RU2078765C1 - 6-оксо-азепиноиндоловые соединения и их физиологически переносимые кислотные соли присоединения, фармацевтическая композиция на их основе и способы их получения - Google Patents
6-оксо-азепиноиндоловые соединения и их физиологически переносимые кислотные соли присоединения, фармацевтическая композиция на их основе и способы их получения Download PDFInfo
- Publication number
- RU2078765C1 RU2078765C1 SU925052604A SU5052604A RU2078765C1 RU 2078765 C1 RU2078765 C1 RU 2078765C1 SU 925052604 A SU925052604 A SU 925052604A SU 5052604 A SU5052604 A SU 5052604A RU 2078765 C1 RU2078765 C1 RU 2078765C1
- Authority
- RU
- Russia
- Prior art keywords
- compounds
- group
- formula
- oxo
- hydrogen
- Prior art date
Links
- 238000000034 method Methods 0.000 title claims abstract description 81
- 150000003839 salts Chemical class 0.000 title claims abstract description 19
- 239000008194 pharmaceutical composition Substances 0.000 title claims abstract 4
- 239000002253 acid Substances 0.000 title claims description 30
- 230000015572 biosynthetic process Effects 0.000 title abstract description 10
- 238000003786 synthesis reaction Methods 0.000 title abstract description 4
- 150000001875 compounds Chemical class 0.000 claims abstract description 234
- 125000000217 alkyl group Chemical group 0.000 claims abstract description 67
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims abstract description 28
- 150000002367 halogens Chemical class 0.000 claims abstract description 21
- 229910052736 halogen Inorganic materials 0.000 claims abstract description 20
- 125000003545 alkoxy group Chemical group 0.000 claims abstract description 16
- 230000000694 effects Effects 0.000 claims abstract description 8
- 208000019695 Migraine disease Diseases 0.000 claims abstract description 6
- 206010027599 migraine Diseases 0.000 claims abstract description 4
- 125000005913 (C3-C6) cycloalkyl group Chemical group 0.000 claims abstract 3
- 239000001257 hydrogen Substances 0.000 claims description 68
- 229910052739 hydrogen Inorganic materials 0.000 claims description 68
- -1 methoxyphenyl group Chemical group 0.000 claims description 47
- 150000002431 hydrogen Chemical class 0.000 claims description 36
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 32
- 125000006239 protecting group Chemical group 0.000 claims description 23
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 21
- 229910052757 nitrogen Inorganic materials 0.000 claims description 21
- 125000003277 amino group Chemical group 0.000 claims description 17
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 claims description 17
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 claims description 15
- 230000003993 interaction Effects 0.000 claims description 15
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 10
- 125000004453 alkoxycarbonyl group Chemical group 0.000 claims description 7
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 claims description 7
- 230000002460 anti-migrenic effect Effects 0.000 claims description 5
- 125000004093 cyano group Chemical group *C#N 0.000 claims description 5
- 230000030135 gastric motility Effects 0.000 claims description 5
- 125000004202 aminomethyl group Chemical group [H]N([H])C([H])([H])* 0.000 claims description 3
- 125000000623 heterocyclic group Chemical group 0.000 claims description 3
- 125000001841 imino group Chemical group [H]N=* 0.000 claims description 3
- 230000000269 nucleophilic effect Effects 0.000 claims description 3
- 229910052760 oxygen Inorganic materials 0.000 claims description 3
- 238000011084 recovery Methods 0.000 claims description 3
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 claims description 2
- 238000003776 cleavage reaction Methods 0.000 claims description 2
- 125000001570 methylene group Chemical group [H]C([H])([*:1])[*:2] 0.000 claims description 2
- 239000001301 oxygen Substances 0.000 claims description 2
- 230000007017 scission Effects 0.000 claims description 2
- 239000004480 active ingredient Substances 0.000 claims 4
- XTFIVUDBNACUBN-UHFFFAOYSA-N 1,3,5-trinitro-1,3,5-triazinane Chemical compound [O-][N+](=O)N1CN([N+]([O-])=O)CN([N+]([O-])=O)C1 XTFIVUDBNACUBN-UHFFFAOYSA-N 0.000 claims 2
- 239000003937 drug carrier Substances 0.000 claims 2
- 229940100198 alkylating agent Drugs 0.000 claims 1
- 239000002168 alkylating agent Substances 0.000 claims 1
- IZFMRMZLDYSGCO-UHFFFAOYSA-N isoindole-1,3-dione;azide Chemical compound [N-]=[N+]=[N-].C1=CC=C2C(=O)NC(=O)C2=C1 IZFMRMZLDYSGCO-UHFFFAOYSA-N 0.000 claims 1
- 230000009471 action Effects 0.000 abstract description 7
- 210000002784 stomach Anatomy 0.000 abstract description 7
- 239000000126 substance Substances 0.000 abstract description 6
- AGPZUEDYVLUKMF-UHFFFAOYSA-N 1,3,4,5-tetrahydro-6h-azepino[5,4,3-cd]indol-6-one Chemical class O=C1NCCC2=CNC3=CC=CC1=C23 AGPZUEDYVLUKMF-UHFFFAOYSA-N 0.000 abstract description 4
- 239000003814 drug Substances 0.000 abstract description 3
- 125000006527 (C1-C5) alkyl group Chemical group 0.000 abstract 2
- 230000037023 motor activity Effects 0.000 abstract 1
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 207
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 99
- 239000000243 solution Substances 0.000 description 91
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 88
- 239000011541 reaction mixture Substances 0.000 description 85
- 239000000203 mixture Substances 0.000 description 76
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 74
- 238000006243 chemical reaction Methods 0.000 description 59
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 46
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 45
- 239000000047 product Substances 0.000 description 42
- 238000002844 melting Methods 0.000 description 41
- 230000008018 melting Effects 0.000 description 41
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 36
- 238000002360 preparation method Methods 0.000 description 34
- 239000002585 base Substances 0.000 description 33
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 33
- 238000012545 processing Methods 0.000 description 32
- 230000002829 reductive effect Effects 0.000 description 28
- QZAYGJVTTNCVMB-UHFFFAOYSA-N serotonin Chemical compound C1=C(O)C=C2C(CCN)=CNC2=C1 QZAYGJVTTNCVMB-UHFFFAOYSA-N 0.000 description 26
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 25
- 125000004432 carbon atom Chemical group C* 0.000 description 25
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 23
- 239000012074 organic phase Substances 0.000 description 23
- 238000004587 chromatography analysis Methods 0.000 description 22
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 20
- 239000003480 eluent Substances 0.000 description 20
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 18
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 18
- 229910052938 sodium sulfate Inorganic materials 0.000 description 18
- 235000011152 sodium sulphate Nutrition 0.000 description 18
- 239000002904 solvent Substances 0.000 description 18
- 238000003756 stirring Methods 0.000 description 18
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 18
- 238000011282 treatment Methods 0.000 description 18
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 16
- 239000012442 inert solvent Substances 0.000 description 16
- 239000000741 silica gel Substances 0.000 description 16
- 229910002027 silica gel Inorganic materials 0.000 description 16
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 15
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 15
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 15
- 239000003054 catalyst Substances 0.000 description 15
- 238000001816 cooling Methods 0.000 description 15
- OAKJQQAXSVQMHS-UHFFFAOYSA-N Hydrazine Chemical compound NN OAKJQQAXSVQMHS-UHFFFAOYSA-N 0.000 description 14
- 239000008346 aqueous phase Substances 0.000 description 14
- 230000009467 reduction Effects 0.000 description 14
- 238000006722 reduction reaction Methods 0.000 description 14
- 238000007792 addition Methods 0.000 description 13
- 239000003638 chemical reducing agent Substances 0.000 description 13
- 230000003287 optical effect Effects 0.000 description 13
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 12
- NPXOKRUENSOPAO-UHFFFAOYSA-N Raney nickel Chemical compound [Al].[Ni] NPXOKRUENSOPAO-UHFFFAOYSA-N 0.000 description 12
- 229910000564 Raney nickel Inorganic materials 0.000 description 12
- 238000003818 flash chromatography Methods 0.000 description 12
- GQHTUMJGOHRCHB-UHFFFAOYSA-N 2,3,4,6,7,8,9,10-octahydropyrimido[1,2-a]azepine Chemical compound C1CCCCN2CCCN=C21 GQHTUMJGOHRCHB-UHFFFAOYSA-N 0.000 description 11
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 11
- 239000007868 Raney catalyst Substances 0.000 description 11
- 230000029936 alkylation Effects 0.000 description 11
- 238000005804 alkylation reaction Methods 0.000 description 11
- 239000012071 phase Substances 0.000 description 11
- 230000001681 protective effect Effects 0.000 description 11
- 239000007864 aqueous solution Substances 0.000 description 10
- 238000001035 drying Methods 0.000 description 10
- 238000005984 hydrogenation reaction Methods 0.000 description 10
- 239000000543 intermediate Substances 0.000 description 10
- 239000012279 sodium borohydride Substances 0.000 description 10
- 229910000033 sodium borohydride Inorganic materials 0.000 description 10
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 9
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 9
- 229960000583 acetic acid Drugs 0.000 description 9
- 238000009903 catalytic hydrogenation reaction Methods 0.000 description 9
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 9
- LYGJENNIWJXYER-UHFFFAOYSA-N nitromethane Chemical compound C[N+]([O-])=O LYGJENNIWJXYER-UHFFFAOYSA-N 0.000 description 9
- 125000004044 trifluoroacetyl group Chemical group FC(C(=O)*)(F)F 0.000 description 9
- OUBIMSKBCIHOJI-UHFFFAOYSA-N 3-aminomethyl-3,4,5,6-tetrahydro-6-oxo-1h-azepino[5,4,3-cd]indole hydrate Chemical compound O.NCC1CNC(=O)C2=CC=CC3=C2C1=CN3 OUBIMSKBCIHOJI-UHFFFAOYSA-N 0.000 description 8
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 8
- 150000001298 alcohols Chemical class 0.000 description 8
- 235000011114 ammonium hydroxide Nutrition 0.000 description 8
- 239000012043 crude product Substances 0.000 description 8
- 150000002148 esters Chemical class 0.000 description 8
- 239000000706 filtrate Substances 0.000 description 8
- 150000008282 halocarbons Chemical class 0.000 description 8
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 8
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 8
- 125000001424 substituent group Chemical group 0.000 description 8
- WFDIJRYMOXRFFG-UHFFFAOYSA-N Acetic anhydride Chemical compound CC(=O)OC(C)=O WFDIJRYMOXRFFG-UHFFFAOYSA-N 0.000 description 7
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical class O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 7
- SIKJAQJRHWYJAI-UHFFFAOYSA-N Indole Chemical compound C1=CC=C2NC=CC2=C1 SIKJAQJRHWYJAI-UHFFFAOYSA-N 0.000 description 7
- 241001465754 Metazoa Species 0.000 description 7
- 235000011054 acetic acid Nutrition 0.000 description 7
- 150000007513 acids Chemical class 0.000 description 7
- 150000004945 aromatic hydrocarbons Chemical class 0.000 description 7
- 210000001367 artery Anatomy 0.000 description 7
- 230000008602 contraction Effects 0.000 description 7
- 150000004292 cyclic ethers Chemical class 0.000 description 7
- 125000001316 cycloalkyl alkyl group Chemical group 0.000 description 7
- 125000000753 cycloalkyl group Chemical group 0.000 description 7
- 238000000354 decomposition reaction Methods 0.000 description 7
- 150000002475 indoles Chemical class 0.000 description 7
- 239000003921 oil Substances 0.000 description 7
- 229920006395 saturated elastomer Polymers 0.000 description 7
- 229940076279 serotonin Drugs 0.000 description 7
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Chemical compound OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 6
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 6
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 6
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 6
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 6
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 6
- IETKFWIJKMWBKU-UHFFFAOYSA-N ac1l4b9k Chemical compound NCC1CNC(=O)C2=CC=CC3=C2C1=CN3 IETKFWIJKMWBKU-UHFFFAOYSA-N 0.000 description 6
- 150000001412 amines Chemical class 0.000 description 6
- 125000004122 cyclic group Chemical group 0.000 description 6
- IXCSERBJSXMMFS-UHFFFAOYSA-N hydrogen chloride Substances Cl.Cl IXCSERBJSXMMFS-UHFFFAOYSA-N 0.000 description 6
- 229910000041 hydrogen chloride Inorganic materials 0.000 description 6
- 239000003960 organic solvent Substances 0.000 description 6
- 230000008569 process Effects 0.000 description 6
- 239000003826 tablet Substances 0.000 description 6
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 6
- NWZSZGALRFJKBT-KNIFDHDWSA-N (2s)-2,6-diaminohexanoic acid;(2s)-2-hydroxybutanedioic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O.NCCCC[C@H](N)C(O)=O NWZSZGALRFJKBT-KNIFDHDWSA-N 0.000 description 5
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 5
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 5
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 5
- CPELXLSAUQHCOX-UHFFFAOYSA-N Hydrogen bromide Chemical compound Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 description 5
- 150000001299 aldehydes Chemical class 0.000 description 5
- 150000001540 azides Chemical class 0.000 description 5
- 239000003795 chemical substances by application Substances 0.000 description 5
- 239000000284 extract Substances 0.000 description 5
- 238000005187 foaming Methods 0.000 description 5
- IKDUDTNKRLTJSI-UHFFFAOYSA-N hydrazine monohydrate Substances O.NN IKDUDTNKRLTJSI-UHFFFAOYSA-N 0.000 description 5
- 125000002768 hydroxyalkyl group Chemical group 0.000 description 5
- RGHXWDVNBYKJQH-UHFFFAOYSA-N nitroacetic acid Chemical compound OC(=O)C[N+]([O-])=O RGHXWDVNBYKJQH-UHFFFAOYSA-N 0.000 description 5
- 230000000144 pharmacologic effect Effects 0.000 description 5
- 238000012360 testing method Methods 0.000 description 5
- QAEDZJGFFMLHHQ-UHFFFAOYSA-N trifluoroacetic anhydride Chemical compound FC(F)(F)C(=O)OC(=O)C(F)(F)F QAEDZJGFFMLHHQ-UHFFFAOYSA-N 0.000 description 5
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 4
- BZLVMXJERCGZMT-UHFFFAOYSA-N Methyl tert-butyl ether Chemical compound COC(C)(C)C BZLVMXJERCGZMT-UHFFFAOYSA-N 0.000 description 4
- 229920002472 Starch Polymers 0.000 description 4
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 4
- 229910052783 alkali metal Inorganic materials 0.000 description 4
- 150000003973 alkyl amines Chemical class 0.000 description 4
- 150000001408 amides Chemical class 0.000 description 4
- HUMNYLRZRPPJDN-UHFFFAOYSA-N benzaldehyde Chemical compound O=CC1=CC=CC=C1 HUMNYLRZRPPJDN-UHFFFAOYSA-N 0.000 description 4
- SIPUZPBQZHNSDW-UHFFFAOYSA-N bis(2-methylpropyl)aluminum Chemical compound CC(C)C[Al]CC(C)C SIPUZPBQZHNSDW-UHFFFAOYSA-N 0.000 description 4
- 238000004440 column chromatography Methods 0.000 description 4
- 238000001704 evaporation Methods 0.000 description 4
- 230000008020 evaporation Effects 0.000 description 4
- 238000002474 experimental method Methods 0.000 description 4
- 235000019253 formic acid Nutrition 0.000 description 4
- 230000002496 gastric effect Effects 0.000 description 4
- PZOUSPYUWWUPPK-UHFFFAOYSA-N indole Natural products CC1=CC=CC2=C1C=CN2 PZOUSPYUWWUPPK-UHFFFAOYSA-N 0.000 description 4
- RKJUIXBNRJVNHR-UHFFFAOYSA-N indolenine Natural products C1=CC=C2CC=NC2=C1 RKJUIXBNRJVNHR-UHFFFAOYSA-N 0.000 description 4
- 150000003951 lactams Chemical group 0.000 description 4
- ZCSHNCUQKCANBX-UHFFFAOYSA-N lithium diisopropylamide Chemical compound [Li+].CC(C)[N-]C(C)C ZCSHNCUQKCANBX-UHFFFAOYSA-N 0.000 description 4
- HWQJAOMFBDZMPB-UHFFFAOYSA-N methyl 3-formyl-1h-indole-4-carboxylate Chemical compound COC(=O)C1=CC=CC2=C1C(C=O)=CN2 HWQJAOMFBDZMPB-UHFFFAOYSA-N 0.000 description 4
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 4
- 150000002825 nitriles Chemical class 0.000 description 4
- 239000012299 nitrogen atmosphere Substances 0.000 description 4
- 125000005543 phthalimide group Chemical group 0.000 description 4
- 229910000027 potassium carbonate Inorganic materials 0.000 description 4
- 239000008107 starch Substances 0.000 description 4
- 235000019698 starch Nutrition 0.000 description 4
- 239000007858 starting material Substances 0.000 description 4
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 4
- CSRZQMIRAZTJOY-UHFFFAOYSA-N trimethylsilyl iodide Chemical compound C[Si](C)(C)I CSRZQMIRAZTJOY-UHFFFAOYSA-N 0.000 description 4
- BASYBBIPCGCPCM-UHFFFAOYSA-N 12-(aminomethyl)-10-methyl-3,10-diazatricyclo[6.4.1.04,13]trideca-1,4,6,8(13)-tetraen-9-one Chemical compound O=C1N(C)CC(CN)C2=CNC3=CC=CC1=C23 BASYBBIPCGCPCM-UHFFFAOYSA-N 0.000 description 3
- XQBIHHWYXCNQEH-UHFFFAOYSA-N 12-(aminomethyl)-3,10-diazatricyclo[6.4.1.04,13]trideca-1,4,6,8(13)-tetraen-9-one hydrochloride Chemical compound Cl.NCC1CNC(=O)C2=CC=CC3=C2C1=CN3 XQBIHHWYXCNQEH-UHFFFAOYSA-N 0.000 description 3
- IAKQRFKTQDYKDK-UHFFFAOYSA-N 12-[(benzylamino)methyl]-3,10-diazatricyclo[6.4.1.04,13]trideca-1,4,6,8(13)-tetraen-9-one Chemical compound C=12C3=CNC2=CC=CC=1C(=O)NCC3CNCC1=CC=CC=C1 IAKQRFKTQDYKDK-UHFFFAOYSA-N 0.000 description 3
- ONLMSCRONKULEK-UHFFFAOYSA-N 3-(n-benzyl-n-methylaminomethyl)-3,4,5,6-tetrahydro-6-oxo-1h-azepino[5,4,3-cd]indole Chemical compound C1NC(=O)C(C2=3)=CC=CC=3NC=C2C1CN(C)CC1=CC=CC=C1 ONLMSCRONKULEK-UHFFFAOYSA-N 0.000 description 3
- WCNLDSVELYMBQX-UHFFFAOYSA-N 3-benzyl-12-[(benzylamino)methyl]-10-methyl-3,10-diazatricyclo[6.4.1.04,13]trideca-1,4,6,8(13)-tetraen-9-one Chemical compound C=12C3=CN(CC=4C=CC=CC=4)C2=CC=CC=1C(=O)N(C)CC3CNCC1=CC=CC=C1 WCNLDSVELYMBQX-UHFFFAOYSA-N 0.000 description 3
- QCQCHGYLTSGIGX-GHXANHINSA-N 4-[[(3ar,5ar,5br,7ar,9s,11ar,11br,13as)-5a,5b,8,8,11a-pentamethyl-3a-[(5-methylpyridine-3-carbonyl)amino]-2-oxo-1-propan-2-yl-4,5,6,7,7a,9,10,11,11b,12,13,13a-dodecahydro-3h-cyclopenta[a]chrysen-9-yl]oxy]-2,2-dimethyl-4-oxobutanoic acid Chemical compound N([C@@]12CC[C@@]3(C)[C@]4(C)CC[C@H]5C(C)(C)[C@@H](OC(=O)CC(C)(C)C(O)=O)CC[C@]5(C)[C@H]4CC[C@@H]3C1=C(C(C2)=O)C(C)C)C(=O)C1=CN=CC(C)=C1 QCQCHGYLTSGIGX-GHXANHINSA-N 0.000 description 3
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 3
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 3
- USFZMSVCRYTOJT-UHFFFAOYSA-N Ammonium acetate Chemical compound N.CC(O)=O USFZMSVCRYTOJT-UHFFFAOYSA-N 0.000 description 3
- 239000005695 Ammonium acetate Substances 0.000 description 3
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonium chloride Substances [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 3
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 3
- 0 C*c1cc(C(N(*)C(*)CC2=CC3*I)=O)c2c3c1 Chemical compound C*c1cc(C(N(*)C(*)CC2=CC3*I)=O)c2c3c1 0.000 description 3
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 3
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 3
- 241000699670 Mus sp. Species 0.000 description 3
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 3
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical compound C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 3
- 239000002262 Schiff base Substances 0.000 description 3
- 150000004753 Schiff bases Chemical class 0.000 description 3
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical class [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 3
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 3
- 206010070863 Toxicity to various agents Diseases 0.000 description 3
- QNZHUGYZWMFBGE-UHFFFAOYSA-N ac1l4b9n Chemical compound Cl.CNCC1CNC(=O)C2=CC=CC3=C2C1=CN3 QNZHUGYZWMFBGE-UHFFFAOYSA-N 0.000 description 3
- ZOPLDNOMWNCKNU-UHFFFAOYSA-N ac1l4b9q Chemical compound CNCC1CNC(=O)C2=CC=CC3=C2C1=CN3 ZOPLDNOMWNCKNU-UHFFFAOYSA-N 0.000 description 3
- 230000002378 acidificating effect Effects 0.000 description 3
- 125000002252 acyl group Chemical group 0.000 description 3
- 230000010933 acylation Effects 0.000 description 3
- 238000005917 acylation reaction Methods 0.000 description 3
- 125000005907 alkyl ester group Chemical group 0.000 description 3
- 230000002152 alkylating effect Effects 0.000 description 3
- 125000002947 alkylene group Chemical group 0.000 description 3
- 150000001409 amidines Chemical class 0.000 description 3
- 235000019257 ammonium acetate Nutrition 0.000 description 3
- 229940043376 ammonium acetate Drugs 0.000 description 3
- 150000008107 benzenesulfonic acids Chemical group 0.000 description 3
- 238000009835 boiling Methods 0.000 description 3
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 3
- 229910052794 bromium Inorganic materials 0.000 description 3
- 239000003153 chemical reaction reagent Substances 0.000 description 3
- 239000000460 chlorine Substances 0.000 description 3
- 229910052801 chlorine Inorganic materials 0.000 description 3
- 230000034994 death Effects 0.000 description 3
- 231100000517 death Toxicity 0.000 description 3
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 3
- 208000035475 disorder Diseases 0.000 description 3
- 230000022244 formylation Effects 0.000 description 3
- 238000006170 formylation reaction Methods 0.000 description 3
- 210000001035 gastrointestinal tract Anatomy 0.000 description 3
- 238000011065 in-situ storage Methods 0.000 description 3
- 210000000936 intestine Anatomy 0.000 description 3
- 229910052744 lithium Inorganic materials 0.000 description 3
- 229940098779 methanesulfonic acid Drugs 0.000 description 3
- 150000004702 methyl esters Chemical class 0.000 description 3
- 150000007524 organic acids Chemical class 0.000 description 3
- 150000007530 organic bases Chemical class 0.000 description 3
- TYJJADVDDVDEDZ-UHFFFAOYSA-M potassium hydrogencarbonate Chemical compound [K+].OC([O-])=O TYJJADVDDVDEDZ-UHFFFAOYSA-M 0.000 description 3
- 239000012264 purified product Substances 0.000 description 3
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 3
- 150000003254 radicals Chemical class 0.000 description 3
- 238000007363 ring formation reaction Methods 0.000 description 3
- 238000000926 separation method Methods 0.000 description 3
- 229910000029 sodium carbonate Inorganic materials 0.000 description 3
- 229910000104 sodium hydride Inorganic materials 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- 125000000542 sulfonic acid group Chemical group 0.000 description 3
- 239000011975 tartaric acid Substances 0.000 description 3
- 235000002906 tartaric acid Nutrition 0.000 description 3
- 229940095064 tartrate Drugs 0.000 description 3
- 238000005406 washing Methods 0.000 description 3
- ODIGIKRIUKFKHP-UHFFFAOYSA-N (n-propan-2-yloxycarbonylanilino) acetate Chemical compound CC(C)OC(=O)N(OC(C)=O)C1=CC=CC=C1 ODIGIKRIUKFKHP-UHFFFAOYSA-N 0.000 description 2
- VOKHNQLNPTWRPI-UHFFFAOYSA-N 1,2,3,3a-tetrahydropyrrolo[2,3-g][1]benzazepine Chemical class C1=CC2=NC=CC=CC2=C2C1CCN2 VOKHNQLNPTWRPI-UHFFFAOYSA-N 0.000 description 2
- YRFBLZCKYULYBG-UHFFFAOYSA-N 11-(aminomethyl)-3,10-diazatricyclo[6.4.1.04,13]trideca-1,4,6,8(13)-tetraen-9-one Chemical compound O=C1NC(CN)CC2=CNC3=CC=CC1=C23 YRFBLZCKYULYBG-UHFFFAOYSA-N 0.000 description 2
- YATLYEGMYHLWQU-UHFFFAOYSA-N 11-(aminomethyl)-3,10-diazatricyclo[6.4.1.04,13]trideca-1,4,6,8(13)-tetraen-9-one hydrochloride Chemical compound Cl.O=C1NC(CN)CC2=CNC3=CC=CC1=C23 YATLYEGMYHLWQU-UHFFFAOYSA-N 0.000 description 2
- FILWJKSXAZUBGZ-UHFFFAOYSA-N 12-(aminomethyl)-3-benzyl-3,10-diazatricyclo[6.4.1.04,13]trideca-1,4,6,8(13)-tetraen-9-one Chemical compound C1=C(C2=3)C(CN)CNC(=O)C2=CC=CC=3N1CC1=CC=CC=C1 FILWJKSXAZUBGZ-UHFFFAOYSA-N 0.000 description 2
- NERKFGLFXIXWFT-UHFFFAOYSA-N 2,2,2-trifluoro-N-[(9-oxo-3,10-diazatricyclo[6.4.1.04,13]trideca-1,4,6,8(13)-tetraen-12-yl)methyl]acetamide Chemical compound FC(F)(F)C(=O)NCC1CNC(=O)C2=CC=CC3=C2C1=CN3 NERKFGLFXIXWFT-UHFFFAOYSA-N 0.000 description 2
- HPDQJWITOVDCHV-UHFFFAOYSA-N 3-(1-piperidinylmethyl)-3,4,5,6-tetrahydro-6-oxo-1h-azepino[5,4,3-cd]indole Chemical compound C=12C3=CNC2=CC=CC=1C(=O)NCC3CN1CCCCC1 HPDQJWITOVDCHV-UHFFFAOYSA-N 0.000 description 2
- OVKALOQTHXBFPP-UHFFFAOYSA-N 3-aminomethyl-5-methoxymethyl-3,4,5,6-tetrahydro-6-oxo-1h-azepino[5,4,3-cd]indole Chemical compound O=C1N(COC)CC(CN)C2=CNC3=CC=CC1=C23 OVKALOQTHXBFPP-UHFFFAOYSA-N 0.000 description 2
- PJHBTAHSBNNPKN-UHFFFAOYSA-N 4-(4-phenylpiperazin-1-ylmethyl)-3,4,5,6-tetrahydro-6-oxo-1h-azepino[5,4,3-cd]indole Chemical compound C1C(C=23)=CNC3=CC=CC=2C(=O)NC1CN(CC1)CCN1C1=CC=CC=C1 PJHBTAHSBNNPKN-UHFFFAOYSA-N 0.000 description 2
- GUQRPODJFHTNGU-UHFFFAOYSA-N 4-(p-toluenesulfonyloxymethyl)-3,4,5,6-tetrahydro-6-oxo-1h-azepino[5,4,3-cd]indole Chemical compound C1=CC(C)=CC=C1S(=O)(=O)OCC(C1)NC(=O)C2=C3C1=CNC3=CC=C2 GUQRPODJFHTNGU-UHFFFAOYSA-N 0.000 description 2
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- ROSDSFDQCJNGOL-UHFFFAOYSA-N Dimethylamine Chemical compound CNC ROSDSFDQCJNGOL-UHFFFAOYSA-N 0.000 description 2
- 108010010803 Gelatin Proteins 0.000 description 2
- YQEZLKZALYSWHR-UHFFFAOYSA-N Ketamine Chemical compound C=1C=CC=C(Cl)C=1C1(NC)CCCCC1=O YQEZLKZALYSWHR-UHFFFAOYSA-N 0.000 description 2
- 241000124008 Mammalia Species 0.000 description 2
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical compound C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 2
- ATHHXGZTWNVVOU-UHFFFAOYSA-N N-methylformamide Chemical compound CNC=O ATHHXGZTWNVVOU-UHFFFAOYSA-N 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 2
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 2
- PXIPVTKHYLBLMZ-UHFFFAOYSA-N Sodium azide Chemical compound [Na+].[N-]=[N+]=[N-] PXIPVTKHYLBLMZ-UHFFFAOYSA-N 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 150000001241 acetals Chemical class 0.000 description 2
- 239000013543 active substance Substances 0.000 description 2
- 125000001931 aliphatic group Chemical group 0.000 description 2
- 150000001340 alkali metals Chemical class 0.000 description 2
- 238000007281 aminoalkylation reaction Methods 0.000 description 2
- 150000008064 anhydrides Chemical class 0.000 description 2
- 150000001450 anions Chemical class 0.000 description 2
- 125000002785 azepinyl group Chemical group 0.000 description 2
- 230000009286 beneficial effect Effects 0.000 description 2
- ILAHWRKJUDSMFH-UHFFFAOYSA-N boron tribromide Chemical compound BrB(Br)Br ILAHWRKJUDSMFH-UHFFFAOYSA-N 0.000 description 2
- 210000004556 brain Anatomy 0.000 description 2
- 125000001589 carboacyl group Chemical group 0.000 description 2
- 239000000969 carrier Substances 0.000 description 2
- 230000003197 catalytic effect Effects 0.000 description 2
- MVPPADPHJFYWMZ-UHFFFAOYSA-N chlorobenzene Chemical compound ClC1=CC=CC=C1 MVPPADPHJFYWMZ-UHFFFAOYSA-N 0.000 description 2
- 239000013065 commercial product Substances 0.000 description 2
- 238000007796 conventional method Methods 0.000 description 2
- 230000001186 cumulative effect Effects 0.000 description 2
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 2
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 2
- HPNMFZURTQLUMO-UHFFFAOYSA-N diethylamine Chemical compound CCNCC HPNMFZURTQLUMO-UHFFFAOYSA-N 0.000 description 2
- 229940079593 drug Drugs 0.000 description 2
- 125000004185 ester group Chemical group 0.000 description 2
- 125000002485 formyl group Chemical group [H]C(*)=O 0.000 description 2
- 239000001530 fumaric acid Substances 0.000 description 2
- 235000011087 fumaric acid Nutrition 0.000 description 2
- 239000008273 gelatin Substances 0.000 description 2
- 229920000159 gelatin Polymers 0.000 description 2
- 235000019322 gelatine Nutrition 0.000 description 2
- 235000011852 gelatine desserts Nutrition 0.000 description 2
- 239000012362 glacial acetic acid Substances 0.000 description 2
- 239000008187 granular material Substances 0.000 description 2
- 229940093915 gynecological organic acid Drugs 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- 238000004128 high performance liquid chromatography Methods 0.000 description 2
- 150000004678 hydrides Chemical class 0.000 description 2
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 2
- 229910000042 hydrogen bromide Inorganic materials 0.000 description 2
- 238000000338 in vitro Methods 0.000 description 2
- CGIGDMFJXJATDK-UHFFFAOYSA-N indomethacin Chemical compound CC1=C(CC(O)=O)C2=CC(OC)=CC=C2N1C(=O)C1=CC=C(Cl)C=C1 CGIGDMFJXJATDK-UHFFFAOYSA-N 0.000 description 2
- 150000007529 inorganic bases Chemical class 0.000 description 2
- 238000007912 intraperitoneal administration Methods 0.000 description 2
- INQOMBQAUSQDDS-UHFFFAOYSA-N iodomethane Chemical compound IC INQOMBQAUSQDDS-UHFFFAOYSA-N 0.000 description 2
- 238000002955 isolation Methods 0.000 description 2
- 229960003299 ketamine Drugs 0.000 description 2
- 150000002576 ketones Chemical class 0.000 description 2
- SXQFCVDSOLSHOQ-UHFFFAOYSA-N lactamide Chemical group CC(O)C(N)=O SXQFCVDSOLSHOQ-UHFFFAOYSA-N 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 2
- 238000003819 low-pressure liquid chromatography Methods 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 150000007522 mineralic acids Chemical class 0.000 description 2
- 239000012452 mother liquor Substances 0.000 description 2
- 230000004899 motility Effects 0.000 description 2
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 2
- RPMXALUWKZHYOV-UHFFFAOYSA-N nitroethene Chemical group [O-][N+](=O)C=C RPMXALUWKZHYOV-UHFFFAOYSA-N 0.000 description 2
- 235000005985 organic acids Nutrition 0.000 description 2
- 125000001979 organolithium group Chemical group 0.000 description 2
- QNGNSVIICDLXHT-UHFFFAOYSA-N para-ethylbenzaldehyde Natural products CCC1=CC=C(C=O)C=C1 QNGNSVIICDLXHT-UHFFFAOYSA-N 0.000 description 2
- YZTJYBJCZXZGCT-UHFFFAOYSA-N phenylpiperazine Chemical group C1CNCCN1C1=CC=CC=C1 YZTJYBJCZXZGCT-UHFFFAOYSA-N 0.000 description 2
- XHXFXVLFKHQFAL-UHFFFAOYSA-N phosphoryl trichloride Chemical compound ClP(Cl)(Cl)=O XHXFXVLFKHQFAL-UHFFFAOYSA-N 0.000 description 2
- LPNYRYFBWFDTMA-UHFFFAOYSA-N potassium tert-butoxide Chemical compound [K+].CC(C)(C)[O-] LPNYRYFBWFDTMA-UHFFFAOYSA-N 0.000 description 2
- 238000005932 reductive alkylation reaction Methods 0.000 description 2
- 238000010992 reflux Methods 0.000 description 2
- BEOOHQFXGBMRKU-UHFFFAOYSA-N sodium cyanoborohydride Chemical compound [Na+].[B-]C#N BEOOHQFXGBMRKU-UHFFFAOYSA-N 0.000 description 2
- 239000012312 sodium hydride Substances 0.000 description 2
- 239000011877 solvent mixture Substances 0.000 description 2
- 230000004936 stimulating effect Effects 0.000 description 2
- 150000003460 sulfonic acids Chemical class 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- 239000000454 talc Substances 0.000 description 2
- 235000012222 talc Nutrition 0.000 description 2
- 229910052623 talc Inorganic materials 0.000 description 2
- FYSNRJHAOHDILO-UHFFFAOYSA-N thionyl chloride Chemical compound ClS(Cl)=O FYSNRJHAOHDILO-UHFFFAOYSA-N 0.000 description 2
- 231100000816 toxic dose Toxicity 0.000 description 2
- TUQOTMZNTHZOKS-UHFFFAOYSA-N tributylphosphine Chemical compound CCCCP(CCCC)CCCC TUQOTMZNTHZOKS-UHFFFAOYSA-N 0.000 description 2
- AQRLNPVMDITEJU-UHFFFAOYSA-N triethylsilane Chemical compound CC[SiH](CC)CC AQRLNPVMDITEJU-UHFFFAOYSA-N 0.000 description 2
- 230000002792 vascular Effects 0.000 description 2
- 238000005303 weighing Methods 0.000 description 2
- BPICBUSOMSTKRF-UHFFFAOYSA-N xylazine Chemical compound CC1=CC=CC(C)=C1NC1=NCCCS1 BPICBUSOMSTKRF-UHFFFAOYSA-N 0.000 description 2
- 229960001600 xylazine Drugs 0.000 description 2
- JIAARYAFYJHUJI-UHFFFAOYSA-L zinc dichloride Chemical compound [Cl-].[Cl-].[Zn+2] JIAARYAFYJHUJI-UHFFFAOYSA-L 0.000 description 2
- SHAHPWSYJFYMRX-GDLCADMTSA-N (2S)-2-(4-{[(1R,2S)-2-hydroxycyclopentyl]methyl}phenyl)propanoic acid Chemical compound C1=CC([C@@H](C(O)=O)C)=CC=C1C[C@@H]1[C@@H](O)CCC1 SHAHPWSYJFYMRX-GDLCADMTSA-N 0.000 description 1
- RPFNQFNIFCRPHP-UHFFFAOYSA-N (9-oxo-3,10-diazatricyclo[6.4.1.04,13]trideca-1,4,6,8(13)-tetraen-3-yl)methyl 4-methylbenzenesulfonate Chemical compound CC1=CC=C(C=C1)S(=O)(=O)OCN1C=C2C=3C(=CC=CC1=3)C(NCC2)=O RPFNQFNIFCRPHP-UHFFFAOYSA-N 0.000 description 1
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 1
- SCZNXLWKYFICFV-UHFFFAOYSA-N 1,2,3,4,5,7,8,9-octahydropyrido[1,2-b]diazepine Chemical compound C1CCCNN2CCCC=C21 SCZNXLWKYFICFV-UHFFFAOYSA-N 0.000 description 1
- GVUOUPMJAPXKFT-UHFFFAOYSA-N 1-benzyl-3-aminomethyl-3,4,5,6-tetrahydro-6-oxo-1h-azepino[5,4,3-cd]indole hydrochloride Chemical compound Cl.C1=C(C2=3)C(CN)CNC(=O)C2=CC=CC=3N1CC1=CC=CC=C1 GVUOUPMJAPXKFT-UHFFFAOYSA-N 0.000 description 1
- OOUZDWNMZJVAGK-UHFFFAOYSA-N 11-(2-aminoethyl)-3,10-diazatricyclo[6.4.1.04,13]trideca-1,4,6,8(13)-tetraen-9-one Chemical compound O=C1NC(CCN)CC2=CNC3=CC=CC1=C23 OOUZDWNMZJVAGK-UHFFFAOYSA-N 0.000 description 1
- JGXCIBWFJLGJCN-UHFFFAOYSA-N 11-(hydroxymethyl)-3,10-diazatricyclo[6.4.1.04,13]trideca-1,4,6,8(13)-tetraen-9-one Chemical compound O=C1NC(CO)CC2=CNC3=CC=CC1=C23 JGXCIBWFJLGJCN-UHFFFAOYSA-N 0.000 description 1
- SKICPKRSCWTXTC-UHFFFAOYSA-N 12-(aminomethyl)-3,10-diazatricyclo[6.4.1.04,13]trideca-1,4,6,8(13)-tetraen-9-one hydrate hydrochloride Chemical compound O.Cl.NCC1CNC(=O)C2=CC=CC3=C2C1=CN3 SKICPKRSCWTXTC-UHFFFAOYSA-N 0.000 description 1
- DSTRRFRKDPBVPK-UHFFFAOYSA-N 12-(aminomethyl)-3-(3-phenylpropyl)-3,10-diazatricyclo[6.4.1.04,13]trideca-1,4,6,8(13)-tetraen-9-one Chemical compound C1=C(C2=3)C(CN)CNC(=O)C2=CC=CC=3N1CCCC1=CC=CC=C1 DSTRRFRKDPBVPK-UHFFFAOYSA-N 0.000 description 1
- GEWJXCGKSRCLCR-UHFFFAOYSA-N 12-(aminomethyl)-3-(3-phenylpropyl)-3,10-diazatricyclo[6.4.1.04,13]trideca-1,4,6,8(13)-tetraen-9-one hydrochloride Chemical compound Cl.C1=C(C2=3)C(CN)CNC(=O)C2=CC=CC=3N1CCCC1=CC=CC=C1 GEWJXCGKSRCLCR-UHFFFAOYSA-N 0.000 description 1
- IKYMKJFORLWACJ-UHFFFAOYSA-N 12-(aminomethyl)-3-methyl-3,10-diazatricyclo[6.4.1.04,13]trideca-1,4,6,8(13)-tetraen-9-one Chemical compound NCC1CNC(=O)C2=CC=CC3=C2C1=CN3C IKYMKJFORLWACJ-UHFFFAOYSA-N 0.000 description 1
- RCFRBOGCYIBUCD-UHFFFAOYSA-N 12-(aminomethyl)-3-methyl-3,10-diazatricyclo[6.4.1.04,13]trideca-1,4,6,8(13)-tetraen-9-one hydrochloride Chemical compound Cl.NCC1CNC(=O)C2=CC=CC3=C2C1=CN3C RCFRBOGCYIBUCD-UHFFFAOYSA-N 0.000 description 1
- WPZGUMXESHZVFM-UHFFFAOYSA-N 12-(diethylaminomethyl)-3,10-diazatricyclo[6.4.1.04,13]trideca-1,4,6,8(13)-tetraen-9-one Chemical compound CCN(CC)CC1CNC(=O)C2=CC=CC3=C2C1=CN3 WPZGUMXESHZVFM-UHFFFAOYSA-N 0.000 description 1
- ITPPUDJVOOBTLV-UHFFFAOYSA-N 12-(ethylaminomethyl)-3,10-diazatricyclo[6.4.1.04,13]trideca-1,4,6,8(13)-tetraen-9-one Chemical compound CCNCC1CNC(=O)C2=CC=CC3=C2C1=CN3 ITPPUDJVOOBTLV-UHFFFAOYSA-N 0.000 description 1
- ZXESTJDOQYNNFQ-UHFFFAOYSA-N 12-[(benzylamino)methyl]-3,10-diazatricyclo[6.4.1.04,13]trideca-1,4,6,8(13)-tetraen-9-one hydrochloride Chemical compound Cl.C=12C3=CNC2=CC=CC=1C(=O)NCC3CNCC1=CC=CC=C1 ZXESTJDOQYNNFQ-UHFFFAOYSA-N 0.000 description 1
- MFKKNWJTSJMVPG-UHFFFAOYSA-N 12-[[(4-hydroxyphenyl)methylamino]methyl]-3,10-diazatricyclo[6.4.1.04,13]trideca-1,4,6,8(13)-tetraen-9-one Chemical compound C1=CC(O)=CC=C1CNCC(CNC1=O)C2=CNC3=C2C1=CC=C3 MFKKNWJTSJMVPG-UHFFFAOYSA-N 0.000 description 1
- PZFODDDHMDBREA-UHFFFAOYSA-N 12-amino-3-methyl-3,10-diazatricyclo[6.4.1.04,13]trideca-1,4,6,8(13)-tetraen-9-one Chemical compound NC1CNC(C=2C=3C1=CN(C=3C=CC=2)C)=O PZFODDDHMDBREA-UHFFFAOYSA-N 0.000 description 1
- BQLKDRKXLYBIQR-UHFFFAOYSA-N 1h-indol-1-ium;hydroxide Chemical compound O.C1=CC=C2NC=CC2=C1 BQLKDRKXLYBIQR-UHFFFAOYSA-N 0.000 description 1
- JKXBPYWMWCKBHA-UHFFFAOYSA-N 2,2,2-trifluoro-N-[[9-oxo-3-(3-phenylpropyl)-3,10-diazatricyclo[6.4.1.04,13]trideca-1,4,6,8(13)-tetraen-12-yl]methyl]acetamide Chemical compound C1=C(C2=3)C(CNC(=O)C(F)(F)F)CNC(=O)C2=CC=CC=3N1CCCC1=CC=CC=C1 JKXBPYWMWCKBHA-UHFFFAOYSA-N 0.000 description 1
- KGLPWQKSKUVKMJ-UHFFFAOYSA-N 2,3-dihydrophthalazine-1,4-dione Chemical compound C1=CC=C2C(=O)NNC(=O)C2=C1 KGLPWQKSKUVKMJ-UHFFFAOYSA-N 0.000 description 1
- OBJYGYSEDOUCGU-UHFFFAOYSA-N 2-(9-oxo-3,10-diazatricyclo[6.4.1.04,13]trideca-1,4,6,8(13)-tetraen-11-yl)acetonitrile Chemical compound O=C1NC(CC#N)CC2=CNC3=CC=CC1=C23 OBJYGYSEDOUCGU-UHFFFAOYSA-N 0.000 description 1
- WJYLMMNPQWEDQG-UHFFFAOYSA-N 2-(ethoxycarbonylamino)-4-methylpentanoic acid Chemical compound CCOC(=O)NC(C(O)=O)CC(C)C WJYLMMNPQWEDQG-UHFFFAOYSA-N 0.000 description 1
- LBLYYCQCTBFVLH-UHFFFAOYSA-N 2-Methylbenzenesulfonic acid Chemical compound CC1=CC=CC=C1S(O)(=O)=O LBLYYCQCTBFVLH-UHFFFAOYSA-N 0.000 description 1
- 125000000022 2-aminoethyl group Chemical group [H]C([*])([H])C([H])([H])N([H])[H] 0.000 description 1
- JUSXLWAFYVKNLT-UHFFFAOYSA-N 2-bromobenzenesulfonic acid Chemical compound OS(=O)(=O)C1=CC=CC=C1Br JUSXLWAFYVKNLT-UHFFFAOYSA-N 0.000 description 1
- JFLUOXBOIZOSRC-UHFFFAOYSA-N 2-ethyl-1h-indole-4-carboxylic acid Chemical compound C1=CC=C2NC(CC)=CC2=C1C(O)=O JFLUOXBOIZOSRC-UHFFFAOYSA-N 0.000 description 1
- SZMXXBSCVLNOCZ-UHFFFAOYSA-N 3-(1,3-dinitropropan-2-yl)-1H-indole-4-carboxylic acid Chemical compound [N+](=O)([O-])CC(C[N+](=O)[O-])C1=CNC=2C=CC=C(C1=2)C(=O)O SZMXXBSCVLNOCZ-UHFFFAOYSA-N 0.000 description 1
- UYZHCASXEHRCRF-UHFFFAOYSA-N 3-(1,3-dinitropropan-2-yl)-1h-indole Chemical compound C1=CC=C2C(C(C[N+]([O-])=O)C[N+](=O)[O-])=CNC2=C1 UYZHCASXEHRCRF-UHFFFAOYSA-N 0.000 description 1
- LDFQPSKVEGLCPF-UHFFFAOYSA-N 3-(dimethylaminomethylideneaminomethyl)-3,4,5,6-tetrahydro-6-oxo-1h-azepino[5,4,3-cd]indole Chemical compound CN(C)C=NCC1CNC(=O)C2=CC=CC3=C2C1=CN3 LDFQPSKVEGLCPF-UHFFFAOYSA-N 0.000 description 1
- FOEIERVBCCAEPF-UHFFFAOYSA-N 3-(n-diphenylmethyl-n-methylamino)-3,4,5,6-tetrahydro-6-oxo-1h-azepino[5,4,3-cd]indole Chemical compound C1NC(=O)C(C2=3)=CC=CC=3NC=C2C1N(C)C(C=1C=CC=CC=1)C1=CC=CC=C1 FOEIERVBCCAEPF-UHFFFAOYSA-N 0.000 description 1
- IETACHKVJHNQID-UHFFFAOYSA-N 3-[n-(diphenylmethyl)aminomethyl]-3,4,5,6-tetrahydro-6-oxo-1h-azepino[5,4,3-cd]indole Chemical compound C=12C3=CNC2=CC=CC=1C(=O)NCC3CNC(C=1C=CC=CC=1)C1=CC=CC=C1 IETACHKVJHNQID-UHFFFAOYSA-N 0.000 description 1
- XMZQWZJMTBCUFT-UHFFFAOYSA-N 3-bromopropylbenzene Chemical compound BrCCCC1=CC=CC=C1 XMZQWZJMTBCUFT-UHFFFAOYSA-N 0.000 description 1
- YBGLTBUHWAZATH-UHFFFAOYSA-N 3-isopropylaminomethyl-3,4,5,6-tetrahydro-6-oxo-1h-azepino[5,4,3-cd]indole Chemical compound CC(C)NCC1CNC(=O)C2=CC=CC3=C2C1=CN3 YBGLTBUHWAZATH-UHFFFAOYSA-N 0.000 description 1
- QEJZJCKTZMWECY-UHFFFAOYSA-N 3-trifluoroacetamidomethyl-5-hydroxymethyl-3,4,5,6-tetrahydro-6-oxo-1h-azepino[5,4,3-cd]indole Chemical compound O=C1N(CO)CC(CNC(=O)C(F)(F)F)C2=CNC3=CC=CC1=C23 QEJZJCKTZMWECY-UHFFFAOYSA-N 0.000 description 1
- 125000003143 4-hydroxybenzyl group Chemical group [H]C([*])([H])C1=C([H])C([H])=C(O[H])C([H])=C1[H] 0.000 description 1
- YYROPELSRYBVMQ-UHFFFAOYSA-N 4-toluenesulfonyl chloride Chemical compound CC1=CC=C(S(Cl)(=O)=O)C=C1 YYROPELSRYBVMQ-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- 208000004998 Abdominal Pain Diseases 0.000 description 1
- 229930003347 Atropine Natural products 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-M Bicarbonate Chemical class OC([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-M 0.000 description 1
- LSNNMFCWUKXFEE-UHFFFAOYSA-M Bisulfite Chemical compound OS([O-])=O LSNNMFCWUKXFEE-UHFFFAOYSA-M 0.000 description 1
- DKPFZGUDAPQIHT-UHFFFAOYSA-N Butyl acetate Natural products CCCCOC(C)=O DKPFZGUDAPQIHT-UHFFFAOYSA-N 0.000 description 1
- BMTAFVWTTFSTOG-UHFFFAOYSA-N Butylate Chemical compound CCSC(=O)N(CC(C)C)CC(C)C BMTAFVWTTFSTOG-UHFFFAOYSA-N 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- 208000017228 Gastrointestinal motility disease Diseases 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 206010019233 Headaches Diseases 0.000 description 1
- RKUNBYITZUJHSG-UHFFFAOYSA-N Hyosciamin-hydrochlorid Natural products CN1C(C2)CCC1CC2OC(=O)C(CO)C1=CC=CC=C1 RKUNBYITZUJHSG-UHFFFAOYSA-N 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-M L-tartrate(1-) Chemical compound OC(=O)[C@H](O)[C@@H](O)C([O-])=O FEWJPZIEWOKRBE-JCYAYHJZSA-M 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- 239000012448 Lithium borohydride Substances 0.000 description 1
- 238000006683 Mannich reaction Methods 0.000 description 1
- CXFAYTSBUJGUEI-UHFFFAOYSA-N N,N-dimethyl-N'-[(9-oxo-3,10-diazatricyclo[6.4.1.04,13]trideca-1,4,6,8(13)-tetraen-12-yl)methyl]methanimidamide hydrochloride Chemical compound Cl.CN(C)C=NCC1CNC(=O)C2=CC=CC3=C2C1=CN3 CXFAYTSBUJGUEI-UHFFFAOYSA-N 0.000 description 1
- ZSXGLVDWWRXATF-UHFFFAOYSA-N N,N-dimethylformamide dimethyl acetal Chemical compound COC(OC)N(C)C ZSXGLVDWWRXATF-UHFFFAOYSA-N 0.000 description 1
- XXIPFVRNOPTHDA-UHFFFAOYSA-N N-benzyl-N-[(3-benzyl-9-oxo-3,10-diazatricyclo[6.4.1.04,13]trideca-1,4,6,8(13)-tetraen-12-yl)methyl]-2,2,2-trifluoroacetamide Chemical compound C=1C=CC=CC=1CN(C(=O)C(F)(F)F)CC(C(=C1)C2=3)CNC(=O)C2=CC=CC=3N1CC1=CC=CC=C1 XXIPFVRNOPTHDA-UHFFFAOYSA-N 0.000 description 1
- TZYWCYJVHRLUCT-VABKMULXSA-N N-benzyloxycarbonyl-L-leucyl-L-leucyl-L-leucinal Chemical compound CC(C)C[C@@H](C=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(C)C)NC(=O)OCC1=CC=CC=C1 TZYWCYJVHRLUCT-VABKMULXSA-N 0.000 description 1
- 206010028813 Nausea Diseases 0.000 description 1
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 1
- HLOAQVYSVOPSTF-WLHGVMLRSA-N OC(=O)\C=C\C(O)=O.C1NC(=O)C(C2=3)=CC=CC=3NC=C2C1CN(C)CC1=CC=CC=C1 Chemical compound OC(=O)\C=C\C(O)=O.C1NC(=O)C(C2=3)=CC=CC=3NC=C2C1CN(C)CC1=CC=CC=C1 HLOAQVYSVOPSTF-WLHGVMLRSA-N 0.000 description 1
- 208000002193 Pain Diseases 0.000 description 1
- YGYAWVDWMABLBF-UHFFFAOYSA-N Phosgene Chemical compound ClC(Cl)=O YGYAWVDWMABLBF-UHFFFAOYSA-N 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- UIIMBOGNXHQVGW-DEQYMQKBSA-M Sodium bicarbonate-14C Chemical compound [Na+].O[14C]([O-])=O UIIMBOGNXHQVGW-DEQYMQKBSA-M 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- 206010046996 Varicose vein Diseases 0.000 description 1
- 150000001242 acetic acid derivatives Chemical class 0.000 description 1
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 1
- 150000008065 acid anhydrides Chemical class 0.000 description 1
- 125000004423 acyloxy group Chemical group 0.000 description 1
- 239000000443 aerosol Substances 0.000 description 1
- 230000001270 agonistic effect Effects 0.000 description 1
- 229910000288 alkali metal carbonate Inorganic materials 0.000 description 1
- 150000008041 alkali metal carbonates Chemical class 0.000 description 1
- 229910000102 alkali metal hydride Inorganic materials 0.000 description 1
- 150000008046 alkali metal hydrides Chemical class 0.000 description 1
- 150000008044 alkali metal hydroxides Chemical class 0.000 description 1
- 125000005234 alkyl aluminium group Chemical group 0.000 description 1
- 150000005215 alkyl ethers Chemical class 0.000 description 1
- 150000001351 alkyl iodides Chemical class 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 125000006295 amino methylene group Chemical group [H]N(*)C([H])([H])* 0.000 description 1
- 125000004103 aminoalkyl group Chemical group 0.000 description 1
- 229910021529 ammonia Inorganic materials 0.000 description 1
- 239000001099 ammonium carbonate Substances 0.000 description 1
- 235000012501 ammonium carbonate Nutrition 0.000 description 1
- 230000003444 anaesthetic effect Effects 0.000 description 1
- 239000011260 aqueous acid Substances 0.000 description 1
- 239000012736 aqueous medium Substances 0.000 description 1
- 238000006565 aromatic formylation reaction Methods 0.000 description 1
- 239000010425 asbestos Substances 0.000 description 1
- RKUNBYITZUJHSG-SPUOUPEWSA-N atropine Chemical compound O([C@H]1C[C@H]2CC[C@@H](C1)N2C)C(=O)C(CO)C1=CC=CC=C1 RKUNBYITZUJHSG-SPUOUPEWSA-N 0.000 description 1
- 229960000396 atropine Drugs 0.000 description 1
- CBHOOMGKXCMKIR-UHFFFAOYSA-N azane;methanol Chemical compound N.OC CBHOOMGKXCMKIR-UHFFFAOYSA-N 0.000 description 1
- DXZDEAJXVCLRLE-UHFFFAOYSA-N azepin-2-one Chemical group O=C1C=CC=CC=N1 DXZDEAJXVCLRLE-UHFFFAOYSA-N 0.000 description 1
- SRSXLGNVWSONIS-UHFFFAOYSA-N benzenesulfonic acid Chemical compound OS(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-N 0.000 description 1
- 229940092714 benzenesulfonic acid Drugs 0.000 description 1
- RWCCWEUUXYIKHB-UHFFFAOYSA-N benzophenone Chemical compound C=1C=CC=CC=1C(=O)C1=CC=CC=C1 RWCCWEUUXYIKHB-UHFFFAOYSA-N 0.000 description 1
- 239000012965 benzophenone Substances 0.000 description 1
- AGEZXYOZHKGVCM-UHFFFAOYSA-N benzyl bromide Chemical compound BrCC1=CC=CC=C1 AGEZXYOZHKGVCM-UHFFFAOYSA-N 0.000 description 1
- 230000008033 biological extinction Effects 0.000 description 1
- UORVGPXVDQYIDP-BJUDXGSMSA-N borane Chemical compound [10BH3] UORVGPXVDQYIDP-BJUDXGSMSA-N 0.000 description 1
- 229910000085 borane Inorganic materials 0.000 description 1
- RJTANRZEWTUVMA-UHFFFAOYSA-N boron;n-methylmethanamine Chemical compound [B].CNC RJTANRZEWTUVMA-UHFFFAOYSA-N 0.000 description 1
- 125000001246 bromo group Chemical group Br* 0.000 description 1
- RDHPKYGYEGBMSE-UHFFFAOYSA-N bromoethane Chemical compound CCBr RDHPKYGYEGBMSE-UHFFFAOYSA-N 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 229910002091 carbon monoxide Inorganic materials 0.000 description 1
- 150000004649 carbonic acid derivatives Chemical class 0.000 description 1
- 150000001244 carboxylic acid anhydrides Chemical class 0.000 description 1
- 230000002490 cerebral effect Effects 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 150000008280 chlorinated hydrocarbons Chemical class 0.000 description 1
- 125000001309 chloro group Chemical group Cl* 0.000 description 1
- 238000013375 chromatographic separation Methods 0.000 description 1
- 230000001595 contractor effect Effects 0.000 description 1
- 150000001923 cyclic compounds Chemical class 0.000 description 1
- 125000004210 cyclohexylmethyl group Chemical group [H]C([H])(*)C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- HCAJEUSONLESMK-UHFFFAOYSA-N cyclohexylsulfamic acid Chemical compound OS(=O)(=O)NC1CCCCC1 HCAJEUSONLESMK-UHFFFAOYSA-N 0.000 description 1
- 125000004186 cyclopropylmethyl group Chemical group [H]C([H])(*)C1([H])C([H])([H])C1([H])[H] 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 238000006264 debenzylation reaction Methods 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 238000007257 deesterification reaction Methods 0.000 description 1
- 238000012217 deletion Methods 0.000 description 1
- 230000037430 deletion Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 239000012973 diazabicyclooctane Substances 0.000 description 1
- FJBFPHVGVWTDIP-UHFFFAOYSA-N dibromomethane Chemical compound BrCBr FJBFPHVGVWTDIP-UHFFFAOYSA-N 0.000 description 1
- 150000001991 dicarboxylic acids Chemical class 0.000 description 1
- 125000006264 diethylaminomethyl group Chemical group [H]C([H])([H])C([H])([H])N(C([H])([H])*)C([H])([H])C([H])([H])[H] 0.000 description 1
- VAYGXNSJCAHWJZ-UHFFFAOYSA-N dimethyl sulfate Chemical compound COS(=O)(=O)OC VAYGXNSJCAHWJZ-UHFFFAOYSA-N 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 238000004821 distillation Methods 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 230000032050 esterification Effects 0.000 description 1
- 238000005886 esterification reaction Methods 0.000 description 1
- DZGCGKFAPXFTNM-UHFFFAOYSA-N ethanol;hydron;chloride Chemical compound Cl.CCO DZGCGKFAPXFTNM-UHFFFAOYSA-N 0.000 description 1
- UYMKPFRHYYNDTL-UHFFFAOYSA-N ethenamine Chemical group NC=C UYMKPFRHYYNDTL-UHFFFAOYSA-N 0.000 description 1
- 125000001033 ether group Chemical group 0.000 description 1
- 150000002170 ethers Chemical class 0.000 description 1
- ADTFTNVSZFZSSV-UHFFFAOYSA-N ethyl 9-oxo-3,10-diazatricyclo[6.4.1.04,13]trideca-1,4,6,8(13)-tetraene-11-carboxylate Chemical compound C(C)OC(=O)C1CC2=CNC=3C=CC=C(C23)C(N1)=O ADTFTNVSZFZSSV-UHFFFAOYSA-N 0.000 description 1
- IIEWJVIFRVWJOD-UHFFFAOYSA-N ethyl cyclohexane Natural products CCC1CCCCC1 IIEWJVIFRVWJOD-UHFFFAOYSA-N 0.000 description 1
- 125000004494 ethyl ester group Chemical group 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 238000001640 fractional crystallisation Methods 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 231100000869 headache Toxicity 0.000 description 1
- FUZZWVXGSFPDMH-UHFFFAOYSA-N hexanoic acid Chemical compound CCCCCC(O)=O FUZZWVXGSFPDMH-UHFFFAOYSA-N 0.000 description 1
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical compound I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 1
- 229910000043 hydrogen iodide Inorganic materials 0.000 description 1
- 238000007327 hydrogenolysis reaction Methods 0.000 description 1
- RJTZUHVCZIGJMB-UHFFFAOYSA-N hydron;1h-indole;chloride Chemical compound Cl.C1=CC=C2NC=CC2=C1 RJTZUHVCZIGJMB-UHFFFAOYSA-N 0.000 description 1
- 125000004029 hydroxymethyl group Chemical group [H]OC([H])([H])* 0.000 description 1
- 229960000905 indomethacin Drugs 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 150000002484 inorganic compounds Chemical class 0.000 description 1
- PNDPGZBMCMUPRI-UHFFFAOYSA-N iodine Chemical compound II PNDPGZBMCMUPRI-UHFFFAOYSA-N 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 239000003456 ion exchange resin Substances 0.000 description 1
- 229920003303 ion-exchange polymer Polymers 0.000 description 1
- 208000002551 irritable bowel syndrome Diseases 0.000 description 1
- JMMWKPVZQRWMSS-UHFFFAOYSA-N isopropanol acetate Natural products CC(C)OC(C)=O JMMWKPVZQRWMSS-UHFFFAOYSA-N 0.000 description 1
- 239000004310 lactic acid Substances 0.000 description 1
- 235000014655 lactic acid Nutrition 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- 239000001630 malic acid Substances 0.000 description 1
- 235000011090 malic acid Nutrition 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 125000004184 methoxymethyl group Chemical group [H]C([H])([H])OC([H])([H])* 0.000 description 1
- WEAXQUBYRSEBJD-UHFFFAOYSA-N methyl 1h-indole-4-carboxylate Chemical compound COC(=O)C1=CC=CC2=C1C=CN2 WEAXQUBYRSEBJD-UHFFFAOYSA-N 0.000 description 1
- FIHLULIAWLUDIW-UHFFFAOYSA-N methyl 3-(1,3-dinitropropan-2-yl)-1h-indole-4-carboxylate Chemical compound COC(=O)C1=CC=CC2=C1C(C(C[N+]([O-])=O)C[N+]([O-])=O)=CN2 FIHLULIAWLUDIW-UHFFFAOYSA-N 0.000 description 1
- KWKAKUADMBZCLK-UHFFFAOYSA-N methyl heptene Natural products CCCCCCC=C KWKAKUADMBZCLK-UHFFFAOYSA-N 0.000 description 1
- GRVDJDISBSALJP-UHFFFAOYSA-N methyloxidanyl Chemical group [O]C GRVDJDISBSALJP-UHFFFAOYSA-N 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- JKOVQYWMFZTKMX-UHFFFAOYSA-N n,n-dimethyl-2-nitroethenamine Chemical group CN(C)C=C[N+]([O-])=O JKOVQYWMFZTKMX-UHFFFAOYSA-N 0.000 description 1
- TVMXDCGIABBOFY-UHFFFAOYSA-N n-Octanol Natural products CCCCCCCC TVMXDCGIABBOFY-UHFFFAOYSA-N 0.000 description 1
- 230000008693 nausea Effects 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 150000002894 organic compounds Chemical class 0.000 description 1
- 239000012044 organic layer Substances 0.000 description 1
- 230000036407 pain Effects 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 230000002572 peristaltic effect Effects 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 239000003444 phase transfer catalyst Substances 0.000 description 1
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N phenol group Chemical group C1(=CC=CC=C1)O ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 1
- WKFBZNUBXWCCHG-UHFFFAOYSA-N phosphorus trifluoride Chemical compound FP(F)F WKFBZNUBXWCCHG-UHFFFAOYSA-N 0.000 description 1
- XKJCHHZQLQNZHY-UHFFFAOYSA-N phthalimide Chemical compound C1=CC=C2C(=O)NC(=O)C2=C1 XKJCHHZQLQNZHY-UHFFFAOYSA-N 0.000 description 1
- 150000004885 piperazines Chemical group 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- NNFCIKHAZHQZJG-UHFFFAOYSA-N potassium cyanide Chemical compound [K+].N#[C-] NNFCIKHAZHQZJG-UHFFFAOYSA-N 0.000 description 1
- FYRHIOVKTDQVFC-UHFFFAOYSA-M potassium phthalimide Chemical compound [K+].C1=CC=C2C(=O)[N-]C(=O)C2=C1 FYRHIOVKTDQVFC-UHFFFAOYSA-M 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- 238000011321 prophylaxis Methods 0.000 description 1
- AQHHHDLHHXJYJD-UHFFFAOYSA-N propranolol Chemical compound C1=CC=C2C(OCC(O)CNC(C)C)=CC=CC2=C1 AQHHHDLHHXJYJD-UHFFFAOYSA-N 0.000 description 1
- 210000001187 pylorus Anatomy 0.000 description 1
- 150000003242 quaternary ammonium salts Chemical class 0.000 description 1
- 238000006476 reductive cyclization reaction Methods 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 229910052895 riebeckite Inorganic materials 0.000 description 1
- 239000000523 sample Substances 0.000 description 1
- 239000012047 saturated solution Substances 0.000 description 1
- 239000000952 serotonin receptor agonist Substances 0.000 description 1
- 238000010898 silica gel chromatography Methods 0.000 description 1
- 239000010802 sludge Substances 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- HUAUNKAZQWMVFY-UHFFFAOYSA-M sodium;oxocalcium;hydroxide Chemical compound [OH-].[Na+].[Ca]=O HUAUNKAZQWMVFY-UHFFFAOYSA-M 0.000 description 1
- 230000006641 stabilisation Effects 0.000 description 1
- 238000011105 stabilization Methods 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 150000005621 tetraalkylammonium salts Chemical class 0.000 description 1
- UGQWDFALGKAXTL-UHFFFAOYSA-M tetraoctylazanium;acetate Chemical compound CC([O-])=O.CCCCCCCC[N+](CCCCCCCC)(CCCCCCCC)CCCCCCCC UGQWDFALGKAXTL-UHFFFAOYSA-M 0.000 description 1
- 230000002110 toxicologic effect Effects 0.000 description 1
- 231100000759 toxicological effect Toxicity 0.000 description 1
- IMNIMPAHZVJRPE-UHFFFAOYSA-N triethylenediamine Chemical compound C1CN2CCN1CC2 IMNIMPAHZVJRPE-UHFFFAOYSA-N 0.000 description 1
- UORVGPXVDQYIDP-UHFFFAOYSA-N trihydridoboron Substances B UORVGPXVDQYIDP-UHFFFAOYSA-N 0.000 description 1
- YFTHZRPMJXBUME-UHFFFAOYSA-N tripropylamine Chemical compound CCCN(CCC)CCC YFTHZRPMJXBUME-UHFFFAOYSA-N 0.000 description 1
- 208000027185 varicose disease Diseases 0.000 description 1
- 230000024883 vasodilation Effects 0.000 description 1
- 239000008096 xylene Substances 0.000 description 1
- 239000011592 zinc chloride Substances 0.000 description 1
- 235000005074 zinc chloride Nutrition 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/06—Peri-condensed systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/14—Prodigestives, e.g. acids, enzymes, appetite stimulants, antidyspeptics, tonics, antiflatulents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/04—Centrally acting analgesics, e.g. opioids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/06—Antimigraine agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/02—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom condensed with one carbocyclic ring
- C07D209/04—Indoles; Hydrogenated indoles
- C07D209/10—Indoles; Hydrogenated indoles with substituted hydrocarbon radicals attached to carbon atoms of the hetero ring
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Engineering & Computer Science (AREA)
- Public Health (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Pain & Pain Management (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Nutrition Science (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
- Plural Heterocyclic Compounds (AREA)
- Indole Compounds (AREA)
Abstract
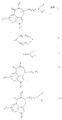
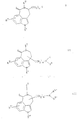
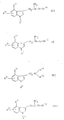
Использование: в фармацевтической промышленности в поиске лекарств, регулирующих моторику желудка или обладающих эффективным против мигрени серотонин-агонистическим действием. Сущность изобретения: производное 3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индола формулы:
где R1 - H, низший алкил или фенил-низшая алкильная группа, которая может быть моно- или дизамещена в фенильном кольце низшим алкокси или низшим алкилом; R2 - H или низший алкил; R3 - H или галоген; n = 1 или, если - (CH2)n - цепь расположена в положении кольца, также 2; R4 - H, C1-5-алкил, C3-6-циклоалкил, C4-циклоалкил, фенил-низшая алкильная группа; R5 - H, C1-5-алкил или фенил-низшая алкильная группа; D - связь или -N=CH-группа, и их физиологически приемлемые соли, способы их получения и фармацевтические композиции, содержащие их в качестве активного ингредиента. 9 с. и 5 з.п. ф-лы, 3 табл.
где R1 - H, низший алкил или фенил-низшая алкильная группа, которая может быть моно- или дизамещена в фенильном кольце низшим алкокси или низшим алкилом; R2 - H или низший алкил; R3 - H или галоген; n = 1 или, если - (CH2)n - цепь расположена в положении кольца, также 2; R4 - H, C1-5-алкил, C3-6-циклоалкил, C4-циклоалкил, фенил-низшая алкильная группа; R5 - H, C1-5-алкил или фенил-низшая алкильная группа; D - связь или -N=CH-группа, и их физиологически приемлемые соли, способы их получения и фармацевтические композиции, содержащие их в качестве активного ингредиента. 9 с. и 5 з.п. ф-лы, 3 табл.
Description
Изобретение относится к 6-оксо-азепиноиндоловым соединениям, а именно к новым производным 6-оксо-3,4,5,6-тетрагидро-1H-азепино [5,4,3-cd] индола, имеющим в случае необходимости в 3-ем или 4-ом положении остова кольца замещенный аминоалкильный остаток, и их кислотным солям присоединения, а также к фармацевтическим препаратам, содержащим эти соединения, способу получения этих соединений и полупродуктов для их получения.
В японской патентной заявке N 1034988 описаны 6-оксо-тетерагидроазепино-индолы в качестве полупродуктов для получения диуретически действующих тетрагидроазепиноиндолов. Из японской патентной заявки N 57144286 известны тетрагидроазепиноиндолы с коронарно-сосудорасширяющими свойствами.
Задача изобретения получить новые соединения 6-оксо-3,4,5,6-тетрагидро-1H-азепино [5,4,3-cd] индола с ценными фармакологическими свойствами.
Было обнаружено, что новые производные 6-оксо-3,4,5,6-тетрагидро-1H-азепино [5,4,3-cd] индола, имеющие в 3-ем и 4-ом положении остова кольца, в случае необходимости несущие замещенные аминометильную или аминоэтильную группы, обладают ценными фармакологическими свойствами, и, в особенности, оказывают благоприятное фармакологическое действие на желудочно-кишечный тракт и отличаются действием, способствующим желудочной подвижности. Соединения обладают, кроме того, серотонин-агонистическим действием на рецепторы вида 5-HT1, оказывающим благоприятное влияние при мигренях. На основе их действия соединения согласно изобретению пригодны для лечения нарушений желудочной подвижности, а также для лечения мигреней.
Поэтому настоящее изобретение касается новых соединений общей формулы
где R1 означает водород, низшие алкил- или циклоалкил-алкил-группы или фенил-низшую алкил-группу, которые в случае необходимости могут быть моно- или дизамещенными в фенильном кольце низшими алкоксилом, гидроксилом, галогеном или низшим алкилом;
R2 означает водород или в случае необходимости низшую алкильную группу, замещенную в α-положении к атому азота низшим алкоксилом;
R3 означает водород, низший алкил, галоген или, в случае если заместители R1, R2, R4 и/или R5 не содержат низших алкокси-групп, также гидроксил;
n означает 1 или, в случае если в 4-ом положении кольца имеется - (CH2)n-цепь, также и 2.
где R1 означает водород, низшие алкил- или циклоалкил-алкил-группы или фенил-низшую алкил-группу, которые в случае необходимости могут быть моно- или дизамещенными в фенильном кольце низшими алкоксилом, гидроксилом, галогеном или низшим алкилом;
R2 означает водород или в случае необходимости низшую алкильную группу, замещенную в α-положении к атому азота низшим алкоксилом;
R3 означает водород, низший алкил, галоген или, в случае если заместители R1, R2, R4 и/или R5 не содержат низших алкокси-групп, также гидроксил;
n означает 1 или, в случае если в 4-ом положении кольца имеется - (CH2)n-цепь, также и 2.
R4 означает водород, алкил с 1 5 атомами углерода, циклоалкил с 3 6 атомами углерода, циклоалкилалкил с 4 9 атомами углерода или в случае необходимости фенил-низшую алкильную группу, моно- или дизамещенную в фенильном кольце на низший алкил, низший алкоксил, гидроксил или галоген;
R5 означает водород, алкил с 1 5 атомами углерода, циклоалкил с 3 6 атомами углерода, циклоалкилалкил с 4 9 атомами углерода или в случае необходимости фенил-низшую алкильную группу, моно- или дизамещенную в фенильном кольце низшим алкилом, низшим алкоксилом, гидроксилом или галогеном; или
R4 и R5 вместе с атомом азота, с которым они связаны, образуют гетероцикл общей формулы a
где B означает связь, метиленовую группу, кислород или имино-группу -NR6-, где
R6 означает водород, низший алкил или в случае необходимости фенил или бензил, замещенный в фенильном кольце на низший алкил, низший алкоксил, гидроксил или галоген; и
D связь или, если R4 и R5 не означают водород, представляет собой -N= CH-группу или их физиологически совместимые кислотные соли присоединения.
R5 означает водород, алкил с 1 5 атомами углерода, циклоалкил с 3 6 атомами углерода, циклоалкилалкил с 4 9 атомами углерода или в случае необходимости фенил-низшую алкильную группу, моно- или дизамещенную в фенильном кольце низшим алкилом, низшим алкоксилом, гидроксилом или галогеном; или
R4 и R5 вместе с атомом азота, с которым они связаны, образуют гетероцикл общей формулы a
где B означает связь, метиленовую группу, кислород или имино-группу -NR6-, где
R6 означает водород, низший алкил или в случае необходимости фенил или бензил, замещенный в фенильном кольце на низший алкил, низший алкоксил, гидроксил или галоген; и
D связь или, если R4 и R5 не означают водород, представляет собой -N= CH-группу или их физиологически совместимые кислотные соли присоединения.
Поскольку соединения формулы I содержат в качестве заместителей низшие алкильные группы, то эти алкильные группы могут быть линейными или разветвленными и содержать, в частности, 1 4, предпочтительно 1 2, атома углерода, и представляют собой предпочтительно метил. Если заместители являются галогеном или содержат галогеновые заместители, то речь идет, в особенности, о фторе, хлоре или броме, предпочтительно хлоре.
Заместитель R1 представляет собой предпочтительно водород. Если R1 является низшей алкильной группой, она может быть линейной, разветвленной или циклической и содержать, предпочтительно, 1 4 атома углерода и представляет собой, предпочтительно, метил. Если R1 представляет собой фенил-низшую алкильную группу, то он может содержать алкиленовую цепь с 1 4 атомами углерода, фенильное кольцо может быть незамещенным или моно- или дизамещенным низшим алкоксилом, предпочтительно, метоксилом или также галогеном, гидроксилом или низшим алкилом. Циклоалкилалкильные остатки R1 могут содержать циклоалкильные группы с 3 6 атомами углерода и алкиленовую цепь с 1 3 атомами углерода.
Заместитель R2 является предпочтительно водородом. Если R2 представляет собой низшую алкильную группу, то он может содержать 1 4, особенно 1 или 2 атома углерода, и может быть замещен предпочтительно низшим алкилом, в особенности метоксилом и представляет собой, к примеру, метоксиметильную группу.
Заместитель в азепиновом кольце расположен предпочтительно в 3-ем положении. R4 и/или R5 могут представлять собой водород или линейный или разветвленный алкил, имеющий до 5 атомов углерода, циклоалкил с 3 6 атомами углерода, например циклопропил или циклогексил, или циклоалкилалкил с 4 9, в особенности с 4 7 углеродными атомами, например циклопропилметил или циклогексилметил, или также в случае необходимости означает замещенную фенил-низшую алкильную группу, которая может содержать алкильную цепь, с 1 4 атомами углерода и фенильное кольцо может быть незамещенным или моно- или дизамещенным низшим алкоксилом, в особенности метоксилом, или также галогеном, гидроксилом или низшим алкилом. Наиболее благоприятными оказываются заместители азепинового кольца, где D означает связь и один из заместителей R4 и R5 является водородом, например R4 означает водород или алкил-, циклоалкил- или циклоалкилалкильную группу, имеющую до 5 углеродных атомов, и R5 означает водород. Поскольку R4 в случае необходимости представляет собой замещенную фенил-низшую алкильную группу, предпочтительно в случае необходимости замещенный бензил, R5 является предпочтительно водородом. Поскольку R4 и R5 вместе с атомом азота, с которым они соединены, образуют гетероцикл, они могут быть пирролидином, пиперидином, морфолином или в случае необходимости замещенным пиперазиновым кольцом. Так, пригодны, например, незамещенные или замещенные в случае необходимости замещенным фенилом пиперазиновые кольца.
Согласно изобретению новые соединения формулы I и их кислотные соли присоединения получают по известным ранее способам, тем что:
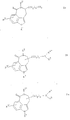
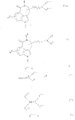
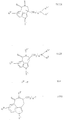
a) для получения соединений общей формулы Ia
где R1 имеет вышеуказанное значение и R3 имеет значение, указываемое для R3 за исключением гидроксила, соединения общей формулы II
где R1 и R3 имеют вышеуказанное значение и R7 означает низшую алкоксикарбонильную группу или CN-группу, циклизуют при условиях восстановления или
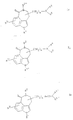
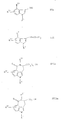
b) для получения соединений общей формулы Ib
где R1, R3, R4, R5 и n имеют вышеуказанное значение и R2 представляет собой водород или низший алкил, соединения общей формулы III
где R1, R2, R3 и n имеют вышеназванное значение и X представляет собой нуклеофильно отщепляемую летучую группу, вступают во взаимодействие с соединениями общей формулы IV
где R4 и R5 имеют вышеназванное значение, или
c) для получения соединений общей формулы Ic
где R1, R2, R3 и n имеют вышеназванное значение, переводят группу Y в амино-группу, в соединениях общей формулы V
где R1, R2, R3 и n имеют вышеназванное значение и Y означает азид- или фталимидную группу, если n равно 1, то 3 также циан-группу, или
d) для получения соединений общей формулы Id
где R1, R2, R3, R5 и n имеют вышеназванное значение и R4'' вышеназванное для R4 за исключением водорода, соединения общей формулы VI
где R1, R2, R3 и n имеют вышеназванное значение и R8 означает водород, алкил с 1 5 атомами углерода, циклоалкил с 3 6 атомами углерода, циклоалкилалкил с 4 9 атомами углерода, фенил-низшую алкильную группу, моно- или дизамещенную в случае необходимости низшим алкилом, низшим алкоксилом, гидроксилом или галогеном, или защитной алкиногруппой алкилируют и все защитные аминогруппы снова отщепляют, или
е) для получения соединений общей формулы Ie
где R1, R3, R4, R5 и n имеют вышеуказанные значения и R2'' в случае необходимости низшую алкильную группу, замещенную в 2-положении относительно атома азота низшим алкилом
где R3 и n имеют вышеназванное значение, R1 имеет значение, указанное для R1 или означает защитную аминогруппу, R4 и R5 имеют значения, названные для R4 и R5, при этом однако NR4R5-группа, где R4 и/или R5 означают водород, настолько защищена наименее легко отщепляемой амино защитной группой, что она не реагирует с ацилирующими алкилирующими реагентами, и R9 является низшей 1-гидроксиалкил-группой, переводом 1-гидроксиалкил-группы в остаток R2 и снова отщепляют полностью аминозащитные группы, или
f) для получения соединений общей формулы If
где R1, R3, R4, R5 и n имеют вышеназванное значение и R2 означает низший алкил, соединения общей формулы VIII
где R3 и n имеют вышеназванное значение и R1''', R4''' и R5''' имеют значения, указанные для R1, R4 и R5, за исключением водорода, или представляют собой амино защитную группу, взаимодействуют с соединениями общей формулы XII
R2''' X
где R2''' и X имеют вышеназванное значение, и затем снова отщепляют амино-защитные группы, или
g) для получения соединений общей формулы Ig
где R2, R3', R4, R5 и n имеют вышеназванное значение и R1'' имеет указанное для R1 значение, за исключением водорода, соединения общей формулы IX
где R2, R3', R4', R5' и n имеют вышеназванное значение, взаимодействуют с соединениями общей формулы X
R1'' X
где R1'' и X имеют вышеназванное значение, и затем снова отщепляют все амино-защитные группы, или
h) для получения соединений общей формулы Ih
где R1, R2, R3', R4'' и n имеют вышеназванное значение и R5'' имеет указанное для R5 значение, за исключением водорода, соединения общей формулы Ii
где R1, R2, R3' и n имеют вышеназванное значение, вводят аминоэтиленовый остаток общей формулы b
где R4'' и R5'' имеют вышеназванное значение, и при желании в полученных соединениях формулы I, где R3' означает и/или R1, R4 и/или R5 содержат метоксигруппу, метоксигруппа расщепляется до гидроксигруппы и/или в полученных соединениях формулы I, где R1, R4, R5 и/или в полученных соединениях формулы I, где R1, R4, R5 и/или R6 представляют собой замещенную в случае необходимости бензильную группу, эта бензильная группа гидролитически отщепляется и свободные соединения формулы I переводят по желанию в их кислотные соли присоединения или кислотные соли присоединения переводят в свободные соединения формулы I.
a) для получения соединений общей формулы Ia
где R1 имеет вышеуказанное значение и R3 имеет значение, указываемое для R3 за исключением гидроксила, соединения общей формулы II
где R1 и R3 имеют вышеуказанное значение и R7 означает низшую алкоксикарбонильную группу или CN-группу, циклизуют при условиях восстановления или
b) для получения соединений общей формулы Ib
где R1, R3, R4, R5 и n имеют вышеуказанное значение и R2 представляет собой водород или низший алкил, соединения общей формулы III
где R1, R2, R3 и n имеют вышеназванное значение и X представляет собой нуклеофильно отщепляемую летучую группу, вступают во взаимодействие с соединениями общей формулы IV
где R4 и R5 имеют вышеназванное значение, или
c) для получения соединений общей формулы Ic
где R1, R2, R3 и n имеют вышеназванное значение, переводят группу Y в амино-группу, в соединениях общей формулы V
где R1, R2, R3 и n имеют вышеназванное значение и Y означает азид- или фталимидную группу, если n равно 1, то 3 также циан-группу, или
d) для получения соединений общей формулы Id
где R1, R2, R3, R5 и n имеют вышеназванное значение и R4'' вышеназванное для R4 за исключением водорода, соединения общей формулы VI
где R1, R2, R3 и n имеют вышеназванное значение и R8 означает водород, алкил с 1 5 атомами углерода, циклоалкил с 3 6 атомами углерода, циклоалкилалкил с 4 9 атомами углерода, фенил-низшую алкильную группу, моно- или дизамещенную в случае необходимости низшим алкилом, низшим алкоксилом, гидроксилом или галогеном, или защитной алкиногруппой алкилируют и все защитные аминогруппы снова отщепляют, или
е) для получения соединений общей формулы Ie
где R1, R3, R4, R5 и n имеют вышеуказанные значения и R2'' в случае необходимости низшую алкильную группу, замещенную в 2-положении относительно атома азота низшим алкилом
где R3 и n имеют вышеназванное значение, R1 имеет значение, указанное для R1 или означает защитную аминогруппу, R4 и R5 имеют значения, названные для R4 и R5, при этом однако NR4R5-группа, где R4 и/или R5 означают водород, настолько защищена наименее легко отщепляемой амино защитной группой, что она не реагирует с ацилирующими алкилирующими реагентами, и R9 является низшей 1-гидроксиалкил-группой, переводом 1-гидроксиалкил-группы в остаток R2 и снова отщепляют полностью аминозащитные группы, или
f) для получения соединений общей формулы If
где R1, R3, R4, R5 и n имеют вышеназванное значение и R2 означает низший алкил, соединения общей формулы VIII
где R3 и n имеют вышеназванное значение и R1''', R4''' и R5''' имеют значения, указанные для R1, R4 и R5, за исключением водорода, или представляют собой амино защитную группу, взаимодействуют с соединениями общей формулы XII
R2''' X
где R2''' и X имеют вышеназванное значение, и затем снова отщепляют амино-защитные группы, или
g) для получения соединений общей формулы Ig
где R2, R3', R4, R5 и n имеют вышеназванное значение и R1'' имеет указанное для R1 значение, за исключением водорода, соединения общей формулы IX
где R2, R3', R4', R5' и n имеют вышеназванное значение, взаимодействуют с соединениями общей формулы X
R1'' X
где R1'' и X имеют вышеназванное значение, и затем снова отщепляют все амино-защитные группы, или
h) для получения соединений общей формулы Ih
где R1, R2, R3', R4'' и n имеют вышеназванное значение и R5'' имеет указанное для R5 значение, за исключением водорода, соединения общей формулы Ii
где R1, R2, R3' и n имеют вышеназванное значение, вводят аминоэтиленовый остаток общей формулы b
где R4'' и R5'' имеют вышеназванное значение, и при желании в полученных соединениях формулы I, где R3' означает и/или R1, R4 и/или R5 содержат метоксигруппу, метоксигруппа расщепляется до гидроксигруппы и/или в полученных соединениях формулы I, где R1, R4, R5 и/или в полученных соединениях формулы I, где R1, R4, R5 и/или R6 представляют собой замещенную в случае необходимости бензильную группу, эта бензильная группа гидролитически отщепляется и свободные соединения формулы I переводят по желанию в их кислотные соли присоединения или кислотные соли присоединения переводят в свободные соединения формулы I.
Восстановительная циклизация соединений формулы II в соединения формулы Ia может быть осуществлена по известному методу согласно варианту способа а) тем, что соединения формулы II с помощью восстановителя способны восстанавливать селективную алифатическую нитрогруппу до аминогруппы, не подвергая восстановлению циан-группы или алкоксикарбонильный остаток, обрабатывая подходящим для условий реакций инертным растворителем. В качестве восстанавливающего агента пригодны, например, гидразин в присутствии никеля Ренея или, если R7 не является цианом, также и водород, в присутствии катализатора гидрирования, предпочтительно палладия на угле. В качестве растворителей пригодны, в частности, низшие спирты такие, как метанол или этанол, которые в случае гидрирующей обработки с водородом можно вводить также в смеси с водой. Восстановление гидразином в присутствии катализатора никеля Ренея может происходить при температуре между комнатной температурой и примерно 80oC, предпочтительно при температуре кипения растворителя. Восстановление посредством каталитического гидрирования можно проводить при давлении водорода от 3 до 120 бар и температуре между комнатной и примерно 120oC. Когда по роду условий гидрирования замещенный в случае необходимости бензильный остаток R1 может также отщепиться при каталитическом гидрировании, то в таком случае целесообразно выбирать восстановление гидразином. Взаимодействие соединений формулы III с амино-соединениями формулы IV согласно варианту способа b) можно проводить по обычным методам аминоалкилирования. Взаимодействие проводят по условиям реакции целесообразнее всего в инертных растворителях при основных условиях.
В качестве нуклеофильно отщепляемого остатка X соединений формулы III пригодными являются галогены, такие как хлор, бром или йод, или также ацилокси-остаток O-E, где E представляет собой низший алканоил-остаток или сульфокислотный остаток, например остаток низшей алкансульфокислоты, как например метансульфокислоты или ароматических сульфокислот, как бензолсульфокислота или бензолсульфокислот, замещенных низшим алкилом или галогеном, например толуолсульфокислоты или бромбензолсульфокислоты. В качестве инертных растворителей пригодны, в частности, диметилформамид, низшие спирты, такие как этанол, циклические простые эфиры, такие как диоксан или тетрагидрофуран, галогенированные углеводороды, ароматические углеводороды или смеси из ранее названных растворителей. Для фиксирования образующейся во время реакции кислоты целесообразно добавлять органические или неорганические основания. При этом можно применять также избыток амина формулы IV и использовать его в качестве инертного основания. Примерами органических оснований являются третичные органические амины, в частности третичные низшие алкиламины, такие как триэтиламин, трипропиламин, N-низшие алкилморфолины или N-низшие алкил-пиперидины. Пригодными неорганическими основаниями являются, в частности, карбонаты или бикарбонаты щелочных металлов. Температура реакции может лежать между комнатной температурой и 100oC, предпочтительнее работают при повышенных температурах, например при температурах между 50 и 80oC.
Выделение аминосоединений формулы Ic, согласно варианту способа c) из соответствующих азидов, цианидов и фталимидов формулы V может происходить по известному ранее способу превращением азидов, цианидов или фталимидов в соответствующие амины обычным методом. Так можно гидролизовать, например, фталимиды формулы V по ранее известному способу и расщепить, например, обработкой гидразином до соединений формулы Ic. Азиды и цианиды формулы V можно восстановить известным самим по себе способом в инертном растворителе согласно условиям реакции до соответствующих аминосоединений. При этом следует выбрать условия реакции таким образом, чтобы не разрушалась лактамная связь кольцевого скелета. Для восстановления азидов формулы V пригодны, например, обработка гидразином в присутствии никеля Ренея, обработка хлоридом цинка в метаноле, обработка натрийборгидридом в двухфазной системе из водной фазы и не смешивающегося с водой органического растворителя, например галогенированного углеводорода, как дихлорметан, или ароматического углеводорода, как толуол, в присутствии катализатора фазового перевода, например солей тетраалкиламмония, как тетраоктиламмонийацетат, обработка трифторфосфином в водной среде или каталитическое гидрирование. Каталитическое гидрирование можно проводить по известному ранее способу в подходящем по условиям реакции инертном растворителе, например, в низших спиртах, в присутствии катализатора гидрирования при давлении водорода в интервале 1 50 бар. В качестве катализаторов гидрирования пригодны никель Ренея или, если R1 в случае необходимости не является замещенной бензильной группой, также палладий на угле. Восстановление цианидов формулы V предпочтительнее проводить каталитическим гидрированием в присутствии никеля Ренея в смеси из низшего спирта и аммиака при давлении водорода между 50 и 150 бар.
Получение соединений формулы Id может происходить, согласно варианту способа d), путем алкилирования соединений формулы VI известным самим по себе методом, обычным для алкилирования аминов. Так, соединения формулы Id можно получать взаимодействием соединений формулы VI с соединениями общей формулы XIIIa или, если R8 в соединениях формулы VI означает водород, также соединений общей формулы XIIIb
R4IV X
X-CH2-CH2-B-CH2-CH2-X
где B и X имеют выше названное значение и R4IV означает алкил с 1 5 атомами углерода, циклоалкил с 3 6 атомами углерода, циклоалкилалкил с 4 9 атомами углерода или фенил-низшую алкильную группу, моно- или дизамещенную, в случае необходимости, в фенильном кольце низшим алкилом, низшим алкоксилом, гидроксилом или галогеном, в обычных для аминоалкилирования условиях или восстановительным алкилированием соединений формулы VI с альдегидами или кетонами формулы XIIIc
R4V 0
где R4V представляет собой радикал, соответствующий радикалу R4IV, однако содержащий на 1 атом водорода меньше C по меньшей мере 2-я атомами углерода.
R4IV X
X-CH2-CH2-B-CH2-CH2-X
где B и X имеют выше названное значение и R4IV означает алкил с 1 5 атомами углерода, циклоалкил с 3 6 атомами углерода, циклоалкилалкил с 4 9 атомами углерода или фенил-низшую алкильную группу, моно- или дизамещенную, в случае необходимости, в фенильном кольце низшим алкилом, низшим алкоксилом, гидроксилом или галогеном, в обычных для аминоалкилирования условиях или восстановительным алкилированием соединений формулы VI с альдегидами или кетонами формулы XIIIc
R4V 0
где R4V представляет собой радикал, соответствующий радикалу R4IV, однако содержащий на 1 атом водорода меньше C по меньшей мере 2-я атомами углерода.
Взаимодействие соединений формулы VI с соединениями формулы XIIIf или XIIIb может быть выполнено методом, известным самим по себе обычным для алкилирования аминов, в подходящем для условий реакции инертном растворителе при основных условиях. Оно может происходить, например, по способу, описанному для взаимодействия соединений формулы III с соединениями формулы IV. Поскольку R8 представляет собой защитную амино-группу, он может быть известной ранее гидрогенолитически или гидролитически отщепляемой защитной группой. В качестве гидрогенолитически отщепляемых групп пригодны, в частности, в данном случае замещенные бензил- или бензилгидрил-группы, которые затем легко можно снова гидрировать, например, в присутствии палладий/угольного катализатора. В качестве примера гидролитически отщепляемой защитной группы пригодны низшие ацилгруппы, такие как формил-, ацетил- или трифторацетил-группы. Поскольку R8 в соединениях формулы VI представляет собой водород, то вообще при взаимодействии с соединениями формулы XIIIa образуется смесь моно- и дизамещенных соединений, где содержание дизамещенных соединений можно варьировать в зависимости от вступаемого в реакцию количества соединения формулы XIIIa и условий реакции. Монозамещенные и дизамещенные соединения могут быть отделены друг от друга, известными сами по себе методами, например, посредством хроматографии на кизельгеле.
Восстановительное алкилирование соединений формулы VI может происходить известным самим по себе способом путем взаимодействий формулы VI с альдегидом или кетоном формулы XIIIc в восстановительных условиях. Например, соединения формулы VI могут взаимодействовать с соединениями формулы XIIIc в проходящем по условиям реакции инертном растворителе в присутствии восстановителя, например муравьиной кислоты, боран-ди-низшего алкиламинкомплекса или натрийцианоборгидрида. Соединения формулы VI могут, однако, взаимодействовать также прежде всего с соединениями формулы XIIIa в подходящем по условиям реакции инертном растворителе и восстанавливаться затем в промежутоно образующиеся основания Шиффа in situ или после изоляции обработкой с восстановителем, не разрушающим лактамную связь в кольцевом скелете. Восстановление промежуточных иминосоединений может происходить по известному самим по себе способу путем обработки боран-ди-низшим алкиламинкомплексом, например боран-деметиламином, или диборан/пиридиновым комплексом, натрийборгидридом в уксусной кислоте или натрийцианборгидридом в кислой и нейтральной среде, например в уксусной кислоте и низшем спирте. По желанию восстановление оснований Шиффа можно проводить посредством каталитического гидрирования. Каталитическое гидрирование можно проводить, например, в присутствии никеля Ренея или палладия на угле в низшем спирте при мягких условиях, например при давлении водорода 1 3 бар при комнатной температуре.
Перевод 1-гидроксиалкильного остатка R9 соединений формулы VII в остаток R2'', согласно варианту способа e) для получения соединений формулы Ie можно осуществить известными самими по себе методами.
Так гидроксильную группу R9 известным самим по себе методом можно восстановить до соответствующей алкильной группы и гидроксиалкильную группу R9 в присутствии кислоты переэтерифицировать низшим спиртом в кислых условиях известным самим по себе способом.
Восстановление гидроксиалкильной группы до алкильной группы можно проводить в подходящем для условий реакции инертном органическом растворителе с помощью гидрирующего агента, который делает способным гидроксиалкильную группу восстанавливаться без разрушения лактамной связи. В качестве восстановителя пригоден, в частности, натрийборгидрид в присутствии сильной органической кислоты, например галогенуксусной кислоты, как трифторуксусной кислоты, или также триэтилсилан. В качестве растворителя пригодны, например, эфиры с открытой цепью или циклические сложные эфиры, в частности циклические эфиры, такие как тетерагидрофуран или диоксан, или галогенированные углеводороды, также как дихлорметан. Реакцию можно проводить при нескольких повышенных температурах, например при температурах между примерно 30 и 100oC, предпочтительно при температуре флегмы реакционной смеси.
Этерификацию гидроксилалкильной группы R9 низшим спиртом можно проводить в обычных для кислотами катализируемого образования эфира условиях. Так соединение формулы VII может взаимодействовать с низшим спиртом при добавлении каталитических количеств сильной кислоты. Взаимодействие целесообразнее проводить при повышенной температуре, например путем нагревания соединения формулы VII, в низшем спирте при температуре флегмы реакционной смеси. В качестве кислот пригодны неорганические кислоты, такие как серная кислота, или сильные органические кислоты, целесообразнее органические сульфокислоты, например низшие алкансульфокислоты, такие как метансульфокислота, или ароматические сульфокислоты, такие как бензолсульфокислоты или замещенные низшим алкилом, или галогеном бензолсульфокислоты, или также галогенуксусные кислоты.
После достигнутого превращения остатка R9 в остаток R2'' амино-защитная группа полностью отщепляется известным самим по себе способом.
Взаимодействие соединений формулы VIII с соединениями формулы XII может происходить, согласно варианту способа f), известным самим по себе способом в условиях, обычных для алкилирования амидов. Так взаимодействие можно проводить в подходящем по условиям реакции инертном растворителе в присутствии сильного основания, который делает способным депротонировать атом азота лактамной группы. В качестве оснований пригодны, например, литийорганические основания, например низший алкиллитий, в частности бутиллитий, или литийдиизопропиламид, трет. бутилат калия. В качестве растворителя пригодны, например, эфиры с открытой цепью и циклические, такие как диэтиловый эфир, тетерагидрофуран или диоксан. Взаимодействие целесообразно проводить при температурах в интервале от -78oC до комнатной температуры. После окончания реакции амино-защитные группы полностью отщепляются известным самим по себе способом.
Взаимодействие соединений формулы IX с соединениями формулы X, согласно варианту способа g), может происходить методом, обычным самим по себе для алкилирования индолов. В соединениях формулы X нуклеофильный отщепляемый остаток X может иметь значения, указываемые для соответствующего остатка в соединениях формулы III. В частности пригодны галогены, предпочтительно йод или бром, или также органические сульфокислотные остатки. Взаимодействие целесообразнее проводить в подходящем по условиям реакции инертном органическом растворителе в присутствии сильных оснований. В качестве сильного основания пригодны, например, гидриды щелочных металлов, такие как гидрид натрия, или литийорганические основания, например низший алкиллитий, в особенности бутиллитий, или литийдиизопропиламид, трет.бутилат калия. Поскольку R2 означает водород, то сначала реагирует сильный нуклеофильный азот индола. Чтобы избежать дополнительного алкилирования лактамного азота, количество основания целесообразно ограничить так, чтобы его было недостаточно для двойного алкилирования. При необходимости свободную амино-группу можно защитить также известным самим по себе способом, введением защитной формилгруппы, которая снова гидролитически отщепляется при последующей обработке.
В качестве растворителя пригодны диметилформамид или сложные эфиры с открытой цепью или циклические сложные эфиры, такие как диэтиловый эфир, тетерагидрофуран или диоксан. Реакцию целесообразно проводить при повышенных температурах, например при температуре между 30 и 100oC. Все защитные аминогруппы можно после реакции отщепить известным самим по себе способом.
Введение аминометиленового остатка b) в аминосоединения формулы Ii согласно варианту способа h) можно осуществить способом обычной для образования амидинов. Так соединения формулы Ii могут взаимодействовать известным самим по себе способом с галогениминиевыми солями общей формулы XIa
где R4'' и R5'' имеют вышеуказанное значение, Hal означает хлор или бром и A означает кислотный анион, или с ацеталями общей формулы XIb
где R4'' и R5'' имеют вышеуказанное значение и R13 означает низший алкил.
где R4'' и R5'' имеют вышеуказанное значение, Hal означает хлор или бром и A означает кислотный анион, или с ацеталями общей формулы XIb
где R4'' и R5'' имеют вышеуказанное значение и R13 означает низший алкил.
Взаимодействие соединений формулы Ii с галогениминиевыми солями формулы XIa может осуществляться до соединений формулы Ih известным самим по себе способом при условиях, обычных для образования амидинов. В солях формулы XIa радикал A может быть анионом галогенводородной кислоты, в частности хлоридом. Взаимодействие целесообразно проводить в подходящем по условиям реакции инертном растворителе, например диметилформамиде, в сложном эфире с открытой цепью или циклическом, в галогенированном углеводороде или в смеси этих растворителей при температурах от комнатной температуры до 100oC.
Взаимодействие соединений формулы Ii с ацеталями формулы XIb может происходить известным самим по себе способом при условиях, обычных для образования амидинов, например условиях, указанных выше для реакции соединений формулы Ii с соединениями формулы XIa.
В качестве амино-защитных групп в вышеуказанных соединениях можно выбрать известные сами по себе защитные группы, которые затем известным самим по себе методом можно отщепить сольволитически или гидрогенолитически. Пригодные легко снова отщепляющиеся защитные группы для аминогрупп известны, например, из E.Mc Omie "Protective Groupe in Organic Chemistry" Plenum Press 1971.
В качестве амино-защитных групп пригодны, например, гидролитически отщепляемые ацил-группы, предпочтительно трифторацетилгруппа, или также замещенные в случае необходимости бензильные группы, которые могут известным самим по себе способом вторично отщепляться. Однако амино-защитные группы должны выбираться, естественно, принимая во внимание прочие остатки, содержащиеся в защищаемых соединениях так, чтобы амино-группа была достаточно защищена по условиям реакции, превалирующим для получения и/или дальнейшей обработки, и что затем защитные группы легко отщепляются при условиях, при которых другие остатки, содержащиеся в молекуле, не разрушаются. В качестве гидрогенолитически отщепляемой защитной группы применяется предпочтительнее бензильная группа. В качестве гидролитически отщепляемой группы вводится преимущественно трифторацетильная группа. Поскольку NR4R5-группа представляет собой NH2-группу, то при применении защитной трифторацетильной группы достаточно, если один из водородных атомов замещен этой защитной группой. Для введения защитной трифторацетильной группы защищаемое соединение может взаимодействовать с трифторацетангидридом известным самим по себе способом. Если R2 означает водород, то при таком ацилировании может иметь место также частичное ацилирование на амидном азоте, причем образуется лактамамидная функция. Такого вида лактамамидная функция однако снова отщепляется при дальнейшей обработке ацилированного продукта водным насыщенным раствором бикарбоната натрия для нейтралазации образовавшейся кислоты и для избавления от избыточного ангидрида кислоты. Поскольку заместители R1, R4 и/или R5 содержат фенольные гидрокси-группы, то их можно при необходимости защитить в процессе вышеописанных реакций отщепляемыми при дальнейшей обработке известными ранее эфирными защитными группами, такими как бензил.
В соединениях формулы I, где R3 означает метоксил и/или R1, и/или R4, и/или R5 содержат метоксифенильную группу, метокси-группа может отщепляться пригодными для расщепления метоксиарилэфиров методами до гидрокси-группы известным самим по себе способом. Например, расщепление эфира может происходить путем обработки йодистым водородом или бромистым водородом в подходящем для условий реакции инертном растворителе, например ацетангидриде или уксусной кислоте, или путем обработки йодтриметилсиланом в присутствии основания или бортрибромидом в галогенированном углеводороде, таком как дихлорметан.
В соединениях формулы I, где R1, и/или R4, и/или R5, и/или R6 представляет собой бензил группу, замещенную в случае необходимости в фенильном кольце, то эта группа по необходимости может быть гидрогенолитически отщеплена известным самим по себе способом. Гидрогенолиз может осуществляться в подходящем по условиям реакции инертном растворителе, например в низшем спирте, каталитическим гидрированием при давлении водорода от 3 до 50 бар и температурах между комнатной и примерно 120oC в присутствии катализатора гидрирования, например палладия на угле. Отщепление бензила можно также производить обработкой с муравьиной кислотой в присутствии спирта или обработкой с натрием в жидком аммиаке.
Соединения формулы I можно известным самим по себе способом изолировать из реакционной смеси и очистить. Кислотные соли присоединения могут быть переведены обычным способом в свободные основания и они по необходимости переводят известным способом в фармакологически переносимые кислотные соли присоединения.
В качестве фармакологически приемлемых кислотных солей присоединения формулы I пригодны, например, их соли с неорганическими кислотами, например галогенводородными кислотами, предпочтительно хлорводородная кислота, серная кислота или фосфорная кислота, или с органическими кислотами, например низшими алифатическими моно- или дикарбоновыми кислотами, такими как малеиновая кислота, фумаровая кислота, молочная кислота, винная кислота или уксусная кислота, или сульфокислоты, например низшие алкансульфокислоты, такие как метансульфокислота, или бензолсульфокислоты, замещенные в случае необходимости в бензольном кольце галогеном или низшим алкилом, такие как п-толуолсульфокислота, или циклогексиламинсульфокислота.
Соединения формулы I содержат хиральный центр в положении, в котором боковая цепь -(CH2)n-D-NR4R5 связана с азепиновым кольцом, и могут существовать в нескольких оптических активных энантиомерных формах или рацематах. Данное изобретение охватывает как рацемические смеси, так и чистые оптические изомеры соединений формулы I. Если при синтезе рацематов водят исходные соединения формулы III, V, VI, VII, VIII или IX, то получают соединения формулы I в виде рацематов. Исходя из оптически активных форм этих исходных соединений, можно получить оптически активные соединения формулы I. Оптически активные соединения формулы I могут получены из рацемических смесей известным самим по себе способом, например хроматографическим разделением на хиральных разделительных носителях или взаимодействием с пригодными для этой цели оптически активными кислотами, винной кислотой или яблочной кислотой, на их оптические антиподы путем фракционированной кристаллизации полученных солей.
Исходные продукты формулы II представляют собой ценные полупродукты для получения фармакологически действующих соединений, например соединения формулы I.
Соединения формулы II могут быть получены известным самим по себе способом, исходя из соединений индола общей формулы XIV
где R1, R3' и R7 имеют вышеназванное значение, в то время как соединения формулы XIV прежде всего формилируются до альдегидов общей формулы XV
где R1, R3' и R7 имеют вышеназванное значение, и образовавшиеся альдегидные соединения формулы XV реагируют с нитрометаном.
где R1, R3' и R7 имеют вышеназванное значение, в то время как соединения формулы XIV прежде всего формилируются до альдегидов общей формулы XV
где R1, R3' и R7 имеют вышеназванное значение, и образовавшиеся альдегидные соединения формулы XV реагируют с нитрометаном.
Формилирование соединений индола формулы XIV можно проводить взаимодействием с известными формилирующими средствами методами, обычными для формилирования ароматики. Целесообразным оказывается формилирование с N,N-дизамещенным формамидом, таким как диметилформамид или с N-метилформамид в присутствии фосфороксихлорида или фосгена по Vilsmeier-методу. В качестве растворителя при этом может служить избыток диметилформамида или можно вводить также ароматические углеводороды, такие как бензол или хлорбензол. Взаимодействие можно проводить при температурах между комнатной и примерно 80oC.
Полученные формальдегидные соединения формулы XV, где R1 означает водород, по необходимости могут быть переведены путем взаимодействия с соединениями формулы X в такие соединения формулы XV, где R1 имеет такое же значение, как и R1'' остаток. Взаимодействие может быть проведено, например, в условиях, представленных выше для взаимодействия соединений формулы IX с соединениями формулы X.
Реакцию взаимодействия соединений формулы XV с нитрометаном можно проводить в присутствии основания в условиях, обычных для взаимодействия альдегидов с C-H-ацидными соединениями. В качестве растворителя может служить избыток нитрометана. По желанию можно также применять следующие органические растворители, такие как, например, низшие спирты, галогенированные углеводороды, такие как дихлорметан, или циклический сложный эфир, такой как тетрагидрофуран. Взаимодействие может протекать при температурах между комнатной и примерно 80oC. В качестве оснований можно вводить неорганические или органические соединения, реагирующие как основания. Так пригодны, например, гидроксиды щелочных металлов, их карбонаты или ацетаты, аммония ацетат или карбонат, основные ионообменные смолы или третичные органические основания, как например три-низш.алкиламины или в особенности 1,8-диазабицикло [5.4.0] ундец-7-ен (1,5 5) (=DBU) или 1,5-дииазабицикло [4.3.0) нонен-5-ен (=DBN). При взаимодействии может образовываться смесь из соединений 3-(1,3-динитропропан-2-ил)-индола формулы II и соответствующих соединений 3-(2-нитроэтилен)-индола общей формулы XVI
где R1, R3' и R7 имеют вышеуказанное значение. Смесь из соединений формулы II и соединений формулы XVI можно разделить известным ранее способом дистилляцией или посредством колоночной хроматографии. Соотношение соединений формулы XVI к соединениям формулы II в реакционной смеси может варьироваться в зависимости от вида и силы применяемого основания или реакционных условий. Для того чтобы сразу получить соединения формулы II или смеси с очень высоким содержанием соединения формулы II, в качестве основания целесообразно вводить 1,8-диазабицикло [5.4.0] ундец-7-ен (1,5-5) или 1,5-диазабицикло [4.3.0] нонен-5-ен. Чтобы получить соединения формулы XVI или смесь с очень высоким содержанием соединения формулы XVI, целесообразно вводить слабые основания предпочтительно аммонийацетат.
где R1, R3' и R7 имеют вышеуказанное значение. Смесь из соединений формулы II и соединений формулы XVI можно разделить известным ранее способом дистилляцией или посредством колоночной хроматографии. Соотношение соединений формулы XVI к соединениям формулы II в реакционной смеси может варьироваться в зависимости от вида и силы применяемого основания или реакционных условий. Для того чтобы сразу получить соединения формулы II или смеси с очень высоким содержанием соединения формулы II, в качестве основания целесообразно вводить 1,8-диазабицикло [5.4.0] ундец-7-ен (1,5-5) или 1,5-диазабицикло [4.3.0] нонен-5-ен. Чтобы получить соединения формулы XVI или смесь с очень высоким содержанием соединения формулы XVI, целесообразно вводить слабые основания предпочтительно аммонийацетат.
Соединения формулы XVI, где R1 означает водород по желанию, можно путем взаимодействия с соединением в формулы X перевести в такие соединения формулы XVI, где R1 означает R1''. Реакцию взаимодействия можно осуществлять обычным самим по себе методом для алкилирования индолов и, например, проводить в условиях, описанных выше для взаимодействия соединений формулы IX с соединениями формулы X.
Соединения формулы XVI можно переводить взаимодействием с другим нитрометаном в присутствии основания, предложенного выше для получения соединений формулы II в качестве особенно пригодных, в соединения формулы II.
Соединения формулы XVI можно также получать взаимодействием соединений формулы XIV с 1-нитро-2-диметиламиноэтиленом.
Индольные соединения формулы XIV известны или могут быть получены известными методами или аналогично известным методам. Получение соединений формулы XIV описаны, например, в патенте США N 3732245.
Исходные соединения формулы III представляют собой новые соединения, которые являются ценными полупродуктами для получения фармакологически действующих соединений, например соединения формулы I. Соединения формулы III могут быть получены известным само по себе способом из соответствующих спиртов общей формулы XVII
где R1, R3', R2' и n имеет вышеуказанное значение, путем перевода гидрокси-группы в летучую группу. Так, известным самим по себе способом соединения формулы XVII вступают во взаимодействие, например, для введения галогенового остатка X с тионилхлоридом или с фосфоргалогенидами, например фосфортрибромидом, известным самим по себе способом в инертном растворителе, подходящим по условиям реакции, например галогенированном углеводороде, таком как хлороформ. Сульфокислотные остатки X могут быть введены известным самим по себе способом ацилированием соединений формулы XVII с соответствующими галогенидами сульфокислоты. Так, спирты формулы XVII могут взаимодействовать с галогенидом сульфокислоты, предпочтительно с хлоридом сульфокислоты по методам, обычным для образования сложных эфиров. Например, реакцию взаимодействия можно проводить в присутствии основания при температурах между примерно комнатной и 100oC в инертном растворителе, подходящем по условиям реакции. В качестве оснований пригодны, например, третичные органические амины, такие как триэтиламин или пиридин, которые одновременно могут служить растворителями для реакции.
где R1, R3', R2' и n имеет вышеуказанное значение, путем перевода гидрокси-группы в летучую группу. Так, известным самим по себе способом соединения формулы XVII вступают во взаимодействие, например, для введения галогенового остатка X с тионилхлоридом или с фосфоргалогенидами, например фосфортрибромидом, известным самим по себе способом в инертном растворителе, подходящим по условиям реакции, например галогенированном углеводороде, таком как хлороформ. Сульфокислотные остатки X могут быть введены известным самим по себе способом ацилированием соединений формулы XVII с соответствующими галогенидами сульфокислоты. Так, спирты формулы XVII могут взаимодействовать с галогенидом сульфокислоты, предпочтительно с хлоридом сульфокислоты по методам, обычным для образования сложных эфиров. Например, реакцию взаимодействия можно проводить в присутствии основания при температурах между примерно комнатной и 100oC в инертном растворителе, подходящем по условиям реакции. В качестве оснований пригодны, например, третичные органические амины, такие как триэтиламин или пиридин, которые одновременно могут служить растворителями для реакции.
Соединения формулы XVII представляют собой новые соединения, являющиеся ценными полупродуктами для получения фармакологически действующих соединений, например соединения формулы I. Спирты общей формулы XVIIa
где R1, R2' и R3' имеют вышеуказанное значение, могут быть получены известным самим по себе способом, селективным восстановлением сложной эфирной группы в соответствующих сложных эфирах общей формулы XVIII
где R1, R2' и R3' имеют вышеуказанное значение и R10 означает низший алкил. В качестве восстановителя пригодны, например, гидридные восстановители, способные к восстановлению сложных эфиров, которые однако не разрушают лактамную связь кольцевого скелета. Так, оказывается целесообразным, например, восстановление диизобутилалюминийборгидридом или боргидридами щелочных металлов, такими как натрийборгидрид, литийборгидрид или литийтри-низш.алкилборгидрид, или натрийтриэтоксиалюминийгидридом в смеси растворителей из циклического эфира, такого как тетрагидрофуран или диоксан, и низшего спирта при температурах между комнатной и температурой кипения реакционной смеси. При применении диизобутилалюминийгидрада в качестве восстановителя можно восстановление проводить в циклическом эфире, таком как тетрагидрофуран, или ароматическом углеводороде, таком как бензол или толуол, при температурах между -20oC и комнатной температурой.
где R1, R2' и R3' имеют вышеуказанное значение, могут быть получены известным самим по себе способом, селективным восстановлением сложной эфирной группы в соответствующих сложных эфирах общей формулы XVIII
где R1, R2' и R3' имеют вышеуказанное значение и R10 означает низший алкил. В качестве восстановителя пригодны, например, гидридные восстановители, способные к восстановлению сложных эфиров, которые однако не разрушают лактамную связь кольцевого скелета. Так, оказывается целесообразным, например, восстановление диизобутилалюминийборгидридом или боргидридами щелочных металлов, такими как натрийборгидрид, литийборгидрид или литийтри-низш.алкилборгидрид, или натрийтриэтоксиалюминийгидридом в смеси растворителей из циклического эфира, такого как тетрагидрофуран или диоксан, и низшего спирта при температурах между комнатной и температурой кипения реакционной смеси. При применении диизобутилалюминийгидрада в качестве восстановителя можно восстановление проводить в циклическом эфире, таком как тетрагидрофуран, или ароматическом углеводороде, таком как бензол или толуол, при температурах между -20oC и комнатной температурой.
Спирты общей формулы XVIIb
где R1, R2' и R3' имеют вышеуказанное значение, можно получить, исходя из таких соединений формулы V, где Y означает цианогруппу, переводом цианогруппы известным способом в алкоксикарбонильную группу и последующим селективным гидрированием до гидроксиметильной группы. В качестве восстановителя пригодны гидридные восстановители, описанные выше для селективного восстановления сложноэфирной группы в соединениях формулы XVIII.
где R1, R2' и R3' имеют вышеуказанное значение, можно получить, исходя из таких соединений формулы V, где Y означает цианогруппу, переводом цианогруппы известным способом в алкоксикарбонильную группу и последующим селективным гидрированием до гидроксиметильной группы. В качестве восстановителя пригодны гидридные восстановители, описанные выше для селективного восстановления сложноэфирной группы в соединениях формулы XVIII.
Соединения общей формулы XVIIIa
где R1, R3' и R10 имеют вышеуказанное значение, могут быть получены известным самим по себе способом, исходя из соединений общей формулы XIX
где R1, R3' и R10 имеют вышеуказанное значение и R7' означает низшую алкоксикарбонильную группу, тем что соединения формулы XIX восстанавливают в условиях циклизации. Для этого соединения формулы XIX подвергают взаимодействию в инертном растворителе, подходящем по условиям реакции, с восстановителем, который способен селективно восстанавливать алифатическую нитро-группу до амино-группы без восстановительного разрушения алкоксикарбонильного остатка. В качестве восстановителя пригодны, например, водород в присутствии катализатора гидрирования или гидразин в присутствии никеля Ренея. Восстановление каталитическим гидрированием целесообразно проводить при давлении водорода от 3 до 50 бар и при температурах между комнатной и примерно 120oC. В качестве катализатора гидрирования пригоден, в частности, палладий на угле. В качестве растворителей пригодны предпочтительно ароматические углеводороды, такие как толуол или ксилол. Если по роду условий гидрирования может также расщепиться и замещенное в случае необходимости фенильное кольцо R1 при каталитическом гидрировании, то в этом случае целесообразнее выбрать восстановление гидразином. При восстановлении соединений формулы XIX при указанных условиях возникает, в общем, смесь из соединений общей формулы XX
где R1, R3', R7' и R10 имеют вышеуказанное значение, и соответствующего циклического соединения формулы XVIIIa. Для завершения циклизации эту смесь нагревают в течение 0,5 3 ч до температур между 100 и 150oC.
где R1, R3' и R10 имеют вышеуказанное значение, могут быть получены известным самим по себе способом, исходя из соединений общей формулы XIX
где R1, R3' и R10 имеют вышеуказанное значение и R7' означает низшую алкоксикарбонильную группу, тем что соединения формулы XIX восстанавливают в условиях циклизации. Для этого соединения формулы XIX подвергают взаимодействию в инертном растворителе, подходящем по условиям реакции, с восстановителем, который способен селективно восстанавливать алифатическую нитро-группу до амино-группы без восстановительного разрушения алкоксикарбонильного остатка. В качестве восстановителя пригодны, например, водород в присутствии катализатора гидрирования или гидразин в присутствии никеля Ренея. Восстановление каталитическим гидрированием целесообразно проводить при давлении водорода от 3 до 50 бар и при температурах между комнатной и примерно 120oC. В качестве катализатора гидрирования пригоден, в частности, палладий на угле. В качестве растворителей пригодны предпочтительно ароматические углеводороды, такие как толуол или ксилол. Если по роду условий гидрирования может также расщепиться и замещенное в случае необходимости фенильное кольцо R1 при каталитическом гидрировании, то в этом случае целесообразнее выбрать восстановление гидразином. При восстановлении соединений формулы XIX при указанных условиях возникает, в общем, смесь из соединений общей формулы XX
где R1, R3', R7' и R10 имеют вышеуказанное значение, и соответствующего циклического соединения формулы XVIIIa. Для завершения циклизации эту смесь нагревают в течение 0,5 3 ч до температур между 100 и 150oC.
Соединения формулы XVIIIa, где R1 означает водород могут по желанию путем взаимодействия с соединениями формулы X переведены в такие соединения формулы XVIIIa, где R1 означает остаток R1''. Реакцию взаимодействия можно проводить методом, обычным самим по себе для алкилирования индолов, и, например, по условиям, описанным выше для реакции соединений формулы IX с соединениями формулы X.
При желании можно в соединения формулы XVIIIa известным самим по себе способом ввести алкильную группу R2''. Так, соединения формулы XVIIIa могут взаимодействовать при условиях, обычных для алкилирования амидов, с соединениями формулы XII. Реакцию взаимодействия можно проводить в инертном, подходящем по условиям реакции, растворителе в присутствии сильного основания, которое способно депротонировать атом азота лактамной группы. В качестве основания пригодны названные выше для алкилирования соединений формулы VII согласно способу f) основания, в частности бутиллитий. В качестве растворителя пригодны, например, циклические эфиры или эфиры с открытой цепью, такие как тетрагидрофуран или диоксан или также диэтиловый эфир. Реакцию целесообразно проводить при температурах в интервале от -80oC до комнатной температуры. Поскольку R1 означает водород, то нужно защитить известным способом индольную связь обычной амино-группой, которую затем снова отщепляют.
Соединения формулы XIX могут быть получены известным самим по себе способом, исходя из соединений общей формулы XXI
где R1, R3' и R7' имеют вышеуказанное значение и R11 и R12 соответственно означают низший алкил или оба вместе представляют собой алкиленовую цепь с 1-4 атомами углерода, тем что NR11R12-группу соединения формулы XXi переводит в нуклеофильно отщепляемую летучую группу и продукт реакции в колбе подвергают взаимодействию с низшим алкиловым эфиром нитроуксусной кислоты. Так можно, например, соединение формулы XXI подвергнуть взаимодействию с алкиловым эфиром нитроуксусной кислоты в инертном, подходящем по условиям реакции растворителе в присутствии три-низшем алкилфосфина, в частности трибутилфосфина, который промежуточно реагирует с аминогруппой соединения формулы XXI до нуклеофильно способного к отщеплению остатка. В качестве растворителя пригодны, например, ацетонитрил, диметилформамид или циклический эфир. Реакцию целесообразно проводить при повышенных температурах, например при температурах в интервале 50 80oC. По желанию соединение формулы XXI можно также сначала перевести путем взаимодействия с низшим алкилйодидом известным самим по себе способом в соответствующую четвертичную аммониевую соль и затем ее подвергнуть взаимодействию с низшим алкиловым эфиром нитроуксусной кислоты.
где R1, R3' и R7' имеют вышеуказанное значение и R11 и R12 соответственно означают низший алкил или оба вместе представляют собой алкиленовую цепь с 1-4 атомами углерода, тем что NR11R12-группу соединения формулы XXi переводит в нуклеофильно отщепляемую летучую группу и продукт реакции в колбе подвергают взаимодействию с низшим алкиловым эфиром нитроуксусной кислоты. Так можно, например, соединение формулы XXI подвергнуть взаимодействию с алкиловым эфиром нитроуксусной кислоты в инертном, подходящем по условиям реакции растворителе в присутствии три-низшем алкилфосфина, в частности трибутилфосфина, который промежуточно реагирует с аминогруппой соединения формулы XXI до нуклеофильно способного к отщеплению остатка. В качестве растворителя пригодны, например, ацетонитрил, диметилформамид или циклический эфир. Реакцию целесообразно проводить при повышенных температурах, например при температурах в интервале 50 80oC. По желанию соединение формулы XXI можно также сначала перевести путем взаимодействия с низшим алкилйодидом известным самим по себе способом в соответствующую четвертичную аммониевую соль и затем ее подвергнуть взаимодействию с низшим алкиловым эфиром нитроуксусной кислоты.
Соединения формулы XXI можно получать известным способом из индольных соединений общей формулы XIVa
где R1, R3' и R7' имеют вышеуказанное значение, путем взаимодействия соединений формулы XIVa с формальдегидом и амином HNR11R12, где R11 и R12 имеют вышеуказанные значения, по методам, обычным для алкилирования, например, в условиях реакции Манниха.
где R1, R3' и R7' имеют вышеуказанное значение, путем взаимодействия соединений формулы XIVa с формальдегидом и амином HNR11R12, где R11 и R12 имеют вышеуказанные значения, по методам, обычным для алкилирования, например, в условиях реакции Манниха.
Соединения формулы XIX можно также получать из соединений общей формулы XXII
где R1, R3' и R10 имеют вышеуказанное значение, тем что восстанавливают двойную связь в соединениях формулы XXII известным самим по себе способом, например, обрабатывая соединения формулы XXII с натрийтриметоксиборгидридом, полученным in situ из натрийборгидрида и метанола в тетрагидрофуране. Соединения формулы XXII могут быть получены известным самим по себе способом при взаимодействии соединений общей формулы XVa
где R1, R3' и R7 имеют вышеуказанные значения, с низшим алкиловым эфиром нитроуксусной кислоты. Реакция может быть проведена известными самим по себе методами в присутствии основания при обычных для реакции альдегидов с C-H-ацидными соединениями условиях, например, в условиях, предложенных выше для реакции соединений формулы XV с нитрометаном.
где R1, R3' и R10 имеют вышеуказанное значение, тем что восстанавливают двойную связь в соединениях формулы XXII известным самим по себе способом, например, обрабатывая соединения формулы XXII с натрийтриметоксиборгидридом, полученным in situ из натрийборгидрида и метанола в тетрагидрофуране. Соединения формулы XXII могут быть получены известным самим по себе способом при взаимодействии соединений общей формулы XVa
где R1, R3' и R7 имеют вышеуказанные значения, с низшим алкиловым эфиром нитроуксусной кислоты. Реакция может быть проведена известными самим по себе методами в присутствии основания при обычных для реакции альдегидов с C-H-ацидными соединениями условиях, например, в условиях, предложенных выше для реакции соединений формулы XV с нитрометаном.
Соединения формулы V являются новыми и представляют собой ценные промежуточные продукты для получения фармакологически активных соединений формулы I.
Соединения формулы V могут быть получены тем, что соответствующие соединения формулы III взаимодействуют известным самим по себе способом с азидом щелочного металла, фталимидом щелочного металла или цианидом щелочного металла.
Соединения формулы VI охватывают такие соединения формулы I, где R4 означает водород, D представляет собой связь и R3 является не гидроксилом или могут быть получены из соответствующих соединений формулы I, где R5 означает водород, путем введения защитной амино-группы.
Соединения формулы VII представляют собой новые соединения, которые являются ценными полупродуктами для получения фармакологически действующих соединений, например соединения формулы I. Соединения формулы VII могут быть получены тем, что соединения общей формулы XXIII
где R1', R3', R4', R5' и n имеют вышеуказанные значения, ацилируют до соединений общей формулы XXIV
где R1', R3', R4', R5' и n имеют вышеуказанные значения и R9' представляет собой ацил-группу, соответствующую остатку R9, и полученные соединения формулы XXIV затем восстанавливают до соединения формулы VII.
где R1', R3', R4', R5' и n имеют вышеуказанные значения, ацилируют до соединений общей формулы XXIV
где R1', R3', R4', R5' и n имеют вышеуказанные значения и R9' представляет собой ацил-группу, соответствующую остатку R9, и полученные соединения формулы XXIV затем восстанавливают до соединения формулы VII.
Для ацилирования соединения формулы XXIII можно подвергнуть взаимодействию с ацилирующим средством общей формулы XXV
R9' X'
где R9' имеет вышеуказанное значение и X' означает галоген или низшую алкоксикарбонильную группу, при повышенных температурах, например при температурах между 30 и 100oC. В качестве растворителя может служить избыток ацилирующего средства, к которому по желанию можно добавить следующие органические растворители такие, как эфиры с открытой цепью или циклические, хлорированные углеводороды, такие как дихлорметан или ароматические углеводороды, такие как бензол. Предпочтительнее в качестве алкилирующего реагента вводят ангидрид соответствующей кислоты. Для формилирования целесообразно применять смешанный ангидрид, образующийся in situ из муравьиной кислоты и низшего ангидрида карбоновой кислоты, предпочтительнее ацетангидрида.
R9' X'
где R9' имеет вышеуказанное значение и X' означает галоген или низшую алкоксикарбонильную группу, при повышенных температурах, например при температурах между 30 и 100oC. В качестве растворителя может служить избыток ацилирующего средства, к которому по желанию можно добавить следующие органические растворители такие, как эфиры с открытой цепью или циклические, хлорированные углеводороды, такие как дихлорметан или ароматические углеводороды, такие как бензол. Предпочтительнее в качестве алкилирующего реагента вводят ангидрид соответствующей кислоты. Для формилирования целесообразно применять смешанный ангидрид, образующийся in situ из муравьиной кислоты и низшего ангидрида карбоновой кислоты, предпочтительнее ацетангидрида.
Восстановление соединений формулы XXIV до соединений формулы VII может происходить известным самим по себе способом в подходящем по условиям реакции инертном органическом растворителе с помощью гидрид-восстанавливающих средств, которые делают способным алканоильный остаток R9' смешанной имидиновой группировки соединений формулы XXIV восстанавливать до гидроксиалкилгруппы без разрушения лактамной группы оксо-азепинового кольца или подлежащей отщеплению амидной защитной группы. Целесообразно, например, проводить восстановление динизшим алкилалюминийгидридом, предпочтительнее диизобутилалюминийгидридом, дибораном или ди-низшим алкилборгидридом при низких температурах, например температурах между -80oC и комнатной температурой. В качестве растворителя пригодны, например, эфиры с открытой цепью и циклические, такие как диэтиловый эфир или тетрагидрофуран, ароматические углеводороды, такие как бензол или толуол, или галогенированные углеводороды, такие как дихлорметан или смесь подобных растворителей.
Соединения формулы XXIII охватывают соединения формулы I, где R2 означает водород, D представляет собой связь и R4 и/или R5 не означают водород, или могут быть получены известным способом из соответствующих соединений формулы I, где R4, R5 и/или R1 означают водород, введением защитной амино-группы.
Соединения формулы VIII охватывают соединения формулы I, где R2 означает водород, D представляет собой связь и R3 не является гидроксилом, или могут быть получены известным способом из соответствующих соединений формулы I, где R1, R4 и/или R5 означают водород, введением защитной амино-группы.
Соединения общей формулы IX охватывают соединения формулы I, где R1 означает водород, D представляет собой связь и R3 не является гидроксилом и остатки R4 и R5 не являются водородом, или могут быть получены известным способом из соответствующих соединений формулы I, где R4 и/или R5 означают водород, введением защитной амино-группы.
Соединения общей формулы XXVI
где R1, R2', R3' и n имеют вышеуказанное значение и Z является гидроксилом или ранее определенным остатком X или Y, охватывают соединения формулы III, V и VII и представляют собой ценные полупродукты для получения фармакологически активных соединений формулы I.
где R1, R2', R3' и n имеют вышеуказанное значение и Z является гидроксилом или ранее определенным остатком X или Y, охватывают соединения формулы III, V и VII и представляют собой ценные полупродукты для получения фармакологически активных соединений формулы I.
Соединения формулы I и их фармацевтически приемлемые кислотные соли присоединения обладают интересными фармакологическими свойствами и оказывают селективное средство к 5-HT1-рецепторам. Они отличаются особо важным действием на подвижность желудочно-кишечного тракта, особенно желудка. Так, в экспериментах на животных перистальтические волны желудка усиливались под влиянием соединений формулы I, причем частота движений изменялась незначительно. Кроме того, соединения обладают серотинин-агонистическим стимулирующим действием на рецепторы вида 5-HT1 в артерии basilaris, которая представляет собой хороший объект для антимигреневой эффективности соединений.
Описание фармакологических методов исследования.
1. Определение минимальной токсической дозы.
Мышам самцам весом 20 25 г дают перорально максимальную дозу до 300 мг/кг исследуемого вещества. Животные тщательно наблюдаются в течение 3 ч на проявление токсилогического эффекта. На протяжении 72 ч после аппликации регистрируют дополнительно все симптомы и смертельные случаи. Также наблюдаются и регистрируются все сопутствующие симптомы. Если наблюдают смерть или сильный токсический симптом, то следующим мышам дают убывающую дозу до прекращения появления токсических симптомов. Самая низкая доза, вызывающая смерть или сильные токсические симптомы, приведена в табл.A в качестве минимальной токсической дозы. Приведенные в табл.A номера примеров соотносятся со следующими примерами получения.
2. Определение действия на подвижность желудка на наркотизированных мышах.
Для тестов используются группы соответственно из 5 6 чистых крыс штамма SIV 50 весом по 220 290 г, которые анестизируются смесью кетамин/ксилазин. Животные получают внутрибрюшинно начальную дозу раствора 50 мг/мл кетамина и 10 мг/мл ксилазина из расчета 1 мл/кг веса и анестезионный уровень поддерживается путем непрерывной внутрибрюшной инфузии того же раствора в количестве 1 мл/кг/ч. Животные трахеотомируются и лапаротомируются. После наложения Pylorus-лигатуры в желудок вводится желудочный зонд, а на другом конце присоединяются через трехходовой кран к калиброванному прибору для измерения давления (Statham-элемент P 23 ID). Соответствующий зонд вводится реактивно на глубину 8 9 см в кишечник и таким же образом подключают к калиброванному тонометру того же типа. Затем желудок животных заполняется 2 мл воды. После 40-минутной фазы стабилизации измеряются колебания давления в желудке и кишечнике в течение 2 ч 20 мин и с помощью мультирекордера Watanabe (MC 6621) записываются амплитуды, полученные в результате фазовой моторики желудка. Для отдельных животных определяются средне-геометрические значения в течение первых 20 мин, которые служат контрольными амплитудными значениями. После этих 20 мин вводят испытываемое вещество. Максимальное повышение амплитуды (среднее значение из того 20-минутного промежутка времени, когда наступает наибольшее повышение амплитуды), вызванное введением исследуемых композиций, определяют в процентном отношении к контрольным значениям до применения испытываемых композиций, и в табл.A дается среднее значение. Кроме того, значения максимального повышения среднего желудочного тонуса, вызванного применением испытываемых композиций в течение опыта, могут быть записаны в сравнении с существующим средним желудочным тонусом до применения испытываемых композиций. Это повышение желудочного тонуса дается в табл.A в см H2O (среднее значение группы животных). В кишечнике испытываемые композиции вызывают угасание амплитудных колебаний.
3. Исследование свойств, указывающих на антимигреневое действие испытываемых композиций.
Мигреневые боли ассоциируются с чрезмерной делатацией сосудистой системы головного мозга.
Испытываемые композиции обладают стимулирующим сосудистую систему серотонин-агонистически действием на рецепторы типа 5-HT1 в артерии basilaris, на базе которого можно сделать вывод об антимигреневом действии композиций. Серотонин-агонистическое действие композиций на рецепторы вида 5-HT1 может быть определено in vitro на изолированных полосках органов артерии basilaris свиньи. Серотонин вызывает путем стимуляции 5-HT1-рецепторов зависимую от концентрации контракцию на изолированной полоске артерии basilaris свиньи. Такого вида контракция вызывается также испытываемыми композициями и является, таким образом, хорошим доказательством антимигреневого действия композиции. Исследование проводится по методу, описанному (Naunyn-Schmiebleb. Avch. Pharmacol. supp. zu Band 341, R 89, 1990 u Eur. J. Pharmacol. 183, 1106 1107, 1990) von van Charldorp и другими.
Описание опыта для определения in vitro действия, индуцирующего серотонин-агонистические контракции на сегментах изолированной артерии basilaris свиньи.
Для опыта применяются спиралеобразные сегменты артерии basilaris свиньи, которые изолируются из мозга свиней, поступающих с бойни.
Каждая полоска закрепляется в ванне из 10 мл модифицированного Tyrode-раствора (Tyrode-раствор это водный раствор, содержащий в литре 150,0 ммоля NaCl, 4,0 ммоля KCl, 1,8 ммоля CaCl2•2H2O, 1,1 моля MgCl2•6H2O, 25,0 ммоля NaHCO3, 0,3 ммоля NaH2PO4•H2O и 11,1 моля глюкозы), имеющего pH 7 (= Tyrode-раствор с добавкой 10-8 моль/л индометацина, 10-7 моль/л атропина и 10-7 моль/л пропанолола) таким образом, что ткань находится под давлением 10 мН. Ванна заполняется смесью из 95% O2 и 5% CO2. После эквилибрированной фазы в течение 1 ч посредством двухкратного добавления серотонина в концентрации 10-5 моль/л вызывается контракция ткани, а затем препарат вымывается. Далее контракционное действие измеряется при повышенной концентрации серотонина и строится кумулятивная кривая действия концентрации для серотонина. На этом же препарате после повторного вымывания строится кумулятивная кривая действия концентрации для испытываемой композиции.
В табл. B даны максимальная контракция, обусловленная испытываемыми композициями в соотношении с максимальной, вызванной серотонином контракцией, а также негативный логаритм той концентрации испытываемой композиции, которая вызывает 50% максимальной контракции, получаемой посредством этой испытываемой композиции (=pD2), и относительная сила действия, пересчитанная как pD2 испытываемой композиции по сравнению с pD2 серотонина, полученным на том же куске артерии.
На основе своего действия соединения формулы I и их фармакологически переносимые кислотные соли присоединения пригодны в гастроэнторологии в качестве лекарственных средств, для крупных млекопитающих, в особенности, людей, для профилактики и лечения нарушения подвижности желудочно-кишечного тракта. Так, например, пригодны для лечения различных недугов, вызванных нарушениями желудочно-кишечного тракта, таких как тошнота, чувство переполненности, боли в животе или синдром раздражения кишечника. Кроме того, соединения, пригодные для профилактики и лечения мигрени и сходных нарушений и головных болей, вызванных делатацией сосудов головного мозга, обладают при этом и болеутоляющим эффектом.
Применяемые дозы могут быть индивидуальными и варьируются в зависимости от состояния больного, применяемой композиции и формы аппликации. Например, парентеральные составы содержат, в общем, меньше действующего вещества, чем препараты, принимаемые внутрь. Однако для применения для крупных млекопитающих, особенно людей, в основном все же используются лекарственные формы с содержанием активного вещества от 25 до 300 мг на пероральную разовую дозу.
В качестве лекарственного соединения формулы I могут сочетаться в композиции с обычными веществами в галеновых препаратах, таких как, например, таблетках, капсулах, суппозиториях или растворах, например растворах для инъекций или растворах для орального приема, или для ингаляции, например, в аэрозольной форме. Эти галеновые препараты могут быть получены известными ранее способами с применением обычных твердых носителей, таких как, например, молочный сахар, крахмал или тальк, или жидкие парафины, и с применением обычных фармацевтических веществ, например средств для изготовления таблеток, реагентов растворения или консерваторов.
Изобретение характеризуется следующими примерами, которые, однако, ни в коей мере не должны ограничивать объем данного изобретения.
Пример 1. 3-Аминометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол.
а) К раствору 100 г метилового эфира индол-4-карбоновой кислоты в 1000 мл диметилформамида при охлаждении льдом прикапали в течение 30 мин 90 мл фосфороксихлорида. По окончании ледяную баню удалили и реакционную смесь перемешивали при комнатной температуре в течение 3 ч. Для дальнейшей обработки реакционную смесь при охлаждении льдом и сильном перемешивании разбавили 1000 мл дихлорметана. Далее прибавляли 200 мл воды и 100 мл 40%-ного гидроксида натрия с такой скоростью, чтобы температура не превышала 40oC. Органический слой отделили, промыли дважды по 50 мл 10%-ным раствором гидроксида натрия и сконцентрировали. Оставшийся маслообразный сырой метиловый эфир 3-формилиндол-4-карбоновой кислоты растворили в диэтиловом эфире. Из эфирного раствора выкристаллизовался продукт, который затем был отфильтрован. После высушивания получено 83,4 г метилового эфира 3-формилиндол-4-карбоновой кислоты с точкой плавления 134 135oC.
b) 60 г полученного выше продукта смешали при комнатной температуре при перемешивании с 350 мл нитрометана и 5 мл 1,8-диазабицикло [5,4,0] ундец-7-ена (1,5-5) (=DBU) и реакционную смесь оставили реагировать при температуре 65oC в течение 6 ч. По окончании для дальнейшей обработки реакционную смесь сконцентрировали досуха и остаток растворили в этилацетате. Раствор дважды промыли водой, высушили над сульфатом натрия, отфильтровали и сконцентрировали. Оставшийся маслообразный сырой метиловый эфир 3-(1,3-динитро-пропан-2-ил) индол-4-карбоновой кислоты растворили в диэтиловом эфире. Из эфирного раствора выкристаллизовался продукт. Кристаллизат отфильтровали, окончательно промыли диэтиловым эфиром и высушили. Получено 67 г метилового эфира 3-(1,3-динитропропан-2-ил)индол-4-карбоновой кислоты с точкой плавления 110 112oC.
c) 67 г полученного выше продукта растворили в литре метанола. К раствору добавили 5 г никеля Ренея. Затем к реакционной смеси прикапали 150 мл гидразин-гидрата. При этом температура поднялась до 40oC (наблюдалось быстрое выделение газа). По окончании реакционную смесь нагревали в течение 1,5 ч до 55oC. Для дальнейшей обработки реакционную смесь охладили, отфильтровали от катализатора и сконцентрировали досуха. Остаток сырое основное вещество очистили посредством колоночной хроматографии при слабо повышенном давлении (Flash-хроматография) с применением метанола/25%-водного аммиака 96: 4 в качестве элюента. Пенистый остаток, образовавшийся после упаривания смеси растворителей, растворили в метаноле и кристаллизовали. Кристаллизат подкислили и окончательно промыли смесью метанол/диэтиловый эфир 9:1 и высушили. Получено 36,4 г 3-аминометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd]индол-гидрата с точкой плавления 119 120oC.
Для перевода в гидрохлорид 13 г полученного выше гидрата растворили в 200 мл метанола. К раствору при перемешивании по каплям добавили избыток эфирного раствора хлористого водорода. Образовавшийся при комнатной температуре кристаллизат отфильтровали, отмыли смесью метанол/диэтиловый эфир 9:2 и высушили. Получено 12 г 3-аминометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd]индол-гидрохлорид-гидрата с точкой плавления 193 204oC.
d) Разделение энантиомеров:
Рацемическое целевое соединение, как следует из его оптических антиподов, разделили на
1a) 3R(+)-3-аминометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол и
1b) 3S(-)-3-аминометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол.
Рацемическое целевое соединение, как следует из его оптических антиподов, разделили на
1a) 3R(+)-3-аминометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол и
1b) 3S(-)-3-аминометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол.
Da1) 8,2 г рацемического 3-аминометил-3,4,5,6- тетрагидро-6-оксо-1H-азепино[5,4,3-cd] индол-гидрата растворили в 50 мл кипящего метанола и при перемешивании к раствору прибавили 5,12 г D(-) -винной кислоты. Затем добавили 5 мл воды и реакционную смесь перемешивали при температуре водяной бани 70oC до тех пор, пока раствор не стал прозрачным. Далее этот раствор перемешивали при комнатной температуре в открытом сосуде. Образовавшийся кристаллизат отделили от маточного раствора и промыли небольшим количеством метанола. После высушивания получено 5,9 г кристаллизата, который перекристаллизовали из смеси метанол/вода 9:1 и высушили. Получено 3,5 г 3R(+)-3- аминометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино[5,4,3-cd] индол-D- тартрата с величиной удельного угла оптического вращения [α] = +92,8° (c=0,25 в воде).
Da2) 2,12 г полученного выше тартрата растворили в 6,3 мл воды при температуре до 95oC. Раствор имел значение pH до 3,5. Прибавлением 25%-ного изопропанольного раствора хлористого водорода снизили значение pH до 0,4 и затем раствор сконцентрировали при пониженном давлении (вакуум водоструйного насоса) до 4 мл. Образовавшийся кристаллизат спустя 24 часа отфильтровали из водной реакционной смеси, промыли небольшим количеством метанола и высушили. Получено 0,94 г 3R(+)-3-аминометил-3,4,5,6-тетрагидро-6- оксо-1H-азепино [5,4,3-cd] индол-гидрохлорида с точки плавления до 295oC (разложение) и величиной удельного угла оптического вращения [α] = +232,4° (c=0,25 в воде).
Da3) Оставшийся в Da2) водный фильтрат довели до значения pH, равного 11, добавлением насыщенного раствора водного раствора карбоната натрия и затем упарили при пониженном давлении (вакуум водоструйного насоса). Остаток очистили посредством хроматографии при слегка повышенном давлении (Flash-хроматография) на кизельгеле с использованием смеси метанол/ 25%-ный водный раствор аммиака 96:4 в качестве элюента. Получено 0,32 г аморфного 3R(+)-3-аминометил-3,4,5,6-тетрагидро-6-оксо-1H -азепино[5,4,3-cd] индола с величиной удельного угла оптического вращения [α] = +104°C (c=1 в метаноле).
Db1) Маточный раствор, полученный на стадии DaI), упарили и остаток растворили в 20 мг воды при температуре до 80oC. После охлаждения раствора до комнатной температуры к нему добавили 4 мг изопропанола. Раствор перемешивали в течение 48 ч при комнатной температуре в открытом сосуде. Образовавшийся кристаллизат отфильтровали, высушили и дважды перекристаллизовали из смеси вода/изопропанол 20:4. Получено 1,05 г 3S(-)-3-аминометил-3,4,5,6 -тетрагидро-6-оксо-1H-азепино[5,4,3-cd]индол-B-тартрата с величиной удельного угла оптического вращения [α] = -143° (c=1 в метаноле).
Db2) 0,95 г полученного выше тартрата перевели непосредственно в гидрохлорид методом, аналогичным описанному в стадии Da2). Получено 0,3 г 3S(-)-3-аминометил-3,4,5,6 -тетрагидро-6-оксо-1H-азепино [5,4,3-cd]индол-гидрохлорида с величиной удельного угла оптического вращения [α] = -222° (c=0,25 в воде).
Db3) Из водного фильтрата, оставшегося в стадии Db2), методом, аналогичным описанному в стадии Da3), освободили основание и почистили его. Получено 0,15 г аморфного 3S(-)-3-аминометил-3,4,5,6 -тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индола с величиной удельного угла оптического вращения [α] = -103° (c=1 в метаноле).
Пример 2. 3-бензиламинометил-3,4,5,6-тетрагидро-6 оксо-1H-азепино-[5,4,3-cd] индол.
6,2 г 3-Аминометил-3,4,5,6-тетрагидро-6-оксо-1H -азепино-[5,4,3-cd] индол-гидрата (получение см. в примере 1с) поместили в 120 мл бензола и к смеси добавили 3,3 мл бензальдегида. Эту реакционную смесь кипятили с водоотделителем в течение 3 ч. По окончании реакционную смесь сконцентрировали досуха. Сырой, в виде маслообразного остатка, 3-бензил-иденаминометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол сразу же подвергли дальнейшей обработке. Для этого его растворили в 40 мл уксусной кислоты и к раствору при охлаждении льдом и перемешивании порциями добавили 1,2 г натрийборгидрида. Затем реакционную смесь перемешивали 30 мин при комнатной температуре. Для дальнейшей обработки уксусную кислоту упарили при пониженном давлении (вакуум водоструйного насоса). Маслообразный остаток растворили в 100 мл воды и смесь подщелочили путем добавления насыщенного водного раствора карбоната натрия до pH 9. Сырой целевой продукт, осажденный в виде масла, отделили и водную фазу экстрагировали трижды по 100 мл хлористым метиленом. Органические фазы объединили, высушили над сульфатом натрия, отфильтровали и сконцентрировали досуха. Оставшийся сырой целевой продукт очистили посредством колоночной хроматографии на кизельгеле при слабо повышенном давлении (Flash-хроматография), используя в качестве элюента смесь этилацетат/метанол 4:1. После упаривания растворителей получено 7 г 3-бензиламинометил-3,4,5,6-тетрагидро-6-оксо-1H- азепино-[5,4,3-cd] индола в виде пенящегося продукта.
3г полученного выше целевого соединения растворили в метаноле и, как описано в примере 1с), перевели в гидрохлорид. Получено 2,9 г 3-бензиламинометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино[5,4,3-cd] индол-гидрохлорида с точкой плавления 179-181oC.
Пример 3. 3-(N-бензил-N-метиламинометил)-3,4,5,6- тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол.
6,2 г 3-бензиламинометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индола (получением см.пример 2) растворили в 250 мл диметилформамида. К раствору при комнатной температуре и при перемешивании добавили 0,81 мл йодистого метила и 1,81 г карбоната калия. Реакционную смесь в течение 3 ч перемешивали при комнатной температуре. Затем для дальнейшей обработки при пониженном давлении в вакууме водоструйного насоса удалили при 50oC диметилформамид. Маслообразный остаток растворили в смеси вода/дихлорметан 1:1, отделили дихлорметановую фазу и водную фазу еще дважды экстрагировали дихлорметаном. Органическую фазу очистили, высушили над сульфатом натрия, отфильтровали и упарили. В остатке 3,84 г маслообразного сырого продукта. Его очистили посредством хроматографии при умеренно повышенном давлении (= хроматографии низкого давленияLPLC при 3-6 барах) на кизельгеле (продажный продукт Zichroprer R Si 60), используя в качестве элютена смесь дихлорметан/метанол 9: 1. Получено 3,26 г маслообразного 3-(N-бензил-N-метиламинометил)-3,4,5,6-тетрагидро -6-оксо-1H-азепино [5,4,3-cd] индола.
0,88 г полученного выше целевого соединения при легком нагревании растворили в 5 мл изопропанола. К этому раствору добавили раствор 0,44 г фумаровой кислоты в смеси с 9 мл изопропанола и 1 мл метанола. Затем смесь смешали с 1 мл метилтрет.бутилового эфира до легкого помутнения. Из этой реакционной смеси выкристаллизовался фумарат. После фильтрации кристаллизата, промывания его метилтрет.бутиловым эфиром и высушивания получено 1,07 г 3-(N-бензилN-метиламинометил)-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол-гидрогенфумарат-семигидрат с точкой плавления 191-193oC.
Пример 4. 3-метиламинометил-3,4,5,6-тетрагидро-6-оксо -1H-азепино-[5,4,3-cd] индол.
A1) 2,38 г 3-(N-бензил-N-метиламинометил)-3,4,5,6- тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол (получение см. в примере 3) растворили в 150 мл метанола. К раствору в токе азота на кончике шпателя добавили катализатор палладий/на угле (10% ). Затем смесь гидрировали в автоклаве при давлении водорода до 3,5 бар при температуре до 50oC при перемешивании. Спустя 3 ч водород удалили, реакционный объем заполнили азотом и отфильтровали катализатор. Оставшийся раствор упарили и остаток - маслообразный сырой продукт очистили хроматографией низкого давления на кизельгеле с использованием смеси метанол/25%-ный водный раствор аммиака 96:4 в качестве элюента. Получено 0,9 г 3 -метиламинометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd]индола в виде пенящегося продукта.
0,62 г полученного выше целевого основания перевели в гидрохлорид, аналогично описанному в примере 1с). Получено 0,56 г 3 -метиламинометил-3,4,5,5-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол-гидрохлорида с точкой плавления от 274 до 277oC.
A2) Введение 3-(N-бензил-N -метиламинометил)-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3 -cd]индола можно осуществить, используя в качестве исходного вещества также 3-(N-дифенилметил-N -метиламино)-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол (точка плавления 192oC, с разложением), который можно получить аналогично примеру 3, исходя из 3-[N-(дифенилметил)-амино-метил] -3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индола (точка плавления гидрохлорида 291oC, с разложением, получение аналогично примеру 2, исходя из 3-аминометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd]индол-гидрата и бензофенона).
B) Разделение энантиомеров.
Рацемическое соединение можно разделить на его оптические антиподы аналогично методу, описанному в примере 10. Получено:
4a) 3R(+)-3-метиламинометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол-гидрохлорид, точка плавления 310oC (разложение), [α] =218,6° (c=1 в метаноле) и
4b) 3S(-)-3-метиламинометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd]индол-гидрохлорид, точка плавления >280oC (разложение), [α] = -224,9° (с=1 в метаноле).
4a) 3R(+)-3-метиламинометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол-гидрохлорид, точка плавления 310oC (разложение), [α]
4b) 3S(-)-3-метиламинометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd]индол-гидрохлорид, точка плавления >280oC (разложение), [α]
C) 2-ой метод разделения энантиомеров.
Ca1) 2,14 г N-этоксикарбонил-L-лейцина и 2,94 мл триэтиламина растворили в 75 мл сухого тетрагидрофурана. Раствор охладили до примерно -15oC. Затем в атмосфере азота частями в течение 10 мин добавляли 1,37 мл изобутилового эфира хлормуравьиной кислоты в 10 мл сухого тетрагидрофурана. Далее реакционная смесь перемешивалась в течение 10 мин. Потом порциями в течение 15 мин при примерно -15oC добавили 2,8 г рацемического 3-метиламинометил-3,4,5,6-тетрагидро -6-оксо-1H-азепино [5,4,3-cd] индола. Реакционную смесь медленно нагрели до комнатной температуры и перемешивали в течение 3 ч. По окончании ее упарили и остаток очистили посредством хроматографии при слабо повышенном давлении (Flash-хроматография), используя в качестве элюента смесь этилацетат/метанол 99: 1. 3 г очищенного продукта разделили посредством препаративной жидкостной хроматограии высокого давления (HPLC) на (+)- и (-)-энантиомеры.
C2) 1,8 г (+)-энантиомера растворили в 25 мл концентрированной соляной кислоты и раствор нагрели на масляной бане до 100oC. Спустя 24 ч раствор упарили при пониженном давлении, остаток растворили в этаноле и снова упарили. Остаток растворили в водном этаноле и к нему добавили 1,18 г карбоната калия. Смесь сконцентрировали при пониженном давлении и остаток очистили посредством хроматографии при слабо повышенном давлении (Flash-хроматография), используя в качестве элюента смесь метанол/водный раствор аммиака 99,5:0,5. Полученный сиропообразный продукт растворили в небольшом количестве абсолютного этанола и к раствору добавили избыток этанольного раствора соляной кислоты. Образовавшийся осадок отсосали на фильтре и промыли абсолютным этанолом и диэтиловым эфиром. Полученный 3R(+) -3-метиламинометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол-гидрохлорид имел точку плавления до 310oC (разложение) и величину удельного угла оптического вращения [α] = +218,6° (метанол).
Cb) Полученный на стадии Ca1) (-)-энантиомер аналогично методу, описанному в стадии Ca2), переведен в 3S(-) -3-метиламинометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] -индол-гидрохлорид с точкой плавления выше 280oC (разложение) и величиной удельного угла оптического вращения [α] = -224,9° (метанол).
Пример 5.
a) 3-этиламинометилметил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол.
b) 3-диэтиламинометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол.
A) 6г 3-Аминометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd]индол-гидрата (получение см. пример 1C) растворили в 60 мл диметилформамида. К раствору добавили одновременно 2,5 мл этилбромида и 5,1 мл триэтиламина четырьмя равными порциями в течение 6,5 ч. В течение всего этого времени температура реакционной смеси поддерживалась 60oC. Для дальнейшей обработки реакционную смесь упарили досуха и оставшуюся красную реакционную смесь, состоящую из обоих целевых соединений, разделили посредством хроматографии при слабо повышенном давлении (Flash-хроматография) на кизельгеле, используя смесь дихлорметана/метанола/диэтиламина 80:17:3. Получено 3,4 г маслообразного сырого моноэтиламино-метильного продукта (=соединению 5a) и 4,1 г маслообразного диэтиламинометильного продукта (=соединению 5b).
Маслообразный продукт 5a) растворили в метаноле. Из раствора при добавлении небольшого количества диэтилового эфира выкристаллизовалось 2,3 г 3-этиламинометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индола с точкой плавления 90 92oC.
Маслообразный сырой продукт 5b) растворили в этаноле и при добавлении эфирного раствора хлористого водорода получили, как описано в примере 1C), гидрохлорид. Получено 2,5 г 3-диэтил -аминометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол-гидрохлорида с точкой плавления 150 153oC.
ПРИМЕР 6. 3-изопропиламинометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd]-индол.
К раствору 3-аминометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол-гидрата (получение см. пример 1C) в 80 мл тетрагидрофурана при перемешивании добавили 0,82 г комплекса боран-диметиламина. Раствор кипятили в течение 1 ч с обратным холодильником и по окончании прикапали при температуре до 45oC 10 мл ацетона. Реакционную смесь перемешивали 2,5 ч при температуре до 60oC. Затем для дальнейшей обработки реакционную смесь упарили досуха и остаток растворили в смеси из воды и дихлорметана. Отделили дихлорметановую фазу и водную фазу экстрагировали трижды по 50 мл смесью из дихлорметана/метанола 9:1. Органические фазы объединили и упарили досуха. Остаток сырой продукт очистили посредством хроматографии при слабо повышенном давлении (Flash-хроматография) на кизельгеле с использованием в качестве элюента смеси метанол/этилацетат 4:1. Целевое соединение получено в виде масла.
Маслообразное целевое соединение переведено в гихрохлорид методом, описанным в примере 1C). Получено 1,6 г 3-изопропил -аминометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол -гидрата с точкой плавления 180-183oC.
Пример 7. 4-аминометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол.
А) 100 г этилового эфира индол-4-карбоновой кислоты растворили в 500 мл ледяной уксусной кислоты. К раствору при комнатной температуре прикапали смесь из 86 мл 40%-ного водного раствора диметиламина, 55 мл 37%-ного водного раствора формальдегида и 250 мл ледяной уксусной кислоты. По окончании реакционную смесь перемешивали при комнатной температуре в течение 20 ч. Для дальнейшей обработки к реакционной смеси при охлаждении льдом для достижения pH 9 прибавили 20% -ный водный раствор гидроксида натрия. Затем трижды экстрагировали дихлорметаном, объединенные органические фазы высушили над сульфатом натрия, отфильтровали и сконцентрировали. Получено 127 г сырого метилового эфира 3-диметил-аминометилиндол-4-карбоновой кислоты в виде светло-желтого масла.
В) 127 г полученного выше продукта растворили в 600 мл ацетонитрила. К раствору прилили 68 мл этилового эфира нитроуксусной кислоты. Затем при комнатной температуре прикапали раствор из 40 мл трибутилфосфина в 350 мл ацетонитрила. Реакционную смесь кипятили с обратным холодильником в течение 2,5 ч. По окончании для дальнейшей обработки реакционную смесь упарили досуха и остаток растворили в 10%-ной водной соляной кислоте. Раствор трижды экстрагировали этилацетатом и объединенные органические экстракты высушили над сульфатом натрия, отфильтровали и сконцентрировали. Оставшийся сырой продукт очистили посредством колоночной хроматографии на кизельгеле при слабо повышенном давлении (Flash-хроматография), используя в качестве элюента смесь циклогенсан/этилацетат 2:1. После упаривания элюента остаток кристаллизовали из диэтилового эфира. Получено 66 г 3-(этоксикарбонил-2-нитропропил)-индол-4-карбоновой кислоты метиловый эфир с точкой плавления 106-110oC.
С) 66 г полученного выше продукта растворили в 2 л толуола. К раствору добавили 5 г палладий/угольного катализатора. Затем реакционную смесь 6 ч гидрировали под давлением водорода до 50 бар при температуре до 70oC. По окончании смесь охладили, отфильтровали катализатор и фильтрат упарили. Маслообразный остаток для окончательной циклизации нагревали при 130oC в течение 1 ч. Образовавшийся при последующем охлаждении кристаллизат смешали с этанолом, отфильтровали и промыли смесью из диэтилового эфира/этанола 1:1. После высушивания получено 41,5 г 3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол-4-карбоновой кислоты этиловый эфир с точкой плавления 185-188oC.
Д) 41,5 г полученного выше продукта растворили в 1,2 л тетрагидрофурана. К раствору порциями при перемешивании добавили при комнатной температуре 48,7 г натрийборгидрида. По окончании прикапали 780 мл этанола и реакционную смесь 1,5 ч нагревали при 50oC. Для дальнейшей обработки реакционную смесь разбавили дихлорметаном и органические фазы экстрагировали водой. Вслед за тем водные фазы четырежды экстрагировали смесью из дихлорметана/метанола 95: 5. Объединенные органические фазы высушили над сульфатом натрия, отфильтровали и фильтрат упарили. Выпавший твердый остаток растворили в метаноле и кристаллизовали. Кристаллизат отфильтровали, промыли смесью из метанола/диэтилового эфира 8: 2 и высушили. Получено 31,3 г 4 -гидроксиметил-3,4,5,6-тетрагидро-6-оксо-1H-азепино[5,4,3-cd] индол с точкой плавления 186-187oC.
Е) 31,3 г полученного выше продукта растворили в 190 мл пиридина. Вслед за тем раствору при охлаждении и перемешивании добавили 33 г п-толуолсульфокислоты хлорида. Реакционную смесь перемешивали при комнатной температуре 24 ч. Для дальнейшей обработки реакционную смесь влили в 300 мл ледяного, насыщенного водного раствора лимонной кислоты. Водную кислую фазу трижды экстрагировали дихлорметаном. Объединенные органические экстракты высушили над сульфатом натрия, отфильтровали и упарили. Остаток растворили в метаноле и кристаллизовали при добавлении диэтилового эфира. Кристаллизат отфильтровали, промыли смесью из метанол/диэтилоовго эфира 7:3 и высушили. Получено 36,5 г 4-(p-толуолсульфонилоксиметил-3,4,5,6-тетрагидро -6-оксо-1H-азепино[5,4,3-cd]индола с точкой плавления 175-178oC.
F) 5 г полученного выше продукта растворили в 50 мл диметил формамида. К раствору добавили 5,3 г азида натрия. Затем реакционную смесь нагревали до 100oC при перемешивании 2 ч. Для дальнейшей обработки ее охладили, реакционную смесь упарили, остаток растворили в дихлорметане и дихлорметановую фазу дважды промыли водой, высушили над сульфатом натрия, отфильтровали и упарили. Маслообразный остаток растворили в этилацетате и кристаллизовали при добавлении диэтилового эфира. Получено 2,8 г 4-азидометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино[5,4,3,-cd]индола с точкой плавления 152-153oC.
G) 2,8 г полученного выше продукта растворили в 30 мл метанола. В раствор внесли на кончике шпателя никель Ренея, затем при перемешивании добавили 2,3 мл гидразин-гидрата и в течение 2 ч реакционная смесь перемешивалась при комнатной температуре. Для дальнейшей обработки катализатор отсосали на асбестовом шламе (продажный продукт ThevritR) и фильтрат упарили. Остаток сырое целевое соединение растворили в метаноле и, как описано в примере IC), перевели в свой гидрохлорид. Полученный кристаллизат отфильтровали, промыли смесью из метанола/диэтилового эфира 8:2 и высушили. Получено 2,8 г 4-аминометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино[5,4,3 -cd] индол-гидрохлорида с точкой плавления 259-265oC.
Пример 8. 4-(2-аминоэтил)-3,4,5,6-тетрагидро -6-оксо-1H-азепино-[5,4,3-cd]индол.
А) 5 г 4-(p-толуолсульфонилоксиметил) -3,4,5,6-тетрагидро-6-оксо-1H-азепино[5,4,3-cd] индола (получение см. пример 7Е) растворили в 25 мл диметилформамида. К раствору добавили 970 мг цианида калия. Реакционную смесь при перемешивании нагревали 3 ч при 65oC. Для дальнейшей обработки реакционную смесь при охлаждении разбавили водой и трижды экстрагировали этилацетатом. Объединенные органические фазы высушили над сульфатом натрия, отфильтровали и упарили. Маслообразный остаток растворили в метаноле и раствор довели до кристаллизации путем добавления диэтилового эфира. Кристаллизат отсосали, промывали на фильтре смесью из метанол/диэтилового эфира 8:2 и высушивали. Получено 2,4 г 4-цианометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индола с точкой правления 197-198oC.
B) 1,8 г полученного выше продукта растворили в 250 мл насыщенного при 0oC аммиаком метаноле. К раствору на кончике шпателя добавили никель Ренея. Затем реакционную смесь поместили в автоклав и 5 ч гидрировали при перемешивании при 50oC под давлением водорода до 50 бар. Для дальнейшей обработки катализатор отфильтровали и фильтрат упарили. Остаток очистили посредством хроматографии низкого давления на кизельгеле с использованием в качестве элюента смеси метанол/дихлорметан/диэтиламин 17:80:3. Целевое соединение получено в виде масла.
Полученное выше целевое основание растворили в метаноле и аналогично методу, описанному в примере 3, подвергли взаимодействию с малоновой кислотой. Получено 1,4 г 4-(2-амино-метил)-3,4,5,6-тетрагидро -6-оксо-1H-азепино [5,4,3-cd]индол-гидромалеината с точкой плавления 209-210oC.
Пример 9. 1-метил-3-аминометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол.
А) к раствору 7 г метилового эфира 3-формилиндол-4-карбоновой кислоты (получение см. пример IA) в атмосфере азота при комнатной температуре порциями добавляли 2,1 г 80%-ного гидрида натрия. Реакционную смесь в течение 1 ч перемешивали при 50oC. По окончании из капельной воронки добавляли 7 мл йодистого метила и реакционную смесь перемешивали еще в течение 2 ч при 50oC. Для дальнейшей обработки реакционную смесь упаривали при пониженном давлении досуха и смесь растворили в 50 мл воды и 50 мл дихлорметана. Дихлорметановую фазу отделили и водную фазу еще раз экстрагировали дихлорметаном. Органические фазы объедининли, высушили над сульфатом натрия, отфильтровали и упарили. Оставшийся кристаллический сырой продукт перекристаллизовали из диэтилового эфира. После высушивания кристаллизата получено 6,9 г метилового эфира 1-метил-3-формилидон-4-карбоновой кислоты с точкой плавления 128-129oC.
В) 6,9 г полученного выше продукта смешали при комнатной температуре с 70 мл нитрометана и 1 мл 1,8-диазабицикло [5.4.0]-ундец-7-еном(1,5-5) и реакционную смесь 4 ч перемешивали при температуре до 65oC. По окончании реакционную смесь обработали так же, как описано в примере IB). Получено 5,1 г метилового эфира 1-метил-3(1,3-динитропропан -2-ил)индол-4-карбоновой кислоты с точкой плавления 142-145oC.
С) 5,1 г полученного выше продукта растворили в 60 мл метанола и в присутствии никеля Ренея (на кончике шпателя) подвергли взаимодействию с 10 мл гидразин-гидрата по методу, описанному в примере IC). После окончания реакции катализатор отфильтровали и фильтрат упарили при пониженном давлении. Сырой целевой продукт, в виде пенящегося остатка, растворили в метаноле и, как описано в примере IC), перевели в гидрохлорид. Получено 3,2 г 1-метил-3-аминометил-3,4,5,6 -тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол-гидрохлорида с точкой плавления 256-261oC.
Пример 10. 1-бензил-3-аминометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-сd] индол.
A) 28 г метилового эфира 3-формилиндол-4-карбоновой кислоты (получение см. пример IA) растворили в 230 мл нитрометана. К раствору добавили 4,2 г ацетата аммония и реакционную смесь кипятили с обратным холодильником в течение 1 ч. Для дальнейшей обработки реакционную смесь охладили до комнатной температуры, разбавили смесью из этилацетат/метанола 9:1 и затем вылили в 150 мл воды. Отделили органическую фазу, высушили ее над сульфатом натрия, отфильтровали и сконцентрировали при слабо пониженном давлении. Продукт, выкристаллизовавшийся из сконцентрированного раствора, отфильтровали и высушили. Получено 25 г метилового эфира 3-(2-нитроэтилен)-индол-4-карбоновой кислоты с точкой плавления 187-190oC.
В) 12 г полученного выше продукта растворили в 200 мл сухого диметилформамида. К раствору в атмосфере азота при комнатной температуре порциями добавляли 3 г натрийборгидрида. Затем реакционную смесь нагрели до 60oC и из капельной воронки прикапали 6,3 мл бензилбромида. Далее реакционную смесь нагревали до 80oC и 1 ч перемешивали при этой температуре. Для дальнейшей обработки реакционную смесь упарили при пониженном давлении и остаток растворили в смеси из воды/этилацетата. Органическую фазу отделили и сконцентрировали. Остаток очистили посредством колоночной хроматографии на кизельгеле при слабо повышенном давлении (Flash-хроматография), используя в качестве элюента этилацетат. Остаток, образовавшийся после концентрирования элюента, кристаллизовали из смеси дихлорметан/диэтиловый эфир 1:9. После высушивания получено 10,8 г кристаллического метилового эфира 1-бензил -3-(2-нитроэтилен)индол-4-карбоновой кислоты, который сразу же подвергли дальнейшей обработке.
C) 10,8 г полученного выше продукта растворили в 150 мл метанола. К раствору при комнатной температуре добавили 33 мл нитрометана и затем медленно прилили 2 мл диазабицикло [5.4.0] ундец-7-ена (1,5 5). По окончании реакционную смесь перемешивали при комнатной температуре в течение 1 ч. Для дальнейшей обработки реакционную смесь разбавили 150 мл воды и трижды по 100 мл экстрагировали дихлорметаном. Органические фазы объединили, высушили над сульфатом натрия, отфильтровали и упарили. Остаток маслообразный продукт - очистили Flash-хроматографией на кизельгеле с применением в качестве элюента этилацетата. Остаток после концентрирования элюата кристаллизовали из смеси изопропанол/этилацетат 2:8. После высушивания получено 10,3 г кристаллического метилового эфира 1-бензил -3-(1,3-динитропропан-2-ил)-индол-4-карбоновой кислоты, который сразу же подвергли дальнейшей обработке.
D) 10,3 г полученного выше продукта растворили в 250 мл метанола и в присутствии 3 г промытого метанолом никеля Ренея подвергли взаимодействию с 34 мл гидразин-гидрата по примеру 1C). Реакционную смесь обработали, как описано в примере 1C). Целевое соединение получено в виде масла. Полученное выше целевое основание методом, описанным в примере 1C), переведено в гидрохлорид. Получено 7,4 г 1-бензил -3-аминометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол-гидрохлорида с точкой плавления 167 169oC.
Пример 11. 3-аминометил-5-метил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол.
А) К 50 мл ангидрида трифторуксусной кислоты при перемешивании и охлаждении льдом прибавили порциями 16 г 3-амино-метил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол-гидрата (получение см. пример C) в течение 30 мин. Реакционную смесь 2 ч перемешивали в атмосфере азота. По окончании реакционную смесь упарили при пониженном давлении досуха. Остаток растворили в 200 мл этилацетата. Прибавлением насыщенного водного раствора бикарбоната натрия довели раствор до значения pH 8,5. Обработкой водным насыщенным раствором бикарбоната натрия нейтрализовали образовавшуюся трифторуксусную кислоту и избыточный ангидрид трифторуксусной кислоты и одновременно отщепили вновь трифторацетильный остаток, расположенный в 5 положении у атома азота. По окончании органическую фазу отделили, водную фазу еще дважды проэкстрагировали этилацетатом и органические фазы объединили, высушили над сульфатом натрия, отфильтровали и упарили. Остаток кристаллизовали путем добавления диэтилового эфира. После высушивания получено 18 г 3-трифторацетамидометил-3,4,5,6-тетрагидро-6-оксо-1H -азепино [5,4,3-cd] индол с точкой плавления 228 232oC.
B) 6 г полученного выше продукта растворили при комнатной температуре в 40 мл муравьиной кислоты (98 до 100%). К раствору при температуре от 55 до 65oC в течение 8 ч прикапали 95 мл ангидрида уксусной кислоты. Реакционную смесь перемешивали 12 ч при комнатной температуре. Затем раствор упарили при пониженном давлении (в вакууме водоструйного насоса) и остаток растворили в этилацетате и обработали, как описано в примере 11А). Получено 5,3 г кристаллического 3-трифторацетами-дометил -5-формил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол с точкой плавления 198 205oC.
C) 4 г полученного выше продукта растворили в 80 мл абсолютного тетрагидрофурана, и раствор в атмосфере азота охладили до -78oC. При этой температуре медленно прикапали 11,8 г 1М раствора диизобутилалюминийгидрида в толуоле. По окончании охлаждение сняли. Спустя 2 ч раствор обработали 80 мл этилацетата и 60 мл 10%-ного водного раствора лимонной кислоты. Органическую фазу отделили, а водную фазу еще два раза по 80 мл экстрагировали этилацетатом. Органические фазы объединили, высушили над сульфатом натрия и упарили в вакууме водоструйного насоса. После высушивания получено 3,4 г 3-трифторацетамидометил -5-гидроксиметил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол с точкой плавления 150 151,5oC.
D) К суспензии 1,08 г натрийборгидирида в 60 мл тетрагидрофурана при охлаждении льдом и сильном перемешивании прикапали 25,2 мл трифторуксусной кислоты. К этому раствору при охлаждении льдом в течение 30 мин прикапали 1,8 г полученного выше продукта в 60 мл тетрагидрофурана. По окончании охлаждение убрали и реакционную смесь нагревали при 60oC в течение 1 ч. Затем реакционную смесь сконцентрировали в вакууме водоструйного насоса до 10 мл, и обработали, как описано в примере 11А). Полученный маслообразный продукт очистили посредством хроматографии при умеренно повышенном давлении (хроматография низкого давления при 3 5 барах). Полученный продукт кристаллизовали из смеси этилацетат/диэтиловый эфир. Получено 1,2 г 3 -фторацетамидометил-5-метил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол с точкой плавления 174 177oC.
E) 1,2 г полученного выше продукта растворили в 40 мл метанола. К раствору прилили 40 мл 5%-ного водного раствора карбоната калия. Реакционную смесь перемешивали 8 ч при комнатной температуре. Затем для дальнейшей обработки реакционную смесь очистили посредством хроматографии при умеренно повышенном давлении ( хроматографии низкого давления при 3 6 барах) на кизельгеле с применением в качестве элюента смеси метанол/25%-ный водный раствор аммиака 97:3. Очищенный продукт кристаллизовали из смеси метанол/диэтиловый эфир. Получено 0,82 г 3-аминометил-5-метил-3,4,5,6 -тетрагидро-6-оксо-1H-азепино[5,4,3-cd] индола с точкой плавления 85 - 87oC.
F) 3-Аминометил-5-метил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол можно также получить путем гидрогенолитического дебензилирования 1-бензил-3-бензиламинометил -5-метил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индола (получение см. пример 18) аналогично методу, описанному в примере 4, при давлении водорода до 10 бар.
Пример 12. 3-аминометил-5-метоксиметил-3,4,5,6-тетргидро-6-оксо-1H-азепино [5,4,3-cd] индол.
К раствору 1,5 г 3-фторацетамидометил -5-гидроксиметил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индола (получение см. пример 11C) в 25 мл метанола добавили 0,1 п-толуолсульфокислоты и раствор кипятили с обратным холодильником в течение 2 ч. Затем реакционную смесь сконцентрировали и остаток путем добавления водного насыщенного раствора карбоната калия до достижения значения pH 11 и 4 ч перемешивали при комнатной температуре. Посредством обработки водным насыщенным раствором карбоната калия отщепили трифторацетильную защитную группу и нейтрализовали п-толуолсульфокислоту. Для дальнейшей обработки реакционную смесь упарили, остаток растворили в метаноле и отфильтровали от нерастворимых частиц и отфильтрованный остаток промыли дважды по 30 мл метанола. Объединенные метанольные фазы упарили и остаток очистили посредством хроматографии при умеренно повышенном давлении ( хроматография низкого давления при 3 6 барах) на кизельгеле с применением в качестве элюента метанол/25%-ный водный раствор аммиака 97:3. Целевое соединение, оставшееся после концентрирования элюата, кристаллизовали из смеси этанол/эфир 9:1. Получено 0,5 г 3-аминометил-5-метоксиметил-3,4,5,6-тетрагидро-6-оксо-1H -азепино-[5,4,3-cd] индол с точкой плавления 160 163oC.
Пример 13. 3-аминометил-1-(3-фенилпропил)-3,4,5,6-тетрагидро -6-оксо-1H-азепино-[5,4,3-cd] индол.
2 г 3-Трифторацетамидометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино[5,4,3-cd] индола (получение см. пример 11А) растворили в 40 мл сухого деметилформамида. К раствору добавили 0,8 г натрийборгидрида и в атмосфере азота перемешивали реакционную смесь в течение 1 ч. По окончании прикапали 3,9 мл 3-фенилпропилбромида и реакционную смесь 6 ч кипятили с обратным холодильником. После этого реакционную смесь упарили при пониженном давлении в вакууме водоструйного насоса и маслообразный остаток растворили в смеси из 40 мл этилацетата и 40 мл 5%-ного раствора лимонной кислоты. Органическую фазу отделили и еще дважды по 30 мл экстрагировали этилацетатом. Объединенные органические экстракты высушили над сульфатом натрия, отфильтровали и сконцентрировали. Полученный маслообразный сырой 3-трифторацетамидометил-1-(3 -фенилпропил)-3,4,5,6-тетрагидро-6-оксо-1H-азепино-[5,4,3-cd] индол очистили посредством хроматографии при умеренно повышенном давлении (хроматография низкого давления) на кизельгеле с применением в качестве элюента смеси циклогексан/этилацетат 1: 1. Фракции, содержащие очищенный продукт, объединили и сконцентрировали. Для отщепления трифторацетильной защитной группы полученный продукт растворили в 40 мл метанола и прибавили к 40 мл насыщенного водного раствора карбоната калия и перемешивали 8 ч при комнатной температуре. Затем реакционную смесь обработали методом, описанным в примере 11Е). Полученное маслообразное целевое основание растворили в изопропаноле и раствор прибавили к эфирному раствору хлористого водорода. Получено 1,0 г 3 -аминометил-1-(3 -фенилпропил)-3,4,5,6-тетрагидро-6-оксо-1H-азепино-[5,4,3-cd]индол -хлорида с точкой плавления 118oC.
Пример 14. 3-(пиперидин-1-илметил) -3,4,5,6 -тетрагидро-6-оксо-1H-азепино-[5,4,3-cd]индол.
4 г 3-аминометил-3,4,5,6 -тетрагидро -6-оксо-1H-азепино-[5,4,3-cd)индол-гидрата (получение см. пример IC) растворили в 40 мл диметилфомамида. К раствору прибавили 2,6 г триэтиламина и затем при комнатной температуре и перемешивании добавили 2,4 г дибромметана. Реакционную смесь 3,5 ч нагревали при 50oC. Для дальнейшей обработки реакционную смесь упарили при пониженном давлении в вакууме водоструйного насоса и остаток растворили в смеси из дихлорметан/метанол 9:1. Затем для достижения pH 11 добавили насыщенный водный раствор карбоната натрия. Органическую фазу отделили, а водную фазу промывали еще два раза по 50 мл смесью дихлорметан/метанол. Объединенные органические фазы высушили над сульфатом натрия, отфильтровали и упарили. Остаток растворили в этаноле и разбавили эфиром до легкого помутнения. Получившийся кристаллизат отфильтровали и высушили. Получено 3,5 г 3-(пиперидин -1-илметил)-3,4,5,6-тетрагидро-6-оксо-1H-азепино-[5,4,3 -cd]индола с точкой плавления 119-122oC.
Пример 15. 3-(диметиламинометилиденаминодиметил)-3,4,5,6 -тетрагидро-6-оксо-1H-азепино-[5,4,3-cd]индол.
2 г 3-аминометил-3,4,5,6-тетрагидро -6-оксо-1H-азепино[5,4,3, -cd]индол-гидрата (получение см. пример IC) растворили при комнатной температуре в 20 мл диметилформамида. К раствору при перемешивании прибавили 2,6 г диметилформамид-диметилацеталя. Реакционную смесь перемешивали при комнатной температуре в течение 4 ч. Затем реакционную смесь сконцентрировали при пониженном давлении в вакууме водоструйного насоса и маслообразный остаток растворили в 50 мл этилацетата. Раствор разбавили диэтиловым эфиром до легкого помутнения. Выкристаллизовались 2,2 г сырого целевого основания.
2,2г полученного выше сырого целевого основания растворили в метаноле и раствор добавлением эфирного раствора хлористого водорода довели значение pH до примерно равного 1. Затем раствор упарили и оставшееся целевое соединение кристаллизовали из бутилацетата при добавлении изопропанола. После высушивания кристаллизата получено 1,3 г 3 -(диметиламинометилиденаминометил)-3,4,5,6-тетрагидро-6-оксо-1H-азепино[5,4,3-cd] индол-гидрохлорида с точкой плавления 178-179oC.
Пример 16. 3-(Диметиламинометилиденаминометил) -3,4,5,6-тетрагидро-6-оксо-1H-азепино-[5,4,3-cd] индол.
1 г 3-аминометил-3,4,5,6-тетрагидро -6-оксо-1H-азепино-[5,4,3-cd] индол-гидрата (получение см. пример IC) растворили при комнатной температуре в 10 мл диметилформамида. К этому раствору прибавили 1 г N-хлорметилен-N,N-диметилиминохлорида. По окончании реакционную смесь перемешивали 2 ч при комнатной температуре. Для дальнейшей обработки реакционную смесь упарили при пониженном давлении в вакууме водоструйного насоса и остаток растворили в смеси из равных частей воды и этилацетата. Путем добавления насыщенного раствора бикарбоната натрия достигли pH водной фазы 8,5, затем отделили органическую фазу, а водную фазу экстрагировали этилацетатом еще три раза по 50 мл. Объединенные органические экстракты сконцентрировали до 25 мл. Полученный таким образом раствор целевого соединения далее обрабатывали, как описано в примере 15. Получено 0,5 г 3 -(диметиламинометилиденаминометил)-3,4,5,6-тетрагидро-6-оксо-1H -азепино-[5,4,3-cd]индол-гидрохлорида с точкой плавления 178-179oC.
Пример 17. 4-(4-фенилпиперазин-1-илметил)-3,4,5,6 -тетрагидро-6-оксо-1H-азепино-[5,4,3-cd]индол.
2,2 г 4-(п-толуолсульфонилоксиметил) -3,4,5,6-тетрагидро-6-оксо-1H-азепино-[5,4,3-cd] индола (получение см. пример 7Е) смешали с 9 мл 1-фенилпиперазина и далее смесь перемешивали 4 ч при температуре до 80oC. При последующем охлаждении выкристаллизовалось сырое целевое соединение. Его отфильтровали и промыли смесью из равных частей метанола и воды. После высушивания получено 1,7 г 4-(4-фенилпиперазин-1-илметил)-3,4,5,6 -тетрагидро-6-оксо-1H-азепино-[5,4,3-cd]индола с точкой плавления 184-185oC.
Пример 18. 1-бензил-3-бензиламинометил -5-метил-3,4,5,6-тетрагидро-6-оксо-1H-азепино-[5,4,3-cd]индол.
A) 4 г маслообразного 1-бензил-3- аминометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индола (получение см. пример 10) по методу, описанному в примере 2, подвергли взаимодействию с бензальдегидом и образовавшееся Шиффовое основание гидрировали по методу, описанному в примере 2. Реакционную смесь далее обработали, как в примере 2. Получено 4,3 г 1-бензил -3-бензиламинометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индола.
B) 4,3 г полученного выше продукта подвергали взаимодействию с ангидридом трифторуксусной кислоты по методу, описанному в примере 11A и реакционную смесь обработали, как описано в примере 11A. Получено 4,1 г 1-бензил-3-[N-(бензил)-трифторацетамидометил] -3,4,5,6-тетрагидро -6-оксо-1H-азепино-[5,4,3-cd] индола в виде пенящегося продукта.
C) 4,1 г полученного выше продукта растворили в 100 мл абсолютного татрагидрофурана. Раствор прикапали при температуре до -20oC в атмосфере азота к раствору 1,15 г трет.-бутилата калия в 10 мл тетрагидрофурана. Реакционную смесь перемешивали при температуре -20oC в течение 1 ч и затем при этой температуре прикапали раствор из 0,85 мл диметилсульфата в 5 мл тетрагидрофурана. Далее реакционную смесь перемешивали при -20oC один час в атмосфере азота. По окончании охлаждение удалили. После достижения комнатной температуры реакционную смесь сконцентрировали при пониженном давлении в вакууме водоструйного насоса до объема примерно 20 мл и затем разбавили путем добавления насыщенного водного раствора карбоната калия до значения pH, не превышающего 11. Далее реакционную смесь в течение часов сильно перемешивали, так чтобы осуществлялось хорошее смешение двух фаз, при этом также происходило отщепление трифторацетильной защитной группы. По окончании органическую фазу отделили, а водную экстрагировали дихлорметаном дважды по 50 мл. Объединенные органические фазы высушили над сульфатом натрия, отфильтровали и упарили. Оставшийся сырой продукт очистили посредством хроматографии при слабо повышенном давлении (Flash-хроматография) на кизельгеле с использованием в качестве элюента смеси этилацетат/циклогегсан 7:3. Получено 2,1 г 1-бензил-3-бензиламинометил-5-метил-3,4,5,6- тетрагидро-6-оксо-1H-азепино-[5,4,3-cd] индола в виде пенящегося продукта.
Пример 19. 3-[N-гидроксибензил] -аминометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино-[5,4,3-cd] индол.
К раствору из 1,5 г 3-[N -метоксибензил]-аминометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино-[5,4,3 -cd] индола и 2,5 г 1,4-диазабицикло 2,2,1 октана (= DABCO) добавили 2 мл триметилсилилиодида. Реакционную смесь нагревали 24 ч в атмосфере азота при 150oC. После охлаждения до комнатной температуры реакционную смесь разбавили 25 мл метанола и подкислили 20%-ной водной соляной кислотой. Затем реакционную смесь сильно перемешивали при комнатной температуре. Для дальнейшей обработки реакционную смесь разбавили 30 мл воды, водную фазу отделили, а органическую фазу промыли водой дважды по 20 мл. Объединенные водные фазы нейтрализовали разбавленной натронной известью и затем упарили при пониженном давлении в вакууме водоструйного насоса. Остаток маслообразный сырой продукт очистили посредством хроматографии на кизельгеле при слабо повышенном давлении (Flash-хроматография) с использованием в качестве элюента смеси метанол/25%-ный водный раствор аммиака 98:2. Получено 0,6 г 3-[N-(4-гидроксибензил)-аминометил] -3,4,5,6-тетрагидро-6-оксо-1H- азепино-[5,4,3,-cd] индола в виде масла.
0,6 г полученного выше целевого основания растворили в 20 мл метанола и прибавили к раствору 0,27 г винной кислоты. После упаривания этой смеси получено 0,87 г аморфного 3-[N-(4-гидроксибензил)-аминометил] 3,4,5,6-тетрагидро-6-оксо-1H-азепино-[5,4,3-cd] индола.
Пример 20. 4-аминометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино -[5,4,3-cd] -индола.
A) 2,5 г -(п-Толуолсульфонилоксиметил)-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3 -cd] индола растворили в 40 мл метанола. К раствору добавили 1,4 г фталимида калия. Реакционную смесь кипятили с обратным холодильником 6 ч. Для дальнейшей обработки реакционную смесь упарили досуха при пониженном давлении в вакууме водоструйного насоса. Твердый остаток растворили в смеси дихлорметана и воды 1:1. Органическую фазу отделили, а водную промыли дихлорметаном три раза по 50 мл. Объединенные органические экстракты высушили над сульфатом натрия, отфильтровали и упарили. Получено 1,9 г 4 -(N-фталимидометил)-3,4,5,6-тетрагидро-6-оксо-1H-азепино-[5,4,3-cd] индола, который тут же использовали в следующей стадии.
B) 1,9 г полученного выше продукта растворили в 50 мл этанола. К раствору прибавили 1 мл гидразин-гидрата. Реакционную смесь 4 ч кипятили с обратным холодильником. Для дальнейшей обработки образовавшийся охлажденный до комнатной температуры фталгидразид отфильтровали и промыли этанолом дважды по 20 мл. Фильтрат и промывные растворы объединили, упарили. Оставшееся целевое соединение очистили посредством хроматографии при умеренно повышенном давлении (=хроматографии низкого давленияLPLC при 3-6 барах) на кизельгеле с использованием в качестве элюента смеси метанол/водный раствор аммиака 98:2. Полученное таким образом целевое основание переведено в свой гидрохлорид методом, описанным в примере 7G). Получено 0,7 г 4-аминометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол-гидрохлорида с точкой плавления 256-260oC.
По методам, описанным в предложенных выше примерах, можно также представить соединения формулы 1, приведенные в нижеследующей табл.1.
Обозначения в табл. 1: Поз. положение боковой цепи в кольцевом остове, HCl гидрохлорид, B основание, HBr гидробромид, Hta гидрогентартрат, bi связь, Ph фенил, Cycloprop циклопропил, Cyclohex циклогексил, z - разложение.
Пример. 3-аминометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол содержащие таблетки.
Производились таблетки в следующем составе на таблетку, мг:
3-Аминометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол-гидрохлорид 20
Крахмал 60
Молочный сахар 135
Желатин (в виде 10%-ного раствора) 6
Основное вещество, крахмал и молочный сахар сгустили в 10%-ном желатиновом растворе. Пасту размельчили и получившийся гранулят поместили на подходящую посуду и высушили при 45oC. Высушенный гранулят пропустили через мельницу и смешали в миксере со вспомогательными материалами, мг:
Тальк 5
Стеарат магния 5
Крахмал 9
и затем спрессовали в таблетки по 240 мг.
3-Аминометил-3,4,5,6-тетрагидро-6-оксо-1H-азепино [5,4,3-cd] индол-гидрохлорид 20
Крахмал 60
Молочный сахар 135
Желатин (в виде 10%-ного раствора) 6
Основное вещество, крахмал и молочный сахар сгустили в 10%-ном желатиновом растворе. Пасту размельчили и получившийся гранулят поместили на подходящую посуду и высушили при 45oC. Высушенный гранулят пропустили через мельницу и смешали в миксере со вспомогательными материалами, мг:
Тальк 5
Стеарат магния 5
Крахмал 9
и затем спрессовали в таблетки по 240 мг.
Claims (14)
1. 6-Оксо-азепиноиндоловые соединения формулы I
где R1 водород, низший алкил или фенилнизшая алкильная группа, которая может быть моно- или дизамещена в фенильном кольце низшим алкоксилом или низшим алкилом;
R2 водород или низший алкил, который может быть замещен в α-положении к атому азота низшим алкоксилом;
R3 водород или галоген;
n 1 или, если -(CH2)-цепь расположена в 4-м положении кольца, также и 2;
R4 водород, C1 C5-алкил, C3 - C6-циклоалкил, C4-циклоалкилалкил, фенилнизшая алкильная группа, которая может быть моно- или дизамещена в фенильном кольце низшим алкилом, низшим алкоксилом, гидроксилом или галогеном;
R5 водород, C1 C5-алкил или фенилнизшая алкильная группа, которая может быть замещена низшим алкоксиломб или R4 и R5 вместе с атомом азота, с которым они соединены, образуют гетероцикл общей формулы
где B связь, метиленовая группа, кислород или иминогруппа -NR6, где R6 низший алкил или фенил;
D связь или в случае, если R4 и R5 не водород, также -N CH-группа,
и их физиологически переносимые кислотные соли присоединения.
где R1 водород, низший алкил или фенилнизшая алкильная группа, которая может быть моно- или дизамещена в фенильном кольце низшим алкоксилом или низшим алкилом;
R2 водород или низший алкил, который может быть замещен в α-положении к атому азота низшим алкоксилом;
R3 водород или галоген;
n 1 или, если -(CH2)-цепь расположена в 4-м положении кольца, также и 2;
R4 водород, C1 C5-алкил, C3 - C6-циклоалкил, C4-циклоалкилалкил, фенилнизшая алкильная группа, которая может быть моно- или дизамещена в фенильном кольце низшим алкилом, низшим алкоксилом, гидроксилом или галогеном;
R5 водород, C1 C5-алкил или фенилнизшая алкильная группа, которая может быть замещена низшим алкоксиломб или R4 и R5 вместе с атомом азота, с которым они соединены, образуют гетероцикл общей формулы
где B связь, метиленовая группа, кислород или иминогруппа -NR6, где R6 низший алкил или фенил;
D связь или в случае, если R4 и R5 не водород, также -N CH-группа,
и их физиологически переносимые кислотные соли присоединения.
2. 6-Оксо-азепиноиндоловые соединения по п. 1, отличающиеся тем, что в общей формуле I R1 водород.
3. 6-Окс-оазепиноиндоловые соединения по п. 1 или 2, отличающиеся тем, что в общей формуле I R4 водород.
4. 6-Оксо-азепиноиндоловые соединения по пп. 1 3, отличающиеся тем, что в общей формуле I R4 водород, низший алкил или замещенный в случае необходимости бензил и R5 водород.
5. 6-Оксо-азепиноиндоловые соединения по пп. 1 4, отличающиеся тем, что в общей формуле I D связь.
6. 6-Оксо-азепиноиндоловые соеднения по пп. 1 5, отличающиеся тем, что в общей формуле I они содержат CH2 D NR4R5-группу в 3-м положении остова кольца.
7. Фармацевтическая композиция, регулирующая моторику желудка, включающая активный ингредиент и фармацевтически приемлемый носитель, отличающаяся тем, что в качестве активного ингредиента она содержит эффективное для содействия моторике желудка количество соединения по п. 1.
8. Фармацевтическая композиция, обладающая эффективным против мигрени серотонин-агонистическим действием, включающая активный ингредент и фармацевтически приемлемый носитель, отличающаяся тем, что в качестве активного ингредиента содержит активное пртив мигрени количество соединения по п. 1.
10. Способ получения соединения формулы Ib
где R1, R3, R4, R5 и n имеют указанные в п. 1 значения;
R2′- водород или низший алкил,
отличающийся тем, что соединение формулы III
где R1,R3,R2′, n имеют указанные значения;
X нуклеофильно отщепляющая группа,
подвергают взаимодействию с соединениями общей формулы IV
где R4 и R5 имеют указанные значения,
и по желанию в полученных соединениях формулы I, где R1, R4 и/или R5 содержат метоксифенильную группу, отщепляют метоксигруппу до гидроксигруппы и в полученных соединениях I, где R1, R4 или R5 представляют замещенную бензильную группу, эту бензильную группу гидрогенолитически отщепляют с получением целевого соединения в свободном виде или в виде их кислотной соли присоединения.
где R1, R3, R4, R5 и n имеют указанные в п. 1 значения;
R2′- водород или низший алкил,
отличающийся тем, что соединение формулы III
где R1,R3,R2′, n имеют указанные значения;
X нуклеофильно отщепляющая группа,
подвергают взаимодействию с соединениями общей формулы IV
где R4 и R5 имеют указанные значения,
и по желанию в полученных соединениях формулы I, где R1, R4 и/или R5 содержат метоксифенильную группу, отщепляют метоксигруппу до гидроксигруппы и в полученных соединениях I, где R1, R4 или R5 представляют замещенную бензильную группу, эту бензильную группу гидрогенолитически отщепляют с получением целевого соединения в свободном виде или в виде их кислотной соли присоединения.
12. Способ получения соединений общей формулы Id
где R1, R2, R3, R5 и n имеют указанные значения;
R4″ имеет значения, указанные для R4, кроме водорода,
отличающийся тем, что соединения общей формулы VI
где R1, R2, R3 и n имеют указанные значения;
R8 водород, C1 C5-алкил, C3 - C6-циклоалкил, C4-циклоалкилалкил, фенилнизшая алкильная группа, моно- или дизамещенная в фенильном кольце низшим алкилом, низшим алкоксилом, гидроксилом или галогеном, или аминозащитная группа,
алкилируют и снова отщепляют аминозащитную группу R8.
где R1, R2, R3, R5 и n имеют указанные значения;
R4″ имеет значения, указанные для R4, кроме водорода,
отличающийся тем, что соединения общей формулы VI
где R1, R2, R3 и n имеют указанные значения;
R8 водород, C1 C5-алкил, C3 - C6-циклоалкил, C4-циклоалкилалкил, фенилнизшая алкильная группа, моно- или дизамещенная в фенильном кольце низшим алкилом, низшим алкоксилом, гидроксилом или галогеном, или аминозащитная группа,
алкилируют и снова отщепляют аминозащитную группу R8.
13. Способ получения соединений формулы Iе
где R1, R3, R4, R5 и n имеют указанные значения;
R2″ низшая алкильная группа, замещенная низшим алкоксилом в α-положении к атому азота,
отличающийся тем, что в соединениях общей формулы VII
где R3, n имеют указанные значения;
R1 имеет значения, указанные для R1, или аминозащитная группа;
R4′ и R5′ имеют значения, указанные для R4 и R5, при этом NR4R5 группа, где R4 и/или R5 водород, настолько защищена по меньшей мере одной легко отщепляемой защитной аминогруппой, что она не реагирует ацилирующими и алкилирующими средствами;
R9 1-гидроксильная группа,
1-гидроксильную группу переводят в остаток R2″ и снова отщепляют аминозащитную группу.
где R1, R3, R4, R5 и n имеют указанные значения;
R2″ низшая алкильная группа, замещенная низшим алкоксилом в α-положении к атому азота,
отличающийся тем, что в соединениях общей формулы VII
где R3, n имеют указанные значения;
R1 имеет значения, указанные для R1, или аминозащитная группа;
R4′ и R5′ имеют значения, указанные для R4 и R5, при этом NR4R5 группа, где R4 и/или R5 водород, настолько защищена по меньшей мере одной легко отщепляемой защитной аминогруппой, что она не реагирует ацилирующими и алкилирующими средствами;
R9 1-гидроксильная группа,
1-гидроксильную группу переводят в остаток R2″ и снова отщепляют аминозащитную группу.
14. Способ получения соединений общей формулы I
где R1, R2, R3, R4″ и n имеют указанные значения;
R5″ имеет значения, указанные для R5, кроме водорода,
отличающийся тем, что в соединении общей формулы Ii
где R1, R2, R3 и n имеют указанные значения,
вводят аминометиловый остаток общей формулы
где R4″ и R5″ имеют указанное значение.
где R1, R2, R3, R4″ и n имеют указанные значения;
R5″ имеет значения, указанные для R5, кроме водорода,
отличающийся тем, что в соединении общей формулы Ii
где R1, R2, R3 и n имеют указанные значения,
вводят аминометиловый остаток общей формулы
где R4″ и R5″ имеют указанное значение.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DEP4125292.6 | 1991-07-31 | ||
| DE4125292A DE4125292A1 (de) | 1991-07-31 | 1991-07-31 | 6-oxo-azepinoindol-verbindungen sowie verfahren und zwischenprodukte zu ihrer herstellung und diese verbindungen enthaltende arzneimittel |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2078765C1 true RU2078765C1 (ru) | 1997-05-10 |
Family
ID=6437366
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| SU925052604A RU2078765C1 (ru) | 1991-07-31 | 1992-07-30 | 6-оксо-азепиноиндоловые соединения и их физиологически переносимые кислотные соли присоединения, фармацевтическая композиция на их основе и способы их получения |
Country Status (21)
| Country | Link |
|---|---|
| US (1) | US5272143A (ru) |
| EP (1) | EP0525584B1 (ru) |
| JP (1) | JP3174158B2 (ru) |
| KR (1) | KR930002353A (ru) |
| CN (2) | CN1069733A (ru) |
| AT (1) | ATE161012T1 (ru) |
| AU (1) | AU649153B2 (ru) |
| CA (1) | CA2075102A1 (ru) |
| CZ (1) | CZ239392A3 (ru) |
| DE (2) | DE4125292A1 (ru) |
| ES (1) | ES2110454T3 (ru) |
| FI (1) | FI923440A7 (ru) |
| HU (2) | HU211105B (ru) |
| IE (1) | IE922310A1 (ru) |
| IL (1) | IL102503A (ru) |
| MX (1) | MX9204457A (ru) |
| NO (1) | NO300375B1 (ru) |
| NZ (1) | NZ243715A (ru) |
| RU (1) | RU2078765C1 (ru) |
| TW (1) | TW207541B (ru) |
| ZA (1) | ZA925093B (ru) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2344138C2 (ru) * | 2004-09-22 | 2009-01-20 | Пфайзер Инк. | Способ получения ингибиторов поли(адф-рибоза)полимераз |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5414130A (en) * | 1993-12-23 | 1995-05-09 | The Dow Chemical Company | Process for the preparation of diaminoresorcinol |
| ES2218110T3 (es) * | 1999-01-11 | 2004-11-16 | Agouron Pharmaceuticals, Inc. | Inhibidores triciclicos de poli(adp-ribosa)polimerasas. |
| ECSP003637A (es) | 1999-08-31 | 2002-03-25 | Agouron Pharma | Inhibidores triciclicos de poli (adp-ribosa) polimerasas |
| CA2581200A1 (en) * | 2004-09-22 | 2006-03-30 | Pfizer Inc. | Therapeutic combinations comprising poly(adp-ribose) polymerases inhibitor |
| JP5465241B2 (ja) | 2008-05-29 | 2014-04-09 | アルバニー モレキュラー リサーチ, インコーポレイテッド | 5−ht3受容体調節物質ならびにその作製方法および使用 |
| EP3597651A1 (en) * | 2010-02-12 | 2020-01-22 | Pfizer Inc | Salts and polymorphs of 8-fluoro-2-{4- [(methylamino)methyl]phenyl}-1 ,3,4,5-tetrahydro-6h-azepino[5,4,3- cd]indol-6-one |
| US10513515B2 (en) | 2017-08-25 | 2019-12-24 | Biotheryx, Inc. | Ether compounds and uses thereof |
| CA3106239A1 (en) | 2018-07-27 | 2020-01-30 | Biotheryx, Inc. | Bifunctional compounds as cdk modulators |
| US11897930B2 (en) | 2020-04-28 | 2024-02-13 | Anwita Biosciences, Inc. | Interleukin-2 polypeptides and fusion proteins thereof, and their pharmaceutical compositions and therapeutic applications |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4910193A (en) * | 1985-12-16 | 1990-03-20 | Sandoz Ltd. | Treatment of gastrointestinal disorders |
-
1991
- 1991-07-31 DE DE4125292A patent/DE4125292A1/de not_active Withdrawn
-
1992
- 1992-07-08 ZA ZA925093A patent/ZA925093B/xx unknown
- 1992-07-15 IL IL10250392A patent/IL102503A/en not_active IP Right Cessation
- 1992-07-15 IE IE231092A patent/IE922310A1/en not_active Application Discontinuation
- 1992-07-21 EP EP92112431A patent/EP0525584B1/de not_active Expired - Lifetime
- 1992-07-21 AT AT92112431T patent/ATE161012T1/de not_active IP Right Cessation
- 1992-07-21 DE DE59209055T patent/DE59209055D1/de not_active Expired - Fee Related
- 1992-07-21 ES ES92112431T patent/ES2110454T3/es not_active Expired - Lifetime
- 1992-07-24 NZ NZ243715A patent/NZ243715A/en unknown
- 1992-07-24 HU HU9202430A patent/HU211105B/hu not_active IP Right Cessation
- 1992-07-30 KR KR1019920013719A patent/KR930002353A/ko not_active Withdrawn
- 1992-07-30 MX MX9204457A patent/MX9204457A/es not_active IP Right Cessation
- 1992-07-30 AU AU20677/92A patent/AU649153B2/en not_active Ceased
- 1992-07-30 FI FI923440A patent/FI923440A7/fi not_active Application Discontinuation
- 1992-07-30 RU SU925052604A patent/RU2078765C1/ru active
- 1992-07-30 JP JP20377092A patent/JP3174158B2/ja not_active Expired - Fee Related
- 1992-07-30 NO NO923004A patent/NO300375B1/no unknown
- 1992-07-30 CN CN92108977A patent/CN1069733A/zh active Pending
- 1992-07-31 CZ CS922393A patent/CZ239392A3/cs unknown
- 1992-07-31 CA CA002075102A patent/CA2075102A1/en not_active Abandoned
- 1992-07-31 US US07/922,527 patent/US5272143A/en not_active Expired - Lifetime
- 1992-09-10 TW TW081107187A patent/TW207541B/zh active
-
1994
- 1994-09-30 HU HU94P/P00032P patent/HU210217A9/hu unknown
-
1996
- 1996-01-19 CN CN96100699A patent/CN1141773A/zh active Pending
Non-Patent Citations (1)
| Title |
|---|
| Патент СССР N 1537139, кл. С 07 D 487/04, 1986. * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2344138C2 (ru) * | 2004-09-22 | 2009-01-20 | Пфайзер Инк. | Способ получения ингибиторов поли(адф-рибоза)полимераз |
Also Published As
| Publication number | Publication date |
|---|---|
| IL102503A (en) | 1995-12-31 |
| FI923440A0 (fi) | 1992-07-30 |
| JP3174158B2 (ja) | 2001-06-11 |
| ATE161012T1 (de) | 1997-12-15 |
| CN1069733A (zh) | 1993-03-10 |
| NO300375B1 (no) | 1997-05-20 |
| HU211105B (en) | 1995-10-30 |
| TW207541B (ru) | 1993-06-11 |
| AU649153B2 (en) | 1994-05-12 |
| NO923004L (no) | 1993-02-01 |
| DE4125292A1 (de) | 1993-02-04 |
| DE59209055D1 (de) | 1998-01-22 |
| ZA925093B (en) | 1993-04-28 |
| CN1141773A (zh) | 1997-02-05 |
| NZ243715A (en) | 1995-03-28 |
| HU210217A9 (en) | 1995-02-28 |
| IL102503A0 (en) | 1993-01-14 |
| EP0525584B1 (de) | 1997-12-10 |
| HU9202430D0 (en) | 1992-10-28 |
| IE922310A1 (en) | 1993-02-10 |
| CA2075102A1 (en) | 1993-02-01 |
| HUT65453A (en) | 1994-06-28 |
| EP0525584A1 (de) | 1993-02-03 |
| JPH05202052A (ja) | 1993-08-10 |
| US5272143A (en) | 1993-12-21 |
| FI923440A7 (fi) | 1993-02-01 |
| ES2110454T3 (es) | 1998-02-16 |
| NO923004D0 (no) | 1992-07-30 |
| MX9204457A (es) | 1993-05-01 |
| CZ239392A3 (en) | 1993-04-14 |
| AU2067792A (en) | 1993-02-04 |
| KR930002353A (ko) | 1993-02-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US5037845A (en) | Indole derivative | |
| US5571833A (en) | Tryptamine analogues, their synthesis and their use as 5-HT1 -like or 5-HT2 receptor agonists | |
| US4816470A (en) | Heterocyclic compounds | |
| GB2162522A (en) | An indole derivative | |
| CZ282061B6 (cs) | Tetrahydrokarbazolové deriváty, způsob jejich výroby a farmaceutické prostředky s jejich obsahem | |
| RU2078765C1 (ru) | 6-оксо-азепиноиндоловые соединения и их физиологически переносимые кислотные соли присоединения, фармацевтическая композиция на их основе и способы их получения | |
| NZ197998A (en) | 5-amino(methyl)-1h-indol-3-ylalkaneamines | |
| PL199351B1 (pl) | Związki pochodne fenylopiperazyny, zawierająca je kompozycja farmaceutyczna i ich zastosowanie | |
| EP1615634B1 (en) | Substituted azabicyclo hexane derivatives as muscarinic receptor antagonists | |
| EP1075471B1 (en) | Indolyl derivatives as serotonergic agents | |
| EP0666847B1 (en) | Tryptamine analogs with 5-ht1d selectivity | |
| WO1995007260A1 (en) | Tetrahydroisoquinolines as alpha-2 antagonists and biogenic amine uptake inhibitors | |
| CA1145747A (en) | N-aminoalkylindol derivatives, their salts and pharmaceutical compositions thereof and process for their preparation | |
| EP0004342A1 (en) | Carbazoles, process for their preparation, pharmaceutical compositions containing them, and intermediates thereto | |
| JPH04308557A (ja) | アルキルアミノアルキルアミン−および−エーテル化合物、その製造方法、およびそれを含有する胃腸管の鎮痙用の医薬 | |
| PL182361B1 (pl) | Pochodne 6-metoksy-1H-benzotriazolo-5-karboksyamidu, sposoby ich wytwarzaniai kompozycje farmaceutyczne zawierajace te pochodne PL PL PL PL PL PL PL PL | |
| JP3222051B2 (ja) | 6−メトキシ−1h−ベンゾトリアゾール−5−カルボキサミド誘導体 | |
| JPH08225571A (ja) | 6−アルコキシ−1h−ベンゾトリアゾール−5−カルボキサミド誘導体及びその中間体並びに該化合物を含有する医薬組成物 |