KR20190105590A - 화학 생산으로부터 염산의 사용을 유연하게 제어하는 방법 - Google Patents
화학 생산으로부터 염산의 사용을 유연하게 제어하는 방법 Download PDFInfo
- Publication number
- KR20190105590A KR20190105590A KR1020197020805A KR20197020805A KR20190105590A KR 20190105590 A KR20190105590 A KR 20190105590A KR 1020197020805 A KR1020197020805 A KR 1020197020805A KR 20197020805 A KR20197020805 A KR 20197020805A KR 20190105590 A KR20190105590 A KR 20190105590A
- Authority
- KR
- South Korea
- Prior art keywords
- hydrochloric acid
- neutralization
- reaction mixture
- stage
- station
- Prior art date
Links
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 title claims abstract description 518
- 238000012824 chemical production Methods 0.000 title claims abstract description 26
- 238000006386 neutralization reaction Methods 0.000 claims abstract description 144
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 claims abstract description 117
- 238000000034 method Methods 0.000 claims abstract description 115
- 230000008569 process Effects 0.000 claims abstract description 90
- 238000005868 electrolysis reaction Methods 0.000 claims abstract description 69
- 239000003513 alkali Substances 0.000 claims abstract description 16
- 239000000243 solution Substances 0.000 claims abstract description 14
- 229910052739 hydrogen Inorganic materials 0.000 claims abstract description 10
- 239000012266 salt solution Substances 0.000 claims abstract description 5
- IXCSERBJSXMMFS-UHFFFAOYSA-N hcl hcl Chemical compound Cl.Cl IXCSERBJSXMMFS-UHFFFAOYSA-N 0.000 claims description 84
- 239000011541 reaction mixture Substances 0.000 claims description 65
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 claims description 46
- 238000006243 chemical reaction Methods 0.000 claims description 38
- 238000004519 manufacturing process Methods 0.000 claims description 35
- 238000002156 mixing Methods 0.000 claims description 34
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 claims description 29
- 239000000460 chlorine Substances 0.000 claims description 29
- 229910052801 chlorine Inorganic materials 0.000 claims description 29
- 239000011780 sodium chloride Substances 0.000 claims description 23
- 238000001816 cooling Methods 0.000 claims description 22
- 150000008044 alkali metal hydroxides Chemical class 0.000 claims description 18
- 239000012948 isocyanate Substances 0.000 claims description 12
- 150000002513 isocyanates Chemical class 0.000 claims description 12
- 238000004064 recycling Methods 0.000 claims description 12
- 230000003472 neutralizing effect Effects 0.000 claims description 11
- 230000003068 static effect Effects 0.000 claims description 11
- 238000010517 secondary reaction Methods 0.000 claims description 10
- 238000012544 monitoring process Methods 0.000 claims description 6
- 239000003795 chemical substances by application Substances 0.000 claims description 5
- SUKJFIGYRHOWBL-UHFFFAOYSA-N sodium hypochlorite Chemical compound [Na+].Cl[O-] SUKJFIGYRHOWBL-UHFFFAOYSA-N 0.000 claims description 5
- 229910019093 NaOCl Inorganic materials 0.000 claims description 4
- 229910001514 alkali metal chloride Inorganic materials 0.000 claims description 4
- 230000014759 maintenance of location Effects 0.000 claims description 4
- YGYAWVDWMABLBF-UHFFFAOYSA-N Phosgene Chemical compound ClC(Cl)=O YGYAWVDWMABLBF-UHFFFAOYSA-N 0.000 claims description 3
- KIQKWYUGPPFMBV-UHFFFAOYSA-N diisocyanatomethane Chemical compound O=C=NCN=C=O KIQKWYUGPPFMBV-UHFFFAOYSA-N 0.000 claims description 3
- 229920000515 polycarbonate Polymers 0.000 claims description 3
- 239000004417 polycarbonate Substances 0.000 claims description 3
- 239000002699 waste material Substances 0.000 claims description 3
- BZHJMEDXRYGGRV-UHFFFAOYSA-N Vinyl chloride Chemical compound ClC=C BZHJMEDXRYGGRV-UHFFFAOYSA-N 0.000 claims description 2
- 238000005660 chlorination reaction Methods 0.000 claims description 2
- 150000002894 organic compounds Chemical class 0.000 claims description 2
- 238000003908 quality control method Methods 0.000 claims description 2
- 238000003756 stirring Methods 0.000 claims description 2
- 125000005628 tolylene group Chemical group 0.000 claims 1
- 238000012545 processing Methods 0.000 abstract description 4
- 239000012670 alkaline solution Substances 0.000 abstract 1
- 235000011167 hydrochloric acid Nutrition 0.000 description 196
- 229910000041 hydrogen chloride Inorganic materials 0.000 description 83
- 238000003860 storage Methods 0.000 description 35
- 238000010521 absorption reaction Methods 0.000 description 26
- 238000000746 purification Methods 0.000 description 23
- 230000003647 oxidation Effects 0.000 description 13
- 238000007254 oxidation reaction Methods 0.000 description 13
- 238000010979 pH adjustment Methods 0.000 description 13
- 239000012071 phase Substances 0.000 description 13
- 239000002253 acid Substances 0.000 description 12
- 239000007789 gas Substances 0.000 description 12
- 239000012535 impurity Substances 0.000 description 12
- DVKJHBMWWAPEIU-UHFFFAOYSA-N toluene 2,4-diisocyanate Chemical compound CC1=CC=C(N=C=O)C=C1N=C=O DVKJHBMWWAPEIU-UHFFFAOYSA-N 0.000 description 12
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 12
- 229910001868 water Inorganic materials 0.000 description 12
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 11
- 238000005259 measurement Methods 0.000 description 10
- 238000001139 pH measurement Methods 0.000 description 9
- 239000000126 substance Substances 0.000 description 9
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 8
- 230000033228 biological regulation Effects 0.000 description 8
- 238000001311 chemical methods and process Methods 0.000 description 8
- 239000012267 brine Substances 0.000 description 7
- 239000000498 cooling water Substances 0.000 description 7
- 238000009434 installation Methods 0.000 description 7
- 239000000047 product Substances 0.000 description 7
- 230000001105 regulatory effect Effects 0.000 description 7
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 7
- 239000002585 base Substances 0.000 description 6
- 239000002826 coolant Substances 0.000 description 6
- 239000001257 hydrogen Substances 0.000 description 6
- 238000007138 Deacon process reaction Methods 0.000 description 5
- 239000006227 byproduct Substances 0.000 description 5
- 238000004821 distillation Methods 0.000 description 5
- 238000000926 separation method Methods 0.000 description 5
- 229910021529 ammonia Inorganic materials 0.000 description 4
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 4
- 238000009529 body temperature measurement Methods 0.000 description 4
- 238000010586 diagram Methods 0.000 description 4
- 230000000694 effects Effects 0.000 description 4
- 238000000265 homogenisation Methods 0.000 description 4
- 150000002431 hydrogen Chemical class 0.000 description 4
- -1 hydronium ions Chemical class 0.000 description 4
- 239000001301 oxygen Substances 0.000 description 4
- 229910052760 oxygen Inorganic materials 0.000 description 4
- 238000004886 process control Methods 0.000 description 4
- 239000002351 wastewater Substances 0.000 description 4
- KZBUYRJDOAKODT-UHFFFAOYSA-N Chlorine Chemical compound ClCl KZBUYRJDOAKODT-UHFFFAOYSA-N 0.000 description 3
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 3
- 239000008346 aqueous phase Substances 0.000 description 3
- 239000007864 aqueous solution Substances 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- 230000003197 catalytic effect Effects 0.000 description 3
- 239000003638 chemical reducing agent Substances 0.000 description 3
- 239000004035 construction material Substances 0.000 description 3
- 230000007423 decrease Effects 0.000 description 3
- 238000013461 design Methods 0.000 description 3
- 238000011049 filling Methods 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 239000007858 starting material Substances 0.000 description 3
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 230000002378 acidificating effect Effects 0.000 description 2
- 230000002411 adverse Effects 0.000 description 2
- 238000013459 approach Methods 0.000 description 2
- 238000009530 blood pressure measurement Methods 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 239000007795 chemical reaction product Substances 0.000 description 2
- 239000001279 citrus aurantifolia swingle expressed oil Substances 0.000 description 2
- 238000010924 continuous production Methods 0.000 description 2
- 230000001276 controlling effect Effects 0.000 description 2
- 238000009826 distribution Methods 0.000 description 2
- 238000007710 freezing Methods 0.000 description 2
- 230000008014 freezing Effects 0.000 description 2
- 238000012423 maintenance Methods 0.000 description 2
- 229910000000 metal hydroxide Inorganic materials 0.000 description 2
- 150000004692 metal hydroxides Chemical class 0.000 description 2
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 description 2
- 238000010327 methods by industry Methods 0.000 description 2
- 239000000203 mixture Substances 0.000 description 2
- 239000012074 organic phase Substances 0.000 description 2
- 230000010355 oscillation Effects 0.000 description 2
- 230000020477 pH reduction Effects 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- 238000011144 upstream manufacturing Methods 0.000 description 2
- 241000283707 Capra Species 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 1
- DWAQJAXMDSEUJJ-UHFFFAOYSA-M Sodium bisulfite Chemical compound [Na+].OS([O-])=O DWAQJAXMDSEUJJ-UHFFFAOYSA-M 0.000 description 1
- 239000005708 Sodium hypochlorite Substances 0.000 description 1
- 239000002250 absorbent Substances 0.000 description 1
- 230000002745 absorbent Effects 0.000 description 1
- 238000010306 acid treatment Methods 0.000 description 1
- 239000003929 acidic solution Substances 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 230000003213 activating effect Effects 0.000 description 1
- 239000003463 adsorbent Substances 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 150000001342 alkaline earth metals Chemical class 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 230000003139 buffering effect Effects 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 239000003054 catalyst Substances 0.000 description 1
- 239000013522 chelant Substances 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 238000012937 correction Methods 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 238000009792 diffusion process Methods 0.000 description 1
- ZZTCPWRAHWXWCH-UHFFFAOYSA-N diphenylmethanediamine Chemical compound C=1C=CC=CC=1C(N)(N)C1=CC=CC=C1 ZZTCPWRAHWXWCH-UHFFFAOYSA-N 0.000 description 1
- 238000011438 discrete method Methods 0.000 description 1
- 238000006073 displacement reaction Methods 0.000 description 1
- 238000010494 dissociation reaction Methods 0.000 description 1
- 230000005593 dissociations Effects 0.000 description 1
- 239000003792 electrolyte Substances 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 238000005530 etching Methods 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 235000013373 food additive Nutrition 0.000 description 1
- 239000002778 food additive Substances 0.000 description 1
- 150000004679 hydroxides Chemical class 0.000 description 1
- 238000011065 in-situ storage Methods 0.000 description 1
- 238000009776 industrial production Methods 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 238000011031 large-scale manufacturing process Methods 0.000 description 1
- 230000007257 malfunction Effects 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 229910021645 metal ion Inorganic materials 0.000 description 1
- 150000007522 mineralic acids Chemical class 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 239000003345 natural gas Substances 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 238000005457 optimization Methods 0.000 description 1
- 239000005416 organic matter Substances 0.000 description 1
- 239000003209 petroleum derivative Substances 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 238000005554 pickling Methods 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- 150000003304 ruthenium compounds Chemical class 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 229910052709 silver Inorganic materials 0.000 description 1
- 239000004332 silver Substances 0.000 description 1
- 229940079827 sodium hydrogen sulfite Drugs 0.000 description 1
- 235000010267 sodium hydrogen sulphite Nutrition 0.000 description 1
- 238000005476 soldering Methods 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 238000004448 titration Methods 0.000 description 1
- 238000005303 weighing Methods 0.000 description 1
- 238000010626 work up procedure Methods 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B7/00—Halogens; Halogen acids
- C01B7/01—Chlorine; Hydrogen chloride
- C01B7/03—Preparation from chlorides
- C01B7/04—Preparation of chlorine from hydrogen chloride
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B7/00—Halogens; Halogen acids
- C01B7/01—Chlorine; Hydrogen chloride
- C01B7/07—Purification ; Separation
- C01B7/0706—Purification ; Separation of hydrogen chloride
-
- C—CHEMISTRY; METALLURGY
- C02—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F1/00—Treatment of water, waste water, or sewage
- C02F1/46—Treatment of water, waste water, or sewage by electrochemical methods
- C02F1/461—Treatment of water, waste water, or sewage by electrochemical methods by electrolysis
-
- C—CHEMISTRY; METALLURGY
- C02—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F1/00—Treatment of water, waste water, or sewage
- C02F1/66—Treatment of water, waste water, or sewage by neutralisation; pH adjustment
-
- C—CHEMISTRY; METALLURGY
- C02—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F2101/00—Nature of the contaminant
- C02F2101/10—Inorganic compounds
- C02F2101/12—Halogens or halogen-containing compounds
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02W—CLIMATE CHANGE MITIGATION TECHNOLOGIES RELATED TO WASTEWATER TREATMENT OR WASTE MANAGEMENT
- Y02W90/00—Enabling technologies or technologies with a potential or indirect contribution to greenhouse gas [GHG] emissions mitigation
-
- Y02W90/20—
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Inorganic Chemistry (AREA)
- Environmental & Geological Engineering (AREA)
- Life Sciences & Earth Sciences (AREA)
- Hydrology & Water Resources (AREA)
- Engineering & Computer Science (AREA)
- Water Supply & Treatment (AREA)
- Electrochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Electrolytic Production Of Non-Metals, Compounds, Apparatuses Therefor (AREA)
Abstract
Description
도 1 염산의 3-단계 중화(G)의 개략도
도 2 제1 중화 단계의 세부사항의 개략도
도 3 제2 중화 단계의 세부사항의 개략도
도 4 제3 중화 단계의 세부사항의 개략도
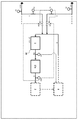
도 5 염산 관리를 위한 전체 공정의 개략도
도 6 염산 관리의 특정한 실시양태의 개략도
도면에서, 참조 부호는 다음의 의미를 갖는다:
1 제1 중화 단계
2 제2 중화 단계
3 제3 중화 단계
4 중화될 염산
4' 제2 및 제3 단계에서 목표 pH를 세팅하기 위한 염산 스트림
5 수산화나트륨
5' 제2 및 제3 단계에서 목표 pH를 세팅하기 위한 수산화나트륨 스트림
6 제1 단계로부터 나온 반응 혼합물
7 제2 중화 단계로부터의 메인 스트림
7' 메인 스트림(7)으로부터의 부분 중화된 염산의 더 작은 2차 회로
7" 제2 중화 단계의 2차 회로로의 수산화나트륨의 도입
7"' 제2 중화 단계의 2차 회로로의 염산의 도입
8 제1 및 제2 중화 단계의 냉각
9 제2 단계의 냉각된 반응 혼합물의 재순환
10 제2 단계로부터 나온 반응 혼합물
11 제3 단계로부터 나온 반응 혼합물
11' 스트림(11)으로부터의 중화된 염산의 더 작은 2차 회로
11" 제3 중화 단계의 2차 회로로의 수산화나트륨의 도입
11"' 제3 중화 단계의 2차 회로로의 염산의 도입
12 제3 중화 단계의 냉각
13 제3 단계의 냉각된 반응 혼합물
14 생성물 스트림의 방출 기준 또는 품질의 모니터링
15 품질 윈도우 내의 중화로부터의 배출된 생성물 스트림
16 품질 윈도우 밖의 재순환된 반응 혼합물
17a 제1 단계의 하류에서의 체류 시간 및 중화 구역
17b 제2 단계의 중화 구역
17c 제3 단계의 중화 구역
18a 제1 단계의 (1차) 반응 혼합물
18b 제2 단계의 (2차) 반응 혼합물
18c 제3 단계의 (3차) 반응 혼합물
20 제1 단계의 정적 혼합기
21 제2 단계의 혼합 노즐
22 제3 단계의 혼합 노즐
F1 제1 중화 단계로의 염산 공급물의 유동 측정
F2 제2 중화 단계로의 염산 공급물의 유동 측정
F3 제3 중화 단계로의 염산 공급물의 유동 측정
F4 제1 중화 단계로의 수산화나트륨 공급물에 대한 유동 측정
F5 제2 중화 단계로의 수산화나트륨 공급물에 대한 유동 측정
F6 제3 중화 단계로의 수산화나트륨 공급물에 대한 유동 측정
K1 제1 중화 단계로의 염산 공급을 위한 조절 장치
K2 제2 중화 단계로의 염산 공급을 위한 조절 장치
K3 제3 중화 단계로의 염산 공급을 위한 조절 장치
K4 제1 중화 단계로의 수산화나트륨 공급을 위한 조절 밸브 쌍
K5 제2 중화 단계로의 수산화나트륨 공급을 위한 조절 밸브 쌍
K6 제3 중화 단계로의 수산화나트륨 공급을 위한 조절 밸브 쌍
P1 염산에 대한 유입 압력 측정
P2 수산화나트륨에 대한 유입 압력 측정
PH1 pH 조절을 위한 제1 중화 단계 후의 pH 측정
PH2 pH 조절을 위한 제2 중화 단계 후의 pH 측정
PH3 pH 조절을 위한 제3 중화 단계 후의 pH 측정
PH4 목표 pH의 모니터링
T1 냉각수 조절을 위한 제1 중화 단계 후의 온도 측정
T2 냉각수 조절을 위한 제3 중화 단계 후의 온도 측정
T3 목표 온도의 모니터링
A 화학 생산 (이소시아네이트 생산)
E 염산 저장 시설
F HCl 전기분해 스테이션
G 중화 스테이션
L 클로르알칼리 전기분해 스테이션
M 처분 스테이션
40, 41 염화수소
42, 43 정제된 염화수소
44, 49 염산, 조질
48 염산, 20 중량%
54, 54a, 54b, 54c 정제된 염산
55 농축 수산화나트륨
56, 56a 염 용액
57, 58 염소
59 수소 가스
60 염산, 정제되지 않음
61 물
Claims (14)
- 연속 화학 생산 공정(A)으로부터 수득된, 적어도 10 중량%의 HCl 농도를 갖고, 특히 적어도 1 ㎥/h의 체적 유량을 갖는 염산(54)의 사용을 유연하게 제어하는 방법으로서, 정제된 염산(54)은 염산 저장소(E)로부터, 임의적으로, 염산에 대한 인취 지점인, 수송 스테이션(H), HCl 전기분해 스테이션(F) 및 클로르알칼리 전기분해 스테이션(L), 또는 중화 스테이션(G)으로 공급되며, 여기서 전술한 인취 지점(H, F, L) 중 하나 이상의 고장 시 또는 인취 지점(H, F, L)에서의 인취 병목현상의 경우에, 염산(54)은 중화 스테이션(G)으로 공급되고 농축 알칼리 금속 수산화물(55), 특히 농축 수산화나트륨으로 중화되고, 형성된 염 용액(56)은 임의적으로 클로르알칼리 전기분해 스테이션(L) 또는 처분 스테이션(M)으로 공급되는 것을 특징으로 하는 방법.
- 제1항에 있어서, 화학 생산 공정(A)이 유기 화합물의 염소화 (예를 들어 염화비닐의 생산), 포스겐 생산 및 포스겐화, 특히 이소시아네이트, 특히 바람직하게는 메틸렌 디이소시아네이트 (MDI), 톨릴렌 디이소시아네이트 (TDI)의 생산을 위한 위한 생산 공정, 또는 폴리카르보네이트 (PC)의 생산 공정, 또는 염소-함유 폐기물의 소각 공정인 것을 특징으로 하는 방법.
- 제1항 또는 제2항에 있어서, 염산(54)이 HCl 전기분해 스테이션(F)에서 염소(57)로 전환되고, 염소가 화학 생산 공정(A)으로 리사이클링되고 거기서 화학적으로 반응하는 것을 특징으로 하는 방법.
- 제1항 내지 제3항 중 어느 한 항에 있어서, 중화 스테이션(G)으로부터 임의적으로 수득된, 알칼리 금속 염화물(56), 특히 염화나트륨, 및 알칼리 금속 염화물 용액을 산성화시키기 위한 염산이 클로르알칼리 전기분해 스테이션(L)에서 염소(57)로 전환되고, 염소가 화학 생산 공정(A)으로 리사이클링되고 거기서 화학적으로 반응하는 것을 특징으로 하는 방법.
- 제1항 내지 제4항 중 어느 한 항에 있어서, 다단계, 특히 삼중 중화 공정이 중화 스테이션(G)에서 사용되는 것을 특징으로 하는 방법.
- 제5항에 있어서, 적어도 10 중량%의 HCl 농도를 갖고 적어도 1 ㎥/h, 바람직하게는 적어도 5 ㎥/h의 체적 유량을 갖는 염산(4, 54)의 다단계, 특히 삼중 연속 중화(G)가 3 내지 9 범위의 목표 pH까지, 하기 단계에 의해 수행되는 것을 특징으로 하는 방법:
A) 제1 단계(1)에서, 중화될 염산(4) 및 95%, 바람직하게는 적어도 99%의 구성비율의 화학량론적으로 필요한 알칼리 금속 수산화물(5)을, 제2 단계(2)로부터 재순환되어 냉각된, 중화된 염산의 체적 유량(9)에 도입하고, 후속적으로 스트림(4, 5, 9)을 혼합하고, 중화 및 체류 구역(17a)에서 1차 반응 혼합물(18a)을 완전히 반응시키는 단계로서, 여기서 제1 단계(1)로부터 유출되는 스트림(6)의 pH는 적어도 1의 pH를 갖고, 제2 단계(2)로부터 재순환되어 냉각된 체적 유량(7)은 제1 단계(1)에 공급된 염산 체적 유량의 적어도 3배에 상응하는 것인 단계,
B) 제1 단계(1)로부터의 체적 유량(6)을 제2 중화 단계(2)의 중화 구역(17b)에 이송하고, 2차 회로(7')에서 알칼리 금속 수산화물(5') 또는 염산(4')의 첨가에 의해 2차 반응 혼합물(18b)의 pH를 바람직하게는 pH 3의 값으로 추가 세팅하고, 여기서 이 2차 회로(7')는 제2 반응 단계(2)의 냉각될 메인 스트림(7)으로부터 취출된 서브스트림에서 비롯되고 중화된 염산의 체적 유량(7) 대 서브스트림(7')의 체적 유량의 비는 적어도 10:1이며, 제2 단계에서의 메인 스트림의 냉각(8) 후에, 반응 A)를 수행하기 위해 제1 중화 단계(1)로 제2 단계(2)의 2차 반응 혼합물(18b)의 보다 더 큰 서브스트림(9)을 재순환시키는 단계,
C) 제2 단계(2)의 2차 반응 혼합물(18b)로부터의 추가 서브스트림(10)을 제3 중화 단계(3)의 중화 구역(17c)에 도입하고, 중화 구역(17c)에 연결된 추가 2차 회로(11')에서 알칼리 금속 수산화물(5') 또는 염산(4')의 첨가에 의해 제3 중화 단계(3)의 3차 반응 혼합물(18c)의 pH를 pH 3 내지 pH 9 범위의 pH로 추가 세팅하고, 여기서 여기서 이 2차 회로(11')는 제3 단계로부터 나온 반응 혼합물(17c)의 메인 스트림(11)의 더 작은 서브스트림으로 이루어지고, 이것은 냉각(12)을 통과한 것이며, 제3 단계로부터 나온 메인 스트림(11)의 더 큰 서브스트림(13)을, 냉각(12) 후에, 온도 및 pH 모니터링을 위해 최종 품질 제어로 전달하고, 3차 반응 혼합물(18c)의 이 냉각된 스트림(13)이 품질 기준을 충족하는 경우, 이 스트림(13)을 생성물 스트림(15)으로서 취출하거나, 또는 그렇지 않으면 추가 pH 조정을 위해 3차 반응 혼합물(18c)을 재순환 스트림(16)으로서 제3 단계(3)에 도입해야 하는 단계. - 제6항에 있어서, 수산화나트륨, 특히 100 ppm 미만의 NaOCl의 함량을 갖는 수산화나트륨을 중화제로서 사용하는 것을 특징으로 하는 방법.
- 제7항에 있어서, 제1 중화 단계(1)에서의 1차 반응 혼합물(18a)의 평균 체류 시간이 20초 내지 3분인 것을 특징으로 하는 방법.
- 제6항 내지 제8항 중 어느 한 항에 있어서, 제2 중화 단계(2)에서의 2차 반응 혼합물(18b)의 평균 체류 시간이 15 내지 100분인 것을 특징으로 하는 방법.
- 제6항 내지 제9항 중 어느 한 항에 있어서, 제3 중화 단계(3)에서의 3차 반응 혼합물(18c)의 평균 체류 시간이 45 내지 250분인 것을 특징으로 하는 방법.
- 제6항 내지 제10항 중 어느 한 항에 있어서, 서로 독립적으로, 제1 단계(1)로부터의 출구에서의 1차 반응 혼합물(18a)의 온도를 45℃ 내지 80℃, 바람직하게는 65℃ 내지 70℃ 범위의 값으로 세팅하고, 제2 반응 단계(2)에서 직접 측정되는, 2차 반응 혼합물(18b)의 온도를 40℃ 내지 75℃, 바람직하게는 60℃ 내지 65℃ 범위의 값으로 세팅하고, 제3 단계의 냉각(12)으로부터의 출구에서의 3차 반응 혼합물(18c)의 온도를 15℃ 내지 55℃, 바람직하게는 25℃ 내지 50℃ 범위의 값으로 세팅하는 것을 특징으로 하는 방법.
- 제6항 내지 제11항 중 어느 한 항에 있어서, 제1 중화 단계(1)에서의 스트림(4, 5, 9)의 혼합을 정적 혼합기에서 수행하며, 여기서 정적 혼합기는 적어도 98%, 바람직하게는 99%의 혼합 품질을 갖는 것을 특징으로 하는 방법.
- 제6항 내지 제12항 중 어느 한 항에 있어서, +/-20%의 범위의 유입 체적 스트림에서의 변동을 보상하기 위한 버퍼 체적을 중화 구역(17b) 및 중화 구역(17c)에 제공하는 것을 특징으로 하는 방법.
- 제6항 내지 제13항 중 어느 한 항에 있어서, 2차 반응 혼합물(18b)과 서브스트림(4', 5', 7')과의 혼합 및 3차 반응 혼합물(18c)과 서브스트림(4', 5', 11')과의 혼합을 중화 구역(17b) 또는 (17c)에서 교반 도구(19)를 사용하거나 또는 서브스트림(7') 또는 (11')을 위한 공급 도관의 중화 구역(17b) 또는 (17c)으로의 진입 영역에 제공된 혼합 노즐(20)을 사용하여 서로 독립적으로 수행하는 것을 특징으로 하는 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP17152417.6A EP3351505A1 (de) | 2017-01-20 | 2017-01-20 | Verfahren zur flexiblen steuerung der verwendung von salzsäure aus chemischer produktion |
| EP17152417.6 | 2017-01-20 | ||
| PCT/EP2018/051088 WO2018134239A1 (de) | 2017-01-20 | 2018-01-17 | Verfahren zur flexiblen steuerung der verwendung von salzsäure aus chemischer produktion |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20190105590A true KR20190105590A (ko) | 2019-09-17 |
Family
ID=58017897
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020197020805A KR20190105590A (ko) | 2017-01-20 | 2018-01-17 | 화학 생산으로부터 염산의 사용을 유연하게 제어하는 방법 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US11040878B2 (ko) |
| EP (2) | EP3351505A1 (ko) |
| JP (1) | JP2020506859A (ko) |
| KR (1) | KR20190105590A (ko) |
| CN (1) | CN110198914A (ko) |
| WO (1) | WO2018134239A1 (ko) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN109399567B (zh) * | 2018-12-28 | 2021-08-13 | 甘肃金川恒信高分子科技有限公司 | 一种自动补偿氯化氢发生器 |
| BR102020009844A2 (pt) * | 2020-05-15 | 2021-11-23 | Petróleo Brasileiro S.A. - Petrobras | Método e aparato para avaliação da evolução de cloreto de hidrogênio em função da temperatura |
Family Cites Families (28)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AT234639B (de) * | 1961-10-14 | 1964-07-10 | Siegener Ag Eisenkonstruktion | Verfahren zur Gewinnung von gasförmigem Chlor und gasförmigem Wasserstoff |
| JPS5311238B2 (ko) * | 1972-09-14 | 1978-04-20 | ||
| US4247532A (en) * | 1979-08-13 | 1981-01-27 | Shell Oil Company | Purification of electrolytically-produced chlorine |
| DE3714439A1 (de) | 1987-04-30 | 1988-11-10 | Bayer Ag | Verfahren zur herstellung von (cyclo)aliphatischen diisocyanaten |
| EP0371201A1 (de) * | 1988-12-01 | 1990-06-06 | Ruhrkohle Aktiengesellschaft | Verfahren zur Hydrierung von Organochlorverbindungen und Neutralisation des anfallenden Chlorwasserstoffs sowie Neutralisationsmittel für aus Organochlorverbindungen anfallenden Clorwasserstoff |
| FI85007C (fi) * | 1990-10-24 | 1992-02-25 | Nokia Ab Chemicals Oy | Foerfarande foer framstaellning av saltsyra. |
| US5616234A (en) * | 1995-10-31 | 1997-04-01 | Pepcon Systems, Inc. | Method for producing chlorine or hypochlorite product |
| IT1282367B1 (it) * | 1996-01-19 | 1998-03-20 | De Nora Spa | Migliorato metodo per l'elettrolisi di soluzioni acquose di acido cloridrico |
| JPH1081986A (ja) * | 1996-09-03 | 1998-03-31 | Permelec Electrode Ltd | 水平型複極式電解槽 |
| US6719957B2 (en) | 2002-04-17 | 2004-04-13 | Bayer Corporation | Process for purification of anhydrous hydrogen chloride gas |
| US20040152929A1 (en) * | 2002-05-08 | 2004-08-05 | Clarke William D | Process for vinyl chloride manufacture from ethane and ethylene with air feed and alternative hcl processing methods |
| DE102005032663A1 (de) | 2005-07-13 | 2007-01-18 | Bayer Materialscience Ag | Verfahren zur Herstellung von Isocyanaten |
| DE102006023581A1 (de) * | 2006-05-19 | 2007-11-22 | Bayer Materialscience Ag | Verfahren zur Abtrennung von Chlor aus dem Produktgas eines HCI-Oxidationsprozesses |
| DE102006024516A1 (de) * | 2006-05-23 | 2007-11-29 | Bayer Materialscience Ag | Verfahren zur Herstellung von Chlor aus Chlorwasserstoff und Sauerstoff |
| CN101583591B (zh) | 2007-01-08 | 2014-01-08 | 巴斯夫欧洲公司 | 制备二苯甲烷二胺的方法 |
| CA2682402C (en) * | 2007-04-12 | 2015-07-14 | Cefco, Llc | Process and apparatus for carbon capture and elimination of multi-pollutants in flue gas from hydrocarbon fuel sources and recovery of multiple by-products |
| TWI478875B (zh) * | 2008-01-31 | 2015-04-01 | Solvay | 使水性組成物中之有機物質降解之方法 |
| WO2009105566A2 (en) * | 2008-02-19 | 2009-08-27 | Global Research Technologies, Llc | Extraction and sequestration of carbon dioxide |
| DE102008012037A1 (de) * | 2008-03-01 | 2009-09-03 | Bayer Materialscience Ag | Verfahren zur Herstellung von Methylen-diphenyl-diisocyanaten |
| DE102008015901A1 (de) * | 2008-03-27 | 2009-10-01 | Bayer Technology Services Gmbh | Elektrolysezelle zur Chlorwasserstoffelektrolyse |
| JP5484689B2 (ja) * | 2008-04-25 | 2014-05-07 | 三菱重工業株式会社 | 排ガス処理システム及び排ガス中の水銀除去方法 |
| JP5391577B2 (ja) * | 2008-05-14 | 2014-01-15 | Jfeスチール株式会社 | 廃塩酸液から塩酸を回収する塩酸回収装置および塩酸回収方法 |
| US20110091366A1 (en) * | 2008-12-24 | 2011-04-21 | Treavor Kendall | Neutralization of acid and production of carbonate-containing compositions |
| SG174714A1 (en) | 2010-03-30 | 2011-10-28 | Bayer Materialscience Ag | Process for preparing diaryl carbonates and polycarbonates |
| CN102602892B (zh) * | 2012-04-11 | 2015-04-01 | 万华化学集团股份有限公司 | 通过氯化氢的催化氧化制备氯气的方法 |
| WO2014039929A1 (en) * | 2012-09-07 | 2014-03-13 | Clean Chemistry, Llc | Systems and methods for generation of reactive oxygen species and applications thereof |
| CN104512865B (zh) * | 2013-09-26 | 2016-08-17 | 宝山钢铁股份有限公司 | 除硅中和反应的中和药剂氨水添加量的控制方法 |
| US10934627B2 (en) * | 2016-05-06 | 2021-03-02 | Malvi Technologies, Llc | Methods and systems for making hypochlorite solution from reverse osmosis brine |
-
2017
- 2017-01-20 EP EP17152417.6A patent/EP3351505A1/de not_active Withdrawn
-
2018
- 2018-01-17 US US16/479,083 patent/US11040878B2/en active Active
- 2018-01-17 WO PCT/EP2018/051088 patent/WO2018134239A1/de unknown
- 2018-01-17 JP JP2019538621A patent/JP2020506859A/ja active Pending
- 2018-01-17 KR KR1020197020805A patent/KR20190105590A/ko not_active Application Discontinuation
- 2018-01-17 CN CN201880007462.2A patent/CN110198914A/zh active Pending
- 2018-01-17 EP EP18700374.4A patent/EP3571157A1/de not_active Ceased
Also Published As
| Publication number | Publication date |
|---|---|
| US11040878B2 (en) | 2021-06-22 |
| EP3571157A1 (de) | 2019-11-27 |
| CN110198914A (zh) | 2019-09-03 |
| JP2020506859A (ja) | 2020-03-05 |
| WO2018134239A1 (de) | 2018-07-26 |
| EP3351505A1 (de) | 2018-07-25 |
| US20190375635A1 (en) | 2019-12-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US7604720B2 (en) | Process for the on-site production of chlorine and high strength sodium hypochlorite | |
| KR20190105590A (ko) | 화학 생산으로부터 염산의 사용을 유연하게 제어하는 방법 | |
| CN106414321A (zh) | 用于光气的安全生产的方法 | |
| EP2468387A1 (en) | Gas treatment apparatus, particularly for polyisocyanate production system. | |
| RU2292298C2 (ru) | Способ управления процессом получения диоксида хлора | |
| US4105751A (en) | Process and installation for the manufacture of chlorine dioxide | |
| US10125087B2 (en) | Method for preparation of n-butyl nitrite | |
| KR102478404B1 (ko) | 염산의 연속 중화를 위한 방법 및 장치 | |
| Shemer et al. | Re-mineralization of desalinated water using a mixture of CO2 and H2SO4 | |
| CN106007099A (zh) | 一种含铜刻蚀废液处理及回收工艺 | |
| RU2366651C1 (ru) | Способ управления производством капролактама | |
| US20190194018A1 (en) | A method and a system for separating and treating impurities from a hydrogen chloride liquid mixture | |
| US20050260108A1 (en) | On-site generation, purification, and distribution of ultra-pure anhydrous ammonia | |
| CN101588857A (zh) | 碳酰氯的中和处理方法 | |
| US2965443A (en) | Process for production of calcium hypochlorite bleach liquor | |
| CN215163197U (zh) | 一种将冷凝酸回用于二次盐水氯酸盐分解槽的系统 | |
| JP2579533B2 (ja) | 水硫化ソーダの製造方法 | |
| CN112912366B (zh) | 用于生产肟的改良方法 | |
| SU1361154A1 (ru) | Способ регулировани процесса очистки растворител от примесей в производстве синтетического каучука | |
| RU2296741C1 (ru) | Способ управления процессами получения циклогексанола или циклогексанона | |
| JP4601644B2 (ja) | 晶析反応装置及び晶析反応方法 | |
| JP2765122B2 (ja) | 水素製造用メタノール水溶液及びその使用法 | |
| Bagheri et al. | Plantwide Control Structure of the Diethyl Oxalate Process Concerning: Safety and Process Improvement | |
| JP2015203573A (ja) | 放射性廃液の処理装置 | |
| TWM329055U (en) | Fluidized-bed reactor processing method for fluorine-containing wastewater treatment |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
Patent event date: 20190717 Patent event code: PA01051R01D Comment text: International Patent Application |
|
| PG1501 | Laying open of application | ||
| A201 | Request for examination | ||
| PA0201 | Request for examination |
Patent event code: PA02012R01D Patent event date: 20210115 Comment text: Request for Examination of Application |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
Comment text: Notification of reason for refusal Patent event date: 20220725 Patent event code: PE09021S01D |
|
| E601 | Decision to refuse application | ||
| PE0601 | Decision on rejection of patent |
Patent event date: 20230104 Comment text: Decision to Refuse Application Patent event code: PE06012S01D Patent event date: 20220725 Comment text: Notification of reason for refusal Patent event code: PE06011S01I |