KR20170140182A - 공간적 범위를 갖는 생물학적 샘플의 움직임에 대한 광학적 검출 방법 및 장치 - Google Patents
공간적 범위를 갖는 생물학적 샘플의 움직임에 대한 광학적 검출 방법 및 장치 Download PDFInfo
- Publication number
- KR20170140182A KR20170140182A KR1020177027379A KR20177027379A KR20170140182A KR 20170140182 A KR20170140182 A KR 20170140182A KR 1020177027379 A KR1020177027379 A KR 1020177027379A KR 20177027379 A KR20177027379 A KR 20177027379A KR 20170140182 A KR20170140182 A KR 20170140182A
- Authority
- KR
- South Korea
- Prior art keywords
- sample
- detector
- light source
- light
- radiation
- Prior art date
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/17—Systems in which incident light is modified in accordance with the properties of the material investigated
- G01N21/21—Polarisation-affecting properties
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/17—Systems in which incident light is modified in accordance with the properties of the material investigated
- G01N21/47—Scattering, i.e. diffuse reflection
- G01N21/4788—Diffraction
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/17—Systems in which incident light is modified in accordance with the properties of the material investigated
- G01N21/47—Scattering, i.e. diffuse reflection
- G01N21/49—Scattering, i.e. diffuse reflection within a body or fluid
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01P—MEASURING LINEAR OR ANGULAR SPEED, ACCELERATION, DECELERATION, OR SHOCK; INDICATING PRESENCE, ABSENCE, OR DIRECTION, OF MOVEMENT
- G01P13/00—Indicating or recording presence, absence, or direction, of movement
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/17—Systems in which incident light is modified in accordance with the properties of the material investigated
- G01N21/47—Scattering, i.e. diffuse reflection
- G01N21/4788—Diffraction
- G01N2021/479—Speckle
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/17—Systems in which incident light is modified in accordance with the properties of the material investigated
- G01N21/47—Scattering, i.e. diffuse reflection
- G01N2021/4792—Polarisation of scatter light
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/15—Medicinal preparations ; Physical properties thereof, e.g. dissolubility
Landscapes
- Health & Medical Sciences (AREA)
- General Physics & Mathematics (AREA)
- Physics & Mathematics (AREA)
- Life Sciences & Earth Sciences (AREA)
- Immunology (AREA)
- Chemical & Material Sciences (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Analytical Chemistry (AREA)
- Pathology (AREA)
- Engineering & Computer Science (AREA)
- Molecular Biology (AREA)
- Biomedical Technology (AREA)
- Hematology (AREA)
- Urology & Nephrology (AREA)
- Medicinal Chemistry (AREA)
- Food Science & Technology (AREA)
- Cell Biology (AREA)
- Microbiology (AREA)
- Biotechnology (AREA)
- Tropical Medicine & Parasitology (AREA)
- Investigating Or Analysing Materials By Optical Means (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biophysics (AREA)
- Pharmacology & Pharmacy (AREA)
- Length Measuring Devices By Optical Means (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Abstract
본 발명은 3 차원 세포 및/또는 조직 배양물 또는 세포 클러스터 또는 자유롭게 수영하는 것으로 제조된 샘플의 형태로 공간 범위를 갖는 생물학적 샘플에서의 움직임의 광학적인 시험관내 검출 방법 및 장치에 관한 것이다. 상기 방법은 a) 샘플(1), 광원(6), 광학기구(7, 8; 3, 3a, 3b, 4, 5a, 5b) 및 검출기(2)를 위한 리셉터클을 제공하는 단계로서, a1) 상기 광학기구(7, 8)는 상기 광원으로부터 나오는 방사선으로 상기 리셉터클 내의 전체 샘플(1)을 조명하고 상기 광원(6)으로부터 상기 방사선의 적어도 일부를 유도하도록 구성되고, 샘플(1)과의 상호 작용을 통해 샘플(1) 내의 임의의 지점에서 검출기(2)의 검출 표면(2a)으로 방사 방향, 편광 상태 및/또는 회절 패턴이 변경되며, a2) 상기 검출기(2)는 검출된 방사선에 따라 측정 신호(9)를 생성하도록 구성되는 것으로, 상기 검출된 방사선의 강도의 시간 프로파일을 특정하고 그리고/또는 검출된 방사선(11)의 강도의 시간 프로파일이 도출될 수 있고; b) 상기 광원로부터의 방사선으로 상기 샘플(1)을 조명하는 단계; 및 c) 측정 신호(9)의 시간 변화에 따라 생물학적 샘플(1)에서의 움직임을 검출하는 단계를 포함한다.
Description
본 발명은 공간적 범위를 갖는 생물학적 샘플의 움직임에 대한 광학적인 시험관내 검출을 위한 방법 및 장치에 관한 것이다.
발달 생물학, 독성 시험 및 제약 연구와 같은 분야에서 폐쇄 및 3 차원 세포 및 조직 배양의 능동 역학을 모니터링 하기 위한 요구 사항이 존재한다는 것이 실제 사례로부터 알려져 있다.
근육 조직으로 분화된 배아 줄기 세포에서 추출한 조직 샘플은 예를 들어 시험할 물질의 유해성을 확인하기 위해 독성 시험의 일부로 사용된다. 여기서 근육 조직에 적용되는 물질이 근육 조직의 근육 수축에 영향을 미치는지 여부가 조사된다. 근육 조직의 수축은 물질의 독성을 나타내는 지표가 될 수 있다. 세포 클러스터(cell cluster)의 형태와 같은 3 차원 생물학적 샘플에서 움직임, 예를 들어 수축을 검출하기 위한 측정 방법이 필요하다. 이러한 세포 클러스터의 일반적인 직경은 100 ~ 400㎛이며, 밀리미터 범위 내의 직경도 가능하다.
이 연구는 주로 시각적인 관찰을 통해 주로 수행되며 비디오 현미경과 후속 이미지 분석을 사용하는 경우는 드물다. 첫 번째는 시간 소모적이며 항상 주관적인 평가와 관련이 있다. 후자는 복잡한 이미징 광학 및 상당한 연구 노력으로 연결된 복잡한 이미지 분석이 요구된다는 단점이 있다. 작은 변위에 대한 그들의 고유한 민감성은 또 다른 단점이다.
임피던스 측정과 같은 비 광학적인 방법은 오직 샘플과 접촉하여 작동한다. 샘플 형태가 레벨(부착성 단분자층)에서 벗어나거나 심지어 입체적이며 또한 매체에서 자유롭게 헤엄치는 경우, 위에서 언급한 기술을 적용할 수 없다.
자동 이미징 방법은, 예를 들어, 10㎛의 초점 깊이 및 100 내지 400㎛의 셀 클러스터의 상기 언급된 전형적인 크기에 대해 샘플의 10 내지 40 이미지 레벨이 측정되어야 한다는 단점을 갖는다. 일반적인 최소 측정 기간은 약 1년이다. 움직임을 감지할 수 있는 데 10초, 및 재위치 지정 또는 초점 맞추기에 필요한 추가 시간이 필요하므로 이러한 방법은 여러 샘플을 신속하게 모니터링 하는데 적합하지 않다.
생물학적 역동성의 시간 척도로 인해 모니터링 기간이 길기 때문에 많은 수의 샘플을 연속적으로 측정하지 않는다. 그러나 실제로, 예를 들어 96 또는 384와 같은 마이크로-역가 플레이트(micro-titre plate)로도 알려진, 멀티-웰 플레이트(multi-well plate)에 저장되어 있는, 서로 분리된 다수의 샘플에 대해 이러한 움직임 검출을 수행할 필요가 있다. 이미징 방법은 기하학적인 이유로 멀티-웰 플레이트의 모든 캐비티(cavity)에서 이미징 광학 장치의 배열을 실현하는 것이 어렵고 건축 공간이 부족하기 때문에 다수의 샘플을 병렬로 측정하는 데 적합하지 않다.
따라서, 본 발명의 목적은 종래 기술의 단점을 피할 수 있는 공간적 범위를 갖는 생물학적 샘플에서의 움직임을 검출하기 위한 개선된 방법을 제공하는 것이다.
본 발명은 특히 복잡한 이미지 분석을 필요로 하지 않는 강건하고 비접촉식의 움직임 검출 방법을 제공하는 것을 목적으로 한다.
본 발명의 또 다른 목적은 스크리닝 환경에서 다수의 샘플의 병행 분석에 적합한 방법을 제공하는 것이다.
또 다른 목적은 종래의 장치의 단점을 피할 수 있는 공간적 범위를 갖는 생물학적 샘플 내의 움직임을 검출하기 위한 장치를 제공하는 것으로 구성된다.
이러한 목적은 독립 청구항의 특징을 가진 장치 및 방법으로 해결된다.
본 발명의 유리한 실시예 및 응용예는 종속 청구항에 기인하며, 도면을 부분적으로 참조하여 이하의 상세한 설명에서 보다 구체적으로 설명된다.
본 발명은 광학적 방법이 비접촉 모니터링에 가장 적합하고 샘플 내의 가능한 움직임의 정확한 위치가 미리 알려지지 않았기 때문에 전체 샘플을 조명하는 것이 필수적이라는 기술적 통찰력에 기초한다. 샘플은 통상적으로 상당한 깊이, 즉 이미징 광학기구의 초점 깊이보다 크므로 샘플과의 상호 작용은 전체 길이를 따라 샘플을 통해 누적적으로 측정되어야 한다. 따라서 전송 방식은 특히 빛의 비-상호작용형 부분이 여기에서 측정되고 예상되는 변동에 높은 배경 노이즈 및 간섭이 수반되므로 이 기법을 민감하게 만들지 않으므로 이 전송 방법이 적합하지 않다. 따라서, 본 발명에 따른 접근법은 조명된 샘플의 산란된 방사선, 편광 방사선 및/또는 회절 방사선의 검출에 기초하며, 샘플 움직임에 의해 야기된 변동은 그것의 방사 방향, 그것의 편광 상태 및/또는 그것의 회절 패턴에서 샘플과의 상호 작용에 의해 변화되는 광의 부분에서 검출된다. 적절한 필터를 통해 산란된, 편광 및/또는 회절 방사선으로부터 투과광을 분리하는 것이 여기서 바람직하다. 용어 "광(light)"은 또한 본 발명의 일부로서 "방사선"이라는 용어 대신에 사용되기도 ㅎ한. 이들 두 용어는 본 발명의 일부로서 동등한 것으로 간주될 수 있고 가시 광선, IR 및 UV 범위 내의 전자기 방사선을 포함한다.
따라서, 본 발명의 일반적인 태양에 따라, 공간적 범위를 갖는 생물학적 샘플에서의 움직임의 광학적인 시험관내 검출 방법을 제공한다.
본 발명에 따른 방법은 샘플용 리셉터클, 광원, 광학기구 및 검출기를 제공하는 단계를 포함한다. 상기 광학기구는 여기에서 광원로부터 방사되는 방사선으로 상기 용기 내의 전체 샘플을 조명하고 샘플과의 상호 작용을 통해 샘플 내부의 임의의 지점에서 변화되는 광원의 방사선의 적어도 일부를 안내하도록 구성된다 그 편광 방향 및/또는 그 회절 패턴을 검출기의 검출기 표면 상에 투영함으로써, 상기 광원로부터 상기 샘플로 방출되는 방사선의 상호 작용이 상기 샘플을 통한 전체 경로를 따라 누적적으로 측정되도록 한다. 검출기는 검출된 방사선에 따라 측정 신호를 생성하도록 구성되며, 그 시간 프로파일은 검출된 방사선의 강도의 시간 프로파일을 나타내고, 그리고/또는 검출된 방사선의 강도의 시간 프로파일이 유도될 수 있다.
본 발명에 따른 방법은 측정 신호의 시간 변화에 따라 광원로부터의 방사선으로 샘플을 조명하고 생물학적 샘플에서 움직임을 검출하는 단계를 더 포함한다.
본 발명에 따른 접근법의 하나의 특별한 이점은 샘플 역학(sample dynamics)이 그 방법의 측정된 값으로부터 직접적으로 도출될 수 있으며, 방사선의 방향으로 변화된 광의 부분에서 샘플 움직임에 의해 야기되는 변동으로서, 샘플과의 상호 작용을 통한 편광 상태 및/또는 회절 패턴은 측정 신호의 변동으로서 직접 가시적이라는 것이다. 따라서 이미징 방법에서 요구되는 복잡한 측정 데이터 처리가 생략 될 수 있다.
이 방법은 예를 들어, 측정 신호의 변화가 미리 결정된 임계 값을 초과하면 샘플 내의 움직임을 검출하도록 설계될 수 있다. 측정 신호의 시간 변화가 주기성을 가지면 근육 조직의 모순을 검사할 때 움직임을 더 감지할 수 있다.
이 방법은 비교적 간단한 광학 요소들을 사용하여 수행될 수 있다. 개별 이미지 레벨에 초점을 맞추고 샘플 볼륨을 연속적으로 스캔하기 위한 광학기구는 필요하지 않다. 따라서, 본 방법을 수행하기 위한 장치는 비용면에서 효율적으로 실현될 수 있고 콤팩트한 구조로 구현될 수 있다.
측정 신호의 단순한 평가 및 컴팩트한 구조 덕분에 이 방법은 다수의 샘플을 동시에 모니터링 하는 데 적합하며 선별적인 환경이나 자동화된 고 처리 공정, 예를 들어 고 처리 스크리닝 공정에 프로세스-효율 방식으로 통합될 수 있다.
특히 바람직한 실시예에 따르면, 검출기는 단일 채널 검출기로서 제공되거나 검출기는 단일-채널 측정 신호를 발생시킨다. 측정 신호는 바람직하게는 시간 단위당 검출기 표면에 충돌하는 방사선 강도만을 표시한다. 따라서 샘플의 움직임은 신호의 시간적 변화 또는 변동에 의해 직접 검출될 수 있다.
검출기는 바람직하게는 비- 촬상 검출기 또는 공간적으로 분해되지 않은 측정 신호를 갖는 검출기, 예를 들어 포토다이오드와 같은 비-공간적으로 분해되는 광 검출기이다. 이러한 검출기는 콤팩트하고 비용면에서 효율적이다.
공간적 범위를 갖는 생물학적 샘플은 3 차원 생물학적 샘플, 예를 들어 3 차원 세포 및/또는 조직 배양물 또는 세포 클러스터(cell cluster)의 형태로 이해된다.
생물학적 샘플의 직경은 모든 공간 방향에서 적어도 하나의 공간 방향에서 적어도 50 마이크로미터(㎛), 보다 바람직하게는 적어도 50 마이크로미터 일 수 있으며, 모든 공간 방향에서 종종 100 ㎛ 이상이다.
샘플의 직경은 바람직하게는 100 ㎛ 내지 5 ㎜의 범위 내에 있고, 보다 바람직하게는 100 ㎛ 내지 1 ㎜의 범위 내에 있다. 생물학적 샘플은 특히 근육 조직 및/또는 살아 있는 세포의 샘플, 즉 활성 동역학을 갖는 세포, 즉 운동을 유발할 수 있는 세포일 수 있다.
생물학적 샘플에서의 움직임의 검출은 특히 샘플 내의 움직임 또는 생물학적 샘플의 샘플 성분의 움직임으로 이해되어야 한다. 다시 말해, 공간적 범위를 지닌 생물학적 샘플 내 또는 내부의 동적 현상이 일반적으로 감지 가능해야 한다. 근육 세포의 세포 배양과 함께 이러한 움직임은 예를 들어 개별적인 근육 세포의 수축에 의해 촉발될 수 있다.
그러나 생물학적 샘플은 또한 자유로이 수영하는 미생물 샘플, 예를 들어 정자일 수 있다. 이 경우 자유로이 수영하는 미생물의 움직임을 검출하는 방법은 예를 들어 정자의 경우 정자 운동성을 결정하는 데 사용될 수 있다.
상기 광학 요소는 조명 측에 배치된 조명 광학기구를 포함할 수 있으며, 상기 광원은 상기 샘플을 완전히 그리고 가능한 한 고르게 조명하기 위해 상기 샘플 전체를 지향한다.
또한, 광학 요소는 샘플로부터 나오는 광, 방사선 방향, 편광 상태 및/또는 회절 패턴이 샘플과의 상호 작용에 의해 변화되어 검출기의 검출면으로 지향되는 검출 광학기구를 포함할 수 있다.
광학기구의 이러한 기능적 특성은 이후의 실시예를 참조하여 이후에 설명되는 바와 같이, 예를 들어 필터, 렌즈, 조리개(어퍼쳐), 굴절 소자 등과 같은 하나 이상의 적절하게 배열되고 설계된 공지된 광학 구성 요소를 사용하여 실현될 수 있다.
하나의 유리한 실시 변형예는 여기에서, 광학기구가 구성되고 그리고/또는 검출기가 조명 빔 경로 및 샘플에 대해 샘플을 통해 투과된 광원의 어떠한 투과 방사선도 검출기에 도달하지 않는 방식으로 그리고/또는 검출기 및/또는 광원으로부터의 광이 샘플을 바이패싱하는 동안 검출기에 도달하지 않는 방식으로 배치되는 것으로 가정한다.
이 실시예에 따르면, 샘플과의 상호 작용을 통해 방사선 방향, 편광 상태 및/또는 회절 패턴이 변경된 광원으로부터의 광 만이 검출기에 도달하는 반면, 광학기구는 투과 방사선 또는 샘플을 우회하는 방사선이 검출기의 검출 표면에 도달하는 것을 방지한다. 이러한 방식으로 간섭하는 배경 신호들이 감소되고 측정의 민감도가 증가하게 된다.
바람직한 실시예에 따르면, 샘플 내의 움직임은 회절 패턴의 변화에 의해 인식된다. 이 실시예에 따르면, 광원은 간섭성 광을 생성한다. 또한, 광학기구는 예를 들어 공간형 필터에 의해, 샘플에 의해 회절된 광원로부터의 광에 의해 생성된 회절 패턴의 에지 영역을 검출기 상에 맵핑하도록 구성된다. 샘플 내의 움직임은 회절 패턴, 예를 들어 스페클 패턴(speckle pattern)의 변화를 생성한다. 본 발명의 일부로서 수행된 조사는 회절 패턴의 변화가 방사선 강도의 상대적 변화가 작기 때문에 그 중심에서 측정하기가 어렵다는 것을 보여 주었다. 에지 영역에서, 변화는 신뢰성 있게 인식될 수 있고, 예를 들어, 회절 패턴에서 국소 회절 최대값으로부터 국부 회절 최소값으로 또는 그 반대로 일시적으로 변화할 수 있다. 회절 패턴을 사용하면 패턴의 각 점은 전체 샘플의 회절 정보를 포함한다.
이 실시예의 유리한 변형예에서, 광학기구는 샘플에 의해 생성된 회절 패턴의 에지 영역에 핀홀 조리개(어퍼쳐)(pinhole aperture)의 핀홀이 배치되는 방식으로 샘플과 검출기 사이에 배치되는 핀홀 조리개(어퍼쳐)를 포함한다.
핀홀 조리개(어퍼쳐)는 홀 모양의 조리개(어퍼쳐), 바람직하게는 작은 조리개(어퍼쳐) 모양의 개구, 바람직하게는 렌즈가 없는 것으로 이해된다. 핀홀 조리개(어퍼쳐)는 국부적으로 구분된 광의 수집에 사용된다. 광섬유의 전방면은 특히 공동초점 현미경에서 동일한 목적으로 오랫동안 사용되어 왔다.
투과광이 수신되지 않는 모든 관측 각은 바람직하게는 회절 패턴의 에지 영역으로 간주되어야 한다. 회절 패턴은 물체(여기서는 샘플)에서 회절된 광파의 양과 음의 간섭에 의해 발생한다. 간섭이 양 또는 음인지 여부에 따라 물체의 크기, 빛의 파장 및 관찰 각도에 따라 다르다. 상호작용 없이 샘플을 통과하는 빛, 즉 투과 광, 탄도 광자는 0°의 관측각을 가지며 회절 패턴의 중간에 도달한다. 회절 패턴은 투과 광과 S/B (S/B : 신호 대 배경, 신호 배경) 비 및 S/N (S/N : 신호 대 잡음) 비가 대폭 떨어진다는 것을 보여준다. 따라서, 투과 광이 수신되지 않는 모든 관측각은 바람직하게는 회절 패턴의 에지 영역을 나타내는 것으로 고려되어야 한다. 전체 샘플이 여기에 조사되고 조명이 조준되지 않으면 전송된 방사선의 "수신 영역"은 단 하나의 지점보다 크다.
이 실시예의 다른 변형예에 따르면, 핀홀 조리개(어퍼쳐)는 핀홀 조리개(어퍼쳐)가 회절 패턴의 에지 영역에 위치하도록 회절 패턴에 대해 배치된 수 개의 핀홀을 가질 수 있다. 이를 위해, 핀홀은 핀홀을 통해 검출기에 영향을 주는 회절 방사선의 오버레이(overlaying)가 회절 효과를 악화시키기보다는 증가하는 방식으로 배열되어야 한다.
회절 패턴의 변화에 의해 샘플 내의 움직임을 검출하는 본 실시예의 또 다른 변형예에 따르면, 광학기구는 광원과 샘플 사이에 조리개(어퍼쳐)를 포함할 수 있으며, 상기 조리개(어퍼쳐)는 방사선 조리개(어퍼쳐)의 개구를 통해 나오는 광원으로부터의 방사선이 핀홀 조리개(어퍼쳐)의 핀홀에 직접적으로 영향을 주지 않고, 즉 샘플을 바이패스한다. 광학은 굴절 광학 요소, 즉, 굴절에 의해 편향된 방사선이 굴절되도록 구성되는, 예를 들어 볼록 렌즈 또는 프리즘과 같은 방사선을 굴절시키는 요소를 더 포함할 수 있다. 이 요소는 핀홀 조리개(어퍼쳐)의 핀홀에 직접적으로 영향을 미치지 않는다. 이러한 변형예는 회절된 방사선 만을 핀홀 조리개(어퍼쳐)의 핀홀로 조정 및 유도하기 용이하게 하는 광학의 비용 효과적인 예를 나타낸다.
또 다른 바람직한 실시예에 따르면, 샘플에 있어서의 움직임은 움직임에 의해 야기된 편광의 변동에 의해 검출된다. 이 실시예에 따르면, 광학기구는 상이한 편광 방향을 갖는 제 1 편광 필터 및 제 2 편광 필터를 포함하며, 제 1 편광 필터는 광원와 샘플 사이에 배치되고, 제 2 편광 필터는 샘플과 검출기 사이에 배치된다. 샘플에서의 움직임은 샘플과 편광된 빛 사이의 변화된 상호작용 및 편광 상태의 변화를 유도하여, 검출기 신호의 변동을 유도한다.
검출기 및 제 2 편광 필터는 광원에 대해 샘플의 반대측, 샘플의 측면 또는 여기에서 광원와 동일한 측면 상에 배치될 수 있다.
또 다른 바람직한 실시예에 따르면, 샘플에서의 움직임은 샘플에 의해 산란 된 광의 변동에 의해 검출되며, 이는 움직임에 의해 야기된다. 검출기는 여기에서 샘플에 의해 산란된 광의 표면 검출을 위한 광원와 같이 샘플(1)의 동일한 측면 상에 배치될 수 있다. 대안적으로, 검출기는 샘플의 측면으로 산란된 방사선의 검출을 위해 조명 빔 경로의 방향 및/또는 샘플의 측면에 대해 경사각(tilt angle)으로 배치될 수 있다.
이러한 변형예는 투과 방사가 검출기에 충돌하는 것을 방지하는 조리개(어퍼쳐)들과 같은 광학 구성 요소가 필요 없다는 이점을 제공한다.
검출기는 샘플에 의해 산란된 광의 투과광 검출을 위해 샘플에 투과된 광 방향으로 추가로 배열될 수 있다. 이 변형예에 따르면, 광학기구는 샘플을 통해 투과되는 빔으로서 검출기에 충돌할 수 있는 조명 빔 경로 내의 광선을 차단하도록 구성된 광원과 샘플 사이에 배치된 조리개(어퍼쳐)를 포함한다. 선택적으로 또는 부가적으로, 광학기구는 샘플을 통해 투과된 광선이 검출기에 충돌하지 않도록 조명 광선 경로의 방향을 변화시키도록 구성된, 광원과 샘플 사이에 배치된 굴절 광학 요소를 포함할 수 있다.
또한 광학기구가 검출기 앞에 배치된 대역 통과 필터(bandpass filter)를 가지고 있고, 이 대역 필터는 실내 조명 억제용으로 설계된 경우 이점이 있다. 이러한 방식으로 검출 감도가 더 증가될 수 있다.
또 다른 바람직한 변형예에 따르면, 광학기구, 특히 조명 광학 요소는 엑시콘(axicon)을 포함한다. 엑시콘의 사용은 기존의 렌즈에 비해 공간적으로 더 깊은 샘플의 균일한 조명 효과를 제공한다. 그 이유는 엑시콘의 초점은 한 지점이 아닌 광축을 따라 연장되기 때문이다. 엑시콘의 또 다른 장점은 입사광(영향을 받지 않는 빛)을 광축에 일정한 각도로 회절시키므로 쉽게 필터링할 수 있다는 점이다.
본 발명에 따른 한 가지 실현가능성은 샘플이 캐리어 매트릭스 상에 위치될 수 있다. 따라서 샘플의 리셉터클은 캐리어 매트릭스, 바람직하게는 바이오폴리머를 포함할 수 있다. 샘플은 현적형 드롭(hanging drop)에 위치할 수도 있다. 따라서 샘플의 리셉터클은 현적형 드롭(hanging drop)을 포함할 수 있다. 샘플의 리셉터클은 또한 현적형 드롭 내에 위치하는 캐리어 매트릭스로서 설계될 수 있으며, 캐리어 매트릭스는 바람직하게는 예를 들어 알긴산과 같은 바이오폴리머이다.
샘플의 리셉터클은 스크리닝 환경에서 상기 방법을 사용하기 위한 멀티-웰 플레이트(multi-well plate)(micro-titre plate))의 캐비티 일 수 있다. 리셉터클 또한 개별 캐비티에 현적형 드롭을 형성하도록 설계된 멀티-웰 플레이트의 캐비티가 될 수 있다. 이러한 현적형 드롭 멀티 웰 플레이트는 예를 들어, Insphero AG, CH-8952 Schlieren에 의해 "GravityPLUSTM 3d Culture and Assay Platform"이라는 이름으로 제공된다. 특허문헌 EP 2342317 B1 또한 그러한 플레이트를 개시한다.
이미 상기 방법은 자동화된 고 처리량 방법의 일부로서 검사될 샘플, 예컨대 다수의 샘플의 병렬 모니터링에 특히 적합하다는 것이 이미 언급되었다.
따라서, 본 방법의 또 다른 유리한 개선점은 움직임의 병행 광학 검출이 서로 분리된 몇몇 생물학적 샘플에서 동일하게 수행된다는 것이 고려된다. 생물학적 샘플용 리셉터클은 바람직하게는 여기에 멀티-웰 플레이트이고, 샘플을 수용하기 위해 행과 열로 배열된 다수의 캐비티를 갖는다. 검출기는 검출기 어레이로서, 바람직하게는 포토다이오드 어레이로서 설계되며, 개별 검출기의 그리드 거리는 멀티 웰 플레이트의 캐비티의 그리드 거리와 동일하다.
광원은 개개의 캐비티를 조명하도록 구성된다. 유리한 변형예에 따르면, 캐비티 내의 샘플을 조명하기 위한 광원은 레이저 다이오드 어레이로서 구성되며, 개별 레이저 다이오드의 그리드 거리는 멀티 웰 플레이트의 캐비티의 그리드 거리와 동일하다. 레이저 다이오드 어레이는 공간 절약 및 에너지 효율적인 조명 소스를 나타낸다.
양호한 방열을 가능하게 하기 위해, 레이저 다이오드 어레이의 브라킷은 열전도성 재료, 바람직하게는 알루미늄으로 제조될 수 있다. 이 변형예에 따른 광학 기는 또한 렌즈 어레이의 각각의 렌즈가 레이저 다이오드 중 하나에 할당되고 렌즈가 레이저 다이오드의 광을 캐비티로 안내하는 렌즈 어레이, 예를 들어 마이크로 렌즈 어레이를 포함할 수 있다.
광원은 레이저 다이오드 어레이 대신에 광원로서 종래의 광원(레이저, 아크 램프 등)으로 설계될 수 있으며, 여기서 광원의 광은 샘플을 광섬유 번들에 의해 조명하기 위한 샘플을 내포하는 개별 캐비티에 결합된다. 각 광섬유는 여기서 캐비티에 할당된다. 이것은 샘플 근처에서 과도한 열 발산을 피하기 위해 샘플로부터 충분한 거리에서 광원을 작동시킬 수 있다는 이점을 제공하는 것이다.
또 다른 변형예에 따르면, 단순한 실현 변형예을 나타내는 것으로, 광원이 대응 성능 용량을 가져야 하므로, 에너지 효율의 단점을 갖는 광원을 갖는 멀티-웰 플레이트를 표면에 조명하는 가능성이 존재한다. 빛이 편리하게 설계된 응축기 광학기구를 통해 안내되고 여기에 병행하게 되고 캐비티에서 목표로 하는 각도 의존적인 통과 필터가 있을 경우 이점이 있다.
본 발명의 또 다른 태양에 따르면, 공간적 범위를 갖는 생물학적 샘플에서 움직임의 비접촉식 시험관내 검출을 위한 장치가 제공된다. 상기 장치는 생물학적 샘플용 리셉터클, 광원, 검출기 및 광학기구를 포함하며, 이들은 상기 광원으로부터 나오는 방사선으로 상기 리셉터클 내의 전체 샘플을 조명하고 상기 광선의 방사선의 적어도 일부를 안내하도록 구성되고, 샘플과의 상호 작용을 통해 샘플 내의 임의의 지점에서 그 방사 방향, 편광 상태 및/또는 회절 패턴이 검출기의 검출기 표면 상으로 변화되는 광원을 포함한다. 검출기는 검출된 방사선의 강도의 시간 프로파일을 나타내고 그리고/또는 검출된 방사선의 강도의 시간 프로파일이 유도될 수 있는 측정 신호를 검출된 방사선에 따라 생성하도록 구성된다.
상기 장치는 또한 검출된 방사선의 시간 변화를 디스플레이 및/또는 평가함으로써 생물학적 샘플 내의 움직임을 검출하도록 구비된 평가 유닛을 가질 수 있다.
순수하게 방법의 일부로서 공개된 특징들은 또한 반복을 피하기 위해 장치에 대해 공개되고 청구된 것으로 간주되어야 한다. 본 발명의 상기 언급된 양태 및 특징은, 특히 광학기구, 검출기, 리셉터클, 예를 들어 멀티-웰 플레이트, 현적형 드롭 또는 현적형 멀티-웰 플레이트, 및 광원도 따라서 장치에도 역시 적용된다.
전술한 바람직한 실시예 및 본 발명의 특징은 임의의 방식으로 서로 결합될 수 있다. 본 발명의 추가의 세부 사항 및 이점은 첨부된 도면을 참조하여 후술될 것이다. 동일한 부분들은 도면들에서 동일한 참조 번호들로 식별되고 별도로 설명되지 않을 것이다.
본 발명에 따른 검출 방법은 비교적 간단한 광학 요소들을 사용하여 수행될 수 있고, 개별 이미지 레벨에 초점을 맞추고 샘플 볼륨을 연속적으로 스캔하기 위한 광학기구는 필요하지 않으며, 따라서, 본 방법을 수행하기 위한 장치는 비용면에서 효율적으로 실현될 수 있고 콤팩트한 구조로 구현될 수 있다.
측정 신호의 단순한 평가 및 컴팩트한 구조 덕분에 본 발명에 따른 검출 방법은 다수의 샘플을 동시에 모니터링 하는 데 적합하며 선별적인 환경이나 자동화된 고 처리 공정, 예를 들어 고 처리 스크리닝 공정에 프로세스-효율 방식으로 통합될 수 있다.
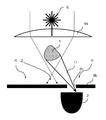
도 1은 본 발명의 일 실시예에 따른 방법 및 장치의 개략도,
도 2a-2e는 움직임 검출을 위해 샘플에 의해 산란된 광을 사용하는 본 발명의 실시예,
도 3a-3c는 움직임 검출을 위해 편광된 광을 사용하는 본 발명의 실시예,
도 4a-4c는 움직임 검출을 위한 샘플의 회절 패턴을 이용하는 본 발명의 실시예,
도 5a는 캐리어 매트릭스 상의 심장 근육 조직 모델 형태의 샘플,
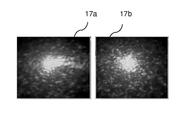
도 5b는 두 개의 연속적인 시점에서의 스펙클 패턴의 예시도, 및
도 5c는 측정 신호의 시간 프로파일 예.
도 2a-2e는 움직임 검출을 위해 샘플에 의해 산란된 광을 사용하는 본 발명의 실시예,
도 3a-3c는 움직임 검출을 위해 편광된 광을 사용하는 본 발명의 실시예,
도 4a-4c는 움직임 검출을 위한 샘플의 회절 패턴을 이용하는 본 발명의 실시예,
도 5a는 캐리어 매트릭스 상의 심장 근육 조직 모델 형태의 샘플,
도 5b는 두 개의 연속적인 시점에서의 스펙클 패턴의 예시도, 및
도 5c는 측정 신호의 시간 프로파일 예.
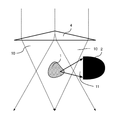
도 1은 본 발명의 일 실시예에 따른 방법 및 장치에 대한 개략도이다.
공간적 범위를 갖는 생물학적 샘플(1)에서의 움직임의 광학적인 시험관내 검출을 위한 검출장치(100)가 상기 방법을 수행하기 위해 제공된다.
검출장치(100)는 3 차원 샘플(1) 용의 리셉터클(도시되지 않음), 광원(6), 광학 요소(7, 8) 및 검출기(2)를 포함한다.
리셉터클은 특정 유형의 리셉터클에 국한되지 않고, 예를 들어 캐리어, 캐리어 플레이트, 용기로서, 멀티 웰 플레이트의 캐비티로서 또는 샘플의 적용 및 유형에 따라 편리하게 설계될 수 있다. 샘플이 성장되는 생체 고분자의 형태, 예를 들어 알긴산 염 형태의 캐리어 매트릭스로서 존재할 수 있다.
광원(6)은 간섭성(coherent) 광원, 예를 들면 레이저 일 수 있지만, 반드시 그러할 필요는 없다. 움직임 검출을 위해 샘플의 회절 패턴을 사용하는 실시예(도 4a 내지 도 4c, 도 5a 내지 도 5c를 비교)는 간섭형 방사선을 필요로 한다.
도 1의 광학 요소(7, 8)의 설명은 단지 개략적인 것으로서, 특정한 광학 요소 변형예가 다수 가능하므로 특정 광학 요소를 설명하기보다는 광학 요소의 기능적 특성을 설명하기 위한 것이다. 이하의 도면에서는 예시로서 도시되어 있다.
광학 요소의 이러한 기능 특성은 하나 이상의 적절하게 배열되고 설계된 공지된 광학 구성 요소, 예를 들어 필터, 렌즈, 개구, 굴절 소자 등과 같은 구성 요소를 사용하여 실현될 수 있다.
광학 요소(7, 8)는 조사 측에 배치된 조명 광학 요소(7)를 포함하며, 상기 광학 요소를 사용하여 샘플을 완전히 균일하게 가능한 한 조명하기 위해 광선 광원(6)의 방사선(10)이 전체 샘플(1) 상에 안내된다. 조명 광학 요소는 이에 대한 방사선을 형성하기 위한 개구, 렌즈 및/또는 필터와 같은 적절한 광학 요소 또는 구성 요소를 포함할 수 있다. 액시콘(axicon)의 사용은 특히 유리하다.
광학 요소(7, 8)는 검출 광학 요소(8)를 더 포함하며, 상기 검출 광학 요소(8)에 의해 샘플로부터 방출되는 광(11), 즉 방사 방향, 편광 상태 및/또는 샘플(1)과의 상호 작용에 의한 회절 패턴으로 변경된 광원(6)으로부터의 광은 검출기(2)의 검출 표면(2a) 상으로 유도된다. 도 1에서, 산란 이벤트는 예를 들어 포인트 (P1)에서 도시되고, 여기서 광(11)은 검출기(2)의 방향으로 산란되고 그리고 검출 광학 요소(8)에 의해 검출기(2)에 맵핑된다. 전체 샘플(1)이 균일하게 조명됨에 따라, 샘플(1) 내의 임의의 지점에서 입사광(10)이 상호 작용이 발생할 수 있으므로 샘플과 광과의 상호 작용이 검출기 (2)에 의해 누적된 방식으로 샘플을 통과하는 전체 경로를 가로질러 측정된다.
검출 광학 요소(8)는 또한 샘플과의 상호 작용을 통해 방사선 방향, 편광 상태 및/또는 회절 패턴이 변경되지 않은 광이 검출기(2)에 도달하지 않도록 하는 광학 요소를 더 포함할 수 있다. 검출 광학 요소(8)는 예를 들어, 실내 광을 걸러내거나 억제하지만 광원(6)의 파장을 갖는 광을 통과시키는 검출기 입구 앞에 배치된 대역 통과 필터를 포함할 수 있다. 이것은 단색광 광원이 사용되거나 상응하는 필터가 특정 광 파장 만을 갖는 샘플을 조명하기 위해 광원의 출구에 배열된다는 것으로 가정한다.
검출 광학 요소(8)는 또한 조리개(어퍼쳐)(aperture), 렌즈 등에 의해 광선 경로를 차단할 수 있으며, 샘플(1)에 의해 투과된 광원(6)로부터의 방사선을 검출기에 도달시키고 그리고/또는 광원(6)으로부터의 광을 샘플을 우회하는 동안 검출기(2)에 도달시킨다.
부가적으로 또는 대안적으로, 검출기는 예를 들어 도 1에 도시된 바와 같이 조명 빔 경로(10)에 대해 측면 상에 검출기(2)를 배치함으로써 투과광(12)이 그 검출기 표면(2a)에 도달하지 않도록 배열될 수 있다.
검출기(2)는 검출된 방사선(11)에 따라 측정 신호(9)를 생성하도록 구성되며, 이것의 시간 프로파일은 검출된 방사선(11)의 강도의 시간 프로파일을 특정한다.
따라서 검출기 신호(9)는 샘플의 체적 측정(전체 체적 측정)과 동일하다. 검출기(2)는 단일 채널 검출기인 것이 바람직하며, 따라서 시간 단위당 검출기에 의해 기록된 광 강도의 변동과 동일한 단 하나의 측정 파라미터(9)만이 생성된다. 검출기(2)는 예를 들어 종래의 포토다이오드(2)이다.
샘플(1)은 도 1에 도시된 검출 장치(100)로 조명되고 대응하는 측정 신호(9)가 평가된다.
움직임이 현재 샘플(1)에서 발생하는 경우, 예를 들어 배양된 근육 조직의 경우 수축인 경우 샘플에 도달하는 빛과 샘플(1)의 상호 작용 또한 움직임에 의해 변경된다. 즉 샘플(1)과의 상호 작용을 통해 방사선 방향, 그것의 편광 상태 및/또는 회절 패턴으로 변화된 샘플 상에 낙하하는 빛(11)의 비율은 변화하여 검출기 신호(9)에 변화를 발생시킬 수 있다. 상기 방법에 따르면, 생물학적 샘플에서의 움직임은 따라서 검출기 신호(9)의 변동에 의해 검출될 수 있다.
이하, 도 1에 도시된 솔루션 접근법의 특정 설계를 나타내는 본 발명의 실시예의 일부 예를 설명할 것이다. 광원(6)는 도 2a 내지 도 3c에는 도시되어 있지 않지만, 빔 경로(10)로부터 명확한 도시된 광학 및 검출기 구성 위에 위치된다.
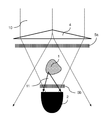
도 2a 내지 도 2e는 움직임 검출을 위해 샘플에 의해 산란된 광을 사용하는 본 발명의 실시예를 나타낸다. 도 2a 내지 도 2b에서, 검출기(2)는 샘플(2)의 산란광(11)의 투과광 검출을 위해 샘플(1)에 투과된 광 방향으로 배열된다. 샘플(2)을 통해 투과된 빔이 검출기(2)에 도달하는 것을 막기 위해 샘플(2)을 통해 투과된 빔 또는 샘플의 측면을 통과하여 검출기(2)에 도달할 수 있는 빔으로서 검출기(2)에 도달할 광 빔을 차단하는 조리개(어퍼쳐)(3)가 도 2a에 배열된다. 따라서, 조리개(어퍼쳐)(3) 형태의 조명 광학 요소는 검출기(12)에 도달하지 않을 샘플을 통해 투과된 방사선(12)만을 허용한다.
도 2b에 도시된 실시예의 특수성은 조명의 방향을 변화시키는 굴절 광학 요소, 예를 들어 렌즈, 액시콘 등에 의해 추종되는 큰 조리개(어퍼쳐)(3)의 대신에 작은 조리개(어퍼쳐)(3)가 사용되며, 이는 샘플(2)을 통해 투과된 광(12)이 검출기(2)에 도달할 수 없도록 조리개(어퍼쳐)(3)를 통해 입사되는 빔 경로(10)의 방향으로 변화한다는 것이다.
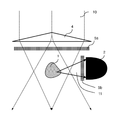
도 2c에 도시된 실시예의 특수성은 샘플(1)로부터의 반사 형태의 산란광의 표면 검출을 위한 광원(6)와 동일한 샘플(1)의 측면 상에 검출기(2)가 배치되고, 검출기 표면(2a)은 차례로 샘플(2)에 대면한다. 이는 투과광을 차단하기 위한 조리개(어퍼쳐)이 필요 없다는 이점을 제공한다. 그럼에도 불구하고, 검출기(2)를 에워싸는 조리개(어퍼쳐)가 여기에서 구상되고, 간섭 광 영향의 영향을 감소시킬 수 있다.
도 2d 및 도 2e에 도시된 실시예 변형의 특징은 산란된 광(11)이 측면에서 검출된다는 것이다. 이를 위해, 검출기(2)는 조명 방향 측에 배치된다. 도 2d에서, 굴절 광학 요소, 예를 들어 렌즈 또는 프리즘(4)은 광선 경로와 샘플(1) 사이에 배치되어, 광선 경로의 방향을 변화시켜 조명 광선 경로(10)의 광선이 도달하지 못하도록 한다. 즉 샘플(1)을 우회하는 동안 검출기(2)에 직접 연결된다.
도 2e에 도시된 실시예는 굴절 광학 요소(4) 대신에 조리개(어퍼쳐)(3a)가 사용되는데, 굴절 광학 요소(4)는 빔 경로(10)를 좁히기 위한 개구를 가지므로, 조명 빔 경로(10)의 광이 샘플(1)을 우회하는 동안 다시 검출기(2)에 직접 도달하지 않게끔 한다.
도 3a 내지 도 3c는 움직임 검출을 위해 편광된 광을 사용하는 본 발명의 실시예를 나타낸다. 이를 위해, 조명 광학 요소는 광원와 샘플 (1) 사이에 배치된 제 1 편광 필터 (5a)를 포함한다. 검출 광학 요소는 제 1 편광 필터(5a)와 비교하여 상이한 편광 방향을 갖는 제 2 편광 필터(5b)를 포함하여 샘플(1)과 검출기(2), 바람직하게는 검출기 입구에 위치한다.
검출기(2) 및 제 2 편광 필터(5b)는 광원 소스에 대해 샘플(1)의 반대측, 샘플(1)의 측면 또는 광원과 동일한 측면 상에 배치될 수 있으며, 도 3a 내지 도 3c에서 다른 변형예를 도시한다.
2 개의 편광 필터(5a 및 5b)의 상이한 편광 방향으로 인해, 편광 필터(5b)는 샘플 통과와의 상호 작용을 통해 "편광없는" 광 만을 허용한다. 따라서, 2 개의 편광 필터(5a 및 5b)의 배열은 샘플을 통해 투과된 광 또는 샘플을 바이패스한 광이 검출되지 않도록 보장한다.
샘플에서의 움직임은 무 편광 광의 비율을 변화시키고 검출기 신호의 변동을 야기하므로, 샘플(1)에서의 움직임은 검출기 신호의 변동으로부터 직접 검출될 수 있다.
샘플상의 조명 빔 경로(10)를 포커싱하는 굴절 광학 요소(4), 예를 들어 볼록 렌즈 또는 프리즘은 산란 광 효과를 감소시키기 위해 제 1 편광 필터(5a) 앞에 배열될 수 있다(도 3a 및 도 3c).
도 3b의 실시예에서, 검출기(2)는 샘플(1)로부터의 반사의 형태로 산란된 광의 표면 검출을 위해 광원(6)과 같은 샘플(1)의 측면 상에 배치된다. 검출기(2)를 둘러싸는 조리개(어퍼쳐)(3)는 여기서 예상되는 간섭성 광 영향의 영향을 줄일 수 있다.
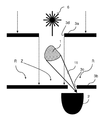
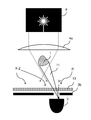
도 4a 내지 도 4c는 움직임 검출을 위해, 예를 들어 스펙클 패턴의 형태로 샘플의 회절 패턴을 사용하는 본 발명의 실시예를 나타낸다. 광원(6)은 예를 들어 레이저 다이오드와 같은 간섭성 광원이다. 샘플에서 회절된 광원(6)의 광은 강도가 높은 중심(Z) 및 낮은 강도의 에지 영역(R)을 갖는 회절 패턴을 생성한다.
검출 광학기구는 핀홀 조리개(어퍼쳐)(3b)의 핀홀(3c)이 샘플에 의해 생성된 회절 패턴의 에지 영역(R)에 배치되도록 샘플(1)과 검출기(2) 사이에 배치된 검출기(2)의 전방에 배치된 핀홀 조리개(어퍼쳐)(3b)를 포함한다.
도 4a의 변형예에 따르면, 조명 광학기구는 광원과 샘플 사이에 배치된 조리개(어퍼쳐)(3a)를 포함하며, 조리개(어퍼쳐)(3a)의 조리개(어퍼쳐) 개구(3d)를 통해 방출하는 상기 광원(6)로부터의 방사선은 핀홀 조리개(어퍼쳐)(3b)의 핀홀(3c)에 직접적으로 도달하지 않는 형식으로 형성된다.
도 4b 및 도 4c의 변형예에 따르면, 조명 광학기구는 광원(6)과 샘플(1) 사이에, 예를 들어 오목 렌즈와 같은 굴절 광학 요소(4a)를 포함하며, 굴절 광학 요소(4a)는 핀홀 조리개(어퍼쳐)(3b)의 핀홀(3c)에 직접 도달하지 않고, 즉 샘플을 바이패스한다.
도 4c의 변형예에서, 대역 통과 필터(13)는 또한 샘플(1)과 광원(6)의 파장과 동일하지 않은 실내 광을 걸러내는 핀홀 조리개(어퍼쳐)(3b) 사이에 배치된다. 심장 박동은 현재 도 4c에 도시된 구성으로 육안 관찰(현미경으로 관찰)에 필적하는 감도로 검출될 수 있다.
도 5c는 세포 클러스터(cell cluster) 형태의 샘플(1)의 예를 도시한다. 세포 클러스터는 현적형 드롭에 위치하며, 그 일부만이 도 5a에서 볼 수 있으며, 현적형 드롭 다중 역가 플레이트의 캐비티 내에 형성된다. 샘플은 줄기 세포로부터 분화된 심장 근육 조직 모델로 구성되며, 알긴산 염 형태로 캐리어 비드(15)에 부착한다. 도 5a에 도시된 샘플은 약 1 밀리미터의 직경을 갖는다.
샘플(1)은 레이저 다이오드로 650nm 파장의 광으로 완전히 조명된다. 서로 다른 크기의 스케일로 구성된 샘플(1)은 다양한 방식으로 간섭성 광을 회절시키고 투과광 방향으로 복잡한 회절 패턴(소위 "스펙클 패턴")을 생성한다. 국소 심장 근육 수축으로 인한 조직 내에서의 이러한 구조의 작은 변형은 전체 스펙클 패턴의 변화로 이어진다.
도 5b는 수축의 최소 및 최대 편향에서의 스펙클 패턴의 2 개의 상이한 조건을 나타내는 예로서의 이미지(17a 및 17b)를 도시한다. 이미지(17a 및 17b)는 설명을 위해서만 사용되며, 다른 실험에서 기인한 것으로,도 5a의 샘플(1)의 스펙클 패턴을 나타내지 않는다. 그러나 측정 원리는 동일하다. 회절 패턴(17a, 17b)의 에지 영역(R)의 점은 공간 필터, 예를 들어 핀홀 조리개(어퍼쳐)(3b)에 의해 검출기(2) 상에 도시된다. 패턴(17a, 17b)의 변화는 이제 핀홀 조리개(어퍼쳐)(3b)에 의해 통과하는 변동 광량으로 이어지고, 따라서 도 5c에 도시된 변동하는 검출기 신호(9)로 이어진다. 신호(9)의 주기적인 변동은 근육 조직의 주기적인 수축과 동일하다. 도 5c의 예시는 설명을 위한 것일 뿐이며,도 1a에 도시된 샘플의 조명 동안 측정된 측정 신호도 나타내지 않는다.
본 발명이 특정 실시예를 참조하여 설명되었지만, 본 발명의 범위를 벗어나지 않고 다른 변경이 수행될 수 있고 등가물이 대체물로서 사용될 수 있음은 당업자에게 명백하다. 또한 많은 수정이 관련 범위를 벗어나지 않고 수행될 수 있다. 결론적으로, 본 발명은 개시된 실시예에 한정되지 않고, 첨부된 특허청구범위에 속하는 모든 실시예를 포함해야 한다. 본 발명은 특히, 청구된 청구범위에 관계없이, 대상에 대한 보호 및 종속 관계의 특성을 모두 청구한다.
Claims (19)
- 3 차원 세포 및/또는 조직 배양물 또는 세포 클러스터 또는 자유롭게 수영하는 미생물 샘플의 형태로 공간적 범위를 갖는 생물학적 샘플(1)에서의 움직임에 대한 광학적인 시험관내 검출 방법으로서,
a) 샘플(1), 광원(6), 광학기구(7, 8; 3, 3a, 3b, 4, 5a, 5b) 및 검출기(2)를 위한 리셉터클을 제공하는 단계로서,
a1) 상기 광학기구(7, 8)는 상기 광원으로부터 나오는 방사선으로 상기 리셉터클 내의 전체 샘플(1)을 조명하고 상기 광원(6)으로부터 상기 방사선의 적어도 일부를 유도하도록 구성되고, 샘플(1)과의 상호 작용을 통해 샘플(1) 내의 임의의 지점에서 검출기(2)의 검출 표면(2a)으로 방사 방향, 편광 상태 및/또는 회절 패턴이 변경되며,
a2) 상기 검출기(2)는 검출된 방사선에 따라 측정 신호(9)를 생성하도록 구성되는 것으로, 상기 검출된 방사선의 강도의 시간 프로파일을 특정하고 그리고/또는 검출된 방사선(11)의 강도의 시간 프로파일이 도출될 수 있고;
b) 상기 광원으로부터의 방사선으로 상기 샘플(1)을 조명하는 단계; 및
c) 측정 신호(9)의 시간 변화에 따라 생물학적 샘플(1)에서의 움직임을 검출하는 단계를 포함하는 것을 특징으로 하는 검출 방법.
- 제 1 항에 있어서,
상기 샘플의 직경은
a) 적어도 하나의 공간 방향에서 적어도 50 마이크로미터(㎛), 또는
b) 100 ㎛에서 1 mm의 범위 내에 있는 것을 특징으로 하는 검출 방법.
- 제 1 항 또는 제 2 항에 있어서,
상기 샘플은
a) 생체 세포, 예를 들어 근육 세포, 및/또는
b) 움직임을 유발할 수 있는 세포를 포함하는 것을 특징으로 하는 검출 방법. - 전술한 항들 중 어느 한 항에 있어서,
a) 상기 검출기(2)는 단일-채널 측정 신호(9)를 방출하고; 그리고/또는
b) 상기 검출기(2)는 포토다이오드이고; 그리고/또는
c) 상기 검출기(2)는 비-이미징 검출기 또는 비 공간적으로 분해된 측정 신호를 갖는 검출기 인 것을 특징으로 하는 검출 방법.
- 전술한 항들 중 어느 한 항에 있어서,
a) 상기 광학기구(7, 8)는 샘플(1)을 통해 투과된 광원(6)의 상기 방사선(12)이 상기 검출기에 도달하는 위치에 그리고/또는 샘플을 우회하는 동안 상기 광원로부터의 광이 상기 검출기에 도달하는 위치에 어떠한 빔 경로도 존재하지 않게끔 구성되는 방도로 상기 조명 빔 경로(10) 및 상기 샘플(2)에 대해 배치되고; 그리고/또는
b) 상기 샘플(1)이 완전히 조명되는 것을 특징으로 하는 검출 방법.
- 전술한 항들 중 어느 한 항에 있어서,
상기 샘플(1)에서의 움직임이 상기 측정 신호(9)의 변화가 미리 결정된 임계 값을 초과하는 경우 및/또는 상기 측정 신호(9)의 시간적 변화가 측정 신호(9)는 주기성을 갖는 경우에 검출되는 것을 특징으로 하는 검출 방법.
- 전술한 항들 중 어느 한 항에 있어서,
a) 상기 광원(6)은 간섭성 광선을 생성하고, 그리고
b) 상기 광학기구(7, 8)는 상기 샘플에 의해 회절된 상기 광원으로부터의 광에 의해 생성된 회절 패턴의 에지 영역을 상기 검출기 상에 맵핑하도록 구성되는 것을 특징으로 하는 검출 방법.
- 제 7 항에 있어서,
상기 광학기구는 상기 샘플(1)과 상기 검출기(2) 사이에 배치된 핀홀 조리개(어퍼쳐)(3b)를 포함하여 상기 핀홀 조리개(어퍼쳐)(3b)의 핀 홀(3c)이 샘플에 의해 생성된 회절 패턴의 에지 영역 (R)에 배치되도록 한 것을 특징으로 하는 검출 방법.
- 제 8 항에 있어서,
상기 광학기구는,
a) 조리개(어퍼쳐) 개구(3d)를 통해 존재하는 상기 광원(6)으로부터의 방사선이 핀홀 조리개(어퍼쳐)(3b)의 핀홀 (3c)을 직접 도달하지 않는 방도로 상기 광원과 상기 샘플 사이에 배치된 조리개(어퍼쳐)(3a), 및/또는
b) 회절된 방사선이 핀홀 조리개(어퍼쳐)(3b)의 핀홀(3c)에 도달하지 않는 방도로 광원(6)과 샘플(1) 사이에 배치된 굴절 광학 요소(4a)를 포함하는 것을 특징으로 하는 검출 방법.
- 전술한 항들 중 어느 한 항에 있어서,
상기 광학기구는 상이한 편광 방향을 갖는 제 1 편광 필터(5a) 및 제 2 편광 필터(5b)를 포함하고, 상기 제 1 편광 필터(5a)는 광원(6)과 샘플(1) 사이에 그리고 제 2 편광 필터(5b)는 샘플(1)과 검출기(2) 사이에 배치되는 것을 특징으로 하는 검출 방법.
- 전술한 항들 중 어느 한 항에 있어서,
a) 상기 검출기(2)는 상기 샘플(1)에 의해 확산된 광의 에피디텍션(epidetection)을 위해 상기 광원(6)과 동일한 상기 샘플(1) 측에 배치되고; 그리고/또는
b) 상기 검출기(2)는 상기 조명 빔 경로(10)의 방향에 대해 상기 샘플(1)의 확산 측면 방사선을 검출하기 위해 상기 샘플(2)의 측면에 배치되고; 그리고/또는
c) 상기 검출기(2)는 샘플(2)에 의해 확산된 광의 투과광 검출을 위해 샘플(1)의 투과광 방향으로 배열되고, 상기 광학기구는
c1) 샘플을 통해 투과된 빔으로서 검출기(2)에 도달할 수 있는 조명 빔 경로 내의 광 빔을 차단하도록 설계된 광원(6)와 샘플(1) 사이에 배치된 것으로, 샘플을 통해 투과된 빔으로서 검출기(2)에 도달할 수 있는 조명 빔 경로 내의 광 빔을 차단하도록 설계된 조리개(어퍼쳐)(3)을 포함하고, 그리고/또는
c2) 상기 광원(6)과 상기 샘플(2) 사이에 배치된 것으로서, 상기 샘플(1)을 통해 투과된 광선이 검출기(2)에 도달하지 않는 방도로 상기 조명 빔 경로의 방향을 변경시키도록 설계된 굴절 요소(4)를 포함하는 것을 특징으로 하는 검출 방법.
- 전술한 항들 중 어느 한 항에 있어서,
상기 광학기구는 상기 검출기(2) 앞에 배치되고 실내 광을 억제하도록 설계된 대역 통과 필터(13)를 포함하는 것을 특징으로 하는 검출 방법.
- 전술한 항들 중 어느 한 항에 있어서,
a) 샘플용 리셉터클이 캐리어 매트릭스, 바람직하게는 바이오폴리머(15)를 포함하고; 그리고/또는
b) 샘플용 리셉터클이 현적형 드롭(hanging drop)을 포함하는 것을 특징으로 하는 검출 방법.
- 전술한 항들 중 어느 한 항에 있어서,
상기 샘플용 리셉터클은 멀티-웰 플레이트 또는 현적형 드롭 멀티-웰 플레이트의 캐비티 인 것을 특징으로 하는 검출 방법.
- 전술한 항들 중 어느 한 항에 있어서,
움직임의 병행 광학 검출이 서로 분리된 몇몇 생물학적 샘플에서 수행되고,
샘플용 리셉터클은 멀티-웰 플레이트 또는 현적형 드롭 멀티-웰 플레이트로서, 행렬로 배열된, 샘플을 수용하기 위한 다수의 캐비티를 가지며,
검출기는 검출기 어레이로서, 바람직하게는 포토다이오드 어레이로서 설계되며, 개별 검출기의 그리드 거리는 멀티-웰 플레이트의 캐비티의 그리드 거리와 동일한 것을 특징으로 하는 검출 방법.
- 제 15 항에 있어서,
상기 광원은 캐비티 내의 샘플을 조명하기 위한 레이저 다이오드 어레이로서 설계되고, 개별 레이저 다이오드의 그리드 거리는 멀티-웰 플레이트의 캐비티의 그리드 거리와 동일하고 렌즈는 레이저 다이오드의 빛을 캐비티로 안내하는 것을 특징으로 하는 검출 방법.
- 제 16 항에 있어서,
a) 상기 레이저 다이오드 어레이의 홀더는 열전도성 재료, 바람직하게는 알루미늄으로 제조되며; 그리고/또는
b) 상기 광학기구는 마이크로 렌즈 어레이를 포함하며, 상기 렌즈 어레이의 각 렌즈는 상기 레이저 다이오드 중 하나에 할당되는 것을 특징으로 하는 검출 방법.
- 제 15 항에 있어서,
상기 광원의 광은 광섬유 번들에 의해 상기 샘플을 조명하기 위해 상기 샘플을 포함하는 개별 캐비티에 결합되는 것을 특징으로 하는 검출 방법.
- 3 차원 세포 및/또는 조직 배양물 또는 세포 클러스터 또는 자유롭게 수영하는 미생물 샘플의 형태로 공간적 범위를 갖는 생물학적 샘플에서의 움직임에 대한 비접촉 시험관내 검출 장치로서,
- 생물학적 샘플 (1) 용 리셉터클 (15, 16),
- 광원(6),
- 검출기 (2),
- 광학기구(7, 8)를 포함하고,
상기 광학기구(7, 8)는 상기 광원으로부터 나오는 방사선으로 상기 리셉터클 내의 전체 샘플(1)을 조명하고 상기 광원(6)으로부터 상기 방사선(11)의 적어도 일부를 유도하도록 구성되고, 샘플(1)과의 상호 작용을 통해 샘플(1) 내의 임의의 지점에서 검출기(2)의 검출 표면(2a)으로 방사 방향, 편광 상태 및/또는 회절 패턴이 변경되며, 상기 검출기(2)는 검출된 방사선(11)에 따라 측정 신호(9)를 생성하도록 구성되는 것으로, 상기 검출된 방사선의 강도의 시간 프로파일을 특정하고 그리고/또는 검출된 방사선(11)의 강도의 시간 프로파일이 도출될 수 있고, 상기 검출된 방사선의 시간 변화를 디스플레이 및/또는 평가함으로써 상기 생물학적 샘플 내의 움직임을 검출하도록 구성된 평가 유닛을 더 포함하는 것을 특징으로 하는 검출 장치.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102015003019.1A DE102015003019A1 (de) | 2015-03-06 | 2015-03-06 | Verfahren und Vorrichtung zur optischen Detektion einer Bewegung in einer biologischen Probe mit räumlicher Ausdehnung |
| DE102015003019.1 | 2015-03-06 | ||
| PCT/EP2016/000377 WO2016142043A1 (de) | 2015-03-06 | 2016-03-02 | Verfahren und vorrichtung zur optischen detektion einer bewegung in einer biologischen probe mit räumlicher ausdehnung |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20170140182A true KR20170140182A (ko) | 2017-12-20 |
Family
ID=55456746
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020177027379A KR20170140182A (ko) | 2015-03-06 | 2016-03-02 | 공간적 범위를 갖는 생물학적 샘플의 움직임에 대한 광학적 검출 방법 및 장치 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US10488400B2 (ko) |
| EP (2) | EP3265779B1 (ko) |
| JP (1) | JP6851328B2 (ko) |
| KR (1) | KR20170140182A (ko) |
| CN (1) | CN107430064B (ko) |
| DE (1) | DE102015003019A1 (ko) |
| ES (1) | ES2961352T3 (ko) |
| WO (1) | WO2016142043A1 (ko) |
Families Citing this family (30)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA3049524A1 (en) * | 2017-02-10 | 2018-08-16 | Amgen Inc. | Imaging system for counting and sizing particles in fluid-filled vessels |
| US10088660B2 (en) | 2017-02-10 | 2018-10-02 | Amgen Inc. | Imaging system for counting and sizing particles in fluid-filled vessels |
| BR112020012744A2 (pt) | 2017-12-27 | 2020-12-01 | Ethicon Llc | imageamento por fluorescência em ambiente com deficiência de luz |
| DE102018111033A1 (de) * | 2018-05-08 | 2019-11-14 | Byonoy Gmbh | Transmissionsvorrichtung zur Untersuchung von Proben in Kavitäten einer Mikrotiterplatte und Verfahren zum Untersuchen von Proben in Kavitäten einer Mikrotiterplatte mittels Transmission |
| US11237270B2 (en) | 2019-06-20 | 2022-02-01 | Cilag Gmbh International | Hyperspectral, fluorescence, and laser mapping imaging with fixed pattern noise cancellation |
| US11925328B2 (en) | 2019-06-20 | 2024-03-12 | Cilag Gmbh International | Noise aware edge enhancement in a pulsed hyperspectral imaging system |
| US11291358B2 (en) | 2019-06-20 | 2022-04-05 | Cilag Gmbh International | Fluorescence videostroboscopy of vocal cords |
| US11686847B2 (en) | 2019-06-20 | 2023-06-27 | Cilag Gmbh International | Pulsed illumination in a fluorescence imaging system |
| US11754500B2 (en) | 2019-06-20 | 2023-09-12 | Cilag Gmbh International | Minimizing image sensor input/output in a pulsed fluorescence imaging system |
| US11622094B2 (en) | 2019-06-20 | 2023-04-04 | Cilag Gmbh International | Wide dynamic range using a monochrome image sensor for fluorescence imaging |
| US11758256B2 (en) | 2019-06-20 | 2023-09-12 | Cilag Gmbh International | Fluorescence imaging in a light deficient environment |
| US11671691B2 (en) | 2019-06-20 | 2023-06-06 | Cilag Gmbh International | Image rotation in an endoscopic laser mapping imaging system |
| US11716543B2 (en) | 2019-06-20 | 2023-08-01 | Cilag Gmbh International | Wide dynamic range using a monochrome image sensor for fluorescence imaging |
| US11624830B2 (en) | 2019-06-20 | 2023-04-11 | Cilag Gmbh International | Wide dynamic range using a monochrome image sensor for laser mapping imaging |
| US11903563B2 (en) | 2019-06-20 | 2024-02-20 | Cilag Gmbh International | Offset illumination of a scene using multiple emitters in a fluorescence imaging system |
| US11898909B2 (en) | 2019-06-20 | 2024-02-13 | Cilag Gmbh International | Noise aware edge enhancement in a pulsed fluorescence imaging system |
| US11360028B2 (en) | 2019-06-20 | 2022-06-14 | Cilag Gmbh International | Super resolution and color motion artifact correction in a pulsed hyperspectral, fluorescence, and laser mapping imaging system |
| US11793399B2 (en) | 2019-06-20 | 2023-10-24 | Cilag Gmbh International | Super resolution and color motion artifact correction in a pulsed hyperspectral imaging system |
| US11740448B2 (en) | 2019-06-20 | 2023-08-29 | Cilag Gmbh International | Driving light emissions according to a jitter specification in a fluorescence imaging system |
| US11284785B2 (en) | 2019-06-20 | 2022-03-29 | Cilag Gmbh International | Controlling integral energy of a laser pulse in a hyperspectral, fluorescence, and laser mapping imaging system |
| US11931009B2 (en) | 2019-06-20 | 2024-03-19 | Cilag Gmbh International | Offset illumination of a scene using multiple emitters in a hyperspectral imaging system |
| US11187658B2 (en) | 2019-06-20 | 2021-11-30 | Cilag Gmbh International | Fluorescence imaging with fixed pattern noise cancellation |
| US11700995B2 (en) | 2019-06-20 | 2023-07-18 | Cilag Gmbh International | Speckle removal in a pulsed fluorescence imaging system |
| US11674848B2 (en) | 2019-06-20 | 2023-06-13 | Cilag Gmbh International | Wide dynamic range using a monochrome image sensor for hyperspectral imaging |
| US11147436B2 (en) | 2019-06-20 | 2021-10-19 | Cilag Gmbh International | Image rotation in an endoscopic fluorescence imaging system |
| US11550057B2 (en) | 2019-06-20 | 2023-01-10 | Cilag Gmbh International | Offset illumination of a scene using multiple emitters in a fluorescence imaging system |
| US20200397239A1 (en) | 2019-06-20 | 2020-12-24 | Ethicon Llc | Offset illumination of a scene using multiple emitters in a fluorescence imaging system |
| CN114514309A (zh) * | 2019-09-26 | 2022-05-17 | 京瓷株式会社 | 细胞检测装置和细胞检测方法 |
| WO2021257457A1 (en) * | 2020-06-15 | 2021-12-23 | Bragg Analytics, Inc. | Diffraction-based global in vitro diagnostic system |
| EP4165397A1 (en) | 2020-06-15 | 2023-04-19 | EosDx Inc. | Diffractometer-based global in situ diagnostic system |
Family Cites Families (39)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS54109488A (en) * | 1978-02-08 | 1979-08-28 | Fuji Photo Optical Co Ltd | Analyzing method and device of optically scattered image information |
| DE7836339U1 (de) * | 1978-12-07 | 1981-07-16 | Kaufmann, Raimund, Dr., 4005 Meerbusch | Vorrichtung zur bestimmung der geschwindigkeit von in einer fluessigkeit bewegten teilchen |
| JPS6259841A (ja) * | 1985-09-10 | 1987-03-16 | Res Dev Corp Of Japan | 直線偏光を用いる免疫反応の測定方法および装置 |
| JPS62116263A (ja) * | 1985-11-15 | 1987-05-27 | Olympus Optical Co Ltd | 直線偏光の多重散乱を用いる免疫反応の測定方法および装置 |
| JPH0623749B2 (ja) | 1986-03-10 | 1994-03-30 | 新技術事業団 | 毒素、薬剤による細胞損傷の新しい分光測定による検査法 |
| JP2949286B2 (ja) * | 1987-08-26 | 1999-09-13 | 松下電工株式会社 | 減光式二酸化炭素濃度感知器 |
| DE68924749T2 (de) * | 1988-09-15 | 1996-07-04 | Univ Arkansas | Kennzeichnung von Teilchen durch modulierte dynamische Lichtstreuung. |
| US5061075A (en) | 1989-08-07 | 1991-10-29 | Alfano Robert R | Optical method and apparatus for diagnosing human spermatozoa |
| US6671540B1 (en) * | 1990-08-10 | 2003-12-30 | Daryl W. Hochman | Methods and systems for detecting abnormal tissue using spectroscopic techniques |
| DE4215908A1 (de) * | 1992-05-14 | 1993-11-18 | Ubbo Prof Dr Ricklefs | Optische Einrichtung zur Bestimmung der Größe von Partikeln |
| US5627308A (en) * | 1995-05-31 | 1997-05-06 | Dahneke; Barton E. | Method and apparatus for measuring motion of a suspended particle or a suspending fluid |
| US6096510A (en) * | 1995-10-04 | 2000-08-01 | Cytoscan Sciences, Llc | Methods and systems for assessing biological materials using optical detection techniques |
| JP4169827B2 (ja) * | 1997-05-28 | 2008-10-22 | ミクロナス ゲーエムベーハー | 測定装置 |
| US20060105357A1 (en) * | 1998-02-18 | 2006-05-18 | Myomics, Inc. | Tissue sensor and uses thereof |
| DE19836183A1 (de) * | 1998-08-03 | 1999-03-18 | Gimsa Jan Priv Doz Dr | Verfahren und Vorrichtung zur räumlich (nm) und zeitlich (ms) aufgelösten Verfolgung der Bewegung mikroskopischer und submikroskopischer Objekte in mikroskopischen Volumina |
| DE59915204D1 (de) * | 1998-08-28 | 2010-10-28 | Febit Holding Gmbh | Verfahren zur herstellung von biochemischen reaktionsträgern |
| US6100976A (en) * | 1998-09-21 | 2000-08-08 | The Board Of Regents For Oklahoma State University | Method and apparatus for fiber optic multiple scattering suppression |
| GB2361772B (en) * | 2000-04-29 | 2004-05-19 | Malvern Instr Ltd | Mobility and effects arising from surface charge |
| JP4384344B2 (ja) * | 2000-08-09 | 2009-12-16 | 拓之 今野 | レーザ反射光による粒状斑点模様を利用した血液凝固時間測定方法とその装置 |
| DE10041596A1 (de) * | 2000-08-24 | 2002-03-21 | Cellcontrol Biomedical Lab Gmb | Vorrichtung und Verfahren zum ortsaufgelösten Untersuchen vernetzter Zellen und/oder Zellsystemen und Verwendung für die Wirkstoffuntersuchung |
| JP4334899B2 (ja) | 2003-02-25 | 2009-09-30 | 大塚電子株式会社 | 電気泳動速度測定装置 |
| GB0307756D0 (en) * | 2003-04-03 | 2003-05-07 | Suisse Electronique Microtech | Measuring the concentration and motility of light scattering particles |
| DE102006003877B4 (de) * | 2005-12-09 | 2007-10-31 | Diehl Bgt Defence Gmbh & Co. Kg | Vibrometer |
| WO2008053474A2 (en) * | 2006-10-30 | 2008-05-08 | Elfi-Tech Ltd. | System and method for in vivo measurement of biological parameters |
| JP5024935B2 (ja) | 2007-01-16 | 2012-09-12 | 富士フイルム株式会社 | 光透過性部材の欠陥検出装置及び方法 |
| GB0701201D0 (en) * | 2007-01-22 | 2007-02-28 | Cancer Rec Tech Ltd | Cell mapping and tracking |
| US8821799B2 (en) * | 2007-01-26 | 2014-09-02 | Palo Alto Research Center Incorporated | Method and system implementing spatially modulated excitation or emission for particle characterization with enhanced sensitivity |
| ES2401640T3 (es) | 2008-09-22 | 2013-04-23 | University Of Zurich Prorektorat Forschung | Placa para gotas en suspensión |
| CN201311392Y (zh) | 2008-12-11 | 2009-09-16 | 成都恩普生医疗科技有限公司 | 一种基于led冷光源的酶标仪光路检测系统 |
| EP2376896B1 (en) | 2009-01-08 | 2021-05-19 | IT-IS International Ltd | Optical system for chemical and/or biochemical reactions |
| US8702942B2 (en) * | 2010-12-17 | 2014-04-22 | Malvern Instruments, Ltd. | Laser doppler electrophoresis using a diffusion barrier |
| JP5883233B2 (ja) * | 2011-03-16 | 2016-03-09 | 英光 古川 | 走査型顕微光散乱測定解析装置および光散乱解析方法 |
| US8772039B2 (en) * | 2011-05-26 | 2014-07-08 | The General Hospital Corporation | Optical thromboelastography system and method for evaluation of blood coagulation metrics |
| DE102011085599B3 (de) | 2011-11-02 | 2012-12-13 | Polytec Gmbh | Vorrichtung und Verfahren zur interferometrischen Vermessung eines Objekts |
| JP5981443B2 (ja) * | 2011-11-02 | 2016-08-31 | 浜松ホトニクス株式会社 | 観察装置 |
| DE102012016122A1 (de) * | 2012-08-15 | 2014-02-20 | Westfälische Wilhelms-Universität Münster | Verfahren und Vorrichtung zur Erfassung wenigsten eines Tieres |
| JP6076111B2 (ja) * | 2013-02-07 | 2017-02-08 | 浜松ホトニクス株式会社 | 塊状細胞評価方法および塊状細胞評価装置 |
| DE102013211885A1 (de) * | 2013-06-24 | 2014-12-24 | Siemens Aktiengesellschaft | Partikeldetektor und Verfahren zur Detektion von Partikeln |
| DE202014004218U1 (de) * | 2014-05-19 | 2014-05-28 | Particle Metrix Gmbh | Vorrichtung der Partikel Tracking Analyse mit Hilfe von Streulicht (PTA) und zur Erfassung und Charakterisierung von Partikeln in Flüssigkeiten aller Art in der Größenordnung von Nanometern |
-
2015
- 2015-03-06 DE DE102015003019.1A patent/DE102015003019A1/de active Pending
-
2016
- 2016-03-02 ES ES16708082T patent/ES2961352T3/es active Active
- 2016-03-02 KR KR1020177027379A patent/KR20170140182A/ko unknown
- 2016-03-02 CN CN201680014161.3A patent/CN107430064B/zh active Active
- 2016-03-02 EP EP16708082.9A patent/EP3265779B1/de active Active
- 2016-03-02 EP EP23182756.9A patent/EP4242637A3/de active Pending
- 2016-03-02 JP JP2017564793A patent/JP6851328B2/ja active Active
- 2016-03-02 US US15/555,773 patent/US10488400B2/en active Active
- 2016-03-02 WO PCT/EP2016/000377 patent/WO2016142043A1/de active Application Filing
Also Published As
| Publication number | Publication date |
|---|---|
| JP6851328B2 (ja) | 2021-03-31 |
| CN107430064B (zh) | 2020-10-20 |
| ES2961352T3 (es) | 2024-03-11 |
| EP3265779C0 (de) | 2023-08-09 |
| EP4242637A2 (de) | 2023-09-13 |
| US20180038845A1 (en) | 2018-02-08 |
| US10488400B2 (en) | 2019-11-26 |
| CN107430064A (zh) | 2017-12-01 |
| WO2016142043A1 (de) | 2016-09-15 |
| EP4242637A3 (de) | 2023-10-04 |
| DE102015003019A1 (de) | 2016-09-08 |
| EP3265779A1 (de) | 2018-01-10 |
| EP3265779B1 (de) | 2023-08-09 |
| JP2018515787A (ja) | 2018-06-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20170140182A (ko) | 공간적 범위를 갖는 생물학적 샘플의 움직임에 대한 광학적 검출 방법 및 장치 | |
| KR100190312B1 (ko) | 이물검사장치 | |
| KR102162213B1 (ko) | 이미지 형성 세포 계수기 | |
| EP3593110B1 (en) | Particle characterisation with a focus tuneable lens | |
| CN103364348A (zh) | 用于检测样本内的不均匀性的光学设备,特别是偏振计 | |
| US8637803B2 (en) | Method and apparatus for measuring the optical forces acting on a particle | |
| CN110389021A (zh) | 透镜图像产生系统及屈光能力和厚度确定与缺陷检测方法 | |
| JP2019512701A5 (ko) | ||
| EP3189321B1 (en) | A particle characterization method and apparatus | |
| EP2960635A1 (en) | Dynamic light scattering measurement device and dynamic light scattering measurement method | |
| KR20120013297A (ko) | 매질 내의 고체 입자를 분석하는 방법 및 시스템 | |
| US20080018893A1 (en) | Instrument using near-field intensity correlation measurements for characterizing scattering of light by suspensions | |
| CN106066315A (zh) | 用于表征和量化微粒样本的图像细胞仪 | |
| JP2016540237A (ja) | 自由表面を有する液体の光学測定 | |
| JP2021517963A (ja) | 光回折により改良された粒子サイジング | |
| US9958319B2 (en) | Method and device for determining a critical angle of an excitation light beam | |
| JP2007333409A (ja) | 浮遊粒子測定装置 | |
| CN107478332B (zh) | 一种环形光束共聚焦纵向高分辨成像装置 | |
| US20150049348A1 (en) | Measurement Method For Height Profiles Of Surfaces | |
| JP2010156557A (ja) | 入射光学系及びラマン散乱光測定装置 | |
| US20210348998A1 (en) | Method and apparatus for detecting nanoparticles and biological molecules | |
| CZ2012499A3 (cs) | Zarízení pro sledování kvality pohybujícího se lineárního textilního materiálu na pracovním míste textilního stroje | |
| WO2012033723A1 (en) | Optical measuring system with illumination provided through a void in a collecting lens | |
| US20110057093A1 (en) | Method for calibrating a deflection unit in a tirf microscope, tirf microscope, and method for operating the same | |
| KR102255060B1 (ko) | 생물학적 시료의 움직임 및/또는 생물학적 시료 성분의 움직임에 대한 광학적인 시험관내 검출 방법 및 장치 |