KR20140057523A - 비특이 반응 억제제, 비특이 반응 억제 방법 및 키트 - Google Patents
비특이 반응 억제제, 비특이 반응 억제 방법 및 키트 Download PDFInfo
- Publication number
- KR20140057523A KR20140057523A KR1020147001570A KR20147001570A KR20140057523A KR 20140057523 A KR20140057523 A KR 20140057523A KR 1020147001570 A KR1020147001570 A KR 1020147001570A KR 20147001570 A KR20147001570 A KR 20147001570A KR 20140057523 A KR20140057523 A KR 20140057523A
- Authority
- KR
- South Korea
- Prior art keywords
- specific
- inhibitor
- group
- specific reaction
- measurement
- Prior art date
Links
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/5306—Improving reaction conditions, e.g. reduction of non-specific binding, promotion of specific binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D207/00—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D207/02—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D207/30—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having two double bonds between ring members or between ring members and non-ring members
- C07D207/34—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having two double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D207/36—Oxygen or sulfur atoms
- C07D207/40—2,5-Pyrrolidine-diones
- C07D207/416—2,5-Pyrrolidine-diones with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to other ring carbon atoms
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Immunology (AREA)
- Urology & Nephrology (AREA)
- Molecular Biology (AREA)
- Biomedical Technology (AREA)
- Hematology (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- Biochemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Food Science & Technology (AREA)
- Cell Biology (AREA)
- Physics & Mathematics (AREA)
- Analytical Chemistry (AREA)
- Microbiology (AREA)
- General Health & Medical Sciences (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Biotechnology (AREA)
- Peptides Or Proteins (AREA)
- Investigating Or Analysing Biological Materials (AREA)
Abstract
Description
본 발명은 면역학적 측정법에서 사용하는, 미량의 표적 물질을 정확하게 검출, 정량하는데 장해가 되는 비특이적 반응을 억제하기 위한 비특이 반응 억제제, 이것을 이용하는 비특이 반응 억제 방법 및 이를 포함하는 면역 측정 키트에 관한 것이다.
항원 항체 반응을 이용한 면역학적 측정법은 측정 대상으로 하는 미량 성분을 특이적으로 검출 또는 정밀하게 측정할 수 있기 때문에, 임상 검사에 널리 이용되고 있다. 이러한 면역학적 측정법에서는, 본래의 목적으로 하는 표적 물질의 특이적인 항원 항체 반응 이외의 비특이 반응에 의해, 측정 값의 신뢰성이 손상되어 버리는 것이 종종 확인되고 있다. 이 문제는 검체 중에 포함되는 표적 물질 (항원) 이외의 성분이 측정계의 성분과 반응함에 의해 야기된다.
종래로부터, 비특이 반응을 억제하고 올바른 측정값을 얻기 위해 다양한 시도를 해왔다. 예를 들면, 측정될 검체를 가열이나 적당한 시약에 의해 전처리하고, 각종 동물 혈청, 면역 글로불린 분획, 알부민, 탈지 우유(スキムミルク), 젤라틴, 계면 활성제 등을 측정계에 첨가하기도 함에 일반적으로 행해져왔다. 류마티스 인자와 같은 항체의 Fc 부위에 결합함으로써 발생되는 비특이 반응을 회피하기 위하여는, Fab이나 F(ab')2 등의 항체 단편을 특이 반응에 사용하는 것도 행해지고 있다. 또한 측정계에 사용되는 모노클론 항체와는 반응 특이성이 다르며 측정계에 관련된 반응을 저해하지 않는 모노클론 항체를 측정계에 첨가하는 것도 행해지고 있다.
또한 특허 문헌 1과 같이, 스트렙토 아비딘을 말레이미드 등을 사용하여 가교/중합한 것을 이용하거나, 특허 문헌 2와 같이, 아실화 단백질 응집체를 이용하기도 하는 것도 알려져 있다. 또한 N치환 말레이미드 화합물의 존재 하에서, 검출 가능한 물질로 표지된 제 1항체와 제 2항체와 시료를 반응시켜, 이것에 의해, 검출 가능한 물질과 시료에 포함된 티올기 (즉, SH기)에 의한 비특이적인 결합을 억제하는 것도 알려져 있다 (특허 문헌3). 또한 담체에 대한 생체 관련 분자의 비특이적 흡착을 저해하는 방법으로는, N-히드록시 숙신이미드 에스테르(N-ヒドロキシスクシンイミドエステル)기, 카르복실기, 말레이미드기 및 아미노기로 이루어진 군에서 선택되는 화학 수식기를 표면에 갖는 담체에 대하여, 상기 담체 상의 화학적 수식기와 반응할 수 있는 관능기이고, N-히드록시 숙신이미드 에스테르기, 메르캅토기 및 아미노기로 이루어진 군에서 선택되는 관능기를 말단에 갖는 폴리알킬렌 옥사이드를 포함하는 블로킹제를 사용하는 것이 개시되어 있다 (특허 문헌4).
그러나, 이러한 방법은 비특이 반응 억제에 어느 정도 효과가 있지만, 일부 검체에서는 그 효과는 아직 불충분하고, 오진단이 심각한 결과를 초래하게 되어 임상 검사의 현장에서는, 아직 만족할 수 있는 것은 아니었다.
이러한 상황을 감안하여, 면역학적 측정법에서, 측정에 따르는 비특이 반응을 간편하고 효과적으로 억제하여, 검체 중의 미량 성분 (표적 물질)의 정확한 검출 및 정량을 실현하기 위한 비특이 반응 억제제와 그의 사용 방법, 및 측정 키트를 제공하는 것이 본 발명의 목적이다.
본 발명자들은, 상기의 문제점을 해결하기 위해 비특이 반응에 대해 예의 검토한 결과, 말레이미드기를 가지는 물질 (Sulfo-SMCC: 술포석신이미딜-4-(N-말레이미드메틸)시클로헥산-1-카르복실레이트(スルホサクシイミジル-4-(N-マレイミドメチル)シクロヘキサン-1-カルボキシレ-ト) 또는 Sulfo-HMCS: N-(8-말레이미드 카프릴옥시)술포석신이미드)(N-(8-マレイミドカプリルオキシ)スルホスクシニミド)을 결합시킨 캐리어 단백질을 반응액 중에 첨가함에 의해, 검체 중의 간섭 물질 (비특이 반응 물질)의 영향을 회피할 수 있음을 발견하여, 본 발명에 이르렀다. 즉, 후술하는 실시예에서 상술하겠지만, 검체 중에 비특이 반응 물질로서, 말레이미드기를 결합한 캐리어 단백질에 반응하는 물질이 존재하는 것이 판명됐다. 본 발명은 이 지견에 기초하여, 검체 중의 표적 물질을 정확히 측정하기 위한 비특이 반응 억제제 및 해당 비특이 반응 억제제를 사용하는 측정 방법 및 측정 시약을 완성시킨 것이다.
즉, 본 발명은
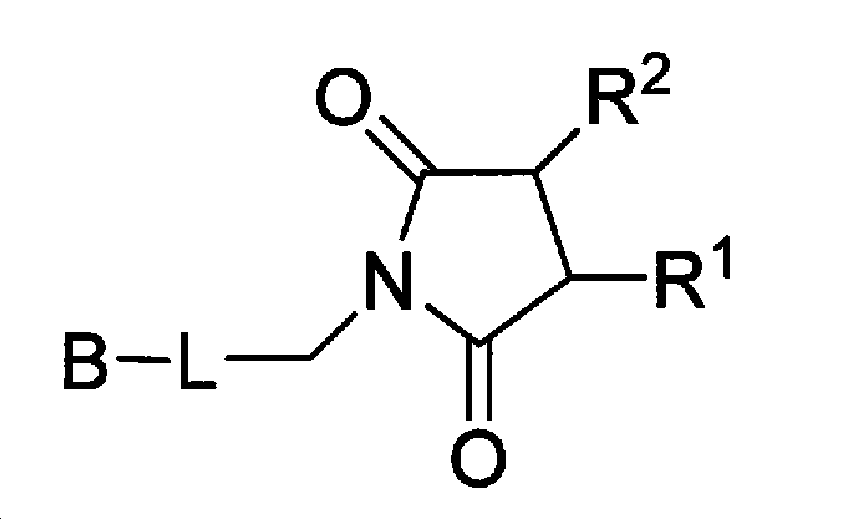
[1] 식 1:
[식 중, R1 및 R2는, 하나가 되어, 각각이 직접 결합하는 탄소 사이에 이중 결합을 형성하거나, 또는 R1이 수소 원자이며, 그리고, R2가 SH기 함유 화합물에서 H를 제거한 기이고, B는 지지체이며, L은 스페이서 암(スペ-サ-ア-ム) 부분이다]
로 표시되는 물질을 포함하는, 면역학적 측정용의 비특이 반응 억제제,
[2] 지지체가 캐리어 단백질 또는 캐리어 고상(固相) 담체인 [1]의 비특이 반응 억제제,
[3] 캐리어 단백질이 알부민인 [2]의 비특이 반응 억제제,
[4] 캐리어 고상 담체가 입자인 [2]의 비특이 반응 억제제,
[5] [1] ~ [4]의 어느 하나의 비특이 반응 억제제를 사용하는, 면역학적 측정 방법,
[6] 면역학적 측정 방법이, 라텍스 응집 광학적 측정법, 효소 면역 분석법(エンザイムイムノアッセイ), 면역 비탁 분석법(免疫比ろう法), 효소 면역 측정법, 형광 면역 측정법, 또는 방사 면역 측정법인 [5]의 면역학적 측정 방법,
[7] 검체에 포함된 표적 물질과의 특이적인 면역 반응 공정을 수행하기 전에, 해당 검체와 비특이 반응 억제제를 반응시키는, [5] 또는 [6]의 면역학적 측정 방법,
[8] 비특이 반응 억제제의 공존 하에, 검체에 포함된 표적 물질과의 특이적인 면역 반응 공정을 수행하는, [5] 또는 [6]의 면역학적 측정 방법,
[9] 면역 측정이 샌드위치법에 의한 측정이며, 검체에 포함된 표적 물질과의 특이적인 면역 반응 공정의 하나 이상의 공정을 비특이 반응 억제제의 공존 하에서 실시하는, [5] 또는 [6]의 면역학적 측정 방법,
[10] [1]~ [4]의 어느 하나의 비특이 반응 억제제를 함유하는, 면역학적 측정 키트, 에 관한 것이다.
본 발명의 비특이 반응 억제제와 그 사용 방법, 및 측정 키트를 이용함에 의해, 검체 중의 비특이 반응 물질의 영향을 간편하고 효과적으로 억제하여, 검체 중의 미량 성분 (표적 물질)을 정확하게 측정할 수 있다.
본 발명에서 발견한 비특이 반응 물질은, 본 발명의 비특이 반응 억제 물질 인, 말레이미드기 또는 그 유도체가 결합된 지지체 (특히 단백질)에 잘 반응하기 때문에, 특이적인 면역 반응 공정 중에 말레이미드기가 결합된 지지체가 존재하는 경우에 특히 효과가 높다. 따라서, 면역학적 측정법 중 말레이미드법을 이용하여 항체나 항원등을 고상화(固相化) 또는 표지화하여 제조되는 시약에서는, 특히 본 발명이 유효하다고 생각된다.
본 발명의 비특이 반응 억제제는, 공지의 면역학적 측정법에 이용할 수 있다.
면역학적 측정법으로는, 일원(一元) 방사 면역 확산법, 비탁법(比濁法), 비탁 분석법(比ろう法), 응집법, 방사 면역 측정법, 효소 면역 측정법, 형광 면역 측정법 등이 있지만, 방사 면역 측정법, 효소 면역 측정법, 형광 면역 측정법은 측정 감도도 높고, 특히 극미량 성분의 측정에 적합하다.
방사 면역 측정법, 효소 면역 측정법, 형광 면역 측정법은 각각 방사성 물질 , 효소, 형광 물질을, 표적 물질에 특이적으로 반응하는 항체에 결합한 표지 항체를 이용하는 방법으로, 일반적으로는, 항체나 항원을 불용성 담체에 결합한 고상 화 항체 또는 고상화 항원과 조합시킨 고상법(固相法)으로 사용된다. 고상법에는 「고상화 항체-항원-표지 항체」 복합물을 만들어서 측정하는 샌드위치법이나, 고상화 항원과 검체 중의 유리(遊離) 항원이 반응계 내에 첨가된 일정량의 표지 항체에 대해 경합적으로 반응함을 원리로 하는 경합법이 있다.
본 발명에서 사용되는 검체로서는, 예를 들면 전혈, 혈청, 혈장, 수액, 타액 등의 체액이나 소변, 대변 추출액 등을 들 수 있다.
표적 물질로서는, 검체 중에 함유될 수 있고, 면역학적 반응성을 갖는 것이면 제한은 없으나, 질병의 진단이나 병 상태의 파악에 도움이 되는 것이 바람직하다. 예를 들어, B형 간염 바이러스 표면 항원 (HBsAg), C형 간염 바이러스(HCV) 항체 및 항원, 인간 면역 결핍 바이러스 (HIV) 항체, 인간 T세포 백혈병 바이러스-1 (HTLV-1) 항체, 매독 트레포네마(トレポネ-マ, TP) 항체 등을 들 수 있다. 또한 각종 심근 마커 (크레아틴 키나제(CKMB), 미오글로빈, 트로포닌), 각종 호르몬류, 혈청 단백 등을 들 수 있다.
본 발명의 비특이 반응 억제제는, 상기 화학식 1로 표시되는, 지지체에 말레이미드기 또는 그 유도체를 직접 또는 간접적으로 결합시킨 것을, 비특이 반응 억제 물질로서 포함한다. 또한, 본 명세서에서, 말레이미드기의 유도체로는, 말레이 미드기(설프히드릴기(スルフヒドリル)와 반응)를 SH기 함유 화합물로 블로킹(ブロッキング)한 것을 의미한다. 지지체로서는, 측정계에서 불활성인 물질 (이하, 캐리어라고 칭하는 경우가 있음)이면 특별히 한정하지 않지만, 예를 들어, 단백질, 고상 담체 등 을 들 수 있다. 캐리어 단백질로서는, 알부민 (소 혈청 알부민: BSA나 인간 혈청 알부민: HSA 등), 불활성화 알칼리 포스파타제 (불활성화 ALP), 불활성화 호스라디쉬 퍼옥시다아제 (不活性化ホ-スラディッシュペルオキシダ-ゼ; 불활성 HRP), 스트렙토아비딘, 아비딘, 젤라틴, 카제인, 항체 등을 들 수 있다. 캐리어 고상 담체로서는, 마이크로타이터 플레이트(マイクロタイタ-プレ-ト), 시험관, 비즈, 입자, 나노 입자, 막 등을 들 수 있다. 입자로서는, 자성 입자, 폴리스티렌 라텍스와 같은 소수성 입자, 입자 표면에 아미노기, 카르복실기 등의 친수기를 갖는 공중합 라텍스 입자, 적혈구, 젤라틴 입자 등을 들 수 있다. 측정계에서 불활성으로는, 측정 대상의 물질과의 면역학적 반응에 영향을 주지 않는 것이나, 효소 반응에 영향을 주지 않는 것 등을 가리킨다. 당업자이면, 측정 원리에 맞게, 적절하게 적합한 캐리어를 선택할 수 있다.
캐리어 단백질로로서는, 생체 시료로부터 정제한 것이어도, 유전자 조작에 의해 바람직한 단백질로서 제작한 것이어도 좋다.
캐리어 단백질로의 말레이미드기의 결합은, 공지의 가교제를 사용할 수 있다. 가교제는, 말레이미드기와, 캐리어 단백질로의 결합용 관능기 (예를 들면, 아미노기 반응성 관능기, 카르복실기 반응성 관능기, 비오틴)를 포함하면, 말레이미드기와 캐리어 단백질의 사이에, 환상 또는 직선상의 관능기를 가지고 있어도 좋다.
사용 가능한 가교제의 구체적인 예로서는, 아미노기 반응성 관능기를 갖는 가교제로서, 예를 들면, 식: S-L-M (S는 아미노기 반응성 관능기이고, M은 말레이미드기이고, L은 스페이서 암 부분이다)로 표시되는 화합물, 보다 구체적으로는, succinimidyl 4-[N-maleimidomethyl]cyclohexane-1-carboxylate (SMCC), sulfosuccinimidyl 4-[N-maleimidomethyl]cyclohexane-1-carboxylate (Sulfo-SMCC), Succinimidyl-4-[N-Maleimidomethyl]cyclohexane-1-carboxy-[6-amidocaproate] (LC-SMCC), N-[e-Maleimidocaproyloxy]succinimide ester (EMCS), N-[e-Maleimidocaproyloxy]sulfosuccinimide ester (Sulfo-EMCS), N-[γ-maleimidobutyryloxy]succinimide ester (GMBS), N-[γ-maleimidobutyryloxy]sulfosuccinimide ester (Sulfo-GMBS), N-(11-Maleimidoundecanoyloxy)succinimide (KMUS), N-[k-Maleimidoundecanoyloxy]-sulfosuccinimide ester (Sulfo-KMUS), m-maleimidobenzoyl-N-hydoxysuccinimide ester (MBS), m-maleimidobenzoyl-N-hydoxysulfosuccinimide ester (Sulfo-MBS), succinimidyl 4-[p-maleimidophenyl]butyrate (SMPB), sulfosuccinimidyl 4-[p-maleimidophenyl]butyrate (Sulfo-SMPB), N-[α-Maleimidoacetoxy]succinimide ester (AMAS), N-[β-Maleimidopropyloxy]succinimide ester (BMPS), Succinimidyl-6-[β-maleimidopropionamido]hexanoate (SMPH), N-(8-Maleimidocapryloxy)succinimide (HMCS), N-(8-Maleimidocapryloxy)sulfosuccinimide (Sulfo-HMCS) 등을 들 수 있다.
카르복실기 반응성 관능기를 갖는 가교제로서, 예를 들면 식: H-L-M (H는 카르복실기 반응성 관능기이고, M은 말레이미드기이고, L은 스페이서 암 부분이다)로 표시되는 화합물, 보다 구체적으로는, β-Maleimidopropionic acid hydrazide (BMPH), 3,3'-N-[e-Maleimidocaproic acid] hydrazide (EMCH), N-[k-Maleimidoundecanoic acid]-hydrazide (KMUH), 4-[4-N-maleimidophenyl] butyric acid hydrazide hydrochloride (MPBH), 3-[2-Pyridyldithio] propionyl hydrazide (PDPH) 등을 들 수 있다.
비오틴을 갖는 가교제로서, 예를 들면 식: X-L-M (X는 비오틴이며, M은 말레이미드기이고, L은 스페이서 암 부분이다)로 표시되는 화합물, 보다 구체적으로는, 1-Biotinamido-4-[4'-(maleimidomethyl) cyclohexanecarboxamido] butane (Biotin-BMCC), Maleimide-PEG11-Biotin, Maleimide-PEG2-Biotin 등을 들 수 있다.
또한, 상기 가교제의 스페이서 암 부분의 길이는, 통상의 가교제와 동일하며, 예를 들어 4 ~ 52 옴스트롱(オ-ムストロング), 바람직하게는 9 ~ 20 옴스트롱이다.
이러한 가교제의 결합은, 공지의 방법에 따라 할 수 있다. 상기 말레이미드기는, 상기 가교제를 결합시킨 후, SH기 함유 화합물 (예를 들면, 단백질, 아미노산)을 이용하여 공지의 방법으로 블로킹하여도 좋다. 상기 SH기 함유 화합물로서는 SH기를 가지며, 상기 SH기를 통해 말레이미드기와 반응함에 의해, 상기 말레이미드기로의 반응성을 블로킹할 수 있는 화합물이면 특별히 한정되는 것은 아니다.
캐리어 입자로의 말레이미드기의 결합은, 캐리어 입자의 제작시에 말레이미드기를 갖는 화합물을 사용하는 것으로 행해도 좋고, 아미노기 또는 카르복실기를 갖는 화합물을 사용하고, 더욱 더 아미노기 반응성 관능기 또는 카르복실기 반응성 관능기 및 말레이미드기을 갖는 가교제를 결합시켜도 좋고, 상기 말레이미드기를 갖는 캐리어 단백질을 결합시켜도 좋다. 캐리어 입자의 제작 입자로의 캐리어 단백질의 결합은, 물리 흡착 또는 공유 결합 모두 사용할 수 있다. 공지의 화합물 또는 상기 가교제를 사용할 수 있다.
본 발명의 측정 원리는 상술한 면역학적 측정 방법을 사용할 수 있다.
상기 면역학적 측정 방법에 사용 가능한 항체는, 폴리클론 항체이어도, 모노클론 항체이어도 좋고, 항체를 생산하는 임의의 동물종, 예를 들면 집토끼, 염소, 양, 돼지, 말, 마우스(マウス) 또는 랫트(ラット)등 유래의 항체를 사용할 수 있다.
또한 사용 가능한 항체로서는 완전 항체나, 이것을 효소 처리나 화학 처리에 의해 절단한 F(ab')2 나 Fab'등과 같은 항체 단편을 들 수 있다.
「고상화 항체-항원-표지 항체」복합물을 만들어서 측정하는 샌드위치법 의 경우, 이들 항체는, 고상 담체 또는 표지 물질에 고정화된다. 고상 담체로서는, 마이크로타이터 플레이트, 시험관, 비즈, 입자, 나노 입자, 막 등을 들 수 있다. 입자로서는, 자성 입자, 폴리스티렌 라텍스와 같은 소수성 입자, 입자 표면에 아미노기, 카르복실기 등의 친수기를 갖는 공중합 라텍스 입자, 적혈구, 젤라틴 입자 등을 들 수 있다. 그 중에서도 신속 간편한 B/F 분리를 실현하는 관점에서는 자성 입자가 특히 바람직하며, 구체적으로는 예를 들어, 사산화삼철 (Fe3O4), 산화제2 철 (Fe2O3), 각종 페라이트, 철, 망간, 니켈, 코발트, 크롬 등의 금속, 코발트, 니켈, 망간 등의 합금으로 이루어진 미립자 등의 자성 입자가 바람직하게 사용된다. 또한 이러한 자성 입자를, 폴리스티렌 등의 고분자의 라텍스나, 젤라틴, 리포솜 등의 내부에 포함되는 형태로 조제하거나, 표면에 고정화하거나 한 것을 바람직하게 사용할 수 있다. 막으로는, 니트로셀룰로오스막, 셀룰로오스 여과지, 나일론막 등을 들 수 있고, 면역 크로마토그래피 등을 원리로 하는 간이 측정 키트의 시험편에도 사용하는 것도 가능 하다.
상기 면역학적 측정 방법에 사용 가능한 표지 물질로서는, 예를 들면, 효소, 형광 물질, 방사성 동위 원소, 불용성 입상(粒狀) 물질 등을 들 수 있다. 상기 표 지용 효소로서는, 알칼리 포스파타아제, 퍼옥시다아제, 글리코스옥시다아제, 티로시나아제, 산성 포스파타아제 등을 들 수 있다. 형광 물질로서는, 플루오레세인 이소티오시아네이트 (FITC), 그린 형광 단백질 (GFP), 루시페린 등을 들 수 있다. 방사성 동위 원소로서는, 125I, 14C, 32P 등을 들 수 있다.
또한, 표지 물질이 효소인 경우, 상기 효소에 대한 기질을 이용해서 발광, 형광 또는 발색 반응을 수행하여, 표지 물질을 측정할 수 있다. 예를 들면, 효소가 알칼리 포스파타아제인 경우, 기질로서는, CDP-star (등록 상표) (4-클로로-3-(메 톡시스피로 {1,2-디옥세탄-3,2'-(5'-클로로) 트리시클로 [3.3.1.13,7] 데칸}-4-일) 페닐인산2나트륨, (4-クロロ-3-(メトキシスピロ{1,2-ジオキセタン-3,2'-(5'-クロロ)トリシクロ[3.3.1.13,7]デカン}-4-イル)フェニルリン酸2ナトリウム)), CSPD (등록 상표) (3-(4-메톡시스피로 {1,2-디옥세탄-3,2-(5'-클로로)트리시클로 [3.3.1.13,7] 데칸}-4-일)페닐인산2나트륨, (3-(4-メトキシスピロ{1,2-ジオキセタン-3,2-(5'-クロロ)トリシクロ[3.3.1.13,7]デカン}-4-イル)フェニルリン酸2ナトリウム)), AMPPD (등록 상표) (아다만틸 메톡시 페닐 포스포릴 디옥시세탄, (アダマンチルメトキシフェニルホスホリルジオキシセタン)), APS-5 등의 화학 발광 기질; 4-메틸 운벨리 페릴 포스페이트 (4-methylumbelliferylphosphate) 등의 형광 기질; p-니트로 페닐포스페이트, BCIP (5-브로모-4-클로로-3-인돌릴-인산), NBT (4-니트로 블루 테트라졸륨 클로라이드), INT (요오드 니트로 테트라졸륨) 등의 발색 기질을 사용할 수 있다.
상기 항체(단편)은 그것만으로, 또는 단백질, 다당류 또는 합성 고분자 물질 등의 다른 고분자 물질과 함께, 유기 화학적 방법 또는 생물학적 친화성을 기반으로 하는 상호 작용 등을 통해 문헌에서 공지된 방법에 의해 결합체를 제조할 수 있다.
유기 화학적 방법으로는, 예를 들면, 가교 시약을 사용하여 공유결합시킴으로써 결합체를 제조할 수 있다. 주요한 가교 시약으로는 카르보디이미드, 이소시아네이트, 디아조 화합물, 벤조 퀴논, 글루타르 알데히드, 과요오드산, N-히드록시 숙신이미드 에스테르 화합물, 말레이미드 화합물, 피리딜·디설피드 화합물 등을 들 수 있다. 이러한 가교 시약을 사용한 결합체의 제조는, 예를 들어 효소 표지 항체에서 효소와 항체를 결합하는 방법과 동일한 방법으로 할 수 있고, 이시카와(石川) 등의 「효소 면역 측정법 제 3 판 (의학 서원, 1987년 ) 75 ~ 126 페이지」나 P. Tijssen 의 「효소 면역 분석법 (생화학 실험법 11, 도쿄 화학 동인, 1989년) 196 ~ 251 페이지 」 등에 상세하게 기재 되어 있다.
생물학적 친화성을 이용한 결합체의 제조 방법의 예로서는, 아비딘과 비오틴의 결합을 이용한 방법이 있다. 예를 들면 동일한 항체의 항체 (단편)와 알부민 등의 다른 고분자 물질의 양방에 비오틴 분자를 도입하고 아비딘에 의해 가교하는 방법이나, 또는 양자의 한쪽에 아비딘을 도입하고, 다른 한쪽에 비오틴을 도입하여 가교하는 방법이 있다. 비오틴 분자의 도입에는 비오티닐-ε-아미노카프론산-N- 히드록시 석신미니도 에스테르(ビオチニル-ε-アミノカプロン酸-N-ヒドロキシスクシミニドエステル) 등이 시약으로 사용된다.
본 발명의 비특이적 반응 억제제의 사용 방법으로는, 표적 물질과 그에 대한 특이적인 항체와 특이적인 면역 반응 공정 전에, 미리 적당한 완충액 중에서 비특이 반응 억제제와 검체를 접촉시켜, 적당한 시간 (예를 들면: 1 분 ~ 2 시간 ) 인큐베이트 하는 방법이 있다. 이 사이에, 검체 중의 비특이 반응을 일으키는 물질 ( 비특이 반응 물질)은 비특이 반응 억제제와 반응하여, 특이적인 면역 반응 공정에서의 표지 항체와의 비특이 반응 활성은 잃게 된다.
비특이 반응 억제제가, 특이적 면역 반응 공정에 영향을 주지 않는 측정법을 사용하는 경우에는, 인큐베이트를 완료한 검체와 비특이 반응 억제제의 혼합액을 그대로 이용하면 좋고, 한편 특이적 면역 반응 공정에 영향을 주는 측정법을 사용하는 경우에는, 특이적 면역 반응 공정을 수행하기 전에, 인큐베이트를 완료한 후의 비특이 반응 억제제를 제거하면 좋다.
특이적 면역 반응 공정에 영향을 주지 않는 측정법으로는, 예를 들어, 가장 일반적으로 사용되는 샌드위치법의 경우, 특이적 면역 반응에서 분리되는 「고상화 항체-비특이 반응 물질-표지 항체」샌드위치 복합체에 관련되지 않는 측정법이다. 이와 같은 경우, 구체적으로는, 상기 복합체와 함께 분리되지 않는 비특이 반응 억제제 (예를 들어, 유리(遊離))의 단백질이나 분리되지 않는 입자 등을 포함함)를 사용할 수 있다.
특이적 면역 반응 공정에 영향을 주는 측정법은, 예를 들어, 가장 일반적으로 사용되는 샌드위치법의 경우, 특이적 면역 반응에서 분리되는 「고상화 항체-비특이 반응 물질-표지 항체」샌드위치 복합체에 관련되는 측정법이다. 이와 같은 경우, 구체적으로는, 상기 복합체와 함께 분리되는 비특이 반응 억제제 (예를 들어, 상기 복합체가 자성 입자를 포함하고 자력체에서 분리되는 경우, 동일한 자성 입자 등을 포함함)를 사용할 수 있다.
본 발명의 비특이 반응 억제제의 다른 사용 방법으로서는, 비특이 반응 억제제의 공존하에 특이적 면역 반응 공정을 수행하는 방법이 있다. 예를 들어, 가장 일반적으로 사용되는 샌드위치법의 경우, 고상화 항체와 검체 중의 항원 (표적 물질)을 반응시키는 제 1 면역 반응 공정의 완충액에 비특이 반응 억제제를 첨가한다. 비특이 반응이 검출되는 것은, 항체의 특이적 반응 부위를 통하지 않고 「고상화 항체-비특이 반응 물질- 표지 항체」샌드위치 복합체를 형성하기 때문이나, 이 경우 제 1 면역 반응 중에 비특이 반응 물질의 표지 항체에 대한 반응 활성이 비특이 반응 억제제에 의해 흡수된다. 또한 항체의 특이 반응 부위를 통해 고정화된 항원과 표지 항체를 반응시키는 제 2 면역 반응 공정의 완충액에도 첨가하면, 제 1 면역 반응 공정에서 완전히 흡수되지 않았던 비특이 반응 물질도 흡수되기 때문에, 측정의 신뢰성을 보다 더욱 높일 수 있다.
위와 같이, 어느 측정법도 사용 가능하지만, 특이적 면역 반응 공정에서 비특이 반응 억제제가 사용되기 때문에, 상기 특이적 면역 반응 공정에 영향을 주지 않는 측정법으로 수행하는 쪽이 바람직하다.
또한, 1 단계 샌드위치법에서도 면역 반응 공정의 완충액에 비특이 반응 억제제를 첨가하여 반응시킴으로써, 비특이 반응은 회피된다.
상기와 같이, 어느 측정법도 사용 가능하지만, 특이적 면역 반응 공정에서 비특이 반응 억제제가 사용되기 때문에, 상기 특이적 면역 반응 공정에 영향을 주지 않는 측정법으로 수행하는 쪽이 바람직하다.
비특이 반응 억제제의 첨가 시기는, 표적 물질이나 측정법에 맞추어서, 적합한 방법을 적절하게 선택하면 좋다.
예를 들면, 본 발명에서 발견한 비특이 반응 물질은, 본 발명의 비특이 반응 억제 물질인, 말레이미드기 또는 그의 유도체가 직접 또는 간접적으로 결합된 지지체 (특히는 캐리어 단백질)에 잘 반응하기 때문에, 특이적인 면역 반응 중에 말레이미드기 또는 그의 유도체가 결합된 지지체 (특히 단백질)이 존재하는 경우에 특히 효과가 높다. 따라서, 면역학적 측정법 중 말레이미드법을 이용하여 항체나 항원 등을 고상화 또는 표지화하여 제조되는 시약에서는, 특히 바람직하다.
예를 들어, 앞서 서술한 바와 같은, 식: S-L-M 또는 H-L-M 또는 X-L-M으로 표시되는 가교제를 사용하여 제작한 항체 함유 물질 (항체 결합 담체, 표지화 항체 등)를 사용하는 면역학적 측정에 있어서는, 상기 식 1로 표시되는 비특이 반응 억제 물질을, 반응 공정의 적어도 하나에 공존시킬 수 있다. 따라서, 본 발명에는, 식: S-L-M 또는 H-L-M 또는 X-L-M으로 표시되는 가교제를 사용하여 제작한 항체 함유 물질과, 상기 화학식 1로 표시되는 비특이 반응 억제 물질을 포함하는, 면역학적 측정 키트가 포함된다. 또한, 상기 가교제의 화학식과, 상기 화학식 1에는, 스페이서 암 부분을 나타내는 기호로서, 동일한 「L」을 사용하고 있지만, 가교제의 관능기 S 또는 H의 종류나 지지체 B의 구조에 의해, 스페이서 암 부분의 구조가 다른 경우가 있다.
본 발명의 비특이 반응 억제제는, 면역 반응 공정 전에 미리 적당한 완충액에 첨가하여 사용하거나, 또는 면역 반응 공정의 완충액에 첨가하여 사용된다. 비특이 반응 억제제의 지지체가, 캐리어 단백질인 경우, 비특이 반응 물질과 반응시키는 계의 비특이 반응 억제 물질의 농도는 0.1 ~ 1000 μg/mL인 것이 바람직하고, 더욱 바람직하게는 1 ~ 500 μg/mL이다. 사용되는 완충액은 공지의 통상의 면역 반응에 사용되는 적당한 완충액이어도 좋다. 비특이 반응 억제 물질의 지지체가, 캐리어 고상 담체인 경우도, 당업자라면, 상기 캐리어 단백질과 동등한 활성을 갖는 농도나 사용 조건을 쉽게 결정할 수 있다.
또한 완충액 중에 통상적으로 사용되는 첨가제 예를 들어 반응 촉진제, 세정제 또는 안정제와 함께 사용할 수 있다. 또한 다른 비특이 반응 억제제와 함께 사용할 수도 있다. 적당한 완충액으로는 예를 들어, 20 ~ 100 mmol/L 인산염 완충액 (pH6 ~ 8) 또는 50 mmol/L 트리스-염산/100 mmol/L NaCl (pH7 ~ 8) 등이 사용될 수 있다. 반응 촉진제로서는 예를 들면 덱스트란 설페이트 또는 폴리에틸렌 글리콜 등, 세정제로서는 예를 들면 TritonX-100, Tween20 등을, 또한 안정 화제로서 알부민, 탈지 우유, 젤라틴 등의 단백질이나 아지화 나트륨, 티메로살(チメロサ-ル), 케이슨 CG(ケ-ソンCG), 프로클린(プロクリン) 등의 방부제를 들 수 있다.
본 발명의 비특이 반응 억제제를 포함하는 측정 키트로서는, 종래의 면역학적 측정 키트에 비특이 반응 억제제를 더욱 포함시킨 것이 가능하다. 일반적으로, ELISA법에 의한 측정 키트는 표지 항체액, 고상화 항체, 표준 물질 등의 시약으로 구성되고, 또한 필요에 따라, 샌드위치법으로 검체와 고상화 항체를 반응시키기 위한 완충액, 효소 반응을 위한 발색액과 반응 정지액, 고상(固相)을 세정하기 위한 세정액, 검체의 전처리제(前處理劑) 등을 포함하여 구성된다. 이러한 구성 시약이 동결 건조품의 경우, 복원을 위한 용액도 첨부되는 경우가 있다.
본 발명의 비특이 반응 억제제는 단독으로 키트의 구성 시약으로 하여도 좋고, 다른 구성 시약에 미리 첨가해도 좋다. 하지만 측정 조작을 늘리는 것 없이 비특이 반응 억제 효과를 얻는 것을 고려하면, 구성 시약의 일 성분으로서 첨가하는 것이 바람직하다. 예를 들면, 본 발명의 비특이 반응 억제제는, 검체 처리액이나 검체와 고상화 항체를 반응하는 완충액이나 표지 항체 용액에 첨가하여 키트의 구성 시약으로 하는 것을 들 수 있다. 이러한 구성 시약이 동결 건조품인 경우에는 복원액에 첨가할 수도 있다. 표지 항체에 대해서 비특이 반응 억제제는 0.1 ~ 1000 중량배 사용하는 것이 바람직하고, 특히 1 ~ 500 중량배 사용하는 것이 바람직하다.
[실시예]
이하, 실시예에 의해 본 발명을 구체적으로 설명하지만, 이들은 본 발명의 범위를 한정하는 것은 아니다.
《실시예 1 : 비특이 반응 억제제 (SMCC-BSA)의 제작》
소 혈청 알부민 (BSA: 시그마 사)을 0.1 mol/L HEPES (pH7.0)로 10 mg/mL가 되도록 용해하고, 또한, 디메틸 설폭시드(DMSO)로 용해한 50 mg/mL Sulfo - SMCC (술포삭시이미딜-4-(N-말레이미드메틸)시클로헥산-1-카르복실레이트) (피어스 사) 용액과 혼합하고, 37℃에서 하룻밤 방치했다. 이 반응액에 114 mg/mL 시스테아민(システアミン) HCl 용액을 첨가하고, 말단의 말레이미드기를 블로킹(ブロッキング)했다. 이것을 비특이 반응 억제제로서 이하의 검토에 사용했다.
《실시예 2: HBs 항원 측정계의 구축》
(1) 자성 입자 결합 항체 용액의 제작
(1-1) 말레이미드법을 이용하여 제작을 수행한 자성 입자 결합 항체 용액
자성 입자 (JSR 사)와 BSA (시그마 사)를 결합시킨 후, 추가로 항HBs 마우스 모노클론 항체를 Sulfo-SMCC (피어스 사)를 이용하여 결합시킨 자성 입자 용액을 제조하였다. 또한 항HBs 마우스 모노클론 항체는, 공지의 방법에 따라, CH1 세포에 의해 재조합 HBs 항원을 제작하고, 이를 마우스에 면역하여 제작하였다.
(1-2) EDC법을 이용하여 제작을 한 자성 입자 결합 항체 용액
자성 입자 (JSR 사)와 항HBs 마우스 모노클론 항체를, 카르복시이미드 (시그마 사)를 사용하여 결합시킨 자성 입자 용액을 제조하였다.
(2) 표지 항체 용액의 제작
항HBs 토끼 폴리클론 항체를 말레이미드법에 의해 알칼리 포스파타아제 (ALP) 표지한 표지 항체 용액을 제조하였다. 항HBs 토끼 폴리클론 항체는, (1-1)에서 제작한 재조합 HBs 항원을 토끼에 면역해서 제작했다.
(3) 발광 기질 용액
2-클로로-5-(4-메톡시스피로{1,2-디옥시세탄-3,2'-(5'-클로로)-트리시클로 [3.3.1.13,7]데칸}-4-일)-1-페닐포스페이트·나트륨 (2-クロロ-5-(4-メトキシスピロ{1,2-ジオキセタン-3,2'-(5'-クロロ)-トリシクロ[3.3.1.13,7]デカン}-4-イル)-1-フェニルホスフェ-ト·二ナトリウム) (CDP-Star (등록 상표):어플라이드바이오시스템 사)을 사용했다.
(4) 측정법
측정은, 전자동 임상 검사 시스템 STACIA (미츠비시 화학 메디엔스 사 제조)을 사용했다.
50 μL의 검체에 말레이미드법 또는 EDC법으로 제작한 60 μL의 자성 입자 결합 항체 용액을 첨가하여, 37 ℃에서 3.5 분간 가온한 후, 60 μL의 표지 항체 용액을 첨가하여, 37 ℃에서 8.6 분간 가압 가온하고, BF 분리, 세정한 후, 100 μL의 발광 기질 용액을 가하여, 37 ℃에서 2.7 분 반응 후에 발광량(counts)을 측정했다.
《실시예 3: 비특이 반응 억제제에 의한 검체 중의 간섭 물질의 영향 회피 효과의 확인》
실시예 2의 방법에 있어서, 실시예 1에서 제작한 비특이 반응 억제제를 최종 농도가 0.03%가 되도록 첨가하여, 그 효과의 유무를 검토했다.
HBs 항원 검사 의뢰가 있었던 환자군에서 얻은 HBs 항원 양성 검체 1예, 및 비특이 반응이 확인된 HBs 항원 음성 검체 5예에 대해서, 각 조건에서 측정을 실시했다. 말레이미드법에 의해 감작된 자성 입자 결합 항체를 사용하는 경우에는, EDC법 (카르복시이미드법)에 의해 감작된 자성 입자 결합 항체를 사용한 경우에 비해, 높은 비특이 반응이 인정되었지만, 말레이미드법 감작 자성 입자 결합 항체에, 비특이 반응 억제제를 첨가한 바, 그의 비특이 반응이 유의하게 억제되었다.
이 때문에, 검토에 사용한 비특이 검체에는, 자성 입자로의 고정화 방법에 기인하는 비특이 반응 물질이 포함되어 있는 것이 시사되었다. 또한 말레이미드법에서 현저하게 일어나므로, 자성 입자에 고정된 말레이미드기에 대해 비특이 반응이 일어나고 있는 것으로 예상되었다.
《실시예 4: 비특이 반응 억제제의 첨가 농도의 검토》
실시예 2에 따라서, 검체 중의 HBs 항원을 측정했다. 구성 시약 중의 자성 입자 결합 항체 용액에 실시예 1에서 제작한 SMCC-BSA를 각각 0.00003 %, 0.0003 %, 0.003 %, 0.03 %, 0.3 % 농도가 되도록 첨가하여, 실시예 3과 동일한 비특이 반응을 보이는 비특이 검체 6를 측정하여 그의 반응성을 비교했다. 그 결과, SMCC-BSA를 자성 입자 결합 항체 용액에 0.0003 % 이상 첨가함으로써, 비특이 검체의 영향을 회피할 수 있음을 확인할 수 있었다.
《실시예 5: 비특이적 반응의 원인 검토 1》
실시예 2에 따라서, 검체 중의 HBs 항원을 측정했다. 검토를 함에 있어서, MGLTX (magnetic latex)-BSA-SMCC-Ab, MGLTX-BSA-SMCC, MGLTX-BSA의 제작을, 다음과 같이 실시했다.
(1) MGLTX-BSA-SMCC-Ab
자성 입자 (JSR 사)와 BSA (시그마 사)를 결합시킨 후, 추가로 실시예 2에서 제작한 항HBs 마우스 모노클론 항체를 Sulfo-SMCC (피어스 사)를 이용하여 결합시켜 자성 입자 용액을 제조하였다.
(2) MGLTX-BSA-SMCC
자성 입자 (JSR 사)와 BSA (시그마 사)를 결합시킨 후에, Sulfo-SMCC (피어스 사)를 결합시켜 자성 입자 용액을 제조하였다.
(3) MGLTX-BSA
자성 입자 (JSR 사)와 BSA (시그마 사)를 결합시켜 자성 입자 용액을 제조하였다.
구성 시약 중의 자성 입자 결합 항체 용액을 상기 자성 입자의 제작 과정에서 할 수 있는 MGLTX-BSA-SMCC-Ab 또는 MGLTX-BSA-SMCC 또는 MGLTX-BSA로 변경하고, 이하의 조건에서 HBs 항원 음성 검체와 비특이 검체 1의 측정을 실시했다.
(A) (1)만
(B) (1) 및 최종 농도 0.03 % SMCC-BSA
(C) (2)만
(D) (3)만
그 결과, (A) 및 (C)의 비특이 검체에서 측정값의 상승이 인정되고, 또한 (B)에서는, (A)에 대해 비특이 반응 억제제 (SMCC-BSA)를 추가함에 의해, (A)에서 인정된 측정값의 상승이 억제되고, 음성 검체와 동등한 측정값을 얻었다. 이상에 의해, 자성 입자에 결합된 가교제(SMCC)가 비특이 반응의 발생에 크게 관여하는 것이 시사되었다.
《실시예 6: 비특이 반응의 원인 검토 2》
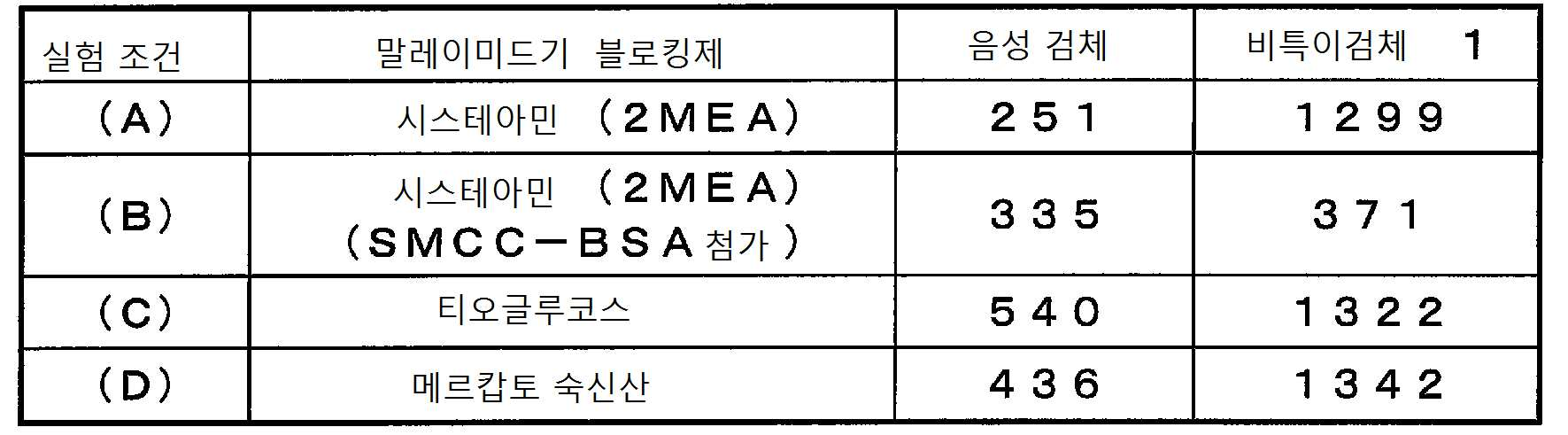
실시예 2에 따라서, 검체 중의 HBs 항원을 측정했다. 검토를 함에 있어서, 실시예 5(2)와 동일하게 제작한 MGLTX-BSA-SMCC를, 더욱 세 종류의 말레이미드기 블로킹제로서 처리한 자성 입자를 다음과 같이 제작하였다.
(1) 시스테아민 (2MEA)
자성 입자 (JSR 사)와 BSA (시그마 사)를 결합시킨 후에, Sulfo-SMCC를 결합시킨 자성 입자 용액에 대해 시스테아민 (Wako 사)으로 블로킹 처리를 실시해서, 조제하였다.
(2) 티오글루코스
자성 입자 (JSR 사)와 BSA (시그마 사)를 결합시킨 후에, Sulfo-SMCC를 결합시킨 자성 입자 용액에 대해 티오글루코스 (Wako 사)로 블로킹 처리를 실시해서, 조제하였다.
(3) 메르캅토 숙신산(メルカプトこはく酸)
자성 입자 (JSR 사)와 BSA (시그마 사)를 결합시킨 후에, Sulfo-SMCC를 결합시킨 자성 입자 용액에 대해 메르캅토 숙신산 (Wako 사)으로 블로킹 처리를 실시해서, 조제하였다.
구성 시약 중의 자성 입자 결합 항체 용액을 상기 자성 입자의 제작시에 사용하는 말레이미드기 블로킹제의 종류를 상기와 같이 하여 변경하고, HBs 항원 음성 검체 및 비특이 검체 1의 측정을 실시했다. 실험 조건으로는 이하를 실시했다.
(A) (1)만
(B) (1) 및 최종 농도 0.03 % SMCC - BSA
(C) (2)만
(D) (3)만
그 결과, (A) (C) (D)의 어느 것에서도 비특이 검체에서 측정값의 상승이 인정되었고 또한 (B)에서는, (A)에 대해 비특이 반응 억제제 (SMCC-BSA)를 추가함에 의해, (A)에서 인정된 측정값의 상승이 억제되고, 음성 검체와 동등의 측정값을 얻었다. 따라서, 말레이미드기의 블로킹제의 종류에 관계없이 비특이 반응이 발생하는 것으로 나타났다.
이상으로부터, 자성 입자에 결합된 가교제(SMCC)가 비특이 반응의 발생에 크게 관여하는 것이 시사되었다.
《실시예 7: 비특이 반응의 원인 검토 3》
실시예 2에 따라서, 검체 중의 HBs 항원을 측정했다. 검토를 함에 있어서, 실시예 1과 마찬가지로 시스테아민 HCl로 블로킹한 SMCC-BSA와 시스테아민 HCl로 블로킹하지 않은 SMCC-BSA의 2 종류의 비특이 반응 억제제를 제작했다. 이러한 비특이 반응 억제제를 첨가하여 비특이 검체의 측정을 실시했지만, 모두 같은 정도로 비특이 반응 억제 효과가 있는 것으로 나타났다.
이상으로부터, 말레이미드기를 갖는 캐리어 단백질에 의해, 비특이 반응을 억제할 수 있는 것으로 나타났다.
[산업상 이용 가능성]
본 발명자들에 의해, 본 발명에서 발견한 비특이 반응 물질에 의한 비특이 반응은, 질병에 관계없이, 정상인 검체의 300 ~ 1000 건에 1 건의 빈도로 발생하는 것이 판명되고 있다.
본 발명의 비특이 반응 억제제와 그의 사용 방법, 및 측정 키트를 이용함으로써, 이러한 고빈도로 일어나는 검체 중의 비특이 반응 물질의 영향을 간편하고 효과적으로 억제하여, 검체 중의 미량 성분을 정확하게 측정하는 것이 가능해져, 다양한 질환의 진단에 유용하다.
이상, 본 발명을 특정 형태에 따라 설명했지만, 당업자에게 자명한 변형이나 개량은 본 발명의 범위에 포함된다.
Claims (10)
- 청구항 1에 있어서, 지지체가 캐리어 단백질 또는 캐리어 고상 담체인, 비특이 반응 억제제.
- 청구항 2에 있어서, 캐리어 단백질이 알부민인, 비특이 반응 억제제.
- 청구항 2에 있어서, 캐리어 고상 담체가 입자인, 비특이 반응 억제제.
- 청구항 1 ~ 4 중 어느 한 항에 기재된 비특이 반응 억제제를 사용하는, 면역 학적 측정 방법.
- 청구항 5에 있어서, 면역학적 측정 방법이, 라텍스 응집 광학적 측정법, 효소 면역 분석법, 면역 비탁 분석법, 효소 면역 측정법, 형광 면역 측정법, 또는 방사 면역 측정법인, 면역학적 측정 방법.
- 청구항 5 또는 청구항 6에 있어서, 검체에 포함된 표적 물질과의 특이적인 면역 반응 공정을 수행하기 전에, 해당 검체와 비특이 반응 억제제를 반응시키는, 면역학적 측정 방법.
- 청구항 5 또는 청구항 6에 있어서, 비특이 반응 억제제의 공존 하에, 검체에 포함된 표적 물질과의 특이적인 면역 반응 공정을 수행하는, 면역학적 측정 방법.
- 청구항 5 또는 청구항 6에 있어서, 면역 측정이 샌드위치법에 의한 측정이며, 검체에 포함된 표적 물질과의 특이적인 면역 반응 공정의 하나 이상의 공정을 비특이 반응 억제제의 공존 하에서 실시하는, 면역 학적 측정 방법.
- 청구항 1 ~ 4 중 어느 한 항에 기재된 비특이 반응 억제제를 함유하는 면역 학적 측정 키트.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JPJP-P-2011-144464 | 2011-06-29 | ||
| JP2011144464 | 2011-06-29 | ||
| PCT/JP2012/066484 WO2013002309A1 (ja) | 2011-06-29 | 2012-06-28 | 非特異反応抑制剤、非特異反応抑制方法及びキット |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20140057523A true KR20140057523A (ko) | 2014-05-13 |
| KR101988600B1 KR101988600B1 (ko) | 2019-06-12 |
Family
ID=47424196
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020147001570A KR101988600B1 (ko) | 2011-06-29 | 2012-06-28 | 비특이 반응 억제제, 비특이 반응 억제 방법 및 키트 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US11125742B2 (ko) |
| EP (1) | EP2728354B1 (ko) |
| JP (1) | JP5808808B2 (ko) |
| KR (1) | KR101988600B1 (ko) |
| CN (1) | CN103620407B (ko) |
| WO (1) | WO2013002309A1 (ko) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3028043A4 (en) * | 2013-07-30 | 2017-04-19 | Bio-rad Laboratories, Inc. | Multiplex blocker beads for immunoassays |
| CN104860865B (zh) * | 2015-05-28 | 2019-04-05 | 江苏省原子医学研究所 | 一种非典型性荧光材料琥珀酰亚胺衍生物的制备方法 |
| CA3029989A1 (en) | 2016-07-06 | 2018-01-11 | Aluma Safety, Inc. | Mobile device accessory |
| US20190302115A1 (en) * | 2016-09-30 | 2019-10-03 | Biopromic Ab | Method for removing inhibitory components |
| CN106950363A (zh) * | 2017-03-31 | 2017-07-14 | 四川迈克生物科技股份有限公司 | 抑制类风湿因子干扰的胶乳增强免疫比浊试剂 |
| WO2020113521A1 (zh) * | 2018-12-06 | 2020-06-11 | 深圳迈瑞生物医疗电子股份有限公司 | 免疫检测中消除阿霉素干扰的方法及免疫检测试剂盒 |
| CN112269024A (zh) * | 2020-10-15 | 2021-01-26 | 上海捷门生物技术有限公司 | 白细胞介素-6的检测试剂、试纸、试剂盒及其应用 |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5169754A (en) * | 1990-10-31 | 1992-12-08 | Coulter Corporation | Biodegradable particle coatings having a protein covalently immobilized by means of a crosslinking agent and processes for making same |
| JPH06506688A (ja) * | 1991-04-10 | 1994-07-28 | バイオサイト・ダイアグノスティックス・インコーポレイテッド | クロストークインヒビターおよびその使用 |
| JPH08506907A (ja) | 1993-12-21 | 1996-07-23 | ベーリンガー マンハイム ゲーエムベーハー | アシル化タンパク質凝集体および免疫検定における干渉の抑制についてのそれらの使用 |
| JP3027770B2 (ja) | 1994-03-05 | 2000-04-04 | ロシュ ダイアグノスティックス ゲーエムベーハー | イムノアッセイで使用するための干渉除去剤 |
| JP2006308307A (ja) | 2005-04-26 | 2006-11-09 | Toyo Kohan Co Ltd | 生体関連分子の非特異的吸着を阻害する方法および生体関連分子検出用キット |
| EP2184608A1 (en) * | 2007-08-23 | 2010-05-12 | Mitsubishi Chemical Medience Corporation | Non-specific reaction inhibitor |
| JP4571999B1 (ja) | 2009-11-06 | 2010-10-27 | 森永製菓株式会社 | 検体に由来する偽陽性を抑制する方法 |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6777190B1 (en) * | 1991-04-10 | 2004-08-17 | Biosite, Inc. | Crosstalk inhibitors and their uses |
| DE4407423A1 (de) * | 1994-03-05 | 1995-09-07 | Boehringer Mannheim Gmbh | Entstörmittel zum Einsatz bei Immunoassays |
| BR0207290A (pt) | 2001-02-16 | 2005-06-07 | Immunivest Corp | Método para analisar um paciente quanto à presença de uma malignidade, célula maligna isolada das células cultivadas, vacina de tumor, molécula associada com diátese de tumor alterada, métodos para determinar alterações em moléculas associadas com diátese de tumor como um meio para predizer a eficácia da terapia, como um meio para analisar dosagem apropriada para terapia, como um meio para monitorar eficácia da terapia, como um meio para analisar progressão de câncer, para realizar uma biópsia de corpo inteiro em um paciente, e para identificar alterações em uma célula de tumor circulante relativamente a células presentes numa massa de tumor in situ, e, kit de teste para analisar uma amostra de paciente quanto à presença de uma célula maligna não-hematopoiética |
| CN100451651C (zh) * | 2001-03-09 | 2009-01-14 | 株式会社三菱化学药得论 | 测试全血的方法 |
| AU2004318223B8 (en) * | 2004-03-05 | 2009-09-17 | Bio-Rad Laboratories, Inc. | HSV-2 type-specific immunoassays using glycoprotein G2 peptides |
| US7342093B2 (en) | 2004-07-23 | 2008-03-11 | University Of Massachusetts | Compounds that inhibit Hsp90 protein-protein interactions with IAP proteins |
| JP2006177914A (ja) | 2004-12-20 | 2006-07-06 | Yukio Nagasaki | 高分子密生層を有する表面およびその調製方法 |
-
2012
- 2012-06-28 WO PCT/JP2012/066484 patent/WO2013002309A1/ja active Application Filing
- 2012-06-28 CN CN201280032103.5A patent/CN103620407B/zh active Active
- 2012-06-28 EP EP12803782.7A patent/EP2728354B1/en active Active
- 2012-06-28 KR KR1020147001570A patent/KR101988600B1/ko active IP Right Grant
- 2012-06-28 JP JP2013522925A patent/JP5808808B2/ja active Active
- 2012-06-28 US US14/129,510 patent/US11125742B2/en active Active
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5169754A (en) * | 1990-10-31 | 1992-12-08 | Coulter Corporation | Biodegradable particle coatings having a protein covalently immobilized by means of a crosslinking agent and processes for making same |
| JPH06506688A (ja) * | 1991-04-10 | 1994-07-28 | バイオサイト・ダイアグノスティックス・インコーポレイテッド | クロストークインヒビターおよびその使用 |
| JPH08506907A (ja) | 1993-12-21 | 1996-07-23 | ベーリンガー マンハイム ゲーエムベーハー | アシル化タンパク質凝集体および免疫検定における干渉の抑制についてのそれらの使用 |
| JP3027770B2 (ja) | 1994-03-05 | 2000-04-04 | ロシュ ダイアグノスティックス ゲーエムベーハー | イムノアッセイで使用するための干渉除去剤 |
| JP2006308307A (ja) | 2005-04-26 | 2006-11-09 | Toyo Kohan Co Ltd | 生体関連分子の非特異的吸着を阻害する方法および生体関連分子検出用キット |
| EP2184608A1 (en) * | 2007-08-23 | 2010-05-12 | Mitsubishi Chemical Medience Corporation | Non-specific reaction inhibitor |
| JP4571999B1 (ja) | 2009-11-06 | 2010-10-27 | 森永製菓株式会社 | 検体に由来する偽陽性を抑制する方法 |
Non-Patent Citations (1)
| Title |
|---|
| Annals of the New York Academy of Sciences, 2006, Vol. 420, pp 74-89. * |
Also Published As
| Publication number | Publication date |
|---|---|
| EP2728354A1 (en) | 2014-05-07 |
| EP2728354B1 (en) | 2018-06-13 |
| JP5808808B2 (ja) | 2015-11-10 |
| US11125742B2 (en) | 2021-09-21 |
| US20140193842A1 (en) | 2014-07-10 |
| KR101988600B1 (ko) | 2019-06-12 |
| CN103620407A (zh) | 2014-03-05 |
| JPWO2013002309A1 (ja) | 2015-02-23 |
| WO2013002309A1 (ja) | 2013-01-03 |
| CN103620407B (zh) | 2016-09-21 |
| EP2728354A4 (en) | 2015-07-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101988600B1 (ko) | 비특이 반응 억제제, 비특이 반응 억제 방법 및 키트 | |
| US11268956B2 (en) | Method for producing antibody reagent | |
| JP7398366B2 (ja) | 対称性ジメチルアルギニンの検出 | |
| JP4920415B2 (ja) | プローブ複合体 | |
| JP7320492B2 (ja) | B型肝炎ウイルス抗原の免疫測定方法 | |
| US10458981B2 (en) | Three-step acid dissociation enzyme linked immunosorbent (TADELIS) assay | |
| JPH04503109A (ja) | アビジン―ビオチン助力のイムノアッセイ | |
| US11768209B2 (en) | Method and reagent for measuring thyroglobulin | |
| US11543413B2 (en) | Kit and method for quantitative detection of HBsAg | |
| JPS6223823B2 (ko) | ||
| JPH03503566A (ja) | 天然結合タンパク質に対するモノクローナル抗体を用いたイムノアツセイ | |
| JPH11295313A (ja) | 抗体または抗体断片の重合体とその利用 | |
| US5998157A (en) | Acylated protein aggregates and their use as signal enhancers in an immunoassay for the detection of antibodies | |
| Josephson | Immunoenzyme techniques |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal | ||
| E701 | Decision to grant or registration of patent right | ||
| GRNT | Written decision to grant |