KR20140035492A - 열 처리된 헤테로원자 아민 전구체로부터 유도된 연료 전지 응용을 위한 비-pgm 캐소드 촉매 - Google Patents
열 처리된 헤테로원자 아민 전구체로부터 유도된 연료 전지 응용을 위한 비-pgm 캐소드 촉매 Download PDFInfo
- Publication number
- KR20140035492A KR20140035492A KR1020147000718A KR20147000718A KR20140035492A KR 20140035492 A KR20140035492 A KR 20140035492A KR 1020147000718 A KR1020147000718 A KR 1020147000718A KR 20147000718 A KR20147000718 A KR 20147000718A KR 20140035492 A KR20140035492 A KR 20140035492A
- Authority
- KR
- South Korea
- Prior art keywords
- silica
- aapyr
- catalyst
- precursor
- precursors
- Prior art date
Links
- 239000003054 catalyst Substances 0.000 title claims abstract description 186
- 239000002243 precursor Substances 0.000 title claims abstract description 58
- 239000000446 fuel Substances 0.000 title claims description 16
- 150000001412 amines Chemical class 0.000 title description 2
- RLFWWDJHLFCNIJ-UHFFFAOYSA-N 4-aminoantipyrine Chemical compound CN1C(C)=C(N)C(=O)N1C1=CC=CC=C1 RLFWWDJHLFCNIJ-UHFFFAOYSA-N 0.000 claims abstract description 48
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 claims abstract description 30
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 claims abstract description 28
- 229910052799 carbon Inorganic materials 0.000 claims abstract description 17
- 230000003197 catalytic effect Effects 0.000 claims abstract description 16
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 claims abstract description 15
- 229910052757 nitrogen Inorganic materials 0.000 claims abstract description 14
- 229910052742 iron Inorganic materials 0.000 claims abstract description 8
- 238000004519 manufacturing process Methods 0.000 claims abstract description 7
- 150000004032 porphyrins Chemical class 0.000 claims abstract description 6
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 claims description 205
- 239000000377 silicon dioxide Substances 0.000 claims description 89
- 238000000034 method Methods 0.000 claims description 59
- 239000011148 porous material Substances 0.000 claims description 54
- 238000010438 heat treatment Methods 0.000 claims description 52
- 229910052751 metal Inorganic materials 0.000 claims description 52
- 239000002184 metal Substances 0.000 claims description 52
- 239000000463 material Substances 0.000 claims description 35
- 239000010411 electrocatalyst Substances 0.000 claims description 20
- 239000000203 mixture Substances 0.000 claims description 19
- 239000002245 particle Substances 0.000 claims description 17
- 229910052723 transition metal Inorganic materials 0.000 claims description 13
- 150000003624 transition metals Chemical class 0.000 claims description 13
- 239000000843 powder Substances 0.000 claims description 12
- 239000012692 Fe precursor Substances 0.000 claims description 9
- OOOQNKMJLOLMHC-UHFFFAOYSA-N 5-[[3,4-diethyl-5-[[5-formyl-3-(3-hydroxypropyl)-4-methyl-1h-pyrrol-2-yl]methyl]-1h-pyrrol-2-yl]methyl]-4-(3-hydroxypropyl)-3-methyl-1h-pyrrole-2-carbaldehyde Chemical group N1C(CC2=C(C(C)=C(C=O)N2)CCCO)=C(CC)C(CC)=C1CC=1NC(C=O)=C(C)C=1CCCO OOOQNKMJLOLMHC-UHFFFAOYSA-N 0.000 claims description 7
- 238000009826 distribution Methods 0.000 claims description 7
- 238000006243 chemical reaction Methods 0.000 claims description 4
- 230000007246 mechanism Effects 0.000 claims description 4
- 239000003863 metallic catalyst Substances 0.000 claims description 4
- 229910052759 nickel Inorganic materials 0.000 claims description 4
- 229910052802 copper Inorganic materials 0.000 claims description 3
- 229910052721 tungsten Inorganic materials 0.000 claims description 3
- 229910052750 molybdenum Inorganic materials 0.000 claims description 2
- 229910052707 ruthenium Inorganic materials 0.000 claims description 2
- 229910052715 tantalum Inorganic materials 0.000 claims description 2
- 229910052719 titanium Inorganic materials 0.000 claims description 2
- 229910052720 vanadium Inorganic materials 0.000 claims description 2
- 229910052726 zirconium Inorganic materials 0.000 claims description 2
- 230000001376 precipitating effect Effects 0.000 claims 1
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 abstract description 4
- 238000013459 approach Methods 0.000 abstract description 4
- 229920000642 polymer Polymers 0.000 abstract description 3
- GEYOCULIXLDCMW-UHFFFAOYSA-N 1,2-phenylenediamine Chemical compound NC1=CC=CC=C1N GEYOCULIXLDCMW-UHFFFAOYSA-N 0.000 abstract description 2
- NQTADLQHYWFPDB-UHFFFAOYSA-N N-Hydroxysuccinimide Chemical compound ON1C(=O)CCC1=O NQTADLQHYWFPDB-UHFFFAOYSA-N 0.000 abstract description 2
- 238000001878 scanning electron micrograph Methods 0.000 description 66
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 41
- 239000001301 oxygen Substances 0.000 description 41
- 229910052760 oxygen Inorganic materials 0.000 description 41
- 238000006722 reduction reaction Methods 0.000 description 38
- 230000009467 reduction Effects 0.000 description 36
- 239000000243 solution Substances 0.000 description 21
- 238000011068 loading method Methods 0.000 description 20
- 229920006395 saturated elastomer Polymers 0.000 description 19
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 18
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 16
- 238000001075 voltammogram Methods 0.000 description 13
- 210000004027 cell Anatomy 0.000 description 12
- 238000000527 sonication Methods 0.000 description 11
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 10
- 230000000694 effects Effects 0.000 description 9
- MVFCKEFYUDZOCX-UHFFFAOYSA-N iron(2+);dinitrate Chemical compound [Fe+2].[O-][N+]([O-])=O.[O-][N+]([O-])=O MVFCKEFYUDZOCX-UHFFFAOYSA-N 0.000 description 9
- 229910052697 platinum Inorganic materials 0.000 description 8
- 229910000608 Fe(NO3)3.9H2O Inorganic materials 0.000 description 7
- 229910004298 SiO 2 Inorganic materials 0.000 description 7
- 239000002253 acid Substances 0.000 description 7
- 239000007864 aqueous solution Substances 0.000 description 7
- 229910021485 fumed silica Inorganic materials 0.000 description 7
- 238000005470 impregnation Methods 0.000 description 7
- 239000004570 mortar (masonry) Substances 0.000 description 7
- 239000012299 nitrogen atmosphere Substances 0.000 description 7
- 239000007787 solid Substances 0.000 description 7
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 6
- 238000012360 testing method Methods 0.000 description 6
- 239000012298 atmosphere Substances 0.000 description 5
- 239000011572 manganese Substances 0.000 description 5
- 150000002739 metals Chemical class 0.000 description 5
- 230000000877 morphologic effect Effects 0.000 description 5
- PXHVJJICTQNCMI-UHFFFAOYSA-N nickel Substances [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 5
- 229910002848 Pt–Ru Inorganic materials 0.000 description 4
- 239000011651 chromium Substances 0.000 description 4
- PHFQLYPOURZARY-UHFFFAOYSA-N chromium trinitrate Chemical compound [Cr+3].[O-][N+]([O-])=O.[O-][N+]([O-])=O.[O-][N+]([O-])=O PHFQLYPOURZARY-UHFFFAOYSA-N 0.000 description 4
- 239000010949 copper Substances 0.000 description 4
- 239000012528 membrane Substances 0.000 description 4
- 238000012986 modification Methods 0.000 description 4
- 230000004048 modification Effects 0.000 description 4
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- 229910015136 FeMn Inorganic materials 0.000 description 3
- 229910002555 FeNi Inorganic materials 0.000 description 3
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 239000003513 alkali Substances 0.000 description 3
- 238000010586 diagram Methods 0.000 description 3
- 239000001257 hydrogen Substances 0.000 description 3
- 229910052739 hydrogen Inorganic materials 0.000 description 3
- 229910052748 manganese Inorganic materials 0.000 description 3
- 239000010970 precious metal Substances 0.000 description 3
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 2
- 229910002546 FeCo Inorganic materials 0.000 description 2
- -1 Vulcan Chemical compound 0.000 description 2
- 238000002441 X-ray diffraction Methods 0.000 description 2
- CKUAXEQHGKSLHN-UHFFFAOYSA-N [C].[N] Chemical compound [C].[N] CKUAXEQHGKSLHN-UHFFFAOYSA-N 0.000 description 2
- 230000002378 acidificating effect Effects 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 150000001768 cations Chemical class 0.000 description 2
- HSJPMRKMPBAUAU-UHFFFAOYSA-N cerium(3+);trinitrate Chemical compound [Ce+3].[O-][N+]([O-])=O.[O-][N+]([O-])=O.[O-][N+]([O-])=O HSJPMRKMPBAUAU-UHFFFAOYSA-N 0.000 description 2
- 229910052804 chromium Inorganic materials 0.000 description 2
- 230000001788 irregular Effects 0.000 description 2
- 238000002386 leaching Methods 0.000 description 2
- MIVBAHRSNUNMPP-UHFFFAOYSA-N manganese(2+);dinitrate Chemical compound [Mn+2].[O-][N+]([O-])=O.[O-][N+]([O-])=O MIVBAHRSNUNMPP-UHFFFAOYSA-N 0.000 description 2
- 239000002923 metal particle Substances 0.000 description 2
- 230000007935 neutral effect Effects 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 238000000197 pyrolysis Methods 0.000 description 2
- 238000005118 spray pyrolysis Methods 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- OERNJTNJEZOPIA-UHFFFAOYSA-N zirconium nitrate Chemical compound [Zr+4].[O-][N+]([O-])=O.[O-][N+]([O-])=O.[O-][N+]([O-])=O.[O-][N+]([O-])=O OERNJTNJEZOPIA-UHFFFAOYSA-N 0.000 description 2
- PAWQVTBBRAZDMG-UHFFFAOYSA-N 2-(3-bromo-2-fluorophenyl)acetic acid Chemical compound OC(=O)CC1=CC=CC(Br)=C1F PAWQVTBBRAZDMG-UHFFFAOYSA-N 0.000 description 1
- PWHULOQIROXLJO-UHFFFAOYSA-N Manganese Chemical compound [Mn] PWHULOQIROXLJO-UHFFFAOYSA-N 0.000 description 1
- 229910001260 Pt alloy Inorganic materials 0.000 description 1
- 230000010757 Reduction Activity Effects 0.000 description 1
- 229910000929 Ru alloy Inorganic materials 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 239000012670 alkaline solution Substances 0.000 description 1
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 1
- APUPEJJSWDHEBO-UHFFFAOYSA-P ammonium molybdate Chemical compound [NH4+].[NH4+].[O-][Mo]([O-])(=O)=O APUPEJJSWDHEBO-UHFFFAOYSA-P 0.000 description 1
- 239000011609 ammonium molybdate Substances 0.000 description 1
- 229940010552 ammonium molybdate Drugs 0.000 description 1
- 235000018660 ammonium molybdate Nutrition 0.000 description 1
- 238000000429 assembly Methods 0.000 description 1
- 230000000712 assembly Effects 0.000 description 1
- 238000010923 batch production Methods 0.000 description 1
- 239000006229 carbon black Substances 0.000 description 1
- 239000001569 carbon dioxide Substances 0.000 description 1
- 229910002092 carbon dioxide Inorganic materials 0.000 description 1
- 210000000170 cell membrane Anatomy 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 238000003486 chemical etching Methods 0.000 description 1
- 230000000536 complexating effect Effects 0.000 description 1
- 238000011437 continuous method Methods 0.000 description 1
- XTVVROIMIGLXTD-UHFFFAOYSA-N copper(II) nitrate Chemical compound [Cu+2].[O-][N+]([O-])=O.[O-][N+]([O-])=O XTVVROIMIGLXTD-UHFFFAOYSA-N 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 238000000151 deposition Methods 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 238000005530 etching Methods 0.000 description 1
- 125000005842 heteroatom Chemical group 0.000 description 1
- FBAFATDZDUQKNH-UHFFFAOYSA-M iron chloride Chemical compound [Cl-].[Fe] FBAFATDZDUQKNH-UHFFFAOYSA-M 0.000 description 1
- 229910000358 iron sulfate Inorganic materials 0.000 description 1
- BAUYGSIQEAFULO-UHFFFAOYSA-L iron(2+) sulfate (anhydrous) Chemical compound [Fe+2].[O-]S([O-])(=O)=O BAUYGSIQEAFULO-UHFFFAOYSA-L 0.000 description 1
- PVFSDGKDKFSOTB-UHFFFAOYSA-K iron(3+);triacetate Chemical compound [Fe+3].CC([O-])=O.CC([O-])=O.CC([O-])=O PVFSDGKDKFSOTB-UHFFFAOYSA-K 0.000 description 1
- 239000003273 ketjen black Substances 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 150000001247 metal acetylides Chemical class 0.000 description 1
- 229910044991 metal oxide Inorganic materials 0.000 description 1
- 150000004706 metal oxides Chemical class 0.000 description 1
- 239000002090 nanochannel Substances 0.000 description 1
- 239000002105 nanoparticle Substances 0.000 description 1
- 150000004767 nitrides Chemical class 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 150000002978 peroxides Chemical class 0.000 description 1
- CFQCIHVMOFOCGH-UHFFFAOYSA-N platinum ruthenium Chemical compound [Ru].[Pt] CFQCIHVMOFOCGH-UHFFFAOYSA-N 0.000 description 1
- 239000005518 polymer electrolyte Substances 0.000 description 1
- 238000005381 potential energy Methods 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- KWUQLGUXYUKOKE-UHFFFAOYSA-N propan-2-ol;tantalum Chemical compound [Ta].CC(C)O.CC(C)O.CC(C)O.CC(C)O.CC(C)O KWUQLGUXYUKOKE-UHFFFAOYSA-N 0.000 description 1
- 238000012797 qualification Methods 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- YBCAZPLXEGKKFM-UHFFFAOYSA-K ruthenium(iii) chloride Chemical compound [Cl-].[Cl-].[Cl-].[Ru+3] YBCAZPLXEGKKFM-UHFFFAOYSA-K 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 238000005287 template synthesis Methods 0.000 description 1
- 238000007669 thermal treatment Methods 0.000 description 1
- 239000010936 titanium Substances 0.000 description 1
- JMXKSZRRTHPKDL-UHFFFAOYSA-N titanium ethoxide Chemical compound [Ti+4].CC[O-].CC[O-].CC[O-].CC[O-] JMXKSZRRTHPKDL-UHFFFAOYSA-N 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- WFKWXMTUELFFGS-UHFFFAOYSA-N tungsten Chemical compound [W] WFKWXMTUELFFGS-UHFFFAOYSA-N 0.000 description 1
- VLOPEOIIELCUML-UHFFFAOYSA-L vanadium(2+);sulfate Chemical compound [V+2].[O-]S([O-])(=O)=O VLOPEOIIELCUML-UHFFFAOYSA-L 0.000 description 1
- 239000010457 zeolite Substances 0.000 description 1
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/86—Inert electrodes with catalytic activity, e.g. for fuel cells
- H01M4/8647—Inert electrodes with catalytic activity, e.g. for fuel cells consisting of more than one material, e.g. consisting of composites
- H01M4/8652—Inert electrodes with catalytic activity, e.g. for fuel cells consisting of more than one material, e.g. consisting of composites as mixture
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J23/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00
- B01J23/70—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J23/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00
- B01J23/70—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper
- B01J23/76—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper combined with metals, oxides or hydroxides provided for in groups B01J23/02 - B01J23/36
- B01J23/84—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper combined with metals, oxides or hydroxides provided for in groups B01J23/02 - B01J23/36 with arsenic, antimony, bismuth, vanadium, niobium, tantalum, polonium, chromium, molybdenum, tungsten, manganese, technetium or rhenium
- B01J23/889—Manganese, technetium or rhenium
- B01J23/8892—Manganese
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J35/00—Catalysts, in general, characterised by their form or physical properties
- B01J35/30—Catalysts, in general, characterised by their form or physical properties characterised by their physical properties
- B01J35/33—Electric or magnetic properties
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J37/00—Processes, in general, for preparing catalysts; Processes, in general, for activation of catalysts
- B01J37/08—Heat treatment
- B01J37/082—Decomposition and pyrolysis
- B01J37/084—Decomposition of carbon-containing compounds into carbon
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/86—Inert electrodes with catalytic activity, e.g. for fuel cells
- H01M4/8605—Porous electrodes
- H01M4/8621—Porous electrodes containing only metallic or ceramic material, e.g. made by sintering or sputtering
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/86—Inert electrodes with catalytic activity, e.g. for fuel cells
- H01M4/88—Processes of manufacture
- H01M4/8878—Treatment steps after deposition of the catalytic active composition or after shaping of the electrode being free-standing body
- H01M4/8882—Heat treatment, e.g. drying, baking
- H01M4/8885—Sintering or firing
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/86—Inert electrodes with catalytic activity, e.g. for fuel cells
- H01M4/90—Selection of catalytic material
- H01M4/9041—Metals or alloys
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/86—Inert electrodes with catalytic activity, e.g. for fuel cells
- H01M4/90—Selection of catalytic material
- H01M4/9075—Catalytic material supported on carriers, e.g. powder carriers
- H01M4/9083—Catalytic material supported on carriers, e.g. powder carriers on carbon or graphite
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/86—Inert electrodes with catalytic activity, e.g. for fuel cells
- H01M4/90—Selection of catalytic material
- H01M4/9091—Unsupported catalytic particles; loose particulate catalytic materials, e.g. in fluidised state
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/86—Inert electrodes with catalytic activity, e.g. for fuel cells
- H01M2004/8678—Inert electrodes with catalytic activity, e.g. for fuel cells characterised by the polarity
- H01M2004/8689—Positive electrodes
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/30—Hydrogen technology
- Y02E60/50—Fuel cells
Landscapes
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Electrochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Physics & Mathematics (AREA)
- Thermal Sciences (AREA)
- Manufacturing & Machinery (AREA)
- Ceramic Engineering (AREA)
- Composite Materials (AREA)
- Catalysts (AREA)
- Inert Electrodes (AREA)
Abstract
희생 지지체 접근법을 이용하고 질소 및 탄소의 공급원으로서 저렴하고 용이하게 입수가능한 중합체 전구체를 이용하여 M-N-C 촉매를 제조하는 방법이 개시된다. 예시적인 중합체 전구체에는 초기 촉매 활성을 갖지 않는 비-포르피린 전구체가 포함된다. 적합한 비-촉매성 비-포르피린 전구체의 예에는 철과의 착물을 형성하는 저분자량 전구체, 예컨대, 4-아미노안티피린, 페닐렌디아민, 히드록시숙신이미드, 에탄올아민 등이 포함되지만 반드시 이로 한정되는 것은 아니다.
Description
관련 출원과의 상호 참조
하기의 출원은 2011년 6월 15일자로 출원된 미국 가출원 번호 61/497,444, 2012년 3월 2일자로 출원된 미국 가출원 번호 61/606,109, 2012년 4월 6일자로 출원된 61/621084 및 2012년 4월 6일자로 출원된 61/621,095의 이득을 주장하며, 이들 각각은 그의 전문이 본원에 참고로 포함된다.
실행가능한 연료-대체물로서 연료 전지에 대한 주목이 증가되고 있다. 일반적으로, 연료 전지는 환경적으로 청정하고 효율적인 방식으로 전기화학 에너지를 전기 에너지로 변환시킨다. 연료 전지는 소형 전자장치로부터 자동차 및 주택에 이르기까지 모든 것에 대한 잠재적인 에너지 공급원으로서 고려된다. 상이한 에너지 요건을 충족시키기 위하여, 오늘날 다수의 상이한 유형의 연료 전지가 존재하는데, 이들 각각은 다양한 화학적 성질, 요건, 및 용도를 갖는다.
한 예로서, 직접 메탄올 연료 전지 (DMFC)는 전기촉매(electrocatalyst) 층 상에서 메탄올을 산화시켜 이산화탄소를 형성하는 것을 이용한다. 물이 애노드에서 소비되고 캐소드에서 생성된다. 양이온 (H+)이 양성자 교환막을 가로질러 캐소드로 수송되며, 여기서 이들이 산소와 반응하여 물을 생성한다. 이어서, 전자가 외부 회로를 거쳐 애노드로부터 캐소드로 수송되어 전력을 외부 공급원에 제공할 수 있다.
또 다른 예로서, 중합체 전해질 막 (PEM) 연료 전지 (양성자 교환막 연료 전지라고도 불림)는 연료로서 (전형적으로 수소 탱크에 의해 공급되는) 순수한 수소를 사용한다. 수소의 스트림이 막-전극 조립체 (MEA)의 애노드 측으로 전달되며, 여기서 이는 양성자와 전자로 촉매적으로 분열된다. DMFC에서와 같이, 양이온은 양성자 교환막을 가로질러 캐소드로 수송되며, 여기서 이들은 산소와 반응하여 물을 생성한다.
현재, PEM 및 DMFC 연료 전지의 넓은 규모의 상업화에서의 제한 인자 중 하나는 귀금속과 관련된 비용이다. DMFC 및 PEM 연료 전지 둘 다는 전기촉매로서 백금을 통상 사용한다. 백금과 같은 귀금속은 캐소드에서의 느린 산소 환원 반응 (ORR)을 촉매하는 데 필요로 한다. 이러한 제한을 극복하는 주요 경로 중 하나는 귀금속계 전기촉매에서의 백금 이용률을 증가시키는 것이다. 또 다른 실행가능한 경로는 덜 비싸면서도 여전히 충분히 활성인 촉매를 대량으로 사용하는 것이다. 몇몇 부류의 비-백금 전기촉매가 시판 연료 전지 응용에서 잠재적인 전기촉매로서 고려되기에 적절한 산소 환원 활성을 갖는 것으로 확인되어 있다.
일반적으로, 공지된 비-백금 전기촉매는 고 표면적 카본 블랙 상에 지지된다. 이는 분산, 활성 표면적, 및 촉매 층의 전도도를 증가시키기 위해 행해진다. 합성 절차는 지지 기재에 대한 전구체 분자의 침전 및 지지된 전구체의 열분해를 통상 포함한다.
M-N-C 촉매는 연료 전지 막 전극 조립체 (MEA), 적층체(stack) 및 연료 전지 시스템에서 전기화학 산소 환원 응용에 있어 매우 유망한 것으로 밝혀졌다. 이들 물질의 중요한 측면은 금속 입자, 공액된 탄소-질소-산화물-금속 네트워크, 및 질소-결합된 탄소의 존재를 포함한다. 금속 상(metallic phase)은 금속의 산화물, 탄화물, 질화물, 및 이들 상태의 혼합물을 포함한다. N/C/M 네트워크 및 N/C 네트워크의 화학적 상태 및 결합은 성능에 영향을 주며, 예를 들어 증가된 전체 질소 함량은 ORR 성능을 개선한다. 그러나, 이들 시스템은 여전히 하기를 포함한 몇 가지 상당한 결점을 안고 있다: 산성 환경에서의 낮은 안정성, 산 및 알칼리 환경에서의 낮은 내구성, 질소 전구체의 높은 비용 및 백금과 비교하여 ORR에서의 낮은 활성. 산에서의 낮은 안정성의 문제는 탄소-질소 네트워크로부터의 금속의 침출과 연관된다. 산 및 알칼리 용액 중에서의 낮은 내구성은 이들 환경에서의 상당한 양의 H2O2의 방출에 의해 설명되는데, 이는 금속 및 탄소-질소 네트워크 둘 다에 대해 부식성이다. 낮은 활성은 가능하게는 낮은 금속 로딩에 기인하며, 그러한 촉매에서의 활성 부위의 낮은 농도에서의 결과로서 외부 탄소 공급원 (불칸(Vulcan), 케첸블랙(KetjenBlack)과 같은 고 표면적 탄소)을 사용하는 것에 기인한다.
상기에서 확인된 문제들 중 다수를 극복한 비지지된 M-N-C 촉매를 합성하기 위한 앞서 기재된 열분해-기반 방법은 실리카와 같은 희생 지지체 상에 약간의 초기 촉매 활성을 갖는 것으로 알려진 질소 및 탄소 함유 포르피린을 템플레이팅하고, 템플레이팅된 지지체를 열분해하고, 이어서, 예를 들어 에칭을 통해 지지체를 제거하는 것을 포함하였다. 예를 들어, 2010년 3월 15일자로 허여된 미국 특허 번호 7,678,728를 참조하며, 이는 본원에 참고로 포함된다.
M-N-C 시스템은 산소 환원 반응 (ORR)을 위한 공지된 촉매이다. 그러나, 이들은 하기를 포함한 다수의 상당한 단점을 갖는다: 산 매질에서의 낮은 안정성, 종래의 ORR 촉매 (백금)와 비교하여 낮은 활성, 및 전구체의 높은 비용. 본원에는, 희생 지지체 접근법을 이용하고 저렴하고 용이하게 입수가능한 중합체 전구체를 사용하여 M-N-C 촉매를 제조하는 방법이 기재된다. 이러한 접근법을 사용하여 제조된 합성 촉매는 알칼리 및 산 매질 둘 다의 매질 중에서 잘 기능하며, 고도로 내구성이며, 제조 비용이 저렴하다.
도 1은 본원에 기재된 바와 같이 제조된 Fe-M-C 촉매의 X선 회절도이다.
도 2는 본원에 기재된 방법을 사용하여 제조된 Fe-AAPyr 촉매의 SEM 이미지이다.
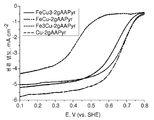
도 3은 본원에 기재된 방법을 사용하여 제조된 Fe-AAPyr 촉매에 대한 산소 환원을 보여주는 회전 디스크 전극(Rotating Disc Electrode) 전압전류곡선(electro-voltamogram)이다.
도 4는 다양한 열 처리 온도로 제조된 Fe-AAPyr 촉매에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다.
도 5는 본원에 기재된 바와 같이 제조된 다양한 Fe-AAPyr 촉매에 대한 ORR에 참여한 전자수의 그래프이다.
도 6은 본원에 기재된 바와 같이 제조된 다양한 Fe-AAPyr 촉매에 대한 과산화수소 수율의 그래프이다.
도 7은 본원에 기재된 바와 같이 제조된 Fe-AAPyr 촉매에 대한 ORR에 참여한 전자수의 그래프이다.
도 8은 본원에 기재된 바와 같이 제조된 다양한 Fe-AAPyr 촉매에 대한 과산화수소 수율의 그래프이다.
도 9는 본원에 기재된 바와 같이 멀티모달 세공 크기 분포를 갖는 촉매의 제조 방법의 개략도이다.
도 10a는 Fe-AAPyr 및 HS5 실리카로부터 유도된 모노-모달 촉매의 SEM 이미지이며, 이때 스케일 바는 500 nm이다.
도 10b는 Fe-AAPyr 및 HS5 실리카로부터 유도된 모노-모달 촉매의 SEM 이미지이며, 이때 스케일 바는 300 nm이다.
도 11a는 Fe-AAPyr 및 M5 실리카로부터 유도된 바이-모달 촉매의 SEM 이미지이며, 이때 스케일 바는 500 nm이다.
도 11b는 Fe-AAPyr 및 M5 실리카로부터 유도된 바이-모달 촉매의 SEM 이미지이며, 이때 스케일 바는 300 nm이다.
도 12a는 Fe-AAPyr 및 LM130 실리카로부터 유도된 바이-모달 촉매의 SEM 이미지이며, 이때 스케일 바는 500 nm이다.
도 12b는 Fe-AAPyr 및 LM130 실리카로부터 유도된 바이-모달 촉매의 SEM 이미지이며, 이때 스케일 바는 300 nm이다.
도 13a는 Fe-AAPyr 및 A90 실리카로부터 유도된 촉매의 SEM 이미지이며, 이때 스케일 바는 500 nm이다.
도 13b는 Fe-AAPyr 및 A90 실리카로부터 유도된 촉매의 SEM 이미지이며, 이때 스케일 바는 300 nm이다.
도 14는 Fe-AAPyr 및 L90과 A90 실리카의 혼합물로부터 유도된 바이-모달 촉매의 SEM 이미지이다.
도 15a는 Fe-AAPyr 및 L90과 EH5 실리카의 혼합물로부터 유도된 트리-모달 촉매의 SEM 이미지이며, 이때 스케일 바는 500 nm이다.
도 15b는 Fe-AAPyr 및 L90과 EH5 실리카의 혼합물로부터 유도된 트리-모달 촉매의 SEM 이미지이며, 이때 스케일 바는 400 nm이다.
도 15c는 Fe-AAPyr 및 L90과 EH5 실리카의 혼합물로부터 유도된 트리-모달 촉매의 SEM 이미지이며, 이때 스케일 바는 300 nm이다.
도 16은 Fe-AAPyr 및 L90과 M5 실리카의 혼합물로부터 유도된 바이-모달 촉매의 SEM 이미지이며, 이때 스케일 바는 500 nm이다.
도 17은 Fe-AAPyr 및 L90과 LM130 실리카의 혼합물로부터 유도된 바이-모달 촉매의 SEM 이미지이며, 이때 스케일 바는 500 nm이다.
도 18은 Fe-AAPyr 및 L90과 A200 실리카의 혼합물로부터 유도된 바이-모달 촉매의 SEM 이미지이다.
도 19는 Fe-AAPy 및 L90과 A380 실리카의 혼합물로부터 유도된 바이-모달 촉매의 SEM 이미지이다.
도 20a는 Fe-AAPyr 및 M5 실리카로부터 유도된 구형 촉매의 SEM 이미지이다.
도 20b는 Fe-AAPyr 및 M5 실리카로부터 유도된 구형 촉매의 또 다른 SEM 이미지이다.
도 20c는 Fe-AAPyr 및 M5 실리카로부터 유도된 구형 촉매의 또 다른 SEM 이미지이다.
도 20e는 Fe-AAPyr 및 M5 실리카로부터 유도된 구형 촉매의 또 다른 SEM 이미지이다.
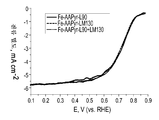
도 21은 Fe-AAPyr 및 HS5, L90 및 L90 + EH5 실리카로부터 제조된 촉매에 대한 RDE 데이터에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다.
도 22는 Fe-AAPyr 및 L90, LM130, 및 L90 + LM130 실리카로부터 제조된 촉매에 대한 RDE 데이터에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다.
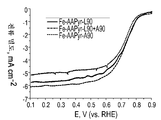
도 23은 Fe-AAPyr 및 L90, L90 + A90, 및 A90 실리카로부터 제조된 촉매에 대한 RDE 데이터에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다.
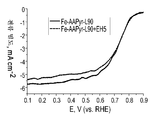
도 24는 Fe-AAPyr 및 L90 및 L90 + EH5 실리카로부터 제조된 촉매에 대한 RDE 데이터에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다.
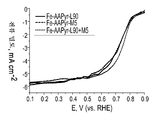
도 25는 Fe-AAPyr 및 L90, M5 및 L90 + M5 실리카로부터 제조된 촉매에 대한 RDE 데이터에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다.
도 26은 본원에 기재된 방법을 사용하여 제조된 Fe3Co-AAPyr 촉매의 SEM 이미지이다.
도 27은 본원에 기재된 방법을 사용하여 제조된 FeCo-AAPyr 촉매의 SEM 이미지이다.
도 28은 본원에 기재된 방법을 사용하여 제조된 FeCo3-AAPyr 촉매의 SEM 이미지이다.
도 29a는 본원에 기재된 방법을 사용하여 제조된 FeCu3-AAPyr 2원-금속(bi-metallic) 촉매의 SEM 이미지이다.
도 29b는 본원에 기재된 방법을 사용하여 제조된 FeCu3-AAPyr 2원-금속 촉매의 또 다른 SEM 이미지이다.
도 30a는 본원에 기재된 방법을 사용하여 제조된 FeMn3-AAPyr 2원-금속 촉매의 SEM 이미지이다.
도 30b는 본원에 기재된 방법을 사용하여 제조된 FeMn3-AAPyr 2원-금속 촉매의 또 다른 SEM 이미지이다.
도 31a는 본원에 기재된 방법을 사용하여 제조된 FeNi3-AAPyr 2원-금속 촉매의 SEM 이미지이다.
도 31b는 본원에 기재된 방법을 사용하여 제조된 FeNi3-AAPyr 2원-금속 촉매의 또 다른 SEM 이미지이다.
도 32a는 본원에 기재된 방법을 사용하여 제조된 FeCoCu-AAPyr 3원-금속(tri-metallic) 촉매의 SEM 이미지이다.
도 32b는 본원에 기재된 방법을 사용하여 제조된 FeCoCu-AAPyr 3원-금속 촉매의 또 다른 SEM 이미지이다.
도 33a는 본원에 기재된 방법을 사용하여 제조된 FeCoMn-AAPyr 3원-금속 촉매의 SEM 이미지이다.
도 33b는 본원에 기재된 방법을 사용하여 제조된 FeCoMn-AAPyr 3원-금속 촉매의 또 다른 SEM 이미지이다.
도 34a는 본원에 기재된 방법을 사용하여 제조된 FeCuMn-AAPyr 3원-금속 촉매의 SEM 이미지이다.
도 34b는 본원에 기재된 방법을 사용하여 제조된 FeCuMn-AAPyr 3원-금속 촉매의 또 다른 SEM 이미지이다.
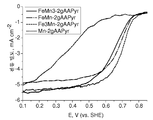
도 35는 Co-AAPyr에 대비하여 FexCoy-AAPyr 2원-금속 촉매에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다.
도 36은 Ni-AAPyr에 대비하여 FexNiy-AAPyr 2원-금속 촉매에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다.
도 37은 Cu-AAPyr에 대비하여 FexCuy-AAPyr 2원-금속 촉매에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다.
도 38은 Cr-AAPyr에 대비하여 FexCry-AAPyr 2원-금속 촉매에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다.
도 39는 Mn-AAPyr에 대비하여 FexMny-AAPyr 2원-금속 촉매에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다.
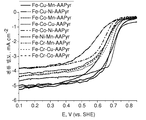
도 40은 FeMIMII-AAPyr 3원-금속 촉매에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다.
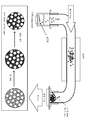
도 41은 본원에 따라 M-N-C 촉매를 제조하기 위한 회분식(batch-wise) 공정의 개략도이다.
도 42a는 저 표면적 실리카 상에 제조된 고도로 다공성인 구형 Fe-N-C 촉매의 SEM 이미지이며, 이때 스케일 바는 10 μm이다.
도 42b는 저 표면적 실리카 상에 제조된 고도로 다공성인 구형 Fe-N-C 촉매의 SEM 이미지이며, 이때 스케일 바는 2 μm이다.
도 42c는 저 표면적 실리카 상에 제조된 고도로 다공성인 구형 Fe-N-C 촉매의 SEM 이미지이며, 이때 스케일 바는 1 μm이다.
도 42d는 저 표면적 실리카 상에 제조된 고도로 다공성인 구형 Fe-N-C 촉매의 SEM 이미지이며, 이때 스케일 바는 500 nm이다.
도 43a는 고 표면적 실리카 상에 제조된 고도로 다공성인 구형 Fe-N-C 촉매의 제1 배치의 SEM 이미지이며, 이때 스케일 바는 5 μm이다.
도 43b는 고 표면적 실리카 상에 제조된 고도로 다공성인 구형 Fe-N-C 촉매의 제1 배치의 SEM 이미지이며, 이때 스케일 바는 2 μm이다.
도 43c는 고 표면적 실리카 상에 제조된 고도로 다공성인 구형 Fe-N-C 촉매의 제1 배치의 SEM 이미지이며, 이때 스케일 바는 500 nm이다.
도 44a는 고 표면적 실리카 상에 제조된 고도로 다공성인 구형 Fe-N-C 촉매의 제2 배치의 SEM 이미지이며, 이때 스케일 바는 3 μm이다.
도 44b는 고 표면적 실리카 상에 제조된 고도로 다공성인 구형 Fe-N-C 촉매의 제2 배치의 SEM 이미지이며, 이때 스케일 바는 2 μm이다.
도 45는 O2로 포화된 0.5M H2SO4 중에서의 본원에 기재된 방법에 의해 제조된 구형 F-N-C 촉매에 대한 RDE 데이터에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다 (촉매 로딩: 600 μg cm-2, 1200 RPM, 5 mV s-1).
도 2는 본원에 기재된 방법을 사용하여 제조된 Fe-AAPyr 촉매의 SEM 이미지이다.
도 3은 본원에 기재된 방법을 사용하여 제조된 Fe-AAPyr 촉매에 대한 산소 환원을 보여주는 회전 디스크 전극(Rotating Disc Electrode) 전압전류곡선(electro-voltamogram)이다.
도 4는 다양한 열 처리 온도로 제조된 Fe-AAPyr 촉매에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다.
도 5는 본원에 기재된 바와 같이 제조된 다양한 Fe-AAPyr 촉매에 대한 ORR에 참여한 전자수의 그래프이다.
도 6은 본원에 기재된 바와 같이 제조된 다양한 Fe-AAPyr 촉매에 대한 과산화수소 수율의 그래프이다.
도 7은 본원에 기재된 바와 같이 제조된 Fe-AAPyr 촉매에 대한 ORR에 참여한 전자수의 그래프이다.
도 8은 본원에 기재된 바와 같이 제조된 다양한 Fe-AAPyr 촉매에 대한 과산화수소 수율의 그래프이다.
도 9는 본원에 기재된 바와 같이 멀티모달 세공 크기 분포를 갖는 촉매의 제조 방법의 개략도이다.
도 10a는 Fe-AAPyr 및 HS5 실리카로부터 유도된 모노-모달 촉매의 SEM 이미지이며, 이때 스케일 바는 500 nm이다.
도 10b는 Fe-AAPyr 및 HS5 실리카로부터 유도된 모노-모달 촉매의 SEM 이미지이며, 이때 스케일 바는 300 nm이다.
도 11a는 Fe-AAPyr 및 M5 실리카로부터 유도된 바이-모달 촉매의 SEM 이미지이며, 이때 스케일 바는 500 nm이다.
도 11b는 Fe-AAPyr 및 M5 실리카로부터 유도된 바이-모달 촉매의 SEM 이미지이며, 이때 스케일 바는 300 nm이다.
도 12a는 Fe-AAPyr 및 LM130 실리카로부터 유도된 바이-모달 촉매의 SEM 이미지이며, 이때 스케일 바는 500 nm이다.
도 12b는 Fe-AAPyr 및 LM130 실리카로부터 유도된 바이-모달 촉매의 SEM 이미지이며, 이때 스케일 바는 300 nm이다.
도 13a는 Fe-AAPyr 및 A90 실리카로부터 유도된 촉매의 SEM 이미지이며, 이때 스케일 바는 500 nm이다.
도 13b는 Fe-AAPyr 및 A90 실리카로부터 유도된 촉매의 SEM 이미지이며, 이때 스케일 바는 300 nm이다.
도 14는 Fe-AAPyr 및 L90과 A90 실리카의 혼합물로부터 유도된 바이-모달 촉매의 SEM 이미지이다.
도 15a는 Fe-AAPyr 및 L90과 EH5 실리카의 혼합물로부터 유도된 트리-모달 촉매의 SEM 이미지이며, 이때 스케일 바는 500 nm이다.
도 15b는 Fe-AAPyr 및 L90과 EH5 실리카의 혼합물로부터 유도된 트리-모달 촉매의 SEM 이미지이며, 이때 스케일 바는 400 nm이다.
도 15c는 Fe-AAPyr 및 L90과 EH5 실리카의 혼합물로부터 유도된 트리-모달 촉매의 SEM 이미지이며, 이때 스케일 바는 300 nm이다.
도 16은 Fe-AAPyr 및 L90과 M5 실리카의 혼합물로부터 유도된 바이-모달 촉매의 SEM 이미지이며, 이때 스케일 바는 500 nm이다.
도 17은 Fe-AAPyr 및 L90과 LM130 실리카의 혼합물로부터 유도된 바이-모달 촉매의 SEM 이미지이며, 이때 스케일 바는 500 nm이다.
도 18은 Fe-AAPyr 및 L90과 A200 실리카의 혼합물로부터 유도된 바이-모달 촉매의 SEM 이미지이다.
도 19는 Fe-AAPy 및 L90과 A380 실리카의 혼합물로부터 유도된 바이-모달 촉매의 SEM 이미지이다.
도 20a는 Fe-AAPyr 및 M5 실리카로부터 유도된 구형 촉매의 SEM 이미지이다.
도 20b는 Fe-AAPyr 및 M5 실리카로부터 유도된 구형 촉매의 또 다른 SEM 이미지이다.
도 20c는 Fe-AAPyr 및 M5 실리카로부터 유도된 구형 촉매의 또 다른 SEM 이미지이다.
도 20e는 Fe-AAPyr 및 M5 실리카로부터 유도된 구형 촉매의 또 다른 SEM 이미지이다.
도 21은 Fe-AAPyr 및 HS5, L90 및 L90 + EH5 실리카로부터 제조된 촉매에 대한 RDE 데이터에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다.
도 22는 Fe-AAPyr 및 L90, LM130, 및 L90 + LM130 실리카로부터 제조된 촉매에 대한 RDE 데이터에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다.
도 23은 Fe-AAPyr 및 L90, L90 + A90, 및 A90 실리카로부터 제조된 촉매에 대한 RDE 데이터에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다.
도 24는 Fe-AAPyr 및 L90 및 L90 + EH5 실리카로부터 제조된 촉매에 대한 RDE 데이터에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다.
도 25는 Fe-AAPyr 및 L90, M5 및 L90 + M5 실리카로부터 제조된 촉매에 대한 RDE 데이터에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다.
도 26은 본원에 기재된 방법을 사용하여 제조된 Fe3Co-AAPyr 촉매의 SEM 이미지이다.
도 27은 본원에 기재된 방법을 사용하여 제조된 FeCo-AAPyr 촉매의 SEM 이미지이다.
도 28은 본원에 기재된 방법을 사용하여 제조된 FeCo3-AAPyr 촉매의 SEM 이미지이다.
도 29a는 본원에 기재된 방법을 사용하여 제조된 FeCu3-AAPyr 2원-금속(bi-metallic) 촉매의 SEM 이미지이다.
도 29b는 본원에 기재된 방법을 사용하여 제조된 FeCu3-AAPyr 2원-금속 촉매의 또 다른 SEM 이미지이다.
도 30a는 본원에 기재된 방법을 사용하여 제조된 FeMn3-AAPyr 2원-금속 촉매의 SEM 이미지이다.
도 30b는 본원에 기재된 방법을 사용하여 제조된 FeMn3-AAPyr 2원-금속 촉매의 또 다른 SEM 이미지이다.
도 31a는 본원에 기재된 방법을 사용하여 제조된 FeNi3-AAPyr 2원-금속 촉매의 SEM 이미지이다.
도 31b는 본원에 기재된 방법을 사용하여 제조된 FeNi3-AAPyr 2원-금속 촉매의 또 다른 SEM 이미지이다.
도 32a는 본원에 기재된 방법을 사용하여 제조된 FeCoCu-AAPyr 3원-금속(tri-metallic) 촉매의 SEM 이미지이다.
도 32b는 본원에 기재된 방법을 사용하여 제조된 FeCoCu-AAPyr 3원-금속 촉매의 또 다른 SEM 이미지이다.
도 33a는 본원에 기재된 방법을 사용하여 제조된 FeCoMn-AAPyr 3원-금속 촉매의 SEM 이미지이다.
도 33b는 본원에 기재된 방법을 사용하여 제조된 FeCoMn-AAPyr 3원-금속 촉매의 또 다른 SEM 이미지이다.
도 34a는 본원에 기재된 방법을 사용하여 제조된 FeCuMn-AAPyr 3원-금속 촉매의 SEM 이미지이다.
도 34b는 본원에 기재된 방법을 사용하여 제조된 FeCuMn-AAPyr 3원-금속 촉매의 또 다른 SEM 이미지이다.
도 35는 Co-AAPyr에 대비하여 FexCoy-AAPyr 2원-금속 촉매에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다.
도 36은 Ni-AAPyr에 대비하여 FexNiy-AAPyr 2원-금속 촉매에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다.
도 37은 Cu-AAPyr에 대비하여 FexCuy-AAPyr 2원-금속 촉매에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다.
도 38은 Cr-AAPyr에 대비하여 FexCry-AAPyr 2원-금속 촉매에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다.
도 39는 Mn-AAPyr에 대비하여 FexMny-AAPyr 2원-금속 촉매에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다.
도 40은 FeMIMII-AAPyr 3원-금속 촉매에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다.
도 41은 본원에 따라 M-N-C 촉매를 제조하기 위한 회분식(batch-wise) 공정의 개략도이다.
도 42a는 저 표면적 실리카 상에 제조된 고도로 다공성인 구형 Fe-N-C 촉매의 SEM 이미지이며, 이때 스케일 바는 10 μm이다.
도 42b는 저 표면적 실리카 상에 제조된 고도로 다공성인 구형 Fe-N-C 촉매의 SEM 이미지이며, 이때 스케일 바는 2 μm이다.
도 42c는 저 표면적 실리카 상에 제조된 고도로 다공성인 구형 Fe-N-C 촉매의 SEM 이미지이며, 이때 스케일 바는 1 μm이다.
도 42d는 저 표면적 실리카 상에 제조된 고도로 다공성인 구형 Fe-N-C 촉매의 SEM 이미지이며, 이때 스케일 바는 500 nm이다.
도 43a는 고 표면적 실리카 상에 제조된 고도로 다공성인 구형 Fe-N-C 촉매의 제1 배치의 SEM 이미지이며, 이때 스케일 바는 5 μm이다.
도 43b는 고 표면적 실리카 상에 제조된 고도로 다공성인 구형 Fe-N-C 촉매의 제1 배치의 SEM 이미지이며, 이때 스케일 바는 2 μm이다.
도 43c는 고 표면적 실리카 상에 제조된 고도로 다공성인 구형 Fe-N-C 촉매의 제1 배치의 SEM 이미지이며, 이때 스케일 바는 500 nm이다.
도 44a는 고 표면적 실리카 상에 제조된 고도로 다공성인 구형 Fe-N-C 촉매의 제2 배치의 SEM 이미지이며, 이때 스케일 바는 3 μm이다.
도 44b는 고 표면적 실리카 상에 제조된 고도로 다공성인 구형 Fe-N-C 촉매의 제2 배치의 SEM 이미지이며, 이때 스케일 바는 2 μm이다.
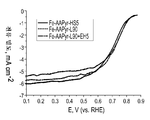
도 45는 O2로 포화된 0.5M H2SO4 중에서의 본원에 기재된 방법에 의해 제조된 구형 F-N-C 촉매에 대한 RDE 데이터에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다 (촉매 로딩: 600 μg cm-2, 1200 RPM, 5 mV s-1).
상세한 설명
한 실시양태에 따르면, 본원은 신규한 촉매 및 그의 제조 방법을 제공한다. M-N-C 촉매를 형성하기 위한 앞서 기재된 방법에서, 질소 및 탄소의 공급원은 전형적으로 초기 촉매 활성을 갖는 포르피린 전구체이다. 이러한 초기 촉매 활성은 이의 금속 입자와의 착물 형성(complexing)시에 개선된다. 본원은 질소 및 탄소의 공급원으로서 초기 촉매 활성을 갖지 않는 비-포르피린 전구체를 사용함으로써 M-N-C 촉매가 합성될 수 있다는 놀랍고도 예기치 않은 발견에 의지한다. 적합한 비-촉매성 비-포르피린 전구체의 예에는 철과의 착물을 형성하는 저분자량 전구체 (예컨대, 4-아미노안티피린, 페닐렌디아민, 히드록시숙신이미드, 에탄올아민 등)이 포함되지만 반드시 이로 한정되는 것은 아니다. 일부 실시양태에 따르면, 비-촉매성 전구체는 철과 착물을 형성할 수 있는 그들의 능력으로 인해 선택될 수 있다. 또 다른 실시양태에 따르면, 비-촉매성 전구체는, 이들이 초기 촉매 활성을 갖는 전구체 내의 활성 부위와 동일하거나 유사한 모이어티(moiety)를 함유하기 때문에 선택될 수 있는데, 이어서 이의 결정 구조는 고온 열 처리에 의해 안정화된다.
한 실시양태에 따르면, 본원에 따른 M-N-C 촉매는 질산철 형태의 철 전구체 및 4-아미노안티피린 (AAPyr) 형태의 C-N 전구체를 발연 실리카의 희생 지지체의 표면 상에 습식 함침시킴으로써 제조될 수 있다. 다른 적합한 철 전구체에는 황산철, 아세트산철, 염화철 등이 포함되지만 이로 한정되는 것은 아니다.
다른 전이 금속, 예컨대 Ce, Cr, Cu Mo, Ni, Ru, Ta, Ti, V, W 및 Zr이, 단순히 그 대신 그러한 금속의 전구체를 사용함으로써, 철 대신 사용될 수 있다는 것을 이해할 것이다. 예시적인 전이 금속 전구체에는 질산세륨, 질산크로뮴, 질산구리, 몰리브데넘산암모늄, 질산니켈, 염화루테늄, 탄탈럼 이소프로폭시드, 티타늄 에톡시드, 황산바나듐, 텅스텐산암모늄 및 질산지르코늄이 포함되지만 이로 한정되는 것은 아니다. 더욱이, 일부 실시양태에 따르면, 그리고 하기에 더 상세히 기재된 바와 같이, 본원에 기재된 방법은 둘 이상의 금속의 전구체를 이용하여 다중-금속(multi-metallic) 촉매를 생성할 수 있다.
적합한 희생 지지체에는 실리카, 제올라이트, 알루미나 등이 포함되지만 이로 한정되는 것은 아니다. 지지체는 구체, 입자, 또는 다른 2차원 또는 3차원적 규칙, 불규칙, 또는 무정형 형상의 형태를 취할 수 있다. 구체, 입자, 또는 다른 형상은 단분산이거나, 또는 불규칙한 크기를 가질 수 있다. 구체, 입자, 또는 다른 형상은 세공을 가질 수 있거나 가질 수 없으며, 그러한 세공은 동일하거나 상이한 크기 및 형상을 가질 수 있다.
하기에 더 상세히 기재된 바와 같이, 실리카 입자의 크기 및 형상은 전기촉매 물질 내의 공극의 원하는 형상(들) 및 크기(들)에 따라 선택될 수 있다는 것을 이해해야 한다. 따라서, 실리카 입자의 특정 크기 및 형상을 선택함으로써, 예측가능한 크기 및 형상의 공극을 갖는 전기촉매를 생성할 수 있다. 예를 들어, 실리카 입자가 구체일 경우, 전기촉매는 복수의 구형 공극을 함유할 것이다. 당업자는 복수의 백금-루테늄 합금 구체로 이루어진 전기촉매 Pt-Ru 블랙에 친숙할 것이다. 상기에 기재된 방법으로 실리카 구체를 사용하여 형성된 전기촉매는 Pt-Ru 블랙의 네거티브 이미지처럼 보이는데; Pt-Ru 블랙 내에 공극으로서 존재했던 공간은 금속 전기촉매로 충전되고, Pt-Ru 블랙 내에 금속 전기촉매로서 존재했던 공간은 공극이다.
상기에 기재된 바와 같이, 일부 실시양태에 따르면, 임의의 직경의 실리카 구체가 사용될 수 있다. 일부 바람직한 실시양태에서는, 특성 길이가 1 nm 내지 100 nm인 실리카 입자, 보다 바람직한 실시양태에서는, 특성 길이가 100 nm 내지 1000 nm인 실리카 입자가 사용될 수 있으며, 다른 바람직한 실시양태에서는, 특성 길이가 1 mm 내지 10 mm인 실리카 입자가 사용될 수 있다. 추가로, 메조다공성 실리카가 또한 템플레이팅 합성 접근법에 사용될 수 있다. 이 경우에, 템플레이팅은 물질의 메조세공들을 삽입하는 것을 포함하며, 그 결과 다공도가 2 내지 20 nm 범위인 자기-지지된 전기촉매가 생성된다. 한 특정 실시양태에서, 실리카 템플레이트는 캅오실(Cabosil) 무정형 발연 실리카 (325 m2/g)이다. 상기에 기재된 바와 같이, 구체는 전기촉매의 형성을 위한 템플레이트로서의 역할을 하기 때문에, 평균 직경이 20 nm인 실리카 입자가 사용되는 실시양태에서, 전기촉매 내의 구형 공극은 전형적으로 대략 20 nm의 직경을 가질 것이다. 당업자는 구매가능한 다양한 실리카 입자에 친숙할 것이며, 그러한 입자가 사용될 수 있다. 대안적으로, 원하는 형상 및/또는 크기의 입자를 수득하기 위해 실리카 입자를 형성하는 공지된 방법이 사용될 수 있다.
C-N 전구체 및 금속 전구체를 희생 지지체 상에 침적 및/또는 함침시킨 후에, 촉매는 N2, Ar 또는 He와 같은 불활성 분위기 내에서, 또는 NH3 또는 아세토니트릴과 같은 반응성 분위기 내에서 열 처리된다. C-N 전구체에 질소가 풍부한 경우에는 불활성 분위기가 전형적으로 사용되는데, 이는 불활성 분위기는 Fe (또는 다른 금속) N4 중심을 갖는 활성 부위를 많이 생성할 수 있게 하기 때문이다. 그러나, C-N 전구체에 탄소가 풍부하고 질소가 결핍된 경우에는 질소 풍부 분위기를 사용하도록 요구될 수 있는데, 이는 질소 풍부 분위기는 Fe (또는 다른 금속) N4 중심의 생성을 가능하게 할 것이기 때문이다.
한 실시양태에 따르면, 열 처리를 위한 최적 온도는 500 내지 1100℃이다. 일부 실시양태에 따르면, 800 내지 900℃의 열 처리가 바람직한데, 이는 이 온도는 물질을 열분해시키기에는 충분히 높지만 전형적으로 활성 부위를 파괴시키기에는 충분히 높지 않기 때문이다.
열 처리 후에는, 적합한 수단을 사용하여 희생 지지체를 제거한다. 예를 들어, 희생 지지체는 화학적 에칭을 통해 제거될 수 있다. 적합한 에천트(etchant)의 예에는 NaOH, KOH, 및 HF가 포함된다. 일부 실시양태에 따르면, KOH를 사용하는 것이 바람직할 수 있는데, 이는 그것이 촉매 내의 모든 금속 및 금속 산화물을 보존하기 때문이며, 이들 종이 촉매 활성일 경우, KOH의 사용은 실제로 촉매 활성을 증가시킬 수 있기 때문이다. 대안적으로, 일부 실시양태에서는, HF가 바람직할 수 있는데, 이는 그것이 매우 공격적이며 촉매의 표면으로부터 일부 독성 종을 제거하는 데 사용될 수 있기 때문이다. 따라서, 당업자는 형성되는 특정 촉매 물질의 특정 요건에 기초하여 원하는 에천트를 선택할 수 있을 것이다.
구체적인 예시적 실시양태에 따르면, 철 전구체 및 아미노안티피린 전구체를 발연 실리카 (캅-오-실(Cab-O-Sil)™ EH-5, 표면적: 약 400 m2 g-1)의 표면 상에 습식 함침시킴으로써 Fe-AAPyr 촉매를 제조하였다. 먼저, 1 g의 실리카를 소노배쓰(sonobath)를 사용하여 물 중에 분산시켰다. 이어서, 물 중 1 g의 AAPyr의 용액을 실리카에 첨가하고 20분 동안 초음파처리하였다. 이어서, 1 g의 질산철 (Fe(NO3)3·9H2O, 시그마-알드리치(Sigma-Aldrich))의 수용액을 SiO2-AAPyr 용액에 첨가하고, 이어서 소노배쓰 내에서 8시간 동안 초음파처리하였다. 초음파처리 후, 실리카 및 Fe-AAPyr의 점성 용액을 T=85℃에서 하룻밤 건조시켰다. 고형물을 마노 유발 내에서 미세 분말로 분쇄하고, 이어서 열 처리 (HT)를 가하였다. HT의 조건은 다음과 같았다: 100 cc min-1의 속도로 유동하는 UHP N2 분위기, HT 온도 800℃, HT 온도 상승률 10℃ min-1, 및 HT 지속시간 1시간.
도 1 및 도 2는 본원에 기재된 방법을 사용하여 제조된 선택된 M-N-C 촉매에 대한 구조적 및 형태학적 데이터를 보여준다.
도 1은 금속 공급원으로서 질산철로부터, 그리고 질소 및 탄소 공급원으로서 AAPyr로부터 제조된 Fe-M-C 촉매가 탄소 매트릭스 내로 매립된 철의 나노입자 (2 nm 미만)로 주로 이루어지는 것을 보여주는 X선 회절도이다.
도 2는 본원에 기재된 방법을 사용하여 제조된 Fe-AAPyr 촉매의 SEM 이미지인데, 이는 이 물질이 세공 크기가 약 50 내지 70 nm인 고도로 발달된 다공성 구조를 갖는다는 것을 보여준다. 이러한 다공성은 산소 환원 쪽으로 촉매 특성을 개선하는 것으로 여겨진다.
도 3 및 도 4는 산소 환원 시험의 결과를 나타내며, 이에 따라 본원에 기재된 물질의 유용성을 입증한다.
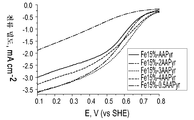
도 3은 O2로 포화된 0.5M H2SO4 중에서의 상이한 양의 아미노안티피린 전구체로 제조된 Fe-AAPyr 촉매에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다 (촉매 로딩 160 mg cm-2, 1600 RPM, 스캔 속도 20 mV s-1).
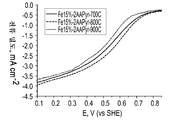
도 4는 O2로 포화된 0.5M H2SO4 중에서의 다양한 열 처리 온도로 제조된 Fe-AAPyr에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다 (촉매 로딩 160 mg cm-2, 1600 RPM, 스캔 속도 20 mV s-1).
이들 반응 시험은 저렴한 헤테로원자 아민 전구체 및 본원에 개시된 방법을 사용하여 제조된 M-N-C 촉매가 알칼리 및 산 매질 둘 다의 매질 중에서 높은 활성을 가지며, 따라서 또한 중성 pH에서도 활성임을 입증한다.
도 5 내지 도 8은 본원에 기재된 바와 같이 제조된 촉매의 메카니즘 연구를 보여주고 낮은 H2O2 생성 수율을 나타내며, 이에 따라 이는 더 효율적인 4 전자 메카니즘을 거쳐 진행되는 반응 경로임을 나타낸다.
도 5는 O2로 포화된 0.5M H2SO4 중에서의 아미노안티피린 전구체의 양의 변동을 갖는 Fe-AAPyr 촉매에 대한 ORR에 참여한 전자수의 그래프이다 (촉매 로딩: 160 mg cm-2, 1600 RPM, 20 mV s-1).
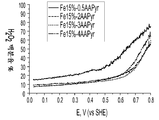
도 6은 O2로 포화된 0.5M H2SO4 중에서의 상이한 양의 아미노안티피린 전구체로 제조된 Fe-AAPyr 촉매에 대한 과산화수소 수율의 그래프이다 (촉매 로딩: 160 mg cm-2, 1600 RPM, 20 mV s-1).
도 7은 O2로 포화된 0.5M H2SO4 중에서의 열 처리 온도를 변동시키면서 제조된 Fe-AAPyr 촉매에 대한 ORR에 참여한 전자수의 그래프이다 (촉매 로딩: 160 mg cm-2, 1600 RPM, 20 mV s-1).
도 8은 O2로 포화된 0.5M H2SO4 중에서의 열 처리 온도를 변동시키면서 제조된 Fe-AAPyr에 대한 과산화수소 수율의 그래프이다 (촉매 로딩: 160 mg cm-2, 1600 RPM, 20 mV s-1).
상기에 기재된 바와 같이, 산소 환원의 메카니즘은 바람직한 4 전자 경로에 의한 산소의 물로의 직접 환원을 나타내며, 이에 따라 부식성 과산화물의 생성을 피하며, 그러므로 생성된 촉매의 안정성 및 내구성을 개선한다.
도 3, 도 5, 및 도 6에서 입증된 바와 같이, 생성된 촉매의 특성은 제조 방법에 사용될 질소-함유 전구체의 양을 선택함으로써 변동될 수 있다. 일반적으로, 촉매 내의 질소의 농도가 더 높을수록, ORR에서의 활성이 더 높다. 더욱이, 도 4, 도 7 및 도 8에서 입증된 바와 같이, 촉매의 특성은 또한 열 처리 온도를 변동시킴으로써 변경될 수 있다. 전이 금속 및 C-N 전구체의 조합 각각에 대하여 열 처리 온도를 최적화하는 것이 바람직하다는 것을 이해할 것인데, 이는 너무 낮은 온도는 활성 부위를 생성시키지 않을 것이며, 너무 높은 온도는 물질을 분해시킬 것이다.
상기에 언급된 바와 같이, 본원에 기재된 방법은 비-철 금속, 예컨대 Co, Ni, Cu, Cr, Mn 등으로부터 촉매를 제조하는 데 사용될 수 있다.
구체적인 비제한적 실시예로서, 철 전구체 및 아미노안티피린 전구체를 발연 실리카 (캅-오-실™ EH-5, 표면적: 약 400 m2 g-1)의 표면 상에 습식 함침시킴으로써 Fe-AAPyr 촉매를 제조하였다. 먼저, 1 g의 실리카를 소노배쓰를 사용하여 물 중에 분산시켰다. 이어서, 물 중 1 g의 AAPyr의 용액을 실리카에 첨가하고 20분 동안 초음파처리하였다. 이어서, 1 g의 질산철 (Fe(NO3)3·9H2O, 시그마-알드리치)의 수용액을 SiO2-AAPyr 용액에 첨가하고, 이어서 소노배쓰 내에서 8시간 동안 초음파처리하였다. 초음파처리 후, 실리카 및 Fe-AAPyr의 점성 용액을 T=85℃에서 하룻밤 건조시켰다. 고형물을 마노 유발 내에서 미세 분말로 분쇄하고, 이어서 열 처리 (HT)를 가하였다. HT의 조건은 다음과 같았다: 100 cc min-1의 속도로 유동하는 UHP N2 분위기, HT 온도 800℃, HT 온도 상승률 10℃ min-1, 및 HT 지속시간 1시간.
또 다른 비제한적 실시예에 따르면, 철 전구체, 망가니즈 전구체 및 아미노안티피린 전구체를 발연 실리카 (캅-오-실™ EH-5, 표면적: 약 400 m2 g-1)의 표면 상에 습식 함침시킴으로써 Fe-Mn-AAPyr 촉매를 제조하였다. 먼저, 3 g의 실리카를 소노배쓰를 사용하여 물 중에 분산시켰다. 이어서, 물 중 1.98 g의 AAPyr의 용액을 실리카에 첨가하고 20분 동안 초음파처리하였다. 이어서, 1.4 g의 질산철 (Fe(NO3)3·9H2O, 시그마-알드리치) 및 3.2g의 질산망가니즈의 수용액을 SiO2-AAPyr 용액에 첨가하고, 이어서 소노배쓰 내에서 8시간 동안 초음파처리하였다. 초음파처리 후, 실리카 및 Fe-Mn-AAPyr의 점성 용액을 T=85℃에서 하룻밤 건조시켰다. 고형물을 마노 유발 내에서 미세 분말로 분쇄하고, 이어서 열 처리 (HT)를 가하였다. HT의 조건은 다음과 같았다: 100 cc min-1의 속도로 유동하는 UHP N2 분위기, HT 온도 800℃, HT 온도 상승률 10℃ min-1, 및 HT 지속시간 1시간.
또 다른 비제한적 실시양태에 따르면, 철 전구체 및 아미노안티피린 전구체를 발연 실리카 (캅-오-실™ EH-5, 표면적: 약 400 m2 g-1)의 표면 상에 습식 함침시킴으로써 Fe-Cr-AAPyr 촉매를 제조하였다. 먼저, 2 g의 실리카를 소노배쓰를 사용하여 물 중에 분산시켰다. 이어서, 물 중 3.5 g의 AAPyr의 용액을 실리카에 첨가하고 20분 동안 초음파처리하였다. 이어서, 1 g의 질산철 (Fe(NO3)3·9H2O, 시그마-알드리치) 및 1.25 g의 질산크로뮴의 수용액을 SiO2-AAPyr 용액에 첨가하고, 이어서 소노배쓰 내에서 8시간 동안 초음파처리하였다. 초음파처리 후, 실리카 및 Fe-AAPyr의 점성 용액을 T=85℃에서 하룻밤 건조시켰다. 고형물을 마노 유발 내에서 미세 분말로 분쇄하고, 이어서 열 처리 (HT)를 가하였다. HT의 조건은 다음과 같았다: 100 cc min-1의 속도로 유동하는 UHP N2 분위기, HT 온도 850℃, HT 온도 상승률 10℃ min-1, 및 HT 지속시간 4시간.
실시양태에 따르면, 본원에 기재된 M-N-C 촉매는 헤테로원자 및 지지체의 전하 이동을 촉진시키는 방식으로 전도성의 분산된 지지체 (탄소 및 비-탄소 둘 다) 상에 침적될 수 있다. 일부 실시양태에 따르면, 전도성 Mo 또는 W 산화물과 같은 비-탄소 지지체의 사용은 과산화수소 생성을 상당히 감소시켜, 산 및 알칼리 매질 내에서의 촉매의 내구성 및 안정성을 증가시킬 수 있다.
상기에 기재된 바와 같이, 상이한 크기 및 형상의 희생 지지체들이 함께 사용되어 다양한 상이한 형태를 갖는 촉매를 생성할 수 있다. 예를 들어, 일부 실시양태에서는, 멀티-모달 다공도를 갖는 촉매를 생성하는 것이 바람직할 수 있는데, 즉 이러한 경우에는 촉매가 둘 이상의 구별되는 세공 집단을 포함하며, 여기서 각 집단은 다른 집단(들)과 구별가능한 평균 직경을 갖는 세공으로 이루어진다. 예를 들어, 대략 10 nm의 평균 직경을 갖는 세공의 한 집단, 대략 50 nm의 평균 직경을 갖는 제2 세공 집단 및 150 내지 200 nm의 평균 직경을 갖는 제3 세공 집단을 갖는 촉매는 멀티-모달 세공 크기 분포를 갖는 것으로 간주될 것이다.
도 9를 보면, 한 실시양태에 따르면, 그러한 멀티-모달 세공 크기 분포는 상기에 기재된 전구체를 상이한 직경을 갖는 구체 (아니면 형상화된 입자)로부터 형성된 희생 지지체 상에 템플레이팅함으로써 생성될 수 있을 것이다. 도시된 바와 같이, 직경 d1을 갖는 더 큰 구체 (10)와 직경 d2를 갖는 더 작은 구체 (12)를 함께 혼합하여 희생 지지체를 형성하며, 이 희생 지지체 상에 전구체 물질이 침적되고 열분해된다. 일단 지지체를 제거하면, 생성된 촉매 물질 (16)은 상이한 입자 직경에 상응하는 상이한 크기의 세공 (18, 20)을 함유한다.
생성된 촉매 물질의 형태에 대한 완전한 제어를 갖기 위하여, 형상 및 크기가 알려진 희생 지지체 내로 전구체를 템플레이팅하는 것이 바람직할 것임을 이해할 것이다. 희생 지지체가 실리카 입자로부터 형성되는 특정 실시양태에 따르면, 희생 지지체의 상이한 형상 및 크기는 상이한 유형의 실리카를 사용하여 상이한 크기의 실리카 입자를 신뢰성있게 그리고 재현가능하게 생성함으로써 생성될 수 있다. 그러면, 생성된 촉매는 멀티-모달 세공 분포를 가질 것이며, 여기서 세공의 특정 크기 및 형상은 알려져 있다.
구체적인 실시예에 따르면, 철 전구체 및 아미노안티피린 전구체를 상이한 발연 실리카 및 그들의 혼합물 (캅-오-실™ 표면적 90 내지 400 m2 g-1)의 표면 상에 습식 함침시킴으로써 EH5 및 LM130 실리카 상에 형성된 본원에 기재된 촉매를 제조하였다. 먼저, 1 g의 실리카 EH5 및 1 g의 실리카 LM130을 소노배쓰를 사용하여 물 중에 분산시켰다. 이어서, 물 중 1 g의 AAPyr의 용액을 실리카에 첨가하고 20분 동안 초음파처리하였다. 이어서, 1 g의 질산철 (Fe(NO3)3·9H2O, 시그마-알드리치)의 수용액을 SiO2-AAPyr 용액에 첨가하고, 이어서 소노배쓰 내에서 8시간 동안 초음파처리하였다. 초음파처리 후, 실리카 및 Fe-AAPyr의 점성 용액을 T=85℃에서 하룻밤 건조시켰다. 고형물을 마노 유발 내에서 미세 분말로 분쇄하고, 이어서 열 처리 (HT)를 가하였다. HT의 조건은 다음과 같았다: 100 cc min-1의 속도로 유동하는 UHP N2 분위기, HT 온도 800℃, HT 온도 상승률 10℃ min-1, 및 HT 지속시간 1시간.
또 다른 구체적인 실시예에 따르면, 철 전구체 및 아미노안티피린 전구체를 상이한 발연 실리카 및 그들의 혼합물 (캅-오-실™ 표면적 90 내지 400 m2 g-1)의 표면 상에 습식 함침시킴으로써 M5D 및 A90 실리카 상에 형성된 본원에 기재된 촉매를 제조하였다. 먼저, 2 g의 실리카 M5D 및 0.25 g의 실리카 A90을 소노배쓰를 사용하여 물 중에 분산시켰다. 이어서, 물 중 1.3 g의 AAPyr의 용액을 실리카에 첨가하고 20분 동안 초음파처리하였다. 이어서, 4 g의 질산철 (Fe(NO3)3·9H2O, 시그마-알드리치)의 수용액을 SiO2-AAPyr 용액에 첨가하고, 이어서 소노배쓰 내에서 8시간 동안 초음파처리하였다. 초음파처리 후, 실리카 및 Fe-AAPyr의 점성 용액을 T=85℃에서 하룻밤 건조시켰다. 고형물을 마노 유발 내에서 미세 분말로 분쇄하고, 이어서 열 처리 (HT)를 가하였다. HT의 조건은 다음과 같았다: 100 cc min-1의 속도로 유동하는 UHP N2 분위기, HT 온도 800℃, HT 온도 상승률 10℃ min-1, 및 HT 지속시간 1시간.
도 10 내지 도 20은 멀티모달 다공도를 갖고 본원에 기재된 바와 같이 제조된 다양한 M-N-C 촉매에 대한 형태학적 데이터를 도시한다.
도 10은 Fe-AAPyr 및 HS5 실리카로부터 유도된 모노-모달 촉매의 SEM 이미지이다. 세공 크기가 40 내지 60 nm의 범위라는 것을 알 수 있다.
도 11은 Fe-AAPyr 및 M5 실리카로부터 유도된 바이-모달 촉매의 SEM 이미지이다. 세공의 제1 유형은 직경이 40 내지 60 nm이며, 세공의 제2 유형은 직경이 <10 nm인 것을 알 수 있다.
도 12는 Fe-AAPyr 및 LM130 실리카로부터 유도된 바이-모달 촉매의 SEM 이미지이다. 세공의 제1 유형은 직경이 약 100 nm이며, 세공의 제2 유형은 직경이 약 30 nm인 것을 알 수 있다.
도 13은 Fe-AAPyr 및 A90 실리카로부터 유도된 촉매의 SEM 이미지이다. 세공은 직경이 약 30 nm이지만, 직경이 40 내지 60 nm인 나노채널이 또한 존재한다는 것을 알 수 있다.
도 14는 Fe-AAPyr 및 L90과 A90 실리카의 혼합물로부터 유도된 바이-모달 촉매의 SEM 이미지이다. 세공의 제1 유형은 직경이 약 150 nm이며, 세공의 제2 유형은 직경이 약 20 nm인 것을 알 수 있다.
도 15는 Fe-AAPyr 및 L90과 EH5 실리카의 혼합물로부터 유도된 트리-모달 촉매의 SEM 이미지이다. 세공의 제1 유형은 직경이 약 150 내지 200 nm이며, 세공의 제2 유형은 직경이 약 40 내지 60 nm이며, 제3 유형은 약 20 nm인 것을 알 수 있다.
도 16은 Fe-AAPyr 및 L90과 M5 실리카의 혼합물로부터 유도된 바이-모달 촉매의 SEM 이미지이다. 세공의 제1 유형은 직경이 약 100 nm이며, 세공의 제2 유형은 직경이 약 25 nm인 것을 알 수 있다.
도 17은 Fe-AAPyr 및 L90과 LM130 실리카의 혼합물로부터 유도된 바이-모달 촉매의 SEM 이미지이다. 세공의 제1 유형은 직경이 약 150 내지 200 nm이며, 세공의 제2 유형은 직경이 약 30 nm인 것을 알 수 있다.
도 18은 Fe-AAPyr 및 L90과 A200 실리카의 혼합물로부터 유도된 바이-모달 촉매의 SEM 이미지이다. 세공의 제1 유형은 직경이 약 100 내지 200 nm이며, 세공의 제2 유형은 직경이 약 50 nm인 것을 알 수 있다.
도 19는 Fe-AAPyr 및 L90과 A380 실리카의 혼합물로부터 유도된 바이-모달 촉매의 SEM 이미지이다. 세공의 제1 유형은 직경이 약 100 nm이며, 세공의 제2 유형은 직경이 <20 nm인 것을 알 수 있다.
도 20은 Fe-AAPyr 및 M5 실리카로부터 유도된 구형 촉매의 SEM 이미지이다. 촉매의 구체는 1 내지 3 μm의 범위이며, 세공은 직경이 약 50 내지 70 nm라는 것을 알 수 있다.
도 21 내지 도 25는 도 10 내지 도 20의 멀티모달 촉매의 선택에 대한 산소 환원 시험의 결과를 나타내며, 이에 따라 본원에 기재된 물질의 유용성을 입증한다.
도 21은 O2로 포화된 0.5M H2SO4 중에서의 Fe-AAPyr 및 HS5, L90 및 L90 + EH5 실리카로부터 제조된 촉매에 대한 RDE 데이터에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다 (촉매 로딩: 600 mg cm-2, 1200 RPM, 5 mV s-1).
도 22는 O2로 포화된 0.5M H2SO4 중에서의 Fe-AAPyr 및 L90, LM130, 및 L90 + LM130 실리카로부터 제조된 촉매에 대한 RDE 데이터에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다 (촉매 로딩: 600 mg cm-2, 1200 RPM, 5 mV s-1).
도 23은 O2로 포화된 0.5M H2SO4 중에서의 Fe-AAPyr 및 L90, L90 + A90, 및 A90 실리카로부터 제조된 촉매에 대한 RDE 데이터에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다 (촉매 로딩: 600 mg cm-2, 1200 RPM, 5 mV s-1).
도 24는 O2로 포화된 0.5M H2SO4 중에서의 Fe-AAPyr 및 L90 및 L90 + EH5 실리카로부터 제조된 촉매에 대한 RDE 데이터에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다 (촉매 로딩: 600 mg cm-2, 1200 RPM, 5 mV s-1).
도 25는 O2로 포화된 0.5M H2SO4 중에서의 Fe-AAPyr 및 L90, M5 및 L90 + M5 실리카로부터 제조된 촉매에 대한 RDE 데이터에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다 (촉매 로딩: 600 mg cm-2, 1200 RPM, 5 mV s-1).
일부 응용에서는 1원-금속 촉매가 전통적인 백금계 또는 백금 합금계 촉매를 대체하기에 충분히 안정하거나 활성을 나타낼 수 없다는 것을 이해할 것이다. 따라서, 상기에 나타낸 바와 같이, 일부 실시양태에 따르면, 본원에 기재된 방법은 원하는 안정성 및/또는 활성을 달성하기 위하여 다수의 금속의 전구체들의 사용을 포함할 수 있다.
다양한 구체적인 실시양태에 따르면, 철 및 제2 전이 금속 전구체, 또는 철, 제2 및 제3 전이 금속 (전이 금속 = Co, Ni, Cu, Cr 및 Mn) 전구체 및 아미노안티피린 전구체를 발연 실리카 (캅-오-실™ EH-5, 표면적: 약 400 m2 g-1)의 표면 상에 습식 함침시킴으로써 Fe-AAPyr 촉매를 제조하였다. 먼저, 1 g의 실리카를 소노배쓰를 사용하여 물 중에 분산시켰다. 이어서, 물 중 1 g의 AAPyr의 용액을 실리카에 첨가하고 20분 동안 초음파처리하였다. 이어서, 1 g의 질산철 (Fe(NO3)3·9H2O, 시그마-알드리치) 및 1 g의 질산망가니즈의 수용액을 SiO2-AAPyr 용액에 첨가하고, 이어서 소노배쓰 내에서 8시간 동안 초음파처리하였다. 초음파처리 후, 실리카 및 Fe-Mn-AAPyr의 점성 용액을 T=85℃에서 하룻밤 건조시켰다. 고형물을 마노 유발 내에서 미세 분말로 분쇄하고, 이어서 열 처리 (HT)를 가하였다. HT의 조건은 다음과 같았다: 100 cc min-1의 속도로 유동하는 UHP N2 분위기, HT 온도 800℃, HT 온도 상승률 10℃ min-1, 및 HT 지속시간 1시간.
도 26 내지 도 34는 상기에 기재된 방법에 의해 제조된 선택된 다중-금속 M-N-C 촉매에 대한 구조적 및 형태학적 데이터를 보여준다.
도 26 내지 도 28은 본원에 기재된 방법을 사용하여 제조된 3개의 상이한 촉매 Fe3Co-AAPyr, FeCo-AAPyr 및 FeCo3-AAPyr을 각각 나타낸다. 이들 물질은 세공 크기가 약 100 nm인 고도로 발달된 다공성 구조를 갖는다.
도 29a 및 도 29b는 FeCu3-AAPyr 2원-금속 촉매의 SEM 이미지이며, 이는 이 물질이 세공 크기가 약 70 nm인 고도로 발달된 다공성 구조를 갖는다는 것을 보여준다.
도 30a 및 도 30b는 FeMn3-AAPyr 2원-금속 촉매의 SEM 이미지이며, 이는 이 물질이 세공 크기가 약 50 nm인 고도로 발달된 다공성 구조를 갖는다는 것을 보여준다.
도 31a 및 도 31b는 FeNi3-AAPyr 2원-금속 촉매의 SEM 이미지이며, 이는 이 물질이 세공 크기가 약 200 nm인 고도로 발달된 다공성 구조를 갖는다는 것을 보여준다.
도 32a 및 도 32b는 FeCoCu-AAPyr 3원-금속 촉매의 SEM 이미지이며, 이는 이 물질이 세공 크기가 약 150 nm인 고도로 발달된 다공성 구조를 갖는다는 것을 보여준다.
도 33a 및 도 33b는 FeCoMn-AAPyr 3원-금속 촉매의 SEM 이미지이며, 이는 이 물질이 세공 크기가 약 100 nm인 고도로 발달된 다공성 구조를 갖는다는 것을 보여준다.
도 34a 및 도 34b는 FeCuMn-AAPyr 3원-금속 촉매의 SEM 이미지이며, 이는 이 물질이 세공 크기가 약 100 nm인 고도로 발달된 다공성 구조를 갖는다는 것을 보여준다.
본원에 기재된 다중-금속 촉매의 유용성은 도 35 내지 도 40에 나타낸 산소 환원 시험의 결과에 의해 입증된다.
도 35는 O2로 포화된 0.5M H2SO4 중에서의, Co-AAPyr에 대비하여 FexCoy-AAPyr 2원-금속 촉매에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다 (촉매 로딩: 600 mg cm-2, 1200 RPM, 5 mV s-1).
도 36은 O2로 포화된 0.5M H2SO4 중에서의, Ni-AAPyr에 대비하여 FexNiy-AAPyr 2원-금속 촉매에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다 (촉매 로딩: 600 mg cm-2, 1200 RPM, 5 mV s-1).
도 37은 O2로 포화된 0.5M H2SO4 중에서의, Cu-AAPyr에 대비하여 FexCuy-AAPyr 2원-금속 촉매에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다 (촉매 로딩: 600 mg cm-2, 1200 RPM, 5 mV s-1).
도 38은 O2로 포화된 0.5M H2SO4 중에서의, Cr-AAPyr에 대비하여 FexCry-AAPyr 2원-금속 촉매에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다 (촉매 로딩: 600 mg cm-2, 1200 RPM, 5 mV s-1).
도 39는 O2로 포화된 0.5M H2SO4 중에서의, Mn-AAPyr에 대비하여 FexMny-AAPyr 2원-금속 촉매에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다 (촉매 로딩: 600 mg cm-2, 1200 RPM, 5 mV s-1).
도 40은 O2로 포화된 0.5M H2SO4 중에서의 FeMIMII-AAPyr 3원-금속 촉매에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다 (촉매 로딩: 600 mg cm-2, 1200 RPM, 5 mV s-1).
이들 반응 시험은 본원에 기재된 방법을 사용하여 저렴한 C-N 전구체로부터 제조된 다중-금속 M-N-C 촉매가 1원-금속 촉매보다 상당히 더 높은 활성을 갖는다는 것을 입증한다. 그러한 높은 활성은 이들 물질을 캐소드 촉매로서 연료 전지 응용에 사용하는 데 적합하게 하는데, 이는 이들이 알칼리성, 중성, 및 산성 환경에서 높은 ORR 활성을 갖기 때문이다.
일부 실시양태에 따르면, 본원에 기재된 촉매를, 예를 들어 회분식 공정으로 대량으로 생성하는 것이 바람직할 수 있다. 따라서, 본원은 본원에 기재된 촉매의 대규모 제조에 대한 방법을 추가로 제공한다. 한 실시양태에 따르면, 본원은 희생 지지체-기반 방법을 분무 열분해와 조합하여 자기-지지된 촉매를 생성하는 방법을 제공한다. 이 방법에 따르면, 분무 열분해 방법은 연속 방법이지만, 희생 지지체-기반 방법은 회분식으로 수행된다. 도 41을 보면, 상기에 기재된 전구체 물질을 실리카 지지체와 혼합하고, 무화(atomize)시키고, 관상로(tube furnace) 내에서 건조시킨다는 것을 알 수 있다. 이어서, 이 절차로부터 수득된 분말을 필터 상에 수집한다. 이어서, 수집된 분말을 촉매의 원하는 응용에 따라 필요하다면 열 처리한다. 마지막으로, 희생 지지체를, 예를 들어 HF 또는 KOH로 침출시킴으로써 제거한다.
상기에 기재된 대규모 제조 방법은 매우 다양한 전구체 및 물질에 사용하기에 적합하며, 이에 따라 반드시 본원에 개시된 촉매로 한정되는 것은 아니라는 것을 이해할 것이다. 도 42 내지 도 44는 상기에 기재된 방법에 의해 제조된 선택된 자기-지지된 금속-질소-탄소 (M-N-C) 촉매에 대한 형태학적 데이터를 보여준다.
도 42a 내지 도 42d는 저 표면적 실리카 상에 제조된 고도로 다공성인 구형 Fe-N-C 촉매의 SEM 이미지이다.
도 43a 내지 도 43c는 고 표면적 실리카 상에 제조된 고도로 다공성인 구형 Fe-N-C 촉매 (배치 1)의 SEM 이미지이다.
도 44는 고 표면적 실리카 상에 제조된 고도로 다공성인 구형 Fe-N-C 촉매 (배치 2)의 SEM 이미지이다.
도 45는 O2로 포화된 0.5M H2SO4 중에서의 본원에 기재된 방법에 의해 제조된 구형 F-N-C 촉매에 대한 RDE 데이터에 대한 산소 환원을 보여주는 회전 디스크 전극 전압전류곡선이다 (촉매 로딩: 600 μg cm-2, 1200 RPM, 5 mV s-1).
이들 물질의 형태학적 특성이 배치 별로 매우 일관성이 있다는 것을 명백히 알 수 있다. 이들 물질의 유용성은 산소 환원 시험에서 나타나 있으며, 이들 중 한 실시예가 도 5에 도시되어 있다.
본원에 기재된 구체적인 방법 및 조성은 대표적인 바람직한 실시양태이고, 예시적이며 본 발명의 범주에 대한 제한으로서 의도되지 않는다. 본 명세서의 고려시에 다른 목적, 측면, 및 실시양태가 당업자에게 떠오를 것이며, 이는 특허청구범위의 범주에 의해 정의된 본 발명의 사상 내에 포함된다. 본 발명의 범주 및 사상으로부터 벗어남이 없이 본원에 개시된 본 발명에 대해 다양한 치환 및 수정이 이루어질 수 있다는 것이 당업자에게 용이하게 명백할 것이다. 본원에 예시적으로 기재된 본 발명은 적합하게는, 본원에서 본질적인 것으로 구체적으로 개시되지 않은 임의의 요소 또는 요소들, 또는 제한 또는 제한들의 부재하에 실시될 수 있다. 본원에 예시적으로 기재된 방법 및 공정은 적합하게는 단계들의 순서를 상이하게 하여 실시될 수 있으며, 이들은 반드시 본원 또는 특허청구범위에 나타낸 단계들의 순서로 제한되지는 않는다. 본원 및 첨부된 특허청구범위에 사용되는 바와 같이, 단수형은 그 맥락에 달리 명백히 나타나 있지 않는 한 복수 지시대상을 포함한다. 따라서, 예를 들어, "촉매"에 대한 언급은 복수의 그러한 촉매를 포함하는 등이다.
어떠한 상황 하에서도 본 발명은 본원에 구체적으로 개시된 구체적인 실시예 또는 실시양태 또는 방법에 제한되는 것으로 해석될 수 없다. 어떠한 상황 하에서도 본 특허는 특허 상표청(Patent and Trademark Office)의 어떠한 심사관, 다른 직원 또는 고용인에 의해 행해진 어떠한 진술도, 구체적으로는 자격 또는 권리 없이 출원인에 의한 서면 응답에서 명백히 채택되지 않는 한, 그에 의해 제한되는 것으로 해석될 수 없다.
사용된 용어 및 표현은 제한이 아니라 설명을 위해 사용되며, 그러한 용어 및 표현의 사용에서, 도시되고 설명된 특징부 또는 그의 일부의 임의의 등가물을 제외시킬 의도는 없으며, 청구된 바와 같은 본 발명의 범주 내에서 다양한 수정이 가능하다는 것이 인식된다. 따라서, 본 발명이 바람직한 실시양태 및 임의적인 특징부에 의해 구체적으로 개시되어 있기는 하지만, 본원에 개시된 개념의 수정 및 변형이 당업자에 의해 이루어질 수 있으며, 그러한 수정 및 변형은 첨부된 특허청구범위에 의해 정의된 바와 같은 본 발명의 범주 내에 있는 것으로 여겨진다는 것을 이해할 것이다.
이하에서 참고되고/되거나 본원에 언급된 모든 특허 및 간행물은 본 발명이 속하는 기술 분야에서의 당업자의 기술 수준의 지표가 되며, 각각의 그러한 참고된 특허 또는 간행물은 마치 그의 전문이 개별적으로 참고로 포함되거나 그의 전문이 본원에 기술된 것처럼 그와 동일한 정도로 본원에 참고로 포함된다. 출원인은 임의의 그러한 인용된 특허 또는 간행물로부터의 임의의 및 모든 자료 및 정보를 본 명세서 내로 물리적으로 포함시킬 권리를 유보한다.
Claims (19)
- 희생 템플레이트 입자를 제공하는 단계;
하나 이상의 전이 금속 전구체 및 초기 촉매 활성을 갖지 않는 비-포르피린 전구체를 희생 템플레이트 입자 상에 침전시켜, 분산된 전구체를 생성하는 단계;
분산된 전구체를 열분해하는 단계; 및
희생 템플레이트 입자를 제거하여 고도로 분산된 자기-지지된 고 표면적 전기촉매 물질을 생성하는 단계
를 포함하는, 연료 전지에 사용하기에 적합한 금속-질소-탄소 촉매의 제조 방법. - 제1항에 있어서, 비-포르피린 전구체가 철과의 착물을 형성하는 것인 방법.
- 제1항에 있어서, 비-포르피린 전구체가 4-아미노안티피린인 방법.
- 제1항에 있어서, 전이 금속 전구체가 철 전구체인 방법.
- 제1항에 있어서, 하나 이상의 전이 금속 전구체가 Ce, Cr, Cu, Mo, Ni, Ru, Ta, Ti, V, W 및 Zr의 전구체로 이루어진 군으로부터 선택된 것인 방법.
- 제1항에 있어서, 적어도 2개의 상이한 금속 전구체를 사용하여, 다중-금속(multi-metallic) 촉매가 생성되는 것인 방법.
- 제1항에 있어서, 희생 템플레이트 입자 및 비-포르피린 전구체가, 전기촉매 물질의 반응 메카니즘을 4 e- 경로 쪽으로 이동시키기 위해 사용되도록 선택된 것인 방법.
- 제1항에 있어서, 희생 템플레이트 입자가 적어도 2개의 입자 집단을 포함하며, 여기서 각 집단은 다른 집단과 상이한 평균 입자 직경을 가져서, 멀티모달 세공 분포를 갖는 전기촉매 물질이 생성되는 것인 방법.
- 제8항에 있어서, 전기촉매 물질이, 20 내지 60 nm의 평균 직경을 갖는 세공 집단 및 100 내지 200 nm의 평균 직경을 갖는 제2 세공 집단을 함유하는 것인 방법.
- 제9항에 있어서, 희생 템플레이트 입자를 실리카로부터 형성하는 방법.
- 제10항에 있어서, 실리카 입자의 각 집단을 상이한 유형의 실리카로부터 형성하는 방법.
- 제11항에 있어서, 각 집단에서 입자를 형성하는 실리카가 HS5, M4, LM130, A90, L90, A200 및 A380 실리카로 이루어진 군으로부터 선택되는 것인 방법.
- 제1항에 있어서,
전이 금속 및 비-포르피린 전구체를 희생 템플레이트 입자와 혼합하는 단계;
혼합물을 무화(atomizing)하여 분말을 형성하는 단계;
분말을 수집하는 단계; 및
분말을 열 처리하는 단계
를 추가로 포함하는 방법. - 제1항의 방법을 사용하여 제조된 열분해된 금속 전구체로부터의 적어도 하나의 전이 금속과 초기 촉매 활성을 갖지 않는 비-포르피린 전구체로부터의 질소 및 탄소로 실질적으로 이루어진 고도로 분산된 비지지된 촉매 물질.
- 열분해된 금속 전구체로부터의 적어도 하나의 전이 금속과 초기 촉매 활성을 갖지 않는 비-포르피린 전구체로부터의 질소 및 탄소로 실질적으로 이루어진 고도로 분산된 비지지된 촉매 물질.
- 제15항에 있어서, 멀티-모달 세공 분포를 추가로 포함하는 물질.
- 제16항에 있어서, 20 내지 60 nm의 평균 직경을 갖는 제1 세공 집단 및 100 내지 200 nm의 평균 직경을 갖는 제2 세공 집단을 포함하는 물질.
- 제16항에 있어서, 트리-모달 세공 분포를 추가로 포함하며, 대략 20 nm 이하의 평균 직경을 갖는 제1 세공 집단, 대략 40 내지 60 nm의 평균 직경을 갖는 제2 세공 집단, 및 150 내지 200 nm의 평균 직경을 갖는 제3 세공 집단을 포함하는 물질.
- 제15항에 있어서, 다수의 전이 금속을 포함하는 물질.
Applications Claiming Priority (9)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201161497444P | 2011-06-15 | 2011-06-15 | |
| US61/497,444 | 2011-06-15 | ||
| US201261606109P | 2012-03-02 | 2012-03-02 | |
| US61/606,109 | 2012-03-02 | ||
| US201261621084P | 2012-04-06 | 2012-04-06 | |
| US201261621095P | 2012-04-06 | 2012-04-06 | |
| US61/621,084 | 2012-04-06 | ||
| US61/621,095 | 2012-04-06 | ||
| PCT/US2012/042609 WO2012174344A2 (en) | 2011-06-15 | 2012-06-15 | Non-pgm cathode catalysts for fuel cell application derived from heat treated heteroatomic amines precursors |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20140035492A true KR20140035492A (ko) | 2014-03-21 |
Family
ID=47357757
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020147000718A KR20140035492A (ko) | 2011-06-15 | 2012-06-15 | 열 처리된 헤테로원자 아민 전구체로부터 유도된 연료 전지 응용을 위한 비-pgm 캐소드 촉매 |
Country Status (11)
| Country | Link |
|---|---|
| US (1) | US9634331B2 (ko) |
| EP (1) | EP2720793B1 (ko) |
| JP (1) | JP6202629B2 (ko) |
| KR (1) | KR20140035492A (ko) |
| CN (1) | CN103998131A (ko) |
| AU (1) | AU2012271494B2 (ko) |
| CA (1) | CA2838267C (ko) |
| DK (1) | DK2720793T3 (ko) |
| HK (1) | HK1201228A1 (ko) |
| IL (1) | IL229855B (ko) |
| WO (1) | WO2012174344A2 (ko) |
Families Citing this family (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2872252A4 (en) * | 2012-07-11 | 2016-02-17 | Stc Unm | CATALYTIC MATERIALS BASED ON CARBENDAZIME |
| US9673456B2 (en) | 2013-01-16 | 2017-06-06 | Alexey Serov | Non-PGM catalysts for ORR based on charge transfer organic complexes |
| CN103326041B (zh) * | 2013-06-19 | 2015-03-25 | 厦门大学 | 一种氧还原电催化剂及其制备方法 |
| DE102013219937A1 (de) * | 2013-10-01 | 2015-04-02 | Volkswagen Aktiengesellschaft | Edemetallfreies Katalysatorsystem für eine Brennstoffzelle |
| WO2016133921A1 (en) | 2015-02-16 | 2016-08-25 | Stc.Unm | Materials with atomically dispersed chemical moieties |
| WO2016149168A1 (en) * | 2015-03-13 | 2016-09-22 | Stc.Unm | Design of smart-meas for high power fuel cells |
| CN105789644B (zh) * | 2016-03-02 | 2018-08-21 | 中南大学 | 一种Fe-N/C氧还原反应复合电催化剂的制备方法 |
| WO2018159622A1 (en) * | 2017-02-28 | 2018-09-07 | Okinawa Institute Of Science And Technology School Corporation | Process for preparing a supported catalytic material, and supported catalytic material |
| CN108889300A (zh) * | 2018-06-04 | 2018-11-27 | 中国科学院生态环境研究中心 | 一种新型水热炭负载纳米双金属催化剂的制备方法及其应用 |
| CN114388802B (zh) * | 2021-12-24 | 2023-03-10 | 合肥国轩高科动力能源有限公司 | 一种单原子负载氮磷共掺杂碳复合材料包覆的磷酸铁锂及其制备方法和应用 |
| DE102023127140A1 (de) | 2023-03-29 | 2024-10-02 | Cornell University | Brennstoffzellenelektrode und brennstoffzellensystem mit dotierstoffen auf zirkoniumbasis |
Family Cites Families (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5240893A (en) | 1992-06-05 | 1993-08-31 | General Motors Corporation | Method of preparing metal-heterocarbon-nitrogen catalyst for electrochemical cells |
| DE10132490B4 (de) * | 2001-07-03 | 2007-04-12 | Hahn-Meitner-Institut Berlin Gmbh | Platinfreies Chelat-Katalysatormaterial für die selektive Sauerstoffreduktion und Verfahren zu seiner Herstellung |
| US20070275160A1 (en) * | 2003-10-10 | 2007-11-29 | Stephen Maldonado | Carbon Nanostructure-Based Electrocatalytic Electrodes |
| CN1299377C (zh) * | 2003-12-31 | 2007-02-07 | 山东理工大学 | 活性炭表面用卟啉、酞菁化学修饰的产品在燃料电池中的应用 |
| US7718155B2 (en) * | 2005-10-06 | 2010-05-18 | Headwaters Technology Innovation, Llc | Carbon nanostructures manufactured from catalytic templating nanoparticles |
| JP4893918B2 (ja) | 2005-11-15 | 2012-03-07 | 株式会社豊田中央研究所 | 含窒素炭素系電極触媒 |
| US7618915B2 (en) | 2006-05-08 | 2009-11-17 | University Of South Carolina | Composite catalysts supported on modified carbon substrates and methods of making the same |
| US7678728B2 (en) * | 2006-10-16 | 2010-03-16 | Stc.Unm | Self supporting structurally engineered non-platinum electrocatalyst for oxygen reduction in fuel cells |
| ATE524843T1 (de) | 2007-04-12 | 2011-09-15 | 3M Innovative Properties Co | Leistungsstarke und langlebige nichtedelmetall- brennstoffzellenkatalysatoren |
| KR101473319B1 (ko) | 2007-10-16 | 2014-12-16 | 삼성에스디아이 주식회사 | 복합 중형 다공성 탄소, 그 제조방법 및 이를 이용한연료전지 |
| WO2009075038A1 (en) | 2007-12-12 | 2009-06-18 | Toyota Jidosha Kabushiki Kaisha | Electrode catalyst for fuel cells, a method of preparing an electrode catalyst for fuel cells, and a polymer electrolyte fuel cell |
| US20100048380A1 (en) | 2008-08-21 | 2010-02-25 | Board Of Trustees Of Michigan State University | Novel catalyst for oxygen reduction reaction in fuel cells |
| US8791043B2 (en) * | 2008-12-31 | 2014-07-29 | Samsung Electronics Co., Ltd. | Ordered mesoporous carbon composite catalyst, method of manufacturing the same, and fuel cell using the same |
| JP5507099B2 (ja) * | 2009-03-11 | 2014-05-28 | 花王株式会社 | メソポーラスシリカ粒子の製造方法 |
| JP5555225B2 (ja) * | 2009-03-12 | 2014-07-23 | 三井化学株式会社 | 金属酸化物多孔質体の製造方法 |
| JP5636171B2 (ja) | 2009-06-19 | 2014-12-03 | 東洋炭素株式会社 | 多孔質炭素及びその製造方法 |
| WO2013040567A2 (en) * | 2011-09-16 | 2013-03-21 | Stc.Unm | Structured cathode catalysts for fuel cell application derived from metal-nitrogen-carbon precursors, using hierarchically structured silica as a sacrificial support |
| WO2013187976A1 (en) * | 2012-06-13 | 2013-12-19 | Stc.Unm | Bi-functional catalysts for oxygen reduction and oxygen evolution |
| EP2872252A4 (en) * | 2012-07-11 | 2016-02-17 | Stc Unm | CATALYTIC MATERIALS BASED ON CARBENDAZIME |
| US9359681B1 (en) * | 2013-03-11 | 2016-06-07 | Alexey Serov | CO2 electroreduction on metals and metal alloys prepared by a sacrificial support-based method |
-
2012
- 2012-06-15 JP JP2014516017A patent/JP6202629B2/ja active Active
- 2012-06-15 EP EP12801152.5A patent/EP2720793B1/en active Active
- 2012-06-15 AU AU2012271494A patent/AU2012271494B2/en active Active
- 2012-06-15 DK DK12801152.5T patent/DK2720793T3/en active
- 2012-06-15 CA CA2838267A patent/CA2838267C/en active Active
- 2012-06-15 US US14/126,788 patent/US9634331B2/en active Active
- 2012-06-15 WO PCT/US2012/042609 patent/WO2012174344A2/en active Application Filing
- 2012-06-15 CN CN201280039823.4A patent/CN103998131A/zh active Pending
- 2012-06-15 KR KR1020147000718A patent/KR20140035492A/ko not_active Application Discontinuation
-
2013
- 2013-12-08 IL IL229855A patent/IL229855B/en active IP Right Grant
-
2015
- 2015-02-18 HK HK15101794.9A patent/HK1201228A1/xx unknown
Also Published As
| Publication number | Publication date |
|---|---|
| EP2720793B1 (en) | 2018-03-07 |
| AU2012271494A1 (en) | 2013-12-19 |
| IL229855B (en) | 2018-01-31 |
| JP6202629B2 (ja) | 2017-09-27 |
| US9634331B2 (en) | 2017-04-25 |
| HK1201228A1 (en) | 2015-08-28 |
| CA2838267C (en) | 2018-10-02 |
| DK2720793T3 (en) | 2018-05-07 |
| AU2012271494B2 (en) | 2017-03-09 |
| US20160181621A1 (en) | 2016-06-23 |
| CA2838267A1 (en) | 2012-12-20 |
| CN103998131A (zh) | 2014-08-20 |
| WO2012174344A2 (en) | 2012-12-20 |
| JP2014523065A (ja) | 2014-09-08 |
| EP2720793A2 (en) | 2014-04-23 |
| WO2012174344A3 (en) | 2013-05-02 |
| EP2720793A4 (en) | 2015-01-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US9634331B2 (en) | Non-PGM cathode catalysts for fuel cell application derived from heat treated heteroatomic amines precursors | |
| US9502719B2 (en) | Cathode catalysts for fuel cell application derived from polymer precursors | |
| Jang et al. | Emerging carbon shell-encapsulated metal nanocatalysts for fuel cells and water electrolysis | |
| JP7364608B2 (ja) | 高出力燃料電池用スマートMEAsの設計 | |
| Daş et al. | Graphene nanoplatelets-carbon black hybrids as an efficient catalyst support for Pt nanoparticles for polymer electrolyte membrane fuel cells | |
| US20130149632A1 (en) | Electrode catalyst for a fuel cell, method of preparing the same, and membrane electrode assembly and fuel cell including the electrode catalyst | |
| US10038196B2 (en) | Active support for cathode catalysts | |
| CN104812488B (zh) | 基于贝芬替的催化材料 | |
| KR20150070141A (ko) | 열분해된 다중 착물 기반의 orr을 위한 비-pgm 촉매 | |
| KR20130067476A (ko) | 연료 전지용 전극 촉매, 이의 제조 방법, 및 이를 포함한 막 전극 접합체 및 연료 전지 | |
| Sudarsono et al. | From catalyst structure design to electrode fabrication of platinum-free electrocatalysts in proton exchange membrane fuel cells: A review | |
| Phan et al. | Highly efficient and durable electrochemical hydrogen evolution reaction based on composition/shape controlled CuTi@ Pt core-shell nanotubes in acidic media | |
| JP6438890B2 (ja) | 非白金族金属(pgm)触媒物質を製造する方法 | |
| Jang et al. | Effect of Fe content on nonprecious cathodic catalysts derived from a metal–organic framework for direct ammonia fuel cells | |
| Serov et al. | Cathode catalysts for fuel cell application derived from polymer precursors | |
| Sui et al. | Nanoporous materials for proton exchange membrane fuel cell applications | |
| Roy et al. | Oxygen reduction reaction in ethanol fuel cells |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| E902 | Notification of reason for refusal | ||
| E601 | Decision to refuse application |