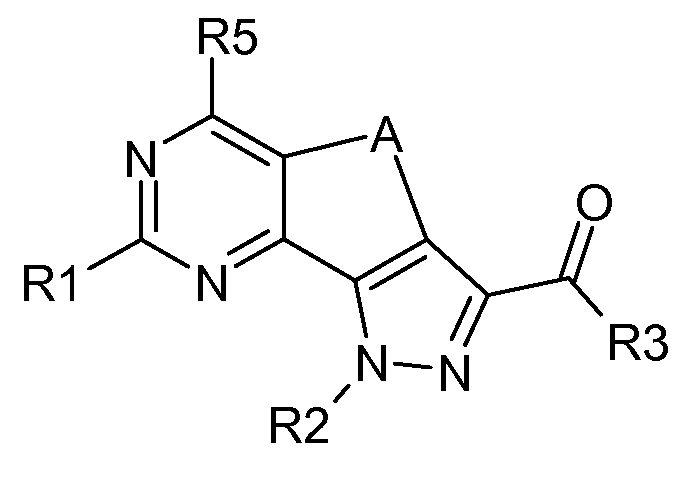
KR20140027902A - 키나제 억제제로서 치환된 피라졸로-퀴나졸린 유도체 - Google Patents
키나제 억제제로서 치환된 피라졸로-퀴나졸린 유도체 Download PDFInfo
- Publication number
- KR20140027902A KR20140027902A KR1020137007627A KR20137007627A KR20140027902A KR 20140027902 A KR20140027902 A KR 20140027902A KR 1020137007627 A KR1020137007627 A KR 1020137007627A KR 20137007627 A KR20137007627 A KR 20137007627A KR 20140027902 A KR20140027902 A KR 20140027902A
- Authority
- KR
- South Korea
- Prior art keywords
- pyrazolo
- quinazolin
- carboxamide
- methylsulfanyl
- compound
- Prior art date
Links
- 229940043355 kinase inhibitor Drugs 0.000 title description 3
- 239000003757 phosphotransferase inhibitor Substances 0.000 title description 3
- GNOYRJIXSUNXIH-UHFFFAOYSA-N N1=CNC2=C3C=NN=C3C=CC2=C1 Chemical class N1=CNC2=C3C=NN=C3C=CC2=C1 GNOYRJIXSUNXIH-UHFFFAOYSA-N 0.000 title description 2
- 150000001875 compounds Chemical class 0.000 claims abstract description 406
- 238000000034 method Methods 0.000 claims abstract description 295
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims abstract description 19
- 230000000694 effects Effects 0.000 claims abstract description 19
- 102000001253 Protein Kinase Human genes 0.000 claims abstract description 14
- 239000008194 pharmaceutical composition Substances 0.000 claims abstract description 14
- 108060006633 protein kinase Proteins 0.000 claims abstract description 14
- 201000010099 disease Diseases 0.000 claims abstract description 12
- -1 2,6-difluorophenyl Chemical group 0.000 claims description 161
- 238000006243 chemical reaction Methods 0.000 claims description 144
- 125000000623 heterocyclic group Chemical group 0.000 claims description 67
- 125000003118 aryl group Chemical group 0.000 claims description 66
- 239000001257 hydrogen Substances 0.000 claims description 66
- 229910052739 hydrogen Inorganic materials 0.000 claims description 66
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 46
- 150000003839 salts Chemical class 0.000 claims description 43
- 210000004027 cell Anatomy 0.000 claims description 39
- 125000003710 aryl alkyl group Chemical group 0.000 claims description 36
- 125000001316 cycloalkyl alkyl group Chemical group 0.000 claims description 33
- 125000004415 heterocyclylalkyl group Chemical group 0.000 claims description 33
- 150000002431 hydrogen Chemical class 0.000 claims description 31
- 125000002816 methylsulfanyl group Chemical group [H]C([H])([H])S[*] 0.000 claims description 30
- 229910052760 oxygen Inorganic materials 0.000 claims description 25
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 24
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 claims description 24
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 24
- 229910052717 sulfur Inorganic materials 0.000 claims description 24
- 101001001642 Xenopus laevis Serine/threonine-protein kinase pim-3 Proteins 0.000 claims description 22
- 101100297651 Mus musculus Pim2 gene Proteins 0.000 claims description 20
- 206010028980 Neoplasm Diseases 0.000 claims description 20
- 108091000080 Phosphotransferase Proteins 0.000 claims description 19
- 229910052757 nitrogen Inorganic materials 0.000 claims description 19
- 102000020233 phosphotransferase Human genes 0.000 claims description 19
- 238000004519 manufacturing process Methods 0.000 claims description 17
- 239000003814 drug Substances 0.000 claims description 16
- 125000005842 heteroatom Chemical group 0.000 claims description 16
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 13
- 150000001412 amines Chemical class 0.000 claims description 12
- 125000001072 heteroaryl group Chemical group 0.000 claims description 12
- 229910052763 palladium Inorganic materials 0.000 claims description 12
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 11
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 claims description 11
- 201000011510 cancer Diseases 0.000 claims description 10
- 125000004482 piperidin-4-yl group Chemical group N1CCC(CC1)* 0.000 claims description 10
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 claims description 9
- UCAVIZKQSBARGL-UHFFFAOYSA-N 2h-quinazoline-3-carboxamide Chemical compound C1=CC=CC2=CN(C(=O)N)CN=C21 UCAVIZKQSBARGL-UHFFFAOYSA-N 0.000 claims description 8
- ZLQWCKMQAILQFX-UHFFFAOYSA-N 8-methylsulfanyl-2h-pyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(SC)=NC=C2C=CC2=C1NN=C2C(N)=O ZLQWCKMQAILQFX-UHFFFAOYSA-N 0.000 claims description 8
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 claims description 8
- 101100297652 Coturnix japonica PIM3 gene Proteins 0.000 claims description 8
- 208000032839 leukemia Diseases 0.000 claims description 8
- 208000031261 Acute myeloid leukaemia Diseases 0.000 claims description 7
- 239000000908 ammonium hydroxide Substances 0.000 claims description 7
- 238000000338 in vitro Methods 0.000 claims description 7
- 230000005764 inhibitory process Effects 0.000 claims description 7
- 125000000951 phenoxy group Chemical group [H]C1=C([H])C([H])=C(O*)C([H])=C1[H] 0.000 claims description 7
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Substances [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 claims description 7
- 125000000022 2-aminoethyl group Chemical group [H]C([*])([H])C([H])([H])N([H])[H] 0.000 claims description 6
- 125000004195 4-methylpiperazin-1-yl group Chemical group [H]C([H])([H])N1C([H])([H])C([H])([H])N(*)C([H])([H])C1([H])[H] 0.000 claims description 6
- 206010025323 Lymphomas Diseases 0.000 claims description 6
- 241000124008 Mammalia Species 0.000 claims description 6
- 208000033776 Myeloid Acute Leukemia Diseases 0.000 claims description 6
- 239000003054 catalyst Substances 0.000 claims description 6
- 230000004663 cell proliferation Effects 0.000 claims description 6
- 229940127089 cytotoxic agent Drugs 0.000 claims description 6
- 208000035475 disorder Diseases 0.000 claims description 6
- 230000002062 proliferating effect Effects 0.000 claims description 6
- JJDCLIXYKUZWCV-UHFFFAOYSA-N 1-methyl-8-methylsulfonyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1CC2=CN=C(S(C)(=O)=O)N=C2C2=C1C(C(N)=O)=NN2C JJDCLIXYKUZWCV-UHFFFAOYSA-N 0.000 claims description 5
- 125000000882 C2-C6 alkenyl group Chemical group 0.000 claims description 5
- 201000004681 Psoriasis Diseases 0.000 claims description 5
- 230000002378 acidificating effect Effects 0.000 claims description 5
- 150000003863 ammonium salts Chemical class 0.000 claims description 5
- 206010003246 arthritis Diseases 0.000 claims description 5
- 229910052799 carbon Inorganic materials 0.000 claims description 5
- 239000003795 chemical substances by application Substances 0.000 claims description 5
- 125000001309 chloro group Chemical group Cl* 0.000 claims description 5
- 125000002147 dimethylamino group Chemical group [H]C([H])([H])N(*)C([H])([H])[H] 0.000 claims description 5
- 230000001404 mediated effect Effects 0.000 claims description 5
- 239000007800 oxidant agent Substances 0.000 claims description 5
- 229910052697 platinum Inorganic materials 0.000 claims description 5
- VKAPJLWEZIYDSK-UHFFFAOYSA-N 1-tert-butyl-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(SC)=NC=C2C=CC2=C1N(C(C)(C)C)N=C2C(N)=O VKAPJLWEZIYDSK-UHFFFAOYSA-N 0.000 claims description 4
- MEYAPIXXJVEGHY-UHFFFAOYSA-N 6-amino-1-tert-butyl-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(SC)=NC(N)=C2C=CC2=C1N(C(C)(C)C)N=C2C(N)=O MEYAPIXXJVEGHY-UHFFFAOYSA-N 0.000 claims description 4
- QIHMJRJFJUQPND-UHFFFAOYSA-N 8-methylsulfanyl-4,5-dihydro-2h-pyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(SC)=NC=C2CCC2=C1NN=C2C(N)=O QIHMJRJFJUQPND-UHFFFAOYSA-N 0.000 claims description 4
- 208000024893 Acute lymphoblastic leukemia Diseases 0.000 claims description 4
- 208000014697 Acute lymphocytic leukaemia Diseases 0.000 claims description 4
- 201000009030 Carcinoma Diseases 0.000 claims description 4
- 208000022559 Inflammatory bowel disease Diseases 0.000 claims description 4
- 208000031481 Pathologic Constriction Diseases 0.000 claims description 4
- 208000006664 Precursor Cell Lymphoblastic Leukemia-Lymphoma Diseases 0.000 claims description 4
- 238000011319 anticancer therapy Methods 0.000 claims description 4
- 239000002246 antineoplastic agent Substances 0.000 claims description 4
- 125000001246 bromo group Chemical group Br* 0.000 claims description 4
- 239000003085 diluting agent Substances 0.000 claims description 4
- 208000037765 diseases and disorders Diseases 0.000 claims description 4
- 239000003937 drug carrier Substances 0.000 claims description 4
- 201000005787 hematologic cancer Diseases 0.000 claims description 4
- 208000024200 hematopoietic and lymphoid system neoplasm Diseases 0.000 claims description 4
- 210000002865 immune cell Anatomy 0.000 claims description 4
- 125000002346 iodo group Chemical group I* 0.000 claims description 4
- 230000036262 stenosis Effects 0.000 claims description 4
- 208000037804 stenosis Diseases 0.000 claims description 4
- 125000001273 sulfonato group Chemical group [O-]S(*)(=O)=O 0.000 claims description 4
- VUNLIWFVLSRDRX-UHFFFAOYSA-N 1-(2-chloroethyl)-8-methylsulfanyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(SC)=NC=C2CCC2=C1N(CCCl)N=C2C(N)=O VUNLIWFVLSRDRX-UHFFFAOYSA-N 0.000 claims description 3
- RNBCWFMUDRQZLJ-UHFFFAOYSA-N 1-(4-aminobutan-2-yl)-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(SC)=NC=C2C=CC2=C1N(C(C)CCN)N=C2C(N)=O RNBCWFMUDRQZLJ-UHFFFAOYSA-N 0.000 claims description 3
- GEOKAEHZKBKPQI-UHFFFAOYSA-N 1-[4-(1,3-dioxoisoindol-2-yl)butan-2-yl]-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound O=C1C2=CC=CC=C2C(=O)N1CCC(C)N1N=C(C(N)=O)C2=C1C1=NC(SC)=NC=C1C=C2 GEOKAEHZKBKPQI-UHFFFAOYSA-N 0.000 claims description 3
- RNHFYZVFJTWGLL-UHFFFAOYSA-N 1-[4-(ethylcarbamoylamino)cyclohexyl]-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1CC(NC(=O)NCC)CCC1N1C2=C3N=C(SC)N=CC3=CC=C2C(C(N)=O)=N1 RNHFYZVFJTWGLL-UHFFFAOYSA-N 0.000 claims description 3
- OUYAXBCNTRYHBH-UHFFFAOYSA-N 1-methyl-8-(3-nitrophenoxy)pyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound N=1C2=C3N(C)N=C(C(N)=O)C3=CC=C2C=NC=1OC1=CC=CC([N+]([O-])=O)=C1 OUYAXBCNTRYHBH-UHFFFAOYSA-N 0.000 claims description 3
- VAYXDRJDBFNMGP-UHFFFAOYSA-N 1-methyl-8-[4-(4-methylpiperazin-1-yl)phenoxy]-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1CN(C)CCN1C(C=C1)=CC=C1OC1=NC=C(CCC2=C3N(C)N=C2C(N)=O)C3=N1 VAYXDRJDBFNMGP-UHFFFAOYSA-N 0.000 claims description 3
- MKRDFCDKKBIATP-UHFFFAOYSA-N 1-methyl-8-[4-(4-methylpiperazin-1-yl)phenoxy]pyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1CN(C)CCN1C(C=C1)=CC=C1OC1=NC=C(C=CC2=C3N(C)N=C2C(N)=O)C3=N1 MKRDFCDKKBIATP-UHFFFAOYSA-N 0.000 claims description 3
- HRBCTOMPVLOHDP-UHFFFAOYSA-N 1-methyl-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(SC)=NC=C2C=CC2=C1N(C)N=C2C(N)=O HRBCTOMPVLOHDP-UHFFFAOYSA-N 0.000 claims description 3
- LELCLNIUIDJOIN-UHFFFAOYSA-N 1-methyl-8-piperidin-1-yl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound N1=C2C=3N(C)N=C(C(N)=O)C=3CCC2=CN=C1N1CCCCC1 LELCLNIUIDJOIN-UHFFFAOYSA-N 0.000 claims description 3
- XDERQDSXXASZLS-UHFFFAOYSA-N 1-tert-butylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1=NC=NC2=C3N(C(C)(C)C)N=C(C(N)=O)C3=CC=C21 XDERQDSXXASZLS-UHFFFAOYSA-N 0.000 claims description 3
- YYDLUFYHSZJENC-UHFFFAOYSA-N 6-amino-1-[2-(dimethylamino)ethyl]-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(SC)=NC(N)=C2C=CC2=C1N(CCN(C)C)N=C2C(N)=O YYDLUFYHSZJENC-UHFFFAOYSA-N 0.000 claims description 3
- SXYDRIGTWYCOCU-UHFFFAOYSA-N 8-[3-(hydroxymethyl)phenoxy]-1-methylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound N=1C2=C3N(C)N=C(C(N)=O)C3=CC=C2C=NC=1OC1=CC=CC(CO)=C1 SXYDRIGTWYCOCU-UHFFFAOYSA-N 0.000 claims description 3
- 201000001320 Atherosclerosis Diseases 0.000 claims description 3
- 206010004446 Benign prostatic hyperplasia Diseases 0.000 claims description 3
- MOIGHUQINXRYRV-WAAGHKOSSA-N C1=2C3=NC(SC)=NC=C3C=CC=2C(C(N)=O)=NN1[C@@H]1C[C@H](CO)C1 Chemical compound C1=2C3=NC(SC)=NC=C3C=CC=2C(C(N)=O)=NN1[C@@H]1C[C@H](CO)C1 MOIGHUQINXRYRV-WAAGHKOSSA-N 0.000 claims description 3
- MOIGHUQINXRYRV-CZMCAQCFSA-N C1=2C3=NC(SC)=NC=C3C=CC=2C(C(N)=O)=NN1[C@H]1C[C@H](CO)C1 Chemical compound C1=2C3=NC(SC)=NC=C3C=CC=2C(C(N)=O)=NN1[C@H]1C[C@H](CO)C1 MOIGHUQINXRYRV-CZMCAQCFSA-N 0.000 claims description 3
- 201000006107 Familial adenomatous polyposis Diseases 0.000 claims description 3
- 206010018364 Glomerulonephritis Diseases 0.000 claims description 3
- 208000009905 Neurofibromatoses Diseases 0.000 claims description 3
- 206010061902 Pancreatic neoplasm Diseases 0.000 claims description 3
- 206010060862 Prostate cancer Diseases 0.000 claims description 3
- 208000004403 Prostatic Hyperplasia Diseases 0.000 claims description 3
- 208000000236 Prostatic Neoplasms Diseases 0.000 claims description 3
- 208000005718 Stomach Neoplasms Diseases 0.000 claims description 3
- 208000029664 classic familial adenomatous polyposis Diseases 0.000 claims description 3
- 239000000824 cytostatic agent Substances 0.000 claims description 3
- 230000001085 cytostatic effect Effects 0.000 claims description 3
- 239000002254 cytotoxic agent Substances 0.000 claims description 3
- 231100000599 cytotoxic agent Toxicity 0.000 claims description 3
- 206010017758 gastric cancer Diseases 0.000 claims description 3
- 230000007062 hydrolysis Effects 0.000 claims description 3
- 238000006460 hydrolysis reaction Methods 0.000 claims description 3
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 claims description 3
- 201000004931 neurofibromatosis Diseases 0.000 claims description 3
- 201000002528 pancreatic cancer Diseases 0.000 claims description 3
- 208000008443 pancreatic carcinoma Diseases 0.000 claims description 3
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 3
- 230000002980 postoperative effect Effects 0.000 claims description 3
- 208000005069 pulmonary fibrosis Diseases 0.000 claims description 3
- 238000001959 radiotherapy Methods 0.000 claims description 3
- 201000011549 stomach cancer Diseases 0.000 claims description 3
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 claims description 3
- 230000002792 vascular Effects 0.000 claims description 3
- 125000006570 (C5-C6) heteroaryl group Chemical group 0.000 claims description 2
- TWTROWDMXIHRPT-UHFFFAOYSA-N 1-(1-amino-2-methyl-1-oxopropan-2-yl)-8-methylsulfanyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(SC)=NC=C2CCC2=C1N(C(C)(C)C(N)=O)N=C2C(N)=O TWTROWDMXIHRPT-UHFFFAOYSA-N 0.000 claims description 2
- LKTGTBCGEUXTAK-UHFFFAOYSA-N 1-(1-azabicyclo[2.2.2]octan-3-yl)-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1N(CC2)CCC2C1N1N=C(C(N)=O)C2=C1C1=NC(SC)=NC=C1C=C2 LKTGTBCGEUXTAK-UHFFFAOYSA-N 0.000 claims description 2
- ZNQSKYQYPXDKGH-UHFFFAOYSA-N 1-(1-hydroxy-2-methylpropan-2-yl)-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(SC)=NC=C2C=CC2=C1N(C(C)(C)CO)N=C2C(N)=O ZNQSKYQYPXDKGH-UHFFFAOYSA-N 0.000 claims description 2
- DMEYJQSLOJUNLH-UHFFFAOYSA-N 1-(2-fluoroethyl)-8-methylsulfanyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(SC)=NC=C2CCC2=C1N(CCF)N=C2C(N)=O DMEYJQSLOJUNLH-UHFFFAOYSA-N 0.000 claims description 2
- QINUFQDJAWPBEV-UHFFFAOYSA-N 1-(2-hydroxyethyl)-8-(3-nitrophenoxy)pyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound NC(=O)C1=NN(CCO)C(C2=N3)=C1C=CC2=CN=C3OC1=CC=CC([N+]([O-])=O)=C1 QINUFQDJAWPBEV-UHFFFAOYSA-N 0.000 claims description 2
- PVXPMCGSVKVEOQ-UHFFFAOYSA-N 1-(2-hydroxyethyl)-8-[3-(4-methylpiperazin-1-yl)phenoxy]pyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1CN(C)CCN1C1=CC=CC(OC=2N=C3C=4N(CCO)N=C(C=4C=CC3=CN=2)C(N)=O)=C1 PVXPMCGSVKVEOQ-UHFFFAOYSA-N 0.000 claims description 2
- OAWRTTNPONQUTR-UHFFFAOYSA-N 1-(2-hydroxyethyl)-8-[4-(4-methylpiperazin-1-yl)phenoxy]pyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1CN(C)CCN1C(C=C1)=CC=C1OC1=NC=C(C=CC2=C3N(CCO)N=C2C(N)=O)C3=N1 OAWRTTNPONQUTR-UHFFFAOYSA-N 0.000 claims description 2
- XKMFPGRFLQHILJ-UHFFFAOYSA-N 1-(2-hydroxyethyl)-8-methoxypyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(OC)=NC=C2C=CC2=C1N(CCO)N=C2C(N)=O XKMFPGRFLQHILJ-UHFFFAOYSA-N 0.000 claims description 2
- CBHXEMXGWPYSBM-UHFFFAOYSA-N 1-(2-hydroxyethyl)-8-methylsulfanyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(SC)=NC=C2CCC2=C1N(CCO)N=C2C(N)=O CBHXEMXGWPYSBM-UHFFFAOYSA-N 0.000 claims description 2
- VZSALDSEPCCIJL-UHFFFAOYSA-N 1-(2-hydroxyethyl)-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(SC)=NC=C2C=CC2=C1N(CCO)N=C2C(N)=O VZSALDSEPCCIJL-UHFFFAOYSA-N 0.000 claims description 2
- MZUSSOCCUWPBAM-UHFFFAOYSA-N 1-(2-hydroxyethyl)-8-phenoxypyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound NC(=O)C1=NN(CCO)C(C2=N3)=C1C=CC2=CN=C3OC1=CC=CC=C1 MZUSSOCCUWPBAM-UHFFFAOYSA-N 0.000 claims description 2
- OAIURKJUXVZWKS-UHFFFAOYSA-N 1-(2-methoxyethyl)-8-methylsulfanyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1CC2=CN=C(SC)N=C2C2=C1C(C(N)=O)=NN2CCOC OAIURKJUXVZWKS-UHFFFAOYSA-N 0.000 claims description 2
- HNPHLZMAYAXKMW-UHFFFAOYSA-N 1-(4-aminocyclohexyl)-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1=2C3=NC(SC)=NC=C3C=CC=2C(C(N)=O)=NN1C1CCC(N)CC1 HNPHLZMAYAXKMW-UHFFFAOYSA-N 0.000 claims description 2
- TWJFLTKVSUVGIB-UHFFFAOYSA-N 1-[2-(dimethylamino)ethyl]-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(SC)=NC=C2C=CC2=C1N(CCN(C)C)N=C2C(N)=O TWJFLTKVSUVGIB-UHFFFAOYSA-N 0.000 claims description 2
- BTUCCAJXLGWWKZ-UHFFFAOYSA-N 1-[3-(dimethylamino)propyl]-8-ethoxy-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(OCC)=NC=C2CCC2=C1N(CCCN(C)C)N=C2C(N)=O BTUCCAJXLGWWKZ-UHFFFAOYSA-N 0.000 claims description 2
- RFAYIBDZFAINQL-UHFFFAOYSA-N 1-[3-(dimethylamino)propyl]-8-methylsulfanyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(SC)=NC=C2CCC2=C1N(CCCN(C)C)N=C2C(N)=O RFAYIBDZFAINQL-UHFFFAOYSA-N 0.000 claims description 2
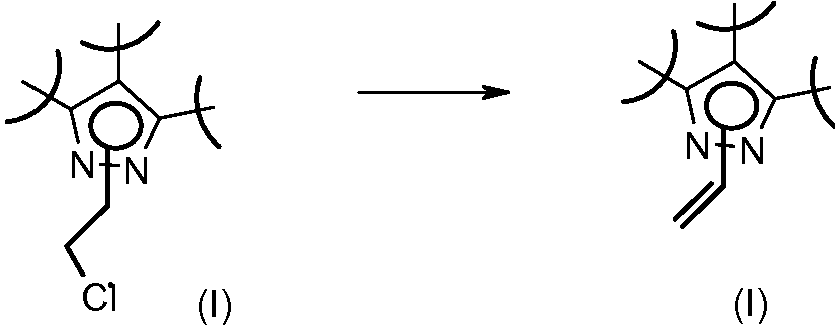
- YXXJXKLYUYCZOS-UHFFFAOYSA-N 1-ethenyl-8-methylsulfanyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(SC)=NC=C2CCC2=C1N(C=C)N=C2C(N)=O YXXJXKLYUYCZOS-UHFFFAOYSA-N 0.000 claims description 2
- STSYKYVCQKPJJV-UHFFFAOYSA-N 1-methyl-8-(3-piperazin-1-ylphenoxy)-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound N1=C2C=3N(C)N=C(C(N)=O)C=3CCC2=CN=C1OC(C=1)=CC=CC=1N1CCNCC1 STSYKYVCQKPJJV-UHFFFAOYSA-N 0.000 claims description 2
- KGBUBMICPNIBPP-UHFFFAOYSA-N 1-methyl-8-(4-nitroimidazol-1-yl)-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound N1=C2C=3N(C)N=C(C(N)=O)C=3CCC2=CN=C1N1C=NC([N+]([O-])=O)=C1 KGBUBMICPNIBPP-UHFFFAOYSA-N 0.000 claims description 2
- CIHNYXLFCKDJCK-UHFFFAOYSA-N 1-methyl-8-[3-(4-methylpiperazin-1-yl)phenoxy]pyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1CN(C)CCN1C1=CC=CC(OC=2N=C3C=4N(C)N=C(C=4C=CC3=CN=2)C(N)=O)=C1 CIHNYXLFCKDJCK-UHFFFAOYSA-N 0.000 claims description 2
- KDFDUWMFEYWXNH-UHFFFAOYSA-N 1-methyl-8-[3-(morpholin-4-ylmethyl)phenoxy]pyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound N=1C2=C3N(C)N=C(C(N)=O)C3=CC=C2C=NC=1OC(C=1)=CC=CC=1CN1CCOCC1 KDFDUWMFEYWXNH-UHFFFAOYSA-N 0.000 claims description 2
- IVWIENHLOGARKE-UHFFFAOYSA-N 1-methyl-8-[3-[(4-methylpiperazin-1-yl)methyl]phenoxy]pyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1CN(C)CCN1CC1=CC=CC(OC=2N=C3C=4N(C)N=C(C=4C=CC3=CN=2)C(N)=O)=C1 IVWIENHLOGARKE-UHFFFAOYSA-N 0.000 claims description 2
- QYOQMWLXSIKXHO-UHFFFAOYSA-N 1-methyl-8-methylsulfanyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(SC)=NC=C2CCC2=C1N(C)N=C2C(N)=O QYOQMWLXSIKXHO-UHFFFAOYSA-N 0.000 claims description 2
- ZCFKVDATEGHYAB-UHFFFAOYSA-N 1-methyl-8-phenoxy-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound N1=C2C=3N(C)N=C(C(N)=O)C=3CCC2=CN=C1OC1=CC=CC=C1 ZCFKVDATEGHYAB-UHFFFAOYSA-N 0.000 claims description 2
- WIRWFGUYSGGQDX-UHFFFAOYSA-N 1-methyl-8-pyrazol-1-yl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound N1=C2C=3N(C)N=C(C(N)=O)C=3CCC2=CN=C1N1C=CC=N1 WIRWFGUYSGGQDX-UHFFFAOYSA-N 0.000 claims description 2
- VESZGMYQLXEVMZ-UHFFFAOYSA-N 1-methyl-8-pyridin-4-yloxy-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound N1=C2C=3N(C)N=C(C(N)=O)C=3CCC2=CN=C1OC1=CC=NC=C1 VESZGMYQLXEVMZ-UHFFFAOYSA-N 0.000 claims description 2
- PKOKOHNNMSBMDU-UHFFFAOYSA-N 1-tert-butyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1CC2=CN=CN=C2C2=C1C(C(N)=O)=NN2C(C)(C)C PKOKOHNNMSBMDU-UHFFFAOYSA-N 0.000 claims description 2
- KULDHYDPVJTULH-UHFFFAOYSA-N 1-tert-butyl-8-(dimethylamino)pyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(N(C)C)=NC=C2C=CC2=C1N(C(C)(C)C)N=C2C(N)=O KULDHYDPVJTULH-UHFFFAOYSA-N 0.000 claims description 2
- OVKKBCIXQQNJFM-UHFFFAOYSA-N 1-tert-butyl-8-[4-(4-methylpiperazin-1-yl)phenoxy]pyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1CN(C)CCN1C(C=C1)=CC=C1OC1=NC=C(C=CC2=C3N(N=C2C(N)=O)C(C)(C)C)C3=N1 OVKKBCIXQQNJFM-UHFFFAOYSA-N 0.000 claims description 2
- JQFBWAFNEIHUMM-UHFFFAOYSA-N 1-tert-butyl-8-methylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(C)=NC=C2C=CC2=C1N(C(C)(C)C)N=C2C(N)=O JQFBWAFNEIHUMM-UHFFFAOYSA-N 0.000 claims description 2
- PWXZOFMDEXLBIQ-UHFFFAOYSA-N 1-tert-butyl-8-methylsulfanyl-6-morpholin-4-ylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C=12C=CC=3C(C(N)=O)=NN(C(C)(C)C)C=3C2=NC(SC)=NC=1N1CCOCC1 PWXZOFMDEXLBIQ-UHFFFAOYSA-N 0.000 claims description 2
- NIQUFIVTWOQRIR-UHFFFAOYSA-N 1-tert-butyl-N-hydroxy-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(SC)=NC=C2C=CC2=C1N(C(C)(C)C)N=C2C(=O)NO NIQUFIVTWOQRIR-UHFFFAOYSA-N 0.000 claims description 2
- UXMSRDKDGKAPSN-UHFFFAOYSA-N 1-tert-butyl-n-(1-methylpiperidin-4-yl)-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound N=1N(C(C)(C)C)C=2C3=NC(SC)=NC=C3C=CC=2C=1C(=O)NC1CCN(C)CC1 UXMSRDKDGKAPSN-UHFFFAOYSA-N 0.000 claims description 2
- QNSOGPZERKLDNN-UHFFFAOYSA-N 1-tert-butyl-n-(2-hydroxyethyl)-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(SC)=NC=C2C=CC2=C1N(C(C)(C)C)N=C2C(=O)NCCO QNSOGPZERKLDNN-UHFFFAOYSA-N 0.000 claims description 2
- UDTKSLIIOSMLRF-UHFFFAOYSA-N 1-tert-butyl-n-[2-(dimethylamino)ethyl]-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(SC)=NC=C2C=CC2=C1N(C(C)(C)C)N=C2C(=O)NCCN(C)C UDTKSLIIOSMLRF-UHFFFAOYSA-N 0.000 claims description 2
- UIXROJRKTQHFSR-UHFFFAOYSA-N 1-tert-butyl-n-methyl-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1=CC2=CN=C(SC)N=C2C2=C1C(C(=O)NC)=NN2C(C)(C)C UIXROJRKTQHFSR-UHFFFAOYSA-N 0.000 claims description 2
- SPRZVNSCNVHWNU-UHFFFAOYSA-N 2-[2-(dimethylamino)ethyl]-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1=CC2=C(C(N)=O)N(CCN(C)C)N=C2C2=NC(SC)=NC=C21 SPRZVNSCNVHWNU-UHFFFAOYSA-N 0.000 claims description 2
- CVTFNRHCAIZJEM-UHFFFAOYSA-N 6-amino-1-methyl-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(SC)=NC(N)=C2C=CC2=C1N(C)N=C2C(N)=O CVTFNRHCAIZJEM-UHFFFAOYSA-N 0.000 claims description 2
- BIXDEHDGXCNLPH-UHFFFAOYSA-N 6-amino-1-tert-butylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound NC1=NC=NC2=C3N(C(C)(C)C)N=C(C(N)=O)C3=CC=C21 BIXDEHDGXCNLPH-UHFFFAOYSA-N 0.000 claims description 2
- VCYLZULDANKZTH-UHFFFAOYSA-N 8-(2-chlorophenoxy)-1-methylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound N=1C2=C3N(C)N=C(C(N)=O)C3=CC=C2C=NC=1OC1=CC=CC=C1Cl VCYLZULDANKZTH-UHFFFAOYSA-N 0.000 claims description 2
- JQZKLMWZZMZHEP-UHFFFAOYSA-N 8-(2-fluoroethoxy)-1-methyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1CC2=CN=C(OCCF)N=C2C2=C1C(C(N)=O)=NN2C JQZKLMWZZMZHEP-UHFFFAOYSA-N 0.000 claims description 2
- UKQZQDCVHIULFP-UHFFFAOYSA-N 8-(2-fluorophenoxy)-1-methylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound N=1C2=C3N(C)N=C(C(N)=O)C3=CC=C2C=NC=1OC1=CC=CC=C1F UKQZQDCVHIULFP-UHFFFAOYSA-N 0.000 claims description 2
- QENWBUNQKHVEKE-UHFFFAOYSA-N 8-(3-aminophenoxy)-1-(2-hydroxyethyl)pyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound NC(=O)C1=NN(CCO)C(C2=N3)=C1C=CC2=CN=C3OC1=CC=CC(N)=C1 QENWBUNQKHVEKE-UHFFFAOYSA-N 0.000 claims description 2
- SOTWQYFXXKKVMT-UHFFFAOYSA-N 8-(3-aminophenoxy)-1-methyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound N1=C2C=3N(C)N=C(C(N)=O)C=3CCC2=CN=C1OC1=CC=CC(N)=C1 SOTWQYFXXKKVMT-UHFFFAOYSA-N 0.000 claims description 2
- PAYSSAVMLZYWBV-UHFFFAOYSA-N 8-(3-aminophenoxy)-1-methylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound N=1C2=C3N(C)N=C(C(N)=O)C3=CC=C2C=NC=1OC1=CC=CC(N)=C1 PAYSSAVMLZYWBV-UHFFFAOYSA-N 0.000 claims description 2
- GFCCWNZUZUSIPA-UHFFFAOYSA-N 8-(3-formylphenoxy)-1-methylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound N=1C2=C3N(C)N=C(C(N)=O)C3=CC=C2C=NC=1OC1=CC=CC(C=O)=C1 GFCCWNZUZUSIPA-UHFFFAOYSA-N 0.000 claims description 2
- BGQNRSJYKSDQNW-UHFFFAOYSA-N 8-(4-aminophenoxy)-1-methyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound N1=C2C=3N(C)N=C(C(N)=O)C=3CCC2=CN=C1OC1=CC=C(N)C=C1 BGQNRSJYKSDQNW-UHFFFAOYSA-N 0.000 claims description 2
- FEGSEUOXIJOJSU-UHFFFAOYSA-N 8-[3-(dimethylamino)phenoxy]-1-methylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound CN(C)C1=CC=CC(OC=2N=C3C=4N(C)N=C(C=4C=CC3=CN=2)C(N)=O)=C1 FEGSEUOXIJOJSU-UHFFFAOYSA-N 0.000 claims description 2
- ANJCTQQJZBVRFX-UHFFFAOYSA-N 8-[3-[(dimethylamino)methyl]phenoxy]-1-methylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound CN(C)CC1=CC=CC(OC=2N=C3C=4N(C)N=C(C=4C=CC3=CN=2)C(N)=O)=C1 ANJCTQQJZBVRFX-UHFFFAOYSA-N 0.000 claims description 2
- UEZIQYIHVRIWQC-UHFFFAOYSA-N 8-cyano-1-methyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1CC2=CN=C(C#N)N=C2C2=C1C(C(N)=O)=NN2C UEZIQYIHVRIWQC-UHFFFAOYSA-N 0.000 claims description 2
- PLAFWAHDXTXYKE-UHFFFAOYSA-N 8-ethoxy-1-(piperidin-4-ylmethyl)-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1=2C3=NC(OCC)=NC=C3CCC=2C(C(N)=O)=NN1CC1CCNCC1 PLAFWAHDXTXYKE-UHFFFAOYSA-N 0.000 claims description 2
- DUZUTTXUYKFNEI-UHFFFAOYSA-N 8-ethoxy-1-[(1-methylpiperidin-4-yl)methyl]-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1=2C3=NC(OCC)=NC=C3CCC=2C(C(N)=O)=NN1CC1CCN(C)CC1 DUZUTTXUYKFNEI-UHFFFAOYSA-N 0.000 claims description 2
- ZEOCCBSKAJINPU-UHFFFAOYSA-N 8-ethoxy-1-methylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(OCC)=NC=C2C=CC2=C1N(C)N=C2C(N)=O ZEOCCBSKAJINPU-UHFFFAOYSA-N 0.000 claims description 2
- MPSCKCKQUYBFEN-UHFFFAOYSA-N 8-imidazol-1-yl-1-methyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound N1=C2C=3N(C)N=C(C(N)=O)C=3CCC2=CN=C1N1C=CN=C1 MPSCKCKQUYBFEN-UHFFFAOYSA-N 0.000 claims description 2
- MOCIUOIBJQISIO-UHFFFAOYSA-N 8-methoxy-1-methylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(OC)=NC=C2C=CC2=C1N(C)N=C2C(N)=O MOCIUOIBJQISIO-UHFFFAOYSA-N 0.000 claims description 2
- STMGLZIHXIYPRM-UHFFFAOYSA-N 8-methoxy-2h-pyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(OC)=NC=C2C=CC2=C1NN=C2C(N)=O STMGLZIHXIYPRM-UHFFFAOYSA-N 0.000 claims description 2
- RVPDBWSVXYWCND-UHFFFAOYSA-N 8-methylsulfanyl-1-(oxan-4-yl)pyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1=2C3=NC(SC)=NC=C3C=CC=2C(C(N)=O)=NN1C1CCOCC1 RVPDBWSVXYWCND-UHFFFAOYSA-N 0.000 claims description 2
- 208000036762 Acute promyelocytic leukaemia Diseases 0.000 claims description 2
- 206010002556 Ankylosing Spondylitis Diseases 0.000 claims description 2
- 206010003571 Astrocytoma Diseases 0.000 claims description 2
- 208000023275 Autoimmune disease Diseases 0.000 claims description 2
- 208000003950 B-cell lymphoma Diseases 0.000 claims description 2
- 208000032791 BCR-ABL1 positive chronic myelogenous leukemia Diseases 0.000 claims description 2
- 206010005003 Bladder cancer Diseases 0.000 claims description 2
- 206010006187 Breast cancer Diseases 0.000 claims description 2
- 208000026310 Breast neoplasm Diseases 0.000 claims description 2
- 206010008342 Cervix carcinoma Diseases 0.000 claims description 2
- 208000010833 Chronic myeloid leukaemia Diseases 0.000 claims description 2
- 206010009900 Colitis ulcerative Diseases 0.000 claims description 2
- 206010009944 Colon cancer Diseases 0.000 claims description 2
- 208000011231 Crohn disease Diseases 0.000 claims description 2
- 206010013786 Dry skin Diseases 0.000 claims description 2
- 208000000461 Esophageal Neoplasms Diseases 0.000 claims description 2
- 201000008808 Fibrosarcoma Diseases 0.000 claims description 2
- 208000022072 Gallbladder Neoplasms Diseases 0.000 claims description 2
- 208000032612 Glial tumor Diseases 0.000 claims description 2
- 206010018338 Glioma Diseases 0.000 claims description 2
- 208000017604 Hodgkin disease Diseases 0.000 claims description 2
- 208000021519 Hodgkin lymphoma Diseases 0.000 claims description 2
- 208000010747 Hodgkins lymphoma Diseases 0.000 claims description 2
- 206010020751 Hypersensitivity Diseases 0.000 claims description 2
- 208000007766 Kaposi sarcoma Diseases 0.000 claims description 2
- 208000008839 Kidney Neoplasms Diseases 0.000 claims description 2
- 206010058467 Lung neoplasm malignant Diseases 0.000 claims description 2
- 206010027406 Mesothelioma Diseases 0.000 claims description 2
- 206010027476 Metastases Diseases 0.000 claims description 2
- 201000003793 Myelodysplastic syndrome Diseases 0.000 claims description 2
- 208000033761 Myelogenous Chronic BCR-ABL Positive Leukemia Diseases 0.000 claims description 2
- 206010029260 Neuroblastoma Diseases 0.000 claims description 2
- 208000015914 Non-Hodgkin lymphomas Diseases 0.000 claims description 2
- 206010030155 Oesophageal carcinoma Diseases 0.000 claims description 2
- 206010033128 Ovarian cancer Diseases 0.000 claims description 2
- 206010061535 Ovarian neoplasm Diseases 0.000 claims description 2
- 206010033645 Pancreatitis Diseases 0.000 claims description 2
- 206010038389 Renal cancer Diseases 0.000 claims description 2
- 206010039710 Scleroderma Diseases 0.000 claims description 2
- 206010041067 Small cell lung cancer Diseases 0.000 claims description 2
- 201000009594 Systemic Scleroderma Diseases 0.000 claims description 2
- 206010042953 Systemic sclerosis Diseases 0.000 claims description 2
- 206010042971 T-cell lymphoma Diseases 0.000 claims description 2
- 208000027585 T-cell non-Hodgkin lymphoma Diseases 0.000 claims description 2
- 208000024770 Thyroid neoplasm Diseases 0.000 claims description 2
- 201000006704 Ulcerative Colitis Diseases 0.000 claims description 2
- 208000007097 Urinary Bladder Neoplasms Diseases 0.000 claims description 2
- 208000006105 Uterine Cervical Neoplasms Diseases 0.000 claims description 2
- 206010047115 Vasculitis Diseases 0.000 claims description 2
- 206010047642 Vitiligo Diseases 0.000 claims description 2
- 230000001154 acute effect Effects 0.000 claims description 2
- 230000007815 allergy Effects 0.000 claims description 2
- 230000001093 anti-cancer Effects 0.000 claims description 2
- 208000006673 asthma Diseases 0.000 claims description 2
- 210000003169 central nervous system Anatomy 0.000 claims description 2
- 201000010881 cervical cancer Diseases 0.000 claims description 2
- 238000002512 chemotherapy Methods 0.000 claims description 2
- 208000029742 colonic neoplasm Diseases 0.000 claims description 2
- 230000037336 dry skin Effects 0.000 claims description 2
- 201000004101 esophageal cancer Diseases 0.000 claims description 2
- 230000003325 follicular Effects 0.000 claims description 2
- 201000010175 gallbladder cancer Diseases 0.000 claims description 2
- 125000000336 imidazol-5-yl group Chemical group [H]N1C([H])=NC([H])=C1[*] 0.000 claims description 2
- 208000027866 inflammatory disease Diseases 0.000 claims description 2
- 230000002757 inflammatory effect Effects 0.000 claims description 2
- 208000002551 irritable bowel syndrome Diseases 0.000 claims description 2
- 201000010982 kidney cancer Diseases 0.000 claims description 2
- 201000007270 liver cancer Diseases 0.000 claims description 2
- 208000014018 liver neoplasm Diseases 0.000 claims description 2
- 201000005202 lung cancer Diseases 0.000 claims description 2
- 208000020816 lung neoplasm Diseases 0.000 claims description 2
- 210000004324 lymphatic system Anatomy 0.000 claims description 2
- 201000001441 melanoma Diseases 0.000 claims description 2
- 230000009401 metastasis Effects 0.000 claims description 2
- 201000006417 multiple sclerosis Diseases 0.000 claims description 2
- 206010028417 myasthenia gravis Diseases 0.000 claims description 2
- 208000007538 neurilemmoma Diseases 0.000 claims description 2
- 201000008482 osteoarthritis Diseases 0.000 claims description 2
- 201000008968 osteosarcoma Diseases 0.000 claims description 2
- 210000001428 peripheral nervous system Anatomy 0.000 claims description 2
- 208000037803 restenosis Diseases 0.000 claims description 2
- 201000009410 rhabdomyosarcoma Diseases 0.000 claims description 2
- 206010039073 rheumatoid arthritis Diseases 0.000 claims description 2
- 206010039667 schwannoma Diseases 0.000 claims description 2
- 208000000587 small cell lung carcinoma Diseases 0.000 claims description 2
- 201000000596 systemic lupus erythematosus Diseases 0.000 claims description 2
- 208000001608 teratocarcinoma Diseases 0.000 claims description 2
- 201000002510 thyroid cancer Diseases 0.000 claims description 2
- 210000001685 thyroid gland Anatomy 0.000 claims description 2
- 230000005747 tumor angiogenesis Effects 0.000 claims description 2
- 201000005112 urinary bladder cancer Diseases 0.000 claims description 2
- LRKOMEWBGLPTEP-UHFFFAOYSA-N 1-(2-aminoethyl)-8-methylsulfanyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(SC)=NC=C2CCC2=C1N(CCN)N=C2C(N)=O LRKOMEWBGLPTEP-UHFFFAOYSA-N 0.000 claims 1
- WTATXACZNSHVCC-UHFFFAOYSA-N 1-(2-aminoethyl)-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(SC)=NC=C2C=CC2=C1N(CCN)N=C2C(N)=O WTATXACZNSHVCC-UHFFFAOYSA-N 0.000 claims 1
- BCXCSCKINDRGDV-UHFFFAOYSA-N 1-(3-amino-2,2-dimethylpropyl)-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(SC)=NC=C2C=CC2=C1N(CC(C)(C)CN)N=C2C(N)=O BCXCSCKINDRGDV-UHFFFAOYSA-N 0.000 claims 1
- SYKBTJQDLFSGCT-UHFFFAOYSA-N 1-(3-aminopropyl)-8-(4-fluorophenyl)-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound N1=C2C=3N(CCCN)N=C(C(N)=O)C=3CCC2=CN=C1C1=CC=C(F)C=C1 SYKBTJQDLFSGCT-UHFFFAOYSA-N 0.000 claims 1
- IYCHKPVQZCIZPH-UHFFFAOYSA-N 1-(3-aminopropyl)-8-methylsulfanyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(SC)=NC=C2CCC2=C1N(CCCN)N=C2C(N)=O IYCHKPVQZCIZPH-UHFFFAOYSA-N 0.000 claims 1
- PLNCXWDLDLWTLR-UHFFFAOYSA-N 1-(3-aminopropyl)-n-(3-hydroxypropyl)-8-(4-methoxyphenyl)-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1=CC(OC)=CC=C1C1=NC=C(CCC2=C3N(CCCN)N=C2C(=O)NCCCO)C3=N1 PLNCXWDLDLWTLR-UHFFFAOYSA-N 0.000 claims 1
- LVARNYMAVJXLNN-UHFFFAOYSA-N 1-(4-aminocyclohexyl)-8-phenylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1CC(N)CCC1N1C2=C3N=C(C=4C=CC=CC=4)N=CC3=CC=C2C(C(N)=O)=N1 LVARNYMAVJXLNN-UHFFFAOYSA-N 0.000 claims 1
- RZYZBMQCFYVCRG-UHFFFAOYSA-N 1-(4-aminocyclohexyl)-8-thiophen-3-ylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1CC(N)CCC1N1C2=C3N=C(C4=CSC=C4)N=CC3=CC=C2C(C(N)=O)=N1 RZYZBMQCFYVCRG-UHFFFAOYSA-N 0.000 claims 1
- JUEUGXCBGVOMGY-UHFFFAOYSA-N 1-[4-(2-aminoethylamino)cyclohexyl]-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1=2C3=NC(SC)=NC=C3C=CC=2C(C(N)=O)=NN1C1CCC(NCCN)CC1 JUEUGXCBGVOMGY-UHFFFAOYSA-N 0.000 claims 1
- ZRQWMQIIJCLHDI-UHFFFAOYSA-N 1-[[1-(2-aminoethyl)piperidin-4-yl]methyl]-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1=2C3=NC(SC)=NC=C3C=CC=2C(C(N)=O)=NN1CC1CCN(CCN)CC1 ZRQWMQIIJCLHDI-UHFFFAOYSA-N 0.000 claims 1
- MJQKMFSXFHMHJO-UHFFFAOYSA-N 1-methyl-8-(3-piperazin-1-ylphenoxy)pyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound N=1C2=C3N(C)N=C(C(N)=O)C3=CC=C2C=NC=1OC(C=1)=CC=CC=1N1CCNCC1 MJQKMFSXFHMHJO-UHFFFAOYSA-N 0.000 claims 1
- FIVYBNHVRIKFQQ-UHFFFAOYSA-N 1-methyl-8-(4-piperazin-1-ylphenoxy)-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound N1=C2C=3N(C)N=C(C(N)=O)C=3CCC2=CN=C1OC(C=C1)=CC=C1N1CCNCC1 FIVYBNHVRIKFQQ-UHFFFAOYSA-N 0.000 claims 1
- OKCZJHNWXOACMJ-UHFFFAOYSA-N 1-methyl-8-(4-piperazin-1-ylphenoxy)pyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound N=1C2=C3N(C)N=C(C(N)=O)C3=CC=C2C=NC=1OC(C=C1)=CC=C1N1CCNCC1 OKCZJHNWXOACMJ-UHFFFAOYSA-N 0.000 claims 1
- FQCXYHUFIJDIOS-UHFFFAOYSA-N 1-piperidin-4-yl-8-pyrrolidin-1-ylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1=CC2=CN=C(N3CCCC3)N=C2C2=C1C(C(=O)N)=NN2C1CCNCC1 FQCXYHUFIJDIOS-UHFFFAOYSA-N 0.000 claims 1
- ACAJLACRJCSBJH-UHFFFAOYSA-N 1-piperidin-4-yl-8-thiophen-3-ylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1=CC2=CN=C(C3=CSC=C3)N=C2C2=C1C(C(=O)N)=NN2C1CCNCC1 ACAJLACRJCSBJH-UHFFFAOYSA-N 0.000 claims 1
- BFWAEPUWLCPSOJ-UHFFFAOYSA-N 1-tert-butyl-8-methyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(C)=NC=C2CCC2=C1N(C(C)(C)C)N=C2C(N)=O BFWAEPUWLCPSOJ-UHFFFAOYSA-N 0.000 claims 1
- RMGSJAWOCSTGBU-UHFFFAOYSA-N 2-(2-aminoethyl)-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1=CC2=C(C(N)=O)N(CCN)N=C2C2=NC(SC)=NC=C21 RMGSJAWOCSTGBU-UHFFFAOYSA-N 0.000 claims 1
- QZTUMBOHVDZAQZ-UHFFFAOYSA-N 2-(3-aminopropyl)-8-(4-fluorophenyl)-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound NC(=O)C=1N(CCCN)N=C(C2=N3)C=1CCC2=CN=C3C1=CC=C(F)C=C1 QZTUMBOHVDZAQZ-UHFFFAOYSA-N 0.000 claims 1
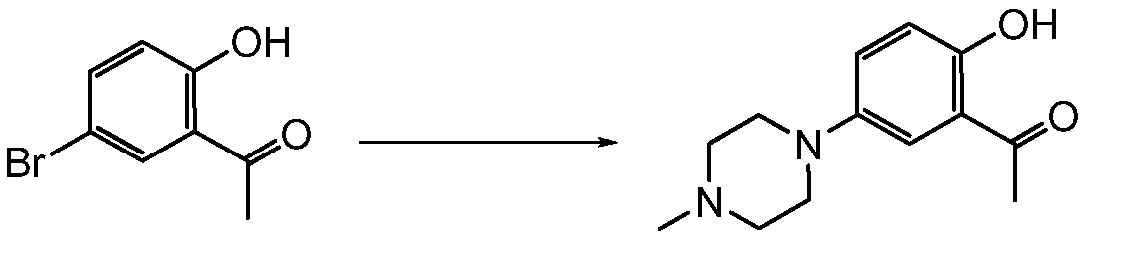
- XUSTXVKBPPEJTB-UHFFFAOYSA-N 8-(2-acetyl-4-piperazin-1-ylphenoxy)-1-methylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C=1C=C(OC=2N=C3C=4N(C)N=C(C=4C=CC3=CN=2)C(N)=O)C(C(=O)C)=CC=1N1CCNCC1 XUSTXVKBPPEJTB-UHFFFAOYSA-N 0.000 claims 1
- JEQSKHMTQOZZCJ-UHFFFAOYSA-N 8-[2-bromo-4-(4-methylpiperazin-1-yl)phenoxy]-1-methyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1CN(C)CCN1C(C=C1Br)=CC=C1OC1=NC=C(CCC2=C3N(C)N=C2C(N)=O)C3=N1 JEQSKHMTQOZZCJ-UHFFFAOYSA-N 0.000 claims 1
- YLHNUZKKPKEXKG-UHFFFAOYSA-N 8-[2-bromo-4-(4-methylpiperazin-1-yl)phenoxy]-1-methylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1CN(C)CCN1C(C=C1Br)=CC=C1OC1=NC=C(C=CC2=C3N(C)N=C2C(N)=O)C3=N1 YLHNUZKKPKEXKG-UHFFFAOYSA-N 0.000 claims 1
- RDWJXFCCAHEKOR-UHFFFAOYSA-N 8-[2-cyano-4-(4-methylpiperazin-1-yl)phenoxy]-1-methylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1CN(C)CCN1C(C=C1C#N)=CC=C1OC1=NC=C(C=CC2=C3N(C)N=C2C(N)=O)C3=N1 RDWJXFCCAHEKOR-UHFFFAOYSA-N 0.000 claims 1
- JRAAQCHOYNCFFZ-UHFFFAOYSA-N 8-[2-fluoro-4-(4-methylpiperazin-1-yl)phenoxy]-1-methyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1CN(C)CCN1C(C=C1F)=CC=C1OC1=NC=C(CCC2=C3N(C)N=C2C(N)=O)C3=N1 JRAAQCHOYNCFFZ-UHFFFAOYSA-N 0.000 claims 1
- RBJDZNDMORCREZ-UHFFFAOYSA-N 8-[2-fluoro-4-(4-methylpiperazin-1-yl)phenoxy]-1-methylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1CN(C)CCN1C(C=C1F)=CC=C1OC1=NC=C(C=CC2=C3N(C)N=C2C(N)=O)C3=N1 RBJDZNDMORCREZ-UHFFFAOYSA-N 0.000 claims 1
- VQNFZMWEOSUDLJ-UHFFFAOYSA-N 8-ethoxy-1-piperidin-4-yl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1=2C3=NC(OCC)=NC=C3CCC=2C(C(N)=O)=NN1C1CCNCC1 VQNFZMWEOSUDLJ-UHFFFAOYSA-N 0.000 claims 1
- IEHSRRWGTPBPBS-UHFFFAOYSA-N 8-methoxy-1-(piperidin-4-ylmethyl)pyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1=2C3=NC(OC)=NC=C3C=CC=2C(C(N)=O)=NN1CC1CCNCC1 IEHSRRWGTPBPBS-UHFFFAOYSA-N 0.000 claims 1
- ASNUCCUQVOWYJK-UHFFFAOYSA-N 8-methoxy-1-piperidin-4-ylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1=2C3=NC(OC)=NC=C3C=CC=2C(C(N)=O)=NN1C1CCNCC1 ASNUCCUQVOWYJK-UHFFFAOYSA-N 0.000 claims 1
- MAOPRIAVJYUOAS-UHFFFAOYSA-N 8-methylsulfanyl-1-(piperidin-3-ylmethyl)pyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1=2C3=NC(SC)=NC=C3C=CC=2C(C(N)=O)=NN1CC1CCCNC1 MAOPRIAVJYUOAS-UHFFFAOYSA-N 0.000 claims 1
- DISAVFVQPMPLTA-UHFFFAOYSA-N 8-methylsulfanyl-1-(piperidin-4-ylmethyl)-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1=2C3=NC(SC)=NC=C3CCC=2C(C(N)=O)=NN1CC1CCNCC1 DISAVFVQPMPLTA-UHFFFAOYSA-N 0.000 claims 1
- YDPXWMLSPPALQZ-UHFFFAOYSA-N 8-methylsulfanyl-1-(piperidin-4-ylmethyl)pyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1=2C3=NC(SC)=NC=C3C=CC=2C(C(N)=O)=NN1CC1CCNCC1 YDPXWMLSPPALQZ-UHFFFAOYSA-N 0.000 claims 1
- PFQKTVGKNDEUFN-UHFFFAOYSA-N 8-methylsulfanyl-1-piperidin-3-ylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1=2C3=NC(SC)=NC=C3C=CC=2C(C(N)=O)=NN1C1CCCNC1 PFQKTVGKNDEUFN-UHFFFAOYSA-N 0.000 claims 1
- HGSBPQDWGFYNNP-UHFFFAOYSA-N 8-methylsulfanyl-1-piperidin-4-yl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1=2C3=NC(SC)=NC=C3CCC=2C(C(N)=O)=NN1C1CCNCC1 HGSBPQDWGFYNNP-UHFFFAOYSA-N 0.000 claims 1
- HJQKTMCQWAPCGN-UHFFFAOYSA-N 8-methylsulfanyl-1-piperidin-4-ylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1=2C3=NC(SC)=NC=C3C=CC=2C(C(N)=O)=NN1C1CCNCC1 HJQKTMCQWAPCGN-UHFFFAOYSA-N 0.000 claims 1
- XSTHZLJONIIAPY-UHFFFAOYSA-N 8-methylsulfanyl-2-(piperidin-4-ylmethyl)pyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound N1=C2C3=NC(SC)=NC=C3C=CC2=C(C(N)=O)N1CC1CCNCC1 XSTHZLJONIIAPY-UHFFFAOYSA-N 0.000 claims 1
- DPUDZUHBRIBMIF-UHFFFAOYSA-N 8-morpholin-4-yl-1-piperidin-4-ylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1=CC2=CN=C(N3CCOCC3)N=C2C2=C1C(C(=O)N)=NN2C1CCNCC1 DPUDZUHBRIBMIF-UHFFFAOYSA-N 0.000 claims 1
- 241000156724 Antirhea Species 0.000 claims 1
- 208000011691 Burkitt lymphomas Diseases 0.000 claims 1
- 206010013554 Diverticulum Diseases 0.000 claims 1
- 206010041349 Somnolence Diseases 0.000 claims 1
- 208000026935 allergic disease Diseases 0.000 claims 1
- 230000001771 impaired effect Effects 0.000 claims 1
- 201000001513 prostate squamous cell carcinoma Diseases 0.000 claims 1
- 230000004952 protein activity Effects 0.000 claims 1
- 238000004383 yellowing Methods 0.000 claims 1
- 108010083755 proto-oncogene proteins pim Proteins 0.000 abstract description 5
- JWVCLYRUEFBMGU-UHFFFAOYSA-N quinazoline Chemical class N1=CN=CC2=CC=CC=C21 JWVCLYRUEFBMGU-UHFFFAOYSA-N 0.000 abstract description 2
- IAZDPXIOMUYVGZ-WFGJKAKNSA-N Dimethyl sulfoxide Chemical compound [2H]C([2H])([2H])S(=O)C([2H])([2H])[2H] IAZDPXIOMUYVGZ-WFGJKAKNSA-N 0.000 description 284
- 238000004128 high performance liquid chromatography Methods 0.000 description 209
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 172
- 238000005481 NMR spectroscopy Methods 0.000 description 167
- 238000000132 electrospray ionisation Methods 0.000 description 166
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 144
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 144
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 132
- 239000000203 mixture Substances 0.000 description 91
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 81
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 80
- 239000000243 solution Substances 0.000 description 75
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 71
- 235000019439 ethyl acetate Nutrition 0.000 description 63
- 238000002360 preparation method Methods 0.000 description 59
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 58
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 56
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 55
- 239000011734 sodium Substances 0.000 description 48
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 47
- 239000002904 solvent Substances 0.000 description 44
- 239000007787 solid Substances 0.000 description 40
- 239000000047 product Substances 0.000 description 38
- 239000012267 brine Substances 0.000 description 29
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 29
- 238000012360 testing method Methods 0.000 description 29
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 27
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 26
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 26
- 239000003039 volatile agent Substances 0.000 description 26
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 25
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 25
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 24
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 24
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 23
- 239000012044 organic layer Substances 0.000 description 21
- 101000595531 Homo sapiens Serine/threonine-protein kinase pim-1 Proteins 0.000 description 19
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 19
- 102100036077 Serine/threonine-protein kinase pim-1 Human genes 0.000 description 19
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 18
- FJDQFPXHSGXQBY-UHFFFAOYSA-L caesium carbonate Chemical compound [Cs+].[Cs+].[O-]C([O-])=O FJDQFPXHSGXQBY-UHFFFAOYSA-L 0.000 description 18
- 229910000024 caesium carbonate Inorganic materials 0.000 description 18
- 239000012074 organic phase Substances 0.000 description 18
- 229920006395 saturated elastomer Polymers 0.000 description 18
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Substances [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 17
- 239000003643 water by type Substances 0.000 description 17
- 125000000954 2-hydroxyethyl group Chemical group [H]C([*])([H])C([H])([H])O[H] 0.000 description 16
- 239000000872 buffer Substances 0.000 description 16
- 238000010898 silica gel chromatography Methods 0.000 description 16
- 125000001255 4-fluorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1F 0.000 description 15
- 239000011541 reaction mixture Substances 0.000 description 15
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical compound [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 14
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 14
- 238000003818 flash chromatography Methods 0.000 description 14
- 150000002500 ions Chemical class 0.000 description 14
- 238000010992 reflux Methods 0.000 description 14
- 229910052796 boron Inorganic materials 0.000 description 13
- 239000003112 inhibitor Substances 0.000 description 13
- 230000002401 inhibitory effect Effects 0.000 description 13
- 238000011282 treatment Methods 0.000 description 13
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 12
- 239000002585 base Substances 0.000 description 12
- 229940079593 drug Drugs 0.000 description 12
- 239000012071 phase Substances 0.000 description 12
- 230000008569 process Effects 0.000 description 12
- 101001064870 Homo sapiens Lon protease homolog, mitochondrial Proteins 0.000 description 11
- 238000004440 column chromatography Methods 0.000 description 11
- 229910000027 potassium carbonate Inorganic materials 0.000 description 11
- 239000011347 resin Substances 0.000 description 11
- 229920005989 resin Polymers 0.000 description 11
- 239000007858 starting material Substances 0.000 description 11
- 239000000758 substrate Substances 0.000 description 11
- 230000007704 transition Effects 0.000 description 11
- 239000003153 chemical reaction reagent Substances 0.000 description 10
- 238000002953 preparative HPLC Methods 0.000 description 10
- HEMHJVSKTPXQMS-UHFFFAOYSA-M sodium hydroxide Inorganic materials [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 10
- 125000002221 trityl group Chemical group [H]C1=C([H])C([H])=C([H])C([H])=C1C([*])(C1=C(C(=C(C(=C1[H])[H])[H])[H])[H])C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 10
- 102000004190 Enzymes Human genes 0.000 description 9
- 108090000790 Enzymes Proteins 0.000 description 9
- 239000007864 aqueous solution Substances 0.000 description 9
- 239000003638 chemical reducing agent Substances 0.000 description 9
- 230000004048 modification Effects 0.000 description 9
- 238000012986 modification Methods 0.000 description 9
- 239000000725 suspension Substances 0.000 description 9
- LMDZBCPBFSXMTL-UHFFFAOYSA-N 1-ethyl-3-(3-dimethylaminopropyl)carbodiimide Chemical compound CCN=C=NCCCN(C)C LMDZBCPBFSXMTL-UHFFFAOYSA-N 0.000 description 8
- HZNVUJQVZSTENZ-UHFFFAOYSA-N 2,3-dichloro-5,6-dicyano-1,4-benzoquinone Chemical compound ClC1=C(Cl)C(=O)C(C#N)=C(C#N)C1=O HZNVUJQVZSTENZ-UHFFFAOYSA-N 0.000 description 8
- 101001001648 Homo sapiens Serine/threonine-protein kinase pim-2 Proteins 0.000 description 8
- 102100036120 Serine/threonine-protein kinase pim-2 Human genes 0.000 description 8
- 229960000583 acetic acid Drugs 0.000 description 8
- 150000001299 aldehydes Chemical class 0.000 description 8
- XTEOJPUYZWEXFI-UHFFFAOYSA-N butyl n-[3-[4-(imidazol-1-ylmethyl)phenyl]-5-(2-methylpropyl)thiophen-2-yl]sulfonylcarbamate Chemical compound S1C(CC(C)C)=CC(C=2C=CC(CN3C=NC=C3)=CC=2)=C1S(=O)(=O)NC(=O)OCCCC XTEOJPUYZWEXFI-UHFFFAOYSA-N 0.000 description 8
- 238000007796 conventional method Methods 0.000 description 8
- 125000004170 methylsulfonyl group Chemical group [H]C([H])([H])S(*)(=O)=O 0.000 description 8
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 8
- 230000002829 reductive effect Effects 0.000 description 8
- 239000000741 silica gel Substances 0.000 description 8
- 229910002027 silica gel Inorganic materials 0.000 description 8
- 239000000377 silicon dioxide Substances 0.000 description 8
- 0 **(CCC1)CC1N1NC2c3nc(*)nc(*)c3*C2C1C(*)=O Chemical compound **(CCC1)CC1N1NC2c3nc(*)nc(*)c3*C2C1C(*)=O 0.000 description 7
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 7
- CLZISMQKJZCZDN-UHFFFAOYSA-N [benzotriazol-1-yloxy(dimethylamino)methylidene]-dimethylazanium Chemical compound C1=CC=C2N(OC(N(C)C)=[N+](C)C)N=NC2=C1 CLZISMQKJZCZDN-UHFFFAOYSA-N 0.000 description 7
- 235000019270 ammonium chloride Nutrition 0.000 description 7
- 235000011114 ammonium hydroxide Nutrition 0.000 description 7
- 238000004458 analytical method Methods 0.000 description 7
- 238000004587 chromatography analysis Methods 0.000 description 7
- 238000001816 cooling Methods 0.000 description 7
- 238000002347 injection Methods 0.000 description 7
- 239000007924 injection Substances 0.000 description 7
- 238000002156 mixing Methods 0.000 description 7
- 239000002244 precipitate Substances 0.000 description 7
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 description 7
- QOXOZONBQWIKDA-UHFFFAOYSA-N 3-hydroxypropyl Chemical group [CH2]CCO QOXOZONBQWIKDA-UHFFFAOYSA-N 0.000 description 6
- 125000004172 4-methoxyphenyl group Chemical group [H]C1=C([H])C(OC([H])([H])[H])=C([H])C([H])=C1* 0.000 description 6
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 6
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 6
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 6
- OAKJQQAXSVQMHS-UHFFFAOYSA-N Hydrazine Chemical compound NN OAKJQQAXSVQMHS-UHFFFAOYSA-N 0.000 description 6
- 150000001204 N-oxides Chemical class 0.000 description 6
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 6
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical compound C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 6
- 239000012317 TBTU Substances 0.000 description 6
- 125000003545 alkoxy group Chemical group 0.000 description 6
- 150000003857 carboxamides Chemical class 0.000 description 6
- MVPPADPHJFYWMZ-UHFFFAOYSA-N chlorobenzene Chemical compound ClC1=CC=CC=C1 MVPPADPHJFYWMZ-UHFFFAOYSA-N 0.000 description 6
- 239000000463 material Substances 0.000 description 6
- SCVFZCLFOSHCOH-UHFFFAOYSA-M potassium acetate Chemical compound [K+].CC([O-])=O SCVFZCLFOSHCOH-UHFFFAOYSA-M 0.000 description 6
- 108090000623 proteins and genes Proteins 0.000 description 6
- 238000000746 purification Methods 0.000 description 6
- 150000003335 secondary amines Chemical class 0.000 description 6
- 239000012321 sodium triacetoxyborohydride Substances 0.000 description 6
- 239000000126 substance Substances 0.000 description 6
- RMZDXTBIBYDFHR-UHFFFAOYSA-N 2h-quinazoline-3-carboxylic acid Chemical compound C1=CC=CC2=CN(C(=O)O)CN=C21 RMZDXTBIBYDFHR-UHFFFAOYSA-N 0.000 description 5
- KXDHJXZQYSOELW-UHFFFAOYSA-M Carbamate Chemical compound NC([O-])=O KXDHJXZQYSOELW-UHFFFAOYSA-M 0.000 description 5
- 239000007995 HEPES buffer Substances 0.000 description 5
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 5
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 5
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 5
- 230000015572 biosynthetic process Effects 0.000 description 5
- 125000004093 cyano group Chemical group *C#N 0.000 description 5
- 238000010790 dilution Methods 0.000 description 5
- 239000012895 dilution Substances 0.000 description 5
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 5
- WMFOQBRAJBCJND-UHFFFAOYSA-M lithium hydroxide Inorganic materials [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 5
- 235000019988 mead Nutrition 0.000 description 5
- 239000002207 metabolite Substances 0.000 description 5
- 238000006366 phosphorylation reaction Methods 0.000 description 5
- 150000003141 primary amines Chemical class 0.000 description 5
- 238000012545 processing Methods 0.000 description 5
- 102000004169 proteins and genes Human genes 0.000 description 5
- 150000003254 radicals Chemical class 0.000 description 5
- 125000000467 secondary amino group Chemical group [H]N([*:1])[*:2] 0.000 description 5
- 238000000926 separation method Methods 0.000 description 5
- 235000015424 sodium Nutrition 0.000 description 5
- 229940083542 sodium Drugs 0.000 description 5
- 210000004881 tumor cell Anatomy 0.000 description 5
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 5
- BYYRKLKNJKBDCR-UHFFFAOYSA-N 1-(4-aminocyclohexyl)-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide;hydrochloride Chemical compound Cl.C1=2C3=NC(SC)=NC=C3C=CC=2C(C(N)=O)=NN1C1CCC(N)CC1 BYYRKLKNJKBDCR-UHFFFAOYSA-N 0.000 description 4
- PVOAHINGSUIXLS-UHFFFAOYSA-N 1-Methylpiperazine Chemical compound CN1CCNCC1 PVOAHINGSUIXLS-UHFFFAOYSA-N 0.000 description 4
- NHQDETIJWKXCTC-UHFFFAOYSA-N 3-chloroperbenzoic acid Chemical compound OOC(=O)C1=CC=CC(Cl)=C1 NHQDETIJWKXCTC-UHFFFAOYSA-N 0.000 description 4
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 4
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 4
- GQHTUMJGOHRCHB-UHFFFAOYSA-N DBU Substances C1CCCCN2CCCN=C21 GQHTUMJGOHRCHB-UHFFFAOYSA-N 0.000 description 4
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical compound C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 4
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 4
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 4
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 4
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 4
- 229930006000 Sucrose Natural products 0.000 description 4
- DTQVDTLACAAQTR-UHFFFAOYSA-M Trifluoroacetate Chemical compound [O-]C(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-M 0.000 description 4
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 4
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 4
- 239000002253 acid Substances 0.000 description 4
- 239000004037 angiogenesis inhibitor Substances 0.000 description 4
- 239000006227 byproduct Substances 0.000 description 4
- 239000000969 carrier Substances 0.000 description 4
- 239000013058 crude material Substances 0.000 description 4
- 238000006356 dehydrogenation reaction Methods 0.000 description 4
- 239000003480 eluent Substances 0.000 description 4
- RXXABMLMKKIICJ-UHFFFAOYSA-N ethyl 1-tert-butyl-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxylate Chemical compound C1=CC2=CN=C(SC)N=C2C2=C1C(C(=O)OCC)=NN2C(C)(C)C RXXABMLMKKIICJ-UHFFFAOYSA-N 0.000 description 4
- HOHJFALABWNCJK-UHFFFAOYSA-N ethyl 8-methylsulfanyl-2h-pyrazolo[4,3-h]quinazoline-3-carboxylate Chemical compound C1=CC2=CN=C(SC)N=C2C2=C1C(C(=O)OCC)=NN2 HOHJFALABWNCJK-UHFFFAOYSA-N 0.000 description 4
- 239000012091 fetal bovine serum Substances 0.000 description 4
- 238000001914 filtration Methods 0.000 description 4
- 150000003840 hydrochlorides Chemical class 0.000 description 4
- 239000002609 medium Substances 0.000 description 4
- 229920001467 poly(styrenesulfonates) Polymers 0.000 description 4
- 239000011591 potassium Substances 0.000 description 4
- 239000000651 prodrug Substances 0.000 description 4
- 229940002612 prodrug Drugs 0.000 description 4
- 230000035755 proliferation Effects 0.000 description 4
- WGYKZJWCGVVSQN-UHFFFAOYSA-N propylamine Chemical group CCCN WGYKZJWCGVVSQN-UHFFFAOYSA-N 0.000 description 4
- 229910000104 sodium hydride Inorganic materials 0.000 description 4
- 229960004793 sucrose Drugs 0.000 description 4
- 230000004083 survival effect Effects 0.000 description 4
- 238000003786 synthesis reaction Methods 0.000 description 4
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 4
- 229920002554 vinyl polymer Polymers 0.000 description 4
- PNYZSOIVSRGIAZ-UHFFFAOYSA-N 1-methyl-8-methylsulfonylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1=NC(S(C)(=O)=O)=NC2=C3N(C)N=C(C(N)=O)C3=CC=C21 PNYZSOIVSRGIAZ-UHFFFAOYSA-N 0.000 description 3
- 125000004214 1-pyrrolidinyl group Chemical group [H]C1([H])N(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 3
- XZLRJCSXDLXBSC-UHFFFAOYSA-N 3-[(2-methylpropan-2-yl)oxycarbonylamino]propyl 2-cyanoacetate Chemical group CC(C)(C)OC(=O)NCCCOC(=O)CC#N XZLRJCSXDLXBSC-UHFFFAOYSA-N 0.000 description 3
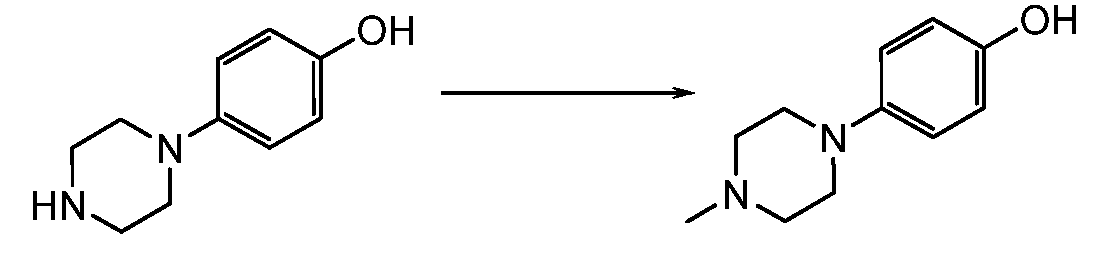
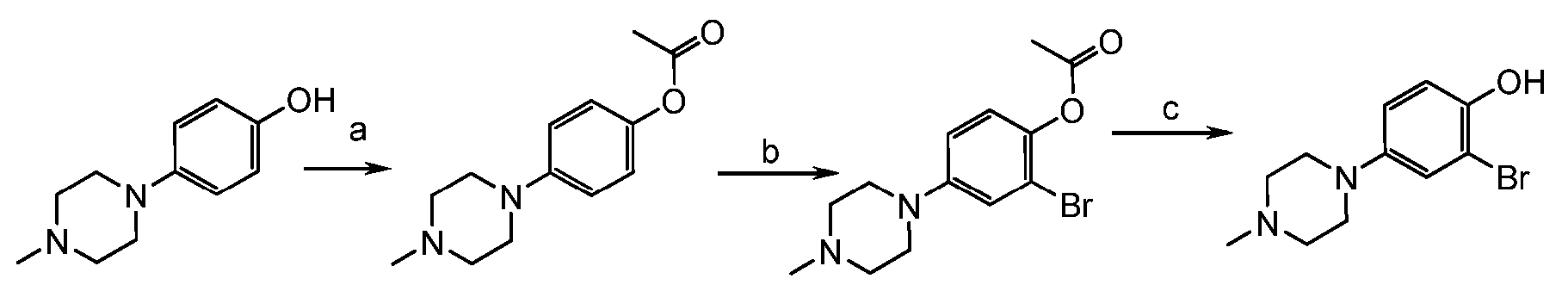
- RWDJMTACZOUIAI-UHFFFAOYSA-N 4-(4-methylpiperazin-1-yl)phenol Chemical compound C1CN(C)CCN1C1=CC=C(O)C=C1 RWDJMTACZOUIAI-UHFFFAOYSA-N 0.000 description 3
- IYBFLPBNFZDLGO-UHFFFAOYSA-N 8-(4-fluorophenyl)-1-[3-[(2-methylpropan-2-yl)oxycarbonylamino]propyl]-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxylic acid Chemical compound N1=C2C=3N(CCCNC(=O)OC(C)(C)C)N=C(C(O)=O)C=3CCC2=CN=C1C1=CC=C(F)C=C1 IYBFLPBNFZDLGO-UHFFFAOYSA-N 0.000 description 3
- WFDIJRYMOXRFFG-UHFFFAOYSA-N Acetic anhydride Chemical compound CC(=O)OC(C)=O WFDIJRYMOXRFFG-UHFFFAOYSA-N 0.000 description 3
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 3
- RGSFGYAAUTVSQA-UHFFFAOYSA-N Cyclopentane Chemical compound C1CCCC1 RGSFGYAAUTVSQA-UHFFFAOYSA-N 0.000 description 3
- QOSSAOTZNIDXMA-UHFFFAOYSA-N Dicylcohexylcarbodiimide Chemical compound C1CCCCC1N=C=NC1CCCCC1 QOSSAOTZNIDXMA-UHFFFAOYSA-N 0.000 description 3
- 101000610640 Homo sapiens U4/U6 small nuclear ribonucleoprotein Prp3 Proteins 0.000 description 3
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 3
- 229930182816 L-glutamine Natural products 0.000 description 3
- OFOBLEOULBTSOW-UHFFFAOYSA-N Malonic acid Chemical compound OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 3
- 108700020796 Oncogene Proteins 0.000 description 3
- 102000043276 Oncogene Human genes 0.000 description 3
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 3
- 206010035226 Plasma cell myeloma Diseases 0.000 description 3
- 102000001708 Protein Isoforms Human genes 0.000 description 3
- 108010029485 Protein Isoforms Proteins 0.000 description 3
- 239000006146 Roswell Park Memorial Institute medium Substances 0.000 description 3
- 101001110823 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) 60S ribosomal protein L6-A Proteins 0.000 description 3
- 101000712176 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) 60S ribosomal protein L6-B Proteins 0.000 description 3
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 3
- 102100040374 U4/U6 small nuclear ribonucleoprotein Prp3 Human genes 0.000 description 3
- 125000003342 alkenyl group Chemical group 0.000 description 3
- 125000000217 alkyl group Chemical group 0.000 description 3
- 125000000304 alkynyl group Chemical group 0.000 description 3
- 230000027455 binding Effects 0.000 description 3
- 239000011230 binding agent Substances 0.000 description 3
- 238000006664 bond formation reaction Methods 0.000 description 3
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Chemical compound BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 3
- 150000007942 carboxylates Chemical class 0.000 description 3
- 238000012054 celltiter-glo Methods 0.000 description 3
- KXZJHVJKXJLBKO-UHFFFAOYSA-N chembl1408157 Chemical compound N=1C2=CC=CC=C2C(C(=O)O)=CC=1C1=CC=C(O)C=C1 KXZJHVJKXJLBKO-UHFFFAOYSA-N 0.000 description 3
- 239000000460 chlorine Substances 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 239000011248 coating agent Substances 0.000 description 3
- 238000000576 coating method Methods 0.000 description 3
- 238000006880 cross-coupling reaction Methods 0.000 description 3
- 239000012043 crude product Substances 0.000 description 3
- 235000013681 dietary sucrose Nutrition 0.000 description 3
- XWAZKFWFTMMONG-UHFFFAOYSA-N ethyl 1-tert-butyl-7-oxo-5,6-dihydro-4h-indazole-3-carboxylate Chemical compound C1CCC(=O)C2=C1C(C(=O)OCC)=NN2C(C)(C)C XWAZKFWFTMMONG-UHFFFAOYSA-N 0.000 description 3
- 238000002474 experimental method Methods 0.000 description 3
- 125000000524 functional group Chemical group 0.000 description 3
- 229910052736 halogen Chemical group 0.000 description 3
- 125000005843 halogen group Chemical group 0.000 description 3
- 150000002367 halogens Chemical group 0.000 description 3
- DMEGYFMYUHOHGS-UHFFFAOYSA-N heptamethylene Natural products C1CCCCCC1 DMEGYFMYUHOHGS-UHFFFAOYSA-N 0.000 description 3
- 150000004677 hydrates Chemical class 0.000 description 3
- NPZTUJOABDZTLV-UHFFFAOYSA-N hydroxybenzotriazole Substances O=C1C=CC=C2NNN=C12 NPZTUJOABDZTLV-UHFFFAOYSA-N 0.000 description 3
- 238000001727 in vivo Methods 0.000 description 3
- 239000011777 magnesium Substances 0.000 description 3
- 125000000325 methylidene group Chemical group [H]C([H])=* 0.000 description 3
- 230000035772 mutation Effects 0.000 description 3
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 3
- 230000002246 oncogenic effect Effects 0.000 description 3
- DNUTZBZXLPWRJG-UHFFFAOYSA-M piperidine-1-carboxylate Chemical compound [O-]C(=O)N1CCCCC1 DNUTZBZXLPWRJG-UHFFFAOYSA-M 0.000 description 3
- 235000011056 potassium acetate Nutrition 0.000 description 3
- NNFCIKHAZHQZJG-UHFFFAOYSA-N potassium cyanide Chemical compound [K+].N#[C-] NNFCIKHAZHQZJG-UHFFFAOYSA-N 0.000 description 3
- 108090000765 processed proteins & peptides Proteins 0.000 description 3
- 125000003226 pyrazolyl group Chemical group 0.000 description 3
- 238000006268 reductive amination reaction Methods 0.000 description 3
- 238000004007 reversed phase HPLC Methods 0.000 description 3
- 150000003384 small molecules Chemical class 0.000 description 3
- 239000012279 sodium borohydride Substances 0.000 description 3
- 229910000033 sodium borohydride Inorganic materials 0.000 description 3
- BEOOHQFXGBMRKU-UHFFFAOYSA-N sodium cyanoborohydride Chemical compound [Na+].[B-]C#N BEOOHQFXGBMRKU-UHFFFAOYSA-N 0.000 description 3
- 239000012453 solvate Substances 0.000 description 3
- 125000005931 tert-butyloxycarbonyl group Chemical group [H]C([H])([H])C(OC(*)=O)(C([H])([H])[H])C([H])([H])[H] 0.000 description 3
- 238000004809 thin layer chromatography Methods 0.000 description 3
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 3
- 229940121358 tyrosine kinase inhibitor Drugs 0.000 description 3
- 239000005483 tyrosine kinase inhibitor Substances 0.000 description 3
- OSGACEPPJOFGDS-UHFFFAOYSA-N 1-(3-aminopropyl)-8-(4-fluorophenyl)-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide;2,2,2-trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.N1=C2C=3N(CCCN)N=C(C(N)=O)C=3CCC2=CN=C1C1=CC=C(F)C=C1 OSGACEPPJOFGDS-UHFFFAOYSA-N 0.000 description 2
- ASOKPJOREAFHNY-UHFFFAOYSA-N 1-Hydroxybenzotriazole Chemical compound C1=CC=C2N(O)N=NC2=C1 ASOKPJOREAFHNY-UHFFFAOYSA-N 0.000 description 2
- 125000004973 1-butenyl group Chemical group C(=CCC)* 0.000 description 2
- 125000006039 1-hexenyl group Chemical group 0.000 description 2
- IIZPXYDJLKNOIY-JXPKJXOSSA-N 1-palmitoyl-2-arachidonoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCC\C=C/C\C=C/C\C=C/C\C=C/CCCCC IIZPXYDJLKNOIY-JXPKJXOSSA-N 0.000 description 2
- 125000006017 1-propenyl group Chemical group 0.000 description 2
- HCCQJTAQYCXAGM-UHFFFAOYSA-N 1-tert-butyl-8-methylsulfanyl-n-(oxan-2-yloxy)pyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound N=1N(C(C)(C)C)C=2C3=NC(SC)=NC=C3C=CC=2C=1C(=O)NOC1CCCCO1 HCCQJTAQYCXAGM-UHFFFAOYSA-N 0.000 description 2
- 125000000453 2,2,2-trichloroethyl group Chemical group [H]C([H])(*)C(Cl)(Cl)Cl 0.000 description 2
- YTMCJARGEHWXRH-UHFFFAOYSA-N 2-(3-aminopropyl)-8-(4-fluorophenyl)-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide;2,2,2-trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.NC(=O)C=1N(CCCN)N=C(C2=N3)C=1CCC2=CN=C3C1=CC=C(F)C=C1 YTMCJARGEHWXRH-UHFFFAOYSA-N 0.000 description 2
- 125000004974 2-butenyl group Chemical group C(C=CC)* 0.000 description 2
- 125000004777 2-fluoroethyl group Chemical group [H]C([H])(F)C([H])([H])* 0.000 description 2
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 2
- LJGHYPLBDBRCRZ-UHFFFAOYSA-N 3-(3-aminophenyl)sulfonylaniline Chemical group NC1=CC=CC(S(=O)(=O)C=2C=C(N)C=CC=2)=C1 LJGHYPLBDBRCRZ-UHFFFAOYSA-N 0.000 description 2
- 125000004975 3-butenyl group Chemical group C(CC=C)* 0.000 description 2
- HJBLUNHMOKFZQX-UHFFFAOYSA-N 3-hydroxy-1,2,3-benzotriazin-4-one Chemical compound C1=CC=C2C(=O)N(O)N=NC2=C1 HJBLUNHMOKFZQX-UHFFFAOYSA-N 0.000 description 2
- IAVREABSGIHHMO-UHFFFAOYSA-N 3-hydroxybenzaldehyde Chemical compound OC1=CC=CC(C=O)=C1 IAVREABSGIHHMO-UHFFFAOYSA-N 0.000 description 2
- 125000001541 3-thienyl group Chemical group S1C([H])=C([*])C([H])=C1[H] 0.000 description 2
- GPEOAEVZTOQXLG-UHFFFAOYSA-N 4-piperazin-1-ium-1-ylphenolate Chemical compound C1=CC(O)=CC=C1N1CCNCC1 GPEOAEVZTOQXLG-UHFFFAOYSA-N 0.000 description 2
- CLCPDSJUXHDRGX-UHFFFAOYSA-N 6-(1,3-dihydroxyisobutyl)thymine Chemical compound CC1=C(CC(CO)CO)NC(=O)NC1=O CLCPDSJUXHDRGX-UHFFFAOYSA-N 0.000 description 2
- WDYVUKGVKRZQNM-UHFFFAOYSA-N 6-phosphonohexylphosphonic acid Chemical compound OP(O)(=O)CCCCCCP(O)(O)=O WDYVUKGVKRZQNM-UHFFFAOYSA-N 0.000 description 2
- BIRPIGJJJTXZIP-UHFFFAOYSA-N 8-(2-acetylphenoxy)-1-methyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound CC(=O)C1=CC=CC=C1OC1=NC=C(CCC2=C3N(C)N=C2C(N)=O)C3=N1 BIRPIGJJJTXZIP-UHFFFAOYSA-N 0.000 description 2
- INMDGYIZAPMJJL-UHFFFAOYSA-N 8-(4-fluorophenyl)-1-trityl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxylic acid Chemical compound OC(=O)C1=NN(C(C=2C=CC=CC=2)(C=2C=CC=CC=2)C=2C=CC=CC=2)C(C2=N3)=C1CCC2=CN=C3C1=CC=C(F)C=C1 INMDGYIZAPMJJL-UHFFFAOYSA-N 0.000 description 2
- UTXUXEPUTHIWGZ-UHFFFAOYSA-N 8-(4-fluorophenyl)-n-(3-hydroxypropyl)-1-trityl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound OCCCNC(=O)C1=NN(C(C=2C=CC=CC=2)(C=2C=CC=CC=2)C=2C=CC=CC=2)C(C2=N3)=C1CCC2=CN=C3C1=CC=C(F)C=C1 UTXUXEPUTHIWGZ-UHFFFAOYSA-N 0.000 description 2
- BHNBLEKOCWIXNL-UHFFFAOYSA-N 8-[2-(2-hydroxyphenyl)-2-oxoethyl]-1-methyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound N1=C2C=3N(C)N=C(C(N)=O)C=3CCC2=CN=C1CC(=O)C1=CC=CC=C1O BHNBLEKOCWIXNL-UHFFFAOYSA-N 0.000 description 2
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 2
- MVPMGXJVHLRWPB-UHFFFAOYSA-N 8-iodo-4,5-dihydro-2h-pyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1CC2=CN=C(I)N=C2C2=C1C(C(=O)N)=NN2 MVPMGXJVHLRWPB-UHFFFAOYSA-N 0.000 description 2
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 2
- KXDHJXZQYSOELW-UHFFFAOYSA-N Carbamic acid Chemical compound NC(O)=O KXDHJXZQYSOELW-UHFFFAOYSA-N 0.000 description 2
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 2
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 2
- 229940123587 Cell cycle inhibitor Drugs 0.000 description 2
- 102100033270 Cyclin-dependent kinase inhibitor 1 Human genes 0.000 description 2
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 2
- 229940123780 DNA topoisomerase I inhibitor Drugs 0.000 description 2
- 229940124087 DNA topoisomerase II inhibitor Drugs 0.000 description 2
- ROSDSFDQCJNGOL-UHFFFAOYSA-N Dimethylamine Chemical compound CNC ROSDSFDQCJNGOL-UHFFFAOYSA-N 0.000 description 2
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 2
- QUSNBJAOOMFDIB-UHFFFAOYSA-N Ethylamine Chemical compound CCN QUSNBJAOOMFDIB-UHFFFAOYSA-N 0.000 description 2
- 102100022466 Eukaryotic translation initiation factor 4E-binding protein 1 Human genes 0.000 description 2
- 108050000946 Eukaryotic translation initiation factor 4E-binding protein 1 Proteins 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 2
- AEMRFAOFKBGASW-UHFFFAOYSA-N Glycolic acid Chemical compound OCC(O)=O AEMRFAOFKBGASW-UHFFFAOYSA-N 0.000 description 2
- 101000932478 Homo sapiens Receptor-type tyrosine-protein kinase FLT3 Proteins 0.000 description 2
- 208000031671 Large B-Cell Diffuse Lymphoma Diseases 0.000 description 2
- 108091054455 MAP kinase family Proteins 0.000 description 2
- 102000043136 MAP kinase family Human genes 0.000 description 2
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 2
- 208000025205 Mantle-Cell Lymphoma Diseases 0.000 description 2
- BZLVMXJERCGZMT-UHFFFAOYSA-N Methyl tert-butyl ether Chemical compound COC(C)(C)C BZLVMXJERCGZMT-UHFFFAOYSA-N 0.000 description 2
- BAVYZALUXZFZLV-UHFFFAOYSA-N Methylamine Chemical compound NC BAVYZALUXZFZLV-UHFFFAOYSA-N 0.000 description 2
- 208000034578 Multiple myelomas Diseases 0.000 description 2
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 2
- 229940122907 Phosphatase inhibitor Drugs 0.000 description 2
- XYFCBTPGUUZFHI-UHFFFAOYSA-N Phosphine Chemical compound P XYFCBTPGUUZFHI-UHFFFAOYSA-N 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- GLUUGHFHXGJENI-UHFFFAOYSA-N Piperazine Chemical compound C1CNCCN1 GLUUGHFHXGJENI-UHFFFAOYSA-N 0.000 description 2
- 239000004793 Polystyrene Substances 0.000 description 2
- 102100020718 Receptor-type tyrosine-protein kinase FLT3 Human genes 0.000 description 2
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- 239000004280 Sodium formate Substances 0.000 description 2
- 229920002472 Starch Polymers 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 238000006069 Suzuki reaction reaction Methods 0.000 description 2
- 108010065917 TOR Serine-Threonine Kinases Proteins 0.000 description 2
- 102000013530 TOR Serine-Threonine Kinases Human genes 0.000 description 2
- 239000000365 Topoisomerase I Inhibitor Substances 0.000 description 2
- 239000000317 Topoisomerase II Inhibitor Substances 0.000 description 2
- 239000007983 Tris buffer Substances 0.000 description 2
- 102000004243 Tubulin Human genes 0.000 description 2
- 108090000704 Tubulin Proteins 0.000 description 2
- KRFKGTLZIBAQBL-UHFFFAOYSA-N [2-bromo-4-(4-methylpiperazin-1-yl)phenyl] acetate Chemical compound C1CN(C)CCN1C1=CC=C(OC(C)=O)C(Br)=C1 KRFKGTLZIBAQBL-UHFFFAOYSA-N 0.000 description 2
- IQOMXJYLDDBSQL-UHFFFAOYSA-N [4-(4-methylpiperazin-1-yl)phenyl] acetate Chemical compound C1CN(C)CCN1C1=CC=C(OC(C)=O)C=C1 IQOMXJYLDDBSQL-UHFFFAOYSA-N 0.000 description 2
- WRWYGOVGIGCDLE-UHFFFAOYSA-N [O]c1ccccc1F Chemical group [O]c1ccccc1F WRWYGOVGIGCDLE-UHFFFAOYSA-N 0.000 description 2
- DHKHKXVYLBGOIT-UHFFFAOYSA-N acetaldehyde Diethyl Acetal Natural products CCOC(C)OCC DHKHKXVYLBGOIT-UHFFFAOYSA-N 0.000 description 2
- 150000001241 acetals Chemical class 0.000 description 2
- 239000008351 acetate buffer Substances 0.000 description 2
- HSEMWALZGKQWLK-SWWIKBNJSA-N aktide-2t Chemical compound C([C@H](NC(=O)[C@@H](NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](C)N)[C@H](O)C)C(=O)N[C@@H](CO)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)NCC(=O)N[C@@H](CC=1N=CNC=1)C(=O)N[C@@H](CC=1N=CNC=1)C(=O)N[C@@H](C)C(O)=O)C1=CC=C(O)C=C1 HSEMWALZGKQWLK-SWWIKBNJSA-N 0.000 description 2
- 235000010443 alginic acid Nutrition 0.000 description 2
- 229920000615 alginic acid Polymers 0.000 description 2
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 2
- 125000004453 alkoxycarbonyl group Chemical group 0.000 description 2
- 125000004466 alkoxycarbonylamino group Chemical group 0.000 description 2
- 125000003282 alkyl amino group Chemical group 0.000 description 2
- 125000004414 alkyl thio group Chemical group 0.000 description 2
- 239000002168 alkylating agent Substances 0.000 description 2
- 229940100198 alkylating agent Drugs 0.000 description 2
- 150000001409 amidines Chemical class 0.000 description 2
- 125000003277 amino group Chemical group 0.000 description 2
- 239000001099 ammonium carbonate Substances 0.000 description 2
- 229940121369 angiogenesis inhibitor Drugs 0.000 description 2
- 150000008064 anhydrides Chemical class 0.000 description 2
- 229940124650 anti-cancer therapies Drugs 0.000 description 2
- 230000002942 anti-growth Effects 0.000 description 2
- 239000002256 antimetabolite Substances 0.000 description 2
- 229910052786 argon Inorganic materials 0.000 description 2
- 239000012300 argon atmosphere Substances 0.000 description 2
- 125000001769 aryl amino group Chemical group 0.000 description 2
- 125000004104 aryloxy group Chemical group 0.000 description 2
- 238000003556 assay Methods 0.000 description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 2
- 210000003719 b-lymphocyte Anatomy 0.000 description 2
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 2
- YNHIGQDRGKUECZ-UHFFFAOYSA-L bis(triphenylphosphine)palladium(ii) dichloride Chemical compound [Cl-].[Cl-].[Pd+2].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 YNHIGQDRGKUECZ-UHFFFAOYSA-L 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- 229910052794 bromium Inorganic materials 0.000 description 2
- 125000002837 carbocyclic group Chemical group 0.000 description 2
- 239000011203 carbon fibre reinforced carbon Substances 0.000 description 2
- 229910002091 carbon monoxide Inorganic materials 0.000 description 2
- 239000001768 carboxy methyl cellulose Substances 0.000 description 2
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 2
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 2
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 2
- 229940125904 compound 1 Drugs 0.000 description 2
- 229940125782 compound 2 Drugs 0.000 description 2
- 229940126214 compound 3 Drugs 0.000 description 2
- FDIRIOAEXPIEBL-UHFFFAOYSA-L copper;thiophene-2-carboxylate Chemical compound [Cu+2].[O-]C(=O)C1=CC=CS1.[O-]C(=O)C1=CC=CS1 FDIRIOAEXPIEBL-UHFFFAOYSA-L 0.000 description 2
- 239000007822 coupling agent Substances 0.000 description 2
- 229940111134 coxibs Drugs 0.000 description 2
- 125000005170 cycloalkyloxycarbonyl group Chemical group 0.000 description 2
- MGNZXYYWBUKAII-UHFFFAOYSA-N cyclohexa-1,3-diene Chemical compound C1CC=CC=C1 MGNZXYYWBUKAII-UHFFFAOYSA-N 0.000 description 2
- HGCIXCUEYOPUTN-UHFFFAOYSA-N cyclohexene Chemical compound C1CCC=CC1 HGCIXCUEYOPUTN-UHFFFAOYSA-N 0.000 description 2
- 239000003255 cyclooxygenase 2 inhibitor Substances 0.000 description 2
- LPIQUOYDBNQMRZ-UHFFFAOYSA-N cyclopentene Chemical compound C1CC=CC1 LPIQUOYDBNQMRZ-UHFFFAOYSA-N 0.000 description 2
- 230000001419 dependent effect Effects 0.000 description 2
- 238000001514 detection method Methods 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 230000018109 developmental process Effects 0.000 description 2
- 125000004663 dialkyl amino group Chemical group 0.000 description 2
- FAMRKDQNMBBFBR-BQYQJAHWSA-N diethyl azodicarboxylate Substances CCOC(=O)\N=N\C(=O)OCC FAMRKDQNMBBFBR-BQYQJAHWSA-N 0.000 description 2
- 206010012818 diffuse large B-cell lymphoma Diseases 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 2
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical compound C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 2
- 230000004064 dysfunction Effects 0.000 description 2
- 239000000839 emulsion Substances 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- ZIQJJUFYWGFIOT-UHFFFAOYSA-N ethyl 1-(2-hydroxyethyl)-8-methoxypyrazolo[4,3-h]quinazoline-3-carboxylate Chemical compound C1=CC2=CN=C(OC)N=C2C2=C1C(C(=O)OCC)=NN2CCO ZIQJJUFYWGFIOT-UHFFFAOYSA-N 0.000 description 2
- RRICKXFUMPSCDM-UHFFFAOYSA-N ethyl 1-[(4-methoxyphenyl)methyl]-7-oxo-5,6-dihydro-4h-indazole-3-carboxylate Chemical compound C1CCC(=O)C2=C1C(C(=O)OCC)=NN2CC1=CC=C(OC)C=C1 RRICKXFUMPSCDM-UHFFFAOYSA-N 0.000 description 2
- NZZUPYUHSNPFEE-UHFFFAOYSA-N ethyl 1-[2-(dimethylamino)ethyl]-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxylate Chemical compound C1=CC2=CN=C(SC)N=C2C2=C1C(C(=O)OCC)=NN2CCN(C)C NZZUPYUHSNPFEE-UHFFFAOYSA-N 0.000 description 2
- LNTBKFWXZZGIHN-UHFFFAOYSA-N ethyl 2-[(4-methoxyphenyl)methyl]-7-oxo-5,6-dihydro-4h-indazole-3-carboxylate Chemical compound CCOC(=O)C1=C2CCCC(=O)C2=NN1CC1=CC=C(OC)C=C1 LNTBKFWXZZGIHN-UHFFFAOYSA-N 0.000 description 2
- UKPYNHZOVFKBHN-UHFFFAOYSA-N ethyl 2-[2-(dimethylamino)ethyl]-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxylate Chemical compound N1=C(SC)N=C2C3=NN(CCN(C)C)C(C(=O)OCC)=C3C=CC2=C1 UKPYNHZOVFKBHN-UHFFFAOYSA-N 0.000 description 2
- XFLFPYFSAQLHCN-UHFFFAOYSA-N ethyl 7-oxo-2,4,5,6-tetrahydroindazole-3-carboxylate Chemical compound C1CCC(=O)C2=C1C(C(=O)OCC)=NN2 XFLFPYFSAQLHCN-UHFFFAOYSA-N 0.000 description 2
- PZCSLMALLIALHH-UHFFFAOYSA-N ethyl 8-methylsulfanyl-1-trityl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxylate Chemical compound C1CC2=CN=C(SC)N=C2C2=C1C(C(=O)OCC)=NN2C(C=1C=CC=CC=1)(C=1C=CC=CC=1)C1=CC=CC=C1 PZCSLMALLIALHH-UHFFFAOYSA-N 0.000 description 2
- MIYFTJQBWSPQHR-UHFFFAOYSA-N ethyl 8-methylsulfanyl-4,5-dihydro-2h-pyrazolo[4,3-h]quinazoline-3-carboxylate Chemical compound C1CC2=CN=C(SC)N=C2C2=C1C(C(=O)OCC)=NN2 MIYFTJQBWSPQHR-UHFFFAOYSA-N 0.000 description 2
- FAMRKDQNMBBFBR-UHFFFAOYSA-N ethyl n-ethoxycarbonyliminocarbamate Chemical compound CCOC(=O)N=NC(=O)OCC FAMRKDQNMBBFBR-UHFFFAOYSA-N 0.000 description 2
- 239000011737 fluorine Substances 0.000 description 2
- 229910052731 fluorine Inorganic materials 0.000 description 2
- 125000002485 formyl group Chemical group [H]C(*)=O 0.000 description 2
- XKUKSGPZAADMRA-UHFFFAOYSA-N glycyl-glycyl-glycine Chemical compound NCC(=O)NCC(=O)NCC(O)=O XKUKSGPZAADMRA-UHFFFAOYSA-N 0.000 description 2
- 239000003102 growth factor Substances 0.000 description 2
- 125000004969 haloethyl group Chemical group 0.000 description 2
- 210000003958 hematopoietic stem cell Anatomy 0.000 description 2
- 125000006517 heterocyclyl carbonyl group Chemical group 0.000 description 2
- 125000005844 heterocyclyloxy group Chemical group 0.000 description 2
- 239000008240 homogeneous mixture Substances 0.000 description 2
- 229940088597 hormone Drugs 0.000 description 2
- 239000005556 hormone Substances 0.000 description 2
- 150000002429 hydrazines Chemical class 0.000 description 2
- 229930195733 hydrocarbon Natural products 0.000 description 2
- 239000000677 immunologic agent Substances 0.000 description 2
- 229940124541 immunological agent Drugs 0.000 description 2
- 238000001802 infusion Methods 0.000 description 2
- SUMDYPCJJOFFON-UHFFFAOYSA-N isethionic acid Chemical compound OCCS(O)(=O)=O SUMDYPCJJOFFON-UHFFFAOYSA-N 0.000 description 2
- 125000000555 isopropenyl group Chemical group [H]\C([H])=C(\*)C([H])([H])[H] 0.000 description 2
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 2
- 239000010410 layer Substances 0.000 description 2
- 239000000787 lecithin Substances 0.000 description 2
- 235000010445 lecithin Nutrition 0.000 description 2
- 229940067606 lecithin Drugs 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- YNESATAKKCNGOF-UHFFFAOYSA-N lithium bis(trimethylsilyl)amide Chemical compound [Li+].C[Si](C)(C)[N-][Si](C)(C)C YNESATAKKCNGOF-UHFFFAOYSA-N 0.000 description 2
- KWGKDLIKAYFUFQ-UHFFFAOYSA-M lithium chloride Chemical compound [Li+].[Cl-] KWGKDLIKAYFUFQ-UHFFFAOYSA-M 0.000 description 2
- 229910052749 magnesium Inorganic materials 0.000 description 2
- 230000003211 malignant effect Effects 0.000 description 2
- 239000011159 matrix material Substances 0.000 description 2
- 239000012528 membrane Substances 0.000 description 2
- 239000003475 metalloproteinase inhibitor Substances 0.000 description 2
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 2
- 229920000609 methyl cellulose Polymers 0.000 description 2
- 239000001923 methylcellulose Substances 0.000 description 2
- 235000010981 methylcellulose Nutrition 0.000 description 2
- FBUKVWPVBMHYJY-UHFFFAOYSA-N nonanoic acid Chemical compound CCCCCCCCC(O)=O FBUKVWPVBMHYJY-UHFFFAOYSA-N 0.000 description 2
- 239000012038 nucleophile Substances 0.000 description 2
- 239000003921 oil Substances 0.000 description 2
- 235000019198 oils Nutrition 0.000 description 2
- 231100000590 oncogenic Toxicity 0.000 description 2
- 210000000056 organ Anatomy 0.000 description 2
- 125000002524 organometallic group Chemical group 0.000 description 2
- 230000001582 osteoblastic effect Effects 0.000 description 2
- 239000001301 oxygen Substances 0.000 description 2
- VLTRZXGMWDSKGL-UHFFFAOYSA-N perchloric acid Chemical compound OCl(=O)(=O)=O VLTRZXGMWDSKGL-UHFFFAOYSA-N 0.000 description 2
- HXITXNWTGFUOAU-UHFFFAOYSA-N phenylboronic acid Chemical compound OB(O)C1=CC=CC=C1 HXITXNWTGFUOAU-UHFFFAOYSA-N 0.000 description 2
- 230000026731 phosphorylation Effects 0.000 description 2
- 125000004194 piperazin-1-yl group Chemical group [H]N1C([H])([H])C([H])([H])N(*)C([H])([H])C1([H])[H] 0.000 description 2
- 229920001223 polyethylene glycol Polymers 0.000 description 2
- 229920002223 polystyrene Polymers 0.000 description 2
- 229910052700 potassium Inorganic materials 0.000 description 2
- 235000007686 potassium Nutrition 0.000 description 2
- LPNYRYFBWFDTMA-UHFFFAOYSA-N potassium tert-butoxide Chemical compound [K+].CC(C)(C)[O-] LPNYRYFBWFDTMA-UHFFFAOYSA-N 0.000 description 2
- BXKKKVYZUPKLHC-UHFFFAOYSA-M potassium;1-methyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxylate Chemical compound [K+].C1CC2=CN=CN=C2C2=C1C(C([O-])=O)=NN2C BXKKKVYZUPKLHC-UHFFFAOYSA-M 0.000 description 2
- WKZRHMMQZLIYMN-UHFFFAOYSA-M potassium;1-tert-butyl-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxylate Chemical compound [K+].C12=NC(SC)=NC=C2C=CC2=C1N(C(C)(C)C)N=C2C([O-])=O WKZRHMMQZLIYMN-UHFFFAOYSA-M 0.000 description 2
- VVWRJUBEIPHGQF-UHFFFAOYSA-N propan-2-yl n-propan-2-yloxycarbonyliminocarbamate Chemical compound CC(C)OC(=O)N=NC(=O)OC(C)C VVWRJUBEIPHGQF-UHFFFAOYSA-N 0.000 description 2
- 239000002599 prostaglandin synthase inhibitor Substances 0.000 description 2
- 125000006239 protecting group Chemical group 0.000 description 2
- 239000003528 protein farnesyltransferase inhibitor Substances 0.000 description 2
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 2
- 108020003175 receptors Proteins 0.000 description 2
- 102000005962 receptors Human genes 0.000 description 2
- 230000001105 regulatory effect Effects 0.000 description 2
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 2
- 239000000523 sample Substances 0.000 description 2
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 2
- 238000013207 serial dilution Methods 0.000 description 2
- 230000019491 signal transduction Effects 0.000 description 2
- QFJCIRLUMZQUOT-HPLJOQBZSA-N sirolimus Chemical compound C1C[C@@H](O)[C@H](OC)C[C@@H]1C[C@@H](C)[C@H]1OC(=O)[C@@H]2CCCCN2C(=O)C(=O)[C@](O)(O2)[C@H](C)CC[C@H]2C[C@H](OC)/C(C)=C/C=C/C=C/[C@@H](C)C[C@@H](C)C(=O)[C@H](OC)[C@H](O)/C(C)=C/[C@@H](C)C(=O)C1 QFJCIRLUMZQUOT-HPLJOQBZSA-N 0.000 description 2
- 229910052708 sodium Inorganic materials 0.000 description 2
- 229910000029 sodium carbonate Inorganic materials 0.000 description 2
- HLBBKKJFGFRGMU-UHFFFAOYSA-M sodium formate Chemical compound [Na+].[O-]C=O HLBBKKJFGFRGMU-UHFFFAOYSA-M 0.000 description 2
- 235000019254 sodium formate Nutrition 0.000 description 2
- 229910052938 sodium sulfate Inorganic materials 0.000 description 2
- GEHJYWRUCIMESM-UHFFFAOYSA-L sodium sulfite Chemical compound [Na+].[Na+].[O-]S([O-])=O GEHJYWRUCIMESM-UHFFFAOYSA-L 0.000 description 2
- 235000011152 sodium sulphate Nutrition 0.000 description 2
- SNOOUWRIMMFWNE-UHFFFAOYSA-M sodium;6-[(3,4,5-trimethoxybenzoyl)amino]hexanoate Chemical compound [Na+].COC1=CC(C(=O)NCCCCCC([O-])=O)=CC(OC)=C1OC SNOOUWRIMMFWNE-UHFFFAOYSA-M 0.000 description 2
- 239000008107 starch Substances 0.000 description 2
- 235000019698 starch Nutrition 0.000 description 2
- 229940032147 starch Drugs 0.000 description 2
- 239000008223 sterile water Substances 0.000 description 2
- 239000006228 supernatant Substances 0.000 description 2
- 239000000829 suppository Substances 0.000 description 2
- 239000006188 syrup Substances 0.000 description 2
- 235000020357 syrup Nutrition 0.000 description 2
- LMBFAGIMSUYTBN-MPZNNTNKSA-N teixobactin Chemical compound C([C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CO)C(=O)N[C@H](CCC(N)=O)C(=O)N[C@H]([C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CO)C(=O)N[C@H]1C(N[C@@H](C)C(=O)N[C@@H](C[C@@H]2NC(=N)NC2)C(=O)N[C@H](C(=O)O[C@H]1C)[C@@H](C)CC)=O)NC)C1=CC=CC=C1 LMBFAGIMSUYTBN-MPZNNTNKSA-N 0.000 description 2
- 239000003277 telomerase inhibitor Substances 0.000 description 2
- UMGDCJDMYOKAJW-UHFFFAOYSA-N thiourea Chemical compound NC(N)=S UMGDCJDMYOKAJW-UHFFFAOYSA-N 0.000 description 2
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 2
- ITMCEJHCFYSIIV-UHFFFAOYSA-M triflate Chemical compound [O-]S(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-M 0.000 description 2
- PYOKUURKVVELLB-UHFFFAOYSA-N trimethyl orthoformate Chemical compound COC(OC)OC PYOKUURKVVELLB-UHFFFAOYSA-N 0.000 description 2
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 2
- 238000004704 ultra performance liquid chromatography Methods 0.000 description 2
- 238000001262 western blot Methods 0.000 description 2
- ASGMFNBUXDJWJJ-JLCFBVMHSA-N (1R,3R)-3-[[3-bromo-1-[4-(5-methyl-1,3,4-thiadiazol-2-yl)phenyl]pyrazolo[3,4-d]pyrimidin-6-yl]amino]-N,1-dimethylcyclopentane-1-carboxamide Chemical compound BrC1=NN(C2=NC(=NC=C21)N[C@H]1C[C@@](CC1)(C(=O)NC)C)C1=CC=C(C=C1)C=1SC(=NN=1)C ASGMFNBUXDJWJJ-JLCFBVMHSA-N 0.000 description 1
- UAOUIVVJBYDFKD-XKCDOFEDSA-N (1R,9R,10S,11R,12R,15S,18S,21R)-10,11,21-trihydroxy-8,8-dimethyl-14-methylidene-4-(prop-2-enylamino)-20-oxa-5-thia-3-azahexacyclo[9.7.2.112,15.01,9.02,6.012,18]henicosa-2(6),3-dien-13-one Chemical compound C([C@@H]1[C@@H](O)[C@@]23C(C1=C)=O)C[C@H]2[C@]12C(N=C(NCC=C)S4)=C4CC(C)(C)[C@H]1[C@H](O)[C@]3(O)OC2 UAOUIVVJBYDFKD-XKCDOFEDSA-N 0.000 description 1
- AOSZTAHDEDLTLQ-AZKQZHLXSA-N (1S,2S,4R,8S,9S,11S,12R,13S,19S)-6-[(3-chlorophenyl)methyl]-12,19-difluoro-11-hydroxy-8-(2-hydroxyacetyl)-9,13-dimethyl-6-azapentacyclo[10.8.0.02,9.04,8.013,18]icosa-14,17-dien-16-one Chemical compound C([C@@H]1C[C@H]2[C@H]3[C@]([C@]4(C=CC(=O)C=C4[C@@H](F)C3)C)(F)[C@@H](O)C[C@@]2([C@@]1(C1)C(=O)CO)C)N1CC1=CC=CC(Cl)=C1 AOSZTAHDEDLTLQ-AZKQZHLXSA-N 0.000 description 1
- ABJSOROVZZKJGI-OCYUSGCXSA-N (1r,2r,4r)-2-(4-bromophenyl)-n-[(4-chlorophenyl)-(2-fluoropyridin-4-yl)methyl]-4-morpholin-4-ylcyclohexane-1-carboxamide Chemical compound C1=NC(F)=CC(C(NC(=O)[C@H]2[C@@H](C[C@@H](CC2)N2CCOCC2)C=2C=CC(Br)=CC=2)C=2C=CC(Cl)=CC=2)=C1 ABJSOROVZZKJGI-OCYUSGCXSA-N 0.000 description 1
- GLGNXYJARSMNGJ-VKTIVEEGSA-N (1s,2s,3r,4r)-3-[[5-chloro-2-[(1-ethyl-6-methoxy-2-oxo-4,5-dihydro-3h-1-benzazepin-7-yl)amino]pyrimidin-4-yl]amino]bicyclo[2.2.1]hept-5-ene-2-carboxamide Chemical compound CCN1C(=O)CCCC2=C(OC)C(NC=3N=C(C(=CN=3)Cl)N[C@H]3[C@H]([C@@]4([H])C[C@@]3(C=C4)[H])C(N)=O)=CC=C21 GLGNXYJARSMNGJ-VKTIVEEGSA-N 0.000 description 1
- SZUVGFMDDVSKSI-WIFOCOSTSA-N (1s,2s,3s,5r)-1-(carboxymethyl)-3,5-bis[(4-phenoxyphenyl)methyl-propylcarbamoyl]cyclopentane-1,2-dicarboxylic acid Chemical compound O=C([C@@H]1[C@@H]([C@](CC(O)=O)([C@H](C(=O)N(CCC)CC=2C=CC(OC=3C=CC=CC=3)=CC=2)C1)C(O)=O)C(O)=O)N(CCC)CC(C=C1)=CC=C1OC1=CC=CC=C1 SZUVGFMDDVSKSI-WIFOCOSTSA-N 0.000 description 1
- DBZAICSEFBVFHL-UHFFFAOYSA-N (2,6-difluorophenyl)boronic acid Chemical compound OB(O)C1=C(F)C=CC=C1F DBZAICSEFBVFHL-UHFFFAOYSA-N 0.000 description 1
- QBYIENPQHBMVBV-HFEGYEGKSA-N (2R)-2-hydroxy-2-phenylacetic acid Chemical compound O[C@@H](C(O)=O)c1ccccc1.O[C@@H](C(O)=O)c1ccccc1 QBYIENPQHBMVBV-HFEGYEGKSA-N 0.000 description 1
- GHYOCDFICYLMRF-UTIIJYGPSA-N (2S,3R)-N-[(2S)-3-(cyclopenten-1-yl)-1-[(2R)-2-methyloxiran-2-yl]-1-oxopropan-2-yl]-3-hydroxy-3-(4-methoxyphenyl)-2-[[(2S)-2-[(2-morpholin-4-ylacetyl)amino]propanoyl]amino]propanamide Chemical compound C1(=CCCC1)C[C@@H](C(=O)[C@@]1(OC1)C)NC([C@H]([C@@H](C1=CC=C(C=C1)OC)O)NC([C@H](C)NC(CN1CCOCC1)=O)=O)=O GHYOCDFICYLMRF-UTIIJYGPSA-N 0.000 description 1
- IUSARDYWEPUTPN-OZBXUNDUSA-N (2r)-n-[(2s,3r)-4-[[(4s)-6-(2,2-dimethylpropyl)spiro[3,4-dihydropyrano[2,3-b]pyridine-2,1'-cyclobutane]-4-yl]amino]-3-hydroxy-1-[3-(1,3-thiazol-2-yl)phenyl]butan-2-yl]-2-methoxypropanamide Chemical compound C([C@H](NC(=O)[C@@H](C)OC)[C@H](O)CN[C@@H]1C2=CC(CC(C)(C)C)=CN=C2OC2(CCC2)C1)C(C=1)=CC=CC=1C1=NC=CS1 IUSARDYWEPUTPN-OZBXUNDUSA-N 0.000 description 1
- YJLIKUSWRSEPSM-WGQQHEPDSA-N (2r,3r,4s,5r)-2-[6-amino-8-[(4-phenylphenyl)methylamino]purin-9-yl]-5-(hydroxymethyl)oxolane-3,4-diol Chemical compound C=1C=C(C=2C=CC=CC=2)C=CC=1CNC1=NC=2C(N)=NC=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@H]1O YJLIKUSWRSEPSM-WGQQHEPDSA-N 0.000 description 1
- BSVHTRRLCAVQCZ-JDEXMCKMSA-N (2s)-1-[(2s)-1-[(2s)-1-[(2s)-1-[(2s)-1-[(2s)-1-[(2s)-2-[[(2s)-1-[(2s)-2-[[(2s)-2-amino-3-(4-hydroxyphenyl)propanoyl]amino]-3-carboxypropanoyl]pyrrolidine-2-carbonyl]amino]propanoyl]pyrrolidine-2-carbonyl]pyrrolidine-2-carbonyl]pyrrolidine-2-carbonyl]pyrro Chemical compound C([C@H](N)C(=O)N[C@@H](CC(O)=O)C(=O)N1CCC[C@H]1C(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(O)=O)C1=CC=C(O)C=C1 BSVHTRRLCAVQCZ-JDEXMCKMSA-N 0.000 description 1
- VIJSPAIQWVPKQZ-BLECARSGSA-N (2s)-2-[[(2s)-2-[[(2s)-2-[[(2s)-2-[[(2s)-2-[[(2s)-2-acetamido-5-(diaminomethylideneamino)pentanoyl]amino]-4-methylpentanoyl]amino]-4,4-dimethylpentanoyl]amino]-4-methylpentanoyl]amino]propanoyl]amino]-5-(diaminomethylideneamino)pentanoic acid Chemical compound NC(=N)NCCC[C@@H](C(O)=O)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(C)(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCNC(N)=N)NC(C)=O VIJSPAIQWVPKQZ-BLECARSGSA-N 0.000 description 1
- WWTBZEKOSBFBEM-SPWPXUSOSA-N (2s)-2-[[2-benzyl-3-[hydroxy-[(1r)-2-phenyl-1-(phenylmethoxycarbonylamino)ethyl]phosphoryl]propanoyl]amino]-3-(1h-indol-3-yl)propanoic acid Chemical compound N([C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)O)C(=O)C(CP(O)(=O)[C@H](CC=1C=CC=CC=1)NC(=O)OCC=1C=CC=CC=1)CC1=CC=CC=C1 WWTBZEKOSBFBEM-SPWPXUSOSA-N 0.000 description 1
- STBLNCCBQMHSRC-BATDWUPUSA-N (2s)-n-[(3s,4s)-5-acetyl-7-cyano-4-methyl-1-[(2-methylnaphthalen-1-yl)methyl]-2-oxo-3,4-dihydro-1,5-benzodiazepin-3-yl]-2-(methylamino)propanamide Chemical compound O=C1[C@@H](NC(=O)[C@H](C)NC)[C@H](C)N(C(C)=O)C2=CC(C#N)=CC=C2N1CC1=C(C)C=CC2=CC=CC=C12 STBLNCCBQMHSRC-BATDWUPUSA-N 0.000 description 1
- QFLWZFQWSBQYPS-AWRAUJHKSA-N (3S)-3-[[(2S)-2-[[(2S)-2-[5-[(3aS,6aR)-2-oxo-1,3,3a,4,6,6a-hexahydrothieno[3,4-d]imidazol-4-yl]pentanoylamino]-3-methylbutanoyl]amino]-3-(4-hydroxyphenyl)propanoyl]amino]-4-[1-bis(4-chlorophenoxy)phosphorylbutylamino]-4-oxobutanoic acid Chemical compound CCCC(NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](Cc1ccc(O)cc1)NC(=O)[C@@H](NC(=O)CCCCC1SC[C@@H]2NC(=O)N[C@H]12)C(C)C)P(=O)(Oc1ccc(Cl)cc1)Oc1ccc(Cl)cc1 QFLWZFQWSBQYPS-AWRAUJHKSA-N 0.000 description 1
- IWZSHWBGHQBIML-ZGGLMWTQSA-N (3S,8S,10R,13S,14S,17S)-17-isoquinolin-7-yl-N,N,10,13-tetramethyl-2,3,4,7,8,9,11,12,14,15,16,17-dodecahydro-1H-cyclopenta[a]phenanthren-3-amine Chemical compound CN(C)[C@H]1CC[C@]2(C)C3CC[C@@]4(C)[C@@H](CC[C@@H]4c4ccc5ccncc5c4)[C@@H]3CC=C2C1 IWZSHWBGHQBIML-ZGGLMWTQSA-N 0.000 description 1
- UDQTXCHQKHIQMH-KYGLGHNPSA-N (3ar,5s,6s,7r,7ar)-5-(difluoromethyl)-2-(ethylamino)-5,6,7,7a-tetrahydro-3ah-pyrano[3,2-d][1,3]thiazole-6,7-diol Chemical compound S1C(NCC)=N[C@H]2[C@@H]1O[C@H](C(F)F)[C@@H](O)[C@@H]2O UDQTXCHQKHIQMH-KYGLGHNPSA-N 0.000 description 1
- OOKAZRDERJMRCJ-KOUAFAAESA-N (3r)-7-[(1s,2s,4ar,6s,8s)-2,6-dimethyl-8-[(2s)-2-methylbutanoyl]oxy-1,2,4a,5,6,7,8,8a-octahydronaphthalen-1-yl]-3-hydroxy-5-oxoheptanoic acid Chemical compound C1=C[C@H](C)[C@H](CCC(=O)C[C@@H](O)CC(O)=O)C2[C@@H](OC(=O)[C@@H](C)CC)C[C@@H](C)C[C@@H]21 OOKAZRDERJMRCJ-KOUAFAAESA-N 0.000 description 1
- HUWSZNZAROKDRZ-RRLWZMAJSA-N (3r,4r)-3-azaniumyl-5-[[(2s,3r)-1-[(2s)-2,3-dicarboxypyrrolidin-1-yl]-3-methyl-1-oxopentan-2-yl]amino]-5-oxo-4-sulfanylpentane-1-sulfonate Chemical compound OS(=O)(=O)CC[C@@H](N)[C@@H](S)C(=O)N[C@@H]([C@H](C)CC)C(=O)N1CCC(C(O)=O)[C@H]1C(O)=O HUWSZNZAROKDRZ-RRLWZMAJSA-N 0.000 description 1
- MPDDTAJMJCESGV-CTUHWIOQSA-M (3r,5r)-7-[2-(4-fluorophenyl)-5-[methyl-[(1r)-1-phenylethyl]carbamoyl]-4-propan-2-ylpyrazol-3-yl]-3,5-dihydroxyheptanoate Chemical compound C1([C@@H](C)N(C)C(=O)C2=NN(C(CC[C@@H](O)C[C@@H](O)CC([O-])=O)=C2C(C)C)C=2C=CC(F)=CC=2)=CC=CC=C1 MPDDTAJMJCESGV-CTUHWIOQSA-M 0.000 description 1
- YQOLEILXOBUDMU-KRWDZBQOSA-N (4R)-5-[(6-bromo-3-methyl-2-pyrrolidin-1-ylquinoline-4-carbonyl)amino]-4-(2-chlorophenyl)pentanoic acid Chemical compound CC1=C(C2=C(C=CC(=C2)Br)N=C1N3CCCC3)C(=O)NC[C@H](CCC(=O)O)C4=CC=CC=C4Cl YQOLEILXOBUDMU-KRWDZBQOSA-N 0.000 description 1
- STPKWKPURVSAJF-LJEWAXOPSA-N (4r,5r)-5-[4-[[4-(1-aza-4-azoniabicyclo[2.2.2]octan-4-ylmethyl)phenyl]methoxy]phenyl]-3,3-dibutyl-7-(dimethylamino)-1,1-dioxo-4,5-dihydro-2h-1$l^{6}-benzothiepin-4-ol Chemical compound O[C@H]1C(CCCC)(CCCC)CS(=O)(=O)C2=CC=C(N(C)C)C=C2[C@H]1C(C=C1)=CC=C1OCC(C=C1)=CC=C1C[N+]1(CC2)CCN2CC1 STPKWKPURVSAJF-LJEWAXOPSA-N 0.000 description 1
- VUEGYUOUAAVYAS-JGGQBBKZSA-N (6ar,9s,10ar)-9-(dimethylsulfamoylamino)-7-methyl-6,6a,8,9,10,10a-hexahydro-4h-indolo[4,3-fg]quinoline Chemical compound C1=CC([C@H]2C[C@@H](CN(C)[C@@H]2C2)NS(=O)(=O)N(C)C)=C3C2=CNC3=C1 VUEGYUOUAAVYAS-JGGQBBKZSA-N 0.000 description 1
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 description 1
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 1
- DYLIWHYUXAJDOJ-OWOJBTEDSA-N (e)-4-(6-aminopurin-9-yl)but-2-en-1-ol Chemical compound NC1=NC=NC2=C1N=CN2C\C=C\CO DYLIWHYUXAJDOJ-OWOJBTEDSA-N 0.000 description 1
- DEVSOMFAQLZNKR-RJRFIUFISA-N (z)-3-[3-[3,5-bis(trifluoromethyl)phenyl]-1,2,4-triazol-1-yl]-n'-pyrazin-2-ylprop-2-enehydrazide Chemical compound FC(F)(F)C1=CC(C(F)(F)F)=CC(C2=NN(\C=C/C(=O)NNC=3N=CC=NC=3)C=N2)=C1 DEVSOMFAQLZNKR-RJRFIUFISA-N 0.000 description 1
- WBYWAXJHAXSJNI-VOTSOKGWSA-M .beta-Phenylacrylic acid Natural products [O-]C(=O)\C=C\C1=CC=CC=C1 WBYWAXJHAXSJNI-VOTSOKGWSA-M 0.000 description 1
- KZPYGQFFRCFCPP-UHFFFAOYSA-N 1,1'-bis(diphenylphosphino)ferrocene Chemical compound [Fe+2].C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1 KZPYGQFFRCFCPP-UHFFFAOYSA-N 0.000 description 1
- SCYULBFZEHDVBN-UHFFFAOYSA-N 1,1-Dichloroethane Chemical compound CC(Cl)Cl SCYULBFZEHDVBN-UHFFFAOYSA-N 0.000 description 1
- VNUPRKZUPUBXOD-UHFFFAOYSA-N 1,2-dimethoxyethane;1,4-dioxane Chemical compound COCCOC.C1COCCO1 VNUPRKZUPUBXOD-UHFFFAOYSA-N 0.000 description 1
- GWYPDXLJACEENP-UHFFFAOYSA-N 1,3-cycloheptadiene Chemical compound C1CC=CC=CC1 GWYPDXLJACEENP-UHFFFAOYSA-N 0.000 description 1
- BDNKZNFMNDZQMI-UHFFFAOYSA-N 1,3-diisopropylcarbodiimide Chemical compound CC(C)N=C=NC(C)C BDNKZNFMNDZQMI-UHFFFAOYSA-N 0.000 description 1
- DJMOXMNDXFFONV-UHFFFAOYSA-N 1,3-dimethyl-7-[2-(n-methylanilino)ethyl]purine-2,6-dione Chemical compound C1=NC=2N(C)C(=O)N(C)C(=O)C=2N1CCN(C)C1=CC=CC=C1 DJMOXMNDXFFONV-UHFFFAOYSA-N 0.000 description 1
- KKHFRAFPESRGGD-UHFFFAOYSA-N 1,3-dimethyl-7-[3-(n-methylanilino)propyl]purine-2,6-dione Chemical compound C1=NC=2N(C)C(=O)N(C)C(=O)C=2N1CCCN(C)C1=CC=CC=C1 KKHFRAFPESRGGD-UHFFFAOYSA-N 0.000 description 1
- WNXJIVFYUVYPPR-UHFFFAOYSA-N 1,3-dioxolane Chemical compound C1COCO1 WNXJIVFYUVYPPR-UHFFFAOYSA-N 0.000 description 1
- OGYGFUAIIOPWQD-UHFFFAOYSA-N 1,3-thiazolidine Chemical compound C1CSCN1 OGYGFUAIIOPWQD-UHFFFAOYSA-N 0.000 description 1
- AZQWKYJCGOJGHM-UHFFFAOYSA-N 1,4-benzoquinone Chemical compound O=C1C=CC(=O)C=C1 AZQWKYJCGOJGHM-UHFFFAOYSA-N 0.000 description 1
- OCJBOOLMMGQPQU-UHFFFAOYSA-N 1,4-dichlorobenzene Chemical compound ClC1=CC=C(Cl)C=C1 OCJBOOLMMGQPQU-UHFFFAOYSA-N 0.000 description 1
- XLYWBOUWPLIGEF-UHFFFAOYSA-N 1-(2-aminoethyl)-8-methylsulfanyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide;2,2,2-trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.C12=NC(SC)=NC=C2CCC2=C1N(CCN)N=C2C(N)=O XLYWBOUWPLIGEF-UHFFFAOYSA-N 0.000 description 1
- JEMZZSLLLFWLBD-UHFFFAOYSA-N 1-(2-aminoethyl)-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide;hydrochloride Chemical compound Cl.C12=NC(SC)=NC=C2C=CC2=C1N(CCN)N=C2C(N)=O JEMZZSLLLFWLBD-UHFFFAOYSA-N 0.000 description 1
- QNEXFOBAFPBAFA-UHFFFAOYSA-N 1-(2-hydroxyethyl)-8-methylsulfonylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(S(=O)(=O)C)=NC=C2C=CC2=C1N(CCO)N=C2C(N)=O QNEXFOBAFPBAFA-UHFFFAOYSA-N 0.000 description 1
- LLLZUMCXZOPOGX-UHFFFAOYSA-N 1-(3-amino-2,2-dimethylpropyl)-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide;hydrochloride Chemical compound Cl.C12=NC(SC)=NC=C2C=CC2=C1N(CC(C)(C)CN)N=C2C(N)=O LLLZUMCXZOPOGX-UHFFFAOYSA-N 0.000 description 1
- RFBXROMGOJAXNH-UHFFFAOYSA-N 1-(3-aminopropyl)-8-methylsulfanyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide;hydrochloride Chemical compound Cl.C12=NC(SC)=NC=C2CCC2=C1N(CCCN)N=C2C(N)=O RFBXROMGOJAXNH-UHFFFAOYSA-N 0.000 description 1
- SHJCXGWLRLZQJQ-UHFFFAOYSA-N 1-(3-aminopropyl)-n-(3-hydroxypropyl)-8-(4-methoxyphenyl)-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide;2,2,2-trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.C1=CC(OC)=CC=C1C1=NC=C(CCC2=C3N(CCCN)N=C2C(=O)NCCCO)C3=N1 SHJCXGWLRLZQJQ-UHFFFAOYSA-N 0.000 description 1
- GCPZUXYAEFKFEX-UHFFFAOYSA-N 1-(3-methylcyclobutyl)-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound CSc1ncc2ccc3c(nn(C4CC(C)C4)c3c2n1)C(N)=O GCPZUXYAEFKFEX-UHFFFAOYSA-N 0.000 description 1
- FZYHMVRMPVVKDB-UHFFFAOYSA-N 1-(4-aminocyclohexyl)-8-phenylpyrazolo[4,3-h]quinazoline-3-carboxamide;hydrochloride Chemical compound Cl.C1CC(N)CCC1N1C2=C3N=C(C=4C=CC=CC=4)N=CC3=CC=C2C(C(N)=O)=N1 FZYHMVRMPVVKDB-UHFFFAOYSA-N 0.000 description 1
- ONULAMBUKBCQQX-UHFFFAOYSA-N 1-(4-aminocyclohexyl)-8-thiophen-3-ylpyrazolo[4,3-h]quinazoline-3-carboxamide;2,2,2-trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.C1CC(N)CCC1N1C2=C3N=C(C4=CSC=C4)N=CC3=CC=C2C(C(N)=O)=N1 ONULAMBUKBCQQX-UHFFFAOYSA-N 0.000 description 1
- HQCCNFFIOWYINW-UHFFFAOYSA-N 1-(5-bromo-2-hydroxyphenyl)ethanone Chemical compound CC(=O)C1=CC(Br)=CC=C1O HQCCNFFIOWYINW-UHFFFAOYSA-N 0.000 description 1
- GIGRWGTZFONRKA-UHFFFAOYSA-N 1-(bromomethyl)-4-methoxybenzene Chemical compound COC1=CC=C(CBr)C=C1 GIGRWGTZFONRKA-UHFFFAOYSA-N 0.000 description 1
- KQZLRWGGWXJPOS-NLFPWZOASA-N 1-[(1R)-1-(2,4-dichlorophenyl)ethyl]-6-[(4S,5R)-4-[(2S)-2-(hydroxymethyl)pyrrolidin-1-yl]-5-methylcyclohexen-1-yl]pyrazolo[3,4-b]pyrazine-3-carbonitrile Chemical compound ClC1=C(C=CC(=C1)Cl)[C@@H](C)N1N=C(C=2C1=NC(=CN=2)C1=CC[C@@H]([C@@H](C1)C)N1[C@@H](CCC1)CO)C#N KQZLRWGGWXJPOS-NLFPWZOASA-N 0.000 description 1
- WZZBNLYBHUDSHF-DHLKQENFSA-N 1-[(3s,4s)-4-[8-(2-chloro-4-pyrimidin-2-yloxyphenyl)-7-fluoro-2-methylimidazo[4,5-c]quinolin-1-yl]-3-fluoropiperidin-1-yl]-2-hydroxyethanone Chemical compound CC1=NC2=CN=C3C=C(F)C(C=4C(=CC(OC=5N=CC=CN=5)=CC=4)Cl)=CC3=C2N1[C@H]1CCN(C(=O)CO)C[C@@H]1F WZZBNLYBHUDSHF-DHLKQENFSA-N 0.000 description 1
- ONBQEOIKXPHGMB-VBSBHUPXSA-N 1-[2-[(2s,3r,4s,5r)-3,4-dihydroxy-5-(hydroxymethyl)oxolan-2-yl]oxy-4,6-dihydroxyphenyl]-3-(4-hydroxyphenyl)propan-1-one Chemical compound O[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1OC1=CC(O)=CC(O)=C1C(=O)CCC1=CC=C(O)C=C1 ONBQEOIKXPHGMB-VBSBHUPXSA-N 0.000 description 1
- WJLAADKXXJWFDP-UHFFFAOYSA-N 1-[2-[4-(dimethylamino)piperidin-1-yl]ethyl]-8-methylsulfanyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1=2C3=NC(SC)=NC=C3CCC=2C(C(N)=O)=NN1CCN1CCC(N(C)C)CC1 WJLAADKXXJWFDP-UHFFFAOYSA-N 0.000 description 1
- SQPVSDOHSWJABQ-UHFFFAOYSA-N 1-[2-hydroxy-5-(4-methylpiperazin-1-yl)phenyl]ethanone Chemical compound C1CN(C)CCN1C1=CC=C(O)C(C(C)=O)=C1 SQPVSDOHSWJABQ-UHFFFAOYSA-N 0.000 description 1
- IIRKKTFPOMXKEA-UHFFFAOYSA-N 1-[4-(2-aminoethylamino)cyclohexyl]-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide;hydrochloride Chemical compound Cl.C1=2C3=NC(SC)=NC=C3C=CC=2C(C(N)=O)=NN1C1CCC(NCCN)CC1 IIRKKTFPOMXKEA-UHFFFAOYSA-N 0.000 description 1
- UNILWMWFPHPYOR-KXEYIPSPSA-M 1-[6-[2-[3-[3-[3-[2-[2-[3-[[2-[2-[[(2r)-1-[[2-[[(2r)-1-[3-[2-[2-[3-[[2-(2-amino-2-oxoethoxy)acetyl]amino]propoxy]ethoxy]ethoxy]propylamino]-3-hydroxy-1-oxopropan-2-yl]amino]-2-oxoethyl]amino]-3-[(2r)-2,3-di(hexadecanoyloxy)propyl]sulfanyl-1-oxopropan-2-yl Chemical compound O=C1C(SCCC(=O)NCCCOCCOCCOCCCNC(=O)COCC(=O)N[C@@H](CSC[C@@H](COC(=O)CCCCCCCCCCCCCCC)OC(=O)CCCCCCCCCCCCCCC)C(=O)NCC(=O)N[C@H](CO)C(=O)NCCCOCCOCCOCCCNC(=O)COCC(N)=O)CC(=O)N1CCNC(=O)CCCCCN\1C2=CC=C(S([O-])(=O)=O)C=C2CC/1=C/C=C/C=C/C1=[N+](CC)C2=CC=C(S([O-])(=O)=O)C=C2C1 UNILWMWFPHPYOR-KXEYIPSPSA-M 0.000 description 1
- KLXAVGUFAPKCFH-UHFFFAOYSA-N 1-[[1-(2-aminoethyl)piperidin-4-yl]methyl]-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide;hydrochloride Chemical compound Cl.C1=2C3=NC(SC)=NC=C3C=CC=2C(C(N)=O)=NN1CC1CCN(CCN)CC1 KLXAVGUFAPKCFH-UHFFFAOYSA-N 0.000 description 1
- OCWRKTTWVBYXAQ-UHFFFAOYSA-N 1-azabicyclo[2.2.2]octan-3-yl 4-methylbenzenesulfonate Chemical compound C1=CC(C)=CC=C1S(=O)(=O)OC1C(CC2)CCN2C1 OCWRKTTWVBYXAQ-UHFFFAOYSA-N 0.000 description 1
- IXPNQXFRVYWDDI-UHFFFAOYSA-N 1-methyl-2,4-dioxo-1,3-diazinane-5-carboximidamide Chemical compound CN1CC(C(N)=N)C(=O)NC1=O IXPNQXFRVYWDDI-UHFFFAOYSA-N 0.000 description 1
- LTMPOWBIFCSVQK-UHFFFAOYSA-N 1-methyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1CC2=CN=CN=C2C2=C1C(C(N)=O)=NN2C LTMPOWBIFCSVQK-UHFFFAOYSA-N 0.000 description 1
- GLDDPJPBFUFFPL-UHFFFAOYSA-N 1-methyl-8-(2-oxopropoxy)-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(OCC(=O)C)=NC=C2CCC2=C1N(C)N=C2C(N)=O GLDDPJPBFUFFPL-UHFFFAOYSA-N 0.000 description 1
- ZZEHYOQBNUYTLI-UHFFFAOYSA-N 1-methyl-8-(3-piperazin-1-ylphenoxy)pyrazolo[4,3-h]quinazoline-3-carboxamide;2,2,2-trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.N=1C2=C3N(C)N=C(C(N)=O)C3=CC=C2C=NC=1OC(C=1)=CC=CC=1N1CCNCC1 ZZEHYOQBNUYTLI-UHFFFAOYSA-N 0.000 description 1
- PSJKEAVPPPPZSA-UHFFFAOYSA-N 1-methyl-8-(4-piperazin-1-ylphenoxy)pyrazolo[4,3-h]quinazoline-3-carboxamide;2,2,2-trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.N=1C2=C3N(C)N=C(C(N)=O)C3=CC=C2C=NC=1OC(C=C1)=CC=C1N1CCNCC1 PSJKEAVPPPPZSA-UHFFFAOYSA-N 0.000 description 1
- HHUQJUJLSWZLOQ-UHFFFAOYSA-N 1-methyl-8-propan-2-yloxy-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(OC(C)C)=NC=C2CCC2=C1N(C)N=C2C(N)=O HHUQJUJLSWZLOQ-UHFFFAOYSA-N 0.000 description 1
- 125000004484 1-methylpiperidin-4-yl group Chemical group CN1CCC(CC1)* 0.000 description 1
- HAXUPMBANZSOIK-UHFFFAOYSA-N 1-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound CSN1N=C(C=2C=CC=3C=NC=NC=3C=21)C(=O)N HAXUPMBANZSOIK-UHFFFAOYSA-N 0.000 description 1
- KKVYYGGCHJGEFJ-UHFFFAOYSA-N 1-n-(4-chlorophenyl)-6-methyl-5-n-[3-(7h-purin-6-yl)pyridin-2-yl]isoquinoline-1,5-diamine Chemical compound N=1C=CC2=C(NC=3C(=CC=CN=3)C=3C=4N=CNC=4N=CN=3)C(C)=CC=C2C=1NC1=CC=C(Cl)C=C1 KKVYYGGCHJGEFJ-UHFFFAOYSA-N 0.000 description 1
- OVMWSSGAVNRYET-UHFFFAOYSA-N 1-piperidin-4-yl-8-pyrrolidin-1-ylpyrazolo[4,3-h]quinazoline-3-carboxamide;hydrochloride Chemical compound Cl.C1=CC2=CN=C(N3CCCC3)N=C2C2=C1C(C(=O)N)=NN2C1CCNCC1 OVMWSSGAVNRYET-UHFFFAOYSA-N 0.000 description 1
- TYNFDQQQAVKFFI-UHFFFAOYSA-N 1-piperidin-4-yl-8-thiophen-3-ylpyrazolo[4,3-h]quinazoline-3-carboxamide;2,2,2-trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.C1=CC2=CN=C(C3=CSC=C3)N=C2C2=C1C(C(=O)N)=NN2C1CCNCC1 TYNFDQQQAVKFFI-UHFFFAOYSA-N 0.000 description 1
- ULYUCPHWEYFFMQ-UHFFFAOYSA-N 1-tert-butyl-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxylic acid Chemical compound C12=NC(SC)=NC=C2C=CC2=C1N(C(C)(C)C)N=C2C(O)=O ULYUCPHWEYFFMQ-UHFFFAOYSA-N 0.000 description 1
- UUVHHSFQAIWREJ-UHFFFAOYSA-N 1-tert-butyl-8-methylsulfonylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1=NC(S(C)(=O)=O)=NC2=C3N(C(C)(C)C)N=C(C(N)=O)C3=CC=C21 UUVHHSFQAIWREJ-UHFFFAOYSA-N 0.000 description 1
- 238000005160 1H NMR spectroscopy Methods 0.000 description 1
- YBYIRNPNPLQARY-UHFFFAOYSA-N 1H-indene Natural products C1=CC=C2CC=CC2=C1 YBYIRNPNPLQARY-UHFFFAOYSA-N 0.000 description 1
- BHXVYTQDWMQVBI-UHFFFAOYSA-N 1h-indazole-3-carboxylic acid Chemical compound C1=CC=C2C(C(=O)O)=NNC2=C1 BHXVYTQDWMQVBI-UHFFFAOYSA-N 0.000 description 1
- YVARNMRPPSXNCI-UHFFFAOYSA-N 1h-pyrazolo[4,3-h]quinazoline Chemical class C1=CC2=CN=CN=C2C2=C1C=NN2 YVARNMRPPSXNCI-UHFFFAOYSA-N 0.000 description 1
- ONEKSCQALFOIGK-UHFFFAOYSA-N 2,2,2-trichloroethyl 3-methylsulfonyloxy-8-azabicyclo[3.2.1]octane-8-carboxylate Chemical compound C1C(OS(=O)(=O)C)CC2CCC1N2C(=O)OCC(Cl)(Cl)Cl ONEKSCQALFOIGK-UHFFFAOYSA-N 0.000 description 1
- JKTCBAGSMQIFNL-UHFFFAOYSA-N 2,3-dihydrofuran Chemical compound C1CC=CO1 JKTCBAGSMQIFNL-UHFFFAOYSA-N 0.000 description 1
- WGFNXGPBPIJYLI-UHFFFAOYSA-N 2,6-difluoro-3-[(3-fluorophenyl)sulfonylamino]-n-(3-methoxy-1h-pyrazolo[3,4-b]pyridin-5-yl)benzamide Chemical compound C1=C2C(OC)=NNC2=NC=C1NC(=O)C(C=1F)=C(F)C=CC=1NS(=O)(=O)C1=CC=CC(F)=C1 WGFNXGPBPIJYLI-UHFFFAOYSA-N 0.000 description 1
- FQMZXMVHHKXGTM-UHFFFAOYSA-N 2-(1-adamantyl)-n-[2-[2-(2-hydroxyethylamino)ethylamino]quinolin-5-yl]acetamide Chemical compound C1C(C2)CC(C3)CC2CC13CC(=O)NC1=CC=CC2=NC(NCCNCCO)=CC=C21 FQMZXMVHHKXGTM-UHFFFAOYSA-N 0.000 description 1
- NZOKQORJUXWPNX-UHFFFAOYSA-N 2-(2-aminoethyl)-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxamide;hydrochloride Chemical compound Cl.C1=CC2=C(C(N)=O)N(CCN)N=C2C2=NC(SC)=NC=C21 NZOKQORJUXWPNX-UHFFFAOYSA-N 0.000 description 1
- VCUXVXLUOHDHKK-UHFFFAOYSA-N 2-(2-aminopyrimidin-4-yl)-4-(2-chloro-4-methoxyphenyl)-1,3-thiazole-5-carboxamide Chemical compound ClC1=CC(OC)=CC=C1C1=C(C(N)=O)SC(C=2N=C(N)N=CC=2)=N1 VCUXVXLUOHDHKK-UHFFFAOYSA-N 0.000 description 1
- QEBYEVQKHRUYPE-UHFFFAOYSA-N 2-(2-chlorophenyl)-5-[(1-methylpyrazol-3-yl)methyl]-4-[[methyl(pyridin-3-ylmethyl)amino]methyl]-1h-pyrazolo[4,3-c]pyridine-3,6-dione Chemical compound C1=CN(C)N=C1CN1C(=O)C=C2NN(C=3C(=CC=CC=3)Cl)C(=O)C2=C1CN(C)CC1=CC=CN=C1 QEBYEVQKHRUYPE-UHFFFAOYSA-N 0.000 description 1
- YCHZPWGYTIFELL-UHFFFAOYSA-N 2-(3-aminopropyl)-8-(4-fluorophenyl)-1,3,4,5-tetrahydropyrazolo[4,3-h]quinazoline-3-carboxylic acid;2,2,2-trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.OC(=O)C1N(CCCN)NC(C2=N3)=C1CCC2=CN=C3C1=CC=C(F)C=C1 YCHZPWGYTIFELL-UHFFFAOYSA-N 0.000 description 1
- WUVYBRUWDBUPIT-UHFFFAOYSA-N 2-(4-bromo-3-methylbutyl)isoindole-1,3-dione Chemical compound C1=CC=C2C(=O)N(CCC(CBr)C)C(=O)C2=C1 WUVYBRUWDBUPIT-UHFFFAOYSA-N 0.000 description 1
- VRPJIFMKZZEXLR-UHFFFAOYSA-N 2-[(2-methylpropan-2-yl)oxycarbonylamino]acetic acid Chemical compound CC(C)(C)OC(=O)NCC(O)=O VRPJIFMKZZEXLR-UHFFFAOYSA-N 0.000 description 1
- IEQAICDLOKRSRL-UHFFFAOYSA-N 2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-[2-(2-dodecoxyethoxy)ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethoxy]ethanol Chemical compound CCCCCCCCCCCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCOCCO IEQAICDLOKRSRL-UHFFFAOYSA-N 0.000 description 1
- PYRKKGOKRMZEIT-UHFFFAOYSA-N 2-[6-(2-cyclopropylethoxy)-9-(2-hydroxy-2-methylpropyl)-1h-phenanthro[9,10-d]imidazol-2-yl]-5-fluorobenzene-1,3-dicarbonitrile Chemical compound C1=C2C3=CC(CC(C)(O)C)=CC=C3C=3NC(C=4C(=CC(F)=CC=4C#N)C#N)=NC=3C2=CC=C1OCCC1CC1 PYRKKGOKRMZEIT-UHFFFAOYSA-N 0.000 description 1
- FMKGJQHNYMWDFJ-CVEARBPZSA-N 2-[[4-(2,2-difluoropropoxy)pyrimidin-5-yl]methylamino]-4-[[(1R,4S)-4-hydroxy-3,3-dimethylcyclohexyl]amino]pyrimidine-5-carbonitrile Chemical compound FC(COC1=NC=NC=C1CNC1=NC=C(C(=N1)N[C@H]1CC([C@H](CC1)O)(C)C)C#N)(C)F FMKGJQHNYMWDFJ-CVEARBPZSA-N 0.000 description 1
- VVCMGAUPZIKYTH-VGHSCWAPSA-N 2-acetyloxybenzoic acid;[(2s,3r)-4-(dimethylamino)-3-methyl-1,2-diphenylbutan-2-yl] propanoate;1,3,7-trimethylpurine-2,6-dione Chemical compound CC(=O)OC1=CC=CC=C1C(O)=O.CN1C(=O)N(C)C(=O)C2=C1N=CN2C.C([C@](OC(=O)CC)([C@H](C)CN(C)C)C=1C=CC=CC=1)C1=CC=CC=C1 VVCMGAUPZIKYTH-VGHSCWAPSA-N 0.000 description 1
- YSUIQYOGTINQIN-UZFYAQMZSA-N 2-amino-9-[(1S,6R,8R,9S,10R,15R,17R,18R)-8-(6-aminopurin-9-yl)-9,18-difluoro-3,12-dihydroxy-3,12-bis(sulfanylidene)-2,4,7,11,13,16-hexaoxa-3lambda5,12lambda5-diphosphatricyclo[13.2.1.06,10]octadecan-17-yl]-1H-purin-6-one Chemical compound NC1=NC2=C(N=CN2[C@@H]2O[C@@H]3COP(S)(=O)O[C@@H]4[C@@H](COP(S)(=O)O[C@@H]2[C@@H]3F)O[C@H]([C@H]4F)N2C=NC3=C2N=CN=C3N)C(=O)N1 YSUIQYOGTINQIN-UZFYAQMZSA-N 0.000 description 1
- TVTJUIAKQFIXCE-HUKYDQBMSA-N 2-amino-9-[(2R,3S,4S,5R)-4-fluoro-3-hydroxy-5-(hydroxymethyl)oxolan-2-yl]-7-prop-2-ynyl-1H-purine-6,8-dione Chemical compound NC=1NC(C=2N(C(N(C=2N=1)[C@@H]1O[C@@H]([C@H]([C@H]1O)F)CO)=O)CC#C)=O TVTJUIAKQFIXCE-HUKYDQBMSA-N 0.000 description 1
- PJYJPVQRVUHVOR-UHFFFAOYSA-N 2-bromo-4-(4-methylpiperazin-1-yl)phenol Chemical compound C1CN(C)CCN1C1=CC=C(O)C(Br)=C1 PJYJPVQRVUHVOR-UHFFFAOYSA-N 0.000 description 1
- LVCHXPHUKPLVRQ-UHFFFAOYSA-N 2-bromo-n,n-dimethylethanamine Chemical compound CN(C)CCBr LVCHXPHUKPLVRQ-UHFFFAOYSA-N 0.000 description 1
- 125000001340 2-chloroethyl group Chemical group [H]C([H])(Cl)C([H])([H])* 0.000 description 1
- GNRWQDOUORMQMO-UHFFFAOYSA-N 2-fluoro-4-(4-methylpiperazin-1-yl)phenol Chemical compound C1CN(C)CCN1C1=CC=C(O)C(F)=C1 GNRWQDOUORMQMO-UHFFFAOYSA-N 0.000 description 1
- 125000004791 2-fluoroethoxy group Chemical group FCCO* 0.000 description 1
- KQMFTCFZNVYSQH-UHFFFAOYSA-N 2-hydroxy-5-(4-methylpiperazin-1-yl)benzonitrile Chemical compound C1CN(C)CCN1C1=CC=C(O)C(C#N)=C1 KQMFTCFZNVYSQH-UHFFFAOYSA-N 0.000 description 1
- ZWVHTXAYIKBMEE-UHFFFAOYSA-N 2-hydroxyacetophenone Chemical compound OCC(=O)C1=CC=CC=C1 ZWVHTXAYIKBMEE-UHFFFAOYSA-N 0.000 description 1
- LFOIDLOIBZFWDO-UHFFFAOYSA-N 2-methoxy-6-[6-methoxy-4-[(3-phenylmethoxyphenyl)methoxy]-1-benzofuran-2-yl]imidazo[2,1-b][1,3,4]thiadiazole Chemical compound N1=C2SC(OC)=NN2C=C1C(OC1=CC(OC)=C2)=CC1=C2OCC(C=1)=CC=CC=1OCC1=CC=CC=C1 LFOIDLOIBZFWDO-UHFFFAOYSA-N 0.000 description 1
- 125000004200 2-methoxyethyl group Chemical group [H]C([H])([H])OC([H])([H])C([H])([H])* 0.000 description 1
- 125000006024 2-pentenyl group Chemical group 0.000 description 1
- 125000001494 2-propynyl group Chemical group [H]C#CC([H])([H])* 0.000 description 1
- RSEBUVRVKCANEP-UHFFFAOYSA-N 2-pyrroline Chemical compound C1CC=CN1 RSEBUVRVKCANEP-UHFFFAOYSA-N 0.000 description 1
- MGADZUXDNSDTHW-UHFFFAOYSA-N 2H-pyran Chemical compound C1OC=CC=C1 MGADZUXDNSDTHW-UHFFFAOYSA-N 0.000 description 1
- JHUUPUMBZGWODW-UHFFFAOYSA-N 3,6-dihydro-1,2-dioxine Chemical compound C1OOCC=C1 JHUUPUMBZGWODW-UHFFFAOYSA-N 0.000 description 1
- DFRAKBCRUYUFNT-UHFFFAOYSA-N 3,8-dicyclohexyl-2,4,7,9-tetrahydro-[1,3]oxazino[5,6-h][1,3]benzoxazine Chemical compound C1CCCCC1N1CC(C=CC2=C3OCN(C2)C2CCCCC2)=C3OC1 DFRAKBCRUYUFNT-UHFFFAOYSA-N 0.000 description 1
- AISHPJPGKBKMGV-UHFFFAOYSA-N 3-(4-methylpiperazin-1-yl)phenol Chemical compound C1CN(C)CCN1C1=CC=CC(O)=C1 AISHPJPGKBKMGV-UHFFFAOYSA-N 0.000 description 1
- FPQQSJJWHUJYPU-UHFFFAOYSA-N 3-(dimethylamino)propyliminomethylidene-ethylazanium;chloride Chemical compound Cl.CCN=C=NCCCN(C)C FPQQSJJWHUJYPU-UHFFFAOYSA-N 0.000 description 1
- QBWKPGNFQQJGFY-QLFBSQMISA-N 3-[(1r)-1-[(2r,6s)-2,6-dimethylmorpholin-4-yl]ethyl]-n-[6-methyl-3-(1h-pyrazol-4-yl)imidazo[1,2-a]pyrazin-8-yl]-1,2-thiazol-5-amine Chemical compound N1([C@H](C)C2=NSC(NC=3C4=NC=C(N4C=C(C)N=3)C3=CNN=C3)=C2)C[C@H](C)O[C@H](C)C1 QBWKPGNFQQJGFY-QLFBSQMISA-N 0.000 description 1
- WFOVEDJTASPCIR-UHFFFAOYSA-N 3-[(4-methyl-5-pyridin-4-yl-1,2,4-triazol-3-yl)methylamino]-n-[[2-(trifluoromethyl)phenyl]methyl]benzamide Chemical compound N=1N=C(C=2C=CN=CC=2)N(C)C=1CNC(C=1)=CC=CC=1C(=O)NCC1=CC=CC=C1C(F)(F)F WFOVEDJTASPCIR-UHFFFAOYSA-N 0.000 description 1
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 1
- 102100037263 3-phosphoinositide-dependent protein kinase 1 Human genes 0.000 description 1
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 1
- WYFCZWSWFGJODV-MIANJLSGSA-N 4-[[(1s)-2-[(e)-3-[3-chloro-2-fluoro-6-(tetrazol-1-yl)phenyl]prop-2-enoyl]-5-(4-methyl-2-oxopiperazin-1-yl)-3,4-dihydro-1h-isoquinoline-1-carbonyl]amino]benzoic acid Chemical compound O=C1CN(C)CCN1C1=CC=CC2=C1CCN(C(=O)\C=C\C=1C(=CC=C(Cl)C=1F)N1N=NN=C1)[C@@H]2C(=O)NC1=CC=C(C(O)=O)C=C1 WYFCZWSWFGJODV-MIANJLSGSA-N 0.000 description 1
- MPMKMQHJHDHPBE-RUZDIDTESA-N 4-[[(2r)-1-(1-benzothiophene-3-carbonyl)-2-methylazetidine-2-carbonyl]-[(3-chlorophenyl)methyl]amino]butanoic acid Chemical compound O=C([C@@]1(N(CC1)C(=O)C=1C2=CC=CC=C2SC=1)C)N(CCCC(O)=O)CC1=CC=CC(Cl)=C1 MPMKMQHJHDHPBE-RUZDIDTESA-N 0.000 description 1
- QCQCHGYLTSGIGX-GHXANHINSA-N 4-[[(3ar,5ar,5br,7ar,9s,11ar,11br,13as)-5a,5b,8,8,11a-pentamethyl-3a-[(5-methylpyridine-3-carbonyl)amino]-2-oxo-1-propan-2-yl-4,5,6,7,7a,9,10,11,11b,12,13,13a-dodecahydro-3h-cyclopenta[a]chrysen-9-yl]oxy]-2,2-dimethyl-4-oxobutanoic acid Chemical compound N([C@@]12CC[C@@]3(C)[C@]4(C)CC[C@H]5C(C)(C)[C@@H](OC(=O)CC(C)(C)C(O)=O)CC[C@]5(C)[C@H]4CC[C@@H]3C1=C(C(C2)=O)C(C)C)C(=O)C1=CN=CC(C)=C1 QCQCHGYLTSGIGX-GHXANHINSA-N 0.000 description 1
- DQAZPZIYEOGZAF-UHFFFAOYSA-N 4-ethyl-n-[4-(3-ethynylanilino)-7-methoxyquinazolin-6-yl]piperazine-1-carboxamide Chemical compound C1CN(CC)CCN1C(=O)NC(C(=CC1=NC=N2)OC)=CC1=C2NC1=CC=CC(C#C)=C1 DQAZPZIYEOGZAF-UHFFFAOYSA-N 0.000 description 1
- LBUNNMJLXWQQBY-UHFFFAOYSA-N 4-fluorophenylboronic acid Chemical compound OB(O)C1=CC=C(F)C=C1 LBUNNMJLXWQQBY-UHFFFAOYSA-N 0.000 description 1
- VKLKXFOZNHEBSW-UHFFFAOYSA-N 5-[[3-[(4-morpholin-4-ylbenzoyl)amino]phenyl]methoxy]pyridine-3-carboxamide Chemical compound O1CCN(CC1)C1=CC=C(C(=O)NC=2C=C(COC=3C=NC=C(C(=O)N)C=3)C=CC=2)C=C1 VKLKXFOZNHEBSW-UHFFFAOYSA-N 0.000 description 1
- XFJBGINZIMNZBW-CRAIPNDOSA-N 5-chloro-2-[4-[(1r,2s)-2-[2-(5-methylsulfonylpyridin-2-yl)oxyethyl]cyclopropyl]piperidin-1-yl]pyrimidine Chemical compound N1=CC(S(=O)(=O)C)=CC=C1OCC[C@H]1[C@@H](C2CCN(CC2)C=2N=CC(Cl)=CN=2)C1 XFJBGINZIMNZBW-CRAIPNDOSA-N 0.000 description 1
- RSIWALKZYXPAGW-NSHDSACASA-N 6-(3-fluorophenyl)-3-methyl-7-[(1s)-1-(7h-purin-6-ylamino)ethyl]-[1,3]thiazolo[3,2-a]pyrimidin-5-one Chemical compound C=1([C@@H](NC=2C=3N=CNC=3N=CN=2)C)N=C2SC=C(C)N2C(=O)C=1C1=CC=CC(F)=C1 RSIWALKZYXPAGW-NSHDSACASA-N 0.000 description 1
- GDUANFXPOZTYKS-UHFFFAOYSA-N 6-bromo-8-[(2,6-difluoro-4-methoxybenzoyl)amino]-4-oxochromene-2-carboxylic acid Chemical compound FC1=CC(OC)=CC(F)=C1C(=O)NC1=CC(Br)=CC2=C1OC(C(O)=O)=CC2=O GDUANFXPOZTYKS-UHFFFAOYSA-N 0.000 description 1
- FHVDTGUDJYJELY-UHFFFAOYSA-N 6-{[2-carboxy-4,5-dihydroxy-6-(phosphanyloxy)oxan-3-yl]oxy}-4,5-dihydroxy-3-phosphanyloxane-2-carboxylic acid Chemical compound O1C(C(O)=O)C(P)C(O)C(O)C1OC1C(C(O)=O)OC(OP)C(O)C1O FHVDTGUDJYJELY-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical group [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- LYFSIDGSUHKDBV-UHFFFAOYSA-N 8-(2,6-difluorophenyl)-1-(2-fluoroethyl)-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound NC(=O)C1=NN(CCF)C(C2=N3)=C1CCC2=CN=C3C1=C(F)C=CC=C1F LYFSIDGSUHKDBV-UHFFFAOYSA-N 0.000 description 1
- WFGZJAQGZPUVCK-UHFFFAOYSA-N 8-(2,6-difluorophenyl)-1-(piperidin-4-ylmethyl)-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide;hydrochloride Chemical compound Cl.C1CC2=CN=C(C=3C(=CC=CC=3F)F)N=C2C2=C1C(C(=O)N)=NN2CC1CCNCC1 WFGZJAQGZPUVCK-UHFFFAOYSA-N 0.000 description 1
- BNSRYEBCTSZWNA-UHFFFAOYSA-N 8-(2-acetyl-4-piperazin-1-ylphenoxy)-1-methylpyrazolo[4,3-h]quinazoline-3-carboxamide;2,2,2-trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.C=1C=C(OC=2N=C3C=4N(C)N=C(C=4C=CC3=CN=2)C(N)=O)C(C(=O)C)=CC=1N1CCNCC1 BNSRYEBCTSZWNA-UHFFFAOYSA-N 0.000 description 1
- XFARNFRXMBXRLP-UHFFFAOYSA-N 8-(2-chlorophenoxy)-1-methyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound N1=C2C=3N(C)N=C(C(N)=O)C=3CCC2=CN=C1OC1=CC=CC=C1Cl XFARNFRXMBXRLP-UHFFFAOYSA-N 0.000 description 1
- FCXRZXVVSAKQQX-UHFFFAOYSA-N 8-(2-fluorophenoxy)-1-methyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound N1=C2C=3N(C)N=C(C(N)=O)C=3CCC2=CN=C1OC1=CC=CC=C1F FCXRZXVVSAKQQX-UHFFFAOYSA-N 0.000 description 1
- NSBGDLHFUYXQMI-UHFFFAOYSA-N 8-(4-fluorophenyl)-2-[3-[(2-methylpropan-2-yl)oxycarbonylamino]propyl]-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxylic acid Chemical compound OC(=O)C=1N(CCCNC(=O)OC(C)(C)C)N=C(C2=N3)C=1CCC2=CN=C3C1=CC=C(F)C=C1 NSBGDLHFUYXQMI-UHFFFAOYSA-N 0.000 description 1
- IKUPJXBBYULYST-UHFFFAOYSA-N 8-(4-fluorophenyl)-n-(3-hydroxypropyl)-4,5-dihydro-2h-pyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound OCCCNC(=O)C1=NNC(C2=N3)=C1CCC2=CN=C3C1=CC=C(F)C=C1 IKUPJXBBYULYST-UHFFFAOYSA-N 0.000 description 1
- HGXGUNKPERHVPE-UHFFFAOYSA-N 8-(4-methoxyphenyl)-1-trityl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxylic acid Chemical compound C1=CC(OC)=CC=C1C1=NC=C(CCC2=C3N(N=C2C(O)=O)C(C=2C=CC=CC=2)(C=2C=CC=CC=2)C=2C=CC=CC=2)C3=N1 HGXGUNKPERHVPE-UHFFFAOYSA-N 0.000 description 1
- JLZAGSOGYVWISD-UHFFFAOYSA-N 8-[2-acetyl-4-(4-methylpiperazin-1-yl)phenoxy]-1-methyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide;2,2,2-trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.C1CN(C)CCN1C(C=C1C(C)=O)=CC=C1OC1=NC=C(CCC2=C3N(C)N=C2C(N)=O)C3=N1 JLZAGSOGYVWISD-UHFFFAOYSA-N 0.000 description 1
- ILJVZHMDRUFAJA-UHFFFAOYSA-N 8-[2-acetyl-4-(4-methylpiperazin-1-yl)phenoxy]-1-methylpyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1CN(C)CCN1C(C=C1C(C)=O)=CC=C1OC1=NC=C(C=CC2=C3N(C)N=C2C(N)=O)C3=N1 ILJVZHMDRUFAJA-UHFFFAOYSA-N 0.000 description 1
- YMKRGHWSVONYDW-UHFFFAOYSA-N 8-[2-bromo-4-(4-methylpiperazin-1-yl)phenoxy]-1-methyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide;2,2,2-trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.C1CN(C)CCN1C(C=C1Br)=CC=C1OC1=NC=C(CCC2=C3N(C)N=C2C(N)=O)C3=N1 YMKRGHWSVONYDW-UHFFFAOYSA-N 0.000 description 1
- FNXSNVGNDAYFFV-UHFFFAOYSA-N 8-[2-cyano-4-(4-methylpiperazin-1-yl)phenoxy]-1-methyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide;2,2,2-trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.C1CN(C)CCN1C(C=C1C#N)=CC=C1OC1=NC=C(CCC2=C3N(C)N=C2C(N)=O)C3=N1 FNXSNVGNDAYFFV-UHFFFAOYSA-N 0.000 description 1
- RMHHYAQFYRNSAJ-UHFFFAOYSA-N 8-[2-fluoro-4-(4-methylpiperazin-1-yl)phenoxy]-1-methyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide;2,2,2-trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.C1CN(C)CCN1C(C=C1F)=CC=C1OC1=NC=C(CCC2=C3N(C)N=C2C(N)=O)C3=N1 RMHHYAQFYRNSAJ-UHFFFAOYSA-N 0.000 description 1
- KOKGVLMMSFWSEJ-UHFFFAOYSA-N 8-[3-(dimethylamino)phenoxy]-1-methyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound CN(C)C1=CC=CC(OC=2N=C3C=4N(C)N=C(C=4CCC3=CN=2)C(N)=O)=C1 KOKGVLMMSFWSEJ-UHFFFAOYSA-N 0.000 description 1
- GVXTVQRBKFPRNF-UHFFFAOYSA-N 8-ethoxy-1-(piperidin-4-ylmethyl)-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide;hydrochloride Chemical compound Cl.C1=2C3=NC(OCC)=NC=C3CCC=2C(C(N)=O)=NN1CC1CCNCC1 GVXTVQRBKFPRNF-UHFFFAOYSA-N 0.000 description 1
- OOHMVWZUVFZRFS-UHFFFAOYSA-N 8-ethoxy-1-methyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(OCC)=NC=C2CCC2=C1N(C)N=C2C(N)=O OOHMVWZUVFZRFS-UHFFFAOYSA-N 0.000 description 1
- MVGWVEHAKJQCTJ-UHFFFAOYSA-N 8-ethoxy-1-piperidin-4-yl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide;hydrochloride Chemical compound Cl.C1=2C3=NC(OCC)=NC=C3CCC=2C(C(N)=O)=NN1C1CCNCC1 MVGWVEHAKJQCTJ-UHFFFAOYSA-N 0.000 description 1
- CAWGRADRGCYQKM-UHFFFAOYSA-N 8-ethoxy-4,5-dihydro-2h-pyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(OCC)=NC=C2CCC2=C1NN=C2C(N)=O CAWGRADRGCYQKM-UHFFFAOYSA-N 0.000 description 1
- KXZRTDOSWZGEEF-UHFFFAOYSA-N 8-methoxy-1-(piperidin-4-ylmethyl)pyrazolo[4,3-h]quinazoline-3-carboxamide;hydrochloride Chemical compound Cl.C1=2C3=NC(OC)=NC=C3C=CC=2C(C(N)=O)=NN1CC1CCNCC1 KXZRTDOSWZGEEF-UHFFFAOYSA-N 0.000 description 1
- HEJBFZFDMZJATP-UHFFFAOYSA-N 8-methoxy-1-piperidin-4-ylpyrazolo[4,3-h]quinazoline-3-carboxamide;hydrochloride Chemical compound Cl.C1=2C3=NC(OC)=NC=C3C=CC=2C(C(N)=O)=NN1C1CCNCC1 HEJBFZFDMZJATP-UHFFFAOYSA-N 0.000 description 1
- XASOHFCUIQARJT-UHFFFAOYSA-N 8-methoxy-6-[7-(2-morpholin-4-ylethoxy)imidazo[1,2-a]pyridin-3-yl]-2-(2,2,2-trifluoroethyl)-3,4-dihydroisoquinolin-1-one Chemical compound C(N1C(=O)C2=C(OC)C=C(C=3N4C(=NC=3)C=C(C=C4)OCCN3CCOCC3)C=C2CC1)C(F)(F)F XASOHFCUIQARJT-UHFFFAOYSA-N 0.000 description 1
- JZLWBUHPDGCMJS-UHFFFAOYSA-N 8-methylsulfanyl-1-(piperidin-3-ylmethyl)pyrazolo[4,3-h]quinazoline-3-carboxamide;hydrochloride Chemical compound Cl.C1=2C3=NC(SC)=NC=C3C=CC=2C(C(N)=O)=NN1CC1CCCNC1 JZLWBUHPDGCMJS-UHFFFAOYSA-N 0.000 description 1
- VIWHPKVHKSTGBD-UHFFFAOYSA-N 8-methylsulfanyl-1-(piperidin-4-ylmethyl)pyrazolo[4,3-h]quinazoline-3-carboxamide;hydrochloride Chemical compound Cl.C1=2C3=NC(SC)=NC=C3C=CC=2C(C(N)=O)=NN1CC1CCNCC1 VIWHPKVHKSTGBD-UHFFFAOYSA-N 0.000 description 1
- XUWGWBJDBPLUMB-UHFFFAOYSA-N 8-methylsulfanyl-1-piperidin-3-ylpyrazolo[4,3-h]quinazoline-3-carboxamide;hydrochloride Chemical compound Cl.C1=2C3=NC(SC)=NC=C3C=CC=2C(C(N)=O)=NN1C1CCCNC1 XUWGWBJDBPLUMB-UHFFFAOYSA-N 0.000 description 1
- SJERRKSOHUGCGO-UHFFFAOYSA-N 8-methylsulfanyl-1-piperidin-4-yl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxamide;2,2,2-trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.C1=2C3=NC(SC)=NC=C3CCC=2C(C(N)=O)=NN1C1CCNCC1 SJERRKSOHUGCGO-UHFFFAOYSA-N 0.000 description 1
- AHXOSGABXOMIIT-UHFFFAOYSA-N 8-methylsulfanyl-1-piperidin-4-ylpyrazolo[4,3-h]quinazoline-3-carboxamide;hydrochloride Chemical compound Cl.C1=2C3=NC(SC)=NC=C3C=CC=2C(C(N)=O)=NN1C1CCNCC1 AHXOSGABXOMIIT-UHFFFAOYSA-N 0.000 description 1
- HEIPYWFUKNUGAG-UHFFFAOYSA-N 8-methylsulfanyl-2-(piperidin-4-ylmethyl)pyrazolo[4,3-h]quinazoline-3-carboxamide;hydrochloride Chemical compound Cl.N1=C2C3=NC(SC)=NC=C3C=CC2=C(C(N)=O)N1CC1CCNCC1 HEIPYWFUKNUGAG-UHFFFAOYSA-N 0.000 description 1
- XFTJEPWHFQPBRW-UHFFFAOYSA-N 8-methylsulfonyl-2h-pyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C12=NC(S(=O)(=O)C)=NC=C2C=CC2=C1NN=C2C(N)=O XFTJEPWHFQPBRW-UHFFFAOYSA-N 0.000 description 1
- XWNKTTWLOGXVED-UHFFFAOYSA-N 8-morpholin-4-yl-1-piperidin-4-ylpyrazolo[4,3-h]quinazoline-3-carboxamide;hydrochloride Chemical compound Cl.C1=CC2=CN=C(N3CCOCC3)N=C2C2=C1C(C(=O)N)=NN2C1CCNCC1 XWNKTTWLOGXVED-UHFFFAOYSA-N 0.000 description 1
- PCJDPTAMZRVZKI-UHFFFAOYSA-N 8-phenyl-1-piperidin-4-ylpyrazolo[4,3-h]quinazoline-3-carboxamide;hydrochloride Chemical compound Cl.C1=CC2=CN=C(C=3C=CC=CC=3)N=C2C2=C1C(C(=O)N)=NN2C1CCNCC1 PCJDPTAMZRVZKI-UHFFFAOYSA-N 0.000 description 1
- IRBAWVGZNJIROV-SFHVURJKSA-N 9-(2-cyclopropylethynyl)-2-[[(2s)-1,4-dioxan-2-yl]methoxy]-6,7-dihydropyrimido[6,1-a]isoquinolin-4-one Chemical compound C1=C2C3=CC=C(C#CC4CC4)C=C3CCN2C(=O)N=C1OC[C@@H]1COCCO1 IRBAWVGZNJIROV-SFHVURJKSA-N 0.000 description 1
- 244000215068 Acacia senegal Species 0.000 description 1
- OQLZINXFSUDMHM-UHFFFAOYSA-N Acetamidine Chemical compound CC(N)=N OQLZINXFSUDMHM-UHFFFAOYSA-N 0.000 description 1
- 229920001817 Agar Polymers 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- USFZMSVCRYTOJT-UHFFFAOYSA-N Ammonium acetate Chemical compound N.CC(O)=O USFZMSVCRYTOJT-UHFFFAOYSA-N 0.000 description 1
- 239000005695 Ammonium acetate Substances 0.000 description 1
- 108010063104 Apoptosis Regulatory Proteins Proteins 0.000 description 1
- 102000010565 Apoptosis Regulatory Proteins Human genes 0.000 description 1
- 108090000461 Aurora Kinase A Proteins 0.000 description 1
- 102100032311 Aurora kinase A Human genes 0.000 description 1
- 102100032306 Aurora kinase B Human genes 0.000 description 1
- 108090000749 Aurora kinase B Proteins 0.000 description 1
- 208000010839 B-cell chronic lymphocytic leukemia Diseases 0.000 description 1
- IYHHRZBKXXKDDY-UHFFFAOYSA-N BI-605906 Chemical compound N=1C=2SC(C(N)=O)=C(N)C=2C(C(F)(F)CC)=CC=1N1CCC(S(C)(=O)=O)CC1 IYHHRZBKXXKDDY-UHFFFAOYSA-N 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- ZBJJDYGJCNTNTH-UHFFFAOYSA-N Betahistine mesilate Chemical group CS(O)(=O)=O.CS(O)(=O)=O.CNCCC1=CC=CC=N1 ZBJJDYGJCNTNTH-UHFFFAOYSA-N 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-M Bicarbonate Chemical compound OC([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-M 0.000 description 1
- ZOXJGFHDIHLPTG-UHFFFAOYSA-N Boron Chemical compound [B] ZOXJGFHDIHLPTG-UHFFFAOYSA-N 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- JQUCWIWWWKZNCS-LESHARBVSA-N C(C1=CC=CC=C1)(=O)NC=1SC[C@H]2[C@@](N1)(CO[C@H](C2)C)C=2SC=C(N2)NC(=O)C2=NC=C(C=C2)OC(F)F Chemical compound C(C1=CC=CC=C1)(=O)NC=1SC[C@H]2[C@@](N1)(CO[C@H](C2)C)C=2SC=C(N2)NC(=O)C2=NC=C(C=C2)OC(F)F JQUCWIWWWKZNCS-LESHARBVSA-N 0.000 description 1
- 102100021935 C-C motif chemokine 26 Human genes 0.000 description 1
- PGRIMIBFRLIEDK-UHFFFAOYSA-N CC(C)(C)OC(N1CCC(C[n]2nc(C(N)=O)c3c2-c2nc(I)ncc2CC3)CC1)=O Chemical compound CC(C)(C)OC(N1CCC(C[n]2nc(C(N)=O)c3c2-c2nc(I)ncc2CC3)CC1)=O PGRIMIBFRLIEDK-UHFFFAOYSA-N 0.000 description 1
- ZGQXUEYSVBGEDX-UHFFFAOYSA-N CC(C)CNC(c1n[n](C(CC2)CCC2N)c2c1ccc(cn1)c2nc1SC)=O Chemical compound CC(C)CNC(c1n[n](C(CC2)CCC2N)c2c1ccc(cn1)c2nc1SC)=O ZGQXUEYSVBGEDX-UHFFFAOYSA-N 0.000 description 1
- UHNRLQRZRNKOKU-UHFFFAOYSA-N CCN(CC1=NC2=C(N1)C1=CC=C(C=C1N=C2N)C1=NNC=C1)C(C)=O Chemical compound CCN(CC1=NC2=C(N1)C1=CC=C(C=C1N=C2N)C1=NNC=C1)C(C)=O UHNRLQRZRNKOKU-UHFFFAOYSA-N 0.000 description 1
- BQXUPNKLZNSUMC-YUQWMIPFSA-N CCN(CCCCCOCC(=O)N[C@H](C(=O)N1C[C@H](O)C[C@H]1C(=O)N[C@@H](C)c1ccc(cc1)-c1scnc1C)C(C)(C)C)CCOc1ccc(cc1)C(=O)c1c(sc2cc(O)ccc12)-c1ccc(O)cc1 Chemical compound CCN(CCCCCOCC(=O)N[C@H](C(=O)N1C[C@H](O)C[C@H]1C(=O)N[C@@H](C)c1ccc(cc1)-c1scnc1C)C(C)(C)C)CCOc1ccc(cc1)C(=O)c1c(sc2cc(O)ccc12)-c1ccc(O)cc1 BQXUPNKLZNSUMC-YUQWMIPFSA-N 0.000 description 1
- 101150006084 CHKB gene Proteins 0.000 description 1
- PCBZRNYXXCIELG-WYFCWLEVSA-N COC1=CC=C(C[C@H](NC(=O)OC2CCCC3(C2)OOC2(O3)C3CC4CC(C3)CC2C4)C(=O)N[C@@H]2[C@@H](CO)O[C@H]([C@@H]2O)N2C=NC3=C2N=CN=C3N(C)C)C=C1 Chemical compound COC1=CC=C(C[C@H](NC(=O)OC2CCCC3(C2)OOC2(O3)C3CC4CC(C3)CC2C4)C(=O)N[C@@H]2[C@@H](CO)O[C@H]([C@@H]2O)N2C=NC3=C2N=CN=C3N(C)C)C=C1 PCBZRNYXXCIELG-WYFCWLEVSA-N 0.000 description 1
- BCACBOOQAUYFDU-UHFFFAOYSA-N CSc1nc2c3[n](C(CC4)CCC4NC(N)=N)nc(C(N)=O)c3ccc2cn1 Chemical compound CSc1nc2c3[n](C(CC4)CCC4NC(N)=N)nc(C(N)=O)c3ccc2cn1 BCACBOOQAUYFDU-UHFFFAOYSA-N 0.000 description 1
- PKMUHQIDVVOXHQ-HXUWFJFHSA-N C[C@H](C1=CC(C2=CC=C(CNC3CCCC3)S2)=CC=C1)NC(C1=C(C)C=CC(NC2CNC2)=C1)=O Chemical compound C[C@H](C1=CC(C2=CC=C(CNC3CCCC3)S2)=CC=C1)NC(C1=C(C)C=CC(NC2CNC2)=C1)=O PKMUHQIDVVOXHQ-HXUWFJFHSA-N 0.000 description 1
- 101100326430 Caenorhabditis elegans bub-1 gene Proteins 0.000 description 1
- 101100220616 Caenorhabditis elegans chk-2 gene Proteins 0.000 description 1
- 101100498823 Caenorhabditis elegans ddr-2 gene Proteins 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 239000004215 Carbon black (E152) Substances 0.000 description 1
- 208000005623 Carcinogenesis Diseases 0.000 description 1
- 241000206601 Carnobacterium mobile Species 0.000 description 1
- 102000009410 Chemokine receptor Human genes 0.000 description 1
- 108050000299 Chemokine receptor Proteins 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- KZBUYRJDOAKODT-UHFFFAOYSA-N Chlorine Chemical compound ClCl KZBUYRJDOAKODT-UHFFFAOYSA-N 0.000 description 1
- WBYWAXJHAXSJNI-SREVYHEPSA-N Cinnamic acid Chemical compound OC(=O)\C=C/C1=CC=CC=C1 WBYWAXJHAXSJNI-SREVYHEPSA-N 0.000 description 1
- 229940126657 Compound 17 Drugs 0.000 description 1
- 229940126639 Compound 33 Drugs 0.000 description 1
- 229940127007 Compound 39 Drugs 0.000 description 1
- 229920002261 Corn starch Polymers 0.000 description 1
- VMQMZMRVKUZKQL-UHFFFAOYSA-N Cu+ Chemical compound [Cu+] VMQMZMRVKUZKQL-UHFFFAOYSA-N 0.000 description 1
- 108050006400 Cyclin Proteins 0.000 description 1
- 102000016736 Cyclin Human genes 0.000 description 1
- 102100033233 Cyclin-dependent kinase inhibitor 1B Human genes 0.000 description 1
- PMPVIKIVABFJJI-UHFFFAOYSA-N Cyclobutane Chemical compound C1CCC1 PMPVIKIVABFJJI-UHFFFAOYSA-N 0.000 description 1
- LVZWSLJZHVFIQJ-UHFFFAOYSA-N Cyclopropane Chemical compound C1CC1 LVZWSLJZHVFIQJ-UHFFFAOYSA-N 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- IGXWBGJHJZYPQS-SSDOTTSWSA-N D-Luciferin Chemical compound OC(=O)[C@H]1CSC(C=2SC3=CC=C(O)C=C3N=2)=N1 IGXWBGJHJZYPQS-SSDOTTSWSA-N 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- 101100440695 Dictyostelium discoideum corB gene Proteins 0.000 description 1
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 description 1
- FVIGODVHAVLZOO-UHFFFAOYSA-N Dixanthogen Chemical compound CCOC(=S)SSC(=S)OCC FVIGODVHAVLZOO-UHFFFAOYSA-N 0.000 description 1
- 102100031480 Dual specificity mitogen-activated protein kinase kinase 1 Human genes 0.000 description 1
- 101710146526 Dual specificity mitogen-activated protein kinase kinase 1 Proteins 0.000 description 1
- 239000006145 Eagle's minimal essential medium Substances 0.000 description 1
- LVGKNOAMLMIIKO-UHFFFAOYSA-N Elaidinsaeure-aethylester Natural products CCCCCCCCC=CCCCCCCCC(=O)OCC LVGKNOAMLMIIKO-UHFFFAOYSA-N 0.000 description 1
- 102100034174 Eukaryotic translation initiation factor 2-alpha kinase 3 Human genes 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- PNKUSGQVOMIXLU-UHFFFAOYSA-N Formamidine Chemical compound NC=N PNKUSGQVOMIXLU-UHFFFAOYSA-N 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 208000009329 Graft vs Host Disease Diseases 0.000 description 1
- 229920000084 Gum arabic Polymers 0.000 description 1
- 244000043261 Hevea brasiliensis Species 0.000 description 1
- 101000600756 Homo sapiens 3-phosphoinositide-dependent protein kinase 1 Proteins 0.000 description 1
- 101000897493 Homo sapiens C-C motif chemokine 26 Proteins 0.000 description 1
- 101000944380 Homo sapiens Cyclin-dependent kinase inhibitor 1 Proteins 0.000 description 1
- 101000944361 Homo sapiens Cyclin-dependent kinase inhibitor 1B Proteins 0.000 description 1
- 101001012157 Homo sapiens Receptor tyrosine-protein kinase erbB-2 Proteins 0.000 description 1
- 101001059454 Homo sapiens Serine/threonine-protein kinase MARK2 Proteins 0.000 description 1
- 101001001645 Homo sapiens Serine/threonine-protein kinase pim-3 Proteins 0.000 description 1
- 101001117146 Homo sapiens [Pyruvate dehydrogenase (acetyl-transferring)] kinase isozyme 1, mitochondrial Proteins 0.000 description 1
- WRYCSMQKUKOKBP-UHFFFAOYSA-N Imidazolidine Chemical compound C1CNCN1 WRYCSMQKUKOKBP-UHFFFAOYSA-N 0.000 description 1
- 108010002386 Interleukin-3 Proteins 0.000 description 1
- 102000000646 Interleukin-3 Human genes 0.000 description 1
- 238000005577 Kumada cross-coupling reaction Methods 0.000 description 1
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- 239000012448 Lithium borohydride Substances 0.000 description 1
- 108060001084 Luciferase Proteins 0.000 description 1
- 239000005089 Luciferase Substances 0.000 description 1
- 229940124647 MEK inhibitor Drugs 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 239000012359 Methanesulfonyl chloride Substances 0.000 description 1
- 102100026907 Mitogen-activated protein kinase kinase kinase 8 Human genes 0.000 description 1
- 241001529936 Murinae Species 0.000 description 1
- 101100381978 Mus musculus Braf gene Proteins 0.000 description 1
- 101100335081 Mus musculus Flt3 gene Proteins 0.000 description 1
- 101001033276 Mus musculus Interleukin-3 Proteins 0.000 description 1
- ZKGNPQKYVKXMGJ-UHFFFAOYSA-N N,N-dimethylacetamide Chemical compound CN(C)C(C)=O.CN(C)C(C)=O ZKGNPQKYVKXMGJ-UHFFFAOYSA-N 0.000 description 1
- KQJQICVXLJTWQD-UHFFFAOYSA-N N-Methylthiourea Chemical compound CNC(N)=S KQJQICVXLJTWQD-UHFFFAOYSA-N 0.000 description 1
- LVDRREOUMKACNJ-BKMJKUGQSA-N N-[(2R,3S)-2-(4-chlorophenyl)-1-(1,4-dimethyl-2-oxoquinolin-7-yl)-6-oxopiperidin-3-yl]-2-methylpropane-1-sulfonamide Chemical compound CC(C)CS(=O)(=O)N[C@H]1CCC(=O)N([C@@H]1c1ccc(Cl)cc1)c1ccc2c(C)cc(=O)n(C)c2c1 LVDRREOUMKACNJ-BKMJKUGQSA-N 0.000 description 1
- AVYVHIKSFXVDBG-UHFFFAOYSA-N N-benzyl-N-hydroxy-2,2-dimethylbutanamide Chemical compound C(C1=CC=CC=C1)N(C(C(CC)(C)C)=O)O AVYVHIKSFXVDBG-UHFFFAOYSA-N 0.000 description 1
- POFVJRKJJBFPII-UHFFFAOYSA-N N-cyclopentyl-5-[2-[[5-[(4-ethylpiperazin-1-yl)methyl]pyridin-2-yl]amino]-5-fluoropyrimidin-4-yl]-4-methyl-1,3-thiazol-2-amine Chemical compound C1(CCCC1)NC=1SC(=C(N=1)C)C1=NC(=NC=C1F)NC1=NC=C(C=C1)CN1CCN(CC1)CC POFVJRKJJBFPII-UHFFFAOYSA-N 0.000 description 1
- OPFJDXRVMFKJJO-ZHHKINOHSA-N N-{[3-(2-benzamido-4-methyl-1,3-thiazol-5-yl)-pyrazol-5-yl]carbonyl}-G-dR-G-dD-dD-dD-NH2 Chemical compound S1C(C=2NN=C(C=2)C(=O)NCC(=O)N[C@H](CCCN=C(N)N)C(=O)NCC(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC(O)=O)C(N)=O)=C(C)N=C1NC(=O)C1=CC=CC=C1 OPFJDXRVMFKJJO-ZHHKINOHSA-N 0.000 description 1
- OVNYIUWEKOXLOF-UHFFFAOYSA-N N1=C2C=3N(CCCN)N=C(C(O)=O)C=3CCC2=CN=C1C1=CC=C(F)C=C1 Chemical compound N1=C2C=3N(CCCN)N=C(C(O)=O)C=3CCC2=CN=C1C1=CC=C(F)C=C1 OVNYIUWEKOXLOF-UHFFFAOYSA-N 0.000 description 1
- QOVYHDHLFPKQQG-NDEPHWFRSA-N N[C@@H](CCC(=O)N1CCC(CC1)NC1=C2C=CC=CC2=NC(NCC2=CN(CCCNCCCNC3CCCCC3)N=N2)=N1)C(O)=O Chemical compound N[C@@H](CCC(=O)N1CCC(CC1)NC1=C2C=CC=CC2=NC(NCC2=CN(CCCNCCCNC3CCCCC3)N=N2)=N1)C(O)=O QOVYHDHLFPKQQG-NDEPHWFRSA-N 0.000 description 1
- 238000006411 Negishi coupling reaction Methods 0.000 description 1
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 1
- KKQQPIMIJPRLAH-UHFFFAOYSA-N OCCN1N=CC=2C=CC=3C=NC(=NC3C21)S(=O)(=O)C Chemical compound OCCN1N=CC=2C=CC=3C=NC(=NC3C21)S(=O)(=O)C KKQQPIMIJPRLAH-UHFFFAOYSA-N 0.000 description 1
- 108091008606 PDGF receptors Proteins 0.000 description 1
- 108091008010 PERKs Proteins 0.000 description 1
- 102000038030 PI3Ks Human genes 0.000 description 1
- 108091007960 PI3Ks Proteins 0.000 description 1
- 239000002033 PVDF binder Substances 0.000 description 1
- 108010077495 Peptide oostatic hormone Proteins 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 229920001213 Polysorbate 20 Polymers 0.000 description 1
- 229920001214 Polysorbate 60 Polymers 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- WUGQZFFCHPXWKQ-UHFFFAOYSA-N Propanolamine Chemical compound NCCCO WUGQZFFCHPXWKQ-UHFFFAOYSA-N 0.000 description 1
- 229940124158 Protease/peptidase inhibitor Drugs 0.000 description 1
- 108090000315 Protein Kinase C Proteins 0.000 description 1
- 102000003923 Protein Kinase C Human genes 0.000 description 1
- 108700020978 Proto-Oncogene Proteins 0.000 description 1
- 102000052575 Proto-Oncogene Human genes 0.000 description 1
- 108010014608 Proto-Oncogene Proteins c-kit Proteins 0.000 description 1
- 102000016971 Proto-Oncogene Proteins c-kit Human genes 0.000 description 1
- 108010017121 Proto-Oncogene Proteins c-pim-1 Proteins 0.000 description 1
- 102000004433 Proto-Oncogene Proteins c-pim-1 Human genes 0.000 description 1
- WTKZEGDFNFYCGP-UHFFFAOYSA-N Pyrazole Chemical compound C=1C=NNC=1 WTKZEGDFNFYCGP-UHFFFAOYSA-N 0.000 description 1
- IWYDHOAUDWTVEP-UHFFFAOYSA-N R-2-phenyl-2-hydroxyacetic acid Natural products OC(=O)C(O)C1=CC=CC=C1 IWYDHOAUDWTVEP-UHFFFAOYSA-N 0.000 description 1
- 108091030071 RNAI Proteins 0.000 description 1
- 102100030086 Receptor tyrosine-protein kinase erbB-2 Human genes 0.000 description 1
- 108091006627 SLC12A9 Proteins 0.000 description 1
- LDEBVRIURYMKQS-WISUUJSJSA-N Ser-Thr Chemical compound C[C@@H](O)[C@@H](C(O)=O)NC(=O)[C@@H](N)CO LDEBVRIURYMKQS-WISUUJSJSA-N 0.000 description 1
- 102100028904 Serine/threonine-protein kinase MARK2 Human genes 0.000 description 1
- 102100027940 Serine/threonine-protein kinase PAK 4 Human genes 0.000 description 1
- 101710148155 Serine/threonine-protein kinase PAK 4 Proteins 0.000 description 1
- 101710148159 Serine/threonine-protein kinase PAK 5 Proteins 0.000 description 1
- 102100026840 Serine/threonine-protein kinase PAK 6 Human genes 0.000 description 1
- 102100036119 Serine/threonine-protein kinase pim-3 Human genes 0.000 description 1
- PNUZDKCDAWUEGK-CYZMBNFOSA-N Sitafloxacin Chemical compound C([C@H]1N)N(C=2C(=C3C(C(C(C(O)=O)=CN3[C@H]3[C@H](C3)F)=O)=CC=2F)Cl)CC11CC1 PNUZDKCDAWUEGK-CYZMBNFOSA-N 0.000 description 1
- 208000000453 Skin Neoplasms Diseases 0.000 description 1
- UIIMBOGNXHQVGW-DEQYMQKBSA-M Sodium bicarbonate-14C Chemical compound [Na+].O[14C]([O-])=O UIIMBOGNXHQVGW-DEQYMQKBSA-M 0.000 description 1
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- 238000006619 Stille reaction Methods 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical group [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 description 1
- 206010052779 Transplant rejections Diseases 0.000 description 1
- 241000700605 Viruses Species 0.000 description 1
- LJOOWESTVASNOG-UFJKPHDISA-N [(1s,3r,4ar,7s,8s,8as)-3-hydroxy-8-[2-[(4r)-4-hydroxy-6-oxooxan-2-yl]ethyl]-7-methyl-1,2,3,4,4a,7,8,8a-octahydronaphthalen-1-yl] (2s)-2-methylbutanoate Chemical compound C([C@H]1[C@@H](C)C=C[C@H]2C[C@@H](O)C[C@@H]([C@H]12)OC(=O)[C@@H](C)CC)CC1C[C@@H](O)CC(=O)O1 LJOOWESTVASNOG-UFJKPHDISA-N 0.000 description 1
- SPXSEZMVRJLHQG-XMMPIXPASA-N [(2R)-1-[[4-[(3-phenylmethoxyphenoxy)methyl]phenyl]methyl]pyrrolidin-2-yl]methanol Chemical compound C(C1=CC=CC=C1)OC=1C=C(OCC2=CC=C(CN3[C@H](CCC3)CO)C=C2)C=CC=1 SPXSEZMVRJLHQG-XMMPIXPASA-N 0.000 description 1
- IOSLINNLJFQMFF-XMMPIXPASA-N [(2R)-1-[[4-[[3-[(4-fluorophenyl)methylsulfanyl]phenoxy]methyl]phenyl]methyl]pyrrolidin-2-yl]methanol Chemical compound FC1=CC=C(CSC=2C=C(OCC3=CC=C(CN4[C@H](CCC4)CO)C=C3)C=CC=2)C=C1 IOSLINNLJFQMFF-XMMPIXPASA-N 0.000 description 1
- LNUFLCYMSVYYNW-ZPJMAFJPSA-N [(2r,3r,4s,5r,6r)-2-[(2r,3r,4s,5r,6r)-6-[(2r,3r,4s,5r,6r)-6-[(2r,3r,4s,5r,6r)-6-[[(3s,5s,8r,9s,10s,13r,14s,17r)-10,13-dimethyl-17-[(2r)-6-methylheptan-2-yl]-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1h-cyclopenta[a]phenanthren-3-yl]oxy]-4,5-disulfo Chemical compound O([C@@H]1[C@@H](COS(O)(=O)=O)O[C@@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@@H]1[C@@H](COS(O)(=O)=O)O[C@@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@@H]1[C@@H](COS(O)(=O)=O)O[C@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@@H]1C[C@@H]2CC[C@H]3[C@@H]4CC[C@@H]([C@]4(CC[C@@H]3[C@@]2(C)CC1)C)[C@H](C)CCCC(C)C)[C@H]1O[C@H](COS(O)(=O)=O)[C@@H](OS(O)(=O)=O)[C@H](OS(O)(=O)=O)[C@H]1OS(O)(=O)=O LNUFLCYMSVYYNW-ZPJMAFJPSA-N 0.000 description 1
- PSLUFJFHTBIXMW-WYEYVKMPSA-N [(3r,4ar,5s,6s,6as,10s,10ar,10bs)-3-ethenyl-10,10b-dihydroxy-3,4a,7,7,10a-pentamethyl-1-oxo-6-(2-pyridin-2-ylethylcarbamoyloxy)-5,6,6a,8,9,10-hexahydro-2h-benzo[f]chromen-5-yl] acetate Chemical compound O([C@@H]1[C@@H]([C@]2(O[C@](C)(CC(=O)[C@]2(O)[C@@]2(C)[C@@H](O)CCC(C)(C)[C@@H]21)C=C)C)OC(=O)C)C(=O)NCCC1=CC=CC=N1 PSLUFJFHTBIXMW-WYEYVKMPSA-N 0.000 description 1
- SMNRFWMNPDABKZ-WVALLCKVSA-N [[(2R,3S,4R,5S)-5-(2,6-dioxo-3H-pyridin-3-yl)-3,4-dihydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl] [[[(2R,3S,4S,5R,6R)-4-fluoro-3,5-dihydroxy-6-(hydroxymethyl)oxan-2-yl]oxy-hydroxyphosphoryl]oxy-hydroxyphosphoryl] hydrogen phosphate Chemical compound OC[C@H]1O[C@H](OP(O)(=O)OP(O)(=O)OP(O)(=O)OP(O)(=O)OC[C@H]2O[C@H]([C@H](O)[C@@H]2O)C2C=CC(=O)NC2=O)[C@H](O)[C@@H](F)[C@@H]1O SMNRFWMNPDABKZ-WVALLCKVSA-N 0.000 description 1
- 235000010489 acacia gum Nutrition 0.000 description 1
- 239000000205 acacia gum Substances 0.000 description 1
- XPOLVIIHTDKJRY-UHFFFAOYSA-N acetic acid;methanimidamide Chemical compound NC=N.CC(O)=O XPOLVIIHTDKJRY-UHFFFAOYSA-N 0.000 description 1
- WETWJCDKMRHUPV-UHFFFAOYSA-N acetyl chloride Chemical compound CC(Cl)=O WETWJCDKMRHUPV-UHFFFAOYSA-N 0.000 description 1
- 239000012346 acetyl chloride Substances 0.000 description 1
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 125000002015 acyclic group Chemical group 0.000 description 1
- 239000008272 agar Substances 0.000 description 1
- 235000010419 agar Nutrition 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- QBYJBZPUGVGKQQ-SJJAEHHWSA-N aldrin Chemical compound C1[C@H]2C=C[C@@H]1[C@H]1[C@@](C3(Cl)Cl)(Cl)C(Cl)=C(Cl)[C@@]3(Cl)[C@H]12 QBYJBZPUGVGKQQ-SJJAEHHWSA-N 0.000 description 1
- 229940072056 alginate Drugs 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 150000004781 alginic acids Chemical class 0.000 description 1
- 239000003513 alkali Substances 0.000 description 1
- 150000001342 alkaline earth metals Chemical class 0.000 description 1
- 125000000676 alkoxyimino group Chemical group 0.000 description 1
- 150000003973 alkyl amines Chemical class 0.000 description 1
- 125000004457 alkyl amino carbonyl group Chemical group 0.000 description 1
- 125000004471 alkyl aminosulfonyl group Chemical group 0.000 description 1
- 125000003806 alkyl carbonyl amino group Chemical group 0.000 description 1
- 125000004448 alkyl carbonyl group Chemical group 0.000 description 1
- 125000005196 alkyl carbonyloxy group Chemical group 0.000 description 1
- 125000005600 alkyl phosphonate group Chemical group 0.000 description 1
- 125000004390 alkyl sulfonyl group Chemical group 0.000 description 1
- 125000004656 alkyl sulfonylamino group Chemical group 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 230000009435 amidation Effects 0.000 description 1
- 238000007112 amidation reaction Methods 0.000 description 1
- BIVUUOPIAYRCAP-UHFFFAOYSA-N aminoazanium;chloride Chemical compound Cl.NN BIVUUOPIAYRCAP-UHFFFAOYSA-N 0.000 description 1
- 125000004397 aminosulfonyl group Chemical group NS(=O)(=O)* 0.000 description 1
- 229910021529 ammonia Inorganic materials 0.000 description 1
- 235000019257 ammonium acetate Nutrition 0.000 description 1
- 229940043376 ammonium acetate Drugs 0.000 description 1
- 235000012538 ammonium bicarbonate Nutrition 0.000 description 1
- 235000012501 ammonium carbonate Nutrition 0.000 description 1
- 230000000340 anti-metabolite Effects 0.000 description 1
- 230000001028 anti-proliverative effect Effects 0.000 description 1
- 230000000259 anti-tumor effect Effects 0.000 description 1
- 229940100197 antimetabolite Drugs 0.000 description 1
- 229940045988 antineoplastic drug protein kinase inhibitors Drugs 0.000 description 1
- 230000006907 apoptotic process Effects 0.000 description 1
- 239000008346 aqueous phase Substances 0.000 description 1
- 125000005100 aryl amino carbonyl group Chemical group 0.000 description 1
- 125000005141 aryl amino sulfonyl group Chemical group 0.000 description 1
- 125000004658 aryl carbonyl amino group Chemical group 0.000 description 1
- 125000005129 aryl carbonyl group Chemical group 0.000 description 1
- 125000005199 aryl carbonyloxy group Chemical group 0.000 description 1
- 125000005161 aryl oxy carbonyl group Chemical group 0.000 description 1
- 125000004657 aryl sulfonyl amino group Chemical group 0.000 description 1
- 125000004391 aryl sulfonyl group Chemical group 0.000 description 1
- 125000005110 aryl thio group Chemical group 0.000 description 1
- XRWSZZJLZRKHHD-WVWIJVSJSA-N asunaprevir Chemical compound O=C([C@@H]1C[C@H](CN1C(=O)[C@@H](NC(=O)OC(C)(C)C)C(C)(C)C)OC1=NC=C(C2=CC=C(Cl)C=C21)OC)N[C@]1(C(=O)NS(=O)(=O)C2CC2)C[C@H]1C=C XRWSZZJLZRKHHD-WVWIJVSJSA-N 0.000 description 1
- 230000035578 autophosphorylation Effects 0.000 description 1
- 125000005604 azodicarboxylate group Chemical group 0.000 description 1
- 102000007348 bcl-Associated Death Protein Human genes 0.000 description 1
- 108010007734 bcl-Associated Death Protein Proteins 0.000 description 1
- 125000002047 benzodioxolyl group Chemical group O1OC(C2=C1C=CC=C2)* 0.000 description 1
- 125000000499 benzofuranyl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- 125000004196 benzothienyl group Chemical group S1C(=CC2=C1C=CC=C2)* 0.000 description 1
- HSDAJNMJOMSNEV-UHFFFAOYSA-N benzyl chloroformate Chemical compound ClC(=O)OCC1=CC=CC=C1 HSDAJNMJOMSNEV-UHFFFAOYSA-N 0.000 description 1
- KGNDCEVUMONOKF-UGPLYTSKSA-N benzyl n-[(2r)-1-[(2s,4r)-2-[[(2s)-6-amino-1-(1,3-benzoxazol-2-yl)-1,1-dihydroxyhexan-2-yl]carbamoyl]-4-[(4-methylphenyl)methoxy]pyrrolidin-1-yl]-1-oxo-4-phenylbutan-2-yl]carbamate Chemical compound C1=CC(C)=CC=C1CO[C@H]1CN(C(=O)[C@@H](CCC=2C=CC=CC=2)NC(=O)OCC=2C=CC=CC=2)[C@H](C(=O)N[C@@H](CCCCN)C(O)(O)C=2OC3=CC=CC=C3N=2)C1 KGNDCEVUMONOKF-UGPLYTSKSA-N 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- 238000010876 biochemical test Methods 0.000 description 1
- 238000012925 biological evaluation Methods 0.000 description 1
- 239000004305 biphenyl Substances 0.000 description 1
- 235000010290 biphenyl Nutrition 0.000 description 1
- 229940098773 bovine serum albumin Drugs 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 235000001465 calcium Nutrition 0.000 description 1
- CJZGTCYPCWQAJB-UHFFFAOYSA-L calcium stearate Chemical compound [Ca+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O CJZGTCYPCWQAJB-UHFFFAOYSA-L 0.000 description 1
- 239000008116 calcium stearate Substances 0.000 description 1
- 235000013539 calcium stearate Nutrition 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 230000036952 cancer formation Effects 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 239000004202 carbamide Substances 0.000 description 1
- 125000004432 carbon atom Chemical group C* 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 150000001733 carboxylic acid esters Chemical class 0.000 description 1
- 231100000504 carcinogenesis Toxicity 0.000 description 1
- 230000022131 cell cycle Effects 0.000 description 1
- 230000005754 cellular signaling Effects 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 238000009104 chemotherapy regimen Methods 0.000 description 1
- 238000004296 chiral HPLC Methods 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 125000002603 chloroethyl group Chemical group [H]C([*])([H])C([H])([H])Cl 0.000 description 1
- 235000013985 cinnamic acid Nutrition 0.000 description 1
- 229930016911 cinnamic acid Natural products 0.000 description 1
- 235000015165 citric acid Nutrition 0.000 description 1
- 238000003776 cleavage reaction Methods 0.000 description 1
- 229940110456 cocoa butter Drugs 0.000 description 1
- 235000019868 cocoa butter Nutrition 0.000 description 1
- 229940125773 compound 10 Drugs 0.000 description 1
- 229940125797 compound 12 Drugs 0.000 description 1
- 229940126543 compound 14 Drugs 0.000 description 1
- 229940125758 compound 15 Drugs 0.000 description 1
- 229940126142 compound 16 Drugs 0.000 description 1
- 229940125810 compound 20 Drugs 0.000 description 1
- 229940126086 compound 21 Drugs 0.000 description 1
- 229940126208 compound 22 Drugs 0.000 description 1
- 229940125833 compound 23 Drugs 0.000 description 1
- 229940125961 compound 24 Drugs 0.000 description 1
- 229940125846 compound 25 Drugs 0.000 description 1
- 229940125851 compound 27 Drugs 0.000 description 1
- 229940127204 compound 29 Drugs 0.000 description 1
- 229940125877 compound 31 Drugs 0.000 description 1
- 229940125878 compound 36 Drugs 0.000 description 1
- 229940125807 compound 37 Drugs 0.000 description 1
- 229940127573 compound 38 Drugs 0.000 description 1
- 229940126540 compound 41 Drugs 0.000 description 1
- 229940125936 compound 42 Drugs 0.000 description 1
- 229940125844 compound 46 Drugs 0.000 description 1
- 229940127271 compound 49 Drugs 0.000 description 1
- 229940125898 compound 5 Drugs 0.000 description 1
- 229940126545 compound 53 Drugs 0.000 description 1
- 229940127113 compound 57 Drugs 0.000 description 1
- 229940125900 compound 59 Drugs 0.000 description 1
- 229940126179 compound 72 Drugs 0.000 description 1
- 238000012790 confirmation Methods 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- 239000008120 corn starch Substances 0.000 description 1
- 239000006184 cosolvent Substances 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 125000004465 cycloalkenyloxy group Chemical group 0.000 description 1
- 125000006254 cycloalkyl carbonyl group Chemical group 0.000 description 1
- ZXIJMRYMVAMXQP-UHFFFAOYSA-N cycloheptene Chemical compound C1CCC=CCC1 ZXIJMRYMVAMXQP-UHFFFAOYSA-N 0.000 description 1
- SNRCKKQHDUIRIY-UHFFFAOYSA-L cyclopenta-1,4-dien-1-yl(diphenyl)phosphane;dichloromethane;dichloropalladium;iron(2+) Chemical compound [Fe+2].ClCCl.Cl[Pd]Cl.C1=C[CH-]C(P(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1.C1=C[CH-]C(P(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1 SNRCKKQHDUIRIY-UHFFFAOYSA-L 0.000 description 1
- 231100000135 cytotoxicity Toxicity 0.000 description 1
- 230000003013 cytotoxicity Effects 0.000 description 1
- DEZRYPDIMOWBDS-UHFFFAOYSA-N dcm dichloromethane Chemical compound ClCCl.ClCCl DEZRYPDIMOWBDS-UHFFFAOYSA-N 0.000 description 1
- 230000034994 death Effects 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- 125000004473 dialkylaminocarbonyl group Chemical group 0.000 description 1
- 125000004986 diarylamino group Chemical group 0.000 description 1
- 229940117389 dichlorobenzene Drugs 0.000 description 1
- 235000014113 dietary fatty acids Nutrition 0.000 description 1
- HPNMFZURTQLUMO-UHFFFAOYSA-N diethylamine Chemical compound CCNCC HPNMFZURTQLUMO-UHFFFAOYSA-N 0.000 description 1
- 125000005046 dihydronaphthyl group Chemical group 0.000 description 1
- 229940113088 dimethylacetamide Drugs 0.000 description 1
- UXGNZZKBCMGWAZ-UHFFFAOYSA-N dimethylformamide dmf Chemical compound CN(C)C=O.CN(C)C=O UXGNZZKBCMGWAZ-UHFFFAOYSA-N 0.000 description 1
- 230000008034 disappearance Effects 0.000 description 1
- 239000007884 disintegrant Substances 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 208000007784 diverticulitis Diseases 0.000 description 1
- CETRZFQIITUQQL-UHFFFAOYSA-N dmso dimethylsulfoxide Chemical compound CS(C)=O.CS(C)=O CETRZFQIITUQQL-UHFFFAOYSA-N 0.000 description 1
- MOTZDAYCYVMXPC-UHFFFAOYSA-N dodecyl hydrogen sulfate Chemical compound CCCCCCCCCCCCOS(O)(=O)=O MOTZDAYCYVMXPC-UHFFFAOYSA-N 0.000 description 1
- 229940043264 dodecyl sulfate Drugs 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 230000007783 downstream signaling Effects 0.000 description 1
- 239000008298 dragée Substances 0.000 description 1
- 238000007876 drug discovery Methods 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 230000008482 dysregulation Effects 0.000 description 1
- 238000001962 electrophoresis Methods 0.000 description 1
- BJXYHBKEQFQVES-NWDGAFQWSA-N enpatoran Chemical compound N[C@H]1CN(C[C@H](C1)C(F)(F)F)C1=C2C=CC=NC2=C(C=C1)C#N BJXYHBKEQFQVES-NWDGAFQWSA-N 0.000 description 1
- HKSZLNNOFSGOKW-UHFFFAOYSA-N ent-staurosporine Natural products C12=C3N4C5=CC=CC=C5C3=C3CNC(=O)C3=C2C2=CC=CC=C2N1C1CC(NC)C(OC)C4(C)O1 HKSZLNNOFSGOKW-UHFFFAOYSA-N 0.000 description 1
- 238000006911 enzymatic reaction Methods 0.000 description 1
- 238000011067 equilibration Methods 0.000 description 1
- RKZRCSHSYSYDSR-UHFFFAOYSA-N ethyl 1,8-dimethyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxylate Chemical compound C1CC2=CN=C(C)N=C2C2=C1C(C(=O)OCC)=NN2C RKZRCSHSYSYDSR-UHFFFAOYSA-N 0.000 description 1
- MLZXGZLFSYJMDH-UHFFFAOYSA-N ethyl 1-(2-hydroxyethyl)-8-methoxy-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxylate Chemical compound C1CC2=CN=C(OC)N=C2C2=C1C(C(=O)OCC)=NN2CCO MLZXGZLFSYJMDH-UHFFFAOYSA-N 0.000 description 1
- DQWJANBYFFPPKD-UHFFFAOYSA-N ethyl 1-(2-hydroxyethyl)-8-methylsulfanyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxylate Chemical compound C1CC2=CN=C(SC)N=C2C2=C1C(C(=O)OCC)=NN2CCO DQWJANBYFFPPKD-UHFFFAOYSA-N 0.000 description 1
- DOQZDBICCMKIBS-UHFFFAOYSA-N ethyl 1-(2-hydroxyethyl)-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxylate Chemical compound C1=CC2=CN=C(SC)N=C2C2=C1C(C(=O)OCC)=NN2CCO DOQZDBICCMKIBS-UHFFFAOYSA-N 0.000 description 1
- AQLKKHFTRSCWMX-UHFFFAOYSA-N ethyl 1-[2-[(2-methylpropan-2-yl)oxycarbonylamino]ethyl]-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxylate Chemical compound C1=CC2=CN=C(SC)N=C2C2=C1C(C(=O)OCC)=NN2CCNC(=O)OC(C)(C)C AQLKKHFTRSCWMX-UHFFFAOYSA-N 0.000 description 1
- NCAUDJHUBRKYAW-UHFFFAOYSA-N ethyl 1-methyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxylate Chemical compound C1CC2=CN=CN=C2C2=C1C(C(=O)OCC)=NN2C NCAUDJHUBRKYAW-UHFFFAOYSA-N 0.000 description 1
- XTQZFGZEXAFLJN-UHFFFAOYSA-N ethyl 1-methyl-8-methylsulfanyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxylate Chemical compound C1CC2=CN=C(SC)N=C2C2=C1C(C(=O)OCC)=NN2C XTQZFGZEXAFLJN-UHFFFAOYSA-N 0.000 description 1
- WIWOFRYCHIWMNM-UHFFFAOYSA-N ethyl 1-methyl-8-methylsulfanylpyrazolo[4,3-h]quinazoline-3-carboxylate Chemical compound C1=CC2=CN=C(SC)N=C2C2=C1C(C(=O)OCC)=NN2C WIWOFRYCHIWMNM-UHFFFAOYSA-N 0.000 description 1
- AXJWUDNSBLMMJH-UHFFFAOYSA-N ethyl 1-tert-butyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxylate Chemical compound C1CC2=CN=CN=C2C2=C1C(C(=O)OCC)=NN2C(C)(C)C AXJWUDNSBLMMJH-UHFFFAOYSA-N 0.000 description 1
- ROBIRYRHZYWANU-UHFFFAOYSA-N ethyl 1-tert-butyl-8-methyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxylate Chemical compound C1CC2=CN=C(C)N=C2C2=C1C(C(=O)OCC)=NN2C(C)(C)C ROBIRYRHZYWANU-UHFFFAOYSA-N 0.000 description 1
- UMHRGOOZJYOURO-UHFFFAOYSA-N ethyl 1-tert-butyl-8-methylpyrazolo[4,3-h]quinazoline-3-carboxylate Chemical compound C1=CC2=CN=C(C)N=C2C2=C1C(C(=O)OCC)=NN2C(C)(C)C UMHRGOOZJYOURO-UHFFFAOYSA-N 0.000 description 1
- DXWOAPLLSSUKNC-UHFFFAOYSA-N ethyl 1-tert-butyl-8-methylsulfanyl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxylate Chemical compound C1CC2=CN=C(SC)N=C2C2=C1C(C(=O)OCC)=NN2C(C)(C)C DXWOAPLLSSUKNC-UHFFFAOYSA-N 0.000 description 1
- RVMWXUZBBYTRCA-UHFFFAOYSA-N ethyl 1-tert-butylpyrazolo[4,3-h]quinazoline-3-carboxylate Chemical compound C1=CC2=CN=CN=C2C2=C1C(C(=O)OCC)=NN2C(C)(C)C RVMWXUZBBYTRCA-UHFFFAOYSA-N 0.000 description 1
- CEAKAIYDERWAJF-UHFFFAOYSA-N ethyl 2-(3-ethoxy-2-oxocyclohex-3-en-1-yl)-2-oxoacetate Chemical compound CCOC(=O)C(=O)C1CCC=C(OCC)C1=O CEAKAIYDERWAJF-UHFFFAOYSA-N 0.000 description 1
- GWNFQAKCJYEJEW-UHFFFAOYSA-N ethyl 3-[8-[[4-methyl-5-[(3-methyl-4-oxophthalazin-1-yl)methyl]-1,2,4-triazol-3-yl]sulfanyl]octanoylamino]benzoate Chemical compound CCOC(=O)C1=CC(NC(=O)CCCCCCCSC2=NN=C(CC3=NN(C)C(=O)C4=CC=CC=C34)N2C)=CC=C1 GWNFQAKCJYEJEW-UHFFFAOYSA-N 0.000 description 1
- ZXVMKJSZINVCPQ-UHFFFAOYSA-N ethyl 8-(4-fluorophenyl)-1-[3-[(2-methylpropan-2-yl)oxycarbonylamino]propyl]-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxylate Chemical compound CCOC(=O)C1=NN(CCCNC(=O)OC(C)(C)C)C(C2=N3)=C1CCC2=CN=C3C1=CC=C(F)C=C1 ZXVMKJSZINVCPQ-UHFFFAOYSA-N 0.000 description 1
- BHDQABOIKBOGJL-UHFFFAOYSA-N ethyl 8-(4-fluorophenyl)-1-trityl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxylate Chemical compound CCOC(=O)C1=NN(C(C=2C=CC=CC=2)(C=2C=CC=CC=2)C=2C=CC=CC=2)C(C2=N3)=C1CCC2=CN=C3C1=CC=C(F)C=C1 BHDQABOIKBOGJL-UHFFFAOYSA-N 0.000 description 1
- GNIPHBLLPQTGOL-UHFFFAOYSA-N ethyl 8-(4-fluorophenyl)-2-[3-[(2-methylpropan-2-yl)oxycarbonylamino]propyl]-1,3,4,5-tetrahydropyrazolo[4,3-h]quinazoline-3-carboxylate Chemical compound CCOC(=O)C1N(CCCNC(=O)OC(C)(C)C)NC(C2=N3)=C1CCC2=CN=C3C1=CC=C(F)C=C1 GNIPHBLLPQTGOL-UHFFFAOYSA-N 0.000 description 1
- VYRVUOIDLIZSOZ-UHFFFAOYSA-N ethyl 8-(4-methoxyphenyl)-1-trityl-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxylate Chemical compound CCOC(=O)C1=NN(C(C=2C=CC=CC=2)(C=2C=CC=CC=2)C=2C=CC=CC=2)C(C2=N3)=C1CCC2=CN=C3C1=CC=C(OC)C=C1 VYRVUOIDLIZSOZ-UHFFFAOYSA-N 0.000 description 1
- JAWAWHCHSUCPDG-UHFFFAOYSA-N ethyl 8-iodo-1-[3-[(2-methylpropan-2-yl)oxycarbonylamino]propyl]-4,5-dihydropyrazolo[4,3-h]quinazoline-3-carboxylate Chemical compound C1CC2=CN=C(I)N=C2C2=C1C(C(=O)OCC)=NN2CCCNC(=O)OC(C)(C)C JAWAWHCHSUCPDG-UHFFFAOYSA-N 0.000 description 1
- WUDNUHPRLBTKOJ-UHFFFAOYSA-N ethyl isocyanate Chemical compound CCN=C=O WUDNUHPRLBTKOJ-UHFFFAOYSA-N 0.000 description 1
- LVGKNOAMLMIIKO-QXMHVHEDSA-N ethyl oleate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OCC LVGKNOAMLMIIKO-QXMHVHEDSA-N 0.000 description 1
- 229940093471 ethyl oleate Drugs 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 239000000194 fatty acid Substances 0.000 description 1
- 229930195729 fatty acid Natural products 0.000 description 1
- 239000007941 film coated tablet Substances 0.000 description 1
- 239000007888 film coating Substances 0.000 description 1
- 238000009501 film coating Methods 0.000 description 1
- 125000001153 fluoro group Chemical group F* 0.000 description 1
- 235000003599 food sweetener Nutrition 0.000 description 1
- 235000019253 formic acid Nutrition 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 238000013467 fragmentation Methods 0.000 description 1
- 238000006062 fragmentation reaction Methods 0.000 description 1
- 239000012458 free base Substances 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 235000011087 fumaric acid Nutrition 0.000 description 1
- 125000002541 furyl group Chemical group 0.000 description 1
- 102000037865 fusion proteins Human genes 0.000 description 1
- 108020001507 fusion proteins Proteins 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 230000009368 gene silencing by RNA Effects 0.000 description 1
- 239000012362 glacial acetic acid Substances 0.000 description 1
- 229960001031 glucose Drugs 0.000 description 1
- 235000011187 glycerol Nutrition 0.000 description 1
- 150000002334 glycols Chemical class 0.000 description 1
- 108010067216 glycyl-glycyl-glycine Proteins 0.000 description 1
- 208000024908 graft versus host disease Diseases 0.000 description 1
- 230000005484 gravity Effects 0.000 description 1
- JAXFJECJQZDFJS-XHEPKHHKSA-N gtpl8555 Chemical compound OC(=O)C[C@H](N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](C(C)C)C(=O)N1CCC[C@@H]1C(=O)N[C@H](B1O[C@@]2(C)[C@H]3C[C@H](C3(C)C)C[C@H]2O1)CCC1=CC=C(F)C=C1 JAXFJECJQZDFJS-XHEPKHHKSA-N 0.000 description 1
- 150000002357 guanidines Chemical class 0.000 description 1
- 229940083094 guanine derivative acting on arteriolar smooth muscle Drugs 0.000 description 1
- 229940093915 gynecological organic acid Drugs 0.000 description 1
- 125000000592 heterocycloalkyl group Chemical group 0.000 description 1
- 238000000589 high-performance liquid chromatography-mass spectrometry Methods 0.000 description 1
- 125000002768 hydroxyalkyl group Chemical group 0.000 description 1
- 150000002443 hydroxylamines Chemical class 0.000 description 1
- 125000002962 imidazol-1-yl group Chemical group [*]N1C([H])=NC([H])=C1[H] 0.000 description 1
- MTNDZQHUAFNZQY-UHFFFAOYSA-N imidazoline Chemical compound C1CN=CN1 MTNDZQHUAFNZQY-UHFFFAOYSA-N 0.000 description 1
- 125000002883 imidazolyl group Chemical group 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 125000003392 indanyl group Chemical group C1(CCC2=CC=CC=C12)* 0.000 description 1
- 125000003454 indenyl group Chemical group C1(C=CC2=CC=CC=C12)* 0.000 description 1
- 125000001041 indolyl group Chemical group 0.000 description 1
- 230000004968 inflammatory condition Effects 0.000 description 1
- 238000011081 inoculation Methods 0.000 description 1
- 150000007529 inorganic bases Chemical class 0.000 description 1
- 230000002452 interceptive effect Effects 0.000 description 1
- 229940076264 interleukin-3 Drugs 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000010255 intramuscular injection Methods 0.000 description 1
- 239000007927 intramuscular injection Substances 0.000 description 1
- 238000007913 intrathecal administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 238000010253 intravenous injection Methods 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 238000005342 ion exchange Methods 0.000 description 1
- 238000005040 ion trap Methods 0.000 description 1
- 229940045996 isethionic acid Drugs 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 239000012948 isocyanate Substances 0.000 description 1
- 150000002513 isocyanates Chemical class 0.000 description 1
- 125000005956 isoquinolyl group Chemical group 0.000 description 1
- 125000001786 isothiazolyl group Chemical group 0.000 description 1
- 125000000842 isoxazolyl group Chemical group 0.000 description 1
- ZLVXBBHTMQJRSX-VMGNSXQWSA-N jdtic Chemical compound C1([C@]2(C)CCN(C[C@@H]2C)C[C@H](C(C)C)NC(=O)[C@@H]2NCC3=CC(O)=CC=C3C2)=CC=CC(O)=C1 ZLVXBBHTMQJRSX-VMGNSXQWSA-N 0.000 description 1
- 239000004310 lactic acid Substances 0.000 description 1
- 235000014655 lactic acid Nutrition 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 229960001375 lactose Drugs 0.000 description 1
- 229960004393 lidocaine hydrochloride Drugs 0.000 description 1
- YECIFGHRMFEPJK-UHFFFAOYSA-N lidocaine hydrochloride monohydrate Chemical compound O.[Cl-].CC[NH+](CC)CC(=O)NC1=C(C)C=CC=C1C YECIFGHRMFEPJK-UHFFFAOYSA-N 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 239000006193 liquid solution Substances 0.000 description 1
- 239000006194 liquid suspension Substances 0.000 description 1
- 239000012280 lithium aluminium hydride Substances 0.000 description 1
- RENRQMCACQEWFC-UGKGYDQZSA-N lnp023 Chemical compound C1([C@H]2N(CC=3C=4C=CNC=4C(C)=CC=3OC)CC[C@@H](C2)OCC)=CC=C(C(O)=O)C=C1 RENRQMCACQEWFC-UGKGYDQZSA-N 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 238000004020 luminiscence type Methods 0.000 description 1
- 239000006166 lysate Substances 0.000 description 1
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Substances [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- 230000014759 maintenance of location Effects 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- 239000001630 malic acid Substances 0.000 description 1
- 235000011090 malic acid Nutrition 0.000 description 1
- 230000036210 malignancy Effects 0.000 description 1
- 229960002510 mandelic acid Drugs 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 101150054634 melk gene Proteins 0.000 description 1
- COTNUBDHGSIOTA-UHFFFAOYSA-N meoh methanol Chemical compound OC.OC COTNUBDHGSIOTA-UHFFFAOYSA-N 0.000 description 1
- QSHDDOUJBYECFT-UHFFFAOYSA-N mercury Chemical compound [Hg] QSHDDOUJBYECFT-UHFFFAOYSA-N 0.000 description 1
- 229910052753 mercury Inorganic materials 0.000 description 1
- 230000037353 metabolic pathway Effects 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- QARBMVPHQWIHKH-UHFFFAOYSA-N methanesulfonyl chloride Chemical compound CS(Cl)(=O)=O QARBMVPHQWIHKH-UHFFFAOYSA-N 0.000 description 1
- NXKMGLPAVNNCKB-UHFFFAOYSA-N methyl 2-(3-carbamoyl-8-methylsulfanylpyrazolo[4,3-h]quinazolin-1-yl)-2-methylpropanoate Chemical compound C1=NC(SC)=NC2=C3N(C(C)(C)C(=O)OC)N=C(C(N)=O)C3=CC=C21 NXKMGLPAVNNCKB-UHFFFAOYSA-N 0.000 description 1
- NNBBQNFHCVVQHZ-UHFFFAOYSA-N methyl carbamimidothioate;sulfuric acid Chemical compound CSC(N)=N.OS(O)(=O)=O NNBBQNFHCVVQHZ-UHFFFAOYSA-N 0.000 description 1
- CBTGNLZUIZHUHY-UHFFFAOYSA-N methyl cyclobutanecarboxylate Chemical group COC(=O)C1CCC1 CBTGNLZUIZHUHY-UHFFFAOYSA-N 0.000 description 1
- WBYWAXJHAXSJNI-UHFFFAOYSA-N methyl p-hydroxycinnamate Natural products OC(=O)C=CC1=CC=CC=C1 WBYWAXJHAXSJNI-UHFFFAOYSA-N 0.000 description 1
- NQMRYBIKMRVZLB-UHFFFAOYSA-N methylamine hydrochloride Chemical compound [Cl-].[NH3+]C NQMRYBIKMRVZLB-UHFFFAOYSA-N 0.000 description 1
- GIHFHHKDKVDQIT-UHFFFAOYSA-N methylurea;sulfuric acid Chemical compound CNC(O)=N.OS(O)(=O)=O GIHFHHKDKVDQIT-UHFFFAOYSA-N 0.000 description 1
- 238000013508 migration Methods 0.000 description 1
- 230000005012 migration Effects 0.000 description 1
- 239000002480 mineral oil Substances 0.000 description 1
- 235000010446 mineral oil Nutrition 0.000 description 1
- 150000007522 mineralic acids Chemical class 0.000 description 1
- 238000006011 modification reaction Methods 0.000 description 1
- 125000002950 monocyclic group Chemical group 0.000 description 1
- 125000004573 morpholin-4-yl group Chemical group N1(CCOCC1)* 0.000 description 1
- 238000010172 mouse model Methods 0.000 description 1
- 238000002703 mutagenesis Methods 0.000 description 1
- 231100000350 mutagenesis Toxicity 0.000 description 1
- 210000000066 myeloid cell Anatomy 0.000 description 1
- 201000000050 myeloid neoplasm Diseases 0.000 description 1
- DBNQIOANXZVWIP-UHFFFAOYSA-N n,n-dimethyl-1,1-bis[(2-methylpropan-2-yl)oxy]methanamine Chemical compound CC(C)(C)OC(N(C)C)OC(C)(C)C DBNQIOANXZVWIP-UHFFFAOYSA-N 0.000 description 1
- YFJAIURZMRJPDB-UHFFFAOYSA-N n,n-dimethylpiperidin-4-amine Chemical compound CN(C)C1CCNCC1 YFJAIURZMRJPDB-UHFFFAOYSA-N 0.000 description 1
- YCJZWBZJSYLMPB-UHFFFAOYSA-N n-(2-chloropyrimidin-4-yl)-2,5-dimethyl-1-phenylimidazole-4-carboxamide Chemical compound CC=1N(C=2C=CC=CC=2)C(C)=NC=1C(=O)NC1=CC=NC(Cl)=N1 YCJZWBZJSYLMPB-UHFFFAOYSA-N 0.000 description 1
- JSKQBIIYZUWIQC-UHFFFAOYSA-N n-(3-hydroxypropyl)-8-(4-methoxyphenyl)-4,5-dihydro-2h-pyrazolo[4,3-h]quinazoline-3-carboxamide Chemical compound C1=CC(OC)=CC=C1C1=NC=C(CCC2=C3NN=C2C(=O)NCCCO)C3=N1 JSKQBIIYZUWIQC-UHFFFAOYSA-N 0.000 description 1
- SYSQUGFVNFXIIT-UHFFFAOYSA-N n-[4-(1,3-benzoxazol-2-yl)phenyl]-4-nitrobenzenesulfonamide Chemical class C1=CC([N+](=O)[O-])=CC=C1S(=O)(=O)NC1=CC=C(C=2OC3=CC=CC=C3N=2)C=C1 SYSQUGFVNFXIIT-UHFFFAOYSA-N 0.000 description 1
- YGBMCLDVRUGXOV-UHFFFAOYSA-N n-[6-[6-chloro-5-[(4-fluorophenyl)sulfonylamino]pyridin-3-yl]-1,3-benzothiazol-2-yl]acetamide Chemical compound C1=C2SC(NC(=O)C)=NC2=CC=C1C(C=1)=CN=C(Cl)C=1NS(=O)(=O)C1=CC=C(F)C=C1 YGBMCLDVRUGXOV-UHFFFAOYSA-N 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- WOOWBQQQJXZGIE-UHFFFAOYSA-N n-ethyl-n-propan-2-ylpropan-2-amine Chemical compound CCN(C(C)C)C(C)C.CCN(C(C)C)C(C)C WOOWBQQQJXZGIE-UHFFFAOYSA-N 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 229920003052 natural elastomer Polymers 0.000 description 1
- 229920001194 natural rubber Polymers 0.000 description 1
- IOMMMLWIABWRKL-WUTDNEBXSA-N nazartinib Chemical compound C1N(C(=O)/C=C/CN(C)C)CCCC[C@H]1N1C2=C(Cl)C=CC=C2N=C1NC(=O)C1=CC=NC(C)=C1 IOMMMLWIABWRKL-WUTDNEBXSA-N 0.000 description 1
- 208000015122 neurodegenerative disease Diseases 0.000 description 1
- 229910017604 nitric acid Inorganic materials 0.000 description 1
- 239000012299 nitrogen atmosphere Substances 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- VWBWQOUWDOULQN-UHFFFAOYSA-N nmp n-methylpyrrolidone Chemical compound CN1CCCC1=O.CN1CCCC1=O VWBWQOUWDOULQN-UHFFFAOYSA-N 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 239000004006 olive oil Substances 0.000 description 1
- 235000008390 olive oil Nutrition 0.000 description 1
- PIDFDZJZLOTZTM-KHVQSSSXSA-N ombitasvir Chemical compound COC(=O)N[C@@H](C(C)C)C(=O)N1CCC[C@H]1C(=O)NC1=CC=C([C@H]2N([C@@H](CC2)C=2C=CC(NC(=O)[C@H]3N(CCC3)C(=O)[C@@H](NC(=O)OC)C(C)C)=CC=2)C=2C=CC(=CC=2)C(C)(C)C)C=C1 PIDFDZJZLOTZTM-KHVQSSSXSA-N 0.000 description 1
- 238000005580 one pot reaction Methods 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 150000007530 organic bases Chemical class 0.000 description 1
- FIYYMXYOBLWYQO-UHFFFAOYSA-N ortho-iodylbenzoic acid Chemical compound OC(=O)C1=CC=CC=C1I(=O)=O FIYYMXYOBLWYQO-UHFFFAOYSA-N 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- GSEZHCLWHDZJAB-UHFFFAOYSA-N oxan-4-yl methanesulfonate Chemical compound CS(=O)(=O)OC1CCOCC1 GSEZHCLWHDZJAB-UHFFFAOYSA-N 0.000 description 1
- 125000002971 oxazolyl group Chemical group 0.000 description 1
- 230000001590 oxidative effect Effects 0.000 description 1
- 125000004043 oxo group Chemical group O=* 0.000 description 1
- 125000004430 oxygen atom Chemical group O* 0.000 description 1
- PIBWKRNGBLPSSY-UHFFFAOYSA-L palladium(II) chloride Chemical compound Cl[Pd]Cl PIBWKRNGBLPSSY-UHFFFAOYSA-L 0.000 description 1
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 1
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 1
- 244000045947 parasite Species 0.000 description 1
- 239000001814 pectin Substances 0.000 description 1
- 229920001277 pectin Polymers 0.000 description 1
- 235000010987 pectin Nutrition 0.000 description 1
- 239000000137 peptide hydrolase inhibitor Substances 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- UEZVMMHDMIWARA-UHFFFAOYSA-M phosphonate Chemical compound [O-]P(=O)=O UEZVMMHDMIWARA-UHFFFAOYSA-M 0.000 description 1
- 229910000073 phosphorus hydride Inorganic materials 0.000 description 1
- 125000004483 piperidin-3-yl group Chemical group N1CC(CCC1)* 0.000 description 1
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 1
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 1
- 229920000136 polysorbate Polymers 0.000 description 1
- 229940068965 polysorbates Drugs 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 235000019422 polyvinyl alcohol Nutrition 0.000 description 1
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 229920001592 potato starch Polymers 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 150000003138 primary alcohols Chemical class 0.000 description 1
- 235000019260 propionic acid Nutrition 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 239000003909 protein kinase inhibitor Substances 0.000 description 1
- 238000001243 protein synthesis Methods 0.000 description 1
- 125000003373 pyrazinyl group Chemical group 0.000 description 1
- USPWKWBDZOARPV-UHFFFAOYSA-N pyrazolidine Chemical compound C1CNNC1 USPWKWBDZOARPV-UHFFFAOYSA-N 0.000 description 1
- DNXIASIHZYFFRO-UHFFFAOYSA-N pyrazoline Chemical compound C1CN=NC1 DNXIASIHZYFFRO-UHFFFAOYSA-N 0.000 description 1
- 125000002098 pyridazinyl group Chemical group 0.000 description 1
- 125000004076 pyridyl group Chemical group 0.000 description 1
- 125000000714 pyrimidinyl group Chemical group 0.000 description 1
- ZVJHJDDKYZXRJI-UHFFFAOYSA-N pyrroline Natural products C1CC=NC1 ZVJHJDDKYZXRJI-UHFFFAOYSA-N 0.000 description 1
- 125000000168 pyrrolyl group Chemical group 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 1
- 125000005493 quinolyl group Chemical group 0.000 description 1
- 125000001567 quinoxalinyl group Chemical group N1=C(C=NC2=CC=CC=C12)* 0.000 description 1
- 239000002516 radical scavenger Substances 0.000 description 1
- 230000002285 radioactive effect Effects 0.000 description 1
- ZAHRKKWIAAJSAO-UHFFFAOYSA-N rapamycin Natural products COCC(O)C(=C/C(C)C(=O)CC(OC(=O)C1CCCCN1C(=O)C(=O)C2(O)OC(CC(OC)C(=CC=CC=CC(C)CC(C)C(=O)C)C)CCC2C)C(C)CC3CCC(O)C(C3)OC)C ZAHRKKWIAAJSAO-UHFFFAOYSA-N 0.000 description 1
- 239000000376 reactant Substances 0.000 description 1
- 239000011535 reaction buffer Substances 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 238000006722 reduction reaction Methods 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 229960004889 salicylic acid Drugs 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- 238000012216 screening Methods 0.000 description 1
- 238000007086 side reaction Methods 0.000 description 1
- 229960002930 sirolimus Drugs 0.000 description 1
- 201000000849 skin cancer Diseases 0.000 description 1
- 235000010413 sodium alginate Nutrition 0.000 description 1
- 239000000661 sodium alginate Substances 0.000 description 1
- 229940005550 sodium alginate Drugs 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- MNWBNISUBARLIT-UHFFFAOYSA-N sodium cyanide Chemical compound [Na+].N#[C-] MNWBNISUBARLIT-UHFFFAOYSA-N 0.000 description 1
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 1
- 239000012312 sodium hydride Substances 0.000 description 1
- KSAVQLQVUXSOCR-UHFFFAOYSA-M sodium lauroyl sarcosinate Chemical compound [Na+].CCCCCCCCCCCC(=O)N(C)CC([O-])=O KSAVQLQVUXSOCR-UHFFFAOYSA-M 0.000 description 1
- 229920003109 sodium starch glycolate Polymers 0.000 description 1
- 239000008109 sodium starch glycolate Substances 0.000 description 1
- 229940079832 sodium starch glycolate Drugs 0.000 description 1
- 235000010265 sodium sulphite Nutrition 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 210000000278 spinal cord Anatomy 0.000 description 1
- 206010041823 squamous cell carcinoma Diseases 0.000 description 1
- 102000009076 src-Family Kinases Human genes 0.000 description 1
- 108010087686 src-Family Kinases Proteins 0.000 description 1
- HKSZLNNOFSGOKW-FYTWVXJKSA-N staurosporine Chemical compound C12=C3N4C5=CC=CC=C5C3=C3CNC(=O)C3=C2C2=CC=CC=C2N1[C@H]1C[C@@H](NC)[C@@H](OC)[C@]4(C)O1 HKSZLNNOFSGOKW-FYTWVXJKSA-N 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 125000001424 substituent group Chemical group 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 235000000346 sugar Nutrition 0.000 description 1
- 239000007940 sugar coated tablet Substances 0.000 description 1
- 238000009495 sugar coating Methods 0.000 description 1
- 239000011593 sulfur Chemical group 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 239000003765 sweetening agent Substances 0.000 description 1
- 238000001308 synthesis method Methods 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 230000009897 systematic effect Effects 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- 235000012222 talc Nutrition 0.000 description 1
- 230000008685 targeting Effects 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- YLXNIRRSRXUTCK-UHFFFAOYSA-N tert-butyl 3-hydroxyazepane-1-carboxylate Chemical compound CC(C)(C)OC(=O)N1CCCCC(O)C1 YLXNIRRSRXUTCK-UHFFFAOYSA-N 0.000 description 1
- CFMHVVHPIGIIKI-UHFFFAOYSA-N tert-butyl 4-(3-acetyl-4-hydroxyphenyl)piperazine-1-carboxylate Chemical compound C1=C(O)C(C(=O)C)=CC(N2CCN(CC2)C(=O)OC(C)(C)C)=C1 CFMHVVHPIGIIKI-UHFFFAOYSA-N 0.000 description 1
- QJNRGHRAGOKNEC-UHFFFAOYSA-N tert-butyl 4-(3-carbamoyl-8-methylsulfonylpyrazolo[4,3-h]quinazolin-1-yl)piperidine-1-carboxylate Chemical compound C1CN(C(=O)OC(C)(C)C)CCC1N1C2=C3N=C(S(C)(=O)=O)N=CC3=CC=C2C(C(N)=O)=N1 QJNRGHRAGOKNEC-UHFFFAOYSA-N 0.000 description 1
- DOTUESCTWPPNEO-UHFFFAOYSA-N tert-butyl 4-(3-carbamoyl-8-pyrrolidin-1-ylpyrazolo[4,3-h]quinazolin-1-yl)piperidine-1-carboxylate Chemical compound C1CN(C(=O)OC(C)(C)C)CCC1N1C2=C3N=C(N4CCCC4)N=CC3=CC=C2C(C(N)=O)=N1 DOTUESCTWPPNEO-UHFFFAOYSA-N 0.000 description 1
- YGJXBTRLYHCWGD-UHFFFAOYSA-N tert-butyl 4-(bromomethyl)piperidine-1-carboxylate Chemical compound CC(C)(C)OC(=O)N1CCC(CBr)CC1 YGJXBTRLYHCWGD-UHFFFAOYSA-N 0.000 description 1
- YWLPFSAEXOQNHN-UHFFFAOYSA-N tert-butyl 4-[[3-carbamoyl-8-(2,6-difluorophenyl)-4,5-dihydropyrazolo[4,3-h]quinazolin-1-yl]methyl]piperidine-1-carboxylate Chemical compound C1CN(C(=O)OC(C)(C)C)CCC1CN1C(C2=NC(=NC=C2CC2)C=3C(=CC=CC=3F)F)=C2C(C(N)=O)=N1 YWLPFSAEXOQNHN-UHFFFAOYSA-N 0.000 description 1
- KZBWIYHDNQHMET-UHFFFAOYSA-N tert-butyl 4-bromopiperidine-1-carboxylate Chemical compound CC(C)(C)OC(=O)N1CCC(Br)CC1 KZBWIYHDNQHMET-UHFFFAOYSA-N 0.000 description 1
- OXSSNJRGXRJNPX-UHFFFAOYSA-N tert-butyl 4-methylpiperidine-1-carboxylate Chemical compound CC1CCN(C(=O)OC(C)(C)C)CC1 OXSSNJRGXRJNPX-UHFFFAOYSA-N 0.000 description 1
- TZRQZPMQUXEZMC-UHFFFAOYSA-N tert-butyl n-(2-bromoethyl)carbamate Chemical compound CC(C)(C)OC(=O)NCCBr TZRQZPMQUXEZMC-UHFFFAOYSA-N 0.000 description 1
- ACNRTYKOPZDRCO-UHFFFAOYSA-N tert-butyl n-(2-oxoethyl)carbamate Chemical compound CC(C)(C)OC(=O)NCC=O ACNRTYKOPZDRCO-UHFFFAOYSA-N 0.000 description 1
- FUYBPBOHNIHCHM-UHFFFAOYSA-N tert-butyl piperidine-4-carboxylate Chemical group CC(C)(C)OC(=O)C1CCNCC1 FUYBPBOHNIHCHM-UHFFFAOYSA-N 0.000 description 1
- 150000003512 tertiary amines Chemical class 0.000 description 1
- 125000001302 tertiary amino group Chemical group 0.000 description 1
- 238000010998 test method Methods 0.000 description 1
- WHRNULOCNSKMGB-UHFFFAOYSA-N tetrahydrofuran thf Chemical compound C1CCOC1.C1CCOC1 WHRNULOCNSKMGB-UHFFFAOYSA-N 0.000 description 1
- DGQOCLATAPFASR-UHFFFAOYSA-N tetrahydroxy-1,4-benzoquinone Chemical compound OC1=C(O)C(=O)C(O)=C(O)C1=O DGQOCLATAPFASR-UHFFFAOYSA-N 0.000 description 1
- WROMPOXWARCANT-UHFFFAOYSA-N tfa trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.OC(=O)C(F)(F)F WROMPOXWARCANT-UHFFFAOYSA-N 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 125000000335 thiazolyl group Chemical group 0.000 description 1
- 125000001544 thienyl group Chemical group 0.000 description 1
- 125000004149 thio group Chemical group *S* 0.000 description 1
- 125000003396 thiol group Chemical group [H]S* 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 230000014616 translation Effects 0.000 description 1
- 230000005945 translocation Effects 0.000 description 1
- 125000001425 triazolyl group Chemical group 0.000 description 1
- 125000004205 trifluoroethyl group Chemical group [H]C([H])(*)C(F)(F)F 0.000 description 1
- 125000000876 trifluoromethoxy group Chemical group FC(F)(F)O* 0.000 description 1
- 230000000381 tumorigenic effect Effects 0.000 description 1
- JABYJIQOLGWMQW-UHFFFAOYSA-N undec-4-ene Chemical compound CCCCCCC=CCCC JABYJIQOLGWMQW-UHFFFAOYSA-N 0.000 description 1
- 238000011144 upstream manufacturing Methods 0.000 description 1
- 150000003672 ureas Chemical class 0.000 description 1
- 125000005500 uronium group Chemical group 0.000 description 1
- NQPDZGIKBAWPEJ-UHFFFAOYSA-N valeric acid Chemical compound CCCCC(O)=O NQPDZGIKBAWPEJ-UHFFFAOYSA-N 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
- 239000011701 zinc Substances 0.000 description 1
- 229910052726 zirconium Inorganic materials 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/519—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/18—Drugs for disorders of the alimentary tract or the digestive system for pancreatic disorders, e.g. pancreatic enzymes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/08—Drugs for disorders of the urinary system of the prostate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
Abstract
본 발명은 단백질 키나제의 활성을 변조시키며, 따라서 조절장애된 단백질 키나제 활성, 특히 PIM 키나제에 의해서 야기된 질병을 치료하는데 유용한 치환된 파라졸로[4,3-h]퀴나졸린 화합물에 관한 것이다. 본 발명은 또한, 이들 화합물을 제조하는 방법, 이들 화합물을 포함하는 약제학적 조성물, 및 이러한 이들 화합물 또는 이들을 함유하는 약제학적 조성물을 이용하여 질병을 치료하는 방법을 제공한다.
Description
본 출원은 전체가 참고로 포함된 2010년 12월 17일자 유럽특허출원 제 10195675.3호를 35 USC § 119(a) 하에서 우선권으로 주장한다.
본 발명은 단백질 키나제, 특히 Pim 키나제(Pim-1, Pim-2, 및/또는 Pim-3) 억제제의 활성을 변조시키는 특정의 치환된 파라졸로[4,3-h]퀴나졸린 화합물에 관한 것이다. 따라서 본 발명의 화합물은 조절장애된 단백질 키나제 활성에 의해서 야기된 질병을 치료하는데 유용하다. 본 발명은 또한, 이들 화합물을 제조하는 방법, 이들 화합물을 포함하는 약제학적 조성물, 및 이들 화합물을 포함하는 약제학적 조성물을 이용하여 질병을 치료하는 방법을 제공한다.
단백질 키나제(PK)의 기능부전은 다수의 질병의 특징(hallmark)이다. 인간 암에 포함된 대부분의 종양유전자 및 원-종양유전자(proto-oncogene)는 PK를 암호화한다. PK의 증진된 활성은 또한, 양성 전립선 비대증, 가족성 선종성 용종증, 신경섬유종증, 건선, 혈관 평활세포 증식과 연관된 아테롬성 경화증, 폐섬유증, 관절염, 사구체신염, 및 수술-후 협착증 및 재발협착증과 같은 다수의 비-악성 질환에도 연루된다.
PK는 또한, 염증성 상태 및 바이러스 및 기생충의 증식에도 연루된다. PK는 또한, 신경변성 장애의 병인론 및 발현에 중요한 역할을 할 수 있다.
PK 기능부전 또는 조절장애에 대한 일반적인 참조를 위해서는 예를 들어, 문헌 [Current Opinion in Chemical Biology 1999, 3, 459-465; 및 Carcinogenesis 2008, 29, 1087-1091]을 참고로 한다.
림프종 마우스 모델에서 프로바이러스 돌연변이유발에 의해 활성화된 유전자로서 최초로 확인된 PIM(본 발명 전체에서 PIM1, PIM2 및/또는 PIM-3)는 단백질-세린/트레오닌 키나제이다. PIM 키나제는 정상 조직에서는 열등하게 발현되며, 림프종, 백혈병, 전립선암, 췌장암 및 위암을 포함하는 다수의 인간 암에서 과발현되거나 돌연변이까지 된다[Shah et al. Eur . J. Cancer, 44, 2144-51,(2008)].
PIM 키나제는 구성적으로 활성이며, 그들의 활성은 몇 가지 세포 주기 조절인자 및 세포소멸 매개자를 포함하는 이소형태-특이적 기질뿐만 아니라 공통적인 것의 증가하는 수의 변형을 통해서 시험관내 및 생체내 종양 세포 성장 및 생존을 유지시킨다. PIM1은 또한, 케모카인 수용체 표면 발현을 조절함으로써 정상 및 악성 조혈세포의 귀소(homing) 및 이동을 매개하는 것으로 보이지만, PIM2는 그렇지 않다[Brault et al. Haematologica 95 1004-1015(2010)].
PIM1 및 PIM2 키나제가 일부의 급성 골수성 백혈병(AML)-연관된 종양유전자의 종양원성 효과, 특히 FLT3-돌연변이(AML의 30%에 존재하는, ITD 및 KD 돌연변이) 및/또는 MLL 유전자를 포함하는 전위(AML의 20%에서 나타남)의 종양원성 역할을 매개하는데 포함될 수 있다는 증거가 증가하고 있다[Kumar, et al.(2005) J. Mol. Biol. 348, 183-193]. PIM1은 WT 골수세포에서보다 FLT3-ITD-변형된 AML 세포에서 더 많이 발현된다. 데이터는 PIM1뿐만 아니라 PIM2 억제가 AML 세포의 FLT3ITD-의존성 사망을 매개할 수 있음을 시사한다. 흥미롭게도, 소분자 티로신 키나제 억제제에 대한 저항성을 부여하는 FLT3 돌연변이에 의해서 변형된 세포는 PIM2, 또는 RNAi에 의한 PIM-1 및 PIM-2의 녹다운(knockdown)에 대해서 여전히 민감하였다[Kim et al.(2005) Blood 105: 1759-67].
또한, PIM2는 만성 림프구성 백혈병(CLL), 미만성 거대 B-세포 림프종(DLBCL), 맨틀세포(mantle cell) 림프종(MCL) 또는 골수종과 같은 B-세포계로부터 유래하는 몇 가지의 악성종양의 진행과 연관되고 과발현되는 것으로 보고되었다 [Cohen et al.(2004) Leuk . Lymphoma 94:51; Huttmann et al(2006) Leukemia 20 1774].
흥미롭게도, PIM 및 AKT/PKB는 아마도 십중팔구 BAD, p21WAF1 / CIP1, p27KIP1, 또는 Cot/Tpl-2와 같은 중복성 기질에 기인하여 조혈세포의 성장 및 생존을 매개하는데 부분적으로 과다한 역할을 하는 것으로 보인다 [Choudhary et al, Mol Cell. 36 326-39(2009)].
PIM 키나제는 mTOR 억제(라파마이신) 저항성, 증식 및 생존을 조절하는 것으로 나타났다. 따라서, 몇 개의 생존 키나제를 표적으로 하는 소분자 억제제의 조합이 강력한 암 치료 플랫폼을 위해서 필수적일 수 있다 [Amaravadi R., et al. J. Clin. Invest. 2005, 115(10) 2618-24]. eIF4E 결합 단백질 1(4E-BP1)을 통한 종양원성 단백질 합성은 mTOR-독립적이고 PIM-2에 의해서 조절되는 것으로 보인다. 이러한 관찰결과는 종양원성 eIF4F 해독-개시 컴플렉스가 소분자 PIM-2 억제제에 의해서 차단될 수 있었음을 시사한다 [Tamburini J. et al. Blood 2009, 114(8), 1718-27; 및 Brault L. et al. Haematologica 2010, 95(6) 1004-1015].
키나제 억제활성을 갖는 피라졸로-퀴나졸린 유도체는 또한, Pharmacia Italia S.P.A.의 이름으로 WO 04/104007에 개시되었다. 전술한 WO 04/104007의 몇 가지 특정한 화합물은 본 발명의 일반 화학식으로부터 제외된다.
이들 발전에도 불구하고, 상기 질병에 대한 효과적인 약제에 대한 필요성은 여전하다.
발명의 요약
본 발명에서, 신규 부류의 치환된 피라졸로[4,3-h]퀴나졸린 화합물은 이전에 선행기술에서 달성된 것보다 더 높은 활성을 갖는 것으로 확인되었다. 이들 화합물은 현저하게 낮은 농도에서 인간 종양세포의 증식을 방지함으로써 항종양 효능을 최대화하면서 동시에 대량의 약물의 투여와 관련된 부작용의 위험을 감소시킬 수 있는 것으로 밝혀졌다.
신규의 화합물은 하기 화학식 I로 나타낸 구조를 갖는 화합물, 및 그의 약제학적으로 허용되는 염이다:
[화학식 I]
상기 식에서,
R1은 수소, CN, 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기, 또는 XR4기이며, 여기에서
X는 O, S, SO, S02 및 NR6으로부터 선택된 2가 래디칼이고, 여기에서
R6은 임의로 치환된 직쇄 또는 분지된 C1-C6 알킬이거나, R6 및 R4는 이들이 결합된 질소 원자와 함께 임의로 N, O 및 S로부터 선택된 1개의 추가의 헤테로 원자를 함유하는, 5 내지 6 원 헤테로아릴 또는 헤테로사이클릴기를 형성할 수 있으며;
R2는 수소, 또는 직쇄 또는 분지된 C1-C6 알킬, 직쇄 또는 분지된 C2-C6 알케닐, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기이고;
R3은 NR'R" 및 N(OH)R'로부터 선택된 기이며, 여기에서
R' 및 R"는 각각 독립적으로 수소, 또는 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기이고;
R4는 임의로 치환된 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 기이며;
R5는 수소 또는 NR'R"이고, 여기에서
R' 및 R"는 각각 독립적으로 수소, 또는 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기이거나, R' 및 R"는 이들이 결합된 질소 원자와 함께 임의로 N, O 및 S로부터 선택된 1개의 추가의 헤테로 원자를 함유하는, 5 내지 6 원 헤테로아릴 또는 헤테로사이클릴기를 형성할 수 있으며;
A는 -(CH2)2- 및 -CH=CH-로부터 선택된 2가의 기이고;
단, 여기에서
1-메틸-8-(피페리딘-1-일)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-메틸-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드, 및
1-메틸-8-(메틸설포닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드는 제외된다.
본 발명은 또한, 표준 합성 변형 및 이성체, 호변이성체, 수화물, 용매화물, 컴플렉스, 대사산물, 프로드럭, 담체, N-옥사이드로 구성된 방법을 통해서 제조되는, 화학식 I로 나타낸 치환된 피라졸로[4,3-h]퀴나졸린 화합물을 합성하는 방법을 제공한다.
본 발명은 또한, 상기 정의된 바와 같은 화학식 I로 나타낸 치환된 피라졸로[4,3-h]퀴나졸린 화합물의 유효량을 이를 필요로 하는 포유동물에게 투여하는 단계를 포함하는, 조절장애된 단백질 키나제 활성, 특히 인간 PIM-1, PIM-2, PIM-3, Flt-3, c-Kit, MPSl(TTK), PLK 패밀리 구성원, 다양한 이소형태의 단백질 키나제 C, Met, PAK-4, PAK-5, PERK, STLK-2, DDR-2, 오로라(Aurora) 1, 오로라 2, Bub-1, Chkl, Chk2, HER2, C-raf, B-raf rafl, Melk, PDK1, MEK1, MAPK, EGF-R, PDGF-R, FGF-R, IGF-R, PI3K, 윌(weel) 키나제, Src, Abl, Akt, MAPK, ILK, MK-2, IKK-2, Cdc7, Nek, Cdk/사이클린 키나제 패밀리, 더욱 특히 인간 PIM-1, PIM-2, PIM-3에 의해서 야기되고/되거나 이들과 관련된 질병을 치료하는 방법을 제공한다.
본 발명의 방법은 암, 세포 증식 장애, 및 면역세포-관련된 질병 및 장애로 구성된 군으로부터 선택된, 조절장애된 단백질 키나제 활성에 의해서 야기되고/되거나 그와 관련된 질병을 치료하는 것이다.
본 발명의 다른 방법은 방광암, 유방암, 결장암, 신장암, 간암, 소세포 폐암을 포함한 폐암, 식도암, 담낭암, 난소암, 췌장암, 위암, 경부암, 갑상선암, 전립선암 및 편평세포 암종을 포함한 피부암과 같은 암종; 백혈병, 급성 림프구성 백혈병, 급성 림프아구성 백혈병, B-세포 림프종, T-세포-림프종, 호지킨(Hodgkin) 림프종, 비-호지킨 림프종, 모발성 세포(hairy cell) 림프종 및 버킷(Burkett) 림프종을 포함한 림프계의 조혈성 종양; 급성 및 만성 골수성 백혈병, 골수이형성 증후군 및 전골수성 백혈병을 포함한 골수계의 조혈성 종양; 섬유육종 및 횡문근육종을 포함한 간엽 기원의 종양; 성상세포종, 신경아세포종, 신경교종 및 신경초종을 포함한 중추 및 말초 신경계의 종양; 흑색종, 정상피종, 기형암종, 골육종, 색소성 건피증, 각막황색종(keratoxanthoma), 갑상선 여포암, 카포시(Kaposi) 육종 및 중피종 등을 포함한 그 밖의 다른 종양을 포함하나, 이들로 제한되지 않는, 특정한 유형의 암을 치료하는 것이다.
본 발명의 또 다른 방법은 예를 들어, 양성 전립선 비대증, 가족성 선종성 용종증, 신경섬유종증, 건선, 혈관 평활세포 증식과 관련된 아테롬성 경화증, 폐섬유증, 관절염, 사구체신염, 및 수술-후 협착증 및 재발협착증과 같은 특정의 세포 증식 장애를 치료하는 것이다.
본 발명의 또 다른 방법은 염증성 및 자가면역 질환, 예를 들어, 다발성 경화증, 전신성 홍반성 낭창, 염증성 장질환(IBD), 크론(Crohn)병, 과민성 장 증후군, 췌장염, 궤양성 대장염, 게실증, 중증 근무력증, 맥관염, 건선, 공피증, 천식, 알레르기, 전신 경화증, 백반증(vitiligo), 골관절염, 연소기 류마티스성 관절염과 같은 관절염, 강직성 척추염과 같은 면역세포-관련된 질환 및 장애를 치료하는 것이다.
또한, 본 발명의 방법은 역시 종양 혈관형성 및 전이 억제뿐만 아니라 기관 이식 거부반응 및 이식편대숙주질환의 치료를 제공한다.
본 발명은 또한, 하나 이상의 화학식 I의 화합물 또는 그의 약제학적으로 허용되는 염, 및 약제학적으로 허용되는 부형제, 담체 또는 희석제를 포함하는 약제학적 조성물을 제공한다.
본 발명은 더 나아가 세포증식억제 또는 세포독성제, 항생제-유형 약제, 알킬화제, 항대사물질제, 호르몬제, 면역학적 약제, 인터페론-유형 약제, 사이클로옥시게나제 억제제(예를 들어, COX-2 억제제), 매트릭스메탈로프로테아제 억제제, 텔로머라제 억제제, 티로신 키나제 억제제, 항-성장인자 수용체 약제, 항-HER 약제, 항-EGFR 약제, 항-혈관형성제(예를 들어, 혈관형성 억제제), 파르네실 트랜스퍼라제 억제제, ras-raf 시그날 전달경로 억제제, 세포 주기 억제제, 그 밖의 다른 cdks 억제제, 튜불린 결합제, 토포이소머라제 I 억제제, 토포이소머라제 II 억제제 등과 조합한 방사선요법 또는 화학요법 레지멘과 같은 공지의 항암 치료법과 조합한, 화학식 I의 화합물을 포함하는 약제학적 조성물을 제공한다.
본 발명은 추가로, 키나제를 상기 정의한 바와 같은 화학식 I의 화합물의 유효량과 접촉시키는 단계를 포함하는, PIM-1, PIM-2, PIM-3 단백질 키나제 활성을 억제하는 시험관내 방법을 제공한다.
추가로, 본 발명은 항암 요법에서 동시에, 별도로 또는 순차적으로 사용하기 위한 복합제제로서 상기 정의된 바와 같은 화학식 I의 화합물 또는 그의 약제학적으로 허용되는 염, 또는 그의 약제학적 조성물 및 하나 이상의 화학요법제를 포함하는 제품 또는 키트를 제공한다.
다른 관점에서, 본 발명은 의약으로 사용하기 위한, 상기 정의된 바와 같은 화학식 I의 화합물 또는 그의 약제학적으로 허용되는 염을 제공한다.
더 나아가, 본 발명은 항암 활성을 갖는 의약의 제조에 있어서의 상기 정의된 바와 같은 화학식 I의 화합물 또는 그의 약제학적으로 허용되는 염의 용도를 제공한다.
마지막으로, 본 발명은 암을 치료하는 방법에서 사용하기 위한 상기 정의된 바와 같은 화학식 I의 화합물 또는 그의 약제학적으로 허용되는 염을 제공한다.
도 1은 화학식 I의 화합물의 제조를 포함한 화합물 I-VIII의 전환을 나타내며, 여기에서 R1은 수소, 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기, 또는 SR4기 또는 OR4기이고; R2, R3, R4, R5, R', R" 및 A는 상기 정의된 바와 같다.
도 2는 DMSO 처리된 세포(대조군 제1 레인)와 비교하여 화합물 85로 예시된 화학식 I의 화합물로 처리한 경우에, MV-4-11 세포(FLT3/ITD 돌연변이를 함유하는 인간 백혈병 세포주)에서의 BAD 단백질(포스포BAD)의 용량 의존적 감소를 측정하는 웨스턴 블럿 분석에 의한 pBAD(s112)의 수준을 나타낸다.
도 2는 DMSO 처리된 세포(대조군 제1 레인)와 비교하여 화합물 85로 예시된 화학식 I의 화합물로 처리한 경우에, MV-4-11 세포(FLT3/ITD 돌연변이를 함유하는 인간 백혈병 세포주)에서의 BAD 단백질(포스포BAD)의 용량 의존적 감소를 측정하는 웨스턴 블럿 분석에 의한 pBAD(s112)의 수준을 나타낸다.
이하, 본 발명의 특정한 구체예가 상세히 언급되며, 그의 예는 첨부된 구조 및 화학식에 예시되 어 있다. 본 발명은 열거된 구체예와 함께 기술될 것이지만, 이들은 본 발명을 이들 구체예로 제한하고자 하는 것이 아닌 것으로 이해될 것이다. 그와는 반대로, 본 발명은 특허청구범위에 의해서 정의된 바와 같은 본 발명의 범위 내에 포함될 수 있는 모든 대안, 변형 및 등가물을 포함하고자 한다. 본 기술분야에서 숙련된 전문가는 본 발명을 실시하는데 사용될 수 있는 것으로 본 명세서에 기술된 것과 유사하거나 동등한 다수의 방법 및 물질을 인식할 것이다. 본 발명은 결코 기술된 방법 및 물질로 제한되지 않는다. 인용된 문헌, 특허 및 유사한 자료 중의 하나 이상이 정의된 용어, 용어 용법, 개시된 기술 등을 포함하나, 이들로 제한되지 않는, 본 발명과 상이하거나 모순되는 경우에, 본 출원이 컨트롤한다. 다른 식으로 정의되지 않는 한, 본 발명에서 사용된 모든 기술적 및 과학적 용어들은 본 발명이 속하는 기술분야에서 통상적으로 숙련된 전문가에 의해서 통상적으로 이해되는 것과 같은 의미를 갖는다. 본 발명에 기술된 것과 유사하거나 동등한 방법 및 물질이 본 발명의 실시 또는 시험에 사용될 수 있지만, 적합한 방법 및 물질은 이하에 기술된다. 본 출원에 언급된 모든 간행물, 특허출원, 특허, 및 그 밖의 다른 문헌은 온전히 참고로 포함된다. 본 발명에서 사용된 명명법은 다른 식으로 나타내지 않는 한, IUPAC 체계적 명명법을 기초로 한다.
다른 식으로 명시되지 않는 한, 화학식 I의 화합물 그 자체뿐만 아니라 그의 모든 약제학적 조성물 또는 이들을 포함하는 모든 치료학적 처리를 언급하는 경우에, 본 발명은 본 발명의 화합물의 이성체, 호변이성체, 수화물, 용매화물, 복합체, 대사산물, 전구약물, 담체, N-옥사이드 및 약제학적으로 허용되는 염 모두를 포함한다.
다시 말해서, 상기 정의된 바와 같은 화학식 I의 화합물로부터 용이하게 수득될 수 있다면, 이들의 이성체, 호변이성체, 수화물, 용매화물, 복합체, 대사산물, 전구약물, 담체 및 N-옥사이드도 또한 본 발명의 목적이다.
화학식 I이 화합물의 대사 산물은 생체 내에서, 예를 들어, 필요한 포유동물에게 투여하였을 때 이 화학식 I의 화합물이 전환되는 모든 화합물이다. 제한적인 예를 나타내지는 않지만 전형적으로, 화학식 I의 화합물을 투여하면 이 동일한 유도체는 예를 들어, 쉽게 배설되는 하이드록실화된 유도체와 같은 더욱 가용성인 유도체를 포함한 다양한 종류의 화합물로 전환될 수 있다. 따라서, 이렇게 하여 나타나는 대사경로에 따라 임의의 이들 하이드록실화된 유도체는 하나에 화학식 I의 화합물의 대사산물로 간주될 수 있다.
전구약물은 생체내에서 화학식 I에 따르는 활성 모약물(parent drug)을 방출하는 임의의 공유적으로 결합된 화합물이다.
N-옥사이드는 질소 및 산소가 부여결합(dative bond)을 통해서 속박된 화학식 I의 화합물이다.
하기 화학식 I에서 R2는 하기 화학식 Ia 및 Ib에 따라 피라졸 환의 질소 원자 중의 임의의 하나에 결합될 수 있다:
[화학식 I]
[화학식 Ia]
[화학식 Ib]
입체 중심, 또는 이성체 중심의 또 다른 형태가 본 발명의 화합물에 존재한다면, 에난티오머 및 부분입체이성체를 포함한 이러한 이성체 또는 이성체들의 모든 형태는 본 발명에 포함된다. 입체 중심을 함유하는 화합물은 라세미 혼합물, 에난티오머적으로 풍부한 혼합물로 사용될 수 있거나, 라세미 혼합물은 잘 알려진 기술을 사용하여 분리될 수 있고, 개별적인 에난티오머는 단독으로 사용될 수 있다. 화합물이 불포화된 탄소-탄소 이중결합을 갖는 경우에는 시스(Z) 및 트랜스(E) 이성체 둘 다가 본 발명의 범위 내에 포함된다.
화합물이 호변이성체 형태로 존재할 수 있는 경우에, 각각의 형태는 평형 상태로 존재하든지 하나의 형태가 주로 존재하든지 본 발명에 포함되는 것으로 생각된다.
따라서, 다른 식으로 제시되지 않는 한, 화학식 I의 화합물에서 R2가 수소인 경우에는 하기 화학식 Ia' 또는 Ib'의 호변이성체 형태 중의 단지 하나가 표시되며, 나머지 하나도 여전히 본 발명의 범위 내에 포함되는 것으로 한다:
[화학식 Ia']
[화학식 Ib']
화합물이 케토-에놀 호변이성체와 같은 다른 호변이성체 형태로 존재할 수 있는 경우에, 각각의 호변이성체 형태는 평형 상태로 존재하든지 하나의 형태가 주로 존재하든지 본 발명에 포함되는 것으로 생각된다.
용어 아릴은 융합되거나 단일 결합에 의해서 서로에 연결된 1 내지 2 개의 환 부분을 갖는 카보사이클릭 또는 헤테로사이클릭 탄화수소를 포함하며, 여기에서 환 중의 적어도 하나는 방향족이고; 존재하는 경우에 임의의 방향족 헤테로사이클릭 탄화수소는 또한 헤테로아릴기로도 불리며, N, O 및 S로부터 선택된 1 내지 3 개의 헤테로 원자를 갖는 5 내지 6 원 환을 포함한다.
본 발명에 따르는 아릴기의 예는 예를 들어, 페닐, 비페닐, α- 또는 β-나프틸, 디하이드로나프틸, 티에닐, 벤조티에닐, 푸릴, 벤조푸라닐, 피롤릴, 이미다졸릴, 피라졸릴, 티아졸릴, 이소티아졸릴, 옥사졸릴, 이속사졸릴, 피리딜, 피라지닐, 피리미디닐, 피리다지닐, 인돌릴, 이소인돌릴, 푸리닐, 퀴놀릴, 이소퀴놀릴, 디하이드로퀴놀리닐, 퀴녹살리닐, 벤조디옥솔릴, 인다닐, 인데닐, 트리아졸릴 등이다.
용어 "헤테로사이클릴"(또한 "헤테로사이클로알킬"로 알려짐)은 하나 이상의 탄소 원자가 질소, 산소 및 황과 같은 헤테로 원자에 의해서 대체된 3- 내지 7-원의 포화 또는 부분적으로 불포화된 카보사이클릭 환을 의미한다. 헤테로사이클릴기의 비-제한적 예는 예를 들어, 피란, 피롤리딘, 피롤린, 이미다졸린, 이미다졸리딘, 피라졸리딘, 피라졸린, 티아졸린, 티아졸리딘, 디하이드로푸란, 테트라하이드로푸란, 1,3-디옥솔란, 피페리딘, 피페라진, 모르폴린 등이다.
C4-C7 사이클로알킬을 포함하는 용어 "C3-C7 사이클로알킬"은 다른 식으로 제시되지 않는 한, 하나 이상의 이중결합을 함유할 수 있지만 완전히 접합된 π-전자 시스템을 갖지 않는 3- 내지 7-원의 모두 탄소인 모노사이클릭 환을 의미한다. 사이클로알킬기의 예로는 제한이 없이 사이클로프로판, 사이클로부탄, 사이클로펜탄, 사이클로펜텐, 사이클로헥산, 사이클로헥센, 사이클로헥사디엔, 사이클로헵탄, 사이클로헵텐, 사이클로헵타디엔이다.
C1-C4 알킬을 포함하는, 용어 "직쇄 또는 분지된 C1-C6 알킬"은 예를 들어, 메틸, 에틸, n-프로필, 이소프로필, n-부틸, 이소부틸, tert-부틸, sec-부틸, n-펜틸, n-헥실 등과 같은 임의의 기를 의미한다.
용어 "직쇄 또는 분지된 C2-C6 알케닐"은 예를 들어, 비닐, 알릴, 1-프로페닐, 이소프로페닐, 1-부테닐, 2-부테닐, 3-부테닐, 2-펜테닐, 1-헥세닐 등과 같은 임의의 기를 의미한다.
본 발명에 따라 다른 식으로 제시되지 않는 한, 임의의 상기 R1, R2, R4, R6, R' 및 R"기는 임의의 그들의 자유 위치에서 할로겐 원자, 니트로, 옥소기(=0), 시아노, C1-C6 알킬, 폴리불소화 알킬, 폴리불소화 알콕시, 알케닐, 알키닐, 하이드록시알킬, 아릴, 아릴알킬, 헤테로사이클릴, C3-C7 사이클로알킬, 하이드록시, 알콕시, 아릴옥시, 헤테로사이클릴옥시, 메틸렌디옥시, 알킬카보닐옥시, 아릴카보닐옥시, 사이클로알케닐옥시, 헤테로사이클릴카보닐옥시, 알킬리덴아미노옥시, 카복시, 알콕시카보닐, 아릴옥시카보닐, 사이클로알킬옥시카보닐, 헤테로사이클릴옥시카보닐, 아미노, 우레이도, 알킬아미노, 디알킬아미노, 아릴아미노, 디아릴아미노, 헤테로사이클릴아미노, 포르밀아미노, 알킬카보닐아미노, 아릴카보닐아미노, 헤테로사이클릴카보닐아미노, 아미노카보닐, 알킬아미노카보닐, 디알킬아미노카보닐, 아릴아미노카보닐, 헤테로사이클릴아미노카보닐, 알콕시카보닐아미노, 하이드록시아미노카보닐, 알콕시이미노, 알킬설포닐아미노, 아릴설포닐아미노, 헤테로사이클릴설포닐아미노, 포르밀, 알킬카보닐, 아릴카보닐, 사이클로알킬카보닐, 헤테로사이클릴카보닐, 알킬설포닐, 아릴설포닐, 아미노설포닐, 알킬아미노설포닐, 디알킬아미노설포닐, 아릴아미노설포닐, 헤테로사이클릴아미노설포닐, 아릴티오, 알킬티오, 포스포네이트 및 알킬포스포네이트로부터 독립적으로 선택된 하나 이상의 기, 예를 들어, 1 내지 6 개의 기에 의해서 임의로 치환될 수 있다.
마찬가지로, 적절한 경우에는 언제라도 상기 치환체 각각은 하나 이상의 전술한 기에 의해 추가로 치환될 수 있다.
이 점에 있어서, 용어 "할로겐 원자"는 불소, 염소, 브롬 또는 요오드 원자를 의미한다.
용어 "시아노"는 -CN 잔기를 의미한다.
용어 "니트로"는 -N02 기를 의미한다.
용어 "알케닐" 및 "알키닐"은 각각 이중 또는 삼중 결합을 더 갖는 임의의 전술한 직쇄 또는 분지된 C2-C6 알킬기를 의미한다. 본 발명의 알케닐 또는 알키닐기의 비-제한적 예는 예를 들어, 비닐, 알릴, 1-프로페닐, 이소프로페닐, 1-부테닐, 2-부테닐, 3-부테닐, 2-펜테닐, 1-헥세닐, 에티닐, 2-프로피닐, 4-펜티닐 등이다.
용어 "폴리불소화 알킬" 또는 "폴리불소화 알콕시"는 예를 들어, 트리플루오로메틸, 트리플루오로에틸, 1,1,1,3,3,3-헥사플루오로프로필, 트리플루오로메톡시 등과 같이 한 개 이상의 불소 원자에 의해서 치환된 상기의 직쇄 또는 분지된 C1-C6 알킬 또는 알콕시기 중의 어떤 것을 의미한다.
용어 "알콕시", "아릴옥시", "헤테로사이클릴옥시" 및 그의 파생어들은 산소 원자(-O-)를 통해서 분자의 나머지에 연결된 임의의 상기의 C1-C6 알킬, 아릴 또는 헤테로사이클릴기를 의미한다.
상기한 모든 것으로부터, 명칭이 예를 들어, 아릴아미노와 같은 복합 명칭인 임의의 기는 이것이 유래하는 부분에 의해서, 예를 들어, 아릴에 의해서 추가로 치환된 아미노기에 의해서 통상적으로 이해되는 것으로 쓰인다는 것은 숙련된 전문가에게 명백하다.
마찬가지로, 예를 들어, 알킬티오, 알킬아미노, 디알킬아미노, 알콕시카보닐, 알콕시카보닐아미노, 헤테로사이클릴카보닐, 헤테로사이클릴카보닐아미노, 사이클로알킬옥시카보닐 등과 같은 임의의 용어는 알킬, 알콕시, 아릴, C3-C7 사이클로알킬 및 헤테로사이클릴 부분이 상기 정의된 바와 같은 기를 포함한다.
화학식 I의 화합물의 약제학적으로 허용되는 염은 무기 또는 유기산, 예를 들어, 질산, 염산, 브롬화수소산, 황산, 과염소산, 인산, 아세트산, 트리플루오로아세트산, 프로피온산, 글리콜산, 푸마르산, 락트산, 옥살산, 말론산, 말산, 말레산, 타르타르산, 시트르산, 벤조산, 신남산, 만델산, 메탄설폰산, 이세티온산 및 살리실산에 의한 산부가염을 포함한다. 바람직하게는, 본 발명의 화합물의 산부가염은 하이드로클로라이드 및 메실레이트 염 사이에서 선택된다.
화학식 I의 화합물의 약제학적으로 허용되는 염은 또한, 무기 또는 유기 염기, 예를 들어, 알칼리 또는 알칼리토 금속, 특히 나트륨, 칼륨, 칼슘, 암모늄 하이드록사이드, 카보네이트 또는 바이카보네이트, 아사이클릭 또는 사이클릭 아민, 바람직하게는 메틸아민, 에틸아민, 디에틸아민, 트리에틸아민, 피페리딘 등에 의한 염을 포함한다.
화학식 I의 바람직한 화합물은
R1이 CN, 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기, 또는 XR4기이며, 여기에서
X는 O, S, SO, S02 및 NR6으로부터 선택된 2가 래디칼이고, 여기에서
R6은 임의로 치환된 직쇄 또는 분지된 C1-C6 알킬이거나, R6 및 R4는 이들이 결합된 질소 원자와 함께 임의로 N, O 및 S로부터 선택된 한 개의 추가의 헤테로 원자를 함유하는, 5 내지 6 원 헤테로아릴 또는 헤테로사이클릴기를 형성할 수 있으며;
R2는 직쇄 또는 분지된 C1-C6 알킬, 직쇄 또는 분지된 C2-C6 알케닐, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기이고;
R5는 수소 또는 NR'R"이며, 여기에서
R' 및 R"는 수소이고,
R3, R4 및 A는 상기 정의된 바와 같은 화합물이다.
화학식 I의 화합물의 또 다른 바람직한 부류는
R1이 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기, 또는 XR4기이며, 여기에서
X는 O, S, SO, S02 및 NR6으로부터 선택된 2가 래디칼이고, 여기에서
R6은 임의로 치환된 직쇄 또는 분지된 C1-C6 알킬이거나, R6 및 R4는 이들이 결합된 질소 원자와 함께 임의로 N, O 및 S로부터 선택된 한 개의 추가의 헤테로 원자를 함유하는, 5 내지 6 원 헤테로아릴 또는 헤테로사이클릴기를 형성할 수 있으며;
R2는 직쇄 또는 분지된 C1-C6 알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기이고;
R3은 NR'R" 및 N(OH)R'로부터 선택된 기이며, 여기에서
R' 및 R"는 수소이고,
R4, R5 및 A는 상기 정의된 바와 같은 화합물이다.
화학식 I의 화합물의 추가의 바람직한 부류는
R1이 직쇄 또는 분지된 C1-C6 알킬, 아릴 및 헤테로사이클릴로부터 선택된 임의로 치환된 기, 또는 XR4기이며, 여기에서
X는 O, S, 및 NR6으로부터 선택된 2가 래디칼이고, 여기에서
R6은 임의로 치환된 직쇄 또는 분지된 C1-C6 알킬이거나, R6 및 R4는 이들이 결합된 질소 원자와 함께 임의로 N, O 및 S로부터 선택된 한 개의 추가의 헤테로 원자를 함유하는, 5 내지 6 원 헤테로아릴 또는 헤테로사이클릴기를 형성할 수 있으며;
R3은 NR'R"이고, 여기에서
R' 및 R"는 수소이며;
R4는 임의로 치환된 직쇄 또는 분지된 C1-C6 알킬, 아릴, 아릴알킬, 및 헤테로사이클릴로부터 선택된 기이고;
R5는 수소이며,
R2 및 A는 상기 정의된 바와 같은 화합물이다.
화학식 I의 화합물의 특히 바람직한 부류는
R1이 직쇄 또는 분지된 C1-C6 알킬 및 아릴로부터 선택된 임의로 치환된 기, 또는 XR4기이며, 여기에서
X는 O, S, 및 NR6으로부터 선택된 2가 래디칼이고, 여기에서
R6은 임의로 치환된 직쇄 또는 분지된 C1-C6 알킬이거나, R6 및 R4는 이들이 결합된 질소 원자와 함께 임의로 N, O 및 S로부터 선택된 한 개의 추가의 헤테로 원자를 함유하는, 5 내지 6 원 헤테로아릴 또는 헤테로사이클릴기를 형성할 수 있으며;
R4는 임의로 치환된 직쇄 또는 분지된 C1-C6 알킬, 아릴, 및 헤테로사이클릴로부터 선택된 기이고;
A는 2가의 -CH=CH-기이며,
R2, R3 및 R5는 상기 정의된 바와 같은 화합물이다.
생물학적 평가
화학식 I의 화합물의 Pim 키나제 활성의 측정은 다수의 직접 및 간접 검출방법에 의해서 가능하다. 본 발명에 기술된 특정한 예시적 화합물을 이소형태 Pim-1, Pim-2, 및 Pim-3을 포함한 그들의 Pim 키나제 결합 활성(실시예 901), 및 종양 세포에 대한 시험관내 활성(실시예 902)에 대해서 시험하였다. 본 발명의 특정한 예시적 화합물은 약 1 마이크로몰(μM) 미만의 Pim 결합 활성 IC50 값을 가졌다. 본 발명의 특정한 화합물은 약 1 마이크로몰(μΜ) 미만의 종양 세포-기본 활성 EC50 값을 가졌다. 실시예 901 및 902에 기술된 시험에서 1 μΜ 미만의 Ki/IC50/EC50을 갖는 화학식 I의 화합물은 Pim 키나제 억제제(Pim-1, Pim-2 및/또는 Pim-3)로서 치료학적으로 유용할 수 있다.
표 1에서의 예시적인 화학식 I의 화합물을 제조하고, 특성화하고, 본 발명의 방법에 따라 Pim 키나제의 억제에 관해서 시험하였으며, 이들은 다음의 구조 및 해당하는 명칭을 갖는다[ChemBioDraw Ultra, Version 11.0, CambridgeSoft Corp., Cambridge MA].
[표 1]
임의로 약제학적으로 허용되는 염의 형태인 본 발명의 화학식 I의 임의의 특정한 화합물에 대한 참조를 위해서는 실험 항목 및 특허청구범위를 참고한다.
본 발명은 또한, 본 기술분야에서 이용가능한 기술 및 쉽게 입수할 수 있는 출발물질을 이용하여 이하에 기술된 반응 경로 및 합성 반응식을 사용함으로써 상기 정의된 바와 같은 화학식 I의 화합물의 제조방법을 제공한다. 본 발명의 특정한 구체예의 제조는 이하의 실시예에 기술되지만, 본 기술분야에서 통상적으로 숙련된 전문가는 기술된 제조방법이 본 발명의 다른 구체예를 제조하기 위해서 쉽게 적용될 수 있다는 것을 인식할 것이다. 예를 들어, 본 발명에 따르는 비-예시된 화합물의 합성은 본 기술분야에서 숙련된 전문가에게 명백한 변형에 의해서, 예를 들어, 간섭성 기를 적절하게 보호하거나, 본 기술분야에서 공지된 다른 적합한 시약으로 변화시키거나, 반응조건을 일상적으로 변형시킴으로써 수행될 수 있다. 대안적으로, 본 발명에 언급되거나 본 기술분야에서 공지된 다른 반응들은 본 발명의 다른 화합물을 제조하기 위한 적응성을 갖는 것으로 인식될 것이다.
도 1은 R1이 수소, 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기, 또는 SR4기 또는 OR4기이며; R2, R3, R4, R5, R', R" 및 A는 상기 정의된 바와 같은 화학식 I의 화합물의 제조방법을 나타낸다.
본 기술분야에서 통상적으로 숙련된 모든 전문가는 상기한 방법에 따라 수행되는 임의의 변형반응은 예를 들어, 방해기의 보호, 본 기술분야에서 공지된 다른 적합한 시약으로의 변화, 또는 반응조건에 대한 일상적인 변형과 같은 필요한 변형을 필요로 할 수 있음을 인식할 것이다.
따라서, 본 발명의 방법은 하기 단계를 포함한다:
단계(st.) 1) 하기 화학식 II의 화합물을 산성 조건 하에서 하기 화학식 III의 하이드라진 유도체와 혼합시켜 하기 화학식 IV의 화합물을 제공하는 단계:
[화학식 II]
상기 식에서, A는 -(CH2)2-이고,
[화학식 III]
상기 식에서, R2는 상기 정의된 바와 같고,
[화학식 IV]
상기 식에서, A는 -(CH2)2-이고 R2는 상기 정의된 바와 같음; 또는
단계 1a) R2가 수소인 화학식 IV의 화합물을 하기 화학식 V의 화합물과 혼합시켜 R2가 상기 정의된 바와 같지만 수소는 아닌 화학식 IV의 화합물을 제공하는 단계:
[화학식 V]
상기 식에서, R2는 상기 정의된 바와 같으나, 수소가 아니고, Y는 요오도, 브로모, 클로로 또는 설포네이트기(예를 들어, -OS(0)2CF3, -OS(0)2CH3 또는 -OS(0)2PhMe)와 같은 적합한 이탈기임;
단계 2) 생성된 화학식 IV의 화합물을 디메틸포름아미드-디-알킬아세탈과 혼합시켜 하기 화학식 VI의 화합물을 제공하는 단계:
[화학식 VI]
상기 식에서, -(CH2)2-이고 R2는 상기 정의된 바와 같음;
단계 3) 생성된 화학식 VI의 화합물을 하기 대체 단계(단계 3a),(단계 3b) 또는 (단계 3c) 중 어느 하나에 따라 반응시켜 하기 화학식 VIII의 화합물을 제공하는 단계:
단계 3a) 하기 화학식 VIIa의 이소티오우레아 또는 그의 염과 반응시키는 단계:
[화학식 VIIa]
상기 식에서, R4는 상기 정의된 바와 같음,
단계 3b) 하기 화학식 VIIb의 이소우레아 또는 그의 염과 반응시키는 단계:
[화학식 VIIb]
상기 식에서, R4는 상기 정의된 바와 같음,
단계 3c) 하기 화학식 IX의 적합한 아미딘 또는 그의 염과 반응시키는 단계:
[화학식 IX]
상기 식에서, R1은 수소, 또는 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기임,
[화학식 VIII]
상기 식에서, R1은 각각 SR4, OR4, 수소, 또는 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기이며, A는 -(CH2)2-이고 R2 및 R4는 상기 정의된 바와 같음;
단계 4) 생성된 상기 화학식 VIII의 화합물을 산화제와 혼합시키거나, Pd 또는 Pt 촉매의 존재 하에서 탈수소화 작업조건 하에 처리하여 화학식 VIII의 화합물을 제공하는 단계로서, 여기에서 R1은 각각 SR4, OR4, 수소, 또는 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기이고, A가 -CH=CH-이며, R2 및 R4는 상기 정의된 바와 같은 단계;
단계 5) 단계 3a), 단계 3b), 단계 3c) 또는 단계 4)에 기술된 바와 같이 수득되고, R2가 t-부틸 또는 트리틸과 같은 보호기인 화학식 VIII의 화합물을 산성 조건 하에서 반응시켜, R2가 수소인 화학식 VIII의 화합물을 수득하고, 생성된 화학식 VIII의 화합물을 하기 화학식 V의 화합물과의 반응을 통해서 R2가 상기 정의된 바와 같지만 수소는 아닌 화학식 VIIIa 및 화학식 VIIIb의 두 가지 화합물의 혼합물로 전환시키는 단계:
[화학식 V]
상기 식에서, Y는 상기 정의된 바와 같고 R2는 상기 정의된 바와 같지만 수소는 아님:
단계 6) 단계 3a), 단계 3b), 단계 3c), 단계 4) 또는 단계 5)에 기술된 바와 같이 수득된 화학식 VIII의 화합물을 대체 단계 6a), 단계 6b) 또는 단계 6c) 중 어느 하나에 따라 반응시키는 단계:
단계 6a) 암모늄 하이드록사이드 또는 하기 화학식 XII의 아민과 반응시켜 하기 화학식 I의 화합물을 수득하는 단계:
[화학식 XII]
상기 식에서, R' 및 R"는 상기 정의된 바와 같음:
[화학식 I]
상기 식에서, R1은 수소, 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기, 또는 SR4기 또는 OR4기이며, R3은 NR'R"이고, R5는 수소이며, R2, R4 및 A는 상기 정의된 바와 같음;
단계 6b1) 산성 또는 염기성 가수분해 조건 하에서 반응시켜 하기 화학식 XI의 화합물 또는 그의 염을 제공하는 단계:
[화학식 XI]
상기 식에서, R1은 수소, 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기, 또는 SR4기 또는 OR4기이며, R2, R4 및 A는 상기 정의된 바와 같음;
단계 6b2) 생성된 화학식 XI의 화합물 또는 그의 염을 염기성 조건 및 적합한 축합제의 존재 하에서, 암모늄염 또는 화학식 XII의 유도체 또는 화학식 X의 유도체와 혼합시켜 하기 화학식 I의 화합물을 제공하는 단계:
[화학식 X]
[화학식 I]
상기 식에서, R1은 수소, 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기, 또는 SR4기 또는 OR4기이며, R5는 수소이고, R2, R4, R3 및 A는 상기 정의된 바와 같음;
단계 6c) 강염기의 존재 하에서 암모늄염 또는 화학식 XII의 적합한 아민과 반응시켜 하기 화학식 I의 화합물을 제공하는 단계:
[화학식 I]
상기 식에서, R1은 수소, 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기, 또는 SR4기 또는 OR4기이며, R3은 NR'R"이고, R2, R4, R5, A, R' 및 R"는 상기 정의된 바와 같음;
임의로 화학식 I의 화합물을 화학식 I의 또 다른 상이한 화합물로 전환시키고, 필요한 경우에, 화학식 I의 화합물을 그의 약제학적으로 허용되는 염으로 전환시키거나 염을 유리 화합물 I로 전환시키는 단계.
본 발명은 추가로 하기의 반응식 2에 제시된 것으로서, 상기 정의된 바와 같은 화학식 I의 화합물의 제조를 위한 대체 방법을 제공한다.
[반응식 2]
상기 반응식에서, R1은 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 아릴, 및 헤테로사이클릴로부터 선택된 임의로 치환된 기이며, R2는 상기 정의된 바와 같지만 수소는 아니고, R3 및 A는 상기 정의된 바와 같으며; 이 대체 방법은 다음의 단계를 포함한다:
단계 7) 하기 화학식 XIII의 화합물을 하기 화학식 V의 화합물과 반응시키는 단계:
[화학식 XIII]
상기 식에서, R3 및 A는 상기 정의된 바와 같고,
[화학식 V]
상기 식에서, Y는 상기 정의된 바와 같고, R2는 상기 정의된 바와 같지만, 수소는 아님;
단계 8) 생성된 하기 화학식 XIV의 화합물을 하기 화학식 XV의 화합물과 반응시켜 하기 화학식 I의 화합물을 제공하는 단계:
[화학식 XIV]
상기 식에서, R2는 상기 정의된 바와 같지만 수소는 아니며, R3 및 A는 상기 정의된 바와 같고,
[화학식 XV]
상기 식에서, R1은 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 아릴, 및 헤테로사이클릴로부터 선택된 임의로 치환된 기이며, Q는 -B(OH)2, -B(OAlk)2, -Sn(Alk)4, -Al(Alk)3, ZnHal, MgHal, 또는 ZrCp2Hal과 같은, 팔라듐 매개된 탄소 결합 형성을 겪을 수 있는 적합한 기이며,
[화학식 I]
상기 식에서, R1은 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 아릴, 및 헤테로사이클릴로부터 선택된 임의로 치환된 기이며, R2는 상기 정의된 바와 같지만 수소는 아니고, R3 및 A는 상기 정의된 바와 같으며, R5는 수소임;
임의로 화학식 I의 화합물을 화학식 I의 다른 상이한 화합물로 전환시키고, 필요한 경우에, 화학식 I의 화합물을 그의 약제학적으로 허용되는 염으로 전환시키거나 염을 유리 화합물 I로 전환시키는 단계.
본 발명은 추가로 하기의 반응식 3에 제시된 것으로서, 상기 정의된 바와 같은 화학식 VIII의 화합물의 제조를 위한 대체 방법을 제공한다.
[반응식 3]
상기 반응식에서, R1은 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 아릴, 및 헤테로사이클릴로부터 선택된 임의로 치환된 기이고, R2는 상기 정의된 바와 같지만 수소는 아니며, A는 상기 정의된 바와 같고; 이 대체 방법은 다음의 단계를 포함한다:
단계 9) 하기 화학식 XVIII의 화합물을 화학식 R1-Q(XV)의 화합물과 반응시켜 화학식 VIII의 화합물을 제공하는 단계:
[화학식 XVIII]
상기 식에서, R2는 상기 정의된 바와 같지만 수소는 아니며, A는 상기 정의된 바와 같고,
[화학식 XV]
상기 식에서, R1은 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 아릴, 및 헤테로사이클릴로부터 선택된 임의로 치환된 기이며, Q는 팔라듐 매개된 탄소 결합 형성을 겪을 수 있는 상기 정의된 바와 같음.
상기 정의된 바와 같이, 본 발명의 목적인 방법에 따라 제조된 화학식 I의 화합물은 잘 알려진 합성 조건에 따라 작업함으로써 화학식 I의 다른 화합물로 편리하게 전환될 수 있으며, 가능한 전환반응의 예는 다음과 같다:
전환(Conv.) a) R1이 R4-S-와 같은 기이고, 여기에서 R4는 상기 정의된 바와 같은 화학식 I의 화합물을 산화 조건 하에서 R1이 R4-S(0)2-기인 화학식 I의 화합물로 전환시키는 것:
전환 b) 설포닐 유도체를 화학식 R4-OH(XVI)의 화합물과 반응시킴으로써 R1이 R4-S(0)2-와 같은 기이고, 여기에서 R4는 상기 정의된 바와 같은 화학식 I의 화합물을 R1이 R4-0- 기인 화학식 I의 화합물로 전환시키는 것:
전환 c) 설포닐 유도체를 화학식 R4R6-NH(XVII)의 화합물과 반응시킴으로써 R1이 R4-S(0)2-와 같은 기인 화학식 I의 화합물을 R1이 R4-NR6기이고, 여기에서 R4 및 R6은 상기 정의된 바와 같은 화학식 I의 화합물로 전환시키는 것:
상기 식에서, R4 및 R6은 상기 정의된 바와 같음,
전환 d) 설포닐 유도체를 나트륨 시아나이드(NaCN) 또는 칼륨 시아나이드(KCN)와 반응시킴으로써 R1이 R4-S(0)2-와 같은 기인 화학식 I의 화합물을 R1이 -CN인 화학식 I의 화합물로 전환시키는 것:
전환 e) R1, R3 및 A가 상기 정의된 바와 같고, R2는 수소인 화학식 I의 화합물을 하기 화학식 V의 화합물과의 반응을 통해서 R2가 상기 정의된 바와 같지만 수소는 아닌 화학식 I의 화합물로 전환시키는 것:
[화학식 V]
상기 식에서, Y'는 OH, 또는 임의로 활성화시키면 요오도, 브로모, 클로로 또는 설포네이트기(예를 들어, -OS(0)2CF3, -OS(0)2CH3 또는 -OS(0)2PhMe)와 같은 적합한 이탈기로 작용할 수 있는 기이며, R2는 상기 정의된 바와 같지만 수소는 아님,
전환 f) R2가 할로에틸인 화학식 I의 화합물을 염기성 조건을 적용함으로써 R2가 비닐인 화학식 I의 화합물로 전환시키는 것:
전환 g) R2가 클로로로 치환된 화학식 L-CH2C1의 기이고, 여기에서 L은 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기인 화학식 I의 화합물을 화학식 R'R"NH(XII)의 화합물과 반응시킴으로써 R2가 L-CH2NR'R"기이고, R' 및 R"는 상기 정의된 바와 같은 화학식 I의 화합물로 전환시키는 것:
전환 h) R2가 화학식 L-CH2OH의 기이고, 여기에서 L은 상기 정의된 바와 같은 화학식 I의 화합물을, 우선 CH2OH기를 CHO로 전환시킨 다음에 생성된 알데히드 유도체를 적합한 환원제의 존재 하에서 화학식 R'R"NH(XII)의 화합물과 반응시킴으로써 R2가 L-CH2NR'R"기인 화학식 I의 화합물로 전환시키는 방법:
전환 i) R2가 화학식 L-COO알킬의 기이고, 여기에서 L은 상기 정의된 바와 같은 화학식 I의 화합물을 적합한 환원제와 반응시킴으로써 R2가 L-CH2OH인 화학식 I의 화합물로 전환시키는 것:
전환 j) X가 O이고, R4가 -CHO에 의해서 치환된 아릴, 즉 페닐인 화학식 I의 화합물을 적합한 환원제의 존재 하에서 화학식 R'R"-NH(XII)의 아민으로 처리함으로써 R4가 CH2NR'R"에 의해서 치환된 아릴, 즉 페닐이고, 여기에서 R' 및 R"는 상기 정의된 바와 같은 화학식 I의 화합물로 전환시키는 것:
전환 k) X가 O이고, R4가 -NO2에 의해서 치환된 아릴, 즉 페닐인 화학식 I의 화합물을 적합한 환원제로 처리함으로써 R4가 NH2에 의해서 치환된 아릴, 즉 페닐인 화학식 I의 화합물로 전환시키는 것:
전환 l) R2, R3 및 A가 상기 정의된 바와 같고 R1은 Me-S-와 같은 기인 화학식 I의 화합물을, R1은 상기 정의된 바와 같고 Q'는 팔라듐 매개된 탄소 결합 형성을 겪을 수 있는 -B(OH)2, -MgHal, -ZnHal과 같은 적합한 기인 화학식 R1-Q'(XV)의 화합물과 반응시킴으로써, R1이 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 아릴, 및 헤테로사이클릴로부터 선택된 임의로 치환된 기인 화학식 I의 화합물로 전환시키는 것:
전환 m) R1 및 R2가 상기 정의된 바와 같고, R5는 수소이며, A는 -CH=CH-인 화학식 I의 화합물을, 강염기의 존재 하에서 암모늄염 또는 화학식 R'R"NH(XII)의 적합한 아민과 반응시킴으로써 R5가 NR'R"인 화학식 I의 화합물로 전환시키는 것:
전환 n) R2가 화학식 L-N(H)R'의 기이고, 여기에서 L 및 R'는 상기 정의된 바와 같은 화학식 I의 화합물을, R2가 화학식 L-NR'R"의 기이고, 여기에서 R' 및 R"는 상기 정의된 바와 같은 화학식 I의 화합물이 형성되도록 하는 조건 하에서 화학식 R"-CHO(XIX)의 화합물로 처리함으로써 전환시키는 것:
전환 o) R2가 화학식 L-N(H)R'의 기이고, 여기에서 L 및 R'는 상기 정의된 바와 같은 화학식 I의 화합물을, R2가 화학식 L-N(R')COR7의 기이고, 여기에서 R'는 상기 정의된 바와 같은 화학식 I의 화합물이 형성되도록 하는 조건 하에서, R7은 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬이고, W는 하이드록실 또는 할로겐인 화학식 R7-COW(XX)의 화합물로 처리함으로써 전환시키는 것:
전환 p) R2가 화학식 L-N(H)R'의 기이고, 여기에서 L 및 R'는 상기 정의된 바와 같은 화학식 I의 화합물을, R2가 화학식 L-N(R')CONHR8의 기이고, 여기에서 R'는 상기 정의된 바와 같은 화학식 I의 화합물이 형성되도록 하는 조건 하에서, R8은 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기인 화학식 R8-N=C=0(XXI)의 화합물로 처리함으로써 전환시키는 것:
전환 q) R2가 화학식 L-N(H)R'의 기이고, 여기에서 L 및 R'는 상기 정의된 바와 같은 화학식 I의 화합물을, R2가 화학식 L-N(R')NHCNHR8의 기이고, 여기에서 R'는 상기 정의된 바와 같은 화학식 I의 화합물이 형성되도록 하는 조건 하에서 화학식 R8-NHC(NH)G(XXII)의 화합물로 처리함으로써 전환시키는 것:
전환 r) R1, R2 및 R3은 상기 정의된 바와 같고 A는 -CH2-CH2-와 같은 2가 기인 화학식 I의 화합물을, 산화제로 처리하거나, Pd 또는 Pt 촉매의 존재 하에서 탈수소화 작업 조건 하에서 처리함으로써 A가 -CH=CH-기인 화학식 I의 화합물로 전환시키는 것:
전술한 합성방법에 따른 화학식 I의 화합물의 합성은 단계적 방식으로 수행될 수 있으며, 따라서 각각의 중간체는 후속 반응을 수행하기 전에 예를 들어, 칼럼 크로마토그래피와 같은 표준 정제기술에 의해서 분리 및 정제된다. 대안적으로, 합성 순서의 2 개 이상의 단계는 본 기술분야에서 공지된 것으로서 소위 "원-포트(one-pot)" 공정으로 수행될 수 있으며, 따라서 2 개 이상의 단계로부터 생성된 화합물만이 분리 및 정제된다.
제조방법의 단계(단계 1(st.1))에 따르면, 화학식 II의 화합물을 아세트산의 존재 하에 에탄올과 같은 용매 중에서 화학식 III의 하이드라진 또는 하이드라진 유도체와 반응시키고, 이 반응은 실온 내지 80℃ 범위의 온도에서 수행됨으로써 화학식 IV의 화합물을 수득한다.
임의로, R2가 수소인 화학식 IV의 화합물을 적합한 용매, 예를 들어, 아세토니트릴, 테트라하이드로푸란, 디메틸포름아미드 등에 용해시키고, 나트륨 하이드라이드 또는 세슘 카보네이트와 같은 적합한 염기를 그에 첨가한다. 그 후, 화학식 R2Y(V)의 화합물을 첨가하고, 혼합물을 약 2 시간 내지 약 15 시간의 시간 동안, 약 20℃ 내지 약 80℃ 범위의 온도에서 교반한다.
제조방법의 단계(단계 2)에 따르면, 화학식 IV의 엔아미논 유도체의 합성은 실온 내지 100℃ 범위의 온도에서 30 분 내지 약 24 시간 범위의 시간 동안, N,N-디메틸포름아미드, N,N-디메틸아세트아미드, 톨루엔 등과 같은 적합한 용매 중에서, 예를 들어, 디메틸포름아미드-디-tert-부틸아세탈, 디메티포름아미드-디에틸아세탈 등과 같은 N,N-디메틸포름아미드 디알킬 아세탈을 사용하여 성취된다.
제조방법의 대체 단계(단계 3a),(단계 3b) 또는(단계 3c) 중의 하나에 따르면, 화학식 VI의 화합물의 화학식 VIII의 화합물로의 전환은 화학식 VIIa의 이소티오우레아, 또는 화학식 VIIb의 이소우레아, 또는 화학식 IX의 적합한 아미딘을 사용하여 성취된다. 상기 반응들은 모두 통상적인 방법에 따라 수행된다. 예를 들어, 메틸이소티오우레아, 또는 설페이트와 같은 그의 염을 사용하는 반응은 50℃ 내지 100℃ 범위의 온도에서 2 시간 내지 약 48시간 범위의 시간 동안, 칼륨 아세테이트, 나트륨 바이카보네이트, 나트륨 또는 칼륨 카보네이트 등과 같은 염기의 존재 하에 N,N-디메틸포름아미드, 테트라하이드로푸란, 아세토니트릴 등과 같은 적합한 용매 중에서 수행된다.
제조방법의 단계(단계 4)에 따르면, 화학식 VIII의 화합물은 90℃ 내지 환류 온도 범위의 온도에서 2 시간 내지 8 시간 사이의 시간 동안 톨루엔, 1,4-디옥산, 클로로벤젠, 디클로로벤젠과 같은 적합한 용매 중에서 작업함으로써, 임의로 지지된(supported) 팔라듐 또는 백금 또는 2,3-디클로로-5,6-디시아노-l,4-벤조퀴논(DDQ)의 존재 하에서 탈수소화 반응을 겪어 화학식 VIII의 상응하는 방향족 유도체를 수득할 수 있다.
제조방법의 단계(단계 5)에 따르면, R2가 t-부틸 또는 트리틸과 같은 보호 r기인 화학식 VIII의 화합물에서 이들의 분해는 통상적인 방법에 따른 다양한 방식으로 성취될 수 있다. 바람직하게는, R2가 수소인 화학식 VIII의 화합물이 발생하도록 디클로로메탄 등과 같은 적합한 용매의 존재 하에서 염산 또는 트리플루오로아세트산과 혼합시킴으로써 수행된다.
따라서, 화학식 VIII의 수득된 화합물을 아세토니트릴 또는 N,N-디메틸포름아미드와 같은 적합한 용매 중에서 칼륨 또는 세슘 카보네이트와 같은 염기의 존재 하에 R2는 상기 정의된 바와 같지만 수소는 아니며, Y는 상기 정의된 바와 같은 화학식 R2Y(V)의 화합물과 반응시킨다. 후자의 반응은 실리카겔 크로마토그래피 또는 분취용 HPLC와 같은 공지된 방법에 의해서 분할될 수 있는 화학식 VIIIa 및 VIIIb의 위치이성체의 혼합물을 제공할 수 있다.
제조방법의 단계(단계 6a)에 따르면, 화학식 VIII의 화합물은 카복시에스테르기(-COOEt)를 카복사미드(-CONH2), N-치환된 카복사미드(-CONHR'), 또는 N,N-이치환된 카복사미드(-CONRR")로 전환시키는 본 기술분야에서 잘 알려진 방법에 따라 화학식 I의 화합물로 변형시킨다. 바람직하게는, 이 반응은 약 50℃ 내지 약 100℃ 범위의 온도에서 메탄올/N,N-디메틸포름아미드 혼합물 중의 암모늄 하이드록사이드를 사용하여 수행된다.
유사한 작업조건이 N-치환된 카복사미드 또는 N,N-이치환된 카복사미드의 제조에 적용되며, 여기에서 적합한 일급 또는 이급 아민이 암모니아 또는 암모늄 하이드록사이드 대신에 사용된다.
바람직하게는, 제조방법의 단계(단계 6b1)에 따르면, 화학식 XI의 화합물의 상응하는 카복실산을 제공하는 화학식 VIII의 화합물의 가수분해는 산성 또는 염기성 조건 하에서 수행된다. 바람직하게는, 반응은 저급 알콜, 테트라하이드로푸란, N,N-디메틸포름아미드 또는 이들의 혼합물과 같은 적합한 용매의 존재 하에서 수성 리튬, 나트륨 또는 칼륨 하이드록사이드와 같은 알칼리성 수용액을 사용하여 수행되고; 바람직하게는 반응은 대략 실온 내지 약 100℃ 범위의 온도에서 메탄올/N,N-디메틸포름아미드 혼합물 중의 칼륨 하이드록사이드를 사용하여 수행된다. 사용된 작업조건에 따라, 화학식 XI의 화합물은 그의 산성 형태, 또는 대신으로 염으로 수득될 수 있다.
바람직하게는 제조방법의 단계(단계 6b2)에 따르면, 화학식 I의 상응하는 화합물을 제공하는 화학식 XI의 카복실산의 아미드화는 적합한 축합제, 예를 들어, 디사이클로헥실카보디이미드(DCC), 1-에틸-3-(3'-디메틸아미노프로필)카보디이미드(EDC), 3,4-디하이드로-3-하이드록시-4-옥소-1,2,3-벤조트리아진(DHBT), O-벤조트리아졸릴테트라메틸이소우로늄 테트라플루오로보레이트(TBTU), 벤조트리아졸-1-일옥시트리피롤리디노포스포늄 헥사플루오로포스페이트(PyBOP), 또는 2-(1H-벤조트리아졸-1-일)-1,1,3,3-테트라메틸우로늄 헥사플루오로포스페이트(HBTU)의 존재 하에, 디클로로메탄, N,N-디메틸포름아미드, 테트라하이드로푸란, 1,4-디옥산 또는 N,N-디메틸아세트아미드와 같은 적합한 용매 중에서 염기성 조건 하에, 바람직하게는 N,N-디이소프로필-N-에틸아민 또는 트리에틸아민을 사용하여, 암모늄 클로라이드 또는 화학식 R'R"NH(XII)의 적합한 일급 또는 이급 아민 또는 화학식 R'NHOH(X)의 치환된 하이드록실아민 유도체의 존재 하에서 수행된다. 상기의 반응은 임의로, 4-디메틸아미노피리딘과 같은 적합한 촉매의 존재 하에서, 또는 N-하이드록시벤조트리아졸과 같은 추가의 커플링제의 존재 하에서 수행된다. 대안적으로, 동일한 이 반응은 또한 예를 들어, 혼합 무수물 방법(mixed anhydride method)을 통해, 실온에서 트리에틸아민, N,N-디이소프로필에틸아민 또는 피리딘과 같은 3급 아민의 존재 하에, 예를 들어, 톨루엔, 디클로로메탄, 테트라하이드로푸란, N,N-디메틸포름아미드 등과 같은 적합한 용매 중에서 에틸, 이소-프로필, 벤질 클로로포르메이트와 같은 알킬 클로로포르메이트를 사용함으로써 수행된다.
제조방법의 단계(단계 6c)에 따르면, 화학식 VIII의 화합물의 카복시에스테르 기는 암모늄 클로라이드 또는 적합한 일급 또는 이급 아민을 사용하여 THF 중의 1 N 리튬 비스-트리메틸실릴아미드와 같은 염기성 조건 하에서 카복사미드 또는 N-치환된 카복사미드 또는 N,N-이치환된 카복사미드로 전환시킬 수 있으며; 바람직하게는 이 반응은 0℃ 내지 환류 온도 범위의 온도에서 테트라하이드로푸란 중에서 수행된다.
흥미롭게도, 이 반응에서 A가 -CH=CH-인 경우에는 R3가 R'R"N-이고, R5가 수소 또는 R'R"N-기인 화학식 I의 목적하는 생성물의 혼합물이 수득되었다. 그 후에, 이들 두 가지 유도체는 통상적인 방법에 따라, 예를 들어, 크로마토그래피 또는 분취용 HPLC에 의해서 반응 혼합물로부터 분할된다.
제조방법의 단계(단계 7)에 따르면, 화학식 XIII의 화합물을 칼륨 또는 세슘 카보네이트와 같은 염기의 존재 하에 아세토니트릴 또는 디메틸포름아미드와 같은 적합한 용매 중에서 R2는 상기 정의된 바와 같지만 수소는 아니고, Y는 상기 정의된 바와 같은 화학식 R2Y(V)의 화합물과 반응시켜 화학식 XIV의 유도체를 수득한다.
제조방법의 단계(단계 8)에 따르면, 화학식 XIV의 화합물은 탄소-탄소 결합의 형성에 적합한 교차-커플링 반응 중 어느 것을 이용하여서라도 화학식 I의 화합물로 변형시킬 수 있다. 본 기술분야에서 잘 알려져 있는 상기의 반응은 예를 들어, 유기 붕소(스즈키(Suzuki) 반응), 유기 주석(스틸(Stille) 반응), 유기 마그네슘(쿠마다(Kumada) 반응), 유기 아연, 또는 유기 알루미늄, 또는 유기 지르코늄(네기쉬(Negishi) 반응) 등과 같은 적합한 유기 금속 시약을 사용한 커플링을 포함한다. 바람직한 반응은 스즈키 반응이며, 여기에서는 적절한 아릴 또는 헤테로아릴보론 유도체를 실온 내지 80℃로 변화하는 온도에서 2 시간 내지 하룻밤의 시간 동안, 디메톡시에탄 및 물과 같은 용매의 혼합물 중에서 [1,1'-비스(디페닐포스피노)페로센]팔라듐(II) 디클로라이드 디클로로메탄 복합체(PdCl2(dppf)2ㆍCH2Cl2)와 같은 팔라듐 기본 촉매 및 나트륨 또는 세슘 카보네이트와 같은 염기의 존재 하에 사용한다.
제조방법의 단계(단계 9)에 따르면, 화학식 XVIII의 화합물은 단계 8에서 이미 기술된 바와 같은 탄소-탄소 결합의 형성에 적합한 교차-커플링 반응 중의 어떤 것을 이용함으로써 화학식 VIII의 화합물로 변형시킬 수 있다.
제조방법의 전환반응(전환 a)에 따르면, 티오기의 설포닐기로의 변형은 실온에서 예를 들어, 임의로 공용매로서 물의 존재 하에서 테트라하이드로푸란, 1,4-디옥산 또는 아세톤과 같은 적합한 용매 중의 옥손, 또는 적합한 용매, 바람직하게는 DCM의 존재 하의 m-클로로퍼벤조산과 같은 본 기술분야에서 숙련된 전문가에게 잘 알려진 산화제와의 반응에 의해 수득될 수 있다.
제조방법의 전환반응(전환 b)에 따르면, R4가 상기 정의된 바와 같고, X가 -O-인 화학식 I의 화합물은 상응하는 설포닐 유도체를 화학식 R4-OH(XVI)의 유도체와 반응시킴으로써 쉽게 수득할 수 있다. 반응은 아세토니트릴, N,N-디메틸포름아미드 또는 디메틸설폭사이드와 같은 적합한 용매 중에서 칼륨 또는 나트륨 카보네이트, 나트륨 또는 리튬 하이드록사이드 등과 같은 염기의 존재 하에 실온 내지 약 100℃ 범위의 온도에서 작업함으로써 수행될 수 있다.
흥미롭게도, 이 반응이 A가 -CH2-CH2-인 화학식 I의 화합물을 사용하여 수행되는 경우에는, A가 -CH2-CH2-기 또는 -CH=CH-기인 화학식 I의 목적하는 생성물의 혼합물이 수득되었다. 그 후에, 이들 2 개의 유도체는 통상적인 방법에 따라, 예를 들어, 크로마토그래피 또는 분취용 HPLC에 의해서 반응 혼합물로부터 분할된다.
제조방법의 전환반응(전환 c)에 따르면, 화학식 I의 설포닐 유도체를 화학식 R4R6NH의 이급 아민과 같은 적합한 친핵체로 처리하여 R1이 R4R6N-인 화학식 I의 화합물을 생성시킨다. 상기의 반응은 동일한 아민을 과량으로 사용하거나, 대안적으로 예를 들어, 아세토니트릴, N,N-디메틸포름아미드, 디메틸설폭사이드와 같은 적합한 용매 중에서, 실온 내지 약 100℃ 범위의 온도에서 2 시간 내지 24 시간 동안 작업함으로써 성취된다.
제조방법의 전환반응(전환 d)에 따르면, 화학식 I의 설포닐 유도체의 R1이 -CN인 화학식 I의 화합물로의 전환은 예를 들어, 20℃ 내지 환류 온도 범위의 온도에서 2 시간 내지 24 시간의 시간 동안 아세토니트릴, N,N-디메틸포름아미드 또는 이들의 혼합물과 같은 적합한 용매 중에서 나트륨 시아나이드를 사용하여 성취될 수 있다.
제조방법의 전환반응(전환 e)에 따르면, 화학식 I의 화합물의 화학식 I의 또 다른 화합물로의 전환은 화학식 R2-Y'(V)의 화합물을 사용하여 성취될 수 있으며, 여기에서 Y'는 미츠노부(Mitsunobu) 조건이 사용될 수 있는 경우에는 OH이거나, Y는 할로겐 원자, 토실레이트, 메실레이트 또는 트리플레이트와 같이 임의로 활성화되면 이탈기로 작용할 수 있는 기이다.
전자의 경우에, 즉 미츠노부 프로토콜이 사용되는 경우에, 반응은 테트라하이드로푸란, 1,4-디옥산 1,2-디메톡시에탄, 아세토니트릴과 같은 적합한 용매 중에서 트리알킬 또는 트리아릴 포스핀, 바람직하게는 트리페닐 포스핀의 존재 하에 디에틸아조디카복실레이트(DEAD), 디이소프로필 아조디카복실레이트(DIAD) 등과 같은 디알킬 아조디카복실레이트를 사용하여 성취될 수 있다. Y가 할로겐, 또는 토실레이트, 메실레이트 또는 트리플레이트 등과 같은 기인 경우에, 전환반응은 테트라하이드로푸란, 아세토니트릴, N,N-디메틸포름아미드, N,N-디메틸아세트아미드 등과 같은 적합한 용매 중에서 예를 들어, NaH, K2CO3, Cs2CO3, DBU, KO-t-Bu 등과 같은 적합한 염기를 사용하여 성취될 수 있다. 상기의 반응들은 0℃ 내지 환류 온도 범위의 온도에서 30 분 내지 약 48 시간 범위의 시간 동안 수행될 수 있다.
제조방법의 전환반응(전환 f)에 따르면, R2가 할로에틸, 바람직하게는 클로로에틸인 화학식 I의 화합물을 20℃ 내지 80℃ 범위의 온도에서 염기, 바람직하게는 1,8-디아자비사이클로[5.4.0]운데크-7-엔(DBU)으로 처리하여 R2가 비닐인 화학식 I의 상응하는 화합물을 수득한다.
제조방법의 전환반응(전환 g)에 따르면, R2가 화학식 L-CH2C1인 화학식 I의 화합물을 50℃ 내지 100℃ 범위의 온도에서 적합한 시간, 예를 들어, 2 시간 내지 24 시간 동안 테트라하이드로푸란, 아세토니트릴, N,N-디메틸포름아미드 및 이들의 혼합물과 같은 적합한 용매 중에서, 예를 들어, 칼륨 카보네이트, 세슘 카보네이트, 트리에틸아민, 또는 DBU와 같은 염기의 존재 하에 화학식 NHR'R"(XII)의 일급 또는 이급 아민과 같은 적합한 친핵체와 혼합시킨다.
제조방법의 전환반응(전환 h)에 따르면, R2가 L-CH2OH 기인 화학식 I의 화합물의 R2가 L-CH2NR'R"기인 화학식 I의 화합물로의 전환반응은 본 기술분야에서 숙련된 전문가들 사이에서 잘 정립된 다수의 방식 및 작업 조건으로 성취될 수 있다. 단지 예로서, 우선 R2가 L-CHO기인 화학식 I의 알데히드를 형성시키고, 그 후에 이것을 환원적 아미노화 조건 하에서 화학식 NHR'R"(XII)의 아민과 반응시키는 것을 포함하는 2-단계 절차가 여기에 보고된다. 따라서, L-CH2OH기를 갖는 화학식 I의 화합물을 우선 50℃ 내지 환류 온도 범위의 온도에서 적합한 시간, 예를 들어, 30 분 내지 4 시간 동안 에틸 아세테이트, 테트라하이드로푸란 등과 같은 적합한 용매 중에서, 예를 들어, 2-요오독시벤조산(IBX)과 같은 산화제로 처리함으로써 상응하는 알데히드로 전환시킨다. 수득된 알데히드는 그 후에 0℃ 내지 실온 사이의 온도에서 30 분 내지 6 시간 동안, 테트라하이드로푸란, 1,4-디옥산, N,N-디메틸포름아미드, 또는 이들의 혼합물과 같은 적합한 용매 중에서 예를 들어, 나트륨 시아노보로하이드라이드, 나트륨 트리아세톡시보로하이드라이드 또는 테트라메틸암모늄 트리아세톡시보로하이드라이드와 같은 환원제의 존재 하에 화학식 NHR'R"(XII)의 적합한 아민과 반응시킨다.
제조방법의 전환반응(전환 i)에 따르면, 카복실산 에스테르의 상응하는 일급 알콜로의 환원반응은 0℃ 내지 실온 범위의 온도에서 30 분 내지 24 시간의 적합한 반응시간 동안, 테트라하이드로푸란, 디에틸 에테르, 톨루엔, 에탄올 등과 같은 적합한 용매 중에서 예를 들어, 리튬 알루미늄 하이드라이드, 리튬 보로하이드라이드, 나트륨 보로하이드라이드 등과 같은 적합한 환원제를 사용함으로써 성취된다.
제조방법의 전환반응(전환 j)에 따르면, R' 및 R"가 상기 정의된 바와 같은 알데히드 잔기의 상응하는 알킬아민 유도체 -CH2NR'R"로의 변형은 0℃ 내지 실온 범위의 온도에서 30 분 내지 6 시간 동안, 테트라하이드로푸란, 1,4-디옥산, N,N-디메틸포름아미드 또는 이들의 혼합물과 같은 적합한 용매 중에서, 환원적 아미노화 조건 하에, 바람직하게는 예를 들어, 나트륨 시아노보로하이드라이드, 나트륨 트리아세톡시보로하이드라이드, 또는 테트라메틸암모늄 트리아세톡시보로하이드라이드와 같은 환원제를 사용하여 알데히드 유도체를 화학식 XII의 아민과 반응시킴으로써 수득될 수 있다.
제조방법의 전환반응(전환 k)에 따르면, 니트로기를 갖는 화학식 I의 화합물은 50℃ 내지 환류 온도 범위의 온도에서 30 분 내지 6 시간 동안 테트라하이드로푸란, 1,4-디옥산, 에탄올 및 물 또는 이들의 혼합물과 같은 적합한 용매 중에서 암모늄 클로라이드의 존재 하에, 환원적 조건 하에서, 바람직하게는 예를 들어, 아연 분말과 같은 환원제를 사용하여 아미노기를 갖는 화학식 I의 화합물로 전환시킨다.
제조방법의 전환반응(전환 l)에 따르면, R1이 Me-S-인 화학식 I의 화합물의 R1이 예를 들어, 아릴 또는 헤테로아릴인 화학식 I의 화합물로의 변형은 예를 들어, 화학식 R1-B(OH)2의 유기 보론산과 같은 적합한 유기 금속 시약과의 반응에 의해서 성취된다. 이 반응은 "리베스킨드-스로글(Liebeskind-Srogl) 반응"으로 일반적으로 알려진 Pd-촉매화된 Cu-매개 탈설파이트화(desulfitative) C-C 교차 커플링이다. 상기의 반응은 환류 온도에서 30 분 내지 6 시간 동안, 테트라하이드로푸란, 1,4-디옥산, N,N-디메틸포름아미드와 같은 적합한 용매 중에서, 예를 들어, 테트라키스 트리페닐포스피노 팔라듐 [Pd(PPh3)4] 등과 같은 적합한 팔라듐 공급원 및 구리 티오펜-2-카복실레이트와 같은 금속 보조-인자로서 구리(I)-카복실레이트의 존재 하에서 성취된다.
제조방법의 전환반응(전환 m)에 따르면, R5가 수소인 화학식 I의 화합물은 암모늄 클로라이드 또는 적합한 일급 또는 이급 아민을 사용하여, THF 중의 1 N 리튬 비스-트리메틸실릴아미드와 같은 강염기성 조건 하에서 R5가 R'R"N-인 화학식 I의 화합물로 전환시킬 수 있으며; 바람직하게는 이 반응은 0℃ 내지 환류 온도 범위의 온도에서 테트라하이드로푸란 중에서 수행된다.
제조방법의 전환반응(전환 n)에 따르면, L-N(H)R'와 같은 일급 또는 이급 아미노기가 존재하는 화학식 I의 화합물을 상응하는 이급 또는 삼급 아미노 유도체로 변형시킨다. 바람직하게는, 이 반응은 0℃ 내지 실온 범위의 온도에서 30 분 내지 6 시간 동안, 테트라하이드로푸란, 1,4-디옥산, N,N-디메틸포름아미드 또는 이들의 혼합물과 같은 적합한 용매 중에서, 환원적 아미노화 조건 하에서, 바람직하게는 예를 들어, 나트륨 시아노보로하이드라이드, 나트륨 트리아세톡시보로하이드라이드, 또는 테트라메틸암모늄 트리아세톡시보로하이드라이드와 같은 환원제를 사용하여 화학식 R"CHO(XIX)의 알데히드에 의해 수행된다.
제조방법의 전환반응(전환 o)에 따르면, L-N(H)R'와 같은 일급 또는 이급 아미노기가 존재하는 화학식 I의 화합물을 화학식 R7-COW(XX)의 화합물과 반응시킴으로써 상응하는 카복사미드 유도체로 전환시킨다. 이 반응을 카복사미드의 제조에 관해서 본 기술분야에서 광범하게 공지된 다양한 방식 및 작업 조건으로 수행할 수 있음은 숙련된 전문가에게 명백하다. 예를 들어, W가 클로라이드와 같은 할로겐인 경우에, 반응은 약 -10℃ 내지 환류 온도 범위의 온도에서, 적합한 시간, 예를 들어, 약 30 분 내지 약 96 시간 동안, 예를 들어, 디클로로메탄, 테트라하이드로푸란, 1,4-디옥산, 아세토니트릴, 또는 N,N-디메틸포름아미드 등과 같은 적합한 용매 중에서 수행된다. 반응은 트리에틸아민, N,N-디이소프로필에틸아민 또는 피리딘과 같은 적절한 양자 스캐빈저(proton scavenger)이 존재 하에서 수행된다. W가 하이드록실기인 경우에, 반응은 약 -10℃ 내지 환류 온도 범위의 온도에서 적합한 시간, 예를 들어, 약 30 분 내지 약 48 시간 동안, 예를 들어, 디클로로메탄, 테트라하이드로푸란, 1,4-디옥산, 아세토니트릴, N,N-디메틸포름아미드와 같은 적합한 용매 중에서, 예를 들어, 2-(1H-벤조트리아졸-1-일)-1,1,3,3-테트라메틸우로늄 테트라플루오로보레이트(TBTU), 1,3-디사이클로헥실카보디이미드, 1,3-디이소프로필카보디이미드, 1-(3-디메틸아미노프로필)-3-에틸카보디이미드, N-사이클로헥실카보디이미드-N'-프로필메틸 폴리스티렌 또는 N-사이클로헥실카보디이미드-N'-메틸 폴리스티렌과 같은 커플링제의 존재 하에서 수행된다. 상기의 반응은 임의로, 적합한 촉매, 예를 들어, 4-디메틸아미노피리딘의 존재 하에서, 또는 N-하이드록시벤조트리아졸과 같은 추가의 커플링제의 존재 하에서 수행된다.
제조방법의 전환반응(전환 p)에 따르면, L-N(H)R'와 같은 일급 또는 이급 아미노기가 존재하는 화학식 I의 화합물은 화학식 R8-N=C=0(XXI)의 적절한 이소시아네이트와 반응시켜 상응하는 우레아를 수득함으로써 상응하는 우레아 유도체로 변형된다. 이 반응은 바람직하게는 약 20℃ 내지 환류 온도 범위의 온도에서 약 30 분 내지 약 48 시간의 시간 동안, 디클로로메탄, 테트라하이드로푸란 등과 같은 적합한 용매 중에서 수행된다.
제조방법의 전환반응(전환 q)에 따르면, L-N(H)R'와 같은 일급 또는 이급 아미노기가 존재하는 화학식 I의 화합물을 G가 -S-Me, N-S(0)2CF3, 또는 1H-피라졸릴과 같은 적합한 이탈기인 화학식 R8NHC(NH)-G의 화합물과 반응시킴으로써 상응하는 구아니딘 유도체로 변형시킨다. 예를 들어, 이 반응은 메탄올, 에탄올, N,N-디메틸포름아미드 및 이들의 혼합물과 같은 적합한 용매 중에서 염기성 조건 하에, 예를 들어, 트리에틸아민 또는 칼륨 카보네이트의 존재 하에서 수행될 수 있다. 우선적으로, 이 반응은 실온 내지 약 80℃ 범위의 온도에서 약 30 분 내지 약 24 시간의 시간 동안 수행된다.
제조방법의 전환반응(전환 r)에 따르면, A가 -(CH2)2-인 화학식 I의 화합물은 임의로 지지된 팔라듐 또는 백금 또는 2,3-디클로로-5,6-디시아노-1,4-벤조퀴논(DDQ)의 존재 하에 90℃ 내지 환류 온도 범위의 온도에서 2 시간 내지 8 시간의 시간 동안 톨루엔, 1,4-디옥산, 클로로벤젠과 같은 적합한 용매 중에서 작업함으로써 탈수소화를 겪어 화학식 I의 상응하는 방향족 유도체를 수득할 수 있다.
말할 필요도 없이, 또한 상술한 제조방법의 임의의 중간체는 원하고 필요하다면, 본 발명에서 상술한 전환반응 중의 어느 하나에서와 유사한 방식으로 작업함으로써 상이한 유도체로 전환될 수 있다.
상기한 모든 것으로부터, 본 기술분야에서 잘 알려진 방법에 따라 작업함으로써 또 다른 작용기로 더 유도체화되어 화학식 I의 다른 화합물을 유도할 수 있는 작용기를 갖는 화학식 I의 모든 화합물이 본 발명의 범위 내에 포함된다는 것은 숙련된 전문가에게 명백하다.
또한, 필요한 경우에, 반응성기는 문헌 [예를 들어,, Protective groups in organic synthesis]에 잘 알려진 방법에 따라 보호된 다음에 제거될 수 있다는 것은 숙련된 전문가에게 명백하다.
화학식 I의 화합물을 제조하는 방법의 모든 변형방법에 따르면, 출발물질 및 모든 다른 반응물들은 공지되어 있거나, 공지된 방법에 따라 쉽게 제조된다.
화학식 II의 화합물은 WO 2004/104007에 기술된 바와 같이 제조될 수 있다.
화학식 XIII 및 XVIII의 화합물은 WO 2008/074788에 기술된 바와 같이 제조될 수 있다.
화학식 III, VIIa, VIIb, IX, X, XII, XV, XVII, XIX, XX, XXI 및 XXII의 화합물은 상업적으로 이용할 수 있거나, 공지의 방법으로 제조될 수 있다.
화학식 V 및 XVI의 화합물은 상업적으로 이용할 수 있거나, 공지의 방법으로 제조할 수 있거나, 또는 이하의 실험부(제조예 O 내지 제조예 R)에 기술된 바와 같이 제조될 수 있다.
상기한 모든 것으로부터, 전술한 제조방법 변형 중의 어느 하나에 따라 화학식 I의 화합물을 제조하는 경우에는, 원치 않는 부반응을 야기할 수 있는 출발물질 또는 그의 중간체 내의 임의의 작용기는 통상적인 기술에 따라 적절하게 보호하는 것이 필요하다는 것은 숙련된 전문가에게 명백하다. 마찬가지로, 이들 후자의 탈보호된 화합물로의 전환은 공지된 절차에 따라 수행될 수 있다.
쉽게 이해될 수 있는 바와 같이, 상술한 제조방법에 따라 제조된 화학식 I의 화합물이 이성체의 혼합물로서 수득된다면, 통상적인 기술을 사용한 이들의 화학식 I의 단일 이성체로의 분리가 본 발명의 범위 내에 포함된다.
라세메이트 분할을 위한 통상적인 기술은 예를 들어, 부분입체이성체 염 유도체의 분배 결정화 또는 분취용 키랄 HPLC를 포함한다.
본 발명의 화합물은 단일 약제로서, 또는 대신에 세포증식억제 또는 세포독성제, 항생제-유형 약제, 알킬화제, 항대사물질제, 호르몬제, 면역학적 약제, 인터페론-유형 약제, 사이클로옥시게나제 억제제(예를 들어, COX-2 억제제), 매트릭스메탈로프로테아제 억제제, 텔로머라제 억제제, 티로신 키나제 억제제, 항-성장인자 수용체 약제, 항-HER 약제, 항-EGFR 약제, 항-혈관형성제(예를 들어, 혈관형성 억제제), 파르네실 트랜스퍼라제 억제제, ras-raf 시그날 전달경로 억제제, 세포 주기 억제제, 그 밖의 다른 cdks 억제제, 튜불린 결합제, 토포이소머라제 I 억제제, 토포이소머라제 II 억제제 등과 조합한 방사선요법 또는 화학요법 레지멘과 같은 공지의 항암 치료법과 조합하여 투여될 수 있다.
고정 용량으로 제형화된 경우에, 이러한 조합 생성물은 이하에 기술된 투약량 범위 내의 본 발명의 화합물 및 공인된 투약량 범위 내의 다른 약제학적 활성제를 사용한다.
조합 제형이 부적절한 경우에, 화학식 I의 화합물은 공지의 항암제와 순차적으로 사용될 수 있다.
포유동물에게, 예를 들어, 인간에게 투여하는데 적합한 본 발명의 화학식 I의 화합물은 통상적인 경로로 투여될 수 있으며, 투약량 수준은 환자의 연령, 체중, 상태, 및 투여 경로에 따라 좌우된다.
예를 들어, 화학식 I의 화합물의 경구 투여를 위해서 채택된 적합한 투약량은 1일에 1 내지 5 회, 용량당 약 10 내지 약 500 ㎎의 범위일 수 있다. 본 발명의 화합물은 다양한 투약형으로, 예를 들어, 정제, 캅셀제, 당 또는 필름 코팅 정제, 액체 용액 또는 현탁액의 형태로 경구로; 좌제의 형태로 직장으로; 비경구적으로, 예를 들어, 근육내 또는 정맥내 및/또는 척수강내 및/또는 척수내 주사 또는 주입을 통해서 투여될 수 있다.
본 발명은 또한, 담체 또는 희석제일 수 있는 약제학적으로 허용되는 부형제와 함께 화학식 I의 화합물 또는 그의 약제학적으로 허용되는 염을 포함하는 약제학적 조성물을 포함한다.
본 발명의 화합물을 함유하는 약제학적 조성물은 통상적으로 통상적인 방법에 따라 제조되며, 적합한 약제학적 형태로 투여된다. 예를 들어, 고체 경구용 형태는 활성 화합물과 함께 희석제, 예를 들어, 락토즈, 덱스트로즈, 사카로즈, 슈크로즈, 셀룰로오즈, 옥수수 전분 또는 감자 전분; 윤활제, 예를 들어, 실리카, 탈크, 스테아르산, 마그네슘 또는 칼슘 스테아레이트, 및/또는 폴리에틸렌 글리콜; 결합제, 예를 들어, 전분, 아라비아 고무, 젤라틴 메틸셀룰로즈, 카복시메틸셀룰로즈 또는 폴리비닐 피롤리돈; 붕해제, 예를 들어, 전분, 알긴산, 알기네이트 또는 나트륨 전분 글리콜레이트; 발포성 혼합물(effervescing mixtures); 염료; 감미제; 레시틴, 폴리소르베이트, 라우릴설페이트와 같은 습윤제; 및 일반적으로, 약제학적 제제에서 사용되는 비독성이며 약제학적으로 불활성인 물질을 함유할 수 있다. 이들 약제학적 제제는 공지의 방식으로, 예를 들어, 혼합, 과립화, 타정, 당-코팅, 또는 필름-코팅 방법을 이용하여 제조할 수 있다.
경구 투여를 위한 액체 분산액은 예를 들어, 시럽, 에멀션 및 현탁액일 수 있다. 예를 들어, 시럽제는 담체로서 사카로즈, 또는 글리세린 및/또는 만니톨 및 소르비톨과 함께 사카로즈를 함유할 수 있다.
현탁액 및 에멀션은 담체의 예로서 천연 고무, 한천, 나트륨 알기네이트, 펙틴, 메틸셀룰로즈, 카복시메틸셀룰로즈, 또는 폴리비닐 알콜을 함유할 수 있다. 근육내 주사를 위한 현탁액 또는 용액은 활성 화합물과 함께 약제학적으로 허용되는 담체, 예를 들어, 멸균수, 올리브유, 에틸 올리에이트, 글리콜, 예를 들어, 프로필렌 글리콜, 및 필요에 따라, 적합한 양의 리도카인 하이드로클로라이드를 함유할 수 있다.
정맥내 주사 또는 주입을 위한 용액은 담체로서 멸균수를 함유할 수 있거나, 바람직하게는 이들은 멸균, 수성, 등장성, 식염수 용액의 형태일 수 있거나, 이들은 담체로서 프로필렌 글리콜을 함유할 수 있다.
좌제는 활성 화합물과 함께 약제학적으로 허용되는 담체, 예를 들어, 코코아 버터, 폴리에틸렌 글리콜, 폴리옥시에틸렌 소르비탄 지방산 에스테르 계면활성제 또는 레시틴을 함유할 수 있다.
본 발명에 대한 어떤 제한도 두지 않으면서 본 발명을 더 잘 설명할 목적으로 이하의 실시예가 제시된다.
실험 항목
약물학
화학식 I의 화합물은 단백질 키나제 억제제로서 활성이 있으며, 따라서 예를 들어, 종양 세포의 비조절된 증식을 제한하는데 유용하다.
치료법에서, 이들은 이전에 정의된 것과 같은 다양한 종양의 치료뿐만 아니라 그 밖의 다른 세포 증식 장애 및 면역 세포-관련된 질환 및 장애의 치료에 사용될 수 있다.
PIM-1 및 2 억제제의 억제활성 및 선택된 화합물의 효력은 이하에 기술된 시험방법을 통해서 결정되었다.
임의로 약제학적으로 허용되는 염의 형태인 본 발명의 화학식 I의 어떤 특정한 화합물에 관해서는 실험 항목 및 특허청구범위를 참고로 한다. 이하의 실시예를 참고로 하여, 본 발명의 화합물은 본 발명에 기술된 방법, 또는 본 기술분야에서 잘 알려진 다른 방법을 사용하여 합성하였다.
본 발명에서 사용된 단축 용어 및 약어는 다음의 의미를 갖는다:
BSA 소혈청 알부민
Tris 2-아미노-2-(하이드록시메틸)-1,3-프로판디올
Hepes N-(2-하이드록시에틸)피페라진-N'-(2-에탄설폰산)
THF 테트라하이드로푸란
MTBE 메틸 3급 부틸 에테르
DIPEA N,N-디이소프로필에틸아민
PyBOP 벤조트리아졸-1-일옥시트리스(피롤리디노)포스포늄 헥사플루오 로포스페이트
EDC 1-에틸-3-(3'-디메틸아미노프로필)카보디이미드
DHBT 3,4-디하이드로-3-하이드록시-4-옥소-1,2,3-벤조트리아진
HBTU 2-(1H-벤조트리아졸-1-일)-1,1,3,3-테트라메틸우로늄 헥사플루오로포스페이트
TFA 트리플루오로아세트산
TMOF 트리메틸오르토포르메이트
DCE 디클로로에탄
DCM 디클로로메탄
DMF N,N-디메틸포름아미드
DMA N,N-디메틸아세트아미드
DMSO 디메틸설폭사이드
KDa 킬로달톤
mg 밀리그램
㎍ 마이크로그램
ng 나노그램
L 리터
㎖ 밀리리터
㎕ 마이크로리터
M 몰
mM 밀리몰
μM 마이크로몰
nM 나노몰
MHz 메가-헤르츠
Hz 헤르츠
min 분
mol 몰(moles)
TLC 박층 크로마토그래피
r.t. 실온
TEA 트리에틸아민
Hex 헥산
MeOH 메탄올
bs 브로드한 단일선(broad singlet)
Ac 아세틸
BOC tert-부틸옥시카보닐
Ac20 아세트산 무수물
ESI 전자분무 이온화
NaH 나트륨 하이드라이드, 광유 중의 60%
NMP N-메틸-피롤리돈
RP-HPLC 역상 고성능 액체 크로마토그래피
본 발명에 어떤 제한을 부여하지 않으면서 본 발명을 더 잘 설명할 목적으로, 이하의 실시예가 제공된다.
본 발명에서 사용된 것으로서, 제조방법, 반응식 및 실시예에서 사용된 기호(symbols) 및 관습은 동시대의 과학 문헌, 예를 들어, Journal of the American Chemical Society 또는 Journal of Biological Chemistry에서 사용된 것과 일치한다.
다른 식으로 명시되지 않는 한, 모든 물질들은 상업적 공급자들로부터 최상 등급으로 획득하여, 더 정제하지 않고 사용하였다. DMF, THF, CH2Cl2 및 톨루엔과 같은 무수 용매는 Aldrich Chemical Company로부터 획득하였다. 공기- 또는 수분-민감성 화합물을 포함하는 모든 반응은 질소 또는 아르곤 대기 하에서 수행하였다.
PIM-1 키나제 활성의 억제제에 대한 생화학적 시험
추정상의 키나제 억제제의 억제활성 및 선택된 화합물의 효력은 트랜스-포스포릴화 시험을 사용하여 결정되었다.
특정한 펩타이드 또는 단백질 기질은 33P-γ-ATP로 추적되는 ATP의 존재 하, 및 그들 자신의 최적 완충액 및 보조인자의 존재 하에서 그들의 특정한 ser-thr 또는 tyr 키나제에 의해서 트랜스-포스포릴화된다.
포스포릴화 반응의 종료 시에, 98% 이상의 비표지된 ATP 및 방사성 ATP가 과량의 이온교환 다우엑스®(Dowex®) 수지에 의해서 포착되며; 그 후, 수지는 중력에 의해서 반응 플레이트의 바닥에 침강한다.
이어서 상등액을 배출시키고, 계수 플레이트(counting plate) 내로 옮긴 다음에 β-계수에 의해서 평가한다.
시약/시험 조건
다우엑스
®(
Dowex
®) 수지 제조:
500 g의 습윤 수지(SIGMA, 주문 제조된 수지 다우엑스®(DOWEX®) 1x8 200-400 메쉬, 2.5 Kg)를 정량하고, 150 mM 나트륨 포르메이트 pH 3.00 내에서 2 ℓ로 희석한다.
수지를 침강시킨(몇 시간) 다음에 상청액은 버린다.
2일 정도에 걸쳐서 상기한 바와 같이 3 회 세척한 후에, 수지를 침강시키고, 2 용적(wrt 수지 용적)의 150 mM 나트륨 포르메이트 완충액을 첨가한다.
그 후, pH를 측정하고, 대략 3.00이어야 한다.
세척된 수지는 1 주일 이상 동안 안정하며; 저장 수지는 사용하기 전에 4℃에서 유지시킨다.
키나제
완충액
(
KB
):
PIM-1 시험을 위한 완충액은 10 mM MgCl2, 1 mM DTT, 3 μM NaV03, 및 0.2 ㎎/㎖ BSA와 함께 pH 7.5에서 HEPES 50 mM로 구성되었다.
전장 인간 PIM-1은 문헌 [Bullock AN, et al., J. Biol. Chem. 2005, 280, 41675-82]에 기술된 바와 같이 발현시키고 정제하였다.
효소는 다음의 조건에서 자동-포스포릴화에 의한 전-활성화의 단계 후에 선형 동력학을 나타내었다:
1.7 μM PIM1은 125 μM ATP의 존재 하에 RT 28℃에서 1 시간 동안 배양한다.
시험 조건:
ATP 농도: 200 μM
33P-γ-ATP: 6 nM
효소 농도: 1 nM
기질 농도 액타이드(Aktide)(Chemical Abstract Service Registry Number 324029-01-8): 25 μM
로봇화된
다우엑스
®(
Dowex
®) 시험:
시험 믹스(mix)는 다음으로 구성되었다:
1) 3x 효소 믹스(키나제 완충액 3X 내에서 이루어짐), 5 ㎕/웰
2) 33P-γ-ATP와 함께 3x 기질 및 ATP 믹스(ddH20 중에서 이루어짐), 5 ㎕/웰
3) 3x 시험 화합물(ddH20 - 3% DMSO 내에 희석됨) - 5 ㎕/웰
화합물 희석 및 시험 체계에 대해서는 이하를 참조한다.
화합물의 희석
IC50 결정을 위해서, 시험 화합물을 100% DMSO 중의 1 mM 용액으로 수용하고, 96-웰 플레이트 내에 분배시킨다: 그 후, 화합물(100 ㎕/웰)을 새로운 96-웰 플레이트(A1 내지 G1)의 제1 칼럼 내에 플레이팅한다.
일련의 희석을 위해서 자동화 스테이션(Biomek FX®, Beckman)을 사용하여 칼럼 내의 모든 화합물에 대해 라인 A1부터 A10까지 100% DMSO 내에서 1:3 희석액을 생성시킨다. 또한, 4-5 카피(copies)의 딸 플레이트는 5 ㎕의 상기 제1 세트의 100% DMSO 희석 플레이트를 384-딥웰(deep well) 플레이트 내에 재포맷팅함으로써 제조한다: 시험 화합물을 갖는 이들 일련의 희석 플레이트의 하나의 카피를 시험일에 해동시키고, 작업 농도(최종 농도의 3-배)에서 162 ㎕/웰의 물로 재구성하고, IC50 측정시험을 위해서 사용한다. 표준 실험에서, 화합물의 최고 농도(3X)는 전형적으로 30 μM인 반면에, 최저 농도는 전형적으로 1.5 nM이다.
각각의 384-웰 플레이트는 Z' 및 시그날 대 배경(S/B) 비의 평가를 위한 표준 억제제 스타우로스포린 및 대조 웰의 적어도 하나의 곡선(총 효소 활성 대 비 효소 활성)를 생성시킨다.
시험 체계:
V 바닥 384-웰 플레이트(시험 플레이트)는 전술한 바와 같이 희석된(3X) 화합물 5 ㎕를 사용하여 준비한 다음에, 플레이트트랙(PlateTrak®) 12 로봇화 스테이션(Perkin Elmer; 로봇은 효소 믹스(3X)를 위한 하나의 저장소 및 ATP 믹스(3X)를 위한 하나의 저장소와 함께, 수지 분배를 위한 하나의 96-팁(tip) 헤드와 시험 시작을 위한 하나의 384-팁 피펫팅(pipetting) 헤드를 갖는다.
데이터는 통상적인 이차 시험/히트 확인(hit confirmation)에서 IC50 결정을 위한 10-희석 곡선의 s자형 피팅(sigmoidal fitting)을 제공하는 "에세이 익스플로러®(Assay Explorer®)" SW 패키지의 내부적으로 맞춤형인 버전에 의해서 분석한다.
PIM-2 키나제 억제 시험: 다우엑스 기술
키나제
완충액
(
KB
):
PIM-2 시험을 위한 완충액은 1 mM MgCl2, 1 mM DTT, 3 μM Na3V04, 및 0.2 ㎎/㎖ BSA와 함께 pH 7.5에서 HEPES 50 mM로 구성되었다.
전장 인간 PIM-2는 문헌 [Fedorov O, et al.(2007) PNAS 104, 51, 20523-28]에 기술된 바와 같이 발현시키고 정제하였다.
시험 조건(최종 농도):
효소 농도 = 1.5 nM
액타이드 기질(Chemical Abstract Service Registry Number 324029-01-8) = 5 μM
ATP = 4 μM
33P-γ-ATP = 1 nM
로봇화된
다우엑스
시험:
상기 참조: PIM-1에 대해 기술된 바와 같은 동일한 절차.
시험관내
세포 증식시험:
MV-4-11(이표현성(biphenotypic) B 골수단구성 백혈병) 세포(1250 세포/웰)를 완전 배지(10% 소 태아 혈청과 함께 RPMI 1640 또는 EMEM) 내의 백색 384 웰-플레이트 내에 접종하고, 접종한 지 24 시간 후에 0.1% DMSO에 용해된 화합물로 처리하였다. 세포를 37℃ 및 5% CO2 하에서 인큐베이션시키고, 72 시간 후에 플레이트를 제조자의 사용설명서에 따라 셀타이터-글로®(CellTiter-Glo®) 시험(Promega)을 사용하여 처리하였다. 셀타이터 글로®(CellTiter-Glo®)는 대사적으로 활성인 세포의 지표인 존재하는 ATP의 정량을 기초로 하는 균일한 방법이다. ATP는 광 생성을 야기하는 루시퍼라제 및 D-루시페린을 기초로 하는 시스템을 사용하여 정량화된다.
요컨대, 25 ㎕/웰의 시약 용액을 각각의 웰에 첨가하고, 5 분 진탕한 후에 마이크로플레이트는 엔비전®(Envision®; PerkinElmer) 발광측정기에 의해서 적색이었다. 발광 시그날은 배양물 내에 존재하는 세포의 수에 비례하였다.
억제활성은 에세이 익스플로러(MDL) 프로그램을 사용하여 처리군 대 대조군 데이터를 비교함으로써 평가하였다. IC50은 s자형 내삽 곡선(sigmoidal interpolation curve)을 사용하여 계산하였다.
상기 억제시험의 경우에, 본 발명의 화학식 I의 화합물은 전형적으로 1 μM보다 훨씬 작은 IC50을 갖는 우수한 PIM-1 억제활성, 및 전형적으로 10 μM 이하의 IC50을 갖는 우수한 PIM-2 억제활성을 갖는 것으로 결론이 지어졌다. 또한, 본 발명의 화학식 I의 화합물은 전형적으로 MV-4-11 세포에서 0.010 내지 2 μM 범위의 IC50을 갖는 우수한 세포 증식 억제활성을 나타낸다.
이하의 표 A는 상술한 특이적 시험관내 키나제 시험에서 PIM-1, 및 2 효소에 대해서 시험한 화학식 I의 본 발명의 몇 가지 대표적 화합물의 실험 데이터를 보고한다(IC50 μM).
이하의 표 A는 또한, 선행기술의 가장 근접한 화합물 중의 몇 가지의 PIM-1 및 PIM-2에 대한 억제활성을 보고한다.
대조 화합물 1은 1-메틸-8-(피페리딘-1-일)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드(화합물 코드 B76-X06-M00(C01)-D03)이고; 대조 화합물 2는 상기 인용된 특허출원 WO 2004/104007에서의 1-메틸-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드(화합물 코드 B67-X04-M00(C01-D03)이다. 대조 화합물 1 및 2는 각각 본 발명의 특허청구에서 제외된 첫 번째 및 두 번째 화합물이다.
이하의 표 A는 또한, 골수단구성 백혈병 MV-4-11 세포에 대한 본 발명의 몇 가지 대표적 화합물의 항증식 활성을 보고한다.
[표 A]
놀랍게도, 본 발명의 화합물의 PIM-1 및 PIM-2 억제활성은 대조 화합물의 억제활성에 비해 현저하게 탁월한 것으로 결론이 지어졌다.
본 발명의 신규 화합물은 예기치 않게, 전술한 WO 2004/104007의 구조적으로 가장 근접한 선행기술 화합물에 비해서 훨씬 더 큰 PIM-1 및 PIM-2 억제활성이 부여되며, 따라서 변화된 키나제 활성과 관련된 증식 장애에 대한 치료방법에 특히 유리하다.
본 발명의 화합물의 세포독성이 PIM 키나제의 억제로부터 유래하였음을 더 입증하기 위해서, 본 발명자들은 MV-4-11 백혈병 세포주에서 PIM 억제제의 존재 또는 부재 하에서 PIM 키나제에 의한 전-세포소멸성 단백질 BAD의 포스포릴화를 검사하였다.
PIM 키나제의 하류 표적인 BAD는 Ser 112에서 PIM-1, PIM-2 및 PIM-3에 의해서 직접 포스포릴화되는 것으로 입증되었다 [Pogacic V. et al(2007) Cancer Research, 67(14); 6916-24].
본 발명의 화합물은 MV-4-11 내의 Ser 112에서 BAD의 포스포릴화를 효율적으로 및 용량-의존적으로 억제하였고, 따라서 이들 화합물은 PIM 억제제인 것으로 밝혀졌으며, 결과는 도 2에 나타내었다.
MV-4-11 세포를 6 웰 플레이트 내에 1.5 x106 세포/㎖로 플레이팅하고, 3 시간 동안 상이한 농도의 PIM-억제제로 처리하였다. 세포를 수확하고, PBS 완충액으로 세척하고, 용해 완충액(2% SDS, 1OO mM Tris ph 7.5, 1:100 포스파타제 억제제 칵테일 1(SIGMA) 및 1:100 포스파타제 억제제 칵테일 2(SIGMA) 및 완전 프로테아제 억제제(Roche))로 용해시켰다. 용해물 내의 단백질 농도는 BCA 단백질 시험 키트(Pierce)를 사용하여 정량화하였다. 동등한 양의 단백질을 SDS-PAGE 분석을 위한 4-12% 구배 트리-글리신 겔 상에 부하시켰다. 그 후에, 단백질을 웨스턴 블럿팅(Western Blotting)을 위해서 PVDF 막(Millipore)으로 전이시켰다. 막을 포스포-Bad(Ser112)에 대한 항체로 프로브화시켰다(세포 시그날링 기술).
실시예
본 발명의 일부의 화학식 I의 화합물의 합성 제조는 이하의 실시예에 기술된다.
이하의 실시예에 따라서 제조된 본 발명의 화합물은 또한 1H NMR 또는 HPLC/MS 분석 데이터에 의해서 특정화되었으며; HPLC/MS 데이터는 방법 1, 2, 3 및 4 중 임의의 하나에 따라 수집하였다.
HPLC
MS
분석 방법 1
HPLC 장치는 2996 워터스(Waters) PDA 검출기가 장착된 워터스 액퀴티TM(Waters AcquityTM) UPLC 시스템, 및 전자분무(ESI) 이온 공급원이 장착된 마이크로매스 모드(Micromass mod.) ZQ 단일 사중극 질량 분석기로 구성하였다. 기기 제어, 데이터 획득 및 데이터 처리는 엠파워®(Empower®) 및 매스린스®(MassLynx®) 4.0 소프트웨어에 의해서 제공하였다.
HPLC는 BEH C18 1.7 미크론 워터스 액퀴티®(Waters Acquity®) UPLC(2.1 x 50 ㎜) 칼럼을 사용하여 45℃에서 0.8 ㎖/min의 유속으로 수행하였다. 이동상 A는 포름산 0.1% pH=3.3 완충액과 아세토니트릴(98:2)이었으며, 이동상 B는 H20/아세토니트릴(5:95)이었고; 구배는 2 분에 걸쳐서 5 내지 95% B였으며, 그 다음에는 0.1 분에 걸쳐서 95% B였다. 주입 용적은 2 ㎕였다. 질량 분석기는 양이온 및 음이온 모드에서 작동하였으며, 모세관 전압(capillary voltage)은 3.5 KV(ES+) 및 28 V(ES~)로 설정되었고; 공급원 온도는 120℃였으며; 콘(cone)은 14 V(ES+) 및 2.8 KV(ES-)였고; 질량 범위 100 내지 800 amu의 풀 스캔(full scan)이 설정되었다.
HPLC
/
MS
분석 방법 2
HPLC-MS 분석은 ESI(전자분무) 이온 공급원이 장치된 피니간 MAT 모드(Finnigan MAT mod.) LCQ® 이온 트랩 질량 분석기 상에서 수행되었으며, 질량 분석기는 오토샘플러(autosampler) Lc Pal(CTC Analytics) 및 UV6000LP PDA 검출기가 장치된 HPLC SSP4000(Thermo Separation)에 직접 연결된다.
HPLC는 페노메넥스 제미니(Phenomenex Gemini) C18, 3 ㎛, 50 x 4.6 ㎜ 칼럼을 사용하여 40℃에서 1.0 ㎖/min의 유속으로 수행되었다. 이동상 A는 아세테이트 완충액 5 mM pH 4.5 : 아세토니트릴 95:5(v:v)이었으며, 이동상 B는 아세테이트 완충액 5 mM pH 4.5 : 아세토니트릴 5:95(v:v)이었고, 구배는 7 분에 걸쳐서 0 내지 100% B였으며, 그 다음에 평형화시키기 전에 2 분에 걸쳐서는 100% B로 유지시켰다. 총 LC 시간은 10 분이었다. 주입 용적은 10 ㎕였다.
MS 조건: LCQ 질량 분석기는 양이온 및 음이온 모드의 전자분무 이온화(ESI) 계면과 함께 작동한다. ESI 분무기 전압 4.0 kV, 가열된 모세관 온도 255℃, 5.0 바(bar)의 압력을 갖는 외장(sheath) 가스 질소. 풀 스캔 검출 모드(50 내지 1000 amu)가 사용되었다.
MS/MS 실험은 엑스칼리버®(Xcalibur®) 소프트웨어에 의해서 자동적으로 각 스캔의 가장 강력한 이온 상에서 수행되었다. 45% 충돌 에너지가 전구체 이온의 단편화(fragmentation)를 위해서 사용되었다.
HPLC
/
MS
분석 방법 3
HPLC 장치는 2996 워터스 PDA 검출기가 장치된 워터스 2795 알리안스(Alliance) 시스템, 및 전자분무(ESI) 이온 공급원이 장치된 마이크로매스 모드. ZQ 단일 사중극 질량 분석기로 구성되었다. 기기 제어, 데이터 획득 및 데이터 처리는 임파워®(Empower®) 및 매스린스®(MassLynx®) 4.0 소프트웨어에 의해서 제공되었다.
HPLC는 C18, 3 미크론 페노메넥스(Phenomenex)(4.6 x 50 ㎜) 칼럼을 사용하여 30℃에서 1.0 ㎖/min의 유속으로 수행되었다. 이동상 A는 암모늄 아세테이트 5 mM pH=5.2 완충액과 아세토니트릴(95:5)이었으며, 이동상 B는 H2O/아세토니트릴(5:95)이었고; 구배는 8 분에 걸쳐서 10 내지 90% B였고, 그 다음에 1.0 분에 걸쳐서 100% B까지 상승시켰다. 주입 용적은 10 ㎕였다. 질량 분석기는 양이온 및 음이온 모드로 작동하였으며, 모세관 전압은 3.5 KV(ES+) 및 28 V(ES~)로 설정되었고; 공급원 온도는 120℃였으며; 콘은 14 V(ES+) 및 2.8 KV(ES~)였고; 질량 범위 100 내지 800 amu의 풀 스캔이 설정되었다.
HPLC
/
MS
분석 방법 4
HPLC 장치는 996 워터스 PDA 검출기가 장치된 워터스 2790 HPLC 시스템, 및 전자분무(ESI) 이온 공급원이 장치된 마이크로매스 모드. ZQ 단일 사중극 질량 분석기로 구성되었다. 기기 제어, 데이터 획득 및 데이터 처리는 임파워 및 매스린스 4.0 소프트웨어에 의해서 제공되었다.
HPLC는 RP18 워터스 X 테라(Waters X Terra)(3.0 x 20 ㎜) 칼럼을 사용하여 25℃에서 1 ㎖/min의 유속으로 수행되었다. 이동상 A는 암모늄 하이드록사이드 0.05% pH=10 완충액과 아세토니트릴(95:5)이었으며, 이동상 B는 H20/아세토니트릴(5:95)이었고; 구배는 4 분에 걸쳐서 10 내지 90% B였고, 그 다음에는 1 분에 걸쳐서 90% B로 유지시켰다. 주입 용적은 10 ㎕였다. 질량 분석기는 양이온 및 음이온 모드로 작동하였으며, 모세관 전압은 2.5 KV로 설정되었고; 공급원 온도는 120℃였으며; 콘은 10 V였고; 질량 범위 100 내지 800 amu의 풀 스캔이 설정되었다.
이하의 실시예에 따라 제조된 화학식 I의 본 발명의 몇 가지 화합물은 분취용 HPLC에 의해서 정제되었다.
작업 조건은 이하에 정의되었다:
HPLC
/
MS
분취용
방법 1
HPLC 장치는 996 워터스 PDA 검출기가 장치된 워터스 2790 HPLC 시스템, 및 전자분무(ESI) 이온 공급원이 장치된 마이크로매스 모드. ZQ 단일 사중극 질량 분석기로 구성되었다. 기기 제어, 데이터 획득 및 데이터 처리는 임파워 및 매스린스 4.0 소프트웨어에 의해서 제공되었다.
HPLC는 RP18 워터스 X 테라 10 미크론(19 x 250 ㎜) 칼럼을 사용하여 25℃에서 20 ㎖/min의 유속으로 수행되었다. 이동상 A는 암모늄 하이드록사이드 0.05% pH=10 완충액과 아세토니트릴(95:5)이었으며, 이동상 B는 아세토니트릴이었고; 구배는 15 분에 걸쳐서 10 내지 90% B였고, 그 다음에는 3 분에 걸쳐서 90% B로 유지시켰다. 주입 용적은 10 ㎕였다.
질량 분석기는 양이온 및 음이온 모드로 작동하였으며, 모세관 전압은 2.5 KV로 설정되었고; 공급원 온도는 120℃였으며; 콘은 10 V였고; 질량 범위 100 내지 800 amu의 풀 스캔이 설정되었다.
HPLC
/
MS
분취용
방법 2
HPLC 장치는 996 워터스 PDA 검출기가 장치된 워터스 2790 HPLC 시스템, 및 전자분무(ESI) 이온 공급원이 장치된 마이크로매스 모드. ZQ 단일 사중극 질량 분석기로 구성되었다. 기기 제어, 데이터 획득 및 데이터 처리는 임파워 및 매스린스 4.0 소프트웨어에 의해서 제공되었다.
HPLC는 RP18 워터스 X 테라 10 미크론(19 x 250 ㎜) 칼럼을 사용하여 25℃에서 20 ㎖/min의 유속으로 수행되었다. 이동상 A는 물 중의 0.1% 트리플루오로아세트산/아세토니트릴(95:5)이었으며, 이동상 B는 아세토니트릴이었고; 구배는 15 분에 걸쳐서 10 내지 90% B였고, 그 다음에는 3 분에 걸쳐서 90% B로 유지시켰다. 주입 용적은 10 ㎕였다.
질량 분석기는 양이온 및 음이온 모드로 작동하였으며, 모세관 전압은 2.5 KV로 설정되었고; 공급원 온도는 120℃였으며; 콘은 10 V였고; 질량 범위 100 내지 800 amu의 풀 스캔이 설정되었다.
정확한
MS
정확한 질량 데이터 ESI(+)는 이전에 기술된 바와 같이 마이크로 HPLC 1100 애질런트(Agilent)와 직접적으로 연결된 워터스 Q-토프 울티마®(Waters Q-Tof Ultima®) 상에서 획득하였다 [M. Colombo, F. Riccardi-Sirtori, V. Rizzo, Rapid Commun. Mass Spectrom . 2004, 18, 511-517].
1H-NMR 분광분석은 구배를 사용한 브루커 어밴스®(Bruker AVANCE®) 400MHz 단일 베이(bay) 기기 상에서 수행되었다. 이것은 QNP 프로브(상호교환가능한 4 개의 핵 프로브 - 1H, 13C, 19F 및 31P)(NMR 방법 1)가 장치되었거나, 5 ㎜ 이중 공명 프로브 [1H(15N-31P) ID_PFG Varian]가 장치된 400.45 MHz에서 작동하는 머큐리(Mercury) VX 400 상에 장치되었다.
제조예
A
에틸 1-tert-부틸-7-옥소-4,5,6,7-테트라하이드로-1H-인다졸-3-카복실레이트[(IV), R2 = t-부틸, A = -(CH2)2-]
단계 1
실온에서 무수 에탄올(150 ㎖) 중의 에틸(3-에톡시-2-옥소사이클로헥스-3-엔-1-일)(옥소)아세테이트 10 g(42.6 mmol) 및 아세트산 5 ㎖의 용액에 tert-부틸 하이드라진 하이드로클로라이드 6 g(48 mmol)을 첨가하였다. 혼합물을 60℃에서 3 시간 동안 교반하였다. 휘발성 물질을 진공 하에서 제거하고, 잔류물을 DCM으로 희석하고, NaHCO3의 포화 수용액 및 염수로 세척하였다. 유기상을 나트륨 설페이트로 건조시키고, 여과하고, 농축시켰다. 조물질을 에틸 아세테이트 및 헥산(1:2)으로 용출시키는 실리카겔 칼럼 크로마토그래피에 의해서 정제하여 에틸 1-tert-부틸-7-옥소-4,5,6,7-테트라하이드로-1H-인다졸-3-카복실레이트를 90% 수율로 제공하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 6.08 min. 1H NMR(400 MHz, DMSO-d6) δ ppm 4.18(q, J=6.83 Hz, 2H), 2.93-2.30(3m, 6H), 1.58(s, 9H), 1.16(t, J=6.83 Hz, 3H). HRMS(ESI) C14H20N2O3에 대한 계산치 [M+H]+ 287.1366, 실측치 287.1356.
동일한 방법에 따르지만 하이드라진을 사용하여 다음의 화합물을 제조하였다:
에틸 7-옥소-4,5,6,7-테트라하이드로-1H-인다졸-3-카복실레이트 [(IV), R2 = H, A = -(CH2)2-]. 1H NMR(400 MHz, DMSO-d6) δ ppm 14.39(s, 1H), 4.27(q, J=7.11 Hz, 2H), 2.87(t, J=6.10 Hz, 2H), 2.51(m, 2H), 2.04(m, 2H), 1.28(t, J=7.07 Hz, 3H).
제조예
B
에틸 1-(4-메톡시벤질)-7-옥소-4,5,6,7-테트라하이드로-1H-인다졸-3-카복실레이트[(IVa), R2 = p 메톡시벤질, A = -(CH2)2-] 및 에틸 2-(4-메톡시벤질)-7-옥소-4,5,6,7-테트라하이드로-2H-인다졸-3-카복실레이트 [(IVb), R2 = p 메톡시벤질, A = -(CH2)2-].
단계 1a
50 mg의 에틸 7-옥소-4,5,6,7-테트라하이드로-1H-인다졸-3-카복실레이트 및 120 ㎎(0.37 mmol)의 세슘 카보네이트를 1 ㎖의 무수 DMF에 용해시키고, 42 ㎕(0.288 mmol)의 p-메톡시벤질 브로마이드를 첨가하고, 실온에서 밤새 교반하였다. 혼합물을 H20와 DCM 사이에 분배시켰다. 유기층을 염수로 세척하고, Na2SO4 상에서 건조시키고, 여과하고, 감압 하에서 농축시켰다. 잔류물을 섬광 칼럼 크로마토그래피(DCM/아세톤 95/5)에 의해서 정제하여 2 개의 위치이성체를 제공하였다:
에틸 1-(4-메톡시벤질)-7-옥소-4,5,6,7-테트라하이드로-1H-인다졸-3-카복실레이트, 20% 수율. 1H NMR(400 MHz, DMSO-d6) δ ppm 7.10-7.30(m, 2H), 6.75-6.96(m, 2H), 5.64(s, 2H), 4.29(q, J=7.16 Hz, 2H), 3.71(s, 3H), 2.93(t, J=6.10 Hz, 2H), 2.55(dd, J=5.55, 7.26 Hz, 2H), 1.90-2.15(m, 2H), 1.30(t, J=7.14 Hz, 3H).
에틸 2-(4-메톡시벤질)-7-옥소-4,5,6,7-테트라하이드로-2H-인다졸-3-카복실레이트, 25% 수율. 1H NMR(401 MHz, DMSO-d6) δ 7.12-7.32(m, 2H), 6.76-6.97(m, 2H), 5.70(s, 2H), 4.32(q, J=7.12 Hz, 2H), 3.71(s, 3H), 2.91(t, J=6.10 Hz, 2H), 2.52-2.57(m, 2H), 1.97-2.09(m, 2H), 1.30(t, J=7.08 Hz, 3H).
제조예
C
에틸(6E)-1-tert-부틸-6-[(디메틸아미노)메틸리덴]-7-옥소-4,5,6,7-테트라하이드로-1H-인다졸-3-카복실레이트[(VI), R2 = t-부틸, A = -(CH2)2-]
단계 2
중간체 에틸 1-tert-부틸-7-옥소-4,5,6,7-테트라하이드로-1H-인다졸-3-카복실레이트 10 g(37.8 mmol)을 50 ㎖의 N,N-디메틸포름아미드 디메틸 아세탈에 용해시키고, 110℃에서 교반하였다. 반응액을 그 온도에서 16 시간 동안 교반하였다. 반응 혼합물을 농축시킨 다음에 H2O와 DCM 사이에 분배시켰다. 유기층을 염수로 세척하고, Na2S04 상에서 건조시키고, 여과하고, 감압 하에서 농축시켜 정량적 수율로 표제 화합물을 수득하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 5.85 min. 1H NMR(401 MHz, DMSO-d6) δ 7.55(s, 1H), 4.22-4.33(m, 2H), 3.11(s, 6H), 2.82(s, 4H), 1.66(s, 9H), 1.25-1.32(m, 3H).
제조예
D
에틸 1-tert-부틸-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트[(VIII), R1 = Me-S-, R2 = t-부틸, A = -(CH2)2-]
단계 3a
50 ㎖의 무수 DMF 중의 9 g(28.17 mmol)의 에틸(6E)-1-tert-부틸-6-[(디메틸아미노)메틸리덴]-7-옥소-4,5,6,7-테트라하이드로-1H-인다졸-3-카복실레이트의 용액에 9.2 g(112 mmol)의 무수 칼륨 아세테이트 및 23.52 g( 84.51 mmol)의 메틸이소티오우레아 설페이트를 첨가하였다. 반응액을 100℃에서 8 시간 동안 교반하였다. 혼합물을 에틸 아세테이트로 희석하고, H2O로 세척하고, Na2S04 상에서 건조시키고, 여과하고, 증발시켰다. 조물질을 실리카겔 크로마토그래피(에틸 아세테이트:헥산 1:3)에 의해서 정제하여 표제 화합물을 제공하였다(50%). LC/MS(254 ㎚) HPLC 방법 2 Rt 7.46 min. 1H NMR(401 MHz, DMSO-d6) δ 8.58(s, 1H), 4.22-4.38(m, 2H), 2.95-3.01(m, 2H), 2.80-2.86(m, 2H), 2.57(s, 2H), 1.76-1.83(m, 9H). HRMS(ESI) C17H22N402S에 대한 계산치 [M+H]+ 347.1536, 실측치 347.1523.
동일한 방법을 적용하여 다음의 화합물들을 제조하였다:
에틸 8-(메틸설파닐)-1-트리틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트[(VIII), R1 = Me-S-, R2 = 트리틸, A = -(CH2)2-]. 1H NMR(401 MHz, DMSO-d6) δ 7.19-7.35(m, 10H), 6.92-7.01(m, 6H), 4.22-4.31(m, 2H), 3.04(t, J=6.59 Hz, 1H), 2.55-2.60(m, 2H), 2.41(s, 3H), 1.22-1.30(m, 4H).
에틸 1-메틸-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트 [(VIII), R1 = Me-S-, R2 = 메틸, A = -(CH2)2-]. 1H NMR(401 MHz, DMSO-d6) δ 8.55(s, 1H), 4.33(s, 3H), 4.29(q, J=7.08 Hz, 2H), 2.97-3.04(m, J=1.10, 6.84 Hz, 2H), 2.88-2.95(m, 2H), 2.56(s, 3H), 1.31(t, J=7.08 Hz, 3H).
에틸 1-(2-하이드록시에틸)-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트[(VIII), R1 = Me-S-, R2 = 2-하이드록시에틸, A = -(CH2)2-]. LC/MS(254 ㎚) HPLC 방법 2 Rt 5.27 min. 1H NMR(401 MHz, DMSO-d6) δ 8.55(s, 1H), 4.87(br. s., 1H), 4.83(t, J=6.04 Hz, 2H), 4.30(q, J=7.08 Hz, 2H), 3.82(t, J=5.80 Hz, 2H), 2.97-3.06(m, 2H), 2.85-2.95(m, 2H), 2.55(s, 3H), 1.32(t, J=7.08 Hz, 3H). HRMS(ESI) C15H18N403S에 대한 계산치 [M+H]+ 335.1172, 실측치 335.1175.
제조예
E
에틸 1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트[(VIII), R1 = H, R2 = Me, A = -(CH2)2-]
단계 3c
20 ㎖의 무수 DMF 중의 0.5 g(1.80 mmol)의 에틸(6E)-6-[(디메틸아미노)메틸리덴]-1-메틸-7-옥소-4,5,6,7-테트라하이드로-1H-인다졸-3-카복실레이트의 용액에 746 ㎎(5.4 mmol)의 칼륨 카보네이트 및 510 ㎎(5.4 mmol)의 포름아미딘 아세테이트를 첨가하였다. 반응액을 100℃에서 8 시간 동안 교반하였다. 혼합물을 에틸 아세테이트로 희석하고, H2O로 세척하고, Na2S04 상에서 건조시키고, 여과하고, 증발시켰다. 잔류물을 디에틸 에테르와 함께 분쇄하여 표제 화합물 450 ㎎(95%)을 제공하였다. 1H NMR(401 MHz, DMSO-d6) δ 9.09(s, 1H), 8.74(s, 1H), 4.35(s, 3H), 4.31(q, J=7.08 Hz, 2H), 2.98-3.05(m, 4H), 1.33(t, J=7.08 Hz, 3H).
동일한 방법을 적용하여 다음의 화합물들을 제조하였다:
에틸 1-tert-부틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트[(VIII), R1 = H, R2 = tert-부틸, A = -(CH2)2-]. LC/MS(m/z): 301.1 [M+H]+, HPLC(254 ㎚) 방법 2 Rt 5.89 min. 1H NMR(500 MHz, DMSO-d6) δ 9.13(s, 1H), 8.75(s, 1H), 4.31(q, J=7.14 Hz, 2H), 2.95-3.06(m, 2H), 1.81(s, 9H), 2.85-2.95(m, 2H), 1.31(t, J=7.14 Hz, 3H). HRMS(ESI) C16H20N4O2에 대한 계산치 [M+H]+ 301.1659, 실측치 301.1663
포름아미딘 대신에 아세트아미딘을 사용하여 제조예 E에 기술된 바와 같이 제조하였다:
에틸 1,8-디메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트[(VIII), R1 = Me, R2 = Me, A = -(CH2)2-]. 1H NMR(401 MHz, DMSO-d6) δ 8.62(s, 1H), 4.36(s, 3H), 4.30(q, J=7.08 Hz, 2H), 2.91-3.05(m, 4H), 2.65(s, 3H), 1.32(t, J=7.08 Hz, 3H).
에틸 1-tert-부틸-8-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트 [(VIII), R1 = Me, R2 = tert-부틸, A = -(CH2)2-]. LC/MS(m/z): 315.3 [M+H]+, HPLC(254 ㎚) 방법 3 Rt 6.52 분.
제조예
F
에틸 1-tert-부틸-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트 [(VIII), R1 = Me-S-, R2 = t-부틸, A = -CH=CH-]
단계 4
클로로벤젠 중의 1.5 g(4.35 mmol)의 에틸 1-tert-부틸-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트 및 1.97 g(8.7 mmol)의 DDQ의 용액을 4 시간 동안 환류 하에 가열하였다. 휘발성 물질을 진공 중에서 제거하고, 잔류물을 에틸 아세테이트로 용해시키고, NaHCO3의 포화 수용액으로 세척하였다. 유기상을 Na2S04로 건조시키고, 여과하고, 농축시켰다. 조물질을 에틸 아세테이트 및 헥산(1:4)으로 용출시키는 실리카겔 칼럼 크로마토그래피에 의해서 정제하여 1.19 g(80%)의 표제 화합물을 수득하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 7.78 min. 1H NMR(401 MHz, DMSO-d6) δ 9.52(s, 1H), 8.18-8.43(m, 1H), 7.89(d, J=8.79 Hz, 1H), 4.24-4.61(m, 2H), 2.74(s, 3H), 2.00(s, 9H), 1.40(t, J=7.08 Hz, 3H). HRMS(ESI) C17H20N4O2S에 대한 계산치 [M+H]+ 345.1380, 실측치 345.1371.
상기 예에 기술된 것과 동일한 방법을 사용하여 이하의 유사체를 또한 합성하였다:
에틸 1-메틸-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트[(VIII), R1 = Me-S-, R2 = 메틸, A = -CH=CH-]. 1H NMR(401 MHz, DMSO-d6) 시프트(Shift) 9.49(s, 1H), 8.15(d, J=8.79 Hz, 1H), 7.82(d, J=8.79 Hz, 1H), 4.74(s, 3H), 4.44(q, J=7.20 Hz, 2H), 2.73(s, 3H), 1.40(t, J=7.14 Hz, 3H)
에틸 1-(2-하이드록시에틸)-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트 [(VIII), R1 = Me-S-, R2 = 2-하이드록시에틸, A = -CH=CH-]. LC/MS(254 ㎚) HPLC 방법 2 Rt 5.49 min. 1H NMR(401 MHz, DMSO-d6) δ 9.49(s, 1H), 8.17(d, J=8.67 Hz, 1H), 7.83(d, J=8.79 Hz, 1H), 5.24(t, J=5.92 Hz, 2H), 4.39-4.49(m, 2H), 3.98(t, J=5.80 Hz, 2H), 2.70(s, 3H), 1.41(t, J=7.14 Hz, 3H). HRMS(ESI) C15H16N403S에 대한 계산치 [M+H]+ 333.1016, 실측치 333.1017.
에틸 1-tert-부틸-8-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트[(VIII), R1 = Me-, R2 = tert-부틸, A = -CH=CH-]. LC/MS(m/z): 313.2 [M+H]+, HPLC(254 ㎚) 방법 2 Rt 6.79. 1H NMR(401 MHz, DMSO-d6) δ 9.62(s, 1H), 8.33(d, J=8.67 Hz, 1H), 7.92(d, J=8.79 Hz, 1H), 4.39-4.50(m, 2H), 2.92(s, 3H), 2.02(s, 9H), 1.41(t, J=7.08 Hz, 3H). HRMS(ESI) C17H20N4O2에 대한 계산치 [M+H]+ 313.1659, 실측치 313.1653.
에틸 1-tert-부틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트 [(VIII), R1 = H, R2 = tert-부틸, A = -CH=CH-]. LC/MS(m/z): 299.1 [M+H]+, HPLC(254 ㎚) 방법 2 Rt 6.36 min. 1H NMR(500 MHz, DMSO-d6) δ 9.75(s, 1H), 9.56(s, 1H), 8.44(d, J=8.79 Hz, 1H), 7.98(d, J=8.79 Hz, 1H), 4.46(q, J=7.14 Hz, 2H), 2.01(s, 9H), 1.41(t, J=7.00 Hz, 3H). HRMS(ESI) C16H18N402에 대한 계산치 [M+H]+ 299.1503, 실측치 299.1502
실시예 1: 1-(2-하이드록시에틸)-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-S-, R2= 2-하이드록시에틸, R3 = NH2, A = -CH=CH-](화합물 1)
단계 6a
메탄올 중의 7 N NH3 10 ㎖ 중의 1.2 g(3.61 mmol)의 에틸 1-(2-하이드록시에틸)-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트의 현탁액을 120℃에서 4 시간 동안 마이크로웨이브 조사에 적용하였다. 휘발성 물질을 진공 하에서 제거하고, 잔류물을 디에틸 에테르로 희석하고, 고체를 여과하여 0.6 g(55%)의 표제 화합물을 제공하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 4.29 min. 1H NMR(401 MHz, DMSO-d6) δ 9.46(s, 1H), 8.28(d, J=8.67 Hz, 1H), 7.84(s, 1H), 7.73(d, J=8.79 Hz, 1H), 7.52(br. s., 1H), 5.21(t, J=5.98 Hz, 2H), 4.82-4.96(m, J=0.61 Hz, 1H), 3.94-4.07(m, 2H), 2.70(s, 3H). HRMS(ESI) C13H13N502S에 대한 계산치 [M+H]+ 304.0863, 실측치 304.0857.
상기 실시예에 기술된 것과 동일한 방법을 사용하여 이하의 유사체들을 또한 합성하였다:
1-tert-부틸-8-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-, R2= tert-부틸, R3 = NH2, A = -CH=CH-](화합물 5) LC/MS(m/z): 284.1 [M+H]+, HPLC(254 ㎚) 방법 3 Rt 5.95 분.
1-tert-부틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R2= tert-부틸, R3 = NH2, A = -CH=CH-](화합물 3) LC/MS(m/z): 270.1 [M+H]+, HPLC(254 ㎚) 방법 3 Rt 4.55 분.
실시예 2: 1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 [(I), R1 = H, R2= Me, R3 = NH2, A = -(CH2)2-]
단계 6b1 및 단계 6b2
단계 a. 에탄올(30 ㎖) 및 300 ㎎(5.2 mmol)의 칼륨 하이드록사이드 중의 440 ㎎(1.74 mmol)의 에틸 1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트의 현탁액을 2 시간 동안 환류 하에 가열하였다. 휘발성 물질을 진공 하에서 제거하고, 잔류물을 에탄올(3 ㎖)로 희석하고, 고체를 여과하여 374 ㎎(80%)의 칼륨 1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트를 제공하였다.
단계 b. DMF(10 ㎖) 중의 200 ㎎(0.74 mmol)의 칼륨 1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트의 현탁액에 286 ㎎(1.49 mmol)의 EDCI, 1 ㎖(10 mmol)의 DIPEA, 및 300 ㎎(1.98 mmol)의 HOBt-NH4를 첨가하였다. 혼합물을 실온에서 18 시간 동안 교반하고, 이어서 용액을 DCM으로 희석하고, NaHCO3의 포화 수용액으로 세척하였다. 유기층을 Na2S04 상에서 건조시키고, 증발시켰다. 조물질을 사이클로헥산/EtOAc 4/1로 용출시키는 섬광 크로마토그래피에 의해서 정제하여 백색 고체로서 118 ㎎(70%)의 표제 화합물을 수득하였다. 1H NMR(401 MHz, DMSO-d6) δ 9.08(s, 1H), 8.73(s, 1H), 7.51(bs, 2H), 4.33(s, 3H), 3.05(m, 2H), 2.97(m, 2H).
상기 실시예에 기술된 것과 동일한 방법을 사용하여 이하의 유사체를 또한 합성하였다:
1-tert-부틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 [(I), R1 = H, R2= tert-부틸, R3 = NH2, A = -(CH2)2-](화합물 2) LC/MS(m/z): 272 [M+H]+, HPLC(254 ㎚) 방법 2 Rt 4.28 min. 1H NMR(500 MHz, DMSO-d6) 9.10(s, 1H), 8.73(s, 1H), 7.41(br. s., 1H), 7.31(br. s., 1H), 2.97-3.03(m, 2H), 2.83-2.91(m, 2H), 1.81(s, 9H). HRMS(ESI) C14H7N50에 대한 계산치 [M+H]+ 272.1506, 실측치 272.1514
실시예
3
1-(2-하이드록시에틸)-8-메톡시-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = R4 = Me, X = O, R2= 2-하이드록시에틸, R3 = NH2, A = -CH=CH-](화합물 6)
단계 3b, 단계 4, 단계 6a
에틸 1-(2-하이드록시에틸)-8-메톡시-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트의 제조(단계 3b)
50 ㎖의 무수 DMF 중의 15 g(49 mmol)의 에틸(6E)-6-[(디메틸아미노)메틸리덴]-1-(2-하이드록시에틸)-7-옥소-4,5,6,7-테트라하이드로-1H-인다졸-3-카복실레이트의 용액에 14.4 g(147 mmol)의 무수 칼륨 아세테이트 및 12.60 g(73.0 mmol)의 메틸이소우레아 설페이트를 첨가하였다. 반응액을 100℃에서 16 시간 동안 교반하였다. 혼합물을 에틸 아세테이트로 희석하고, H2O로 세척하고, Na2S04 상에서 건조시키고, 여과하고, 증발시켰다. 조물질을 칼럼(에틸 아세테이트:헥산 1:3)에 의해서 정제하여 1.2 g(10%)의 표제 화합물을 제공하였다. HRMS(ESI) C15H18N404에 대한 계산치 [M+H]+ 319.3278, 실측치 319.3256.
에틸 1-(2-하이드록시에틸)-8-메톡시-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트의 제조(단계 4)
톨루엔(20 ㎖) 중의 1.2 g(3.76 mmol)의 에틸 1-(2-하이드록시에틸)-8-메톡시-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트의 현탁액에 500 ㎎(2.2 mmol)의 4,5-디클로로-3,6-디옥소사이클로헥사-1,4-디엔-1,2-디카보니트릴을 첨가하였다. 혼합물을 밀봉된 바이알 내에서 3 시간 동안 100℃에서 마이크로웨이브 조사에 적용하였다. 휘발성 물질을 증발시키고, 조물질을 에틸 아세테이트로 용해시키고, 포화 NaHC03로 분배시키고, 유기층을 농축 건조시켰다. 잔류물을 크로마토그래피(에틸 아세테이트/헥산 7/3)에 의해서 정제하여 520 ㎎(46%)의 목적하는 화합물을 수득하였다. HRMS(ESI) C15H16N404에 대한 계산치 [M+H]+ 317.3119, 실측치 317.3126.
제조된 250 ㎎(0.79 mmol)의 에틸 1-(2-하이드록시에틸)-8-메톡시-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트를 메탄올 중의 7 M NH3 (8 ㎖)에 용해시켰다. 혼합물을 밀봉된 바이알 내에서 4 시간 동안 120℃에서 마이크로웨이브 조사에 적용하였다. 휘발성 물질을 증발시키고, 조물질을 크로마토그래피(용출제 DCM/MeOH 95/5)에 의해서 정제하여 136 ㎎(60%)의 목적하는 화합물을 수득하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 3.75 min. 1H NMR(401 MHz, DMSO-d6) δ 9.51(s, 1H), 8.20(d, J=8.67 Hz, 1H), 7.82(br. s., 1H), 7.74(d, J=8.79 Hz, 1H), 7.51(br. s., 1H), 5.19(t, J=5.92 Hz, 1H), 4.90(t, J=6.29 Hz, 3H), 4.12(s, 3H), 3.97-4.07(m, J=5.00 Hz, 2H). HRMS(ESI) C13H13N503에 대한 계산치 [M+H]+ 288.1091, 실측치 288.1086.
제조예
G
칼륨 1-tert-부틸-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트[(XI), R1 = Me-S-, R2= tert-부틸, A = -CH=CH-]
단계 6b1
에틸 1-tert-부틸-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트(300 ㎎, 0.87 mmol)를 2 ㎖의 무수 에탄올에 현탁시키고, 실온에서 2 시간 동안 에탄올 중의 칼륨 하이드록사이드의 1.5 M 용액(5 ㎖, 7.5 mmol)으로 처리하였다.생성된 침전을 여과에 의해 수거하여 회백색 고체로서 215 ㎎(70%)의 표제 화합물을 제공하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 4.79 min. 1H NMR(401 MHz, DMSO-d6) δ 9.38(s, 1H), 8.61(d, J=8.54 Hz, 1H), 7.58(d, J=8.67 Hz, 1H), 2.72(s, 3H), 1.95(s, 9H). HRMS(ESI) C15H16N402S에 대한 계산치 [M+H]+ 317.1067, 실측치 317.1052.
실시예
4
1-tert-부틸-N-메틸-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-S-, R2= tert-부틸, R' = Me, A = -CH=CH-](화합물 7)
단계 6b2
무수 N,N-디메틸포름아미드(2 ㎖) 중의 칼륨 1-tert-부틸-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트(50 ㎎, 0.142 mmol)의 현탁액을 N,N-디이소프로필에틸아민(100 ㎕, 0.71 mmol)의 존재 하에서, 2-(1H-벤조트리아졸-1-일)-1,1,3,3-테트라메틸우로늄 헥사플루오로포스페이트(HBTU)(82 ㎎, 0.255 mmol) 및 메틸아민 하이드로클로라이드(15 ㎎, 0.213 mmol)로 처리하였다. 반응액을 3 시간 동안 실온에서 교반하였다. 반응 혼합물을 에틸 아세테이트와 물 사이에 분배시키고, 유기층을 Na2SO4 상에서 건조시키고, 여과하고, 농축시켰다. 조생성물을 칼럼 크로마토그래피(EtOAc/헥산 7/3)에 의해서 정제하여 회백색 고체로서 20 ㎎(45%)의 표제 화합물을 제공하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 6.89 min. 1H NMR(401 MHz, DMSO-d6) δ 9.49(s, 1H), 8.42(d, J=8.67 Hz, 1H), 8.32(d, J=4.52 Hz, 1H), 7.80(d, J=8.67 Hz, 1H), 2.87(d, J=4.76 Hz, 3H), 2.74(s, 3H), 1.98-2.04(m, 9H). HRMS(ESI) C16H19N50S에 대한 계산치 [M+H]+ 330.1383, 실측치 330.1383.
유사한 방식으로 수행하여 이하의 화합물을 제조하였다:
1-tert-부틸-N-[2-(디메틸아미노)에틸]-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-S-, R2= tert-부틸, R' = 2-(디메틸아미노)에틸, A = -CH=CH-](화합물 8) LC/MS(254 ㎚) HPLC 방법 2 Rt 5.28 min. 1H NMR(401 MHz, DMSO-d6) δ 9.49(s, 1H), 8.43(d, J=8.67 Hz, 1H), 8.22(t, J=5.86 Hz, 1H), 7.81(d, J=8.67 Hz, 1H), 3.44(q, J=6.59 Hz, 2H), 2.74(s, 3H), 2.46(t, J=6.77 Hz, 2H), 2.21(s, 6H), 2.01(s, 9H). HRMS(ESI) C19H26N60S에 대한 계산치 [M+H]+ 387.1962, 실측치 387.1974.
1-tert-부틸-N-(2-하이드록시에틸)-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 [(I), R1 = Me-S-, R2= tert-부틸, R' = 2-하이드록시에틸, A = -CH=CH-](화합물 9) LC/MS(254 ㎚) HPLC 방법 2 Rt 6.07 min. 1H NMR(401 MHz, DMSO-d6) δ 9.49(s, 1H), 8.43(d, J=8.54 Hz, 1H), 8.22(t, J=5.92 Hz, 1H), 7.81(d, J=8.67 Hz, 1H), 4.80(t, J=5.43 Hz, 1H), 3.58(q, J=6.02 Hz, 2H), 3.43(q, J=6.27 Hz, 2H), 2.74(s, 3H), 2.01(s, 9H). HRMS(ESI) C17H21N502S에 대한 계산치 [M+H]+ 360.1489, 실측치 360.1495.
1-tert-부틸-N-(1-메틸피페리딘-4-일)-8-(메틸설파닐)-1H-피라졸로[4,3 -h]퀴나졸린-3-카복사미드 [R1= [(I), R1 = Me-S-, R2= tert-부틸, R' = 1-메틸피페리딘-4-일, A = -CH=CH-](화합물 10) LC/MS(254 ㎚) HPLC 방법 2 Rt 5.09 min. 1H NMR(401 MHz, DMSO-d6) δ 9.48(s, 1H), 8.40(d, J=8.67 Hz, 1H), 8.06(d, J=8.06 Hz, 1H), 7.80(d, J=8.79 Hz, 1H), 3.84(dd, J=3.30, 7.57 Hz, 1H), 2.74-2.83(m, 2H), 2.73(s, 3H), 2.18(s, 3H), 2.01(s, 9H), 1.94-1.99(m, 2H), 1.63-1.84(m, 4H). HRMS(ESI) C21H28N60S에 대한 계산치 [M+H]+ 413.2118, 실측치 413.2112.
1-tert-부틸-N-[2-(1H-이미다졸-5-일)에틸]-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[R1[(I), R1 = Me-S-, R2= tert-부틸, R' = 2-(1H-이미다졸-5-일)에틸, A = -CH=CH-](화합물 11) LC/MS(254 ㎚) HPLC 방법 2 Rt 5.49 min. 1H NMR(401 MHz, DMSO-d6) δ 9.49(s, 1H), 8.55(d, J=2.93 Hz, 1H), 8.43(d, J=8.67 Hz, 1H), 7.81(d, J=8.67 Hz, 1H), 7.57(d, J=0.98 Hz, 1H), 6.89(s, 1H), 3.51-3.64(m, 2H), 2.82(t, J=7.38 Hz, 2H), 2.70-2.76(m, 3H), 2.01(s, 9H). HRMS(ESI) C20H23N7OS에 대한 계산치 [M+H]+ 410.1758, 실측치 410.1751.
제조예
H
에틸 8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트 [(VIII), R1= Me-S-, R2 = H, A = -CH=CH-]
단계 5
에틸 1-tert-부틸-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트(800 ㎎, 2.32 mmol)를 트리플루오로아세트산(5 ㎖)으로 처리하였다. 생성된 혼합물을 70℃로 가열하고, 4 시간 동안 교반하였다. 휘발성 물질을 진공 중에서 제거한 후에, 잔류물을 DCM으로 용해시키고, 포화 NaHC03로 세척하고, Na2S04 상에서 건조시키고, 여과하고, 농축시켜 연황색 고체로서 표제 화합물(670 ㎎, >99%)을 수득하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 5.66 min. 1H NMR(401 MHz, DMSO-d6) δ 9.50(s, 1H), 8.14(d, J=8.67 Hz, 1H), 7.80(d, J=8.79 Hz, 1H), 4.41-4.47(m, 2H), 2.75(s, 3H), 1.41(t, J=7.14 Hz, 3H). HRMS(ESI) C13H12N402S에 대한 계산치 [M+H]+ 289.0754, 실측치 289.0752.
제조예
I
에틸 1-[2-(디메틸아미노)에틸]-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트[(VIIIa), R1 = Me-S-, R2 = 2-(디메틸아미노)에틸, A = -CH=CH-], 및
에틸 2-[2-(디메틸아미노)에틸]-8-(메틸설파닐)-2H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트[(VIIIb), R1 = Me-S-, R2 = 2-(디메틸아미노)에틸, A = -CH=CH-]
단계 5
무수 디메틸포름아미드(4 ㎖) 중의 에틸 8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트(150 ㎎, 0.52 mmol)의 용액에 세슘 카보네이트(339 ㎎, 1.04 mmol)를 첨가하고, 이어서 2-브로모-N,N-디메틸에탄아민(135 ㎎, 0.88 mmol)을 첨가하였다. 균질한 혼합물을 실온에서 24 시간 동안 교반하였다. 혼합물을 물로 처리하고, EtOAc로 추출하였다. 유기층을 염수로 세척하고, Na2S04 상에서 건조시키고, 농축시켰다. 조물질을 EtOAc/에탄올 85/15로 용출시키는 실리카겔 크로마토그래피에 의해서 정제하여 주이성체로서 에틸 1-[2-(디메틸아미노)에틸]-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트(60 ㎎, 32%) [1H NMR(401 MHz, DMSO-d6) δ 9.51(s, 1H), 8.16(d, J=8.67 Hz, 1H), 7.83(d, J=8.79 Hz, 1H), 5.29(t, J=6.59 Hz, 1H), 4.32-4.49(m, 2H), 2.94(br. s., 2H), 2.71(s, 3H), 2.24(br. s., 6H), 1.41(t, J=7.08 Hz, 3H)]; 및
부이성체로서 에틸 2-[2-(디메틸아미노)에틸]-8-(메틸설파닐)-2H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트(20 ㎎, 10%) [1H NMR(401 MHz, DMSO-d6) δ 9.39(s, 1H), 8.26(d, J=8.78 Hz, 1H), 7.87(d, J=8.78 Hz, 1H), 4.66(t, J=6.57 Hz, 1H), 4.45(q, J=7.06 Hz, 2H), 2.71(br. s., 3H), 2.67(s, 2H), 2.37(br. s., 6H), 1.46(t, J=7.08 Hz, 3H)]를 제공하였다.
실시예
5
1-[2-(디메틸아미노)에틸]-8-(메틸설파닐)-1H-피라졸로[4,3 -h]퀴나졸린-3-카복사미드[(I), R1 = Me-S-, R2= 2-(디i메틸아미노)에틸, R3 = NH2, A = -CH=CH-](화합물 12)
단계 6c
에틸 1-[2-(디메틸아미노)에틸]-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트(46 ㎎, 0.128 mmol)를 2 ㎖의 테트라하이드로푸란에 현탁시켰다. 암모늄 클로라이드(20 ㎎, 0.384 mmol), 및 THF 중의 1 N LiN(TMS)2(0.8 ㎖, 0.8 mmol)를 첨가하였다. 혼합물을 실온에서 1 시간 동안 교반하였다. 그 후, 용매를 증발 건조시키고,잔류물을 실리카겔 상에서 섬광 크로마토그래피(용출제: DCM/MeOH/NH4OH 95/5/0.1)에 의해서 정제하여 18 ㎎(42%)의 표제 화합물 및 2 ㎎의 부생성물 6-아미노-1-[2-(디메틸아미노)에틸]-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드를 제공하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 3.75 min. 1H NMR(401 MHz, DMSO-d6) δ 9.48(s, 1H), 8.27(d, J=8.67 Hz, 1H), 7.84(br. s., 1H), 7.74(d, J=8.67 Hz, 1H), 7.54(br. s., 1H), 5.25(t, J=6.71 Hz, 2H), 2.93(br. s., 2H), 2.71(s, 3H), 2.23(br. s., 6H). HRMS(ESI) C15H18N60S에 대한 계산치 [M+H]+ 331.1336, 실측치 331.1334.
6-아미노-1-[2-(디메틸아미노)에틸]-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 [R1= [(I), R1 = Me-S-, R2= 2-(디메틸아미노)에틸, R3 = NH2, R5= NH2, A = -CH=CH-](화합물 13)
LC/MS(254 ㎚) HPLC 방법 2 Rt 3.97 분. 1H NMR(401 MHz, DMSO-d6) δ 8.01(d, J=8.79 Hz, 1H), 7.88(br. s., 1H), 7.84(d, J=8.91 Hz, 1H), 7.74(br. s., 1H), 7.45(br. s., 1H), 5.22(t, J=5.61 Hz, 2H), 2.88(br. s., 2H), 2.58(s, 3H), 2.15-2.29(m, J=6.47 Hz, 6H). HRMS(ESI) C15H19N70S에 대한 계산치 [M+H]+ 346.1445, 실측치 346.1439.
실시예 6: 2-[2-(디메틸아미노)에틸]-8-(메틸설파닐)-2H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-S-, R2= 2-(디메틸아미노)에틸, R3 = NH2, A = -CH=CH-](화합물 14)
단계 6a
메탄올 중의 7 N NH3 4 ㎖ 중의 20 ㎎(0.055 mmol)의 에틸 2-[2-(디메틸아미노)에틸]-8-(메틸설파닐)-2H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트의 현탁액을 120℃에서 4 시간 동안 마이크로웨이브 조사에 적용하였다. 휘발성 물질을 진공 하에서 제거하고, 잔류물을 실리카겔 크로마토그래피(용출제 DCM/MeOH/NH3 97/3/1)에 의해서 정제하여 2.6 ㎎(15%)의 표제 화합물을 수득하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 3.13 min. 1H NMR(401 MHz, DMSO-d6) δ 9.34(s, 1H), 8.34(br. S., 1H), 8.04(br. S., 1H), 7.80(d, J=8.91 Hz, 1H), 7.59(d, J=9.03 Hz, 1H), 4.89(t, J=6.47 Hz, 2H), 2.80(t, J=6.41 Hz, 2H), 2.69(s, 3H), 2.18(s, 6H). HRMS(ESI) C15H18N60S에 대한 계산치 [M+H]+ 331.1336, 실측치 331.1331.
실시예 7: tert-부틸{2-[3-카바모일-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-1-일]에틸}카바메이트[(I), R1 = Me-S-, R2= N1-2-[(tert-부톡시카보닐)아미노]에틸, R3 = NH2, A = -CH=CH-], 및
tert-부틸{2-[3-카바모일-8-(메틸설파닐)-2H-피라졸로[4,3-h]퀴나졸린-2-일]에틸}카바메이트[(I), R1 = Me-S-, R2= N2-2-[(tert-부톡시카보닐)아미노]에틸, R3 = NH2, A = -CH=CH-]
무수 디메틸포름아미드(4 ㎖) 중의 에틸 8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트(200 ㎎, 0.69 mmol)의 용액에 세슘 카보네이트(337 ㎎, 1.03 mmol)에 이어서 tert-부틸(2-브로모에틸)카바메이트(186 ㎎, 0.83 mmol)를 첨가하였다. 균질한 혼합물을 실온에서 48 시간 동안 교반하였다. 혼합물을 물로 처리하고, EtOAc로 추출하였다. 유기층을 염수로 세척하고, Na2S04 상에서 건조시키고, 농축시켰다. 조물질을 EtOAc/에탄올 85/15로 용출시키는 실리카겔 크로마토그래피에 의해서 정제하여 2 가지 미분할된 위치이성체 에틸 1-{2-[(tert-부톡시카보닐)아미노]에틸}-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트 및 에틸 2-{2-[(tert-부톡시카보닐)아미노]에틸}-8-(메틸설파닐)-2H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트의 혼합물(282 ㎎, 95%)을 제공하였다.
수득된 2 개의 위치이성체의 혼합물을 메탄올 중의 7 N NH3 10 ㎖에 현탁시키고, 120℃에서 5 시간 동안 마이크로웨이브 조사에 적용하였다. 휘발성 물질을 진공 하에서 제거하고, 잔류물을 실리카겔 크로마토그래피(용출제 DCM/MeOH/NH3 97/3/1)에 의해서 정제하여 주이성체로서 145 ㎎(55%)의 tert-부틸{2-[3-카바모일-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-1-일]에틸}카바메이트 [LC/MS(254 ㎚) HPLC 방법 2 Rt 5.53 min. 1H NMR(401 MHz, DMSO-d6) δ 9.46(s, 1H), 8.27(d, J=8.79 Hz, 1H), 7.74(s, 2H), 7.54(br. S., 1H), 6.91(t, J=6.29 Hz, 1H), 5.21(t, J=5.86 Hz, 2H), 3.58(q, J=6.14 Hz, 2H), 2.71(s, 3H), 1.23(s, 9H). HRMS(ESI) C18H22N603S에 대한 계산치 [M+H]+ 403.1547, 실측치 403.1534; 및
부이성체로서 18 ㎎(7%)의 tert-부틸 {2-[3-카바모일-8-(메틸설파닐)-2H-피라졸로[4,3-h]퀴나졸린-2-일]에틸}카바메이트 [LC/MS(254 ㎚) HPLC 방법 2 Rt 5.08 min. 1H NMR(401 MHz, DMSO-d6) δ 9.33(s, 1H), 8.08(d, J=15.01 Hz, 2H), 7.84(d, J=8.91 Hz, 1H), 7.60(d, J=8.91 Hz, 1H), 6.95(t, J=6.71 Hz, 1H), 4.82(t, J=6.29 Hz, 2H), 3.49(q, J=6.51 Hz, 2H), 2.69(s, 3H), 1.28(s, 9H). HRMS(ESI) C18H22N603S에 대한 계산치 [M+H]+ 403.1547, 실측치 403.1552]를 수득하였다.
이 방법에 따라 수행함으로써, 이하의 화합물을 제조하였다:
tert-부틸 4-{[3-카바모일-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-1-일]메틸}피페리딘-1-카복실레이트 [(I), R1 = Me-S-, R2= N1-tert-부틸 4-메틸피페리딘-1-카복실레이트, R3 = NH2, A = -CH=CH-] LC/MS(254 ㎚) HPLC 방법 2 Rt 6.56 min. 1H NMR(401 MHz, DMSO-d6) δ 9.47(s, 1H), 8.28(d, J=8.79 Hz, 1H), 7.81(s, 1H), 7.74(d, J=8.67 Hz, 1H), 7.55(s, 1H), 5.07(d, J=7.57 Hz, 2H), 3.90(d, J=12.08 Hz, 2H), 2.69-2.70(m, 3H), 2.59-2.68(m, J=2.01, 3.72 Hz, 2H), 2.22-2.41(m, 1H), 1.41-1.51(m, J=6.10 Hz, 2H), 1.38(s, 9H), 1.22(dq, J=4.33, 12.31 Hz, 2H). HRMS(ESI) C22H28N603S에 대한 계산치 [M+H]+ 479.1836, 실측치 479.1849.
실시예 8: 1-(2-아미노에틸)-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드[(I), R1 = Me-S-, R2= N1 2-아미노에틸, R3 = NH2, A = -CH=CH-](화합물 15)
tert-부틸{2-[3-카바모일-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-1-일]에틸}카바메이트(40 ㎎, 0.1 mmol)를 1,4-디옥산 중의 4 M HCl 1 ㎖로 처리하였다. 생성된 혼합물을 실온에서 1 시간 동안 교반하였다. 휘발성 물질을 진공 중에서 제거하고, 수득된 잔류물을 디에틸 에테르와 함께 분쇄하고, 여과하고, Et20로 세척하고, 진공 중에서 건조시켜 백색 고체로서 32 ㎎(97%)의 표제 화합물을 제공하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 3.59 min. HCl염, 1H NMR(401 MHz, DMSO-d6) δ 9.50(s, 1H), 8.29(d, J=8.67 Hz, 1H), 8.12(br. s., 2H), 8.04(br. s., 1H), 7.78(d, J=8.67 Hz, 1H), 7.65(s, 1H), 5.32-5.58(m, 2H), 3.57-3.72(m, 2H), 2.72(s, 3H). HRMS(ESI) C13H14N60S에 대한 계산치 [M+H]+ 303.1023, 실측치 303.1021.
이 방법에 따라 수행하여 이하의 화합물들을 제조하였다:
2-(2-아미노에틸)-8-(메틸설파닐)-2H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드[(I), R1 = Me-S-, R2= N2 2-아미노에틸, R3 = NH2, A = -CH=CH-](화합물 16) LC/MS(254 ㎚) HPLC 방법 2 Rt 3.33 min. HCl 염, 1H NMR(401 MHz, DMSO-d6) δ 9.34-9.40(m, 1H), 7.93-8.29(m, 5H), 7.85-7.91(m, 1H), 7.66(d, J=9.03 Hz, 1H), 5.01(t, J=6.16 Hz, 2H), 3.43-3.53(m, 2H), 2.67-2.71(m, 3H). HRMS(ESI) C13H14N60S에 대한 계산치 [M+H]+ 303.1023, 실측치 303.1017;
8-(메틸설파닐)-1-(피페리딘-4-일메틸)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드[(I), R1 = Me-S-, N1 R2= 피페리딘-4-일메틸, R3 = NH2, A = -CH=CH-](화합물 17). LC/MS(254 ㎚) HPLC 방법 2 Rt 3.94 min. HCl 염, 1H NMR(401 MHz, DMSO-d6) δ 9.49(s, 1H), 8.62(br. s., 1H), 8.47(d, J=10.25 Hz, 1H), 8.29(d, J=8.67 Hz, 1H), 7.81(s, 1H), 7.76(d, J=8.67 Hz, 1H), 7.59(s, 1H), 5.13(d, J=7.32 Hz, 2H), 3.23(d, J=12.21 Hz, 2H), 2.81(q, J=11.76 Hz, 2H), 2.74(s, 3H), 2.36-2.48(m, 1H), 1.43-1.68(m, 4H). HRMS(ESI) C17H20N6OS에 대한 계산치 [M+H]+ 357.1492, 실측치 357.149; 및
8-(메틸설파닐)-2-(피페리딘-4-일메틸)-2H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드[(I), R1 = Me-S-, N2 R2= 피페리딘-4-일메틸, R3 = NH2, A = -CH=CH-](화합물 18). LC/MS(254 ㎚) HPLC 방법 2 Rt 3.7 min. HCl 염, 1H NMR(401 MHz, DMSO-d6) δ 9.36(s, 1H), 8.64(d, J=10.37 Hz, 1H), 7.94-8.39(m, 3H), 7.83(d, J=9.03 Hz, 1H), 7.62(d, J=9.03 Hz, 1H), 4.67-4.90(m, 2H), 2.78-2.94(m, 2H), 2.69(s, 3H), 2.34-2.43(m, 1H), 1.58-1.71(m, J=12.45 Hz, 2H), 1.41-1.56(m, 2H). HRMS(ESI) C17H20N6OS에 대한 계산치 [M+H]+ 357.1492, 실측치 357.1481.
실시예 9: 1-메틸-8-[4-(피페라진-1-일)페녹시]-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 4-(피페라진-1-일)페녹시, R2 = 메틸, R3 = NH2, A = -(CH2)2-](화합물 19)
전환 b
154 ㎎(0.5 mmol)의 1-메틸-8-(메틸설포닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드(WO 2004/104007A1에 기술된 바와 같이 제조) 및 107 ㎎(0.6 mmol)의 4-(피페라진-1-일)페놀을 70℃에서 2 시간 동안, Cs2C03(0.487 g, 1.5 mmol)의 존재 하에 5 ㎖의 무수 DMF 중에서 반응시켰다. 냉각시킨 후에, 반응액을 진공 하에서 건조시키고, 한 스푼의 실리카와 혼합시키고, 섬광 크로마토그래피(DCM/MeOH/MeOH 중의 7 N NH3 9/1/0.4%)에 의해서 용출시켜 목적하는 생성물을 제공하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 3.73 min. 1H NMR(401 MHz, DMSO-d6) δ 8.68(br. s., 2H), 8.49(s, 1H), 7.44(s, 1H), 7.29(s, 1H), 7.12-7.19(m, 2H), 7.03-7.08(m, 2H), 4.06(s, 3H), 3.20-3.39(m, 8H), 2.97-3.04(m, 2H), 2.85-2.92(m, 2H). HRMS(ESI) C21H23N702에 대한 계산치 [M+H]+ 406.1986, 실측치 406.19825.
유사한 방식으로 수행하여 이하의 화합물들을 제조하였다:
1-메틸-8-페녹시-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 페녹시, R2= 메틸, R3 = NH2, A = -(CH2)2-](화합물 20) LC/MS(254 ㎚) HPLC 방법 2 Rt 5.23 min. 1H NMR(401 MHz, DMSO-d6) δ 8.53(s, 1H), 7.42-7.49(m, 3H), 7.22-7.30(m, 4H), 3.99(s, 3H), 2.98-3.04(m, 2H), 2.85-2.93(m, 2H). HRMS(ESI) C17H15N502에 대한 계산치 [M+H]+ 322.1299, 실측치 322.1293;
8-(3-아미노페녹시)-1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 3-아미노페녹시, R2= 메틸, R3 = NH2, A = -(CH2)2-](화합물 21) LC/MS(254 ㎚) HPLC 방법 2 Rt 4.43 min. 1H NMR(401 MHz, DMSO-d6) δ 8.51(s, 1H), 7.45-7.51(m, 1H), 7.26(br. s., 1H), 7.04(t, J=7.99 Hz, 1H), 6.43(ddd, J=0.85, 2.08, 8.06 Hz, 1H), 6.38(t, J=2.14 Hz, 1H), 6.32(ddd, J=0.79, 2.23, 7.96 Hz, 1H), 5.21(br. s., 2H), 4.06(s, 3H), 2.98-3.04(m, 2H), 2.85-2.92(m, 2H). HRMS(ESI) C17H16N602에 대한 계산치 [M+H]+ 337.1408, 실측치 337.1411;
8-(4-아미노페녹시)-1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 4-아미노페녹시, R2= 메틸, R3 = NH2, A = -(CH2)2-](화합물 22) LC/MS(254 ㎚) HPLC 방법 2 Rt 4.23 min. δH NMR(401 MHz, DMSO-d6) 쉬프트 8.48(s, 1H), 7.47(s, 1H), 7.25(br. s., 1H), 6.84-6.94(m, 2H), 6.54-6.63(m, 2H), 4.99(s, 2H), 4.04(s, 3H), 2.95-3.04(m, 2H), 2.83-2.91(m, 2H). HRMS(ESI) C17H16N602에 대한 계산치 [M+H]+ 337.1408, 실측치 337.1405;
1-메틸-8-(피리딘-4-일옥시)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 피리딘-4-일옥시, R2= 메틸, R3 = NH2, A = -(CH2)2-](화합물 23) LC/MS(254 ㎚) HPLC 방법 2 Rt 3.68 min. 1H NMR(401 MHz, DMSO-d6) δ 8.81-8.86(m, 2H), 8.79(s, 1H), 7.53(s, 1H), 7.32(br. s., 1H), 6.30-6.36(m, 2H), 4.36(s, 3H), 3.04-3.11(m, 2H), 3.00(br. s., 2H). HRMS(ESI) C16H14N602에 대한 계산치 [M+H]+ 323.1251, 실측치 323.1238;
8-에톡시-1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 에틸, R2= 메틸, R3 = NH2, A = -(CH2)2-] LC/MS(254 ㎚) HPLC 방법 2 Rt 4.47 min. 1H NMR(401 MHz, DMSO-d6) δ 8.48(s, 1H), 7.45-7.48(m, 1H), 7.26(br. s., 1H), 4.39(q, J=7.04 Hz, 2H), 4.29(s, 3H), 2.95-3.03(m, 2H), 2.81-2.90(m, 2H), 1.36(t, J=7.02 Hz, 3H). HRMS(ESI) C13H15N502에 대한 계산치 [M+H]+ 274.1299, 실측치 274.1296;
1-메틸-8-(프로판-2-일옥시)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 프로판-2-일옥시, R2= 메틸, R3 = NH2, A = -(CH2)2-] LC/MS(254 ㎚) HPLC 방법 2 Rt 4.84 min. 1H NMR(401 MHz, DMSO-d6) δ 8.47(s, 1H), 7.47(br. s., 1H), 7.26(br. s., 1H), 5.21(quin, J=6.16 Hz, 1H), 4.28(s, 3H), 2.96-3.03(m, 2H), 2.80-2.89(m, 2H), 1.35(d, J=6.10 Hz, 6H). HRMS(ESI) C14H17N502에 대한 계산치 [M+H]+ 288.1455, 실측치 288.144;
1-메틸-8-(2-옥소프로폭시)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 2-옥소프로폭시, R2= 메틸, R3 = NH2, A = -(CH2)2-] LC/MS(254 ㎚) HPLC 방법 2 Rt 3.81 min. 1H NMR(401 MHz, DMSO-d6) δ 8.42-8.50(m, 1H), 7.49(s, 1H), 7.27(br. s., 1H), 5.07(s, 2H), 4.22(s, 3H), 2.96-3.04(m, 2H), 2.81-2.89(m, 2H), 2.14(s, 3H). HRMS(ESI) C14H15N503에 대한 계산치 [M+H]+ 302.1248, 실측치 302.1249; 및
8-(2-플루오로에톡시)-1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 2-플루오로에톡시, R2= 메틸, R3 = NH2, A = -(CH2)2-](화합물 24) LC/MS(254 ㎚) HPLC 방법 2 Rt 4.23 min. 1H NMR(401 MHz, DMSO-d6) δ 8.51(s, 1H), 7.41-7.59(m, 1H), 7.28(br. s., 1H), 4.80-4.88(m, 1H), 4.69-4.76(m, 1H), 4.61-4.67(m, 1H), 4.53-4.59(m, 1H), 4.29(s, 3H), 2.95-3.05(m, 2H), 2.83-2.92(m, 2H). HRMS(ESI) C13H14FN502에 대한 계산치 [M+H]+ 292.1205, 실측치 292.1209.
실시예 10: 1-메틸-8-[4-(4-메틸피페라진-1-일)페녹시]-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 4-(4-메틸피페라진-1-일)페녹시, R2 = 메틸, R3 = NH2, A = -(CH2)2-](화합물 25) 및
1-메틸-8-[4-(4-메틸피페라진-1-일)페녹시]-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 [(I), R1 = 4-(4-메틸피페라진-1-일)페녹시, R2 = 메틸, R3 = NH2, A = -CH=CH-](화합물 26)
전환b
400 ㎎(1.3 mmol)의 1-메틸-8-(메틸설포닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 및 360 ㎎(1.43 mmol)의 4-(4-메틸피페라진-1-일)페놀을 70℃에서 4 시간 동안 717 ㎎(5.2 mmol)의 K2C03의 존재 하에 25 ㎖의 무수 DMF 중에서 반응시켰다. 냉각시킨 후에, 반응액을 진공 하에서 건조시키고, 한 스푼의 실리카와 혼합시키고, 섬광 크로마토그래피(DCM/MeOH/MeOH 중의 7 N NH3 9/1/0.4%)에 의해서 용출시켜 두 가지 화합물의 1:1 혼합물을 제공하였다. 그 후에, 각각의 생성물을 분취용 HPLC 방법 2에 의해서 분리시켰다:
1-메틸-8-[4-(4-메틸피페라진-1-일)페녹시]-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드. LC/MS(254 ㎚) HPLC 방법 2 Rt 3.88 min. 1H NMR(401 MHz, DMSO-d6) δ 8.46(s, 1H), 7.44(s, 1H), 7.24(s, 1H), 7.01-7.09(m, 2H), 6.91-6.98(m, 2H), 4.02(s, 3H), 3.06-3.11(m, 4H), 2.94-3.01(m, 2H), 2.81-2.88(m, 2H), 2.42-2.45(m, 4H), 2.20(s, 3H). HRMS(ESI) C22H25N702에 대한 계산치 [M+H]+ 420.2143, 실측치 420.2148; 및
1-메틸-8-[4-(4-메틸피페라진-1-일)페녹시]-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드. LC/MS(254 ㎚) HPLC 방법 2 Rt 4.03 min. 1H NMR(401 MHz, DMSO-d6) δ 9.56(s, 1H), 8.21(d, J=8.67 Hz, 1H), 7.83(s, 1H), 7.76(d, J =8.91Hz, 1H), 7.49(s, 1H), 7.18-7.24(m, 1H), 6.99-7.07(m, 2H), 4.35(s, 3H), 3.12-3.19(m, 4H), 2.45-2.49(m, 4H), 2.22-2.26(m, 3H). HRMS(ESI) C22H23N702에 대한 계산치 [M+H]+ 418.1986, 실측치 418.1985.
동일한 방법에 따라 적합한 출발물질을 사용하여 다음의 화합물들을 제조하였다:
1-메틸-8-[4-(피페라진-1-일)페녹시]-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 트리플루오로아세테이트[(I), R1 = 4-(4-메틸피페라진-1-일)페녹시, R2= 메틸, R3 = NH2, A = -(CH2)2-](화합물 27). LC/MS(254) HPLC 방법 2 Rt 3.91 min. 1H NMR(401 MHz, DMSO-d6) δ 9.57(s, 1H), 8.70(br. s., 2H), 8.23(d, J=8.67 Hz, 1H), 7.79(br. s., 1H), 7.77(d, J=8.79 Hz, 2H), 7.52(s, 1H), 7.25-7.31(m, 2H), 7.09-7.14(m, 2H), 4.36(s, 3H), 3.25-3.40(m, 8H). HRMS(ESI) C21H21N704에 대한 계산치 [M+H]+ 404.183, 실측치 404.1836;
8-[2-브로모-4-(4-메틸피페라진-1-일)페녹시]-1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 트리플루오로아세테이트 [(I), R1 = 2-브로모-4-(4-메틸피페라진-1-일)페녹시, R2= 메틸, R3 = NH2, A = -(CH2)2-](화합물 28). LC/MS(254 ㎚) HPLC 방법 2 Rt 4.35 min. TFA 염, 1H NMR(401 MHz, DMSO-d6) δ 8.52(s, 1H), 7.57(d, J=2.07 Hz, 1H), 7.47(s, 1H), 7.28(br. s., 1H), 7.20-7.27(m, 2H), 4.06(s, 3H), 2.94-3.04(m, 6H), 2.84-2.94(m, 2H), 2.54(br. s., 4H), 2.26(s, 3H). HRMS(ESI) C22H24BrN702에 대한 계산치 [M+H]+ 498.1248, 실측치 498.1239;
8-[2-브로모-4-(4-메틸피페라진-1-일)페녹시]-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 트리플루오로아세테이트 [(I), R1 = 2-브로모-4-(4-메틸피페라진-1-일)페녹시, R2= 메틸, R3 = NH2, A = -CH=CH-](화합물 29). LC/MS(254 ㎚) HPLC 방법 2 Rt 4.55 min. TFA 염, 1H NMR(401 MHz, DMSO-d6) δ 9.59(s, 1H), 8.24(d, J=8.67 Hz, 1H), 7.83(s, 1H), 7.78(d, J=8.91 Hz, 1H), 7.73(d, J=2.69 Hz, 1H), 7.51(s, 1H), 7.35-7.42(m, 1H), 7.26-7.32(m, 1H), 4.36(s, 2H), 2.95-3.08(m, 2H), 2.54-2.61(m, 2H), 2.29(br. s., 2H). HRMS(ESI) C22H22BrN702에 대한 계산치 [M+H]+ 496.1091, 실측치 496.1082;
1-메틸-8-[3-(피페라진-1-일)페녹시]-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 [(I), R1 = 3-(피페라진-1-일)페녹시, R2= 메틸, R3 = NH2, A = -(CH2)2-](화합물 30). LC/MS(254 ㎚) HPLC 방법 2 Rt 3.9 min. 1H NMR(401 MHz, DMSO-d6) δ 8.51(s, 1H), 7.47(br. s., 1H), 7.26-7.28(m, 1H), 7.17-7.28(m, 1H), 6.77-6.83(m, J=1.22, 1.22, 8.42 Hz, 1H), 6.75(t, J=2.26 Hz, 1H), 6.55-6.63(m, 1H), 4.03(s, 3H), 3.05(dd, J=4.09, 5.92 Hz, 4H), 2.97-3.03(m, 2H), 2.89(s, 1H), 2.86-2.93(m, 2H), 2.77-2.84(m, J=4.09, 5.92 Hz, 4H). HRMS(ESI) C21H23N702에 대한 계산치 [M+H]+ 406.1986, 실측치 406.1980;
1-메틸-8-[3-(피페라진-1-일)페녹시]-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 트리플루오로아세테이트[(I), R1 = 3-(피페라진-1-일)페녹시, R2= 메틸, R3 = NH2, A = -CH=CH-](화합물 31). LC/MS(254 ㎚) HPLC 방법 2 Rt 4.1 min. TFA 염, 1H NMR(401 MHz, DMSO-d6) δ 9.59(s, 1H), 8.65(br. s., 2H), 8.24(d, J=8.67 Hz, 1H), 7.79(d, J=8.79 Hz, 2H), 7.51-7.54(m, 1H), 7.38(t, J=8.12 Hz, 1H), 7.01(t, J=2.20 Hz, 1H), 6.96(d, J=2.44 Hz, 1H), 6.86(dd, J=1.59, 7.93 Hz, 1H), 4.34(s, 3H), 3.36-3.41(m, 4H), 3.22(br. s., 4H). HRMS(ESI) C21H21N702에 대한 계산치 [M+H]+ 404.183, 실측치 404.1835;
8-[3-(디메틸아미노)페녹시]-1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 3-(디메틸아미노)페녹시, R2= 메틸, R3 = NH2, A = -(CH2)2-]. LC/MS(254 ㎚) HPLC 방법 2 Rt 5.53 min. 1H NMR(401 MHz, DMSO-d6) δ 8.51(s, 1H), 7.47(br. s., 1H), 7.26(br. s., 1H), 7.22(t, J=8.18 Hz, 1H), 6.62(dd, J=2.08, 8.30 Hz, 1H), 6.57(t, J=2.20 Hz, 1H), 6.51(dd, J=1.77, 7.87 Hz, 1H), 4.05(s, 3H), 2.98-3.04(m, 2H), 2.85-2.94(m, 8H). HRMS(ESI) C19H20N6O2에 대한 계산치 [M+H]+ 365.1721, 실측치 365.171;
8-[3-(디메틸아미노)페녹시]-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 3-(디메틸아미노)페녹시, R2= 메틸, R3 = NH2, A = -CH=CH-](화합물 32). LC/MS(254 ㎚) HPLC 방법 2 Rt 5.8 min. 1H NMR(401 MHz, DMSO-d6) δ 9.57(s, 1H), 8.22(d, J=8.79 Hz, 1H), 7.83(br. s., 1H), 7.77(d, J=8.91 Hz, 1H), 7.45-7.52(m, 1H), 7.25-7.30(m, 1H), 6.60-6.74(m, 3H), 4.35(s, 3H), 2.92(s, 6H). HRMS(ESI) C19H18N602에 대한 계산치 [M+H]+ 363.1564, 실측치 363.1574;
8-(2-클로로페녹시)-1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 2-클로로페녹시, R2= 메틸, R3 = NH2, A = -(CH2)2-]. LC/MS(254 ㎚) HPLC 방법 2 Rt 5.55 min. 1H NMR(401 MHz, DMSO-d6) δ 8.55(s, 1H), 7.62(dd, J=0.92, 7.99 Hz, 1H), 7.48(d, J=2.81 Hz, 1H), 7.40-7.46(m, 2H), 7.33(ddd, J=2.75, 6.26, 7.96 Hz, 1H), 7.27(br. s., 1H), 3.95(s, 3H), 2.98-3.07(m, 2H), 2.86-2.94(m, J=7.93 Hz, 2H). HRMS(ESI) C17H14C1N502에 대한 계산치 [M+H]+ 356.0909, 실측치 356.0898;
8-(2-클로로페녹시)-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 [(I), R1 = 2-클로로페녹시, R2= 메틸, R3 = NH2, A = -CH=CH-](화합물 33). LC/MS(254 ㎚) HPLC 방법 2 Rt 5.81 min. 1H NMR(401 MHz, DMSO-d6) δ 9.63(s, 1H), 8.25(d, J=8.79 Hz, 1H), 7.85(br. s., 1H), 7.80(d, J=8.79 Hz, 1H), 7.68(dd, J=1.46, 7.93 Hz, 1H), 7.55(dt, J=1.53, 8.15 Hz, 1H), 7.46-7.53(m, 2H), 7.34-7.43(m, 1H), 4.23(s, 3H). HRMS(ESI) C17H12C1N502에 대한 계산치 [M+H]+ 354.0753, 실측치 354.0746;
8-(2-플루오로페녹시)-1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 2-플루오로페녹시, R2= 메틸, R3 = NH2, A = -(CH2)2-]. LC/MS(254 ㎚) HPLC 방법 2 Rt 5.33 min. 1H NMR(401 MHz, DMSO-d6) δ 8.55(s, 1H), 7.48(br. s., 1H), 7.28-7.46(m, 4H), 7.26-7.28(m, 1H), 3.97(s, 3H), 2.97-3.05(m, 2H), 2.87-2.94(m, 2H). HRMS(ESI) C17H14FN502에 대한 계산치 [M+H]+ 340.1205, 실측치 340.1208;
8-(2-플루오로페녹시)-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 2-플루오로페녹시, R2= 메틸, R3 = NH2, A = -CH=CH-](화합물 34). LC/MS(254 ㎚) HPLC 방법 2 Rt 5.58 min. 1H NMR(401 MHz, DMSO-d6) δ 9.63(s, 1H), 8.26(d, J=8.79 Hz, 1H), 7.85(s, 1H), 7.80(d, J=8.79 Hz, 1H), 7.55(dt, J=1.89, 7.90 Hz, 1H), 7.50(br. s., 1H), 7.44-7.49(m, 1H), 7.38-7.44(m, J=2.14, 4.64, 6.68, 6.68 Hz, 1H), 7.31-7.38(m, 1H), 4.26(s, 3H). HRMS(ESI) C17H12FN502에 대한 계산치 [M+H]+ 338.1048, 실측치 338.1037;
8-[2-플루오로-4-(4-메틸피페라진-1-일)페녹시]-1-메틸-4,5-디하이드로- 1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 트리플루오로아세테이트[(I), R1 = 2-플루오로-4-(4-메틸피페라진-1-일)페녹시, R2= 메틸, R3 = NH2, A = -(CH2)2-](화합물 35). LC/MS(254 ㎚) HPLC 방법 2 Rt 4.06 min. 1H NMR(401 MHz, DMSO-d6) δ 9.65(br. s., 1H), 8.50(s, 1H), 7.45(s, 1H), 7.23-7.34(m, J=9.09, 9.09 Hz, 2H), 7.07(dd, J=2.81, 13.79 Hz, 1H), 6.87(dd, J=2.08, 9.03 Hz, 1H), 4.07(s, 3H), 3.78-3.98(m, J=13.79 Hz, 2H), 3.46-3.59(m, 2H), 3.08-3.23(m, 2H), 2.94-3.07(m, 4H), 2.84-2.94(m, 5H). HRMS(ESI) C22H24FN702에 대한 계산치 [M+H]+ 438.2049, 실측치 438.2039;
8-[2-플루오로-4-(4-메틸피페라진-1-일)페녹시]-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 트리플루오로아세테이트[(I), R1 = 2-플루오로-4-(4-메틸피페라진-1-일)페녹시, R2= 메틸, R3 = NH2, A = -CH=CH-](화합물 36). LC/MS(254 ㎚) HPLC 방법 2 Rt 4.25 min. 1H NMR(401 MHz, DMSO-d6) δ 9.68(br. s., 1H), 9.56-9.61(m, 1H), 8.25(d, J=8.67 Hz, 1H), 7.79(d, J=8.91 Hz, 2H), 7.53(s, 1H), 7.41(t, J=9.09 Hz, 1H), 7.14(dd, J=2.81, 13.79 Hz, 1H), 6.93(dd, J=2.26, 8.97 Hz, 1H), 4.37(s, 3H), 3.79-4.05(m, J=8.79 Hz, 2H), 3.47-3.61(m, 2H), 3.17(br. s., 2H), 3.03(br. s., 2H), 2.88(s, 3H). HRMS(ESI) C22H22FN702에 대한 계산치 [M+H]+ 436.1892, 실측치 436.1875;
8-[2-아세틸-4-(4-메틸피페라진-1-일)페녹시]-1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 트리플루오로아세테이트[(I), R1 = 2-아세틸-4-(4-메틸피페라진-1-일)페녹시, R2= 메틸, R3 = NH2, A = -(CH2)2-]. LC/MS(254 ㎚) HPLC 방법 2 Rt 3.83 min. 1H NMR(401 MHz, DMSO-d6) δ 9.57(br. s., 1H), 8.48(s, 1H), 7.44(s, 1H), 7.36(d, J=2.93 Hz, 1H), 7.27-7.32(m, 2H), 7.23-7.27(m, 1H), 4.03(s, 3H), 3.84-3.96(m, J=12.45 Hz, 2H), 3.48-3.61(m, J=11.23 Hz, 2H), 2.98-3.06(m, J=7.32 Hz, 4H), 2.85-2.92(m, 5H), 2.45(s, 3H). HRMS(ESI) C24H27N703에 대한 계산치 [M+H]+ 462.2248, 실측치 462.2229;
8-[2-아세틸-4-(4-메틸피페라진-1-일)페녹시]-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 트리플루오로아세테이트[(I), R1 = 2-아세틸-4-(4-메틸피페라진-1-일)페녹시, R2= 메틸, R3 = NH2, A = -CH=CH-](화합물 37). LC/MS(254 ㎚) HPLC 방법 2 Rt 3.99 min. 1H NMR(401 MHz, DMSO-d6) δ 9.60(br. s., 1H), 9.57(s, 1H), 8.24(d, J=8.79 Hz, 1H), 7.78(d, J=8.79 Hz, 2H), 7.53(s, 1H), 7.42(d, J=2.93 Hz, 1H), 7.36-7.40(m, 2H), 4.32(s, 3H), 3.88-4.04(m, J=15.01 Hz, 2H), 3.47-3.65(m, J=11.47 Hz, 2H), 2.96-3.12(m, 2H), 2.90(br. s., 3H), 2.46(s, 3H). HRMS(ESI) C24H25N703에 대한 계산치 [M+H]+ 460.2092, 실측치 460.207;
8-[2-아세틸-4-(피페라진-1-일)페녹시]-1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 트리플루오로아세테이트[(I), R1 = 2-아세틸-4-(피페라진-1-일)페녹시)페녹시, R2= 메틸, R3 = NH2, A = -(CH2)2-]. LC/MS(254 ㎚) HPLC 방법 2 Rt 3.75 min. 1H NMR(401 MHz, DMSO-d6) δ 8.72(d, J=5.37 Hz, 2H), 8.49(s, 1H), 7.44(s, 1H), 7.35(d, J=2.93 Hz, 1H), 7.26-7.32(m, 2H), 7.22-7.26(m, 1H), 4.02(s, 3H), 3.37-3.42(m, 4H), 3.28(br. s., 4H), 2.98-3.04(m, 2H), 2.85-2.92(m, 2H), 2.41-2.46(m, 3H). HRMS(ESI) C23H25N703에 대한 계산치 [M+H]+ 448.2092, 실측치 448.2071;
8-[2-아세틸-4-(피페라진-1-일)페녹시]-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 트리플루오로아세테이트[(I), R1 = 2-아세틸-4-(피페라진-1-일)페녹시, R2= 메틸, R3 = NH2, A = -CH=CH-](화합물 38). LC/MS(254 ㎚) HPLC 방법 2 Rt 3.9 min. 1H NMR(401 MHz, DMSO-d6) δ 9.57(s, 1H), 8.74(br. s., 2H), 8.23(d, J=8.67 Hz, 1H), 7.78(d, J=8.91 Hz, 2H), 7.51-7.54(m, 1H), 7.42(d, J=2.69 Hz, 1H), 7.37-7.40(m, 1H), 7.32-7.37(m, 1H), 4.31(s, 3H), 3.41-3.45(m, 4H), 3.30(d, J=5.13 Hz, 4H), 2.45-2.47(m, 3H). HRMS(ESI) C23H23N703에 대한 계산치 [M+H]+ 446.1935, 실측치 446.1927;
8-[2-시아노-4-(4-메틸피페라진-1-일)페녹시]-1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 트리플루오로아세테이트[(I), R1 = 2-시아노-4-(4-메틸피페라진-1-일, R2= 메틸, R3 = NH2, A = -(CH2)2-]. LC/MS(254 ㎚) HPLC 방법 2 Rt 4.7 min. 1H NMR(401 MHz, DMSO-d6) δ 9.69(br. s., 1H), 8.54(s, 1H), 7.53-7.56(m, 1H), 7.47(br. s., 1H), 7.42-7.44(m, 1H), 7.31(s, 1H), 4.08(s, 3H), 3.00-3.05(m, 2H), 2.89-2.95(m, J=7.81 Hz, 2H), 2.87(s, 3H). HRMS(ESI) C23H24N802에 대한 계산치 [M+H]+ 445.2095, 실측치 445.2090; 및
8-[2-시아노-4-(4-메틸피페라진-1-일)페녹시]-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 트리플루오로아세테이트[(I), R1 = 2-시아노-4-(4-메틸피페라진-1-일, R2= 메틸, R3 = NH2, A = -CH=CH-](화합물 39). LC/MS(254 ㎚) HPLC 방법 2 Rt 4.1 min. 1H NMR(401 MHz, DMSO-d6) 쉬프트 9.71(br. s., 1H), 9.63(s, 1H), 8.29(d, J=8.79 Hz, 1H), 7.75-7.87(m, 2H), 7.60(d, J=2.93 Hz, 1H), 7.55-7.59(m, 1H), 7.54(br. s., 1H), 7.45-7.52(m, 1H), 4.37(s, 3H), 3.89-4.05(m, J=13.79 Hz, 2H), 3.50-3.61(m, J=14.28 Hz, 2H), 3.19(br. s., 2H), 3.03-3.13(m, J=13.43 Hz, 2H), 2.88(s, 3H). HRMS(ESI) C23H22N802에 대한 계산치 [M+H]+ 443.1939, 실측치 443.1938.
실시예 11: 8-(2-아세틸페녹시)-1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드, 및
8-[2-(2-하이드록시페닐)-2-옥소에틸]-1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드
전환 b
약 15 ㎖의 NMP 중의 307 ㎎(1 mmol)의 1-메틸-8-(메틸설포닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드, 322 ㎎(1.5 mmoles)의 2-하이드록시아세토페논, 975 ㎎(3.0 mmoles)의 세슘 카보네이트의 용액을 95℃에서 1 시간 동안 가열하였다. 출발물질의 소실 후에, 반응액을 냉각시키고, 물 및 에틸 아세테이트로 추출하였다. 형성된 침전물을 여과에 의해서 분리시키고, 분취용 역상 HPLC에 의해서 회수하여 다음의 2 가지 화합물을 유도하였다:
8-(2-아세틸페녹시)-1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 2-아세틸페녹시, R2= 메틸, R3 = NH2, A = -(CH2)2-]. LC/MS(254 ㎚) HPLC 방법 2 Rt 5.0 min. 1H NMR(401 MHz, DMSO-d6) δ 8.52(s, 1H), 7.87(dd, J=1.71, 7.81 Hz, 1H), 7.67(ddd, J=1.71, 7.45, 8.06 Hz, 1H), 7.48(br. s., 1H), 7.41(dt, J=1.10, 7.57 Hz, 1H), 7.35(dd, J=0.85, 8.18 Hz, 1H), 7.26(br. s., 1H), 3.94(s, 3H), 2.96-3.06(m, 2H), 2.89(t, J=7.90 Hz, 2H), 2.46(s, 3H). HRMS(ESI) C19H17N503에 대한 계산치 [M+H]+ 364.1404, 실측치 364.1406; 및
8-[2-(2-하이드록시페닐)-2-옥소에틸]-1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 2-아세틸페녹시, R2= 메틸, R3 = NH2, A = -(CH2)2-]. LC/MS(254 ㎚) HPLC 방법 2 Rt 4.12 min. 1H NMR(500 MHz, DMSO-d6) δ 11.62(s, 1H), 8.66(s, 1H), 7.92-7.97(m, 1H), 7.52(s, 1H), 7.48(br. s., 1H), 7.27(br. s., 1H), 6.98(d, J=7.48 Hz, 1H), 6.94-6.97(m, 1H), 4.70(s, 2H), 4.11(s, 3H), 2.97-3.06(m, 2H), 2.89-2.95(m, 2H). HRMS(ESI) C19H17N503에 대한 계산치 [M+H]+ 363.3770, 실측치 363.3774.
실시예 12: 8-시아노-1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = CN, R2 = Me, R3 = NH2, A = -(CH2)2-](화합물 40)
전환 d
136 ㎎(0.44 mmol)의 1-메틸-8-(메틸설포닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드를 약 8 ㎖의 DMF에 용해시키고, 116 ㎎(1.77 mmol)의 칼륨 시아나이드의 존재 하에 70℃에서 가열하였다. 30 분 후에, 출발물질이 소실되었으며, 이렇게 하여 반응액을 냉각시키고, 물 및 에틸 아세테이트로 추출하였다. 유기상을 Na2S04 상에서 건조시키고, 증발시키고, 무수 에탄올에 현탁시키고, 65℃에서 2 시간 동안 교반하였다. 생성물을 여과에 의해서 35 ㎎(31%)의 황색 분말로서 분리시켰다. LC/MS(254 ㎚) HPLC 방법 2 Rt 3.67 min. 1H NMR(401 MHz, DMSO-d6) δ 8.89(s, 1H), 7.56(br. s., 1H), 7.33(br. s., 1H), 4.28(s, 3H), 3.06(s, 4H). HRMS(ESI) C12H10N6O에 대한 계산치 [M+H]+ 255.0989, 실측치 255.0978.
실시예 13: 1-메틸-8-(1H-피라졸-1-일)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 [(I), R1 = 1H-피라졸-1-일, R2 = Me, R3 = NH2, A = -(CH2)2-](화합물 41)
전환 c
DMSO(3 ㎖) 중의 100 ㎎(0.32 mmol)의 1-메틸-8-(메틸설포닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드의 용액에 44 ㎎(0.65 mmol)의 피라졸 및 134.9 ㎎(0.976 mmol)의 K2CO3을 첨가하였다. 혼합물을 70℃에서 4 시간 동안 교반하였다. 반응은 물을 첨가함으로써 진행시키고, 침전을 여과하여 물로 세척하였다. 고체를 뜨거운 에탄올로 세척하고, 여과하여 65 ㎎(67%)의 표제 화합물을 수득하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 3.38 min. 1H NMR(401 MHz, DMSO-d6) δ 8.74(s, 1H), 8.69(d, J=2.44 Hz, 1H), 7.88(d, J=0.85 Hz, 1H), 7.51(br. s., 1H), 7.31(br. s., 1H), 6.62(dd, J=1.59, 2.56 Hz, 1H), 4.40(s, 3H), 3.06(d, J=6.96 Hz, 2H), 2.97-3.02(m, 2H). HRMS(ESI) C14H13N70에 대한 계산치 [M+H]+ 296.1255, 실측치 296.1261.
유사한 방법에 따라서 적합한 출발물질을 사용하여 다음의 화합물들을 제조하였다:
1-메틸-8-[3-(트리플루오로메틸)-1H-피라졸-1-일]-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 3-(트리플루오로메틸)-1H-피라졸-1-일, R2 = Me, R3 = NH2, A = -(CH2)2-](화합물 42). LC/MS(254 ㎚) HPLC 방법 2 Rt 4.7 min. 1H NMR(401 MHz, DMSO-d6) δ 8.91(dd, J=0.98, 2.69 Hz, 1H), 8.82(s, 1H), 7.54(br. s., 1H), 7.32(br. s., 1H), 7.10(d, J=2.56 Hz, 1H), 4.38-4.40(m, 3H), 2.96-3.15(m, 4H). HRMS(ESI) C15H12F3N70에 대한 계산치 [M+H]+ 364.1128, 실측치 364.1134;
8-(1H-이미다졸-1-일)-1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 1H-이미다졸-1-일, R2 = Me, R3 = NH2, A = -(CH2)2-](화합물 43). LC/MS(254 ㎚) HPLC 방법 2 Rt 3.33 min. 1H NMR(401 MHz, DMSO-d6) δ 8.74(s, 1H), 8.64(t, J=0.98 Hz, 1H), 7.99(t, J=1.34 Hz, 1H), 7.52(br. s., 1H), 7.31(br. s., 1H), 7.10-7.21(m, 1H), 4.34-4.38(m, 3H), 3.03-3.10(m, 2H), 2.94-3.02(m, 2H). HRMS(ESI) C14H13N70에 대한 계산치 [M+H]+ 296.1255, 실측치 296.1249; 및
1-메틸-8-(4-니트로-1H-이미다졸-1-일)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 4-니트로-1H-이미다졸-1-일, R2 = Me, R3 = NH2, A = -(CH2)2-](화합물 44). LC/MS(254 ㎚) HPLC 방법 2 Rt 3.82 min. 1H NMR(401 MHz, DMSO-d6) δ 8.93(d, J=1.46 Hz, 1H), 8.84(s, 1H), 8.81(d, J=1.46 Hz, 1H), 7.51-7.61(m, 1H), 7.20-7.41(m, 1H), 4.39(s, 3H), 3.06(dd, J=6.23, 12.94 Hz, 4H). HRMS(ESI) C14H12N803에 대한 계산치 [M+H]+ 341.1105, 실측치 341.1103.
실시예 14: 1-메틸-8-(메틸설포닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R4 = Me, X= S02-, R2= Me, R3 = NH2, A = -CH=CH-]
전환 a
0.2 g(0.74 mmol)의 1-메틸-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드를 10 ㎖의 DCM에 현탁시키고, 0.52 g(3.04 mmol)의 MCPBA와 3 시간 동안 반응시켰다. 물 및 NaHC03를 첨가하고, 고체를 분리시키고, 여과하고, NaHC03의 포화 수용액으로 세척하여 180 ㎎(80%)의 백색 화합물을 수득하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 3.72 min. 1H NMR(401 MHz, DMSO-d6) δ 9.97(s, 1H), 8.60(d, J=8.67 Hz, 1H), 7.99(d, J=8.79 Hz, 2H), 7.63(br. s., 1H), 4.72(s, 3H), 3.61(s, 3H). HRMS(ESI) C12H11N503S에 대한 계산치 [M+H]+ 306.0656, 실측치 306.0645
유사한 방식으로 수행하여 다음의 화합물들을 제조하였다:
1-(2-하이드록시에틸)-8-(메틸설포닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R4 = Me, X= SO2-, R2= 2-하이드록시에틸, R3 = NH2, A = -CH=CH-]. LC/MS(254 ㎚) HPLC 방법 2 Rt 3.39. HRMS(ESI) C13H13N504S에 대한 계산치 [M+H]+ 336.0761, 실측치 336.0776;
1-tert-부틸-8-(메틸설포닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R4 = Me, X= SO2-, R2= t-부틸, R3 = NH2, A = -CH=CH-]. LC/MS(m/z): 348.2 [M+H]+, HPLC(254 ㎚) 방법 3 Rt 4.59; 및
8-(메틸설포닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R4 = Me, X= S02-, R2= H, R3 = NH2, A = -CH=CH-]. LC/MS(m/z): 292.2 [M+H]+, HPLC(254 ㎚) 방법 3 Rt 2.21.
실시예 15: 1-(2-하이드록시에틸)-8-페녹시-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 페녹시, R2= 2-하이드록시에틸, R3 = NH2, A = -CH=CH-](화합물 45)
전환 b
N,N-디메틸포름아미드(5 ㎖) 중의 100 ㎎(0.298 mmol)의 1-(2-하이드록시에틸)-8-(메틸설포닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드의 용액에 160 ㎎(1.2 mmol)의 칼륨 카보네이트 및 35 ㎎(0.36 mmol)의 페놀을 첨가하였다. 혼합물을 70℃에서 3 시간 동안 교반하고, 그 후에 이것을 EtOAc와 H20 사이에 분배시켰다. 유기층을 합하여 Na2S04 상에서 건조시키고, 진공 중에서 농축시켰다. 조물질을 크로마토그래피(DCM/MeOH 9/1)에 의해서 정제하여 목적하는 생성물을 제공하였다(40 ㎎, 40%). LC/MS(254 ㎚) HPLC 방법 2 Rt 4.79 min. 1H NMR(401 MHz, DMSO-d6) δ 9.61(s, 1H), 8.25(d, J=8.79 Hz, 1H), 7.75-7.84(m, J=8.79 Hz, 1H), 7.45-7.57(m, 3H), 7.31-7.40(m, 3H), 4.69-4.75(m, 2H), 4.55-4.63(m, 1H), 3.59(q, J=5.61 Hz, 2H). HRMS(ESI) C18H15N503에 대한 계산치 [M+H]+ 350.1248, 실측치 350.1247.
상기 실시예에 기술된 것과 유사한 방법을 사용하여, 다음의 유사체들을 또한 합성하였다:
1-(2-하이드록시에틸)-8-[4-(4-메틸피페라진-1-일)페녹시]-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 4-(4-메틸피페라진-1-일)페녹시, R2= 2-하이드록시에틸, R3 = NH2, A = -CH=CH-](화합물 46). LC/MS(254 ㎚) HPLC 방법 2 Rt 3.78 min. 1H NMR(401 MHz, DMSO-d6) δ 9.57(s, 1H), 8.23(d, J=8.79 Hz, 1H), 7.77(d, J=8.91 Hz, 2H), 7.46-7.53(m, 1H), 7.16-7.27(m, 2H), 6.98-7.10(m, 2H), 4.77(t, J=5.19 Hz, 2H), 4.55-4.63(m, 1H), 3.64(q, J=5.53 Hz, 2H), 3.13-3.21(m, 4H), 2.52(br. s., 4H), 2.26(s, 3H). HRMS(ESI) C23H25N703에 대한 계산치 [M+H]+ 448.2092, 실측치 448.2082;
1-(2-하이드록시에틸)-8-[3-(4-메틸피페라진-1-일)페녹시]-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 3-(4-메틸피페라진-1-일)페녹시, R2= 2-하이드록시에틸, R3 = NH2, A = -CH=CH-](화합물 47). LC/MS(254 ㎚) HPLC 방법 2 Rt 3.92 min. 1H NMR(401 MHz, DMSO-d6) δ 9.59(s, 1H), 8.24(d, J=8.79 Hz, 1H), 7.79(s, 1H), 7.77(s, 2H), 7.48-7.50(m, 1H), 7.28-7.36(m, 1H), 6.84-6.93(m, 2H), 6.68-6.77(m, 1H), 4.70-4.78(m, 2H), 4.57(t, J=5.68 Hz, 1H), 3.62(q, J=5.53 Hz, 2H), 3.15-3.22(m, 4H), 2.39-2.47(m, 4H), 2.21(s, 3H). HRMS(ESI) C23H25N703에 대한 계산치 [M+H]+ 448.2092, 실측치 448.2086;
1-(2-하이드록시에틸)-8-(3-니트로페녹시)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 [(I), R1 = 3-니트로페녹시, R2= 2-하이드록시에틸, R3 = NH2, A = -CH=CH-](화합물 48). LC/MS(254 ㎚) HPLC 방법 2 Rt 4.9 min. 1H NMR(401 MHz, DMSO-d6) δ 9.66(s, 1H), 8.30(t, J=2.14 Hz, 1H), 8.28(d, J=8.79 Hz, 1H), 8.20-8.24(m, 1H), 7.89-7.93(m, 1H), 7.80-7.86(m, 2H), 7.50-7.52(m, 1H), 4.69(t, J=5.74 Hz, 1H), 4.61-4.65(m, 1H), 3.57(q, J=5.45 Hz, 1H). HRMS(ESI) C18H14N605에 대한 계산치 [M+H]+ 395.1099, 실측치 395.1098;
1-메틸-8-(3-니트로페녹시)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 3-니트로페녹시, R2= 메틸, R3 = NH2, A = -CH=CH-](화합물 49). 1H NMR(401 MHz, DMSO-d6) δ 9.65(s, 1H), 8.34(t, J=2.14 Hz, 1H), 8.27(d, J=8.67 Hz, 1H), 8.21(ddd, J=0.98, 2.20, 8.18 Hz, 2H), 7.91-7.95(m, 2H), 7.86(br. s., 1H), 7.78-7.85(m, 4H), 7.51(br. s., 3H), 4.29(s, 3H). HRMS(ESI) C17H12N604에 대한 계산치 [M+H]+ 365.0993, 실측치 365.0997;
1-메틸-8-[3-(4-메틸피페라진-1-일)페녹시]-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 3-(4-메틸피페라진-1-일)페녹시, R2= 메틸, R3 = NH2, A = -CH=CH-](화합물 50). LC/MS(254 ㎚) HPLC 방법 2 Rt 4.24 min. 1H NMR(401 MHz, DMSO-d6) δ 9.58(s, 1H), 8.22(d, J=8.67 Hz, 1H), 7.83(s, 1H), 7.77(d, J=8.79 Hz, 1H), 7.49(s, 1H), 7.31(t, J=8.18 Hz, 1H), 6.90-6.93(m, 1H), 6.87(dd, J=1.77, 8.36 Hz, 1H), 6.71-6.77(m, 1H), 4.31-4.35(m, 3H), 3.12-3.20(m, 4H), 2.44(d, J=9.28 Hz, 4H), 2.21(s, 3H). HRMS(ESI) C22H23N702에 대한 계산치 [M+H]+ 418.1986, 실측치 418.1983; 및
1-tert-부틸-8-[4-(4-메틸피페라진-1-일)페녹시]-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 4-(4-메틸피페라진-1-일)페녹시, R2= tert-부틸, R3 = NH2, A = -CH=CH-](화합물 51). LC/MS(254 ㎚) HPLC 방법 2 Rt 4.63 min. 1H NMR(401 MHz, DMSO-d6) δ 9.60(s, 1H), 8.34(d, J=8.54 Hz, 1H), 7.82(d, J=8.79 Hz, 1H), 7.67(s, 1H), 7.43-7.57(m, 1H), 7.12-7.20(m, 2H), 6.99-7.09(m, 2H), 3.09-3.21(m, 4H), 2.25(s, 3H), 1.55(s, 9H). HRMS(ESI) C25H29N702에 대한 계산치 [M+H]+ 460.2456, 실측치 460.2448.
실시예 16: 1-tert-부틸-8-(디메틸아미노)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = R4 및 R6 = Me, X = N, R2= tert-부틸, R3 = NH2, A = -CH=CH-](화합물 52)
전환 c
N,N-디메틸포름아미드(2 ㎖) 중의 10 ㎎(0.028 mmol)의 1-tert-부틸-8-(메틸설포닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드의 용액에 160 ㎎(0.112 mmol)의 칼륨 카보네이트 및 10 ㎕ ㎎(0.36 mmol)의 40% 수성 디메틸아민을 첨가하였다. 혼합물을 실온에서 18 시간 동안 교반하고, 그 후에 이것을 H2O로 희석하였다. 침전을 여과하고, 물로 세척하고, 진공 중에서 건조시켜 5 ㎎(65%)의 목적하는 생성물을 제공하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 6.44 min. 1H NMR(401 MHz, DMSO-d6) δ 9.23(s, 1H), 8.05(d, J=8.54 Hz, 1H), 7.61(br. s., 1H), 7.56(d, J=8.67 Hz, 1H), 7.41(br. s., 1H), 2.00(s, 9H). HRMS(ESI) C16H20N6O에 대한 계산치 [M+H]+ 313.1772, 실측치 313.1777.
실시예 17: 8-메톡시-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R4 = Me, X= O, R2= 메틸, A = -CH=CH-](화합물 53)
전환 b
1-메틸-8-(메틸설포닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드(30 ㎎, 0.1 mmol)를 3 ㎖의 메탄올에 용해시키고, 칼륨 카보네이트(27 ㎎, 0.2 mmol)를 첨가하였다. 혼합물을 실온에서 1 시간 동안 교반하였다. 용매를 감압 하에서 제거하고, 잔류물을 디에틸 에테르와 함께 분쇄하고, 여과하고, 건조시켜 20 ㎎(80%)의 표제 생성물을 수득하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 4.28 min. 1H NMR(401 MHz, DMSO-d6) δ 9.51(s, 1H), 8.18(d, J=8.67 Hz, 1H), 7.83(br. s., 1H), 7.73(d, J=8.67 Hz, 1H), 7.47-7.57(m, 1H), 4.70(s, 3H), 4.14(s, 3H). HRMS(ESI) C12H11N502에 대한 계산치 [M+H]+ 258.0986, 실측치 258.0987
유사한 방식으로 수행하여 다음의 화합물들을 제조하였다:
8-에톡시-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R4 = Et, X= O, R2= 메틸, A = -CH=CH-](화합물 54). LC/MS(254 ㎚) HPLC 방법 2 Rt 4.71 min. 1H NMR(401 MHz, DMSO-d6) δ 9.46-9.55(m, 1H), 8.17(d, J=8.79 Hz, 1H), 7.79-7.89(m, 1H), 7.72(d, J=8.79 Hz, 1H), 7.50(br. s., 1H), 4.68(s, 3H), 4.55-4.63(m, 2H), 1.46(t, J=7.08 Hz, 3H). HRMS(ESI) C13H13N502에 대한 계산치 [M+H]+ 272.1142, 실측치 272.1149; 및
8-메톡시-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R4 = Me, X= O, R2= H, A = -CH=CH-](화합물 55). LC/MS(m/z): 244.2 [M+H]+, HPLC(254 ㎚) 방법 3 Rt 2.89 min.
실시예 18: 8-(3-포르밀페녹시)-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R4 = 3-포르밀페닐, X= O, R2= 메틸, A = -CH=CH-](화합물 56)
전환 b
N,N-디메틸포름아미드(3 ㎖) 중의 120 ㎎(0.39 mmol)의 1-메틸-8-(메틸설포닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드의 용액에 칼륨 카보네이트(108 ㎎, 0.78 mmol) 및 m-하이드록시벤즈알데히드(70 ㎎, 0.58 mmol)를 첨가하였다. 혼합물을 70℃에서 4 시간 동안 교반한 다음에, EtOAc와 H20 사이에 분배시켰다. 유기층을 합하여 Na2S04 상에서 건조시키고, 진공 중에서 농축시켜 목적하는 생성물(100 ㎎, 74%)을 제공하였다. LC/MS(m/z): 348.0 [M+H]+, HPLC(254 ㎚) 방법 3 Rt 5.05 min.
실시예 19: 1-메틸-8-{3-[(4-메틸피페라진-1-일)메틸]페녹시}-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R4 = 3-[(4-메틸피페라진-1-일)메틸]페닐, X= O, R2= 메틸, A = -CH=CH-](화합물 57), 및
8-[3-(하이드록시메틸)페녹시]-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 [(I), R4 = 3-하이드록시메틸페닐, X= O, R2= 메틸, A = -CH=CH-](화합물 58)
전환 j
N,N-디메틸포름아미드(2 ㎖) 및 아세트산(50 ㎕)중의 30 ㎎(0.086 mmol)의 8-(3-포르밀페녹시)-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드의 용액에 N-메틸 피페라진(13 ㎕, 0.13 mmol) 및 나트륨 시아노보로하이드라이드(6 ㎎, 0.26 mmol)를 첨가하였다. 용액을 실온에서 3 시간 동안 교반하고, TLC 및 LC/MS 둘 다에 의해서 모니터링하였다(방법 1). 반응액을 에틸 아세테이트로 희석하고, 물 및 염수로 세척하고, Na2S04 상에서 건조시키고, 여과하고 농축시켰다. 잔류물을 칼럼(DCM/MeOH/NH4OH 95/5/0.1)으로 정제하여 주생성물로서 1-메틸-8-{3-[(4-메틸피페라진-1-일)메틸]페녹시}-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드(15 ㎎, 40%) [LC/MS(254 ㎚) HPLC 방법 2 Rt 4.14 min. 1H NMR(401 MHz, DMSO-d6) δ 9.60(s, 1H), 8.23(d, J=8.79 Hz, 1H), 7.83(s, 1H), 7.78(d, J=8.79 Hz, 1H), 7.49-7.50(m, 1H), 7.46(t, J=7.81 Hz, 1H), 7.26(dt, J=1.71, 7.69 Hz, 3H), 4.27(s, 3H), 3.53(s, 2H), 2.30-2.47(m, 8H), 2.17(br. s., 3H). HRMS(ESI) C23H25N702에 대한 계산치 [M+H]+ 432.2143, 실측치 432.2141; 및
부산물로서 8-[3-(하이드록시메틸)페녹시]-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드(10 ㎎, 33%) [LC/MS(254 ㎚) HPLC 방법 2 Rt 4.54 min. 1H NMR(401 MHz, DMSO-d6) δ 9.60(s, 1H), 8.23(d, J=8.79 Hz, 1H), 7.83(s, 1H), 7.78(d, J=8.79 Hz, 1H), 7.49(s, 1H), 7.42-7.48(m, 1H), 7.30-7.33(m, J=1.83 Hz, 1H), 7.20-7.28(m, 2H), 5.27(t, J=5.80 Hz, 1H), 4.56(d, J=5.74 Hz, 2H), 4.30(s, 3H). HRMS(ESI) C18H15N503에 대한 계산치 [M+H]+ 350.1248, 실측치 350.1253]를 제공하였다.
동일한 방법에 따라 수행하여 다음의 화합물들을 제조하였다:
8-{3-[(디메틸아미노)메틸]페녹시}-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R4 = 3-[(디메틸아미노)메틸]페닐, X= O, R2= 메틸, A = -CH=CH-](화합물 59). LC/MS(254 ㎚) HPLC 방법 2 Rt 3.89 min. 1H NMR(401 MHz, DMSO-d6) δ 9.61(s, 1H), 8.23(d, J=8.79 Hz, 1H), 7.82(s, 1H), 7.78(d, J=8.91 Hz, 1H), 7.49-7.50(m, 1H), 7.46(t, J=7.81 Hz, 1H), 7.29(d, J=1.46 Hz, 1H), 7.21-7.28(m, 2H), 4.27(s, 3H), 3.46(s, 2H), 2.18(s, 6H). HRMS(ESI) C20H20N6O2에 대한 계산치 [M+H]+ 377.1721, 실측치 377.1719; 및
1-메틸-8-[3-(모르폴린-4-일메틸)페녹시]-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R4 = 3-(모르폴린-4-일메틸)페닐, X= O, R2= 메틸, A = -CH=CH-](화합물 60). LC/MS(254 ㎚) HPLC 방법 2 Rt 4.72 min. 1H NMR(401 MHz, DMSO-d6) δ 9.60(s, 1H), 8.23(d, J=8.67 Hz, 1H), 7.83(s, 1H), 7.78(d, J=8.79 Hz, 1H), 7.49-7.50(m, 1H), 7.46(t, J=7.87 Hz, 1H), 7.29-7.32(m, 1H), 7.23-7.29(m, 2H), 4.27(s, 3H), 3.55-3.60(m, 4H), 3.53(s, 2H), 2.36-2.41(m, 4H). HRMS(ESI) C22H22N603에 대한 계산치 [M+H]+ 419.1826, 실측치 419.1815.
실시예 20: 8-(3-아미노페녹시)-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R4 = 3-아미노페닐, X= O, R2= 메틸, A = -CH=CH-](화합물 61)
전환 k
55 ㎎(0.15 mmol)의 1-메틸-8-(3-니트로페녹시)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드를 1,4-디옥산(5 ㎖) 및 물(1 ㎖)에 현탁시키고, 43 mg(0.6 mmol)의 아연 분말 및 88 ㎎(1.5 mmol)의 암모늄 클로라이드를 첨가하였다. 혼합물을 100℃에서 2 시간 동안 교반하였다. 휘발성 물질을 진공 중에서 제거하고, 잔류물을 에틸 아세테이트 및 물에 용해시키고, 유기물질을 추출하여 염수로 세척하고, Na2S04 상에서 건조시키고, 농축시켰다. 조 고체를 실리카겔 상에서의 섬광 크로마토그래피(디클로로메탄/메탄올 95/5)에 의해서 정제하여 10 ㎎(20% 수율)의 표제 화합물을 수득하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 4.7 min. 1H NMR(401 MHz, DMSO-d6) δ 9.57(s, 1H), 8.22(d, J=8.79 Hz, 1H), 7.84(s, 1H), 7.77(d, J=8.79 Hz, 1H), 7.49(s, 1H), 7.11(t, J=7.99 Hz, 1H), 6.50-6.53(m, 1H), 6.41-6.50(m, J=0.92, 2.23, 8.68, 8.68 Hz, 2H), 5.26(s, 2H), 4.38(s, 3H). HRMS(ESI) C17H14N602에 대한 계산치 [M+H]+ 335.1251, 실측치 335.1258.
동일한 방법에 따라 수행하여 다음의 화합물을 제조하였다:
8-(3-아미노페녹시)-1-(2-하이드록시에틸)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R4 = 3-아미노페닐, X= O, R2= 2-하이드록시에틸, A = -CH=CH-](화합물 62). LC/MS(254 ㎚) HPLC 방법 2 Rt 4.26 min. 1H NMR(401 MHz, DMSO-d6) δ 9.58(s, 1H), 8.23(d, J=8.79 Hz, 1H), 7.74-7.83(m, J=8.79 Hz, 1H), 7.49(s, 1H), 7.12(t, J=8.12 Hz, 1H), 6.47-6.55(m, 2H), 6.40-6.47(m, 1H), 5.27(s, 2H), 4.81(t, J=5.19 Hz, 2H), 4.61(t, J=5.68 Hz, 1H), 3.69(q, J=5.57 Hz, 2H). HRMS(ESI) C18H16N603에 대한 계산치 [M+H]+ 365.1357, 실측치 365.1363.
제조예 J: 에틸 8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트[(VIII), R1 = Me-S-, R2 = H]
단계 5
DCM(20 ㎖) 중의 에틸 8-(메틸설파닐)-1-트리틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트(1.0 g, 1.99 mmol)를 트리플루오로아세트산(5 ㎖)으로 처리하였다. 생성된 혼합물을 실온에서 1 시간 동안 교반하고, 용매를 진공 중에서 제거하였다. 잔류물을 디에틸 에테르와 함께 분쇄하고, 여과하고, 건조시켜 500 ㎎(96%)의 표제 화합물을 제공하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 3.62 min.
실시예 21: 8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-S-, R2 = H, R3 = NH2, A = -(CH2)2-](화합물 63)
단계 6a
메탄올 중의 7 N NH3 5 ㎖ 중의 0.5 g(1.91 mmol)의 에틸 8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트의 현탁액을 60℃에서 72 시간 동안 가열하였다. 휘발성 물질을 진공 하에서 제거하고, 잔류물을 디에틸 에테르와 함께 분쇄하고, 고체를 여과하여 0.4 g(80%)의 표제 화합물을 제공하였다. 1H NMR(401 MHz, DMSO-d6) δ 14.13(br. s., 1H), 8.52(s, 1H), 7.53(br. s., 1H), 7.26(br. s., 1H), 2.96-3.08(m, J=7.45 Hz, 2H), 2.83-2.94(m, 2H), 2.56(s, 3H). HRMS(ESI) C11H11N50S에 대한 계산치 [M+H]+ 262.0757, 실측치 262.07575.
실시예 22: 1-(2-플루오로에틸)-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-S-, R2 = 2-플루오로에틸, R3 = NH2, A = -(CH2)2-](화합물 64)
전환 e
아세토니트릴 중의 8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드(50 ㎎, 0.191 mmol)의 용액에 2-플루오로-1-요오도에탄(66.7 ㎎, 0.38 mmol) 및 세슘 카보네이트(124 ㎎, 0.38 mmol)를 첨가하였다. 생성된 혼합물을 60℃에서 4 시간 동안 가열하였다. 실온으로 냉각시킨 후에, 반응 혼합물을 에틸 아세테이트와 물 사이에 분배시켰다. 유기층을 염수로 세척하고, Na2S04 상에서 건조시키고, 농축시켰다. 조물질을 실리카겔 크로마토그래피(DCM/EtOH 9/1)에 의해서 정제하여 표제 화합물을 제공하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 4.82 min. 1H NMR(401 MHz, DMSO-d6) δ 8.52-8.58(m, 1H), 7.50(br. s., 1H), 7.33(br. s., 1H), 5.07-5.15(m, J=4.88 Hz, 1H), 5.03(t, J=4.94 Hz, 1H), 4.93-4.99(m, 1H), 4.85(t, J=4.88 Hz, 1H), 3.00-3.06(m, J=7.69 Hz, 2H), 2.85-2.93(m, J=8.06 Hz, 2H), 2.53(s, 3H). HRMS(ESI) C13H14FN50S에 대한 계산치 [M+H]+ 308.0976, 실측치 308.0976.
동일한 방법에 따라 수행하여 다음의 화합물들을 제조하였다:
1-(2-클로로에틸)-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-S-, R2 = 2-클로로에틸, R3 = NH2, A = -(CH2)2-](화합물 65). LC/MS(254 ㎚) HPLC 방법 2 Rt 5.25 min. 1H NMR(401 MHz, DMSO-d6) δ 8.55(s, 1H), 7.53(br. s., 1H), 7.35(br. s., 1H), 5.09(t, J=6.23 Hz, 2H), 4.11(t, J=6.29 Hz, 2H), 2.98-3.06(m, 2H), 2.86-2.92(m, 2H), 2.56(s, 3H). HRMS(ESI) C13H14ClN50S에 대한 계산치 [M+H]+ 324.0681, 실측치 324.0676;
1-(2-하이드록시에틸)-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 [(I), R1 = Me-S-, R2 = 2-하이드록시에틸, R3 = NH2, -(CH2)2-](화합물 66). LC/MS(254 ㎚) HPLC 방법 2 Rt 4.1 min. 1H NMR(401 MHz, DMSO-d6) δ 8.53(s, 1H), 7.35-7.60(m, 1H), 7.28(br. s., 1H), 4.84-4.90(m, 1H), 4.79(t, J=6.16 Hz, 2H), 3.79-3.90(m, 2H), 2.95-3.08(m, 2H), 2.82-2.94(m, 2H), 2.55(s, 3H). HRMS(ESI) C13H15N502S에 대한 계산치 [M+H]+ 306.1019, 실측치 306.1023;
1-(2-메톡시에틸)-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-S-, R2 = 2-메톡시에틸, R3 = NH2, A = -(CH2)2-](화합물 67). LC/MS(254 ㎚) HPLC 방법 2 Rt 4.76 min. 1H NMR(401 MHz, DMSO-d6) δ 8.54(s, 1H), 7.47(br. s., 1H), 7.30(br. s., 1H), 4.90(t, J=5.86 Hz, 2H), 3.76-3.89(m, 2H), 3.23(s, 3H), 2.98-3.06(m, 2H), 2.84-2.91(m, 2H), 2.54(s, 3H). HRMS(ESI) C14H17N502S에 대한 계산치 [M+H]+ 320.1176, 실측치 320.1187;
1-[3-(디메틸아미노)프로필]-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-S-, R2 = 3-(디메틸아미노)프로필, R3 = NH2, A = -(CH2)2-](화합물 68). LC/MS(254 ㎚) HPLC 방법 2 Rt 3.69 min. 1H NMR(401 MHz, DMSO-d6) δ 8.53(s, 1H), 7.46(br. s., 1H), 7.29(br. s., 1H), 4.70-4.77(m, 2H), 2.97-3.05(m, 2H), 2.83-2.91(m, 2H), 2.54-2.58(m, 3H), 2.22-2.31(m, 2H), 2.11(s, 6H), 1.92-2.03(m, 2H). HRMS(ESI) C16H22N60S에 대한 계산치 [M+H]+ 347.1649, 실측치 347.1638; 및
1-(1-아미노-2-메틸-1-옥소프로판-2-일)-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-S-, R2 = 1-아미노-2-메틸-1-옥소프로판-2-일, R3 = NH2, A = -(CH2)2-](화합물 69). LC/MS(254 ㎚) HPLC 방법 2 Rt 4.13 min. 1H NMR(401 MHz, DMSO-d6) δ 8.49(s, 1H), 7.42(s, 1H), 7.29(s, 1H), 6.96-7.14(m, 1H), 2.94-3.05(m, 2H), 2.75-2.85(m, 2H), 2.55(s, 3H), 1.90(s, 6H). HRMS(ESI) C15H18N602S에 대한 계산치 [M+H]+ 347.1285, 실측치 347.1282.
실시예 23: 8-(메틸설파닐)-1-(피페리딘-4-일메틸)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드[(I), R1 = Me-S-, R2 = 피페리딘-4-일메틸, R3 = NH2, A = -(CH2)2-](화합물 70)
아세토니트릴 중의 8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드(50 ㎎, 0.191 mmol)의 용액에 tert-부틸-피페리딘-4-일메틸브로뮤로 카바메이트(105.71 ㎎, 0.38 mmol) 및 세슘 카보네이트(124 ㎎, 0.38 mmol)를 첨가하였다. 생성된 혼합물을 60℃에서 4 시간 동안 가열하였다. 실온으로 냉각시킨 후에, 반응 혼합물을 에틸 아세테이트와 물 사이에 분배시켰다. 유기층을 염수로 세척하고, Na2S04 상에서 건조시키고 농축시켰다. 조물질을 실리카겔 크로마토그래피(DCM/EtOH 9/1)에 의해서 정제하여 tert-부틸 4-{[3-카바모일-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-1-일]메틸}피페리딘-1-카복실레이트(30 ㎎, 0.65 mmol)를 제공하였다. 그 후, 이 화합물을 1,4-디옥산 중의 4 M HC1 2 ㎖로 처리하였다. 생성된 혼합물을 실온에서 1 시간 동안 교반하였다. 휘발성 물질을 진공 중에서 제거하고, 수득된 잔류물을 디에틸 에테르와 함께 분쇄하고, 여과하고, Et20로 세척하고, 진공 중에서 건조시켜 백색 고체로서 32 ㎎(97%)의 표제 화합물을 제공하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 3.83 min. 1H NMR(401 MHz, DMSO-d6) δ 8.62(d, J=10.01 Hz, 1H), 8.55(s, 1H), 8.27-8.49(m, J=8.42 Hz, 1H), 7.44(s, 1H), 7.35(s, 1H), 4.63-4.78(m, 2H), 3.18-3.28(m, J=6.10 Hz, 2H), 2.99-3.07(m, 2H), 2.85-2.92(m, J=7.93 Hz, 2H), 2.74-2.85(m, J=10.38 Hz, 2H), 2.57(s, 3H), 2.18-2.31(m, 1H), 1.56-1.70(m, 2H), 1.37-1.51(m, J=3.72, 13.98 Hz, 2H). HRMS(ESI) C17H22N60S에 대한 계산치 [M+H]+ 359.1649, 실측치 359.1634.
동일한 방법에 따라 수행하여 다음의 화합물들을 제조하였다:
1-(3-아미노프로필)-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드[(I), R1 = Me-S-, R2 = 3-아미노프로필, R3 = NH2, A = -(CH2)2-](화합물 71). LC/MS(254 ㎚) HPLC 방법 2 Rt 3.58 min. 1H NMR(401 MHz, DMSO-d6) δ 8.56(s, 1H), 7.79(br. s., 3H), 7.47-7.50(m, 1H), 7.38(br. s., 1H), 4.77(t, J=6.53 Hz, 2H), 2.99-3.06(m, 2H), 2.86-2.93(m, 2H), 2.76-2.83(m, 2H), 2.54-2.59(m, 3H), 2.17(br. s., 2H). HRMS(ESI) C14H18N60S [M+H]+ 319.1336, 실측치 319.1344;
8-(메틸설파닐)-1-(피페리딘-4-일)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 트리플루오로아세테이트[(I), R1 = Me-S-, R2 = 피페리딘-4-일, R3 = NH2, A = -(CH2)2-](화합물 72). LC/MS(254 ㎚) HPLC 방법 2 Rt 3.65 min. 1H NMR(401 MHz, DMSO-d6) δ 8.58-8.65(m, 1H), 8.56(s, 1H), 8.46(br. s., 1H), 7.41(br. s., 1H), 7.38(br. s., 1H), 5.52-5.73(m, J=6.84, 6.84 Hz, 1H), 3.46-3.62(m, 2H), 3.04-3.13(m, J=6.84 Hz, 2H), 2.97-3.04(m, 2H), 2.82-2.91(m, J=8.18 Hz, 2H), 2.58(s, 3H), 2.19-2.32(m, J=7.32 Hz, 4H). HRMS(ESI) C16H20N6OS에 대한 계산치 [M+H]+ 345.1492, 실측치 345; 및
1-(2-아미노에틸)-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 트리플루오로아세테이트[(I), R1 = Me-S-, R2 = 2-아미노에틸, R3 = NH2, A = -(CH2)2-](화합물 73). LC/MS(254 ㎚) HPLC 방법 2 Rt 3.46 min. 1H NMR(401 MHz, DMSO-d6) δ 8.58(s, 1H), 7.92(br. s., 3H), 7.74(s, 1H), 7.43(s, 1H), 4.85-5.09(m, 2H), 3.42-3.57(m, J=5.98 Hz, 2H), 2.96-3.09(m, 2H), 2.80-2.94(m, 2H), 2.56(s, 3H). HRMS(ESI) C13H16N60S에 대한 계산치 [M+H]+ 305.1179, 실측치 305.1191.
실시예 24: 1-[2-(4-메틸피페라진-1-일)에틸]-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-S-, R2 = 2-(4-메틸피페라진-1-일)에틸, R3 = NH2, A = -(CH2)2-](화합물 74), 및
1-에테닐-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-S-, R2 = 에테닐, R3 = NH2, A = -(CH2)2-](화합물 75)
전환 f 및 g
메탄올(3 ㎖) 중의 1-(2-클로로에틸)-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드(50 ㎎, 0.15 mmol)의 용액에 N-메틸피페라진(62 ㎕, 0.61 mmol) 및 세슘 카보네이트(97 ㎎, 0.3 mmol)를 첨가하였다. 생성된 혼합물을 60℃에서 48 시간 동안 가열하였다. 휘발성 물질을 진공 하에서 제거하고, 조 고체를 에틸 아세테이트 및 물로 용해시키고, 유기층을 염수로 세척하고, Na2S04 상에서 건조시키고 농축시켰다. 조물질을 실리카겔 크로마토그래피(DCM/EtOAc 8/2)에 의해서 정제하여 황색 고체로서 화합물 1-에테닐-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드를 제공하였다(15 ㎎, 35% 수율). LC/MS(254 ㎚) HPLC 방법 2 Rt 5.34 min. 1H NMR(401 MHz, DMSO-d6) δ 8.58(s, 1H), 8.35(dd, J=8.73, 15.44 Hz, 1H), 7.71(s, 1H), 7.46(br. s., 1H), 5.96(d, J=15.38 Hz, 1H), 5.15(d, J=8.67 Hz, 1H), 3.00-3.09(m, 2H), 2.86-2.94(m, 2H), 2.56(s, 3H). HRMS(ESI) C13H13N50S에 대한 계산치 [M+H]+ 288.0914, 실측치 288.0913.
DCM/MeOH/NH4OH 9/1/0.1과 같은 용출제를 변화시켜 극성 화합물 1-(2-[N-메틸피페라진]에틸)-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드를 황색 고체로서 수집하였다(17 ㎎, 30% 수율). LC/MS(254 ㎚) HPLC 방법 2 Rt 3.79 min. 1H NMR(401 MHz, DMSO-d6) δ 8.35(s, 1H), 7.46(s, 1H), 7.28(s, 1H), 4.82(t, J=6.84 Hz, 2H), 2.98-3.04(m, 2H), 2.88(d, J=7.93 Hz, 2H), 2.55(s, 3H). HRMS(ESI) C18H25N70S에 대한 계산치 [M+H]+ 388.1914, 실측치 388.1909
실시예 25: 1-{2-[4-(디메틸아미노)피페리딘-1-일]에틸}-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-S-, R2 = 2-[4-(디메틸아미노)피페리딘-1-일]에틸, R3 = NH2, A = -(CH2)2-](화합물 76)
전환 h
에틸 아세테이트(2 ㎖) 중의 1-(2-하이드록시에틸)-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드(20 ㎎, 0.077 mmol)의 용액에 IBX(64 ㎎, 0.23 mmol)를 첨가하였다. 생성된 혼합물을 80℃에서 4 시간 동안 가열하였다. 실온으로 냉각시킨 후에, 반응 혼합물을 여과하고, 휘발성 물질을 진공 중에서 제거하고, 조물질로서 알데히드를 다음 반응을 위해서 사용하였다. 알데히드를 THF/DMF(3/1 ㎖)로 용해시키고, 나트륨 트리아세톡시보로하이드라이드(49 ㎎, 0.233 mmol) 및 4-디메틸아미노피페리딘(20 ㎕, 0.156 mmol)을 첨가하였다. 반응 혼합물을 실온에서 72 시간 동안 교반하였다. 용매를 증발시키고, 수득된 조물질을 크로마토그래피(DCM/MeOH/NH4OH 8/2/0.2)에 의해서 정제하여 15 ㎎(48%)의 표제 화합물을 제공하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 3.93 min. 1H NMR(401 MHz, DMSO-d6) δ 8.55(s, 1H), 7.46(s, 1H), 7.29(s, 1H), 4.81(t, J=6.90 Hz, 2H), 2.96-3.04(m, 2H), 2.79-2.93(m, J=8.18 Hz, 5H), 2.71(t, J=6.59 Hz, 2H), 2.56(s, 3H), 2.14(s, 6H), 1.93-2.06(m, J=16.11 Hz, 3H), 1.53-1.68(m, J=14.16 Hz, 2H), 1.04-1.20(m, J=3.17 Hz, 2H). HRMS(ESI) C20H29N7OS에 대한 계산치 [M+H]+ 416.2227, 실측치 416.2234.
실시예 26: 8-에톡시-1-(피페리딘-4-일메틸)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드[(I), R4 = Et, X = O, R2 = 2-[4-(디메틸아미노)피페리딘-1-일]에틸, R3 = NH2, A = -(CH2)2-](화합물 77)
전환 e
DMF(3 ㎖) 중의 8-에톡시-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드(40 ㎎, 0.154 mmol)의 용액에 tert-부틸-피페리딘-4-일메틸브로뮤로 카바메이트(85 ㎎, 0.308 mmol) 및 Cs2C03 (121 ㎎, 0.370 mmol)를 첨가하였다. 혼합물을 70℃에서 가열하고, 4 시간 동안 교반하였다. 냉각된 혼합물을 물(10 ㎖)로 처리하고, 에틸 아세테이트로 추출하였다. 유기상을 합하여 물 및 염수로 세척하고, Na2S04 상에서 건조시키고, 농축시켰다. 조물질을 DCM/EtOAc/EtOH 7/2/1로 용출시키는 섬광 크로마토그래피에 의해서 정제하여 백색 고체로서 50 ㎎(70%)의 목적 생성물 tert-부틸 4-{[3-카바모일-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-1-일]메틸}-피페리딘-1-카복실레이트를 수득하였다. 후자의 생성물을 DCM(2 ㎖)에 용해시키고, 1,4-디옥산 중의 4 M HCl(2 ㎖)을 첨가하였다. 용액을 실온에서 1 시간 동안 교반하고, 증발 건조시켰다. 고체를 디에틸 에테르와 함께 분쇄하고, 여과하고, 진공 중에서 건조시켜 40 ㎎(95%)의 목적 생성물을 제공하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 3.65 min. 1H NMR(401 MHz, DMSO-d6) δ 8.65(d, J=11.60 Hz, 1H), 8.51(s, 1H), 8.31-8.46(m, J=15.38 Hz, 1H), 7.42(br. s., 1H), 7.34(s, 1H), 4.69(d, J=7.20 Hz, 1H), 4.39(q, J=6.96 Hz, 1H), 3.18-3.27(m, 2H), 2.97-3.04(m, 2H), 2.74-2.90(m, J=7.93 Hz, 4H), 2.18-2.32(m, J=5.98 Hz, 1H), 1.59-1.70(m, J=11.84 Hz, 2H), 1.40-1.53(m, J=4.03 Hz, 2H), 1.38(t, J=7.02 Hz, 3H). HRMS(ESI) C18H24N602에 대한 계산치 [M+H]+ 357.2033, 실측치 357.2041.
동일한 방법에 따라 수행하여 다음의 화합물들을 제조하였다:
1-[3-(디메틸아미노)프로필]-8-에톡시-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R4 = Et, X = O, R2 = 3-(디메틸아미노)프로필, R3 = NH2, A = -(CH2)2-](화합물 78). LC/MS(254 ㎚) HPLC 방법 2 Rt 3.63 min. 1H NMR(401 MHz, DMSO-d6) δ 8.49(s, 1H), 7.44(s, 1H), 7.29(br. s., 1H), 4.67-4.78(m, 2H), 4.39(q, J=7.08 Hz, 2H), 2.93-3.05(m, 2H), 2.81-2.93(m, 2H), 2.32-2.42(m, J=1.92, 1.92, 3.72 Hz, 2H), 2.19(br. s., 6H), 1.90-2.07(m, 2H), 1.36(t, J=7.02 Hz, 3H). HRMS(ESI) C17H24N602에 대한 계산치 [M+H]+ 345.2033, 실측치 345.203; 및
8-에톡시-1-(피페리딘-4-일)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드[(I), R4 = Et, X = O, R2 = 피페리딘-4-일, R3 = NH2, A = -(CH2)2-](화합물 79). LC/MS(254 ㎚) HPLC 방법 2 Rt 3.59 min. 1H NMR(401 MHz, DMSO-d6) δ 8.57-8.95(m, 2H), 8.52(s, 1H), 7.39(br. s., 2H), 5.58(quin, J=7.23 Hz, 1H), 4.36-4.45(m, 2H), 2.96-3.02(m, 3H), 2.82-2.89(m, J=8.18 Hz, 2H), 1.37(t, J=7.02 Hz, 3H). HRMS(ESI) C17H22N602에 대한 계산치 [M+H]+ 343.1877, 실측치 343.1876
실시예 27: 8-에톡시-1-[(1-메틸피페리딘-4-일)메틸]-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R4 = Et, X = O, R2 =(1-메틸피페리딘-4-일)메틸, R3 = NH2, A = -(CH2)2-](화합물 80)
전환 n
DMF(3 ㎖) 중의 8-에톡시-1-(피페리딘-4-일메틸)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드(30 ㎎, 0.084 mmol)의 용액에 1 ㎖의 포름알데히드(물 중의 37%, 12.3 mmol) 및 나트륨 트리아세톡시보로하이드라이드(71 ㎎, 0.33 mmol)를 첨가하였다. 반응 혼합물을 실온에서 4 시간 동안 교반하였다. 혼합물을 물로 희석하고, 에틸 아세테이트로 추출하고, 유기층을 물 및 염수로 세척하고, Na2S04 상에서 건조시키고, 여과하고, 농축 건조시켰다. 조 혼합물을 DCM/EtOAc/EtOH 7/2/1로 용출시키는 실리카 상에서 크로마토그래피하여 20 ㎎(64%)의 목적 생성물을 제공하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 3.7 min. 1H NMR(401 MHz, DMSO-d6) δ 8.49(s, 1H), 7.43(s, 1H), 7.30(br. s., 1H), 4.65(d, J=7.45 Hz, 1H), 4.38(q, J=7.08 Hz, 2H), 2.97-3.04(m, 2H), 2.83-2.90(m, 2H), 2.79(br. s., 1H), 2.18(br. s., 2H), 1.86-2.03(m, 2H), 1.44-1.53(m, 2H), 1.34-1.39(m, 3H), 1.29(d, J=4.03 Hz, 2H). HRMS(ESI) C19H26N602에 대한 계산치 [M+H]+ 371.219, 실측치 371.2191.
제조예 K: tert-부틸 4-[(3-카바모일-8-요오도-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-1-일)메틸]피페리딘-1-카복실레이트 [(XIV)]
단계 7
DMF(3 ㎖) 중의 50 ㎎(0.146 mmol)의 8-요오도-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드(WO2008074788A1에 보고된 방법에 따라 제조)의 용액에 61 ㎎(0.219 mmol)의 tert-부틸 4-(브로모메틸)피페리딘-1-카복실레이트 및 95 ㎎(0.293 mmol)의 Cs2CO3를 첨가하였다. 혼합물을 70℃에서 가열하고, 4 시간 동안 교반하였다. 냉각된 혼합물을 물(10 ㎖)로 처리하고, 에틸 아세테이트로 추출하였다. 유기상을 물 및 염수로 세척하고, Na2S04 상에서 건조시키고, 농축시켰다. 조물질을 DCM/EtOH 9/1로 용출시키는 섬광 크로마토그래피에 의해서 정제하여 백색 고체로서 63 ㎎(80%)의 목적하는 표제 생성물을 수득하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 6.51 min. 1H NMR(401 MHz, DMSO-d6) δ 8.46(s, 1H), 7.47(s, 1H), 7.32(s, 1H), 4.50-4.55(m, 2H), 3.84-3.96(m, 2H), 2.99-3.07(m, 2H), 2.84-2.95(m, 2H), 2.59-2.75(m, 2H), 2.07(s, 1H), 1.56(br. s., 2H), 1.39(s, 9H), 1.08-1.22(m, 2H). HRMS(ESI) C21H27IN603에 대한 계산치 [M+H]+ 539.1262, 실측치 539.1274.
상술한 것과 유사한 방식으로 수행하여 다음의 화합물들을 제조하였다:
에틸 1-{3-[(tert-부톡시카보닐)아미노]프로필}-8-요오도-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트 및 에틸 2-{3-[(tert-부톡시카보닐)아미노]프로필}-8-요오도-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트. LC/MS(m/z): 528.0 [M+H]+, HPLC(254 ㎚) 방법 3 Rt 6.43 min.
실시예 28: 8-(2,6-디플루오로페닐)-1-(피페리딘-4-일메틸)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드[(I), R1 = 2,6-디플루오로페닐, R2 = 피페리딘-4-일메틸, R3 = NH2, A = -(CH2)2-](화합물 81)
단계 8
아르곤 대기 하에서 3 ㎖의 1,4-디옥산 및 1 ㎖의 물 중의 tert-부틸 4-[(3-카바모일-8-요오도-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-1-일)메틸]피페리딘-1-카복실레이트(30 ㎎, 0.036 mmol)의 용액에 17.6 ㎎(0.11 mmol)의 2,6-디플루오로페닐보론산, 13.7 ㎎(0.017 mmol)의 디클로로메탄과 1,1'-비스(디페닐포스피노)페로센팔라듐 복합체, 및 54 ㎎(0.167 mmol)의 세슘 카보네이트를 순차적으로 첨가하였다. 혼합물을 밀봉된 바이알 내에서 1 시간 동안, 80℃에서 마이크로웨이브 조사에 적용하였다. 반응액을 셀라이트 패드를 통해서 여과하고, 용매를 증발 건조시켰다. 그 후, 조물질을 에틸 아세테이트와 물 사이에 분배시키고, 유기층을 황산나트륨 상에서 건조시키고, 용매를 진공 중에서 제거하였다. 실리카겔 칼럼 상에서의 섬광 크로마토그래피(DCM/EtOAc 7/3)에 의해서 정제한 후에, 20 ㎎(70%)의 tert-부틸 4-{[3-카바모일-8-(2,6-디플루오로페닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-1-일]메틸}피페리딘-1-카복실레이트를 수득하였다.생성물을 DCM(2 ㎖)에 용해시키고, 1,4-디옥산 중의 4 M HCl(2 ㎖)을 첨가하였다. 반응액을 실온에서 1 시간 동안 교반하고, 용매를 증발 건조시켰다. 고체를 에틸 에테르로 처리하고, 침전을 여과에 의해서 수거하여 연황색 고체로서 17 ㎎(85%)의 표제 화합물을 제공하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 4.14 min. 1H NMR(401 MHz, DMSO-d6) δ 8.89(s, 1H), 8.57(d, J=9.76 Hz, 1H), 8.30(d, J=10.01 Hz, 1H), 7.55-7.69(m, 1H), 7.45(s, 1H), 7.37(s, 1H), 7.23-7.33(m, 2H), 4.57-4.66(m, 2H), 3.16-3.26(m, 2H), 3.01-3.14(m, 4H), 2.69-2.85(m, J=10.74 Hz, 2H), 2.09-2.29(m, J=7.20 Hz, 1H), 1.56-1.70(m, J=12.94 Hz, 2H), 1.32-1.48(m, 2H). HRMS(ESI) C21H27IN603에 대한 계산치 [M+H]+ 425.1896, 실측치 425.1896
상술한 것과 유사한 방식으로 수행하여 다음의 화합물을 제조하였다:
8-(2,6-디플루오로페닐)-1-(2-플루오로에틸)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 2,6-디플루오로페닐, R2 = 2-플루오로에틸, R3 = NH2, A = -(CH2)2-]. LC/MS(254 ㎚) HPLC 방법 2 Rt 5.31 min. 1H NMR(401 MHz, DMSO-d6) δ 8.89(s, 1H), 7.61(tt, J=6.44, 8.45 Hz, 1H), 7.53(br. S., 1H), 7.35(s, 1H), 7.19-7.32(m, 2H), 4.96-5.11(m, 2H), 4.74-4.96(m, 2H), 2.98-3.18(m, 4H). HRMS(ESI) C18H14F3N50에 대한 계산치 [M+H]+ 374.1223, 실측치 374.1225.
제조예 L: 에틸 8-(4-플루오로페닐)-1-트리틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트[(VIII), R1 = 4-플루오로페닐, R2 = 트리틸, A = -(CH2)2-]
단계 9
톨루엔(10 ㎖) 및 228 ㎎(1.63 mmol)의 4-플루오로벤젠보론산 중의 500 ㎎(0.82 mmol)의 에틸 8-요오도-1-트리틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트(WO2008074788A1에 보고된 방법에 따라 제조)의 용액에 물(0.5 ㎖) 중의 103 ㎎(2.46 mmol)의 리튬 클로라이드 및 339.8 ㎎(2.46 mmol)의 칼륨 카보네이트를 첨가하였다. 반응액을 아르곤으로 탈기(degass)시킨 다음에, 22 ㎎(0.041 mmol, 5% mol)의 비스(트리페닐포스핀)팔라듐(II) 디클로라이드를 첨가하고, 반응액을 100℃에서 60 분 동안 가열하였다. LC/MS 분석은 출발물질의 생성물로의 완전한 전환을 나타내었다. 반응액을 실온으로 냉각시킨 다음에, 진공 중에서 농축시키고, 실리카겔에 융합시켰다. 조생성물을 DCM/EtOH 10/0.5로 용출시키는 섬광 크로마토그래피에 의해서 정제하여 380 ㎎(80%)의 목적 생성물을 제공하였다. LC/MS(m/z): 581.2 [M+H]+, HPLC(254 ㎚) 방법 3 Rt 9.02.
상술한 것과 유사한 방식으로 수행하여 다음의 화합물들을 제조하였다:
에틸 8-(4-메톡시페닐)-1-트리틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트[(VIII), R1 = 4-메톡시페닐, R2 = 트리틸, A = -(CH2)2-]. LC/MS(m/z): 593.2 [M+H]+, HPLC(254 ㎚) 방법 3 Rt 8.91 min.
에틸 1-{3-[(tert-부톡시카보닐)아미노]프로필}-8-(4-플루오로페닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트[(VIII), R1 = 4-플루오로페닐, R2 = 3-(tert-부톡시카보닐)아미노프로필, A = -(CH2)2-], 및
에틸 2-{3-[(tert-부톡시카보닐)아미노]프로필}-8-(4-플루오로페닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트[(VIII), R1 = 4-플루오로페닐, R2 = 3-(tert-부톡시카보닐)아미노프로필, A = -(CH2)2-]. LC/MS(m/z): 496.1 [M+H]+, HPLC(254 ㎚) 방법 3 Rt 7.87 min.
제조예 M: 8-(4-플루오로페닐)-1-트리틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실산[(XI), R1 = 4-플루오로페닐, R2 = 트리틸, A = -(CH2)2-]
단계 6b1
에탄올(20 ㎖) 중의 380 ㎎(0.65 mmol)의 에틸 8-(4-플루오로페닐)-1-트리틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트의 용액에 3 ㎖(6 mmol)의 2 N 수성 NaOH를 첨가하였다. 혼합물을 30 분 동안 80℃로 가열하였다. 실온으로 냉각시킨 후에, 휘발성 물질을 진공 중에서 제거하였다. 잔류물을 물 및 아세트산(pH = 4)으로 희석하고, 형성된 침전을 여과하여 에탄올로 세척하였다. 고체를 오븐(진공 중에서 40℃) 내에서 2 시간 동안 건조시켰다. 360 ㎎(99%). LC/MS(m/z): 553.1 [M+H]+, HPLC(254 ㎚) 방법 3 Rt 5.84.
상술한 것과 유사한 방식으로 수행하여 다음의 화합물들을 제조하였다:
8-(4-메톡시페닐)-1-트리틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실산[(XI), R1 = 4-메톡시페닐, R2 = 트리틸, A = -(CH2)2-]. LC/MS(m/z): 565.2 [M+H]+, HPLC(254 ㎚) 방법 3 Rt 6.03;
1-{3-[(tert-부톡시카보닐)아미노]프로필}-8-(4-플루오로페닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실산[(XI), R1 = 4-플루오로페닐, R2 = 3-(tert-부톡시카보닐)아미노프로필, A = -(CH2)2-]; 및
2-{3-[(tert-부톡시카보닐)아미노]프로필}-8-(4-플루오로페닐)-4,5-디하이드로-2H-피라졸로[4,3-h]퀴나졸린-3-카복실산[(XI), XI R1 = 4-플루오로페닐, R2 = 3-(tert-부톡시카보닐)아미노프로필, A = -(CH2)2-]. LC/MS(m/z): 468.1 [M+H]+, HPLC(254 ㎚) 방법 3 Rt 4.27 min.(주생성물) 및 4.55 min(부생성물).
실시예 29: 8-(4-플루오로페닐)-N-(3-하이드록시프로필)-1-트리틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 4-플루오로페닐, R2 = 트리틸, R' = 3-하이드록시프로필, A = -(CH2)2-]
358 ㎎(0.65 mmol)의 8-(4-플루오로페닐)-1-트리틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실산을 실온에서 3 시간 동안 무수 DMF 중에서 0.060 ㎖(0.78 mmol)의 프로판올아민, 250 ㎎(0.78 mmol)의 TBTU 및 0.268 ㎖(1.5 mmol)의 DIPEA와 반응시켰다. 반응액을 물 및 포화 NaHCO3로 후처리하고, 에틸 아세테이트로 추출하였다. Na2SO4 상에서 건조시키고, 여과하고 증발시킨 유기상을 에틸 아세테이트/헥산 7/3을 사용하여 실리카 상에서 정제하여 300 ㎎(75%)의 순수한 생성물을 제공하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 8.08 min. 1H NMR(401 MHz, DMSO-d6) δ 8.52(s, 1H), 7.34(t, J= 5.73 Hz, 1H), 6.93-6.99(m, 2H), 4.52(t, J=5.00 Hz, 1H), 3.43-3.50(m, 2H), 3.25-3.32(m, 2H), 3.10(d, J=8.05 Hz, 2H), 2.78(t, J=7.44 Hz, 2H), 1.61(quin, J=6.40 Hz, 2H). HRMS(ESI) C38H32FN502에 대한 계산치 [M+H]+ 610.2613, 실측치 610.262.
상술한 것과 유사한 방식으로 수행하여 다음의 화합물을 제조하였다:
N-(3-하이드록시프로필)-8-(4-메톡시페닐)-1-트리틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 4-메톡시페닐, R2 = 트리틸, R' = 3 -하이드록시프로필, A = -(CH2)2-]. LC/MS(m/z): 622.2 [M+H]+, HPLC(254 ㎚) 방법 3 Rt 7.07 min.
실시예 30: 8-(4-플루오로페닐)-N-(3-하이드록시프로필)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 [(I), R1 = 4-플루오로페닐, R2 = H, R' = 3-하이드록시프로필, A = -(CH2)2-]
300 ㎎(0.5 mmol)의 8-(4-플루오로페닐)-N-(3-하이드록시프로필)-1-트리틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드를 DCM에 용해시키고, 실온에서 2 ㎖의 트리플루오로아세트산과 반응시켰다. 반응액을 증발 건조시키고, MeOH 및 포화 NaHC03로 30 분 동안 처리하였다. 그 후에, MeOH를 증발시키고, 수성상을 NaH2P03로 pH = 5.0으로 산성화시키고, DCM으로 추출하였다. 건조된 조물질을 에틸 아세테이트를 사용하여 실리카겔 상에서 정제하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 5.29 min. 1H NMR(401 MHz, DMSO-d6) δ 14.20(s, 1H), 8.77(s, 1H), 8.52-8.59(m, 2H), 8.23(t, J=5.74 Hz, 1H), 7.35-7.43(m, 2H), 4.51(t, J=5.25 Hz, 2H), 3.48(q, J=6.18 Hz, 2H), 3.06-3.11(m, 2H), 3.00-3.06(m, 2H), 1.60-1.76(m, 2H). HRMS(ESI) C19H18FN502에 대한 계산치 [M+H]+ 368.1518, 실측치 368.153.
상술한 것과 유사한 방식으로 수행하여 다음의 화합물을 제조하였다:
N-(3-하이드록시프로필)-8-(4-메톡시페닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = 4-메톡시페닐, R2 = 트리틸, R' = 3-하이드록시프로필, A = -(CH2)2-]. LC/MS(m/z): 380.1 [M+H]+, HPLC(254 ㎚) 방법 3 Rt 4.41 min.
실시예 31: tert-부틸 {3-[3-카바모일-8-(4-플루오로페닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-1-일]프로필}카바메이트[(I), R1 = 4-플루오로페닐, N1 R2 = tert-부틸 3-카바모일프로필, R3 = NH2, A = -(CH2)2-], 및
tert-부틸 {3-[3-카바모일-8-(4-플루오로페닐)-4,5-디하이드로-2H-피라졸로[4,3-h]퀴나졸린-2-일]프로필}카바메이트[(I), R1 = 4-플루오로페닐, N2 R2 = tert-부틸 3-카바모일프로필, R3 = NH2, A = -(CH2)2-]
단계 6b2
1-{3-[(tert-부톡시카보닐)아미노]프로필}-8-(4-플루오로페닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실산 및 2-{3-[(tert-부톡시카보닐)아미노]프로필}-8-(4-플루오로페닐)-4,5-디하이드로-2H-피라졸로[4,3-h]퀴나졸린-3-카복실산 358 ㎎(0.65 mmol)을 실온에서 3 시간 동안 무수 DMF(5 ㎖) 중에서 147 ㎎(0.975 mmol)의 HOBt*NH4, 250 ㎎(0.78 mmol)의 TBTU, 및 0.268 ㎖(1.5 mmol)의 DIPEA와 반응시켰다. 반응액을 물 및 포화 NaHCO3로 후처리하고, 에틸 아세테이트로 추출하였다. Na2SO4 상에서 건조시키고, 여과하고 증발시킨 유기상을 에틸 아세테이트/헥산 7/3을 사용하여 실리카 상에서 정제하여 212 ㎎(70%)의 위치이성체의 순수한 혼합물을 제공하였다. LC/MS(m/z): 467.2 [M+H]+, 및 467.2 [M+H]+, HPLC(254 ㎚) 방법 3 Rt 5.62 및 6.12 min.
실시예 32: 1-(3-아미노프로필)-8-(4-플루오로페닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 트리플루오로아세테이트 [(I), R1 = 4-플루오로페닐, N1 R2 = 3-아미노프로필, R3 = NH2, A = -(CH2)2-](화합물 82), 및
2-(3-아미노프로필)-8-(4-플루오로페닐)-4,5-디하이드로-2H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 트리플루오로아세테이트[(I), R1 = 4-플루오로페닐, N2 R2 = 3-아미노프로필, R3 = NH2, A = -(CH2)2-](화합물 83)
tert-부틸 {3-[3-카바모일-8-(4-플루오로페닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-1-일]프로필}카바메이트 및 tert-부틸 {3-[3-카바모일-8-(4-플루오로페닐)-4,5-디하이드로-2H-피라졸로[4,3-h]퀴나졸린-2-일]프로필}카바메이트를 DCM에 현탁시키고, 60℃에서 2 ㎖의 TFA와 반응시켰다. 90 분 동안에 완결된 반응액을 증발시켰다. 조물질을 분취용-HPLC 방법 2에 의해서 정제하고, 다음의 2 개의 위치이성체를 분할시켰다:
1-(3-아미노프로필)-8-(4-플루오로페닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 트리플루오로아세테이트(주생성물). LC/MS(254 ㎚) HPLC 방법 2 Rt 4.32 min. 1H NMR(401 MHz, DMSO-d6) δ 8.83(s, 1H), 8.43(dd, J=5.68, 8.97 Hz, 2H), 7.64(br. s., 3H), 7.48(br. s., 1H), 7.40(br. s., 1H), 7.38(t, J=8.85 Hz, 2H), 4.93(t, J=6.47 Hz, 2H), 3.05-3.13(m, 2H), 3.01(t, J=7.20 Hz, 2H), 2.82-2.91(m, 2H), 2.25(quin, J=7.20 Hz, 2H). HRMS(ESI) C19H19FN60에 대한 계산치 [M+H]+ 367.1677, 실측치 367.16785; 및
2-(3-아미노프로필)-8-(4-플루오로페닐)-4,5-디하이드로-2H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 트리플루오로아세테이트(부생성물). LC/MS(254 ㎚) HPLC 방법 2 Rt 4.14 min. 1H NMR(401 MHz, DMSO-d6) δ 8.78(s, 1H), 8.46(dd, J=5.68, 8.97 Hz, 2H), 7.92(br. s., 1H), 7.78(br. s., 1H), 7.74(br. s., 3H), 7.37(t, J=8.91 Hz, 2H), 4.53(t, J=6.84 Hz, 2H), 2.93-3.05(m, 4H), 2.81-2.92(m, 2H), 2.16(quin, J=7.26 Hz, 2H). HRMS(ESI) C19H19FN60에 대한 계산치 [M+H]+ 367.1677, 실측치 367.16784.
이와 동일한 방법에 따라 적합한 치환된 유도체를 사용하여 다음의 화합물을 제조하였다:
1-(3-아미노프로필)-N-(3-하이드록시프로필)-8-(4-메톡시페닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 트리플루오로아세테이트[(I), R1 = 4-메톡시페닐, R2 = 3-아미노프로필, R' = 3-하이드록시프로필, A = -(CH2)2-](화합물 84). LC/MS(254 ㎚) HPLC 방법 2 Rt = 3.52 min. 1H NMR(401 MHz, DMSO-d6) δ 8.79(s, 1H), 8.32-8.37(m, 2H), 8.11(t, J=5.86 Hz, 1H), 7.67(br. s., 3H), 7.06-7.14(m, 2H), 4.94(t, J=6.53 Hz, 2H), 3.86(s, 3H), 3.49(t, J=6.23 Hz, 2H), 3.31(br. s., 2H), 3.03-3.13(m, 2H), 3.00(d, J=7.81 Hz, 2H), 2.81-2.92(m, 2H), 2.26(d, J=2.56 Hz, 2H), 1.69(quin, J= 6.56 Hz, 2H). 질량 계산치: 437.2296, 질량 실측치: 437.2291.
제조예 N: 1-(3-아미노프로필)-8-(4-플루오로페닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실산 트리플루오로아세테이트 및 2-(3-아미노프로필)-8-(4-플루오로페닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실산 트리플루오로아세테이트
1-{3-[(tert-부톡시카보닐)아미노]프로필}-8-(4-플루오로페닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실산 및 2-{3-[(tert-부톡시카보닐)아미노]프로필}-8-(4-플루오로페닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복실산의 혼합물 165 ㎎(0.35 mmol)을 DCM에 현탁시키고, 60℃에서 2 ㎖의 TFA와 반응시켰다. 90 분 이내에 완결된 반응액을 증발시켰다. 조물질을 분취용-HP LC 방법 2에 의해서 정제하고, 2 개의 위치이성체의 혼합물로서 유도하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 4.2 min, 2 개의 위치이성체에 대해서 동일한 체류시간. 1H NMR(401 MHz, DMSO-d6) δ 8.83(s, 1H, 주), 8.71(s, 1H, 주), 8.41-8.51(m, 2H), 8.34(br. s., 3H), 7.26-7.42(m, 2H), 4.96(m, 2H, 부), 4.70-4.77(m, 2H, 주), 2.96-3.02(m, 2H), 2.88-2.95(m, 2H), 2.61(t, J=5.92 Hz, 2H), 2.11-2.21(m, 2H). HRMS(ESI) C19H18FN502에 대한 계산치 [M+H]+ 368.1518, 실측치 368.153.
실시예 33: 1-tert-부틸-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-S-, R2= tert-부틸, R3 = NH2, A = -CH=CH-](화합물 85), 및
6-아미노-1-tert-부틸-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-S-, R2= tert-부틸, R3 = NH2, R5 = NH2, A= -CH=CH-](화합물 86)
단계 6c
에틸 1-tert-부틸-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트(170 ㎎, 0.494 mmol)를 4 ㎖의 무수 THF에 현탁시키고, 암모늄 클로라이드(80 ㎎, 1.48 mmol)를 첨가하였다. 반응 혼합물을 0℃로 냉각시키고, THF 중의 1 M LiN(TMS)2(3 ㎖, 3 mmol)를 첨가하였다; 반응액을 2 시간 동안 교반하였다. 그 후, 용매를 증발 건조시키고, 잔류물을 물에 현탁시키고, 여과하였다. 조물질을 DCM/MeOH 97/3으로 용출시키는 실리카겔 칼럼 크로마토그래피에 의해서 정제하여 100 ㎎(65% 수율)의 1-tert-부틸-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 및 10 ㎎(6%)의 6-아미노-1-tert-부틸-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드를 제공하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 6.07 min. 1H NMR(401 MHz, DMSO-d6) δ 9.49(s, 1H), 8.42(d, J=8.54 Hz, 1H), 7.80(d, J=8.79 Hz, 1H), 7.75(br. s., 1H), 7.53(br. s., 1H), 2.74(s, 3H), 2.00(s, 9H). HRMS(ESI) C15H17N50S에 대한 계산치 [M+H]+ 316.1227, 실측치 316.1224.
6-아미노-1-tert-부틸-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[R1 = Me-S-, R2= tert-부틸, R3 = NH2, R5 = NH2, A= -CH=CH-]. LC/MS(254 ㎚) HPLC 방법 2 Rt 5.08 min. 1H NMR(401 MHz, DMSO-d6) δ 8.16(d, J=8.79 Hz, 1H), 7.91(d, J=8.79 Hz, 1H), 7.84(br. s., 2H), 7.62(br. s., 1H), 7.42(br. s., 1H), 2.61(s, 3H), 1.98(s, 9H). HRMS(ESI) C15H18N60S에 대한 계산치 [M+H]+ 331.1336, 실측치 331.1340
유사한 방식으로 수행하여 다음의 화합물들을 제조하였다:
1-메틸-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-S-, R2= Me, R3 = NH2, A= -CH=CH-](화합물 87). LC/MS(254 ㎚) HPLC 방법 2 Rt 4.96 min. 1H NMR(401 MHz, DMSO-d6) δ 9.46(s, 1H), 8.26(d, J=8.67 Hz, 1H), 7.85(br. s., 1H), 7.73(d, J=8.79 Hz, 1H), 7.52(br. s., 1H), 4.71(s, 3H), 2.73(s, 3H). HRMS(ESI) C12H11N50S에 대한 계산치 [M+H]+ 274.0757, 실측치 274.0757;
6-아미노-1-메틸-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-S-, R2= Me, R3 = NH2, R5 = NH2, A= -CH=CH-](화합물 88). LC/MS(254 ㎚) HPLC 방법 2 Rt 4.59. 1H NMR(401 MHz, DMSO-d6) δ 8.00(d, J=8.91 Hz, 1H), 7.85(br. s., 1H), 7.83(d, J=8.91 Hz, 1H), 7.74(br. s., 1H), 7.42(br. s., 1H), 4.65(s, 3H), 2.59(s, 3H). HRMS(ESI) C12H12N60S에 대한 계산치 [M+H]+ 289.0866, 실측치 289.0859;
1-tert-부틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Η, R2= tert-부틸, R3 = NH2, A = -CH=CH-](화합물 3). LC/MS(254 ㎚) HPLC 방법 2 Rt 4.63 min. 1H NMR(500 MHz, DMSO-d6) δ 9.71(s, 1H), 9.53(s, 1H), 8.55(d, J=8.79 Hz, 1H), 7.89(d, J=8.78 Hz, 1H), 7.80(br. s., 1H), 7.58(br. s., 1H), 2.01(s, 9H). HRMS(ESI) C14H15N50에 대한 계산치 [M+H]+ 270.1350, 실측치 270.1357; 및
6-아미노-1-tert-부틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Η, R2= tert-부틸, R3 = NH2, R5 = NH2, A = -CH=CH-](화합물 122). LC/MS(254 ㎚) HPLC 방법 2 Rt 4.29 min. 1H NMR(500 MHz, DMSO-d6) δ 8.65(s, 1H), 8.30(d, J=9.06 Hz, 1H), 8.12(br. s., 1H), 8.02(d, J=8.79 Hz, 1H), 7.70(br. s., 1H), 7.46-7.52(m, 1H), 1.98(s, 9H). HRMS(ESI) C14H16N60에 대한 계산치 [M+H]+ 285.1459, 실측치 285.1466.
실시예 34: 1-tert-부틸-N-하이드록시-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-S-, R2= tert-부틸, R3 = N(H)OH, A= -CH=CH-](화합물 89)
단계 6b2
40 ㎎(0.112 mmol)의 1-tert-부틸-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복실산을 실온에서 3 시간 동안, 무수 DMF(2 ㎖) 중에서 25 ㎎(0.21 mmol)의 0-(테트라하이드로-2H-피란-2-일)하이드록실아민, 70 ㎎(0.21 mmol)의 TBTU 및 0.110 ㎖(1.19 mmol)의 DIPEA와 반응시켰다. 반응액을 물 및 포화 NaHCO3로 후처리하고, 에틸 아세테이트로 추출하였다. Na2S04 상에서 건조시키고, 여과하고, 증발시킨 유기상을 DCM/EtOAc 7/3를 사용하여 실리카 상에서 정제하여 23 ㎎(50%)의 1-tert-부틸-8-(메틸설파닐)-N-(테트라하이드로-2H-피란-2-일옥시)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드를 제공하였다. LC/MS(m/z): 416.1 [M+H]+, HPLC(254 ㎚) 방법 3 Rt 6.94 min.
1-tert-부틸-8-(메틸설파닐)-N-(테트라하이드로-2H-피란-2-일옥시)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드를 메탄올(2 ㎖)에 용해시키고, 디옥산 중의 4 M HCl(2 ㎖)을 첨가하였다. 용액을 실온에서 2 시간 동안 교반하고, 이에 따라 휘발성 물질을 진공 중에서 제거하였다. 조물질을 우선, DCM/MeOH 6/1로 용출시키는 실리카겔에 의해서 정제하여 목적 생성물을 수득하고, 이것을 분취용 HPLC 정제방법 1에 적용하여 5 ㎎(30%)의 표제 생성물을 수득하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 4.95 min. 1H NMR(401 MHz, DMSO-d6) δ 11.16(s, 1H), 9.49(s, 1H), 9.15(br. s., 1H), 8.33(d, J=8.67 Hz, 1H), 7.80(d, J=8.67 Hz, 1H), 2.73(s, 3H), 1.99(s, 9H). HRMS(ESI) C15H17N502S에 대한 계산치[M+H]+ 332.1176, 실측치 332.1185.
실시예 35: 8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 [(I), R1 = Me-S-, R2= H, R3 = NH2, A = -CH=CH-](화합물 90)
단계 6c
에틸 8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복실레이트(210 ㎎, 0.76 mmol)를 4 ㎖의 무수 THF에 현탁시키고, 암모늄 클로라이드(120 ㎎, 2.28 mmol)를 첨가하였다. 반응 혼합물을 0℃로 냉각시키고, THF 중의 LiN(TMS)2(8 ㎖, 8.0 mmol)를 반응액에 첨가하고, 2 시간 동안 교반하였다. 그 후, 용매를 증발 건조시키고, 잔류물을 DCM으로 녹이고, 물 및 염수로 세척하였다. 유기층을 Na2S04 상에서 건조시키고, 여과하고, 진공 하에서 증발시켰다. 조물질을 DCM/MeOH 9/1로 용출시키는 실리카겔 칼럼 크로마토그래피에 의해서 정제하여 180 ㎎(86% 수율)의 표제 화합물을 제공하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 4.46 min. 1H NMR(401 MHz, DMSO-d6) δ 9.48(s, 1H), 8.24(d, J=8.79 Hz, 1H), 7.91(br. s., 1H), 7.71(d, J=8.67 Hz, 1H), 7.49(s, 1H), 2.75(s, 3H). HRMS(ESI) C11H9N50S에 대한 계산치[M+H]+ 260.0601, 실측치 260.0598
실시예 36: tert-부틸 4-[3-카바모일-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-1-일]피페리딘-1-카복실레이트 [(I), R1 = Me-S-, R2= tert-부틸 4-피페리딘 카복실레이트, R3 = NH2, A = -CH=CH-]
DMF(5 ㎖) 중의 150 ㎎(0.58 mmol)의 8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드의 용액, 205 ㎎(1.16 mmol)의 tert-부틸 4-브로모피페리딘-1-카복실레이트 및 377 ㎎(1.16 mmol)의 세슘 카보네이트를 80℃에서 18 시간 동안 반응시켰다. 혼합물을 실온으로 냉각시키고, 에틸 아세테이트와 물 사이에 분배시켰다. 유기상을 염수로 세척하고, Na2S04 상에서 건조시키고, 증발시켰다. 조물질을 DCM/EtOAc/EtOH 6/4/0.5로 용출시키는 칼럼 크로마토그래피에 의해서 정제하여 백색 고체로서 200 ㎎(78%)의 목적 화합물을 제공하였다. LC/MS(m/z): 443.1 [M+H]+, HPLC(254 ㎚) 방법 4 Rt 2.53.
유사한 방식으로 수행하여 다음의 화합물을 제조하였다:
tert-부틸 4-(3-카바모일-8-메톡시-1H-피라졸로[4,3-h]퀴나졸린-1-일)피페리딘-1-카복실레이트. LC/MS(m/z): 427.2 [M+H]+, HPLC(254 ㎚) 방법 3 Rt 5.61.
실시예 37: 8-(메틸설파닐)-1-(피페리딘-4-일)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드[(I), R1 = Me-S-, R2= 피페리딘-4-일, R3 = NH2, A = -CH=CH-](화합물 91)
tert-부틸 4-[3-카바모일-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-1-일]피페리딘-1-카복실레이트를 1,4-디옥산(2 ㎖)에 용해시키고, 1,4-디옥산 중의 4 M HCl(3 ㎖)을 첨가하였다. 용액을 실온에서 1 시간 동안 교반하였다. 휘발성 물질을 진공 중에서 제거하고, 잔류물을 디에틸 에테르와 함께 분쇄하고, 여과하고, 진공 하에 오븐(40℃ 내에서 2 시간 동안 건조시켜 25 ㎎(99%)의 표제 화합물을 수득하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 3.73 min. 1H NMR(401 MHz, DMSO-d6) δ 9.50(s, 1H), 8.85(br. s., 1H), 8.64-8.78(m, 1H), 8.29(d, J=8.67 Hz, 1H), 7.73-7.82(m, 2H), 7.64(s, 1H), 6.16(quin, J=7.05 Hz, 1H), 3.52-3.61(m, J=13.06 Hz, 2H), 3.08-3.21(m, 2H), 2.75(s, 3H), 2.37-2.47(m, 4H). HRMS(ESI) C16H18N60S에 대한 계산치 [M+H]+ 343.1336, 실측치 343.1326.
동일한 방법에 따라 적합한 출발물질을 사용하여 다음의 화합물들을 제조하였다:
8-(메틸설파닐)-1-(피페리딘-3-일)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드[(I), R1 = Me-S-, R2 = 피페리딘-3-일, R3 = NH2, A = -CH=CH-](화합물 92). LC/MS(254 ㎚) HPLC 방법 2 Rt 3.86 min. 1H NMR(401 MHz, DMSO-d6) δ 9.41-9.59(m, 1H), 9.27(br. s., 1H), 8.43(br. s., 1H), 8.20-8.38(m, 2H), 7.75-7.84(m, 1H), 7.69(s, 1H), 6.30(t, J=4.88 Hz, 1H), 3.90(d, J=12.33 Hz, 2H), 3.78(d, J=4.52 Hz, 2H), 2.74(br. s., 3H), 2.27-2.42(m, 3H), 2.14(dd, J=5.61, 14.16 Hz, 2H), 1.78(d, J=5.37 Hz, 2H). HRMS(ESI) C16H18N60S에 대한 계산치 [M+H]+ 343.1336, 실측치 343.1329;
1-(4-아미노사이클로헥실)-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드[(I), R1 = Me-S-, R2 = 4-아미노사이클로헥실, R3 = NH2, A = -CH=CH-](화합물 93). LC/MS(254 ㎚) HPLC 방법 2 Rt 4.05 min. 1H NMR(401 MHz, DMSO-d6) δ 9.48(s, 1H), 8.28(d, J=8.67 Hz, 1H), 8.00(br. s., 3H), 7.76(d, J=8.79 Hz, 1H), 7.72(s, 1H), 7.64(s, 1H), 6.18(br. s., 1H), 2.69(s, 3H), 2.25-2.37(m, 2H), 2.06-2.19(m, 4H), 1.79-1.95(m, 2H). HRMS(ESI) C17H20N6OS에 대한 계산치 [M+H]+ 357.1492, 실측치 357.1491;
8-(메틸설파닐)-1-(피페리딘-3-일메틸)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드[(I), R1 = Me-S-, R2 = 피페리딘-3-일메틸, R3 = NH2, A = -CH=CH-](화합물 94). LC/MS(254 ㎚) HPLC 방법 2 Rt 3.94 min. 1H NMR(401 MHz, DMSO-d6) δ 1H 9.50(s, 1H), 8.63(d, J=10.99 Hz, 1H), 8.34-8.40(m, 1H), 8.30(d, J=8.67 Hz, 1H), 7.80(s, 1H), 7.78(d, J=8.79 Hz, 1H), 7.63(s, 1H), 5.01-5.19(m, 2H), 3.20(d, J=13.79 Hz, 2H), 3.02(d, J=12.45 Hz, 1H), 2.76-2.88(m, 2H), 2.74(s, 3H), 2.55-2.66(m, 1H), 1.67-1.85(m, 2H), 1.31-1.64(m, 2H). HRMS(ESI) C17H20N6OS에 대한 계산치 [M+H]+ 357.1492, 실측치 357.1489;
1-(아제판-4-일)-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드[(I), R1 = Me-S-, R2 = 아제판-4-일, R3 = NH2, A = -CH=CH-](화합물 95). LC/MS(254 ㎚) HPLC 방법 2 Rt 3.94 min. 1H NMR(401 MHz, DMSO-d6) δ 9.49(m, 1H), 8.87(br. s., 2H), 8.28(d, J=8.79 Hz, 1H), 7.83(s, 1H), 7.76(d, J=8.79 Hz, 1H), 7.63(s, 1H), 6.05-6.59(m, 1H), 3.46-3.66(m, 2H), 3.10-3.24(m, 1H), 2.72(s, 3H), 2.53-2.59(m, 2H), 2.39-2.46(m, 1H), 2.25-2.35(m, 1H), 2.04-2.17(m, 1H), 1.75-1.95(m, 1H). HRMS(ESI) C17H20N6OS에 대한 계산치 [M+H]+ 357.1492, 실측치 357.1509;
1-(3-아미노-2,2-디메틸프로필)-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드[(I), R1 = Me-S-, R2 = 3-아미노-2,2-디메틸프로필, R3 = NH2, A = -CH=CH-](화합물 96). LC/MS(254 ㎚) HPLC 방법 2 Rt 4.08 분. 1H NMR(401 MHz, DMSO-d6) δ 9.50(s, 1H), 8.32(d, J=8.67 Hz, 1H), 7.99(br. s., 3H), 7.94(s, 1H), 7.78(d, J=8.79 Hz, 1H), 7.71(s, 1H), 5.29(s, 2H), 2.89(q, J=6.43 Hz, 1H), 2.75(s, 3H), 1.02(s, 6H). HRMS(ESI) C16H20N6OS에 대한 계산치 [M+H]+ 345.1492, 실측치 345.1502;
8-메톡시-1-(피페리딘-4-일)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드[(I), R1 = Me-O-, R2 = 피페리딘-4-일, R3 = NH2, A = -CH=CH-](화합물 97). LC/MS(254 ㎚) HPLC 방법 2 Rt 3.43 min. 1H NMR(401 MHz, DMSO-d6) δ 9.55(s, 1H), 8.65-8.79(m, 1H), 8.68(br. s., 1H), 8.45-8.58(m, 1H), 8.53(br. s., 1H), 8.22(d, J=8.67 Hz, 1H), 7.79(d, J=8.79 Hz, 1H), 7.75(s, 1H), 7.62(s, 1H), 6.10(quind, J=4.66, 9.67 Hz, 1H), 4.16(s, 3H), 3.51-3.65(m, J=12.45 Hz, 1H), 3.18-3.26(m, 2H), 2.37-2.46(m, 4H). HRMS(ESI) C16H18N602에 대한 계산치 [M+H]+ 327.1564, 실측치 327.15575; 및
8-메톡시-1-(피페리딘-4-일메틸)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드[(I), R1 = Me-O-, R2 = 피페리딘-4-일메틸, R3 = NH2, A = -CH=CH-](화합물 98). LC/MS(254 ㎚) HPLC 방법 2 Rt 3.54 min. 1H NMR(401 MHz, DMSO-d6) δ 9.53(s, 1H), 8.72-8.89(m, 1H), 8.57-8.70(m, J=9.52 Hz, 1H), 8.21(d, J=8.67 Hz, 1H), 7.80(br. s., 1H), 7.77(d, J=8.79 Hz, 1H), 7.57(s, 1H), 5.09(d, J=7.32 Hz, 2H), 4.16(s, 3H), 3.18-3.26(m, J=12.69 Hz, 2H), 2.72-2.89(m, 2H), 2.40-2.47(m, 1H), 1.50-1.68(m, 4H). HRMS(ESI) C17H20N6O2에 대한 계산치 [M+H]+ 341.1721, 실측치 341.1721.
실시예 38: 1-[(3-엑소)-8-아자비사이클로[3.2.1]옥트-3-일]-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 [(I), R1 = Me-S-, R2 = 8-아자비사이클로[3.2.1]옥트-3-일, R3 = NH2, A = -CH=CH-](화합물 99)
DMF(8 ㎖) 중의 50 ㎎(0.193 mmol)의 8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드를 90℃에서 4 시간 동안 200 ㎎(0.52 mmol)의 2,2,2-트리클로로에틸 3-[(메틸설포닐)옥시]-8-아자비사이클로[3.2.1]옥탄-8-카복실레이트 및 140 ㎎(0.43 mmol)의 세슘 카보네이트와 반응시켰다. 혼합물을 실온으로 냉각시키고, 에틸 아세테이트와 물 사이에 분배시켰다. 유기상을 염수로 세척하고, Na2S04 상에서 건조시키고, 증발시켰다. 조물질을 DCM/EtOH 9/1로 용출시키는 칼럼 크로마토그래피에 의해서 정제하여 회백색 고체로서 73 ㎎(70%)의 2,2,2-트리클로로에틸 3-[3-카바모일-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-1-일]-8-아자비사이클로[3.2.1]옥탄-8-카복실레이트를 제공하였다. 이 화합물(134 mmol)을 THF(5 ㎖)에 용해시키고, 아세트산(5 ㎖) 및 35 ㎎(0.536 mmol)의 아연 분말을 첨가하였다. 혼합물을 50℃까지 가열하고, 18 시간 동안 교반하였다. 휘발성 물질을 진공 중에서 제거하고, 잔류물을 DCM/MeOH 95/5로 용출시키는 크로마토그래피에 의해서 정제하였다. 추가의 정제가 필요하였으며, 분취용-HPLC 방법 1에 의해서 수행하여 25 ㎎(50%)의 표제 화합물을 수득하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 4.08 min. 1H NMR(401 MHz, DMSO-d6) δ 9.50(s, 1H), 8.25(d, J=8.67 Hz, 1H), 7.62-7.79(m, 3H), 7.52-7.60(m, 1H), 6.21-6.54(m, OH), 3.68(br. s., 2H), 2.76(s, 2H), 2.22-2.36(m, 2H), 2.02(br. s., 2H), 1.78-1.98(m, 5H). HRMS(ESI) C18H20N6OS에 대한 계산치 [M+H]+ 369.1492, 실측치 369.15.
유사한 방식으로 수행하여 다음의 화합물을 제조하였다:
1-[(3-엔도)-8-아자비사이클로[3.2.1]옥트-3-일]-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 트리플루오로아세테이트 [(I), R1 = Me-S-, R2 = 8-아자비사이클로[3.2.1]옥트-3-일, R3 = NH2, A = -CH=CH-](화합물 100). LC/MS(254 ㎚) HPLC 방법 2 Rt 3.0 min. 1H NMR(401 MHz, DMSO-d6) δ 9.49(s, 1H), 8.66(br. s., 1H), 8.32(d, J=8.79 Hz, 1H), 7.85(s, 1H), 7.79(d, J=8.79 Hz, 1H), 7.63(s, 1H), 6.07(t, J=8.12 Hz, 1H), 4.07(br. s., 2H), 2.81(ddd, J=4.09, 8.03, 16.20 Hz, 2H), 2.72(s, 3H), 2.63(d, J=16.36 Hz, 2H), 2.05-2.19(m, 2H), 1.79-1.94(m, 2H). HRMS(ESI) C18H20N6OS에 대한 계산치 [M+H]+ 369.1492, 실측치 369.1484.
실시예 39: 1-[4-(1,3-디옥소-1,3-디하이드로-2H-이소인돌-2-일)부탄-2-일]-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 [(I), R1 = Me-S-, R2 = 4-(1,3-디옥소-1,3-디하이드로-2H-이소인돌-2-일)부탄-2-일, R3 = NH2, A = -CH=CH-](화합물 101)
DMF(3 ㎖) 중의 50 ㎎(0.193 mmol)의 8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드를 80℃에서 3 시간 동안 108 ㎎(0.38 mmol)의 2-(4-브로모-3-메틸부틸)-1H-이소인돌-1,3(2H)-디온 및 132 ㎎(0.38 mmol)의 세슘 카보네이트와 반응시켰다. 혼합물을 실온으로 냉각시키고, 에틸 아세테이트와 물 사이에 분배시켰다. 유기상을 염수로 세척하고, Na2S04 상에서 건조시키고, 농축시켰다. 조물질을 DCM/EtOH 9/1로 용출시키는 칼럼 크로마토그래피에 의해서 정제하여 연황색 고체로서 57 ㎎(65%)의 목적 화합물을 제공하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 6.01 min. 1H NMR(401 MHz, DMSO-d6) δ 9.38(s, 1H), 8.21(d, J=8.67 Hz, 1H), 7.71-7.76(m, 2H), 7.69(d, J=8.79 Hz, 1H), 7.53-7.60(m, 2H), 6.29-6.45(m, 1H), 3.41-3.58(m, 2H), 2.72(dt, J=5.25, 9.70 Hz, 1H), 2.45(d, J=7.57 Hz, 1H), 2.41(s, 3H), 1.59(d, J=6.59 Hz, 3H). HRMS(ESI) C23H20N6O3S에 대한 계산치 [M+H]+ 461.1391, 실측치 461.1412.
실시예 40: 1-(4-아미노부탄-2-일)-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-S-, R2 = 4-아미노부탄-2-일, R3 = NH2, A = -CH=CH-](화합물 102)
THF(5 ㎖) 중의 45 ㎎(0.097 mmol)의 1-[4-(1,3-디옥소-1,3-디하이드로-2H-이소인돌-2-일)부탄-2-일]-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드의 용액에 THF 중의 1 M 하이드라진(5 ㎖)을 첨가하였다. 혼합물을 50℃에서 3 시간 동안 교반하였다. 혼합물을 실온으로 냉각시키고, 여과하고, 휘발성 물질을 진공 하에서 제거하고, 조물질을 분취용-HPLC 방법 1에 적용하여 20 ㎎(60%)의 표제 생성물을 수득하였다. LC/MS(254 ㎚) HPLC 방법 x Rt 3.98 min. 1H NMR(401 MHz, DMSO-d6) δ 9.50(s, 1H), 8.29(d, J=8.67 Hz, 1H), 7.81(s, 1H), 7.77(d, J=8.79 Hz, 1H), 7.62(d, J=10.25 Hz, 2H), 6.23(br. s., 1H), 2.87(td, J=5.66, 11.50 Hz, 1H), 2.71(s, 3H), 2.61(dt, J=6.41, 11.81 Hz, 1H), 2.14-2.30(m, 1H), 1.66(d, J=6.59 Hz, 3H). HRMS(ESI) C15H18N60S에 대한 계산치 [M+H]+ 331.1336, 실측치 331.134.
실시예 41: 1-(1-아자비사이클로[2.2.2]옥트-3-일)-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-S-, R2 = 아자비사이클로[2.2.2]옥트-3-일, R3 = NH2, A = -CH= -](화합물 103)
DMF(3 ㎖) 중의 64 ㎎(0.247 mmol)의 8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드의 용액에 300 ㎎(1.06 mmol)의 1-아자비사이클로[2.2.2]옥트-3-일-4-메틸벤젠설포네이트(문헌 [Tetrahedron . Lett . 2000 41, 271-274]에 기술된 방법에 따라 제조) 및 55 ㎎(0.494 mmol)의 칼륨 tert-부톡사이드를 첨가하였다. 혼합물을 100℃까지 가열하고, 4 시간 동안 교반하였다. 반응 혼합물을 실온에서 냉각시키고, 에틸 아세테이트와 물 사이에 분배시켰다. 유기상을 염수로 세척하고, Na2S04 상에서 건조시키고, 증발시켰다. 조물질을 DCM/MeOH/NH4OH 9/1/0.5로 용출시키는 칼럼 크로마토그래피에 의해서 정제하여 14 ㎎(15%)의 목적 생성물을 수득하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 4.73 min. 1H NMR(401 MHz, DMSO-d6) δ 9.46(s, 1H), 8.17-8.41(m, 1H), 7.87-8.00(m, 1H), 7.68-7.80(m, 1H), 7.54(s, 1H), 5.94-6.38(m, 1H), 4.01(dd, J=4.09, 13.98 Hz, 1H), 3.37-3.48(m, 1H), 2.75-2.95(m, 3H), 2.73(s, 3H), 2.20-2.29(m, 1H), 1.80-1.95(m, 1H), 1.75(ddd, J=4.76, 8.48, 13.12 Hz, 1H), 1.34-1.47(m, 1H), 1.20-1.35(m, 1H). HRMS(ESI) C18H20N6OS에 대한 계산치 [M+H]+ 369.1492, 실측치 369.1508.
실시예 42: 8-(메틸설파닐)-1-(테트라하이드로-2H-피란-4-일)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-S-, R2 = 테트라하이드로-2H-피란-4-일, R3 = NH2, A = -CH= -](화합물 104)
DMF(3 ㎖) 중의 30 ㎎(0.247 mmol)의 8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드의 용액에 62 ㎎(0.34 mmol)의 테트라하이드로-2H-피란-4-일 메탄설포네이트(US 2003/6653489에 따라 제조) 및 87 ㎎(0.266 mmol)의 세슘 카보네이트를 첨가하였다. 혼합물을 80℃까지 가열하고, 4 시간 동안 교반하였다. 반응 혼합물을 실온에서 냉각시키고, 에틸 아세테이트와 물 사이에 분배시켰다. 유기상을 염수로 세척하고, Na2SO4 상에서 건조시키고 증발시켰다. 조물질을 DCM/MeOH/NH4OH 9/1/0.5로 용출시키는 칼럼 크로마토그래피에 의해서 정제하여 32 ㎎(38%)의 목적 생성물을 수득하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 5.41 min. 1H NMR(401 MHz, DMSO-d6) δ 9.47(s, 1H), 8.28(d, J=8.67 Hz, 1H), 7.84(br. s., 1H), 7.75(d, J=8.79 Hz, 1H), 7.54(s, 1H), 6.25(tt, J=4.32, 11.37 Hz, 1H), 4.11(dd, J=4.15, 11.47 Hz, 1H), 3.48-3.65(m, 1H), 2.75(s, 3H), 2.23-2.40(m, 2H), 2.13(dd, J=2.38, 12.39 Hz, 2H). HRMS(ESI) C16H17N502S에 대한 계산치 [M+H]+ 344.1176, 실측치 344.1166.
실시예 43: 메틸 3-[3-카바모일-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-1-yl]사이클로부탄카복실레이트[(I), R1 = Me-S-, R2 = 메틸 3-사이클로부탄카복실레이트, R3 = NH2, A = -C =CH-]
DMF(5 ㎖) 중의 100 ㎎(0.38 mmol)의 8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드의 용액에 200 ㎎(0.89 mmol)의 메틸 2-메틸-4-[(메틸설포닐)옥시]펜타노에이트(WO2009/71509 A1에 기술된 방법에 따라 제조) 및 191 ㎎(0.55 mmol)의 세슘 카보네이트를 첨가하였다. 혼합물을 90℃에서 18 시간 동안 가열하였다. 혼합물을 실온에서 냉각시키고, 에틸 아세테이트와 물 사이에 분배시켰다. 유기상을 염수로 세척하고, Na2SO4 상에서 건조시키고 증발시켰다. 조물질을 DCM/EtOH 9/1로 용출시키는 칼럼 크로마토그래피에 의해서 정제하여 백색 고체로서 100 ㎎(70%)의 목적 화합물을 제공하였다. 생성물은 시스 및 트랜스 이성체의 혼합물을 함유하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 5.55 min. 1H NMR(401 MHz, DMSO-d6) δ 9.44-9.51(m, 1H), 8.26(dd, J=1.89, 8.73 Hz, 1H), 7.87-8.02(m, 1H), 7.72-7.77(m, 1H), 7.58(br. s., 1H), 6.24-6.93(m, 1H), 3.66-3.76(m, 3H), 3.29(s, 3H), 3.04-3.25(m, 2H), 2.79-3.02(m, 3H). HRMS(ESI) C17H17N503S에 대한 계산치 [M+H]+ 372.1125, 실측치 372.1119.
유사한 방식으로 수행하여 다음의 화합물을 제조하였다:
메틸 2-[3-카바모일-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-1-일]-2-메틸프로파노에이트 LC/MS(m/z): 360.1 [M+H]+, HPLC(254 ㎚) 방법 3 Rt 4.75
실시예
44
1-[트랜스-3-(하이드록시메틸)사이클로부틸]-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-S-, R2 = 트랜스-3-(하이드록시메틸)사이클로부틸, R3 = NH2, A = -CH=CH-](화합물 105), 및
1-[시스-3-(하이드록시메틸)사이클로부틸]-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-S-, R2 = 시스-3-(하이드록시메틸)사이클로부틸, R3 = NH2, A = -CH=CH-](화합물 106)
전환 i
에탄올(5 ㎖) 중의 70 ㎎(0.188 mmol)의 메틸 3-[3-카바모일-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-1-일]사이클로부탄카복실레이트(시스 및 트랜스 혼합물)의 용액에 30 ㎎(0.75 mmol)의 나트륨 보로하이드라이드를 조심해서 첨가하였다. 혼합물을 실온에서 18 시간 동안 교반하였다. 용매를 제거한 후에, 잔류물을 에틸 아세테이트(20 ㎖), 물(10 ㎖) 및 포화 NH4Cl 수용액(10 ㎖)로 녹였다. 층들을 혼합시키고, 분리시켰다. 유기 추출물을 염수로 세척하고, Na2SO4 상에서 건조시킨 다음에, 여과하고 농축시켰다. 조생성물을 칼럼 크로마토그래피(DCM/EtOAc/EtOH 7/2/1)에 의해서 정제하여 회백색 고체로서 생성물을 제공하고, 이것을 다음의 시스/트랜스 이성체 분할을 위해 분취용-HPLC에 적용하였다:
1-[시스-3-(하이드록시메틸)사이클로부틸]-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드. LC/MS(254 ㎚) HPLC 방법 2 Rt 5.04 min. 1H NMR(401 MHz, DMSO-d6) δ 9.46(s, 1H), 8.26(d, J=8.67 Hz, 1H), 7.84(s, 1H), 7.73(d, J=8.79 Hz, 1H), 7.57(s, 1H), 6.39(quin, J=8.33 Hz, 1H), 4.55-4.67(m, 1H), 3.55(d, J=6.10 Hz, 2H), 2.73(s, 3H), 2.57-2.65(m, J=6.35 Hz, 1H), 2.51-2.54(m, 2H), 2.31-2.40(m, 1H). HRMS(ESI) C16H17N502S에 대한 계산치 [M+H]+ 344.1176, 실측치 344.1167; 및
1-[트랜스-3-(하이드록시메틸)사이클로부틸]-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드. LC/MS(254 ㎚) HPLC 방법 2 Rt 4.91 min. 1H NMR(401 MHz, DMSO-d6) δ 9.39-9.48(m, 1H), 8.14-8.34(m, 1H), 7.82-8.00(m, 1H), 7.73(d, J=8.79 Hz, 1H), 7.56(s, 1H), 6.64(quin, J=7.78 Hz, 1H), 4.71-4.97(m, 1H), 3.53-3.75(m, 2H), 2.82-2.97(m, 2H), 2.73-2.78(m, 3H), 2.37-2.47(m, 2H). HRMS(ESI) C16H17N502S에 대한 계산치 [M+H]+ 344.1176, 실측치 344.1174.
유사한 방식으로 수행하여 다음의 화합물들을 제조하였다:
1-(1-하이드록시-2-메틸프로판-2-일)-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-S-, R2 = 1-하이드록시-2-메틸프로판-2-일, R3 = NH2, A = -CH=CH-](화합물 107). LC/MS(m/z): 332.08 [M+H]+, HPLC(254 ㎚) 방법 1 Rt 1.14; 및
1-(1-하이드록시-2-메틸프로판-2-일)-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-S-, R2 = 1-하이드록시-2-메틸프로판-2-일, R3 = NH2, A = -(CH2)2-](화합물 108). LC/MS(m/z): 334.1 [M+H]+, HPLC(254 ㎚) 방법 1 Rt 0.63.
실시예 45: tert-부틸 4-(3-카바모일-8-페닐-1H-피라졸로[4,3-h]퀴나졸린-1-일)피페리딘-1-카복실레이트[(I), R1 = 페닐, R2 = tert-부틸 4-피페리딘-1-카복실레이트, R3 = NH2, A = -CH=CH-]
전환 l
건조 마이크로웨이브 처리 바이알을 30 ㎎(0.068 mmol)의 tert-부틸 4-[3-카바모일-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-1-일]피페리딘-1-카복실레이트, 3 ㎖의 무수 THF, 16.5 ㎎(0.138 mmol)의 페닐보론산, 38.7 ㎎(0.203 mmol)의 구리 티오펜카복실레이트, 및 7.8 ㎎(0.007 mmol, 10 mol%)의 Pd(PPh3)4로 충전시켰다. 이어서, 혼합물을 100℃의 마이크로웨이브 반응기 내에서 60 분 동안 가열하였다. 냉각시킨 후에, 혼합물을 에틸 아세테이트로 희석하고, 25% 수성 암모니아로 세척하였다. 수층을 다시 에틸 아세테이트로 추출하고, 유기상을 합하여 Na2S04 상에서 건조시키고, 증발시킨 후의 잔류물을 실리카겔 상에서의 칼럼 크로마토그래피(DCM/EtOAc/EtOH, 6/4/0,2)에 의해서 정제하여 백색 고체로서 29 ㎎(90%)의 표제 생성물을 제공하였다. LC/MS(m/z): 473.0 [M+H]+, HPLC(254 ㎚) 방법 4 Rt 2.95.
실시예 46: 8-페닐-1-(피페리딘-4-일)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드[(I), R1 = 페닐, R2 = 피페리딘-4-일, R3 = NH2, A = -CH=CH-](화합물 109)
tert-부틸 4-(3-카바모일-8-페닐-1H-피라졸로[4,3-h]퀴나졸린-1-일)피페리딘-1-카복실레이트를 1,4-디옥산(2 ㎖)에 용해시키고, 1,4-디옥산 중의 4 M HCl(3 ㎖)을 첨가하였다. 용액을 실온에서 1 시간 동안 교반하였다. 휘발성 물질을 진공 중에서 제거하고, 잔류물을 디에틸 에테르와 함께 분쇄하고, 여과하고, 진공 하에 오븐(40℃) 내에서 2 시간 동안 건조시켜 27 ㎎(99%)의 표제 화합물을 수득하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 4.47 min. 1H NMR(401 MHz, DMSO-d6) δ 9.82(s, 1H), 8.94(br. s., 1H), 8.85(br. s., 1H), 8.52-8.66(m, 2H), 8.41(d, J=8.67 Hz, 1H), 7.89(d, J=8.67 Hz, 1H), 7.84(br. s., 1H), 7.57-7.73(m, 4H), 6.16-6.37(m, 1H), 3.54-3.67(m, 2H). HRMS(ESI) C21H20N6O에 대한 계산치 [M+H]+ 373.1771, 실측치 373.1783
유사한 방식으로 수행하여 다음의 화합물들을 제조하였다:
1-(피페리딘-4-일)-8-(티오펜-3-일)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 트리플루오로아세테이트[(I), R1 = 티오펜-3-일, R2 = 피페리딘-4-일, R3 = NH2, A = -CH=CH-](화합물 110). LC/MS(254 ㎚) HPLC 방법 2 Rt 4.32 min. 1H NMR(401 MHz, DMSO-d6) δ 9.74(s, 1H), 8.69(br. s., 1H), 8.64(dd, J=1.10, 3.05 Hz, 1H), 8.59(br. s., 1H), 8.37(d, J=8.67 Hz, 1H), 8.03(dd, J=0.98, 5.00 Hz, 1H), 7.85(d, J=8.79 Hz, 1H), 7.80(s, 1H), 7.77(dd, J=3.05, 5.00 Hz, 1H), 7.65(s, 1H), 6.11-6.43(m, 1H), 3.48-3.73(m, J=12.94 Hz, 2H), 3.35-3.42(m, 2H). HRMS(ESI) C19H18N60S에 대한 계산치 [M+H]+ 379.1336, 실측치 379.1332;
1-(4-아미노사이클로헥실)-8-페닐-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드[(I), R1 = 페닐, R2 = 4-아미노사이클로헥실, R3 = NH2, A = -CH=CH-](화합물 111). LC/MS(254 ㎚) HPLC 방법 2 Rt 3.91 min. 1H NMR(401 MHz, DMSO-d6) δ 9.79(s, 1H), 8.59(dd, J=1.89, 7.75 Hz, 2H), 8.40(d, J=8.67 Hz, 1H), 8.04(br. s., 3H), 7.86(d, J=8.79 Hz, 1H), 7.73(br. s., 1H), 7.69(br. s., 1H), 7.56-7.67(m, 3H), 6.32(quin, J=4.61 Hz, 1H), 2.10-2.46(m, 6H), 1.85-2.03(m, J=4.52 Hz, 2H). HRMS(ESI) C22H22N60에 대한 계산치 [M+H]+ 387.1928, 실측치 387.1929; 및
1-(4-아미노사이클로헥실)-8-(티오펜-3-일)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 트리플루오로아세테이트[(I), R1 = 티오펜-3-일, R2 = 4-아미노사이클로헥실, R3 = NH2, A = -CH=CH-](화합물 112). LC/MS(254 ㎚) HPLC 방법 2 Rt 3.73 min. 1H NMR(401 MHz, DMSO-d6) δ 9.71(s, 1H), 8.51-8.69(m, 1H), 8.36(d, J=8.67 Hz, 1H), 7.99(d, J=5.13 Hz, 1H), 7.89(br. s., 2H), 7.83(d, J=8.79 Hz, 1H), 7.76(dd, J=3.05, 5.00 Hz, 2H), 7.58(s, 1H), 6.27(quin, J=4.61 Hz, 1H), 3.38-3.46(m, J=4.64 Hz, 1H), 2.31-2.42(m, 2H), 2.20-2.31(m, 2H), 2.04-2.18(m, 2H), 1.96(dd, J=5.00, 13.06 Hz, 1H). HRMS(ESI) C20H20N6OS에 대한 계산치 [M+H]+ 393.1492, 실측치 393.1481.
실시예 47: tert-부틸 4-[3-카바모일-8-(메틸설포닐)-1H-피라졸로[4,3-h]퀴나졸린-1-일]피페리딘-1-카복실레이트[(I), R4 = Me, X = S02, R2 = tert-부틸 4-피페리딘-1-카복실레이트, R3 = NH2, A = -CH=CH-]
100 ㎎(0.225 mmol)의 tert-부틸 4-[3-카바모일-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-1-일]피페리딘-1-카복실레이트를 10 ㎖의 DCM에 용해시켰다. 77.3 ㎎(0.448 mmol)의 mCPBA(m-클로로퍼벤조산)를 실온에서 첨가하고, 동일한 온도에서 60 분 동안 교반하였다. 1 ㎖의 포화 나트륨 설파이트 수용액을 첨가하고, 30 분 동안 교반하였다. 반응 혼합물을 염수로 세척하고, Na2O4 상에서 건조시키고, 감압 하에서 농축시켜 황색 고체로서 100 ㎎(94%)의 표제 화합물을 제공하였다. LC/MS(m/z): 475.0 [M+H]+, HPLC(254 ㎚) 방법 4 Rt 2.01 min.
실시예 48: 1-(피페리딘-4-일)-8-(피롤리딘-1-일)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드[(I), R1 = 피롤리딘-1-일, R2 = 피페리딘-4-일, R3 = NH2, A = -CH=CH-](화합물 113)
THF(3 ㎖) 중의 30 ㎎(0.063 mmol)의 tert-부틸 4-[3-카바모일-8-(메틸설포닐)-1H-피라졸로[4,3-h]퀴나졸린-1-일]피페리딘-1-카복실레이트의 용액에 70 ㎕(1 mmol)의 피롤리딘을 첨가하였다. 용액을 실온에서 1 시간 동안 교반하고, LC/MS에 의해서 모니터링하였다. 반응 혼합물을 실온으로 냉각시키고; 분리된 고체를 여과하고 디에틸 에테르로 세척하여 15 ㎎(50%)의 tert-부틸 4-[3-카바모일-8-(피롤리딘-1-일)-1H-피라졸로[4,3-h]퀴나졸린-1-일]피페리딘-1-카복실레이트를 수득하였다. LC/MS(m/z): 475.0 [M+H]+, HPLC(254 ㎚) 방법 4 Rt 2.01 min.
15 ㎎(0.032 mmol)의 tert-부틸 4-[3-카바모일-8-(피롤리딘-1-일)-1H-피라졸로[4,3-h]퀴나졸린-1-일]피페리딘-1-카복실레이트를 1,4-디옥산(2 ㎖)에 용해시키고, 1,4-디옥산 중의 4 M HCl 3 ㎖(3 mmol)를 첨가하였다. 혼합물을 실온에서 1 시간 동안 교반하였다. 휘발성 물질을 진공 중에서 제거하고, 수득된 잔류물을 디에틸 에테르와 함께 분쇄하고, 여과하고, 건조시켜 12 ㎎(93%)의 표제 화합물을 수득하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 4.11 min. 1H NMR(401 MHz, DMSO-d6) δ 9.11-9.31(m, 1H), 8.89(br. s., 1H), 8.57-8.82(m, 1H), 7.89(d, J=8.67 Hz, 1H), 7.64(br. s., 1H), 7.41-7.58(m, 2H), 5.80-6.23(m, 1H), 3.69(br. s., 4H), 3.50-3.62(m, 2H), 3.07-3.27(m, 2H), 2.35-2.45(m, 4H), 1.94-2.15(m, 4H). HRMS(ESI) C19H23N70에 대한 계산치 [M+H]+ 366.2037, 실측치 366.2047.
유사한 방식으로 수행하여 다음의 화합물을 제조하였다:
8-(모르폴린-4-일)-1-(피페리딘-4-일)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드[(I), R1 = 피롤리딘-1-일, R2 = 피페리딘-4-일, R3 = NH2, A = -CH=CH-](화합물 114). LC/MS(254 ㎚) HPLC 방법 2 Rt 3.92 min. 1H NMR(401 MHz, DMSO-d6) δ 9.31(s, 1H), 8.82(br. s., 1H), 8.73(br. s., 1H), 7.98(d, J=8.67 Hz, 1H), 7.64-7.73(m, 1H), 7.51-7.62(m, 2H), 5.87-6.09(m, 1H), 3.85-3.91(m, 4H), 3.72-3.80(m, 4H), 3.54(d, J=13.43 Hz, 2H), 3.18(d, J=5.86 Hz, 3H), 2.35-2.44(m, 4H). HRMS(ESI) C19H23N702에 대한 계산치 [M+H]+ 382.1986, 실측치 382.2004.
실시예 49: 1-{[1-(2-아미노에틸)피페리딘-4-일]메틸}-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드[(I), R1 = Me-S-, R2 = 1-(2-아미노에틸)피페리딘-4-일]메틸, R3 = NH2, A = -CH=CH-](화합물 115)
전환 n
메탄올(1.5 ㎖) 및 DMF(1 ㎖) 중의 26 ㎎(0.073 mmol)의 8-(메틸설파닐)-1-(피페리딘-4-일메틸)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드의 용액에 13 ㎕(0.219 mmol)의 아세트산, 69.6 ㎎(0.438 mmol)의 tert-부틸(2-옥소에틸)카바메이트 및 28 ㎎(0.438 mmol)의 NaCNBH3를 첨가하였다. 혼합물을 실온에서 18 시간 동안 교반하고, 이에 따라 휘발성 물질을 진공 중에서 제거하였다. 잔류물을 에틸 아세테이트에 용해시키고, 물에 의해서 분배시켰다; 유기층을 염수로 세척하고, Na2S04 상에서 건조시키고, 농축시켰다. 조물질을 섬광 크로마토그래피(DCM/MeOH 95/5)에 의해서 정제하여 백색 고체로서 27 ㎎(75%)의 tert-부틸 [2-(4-{[3-카바모일-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-1-일]메틸}피페리딘-1-일)에틸]카바메이트를 제공하였다. LC/MS(254) HPLC 방법 2 Rt 3.86 min. 1H NMR(401 MHz, DMSO-d6) δ 9.47(s, 1H), 8.28(d, J=8.67 Hz, 1H), 7.81(s, 1H), 7.74(d, J=8.79 Hz, 1H), 7.54(br. s., 1H), 6.56(br. s., 1H), 5.08(d, J=7.32 Hz, 2H), 2.93-3.05(m, 2H), 2.76-2.84(m, J=10.25 Hz, 2H), 2.71(s, 3H), 2.27(br. s., 1H), 2.14(br. s., 1H), 1.75-1.94(m, 2H), 1.12-1.49(m, 17H). HRMS(ESI) C24H33N703S에 대한 계산치 [M+H]+ 500.2439, 실측치 500.2436.
수득된 tert-부틸 [2-(4-{[3-카바모일-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-1-일]메틸}피페리딘-1-일)에틸]카바메이트를 1,4-디옥산 중의 4 M HCl 2 ㎖에 용해시키고, 실온에서 2 시간 동안 교반하였다. 그 후에, 휘발성 물질을 진공 중에서 제거하고, 잔류물을 디에틸 에테르로 현탁시키고, 여과하여 연황색 고체로서 14 ㎎(90%)의 목적 생성물을 제공하였다. LC/MS(254) HPLC 방법 2 Rt 3.29 min. 1H NMR(401 MHz, DMSO-d6) δ 10.78(br. s., 1H), 9.49(s, 1H), 8.30(d, J=8.67 Hz, 1H), 8.12-8.24(m, 2H), 7.86(s, 1H), 7.77(d, J=8.79 Hz, 1H), 7.58(s, 1H), 5.12(d, J=7.32 Hz, 1H), 3.47-3.54(m, 2H), 3.16-3.28(m, 3H), 2.85-3.01(m, 1H), 2.76(s, 2H), 1.73-1.88(m, 2H), 1.60-1.71(m, 2H). HRMS(ESI) C19H25N70S에 대한 계산치 [M+H]+ 400.1914, 실측치 400.1918.
유사한 방식으로 수행하여 다음의 화합물들을 제조하였다:
1-{4-[(2-아미노에틸)아미노]사이클로헥실}-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드[(I), R1 = Me-S- , R2 = 4-(2-아미노에틸)아미노사이클로헥실, R3 = NH2, A = -CH=CH-](화합물 116). HRMS(ESI) C19H25N70S에 대한 계산치 [M+H]+ 400.1914, 실측치 400.1908; 및
1-{4-[(2-아미노에틸)아미노]사이클로헥실}-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드 [(I), R1 = Me-S- , R2 = 4-(2-아미노에틸)아미노사이클로헥실, R3 = NH2, A = -(CH2)2-](화합물 117). HRMS(ESI) C19H27N70S에 대한 계산치 [M+H]+ 402.2071, 실측치 402.2074.
실시예 50: 1-[4-(글리실아미노)사이클로헥실]-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드[(I), R1 = Me-S- , R2 = 4-(글리실아미노)사이클로헥실, R3 = NH2, A = -CH=CH-](화합물 118)
전환 o
30 ㎎(0.084 mmol)의 1-(4-아미노사이클로헥실)-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드를 2 ㎖의 디메틸 아세트아미드에 용해시켰다. 수득된 용액에 21 ㎎(0.126 mmol)의 N-(tert-부톡시카보닐)글리신, 60 ㎕(0.336 mmol)의 DIPEA, 및 40 ㎎(0.126 mmol)의 TBTU를 첨가하였다. 혼합물을 실온에서 18 시간 동안 교반하고, 용액을 에틸 아세테이트와 NaHCO3의 포화 수용액 사이에 분배시키고, 유기층을 염수로 세척하고, Na2SO4 상에서 건조시키고, 진공 하에서 증발시켰다. 조물질을 실리카겔 크로마토그래피(DCM/MeOH/NH40H 95/5/0.1)에 의해서 정제하여 백색 고체로서 35 ㎎(81%)의 tert-부틸 [2-({4-[3-카바모일-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-1-일]사이클로헥실}아미노)-2-옥소에틸]카바메이트를 제공하였다. 1H NMR(401 MHz, DMSO-d6) δ 9.47(s, 1H), 8.27(d, J=8.67 Hz, 1H), 7.78(d, J=6.35 Hz, 1H), 7.74(d, J=8.67 Hz, 1H), 7.64(br. s., 1H), 7.55(br. s., 1H), 6.86(t, J=5.86 Hz, 1H), 6.00(br. s., 1H), 3.96(d, J=2.56 Hz, 1H), 3.62(d, J=5.61 Hz, 2H), 2.72(s, 3H), 2.23-2.36(m, 2H), 1.91-2.11(m, 4H), 1.68-1.82(m, 2H), 1.38(s, 9H).
1,4-디옥산(1 ㎖) 중의 20 ㎎(0.039 mmol)의 tert-부틸 [2-({4-[3-카바모일-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-1-일]사이클로헥실}아미노)-2-옥소에틸]카바메이트의 용액에 1,4-디옥산 중의 4 M HCl(2 ㎖, 8 mmol)을 첨가하였다. 혼합물을 실온에서 2 시간 동안 교반하였다. 용매를 감압 하에서 제거하고, 조물질을 디에틸 에테르로 희석하고, 여과하여 황색 고체로서 15 ㎎(88%)의 최종 하이드로클로라이드 염을 제공하였다. LC/MS(254) HPLC 방법 2 Rt 3.3 min. 1H NMR(401 MHz, DMSO-d6) δ 9.48(s, 1H), 8.46(d, J=6.96 Hz, 1H), 8.27(d, J=8.67 Hz, 1H), 7.93-8.11(m, 3H), 7.75(d, J=8.79 Hz, 1H), 7.67(br. s., 1H), 7.51(br. s., 1H), 5.83-6.10(m, 1H), 3.96-4.12(m, 1H), 3.56-3.71(m, 2H), 2.73(s, 3H), 2.25-2.39(m, 2H), 2.04-2.15(m, 2H), 1.89-2.04(m, 3H), 1.75-1.88(m, 2H). HRMS(ESI) C19H23N702S에 대한 계산치 [M+H]+ 414.1707, 실측치 414.1721.
실시예 51: 1-{4-[(에틸카바모일)아미노]사이클로헥실}-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-S- , R2 = 에틸카바모일)아미노]사이클로헥실, R3 = NH2, A = -CH=CH-](화합물 119)
전환 p
30 ㎎(0.084 mmol)의 1-(4-아미노사이클로헥실)-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드를 2 ㎖의 디메틸포름아미드에 용해시켰다. 수득된 용액에 32 ㎕(0.42 mmol)의 에틸이소시아네이트 및 60 ㎕(0.336 mmol)의 DIPEA를 첨가하였다. 혼합물을 100℃에서 18 시간 동안 교반하고, 용액을 에틸 아세테이트와 NaHCO3의 포화 수용액 사이에 분배시키고, 유기층을 염수로 세척하고, Na2SO4 상에서 건조시키고, 진공 하에서 증발시켰다. 조물질을 실리카겔 크로마토그래피(DCM/MeOH/NH40H 95/5/1)에 의해서 정제하여 백색 고체로서 4 ㎎(11%)의 1-{4-[(에틸카바모일)아미노]사이클로헥실}-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드를 제공하였다. LC/MS(254) HPLC 방법 2 Rt 4.38 min. 1H NMR(401 MHz, DMSO-d6) δ 9.47(s, 1H), 8.27(d, J=8.67 Hz, 1H), 7.74(d, J=8.67 Hz, 1H), 7.59(s, 2H), 6.06(d, J=7.08 Hz, 1H), 5.89-6.02(m, 1H), 5.81(t, J=5.49 Hz, 1H), 3.78-3.88(m, 1H), 3.00-3.07(m, 2H), 2.71-2.74(m, 3H), 2.15-2.29(m, 2H), 1.99-2.11(m, 3H), 1.90(dd, J=3.54, 13.67 Hz, 2H), 1.65-1.79(m, 2H), 1.01(t, J=7.20 Hz, 3H). HRMS(ESI) C20H25N7O2S에 대한 계산치 [M+H]+ 428.1863, 실측치 428.1852.
실시예 52: 1-(4-카바미미드아미도사이클로헥실)-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 [(I), R1 = Me-S- , R2 = 4-카바미미드아미도사이클로헥실, R3 = NH2, A = -CH=CH-](화합물 120)
전환 q
30 ㎎(0.084 mmol)의 1-(4-아미노사이클로헥실)-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드 하이드로클로라이드를 2 ㎖의 디메틸포름아미드에 용해시켰다. 수득된 용액에 70 ㎎(0.34 mmol)의 3,5-디메틸-1H-피라졸-1-카복시이미드아미드 및 93 ㎕(0.67 mmol)의 TEA를 첨가하였다. 혼합물을 100℃에서 48 시간 동안 교반하고, 용액을 에틸 아세테이트와 NaHCO3의 포화 수용액 사이에 분배시키고, 유기층을 염수로 세척하고, Na2SO4 상에서 건조시키고, 진공 하에서 증발시켰다. 조물질을 실리카겔 크로마토그래피(DCM/MeOH/NH4OH 95/5/1)에 의해서 정제하여 황색 고체로서 6 ㎎(11%)의 1-(4-카바미미드아미도사이클로헥실)-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드를 제공하였다. LC/MS(m/z): 399.1 [M+H]+, HPLC(254 ㎚) 방법 3 Rt 4.1 min.
실시예 53: 1-tert-부틸-8-(메틸설파닐)-6-(모르폴린-4-일)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드[(I), R1 = Me-S- , R2 = tert-부틸, R3 = NH2, R5 = 모르폴린-4-일, A = -CH=CH-](화합물 121)
무수 THF(2 ㎖) 중의 50 ㎎(0.158 mmol)의 1-tert-부틸-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드의 용액에 137 ㎕(1.26 mmol)의 모르폴린, 및 THF 중의 1 M LiN(TMS)2(4 ㎖, 4 mmol)를 첨가하였다. 혼합물을 실온에서 48 시간 동안 교반한 다음에, 냉수로 희석하고, 수득된 침전을 여과하였다. 조물질을 HPLC/MS 정제방법 1에 적용하여 5 ㎎(8%)의 목적 생성물을 수득하였다. LC/MS(m/z): 401.0 [M+H]+, HPLC(254 ㎚) 방법 2 Rt 6.39 min. 1H NMR(401 MHz, DMSO-d6) δ 8.20(d, J=8.91 Hz, 1H), 7.67(d, J=8.91 Hz, 2H), 7.44(s, 1H), 3.75-3.82(m, 4H), 3.63-3.69(m, 4H), 2.64(s, 3H), 1.97(s, 9H). HRMS(ESI) C19H25N602S에 대한 계산치 [M+H]+ 401.1754, 실측치 428.1757.
제조예 O: 1-[2-하이드록시-5-(4-메틸피페라진-1-일)페닐]에타논
THF(10 ㎖) 중의 1.0 g(4.65 mmol)의 1-(5-브로모-2-하이드록시페닐)에타논, 0.83 ㎖(7.45 mmol)의 N-메틸피페라진, 16.2 ㎖(16.2 mmol)의 LiHMDSA, 68 ㎎(0.074 mmol)의 Pd2(dba)3, 및 29.3 ㎎(0.074 mmol)의 2-디사이클로헥실포스피노-2'-N,N-디메틸아미노비페닐을 마개가 있는 바이알 내에서 아르곤 하에 배합하고, 70℃에서 40 분 동안 교반하였다. 휘발성 물질을 진공 중에서 제거하고, 수득된 잔류물을 물 및 1 N HCl(pH = 6)로 용해시키고, DCM으로 분배시켰다. 유기상을 염수로 세척하고, Na2S04 상에서 건조시키고, 여과하고, 감압 하에서 농축시켰다. 잔류물을 섬광 칼럼 크로마토그래피(10% MeOH/DCM까지의 DCM 구배)에 의해서 정제하여 갈색 고체로서 532 ㎎(51%)의 목적 생성물을 제공하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 3.34 min. 1H NMR(401 MHz, DMSO-d6) δ 11.45(s, 1H), 7.21-7.28(m, 2H), 6.80-6.93(m, 1H), 2.98-3.10(m, 4H), 2.63(s, 3H), 2.44-2.48(m, 4H), 2.23(s, 3H). HRMS(ESI) C13H18N202에 대한 계산치 [M+H]+ 235.1441, 실측치 235.1448.
동일한 방법에 따라 적합한 출발물질을 사용하여 다음의 화합물들을 제조하였다:
tert-부틸 4-(3-아세틸-4-하이드록시페닐)피페라진-1-카복실레이트. LC/MS(254 ㎚) HPLC 방법 2 Rt 6.61 min. 1H NMR(401 MHz, DMSO-d6) δ 11.49(s, 1H), 7.32(d, J=2.93 Hz, 1H), 7.25-7.30(m, 1H), 6.88(d, J=8.91 Hz, 1H), 3.41-3.52(m, 4H), 2.95-3.05(m, 4H), 2.64(s, 3H), 1.42(s, 9H). HRMS(ESI) C17H24N204에 대한 계산치 [M+H]+ 321.1809, 실측치 321.1805;
2-하이드록시-5-(4-메틸피페라진-1-일)벤조니트릴. LC/MS(254 ㎚) HPLC 방법 2 Rt min. 1H NMR(401 MHz, DMSO-d6) δ 10.38(br. s., 1H), 7.18(dd, J=3.11, 9.09 Hz, 1H), 7.08(d, J=2.93 Hz, 1H), 6.90(d, J=9.15 Hz, 1H). HRMS(ESI) C12H15N30에 대한 계산치 [M+H]+ 218.1288, 실측치 218.1287; 및
2-플루오로-4-(4-메틸피페라진-1-일)페놀. LC/MS(m/z): 211.1[M+H]+, HPLC(254 ㎚) 방법 3 Rt 4.00 min.
제조예 P: 4-(4-메틸피페라진-1-일)페놀
2 g(11.24 mmol)의 4-(피페라진-1-일)페놀 및 4.5 ㎖(물 중의 37%, 56 mmol)의 포름알데히드를 THF/AcOH 5/1의 혼합물에 현탁시키고, 실온에서 교반하였다. 30 분 후에, 4.7 g(22.5 mmol)의 나트륨 트리아세톡시보로하이드라이드를 조금씩 첨가하였다. 반응액을 몇 시간 동안 교반하고, 증발시켰다. 조물질을 메탄올 중의 에틸 아세테이트/에탄올/NH3 7 N 8/2/0.2를 사용하여 실리카겔 상에서 정제하여 유리 염기로서 2.3 g의 분홍색 고체를 제공하였다. LC/MS(254 ㎚) HPLC 방법 2 Rt 2.4 min. 1H NMR(401 MHz, DMSO-d6) δ 8.78(s, 1H), 6.71-6.84(m, 2H), 6.56-6.69(m, 2H), 2.85-3.03(m, 4H), 2.46(br. s., 4H), 2.23(s, 3H). HRMS(ESI) C11H16N20에 대한 계산치 [M+H]+ 193.1336, 실측치 193.1328.
유사한 방식으로 수행하여 다음의 화합물을 제조하였다:
3-(4-메틸피페라진-1-일)페놀. LC/MS(254 ㎚) HPLC 방법 2 Rt min. 1H NMR(401 MHz, DMSO-d6) δ 9.07(s, 1H), 6.96(t, J=8.12 Hz, 1H), 6.34-6.38(m, 1H), 6.28(t, J=2.32 Hz, 1H), 6.19(ddd, J=0.73, 2.20, 7.93 Hz, 1H), 3.02-3.09(m, 4H), 2.41-2.46(m, 4H), 2.22(s, 3H). HRMS(ESI) C11H16N20에 대한 계산치 [M+H]+ 193.1336, 실측치 193.1329.
제조예
Q:
단계 a. 4-(4-메틸피페라진-1-일)페닐 아세테이트의 제조
DCM 중의 1.080 ㎎(5.59 mmol)의 4-(4-메틸피페라진-1-일)페놀 및 1.72 ㎖(12.3 mmol)의 TEA의 혼합물을 빙욕 중에서 냉각시키고, 0.44 ㎖(6.15 mmol)의 아세틸 클로라이드를 적가하였다. 완료 후에, 반응액을 여과하고, 유기상을 물로 빠르게 추출하고, Na2S04 상에서 건조시키고, 증발시켜 연한 분홍색 고체를 제공하였다. LC/MS(m/z): 235.4 [M+H]+, HPLC(254 ㎚) 방법 3 Rt 1.89 min.
단계 b. 2-브로모-4-(4-메틸피페라진-1-일)페닐 아세테이트의 제조
아세토니트릴 중의 247 ㎎(1.05 mmol)의 4-(4-메틸피페라진-1-일)페닐 아세테이트 및 209 ㎎(1.1 mmol)의 p-톨루엔설폰산의 용액을 빙욕 중에서 냉각시키고, 0.056 ㎖(1.1 mmol)의 브롬을 적가하였다. 반응액을 완결될 때까지(3-4 시간) 실온에서 교반하고, 에틸 아세테이트로 희석하고, 물 및 포화 NaHCO3로 추출하였다. Na2SO4 상에서 건조시키고 증발시킨 유기상을 섬광 크로마토그래피(DCM/MeOH 85/15)에 의해서 정제하여 암갈색 오일로서 생성물을 제공하였다. HPLC(254 ㎚) 방법 2 Rt 4.05 min. 1H NMR(400 MHz, DMSO-d6) δ ppm 2.25(s, 3H), 2.36(s, 3H), 2.39(m, 4H), 3.44(m, 4H), 6.50(dd, J=2.1, 8.3 Hz, 1H), 7.03(d, J=8.3 Hz, 1H), 7.21(d, J=2.1 Hz, 1H). 질량 계산치 313.0546, 질량 실측치: 313.0538.
단계 c. 2-브로모-4-(4-메틸피페라진-1-일)페놀의 제조
280 ㎎(1.03 mmol)의 2-브로모-4-(4-메틸피페라진-1-일)페닐 아세테이트를 메탄올에 용해시키고, 2 ㎖의 1 N NaOH와 반응시켰다. 2 시간 후에, 반응액을 빙초산으로 산성화시키고, 증발시키고, DCM/MeOH 9/1 및 MeOH 중의 0.4% 7 M NH3를 사용하여 실리카 상에서 정제하였다. LC/MS(m/z): 273.2 [M+H]+, HPLC(254 ㎚) 방법 3 Rt 2.96 min.
제조예 R: tert-부틸 3-[(메틸설포닐)옥시]아제판-1-카복실레이트
단계 a. tert-부틸 3-하이드록시아제판-1-카복실레이트의 제조
50 ㎖의 MeOH 중의 1.07 g(5 mmol)의 tert-부틸 3-옥소아제판-1-카복실레이트의 용액을 0℃로 냉각시키고, 213 ㎎(6.1 mmol)의 나트륨 보로하이드라이드를 첨가하였다. 용액을 서서히 실온으로 가온하고, 2 시간 동안 교반하였다. 휘발성 물질을 진공 하에서 제거하고, 잔류물을 에틸 아세테이트로 용해시키고, 물로 분배시켰다. 유기층을 염수로 세척하고, Na2SO4 상에서 건조시키고, 증발시켰다. 조물질을 섬광 크로마토그래피(EtOAc/헥산 3/7)에 의해서 정제하여 백색 고체로서 0.75 g(75%)의 tert-부틸 3-하이드록시아제판-1-카복실레이트를 제공하였다. 1H NMR(401 MHz, DMSO-d6) δ 4.34-4.65(m, 1H), 3.52-3.80(m, 1H), 3.05-3.25(m, 2H), 1.70-1.89(m, 2H), 1.58-1.69(m, 1H), 1.43-1.56(m, 3H), 1.39(s, 9H).
단계 b. tert-부틸 3-[(메틸설포닐)옥시]아제판-1-카복실레이트의 제조
0℃로 냉각시킨 DCM(10 ㎖) 중의 200 ㎎(0.93 mmol)의 tert-부틸 3-하이드록시아제판-1-카복실레이트의 용액에 190 ㎕(1.4 mmol)의 TEA 및 114 ㎕(1.4 mmol)의 메실 클로라이드를 첨가하였다. 용액을 실온으로 가온하고, 2 시간 동안 교반하였다. 혼합물을 NaHCO3의 포화 수용액으로 희석하고, 유기층을 분리하여 염수로 세척하고, Na2SO4 상에서 건조시키고, 감압 하에서 농축시키고, 수득된 농후한 연황색 오일을 다음 단계에 직접 적용하였다. LC/MS(m/z) 294.0 [M+H]+, HPLC(254 ㎚) 방법 3 Rt 5.65 min.
동일한 방법에 따라 적합한 출발물질을 사용하여 다음의 화합물을 제조하였다:
2,2,2-트리클로로에틸(3-엑소)-3-[(메틸설포닐)옥시]-8-아자비사이클로[3.2.1]옥탄-8-카복실레이트. LC/MS(m/z): 381.1 [M+H]+, HPLC(254 ㎚) 방법 3 Rt 5.56 min.
실시예 901: Pim 키나제 결합 활성
PIM-1, -2, 및 -3 효소를 박테리아에서 발현된 융합 단백질로서 생성시키고, IMAC 칼럼 크로마토그래피에 의해서 정제하였다[Sun, X., Chiu, J.F., and He, Q.Y.(2005) Expert Rev. Proteomics, 2:649-657]. 형광-표지된 Pim-특이적 펩타이드 기질은 American Peptide Company(Sunnyvale, CA)에 의해서 주문 합성되었다. 반응 완충액은 10 mM HEPES, pH 7.2, 10 mM MgCl2, 0.01% 트윈(Tween) 20, 2 mM DTT를 함유하였다. 종결 완충액은 190 mM HEPES, pH 7.2, 0.015% 브리즈(Brij)-35, 0.2% 코팅 시약 3(Caliper Life Sciences, Hopkinton, MA), 20 mM EDTA를 함유하였다. 분리 완충액은 100 mM HEPES, pH 7.2, 0.015% 브리즈-35, 0.1% 코팅 시약 3, 1:200 코팅 시약 8(Caliper Life Sciences, Hopkinton, MA), 10 mM EDTA 및 5% DMSO를 함유하였다.
PIM 반응은 384-웰 플레이트 내에서 웰당 10 ㎕의 최종 용적으로 수행하였다. 5 ㎕의 2X 효소 및 FAM-펩타이드에 5 ㎕의 2X ATP 및 시험 화합물을 첨가함으로써 개시된 표준 효소반응은 반응 완충액 내에 20 pM PIM1, 50 pM PIM2, 또는 55 pM PIM3, 1 μM FAM-펩타이드, 및 10 μM ATP를 함유하였다. 실온에서 90 분 배양한 후에, 10 ㎕의 종결 완충액을 첨가함으로써 포스포릴화 반응을 중지시켰다. 각각의 독립적인 반응에서 생성물 및 기질을 캘리퍼(Caliper) LC3000®(Caliper Life Sciences, Hopkinton, MA) 상에서 진행되는 12-시퍼(sipper) 마이크로 플루이딕 칩(micro fluidic chip)(Caliper Life Sciences, Hopkinton, MA) 상에서 분리시켰다. 생성물 및 기질의 분리는 캘리퍼 옵티마이저(Caliper's Optimizer) 소프트웨어(Hopkinton, MA)를 사용하여 전압 및 압력을 선택함으로써 최적화되었다. 분리 조건은 -500 V의 하류 전압(downstream voltage), -2150 V의 상류 전압(upstream voltage), 및 -1.2 psi의 선별 압력(screening pressure)을 사용하였다. 생성물 및 기질 형광단은 488 ㎚에서 여기되었으며, 530 ㎚에서 검출되었다. 기질 전환은 HTS 웰 분석기 소프트웨어(Well Analyzer software)(Caliper Life Sciences, Hopkinton, MA)를 사용하여 전기영동도로부터 계산하였다. 시험 화합물에 대한 Ki 값을 계산하였다. 예시된 화합물의 대표적인 PIM1 LC3K Ki에 대한 마이크로몰 값에 대해서는 표 1을 참고로 한다.
실시예 902: 시험관내 세포 증식 효력시험
BaF3은 키나제 종양유전자의 효력 및 하류 시그날링 둘 다를 평가하기 위한 모델 시스템으로서 유용한 쥐 인터류킨-3 의존성 프로-B 세포주이다 ["Ba/F3 cells and their use in kinase drug discovery", Warmuth, M, et al,(January 2007) Current Opinion in Oncology, Vol 19(1):55-60]. BaF3 어버이 세포주는 DSMZ 기탁기관으로부터 획득하였다. PIM1 또는 PIM2로 형질감염된 BaF3 세포주를 생성시켰다. 마우스 IL-3은 R&D Systems로부터 구입하였다. G418은 Clontech로부터 구입하였다. BaF3 어버이 세포주를 위한 배지는 RPMI, 10% FBS, 2 mM L-글루타민, 2 ng/㎖ mIL-3을 함유하였다. BaF3 PIM1 및 2 세포주를 위한 배지는 RPMI, 10% FBS, 2 mM L-글루타민, 250 ㎍/㎖를 함유하였다. MM1.S(다발성 골수종 세포) 세포주를 위한 배지는 RPMI, 10% FBS, 2 mM L-글루타민을 함유하였다.
어버이 세포, BaF3 PIM1 세포, BaF3 PIM2 세포, 및 MM1.S(다발성 골수종) 세포를 45 ㎕/웰로 384-웰 플레이트 내에 각각 2k/웰, 5k/웰, 5k/웰, 및 1Ok/웰로 접종하였다. 시험 화합물은 5 ㎕/웰로 첨가하였다. BaF3 세포(어버이 및 형질감염 세포주)는 밤새 배양하는 반면에, MM1.S 세포는 37℃, 5% CO2 하에서 72 시간 동안 배양하였다. 셀타이터 글로®(CELL TITER GLO®) 시약(Promega)을 50 ㎕/웰로 첨가하고, 플레이트를 30 분 동안 배양하고, 그들의 발광을 HT 아날리스트(Analyst) 상에서 판독하였다. 시험 화합물에 대한 IC50/EC50 값을 계산하였다.
본 발명의 대표적인 화합물을 상술한 바와 같이 시험하였으며, 이하의 표 2에 나타낸 바와 같은 Ki/IC50/EC50을 나타내는 것으로 밝혀졌다.
[표 2]
Claims (25)
- 하기 화학식 I의 화합물 및 그의 약제학적으로 허용되는 염:
[화학식 I]
상기 식에서,
R1은 수소, CN, 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기, 또는 XR4기이며, 여기에서
X는 O, S, SO, S02 및 NR6으로부터 선택된 2가 래디칼이고, 여기에서
R6은 임의로 치환된 직쇄 또는 분지된 C1-C6 알킬이거나, R6 및 R4는 이들이 결합된 질소 원자와 함께 임의로 N, O 및 S로부터 선택된 1개의 추가의 헤테로 원자를 함유하는, 5 내지 6 원 헤테로아릴 또는 헤테로사이클릴 기를 형성할 수 있으며;
R2는 수소, 또는 직쇄 또는 분지된 C1-C6 알킬, 직쇄 또는 분지된 C2-C6 알케닐, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기이고;
R3은 NR'R" 및 N(OH)R'로부터 선택된 기이며, 여기에서
R' 및 R"는 각각 독립적으로 수소, 또는 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기이고;
R4는 임의로 치환된 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 기이며;
R5는 수소 또는 NR'R"이고, 여기에서
R' 및 R"는 각각 독립적으로 수소, 또는 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기이거나, R' 및 R"는 이들이 결합된 질소 원자와 함께 임의로 N, O 및 S로부터 선택된 1개의 추가의 헤테로 원자를 함유하는, 5 내지 6 원 헤테로아릴 또는 헤테로사이클릴 기를 형성할 수 있으며;
A는 -(CH2)2- 및 -CH=CH-로부터 선택된 2가 기이고;
단, 여기에서
1-메틸-8-(피페리딘-1-일)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-메틸-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드, 및
1-메틸-8-(메틸설포닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드는 제외된다. - 제1항에 있어서,
R1이 CN, 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기, 또는 XR4기이며, 여기에서
X는 O, S, SO, S02 및 NR6으로부터 선택된 2가 래디칼이고, 여기에서
R6은 임의로 치환된 직쇄 또는 분지된 C1-C6 알킬이거나, R6 및 R4는 이들이 결합된 질소 원자와 함께 임의로 N, O 및 S로부터 선택된 1 개의 추가의 헤테로 원자를 함유하는, 5 내지 6 원 헤테로아릴 또는 헤테로사이클릴 기를 형성할 수 있으며;
R2는 직쇄 또는 분지된 C1-C6 알킬, 직쇄 또는 분지된 C2-C6 알케닐, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기이고;
R5는 수소 또는 NR'R"이며, 여기에서
R' 및 R"는 수소인 화학식 I의 화합물. - 제1항 또는 제2항에 있어서,
R1이 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기, 또는 XR4 기이며, 여기에서
X는 O, S, SO, S02 및 NR6으로부터 선택된 2가 래디칼이고, 여기에서
R6은 임의로 치환된 직쇄 또는 분지된 C1-C6 알킬이거나, R6 및 R4는 이들이 결합된 질소 원자와 함께 임의로 N, O 및 S로부터 선택된 한 개의 추가의 헤테로 원자를 함유하는, 5 내지 6 원 헤테로아릴 또는 헤테로사이클릴 기를 형성할 수 있으며;
R2는 직쇄 또는 분지된 C1-C6 알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기이고;
R3은 NR'R" 및 N(OH)R'로부터 선택된 기이며, 여기에서
R' 및 R"는 수소인 화학식 I의 화합물. - 제1항 내지 제3항 중 어느 한 항에 있어서,
R1이 직쇄 또는 분지된 C1-C6 알킬, 아릴 및 헤테로사이클릴로부터 선택된 임의로 치환된 기, 또는 XR4기이며, 여기에서
X는 O, S, 및 NR6으로부터 선택된 2가 래디칼이고, 여기에서
R6은 임의로 치환된 직쇄 또는 분지된 C1-C6 알킬이거나, R6 및 R4는 이들이 결합된 질소 원자와 함께 임의로 N, O 및 S로부터 선택된 1개의 추가의 헤테로 원자를 함유하는, 5 내지 6 원 헤테로아릴 또는 헤테로사이클릴 기를 형성할 수 있으며;
R3은 NR'R"이고, 여기에서
R' 및 R"는 수소이며;
R4는 임의로 치환된 직쇄 또는 분지된 C1-C6 알킬, 아릴, 아릴알킬, 및 헤테로사이클릴로부터 선택된 기이고;
R5는 수소인 화학식 I의 화합물. - 제1항 내지 제4항 중 어느 한 항에 있어서,
R1이 직쇄 또는 분지된 C1-C6 알킬 및 아릴로부터 선택된 임의로 치환된 기, 또는 XR4기이며, 여기에서
X는 O, S, 및 NR6으로부터 선택된 2가 래디칼이고, 여기에서
R6은 임의로 치환된 직쇄 또는 분지된 C1-C6 알킬이거나, R6 및 R4는 이들이 결합된 질소 원자와 함께 임의로 N, O 및 S로부터 선택된 한 개의 추가의 헤테로 원자를 함유하는, 5 내지 6 원 헤테로아릴 또는 헤테로사이클릴 기를 형성할 수 있으며;
R4는 임의로 치환된 직쇄 또는 분지된 C1-C6 알킬, 아릴, 및 헤테로사이클릴로부터 선택된 기이고;
A는 2가 -CH=CH- 기인 화학식 I의 화합물. - 제1항에 있어서,
1-(2-하이드록시에틸)-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-tert-부틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-tert-부틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-tert-부틸-8-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-tert-부틸-8-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-(2-하이드록시에틸)-8-메톡시-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-tert-부틸-N-메틸-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-tert-부틸-N-[2-(디메틸아미노)에틸]-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-tert-부틸-N-(2-하이드록시에틸)-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-tert-부틸-N-(1-메틸피페리딘-4-일)-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-tert-부틸-N-[2-(1H-이미다졸-5-일)에틸]-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-[2-(디메틸아미노)에틸]-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
6-아미노-1-[2-(디메틸아미노)에틸]-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
2-[2-(디메틸아미노)에틸]-8-(메틸설파닐)-2H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-(2-아미노에틸)-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
2-(2-아미노에틸)-8-(메틸설파닐)-2H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-(메틸설파닐)-1-(피페리딘-4-일메틸)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-(메틸설파닐)-2-(피페리딘-4-일메틸)-2H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-메틸-8-[4-(피페라진-1-일)페녹시]-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-메틸-8-페녹시-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-(3-아미노페녹시)-1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-(4-아미노페녹시)-1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-메틸-8-(피리딘-4-일옥시)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-(2-플루오로에톡시)-1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-메틸-8-[4-(4-메틸피페라진-1-일)페녹시]-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-메틸-8-[4-(4-메틸피페라진-1-일)페녹시]-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-메틸-8-[4-(피페라진-1-일)페녹시]-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-[2-브로모-4-(4-메틸피페라진-1-일)페녹시]-1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-[2-브로모-4-(4-메틸피페라진-1-일)페녹시]-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-메틸-8-[3-(피페라진-1-일)페녹시]-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-메틸-8-[3-(피페라진-1-일)페녹시]-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-[3-(디메틸아미노)페녹시]-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-(2-클로로페녹시)-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-(2-플루오로페녹시)-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-[2-플루오로-4-(4-메틸피페라진-1-일)페녹시]-1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-[2-플루오로-4-(4-메틸피페라진-1-일)페녹시]-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-[2-아세틸-4-(4-메틸피페라진-1-일)페녹시]-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-[2-아세틸-4-(피페라진-1-일)페녹시]-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-[2-시아노-4-(4-메틸피페라진-1-일)페녹시]-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-시아노-1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-메틸-8-(1H-피라졸-1-일)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-메틸-8-[3-(트리플루오로메틸)-1H-피라졸-1-일]-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-(1H-이미다졸-1-일)-1-메틸-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-메틸-8-(4-니트로-1H-이미다졸-1-일)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-(2-하이드록시에틸)-8-페녹시-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-(2-하이드록시에틸)-8-[4-(4-메틸피페라진-1-일)페녹시]-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-(2-하이드록시에틸)-8-[3-(4-메틸피페라진-1-일)페녹시]-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-(2-하이드록시에틸)-8-(3-니트로페녹시)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-메틸-8-(3-니트로페녹시)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-메틸-8-[3-(4-메틸피페라진-1-일)페녹시]-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-tert-부틸-8-[4-(4-메틸피페라진-1-일)페녹시]-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-tert-부틸-8-(디메틸아미노)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-메톡시-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-에톡시-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-메톡시-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-(3-포르밀페녹시)-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-메틸-8-{3-[(4-메틸피페라진-1-일)메틸]페녹시}-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-[3-(하이드록시메틸)페녹시]-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-{3-[(디메틸아미노)메틸]페녹시}-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-메틸-8-[3-(모르폴린-4-일메틸)페녹시]-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-(3-아미노페녹시)-1-메틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-(3-아미노페녹시)-1-(2-하이드록시에틸)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-(2-플루오로에틸)-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-(2-클로로에틸)-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-(2-하이드록시에틸)-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-(2-메톡시에틸)-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-[3-(디메틸아미노)프로필]-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-(1-아미노-2-메틸-1-옥소프로판-2-일)-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-(메틸설파닐)-1-(피페리딘-4-일메틸)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-(3-아미노프로필)-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-(메틸설파닐)-1-(피페리딘-4-일)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-(2-아미노에틸)-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-[2-(4-메틸피페라진-1-일)에틸]-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-에테닐-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-{2-[4-(디메틸아미노)피페리딘-1-일]에틸}-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-에톡시-1-(피페리딘-4-일메틸)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-[3-(디메틸아미노)프로필]-8-에톡시-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-에톡시-1-(피페리딘-4-일)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-에톡시-1-[(1-메틸피페리딘-4-일)메틸]-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-(2,6-디플루오로페닐)-1-(피페리딘-4-일메틸)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-(3-아미노프로필)-8-(4-플루오로페닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
2-(3-아미노프로필)-8-(4-플루오로페닐)-4,5-디하이드로-2H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-(3-아미노프로필)-N-(3-하이드록시프로필)-8-(4-메톡시페닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-tert-부틸-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
6-아미노-1-tert-부틸-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-메틸-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
6-아미노-1-메틸-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-tert-부틸-N-하이드록시-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-(메틸설파닐)-1-(피페리딘-4-일)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-(메틸설파닐)-1-(피페리딘-3-일)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-(4-아미노사이클로헥실)-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-(메틸설파닐)-1-(피페리딘-3-일메틸)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-(아제판-4-일)-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-(3-아미노-2,2-디메틸프로필)-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-메톡시-1-(피페리딘-4-일)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-메톡시-1-(피페리딘-4-일메틸)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-[(3-엑소)-8-아자비사이클로[3.2.1]옥트-3-일]-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-[(3-엔도)-8-아자비사이클로[3.2.1]옥트-3-일]-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-[4-(1,3-디옥소-1,3-디하이드로-2H-이소인돌-2-일)부탄-2-일]-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-(4-아미노부탄-2-일)-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-(1-아자비사이클로[2.2.2]옥트-3-일)-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-(메틸설파닐)-1-(테트라하이드로-2H-피란-4-일)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-[트랜스-3-(하이드록시메틸)사이클로부틸]-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-[시스-3-(하이드록시메틸)사이클로부틸]-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-(1-하이드록시-2-메틸프로판-2-일)-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-(1-하이드록시-2-메틸프로판-2-일)-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-페닐-1-(피페리딘-4-일)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-(피페리딘-4-일)-8-(티오펜-3-일)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-(4-아미노사이클로헥실)-8-페닐-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-(4-아미노사이클로헥실)-8-(티오펜-3-일)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-(피페리딘-4-일)-8-(피롤리딘-1-일)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
8-(모르폴린-4-일)-1-(피페리딘-4-일)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-{[1-(2-아미노에틸)피페리딘-4-일]메틸}-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-{4-[(2-아미노에틸)아미노]사이클로헥실}-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-{4-[(2-아미노에틸)아미노]사이클로헥실}-8-(메틸설파닐)-4,5-디하이드로-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-[4-(글리실아미노)사이클로헥실]-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-{4-[(에틸카바모일)아미노]사이클로헥실}-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-(4-카바미미드아미도사이클로헥실)-8-(메틸설파닐)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드,
1-tert-부틸-8-(메틸설파닐)-6-(모르폴린-4-일)-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드, 및
6-아미노-1-tert-부틸-1H-피라졸로[4,3-h]퀴나졸린-3-카복사미드로 구성된 군으로부터 선택된 화학식 I의 화합물 또는 그의 약제학적으로 허용되는 염. - 하기 단계를 포함하는 것을 특징으로 하는, 제1항에 정의된 바와 같은 화학식 I의 화합물 또는 그의 약제학적으로 허용되는 염을 제조하는 방법:
단계 6) 하기 화학식 VIII의 화합물을 대체 단계 6a), 6b) 또는 6c) 중 어느 하나에 따라 반응시키는 단계:
[화학식 VIII]
상기 식에서, R1은 SR4, OR4, 수소, 또는 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기이고, R2, R4, A는 제1항에서 정의된 바와 같음:
단계 6a) 암모늄 하이드록사이드 또는 하기 화학식 XII의 아민과 반응시켜 하기 화학식 I의 화합물을 수득하는 단계:
[화학식 XII]
:
상기 식에서, R' 및 R"는 제1항에서 정의된 바와 같음:
[화학식 I]
상기 식에서, R1은 수소, 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기, 또는 SR4기 또는 OR4기이며, R3은 NR'R"이고, R5는 수소이며, R2, R4, A, R' 및 R"는 제1항에서 정의된 바와 같음;
단계 6b1) 산성 또는 염기성 가수분해 조건 하에서 반응시켜 화학식 XI의 화합물 또는 그의 염을 제공하는 단계:
[화학식 XI]
상기 식에서, R1은 수소, 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기, 또는 SR4기 또는 OR4 기이며, R2, R4, A는 제1항에서 정의된 바와 같음;
단계 6b2) 생성된 화학식 XI의 화합물 또는 그의 염을 염기성 조건 및 적합한 축합제의 존재 하에서, 암모늄염 또는 상기에서 정의된 바와 같은 화학식 XII의 유도체, 또는 하기 화학식 X의 유도체와 혼합시켜 하기 화학식 I의 화합물을 제공하는 단계:
[화학식 X]
상기 식에서, R'는 제1항에서 정의된 바와 같음:
[화학식 I]
상기 식에서, R1은 수소, 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기, 또는 SR4기 또는 OR4 기이며, R5는 수소이고, R2, R3, R4 및 A는 제1항에서 정의된 바와 같음;
단계 6c) 강염기의 존재 하에서 암모늄염 또는 상기에서 정의된 화학식 XII의 적합한 아민과 반응시켜 하기 화학식 I의 화합물을 제공하는 단계:
[화학식 I]
상기 식에서, R1은 수소, 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 사이클로알킬알킬, 아릴, 아릴알킬, 헤테로사이클릴 및 헤테로사이클릴알킬로부터 선택된 임의로 치환된 기, 또는 SR4기 또는 OR4 기이며, R3은 NR'R"이고, R2, R4, R5, A, R' 및 R"는 제1항에서 정의된 바와 같음;
임의로 화학식 I의 화합물을 화학식 I의 또 다른 상이한 화합물로 전환시키고, 필요한 경우에, 화학식 I의 화합물을 그의 약제학적으로 허용되는 염으로 전환시키거나 염을 유리 화합물 I로 전환시키는 단계. - 하기 단계를 포함하는 것을 특징으로 하는, 제1항에 정의된 바와 같은 화학식 I의 화합물 또는 그의 약제학적으로 허용되는 염을 제조하는 방법:
단계 7) 하기 화학식 XIII의 화합물을 하기 화학식 V의 화합물과 반응시키는 단계:
[화학식 XIII]
상기 식에서, R3 및 A는 제1항에서 정의된 바와 같음:
[화학식 V]
상기 식에서, Y는 요오도, 브로모, 클로로 또는 설포네이트기(예를 들어, -OS(0)2CF3, -OS(0)2CH3 또는 -OS(0)2PhMe)과 같은 적합한 이탈기임;
단계 8) 생성된 하기 화학식 XIV의 화합물을 화학식 XV의 화합물과 반응시켜 하기 화학식 I의 화합물을 제공하는 단계:
[화학식 XIV]
상기 식에서, R2는 제1항에서 정의된 바와 같지만 수소는 아니며, R3 및 A는 제1항에서 정의된 바와 같음:
[화학식 XV]
상기 식에서, R1은 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 아릴 및 헤테로사이클릴로부터 선택된 임의로 치환된 기이고, Q는 -B(OH)2, -B(OAlk)2, -Sn(Alk)4, -Al(Alk)3, ZnHal, MgHal, 또는 ZrCp2Hal과 같은, 팔라듐 매개된 탄소 결합을 형성할 수 있는 적합한 기임:
[화학식 I]
상기 식에서, R1은 직쇄 또는 분지된 C1-C6 알킬, C3-C7 사이클로알킬, 아릴 및 헤테로사이클릴로부터 선택된 임의로 치환된 기이고, R2는 제1항에서 정의된 바와 같지만 수소는 아니며, R3 및 A는 제1항에서 정의된 바와 같고, R5는 수소임;
임의로 화학식 I의 화합물을 화학식 I의 또 다른 상이한 화합물로 전환시키고, 필요한 경우에, 화학식 I의 화합물을 그의 약제학적으로 허용되는 염으로 전환시키거나 염을 유리 화합물 I로 전환시키는 단계. - 하기 방법 중 하나를 수행하여 화학식 I의 화합물을 화학식 I의 또 다른 상이한 화합물로 전환시키는 것을 특징으로 하는, 제1항에 정의된 바와 같은 화학식 I의 화합물 또는 그의 약제학적으로 허용되는 염을 제조하는 방법:
전환 e) Rl, R3 및 A가 제1항에서 정의된 바와 같고 R2가 수소인 화학식 I의 화합물을, 하기 화학식 V의 화합물과의 반응을 통해서 R2가 제1항에서 정의된 바와 같지만 수소는 아닌 화학식 I의 화합물로 전환시키는 방법:
[화학식 V]
R2-Y'
상기 식에서, Y'는 OH, 또는 임의로 활성화시키면 요오도, 브로모, 클로로 또는 설포네이트기(예를 들어, -OS(0)2CF3, -OS(0)2CH3 또는 -OS(0)2PhMe)과 같은 적합한 이탈기로 작용할 수 있는 기이며, R2는 제1항에서 정의된 바와 같지만 수소는 아님;
전환 r) Rl, R2 및 R3가 제1항에서 정의된 바와 같고 A는 -CH2-CH2-와 같은 2가 기인 화학식 I의 화합물을, 산화제로 처리하거나 Pd 또는 Pt 촉매의 존재 하에서 탈수소화 작업 조건 하에서 처리함으로써, A가 -CH=CH-기인 화학식 I의 화합물로 전환시키는 방법. - 제1항에서 정의된 바와 같은 화학식 I의 화합물의 유효량을 이를 필요로 하는 포유동물에게 투여하는 단계를 포함하는, 조절장애된 단백질 키나제 활성에 의해서 야기되고/되거나 이들과 관련된 질병을 치료하는 방법.
- 제10항에 있어서, 조절장애된 PIM-1, PIM-2, PIM-3 키나제 활성에 의해서 야기되고/되거나 이들과 관련된 질병을 치료하는 방법.
- 제10항에 있어서, 상기 질병이 암, 세포 증식 장애, 및 면역세포-관련된 질병 및 장애로 구성된 군으로부터 선택되는 것인 방법.
- 제12항에 있어서, 상기 암이 방광암, 유방암, 결장암, 신장암, 간암, 소세포 폐암을 포함한 폐암, 식도암, 담낭암, 난소암, 췌장암, 위암, 경부암, 갑상선암, 전립선암 및 편평세포 암종을 포함한 피부암과 같은 암종; 백혈병, 급성 림프구성 백혈병, 급성 림프아구성 백혈병, B-세포 림프종, T-세포-림프종, 호지킨 림프종, 비-호지킨 림프종, 모발성 세포 림프종 및 버킷 림프종을 포함한 림프계의 조혈성 종양; 급성 및 만성 골수성 백혈병, 골수이형성 증후군 및 전골수성 백혈병을 포함한 골수계의 조혈성 종양; 섬유육종 및 횡문근육종을 포함한 간엽 기원의 종양; 성상세포종, 신경아세포종, 신경교종 및 신경초종을 포함한 중추 및 말초 신경계의 종양; 흑색종, 정상피종, 기형암종, 골육종, 색소성 건피증, 각막황색종, 갑상선 여포암, 카포시 육종 및 중피종을 포함한 그 밖의 다른 종양으로 구성된 군으로부터 선택되는 것인 방법.
- 제12항에 있어서, 상기 세포 증식 장애가 양성 전립선 비대증, 가족성 선종성 용종증, 신경섬유종증, 건선, 아테롬성 경화증과 관련된 혈관 평활세포 증식, 폐섬유증, 관절염, 사구체신염, 및 수술-후 협착증 및 재발협착증으로 구성된 군으로부터 선택되는 것인 방법.
- 제12항에 있어서, 염증성 및 자가면역 질환이 다발성 경화증, 전신성 홍반성 낭창, 염증성 장질환(IBD), 크론병, 과민성 장 증후군, 췌장염, 궤양성 대장염, 게실증, 중증 근무력증, 맥관염, 건선, 공피증, 천식, 알레르기, 전신 경화증, 백반, 골관절염, 연소기 류마티스성 관절염과 같은 관절염, 강직성 척추염으로부터 선택되는 것인 방법.
- 제10항에 있어서, 적어도 하나의 세포증식억제제 또는 세포독성제와 함께 방사선요법 또는 화학요법을 이를 필요로 하는 포유동물에게 적용하는 단계를 추가로 포함하는 방법.
- 제17항에 있어서, 이를 필요로 하는 포유동물이 인간인 것인 방법.
- PIM-1, PIM-2, PIM-3 키나제 단백질을 제1항에서 정의된 바와 같은 화학식 I의 화합물의 유효량과 접촉시키는 단계를 포함하는, PIM-1, PIM-2, PIM-3 키나제 단백질 활성을 억제하는 시험관내 방법.
- 제10항에 있어서, 종양 혈관형성 및 전이 억제를 제공하는 방법.
- 제1항에서 정의된 바와 같은 화학식 I의 화합물 또는 그의 약제학적으로 허용되는 염의 치료학적 유효량, 및 적어도 하나의 약제학적으로 허용되는 부형제, 담체 및/또는 희석제를 포함하는 약제학적 조성물.
- 제20항에 있어서, 하나 이상의 화학요법제를 추가로 포함하는 약제학적 조성물.
- 항암 요법에서 동시에, 별도로 또는 순차적으로 사용하기 위한 복합제제로서 제1항에서 정의된 바와 같은 화학식 I의 화합물 또는 그의 약제학적으로 허용되는 염, 또는 제20항에서 정의된 바와 같은 그의 약제학적 조성물, 및 하나 이상의 화학요법제를 포함하는 제품 또는 키트.
- 의약으로 사용하기 위한, 제1항에서 정의된 바와 같은 화학식 I의 화합물 또는 그의 약제학적으로 허용되는 염.
- 암을 치료하는 방법에서 사용하기 위한, 제1항에서 정의된 바와 같은 화학식 I의 화합물 또는 그의 약제학적으로 허용되는 염.
- 항암 활성을 갖는 의약의 제조에 있어서의, 제1항에서 정의된 바와 같은 화학식 I의 화합물 또는 그의 약제학적으로 허용되는 염의 용도.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP10195675 | 2010-12-17 | ||
| EP10195675.3 | 2010-12-17 | ||
| PCT/IB2011/055743 WO2012080990A1 (en) | 2010-12-17 | 2011-12-16 | Substituted pyrazolo-quinazoline derivatives as kinase inhibitors |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20140027902A true KR20140027902A (ko) | 2014-03-07 |
| KR101913441B1 KR101913441B1 (ko) | 2018-10-30 |
Family
ID=45498046
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020137007627A KR101913441B1 (ko) | 2010-12-17 | 2011-12-16 | 키나제 억제제로서 치환된 피라졸로-퀴나졸린 유도체 |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US8541576B2 (ko) |
| EP (1) | EP2614065B1 (ko) |
| JP (1) | JP5980225B2 (ko) |
| KR (1) | KR101913441B1 (ko) |
| CN (1) | CN103298816A (ko) |
| BR (1) | BR112013008527A2 (ko) |
| CA (1) | CA2812223C (ko) |
| MX (1) | MX342873B (ko) |
| RU (1) | RU2652638C2 (ko) |
| WO (1) | WO2012080990A1 (ko) |
Families Citing this family (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN102382106A (zh) * | 2010-08-30 | 2012-03-21 | 黄振华 | 苯胺取代的喹唑啉衍生物 |
| US8916577B2 (en) * | 2011-01-26 | 2014-12-23 | Nerviano Medical Sciences S.R.L. | Tricyclic derivatives, process for their preparation and their use as kinase inhibitors |
| CN103339134B (zh) * | 2011-01-26 | 2015-12-23 | 内尔维阿诺医学科学有限公司 | 三环吡咯并衍生物、它们的制备方法和它们作为激酶抑制剂的应用 |
| JP6105578B2 (ja) | 2011-07-21 | 2017-03-29 | トレロ ファーマシューティカルズ, インコーポレイテッド | 複素環式プロテインキナーゼ阻害剤 |
| AU2013234955A1 (en) | 2012-03-23 | 2014-11-13 | Dennis Brown | Compositions and methods to improve the therapeutic benefit of indirubin and analogs thereof, including meisoindigo |
| US9278950B2 (en) | 2013-01-14 | 2016-03-08 | Incyte Corporation | Bicyclic aromatic carboxamide compounds useful as Pim kinase inhibitors |
| BR122019024759B1 (pt) | 2013-01-15 | 2022-02-08 | Incyte Holdings Corporation | Compostos de tiazolacarboxamidas e piridinacarboxamida, composição compreendendo os mesmos, método de inibição da enzima pim1, pim2, ou pim3, e usos dos referidos compostos |
| JP2016528298A (ja) | 2013-08-23 | 2016-09-15 | インサイト・コーポレイションIncyte Corporation | Pimキナーゼ阻害剤として有用なフロピリジン及びチエノピリジンカルボキシアミド化合物 |
| WO2016010897A1 (en) | 2014-07-14 | 2016-01-21 | Incyte Corporation | Bicyclic heteroaromatic carboxamide compounds useful as pim kinase inhibitors |
| US9580418B2 (en) | 2014-07-14 | 2017-02-28 | Incyte Corporation | Bicyclic aromatic carboxamide compounds useful as Pim kinase inhibitors |
| US9540347B2 (en) | 2015-05-29 | 2017-01-10 | Incyte Corporation | Pyridineamine compounds useful as Pim kinase inhibitors |
| TWI734699B (zh) | 2015-09-09 | 2021-08-01 | 美商英塞特公司 | Pim激酶抑制劑之鹽 |
| US9920032B2 (en) | 2015-10-02 | 2018-03-20 | Incyte Corporation | Heterocyclic compounds useful as pim kinase inhibitors |
| KR20200038286A (ko) * | 2017-08-11 | 2020-04-10 | 셍커 파마슈티컬스 (지앙수) 엘티디. | 단백질 인산화효소 억제제로 작용하는 1h-피라졸로[4,3-h]퀴나졸린 화합물 |
| WO2019113487A1 (en) | 2017-12-08 | 2019-06-13 | Incyte Corporation | Low dose combination therapy for treatment of myeloproliferative neoplasms |
| CA3095580A1 (en) | 2018-04-13 | 2019-10-17 | Sumitomo Dainippon Pharma Oncology, Inc. | Pim kinase inhibitors for treatment of myeloproliferative neoplasms and fibrosis associated with cancer |
| CN108931633B (zh) * | 2018-05-22 | 2021-08-27 | 郑州大学第一附属医院 | 胆囊癌诊断和预后判断标志物pim1 |
| CN111377872A (zh) * | 2018-12-29 | 2020-07-07 | 广东阿格蕾雅光电材料有限公司 | 2-氯-4苯基苯并喹唑啉的合成方法 |
| WO2020167990A1 (en) | 2019-02-12 | 2020-08-20 | Tolero Pharmaceuticals, Inc. | Formulations comprising heterocyclic protein kinase inhibitors |
| CN113354651B (zh) * | 2020-07-30 | 2022-07-22 | 四川大学 | 吡唑并[1,5-a]喹唑啉衍生物及其在药物制备中的用途 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2005526730A (ja) * | 2002-02-19 | 2005-09-08 | ファルマシア・コーポレーション | 炎症の治療のための三環系ピラゾール誘導体 |
| KR20060015294A (ko) * | 2003-05-22 | 2006-02-16 | 파마시아 이탈리아 에스.피.에이. | 피라졸로-퀴나졸린 유도체, 그의 제조 방법 및 상기유도체의 키나제 저해제로서의 용도 |
| KR20090101942A (ko) * | 2006-12-21 | 2009-09-29 | 네르비아노 메디칼 사이언시스 에스.알.엘. | 치환된 피라졸로-퀴나졸린 유도체, 이의 제조방법, 및 키나제 억제제로서의 이의 용도 |
| WO2009156315A1 (en) * | 2008-06-26 | 2009-12-30 | Nerviano Medical Sciences S.R.L. | Pyrazolo-quinazolines |
Family Cites Families (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0831829B1 (en) | 1995-06-07 | 2003-08-20 | Pfizer Inc. | Heterocyclic ring-fused pyrimidine derivatives |
| EP0946523A1 (en) | 1996-12-23 | 1999-10-06 | Celltech Therapeutics Limited | Fused polycyclic 2-aminopyrimidine derivatives, their preparation and their use as protein tyrosine kinase inhibitors |
| GB9713087D0 (en) * | 1997-06-20 | 1997-08-27 | Celltech Therapeutics Ltd | Chemical compounds |
| GB9911053D0 (en) | 1999-05-12 | 1999-07-14 | Pharmacia & Upjohn Spa | 4,5,6,7-tetrahydroindazole derivatives process for their preparation and their use as antitumour agents |
| KR20020060160A (ko) | 1999-08-12 | 2002-07-16 | 파마시아 이탈리아 에스.피.에이. | 3(5)-아미노-피라졸 유도체, 이의 제조 방법 및항종양제로서의 이의 용도 |
| US6387900B1 (en) | 1999-08-12 | 2002-05-14 | Pharmacia & Upjohn S.P.A. | 3(5)-ureido-pyrazole derivatives process for their preparation and their use as antitumor agents |
| AU1734801A (en) | 1999-12-10 | 2001-06-18 | Ube Industries, Ltd. | Processes for producing tetrahydropyranyl-4-sulfonate and 4-aminotetrahydropyrancompound |
| NZ524475A (en) | 2000-08-10 | 2004-11-26 | Pharmacia Italia S | Bicyclo-pyrazoles active as kinase inhibitors, process for their preparation and pharmaceutical compositions comprising them |
| ES2299501T3 (es) | 2000-08-11 | 2008-06-01 | Boehringer Ingelheim Pharmaceuticals Inc. | Compuestos heterociclicos utiles como inhibidores de tirosina-quinasas. |
| JP2004517840A (ja) | 2000-11-27 | 2004-06-17 | フアルマシア・イタリア・エツセ・ピー・アー | フェニルアセトアミド−ピラゾール誘導体およびそれの抗腫瘍薬としての使用 |
| MXPA03006478A (es) | 2001-01-26 | 2003-09-22 | Pharmacia Italia Spa | Derivados de cromano, procedimiento para su preparacion y su uso como agentes antitumorales. |
| US20030100594A1 (en) | 2001-08-10 | 2003-05-29 | Pharmacia Corporation | Carbonic anhydrase inhibitor |
| EP1432416B1 (en) | 2001-09-26 | 2011-01-19 | Pfizer Italia S.r.l. | Aminoindazole derivatives active as kinase inhibitors, process for their preparation and pharmaceutical compositions containing them |
| ES2375527T3 (es) | 2007-12-03 | 2012-03-01 | Novartis Ag | Derivados 1,2-disustituidos-4-bencilamino-pirrolidina como inhibidores cetp útiles para el tratamiento de enfermedades tales como hiperlipidemia o arteriosclerosis. |
| CN103626777B (zh) * | 2009-07-29 | 2015-10-21 | 内尔维阿诺医学科学有限公司 | Plk抑制剂的盐类 |
| DE102009055123A1 (de) * | 2009-12-22 | 2011-06-30 | Osram Gesellschaft mit beschränkter Haftung, 81543 | Keramische Elektrode für eine Hochdruckentladungslampe |
| CN103339134B (zh) * | 2011-01-26 | 2015-12-23 | 内尔维阿诺医学科学有限公司 | 三环吡咯并衍生物、它们的制备方法和它们作为激酶抑制剂的应用 |
-
2011
- 2011-12-16 RU RU2013109776A patent/RU2652638C2/ru not_active IP Right Cessation
- 2011-12-16 WO PCT/IB2011/055743 patent/WO2012080990A1/en active Application Filing
- 2011-12-16 EP EP11810663.2A patent/EP2614065B1/en not_active Not-in-force
- 2011-12-16 JP JP2013543959A patent/JP5980225B2/ja not_active Expired - Fee Related
- 2011-12-16 MX MX2013003328A patent/MX342873B/es active IP Right Grant
- 2011-12-16 CA CA2812223A patent/CA2812223C/en not_active Expired - Fee Related
- 2011-12-16 KR KR1020137007627A patent/KR101913441B1/ko active IP Right Grant
- 2011-12-16 CN CN201180059720XA patent/CN103298816A/zh active Pending
- 2011-12-16 US US13/327,979 patent/US8541576B2/en not_active Expired - Fee Related
- 2011-12-16 BR BR112013008527A patent/BR112013008527A2/pt not_active Application Discontinuation
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2005526730A (ja) * | 2002-02-19 | 2005-09-08 | ファルマシア・コーポレーション | 炎症の治療のための三環系ピラゾール誘導体 |
| KR20060015294A (ko) * | 2003-05-22 | 2006-02-16 | 파마시아 이탈리아 에스.피.에이. | 피라졸로-퀴나졸린 유도체, 그의 제조 방법 및 상기유도체의 키나제 저해제로서의 용도 |
| KR20090101942A (ko) * | 2006-12-21 | 2009-09-29 | 네르비아노 메디칼 사이언시스 에스.알.엘. | 치환된 피라졸로-퀴나졸린 유도체, 이의 제조방법, 및 키나제 억제제로서의 이의 용도 |
| WO2009156315A1 (en) * | 2008-06-26 | 2009-12-30 | Nerviano Medical Sciences S.R.L. | Pyrazolo-quinazolines |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2012080990A1 (en) | 2012-06-21 |
| RU2013109776A (ru) | 2015-01-27 |
| MX342873B (es) | 2016-10-17 |
| US8541576B2 (en) | 2013-09-24 |
| CA2812223A1 (en) | 2012-06-21 |
| EP2614065A1 (en) | 2013-07-17 |
| KR101913441B1 (ko) | 2018-10-30 |
| US20120190678A1 (en) | 2012-07-26 |
| CA2812223C (en) | 2019-03-12 |
| RU2652638C2 (ru) | 2018-04-28 |
| MX2013003328A (es) | 2013-06-24 |
| BR112013008527A2 (pt) | 2016-07-12 |
| JP5980225B2 (ja) | 2016-08-31 |
| JP2014503531A (ja) | 2014-02-13 |
| EP2614065B1 (en) | 2017-04-19 |
| CN103298816A (zh) | 2013-09-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101913441B1 (ko) | 키나제 억제제로서 치환된 피라졸로-퀴나졸린 유도체 | |
| US10478423B2 (en) | Substituted indazole derivatives active as kinase inhibitiors | |
| JP5976778B2 (ja) | キナーゼ阻害剤としてのピラゾリル−ピリミジン誘導体 | |
| JP5925808B2 (ja) | 三環式誘導体、これらの調製方法およびこれらのキナーゼ阻害剤としての使用 | |
| JP5998223B2 (ja) | キナーゼ阻害剤としての置換3,4−ジヒドロピロロ[1,2−a]ピラジン−1(2H)−オン誘導体 | |
| AU2009264431B2 (en) | Pyrazolo-quinazolines | |
| RU2591191C2 (ru) | Трициклические пирроло производные, способ их получения и их применение в качестве ингибиторов киназы | |
| US9333205B2 (en) | Isoxazolo-quinazolines as modulators of protein kinase activity | |
| EP2203442B1 (en) | Substituted pyrrolo-pyrimidine derivatives, process for their preparation and their use as kinase inhibitors | |
| EP2089394A1 (en) | Substituted pyrrolo-pyrazole derivatives as kinase inhibitors |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal | ||
| E701 | Decision to grant or registration of patent right | ||
| GRNT | Written decision to grant |