KR20120128126A - 항응고제 해독제 - Google Patents
항응고제 해독제 Download PDFInfo
- Publication number
- KR20120128126A KR20120128126A KR1020127019086A KR20127019086A KR20120128126A KR 20120128126 A KR20120128126 A KR 20120128126A KR 1020127019086 A KR1020127019086 A KR 1020127019086A KR 20127019086 A KR20127019086 A KR 20127019086A KR 20120128126 A KR20120128126 A KR 20120128126A
- Authority
- KR
- South Korea
- Prior art keywords
- ser
- dabigatran
- seq
- val
- leu
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- IWQJUSCTFXXCDD-UHFFFAOYSA-N C[n](c(CNc(cc1)ccc1C#N)nc1c2)c1ccc2C(N(CCC(OC)=O)c1ccccc1)=O Chemical compound C[n](c(CNc(cc1)ccc1C#N)nc1c2)c1ccc2C(N(CCC(OC)=O)c1ccccc1)=O IWQJUSCTFXXCDD-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/44—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material not provided for elsewhere, e.g. haptens, metals, DNA, RNA, amino acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4427—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems
- A61K31/4439—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems containing a five-membered ring with nitrogen as a ring hetero atom, e.g. omeprazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39583—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials not provided for elsewhere, e.g. haptens, coenzymes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/02—Stomatological preparations, e.g. drugs for caries, aphtae, periodontitis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P39/00—General protective or antinoxious agents
- A61P39/02—Antidotes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/02—Antithrombotic agents; Anticoagulants; Platelet aggregation inhibitors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/04—Antihaemorrhagics; Procoagulants; Haemostatic agents; Antifibrinolytic agents
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/86—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving blood coagulating time or factors, or their receptors
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/54—F(ab')2
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/55—Fab or Fab'
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/569—Single domain, e.g. dAb, sdAb, VHH, VNAR or nanobody®
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/62—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising only variable region components
- C07K2317/622—Single chain antibody (scFv)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/62—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising only variable region components
- C07K2317/626—Diabody or triabody
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2500/00—Screening for compounds of potential therapeutic value
- G01N2500/02—Screening involving studying the effect of compounds C on the interaction between interacting molecules A and B (e.g. A = enzyme and B = substrate for A, or A = receptor and B = ligand for the receptor)
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2500/00—Screening for compounds of potential therapeutic value
- G01N2500/10—Screening for compounds of potential therapeutic value involving cells
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Immunology (AREA)
- Hematology (AREA)
- Molecular Biology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biochemistry (AREA)
- Epidemiology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Biomedical Technology (AREA)
- Microbiology (AREA)
- Urology & Nephrology (AREA)
- Genetics & Genomics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biophysics (AREA)
- Diabetes (AREA)
- Cell Biology (AREA)
- Biotechnology (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Physics & Mathematics (AREA)
- Mycology (AREA)
- Food Science & Technology (AREA)
- Analytical Chemistry (AREA)
- Toxicology (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Peptides Or Proteins (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
Abstract
Description
도 2: 디비가트란에 대한 4 가지 상이한 항체들(A-D)은 모두 사람 혈장중의 다비가트란을 연장된 응고 시간으로 중화시켰다. 사람 혈장의 기준 응고는 10.9초였으며, 200 nM 다비가트란이 혈장과 함께 예비항온처리된 경우 응고는 51초로 연장되었다. 200 nM 다비가트란과 예비항온처리된 혈장에 각 항체를 첨가하고 추가로 5분간 항온처리하였다. 그런 다음 트롬빈을 첨가하여 트롬빈 응고 시간이 개시되었다. 각 항체는 다비가트란의 응고 시간을 상이한 정도로 감소시킬 수 있었다. 농도가 가장 높은 용액이 항응고제 활성을 가장 크게 감소시켰다.
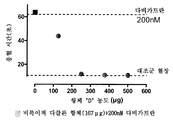
도 3: 200 nM 다비가트란과 예비항온처리된 사람 혈장에 첨가되는 다클론 항체(항체 D)의 농도 증가에 따른 효과를 측정하였다. 기준 응고 시간은 11초였으며 다비가트란의 첨가시 응고는 63.7초로 연장되었다. 그런 다음, 다비가트란에 의해 연장된 트롬빈 응고 시간을 감소시키는 작용에 대한 항체 희석도의 증가에 따른 효과를 시험하였다. 가장 낮은 농도는 트롬빈 응고 시간을 43.9초로 감소시켰다. 보다 높은 농도들은 트롬빈 응고 시간을 기준치 수준으로 완전히 감소시켰고 다비가트란의 항응고 효과를 완전히 중화시켰다. 비특이적 토끼 다클론 항체의 첨가(정사각형)는 다비가트란의 항응고 효과를 감소시키는 효과를 전혀 나타내지 않았다.
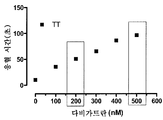
도 4: 500 nM 다비가트란과 예비항온처리된 사람 혈장에 첨가되는 다클론 항체(항체 D)의 농도 증가에 따른 효과를 측정하였다. 기준 응고 시간은 10.9초였으며 이와 같은 좀더 고 농도의 다비가트란 첨가시 응고는 111.7초로 연장되었다(~10배 증가). 원액 또는 항체의 1:2 희석의 효과는 다비가트란에 의해 연장된 트롬빈 응고 시간을 농도 의존적 방식으로 감소시켰다. 최고의 농도는 또한 트롬빈 응고 시간을 기준치 수준으로 완전히 감소시켰고 다비가트란의 과다치료 농도의 항응고 효과를 완전히 중화시켰다.
도 5: 항-다비가트란 항체 분자 중쇄의 가변 영역의 서열.
도 6: 항-다비가트란 항체 분자 경쇄의 가변 영역의 서열.
도 7: 마우스 단클론 항체(클론 22)는 사람 혈장 및 사람 전혈중에서의 다비가트란의 항응고 효과를 감소시킨다. 30 nM 다비가트란과 예비항온처리된 사람 혈장 또는 전혈에 농도가 점증된 마우스 항체를 첨가하였다. 이 검사는 트롬빈 1.5 내지 2 U/mL의 첨가로 시작하여 응고 시간을 측정하였다. 100% 다비가트란 활성은 이 화합물의 유무에 따른 응고 시간의 차이로서 규정되었다. 다비가트란-매개된 응고 시간 연장이 항체 용량에 의존적으로 억제되었다.
도 8: 클론 22 항체로부터 생성된 마우스 Fab는 사람 혈장중에서 다비가트란의 항응고 효과를 감소시킨다. 7 nM 다비가트란과 예비항온처리된 사람 혈장에 농도가 점증된 마우스 Fab를 첨가하였다. 이 검사는 트롬빈 0.4 U/mL의 첨가로 시작하여 응고 시간을 측정하였다. 100% 억제는 다비가트란-매개된 응고 시간 증가의 완전한 차단으로서 규정되었다. 사람 혈장에서의 다비가트란-유도된 응고 시간 연장이 Fab 용량에 의존적으로 억제되었다.
도 9: 마우스 단클론 항체(클론 22)는 사람 혈장중에서 다비가트란 아실글루쿠로나이드의 항응고 효과를 감소시킨다. 7 nM 다비가트란 아실글루쿠로나이드 또는 다비가트란과 예비항온처리된 사람 혈장에 농도가 점증된 마우스 항체를 첨가하였다. 이 검사는 트롬빈 0.4 U/mL의 첨가로 시작하여 응고 시간을 측정하였다. 100% 억제는 해당 화합물-매개된 응고 시간 증가의 완전한 차단으로서 규정되었다. 사람 혈장에서의 다비가트란 아실글루쿠로나이드-유도된 응고 시간 연장이 항체 용량에 의존적으로 억제되었다.
도 10: 인간화 Fab(Fab 18/15)는 사람 혈장중에서 다비가트란의 항응고 효과를 감소시킨다. 7 nM 다비가트란과 예비항온처리된 사람 혈장에 농도가 점증된 Fab 18/15를 첨가하였다. 이 검사는 트롬빈 0.4 U/mL의 첨가로 시작하여 응고 시간을 측정하였다. 100% 억제는 해당 다비가트란-매개된 응고 시간 증가의 완전한 차단으로서 규정되었다. 사람 혈장에서의 다비가트란-유도된 응고 시간 연장이 Fab 용량에 의존적으로 억제되었다.
도 11: t=0에서 등몰 Fab의 일시 투여와 함께 연속 주입으로서 다비가트란이 투여된 랫트에서의 생체외 전혈 트롬빈 응고 시간(3.0 U/mL 트롬빈). 원형 라인은 약물없이 비히클로 처리된 것을 나타낸다. 정사각형 라인은 Fab 투여가 없는 다비가트란 항응고 활성을 나타낸다. 삼각형 라인은 Fab의 투여 후 항응고제 활성을 나타낸다. 데이터는 처리군 당 네마리 동물(n=4)의 평균 ± SE로 표시되었다.
도 12: t=0에서 등몰 Fab의 일시 투여와 함께 연속 주입으로서 다비가트란이 투여된 랫트에서의 생체외 전혈 aPTT. 원형은 약물없이 비히클로 처리된 것을 나타낸다. 정사각형 라인은 Fab 투여가 없는 다비가트란 항응고 활성을 나타낸다. 삼각형 라인은 Fab의 투여 후 항응고제 활성을 나타낸다. 데이터는 처리군 당 네마리 동물(n=4)의 평균 ± SE로 표시되었다.
도 13: t=0에서 점증된 용량의 Fab의 일시 투여와 함께 연속 주입으로서 다비가트란이 투여된 랫트에서의 생체외 전혈 트롬빈 응고 시간(3.0 U/mL 트롬빈). 원형 라인은 약물없이 비히클로 처리된 것을 나타낸다. 정사각형 라인은 Fab 투여가 없는 다비가트란 항응고 활성을 나타낸다. 삼각형 라인은 Fab의 등몰 투여 후 항응고제 활성을 나타내고 파선은 등몰 용량의 50%를 나타낸다. 데이터는 처리군 당 네마리 동물(n=4)의 평균 ± SE로 표시되었다.
도 14: t=0에서 등몰 Fab의 일시 투여와 함께 연속 주입으로서 다비가트란이 투여된 랫트에서의 생체외 전혈 aPTT. 원형 라인은 약물없이 비히클로 처리된 것을 나타낸다. 정사각형 라인은 Fab 투여가 없는 다비가트란 항응고 활성을 나타낸다. 삼각형 라인은 등몰 Fab의 투여 후 항응고제 활성을 나타내고 파선은 등몰 용량의 50%를 나타낸다. 데이터는 처리군 당 네마리 동물(n=4)의 평균 ± SE로 표시되었다.
Claims (38)
- 항응고제의 활성을 중화시킬 수 있는 항체 분자.
- 제1항에 있어서, 상기 항체 분자가 항응고제에 대해 결합 특이성을 갖는, 항체 분자.
- 제1항 또는 제2항에 있어서, 상기 항응고제가 직접 트롬빈 억제제, 인자 Xa 억제제 또는 비타민 K 길항제인, 항체 분자.
- 제1항 내지 3항 중 어느 한 항에 있어서, 상기 항응고제가 다비가트란, 아르가트로반, 멜라가트란, 지멜라가트란, 히루딘, 비발리루딘, 레피루딘, 데시루딘, 아픽사반, 오타믹사반, 리바록사반, 데피브로타이드, 라마트로반, 안티트롬빈 III 또는 드로트레코진 알파인, 항체 분자.
- 제1항 내지 4항 중 어느 한 항에 있어서, 상기 항응고제가 하기 화학식 I의 이치환된 바이사이클릭 헤테로사이클, 이의 호변이성체, 입체이성체 및 염인 항체 분자:
화학식 I
Ra - A - Het - B - Ar - E
상기 화학식 I에서,
A는 그룹 Het의 벤조, 피리도 또는 티에노 모이어티(moiety)에 결합된 카르보닐 또는 설포닐 그룹을 나타내고;
B는 그룹 Ar에 결합된 메틸렌 그룹이 산소 또는 황 원자에 의해 또는 -NR1- 그룹(여기서, R1은 수소 원자 또는 C1 -4-알킬 그룹을 나타낸다)에 의해 대체될 수 있는 에틸렌 그룹을 나타내며;
E는 RbNH-C(=NH)- 그룹(여기서, Rb는 수소 원자, 하이드록시, C1 -9-알콕시카르보닐(여기서, C1 -9-알콕시카르보닐의 2번 위치의 에톡시 모이어티는 C1 -3-알킬설포닐 또는 2-(C1 -3-알콕시)-에틸 그룹에 의해 추가로 치환될 수 있다), 사이클로헥실옥시카르보닐, 페닐-C1 -3-알콕시카르보닐, 벤조일, p-C1 -3-알킬벤조일 또는 피리디노일 그룹을 나타낸다)을 나타내고;
Ar은 염소 원자 또는 메틸, 에틸 또는 메톡시 그룹에 의해 임의로 치환되는 1,4-페닐렌 그룹을 나타내거나 2,5-티에닐렌 그룹을 나타내며;
Het는 1-(C1 -3-알킬)-2,5-벤즈이미다졸릴렌, 1-사이클로프로필-2,5-벤즈이미다졸릴렌, 2,5-벤조티아졸릴렌, 1-(C1 -3-알킬)-2,5-인돌릴렌, 1-(C1 -3-알킬)-2,5-이미다조[4,5-b]피리디닐렌, 3-(C1 -3-알킬)-2,7-이미다조[1,2-a]피리디닐렌 또는 1-(C1 -3-알킬)-2,5-티에노[2,3-d]이미다졸릴렌 그룹을 나타내고;
Ra는 R2NR3- 그룹을 나타낸다(여기서,
R2는 카르복시, C1 -6-알킬옥시카르보닐, 벤질옥시카르보닐, C1 -3-알킬설포닐아미노카르보닐 또는 1H-테트라졸-5-일 그룹에 의해 치환될 수 있는 C1 -4 알킬 그룹;
하이드록시, 벤질옥시, 카르복시-C1 -3-알킬아미노, C1 -3-알콕시카르보닐-C1 -3-알킬아미노, N-(C1 -3-알킬)-카르복시-C1 -3-알킬아미노 또는 N-(C1 -3-알킬)-C1 -3-알콕시카르보닐-C1 -3-알킬아미노 그룹에 의해 치환되는 C2 -4-알킬 그룹(여기서, 상기 그룹들에서 인접한 질소 원자에 대해 α-위치에 있는 탄소 원자는 치환될 수 없다)이고;
R3은 C3 -7-사이클로알킬 그룹, 프로파르길 그룹(여기서, 불포화 부분은 R2NR3 그룹의 질소 원자에 직접적으로 결합될 수 없다), 불소 또는 염소 원자에 의해, 또는 메틸 또는 메톡시 그룹에 의해 임의로 치환되는 페닐 그룹, 메틸 그룹에 의해 임의로 치환되는 피라졸릴, 피리다졸릴 또는 피리디닐 그룹을 나타내거나;
R2와 R3은 이들 사이의 질소 원자와 함께, 카르복시 또는 C1 -4-알콕시카르보닐 그룹에 의해 임의로 치환되고, 페닐 환이 추가로 융합될 수 있는 5- 내지 7-원 사이클로알킬렌이미노 그룹을 나타낸다). - 제5항에 있어서, 상기 항응고제가
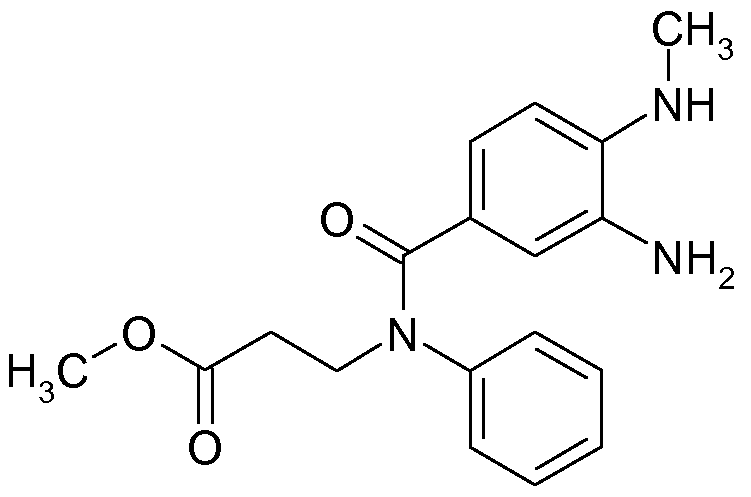
(a) 2-[N-(4-아미디노페닐)-아미노메틸]-벤즈티아졸-5-카르복실산-N-페닐-N-(2-카르복시에틸)-아미드,
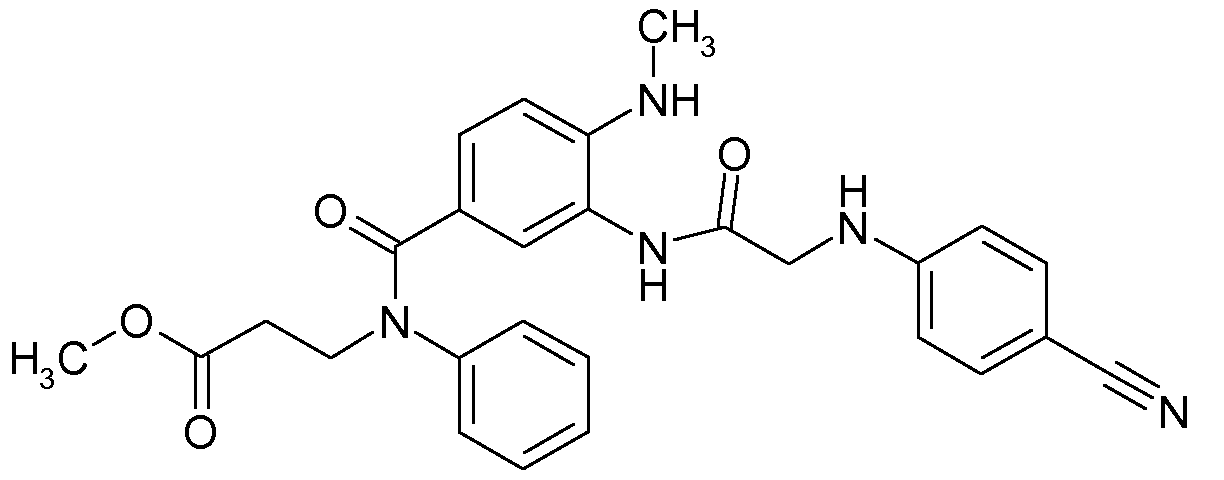
(b) 2-[N-(4-아미디노페닐)-N-메틸-아미노메틸]-벤즈티아졸-5-일-카르복실산-N-페닐-N-(2-카르복시카르보닐에틸)-아미드,
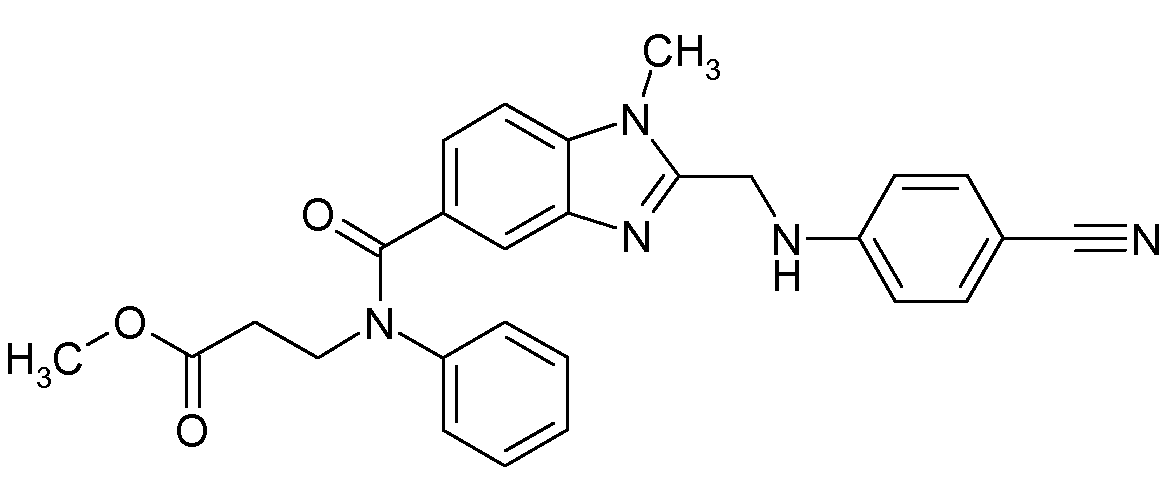
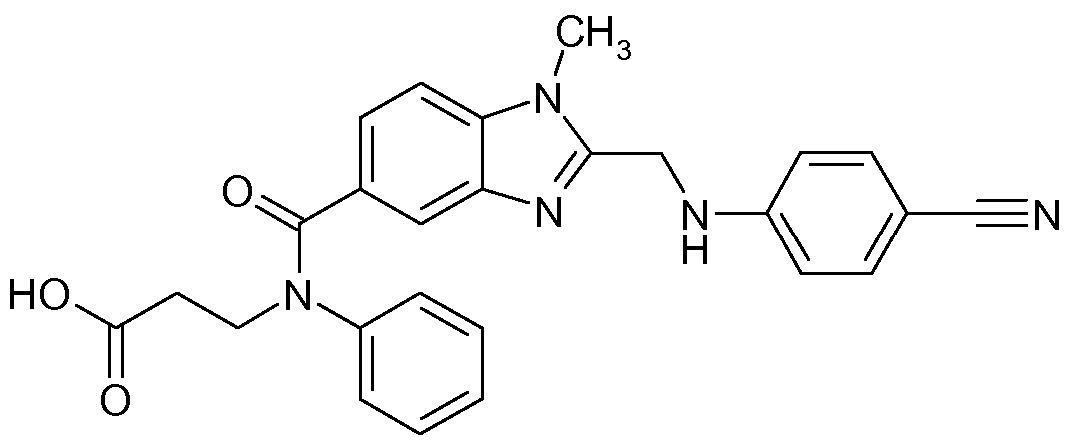
(c) 1-메틸-2-[N-(4-아미디노페닐)-아미노메틸]-벤즈이미다졸-5-일-카르복실산-N-페닐-N-(2-하이드록시카르보닐에틸)-아미드,
(d) 1-메틸-2-[N-(4-아미디노페닐)-아미노메틸]-벤즈이미다졸-5-일-카르복실산-N-페닐-N-(3-하이드록시카르보닐프로필)-아미드,
(e) 1-메틸-2-[N-(4-아미디노페닐)-아미노메틸]-벤즈이미다졸-5-일-카르복실산-N-(2-피리딜)-N-(하이드록시카르보닐메틸)-아미드,
(f) 1-메틸-2-[2-(2-아미디노티오펜-5-일)에틸]-벤즈이미다졸-5-일-카르복실산-N-(2-피리딜)-N-(2-하이드록시카르보닐에틸)-아미드,
(g) 1-메틸-2-[N-(4-아미디노페닐)-아미노메틸]-벤즈이미다졸-5-일-카르복실산-N-(2-피리딜)-N-(2-하이드록시카르보닐에틸)-아미드,
(h) 1-메틸-2-[2-(4-아미디노페닐)에틸]-벤즈이미다졸-5-일-카르복실산-N-(2-피리딜)-N-(2-하이드록시카르보닐에틸)-아미드,
(i) 1-메틸-2-[2-(4-아미디노페닐)에틸]-벤즈이미다졸-5-일-카르복실산-N-페닐-N-(2-하이드록시카르보닐에틸)-아미드,
(j) 1-메틸-2-[2-(4-아미디노페닐)에틸]-벤즈이미다졸-5-일-카르복실산-N-페닐-N-[2-(1H-테트라졸-5-일)에틸]-아미드,
(k) 1-메틸-2-[N-(4-아미디노페닐)-아미노메틸]-벤즈이미다졸-5-일-카르복실산-N-페닐-N-[2-(1H-테트라졸-5-일)에틸]-아미드,
(l) 1-메틸-2-[N-(4-아미디노페닐)-N-메틸-아미노메틸]-벤즈이미다졸-5-일-카르복실산-N-(2-피리딜)-N-(2-하이드록시카르보닐에틸]-아미드,
(m) 1-메틸-2-[N-(4-아미디노페닐)-N-메틸-아미노메틸]-벤즈이미다졸-5-일-카르복실산-N-(3-피리딜)-N-(2-하이드록시카르보닐에틸]-아미드,
(n) 1-메틸-2-[N-(4-아미디노페닐)-N-메틸-아미노메틸]-벤즈이미다졸-5-일-카르복실산-N-페닐-N-(2-하이드록시카르보닐에틸]-아미드,
(o) 1-메틸-2-[N-(4-아미디노페닐)-아미노메틸]-벤즈이미다졸-5-일-카르복실산-N-페닐-N-[(N-하이드록시카르보닐에틸-N-메틸)-2-아미노에틸]-아미드,
(p) 1-메틸-2-[N-(4-아미디노페닐)-아미노메틸]-벤즈이미다졸-5-일-카르복실산-N-(3-플루오로페닐)-N-(2-하이드록시카르보닐에틸)-아미드,
(q) 1-메틸-2-[N-(4-아미디노페닐)-아미노메틸]-벤즈이미다졸-5-일-카르복실산-N-(4-플루오로페닐)-N-(2-하이드록시카르보닐에틸)-아미드,
(r) 1-메틸-2-[N-(4-아미디노-2-메톡시-페닐)-아미노메틸]-벤즈이미다졸-5-일-카르복실산-N-페닐-N-(2-하이드록시카르보닐에틸]-아미드,
(s) 1-메틸-2-[N-(4-아미디노-2-메톡시-페닐)-아미노메틸]-벤즈이미다졸-5-일-카르복실산-N-(2-피리딜)-N-(2-하이드록시카르보닐에틸]-아미드,
(t) 1-메틸-2-[N-(4-아미디노페닐)-아미노메틸]-인돌-5-일-카르복실산-N-페닐-N-(2-메톡시카르보닐에틸)-아미드, 및
(u) 1-메틸-2-[N-(4-아미디노페닐)-아미노메틸]-티에노[2,3-d]이미다졸-5-일-카르복실산-N-페닐-N-(2-하이드록시카르보닐에틸)-아미드,
(v) 1-메틸-2-[N-(4-아미디노페닐)-아미노메틸]-벤즈이미다졸-5-일-카르복실산-N-페닐-N-(2-하이드록시카르보닐에틸)-아미드,
(w) 1-메틸-2-[N-(4-아미디노페닐)-아미노메틸]-벤즈이미다졸-5-일-카르복실산-N-(2-피리딜)-N-(2-하이드록시카르보닐에틸)-아미드,
(x) 1-메틸-2-[N-(4-아미디노-2-메톡시-페닐)-아미노메틸]-벤즈이미다졸-5-일-카르복실산-N-(2-피리딜)-N-(2-하이드록시카르보닐에틸)-아미드,
(y) 1-메틸-2-[N-[4-(N-n-헥실옥시카르보닐아미디노)페닐]-아미노메틸]-벤즈이미다졸-5-일-카르복실산-N-(2-피리딜)-N-(2-에톡시카르보닐에틸)-아미드,
이들의 호변이성체, 입체이성체 및 염중에서 선택되는 화합물인, 항체 분자. - 제2항에 있어서, 상기 항응고제가 다비가트란인, 항체 분자.
- 제7항에 있어서, 다비가트란 및 다비가트란의 1-O-아실글루쿠로나이드의 활성을 중화시킬 수 있는, 항체 분자.
- 제5항 내지 제8항 중 어느 한 항에 있어서, 서열번호 1 및 서열번호 2로 이루어진 그룹에서 선택되는 CDR1, 서열번호 3, 서열번호 4, 서열번호 5, 서열번호 6, 서열번호 7 및 서열번호 8로 이루어진 그룹에서 선택되는 CDR2 및 서열번호 9 및 서열번호 10으로 이루어진 그룹에서 선택되는 CDR3을 갖는 중쇄 가변 도메인과 서열번호 11, 서열번호 12 및 서열번호 13으로 이루어진 그룹에서 선택되는 CDR1, 서열번호 14의 CDR2 및 서열번호 15의 CDR3을 갖는 경쇄 가변 도메인을 포함하는, 항체 분자.
- 제9항에 있어서, 서열번호 1의 CDR1, 서열번호 6, 서열번호 7 및 서열번호 8로 이루어진 그룹에서 선택되는 CDR2 및 서열번호 10의 CDR3을 갖는 중쇄 가변 도메인과 서열번호 13의 CDR1, 서열번호 14의 CDR2 및 서열번호 15의 CDR3을 갖는 경쇄 가변 도메인을 포함하는, 항체 분자.
- 제9항 또는 제10항에 있어서, 서열번호 16, 18, 20, 22, 24 및 26으로 이루어진 그룹에서 선택되는 중쇄 가변 도메인과 서열번호 17, 19, 21, 23, 25 및 27로 이루어진 그룹에서 선택되는 경쇄 가변 도메인을 포함하는, 항체 분자.
- 제11항에 있어서, 서열번호 16의 중쇄 가변 도메인과 서열번호 17의 경쇄 가변 도메인을, 또는 서열번호 18의 중쇄 가변 도메인과 서열번호 19의 경쇄 가변 도메인을, 또는 서열번호 20의 중쇄 가변 도메인과 서열번호 21의 경쇄 가변 도메인을, 또는 서열번호 22의 중쇄 가변 도메인과 서열번호 23의 경쇄 가변 도메인을, 또는 서열번호 24의 중쇄 가변 도메인과 서열번호 25의 경쇄 가변 도메인을, 또는 서열번호 24의 중쇄 가변 도메인과 서열번호 27의 경쇄 가변 도메인을, 또는 서열번호 26의 중쇄 가변 도메인과 서열번호 27의 경쇄 가변 도메인을 포함하는, 항체 분자.
- 제1항 내지 제12항 중 어느 한 항에 있어서, 다클론 항체, 단클론 항체, 인간 항체, 인간화 항체, 키메라 항체, 항체의 단편, 특히 Fab, Fab' 또는 F(ab')2 단편, 단일쇄 항체, 특히 단일쇄 가변 단편(scFv), 소형 모듈 면역약제(SMIP : Small Modular Immunopharmaceutical), 도메인 항체, 나노바디, 디아바디(diabody) 또는 설계된 안키린 반복 단백질(DARPin)인, 항체 분자.
- 제13항에 있어서, 중쇄 가변 도메인과 경쇄 가변 도메인이 서열번호 28, 서열번호 29, 서열번호 30 및 서열번호 31로 이루어진 그룹에서 선택되는 링커 펩타이드를 통해 서로 결합되어 있는 scFv인, 항체 분자.
- 제14항에 있어서, 서열번호 32 또는 서열번호 33을 포함하는, 항체 분자.
- 제13항에 있어서, 서열번호 34 또는 서열번호 40을 포함하는 중쇄와 서열번호 35를 포함하는 경쇄를 갖거나, 서열번호 42를 포함하는 중쇄와 서열번호 43을 포함하는 경쇄를 갖는 항체 분자.
- 제13항에 있어서, 서열번호 36, 서열번호 38 또는 서열번호 41을 포함하는 Fd 단편 및 서열번호 37 또는 서열번호 39를 포함하는 경쇄를 갖는 Fab 분자인, 항체 분자.
- 제1항 내지 제17항 중 어느 한 항에 있어서, 의약으로 사용하기 위한 항체 분자.
- 제1항 내지 제18항 중 어느 한 항에 있어서, 항응고제 치료요법의 부작용의 치료요법 또는 예방에 사용하고/하거나 항응고제의 과다복용을 반전시키기 위한 항체 분자.
- 제19항에 있어서, 상기 부작용이 출혈인, 항체 분자.
- 제1항 내지 제20항 중 어느 한 항에 따른 항체 분자의 유효량을 이를 필요로 하는 환자에게 투여함을 포함하여, 항응고제 치료요법의 부작용 또는 항응고제 치료요법에서의 과다복용 사건을 치료 또는 예방하는 방법.
- 제1항 내지 제21항 중 어느 한 항에 따른 항체 분자의 제조 방법으로서,
(a) 발현 조절 서열과 기능적으로 연계되어 있는 상기 항체 분자를 암호화하는 하나 이상의 핵산을 포함하는 숙주 세포를 제공하고,
(b) 상기 숙주 세포를 배양하고,
(c) 상기 세포 배양물로부터 상기 항체 분자를 회수함을 포함하는,
제1항 내지 제21항 중 어느 한 항에 따른 항체 분자의 제조 방법. - 제1항 내지 제20항 중 어느 한 항에 따른 항체 또는 이의 약제학적 조성물을 포함하는 키트.
- (a) 제1항 내지 제20항 중 어느 한 항에 따른 항체 또는 이의 약제학적 조성물,
(b) 용기 및
(c) 라벨(label)을 포함하는, 키트. - 제7항 내지 제20항 중 어느 한 항에 따른 항체, 및 다비가트란, 다비가트란 에텍실레이트, 다비가트란의 프로드러그 또는 이들의 약제학적으로 허용되는 염을 포함하는 키트.
- 제25항에 있어서, 상기 다비가트란, 다비가트란 에텍실레이트, 다비가트란의 프로드러그 또는 이들의 약제학적으로 허용되는 염의 형태가 고체, 액체 또는 겔의 형태인, 키트.
- 제25항에 있어서, 상기 다비가트란 에텍실레이트의 약제학적으로 허용되는 염이 메실레이트 염인, 키트.
- 제25항 또는 제27항에 있어서, 상기 다비가트란, 다비가트란 에텍실레이트, 다비가트란의 프로드러그 또는 이들의 약제학적으로 허용되는 염의 용량 단위 당 함량이 일일 1회(QD) 또는 일일 2회(BID)로 75 mg 내지 300 mg인, 키트.
- (a) 제7항 내지 제20항 중 어느 한 항에 따른 항체 또는 이의 약제학적 조성물;
(b) 다비가트란, 다비가트란 에텍실레이트, 다비가트란의 프로드러그 또는 이들의 약제학적으로 허용되는 염의 약제학적 조성물;
(c) 용기; 및
(d) 라벨을 포함하는, 키트. - 제29항에 있어서, 상기 다비가트란, 다비가트란 에텍실레이트, 다비가트란의 프로드러그 또는 이들의 약제학적으로 허용되는 염의 형태가 고체, 액체 또는 겔의 형태인, 키트.
- 제29항에 있어서, 상기 다비가트란 에텍실레이트의 약제학적으로 허용되는 염이 메실레이트 염인, 키트.
- 제29항 또는 제31항에 있어서, 상기 다비가트란, 다비가트란 에텍실레이트, 다비가트란의 프로드러그 또는 이들의 약제학적으로 허용되는 염의 용량 단위 당 함량이 일일 1회(QD) 또는 일일 2회(BID)로 75 mg 내지 300 mg인, 키트.
- 키트로서,
상기 키트는
(a) 다비가트란, 다비가트란 에텍실레이트, 다비가트란의 프로드러그 또는 이들의 약제학적으로 허용되는 염을 포함하는 제1 약제학적 조성물;
(b) 제7항 내지 제20항 중 어느 한 항에 따른 항체를 포함하는 제2 약제학적 조성물;
(c) 상기 제1 및 제2 약제학적 조성물을 환자에게 별도로 투여하기 위한 지침서
를 포함하고;
상기 제1 및 제2 약제학적 조성물은 별개의 용기들에 함유되며 상기된 제2 약제학적 조성물이 다비가트란 또는 다비가트란의 1-O-아실글루쿠로나이드의 중화 또는 부분 중화를 필요로 하는 환자에게 투여되는, 키트. - 다비가트란, 다비가트란 에텍실레이트, 다비가트란의 프로드러그 또는 이들의 약제학적으로 허용되는 염으로 치료를 받고 있는 환자에서 다비가트란 또는 다비가트란의 1-O-아실글루쿠로나이드를 중화 또는 부분 중화시키는 방법으로서, 제7항 내지 제20항 중 어느 한 항에 따른 항체 또는 이의 약제학적 조성물을 투여함을 포함하는 방법.
- 환자에서 다비가트란 또는 다비가트란의 1-O-아실글루쿠로나이드를 중화 또는 부분 중화시키는 방법으로서,
(a) 환자가 다비가트란, 다비가트란 에텍실레이트, 다비가트란의 프로드러그 또는 이들의 약제학적으로 허용되는 염으로 치료를 받았었는 지와 환자가 복용한 양을 확인하고;
(b) 다비가트란 또는 다비가트란의 1-O-아실글루쿠로나이드가 응혈 또는 응고 시험 또는 검사 결과의 정밀 판독을 방해하는 응혈 또는 응고 시험 또는 검사를 수행하기 이전에, 다비가트란 또는 1-O-아실글루쿠로나이드를 제7항 내지 제20항 중 어느 한 항에 따른 항체로 중화시키며;
(c) 상기 환자로부터 채취한 시료에 대해 상기 응혈 또는 응고 시험 또는 검사를 수행하여 다비가트란 또는 다비가트란의 1-O-아실글루쿠로나이드 존재없이 응혈의 형성 수준을 측정하고;
(d) 환자에서 응혈 형성과 분해사이의 적절한 균형을 달성하기 위해, 상기 환자에게 투여된 다비가트란, 다비가트란 에텍실레이트, 다비가트란의 프로드러그 또는 이들의 약제학적으로 허용되는 염의 양을 조정함을 포함하는,
환자에서 다비가트란 또는 다비가트란의 1-O-아실글루쿠로나이드를 중화 또는 부분 중화시키는 방법. - 제34항 또는 제35항에 있어서, 다비가트란 또는 다비가트란의 1-O-아실글루쿠로나이드에 대한 항체의 양이 0.1 내지 100의 몰비인, 방법.
- 제36항에 있어서, 다비가트란 또는 다비가트란의 1-O-아실글루쿠로나이드에 대한 항체의 양이 0.1 내지 10의 몰비인, 방법.
- 제35항에 있어서, 상기 시험 또는 검사 결과의 정밀 판독이, 피브리노겐 수준, 활성화된 단백질 C 내성 또는 관련된 시험들의 정밀 판독인, 방법.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP10151239 | 2010-01-20 | ||
| EP10151239.0 | 2010-01-20 | ||
| US38391410P | 2010-09-17 | 2010-09-17 | |
| US61/383,914 | 2010-09-17 | ||
| PCT/EP2011/050749 WO2011089183A2 (en) | 2010-01-20 | 2011-01-20 | Anticoagulant antidotes |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20120128126A true KR20120128126A (ko) | 2012-11-26 |
| KR101781787B1 KR101781787B1 (ko) | 2017-09-26 |
Family
ID=42061991
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020127019086A Active KR101781787B1 (ko) | 2010-01-20 | 2011-01-20 | 항응고제 해독제 |
Country Status (43)
Families Citing this family (25)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AR079944A1 (es) * | 2010-01-20 | 2012-02-29 | Boehringer Ingelheim Int | Anticuerpo neutralizante de la actividad de un anticoagulante |
| EP3252076B1 (en) | 2011-01-14 | 2019-09-04 | The Regents Of The University Of California | Diagnostic use of antibodies against ror-1 protein |
| JP2014506448A (ja) * | 2011-01-19 | 2014-03-17 | バイエル・インテレクチュアル・プロパティ・ゲゼルシャフト・ミット・ベシュレンクテル・ハフツング | 凝固因子の阻害剤に対する結合タンパク質 |
| WO2012130834A1 (en) * | 2011-03-30 | 2012-10-04 | Boehringer Ingelheim International Gmbh | Anticoagulant antidotes |
| CN104080772B (zh) | 2011-11-29 | 2016-10-05 | 佩罗斯菲尔股份有限公司 | 抗凝血逆转剂 |
| PE20160533A1 (es) | 2013-03-14 | 2016-06-09 | Bayer Healthcare Llc | Anticuerpos monoclonales contra antitrombina beta que forma complejos con heparina |
| JP2016539926A (ja) * | 2013-10-25 | 2016-12-22 | ベーリンガー インゲルハイム インターナショナル ゲゼルシャフト ミット ベシュレンクテル ハフツング | 抗凝血薬の解毒剤 |
| TW201623331A (zh) * | 2014-03-12 | 2016-07-01 | 普羅帝納生物科學公司 | 抗黑色素瘤細胞黏著分子(mcam)抗體類及使用彼等之相關方法 |
| CN105223348A (zh) * | 2014-05-26 | 2016-01-06 | 北京九强生物技术股份有限公司 | 人抗凝血酶iii的胶乳增强免疫比浊法检测试剂盒 |
| EP2980218A1 (en) | 2014-07-30 | 2016-02-03 | Rheinische Friedrich-Wilhelms-Universität Bonn | Aptamer thrombin complex for use as an antidote to direct acting thrombin inhibitors |
| WO2016019145A1 (en) * | 2014-07-31 | 2016-02-04 | Haemonetics Corporation | Detection and classification of an anticoagulant using a clotting assay |
| WO2016044645A1 (en) * | 2014-09-17 | 2016-03-24 | Elmaleh David R | Anticoagulant derivatives for cardiovascular imaging |
| EP4205743A1 (en) | 2014-12-31 | 2023-07-05 | Shenzhen Pharmacin Co., Ltd. | Pharmaceutical composition and preparation method therefor |
| US10449195B2 (en) | 2016-03-29 | 2019-10-22 | Shenzhen Pharmacin Co., Ltd. | Pharmaceutical formulation of palbociclib and a preparation method thereof |
| US11879014B2 (en) | 2017-03-17 | 2024-01-23 | Tusk Therapeutics Ltd. | Method of treating cancer or depleting regulatory T cells in a subject by administering a human IGG1 anti-CD25 antibody |
| WO2019124468A1 (ja) * | 2017-12-24 | 2019-06-27 | ノイルイミューン・バイオテック株式会社 | ヒトメソセリンを特異的に認識する細胞表面分子、il-7、及びccl19を発現する免疫担当細胞 |
| US11814434B2 (en) | 2018-03-13 | 2023-11-14 | Tusk Therapeutics Ltd. | Anti-CD25 for tumour specific cell depletion |
| WO2019217705A1 (en) * | 2018-05-11 | 2019-11-14 | Proplex Technologies, LLC | Binding proteins and chimeric antigen receptor t cells targeting gasp-1 granules and uses thereof |
| EP3873916B8 (en) | 2018-10-29 | 2025-03-26 | Shanghai Synergy Pharmaceutical Sciences, Ltd. | Novel dipeptide compounds and uses thereof |
| US12251377B2 (en) | 2019-03-06 | 2025-03-18 | University Of Rochester | Anticoagulant compositions and uses thereof |
| CN114306245A (zh) | 2020-09-29 | 2022-04-12 | 深圳市药欣生物科技有限公司 | 无定形固体分散体的药物组合物及其制备方法 |
| TW202321311A (zh) * | 2021-08-02 | 2023-06-01 | 日商諾伊爾免疫生物科技股份有限公司 | 與scFv等之連接子結合的抗體 |
| US11446286B1 (en) * | 2022-02-28 | 2022-09-20 | King Faisal University | Treatment of fungal infections using dabigatran etexilate |
| NL2036011B1 (en) | 2023-10-12 | 2025-04-30 | Synapse Res Institute | Molecules for reversing anti-coagulant activity of direct oral anticoagulants |
| WO2025149667A1 (en) | 2024-01-12 | 2025-07-17 | Pheon Therapeutics Ltd | Antibody drug conjugates and uses thereof |
Family Cites Families (31)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6087380A (en) | 1949-11-24 | 2000-07-11 | Boehringer Ingelheim Pharma Kg | Disubstituted bicyclic heterocycles, the preparations and the use thereof as pharmaceutical compositions |
| WO1988001649A1 (en) | 1986-09-02 | 1988-03-10 | Genex Corporation | Single polypeptide chain binding molecules |
| FI903489A0 (fi) | 1988-11-11 | 1990-07-10 | Medical Res Council | Ligander med en enda sektion, receptorer innehaollande naemnda ligander, foerfaranden foer deras framstaellning samt anvaendning av liganderna och receptorerna. |
| US5530101A (en) * | 1988-12-28 | 1996-06-25 | Protein Design Labs, Inc. | Humanized immunoglobulins |
| US5427908A (en) | 1990-05-01 | 1995-06-27 | Affymax Technologies N.V. | Recombinant library screening methods |
| JP3490437B2 (ja) * | 1992-01-23 | 2004-01-26 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフトング | 単量体および二量体抗体フラグメント融合タンパク質 |
| DE4203965A1 (de) | 1992-02-11 | 1993-08-12 | Max Planck Gesellschaft | Antidot fuer hirudin und synthetische thrombininhibitoren |
| EP1498427B1 (en) | 1992-08-21 | 2009-12-16 | Vrije Universiteit Brussel | Immunoglobulins devoid of light chains |
| DK0672142T3 (da) | 1992-12-04 | 2001-06-18 | Medical Res Council | Multivalente og multispecifikke bindingsproteiner samt fremstilling og anvendelse af disse |
| ATE183513T1 (de) | 1993-06-03 | 1999-09-15 | Therapeutic Antibodies Inc | Herstellung von antikörperfragmenten |
| AT404357B (de) | 1995-06-13 | 1998-11-25 | Immuno Ag | Prothrombin-derivate |
| DE19605126A1 (de) | 1996-02-12 | 1997-08-14 | Basf Ag | Thrombinmuteine als Antidot für Thrombininhibitoren |
| US6200955B1 (en) | 1996-06-11 | 2001-03-13 | Commonwealth Biotechnologies, Inc. | Heparin binding peptides |
| GB9625640D0 (en) | 1996-12-10 | 1997-01-29 | Celltech Therapeutics Ltd | Biological products |
| PE121699A1 (es) * | 1997-02-18 | 1999-12-08 | Boehringer Ingelheim Pharma | Heterociclos biciclicos disustituidos como inhibidores de la trombina |
| JP2002505574A (ja) | 1997-04-30 | 2002-02-19 | エンゾン,インコーポレイテッド | ポリアルキレンオキシド修飾された単鎖ポリペプチド |
| DE19729544A1 (de) * | 1997-07-10 | 1999-01-14 | Basf Ag | Ancrod spezifische monoklonale Antikörper, Antikörperfragmente, deren Mischung oder Derivate und deren Verwendung |
| US6440417B1 (en) | 1998-11-06 | 2002-08-27 | Conjuchem, Inc. | Antibodies to argatroban derivatives and their use in therapeutic and diagnostic treatments |
| US6624141B1 (en) | 1999-03-17 | 2003-09-23 | The Regents Of The University Of Michigan | Protamine fragment compositions and methods of use |
| JP2003530838A (ja) | 2000-04-12 | 2003-10-21 | ヒューマン ゲノム サイエンシズ インコーポレイテッド | アルブミン融合タンパク質 |
| CA2433877C (en) | 2001-01-17 | 2014-11-18 | Aptevo Research And Development Llc | Binding domain-immunoglobulin fusion proteins |
| US20040097547A1 (en) | 2001-04-16 | 2004-05-20 | Taveras Arthur G. | 3,4-Di-substituted cyclobutene-1,2-diones as CXC-chemokine receptor ligands |
| US20070031438A1 (en) * | 2001-12-10 | 2007-02-08 | Junghans Richard P | Antibodies as chimeric effector cell receptors against tumor antigens |
| AU2002351896A1 (en) | 2001-12-11 | 2003-06-23 | Ablynx N.V. | Method for displaying loops from immunoglobulin domains in different contexts |
| EP1517921B1 (en) | 2002-06-28 | 2006-06-07 | Domantis Limited | Dual specific ligands with increased serum half-life |
| WO2004041862A2 (en) | 2002-11-08 | 2004-05-21 | Ablynx N.V. | Single domain antibodies directed against tumour necrosis factor-alpha and uses therefor |
| SI1639011T1 (sl) | 2003-06-30 | 2009-04-30 | Domantis Ltd | Pegilirana protitelesa z enojno domeno (dAb) |
| BRPI0816837B1 (pt) * | 2007-09-28 | 2022-10-18 | Portola Pharmaceuticals, Inc | Composições farmacêuticas, polipeptídeo isolado de duas cadeias e uso de uma composição farmacêutica |
| AR070141A1 (es) * | 2008-01-23 | 2010-03-17 | Glenmark Pharmaceuticals Sa | Anticuerpos humanizados especificos para el factor von willebrand |
| AR077909A1 (es) | 2009-08-24 | 2011-09-28 | Boehringer Ingelheim Int | Intervenciones de urgencia de carbon vegetal activo con sobredosificacion con etexilato de dabigatran |
| AR079944A1 (es) | 2010-01-20 | 2012-02-29 | Boehringer Ingelheim Int | Anticuerpo neutralizante de la actividad de un anticoagulante |
-
2011
- 2011-01-19 AR ARP110100179A patent/AR079944A1/es active IP Right Grant
- 2011-01-19 TW TW100102006A patent/TWI513466B/zh active
- 2011-01-20 MY MYPI2012002840A patent/MY162323A/en unknown
- 2011-01-20 AP AP2012006242A patent/AP2012006242A0/xx unknown
- 2011-01-20 PT PT117034108T patent/PT2525812T/pt unknown
- 2011-01-20 UA UAA201209779A patent/UA110470C2/ru unknown
- 2011-01-20 PH PH1/2012/501493A patent/PH12012501493A1/en unknown
- 2011-01-20 SI SI201131156A patent/SI2525812T1/sl unknown
- 2011-01-20 NZ NZ599508A patent/NZ599508A/en unknown
- 2011-01-20 RS RS20170195A patent/RS55683B1/sr unknown
- 2011-01-20 UY UY0001033196A patent/UY33196A/es active IP Right Grant
- 2011-01-20 CA CA2787566A patent/CA2787566A1/en not_active Abandoned
- 2011-01-20 WO PCT/EP2011/050749 patent/WO2011089183A2/en not_active Ceased
- 2011-01-20 PE PE2012000997A patent/PE20121516A1/es active IP Right Grant
- 2011-01-20 PL PL11703410T patent/PL2525812T3/pl unknown
- 2011-01-20 GE GEAP201112836A patent/GEP20156341B/en unknown
- 2011-01-20 MA MA35080A patent/MA33936B1/fr unknown
- 2011-01-20 HU HUE11703410A patent/HUE032263T2/en unknown
- 2011-01-20 MX MX2012008360A patent/MX2012008360A/es active IP Right Grant
- 2011-01-20 HR HRP20170613TT patent/HRP20170613T1/hr unknown
- 2011-01-20 KR KR1020127019086A patent/KR101781787B1/ko active Active
- 2011-01-20 LT LTEP11703410.8T patent/LT2525812T/lt unknown
- 2011-01-20 ES ES11703410.8T patent/ES2614992T3/es active Active
- 2011-01-20 DK DK11703410.8T patent/DK2525812T3/en active
- 2011-01-20 EA EA201201016A patent/EA028371B1/ru active Protection Beyond IP Right Term
- 2011-01-20 JP JP2012549355A patent/JP5575923B2/ja active Active
- 2011-01-20 ME MEP-2017-29A patent/ME02602B/me unknown
- 2011-01-20 AU AU2011208719A patent/AU2011208719C1/en active Active
- 2011-01-20 BR BR112012018021-5A patent/BR112012018021B1/pt active IP Right Grant
- 2011-01-20 SG SG2012052445A patent/SG182552A1/en unknown
- 2011-01-20 CN CN201180006616.4A patent/CN102711813B/zh active Active
- 2011-01-20 EP EP16205771.5A patent/EP3195876A1/en not_active Withdrawn
- 2011-01-20 EP EP11703410.8A patent/EP2525812B1/en active Active
- 2011-01-20 US US13/010,403 patent/US8486398B2/en active Active
-
2012
- 2012-04-19 ZA ZA2012/02876A patent/ZA201202876B/en unknown
- 2012-04-25 IL IL219427A patent/IL219427B/en active IP Right Grant
- 2012-07-18 TN TNP2012000366A patent/TN2012000366A1/en unknown
- 2012-07-23 CO CO12123109A patent/CO6571889A2/es active IP Right Grant
- 2012-08-14 EC ECSP12012105 patent/ECSP12012105A/es unknown
-
2013
- 2013-06-13 US US13/916,994 patent/US9034822B2/en active Active
-
2014
- 2014-07-02 JP JP2014136811A patent/JP2014210794A/ja active Pending
-
2015
- 2015-04-13 US US14/684,576 patent/US20150210778A1/en not_active Abandoned
-
2017
- 2017-03-22 CY CY20171100361T patent/CY1118875T1/el unknown
- 2017-07-06 NL NL300882C patent/NL300882I2/nl unknown
- 2017-07-10 CY CY2017025C patent/CY2017025I2/el unknown
- 2017-07-10 FR FR17C1026C patent/FR17C1026I2/fr active Active
- 2017-07-10 LT LTPA2017021C patent/LTC2525812I2/lt unknown
- 2017-07-11 NO NO2017034C patent/NO2017034I1/no unknown
- 2017-07-12 LU LU00028C patent/LUC00028I2/fr unknown
- 2017-07-13 HU HUS1700030C patent/HUS1700030I1/hu unknown
-
2022
- 2022-08-12 NO NO2022036C patent/NO2022036I1/no unknown
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101781787B1 (ko) | 항응고제 해독제 | |
| AU2011208719B2 (en) | Anticoagulant antidotes | |
| KR20140009437A (ko) | 항응고제 해독제 | |
| US9499633B2 (en) | Dabigatran antidotes | |
| HK1173957B (en) | Anticoagulant antidotes | |
| HK1189532A (en) | Anticoagulant antidotes | |
| NZ613543B2 (en) | Anticoagulant antidotes | |
| AU2012234338A1 (en) | Anticoagulant antidotes | |
| OA16600A (en) | Anticoagulant antidotes. |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
Patent event date: 20120719 Patent event code: PA01051R01D Comment text: International Patent Application |
|
| PG1501 | Laying open of application | ||
| PA0201 | Request for examination |
Patent event code: PA02012R01D Patent event date: 20160114 Comment text: Request for Examination of Application |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
Comment text: Notification of reason for refusal Patent event date: 20170324 Patent event code: PE09021S01D |
|
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
Patent event code: PE07011S01D Comment text: Decision to Grant Registration Patent event date: 20170619 |
|
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment |
Comment text: Registration of Establishment Patent event date: 20170920 Patent event code: PR07011E01D |
|
| PR1002 | Payment of registration fee |
Payment date: 20170921 End annual number: 3 Start annual number: 1 |
|
| PG1601 | Publication of registration | ||
| PR1001 | Payment of annual fee |
Payment date: 20200911 Start annual number: 4 End annual number: 4 |
|
| PR1001 | Payment of annual fee |
Payment date: 20210910 Start annual number: 5 End annual number: 5 |
|
| PR1001 | Payment of annual fee |
Payment date: 20220913 Start annual number: 6 End annual number: 6 |
|
| PR1001 | Payment of annual fee |
Payment date: 20240913 Start annual number: 8 End annual number: 8 |