KR20110132369A - 눈물 임플란트 및 관련 방법 - Google Patents
눈물 임플란트 및 관련 방법 Download PDFInfo
- Publication number
- KR20110132369A KR20110132369A KR1020117021082A KR20117021082A KR20110132369A KR 20110132369 A KR20110132369 A KR 20110132369A KR 1020117021082 A KR1020117021082 A KR 1020117021082A KR 20117021082 A KR20117021082 A KR 20117021082A KR 20110132369 A KR20110132369 A KR 20110132369A
- Authority
- KR
- South Korea
- Prior art keywords
- implant
- tear
- fistula
- implant body
- distal
- Prior art date
Links
- ULEZWUGQDAQWPT-UHFFFAOYSA-N CCNC1CC1 Chemical compound CCNC1CC1 ULEZWUGQDAQWPT-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F9/00—Methods or devices for treatment of the eyes; Devices for putting-in contact lenses; Devices to correct squinting; Apparatus to guide the blind; Protective devices for the eyes, carried on the body or in the hand
- A61F9/0008—Introducing ophthalmic products into the ocular cavity or retaining products therein
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F9/00—Methods or devices for treatment of the eyes; Devices for putting-in contact lenses; Devices to correct squinting; Apparatus to guide the blind; Protective devices for the eyes, carried on the body or in the hand
- A61F9/007—Methods or devices for eye surgery
- A61F9/00772—Apparatus for restoration of tear ducts
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2/00—Filters implantable into blood vessels; Prostheses, i.e. artificial substitutes or replacements for parts of the body; Appliances for connecting them with the body; Devices providing patency to, or preventing collapsing of, tubular structures of the body, e.g. stents
- A61F2/02—Prostheses implantable into the body
- A61F2/14—Eye parts, e.g. lenses, corneal implants; Implanting instruments specially adapted therefor; Artificial eyes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F9/00—Methods or devices for treatment of the eyes; Devices for putting-in contact lenses; Devices to correct squinting; Apparatus to guide the blind; Protective devices for the eyes, carried on the body or in the hand
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0048—Eye, e.g. artificial tears
- A61K9/0051—Ocular inserts, ocular implants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/50—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
- A61L27/52—Hydrogels or hydrocolloids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/50—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
- A61L27/54—Biologically active materials, e.g. therapeutic substances
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2250/00—Special features of prostheses classified in groups A61F2/00 - A61F2/26 or A61F2/82 or A61F9/00 or A61F11/00 or subgroups thereof
- A61F2250/0003—Special features of prostheses classified in groups A61F2/00 - A61F2/26 or A61F2/82 or A61F9/00 or A61F11/00 or subgroups thereof having an inflatable pocket filled with fluid, e.g. liquid or gas
Landscapes
- Health & Medical Sciences (AREA)
- Ophthalmology & Optometry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Vascular Medicine (AREA)
- Heart & Thoracic Surgery (AREA)
- Medicinal Chemistry (AREA)
- Epidemiology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmacology & Pharmacy (AREA)
- Surgery (AREA)
- Plastic & Reconstructive Surgery (AREA)
- Transplantation (AREA)
- Oral & Maxillofacial Surgery (AREA)
- Dermatology (AREA)
- Molecular Biology (AREA)
- Dispersion Chemistry (AREA)
- Cardiology (AREA)
- Prostheses (AREA)
- Materials For Medical Uses (AREA)
- Medicinal Preparation (AREA)
Abstract
눈의 누점 및 누소관 내에 견고한 고정가능한 유지를 제공하는 눈물 임플란트 및 관련 방법이 개시된다. 상기 눈물 임플란트는 누점을 통하여 누소관 내로 적어도 부분적으로 삽입하도록 구성되는 임플란트 바디를 포함할 수 있다. 상기 임플란트 바디는 제1 및 제2 부분을 포함할 수 있으며, 세로 근위축을 정의하는 제1 부분의 근위 말단으로부터 세로 원위축을 정의하는 제1 부분의 원위 말단으로 연장할 수 있다. 상기 임플란트 바디는, 일체형 확장기를 이용하여 임플란트될 때, 근위축과 원위축 사이에 경사진 교차지점이 존재하도록 구성될 수 있다. 이러한 방식으로, 임플란트 바디의 적어도 일부가 소관 만곡에 또는 더 원위에 위치하는 누소관의 적어도 일부에 대하여 바이어싱됨으로써, 해부 구조를 이용하여 눈물 임플란트의 임플란트된 위치를 유지할 수 있다.
Description
관련 출원에 대한 참조
본원은 2009. 2. 23 자로 출원된 미국 가출원 제 61/154,693 호 (발명의 명칭 "눈물 임플란트 및 관련 방법"), 2009. 3. 2 자로 출원된 미국 가출원제 61/209,036호 (발명의 명칭 "눈물 임플란트 및 관련 방법"), 2009. 3. 9자로 출원된 미국 가출원 제 61/209,630호 (발명의 명칭 "눈물 임플란트 및 관련 방법"), 2009. 7. 27 자로 출원된 미국 가출원 제 61/271,862호 (발명의 명칭 "눈물 임플란트 및 관련 방법"), 및 2009. 10. 15 자로 출원된 미국 가출원 제 61/252,057호 (발명의 명칭 "눈물 임플란트 및 관련 방법")으로부터의 우선권의 이익을 주장하며, 상기 출원 모두 계류 중이며, 본원에 참조로 그 전체가 포함된다.
본원은 2008. 9. 5 자로 출원된 계류 중인 미국 출원 제 12/231,989 호 (발명의 명칭 "눈물 임플란트 및 관련 방법")와 관련된 것이다.
본 발명은 일반적으로 안과용 기구, 특히 안구 임플란트에 관한 것이다. 보다 구체적으로, 이에 제한되는 것은 아니지만, 본 발명은 눈물 임플란트, 이러한 임플란트의 제조 방법, 및 이러한 임플란트를 이용하여 안구, 호흡, 내이 또는 기타 질환 또는 장애 (예를 들어, 폐 또는 면역 장애)를 치료하는 방법에 관한 것이다.
건성 각결막염을 포함하는 안구 건조증은 치료를 필요로 할 수 있는 통상적인 안구 상태이다. 안구 건조증은 넓은 인구 집단이 경험하고 있으며, 나이 든 사람들에게 흔히 있다. 다양한 현재 치료 양식은 정상적인 루액의 증가, 눈물막 성분 생산의 증진, 및 눈으로부터 누소관 내로 및 이를 통한 눈물 흐름을 차단하는 것과 같은 눈물의 체류 시간을 증가시키는 방법을 포함하는, 안구 건조증에 기여하는 생리적 상태를 표적으로 하고 있다.
현재 많은 눈물 흐름 차단 기법은 본질적으로 비가역적임을 포함하여 결함을 가지고 있다. 예를 들어, 일부 눈물 흐름 차단 기법은 관련 누점 개구 셧을 스티치하거나 또는 전기 또는 레이저 소작을 이용하여 누점 개구를 밀봉함으로써 소관의 관을 폐쇄시키는 것을 수반한다. 이러한 절차는 눈물 흐름을 차단하여 안구 건조증을 치료하는 원하는 결과를 제공할 수 있으나, 이는 재건 수술없이 가역적이지 않다.
안구 건조증 증상 완화 외에도, 환자 및 의사는 안구, 호흡 및 내이 질환 또는 장애 관리에 있어서 눈, 비도 또는 내이에 충분한 약물 또는 기타 치료제 전달을 포함하는 다양한 문제에 직면한다. 안구 관리에 있어서, 예를 들어, 많은 현재 안구 약물 전달 시스템은 반복적인 수동적 투여를 필요로 하며, 종종 환자 순응도 결여 또는 불충분한 약물 농도가 눈에 도달함으로 인하여 비효과적이다. 예를 들어, 점안액이 눈 내에 주입될 때, 이는 종종 결막낭 (즉, 눈과 눈꺼풀 사이의 포켓)을 넘쳐 흘러 눈꺼풀 가장자리의 넘쳐 흐름과 볼에 흘림으로 인하여 상당 부분의 점안액의 손실을 야기한다. 안구 표면에 남아 있는 다량의 점안액이 적용 직후 누소관 내로 및 이를 통하여 씻겨질 수 있으며, 이에 따라 집중적으로 눈을 치료하기 전에 약물 농도가 희석된다. 더욱이, 국소 적용된 약물은 종종 적용 후 약 2 시간 동안 최고 안구 효과를 가지며, 그 후, 원하는 약물 치료 이점을 유지하기 위해서는 약물이 추가적으로 투여되어야 하나 종종 그러하지 않다.
안구 관리와 다른 분야에서, 호흡 관련 (예를 들어, 알레르기) 및 내이 질환 또는 장애의 조절은 종종 반복적인 제제(예를 들어, 약물 또는 기타 치료제)의 수동적 소화 또는 섭취를 필요로 하며, 환자 순응도 결여 또는 비-국소적 약물 전달로 인하여 비효과적일 수 있다.
본 발명자들은 눈에 눈물의 체류 시간 및 약물 또는 기타 치료제의 눈, 비도, 내이 또는 기타 신체 시스템으로의 전달을 증가시키기 위한 다양한 전망 있는 기법을 인식하여 왔다. 이러한 기법들은 제거가능하고 임의로 약물을 방출하는 눈물 임플란트를 누점을 통하여 누소관 내로 배치하는 것을 포함한다. 비루(nasolacrimal) 배출 시스템의 특징을 이용하는 눈물 임플란트를 디자인함으로써 (예를 들어, 누소관의 형상을 모방함으로써), 환자의 편안함 및 안구 해부 구조 내 임플란트의 유지를 충족시킬 수 있다. 이러한 방식으로, 본 발명의 눈물 임플란트는 본질적으로 비가역성, 및 저조한 환자 순응도, 폐기물, 시기적으로 부적절한 적용, 또는 비-국소적 전달과 같은 수동적 드롭 또는 소화에 근거한 약물 투여와 같은 현재 안구 건조증 완화와 관련된 결함 중 일부를 극복할 수 있다.
나아가, 본 발명자들은 눈물 임플란트가 다음 중 하나 이상에서 유용할 수 있음을 인지하였다: 용이하게 임플란트되고 누점 또는 누소관의 지나친 바이어싱 없이 제거될 수 있음, 임의로 특정 누점 또는 소관 직경으로 미리 크기가 정해지지 않고 임플란트시 누소관 내에 견고히 유지될 수 있음, 루액, 약물 또는 기타 제제를 비루 시스템 내로 흐를 수 있도록 함, 및, 약물 전달 시스템으로서 제조되고 이용될 때 하나 이상의 약물 또는 기타 치료제를 연장된 기간 동안 원하는 치료 수준으로 국소적인 서방출될 수 있도록 함.
이러한 인식의 견지에서, 질환 또는 장애를 치료하기 위한 눈물 임플란트가 개시된다. 보다 구체적으로, 눈물 임플란트, 이와 같은 임플란트의 제조 방법, 및 이러한 임플란트를 이용하여 안구, 호흡, 내이, 폐 또는 면역 질환 또는 장애를 치료하는 방법이 개시된다. 본원에 개시되는 다양한 눈물 임플란트의 안전성, 허용성, 편안함, 취급 용이성, 삽입 및 제거, 유지, 효능 및 투여를 평가하려는 임상적 시도는, 도 12, 도 13, 및 도 43a 내지 도 43c에 도시되는 눈물 임플란트와 같은 본 발명의 눈물 임플란트가 임상 시험 환자에게 효과적이며 잘 견딜 수 있음을 나타낸다. 또한, 도 13에 도시되는 유형의 눈물 임플란트와 같은 특정 눈물 임플란트의 유지율은 8주째에 약 60% 이상, 및 12주째에 약 47% 이상인 반면, 도 12, 및 도 43a 내지 도 43c에 도시되는 유형과 같은 눈물 임플란트의 유지율은 8주째에 약 75% 이상인 것으로 밝혀졌다.
본원의 요지를 더 잘 예시하기 위하여, 비제한적인 예시적 측면 및 구현예들이 제공된다:
1. 제1 및 제2 부분을 포함하고, 상기 제1 부분의 근위 말단으로부터 상기 제2 부분의 원위 말단으로 연장하는 임플란트 바디를 포함하는 누소관 내로 삽입가능한 눈물 임플란트로서; 상기 제1 부분의 근위 말단은 세로 근위축을 정의하고, 그 원주 주위로 비-등거리로 측면으로 돌출하는 유지 돌출부를 포함하고; 상기 제2 부분의 원위 말단은 세로 원위축을 정의하고; 및, 상기 임플란트 바디는, 누소관 내에 임플란트될 때, 소관 만곡에 또는 더 원위에 위치하는 누소관의 적어도 일부에 대하여 상기 임플란트 바디의 적어도 일부를 바이어싱하기 위한 상기 근위축과 상기 원위축 사이에 경사진 교차지점이 존재하도록 구성되는 것을 특징으로 하는 눈물 임플란트.
2. 제1 측면에 있어서, 상기 제1 부분의 유지 돌출부의 근위 말단은 그 원주 주위로 비-등 측면 거리로 외부로 측면 돌출되고, 상기 제1 부분의 원위 말단의 외부 직경을 향하여 가늘어지는 것을 특징으로 하는 눈물 임플란트.
3. 제2 측면에 있어서, 상기 제1 부분의 근위 말단으로부터 적어도 부분적으로 연장하고, 상기 임플란트 바디가 임플란트될 때 누점에 대하여 또는 이에 근접하여 배치되도록 구성되는 잡을 수 있는 돌출부를 포함하며; 상기 제1 부분의 유지 돌출부의 근위 말단은 상기 잡을 수 있는 돌출부의 둘레와 수적으로 대략 동일한 둘레를 포함하는 것을 특징으로 하는 눈물 임플란트.
4. 제2 또는 제3 측면에 있어서, 상기 제1 부분의 유지 돌출부의 근위 말단은 마주보는 제3 및 제4 면 상에 외부 직경으로부터 밖을 향하여 돌출됨이 없이 마주보는 제1 및 제2 면 상에서 마주보는 방향으로 외부로 돌출되는 것을 특징으로 하는 눈물 임플란트.
5. 제1-4 측면 중 하나에 있어서, 하나 이상의 치료제를 추가로 포함하는 눈물 임플란트.
6. 제5 측면에 있어서, 상기 하나 이상의 치료제는 상기 제1 부분 내에 적어도 부분적으로 배치되며 상기 하나 이상의 치료제의 서방출을 전달하도록 구성되는 약물 인서트 내에 제공되는 것을 특징으로 하는 눈물 임플란트.
7. 제1-6 측면 중 어느 하나의 눈물 임플란트, 및 안 질환 치료를 위하여 상기 눈물 임플란트를 사용하기 위한 설명서를 포함하는 키트.
8. 제1 및 제2 부분을 포함하고, 상기 제1 부분의 근위 말단으로부터 상기 제2 부분의 원위 말단으로 연장하는 임플란트 바디를 포함하는 누소관 내로 삽입가능한 눈물 임플란트로서; 상기 제1 부분의 근위 말단은 세로 근위축을 정의하고; 상기 제2 부분의 원위 말단은 세로 원위축을 정의하고, 그 원주 주위로 측면 돌출되는 유지 돌출부를 포함하며, 상기 유지 돌출부는 상기 유지 돌출부의 근위 말단 또는 상기 유지돌출부의 원위 말단 중 하나에서 외부를 향하는 측면 스텝을 포함하고; 및, 상기 임플란트 바디는, 누소관 내에 임플란트될 때, 소관 만곡에 또는 더 원위에 위치하는 누소관의 적어도 일부에 대하여 상기 임플란트 바디의 적어도 일부를 바이어싱하기 위한 상기 근위축과 상기 원위축 사이에 경사진 교차지점이 존재하도록 구성되는 것을 특징으로 하는 눈물 임플란트.
9. 제8 측면에 있어서, 상기 측면 스텝은 상기 제2 부분이 연장하는 방향에 수직 방향으로 외부로 측면 연장하며, 상기 측면 스텝은 약 0.14 mm 이상인 것을 특징으로 하는 눈물 임플란트.
10. 제8 또는 제9 측면에 있어서, 상기 측면 스텝은 상기 유지 돌출부의 근위 말단에 배치되며, 상기 유지 돌출부의 원위 말단에서 상기 제2 부분의 외부 직경을 향하여 가늘어지는 것을 특징으로 하는 눈물 임플란트.
11. 제10 측면에 있어서, 상기 유지 돌출부의 원위 말단은 상기 임플란트 바디의 누소관 내로의 삽입을 촉진시키기 위한 일체형 확장기를 포함하는 것을 특징으로 하는 눈물 임플란트.
12. 제8-11 측면 중 어느 하나에 있어서, 하나 이상의 치료제를 추가로 포함하는 눈물 임플란트.
13. 제12 측면에 있어서, 상기 하나 이상의 치료제는 상기 제1 부분 내에 적어도 부분적으로 배치되며 상기 하나 이상의 치료제의 서방출을 전달하도록 구성되는 약물 인서트 내에 제공되는 것을 특징으로 하는 눈물 임플란트.
14. 제13 측면에 있어서, 상기 약물 인서트는 상기 하나 이상의 치료제를 적어도 약 44 마이크로그램 포함하는 것을 특징으로 하는 눈물 임플란트.
15. 제13 측면에 있어서, 상기 약물 인서트는 상기 하나 이상의 치료제를 적어도 약 81 마이크로그램 포함하는 것을 특징으로 하는 눈물 임플란트.
16. 제8-15 측면 중 어느 하나의 눈물 임플란트, 및 안 질환 치료를 위하여 상기 눈물 임플란트를 사용하기 위한 설명서를 포함하는 키트.
17. 누소관의 수직 단면 내에 배치가능한 근위 말단부로부터 상기 누소관의 수평 단면 내에 배치가능한 원위 말단부로 비선형 연장하며, 그들 사이의 중간부를 가지는 임플란트 바디를 포함하는 누소관 내로 삽입하기 위한 눈물 임플란트로서; 상기 누소관 내에 임플란트될 때, 상기 중간부는 상기 근위 말단부를 향하여 제1 방향으로 부분적으로 연장하고, 상기 원위 말단부를 향하여 제2 방향으로 부분적으로 연장하고; 상기 중간부는 팽창가능한 물질을 저장하는 오목부를 포함하고, 상기 팽창가능한 물질은 상기 임플란트 바디가 임플란트될 때 누소관 팽대부를 향하여 상기 제2 방향과 실질적으로 반대인 제3 방향으로 부분적으로 팽창하도록 구성되는 것을 특징으로 하는 눈물 임플란트.
18. 제17 측면에 있어서, 상기 팽창가능한 물질은 하이드로겔을 포함하는 것을 특징으로 하는 눈물 임플란트.
19. 제17 또는 제18 측면에 있어서, 상기 팽창가능한 물질은, 상기 임플란트 바디가 임플란트될 때 상기 제2 방향에 대하여 측면으로 부분적으로 팽창하고, 상기 측면 팽창은 상기 누소관 벽에 대하여 상기 임플란트 바디의 하나 이상의 주변부가 밖을 향하도록 하는 것을 특징으로 하는 눈물 임플란트.
20. 제17-19 측면 중 어느 하나에 있어서, 상기 근위 말단부 또는 원위 말단부 중 적어도 하나가 인접하는 임플란트 바디 부분 보다 큰 크기의 단면을 가지는 적어도 하나의 중간-배치된 유지 돌출부를 포함하는 것을 특징으로 하는 눈물 임플란트.
21. 제17-20 측면 중 어느 하나에 있어서, 하나 이상의 치료제를 추가로 포함하는 눈물 임플란트.
22. 제21 측면에 있어서, 상기 하나 이상의 치료제는 상기 근위 말단부 내에 적어도 부분적으로 배치되며 상기 하나 이상의 치료제의 서방출을 전달하도록 구성되는 적어도 하나의 노출 표면을 포함하는 약물 인서트 내에 제공되는 것을 특징으로 하는 눈물 임플란트.
23. 제17-22 측면 중 어느 하나의 눈물 임플란트, 및 안 질환 치료를 위하여 상기 눈물 임플란트를 사용하기 위한 설명서를 포함하는 키트.
24. 제1 및 제2 부분을 포함하고, 상기 제1 부분의 근위 말단으로부터 상기 제2 부분의 원위 말단으로 연장하는 임플란트 바디를 포함하는 누소관 내로 삽입가능한 눈물 임플란트로서; 상기 제1 부분의 근위 말단은 세로 근위축을 정의하고, 그 원주 주위로 측면 돌출하는 유지 돌출부를 포함하고; 상기 제2 부분의 원위 말단은 세로 원위축을 정의하고; 상기 유지 돌출부는 그 근위 말단에서 밖을 향하는 측면 스텝을 포함하고 상기 제2 부분 내로 직접적으로 테이퍼링되고; 및, 상기 임플란트 바디는, 누소관 내로 임플란트될 때, 소관 만곡에 또는 더 원위에 위치하는 누소관의 적어도 일부에 대하여 상기 임플란트 바디의 적어도 일부를 바이어싱하기 위한, 상기 근위축과 원위축 사이에 경사진 교차 지점이 존재하도록 구성되는 것을 특징으로 하는 눈물 임플란트.
25. 제24 측면에 있어서, 상기 유지 돌출부의 길이는 약 0.96 mm 이상인 것을 특징으로 하는 눈물 임플란트.
26. 제24 또는 제25 측면에 있어서, 상기 유지 돌출부의 원위 말단은 상기 임플란트 바디의 누소관 내로의 삽입을 촉진시키기 위한 일체형 확장기를 포함하는 것을 특징으로 하는 눈물 임플란트.
27. 제24-26 측면 중 어느 하나에 있어서, 하나 이상의 치료제를 추가로 포함하는 눈물 임플란트.
28. 제27 측면에 있어서, 상기 하나 이상의 치료제는 상기 제1 부분 내에 적어도 부분적으로 배치되며 상기 하나 이상의 치료제의 서방출을 전달하도록 구성되는 약물 인서트 내에 제공되는 것을 특징으로 하는 눈물 임플란트.
29. 제28 측면에 있어서, 상기 약물 인서트는 상기 제1 부분의 제1 공동 내에 배치되며, 상기 제1 공동은 적어도 약 0.56 mm의 직경을 가지는 것을 특징으로 하는 눈물 임플란트.
30. 제28 또는 제29 측면에 있어서, 상기 약물 인서트는 상기 하나 이상의 치료제를 적어도 약 81 마이크로그램 포함하는 것을 특징으로 하는 눈물 임플란트.
31. 제24-28 측면 중 어느 하나의 눈물 임플란트, 및 안질환 치료를 위하여 상기 눈물 임플란트를 사용하기 위한 설명서를 포함하는 키트.
32. 누소관의 수직 단면 내에 배치가능한 근위 말단부로부터 상기 누소관의 수평 단면 내에 배치가능한 원위 말단부로 비선형 연장하며, 그들 사이의 중간부를 가지는 임플란트 바디를 포함하는 누소관 내로 삽입하기 위한 눈물 임플란트로서; 상기 중간부는 상기 근위 말단부를 향하여 제1 방향으로 부분적으로 연장하고, 상기 원위 말단부를 향하여 일반적으로 좁아지는 방식으로 제2 방향으로 부분적으로 연장하여, 상기 누소관 내에 임플란트될 때, 상기 임플란트 바디가 소관 만곡에 또는 이로부터 떨어져 위치하는 누소관의 적어도 일부에 대하여 상기 측면으로 직접적으로 바이어스되며; 상기 제2 방향 연장은 제1 방향 연장의 세로 길이의 4 배 미만의 세로 길이를 가지고; 상기 중간부는 상기 임플란트 바디가 임플란트될 때 누소관 팽대부를 향하여, 상기 제2 방향과 실질적으로 반대인 제3 방향으로 부분적으로 연장하며, 상기 제3 방향 연장은 편평한 선체(hull-like) 형상을 포함하는 것을 특징으로 하는 눈물 임플란트.
33. 제32 측면에 있어서, 상기 근위 말단부로부터 적어도 부분적으로 연장하는 잡을 수 있는 돌출부를 포함하고, 상기 잡을 수 있는 돌출부는 타원형을 포함하는 것을 특징으로 하는 눈물 임플란트.
34. 제32 또는 제33 측면에 있어서, 상기 편평 선체 형상은 약 0.4 내지 0.5 밀리미터의 길이 및 약 0.5 내지 0.6 밀리미터의 두께를 포함하는 것을 특징으로 하는 눈물 임플란트.
35. 제32-34 측면 중 어느 하나에 있어서, 치료제를 추가로 포함하는 눈물 임플란트.
36. 제35 측면에 있어서, 치료제를 포함하는 폴리머 매트릭스를 포함하고, 상기 근위 말단부의 공동 내에 배치되는, 상기 임플란트 바디로부터 구분되는 적어도 하나의 약물 인서트를 포함하는 눈물 임플란트.
37. 제35 또는 제36 측면에 있어서, 상기 치료제는 상기 임플란트 바디의 하나 이상의 부분 내로 통합되는 것을 특징으로 하는 눈물 임플란트.
38. 제32-37 측면 중 어느 하나의 눈물 임플란트, 및 안질환 치료를 위하여 상기 눈물 임플란트를 사용하기 위한 설명서를 포함하는 키트.
39. 제1 및 제2 부분을 포함하고, 세로 근위축을 정의하는 제1 부분의 근위 말단으로부터 세로 원위축을 정의하는 제2 부분의 원위 말단으로 연장하는 임플란트 - 상기 임플란트 바디는, 누소관 내로 임플란트될 때, 소관 만곡에 또는 더 원위에 떨어져 위치하는 누소관의 적어도 일부에 대하여 상기 임플란트 바디의 적어도 일부를 바이어싱하기 위한 상기 근위축과 원위축 사이에 경사진 교차 지점이 존재하도록 구성됨 - ; 및, 상기 제1 부분의 근위 말단으로부터 적어도 부분적으로 연장하며, 상기 제1 부분 내 공동에 오버행되는 내부로 연장하는 유지 립을 포함하는 잡을 수 있는 돌출부를 포함하는 누소관 내로 삽입가능한 눈물 임플란트.
40. 제39 측면에 있어서, 상기 눈물 임플란트는 상기 제1 부분의 공동 내에 배치되는, 상기 임플란트 바디로부터 구분되는 적어도 하나의 약물 인서트를 추가로 포함하고, 상기 약물 인서트는 치료제를 포함하는 것을 특징으로 하는 눈물 임플란트.
41. 제40 측면에 있어서, 상기 내부 연장 유지 립은 상기 공동 내에 완전히 배치될 때 상기 약물 인서트의 근위 표면에 오버행되어, 상기 인서트의 배치를 견고히 하는 것을 특징으로 하는 눈물 임플란트.
42. 제41 측면에 있어서, 상기 오버행은 상기 약물 인서트 내에 저장되는 약물의 방출 속도에 감지가능하게 영향을 미치지 않는 것을 특징으로 하는 눈물 임플란트.
43. 누소관 내로 삽입가능한 눈물 임플란트의 제조 방법으로서, 상기 방법은: 제1 바디 부분 내에 공동을 형성하고, 제2 바디 부분을 상기 제1 바디 부분의 세로 길이의 4배 미만의 세로 길이로 연장하고, 근위 말단 및 원위 말단을 각각 누소관 내로 임플란트될 때 일정 각도로 교차하는 세로 근위축 및 세로 원위축을 정의하도록 구성하여 상기 임플란트 바디가 소관 만곡에 또는 더 원위에 위치하는 누소관의 적어도 일부에 대하여 측면으로 직접적으로 바이어스되도록 구성하는 것을 포함하는, 제1 부분의 근위 말단으로부터 제2 부분의 원위 말단으로 연장하는 임플란트 바디를 형성하는 단계; 및, 약물 인서트의 노출 표면을 상기 제1 바디 부분의 근위 말단 위로 배치하는 것을 포함하는, 상기 제1 바디 부분의 공동 내에 상기 임플란트 바디로부터 구분되는 약물 인서트를 배치하는 단계를 포함하는 방법.
44. 누소관의 수직 단면 내에 배치가능한 근위 말단부로부터 누소관의 수평 단면 내에 배치가능한 원위 말단으로 연장하며, 그 사이에 중간부를 가지는 임플란트 바디 - 상기 중간부는 상기 근위 말단부를 향하여 제1 방향으로 부분적으로 연장하고 상기 원위 말단부를 향하여 제2 방향으로 부분적으로 연장하여, 누소관 내에 임플란트될 때, 상기 임플란트 바디가 소관 만곡에 또는 더 원위에 위치하는 누소관의 적어도 일부에 대하여 직접적으로 측면 바이어스되도록 함 - ; 및, 상기 원위 말단부에 또는 이에 근접하여 배치되는 유지 돌출부를 포함하는 누소관 내로 삽입하기 위한 눈물 임플란트.
45. 제44 측면에 있어서, 상기 제2 방향 연장은 상기 제1 방향 연장에 대하여 일반적으로 오목 형상을 포함하고; 일반적으로 오목 형상의 반경은 소관 만곡 반경보다 작은 것을 특징으로 하는 눈물 임플란트.
46. 적어도 하나의 공동을 포함하는 임플란트 바디; 상기 적어도 하나의 공동 내에 배치되며, 폴리머 매트릭스 및 치료제를 포함하는, 상기 임플란트 바디로부터 구분되는 약물 인서트를 포함하는 누소관 내로 삽입하기 위한 눈물 임플란트로서, 상기 임플란트 바디는 하나 이상의 바디 부분과 통합되는 치료제를 포함하는 것을 특징으로 하는 눈물 임플란트.
47. 제46 측면에 있어서, 상기 약물 인서트의 하나 이상의 표면을 둘러싸는 시스체를 추가로 포함하는 눈물 임플란트.
48. 제46 또는 제47 측면에 있어서, 외부 임플란트 바디 표면의 하나 이상의 부분에 적용되는 코팅을 추가로 포함하는 눈물 임플란트.
49. 제48 측면에 있어서, 제1 코팅 두께가 제1 임플란트 바디 표면부에 적용되고, 상기 제1 코팅 두께와 다른 제2 코팅 두께가 제2 임플란트 바디 표면부에 적용되는 것을 특징으로 하는 눈물 임플란트.
50. 제48 또는 제49 측면에 있어서, 상기 코팅은 패럴린, 세라믹 또는 은 중 적어도 하나를 포함하는 것을 특징으로 하는 눈물 임플란트.
51. 제46 측면에 있어서, 상기 약물 인서트는 제1 치료제 공급부를 포함하고, 상기 임플란트 바디는 제2 치료제 공급부를 포함하는 것을 특징으로 하는 눈물 임플란트.
본 발명의 눈물 임플란트 및 방법의 상기 및 기타 구현예들, 이점들, 및 측면들이 이하 상세한 설명에 부분적으로 기재될 것이다. 이러한 예시적 구현예 부분은 본 발명의 요지의 개요를 제공하고자 하는 것이다. 본 발명의 임플란트의 독점적이고 완전한 설명을 제공함을 의도하는 것이 아니다. 상세한 설명은 본 발명에 대한 추가적인 정보를 제공하기 위하여 포함된다.
본 발명에 따르면, 눈물 임플란트, 이러한 임플란트의 제조 방법, 및 이러한 임플란트를 이용하여 안구, 호흡, 내이 또는 기타 질환 또는 장애 (예를 들어, 폐 또는 면역 장애)를 치료하는 방법이 제공된다.
도면에서, 동일 도면 부호는 유사한 구성 요소를 나타내기 위하여 사용될 수 있다. 상이한 접미사를 이용하여 유사한 구성 성분의 상이한 예를 나타낼 수 있다. 도면은 일반적으로 제한적이 아니라 예시적으로 본원에 논의되는 다양한 구현예를 예시한다.
도 1 및 도 2는 눈물 임팔란트가 사용될 수 있는 적합한 환경을 제공하는 눈과 관련된 해부 조직 구조를 예시한다.
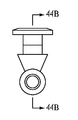
도 3a는 제1 및 제2 임플란트 바디 부분 사이에 경사진 교차 지점을 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예시에 대한 등축도이다.
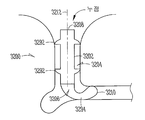
도 3b는 선 3B-3B와 같은 임플란트의 세로축에 평행한 선을 따라 취해진 눈물 임플란트, 및 임플란트를 수용하는 해부 조직 구조의 확대의 예의 단면도이다.
도 4는 일체형 확장기를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예에 대한 측면도이다.
도 5는 적어도 하나의 약물 또는 기타 치료제를 포함하는, 누점 및 누소관 해부 구조 내에 유지되는 눈물 임플란트의 예에 대한 개략도이다.
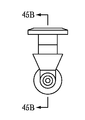
도 6a는 누소관 팽대부 내 사용가능한 부분을 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예에 대한 등축도이다.
도 6b는 선 6B-6B와 같은 임플란트의 세로축에 평행한 선을 따라 취해진 눈물 임플란트의 예에 대한 단면도이다.
도 7a는 환형의 잡을 수 있는 돌출부를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예에 대한 등축도이다.
도 7b는 선 7B-7B와 같은 임플란트의 세로축에 평행한 선을 따라 취해진 눈물 임플란트의 예에 대한 단면도이다.
도 8a는 누소관 팽대부 내 일회용 부분을 포함하고 삽입 촉진 오목부를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예 대한 등축도이다.
도 8b는 선 8B-8B와 같은 임플란트의 세로축에 평행한 선을 따라 취해진 눈물 임플란트의 예에 대한 단면도이다.
도 9는 삽입 촉진 오목부를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예에 대한 측면도이다.
도 10a는 누소관 팽대부 내 일회용 부분을 포함하는, 누점 및 누소관 해부 구조 내 유지되도록 구성되는 눈물 임플란트의 예에 대한 등축도이다.
도 10b는 선 10B-10B와 같은 임플란트의 세로축에 평행한 선을 따라 취해진 눈물 임플란트의 예에 대한 단면도이다.
도 11 내지 17은 각각 적어도 하나의 중간 배치되는 유지 돌출부를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 다양한 눈물 임플란트 예에 대한 측면 또는 등축도이다.
도 18 및 도 19는 각각 비-선형의 제2 임플란트 바디 부분을 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트를 예시한다.
도 20은 제2 바디 부분의 만곡을 허용하는 하나 이상의 물질 컷아웃을 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예이다.
도 21 및 도 22a, 도 22b는 각각 하나 이상의 측면 연장 암을 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예에 대한 측면도이다.
도 23은 하나 이상의 임플란트 바디 부분 주위에 배치되는 팽창가능한 유지 요소를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예에 대한 측면도이다.
도 24는 누점 및 누소관 해부 구조 내에 유지되는 눈물 임플란트의 예에 대한 개략도이다.
도 25a, 도 25b는 각각 일반적으로 오목 형상을 가지는 임플란트 바디 부분을 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예에 대한 등축도이다.
도 26은 일반적으로 볼록 형상을 가지는 임플란트 바디 부분을 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예에 대한 등축도이다.
도 27은 파동 형상을 가지는 임플란트 바디 부분을 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예에 대한 측면도이다.
도 28은 적어도 하나의 중간 배치되는 유지 돌출부를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예에 대한 측면도이다.
도 29 내지 도 32는 각각 유체 팽창가능한 유지 요소를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 다양한 예에 대한 측면도이다.
도 33은 팽창가능한 유지 요소를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예에 대한 측면도이다.
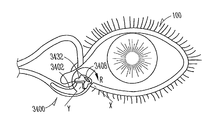
도 34a, 도 34b는 각각 개조된 잡을 수 있는 돌출부를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예에 대한 개략도이다.
도 35 내지 도 38은 각각의 근위 말단부가 잡을 수 있는 돌출부 또는 공극을 포함하는 다양한 눈물 임플란트 근위 말단부의 등축도이다.
도 39a, 도 39b는 약물 인서트 및 제거 촉진 필라멘트의 등축도이다.
도 40은 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 제조 방법을 예시한다.
도 41은 적어도 하나의 중간 배치되는 유지 돌출부를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예에 대한 측면도이다.
도 42a 내지 도 42d는 갑작스런 스텝을 포함할 수 있는 원위 제2 부분 상에 유지 메커니즘을 가지는 것과 같이, 적어도 하나의 중간-배치되는 유지 돌출부를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트를 예시한다.
도 43a 내지 도 43c는 원위 부분으로 가늘어지는 근위 부분에 대한 유지 메커니즘을 가지는 것과 같이, 적어도 하나의 중간 배치되는 유지 돌출부를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트를 예시한다.
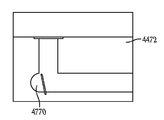
도 44a 내지 도 44c는 원위 부분의 근위 말단으로부터 연장하는 오목부를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트를 예시한다.
도 45a 내지 도 45c는 원위 부분의 근위 말단으로부터 연장하는 오목부를 포함하고 그 안에 팽창가능한 물질을 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트를 예시한다.
도 46, 도 47은 그 안에 팽창가능한 물질을 포함하는 원위 부분의 근위 말단으로부터 연장하는 오목부를 포함하는 눈물 임플란트의 실험 결과를 예시한다.
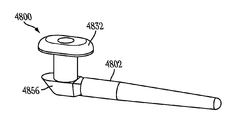
도 48a 내지 도 48e는 누소관 팽대부 내 이용가능한 강성 돌출부를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트를 예시한다.
도 49a 내지 도 49f는 임플란트 바디 공동 내에 구분되는 약물 인서트의 고정을 보조하도록 구성되는 유지 립을 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트를 예시한다.
도 50a 및 도 50b는 상승되는 약물 인서트를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트를 예시한다.
도 51 및 도 52는 근위 말단에 또는 이에 근접하여 유지 요소를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트를 예시한다.
도 53a 내지 도 53d는 구분되는 약물 인서트 또는 임플란트와 통합되는 약물 중 하나 또는 이들 모두를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트를 예시한다.
도 1 및 도 2는 눈물 임팔란트가 사용될 수 있는 적합한 환경을 제공하는 눈과 관련된 해부 조직 구조를 예시한다.
도 3a는 제1 및 제2 임플란트 바디 부분 사이에 경사진 교차 지점을 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예시에 대한 등축도이다.
도 3b는 선 3B-3B와 같은 임플란트의 세로축에 평행한 선을 따라 취해진 눈물 임플란트, 및 임플란트를 수용하는 해부 조직 구조의 확대의 예의 단면도이다.
도 4는 일체형 확장기를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예에 대한 측면도이다.
도 5는 적어도 하나의 약물 또는 기타 치료제를 포함하는, 누점 및 누소관 해부 구조 내에 유지되는 눈물 임플란트의 예에 대한 개략도이다.
도 6a는 누소관 팽대부 내 사용가능한 부분을 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예에 대한 등축도이다.
도 6b는 선 6B-6B와 같은 임플란트의 세로축에 평행한 선을 따라 취해진 눈물 임플란트의 예에 대한 단면도이다.
도 7a는 환형의 잡을 수 있는 돌출부를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예에 대한 등축도이다.
도 7b는 선 7B-7B와 같은 임플란트의 세로축에 평행한 선을 따라 취해진 눈물 임플란트의 예에 대한 단면도이다.
도 8a는 누소관 팽대부 내 일회용 부분을 포함하고 삽입 촉진 오목부를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예 대한 등축도이다.
도 8b는 선 8B-8B와 같은 임플란트의 세로축에 평행한 선을 따라 취해진 눈물 임플란트의 예에 대한 단면도이다.
도 9는 삽입 촉진 오목부를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예에 대한 측면도이다.
도 10a는 누소관 팽대부 내 일회용 부분을 포함하는, 누점 및 누소관 해부 구조 내 유지되도록 구성되는 눈물 임플란트의 예에 대한 등축도이다.
도 10b는 선 10B-10B와 같은 임플란트의 세로축에 평행한 선을 따라 취해진 눈물 임플란트의 예에 대한 단면도이다.
도 11 내지 17은 각각 적어도 하나의 중간 배치되는 유지 돌출부를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 다양한 눈물 임플란트 예에 대한 측면 또는 등축도이다.
도 18 및 도 19는 각각 비-선형의 제2 임플란트 바디 부분을 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트를 예시한다.
도 20은 제2 바디 부분의 만곡을 허용하는 하나 이상의 물질 컷아웃을 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예이다.
도 21 및 도 22a, 도 22b는 각각 하나 이상의 측면 연장 암을 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예에 대한 측면도이다.
도 23은 하나 이상의 임플란트 바디 부분 주위에 배치되는 팽창가능한 유지 요소를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예에 대한 측면도이다.
도 24는 누점 및 누소관 해부 구조 내에 유지되는 눈물 임플란트의 예에 대한 개략도이다.
도 25a, 도 25b는 각각 일반적으로 오목 형상을 가지는 임플란트 바디 부분을 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예에 대한 등축도이다.
도 26은 일반적으로 볼록 형상을 가지는 임플란트 바디 부분을 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예에 대한 등축도이다.
도 27은 파동 형상을 가지는 임플란트 바디 부분을 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예에 대한 측면도이다.
도 28은 적어도 하나의 중간 배치되는 유지 돌출부를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예에 대한 측면도이다.
도 29 내지 도 32는 각각 유체 팽창가능한 유지 요소를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 다양한 예에 대한 측면도이다.
도 33은 팽창가능한 유지 요소를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예에 대한 측면도이다.
도 34a, 도 34b는 각각 개조된 잡을 수 있는 돌출부를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예에 대한 개략도이다.
도 35 내지 도 38은 각각의 근위 말단부가 잡을 수 있는 돌출부 또는 공극을 포함하는 다양한 눈물 임플란트 근위 말단부의 등축도이다.
도 39a, 도 39b는 약물 인서트 및 제거 촉진 필라멘트의 등축도이다.
도 40은 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 제조 방법을 예시한다.
도 41은 적어도 하나의 중간 배치되는 유지 돌출부를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트의 예에 대한 측면도이다.
도 42a 내지 도 42d는 갑작스런 스텝을 포함할 수 있는 원위 제2 부분 상에 유지 메커니즘을 가지는 것과 같이, 적어도 하나의 중간-배치되는 유지 돌출부를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트를 예시한다.
도 43a 내지 도 43c는 원위 부분으로 가늘어지는 근위 부분에 대한 유지 메커니즘을 가지는 것과 같이, 적어도 하나의 중간 배치되는 유지 돌출부를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트를 예시한다.
도 44a 내지 도 44c는 원위 부분의 근위 말단으로부터 연장하는 오목부를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트를 예시한다.
도 45a 내지 도 45c는 원위 부분의 근위 말단으로부터 연장하는 오목부를 포함하고 그 안에 팽창가능한 물질을 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트를 예시한다.
도 46, 도 47은 그 안에 팽창가능한 물질을 포함하는 원위 부분의 근위 말단으로부터 연장하는 오목부를 포함하는 눈물 임플란트의 실험 결과를 예시한다.
도 48a 내지 도 48e는 누소관 팽대부 내 이용가능한 강성 돌출부를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트를 예시한다.
도 49a 내지 도 49f는 임플란트 바디 공동 내에 구분되는 약물 인서트의 고정을 보조하도록 구성되는 유지 립을 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트를 예시한다.
도 50a 및 도 50b는 상승되는 약물 인서트를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트를 예시한다.
도 51 및 도 52는 근위 말단에 또는 이에 근접하여 유지 요소를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트를 예시한다.
도 53a 내지 도 53d는 구분되는 약물 인서트 또는 임플란트와 통합되는 약물 중 하나 또는 이들 모두를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 눈물 임플란트를 예시한다.
본원 명세서에, 눈물 임플란트 및 누점 및 누소관 내에 견고한 고정가능한 유지를 제공하는 관련 방법이 기재된다. 상기 눈물 임플란트는 누점을 통하여 누소관 내로 적어도 부분적으로 삽입되도록 구성되는 임플란트 바디를 포함할 수 있다. 상기 임플란트 바디는 제1 및 제2 부분을 포함하며, 세로 근위축을 정의하는 제1 부분의 근위 말단으로부터 세로 원위축을 정의하는 제2 부분의 원위 말단으로 연장할 수 있다. 상기 임플란트 바디는 일체형 확장기를 이용하여 임플란트될 때, 예를 들어 적어도 45도 경사진 교차 지점이 근위축과 원위축 사이에 존재하도록 구성될 수 있다. 이러한 방식으로, 상기 임플란트 바디의 적어도 일부가 소관 만곡에 또는 더 원위에 위치하는 누소관의 적어도 일부에 대하여 바이어싱되어, 해부학적 구조를 이용하여 눈물 임플란트의 삽입된 위치를 유지할 수 있다.
다양한 실시예에서, 상기 눈물 임플란트는 임플란트 바디의 제1 부분 또는 제2 부분 중 적어도 하나 내에 배치되는 구분되는 약물 인서트 또는 통합된 약물 또는 기타 제제를 추가로 포함하여, 약물 또는 기타 치료제의 눈, 비도 또는 내이 시스템 중 하나 이상으로의 서방출을 제공할 수 있다.
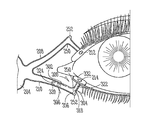
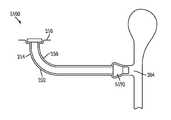
도 1 및 도 2는 눈(100)과 관련된 해부 조직 구조를 예시한다. 도시되는 특정 해부 조직 구조는 본원에 논의되는 다양한 눈물 임플란트 및 방법을 이용하는 치료에 적합할 수 있다. 눈(100)은 바깥쪽 공막(102), 중간 맥락막층(104) 및 내부 망막(106)의 3층을 가지는 벽을 포함하는 구형 구조이다. 상기 공막(102)은 내부층을 보호하는 강성 섬유 코팅을 포함한다. 이는 빛이 눈(100)으로 침입하도록 하는 각막(108)으로 통상적으로 알려진 정면의 투명한 영역을 제외하고 대부분 백색이다.
상기 맥락막층(104)은 공막(102) 내부에 위치하며 많은 혈관을 함유하고 색소침착된 홍채(110)로서 눈(100)의 정면에서 변형된다. 양면 볼록 렌즈(112)가 동공 바로 뒤에 위치한다. 상기 렌즈(112) 뒤의 체임버(114)는 유리체, 젤라틴성 물질로 충전되어 있다. 전안방 및 후안방(116)이 각각 상기 각막(108)과 홍채(110) 사이에 위치하며 안방수로 충전된다. 눈(100)의 후면에 빛을 감지하는 망막(106)이 있다.
상기 각막(108)은 이미지를 눈(100)의 후면에 전달하는 임의로 투명한 조직이다. 이는 영양소 및 산소가 각막(108)과 공막(102) 사이의 연결지점을 연결하는 혈관으로부터 뿐 아니라 루액 및 안방수로 담금을 통하여 공급되는 무혈관 조직을 포함한다. 상기 각막(108)은 약물의 눈(100) 내로의 침투를 위한 경로를 포함한다.
도 2를 참조로 하여, 분비계(230), 분산계 및 배설계를 포함하는, 눈물 배출 시스템을 포함하는 눈(100)과 관련된 기타 해부 조직 구조가 도시된다. 상기 분비계(230)는 눈 깜빡임 및 눈물 증발로 인한 온도 변화에 의하여 자극되는 분비자 및 원심 부교감 신경 공급부를 가지며 물리적 또는 감정적 자극에 반응하여 눈물을 분비하는 반사 분비자를 포함한다. 상기 분산계는 눈꺼풀(202), 및 눈 깜빡임에 의하여 안구 표면 위로 눈물을 분산시킴으로써 건조한 영역이 진전되는 것을 감소시키는, 개방된 눈의 눈꺼풀 가장자리 주위의 눈물 메니스커스를 포함한다.
상기 눈물 배출 시스템의 배설부는, 배출을 위하여, 누점, 누소관, 누낭(204) 및 누관(206)을 포함한다. 누관(206)으로부터, 눈물 및 기타 유동가능한 물질이 비루 시스템의 통로 내로 흘러나간다. 상기 누소관은 상부 누소관(208) 및 하부 누소관(210)을 포함하며, 이들 각각은 상부(212) 및 하부(214) 누점에서 종결된다. 상기 상부(212) 및 하부(214) 누점은 모양체 및 결막낭(218)에 인접하는 눈물 부분의 연결지점(216)에서 눈꺼풀 가장자리의 내측 말단에서 약간 상승된다. 상기 상부(212) 및 하부(214) 누점은 일반적으로 연결 조직 고리에 의하여 둘러싸이는 원형 또는 약간 타원형 개구이다. 누점(212,214) 각각은 그들 각각의 소관의 수직한 부분(220, 222)으로 이어진 후, 소관 만곡(250)에서 더 수평하게 전환되어 누낭(204)의 입구에서 서로 결합된다. 상기 소관(208,210)은 일반적으로 튜브 형상이고, 그들의 팽창을 허용하는 탄성 조직에 의하여 둘러싸인 중층편평상피에 의하여 가장자리를 이룬다. 도시되는 바와 같이, 누소관 팽대부(252)가 각각의 소관 만곡(250)의 외부 가장자리 가까이에 존재한다.
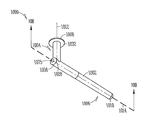
도 3a는 누점(212,214)을 통하여 누소관(208,210)(도 2) 내로 삽입될 수 있는 눈물 임플란트(300)를 예시한다. 상기 눈물 임플란트(300)의 누점(212,214)을 통한 누소관(208,210) 내로의 삽입은 다음 중 하나 이상을 허용한다: 이를 통한 눈물 흐름의 억제 또는 차단 (예를 들어, 안구 건조증 치료를 위함) 또는 약물 또는 기타 치료제의 눈 (예를 들어, 감염, 염증, 녹내장 또는 기타 안구 질환 또는 장애 치료를 위함), 비도 (예를 들어, 부비강 또는 알레르기 질환 치료를 위함) 또는 내이 시스템 (예를 들어, 어지러움 또는 편두통 치료를 위함)으로의 지속적인 전달.
본 실시예에 도시되는 바와 같이, 눈물 임플란트(300)는 제1(304) 및 제2(306) 부분을 포함하는 임플란트 바디(302)를 포함할 수 있고, 상기 제1 부분(304)의 근위 말단(308)으로부터 상기 제2 부분(306)의 원위 말단(310)으로 연장할 수 있다. 다양한 실시예에서, 상기 근위 말단(308)은 세로 근위축(312)을 정의하고, 상기 원위 말단(310)은 세로 원위축(314)을 정의할 수 있다. 상기 임플란트 바디(300)는 누점 및 누소관 내에 임플란트될 때, 소관 만곡(250)에 또는 더 원위에 위치하는 누소관(208,201)(도 2)의 적어도 일부에 대하여 상기 임플란트 바디(302)의 적어도 일부를 바이어싱하기 위한 상기 근위축(312)과 원위축(314) 사이에 적어도 45도 경사진 교차지점(316)이 존재하도록 구성될 수 있다. 일부 실시예에서, 상기 임플란트 바디(302)는 상기 경사진 교차 지점(316)이 약 45도 내지 약 135도 사이가 되도록 구성될 수 있다. 본 실시예에서, 상기 임플란트 바디(302)는 상기 경사진 교차 지점(316)이 약 90 도가 되도록 (즉, 근위축(312)과 원위축(314) 사이의 교차 지점(16)이 대략 수직이 되도록) 구성된다. 다양한 실시예에서, 상기 제1 부분(304)의 원위 말단(326)은 상기 제2 부분(306)의 근위 말단(328)에 또는 이에 근접하여 상기 제 2 부분(306)과 일체화될 수 있다.
특정 실시예에서, 상기 임플란트 바디(302)는 근위 말단(308)에 인접하여 배치되는 제1 공동(318) 또는 원위 말단(310)에 인접하여 배치되는 제2 공동(320) 중 하나 또는 둘 모두를 포함하는 각지게 배치되는 원통형 구조를 포함할 수 있다. 본 실시예에서, 상기 제1 공동(318)은 제1 부분(304)의 근위 말단(308)으로부터 내측으로 연장하고, 상기 제2 공동(320)은 제2 부분(306)의 원위 말단(310)으로부터 내측으로 연장한다. 임의로, 상기 임플란트 바디(302)의 하나 이상의 부분은 해부구조상 피팅 목적을 위하여 타원형 단면 형상을 포함할 수 있다.
제1 약물 방출 또는 기타 제제 방출 인서트 (예를 들어, 약물 코어)(322)가 제1 공동(318) 내에 배치되어 약물 또는 기타 치료제의 눈으로의 서방출을 제공하는 반면, 제2 약물 방출 또는 기타 제제 방출 인서트 (예를 들어, 약물 코어)(324)가 제2 공동(320) 내에 대안적으로 또는 함께 배치되어 약물 또는 기타 치료제의 예를 들어 비도 또는 내이 시스템으로의 서방출을 제공할 수 있다. 임플란트 바디 격막(330)이 제1 공동(318)과 제2 공동(320) 사이에 배치될 수 있으며, 상기 제1 약물 인서트(322)와 제2 약물 인서트(324) 사이에 물질 (예를 들어, 제제)의 소통을 억제 또는 방지하는데에 이용될 수 있다. 다양한 실시예에서, 제1 약물 방출 또는 기타 제제 방출 인서트(322) 또는 제2 약물 방출 또는 기타 제제 방출 인서트(324) 중 하나 또는 이들 모두는 2009. 5. 8 자 출원된 Butuner et al 공동 소유의 미국 특허 출원 제 12/463,279 호 (발명의 명칭 "녹내장 및 고안압증 치료를 위한 활성 제제의 서방형 전달") 및 2009. 9. 18 자 출원된 Utkhede 공동 소유의 미국 특허 출원 제 61/277,000 호 (발명의 명칭 "치료제의 안구 서방출을 위한 향상된 약물 코어")에 추가적으로 논의되는 바와 같이, 적어도 21 마이크로그램, 적어도 42 마이크로그램, 적어도 44 마이크로그램, 적어도 81 마이크로그램, 또는 적어도 95 마이크로그램의 약물 (예를 들어, 라타노프로스트)를 포함할 수 있으며, 상기 문헌들은 약물 또는 기타 제제 농도에 대한 기재를 포함하여 그 전체가 본원에 참조로 포함된다.
일부 실시예에서, 상기 임플란트 바디(302)는 약물 방출 또는 기타 제제 방출 인서트를 수용하기 위한 하나 이상의 공동 또는 기타 공극을 포함하지 않는다는 점에서 실질적으로 고체이다. 그 대신, 상기 임플란트 바디(302)는 하나 이상의 바디 부분을 통하여 통합되는 하나 이상의 약물 또는 기타 제제를 수용하도록 구성될 수 있다. 이러한 방식으로, 전체 임플란트 바디(302) 또는 그 일부가 약물 방출 또는 기타 제제 방출 인서트로서 작용할 수 있으며, 상기 임플란트 바디(302)의 부분들을 둘러싸는 불투과성 또는 실질적으로 불투과성인 커버 (예를 들어, 패릴렌 커버) 내에 미리 형성된 개구(들)을 이용하여 제제 방출을 유도할 수 있다. 다른 실시예에서, 투과성 커버 재료를 이용하여 약물 또는 기타 제제 방출을 허용할 수 있다.
일부 실시예에서, 약물 또는 기타 치료제 방출은 적어도 부분적으로 약물 인서트(322,324)의 노출된 비-시스 커버된 표면을 통하여 일어날 수 있다. 노출된 표면의 기하학을 조절함으로써, 소정의 약물 또는 제제 방출 속도를 달성할 수 있다. 예를 들어, 상기 노출된 표면을, 예를 들어 외래환자 의사 방문 사이에 급성 또는 만성 기준으로, 특정 기하학 또는 약물 또는 기타 치료제의 눈(100)으로의 방출 속도를 조절하기에 적합한 기타 기법을 이용하여 구성할 수 있다. 약물 인서트(322,324)로부터의 하나 이상의 약물 또는 기타 치료제의 효과적인 방출 속도에 대한 추가적인 기재는 DeuJuan et al 공동 소유의 미국 특허 출원 제 11/695,545 호 (발명의 명칭 "약물 치료법을 위한 비루 배출 시스템 임플란트")에서 찾을 수 있으며, 상기 문헌은 특정 방출 속도를 얻는 기재를 포함하여 그 전체가 본원에 참조로 포함된다.
도 3b에 도시되는 바와 같은 일부 실시예에서, 약물 인서트(322,324)의 노출된 표면은 제1 부분(304)의 근위 말단(308) 또는 제2 부분(306)의 원위 말단(310)과 각각 동일 평면이거나 약간 낮아, 약물 인서트가 상기 임플란트 바디(302)의 밖으로 돌출되지 않을 수 있다. 도 4에 도시되는 바와 같은 일부 실시예에서, 제1 약물 인서트(322)의 노출된 표면은 예를 들어 근위 말단(308) 위에 배치되어, 제1 약물 인서트(322)가 적어도 부분적으로 임플란트 바디(302) 밖으로 돌출될 수 있다.
상기 임플란트 바디(302)는 제1 임플란트 바디 부분(304)의 근위 말단(308)으로부터 또는 그 주위에 적어도 부분적으로 측면 연장하는 하나 이상의 돌출부와 같은 잡을 수 있는 또는 기타 돌출부(332)를 포함할 수 있다. 일부 실시예에서, 상기 잡을 수 있는 또는 기타 돌출부(332)는 눈물 임플란트(300)를 임플란트 위치 내로 삽입하거나 상기 눈물 임플란트(300)를 그 위치로부터 제거하는데 사용하기 위한 일 셋트의 날개를 포함할 수 있다. 임플란트 바디(302)의 비-선형 구조가 소관 만곡(250) 및 임의로 누소관 팽대부(252)(도 2)의 크기 또는 형상을 취함으로써 임플란트(300) 이동을 방지할 수 있으므로, 상기 날개 또는 기타 돌출부(332) 세트는이동을 고려하지 않고 구성될 수 있다. 일부 실시예에서, 상기 잡을 수 있는 또는 기타 돌출부(332)는, 예를 들어 상기 눈물 임플란트(300)가 누소관(208,210) 내에 완전히 통과하는 것을 억제 또는 방지하거나 또는 임플란트 사용자에게 예를 들어 임플란트가 완전히 삽입되었는지에 대한 촉각적 또는 가시적 피드백 정보를 제공하기 위하여, 누점 개구(212,214)에 대하여 또는 이에 인접하여 배치되도록 구성될 수 있다.
도 34a, 도 34b에 도시되고 이하 추가로 논의하는 바와 같이, 상기 잡을 수 있는 또는 기타 돌출부(332)는 임플란트될 때 눈(100)에 평행하거나 이로부터 멀어지는 방향으로 측면 연장할 수 있다. 이는 돌출 부분이 눈(100)을 향하여 연장하는 경우와 비교하여 눈(100)에 대한 자극을 감소시킬 수 있는 것으로 믿어진다. 또한, 상기 돌출부(332의 근위 말단(308)으로부터 측면 연장 방향은 도 3a-도 3b에 도시되는 바와 같이, 제1 임플란트 바디 부분(304)의 윈위 말단(326)에 대한 제2 임플란트 바디 부분(306)의 측면 연장 방향과 실질적으로 동일할 수 있다. 이는 또한 눈을 향한 돌출부 연장을 피하고, 임플란트 간병인 의사를 위하여 삽입 배향을 촉진시킬 수 있다. 상기 제1 약물 인서트(322)는, 예를 들어 제1 약물 또는 기타 치료제의 눈으로의 서방출을 제공하기 위하여, 상기 돌출부(332) 영역을 통하여 부분적으로 연장할 수 있다.
다양한 실시예에서, 상기 임플란트 바디(302)는 실리콘, 폴리우레탄 또는 기타 우레탄계 폴리머 또는 코폴리머, NuSil (예를 들어, 2% 6-4800을 가지는 NuSil 4840) 또는 비-생분해성, 부분적으로 생분해성 또는 생분해성 (즉, 신체 내 부식가능한) 아크릴산과 같은 탄성 물질을 이용하여 몰딩되어, 누소관(208,210)내로 임플란트될 때 근위(312) 및 원위(314) 축 사이에 경사진 교차 지점(16)이 형성되도록 임플란트 바디(302)가 구성되도록 할 수 있다. 예를 들어, 실리콘은 환자에게 편안하기에 충분히 연성이고 간병인 의사에 의한 삽입을 촉진시키기에 충분히 강성인 것으로 믿어진다. 다양한 실시예에서, 생체적합성 착색제(예를 들어, 녹색 착색제)를 임플란트 바디(302)의 탄성 재료와 혼합하여 환자 및 간병인이 보다 용이하게 임플란트를 보고 그것이 임플란트된 위치에 유지되는지를 확인할 수 있도록 한다. 일부 실시예에서, 임플란트 피드백을 위하여 또는 임플란트의 유형, 크기, 제제 또는 기타 특성을 나타내기 위하여, 생체적합성 착색제를 약물 인서트(322) 재료와 혼합할 수 있다.
일부 실시예에서, 상기 생분해성 탄성 재료는 폴리(비닐알콜)과 같은 가교결합 폴리머를 포함할 수 있다. 일부 실시예에서, 상기 임플란트 바디(302)는 실리콘/폴리우레탄 코폴리머를 포함할 수 있다. 상기 임플란트 바디(302)를 형성하는데에 사용될 수 있는 기타 코폴리머는 이에 제한되지 않으나, 실리콘/우레탄, 실리콘/폴리(에틸렌글리콜)(PEG), 및 실리콘/2히드록시에틸 메타크릴레이트 (HEMA)를 포함한다. 본원에 그 전체가 참조로 포함되는 2008. 9. 5 자로 출원된 Utkhede et al. 공동 소유의 미국 특허 출원 제 12/231,986 호 (대리인 사건 번호 2755.045US1, 발명의 명칭 "치료제의 서방출을 위한 약물 코어")에 논의되는 바와 같이, 우레탄계 폴리머 및 코폴리머 재료는 다양한 가공 방법 및 서로에 대한 만족스러운 결합을 허용한다.
도 3b는 도 3a의 선 3B-3B와 같은, 임플란트의 세로축에 평행한 선을 따라 취해진 눈물 임플란트(300)의 단면도를 예시한다. 도 3b에 도시되는 바와 같이, 눈물 임플란트(300)는 제1(304) 및 제2(306) 부분을 포함하는 임플란트 바디(302)를 포함할 수 있으며, 제1 부분(304)의 근위 말단(308)으로부터 제2 부분(306)의 원위 말단(310)으로 연장할 수 있다. 다양한 실시예에서, 상기 근위 말단(308)은 세로 근위축(312)을 정의하고, 상기 원위 말단(310)은 세로 원위축(314)을 정의할 수 있다. 상기 임플란트 바디(300)는, 임플란트될 때, 소관 만곡(250)(도 2)에 또는 더 원위에 위치하는 누소관(208,210)(도 2)의 적어도 일부에 대하여 임플란트 바디(302)의 적어도 일부를 바이어싱 하기 위한 근위축(312)과 원위축(314) 사이에 적어도 45 도 경사진 교차지점(316)이 존재하도록 구성될 수 있다. 본 실시예에서, 상기 임플란트 바디(300)는 경사진 교차 지점(316)이 대략 90 도가 되도록 구성된다.
다양한 실시예에서, 제1 부분(304)의 원위 말단(326)이 제2 부분(306)의 근위 말단(328)에서 또는 이에 인접하여 제2 부분(306)과 일체화될 수 있다. 일부 실시예에서, 상기 제2 부분(306)은 제1 부분(304)의 길이의 4 배 미만의 길이를 포함할 수 있다. 일 실시예에서, 제2 부분(306)은 약 10 밀리미터 미만의 길이를 포함하고, 도 3b에 도시되는 것과 유사한 구조를 가질 수 있다. 다른 실시예에서, 제2 부분(306)은 약 2 밀리미터 미만의 길이를 포함하고, 도 24에 도시되는 것과 유사한 구조를 가질 수 있다.
다양한 실시예에서, 제2 부분(306)은 눈물 임플란트(300)가 임플란트되는 동안 누점(212,214)(도 2) 또는 누소관(208,210) 중 하나 또는 이들 모두와 같은 해부 조직(325)을 충분한 직경으로 팽창시키기 위한 일체형 확장기(350)를 포함할 수 있다. 이러한 방식으로, 상기 눈물 임플란트(300)는 별도의 확대 도구를 통한 예비 팽창의 필요없이 다양한 크기의 안구 해부 구조 내로 삽입될 수 있다. 상기 확장기(350)는 누점(212,214) 및 누소관(208,210)의 내벽에 외상을 초래하지 않도록 형성될 수 있다. 일부 실시예에서, 임플란트 바디(302)의 외표면 상에 배치되거나 그 안에 함침되는 윤활 코팅을 사용하여 눈물 임플란트(300)의 해부 조직(352) 내로의 삽입을 추가로 보조할 수 있다. 일 실시예에서, 상기 윤활 코팅은 실리콘 윤활제를 포함할 수 있다.
상기 확장기(350)는 제2 부분(305)의 근위 말단(328)에 인접하는 위치로부터 제2 부분(306)의 근위 말단(310)으로 예를 들어 약 0.6 밀리미터에서 약 0.2 밀리미터 직경으로 좁아질 수 있다. 일부 실시예에서, 상기 확장기(350)의 외표면 경사는, 제2 부분(306)의 근위 말단(328)에 인접하는 위치로부터 제2 부분(306)의 원위 말단(310)까지 측정하여, 세로 원위축(314)에 대하여 약 1 도 내지 약 10 도 (예를 들어, 2 도, 3 도, 4 도, 또는 5 도)일 수 있다. 일부 실시예에서, 상기 확장기(350)의 경사는 세로 원위축(314)에 대하여 45 도 미만일 수 있다. 연성, 유연성의 일치하는 임플란트 바디를 (예를 들어, 누소관 해부구조에 일치) 가지기 위하여 삽입에 바람직한 임플란트 바디(320) 강도를 밸런싱함으로써, 주어진 임플란트 상황에 대하여 원하는 확장기(350) 경사를 결정할 수 있다. 일부 실시예에서, 확장기 팁(354)의 직경은 약 0.2 밀리미터 내지 약 0.5 밀리미터 사이일 수 있다.
특정 실시예에서, 제2 임플란트 바디 부분(306)의 근위 말단(328)은 임플란트될 때 누소관 팽대부(252)(도 2)의 적어도 일부에 대하여 바이어싱되도록 구성되는 유지 요소(356)를 포함할 수 있다. 본 실시예에서, 상기 유지 요소(356)는 제1(304) 및 제2(306) 임플란트 바디 부분 사이의 교차 지점으로부터, 예를 들어 확장기(350)의 연장과 반대 방향으로, 근위로 돌출된다. 팽대부(252) 내에 존재하고 임플란트될 때, 상기 유지 요소(356)는 누점 개구(212,214)에 대하여 잡을 수 있는 또는 기타 돌출부(332)의 배치를 확고히 하는 것을 보조할 수 있다.
특정 실시예에서, 상기 임플란트 바디(302)는 근위 말단(308)에 인접하여 배치되는 제1 공동(318)을 포함한다. 이러한 실시예에서, 상기 제1 공동(318)은 근위 말단(308)으로부터 약 2 밀리미터 이하로 내측 연장하고, 제1 약물 방출 또는 기타 제제 방출 약물 인서트(322)를 수용하여 약물 또는 기타 제제의 눈으로의 서방출을 제공한다. 일부 실시예에서, 상기 약물 인서트(322)는 매트릭스(362) 내에 분포될 수 있는 복수의 치료제 내포물(360)을 포함할 수 있다. 일부 실시예에서, 상기 내포물(360)은 농축된 형태의 (예를 들어, 결정형) 치료제를 포함할 수 있다. 일부 실시예에서, 상기 매트릭스(362)는 실리콘 매트릭스 등을 포함할 수 있으며, 상기 매트릭스 내 내포물(360)의 분포는 실질적으로 균질하거나 비-균질할 수 있다. 일부 실시예에서, 상기 제제 내포물(360)은 라타노프로스트 오일과 같은 오일 액적을 포함할 수 있다. 또 다른 실시예에서, 상기 제제 내포물(360)은 결정형 비마토프로스트 입자와 같은 고체 입자를 포함할 수 있다. 일부 실시예에서, 상기 약물 인서트(322)는 눈 또는 주변 조직 내로 전달할 수 있는 치료제 내포물을 포함하는 우레탄계 (예를 들어, 폴리우레탄) 폴리머 또는 코폴리머를 포함한다. 상기 내포물은 다양한 크기 및 형태일 수 있다. 예를 들어, 상기 내포물은 약 1 마이크로미터 내지 약 100 마이크로미터의 크기를 가지는 미립자를 포함할 수 있다. 약물 방출 또는 기타 제제 방출 약물 인서트에 대한 추가적인 논의는 2008. 9. 5 자로 출원된 Utkhede et al. 공동 소유의 미국 특허 출원 제 12/231,986 호 (대리인 사건 번호 제 2755.045US1호, 발명의 명칭 "치료제의 서방출을 위한 약물 코어")에서 찾을 수 있으며, 상기 문헌은 본원에 그 전체가 참조로 포함된다.
다양한 실시예에서, 상기 약물 인서트(322)는 상기 인서트의 적어도 일부 위에 배치되어 적어도 하나의 인서트 노출 표면(368)을 정의하는 시스체(366)을 포함할 수 있다. 상기 노출 표면(368)은 임플란트 바디(302)의 근위 말단(308)에 또는 이에 인접하여 위치됨으로써, 예를 들어, 눈물 임플란트(300)가 누점(212,214)을 통하여 누소관(208,210) 내로 임플란트될 때, 눈물 또는 눈물막 유체와의 직접적인 접촉 및 지속되는 기간에 걸쳐 약물 인서트(322)로부터 약물 또는 기타 치료제의 방출을 허용할 수 있다.
도 4는 눈물 임플란트(400)의 임플란트 바디(402) 제2 부분(406)의 다른 일체형 확장기(450)의 측면도를 예시한다. 본 실시예에서, 확장기(450)는 제2 부분(406)의 원위 말단(410)에 인접하여 갑작스럽게 좁아진다. 도시되는 바와 같이, 임플란트 바디 제1 부분(404)은 근위 말단(408)에 인접하여 배치되는 제1 공동(418)을 포함할 수 있다. 본 실시에에서, 상기 제1 공동(418)은 상기 근위 말단(408)으로부터 내측 연장하고, 제1 약물 방출 또는 기타 제제 방출 약물 인서트(422)를 수용하여 약물 또는 기타 치료제의 예를 들어 눈으로의 서방출을 제공한다. 일부 실시예에서, 상기 약물 또는 기타 치료제는 약물 인서트(422)의 노출된 비-시스 커버된 표면(468)을 통하여 눈으로 방출될 수 있다. 이러한 실시예에서, 상기 약물 인서트(422)의 노출 표면(468)은 근위 말단(408) 위에 배치되어, 약물 인서트(422)가 임플란트 바디(402) 밖으로 적어도 부분적으로 돌출된다.
다양한 실시예에서, 임플란트 바디(402)의 외표면(482)이 형성되거나, 또는 일반적으로 평활하게 표면 처리되어 박테리아가 눈물 임플란트(400)에 부착되고 인큐베이션되는 것을 억제할 수 있다. 상기 일반적으로 평활한 외표면(482)은 또한 임플란트 중에 누점(212,214)(도 2) 또는 누소관(208,201)(도 2)과 같은 수용 해부 조직의 내벽에의 손상을 방지할 수 있다. 본원에 그 전체가 참조로 포함되는 2008. 9. 5 자로 출원된 Rapacki et al. 공동 소유의 미국 특허 출원 제 12/283,002 호 (대리인 사건 번호 제 2755.035US1, 발명의 명칭 "임플란트의 표면 처리 및 관련 방법")에 추가로 논의되는 바와 같이, 임플란트 바디(402)의 외표면(482)은 연마 공정을 통하여 일반적으로 평활하게 표면 처리될 수 있다. 상기 연마 공정은 상기 바디(420)가 확장되고 팽창된 상태인 진행 중인 기간 동안 몰딩된 임플란트 바디(402)를 연마 매질과 접촉시키는 것을 포함한다. 이는 상기 임플란트 바디(402)의 하나 이상의 표면 또는 가장자리를 평활하게 할 수 있다. 다양한 실시예에서, 상기 연마 매질은 약 3 밀리미터 이상의 직경의 적어도 일부 과립을 포함할 수 있다.
다양한 실시예에서, 항미생물 코팅(484)을 외표면(482)의 적어도 일부 위에 배치하거나 그 안에 함침시켜 임플란트 바디(420) 상에 박테리아 성장을 추가로 방지할 수 있다. 일부 실시예에서, 상기 항미생물 코팅(484)은 2-브로모-2-니트로프로판-1,3-디올, 5-브로모-5-니트로-1,3-디옥산, 7-에틸 비시클로옥사졸리딘, 벤즈알코늄 클로라이드, 벤즈에토늄 클로라이드, 벤조산, 벤질 알콜, 붕산, 브로노폴, 세틸피리디늄 클로라이드, 클로르헥시딘 디글루코네이트, 클로로아세트아미드, 클로로부탄올, 클로로메틸 이소티아졸리논 및 메틸 이소티아졸린, 디메톡산, 디메틸 옥사졸리딘, 디메틸 히드록시메틸 피라졸, 클로르옥실레놀, 디하이드로아세트산, 디아졸리디닐 우레아, 디클로로벤질 알콜, DMDM 히단토인, 에틸알콜, 포름알데히드, 글루타르알데히드, 헥사클로로펜, 헥세티딘, 헥사메틸렌트라민, 이미다졸리디닐 우레아, 요오도프로피닐 부틸카르바메이트, 이소티아졸리논, 메텐암모늄 클로라이드, 메틸디브로모 글루타로니트릴, MDM 히단토인, 미노시클린, 오르토 페닐페놀, p-클로로-m-크레졸, 파라벤 (부틸파라벤, 에틸파라벤, 메틸파라벤), 페네틸 알콜, 페녹시에탄올, 피록탄 올라민, 폴리아미노프로필 바이구아나이드, 폴리메톡시 바이시클릭 옥사졸리딘, 폴리옥시메틸렌, 폴리쿼터늄-42, 포타슘 벤조에이트, 포타슘 소르베이트, 프로피온산, 쿼터늄-15, 리팜핀, 살리실산, 셀레늄 디설파이드, 소듐 보레이트, 소듐 요오데이트, 소듐 히드록시메틸글리시네이트, 소듐 프로피오네이트, 소듐 피리티온, 소르브산, 티메로살, 트리클로산, 트리클로카르반, 운데실렌산, 아연 페노설포네이트, 및 아연 피리티온으로부터 선택되는 제제를 포함할 수 있다. 일부 실시예에서, 상기 항미생물 코팅(484)은 실버 락테이트, 실버 포스페이트, 실버 시트레이트, 실버 아세테이트, 실버 벤조에이트, 실버 플로라이드, 실버 요오다이드, 실버 로데이트, 실버 니트레이트, 실버 설파디아진, 실버 팔미테이트, 또는 하나 이상의 그 혼합물로 이루어지는 군으로부터 선택되는 물질을 포함하 수 있다. 일부 실시예에서, 상기 항미생물 코팅(484)은 항생제 또는 방부제 중 적어도 하나를 포함할 수 있다. 예를 들어, 상기 항미생물 코팅(484)은 평균적으로 수 시간 내지 1일 지속되는 일시적인 마취제를 포함할 수 있다. 또 다른 실시예에서, 상기 항미생물 코팅(484)은 즉각적인 효과를 위한 볼루스와 같은 잠복 질병 치료에 이용되는 약물 또는 기타 치료제를 포함할 수 있다.
도 5는 하부 누점(214) 및 누소관(210) 내에 임플란트되는, 도 3에 도시되는 눈물 임플란트(300)와 같은 눈물 임플란트의 개략도를 예시한다. 일부 실시예에서, 눈물 임플란트(300)는 상부 누점(212) 및 소관(208) 내에 삽입된다. 위에 추가로 논의한 바와 같이, 눈물 임플란트(300)는 제1(304) 및 제2(306) 부분을 포함하는 임플란트 바디(302)를 포함할 수 있다. 다양한 실시예에서, 상기 임플란트 바디(302)는, 임플란트될 때, 임플란트 바디(302)의 적어도 일부가 소관 만곡(250)에 또는 더 원위에 위치하는 누소관(210)의 적어도 일부에 대하여 바이어스되어 임플란트(300)의 임플란트된 위치를 확고히 유지하도록 구성될 수 있다. 도시되는 바와 같이, 제1 부분(304)은 누점(214)을 통하여 누소관(210) 내로 삽입되고 누점 개구 및 누소관 팽대부(252) 사이에 배치되도록 구성되고, 제2 부분은 누점(214)을 통하여 소관(210) 내로 삽입되고 팽대부(252)와 누낭(204) 사이에 배치되도록 구성될 수 있다. 특정 실시예에서, 제2 부분(306)의 근위 말단으로부터 돌출되는 유지 요소(356)가 임플란트될 때 팽대부(252)의 적어도 일부에 대하여 및 그 안으로 바이어스 되도록 구성될 수 있다. 다양한 실시예에서, 상기 제1(304) 및 제2(306) 부분들은 원하는 대로 구부려지거나, 신장되거나 접혀져 과도하게 안구 해부 구조를 신장시키지 않고 적합한 해부학상 임플란트된 피트를 유지하도록 구성될 수 있다.
특정 실시예에서, 임플란트(300)를 누점(214) 및 소관(210) 내에 더욱 고정시키기 위하여 또는 임플란트 바디(302)를 그 크기 조정가능하도록 하기 위하여, 하이드로겔 또는 기타 유체 팽창성 물질을 임플란트 바디(302)의 외표면부에 배치할 수 있다 (예를 들어, 코팅). 상기 유체 팽창성 물질은 임플란트시 임플란트 바디(302)의 외표면 직경부를 효과적으로 팽창시킬 수 있다. 특정 실시예에서, 상기 임플란트 바디(302)의 외표면은 임플란트 바디(302) 주위로 유체 흐름을 허용하도록 세로 채널 또는 홈 또는 심지(wicking) 물질 코팅을 포함할 수 있다. 이러한 기법 중 하나 이상의 조합을 이용하여, 눈물 임플란트(300)는 그 안에 임플란트될 때 누소관(208,210)을 완전히 막거나 부분적으로 막도록 구성될 수 있다. 예를 들어, 임플란트 바디(302)의 제1(304) 또는 제2(306) 부분 중 하나 또는 이들 모두 내에 세로 채널 또는 홈의 이용은 감소된 부피를 허용하거나, 눈물 배출을 야기하여, 약물 인서트로부터 약물 또는 기타 치료제의 방출을 잠재적으로 촉진시킬 수 있다.
겸자 또는 다른 삽입 도구를 이용하여 눈물 임플란트(300)를 누점(212,214)을 통하여 누소관(208,210) 내로 임플란트할 수 있다. 일부 실시예에서, 본원에 그 전체가 참조로 포함되는 2008. 9. 5 자로 출원된 De Juan, et al. 공동 소유의 미국 특허 출원 제 12/231,984 호 (대리인 사건 번호 제 2755.018US1, 발명의 명칭 "눈물 임플란트 삽입 및 추출 도구")에 논의된 바와 같은 삽입 도구를 이용하여 눈물 임플란트(300)를 임플란트할 수 있다. 다양한 실시예에서, 존재한다면 잡을 수 있는 또는 기타 돌출부(332)가 누점 개구(212,214)에 대하여 배치될 수 있을 때까지 삽입기 도구의 조작에 의하여 임플란트 바디(302)의 제2 부분(306)을 누소관(208,210)의 깊이 내로 전진시킬 수 있다.
다양한 실시예에서, 누점 크기를 측정하고 적절한 크기의 임플란트(300) (예를 들어, 소, 중간 또는 대)를 선택한 후, 누점(212,214)을 임의로 삽입 전에 또는 삽입 중에 확장시킬 수 있다 (예를 들어, 임플란트의 일체형 확장기를 통하여). 임플란트(300)를 겸자 또는 다른 삽입 도구를 이용하여 제2 부분(306)에서 잡아 누점(212,214) 내로 수직 도입할 수 있다. 그 다음, 상기 임플란트(300)를 회전시켜 누소관(208,210)의 수평 부분 내로 언덕과 같은 유지 요소(356)까지 전진시킬 수 있다. 상기 겸자 또는 기타 삽입 도구는 임플란트(300)의 유지 요소(356) 부분을 잡고 이를 누점(212,214) 내로 회전시켜 상기 잡을 수 있는 또는 기타 캡형 돌출부(32)가 누점 상에 배치되도록 하는데에 추가적으로 이용될 수 있다.
눈물 임플란트(300)를 제거하는 것이 바람직할 때, 상기 돌출부(332)를 예를 들어 겸자로 잡고 누점 개구(212,214)로부터 가벼운 당김을 통하여 빼낼 수 있다. 임의로, 마취제 한 방울 또는 두 방울을 임플란트(300) 제거 전에 투여할 수 있다. 돌출부(332)의 최외곽 가장자리를 잡는 것은 상기 돌출부(332)의 찢김 또는 분리를 야기할 수 있으므로 그러지 않도록 주의하여야 한다.
특정 구현예에서, 임플란트 바디(302)는 근위 말단(308)에 인접하여 배치되는 제1 공동(318) 및 원위 말단(310)에 인접하여 배치되는 제2 공동(320) 중 하나 또는 이들 모두를 포함할 수 있다. 본 실시예에서, 상기 제1 공동(318)은 제1 부분(304)의 근위 말단(308)으로부터 내측 연장하고, 제2 공동(320)은 제2 부분(306)의 원위 말단(310)으로부터 내측 연장한다. 제1 약물 방출 또는 기타 제제 방출 약물 인서트322)를 제1 공동(318) 내에 배치하여 약물 또는 기타 치료제의 눈으로의 서방출을 제공할 수 있는 반면 (예를 들어, 감염, 염증, 녹내장 또는 기타 안구 질환 또는 장애 치료를 위하여), 제2 약물 방출 또는 기타 제제 방출 약물 인서트(324)를 제2 공동(320) 내에 배치하여 약물 또는 기타 치료제의 비도 (예를 들어, 부비강 또는 알레르기 질환 치료를 위하여) 또는 내이 시스템 (예를 들어, 어지러움 또는 편두통 치료를 위하여)으로의 서방출을 제공할 수 있다.
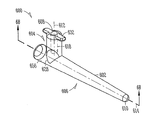
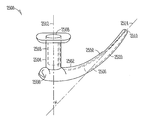
도 6a, 도 6b는 누점(212,214)을 통하여 누소관(208,210)(도 2) 내로 삽입가능한 다른 눈물 임플란트(600)를 예시한다. 본 실시예에서, 상기 눈물 임플란트(600)는 제1(604) 및 제2(606) 부분을 포함하는 임플란트 바디(602)를 포함할 수 있고, 상기 제1 부분(604)의 근위 말단(608)으로부터 상기 제2 부분(606)의 원위 말단(610)으로 연장할 수 있다. 상기 근위 말단(08)은 세로 근위축(612)을 정의하고, 상기 원위 말단(610)은 세로 원위축(614)을 정의할 수 있다. 상기 임플란트 바디(600)는, 임플란트될 때, 소관 만곡(250)(도 2)에 또는 더 원위에 위치하는 누소관(208,210)(도 2)의 적어도 일부에 대하여 상기 임플란트 바디의 적어도 일부를 바이어싱하기 위한 상기 근위축(612)과 원위축(614) 사이에 대략 90 도의 경사진 교차 지점이 존재하도록 구성될 수 있다.
본 실시예에서, 제2 임플란트 바디 부분(606)의 근위 말단(628)은 임플란트시 누소관 팽대부(252)(도 2)의 적어도 일부에 대하여 바이어싱되도록 구성되는 유지 요소(656)를 포함할 수 있다. 이러한 실시예에서, 상기 임플란트 바디(602)는 제1 임플란트 바디 부분(604)의 근위 말단(608)에 인접하여 배치되는, 제1 약물 방출 또는 기타 제제 방출 약물 인서트를 수용하도록 구성되는 제1 공동(618)을 포함한다. 또한, 이러한 실시예에서, 상기 임플란트 바디(602)는 예를 들어 약 1 밀리미터의 결합 길이를 가지며 근위 말단(308)으로부터 측면 연장하는 날개 세트와 같은 잡을 수 있는 또는 기타 돌출부(632)를 포함할 수 있다.
도 6b는 도 6a의 선 6B-6B와 같은 임플란트의 세로축에 평행한 선을 따라 취해진 눈물 임플란트(600)의 단면도를 예시한다. 도 6b에 도시되는 바와 같이, 제1 부분(604)의 원위 말단(626)은 제2 부분(606)의 근위 말단(628)에 또는 이에 인접하여 제2 부분(606)과 일체화될 수 있다. 다양한 실시예에서, 제2 부분(606)은, 근위 말단(608)으로부터 원위축(614)까지 측정되는 제1 부분(604)의 세로 길이의 4 배 미만의 크기를 가지는, 근위축(612)으로부터 원위말단(610)까지 측정되는 세로 길이를 포함할 수 있다. 일부 실시예에서, 상기 제1 부분은 약 1.54 밀리미터의 세로 길이를 포함할 수 있으며, 상기 제2 부분은 약 4.5 밀리미터 내지 약 5.42 밀리미터 사이의 세로 길이를 포함할 수 있다.
다양한 실시예에서, 제2 부분(606)은 눈물 임플란트(600)가 임플란트되는 동안 누점(212,214)(도 2) 또는 누소관(208,201) 중 하나 또는 이들 모두와 같은 해부 조직을 충분한 직경으로 확장시키기 위한 일체형 확장기(650)를 포함할 수 있다. 일부 실시예에서, 제2 부분(606)은 약 0.50 밀리미터 내지 약 0.75 밀리미터 사이의 근위 말단 직경으로부터 약 0.36 밀리미터의 확장기 팁(654)으로 가늘어진다.
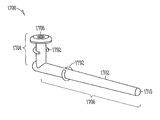
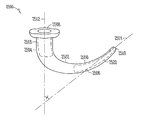
도 7a, 도 7b는 누점(212,214)을 통하여 누소관(208,210)(도 2) 내로 삽입가능한 다른 눈물 임플란트(700)를 예시한다. 본 실시예에서, 눈물 임플란트(700)는 제1(705) 및 제2(706) 부분을 포함하는 임플란트 바디(702)를 포함할 수 있고, 상기 제1 부분(704)의 근위 말단(708)으로부터 상기 제2 부분(706)의 원위 말단(710)으로 연장할 수 있다. 상기 근위 말단(708)은 세로 근위축(712)을 정의하고, 상기 원위 말단(710)은 세로 원위축(714)을 정의할 수 있다. 상기 임플란트 바디(700)는, 임플란트시, 소관 만곡(250)(도 2)에 또는 더 원위에 위치하는 누소관(208,210)(도 2)의 적어도 일부에 대하여 상기 임플란트 바디의 적어도 일부를 바이어싱하기 위한 근위축(712)과 원위축(714) 사이의 대략 90도 경사진 교차 지점이 존재하도록 구성될 수 있다. 도 7a에 도시되는 바와 같이, 상기 제1(704) 및 제2(706) 부분 사이에 평활한 전환 부분이 존재할 수 있다.
이러한 실시예에서, 상기 임플란트 바디(702)는 제1 임플란트 바디 부분(704)의 근위 말단(708)에 인접하여 배치되는, 제1 약물 방출 또는 기타 제제 방출 약물 인서트를 수용하도록 구성되는 제1 공동(718)을 포함한다. 또한, 상기 임플란트 바디(702)는 상기 근위 말단(708)으로부터 및 그 주위로 완전히 측면 연장하는 환상 돌출부와 같은, 잡을 수 있는 또는 기타 돌출부(732)를 포함할 수 있다. 일부 실시예에서, 상기 잡을 수 있는 또는 기타 돌출부(732)는 약 0.75 밀리미터의 트리밍된 폭을 가지며 근위 말단(708) 주위로 변화하는 양으로 연장하는 부분적으로 트리밍된 돌출부를 포함한다.
도 7b는 도 7a의 선 7B-7B과 같은 임플란트의 세로축에 평행한 선을 따라 취해진 눈물 임플란트(700)의 단면도를 예시한다. 도 7b에 도시되는 바와 같이, 제1 부분(704)의 원위 말단(726)은 제2 부분(706)의 근위 말단(728)에 또는 이에 인접하여 제2 부분(706)과 일체화될 수 있다. 다양한 실시예에서, 상기 제2 부분(706)은, 근위 말단(708)으로부터 원위축(714)까지 측정되는 제1 부분(704)의 세로 길이의 4배 미만의 크기를 가지는, 근위축(712)으로부터 원위 말단(710)까지 측정되는 세로 길이를 포함할 수 있다. 일부 실시예에서, 상기 제1 부분은 약 1.5 밀리미터의 세로 길이를 포함할 수 있으며, 상기 제2 부분은 약 5 밀리미터의 세로 길이를 포함할 수 있다.
다양한 실시예에서, 상기 제2 부분(706)은 눈물 임플란트(700)가 임플란트되는 동안 누점(212,214)(도 2) 또는 누소관(208,210) 중 하나 또는 이들 모두와 같은 해부 조직을 충분한 직경으로 확장시키기 위한 일체형 확장기(750)를 포함할 수 있다. 일부 실시예에서, 상기 제2 부분(706)은 약 0.46 밀리미터의 근위 말단으로부터 약 0.36 밀리미터의 확장기 팁(754) 직경으로 가늘어진다.
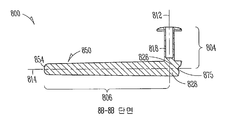
도 8a, 도 8b는 누점(212,214)을 통하여 누소관(208,210)(도 2) 내로 삽입가능한 다른 눈물 임플란트(800)를 예시한다. 본 실시예에서, 눈물 임플란트(800)는 제1(804) 및 제2(806) 부분을 포함하는 임플란트 바디(802)를 포함할 수 있으며, 상기 제1 부분(804)의 근위 말단(808)으로부터 상기 제2 부분(806)의 원위 말단(810)으로 연장할 수 있다. 상기 근위 말단(808)은 세로 근위축(812)을 정의하고, 상기 근위 말단(810)은 세로 근위축(814)을 정의할 수 있다. 상기 임플란트 바디(800)는 임플란트시, 소관 만곡(250)(도 2)에 또는 더 원위에 위치하는 누소관(208,210)(도 2)의 적어도 일부에 대하여 상기 임플란트 바디의 적어도 일부를 바이어싱하기 위한 근위축(812)과 원위축(814) 사이에 대략 90도 경사진 교차지점이 존재하도록 구성될 수 있다.
이러한 실시예에서, 상기 제2 임플란트 바디 부분(806)의 근위 말단(828)은 임플란트시 누소관 팽대부(252)(도 2)의 적어도 일부에 대하여 바이어스되도록 구성되는 유지 요소(856)를 포함할 수 있다. 상기 유지 요소(856)는 삽입 촉진 오목부(875) 또는 임플란트 삽입 또는 제거 중 하나 또는 모두를 보조하기 위한 기타 잡는 수단을 포함할 수 있다. 이러한 실시예에서, 상기 임플란트 바디(802)는 상기 제1 임플란트 바디 부분(804)의 근위 말단(808)에 인접하여 배치되는, 제1 약물 방출 또는 기타 제제 방출 약물 인서트를 수용하도록 구성되는 제1 공동(818)을 포함한다. 또한, 이러한 실시예에서, 상기 임플란트 바디(802)는 근위 말단(808)으로부터 및 그 주위로 완전히 측면 연장하는 환상 돌출부와 같은 잡을 수 있는 또는 기타 돌출부(832)를 포함할 수 있다. 일부 구현예에서, 상기 잡을 수 있는 또는 기타 돌출부(832)는 상기 근위 말단(808) 주위로 변화하는 양으로 연장하는 부분적으로 잘려진 돌출부를 포함한다.
도 8b는 도 8a의 선 8B-8B와 같은 임플란트의 세로축에 평행한 선을 따라 취해진 눈물 임플란트(800)의 단면도를 예시한다. 도 8b에 도시되는 바와 같이, 제1 부분(804)의 원위 말단(826)은 제2 부분(806)의 근위 말단(828)에서 또는 이에 인접하여 제2 부분(806)과 일체화될 수 있다. 다양한 실시예에서, 제2 부분(806)은 근위 말단(808)으로부터 원위축(814)까지 측정되는 제1 부분(804)의 세로 길이의 4배 미만의 크기를 가지는, 근위축(812)으로부터 원위 말단(810)까지 측정되는 세로 길이를 포함할 수 있다. 일부 실시예에서, 상기 제1 부분은 약 1.725 밀리미터 내지 약 1.77 밀리미터의 세로 길이를 포함하고, 제2 부분은 약 4.77 밀리미터 내지 약 5 밀리미터의 세로 길이를 포함할 수 있다.
다양한 실시예에서, 제2 부분(806)은 눈물 임플란트(800)가 임플란트되는 동안, 누점(212,214)(도 2) 또는 누소관(208,210) 중 하나 또는 이들 모두와 같은 해부 조직을 충분한 직경으로 확장시키기 위한 일체형 확장기(850)를 포함할 수 있다. 일부 실시예에서, 상기 제2 부분(806)은 약 0.46 밀리미터의 근위 말단(828) 직경으로부터 약 0.36 밀리미터의 확장기 팁(854) 직경으로 가늘어진다.
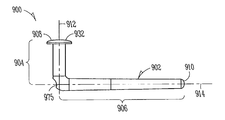
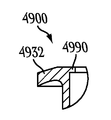
도 9는 누점(212,214)을 통하여 누소관(208,210)(도 2) 내로 삽입가능한 다른 눈물 임플란트(900)를 예시한다. 본 실시예에서, 상기 눈물 임플란트(900)는 제1(904) 및 제2(906) 부분을 포함하는 임플란트 바디(902)를 포함할 수 있으며, 제1 부분(904)의 근위 말단(908)으로부터 제2 부분(906)의 원위 말단(910)으로 연장될 수 있다. 상기 근위 말단(908)은 세로 근위축(912)을 정의하고, 상기 원위 말단(910)은 세로 원위축(914)을 정의할 수 있다. 상기 임플란트 바디(900)는, 임플란트시, 소관 만곡(250)(도 2)에 또는 더 원위에 위치하는 누소관(208,210)(도 2)의 적어도 일부에 대하여 상기 임플란트 바디의 적어도 일부를 바이어싱하기 위한 근위축(912)과 원위축(914) 사이의 대략 90도 경사진 부분이 존재하도록 구성될 수 있다.
도시되는 바와 같이, 제1(904) 및 제2(906) 부분 사이에 평활한 전이 부분이 존재할 수 있다. 이러한 실시예에서, 상기 평활한 전이 부분은 삽입 촉진 오목부(975) 또는 임플란트 삽입 또는 제거 중 하나 또는 이들 모두를 보조하기 위한 기타 잡는 수단을 포함할 수 있다. 또한, 이러한 실시예에서, 상기 임플란트 바디(902)는 근위 말단(908)으로부터 그 주위로 완전히 측면 연장하는 환상 돌출부와 같은, 잡을 수 있는 또는 기타 돌출부(932)를 포함할 수 있다. 일부 실시예에서, 상기 잡을 수 있는 또는 기타 돌출부(932)는 상기 근위 말단(908) 주위로 변화하는 양으로 연장하는 부분적으로 트리밍된 돌출부를 포함한다.
도 10a, 도 10b는 누점(212,214)을 통하여 누소관(208,210)(도 2) 내로 삽입가능한 다른 눈물 임플란트(1000)를 예시한다. 본 실시예에서, 상기 눈물 임플란트(1000)는 제1(1004) 및 제2(1006) 부분들을 포함하는 임플란트 바디(1002)를 포함할 수 있고, 상기 제1 부분(1004)의 근위 말단(1008)으로부터 상기 제2 부분(1006)의 원위 말단(1010)으로 연장할 수 있다. 상기 근위 말단(1008)은 세로 근위축(1012)을 정의하고 상기 원위 말단(1010)은 세로 원위축(1014)을 정의할 수 있다. 상기 임플란트 바디(1000)는 임플란트시, 소관 만곡(250)(도 2)에 또는 더 원위에 위치하는 누소관(208,210)(도 2)의 적어도 일부에 대하여 상기 임플란트 바디의 적어도 일부를 바이어싱하기 위한 근위축(1012)과 원위축(1014) 사이의 대략 90도 경사진 교차 지점이 존재하도록 구성될 수 있다.
본 실시예에서, 상기 제2 임플란트 바디 부분(1006)의 근위 말단(1028)은 임플란트시 누소관 팽대부(252)(도 2)의 적어도 일부에 대하여 바이어스되도록 구성되는 유지 요소(1056)를 포함할 수 있다. 상기 유지 요소(1056)는 삽입 촉진 오목부(1075) 또는 임플란트 삽입 또는 제거 중 하나 또는 이들 모두를 보조하기 위한 기타 잡는 수단을 포함할 수 있다. 이러한 실시예에서, 상기 임플란트 바디(1002)는 상기 제1 임플란트 바디 부분(1004)의 근위 말단(1008)에 인접하여 배치되는, 제1 약물 방출 또는 기타 제제 방출 약물 인서트를 수용하도록 구성되는 제1 공동(1018)을 포함한다. 또한, 이러한 실시예에서, 상기 임플란트 바디(1002)는 상기 근위 말단(1008)으로부터 그 주위로 완전히 측면 연장하는 약 1.3 밀리미터의 직경을 가지는 환상 돌출부와 같은, 잡을 수 있는 또는 기타 돌출부(1032)를 포함할 수 있다. 일부 실시예에서, 상기 잡을 수 있는 또는 기타 돌출부(1032)는 상기 근위 말단(1008) 주위로 변화하는 양으로 연장하는 부분적으로 트리밍된 돌출부를 포함한다.
도 10b는 도 10a의 선 10B-10B와 같은 임플란트의 세로축에 평행한 선을 따라 취해진 눈물 임플란트(1000)의 단면도를 예시한다. 도 10b에 도시되는 바와 같이, 제1 부분(1004)의 원위 말단(1026)은 제2 부분(1006)의 근위 말단(1028)에서 또는 그에 인접하여 제2 부분(1006)과 일체화될 수 있다. 다양한 실시예에서, 상기 제2 부분(1006)은 근위 말단(1008)으로부터 원위축(1014)까지 측정되는 제1 부분(1004)의 세로 길이의 4배 미만의 크기를 가지는, 근위축(1012)으로부터 원위 말단(1010)까지 측정되는 세로 길이를 포함할 수 있다. 일부 실시예에서, 상기 제1 부분은 약 1.5 밀리미터의 세로 길이를 포함하고, 상기 제2 부분은 약 5 밀리미터의 세로 길이를 포함할 수 있다.
다양한 실시예에서, 상기 제2 부분(1006)은 눈물 임플란트(1000)가 임플란트되는 동안 누점(212,214)(도 2) 또는 누소관(208,210) 중 하나 또는 이들 모두와 같은 해부 조직을 충분한 직경으로 확장시키기 위한 일체형 확장기를 포함할 수 있다. 일부 실시예에서, 상기 제2 부분(1006)은 약 0.46 밀리미터의 근위 말단(1028)으로부터 약 0.36 밀리미터의 확장기 팁(1054) 직경으로 가늘어진다.
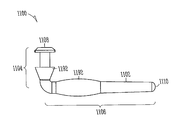
도 11 내지 도 17은 누점(212,214)을 통하여 누소관(208,210)(도 2) 내로 삽입가능한 다른 눈물 임플란트(1100,1200,1300,1400,1500,1600,1700)를 예시한다. 본 실시예에서, 각각의 눈물 임플란트(1100,1200,1300,1400,1500,1600,1700)는 제1(1104, 1204, 1304, 1404, 1504, 1604, 1704) 및 제2(1106, 1206, 1306, 1406, 1506, 1606, 1706) 부분들을 포함하는 임플란트 바디(1102, 1202, 1302, 1402, 1502, 1602, 1702)를 포함할 수 있고, 상기 제1 부분(1104, 1204, 1304, 1404, 1504, 1604, 1704)의 근위 말단(1108, 1208, 1308, 1408, 1508, 1608, 1708)으로부터 상기 제2 부분(1106, 1206, 1306, 1406, 1506, 1606, 1706)의 원위 말단(1110, 1210, 1310, 1410, 1510, 1610, 1710 )으로 연장할 수 있다. 각각의 임플란트 바디(1102, 1202, 1302, 1402, 1502, 1602, 1702)는 눈물 임플란트의 임플란트된 위치를 잠재적으로 더욱 확고히 하기 위하여 적어도 하나의 중간 배치되는 유지 돌출부(1192, 1292, 1392, 1492, 1592, 1692, 1792)를 포함할 수 있다. 상기 중간 배치되는 유지 돌출부(1192, 1292, 1392, 1492, 1592, 1692, 1792)는 상기 제1(1104, 1204, 1304, 1404, 1504, 1604, 1704) 또는 제2(1106, 1206, 1306, 1406, 1506, 1606, 1706) 임플란트 바디 부분들 중 하나 또는 이들 모두에 배치될 수 있으며, 환형, 반-환형, 컬럼형 또는 배럴형 돌출부의 형태를 취할 수 있다. 상기 중간 배치되는 돌출부(1192, 1292, 1392, 1492, 1592, 1692, 1792)는 인접하는 임플란트 바디 부분 보다 큰 단면 크기를 포함할 수 있으며, 소관 벽 일부를 약간 변형시켜 상기 임플란트를 사용 기간 중 제 위치에 유지시키기 위한 추가적인 고정을 제공할 수 있다 (예를 들어, 도 5 참조).
예를 들어, 눈물 임플란트에 의하여 하부 누소관(210)을 막아 소관(210) 내에 배압의 축적을 야기함으로써 임플란트를 임플란트 위치로부터 몰 수 있는 것으로 믿어진다. 이러한 배압은 예를 들어 눈 깜빡임 (눈물이 눈의 전방 표면으로부터 배출 시스템으로 아래로 펌핑되는) 또는 재채기 (압력이 폐 시스템으로부터 나오는) 동안 일어날 수 있다. 따라서, 적어도 하나의 중간 배치되는 유지 돌출부(1192, 1292, 1392, 1492, 1592, 1692, 1792)의 형태로 도시되는 부가적인 유지 특징 중 하나 이상을 이용하여 임플란트 이동을 방지하고 임플란트된 눈물 임플란트 위치를 더욱 고정시킬 수 있다. 이러한 부가적인 유지 특징들은 임플란트의 삽입 어려움을 감지가능한 정도로 증가시키지 않으면서 근위 방향으로 이동을 방지하도록 디자인될 수 있다.
본원에 개시되는 다양한 눈물 임플란트의 안전성, 허용가능성, 편안함, 조작및 삽입/제거 용이성, 유지, 효율성 및 임플란트을 평가하기 위한 임상 실험이 수행되고 있다. 예비 보고서는 도 12, 도 13, 및 도 43a 내지 도 43c에 도시되는 눈물 임플란트와 같은 눈물 임플란트는 효율적이고 시험에 참여하는 환자가 잘 견딜 수 있음을 나타낸다. 예를 들어, 도 13에 도시되는 유형의 눈물 임플란트의 배치 후 4주의 팔로우업에서 측정되는 예비 데이터에 근거하여, 이상 반응이 주목되는 경우, 총 이상 반응은 단지 1.7% 내지 11.% 범위이다. 가장 통상적인 이상 반응은 눈 가려움 (초기 임플란트 착용 및 대개 적응의 일부로 흔히 나타나는), 눈물 흘림 및 눈 자극이다 (각각 11.7%, 6.7% 및 5.0%). 상기한 것들보다 덜 보고되는 빈도수의 기타 이상 반응은 눈 화끈거림, 안구 불편함, 표층 점상 각막염을 포함한다. 4주의 팔로우업에서 결막 또는 안구 충혈이 관측되지 않았다. 44 ㎍ 라타노프로스트 약물 인서트를 포함하는 임플란트에 대한 4주째 환자에서 보고된 편안함 및 눈물 흘림 스코어는 다음과 같았다: 환자의 88%가 편안함을 '자각 없음' 또는 '가벼운 자각'으로 평가한 반면, 환자의 76%가 눈물 흘림을 '없음'으로 평가하였다. 도 12, 도 13, 및 도 43a 내지 도 43c에 도시되는 유형의 눈물 임플란트의 조작 평가는 임플란트가 삽입 및 제거가 용이함을 나타내며, 의사는 도 12, 및 도 43a 내지 도 43c에 도시되는 유형의 눈물 임플란트를 삽입하기 용이함(80%) 및 제거하기 용이함(100%)으로 평가하였다.
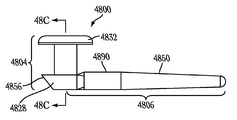
도 12에 일반적으로 도시되는 바와 같은 실시예에서, 근위 말단(1208)은 약 1.2 mm의 외부 직경 및 제1 부분(1204)의 세로 방향으로 약 0.13 mm 내지 약 0.19 mm의 캡 두께를 가지는 캡과 같은 돌출부를 제공한다. 이러한 실시예에서, 상기 근위 말단(1208) 캡 부분은, 예를 들어 약 0.56 mm의 외부 직경 및 약 0.6 mm의 세로샤프트 길이를 가질 수 있는 샤프트 부분에 의해서, 제1 부분(1204)의 유지 돌출부(1292)로부터 분리될 수 있다. 이러한 실시예에서, 제1 부분(1204)의 유지 돌출부(1292)는 약 0.9 mm의 근위 외부 직경을 가질 수 있으며, 이는 샤프트 부분의 외부 직경과 동일하거나 그보다 작은 원위 외부 직경(제1 부분(1204) 및 제2 부분(1206)이 만나는 곳과 같은)으로 갈수록 가늘어질 수 있다. 제1 부분(1204)의 보다 날카롭게 가늘어지는 유지 돌출부(1292)를 이용하여 더 나은 유지를 얻을 수 있으며, 다른 실시예에서, 상기 유지 돌출부는 약 1.1 mm의 근위 외부 직경을 가질 수 있다. 또 다른 실시예에서, 상기 근위 말단(1208)은 약 1.4 mm의 외부 직경을 가지는 캡을 제공하고, 상기 제1 부분(1204)의 유지 돌출부(1292)의 근위 외부 직경은 약 1.4 mm일 수 있다.
유사한 규모 및 규모적 변화를 도 11 내지 17에 일반적으로 도시되는 실시예를 포함하는 본원에 기재되는 다른 실시예들에 적용할 수 있다. 예를 들어, 도 13에 일반적으로 도시되는 바와 같이, 제1 부분(1304)의 유지 돌출부(1392)는 약 0.56 mm 내지 약 0.70 mm의 출발 직경으로부터 밖을 향하는 배럴일 수 있다. 상기 제1 부분(1304) 내 제1 공동은 약 0.42 mm (대략 0.0165 인치)의 직경 및 약 1.22 mm (대략 0.048 인치)의 깊이를 가질 수 있다. 이와 같은 제1 공동 크기는 적어도 약 0.07 mm의 상기 공동을 둘러싸는 제1 부분 벽 두께를 초래할 수 있다. 일부 실시예에서, 약 44 마이크로그램의 라타노프로스트 (대략 33% 약물 적재를 가정)를 가지는 약물 인서트가 제1 공동 내로 삽입되고 고정된다. 임의로, 공동 및 그 안에 배치될 수 있는 약물 인서트의 크기 (예를 들어, 직경 또는 깊이)를 증가 또는 감소시킴으로써, 더 많거나 적은 약물 또는 기타 제제를 상기 제1 공동 내 삽입할 수 있다. 예를 들어, 도 43a 내지 도 43c에 도시되고 이와 관련하여 기재되는 바와 같이, 상기 제1 공동은 약 0.56 mm (대략 0.022 인치)의 직경 및 1.22 mm (대략 0.048 인치)의 깊이를 가질 수 있다. 이와 같은 제1 공동 크기는 약 81 ㎍의 라타노프로스트 (대략 33% 약물 적재를 가정)를 가지는 약물 인서트를 수용할 수 있다.
도 18 및 도 19는 누점(212,214)을 통하여 누소관(208,210)(도 2) 내로 삽입가능한 다른 눈물 임플란트(1800,1900)를 예시한다. 본 실시예에서, 상기 눈물 임플란트(1800,1900)는 제1(1804,1904) 및 제2(1806.1906) 부분들을 포함하는 임플란트 바디(1802.1902)를 포함할 수 있고, 상기 제1 부분(1804,1904)의 근위 말단(1808,1908)으로부터 상기 제2 부분(1806,1906)의 원위 말단(1810,1910)으로 연장할 수 있다. 도시되는 바와 같이, 각각의 임플란트 바디(1802,1902)의 중간부(1896,1996)는 제1(1804,1904) 또는 제2(1806,1906) 임플란트 바디 부분들 중 하나 또는 이들 모두에 대하여 경사져 눈물 임플란트의 임플란트되는 위치를 잠재적으로 더욱 고정시킬 수 있다.
중간부(1896,1996)의 경사가 누점(212,214) 및 누소관(208,210)의 해부 구조를 포획하여, 예를 들어 누소관에 대한 경사에 의하여 적용되는 지향성 힘을 통해서, 눈물 임플란트(1800,1900)를 임플란트된 위치 내에 유지하는 것을 보조할 수 있다. 이러한 지향성 힘은 연속적으로 피드백 또는 기타 돌출부(1832,1932)를 누점(212,214)과 동일 평면이 되도록 할 수 있다.
도 20은 누점(212,214)을 통하여 누소관(208,210)(도 2) 내로 삽입가능한 다른 눈물 임플란트(2000)를 예시한다. 본 실시예에서, 상기 눈물 임플란트(2000)는 제1(2004) 및 제2(2006) 부분들을 포함하는 임플란트 바디(2002)를 포함할 수 있고, 상기 제1 부분(2004)의 근위 말단(2008)으로부터 상기 제2 부분(2006)의 원위 말단(2010)으로 연장할 수 있다. 상기 근위 말단(2008)은 세로 근위축(2012)을 정의하고 상기 원위 말단(2010)은 세로 원위축(2014)을 정의할 수 있다. 상기 임플란트 바디(2000)는 임플란트시, 소관 만곡(250)(도 2)에 또는 더 원위에 위치하는 누소관(208,210)(도 2)의 적어도 일부에 대하여 상기 임플란트 바디의 적어도 일부를 바이어싱하기 위한 근위축(2012)과 원위축(2014) 사이의 대략 90도 경사진 교차 지점이 존재하도록 구성될 수 있다. 다양한 실시예에서, 상기 제1 부분(2004)의 원위 말단(2026)은 상기 제2 부분(2006)의 근위 말단(2028) 또는 이에 인접하여 상기 제2 부분(2006)과 일체화될 수 있다.
상기 실시예에서, 하나 이상의 물질 컷아웃(2080)이 임플란트 바디(2002)의 외표면 내에 만들어진다. 그 결과, 환영으로 도시되는 바와 같이, 근위축(2012)과 원위축(2014) 사이에 경사진 교차 지점이 임플란트 동안 더 선형으로 정렬되어, 누점(212,214)을 통한 누소관(208,210) 내로의 삽입을 촉진시킬 수 있다.
도 21 및 도 22a, 도 22b는 누점(212,214)을 통한 누소관(208,210)(도 2) 내로 삽입가능한 눈물 임플란트(2100,2200)의 측면도를 예시한다. 이러한 실시예에서, 각각의 눈물 임플란트(2100,2200)는 제1(2104,2204) 및 제2(2106,2206) 부분을 포함하는 임플란트 바디(2102,2202)를 포함할 수 있으며, 제1 부분(2104,2204)의 근위 말단(2108,2208)으로부터 제2 부분(2106,2206)의 원위 말단(2110,2210)으로 연장할 수 있다. 제2 부분(2106,2206) 각각은 하나 이상의 암 부재(2170,2270)가 임플란트 바디에 인접하는 제1 배치와 하나 이상의 암 부재(2170,2270)가 임플란트 바디의 측면으로부터 측면 연장하는 제2 배치 사이에서 이동가능한 하나 이상의 암 부재(2170,2270)를 포함할 수 있다. 제1 배치에서, 상기 하나 이상의 암 부재(2170,2270)는 좁은 프로파일을 제공함으로써 눈물 임플란트의 누점(212,214)을 통한 누소관(208,210) 내로의 삽입을 촉진시킨다. 제2 배치에서, 상기 하나 이상의 암 부재(2170,2270)는 임플란트시 누소관 팽대부(252)(도 2) 또는 누소관(208,210) 중 적어도 하나를 채우도록 측면 연장한다. 임의로, 상기 하나 이상의 암 부재(2170,2270)는 하이드로겔과 같은 유체 팽창가능한 물질을 포함하여, 수화시 누소관 팽대부(252) 또는 누소관(208,210) 내 임플란트되는 눈물 임플란트를 더욱 고정시킬 수 있다.
일부 실시예에서, 상기 하나 이상의 암 부재(2170,2270)는 임플란트 바디(2102,2202)를 형성하는데에 또한 사용되는 몰드 내로 혼입될 수 있다. 상기 하나 이상의 암 부재(2170,2270)는 대안적으로 존재하는 임플란트 바디(2102,2202) 상으로 몰딩 또는 접착시킴으로써 부착될 수 있다. 상이한 강성 및 고정/제거 특성을 위하여 상이한 두께 및 형태의 하나 이상의 암 부재(2170,2270)를 사용할 수 있다. 하이드로겔 외에, 상기 하나 이상의 암 부재(2170,2270)는 인공 수정체 위에 촉각을 위하여 사용되는 것과 같은 기타 물질로 형성될 수 있다.
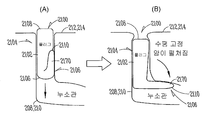
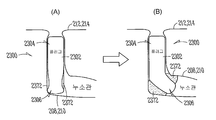
도 23은 누점(212,214)을 통하여 누소관(208,210)(도 2) 내로 삽입가능한 다른 눈물 임플란트(2300)의 측면도를 예시한다. 본 실시예에서, 상기 눈물 임프란트(2300)는 제1(2304) 및 제2(2306) 부분을 포함하는 임플란트 바디(2302)를 포함할 수 있으며, 상기 제1 부분(2304)의 근위 말단(2308)으로부터 제2 부분(2306)의 원위 말단(2310)으로 연장할 수 있다. 상기 제2 부분(2306)은, 팽창시 누소관 벽으로부터 멀어져 제2 부분(2306)을 바이어스하도록 구성되는, 팽창가능한 유지 요소 (예를 들어, 팽창식 벌룬)(2372)에 의하여 적어도 부분적으로 둘러싸여질 수 있다.
일부 실시예에서, 상기 팽창가능한 유지 요소(2372)는 눈 또는 비루 시스템 조직에 전달될 제제를 함유하거나 이에 의하여 부풀려질 수 있다. 일부 실시예에서, 상기 팽창가능한 유지 요소(2372)는 임의의 약물 인서트 또는 기타 제제 유지 구조로부터 분리되는 하나 이상의 벌룬을 사용할 수 있다. 상기 하나 이상의 벌룬은 임의로, 상기 벌룬의 조절된 팽창을 허용하도록 임의로 임플란트 삽입 내에 포함되는 팽창 루멘을 가지는, 벌룬 카테터 상에 사용되는 것들과 유사할 수 있다. 이와 같은 실시예에서, 상기 눈물 임플란트(2300)는 도 23의 (A)에 도시되는 바와 같이 수축된 벌룬과 함께 삽입될 수 있다. 눈물 임플란트(2300)가 제 위치에 놓이면, 상기 벌룬은 도 23의 (B)에 도시되는 바와 같이 부풀려져 임플란트의 임플란트된 위치를 고정시킬 수 있다.
상기 벌룬은 또한 수축되어 눈물 임플란트(2300)의 제거를 더 용이하게 할 수 있다. 상기 벌룬은 임의로 부분적으로 또는 실질적으로 누소관(208,210)의 크기 및 형태 변화에 순응할 수 있다. 대안적인 실시예의 벌룬은 벌룬 내 천공 또는 개구를 통한 물의 흡수에 의한 하이드로겔의 팽창과 같은, 벌룬 내 배치되는 물질의 팽창에 의하여 팽창될 수 있다. 상기 하나 이상의 벌룬은 지지 임플란트 바디 주위에 배치되는 환형 구조이거나, 또는 임플란트 바디의 축 주위에 편심 배치될 수 있다. 도 23의 (B)에 예시되는 바와 같이, 상기 벌룬은 눈물 배출관의 수평 부분 내에 또는 이에 인접하여, 또는 눈물 배출 시스템의 누소관 팽대부 내에 또는 이에 인접하여 있기에 충분히 원위에 배치될 수 있다. 대안적인 실시예는 더 근위의 하나 이상의 벌룬을 포함할 수 있다.]
도 24는 하부 누점(214)을 통하여 누소관(210) 내로 삽입되는 다른 눈물 임플란트(2400)의 개략도를 예시한다. 상기 눈물 임플란트(2400)는 제1(2404) 및 제2(2406) 부분을 포함하는 임플란트 바디(2402)를 포함할 수 있다. 다양한 실시예에서, 상기 임플란트 바디(2402)는 임플란트시, 상기 임플란트 바디(2402)의 적어도 일부가 소관 만곡(250)에 또는 더 원위에 위치하는 누소관(210)의 적어도 일부에 대하여 바이어스 되도록 구성될 수 있다. 이러한 실시예에서, 상기 제2 부분(2406)은 제1 부분(2404)의 직경보다 크나 2 밀리미터 미만인 크기와 같은 약 2 밀리미터 미만의 세로 길이를 포함한다. 또한, 이러한 실시예에서, 상기 임플란트 바디(2402)는 상기 제1 임플란트 바디 부분(2404)의 근위 말단 주위로 적어도 부분적으로 측면 연장하는 것과 같은, 잡을 수 있는 또는 기타 돌출부(2432)를 포함할 수 있다.
도 25a, 도 25b는 누점(212,214)을 통하여 누소관(208,210)(도 2) 내로 삽입가능한 다른 눈물 임플란트(2500)을 예시한다. 이들 실시예에서, 상기 눈물 임플란트(2500)는 제1(2504) 및 제2(2506) 부분을 포함하는 임플란트 바디(2502)를 포함할 수 있으며, 상기 제1 부분(2504)의 근위 말단(2508)으로부터 제2(2506) 부분의 원위 발단(2510)으로 연장할 수 있다. 상기 임플란트 바디는 일반적으로 누소관(208,210)의 해부학적 특징에 매치되어 예를 들어 환자의 편안함 및 고정 유지를 제공할 수 있는 일반적 형상을 포함한다. 상기 근위 말단(2508)은 세로 근위축(2512)을 정의하고, 상기 원위 말단(2510)은 세로 원위축(2514)을 정의할 수 있다. 상기 임플란트 바디(2502) 임플란트시, 상기 임플란트 바디(2502)의 적어도 일부를 소관 만곡(250)(도 2)에 또는 더 원위에 위치하는 누소관(208,210)(도 2)의 적어도 일부에 대하여 바이어싱하기 위한 근위축(2512)과 원위축(2514) 사이에 경사진 교차 지점이 존재하도록 구성될 수 있다.
도 25a, 도 25b의 실시예에서, 상기 임플란트 바디(2502)는 근위 말단(2508)에 인접하여 배치되는 제1 공동(2518) 및 원위 말단(2510)에 인접하여 배치되는 제2 공동(2520) 모두를 포함한다. 상기 제1 공동(2518)은 제1 부분(2504)의 근위 말단(2508)으로부터 내측 연장하고, 상기 제2 공동(2520)은 제2 부분(2506)의 원위 말단(2510)으로부터 내측 연장한다. 제1 약물 방출 또는 기타 제제 방출 약물 인서트가 제1 공동(2518) 내에 삽입되어 눈에 약물 또는 기타 치료제의 서방출을 제공할 수 있으며, 제2 약물 방출 또는 기타 제제 방출 약물 인서트가 제2 공동(2520) 내에 삽입되어 예를 들어 비도 또는 내이 시스템에 약물 또는 기타 치료제의 서방출을 제공할 수 있다. 일부 실시예에서, 상기 제1 공동(2518)은 도 26에 도시되는 바와 같이 상기 제1 부분(2504)의 근위 말단(2508)으로부터 내측 연장하여 제 부분(2506)의 원위 말단(2510) 가까이 위치하며, 제1 약물 방출 또는 기타 제제 방출 약물 인서트로 충전된다. 일부 실시예서, 상기 제2 공동(2520)은 제2 부분(2506)의 원위 말단(2510)으로부터 내측 연장하여 제1 부분(2504)의 근위 말단(2508) 가까이에 위치하며, 제2 약물 방출 또는 기타 제제 방출 약물 인서트로 충전된다.
특정 실시예에서, 제2 부분(2506)은 눈물 임플란트(2500)가 임플란트되는 동안 누점(212,214) 또는 누소관(208,210) 중 하나 또는 이들 모두와 같은 해부 조직을 충분한 직경으로 확작시키기 위한 일체형 확장기(2550)을 포함한다. 이러한 방식으로, 상기 눈물 임플란트(2500)는 별도의 확대 도구를 통한 예비 확장의 필요 없이 다양한 크기의 안구 해부 구조 내에 임플란트될 수 있다. 이들 실시예에서, 상기 일체형 확장기(2550)는 상기 제1 부분(2504)에 연관된 일반적으로 오목 형상을 포함한다. 일부 실시예에서, 상기 오목 형상은 소관 만곡(250)의 반경보다 작은 반경을 포함한다. 일부 실시예에서, 상기 오목 형상은 소관 만곡(250)의 반경과 실질적으로 동일한 반경을 포함한다. 도 25b의 실시예에 도시되는 바와 같이, 평탄한 전이부가 상기 제1(2504) 및 제2(2506) 부분 사이에 존재할 수 있다.
특정 실시예에서, 제2 임플란트 바디 부분(2506)의 근위 말단(2528)은 임플란트시 누소관 팽대부(252)(도 2)의 적어도 일부에 대하여 바이어스되도록 구성되는 유지 요소(2556)를 포함할 수 있다. 도 25a의 실시예에서, 상기 유지 요소(2556)는 제1(2504) 및 제2(2506) 임플란트 바디 부분 사이의 교차 지점으로부터 기부에 돌출한다.
도 26은 누점(212,214)을 통하여 누소관(208,210)(도 2) 내로 삽입가능한 다른 눈물 임플란트(2600)를 예시한다. 본 실시예에서, 상기 눈물 임플란트(2600)는 제1(2604) 및 제2(2606) 부분을 포함하는 임플란트 바디(2602)를 포함하고, 제1 부분(2604)의 근위 말단(2608)으로부터 제2 부분(2606)의 원위 말단(2610)으로 연장한다. 상기 근위 말단(2608)은 세로 근위축(2612)을 정의하고, 상기 원위 말단(2610)은 세로 원위축(2614)을 정의할 수 있다. 상기 임플란트 바디(2600)는 임플란트시, 상기 임플란트 바디(2600)의 적어도 일부를 소관 만곡(250)(도 2)에 또는 보다 원위에 위치하는 누소관(208,210)의 적어도 일부에 대하여 바이어싱하기 위한 근위축(2612)과 원위축(2614) 사이의 90-135 도 경사진 교차 지점이 존재하도록 구성될 수 있다.
특정 실시예에서, 상기 임플란트 바디(2602)는 근위 말단(2608)에 인접하여 배치되는 제1 공동(2618)을 포함할 수 있다. 이러한 실시예에서, 상기 제1 공동(2618)은 제1 부분(2604)의 근위 말단(2608)으로부터 제2 부분(2606)의 원위 말단(2610) 가까이의 위치로 내측 연장한다. 예를 들어 약 0.2 입방 센티미터 내지 약 0.25 입방 센티미터 사이의 부피를 가지는 제1 약물 방출 또는 기타 제제 방출 약물 인서트를 제1 공동(2618) 내에 배치하여 눈에 약물 또는 기타 치료제의 연장된 서방출을 제공할 수 있다.
특정 실시예에서, 상기 제2 부분(2606)은 눈물 임플란트(2600)가 임플란트되는 동안 누점(212,214) 또는 누소관(208,210) 중 하나 또는 이들 모두와 같은 해부 조직을 충분한 직경으로 확장시키기 위한 일체형 확장기(2650)를 포함한다. 이러한 방식으로, 상기 눈물 임플란트(2600)는 별도의 확대 도구를 통한 예비 확장의 필요없이 다양한 크기의 안구 해부구조 내로 임플란트될 수 있다. 이러한 실시예에서, 상기 확장기(2650)는 상기 제1 부분(2604)에 대한 일반적으로 볼록 형상을 포함한다. 일부 실시예에서, 상기 볼록 형상은 소관 만곡(250)의 반경보다 작은 반경을 포함한다. 일부 실시예에서, 상기 볼록 형상은 소관 만곡(250)의 반경과 실질적으로 동일한 반경을 포함한다.
특정 실시예에서, 상기 제2 임플란트 바디 부분(2606)의 근위 말단(2628)은 임플란트시 누소관 팽대부(252)(도 2)의 적어도 일부에 대하여 바이어스되도록 구성되는 유지 요소(2656)을 포함할 수 있다. 본 실시예에서, 상기 유지 요소(2656)는 제1(2604) 및 제2(2606) 임플란트 바디 부분 사이의 교차 지점으로부터 근위로 돌출한다. 도 29 및 도 30에 도시되는 바와 같은 일부 실시예에서, 제2 임플란트 바디 부분(2606)의 근위 말단(2628)은, 임플란트 바디(2602)가 임플란트될 때 팽대부(252) 내로 팽창하도록 구성되는 하이드로겔 유지 요소를 포함하는 유지 요소(2656)를 포함할 수 있다.
도 27은 누점(212,214)을 통하여 누소관(208,210) 내로 삽입가능한 다른 눈물 임플란트(2700)의 측면도를 예시한다. 본 실시예에서, 상기 눈물 임플란트(2700)는 임플란트 전에 서로에 대하여 선형인 제1 및 제2 부분을 포함하는 임플란트 바디(2702)를 포함한다. 상기 임플란트 바디(2702)는 제1 부분의 근위 말단(2708)으로부터 제2 부분의 원위 말단(2710)으로 연장한다. 상기 근위 말단(2708)은 세로 근위축(2712)을 정의하고, 원위 말단(2710)은 세로 원위축(2714)을 정의할 수 있다. 상기 임플란트 바디(2702)는 임플란트시, 상기 임플란트 바디(2702)의 적어도 일부를 소관 만곡(250)(도 2)에 또는 보다 원위에 위치하는 누소관(208,210)의 적어도 일부에 대하여 바이어싱하기 위한 근위축(2712)과 원위축(2714) 사이의 45-135도 경사진 교차 지점이 존재하도록 구성될 수 있다. 이러한 실시예에서, 상기 임플란트 바디(2702)의 제2 부분은 누소관(208,210)의 일부에 대하여 임플란트 바디(2702)의 바이어싱을 촉진하기 위한 적어도 하나의 기복(2790)을 포함한다.
도 28은 누점(212,214)을 통하여 누소관(208,210) 내로 삽입가능한 다른 눈물 임플란트(2800)의 측면도를 예시한다. 본 실시예에서, 상기 눈물 임플란트(2800)는 임플란트 전에 서로에 대하여 선형인 제1 및 제2 부분을 포함하는 임플란트 바디(2802)를 포함한다. 상기 임플란트 바디(2802)는 제1 부분의 근위 말단(2808)으로부터 제2 부분의 원위 말단(2810)으로 연장한다. 상기 근위 말단(2808)은 세로 근위축(2812)을 정의하고, 원위 말단(2810)은 세로 원위축(2814)을 정의할 수 있다. 상기 임플란트 바디(2802)는 임플란트시, 상기 임플란트 바디(2802)의 적어도 일부를 소관 만곡(250)(도 2)에 또는 보다 원위에 위치하는 누소관(208,210)의 적어도 일부에 대하여 바이어싱하기 위한 근위축(2812)과 원위축(2814) 사이의 45-135도 경사진 교차 지점이 존재하도록 구성될 수 있다. 본 실시예에서, 상기 임플란트 바디(2802)의 제2 부분은 환형 립 형태의 돌출부와 같은 적어도 하나의 중간 배치되는 유지 돌출부(2892)를 포함한다. 상기 유지 돌출부(2892)는 인접하는 임플란트 바디 부분보다 큰 단면을 포함하고, 임플란트 바디(2802)의 임플란트된 위치의 고정을 촉진시킬 수 있는 반면, 인접하는 더 좁은 임플란트 바디 부분은 누소관(208,210)의 일부에 대한 임플란트 바디(2802)의 바이어싱을 촉진시킬 수 있다.
도 29 내지 도 32는 누점(212,214)을 통하여 누소관(208,210) 내로 삽입가능한 다른 눈물 임플란트(2900,3000,3100,3200)의 측면도를 예시한다. 본 실시예에서, 상기 눈물 임플란트(2900,3000,3100,3200)는 임플란트 전에 서로에 대하여 선형인 제1(2904,3004,3104,3204) 및 제2(2906,2006,3106,3206) 부분을 포함하는 임플란트 바디(2902, 3002,3102,3202)를 포함하며, 제1 부분(2904,3004,3104,3204)의 근위 말단(2908,3008,3108,3208)으로부터 제2(2906,3006,3106,3206) 부분의 원위 말단(2910,3010,3110,3210)으로 연장한다. 상기 근위 말단(2908,3008,3108,3208)은 세로 근위축(2912,3012,3112,3213)을 정의할 수 있다.
상기 제2 부분(2906,3006,3106,3206)은, 상기 임플란트 바디(2902,3002,3102,3202)가 임플란트 될 때 근위축(2912,3012,3112,3212)에 대하여 측면 팽창하도록 구성되는 유체 팽창가능한 유지 요소(2994,3094,3194,3294)를 포함할 수 있다. 다양한 실시예에서, 상기 유체 팽창가능한 유지 요소(2994,3094,3194,3294)는 팽창 방향 또는 팽창 양 중 하나 또는 이들 모두가 조절되도록 형성될 수 있다. 예를 들어, 상기 유체 팽창가능한 유지 요소(2994,3004,3104,3204)는 다른 평면보다 일 평면으로 더 팽창하여 눈물 임플란트를 확고히 고정시킬 수 있다. 일부 실시예에서, 상기 유체 팽창가능한 유지 요소(2994,3094,3194,3294)는, 임플란트 바디가 임플란트될 때, 누소관 팽대부(252)(도 2)로부터 멀어지는 방향으로 근위축(2912,3012,3112,3212)에 대하여 측면으로 팽창하도록 구성되는 일부를 포함할 수 있다. 도 29-30에 도시되는 바와 같은 일부 실시예에서, 상기 유체 팽창가능한 유지 요소(2994,3004,3104,3204)는, 임플란트 바디가 임플란트될 때 누소관 팽대부(252)(도 2)를 향하는 방향으로 근위축(2912,3012,3112,3212)에 대하여 측면 팽창하도록 구성되는 일부를 포함한다.
일부 실시예에서, 상기 유체 팽창가능한 유지 요소(2994,3004,3104,3204)는 누점(212,214)을 통하여 누소관(208,210) 내로 좁은 프로파일로 삽입가능한 하이드로겔을 포함할 수 있다. 삽입 후, 상기 하이드로겔 또는 기타 유체 팽창가능한 유지 요소는 수화되고 넓은 구조로 팽창될 수 있다. 적어도 하나의 중간 배치되는 유지 요소(2992,3092,3192,3292)와 같은 돌출부를 이용하여 상기 하이드로겔 또는 기타 팽창가능한 요소가 팽창하는 동안 눈물 임플란트의 임플란트된 위치를 유지할 수 있다.
도 33은 누점(212,214)을 통하여 누소관(208,210)(도 2) 내로 삽입가능한 다른 눈물 임플란트(3300)의 측면도를 예시한다. 본 실시예에서, 상기 눈물 임플란트(3300)는 제1(3304) 및 제2(3306) 부분을 포함하는 임플란트 바디(3302)를 포함할 수 있으며, 제1 부분(3304)의 근위 말단(3308)으로부터 제2 부분(3306)의 원위 말단(3310)으로 연장할 수 있다. 도시되는 바와 같이, 제1 부분(3306)은 코일, 브레이드, 스텐트, 메시 튜브, 봉합사, 열경화성 폴리머, 열가소성 열활성화 물질, 또는 형상 기억 재료 중 적어도 하나를 포함하는 팽창가능한 유지 요소(3393)를 포함할 수 있다. 상기 팽창가능한 유지 요소(3393)는, 임플란트 바디가 임플란트될 때 제1 부분(3304)에 의하여 정의되는 근위축(3312)에 대하여 측면 팽창하도록 구성될 수 있다. 적어도 하나의 중간 배치되는 유지 돌출부(3392)와 같은 돌출부를 이용하여 눈물 임플란트의 임플란트된 위치를 잠재적으로 더욱 고정시킬 수 있다.
도 34a, 도 34b는 다른 눈물 임플란트(3400) 및 임플란트 환경의 개략도를 예시한다. 다양한 실시예에서, 임플란트 바디(3402)는 제1 임플란트 바디 부분의 근위 말단(3408)으로부터 또는 그 주위로 적어도 부분적으로 측면 연장하는 하나 이상의 돌출부와 같은, 잡을 수 있는 또는 기타 돌출부(3432)를 포함할 수 있다. 도 34b에 도시되는 것와 같은 일부 실시예에서, 상기 돌출부(3432)는 임플란트되는 위치 내로 눈물 임플란트(3400)을 삽입하거나 또는 이로부터 임플란트를 제거하는데에 사용되는 날개 세트를 포함할 수 있다. 소관 만곡(250) 및 임의로 누소관 팽대부(252)의 크기 및 형상을 가정하여, 상기 임플란트 바디(3402)의 임플란트된 비선형 구조는 이동을 방지할 수 있으므로, 상기 날개 세트는 이동을 고려하지 않고 구성될 수 있다.
도 34a, 도 34b의 실시예에서, 상기 하나 이상의 돌출부(3432)는 임플란트시 눈(100)에 평행하거나 이로부터 멀어지는 방향으로 측면 연장한다. 이러한 방식으로, 상기 돌출부(3432)는 잡을 수 있는 또는 피드백 특징으로서 작용할 수 있으나, 눈물 임플란트(3400)가 임플란트될 때 환자의 불편함을 제한할 수 있다. 또한, 상기 돌출부(3432)는 눈(100)으로부터 멀어져 연장함으로써 조직 내에 묻히지 않을 수 있으며, 환자 또는 의사가 용이하게 인식할 수 있다. 이는 눈(100) 주위의 연질 조직을 파내고 찾을 필요 없이 눈물 임플란트(3400)가 적절한 위치에 유지되고 있는지에 대한 신속한 결정을 허용할 수 있다. 일부 예에서, 하부 눈꺼풀 상에 간단한 잡아당김이 눈(100)으로부터 멀어지는 방향으로 돌출부(3432)를 노출시킬 수 있다. 도 34b의 예에서, 근위 말단(3408)으로부터 적어도 하나의 돌출부(3432)의 측면 팽창은 제1 임플란트 바디 부분의 원위 말단에 대한 제2 임플란트 바디 부분의 측면 연장 방향과 실질적으로 동일하다.
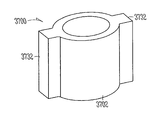
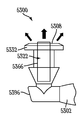
도 35 내지 도38은 눈물 임플란트(3500,3600,3700,3800)의 근위 말단으로부터 연장하는 다양한 잡을 수 있는 돌출부 또는 기타 잡는 수단(3532,3632,3732,3832)의 등축도를 예시한다. 상기 잡을 수 있는 또는 기타 돌출부(3532,3632,3732,3832)는, 사용자가 임플란트 삽입 또는 제거 중에 잡는 구조를 제공하거나, 눈물 임플란트가 누점(212,214)ALC 누소관(208,210)(도 2) 내 완전히 통과하는 것을 억제 또는 방지하거나, 예를 들어 임플란트가 완전히 임플란트되는지에 대한 촉각적 및 시각적 피드백 정보를 사용자에 제공하는 것을 포함하는 다양한 기능을 위하여 사용될 수 있다.
도 35에 도시되는 바와 같은 일부 실시예에서, 상기 잡을 수 있는 돌출부(3532)는 누점의 외면에 있도록 하는 크기를 가지는 두 개 이상의 팽창가능한 암 부재를 포함할 수 있다. 상기 암 부재는 예를 들어 몰딩, 접착 또는 용접을 통하여 임플란트 바디(3502)에 부착될 수 있다. 상기 팽창가능한 암 부재는 눈물 임플란트(3500)의 누점(212,214)을 통한 누소관(208,210) 내로의 침투를 제한하도록 팽창가능하다. 두 개의 암 부재가 도시되나, 일부는 네 개의 암 부재와 같이 두 개 이상의 암 부재를 포함할 수 있다. 상기 팽창가능한 암 부재는 임플란트 바디 직경의 약 두 배에 상응하는 팽창된 프로필 분리 거리(3505)를 가져, 근위 팽창가능한 암 부재의 근위 말단이 누점의 외면에 유지되도록 할 수 있다. 상기 팽창가능한 암 부재는 좁은 프로필 배치로부터 팽창된 프로필 배치로 다양한 방식으로 팽창할 수 있으며, 코일, 브레이드, 봉합사, 열경화성 폴리머, 열가소성 열활성화 물질, 니티놀, 형상기억 재료, 폴리머, 폴리프로필렌, 폴리에스테르, 나일론, 천연 섬유, 스테인레스 스틸, 폴리메틸메타크릴레이트 또는 폴리이미드 중 적어도 하나를 포함할 수 있다. 일부 예에서, 상기 팽창가능한 암 부재는, 눈물 임플란트가 소관 루멘(208,210) 내에 배치된 후, 예를 들어 의사에 의하여 수동적으로 팽창될 수 있다.
도 36에 도시되는 바와 같은 일부 실시예에서, 잡을 수 있는 돌출부(3632)는 눈물 임플란트(3600)의 근위 말단 내에 묻히는 필라멘트의 루프를 포함하여, 예를 들어 겸자를 이용하여 상기 루프를 근위 긴장시켜 임플란트를 제거할 수 있다. 일부 실시예에서, 상기 필라멘트 루프는 루프로 눈물 임플란트로부터 연장하는 주머니 핸들과 유사한 형상을 가져 눈물 임플란트의 제거를 촉진시킬 수 있다. 상기 필라멘트는 열 활성화 물질, 니티놀, 형상 기억 소재, 폴리머, 폴리프로필렌, 폴리에스테르, 나일론, 천연섬유, 스테인레스 스틸, 폴리메틸메타크릴레이트 또는 폴리이미드 중 적어도 하나를 포함할 수 있다. 일부 구현예에서, 상기 필라멘트는 흡수가능한 열가소성 폴리머, 예를 들어, 폴리락트산(PLA), 폴리글리콜산(PGA) 또는 폴리락트 코-글리콜산(PLGA) 중 적어도 하나를 포함할 수 있다. 상기 필라멘트의 원위 말단은 임플란트 바디(3602) 내에 묻히거나, 몰딩되거나 또는 부착되어 필라멘트를 눈물 임플란트에 고정시킬 수 있다.
도 37에 도시되는 바와 같은 일부 실시예에서, 잡을 수 있는 돌출부(3732)는, 누소관(208,210)의 최외곽부를 바이어싱하도록 구성되는, 임플란트 바디(3702)와 결합되는 적어도 하나의 축방향 연장 돌출부를 포함할 수 있다. 상기 누소관의 외측 바이어싱에 대한 본질적인 제한으로 인하여, 상기 축방향 연장 돌출부과 누소관 사이의 상호작용이 눈물 임플란트(3700)의 과도한 삽입을 억제한다.
도 38에 도시되는 바와 같은 일부 실시예에서, 잡을 수 있는 돌출부룰 대신하여 임플란트 바디(3802) 내 세로 압입, 채널 또는 기타 오목부(3832)를 사용하여 눈물 임플란트(3800)의 삽입 또는 제거를 허용할 수 있다. 상기 압입, 채널 또는 기타 오목부(3832)는 임플란트 바디의 일부만을 따라 충분한 거리로 축방향 연장하여 눈물 임플란트의 제거를 촉진시킬 수 있다. 추가적인 실시예에서, 눈물 임플란트는 임플란트 바디 내로 몰딩되고 누점으로부터 임플란트의 제거를 위하여 근위로 연장하는 필라멘트를 포함할 수 있다.
도 39a, 도 39b는 약물 인서트(322) 및 제거 촉진 필라멘트(3999)의 등축도를 예시한다. 도 39a에 도시되는 바와 같은 일부 실시예에서, 상기 필라멘트(3999)는 약물 인서트(322)로부터 연장하고 제거를 위하여 그 안에 몰딩된다. 다른 것들 중, 상기 필라멘트(3999)는 봉합사, 열경화성 폴리머, 또는 형상기억 합금을 포함할 수 있다. 도 39b에 도시되는 바와 같은 일부 실시예에서, 상기 필라멘트(3999)는 임플란트 바디(3902)에 인접하는 약물 인서트(322)를 따라 연장하고, 제거 목적으로 인서트의 원위 말단에 결합된다. 필라멘트를 시아노아크릴레이트, 아크릴산, 에폭시, 우레탄 또는 핫멜트 접착제와 같은 접착제를 이용하여 약물 코어 인서트의 원위 말단에 결합시킬 수 있다.
도 40은 누점을 통하여 누소관 내로 적어도 부분적으로 삽입가능하도록 구성되는 눈물 임플란트를 제조하는 방법(4000)을 예시하는 블록 다이어그램이다. (4002)에서, 제1 부분의 근위 말단으로부터 제2 부분의 원위 말단으로 연장하는 임플란트 바디가 형성된다. 다양한 실시예에서, 상기 근위 말단은 세로 근위축을 정의하도록 형성되고, 상기 원위 말단은 세로 원위축을 정의하도록 형성된다. 임플란트 바디의 형성은, 임플란트시, 임플란트 바디의 적어도 일부를 소관 만곡에 또는 보다 원위에 위치하는 누소관의 적어도 일부에 대하여 측면으로 바이어싱하도록 약 45 도의 경사로 근위축과 원위축이 교차하도록 구성될 수 있다. 임의로, 임플란트 바디의 형성은 하나 이상의 약물 또는 기타 치료제 입자를 바디 내로 포함시키는 것을 포함할 수 있다. 그렇다면, 상기 임플란트 바디는 임의로 투과성 또는 불투과성 물질로 코팅되어 환자의 신체 조직으로 원하는 대로 제제 방출을 지시할 수 있다.
일부 실시예에서, 다양한 크기의 임플란트 바디가 다양한 환자 해부 구조에 피팅되도록 형성된다. 환자의 누점 크기 측정을 위하여, 환자가 짧은 시간 동안 (대략 60 초) 그 눈꺼풀을 닫고 비스듬히 누운 위치에 있을 때, 국소적 안과용 마취제 한두방울을 눈에 적용할 수 있다. 이어서, 누점 게이지를 이용하여 상부 또는 하부 누점 중 하나 또는 이들 모두의 직경을 측정한다. 게이지 상에 약간의 저항이 느껴질 때까지, 누점 게이지를 누점 내로 밀 수 있으며, 이 때 게이지 상의 눈금에 상응하는 측정을 판독하고 기록한다.
일부 실시예에서, 제2 바디 부분이 상기 제2 부분의 근위 말단에 가까운 위치로부터 제2 바디 부분의 원위 말단으로 일반적으로 좁아지는 확장기를 포함하도록 형성된다. 일부 실시예에서, 상기 확장기는 임플란트 바디의 제2 부분의 외표면을 세로 원위축에 대하여 약 1 도 내지 약 10 도 사이로 경사지게 함으로써 형성된다. 일부 실시예에서, 상기 제2 임플란트 바디 부분의 외표면은 약 0.2 밀리미터 내지 약 0.5 밀리미터 확장기 팁에 대하여 경사진다.
일부 실시예에서, 상기 임플란트 바디는 제1 바디 부분의 근위 말단으로부터 측면 연장하는 잡을 수 있는 또는 기타 돌출부를 포함하도록 형성된다. 특정 실시예에서, 상기 돌출부는 제1 바디 부분에 대하여 제2 바디 부분의 측면 연장 방향과 실질적으로 정렬되도록 형성된다. 특정 실시예에서, 상기 돌출부는, 임플란트시, 제1 바디 부분의 근위 말단으로부터 눈과 평행하거나 이로부터 멀어지는 방향으로 측면 연장하도록 형성된다.
(4004)에서, 제1 바디 부분 또는 제2 바디 부분 중 적어도 하나 내에 약물 인서트가 배치될 수 있다. 다양한 실시예에서, 상기 약물 인서트는, 예를 들어, 눈, 비도 또는 내이에 약물 또는 기타 치료제의 서방출을 제공하기 위하여 노출된 약물 인서트 표면이 근위 말단 또는 원위 말단 중 적어도 하나에 인접하여 있도록 배치된다. 특정 실시예에서, 제1 약물 인서트가 제1 바디 부분 내에 배치되고, 제2 약물 인서트가 제2 바디 부분 내에 배치된다. 다양한 실시예에서, 상기 하나 이상의 약물 인서트는 약물 또는 기타 치료제를 포함하는 약물 코어를 포함한다.
(4006)에서, 임플란트 바디 또는 임플란트 바디 코팅의 외표면부를 유체 팽창가능한 물질, 윤활 코팅 또는 항미생물 코팅 중 적어도 하나로 코팅할 수 있다. 다양한 실시예에서, 임플란트 바디의 외표면부는 연마 공정을 이용하여 연마된다.
기타
실시예
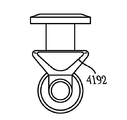
도 41은 도 12의 실시예와 같은 눈물 임플란트가 제1 부분(1204)의 유지 메커니즘(1292)이 그 원주 주위로 등거리로 측면 돌출할 필요가 없도록 변형될 수 있는 실시예를 도시한다. 대신, 도 41에 도시되는 실시예에서는, 제1 부분(1204)의 유지 메커니즘(4192)의 근위 말단이 그 주위로 비-등 측면 거리로 외측으로 측면 돌출하고, 제1 부분(1204)의 유지 메커니즘(4192)은 유지 메커니즘(4192)의 원위 말단에서 제1 부분(1204)의 외부 직경으로 가늘어진다. 일 실시예에서, 상기 유지 메커니즘(4192)의 근위 말단은 제1 부분(1204)의 근위 말단에서 캡(1208) 또는 기타 돌출부의 둘레와 수적으로 동일한 둘레를 포함할 수 있다.
일 실시예에서, 제1 부분(1204)의 유지 메커니즘(4192)의 근위 말단은, 유지 메커니즘의 마주보는 제3 및 제4 면 상에 (상기 제3 및 제4 면은 제1 및 제2 면에 의하여 정의되는 제1 측면 방향에 실질적으로 직각인 제2 측면 방향을 정의함) 샤프트 부분 외부 규모로부터 외측으로 돌출함이 없이, 제1 부분(1204)의 유지 메커니즘(4192)의 마주보는 제1 및 제2 면 상에서 반대 방향으로와 같이, 외측 대측성으로 돌출할 수 있다. 이러한 방식으로, 상기 제1 부분(1204)의 유지 메커니즘(4192)의 대측성 돌출 부분은, 도 12에 도시되고 이와 관련하여 기재되는 바와 같이, 제1 부분(1204)의 유지 메커니즘(1292)의 근위 말단의 돌출 외부 직경과 실질적으로 동일할 수 있는 제1 측면 방향 내 말단 대 말단 측면 거리를 정의할 수 있다.
임플란트를 위한 다양한 기타 옵션이 또한 가능하다. 예를 들어, 조직 자극 또는 손상을 감소시키기 위하여, 부드럽게 한 코너를 임의로 제공할 수 있다. 예를 들어, 유지를 증진시키기 위하여, 날카로운 코너를 임의로 제공할 수 있다. 그러나, 수직 제2 측면 방향으로, 제1 부분(1204)의 유지 메커니즘($192)의 외부 샤프트 직경을 넘어 어떠한 돌출도 있을 수 없다. 일 실시예에서, 상기 제1 부분(1204)의 유지 메커니즘(4192)의 대측 돌출 부분의 제1 측면 방향은, 제2 부분(1206)이 제1 부분(1204)으로부터 연장하는 방향에 실질적으로 직각이며, 이는 더 나은 유지를 제공할 수 있다. 그러나, 다른 실시예에서, 제1 부분(1204)의 유지 메커니즘(4192)의 대측 돌출 부분의 제1 측면 방향은 제2 부분(1206)이 제1 부분(1204)으로부터 연장하는 방향에 실질적으로 평행할 수 있다. 또 다른 실시예에서, 제1 부분(1204)의 유지 메커니즘(4192)의 대측 돌출 부분의 제1 측면 방향은 제2 부분(1206)이 제1 부분(1204)으로부터 연장하는 방향에 대하여 다른 각도 (예를 들어, 0 도 내지 90 도)일 수 있다.
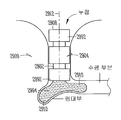
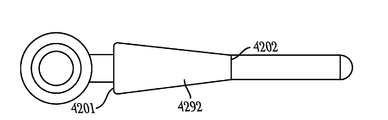
도 42a 내지 도 42d는 도 21 및 41의 실시예에 도시되는 것과 같은 눈물 임플란트가 제2 부분(1206)의 유지 메커니즘(1292)이 제2 부분(1206)의 측면 외부 규모 프로필로부터 서서히 외측으로 불룩하게 될 필요가 없도록 변형되는 예를 도시한다. 보다 구체적으로, 도 42a는 눈물 임플란트의 측면도를 도시하고, 도 42b는 도 42a에 도시되는 커트라인 A-A를 따라 취해진 단면도를 도시하고, 도 42c는 눈물 임플란트의 상면도를 도시하고, 도 42d는 제2 부분(1206)의 근위 말단에서 보이는 눈물 임플란트의 단면도를 도시한다.
도 42a 내지 도 42d의 실시예에서, 제2 부분(1206)은 유지 메커니즘(4292)의 근위 말단부(4201) 또는 유지 메커니즘(4292)의 원위 말단부(4202) 중 하나에서외측 측면 스텝과 같은 더 갑작스러운 변화 프로파일을 가지는 유지 메커니즘(4292)을 포함할 수 있다. 예를 들어, 상기 유지 메커니즘(4292)은 그 근위 말단부(4201)에, 예를 들어, 제2 부분(1206)의 외부 직경(예를 들어, 약 0.46mm 내지 약 0,62mm)으로부터 유지 메커니즘(4292)의 근위 말단부(4201)의 적어도 부분적으로 원주방향으로 돌출하는 외부 직경(예를 들어, 약 0.76mm, 약 0.86mm, 또는 약 0.89mm)으로, 갑작스러운 스텝을 포함할 수 있다. 예를 들어, 조직 자극 또는 손상을 감소시키기 위하여, 부드러운 코너를 임의로 제공할 수 있다. 예를 들어, 유지를 증진시키기 위하여, 날카로운 코너를 임의로 제공할 수 있다. 이러한 실시예에서, 상기 유지 메커니즘(4292)의 원위 말단부(4202)에 근접함에 따라, 상기 유지 메커니즘(4292)의 외부 직경은 제2 부분(1205)의 외부 직경 (예를 들어, 약 0.46mm 내지 약 0.62mm)으로 다시 가늘어질 수 있다.
도 42a 내지 도 42d의 실시예는, 제2 부분(1206)이 제1 부분(1204)으로부터 외측 연장하는 방향에 평행한 방향으로 외측으로 측면 연장함이 없이, 제2 부분(1206)이 제1 부분(1204)으로부터 외측 연장하는 방향에 수직한 방향으로 외측으로 측면 연장하고, 도 41에 대하여 설명한 바와 같이, 상기 제1 부분(1204)의 근위 캡(1208)과 제1 부분(1204)의 유지 메커니즘(4192) 사이에 좁아지고 적어도 부분적으로 원주방향 넥(4203) 부분을 정의하는 샤프트 부분을 제공하는, 제1 부분(1204)의 테이퍼드 유지 메커니즘(4192)를 포함할 수 있다. 좁아지고 적어도 부분적으로 원주방향의 넥 부분(4204)는 또한 유지 목적으로 제1 부분(1204)과 제2 부분(1206) 사이의 접합점에 제공될 수 있다. 소관 조직은 상기 넥 부분(4204) 내로 및 그 주위로 압축됨으로써 눈물 임플란트의 임플란트된 위치의 고정을 보조하는 것으로 믿어진다.
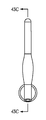
도 43a 내지 도 43c는 도 12, 도 41 및 도 42a 내지 도 42d의 실시예에 도시되는 것과 같은 눈물 임플란트가 제1 부분(1204)의 유지 메커니즘(1292,4192)이 제1 부분(1204) 및 제2 부분(!206) 사이에 접합점에서 넥 부분을 포함할 필요가 없도록 변형될 수 있는 실시예를 도시한다. 보다 구체적으로, 도 43a는 눈물 임플란트의 측면도를 도시하고, 도 43b는 눈물 임플란트의 저면도를 도시하고, 도 43c는 도 43b에 도시되는 커트라인 A-A를 따라 취해진 눈물 임프란트의 단면도를 도시한다.
도 43a 내지 도 43c의 실시예에서, 근위 말단(1208)은 약 1.1 mm의 외부 직경 및 약 0.13 mm의 제1 부분(1204)의 세로 방향 캡 두께를 가지는 캡과 같은 돌출부를 제공할 수 있다. 이러한 실시예에서, 상기 근위 말단(1208) 캡 부분은, 예를 들어, 약 0.56 mm의 외부 직경 및 약 0.66 mm의 세로 샤프트 길이를 가지는 샤프트 부분에 의해서, 제1 부분(1204)의 유지 돌출부(4392)로부터 분리될 수 있다. 이러한 실시예에서, 제1 부분(1204)의 유지 돌출부(4392)는 약 1.1 mm의 근위 외부 직경을 가질 수 있으며, 이는 제2 부분(1206) 내로 직접적으로 약 0.96 mm 가늘어져 제1(1204) 및 제2(1206) 부분 사이에 접합부(4305)에 제공되는 넥 부분이 없도록 할 수 있다. 도 42a 내지 도 42d에 도시되는 바와 같은 넥 부분을 제거함으로써, 유지 돌출부(4392)의 길이를 더 효과적으로 길게 하여 약 1.1 mm 이상의 직경과 같은 더 넓은 근위 외부 직경, 및/또는 더 점진적인 테이퍼 각을 통한 증가된 팽창 및 더 용이한 삽입가능성을 허용할 수 있다. 일부 실시예에서, 근위 외부 둘레는 예를 들어 유지를 증진시키기 위하여 임의로 샤프한 코너를 포함할 수 있다.
도 43a 내지 도 43c의 인서트를 위한 기타 규모 옵션은 다음과 같을 수 있다. 근위 말단(1208)은 약 1.4 mm의 외부 직경을 가지는 캡과 같은 돌출부를 제공할 수 있다. 제1 부분(1204)의 유지 돌출부(4392)는 약 1.3 mm의 근위 외부 직경을 가질 수 있다. 근위 캡(1208)과 유지 돌출부(4392) 사이의 넥 부분은 약 0.7 mm의 직경을 가질 수 있으며, 제1 부분(1304) 내 제1 공동은 약 0.56mm의 직경을 가질 수 있다. 제1(1204) 및 제2(1206) 부분 사이의 접합지점(4305)에서 유지 돌출부의 두께는 상기 돌출부(4392)의 외부 커버 표면에 수직으로 측정하여, 제1 공동의 깊이 및 제1 부분(1204)에 대한 돌출부(4392)의 구조 및 배치에 따라, 예를 들어 0.043 mm, 0.086 mm, 또는 0.175 mm일 수 있다.
특정 실시예에서, 제1 부분(1204)의 유지 메커니즘(1292,4192,4392) 또는 제2 부분(1206)의 유지 메커니즘(1292,4292)은 임의로 마개 바디 위의 자가 팽창 하이드로겔 코팅으로서 임플란트될 수 있으며, 상기 자가 팽창 코팅은 팽창되어 일반적으로 도 41, 도 42a 내지 도 42d, 및 도 43a 내지 도 43c에 도시되는 것과 유사한 형상을 형성한다.
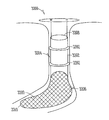
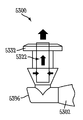
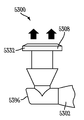
도 44a 내지 도 44c, 및 도 45a 내지 도 45c는 도 12, 도 41, 및 도 42a 내지 도 42d, 및 도 43a 내지 도 43c의 실시예에 도시되는 것과 같은 눈물 임플란트가 비교적 깊은 오목부(4405) 또는 비교적 얕은 오목부(4505)가 제2 부분(1206) 내로 연장하는 것과 같이 제2 부분(1206)의 근위 말단으로부터 연장하도록 변형되는 예를 도시한다. 도 44a 및 도 45a는, 각각 제2 부분(1206)의 원위 말단 및 근위 말단에서 보는 눈물 임플란트의 단면도를 도시하며, 도 44b 및 도 45b는 도 44a 및 도 45a의 커트라인 A-A를 따라 취해진 눈물 임플란트의 단면도를 도시하고, 도 44c 및 도 45c는 눈물 임플란트의 상면도를 도시한다.
일 실시예에서, 상기 오목부(4405,4505)는 기구의 오목부(4405,4505) 내로의 삽입을 허용함으로써 임플란트 동안 보조하기 위하여 사용될 수 있다. 일 실시예에서, 상기 오목부(4405,4505)는 하이드로겔 (예를 들어, Lubrizol Corporation of Cleveland, Ohio에 의하여 제조된 "TG-500" 또는 "TF-2000")과 같은 팽창 가능한 물질을 그 안에 포함할 수 있으며, 상기 물질은 임플란트되고 체액에 노출될 때 팽창할 수 있다. 일 실시예에서, 상기 오목부(4405,4505)는 임플란트 중 기구의 삽입을 허용하고 또한 임플란트시 유지를 보조하기 위하여 하이드로겔의 팽창을 허용하는 두 가지 목적 모두를 수행할 수 있다. 제2 부분(1206)의 근위 말단에 대한 상기 오목부(4405,4505)의 깊이는 존재한다면 팽창가능한 물질(4407)의 적어도 부분적인 팽창을 허용하기에 충분할 수 있다. 일부 실시예에서, 상기 오목부의 깊이는 팽창가능한 물질(4407)의 세로 길이의 두 배이다. 일부 실시예에서, 상기 오목부의 깊이는 팽창가능한 물질(4407)의 세로 길이보다 약간 크다.
상기 팽창가능한 물질(4407)은, 임플란트시 다양한 방향으로 (예를 들어, 측면 및/또는 원주방향으로 벌룬과 유사한 방식으로) 팽창하여 임플란트 바디(1202)의 하나 이상의 부분을 외측으로 누소관 벽에 대하도록 상기 오목부(4405,4505) 내에 구성되고 배치될 수 있다. 상기 임플란트 바디(1202)의 외측으로 팽창된 부분과 소관벽 사이의 맞물림을 통하여, 상기 눈물 임플란트는 누점 내에 보다 확고히 유지될 수 있다. 임의로, 상기 제2 부분(1206)의 오목부(4405,4505) 내에 팽창가능한 물질(4407)의 위치를 필요시 조정하여 원하는 유지 특성을 달성할 수 있다. 일부 실시예에서, 상기 팽창가능한 물질(4407)이 상기 오목부(4405,4505) 내에 배치되어 팽창시 팽창가능한 물질(4407)의 일부가 오목부(4405,4505)에 대하여 외부적으로 돌출되도록 한다. 다른 실시예에서, 상기 팽창가능한 물질(4407)이 상기 오목부(4405,4505) 내에 배치되어 팽창시 상기 팽창가능한 물질(4407)이 상기 오목부 내에 실질적으로 유지되고 상기 오목부(4405,4505)에 대하여 외부적으로 실질적으로 돌출하지 않는다.
다양한 실시예에서, 상기 임플란트 바디(1202)는, 팽창가능한 물질(407)이 유체를 흡수하거나 또는 유지함에 따른 임플란트 바디(1202)의 적어도 부분적인 외측 변형을 허용하기 위하여, 실리콘, 폴리우레탄 또는 기타 우레탄계 물질, 또는 비-생분해성, 부분적 생분해성 또는 생분해성 (즉, 신체 내 부식성) 아크릴산과 같은 탄성 물질을 포함할 수 있다. 일부 실시예에서, 임플란트 바디(1202)의 상이한 부분들이 상이한 재료로 이루어질 수 있다. 예를 들어, 제1 부분(1204)은 보다 강성이고 덜 팽창가능한 물질을 포함할 수 있고, 제2 부분(1206)은 더 탄성 물질을 포함할 수 있다. 상기 제2 부분(1206)은 또한 유체 투과성 물질을 포함하여 유체가 팽창가능한 물질(4407) 내로 더 잘 침투하도록 촉진시키거나 허용할 수 있다. 임의로, 상기 팽창가능한 부재(4407)를 둘러싸는 제2 부분(1206)의 벽 두께는 더 얇게 형성되어, 팽창가능한 부재(4407)가 유체를 흡수 또는 유지함에 따른 외측 변형을 촉진시킬 수 있다.
도 44b 및 도 45b에 도시되는 바와 같이, 팽창가능한 물질(4407)은 비-팽창된 건조 상태일 수 있으며, 이는 누점을 통한 누소관 내로의 삽입을 보조할 수 있다. 누소관 내에 배치되면, 팽창가능한 물질(4407)은 오목부(4405,4505)의 구멍을 통하여 또는 상기 물질(4407)을 둘러싸는 제2 부분(1206)의 유체 투과성 물질 또는 그 안의 루멘을 통하여, 소관 또는 기타 체액을 흡수하거나 유지할 수 있다. 일부 실시예에서, 상기 팽창가능한 물질(4407)은 비-생분해성 물질을 포함할 수 있다. 일부 실시예에서, 상기 팽창가능한 물질(4407)은 생분해성 물질을 포함할 수 있다. 상기 팽창가능한 물질(4407)의 다른 옵션을 또한 이용할 수 있다. 예를 들어, 상기 팽창가능한 물질(4407)은 임플란트 바디(1202)와 단일 조각으로 몰딩되거나, 별도로 형성되고 상기 임플란트 바디(1202)에 연이어 결합되거나, 또는 그 안에 배치될 수 있다.
상기 팽창가능한 물질(4407)의 바람직한 팽창 특성은 적합한 물질 배치 및 가공을 통하여 달성될 수 있다. 일부 실시예에서, 하이드로겔과 같은 팽창가능한 물질을 높은 드로-다운(draw-down) 비율로 압출하여 상기 오목부(4405,4505) 내에 피팅되도록 구성되는 규모(예를 들어, 약 0.3 mm의 직경)를 가지게 한다. 높은 드로-다운 비율로 형성되는 압출은 세로 팽창보다 큰 직경 팽창을 가질 수 있는 것으로 밝혀졌다. 일부 실시예에서, 상기 팽창가능한 물질(4407)은, 직경 팽창보다 더 큰 세로 팽창과 같은, 원하는 팽창 특성을 초래하는 것으로 밝혀진 온도 및 압력에서 몰딩된다. 예를 들어, 일부 실시예에서, 상기 팽창가능한 물질(4407)은 임플란트시 오목부(4405,4505) 밖으로 팽대부 내로 측면 팽창하도록 구성되고 배치되어, 누점 내 눈물 임플란트의 유지를 보조한다. 상기 팽창가능한 물질(4407)의 측면 팽창은 제1 부분(1204)의 근위 말단에서 캡(1208) 또는 기타 돌출부가 누점과 동일 평면 에 있도록 할 수 있는 것으로 밝혀졌다. 일 실시예에서, 상기 팽창가능한 물질(4407)은 그 "건조" 부피의 약 1 배, 그 "건조" 부피의 약 10 배, 또는 그 "건조" 부피의 약 20 배 이하의 팽창 성능을 허용할 수 있다.
임플란트시 상기 오목부(4405,4505) 내 팽창가능한 물질(4407)의 팽창은 임플란트 바디 제1 부분(1204)과 임플란트 바디 제2 부분(1206) 상의 경사진 교차 지점(4450)을 록킹하여 누점 내 눈물 임플란트의 유지를 보조할 수 있는 것으로 밝혀졌다. 상기 오목부(4405,4505) 내 다양한 방향으로 팽창가능한 물질(4407)이 팽창함에 따라, 임플란트 바디(1202)의 일부가 더 커짐에 따라 외측으로 덜 탄성으로 되는 것으로 믿어진다.
도 44b 및 도 45b에 도시되는 바와 같이, 눈물 임플란트는 약물 방출 또는 기타 제제 방출 인서트(예를 들어, 약물 코어)를 수용하도록 구성되는 제1 공동 또는 오목부(4418) 및 제2 오목부(4405,4505) 사이의 격막(4430)을 포함할 수 있다. 상기 격막(4430)은 팽창가능한 물질(4407)의 약물 인서트 수용 오목부(4418) 내로의 팽창을 억제 또는 방지하기 위하여 사용될 수 있다. 그러나, 일 실시예에서, 상기 격막(4430)은 약물 또는 기타 치료제가 인서트로부터 팽창가능한 물질(4407) 내로 및 이를 통하여 주변 소관 조직으로 이동하도록 하는 루멘 또는 다공성 부분을 포함하여, 전신 약물 또는 기타 제제 방출을 제공할 수 있다.
도 48a 내지 도 48e는 임플란트시 누소관 팽대부 내에 배치가능한 강성 유지 요소(4856), 타원형 잡을 수 있는 또는 기타 돌출부(4832)를 포함하고, 제1(4804) 또는 제2(4806) 임플란트 바디 부분 상에 중간 돌출부가 없는 눈물 임플란트(4800)의 예를 도시한다. 보다 구체적으로, 도 8a는 눈물 임플란트의 등축도를 도시하고, 도 48b는 눈물 임플란트의 측면도를 도시하고, 도 48c는 도 48b에 도시되는 커트라인 A-A를 따라 취해진 단면도를 도시하고, 도 48d는 눈물 임플란트의 상면도를 도시하고, 도 48e는 제1 부분(4806)의 근위 말단에서 보는 눈물 임플란트의 단면도를 도시한다. 도 48a 내지 도 48e의 실시예에서, 임플란트 바디(4802)는, 임플란트(4800)가 누점(208,210) 내로 완전히 임플란트될 때 누점 개구(212,214)(도 2)에 대하여 또는 이에 가까이 배치되도록 구성될 수 있는, 타원형 잡을 수 있는 또는 기타 돌출부(4832)를 포함한다. 상기 돌출부(4832)는 상기 임플란트(4800)가 누소관 내를 완전히 통과하는 것을 억제 또는 방지하거나, 임플란트 보조 간병인에게 촉각적 또는 시각적 피드백 정보를 제공할 수 있다. 일부 실시예에서, 상기 타원형은 약 1.36 밀리미터의 폭, 약 1.92 밀리미터의 길이, 및 약 0.30 밀리미터의 두께를 포함할 수 있다.
제2 임플란트 바디 부분(4806)의 근위 말단은, 눈물 임플란트가 임플란트될 때 누소관 팽대부(252)의 적어도 일부에 대하여 바이어스되도록 구성되는, 강성 유지 요소(4856)를 포함할 수 있다. 상기 유지 요소(4856)는 제2 바디 부분의 세로 확장기(4850)의 연장과 반대 방향으로 제1(4804) 및 제2(4806) 바디 부분 사이의 교차 지점으로부터 근위로 돌출한다. 일부 실시예에서, 상기 유지 요소(4856)는 약 0.44 밀리미터 근위로 돌출하고, 약 0.53 밀리미터의 높이 또는 두께를 가진다. 이러한 실시예에서, 상기 유지 요소(4856)는 보트 선체 형상을 포함하고, 삽입 도구에 의하여 잡을 수 있는 삽입 촉진 오목부(4875)를 포함할 수 있다. 팽대부(252) 내에 임플란트될 때, 상기 유지 요소(4856)는 상기 누점 개구(212,214)에 대하여 잡을 수 있는 또는 기타 돌출부의 배치의 고정을 보조할 수 있다.
다양한 실시예에서, 상기 제2 부분(4806)은 제1 부분(4804)의 길이의 4배 미만의 크기를 가지는 길이를 포함할 수 있다. 일 실시예에서, 상기 제2 부분(4806)은 약 10 밀리미터 미만의 길이를 포함하고, 세로 확장기(4850) 및 일정 직경부(4890)을 포함하는 구조를 가질 수 있다. 일부 실시예에서, 상기 임플란트 바디(4802)는 근위 말단(4808)에 가까이 배치되는 제1 공동(4818)을 포함한다. 이러한 실시예에서, 상기 제1 공동(4818)은 근위 말단(4808)으로부터 약 1.22 밀리미터 내측 연장하고, 약 0.56 밀리미터의 외부 직경을 가지는 제1 약물 방출 또는 기타 제제 방출 약물 인서트를 수용한다.
도 49a 내지 도 49f는 도 12의 임플란트와 같은 눈물 임플란트(4900)가 잡을 수 있는 또는 기타 돌출부(4932)가 유지 립(4990)을 포함하도록 변형되는 실시예를 도시한다. 상기 유지 립(4990)은 임플란트 바디 공동(4918) 내에 배치되는 약물 방출 또는 기타 제제 방출 약물 인서트의 배치를 고정하도록 구성될 수 있다. 보다 구체적으로, 도 49a는 눈물 임플란트의 등축도를 도시하고, 도 49b는 눈물 인플란트의 측면도를 도시하고, 도 49c는 도 49b에 도시되는 커트라인 A-A를 따라 취해진 단면도를 도시하고, 도 49d는 눈물 임플란트의 상면도를 도시하고, 도 49d는 제2 부분(4906)의 근위 말단에서 눈물 임플란트의 단면도를 도시하고, 도 49f는 도 49c의 부분 B-B의 확대도를 도시한다.
다양한 실시예에서, 상기 유지 립(4990)은 인서트 내 저장되는 약물 또는 기타 제제의 방출 속도에 감지 가능하게 영향을 미치지 않으면서 임플란트 바디 공동(4918) 내 배치되는 약물 인서트의 위치를 고정하도록 구성될 수 있다. 일부 실시예에서, 상기 유지 립(4990)은 약 0.05 밀리미터 (±0.02 밀리미터) 공동(4918)의 표면으로부터 내측 연장한다. 일부 실시예에서, 상기 유지 립(4990)은 약 0.05 밀리미터(±0.02 밀리미터)의 두께를 포함한다. 임플란트 공동(4918) 내 약물 인서트를 고정하기 위한 기타 옵션은 약물 인서트의 외표면과 공동의 표면 사이의 더 타이트한 개입 피트, 또는 인서트의 중간 또는 원위 부분에서 약물 인서트와 공동 사이의 중첩(예를 들어, 스냅 피트형) 디자인 중 하나 이상을 포함할 수 있다.
유지 립(4990)의 존재로 인하여, 임플란트 공동(4918) 내 완전히 배치되는 약물 인서트의 노출되고 외측을 향하는 표면은 제1 부분(4904)의 근위 말단(4908) 또는 제2 부분(4906)의 원위 말단(4910) 보다 약간 낮을 수 있다; 그러나, 이와 같이 낮은 배치는 인서트로부터 약물 또는 기타 제제 방출 속도를 조절하기 위하여 사용되는 임의의 유형의 기공을 창출하지 않으며 이를 의도하지 않는다.
도 50a 및 50b는 도 44a 내지 도 44c와 같은 (오목부 및 팽창가능한 물질을 제외하고) 눈물 임플란트(5000)가 환자 내 완전히 임플란트되기 전에 약물 인서트(5022)의 근위 표면이 임플란트의 근위 말단(5008) 위에 배치되도록 변형되는 예를 도시한다. 보다 구체적으로, 도 50a는 눈물 임플란트의 측면도를 도시하고, 도 50b는 도 50a의 커트라인 A-A를 따라 취해진 단면도를 도시한다.
일부 실시예에서, 약물 인서트(5022)의 근위 표면은 임플란트의 근위 말단(5008)에서 약 0.25 밀리미터(±0.05 밀리미터) 위에 배치될 수 있다. 상기 약물 인서트(5022)의 원위 말단 표면은 인서트를 수용하도록 구성되는 임플란트 바디 공동(5018)의 기부로부터 유사한 양 위에 배치될 수 있다. 이러한 방식으로, 약물 인서트(5022)의 노출된 부분이 누점을 통하여 누소관 내로 눈물 임플란트(5000)의 삽입을 촉진시키는데 이용될 수 있다. 그렇다면, 포스트-임플란트, 상기 약물 인서트(5022)는 공동(5018) 내에 완전히 또는 거의 완전히 들어갈 수 있다. 약물 인서트(5022)가 공동(5018) 내에 들어가므로, 공동 직경에 비하여 임의로 약간 더 큰 인서트 직경은 누소관의 일부에 대한 외부 임플란트 바디 표면의 바이어싱을 초래하여 추가적인 임플란트 고정을 제공할 수 있다.
도 51 및 52는 도 25a 및 도 25b와 마찬가지로, 누점(212,214)를 통하여 누소관(208,210)(도 2) 내로 삽입가능한 다른 눈물 임플란트(5100)를 예시한다. 본 실시예에서, 상기 눈물 임플란트(5100)는 제1(5104) 및 제2(5106) 부분을 포함하는 임플란트 바디(5102)를 포함하고, 제1 부분(5104)의 근위 말단(5108)으로부터 제2 부분(5106)의 원위 말단(5110)으로 연장할 수 있다. 상기 임플란트 바디는 누소관(208,210)의 해부구조 특징에 일반적으로 매치되는 형상을 포함하여 환자에게 편안함을 제공하고 유지를 고정할 수 있다. 일부 실시예에서, 제1(5104) 및 제2(5106) 부분 사이의 오목 형상은 소관 만곡(250)(도 2)의 반경과 실질적으로 동일한 반경을 포함한다.
특정 실시예에서, 유지 요소(5192)는 제2 임플란트 바디 부분(5106)의 원위 말단에 또는 이에 가까이 배치될 수 있다. 이러한 방식으로, 상기 임플란트(5100)는 보다 강성인 누골 영역 및 더 작고 더 깊은 누소관의 직경 영역을 활용하여 임플란트된 위치의 고정을 보조할 수 있다. 나아가, 눈으로부터 임플란트 주위에 루액 흐름은 원위에 위치하는 유지 요소(5192)의 근위 표면에 대한 힘을 발생시켜 임플란트 유지를 보조할 수 있다. 상기 유지 요소(5192)는 수동적 또는 능동적일 수 있다 (예를 들어, 하이드로겔 또는 기타 팽창가능한 물질을 이용하여). 일부 실시예에서, 상기 제2 임플란트 바디 부분(5106)은 약 6 내지 12 밀리미터, 예를 들어 약 10 밀리미터의 길이를 포함한다.
도 52는 하부 누점(214) 및 누소관(210) 내에 임플란트되는 눈물 임플란트(5100)의 개략도를 예시한다. 일부 실시예에서, 눈물 임플란트(5100)는 상부 누점(212) 및 누소관(208) 내에 임플란트될 수 있다. 도시되는 바와 같이, 제1 부분(5104)는 누점(214)을 통하여 누소관(210) 내로 삽입되고 누점 개구와 누소관 팽대부(252) 사이에 있도록 구성될 수 있으며, 제2 부분(5106)은 누점(214)을 통하여 누소관(210) 내로 삽입되고 상기 팽대부(252)와 누낭(204) 사이에 있도록 구성될 수 있다.
도 41, 도 42a 내지 도 42d, 도 43a 내지 도 43c, 도 44a 내지 도 44d, 도 45a 내지 도 45d, 도 48a 내지 도 48e, 도 49a 내지 도 49f, 및 도 50 내지 도 52 에 도시되고 이와 관련하여 기재되는 바와 유사한 규모 및 규모 변형을 본원 명세서를 통하여 기재되는 다른 실시예들에 적용할 수 있다.
도 53a 내지 도 53d는 구분된 약물 인서트(5322) 또는 하나 이상의 임플란트 바디(5302) 부분과 통합되는 약물 중 하나 또는 이들 모두를 포함하는, 누점 및 누소관 해부 구조 내에 유지되도록 구성되는 추가적인 눈물 임플란트(5300) 실시예를 예시한다. 상기 약물 인서트(5322) 내 저장되거나 임플란트 바디(5302) 내에 통합되는 약물 또는 기타 치료제는 눈, 비도 또는 내이 시스템 중 하나 이상에 원하는 속도로 서방출로 전달될 수 있다. 더 많은 양의 약물 또는 기타 치료제가 요구되는 경우, 그의 더 큰 용량으로 인하여 약물 인서트(5322)와 함께 또는 단독으로 임플란트 바디(5302)를 저장 메커니즘으로 사용할 수 있다.
도 53a, 도 53b 및 도 53c에 도시되는 바와 같은 일부 실시예에서, 제1 양의 치료제가 약물 인서트(5322) 내에 저장되고, 제2 양의 치료제가 임플란트 바디(5302) 내에 저장된다. 약물 적재는 임플란트 바디 물질의 경화 또는 강도에 부정적인 영향을 미칠 수 있으므로, 이와 같은 배열이 가장 큰 치료제 유지 성능을 제공하는 것으로 믿어진다. 따라서, 임플란트 바디(5302) 내에 적재되는 약물의 양은 제한될 것이다. 임의로, 약물 인서트(5322)는 인서트(5322)의 하나 이상의 부분을 덮는 시스체(5366)을 포함하지 않을 수 있으며, 그 결과, 임플란트 바디(5302)와 인서트(5322) 사이의 약물 또는 치료제 확산이 가능하다.
도 53d에 도시되는 바와 같은 일부 실시예에서, 임플란트 바디(5302)는 구분된 약물 방출 또는 기타 제제 방출 인서트를 수용하기 위한 하나 이상의 공동 또는 기타 공극을 포함하지 않는다는 점에서 실질적으로 고체이다. 그 대신, 상기 임플란트 바디(5302)는 하나 이상의 바디 부분을 통하여 통합되는 하나 이상의 약물 또는 기타 제제를 수용하도록 구성될 수 있다. 이러한 방식으로, 전체 임플란트 바디(5302) 또는 그 일부가 약물 방출 또는 기차 제제 방출 인서트로서 작용할 수 있으며, 임플란트 바디(5302) 부분을 둘러싸는 불투과성 또는 실질적으로 불투과성 커버 (예를 들어, 패릴렌 커버) 내 미리 형성된 개구를 이용하여 치료제 방출을 지시할 수 있다. 다른 실시예에서, 투과성 커버 재료를 사용하여 약물 또는 기차 제제 방출을 허용할 수 있다.
코팅 물질(5396)을 원하는 방출 속도 및 방향에 따라 하나 외부 임플란트 바디 표면의 하나 이상의 부분에 다양한 두께로 적용할 수 있다. 도 53a에 도시되는 바와 같은 일부 실시예에서, 코팅 물질(5396)이 근위 말단(5308)에 위치하는 잡을 수 있는 또는 기타 돌출부의 표면을 제외한 대부분의 임플란트 바디 표면에 적용된다. 도 53b에 도시되는 바와 같은 일부 실시예에서, 코팅 물질(5396)이 대부분의 임플란트 바디 표면에 적용되나, 약물 인서트(5322)의 노출 표면을 덮지 않는다. 도 53c에 도시되는 바와 같은 일부 실시예에서, 제1 두께 (예를 들어, 약 5-6㎛)를 가지는 코팅 물질(5396)이 대부분의 임플란트 바디 표면에 적용되고, 제2 두께 (예를 들어, 약 1㎛)를 가지는 코팅 물질(5398)이 임플란트 바디(5302) 및/또는 약물 인서트(5322)의 근위 표면(5398)에 적용된다.
일부 바람직한 코팅 물질은 패릴렌, 세라믹 및 실버인 것으로 믿어지며, 이들 모두 우수한 유연성을 보인다. 일부 실시예에서, 패릴렌 코팅 물질이 사용되며, 비교적 낮은 온도에서 임플란트 바디 위에 유리하게 증착될 수 있다.
실험예
도 44a 내지 도 44c, 및 도 45a 내지 도 45c의 본 발명의 눈물 임플란트를 보다 완전히 이해하기 위하여, 이하 실시예가 제한이 아닌 예시로 제공된다.
실험예
1:
도 46은 임플란트 바디 제2 부분의 근위 말단으로부터 연장하는 오목부를 포함하는 눈물 임플란트를 예시한다. 상기 오목부에 내에, 팽창가능한 하이드로겔 물질이 배치된다. 유체가 상기 하이드로겔 물질에 의하여 수용되도록 하기 위하여, 상기 오목부의 구멍이 좌측 개방된다.
(4602)에서, 하이드로겔 물질 및 이를 부분적으로 둘러싸는 임플란트 바디가 30 분 수화 시간에서 도시된다. (4604)에서, 상기 하이드로겔 물질 및 이를 부분적으로 둘러싸는 임플란트 바디가 120 분의 수화 시간에서 도시된다. (4606)에서, 상기 하이드로겔 물질 및 이를 부분적으로 둘러싸는 임플란트 바디가 240 분의 수화 시간에서 도시된다. (4608)에서, 상기 하이드로겔 물질 및 이를 부분적으로 둘러싸는 임플란트 바디가 1440 분의 수화 시간에서 도시된다. 도시되는 바와 같이, 하이드로겔 물질의 팽창은 임플란트 바디, 특히 임플란트 바디의 제2 부분의 주변부가 소관 벽의 크기 및 형상으로 외측 팽창하도록 하여 임플란트의 원하는 위치를 고정적으로 유지한다. 나아가, 하이드로겔 물질의 팽창은 임플란트 바디 제1 부분과 임플란트 바디 제2 부분 사이의 경사진 교차 지점을 약물 방출 또는 기타 제제 방출 인서트(예를 들어, 약물 코어)를 보유하는 제1 공동 또는 오목부와 하이드로겔 물질을 보유하는 제2 오목부를 분리시키는 격막에 대하여 압착함으로써 록킹한다.
실험예
2:
도 47은 임플란트 바디 제2 부분의 근위 말단으로부터 연장하는 오목부를 포함하는 눈물 임플란트를 예시한다. 상기 오목부 내에, 팽창가능한 하이드로겔 물질이 배치된다. 유체가 상기 하이드로겔 물질에 의하여 수용되도록 하기 위하여, 상기 오목부의 구멍이 좌측 개방된다.
이 실시예에서, 상기 하이드로겔 물질은 임플란트시 오목부 밖으로 및 팽대부와 같은 영역(4770) 내로 측면 팽창하여 누점 내에 눈물 임플란트의 유지를 보조하도록 구성되고 배치된다. 도시되는 바와 같이, 하이드로겔 물질의 측면 팽창은 상기 제1 부분의 근위 말단에서 캡 또는 기타 돌출부가 누점과 같은 표면(4772)과 동일 평면에 있도록 한다.
시스체
실시예
:
다양한 방식으로, 시스체는 약물 또는 기타 치료제의 구분된 약물 인서트 또는 통합되는 약물 또는 기타 제제를 포함하는 임플란트 바디로부터 이동을 조절하기 위한 적합한 형상 및 물질을 포함할 수 있다. 일부 실시예에서, 상기 시스체는 누점 또는 누소관의 해부 구조와 같은 임플란트 해부 구조에 순응하도록 구성된다. 일부 실시예에서, 상기 시스체는 적어도 부분적으로 약물 인서트를 덮거나 둘러싸고, 매트릭스/제제 혼합물의 외표면에 대하여 꼭 맞을 수 있다. 다른 실시예에서, 상기 시스체는 하나 이상의 통합되는 제제를 포함하는 임플라트 바디의 일부를 덮거나 둘러싼다. 상기 시스체는 약물 또는 기타 치료제에 실질적으로 불투과성인 물질로 이루어져, 약물 또는 제제의 이동 속도가 상기 시스체에 의하여 덮이지 않은 임플란트 바디 또는 약물 인서트의 노출된 표면 영역에 의하여 크기 조절된다. 많은 실시예에서, 시스체를 통한 제제의 이동은 약물 인서트의 노출 표면을 통한 제제의 이동의 약 10분의 1 이하일 수 있다.
적합한 시스체 물질은, 무엇보다도, 폴리이미드, 폴리에틸렌테레프탈레이트 (PET), 또는 패릴렌을 포함할 수 있다. 상기 시스체는 외부 매트릭스/제제 혼합물 표면에 인접하는 시스 표면으로부터 상기 외표면으로부터 멀어지는 반대 시스 표면까지 정의되는, 약 0.00025 인치 내지 약 0.0015 인치의 두께를 가질 수 있다. 약물 인서트를 가로질러 연장하는 시스의 총 직경은 약 0.2 밀리미터 내지 약 1.2 밀리미터일 수 있다. 상기 약물 인서트는 매트릭스를 상기 시스체 내에 딥 코팅함으로써 형성될 수 있다. 일부 실시예에서, 상기 시스체는 상기 매트릭스/제제 혼합물이 도입되는 튜브를 포함할 수 있다. 상기 시스체는 또한 상기 매트릭스/제제 혼합물 주위에 딥 코팅, 예를 들어, 미리 형성된 매트릭스/제제 코어 또는 임플란트 바디 주위에 딥 코팅될 수 있다.
상기 시스체는 예를 들어 본원에 논의되는 눈물 임플란트의 임상적 이용을 촉진시키기 위한 하나 이상의 부가적인 특징을 구비할 수 있다. 예를 들어, 상기 시스는 즉석에서 상호교환가능한 약물 인서트를 수용할 수 있는 반면, 상기 임플란트 바디는 환자 내 임플란트된 채로 유지된다. 일부 실시예에서, 상기 시스체는 압착될 때 시스체에 힘을 적용하는 하나 이상의 외부 돌출부를 구비할 수 있으며, 이는 매트릭스/제제 혼합물이 상기 시스체로부터 나오도록 한다. 그 다음, 대체 약물 인서트를 상기 시스체 내에 배치할 수 있다.
치료제
실시예
치료제 (또는 단순히 "제제")는, 무엇보다도, 다음 중 하나 또는 이들의 조합 또는 그 균등물, 유도체 또는 유사체로 이루어지는 약물을 포함할 수 있다: 항녹내장약 (예를 들어, 아드레날린 작용제, 아드레날린 길항제 (베타 블록커), 탄산 탈수효소 저해제 (CAIs, 전신 및 국소적), 부교감신경흥분제, 프로스타글란딘 및 혈압강하 지질, 및 이의 조합), 항미생물제 (예를 들어, 항생체, 항바이러스제, antiparacytic, 항진균제, 등), 코르티코스테로이드 또는 기타 소염제 (예를 들어, NSAID 또는 진통제 및 통증 관리 화합물), 충혈 완화제 (예를 들어, 혈관 수축제), 알레르기 반응을 예방 또는 변경하는 제제 (예를 들어, 항히스타민, 사이토카인 억제제, 류코트리엔 억제제, IgE 억제제, 면역조절제), 매스트 세포 안정화제, 조절마비제, 산동제 등.
유용한 제제의 예는 이에 제한되지 않으나 다음을 포함한다: 트롬빈 억제제; 항혈전제; 혈전용해제; 섬유소용해제; 혈관 경련 억제제; 혈관확장제; 항고혈압제; 항생제 (테트라사이클린, 클로르테트라사이클린, 바시트라신, 네오마이신, 폴리믹신, 그라미시딘, 세팔렉신, 옥시테트라사이클린, 클로르암페니콜, 리팜피신, 시프로플록사신, 토브라마이신, 겐타마이신, 에리트로마이신, 페니실린, 술폰아미드, 술파디아진, 술파세트아미드, 술파메티졸, 술피속사졸, 니트로푸라존, 소듐 프로피오네이트와 같은), 항진균제 (암포테리신 B 및 미코나졸과 같은), 및 항바이러스제 (이독수리딘 트리플루오로티미딘, 아시클로비르, 간시클로비르, 인터페론)와 같은 항미생물제; 표면 당단백질 수용체의 억제제; 항혈소판제; 항유사분열제; 미세소관 억제제; 항분비제; 활성 억제제; 리모델링 억제제; 안티센스 뉴클레오티드; 대사길항제; 증식억제제 (혈관생성억제제를 포함); 항암 화학요법제; 소염제 (히드로코르티손, 히드로코르티손 아세테이트, 덱사메타손 21-포스페이트, 플루오시놀론, 메드리손, 메틸프레드니솔론, 프레드니솔론 21-포스페이트, 프레드니솔론 아세테이트, 플루오로메탈론, 베타메타손, 트리암시놀론, 트리암시놀론 아세토나이드와 같은); 비-스테로이드계 소염제 (NSAIDs) (살리실레이트, 인도메타신, 이부프로펜, 디클로페낙, 플루르비프로펜, 피록시캄 인도메타신, 이부프로펜, 낙소프렌, 피록시캄 및 나부메톤과 같은). 본 발명의 눈물 임플란트와 함께 사용이 고려되는 소염제 스테로이드는, 트리암시놀론 아세토나이드 (일반명), 및 예를 들어, 트리암시놀론, 덱사메타손, 플루오시놀론, 코르티손, 프레드니솔론, 플루메톨론, 및 그 유도체를 포함하는 코르티코스테로이드; 항알레르기 물질 (소듐 크로모글리케이트, 안타졸린, 메타피릴린, 클로르페니라민, 세트리진, 피릴아민, 프로페닐피리다민과 같은); 증식억제제 (1,3-시스 레티노익산, 5-플루오로우라실, 탁솔, 라파마이신, 미토마이신 C 및 시스플라틴과 같은); 충혈완화제 (페닐에프린, 나파졸린, 테트라히드라졸린과 같은); 축동제 및 항콜린에스테라아제 (필로카르핀, 살리실레이트, 카르바콜, 아세틸콜린 클로라이드, 피소스티그민, 에세린, 디이소프로필 플루오로포스페이트, 포스폴린 요오딘, 데메카륨 브로마이드와 같은); 항종양약 (카르무스틴, 시스플라틴, 플루오로우라실5과 같은); 면역약 (백신 및 면역 자극제와 같은); 호르몬제 (에스트로겐, 에스트라디올, 프로게스테론성, 프로게스테론, 인슐린, 칼시토닌, 부갑상성 호르몬, 펩타이드 및 바소프레신 시상하부 방출 인자와 같은); 면역억제제, 성장호르몬 길항제, 성장인자 (표피성장인자, 섬유아세포 성장인자, 혈소판 유도 성장 인자, 형질전환 성장인자 베타, 소마토트로핀, 피브로넥틴과 같은); 혈관생성 억제제 (안지오스타틴, 아네코르바트 아세테이트, 트롬보스폰딘, 항-VEFG 항체); 도파민 작용제; 방사요법제; 펩타이드; 단백질; 효소; 세포외 기질; 성분; ACE 억제제; 자유라디칼 스캐빈저; 킬레이터; 항산화제; 중합효소 억제제; 광역학 치료제; 유전자 치료제; 및, 티몰롤, 베탁솔롤, 레보부놀롤, 아테놀롤, 및, 비마토프로스트, 트라보프로스ㅌ, 라타노프로스트 등과 같은 프로스타글란딘 유사체와 같은 베타 블록커를 포함하는 항녹내장약을 포함하는 프로스타글란딘, 안티프로스타글란딘, 프로스타글란딘 전구체와 같은 기타 치료제; 아세트아졸아미드, 도르졸라미드, 브린졸라미드, 메타졸아미드, 디클로르페나미드, 디아목스와 같은 탄산탈수효소 저해제; 및 루베졸, 니모디핀 및 관련 화합물과 같은 신경보호제; 필로카르핀, 카르바콜, 피소스티그민 등과 같은 부교감신경흥분제를 포함한다.
본 발명의 눈물 임플란트와 함께 사용가능한 부가적인 제제는, 이에 제한되지 않으나, 미국 연방 식품 의약품 및 화장품법 505조 하에 또는 공중보건법 하에 승인된 약을 포함하며, 이들 중 일부는 미국 식품의약국(FDA) 웹사이트: http://www.accessdata.fda.gov/scripts/cder/drugsatfda/index 에서 찾을 수 있다. 본 발명의 눈물 임플란트는 또한 종이 또는 전자 형태의 오렌지북에 열거되는 약과 함께 사용할 수 있으며, 이는 본원의 출원일과 동일자, 이보다 빠른 일자 또는 이후의 일자를 가지거나 기록하는 FDA Orange Book 웹사이트: (http://www.fda.gov/cder/ob/)에서 찾을 수 있다. 예를 들어, 이러한 약물은, 무엇보다도, 도르졸라미드, 올로파타딘, 트라보프로스트, 비마토프로스트, 시클로스포린, 브리모니딘, 목시플록사신, 토브라마이신, 브린졸라미드, 아시클로비르 티몰롤 말레이트, 케토롤락 트로메타민, 프레드니솔론 아세테이트, 소듐 히알루로네이트, 네파페낙, 브롬페낙, 디클로페낙, 플루르비프로펜, 수프로페낙, 비녹산, 파타놀, 덱사메타손/토브라마이신 조합, 목시플록사신, 또는 아시클로비르를 포함할 수 있다.
상기 열거된 제제를 이용하여 치료될 수 있는 질병 또는 장애의 예는 이에 제한되지 않으나, 녹내장, 수술전 및 수술후 안구 치료, 안구건조증, 항-눈 알레르기, 항감염, 수술후 염증 또는 통증, 알레르기와 같은 호흡 관련 장애, 어지러움 또는 편두통과 같은 내이 장애, 또는 고혈압, 콜레스테롤 관리, 폐 장애 또는 면역 장애와 같은 전신 장애를 포함한다. 일부 실시예에서, 상기 치료제는 윤활제 또는 계면활성제, 예를 들어, 안구건조증을 치료하기 위한 윤활제를 포함할 수 있다. 다른 실시예에서, 상기 치료제는 눈으로부터 눈물을 흡수할 수 있는 흡수제를 포함할 수 있다.
약물 인서트
실시예
:
약물 인서트는 하나 이상의 약물 또는 기타 치료제, 및 일부 실시예에서, 약물 또는 기차 제제의 서방출을 제공하기 위한 하나 이상의 매트릭스 물질을 포함할 수 있다. 유사하게, 더 많은 양의 제제가 바람직한 경우, 임플란트 바디의 상당 부분은 하나 이상의 통합되는 약물 또는 기타 제제 및 상기 제제의 방출을 제공하도록 구성되는 매트릭스 물질을 포함한다.
상기 하나 이상의 약물 또는 기타 치료제는 적어도 부분적으로 매트릭스 내 약물 또는 제제의 용해도에 근거하여, 약물 인서트의 노출된 표면으로부터 표적 조직으로 이동할 수 있다. 약물 또는 제제의 노출된 표면으로부터의 이동 속도는 매트릭스 내 용해된 약물 또는 제제의 농도와 관련될 수 있다. 일부 실시예에서, 약물 인서트 내 용해되는 약물 또는 제제의 농도는 원하는 약물 또는 제제의 방출 속도를 제공하도록 조절될 수 있다. 부가적으로 또는 조합하여, 약물 또는 제제의 노출된 표면으로부터의 이동 속도는 실리콘 매트릭스 제제의 특성과 같은, 약물 또는 제제가 용해되어 있는 매트릭스의 하나 이상의 특성과 관련될 수 있다. 일부 실시예에서, 상기 약물 인서트 내 포함되는 약물 또는 제제는 액체, 고체, 고체 겔, 고체 결정, 무결정 고체, 고체 미립자 또는 용해된 형태를 포함할 수 있다. 이와 같은 일 실시예에서, 액체 라타노프로스트 액적 또는 고체 비마토프로스트 입자가 실리콘 매트릭스 내에 분산된다.
상기 약물 인서트는 하나 이상의 약물 또는 제제의 서방출을 제공할 수 있는 하나 이상의 생체적합성 물질을 포함할 수 있다. 상기 약물 인서트는 실질적으로 비-생분해성 실리콘 매트릭스과 그 안에 위치하는 용해가능한 약물 또는 제제 내포물을 포함하는 매트릭스를 포함하는 실시예에 대하여 주로 앞서 논의되지만, 약물 인서트는 약물 또는 제제의 서방출을 제공하는 다른 구조, 예를 들어, 생분해성 매트릭스, 다공성 약물 인서트, 액체 약물 인서트 또는 고체 약물 인서트를 포함할 수 있다. 약물 또는 제제를 포함하는 매트릭스는 생분해성 또는 비-생분해성 폴리머로부터 형성될 수 있다. 일부 실시예에서, 비-생분해성 약물 인서트는 실리콘, 아크릴레이트, 폴리에틸렌, 폴리우레탄, 하이드로겔, 폴리에스테르 (예를 들어, E. I. Du Pont de Nemours and Company, Wilmington, Del로부터 DACRON.RTM), 폴리프로필렌, 폴리테트라플루오로에틸렌 (PTFE), 팽창 PTFE (ePTFE), 폴리에테르 에테르 케톤(PEEK), 나일론, 압출 콜라겐, 폴리머 발포체, 실리콘 고무, 폴리에틸렌 테레프탈레이트, 초고분자량 폴리에틸렌, 폴리카보네이트 우레탄, 폴리우레탄, 폴리이미드, 스테인레스 스틸, 니켈-티타늄 합급 (예를 들어, 니티놀), 티타늄, 코발트-크롬 합금 (예를 들어, Elgin Specialty Metals, Elgin, Ill로부터 ELGILOY.RTM. ; Carpenter Metals Corp., Wyomissing, Pa.로부터 CONICHROME.RTM.)을 포함할 수 있다. 일부 실시예에서, 생분해성 약물 인서트는 단백질, 하이드로겔, 플리글리콜산 (PGA), 폴리락트산 (PLA), 폴리(L-락트산) (PLLA), 폴리(L-글리콜산) (PLGA), 폴리글리콜라이드, 폴리-L-락타이드, 폴리-D-락타이드, 폴리(아미노산), 폴리디옥사논, 폴리카프로락톤, 폴리글루코네이트, 폴리락트산-폴리에틸렌 옥사이드 코폴리머, 개질 셀룰로오스, 콜라겐, 폴리오르토에스테르, 폴리히드록시부티레이트, 폴리안하이드라이드, 폴리포스포에스테르, 폴리(알파-히드록시산) 및 이의 조합과 같은, 하나 이상의 생분해성 폴리머를 포함할 수 있다. 일부 실시예에서, 상기 약물 인서트는 하이드로겔 폴리머를 포함할 수 있다.
클로징
노트:
무엇보다도, 눈의 누점 및 누소관 내 확고한 유지를 제공하는 눈물 임플란트 및 관련 방법이 논의된다. 상기 눈물 임플란트는 누점을 통하여 누소관 내로 적어도 부분적인 삽입을 위하여 구성되는 임플란트 바디를 포함할 수 있다. 상기 임플란트 바디는 제1 및 제2 부분을 포함할 수 있으며, 세로 근위축을 정의하는 제1 부분의 근위 말단으로부터 세로 원위축을 정의하는 제2 부분의 원위 말단으로 연장할 수 있다. 상기 임플란트 바디는, 일체형 확장기를 이용하여 임플란트될 때, 상기 근위축과 원위축 사이에 적어도 45 도 경사진 교차 지점이 존재하도록 구성될 수 있다. 이러한 방식으로, 상기 임플란트 바디의 적어도 일부가 소관 만곡에 또는 더 원위에 위치하는 누소관의 적어도 일부에 대하여 바이어싱되어, 해부 구조를 이용하는 눈물 임플란트의 임플란트된 위치를 유지할 수 있다. 다양한 실시예에서, 상기 눈물 임플란트는 임플란트 바디의 제1 부분 또는 제2 부분 중 적어도 하나 내에 배치되는 약물 인서트를 더 포함하여 약물 또는 기타 치료제의 눈으로의 서방출을 제공할 수 있다. 상기 약물 인서트는 임플란트 바디 공동 내 배치되는 구분되는 약물 코어, 또는 하나 이상의 임플란트 바디 부분을 통하여 약물 또는 기타 제제 입자의 혼합물, 또는 이들 모두를 포함할 수 있다.
유리하게, 일부 실시예에서, 본 발명의 눈물 임플란트는 눈물 흐름을 성공적으로 막거나, 수일 내지 수개월 내지 수년과 같은 다양한 기간 동안 약물 또는 기타 치료제의 눈, 비도, 또는 내이로의 지속적 전달을 제공할 수 있다. 또한, 임의로 제1 및 제2 임플란트 바디 공동 또는 약물 방출 임플란트 바디 부분을 포함함으로써, 이중 약물 또는 기타 제제 방출 프로파일이 가능할 수 있다. 예를 들어, 두 개의 별개의 약물이 두 개의 상이한 임플란트 위치로부터 방출될 수 있다. 나아가, 본 발명의 임플란트 바디의 구조를 유지하는 소관 만곡은 누점 및 누소관의 과도한 신장 및 부주의하게 임플란트가 빠지는 것을 감소시킬 수 있다. 본 발명의 눈물 임플란트는, 그러할 필요는 없으나, 팽창가능한 코팅 또는 기타 팽창가능한 유지 물질을 임플란트 바디 내에 적용하여 다양한 크기의 공동 조직 구조에 대하여 피칭되도록 할 수 있으므로, 한 사이즈가 널리 적용될 수 있도록 실행될 수 있다. 본 발명의 눈물 임플란트의 팽창가능한 성질은, 상기 임플란트의 유지 특징 중 일부가 임플란팅 후에 활성화될 수 있으므로, 보다 용이한 임플란팅을 허용할 수 있다.
본 발명의 눈물 임플란트는 또한 예를 들어 제1 임플란트 부분의 근위 말단에서 캡형 돌출부, 제2 임플란트 부분의 근위 말단에서 힐-형 유지 돌출부, 또는 제1 또는 제2 임플란트 부분 상에 하나 이상의 중간 또는 원위에 위치하는 돌출부의 조합으로 인하여, 환자의 누점 및 누소관 내에 더 잘 유지될 수 있다. 앞서 논의한 바와 같이, 상기 캡형 돌출부는 임플란트가 누점 아래로 누소관 내로 완전히 이동하는 것을 억제할 수 있다. 상기 중간, 원위의 힐-형 돌출부는 간병인이 이를 제거할 때까지 임플란트를 제 위치에 유지하는 것을 보조할 수 있다.
상세한 설명은 그 일부를 형성하는 첨부 도면에 대한 참조를 포함한다. 도면은 예시적으로 본 발명이 실행될 수 있는 특정 구현예들을 도시한다. 이들 구현예들은 또한 본원에서 "실시예"로도 언급된다. 본원에 언급되는 모든 공개 문헌, 특허, 및 특허 문헌들은 참조로 개별적으로 포함되나 본원에 참조로 그 전체가 포함된다. 본원과 상기 문헌들 사이에 모순되는 사용이 있는 경우, 포함되는 참조 문헌에서의 사용은 본원에 대하여 추가적인 것으로 고려될 것이다; 양립불가능한 불일치에 대해서는, 본원의 사용으로 제한한다.
본원 명세서에서, 특허 문헌에 통상적인 단수가 사용되며, 이는 "적어도 하나" 또는 "하나 이상"의 사용 또는 다른 예와 독립적으로, 하나 또는 하나 이상을 포함한다. 본원에 사용되는 용어 "또는"은 달리 기재하지 않는 한 "A 또는 B"는 "A 그러나 B가 아닌", "B 그러나 A가 아닌", 및 "A 및 B"를 포함하는 비-독점적 표현이다. 본원에 사용되는 용어 "약"은 대략, 거의, 또는 소정량 근처인 양을 의미한다.
본원에 사용되는 용어 "근위"는 눈의 각막에 상대적으로 가까운 위치를 의미하고, 용어 "원위는 각막으로부터 상대적으로 멀고 누소관 내로 더 깊게 삽입되는 위치를 의미한다.
본원 명세서에서, 용어 "하이드로겔"은 고흡수성 폴리머, 하이드로콜로이드 및 수-흡수성 친수성 폴리머와 같은 흡수 또는 유지 물질 (예를 들어, 흡수 물질)을 의미한다. 본 발명의 눈물 임플란트와 함께 사용하기 위한 하이드로겔의 에는, 무엇보다도, 친수성, 지방족 및 폴리에테르계 열가소성 폴리우레탄과 같은 지방족 열가소성 폴리우레탄 (TPU)을 포함한다. 적합한 열가소성 폴리우레탄은 상품명 Tecophilic 하에 Lubrizol Corporation of Cleveland, Ohio로부터 상용가능한 것들을 포함한다. 특정 적용에서, 상품명 "Tecophilic TG-500" (또는 단순히 "TG-500") 및 "Tecophilic TG-2000" (또는 단순히 "TG-200") 하에 상용 가능한 하이드로겔을 이용할 수 있다. 용어 "하이드로겔"은, 하이드로겔이 팽창되지 않고 물 중량을 더 적게 함유하거나 함유하지 않을 때와 같은, "건조" 상태의 고흡수성 폴리머 입자를 의미할 수 있다. 상기 용어 "하이드로겔"은 또한 수화되거나 팽창된 상태의 고흡수성 폴리머 입자, 예를 들어, 물 내 몇백 배 그 중량과 같은 (예를 들어, 물 내 약 500 배의 그 중량을 흡수할 수 있는 TG-500, 및 물 내 약 2000 배의 그 중량을 흡수할 수 있는 TG-2000), 물 내 적어도 그 중량으로 흡수된 하이드로겔을 의미할 수 있다. 하이드로겔 물질은 유체를 흡수하므로, 그 크기가 증가할 수 있고 (예를 들어, 팽창), 그 형상이 누소관 벽 또는 누소관 팽대부의 적어도 일부에 대하여 바이어스되도록 또는 이에 대하여 주위 물질을 바이어싱하도록 변화할 수 있다.
첨부하는 청구범위에서, 용어 "포함하는"은 비-제한적이다; 즉, 청구항 내 이와 같은 용어 앞에 열거되는 것들 외의 구성 요소들을 포함하는 시스템, 어셈블리, 장치, 물품 또는 공정이 그 청구항의 범위 내에 속하는 것으로 간주된다. 또한, 이하 청구범위에서, 용어 "제1", "제2" 및 "제3" 등은 단지 라벨로서 사용되며, 그 대상에 대한 수적 요건을 부과하고자 하는 것이 아니다.
상기한 발명의 상세한 설명은 예시적인 것을 의도하는 것이며, 제한적이 아니다. 예를 들어, 상기 실시예들 (또는 이들의 하나 이상의 특징들)은 서로 조합하여 사용될 수 있다. 그 예로서, 도시되거나 기재되는 다양한 임플란트 구현예로부터 하나 이상의 규모를 함께 배열하여 원하는 약물 농도를 제공할 수 있는 임플란트 구현예를 형성할 수 있다. 상기 기재를 읽은 후 당업자에 의하여 다른 구현예들이 사용될 수 있다. 또한, 상기 상세한 설명에서, 다양한 특징들을 함께 조합하여 본원의 개시를 간소화할 수 있다. 청구되지 않은 개시되는 특징이 어떠한 청구항에 필수적임을 의도하는 것으로 해석되지 말아야 한다. 그보다, 발명의 요지는 특히 개시되는 구현예의 특징들보다 훨씬 적을 수 있다. 따라서, 이하 청구범위는 상세한 설명에 포함되며, 각각의 청구항은 별개의 구현예를 구성한다. 본 발명의 범위는 첨부되는 청구범위와 그러한 청구범위에 대한 균등 범위를 참조로 하여 결정될 것이다.
37 C.F.R. §.72(b)에 따라 요약서가 제공되어 읽는 사람이 기술적 개시의 특징을 신속히 확인할 수 있도록 한다. 이는 청구항의 범위 또는 의미를 해석하거나 제한하는데에 이용되지 않을 것이다.
Claims (51)
- 제1 및 제2 부분을 포함하고, 상기 제1 부분의 근위 말단으로부터 상기 제2 부분의 원위 말단으로 연장하는 임플란트 바디
를 포함하는 누소관 내로 삽입가능한 눈물 임플란트로서,
상기 제1 부분의 근위 말단은 세로 근위축을 정의하고, 그 원주 주위로 비-등거리로 측면으로 돌출하는 유지 돌출부를 포함하고;
상기 제2 부분의 원위 말단은 세로 원위축을 정의하고; 및
상기 임플란트 바디는, 누소관 내에 임플란트될 때, 소관 만곡에 또는 더 원위에 위치하는 누소관의 적어도 일부에 대하여 상기 임플란트 바디의 적어도 일부를 바이어싱하기 위한, 상기 근위축과 상기 원위축 사이에 경사진 교차지점이 존재하도록 구성되는 것을 특징으로 하는 눈물 임플란트. - 제1항에 있어서,
상기 제1 부분의 유지 돌출부의 근위 말단은 그 원주 주위로 비-등 측면 거리로 외측으로 측면 돌출하고, 상기 제1 부분의 원위 말단의 외부 직경으로 가늘어지는 것을 특징으로 하는 눈물 임플란트. - 제2항에 있어서,
상기 제1 부분의 근위 말단으로부터 적어도 부분적으로 연장하고, 상기 임플란트 바디가 임플란트될 때 누점에 대하여 또는 이에 가까이 배치되도록 구성되는 잡을 수 있는 돌출부를 포함하며,
상기 제1 부분의 유지 돌출부의 근위 말단은 상기 잡을 수 있는 돌출부의 둘레와 수적으로 대략 동일한 둘레를 포함하는 것을 특징으로 하는 눈물 임플란트. - 제2항에 있어서,
상기 제1 부분의 유지 돌출부의 근위 말단은 마주보는 제3 및 제4 면 상에서 외부 직경으로부터 밖을 향하여 돌출됨이 없이 마주보는 제1 및 제2 면 상에서 마주보는 방향으로 외부로 돌출되는 것을 특징으로 하는 눈물 임플란트. - 제1항에 있어서,
하나 이상의 치료제를 추가로 포함하는 눈물 임플란트. - 제5항에 있어서,
상기 하나 이상의 치료제는 상기 제1 부분 내에 적어도 부분적으로 배치되며 상기 하나 이상의 치료제의 서방출을 전달하도록 구성되는 약물 인서트 내에 제공되는 것을 특징으로 하는 눈물 임플란트. - 제1항의 눈물 임플란트, 및 안질환 치료를 위하여 상기 눈물 임플란트를 사용하기 위한 설명서를 포함하는 키트.
- 제1 및 제2 부분을 포함하고, 상기 제1 부분의 근위 말단으로부터 상기 제2 부분의 원위 말단으로 연장하는 임플란트 바디
를 포함하는 누소관 내로 삽입가능한 눈물 임플란트로서,
상기 제1 부분의 근위 말단은 세로 근위축을 정의하고;
상기 제2 부분의 원위 말단은 세로 원위축을 정의하고, 그 원주 주위로 측면 돌출되는 유지 돌출부를 포함하며, 상기 유지 돌출부는 상기 유지 돌출부의 근위 말단 또는 상기 유지 돌출부의 원위 말단 중 하나에서 외부를 향하는 측면 스텝을 포함하고; 및
상기 임플란트 바디는, 누소관 내에 임플란트될 때, 소관 만곡에 또는 더 원위에 위치하는 누소관의 적어도 일부에 대하여 상기 임플란트 바디의 적어도 일부를 바이어싱하기 위한, 상기 근위축과 상기 원위축 사이에 경사진 교차지점이 존재하도록 구성되는 것을 특징으로 하는 눈물 임플란트. - 제8항에 있어서,
상기 측면 스텝은 상기 제2 부분이 연장하는 방향에 수직 방향으로 외측으로 측면 연장하며, 상기 측면 스텝은 약 0.14 mm 이상인 것을 특징으로 하는 눈물 임플란트. - 제8항에 있어서,
상기 측면 스텝은 상기 유지 돌출부의 근위 말단에 배치되며, 상기 유지 돌출부의 원위 말단에서 상기 제2 부분의 외부 직경으로 가늘어지는 것을 특징으로 하는 눈물 임플란트. - 제10항에 있어서,
상기 유지 돌출부의 원위 말단은 상기 임플란트 바디의 누소관 내로의 삽입을 촉진시키기 위한 일체형 확장기를 포함하는 것을 특징으로 하는 눈물 임플란트. - 제8항에 있어서,
하나 이상의 치료제를 추가로 포함하는 눈물 임플란트. - 제12항에 있어서,
상기 하나 이상의 치료제는 상기 제1 부분 내에 적어도 부분적으로 배치되며 상기 하나 이상의 치료제의 서방출을 전달하도록 구성되는 약물 인서트 내에 제공되는 것을 특징으로 하는 눈물 임플란트. - 제13항에 있어서,
상기 약물 인서트는 상기 하나 이상의 치료제를 적어도 약 44 마이크로그램 포함하는 것을 특징으로 하는 눈물 임플란트. - 제13항에 있어서,
상기 약물 인서트는 상기 하나 이상의 치료제를 적어도 약 81 마이크로그램 포함하는 것을 특징으로 하는 눈물 임플란트. - 제8항의 눈물 임플란트, 및 안질환 치료를 위하여 상기 눈물 임플란트를 사용하기 위한 설명서를 포함하는 키트.
- 누소관의 수직 단면 내에 배치가능한 근위 말단부로부터 상기 누소관의 수평 단면 내에 배치가능한 원위 말단부로 비선형 연장하며, 그들 사이의 중간부를 가지는 임플란트 바디
를 포함하는 누소관 내로 삽입하기 위한 눈물 임플란트로서,
상기 중간부는 상기 근위 말단부를 향하여 제1 방향으로 부분적으로 연장하고, 상기 원위 말단부를 향하여 제2 방향으로 부분적으로 연장하고;
상기 중간부는 팽창가능한 물질을 저장하는 오목부를 포함하고, 상기 팽창가능한 물질은 상기 임플란트 바디가 임플란트될 때 누소관 팽대부를 향하여 상기 제2 방향과 실질적으로 반대인 제3 방향으로 부분적으로 팽창하도록 구성되는 것을 특징으로 하는 눈물 임플란트. - 제17항에 있어서,
상기 팽창가능한 물질은 하이드로겔을 포함하는 것을 특징으로 하는 눈물 임플란트. - 제17항에 있어서,
상기 팽창가능한 물질은, 상기 임플란트 바디가 임플란트될 때, 상기 제2 방향에 대하여 측면으로 부분적으로 팽창하고, 상기 측면 팽창은 상기 누소관 벽에 대하여 상기 임플란트 바디의 하나 이상의 주변부가 밖을 향하도록 하는 것을 특징으로 하는 눈물 임플란트. - 제17항에 있어서,
상기 근위 말단부 또는 원위 말단부 중 적어도 하나가 인접하는 임플란트 바디 부분보다 큰 크기의 단면을 가지는 적어도 하나의 중간-배치되는 유지 돌출부를 포함하는 것을 특징으로 하는 눈물 임플란트. - 제17항에 있어서,
하나 이상의 치료제를 추가로 포함하는 눈물 임플란트. - 제21항에 있어서,
상기 하나 이상의 치료제는 상기 근위 말단부 내에 적어도 부분적으로 배치되며 상기 하나 이상의 치료제의 서방출을 전달하도록 구성되는 적어도 하나의 노출된 표면을 포함하는 약물 인서트 내에 제공되는 것을 특징으로 하는 눈물 임플란트. - 제17항의 눈물 임플란트, 및 안질환 치료를 위하여 상기 눈물 임플란트를 사용하기 위한 설명서를 포함하는 키트.
- 제1 및 제2 부분을 포함하고, 상기 제1 부분의 근위 말단으로부터 상기 제2 부분의 원위 말단으로 연장하는 임플란트 바디
를 포함하는 누소관 내로 삽입가능한 눈물 임플란트로서,
상기 제1 부분의 근위 말단은 세로 근위축을 정의하고, 그 원주 주위로 측면 돌출하는 유지 돌출부를 포함하고;
상기 제2 부분의 원위 말단은 세로 원위축을 정의하고;
상기 유지 돌출부는 그 근위 말단에서 외부를 향하는 측면 스텝을 포함하고 상기 제2 부분 내로 직접적으로 테이퍼링되고; 및
상기 임플란트 바디는, 누소관 내로 임플란트될 때, 소관 만곡에 또는 더 원위에 위치하는 누소관의 적어도 일부에 대하여 상기 임플란트 바디의 적어도 일부를 바이어싱하기 위한, 상기 근위축과 원위축 사이에 경사진 교차 지점이 존재하도록 구성되는 것을 특징으로 하는 눈물 임플란트. - 제24항에 있어서,
상기 유지 돌출부의 길이는 약 0.96 mm 이상인 것을 특징으로 하는 눈물 임플란트. - 제24항에 있어서,
상기 유지 돌출부의 원위 말단은 상기 임플란트 바디의 누소관 내로의 삽입을 촉진시키기 위한 일체형 확장기를 포함하는 것을 특징으로 하는 눈물 임플란트. - 제24항에 있어서,
하나 이상의 치료제를 추가로 포함하는 눈물 임플란트. - 제24항에 있어서,
상기 하나 이상의 치료제는 상기 제1 부분 내에 적어도 부분적으로 배치되며 상기 하나 이상의 치료제의 서방출을 전달하도록 구성되는 약물 인서트 내에 제공되는 것을 특징으로 하는 눈물 임플란트. - 제28항에 있어서,
상기 약물 인서트는 상기 제1 부분의 제1 공동 내에 배치되며, 상기 제1 공동은 적어도 약 0.56 mm의 직경을 가지는 것을 특징으로 하는 눈물 임플란트. - 제29항에 있어서,
상기 약물 인서트는 상기 하나 이상의 치료제를 적어도 약 81 마이크로그램 포함하는 것을 특징으로 하는 눈물 임플란트. - 제24항의 눈물 임플란트, 및 안질환 치료를 위하여 상기 눈물 임플란트를 사용하기 위한 설명서를 포함하는 키트.
- 누소관의 수직 단면 내에 배치가능한 근위 말단부로부터 상기 누소관의 수평 단면 내에 배치가능한 원위 말단부로 비선형 연장하며, 그들 사이의 중간부를 가지는 임플란트 바디
를 포함하는 누소관 내로 삽입하기 위한 눈물 임플란트로서,
상기 중간부는 상기 근위 말단부를 향하여 제1 방향으로 부분적으로 연장하고, 상기 원위 말단부를 향하여 일반적으로 좁아지는 방식으로 제2 방향으로 부분적으로 연장하여, 상기 누소관 내에 임플란트될 때, 상기 임플란트 바디가 소관 만곡에 또는 더 원위에 위치하는 누소관의 적어도 일부에 대하여 측면으로 직접적으로 바이어스되며; 상기 제2 방향 연장은 제1 방향 연장의 세로 길이의 4 배 미만의 세로 길이를 가지고;
상기 중간부는, 상기 임플란트 바디가 임플란트될 때, 누소관 팽대부를 향하여 상기 제2 방향과 실질적으로 반대인 제3 방향으로 부분적으로 연장하며, 상기 제3 방향 연장은 편평한 선체 형상을 포함하는 것을 특징으로 하는 눈물 임플란트. - 제32항에 있어서,
상기 근위 말단부로부터 적어도 부분적으로 연장하는 잡을 수 있는 돌출부를 포함하고, 상기 잡을 수 있는 돌출부는 타원형을 포함하는 것을 특징으로 하는 눈물 임플란트. - 제32항에 있어서,
상기 선체 형상은 약 0.4 내지 0.5 밀리미터의 길이 및 약 0.5 내지 0.6 밀리미터의 두께를 포함하는 것을 특징으로 하는 눈물 임플란트. - 제32항에 있어서,
치료제를 추가로 포함하는 눈물 임플란트. - 제35항에 있어서,
상기 치료제를 포함하는 폴리머 매트릭스를 포함하고, 상기 근위 말단부의 공동 내에 배치되는, 상기 임플란트 바디로부터 구분되는 적어도 하나의 약물 인서트를 포함하는 눈물 임플란트. - 제35항에 있어서,
상기 치료제는 상기 임플란트 바디의 하나 이상의 부분 내로 통합되는 것을 특징으로 하는 눈물 임플란트. - 제32항 내지 제37항 중 어느 한 항의 눈물 임플란트, 및 안질환 치료를 위하여 상기 눈물 임플란트를 사용하기 위한 설명서를 포함하는 키트.
- 제1 및 제2 부분을 포함하고, 세로 근위축을 정의하는 제1 부분의 근위 말단으로부터 세로 원위축을 정의하는 제2 부분의 원위 말단으로 연장하며,
누소관 내로 임플란트될 때, 소관 만곡에 또는 더 원위에 위치하는 누소관의 적어도 일부에 대하여 임플란트 바디의 적어도 일부를 바이어싱하기 위한, 상기 근위축과 원위축 사이에 경사진 교차 지점이 존재하도록 구성되는 임플란트 바디; 및
상기 제1 부분의 원위 말단으로부터 적어도 부분적으로 연장하며, 상기 제1 부분 내 공동에 오버행되는 내측으로 연장하는 유지 립을 포함하는 잡을 수 있는 돌출부
를 포함하는 누소관 내로 삽입가능한 눈물 임플란트. - 제39항에 있어서,
치료제를 포함하고, 상기 제1 부분의 공동 내에 배치되는, 상기 임플란트 바디로부터 구분되는 적어도 하나의 약물 인서트를 추가로 포함하는 눈물 임플란트. - 제40항에 있어서,
상기 내측 연장 유지 립은 상기 공동 내에 완전히 배치될 때 상기 약물 인서트의 근위 표면에 오버행되어, 상기 인서트의 위치를 고정하는 것을 특징으로 하는 눈물 임플란트. - 제41항에 있어서,
상기 오버행은 상기 약물 인서트 내에 저장되는 약물의 방출 속도에 감지가능하게 영향을 미치지 않는 것을 특징으로 하는 눈물 임플란트. - 누소관 내로 삽입가능한 눈물 임플란트의 제조 방법으로서,
제1 바디 부분 내에 공동을 형성하고,
제2 바디 부분을 상기 제1 바디 부분의 세로 길이의 4배 미만의 세로 길이로 연장하고,
제1 부분의 근위 말단 및 제2 부분의 원위 말단을 각각, 누소관 내로 임플란트될 때, 일정 각도로 교차하는 세로 근위축 및 세로 원위축을 정의하도록 구성하여, 상기 임플란트 바디가 소관 만곡에 또는 더 원위에 위치하는 누소관의 적어도 일부에 대하여 측면으로 직접적으로 바이어스되도록 구성하는 것을 포함하는,
제1 부분의 근위 말단으로부터 제2 부분의 원위 말단으로 연장하는 임플란트 바디를 형성하는 단계; 및
약물 인서트의 노출된 표면을 상기 제1 바디 부분의 근위 말단 위로 배치하는 것을 포함하는, 상기 제1 바디 부분의 공동 내에 상기 임플란트 바디로부터 구분되는 약물 인서트를 배치하는 단계
를 포함하는 방법. - 누소관의 수직 단면 내에 배치가능한 근위 말단부로부터 누소관의 수평 단면 내에 배치가능한 원위 말단으로 연장하며, 그들 사이에 중간부를 가지는 임플란트 바디
- 상기 중간부는 상기 근위 말단부를 향하여 제1 방향으로 부분적으로 연장하고 상기 원위 말단부를 향하여 제2 방향으로 부분적으로 연장하여, 누소관 내에 임플란트될 때, 상기 임플란트 바디가 소관 만곡에 또는 더 원위에 위치하는 누소관의 적어도 일부에 대하여 직접적으로 측면 바이어스되도록 함 - ; 및
상기 원위 말단부에 또는 이에 근접하여 배치되는 유지 돌출부
를 포함하는 누소관 내로 삽입하기 위한 눈물 임플란트. - 제44항에 있어서,
상기 제2 방향 연장은 상기 제1 방향 연장에 대하여 일반적으로 오목 형상을 포함하고; 일반적으로 오목 형상의 반경은 소관 만곡 반경보다 작은 것을 특징으로 하는 눈물 임플란트. - 적어도 하나의 공동을 포함하는 임플란트 바디;
상기 적어도 하나의 공동 내에 배치되며, 폴리머 매트릭스 및 치료제를 포함하는, 상기 임플란트 바디로부터 구분되는 약물 인서트
를 포함하는 누소관 내로 삽입하기 위한 눈물 임플란트로서,
상기 임플란트 바디는 하나 이상의 바디 부분과 통합되는 치료제를 포함하는 것을 특징으로 하는 눈물 임플란트. - 제46항에 있어서,
상기 약물 인서트의 하나 이상의 표면을 둘러싸는 시스체를 추가로 포함하는 눈물 임플란트. - 제46항에 있어서,
외부 임플란트 바디 표면의 하나 이상의 부분에 적용되는 코팅을 추가로 포함하는 눈물 임플란트. - 제48항에 있어서,
제1 코팅 두께가 제1 임플란트 바디 표면부에 적용되고, 상기 제1 코팅 두께와 다른 제2 코팅 두께가 제2 임플란트 바디 표면부에 적용되는 것을 특징으로 하는 눈물 임플란트. - 제48항에 있어서,
상기 코팅은 패럴린, 세라믹 또는 은 중 적어도 하나를 포함하는 것을 특징으로 하는 눈물 임플란트. - 제46항에 있어서,
상기 약물 인서트는 제1 치료제 공급부를 포함하고, 상기 임플란트 바디는 제2 치료제 공급부를 포함하는 것을 특징으로 하는 눈물 임플란트.
Applications Claiming Priority (10)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US15469309P | 2009-02-23 | 2009-02-23 | |
| US61/154,693 | 2009-02-23 | ||
| US20903609P | 2009-03-02 | 2009-03-02 | |
| US61/209,036 | 2009-03-02 | ||
| US20963009P | 2009-03-09 | 2009-03-09 | |
| US61/209,630 | 2009-03-09 | ||
| US27186209P | 2009-07-27 | 2009-07-27 | |
| US61/271,862 | 2009-07-27 | ||
| US25205709P | 2009-10-15 | 2009-10-15 | |
| US61/252,057 | 2009-10-15 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20110132369A true KR20110132369A (ko) | 2011-12-07 |
Family
ID=42634499
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020117021082A KR20110132369A (ko) | 2009-02-23 | 2010-02-23 | 눈물 임플란트 및 관련 방법 |
Country Status (15)
| Country | Link |
|---|---|
| US (2) | US10238535B2 (ko) |
| EP (2) | EP3415124A3 (ko) |
| JP (2) | JP5576405B2 (ko) |
| KR (1) | KR20110132369A (ko) |
| CN (2) | CN102361603A (ko) |
| AU (1) | AU2010215745A1 (ko) |
| BR (1) | BRPI1008030A2 (ko) |
| CA (2) | CA2977078C (ko) |
| CO (1) | CO6450672A2 (ko) |
| IL (1) | IL214797A0 (ko) |
| MX (1) | MX2011008875A (ko) |
| RU (1) | RU2011138947A (ko) |
| SG (1) | SG174133A1 (ko) |
| TW (1) | TW201041570A (ko) |
| WO (1) | WO2010096822A2 (ko) |
Families Citing this family (31)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3470108A1 (en) | 2004-07-02 | 2019-04-17 | Mati Therapeutics Inc. | Treatment medium delivery device for delivery of treatment media to the eye |
| CN103393483B (zh) | 2006-03-31 | 2016-08-24 | 玛提治疗有限公司 | 用于鼻泪系统的药物释放方法、结构及组合物 |
| FR2908042B1 (fr) * | 2006-11-08 | 2009-06-05 | Bruno Fayet | Ensemble d'intubation monocanaliculonasal et/ou monocanaliculaire,notamment pour l'imperforation lacrymonasale. |
| JP5524841B2 (ja) | 2007-09-07 | 2014-06-18 | キュー エル ティー インク. | 涙管インプラント及び関連する方法 |
| CN101861135A (zh) | 2007-09-07 | 2010-10-13 | Qlt栓塞输送公司 | 泪道植入物检测 |
| WO2009096855A1 (en) * | 2008-01-28 | 2009-08-06 | Milux Holding Sa | Blood clot removal device, system, and method |
| CN102341144B (zh) * | 2009-01-23 | 2014-10-29 | Qlt股份有限公司 | 一种或多种药剂的持续释放递送 |
| MX2011008875A (es) * | 2009-02-23 | 2011-09-26 | Quadra Logic Tech Inc | Implantes lagrimales y metodos relacionados. |
| US9022967B2 (en) | 2010-10-08 | 2015-05-05 | Sinopsys Surgical, Inc. | Implant device, tool, and methods relating to treatment of paranasal sinuses |
| US20120213840A1 (en) * | 2011-02-18 | 2012-08-23 | Valeant International (Barbados) Srl | Ocular strips |
| US9974685B2 (en) * | 2011-08-29 | 2018-05-22 | Mati Therapeutics | Drug delivery system and methods of treating open angle glaucoma and ocular hypertension |
| JP6100782B2 (ja) * | 2011-08-29 | 2017-03-22 | キューエルティー インコーポレイテッド | 緑内障および高眼圧症を治療するための活性剤の徐放送達 |
| WO2013154843A1 (en) | 2012-04-11 | 2013-10-17 | Sinopsys Surgical, Inc. | Implantation tools, tool assemblies, kits and methods |
| CN105473130A (zh) * | 2012-05-03 | 2016-04-06 | 麦提疗法有限公司 | 治疗开角型青光眼和高眼压症的药物递送系统和方法 |
| WO2014113384A2 (en) * | 2013-01-15 | 2014-07-24 | The Regents Of The University Of Colorado, A Body Corporate | Lacrimal system drug delivery device |
| AU2014209177C1 (en) | 2013-01-25 | 2019-01-24 | Sinopsys Surgical, Inc. | Paranasal sinus access implant devices and related tools, methods and kits |
| EP4302736A3 (en) | 2013-03-28 | 2024-04-03 | ForSight Vision4, Inc. | Ophthalmic implant for delivering therapeutic substances |
| CN104434389A (zh) * | 2013-09-12 | 2015-03-25 | 李进凯 | 充气式全泪道扩张器 |
| US9433763B2 (en) | 2013-09-27 | 2016-09-06 | Acclarent, Inc. | Sinus wall implant |
| US9700459B2 (en) | 2013-10-16 | 2017-07-11 | Sinopsys Surgical, Inc. | Apparatuses, tools and kits relating to fluid manipulation treatments of paranasal sinuses |
| EP3179968B1 (en) * | 2014-07-24 | 2019-09-11 | Sinopsys Surgical, Inc. | Paranasal sinus access implant devices and related products and methods |
| US10500091B2 (en) * | 2014-11-10 | 2019-12-10 | Forsight Vision4, Inc. | Expandable drug delivery devices and methods of use |
| CA2989814A1 (en) | 2015-06-16 | 2016-12-22 | The Regents Of The University Of Colorado, A Body Corporate | Nasolacrimal implants and related methods for tear stimulation |
| US11564833B2 (en) | 2015-09-25 | 2023-01-31 | Glaukos Corporation | Punctal implants with controlled drug delivery features and methods of using same |
| EP3380040B1 (en) * | 2015-11-23 | 2023-04-19 | The Regents of The University of Colorado, A Body Corporate | Lacrimal system for drug delivery |
| CA3024912A1 (en) | 2016-05-20 | 2017-11-23 | The Regents Of The University Of Colorado, A Body Corporate | Lacrimal drug delivery device |
| CN108852614B (zh) * | 2017-05-10 | 2023-09-15 | 上海中医药大学附属龙华医院 | 泪小管栓塞推注器 |
| JP7169104B2 (ja) * | 2017-07-12 | 2022-11-10 | 株式会社カネカ | 涙道チューブ |
| EP3675780A4 (en) | 2017-09-20 | 2021-10-06 | Sinopsys Surgical, Inc. | IMPLANTATION TOOLS, ARRANGEMENTS, KITS, AND PROCEDURES FOR ACCESSING PERIODIC FLUIDS |
| US11147735B2 (en) | 2018-02-26 | 2021-10-19 | Olympic Ophthalmics, Inc. | Therapeutic handheld devices for disorders |
| EP4041129A4 (en) * | 2019-10-07 | 2023-11-15 | Glaukos Corporation | POINT-SHAPED IMPLANTS, DELIVERY SYSTEMS AND METHODS OF USING THE SAME |
Family Cites Families (133)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3865108A (en) | 1971-05-17 | 1975-02-11 | Ortho Pharma Corp | Expandable drug delivery device |
| US3923939A (en) * | 1974-06-07 | 1975-12-02 | Alza Corp | Process for improving release kinetics of a monolithic drug delivery device |
| US3949750A (en) | 1974-10-07 | 1976-04-13 | Freeman Jerre M | Punctum plug and method for treating keratoconjunctivitis sicca (dry eye) and other ophthalmic aliments using same |
| US4014335A (en) | 1975-04-21 | 1977-03-29 | Alza Corporation | Ocular drug delivery device |
| US5053030A (en) | 1984-11-07 | 1991-10-01 | Herrick Robert S | Intracanalicular implant for horizontal canalicular blockade treatment of the eye |
| US4660546A (en) | 1984-11-07 | 1987-04-28 | Robert S. Herrick | Method for treating for deficiency of tears |
| US5049142A (en) | 1984-11-07 | 1991-09-17 | Herrick Robert S | Intracanalicular implant for horizontal canalicular blockade treatment of the eye |
| US5229128A (en) | 1986-06-11 | 1993-07-20 | Haddad Heskel M | Drug delivery ophthalmic insert and method of preparing same |
| US5322691A (en) * | 1986-10-02 | 1994-06-21 | Sohrab Darougar | Ocular insert with anchoring protrusions |
| US4886488A (en) | 1987-08-06 | 1989-12-12 | White Thomas C | Glaucoma drainage the lacrimal system and method |
| US4915684A (en) | 1988-06-21 | 1990-04-10 | Mackeen Donald L | Method and apparatus for modulating the flow of lacrimal fluid through a punctum and associated canaliculus |
| US5133159A (en) | 1989-01-13 | 1992-07-28 | Nestle S.A. | Method for polishing silicone products |
| US4959048A (en) * | 1989-01-17 | 1990-09-25 | Helix Medical, Inc. | Lacrimal duct occluder |
| US5128058A (en) | 1989-05-31 | 1992-07-07 | Hoya Corporation | Contact lens cleaner containing a microcapsular polishing agent |
| IE910450A1 (en) | 1990-02-15 | 1991-08-28 | Bausch & Lomb | Soft contact lens processing aid |
| US5171270A (en) | 1990-03-29 | 1992-12-15 | Herrick Robert S | Canalicular implant having a collapsible flared section and method |
| US5163959A (en) | 1990-03-29 | 1992-11-17 | Herrick Robert S | Method for treating an eye with a canalicular implant having a collapsible flared section |
| US5041081A (en) | 1990-05-18 | 1991-08-20 | Odrich Ronald B | Ocular implant for controlling glaucoma |
| US5283063A (en) | 1992-01-31 | 1994-02-01 | Eagle Vision | Punctum plug method and apparatus |
| US5334137A (en) | 1992-02-21 | 1994-08-02 | Eagle Vision, Inc. | Lacrimal fluid control device |
| US5469867A (en) | 1992-09-02 | 1995-11-28 | Landec Corporation | Cast-in place thermoplastic channel occluder |
| US5318513A (en) | 1992-09-24 | 1994-06-07 | Leib Martin L | Canalicular balloon fixation stent |
| US5707643A (en) | 1993-02-26 | 1998-01-13 | Santen Pharmaceutical Co., Ltd. | Biodegradable scleral plug |
| US5417651A (en) | 1993-07-01 | 1995-05-23 | Guena; Nicolas | Punctum plug and monocanalicular probe for lacrimal pathology |
| US5423777A (en) | 1993-10-27 | 1995-06-13 | Tajiri; Akira | Punctum plug |
| US5466233A (en) | 1994-04-25 | 1995-11-14 | Escalon Ophthalmics, Inc. | Tack for intraocular drug delivery and method for inserting and removing same |
| JP3486758B2 (ja) | 1994-06-24 | 2004-01-13 | 株式会社高研 | 注入可能な涙小管閉鎖剤 |
| US5723005A (en) | 1995-06-07 | 1998-03-03 | Herrick Family Limited Partnership | Punctum plug having a collapsible flared section and method |
| US6149684A (en) * | 1995-06-07 | 2000-11-21 | Herrick; Robert S. | Punctum plug having a thin elongated lip and a distal starting tip and method of using |
| CN2251369Y (zh) * | 1995-08-04 | 1997-04-09 | 李绍君 | 一种治疗泪道堵塞的套管 |
| US5766243A (en) | 1995-08-21 | 1998-06-16 | Oasis Medical, Inc. | Abrasive polished canalicular implant |
| US5773019A (en) | 1995-09-27 | 1998-06-30 | The University Of Kentucky Research Foundation | Implantable controlled release device to deliver drugs directly to an internal portion of the body |
| US5824073A (en) | 1996-03-18 | 1998-10-20 | Peyman; Gholam A. | Macular indentor for use in the treatment of subretinal neovascular membranes |
| JPH1033584A (ja) | 1996-07-26 | 1998-02-10 | M L C:Kk | 涙道挿管器具 |
| US5993407A (en) | 1996-10-25 | 1999-11-30 | Moazed; Kambiz Thomas | Transnasal lacrimal insert |
| CA2269029C (en) | 1996-11-01 | 2003-12-23 | Alcon Laboratories, Inc. | Cryogenic polishing method for soft acrylic articles |
| EP0944371A1 (fr) | 1997-02-04 | 1999-09-29 | Alain Fouere | Tampon meatique vissable pour canal lacrymal |
| US6082362A (en) | 1997-03-27 | 2000-07-04 | Eagle Vision, Inc. | Punctum plug |
| US6041785A (en) | 1997-03-27 | 2000-03-28 | Eaglevision, Inc. | Punctum plug |
| US6027470A (en) | 1998-06-10 | 2000-02-22 | Eagle Vision, Inc. | Punctum plug and method for inserting the same into the punctual opening |
| US6016806A (en) | 1997-03-27 | 2000-01-25 | Eaglevision, Inc | Punctum plug |
| US5961370A (en) | 1997-05-08 | 1999-10-05 | Chiron Vision Corporation | Intraocular lens tumbling process using coated beads |
| MY125870A (en) | 1997-07-25 | 2006-08-30 | Alza Corp | Osmotic delivery system flow modulator apparatus and method |
| US6306426B1 (en) | 1997-08-11 | 2001-10-23 | Allergan Sales, Inc. | Implant device with a retinoid for improved biocompatibility |
| US5830171A (en) | 1997-08-12 | 1998-11-03 | Odyssey Medical, Inc. | Punctal occluder |
| US6060439A (en) | 1997-09-29 | 2000-05-09 | Kyzen Corporation | Cleaning compositions and methods for cleaning resin and polymeric materials used in manufacture |
| NL1008090C2 (nl) | 1998-01-22 | 1999-07-26 | Lubberman Bernardus H M | Plug voor het afsluiten van een traanbuis. |
| WO1999044553A1 (en) | 1998-03-02 | 1999-09-10 | Herrick Family Limited Partnership | A punctum plug having a collapsible flared section and method |
| US6290684B1 (en) * | 1998-03-02 | 2001-09-18 | Herrick Family Limited Partnership | Punctum plug having a collapsible expanded section and distal tip extending substantially perpendicular thereto and method of inserting same |
| US6196993B1 (en) * | 1998-04-20 | 2001-03-06 | Eyelab Group, Llc | Ophthalmic insert and method for sustained release of medication to the eye |
| US6306114B1 (en) * | 1998-06-16 | 2001-10-23 | Eagle Vision, Inc. | Valved canalicular plug for lacrimal duct occlusion |
| JP2000070296A (ja) | 1998-08-27 | 2000-03-07 | M L C:Kk | 涙道内挿管器具 |
| US6095901A (en) | 1998-12-09 | 2000-08-01 | Alcon Laboratories, Inc. | Polishing method for soft acrylic articles |
| US20040121014A1 (en) | 1999-03-22 | 2004-06-24 | Control Delivery Systems, Inc. | Method for treating and/or preventing retinal diseases with sustained release corticosteroids |
| US6234175B1 (en) | 1999-03-23 | 2001-05-22 | Medennium, Inc. | Smart ocular plug design and method of insertion for punctal and intracanalicular implants |
| US6383192B1 (en) | 1999-04-28 | 2002-05-07 | Mlc Limited Company | Apparatus for intubation of lacrimal duct |
| US6428502B1 (en) | 1999-06-25 | 2002-08-06 | Alcon Manufacturing, Ltd. | Punctal cannula |
| US6706275B1 (en) | 1999-09-08 | 2004-03-16 | Matthew W. Camp | Scleral plug system |
| US7943162B2 (en) * | 1999-10-21 | 2011-05-17 | Alcon, Inc. | Drug delivery device |
| US6331313B1 (en) | 1999-10-22 | 2001-12-18 | Oculex Pharmaceticals, Inc. | Controlled-release biocompatible ocular drug delivery implant devices and methods |
| US6264971B1 (en) | 1999-11-04 | 2001-07-24 | Btg International Limited | Ocular insert |
| US7867186B2 (en) | 2002-04-08 | 2011-01-11 | Glaukos Corporation | Devices and methods for treatment of ocular disorders |
| US7708711B2 (en) | 2000-04-14 | 2010-05-04 | Glaukos Corporation | Ocular implant with therapeutic agents and methods thereof |
| US6638239B1 (en) | 2000-04-14 | 2003-10-28 | Glaukos Corporation | Apparatus and method for treating glaucoma |
| US20040175410A1 (en) | 2000-04-26 | 2004-09-09 | Control Delivery Systems, Inc. | Sustained release device and method for ocular delivery of carbonic anhydrase inhibitors |
| US6375972B1 (en) | 2000-04-26 | 2002-04-23 | Control Delivery Systems, Inc. | Sustained release drug delivery devices, methods of use, and methods of manufacturing thereof |
| US6371122B1 (en) | 2000-06-20 | 2002-04-16 | Robert M. Mandelkorn | Gauge/dilator apparatus |
| US6629533B1 (en) * | 2000-06-30 | 2003-10-07 | Eagle Vision, Inc. | Punctum plug with at least one anchoring arm |
| ES2231306T3 (es) | 2000-08-04 | 2005-05-16 | Medennium, Inc. | Tapon ocular para implantar en el punto lagrimal y el canaliculo. |
| WO2002056863A2 (en) | 2000-12-29 | 2002-07-25 | Bausch & Lomb Incorporated | Sustained release drug delivery devices |
| CA2432225C (en) | 2001-01-03 | 2008-01-15 | Michael J. Brubaker | Sustained release drug delivery devices with prefabricated permeable plugs |
| US6991808B2 (en) | 2001-01-26 | 2006-01-31 | Bausch & Lomb Inc. | Process for the production of sustained release drug delivery devices |
| US7431710B2 (en) | 2002-04-08 | 2008-10-07 | Glaukos Corporation | Ocular implants with anchors and methods thereof |
| AU2002258754B2 (en) | 2001-04-07 | 2006-08-17 | Glaukos Corporation | Glaucoma stent and methods thereof for glaucoma treatment |
| US6605108B2 (en) * | 2001-04-13 | 2003-08-12 | Eagle Vision, Inc. | Monocanalicular stent |
| US6982090B2 (en) | 2001-05-10 | 2006-01-03 | Gillespie Donald E | More easily visualized punctum plug configurations |
| US7404825B2 (en) | 2001-06-11 | 2008-07-29 | Herrick Ii Robert S | Implant capable of forming a differential image in an eye |
| FR2829019B3 (fr) | 2001-08-31 | 2003-10-31 | Alain Fouere | Bouchons lacrymaux et methodes de mise en place de ces dispositifs |
| CA2452194A1 (en) | 2001-09-11 | 2003-03-20 | Smart Drug Systems Inc | Sustained release pharmaceutical compositions comprising a silicone support material |
| US6729939B2 (en) | 2001-12-17 | 2004-05-04 | Bausch & Lomb Incorporated | Polishing method for intraocular lens |
| FR2834446B1 (fr) | 2002-01-08 | 2004-02-13 | Ioltechnologie Production | Clou meatique a expansion |
| US7204995B2 (en) | 2002-01-31 | 2007-04-17 | El-Sherif Dalia M | Treatment and control of dry eye by use of biodegradable polymer capsules |
| US20040147870A1 (en) | 2002-04-08 | 2004-07-29 | Burns Thomas W. | Glaucoma treatment kit |
| US9301875B2 (en) * | 2002-04-08 | 2016-04-05 | Glaukos Corporation | Ocular disorder treatment implants with multiple opening |
| US6866563B2 (en) | 2002-06-27 | 2005-03-15 | Bausch & Lomb Incorporated | Apparatus and method for target polishing intraocular lenses |
| FR2841770B1 (fr) | 2002-07-05 | 2004-10-01 | Ioltechnologie Production | Clou meatique d'obturation d'un meat lacrymal |
| FR2844182B1 (fr) | 2002-09-11 | 2004-12-03 | Humanoptics Ag | Bouchon d'obturation d'un canalicule lacrymal |
| US7169163B2 (en) | 2002-09-30 | 2007-01-30 | Bruce Becker | Transnasal method and catheter for lacrimal system |
| US20050283109A1 (en) | 2003-03-07 | 2005-12-22 | Peyman Gholam A | Method and apparatus for lacrimal canal obstruction |
| CN1259894C (zh) * | 2003-04-09 | 2006-06-21 | 周坚强 | 连线弹性泪道扩张器 |
| JP4824549B2 (ja) | 2003-05-02 | 2011-11-30 | サーモディクス,インコーポレイティド | 制御放出型の生体活性物質デリバリー・デバイス |
| US7017580B2 (en) | 2003-05-22 | 2006-03-28 | Clarity Corporation | Punctum plug system including a punctum plug and passive insertion tool therefor |
| US7204253B2 (en) | 2003-05-22 | 2007-04-17 | Clarity Corporation | Punctum plug |
| JP4104137B2 (ja) | 2003-05-30 | 2008-06-18 | 有限会社エム・エル・シー | 涙点プラグ |
| JP4339635B2 (ja) * | 2003-06-12 | 2009-10-07 | 有限会社エム・エル・シー | 涙点プラグ |
| US6994684B2 (en) | 2003-06-16 | 2006-02-07 | Alphamed Inc. | Punctum plugs having fluid collecting recesses and methods of punctal occlusion |
| US20040265356A1 (en) | 2003-06-30 | 2004-12-30 | Bausch & Lomb Incorporated | Drug delivery device |
| JP4280128B2 (ja) | 2003-08-19 | 2009-06-17 | 有限会社エム・エル・シー | 涙点プラグ |
| JP2005110765A (ja) | 2003-10-03 | 2005-04-28 | M L C:Kk | 涙点プラグセット |
| JP2005110930A (ja) | 2003-10-07 | 2005-04-28 | M L C:Kk | 涙点プラグセット |
| US20050095269A1 (en) | 2003-11-04 | 2005-05-05 | Ainpour Parviz R. | Gel plug for blockage of the canaliculus |
| US20050197614A1 (en) | 2004-03-04 | 2005-09-08 | Wilson Pritchard | Occlusive biomedical devices, punctum plugs, and methods of use thereof |
| US20050220882A1 (en) | 2004-03-04 | 2005-10-06 | Wilson Pritchard | Materials for medical implants and occlusive devices |
| US20050232972A1 (en) | 2004-04-15 | 2005-10-20 | Steven Odrich | Drug delivery via punctal plug |
| JP2004202276A (ja) | 2004-04-16 | 2004-07-22 | M L C:Kk | 涙道再建用挿管器具 |
| US20050244469A1 (en) | 2004-04-30 | 2005-11-03 | Allergan, Inc. | Extended therapeutic effect ocular implant treatments |
| JP2005312835A (ja) | 2004-04-30 | 2005-11-10 | M L C:Kk | 糸で補強した涙道ステント |
| JP4644438B2 (ja) | 2004-05-11 | 2011-03-02 | 有限会社エム・エル・シー | ツバつき涙道ステント |
| JP4510511B2 (ja) | 2004-05-18 | 2010-07-28 | 有限会社エム・エル・シー | ツバを円盤で補強した涙道ステント及び涙道プラグ |
| EP3470108A1 (en) | 2004-07-02 | 2019-04-17 | Mati Therapeutics Inc. | Treatment medium delivery device for delivery of treatment media to the eye |
| US20060020253A1 (en) * | 2004-07-26 | 2006-01-26 | Prescott Anthony D | Implantable device having reservoir with controlled release of medication and method of manufacturing the same |
| US7117870B2 (en) | 2004-07-26 | 2006-10-10 | Clarity Corporation | Lacrimal insert having reservoir with controlled release of medication and method of manufacturing the same |
| WO2006031658A2 (en) | 2004-09-10 | 2006-03-23 | Allergan, Inc. | Therapeutic lacrimal canalicular inserts and related methods |
| US20060074370A1 (en) | 2004-09-24 | 2006-04-06 | Medennium, Inc. | Ocular occluder and method of insertion |
| CA2588449A1 (en) | 2004-11-24 | 2006-06-01 | Therakine Corporation | An implant for intraocular drug delivery |
| US20060233858A1 (en) | 2005-03-08 | 2006-10-19 | Allergan, Inc. | Systems and methods providing targeted intraocular drug delivery |
| US7862532B2 (en) | 2005-10-07 | 2011-01-04 | Delta Life Sciences, Inc. | Punctum plugs having insertion guides and strengthening beams |
| US20070132125A1 (en) | 2005-12-08 | 2007-06-14 | Bausch & Lomb Incorporated | Use of a super-cooled fluid in lens processing |
| JP4078371B2 (ja) | 2006-01-27 | 2008-04-23 | 章弘 小栗 | 涙点プラグ |
| CN103393483B (zh) | 2006-03-31 | 2016-08-24 | 玛提治疗有限公司 | 用于鼻泪系统的药物释放方法、结构及组合物 |
| US9173773B2 (en) | 2006-06-21 | 2015-11-03 | Johnson & Johnson Vision Care, Inc. | Punctal plugs for the delivery of active agents |
| US9474645B2 (en) * | 2006-06-21 | 2016-10-25 | Johnson & Johnson Vision Care, Inc. | Punctal plugs for the delivery of active agents |
| US20080045911A1 (en) | 2006-06-21 | 2008-02-21 | Borgia Maureen J | Punctal plugs for the delivery of active agents |
| FR2908042B1 (fr) | 2006-11-08 | 2009-06-05 | Bruno Fayet | Ensemble d'intubation monocanaliculonasal et/ou monocanaliculaire,notamment pour l'imperforation lacrymonasale. |
| CA2674076A1 (en) * | 2006-12-26 | 2008-07-10 | Qlt Plug Delivery, Inc. | Drug delivery implants for inhibition of optical defects |
| UY30883A1 (es) * | 2007-01-31 | 2008-05-31 | Alcon Res | Tapones punctales y metodos de liberacion de agentes terapeuticos |
| JP5524841B2 (ja) * | 2007-09-07 | 2014-06-18 | キュー エル ティー インク. | 涙管インプラント及び関連する方法 |
| US20090104243A1 (en) | 2007-09-07 | 2009-04-23 | Qlt Plug Delivery, Inc. - Qpdi | Drug cores for sustained release of therapeutic agents |
| JP2010537776A (ja) | 2007-09-07 | 2010-12-09 | キューエルティー プラグ デリバリー,インク. | 涙管インプラント用の挿入および抜き取り工具 |
| CN102123713A (zh) | 2008-05-09 | 2011-07-13 | Qlt栓塞输送公司 | 治疗青光眼和眼高血压的活性剂的持续释放递送 |
| WO2009145755A1 (en) | 2008-05-30 | 2009-12-03 | Qlt Plug Delivery, Inc | Surface treated implantable articles and related methods |
| CN102341144B (zh) | 2009-01-23 | 2014-10-29 | Qlt股份有限公司 | 一种或多种药剂的持续释放递送 |
| MX2011008875A (es) * | 2009-02-23 | 2011-09-26 | Quadra Logic Tech Inc | Implantes lagrimales y metodos relacionados. |
-
2010
- 2010-02-23 MX MX2011008875A patent/MX2011008875A/es not_active Application Discontinuation
- 2010-02-23 BR BRPI1008030A patent/BRPI1008030A2/pt not_active IP Right Cessation
- 2010-02-23 TW TW099105205A patent/TW201041570A/zh unknown
- 2010-02-23 CA CA2977078A patent/CA2977078C/en active Active
- 2010-02-23 JP JP2011551300A patent/JP5576405B2/ja active Active
- 2010-02-23 EP EP18168145.3A patent/EP3415124A3/en active Pending
- 2010-02-23 WO PCT/US2010/025089 patent/WO2010096822A2/en active Application Filing
- 2010-02-23 CN CN2010800130359A patent/CN102361603A/zh active Pending
- 2010-02-23 EP EP10744476.2A patent/EP2398431A4/en not_active Withdrawn
- 2010-02-23 KR KR1020117021082A patent/KR20110132369A/ko not_active Application Discontinuation
- 2010-02-23 RU RU2011138947/14A patent/RU2011138947A/ru not_active Application Discontinuation
- 2010-02-23 SG SG2011058716A patent/SG174133A1/en unknown
- 2010-02-23 CN CN201610283712.8A patent/CN105997339B/zh active Active
- 2010-02-23 US US12/710,855 patent/US10238535B2/en active Active
- 2010-02-23 AU AU2010215745A patent/AU2010215745A1/en not_active Abandoned
- 2010-02-23 CA CA2752645A patent/CA2752645C/en active Active
-
2011
- 2011-08-23 IL IL214797A patent/IL214797A0/en unknown
- 2011-09-19 CO CO11121700A patent/CO6450672A2/es not_active Application Discontinuation
-
2014
- 2014-07-03 JP JP2014137749A patent/JP5880986B2/ja active Active
-
2019
- 2019-03-21 US US16/361,046 patent/US11712370B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| CN105997339A (zh) | 2016-10-12 |
| WO2010096822A3 (en) | 2011-02-03 |
| CA2752645C (en) | 2017-10-03 |
| IL214797A0 (en) | 2011-11-30 |
| EP3415124A3 (en) | 2019-02-27 |
| TW201041570A (en) | 2010-12-01 |
| RU2011138947A (ru) | 2013-03-27 |
| SG174133A1 (en) | 2011-10-28 |
| CN102361603A (zh) | 2012-02-22 |
| EP2398431A4 (en) | 2014-06-11 |
| MX2011008875A (es) | 2011-09-26 |
| CO6450672A2 (es) | 2012-05-31 |
| JP5576405B2 (ja) | 2014-08-20 |
| CN105997339B (zh) | 2018-09-04 |
| JP2015013121A (ja) | 2015-01-22 |
| JP2012518494A (ja) | 2012-08-16 |
| BRPI1008030A2 (pt) | 2016-03-15 |
| US10238535B2 (en) | 2019-03-26 |
| US20100274204A1 (en) | 2010-10-28 |
| CA2977078A1 (en) | 2010-08-26 |
| US20190216646A1 (en) | 2019-07-18 |
| WO2010096822A2 (en) | 2010-08-26 |
| EP2398431A2 (en) | 2011-12-28 |
| EP3415124A2 (en) | 2018-12-19 |
| US11712370B2 (en) | 2023-08-01 |
| JP5880986B2 (ja) | 2016-03-09 |
| CA2977078C (en) | 2021-07-20 |
| CA2752645A1 (en) | 2010-08-26 |
| AU2010215745A1 (en) | 2011-09-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11712370B2 (en) | Lacrimal implants and related methods | |
| US11951038B2 (en) | Lacrimal implants and related methods |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WITN | Application deemed withdrawn, e.g. because no request for examination was filed or no examination fee was paid |