KR20100049084A - 질병 진단을 위한 방법 및 조성물 - Google Patents
질병 진단을 위한 방법 및 조성물 Download PDFInfo
- Publication number
- KR20100049084A KR20100049084A KR1020107003992A KR20107003992A KR20100049084A KR 20100049084 A KR20100049084 A KR 20100049084A KR 1020107003992 A KR1020107003992 A KR 1020107003992A KR 20107003992 A KR20107003992 A KR 20107003992A KR 20100049084 A KR20100049084 A KR 20100049084A
- Authority
- KR
- South Korea
- Prior art keywords
- transcription factor
- promoter
- ligand
- polynucleotide
- switch
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6897—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids involving reporter genes operably linked to promoters
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/66—General methods for inserting a gene into a vector to form a recombinant vector using cleavage and ligation; Use of non-functional linkers or adaptors, e.g. linkers containing the sequence for a restriction endonuclease
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/66—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving luciferase
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
- C12Q1/6883—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/15—Medicinal preparations ; Physical properties thereof, e.g. dissolubility
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/158—Expression markers
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/24—Immunology or allergic disorders
- G01N2800/245—Transplantation related diseases, e.g. graft versus host disease
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Genetics & Genomics (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biotechnology (AREA)
- General Engineering & Computer Science (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Physics & Mathematics (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Microbiology (AREA)
- Analytical Chemistry (AREA)
- Biomedical Technology (AREA)
- Immunology (AREA)
- Plant Pathology (AREA)
- Pathology (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Pharmacology & Pharmacy (AREA)
- Food Science & Technology (AREA)
- Medicinal Chemistry (AREA)
- General Physics & Mathematics (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Investigating Or Analysing Biological Materials (AREA)
Abstract
본 발명은 상기 환자의 세포에 진단 유전자 스위치 구조체를 도입 및 리포터 유전자 발현을 모니터하여 환자에서 질병 또는 장애를 진단하는 방법과 조성물에 관한 것이다. 본 발명은 나아가 질병 또는 장애의 진행 및 질병 또는 장애 치료제의 효능을 모니터하기 위한 방법과 조성물에 관한 것이다.
Description
본 발명은 개체의 세포에 진단 유전자 스위치 구조체를 도입하고, 리포터 유전자의 발현을 모니터함으로써 개체에서 질병 또는 장애를 진단하기 위한 방법 및 조성물에 관한 것이다. 나아가, 본 발명은 질병 또는 장애의 진행을 모니터하거나 질병 또는 장애에 대한 치료제의 효능 또는 독성을 모니터하기 위한 방법 및 조성물에 관한 것이다.
개체에서 질병 유무에 대한 진단 테스트는 오랫동안 존재해 왔지만, 연구자들은 지속적으로 높은 감도(초기 진단을 가능하게 함) 및 특이성(위양성 및 위음성을 제거)을 보여주는 향상된 진단 테스트 찾고 있다. 진단 테스트의 다른 바람직한 특성은 사용편의, 빠른 결과, 및 질병의 진행 및 진행중인 치료제의 효능을 지속적으로 모니터할 수 있는 능력을 포함한다.
따라서, 상기의 해당 기술 분야에서는 제공하는 새로운 진단 방법 및 조성물에 대한 요구가 있다.
본 발명은 진단 및 모니터 방법을 제공하기 위해 리간드-의존 유전자 스위치 시스템의 조절적 제어(regulatory control)와 연결된 질병 탐지를 위한 질병 특이적 프로모터를 이용하여 특이성 및 민감성의 조합에 근거한 것이다. 본 발명은 개체에서 질병 또는 장애를 진단하기 위한 방법 및 조성물에 관한 것이다. 나아가 본 발명은 개체에서 질병 또는 장애의 진행을 모니터하거나 개체에서 질병 또는 장애에 대한 투여된 치료제의 효능 또는 독성을 모니터하는 방법 및 조성물에 관한 것이다.
본 발명의 하나의 구현예는 (a) 상기 개체의 세포에 (1) 유전자 스위치를 코딩하는 폴리뉴클레오티드, 이때, 상기 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하며, 여기서 상기 적어도 하나의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하고, 작동가능하게 진단 스위치 프로모터와 연결되며, 여기서 상기 프로모터의 활성은 상기 개체의 질병 또는 장애 기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 도입하여 변형된 세포를 생산하는 단계; (b) 상기 변형된 세포에 리간드를 투여하는 단계; 및 (c) 리포터 유전자 발현을 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현이 상기 개체가 상기 질병 또는 장애를 가짐을 지시하는 것인, 상기 개체에서 질병 또는 장애를 진단하는 방법을 포함한다.
하나의 구현예에서, 상기 진단 방법은 생체 외(ex vivo)에서 상기 개체로부터 분리된 세포에서 수행된다.
하나의 구현예에서, 상기 진단 방법은 상기 개체로부터 분리된 세포로 본 발명의 조성물을 도입하여 변형된 세포를 생산하고, 상기 변형된 세포는 상기 개체로 재도입되어 수행된다.
하나의 구현예에서, 상기 진단 방법은 생체 내(in vivo)에서 수행된다.
다른 구현예에서, 상기 진단 방법은 비-자가 세포, 예를 들면 개체에 동종이계 또는 이종인 세포를 이용하여 수행되며, 상기 변형된 비-자가 세포는 상기 개체내로 도입된다.
본 발명의 하나의 관점에서, 상기 유전자 스위치는 엑디손 수용체(EcR)-기반 유전자 스위치이다.
하나의 구현예에서, 상기 유전자 스위치는 제1 진단 스위치 프로모터의 조절 하에 있는 제1 전사 인자 서열 및 제2 진단 스위치 프로모터의 조절 하에 있는 제2 전사 인자 서열을 포함하고, 여기서 상기 제1 전사 인자 서열 및 상기 제2 전사 인자 서열에 의해 코딩되는 단백질들이 상호작용하여 리간드-의존 전사 인자로서 기능하는 단백질 복합체를 형성한다.
본 발명의 다른 관점에서, 상기 제1 전사 인자 서열은 이형이량체 파트너 및 전사활성화 도메인을 포함하는 단백질을 코딩하고, 상기 제2 전사 인자 서열은 DNA 결합 도메인 및 리간드-결합 도메인을 포함하는 단백질을 코딩한다.
본 발명의 다른 구현예는 (a) 상기 개체의 세포로 (1) 유전자 스위치를 코딩하는 폴리뉴클레오티드, 상기 유전자 스위치는 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 진단 스위치 프로모터에 작동가능하게 연결되며, 여기서 상기 프로모터의 활성은 상기 개체의 질병 또는 장애 기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드 도입하여 변형된 세포를 생산하는 단계; (b) 상기 변형된 세포에 리간드를 투여하는 단계; 및 (c) 리포터 유전자 발현을 적어도 2회 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨의 변화가 상기 개체에서 상기 질병 또는 장애의 진행을 지시하는 것인, 상기 개체에서 질병 또는 장애의 진행을 모니터하는 방법에 관한 것이다.
본 발명의 다른 구현예는 (a) 상기 개체에 치료제를 투여하는 단계; (b) 상기 개체의 세포에 (1) 유전자 스위치를 코딩하는 폴리뉴클레오티드, 이때, 상기 유전자 스위치는 적어도 하나의 전사인자 서열을 포함하며, 여기서 상기 적어도 하나의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하고, 진단 스위치 프로모터에 작동가능하게 연결되며, 여기서 상기 프로모터의 활성은 상기 개체의 질병 또는 장애 기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 도입하여 변형된 세포를 생산하는 단계; (c) 상기 변형된 세포에 리간드를 투여하는 단계; 및 (d) 리포터 유전자 발현을 적어도 2회 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨의 변화가 상기 치료제의 효능을 지시하는 것인, 상기 개체에서 질병 또는 장애에 대한 상기 치료제의 효능을 모니터하는 방법에 관한 것이다.
본 발명의 다른 구현예는 (a) 상기 개체에 치료제를 투여하는 단계; (b) 상기 개체의 세포에 (1) 유전자 스위치를 코딩하는 폴리뉴클레오티드, 상기 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하고, 여기서 상기 적어도 하나의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하고, 진단 스위치 프로모터에 연결되며, 여기서 상기 프로모터의 활성은 독성 조건에 노출되어 있는 세포에서 발견된 인자들에 의해 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 도입하여 변형된 세포를 생산하는 단계; (c) 상기 변형된 세포에 리간드를 투여하는 단계; 및 (d) 리포터 유전자 발현을 적어도 2회 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨의 변화가 상기 치료제의 독성을 지시하는 것인, 상기 개체에서 질병 또는 장애에 대한 투여된 치료제의 잠재적 독성을 모니터하는 방법에 관한 것이다.
본 발명의 다른 구현예는 (a) 상기 개체에 치료제를 투여하는 단계; (b) 상기 개체의 세포에 (1) 유전자 스위치를 코딩하는 폴리펩타이드, 이때, 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하고, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 진단 스위치 프로모터에 연결되며, 여기서 상기 프로모터의 활성은 치료를 위해 투여되어 있는 인자에 의해 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 도입하여 변형된 세포를 생산하는 단계; (c) 상기 변형된 세포에 리간드를 투여하는 단계; 및 (d) 리포터 유전자 발현을 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨은 치료를 위해 투여된 상기 인자의 레벨을 지시하는 것인, 상기 질병 또는 장애에 대한 치료를 위해 상기 개체에 투여되어 있는 상기 인자의 레벨을 모니터하는 방법에 관한 것이다.
다른 구현예에서, 상기 각각의 방법은 비-자가 세포, 예를 들면 개체에 동종이계 또는 이종인 세포를 이용하여 수행될 수 있으며, 상기 변형된 비-자가 세포는 상기 개체 내로 투여된다.
본 발명의 하나의 구현예는 (a) 기관 또는 조직 이식의 세포에 (1) 유전자 스위치를 코딩하는 폴리뉴클레오티드, 이때, 상기 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하고, 상기 적어도 하나의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하고, 진단 스위치 프로모터에 작동가능하게 연결되며, 여기서 상기 프로모터의 활성은 이식 거부기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 도입하여 변형된 세포를 생산하는 단계; (b) 상기 변형된 세포에 리간드를 투여하는 단계; 및 (c) 리포터 유전자 발현을 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현이 이식 거부가 탐지됨을 지시하는 것인, 기관 또는 조직 이식을 받는 개체에서 이식 거부를 탐지하는 방법을 포함한다.
본 발명의 다른 구현예는 (a) 기관 또는 조직 이식의 세포에 (1) 유전자 스위치를 코딩하는 폴리뉴클레오티드, 이때, 상기 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하고, 상기 적어도 하나의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하고, 진단 스위치 프로모터에 작동가능하게 연결되며, 여기서 상기 프로모터의 활성은 이식 거부기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 도입하여 변형된 세포를 생산하는 단계; (b) 상기 변형된 세포에 리간드를 투여하는 단계; 및 (c) 리포터 유전자 발현을 적어도 2회 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨의 변화가 상기 개체에서 상기 이식 거부의 진행을 지시하는 것인, 상기 기관 또는 조직 이식을 받는 개체에서 이식 거부의 진행을 모니터하는 방법에 관한 것이다.
다른 구현예에서, 이식 거부를 탐지하거나 모니터하는 방법은 본 발명의 폴리뉴클레오티드를 비-자가 세포, 예를 들면, 이식되는 기관 또는 조직에 동종이계 또는 이종인 세포에 도입함으로써 수행될 수 있으며, 상기 변형된 비-자가 세포는 이식에 앞서 상기 기관 또는 조직에 도입된다.
상기 기술된 방법들 중, 하나의 구현예에서, 상기 유전자 스위치를 코딩하는 폴리뉴클레오티드 및 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드는 하나의 커다란 폴리뉴클레오티드, 예를 들면, 벡터의 일부이다. 다른 하나의 구체예에서, 상기 유전자 스위치를 코딩하는 폴리뉴클레오티드 및 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드는 별개의 폴리뉴클레오티드이다.
본 발명은 상기 기술한 방법들에 유용한 진단 유전자 스위치 구조체에 관한 것이다.
또한, 본 발명은 본 발명의 상기 진단 유전자 스위치 구조체를 포함하는 벡터에 관한 것이다.
또한, 본 발명은 유전자 스위치 구조체, 벡터, 리간드 등등을 포함하는, 본 발명의 상기 방법들을 수행하는 키트에 관한 것이다. 하나의 구현예에서, 상기 키트는 본발명의 폴리뉴클레오티드를 포함할 수 있는 세포(예를 들면, 자가 또는 비-자가 세포)를 포함할 수 있다.
본 발명은 개체에서 질병 또는 장애의 진단을 위해 진단 스위치를 이용한 방법 및 조성물에 관한 것이다. 나아가 본 발명은 개체에서 질병 또는 장애 진행 또는 그것의 치료제를 모니터하는 방법 및 조성물에 관한 것이다. 본 발명의 방법은 생체 외 (유전자 스위치를 개체의 분리된 세포에 도입함에 의한) 또는 생체 내 (개체의 분리된 세포에 유전자 스위치를 도입 및 상기의 세포를 개체에 재도입 또는 유전자 스위치를 직접 상기 개체의 세포에 도입함에 의한) 로 수행될 수 있다. 다른 구현예에서는, 유전자 스위치를 가지고 있는 세포가 비-자가(non-autologous) 조직 세포(예, 동종이계(allogeneic) 또는 이종(xenogeneic) 세포)일 수 있다. 본 발명의 방법은 하나 이상의 진단 스위치 프로모터 조절하에서 리간드-의존 전사인자가 발현되는 유전자 스위치 사용을 포함한다. 여기에 기술된 방법과 조성물은 상당히 민감하고 특이적인 진단 기술을 제공하며, 여기서 진단 단계의 타이밍은 유전자 스위치를 구성하는 세포에 리간드를 투여, 질병 또는 장애의 존재를 최적으로 탐지, 뿐만 아니라 질병 또는 장애의 진행 또는 치료제의 효능 또는 독성을 지속적으로 또는 간헐적으로 모니터함으로써 조절된다.
하기의 정의들이 제공되어 본 발명의 범위 및 실시를 이해하는데 도움이 되어야 한다.
본 발명의 목적을 위해 사용된 "분리된(isolated)" 이라는 용어는 고유의 환경(자연발생적인 환경)으로부터 제거된 생물학적 물질(세포, 핵산, 또는 단백질)을 가리킨다. 예를 들어, 식물 또는 동물에 자연발생적인 폴리뉴클레오티드는 분리되지 않으나, 자연발생적인 이웃 핵산으로부터 분리된 같은 폴리뉴클레오티드는 "분리된"으로 고려된다.
생물학적 물질에 적용되는 "정제된" 이라는 용어는 다른 물질을 전혀 포함하지 않으며 절대 순도를 나타내는 형태로 존재하는 물질을 필요로 하지 않는다. 이 용어는 다소 상대적인 정의이다.
"핵산", "핵산분자", "올리고뉴클레오티드", 및 "폴리뉴클레오티드"라는 용어는 서로 바뀌어 사용될 수 있으며 단일 가닥 형태 또는 이중 가닥 나선의 리보뉴클레오시드(아데노신, 구아노신, 우리딘,또는 시스티딘; "RNA 분자") 또는 데옥시리보뉴클레오시드(데옥시아데노신, 데옥시구아노신, 데옥시사이미딘, 또는 데옥시시스티딘; "DNA 분자")의 인산 에스터 중합 형태, 또는 포스포로사이올레이트 및 사이오에스터와 같은 그것의 어떠한 인산에스터 유사체를 명칭한다. 이중 가닥의 DNA-DNA, DNA-RNA 및 RNA-RNA 나선도 가능하다. 핵산 분자라는 용어, 특히 특정 DNA 또는 RNA 분자에서의 핵산 분자는 오직 분자의 1차 구조 및 2차 구조만을 가리키고, 어떠한 특정 3차 구조에 제한되지는 않는다. 그리하여, 이 용어는 특히, 선형 또는 원형의 DNA 분자(예, 제한 단편), 플라스미드, 슈퍼코일드(supercoiled) DNA 및 염색체에서 발견되는 이중 가닥 DNA을 포함한다. 특정 이중 가닥 DNA 분자의 구조를 논의할 때, 서열은 DNA의 비전사(non-트랜스cribed) 가닥의 5' 에서 3' 방향으로 서열을 읽는 정규적인 관례에 따라 여기에서 기술될 수 있다(곧, mRNA와 상동인 서열을 지닌 가닥). "재조합 DNA 분자"라는 용어는 분자 생물학적 조작을 거친 DNA 분자이다. DNA는 cDNA, 게놈믹 DNA, 플라스미드 DNA, 합성 DNA, 및 반합성 DNA를 포함하나, 여기에 제한적이지는 않다.
"단편"이라는 용어는, 폴리뉴클레오티드 서열에 적용되는 것과 같이, 레퍼런스 핵산에 대해 상대적으로 감소된 길이의 핵산 서열을 가리키며 공통적인 부분에서 레퍼런스 핵산과 동일한 핵산 서열을 포함한다. 본 발명에 따라 그러한 핵산 단편은 그들이 구성원인 보다 더 큰 폴리뉴클레오티드에 적절하게 포함될 수 있다. 그러한 단편은 본 발명에 따라 적어도 6, 8, 9, 10, 12, 15, 18, 20, 21, 22, 23, 24, 25, 30, 39, 40, 42, 45, 48, 50, 51, 54, 57, 60, 63, 66, 70, 75, 78, 80, 90, 100, 105, 120, 135, 150, 200, 300, 500, 720, 900, 1000, 1500, 2000, 3000, 4000, 5000, 또는 그 이상 길이의 연속적인 핵산의 뉴클레오티드 범위의 올리고뉴클레오티드를 포함하거나, 또는 이들로 이루어진다.
여기서 사용하는 "분리된 핵산 단편"이라는 용어는 선택적으로 합성, 비자연적 또는 변형된 뉴클레오티드 염기를 지닌 단일 또는 이중 가닥의 RNA 또는 DNA의 중합체를 가리킨다. DNA 중합체 형태에서 분리된 핵산 단편은 cDNA, 게놈믹 DNA 또는 합성 DNA의 하나 이상의 단편으로 이루어 질 수 있다.
"유전자"라는 용어는 오직 전사(예, 생물활성이 있는 RNA 종) 또는 전사 및 번역(예, 폴리펩타이드)에 의해 생성된 기능성 분자를 코딩하는 뉴클레오티드를 포함하는 폴리뉴클레오티드를 가리킨다. "유전자"라는 용어는 cDNA 및 게놈믹 DNA를 포함한다. "유전자"라는 용어는 또한 특이한 RNA, 단백질, 또는 폴리펩타이드를 발현하는, 코딩 서열 앞의 조절 서열(5' 비-코딩 서열) 및 코딩 서열 뒤의 조절 서열(3' 비-코딩 서열)을 포함하는, 핵산 단편을 가리킨다. "네이티브 유전자"라는 용어는 자기 자신의 조절 서열을 지닌 자연에서 발견되는 유전자를 가리킨다. 자연발생적으로 함께 발견되지 않는 조절 및/또는 코딩 서열을 포함하는 "키메릭 유전자"라는 용어는 네이티브 유전자가 아닌 임의의 유전자를 가리킨다. 따라서, 키메릭 유전자는 다른 근원으로부터 유래된 조절 서열 및 코딩 서열 또는 같은 근원으로부터 유래된 조절 서열 및 코딩 서열을 포함할 수 있으나, 자연에서 발견되는 것과는 다른 방식으로 배열되어 있다. 키메릭 유전자는 다른 근원으로부터 유래된 코딩 서열 및/또는 다른 근원으로부터 유래된 조절 서열을 포함할 수 있다. "내생적인 유전자"라는 용어는 생명체 게놈에서 자연적 위치에 있는 네이티브 유전자를 가리킨다. "외래" 유전자 또는 "이종 기원의" 유전자라는 용어는 숙주 생명체에는 정상적으로 발견되지 않는 유전자를 가리키나, 그것은 유전자 트랜스퍼에 의해 숙주 생명체내로 도입된다. 외래 유전자는 비-네이티브 생명체, 또는 키메릭 유전자에 도입된 네이티브 유전자를 포함할 수 있다. "이식 유전자"라는 용어는 형질전환 절차에 의해 게놈내로 도입된 유전자를 가리킨다.
"이종 기원의 유전자"라는 용어는 세포 또는 세포의 염색체 위치에 자연발생적으로 위치하지 않은 DNA를 가리킨다. 이종 기원의 DNA는 세포에 외래적인 유전자를 포함할 수 있다.
"게놈"이라는 용어는 염색체 뿐만 아니라 미토콘드리아, 엽록체, 및 바이러스 DNA 또는 RNA를 포함한다.
핵산 분자의 단일 가닥 형태가 적당한 조건의 온도 및 용액의 이온 세기하에서 다른 핵산 분자에 어닐링(anneal)할 수 있을 때, 핵산 분자는 cDNA, 게놈믹 DNA, 또는 RNA와 같은 다른 핵산 분자에 "하이브리다이져블"하다 라는 용어을 사용한다. 하이브리다이제이션 및 세척 조건은 Sambrook et al. in Molecular Cloning: A Laboratory Manual, Second Edition, Cold Spring Harbor Laboratory Press, Cold Spring Harbor (1989)에 특히, 11 장과 표 11.1 에 잘 알려져 있고 예시되어 있다(참고로 여기에 전체적으로 도입됨). 온도 및 이온 세기의 조건이 하이브리다이제이션의 "스트린전시(stringency)"를 결정한다.
스트린전시 조건은 진화적으로 멀리 떨어진 생물체로부터의 상동 서열과 같이 중간 정도로 유사한 단편들부터 진화적으로 서로 밀접한 생물체로부터의 기능성 단백질을 복제하는 유전자들과 같이 상당히 유사한 단편들을 선별하기 위해 조정될 수 있다. 상동의 핵산들을 예비적으로 선별하기 위해, 55℃의 Tm 값에 해당하는 낮은 하이브리다이제이션 조건이 사용될 수 있다, 예를 들어 5X SSC, 0.1% SDS, 0.25% 밀크, 및 비 포름아마이드; 또는 30% 포름아마이드, 5X SSC, 0.5% SDS. 중간 정도의 스트린전시 하이브리다이제이션 조건은 더 높은 Tm 값에 해당한다, 예를 들어 5X 또는 6X SSC를 지닌 40% 포름아마이드. 높은 스트린전시 하이브리다이제이션 조건은 가장 높은 Tm 값에 해당한다, 예를 들어 50% 포름아마이드, 5X 또는 6X SSC.
하이브리다이제이션은 하이브리다이제이션의 스트린전시에 대한 의존에 따라 염기 간의 미스매치가 가능함에도 불구하고 2 개의 핵산이 상보 서열을 포함한다는 것을 요구한다. "상보적"이라는 용어는 서로 하이브리다이징할 수 있는 뉴클레오티드 염기 간의 관계를 기술하기 위해 사용된다. 예를 들면, DNA에 대해, 아데닌은 사이민과 상보적이고 사이토신은 구아닌과 상보적이다. 따라서, 본 발명은 여기에 개시 또는 사용된 완전한 서열뿐만 아니라 이들과 상당히 유사한 핵산 서열에 상보적인 분리된 핵산 단편을 또한 포함한다.
본 발명의 하나의 구현예에서, 폴리뉴클레오티드는 55℃의 Tm에서 하이브리다이제이션하는 하이브리다이제이션 조건 및 상기에 기술된 조건을 사용하여 탐지된다. 다른 구현예에서, Tm은 60℃, 63℃, 또는 65℃ 이다.
포스트-하이브리다이제이션 세척도 또한 스트린전시 조건을 결정한다. 한 세트의 조건은 15 분간 실온에서 6X SSC, 0.5% SDS를 가지고 시작하는 일련의 세척을 사용한다. 그 후, 30분간 45℃에서 2X SSC, 0.5% SDS를 가지고 반복하고, 그 다음 30 분간 50℃에서 0.2X SSC, 0.5%를 가지고 2 번 반복하였다. 바람직한 스트린전시 조건의 세트는 0.2X SSC, 0.5% SDS에서 마지막 2번의 30 분간의 세척의 온도가 60 ℃로 증가 된 것만을 제외하고 상기의 세척과 동일한 더 높은 세척 온도를 사용한다. 다른 바람직한 높은 스트린전시 조건의 세트는 60 ℃하 0.1X SSC, 0.1% SDS에서 2번의 마지막 세척을 사용한다.
핵산을 하이브리다이징하기 위한 알맞은 스트린전시 조건은 핵산의 길이 및 상보성의 정도, 당업자에게 알려진 변수에 의존한다. 두 뉴클레오티드 서열 간의 유사성 또는 상동성의 정도가 클수록, 이들 서열을 지닌 핵산의 하이브리드에 대한 Tm 값이 더 커진다. 핵산 하이브리다이제이션의 상대적 안정성(더 높은 Tm에 해당)은 다음의 순으로 감소한다: RNA:RNA, DNA:RNA, DNA:DNA. 길이에서 100개의 뉴클레오티드가 더 큰 하이브리드에 대해서, Tm을 계산하는 식이 도입되었다(Sambrook et al, 위에서 인용, 9.50-0.51 참조). 올리고뉴클레오티드와 같은 더 짧은 핵산을 이용한 하이브리다이제이션에 대해, 미스매치의 위치가 더욱 중요하게 되고 올리고뉴클레오티드의 길이가 그것의 특이성을 결정한다(Sambrook et ah, 위에서 인용, 11.7-11.8 참조).
본 발명의 하나의 구현예에서, 폴리뉴클레오티드는 적어도 37℃에서 및 500 mM 미만의 염에서 하이브리다이제이션, 및 적어도 63℃ 온도의 2X SSPE 에서 세척 단계를 포함하는 하이브리다이제이션 조건을 사용하여 탐지된다. 다른 구현예에서, 하이브리다이제이션 조건은 하이브리다이제이션 단계를 대해서 적어도 37℃에서 및 200 mM 미만의 염을 포함한다. 보다 구체적인 구현예에서, 하이브리다이제이션 조건은 하이브리다이제이션 및 세척 단계 둘 다에 대하여 63℃ 및 2X SSPE를 포함한다.
다른 구현예에서, 하이브리다이져블 핵산의 길이는 약 10개 뉴클레오티드 이상이다. 하이브리다이져블 핵산에 대한 바람직한 최소 길이는 약 15개 뉴클레오티드 이상이다; 예, 약 20 개 뉴클레오티드 이상; 예, 약 30개 뉴클레오티드 이상. 보다 구체적으로, 당업자는 온도 및 세척 용액 염 농도는 프로브 길이와 같은 인자에 따라 조정될 수 있다.
"프로브"라는 용어는 이중 가닥 분자를 형성하기 위해 상보적인 단일 가닥 타켓 핵산과 염기 쌍을 이룰 수 있는 단일 가닥 핵산 분자를 가리킨다.
여기서 사용하는 "올리고뉴클레오티드"라는 용어는 게놈믹 DNA 분자, cDNA 분자, 플라스미드 DNA 또는 mRNA 분자와 하이브리다이져블한 짧은 핵산을 가리킨다. 올리고뉴클레오티드는 바이오틴과 같은 라벨이 공유결합된 32P-뉴클레오티드 또는 뉴클레오티드를 가지고 레이블링될 수 있다. 레이블링된 올리고뉴클레오티드는 핵산의 존재를 탐지하기 위한 프로브로 사용될 수 있다. 올리고뉴클레오티드(한 가닥 또는 두 가닥이 레이블링될 수 있음)는 핵산의 전체 길이 또는 단편의 클로닝을 위해, DNA 서열 분석을 위해, 또는 핵산 존재를 탐지하기 위해서 PCR 프라이머로 사용될 수 있다. 올리고뉴클레오티드는 DNA 분자를 가지고 삼중 나선 형성하는데 또한 사용될 수 있다. 일반적으로, 올리고뉴클레오티드는 합성적으로 제조되며, 바람직하게는 핵산 합성기에서 제조된다. 따라서, 올리고뉴클레오티드는 사이올에스터 결합 등과 같이 자연발생적으로 일어나지 않는 인산에스터 유사체 결합을 가지고 제조될 수 있다.
"프라이머"는 적당한 조건하에서 DNA 합성의 시작점 역할을 하는 이중 가닥 핵산 부위를 생성하기 위해서 타켓 핵산 서열에 하이브리다이즈하는 올리고뉴클레오티드를 가리킨다. 그러한 프라이머는 중합효소 연쇄반응이나 또는 DNA 서열에 사용될 수 있다.
"중합효소 연쇄 반응"이라는 용어는 축약해서 PCR 이고 특정 핵산 서열을 효소적으로 증폭시키기 위한 시험관 내 방법을 가리킨다. PCR은 3 단계를 포함하는 각 사이클을 가진 반복적인 일련의 온도 사이클을 포함한다: 타켓 분자의 가닥을 분리하기 위해 주형 핵산을 변성, 주형 핵산에 단일 가닥 PCR 올리고뉴클레오티드 프라이머를 어닐링, 및 DNA 중합효소에 의해 어닐링된 프라이머를 확장. PCR은 타켓 분자의 존재를 탐지 및 정량적 또는 반-정량적인 조건하에서 핵산의 초기 공급원에서 그 타켓 분자의 상대적인 양을 결정하는 도구를 제공한다.
"역전사-중합효소 연쇄 반응"은 축약해서 RT-PCR 이고 하나의 RNA 분자 또는 분자들로부터 타켓 cDNA 분자 또는 분자들을 효소적으로 생성하기 위한 시험관 내 방법을 가리키며 이 후, 상기에 기술된 타켓 cDNA 분자 또는 분자들 내에서 특정 핵산 서열 또는 서열들을 효소적으로 증폭시킨다. RT-PCR은 타켓 분자의 존재를 탐지 및 정량적 또는 반-정량적인 조건하에서 핵산의 초기 공급원에서 그 타켓 분자의 상대적인 양을 결정하는 도구를 또한 제공한다.
DNA "코딩서열"이라는 용어는 폴리펩타이드를 코딩하는 이중 가닥 DNA 서열을 가리키며 이들은 적당한 조절 서열의 통제하에 위치되었을 때 세포의 시험관 내 또는 생체 내에서 전사 및 번역되어 폴리펩티드를 형성할 수 있다. "적당한 조절 서열"이라는 용어는 코딩 서열의 상류(5' 비-코딩 서열), 내부, 또는 하류(3' 비-코딩 서열)에 위치한 핵산 서열을 가리키며, 전사, RNA 프로세싱 또는 안정성, 또는 연관된 코딩 서열의 번역에 영향을 준다. 조절 서열은 프로모터, 번역 리더 서열, 인트론, 폴리아데닐레이션 인식 서열, RNA 프로세싱 부위, 이펙터 결합 부위 및 스템-루프 구조를 포함할 수 있다, 코딩 서열의 경계는 5' (아미노) 말단에서 개시 코돈 및 3' (카르복실) 말단에서 번역 종료 코돈에 의해 결정된다. 코딩 서열은 원핵 생물체의 서열, mRNA로 부터의 cDNA, 게놈믹 DNA 서열, 및 심지어는 합성 DNA 서열을 포함하나, 여기에 제한적이지는 않다. 코딩 서열이 진핵 세포에서의 발현을 위한 것이라면, 폴리아데닐레이션 신호 및 전사 종료 서열은 일반적으로 코딩 서열의 3'에 위치할 것이다.
"오픈 리딩 프레임(open reading frame)"이라는 용어는 축약해서 ORF이고 ATG 또는 AUG와 같은 번역 개시 신호 또는 개시 코돈 및 종료 코돈을 포함하는 DNA, cDNA, 또는 RNA인 핵산 서열의 길이를 가리킨다. 그리고 이들은 잠재적으로 폴리펩티드 서열로 번역될 수 있다.
"헤드-투-헤드(head-to-head)"라는 용어는 서로에 관한 2 개의 폴리뉴클레오티드 서열의 방향을 기술하기 위해 여기서 사용된다. 하나의 폴리뉴클레오티드의 코딩 가닥의 5' 말단이 다른 폴리뉴클레오티드의 코딩 가닥의 5' 말단과 이웃하고 있을 때, 2 개의 폴리뉴클레오티드는 헤드-투-헤드 방향으로 위치한다. 그래서 각 폴리뉴클레오티드의 전사 방향은 다른 폴리뉴클레오티드의 5' 말단으로부터 멀어지는 곳으로 진행한다. "헤드-투-헤드"라는 용어는 (5')-to-(5')로 축약될 수 있으며 또한 (<- ->) 또는 (3'<- 5' 5' ->3')의 기호로서 표기될 수 있다.
"테일-투-테일(tail-to-tail)"이라는 용어는 서로에 관한 2 개의 폴리뉴클레오티드 서열의 방향을 기술하기 위해 여기서 사용된다. 하나의 폴리뉴클레오티드의 코딩 가닥의 3' 말단이 다른 폴리뉴클레오티드의 코딩 가닥의 3' 말단과 이웃하고 있을 때, 2 개의 폴리뉴클레오티드는 테일-투-테일 방향으로 위치한다. 그래서 각 폴리뉴클레오티드의 전사 방향은 다른 폴리뉴클레오티드를 향하여 진행한다. "테일-투-테일"이라는 용어는 (3')-to-(3')로 축약될 수 있으며 또한 (-> <-) 또는 (5'->3' 3''<- 5')의 기호로서 표기될 수 있다.
"헤드-투-테일"이라는 용어는 서로에 관한 2 개의 폴리뉴클레오티드 서열의 방향을 기술하기 위해 여기서 사용된다. 하나의 폴리뉴클레오티드의 코딩 가닥의 5' 말단이 다른 폴리뉴클레오티드의 코딩 가닥의 3' 말단과 이웃하고 있을 때, 2 개의 폴리뉴클레오티드는 헤드-투-테일 방향으로 위치한다. 그래서, 그래서 각 폴리뉴클레오티드의 전사 방향은 다른 폴리뉴클레오티드의 전사와 같은 방향으로 진행한다. "헤드-투-테일"이라는 용어는 (5')-to-(3')로 축약될 수 있으며 (-> ->) 또한 (5'->3' '5'->3')의 기호로서 표기될 수 있다.
"하류(downstream)"라는 용어는 레퍼런스 뉴클레오티드 서열의 3'에 위치한 뉴클레오티드 서열을 가리킨다. 특히, 하류 뉴클레오티드 서열은 일반적으로 전사 개시 점을 따르는 서열을 포함한다. 예를 들어, 유전자의 번역 개시 코돈은 전사 개시 점의 하류에 위치한다.
"상류(upstream)"라는 용어는 레퍼런스 뉴클레오티드 서열의 5'에 위치한 뉴클레오티드 서열을 가리킨다. 상류 뉴클레오티드 서열은 일반적으로 코딩 서열의 5' 쪽 또는 전사 개시점에 위치한 서열을 포함한다. 예를 들어, 대다수의 프로모터는 전사 개시점의 상류에 위치한다.
"제한 엔도뉴클레아제" 또는 "제한 효소"라는 용어는 서로 바뀌어 사용될 수 있으며 이중 가닥 DNA 내의 특정 핵산 서열에 결합하고 절단하는 효소를 가리킨다.
"상동 재조합"이라는 용어는 예를 들어, 벡터를 염색체로 삽입하는 것과 같이 외래 DNA 서열을 다른 DNA 분자에 삽입하는 것을 가리킨다. 바람직하게, 벡터는 상동 재조합을 위해 특정 염색체 부위를 타켓할 수 있다. 특이적인 상동 재조합을 위해, 벡터는 상보적 결합과 염색체 내로 벡터의 병합을 위해 염색체 서열에 상동하는 충분히 긴 부위를 포함하고 있을 것이다. 상동 부위가 크면 클수록, 그리고 서열의 유사성이 보다 클수록 상동 재조합의 효율은 증가한다.
당업자에게 알려진 몇 가지 방법들이 본 발명에 따라 폴리뉴클레오티드를 증식시키기 위해 사용될 수 있다. 알맞은 숙주 시스템 및 성장 조건이 확립되면, 재조합 발현 벡터는 대량으로 증식 및 제조될 수 있다. 여기에 기술된 것 같이, 사용될 수 있는 발현 벡터는 하기의 벡터 또는 그들의 도입체를 포함하나, 여기에 제한적이지는 않다: 벡시나 바이러스 또는 아데노바이러스와 같은 인간 또는 동물 바이러스; 바큘로바이러스와 같은 곤충 바이러스; 효모 벡터; 박테리오파아지 벡터(예, 람다), 및 플라스미드 및 코스미드 DNA 벡터 등.
"벡터"라는 용어는 핵산을 숙주세포 내로 클로닝 및/또는 트랜스퍼하기 위한 임의의 운송수단을 가리킨다. 벡터는 부착된 DNA 단편 복제를 위해 다른 DNA 단편이 부착될 수 있는 레플리콘일 수 있다. "레플리콘(replicon)"이라는 용어는 생체 내 에서 DNA 복제의 자발적인 단위로서 기능할 수 있는 곧, 자기 자신의 통제하에 복제를 할 수 있는 임의의 유전 서열을 가르킨다. "벡터"라는 용어는 시험관 내 , 생체 외 또는 생체 내 에서 핵산을 세포 내로 도입하기 위한 바이러스 및 비바이러스 운송수단을 포함한다. 당업자에게 알려진 수 많은 벡터가 핵산을 조작, 반응 서열 및 프로모터를 유전자 내로 병합하기 위해 사용될 수 있다. 예를 들어, 사용 가능한 벡터는 예로, 람다 도입체인 박테리오파아지 또는 pBR322 또는 pUC 플라스미드 도입체인 플라스미드, 또는 블루스크립트 벡터를 포함하는 플라스미드 또는 변현된 바이러스를 포함한다. 본 발명에 유용한 다른 예의 벡터는, 참고로 여기 포함된 제 WO 2007/038276호에 기술된 것과 같이, 울트라 벡터™ 프로덕션 시스템(Intrexon Corp., Blacksburg, VA)이다. 예를 들어, 반응 서열 및 프로모터에 해당하는 DNA 단편의 알맞은 벡터 내로의 삽입은 해당 DNA 단편을 상보적 코히시브(cohesive) 말단을 지닌 선택된 벡터 내로 라이게이션하여 이루어질 수 있다. 다른 대안으로, DNA 분자의 말단은 효소적으로 변형될 수 있거나 또는 뉴클레오티드 서열(링커)을 DNA 말단에 라이게이션하여 임의의 부위도 생성될 수 있다. 그러한 벡터는 게놈상에 마커를 병합한 세포를 선택하게 해주는 선택 마커를 포함하도록 조작될 수 있다. 그러한 마커는 마커에 의해 코딩되는 단백질을 병합 및 발현하는 숙주 세포를 동정 및/또는 선별하게 한다.
바이러스 벡터, 특히 리트로바이러스 벡터는 세포 뿐만 아니라 살아있는 동물체에서의 유전자 전송법으로 다양하게 사용되어 왔다. 사용될 수 있는 바이러스 벡터는 리트로바이러스, 아데노-연관-바이러스, 폭스, 바큘로바이러스, 벡시나, 허피스 심플렉스, 엡스타인-바, 아데노바이러스, 제미니바이러스, 및 칼리모바이러스를 포함하나, 여기에 제한적이지는 않다. 비바이러스 벡터는 플라스미드, 리포솜, 전기로 대전된 지질(사이토펙틴), DNA-단백질 복합체, 및 생물고분자를 포함한다. 핵산 뿐만 아니라, 벡터는 핵산 트랜스퍼(발현 동안 조직으로의 트랜스퍼 등) 결과를 선택, 측정, 모니터하는데 유용한 하나 이상의 조절 부위, 및/또는 선택 마커를 또한 포함할 수 있다.
"플라스미드"라는 용어는 세포의 중간대사의 일부분이 아닌 유전자를 종종 가지고 있는 염색체 외의 서열을 가리키며, 일반적으로 원형의 이중 가닥 DNA 분자 형태이다. 그러한 서열은 자율적으로 복제하는 서열, 게놈 통합 서열, 파아지 또는 핵신 서열, 단일 또는 이중 가닥 DNA 또는 RNA의 선형, 원형, 또는 슈퍼코일드 서열일 수 있다. 이들은 수 많은 핵산 서열이 독특한 구조체로 결합 및 재조합되는 임의의 근원으로부터 도입될 수 있다. 여기서 독특한 구조체는 프로모터 단편 및 선택 유전자 산물의 DNA 서열을 해당 3' 번역 안 된 서열과 함께 세포 내로 도입할 수 있다.
"클로닝 벡터"라는 용어는 단위 길이의 핵산인 "레플리콘"을 가리키며, 바람직하게는 순차적으로 복제하는 DNA이고, 부착된 단편의 복제를 위해 다른 핵산 단편이 부착된 플라스미드, 파아지, 또는 코스미드와 같은 복제 오리진을 포함한다. 클로닝 벡터는 하나의 세포 타입에서는 복제를 할 수 있고 다른 세포에서는 발현을 할 수 있다("셔틀 벡터"). 클로닝 벡터는 벡터 및/또는 관심 서열 삽입을 위한 하나 이상의 다중 클로닝 부위를 지니는 세포의 선택에 사용되는 하나 이상의 서열을 포함할 수 있다.
"발현 벡터"라는 용어는 숙주세포에 형질전환된 후 삽입된 핵산 서열의 발현을 가능하도록 설계된 벡터, 플라스미드, 또는 운송수단을 가리킨다. 삽입된 핵산 서열과 같이 클로닝된 서열은 일반적으로 프로모터, 미니 프로모터, 인핸서 등과 같은 조절 서열의 조절하에 위치한다. 바람직한 숙주 세포에서 핵산 발현을 추진하는데 유용한 초기 조절 부위 또는 프로모터는 수 많은 종류가 있고 당업자에게 익숙하다. 실제적으로, 이들 유전자 발현을 추진할 수 있는 임의의 프로모터도 발현 벡터에 사용될 수 있다. 이들 발현 벡터는 하기를 포함하나, 여기에 제한적이지는 않다: 바이러스 프로모터, 박테리아 프로모터, 동물 프로모터, 포유류 프로모터, 합성 프로모터, 항시적 프로모터, 조직 특이적 프로모터, 발병 또는 질병과 연관된 프로모터, 발생 특이적 프로모터, 유도 프로모터, 광 조절 프로모터; CYCl , HIS3, GALl , GAL4 , GALlO , ADHl , PGK , PH05 , GAPDH , ADCl , TRPl , URA3 , LEU2 , ENO , TPI, 알카라인 포스파타아제 프로모터 (효모에서의 발현에 유용한); AOXl 프로모터 (Pichia 에서의 발현에 유용한); β-락타마아제, lac , ara , tet , trp , IP L , IP R , T7 , tac, 및 trc 프로모터 (대장균에서의 발현에 유용한); 광조절-, 씨 특이-, 꽃가루 특이-, 난소 특이-, 콜리플라워 모자이크 바이러스 35S, CMV 35S 미니멀, 카사바 베인 모자이크 바이러스 (CsVMV), 클로로필 a/b 결합 단백질, 리불로스 1,5-바이포스페이트 카복실라아제, 눈(shoot) 특이, 뿌리 특이, 키틴나아제, 스트레스 유도, 라이스 텅그로 바실리폼 바이러스, 식물 슈퍼-프로모터, 포테이토 류신 아미노펩티다아제, 나이트레이트 환원제, 맨노파인 신사아제, 노팔라인 신사아제, 유비쿼틴, 제인 단백질, 및 안토사이아닌 프로모터 (식물 세포에서의 발현에 유용한); 당업자에게 알려진 동물 및 포유류 프로모터는 하기를 포함하나, 여기에 제한적이지는 않다: SV40 초기 (SV40e) p프로모터 부위, 루 살코마 바이러스(RSV)의 3' 롱 말단 리피트(LTR)에 위치한 프로모터, 아데노바이러스(Ad)의 E1A 또는 메이저 후기 프로모터(MLP)의 프로모터, 사이토메갈로바이러스 (CMV) 초기 프로모터, 허피스 심플렉스 바이러스(HSV) 사이미딘 키나아제 (TK) 프로모터, 바큘로바이러스 IE1 프로모터, 엘롱게이션 인자 1 알파 (EF1) 프로모터, 포스포글라이세레이트 키나아제(PGK) 프로모터, 유비쿼틴(Ubc) 프로모터, 알부민 프로모터, 마우스 메탈로사이오닌-L 프로모터 및 전사조절부위의 조절 서열, 유비쿼터스 프로모터 (HPRT, 비멘틴, α-액틴, 튜불린 등), 인터메디에이트 필라멘트(데스민, 뉴로필라멘트, 케라틴, GFAP 등)의 프로모터, 치료용 유전자(MDR, CFTR E또는 인자 VIII 타입 등)의 프로모터, 발병 또는 질병에 연관된 프로모터, 및 췌장 선포 세포에 활성이 있는 이라스타아제 I 유전자 조절 부위와 같이 조직 특이성을 보여주고 형질전환된 동물에 사용되는 프로모터; 췌장 베타세포에서 활성이 있는 인슐린 유전자 조절 부위, 림프계 세포에서 활성이 있는 면역글로불린 유전자 조절 부위, 정소, 유방, 림프계, 및 비만세포에서 활성이 있는 마우스 유방암 바이러스 조절 부위; 알부민 유전자, 간에서 활성이 있는 Apo AI 및 Apo AII 조절 부위, 간에서 활성이 있는 알파-태아단백질 유전자 조절 부위, 간에서 활성이 있는 알파 1-안티트립신 유전자 조절 부위, 골수세포에서 활성이 있는 베타-글로빈 유전자 조절 부위, 뇌 올리고덴드로사이트에서 활성이 있는 마이엘린 베이직 단백질 유전자 조절 부위, 골격근에서 활성이 있는 마이오신 라이트 체인-2 유전자 조절 부위, 및 시상하부에서 활성이 있는 고나도트로픽 방출 호르몬 유전자 조절 부위, 피루베이트 키나아제 프로모터, 빌린 프로모터, 지방산 결합 소장 단백질의 프로모터, 평활근 세포 α-액틴의 프로모터 등. 뿐만 아니라, 이들 발현 서열은 인핸서 또는 조절 서열 등의 첨가에 의해 변형될 수 있다.
벡터는 바람직한 숙주 세포에 당업자에 알려진 방법으로 도입될 수 있다. 예를 들어 그 방법은 다음을 포함한다: 트랜스펙션, 전기천공법, 마이크로인젝션, 트랜스덕션, 세포 융합, DEAE 덱스트란, 칼슘 인산 침전법, 리포펙션 (리포솜 융합), 유전자 총 사용, 또는 DNA 벡터 트랜스포터(Wu et al, J. Biol. Chem. 267:963 (1992); Wu et al., J. Biol. Chem. 263:14621 (1988); and Hartmut et al., Canadian Patent Application No. 2,012,311 참조).
본 발명에 따른 폴리뉴클레오티드는 리포펙션에 의해 생체 내 로 또한 도입될 수 있다. 지난 십 년 동안, 시험관 내 에서 핵산을 인캡슐레이션 및 트랜스펙션하기 위해 리포솜 사용이 증가 되어왔다. 리포솜-매개 트랜스펙션이 당면한 어려움과 위험을 제한하기 위해 고안된 합성 양이온 지질은 마커를 코딩하는 유전자의 트랜스펙션의 리포솜을 제조하기 위해 사용될 수 있다(Feigner et al., Proc. Natl. Acad. Sci. USA. 84:7413 (1987); Mackey et al., Proc. Natl. Acad. Sci. USA 85:8021 (1988); and Ulmer et al., Science 259:1745 (1993)). 양이온 지질 사용은 음으로 대전된 핵산의 인캡슐레이션을 촉진할 수 있으며, 음으로 대전된 세포막과의 융합 또한 촉진한다(Feigner et al., Science 337:387 (1989)). 특히 핵산 트랜스퍼에 유용한 지질 화합물 및 조성물은 WO95/18863, WO96/17823 및 미국 5,459,127에 기술되어 있다. 생 체 내 에서 외래 유전자를 특이 기관에 도입하는데 리포펙션을 사용하면 임의의 실질적인 이점이 있다. 특정 세포에 대한 리포솜의 분자 타켓팅은 이점의 한 면을 제공한다. 분명하건데, 특정 세포 타입으로 트랜스펙션을 지시하는 것은 예를 들어, 췌장, 간, 신장, 및 뇌와 같이 세포가 이종인 조직에서 특히 바람직하다. 지질은 타켓팅 목적을 위해 다른 분자에 화학적으로 결합될 수 있다(Mackey et al. 1988, 위에서 인용). 예를 들어, 호르몬 또는 신경전달물질, 및 항체 또는 비펩타이드 분자와 단백질과 같은 타켓된 펩티드는 리포솜에 화학적으로 결합될 수 있다.
양이온 올리고펩티드(예, WO95/21931), DNA 결합 단백질로부터 도입된 펩타이드(e.g., WO96/25508)), 양이온 중압체(예, WO95/21931)와 같은 다른 분자들도 생체 내 에서 핵산의 트랜스펙션에 또한 유용하다.
벡터를 생체 내 에서 네이키드 DNA 플라스미드로서 도입하는 것 또한 가능하다(미국 특허 제 5,693,622, 5,589,466 및 5,580,859 호 참조). 수용체-매개 유전자 전송 접근법도 또한 사용될 수 있다(Curiel et al, Hum. Gene Ther. 3:147 (1992); and Wu et al, J. Biol Chem. 262:4429 (1987)).
"트랜스펙션"이라는 용어는 세포에 의해 외래 또는 이종 기원의 RNA 또는 DNA를 흡수하는 것을 가리킨다. 그러한 RNA 또는 DNA가 세포 내로 도입되었을 때, 세포는 외래 또는 이종 기원의 RNA 또는 DNA에 의하여 "트랜스펙션" 된다. 트랜스펙션된 RNA 또는 DNA가 형질 변화를 유발할 때, 세포는 외래 또는 이종 기원의 RNA 또는 DNA에 의하여 "형질전환" 된다. 형질전환 시키는 RNA 또는 DNA는 세포의 게놈을 이루는 염색체 DNA 내로 통합(공유 결합)될 수 있다.
"형질전환"이라는 용어는 유전적으로 안정한 상속을 이끌어내는 숙주 개체의 게놈 내로의 핵산 단편 트랜스퍼를 가리킨다. 형질전환된 핵산을 지닌 숙주 개체는 "이식유전자의" 또는 "재조합", 또는 "형질전환된" 개체로 명칭된다.
뿐만 아니라, 본 발명에 따라 폴리뉴클레오티드를 포함하는 재조합 벡터는 증폭과 그들의 발현을 원하는 세포 숙주에서 하나 이상의 복제 기원, 마커, 또는선택 마커를 포함할 수 있다.
"선택 마커"라는 용어는 마커 유전자의 효과를 바탕으로 선택될 수 있는 일반적으로 항생제 또는 화학적 저항 유전자와 같은 동정 인자를 가리킨다. 여기서 마커 유전자의 효과는 항생제에 대한 내성, 제초제에 대한 내성, 측색 마커, 효소, 형광 마커 등을 포함하며, 여기서 이들의 효과는 관심 핵산의 상속을 추적 및/또는 관심 핵산을 상속하는 세포 또는 생명체를 동정하기 위해 사용된다. 당업자에게 알려진 선택 마커 유전자의 예는 하기를 포함한다: 암피실린, 스트렙토마이신, 젠타마이신, 카나마이신, 하이그로마이신, 비알라포 제초제, 설폰아마이드 등; 및 안토사이아닌 조절 유전자, 이소펜타닐 트랜스퍼라아제 유전자 등과 같이 형질 마커로 사용되는 유전자.
"리포터 유전자"라는 용어는 리포터 유전자 효과를 바탕으로 동정될 수 있는 동정 인자를 코딩하는 핵산 서열을 가리킨다. 여기서 이들의 효과는 관심 유전자의 상속을 추적, 관심 유전자를 상속하는 세포 또는 생명체를 동정, 및/또는 유전자 발현 도입 또는 전사를 측정하기 위해 사용된다. 당업자에게 알려진 리포터 유전자의 예는 하기를 포함한다: 루시퍼라아제 (Luc), 녹색 형광 단백질 (GFP), 클로람페니콜 아세틸트랜스퍼라아제 (CAT), β-갈락토시다아제 (LacZ), β-글루커로니다아제(Gus) 등. 선택 마커 유전자는 또한 리포터 유전자로 고려될 수 있다.
"프로모터 및 프로모터 서열"이라는 용어는 서로 바뀌어 사용될 수 있으며 핵산 전사를 조절할 수 있는 DNA 서열을 가리킨다. 프로모터는 네이티브 유전자로부터 완전하게 도입되거나, 또는 자연에 존재하는 다른 프로모터들로부터 도입된 다른 서열들로 이루어지거나, 또는 합성 DNA 단편을 포함할 수 있다. 당업자들에게 다른 프로모터는 다른 조직 또는 세포 타입에서, 또는 발생의 다른 단계에서, 또는 다른 환경 또는 생리학적 조건에 반응하여 유전자 발현을 지시할 수 있다고 알려져 있다. 항상 대다수의 세포 타입에서 유전자가 발현되도록 하는 프로모터를 흔히 "항시적 프로모터" 라고 명칭한다. 특정 세포 타입에서 유전자가 발현되도록 하는 프로모터를 흔히 "세포-특이적 프로모터" 또는 "조직-특이적 프로모터" 라고 명칭한다. 발생 또는 세포 분화의 특이한 단계에서 유전자가 발현되도록 하는 프로모터를 흔히 "발생-특이적 프로모터" 또는 "세포 분화-특이적 프로모터" 라고 명칭한다. 프로모터를 도입하는 제제, 생물학적 분자, 화합물, 리간드, 빛 등을 세포에 노출 또는 처리할 때, 유전자가 발현되도록 하는 프로모터를 흔히 "유도 프로모터" 또는 "조절가능한 프로모터" 라고 명칭한다. 보다 구체적으로, 대다수의 경우, 조절 서열의 정확한 경계가 완벽히 정의되지 않고 있기 때문에 다른 길이의 DNA 단편들도 동일한 프로모터 서열 활성을 포함할 수 있다.
프로모터 서열은 통상적으로 3' 말단에서 전가 개시점과 경계를 이루고 백그라운드 이상의 수준으로 탐지되는 전사 개시에 필요한 최소 수의 염기 또는 서열을 포함하도록 상류 방향 (5' 방향)으로 확장한다. 프로모터 서열 내에서 전사 개시 점(편의상 예를 들어, Sq 뉴클리아제에 의해 맵핑)된 뿐만 아니라 RNA 중합효소-매개 전사를 이끄는 전사인자가 결합하는 단백질 결합 도메인(컨센서스 서열)이 발견될 것이다.
"진단 스위치 프로모터"라는 용어는 프로모터를 가리키며, 이들의 활성은 본 발명에서 진단 도구로 사용될 수 있는 인자에 의해 조절된다. 상기 용어는 두 방향 중 하나의 프로모터 활성의 변화가 진단 도구가 될 것이기 때문에 질병 또는 장애기간 동안 코딩 서열의 발현을 증가 또는 감소시키는 프로모터를 포함한다. 상기 용어는 질병 특이-프로모터, 특별한 생리학적 또는 병리학적 조건에 반응하는 프로모터, 및 특이 생물 분자에 반응하는 프로모터를 포함하나, 여기에 제한적이지는 않다. 진단 스위치 프로모터는 자연발생적인 프로모터의 서열, 자연발생적인 프로모터로부터 도입된 변형된 서열, 또는 합성 서열(예, 프로모터의 반응성을 변화시키기 위해 프로모터 서열 내에 반응 서열을 삽입).
"코딩 서열"이라는 용어는 폴리펩티드 또는 RNA를 코딩하는 DNA 서열을 가리킨다(예, 기능성 RNA).
코딩 서열은 세포에서 RNA 중합효소가 코딩 서열을 RNA로 전사할 때, 전사 및 번역 조절 서열의 "통제(조절)"하에 있다. 코딩 서열이 단백질 코딩 서열이라면, 일차 RNA 전사체는 보다 더 프로세싱되어(예, 트랜스-RNA 스플라이싱(코딩 서열이 인트론을 포함한다면) 및 폴리아데닐레이션) 세포질로 옮겨진 다음, 코딩 서열로 코딩되는 단백질로 번역된다. 단백질을 코딩하지 않는 생물 활성 RNA 종은 일차 전사체, 스플라이싱된 전사체(폴리아데닐레이션이 있거나 또는 없거나) 및/또는 잘려진 인트론으로서 핵에서 기능적일 수 있다; 또는 핵 밖의 세포 지역에서 핵 밖으로 옮겨진 RNA 형태로서 활성을 나타낼 수 있다.
"전사 및 번역 조절 서열"이라는 용어는 프로모터, 인핸서, 터미네이터, 등 과 같은 DNA 조절 서열을 가리키며, 숙주 세포에서 코딩 서열의 발현을 제공한다. 진핵 세포에서, 폴리아데닐레이션 신호가 조절 서열이다.
"반응 서열"이라는 용어는 전사인자의 DNA-결합 도메인과 작용하여 프로모터에 반응성을 부여하는 하나 이상의 시스-액팅 DNA 서열을 가리킨다. 이러한 DNA 서열은 서열상 대칭(완전 또는 불완전)을 이루거나 또는 다양한 뉴클레오티드로 분리된 서열 모티프 또는 반쪽 부위로 이루어져 있다. 반쪽 부위는 유사하거나 또는 동일할 수 있으며 둘 중 한 방향으로 또는 인버티드 리피트 또는 단일 반쪽 부위로 또는 일렬로 이웃한 반쪽 부위의 멀티머로 배열될 수 있다. 반응 서열은 반응 서열이 병합되는 세포 또는 생명체의 성질에 따라 다른 생명체로부터 분리된 최소의 프로모터를 포함할 수 있다. 전사인자의 DNA-결합 도메인은, 리간드의 존재 또는 부재하에서, 이 반응 서열의 조절하에 있는 하류 유전자의 전사를 개시 또는 억제하기 위해 반응 서열의 DNA 서열에 결합한다. 천연형 엑디손 수용체의 반응 서열의 DNA 서열의 예는 하기를 포함한다: RRGG/TTCANTGAC/ACYY (서열 번호: 1) (Cherbas et. al, Genes Dev. 5:120 (1991) 참조); AGGTCAN(n)AGGTCA, 여기서 N(n)는 하나 이상의 스페이서 뉴클레오티드일 수 있다 (서열 번호: 2) (D'Avino et al., MoI. Cell. Endocrinol. 113:1 (1995) 참조); 및 GGGTTGAATGAATTT (서열 번호: 3) (Antoniewski et al., MoI. Cell Biol. 14:4465 (1994) 참조).
"작동가능하게 연결된"이라는 용어는 단일 핵산 단편상에서 핵산 서열들의 결합을 가리키며 한 서열의 기능이 다른 서열에 의해 영향받는다. 예를 들어, 프로모터는, 그것이 그 코딩 서열의 발현에 영향을 줄 수 있을 때, 코딩 서열에 작동가능하게 연결되어 있다(곧, 코딩 서열은 프로모터의 전사조절 통제하에 있다). 코딩 서열은 센스 또는 안티센스 방향으로 조절 서열에 작동가능하게 연결될 수 있다.
여기서 사용하는 "발현"이라는 용어는 핵산 또는 폴리뉴클레오티드의 전사에 의하여 RNA(예, 센스 RNA, 안티센스 RNA, 마이크로 RNA, 메신저 RNA, 이종 기원의 핵 RNA, 리보솜멀 RNA, 소간섭 RNA, 리보자임 등) 합성을 가리킨다. 발현은 mRNA의 단백질 또는 폴리펩티드로로의 번역도 또한 포함할 수 있다.
"카세트(cassette)", "발현 카세트", 및 "유전자 발현 카세트"라는 용어는 특정 제한 부위에 또는 상동 재조합에 의해 핵산 또는 폴리뉴클레오티드 내에 삽입될 수 있는 DNA 단편을 가리킨다. DNA 단편은 관심 폴리펩타이드를 코딩하는 폴리뉴클레오티드를 포함하고, 카세트 및 제한 부위는 카세트가 전사 및 번역을 위해 올바른 리딩 프레임으로 삽입될 수 있도록 고안되었다. "형질전환 카세트"는 관심 폴리펩티드를 코딩하는 폴리뉴클레오티드를 포함하고 특정 숙주세포의 형질 전환을 용이하게 하는 폴리뉴클레오티드 뿐만 아니라 서열을 갖는 특이한 벡터를 가리킨다. 본 발명의 카세트, 발현 카세트, 유전자 발현 카세트, 및 형질전환 카세트는 숙주세포에서 관심 폴리펩티드를 코딩하는 폴리뉴클레오티드의 강화된 발현을 하는 서열을 또한 포함할 수 있다. 이러한 서열은 하기를 포함하나, 여기에 제한적이지는 않다: 프로모터, 최소 프로모터, 인핸서, 반응 서열, 터미네이터 서열, 폴리아데닐레이션 서열 등.
본 발명의 목적으로서, "유전자 스위치"라는 용어는 프로모터와 연관된 반응 서열, 및 하나 이상의 리간드 존재하에서 반응 서열 및 프로모터가 병합된 유전자의 발현을 조절하는 리간드-의존 전사인자-기반 시스템의 조합을 가리킨다.
유전자 스위치에 대하여 "엑디손-기반(ecdysone-based)"이라는 용어는 자연발생적이거나 또는 적어도 합성 엑디손-수용체 리간드 결합 도메인의 기능성 부분을 포함 및 엑디손 수용체 리간드 결합 도메인에 결합하는 리간드에 반응하여 유전자 발현을 조절하는 유전자 스위치를 가리킨다.
"조절하다" 및 "조절하다"라는 용어는 핵산 또는 유전자 발현을 유도, 감소, 또는 저해하는 것을 의미하며, 결과적으로 단백질 또는 폴리펩티드 합성을 각각 유도, 감소, 또는 저해한다.
본 발명에 따라 폴리뉴클레오티드 또는 벡터는 보다 더 나아가 숙주세포에서 유전자 발현을 추진하는데 적합한 하나 이상의 프로모터를 포함할 수 있다.
본 발명의 구현예에서 사용될 수 있는 인핸서는 하기를 포함하나, 여기에 제한적이지는 않다: SV40 인핸서, 사이토메갈로바이러스(CMV) 인핸서, 엘롱게이션 인자 1 (EF1), 효모 인핸서, 바이러스 유전자 인핸서 등.
터미네이터 또는 폴리아데닐레이션 서열과 같은 종료 조절 부위는 바람직한 숙주에 태생적인 다양한 유전자로부터 또한 도입될 수 있다. 선택적으로, 종료 부위는 불필요할 수 있으나, 포함된다면 가장 바람직하다. 본 발명의 하나의 구현예에서, 종료 조절 부위가 합성 서열, 합성 폴리아데닐레이션 신호, SV40 후기 폴리아데닐레이션 신호, SV40 폴리아데닐레이션 신호, 소 성장 호르몬 (BGH) 폴리아데닐레이션 신호, 바이러스 종료 서열 등으로부터 도입되거나 또는 포함할 수 있다.
"3' 비-코딩 서열" 또는 "3' 번역되지 않은 부위(UTR)"라는 용어는 코당 서열의 하류(3')에 위치한 DNA 서열을 가리키며, 폴리아데닐레이션[poly(A)] 인식 서열과 mRNA 프로세싱 및 유전자 발현에 영향을 줄 수 있는 조절 신호를 코딩하는 다른 서열을 포함한다. 폴리아데닐레이션 신호는 일반적으로 mRNA 전구체 3' 말단의 폴리아데닐릭산 트랙트 첨가에 영향을 주는 것에 의해 특징된다.
"조절 부위"라는 용어는 제2 핵산 서열의 발현을 조절하는 핵산 서열을 가리킨다. 조절 부위는 특별한 핵산(상동 부위)을 발현하는데 자연발생적으로 책임이 있는 서열을 포함할 수 있거나 또는 다른 단백질 또는 심지어 합성 단백질(이종 기원 부위)을 책임지는 다른 근원의 서열을 포함할 수 있다. 특히, 서열은 원핵생물체, 진핵생물체, 또는 바이러스 유전자의 서열 또는 특이 또는 비특이 방식 및 유도 또는 비-유도 방식으로 유전자 전사를 촉진 또는 억제하는 도입된 서열일 수 있다. 조절 부위는 복제 기원, RNA 스플라이싱 부위, 프로모터, 인핸서, 전사 종료 서열, 및 폴리펩티드를 타켓 세포의 분비 경로로 인도하는 신호 서열을 포함한다.
"이종 기원"으로부터의 조절 부위는 발현된 핵산과 자연발생적으로 연관이 되지 않는 조절 부위를 가리킨다. 이종 기원 조절 부위는 다른 종으로부터의 조절 부위, 다른 유전자로부터의 조절 부위, 하이브리드 조절 서열, 및 자연발생적으로 일어나지 않지만 당업자에 의해 고안된 조절 서열을 포함한다.
"RNA 전사체"라는 용어는 DNA의 RNA 중합효소-촉매 전사로부터 얻어진 산물을 가리킨다. RNA 전사체가 DNA 서열의 완전한 상보적 카피일 때, 일차 전사체라고 명칭된다. 또는 일차 전사체의 전사 후 프로세싱으로부터 유래된 RNA 서열일 수 있고, 이들은 성숙한 RNA라고 명칭된다. "전령 RNA (mRNA)"라는 용어는 인트론이 없고 세포에서 단백질로 번역되는 RNA를 가리킨다. "cDNA"라는 용어는 mRNA로 부터 유래되고 이들에 상보적인 이중 가닥의 DNA를 가리킨다. "센스 RNA"는 mRNA를 포함하고 세포에서 단백질로 번역될 수 있는 RNA 전사체를 가리킨다. "안티센스 RNA"는 타켓 일차 전사체 또는 mRNA의 모두 또는 일부분에 상보적인 RNA 전사체를 가리키고 타켓 유전자의 발현을 블로킹한다. 안티센스 RNA의 상보성은 특정 유전자의 곧, 5' 비-코딩 서열, 3' 비-코딩 서열, 또는 코딩 서열과 같은 임의의 부분과도 이룰 수 있다. "기능성 RNA"라는 용어는 안티센스 RNA, 리보자임 RNA, 또는 번역은 되지 않았으나 세포 프로세스에 영향을 주는 다른 RNA를 가리킨다.
"폴리펩티드", "펩티드", 및 "단백질"라는 용어는 서로 바뀌어 사용될 수 있으며 공유결합으로 연결된 아미노산 잔기들로 이루어진 중합체 화합물을 가리킨다.
"분리된 폴리펩티드", "분리된 펩티드", 및 "분리된 단백질"라는 용어는 자연상태에서 단백질들과 같이 정상적으로 연관된 화합물(예, 다른 단백질 또는 폴리펩타이드, 핵산, 탄수화물, 지질)이 전혀 없는 폴리펩티드 또는 단백질을 가리킨다. "분리된"이라는 용어는 다른 화합물을 지닌 인공 또는 합성 혼합물 또는 생물 활성을 방해하지 않는, 예를 들어 불완전한 정제, 안정제의 첨가, 또는 약리학적으로 허용된 제제로의 화합에 기인하여 존재할 수 있는 불순물의 존재를 제외하는것은 아니다.
"치환 변이 폴리펩티드" 또는 "치환 변이"라는 용어는 야생형 또는 자연발생적인 폴리펩티드에 대하여 적어도 하나의 야생형 또는 자연발생적인 아미노산이 다른 아미노산으로 치환된 변이 폴리펩티드를 의미하려고 이해될 것이다. 치환 변이 폴리펩티드는 오직 하나의 야생형 또는 자연발생적인 아미노산 치환을 포함할 수 있으며 이들은 "점 돌연변이" 또는 "단일 점 돌연변이" 폴리펩티드라고 명칭한다. 다르게는, 치환 변이 폴리펩티드는 야생형 또는 자연발생적인 폴리펩티드에 대하여 2 개 이상의 야생형 또는 자연발생적인 아미노산이 다른 아미노산으로 치환 변이된 것을 포함할 수 있다. 본 발명에 따라, 하나의 치환 변이를 포함하는 그룹 H 핵 수용체 리간드 결합 도메인 폴리펩티드는 야생형 또는 자연발생적인 그룹 H 핵 수용체 리간드 결합 도메인 폴리펩티드에 대하여 2 개 이상의 야생형 또는 자연발생적인 아미노산이 다른 아미노산으로 치환 변이된 것을 포함한다.
치환 변이 폴리펩티드가 2 개 이상의 야생형 또는 자연발생적인 아미노산의 치환을 포함한다면, 이들 치환은 치환을 위해 제거된 동일한 수의 야생형 또는 자연발생적인 아미노산, 곧, 2 개 이상의 비-야생형 또는 비-자연발생적인 아미노산으로 치환된 2 개 이상의 야생형 또는 자연발생적인 아미노산을 포함할 수 있다. 또는 이들 치환은 치환을 위해 지워진 동일하지 않은 수의 야생형 아미노산, 곧, 1 개의 비-야생형 아미노산으로 치환된 2 개의 야생형 아미노산(치환+결손 변이) 또는 3 개의 비-야생형 아미노산으로 치환된 2 개의 야생형 아미노산을 포함할 수 있다(치환+삽입 변이).
치환 변이는 축약된 명명법을 사용하여 아미노산 잔기 및 레퍼런스 폴리펩티드 서열 내에서 대체될 숫자 및 새로 치환된 아미노산을 표기하기 위해서 기술될 수 있다. 예를 들어, 폴리펩티드의 20 번째 아미노산이 치환된 치환 변이는 "x20z"로 축약될 수 있고, 여기서 "x"는 대체될 아미노산, "20"은 폴리펩티드 내의 아미노산 위치 또는 숫자, 및 "z"는 새롭게 치환된 아미노산이다. 그리하여, 서로 바뀌어 사용될 수 있게 축약된 치환 변이 "E20A" 또는 "Glu20Ala"는 폴리펩티드 20번째 위치에서 글루타믹 산(흔히 축약하여 "E" 또는 "GIu") 대신에 알라닌 잔기(흔히 축약하여 "A" 또는 "Ala")를 포함하고 있음을 기술한다.
치환 변이는 당업자에게 알려진 임의의 돌연변이 생성 기술에 의해 만들어 질 수 있고 이들은 시험관 내 부위-지시 돌연변이 (Hutchinson et al, J. Biol. Chem. 253:6551 (1978); Zoller et al, DNA 3:479 (1984); Oliphant et al, Gene 44:\11 (1986); Hutchinson et al, Proc. Natl. Acad. Sci. USA 83:710 (1986)), 탭® 링커의 사용(Pharmacia), 제한 엔도뉴클리아제 절단/단편 결손 및 치환, PCR-매개/올리고뉴클레오티드-지시 돌연변이 생성 등을 포함하나, 여기에 제한적이지는 않다. PCR-기반 기술은 부위-지시 돌연변이를 위해서 바람직하다(Higuchi, 1989, "Using PCR to Engineer DNA", in PCR Technology: Principles and Applications for DNA Amplification, H. Erlich, ed., Stockton Press, Chapter 6, pp. 61-70 참조).
폴리펩티드에 적용되는 "단편"이라는 용어는 아미노산의 서열이 레퍼런스 폴리펩티드보다 짧은 폴리펩티드를 가리키며, 레퍼런스 폴리펩티드의 전체 부분에 걸쳐 동일한 아미노산 서열을 포함한다. 그러한 단편들은 그들이 부분인 보다 더 큰 폴리펩티드의 적당한 곳에 포함될 수 있다. 본 발명에 따라 그러한 폴리펩티드 단편들은 2, 3, 4, 5, 6, 8, 10, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 25, 26, 30, 35, 40, 45, 50, 100, 200, 240, 또는 300 또는 그 이상의 아미노산 길이를 가질 수 있다.
폴리펩티드 또는 단백질의 "변이체"라는 용어는 폴리펩티드 또는 단백질로부터 유래된 임의의 유사체, 단편, 도입체 또는 변이체를 가리키며, 폴리펩티드 또는 단백질의 하나 이상의 생물 특성을 지니고 있다. 자연에는 폴리펩티드 또는 단백질의 다른 변이체가 존재할 수 있다. 이들 변이체는 단백질을 코딩하는 구조 유전자의 뉴클레오티드 서열상의 차이점으로 특징 지워지는 대립 유전자 변형체 일 수 있거나 또는 다른 스플라이싱 또는 번역 후 변형을 포함할 수 있다. 당업자들은 단일 또는 복수의 아미노산 치환, 결손, 첨가, 또는 대체를 지닌 변형체를 생성할 수 있다. 이들 변형체는 그 중에서도 특히 (a) 하나 이상의 아미노산 잔기가 보존 또는 비-보존 아미노산으로 치환된 변형체, (b) 하나 이상의 아미노산 잔기가 폴리펩티드 또는 단백질에 첨가된 변형체, (c) 하나 이상의 아미노산 잔기가 치환분 그룹을 포함하는 변형체, 및 (d) 폴리펩티드 또는 단백질이 혈청 알부민과 같은 다른 폴리펩티드와 융합된 변형체를 포함한다. 유전학적(억제, 결손, 변이 등), 화학적, 및 효소적 기술을 포하하는 이들 변형체를 얻는 기술은 당업자들에게 알려져 있다. 하나의 구현예에서, 변형체 폴리펩티드는 약 14 개 이상의 아미노산을 포함한다.
"상동 관계"라는 용어는 2 개의 폴리뉴클레오티드 또는 2 개의 폴리펩티드 반쪽들간의 동일한 정도의 퍼센트를 가리킨다. 한 부분과 다른 부분간의 서열 일치는 당업자에게 알려진 기술로 결정될 수 있다. 예를 들어, 서열 정보를 정렬 및 쉽게 입수가능한 컴퓨터 프로그램을 사용하여 2 개의 폴리펩티드 분자 간의 직접적인 서열 정보 비교를 통하여 상동 관계를 결정할 수 있다. 다르게는, 상동 부위 간에 안정적인 2 분자 복합체를 형성하는 조건하에서 폴리뉴클레오티드를 하이브리다이제이션한 후 단일-가닥-특이 뉴클리아제로 절단 및 절단된 단편의 크기 결정을 통하여 상동 관계를 결정할 수 있다.
여기서 사용하는 모든 문법적 형태 및 철자 변형에서 "상동"이라는 용어는 "공통적인 진화 근원"을 포함하는 단백질 간의 관계를 가리킨다. 이들 단백질은 슈퍼패밀리(예, 면역글로불린 슈퍼패밀리)로부터의 단백질 및 다른 종으로부터의 상동 단백질(예, 마이오신 라이트 체인 등)을 포함한다(Reeck et ah, Cell 50:667 (1987). 그러한 단백질(및 그들의 코딩 유전자)은, 높은 서열 유사성에 의해 반영되듯이, 서열 상동성을 지니고 있다. 그러나 흔히 사용되는 경우 및 본 출원에서는 "상동"이라는 용어는, 부사인 "높게"로 변형되었을 경우에만, 서열 유사성을 가리킬 수 있고 공통적인 진화 근원은 가지고 있지 않다.
따라서, 모든 문법적 형태에서 "서열 유사성"이라는 용어는 공통적인 진화 근원을 공유 또는 공유하지않던 간에 핵산 또는 단백질의 아미노산 서열간의 동일함 또는 일치의 정도를 가리킨다(Reeck et al, Cell 50:667 (1987 참조). 하나의 구현예에서, 뉴클레오티드의 50% 이상(예, 75%, 90%, 또는 95% 이상)이 DNA 서열의 정의된 길이 상에서 일치할 때 2 개의 DNA 서열은 "상당히 상동적이다" 또는 "상당히 유사하다"라고 말한다. 상당히 상동적인 서열은 서열 데이터 뱅크에서 입수 가능한 표준 소프트웨어를 사용한 서열 비교를 통하거나, 또는 예를 들어, 자신의 특정 시스템을 위해 정의된 스트린전트 조건하에서 서던 하이브리다이제이션 실험에서 동정될 수 있다. 정의된 해당 하이브리다이제이션 조건은 당업자에게 알려져 있다(e.g., Sambrook et al., 1989, 위에서 인용).
여기서 사용되는 "상당히 유사한"이라는 용어는 핵산 단편을 가리키며, 여기서 하나 이상의 뉴클레오티드 염기 변화가 하나 이상의 아미노산 치환을 가져오지만 DNA 서열에 의해 코딩되는 단백질의 기능적 성질에는 영향을 주지 않는다. "상당히 유사한"이라는 용어는 또한 다음의 핵산 단편을 가리키며, 여기서 하나 이상의 뉴클레오티드 염기 변화가 안티센스 또는 코-서프레션(co-suppression) 기술에 의한 유전자 발현 조절을 매개하는 핵산 단편의 능력에 영향을 주지 않는다. "상당히 유사한"이라는 용어는 또한 결과적인 전사체의 기능적 성질에는 실질적으로 영향을 주지 않는 하나 이상의 뉴클레오티드 염기의 결손 또는 삽입과 같은 본 발명의 핵산 단편의 변형을 가리킨다. 그러므로 본 발명은 특정적으로 대표적인 서열의 이상 범주를 포함한다. 상기에 제공된 각 변형 기술은 코딩된 산물의 생물 활성 보유의 결정에서처럼 당업자에게 알려진 일상적인 기술에 포함된다.
더우기, 당업자들은 본 발명에 의해 포함되는 상당히 유사한 서열이 스트린전트 조건(0.1X SSC, 0.1% SDS, 65°C 및 2X SSC로 세척, 0.1% SDS 후 0.1 X SSC, 0.1% SDS)하에서 여기에 예로 주어진 서열과 하이브리다이제이션 할 수 있는 능력에 의하여 또한 정의된다고 인식한다. 본 발명의 상당히 유사한 핵산 단편들은 그것의 DNA 서열이 여기에 보고된 핵산 단편의 DNA 서열에 70%, 80%, 90% 또는 95% 이상 동일하다.
2 개의 아미노산 서열은 아미노산의 40% 이상이 동일하거나, 또는 60% 이상 유사(기능적으로 동일)할 때 "상당히 상동적이다" 또는 "상당히 유사하다"라고 명칭한다. 바람직하게는, 유사 또는 상동적인 서열은 예를 들어, GCG(Genetics Computer Group, GCG 패키지의 프로그램 매뉴얼, 버전 7, Madison, Wisconsin) 파일업 프로그램을 사용한 정렬을 통해 동정될 수 있다.
여기서 사용되는 "일치하다"라는 용어는 유사한 또는 상동적인 서열을 가리키며, 유사 또는 상동이 측정되는 분자로부터 정확한 위치가 같은 수도 있거나, 또는 상이할 수 있다. 핵산 또는 아미노산 서열 정렬은 공백을 포함할 수 있다. 그리하여, "일치하다"라는 용어는 서열 유사성을 가리키나, 아미노산 잔기 또는 뉴클레오티드 염기의 숫자를 가리키지는 않는다.
아미노산 또는 핵산 서열의 "상당한 부분"이라는 용어는 그 폴리펩티드 또는 유전자를 잠정적으로 동정하기 위한 폴리펩티드의 충분한 아미노산 서열 또는 유전자의 충분한 핵산 서열을 포함한다. 이러한 동정은 당업자에 의해 수작업 평가, 또는 컴퓨터-자동화 서열 비교 및 BLAST(Basic Local Alignment Search Tool; Altschul et al, J. MoI. Biol. 275:403 (1993); ncbi.nhn.nih.gov/BLAST/에서 입수가능)와 같은 알고리즘을 사용한 동정에 의해 수행된다. 일반적으로, 10 개 이상의 연속적인 아미노산 또는 30 개 이상의 뉴클레오티 서열은 이미 알려진 단백질 또는 유전자에 상동적인 폴리펩티드 또는 핵산을 잠정적으로 동정하기 위해서 필요하다. 더우기, 핵산 서열에 대하여, 20-30개의 연속적인 아미노산을 포함하는 유전자 특이적 올리고뉴클레오티드 프로브는 유전자 동정(예, 서던 하이브리다이제이션) 및 분리(예, 박테리아 콜로니 또는 박테리아파아지 플라크의 in situ 하이브리다이제이션)의 서열-의존 방법에 사용될 수 있다. 뿐만 아니라, 12-15 개 염기의 짧은 올리고뉴클레오티드는 상기 프라이머를 포함하는 특정 핵산 단편을 얻기 위해서 PCR에서 증폭 프라이머로 사용될 수 있다. 따라서, 뉴클레오티드 서열의 "상당한 부분"이라는 용어는 상기 서열을 포함하는 핵산 단편을 특별히동정 및/또는 분리하기 위해서 충분한 서열을 포함한다.
당업자에게 알려진 "퍼센트 동일"이라는 용어는 2 개 이상의 폴리펩티드 서열 또는 2 개 이상의 폴리뉴클레오티드 서열간의 관계를 나타내고 이들은 서열 비교를 통해 결정된다. 당업자에게 "동일"이라는 용어는 폴리펩티드 또는 폴리뉴클레오티드 서열 간의 서열 관계의 정도를 또한 의미하며, 상기의 경우처럼, 그러한 서열의 스트링간의 매치에 의해 결정된다. "동일" 및 "유사성"은 하기를 포함하나, 여기에 제한적이지 않은 알려진 방법으로 쉽게 계산될 수 있다: Computational Molecular Biology (Lesk, A. M., ed.) Oxford University Press, New York (1988); Biocomputing: Informatics and Genome Projects (Smith, D. W., ed.) Academic Press, New York (1993); Computer Analysis of Sequence Data, Part I (Griffin, A. M., and Griffin, H. G., eds.) Humana Press, New Jersey (1994); Sequence Analysis in Molecular Biology (von Heinje, G., ed.) Academic Press (1987); and Sequence Analysis Primer (Gribskov, M. and Devereux, J., eds.) Stockton Press, New York (1991). 동일함(identity)을 결정하기 위한 바람직한 방법이 테스트되는 서열 간의 최적인 매치를 제공하기 위해 고안되었다. 동일함 및 유사성을 결정하기 위한 방법은 공개적으로 입수 가능한 컴퓨터 프로그램에 수록되어 있다. 서열 정렬 및 퍼센트 동일 계산은 LASERGENE 생물정보학 컴퓨팅 스위트(DNASTAR Inc., Madison, WI)의 Megalign 프로그램과 같은 서열 분석 소프트웨어를 사용하여 수행될 수 있다. 서열의 복수 정렬은 디폴트 매개변수(GAP PENALTY=IO, GAP LENGTH PENALTY=IO)를 가지고 정렬의 클러스터 방법(Higgins et al, CABIOS. 5:151 (1989))을 사용하여 수행될 수 있다. 클러스터 방법을 사용한 쌍(pairwise) 정렬을 위한 디폴트 매개변수가 선택될 수 있다: KTUPLE 1, GAP PENALTY=3, WIND0W=5 및 DIAGONALS SAVED=5.
"서열 분석 소프트웨어"라는 용어는 뉴클레오티드 또는 아미노산 서열 분석을 위해 유용한 임의의 컴퓨터 알고리즘 또는 소프트웨어 프로그램을 포함한다. "서열 분석 소프트웨어"라는 용어는 상업적으로 입수가능하거나 또는 독립적으로 개발될 수 있다. 통상적인 서열 분석 소프트웨어는 GCG 스위트 프로그램(Wisconsin 패키지 버전 9.0, Genetics Computer Group (GCG), Madison, WI), BLASTP, BLASTN, BLASTX (Altschul et al., J. MoI. Biol. 275:403 (1990)), 및 DNASTAR(DNASTAR, Inc. 1228 S. Park St. Madison, WI 53715 USA)을 포함하나, 여기에 제한적이지는 않다. 이러한 응용의 관점 내에서, 서열 분석 소프트웨어는 분석을 위해 사용되며, 다르게 언급되어 있지 않는한 분석 결과는 참조된 프로그램의 "디폴트 값"에 기반할 것이다. 여기서 사용하는 "디폴트 값"이라는 용어는 처음 초기화 될 때 소프트웨어와 같이 최초로 로딩되는 임의의 일련의 값 또는 매개변수를 의미할 것이다.
DNA 서열에 관하여, "화학적으로 합성"이라는 용어는 구성원인 뉴클레오티드가 시험관 내 에서 결합되었음을 의미한다. DNA의 수작업 화학적 합성은 잘 확립된 방법을 사용하여 수행될 수 있으며, 또는 자동화된 화학적 합성은 상업적으로 입수가능한 수많은 기계 중의 하나를 사용하여 수행될 수 있다. 따라서, 숙주 세포의 코돈 경향을 반영하기 위해서 뉴클레오티드 서열의 최적화에 기반한 최적의 유전자 발현을 위해 유전자가 제조될 수 있다. 당업자들은 코돈 사용의 경향이 숙주 세포가 사용하는 코돈으로 향할 경우 성공적인 유전자 발현의 가능성을 인식한다. 바람직한 코돈의 결정은 서열 정보가 입수가능한 숙주 세포로부터 유래된 유전자의 조사에 기반을 둘 수 있다.
여기서 사용하는, 2 개 이상의 개별적으로 작동 가능한 유전자 조절 시스템은 하기의 경우에 "올소고날(orthogonal)"이라고 명칭한다; a) 선택된 농도에서 리간드에 의한 주어진 각 시스템의 조절이 그 시스템의 유전자 발현의 크기에서 측정가능한 변화를 유발할 때, 및 b) 상기 변화가 세포, 조직, 또는 생명체에서 동시에 작동 가능한 모든 다른 시스템의 발현의 변화와 동시성 또는 이후의 실제적인 조절에 관계없이 통계학적으로 상당히 다를 때. 바람직하게, 각 개별적으로 작동 가능한 유전자 조절 시스템의 조절은 세포, 조직, 또는 기관에서 모든 다른 작동 가능한 시스템보다 2 배 이상, 예를 들어, 5 배, 10 배, 100 배, 또는 500 배 이상으로 유전자 발현 변화에 영향을 준다. 이상적으로, 선택된 농도에서 각 해당 리간드에 의한 주어진 각 시스템의 조절은 그 시스템의 유전자 발현의 크기에 측정가능한 변화를 유발하고, 세포, 조직, 또는 생명체에서 작동 가능한 모든 다른 시스템의 발현에서는 임의의 측정가능한 변화도 유발하지 않는다. 그러한 경우, 복수의 유도 유전자 조절 시스템은 "완전히 올소고날"이라고 명칭한다. 본 발명은 원문 전체로 참고로 여기에 도입된 미국 2002/0110861 Al에 개시된 것과 같이 올소고날 리간드 및 올소고날 수용체-기반 유전자 발현 시스템을 조사하는데 유용하다.
"외래 유전자"라는 용어는 개체에 이질적인 유전자를 의미한다. 곧, 형질 전환을 통하여 내생적인 변이 유전자의 변이되지 않은 버전 또는 내생적인 변이되지 않은 유전자의 변이된 버전으로 개체에 도입되는 유전자이다. 형질 전환 방법은 본 발명에서 중료하지 않고 당업자에게 알려진 개체에 적당한 임의의 방법일 수 있다. 외래 유전자는 개체에 역전사 효소와 같은 DNA 매개물을 통해 기능할 수 있는 DNA 또는 RNA의 형태로 도입되는 자연적 또는 합성 유전자 및 치료용 유전자일 수 있다. 그러한 유전자는 타켓 세포에 도입될 수 있고, 개체에 직접적으로 도입될 수 있거나 또는 형질 전환된 세포를 개체으로 트랜스퍼하여 간접적으로 도입할 수 있다. "치료용 유전자"라는 용어는 유전자가 발현되는 숙주 세포에 유익한 기능을 부여하는 유전자를 의미한다.
"엑디손-수용체 복합체"라는 용어는 일반적으로 엑디손 수용체("EcR") 및 울트라스피라클("USP") 단백질인 2 개 이상의 핵 수용체 단백질 패밀리를 지닌 이형이량체 단백질을 가리킨다(Yao et al, Nature 366:476 (1993); Yao et al., Cell 77:63 (1992) 참조). 기능성 EcR 복합체는 또한 임뮤노필린과 같은 부가적인 단백질을 포함한다. 전사인자(DHR38, betaFTZ-1 또는 다른 곤충 단백질과 같은)로 알려진 부가적인 핵 수용체 패밀리의 단백질은 EcR 및/또는 USP 에 대해 또한 리간드 의존 또는 리간드에 독립적인 파트너일 수 있다. EcR 복합체는 또한 EcR 단백질의 이형이량체 및 울트라스피라클 단백질의 상동체, 레티노익산-X-수용체("RXR") 단백질일 수 있다. EcR 복합체라는 용어는 EcR 단백질 또는 USP의 동종 2분자 복합체를 또한 포함할 수 있다.
EcR 복합체는 EcR을 포함하나 복합체의 다른 단백질을 제외하는 복합체의 단백질 중 하나에 결합된 활성 엑디스테로이드 또는 비-스테로이드 리간드에 의하여 활성화될 수 있다. EcR-기반 유전자 스위치에 적용되는 것 같이, 여기서 사용하는 "리간드"라는 용어는 코딩된 폴리펩티드의 발현을 촉진하기 위해 유전자 스위치를 활성화할 수 있는 작고 용해가능한 분자를 가리킨다. 리간드의 예는 하기를 포함하나, 여기에 제한적이지는 않다: 엑디손과 같은 엑디스테로이드, 20-하이드록시엑디손, 포나스테론 A, 뮤리스테론 A 등, 9-시스-레티노익 산의 합성 유사체, 미국 특허 제 6,013,836호, 5,117,057, 5,530,028 및 5,378,726 호 및 미국 공개 특허 제 2005/0209283 및 2006/0020146호에 개시된 N,N'-다이아실하이드러진; 미국 공개 특허 제 2004/0171651호에 개시된 옥사다이아졸린; 유럽 특허 출원 제 461,809에 개시된 다이벤조일알킬 사이아노하이드러진; 미국 특허 제 5,225,443에 개시된 N-알킬-N,N'-다이아로일하이드러진; 유럽 특허 출원 제 234,994에 개시된 N-아실-N-알킬카르보닐하이드러진; 미국 특허 제 4,985,461에 개시된 N-아로일-N-알킬-N'-아로일하이드러진; 미국 공개 특허 제 2004/0049037호에 개시된 아미도케톤; 하기를 포함하고 참고로 여기에 도입된 각각의 것 및 다른 유사한 물질: 3,5-다이-tert-부틸-4-하이드록시-N-이소부틸-벤자마이드, 8-O-아세틸하파자이드, 옥시스테롤, 22(R) 하이드록시콜레스테롤, 24(S) 하이드록시콜레스테롤, 25-에폭시콜레스테롤, T0901317, 5-알파-6-알파-에폭시콜레스테롤-3-설페이트(ECHS), 7-케토콜레스테롤-3-셀페이트, 파메솔, 담즙산, 1,1-바이포스포네이트 에스터, 쥬번나일 호르몬 등. 본 발명에서 유용한 다이아실하드러진 리간드의 예는 RG-115819 (3,5-ㄷ다다이메틸-벤조익산 N-(l-에틸-2,2-다이메틸-프로필)-N'-(2-메틸-3-메속시-벤조일)-하이드러자이드), RG-115830 (3,5-다이메틸-벤조익산 N-(l-tert-부틸-부틸)-N'-(2-에틸-3-메속시-벤조일)-하이드러자이드), 및 RG-115932 ((R)-3,5-다이메틸-벤조익산 N-(l-tert-부틸-부틸)-N'-(2-에틸-3-메속시-벤조일)-하이드러자이드). 미국 특허 제 12/ 155, 111를 참조하라.
EcR 복합체는 핵 수용체 슈퍼패밀리의 멤버인 단백질을 포함하고 있고, 이들 모든 멤버는 경첩 부위로 분리된 아미노-말단 전사활성화도메인("TA"), DNA 결합 도메인("DBD"), 및 리간드 결합 도메인("LBD")의 존재로 특징지워진다. 상기 패밀리의 몇몇 멤버는 LBD의 카르복실 말단 쪽에 다른 전사활성화도메인을 또한 가질 수 있다. DBD는 P-박스 및 D-박스인 2개의 아미노산 모티프 사이의 2 개의 시스테인 아연 핑거의 존재로 특징지워진다. 이들 박스는 엑디손 반응 서열에 특이성을 부여한다. 이들 도메인은 자연적, 변형된 또는 이종 기원의 수용체 단백질의 다른 도메인의 키메라일 수 있다.
외래 유전자, 반응 서열, 및 상기 EcR 복합체를 이루는 DNA 서열은 아키박테리아, 대장균, 바실러스 서브틸러스, 또는 다른 엔테로박테리아와 원핵생물체, 또는 식물 또는 동물 세포와 같은 진핵생물체에 병합될 수 있다. 그러나, 유전자에 의해 발현되는 수 많은 단백질들은 박테리아에서는 올바르지 않게 프로세싱되기 때문에, 진핵생물체가 선호된다. 상기의 세포는 단일 세포 또는 다세포 생명체의 형태일 수 있다. 외래 유전자, 반응 서열, 및 수용체 복합체에 대한 뉴클레오티드 서열은 RNA 분자 내에 바람직하게는 담배 모자이크 바이러스와 같은 기능성 바이러스 RNA의 형태로 또한 병합될 수 있다. 진핵 생물체 중에서는, 본 발명의 EcR 리간드에 반응을 부여하는 분자들이 자연발생적으로 부족하기 때문에 척추동물 세포가 선호된다. 결과로서, 그들은 본 발명의 리간드에 "상당히 무감각"하다. 그리하여, 본 발명에 유용한 상기의 리간드는 형질 전환된 세포 또는 전체 생명체에서 무시될 수 있는 효과 또는 다른 효과를 가질 것이다. 그러므로, 세포는 실질적으로 리간드 자체의 영향을 받지 않으면서, 성장할 수 있고 바람직한 산물을 발현할 수 있다.
"개체"이라는 용어는 온전한 곤충, 식물, 또는 동물을 의미한다. 또한 상기의 개체이 곰팡이나 효모일 때 상기의 리간드가 양호하게 작용하리라 예상된다. 개체이 온전한 동물체라면, 바람직한 동물은 척추동물, 가장 바람직하게 포유류이다.
외래 유전자(예, 리포터 유전자)에 연결된 반응 서열에 결합하는 EcR 복합체와 같이 사용되는 EcR 리간드는 외래 유전자 발현의 외부적 시간 조절을 위한 도구를 제공한다. 다양한 구성요소가 서로 결합하는 순서, 곧, 리간드가 수용체 복합체에 결합 및 수용체 복합체가 반응 서열에 결합의 순서는 중요하지 않다. 통상적으로, 외래 유전자 발현의 조절은 EcR 복합체가 특이적인 조절 DNA 서열에 결합함으로써 반응한다. EcR 단백질은, 다른 멤버의 핵 수용체 패밀리 같이, 3 개 이상의 도메인인 전사활성화 도메인, DNA 결합 도메인, 및 리간드 결합 도메인을 포함한다. 핵 수용체 패밀리의 하부그룹과 같이, 이 수용체는 이형이량체화 성질을 책임지는 정교하지 않은 부위를 또한 지니고 있다. USP 또는 RXR 던백질의 이형이량체화 후에, 리간드가 EcR 단백질의 리간드 결합 도메인에 결합하면 이형이량체 단백질의 DNA 결합 도메인으로 하여금 활성화된 형태로 반응 서열에 결합하도록 도입하고, 그리하여 외래유전자 발현 또는 억제를 지시한다. 이러한 기작은 EcR 또는 USP로의 리간드 결합의 잠재적 가능성 또는 결과적으로 생기는 활성화된 동종 2분자 복합체의 형성을 배제하지는 않는다(예, EcR+EcR 또는 USP+USP). 하나의 구현예에서, 하나 이상의 수용체 도메인은 변화되어 키메릭 유전자 스위치를 생성할 수 있다. 통상적으로, 하나 이상의 3 개의 도메인이 다른 도메인들의 근원과 다른 근원으로부터 선택되어 키메릭 수용체가 트랜스액팅 활성, 리간드의 상보적 결합, 및 특이적 반응 서열의 인지를 위하여 선택된 숙주 세포 또는 생명체에서 최적화된다. 뿐 만 아니라, 반응 서열 그 자체도 키메릭 EcR 복합체를 수용하기 위한 효모로부터의 GAL-4 단백질(Sadowski et al, Nature 555:563 (1988) 참조) 및 대장균으로부터의 LexA 단백질(Brent et al, Cell 43:729 (1985) 참조)과 같은 다른 DNA 결합 단백질 도메인에 대한 반응 서열을 가지고 변형 또는 치환될 수 있다. 키메릭 시스템의 다른 이점은 그들이 바람직한 최후 효과에 따라 외래유전자를 추진하는데 사용되는 프로모터의 선택을 가능하게 해주는 것이다. 특히 독성 단백질이 생성될 때, 이들의 발현 및 발현이 일어나는 세포의 타이밍이 조절될 수 있기 때문에 그러한 이중 조절은 유전자 치료법 영역에서 특히 중요할 수 있다. 해당 프로모터에 작동가능하게 연결된 외래 유전자가 개체의 세포 내로 도입되면, 외래 유전자의 발현은 본 발명의 리간드 존재에 의하여 조절된다. 프로모터는 항시적으로 또는 인듀서블하게 조절될 수 있거나 또는 조직 특이적(곧, 특정 타입의 세포에서만 오직 발현되는)이거나 또는 생명체의 특정 발생 단계에 특이적일 수 있다.
전사인자 및 리포터 유전자와 같은 다양한 폴리펩티드를 코딩하는 수 많은 게놈믹 및 cDNA 핵산 서열이 당업자에게 잘 알려져 있다. 당업자에게 알려진 기술은 알려진 모든 유전자에 대한 핵산 서열 정보에 접근할 수 있고, 분자의 서열이나 또는 분자를 제조하는 일상적인 방법을 사용하는 기관인 공공 보관소로부터 직접 핵산 분자를 얻을 수 있다.
생체 내 사용에 대해서, 여기에 기술된 리간드는 예를 들어, 용액, 현탁액, 타블릿, 캡슐, 연고, 연금약액, 및 주사가능한 조성물과 같은 약학적으로 허용된 전송체에 탑재될 수 있다. 약학적 조성물은 리간드의 무게로 0.01% 에서 99%를 포함할 수 있다. 조성물은 단일 또는 복수의 투여 형태일 수 있다. 임의의 특정 약학적 조성물에서의 리간드 양은 효능이 있는 투여량, 곧, 바람직한 유전자 발현 또는 억제를 도입하는데 필요한 양에 의존할 것이다.
약학적 제조물 투여의 알맞은 경로는 경구, 직장, 국소적(예, 피부, 구강 및 혀 밑), 질구, 비경구(예, 피하지방, 근육 내, 정맥 내, 피 내, 수막강 내 및 경막 외), 및 비위관을 포함한다. 당업자들에게 바람직한 투여 경로는 진단이 이루어지는 조건 및 투여자의 상태와 같은 인자에 의해 달라질 수 있다.
본 발명의 하나의 구현예는 상기 개체의 세포에 (1) 유전자 스위치를 코딩하는 폴리뉴클레오티드, 이때, 상기 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하며, 여기서 상기 적어도 하나의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하고, 작동가능하게 진단 스위치 프로모터와 연결되며, 여기서 상기 프로모터의 활성은 상기 개체의 질병 또는 장애 기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 도입하여 변형된 세포를 생산하는 단계; (b) 상기 변형된 세포에 리간드를 투여하는 단계; 및 (c) 리포터 유전자 발현을 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현이 상기 개체가 상기 질병, 장애, 또는 증상을 가짐을 지시하는 것인, 상기 개체에서 질병 또는 장애를 진단하는 방법을 포함한다.
하나의 구현예에서, 상기 개체로부터 분리된 세포에서 생체 외로 진단 방법이 수행된다.
하나의 구현예에서, 상기의 진단 방법은 변형된 세포를 생성하기 위해 본 발명의 조성물을 상기 개체로부터 분리된 세포에 도입함으로써 수행되며, 및 상기의 변형된 세포는 상기 개체에 재도입된다.
하나의 구현예에서, 진단 방법은 생 체 내 에서 수행된다.
다른 구현 예에서, 상기의 진단 방법은 상기 개체로부터 얻은 자가 조직 세포 대신에 상기 개체에게 동종이계 또는 이종인 세포인 비-자가 조직 세포를 사용하여 수행될 수 있다. 변형된 세포를 생성하기 위해 폴리뉴클레오티드가 생체 외에서 상기 비-자가 조직 세포에 도입되고, 그런 다음 상기의 변형된 세포는 상기 개체에 도입된다. 비-자가 조직 세포는 개체에 이식된 후에 살아남는 임의의 세포일 수 있고, 이들은 줄기세포(배아 줄기세포 또는 조혈모 줄기세포와 같은) 및 섬유아세포를 포함하나, 여기에 제한적이지는 않다.
본 발명의 하나의 구현예는 상기 비-자가 조직 세포에 (1) 유전자 스위치를 코딩하는 폴리뉴클레오티드, 이때, 상기 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하며, 여기서 상기 적어도 하나의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하고, 작동가능하게 진단 스위치 프로모터와 연결되며, 여기서 상기 프로모터의 활성은 상기 개체의 질병 또는 장애 기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 도입하여 변형된 세포를 생산하는 단계; (b) 상기 변형 세포를 상기 개체에 도입; (c) 상기 변형된 세포에 리간드를 투여하는 단계; 및 (d) 리포터 유전자 발현을 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현이 상기 개체가 상기 질병, 장애, 또는 증상을 가짐을 지시하는 것인, 상기 개체에서 질병 또는 장애를 진단하는 방법을 포함한다.
하나의 구현예에서, 유전자 스위치를 코딩하는 폴리뉴글레오티드와 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드는 예를 들어, 벡터와 같은 하나의 커다란 뉴클레오티드의 일부분이다. 다른 구현예에서, 유전자 스위치를 코딩하는 폴리뉴글레오티드와 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드는 독립된 폴리뉴클레오티드이다.
진단 방법이 실시되는 개체는 진단이 요구되는 임의의 개체일 수 있다. 예를 들어, 개체는 질병 또는 장애의 한가지 이상의 증상을 보이는 개체일 수 있다. 개체는 또한 질병 또는 장애에 취약하게 노출된 사람일 수도 있으며, 이는 유전, 가족 병력, 또는 환경적 노출에 기인한다. 개체는, 예를 들어 개체군에서 질병 또는 장애의 만연을 스크니닝하는 일부분으로서, 일반 대중의 일원일 수 있다.
본 발명의 방법에 의해 진단되는 질병 또는 장애는 한 가지 이상의 진단 스위치 프로모터가 효력이 있는 임의의 질병 또는 장애일 수 있다. 본 발명의 방법에 의해 진단될 수 있는 질병 또는 장애의 예는 암과 같은 고증식성 질병, 심혈관 질환, 신경 질환, 자가면역 질환, 이식편대숙주병(graft versus host disease), 이식 거부, 골 질환, 소화관 질환, 혈액 질환, 대사 질환, 염증 질환, 그리고 감염을 포함하나, 이에 제한되지 않는다.
본 발명의 한 구현예는 개체에서 질병 또는 장애를 진단하는 변형 세포의 제조방법에, 상기의 개체에게 세포를 도입을 포함한다 (1) 유전자 스위치를 코딩하는 폴리뉴글레오티드, 상기 유전자 스위치는 하나 이상의 전사인자 서열, 여기서 상기 하나 이상의 전사인자 서열은 리간드-의존 전사인자를 코딩한다. 여기서 리간드-의존 전사인자는 작동가능하게 진단 스위치 프로모터와 연결되어있다. 여기서 프로모터의 활성은 상기 질병 또는 장애 동안 조절된다. 그리고 (2) 변형된 세포를 생성하기 위해서 상기 리간드-의존 전사인자에 의해 활성화된 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드.
본 발명의 하나의 구현예는 (a) 상기 개체의 변형된 세포에 리간드를 투여하는 단계; 및 (b) 리포터 유전자 발현을 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현이 상기 개체가 상기 질병 또는 장애를 가짐을 지시하고, 여기서 상기 개체의 변형된 세포는 (1) 유전자 스위치를 코딩하는 폴리뉴클레오티드, 이때, 상기 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하며, 여기서 상기 적어도 하나의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하고, 작동가능하게 진단 스위치 프로모터와 연결되며, 여기서 상기 프로모터의 활성은 상기 개체의 질병 또는 장애 기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인, 상기 개체에서 질병 또는 장애를 진단하는 방법에 관한 것이다.
본 발명의 진단 유전자 프로모터는 특정 질병 또는 장애를 진단, 질병의 진행정도를 모니터, 또는 치료의 효능 또는 독성을 모니터하는데 유용한 임의의 프로모터일 수 있다. 예는 특정 질병 또는 장애 동안 증가 쪼는 감소된 발현을 보이는 유전자의 프로모터 및 특정 세포 조건하에서 증가 또는 감소된 발현을 보이는 유전자의 프로모터를 제한적이지 않지만 포함한다(예를 들어, 세포증식, 세포사멸, pH 변화, 산화 상태, 산소 레벨), 유전자 스위치가 하나 이상의 전사 인자 서열을 포함하는 일부 구현예에서 진단 방법의 특이성은 질병- 또는 조건-특이적 프로모터를 진단 측정이 일어나는 조직을 제한하고자 조직- 또는 세포타입-특이적 프로모터와 결합함으로써 증대될 수 있다. 그리하여, 조직- 또는 세포타입-특이적 프로모터는 진단 스위치 프로모터의 정의 내에 포함된다.
질병-특이적 프로모터의 예로서, 암 진단에 유용한 프로모터는 발암 유전자 프로모터를 포함한다. 발암 유전자 군의 예는 성장인자, 성장인자 수용체, 단백질 키나아제, 세포 예정 사멸(programmed cell death) 조절자, 그리고 전사인자를 포함하나, 여기에 국한하지 않는다. 발암 유전자의 특정 예는 sis, erb B, erb B-2, ras, abl, myc and bcl-2 그리고 TERT를 포함하나, 여기에 국한하지 않는다. 암과 관련한 다른 유전자 예는 종양 관련 항원 유전자 및 신생세포(neoplastic cell)에서 과발현되는 다른 유전자를 포함한다(예를 들어, MAGE-I, 암배아항원, 타이로신나아제, 전립선 특이 항원, 전립선 특이 막 항원, p53, MUC-I, MUC-2, MUC-4, HER-2/neu, T/Tn, MART-I, gplOO, GM2, Tn, sTn, 그리고 톰슨-프리덴라이히 항원(TF)).
본 발명에서 진단 스위치 프로모터로 유용하고 당업자에게 알려진 프로모터 서열과 다른 조절 요소(예, 인핸서)의 예는 표 1 및 2 에 열거된 참조문헌에, 질병/질환(표 1) 또는 각 프로모터와 연관된 조직 특이성(표 2)과 더불어, 개시되어있다. 이 참조 문헌에 개시된 프로모터 서열은 여기에 원문 전체로 참조로 도입되었다.
특이 질병 또는 장애 동안 발현 레벨에서 변화를 보여 본 발명에 유용한 다른 유전자는 표 3에 열거된 유전자(관련 질병/질환과 더불어)를 포함하나, 여기에 제한적이지 않다.
질병 또는 장애 동안 발현패턴이 변화되는 유전자가 동정 되면, 상기 유전자 프로모터는 본 발명의 유전자 스위치에 사용될 수 있다. 프로모터 부위를 포함하는 다수의 유전자 서열이 당업자에게 알려져 있고 진뱅크와 같은 공공 데이터베이스에서 이용할 수 있다. 그리하여, 해당 유전자가 한번 동정 되면, 프로모터 서열도 쉽게 동정 및 획득될 수 있다. 본 발명의 다른 양태는 프로모터가 분리 및 유전자 스위치에 놓일 수 있는 프로모터를 지닌 해당 유전자를 동정하는 것에 관한 것이다. 그러므로, 프로모터가 이후 세팅 또는 환경에서 분리 및 사용될 수 있다면, 유전자의 본질은 본 발명의 특정 구현예에 중요하지 않을 수도 있다. 그리하여, 본 발명은 아직까지 동정 되지 않은 유전자의 프로모터의 사용을 포함한다. 해당 유전자가 한번 동정되면, 프로모터 기능에 필요한 유전자 서열의 결정은 일상 기술 또는 실험의 문제일 수 있다. 사실, 몇 개의 상용 프로토콜이 관심 유전자의 프로모터 부위 결정에 도움을 주고자 존재한다. 한 예로서, 딩 등은 최근 신규 Sprouty4 유전자(참고로 도입된 Am. J. Physiol. Lung Cell. MoI. Physiol. 287: L52 (2004))의 프로모터 서열을, 인간 Sprouty4 유전자의 5' 상류 서열을 점진적으로 제거함으로써, 규명하였다. 간략하게, 전사 개시 위치가 일단 결정되면, 5' 상류 서열 단편들을 단일 방향으로 클로닝하기 위해, PCR 프라이머를 사용하여 PCR 단편들이 생성되었다. 생성된 단편들이 루시퍼라제 리포터 벡터에 클로닝되었고 인간 Sprouty4 유전자의 프로모터 부위를 결정하고자 루시퍼라제 활성도가 측정되었다.
유전자 프로모터를 획득하고 평가하는 프로토콜의 다른 예는 다음 단계를 포함한다: (1) 유사하거나/같은 조직 타입의 질병 및 비질병 세포/조직 샘플을 얻는다; (2) 샘츨로부터 전체 RNA 또는 mRNA를 분리한다; (3) 질병 및 비질병 RNA의 분별 마이크로어레이 분석을 수행한다; (4) 질병-특이 전사체 후보군을 발굴한다; (5) 질병-특이 전사체와 연관된 게놈 서열을 동정한다; (6) 질병-특이 전사체의 전사 개시 예상 위치의 상류 및 하류의 DNA 서열을 획득 또는 합성한다; (7) 단계 6에서 얻은 다른 길이의 DNA를 사용하여 프로모터 리포터 벡터를 디자인 및 생성한다; 그리고 (8) 관련이 없는 세포/조직뿐만 아니라 질병 및 비질병 세포/조직에서 프로모터 리포터 벡터를 테스트한다.
유전자 스위치에 삽입되는 프로모터의 근원은 천연형 또는 합성일 수 있고, 프로모터 근원이 여기에 개시된 발명의 범위를 제약해서는 안 된다. 바꾸어 말하면, 프로모터는 세포로부터 직접 클로닝될 수 있거나, 또는 프로모터는 이전에 다른 근원으로부터 클로닝되었을 수 있었거나, 또는 프로모터는 합성될 수 있다.
유전자 스위치는 특정 리간드를 추가 또는 제거함으로써 유전자 발현을 조절하는 임의의 유전자 스위치일 수 있다. 하나의 구현예에서, 유전자 스위치는 유전자 발현 수준이 존재하는 리간드의 수준에 의존하는 경우이다. 본 발명의 유전자 스위치에 사용될 수 있는 리간드-의존 전사인자의 예는 그들 각 리간드(예, 글루코콜티코이드, 에스트로겐, 프로제스틴, 레티노이드, 엑디손, 그리고 그것의 동족체 및 유사체)에 의해 활성화되는 핵 수용체 슈퍼패밀리(superfamily)의 구성원 및 테트라사이클린에 의해 활성화되는 rTTA를 포함하나, 여기에 제한적이지는 않다. 본 발명의 하나의 양태로서, 유전자 스위치는 EcR-기반 유전자 스위치이다. 그러한 시스템의 예는 미국특허 제 6,258,603호, 7,045,315호, 미국공개특허 제 2006/0014711호, 제 2007/0161086호, 그리고 국제특허 공개번호 제 WO 01/70816호에 기술된 시스템을 포함하나, 여기에 제한적이지는 않다. 키메릭 엑디손 수용체 시스템의 예는 원문 전체로 참고로 도입된 미국특허 제 7,091,038호, 미국공개특허 제 2002/0110861호, 제 2004/0033600호, 제 2004/0096942호, 제 2005/0266457호, 그리고 제 2006/0100416호, 그리고 국제특허 공개번호 제 WO 01/70816호, 제 WO 02/066612호, 제 WO 02/066613호, 제 WO 02/066614호, 제 WO 02/066615호, 제 WO 02/29075호, 그리고 제 WO 2005/108617호에 개시되어 있다. 비스테로이드계 엑디손 작용제-조절 시스템의 예는 리오스위치 포유류 유도 발현 시스템(RheoSwitch Mammalian Inducible Expression System (New England Biolabs, Ipswich, MA))이다.
하나의 구현예에서, 상기 유전자 스위치는 진단 스위치 프로모터 조절하에서 리간드-의존 전사인자를 코딩하는 단일 전사 인자 서열을 포함한다. 전사인자 서열은 자연계에 존재하거나 또는 인공적인 전사인자인 리간드-의존 전사인자를 코딩할 수 있다. 인공적인 전사 인자는 전사인자의 본래 서열이 예를 들어, 변이 또는 다른 전사 인자 도메인과의 결합으로 변형된 경우이다. 하나의 구현예에서, 전사인자는 그룹 H 핵수용체 LBD를 포함한다. 하나의 구현예에서, 그룹 H 핵 수용체 LBD는 EcR, 유비쿼터스 수용체, 고아 수용체 1, NER-I, 스테로이드 호르몬 핵 수용체 1, 레티노이드 X 수용체 상호작용 단백질-15, 간 X 수용체 β, 페임소이드(famesoid) X 수용체, 수용체 상호작용 단백질 14, 또는 파네솔(farnesol) 수용체로부터 유래한다. 다른 구현예에서, 그룹 H 핵 수용체 LBD는 엑디손 수용체로 부터 유래한다.
EcR 및 다른 그룹 H 핵 수용체는 핵 수용체 상위그룹의 구성원이고, 여기서 모든 구성원은 일반적으로 아미노-말단 전사활성화(transactivation) 도메인 (TD), DNA 결합 도메인(DBD), 그리고 경첩부위에 의해 DBD로부터 분리된 LBD의 존재로 특징지워진다. 여기서 사용되는 "DNA 결합 도메인" 이란 용어는 DNA 결합 도메인이 특정 반응 서열(response element)과 연관하여 작용하는 한 DNA 결합 단백질의 폴리펩타이드의 최소 서열, 더 나아가 DNA 결합 단백질의 전체 길이까지도 포함한다. 핵 수용체 상위그룹의 구성원은 4개 또는 5개의 도메인 존재로 또한 특징지워진다: A/B, C, D, E, 그리고 일부 구성원의 경우 F (미국 4,981,784 및 Evans, Science 240:889 (1988)를 참조). "A/B" 도메인은 전사활성화도메인에 해당하고, "C"는 DNA 결합 도메인에 해당하고, "D"는 경첩부위에 해당하고, 그리고 "E"는 리간드 결합 도메인에 해당한다. 상기 그룹의 일부 구성원은 "F".에 해당하는 LBD의 카르복실-말단에 다른 전사활성화 도메인을 또한 가지고 있다.
DBD는 2개의 아미노산 모티프인 P-박스 및 D-박스 사이의 2 시스테인 아연 핑거의 존재로 특징지워진다. 상기의 두 박스는 반응 서열에 특이성을 부여한다. 이들 도메인들은 천연형, 변형된, 또는 이종 수용체 단백질의 다른 도메인의 키메라일 수 있다. 핵 수용체 상위그룹의 하위 구성원과 같이, EcR은 이형이량체화화(heterodimerization) 특성에 해당하는 정의가 덜 된 부위를 포함하고 있다. 핵 수용체의 도메인은 자연발생적으로 모듈로 작용하기 때문에, 상기 LBD, DBD, 및 TD는 상호변환될 수 있다.
다른 구현예에서, 전사인자는 TD, 발현이 조절되어야하는 리포터 유전자와 연관된 반응 서열을 인식하는 DBD, 및 그룹 H 핵 수용체 LBD를 포함한다. 일부 구현예에서 그룹 H 핵 수용체 LBD는 치환 변이를 포함한다.
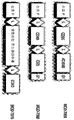
다른 구현예에서, 유전자 스위치는 제1 진단 스위치 프로모터 조절하에 있는 제1 전사인자 서열 및 제2 진단 스위치 프로모터 조절하에 있는 제2 전사인자 서열을 포함한다. 여기서 상기의 제1 및 제2 전사인자 서열에 의해 코딩되는 단백질들은 상호작용을 하여 단백질 복합체를 형성하고, 이들은 리간드-의존 전사인자, 곧, "이중 스위치" 또는 "2개-하이브리드(two-hybrid)"-기반 유전자 스위치로서 기능을 한다. 제1 및 제2 진단 스위치 프로모터는 동일할 수 또는 상이할 수 있다. 이 구현예에서, 리포터 유전자 발현을 위해 요구되는 유전자 스위치에 있는 2개의 다른 진단 스위치 프로모터는 진단 방법의 특이성을 강화한다(도 3). 도 3은 해당 진단 스위치 프로모터를 삽입함으로써 임의의 질병 또는 장애도 간단하게 탐지하기 위해 진단 유전자 스위치를 변형시키는 능력을 또한 제공하고 있다.
더 자세한 구현예에서, 제1 전사인자 서열은 진단 스위치 프로모터(예, 도 1의 P2 또는 P3) 조절 하에 있고 제2 전사인자 서열은 항시적(constitutive) 프로모터(예, 도 1의 Pl) 조절 하에 있다. 이 구현예에서, 리간드-의존 전사인자의 한 부분은 항시적으로 존재할 것이며 제2 부분은 개체자가 질병 또는 장애를 가질 경우에만 합성될 것이다.
다른 구현예에서, 제1 전사인자 서열은 제1 진단 스위치 프로모터(예, 도 2의 P1) 조절하에 있고 2개 이상의 다른 제2 전사인자 서열은 다른 진단 스위치 프로모터(예, 도 2의 P2 및 P3) 조절하에 있다. 이 구현예에서, 각각의 제2 전사인자 서열은 다른 유도(inducible) 프로모터 서열을 인식하는 다른 DBD를 가질수 있다(예, DBD-A는 유도 프로모터 A에 결합하고 DBD-B는 유도 프로모터 B에 결합한다). 각각의 유도 프로모터는 독특한 신호를 생성하는 다른 리포터 유전자에 작동 가능하게 연결될 수 있다. 이러한 방식으로, 복수의 진단이 동시에 이루어질 수 있고 또는 2개 이상의 가능한 질병을 분별할 수 있는 진단법도 이루어진다.
하나의 구현예에서, 제1 전사인자 서열은 TD, 발현이 조절되어야하는 리포터 유전자와 연관된 반응 서열을 인식하는 DBD, 및 그룹 H 핵 수용체 LBD를 포함하는 전사인자를 코딩하고, 제2 전사인자 서열은 척추동물 RXR LBD, 무척추동물 RXR LBD, 울트라스피라클(ultraspiracle) 단백질 LBD, 및 2개의 폴리펩타이드 단편을 포함하는 키메릭 LBD로 이루어진 그룹으로부터 선택된 핵 수용체 LBD를 포함하는 전사인자를 코딩한다. 여기서, 제1 폴리펩타이드 단편은 척추동물 RXR LBD, 무척추동물 RXR LBD, 또는 울트라스피라클(ultraspiracle) 단백질 LBD로부터 유래하고, 제2 폴리펩타이드 단편은 다른 척추동물 RXR LBD, 무척추동물 RXR LBD, 또는 울트라스피라클(ultraspiracle) 단백질 LBD로부터 유래한다.
다른 구현예에서, 유전자 스위치는 핵 수용체 LBD 및 발현이 조절되어야하는 리포터 유전자와 연관된 반응 서열을 인식하는 DBD를 포함하는 제1 폴리펩타이드를 코딩하는 제1 전사인자 서열 및, TD 및 이들 중 하나가 그룹 H 핵 수용체 LBD인 핵 수용체 LBD를 포함하는 제2 폴리펩타이드를 코딩하는 제2 전사인자 서열을 포함한다. 바람직한 구현예에서, 제1 폴리펩타이드는 실질적으로 TD가 없으며 제2 폴리펩타이드는 실질적으로 DBD가 없다. 본 발명의 목적을 위해서, "실질적으로 없다"라는 명칭은 문제의 단백질이 활성화 또는 결합 활성을 제공하기 위해서 문제의 도메인의 충분한 서열을 포함하지 않고 있다는 것을 의미한다.
본 발명의 다른 양태에서는, 제1 전사인자 서열은 이형이량체화 파트너 및 TD를 포함하는 단백질을 코딩하고, 제2 전사인자 서열은 DBD 및 LBD를 포함하는 단백질을 코딩한다.
오직 하나의 핵 수용체 LBD가 그룹 H LBD일 경우, 다른 핵 수용체 LBD는 그룹 H LBD와 2분자를 형성하는 다른 임의의 핵 수용체로부터 유래할 수 있다. 예를 들어, 그룹 H 핵수용체 LBD가 EcR LBD일 경우, 다른 핵 수용체 LBD "파트너"는 EcR, 척추동물 RXR, 무척추동물 RXR, 울트라스피라클 단백질(USP), 또는 척추동물 RXR, 무척추동물 RXR, 및 USP로 이루어진 그룹으로부터 선택된 2개 이상의 다른 핵 수용체 LBD 폴리펩타이드 단편을 포함하는 키메릭 핵 수용체로부터 유래할 수 있다 (원문 전체로 여기에 참고로 도입된 WO 01/70816 A2, 국제특허 출원 제 PCT/US02/05235호 및 US 2004/0096942 A1 참조). "파트너" 핵 수용체 리간드 결합 도메인은 더 나아가 절단 변이, 결손 변이, 치환 변이, 또는 다른 변형을 포함한다.
하나의 구현예에서, 척추 RXR LBD는 인간 호모 사피엔스(Homo sapiens), 생쥐 무스 무스쿨루스(Mus musculus), 집쥐 래터스 노베기커스(Mus musculus), 닭 갈러스 갈러스(Gallus gallus), 돼지 서스 스크로파 도메스티카(Sus scrofa domestica), 개구리 제노퍼스 래비스(Xenopus laevis), 제브라피쉬 다니오 레리오(Danio rerio), 멍게 폴리안드로칼파 미사키엔시스(Polyandrocarpa misakiensis), 또는 젤리피쉬 트리페달리아 시소포라(Tripedalia cysophora) RXR로부터 유래한다.
하나의 구현예에서, 무척추동물 RXR 리간드 결합 도메인은 풀무치 로커스타 미그라토리아(Locusta migratoria) 울트라스피라클 폴리펩타이드("LmUSP"), 이속디드 틱 암블리오마 아메리카넘(Amblyomma americanum) RXR 상동체 1("AmaRXRl"), 이속디드 틱 암블리오마 아메리카넘(Amblyomma americanum) RXR 상동체 2("AmaRXR2"), 피들러 크랩 셀루카 퍼길레이터(Celuca pugilator) RXR 상동체("CpRXR"), 검은 딱정 벌레 테네브리오 몰리터(Tenebrio molitor) RXR 상동체("AmRXR"), 꿀벌 아피스 멜리페라(Apis mellifera) RXR homolog ("AmRXR"), 복숭아혹진딧물 미저스 펄시케(Myzus persicae) RXR 상동체("MpRXR"), 또는 비쌍시류/비인시류(non-Dipteran/non-Lepidopteran) RXR 상동체로부터 유래한다.
하나의 구현예에서, 키메릭 RXR LBD는 척추동물 RXR 폴리펩타이드 단편, 무척추동물 RXR 폴리펩타이드 단편, 및 비쌍시류/비인시류 무척추동물 RXR 상동체 폴리펩타이드 단편으로 이루어진 그룹으로부터 선택된 2개 이상의 폴리펩타이드 단편을 포함한다. 본 발명에서의 용도를 위해 키메릭 RXR 리간드 결합 도메인은 2 개 이상의 다른 종 RXR 폴리펩타이드 단편들을 포함할 수 있고, 또는 종이 같을 경우, 2개 이상의 폴리펩타이드 단편들은 종 RXR 폴리펩타이드 단편의 2개 이상의 다른 동형(isoform)으로부터 유래한다.
하나의 구현예에서, 키메릭 RXR 리간드 결합 도메인은 하나 이상의 척추동물 종의 RXR 폴리펩타이드 단편 및 하나의 무척추동물 종의 RXR 폴리펩타이드 단편을 포함한다.
다른 구현예에서, 키메릭 RXR 리간드 결합 도메인은 하나 이상의 척추동물 종 RXR 폴리펩타이드 단편 및 하나의 비쌍시류/비인시류 무척추동물 종 RXR 상동체 폴리펩타이드 단편을 포함한다.
리간드는 핵 수용체의 LBD와 조합하여 리포터 유전자와 연결된 반응 서열에 결합되어 리포터 유전자 발현에 대한 외부의 시간적 조절을 제공한다. 본 발명의 다양한 구성성분 간의 곧, 리간드와 LBD, DBD와 반응 서열, TD와 프로모터간의 결합 기작 또는 순서는 중요하지 않다.
특별한 예에서, 리간드가 그룹 H 핵 수용체 및 그것의 핵 수용체 LBD 파트너와 결합하면 리포터 유전자를 발현가능하게 한다, 이 기작은 리간드의 그룹 H 핵 수용체(GHNR) 또는 그것의 파트너, 및 결과로 형성된 활성 동종2분자 복합체(예, GHNR + GHNR 또는r partner + partner)와의 결합 잠재능력을 배제하지 않는다. 바람직하게는, 하나 이상의 수용체 도메인이 변형되어 하이브리드 유전자 스위치를 형성한다. 통상적으로, 3개의 도메인인 DBD, LBD, 및 TD의 각 도메인의 하나 이상을 도메인 근원과 다른 근원으로부터 각기 선택하여 하이브리드 유전자 및 결과로 얻어진 하이브리드 단백질을 전사활성도, 리간드의 부가적 결합, 특정 반응 서열의 확인을 위해서 선택된 숙주 세포 또는 생물체에서 최적화한다. 뿐만 아니라, 반응 서열 자체도 효모로부터의 GAL-4(Sadowski et al., Nature 335:563 (1988)) 또는 대장균으로부터의 LexA 단백질(Brent et al., Cell 43:729 (1985)), 또는 하이브리드 수용체를 받아들이기 위해 특정 상호작용을 위해 디자인, 변형, 및 선택된 단백질과의 타켓된 상호작용에 특이한 합성 반응 서열과 같은 다른 DNA 결합 단백질 도메인에 대한 반응 서열을 가지고 변형 또는 치환될 수 있다(예를 들어, Kim et al., Proc. Natl. Acad. ScL USA, 94:3616 (1997)).
기능성 EcR 복합체는 이뮤노필린(immunophilin)과 같은 부가적인 단백질을 또한 포함할 수 있다. 전사인자(DHR38 또는 betaFTZ-1와 같은)로 알려진 단백질의 핵 수용체 그룹의 부가적인 구성원은 EcR, USP, 및/또는 RXR에 대해 리간드 의존 또는 비의존적인 파트너일 수 있다. 게다가, 일반적으로 전사 공동활성화체(coactivator; 또한 어댑터 또는 중재자로 명칭)로 알려진 다른 보조인자가 필요로 될 수 있다. 이들 단백질은 DNA에 서열-특이적으로 결합하지 않으며 기본 전사(basal transcription)에는 관여하지 않는다. 이들은 전사 활성화에 대한 그들의 효과를, 활성화체의 DNA 결합 자극을 포함하는, 염색체 구조에 영향을 주거나 또는 활성화체-개시 복합체 상호작용을 매개함으로써 다양한 기작을 통해 이룰 수 있다. 그런 전사 공동활성화체의 예는 무차별적인 전사 공동활성화체 C 반응 서열 B 결합 단백질인 CBP/p300뿐만 아니라 RIP140, TIFl, RAP46/Bag-1, ARA70, SRC-1 /NCoA-1, TIF2/GRIP/NCoA-2, ACTR/AIBl/RAC3/pCIP를 포함한다(Glass et al., Curr. Opin. Cell Biol. 9:222 (1997) 리뷰 참조). 또한, 일반적으로 코리프레서(또한 리프레서, 사일렌서, 또는 사일렌싱 중재자로 알려진)로 알려진 단백질 보조인자가 리간드가 없을 경우 전사 활성을 효과적으로 저해하기 위해 필요로 될 수 있다. 이들 코리프레서는 반응 서열에서의 활성을 낮추기 위해 리간드가 결합 안된 EcR과 상호작용할 수 있다. 현재의 증거로서, 리간드가 결합하면 수용체의 구조를 변화시켜 코리프레서의 유리 및 상기에 기술된 전사 공동활성화체를 도입하여, 그들의 사일렌싱 활성을 제거해준다. 코리프레서의 예는 N-CoR 및 SMRT를 포함한다(Horwitz et al, MoI Endocrinol. 10:1167 (1996) 리뷰 참조), 이들 보조인잗,fd,s 세포 또는 생물체내에서 내생적일 수 있거나 또는 외부에서 조절 또는 비조절 방식으로 발현되는 이식 유전자로 도입될 수 있다.
리포터 유전자는 탐지할 수 있는 단백질을 코딩하는 임의의 유전자일 수 있다. 단백질은 분비될 수도 있거나 또는 분비되지 않을 수도 있다. 하나의 구현예에서, 단백질은 예를 들어, 면역학적 검사(면역 형광 항체와 같은), 발색법, 형광 검사, 또는 발광 검사와 같은 다양한 표준 정량 방법을 사용하여 분석될 수 있다. 알맞은 리포터 유전자의 예는 루시퍼라아제, 녹색 형광 단백질, β-갈락토시다아제, β-글루코로니다아제, 사이미딘 키나아제, 및 클로람페니콜 아세틸트랜스퍼라아제를 포함하나, 여기에 제한적이지는 않다.
리포터 유전자는 작동 가능하게 유전자 스위치에 의해 코딩되는 리간드-의존 전사인자의 DBD에 의해 인식되는 하나 이상의 반응 서열을 포함하는 프로모터에 연결된다. 하나의 구현예에서, 프로모터는 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 또는 그 이상의 반응 서열 카피를 포함한다. 바람직한 반응 서열을 포함하는 프로모터는 자연발생적으로 일어난 프로모터일 수 있고 또는 당업자에게 잘 알려진 기술, 예를 들어, 최소 프로모터에 작동 가능하게 연결된 하나 이상의 반응 서열로 생성된 인공 프로모터 일 수 있다.
폴리뉴클레오티드를 세포 안으로 도입하기 위해, 벡터가 사용될 수 있다. 벡터는, 예들 들어, 플라스미드 벡터 또는 단일- 또는 이중-가닥 RNA 또는 DNA 바이러스 벡터 일 수 있다. 그러한 벡터는 DNA 및 RNA를 세포 내로 도입하기 위한 잘 알려진 기술을 사용하여 세포 내로 도입될 수 있다. 바이러스 벡터는 복제 가능할 수도 있고 또는 복제 불능일 수도 있다. 후자의 경우, 바이러스 증식은 일반적으로 상보적인 숙주세포(complementing host cell)에서만 일어날 것이다. 여기서 사용되는 "숙주세포(host cell)" 또는 "숙주(host)"라 명칭 된 용어는 본 발명의 하나 이상의 폴리뉴클레오티드를 가진 본 발명의 세포를 의미하기 위해 사용된다.
그리하여, 최소한, 상기 벡터는 본 발명의 폴리뉴클레오티드를 포함해야 한다. 벡터의 다른 구성원은 선택 마커, 염색질 변형 도메인, 벡터에 또한 존재하는 다른 폴리뉴클레오티드의 부가적 프로모터 추진 발현(예, 치사(lethal) 폴리펩티드), 유전자 삽입 위치, 재조합 위치, 및 분자 삽입 피봇(molecular insertion pivot)을 포함할 수 있으나, 여기에 국한되지는 않는다. 상기 벡터는 이들 부가적인 요소의 임의의 수라도 폴리뉴클레오티드 내 또는 밖에 포함할 수 있어, 벡터는 바람직한 진단 방법의 특별한 목적에 맞추어 제조될 수 있다.
본 발명의 하나의 구현예에서, 세포 내로 도입된 벡터는 더 나아가 "선택 마커 유전자"를 포함하고, 이들이 발현이 되었을 때, 본 발명의 진단 유전자 스위치 구조체가 숙주세포의 게놈에 삽입되었다는 것을 의미한다. 이러한 방식으로, 선택 유전자가 게놈 삽입에 대해 양성 마커일 수 있다. 본 발명의 방법에 중요하지 않을 수도 있지만, 선택 마커가 존재하면 당업자로 하여금 살아있는 벡터 구조체가 세포의 게놈에 삽입된 세포군을 선택할 수 있게 한다. 그리하여, 본 발명의 어떤 구현예는 벡터가 성공적으로 삽입된 세포들을 선택하는 것을 포함한다. 여기서 사용되는 세포와 결합하여 사용될 경우, "선택(select)" 또는 그것의 변형체는 특이 유전적 조성 또는 형질의 세포를 선택하기 위한 표준적이고 잘 알려진 방법을 의미하고자 의도된다. 전형적인 방법은 G418, 니오마이신, 암피실린과 같은 항생제 존재하에서 세포를 배양하는 것을 포함하나, 여기에 제한되지는 않는다. 선택 마커 유전자의 다른 예는 다이하이드로폴레이트 리덕타아제, 하이그로마이신, 또는 마이코페놀릭 산에 저항성을 부여하는 유전자를 포함하나, 여기에 제한되지는 않는다. 선택의 다른 방법은 선택 제제로 사이미딘 키나아제, 하이폭젠신-구아닌 포스포리보실트랜스러라아제, 또는 아데닌 포스포리보실트랜스러라아제를 사용하게 해주는 선택 마커 유전자를 포함하나, 여기에 제한되지는 않는다. 항생제 내성 유전자 또는 유전자들을 포함하는 벡터 구조체를 지닌 세포들은 배양액에 있는 항생제를 견딜 수 있다. 이와 유사하게, 항생제 내성 유전자 또는 유전자들을 포함하지 않는 벡터 구조체를 지닌 세포들은 배양액에 있는 항생제를 견딜 수 없다.
여기서 사용되는 "염색질 변형 도메인(chromatin modification domain)" (CMD) 이란 명칭은, 여기에 제한적이지는 않지만, DNA 인슐레이터와 같은 염색체 구조를 유지 및/또는 변형과 연관된 다양한 단백질과 상호작용하는 뉴클레오티드 서열을 가리킨다. 여기에 참고로 도입된 Ciavatta et al, Proc. Nat'l Acad. Sci. U.S.A., 103:9958 (2006)를 참조. CMDs의 예는 닭 β-글로불린 인슐레이터 및 닭 하이퍼센서티브 사이트 4 (cHS4)를 포함하나, 여기에 제한되지는 않는다. 하나 이상의 유전자 프로그램(예, 프로모터, 코딩 서열, 및 3' 조절 부위) 사이에 다른 CMD 서열들을 사용하면, 예를 들어, 존재하는 다인자 및 단일인자 셔틀 벡터들 간의 유전자 프로그램을 "교환(swap)"하는 다양한 미생물 또는 시험관 내 재조합 기술과 조합하여 "미니 상동성 암(mini homology arm)"으로서 차별적인 CMD DNA 서열의 사용을 용이하게 할 수 있다. 염색질 변형 도메인의 다른 예는 당업자에게 알려져 있거나 또는 쉽게 확인될 수 있다.
본 발명을 지닌 용도를 위한 특별한 벡터는 단백질 또는 그것의 일부분을 코딩하는 발현 벡터이다. 일반적으로, 그러한 벡터는 숙주 세포에서의 발현이 효과적이고 기능적으로 발현될 폴리뉴클레오티등레 연결된 시스-액팅 조절 부위를 포함한다. 숙주 세포 내로 도입되자마자 해당 트랜스-액팅 인자가 숙조 세포에 의해 제공, 상보적인 벡터에 의해 제공, 또는 벡터 그 자체에 의해 제공된다.
상당히 다양한 발현 벡터가 단백질을 발현하는데 사용될 수 있다. 그러한 벡터는 염색체, 에피솜, 및 바이러스 유래 벡터를 포함한다. 예를 들어, 대장균 플라스미드, 박테리오파아지, 효모 에피솜, 효모 염색체 요소, 아데노-연관 바이러스, 렌티바이러스, 바쿨로바이러스, SV40와 같은 파포바 바이러스, 벡시니아 바이러스, 아데노바이러스, 파울 폭스 바이러스, 수도레비스 바이러스 및 레트로바이러스로 부터 유래된 벡터들 및 코스미드 및 파아지미드와 같은 플라스미드 및 박테리오파아지 유전 요소로부터 유래된 것과 같이 이들의 조합으로부터 유래된 벡터들이다. 본 발명의 이러한 양태에 따라 발현을 위해서 모든 것이 사용될 수 있다. 그 점에 있어서, 일반적으로, 숙주 세포에서 폴리뉴클레오티드 또는 단백질을 유지, 증식, 발현하기 위해 적합한 임의의 벡터도 발현을 위해 사용될 수 있다.
발현 벡터의 DNA 서열은 기능적으로 예를 들어, mRNA 전사를 지시하는 프로모터를 포함하는 해당 발현 조절 서열에 연결되어 있다. 대표적인 부가적 프로모터는 항시적 프로모터, 및 조직 특이 또는 유도 프로모터를 포함하나, 여기에 제한적이지 않다. 항시적 진핵생물체 프로모터의 예는 마우스 메탈로사이오닌 I 유전자(Hamer et αl., J. MoI. Appl. Gen. 7:273 (1982)); 헤피스 바이러스의 TK 프로모터(McKnight, Cell 37:355 (1982)); SV40 초기 프로모터(Benoist et αl., Nature 290:304 (1981)); 및 벡시니아 바이러스 프로모터를 포함하나, 여기에 제한적이지 않다. 위에 열거된 문헌 모두는 여기 문헌에 의해 도입되어 있다. 단백질 발현을 추진하는데 사용될 수 있는 프로모터의 부가적인 예는 조직-특이적 프로모터 및, 알부민 프로모터(간세포), 프로인슐린 프로모터(췌장 베타 세포) 및 기타 같은 종류의 것과 같은 특이한 단백질에 대한 다른 내생적 프로모터를 포함하나, 여기에 제한적이지 않다. 일반적으로, 발현 구조체는 전사 개시 및 종료, 그리고 전사된 부위에서의 번역을 위한 리보솜 결합 부위를 포함할 것이다. 구조체에 의해 발현된 완전한 전사체의 코딩 부분은 시작에 번역 개시 AUG 및 번역되는 폴리펩타이드 말단에 위치한 종료 코돈(UAA, UGA or UAG)을 포함할 수 있다.
뿐만 아니라, 구조체는 발현을 생기게 할 뿐만 아니라 조절하는 조절 부위를 포함할 수도 있다. 일반적으로, 그런 부위는 여타 다른 것들 중에서 리프레서 결합 부위 및 인핸서와 같은 전사를 조절함으로써 작동할 것이다.
진핵생물체 벡터의 예는 스트라진(Stragene)사로 부터 입수가능한 pW-LNEO, pSV2CAT, pOG44, pXTl 및 pSG; 아머샴 파마시아 바이오텍(Amersham Pharmacia Biotech)으로부터 입수가능한 pSVK3, pBPV, pMSG 및 pSVL; 및 클론텍(Clontech)으로부터 입수가능한 pCMVDsRed2-express, pIRES2-DsRed2, pDsRed2-Mito, pCMV-EGFP를 포함하나, 여기에 제한되지는 않는다. 많은 다른 벡터들이 공지되어 있으며 상업적으로 입수 가능하다.
유전자 프로그램 요소의 신속한 삽입 및 제거를 위한 분자 삽입 피봇을 포함하는 특별히 유용한 벡터는 미국공개특허 제 2004/0185556호, 미국 특허 출원 제 11/233,246호 및 국제 공개 특허 제 WO 2005/040336 및 제 WO 2005/116231호에 개시되어 있다. 이 모두는 참고로 포함되었다. 그러한 벡터의 예는 참고로 여기에 도입된 WO 2007/038276에 개시된 것과 같은 울트라벡터™ 프로덕션 시스템(Intrexon Corp., Blacksburg, VA)이다. 여기서 사용하는 "유전자 프로그램(gene program)"이란 명칭은 프로모터(P), 발현 서열(E), 및 3' 조절 서열의 조합이고 그래서 "PE3"가 유전자 프로그램이다. 유전자 프로그램 내의 요소들은 유전자 프로그램 각 요소의 측면에 위치한 분자 피봇들 사이에서 쉽게 교환될 수 있다. 본 명세서에서 사용된 분자 피봇은 선형으로 나열된 적어도 2개의 불변의 희귀 또는 흔치않은 제한부위를 포함하는 폴리뉴클레오티드로 정의된다. 하나의 구현 예에서, 분자 피봇은 선형으로 나열된 적어도 3개의 비-가변적인 희귀하거나 또는 드문 제한부위를 포함한다. 전형적으로, 임의의 분자 피봇은 동일한 유전자 프로그램 내의 임의의 다른 분자 피봇의 비-가변적인 희귀하거나 또는 드문 제한부위를 포함하지 않는다. 주어진 제한 효소가 작용하는 6개 뉴크레오티드를 초과하는 동족 서열을 "희귀" 제한 부위라 명칭한다. 그러나, 통계적으로 예측된 것보다 더 드물게 나타나는 6 연기쌍(bp)의 제한 부위도 있고, 이들 부위와 이들을 절단하는 엔도뉴클리아제는 "드문" 제한 부위라고 지칭된다. 희귀하거나 드문 제한 효소의 예는 AsiS I, Pac I, Sbf I, Fse I, Asc I, MIu I, SnaB I, Not I, Sal I, Swa I, Rsr II, BSiW I, Sfo I, Sgr AI, AfIIII, Pvu I, Ngo MIV, Ase I, FIp I, Pme I, Sda I, Sgf I, Srf I, 및 Sse8781 I을 포함하나, 여기에 제한되지는 않는다.
벡터는 홈밍 엔도뉴클리아제 (HE) 효소라 불리는 제2 클래스의 제한 효소에 대한 제한 부위를 또한 포함할 수 있다. HE 효소는 큰 비대칭 제한 부위(12-40 염기 쌍)를 가지고 있으며, 그 제한 부위는 자연 상태에서 발생빈도가 낮다. 예를 들어, I-Scel로 알려진 HE는, 무작위 서열의 매 7x1010마다 오직 한번 나타나는 것으로 예측되는, 18 bp의 제한 부위(5 TAGGGATAACAGGGTAATS' (서열 번호:4))를 가지고 있다. 이러한 발생 비율은 포유류 유전제 크기의 20 배인 게놈에서 오직 하나만의 부위에 해당한다, HE 부위의 희귀한 성질은, HE 부위가 클로닝 벡터 플라스미드 내 적당한 위치에 포함될 경우, 유전공학자가 유전자 프로그램의 완전성을 파괴하지 않으면서 유전자 프로그램을 절단할 수 있는 가능성을 대폭 증가시킨다.
숙주세포에서 발현을 위한 적절한 벡터 및 프로모터의 선택은 공지된 절차이고, 숙주세포에서의 발현뿐만 아니라, 벡터 구축 및 숙주세포 내로의 도입에 대한 필요 기술들은 업계의 일상적인 기술이다.
세포 내로 폴리뉴클레오티드 도입은 일시적 트랜스펙션, 안정된 트랜스펙션, 또는 벡터의 유전자위치-특이적 삽입일 수 있다. 숙주 세포 내로 벡터의 일시적 및 안정된 트랜스펙션은 칼슘 인산 트랜스펙션, DEAE-덱스트란 매개 트랜스펙션, 양이온 지질-매개 트랜스펙션, 전기천공법, 트랜스덕션, 감염, 또는 다른 방법들에 의해 이루어질 수 있다. 그러한 방법들은 여기에 참고로 도입된 Davis et al, Basic Methods in Molecular Biology (1986); Keown et al, 1990, Methods Enzymol. 185: 527- 37; Sambrook et al, 2001, Molecular Cloning, A Laboratory Manual, Third Edition, Cold Spring Harbor Laboratory Press, N. Y.와 갈은 수많은 표준 실험 매뉴얼에 기술되어 있다. 이러한 안정된 트랜스펙션 방법은 세포의 게놈내에 벡터를 무작위로 삽입한다. 더 나아가, 벡터의 카피 수와 방향 또한, 일반적으로 말하면, 무작위이다.
본 발명의 하나의 구현예에서, 벡터는 게놈의 생체-중성적(bio-neutral ) 부위에 삽입된다. 바이오-뉴트럴 부위는 폴리뉴클레오티드의 삽입이 세포의 정상 기능에 전혀 영향을 주지 않는 게놈 상의 부위이다. 바이오-뉴트럴 부위는 가용한 생물정보학을 사용하여 분석될 수 있다. 수 많은 바이오-뉴트럴 부위가 당업자에게 알려있다. 예를 들어, 로사-동등 유전자좌(ROSA-equivalent locus). 다른 바이오-뉴트럴 부위도 당업자에게 알려진 일상적인 기술을 사용하여 동정될 수 있다. 유전자 삽입 부위의 특징화 작업은 당업자에게 알려진 방법을 사용하여 실시된다. 벡터를 세포 내로 도입할 때, 폴리뉴클레오티드의 위치, 카피 수, 및/또는 방향을 조절하기 위해서 유전자위치-특이적 삽입 방법이 사용될 수 있다. 유전자위치-특이적 삽입 방법은 당업자에게 잘 알려져 있으며 상동 재조합 및 재조합효소-매개 게놈 삽입을 포함하나, 여기에 제한되지는 않는다. 물론, 유전자위치-특이적 삽입 방법이 본 발명의 방법에서 사용되어야 한다면, 벡터는, 상동 재조합과 동일할 수 있으나 여기에 제한적이지 않는, 이러한 유전자위치-특이적 삽입을 도와주는 요소를 포함할 수 있다. 예를 들어, 벡터는 하나, 둘, 셋, 넷, 또는 그 이상의 유전자 삽입 부위(genomic integration site;GISs)를 포함할 수 있다. 여기서 사용하는 "유전자 삽입 부위"라는 명칭은 뉴클레오티드 서열이 게놈에서 벡터의 삽입을 허용하는 세포 내의 게놈 부분과 동일 또는 거의 동일한 벡터 서열의 부분으로서 정의된다. 특히, 벡터는 폴리뉴클레오티드의 측면에 위치한 적어도 2 개의 유전자 삽입 부위를 포함할 수 있다. 물론, 유전자 삽입 부위는 부가적인 요소의 측면에 위치할 수도 있거나 또는 벡터에 존재하는 모든 요소들 사이에 고르게 위치할 수 있다.
다른 구현예에서, 유전자위치-특이적 삽입은 재조합효소-부위 특이적 유전자 삽입에 의해 수행될 수 있다. 간략하게, PhiC31 삽입효소(integrase)와 같으나 여기에 제한적이지 않은 대장균 재조합효소 효소는 인간 게놈 내에 "슈도(pseudo)" 재조합 부위에 작용할 수 있다. 이들 가성 재조합 부위는 재조합효소를 이용한 유전자위치-특이적 삽입을 위한 타켓일 수 있다. 재조합효소-부위 특이적 유전자 삽입은 참고로 여기에 도입된 hyagarajan et al, MoI. Cell Biol. 21:3926 (2001)에 기술되어 있다. 재조합효소 및 재조합효소-부위 특이적 유전자 삽입에 사용될 수 있는 그들의 각각의 작용 부위의 다른 예들은 R4 및 TP901-1와 같은 세린 재조합효소 및 참고로 여기에 도입된 WO 2006/083253에 개시된 재조합효소를 포함하나, 여기에 제한적이지 않다.
보다 구체적인 구현예에서, 벡터는 예를 들어, 다중약물 저항성(multidrug resistance) 유전자인 mdr1, 다이하이드로촐레이트 리덕타제, 또는 O6-알킬구아닌-DNA 알킬트랜스퍼라제의 화학요법-저항 유전자를 포함할 수 있다. 화학요법-저항 유전자는 항시적(예, CMV) 또는 유도(예, 리오스위치®) 프로모터 조절하에 있을 수 있다. 이러한 구현예에서, 개체 내의 변형 세포를 유지하면서 개체에서 진단된 질병을 치료하고자 한다면, 임상의는 질병 세포를 파괴하기 위해 화학요법 제제를 적용할 수 있으며, 그 동안에 변형 세포는 해당 화학요법-저항 유전자를 발현함으로써 제제로부터 보호되며 질병 진행 또는 치료의 효능을 모니터하기 위해 계속적으로 사용될 수 있다. 화학요법-저항 유전자를 유도 프로모터 하에 위치시켜, 화학요법-저항 유전자의 불필요한 발현이 해결될 수 있으나, 치료 동안 계속적인 진단이 바람직할 경우엔 그 유전자가 아직도 쓸모가 있을 것이다. 변형된 세포 자체가 병적으로 된다면, 하기에 기술된 치사 폴리펩타이드 발현의 도입에 의해 파괴될 수 있다.
본 발명의 방법은 유전자 스위치와 리포터 유전자를 코딩하는 폴리뉴클레오티드를 개체의 세포 내로 도입함으로써 시행한다. 상기에 기술된 것 같이, 당업자에게 알려진 폴리뉴클레오티드를 세포 내로의 도입하는 임의의 방법도 사용될 수 있다.
다른 구현예에서, 유전자 스위치와 리포터 유전자를 코딩하는 폴리뉴클레오티드가 예를 들어, 개체에 동종(allogenei)이거나 또는 이종(xenogeneic)인 비-자가조직(non-autologous) 세포 내로 도입되었다.
폴리뉴클레오티드를 생체 외로 세포 내로 도입할 경우, 세포들은 당업자에게 알려진 임의의 기술에 의하여 개체로부터 회수될 수 있다. 이들 기술은 생검, 스크레이핑(scrapings), 및 외과적 조직 제거를 포함하나, 여기에 제한적이지 않다. 예를 들어, 2, 4, 6, 8, 10, 12, 18, 24, 36, 48 시간 또는 그 이상 폴리뉴클레오티드를 세포 내로 도입하기 위해 분리된 세포들은 충분한 시간 동안 배양될 수 있다. 시간의 짧은 기간 동안 일차 세포를 배양하는 방법은 당업자에게 잘 알려져 있다. 예를 들어, 세포들은 플레이트(예, 마이크로웰 플레이트)에서 부착되거나 또는 부유상태로 배양될 수 있다.
생체 외 진단 방법에 있어서, 세포들은 개체로부터 분리되어 폴리뉴클레오티드를 세포 내로 도입하기 위해 적당한 조건하에서 배양되었다. 폴리뉴클레오티드가 세포 내로 도입되면, 리간드-의존 전사인자가 발현할 수 있도록 세포들을 충분한 시간 동안 예를 들어, 0.5, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 12, 18, or 24 ㅅ시간 또는 그 이상 배양하였다. 리간드-의존 전사인자의 발현이 대조군 레벨과 비교하여 증가되거나 또는 감소된다면(곧, 개체가 질병 또는 장애를 가지고 있고 전사인자 발현을 조절하는 프로모터가 활성화 또는 비활성화된다면), 리간드-의존 전사인자의 존재 및/또는 레벨은 리간드를 첨가함으로써 리간드-의존 전사인자의 레벨에 해당하는 리포터 유전자 발현 레벨을 도입하면서 탐지된다. 리간드는 폴리뉴클레오티드를 세포 내로 도입하기 전, 동안, 또는 후의 어느 시간대에도 세포에 첨가될 수 있다. 각 타입의 세포 및 질병, 또는 질환에 대한 리간드 처리의 최적 시기는 오직 일상적인 기술만을 사용하여 결정될 수 있다. 하나의 구현예에서, 세포의 복수 진단 측정치를 얻기 위해서 리간드는 첨가될 수 있고, 리포터 유전자 발현은 결정될 수 있고, 리간드는 제거될 수 있고, 그리고 프로세스가 하나 또는 두 번 이상 반복될 수 있다. 다른 구현예에서, 리간드는 계속해서 존재하며 리포터 유전자 발현은 주기적으로 측정된다.
분리된 세포를 사용하는 생체 외 방법이 불충분할 경우, 예를 들어 순환인자가 진단 스위치 프로모터 활성이 일어나는데 필요할 경우 본 발명의 첫번째 생체 내 진단 구현예가 사용될 수 있다. 이 구현예에서, 세포들이 개체로부터 분리되어 상기에 기술된 것과 같이 폴리뉴클레오티드가 배양되는 세포 내로 도입되었다. 폴리뉴클레오티드를 세포 내로 도입한 후 어느 시점에서, 세포들을 개체로 다시 재 도입된다. 재도입은 당업자에 알려진 임의의 방법 예를 들어, 정맥내도입 또는 조직 또는 공동(cavity)로의 직접 주사에 의해 수행될 수 있다. 하나의 구현에서, 세포에서 폴리뉴클레오티드의 존재는 세포를 개체로 재도입하기 전에 결정된다. 다른 구현예에서, 폴리뉴클레오티드를 포함하는 세포가 선택(예, 폴리뉴클레오티드에 있는 선택 마커 존재의 기반한)되고 폴리뉴클레오티드를 포함하고 있는 세포들만이 개체에 재도입되었다. 세포가 개체로 재도입된 후, 리간드가 개체에 투여되고 리포터 유전자 발현이 검사되었다. 리간드는 전신(예, 구강으로, 정맥주사로) 또는 국소적(예, 복강내로, 척추관으로, 뇌실내로, 세포가 재도입된 조직 또는 기관 내로 직접 주사)으로 임의의 적당한 방법에 의해서도 투여될 수 있다. 리간드 처리의 최적 시기는 오직 일상적인 기술만을 사용하여 각 타입의 세포 및 질병 또는 장애에 대해 결정될 수 있다. 하나의 구현예에서, 세포의 복수의 진단 측정치를 얻기 위해서 리간드는 첨가될 수 있고, 리포터 유전자 발현은 결정될 수 있고, 리간드는 제거될 수 있고, 그리고 프로세스가 하나 또는 두 번 이상 반복될 수 있다. 다른 구현예에서, 리간드는 계속해서 존재하며 리포터 유전자 발현은 주기적으로 측정된다. 리간드가 투여된 후 리포터 유전자 발현의 탐지는 생 체 내 또는 생 체 외 에서 일어날 수 있다. 예를 들어, 리포터 유전자가 혈액을 순환하는 분비 단백질을 코딩한다면, 단백질 진단은 환자로부터 제거된 혈액샘플에서 일어날 수 있다. 리포터 유전자가 발광 또는 형광 신호를 생성하는 단백질을 코딩한다면, 신호는 생체 내 에서 탐지될 수 있다. 다른 구현예에서는, 변형된 세포의 샘플이 제거될 수 있고 리포터 유전자 발현이 생 체 외 에서 탐지될 수 있다.
본 발명의 두번째 생체 내 진단 구현예는 폴리뉴클레오티드를 개체의 세포내로 직접 생체 내 도입하는 것과 관련한다. 폴리뉴클레오티드는 개체에게 전신 또는 국소적으로 도입될 수 있다(예를 들어, 의심되는 질병 또는 장애 부위에). 일단 폴리뉴클레오티드가 개체 내로 도입되면, 리간드가 투여되어 리포터 유전자 발현이 정량될 수 있다. 리간드는 어느 적당한 방법에 의해서라도 전신(예, 경구, 정맥 내로) 또는 국소적(예, 복강내로, 척추관으로, 뇌실내로, 의심되는 질병이나 질환이 일어나는 조직 또는 기관 내로 직접 주사)으로 투여될 수 있다. 리간드 처리의 최적 시기는 오직 일상적인 기술만을 사용하여 각 타입의 세포 및 질병 또는 장애에 대해 결정될 수 있다. 하나의 구현예에서, 폴리뉴클레오티드를 포함하는 세포의 복수의 진단 측정치를 얻기 위해서 리간드는 첨가될 수 있고, 리포터 유전자 발현은 결정될 수 있고, 리간드는 제거될 수 있고, 그리고 프로세스가 하나 또는 두 번 이상 반복될 수 있다. 다른 구현예에서, 리간드는 계속해서 투여되며 리포터 유전자 발현은 주기적으로 측정된다. 리간드가 투여된 후 리포터 유전자 발현의 탐지는 생 체 내 또는 생 체 외 에서 일어날 수 있다. 예를 들어, 리포터 유전자가 혈액을 순환하는 분비 단백질을 코딩한다면, 단백질 진단은 환자로부터 제거된 혈액샘플에서 일어날 수 있다. 리포터 유전자가 발광 또는 형광 신호를 생성하는 단백질을 코딩한다면, 신호는 생 체 내 에서 탐지될 수 있다. 다른 구현예에서는, 변형된 세포의 샘플이 제거될 수 있고 리포터 유전자 발현이 생 체 외 에서 탐지될 수 있다.
비-자가 조직 세포가 진단 방법에 사용될 경우, 세포들은 임의의 근원으로부터도 얻을 수 있다. 예를 들어, 다른 개체, 세포 주, 또는 동물들. 비-자가 조직 세포는 이식 후 생존 가능한 섬유아세포 또는 줄기세포(예, 배아 줄기 세포, 조혈모 줄기세포)와 같은 임의의 세포일 수 있다. 비-자가 조직 세포는 분리되어 상기에 기술된 바와 같이 폴리뉴클레오티드가 배양액 상의 세포 내로 도입될 수 있다. 폴리뉴클레오티드가 세포 내로 도입된 얼마 후의 시점에, 세포가 개체로 도입이 된다. 도입은 당업자에게 알려진 예를 들어, 정맥내 도입 또는 조직 또는 공동(cavity)으로의 직접적인 주사등의 임의의 방법에 의해서도 이루어 질 수 있다. 하나의 구현예에서, 세포 내의 폴리뉴클레오티드의 존재는 개체로 세포를 다시 도입하기 전에 결정된다. 다른 구현예에서, 폴리뉴클레오티드를 포함하는 세포가 선택(예를 들어, 폴리뉴클레오티드의 선택가능한 마커에 기반한)되어 폴리뉴클레오티드를 포함하는 세포만이 오직 개체에게 도입된다. 세포를 개체에 도입된 후, 리간드가 투여되어 리포터 유전자 발현이 정량된다. 리간드는 어느 적당한 방법에 의해서라도 전신(예, 경구, 정맥 내로) 또는 국소적(예, 복강내로, 척추관으로, 뇌실내로, 세포가 도입된 조직 또는 기관 내로 직접 주사)으로 투여될 수 있다. 리간드 처리의 최적 시기는 오직 일상적인 기술만을 사용하여 각 타입의 세포 및 질병 또는 장애에 대해 결정될 수 있다. 하나의 구현예에서, 세포의 복수의 진단 측정치를 얻기 위해서 리간드는 첨가될 수 있고, 리포터 유전자 발현은 결정될 수 있고, 리간드는 제거될 수 있고, 그리고 프로세스가 하나 또는 두 번 이상 반복될 수 있다. 다른 구현예에서, 리간드는 계속해서 투여되며 리포터 유전자 발현은 주기적으로 측정된다. 리간드가 투여된 후 리포터 유전자 발현의 탐지는 생 체 내 또는 생 체 외 에서 일어날 수 있다. 예를 들어, 리포터 유전자가 혈액을 순환하는 분비 단백질을 코딩한다면, 단백질 진단은 환자로부터 제거된 혈액샘플에서 일어날 수 있다. 리포터 유전자가 발광 또는 형광 신호를 생성하는 단백질을 코딩한다면, 신호는 생 체 내 에서 탐지될 수 있다. 다른 구현예에서는, 변형된 세포의 샘플이 제거될 수 있고 리포터 유전자 발현이 생 체 외 에서 탐지될 수 있다.
모든 생체 내 구현예에서, 폴리뉴클레오티드를 포함하는 폴리뉴클레오티드 또는 벡터는 폴리뉴클레오티드 또는 벡터를 포함하는 세포를 죽이는 산물을 발현하기 위해 활성 화 될 수 있는 치사 폴리펩티드를 코딩하는 서열을 포함할 수 있다. 진단 검사가 더 이상 필요 없거나 또는 변형된 세포(예, 과증식 또는 독성)를 가진 문제 때문에 치사 폴리펩티드 발현은 개체로부터 변형된 세포를 제거하기 위해 사용될 수 있다. 여기서 사용되는 치사 폴리펩티드는, 그것이 발현될 때, 폴리펩티드를 발현하는 세포에 치명적인 폴리펩티드이다. 이것은 폴리펩티드 자체가 치명적이거나 또는 폴리펩티드가 치명적인 화합물을 생성하기 때문이다. 여기서 사용하는 치사 폴리펩티드는 임의의 방식이든지 간에 세포 사멸을 도입하는 폴리펩티드를 포함한다. 이들 방식은 괴사, 사멸, 세포독성을 포함하나, 여기에 제한적이지는 않다. 치사 폴리펩티드의 예는 p53, Rb 및 BRCA-I을 포함하나 여기 제한적이지 않은 종양 억제 유전자를 도입하는 세포 사멸, 디프테리아 독소(DTA), 시겔라 신경독소, 보툴리슴 독소, 테타너스 독소, 콜레라 독소, CSE- V2 및 전갈 단백질 독소의 다른 변형체와 같은 독소, 사이토신 디아미나아제 및 사이미딘 키나아제와 같은 자살 유전자, 그리고 예를 들어 종양 괴사 인자, 인터페론-알파의 세포 독성 유전자를 포함하나, 여기에 제한적이지는 않다. 본 발명은, 폴리펩티드가 발현될 경우 세포에 치명적일 수 있다면, 치사 폴리펩티드의 정체에 의해서 제한되지 않는다. 변형된 세포가 단명인 세포(예를 들어, 제한된 수명을 지닌 세포, 예, 수지상 세포와 같은 10일 또는 적은)라면, 세포들이 짧은 기간에 걸쳐 자연발생적으로 제거될 것이기 때문에 치사 폴리펩티드를 폴리뉴클리오티드 또는 벡터에 포함할 필요가 없다.
다른 양태로서, 본 발명은 개체의 세포에 본 발명의 진단 유전자 스위치를 투여하여 질병 또는 장애의 진행을 모니터하기 위해 리포터 유전자 발현을 측정함으로써 질병 또는 장애의 진행을 모니터하는 방법에 관한 것이다. 하나의 구현예에서, 본 발명은 (a) 상기 개체의 세포에 (1) 유전자 스위치를 코딩하는 폴리뉴클레오티드, 이때, 상기 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하며, 여기서 상기 적어도 하나의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하고, 작동가능하게 진단 스위치 프로모터와 연결되며, 여기서 상기 프로모터의 활성은 상기 개체의 질병 또는 장애 기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 도입하여 변형된 세포를 생산하는 단계; (b) 상기 변형된 세포에 리간드를 투여하는 단계; 및 (c) 리포터 유전자 발현을 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨의 변화가 상기 개체에서 상기 질병 또는 장애의 진행을 지시하는 것인, 상기 개체에서 질병 또는 장애의 진행을 모니터하는 방법에 관한 것이다.
진행과정은 진단 유전자 프로모터가 질병 또는 장애의 진행 동안 증가 또는 감소하는 인자에 반응하는지에 따라서 리포터 유전자의 발현의 증가 또는 감소에 의해 기술 될 수 있다. 이러한 방법은 상기에서 기술된 임의의 진단 방법을 사용하서라도 수행될 수 있다(곧, 생체 외 세포, 생체 외 세포 변형 후 생체 내, 또는 생체 내 로 세포의 재도입). 질병 또는 장애은 질병 또는 장애의 상태의 표시 및 발현 레벨의 변화를 기록하면서 리포터 유전자 발현을 적어도 2 회 측정하여 모니터되었다. 하나의 구현예에서, 모니터은 세포를 라간드에 연속적으로 노출시키면서 리포터 유전자 발현을 간헐적으로 측정함으로써 수행될 수 있다. 다른 구현예에서, 세포를 라간드에 간헐적으로 노출시키면서 리포터 유전자 발현을 각 노출 동안 측정함으로써 수행될 수 있다.
하나의 구현예에서, 상기 개체에서 질병 또는 장애의 진행을 모니터하기 위해 변형된 세포를 제조하는 방법에 관한 것이며, 상기 개체의 세포에 (1) 유전자 스위치를 코딩하는 폴리뉴클레오티드, 이때, 상기 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하며, 여기서 상기 적어도 하나의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하고, 작동가능하게 진단 스위치 프로모터와 연결되며, 여기서 상기 프로모터의 활성은 상기 개체의 질병 또는 장애 기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 도입하여 변형된 세포를 생산하는 단계를 포함한다.
본 발명의 다른 구현예는 (a) 상기 개체의 상기 변형된 세포에 리간드를 투여하는 단계; 및 (c) 리포터 유전자 발현을 적어도 2회 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨의 변화가 상기 개체에서 상기 질병 또는 장애의 진행을 지시하고, 또한, 여기서 상기 개체의 변형된 세포는 (1) 유전자 스위치를 코딩하는 폴리뉴클레오티드, 상기 유전자 스위치는 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 진단 스위치 프로모터에 작동가능하게 연결되며, 여기서 상기 프로모터의 활성은 상기 개체의 질병 또는 장애 기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는, 상기 개체에서 질병 또는 장애의 진행을 모니터하는 방법에 관한 것이다.
보다 구체적인 구현예에서는, 질병 또는 장애의 진행을 모니터하기 위한 방법이 예를 들어 개체에게 동종이계 또는 이종인 세포인 비-자가 조직 세포를 사용하여 수행되었고 변형된 비-자가 조직 세포가 개체 내로 도입되었다. 하나의 구현에서, 본 발명은 (a) 비-자가 세포에 (1) 유전자 스위치를 코딩하는 폴리뉴클레오티드, 상기 유전자 스위치는 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 진단 스위치 프로모터에 작동가능하게 연결되며, 여기서 상기 프로모터의 활성은 상기 개체의 질병 또는 장애 기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 도입하여 변형된 세포를 생산하는 단계;
(b) 상기 개체로 상기 변형된 세포를 도입하는 단계;
(c) 상기 변형된 세포에 리간드를 투여하는 단계; 및
(d) 리포터 유전자 발현을 적어도 2회 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨의 변화가 상기 개체에서 상기 질병 또는 장애의 진행을 지시하는 것인, 상기 개체에서 질병 또는 장애의 진행을 모니터하는 방법에 관한 것이다.
보다 구체적인 양태로서, 본 발명은 개체에서 질병 또는 장애를 위한 치료의 효능을 모니터하는 방법에 관한 것이고, 개체에 치료제를 투여 및 리포터 유전자 발현이 증가, 감소, 또는 동일하게 유지되는지를 결정하고자 본 발명의 진단 방법을 2번 이상 수행하는 것을 포함한다. 하나의 구현예에서, 본 발명은 (a) 상기 개체에 치료제를 투여하는 단계; (b) 상기 개체의 세포에 (1) 유전자 스위치를 코딩하는 폴리뉴클레오티드, 이때, 상기 유전자 스위치는 적어도 하나의 전사인자 서열을 포함하며, 여기서 상기 적어도 하나의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하고, 진단 스위치 프로모터에 작동가능하게 연결되며, 여기서 상기 프로모터의 활성은 상기 개체의 질병 또는 장애 기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 도입하여 변형된 세포를 생산하는 단계; (c) 상기 변형된 세포에 리간드를 투여하는 단계; 및 (d) 리포터 유전자 발현을 적어도 2회 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨의 변화가 상기 치료제의 효능을 지시하는 것인, 상기 개체에서 질병 또는 장애에 대한 상기 치료제의 효능을 모니터하는 방법에 관한 것이다.
치료제가 투여된 후의 리포터 유전자 발현의 레벨 변화는 치료제의 효능을 표시한다. 진단 스위치 프로모터가 질병 또는 장애 동안 증가된 인자에 반응을 한다면, 리포터 유전자 발현의 감소는 치료가 효과적이라는 것을 기술한다. 진단 스위치 프로모터가 질병 또는 장애 동안 감소된 인자에 반응을 한다면, 리포터 유전자 발현의 증가는 치료가 효과적이라는 것을 기술한다. 리포터 유전자 발현이 치료제가 투여된 후에도 변하지 않는다면, 치료제가 질병 또는 장애의 진행을 중지하였다는 것을 기술한다. 이러한 방법은 상기에 기술된 진단 방법의 임의의 변형체를 사용하여 수행될 수 있다(예를 들면, 생체 외 세포, 생체 외 세포 변형 후 생체 내 로 세포의 재도입, 생체 내).
본 발명의 생체 외 구현예에서, 리포터 유전자 발현의 기본 수준을 결정하기 위해 세포는 치료 전에 개체로부터 분리될 수 있다. 치료제가 개체에 투여된 후, 리포터 유전자 발현을 결정하기 위해서 세포는 개체로부터 다양한 간격으로 분리될 수 있다.
본 발명의 생체 내 구현예에서, 변형된 세포 또는 폴리뉴클레오티드는 치료제의 투여 전, 동안, 또는 후에 개체로 도입될 수 있다. 세포 또는 폴리뉴클레오티드가 치료 전에 투여된다면, 리포터 유전자 발현의 기본 수준이 결정될 수 있다.
리포터 유전자 발현의 측정은 생체 외 또는 생체 내 에서 수행될 수 있다. 하나의 구현예에서, 모니터은 세포를 라간드에 연속적으로 노출시키면서 리포터 유전자 발현을 간헐적으로 측정함으로써 수행될 수 있다. 다른 구현예에서, 모니터은 세포를 라간드에 간헐적으로 노출시키면서 리포터 유전자 발현을 각 노출 동안 측정함으로써 수행될 수 있다.
하나의 구현예에서, 유전자 스위치 및 리포터 유전자를 코딩하는 하나 또는 2 개의 폴리뉴클레오티드는 개체에 투여되는 치료용 벡터의 일부분일 수 있다(예를 들어, 치료 단백질을 코딩하는 벡터 또는 유전자 치료법을 위한 핵산). 이러한 구현예에서, 치료 용도의 치료제와 치료 효능을 모니터하기 위한 진단 검사법이 동시에 한 단위로 수행되어, 치료제를 받은 모든 세포가 진단 유전자 스위치를 또한 받을 수 있도록 한다.
본 발명의 하나의 구현예는 개체에서 질병 또는 장애를 위한 치료의 효능을 모니터하기 위한 변형된 세포를 제조하는 방법에 관한 것이고, 변형된 세포를 생성하기 위해서 상기 개체의 세포에 하기를 도입하는 것을 포함한다 (1) 유전자 스위치를 코딩하는 폴리뉴클레오티드, 여기서 상기 유전자 스위치는 하나 이상의 전사 인자 서열을 포함하고, 여기서 상기의 하나 이상의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하며, 이들은 작동가능하게 진단 스위치 프로모터에 연결되어 있고, 여기서 프로모터의 활성은 상기 질병 또는 장애 동안 조절되고, 및 (2) 상기 리간드-의존 전사 인자에 의해 활성화되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드.
본 발명의 다른 구현예는 본 발명은 (a) 상기 개체에 치료제를 투여하는 단계; (b) 상기 변형된 세포에 리간드를 투여하는 단계; 및 (c) 리포터 유전자 발현을 적어도 2회 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨의 변화가 상기 치료제의 효능을 지시하고, 상기 개체의 상기 변형된 세포는 (1) 유전자 스위치를 코딩하는 폴리뉴클레오티드, 이때, 상기 유전자 스위치는 적어도 하나의 전사인자 서열을 포함하며, 여기서 상기 적어도 하나의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하고, 진단 스위치 프로모터에 작동가능하게 연결되며, 여기서 상기 프로모터의 활성은 상기 개체의 질병 또는 장애 기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인, 상기 개체에서 질병 또는 장애에 대한 상기 치료제의 효능을 모니터하는 방법에 관한 것이다.
보다 구체적인 구현예에서는, 질병 또는 장애의 진행을 모니터하기 위한 방법이 예를 들어 개체에게 동종이계 또는 이종인 세포인 비-자가 조직 세포를 사용하여 수행되었고 변형된 비-자가 조직 세포가 개체 내로 도입되었다. 하나의 구현에서, 본 발명은 (a) 비-자가 세포에 (1) 유전자 스위치를 코딩하는 폴리뉴클레오티드, 이때, 상기 유전자 스위치는 적어도 하나의 전사인자 서열을 포함하며, 여기서 상기 적어도 하나의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하고, 진단 스위치 프로모터에 작동가능하게 연결되며, 여기서 상기 프로모터의 활성은 상기 개체의 질병 또는 장애 기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 도입하여 변형된 세포를 생산하는 단계; (b) 상기 개체에 상기 변형된 세포를 도입하는 단계; (c) 상기 변형된 세포에 리간드를 투여하는 단계; 및 (d) 리포터 유전자 발현을 적어도 2회 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨의 변화가 상기 치료제의 효능을 지시하는 것인, 상기 개체에서 질병 또는 장애에 대한 상기 치료제의 효능을 모니터하는 방법에 관한 것이다.
다른 양태로서, 본 발명은 개체의 질병 또는 장애를 위해 투여된 치료제의 잠재적 독성을 모니터하는 방법에 관한 것이다. 하나의 구현예에서, 본 발명은 (a) 상기 개체에 치료제를 투여하는 단계; (b) 상기 개체의 세포에 (1) 유전자 스위치를 코딩하는 폴리뉴클레오티드, 상기 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하고, 여기서 상기 적어도 하나의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하고, 진단 스위치 프로모터에 연결되며, 여기서 상기 프로모터의 활성은 독성 조건에 노출되어 있는 세포에서 발견된 인자들에 의해 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 도입하여 변형된 세포를 생산하는 단계; (c) 상기 변형된 세포에 리간드를 투여하는 단계; 및 (d) 리포터 유전자 발현을 적어도 2회 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨의 변화가 상기 치료제의 독성을 지시하는 것인, 상기 개체에서 질병 또는 장애에 대한 투여된 치료제의 잠재적 독성을 모니터하는 방법에 관한 것이다.
하나의 구현예에서, 본 양태는 스트레스 받거나 또는 죽는 세포, 곧, 독성조건에 노출되어 있는 세포에서 발견되는 인자에 의해 조절되는 프로모터의 조절하에 있는 전사 인자 서열를 지닌 폴리뉴클레오티드와 관련한다. 예는 세포사멸 신호, 괴사 신호, 저산소증, 활성 산소종, DNA 또는 염색체 변형, 단백질 분해, 산화/환원 상태, pH 변화 등을 포함하나, 여기에 제한적이지는 않다. 해당 스트레스 프로모터는 미국공개특허 제 2003/0027127호(참고로 여기에 도입된)에 개시된 것들을 포함하고 다음 유전자로부터의 프로모터를 포함하나, 여기에 제한적이지는 않다: CYPlAl, GST Ya, GADD45, GRP78, JUN, FOS, XHF, HSP70, MT HA, GADDl 53, ALDH 1, HMO, CRE, XRE, NFKBRE, RARE, ThRE, PPRE, TRE, ERE, 및 p53RE. 해당 세포 사멸 반응 프로모터는 Fas/CD95, TRAMP, TNF RI, DRl, DR2, DR3, DR4, DR5, DR6, FADD, RIP, TNFα, Fas ligand, TRAILRl, TRAILR2, TRAILR3, Bcl-2, p53, BAX, BAD, Akt, CAD, PI3 kinase, PPl, 및 caspase 단백질을 포함하나, 여기에 제한적이지는 않다. 치료제 투여에 따른 리포터 유전자 발현 증가의 탐지는 치료제가 세포에 해롭다는 것을 기술한다. 유전자 스위치를 스트레스 또는 사멸 신호에 민감하게 만들어서 개체가 공개적인 독성 증후군을 보여주기 전에 치료 효능을 모니터 및 세포 수준에서 독성 효과를 탐지하는데 사용될할 수 있다.
이러한 방법은 상기에 기술된 진단 방법의 임의의 변형체를 사용하서라도 이루어 질 수 있다(곧, 생체 외 세포, 생체 외 세포 변형 후 생체 내 로 세포의 재도입, 생체 내).
본 발명의 생체 외 구현예에서, 리포터 유전자 발현의 기본 수준을 결정하기 위해 세포는 치료 전에 개체로부터 분리될 수 있다. 치료제가 개체에 투여된 후, 리포터 유전자 발현을 결정하기 위해서 세포는 개체로부터 다양한 간격으로 분리될 수 있다.
본 발명의 생체 내 구현예에서, 변형된 세포 또는 폴리뉴클레오티드는 치료제의 투여 전, 동안, 또는 후에 개체로 도입될 수 있다. 세포 또는 폴리뉴클레오티드가 치료 전에 투여된다면, 리포터 유전자 발현의 기본 수준이 결정될 수 있다.
리포터 유전자 발현의 측정은 생체 외 또는 생체 내 에서 수행될 수 있다. 하나의 구현예에서, 모니터은 세포를 리간드에 연속적으로 노출시키면서 리포터 유전자 발현을 간헐적으로 측정함으로써 수행될 수 있다. 다른 구현예에서, 모니터은 세포를 리간드에 간헐적으로 노출시키면서 리포터 유전자 발현을 각 노출 동안 측정함으로써 수행될 수 있다.
본 발명의 하나의 구현은 개체의 질병 또는 장애를 위해 투여된 치료제의 잠재적 독성을 모니터하기 위한 변형된 세포 제조 방법에 관한 것이다. 하나의 구현예에서, 본 발명은 상기 개체의 세포에 (1) 유전자 스위치를 코딩하는 폴리뉴클레오티드, 상기 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하고, 여기서 상기 적어도 하나의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하고, 진단 스위치 프로모터에 연결되며, 여기서 상기 프로모터의 활성은 독성 조건에 노출되어 있는 세포에서 발견된 인자들에 의해 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 도입하여 변형된 세포를 생산하는 단계를 포함하는, 상기 개체에서 질병 또는 장애에 대한 투여된 치료제의 잠재적 독성을 모니터하는 방법에 관한 것이다.
본 발명의 다른 구현예는 (a) 상기 개체에 치료제를 투여하는 단계; (b) 상기 변형된 세포에 리간드를 투여하는 단계; 및 (c) 리포터 유전자 발현을 적어도 2회 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨의 변화가 상기 치료제의 독성을 지시하고, 상기 개체의 변형된 세포는 (1) 유전자 스위치를 코딩하는 폴리뉴클레오티드, 상기 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하고, 여기서 상기 적어도 하나의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하고, 진단 스위치 프로모터에 연결되며, 여기서 상기 프로모터의 활성은 독성 조건에 노출되어 있는 세포에서 발견된 인자들에 의해 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인, 상기 개체에서 질병 또는 장애에 대한 투여된 치료제의 잠재적 독성을 모니터하는 방법에 관한 것이다.
보다 구체적인 구현예에서는, 질병 또는 장애에 대한 투여된 치료제의 잠재적 독성을 몬터하는 방법은 비-자가 세포, 예를 들어 개체에 동종이계 또는 이종인 세포인 비-자가 조직 세포를 사용하여 수행된다. 하나의 구현예에서, (a) 비-자가 세포에 (1) 유전자 스위치를 코딩하는 폴리뉴클레오티드, 이때, 상기 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하며, 여기서 상기 적어도 하나의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하고, 작동가능하게 진단 스위치 프로모터와 연결되며, 여기서 상기 프로모터의 활성은 상기 개체의 질병 또는 장애 기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 도입하여 변형된 세포를 생산하는 단계; (b) 상기 개체로 상기 변형된 세포를 도입하는 단계; (c) 상기 변형된 세포에 리간드를 투여하는 단계; 및 (c) 리포터 유전자 발현을 적어도 2회 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨의 변화가 상기 치료제의 독성을 지시하는 것인, 상기 개체에서 질병 또는 장애에 대한 투여된 치료제의 잠재적 독성을 모니터하는 방법에 관한 것이다.
본 발명의 다른 구현예에서, 폴리뉴클레오티드는 치료제로서 투여되는 인자에 의해 활성화되는 프로모터의 조절하에 있는 전사 인자 서열을 포함한다(예를 들어, 치료용 단백질 또는 핵산을 이용한 유전자 치료법 치료제). 유전자 스위치를 투여된 치료제에 민감하게 만들어서 개체가 치료 인자의 과발현 또는 저발현의 공개적인 증후군을 보여주기 전에 유전자 치료법 치료제의 발현을 모니터 및 치료제의 바람직하지 않게 높거나 또는 낮은 투여 양 레벨을 탐지하는데 사용될 수 있다. 하나의 구현예에서, 본 발명은 (a) 상기 개체에 치료제를 투여하는 단계; (b) 상기 개체의 세포에 (1) 유전자 스위치를 코딩하는 폴리펩타이드, 이때, 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하고, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 진단 스위치 프로모터에 연결되며, 여기서 상기 프로모터의 활성은 치료를 위해 투여되어 있는 인자에 의해 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 도입하여 변형된 세포를 생산하는 단계; (c) 상기 변형된 세포에 리간드를 투여하는 단계; 및 (d) 리포터 유전자 발현을 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨은 치료를 위해 투여된 상기 인자의 레벨을 지시하는 것인, 상기 질병 또는 장애에 대한 치료를 위해 상기 개체에 투여되어 있는 상기 인자의 레벨을 모니터하는 방법에 관한 것이다.
이러한 방법은 상기에서 기술된 임의의 진단 방법을 사용하서라도 수행될 수 있다(곧, 생체 외 세포, 생체 외 세포 변형 후 생체 내 로 세포의 재도입, 생체 내).
본 발명의 생체 외 구현예에서, 리포터 유전자 발현의 기본 수준을 결정하기 위해 세포는 치료 전에 개체로부터 분리될 수 있다. 치료제가 개체에 투여된 후, 리포터 유전자 발현을 결정하기 위해서 세포는 개체로부터 다양한 간격으로 분리될 수 있다.
본 발명의 생체 내 구현예에서, 변형된 세포 또는 폴리뉴클레오티드는 치료제의 투여 전, 동안, 또는 후에 개체로 도입될 수 있다. 세포 또는 폴리뉴클레오티드가 치료 전에 투여된다면, 리포터 유전자 발현의 기본 수준이 획득될 수 있다.
리포터 유전자 발현의 측정은 생체 외 또는 생체 내 에서 수행될 수 있다. 하나의 구현예에서, 모니터은 세포를 라간드에 연속적으로 노출시키면서 리포터 유전자 발현을 간헐적으로 측정함으로써 수행될 수 있다. 다른 구현예에서, 모니터은 세포를 라간드에 간헐적으로 노출시키면서 리포터 유전자 발현을 각 노출 동안 측정함으로써 수행될 수 있다.
본 발명의 한 구현예는 상기 개체의 세포에 (1) 유전자 스위치를 코딩하는 폴리펩타이드, 이때, 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하고, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 진단 스위치 프로모터에 연결되며, 여기서 상기 프로모터의 활성은 치료를 위해 투여되어 있는 인자에 의해 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 도입하여 변형된 세포를 생산하는 단계를 포함하는, 개체에서 질병 또는 장애의 치료를 위해 투여한 인자의 레벨을 모니터하기 위해 변형된 세포를 제조하는 방법에 관한 것이다.
다른 하나의 구현예에서, 본 발명은 (a) 상기 개체에 치료제를 투여하는 단계; (b) 상기 변형된 세포에 리간드를 투여하는 단계; 및 (c) 리포터 유전자 발현을 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨은 치료를 위해 투여된 상기 인자의 레벨을 지시하고, 상기 개체의 변형된 세포는 (1) 유전자 스위치를 코딩하는 폴리펩타이드, 이때, 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하고, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 진단 스위치 프로모터에 연결되며, 여기서 상기 프로모터의 활성은 치료를 위해 투여되어 있는 인자에 의해 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는, 질병 또는 장애의 치료를 위해 개체에게 투여되어 있는 상기 인자의 레벨을 모니터하는 방법에 관한 것이다.
보다 구체적인 구현예에서, 질병 또는 장애 치료를 위해 투여되고 있는 인자의 레벨을 모니터하기 위한 방법이 예를 들어 개체에게 동종이계 또는 이종인 세포인 비-자가 조직 세포를 사용하여 수행되었고, 변형된 비-자가 조직 세포가 개체 내로 도입되었다. 본 발명은 (a) 비-자가 세포에 (1) 유전자 스위치를 코딩하는 폴리펩타이드, 이때, 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하고, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 진단 스위치 프로모터에 연결되며, 여기서 상기 프로모터의 활성은 치료를 위해 투여되어 있는 인자에 의해 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 도입하여 변형된 세포를 생산하는 단계; (b) 상기 개체에 상기 변형된 세포를 도입하는 단계; (c) 상기 변형된 세포에 리간드를 투여하는 단계; 및 (d) 리포터 유전자 발현을 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨은 치료를 위해 투여된 상기 인자의 레벨을 지시하는 것인, 상기 질병 또는 장애에 대하여 상기 개체에 투여되어 있는 상기 인자의 레벨을 모니터하는 방법에 관한 것이다.
또 다른 양태로서, 본 발명은 (a) 기관 또는 조직 이식의 세포에 (1) 유전자 스위치를 코딩하는 폴리뉴클레오티드, 이때, 상기 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하고, 상기 적어도 하나의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하고, 진단 스위치 프로모터에 작동가능하게 연결되며, 여기서 상기 프로모터의 활성은 이식 거부기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 도입하여 변형된 세포를 생산하는 단계; (b) 상기 변형된 세포에 리간드를 투여하는 단계; 및 (c) 리포터 유전자 발현을 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현이 이식 거부가 탐지됨을 지시하는 것인, 기관 또는 조직 이식을 받는 개체에서 이식 거부를 탐지하는 방법에 관한 것이다.
부가적인 구현예로서, 본 발명은 (a) 기관 또는 조직 이식의 세포에 (1) 유전자 스위치를 코딩하는 폴리뉴클레오티드, 이때, 상기 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하고, 상기 적어도 하나의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하고, 진단 스위치 프로모터에 작동가능하게 연결되며, 여기서 상기 프로모터의 활성은 이식 거부기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 도입하여 변형된 세포를 생산하는 단계; (b) 상기 변형된 세포에 리간드를 투여하는 단계; 및 (c) 리포터 유전자 발현을 적어도 2회 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨의 변화가 상기 개체에서 상기 이식 거부의 진행을 지시하는 것인, 상기 기관 또는 조직 이식을 받는 개체에서 이식 거부의 진행을 모니터하는 방법에 관한 것이다.
이식을 받는 자에서 이식 거부를 탐지 및 모니터하는 방법은 이식된 기관 또는 조직의 생존력을 모니터하는데 사용될 수 있다. 이식 거부의 시작을 탐지하는 능력은 의료인이 예를 들어, 면역 억제제 치료의 레벨을 조정하는 방식으로, 이식 환자의 치료를 조정할 수 있게 한다. 본 방법의 감도는 조직 손상을 조사하는 주기적인 생검을 취하는 현재 방법보다 더 빠르게 거부에 대한 초기 탐지를 가능하게 한다. 개체에서 거부 발생을 초기에 탐지하면 이식된 기관 또는 조직에 대한 추가적인 손상을 보다 빠르게 대처하여 피할 수 있게 한다. 상기의 방법들이 심장, 신장, 폐, 간, 췌장, 소장 및 대장, 피부, 각막, 골수, 뼈, 인대, 힘줄, 신경 조직, 및 줄기 세포 이식을 포함하는 임의의 기관 또는 조직 이식에 사용될 수 있으나, 여기에 제한적이지는 않다.
본 발명의 방법에서, 유전자 스위치는 예를 들어, 거부 프로모터인 이식 거부 동안 활성화되는 하나 이상의 진단 스위치 프로모터를 포함한다. 거부 프로모터는, 거부 반응이 일어나기 시작할 때, 이식된 기관 또는 조직에서 활성화되는 임의의 프로모터이다. 본 발명에서 유용한 거부 프로모터의 예는 표 4에 거부 동안에 발현증가가 탐지된 기관과 더불어 열거된 유전자로부터의 프로모터를 포함하나, 여기에 제한되지 않는다.
본 발명의 하나의 구현예에서, 거부 프로모터를 포함하는 폴리뉴클레오티드는 이식 절차에 앞서 이식될 기관 또는 조직에 투여된다. 통상적으로 이식에 사용되는 기관 또는 조직은 장기 기증자로부터 제거된 24-48 시간 내 수여자(recipient)에게 이식되어야 한다. 하나의 구현예에서, 본 발명의 폴리뉴클레오티드는 장기 기증자로부터 제거된 48 시간 내에 예를 들어, 36, 24, 18, 12, 또는 6 시간 안에 기관 또는 조직에 투여된다. 다른 구현예에서, 폴리뉴클레오티드는 수여자에게 이식되기 전 적어도 48 시간 내에 예를 들어, 적어도 36, 24, 18, 12, 또는 6 시간 안에 기관 또는 조직에 투여된다. 폴리뉴클레오티드는 하나 또는 그 이상의 위치서 예를 들어, 2, 3, 4, 5, 6, 7, 8, 9, 10 또는 더 많은 위치에서 이식되는 기관 또는 조직에 도입될 수 있다.
다른 구현예에서, 폴리뉴클레오티드는 개체로 이식된 후 예를 들어, 이식 후 2, 4, 6, 8, 10, 12, 또는 18 시간, 1, 2, 3, 4, 5, 또는 6 일, 또는 1, 2, 3, 또는 4 주 또는 그 이상 후에 기관 또는 조직에 투여된다.
폴리뉴클레오티드는 직접 주사, 전기천공법, 바이러스 전송등을 포함한 상기에 기술된 임의의 방법에 의해서라도 기관 또는 조직에 투여될 수 있다. 다른 구현예에서, 폴리뉴클레오티드는 예를 들어, 형질전환된 줄기 세포와 같은 형질전환된 세포의 일부분으로서 투여될 수 있다. 세포는 이식 기증자 또는 수여자로 부터 분리될 수 있다. 예를 들어, 이식의 필요로 하여 줄기세포는 개체로부터 분리될 수 있고 본 발명의 폴리뉴클레오티드가 줄기세포 내로 도입될 수 있다. 그 후, 이식을 위한 기관 또는 조직이 입수될 때까지, 형질전환된 세포는 저장될 수 있다(예, 냉동보존). 그 다음 형질전환된 세포는 이식 전후에 기관 또는 조직에 투여될 수 있다.
보다 구체적인 구현예에서, 이식 거부를 탐지하는 방법은 본 발명의 폴리뉴클레오티드를 예들 들어, 이식될 기관 또는 조직에 동종이계 또는 이종인 세포인 비-자가 조직 세포 내로 도입하여 수행될 수 있고, 변형된 비-자가 조직 세포가 이식전에 기관 또는 조직에 도입된다.
본 발명의 하나의 구현예에서, 유전자 스위치는 전사 인자 서열에 작동가능하게 연결된 단일 거부 프로모터를 포함한다. 다른 구현예에서, 유전자 스위치는 리간드-의존 전사인자를 코딩하는 2 개의 다른 전사 인자 서열에 작동가능하게 연결된 2 개의 거부 프로모터를 포함한다. 2 개의 거부 프로모터는 동일하거나 또는 상이할 수 있다.
다른 구현예에서, 유전자 스위치는 보다 구체적으로 유전자 스위치 기능을 모니터하는데 유용한 대조군 단백질의 발현을 조절하는 프로모터를 포함할 수 있다. 곧, 이를 통해 유전자 스위치가 그것의 환경에서 제대로 작동하는지를 예를 들어, 유전자 스위치가 유전자 사일렌싱에 구속되지 않는지를 볼 수 있다. 대조군 단백질의 발현은 유전자 스위치로부터 나오는 부정 오류(false negative) 결과를 제한하는데 사용될 수 있다. 하나의 구현예에서, 대조군 단백질에 연결된 프로모터는 항시적 프로모터이기에 대조군 단백질은 항상 발현된다. 다른 구현예에서는, 대조군 단백질에 연결된 프로모터는 유전자 스위치에 존재하는 거부 프로모터와는 다른 스위치 프로모터이다. 대조군 단백질은 제1 리포터 유전자와는 다른 제2 리포터 유전자에 작동가능하게 연결된 프로모터에 결합하는 리간드-의존 전사인자일 수 있다. 예를 들어, 대조군 단백질은 거부 프로모터로부터 발현된 전사인자와 다른 DNA 결합 도메인을 지니고, 도 4에 개시된 제2 리포터 유전자에 작동가능하게 연결된 프로모터 상의 반응 서열을 인식하는 리간드-의존 전사인자일 수 있다.
이식 거부를 탐지 또는 모니터하는 방법의 하나의 구현예에서, 리포터 유전자는 상기에 기술된 임의의 리포터 유전자이다. 다른 구현예에서, 리포터 유전자는 예를 들어, 이식받은 자의 혈액 또는 소변 샘플에서 쉽게 탐지될 수 있는 분비 단백질을 코딩한다. 다른 구현예에서, 리포터 유전자는 예를 들어, 정상적으로는 낮은 수준으로 발현되다가 거부가 시작되자마자 리포터 유전자 발현이 탐지되는 이식받은 자에 내생적인 단백질을 코딩한다.
본 발명의 폴리뉴클레오티드가 일단 기관 또는 조직 이식체에 투여되면, 이식 거부를 탐지 또는 모니터하는 방법이 리포터 유전자 발현 탐지에 의하여 수행될 수 있다. 하나의 구현예에서, 리포터 유전자 발현의 레벨은 한 번 측정될 수 있다. 다른 구현예에서, 리포터 유전자 발현의 레벨은 한번 이상 예를 들어, 매 1, 2, 3, 4, 5, 6 일 마다, 1, 2, 3, 4 주 마다, 또는 1, 2, 3, 4, 5, 6 또는 그 이상의 매 달 한번씩과 같이 정기적으로 측정될 수 있다. 측정되는 각 시점에서, 리포터 유전자 발현의 측정은 발현의 백그라운드 레벨을 얻기 위해 리간드의 부재하에 이루어질 수 있고, 거부 프로모터 활성화에 기인한 리포터 유전자 발현의 레벨을 얻기 위해서 리간드의 존재하에서도 이루어질 수 있다. 하나의 구현예에서, 리간드의 존재하의 리포터 유전자 발현의 레벨은, 임의의 이식 거부도 일어나기 전의 리포터 유전자 발현의 리간드-도입 기본 수준을 얻기 위해서, 이식 후(예, 1, 2, 3, 4, 5, 6 일 내 또는 1, 2, 3, 또는 4 주 내) 곧바로 결정된다. 측정가능한 리포터 유전자 발현의 레벨을 얻기 위해서 얼마나 많은 리간드를 개체에게 투여하여야 하는지 및 얼마나 오랫동안 리간드가 존재해야 하는지를 결정하기 위해 초기의 시점(또는 이 후의 임의의 시점)이 사용될 수 있다. 투여 양과 시간은 각 개체의 필요에 따라 조정될 수 있다. 그 후 이식 거부를 가리키는 리포터 유전자 발현의 임의의 증가도 탐지하기 위해서 리간드-도입 리포터 유전자 발현의 주기적인 모니터이 수행될 수 있다.
대조군 단백질(항시적이거나 또는 유도이거나)을 코딩하는 폴리뉴클레오티드가 유전자 스위치에 존재한다면, 대조군 단백질 또는 대조군 단백질에 의해 도입되는 리포터 유전자의 레벨은 유전자 스위치가 제대로 작동하는지를 확인하기 위해서 동시에 측정될 수 있다. 유전자 스위치가 최적으로 작동하지 않는다면, 유전자 스위치로부터의 신호를 증가시키기 위해서 리간드 농도 또는 리간드 투여 및 리포터 유전자 탐지 시간 사이의 시간 양을 증가시키는 것이 필요하다. 다른 구현예에서, 유전자 스위치가 더 이상 기능을 하지 않는다면, 부가적인 폴리뉴클레오티드가 기관 또는 조직 이식체에 투여될 수 있고 이식 거부에 대한 모니터이 계속될 수 있다.
보다 구체적인 구현예에서, 이식 거부의 존재를 가리키는 리포터 유전자 발현의 증가가 일단 탐지되면, 이식된 조직의 생검을 얻는 고전적인 방법을 사용하여 진단이 확진될 수 있다.
하나의 구현예는 기관 또는 조직 이식의 세포에 (1) 유전자 스위치를 코딩하는 폴리뉴클레오티드, 이때, 상기 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하며, 여기서 상기 적어도 하나의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하고, 작동가능하게 진단 스위치 프로모터와 연결되며, 여기서 상기 프로모터의 활성은 이식 거부 기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 도입하여 변형된 세포를 생산하는 단계를 포함하는, 상기 개체에서 이식 거부를 탐지하기 위해 기관 또는 조직 이식물(transplant)을 제조하는 방법에 관한 것이다.
또 다른 구현예로서, 본 발명은 (a) 상기 개체에 리간드를 투여하는 단계; 및 (b) 리포터 유전자 발현을 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현은 이식 거부가 탐지됨을 지시하고, 상기 기관 또는 조직 이식체는 (1) 유전자 스위치를 코딩하는 폴리뉴클레오티드, 이때, 상기 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하며, 여기서 상기 적어도 하나의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하고, 작동가능하게 진단 스위치 프로모터와 연결되며, 여기서 상기 프로모터의 활성은 이식 거부 기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 하나 이상의 세포를 포함하는 것인, 기관 또는 조직 이식을 받는 개체에서 이식 거부를 탐지하는 방법에 관한 것이다.
하나의 구현예로서, 본 발명은 상기 기관 또는 조직 이식의 세포로 (1) 유전자 스위치를 코딩하는 폴리뉴클레오티드, 이때, 상기 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하며, 여기서 상기 적어도 하나의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하고, 작동가능하게 진단 스위치 프로모터와 연결되며, 여기서 상기 프로모터의 활성은 이식 거부 기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 도입하여 변형된 세포를 생산하는 단계를 포함하는, 개체에서 이식 거부의 진행을 모니터하기 위해 기관 또는 조직 이식체를 제조하는 방법에 관한 것이다.
또 다른 구현예로서, 본 발명은 (a) 상기 개체에 리간드를 투여하는 단계; 및 (b) 리포터 유전자 발현을 적어도 2회 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨의 변화가 상기 개체에서 상기 이식 거부의 진행을 지시하고, 상기 기관 또는 조직 이식체는 (1) 유전자 스위치를 코딩하는 폴리뉴클레오티드, 이때, 상기 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하고, 상기 적어도 하나의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하고, 진단 스위치 프로모터에 작동가능하게 연결되며, 여기서 상기 프로모터의 활성은 이식 거부기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 하나 이상의 세포를 포함하는 것인, 기관 또는 조직 이식을 받는 개체에서 이식 거부의 진행을 모니터하는 방법에 관한 것이다.
보다 구체적인 구현예에서, 이식 거부를 모니터하기 위한 방법이 예를 들어, 이식되는 기관 또는 조직에 대해 동종이계 또는 이종인 세포인 비-자가 조직 세포에 본 발명의 폴리뉴클레오티드를 도입하여 수행되었고, 변형된 비-자가 조직 세포가 이식에 앞서 상기 기관 또는 조직에 도입되었다.
상기에 기술된 방법의 한 구현예에서, 유전자 스위치 및 리포터 유전자를 코딩하는 하나 또는 2 개의 폴리뉴클레오티드는 개체에 투여되고 있는 치료용 벡터의 일부분일 수 있다(예, 유전자 치료를 위한 치료용 인자(단백질 또는 핵산)를 코딩하는 벡터). 이러한 구현예에서, 상기 인자 및 상기 인자의 레벨을 모니터하기 위한 진단 검사법이 함께 한 단위로 수행되어, 치료제를 받은 모든 세포가 진단 유전자 스위치를 또한 받을 수 있도록 한다.
상기 기술한 각 방법에 대한 하나의 구현예에서, 유전자 스위치를 코딩하는 폴리뉴클레오티드 및 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드는 예를 들어, 벡터와 같은 단일 거대 폴리뉴클레오티드의 일부분이다. 다른 구현예에서, 유전자 스위치를 코딩하는 폴리뉴클레오티드 및 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드는 독립된 폴리뉴클레오티드다.
하나의 양태에서, 본 발명은 본 발명의 방법에 사용될 수 있는 폴리뉴클레오티드에 관한 것이다. 하나의 구현예에서, 상기 폴리뉴클레오티드는 유전자 스위치를 코딩한다. 여기서 상기 유전자 스위치는 하나 이상의 전사 인자 서열을 포함하고, 여기서 상기의 하나 이상의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하며, 이들은 작동가능하게 진단 스위치 프로모터에 연결되어 있고, 여기서 프로모터의 활성은 상기 질병 또는 장애 동안 조절된다. 또 다른 구현예에서, 상기 폴리뉴클레오티드는 더 나아가 상기 리간드-의존 전사 인자에 의해 활성화되는 프로모터에 연결된 리포터 유전자를 코딩한다. 하나의 구현예에서, 유전자 스위치는 EcR-기반 유전자 스위치이다. 또 다른 구현예에서는, 상기 유전자 스위치는 제1 진단 스위치 프로모터 조절하에 있는 제1 전사 인자 서열 및 제2 진단 스위치 프로모터 조절하에 있는 제2 전사 인자 서열을 포함한다. 여기서, 상기 제1 전사 인자 서열 및 상기 제2 전사 인자 서열에 의해 코딩되는 단백질은 서로 상호작용하여 단백질 복합체를 이루고, 이들은 리간드-의존 전사인자로 작용한다. 하나의 구현예에서, 제1 진단 스위치 프로모터 및 제2 진단 스위치 프로모터는 다르다. 다른 구현예에서, 제1 진단 스위치 프로모터 및 제2 진단 스위치 프로모터는 같다. 또 다른 구현예에서, 제1 전사 인자 서열은 이형이량체화 파트너 및 전사활성화도메인을 포함하는 단백질을 코딩하고 제2 전사 인자 서열은 DNA 결합 도메인 및 리간드-결합 도메인을 포함하는 단백질을 코딩한다. 보다 구체적인 구현예에서, 폴리뉴클레오티드는 유도 프로모터에 작동가능하게 연결된 치사 폴리펩티드를 또한 코딩한다.
하나의 양태로서, 본 발명은 유전자 스위치를 코딩하는 폴리뉴클레오티드에 관한 것이다. 여기서 상기 유전자 스위치는 하나 이상의 전사 인자 서열을 포함하고, 여기서 상기의 하나 이상의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하며, 이들은 작동가능하게 진단 스위치 프로모터에 연결되어 있고, 여기서 프로모터의 활성은 상기 독성조건에 노출된 세포에서 발견되는 인자에 의해 조절된다. 또 다른 구현예에서, 폴리뉴클레오티드는 구체적으로 상기 리간드-의존 전사 인자에 의해 활성화되는 프로모터에 연결된 리포터 유전자를 코딩한다. 하나의 구현예에서, 유전자 스위치는 EcR-기반 유전자 스위치이다. 또 다른 구현예에서는, 상기 유전자 스위치는 제1 진단 스위치 프로모터 조절하에 있는 제1 전사 인자 서열 및 제2 진단 스위치 프로모터 조절하에 있는 제2 전사 인자 서열을 포함한다. 여기서, 상기 제1 전사 인자 서열 및 상기 제2 전사 인자 서열에 의해 코딩되는 단백질은 서로 상호작용하여 단백질 복합체를 이루고, 이들은 리간드-의존 전사인자로 작용한다. 하나의 구현예에서, 제1 진단 스위치 프로모터 및 제2 진단 스위치 프로모터는 다르다. 다른 구현예에서, 제1 진단 스위치 프로모터 및 제2 진단 스위치 프로모터는 같다. 또 다른 구현예에서, 제1 전사 인자 서열은 이형이량체화 파트너 및 전사활성화 도메인을 포함하는 단백질을 코딩하고 제2 전사 인자 서열은 DNA 결합 도메인 및 리간드-결합 도메인을 포함하는 단백질을 코딩한다. 보다 구체적인 구현예에서, 폴리뉴클레오티드는 유도 프로모터에 작동가능하게 연결된 치사 폴리펩티드를 또한 코딩한다.
하나의 양태로서, 본 발명은 유전자 스위치를 코딩하는 폴리뉴클레오티드에 관한 것이다. 여기서 상기 유전자 스위치는 하나 이상의 전사 인자 서열을 포함하고, 여기서 상기의 하나 이상의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하며, 이들은 작동가능하게 진단 스위치 프로모터에 연결되어 있고, 여기서 프로모터의 활성은 치료를 위해 투여되고 있는 상기 인자에 의해 조절된다. 다른 구현예에서, 폴리뉴클레오티드는 구체적으로 상기 리간드-의존 전사 인자에 의해 활성화되는 프로모터에 연결된 리포터 유전자를 코딩한다. 하나의 구현예에서, 유전자 스위치는 EcR-기반 유전자 스위치이다. 또 다른 구현예에서는, 상기 유전자 스위치는 제1 진단 스위치 프로모터 조절하에 있는 제1 전사 인자 서열 및 제2 진단 스위치 프로모터 조절하에 있는 제2 전사 인자 서열을 포함한다. 여기서, 상기 제1 전사 인자 서열 및 상기 제2 전사 인자 서열에 의해 코딩되는 단백질은 서로 상호작용하여 단백질 복합체를 이루고, 이들은 리간드-의존 전사인자로 작용한다. 하나의 구현예에서, 제1 진단 스위치 프로모터 및 제2 진단 스위치 프로모터는 다르다. 다른 구현예에서, 제1 진단 스위치 프로모터 및 제2 진단 스위치 프로모터는 같다. 또 다른 구현예에서, 제1 전사 인자 서열은 이형이량체화 파트너 및 전사활성화도메인을 포함하는 단백질을 코딩하고 제2 전사 인자 서열은 DNA 결합 도메인 및 리간드-결합 도메인을 포함하는 단백질을 코딩한다. 보다 구체적인 구현예에서, 폴리뉴클레오티드는 유도 프로모터에 작동가능하게 연결된 치사 폴리펩티드를 또한 코딩한다.
하나의 양태로서, 본 발명은 유전자 스위치를 코딩하는 폴리뉴클레오티드에 관한 것이다. 여기서 상기 유전자 스위치는 하나 이상의 전사 인자 서열을 포함하고, 여기서 상기의 하나 이상의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하며, 이들은 작동가능하게 진단 스위치 프로모터에 연결되어 있고, 여기서 프로모터의 활성은 이식 거부 동안 조절된다. 다른 구현예에서, 폴리뉴클레오티드는 구체적으로 상기 리간드-의존 전사 인자에 의해 활성화되는 프로모터에 연결된 리포터 유전자를 코딩한다. 하나의 구현예에서, 유전자 스위치는 EcR-기반 유전자 스위치이다. 또 다른 구현예에서는, 상기 유전자 스위치는 제1 진단 스위치 프로모터 조절하에 있는 제1 전사 인자 서열 및 제2 진단 스위치 프로모터 조절하에 있는 제2 전사 인자 서열을 포함한다. 여기서, 상기 제1 전사 인자 서열 및 상기 제2 전사 인자 서열에 의해 코딩되는 단백질은 서로 상호작용하여 단백질 복합체를 이루고, 이들은 리간드-의존 전사인자로 작용한다. 하나의 구현예에서, 제1 진단 스위치 프로모터 및 제2 진단 스위치 프로모터는 다르다. 다른 구현예에서, 제1 진단 스위치 프로모터 및 제2 진단 스위치 프로모터는 같다. 또 다른 구현예에서, 제1 전사 인자 서열은 이형이량체화 파트너 및 전사활성화도메인을 포함하는 단백질을 코딩하고 제2 전사 인자 서열은 DNA 결합 도메인 및 리간드-결합 도메인을 포함하는 단백질을 코딩한다. 보다 구체적인 구현예에서, 폴리뉴클레오티드는 유도 프로모터에 작동가능하게 연결된 치사 폴리펩티드를 또한 코딩한다.
다른 양태로서, 본 발명은 상기에 기술된 임의의 폴리뉴클레오티드를 포함하는 벡터에 관한 것이다. 하나의 구현예에서, 벡터는 플라스미드 벡터 또는 바이러스 벡터이다. 하나의 구현예에서, 상기 폴리뉴클레오티드들은 같은 벡터에 존재한다. 보다 구체적인 구현예에서, 각 폴리뉴클레오티드는 독립된 벡터에 있다. 독립된 벡터들은 동일한 벡터(예, 같은 플라스미드), 같은 타입의 벡터(예, 두가지가 플라스미드이지만 같은 플라스미드는 아니다) 또는 다른 타입의 벡터(예, 하나의 벡터는 플라스미드이고, 다른 벡터는 바이러스이다)일 수 있다.
또 다른 양태로서, 본 발명은 본 발명의 방법과 결합해서 사용될 수 있는 키트를 제공한다. 본 발명의 이러한 양태에 따른 키트는 하나 이상의 용기를 포함할 수 있으며, 이들 용기는 하나 이상의 핵산 분자, 제한 효소, 및 그런 핵산을 포함하는 하나 이상의 세포로 이루어진 그룹으로부터 선택된 하나 이상의 구성요소를 포함할 수 있다. 본 발명의 키트는 보다 구체적으로 본 발명의 세포를 배양하는데 적합한 세포배양액을 포함하는 하나 이상의 용기, 본 발명의 세포를 배양하는데 적합한 항생제를 포함하는 하나 이상의 용기, 완충용액을 포함하는 하나 이상의 용기, 형질전환 시약을 포함하는 하나 이상의 용기, 효소 반응의 기질을 포함하는 하나 이상의 용기, 및/또는 유전자 스위치 활성을 위한 하나 이상 리간드를 포함할 수 있다.
본 발명의 키트는 본 발명과 같이 사용될 수 있는 다양한 핵산분자를 포함할 수 있다. 본 발명의 키트에 제공될 수 있는 핵산분자의 예는 프로모터, 유전자 스위치를 코딩하는 서열, 인핸서, 리프레서, 선택 마커, 전사 신호, 번역 신호, 프라이머 하이브리다이제이션 부위(예, 서열결정과 PCR을 위한), 재조합 부위, 및 다중링커, 억제자 tRNA 존재하에서 번역 종료를 억제하는 부위, 억제자 tRNA 코딩 서열, 복제, 텔로미어, 센트로미어의 도메인 및/또는 부위, 오리진을 코딩하는 서열 등을 포함한다. 하나의 구현예에서, 키트는 임의의 진단 스위치 프로모터도 없는 유전자 스위치, 관심 있는 진단 스위치 프로모터 삽입에 적합한 폴리뉴클레오티드를 포함하는 폴리뉴클레오티드를 포함할 수 있다. 본 발명의 핵산분자는 상기에 기술된 폴리뉴클레오티드뿐만 아니라 하나 이상의 임의의 특징도 포함할 수 있다.
본 발명의 키트는 세포를 포함할 수 있다. 세포는 본 발명의 폴리뉴클레오티드를 포함할 수 있다, 또는 세포 및 폴리뉴클레오티드는 독립된 용기에 담겨질 수 있다. 하나의 구현예에서, 세포는 예를 들어, 특정 개체를 위해 고안된 키트의 일부분으로서 자가 조직 세포일 수 있다. 다른 구현예에서, 세포는 예를 들어, 임의의 개체라도 위하게 고안된 키트의 일부분으로서 비-자가 조직 세포일 수 있다.
본 발명의 키트는 하나 이상의 재조합 단백질을 포함하는 용기를 포함할 수 있다. 여기에 적합한 재조합 단백질은 Cre, Int, IHF, Xis, FIp, Fis, Hin, Gin, Cin, Tn3 resolvase, ΦC31, TndX, XerC, 및 XerD를 포함하나, 여기에 제한적이지는 않다. 다른 적합한 재조합 부위 및 단백질은 카나다 칼스바드의 인비트로젠사(Invitrogen Corp.)로부터 입수가능한 게이트웨이™ 클로닝 테크놀로지(GATEWAY™ Cloning Technology)와 연관된 것이고, 참고로 여기에 도입된 전체 개시물인 게이트웨이™ 클로닝 테크놀로지의 제품 소개서(버전 E, 9월 22일, 2003)에 기술되어 있다.
본 발명의 키트는 프라이머와 같이 또한 공급될 수 있다. 이들 프라이머는 일반적으로 특이 핵산 서열을 지닌 분자에 어닐링 되도록 디자인될 것이다. 예를 들어, 이들 프라이머는 특정 핵산 분자를 증폭하기 위한 PCR 용도로 디자인 될 수 있다. 서열 결정 프라이머도 또한 키트와 같이 제공될 수 있다.
하나 이상의 완충 용액(예, 1,2,3,4,5,8,10,15)이 본 발명의 키트에 제공될 수 있다. 이들 완충 용액은 작동 농도(working concentration)로 제공될 수 있거나 또는 농축된 형태로 제공되어 작동 농도로 희석될 수 있다. 이들 완충 용액은 활성 강화 또는 완충용액 자체 또는 완충 용액 내의 분자들의 안정화를 위해서 흔히 염, 금속이온, 보조인자, 금속이온 킬레이트 제제 등을 포함할 것이다. 보다 구체적으로, 이들 완충 용액은 건조 또는 수용액 상태로 제공될 수 있다. 완충 용액이 건조 상태로 제공되면, 사용 전에 물에 일반적으로 용해될 것이다.
본 발명의 키트는 상기에서 상술되거나 본 발명의 어딘가에 기술된 구성물들의 임의의 조합을 사실상 포함할 수 있다. 당업자에게 알려진 바와 같이, 본 발명의 키트와 같이 제공되는 구성물은 키트의 의도된 용도에 따라 달라질 것이다. 그리하여, 키트는 본 출원에 기술된 다양한 기능을 수행하도록 고안될 수 있으며 따라서 그런 키트의 구성물 역시 따라서 변할 것이다.
본 발명은 보다 구체적으로 본 발명의 하나 이상의 방법을 수행하는 지시사항에 관한 것이다. 그런 지시사항은 사용자에게 본 발명의 방법을 수행하는데 적합한 조건을 제공한다. 본 발명의 지시사항은 예를 들어, 서면지시(예, 종이에 필기)와 같은 유형의 형태, 또는 예를 들어, 컴퓨터 디스크 또는 인터넷으로 접근가능한 무형의 형태일 수 있다.
본 발명의 방법을 수행하기 위한 전문의 지시사항, 또는, 상기 지시 사항이 키트와 함께 포함되는 경우, 키트 사용을 위한 키트와 같이 포함된 전문의 지시사항은 제공될 필요가 없음을 인식할 것이다. 예를 들어, 본 발명의 키트가 그런 전문의 지시사항을 포함하지 않는 경우의 예는 제공되는 지시사항이 사용자에게 상기 키트가 사용될 수 있는 방법의 실행을 위한 지시사항을 어디에서 획득할 수 있는지를 알려주는 경우다. 그리하여, 본 발명의 방법을 수행하기 위한 지시사항은 판매되거나 또는 배포된 매뉴얼 또는 제품 소개서 등과는 별도로, 인터넷 웹 페이지로부터 얻을 수 있다. 따라서, 본 발명은 키트 사용자에게 키트와 함께 지시사항이 직접 포장 및/또는 배포되지 않는 지시사항을 구할 수 있는 하나 이상의 위치를 알려주는 키트를 포함한다. 그런 지시 사항은 전자 또는 인쇄된 형태를 포함하나, 여기에 제한적이지는 않은 임의의 형태일 수 있다.
지금, 본 발명을 상세하게 기술하였으므로, 당업자들에 의해서, 같은 발명이 상기의 발명 또는 임의의 구현예의 범위에 영향을 주지 않으면서 다양하고 동일한 범위의 조건, 포뮬레이션, 및 다른 매개변수 하에서 수행될 수 있음이 이해될 것이다. 여기에 인용된 모든 특허, 특허 출원, 및 문헌은 원문 전체로 여기에 참고로 포함되었다.
도 1은 본 발명의 진단 유전자 스위치의 구현예를 도시한다. 여기서 리간드-의존 전사 인자의 2 개의 분리 부분을 코딩하는 2개의 전사인자 서열을 다른 프로모터 조절하에 있다. "Dx-스위치 구성요소"는 유전자 스위치를 나타낸다; "AD"는 전사활성화도메인을 나타낸다; "DBD"는 DNA 결합 도메인을 나타낸다; "LBD"는 리간드 결합 도메인을 나타낸다; "표준 Dx-리포터"는 리포터 유전자를 나타낸다; 및 "P1" 및 "P2"는 2 개의 다른 질병- 또는 질환-반응 서열을 나타낸다. 도 1의 다른 구현예에서, "P1"은 항시적인 프로모터이다; 및 "P2" 및 "P3"는 다른 질병- 또는 질환-반응 서열을 나타낸다.
도 2는 본 발명의 진단 유전자 스위치의 구현예를 도시한다. 여기서 리간드-의존 전사 인자의 2 개의 분리 부분을 코딩하는 2개의 전사인자 서열을 다른 프로모터 조절하에 있다. "Dx-스위치 구성요소"는 유전자 스위치를 나타낸다; "AD"는 전사활성화도메인을 나타낸다; "DBD-A"는 제1 DNA 결합 도메인을 나타낸다; "DBD-B"는 제2 DNA 결합 도메인을 나타낸다; "LBD"는 리간드 결합 도메인을 나타낸다; "표준 Dx-리포터-A"는 제1 리포터 유전자를 나타낸다; "표준 Dx-리포터-B"는 제2 리포터 유전자를 나타낸다; 및 "P1", "P2", 및 "P3"는 3 개의 다른 질병- 또는 질환-반응 서열을 나타낸다. 도 2의 다른 구현예에서, "P1"은 항시적인 프로모터이다; 및 "P2" 및 "P3"는 다른 질병- 또는 질환-반응 서열을 나타낸다.
도 3은 본 발명의 진단 유전자 스위치의 구현예를 도시한다. 여기서 리간드-의존 전사 인자의 2 개의 분리 부분을 코딩하는 2개의 전사인자 서열을 다른 진단 스위치 프로모터 조절하에 있다. "Dx-스위치 구성요소"는 유전자 스위치를 나타낸다; "AD"는 전사활성화도메인을 나타낸다; "DBD"는 DNA 결합 도메인을 나타낸다; "LBD"는 리간드 결합 도메인을 나타낸다; "표준 Dx-리포터"는 리포터 유전자를 나타낸다; 및 "Pl," "P2," "P3," 및 "P4"는 4 개의 다른 질병- 또는 질환-반응 서열을 나타낸다.
도 4는 본 발명의 진단 유전자 스위치의 구현예를 도시한다. 여기서 리간드-의존 전사 인자의 2 개의 분리 부분을 코딩하는 2개의 전사인자 서열을 다른 프로모터 조절하에 있고 대조군 리포터 유전자가 존재한다. "Dx-스위치 구성요소"는 유전자 스위치를 나타낸다; "AD"는 전사활성화도메인을 나타낸다; "DBD-A"는 제1 DNA 결합 도메인을 나타낸다; "DBD-B"는 제2 DNA 결합 도메인을 나타낸다; "LBD"는 리간드 결합 도메인을 나타낸다; "표준 Dx-리포터-A"는 제1 리포터 유전자를 나타낸다; "대조군-Dx-리포터-A"는 제2 리포터 유전자를 나타낸다; 및 "Pl" 및 "P2는 2 개의 다른 질병- 또는 질환-반응 서열을 나타낸다; 및 "P3" 및 "P4는 2 개의 다른 대조군 프로모터를 나타낸다; 도 4의 다른 구현예에서, "P3" 및 "P4"는 항시적인 프로모터이다.
도 5는 단일 프로모터 셔틀 벡터(서열 번호:5)의 구현예를 도시하고, 이 벡터는 IL-24/mda-7 프로모터를 포함한다. 이 벡터를 사용하여 생성되는 아데노바이러스는 림프액 샘플로부터 분리된 세포를 형질전환하기 위해 사용된다.
도 6은 이중 프로모터 벡터(서열 번호: 6)의 구현예를 도시하고, 이 벡터는 TRPM4 및 TRGC1/TARP 프로모터를 포함한다. 이 벡터는 비-바이러스 트랜스덕션 시스템을 사용하여 전립선 생체검사조직을 형질 전환하는데 사용된다.
도 7은 단일 프로모터 벡터(서열 번호: 7)의 구현예를 도시하고, 이 벡터는 ADAM-17 프로모터 및 CD95-ADAM8 이중 리포터 (서열 번호: 10)를 포함한다.
도 8은 이중 프로모터 벡터(서열 번호: 8)의 구현예를 도시하고, 이 벡터는 CXCL9 및 SEMA7A 프로모터 및 CD40-CD3 이중 프로모터(서열 번호: 12)를 포함한다.
도 9은 단일 프로모터 벡터(서열 번호: 9)의 구현예를 도시하고, 이 벡터는 ADAM-17 프로모터 및 알카라인 포스파타아제-c 말단 CD40 리포터(서열 번호: 14)를 포함한다.
도 10은 인체 내에서 발현될 때 면역성 성질을 보여주지 않도록 고안된 혈청-기반 리포터의 구현예를 도시한다. 이들 리포터는 자연발생적으로 세포 표면 또는 혈청 내에 존재하는 인간 기반의 아미노산 서열로 이루어져 있다. 그리하여, 이들 리포터는 면역성 성질을 보여 주지도 않고 인체에서 발현되었을 때 면역 공격을 받지 않는다. 하나의 구현예에서, 혈청-기반 리포터는 예를 들어, ELISA 기반 포획 및 탐지를 가능하게 하는 CD95-ADAM8 리포터(서열 번호: 10-11), CD40-CD3 리포터(서열 번호: 12-13), CD28-CD3 reporter(서열 번호: 16-17) 및 CD28-CD40 리포터(서열 번호: 18-19)인 이중 에피토프 리포터이다. 디자인은 분비 경로로 운송하기 위한 신호 펩티드를 사용하고, 세포 표면 항원으로부터의 에피토프가 링커(L)를 가지고 따른다. 다른 구현예에서, 각 디자인에 대해서 다른 조합의 링커 및 에피토프가 사용된다. 다른 구현예에서, 혈청-기반 리포터는 면역포획에 이은 리포터 활성의 효소적 탐지를 가능하게 하는 예를 들어, 알카라인 포스파타아제-c 말단 CD40 리포터(서열 번호: 14-15)인 알카라인 포스파타아제 리포터이다. 알카라인 포스파타아제 리포터는 분비될 수 있는 효소적 리포터를 위해 조직 비특이적 알카라인 포스파타아제를 사용한다. 세포 표면 항원으로부터의 에피토프는 알카라인 포스파타아제 활성 측정 전에 면역포획을 위해서 카르복실 말단에 포함된다. 도 10의 부가적인 구현예에서, 부가적인 알카라인 포스파타아제 리포터는 하기를 포함한다: 알카라인 포스파타아제-아미노 말단 CD40 리포터(서열 번호: 20-21) 및 알카라인 포스파타아제-c 말단 CD28 리포터(서열 번호: 22-23).
도 2는 본 발명의 진단 유전자 스위치의 구현예를 도시한다. 여기서 리간드-의존 전사 인자의 2 개의 분리 부분을 코딩하는 2개의 전사인자 서열을 다른 프로모터 조절하에 있다. "Dx-스위치 구성요소"는 유전자 스위치를 나타낸다; "AD"는 전사활성화도메인을 나타낸다; "DBD-A"는 제1 DNA 결합 도메인을 나타낸다; "DBD-B"는 제2 DNA 결합 도메인을 나타낸다; "LBD"는 리간드 결합 도메인을 나타낸다; "표준 Dx-리포터-A"는 제1 리포터 유전자를 나타낸다; "표준 Dx-리포터-B"는 제2 리포터 유전자를 나타낸다; 및 "P1", "P2", 및 "P3"는 3 개의 다른 질병- 또는 질환-반응 서열을 나타낸다. 도 2의 다른 구현예에서, "P1"은 항시적인 프로모터이다; 및 "P2" 및 "P3"는 다른 질병- 또는 질환-반응 서열을 나타낸다.
도 3은 본 발명의 진단 유전자 스위치의 구현예를 도시한다. 여기서 리간드-의존 전사 인자의 2 개의 분리 부분을 코딩하는 2개의 전사인자 서열을 다른 진단 스위치 프로모터 조절하에 있다. "Dx-스위치 구성요소"는 유전자 스위치를 나타낸다; "AD"는 전사활성화도메인을 나타낸다; "DBD"는 DNA 결합 도메인을 나타낸다; "LBD"는 리간드 결합 도메인을 나타낸다; "표준 Dx-리포터"는 리포터 유전자를 나타낸다; 및 "Pl," "P2," "P3," 및 "P4"는 4 개의 다른 질병- 또는 질환-반응 서열을 나타낸다.
도 4는 본 발명의 진단 유전자 스위치의 구현예를 도시한다. 여기서 리간드-의존 전사 인자의 2 개의 분리 부분을 코딩하는 2개의 전사인자 서열을 다른 프로모터 조절하에 있고 대조군 리포터 유전자가 존재한다. "Dx-스위치 구성요소"는 유전자 스위치를 나타낸다; "AD"는 전사활성화도메인을 나타낸다; "DBD-A"는 제1 DNA 결합 도메인을 나타낸다; "DBD-B"는 제2 DNA 결합 도메인을 나타낸다; "LBD"는 리간드 결합 도메인을 나타낸다; "표준 Dx-리포터-A"는 제1 리포터 유전자를 나타낸다; "대조군-Dx-리포터-A"는 제2 리포터 유전자를 나타낸다; 및 "Pl" 및 "P2는 2 개의 다른 질병- 또는 질환-반응 서열을 나타낸다; 및 "P3" 및 "P4는 2 개의 다른 대조군 프로모터를 나타낸다; 도 4의 다른 구현예에서, "P3" 및 "P4"는 항시적인 프로모터이다.
도 5는 단일 프로모터 셔틀 벡터(서열 번호:5)의 구현예를 도시하고, 이 벡터는 IL-24/mda-7 프로모터를 포함한다. 이 벡터를 사용하여 생성되는 아데노바이러스는 림프액 샘플로부터 분리된 세포를 형질전환하기 위해 사용된다.
도 6은 이중 프로모터 벡터(서열 번호: 6)의 구현예를 도시하고, 이 벡터는 TRPM4 및 TRGC1/TARP 프로모터를 포함한다. 이 벡터는 비-바이러스 트랜스덕션 시스템을 사용하여 전립선 생체검사조직을 형질 전환하는데 사용된다.
도 7은 단일 프로모터 벡터(서열 번호: 7)의 구현예를 도시하고, 이 벡터는 ADAM-17 프로모터 및 CD95-ADAM8 이중 리포터 (서열 번호: 10)를 포함한다.
도 8은 이중 프로모터 벡터(서열 번호: 8)의 구현예를 도시하고, 이 벡터는 CXCL9 및 SEMA7A 프로모터 및 CD40-CD3 이중 프로모터(서열 번호: 12)를 포함한다.
도 9은 단일 프로모터 벡터(서열 번호: 9)의 구현예를 도시하고, 이 벡터는 ADAM-17 프로모터 및 알카라인 포스파타아제-c 말단 CD40 리포터(서열 번호: 14)를 포함한다.
도 10은 인체 내에서 발현될 때 면역성 성질을 보여주지 않도록 고안된 혈청-기반 리포터의 구현예를 도시한다. 이들 리포터는 자연발생적으로 세포 표면 또는 혈청 내에 존재하는 인간 기반의 아미노산 서열로 이루어져 있다. 그리하여, 이들 리포터는 면역성 성질을 보여 주지도 않고 인체에서 발현되었을 때 면역 공격을 받지 않는다. 하나의 구현예에서, 혈청-기반 리포터는 예를 들어, ELISA 기반 포획 및 탐지를 가능하게 하는 CD95-ADAM8 리포터(서열 번호: 10-11), CD40-CD3 리포터(서열 번호: 12-13), CD28-CD3 reporter(서열 번호: 16-17) 및 CD28-CD40 리포터(서열 번호: 18-19)인 이중 에피토프 리포터이다. 디자인은 분비 경로로 운송하기 위한 신호 펩티드를 사용하고, 세포 표면 항원으로부터의 에피토프가 링커(L)를 가지고 따른다. 다른 구현예에서, 각 디자인에 대해서 다른 조합의 링커 및 에피토프가 사용된다. 다른 구현예에서, 혈청-기반 리포터는 면역포획에 이은 리포터 활성의 효소적 탐지를 가능하게 하는 예를 들어, 알카라인 포스파타아제-c 말단 CD40 리포터(서열 번호: 14-15)인 알카라인 포스파타아제 리포터이다. 알카라인 포스파타아제 리포터는 분비될 수 있는 효소적 리포터를 위해 조직 비특이적 알카라인 포스파타아제를 사용한다. 세포 표면 항원으로부터의 에피토프는 알카라인 포스파타아제 활성 측정 전에 면역포획을 위해서 카르복실 말단에 포함된다. 도 10의 부가적인 구현예에서, 부가적인 알카라인 포스파타아제 리포터는 하기를 포함한다: 알카라인 포스파타아제-아미노 말단 CD40 리포터(서열 번호: 20-21) 및 알카라인 포스파타아제-c 말단 CD28 리포터(서열 번호: 22-23).
실시예
실시예 1
도 5에 도시된 벡터는 IL-24/mda-7 프로모터를 포함한다(서열 번호: 5). 아데노바이러스 셔틀 벡터를 사용하여 생성된 아데노바이러스는 림프관 샘플로부터 분리된 세포를 형질전환하기 위해 사용된다. 형질전환된 세포는 두 그룹으로 나뉘어 활성자 리간드의 존재 또는 부재 하에서 배양된다. 그 후 세포의 두 세트를 파쇄하여 얻어진 세포 용해물을 루시퍼라아제 정량에 사용하였다.
실시예 2
도 6에 도시된 벡터는 TRPM4 및 TRGC1/TARP 프로모터를 포함한다 (서열 번호: 6). DNA 벡터는 비-바이러스 형질전환 시스템을 사용하여 전립선 생체검사조직을 형질전환하는데 사용된다. 형질전환된 생체검사조직은 두 그룹으로 나뉘어 활성자 리간드의 존재 또는 부재하에서 배양된다. 생체검사 조직의 두 세트를 파쇄하여 얻어진 세포 용해물을 루시퍼라아제 정량에 사용하였다.
실시예 3
도 7에 도시된 벡터는 ADAM-17 프로모터(서열 번호: 7) 및 CD95-ADAM8 ㄹ리포터(서열 번호: 10-11)를 포함한다. 아데노바이러스 셔틀 벡터를 사용하여 생성된 아데노바이러스는 이식 전 기증된 신장의 일부분을 형질전환하는데 사용하였다. 이식 후, 내과의에 의해 정의된 시간 동안 혈청 샘플의 리포터 유전자에 대한 검사를 실시하였다. 검사 프로토콜은 활성자 리간드에 노출되지 않은 샘플로부터의 리포터 발현 검사로 이루어져 있다. 비활성 그룹의 정맥 천자 후 곧바로, 24시간 동안 리간드를 투여하였고 그 후 중지하였다; 다른 혈액 샘플은 리간드 처리가 완료되기 전 1 시간 내에 회수하였다. 60 시간을 기다린 후, 이러한 절차를 다시 수행하였다.
실시예 4
도 8에 도시된 벡터는 CXCL9 및 SEMA7A 프로모터(서열 번호: 8) 및 CD40-CD3 리포터(서열 번호: 12-13)를 포함한다. 이 벡터는 이식 전 기증된 심장의 일부분을 직접적인 주사 주입(needle injection)을 통해 형질전화하는데 사용하였다. 이식 후, 내과의에 의해 정의된 시간 동안 혈청 샘플의 리포터 유전자에 대한 검사를 실시하였다. 검사 프로토콜은 활성자 리간드에 노출되지 않은 샘플로부터의 리포터 발현 검사로 이루어져 있다. 비활성 그룹의 정맥 천자 후 곧바로, 24시간 동안 리간드를 투여하였고 그 후 중지하였다; 다른 혈액 샘플은 리간드 처리가 완료되기 전 1 시간 내에 회수하였다. 리간드-처리 샘플과 처리하지 않은 샘플 간의 리포터 검사 결과를 비교하였다. 60 시간을 기다린 후, 이러한 절차를 다시 수행하였다.
실시예 5
도 9에 도시된 벡터는 ADAM- 17 프로모터 및 알카라인 포스파타아제-c 말단 CD40 리포터(서열 번호: 14)를 포함한다. 아데노바이러스 셔틀 벡터를 사용하여 생성된 아데노바이러스는 일차 돼지 신장세포를 형질전화하는데 사용하였다. 그 후 이식 전에 결과로 얻어진 세포를 기증자 신장에 도입하였다. 이식 후, 내과의에 의해 정의된 시간 동안 혈청 샘플의 리포터 유전자에 대한 검사를 실시하였다. 검사 프로토콜은 활성자 리간드에 노출되지 않은 샘플로부터의 리포터 발현 검사로 이루어져 있다. 비활성 그룹의 정맥 천자 후 곧바로, 24시간 동안 리간드를 투여하였고 그 후 중지하였다; 다른 혈액 샘플은 리간드 처리가 완료되기 전 1 시간 내에 회수하였다. 리간드-처리 샘플과 처리하지 않은 샘플 간의 리포터 검사 결과를 비교하였다. 60 시간을 기다린 후, 이러한 절차를 다시 수행하였다.
<110> INTREXON CORPORATION
<120> METHODS AND COMPOSITIONS FOR DIAGNOSING DISEASE
<130> IPA100064
<140> PCT/US2008/010040
<141> 2008-08-25
<150> US 61/047,940
<151> 2008-04-25
<150> US 61/014,654
<151> 2007-12-18
<150> US 60/957,474
<151> 2007-08-23
<160> 23
<170> PatentIn version 3.3
<210> 1
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthetic ecdysone receptor
<220>
<221> VARIANT
<222> (4)
<223> X is Glycine or Threonine
<220>
<221> VARIANT
<222> (12)
<223> X is Cysteine or Alanine
<400> 1
Arg Arg Gly Xaa Thr Cys Ala Asn Thr Gly Ala Xaa Cys Tyr Tyr
1 5 10 15
<210> 2
<211> 13
<212> DNA
<213> Artificial Sequence
<220>
<223> Synthetic ecdysone receptor
<220>
<221> misc_feature
<222> (7)
<223> n can be any nucleotide
<400> 2
aggtcanagg tca 13
<210> 3
<211> 15
<212> DNA
<213> Artificial Sequence
<220>
<223> Synthetic ecdysone receptor
<400> 3
gggttgaatg aattt 15
<210> 4
<211> 18
<212> DNA
<213> Artificial Sequence
<220>
<223> Synthetic homing endonuclease (HE) enzyme known as I-SceI
<400> 4
tagggataac agggtaat 18
<210> 5
<211> 13028
<212> DNA
<213> Artificial Sequence
<220>
<223> Synthetic promoter
<400> 5
taaacaaata ggggttccgc gcacatttcc ccgaaaagtg ccacctgacg tctaagaaac 60
cattattatc atgacattaa cctataaaaa taggcgtatc acgaggccct ttcgtcttca 120
agaaaattaa tcgcaccggt atctatgtcg ggtgcggaga aagaggtaat gaaatggcag 180
ctagcatcat caataatata ccttattttg gattgaagcc aatatgataa tgagggggtg 240
gagtttgtga cgtggcgcgg ggcgtgggaa cggggcgggt gacgtagtag tgtggcggaa 300
gtgtgatgtt gcaagtgtgg cggaacacat gtaagcgacg gatgtggcaa aagtgacgtt 360
tttggtgtgc gccggtgtac acaggaagtg acaattttcg cgcggtttta ggcggatgtt 420
gtagtaaatt tgggcgtaac cgagtaagat ttggccattt tcgcgggaaa actgaataag 480
aggaagtgaa atctgaataa ttttgtgtta ctcatagcgc gtaatagtgc gccggtgtac 540
acaggaagtg acaattttcg cgcggtttta ggcggatgtt gtagtaaatt tgggcgtaac 600
cgagtaagat ttggccattt tcgcgggaaa actgaataag aggaagtgaa atctgaataa 660
ttttgtgtta ctcattttgt ctagggagat ccggtaccga tatcctagac aacgatgctg 720
agctaactat aacggtccta aggtagcgac cgcggagact aggtgtattt atctaagcga 780
tcgcttaatt aaggccggcc gccgcaataa aatatcttta ttttcattac atctgtgtgt 840
tggttttttg tgtgaatcca tagtactaac atacgctctc catcaaaaca aaacgaaaca 900
aaacaaacta gcaaaatagg ctgtccccag tgcaagtcca ggtgccagaa catttctcta 960
tccataatgc aggggtaccg ggtgatgacg gtgaaaacct ccaattgcgg agtactgtcc 1020
tccgagcgga gtactgtcct ccgagcggag tactgtcctc cgagcggagt actgtcctcc 1080
gagcggagta ctgtcctccg agcggagtac tgtcctccga gcggagagtc cccggggacc 1140
tagagggtat ataatgggtg ccttagctgg tgtgtgacct catcttcctg tacgcccctg 1200
caggggcgcg ccacgcgtcg aagaaggtga gtaatcttaa catgctcttt tttttttttt 1260
ttgctaatcc cttttgtgtg ctgatgttag gatgacattt acaacaaatg tttgttcctg 1320
acaggaaaaa ccttgctggg taccttcgtt gccggacact tcttgtcctc tactttggaa 1380
aaaaggaatt gagagccgct agcgccacca tggaagatgc caaaaacatt aagaagggcc 1440
cagcgccatt ctacccactc gaagacggga ccgctggcga gcagctgcac aaagccatga 1500
agcgctacgc cctggtgccc ggcaccatcg cctttaccga cgcacatatc gaggtggaca 1560
ttacctacgc cgagtacttc gagatgagcg ttcggctggc agaagctatg aagcgctatg 1620
ggctgaatac aaaccatcgg atcgtggtgt gcagcgagaa tagcttgcag ttcttcatgc 1680
ccgtgttggg tgccctgttc atcggtgtgg ctgtggcccc agctaacgac atctacaacg 1740
agcgcgagct gctgaacagc atgggcatca gccagcccac cgtcgtattc gtgagcaaga 1800
aagggctgca aaagatcctc aacgtgcaaa agaagctacc gatcatacaa aagatcatca 1860
tcatggatag caagaccgac taccagggct tccaaagcat gtacaccttc gtgacttccc 1920
atttgccacc cggcttcaac gagtacgact tcgtgcccga gagcttcgac cgggacaaaa 1980
ccatcgccct gatcatgaac agtagtggca gtaccggatt gcccaagggc gtagccctac 2040
cgcaccgcac cgcttgtgtc cgattcagtc atgcccgcga ccccatcttc ggcaaccaga 2100
tcatccccga caccgctatt ctcagcgtgg tgccatttca ccacggcttc ggcatgttca 2160
ccacgctggg ctacttgatc tgcggctttc gggtcgtgct catgtaccgc ttcgaggagg 2220
agctattctt gcgcagcttg caagactata agattcaatc tgccctgctg gtgcccacac 2280
tatttagctt cttcgctaag agcactctca tcgacaagta cgacctaagc aacttgcacg 2340
agatcgccag cggcggagcg cctctcagca aggaggtagg tgaggccgtg gccaaacgct 2400
tccacctacc aggcatccgc cagggctacg gcctgacaga aacaaccagc gccattctga 2460
tcacccccga aggggacgac aagcctggcg cagtaggcaa ggtggtgccc ttcttcgagg 2520
ctaaggtggt ggacttggac acaggtaaga ccctgggtgt gaaccagcgc ggcgagctgt 2580
gcgtccgtgg ccccatgatc atgagcggct acgtgaacaa ccccgaggct acaaacgctc 2640
tcatcgacaa ggacggctgg ctgcacagcg gcgacatcgc ctactgggac gaggacgagc 2700
acttcttcat cgtggaccgg ctcaagagcc tgatcaaata caagggctac caggtagccc 2760
cagccgaact ggagagcatc ctgctgcaac accccaacat cttcgacgcc ggggtcgctg 2820
gcctgcccga cgacgatgct ggcgagctgc ccgccgcagt cgtcgtgctg gaacacggta 2880
aaaccatgac cgagaaggag atcgtggact atgtggccag ccaggttaca accgccaaga 2940
agctgcgcgg tggtgttgtg ttcgtggacg aggtgcctaa aggactgacc ggcaagttgg 3000
acgcccgcaa gatccgcgag attctcatta aggccaagaa gggcggcaag atcgccgtgt 3060
aaatcgattg cgcaaagctt tcgcgatagg cgagaccaat gggtgtgtac gtagcggccg 3120
cgtcgacgat agcttgatgg gtggcatccc tgtgacccct ccccagtgcc tctcctggcc 3180
ctggaagttg ccactccagt gcccaccagc cttgtcctaa taaaattaag ttgcatcatt 3240
ttgtctgact aggtgtcctt ctataatatt atggggtgga ggggggtggt atggagcaag 3300
gggcaagttg ggaagacaac ctgtagggcc tgcggggtct attgggaacc aagctggagt 3360
gcagtggcac aatcttggct cactgcaatc tccgcctcct gggttcaagc gattctcctg 3420
cctcagcctc ccgagttgtt gggattccag gcatgcatga ccaggctcag ctaatttttg 3480
tttttttggt agagacgggg tttcaccata ttggccaggc tggtctccaa ctcctaatct 3540
caggtgatct acccaccttg gcctcccaaa ttgctgggat tacaggcgtg aaccactgct 3600
cccttccctg tccttctgat tttaaaataa ctataccagc aggaggacgt ccagacacag 3660
cataggctac ctggccatgc ccaaccggtg ggacatttga gttgcttgct tggcactgtc 3720
ctctcatgcg ttgggtccac tcagtagatg cctgttgaat tctgatttaa atcggtccgc 3780
gtacggcgtg gtaggtccga acgaatccat ggattaccct gttatcccta tccggagtta 3840
acctcgagga cttcggaact tctagaacca gaccgttcag tttaaacgct cttctccccc 3900
tcgagccata tggtctcagt cacaactact catctctgcc tctgtagcac gaaagcaatt 3960
agcaacaata tgtcaacaaa catatgtgac cccatgaaaa ctttatttat tatggatacg 4020
gaaacctgaa aataatgtct ttcttttgat tttttcccca atcattaaaa aacgtaaaaa 4080
ctactcttag gtcgcaaggt taagccattc tcagcttggc agtggcaggc tggatttggc 4140
ttgtgaccta cagttggcca atccctgatt cccaaaatgt attcctcagg gatgtgggca 4200
aatacttatg ggaagtgctg gattaaacag agttaagaag catcagacat ttccaggacg 4260
ggctagcaca tgccagggct ctctaactga cctcattgga ttcatctgtt tcatggagga 4320
tcttgcaaga caagaattcc tcaaacctag agtctgagga ctgtgctttg ggaaacactg 4380
ctctgcttga tgccctcact gggcacatgg tagaatctgg agctgagtgc cttgctagct 4440
ggagataggg tcagagctct tgactgccct ggcagtcttg acacatcacg ctgtctgtgt 4500
cccctgagtg gttcagagct acacaggcca agactagccc accagagcac caggcctccc 4560
agctttctgg gcttgtccat gcgtacattt ccttattctt cctggtttcc agaacctaag 4620
gagaggcaca ttttggttga gtgattataa ccctagggac catgggtagc tgcatgtcag 4680
gaaacactcc tcaacttcct ggccctgatg gattaaagga gaggtactta caggttattt 4740
cttcgctgtg gactactgtc ccagcatgaa tagggcatca ttattgaatt attttgacag 4800
gaaggagact ggtgtatgct gcacagtaat aatgtattta catgtgtaca gagtttacca 4860
agcacctctg tgttgttttt gcctttgttt attacacttg ggacaaattt ttaaaattta 4920
tacatgcaga gactgcagcg cagagaagct aagagacttg cccctgccca cacagccagt 4980
ggtagagcct gaactcaaac ccaggtctca tctcacctca ggggctgctt tccccatcgc 5040
tgtattgtcc ttaaagtgat gggtgactag gcaatgaagt aattctctag gaaagcatga 5100
ccaatttccc tttctccacc tccctctttt tcctccaccc ctcccccatc agcccccata 5160
tatatgccca aatctccaca aagccttgct tgcctgcaaa cctttacttc tgaaatgact 5220
tccacgcatg cggggggggg ggggggcaat tggccaccat gggccccaag aagaaaagga 5280
aggtggcccc ccccaccgac gtgagcctgg gcgacgagct gcacctggac ggcgaggacg 5340
tggccatggc ccacgccgac gccctggacg acttcgacct ggacatgctg ggcgacggcg 5400
acagccccgg ccccggcttc accccccacg acagcgcccc ctacggcgcc ctggacatgg 5460
ccgacttcga gttcgagcag atgttcaccg acgccctggg catcgacgag tacggcggcc 5520
atatggagat gcccgtggac aggattctgg aggccgaact cgccgtggag cagaaaagcg 5580
accagggcgt ggagggcccc ggcggaaccg gcggcagcgg cagcagcccc aacgaccccg 5640
tgaccaacat ctgccaggcc gccgacaagc agctgttcac cctggtggag tgggccaaga 5700
ggattcccca cttcagcagc ctgcccctgg acgaccaggt gatcctgctg agggccggat 5760
ggaacgagct gctgatcgcc agcttcagcc acaggagcat cgacgtgagg gacggcatcc 5820
tgctggccac cggcctgcac gtccatagga acagcgccca cagcgccgga gtgggcgcca 5880
tcttcgacag ggtgctgacc gagctggtga gcaagatgag ggacatgagg atggacaaga 5940
ccgagctggg ctgcctgagg gccatcatcc tgttcaaccc cgaggtgagg ggcctgaaaa 6000
gcgcccagga ggtggagctg ctgagggaga aggtgtacgc cgccctggag gagtacacca 6060
ggaccaccca ccccgacgag cccggcagat tcgccaagct gctgctgagg ctgcccagcc 6120
tgaggagcat cggcctgaag tgcctggagc acctgttctt cttcaggctg atcggcgacg 6180
tgcccatcga caccttcctg atggagatgc tggagagccc cagcgacagc tgagccggca 6240
actcgctgta gtaattccag cgagaggcag agggagcgag cgggcggcgg gctagggtgg 6300
aggagcccgg cgagcagagc tgcgctgcgg gcgtcctggg aagggagatc cggagcgaat 6360
agggggcttc gcctctggcc cagccctccc gctgatcccc cagccagcgg tgcgcaaccc 6420
tagccgcatc cacgaaactt tgcccatagc agcgggcggg cactttgcac tggaacttac 6480
aacacccgag caaggacgcg actctcccga cgcggggagg ctattctgcc catttgggga 6540
cacttccccg ccgctgccag gacccgcttc tctgaaaggc tctccttgca gctgcttaga 6600
cgctggattt ttttcgggta gtggaaaacc agcagcctcc cgcgaccaga tctgccacca 6660
tgaagctgct gagcagcatc gagcaggctt gcgacatctg caggctgaag aagctgaagt 6720
gcagcaagga gaagcccaag tgcgccaagt gcctgaagaa caactgggag tgcagataca 6780
gccccaagac caagaggagc cccctgacca gggcccacct gaccgaggtg gagagcaggc 6840
tggagaggct ggagcagctg ttcctgctga tcttccccag ggaggacctg gacatgatcc 6900
tgaagatgga cagcctgcaa gacatcaagg ccctgctgac cggcctgttc gtgcaggaca 6960
acgtgaacaa ggacgccgtg accgacaggc tggccagcgt ggagaccgac atgcccctga 7020
ccctgaggca gcacaggatc agcgccacca gcagcagcga ggagagcagc aacaagggcc 7080
agaggcagct gaccgtgagc cccgagtttc ccgggatcag gcccgagtgc gtggtgcccg 7140
agacccagtg cgccatgaaa aggaaggaga agaaggccca gaaggagaag gacaagctgc 7200
ccgtgagcac caccaccgtc gatgaccaca tgccccccat catgcagtgc gagccccccc 7260
cccccgaggc cgccaggatt cacgaggtcg tgcccaggtt cctgagcgac aagctgctgg 7320
tgaccaacag gcagaagaac atcccccagc tgaccgccaa ccagcagttc ctgatcgcca 7380
ggctgatctg gtatcaggac ggctacgagc agcccagcga cgaggacctg aaaaggatca 7440
cccagacctg gcagcaggcc gacgacgaga acgaggagag cgacaccccc ttcaggcaga 7500
tcaccgagat gaccatcctg accgtgcagc tgatcgtgga gttcgccaag ggcctgcccg 7560
gattcgccaa gatcagccag cccgaccaga tcaccctgct gaaggcttgc agcagcgagg 7620
tgatgatgct gagggtggcc aggaggtacg acgccgccag cgacagcatc ctgttcgcca 7680
acaaccaggc ttacaccagg gacaactaca ggaaggctgg catggccgag gtgatcgagg 7740
acctcctgca cttctgcaga tgtatgtaca gcatggccct ggacaacatc cactacgccc 7800
tgctgaccgc cgtggtgatc ttcagcgaca ggcccggcct ggagcagccc cagctggtgg 7860
aggagatcca gaggtactac ctgaacaccc tgaggatcta catcctgaac cagctgagcg 7920
gcagcgccag gagcagcgtg atctacggca agatcctgag catcctgagc gagctgagga 7980
ccctgggaat gcagaacagc aatatgtgta tcagcctgaa gctgaagaac aggaagctgc 8040
cccccttcct ggaggagatt tgggacgtgg ccgacatgag ccacacccag ccccccccca 8100
tcctggagag ccccaccaac ctgtgaatcg attagacatg ataagataca ttgatgagtt 8160
tggacaaacc acaactagaa tgcagtgaaa aaaatgctta atttgtgaaa tttgtgatgc 8220
tattgcttaa tttgtaacca ttataagctg caataaacaa gttaataaaa catttgcatt 8280
cattttatgt ttcaggttca gggggagatg tgggaggttt tttaaagcaa gtaaaacctc 8340
tacaaatgtg gtatctagag ctcttccaaa tagatctgga aggtgctgag gtacgatgag 8400
acccgcacca ggtgcagacc ctgcgagtgt ggcggtaaac atattaggaa ccagcctgtg 8460
atgctggatg tgaccgagga gctgaggccc gatcacttgg tgctggcctg cacccgcgct 8520
gagtttggct ctagcgatga agatacagat tgaggtactg aaatgtgtgg gcgtggctta 8580
agggtgggaa agaatatata aggtgggggt cttatgtagt tttgtatctg ttttgcagca 8640
gccgccgccg ccatgagcac caactcgttt gatggaagca ttgtgagctc atatttgaca 8700
acgcgcatgc ccccatgggc cggggtgcgt cagaatgtga tgggctccag cattgatggt 8760
cgccccgtcc tgcccgcaaa ctctactacc ttgacctacg agaccgtgtc tggaacgccg 8820
ttggagactg cagcctccgc cgccgcttca gccgctgcag ccaccgcccg cgggattgtg 8880
actgactttg ctttcctgag cccgcttgca agcagtgcag cttcccgttc atccgcccgc 8940
gatgacaagt tgacggctct tttggcacaa ttggattctt tgacccggga acttaatgtc 9000
gtttctcagc agctgttgga tctgcgccag caggtttctg ccctgaaggc ttcctcccct 9060
cccaatgcgg tttaaaacat aaataaaaaa ccagactctg tttggatttg gatcaagcaa 9120
gtgtcttgct gtctttattt aggggttttg cgcgcgcggt aggcccggga ccagcggtct 9180
cggtcgttga gggtcctgtg tattttttcc aggacgtggt aaaggtgact ctggatgttc 9240
agatacatgg gcataagccc gtctctgggg tggaggtagc accactgcag agcttcatgc 9300
tgcggggtgg tgttgtagat gatccagtcg tagcaggagc gctgggcgtg gtgcctaaaa 9360
atgtctttca gtagcaagct gattgccagg ggcaggccct tggtgtaagt gtttacaaag 9420
cggttaagct gggatgggtg catacgtggg gatatgagat gcatcttgga ctgtattttt 9480
aggttggcta tgttcccagc catatccctc cggggattca tgttgtgcag aaccaccagc 9540
acagtgtatc cggtgcactt gggaaatttg tcatgtagct tagaaggaaa tgcgtggaag 9600
aacttggaga cgcccttgtg acctccaaga ttttccatgc attcgtccat aatgatggca 9660
atgggcccac gggcggcggc ctgggcgaag atatttctgg gatcactaac gtcatagttg 9720
tgttccagga tgagatcgtc ataggccatt tttacaaagc gcgggcggag ggtgccagac 9780
tgcggtataa tggttccatc cggcccaggg gcgtagttac cctcacagat ttgcatttcc 9840
cacgctttga gttcagatgg ggggatcatg tctacctgcg gggcgatgaa gaaaacggtt 9900
tccggggtag gggagatcag ctgggaagaa agcaggttcc tgagcagctg cgacttaccg 9960
cagccggtgg gcccgtaaat cacacctatt accgggtgca actggtagtt aagagagctg 10020
cagctgccgt catccctgag caggggggcc acttcgttaa gcatgtccct gactcgcatg 10080
ttttccctga ccaaatccgc cagaaggcgc tcgccgccca gcgatagcag ttcttgcaag 10140
gaagcaaagt ttttcaacgg tttgagaccg tccgccgtag gcatgctttt gagcgtttga 10200
ccaagcagtt ccaggcggtc ccacagctcg gtcacctgct ctacggcatc tcgatccagc 10260
atatctcctc gtttcgcggg ttggggcggc tttcgctgta cggcagtagt cggtgctcgt 10320
ccagacgggc cagggtcatg tctttccacg ggcgcagggt cctcgtcagc gtagtctggg 10380
tcacggtgaa ggggtgcgct ccgggctgcg cgctggccag ggtgcgcttg aggctggtcc 10440
tgctggtgct gaagcgctgc cggtcttcgc cctgcgcgtc ggccaggtag catttgacca 10500
tggtgtcata gtccagcccc tccgcggcgt ggcccttggc gcgcagcttg cccttggagg 10560
aggcgccgca cgaggggcag tgcagacttt tgagggcgta gagcttgggc gcgagaaata 10620
ccgattccgg ggagtaggca tccgcgccgc aggccccgca gacggtctcg cattccacga 10680
gccaggtgag ctctggccgt tcggggtcaa aaaccaggtt tcccccatgc tttttgatgc 10740
gtttcttacc tctggtttcc atgagccggt gtccacgctc ggtgacgaaa aggctgtccg 10800
tgtccccgta tacagacttg agaggcctgt cctcgaccga tgcccttgag agccttcaac 10860
ccagtcagct ccttccggtg ggcgcggggc atgactatcg tcgccgcact tatgactgtc 10920
ttctttatca tgcaactcgt aggacaggtg ccggcagcgc tctgggtcat tttcggcgag 10980
gaccgctttc gctggagcgc gacgatgatc ggcctgtcgc ttgcggtatt cggaatcttg 11040
cacgccctcg ctcaagcctt cgtcactggt cccgccacca aacgtttcgg cgagaagcag 11100
gccattatcg ccggcatggc ggccgacgcg ctgggctacg tcttgctggc gttcgcgacg 11160
cgaggctgga tggccttccc cattatgatt cttctcgctt ccggcggcat cgggatgccc 11220
gcgttgcagg ccatgctgtc caggcaggta gatgacgacc atcagggaca gcttcaaggc 11280
cagcaaaagg ccaggaaccg taaaaaggcc gcgttgctgg cgtttttcca taggctccgc 11340
ccccctgacg agcatcacaa aaatcgacgc tcaagtcaga ggtggcgaaa cccgacagga 11400
ctataaagat accaggcgtt tccccctgga agctccctcg tgcgctctcc tgttccgacc 11460
ctgccgctta ccggatacct gtccgccttt ctcccttcgg gaagcgtggc gctttctcat 11520
agctcacgct gtaggtatct cagttcggtg taggtcgttc gctccaagct gggctgtgtg 11580
cacgaacccc ccgttcagcc cgaccgctgc gccttatccg gtaactatcg tcttgagtcc 11640
aacccggtaa gacacgactt atcgccactg gcagcagcca ctggtaacag gattagcaga 11700
gcgaggtatg taggcggtgc tacagagttc ttgaagtggt ggcctaacta cggctacact 11760
agaaggacag tatttggtat ctgcgctctg ctgaagccag ttaccttcgg aaaaagagtt 11820
ggtagctctt gatccggcaa acaaaccacc gctggtagcg gtggtttttt tgtttgcaag 11880
cagcagatta cgcgcagaaa aaaaggatct caagaagatc ctttgatctt ttctacgggg 11940
tctgacgctc agtggaacga aaactcacgt taagggattt tggtcatgag attatcaaaa 12000
aggatcttca cctagatcct tttaaattaa aaatgaagtt ttaaatcaat ctaaagtata 12060
tatgagtaaa cttggtctga cagttaccaa tgcttaatca gtgaggcacc tatctcagcg 12120
atctgtctat ttcgttcatc catagttgcc tgactccccg tcgtgtagat aactacgata 12180
cgggagggct taccatctgg ccccagtgct gcaatgatac cgcgagaccc acgctcaccg 12240
gctccagatt tatcagcaat aaaccagcca gccggaaggg ccgagcgcag aagtggtcct 12300
gcaactttat ccgcctccat ccagtctatt aattgttgcc gggaagctag agtaagtagt 12360
tcgccagtta atagtttgcg caacgttgtt gccattgctg caggcatcgt ggtgtcacgc 12420
tcgtcgtttg gtatggcttc attcagctcc ggttcccaac gatcaaggcg agttacatga 12480
tcccccatgt tgtgcaaaaa agcggttagc tccttcggtc ctccgatcgt tgtcagaagt 12540
aagttggccg cagtgttatc actcatggtt atggcagcac tgcataattc tcttactgtc 12600
atgccatccg taagatgctt ttctgtgact ggtgagtact caaccaagtc attctgagaa 12660
tagtgtatgc ggcgaccgag ttgctcttgc ccggcgtcaa cacgggataa taccgcgcca 12720
catagcagaa ctttaaaagt gctcatcatt ggaaaacgtt cttcggggcg aaaactctca 12780
aggatcttac cgctgttgag atccagttcg atgtaaccca ctcgtgcacc caactgatct 12840
tcagcatctt ttactttcac cagcgtttct gggtgagcaa aaacaggaag gcaaaatgcc 12900
gcaaaaaagg gaataagggc gacacggaaa tgttgaatac tcatactctt cctttttcaa 12960
tattattgaa gcatttatca gggttattgt ctcatgagcg gatacatatt tgaatgtatt 13020
tagaaaaa 13028
<210> 6
<211> 12454
<212> DNA
<213> Artificial Sequence
<220>
<223> Synthetic promoter
<400> 6
taaacaaata ggggttccgc gcacatttcc ccgaaaagtg ccacctgacg tactgaggac 60
gccagggttt tcccagtcac gacgttgtaa aacgacggcc agtagcagac aagcccgtca 120
gggcgcgtca gcgggtgttg gccctaggac gaaaggaggt cgtgaaatgg ataaaaaaat 180
acagcgtttt tcatgtacaa ctatactagt tgtagtgcct aaataatgct tttaaaactt 240
aaaaataatc aatgtcctca gcggggtgtc ggggatttag gtgacactat aggctgagcg 300
ccgcacaggc atctagaggc tatggcaggg cctgccgccc cgacgttggc tgcgagccct 360
gggccttcac ccgaacttgg ggggtggggt ggggaaaagg aagaaacgcg ggcgtattgg 420
ccccaatggg gtctcggtgg ggtatcgaca gagtgccagc cctgggaccg aaccccgcgt 480
ttatgaacaa acgacccaac accgtgcgtt ttattctgtc tttttattgc cgtcatagcg 540
cgggttcctt ccggtattgt ctccttccgt gtttcaatcg attcaaaaga actcgtccag 600
cagacggtaa aaagcaatgc gttgagaatc cggtgcagca atgccataca gcaccagaaa 660
gcgatcagcc cattcaccgc ccagttcttc agcaatgtca cgggttgcca gtgcgatgtc 720
ctgatagcga tcagccacgc ccaggcgacc gcagtcgata aagccggaga aacggccgtt 780
ttccaccata atgtttggca gacaagcatc gccgtgggtc acaaccaggt cctcgccatc 840
tggcatacgt gctttcaggc gtgcgaacag ttctgccggt gccagaccct gatgttcctc 900
gtccaggtca tcctgatcaa ccaggccagc ttccatgcga gtgcgtgcgc gctcgatacg 960
gtgtttagct tggtgatcga atgggcaagt agctgggtcc agggtatgca gacggcgcat 1020
agcatcagcc atgatggaaa ccttttctgc cggtgccaga tgagaggaca gcagatcctg 1080
gcctggaacc tcgcccagca gcagccagtc gcggccagcc tcggtcacaa catccagcac 1140
agctgcgcat ggaacgccgg tagtagccag ccaggacaga cgagctgctt catcttgcag 1200
ttcgttcagt gcgccggaca gatcggtctt aacaaacagc accggacggc cttgagcgga 1260
cagacggaac acagctgcgt cggagcaacc gatagtctgt tgagcccagt catagccaaa 1320
cagacgttcc acccaagcag ccggagaacc agcgtgcaga ccgtcttgtt caatcatggt 1380
ggcaattggg tgtctgagcg atgtggctcg gctggcgacg caaaagaaga tgcggctgac 1440
tgtcgaacag gaggagcaga gagcgaagcg ggaggctgcg ggctcaattt gcatgcttta 1500
gttcctcacc ttgtcgtatt atactatgcc gatatactat gccgatgatt aattgtcaac 1560
gtatacggaa tagctctgag gccgaggcag cttcggcctc tgcataaata aaaaaaatta 1620
gtcagccatg gggcggagaa tgggcggaac tgggcggagt taggggcggg atgggcggag 1680
ttaggggcgg gactatggtt gctgactaat tgagatgctt gctttgcata cttctgcctg 1740
ctggggagcc tggggacttt ccacacctgg ttgctgacta attgagatgc ttgctttgca 1800
tacttctgcc tgctggggag cctggggact ttccacaccc taacctcgag gccatcgtgg 1860
cacgccaggg ttttcccagt cacgacgttg taaaacgacg gccagtgctc ttctcccccg 1920
cgggaggttt tataaatccg actgtctaga ttgttgttaa atcacacaaa aaaccaacac 1980
acagatgtaa tgaaaataaa gatattttat tatcgattca gctgtcgctg gggctctcca 2040
gcatctccat caggaaggtg tcgatgggca cgtcgccgat cagcctgaag aagaacaggt 2100
gctccaggca cttcaggccg atgctcctca ggctgggcag cctcagcagc agcttggcga 2160
atctgccggg ctcgtcgggg tgggtggtcc tggtgtactc ctccagggcg gcgtacacct 2220
tctccctcag cagctccacc tcctgggcgc ttttcaggcc cctcacctcg gggttgaaca 2280
ggatgatggc cctcaggcag cccagctcgg tcttgtccat cctcatgtcc ctcatcttgc 2340
tcaccagctc ggtcagcacc ctgtcgaaga tggcgcccac tccggcgctg tgggcgctgt 2400
tcctatggac gtgcaggccg gtggccagca ggatgccgtc cctcacgtcg atgctcctgt 2460
ggctgaagct ggcgatcagc agctcgttcc atccggccct cagcaggatc acctggtcgt 2520
ccaggggcag gctgctgaag tggggaatcc tcttggccca ctccaccagg gtgaacagct 2580
gcttgtcggc ggcctggcag atgttggtca cggggtcgtt ggggctgctg ccgctgccgc 2640
cggttccgcc ggggccctcc acgccctggt cgcttttctg ctccacggcg agttcggcct 2700
ccagaatcct gtccacgggc atctccatat ggccgccgta ctcgtcgatg cccagggcgt 2760
cggtgaacat ctgctcgaac tcgaagtcgg ccatgtccag ggcgccgtag ggggcgctgt 2820
cgtggggggt gaagccgggg ccggggctgt cgccgtcgcc cagcatgtcc aggtcgaagt 2880
cgtccagggc gtcggcgtgg gccatggcca cgtcctcgcc gtccaggtgc agctcgtcgc 2940
ccaggctcac gtcggtgggg ggggccacct tccttttctt cttggggccc atcaattggc 3000
cacccccccc cccccccccg catgctgtgc cacctgtctt cattcttaac ctgaagattt 3060
agtcttttag ggtttctttt gcacttgggg tacttaacat gccactatgc atattgtaga 3120
tttatagata cttttcaact gatactgctc ccacaggcaa acatgcctgg tgaaacactt 3180
gtttcttttt ggcaaacaag aaatgtttgc ataaaagact cgtgtctgga aaaatgtctt 3240
gagaaattga tatgctactc taagccccaa atctcctttt cacttacctt ccccctgctg 3300
caggatgaca atccatgggc ctgtgctttc tgatagtgaa agagaagaaa actcataaat 3360
atagtgtcta ccatgagtca ggcactaact atgcatttat ctctttctgc tttaccctat 3420
aaatggttat taccattaaa agtcatgtga ggaaacagaa ttagggagtt caaactgagc 3480
caggatttca gttcaagttt tccagatcct cgagtaggcg agaccaatgg gtgcgccatg 3540
ggctcttcca aaaatttagg tgacactata gggcaccgct cgcacctgcg cacaggcccg 3600
cggctacaaa ctacgaacga tcattctaga taccacattt gtagaggttt tacttgcttt 3660
aaaaaacctc ccacatctcc ccctgaacct gaaacataaa atgaatgcaa atgttttatt 3720
aacttgttta ttgcagctta taatggttac aaattaagca atagcatcac aaatttcaca 3780
aattaagcat ttttttcact gcattctagt tgtggtttgt ccaaactcat caatgtatct 3840
tatcatgtct aatcgattca caggttggtg gggctctcca ggatgggggg gggctgggtg 3900
tggctcatgt cggccacgtc ccaaatctcc tccaggaagg ggggcagctt cctgttcttc 3960
agcttcaggc tgatacacat attgctgttc tgcattccca gggtcctcag ctcgctcagg 4020
atgctcagga tcttgccgta gatcacgctg ctcctggcgc tgccgctcag ctggttcagg 4080
atgtagatcc tcagggtgtt caggtagtac ctctggatct cctccaccag ctggggctgc 4140
tccaggccgg gcctgtcgct gaagatcacc acggcggtca gcagggcgta gtggatgttg 4200
tccagggcca tgctgtacat acatctgcag aagtgcagga ggtcctcgat cacctcggcc 4260
atgccagcct tcctgtagtt gtccctggtg taagcctggt tgttggcgaa caggatgctg 4320
tcgctggcgg cgtcgtacct cctggccacc ctcagcatca tcacctcgct gctgcaagcc 4380
ttcagcaggg tgatctggtc gggctggctg atcttggcga atccgggcag gcccttggcg 4440
aactccacga tcagctgcac ggtcaggatg gtcatctcgg tgatctgcct gaagggggtg 4500
tcgctctcct cgttctcgtc gtcggcctgc tgccaggtct gggtgatcct tttcaggtcc 4560
tcgtcgctgg gctgctcgta gccgtcctga taccagatca gcctggcgat caggaactgc 4620
tggttggcgg tcagctgggg gatgttcttc tgcctgttgg tcaccagcag cttgtcgctc 4680
aggaacctgg gcacgacctc gtgaatcctg gcggcctcgg gggggggggg ctcgcactgc 4740
atgatggggg gcatgtggtc atcgacggtg gtggtgctca cgggcagctt gtccttctcc 4800
ttctgggcct tcttctcctt ccttttcatg gcgcactggg tctcgggcac cacgcactcg 4860
ggcctcccga gtttcccggg atcgctcacg gtcagctgcc tctggccctt gttgctgctc 4920
tcctcgctgc tgctggtggc gctgatcctg tgctgcctca gggtcagggg catgtcggtc 4980
tccacgctgg ccagcctgtc ggtcacggcg tccttgttca cgttgtcctg cacgaacagg 5040
ccggtcagca gggccttgat gtcttgcagg ctgtccatct tcaggatcat gtccaggtcc 5100
tccctgggga agatcagcag gaacagctgc tccagcctct ccagcctgct ctccacctcg 5160
gtcaggtggg ccctggtcag ggggctcctc ttggtcttgg ggctgtatct gcactcccag 5220
ttgttcttca ggcacttggc gcacttgggc ttctccttgc tgcacttcag cttcttcagc 5280
ctgcagatgt cgcaagcctg ctcgatgctg ctcagcagct tcatggtggc caattgcccc 5340
cccccccccc cgcatgctgc ttccagaccc gcccagagca aaccggatcc tccactttcc 5400
agcctagcct ggggcggggc gaggtctggg gggcggggag tcttggagac tccaaagcgg 5460
gaggcgggga gagggcgggt cccaggccgc gataagggga cagagggaca gcgacctggg 5520
gggtgcagag gtccgggcct gggggagaga gacacacagg ggagactcca agggcaagcg 5580
cgagatggga acagaaggag ttgggggcca gtggcggaga gggaacagac tcagaaagga 5640
ggatgccaga cagggagggg acaatttaac ccaaagaggg ggagacaaag acttagggga 5700
cagagaatca gaaggtgggg cagcagggac ccagggatag acagagagag agggggacag 5760
agacccacag agagaggggg acagagaccc agggagaggg gacagagacc cagagagagt 5820
gggacagaga cccagagaga gtgggacaga gacccacaga gagaggggga cagagaccca 5880
gggagaggag gacagagacc cagagagggg gggacagaga cccagagagg gggggacaga 5940
gacccaggga gggggggaca gagacccagg gagaggggac agagacccac ggagaggggg 6000
acagagaccc agggagaggg gacagagacc cagagagagg gggacagaga cccagagaga 6060
gggggacaga gacccagaga gacagggaca gagacccaga gagaggggga cagagaccca 6120
gagagagggg aacagagacc cagagagaga ggaggacaga gacccagaga gagggggaca 6180
gagacccaga gagacaggga cagagaccca gagagagggg gacagagacc cagagagagg 6240
ggaacagaga cccagagaga gaggaggaca gagacccaga gagaggggga cagagaccca 6300
gagagggggg gacagagacc cagggatggg gggacagaga cccagggaga ggggacagag 6360
acccacggag aggggtacag agacccaggg agaggggaca gagacccaga gagaggggga 6420
cagagactct gagacagagg gggacagaga ccctgagaga gggggacaga gacccagaga 6480
gaggggaaca gagacccaga gagagagggg gacagagacc cacagagaga ggggaacaga 6540
gacccagaga gagggggaca gagatccaca gagagagggg gacagagacc cacagagaga 6600
ggggaacaga gacccagaga gagggggaca gagatccaca gagagagggg gacagagacc 6660
cagggagagg gggacagaga cccagagaga gggggacaga gacccaggga gaggtggaca 6720
gagactctga gacagagggg gacagagact ctgagagaga gtggggacag agacccagag 6780
aggtggatgc cagagatggg gaggagacac cttgactgag gcaaggggca gagggggatg 6840
caaaaaccaa agaattgggg gaagggcagg aactcagaaa ggaggggcca gagatttagg 6900
ggagagagag ggacacagac ttgggggagg actgacacta agataagagt gggacagaag 6960
cccagagtga gagggagagg caatcccatg gaggagggac agggaccctg agagagcaga 7020
tgacagaatt gaagagagag gaggacccgt gaacaggaaa ggagacccta gtgggggcag 7080
tcatgaaggg tgaggagtag gaaatactga cacacagaga caggcaaggc cacttgtctc 7140
ctgccagccc tctgtgatgg ctcgagtggt aatacaatgg ccggttccca tggacctgca 7200
tcgtggtgta actataacgg tcctaaggta gcgaccgcgg agactaggtg tatttatcta 7260
agcgatcgct taattaaggc cggccgccgc aataaaatat ctttattttc attacatctg 7320
tgtgttggtt ttttgtgtga atccatagta ctaacatacg ctctccatca aaacaaaacg 7380
aaacaaaaca aactagcaaa ataggctgtc cccagtgcaa gtccaggtgc cagaacattt 7440
ctctatccat aatgcagggg taccgggtga tgacggtgaa aacctccaat tgcggagtac 7500
tgtcctccga gcggagtact gtcctccgag cggagtactg tcctccgagc ggagtactgt 7560
cctccgagcg gagtactgtc ctccgagcgg agtactgtcc tccgagcgga gagtccccgg 7620
ggacctagag ggtatataat gggtgcctta gctggtgtgt gacctcatct tcctgtacgc 7680
ccctgcaggg gcgcgccacg cgtcgaagaa ggtgagtaat cttaacatgc tctttttttt 7740
tttttttgct aatccctttt gtgtgctgat gttaggatga catttacaac aaatgtttgt 7800
tcctgacagg aaaaaccttg ctgggtacct tcgttgccgg acacttcttg tcctctactt 7860
tggaaaaaag gaattgagag ccgctagcgc caccatggaa gatgccaaaa acattaagaa 7920
gggcccagcg ccattctacc cactcgaaga cgggaccgct ggcgagcagc tgcacaaagc 7980
catgaagcgc tacgccctgg tgcccggcac catcgccttt accgacgcac atatcgaggt 8040
ggacattacc tacgccgagt acttcgagat gagcgttcgg ctggcagaag ctatgaagcg 8100
ctatgggctg aatacaaacc atcggatcgt ggtgtgcagc gagaatagct tgcagttctt 8160
catgcccgtg ttgggtgccc tgttcatcgg tgtggctgtg gccccagcta acgacatcta 8220
caacgagcgc gagctgctga acagcatggg catcagccag cccaccgtcg tattcgtgag 8280
caagaaaggg ctgcaaaaga tcctcaacgt gcaaaagaag ctaccgatca tacaaaagat 8340
catcatcatg gatagcaaga ccgactacca gggcttccaa agcatgtaca ccttcgtgac 8400
ttcccatttg ccacccggct tcaacgagta cgacttcgtg cccgagagct tcgaccggga 8460
caaaaccatc gccctgatca tgaacagtag tggcagtacc ggattgccca agggcgtagc 8520
cctaccgcac cgcaccgctt gtgtccgatt cagtcatgcc cgcgacccca tcttcggcaa 8580
ccagatcatc cccgacaccg ctattctcag cgtggtgcca tttcaccacg gcttcggcat 8640
gttcaccacg ctgggctact tgatctgcgg ctttcgggtc gtgctcatgt accgcttcga 8700
ggaggagcta ttcttgcgca gcttgcaaga ctataagatt caatctgccc tgctggtgcc 8760
cacactattt agcttcttcg ctaagagcac tctcatcgac aagtacgacc taagcaactt 8820
gcacgagatc gccagcggcg gagcgcctct cagcaaggag gtaggtgagg ccgtggccaa 8880
acgcttccac ctaccaggca tccgccaggg ctacggcctg acagaaacaa ccagcgccat 8940
tctgatcacc cccgaagggg acgacaagcc tggcgcagta ggcaaggtgg tgcccttctt 9000
cgaggctaag gtggtggact tggacacagg taagaccctg ggtgtgaacc agcgcggcga 9060
gctgtgcgtc cgtggcccca tgatcatgag cggctacgtg aacaaccccg aggctacaaa 9120
cgctctcatc gacaaggacg gctggctgca cagcggcgac atcgcctact gggacgagga 9180
cgagcacttc ttcatcgtgg accggctcaa gagcctgatc aaatacaagg gctaccaggt 9240
agccccagcc gaactggaga gcatcctgct gcaacacccc aacatcttcg acgccggggt 9300
cgctggcctg cccgacgacg atgctggcga gctgcccgcc gcagtcgtcg tgctggaaca 9360
cggtaaaacc atgaccgaga aggagatcgt ggactatgtg gccagccagg ttacaaccgc 9420
caagaagctg cgcggtggtg ttgtgttcgt ggacgaggtg cctaaaggac tgaccggcaa 9480
gttggacgcc cgcaagatcc gcgagattct cattaaggcc aagaagggcg gcaagatcgc 9540
cgtgttaatc gattgcgcaa agctttcgcg ataggcgaga ccaatgggtg tgtacgtagc 9600
ggccgcgtcg acgatagctt gatgggtggc atccctgtga cccctcccca gtgcctctcc 9660
tggccctgga agttgccact ccagtgccca ccagccttgt cctaataaaa ttaagttgca 9720
tcattttgtc tgactaggtg tccttctata atattatggg gtggaggggg gtggtatgga 9780
gcaaggggca agttgggaag acaacctgta gggcctgcgg ggtctattgg gaaccaagct 9840
ggagtgcagt ggcacaatct tggctcactg caatctccgc ctcctgggtt caagcgattc 9900
tcctgcctca gcctcccgag ttgttgggat tccaggcatg catgaccagg ctcagctaat 9960
ttttgttttt ttggtagaga cggggtttca ccatattggc caggctggtc tccaactcct 10020
aatctcaggt gatctaccca ccttggcctc ccaaattgct gggattacag gcgtgaacca 10080
ctgctccctt ccctgtcctt ctgattttaa aataactata ccagcaggag gacgtccaga 10140
cacagcatag gctacctggc catgcccaac cggtgggaca tttgagttgc ttgcttggca 10200
ctgtcctctc atgcgttggg tccactcagt agatgcctgt tgaattctga tttaaatcgg 10260
tccgcgtacg gcgtggtagg tccgaacgaa tccatggatt accctgttat ccctactcaa 10320
ggacatcatc cctttagtga gggttaattc acgcagtggg tacggaacta aaggcagcac 10380
acatcgtgta atcatggtca tagctgtttc ctgtgtgaaa ttgttatccg ctacgtctct 10440
cccccgcagt aagggctaga ttaactcgtc tcgtgaatat ccggaactcc ctttagtgag 10500
ggttaattgc gttgcgctca ctgcccgctt tccagtcggg aaacctgtcg tgccagctta 10560
atcatggtca tagctgtttc ctgtgtgaaa ttgttatccg ctaccggaaa cgcttccttc 10620
atgtgagcaa aaggccagca aaaggccagg aaccgtaaaa aggccgcgtt gctggcgttt 10680
ttccataggc tccgcccccc tgacgagcat cacaaaaatc gacgctcaag tcagaggtgg 10740
cgaaacccga caggactata aagataccag gcgtttcccc ctggaagctc cctcgtgcgc 10800
tctcctgttc cgaccctgcc gcttaccgga tacctgtccg cctttctccc ttcgggaagc 10860
gtggcgcttt ctcatagctc acgctgtagg tatctcagtt cggtgtaggt cgttcgctcc 10920
aagctgggct gtgtgcacga accccccgtt cagcccgacc gctgcgcctt atccggtaac 10980
tatcgtcttg agtccaaccc ggtaagacac gacttatcgc cactggcagc agccactggt 11040
aacaggatta gcagagcgag gtatgtaggc ggtgctacag agttcttgaa gtggtggcct 11100
aactacggct acactagaag aacagtattt ggtatctgcg ctctgctgaa gccagttacc 11160
ttcggaaaaa gagttggtag ctcttgatcc ggcaaacaaa ccaccgctgg tagcggtggt 11220
ttttttgttt gcaagcagca gattacgcgc agaaaaaaag gatctcaaga agatcctttg 11280
atcttttcta cggggtctga cgctcagtgg aacgaaaact cacgttaagg gattttggtc 11340
atgatctatg tcgggtgcgg agaaagaggt aatgaaatgg catacgagta aacttggtct 11400
gacaccgctg catgagatta tcaaaaagga tcttcaccta gatcctttta aattaaaaat 11460
gaagttttaa atcaatctaa agtatatatg agtaaacttg gtctgacagt taccaatgct 11520
taatcagtga ggcacctatc tcagcgatct gtctatttcg ttcatccata gttgcctgac 11580
tccccgtcgt gtagataact acgatacggg agggcttacc atctggcccc agtgctgcaa 11640
tgataccgcg agacccacgc tcaccggctc cagatttatc agcaataaac cagccagccg 11700
gaagcgccga gcgcagaagt ggtcctgcaa ctttatccgc ctccatccag tctattaact 11760
gttgccggga agctagagta agtagttcgc cagttaatag tttgcggagc gttgttgcca 11820
ttgctacagg catcgtggtg tcacgctcgt cgtttggtat ggcttcattc agctccggtt 11880
cccaacgatc aaggcgagtt acatgatccc ccatgttgtg caaaaaagcg gttagctcct 11940
tcggtcctcc gatggttgtc agaagtaagt tggccgcagt gttatcactc atggttatgg 12000
cagcactgca taattctctt actgtcatgc catccgtaag atgcttttct gtgactggtg 12060
agtattcaac caagtcattc tgagaatagt gtatgcggcg accgagttgc tcttgcccgg 12120
cgtcaatacg ggataatacc gcgccacata gcagaacttt aaaagtgctc atcattggga 12180
agcgttcttc ggggcgaaaa ctctcaagga tcttaccgct gttgagatcc agttcgatgt 12240
aacccacacg agcacccaac tgatcttcag catcttttac tttcaccagc gtttctgggt 12300
gagcaaaaac aggaaggcaa aatgccgcaa aaaagggaat aagggcgaca cggaaatgtt 12360
gaatactcat acgcttcctt tttcaatagt attgaagcat ttatcagggt tattgtctcg 12420
ggagcgaata catatttgaa tgtatttaga aaaa 12454
<210> 7
<211> 12579
<212> DNA
<213> Artificial Sequence
<220>
<223> Synthetic promoter
<400> 7
taaacaaata ggggttccgc gcacatttcc ccgaaaagtg ccacctgacg tctaagaaac 60
cattattatc atgacattaa cctataaaaa taggcgtatc acgaggccct ttcgtcttca 120
agaaaattaa tcgcaccggt atctatgtcg ggtgcggaga aagaggtaat gaaatggcag 180
ctagcatcat caataatata ccttattttg gattgaagcc aatatgataa tgagggggtg 240
gagtttgtga cgtggcgcgg ggcgtgggaa cggggcgggt gacgtagtag tgtggcggaa 300
gtgtgatgtt gcaagtgtgg cggaacacat gtaagcgacg gatgtggcaa aagtgacgtt 360
tttggtgtgc gccggtgtac acaggaagtg acaattttcg cgcggtttta ggcggatgtt 420
gtagtaaatt tgggcgtaac cgagtaagat ttggccattt tcgcgggaaa actgaataag 480
aggaagtgaa atctgaataa ttttgtgtta ctcatagcgc gtaatagtgc gccggtgtac 540
acaggaagtg acaattttcg cgcggtttta ggcggatgtt gtagtaaatt tgggcgtaac 600
cgagtaagat ttggccattt tcgcgggaaa actgaataag aggaagtgaa atctgaataa 660
ttttgtgtta ctcattttgt ctagggagat ccggtaccga tatcctagac aacgatgctg 720
agctaactat aacggtccta aggtagcgac cgcggagact aggtgtattt atctaagcga 780
tcgcttaatt aaggccggcc gccgcaataa aatatcttta ttttcattac atctgtgtgt 840
tggttttttg tgtgaatcca tagtactaac atacgctctc catcaaaaca aaacgaaaca 900
aaacaaacta gcaaaatagg ctgtccccag tgcaagtcca ggtgccagaa catttctcta 960
tccataatgc aggggtaccg ggtgatgacg gtgaaaacct ccaattgcgg agtactgtcc 1020
tccgagcgga gtactgtcct ccgagcggag tactgtcctc cgagcggagt actgtcctcc 1080
gagcggagta ctgtcctccg agcggagtac tgtcctccga gcggagagtc cccggggacc 1140
tagagggtat ataatgggtg ccttagctgg tgtgtgacct catcttcctg tacgcccctg 1200
caggggcgcg ccacgcgtcg aagaaggtga gtaatcttaa catgctcttt tttttttttt 1260
ttgctaatcc cttttgtgtg ctgatgttag gatgacattt acaacaaatg tttgttcctg 1320
acaggaaaaa ccttgctggg taccttcgtt gccggacact tcttgtcctc tactttggaa 1380
aaaaggaatt gagagccgct agcgccacca tgattagccc tttcctcgtg ctcgccattg 1440
gcacatgcct caccaatagc ctcgtgcctg agaaagagaa agacggaggc ggaggctccg 1500
gcggaggcgg aagcggaggc ggaggctccg agtccctgaa actgaggaga agggtgcatg 1560
agacagacaa aaactgtaga tccggcacac cccctcagac cggcctggag aaacccacag 1620
gcacaggcca aagaaaacag ggagccggag cccctaccgc tcccggaccc ggaggctccc 1680
ccggaggcta aatcgattgc gcaaagcttt cgcgataggc gagaccaatg ggtgtgtacg 1740
tagcggccgc gtcgacgata gcttgatggg tggcatccct gtgacccctc cccagtgcct 1800
ctcctggccc tggaagttgc cactccagtg cccaccagcc ttgtcctaat aaaattaagt 1860
tgcatcattt tgtctgacta ggtgtccttc tataatatta tggggtggag gggggtggta 1920
tggagcaagg ggcaagttgg gaagacaacc tgtagggcct gcggggtcta ttgggaacca 1980
agctggagtg cagtggcaca atcttggctc actgcaatct ccgcctcctg ggttcaagcg 2040
attctcctgc ctcagcctcc cgagttgttg ggattccagg catgcatgac caggctcagc 2100
taatttttgt ttttttggta gagacggggt ttcaccatat tggccaggct ggtctccaac 2160
tcctaatctc aggtgatcta cccaccttgg cctcccaaat tgctgggatt acaggcgtga 2220
accactgctc ccttccctgt ccttctgatt ttaaaataac tataccagca ggaggacgtc 2280
cagacacagc ataggctacc tggccatgcc caaccggtgg gacatttgag ttgcttgctt 2340
ggcactgtcc tctcatgcgt tgggtccact cagtagatgc ctgttgaatt ctgatttaaa 2400
tcggtccgcg tacggcgtgg taggtccgaa cgaatccatg gattaccctg ttatccctat 2460
ccggagttaa cctcgaggac ttcggaactt ctagaaccag accgttcagt ttaaacgctc 2520
ttctccccct cgagtatgtc ctacttttat aaactttggt tgaactaaat aaaacagcaa 2580
catgtaccca acgtttttag actgttttat tcagtaccat aaacattcac taaactatac 2640
agagctaaaa tcatgcaaaa gattgcaaaa caaactgcct tgggaaattt ccagtctaag 2700
ctaaatggac caagtatagg attgaatttt aagaagttgg tgggaagatt ccagctcttg 2760
tactcacagg taaggtccta ggattctatt tgttgaagtg tctgcagacc ctctccctac 2820
agcaggggcg tggagcaaat gtgcattcag gaagtgctta ttagtccccc caaaaccttt 2880
ttcgtgacga cagacggatg gaggcctcag acgactccgg cagtaggacc ctgaaccaaa 2940
tgcctgagct gcgctcgaaa ggctcgtctt gcaggagctg gcgagtggca cgggcttcgg 3000
tggccgggct cggggctcgg ggctcggggc ccggagccgg ggggggcggg gggtccgtgc 3060
ccagggcgct ctgtggctcg attcatgtcc ccgccctccc acctgagcac actgggcaga 3120
gagcctgcgg catcgggcca gtcgcgcctc ctcgtccgcc ctgggcgggt cgctgggccc 3180
caggccgctt tctacagctc ctttaataaa atggacagca ggggtcctaa ccagacgtgg 3240
gcatcaagac aaaggaggcg gccagacgcg cttgagggcc tgctcgctag ctcccgcccc 3300
cccattccgc ggtcatccgg ggacagaggc caggccggac tgggtggagt tgggactcat 3360
acgtctgcgt ccaggaaggc gccgggcgag ccccagctag acgtgacggg cggggccgaa 3420
cacggcagcg gaccagaggc ccgcggcgca ccggcgtggg gcggggcaag cggagccttc 3480
cgggatgccg cgcggcagcc ggcttccggc tgtgggtggt gcgggggaca gcggcggccg 3540
gaagctgact gagccggcct ttggtaacgc cgcctgcact tctgggggcg tcgagcctgg 3600
cggtagaatc ttcccagtag gcggcgcggg agggaaaaga ggattgaggg catgcggggg 3660
gggggggggg caattggcca ccatgggccc caagaagaaa aggaaggtgg ccccccccac 3720
cgacgtgagc ctgggcgacg agctgcacct ggacggcgag gacgtggcca tggcccacgc 3780
cgacgccctg gacgacttcg acctggacat gctgggcgac ggcgacagcc ccggccccgg 3840
cttcaccccc cacgacagcg ccccctacgg cgccctggac atggccgact tcgagttcga 3900
gcagatgttc accgacgccc tgggcatcga cgagtacggc ggccatatgg agatgcccgt 3960
ggacaggatt ctggaggccg aactcgccgt ggagcagaaa agcgaccagg gcgtggaggg 4020
ccccggcgga accggcggca gcggcagcag ccccaacgac cccgtgacca acatctgcca 4080
ggccgccgac aagcagctgt tcaccctggt ggagtgggcc aagaggattc cccacttcag 4140
cagcctgccc ctggacgacc aggtgatcct gctgagggcc ggatggaacg agctgctgat 4200
cgccagcttc agccacagga gcatcgacgt gagggacggc atcctgctgg ccaccggcct 4260
gcacgtccat aggaacagcg cccacagcgc cggagtgggc gccatcttcg acagggtgct 4320
gaccgagctg gtgagcaaga tgagggacat gaggatggac aagaccgagc tgggctgcct 4380
gagggccatc atcctgttca accccgaggt gaggggcctg aaaagcgccc aggaggtgga 4440
gctgctgagg gagaaggtgt acgccgccct ggaggagtac accaggacca cccaccccga 4500
cgagcccggc agattcgcca agctgctgct gaggctgccc agcctgagga gcatcggcct 4560
gaagtgcctg gagcacctgt tcttcttcag gctgatcggc gacgtgccca tcgacacctt 4620
cctgatggag atgctggaga gccccagcga cagctgagcc ggcaactcgc tgtagtaatt 4680
ccagcgagag gcagagggag cgagcgggcg gcgggctagg gtggaggagc ccggcgagca 4740
gagctgcgct gcgggcgtcc tgggaaggga gatccggagc gaataggggg cttcgcctct 4800
ggcccagccc tcccgctgat cccccagcca gcggtgcgca accctagccg catccacgaa 4860
actttgccca tagcagcggg cgggcacttt gcactggaac ttacaacacc cgagcaagga 4920
cgcgactctc ccgacgcggg gaggctattc tgcccatttg gggacacttc cccgccgctg 4980
ccaggacccg cttctctgaa aggctctcct tgcagctgct tagacgctgg atttttttcg 5040
ggtagtggaa aaccagcagc ctcccgcgac cagatctgcc accatgaagc tgctgagcag 5100
catcgagcag gcttgcgaca tctgcaggct gaagaagctg aagtgcagca aggagaagcc 5160
caagtgcgcc aagtgcctga agaacaactg ggagtgcaga tacagcccca agaccaagag 5220
gagccccctg accagggccc acctgaccga ggtggagagc aggctggaga ggctggagca 5280
gctgttcctg ctgatcttcc ccagggagga cctggacatg atcctgaaga tggacagcct 5340
gcaagacatc aaggccctgc tgaccggcct gttcgtgcag gacaacgtga acaaggacgc 5400
cgtgaccgac aggctggcca gcgtggagac cgacatgccc ctgaccctga ggcagcacag 5460
gatcagcgcc accagcagca gcgaggagag cagcaacaag ggccagaggc agctgaccgt 5520
gagccccgag tttcccggga tcaggcccga gtgcgtggtg cccgagaccc agtgcgccat 5580
gaaaaggaag gagaagaagg cccagaagga gaaggacaag ctgcccgtga gcaccaccac 5640
cgtcgatgac cacatgcccc ccatcatgca gtgcgagccc cccccccccg aggccgccag 5700
gattcacgag gtcgtgccca ggttcctgag cgacaagctg ctggtgacca acaggcagaa 5760
gaacatcccc cagctgaccg ccaaccagca gttcctgatc gccaggctga tctggtatca 5820
ggacggctac gagcagccca gcgacgagga cctgaaaagg atcacccaga cctggcagca 5880
ggccgacgac gagaacgagg agagcgacac ccccttcagg cagatcaccg agatgaccat 5940
cctgaccgtg cagctgatcg tggagttcgc caagggcctg cccggattcg ccaagatcag 6000
ccagcccgac cagatcaccc tgctgaaggc ttgcagcagc gaggtgatga tgctgagggt 6060
ggccaggagg tacgacgccg ccagcgacag catcctgttc gccaacaacc aggcttacac 6120
cagggacaac tacaggaagg ctggcatggc cgaggtgatc gaggacctcc tgcacttctg 6180
cagatgtatg tacagcatgg ccctggacaa catccactac gccctgctga ccgccgtggt 6240
gatcttcagc gacaggcccg gcctggagca gccccagctg gtggaggaga tccagaggta 6300
ctacctgaac accctgagga tctacatcct gaaccagctg agcggcagcg ccaggagcag 6360
cgtgatctac ggcaagatcc tgagcatcct gagcgagctg aggaccctgg gaatgcagaa 6420
cagcaatatg tgtatcagcc tgaagctgaa gaacaggaag ctgcccccct tcctggagga 6480
gatttgggac gtggccgaca tgagccacac ccagcccccc cccatcctgg agagccccac 6540
caacctgtga atcgattaga catgataaga tacattgatg agtttggaca aaccacaact 6600
agaatgcagt gaaaaaaatg cttaatttgt gaaatttgtg atgctattgc ttaatttgta 6660
accattataa gctgcaataa acaagttaat aaaacatttg cattcatttt atgtttcagg 6720
ttcaggggga gatgtgggag gttttttaaa gcaagtaaaa cctctacaaa tgtggtatct 6780
agagctcttc caaatagatc tggaaggtgc tgaggtacga tgagacccgc accaggtgca 6840
gaccctgcga gtgtggcggt aaacatatta ggaaccagcc tgtgatgctg gatgtgaccg 6900
aggagctgag gcccgatcac ttggtgctgg cctgcacccg cgctgagttt ggctctagcg 6960
atgaagatac agattgaggt actgaaatgt gtgggcgtgg cttaagggtg ggaaagaata 7020
tataaggtgg gggtcttatg tagttttgta tctgttttgc agcagccgcc gccgccatga 7080
gcaccaactc gtttgatgga agcattgtga gctcatattt gacaacgcgc atgcccccat 7140
gggccggggt gcgtcagaat gtgatgggct ccagcattga tggtcgcccc gtcctgcccg 7200
caaactctac taccttgacc tacgagaccg tgtctggaac gccgttggag actgcagcct 7260
ccgccgccgc ttcagccgct gcagccaccg cccgcgggat tgtgactgac tttgctttcc 7320
tgagcccgct tgcaagcagt gcagcttccc gttcatccgc ccgcgatgac aagttgacgg 7380
ctcttttggc acaattggat tctttgaccc gggaacttaa tgtcgtttct cagcagctgt 7440
tggatctgcg ccagcaggtt tctgccctga aggcttcctc ccctcccaat gcggtttaaa 7500
acataaataa aaaaccagac tctgtttgga tttggatcaa gcaagtgtct tgctgtcttt 7560
atttaggggt tttgcgcgcg cggtaggccc gggaccagcg gtctcggtcg ttgagggtcc 7620
tgtgtatttt ttccaggacg tggtaaaggt gactctggat gttcagatac atgggcataa 7680
gcccgtctct ggggtggagg tagcaccact gcagagcttc atgctgcggg gtggtgttgt 7740
agatgatcca gtcgtagcag gagcgctggg cgtggtgcct aaaaatgtct ttcagtagca 7800
agctgattgc caggggcagg cccttggtgt aagtgtttac aaagcggtta agctgggatg 7860
ggtgcatacg tggggatatg agatgcatct tggactgtat ttttaggttg gctatgttcc 7920
cagccatatc cctccgggga ttcatgttgt gcagaaccac cagcacagtg tatccggtgc 7980
acttgggaaa tttgtcatgt agcttagaag gaaatgcgtg gaagaacttg gagacgccct 8040
tgtgacctcc aagattttcc atgcattcgt ccataatgat ggcaatgggc ccacgggcgg 8100
cggcctgggc gaagatattt ctgggatcac taacgtcata gttgtgttcc aggatgagat 8160
cgtcataggc catttttaca aagcgcgggc ggagggtgcc agactgcggt ataatggttc 8220
catccggccc aggggcgtag ttaccctcac agatttgcat ttcccacgct ttgagttcag 8280
atggggggat catgtctacc tgcggggcga tgaagaaaac ggtttccggg gtaggggaga 8340
tcagctggga agaaagcagg ttcctgagca gctgcgactt accgcagccg gtgggcccgt 8400
aaatcacacc tattaccggg tgcaactggt agttaagaga gctgcagctg ccgtcatccc 8460
tgagcagggg ggccacttcg ttaagcatgt ccctgactcg catgttttcc ctgaccaaat 8520
ccgccagaag gcgctcgccg cccagcgata gcagttcttg caaggaagca aagtttttca 8580
acggtttgag accgtccgcc gtaggcatgc ttttgagcgt ttgaccaagc agttccaggc 8640
ggtcccacag ctcggtcacc tgctctacgg catctcgatc cagcatatct cctcgtttcg 8700
cgggttgggg cggctttcgc tgtacggcag tagtcggtgc tcgtccagac gggccagggt 8760
catgtctttc cacgggcgca gggtcctcgt cagcgtagtc tgggtcacgg tgaaggggtg 8820
cgctccgggc tgcgcgctgg ccagggtgcg cttgaggctg gtcctgctgg tgctgaagcg 8880
ctgccggtct tcgccctgcg cgtcggccag gtagcatttg accatggtgt catagtccag 8940
cccctccgcg gcgtggccct tggcgcgcag cttgcccttg gaggaggcgc cgcacgaggg 9000
gcagtgcaga cttttgaggg cgtagagctt gggcgcgaga aataccgatt ccggggagta 9060
ggcatccgcg ccgcaggccc cgcagacggt ctcgcattcc acgagccagg tgagctctgg 9120
ccgttcgggg tcaaaaacca ggtttccccc atgctttttg atgcgtttct tacctctggt 9180
ttccatgagc cggtgtccac gctcggtgac gaaaaggctg tccgtgtccc cgtatacaga 9240
cttgagaggc ctgtcctcga ccgatgccct tgagagcctt caacccagtc agctccttcc 9300
ggtgggcgcg gggcatgact atcgtcgccg cacttatgac tgtcttcttt atcatgcaac 9360
tcgtaggaca ggtgccggca gcgctctggg tcattttcgg cgaggaccgc tttcgctgga 9420
gcgcgacgat gatcggcctg tcgcttgcgg tattcggaat cttgcacgcc ctcgctcaag 9480
ccttcgtcac tggtcccgcc accaaacgtt tcggcgagaa gcaggccatt atcgccggca 9540
tggcggccga cgcgctgggc tacgtcttgc tggcgttcgc gacgcgaggc tggatggcct 9600
tccccattat gattcttctc gcttccggcg gcatcgggat gcccgcgttg caggccatgc 9660
tgtccaggca ggtagatgac gaccatcagg gacagcttca aggccagcaa aaggccagga 9720
accgtaaaaa ggccgcgttg ctggcgtttt tccataggct ccgcccccct gacgagcatc 9780
acaaaaatcg acgctcaagt cagaggtggc gaaacccgac aggactataa agataccagg 9840
cgtttccccc tggaagctcc ctcgtgcgct ctcctgttcc gaccctgccg cttaccggat 9900
acctgtccgc ctttctccct tcgggaagcg tggcgctttc tcatagctca cgctgtaggt 9960
atctcagttc ggtgtaggtc gttcgctcca agctgggctg tgtgcacgaa ccccccgttc 10020
agcccgaccg ctgcgcctta tccggtaact atcgtcttga gtccaacccg gtaagacacg 10080
acttatcgcc actggcagca gccactggta acaggattag cagagcgagg tatgtaggcg 10140
gtgctacaga gttcttgaag tggtggccta actacggcta cactagaagg acagtatttg 10200
gtatctgcgc tctgctgaag ccagttacct tcggaaaaag agttggtagc tcttgatccg 10260
gcaaacaaac caccgctggt agcggtggtt tttttgtttg caagcagcag attacgcgca 10320
gaaaaaaagg atctcaagaa gatcctttga tcttttctac ggggtctgac gctcagtgga 10380
acgaaaactc acgttaaggg attttggtca tgagattatc aaaaaggatc ttcacctaga 10440
tccttttaaa ttaaaaatga agttttaaat caatctaaag tatatatgag taaacttggt 10500
ctgacagctc gagtatgtcc tacttttata aactttggtt gaactaaata aaacagcaac 10560
atgtacccaa cgtttttaga ctgttttatt cagtaccata aacattcact aaactataca 10620
gagctaaaat catgcaaaag attgcaaaac aaactgcctt gggaaatttc cagtctaagc 10680
taaatggacc aagtatagga ttgaatttta agaagttggt gggaagattc cagctcttgt 10740
actcacaggt aaggtcctag gattctattt gttgaagtgt ctgcagaccc tctccctaca 10800
gcaggggcgt ggagcaaatg tgcattcagg aagtgcttat tagtcccccc aaaacctttt 10860
tcgtgacgac agacggatgg aggcctcaga cgactccggc agtaggaccc tgaaccaaat 10920
gcctgagctg cgctcgaaag gctcgtcttg caggagctgg cgagtggcac gggcttcggt 10980
ggccgggctc ggggctcggg gctcggggcc cggagccggg gggggcgggg ggtccgtgcc 11040
cagggcgctc tgtggctcga ttcatgtccc cgccctccca cctgagcaca ctgggcagag 11100
agcctgcggc atcgggccag tcgcgcctcc tcgtccgccc tgggcgggtc gctgggcccc 11160
aggccgcttt ctacagctcc tttaataaaa tggacagcag gggtcctaac cagacgtggg 11220
catcaagaca aaggaggcgg ccagacgcgc ttgagggcct gctcgctagc tcccgccccc 11280
ccattccgcg gtcatccggg gacagaggcc aggccggact gggtggagtt gggactcata 11340
cgtctgcgtc caggaaggcg ccgggcgagc cccagctaga cgtgacgggc ggggccgaac 11400
acggcagcgg accagaggcc cgcggcgcac cggcgtgggg cggggcaagc ggagccttcc 11460
gggatgccgc gcggcagccg gcttccggct gtgggtggtg cgggggacag cggcggccgg 11520
aagctgactg agccggcctt tggtaacgcc gcctgcactt ctgggggcgt cgagcctggc 11580
ggtagaatct tcccagtagg cggcgcggga gggaaaagag gattgagggc atgcttacca 11640
atgcttaatc agtgaggcac ctatctcagc gatctgtcta tttcgttcat ccatagttgc 11700
ctgactcccc gtcgtgtaga taactacgat acgggagggc ttaccatctg gccccagtgc 11760
tgcaatgata ccgcgagacc cacgctcacc ggctccagat ttatcagcaa taaaccagcc 11820
agccggaagg gccgagcgca gaagtggtcc tgcaacttta tccgcctcca tccagtctat 11880
taattgttgc cgggaagcta gagtaagtag ttcgccagtt aatagtttgc gcaacgttgt 11940
tgccattgct gcaggcatcg tggtgtcacg ctcgtcgttt ggtatggctt cattcagctc 12000
cggttcccaa cgatcaaggc gagttacatg atcccccatg ttgtgcaaaa aagcggttag 12060
ctccttcggt cctccgatcg ttgtcagaag taagttggcc gcagtgttat cactcatggt 12120
tatggcagca ctgcataatt ctcttactgt catgccatcc gtaagatgct tttctgtgac 12180
tggtgagtac tcaaccaagt cattctgaga atagtgtatg cggcgaccga gttgctcttg 12240
cccggcgtca acacgggata ataccgcgcc acatagcaga actttaaaag tgctcatcat 12300
tggaaaacgt tcttcggggc gaaaactctc aaggatctta ccgctgttga gatccagttc 12360
gatgtaaccc actcgtgcac ccaactgatc ttcagcatct tttactttca ccagcgtttc 12420
tgggtgagca aaaacaggaa ggcaaaatgc cgcaaaaaag ggaataaggg cgacacggaa 12480
atgttgaata ctcatactct tcctttttca atattattga agcatttatc agggttattg 12540
tctcatgagc ggatacatat ttgaatgtat ttagaaaaa 12579
<210> 8
<211> 11443
<212> DNA
<213> Artificial Sequence
<220>
<223> Synthetic promoter
<400> 8
taaacaaata ggggttccgc gcacatttcc ccgaaaagtg ccacctgacg tactgaggac 60
gccagggttt tcccagtcac gacgttgtaa aacgacggcc agtagcagac aagcccgtca 120
gggcgcgtca gcgggtgttg gccctaggac gaaaggaggt cgtgaaatgg ataaaaaaat 180
acagcgtttt tcatgtacaa ctatactagt tgtagtgcct aaataatgct tttaaaactt 240
aaaaataatc aatgtcctca gcggggtgtc ggggatttag gtgacactat aggctgagcg 300
ccgcacaggc atctagaggc tatggcaggg cctgccgccc cgacgttggc tgcgagccct 360
gggccttcac ccgaacttgg ggggtggggt ggggaaaagg aagaaacgcg ggcgtattgg 420
ccccaatggg gtctcggtgg ggtatcgaca gagtgccagc cctgggaccg aaccccgcgt 480
ttatgaacaa acgacccaac accgtgcgtt ttattctgtc tttttattgc cgtcatagcg 540
cgggttcctt ccggtattgt ctccttccgt gtttcaatcg attcaaaaga actcgtccag 600
cagacggtaa aaagcaatgc gttgagaatc cggtgcagca atgccataca gcaccagaaa 660
gcgatcagcc cattcaccgc ccagttcttc agcaatgtca cgggttgcca gtgcgatgtc 720
ctgatagcga tcagccacgc ccaggcgacc gcagtcgata aagccggaga aacggccgtt 780
ttccaccata atgtttggca gacaagcatc gccgtgggtc acaaccaggt cctcgccatc 840
tggcatacgt gctttcaggc gtgcgaacag ttctgccggt gccagaccct gatgttcctc 900
gtccaggtca tcctgatcaa ccaggccagc ttccatgcga gtgcgtgcgc gctcgatacg 960
gtgtttagct tggtgatcga atgggcaagt agctgggtcc agggtatgca gacggcgcat 1020
agcatcagcc atgatggaaa ccttttctgc cggtgccaga tgagaggaca gcagatcctg 1080
gcctggaacc tcgcccagca gcagccagtc gcggccagcc tcggtcacaa catccagcac 1140
agctgcgcat ggaacgccgg tagtagccag ccaggacaga cgagctgctt catcttgcag 1200
ttcgttcagt gcgccggaca gatcggtctt aacaaacagc accggacggc cttgagcgga 1260
cagacggaac acagctgcgt cggagcaacc gatagtctgt tgagcccagt catagccaaa 1320
cagacgttcc acccaagcag ccggagaacc agcgtgcaga ccgtcttgtt caatcatggt 1380
ggcaattggg tgtctgagcg atgtggctcg gctggcgacg caaaagaaga tgcggctgac 1440
tgtcgaacag gaggagcaga gagcgaagcg ggaggctgcg ggctcaattt gcatgcttta 1500
gttcctcacc ttgtcgtatt atactatgcc gatatactat gccgatgatt aattgtcaac 1560
gtatacggaa tagctctgag gccgaggcag cttcggcctc tgcataaata aaaaaaatta 1620
gtcagccatg gggcggagaa tgggcggaac tgggcggagt taggggcggg atgggcggag 1680
ttaggggcgg gactatggtt gctgactaat tgagatgctt gctttgcata cttctgcctg 1740
ctggggagcc tggggacttt ccacacctgg ttgctgacta attgagatgc ttgctttgca 1800
tacttctgcc tgctggggag cctggggact ttccacaccc taacctcgag gccatcgtgg 1860
cacgccaggg ttttcccagt cacgacgttg taaaacgacg gccagtgctc ttctcccccg 1920
cgggaggttt tataaatccg actgtctaga ttgttgttaa atcacacaaa aaaccaacac 1980
acagatgtaa tgaaaataaa gatattttat tatcgattca gctgtcgctg gggctctcca 2040
gcatctccat caggaaggtg tcgatgggca cgtcgccgat cagcctgaag aagaacaggt 2100
gctccaggca cttcaggccg atgctcctca ggctgggcag cctcagcagc agcttggcga 2160
atctgccggg ctcgtcgggg tgggtggtcc tggtgtactc ctccagggcg gcgtacacct 2220
tctccctcag cagctccacc tcctgggcgc ttttcaggcc cctcacctcg gggttgaaca 2280
ggatgatggc cctcaggcag cccagctcgg tcttgtccat cctcatgtcc ctcatcttgc 2340
tcaccagctc ggtcagcacc ctgtcgaaga tggcgcccac tccggcgctg tgggcgctgt 2400
tcctatggac gtgcaggccg gtggccagca ggatgccgtc cctcacgtcg atgctcctgt 2460
ggctgaagct ggcgatcagc agctcgttcc atccggccct cagcaggatc acctggtcgt 2520
ccaggggcag gctgctgaag tggggaatcc tcttggccca ctccaccagg gtgaacagct 2580
gcttgtcggc ggcctggcag atgttggtca cggggtcgtt ggggctgctg ccgctgccgc 2640
cggttccgcc ggggccctcc acgccctggt cgcttttctg ctccacggcg agttcggcct 2700
ccagaatcct gtccacgggc atctccatat ggccgccgta ctcgtcgatg cccagggcgt 2760
cggtgaacat ctgctcgaac tcgaagtcgg ccatgtccag ggcgccgtag ggggcgctgt 2820
cgtggggggt gaagccgggg ccggggctgt cgccgtcgcc cagcatgtcc aggtcgaagt 2880
cgtccagggc gtcggcgtgg gccatggcca cgtcctcgcc gtccaggtgc agctcgtcgc 2940
ccaggctcac gtcggtgggg ggggccacct tccttttctt cttggggccc atcaattggc 3000
cacccccccc cccccccccg catgcccggc gggtcaggga cgcgggcgcg cggtgcgctg 3060
ggggcggcac gtccgggcgg aggaggcgtc atcccgtggc cccaggagcg gcaatcagcc 3120
gagactgagc cagcgcccgg ccgcaggcag acccaagcgc caggaggcgg agccagcgct 3180
gaccccaccc cgcccctccc cccgcccctc gcagcctttt ctcacctcac tggctttcct 3240
gagcgagagc ggaactgctg ggggaacctt cgccaccctc tcccggacaa ctctacgggg 3300
aaagcccagc tgcggacaag ccagacttgt ggtcttctgc caggggcggc aggccctatc 3360
ccctctctgg gcctcagttc cactccccgc accccgtaaa aagattggcg tagaagtcgt 3420
ggaggacctc tctccaaggg cgcagaggag tccaacaccc aacaaccttg ctatggccag 3480
ctaagtggtt cgcaccctga ggactatggt cctcggagga tgcgttcgcc taagtggaca 3540
cggctccctg ccgagcctac cagcaggcac aacgatgata tgtggggagc actcagggac 3600
ccgctgttgc tttgcctggg agaacactgg aaatttttca tcttggcctg gctccttccc 3660
ctccctctcc tttctcctcc ctttcccagc cagcagcttt ctgggctgcc tccccccaag 3720
ccagctggtg tacgctcaga aaatccaaac tcatttccat gtgagtggag ggggatataa 3780
ttaggaaggc cccttcccca agtagagagg ggagcatccc ccgtgcccca ctcactgtgg 3840
gggagggagg gtcaaagcag cttaagggga tctctgcccg caaagtgcct agggctcaac 3900
tatctcaggc aacctgacca ttcagtgggg actcccttgg ggggtccagg cccagaccct 3960
ctgcagttac ctgagcagtc cagccagctc tgccatcagc tcctcctctc agaactacgt 4020
gcctgccctt tgtaaaaggg tctcctctct ctaaaccaga cagggcccag acctaccact 4080
tccacttgtg ccccagggaa ccatgaatgg aaaatccacc cagctcagta agtacttatc 4140
tagtgtttac tggatgtcta gctgcactga gaggagacag gccgaggaag gagtagaggt 4200
gaacatccaa ccttcagaac tcacagacct agacacgatt cacgcactgc agacaccagc 4260
aaaggcggtg ggctggctgc cctctgccct ctgccctgct ccatggggcc aggaccattt 4320
ggttgttgtt tttacctcct ggaaccagga aagttttgct accaagaagt ttggctttac 4380
cattctacat tttgcttcca gttgtcccct ccttcttccc tcagagtcct gaggcacccc 4440
agcaggccag gaaggtaaac tcaaggcacc tccagagaca gtgcagagtg aggttcctgg 4500
cccactggga gaagccaaca gccctcgagt aggcgagacc aatgggtgcg ccatgggctc 4560
ttccaaaaat ttaggtgaca ctatagggca ccgctcgcac ctgcgcacag gcccgcggct 4620
acaaactacg aacgatcatt ctagatacca catttgtaga ggttttactt gctttaaaaa 4680
acctcccaca tctccccctg aacctgaaac ataaaatgaa tgcaaatgtt ttattaactt 4740
gtttattgca gcttataatg gttacaaatt aagcaatagc atcacaaatt tcacaaatta 4800
agcatttttt tcactgcatt ctagttgtgg tttgtccaaa ctcatcaatg tatcttatca 4860
tgtctaatcg attcacaggt tggtggggct ctccaggatg ggggggggct gggtgtggct 4920
catgtcggcc acgtcccaaa tctcctccag gaaggggggc agcttcctgt tcttcagctt 4980
caggctgata cacatattgc tgttctgcat tcccagggtc ctcagctcgc tcaggatgct 5040
caggatcttg ccgtagatca cgctgctcct ggcgctgccg ctcagctggt tcaggatgta 5100
gatcctcagg gtgttcaggt agtacctctg gatctcctcc accagctggg gctgctccag 5160
gccgggcctg tcgctgaaga tcaccacggc ggtcagcagg gcgtagtgga tgttgtccag 5220
ggccatgctg tacatacatc tgcagaagtg caggaggtcc tcgatcacct cggccatgcc 5280
agccttcctg tagttgtccc tggtgtaagc ctggttgttg gcgaacagga tgctgtcgct 5340
ggcggcgtcg tacctcctgg ccaccctcag catcatcacc tcgctgctgc aagccttcag 5400
cagggtgatc tggtcgggct ggctgatctt ggcgaatccg ggcaggccct tggcgaactc 5460
cacgatcagc tgcacggtca ggatggtcat ctcggtgatc tgcctgaagg gggtgtcgct 5520
ctcctcgttc tcgtcgtcgg cctgctgcca ggtctgggtg atccttttca ggtcctcgtc 5580
gctgggctgc tcgtagccgt cctgatacca gatcagcctg gcgatcagga actgctggtt 5640
ggcggtcagc tgggggatgt tcttctgcct gttggtcacc agcagcttgt cgctcaggaa 5700
cctgggcacg acctcgtgaa tcctggcggc ctcggggggg gggggctcgc actgcatgat 5760
ggggggcatg tggtcatcga cggtggtggt gctcacgggc agcttgtcct tctccttctg 5820
ggccttcttc tccttccttt tcatggcgca ctgggtctcg ggcaccacgc actcgggcct 5880
cccgagtttc ccgggatcgc tcacggtcag ctgcctctgg cccttgttgc tgctctcctc 5940
gctgctgctg gtggcgctga tcctgtgctg cctcagggtc aggggcatgt cggtctccac 6000
gctggccagc ctgtcggtca cggcgtcctt gttcacgttg tcctgcacga acaggccggt 6060
cagcagggcc ttgatgtctt gcaggctgtc catcttcagg atcatgtcca ggtcctccct 6120
ggggaagatc agcaggaaca gctgctccag cctctccagc ctgctctcca cctcggtcag 6180
gtgggccctg gtcagggggc tcctcttggt cttggggctg tatctgcact cccagttgtt 6240
cttcaggcac ttggcgcact tgggcttctc cttgctgcac ttcagcttct tcagcctgca 6300
gatgtcgcaa gcctgctcga tgctgctcag cagcttcatg gtggccaatt gccccccccc 6360
ccccccgcat gccttgcact ccaatcagaa ccagcaagat gatgcccaag aggaaaagaa 6420
caccactttt cttcatagtg atagaatgga gttccaagtc actcctgtat tggattttga 6480
gcctgagaaa ttctttagag aacacatttt ggggatcata tttatttagg atattcattt 6540
ctctcctaaa ctctgattgg ctagtatctt tagccgagct aactaaattg accacaaact 6600
tgattgtgct gggggaaacc ctagtctcag atccaaggga atttctgcat gtttttattt 6660
ccatttcaca taaatgggtg gtttatagta agggatgtga aactagcaac actgatagcc 6720
tttggcacat tcacagttgc tcacctgtgt gaagaatagg ttatataatg aatatactaa 6780
tgttatacaa caaaggttgg agatgtggtt tccagatggg aaatattaaa gtccagataa 6840
ataatatact tttcaaattc ccttactatt tatggcatat tcttctgtat aatagatggc 6900
tacattgata ttttcttata ttgcccactt aacaacttaa agcaccttaa tttcctctgg 6960
gaccaggtca ttttctacta gtggtaagct cattctgtat cattcctgct acagtattat 7020
tttttaaact aataaattgg ttagaataag gggtcagttg catgtaagag acccaaatta 7080
acagtggcta agaaatgcaa taaaaatgaa gataaatagc tgggacctaa ttaaagagct 7140
tttgcacagc aaaaggaaca gtcagcagag taaacagaca acccacagag cgggagaaaa 7200
tcttcacaat ctatatacct gacaaaggac taatatccag aatccagaat gaattcaaac 7260
aaatcattaa gtaaaaaaca aacaatccca ttaaaaagtg ggctaaggac atcaatatac 7320
aattctcaaa agaagataca cgaatagcca acaaacatat gaaaaaatgc tcatcactaa 7380
tgatcaggga aatgcaaatc aaaaccacgg tgcgatacca ccttacaccc gcaagaatgg 7440
ccataatcaa aaaatcaaaa aacagcagat gttggtgtgg actcgagtgg taatacaatg 7500
gccggttccc atggacctgc atcgtggtgt aactataacg gtcctaaggt agcgaccgcg 7560
gagactaggt gtatttatct aagcgatcgc ttaattaagg ccggccgccg caataaaata 7620
tctttatttt cattacatct gtgtgttggt tttttgtgtg aatccatagt actaacatac 7680
gctctccatc aaaacaaaac gaaacaaaac aaactagcaa aataggctgt ccccagtgca 7740
agtccaggtg ccagaacatt tctctatcca taatgcaggg gtaccgggtg atgacggtga 7800
aaacctccaa ttgcggagta ctgtcctccg agcggagtac tgtcctccga gcggagtact 7860
gtcctccgag cggagtactg tcctccgagc ggagtactgt cctccgagcg gagtactgtc 7920
ctccgagcgg agagtccccg gggacctaga gggtatataa tgggtgcctt agctggtgtg 7980
tgacctcatc ttcctgtacg cccctgcagg ggcgcgccac gcgtcgaaga aggtgagtaa 8040
tcttaacatg ctcttttttt ttttttttgc taatcccttt tgtgtgctga tgttaggatg 8100
acatttacaa caaatgtttg ttcctgacag gaaaaacctt gctgggtacc ttcgttgccg 8160
gacacttctt gtcctctact ttggaaaaaa ggaattgaga gccgctagcg ccaccatgat 8220
tagccctttc ctcgtgctcg ccattggcac atgcctcacc aatagcctcg tgcctggcgg 8280
aggcggaagc ggaggcggag gctccggcgg aggcggaagc tgtcagcctg tgacacagga 8340
ggacggaaag gaaagcagga tctccgtgca agagaggcag cctgccccta cccctagcaa 8400
tggctccccc aaagacggac ccgaaatccc tcccacaggc ggaaaggcta aggccaagcc 8460
cgtgacaaga ggagccggag ccaggagcgg aacccctccc caaaccggac tggaaaagcc 8520
taccggaacc ggatgaatcg attgcgcaaa gctttcgcga taggcgagac caatgggtgt 8580
gtacgtagcg gccgcgtcga cgatagcttg atgggtggca tccctgtgac ccctccccag 8640
tgcctctcct ggccctggaa gttgccactc cagtgcccac cagccttgtc ctaataaaat 8700
taagttgcat cattttgtct gactaggtgt ccttctataa tattatgggg tggagggggg 8760
tggtatggag caaggggcaa gttgggaaga caacctgtag ggcctgcggg gtctattggg 8820
aaccaagctg gagtgcagtg gcacaatctt ggctcactgc aatctccgcc tcctgggttc 8880
aagcgattct cctgcctcag cctcccgagt tgttgggatt ccaggcatgc atgaccaggc 8940
tcagctaatt tttgtttttt tggtagagac ggggtttcac catattggcc aggctggtct 9000
ccaactccta atctcaggtg atctacccac cttggcctcc caaattgctg ggattacagg 9060
cgtgaaccac tgctcccttc cctgtccttc tgattttaaa ataactatac cagcaggagg 9120
acgtccagac acagcatagg ctacctggcc atgcccaacc ggtgggacat ttgagttgct 9180
tgcttggcac tgtcctctca tgcgttgggt ccactcagta gatgcctgtt gaattctgat 9240
ttaaatcggt ccgcgtacgg cgtggtaggt ccgaacgaat ccatggatta ccctgttatc 9300
cctactcaag gacatcatcc ctttagtgag ggttaattca cgcagtgggt acggaactaa 9360
aggcagcaca catcgtgtaa tcatggtcat agctgtttcc tgtgtgaaat tgttatccgc 9420
tacgtctctc ccccgcagta agggctagat taactcgtct cgtgaatatc cggaactccc 9480
tttagtgagg gttaattgcg ttgcgctcac tgcccgcttt ccagtcggga aacctgtcgt 9540
gccagcttaa tcatggtcat agctgtttcc tgtgtgaaat tgttatccgc taccggaaac 9600
gcttccttca tgtgagcaaa aggccagcaa aaggccagga accgtaaaaa ggccgcgttg 9660
ctggcgtttt tccataggct ccgcccccct gacgagcatc acaaaaatcg acgctcaagt 9720
cagaggtggc gaaacccgac aggactataa agataccagg cgtttccccc tggaagctcc 9780
ctcgtgcgct ctcctgttcc gaccctgccg cttaccggat acctgtccgc ctttctccct 9840
tcgggaagcg tggcgctttc tcatagctca cgctgtaggt atctcagttc ggtgtaggtc 9900
gttcgctcca agctgggctg tgtgcacgaa ccccccgttc agcccgaccg ctgcgcctta 9960
tccggtaact atcgtcttga gtccaacccg gtaagacacg acttatcgcc actggcagca 10020
gccactggta acaggattag cagagcgagg tatgtaggcg gtgctacaga gttcttgaag 10080
tggtggccta actacggcta cactagaaga acagtatttg gtatctgcgc tctgctgaag 10140
ccagttacct tcggaaaaag agttggtagc tcttgatccg gcaaacaaac caccgctggt 10200
agcggtggtt tttttgtttg caagcagcag attacgcgca gaaaaaaagg atctcaagaa 10260
gatcctttga tcttttctac ggggtctgac gctcagtgga acgaaaactc acgttaaggg 10320
attttggtca tgatctatgt cgggtgcgga gaaagaggta atgaaatggc atacgagtaa 10380
acttggtctg acaccgctgc atgagattat caaaaaggat cttcacctag atccttttaa 10440
attaaaaatg aagttttaaa tcaatctaaa gtatatatga gtaaacttgg tctgacagtt 10500
accaatgctt aatcagtgag gcacctatct cagcgatctg tctatttcgt tcatccatag 10560
ttgcctgact ccccgtcgtg tagataacta cgatacggga gggcttacca tctggcccca 10620
gtgctgcaat gataccgcga gacccacgct caccggctcc agatttatca gcaataaacc 10680
agccagccgg aagcgccgag cgcagaagtg gtcctgcaac tttatccgcc tccatccagt 10740
ctattaactg ttgccgggaa gctagagtaa gtagttcgcc agttaatagt ttgcggagcg 10800
ttgttgccat tgctacaggc atcgtggtgt cacgctcgtc gtttggtatg gcttcattca 10860
gctccggttc ccaacgatca aggcgagtta catgatcccc catgttgtgc aaaaaagcgg 10920
ttagctcctt cggtcctccg atggttgtca gaagtaagtt ggccgcagtg ttatcactca 10980
tggttatggc agcactgcat aattctctta ctgtcatgcc atccgtaaga tgcttttctg 11040
tgactggtga gtattcaacc aagtcattct gagaatagtg tatgcggcga ccgagttgct 11100
cttgcccggc gtcaatacgg gataataccg cgccacatag cagaacttta aaagtgctca 11160
tcattgggaa gcgttcttcg gggcgaaaac tctcaaggat cttaccgctg ttgagatcca 11220
gttcgatgta acccacacga gcacccaact gatcttcagc atcttttact ttcaccagcg 11280
tttctgggtg agcaaaaaca ggaaggcaaa atgccgcaaa aaagggaata agggcgacac 11340
ggaaatgttg aatactcata cgcttccttt ttcaatagta ttgaagcatt tatcagggtt 11400
attgtctcgg gagcgaatac atatttgaat gtatttagaa aaa 11443
<210> 9
<211> 12844
<212> DNA
<213> Artificial Sequence
<220>
<223> Synthetic promoter
<400> 9
taaacaaata ggggttccgc gcacatttcc ccgaaaagtg ccacctgacg tctaagaaac 60
cattattatc atgacattaa cctataaaaa taggcgtatc acgaggccct ttcgtcttca 120
agaaaattaa tcgcaccggt atctatgtcg ggtgcggaga aagaggtaat gaaatggcag 180
ctagcatcat caataatata ccttattttg gattgaagcc aatatgataa tgagggggtg 240
gagtttgtga cgtggcgcgg ggcgtgggaa cggggcgggt gacgtagtag tgtggcggaa 300
gtgtgatgtt gcaagtgtgg cggaacacat gtaagcgacg gatgtggcaa aagtgacgtt 360
tttggtgtgc gccggtgtac acaggaagtg acaattttcg cgcggtttta ggcggatgtt 420
gtagtaaatt tgggcgtaac cgagtaagat ttggccattt tcgcgggaaa actgaataag 480
aggaagtgaa atctgaataa ttttgtgtta ctcatagcgc gtaatagtgc gccggtgtac 540
acaggaagtg acaattttcg cgcggtttta ggcggatgtt gtagtaaatt tgggcgtaac 600
cgagtaagat ttggccattt tcgcgggaaa actgaataag aggaagtgaa atctgaataa 660
ttttgtgtta ctcattttgt ctagggagat ccggtaccga tatcctagac aacgatgctg 720
agctaactat aacggtccta aggtagcgac cgcggagact aggtgtattt atctaagcga 780
tcgcttaatt aaggccggcc gccgcaataa aatatcttta ttttcattac atctgtgtgt 840
tggttttttg tgtgaatcca tagtactaac atacgctctc catcaaaaca aaacgaaaca 900
aaacaaacta gcaaaatagg ctgtccccag tgcaagtcca ggtgccagaa catttctcta 960
tccataatgc aggggtaccg ggtgatgacg gtgaaaacct ccaattgcgg agtactgtcc 1020
tccgagcgga gtactgtcct ccgagcggag tactgtcctc cgagcggagt actgtcctcc 1080
gagcggagta ctgtcctccg agcggagtac tgtcctccga gcggagagtc cccggggacc 1140
tagagggtat ataatgggtg ccttagctgg tgtgtgacct catcttcctg tacgcccctg 1200
caggggcgcg ccacgcgtcg aagaaggtga gtaatcttaa catgctcttt tttttttttt 1260
ttgctaatcc cttttgtgtg ctgatgttag gatgacattt acaacaaatg tttgttcctg 1320
acaggaaaaa ccttgctggg taccttcgtt gccggacact tcttgtcctc tactttggaa 1380
aaaaggaatt gagagccgct agcgccacca tgattagccc tttcctcgtg ctcgccattg 1440
gcacatgcct caccaatagc ctcgtgcctg agaaagagaa agaccctaag tattggaggg 1500
accaagccca agagacactg aaatacgctc tggaactgca aaagctcaac acaaacgtcg 1560
ccaaaaacgt catcatgttc ctcggcgatg gcatgggcgt cagcacagtg acagccgcta 1620
gaatcctgaa aggccaactg catcacaatc ccggagagga aaccaggctg gaaatggata 1680
agtttccctt tgtggctctg tccaagacat acaataccaa tgcccaagtg cctgactccg 1740
ccggaaccgc taccgcctac ctgtgcggag tgaaagccaa tgagggaacc gtcggcgtca 1800
gcgctgccac agagaggagc agatgcaata ccacacaggg aaacgaagtg acaagcattc 1860
tgaggtgggc taaggatgcc ggaaagtccg tgggaatcgt caccacaacc agggtgaatc 1920
acgctacccc tagcgctgcc tatgcccata gcgctgacag ggactggtac tccgacaatg 1980
agatgccccc tgaggctctg tcccagggat gcaaagacat tgcctatcag ctcatgcaca 2040
acattagaga catcgacgtg attatgggag gcggaagaaa atatatgtac cctaagaata 2100
agacagacgt ggagtatgag tccgacgaaa aggctagagg aaccaggctg gatggcctcg 2160
acctcgtgga tacctggaag tccttcaaac ccaggtacaa acactcccac tttatctgga 2220
acaggaccga actgctgacc ctggaccctc acaacgtcga ttacctcctg ggactgtttg 2280
agcctggcga tatgcaatac gaactgaata gaaataacgt caccgatccc tccctgtccg 2340
agatggtggt cgtggctatc caaatcctca gaaaaaaccc taagggattc tttctgctcg 2400
tggaaggcgg aagaattgac cacggccatc acgaaggcaa agccaagcaa gctctccacg 2460
aggctgtgga aatggataga gctatcggac aggctggctc cctgacaagc tccgaggata 2520
ccctcaccgt cgtgacagcc gatcactccc acgtttttac attcggaggc tataccccta 2580
gaggaaactc catctttggc ctcgccccta tgctgtccga taccgataag aaacccttta 2640
ccgctatcct ctacggaaac ggacccggat acaaagtggt cggcggagag agggagaatg 2700
tgagcatggt ggactatgcc cataacaatt accaagccca aagcgctgtg cccctgagac 2760
acgaaaccca cggcggagag gatgtggctg tgtttagcaa aggccctatg gcccacctgt 2820
tgcatggcgt ccacgaacag aattacgtcc cccatgtgat ggcctatgcc gcttgcattg 2880
gcgctaacct cggccattgc gctcccgcca gctccgccgg aagcctcgcc gctggccctc 2940
tgctcctggc tctggctctg tatcccctga gcgtcctgtt tggcggaggc ggaagcggag 3000
gcggaggctc cggcggaggc ggaagctgtc agcctgtgac acaggaggac ggaaaggaaa 3060
gcaggatctc cgtgcaagag taaatcgatt gcgcaaagct ttcgcgatag gcgagaccaa 3120
tgggtgtgta cgtagcggcc gcgtcgacga tagcttgatg ggtggcatcc ctgtgacccc 3180
tccccagtgc ctctcctggc cctggaagtt gccactccag tgcccaccag ccttgtccta 3240
ataaaattaa gttgcatcat tttgtctgac taggtgtcct tctataatat tatggggtgg 3300
aggggggtgg tatggagcaa ggggcaagtt gggaagacaa cctgtagggc ctgcggggtc 3360
tattgggaac caagctggag tgcagtggca caatcttggc tcactgcaat ctccgcctcc 3420
tgggttcaag cgattctcct gcctcagcct cccgagttgt tgggattcca ggcatgcatg 3480
accaggctca gctaattttt gtttttttgg tagagacggg gtttcaccat attggccagg 3540
ctggtctcca actcctaatc tcaggtgatc tacccacctt ggcctcccaa attgctggga 3600
ttacaggcgt gaaccactgc tcccttccct gtccttctga ttttaaaata actataccag 3660
caggaggacg tccagacaca gcataggcta cctggccatg cccaaccggt gggacatttg 3720
agttgcttgc ttggcactgt cctctcatgc gttgggtcca ctcagtagat gcctgttgaa 3780
ttctgattta aatcggtccg cgtacggcgt ggtaggtccg aacgaatcca tggattaccc 3840
tgttatccct atccggagtt aacctcgagg acttcggaac ttctagaacc agaccgttca 3900
gtttaaacgc tcttctcccc ctcgagtatg tcctactttt ataaactttg gttgaactaa 3960
ataaaacagc aacatgtacc caacgttttt agactgtttt attcagtacc ataaacattc 4020
actaaactat acagagctaa aatcatgcaa aagattgcaa aacaaactgc cttgggaaat 4080
ttccagtcta agctaaatgg accaagtata ggattgaatt ttaagaagtt ggtgggaaga 4140
ttccagctct tgtactcaca ggtaaggtcc taggattcta tttgttgaag tgtctgcaga 4200
ccctctccct acagcagggg cgtggagcaa atgtgcattc aggaagtgct tattagtccc 4260
cccaaaacct ttttcgtgac gacagacgga tggaggcctc agacgactcc ggcagtagga 4320
ccctgaacca aatgcctgag ctgcgctcga aaggctcgtc ttgcaggagc tggcgagtgg 4380
cacgggcttc ggtggccggg ctcggggctc ggggctcggg gcccggagcc ggggggggcg 4440
gggggtccgt gcccagggcg ctctgtggct cgattcatgt ccccgccctc ccacctgagc 4500
acactgggca gagagcctgc ggcatcgggc cagtcgcgcc tcctcgtccg ccctgggcgg 4560
gtcgctgggc cccaggccgc tttctacagc tcctttaata aaatggacag caggggtcct 4620
aaccagacgt gggcatcaag acaaaggagg cggccagacg cgcttgaggg cctgctcgct 4680
agctcccgcc cccccattcc gcggtcatcc ggggacagag gccaggccgg actgggtgga 4740
gttgggactc atacgtctgc gtccaggaag gcgccgggcg agccccagct agacgtgacg 4800
ggcggggccg aacacggcag cggaccagag gcccgcggcg caccggcgtg gggcggggca 4860
agcggagcct tccgggatgc cgcgcggcag ccggcttccg gctgtgggtg gtgcggggga 4920
cagcggcggc cggaagctga ctgagccggc ctttggtaac gccgcctgca cttctggggg 4980
cgtcgagcct ggcggtagaa tcttcccagt aggcggcgcg ggagggaaaa gaggattgag 5040
ggcatgcggg gggggggggg ggcaattggc caccatgggc cccaagaaga aaaggaaggt 5100
ggcccccccc accgacgtga gcctgggcga cgagctgcac ctggacggcg aggacgtggc 5160
catggcccac gccgacgccc tggacgactt cgacctggac atgctgggcg acggcgacag 5220
ccccggcccc ggcttcaccc cccacgacag cgccccctac ggcgccctgg acatggccga 5280
cttcgagttc gagcagatgt tcaccgacgc cctgggcatc gacgagtacg gcggccatat 5340
ggagatgccc gtggacagga ttctggaggc cgaactcgcc gtggagcaga aaagcgacca 5400
gggcgtggag ggccccggcg gaaccggcgg cagcggcagc agccccaacg accccgtgac 5460
caacatctgc caggccgccg acaagcagct gttcaccctg gtggagtggg ccaagaggat 5520
tccccacttc agcagcctgc ccctggacga ccaggtgatc ctgctgaggg ccggatggaa 5580
cgagctgctg atcgccagct tcagccacag gagcatcgac gtgagggacg gcatcctgct 5640
ggccaccggc ctgcacgtcc ataggaacag cgcccacagc gccggagtgg gcgccatctt 5700
cgacagggtg ctgaccgagc tggtgagcaa gatgagggac atgaggatgg acaagaccga 5760
gctgggctgc ctgagggcca tcatcctgtt caaccccgag gtgaggggcc tgaaaagcgc 5820
ccaggaggtg gagctgctga gggagaaggt gtacgccgcc ctggaggagt acaccaggac 5880
cacccacccc gacgagcccg gcagattcgc caagctgctg ctgaggctgc ccagcctgag 5940
gagcatcggc ctgaagtgcc tggagcacct gttcttcttc aggctgatcg gcgacgtgcc 6000
catcgacacc ttcctgatgg agatgctgga gagccccagc gacagctgag ccggcaactc 6060
gctgtagtaa ttccagcgag aggcagaggg agcgagcggg cggcgggcta gggtggagga 6120
gcccggcgag cagagctgcg ctgcgggcgt cctgggaagg gagatccgga gcgaataggg 6180
ggcttcgcct ctggcccagc cctcccgctg atcccccagc cagcggtgcg caaccctagc 6240
cgcatccacg aaactttgcc catagcagcg ggcgggcact ttgcactgga acttacaaca 6300
cccgagcaag gacgcgactc tcccgacgcg gggaggctat tctgcccatt tggggacact 6360
tccccgccgc tgccaggacc cgcttctctg aaaggctctc cttgcagctg cttagacgct 6420
ggattttttt cgggtagtgg aaaaccagca gcctcccgcg accagatctg ccaccatgaa 6480
gctgctgagc agcatcgagc aggcttgcga catctgcagg ctgaagaagc tgaagtgcag 6540
caaggagaag cccaagtgcg ccaagtgcct gaagaacaac tgggagtgca gatacagccc 6600
caagaccaag aggagccccc tgaccagggc ccacctgacc gaggtggaga gcaggctgga 6660
gaggctggag cagctgttcc tgctgatctt ccccagggag gacctggaca tgatcctgaa 6720
gatggacagc ctgcaagaca tcaaggccct gctgaccggc ctgttcgtgc aggacaacgt 6780
gaacaaggac gccgtgaccg acaggctggc cagcgtggag accgacatgc ccctgaccct 6840
gaggcagcac aggatcagcg ccaccagcag cagcgaggag agcagcaaca agggccagag 6900
gcagctgacc gtgagccccg agtttcccgg gatcaggccc gagtgcgtgg tgcccgagac 6960
ccagtgcgcc atgaaaagga aggagaagaa ggcccagaag gagaaggaca agctgcccgt 7020
gagcaccacc accgtcgatg accacatgcc ccccatcatg cagtgcgagc cccccccccc 7080
cgaggccgcc aggattcacg aggtcgtgcc caggttcctg agcgacaagc tgctggtgac 7140
caacaggcag aagaacatcc cccagctgac cgccaaccag cagttcctga tcgccaggct 7200
gatctggtat caggacggct acgagcagcc cagcgacgag gacctgaaaa ggatcaccca 7260
gacctggcag caggccgacg acgagaacga ggagagcgac acccccttca ggcagatcac 7320
cgagatgacc atcctgaccg tgcagctgat cgtggagttc gccaagggcc tgcccggatt 7380
cgccaagatc agccagcccg accagatcac cctgctgaag gcttgcagca gcgaggtgat 7440
gatgctgagg gtggccagga ggtacgacgc cgccagcgac agcatcctgt tcgccaacaa 7500
ccaggcttac accagggaca actacaggaa ggctggcatg gccgaggtga tcgaggacct 7560
cctgcacttc tgcagatgta tgtacagcat ggccctggac aacatccact acgccctgct 7620
gaccgccgtg gtgatcttca gcgacaggcc cggcctggag cagccccagc tggtggagga 7680
gatccagagg tactacctga acaccctgag gatctacatc ctgaaccagc tgagcggcag 7740
cgccaggagc agcgtgatct acggcaagat cctgagcatc ctgagcgagc tgaggaccct 7800
gggaatgcag aacagcaata tgtgtatcag cctgaagctg aagaacagga agctgccccc 7860
cttcctggag gagatttggg acgtggccga catgagccac acccagcccc cccccatcct 7920
ggagagcccc accaacctgt gaatcgatta gacatgataa gatacattga tgagtttgga 7980
caaaccacaa ctagaatgca gtgaaaaaaa tgcttaattt gtgaaatttg tgatgctatt 8040
gcttaatttg taaccattat aagctgcaat aaacaagtta ataaaacatt tgcattcatt 8100
ttatgtttca ggttcagggg gagatgtggg aggtttttta aagcaagtaa aacctctaca 8160
aatgtggtat ctagagctct tccaaataga tctggaaggt gctgaggtac gatgagaccc 8220
gcaccaggtg cagaccctgc gagtgtggcg gtaaacatat taggaaccag cctgtgatgc 8280
tggatgtgac cgaggagctg aggcccgatc acttggtgct ggcctgcacc cgcgctgagt 8340
ttggctctag cgatgaagat acagattgag gtactgaaat gtgtgggcgt ggcttaaggg 8400
tgggaaagaa tatataaggt gggggtctta tgtagttttg tatctgtttt gcagcagccg 8460
ccgccgccat gagcaccaac tcgtttgatg gaagcattgt gagctcatat ttgacaacgc 8520
gcatgccccc atgggccggg gtgcgtcaga atgtgatggg ctccagcatt gatggtcgcc 8580
ccgtcctgcc cgcaaactct actaccttga cctacgagac cgtgtctgga acgccgttgg 8640
agactgcagc ctccgccgcc gcttcagccg ctgcagccac cgcccgcggg attgtgactg 8700
actttgcttt cctgagcccg cttgcaagca gtgcagcttc ccgttcatcc gcccgcgatg 8760
acaagttgac ggctcttttg gcacaattgg attctttgac ccgggaactt aatgtcgttt 8820
ctcagcagct gttggatctg cgccagcagg tttctgccct gaaggcttcc tcccctccca 8880
atgcggttta aaacataaat aaaaaaccag actctgtttg gatttggatc aagcaagtgt 8940
cttgctgtct ttatttaggg gttttgcgcg cgcggtaggc ccgggaccag cggtctcggt 9000
cgttgagggt cctgtgtatt ttttccagga cgtggtaaag gtgactctgg atgttcagat 9060
acatgggcat aagcccgtct ctggggtgga ggtagcacca ctgcagagct tcatgctgcg 9120
gggtggtgtt gtagatgatc cagtcgtagc aggagcgctg ggcgtggtgc ctaaaaatgt 9180
ctttcagtag caagctgatt gccaggggca ggcccttggt gtaagtgttt acaaagcggt 9240
taagctggga tgggtgcata cgtggggata tgagatgcat cttggactgt atttttaggt 9300
tggctatgtt cccagccata tccctccggg gattcatgtt gtgcagaacc accagcacag 9360
tgtatccggt gcacttggga aatttgtcat gtagcttaga aggaaatgcg tggaagaact 9420
tggagacgcc cttgtgacct ccaagatttt ccatgcattc gtccataatg atggcaatgg 9480
gcccacgggc ggcggcctgg gcgaagatat ttctgggatc actaacgtca tagttgtgtt 9540
ccaggatgag atcgtcatag gccattttta caaagcgcgg gcggagggtg ccagactgcg 9600
gtataatggt tccatccggc ccaggggcgt agttaccctc acagatttgc atttcccacg 9660
ctttgagttc agatgggggg atcatgtcta cctgcggggc gatgaagaaa acggtttccg 9720
gggtagggga gatcagctgg gaagaaagca ggttcctgag cagctgcgac ttaccgcagc 9780
cggtgggccc gtaaatcaca cctattaccg ggtgcaactg gtagttaaga gagctgcagc 9840
tgccgtcatc cctgagcagg ggggccactt cgttaagcat gtccctgact cgcatgtttt 9900
ccctgaccaa atccgccaga aggcgctcgc cgcccagcga tagcagttct tgcaaggaag 9960
caaagttttt caacggtttg agaccgtccg ccgtaggcat gcttttgagc gtttgaccaa 10020
gcagttccag gcggtcccac agctcggtca cctgctctac ggcatctcga tccagcatat 10080
ctcctcgttt cgcgggttgg ggcggctttc gctgtacggc agtagtcggt gctcgtccag 10140
acgggccagg gtcatgtctt tccacgggcg cagggtcctc gtcagcgtag tctgggtcac 10200
ggtgaagggg tgcgctccgg gctgcgcgct ggccagggtg cgcttgaggc tggtcctgct 10260
ggtgctgaag cgctgccggt cttcgccctg cgcgtcggcc aggtagcatt tgaccatggt 10320
gtcatagtcc agcccctccg cggcgtggcc cttggcgcgc agcttgccct tggaggaggc 10380
gccgcacgag gggcagtgca gacttttgag ggcgtagagc ttgggcgcga gaaataccga 10440
ttccggggag taggcatccg cgccgcaggc cccgcagacg gtctcgcatt ccacgagcca 10500
ggtgagctct ggccgttcgg ggtcaaaaac caggtttccc ccatgctttt tgatgcgttt 10560
cttacctctg gtttccatga gccggtgtcc acgctcggtg acgaaaaggc tgtccgtgtc 10620
cccgtataca gacttgagag gcctgtcctc gaccgatgcc cttgagagcc ttcaacccag 10680
tcagctcctt ccggtgggcg cggggcatga ctatcgtcgc cgcacttatg actgtcttct 10740
ttatcatgca actcgtagga caggtgccgg cagcgctctg ggtcattttc ggcgaggacc 10800
gctttcgctg gagcgcgacg atgatcggcc tgtcgcttgc ggtattcgga atcttgcacg 10860
ccctcgctca agccttcgtc actggtcccg ccaccaaacg tttcggcgag aagcaggcca 10920
ttatcgccgg catggcggcc gacgcgctgg gctacgtctt gctggcgttc gcgacgcgag 10980
gctggatggc cttccccatt atgattcttc tcgcttccgg cggcatcggg atgcccgcgt 11040
tgcaggccat gctgtccagg caggtagatg acgaccatca gggacagctt caaggccagc 11100
aaaaggccag gaaccgtaaa aaggccgcgt tgctggcgtt tttccatagg ctccgccccc 11160
ctgacgagca tcacaaaaat cgacgctcaa gtcagaggtg gcgaaacccg acaggactat 11220
aaagatacca ggcgtttccc cctggaagct ccctcgtgcg ctctcctgtt ccgaccctgc 11280
cgcttaccgg atacctgtcc gcctttctcc cttcgggaag cgtggcgctt tctcatagct 11340
cacgctgtag gtatctcagt tcggtgtagg tcgttcgctc caagctgggc tgtgtgcacg 11400
aaccccccgt tcagcccgac cgctgcgcct tatccggtaa ctatcgtctt gagtccaacc 11460
cggtaagaca cgacttatcg ccactggcag cagccactgg taacaggatt agcagagcga 11520
ggtatgtagg cggtgctaca gagttcttga agtggtggcc taactacggc tacactagaa 11580
ggacagtatt tggtatctgc gctctgctga agccagttac cttcggaaaa agagttggta 11640
gctcttgatc cggcaaacaa accaccgctg gtagcggtgg tttttttgtt tgcaagcagc 11700
agattacgcg cagaaaaaaa ggatctcaag aagatccttt gatcttttct acggggtctg 11760
acgctcagtg gaacgaaaac tcacgttaag ggattttggt catgagatta tcaaaaagga 11820
tcttcaccta gatcctttta aattaaaaat gaagttttaa atcaatctaa agtatatatg 11880
agtaaacttg gtctgacagt taccaatgct taatcagtga ggcacctatc tcagcgatct 11940
gtctatttcg ttcatccata gttgcctgac tccccgtcgt gtagataact acgatacggg 12000
agggcttacc atctggcccc agtgctgcaa tgataccgcg agacccacgc tcaccggctc 12060
cagatttatc agcaataaac cagccagccg gaagggccga gcgcagaagt ggtcctgcaa 12120
ctttatccgc ctccatccag tctattaatt gttgccggga agctagagta agtagttcgc 12180
cagttaatag tttgcgcaac gttgttgcca ttgctgcagg catcgtggtg tcacgctcgt 12240
cgtttggtat ggcttcattc agctccggtt cccaacgatc aaggcgagtt acatgatccc 12300
ccatgttgtg caaaaaagcg gttagctcct tcggtcctcc gatcgttgtc agaagtaagt 12360
tggccgcagt gttatcactc atggttatgg cagcactgca taattctctt actgtcatgc 12420
catccgtaag atgcttttct gtgactggtg agtactcaac caagtcattc tgagaatagt 12480
gtatgcggcg accgagttgc tcttgcccgg cgtcaacacg ggataatacc gcgccacata 12540
gcagaacttt aaaagtgctc atcattggaa aacgttcttc ggggcgaaaa ctctcaagga 12600
tcttaccgct gttgagatcc agttcgatgt aacccactcg tgcacccaac tgatcttcag 12660
catcttttac tttcaccagc gtttctgggt gagcaaaaac aggaaggcaa aatgccgcaa 12720
aaaagggaat aagggcgaca cggaaatgtt gaatactcat actcttcctt tttcaatatt 12780
attgaagcat ttatcagggt tattgtctca tgagcggata catatttgaa tgtatttaga 12840
aaaa 12844
<210> 10
<211> 300
<212> DNA
<213> Artificial Sequence
<220>
<223> Synthetic CD95-ADAM8 reporter
<400> 10
gctagcgcca ccatgattag ccctttcctc gtgctcgcca ttggcacatg cctcaccaat 60
agcctcgtgc ctgagaaaga gaaagacgga ggcggaggct ccggcggagg cggaagcgga 120
ggcggaggct ccgagtccct gaaactgagg agaagggtgc atgagacaga caaaaactgt 180
agatccggca caccccctca gaccggcctg gagaaaccca caggcacagg ccaaagaaaa 240
cagggagccg gagcccctac cgctcccgga cccggaggct cccccggagg ctaaatcgat 300
300
<210> 11
<211> 93
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthetic CD95-ADAM8 reporter
<400> 11
Met Ile Ser Pro Phe Leu Val Leu Ala Ile Gly Thr Cys Leu Thr Asn
1 5 10 15
Ser Leu Val Pro Glu Lys Glu Lys Asp Gly Gly Gly Gly Ser Gly Gly
20 25 30
Gly Gly Ser Gly Gly Gly Gly Ser Glu Ser Leu Lys Leu Arg Arg Arg
35 40 45
Val His Glu Thr Asp Lys Asn Cys Arg Ser Gly Thr Pro Pro Gln Thr
50 55 60
Gly Leu Glu Lys Pro Thr Gly Thr Gly Gln Arg Lys Gln Gly Ala Gly
65 70 75 80
Ala Pro Thr Ala Pro Gly Pro Gly Gly Ser Pro Gly Gly
85 90
<210> 12
<211> 339
<212> DNA
<213> Artificial Sequence
<220>
<223> Synthetic CD40-CD3 reporter
<400> 12
gctagcgcca ccatgattag ccctttcctc gtgctcgcca ttggcacatg cctcaccaat 60
agcctcgtgc ctggcggagg cggaagcgga ggcggaggct ccggcggagg cggaagctgt 120
cagcctgtga cacaggagga cggaaaggaa agcaggatct ccgtgcaaga gaggcagcct 180
gcccctaccc ctagcaatgg ctcccccaaa gacggacccg aaatccctcc cacaggcgga 240
aaggctaagg ccaagcccgt gacaagagga gccggagcca ggagcggaac ccctccccaa 300
accggactgg aaaagcctac cggaaccgga tgaatcgat 339
<210> 13
<211> 106
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthetic CD40-CD3 reporter
<400> 13
Met Ile Ser Pro Phe Leu Val Leu Ala Ile Gly Thr Cys Leu Thr Asn
1 5 10 15
Ser Leu Val Pro Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
20 25 30
Gly Gly Ser Cys Gln Pro Val Thr Gln Glu Asp Gly Lys Glu Ser Arg
35 40 45
Ile Ser Val Gln Glu Arg Gln Pro Ala Pro Thr Pro Ser Asn Gly Ser
50 55 60
Pro Lys Asp Gly Pro Glu Ile Pro Pro Thr Gly Gly Lys Ala Lys Ala
65 70 75 80
Lys Pro Val Thr Arg Gly Ala Gly Ala Arg Ser Gly Thr Pro Pro Gln
85 90 95
Thr Gly Leu Glu Lys Pro Thr Gly Thr Gly
100 105
<210> 14
<211> 1692
<212> DNA
<213> Artificial Sequence
<220>
<223> Synthetic alkaline phosphatase - c terminal
<400> 14
gctagcgcca ccatgattag ccctttcctc gtgctcgcca ttggcacatg cctcaccaat 60
agcctcgtgc ctgagaaaga gaaagaccct aagtattgga gggaccaagc ccaagagaca 120
ctgaaatacg ctctggaact gcaaaagctc aacacaaacg tcgccaaaaa cgtcatcatg 180
ttcctcggcg atggcatggg cgtcagcaca gtgacagccg ctagaatcct gaaaggccaa 240
ctgcatcaca atcccggaga ggaaaccagg ctggaaatgg ataagtttcc ctttgtggct 300
ctgtccaaga catacaatac caatgcccaa gtgcctgact ccgccggaac cgctaccgcc 360
tacctgtgcg gagtgaaagc caatgaggga accgtcggcg tcagcgctgc cacagagagg 420
agcagatgca ataccacaca gggaaacgaa gtgacaagca ttctgaggtg ggctaaggat 480
gccggaaagt ccgtgggaat cgtcaccaca accagggtga atcacgctac ccctagcgct 540
gcctatgccc atagcgctga cagggactgg tactccgaca atgagatgcc ccctgaggct 600
ctgtcccagg gatgcaaaga cattgcctat cagctcatgc acaacattag agacatcgac 660
gtgattatgg gaggcggaag aaaatatatg taccctaaga ataagacaga cgtggagtat 720
gagtccgacg aaaaggctag aggaaccagg ctggatggcc tcgacctcgt ggatacctgg 780
aagtccttca aacccaggta caaacactcc cactttatct ggaacaggac cgaactgctg 840
accctggacc ctcacaacgt cgattacctc ctgggactgt ttgagcctgg cgatatgcaa 900
tacgaactga atagaaataa cgtcaccgat ccctccctgt ccgagatggt ggtcgtggct 960
atccaaatcc tcagaaaaaa ccctaaggga ttctttctgc tcgtggaagg cggaagaatt 1020
gaccacggcc atcacgaagg caaagccaag caagctctcc acgaggctgt ggaaatggat 1080
agagctatcg gacaggctgg ctccctgaca agctccgagg ataccctcac cgtcgtgaca 1140
gccgatcact cccacgtttt tacattcgga ggctataccc ctagaggaaa ctccatcttt 1200
ggcctcgccc ctatgctgtc cgataccgat aagaaaccct ttaccgctat cctctacgga 1260
aacggacccg gatacaaagt ggtcggcgga gagagggaga atgtgagcat ggtggactat 1320
gcccataaca attaccaagc ccaaagcgct gtgcccctga gacacgaaac ccacggcgga 1380
gaggatgtgg ctgtgtttag caaaggccct atggcccacc tgttgcatgg cgtccacgaa 1440
cagaattacg tcccccatgt gatggcctat gccgcttgca ttggcgctaa cctcggccat 1500
tgcgctcccg ccagctccgc cggaagcctc gccgctggcc ctctgctcct ggctctggct 1560
ctgtatcccc tgagcgtcct gtttggcgga ggcggaagcg gaggcggagg ctccggcgga 1620
ggcggaagct gtcagcctgt gacacaggag gacggaaagg aaagcaggat ctccgtgcaa 1680
gagtaaatcg at 1692
<210> 15
<211> 557
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthetic alkaline phosphatase - c terminal CD40
<400> 15
Met Ile Ser Pro Phe Leu Val Leu Ala Ile Gly Thr Cys Leu Thr Asn
1 5 10 15
Ser Leu Val Pro Glu Lys Glu Lys Asp Pro Lys Tyr Trp Arg Asp Gln
20 25 30
Ala Gln Glu Thr Leu Lys Tyr Ala Leu Glu Leu Gln Lys Leu Asn Thr
35 40 45
Asn Val Ala Lys Asn Val Ile Met Phe Leu Gly Asp Gly Met Gly Val
50 55 60
Ser Thr Val Thr Ala Ala Arg Ile Leu Lys Gly Gln Leu His His Asn
65 70 75 80
Pro Gly Glu Glu Thr Arg Leu Glu Met Asp Lys Phe Pro Phe Val Ala
85 90 95
Leu Ser Lys Thr Tyr Asn Thr Asn Ala Gln Val Pro Asp Ser Ala Gly
100 105 110
Thr Ala Thr Ala Tyr Leu Cys Gly Val Lys Ala Asn Glu Gly Thr Val
115 120 125
Gly Val Ser Ala Ala Thr Glu Arg Ser Arg Cys Asn Thr Thr Gln Gly
130 135 140
Asn Glu Val Thr Ser Ile Leu Arg Trp Ala Lys Asp Ala Gly Lys Ser
145 150 155 160
Val Gly Ile Val Thr Thr Thr Arg Val Asn His Ala Thr Pro Ser Ala
165 170 175
Ala Tyr Ala His Ser Ala Asp Arg Asp Trp Tyr Ser Asp Asn Glu Met
180 185 190
Pro Pro Glu Ala Leu Ser Gln Gly Cys Lys Asp Ile Ala Tyr Gln Leu
195 200 205
Met His Asn Ile Arg Asp Ile Asp Val Ile Met Gly Gly Gly Arg Lys
210 215 220
Tyr Met Tyr Pro Lys Asn Lys Thr Asp Val Glu Tyr Glu Ser Asp Glu
225 230 235 240
Lys Ala Arg Gly Thr Arg Leu Asp Gly Leu Asp Leu Val Asp Thr Trp
245 250 255
Lys Ser Phe Lys Pro Arg Tyr Lys His Ser His Phe Ile Trp Asn Arg
260 265 270
Thr Glu Leu Leu Thr Leu Asp Pro His Asn Val Asp Tyr Leu Leu Gly
275 280 285
Leu Phe Glu Pro Gly Asp Met Gln Tyr Glu Leu Asn Arg Asn Asn Val
290 295 300
Thr Asp Pro Ser Leu Ser Glu Met Val Val Val Ala Ile Gln Ile Leu
305 310 315 320
Arg Lys Asn Pro Lys Gly Phe Phe Leu Leu Val Glu Gly Gly Arg Ile
325 330 335
Asp His Gly His His Glu Gly Lys Ala Lys Gln Ala Leu His Glu Ala
340 345 350
Val Glu Met Asp Arg Ala Ile Gly Gln Ala Gly Ser Leu Thr Ser Ser
355 360 365
Glu Asp Thr Leu Thr Val Val Thr Ala Asp His Ser His Val Phe Thr
370 375 380
Phe Gly Gly Tyr Thr Pro Arg Gly Asn Ser Ile Phe Gly Leu Ala Pro
385 390 395 400
Met Leu Ser Asp Thr Asp Lys Lys Pro Phe Thr Ala Ile Leu Tyr Gly
405 410 415
Asn Gly Pro Gly Tyr Lys Val Val Gly Gly Glu Arg Glu Asn Val Ser
420 425 430
Met Val Asp Tyr Ala His Asn Asn Tyr Gln Ala Gln Ser Ala Val Pro
435 440 445
Leu Arg His Glu Thr His Gly Gly Glu Asp Val Ala Val Phe Ser Lys
450 455 460
Gly Pro Met Ala His Leu Leu His Gly Val His Glu Gln Asn Tyr Val
465 470 475 480
Pro His Val Met Ala Tyr Ala Ala Cys Ile Gly Ala Asn Leu Gly His
485 490 495
Cys Ala Pro Ala Ser Ser Ala Gly Ser Leu Ala Ala Gly Pro Leu Leu
500 505 510
Leu Ala Leu Ala Leu Tyr Pro Leu Ser Val Leu Phe Gly Gly Gly Gly
515 520 525
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Cys Gln Pro Val Thr
530 535 540
Gln Glu Asp Gly Lys Glu Ser Arg Ile Ser Val Gln Glu
545 550 555
<210> 16
<211> 354
<212> DNA
<213> Artificial Sequence
<220>
<223> Synthetic CD28-CD3 reporter
<400> 16
gctagcgcca ccatgattag ccctttcctc gtgctcgcca ttggcacatg cctcaccaat 60
agcctcgtgc ctagatccga cgtgaactcc agaacaggcc ctagcggagc cacaccccct 120
agcggaaacc cttacacaat cacaggctcc cagcaactgc aagtgtatag caaaaccgga 180
ttcaatcccg ctcccacacc ctccaacgga agccctaagg atggccctga gattccccct 240
accggaggct ccggcggagg cggaagcgga ggcggaggct ccaaggctaa ggccaagccc 300
gtgacaagag gagccggagc cggacccgga ggctcccccg gaggctaaat cgat 354
<210> 17
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthetic CD28-CD3 reporter
<400> 17
Met Ile Ser Pro Phe Leu Val Leu Ala Ile Gly Thr Cys Leu Thr Asn
1 5 10 15
Ser Leu Val Pro Arg Ser Asp Val Asn Ser Arg Thr Gly Pro Ser Gly
20 25 30
Ala Thr Pro Pro Ser Gly Asn Pro Tyr Thr Ile Thr Gly Ser Gln Gln
35 40 45
Leu Gln Val Tyr Ser Lys Thr Gly Phe Asn Pro Ala Pro Thr Pro Ser
50 55 60
Asn Gly Ser Pro Lys Asp Gly Pro Glu Ile Pro Pro Thr Gly Gly Ser
65 70 75 80
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Lys Ala Lys Ala Lys Pro
85 90 95
Val Thr Arg Gly Ala Gly Ala Gly Pro Gly Gly Ser Pro Gly Gly
100 105 110
<210> 18
<211> 375
<212> DNA
<213> Artificial Sequence
<220>
<223> Synthetic CD28-CD40 reporter
<400> 18
gctagcgcca ccatgattag ccctttcctc gtgctcgcca ttggcacatg cctcaccaat 60
agcctcgtgc ctagatccga cgtgaactcc agaacaggcc ctagcggagc cacaccccct 120
agcggaaacc cttacacaat cacaggctcc cagcaactgc aagtgtatag caaaaccgga 180
ttcaatcccg ctcccacacc ctccaacgga agccctaagg atggccctga gattccccct 240
accggaggct ccggcggagg cggaagcgga ggcggaggct cctgccaacc cgtcacccag 300
gaggacggca aagagtccag aattagcgtc caggaaagac aaggccctgg cggaagccct 360
ggcggatgaa tcgat 375
<210> 19
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthetic CD28-CD40 reporter
<400> 19
Met Ile Ser Pro Phe Leu Val Leu Ala Ile Gly Thr Cys Leu Thr Asn
1 5 10 15
Ser Leu Val Pro Arg Ser Asp Val Asn Ser Arg Thr Gly Pro Ser Gly
20 25 30
Ala Thr Pro Pro Ser Gly Asn Pro Tyr Thr Ile Thr Gly Ser Gln Gln
35 40 45
Leu Gln Val Tyr Ser Lys Thr Gly Phe Asn Pro Ala Pro Thr Pro Ser
50 55 60
Asn Gly Ser Pro Lys Asp Gly Pro Glu Ile Pro Pro Thr Gly Gly Ser
65 70 75 80
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Cys Gln Pro Val Thr Gln
85 90 95
Glu Asp Gly Lys Glu Ser Arg Ile Ser Val Gln Glu Arg Gln Gly Pro
100 105 110
Gly Gly Ser Pro Gly Gly
115
<210> 20
<211> 1737
<212> DNA
<213> Artificial Sequence
<220>
<223> Synthetic alkaline phosphatase - amino terminal CD40
<400> 20
gctagcgcca ccatgattag ccctttcctc gtgctcgcca ttggcacatg cctcaccaat 60
agcctcgtgc cttgccaacc cgtcacccag gaggacggca aagagtccag aattagcgtc 120
caggaaggcg gaggcggaag cggaggcgga ggctccggcg gaggcggaag cgaaaaggaa 180
aaggacccca aatactggag agatcaggct caggaaaccc tcaagtatgc cctggaactc 240
cagaaactga ataccaatgt ggctaagaat gtgattatgt ttctgggcga cggcatggga 300
gtgtccaccg tcaccgctgc cagaatcctg aagggacagc tccaccacaa ccccggcgag 360
gagacaagac tggagatgga caaattccct ttcgtcgccc tgtccaaaac ctataacaca 420
aacgctcagg tccccgatag cgctggcaca gccacagcct atctgtgtgg cgtcaaggct 480
aacgaaggca cagtgggagt gtccgccgct accgaaagat ccagatgtaa cacaacccaa 540
ggcaatgagg tcacctccat cctcagatgg gccaaagacg ctggcaaaag cgtcggcatt 600
gtgacaacca caagagtcaa ccatgccaca ccctccgccg cttacgctca ctccgccgat 660
agagattggt atagcgataa cgaaatgcct cccgaagccc tgagccaagg ctgtaaggac 720
atcgcttacc aactgatgca caatatcagg gacattgacg ttatcatggg cggaggcagg 780
aagtatatgt atcccaaaaa caaaaccgat gtggaatacg aaagcgatga gaaagccagg 840
ggcacaagac tcgacggact ggatctggtg gatacatgga agtccttcaa gcctagatat 900
aagcatagcc atttcatttg gaatagaaca gagcttctga cactggaccc ccataacgtg 960
gactatctgc tcggcctgtt cgagcccgga gacatgcagt atgagctgaa caggaacaat 1020
gtgacagacc ctagcctgag cgaaatggtc gtggtcgcca ttcagattct gaggaagaat 1080
cccaaaggct ttttcctcct ggtcgaggga ggcagaatcg accacggcca ccacgaggga 1140
aaggccaagc aagccctcca cgaagccgtc gagatggaca gggccattgg ccaagccgga 1200
agcctcacct ccagcgagga tacactgaca gtggtcaccg ctgaccatag ccatgtgttt 1260
acctttggcg gatacacacc caggggcaat agcattttcg gactggctcc catgctgtcc 1320
gacacagaca aaaagccttt cacagccatt ctgtatggca atggccctgg ctataaggtc 1380
gtgggaggcg aaagagaaaa cgtcagcatg gtggattacg ctcacaataa ctatcaggct 1440
cagtccgccg tccccctcag acatgagaca cacggaggcg aggacgtggc cgtgttctcc 1500
aagggaccta tggcccatct gctccacggc gtccatgagc aaaactatgt gcctcacgtc 1560
atggcttacg ctgcctgtat cggagccaat ctgggacact gtgcccctgc ctccagcgct 1620
ggctccctgg ctgccggacc cctcctgctc gccctcgccc tctaccctct gtccgtgctg 1680
ttcggaggcg gaggctccgg cggaggcgga agcggaggcg gaggctcctg aatcgat 1737
<210> 21
<211> 572
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthetic alkaline phosphatase - amino terminal CD40
<400> 21
Met Ile Ser Pro Phe Leu Val Leu Ala Ile Gly Thr Cys Leu Thr Asn
1 5 10 15
Ser Leu Val Pro Cys Gln Pro Val Thr Gln Glu Asp Gly Lys Glu Ser
20 25 30
Arg Ile Ser Val Gln Glu Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
35 40 45
Gly Gly Gly Gly Ser Glu Lys Glu Lys Asp Pro Lys Tyr Trp Arg Asp
50 55 60
Gln Ala Gln Glu Thr Leu Lys Tyr Ala Leu Glu Leu Gln Lys Leu Asn
65 70 75 80
Thr Asn Val Ala Lys Asn Val Ile Met Phe Leu Gly Asp Gly Met Gly
85 90 95
Val Ser Thr Val Thr Ala Ala Arg Ile Leu Lys Gly Gln Leu His His
100 105 110
Asn Pro Gly Glu Glu Thr Arg Leu Glu Met Asp Lys Phe Pro Phe Val
115 120 125
Ala Leu Ser Lys Thr Tyr Asn Thr Asn Ala Gln Val Pro Asp Ser Ala
130 135 140
Gly Thr Ala Thr Ala Tyr Leu Cys Gly Val Lys Ala Asn Glu Gly Thr
145 150 155 160
Val Gly Val Ser Ala Ala Thr Glu Arg Ser Arg Cys Asn Thr Thr Gln
165 170 175
Gly Asn Glu Val Thr Ser Ile Leu Arg Trp Ala Lys Asp Ala Gly Lys
180 185 190
Ser Val Gly Ile Val Thr Thr Thr Arg Val Asn His Ala Thr Pro Ser
195 200 205
Ala Ala Tyr Ala His Ser Ala Asp Arg Asp Trp Tyr Ser Asp Asn Glu
210 215 220
Met Pro Pro Glu Ala Leu Ser Gln Gly Cys Lys Asp Ile Ala Tyr Gln
225 230 235 240
Leu Met His Asn Ile Arg Asp Ile Asp Val Ile Met Gly Gly Gly Arg
245 250 255
Lys Tyr Met Tyr Pro Lys Asn Lys Thr Asp Val Glu Tyr Glu Ser Asp
260 265 270
Glu Lys Ala Arg Gly Thr Arg Leu Asp Gly Leu Asp Leu Val Asp Thr
275 280 285
Trp Lys Ser Phe Lys Pro Arg Tyr Lys His Ser His Phe Ile Trp Asn
290 295 300
Arg Thr Glu Leu Leu Thr Leu Asp Pro His Asn Val Asp Tyr Leu Leu
305 310 315 320
Gly Leu Phe Glu Pro Gly Asp Met Gln Tyr Glu Leu Asn Arg Asn Asn
325 330 335
Val Thr Asp Pro Ser Leu Ser Glu Met Val Val Val Ala Ile Gln Ile
340 345 350
Leu Arg Lys Asn Pro Lys Gly Phe Phe Leu Leu Val Glu Gly Gly Arg
355 360 365
Ile Asp His Gly His His Glu Gly Lys Ala Lys Gln Ala Leu His Glu
370 375 380
Ala Val Glu Met Asp Arg Ala Ile Gly Gln Ala Gly Ser Leu Thr Ser
385 390 395 400
Ser Glu Asp Thr Leu Thr Val Val Thr Ala Asp His Ser His Val Phe
405 410 415
Thr Phe Gly Gly Tyr Thr Pro Arg Gly Asn Ser Ile Phe Gly Leu Ala
420 425 430
Pro Met Leu Ser Asp Thr Asp Lys Lys Pro Phe Thr Ala Ile Leu Tyr
435 440 445
Gly Asn Gly Pro Gly Tyr Lys Val Val Gly Gly Glu Arg Glu Asn Val
450 455 460
Ser Met Val Asp Tyr Ala His Asn Asn Tyr Gln Ala Gln Ser Ala Val
465 470 475 480
Pro Leu Arg His Glu Thr His Gly Gly Glu Asp Val Ala Val Phe Ser
485 490 495
Lys Gly Pro Met Ala His Leu Leu His Gly Val His Glu Gln Asn Tyr
500 505 510
Val Pro His Val Met Ala Tyr Ala Ala Cys Ile Gly Ala Asn Leu Gly
515 520 525
His Cys Ala Pro Ala Ser Ser Ala Gly Ser Leu Ala Ala Gly Pro Leu
530 535 540
Leu Leu Ala Leu Ala Leu Tyr Pro Leu Ser Val Leu Phe Gly Gly Gly
545 550 555 560
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
565 570
<210> 22
<211> 1677
<212> DNA
<213> Artificial Sequence
<220>
<223> Synthetic alkaline phosphatase - c terminal CD28
<400> 22
gctagcgcca ccatgattag ccctttcctc gtgctcgcca ttggcacatg cctcaccaat 60
agcctcgtgc ctgagaaaga gaaagaccct aagtattgga gggaccaagc ccaagagaca 120
ctgaaatacg ctctggaact gcaaaagctc aacacaaacg tcgccaaaaa cgtcatcatg 180
ttcctcggcg atggcatggg cgtcagcaca gtgacagccg ctagaatcct gaaaggccaa 240
ctgcatcaca atcccggaga ggaaaccagg ctggaaatgg ataagtttcc ctttgtggct 300
ctgtccaaga catacaatac caatgcccaa gtgcctgact ccgccggaac cgctaccgcc 360
tacctgtgcg gagtgaaagc caatgaggga accgtcggcg tcagcgctgc cacagagagg 420
agcagatgca ataccacaca gggaaacgaa gtgacaagca ttctgaggtg ggctaaggat 480
gccggaaagt ccgtgggaat cgtcaccaca accagggtga atcacgctac ccctagcgct 540
gcctatgccc atagcgctga cagggactgg tactccgaca atgagatgcc ccctgaggct 600
ctgtcccagg gatgcaaaga cattgcctat cagctcatgc acaacattag agacatcgac 660
gtgattatgg gaggcggaag aaaatatatg taccctaaga ataagacaga cgtggagtat 720
gagtccgacg aaaaggctag aggaaccagg ctggatggcc tcgacctcgt ggatacctgg 780
aagtccttca aacccaggta caaacactcc cactttatct ggaacaggac cgaactgctg 840
accctggacc ctcacaacgt cgattacctc ctgggactgt ttgagcctgg cgatatgcaa 900
tacgaactga atagaaataa cgtcaccgat ccctccctgt ccgagatggt ggtcgtggct 960
atccaaatcc tcagaaaaaa ccctaaggga ttctttctgc tcgtggaagg cggaagaatt 1020
gaccacggcc atcacgaagg caaagccaag caagctctcc acgaggctgt ggaaatggat 1080
agagctatcg gacaggctgg ctccctgaca agctccgagg ataccctcac cgtcgtgaca 1140
gccgatcact cccacgtttt tacattcgga ggctataccc ctagaggaaa ctccatcttt 1200
ggcctcgccc ctatgctgtc cgataccgat aagaaaccct ttaccgctat cctctacgga 1260
aacggacccg gatacaaagt ggtcggcgga gagagggaga atgtgagcat ggtggactat 1320
gcccataaca attaccaagc ccaaagcgct gtgcccctga gacacgaaac ccacggcgga 1380
gaggatgtgg ctgtgtttag caaaggccct atggcccacc tgttgcatgg cgtccacgaa 1440
cagaattacg tcccccatgt gatggcctat gccgcttgca ttggcgctaa cctcggccat 1500
tgcgctcccg ccagctccgc cggaagcctc gccgctggcc ctctgctcct ggctctggct 1560
ctgtatcccc tgagcgtcct gtttggcgga ggcggaagcg gaggcggagg ctccggcgga 1620
ggcggaagct cccagcaact gcaagtgtat agcaaaaccg gattcaactg aatcgat 1677
<210> 23
<211> 552
<212> PRT
<213> Artificial Sequence
<220>
<223> Synthetic alkaline phosphatase - c terminal CD28
<400> 23
Met Ile Ser Pro Phe Leu Val Leu Ala Ile Gly Thr Cys Leu Thr Asn
1 5 10 15
Ser Leu Val Pro Glu Lys Glu Lys Asp Pro Lys Tyr Trp Arg Asp Gln
20 25 30
Ala Gln Glu Thr Leu Lys Tyr Ala Leu Glu Leu Gln Lys Leu Asn Thr
35 40 45
Asn Val Ala Lys Asn Val Ile Met Phe Leu Gly Asp Gly Met Gly Val
50 55 60
Ser Thr Val Thr Ala Ala Arg Ile Leu Lys Gly Gln Leu His His Asn
65 70 75 80
Pro Gly Glu Glu Thr Arg Leu Glu Met Asp Lys Phe Pro Phe Val Ala
85 90 95
Leu Ser Lys Thr Tyr Asn Thr Asn Ala Gln Val Pro Asp Ser Ala Gly
100 105 110
Thr Ala Thr Ala Tyr Leu Cys Gly Val Lys Ala Asn Glu Gly Thr Val
115 120 125
Gly Val Ser Ala Ala Thr Glu Arg Ser Arg Cys Asn Thr Thr Gln Gly
130 135 140
Asn Glu Val Thr Ser Ile Leu Arg Trp Ala Lys Asp Ala Gly Lys Ser
145 150 155 160
Val Gly Ile Val Thr Thr Thr Arg Val Asn His Ala Thr Pro Ser Ala
165 170 175
Ala Tyr Ala His Ser Ala Asp Arg Asp Trp Tyr Ser Asp Asn Glu Met
180 185 190
Pro Pro Glu Ala Leu Ser Gln Gly Cys Lys Asp Ile Ala Tyr Gln Leu
195 200 205
Met His Asn Ile Arg Asp Ile Asp Val Ile Met Gly Gly Gly Arg Lys
210 215 220
Tyr Met Tyr Pro Lys Asn Lys Thr Asp Val Glu Tyr Glu Ser Asp Glu
225 230 235 240
Lys Ala Arg Gly Thr Arg Leu Asp Gly Leu Asp Leu Val Asp Thr Trp
245 250 255
Lys Ser Phe Lys Pro Arg Tyr Lys His Ser His Phe Ile Trp Asn Arg
260 265 270
Thr Glu Leu Leu Thr Leu Asp Pro His Asn Val Asp Tyr Leu Leu Gly
275 280 285
Leu Phe Glu Pro Gly Asp Met Gln Tyr Glu Leu Asn Arg Asn Asn Val
290 295 300
Thr Asp Pro Ser Leu Ser Glu Met Val Val Val Ala Ile Gln Ile Leu
305 310 315 320
Arg Lys Asn Pro Lys Gly Phe Phe Leu Leu Val Glu Gly Gly Arg Ile
325 330 335
Asp His Gly His His Glu Gly Lys Ala Lys Gln Ala Leu His Glu Ala
340 345 350
Val Glu Met Asp Arg Ala Ile Gly Gln Ala Gly Ser Leu Thr Ser Ser
355 360 365
Glu Asp Thr Leu Thr Val Val Thr Ala Asp His Ser His Val Phe Thr
370 375 380
Phe Gly Gly Tyr Thr Pro Arg Gly Asn Ser Ile Phe Gly Leu Ala Pro
385 390 395 400
Met Leu Ser Asp Thr Asp Lys Lys Pro Phe Thr Ala Ile Leu Tyr Gly
405 410 415
Asn Gly Pro Gly Tyr Lys Val Val Gly Gly Glu Arg Glu Asn Val Ser
420 425 430
Met Val Asp Tyr Ala His Asn Asn Tyr Gln Ala Gln Ser Ala Val Pro
435 440 445
Leu Arg His Glu Thr His Gly Gly Glu Asp Val Ala Val Phe Ser Lys
450 455 460
Gly Pro Met Ala His Leu Leu His Gly Val His Glu Gln Asn Tyr Val
465 470 475 480
Pro His Val Met Ala Tyr Ala Ala Cys Ile Gly Ala Asn Leu Gly His
485 490 495
Cys Ala Pro Ala Ser Ser Ala Gly Ser Leu Ala Ala Gly Pro Leu Leu
500 505 510
Leu Ala Leu Ala Leu Tyr Pro Leu Ser Val Leu Phe Gly Gly Gly Gly
515 520 525
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ser Gln Gln Leu Gln
530 535 540
Val Tyr Ser Lys Thr Gly Phe Asn
545 550
Claims (170)
- (a) 폴리뉴클레오티드를 개체의 세포에 도입하여 변형된 세포를 생산하는 단계로서, 여기서 상기 폴리뉴클레오티드는 유전자 스위치를 코딩하며, 또한 상기 폴리뉴클레오티드는 (1) 진단 스위치 프로모터에 작동가능하게 연결된 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 상기 프로모터의 활성은 상기 개체의 질병 또는 장애 기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인 단계;
(b) 상기 변형된 세포에 리간드를 투여하는 단계; 및
(c) 리포터 유전자 발현을 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현이 상기 개체가 상기 질병 또는 장애를 가짐을 지시하는 것인, 상기 개체에서 질병 또는 장애를 진단하는 방법.
- 제1항에 있어서, 상기 방법은 생체 외(ex vivo)에서 상기 개체로부터 분리된 세포에서 수행되는 것인 방법.
- 제1항에 있어서, 상기 폴리뉴클레오티드는 상기 개체로부터 분리된 세포에 도입되어 변형된 세포를 생산하고, 상기 변형된 세포는 상기 개체로 재도입되는 것인 방법.
- 제1항에 있어서, 상기 방법은 생체 내(in vivo)에서 수행되는 것인 방법.
- 제1항에 있어서, 상기 유전자 스위치는 엑디손 수용체(EcR)-기반 유전자 스위치인 방법.
- 제5항에 있어서, 상기 리간드는 상기 EcR 리간드 결합 도메인에 결합하는 것인 방법.
- 제6항에 있어서, 상기 리간드는 디아실하이드라진인 방법.
- 제7항에 있어서, 상기 리간드는 RG- 115819, RG-115830, 및 RG-115932로 이루어진 군으로부터 선택된 것인 방법.
- 제6항에 있어서, 상기 리간드는 아미도케톤 또는 옥사디아졸린인 방법.
- 제1항에 있어서, 상기 유전자 스위치는 제1 진단 스위치 프로모터의 조절 하에 있는 제1 전사 인자 서열 및 제2 진단 스위치 프로모터의 조절 하에 있는 제2 전사 인자 서열을 포함하고, 여기서 상기 제1 전사 인자 서열 및 상기 제2 전사 인자 서열에 의해 코딩되는 단백질들이 상호작용하여 리간드-의존 전사 인자로서 기능하는 단백질 복합체를 형성하는 것인 방법.
- 제10항에 있어서,상기 제1 진단 스위치 프로모터와 상기 제2 진단 스위치 프로모터가 상이한 것인 방법.
- 제10항에 있어서, 상기 제1 진단 스위치 프로모터와 상기 제2 진단 스위치 프로모터가 동일한 것인 방법.
- 제10항에 있어서, 상기 제1 전사 인자 서열은 이형이량체 파트너 및 전사활성화 도메인을 포함하는 단백질을 코딩하는 것인 방법.
- 제10항에 있어서, 상기 제2 전사 인자 서열은 DNA 결합 도메인 및 리간드-결합 도메인을 포함하는 단백질을 코딩하는 것인 방법.
- 제1항에 있어서, 상기 폴리뉴클레오티드 중 하나는 유도 프로모터에 작동가능하게 연결된 치사 폴리펩타이드를 추가로 코딩하는 것인 방법.
- 폴리뉴클레오티드를 개체의 세포에 도입하여 변형된 세포를 생산하는 단계로서, 여기서 상기 폴리뉴클레오티드는 유전자 스위치를 코딩하며, 또한 상기 폴리뉴클레오티드는 (1) 진단 스위치 프로모터에 작동가능하게 연결된 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 상기 프로모터의 활성은 상기 개체의 질병 또는 장애 기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인 단계를 포함하는, 상기 개체에서 질병 또는 장애를 진단하기 위해 변형된 세포를 제조하는 방법.
- (a) 개체의 변형된 세포에 리간드를 투여하는 단계; 및
(b) 리포터 유전자 발현을 탐지하는 단계를 포함하고,
여기서 상기 리포터 유전자의 발현이 상기 개체가 상기 질병 또는 장애를 가짐을 지시하고; 또한
상기 개체의 상기 변형된 세포는 폴리뉴클레오티드를 포함하며, 상기 폴리뉴클레오티드는 유전자 스위치를 코딩하며, 또한 상기 폴리뉴클레오티드는 (1) 진단 스위치 프로모터에 작동가능하게 연결된 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 상기 프로모터의 활성은 상기 개체의 질병 또는 장애 기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인, 상기 개체에서 질병 또는 장애를 진단하는 방법.
- (a) 폴리뉴클레오티드를 비-자가 세포에 도입하여 변형된 세포를 생산하는 단계로서, 여기서 상기 폴리뉴클레오티드는 유전자 스위치를 코딩하며, 또한 상기 폴리뉴클레오티드는 (1) 진단 스위치 프로모터에 작동가능하게 연결된 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 상기 프로모터의 활성은 개체의 질병 또는 장애 기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인 단계;
(b) 상기 개체에 상기 변형된 세포를 도입하는 단계;
(c) 상기 변형된 세포에 리간드를 투여하는 단계; 및
(c) 리포터 유전자 발현을 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현이 상기 개체가 상기 질병 또는 장애를 가짐을 지시하는 것인, 상기 개체에서 질병 또는 장애를 진단하는 방법.
- (a) 폴리뉴클레오티드를 개체의 세포에 도입하여 변형된 세포를 생산하는 단계로서, 여기서 상기 폴리뉴클레오티드는 유전자 스위치를 코딩하며, 또한 상기 폴리뉴클레오티드는 (1) 진단 스위치 프로모터에 작동가능하게 연결된 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 상기 프로모터의 활성은 상기 개체의 질병 또는 장애 기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인 단계;
(b) 상기 변형된 세포에 리간드를 투여하는 단계; 및
(c) 리포터 유전자 발현을 적어도 2회 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨의 변화가 상기 개체에서 상기 질병 또는 장애의 진행을 지시하는 것인, 상기 개체에서 질병 또는 장애의 진행을 모니터하는 방법.
- 제19항에 있어서, 상기 방법은 생체 외에서 상기 개체로부터 분리된 세포에서 수행되는 것인 방법.
- 제19항에 있어서, 상기 폴리뉴클레오티드는 상기 개체로부터 분리된 세포로 도입되어 변형된 세포를 생산하고, 상기 변형된 세포는 상기 개체로 재도입되는 것인 단계.
- 제19항에 있어서, 상기 방법은 생체 내에서 수행되는 것인 방법.
- 제19항에 있어서, 상기 유전자 스위치는 EcR-기반 유전자 스위치인 방법.
- 제23항에 있어서, 상기 리간드는 상기 EcR 리간드 결합 도메인에 결합하는 것인 방법.
- 제24항에 있어서, 상기 리간드는 디아실하이드라진인 방법.
- 제25항에 있어서, 상기 리간드는 RG- 115819, RG-115830, 및 RG-115932로 이루어진 군으로부터 선택된 것인 방법.
- 제24항에 있어서, 상기 리간드는 아미도케톤 또는 옥사디아졸린인 방법.
- 제19항에 있어서, 상기 유전자 스위치는 제1 진단 스위치 프로모터의 조절 하에 있는 제1 전사 인자 서열 및 제2 진단 스위치 프로모터의 조절 하에 있는 제2 전사 인자 서열을 포함하고, 여기서 상기 제1 전사 인자 서열 및 상기 제2 전사 인자 서열에 의해 코딩되는 단백질들이 상호작용하여 리간드-의존 전사 인자로서 기능하는 단백질 복합체를 형성하는 것인 방법.
- 제28항에 있어서,상기 제1 진단 스위치 프로모터와 상기 제2 진단 스위치 프로모터가 상이한 것인 방법.
- 제28항에 있어서, 상기 제1 진단 스위치 프로모터와 상기 제2 진단 스위치 프로모터가 동일한 것인 방법.
- 제28항에 있어서, 상기 제1 전사 인자 서열은 이형이량체 파트너 및 전사활성화 도메인을 포함하는 단백질을 코딩하는 것인 방법.
- 제28항에 있어서, 상기 제2 전사 인자 서열은 DNA 결합 도메인 및 리간드-결합 도메인을 포함하는 단백질을 코딩하는 것인 방법.
- 제19항에 있어서, 상기 폴리뉴클레오티드 중 하나는 유도 프로모터에 작동가능하게 연결된 치사 폴리펩타이드를 추가로 코딩하는 것인 방법.
- 폴리뉴클레오티드를 개체의 세포에 도입하여 변형된 세포를 생산하는 단계로서, 여기서 상기 폴리뉴클레오티드는 유전자 스위치를 코딩하며, 또한 상기 폴리뉴클레오티드는 (1) 진단 스위치 프로모터에 작동가능하게 연결된 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 상기 프로모터의 활성은 상기 개체의 질병 또는 장애기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인 단계를 포함하는, 상기 개체에서 질병 또는 장애의 진행을 모니터하기 위해 변형된 세포를 제조하는 방법.
- (a) 개체의 변형된 세포에 리간드를 투여하는 단계; 및
(b) 리포터 유전자 발현을 적어도 2회 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨의 변화가 상기 개체에서 상기 질병 또는 장애의 진행을 지시하고; 또한
여기서 상기 개체의 상기 변형된 세포는 폴리뉴클레오티드를 포함하고, 상기 폴리뉴클레오티드는 유전자 스위치를 코딩하며, 또한 상기 폴리뉴클레오티드는 (1) 진단 스위치 프로모터에 작동가능하게 연결된 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 상기 프로모터의 활성은 상기 개체의 질병 또는 장애 기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인, 상기 개체에서 질병 또는 장애의 진행을 모니터하는 방법.
- (a) 폴리뉴클레오티드를 비-자가 세포에 도입하여 변형된 세포를 생산하는 단계로서, 여기서 상기 폴리뉴클레오티드는 유전자 스위치를 코딩하며, 또한 상기 폴리뉴클레오티드는 (1) 진단 스위치 프로모터에 작동가능하게 연결된 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 상기 프로모터의 활성은 개체의 질병 또는 장애 기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인 단계;
(b) 상기 개체가 상기 변형된 세포를 도입하는 단계;
(c) 상기 변형된 세포에 리간드를 투여하는 단계; 및
(d) 리포터 유전자 발현을 적어도 2회 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨의 변화가 상기 개체에서 상기 질병 또는 장애의 진행을 지시하는 것인, 상기 개체에서 질병 또는 장애의 진행을 모니터하는 방법.
- (a) 개체에 치료제를 투여하는 단계;
(b) 폴리뉴클레오티드를 상기 개체의 세포에 도입하여 변형된 세포를 생산하는 단계로서, 상기 폴리뉴클레오티드는 유전자 스위치를 코딩하며, 또한 상기 폴리뉴클레오티드는 (1) 진단 스위치 프로모터에 작동가능하게 연결된 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 상기 프로모터의 활성은 상기 개체의 질병 또는 장애 기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인 단계;
(c) 상기 변형된 세포에 리간드를 투여하는 단계; 및
(d) 리포터 유전자 발현을 적어도 2회 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨의 변화가 상기 치료제의 효능을 지시하는 것인, 상기 개체에서 질병 또는 장애에 대한 상기 치료제의 효능을 모니터하는 방법.
- 제37항에 있어서, 상기 단계 (b)는 단계 (a)에 앞서 수행되는 것인 방법.
- 제38항에 있어서, 리포터 유전자 발현의 기준선 레벨은 단계 (a)에 앞서 결정되는 것인 방법.
- 제37항에 있어서, 상기 방법은 생체 외에서 상기 개체로부터 분리된 세포에서 수행되는 것인 방법.
- 제37항에 있어서, 상기 폴리뉴클레오티드는 상기 개체로부터 분리된 세포로 도입되어 변형된 세포를 생산하고, 상기 변형된 세포는 상기 개체에 재도입되는 것인 방법.
- 제37항에 있어서, 상기 방법은 생체 내에서 수행되는 것인 방법.
- 제37항에 있어서, 상기 유전자 스위치는 EcR-기반 유전자 스위치인 방법.
- 제43항에 있어서, 상기 리간드는 상기 EcR 리간드 결합 도메인에 결합하는 것인 방법.
- 제44항에 있어서, 상기 리간드는 디아실하이드라진인 방법.
- 제45항에 있어서, 상기 리간드는 RG- 115819, RG-115830, 및 RG-115932로 이루어진 군으로부터 선택된 것인 방법.
- 제44항에 있어서, 상기 리간드는 아미도케톤 또는 옥사디아졸린인 방법.
- 제37항에 있어서, 상기 유전자 스위치는 제1 진단 스위치 프로모터의 조절 하에 있는 제1 전사 인자 서열 및 제2 진단 스위치 프로모터의 조절 하에 있는 제2 전사 인자 서열을 포함하고, 여기서 상기 제1 전사 인자 서열 및 상기 제2 전사 인자 서열에 의해 코딩되는 단백질들이 상호작용하여 리간드-의존 전사 인자로서 기능하는 단백질 복합체를 형성하는 것인 방법.
- 제48항에 있어서, 상기 제1 진단 스위치 프로모터와 상기 제2 진단 스위치 프로모터가 상이한 것인 방법.
- 제48항에 있어서, 상기 제1 진단 스위치 프로모터와 상기 제2 진단 스위치 프로모터가 동일한 것인 방법.
- 제48항에 있어서, 상기 제1 전사 인자 서열은 이형이량체 파트너 및 전사활성화 도메인을 포함하는 단백질을 코딩하는 것인 방법.
- 제48항에 있어서, 상기 제2 전사 인자 서열은 DNA 결합 도메인 및 리간드-결합 도메인을 포함하는 단백질을 코딩하는 것인 방법.
- 제37항에 있어서, 상기 폴리뉴클레오티드 중 하나는 유도 프로모터에 작동가능하게 연결된 치사 폴리펩타이드를 추가로 코딩하는 것인 방법.
- 폴리뉴클레오티드를 개체의 세포에 도입하여 변형된 세포를 생산하는 단계로서, 여기서 상기 폴리뉴클레오티드는 유전자 스위치를 코딩하며, 또한 상기 폴리뉴클레오티드는 (1) 진단 스위치 프로모터에 작동가능하게 연결된 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 상기 프로모터의 활성은 상기 개체의 질병 또는 장애기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인 단계를 포함하는, 상기 개체에서 질병 또는 장애에 대한 치료제의 효능을 모니터하기 위해 변형된 세포를 제조하는 방법.
- (a) 개체에 치료제를 투여하는 단계;
(b) 상기 개체의 변형된 세포에 리간드를 투여하는 단계; 및
(c) 리포터 유전자 발현을 적어도 2회 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨의 변화가 상기 치료제의 효능을 지시하고;
여기서 상기 개체의 변형된 세포는 폴리뉴클레오티드를 포함하고, 상기 폴리뉴클레오티드는 유전자 스위치를 코딩하며, 또한 상기 폴리뉴클레오티드는 (1) 진단 스위치 프로모터에 작동가능하게 연결된 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 상기 프로모터의 활성은 상기 개체의 질병 또는 장애 기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인, 상기 개체에서 질병 또는 장애에 대한 상기 치료제의 효능을 모니터하는 방법.
- (a) 폴리뉴클레오티드를 비-자가 세포에 도입하여 변형된 세포를 생산하는 단계로서, 상기 폴리뉴클레오티드는 유전자 스위치를 코딩하며, 또한 상기 폴리뉴클레오티드는 (1) 진단 스위치 프로모터에 작동가능하게 연결된 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 상기 프로모터의 활성은 상기 개체의 질병 또는 장애 기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인 단계;
(b) 상기 개체에 상기 변형된 세포를 도입하는 단계;
(c) 상기 변형된 세포에 리간드를 투여하는 단계; 및
(d) 리포터 유전자 발현을 적어도 2회 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨의 변화가 상기 치료제의 효능을 지시하는 것인, 상기 개체에서 질병 또는 장애에 대한 상기 치료제의 효능을 모니터하는 방법.
- (a) 개체에 치료제를 투여하는 단계;
(b) 폴리뉴클레오티드를 상기 개체의 세포에 도입하여 변형된 세포를 생산하는 단계로서, 상기 폴리뉴클레오티드는 유전자 스위치를 코딩하며, 또한 상기 폴리뉴클레오티드는 (1) 진단 스위치 프로모터에 작동가능하게 연결된 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 상기 프로모터의 활성은 독성 조건에 노출되어 있는 세포에서 발견된 인자들에 의해 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인 단계;
(c) 상기 변형된 세포에 리간드를 투여하는 단계; 및
(d) 리포터 유전자 발현을 적어도 2회 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨의 변화가 상기 치료제의 독성을 지시하는 것인, 상기 개체에서 질병 또는 장애에 대한 투여된 치료제의 잠재적 독성을 모니터하는 방법.
- 제57항에 있어서, 상기 단계 (b)는 단계 (a)에 앞서 수행되는 것인 방법.
- 제58항에 있어서, 리포터 유전자 발현의 기준선 레벨은 단계 (a)에 앞서 결정되는 것인 방법.
- 제57항에 있어서, 상기 방법은 생체 외에서 상기 개체로부터 분리된 세포에서 수행되는 것인 방법.
- 제57항에 있어서, 상기 폴리뉴클레오티드는 상기 개체로부터 분리된 세포가 도입되어 변형된 세포를 생산하고, 상기 변형된 세포는 상기 개체가 재도입되는 것인 방법.
- 제57항에 있어서, 상기 방법은 생체 내에서 수행되는 것인 방법.
- 제57항에 있어서, 상기 유전자 스위치는 EcR-기반 유전자 스위치인 방법.
- 제63항에 있어서, 상기 리간드는 상기 EcR 리간드 결합 도메인에 결합하는 것인 방법.
- 제64항에 있어서, 상기 리간드는 디아실하이드라진인 방법.
- 제65항에 있어서, 상기 리간드는 RG- 115819, RG-115830, 및 RG-115932로 이루어진 군으로부터 선택된 것인 방법.
- 제64항에 있어서, 상기 리간드는 아미도케톤 또는 옥사디아졸린인 방법.
- 제57항에 있어서, 상기 유전자 스위치는 제1 진단 스위치 프로모터의 조절 하에 있는 제1 전사 인자 서열 및 제2 진단 스위치 프로모터의 조절 하에 있는 제2 전사 인자 서열을 포함하고, 여기서 상기 제1 전사 인자 서열 및 상기 제2 전사 인자 서열에 의해 코딩되는 단백질들이 상호작용하여 리간드-의존 전사 인자로서 기능하는 단백질 복합체를 형성하는 것인 방법.
- 제68항에 있어서,상기 제1 진단 스위치 프로모터와 상기 제2 진단 스위치 프로모터가 상이한 것인 방법.
- 제68항에 있어서, 상기 제1 진단 스위치 프로모터와 상기 제2 진단 스위치 프로모터가 동일한 것인 방법.
- 제68항에 있어서, 상기 제1 전사 인자 서열은 이형이량체 파트너 및 전사활성화 도메인을 포함하는 단백질을 코딩하는 것인 방법.
- 제68항에 있어서, 상기 제2 전사 인자 서열은 DNA 결합 부위 및 리간드-결합 부위를 포함하는 단백질을 코딩하는 것인 방법.
- 제57항에 있어서, 상기 폴리뉴클레오티드 중 하나는 유도 프로모터에 작동가능하게 연결된 치사 폴리펩타이드를 추가로 코딩하는 것인 방법.
- 폴리뉴클레오티드를 개체의 세포에 도입하여 변형된 세포를 생산하는 단계로서, 여기서 상기 폴리뉴클레오티드는 유전자 스위치를 코딩하며, 또한 상기 폴리뉴클레오티드는 (1) 진단 스위치 프로모터에 작동가능하게 연결된 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 상기 프로모터의 활성은 독성 조건에 노출되어 있는 세포에서 발견된 인자들에 의해 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인 단계를 포함하는, 상기 개체에서 질병 또는 장애에 대한 투여된 치료제의 잠재적 독성을 모니터하기 위해 변형된 세포를 제조하는 방법.
- (a) 개체에 치료제를 투여하는 단계;
(b) 상기 개체의 변형된 세포에 리간드를 투여하는 단계; 및
(c) 리포터 유전자 발현을 적어도 2회 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨의 변화가 상기 치료제의 독성을 지시하고; 또한
여기서 상기 개체의 변형된 세포는 폴리뉴클레오티드를 포함하고, 상기 폴리뉴클레오티드는 유전자 스위치를 코딩하며, 또한 상기 폴리뉴클레오티드는 (1) 진단 스위치 프로모터에 작동가능하게 연결된 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 상기 프로모터의 활성은 독성 조건에 노출되어 있는 세포에서 발견되는 인자들에 의해 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인, 상기 개체에서 질병 또는 장애에 대해 투여된 치료제의 잠재적 독성을 모니터하는 방법.
- (a) 폴리뉴클레오티드를 비-자가 세포에 도입하여 변형된 세포를 생산하는 단계로서, 여기서 상기 폴리뉴클레오티드는 유전자 스위치를 코딩하며, 또한 상기 폴리뉴클레오티드는 (1) 진단 스위치 프로모터에 작동가능하게 연결된 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 상기 프로모터의 활성은 독성 조건에 노출되어 있는 세포에서 발견되는 인자들에 의해 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인 단계;
(b) 개체에 상기 변형된 세포를 도입하는 단계;
(c) 상기 변형된 세포에 리간드를 투여하는 단계; 및
(d) 리포터 유전자 발현을 적어도 2회 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨의 변화가 상기 치료제의 독성을 지시하는 것인, 상기 개체에서 질병 또는 장애에 대한 투여된 치료제의 잠재적 독성을 모니터하는 방법.
- (a) 개체에 치료제를 투여하는 단계;
(b) 폴리뉴클레오티드를 상기 개체의 세포에 도입하여 변형된 세포를 생산하는 단계로서, 상기 폴리뉴클레오티드는 유전자 스위치를 코딩하며, 또한 상기 폴리뉴클레오티드는 (1) 진단 스위치 프로모터에 작동가능하게 연결된 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 상기 프로모터의 활성은 치료를 위해 투여되어 있는 인자에 의해 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인 단계;
(c) 상기 변형된 세포에 리간드를 투여하는 단계; 및
(d) 리포터 유전자 발현을 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨은 치료를 위해 투여된 상기 인자의 레벨을 지시하는 것인, 상기 질병 또는 장애에 대한 치료를 위해 상기 개체에 투여되어 있는 상기 인자의 레벨을 모니터하는 방법.
- 제77항에 있어서, 상기 단계 (b)는 단계 (a)에 앞서 수행되는 방법.
- 제78항에 있어서, 리포터 유전자 발현의 기준선 레벨은 단계 (a)에 앞서 결정되는 것인 방법.
- 제77항에 있어서, 단계 (d)에서 탐지된 리포터 유전자 발현의 레벨에 기반하여 투여된 인자의 양을 변경하는 단계를 추가로 포함하는 방법.
- 제77항에 있어서, 상기 방법은 생체 외에서 상기 개체로부터 분리된 세포에서 수행되는 것인 방법.
- 제77항에 있어서, 상기 폴리뉴클레오티드는 상기 개체로부터 분리된 세포로 도입되어 변형된 세포를 생산하고, 상기 변형된 세포는 상기 개체로 재도입되는 것인 단계.
- 제77항에 있어서, 상기 방법은 생체 내에서 수행되는 것인 방법.
- 제77항에 있어서, 상기 유전자 스위치는 EcR-기반 유전자 스위치인 방법.
- 제84항에 있어서, 상기 리간드는 상기 EcR 리간드 결합 도메인에 결합하는 것인 방법.
- 제85항에 있어서, 상기 리간드는 디아실하이드라진인 방법.
- 제86항에 있어서, 상기 리간드는 RG- 115819, RG-115830, 및 RG-115932로 이루어진 군으로부터 선택된 것인 방법.
- 제85항에 있어서, 상기 리간드는 아미도케톤 또는 옥사디아졸린인 방법.
- 제77항에 있어서, 상기 유전자 스위치는 제1 진단 스위치 프로모터의 조절 하의 제1 전사 인자 서열 및 제2 진단 스위치 프로모터의 조절 하의 제2 전사 인자 서열을 포함하고, 상기 제1 전사 인자 서열 및 상기 제2 전사 인자 서열에 의해 코딩되는 단백질들은 상호작용하여 리간드-의존 전사 인자로서 기능하는 단백질 복합체를 형성하는 것인 방법.
- 제89항에 있어서,상기 제1 진단 스위치 프로모터와 상기 제2 진단 스위치 프로모터가 상이한 것인 방법.
- 제89항에 있어서, 상기 제1 진단 스위치 프로모터와 상기 제2 진단 스위치 프로모터가 동일한 것인 방법.
- 제89항에 있어서, 상기 제1 전사 인자 서열은 이형이량체 파트너 및 전사활성화 도메인를 포함하는 단백질을 코딩하는 것인 방법.
- 제89항에 있어서, 상기 제2 전사 인자 서열은 DNA 결합 도메인 및 리간드-결합 도메인을 포함하는 단백질을 코딩하는 것인 방법.
- 제89항에 있어서, 상기 폴리뉴클레오티드 중 하나는 유도 프로모터에 작동가능하게 연결된 치사 폴리펩타이드를 추가로 코딩하는 것인 방법.
- 폴리뉴클레오티드를 개체의 세포에 도입하여 변형된 세포를 생산하는 단계로서, 여기서 상기 폴리뉴클레오티드는 유전자 스위치를 코딩하며, 또한 상기 폴리뉴클레오티드는 (1) 진단 스위치 프로모터에 작동가능하게 연결된 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 상기 프로모터의 활성은 치료를 위해 투여되어 있는 인자에 의해 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인 단계를 포함하는, 상기 질병 또는 장애에 대한 치료를 위해 상기 개체에 투여되어 있는 상기 인자의 레벨을 모니터하기 위해 변형된 세포를 제조하는 방법.
- (a) 개체에 치료제를 투여하는 단계;
(b) 상기 개체의 변형된 세포에 리간드를 투여하는 단계; 및
(c) 리포터 유전자 발현을 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨이 치료를 위해 투여되어 있는 인자의 레벨을 지시하고; 또한
여기서 상기 개체의 상기 변형된 세포는 폴리뉴클레오티드를 포함하고, 상기 폴리뉴클레오티드는 유전자 스위치를 코딩하며, 또한 상기 폴리뉴클레오티드는 (1) 진단 스위치 프로모터에 작동가능하게 연결된 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 상기 프로모터의 활성은 치료를 위해 투여되어 있는 상기 인자에 의해 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인, 상기 질병 또는 장애에 대한 치료를 위해 개체에 투여되어 있는 상기 인자의 레벨을 모니터하는 방법.
- (a) 폴리뉴클레오티드를 비-자가 세포에 도입하여 변형된 세포를 생산하는 단계로서, 여기서 상기 폴리뉴클레오티드는 유전자 스위치를 코딩하며, 또한 상기 폴리뉴클레오티드는 (1) 진단 스위치 프로모터에 작동가능하게 연결된 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 상기 프로모터의 활성은 치료를 위해 투여되어 있는 인자에 의해 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인 단계;
(b) 상기 개체로 상기 변형된 세포를 도입하는 단계;
(c) 상기 변형된 세포에 리간드를 투여하는 단계; 및
(d) 리포터 유전자 발현을 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨이 치료를 위해 투여되어 있는 상기 인자의 레벨을 지시하는 것인, 상기 개체의 질병 또는 장애에 대해 개체에 투여되어 있는 상기 인자의 레벨을 모니터하는 방법.
- (a) 폴리뉴클레오티드를 기관 또는 조직 이식의 세포에 도입하여 변형된 세포를 생산하는 단계로서, 여기서 상기 폴리뉴클레오티드는 유전자 스위치를 코딩하며, 또한 상기 폴리뉴클레오티드는 (1) 진단 스위치 프로모터에 작동가능하게 연결된 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 상기 프로모터의 활성은 이식 거부기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인 단계;
(b) 상기 변형된 세포에 리간드를 투여하는 단계; 및
(c) 리포터 유전자 발현을 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현이 이식 거부가 탐지됨을 지시하는 것인, 기관 또는 조직 이식을 받는 개체에서 이식 거부를 탐지하는 방법.
- 제98항에 있어서, 상기 폴리뉴클레오티드는 이식에 앞서 상기 세포에 도입되는 것인 방법.
- 제98항에 있어서, 상기 폴리뉴클레오티드는 이식 후에 상기 세포에 도입되는 것인 방법.
- 제98항에 있어서, 상기 유전자 스위치는 엑디손 수용체(EcR)-기반 유전자 스위치인 방법.
- 제101항에 있어서, 상기 리간드는 상기 EcR 리간드 결합 도메인에 결합하는 것인 방법.
- 제102항에 있어서, 상기 리간드는 디아실하이드라진인 방법.
- 제103항에 있어서, 상기 리간드는 RG-115819, RG-115830, 및 RG-115932로 이루어진 군으로부터 선택된 것인 방법.
- 제102항에 있어서, 상기 리간드는 아미도케톤 또는 옥사디아졸린인 방법.
- 제98항에 있어서, 상기 유전자 스위치는 제1 진단 스위치 프로모터의 조절 하에 있는 제1 전사 인자 서열 및 제2 진단 스위치 프로모터의 조절 하에 있는 제2 전사 인자 서열을 포함하고, 여기서 상기 제1 전사 인자 서열 및 상기 제2 전사 인자 서열에 의해 코딩되는 단백질들이 상호작용하여 리간드-의존 전사 인자로서 기능하는 단백질 복합체를 형성하는 것인 방법.
- 제106항에 있어서,상기 제1 진단 스위치 프로모터와 상기 제2 진단 스위치 프로모터가 상이한 것인 방법.
- 제106항에 있어서, 상기 제1 진단 스위치 프로모터와 상기 제2 진단 스위치 프로모터가 동일한 것인 방법.
- 제106항에 있어서, 상기 제1 전사 인자 서열은 이형이량체 파트너 및 전사활성화 도메인을 포함하는 단백질을 코딩하는 것인 방법.
- 제106항에 있어서, 상기 제2 전사 인자 서열은 DNA 결합 도메인 및 리간드-결합 도메인을 포함하는 단백질을 코딩하는 것인 방법.
- 제98항에 있어서, 상기 폴리뉴클레오티드 중 하나는 유도 프로모터에 작동가능하게 연결된 치사 폴리펩타이드를 추가로 코딩하는 것인 방법.
- 폴리뉴클레오티드를 기관 또는 조직 이식의 세포에 도입하여 변형된 세포를 생산하는 단계로서, 여기서 상기 폴리뉴클레오티드는 유전자 스위치를 코딩하며, 또한 상기 폴리뉴클레오티드는 (1) 진단 스위치 프로모터에 작동가능하게 연결된 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 상기 프로모터의 활성은 조직 이식기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인 단계를 포함하는, 상기 개체에서 이식 거부를 탐지하기 위해 기관 또는 조직 이식물(transplant)을 제조하는 방법.
- (a) 개체에 리간드를 투여하는 단계; 및
(b) 리포터 유전자 발현을 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현이 이식 거부가 탐지됨을 지시하는 것이고; 또한
여기서 기관 또는 조직 이식은 폴리뉴클레오티드를 포함하는 하나 이상의 세포를 포함하고, 상기 폴리뉴클레오티드는 유전자 스위치를 코딩하며, 또한 상기 폴리뉴클레오티드는 (1) 진단 스위치 프로모터에 작동가능하게 연결된 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 상기 프로모터의 활성은 이식 거부기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인, 상기 기관 또는 조직 이식을 받는 개체에서 이식 거부를 탐지하는 방법.
- (a) 폴리뉴클레오티드를 기관 또는 조직 이식의 세포에 도입하여 변형된 세포를 생산하는 단계로서, 여기서 상기 폴리뉴클레오티드는 유전자 스위치를 코딩하며, 또한 상기 폴리뉴클레오티드는 (1) 진단 스위치 프로모터에 작동가능하게 연결된 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 상기 프로모터의 활성은 이식 거부기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인 단계;
(b) 상기 변형된 세포에 리간드를 투여하는 단계; 및
(c) 리포터 유전자 발현을 적어도 2회 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨의 변화가 상기 개체에서 상기 이식 거부의 진행을 지시하는 것인, 상기 기관 또는 조직 이식을 받는 개체에서 이식 거부의 진행을 모니터하는 방법.
- 제114항에 있어서, 상기 폴리뉴클레오티드는 이식에 앞서 상기 세포에 도입되는 것인 방법.
- 제114항에 있어서, 상기 폴리뉴클레오티드는 이식 후에 상기 세포에 도입되는 것인 방법.
- 제114항에 있어서, 상기 유전자 스위치는 엑디손 수용체(EcR)-기반 유전자 스위치인 방법.
- 제117항에 있어서, 상기 리간드는 상기 EcR 리간드 결합 도메인에 결합하는 것인 방법.
- 제118항에 있어서, 상기 리간드는 디아실하이드라진인 방법.
- 제119항에 있어서, 상기 리간드는 RG- 115819, RG-115830, 및 RG-115932로 이루어진 군으로부터 선택된 것인 방법.
- 제118항에 있어서, 상기 리간드는 아미도케톤 또는 옥사디아졸린인 방법.
- 제114항에 있어서, 상기 유전자 스위치는 제1 진단 스위치 프로모터의 조절 하에 있는 제1 전사 인자 서열 및 제2 진단 스위치 프로모터의 조절 하에 있는 제2 전사 인자 서열을 포함하고, 여기서 상기 제1 전사 인자 서열 및 상기 제2 전사 인자 서열에 의해 코딩되는 단백질들이 상호작용하여 리간드-의존 전사 인자로서 기능하는 단백질 복합체를 형성하는 것인 방법.
- 제122항에 있어서,상기 제1 진단 스위치 프로모터와 상기 제2 진단 스위치 프로모터가 상이한 것인 방법.
- 제122항에 있어서, 상기 제1 진단 스위치 프로모터와 상기 제2 진단 스위치 프로모터가 동일한 것인 방법.
- 제122항에 있어서, 상기 제1 전사 인자 서열은 이형이량체 파트너 및 전사활성화 도메인을 포함하는 단백질을 코딩하는 것인 방법.
- 제122항에 있어서, 상기 제2 전사 인자 서열은 DNA 결합 도메인 및 리간드-결합 도메인을 포함하는 단백질을 코딩하는 것인 방법.
- 제114항에 있어서, 상기 폴리뉴클레오티드 중 하나는 유도 프로모터에 작동가능하게 연결된 치사 폴리펩타이드를 추가로 코딩하는 것인 방법.
- 폴리뉴클레오티드를 기관 또는 조직 이식의 세포에 도입하여 변형된 세포를 생산하는 단계로서, 여기서 상기 폴리뉴클레오티드는 유전자 스위치를 코딩하며, 또한 상기 폴리뉴클레오티드는 (1) 진단 스위치 프로모터에 작동가능하게 연결된 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 상기 프로모터의 활성은 이식 거부기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인 단계를 포함하는, 상기 개체에서 이식 거부의 진행을 모니터하기 위해 기관 또는 조직 이식물(transplant)을 제조하는 방법.
- (a) 개체에 리간드를 투여하는 단계; 및
(b) 리포터 유전자 발현을 적어도 2회 탐지하는 단계를 포함하며, 여기서 상기 리포터 유전자의 발현 레벨의 변화가 상기 개체에서 이식 거부의 진행을 지시하고, 또한, 기관 또는 조직 이식물(transplant)은 폴리뉴클레오티드를 포함하는 하나 이상의 세포를 포함하고, 여기서 상기 폴리뉴클레오티드는 유전자 스위치를 코딩하며, 또한 상기 폴리뉴클레오티드는 (1) 진단 스위치 프로모터에 작동가능하게 연결된 적어도 하나의 전사 인자 서열, 이때, 상기 적어도 하나의 전사 인자 서열이 리간드-의존 전사 인자를 코딩하고, 상기 프로모터의 활성은 이식 거부기간 동안 조절됨; 및 (2) 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 코딩하는 폴리뉴클레오티드를 포함하는 것인 단계를 포함하는, 상기 기관 또는 조직 이식을 받는 개체에서 이식 거부의 진행을 모니터하는 방법.
- 유전자 스위치를 코딩하는 폴리뉴클레오티드로서, 상기 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하며, 상기 적어도 하나의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하고, 진단 스위치 프로모터에 작동가능하게 연결되며, 여기서 상기 프로모터의 활성은 상기 질병 또는 장애 기간 동안 조절되는 것인 폴리뉴클레오티드.
- 제130항에 있어서, 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 추가로 코딩하는 것인 폴리뉴클레오티드.
. - 제130항에 있어서, 상기 유전자 스위치는 EcR-기반 유전자 스위치인 폴리뉴클레오티드.
- 제130항에 있어서, 상기 유전자 스위치는 제1 진단 스위치 프로모터의 조절 하에 있는 제1 전사 인자 서열 및 제2 진단 스위치 프로모터의 조절 하에 있는 제2 전사 인자 서열을 포함하고, 여기서 상기 제1 전사 인자 서열 및 상기 제2 전사 인자 서열에 의해 코딩되는 단백질들이 상호작용하여 리간드-의존 전사 인자로서 기능하는 단백질 복합체를 형성하는 것인 폴리뉴클레오티드.
- 제133항에 있어서, 상기 제1 진단 스위치 프로모터와 상기 제2 진단 스위치 프로모터가 상이한 것인 폴리뉴클레오티드.
- 제133항에 있어서, 상기 제1 진단 스위치 프로모터와 상기 제2 진단 스위치 프로모터가 동일한 것인 폴리뉴클레오티드.
- 제133항에 있어서, 상기 제1 전사 인자 서열은 이형이량체 파트너 및 전사활성화 도메인을 포함하는 단백질을 코딩하는 것인 폴리뉴클레오티드.
- 제133항에 있어서, 상기 제2 전사 인자 서열은 DNA 결합 도메인 및 리간드-결합 도메인을 포함하는 단백질을 코딩하는 것인 폴리뉴클레오티드.
- 제130항에 있어서, 상기 폴리뉴클레오티드는 유도 프로모터에 작동가능하게 연결된 치사 폴리펩타이드를 추가로 코딩하는 것인 폴리뉴클레오티드.
- 유전자 스위치를 코딩하는 폴리뉴클레오티드로서, 상기 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하며, 상기 적어도 하나의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하고, 진단 스위치 프로모터에 작동가능하게 연결되며, 여기서 상기 프로모터의 활성은 독성 조건에 노출되어 있는 세포에서 발견되는 인자들에 의해 조절되는 것인 폴리뉴클레오티드.
- 제139항에 있어서, 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 추가로 코딩하는 폴리뉴클레오티드.
- 제130항에 있어서, 상기 유전자 스위치는 EcR-기반 유전자 스위치인 폴리뉴클레오티드.
- 제139항에 있어서, 상기 유전자 스위치는 제1 진단 스위치 프로모터의 조절 하에 있는 제1 전사 인자 서열 및 제2 진단 스위치 프로모터의 조절 하에 있는 제2 전사 인자 서열을 포함하고, 여기서 상기 제1 전사 인자 서열 및 상기 제2 전사 인자 서열에 의해 코딩되는 단백질들이 상호작용하여 리간드-의존 전사 인자로서 기능하는 단백질 복합체를 형성하는 것인 폴리뉴클레오티드.
- 제142항에 있어서, 상기 제1 진단 스위치 프로모터와 상기 제2 진단 스위치 프로모터가 상이한 것인 폴리뉴클레오티드.
- 제142항에 있어서, 상기 제1 진단 스위치 프로모터와 상기 제2 진단 스위치 프로모터가 동일한 것인 폴리뉴클레오티드.
- 제142항에 있어서, 상기 제1 전사 인자 서열은 이형이량체 파트너 및 전사활성화 도메인을 포함하는 단백질을 코딩하는 것인 폴리뉴클레오티드.
- 제142항에 있어서, 상기 제2 전사 인자 서열은 DNA 결합 도메인 및 리간드-결합 도메인을 포함하는 단백질을 코딩하는 것인 폴리뉴클레오티드.
- 제139항에 있어서, 상기 폴리뉴클레오티드는 유도 프로모터에 작동가능하게 연결된 치사 폴리펩타이드를 추가로 코딩하는 것인 폴리뉴클레오티드.
- 유전자 스위치를 코딩하는 폴리뉴클레오티드로서, 상기 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하며, 상기 적어도 하나의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하고, 진단 스위치 프로모터에 작동가능하게 연결되며, 여기서 상기 프로모터의 활성은 치료를 위해 개체에 투여된 인자에 의해 조절되는 것인 폴리뉴클레오티드.
- 제148항에 있어서, 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 추가로 코딩하는 폴리뉴클레오티드.
- 제148항에 있어서, 상기 유전자 스위치는 EcR-기반 유전자 스위치인 폴리뉴클레오티드.
- 제148항에 있어서, 상기 유전자 스위치는 제1 진단 스위치 프로모터의 조절 하에 있는 제1 전사 인자 서열 및 제2 진단 스위치 프로모터의 조절 하에 있는 제2 전사 인자 서열을 포함하고, 여기서 상기 제1 전사 인자 서열 및 상기 제2 전사 인자 서열에 의해 코딩되는 단백질들이 상호작용하여 리간드-의존 전사 인자로서 기능하는 단백질 복합체를 형성하는 것인 폴리뉴클레오티드.
- 제151항에 있어서, 상기 제1 진단 스위치 프로모터와 상기 제2 진단 스위치 프로모터가 상이한 것인 폴리뉴클레오티드.
- 제151항에 있어서, 상기 제1 진단 스위치 프로모터와 상기 제2 진단 스위치 프로모터가 동일한 것인 폴리뉴클레오티드.
- 제151항에 있어서, 상기 제1 전사 인자 서열은 이형이량체 파트너 및 전사활성화 도메인을 포함하는 단백질을 코딩하는 것인 폴리뉴클레오티드.
- 제151항에 있어서, 상기 제2 전사 인자 서열은 DNA 결합 도메인 및 리간드-결합 도메인을 포함하는 단백질을 코딩하는 것인 폴리뉴클레오티드.
- 제148항에 있어서, 상기 폴리뉴클레오티드는 유도 프로모터에 작동가능하게 연결된 치사 폴리펩타이드를 추가로 코딩하는 것인 폴리뉴클레오티드.
- 유전자 스위치를 코딩하는 폴리뉴클레오티드로서, 상기 유전자 스위치는 적어도 하나의 전사 인자 서열을 포함하며, 상기 적어도 하나의 전사 인자 서열은 리간드-의존 전사 인자를 코딩하고, 진단 스위치 프로모터에 작동가능하게 연결되며, 여기서 상기 프로모터의 활성은 이식 거부기간 동안 조절되는 것인 폴리뉴클레오티드.
- 제157항에 있어서, 상기 리간드-의존 전사 인자에 의해 활성되는 프로모터에 연결된 리포터 유전자를 추가로 코딩하는 폴리뉴클레오티드.
- 제159항에 있어서, 상기 유전자 스위치는 EcR-기반 유전자 스위치인 폴리뉴클레오티드.
- 제157항에 있어서, 상기 유전자 스위치는 제1 진단 스위치 프로모터의 조절 하에 있는 제1 전사 인자 서열 및 제2 진단 스위치 프로모터의 조절 하에 있는 제2 전사 인자 서열을 포함하고, 여기서 상기 제1 전사 인자 서열 및 상기 제2 전사 인자 서열에 의해 코딩되는 단백질들이 상호작용하여 리간드-의존 전사 인자로서 기능하는 단백질 복합체를 형성하는 것인 폴리뉴클레오티드.
- 제160항에 있어서, 상기 제1 진단 스위치 프로모터와 상기 제2 진단 스위치 프로모터가 상이한 것인 폴리뉴클레오티드.
- 제160항에 있어서, 상기 제1 진단 스위치 프로모터와 상기 제2 진단 스위치 프로모터가 동일한 것인 폴리뉴클레오티드.
- 제160항에 있어서, 상기 제1 전사 인자 서열은 이형이량체 파트너 및 전사활성화 도메인을 포함하는 단백질을 코딩하는 것인 폴리뉴클레오티드.
- 제160항에 있어서, 상기 제2 전사 인자 서열은 DNA 결합 도메인 및 리간드-결합 도메인을 포함하는 단백질을 코딩하는 것인 폴리뉴클레오티드.
- 제157항에 있어서, 상기 폴리뉴클레오티드는 유도 프로모터에 작동가능하게 연결된 치사 폴리펩타이드를 추가로 코딩하는 것인 폴리뉴클레오티드.
- 제130, 139, 148 또는 157 중 어느 한 항의 폴리뉴클레오티드를 포함하는 벡터.
- 제166항에 있어서, 상기 벡터는 플라스미드 벡터인 벡터.
- 제166항에 있어서, 상기 벡터는 바이러스 벡터인 벡터.
- 제130, 139, 148, 또는 157 중 어느 한 항의 폴리뉴클레오티드를 포함하는 키트.
- 제166항의 벡터를 포함하는 키트.
Applications Claiming Priority (6)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US95747407P | 2007-08-23 | 2007-08-23 | |
| US60/957,474 | 2007-08-23 | ||
| US1465407P | 2007-12-18 | 2007-12-18 | |
| US61/014,654 | 2007-12-18 | ||
| US4794008P | 2008-04-25 | 2008-04-25 | |
| US61/047,940 | 2008-04-25 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20100049084A true KR20100049084A (ko) | 2010-05-11 |
Family
ID=40378488
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020107003992A KR20100049084A (ko) | 2007-08-23 | 2008-08-25 | 질병 진단을 위한 방법 및 조성물 |
Country Status (11)
| Country | Link |
|---|---|
| US (5) | US20090098055A1 (ko) |
| EP (1) | EP2185730A4 (ko) |
| JP (1) | JP2010536373A (ko) |
| KR (1) | KR20100049084A (ko) |
| CN (1) | CN101835908A (ko) |
| AU (1) | AU2008289461A1 (ko) |
| CA (1) | CA2698212A1 (ko) |
| MX (1) | MX2010001993A (ko) |
| NZ (1) | NZ583430A (ko) |
| WO (1) | WO2009025866A1 (ko) |
| ZA (1) | ZA201000983B (ko) |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2205618B1 (en) * | 2007-09-26 | 2016-11-09 | Intrexon Corporation | Synthetic 5'utrs, expression vectors, and methods for increasing transgene expression |
| CA2715080C (en) | 2007-09-28 | 2021-09-28 | Intrexon Corporation | Therapeutic gene-switch constructs and bioreactors for the expression of biotherapeutic molecules, and uses thereof |
| RU2573912C2 (ru) | 2008-10-08 | 2016-01-27 | Интрексон Корпорейшн | Сконструированные клетки, экспрессирующие множественные иммуномодуляторы, и их применения |
| JP5952815B2 (ja) * | 2010-08-04 | 2016-07-13 | シズル バイオテクノロジー リミテッド | ガンの診断および処置のための方法および化合物 |
| CN103534355A (zh) | 2011-03-04 | 2014-01-22 | 英特瑞克斯顿股份有限公司 | 条件性表达蛋白质的载体 |
| MX369690B (es) * | 2011-09-08 | 2019-11-19 | Intrexon Corp | Diacilhidrazina cristalina y sus usos. |
| CN105510586B (zh) * | 2015-12-22 | 2017-09-12 | 湖北鹊景生物医学有限公司 | 用于肺癌诊断的试剂盒及其使用方法 |
| CN111848733B (zh) * | 2019-04-30 | 2024-03-12 | 上海细胞治疗集团有限公司 | 一种多肽组合物及疫苗 |
| CN111848732B (zh) * | 2019-04-30 | 2024-03-12 | 上海细胞治疗集团有限公司 | 多肽组合物及疫苗 |
| CN110051841B (zh) * | 2019-05-28 | 2021-02-02 | 北京大学 | Nat10抑制剂在制备用于抑制hif表达的药物中的应用 |
| CN111304226A (zh) * | 2019-11-21 | 2020-06-19 | 福州福瑞医学检验实验室有限公司 | 一种编码cyp1b1基因突变体的核酸及其应用 |
| RU2728683C1 (ru) * | 2019-12-03 | 2020-07-30 | Федеральное государственное бюджетное образовательное учреждение высшего образования "Кубанский государственный медицинский университет" Министерства здравоохранения Российской Федерации (ФГБОУ ВО КубГМУ Минздрава России) | Способ ранней диагностики отторжения трансплантата |
| AU2021338361A1 (en) * | 2020-09-03 | 2023-04-06 | Chen, Irvin S.Y | Soluble alkaline phosphatase constructs and expression vectors including a polynucleotide encoding for soluble alkaline phosphatase constructs |
| CN115770296B (zh) * | 2022-07-15 | 2024-05-10 | 青岛大学 | circEYA3在制备先天性心脏病诊断/治疗的产品中的应用 |
Family Cites Families (93)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4352883A (en) | 1979-03-28 | 1982-10-05 | Damon Corporation | Encapsulation of biological material |
| US4409331A (en) | 1979-03-28 | 1983-10-11 | Damon Corporation | Preparation of substances with encapsulated cells |
| CA1196862A (en) | 1983-06-01 | 1985-11-19 | Anthony M.F. Sun | Microencapsulation of living tissue and cells |
| US4806355A (en) | 1983-06-06 | 1989-02-21 | Connaught Laboratories Limited | Microencapsulation of living tissue and cells |
| US4689293A (en) | 1983-06-06 | 1987-08-25 | Connaught Laboratories Limited | Microencapsulation of living tissue and cells |
| US4680174A (en) | 1984-05-24 | 1987-07-14 | Damon Biotech, Inc. | Induction of immune response by immunization with encapsulated antigen-producing cells |
| US5117057A (en) | 1985-10-21 | 1992-05-26 | Rohm And Haas Company | Insecticidal N' substituted-N-N'-disubstituted-hydrazines |
| US4985461A (en) | 1985-10-21 | 1991-01-15 | Rohm And Haas Company | Insecticidal N'-substituted-N,N'-diacylhydrazines |
| US5225443A (en) | 1986-05-01 | 1993-07-06 | Rohm And Haas Company | Insecticidal N'-substituted-N'-substituted N,N'-diacylhydrazines |
| US5773286A (en) | 1987-11-17 | 1998-06-30 | Cytotherapeutics, Inc. | Inner supported biocompatible cell capsules |
| US5786216A (en) | 1987-11-17 | 1998-07-28 | Cytotherapeutics, Inc. | Inner-supported, biocompatible cell capsules |
| US4981784A (en) | 1987-12-02 | 1991-01-01 | The Salk Institute For Biological Studies | Retinoic acid receptor method |
| US5354844A (en) | 1989-03-16 | 1994-10-11 | Boehringer Ingelheim International Gmbh | Protein-polycation conjugates |
| US5693622A (en) | 1989-03-21 | 1997-12-02 | Vical Incorporated | Expression of exogenous polynucleotide sequences cardiac muscle of a mammal |
| US5703055A (en) | 1989-03-21 | 1997-12-30 | Wisconsin Alumni Research Foundation | Generation of antibodies through lipid mediated DNA delivery |
| US5264618A (en) | 1990-04-19 | 1993-11-23 | Vical, Inc. | Cationic lipids for intracellular delivery of biologically active molecules |
| US5529914A (en) | 1990-10-15 | 1996-06-25 | The Board Of Regents The Univeristy Of Texas System | Gels for encapsulation of biological materials |
| IL100643A (en) | 1991-01-25 | 1996-10-31 | Nippon Kayaku Kk | History of hydrazine and pesticides containing these histories as an active ingredient |
| WO1992019195A1 (en) | 1991-04-25 | 1992-11-12 | Brown University Research Foundation | Implantable biocompatible immunoisolatory vehicle for delivery of selected therapeutic products |
| US5800829A (en) | 1991-04-25 | 1998-09-01 | Brown University Research Foundation | Methods for coextruding immunoisolatory implantable vehicles with a biocompatible jacket and a biocompatible matrix core |
| JPH07503943A (ja) | 1991-10-29 | 1995-04-27 | クローバー コンソリデイテッド,リミテッド | 封入及び薬剤放出に有用な架橋性の多糖類、ポリカチオン及び脂質 |
| US5545423A (en) | 1991-11-25 | 1996-08-13 | Vivorx, Inc. | Cytoprotective, biocompatible, retrievable macrocapsule containment systems for biologically active materials |
| US5530028A (en) | 1992-11-23 | 1996-06-25 | Rohm And Haas Company | Insecticidal N'-substituted-N,N'-diacylhydrazines |
| US6013836A (en) | 1992-02-28 | 2000-01-11 | Rohm And Haas Company | Insecticidal N'-substituted-N,N'-disubstitutedhydrazines |
| US5573934A (en) | 1992-04-20 | 1996-11-12 | Board Of Regents, The University Of Texas System | Gels for encapsulation of biological materials |
| US5334640A (en) | 1992-04-08 | 1994-08-02 | Clover Consolidated, Ltd. | Ionically covalently crosslinked and crosslinkable biocompatible encapsulation compositions and methods |
| US5286495A (en) | 1992-05-11 | 1994-02-15 | University Of Florida | Process for microencapsulating cells |
| JPH08510274A (ja) | 1993-04-27 | 1996-10-29 | サイトセラピュティックス インコーポレイテッド | アクリロニトリルベースのポリマーにより形成された膜 |
| EP0708670A4 (en) | 1993-06-23 | 1998-07-01 | Cytotherapeutics Inc | METHOD AND APPARATUS FOR HERMETICALLY CLOSING IMPLANTABLE MEMBRANE ENCAPSULATING DEVICES |
| US5908623A (en) | 1993-08-12 | 1999-06-01 | Cytotherapeutics, Inc. | Compositions and methods for the delivery of biologically active molecules using genetically altered cells contained in biocompatible immunoisolatory capsules |
| WO1995005452A2 (en) | 1993-08-12 | 1995-02-23 | Cytotherapeutics, Inc. | Improved compositions and methods for the delivery of biologically active molecules using genetically altered cells contained in biocompatible immunoisolatory capsules |
| US5858350A (en) | 1993-12-01 | 1999-01-12 | Marine Polymer Technologies | Methods and compositions for poly-β-1→4-N-acetylglucosamine cell therapy system |
| FR2714830B1 (fr) | 1994-01-10 | 1996-03-22 | Rhone Poulenc Rorer Sa | Composition contenant des acides nucléiques, préparation et utilisations. |
| ATE320482T1 (de) | 1994-01-13 | 2006-04-15 | Rogosin Inst | Makroeingekapselte sekretorische zellen |
| USRE39542E1 (en) | 1994-01-13 | 2007-04-03 | The Rogosin Institute | Preparation of agarose coated, solid agarose-collagen beads containing secretory cells |
| FR2715847B1 (fr) | 1994-02-08 | 1996-04-12 | Rhone Poulenc Rorer Sa | Composition contenant des acides nucléiques, préparation et utilisations. |
| US5651980A (en) | 1994-04-15 | 1997-07-29 | Biohybrid Technologies, Inc. | Methods of use of uncoated gel particles |
| US6306454B1 (en) | 1994-10-17 | 2001-10-23 | Baxter International Inc. | Method for producing improved medical devices and devices so produced |
| FR2727679B1 (fr) | 1994-12-05 | 1997-01-03 | Rhone Poulenc Rorer Sa | Nouveaux agents de transfection et leurs applications pharmaceutiques |
| US6281015B1 (en) | 1994-12-16 | 2001-08-28 | Children's Medical Center Corp. | Localized delivery of factors enhancing survival of transplanted cells |
| FR2730637B1 (fr) | 1995-02-17 | 1997-03-28 | Rhone Poulenc Rorer Sa | Composition pharmaceutique contenant des acides nucleiques, et ses utilisations |
| US5916790A (en) | 1995-03-03 | 1999-06-29 | Metabolex, Inc. | Encapsulation compositions, and methods |
| US6126936A (en) | 1995-03-10 | 2000-10-03 | Biohybrid Technologies Llc | Microcapsules and composite microreactors for immunoisolation of cells |
| US5837234A (en) | 1995-06-07 | 1998-11-17 | Cytotherapeutics, Inc. | Bioartificial organ containing cells encapsulated in a permselective polyether suflfone membrane |
| WO1997010807A1 (en) | 1995-09-22 | 1997-03-27 | Gore Hybrid Technologies, Inc. | Improved cell encapsulation device |
| US6224912B1 (en) | 1996-04-03 | 2001-05-01 | The Rogo Institute | Cancer-cell proliferation-suppressing material produced by cancer cells restricted by entrapment |
| US6723531B2 (en) | 1996-04-05 | 2004-04-20 | The Salk Institute For Biological Studies | Method for modulating expression of exogenous genes in mammalian systems, and products related thereto |
| US20040086494A1 (en) * | 1996-10-07 | 2004-05-06 | John Constance Mary | Immune privileged cells for delivery of proteins and peptides |
| US6287558B1 (en) | 1997-08-01 | 2001-09-11 | Biohybrio Technologies Llc | Devices containing cells or tissue and an agent that inhibits damage by a host cell molecule |
| US6368612B1 (en) | 1997-12-12 | 2002-04-09 | Biohybrid Technologies Llc | Devices for cloaking transplanted cells |
| US6342596B1 (en) * | 1998-05-05 | 2002-01-29 | Hsf Pharmaceuticals S.A. | Molecular regulatory circuits to achieve sustained activation of genes of interest by a single stress |
| US6333318B1 (en) | 1998-05-14 | 2001-12-25 | The Salk Institute For Biological Studies | Formulations useful for modulating expression of exogenous genes in mammalian systems, and products related thereto |
| US6258603B1 (en) | 1998-06-17 | 2001-07-10 | Rohm And Haas Company | Ligands for modulating the expression of exogenous genes via an ecdysone receptor complex |
| US6818018B1 (en) | 1998-08-14 | 2004-11-16 | Incept Llc | In situ polymerizable hydrogels |
| US6495161B1 (en) | 1999-03-09 | 2002-12-17 | Vivorx, Inc. | Cytoprotective biocompatible containment systems for biologically active materials and methods of making same |
| US6342896B1 (en) | 1999-03-19 | 2002-01-29 | Microsoft Corporation | Methods and apparatus for efficiently implementing and modifying foreground and background color selections |
| US6303355B1 (en) | 1999-03-22 | 2001-10-16 | Duke University | Method of culturing, cryopreserving and encapsulating pancreatic islet cells |
| US6365385B1 (en) | 1999-03-22 | 2002-04-02 | Duke University | Methods of culturing and encapsulating pancreatic islet cells |
| US6558665B1 (en) | 1999-05-18 | 2003-05-06 | Arch Development Corporation | Encapsulating particles with coatings that conform to size and shape of the particles |
| CA2374365A1 (en) * | 1999-05-28 | 2000-12-07 | Sangamo Biosciences, Inc. | Gene switches |
| ATE338135T1 (de) | 2000-03-22 | 2006-09-15 | Rheogene Holdings Inc | Induziertes genexpressionssystem basierend auf ecdysonrezeptoren |
| US20040033600A1 (en) * | 2001-03-21 | 2004-02-19 | Palli Subba Reddy | Ecdysone receptor-based inducible gene expression system |
| US6337008B1 (en) | 2000-06-12 | 2002-01-08 | Alcan International Limited | Electrolysis cells |
| US8105825B2 (en) * | 2000-10-03 | 2012-01-31 | Intrexon Corporation | Multiple inducible gene regulation system |
| AU2002213143A1 (en) | 2000-10-12 | 2002-04-22 | Institute Of Materials Research And Engineering | Non-disruptive three-dimensional culture and harvest system for anchorage-dependent cells |
| MXPA03007493A (es) * | 2001-02-20 | 2004-10-15 | Rheogene Holdings Inc | Nuevo sistema de expresion genetica inducible a base de receptor de ecdisona/receptor x retinoide de invertebrado. |
| ES2392508T3 (es) * | 2001-02-20 | 2012-12-11 | Intrexon Corporation | Receptores X retinoides quiméricos y su uso en un sistema inducible de expresión génica basado en receptores de ecdisona novedoso |
| WO2002066615A2 (en) | 2001-02-20 | 2002-08-29 | Rheogene, Inc. | Novel substitution mutant receptors and their use in a nuclear receptor-based inducible gene expression system |
| US8715959B2 (en) * | 2001-02-20 | 2014-05-06 | Intrexon Corporation | Substitution mutant receptors and their use in a nuclear receptor-based inducible gene expression system |
| KR100453853B1 (ko) | 2001-08-28 | 2004-10-20 | 삼성전자주식회사 | 저전압 불 휘발성 반도체 메모리 장치 및 그것의 독출 방법 |
| US7919269B2 (en) * | 2001-09-26 | 2011-04-05 | Intrexon Corporation | Whitefly ecdysone receptor nucleic acids, polypeptides, and uses thereof |
| US20040266708A1 (en) * | 2002-01-29 | 2004-12-30 | Paul Diamond | Regulation of polynucleic acid activity and expression |
| US6727322B2 (en) | 2002-04-01 | 2004-04-27 | The University Of Akron | Amphiphilic networks, implantable immunoisolatory devices, and methods of preparation |
| EP1501541A1 (en) | 2002-04-30 | 2005-02-02 | Canadian Blood Services | Encapsulated cells to elicit immune responses |
| US7226978B2 (en) | 2002-05-22 | 2007-06-05 | Dexcom, Inc. | Techniques to improve polyurethane membranes for implantable glucose sensors |
| US7375093B2 (en) | 2002-07-05 | 2008-05-20 | Intrexon Corporation | Ketone ligands for modulating the expression of exogenous genes via an ecdysone receptor complex |
| US7785871B2 (en) | 2002-10-09 | 2010-08-31 | Intrexon Corporation | DNA cloning vector plasmids and methods for their use |
| US20080050808A1 (en) | 2002-10-09 | 2008-02-28 | Reed Thomas D | DNA modular cloning vector plasmids and methods for their use |
| US7304161B2 (en) | 2003-02-10 | 2007-12-04 | Intrexon Corporation | Diaclhydrazine ligands for modulating the expression of exogenous genes in mammalian systems via an ecdysone receptor complex |
| US7304162B2 (en) * | 2003-02-21 | 2007-12-04 | Intrexon Corporation | Oxadiazoline ligands for modulating the expression of exogenous genes via an ecdysone receptor complex |
| EP1639108A2 (en) * | 2003-02-28 | 2006-03-29 | McGILL UNIVERSITY | Cell and enzyme compositions for modulating bile acids, cholesterol and triglycerides |
| US7456315B2 (en) * | 2003-02-28 | 2008-11-25 | Intrexon Corporation | Bioavailable diacylhydrazine ligands for modulating the expression of exogenous genes via an ecdysone receptor complex |
| DK1651161T3 (da) * | 2003-08-07 | 2012-01-30 | Healor Ltd | Farmaceutiske præparater og fremgangsmåder til at fremme sårheling |
| EP1654366A1 (en) * | 2003-08-11 | 2006-05-10 | University Of South Florida | Stem cell beacon |
| SE526959C2 (sv) | 2003-10-02 | 2005-11-29 | Tikomed Ab | Bioartificellt implantat innefattande en semipermeabel barriär samt förfarande för reducering av risken för bildning av bindrväv vid implantatet efter implantering genom att barriären förses med en permeabel beläggning av bioaktiv metall |
| US7935510B2 (en) | 2004-04-30 | 2011-05-03 | Intrexon Corporation | Mutant receptors and their use in a nuclear receptor-based inducible gene expression system |
| NZ583974A (en) | 2004-05-18 | 2011-11-25 | Intrexon Corp | Methods for dynamic vector assembly of DNA cloning vector plasmids |
| US20060228776A1 (en) * | 2004-10-22 | 2006-10-12 | Neurologix, Inc. | PINK-1 promoter |
| US9034650B2 (en) | 2005-02-02 | 2015-05-19 | Intrexon Corporation | Site-specific serine recombinases and methods of their use |
| US7868159B2 (en) * | 2005-06-23 | 2011-01-11 | Baylor College Of Medicine | Modulation of negative immune regulators and applications for immunotherapy |
| NZ567216A (en) | 2005-10-21 | 2010-03-26 | Living Cell Products Pty Ltd | Encapsulation system |
| CA2715080C (en) * | 2007-09-28 | 2021-09-28 | Intrexon Corporation | Therapeutic gene-switch constructs and bioreactors for the expression of biotherapeutic molecules, and uses thereof |
| CA2702058A1 (en) * | 2007-10-08 | 2009-04-16 | Intrexon Corporation | Engineered dendritic cells and uses for the treatment of cancer |
-
2008
- 2008-08-25 JP JP2010521896A patent/JP2010536373A/ja not_active Withdrawn
- 2008-08-25 EP EP08827870A patent/EP2185730A4/en not_active Withdrawn
- 2008-08-25 WO PCT/US2008/010040 patent/WO2009025866A1/en active Application Filing
- 2008-08-25 CA CA2698212A patent/CA2698212A1/en not_active Abandoned
- 2008-08-25 AU AU2008289461A patent/AU2008289461A1/en not_active Abandoned
- 2008-08-25 MX MX2010001993A patent/MX2010001993A/es not_active Application Discontinuation
- 2008-08-25 KR KR1020107003992A patent/KR20100049084A/ko not_active Application Discontinuation
- 2008-08-25 CN CN200880113476A patent/CN101835908A/zh active Pending
- 2008-08-25 NZ NZ583430A patent/NZ583430A/en not_active IP Right Cessation
- 2008-08-25 US US12/197,559 patent/US20090098055A1/en not_active Abandoned
-
2010
- 2010-02-10 ZA ZA2010/00983A patent/ZA201000983B/en unknown
-
2012
- 2012-12-17 US US13/717,483 patent/US20130266947A1/en not_active Abandoned
-
2014
- 2014-08-14 US US14/459,480 patent/US9222121B2/en not_active Expired - Fee Related
-
2015
- 2015-11-23 US US14/948,522 patent/US9605316B2/en not_active Expired - Fee Related
-
2016
- 2016-12-05 US US15/369,105 patent/US20170145520A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| WO2009025866A1 (en) | 2009-02-26 |
| EP2185730A4 (en) | 2010-10-27 |
| US20090098055A1 (en) | 2009-04-16 |
| EP2185730A1 (en) | 2010-05-19 |
| US20170145520A1 (en) | 2017-05-25 |
| MX2010001993A (es) | 2010-03-11 |
| NZ583430A (en) | 2012-06-29 |
| CN101835908A (zh) | 2010-09-15 |
| ZA201000983B (en) | 2011-04-28 |
| US20150056631A1 (en) | 2015-02-26 |
| JP2010536373A (ja) | 2010-12-02 |
| US20130266947A1 (en) | 2013-10-10 |
| US9605316B2 (en) | 2017-03-28 |
| CA2698212A1 (en) | 2009-02-26 |
| AU2008289461A1 (en) | 2009-02-26 |
| US9222121B2 (en) | 2015-12-29 |
| US20160145688A1 (en) | 2016-05-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20100049084A (ko) | 질병 진단을 위한 방법 및 조성물 | |
| KR102606929B1 (ko) | 동족 항원과 t-세포 수용체 상호작용의 발견 및 특징규명을 위한 조작된 2-부분 세포 디바이스 | |
| KR101666228B1 (ko) | 생물치료학적 분자를 발현시키기 위한 치료학적 유전자-스위치 작제물 및 생물반응기, 및 이의 용도 | |
| AU2020264412B2 (en) | Dna-binding protein using ppr motif, and use thereof | |
| AU2022200903B2 (en) | Engineered Cascade components and Cascade complexes | |
| KR20230091894A (ko) | 부위 특이적 표적화 요소를 통한 프로그램 가능한 첨가(paste)를 사용하는 부위 특이적 유전 공학을 위한 시스템, 방법, 및 조성물 | |
| KR102614328B1 (ko) | T-세포 수용체 합성 및 tcr-제시 세포에 대한 안정적인 게놈 통합을 위한 2-부분 디바이스 | |
| KR102652494B1 (ko) | 전장 t-세포 수용체 오픈 리딩 프레임의 신속한 조립 및 다양화를 위한 2-성분 벡터 라이브러리 시스템 | |
| DK2623594T3 (da) | Antistof mod human prostaglandin-E2-receptor EP4 | |
| KR102584628B1 (ko) | T-세포 수용체, t-세포 항원 및 이들의 기능성 상호작용의 식별 및 특징규명을 위한 조작된 다성분 시스템 | |
| US20240207318A1 (en) | Chimeric costimulatory receptors, chemokine receptors, and the use of same in cellular immunotherapies | |
| JP2023025182A (ja) | T細胞レセプター及びt細胞抗原の同定及び特徴決定のための遺伝子操作された多成分システム | |
| AU2017252409A1 (en) | Compositions and methods for nucleic acid expression and protein secretion in bacteroides | |
| DK2935601T3 (en) | RECOMBINANT MICROBELL CELLS PRODUCING AT LEAST 28% EICOSAPENTAIC ACID AS DRY WEIGHT | |
| KR20240022571A (ko) | Rna-가이드된 이펙터 동원을 위한 시스템, 방법 및 성분 | |
| US11814412B2 (en) | Artificial proteins and compositions and methods thereof | |
| RU2774631C1 (ru) | Сконструированные компоненты cascade и комплексы cascade | |
| RU2827658C2 (ru) | Сконструированные компоненты cascade и комплексы cascade | |
| TW202309287A (zh) | 調節基因表現之組合物及方法 | |
| CN115003815A (zh) | 小麦转基因事件ind-øø412-7 | |
| Lai | Analysis of Drosophila melanogaster snRNA activating protein complex binding to the U1 gene promoter |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WITN | Withdrawal due to no request for examination |