KR20100037615A - 대전된 분자 조작을 위한 방법 및 이를 위한 장치 - Google Patents
대전된 분자 조작을 위한 방법 및 이를 위한 장치 Download PDFInfo
- Publication number
- KR20100037615A KR20100037615A KR1020107001996A KR20107001996A KR20100037615A KR 20100037615 A KR20100037615 A KR 20100037615A KR 1020107001996 A KR1020107001996 A KR 1020107001996A KR 20107001996 A KR20107001996 A KR 20107001996A KR 20100037615 A KR20100037615 A KR 20100037615A
- Authority
- KR
- South Korea
- Prior art keywords
- needle structure
- locus
- molecular material
- needle
- dna
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M35/00—Means for application of stress for stimulating the growth of microorganisms or the generation of fermentation or metabolic products; Means for electroporation or cell fusion
- C12M35/02—Electrical or electromagnetic means, e.g. for electroporation or for cell fusion
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/87—Introduction of foreign genetic material using processes not otherwise provided for, e.g. co-transformation
- C12N15/89—Introduction of foreign genetic material using processes not otherwise provided for, e.g. co-transformation using microinjection
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
Abstract
분자 물질을 조작하기 위한 방법 및 시스템이 제공된다. 한 양상에 있어서, 분자 물질을 조작하는 방법 및 시스템은 대전된 분자 물질과의 전기적 유사성을 갖는 미-대전된 바늘 구조물을 액체 환경 내 제1 유전자자리에 위치시키는 단계, 대전된 분자 물질의 적어도 일부가 상기 바늘 구조물과 결합하도록 상기 바늘 구조물을 대전시키는 단계, 상기 바늘 구조물 및 상기 제1 유전자자리를 서로에 대해 이동시키는 단계, 및 상기 바늘 구조물을 방전시켜 상기 대전된 분자 물질을 제2 유전자자리에서 분리시키는 단계를 포함할 수 있다.
Description
발명의 분야
본 발명은 대전된 분자의 미세조작(micromanipulation)에 관한 것이다. 따라서, 본 발명은 생물공학, 화학, 및 미세조작 분야를 포함한다.
발명이 배경
이종 물질(foreign materials)의 현미주사(Microinjection)는 종종 다루기 어려운데, 특히 살아있는 세포와 같은 생물학적 구조물 상에서 수행될 때 그러하다. 다양한 트랜스펙션 기술은 이종 DNA의 발현을 촉진하기 위하여 세포의 핵에 DNA와 같은 이종 유전 물질(foreign genetic material)을 현미주사 하는 것을 포함한다. 예를 들면, 수정된 난모세포(난자)가 트랜스펙션될 때, 상기 난모세포로부터 발생한 세포는 이종 유전 물질을 운반한다. 따라서 한 응용에 있어서, 추가적인, 강화된, 또는 억제된 유전 형질을 나타내는 미생물이 생성될 수 있다. 한 예로서, 연구자들은, 특정 약물에 노출될 때 탐식세포(macrophage)가 세포 사멸 및 자가 형광을 일으키도록 하는 이종 유전 구조물을 운반하는 쥐의 종(strain)을 발생시키기 위한 현미주사를 사용하여 왔다. 이러한 유전자형질변환 쥐(transgenic mice)는 면역 반응 동안의 탐식세포 활성 및 종양 성장 동안의 탐식세포 활성의 연구에 있어서 중요한 역할을 해왔다.
종래 기술의 마이크로주사기(microinjector)가 마크로-규모 주사기(macro-scale syringe)와 유사한 방식으로 작동하는데: 압력 차이가 액체를 바늘을 통하여 세포 내로 밀어넣는다. 일부 경우에 있어서, 모세관 튜브로부터 불꽃을 사용하여 당겨진 유리 바늘이 난모세포의 세포막 및 핵막을 꿰뚫기 위해 사용될 수 있다. 그 후 정밀한 펌프가 바늘로부터 아주 소량의 유전 물질을 핵 내부로 방출시킨다.
최근에, 연구자들은 불꽃을 사용하여 당겨진 모세관(fire drawn capillaries)보다 더 작은, 실리콘 질화물 및 실리카 유리를 사용한 미세 현미주사 바늘을 제조하였다. 그렇지만 이들 더 미세한 바늘은 여전히 전통적인 마이크로주사기에서 사용된 것과 유사한 마크로-규모 펌프를 사용한다.
발명의 개요
따라서, 본 발명은 분자 물질을 조작하기 위한 시스템 및 방법을 제공한다. 예를 들면 한 양상에 있어서, 분자 물질을 조작하는 방법은 대전된 분자 물질과의 전기적 유사성을 갖는 미-대전된(uncharged) 바늘 구조물을 액체 환경 내 제1 유전자자리(locus)에 위치시키는 단계, 대전된 분자 물질의 적어도 일부가 상기 바늘 구조물과 결합하도록 상기 바늘 구조물을 대전시키는 단계, 상기 바늘 구조물 및 상기 제1 유전자자리를 서로에 대해 이동시키는 단계, 및 상기 바늘 구조물을 방전시켜 상기 대전된 분자 물질을 제2 유전자자리에서 분리시키는 단계를 포함할 수 있다. 바늘 구조물을 방전시키는 것은 다양한 방법으로 일어날 수 있음이 이해되어야 한다. 예를 들면, 한 양상에 있어서, 바늘 구조물은 결합된 대전된 분자 물질을 방출시키기에 충분한 정도로 방전될 수 있다. 또 다른 면에 있어서, 바늘 구조물을 방전시키는 것은 대전된 분자 물질이 바늘 구조물로부터 멀리 떨어지도록 하기 위하여 바늘 구조물 하전의 극성을 전환시키는 것을 포함할 수 있다.
본 발명의 양상에 따라 조작될 수 있는 다양한 대전된 분자 물질이 고찰된다. 이러한 예에는 DNA, RNA, 펩티드, 폴리머, 유기 분자, 무기 분자, 이온, 및 이들의 조합이 있으며, 여기에 제한되는 것은 아니다. 본 발명의 한 특정 면에 있어서, 대전된 분자 물질은 DNA, RNA, 펩티드, 및 이들의 조합을 포함할 수 있다. 또 다른 특정 면에서, 대전된 분자 물질은 DNA를 포함할 수 있다.
더욱이, 다수의 제1 및 제2 유전자자리가 고찰되며, 분자 물질 조작의 특성 및 정도는 환경 및 본 발명의 기술의 의도적인 사용에 의존하여 변화할 수 있다. 예를 들면 한 양상에서, 제2 유전자자리는 단일 세포 내에 위치될 수 있다. 또 다른 면에서, 제2 유전자자리는 단일 세포의 세포 핵 내에 위치될 수 있다. 또 다른 면에서, 제1 유전자자리는 단일 세포의 외부에 위치될 수 있다.
부가적으로, 바늘 구조물 및 제1 유전자자리를 서로에 대해 이동시키는 것은 제1 및 제2 유전자자리의 상대적 위치 및 이동 장치의 특성 및 배열에 따라 변화할 수 있다. 예를 들면 한 양상에 있어서, 바늘 구조물 및 제1 유전자자리를 서로에 대해 이동시키는 것은 바늘 구조물을 제1 유전자자리로부터 제2 유전자자리로 이동시키는 것을 포함한다. 또 다른 면에 있어서, 바늘 구조물은 연장 축을 포함하고 유전자자리 축은 제1 유전자자리와 제2 유전자자리 사이에서 정의된다. 바늘 구조물 및 제1 유전자자리가 서로에 대해 이동할 때, 상기 연장 축과 유전자자리 축 사이의 각도 상관관계(angular relationship)가 일정하게 유지된다.
본 발명은 또한 분자 물질을 조작하기 위한 시스템을 제공한다. 예를 들면 한 양상에 있어서, 분자 물질 조작 시스템은 바늘 구조물, 상기 바늘 구조물과 전기적으로 연결된(coupled) 대전 시스템, 상기 대전 시스템은 상기 바늘 구조물을 대전(charge) 및 방전(discharge)시키도록 작동될 수 있으며, 그리고 상기 바늘 구조물을 제1 유전자자리로부터 제2 유전자자리로 이동시키기 위하여 작동될 수 있는 이동 시스템을 포함할 수 있다. 한 특정 면에 있어서, 상기 시스템은 바늘 구조물과 결합한 대전된 분자 물질 샘플을 더욱 포함할 수 있다. 또 다른 특정 면에서, 상기 시스템은 이동 시스템의 작동 동안 바늘 구조물을 수용하도록 위치된 단일 세포를 더욱 포함할 수 있다. 한 양상에 있어서 상기 단일 세포는 난모세포일 수 있다.
또 다른 면에서, 분자 물질을 조작하기 위한 시스템은 이동가능한 지지 프레임 및 상기 이동가능한 지지 프레임에 결합된 바늘 구조물을 포함할 수 있는데, 여기서 상기 바늘 구조물은 그 위에서 분자 물질을 운송시키기 위해 작동가능하다. 더욱이, 상기 이동가능한 지지 프레임은 상기 바늘 구조물을 초기 위치에서 연장된 위치로 이동시키도록 작동가능하며, 여기서 상기 이동가능한 지지 프레임이 상기 바늘 구조물을 초기 위치에서 연장된 위치로 이동시킬 때 상기 바늘 구조물의 연장 축은 실질적으로 일정한 방향으로 유지된다. 한 구체 면에 있어서, 연장된 위치에 있는 바늘 구조물의 수직 상승은 초기 위치에 있는 바늘 구조물의 수직 상승과는 상이하다. 또 다른 구체 면에서, 상기 시스템은 바늘 구조물과 전기적으로 연결된 대전 시스템을 포함할 수 있는데, 여기서 상기 대전 시스템은 바늘 구조물을 대전 및 방전시키도록 작동가능하다. 또 다른 구체 면에서, 상기 시스템은 이동가능한 지지 프레임과 인접하여 위치된 지지체 구조물을 포함할 수 있는데, 여기서 상기 지지체 구조물은 연장된 위치일 때 바늘 구조물을 수용하는 위치에서 단일 세포를 고정하도록 작동될 수 있다.
또 다른 면에서, 분자 물질을 조작하기 위한 시스템은 이동가능한 지지 프레임, 및 상기 이동가능한 지지 프레임에 결합된 바늘 구조물을 포함할 수 있는데, 여기서 상기 바늘 구조물은 제1 대전 상태와 제2 대전 상태 사이에서 대전 가능하다. 더욱이, 상기 이동가능한 지지 프레임은 상기 바늘 구조물을 초기 위치에서 연장된 위치로 이동시키도록 작동가능하며, 여기서 상기 이동가능한 지지 프레임이 상기 바늘 구조물을 초기 위치에서 연장된 위치로 이동시킬 때 상기 바늘 구조물의 연장 축은 실질적으로 일정한 방향으로 유지된다. 한 구체 면에 있어서, 연장된 위치에 있는 바늘 구조물의 수직 상승은 초기 위치에 있는 바늘 구조물의 수직 상승과는 상이하다.
용어의 정의
본 발명을 설명하고 청구함에 있어서, 다음의 용어들이 아래에 제시된 정의에 따라 사용될 것이다.
단수 형태는 명확한 다른 지시가 없는 한 복수형태를 포함한다. 따라서, "지지체"는 하나 이상의 이러한 지지체를 의미하는 것을 포함하며, "난모세포"는 이러한 난모세포의 하나 이상을 의미한다.
본 명세서에서 사용된 바와 같이, 용어 "대전된 분자 물질"은 전기적으로 대전된 구조물에 끌리거나 또는 결합될 수 있는 임의 분자 물질을 의미하는 것으로 사용될 수도 있다. 따라서, 대전된 분자 물질은 알짜 전하(net charge)를 갖는 분자들뿐만 아니라 알짜 중성 전하를 갖지만 구조물에 대하여 인력을 가능하게 하는 전하 분포를 소유하는 분자들을 의미하는 것으로 사용될 수도 있다.
본 명세서에서 사용된 바와 같이, 용어 "펩티드"는 아미노산의 카르복실기에 의해 또 다른 아미노산의 알파 아미노기에 연결된 하나 이상의 아미노산을 포함하는 천연 또는 합성 분자를 의미하는 것으로 사용될 수 있다. 본 발명의 펩티드는 길이에 의해 제한되지 않으며, 따라서 "펩티드"는 폴리펩티드 또는 단백질을 포함할 수 있다.
본 명세서에서 사용된 바와 같이, 바늘 구조물과 관련하여 사용될 때 용어 "미-대전된(uncharged)"은 대전된 분자 물질과 비교하여 바늘 구조물에서 전하량의 상대적 수준을 의미하는 것으로 사용될 수 있다. 환언하면, 바늘 구조물의 전하량이 대전된 분자 물질의 이용가능한 부분을 끌어당기기에 충분하지않는 한 바늘 구조물은 "미-대전된" 것으로 고려될 수 있다. 물론 이용가능한 부분이라는 것은 분자 물질의 의도된 사용에 따라 변화할 수 있으며, 당해 기술분야의 통상의 기술자들이 이러한 의도된 사용에 대하여 어떤 이용가능한 부분이 제공되는지에 대하여 알 수 있음이 이해되어야 한다. 또한 측정가능한 전하가 없는 바늘 구조물이 본 정의에 따라 "미-대전된" 것으로 고려될 수 있음에 주의하여야 한다.
본 명세서에서 사용된 바와 같이, 분자 물질의 샘플과 관련사여 사용될 때 용어 "샘플"은 바늘 구조물 쪽으로 의도적으로 끌어 당겨졌거나 또는 바늘 구조물과 결합된 분자 물질의 일부를 의미하는 것으로 사용될 수 있다. 예를 들면, 바늘 구조물과 결합된 것으로 설명되는 DNA과 같은 분자 물질의 샘플은 바늘 구조물로 의도적으로 끌어 당겨진 DNA를 포함할 수 있으나, 단순히 바늘 구조물이 환경에 노출됨에 따라 바늘 구조물로 끌어 당겨진 DNA는 포함하지 않는다. "샘플"로 고려되지 않는 DNA의 한 예는 후속하여 공기에 노출되는 바늘 구조물과 결합할 수 있는 공기 중의 DNA 단편을 포함한다.
본 명세서에서 사용된 바와 같이, "인접하는(adjacent)"은 의도된 효과를 달성하기에 충분히 가깝거나 근접함을 의미한다.
본 명세서에서 사용된 바와 같이, "결합하다(associate)"는 반대 전하의 인력으로 인하여 구조물에 정전기 적으로 접촉하고 있는 분자 물질을 설명하기 위하여 사용된다. 예를 들면, 양 전하에 의해 구조물에 끌어 당겨진 DNA는 구조물에 결합되어 있다라고 말한다.
본 명세서에서 사용된 바와 같이, 용어 "실질적으로"는 활성, 특정, 물성, 상태, 구조, 항목, 또는 결과의 완전한 또는 거의 완전한 정도를 의미한다. 예를 들면, "실질적으로" 첨부된 물체는 완전하게 첨부되거나 또는 거의 완전하게 첨부된 물체를 의미한다. 완벽한 완전성으로부터 정확한 허용가능한 편차 정도는 일부 경우에 있어서 구체적인 내용에 의존할 수 있다. 그렇지만, 일반적으로 말해서 거의 완전성이라는 것은 완벽하고 전반적인 완전성이 달성되는 것과 동일한 결과를 낳는다. "실질적으로"의 사용은 활성, 특정, 물성, 상태, 구조, 항목, 또는 결과의 완전한 또는 거의 완전한 부재를 의미하는 부정적인 의미로 사용될 때 동일하게 적용된다. 예를 들면, 입자가 "실질적으로 없는" 조성물은 입자가 완전하게 없거나 또는 거의 완전하게 입자가 없어서 입자가 완전하게 없는 경우와 동일한 효과를 산출하는 것을 의미한다. 환언하면, 구성요소 또는 성분이 "실질적으로 없는" 조성물이라 함은 현실적으로는 측정될만한 효과가 없는 한도에서 이러한 구성요소 또는 성분을 함유할 수도 있다.
본 명세서에서 사용된 바와 같이, 용어 "약"은 주어진 수치가 바람직한 결과에 대한 영향을 미치지 않으면서 수치 범위 말단의 "조금 위" 또는 "조금 아래"일 수 있음을 제공하면서 수치 범위 말단에 대한 융통성을 제공하기 위하여 사용된다.
본 명세서에서 사용된 바와 같이, 복수의 항목, 구조 성분, 조성 성분, 및/또는 물질은 편의를 위하여 통상적인 리스트로 제시될 수 있다. 그렇지만, 이러한 리스트들은 각 리스트의 멤버들이 개별적이고 전형적인 멤버로서 개별적으로 정의되는 것으로 해석되어야 한다. 따라서, 이러한 리스트의 개개의 멤버들은, 상반되는 지시 없이는 단지 통상적인 그룹으로 제시되는 것에 기초하여 동일 리스트의 다른 멤버들과 사실상 균등한 것으로 해석되어서는 안 된다.
농도, 용량, 및 또 다른 수치 데이터는 범위 형식으로 표현되거나 제시될 수 있다. 이러한 범위 형식은 단지 편의 및 간결성을 위하여 사용되며 따라서 범위의 한계점으로 명확하게 언급된 수치를 포함할 뿐만 아니라 각각의 수치 및 하부 범위가 명확하게 언급된 것처럼 범위 내에 포함되는 모든 개별적인 수치 또는 하부-범위를 포함하는 것으로 유연성 있게 해석되어야만 한다는 것이 이해되어야 한다. 한 예로서, "약 1 내지 약 5"의 범위는 약 1 내지 약 5라는 명확하게 제시된 수치뿐만 아니라 제시된 범위 내 개별적인 수치 및 하부-범위를 포함하는 것으로 해석되어야 한다. 따라서, 이러한 수치 범위에 포함된 것은 2, 3, 및 4와 같은 개별적인 수치 및 개별적으로 1, 2, 3, 4, 및 5뿐만 아니라 1-3, 2-4, 및 3-5 등과 같은 하부-범위이다.
이러한 동일한 원칙은 최소값 또는 최대값으로 단지 하나의 수치를 언급하는 범위에도 적용된다. 더욱이, 이러한 해석은 범위의 폭 또는 설명되는 특정에 상관없이 적용되어야 한다.
도면의 간단한 설명
도 1은 본 발명의 한 구체예에 따르는 분자 물질 조작 시스템의 도면이다.
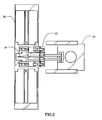
도 2는 본 발명의 또 다른 한 구체예에 따르는 분자 물질 조작 시스템의 도면이다.
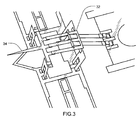
도 3은 본 발명의 또 다른 한 구체예에 따르는 분자 물질 조작 시스템의 도면이다.
도 4는 본 발명의 또 다른 한 구체예에 따르는 분자 물질 조작 시스템의 도면이다.
도 5는 본 발명의 또 다른 한 구체예에 따르는 픽셀 강도에 대한 DNA 농도의 그래프이다.
도 1은 본 발명의 한 구체예에 따르는 분자 물질 조작 시스템의 도면이다.
도 2는 본 발명의 또 다른 한 구체예에 따르는 분자 물질 조작 시스템의 도면이다.
도 3은 본 발명의 또 다른 한 구체예에 따르는 분자 물질 조작 시스템의 도면이다.
도 4는 본 발명의 또 다른 한 구체예에 따르는 분자 물질 조작 시스템의 도면이다.
도 5는 본 발명의 또 다른 한 구체예에 따르는 픽셀 강도에 대한 DNA 농도의 그래프이다.
상세한 설명
본 발명의 양상은 분자 물질을 조작하기 위한 방법 및 시스템을 제공한다. 이러한 방법 및 시스템은 분자 물질의 현실적인 조작뿐만 아니라 조작을 위하여 사용되는 장치 또는 장치들의 이동 및 배치를 포함할 수 있다.
따라서 분자 물질이 펌프 메커니즘의 사용 없이 바늘 구조물의 사용을 통하여 조작될 수 있음이 밝혀졌다. 이러한 "펌프-없는" 바늘 구조물은 대전된 분자 물질을 결합시키거나 방출시키기 위하여 전기 전하를 이용한다. 예를 들면 한 양상에 있어서, 분자 물질을 조작하기 위한 한 방법은 대전된 분자 물질과의 전기적 유사성을 갖는 미-대전된 바늘 구조물을 액체 환경 내 제1 유전자자리(locus)에 위치시키는 단계, 대전된 분자 물질의 적어도 일부가 상기 바늘 구조물과 결합하도록 상기 바늘 구조물을 대전시키는 단계, 상기 바늘 구조물 및 상기 제1 유전자자리를 서로에 대해 이동시키는 단계, 및 상기 바늘 구조물을 방전시켜 상기 대전된 분자 물질을 제2 유전자자리에서 분리시키는 단계를 포함할 수 있다. 이러한 방법은 제1 유전자자리로부터 제2 유전자자리로의 이동을 촉진시키기 위하여 분자 물질의 전하를 이용한다. 예를 들면 DNA의 경우, 이러한 이동은 DNA 분자들 내의 동등하지 않은 전하 분포에 의해 이루어진다. 더욱 상세하게는, DNA의 인산염 골격(backbone)은 인산염 당(per) 전자 하나인 알짜 전하를 가지며, 염기 쌍 당(per) 전체 전자 두 개를 제공한다. 이러한 DNA 분자의 외부 골격 상의 알짜 음성 전하는 대전된 바늘 구조물을 사용하여 DNA를 제1 유전자자리로부터 제2 유전자자리로 이동시키는 것을 가능하게 한다.
더욱 설명하면, 전기 하전이 바늘 구조물 내로 인가되고 대전된 분자 물질을 자신의 외부 표면으로 끌어당긴다. 그 후 바늘 구조물은 결합된 분자 물질과 함께 제1 유전자자리로부터 제2 유전자자리로 이동될 수 있다. 이러한 이동은 바늘 구조물을 제2 유전자자리로 이동시키는 것, 제2 유전자자리를 바늘 구조물로 이동시키는 것, 또는 이들 둘의 조합을 포함할 수도 있다는 점에 유의하여야 한다. 제2 유전자자리로의 이동은 또한 세포의 외부로부터 세포의 내부로의 이동, 액체의 한 부분으로부터 동일 액체의 또 다른 부분으로의 이동, 한 액체로부터 또 다른 액체로의 이동, 및 이들과 유사한 것을 포함할 수도 있다. 제2 유전자자리에 도달한 이후에, 그 후 분자 물질은 바늘 구조물의 표면으로부터 방출될 수 있다. 한 양상에 있어서, 이러한 방출은 바늘 구조물의 전하를 방출시켜 상기 분자 물질이 상기 구조물로부터 멀리 확산되도록 함으로써 달성될 수 있다. 또 다른 면에서, 바늘의 전하 극성이 역전되어서 제2 유전자자리에서 상기 분자 물질을 상기 바늘의 외부 표면으로부터 정전기 적으로 반발시킬 수 있다.
다양한 유형의 대전된 분자 물질이 본 발명의 양상에 따른 사용을 위하여 고려되며, 이러한 모든 대전된 분자 물질은 본 발명의 범위에 포함되는 것으로 해석된다. 비-제한적 실시예는 DNA, RNA, 펩티드, 폴리머, 유기 분자, 무기 분자, 이온, 및 이들의 조합을 포함한다. 한 구체 면에 있어서, DNA는 모든 형태의 천연 또는 합성 DNA일 수 있으며, 유전자 DNA(genomic DNA), cDNA, 플라스미드 DNA, 및 이와 유사한 것을 포함한다. 또 다른 구체 면에서, RNA는 모든 형태의 RNA이 있으며, RNAi, siRNA, shRNA, mRNA, tRNA, rRNA, 마이크로RNA, 및 이들의 혼성 시퀀스 또는 합성 또는 반-합성 시퀀스를 포함한다.
본 발명의 양상에 따르는 분자 물질의 조작은 다양한 상황 및 환경에서 유용할 수 있다. 예를 들면, 이러한 물질의 운송은 분자 물질을 단일 세포 내로 운송시키기 위해 사용될 수도 있다. 비록 임의 단일 세포가 본 발명이 범위에 포함되는 것으로 여겨질 수 있지만, 한 구체 면에서 단일 세포는 난모세포일 수 있다. 단일 세포의 또 다른 비-제한적 실시예는 신경 세포(neuronal cell), 피브로블라스트, 암 세포, 및 이와 유사한 것을 포함한다. 추가로, 분자 물질이 단일 세포 내의 특정 영역 또는 생물학적 구조물로 운송될 수 있음이 고려된다. 한 구체적 예에서, 분자 물질은 단일 세포의 핵으로 운송될 수도 있다.
결합된 분자 물질 및 바늘 구조물을 제1 유전자자리로부터 제2 유전자자리로 이동시키기 위한 다양한 움직임이 고려된다. 예를 들면 한 양상에서, 바늘 구조물은 선형 또는 실질적으로 선형인 경로를 따라서 제1 유전자자리로부터 제2 유전자자리로 이동될 수 있다. 이러한 움직임의 한 예는 제1 유전자자리 및 제2 유전자자리가 바늘 구조물의 연장 축에 실질적으로 배열되고, 제1 유전자자리는 바늘 구조물의 팁(tip)에 또는 팁 근처에 위치하는 상황을 포함할 수 있다. 바늘 구조물을 연장 축을 따라 앞으로 이동시킴에 의해, 바늘의 팁이 선형 경로를 따라 제1 유전자자리로부터 제2 유전자자리로 이동할 것이다. 그 대신에, 또 다른 양상에서, 바늘 구조물은 또한 바늘 구조물의 선형 경로로부터 이탈된 또 다른 방향으로 이동될 수도 있다. 그렇지만, 이러한 경우, 특히 분자 물질이 세포 내로 운송되는 경우에 있어서, 바늘 구조물의 방향을 유지시키는 것이 유리할 수 있다. 이러한 방향이 유지되지 않으면, 주입을 당하는 세포를 손상시킬 위험이 있을 수 있다. 더욱 상세하게는, 유전자자리 축이 제1 유전자자리와 제2 유전자자리 사이에서 정의된다면, 바늘 구조물과 제1 유전자자리가 서로에 대해 이동될 때 바늘 구조물의 연장 축과 상기 유전자자리 축 사이의 각도 관계가 일정하게 유지되어야 한다. 이렇게 함으로써, 바늘 구조물이 유전자자리 축으로부터 멀어지는 방향으로 이동되는 상황에서, 바늘 구조물의 방향이 이동 이전에 형성된 연장 축에 대하여 평행하게 유지될 것이다. 또 다른 면에서, 연장 축을 따르는 방향으로 제2 유전자자리가 접근되도록 바늘 구조물이 위치되는 조건에서는, 유전자자리 축과 연장 축 사이의 각도 관계는 일정하게 유지될 필요가 없다. 환언하면, 바늘 구조물이 중간 유전자자리(intermediate locus)로 이동될 수 있고, 상기 중간 유전자자리로부터 제2 유전자자리로의 바늘 구조물의 이동이 상기 중간 유전자자리에서 바늘 구조물의 연장 축을 따르는 방향으로 일어날 수 있다.
바늘 구조물이 제2 유전자자리에 도달하면, 분자 물질이 방출될 수 있다. 이러한 것은 다양한 방법으로 달성될 수 있으며, 분자 물질을 방출하는 모든 방법이 본 발명의 범위 내에 포함되도록 고려되어야 한다. 한 양상에 있어서, 바늘 구조물의 전하는 간단하게 방출될 수 있으며, 그에 따라 분자 물질이 제2 유전자자리에서 확산되는 것을 가능하게 한다. 바늘 구조물이 반드시 완전하게 방전되지 않을 수 있으며, 일부 경우에 있어서 바늘 구조물과 결합된 대전된 분자 물질을 실질적으로 방출하기에 충분한 정도로 방전될 수 있음을 유념하여야 한다. 또 다른 양상에 있어서, 바늘 구조물을 방전시키는 것은 바늘 구조물의 전하의 극성을 역전시키는 것을 포함할 수 있다. 이러한 방법을 사용함으로써, 분자 물질은 바늘 구조물로부터 능동적으로 방출될 수 있으며, 그에 따라 바늘 구조물이 제2 유전자자리에 존재하는 시간을 최소화한다.
본 발명은 또한 분자 물질을 조작하기 위한 시스템을 제공한다. 예를 들면 한 양상에 있어서, 분자 물질 조작 시스템은 바늘 구조물, 상기 바늘 구조물과 전기적으로 연결된 대전 시스템, 상기 대전 시스템은 상기 바늘 구조물을 대전 및 방전시키도록 작동될 수 있으며, 그리고 상기 바늘 구조물을 제1 유전자자리로부터 제2 유전자자리로 이동시키기 위하여 작동될 수 있는 이동 시스템을 포함할 수 있다. 한 특정 면에 있어서, 상기 시스템은 바늘 구조물과 결합한 대전된 분자 물질 샘플을 더욱 포함할 수 있다. 전술한 바와 같이, 이러한 분자 물질은 바늘 구조물에 의도적으로 끌어 당겨지거나 또는 바늘 구조물에 결합하는 임의 분자 물질을 포함할 수 있다. 이러한 샘플의 비-제한적 실시예는 DNA, RNA, 펩티드, 폴리머, 유기 분자, 무기 분자, 이온, 및 이들의 조합을 포함한다. 비-제한적 실시예의 더욱 구체적인 목록은 DNA, RNA, 펩티드, 및 이들의 조합을 포함한다.
한 구체적 양상에 있어서, 상기 시스템은 이동 시스템이 작동할 때 바늘 구조물을 수용하도록 위치된 단일 세포를 더욱 포함할 수 있다. 비록 다양한 단일 세포가 고려되더라도, 한 양상에 있어서 단일 세포는 난모세포이다.
무수한 바늘 구조물 배열 및 재료가 고려되며, 전기 대전 및 방전을 통하여 분자 물질의 조작을 가능하게 하는 임의 재료 및 배열이 본 발명의 범위에 포함되도록 고려되어야 한다는 것에 유념해야 한다. 한 양상에 있어서, 예를 들면, 바늘 구조물의 재료는 금속 또는 금속 합금, 전도성 유리, 폴리머성 물질, 반도체 물질, 및 이들의 조합을 포함할 수 있다. 바늘 구조물에서 사용하기 위한 물질의 비-제한적 실시예는 인듐, 금, 백금, 은, 구리, 결합 합금(associated alloy), 팔라듐, 텅스텐, 알루미늄, 티타늄, 및 이들의 조합을 포함한다. 바늘 구조물을 제조하기 위하여 사용될 수 있는 폴리머성 물질은 임의 전도성 폴리머를 포함할 수 있으며, 이러한 것의 비-제한적 실시예는 도데실 벤젠 설포네이트 이온이 첨가된(doped) 폴리피롤, 침적된 금속 입자를 갖는 SU-폴리머, 및 이들의 조합을 포함한다. 유용한 반도체 물질의 비-제한적 실시예는 단결정 실리콘, 다결정 실리콘, 게르마늄, 갈륨 비소, 인듐-주석 산화물, 및 이들의 조합을 포함할 수 있다. 일부 양상에 있어서 전도성 물질이 제2 물질의 상부에 코팅되는 전도성 층이 될 수 있는데, 여기서 상기 제2 물질은 바늘 구조물의 물리적 구조를 제공한다는 점 역시 유념하여야 한다. 추가로, 바늘 구조물은 유리와 같은 공동(hollow)의 비-전도성 물질로 구성될 수 있으며, 여기서 상기 공동 물질(hollow material)은 전도성 액체와 같은 전도성 물질로 채워진다. 바늘 구조물은 장치의 의도된 용도에 따라 다양한 크기일 수 있다. 그렇지만, 한 양상에 있어서, 바늘 구조물의 팁은 직경이 약 5 마이크론(microns) 미만일 수 있다. 또 다른 면에 있어서, 바늘 구조물의 팁은 직경이 약 1 마이크론 미만일 수 있다. 또 다른 면에 있어서, 바늘 구조물의 팁은 직경이 약 100 나노미터 미만일 수 있다.
바늘 구조물와 효과적으로 연결된 대전 시스템은 상기 장치를 전기적으로 대전시키고, 전하를 유지하고, 그리고 후속하여 방전시킬 수 있는 임의 시스템을 포함할 수도 있다. 비-제한적 실시예는 배터리, DC 전력원, 태양 전지, 정전기 발전기, 축전기(capacitor), 및 이와 유사한 것을 포함할 수 있다. 대전 시스템은 활성화 및 비활성화를 위한 스위치를 포함할 수 있으며, 일부 경우에 있어서 바늘 구조물에 대한 하전의 극성을 역전시키기 위한 극성 스위치를 또한 포함할 수도 있다. 한 양상에 있어서 상기 시스템은 추가로 다중 대전 시스템을 포함할 수도 있는데, 한 시스템은 바늘 구조물에 하전을 대전시키기 위한 것이며, 다른 대전 시스템은 바늘 구조물에 반대 극성의 하전을 대전시키기 위한 것이다. 한 실시예에 있어서, 초기에 비대전된 바늘 구조물은 대전된 분자 물질의 샘플에 접촉하도록 이동된다. 분자 물질은 물, 염수, 또는 분자 물질 조작에 유용한 또 다른 액체일 수 있다. 대전된 분자 물질의 전하의 극성에 반대되는 하전이 바늘 구조물에 인가되고, 그 결과 바늘 구조물로 분자 물질 샘플의 일부를 끌어당긴다. 그 후 분자 물질이 하전에 의해 제자리에서 유지되면서 바늘 구조물이 제1 유전자자리로부터 제2 유전자자리로 이동된다. 일단 제2 유전자자리에 도달하면, 바늘 구조물의 하전의 극성이 역전될 수 있고, 그에 따라 분자 물질을 바늘 구조물로부터 방출하고, 일부 경우에 있어서 분자 물질을 제2 유전자자리를 둘러싸는 영역 내로 능동적으로 밀어낸다. 후속하여 바늘 구조물은 제2 유전자자리로부터 철수될 수 있다.
바늘 구조물을 제1 유전자자리로부터 제2 유전자자리로 이동시키기 위한 다양한 이동 시스템이 고려된다. 분자 물질의 조절을 가능하게 하기에 충분한 정확성을 가지면서 바늘 구조물을 이동시킬 수 있는 임의 기술이 본 발명의 범위에 포함되는 것으로 고려된다. 이동 시스템의 비-제한적 실시예는 기계적 시스템, 자기적 시스템(magnetic system), 압전성 시스템(piezoelectric system), 정전기적 시스템(electrostatic system), 열-기계적 시스템, 공기역학 시스템(pneumatic system), 수력 시스템(hydraulic system), 및 이와 유사한 것을 포함한다. 바늘 구조물은 또한 사용자에 의해 수동으로 이동될 수 있다. 예를 들면, 사용자는 트랙을 따라 제1 유전자자리로부터 제2 유전자자리로 바늘 구조물을 밀 수 있다. 또한, 이동 시스템은 아래에서 더욱 상세하게 설명된다.
본 발명의 또 다른 양상에 있어서, 이동가능한 지지 프레임, 상기 이동가능한 지지 프레임과 결합된 바늘 구조물을 포함하는 분자 물질 조작 시스템이 제공되는데, 여기서 상기 바늘 구조물은 분자 물질을 운송하도록 작동되고, 상기 이동가능한 지지 프레임은 상기 바늘 구조물을 초기 위치에서부터 연장된 위치로 이동시키도록 작동되고, 여기서 상기 이동가능한 지지 프레임이 상기 바늘 구조물을 초기 위치에서 연장된 위치로 이동시킬 때 상기 바늘 구조물의 연장 축은 실질적으로 일정한 방향으로 유지된다. 한 구체 면에 있어서, 연장된 위치에 있는 바늘 구조물의 수직 상승은 초기 위치에 있는 바늘 구조물의 수직 상승과는 상이하다.이러한 경우, 연장된 위치에 있는 바늘 구조물의 연장 축은 초기 위치에 있는 바늘 구조물의 연장 축에 평행하거나 또는 실질적으로 평행하다. 더욱이, 상기 시스템은 전술한 대전 시스템을 포함할 수 있다. 본 명세서에서 사용된 용어 "수직"은 초기 위치에 있는 바늘 구조물의 연장 축에 따른 이동을 의미한다는 점에 유의하여야 한다.
분자 물질 조작의 특성에 따라 상기 시스템의 추가적인 구성성분이 고려된다. 예를 들면, DNA와 같은 분자 물질을 단일 세포의 핵으로 운송하기 위하여 사용되는 시스템은 이동가능한 지지 프레임에 인접하여 위치된 지지체 구조물을 포함할 수 있는데, 여기서 상기 지지체 구조물은 연장된 위치일 때 바늘 구조물을 수용하는 위치에서 단일 세포를 고정하도록 작동될 수 있다. 난모세포를 붙잡기 위한 이러한 지지체 구조물을 갖는 시스템의 한 예가 도 1에 도시되어 있다. 이동가능한 지지 프레임(16)에 의해서 바늘 구조물(14)이 연장된 위치로 이동될 때, 바늘 구조물(14)을 수용하는 위치에서 난모세포(18)를 붙잡기 위하여 한 쌍의 난모세포 지지체(12)가 사용된다. 이러한 예에서, 바늘 구조물이 연장된 위치로 이동되었을 때 난모세포의 핵이 바늘 구조물과 일렬이 되도록 난모세포(18)의 중앙이 위치된다. 또 다른 예에서, 초기 위치(도시되지 않음)일 때 난모세포의 대략적인 중앙이 바늘 구조물의 연장 축에 일렬이 되도록, 이동가능한 지지 프레임을 보유하는 기판의 움푹한 곳(recess)에 난모세포가 위치될 수도 있다. 따라서 이러한 배열에서 상기 연장된 위치는 바늘 구조물을 연장 축을 따라 난모세포를 향하여 이동시킴에 따라 달성될 수 있다. 지지체 구조물에 대한 추가적인 배열은 본 발명의 설명을 이해하는 당해 기술분야의 통상의 기술자들에게 명백할 것이며, 이러한 배열은 본 발명의 범위에 포함된다고 여겨진다.
본 발명의 또 다른 면에서, 분자 물질을 조작하기 위한 시스템은 이동가능한 지지 프레임, 및 상기 이동가능한 지지 프레임에 결합된 바늘 구조물을 포함할 수 있는데, 여기서 상기 바늘 구조물은 제1 대전 상태와 제2 대전 상태 사이에서 대전 가능하며, 상기 이동가능한 지지 프레임은 상기 바늘 구조물을 초기 위치에서 연장된 위치로 이동시키도록 작동가능하며, 여기서 상기 이동가능한 지지 프레임이 상기 바늘 구조물을 초기 위치에서 연장된 위치로 이동시킬 때 상기 바늘 구조물의 연장 축은 실질적으로 일정한 방향으로 유지된다. 더욱이, 한 구체 면에 있어서, 연장된 위치에 있는 바늘 구조물의 수직 상승은 초기 위치에 있는 바늘 구조물의 수직 상승과는 상이하다.
전술한 바와 같이, 본 발명의 양상에 따르는 분자 물질 조작을 위한 다양한 배치가 고려된다. 구체적인 예에서, 이종 분자 물질을 단일 세포 내로 유입시키기 위하여 무-펌프 마이크로 전기기계 시스템(micro electromechanical system, MEMS) 장치가 제공된다. 이러한 장치의 작은 크기 때문에, 적어도 실질적으로 자급자족인(self-contained) 시스템을 고안하는 것이 유리할 수도 있다. 본 발명의 분자 물질 조작 기술의 이용은 정밀 주사 펌프에 대한 요구를 제거하며, 그에 따라 이러한 자급자족 시스템(self-contained system)을 촉진시킨다.
이종 분자 물질을 난모세포와 같은 단일 세포 내에 주입시키기 위하여, 시스템은 세포를 효과적으로 감금하고 이종 분자 물질을 세포의 핵 내로 유입시켜야 한다. 도 1에 도시된 바와 같이, 시스템은 난모세포 주위에 배치된 세 개의 폴리실리콘 아암(arm)을 사용할 수 있다. 세 개의 아암 중 두 개(지지체 구조물(12))는 세포를 감금하도록 배치되고 배열되는 반면, 세 번째(이동가능한 지지 프레임(16))는 분자 물질을 세포 내로 유입시키기 위한 바늘 구조물을 포함한다. 한 양상에 있어서, 상기 세 개의 아암은 이들이 서로 접촉함에 따라 난모세포를 적절한 위치에 배치시킬 것이다. 전술한 바와 같이, 상기 세 개의 아암 모두는 사용자에 의해 수동으로 움직여질 수 있거나, 또는 이들은 모터 또는 또 다른 이동 시스템에 의해 움직여질 수 있다.
난모세포를 제 위치에서 붙잡기 위하여, 상기 두 개의 지지체 구조물 아암은 평면으로부터 상승하고 세포 쪽으로 이동한다. 상기 아암들은 박편(lamina-emergent)이고, 포인트를 변화시키며(change point), 평행-안내(parallel-guiding)되고, 6-바((six-bar)인 메커니즘이며, 운동학적으로 칩 기판에 근거하며, 슬라이더로부터 나오는 선형적 투입을 수용한다. 분자 물질을 운송하는 동안 좌우 및 수직으로의 이동을 방지하기 위하여, 감금 아암들은 세포의 정중선(midline) 상부에서 세포 벽(cell wall)에 접촉하도록 고안된다. 쥐 세포(직경 80-100 μm)와 같은 난모세포에 대하여, 감금 아암들은 그 규격 위치로부터 68.2 μm의 전체 수직 이동 및 84.6 μm의 전체 수평 이동을 갖도록 고안된다. 이러한 치수를 고려하면, 이 발명이 속하는 기술분야의 통상의 기술자들은 또 다른 세포 크기에 적용가능하도록 본 발명의 시스템을 용이하게 변형시킬 수 있을 것이다. 따라서 감금 아암의 큰 수평 이동은 세포가 초기에 위치할 수 있는 넓은 면적을 고려한 것이다. 감금 아암과 유사하게, 바늘 아암은 슬라이더로부터 나오는 선형적 투입을 수용하는 박편이고, 포인트를 변화시키며, 평행-안내되고, 6-바 인 메커니즘으로 제조될 수 있다. 그렇지만, 바늘 구조물 메커니즘은 이동가능한 지지 프레임에 부착된다. 상기 이동가능한 지지 프레임은 쥐 난모세포에 대하여 50 μm의 평면-내 이동을 갖는 컴플라이언트 평행 안내 메커니즘이다. 한 양상에 있어서, 상기 이동가능한 지지 프레임은 충분히 경직되어 그 결과 슬라이더가 앞쪽으로 이동할 때, 운송 단계에서 바늘은 최소한의 수평 이동을 동반하면서 평면으로부터 상승한다. 더욱이, 앞쪽으로의 이동은 상기 이동가능한 지지 프레임을 빗겨가게 하고 바늘 구조물을 그 연장된 위치에서 수평으로 제2 유전자자리 쪽으로 이동하게 하며, 그 결과 초기 위치에서의 바늘 구조물의 연장 축과 연장된 위치에서의 연장 축 사이의 평행 관계를 유지시킨다. 전술한 시스템은 도 2 및 도 3에 도시된다. 도 2는 초기 위치에서의 시스템을 도시하며, 이 시스템은 연장된 위치에서 바늘 구조물(24)의 수평 이동을 촉진하기 위하여 이동가능한 지지 프레임(22), 바늘 구조물(24), 및 겹쳐진 컴플라이언트 빔 서스펜션(26)을 포함한다. 도 2에 도시된 양상에 있어서, 사용자가 장치를 초기 위치에서부터 연장된 위치로 수동으로 이동시키는 것을 가능하게 하는 수동 슬라이드(28)가 추가로 도시되어 있다. 본 시스템은 바늘 구조물을 대전시키는 전기 접촉기(electrical contact)를 추가로 포함할 수 있다(도시되지 않음).
도 3은 연장된 위치에서의 시스템을 도시한다. 이동가능한 지지 프레임(32)이 도 2에 도시된 초기 위치에서부터 이동함에 따라, 바늘 구조물(34)은 초기 위치에서의 바늘 구조물과 평행한 방향으로 유지된다는 점에 유의하라.
이하의 설명은 DNA에 관한 것이지만, 본 발명의 범위는 여기에 제한되지 않는다. DNA는 편의상 다양한 구체 예를 설명하기 위하여 사용된다. 비록 DNA가 0(zero)의 알짜 전하를 갖지만, DNA는 모든 염기 쌍에 대하여 두 개의 전자와 동일한 음성 특성을 결과하는 내부 전하의 불균형 분포를 갖는다. DNA의 전기적 특성을 이용하여, 바늘 구조물이 정전기적 전하를 사용하여 분자 물질을 끌고, 결합하고, 방출하도록 고안될 수 있다. 따라서, 바늘은 펌프와 모세관을 요구하지 않으며, 단지 용이하게 제조된, 고체의 뾰족한 몸체로 구성된다. MEMS 칩의 밑바닥 모노실리콘 층과 바늘은 축전기를 형성할 수 있다. 이동가능한 지지 프레임의 어느 한쪽 면에 부착된 컴플라이언트 빔(compliant beam)을 사용하여 전압이 바늘 구조물에 인가된다. 상기 컴플라이언트 빔은 고도로 겹쳐질 수 있으며, 바늘 구조물이 수평 축에 대하여 회전하는 것을 야기할 수 있는 모멘트(moment)의 발생을 방지하기 위하여 두 개의 수직 다리 사이의 대략적인 중간 지점에서 바늘 구조물에 부착될 수 있다. 상기 컴플라이언트 빔은 장치 근처에 있는 고정된 전기 결합 패드에 전기적으로 연결되어 있어서 이를 통하여 전하가 인가될 수 있다. 이러한 경우에, 음성으로 하전된 DNA 분자를 끌기 위하여 양성 전하가 인가될 수 있다. 전압공급원의 음극 단자(negative terminal)가 밑에 놓인 모노 실리콘 기판에 연결된 결합 패드에 부착될 수 있다.
MEMS 구조는 다양한 방법에 의해 달성될 수 있다. MEMS 방법은 그 자체로 잘 알려져 있으며, 상세하게 설명될 것이다. 그렇지만, 대표적인 예는 표면이 마이크로기계가공된(micromachined) 폴리실리콘 구조물을 위한 제작 공정인 폴리MUMP (폴리실리콘 MEMS 다중-사용자 공정, Polysilicon MEMS Multi-User Processes)이다(MEMSCAP USA).
따라서, 개시된 MEMS 시스템은 다음과 같이 작동될 수 있다: 바늘 구조물을 함유하는 용액에 유입된다. 바늘 구조물에 양성 전하가 인가되어 DNA 샘플을 끌어당긴다. 난모세포와 같은 단일 세포가 바늘 구조물 및 결합된 DNA를 수용하는 지점에 위치된다. 도 4에 도시된 바와 같이, 감금 구조물(42)이 상승하여 정렬되어 난모세포를 감금한다. 도 4에서, 난모세포는 패드(44) 상부에 위치될 수 있다. 이동가능한 지지 프레임(46)이 연장된 위치로 상승하고, 바늘에 의해 핵에 구멍이 뚫릴 때까지 바늘 구조물(48)이 난모세포 내를 향하여 수평으로 연장된다. 그 후 전기 전하의 극성이 역전되어 DNA를 난모세포 핵 내에 방출하고, 바늘 구조물은 세포로부터 철수될 수 있다.
한 양상에 있어서, 실제로 유용하기 위하여, 자급자족인 펌프없는 MEMS 주사 장치는 세 가지 주된 제약을 만족해야 한다. 첫째, 실제로 유용하기 위하여, MEMS 장치는 상당히 짧은 시간에 적당량의 DNA를 그 표면상에 집결시켜야 한다. 둘째, 세포 생존의 가능성을 증가시키기 위하여, MEMS 바늘 구조물은 가능한 한 짧은 시간 동안 세포 내부에 존재해야 한다; 예를 들면, MEMS 바늘 구조물은 그 표면에 집결된 DNA를 수 초 내에 반발시킬 수 있어야 한다. 셋째, 장치 또는 세포의 피해를 방지하기 위하여, 그리고 의도되지 않은 거품의 형성을 방지하기 위하여, MEMS 바늘 구조물은 주변의 물의 전기분해를 일으키지 말아야 한다. 일부 경우에 있어서, MEMS 바늘 구조물을 둘러싸는 물의 전기분해를 방생시키지 않는 것은 특히 제한적일 수 있다. 초기 시행가능성 시험에 있어서, 0.9% NaCl의 수용액(즉, 염 용액) 내에 침적된 금이 결합된 패드(gold bond pad)의 1.8 V에서 전기분해가 발생하였다. 초기 시험에서, 전기분해가 발생하는 것이 허용될 때, 폴리실리콘-상의-금 결합 패드(gold-on-polysilicon bond pad)의 탈박막화(delamination), 및 폴리실리콘-상의-금 결합 패드로부터의 금의 거의 완전한 제거가 관찰되었다. 따라서, 몇몇 응용에 있어서, MEMS 바늘 구조물에 대한 작동 전압은 1.8 V 미만이어야 한다.
실시예
다음의 실시예는 본 발명의 일부 구체 예에 대한 더욱 명확한 이해를 도모하기 위하여 제공되며, 본 발명을 제한하고자 하는 의도는 없다.
실시예
1:
DNA
시각화 및 영상화 방법
다음의 실시예에서 DNA를 시각화하기 위하여 4',6-디아미디노-2-페닐인돌 디하이드로 클로라이드(DAPI)를 사용하였다. DAPI는 낮은 독성을 나타내며 자외선 조사 하에서 강한 형광을 나타낸다. 물에 용해되고 DNA에 결합하지 않았을 때, DAPI는 355 nm(자외선)의 여기 최대값(excitation maximum) 및 453 nm(청색 빛)의 방출 최대값을 갖는다. DAPI가 DNA에 결합할 때, 그 여기 최대값은 388 nm로 변하고, 그 방출 최대값은 454 nm로 이동하며, 방출된 빛의 밝기(intensity)는 자유 DAPI와 비교하여 대략 20배 증가한다. DAPI가 DNA에 결합할 때 방출 밝기에 있어서의 증가는 미결합 DAPI와 DAPI-착색된 DNA를 구별 가능하게 한다.
DAPI-착색된 DNA는 DAPI 착색된 샘플을 영상화하기 위한 의도적으로-구성된 청색 빛 필터 및 UV 조사를 동반하는 자스 악시오스콥 형광 현미경(Zeiss Axioskop Fluorescence Microscope)을 사용하여 가시화되었다. DAPI-DNA 착물이 가시광선 스펙트럼의 청색 영역에서 형광을 발하기 때문에, 영상 분석을 단순화하기 위하여 청색 채널은 미가공 RGB 영상으로부터 제거된다. 바늘 구조물 상부 또는 그 근처에서 DNA 농도의 정량적인 평가를 제공하기 위하여, 회귀모델(regression model)이 DNA 농도(C)에 대한 함수로서 청색 화소 밝기(I)로 구성된다. 공지되고 균일한 농도의 DAPI 착색된 DNA 샘플이 전술한 파라미터를 이용하여 영상화되며, 영상의 평균 청색 채널 화소 밝기가 MATLAB 스크립트를 사용하여 계산된다. ng/μL 단위의 농도와 청색 화소 밝기 사이의 관계는 도 5에 제시된 선형이다. 데이터에 대하여 적합한 선은 방정식 I에 제시된 관계를 나타낸다.
청색 채널 밝기 측정은 95% 오차 한계로 제시되며, 방정식 I에서 제시된 데이터의 선형 모델은 실선에 의해 제시된다. 사용된 장기간의 노출(6초) 때문에, 절편 값(intercept value)(0 ng/μL에서의 청색 화소 밝기)은 주변 조명 조건에서 변화하기 매우 쉽다. 주변 조명 조건이 절편값을 방정식 I에 제시된 83.07로부터 벗어나게 하는 경우, DNA가 존재하지 않는 적절한 매질(증류수 또는 0.9% NaCl)에 침적된 MEMS 염료의 참조 영상(reference image)이 이러한 조명 조건하에서의 절편 값을 계산하기 위하여 사용될 수 있다.
실시예
2:
DNA
인력 실험
DNA 인력 및 반발 실험은 증류수 및 0.9% 염 용액 양쪽 모두에서 수행된다. 두 경우 모두에서, 실험은 동일한 기준을 따르며, 다만 장치가 침적되는 매질만 예외이다. 본 명세서에서 설명된 MEMS 장치를 증류수 또는 0.9% 염 용액 대략 2 mm로 덮는다. 306 ng/μL DAPI 착색된 DNA의 1-2 μL 방울을 눈금 피펫을 사용하여 장치 근처의 용액에 놓는다. MEMS 장치의 바늘 구조물을 1.5 V DC를 제공하는 전압원의 양극 단자에 접촉시킨다. MEMS 장치의 기판을 전압원의 음극 단자에 접촉시킨다. 바늘 구조물 표면상의 DAPI-착색된 DNA를 검증하기 위하여 영상이 얻어질 수 있다. DNA의 대략적인 농도가 방정식 I의 선형 모델을 사용하여 계산될 수 있다.
실시예
3:
DNA
반발 실험
실시예 2에서 설명한 바와 같이, 바늘 구조물을 1.5 V DC 전압원의 양극 단자에 접촉시키고 MEMS 장치 기판을 전압원의 음극 단자에 접촉시킴으로써, DNA가 MEMS 바늘 구조물의 팁(tip)으로 끌어 당겨진다. DNA를 끌어당긴 이후, 전기 전하의 극성이 역전되어 양극 단자가 MEMS 장치 기판에 접촉되고 음극 단자가 바늘 구조물에 접촉된다. DNA 방출 및 반발을 검증하기 위하여 극성이 역전되는 시간으로부터 영상이 얻어질 수 있다. 더욱이, MEMS 바늘 구조물을 음극 단자에 접촉시킬 때와 DNA가 바늘 구조물로부터 명확하게 반발 될 때 사이의 시간이 계산될 수 있고, 대략적인 농도가 방정식 I에서 주어진 선형 모델을 사용하여 계산될 수 있다.
실시예
4: 증류수 실험
본 명세서에서 설명된 MEMS 장치를 증류수 약 2 mm로 덮는다. 306 ng/μL DAPI 착색된 DNA의 1-2 μL 방울을 눈금 피펫을 사용하여 장치 근처의 증류수에 놓는다. MEMS 장치의 바늘 구조물을 1.5 V DC를 제공하는 전압원의 양극 단자에 접촉시킨다. MEMS 장치의 기판을 전압원의 음극 단자에 접촉시킨다. 바늘 구조물 표면상의 DAPI-착색된 DNA를 검증하기 위하여 영상이 얻어질 수 있다. 배양 후 1시간 17분 이후에, 약 2.4-2.5 ng/μL가 대전된 바늘 구조물의 팁에 끌어 당겨진다. 근사치는 방정식 I의 선형 모델로부터 유도된다.
DNA를 끌어당긴 이후, 전기 전하의 극성이 역전되어 양극 단자가 MEMS 장치 기판에 접촉되고 음극 단자가 바늘 구조물에 접촉된다. 음성으로 대전된 바늘 구조물은 극성 변화 후 6초 이내에 그 팁으로부터 상당량의 DNA를 반발시킨다.
실시예
5: 0.9% 염 용액 실험
본 명세서에서 설명된 MEMS 장치를 0.9% 염 용액 약 2 mm로 덮는다. 306 ng/μL DAPI 착색된 DNA의 1-2 μL 방울을 눈금 피펫을 사용하여 장치 근처의 염 용액에 놓는다. MEMS 장치의 바늘 구조물을 1.5 V DC를 제공하는 전압원의 양극 단자에 접촉시킨다. MEMS 장치의 기판을 전압원의 음극 단자에 접촉시킨다. 이러한 식으로 접촉되고 0.9% NaCl 용액에 침적되었을 때, MEMS 바늘 구조물은 약 230 pf의 전기용량(capacitance)을 갖는다. 바늘 구조물 표면상의 DAPI-착색된 DNA를 검증하기 위하여 영상이 얻어질 수 있다. 배양 후 5분 46초 이후에, 약 2.2-2.4 ng/μL가 대전된 바늘 구조물의 팁에 끌어 당겨진다. 근사치는 방정식 I의 선형 모델로부터 유도된다.
DNA를 끌어당긴 이후, 전기 전하의 극성이 역전되어 양극 단자가 MEMS 장치 기판에 접촉되고 음극 단자가 바늘 구조물에 접촉된다. 음성으로 대전된 바늘 구조물은 극성 변화 후 6초 이내에 그 팁으로부터 상당량의 DNA를 반발시킨다.
전술한 응용의 조성 및 방식은 단지 본 발명의 바람직한 구체 예의 예시적인 것이다. 수많은 변형 및 대안이 본 발명의 범위 및 개념을 벗어나지 않으면서 통상의 기술자에 의해 고안될 수 있으며 첨부된 청구범위가 이러한 변형 및 대안을 포함하도록 의도된다. 따라서 본 발명이 가장 실현 가능하고 바람직한 구체 예와 관련하여 구체적이고 상세하게 설명되었지만, 크기, 재료, 모양, 형태, 기능 및 작동 및 조립 방식에 있어서의 변화를 포함하여 다양한 변형이 있을 수 있다는 것은 통상의 기술자에게 명확할 것이며, 그 용도는 본 명세서에서 제시된 원칙 및 개념의 범위로부터 벗어나지 않을 것이다.
Claims (23)
- 대전된 분자 물질과의 전기적 유사성을 갖는 미-대전된(uncharged) 바늘 구조물을 액체 환경 내 제1 유전자자리(locus)에 위치시키는 단계;
상기 대전된 분자 물질의 적어도 일부가 상기 바늘 구조물과 결합하도록 상기 바늘 구조물을 대전시키는 단계;
상기 바늘 구조물 및 상기 제1 유전자자리를 서로에 대해 이동시키는 단계; 및
상기 바늘 구조물을 방전시켜 상기 대전된 분자 물질을 제2 유전자자리에서 분리시키는 단계;
를 포함하는, 분자 물질 조작 방법. - 청구항 1에 있어서, 상기 대전된 분자 물질은 DNA, RNA, 펩티드, 폴리머, 유기 분자, 무기 분자 및 이온으로 구성된 군으로부터 하나 이상 선택되는 멤버를 포함함을 특징으로 하는, 분자 물질 조작 방법.
- 청구항 1에 있어서, 상기 대전된 분자 물질은 DNA를 포함함을 특징으로 하는, 분자 물질 조작 방법.
- 청구항 1에 있어서, 상기 제2 유전자자리는 단일 세포 내에 있음을 특징으로 하는, 분자 물질 조작 방법.
- 청구항 4에 있어서, 상기 제2 유전자자리는 단일 세포의 세포 핵 내에 있음을 특징으로 하는, 분자 물질 조작 방법.
- 청구항 4에 있어서, 상기 제1 유전자자리는 단일 세포의 외부에 있음을 특징으로 하는, 분자 물질 조작 방법.
- 청구항 4에 있어서, 상기 바늘 구조물 및 상기 제1 유전자자리를 서로에 대해 이동시키는 단계는 상기 바늘 구조물을 상기 제1 유전자자리로부터 상기 제2 유전자자리로 이동시키는 단계를 포함함을 특징으로 하는, 분자 물질 조작 방법.
- 청구항 7에 있어서,
상기 바늘 구조물은 연장 축을 포함하며;
유전자자리 축은 제1 유전자자리와 제2 유전자자리 사이에서 정의되며;
여기서 상기 바늘 구조물 및 제1 유전자자리가 서로에 대해 이동할 때, 상기 연장 축과 상기 유전자자리 축 사이의 각도 상관관계가 일정하게 유지됨;
을 특징으로 하는, 분자 물질 조작 방법. - 청구항 7에 있어서,
상기 바늘 구조물은 연장 축을 포함하며;
상기 바늘 구조물은 중간 유전자자리(intermediate locus)로 이동되며;
상기 중간 유전자자리로부터 상기 제2 유전자자리로의 바늘 구조물의 이동이 상기 중간 유전자자리에서 바늘 구조물의 연장 축을 따르는 방향으로 일어남;
을 특징으로 하는, 분자 물질 조작 방법. - 청구항 1에 있어서, 상기 바늘 구조물을 방전시키는 것은 바늘 구조물 하전의 극성을 역전시키는 것을 추가로 포함함을 특징으로 하는, 분자 물질 조작 방법.
- 청구항 1에 있어서, 상기 바늘 구조물을 방전시키는 것은 상기 바늘 구조물과 결합된 상기 대전된 분자 물질을 실질적으로 방출하기에 충분한 정도로 상기 바늘 구조물을 방전시키는 것을 포함함을 특징으로 하는, 분자 물질 조작 방법.
- 바늘 구조물;
상기 바늘 구조물과 전기적으로 연결된 대전 시스템, 여기서 대전 시스템은 상기 바늘 구조물을 대전 및 방전시키도록 작동될 수 있으며; 그리고
상기 바늘 구조물을 제1 유전자자리로부터 제2 유전자자리로 이동시키기 위하여 작동될 수 있는 이동 시스템;
을 포함하는, 분자 물질 조작 시스템. - 청구항 12에 있어서, 상기 바늘 구조물과 결합된 대전된 분자 물질 샘플을 추가로 포함함을 특징으로 하는, 분자 물질 조작 시스템.
- 청구항 13에 있어서, 상기 대전된 분자 물질 샘플은 DNA, RNA, 펩티드, 폴리머, 유기 분자, 무기 분자 및 이온으로 구성된 군으로부터 하나 이상 선택되는 멤버를 포함함을 특징으로 하는, 분자 물질 조작 시스템.
- 청구항 13에 있어서, 상기 대전된 분자 물질 샘플은 DNA, RNA 및 펩티드로 구성된 군으로부터 하나 이상 선택되는 멤버를 포함함을 특징으로 하는, 분자 물질 조작 시스템.
- 청구항 12에 있어서, 상기 이동 시스템이 작동할 때 상기 바늘 구조물을 수용하도록 위치된 단일 세포를 더욱 포함함을 특징으로 하는, 분자 물질 조작 시스템.
- 청구항 16에 있어서, 상기 단일 세포는 난모세포임을 특징으로 하는, 분자 물질 조작 시스템.
- 이동가능한 지지 프레임;
상기 이동가능한 지지 프레임에 결합된 바늘 구조물, 여기서 바늘 구조물은 분자 물질을 운송시키도록 작동가능함;을 포함하며,
상기 이동가능한 지지 프레임은 상기 바늘 구조물을 초기 위치로부터 연장된 위치로 이동시키도록 작동가능하며;
여기서 상기 이동가능한 지지 프레임이 상기 바늘 구조물을 상기 초기 위치로부터 상기 연장된 위치로 이동시킬 때, 상기 바늘 구조물의 연장 축은 실질적으로 일정한 방향으로 유지되는;
분자 물질 조작 시스템. - 청구항 18에 있어서, 상기 연장된 위치에 있는 바늘 구조물의 수직 상승이 상기 초기 위치에 있는 바늘 구조물의 수직 상승과 상이함을 특징으로 하는, 분자 물질 조작 시스템.
- 청구항 18에 있어서, 상기 바늘 구조물과 전기적으로 결합된 대전 시스템을 더욱 포함하며, 여기서 대전 시스템은 상기 바늘 구조물을 대전 및 방전시키도록 작동가능함을 특징으로 하는, 분자 물질 조작 시스템.
- 청구항 18에 있어서, 상기 이동가능한 지지 프레임과 인접하여 위치된 지지체 구조물을 더욱 포함하며, 여기서 지지체 구조물은 연장된 위치일 때 상기 바늘 구조물을 수용하는 위치에서 단일 세포를 고정하도록 작동될 수 있음을 특징으로 하는, 분자 물질 조작 시스템.
- 이동가능한 지지 프레임;
상기 이동가능한 지지 프레임에 결합된 바늘 구조물, 여기서 바늘 구조물은 제1 대전 상태와 제2 대전 상태 사이에서 대전 가능함;을 포함하며,
상기 이동가능한 지지 프레임은 상기 바늘 구조물을 초기 위치로부터 연장된 위치로 이동시키도록 작동가능하며;
여기서 상기 이동가능한 지지 프레임이 상기 바늘 구조물을 상기 초기 위치로부터 상기 연장된 위치로 이동시킬 때 상기 바늘 구조물의 연장 축은 실질적으로 일정한 방향으로 유지되는,
분자 물질 조작 시스템. - 청구항 22에 있어서, 연장된 위치에 있는 바늘 구조물의 수직 상승이 초기 위치에 있는 바늘 구조물의 수직 상승과 상이함을 특징으로 하는, 분자 물질 조작 시스템.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US95862407P | 2007-07-09 | 2007-07-09 | |
| US60/958,624 | 2007-07-09 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20100037615A true KR20100037615A (ko) | 2010-04-09 |
Family
ID=40229464
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020107001996A KR20100037615A (ko) | 2007-07-09 | 2008-07-09 | 대전된 분자 조작을 위한 방법 및 이를 위한 장치 |
Country Status (7)
| Country | Link |
|---|---|
| US (3) | US20100323419A1 (ko) |
| EP (1) | EP2167632A4 (ko) |
| JP (1) | JP2010532997A (ko) |
| KR (1) | KR20100037615A (ko) |
| AU (1) | AU2008275064A1 (ko) |
| CA (1) | CA2692742A1 (ko) |
| WO (1) | WO2009009610A2 (ko) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20160010067A (ko) | 2014-07-18 | 2016-01-27 | 인제대학교 산학협력단 | 양말 착용 보조장치 |
Families Citing this family (23)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20100323419A1 (en) | 2007-07-09 | 2010-12-23 | Aten Quentin T | Methods and Devices for Charged Molecule Manipulation |
| US9305735B2 (en) | 2007-09-28 | 2016-04-05 | Brigham Young University | Reinforced polymer x-ray window |
| US8736138B2 (en) | 2007-09-28 | 2014-05-27 | Brigham Young University | Carbon nanotube MEMS assembly |
| US8498381B2 (en) | 2010-10-07 | 2013-07-30 | Moxtek, Inc. | Polymer layer on X-ray window |
| US8247971B1 (en) | 2009-03-19 | 2012-08-21 | Moxtek, Inc. | Resistively heated small planar filament |
| US7983394B2 (en) | 2009-12-17 | 2011-07-19 | Moxtek, Inc. | Multiple wavelength X-ray source |
| US8526574B2 (en) | 2010-09-24 | 2013-09-03 | Moxtek, Inc. | Capacitor AC power coupling across high DC voltage differential |
| US8804910B1 (en) | 2011-01-24 | 2014-08-12 | Moxtek, Inc. | Reduced power consumption X-ray source |
| US8750458B1 (en) | 2011-02-17 | 2014-06-10 | Moxtek, Inc. | Cold electron number amplifier |
| US8929515B2 (en) | 2011-02-23 | 2015-01-06 | Moxtek, Inc. | Multiple-size support for X-ray window |
| WO2012149166A1 (en) * | 2011-04-27 | 2012-11-01 | Brigham Young University | Delivery of biological materials into cellular organelles |
| US9076628B2 (en) | 2011-05-16 | 2015-07-07 | Brigham Young University | Variable radius taper x-ray window support structure |
| US9174412B2 (en) | 2011-05-16 | 2015-11-03 | Brigham Young University | High strength carbon fiber composite wafers for microfabrication |
| US8989354B2 (en) | 2011-05-16 | 2015-03-24 | Brigham Young University | Carbon composite support structure |
| US20120295345A1 (en) * | 2011-05-18 | 2012-11-22 | Aten Quentin T | Apparatuses and related methods for delivering biological material into a cell |
| US20130177977A1 (en) * | 2011-06-29 | 2013-07-11 | Brigham Young University | Systems and Devices for Restraining a Cell and Associated Methods |
| US20130101482A1 (en) * | 2011-10-21 | 2013-04-25 | Nanoinjection Technologies, L.L.C. | Systems and devices for restraining a micro-object and associated methods |
| US20130102078A1 (en) * | 2011-10-21 | 2013-04-25 | Nanoinjection Technologies, L.L.C. | Nanoinjection system dna placement pipette coupler |
| WO2013059824A1 (en) * | 2011-10-21 | 2013-04-25 | Nanoinjection Technologies, L.L.C. | Lance device and associated methods for delivering a biological material into a biological structure |
| US20130177988A1 (en) * | 2011-11-17 | 2013-07-11 | Brigham Young University | Cytoplasm to organelle delivery system and associated methods |
| US9173623B2 (en) | 2013-04-19 | 2015-11-03 | Samuel Soonho Lee | X-ray tube and receiver inside mouth |
| US11788042B2 (en) * | 2015-07-31 | 2023-10-17 | Redwire Space Technologies, Inc. | Biomanufacturing system, method, and 3D bioprinting hardware in a reduced gravity environment |
| US11377631B2 (en) * | 2016-10-13 | 2022-07-05 | Sinfonia Technology Co., Ltd. | Culture container linkage device, culture system, and method for washing needle |
Family Cites Families (122)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US1946288A (en) * | 1929-09-19 | 1934-02-06 | Gen Electric | Electron discharge device |
| US2316214A (en) * | 1940-09-10 | 1943-04-13 | Gen Electric X Ray Corp | Control of electron flow |
| US2340363A (en) * | 1942-03-03 | 1944-02-01 | Gen Electric X Ray Corp | Control for focal spot in X-ray generators |
| US2502070A (en) * | 1949-01-19 | 1950-03-28 | Dunlee Corp | Getter for induction flashing |
| US3741797A (en) * | 1970-04-30 | 1973-06-26 | Gen Technology Corp | Low density high-strength boron on beryllium reinforcement filaments |
| US3665236A (en) * | 1970-12-09 | 1972-05-23 | Atomic Energy Commission | Electrode structure for controlling electron flow with high transmission efficiency |
| DE2154888A1 (de) * | 1971-11-04 | 1973-05-17 | Siemens Ag | Roentgenroehre |
| US3882339A (en) * | 1974-06-17 | 1975-05-06 | Gen Electric | Gridded X-ray tube gun |
| US3962583A (en) * | 1974-12-30 | 1976-06-08 | The Machlett Laboratories, Incorporated | X-ray tube focusing means |
| US4007375A (en) * | 1975-07-14 | 1977-02-08 | Albert Richard D | Multi-target X-ray source |
| FR2333344A1 (fr) * | 1975-11-28 | 1977-06-24 | Radiologie Cie Gle | Tube radiogene a cathode chaude avec anode en bout et appareil comportant un tel tube |
| US4184097A (en) * | 1977-02-25 | 1980-01-15 | Magnaflux Corporation | Internally shielded X-ray tube |
| US4368538A (en) * | 1980-04-11 | 1983-01-11 | International Business Machines Corporation | Spot focus flash X-ray source |
| US4576679A (en) * | 1981-03-27 | 1986-03-18 | Honeywell Inc. | Method of fabricating a cold shield |
| US4443293A (en) * | 1981-04-20 | 1984-04-17 | Kulite Semiconductor Products, Inc. | Method of fabricating transducer structure employing vertically walled diaphragms with quasi rectangular active areas |
| DE3222511C2 (de) * | 1982-06-16 | 1985-08-29 | Feinfocus Röntgensysteme GmbH, 3050 Wunstorf | Feinfokus-Röntgenröhre |
| US4521902A (en) * | 1983-07-05 | 1985-06-04 | Ridge, Inc. | Microfocus X-ray system |
| CH654686A5 (fr) * | 1983-11-18 | 1986-02-28 | Centre Electron Horloger | Procede de fabrication d'un dispositif a volets miniatures et application d'un tel procede pour l'obtention d'un dispositif de modulation de lumiere. |
| US4645977A (en) * | 1984-08-31 | 1987-02-24 | Matsushita Electric Industrial Co., Ltd. | Plasma CVD apparatus and method for forming a diamond like carbon film |
| FR2577073B1 (fr) * | 1985-02-06 | 1987-09-25 | Commissariat Energie Atomique | Dispositif matriciel de detection d'un rayonnement lumineux a ecrans froids individuels integres dans un substrat et son procede de fabrication |
| US4591756A (en) * | 1985-02-25 | 1986-05-27 | Energy Sciences, Inc. | High power window and support structure for electron beam processors |
| JPH0617474B2 (ja) * | 1985-05-31 | 1994-03-09 | チッソ株式会社 | 高接着性シリコン含有ポリアミド酸の製造法 |
| DE3542127A1 (de) * | 1985-11-28 | 1987-06-04 | Siemens Ag | Roentgenstrahler |
| WO1988004588A1 (en) * | 1986-12-18 | 1988-06-30 | Itokazu, Kowa | Hole saw |
| DE3718066A1 (de) * | 1987-05-29 | 1988-12-08 | Zeiss Carl Fa | Verfahren zur mikroinjektion in zellen bzw. zum absaugen aus einzelnen zellen oder ganzer zellen aus zellkulturen |
| JPH0787082B2 (ja) * | 1987-07-24 | 1995-09-20 | 株式会社日立製作所 | X線管用回転陽極ターゲット |
| US4797907A (en) * | 1987-08-07 | 1989-01-10 | Diasonics Inc. | Battery enhanced power generation for mobile X-ray machine |
| US4933557A (en) * | 1988-06-06 | 1990-06-12 | Brigham Young University | Radiation detector window structure and method of manufacturing thereof |
| JPH02199099A (ja) * | 1988-10-21 | 1990-08-07 | Crystallume | 連続ダイヤモンド薄膜およびその製法 |
| US5105456A (en) * | 1988-11-23 | 1992-04-14 | Imatron, Inc. | High duty-cycle x-ray tube |
| FI885554A (fi) * | 1988-11-30 | 1990-05-31 | Outokumpu Oy | Indikationsfoenster foer analysator och dess framstaellningsfoerfarande. |
| US5117829A (en) * | 1989-03-31 | 1992-06-02 | Loma Linda University Medical Center | Patient alignment system and procedure for radiation treatment |
| US4907258A (en) | 1989-04-12 | 1990-03-06 | Matsushita Electric Industrial Co., Ltd. | Key telephone apparatus |
| US5302523A (en) * | 1989-06-21 | 1994-04-12 | Zeneca Limited | Transformation of plant cells |
| JP2886588B2 (ja) * | 1989-07-11 | 1999-04-26 | 日本碍子株式会社 | 圧電/電歪アクチュエータ |
| US5010562A (en) * | 1989-08-31 | 1991-04-23 | Siemens Medical Laboratories, Inc. | Apparatus and method for inhibiting the generation of excessive radiation |
| US5217817A (en) * | 1989-11-08 | 1993-06-08 | U.S. Philips Corporation | Steel tool provided with a boron layer |
| US5442678A (en) * | 1990-09-05 | 1995-08-15 | Photoelectron Corporation | X-ray source with improved beam steering |
| GB9200828D0 (en) * | 1992-01-15 | 1992-03-11 | Image Research Ltd | Improvements in and relating to material identification using x-rays |
| US5391958A (en) * | 1993-04-12 | 1995-02-21 | Charged Injection Corporation | Electron beam window devices and methods of making same |
| US5521851A (en) * | 1993-04-26 | 1996-05-28 | Nihon Kohden Corporation | Noise reduction method and apparatus |
| JPH06343478A (ja) * | 1993-06-08 | 1994-12-20 | Hitachi Ltd | マイクロインジェクション方法及び装置 |
| US5627871A (en) * | 1993-06-10 | 1997-05-06 | Nanodynamics, Inc. | X-ray tube and microelectronics alignment process |
| US5400385A (en) * | 1993-09-02 | 1995-03-21 | General Electric Company | High voltage power supply for an X-ray tube |
| US5602507A (en) * | 1993-11-05 | 1997-02-11 | Ntt Mobile Communications Network Inc. | Adaptive demodulating method for generating replica and demodulator thereof |
| US5457041A (en) * | 1994-03-25 | 1995-10-10 | Science Applications International Corporation | Needle array and method of introducing biological substances into living cells using the needle array |
| DE69523457D1 (de) * | 1994-07-12 | 2001-11-29 | Photoelectron Corp | Röntgenstrahlgerät zum dosieren eines vorbestimmten strahlungsflusses auf innere flächen von körperhöhlen |
| US5706354A (en) * | 1995-07-10 | 1998-01-06 | Stroehlein; Brian A. | AC line-correlated noise-canceling circuit |
| US6073484A (en) * | 1995-07-20 | 2000-06-13 | Cornell Research Foundation, Inc. | Microfabricated torsional cantilevers for sensitive force detection |
| US5870051A (en) * | 1995-08-14 | 1999-02-09 | William K. Warburton | Method and apparatus for analog signal conditioner for high speed, digital x-ray spectrometer |
| US5774522A (en) * | 1995-08-14 | 1998-06-30 | Warburton; William K. | Method and apparatus for digitally based high speed x-ray spectrometer for direct coupled use with continuous discharge preamplifiers |
| US5729583A (en) * | 1995-09-29 | 1998-03-17 | The United States Of America As Represented By The Secretary Of Commerce | Miniature x-ray source |
| US5631943A (en) * | 1995-12-19 | 1997-05-20 | Miles; Dale A. | Portable X-ray device |
| JP3594716B2 (ja) * | 1995-12-25 | 2004-12-02 | 浜松ホトニクス株式会社 | 透過型x線管 |
| US6205200B1 (en) * | 1996-10-28 | 2001-03-20 | The United States Of America As Represented By The Secretary Of The Navy | Mobile X-ray unit |
| US5898754A (en) * | 1997-06-13 | 1999-04-27 | X-Ray And Specialty Instruments, Inc. | Method and apparatus for making a demountable x-ray tube |
| US5907595A (en) * | 1997-08-18 | 1999-05-25 | General Electric Company | Emitter-cup cathode for high-emission x-ray tube |
| JP4043571B2 (ja) * | 1997-12-04 | 2008-02-06 | 浜松ホトニクス株式会社 | X線管 |
| WO1999036462A1 (en) * | 1998-01-16 | 1999-07-22 | Maverick Corporation | Low-toxicity, high-temperature polyimides |
| US5939521A (en) * | 1998-01-23 | 1999-08-17 | The United States Of America As Represented By The Administrator Of The National Aeronautics And Space Administration | Polyimides based on 4,4'-bis (4-aminophenoxy)-2,2'or 2,2', 6,6'-substituted biphenyl |
| JP4164233B2 (ja) | 1998-03-12 | 2008-10-15 | 株式会社東京大学Tlo | 自動微小膜電位計測装置 |
| US6027115A (en) * | 1998-03-25 | 2000-02-22 | International Game Technology | Slot machine reels having luminescent display elements |
| JP3902883B2 (ja) * | 1998-03-27 | 2007-04-11 | キヤノン株式会社 | ナノ構造体及びその製造方法 |
| DE59800215D1 (de) * | 1998-06-05 | 2000-08-31 | Lummel Wolfgang | Mikroinjektionsverfahren zum Einbringen eines Injektionsstoffes, insbes. fremdes, genetisches Material, in Prokaryoten-und Eukaryotenzellen, sowie Zellkompartimente von letzteren (Plastiden, Zellkerne), sowie Nanopipette hierzu |
| JP4334639B2 (ja) * | 1998-07-30 | 2009-09-30 | 浜松ホトニクス株式会社 | X線管 |
| US6232706B1 (en) * | 1998-11-12 | 2001-05-15 | The Board Of Trustees Of The Leland Stanford Junior University | Self-oriented bundles of carbon nanotubes and method of making same |
| US6713291B2 (en) * | 1999-01-28 | 2004-03-30 | Alan D. King | Electrodes coated with treating agent and uses thereof |
| FR2789401B1 (fr) * | 1999-02-08 | 2003-04-04 | Cis Bio Int | Procede de fabrication de matrices de ligands adresses sur un support |
| US6062931A (en) * | 1999-09-01 | 2000-05-16 | Industrial Technology Research Institute | Carbon nanotube emitter with triode structure |
| AUPQ304199A0 (en) * | 1999-09-23 | 1999-10-21 | Commonwealth Scientific And Industrial Research Organisation | Patterned carbon nanotubes |
| US6388359B1 (en) * | 2000-03-03 | 2002-05-14 | Optical Coating Laboratory, Inc. | Method of actuating MEMS switches |
| DE10048833C2 (de) * | 2000-09-29 | 2002-08-08 | Siemens Ag | Vakuumgehäuse für eine Vakuumröhre mit einem Röntgenfenster |
| US6876724B2 (en) * | 2000-10-06 | 2005-04-05 | The University Of North Carolina - Chapel Hill | Large-area individually addressable multi-beam x-ray system and method of forming same |
| US6546077B2 (en) * | 2001-01-17 | 2003-04-08 | Medtronic Ave, Inc. | Miniature X-ray device and method of its manufacture |
| US6645757B1 (en) * | 2001-02-08 | 2003-11-11 | Sandia Corporation | Apparatus and method for transforming living cells |
| US20080124787A1 (en) | 2001-02-13 | 2008-05-29 | Avigenics, Inc. | Microinjection devices and methods of use |
| JP4697829B2 (ja) * | 2001-03-15 | 2011-06-08 | ポリマテック株式会社 | カーボンナノチューブ複合成形体及びその製造方法 |
| US20020176984A1 (en) * | 2001-03-26 | 2002-11-28 | Wilson Smart | Silicon penetration device with increased fracture toughness and method of fabrication |
| DE10120335C2 (de) * | 2001-04-26 | 2003-08-07 | Bruker Daltonik Gmbh | Ionenmobilitätsspektrometer mit nicht-radioaktiver Ionenquelle |
| US7682249B2 (en) * | 2001-05-04 | 2010-03-23 | Igt | Light emitting interface displays for a gaming machine |
| JP4772212B2 (ja) * | 2001-05-31 | 2011-09-14 | 浜松ホトニクス株式会社 | X線発生装置 |
| US20020191746A1 (en) * | 2001-06-19 | 2002-12-19 | Mark Dinsmore | X-ray source for materials analysis systems |
| JP2003125750A (ja) | 2001-07-10 | 2003-05-07 | Narishige:Kk | マイクロピペット、インジェクション装置およびマイクロインジェクションの方法 |
| JP3837480B2 (ja) * | 2001-09-19 | 2006-10-25 | 国立大学法人東京工業大学 | 生細胞からの生体分子の採取方法 |
| EP1488441A2 (en) * | 2002-01-31 | 2004-12-22 | The Johns Hopkins University | X-ray source and method for more efficiently producing selectable x-ray frequencies |
| JP2005517537A (ja) * | 2002-02-11 | 2005-06-16 | レンセラー・ポリテクニック・インスティチュート | 高度に組織化されたカーボン・ナノチューブ構造の指向性アセンブリ |
| US20070010318A1 (en) * | 2005-07-11 | 2007-01-11 | Gene Rigsby | Light sources and displays in a gaming machine |
| US7448801B2 (en) * | 2002-02-20 | 2008-11-11 | Inpho, Inc. | Integrated X-ray source module |
| US7448802B2 (en) * | 2002-02-20 | 2008-11-11 | Newton Scientific, Inc. | Integrated X-ray source module |
| JP4051440B2 (ja) * | 2002-03-06 | 2008-02-27 | 独立行政法人産業技術総合研究所 | 細胞操作装置及び方法 |
| AU2003212636A1 (en) | 2002-03-14 | 2003-09-22 | Memlink Ltd | A microelectromechanical device having an analog system for positioning sensing |
| EP1547116A4 (en) * | 2002-09-13 | 2006-05-24 | Moxtek Inc | RADIATION WINDOW AND METHOD OF MANUFACTURING |
| US20040063100A1 (en) | 2002-09-30 | 2004-04-01 | Wang Chung Lin | Nanoneedle chips and the production thereof |
| JP2004265602A (ja) * | 2003-01-10 | 2004-09-24 | Toshiba Corp | X線装置 |
| US6987835B2 (en) * | 2003-03-26 | 2006-01-17 | Xoft Microtube, Inc. | Miniature x-ray tube with micro cathode |
| WO2004092369A1 (ja) * | 2003-04-11 | 2004-10-28 | Riken | マイクロインジェクション方法および装置 |
| WO2005067004A1 (ja) * | 2004-01-07 | 2005-07-21 | Matsushita Electric Industrial Co., Ltd. | 白熱電球及び白熱電球用フィラメント |
| US7224769B2 (en) * | 2004-02-20 | 2007-05-29 | Aribex, Inc. | Digital x-ray camera |
| JP2005276760A (ja) * | 2004-03-26 | 2005-10-06 | Shimadzu Corp | X線発生装置 |
| US20060052751A1 (en) * | 2004-04-20 | 2006-03-09 | Sepehr Eskandari | Fast perfusion cell chamber |
| US7358593B2 (en) * | 2004-05-07 | 2008-04-15 | University Of Maine | Microfabricated miniature grids |
| US7233071B2 (en) * | 2004-10-04 | 2007-06-19 | International Business Machines Corporation | Low-k dielectric layer based upon carbon nanostructures |
| US7680652B2 (en) * | 2004-10-26 | 2010-03-16 | Qnx Software Systems (Wavemakers), Inc. | Periodic signal enhancement system |
| US7428298B2 (en) * | 2005-03-31 | 2008-09-23 | Moxtek, Inc. | Magnetic head for X-ray source |
| US7486774B2 (en) * | 2005-05-25 | 2009-02-03 | Varian Medical Systems, Inc. | Removable aperture cooling structure for an X-ray tube |
| JP4652906B2 (ja) | 2005-06-30 | 2011-03-16 | 富士夫 宮脇 | 振動型マイクロインジェクション装置 |
| US7618906B2 (en) * | 2005-11-17 | 2009-11-17 | Oxford Instruments Analytical Oy | Window membrane for detector and analyser devices, and a method for manufacturing a window membrane |
| US7650050B2 (en) * | 2005-12-08 | 2010-01-19 | Alstom Technology Ltd. | Optical sensor device for local analysis of a combustion process in a combustor of a thermal power plant |
| WO2007076458A1 (en) | 2005-12-21 | 2007-07-05 | Primegen Biotech Llc | Microinjector chip |
| US7657002B2 (en) * | 2006-01-31 | 2010-02-02 | Varian Medical Systems, Inc. | Cathode head having filament protection features |
| US7203283B1 (en) * | 2006-02-21 | 2007-04-10 | Oxford Instruments Analytical Oy | X-ray tube of the end window type, and an X-ray fluorescence analyzer |
| US7693265B2 (en) * | 2006-05-11 | 2010-04-06 | Koninklijke Philips Electronics N.V. | Emitter design including emergency operation mode in case of emitter-damage for medical X-ray application |
| JP5086620B2 (ja) | 2006-11-30 | 2012-11-28 | オリンパス株式会社 | 遺伝子導入装置及び方法 |
| JP4504344B2 (ja) * | 2006-12-04 | 2010-07-14 | 国立大学法人 東京大学 | X線源 |
| US8257932B2 (en) | 2007-02-21 | 2012-09-04 | The Regents Of The University Of California | Interfacing nanostructures to biological cells |
| US7709820B2 (en) * | 2007-06-01 | 2010-05-04 | Moxtek, Inc. | Radiation window with coated silicon support structure |
| US20100323419A1 (en) | 2007-07-09 | 2010-12-23 | Aten Quentin T | Methods and Devices for Charged Molecule Manipulation |
| US7529345B2 (en) * | 2007-07-18 | 2009-05-05 | Moxtek, Inc. | Cathode header optic for x-ray tube |
| US8736138B2 (en) * | 2007-09-28 | 2014-05-27 | Brigham Young University | Carbon nanotube MEMS assembly |
| WO2009085351A2 (en) * | 2007-09-28 | 2009-07-09 | Brigham Young University | X-ray window with carbon nanotube frame |
| JP2009136261A (ja) | 2007-12-10 | 2009-06-25 | Olympus Corp | チップ駆動装置 |
| US20100126660A1 (en) * | 2008-10-30 | 2010-05-27 | O'hara David | Method of making graphene sheets and applicatios thereor |
-
2008
- 2008-07-09 US US12/668,369 patent/US20100323419A1/en not_active Abandoned
- 2008-07-09 CA CA 2692742 patent/CA2692742A1/en not_active Abandoned
- 2008-07-09 EP EP08796124.9A patent/EP2167632A4/en not_active Withdrawn
- 2008-07-09 WO PCT/US2008/069550 patent/WO2009009610A2/en active Application Filing
- 2008-07-09 JP JP2010516228A patent/JP2010532997A/ja active Pending
- 2008-07-09 KR KR1020107001996A patent/KR20100037615A/ko not_active Application Discontinuation
- 2008-07-09 AU AU2008275064A patent/AU2008275064A1/en not_active Abandoned
-
2010
- 2010-06-15 US US12/816,183 patent/US20100248343A1/en not_active Abandoned
-
2013
- 2013-12-11 US US14/103,618 patent/US10119151B2/en not_active Expired - Fee Related
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20160010067A (ko) | 2014-07-18 | 2016-01-27 | 인제대학교 산학협력단 | 양말 착용 보조장치 |
Also Published As
| Publication number | Publication date |
|---|---|
| CA2692742A1 (en) | 2009-01-15 |
| US10119151B2 (en) | 2018-11-06 |
| EP2167632A4 (en) | 2013-12-18 |
| US20100323419A1 (en) | 2010-12-23 |
| US20100248343A1 (en) | 2010-09-30 |
| JP2010532997A (ja) | 2010-10-21 |
| US20140227785A1 (en) | 2014-08-14 |
| AU2008275064A1 (en) | 2009-01-15 |
| EP2167632A2 (en) | 2010-03-31 |
| WO2009009610A3 (en) | 2009-03-12 |
| WO2009009610A2 (en) | 2009-01-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20100037615A (ko) | 대전된 분자 조작을 위한 방법 및 이를 위한 장치 | |
| US11365381B2 (en) | Microfluidic cell culture | |
| US10101250B2 (en) | Manipulation of cell nuclei in a micro-fluidic device | |
| Huang et al. | On-demand intracellular delivery of single particles in single cells by 3D hollow nanoelectrodes | |
| US20090233327A1 (en) | Surface Modification in a Manipulation Chamber | |
| McKnight et al. | Tracking gene expression after DNA delivery using spatially indexed nanofiber arrays | |
| KR20180091062A (ko) | 미세유체 디바이스들 및 키트들 및 그것의 사용을 위한 방법들 | |
| WO2004092369A1 (ja) | マイクロインジェクション方法および装置 | |
| CN113186149A (zh) | Dna-细胞缀合物 | |
| US20140256047A1 (en) | Dose and location controlled drug/gene/particle delivery to individual cells by nanoelectroporation | |
| TW201643241A (zh) | 微流體細胞培養 | |
| Aten et al. | Electrostatic accumulation and release of DNA using a micromachined lance | |
| CN1954064B (zh) | 生物试样操作方法 | |
| US20140199765A1 (en) | Lance device and associated methods for delivering a biological material into a cell | |
| US10843148B2 (en) | Integrated electrowetting nano-injector and aspirator | |
| WO2004033614A1 (ja) | 分子放出装置及び分子放出方法 | |
| Shekaramiz | Integrated Electrowetting Nanoinjector/Aspirator for Single Cell Studies | |
| CN111363762A (zh) | 一种向细胞内传递外源性分子的方法 | |
| US20130102060A1 (en) | Lance device and associated methods for delivering a biological material into a biological structure | |
| Zhao | Micro/Nanofluidics Based Electroporation for Precise Material Delivery to Cells | |
| US20120295345A1 (en) | Apparatuses and related methods for delivering biological material into a cell | |
| KR20120021549A (ko) | 주사 탐침 현미경을 이용하는 전기 천공법 및 전기 천공 장치 | |
| Class et al. | Patent application title: METHODS FOR NANO-MECHANOPORATION Inventors: Min-Feng Yu (Norcross, GA, US) Kyungsuk Yum (Berkeley, CA, US) Ning Wang (Champaign, IL, US) |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WITN | Application deemed withdrawn, e.g. because no request for examination was filed or no examination fee was paid |