JP7614331B2 - 含フッ素ピリミジン化合物およびその製造方法 - Google Patents
含フッ素ピリミジン化合物およびその製造方法 Download PDFInfo
- Publication number
- JP7614331B2 JP7614331B2 JP2023509065A JP2023509065A JP7614331B2 JP 7614331 B2 JP7614331 B2 JP 7614331B2 JP 2023509065 A JP2023509065 A JP 2023509065A JP 2023509065 A JP2023509065 A JP 2023509065A JP 7614331 B2 JP7614331 B2 JP 7614331B2
- Authority
- JP
- Japan
- Prior art keywords
- integer
- group
- general formula
- fluorine
- carbon atoms
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings directly linked by a ring-member-to-ring-member bond
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Plural Heterocyclic Compounds (AREA)
Description
[1]下記一般式(1a)または(1b)で表される、含フッ素ピリミジン化合物。
R1は炭素数1~12の炭化水素基を表し、
R2はハロゲン原子、炭素数1~10の炭化水素基、-CnF2n+1(nは1~10の整数である)、ニトロ基、ボロン酸基、シアノ基、-OA1、-OlSOmA1(lは0~1の整数、mは0~3の整数である)、-NA1A2、-OlCOOA1(lは0~1の整数である)、または-OlCONA1A2(lは0~1の整数である)を表し、A1、A2はそれぞれ独立して、水素原子または炭素数1~10の炭化水素基を表し、AlとA2は結合して環構造を形成しても良く、R2が複数存在する場合、それらは同一であっても異なっていても良く、
環Zは酸素原子を1個含み、窒素原子を1個以上含む5員芳香族複素環である。)
[2]前記環Zが、下記式(c1)~(c14)のうち何れか一つの構造を有する、上記[1]に記載の含フッ素ピリミジン化合物。
下記一般式(2)で表されるフルオロイソブチレン誘導体と、下記一般式(3b)で表される化合物またはその塩とを反応させることにより、下記一般式(1b)で表される含フッ素ピリミジン化合物を得る工程、
を有する、含フッ素ピリミジン化合物の製造方法。
R1は炭素数1~12の炭化水素基を表し、
R2はハロゲン原子、炭素数1~10の炭化水素基、-CnF2n+1(nは1~10の整数である)、ニトロ基、ボロン酸基、シアノ基、-OA1、-OlSOmA1(lは0~1の整数、mは0~3の整数である)、-NA1A2、-OlCOOA1(lは0~1の整数である)、または-OlCONA1A2(lは0~1の整数である)を表し、A1、A2はそれぞれ独立して、水素原子または炭素数1~10の炭化水素基を表し、AlとA2は結合して環構造を形成しても良く、R2が複数存在する場合、それらは同一であっても異なっていても良く、
環Zは酸素原子を1個含み、窒素原子を1個以上含む5員芳香族複素環である。)
[4]下記一般式(4)で表されるフルオロイソブタン誘導体と、下記一般式(3a)で表される化合物またはその塩とを反応させることにより、下記一般式(1a)で表される含フッ素ピリミジン化合物を得る工程、または
下記一般式(4)で表されるフルオロイソブタン誘導体と、下記一般式(3b)で表される化合物またはその塩とを反応させることにより、下記一般式(1b)で表される含フッ素ピリミジン化合物を得る工程、
を有する、含フッ素ピリミジン化合物の製造方法。
R1は炭素数1~12の炭化水素基を表し、
R2はハロゲン原子、炭素数1~10の炭化水素基、-CnF2n+1(nは1~10の整数である)、ニトロ基、ボロン酸基、シアノ基、-OA1、-OlSOmA1(lは0~1の整数、mは0~3の整数である)、-NA1A2、-OlCOOA1(lは0~1の整数である)、または-OlCONA1A2(lは0~1の整数である)を表し、A1、A2はそれぞれ独立して、水素原子または炭素数1~10の炭化水素基を表し、AlとA2は結合して環構造を形成しても良く、R2が複数存在する場合、それらは同一であっても異なっていても良く、
環Zは酸素原子を1個含み、窒素原子を1個以上含む5員芳香族複素環であり、
Xは、ハロゲン原子、シアノ基、-OA3、-NA3A4、-OCOOA3、-OCONA3A4、または-OlSOmA5(lは0~1の整数、mは0~3の整数である)を表し、A3、A4はそれぞれ独立して炭素数1~10の炭化水素基を表し、A3とA4が結合して環構造を形成しても良く、A5は水素原子または炭素数1~10の炭化水素基を表す。)
[5]前記環Zが、下記式(c1)~(c14)のうち何れか一つの構造を有する、上記[3]または[4]に記載の含フッ素ピリミジン化合物の製造方法。
一実施形態の含フッ素ピリミジン化合物は下記一般式(1a)または(1b)で表される。
R1は炭素数1~12の炭化水素基を表し、
R2はハロゲン原子、炭素数1~10の炭化水素基、-CnF2n+1(nは1~10の整数である)、ニトロ基、ボロン酸基、シアノ基、-OA1、-OlSOmA1(lは0~1の整数、mは0~3の整数である)、-NA1A2、-OlCOOA1(lは0~1の整数である)、または-OlCONA1A2(lは0~1の整数である)を表し、A1、A2はそれぞれ独立して、水素原子または炭素数1~10の炭化水素基を表し、AlとA2は結合して環構造を形成しても良く、R2が複数存在する場合、それらは同一であっても異なっていても良く、
環Zは酸素原子を1個含み、窒素原子を1個以上含む5員芳香族複素環である。)
エテニル基、プロペニル基、ブテニル基、ペンテニル基、ヘキセニル基、ヘプテニル基、オクテニル基、ノネニル基、デセニル基、ウンデセニル基、ドデセニル基等のアルケニル基;
エチニル基、プロピニル基、ブチニル基、ペンチニル基、ヘキシニル基、ヘプチニル基、オクチニル基、ノニニル基、デシニル基、ウンデシニル基、ドデシニル基等のアルキニル基等を挙げることができる。
一実施形態の含フッ素ピリミジン化合物の製造方法は、
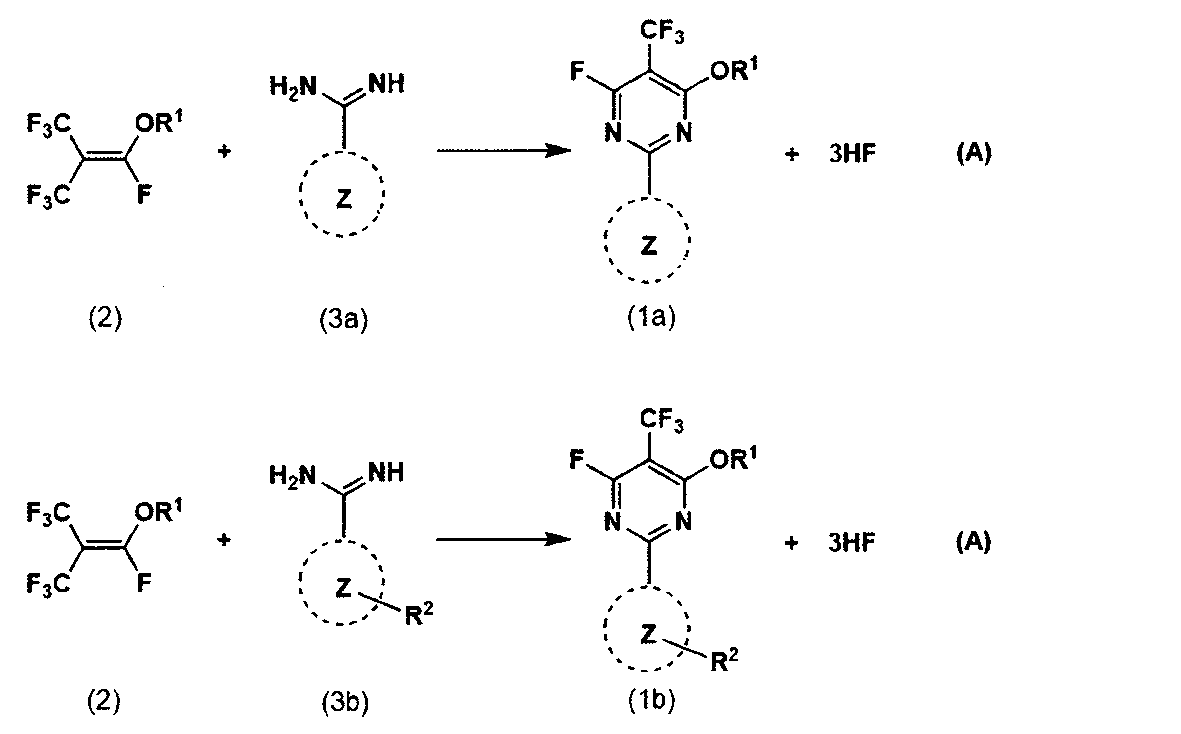
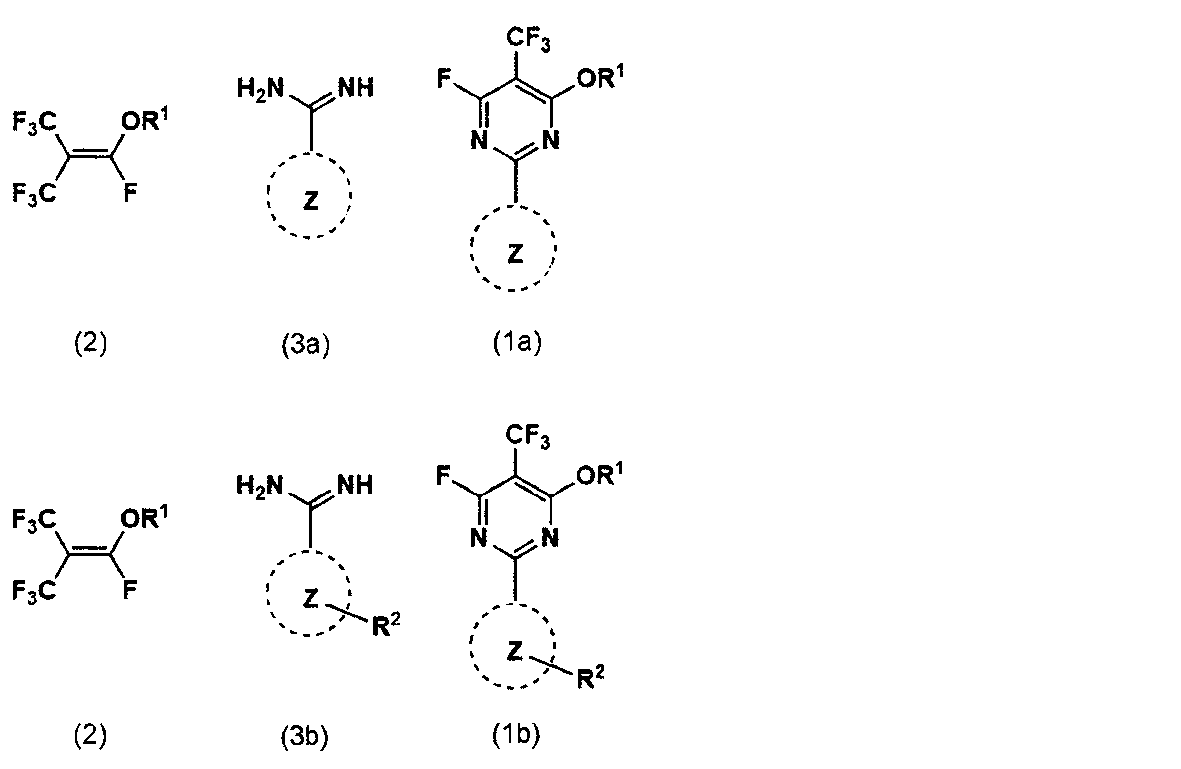
(a)下記一般式(2)で表されるフルオロイソブチレン誘導体と、下記一般式(3a)で表される化合物またはその塩とを反応させることにより、下記一般式(1a)で表される含フッ素ピリミジン化合物を得る工程、または
下記一般式(2)で表されるフルオロイソブチレン誘導体と、下記一般式(3b)で表される化合物またはその塩とを反応させることにより、下記一般式(1b)で表される含フッ素ピリミジン化合物を得る工程、を有する。
R1は炭素数1~12の炭化水素基を表し、
R2はハロゲン原子、炭素数1~10の炭化水素基、-CnF2n+1(nは1~10の整数である)、ニトロ基、ボロン酸基、シアノ基、-OA1、-OlSOmA1(lは0~1の整数、mは0~3の整数である)、-NA1A2、-OlCOOA1(lは0~1の整数である)、または-OlCONA1A2(lは0~1の整数である)を表し、A1、A2はそれぞれ独立して、水素原子または炭素数1~10の炭化水素基を表し、AlとA2は結合して環構造を形成しても良く、R2が複数存在する場合、それらは同一であっても異なっていても良く、
環Zは酸素原子を1個含み、窒素原子を1個以上含む5員芳香族複素環である。)
(b)下記一般式(4)で表されるフルオロイソブタン誘導体と、下記一般式(3a)で表される化合物またはその塩とを反応させることにより、下記一般式(1a)で表される含フッ素ピリミジン化合物を得る工程、または
下記一般式(4)で表されるフルオロイソブタン誘導体と、下記一般式(3b)で表される化合物またはその塩とを反応させることにより、下記一般式(1b)で表される含フッ素ピリミジン化合物を得る工程、を有する。
R1は炭素数1~12の炭化水素基を表し、
R2はハロゲン原子、炭素数1~10の炭化水素基、-CnF2n+1(nは1~10の整数である)、ニトロ基、ボロン酸基、シアノ基、-OA1、-OlSOmA1(lは0~1の整数、mは0~3の整数である)、-NA1A2、-OlCOOA1(lは0~1の整数である)、または-OlCONA1A2(lは0~1の整数である)を表し、A1、A2はそれぞれ独立して、水素原子または炭素数1~10の炭化水素基を表し、AlとA2は結合して環構造を形成しても良く、R2が複数存在する場合、それらは同一であっても異なっていても良く、
環Zは酸素原子を1個含み、窒素原子を1個以上含む5員芳香族複素環であり、
Xは、ハロゲン原子、シアノ基、-OA3、-NA3A4、-OCOOA3、-OCONA3A4、または-OlSOmA5(lは0~1の整数、mは0~3の整数である)を表し、A3、A4はそれぞれ独立して炭素数1~10の炭化水素基を表し、A3とA4が結合して環構造を形成しても良く、A5は水素原子または炭素数1~10の炭化水素基を表す。)
6-フルオロ-4-メトキシ-2-(5-オキサゾリル)-5-(トリフルオロメチル)ピリミジンの製造
5-オキサゾールカルボキシイミドアミド塩酸塩0.8g(4.9mmol)をアセトニトリル50ml中に溶解させてアセトニトリル溶液とした。該アセトニトリル溶液中に、1,3,3,3-テトラフルオロ-1-メトキシ-2-(トリフルオロメチル)-1-プロペン1.2g(5.7mmol)およびジイソプロピルエチルアミン3.3g(25.5mmol)を加え、室温で19.1時間攪拌後、反応液をカラム精製し、下記式(5)で示される化合物(化学式:C9H5F4N3O2、分子量:263.15g/mol)0.4g(1.5mmol)を得た。得られた化合物の単離収率は31.1%であった。
マススペクトル(APCI、m/z):263.4([M]+)
1H-NMR(400MHz、CDCl3) δppm:8.10(s,1H),8.03(s,1H),4.22(s,3H)
6-フルオロ-4-メトキシ-2-(3-(5-メチルイソオキサゾリル))-5-(トリフルオロメチル)ピリミジンの製造
氷水冷却下、3-アミジノ-5-メチルイソオキサゾール塩酸塩0.5g(3.1mmol)をアセトニトリル10gに溶解させ、1,3,3,3-テトラフルオロ-1-メトキシ-2-(トリフルオロメチル)-1-プロペン0.8g(3.6mmol)を滴下した。続いてジイソプロピルエチルアミン2.1g(16.1mmol)とアセトニトリル5gの混合溶液を滴下し室温まで昇温した。16時間攪拌後、得られた反応液をカラム精製し、下記式(6)で示される化合物(化学式:C10H7F4N3O2、分子量:277.18g/mol)0.3g(1.2mmol)を得た。得られた化合物の単離収率は40%であった。
マススペクトル(APCI、m/z):277.5([M]+)
1H-NMR(400MHz、CDCl3) δppm:6.69(s,1H),4.27(s,3H),2.56(s,3H)
6-フルオロ-4-メトキシ-2-(2-(1,3,4-オキサジアゾリル))-5-(トリフルオロメチル)ピリミジンの製造
氷水冷却下、2-アミジノ-1,3,4-オキサジアゾール塩酸塩0.3 g(2.0mmol)をアセトニトリル8gに溶解させ、1,3,3,3-テトラフルオロ-1-メトキシ-2-(トリフルオロメチル)-1-プロペン0.5g(2.3mmol)を滴下した。続いてジイソプロピルエチルアミン1.3g(10mmol)とアセトニトリル5gの混合溶液を滴下し室温まで昇温した。16時間攪拌後、得られた反応液をカラム精製し、下記式(7)で示される化合物(化学式:C8H4F4N4O2、分子量:264.14g/mol)0.1g(0.4mmol)を得た。得られた化合物の収率は22%であった。
マススペクトル(APCI、m/z):264.3([M]+)
実施例1の1,3,3,3-テトラフルオロ-1-メトキシ-2-(トリフルオロメチル)-1-プロペンの代わりに1,1,1,3,3-ペンタフルオロ-3-メトキシ-2-(トリフルオロメチル)-プロパンを使用した、6-フルオロ-4-メトキシ-2-(5-オキサゾリル)-5-(トリフルオロメチル)ピリミジンの製造
氷水冷却下、5-オキサゾールカルボキシイミドアミド塩酸塩0.8g(4.9mmol)をアセトニトリル20gに溶解させ、1,1,1,3,3-ペンタフルオロ-3-メトキシ-2-(トリフルオロメチル)-プロパン1.3g(5.6mmol)を滴下した。続いてジイソプロピルエチルアミン4.1g(32mmol)とアセトニトリル10gの混合溶液を滴下し室温まで昇温した。約16時間後、内容物のカラム精製を行った。得られた化合物の分析結果は、実施例1の生成物と同様であった。
実施例2の1,3,3,3-テトラフルオロ-1-メトキシ-2-(トリフルオロメチル)-1-プロペンの代わりに1,1,1,3,3-ペンタフルオロ-3-メトキシ-2-(トリフルオロメチル)-プロパンを使用した、6-フルオロ-4-メトキシ-2-(3-(5-メチルイソオキサゾリル))-5-(トリフルオロメチル)ピリミジンの製造
氷水冷却下、3-アミジノ-5-メチルイソオキサゾール塩酸塩0.5g(3.1mmol)をアセトニトリル10gに溶解させ、1,1,1,3,3-ペンタフルオロ-3-メトキシ-2-(トリフルオロメチル)-プロパン0.8g(3.6mmol)を滴下した。続いてジイソプロピルエチルアミン2.6g(20mmol)とアセトニトリル10gの混合溶液を滴下し室温まで昇温した。約16時間後、内容物のカラム精製を行った。得られた化合物の分析結果は、実施例2の生成物と同様であった。
2-(4-(3-エチル-5-メチルイソオキサゾリル))-6-フルオロ-4-メトキシ-5-(トリフルオロメチル)ピリミジンの製造
氷水冷却下、4-アミジノ-3-エチル-5-メチルイソオキサゾール塩酸塩0.3g(1.5mmol)をアセトニトリル15gに溶解させ、1,3,3,3-テトラフルオロ-1-メトキシ-2-(トリフルオロメチル)-1-プロペン0.4g(1.7mmol)を滴下した。続いてジイソプロピルエチルアミン1.0g(7.8mmol)とアセトニトリル5gの混合溶液を滴下し室温まで昇温した。16時間攪拌後、得られた反応液をカラム精製し、下記式(8)で示される化合物(化学式:C12H11F4N3O2、分子量:305.23g/mol)0.3g(1.1mmol)を得た。得られた化合物の単離収率は74%であった。
マススペクトル(APCI、m/z):305.6([M]―)
1H-NMR(400MHz、CDCl3) δppm:4.17(s,3H), 3.1(q,2H),2.84(s,3H),1.34(t,3H)
6-フルオロ-4-メトキシ-2-(3-イソオキサゾリル)-5-(トリフルオロメチル)ピリミジンの製造
3-イソオキサゾールカルボキシイミドアミド塩酸塩0.7g(4.4mmol)をアセトニトリル44mlに溶解し、1,3,3,3-テトラフルオロ-1-メトキシ-2-(トリフルオロメチル)-1-プロペン1.1g(5.2mmol)とジイソプロピルエチルアミン3.0g(23.2mmol)を加え室温で16.3時間攪拌後、反応液をカラム精製し、下記式(9)で示される化合物(化学式:C9H5F4N3O2、分子量:263.15g/mol)0.5g(1.7mmol)を得た。得られた化合物の単離収率は39.3%であった。
マススペクトル(APCI、m/z):264.1([M+H]+)
1H-NMR(400MHz、CDCl3) δppm:8.59(d,J=1.5Hz,1H),7.04(d,J=1.8Hz,1H),4.26(s,3H)
6-フルオロ-4-メトキシ-2-(5-イソオキサゾリル)-5-(トリフルオロメチル)ピリミジンの製造
5-イソオキサゾールカルボキシイミドアミド塩酸塩0.7g(3.1mmol)をアセトニトリル31mlに溶解し、1,3,3,3-テトラフルオロ-1-メトキシ-2-(トリフルオロメチル)-1-プロペン1.1g(5.2mmol)とジイソプロピルエチルアミン2.1g(16.2mmol)を加え室温で15.3時間攪拌後、反応液をカラム精製し、下記式(10)で示される化合物(化学式:C9H5F4N3O2、分子量:263.15g/mol)0.1 g(0.3 mmol)を得た。得られた化合物の単離収率は9.9%であった。
得られた化合物の分析結果は、下記の通りであった。
マススペクトル(APCI、m/z):264.1([M+H]+)
1H-NMR(400MHz、CDCl3) δppm:8.44(d,J=1.8Hz,1H),7.19(d,J=1.8Hz,1H),4.26(s,3H)
6-フルオロ-4-メトキシ-2-(2-オキサゾリル)-5-(トリフルオロメチル)ピリミジンの製造
2-オキサゾールカルボキシイミドアミド塩酸塩0.8g(5.2mmol)をアセトニトリル52mlに溶解し、1,3,3,3-テトラフルオロ-1-メトキシ-2-(トリフルオロメチル)-1-プロペン1.3g(6.1 mmol)とジイソプロピルエチルアミン3.5g(27.1mmol)を加え室温で18時間攪拌後、反応液をカラム精製し、下記式(11)で示される化合物(化学式:C9H5F4N3O2、分子量:263.15g/mol)0.7g(2.6mmol)を得た。得られた化合物の単離収率は50.5%であった。
マススペクトル(APCI、m/z):264.2([M+H]+)
1H-NMR(400MHz、CDCl3) δppm:7.92(s,1H),7.47(s,1H),4.29(s,3H)
6-フルオロ-4-メトキシ-2-(4-オキサゾリル)-5-(トリフルオロメチル)ピリミジンの製造
1,3-オキサゾール-4-カルボキシイミドアミド塩酸塩0.5g(3.5mmol)をアセトニトリル30mlに溶解し、1,3,3,3-テトラフルオロ-1-メトキシ-2-(トリフルオロメチル)-1-プロペン0.7 g(3.3mmol)とジイソプロピルエチルアミン2.0g(15.5mmol)を加え室温で18.2時間攪拌後、反応液をカラム精製し、下記式(12)で示される化合物(化学式:C9H5F4N3O2、分子量:263.15g/mol)0.4g(1.4mmol)を得た。得られた化合物の単離収率は41.7%であった。
得られた化合物の分析結果は、下記の通りであった。
マススペクトル(APCI、m/z):264.0([M]+)
1H-NMR(400MHz、CDCl3) δppm:78.52(d,J=0.9Hz,1H),8.03(d,J=0.9Hz,1H),4.23(s,3H)
Claims (5)
- 下記一般式(1a)または(1b)で表される、含フッ素ピリミジン化合物。
R1は炭素数1~12の炭化水素基を表し、
R2はハロゲン原子、炭素数1~10の炭化水素基、-CnF2n+1(nは1~10の整数である)、ニトロ基、ボロン酸基、シアノ基、-OA1、-OlSOmA1(lは0~1の整数、mは0~3の整数である)、-NA1A2、-OlCOOA1(lは0~1の整数である)、または-OlCONA1A2(lは0~1の整数である)を表し、A1、A2はそれぞれ独立して、水素原子または炭素数1~10の炭化水素基を表し、AlとA2は結合して環構造を形成しても良く、R2が複数存在する場合、それらは同一であっても異なっていても良く、
環Zは酸素原子を1個含み、窒素原子を1個以上含む5員芳香族複素環である。) - 下記一般式(2)で表されるフルオロイソブチレン誘導体と、下記一般式(3a)で表される化合物またはその塩とを反応させることにより、下記一般式(1a)で表される含フッ素ピリミジン化合物を得る工程、または
下記一般式(2)で表されるフルオロイソブチレン誘導体と、下記一般式(3b)で表される化合物またはその塩とを反応させることにより、下記一般式(1b)で表される含フッ素ピリミジン化合物を得る工程、
を有する、含フッ素ピリミジン化合物の製造方法。
R1は炭素数1~12の炭化水素基を表し、
R2はハロゲン原子、炭素数1~10の炭化水素基、-CnF2n+1(nは1~10の整数である)、ニトロ基、ボロン酸基、シアノ基、-OA1、-OlSOmA1(lは0~1の整数、mは0~3の整数である)、-NA1A2、-OlCOOA1(lは0~1の整数である)、または-OlCONA1A2(lは0~1の整数である)を表し、A1、A2はそれぞれ独立して、水素原子または炭素数1~10の炭化水素基を表し、AlとA2は結合して環構造を形成しても良く、R2が複数存在する場合、それらは同一であっても異なっていても良く、
環Zは酸素原子を1個含み、窒素原子を1個以上含む5員芳香族複素環である。) - 下記一般式(4)で表されるフルオロイソブタン誘導体と、下記一般式(3a)で表される化合物またはその塩とを反応させることにより、下記一般式(1a)で表される含フッ素ピリミジン化合物を得る工程、または
下記一般式(4)で表されるフルオロイソブタン誘導体と、下記一般式(3b)で表される化合物またはその塩とを反応させることにより、下記一般式(1b)で表される含フッ素ピリミジン化合物を得る工程、
を有する、含フッ素ピリミジン化合物の製造方法。
R1は炭素数1~12の炭化水素基を表し、
R2はハロゲン原子、炭素数1~10の炭化水素基、-CnF2n+1(nは1~10の整数である)、ニトロ基、ボロン酸基、シアノ基、-OA1、-OlSOmA1(lは0~1の整数、mは0~3の整数である)、-NA1A2、-OlCOOA1(lは0~1の整数である)、または-OlCONA1A2(lは0~1の整数である)を表し、A1、A2はそれぞれ独立して、水素原子または炭素数1~10の炭化水素基を表し、AlとA2は結合して環構造を形成しても良く、R2が複数存在する場合、それらは同一であっても異なっていても良く、
環Zは酸素原子を1個含み、窒素原子を1個以上含む5員芳香族複素環であり、
Xは、ハロゲン原子、シアノ基、-OA3、-NA3A4、-OCOOA3、-OCONA3A4、または-OlSOmA5(lは0~1の整数、mは0~3の整数である)を表し、A3、A4はそれぞれ独立して炭素数1~10の炭化水素基を表し、A3とA4が結合して環構造を形成しても良く、A5は水素原子または炭素数1~10の炭化水素基を表す。)
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021047661 | 2021-03-22 | ||
| JP2021047661 | 2021-03-22 | ||
| PCT/JP2022/011917 WO2022202537A1 (ja) | 2021-03-22 | 2022-03-16 | 含フッ素ピリミジン化合物およびその製造方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2022202537A1 JPWO2022202537A1 (ja) | 2022-09-29 |
| JP7614331B2 true JP7614331B2 (ja) | 2025-01-15 |
Family
ID=83396155
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2023509065A Active JP7614331B2 (ja) | 2021-03-22 | 2022-03-16 | 含フッ素ピリミジン化合物およびその製造方法 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US12583847B2 (ja) |
| EP (1) | EP4317154A4 (ja) |
| JP (1) | JP7614331B2 (ja) |
| CN (1) | CN117043158A (ja) |
| WO (1) | WO2022202537A1 (ja) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP4628482A1 (en) * | 2022-11-28 | 2025-10-08 | Unimatec Co., Ltd. | Fluorine-containing pyridone compound and method for producing same |
| WO2026048597A1 (ja) * | 2024-08-27 | 2026-03-05 | ユニマテック株式会社 | 含フッ素ピリミジン化合物、含フッ素ピリミジノン化合物および殺菌剤 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015085909A1 (zh) | 2013-12-10 | 2015-06-18 | 苏州大学 | 一种具有腺苷受体拮抗活性的氨基嘧啶杂环化合物 |
| WO2019007140A1 (zh) | 2017-07-05 | 2019-01-10 | 上海肇钰医药科技有限公司 | 作为腺苷a 2a受体拮抗剂的4-氨基嘧啶衍生物及其用途 |
| WO2020116296A1 (ja) | 2018-12-07 | 2020-06-11 | ユニマテック株式会社 | 含フッ素ピリミジン化合物およびその製造方法 |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS59104364A (ja) | 1982-12-03 | 1984-06-16 | Nippon Mektron Ltd | 新規ピリミジン誘導体およびその製造法 |
| JPS63216877A (ja) | 1987-03-06 | 1988-09-09 | Nippon Kayaku Co Ltd | 含フツ素ピリミジン誘導体 |
| EP4059927A4 (en) | 2019-11-14 | 2023-10-04 | Unimatec Co., Ltd. | FLUORINE-CONTAINING PYRAZOLE COMPOUND AND PRODUCTION PROCESS THEREOF |
-
2022
- 2022-03-16 EP EP22775325.8A patent/EP4317154A4/en active Pending
- 2022-03-16 US US18/282,718 patent/US12583847B2/en active Active
- 2022-03-16 CN CN202280021436.1A patent/CN117043158A/zh active Pending
- 2022-03-16 WO PCT/JP2022/011917 patent/WO2022202537A1/ja not_active Ceased
- 2022-03-16 JP JP2023509065A patent/JP7614331B2/ja active Active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015085909A1 (zh) | 2013-12-10 | 2015-06-18 | 苏州大学 | 一种具有腺苷受体拮抗活性的氨基嘧啶杂环化合物 |
| WO2019007140A1 (zh) | 2017-07-05 | 2019-01-10 | 上海肇钰医药科技有限公司 | 作为腺苷a 2a受体拮抗剂的4-氨基嘧啶衍生物及其用途 |
| WO2020116296A1 (ja) | 2018-12-07 | 2020-06-11 | ユニマテック株式会社 | 含フッ素ピリミジン化合物およびその製造方法 |
Non-Patent Citations (1)
| Title |
|---|
| INOUYE, Y. et al.,A Facile One-pot Preparation of 2-Methyl- and 2-Phenyl-4-fluoro-5-trifluoromethyl-6-methoxypyrimidin,Journal of Fluorine Chemistry,1985年,27,231-236 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP4317154A1 (en) | 2024-02-07 |
| EP4317154A4 (en) | 2025-03-12 |
| JPWO2022202537A1 (ja) | 2022-09-29 |
| WO2022202537A1 (ja) | 2022-09-29 |
| US20240190853A1 (en) | 2024-06-13 |
| US12583847B2 (en) | 2026-03-24 |
| CN117043158A (zh) | 2023-11-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7439124B2 (ja) | 含フッ素ピラゾール化合物およびその製造方法 | |
| JP6802416B2 (ja) | 含フッ素ピリミジン化合物およびその製造方法 | |
| JP7614331B2 (ja) | 含フッ素ピリミジン化合物およびその製造方法 | |
| JP7595153B2 (ja) | 含フッ素ピラゾール化合物およびその製造方法 | |
| TWI621609B (zh) | 製備4-鹵烷基-3-巰基-取代之2-羥基苯甲酸衍生物 | |
| JP7159485B2 (ja) | 含フッ素ピリミジン化合物およびその製造方法 | |
| JP7230274B2 (ja) | 含フッ素ピリミジン化合物およびその製造方法 | |
| JP7109684B2 (ja) | 含フッ素ピリミジン化合物およびその製造方法 | |
| JP7349551B2 (ja) | 含フッ素ピリミジン化合物およびその製造方法 | |
| JP7085697B2 (ja) | 含フッ素ピリミジン化合物およびその製造方法 | |
| JP7649872B2 (ja) | 含フッ素ピラゾール化合物およびその製造方法 | |
| CN108218758B (zh) | 一种2,4-二取代吡咯衍生物的制备方法 | |
| JP2024005443A (ja) | 塩素化された含フッ素ピリミジン化合物の製造方法 | |
| JP7224548B2 (ja) | 含フッ素縮環ピリミジン化合物およびその製造方法 | |
| EP3287448A1 (en) | Method for producing dicarboxylic acid compound | |
| CN120641400A (zh) | 含氟吡唑啉酮化合物及其制造方法 | |
| JPH0578286A (ja) | N−トリフルオロメチル芳香族アミン誘導体及びその製造法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20230912 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240924 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20241211 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20241226 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7614331 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |