JP7541748B2 - 心筋細胞の富化方法 - Google Patents
心筋細胞の富化方法 Download PDFInfo
- Publication number
- JP7541748B2 JP7541748B2 JP2021540957A JP2021540957A JP7541748B2 JP 7541748 B2 JP7541748 B2 JP 7541748B2 JP 2021540957 A JP2021540957 A JP 2021540957A JP 2021540957 A JP2021540957 A JP 2021540957A JP 7541748 B2 JP7541748 B2 JP 7541748B2
- Authority
- JP
- Japan
- Prior art keywords
- cells
- cell
- atrial
- ventricular
- cell population
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 210000004413 cardiac myocyte Anatomy 0.000 title claims description 51
- 238000000034 method Methods 0.000 title claims description 47
- 210000004027 cell Anatomy 0.000 claims description 317
- 210000002072 atrial myocyte Anatomy 0.000 claims description 82
- 210000001567 regular cardiac muscle cell of ventricle Anatomy 0.000 claims description 71
- 230000001746 atrial effect Effects 0.000 claims description 67
- 230000014509 gene expression Effects 0.000 claims description 66
- 210000000663 muscle cell Anatomy 0.000 claims description 66
- 210000000130 stem cell Anatomy 0.000 claims description 58
- 230000002861 ventricular Effects 0.000 claims description 58
- 210000004263 induced pluripotent stem cell Anatomy 0.000 claims description 28
- 239000000523 sample Substances 0.000 claims description 17
- 238000001514 detection method Methods 0.000 claims description 16
- 238000004519 manufacturing process Methods 0.000 claims description 15
- 230000001939 inductive effect Effects 0.000 claims description 8
- 239000003153 chemical reaction reagent Substances 0.000 claims description 7
- 108090000623 proteins and genes Proteins 0.000 description 46
- 239000003550 marker Substances 0.000 description 44
- 230000036982 action potential Effects 0.000 description 36
- 230000004069 differentiation Effects 0.000 description 36
- 239000002609 medium Substances 0.000 description 35
- 102000004169 proteins and genes Human genes 0.000 description 26
- 239000003814 drug Substances 0.000 description 23
- 239000003112 inhibitor Substances 0.000 description 20
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 18
- 230000006698 induction Effects 0.000 description 12
- 229940079593 drug Drugs 0.000 description 11
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 10
- 229910052760 oxygen Inorganic materials 0.000 description 10
- 239000001301 oxygen Substances 0.000 description 10
- 229960005070 ascorbic acid Drugs 0.000 description 9
- 235000010323 ascorbic acid Nutrition 0.000 description 9
- 239000011668 ascorbic acid Substances 0.000 description 9
- AIXAANGOTKPUOY-UHFFFAOYSA-N carbachol Chemical compound [Cl-].C[N+](C)(C)CCOC(N)=O AIXAANGOTKPUOY-UHFFFAOYSA-N 0.000 description 9
- 229960004484 carbachol Drugs 0.000 description 9
- 210000001671 embryonic stem cell Anatomy 0.000 description 9
- PJUIMOJAAPLTRJ-UHFFFAOYSA-N monothioglycerol Chemical compound OCC(O)CS PJUIMOJAAPLTRJ-UHFFFAOYSA-N 0.000 description 9
- 230000004044 response Effects 0.000 description 9
- 238000012360 testing method Methods 0.000 description 9
- 102100024505 Bone morphogenetic protein 4 Human genes 0.000 description 8
- 101000762379 Homo sapiens Bone morphogenetic protein 4 Proteins 0.000 description 8
- 102000004338 Transferrin Human genes 0.000 description 8
- 108090000901 Transferrin Proteins 0.000 description 8
- 102000005789 Vascular Endothelial Growth Factors Human genes 0.000 description 8
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 description 8
- 102000013814 Wnt Human genes 0.000 description 8
- 108050003627 Wnt Proteins 0.000 description 8
- 238000004458 analytical method Methods 0.000 description 8
- 230000024245 cell differentiation Effects 0.000 description 8
- 239000012581 transferrin Substances 0.000 description 8
- NUKYPUAOHBNCPY-UHFFFAOYSA-N 4-aminopyridine Chemical compound NC1=CC=NC=C1 NUKYPUAOHBNCPY-UHFFFAOYSA-N 0.000 description 7
- 229960004979 fampridine Drugs 0.000 description 7
- 239000000203 mixture Substances 0.000 description 7
- 210000001778 pluripotent stem cell Anatomy 0.000 description 7
- 239000000243 solution Substances 0.000 description 7
- 108091006146 Channels Proteins 0.000 description 6
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 6
- 229930182816 L-glutamine Natural products 0.000 description 6
- 239000007640 basal medium Substances 0.000 description 6
- FHYUGAJXYORMHI-UHFFFAOYSA-N SB 431542 Chemical compound C1=CC(C(=O)N)=CC=C1C1=NC(C=2C=C3OCOC3=CC=2)=C(C=2N=CC=CC=2)N1 FHYUGAJXYORMHI-UHFFFAOYSA-N 0.000 description 5
- 102000004887 Transforming Growth Factor beta Human genes 0.000 description 5
- 108090001012 Transforming Growth Factor beta Proteins 0.000 description 5
- 230000001413 cellular effect Effects 0.000 description 5
- 238000000684 flow cytometry Methods 0.000 description 5
- 208000019622 heart disease Diseases 0.000 description 5
- 210000004379 membrane Anatomy 0.000 description 5
- 239000012528 membrane Substances 0.000 description 5
- 239000013642 negative control Substances 0.000 description 5
- 108020004707 nucleic acids Proteins 0.000 description 5
- 102000039446 nucleic acids Human genes 0.000 description 5
- 150000007523 nucleic acids Chemical class 0.000 description 5
- ZRKFYGHZFMAOKI-QMGMOQQFSA-N tgfbeta Chemical compound C([C@H](NC(=O)[C@H](C(C)C)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CC(C)C)NC(=O)CNC(=O)[C@H](C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](N)CCSC)C(C)C)[C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(O)=O)C1=CC=C(O)C=C1 ZRKFYGHZFMAOKI-QMGMOQQFSA-N 0.000 description 5
- 210000001519 tissue Anatomy 0.000 description 5
- 108010065376 COUP Transcription Factor I Proteins 0.000 description 4
- 102100028228 COUP transcription factor 1 Human genes 0.000 description 4
- 102100028226 COUP transcription factor 2 Human genes 0.000 description 4
- 101710188750 COUP transcription factor 2 Proteins 0.000 description 4
- 108090000379 Fibroblast growth factor 2 Proteins 0.000 description 4
- 102100024785 Fibroblast growth factor 2 Human genes 0.000 description 4
- 102100033063 G protein-activated inward rectifier potassium channel 1 Human genes 0.000 description 4
- 102100039990 Hairy/enhancer-of-split related with YRPW motif protein 2 Human genes 0.000 description 4
- 241000282412 Homo Species 0.000 description 4
- 101000944266 Homo sapiens G protein-activated inward rectifier potassium channel 1 Proteins 0.000 description 4
- 101001035089 Homo sapiens Hairy/enhancer-of-split related with YRPW motif protein 2 Proteins 0.000 description 4
- 101000780028 Homo sapiens Natriuretic peptides A Proteins 0.000 description 4
- 241000699666 Mus <mouse, genus> Species 0.000 description 4
- 102100026925 Myosin regulatory light chain 2, ventricular/cardiac muscle isoform Human genes 0.000 description 4
- 102100034296 Natriuretic peptides A Human genes 0.000 description 4
- 102100037445 Potassium voltage-gated channel subfamily A member 5 Human genes 0.000 description 4
- 101710167708 T-box transcription factor TBX5 Proteins 0.000 description 4
- 102100024755 T-box transcription factor TBX5 Human genes 0.000 description 4
- 239000012190 activator Substances 0.000 description 4
- 108010023082 activin A Proteins 0.000 description 4
- 238000005138 cryopreservation Methods 0.000 description 4
- 238000012258 culturing Methods 0.000 description 4
- 238000010195 expression analysis Methods 0.000 description 4
- 230000006870 function Effects 0.000 description 4
- 108010065781 myosin light chain 2 Proteins 0.000 description 4
- 230000008569 process Effects 0.000 description 4
- 230000002336 repolarization Effects 0.000 description 4
- XVMHQSDMKWQNBK-UHFFFAOYSA-N 2-[[3-(4-fluorophenyl)-4-oxo-6,7-dihydrothieno[3,2-d]pyrimidin-2-yl]sulfanyl]-n-(6-methyl-1,3-benzothiazol-2-yl)acetamide Chemical compound S1C2=CC(C)=CC=C2N=C1NC(=O)CSC1=NC=2CCSC=2C(=O)N1C1=CC=C(F)C=C1 XVMHQSDMKWQNBK-UHFFFAOYSA-N 0.000 description 3
- 208000020446 Cardiac disease Diseases 0.000 description 3
- 238000000018 DNA microarray Methods 0.000 description 3
- 238000002965 ELISA Methods 0.000 description 3
- 101001026214 Homo sapiens Potassium voltage-gated channel subfamily A member 5 Proteins 0.000 description 3
- 241000699670 Mus sp. Species 0.000 description 3
- 239000003855 balanced salt solution Substances 0.000 description 3
- 239000000560 biocompatible material Substances 0.000 description 3
- XHBVYDAKJHETMP-UHFFFAOYSA-N dorsomorphin Chemical compound C=1C=C(C2=CN3N=CC(=C3N=C2)C=2C=CN=CC=2)C=CC=1OCCN1CCCCC1 XHBVYDAKJHETMP-UHFFFAOYSA-N 0.000 description 3
- 230000000694 effects Effects 0.000 description 3
- 210000002242 embryoid body Anatomy 0.000 description 3
- 210000002950 fibroblast Anatomy 0.000 description 3
- 239000011521 glass Substances 0.000 description 3
- 238000010324 immunological assay Methods 0.000 description 3
- 238000012744 immunostaining Methods 0.000 description 3
- 230000001965 increasing effect Effects 0.000 description 3
- 239000007924 injection Substances 0.000 description 3
- 238000002347 injection Methods 0.000 description 3
- 238000012423 maintenance Methods 0.000 description 3
- 238000002493 microarray Methods 0.000 description 3
- 210000003205 muscle Anatomy 0.000 description 3
- 238000003199 nucleic acid amplification method Methods 0.000 description 3
- 230000001172 regenerating effect Effects 0.000 description 3
- 238000003757 reverse transcription PCR Methods 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 2
- BDCBRQYHYNUWAM-UHFFFAOYSA-N 2-phenyl-4-(5-pyridin-2-yl-1h-pyrazol-4-yl)pyridine Chemical compound C1=NNC(C=2N=CC=CC=2)=C1C(C=1)=CC=NC=1C1=CC=CC=C1 BDCBRQYHYNUWAM-UHFFFAOYSA-N 0.000 description 2
- RYKSGWSKILPDDY-UHFFFAOYSA-N 3-[[5-(6-methylpyridin-2-yl)-4-quinoxalin-6-yl-1h-imidazol-2-yl]methyl]benzamide Chemical compound CC1=CC=CC(C2=C(N=C(CC=3C=C(C=CC=3)C(N)=O)N2)C=2C=C3N=CC=NC3=CC=2)=N1 RYKSGWSKILPDDY-UHFFFAOYSA-N 0.000 description 2
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 2
- 102100037362 Fibronectin Human genes 0.000 description 2
- 108010067306 Fibronectins Proteins 0.000 description 2
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 2
- 101000851334 Homo sapiens Troponin I, cardiac muscle Proteins 0.000 description 2
- 101000680020 Homo sapiens Troponin I, slow skeletal muscle Proteins 0.000 description 2
- 101710135898 Myc proto-oncogene protein Proteins 0.000 description 2
- 102100038895 Myc proto-oncogene protein Human genes 0.000 description 2
- -1 NANOG Proteins 0.000 description 2
- 229920000954 Polyglycolide Polymers 0.000 description 2
- 239000004372 Polyvinyl alcohol Substances 0.000 description 2
- 238000003559 RNA-seq method Methods 0.000 description 2
- WGZOTBUYUFBEPZ-UHFFFAOYSA-N SB 505124 Chemical compound CC1=CC=CC(C2=C(N=C(N2)C(C)(C)C)C=2C=C3OCOC3=CC=2)=N1 WGZOTBUYUFBEPZ-UHFFFAOYSA-N 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 108091023040 Transcription factor Proteins 0.000 description 2
- 102000040945 Transcription factor Human genes 0.000 description 2
- 101710150448 Transcriptional regulator Myc Proteins 0.000 description 2
- 102100036859 Troponin I, cardiac muscle Human genes 0.000 description 2
- 102100022171 Troponin I, slow skeletal muscle Human genes 0.000 description 2
- 102000006757 Wnt Receptors Human genes 0.000 description 2
- 108010047118 Wnt Receptors Proteins 0.000 description 2
- 239000000654 additive Substances 0.000 description 2
- SHGAZHPCJJPHSC-YCNIQYBTSA-N all-trans-retinoic acid Chemical compound OC(=O)\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C SHGAZHPCJJPHSC-YCNIQYBTSA-N 0.000 description 2
- 239000003242 anti bacterial agent Substances 0.000 description 2
- 239000002585 base Substances 0.000 description 2
- 238000004113 cell culture Methods 0.000 description 2
- 230000030833 cell death Effects 0.000 description 2
- 230000004663 cell proliferation Effects 0.000 description 2
- 239000002458 cell surface marker Substances 0.000 description 2
- 239000006285 cell suspension Substances 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 239000003795 chemical substances by application Substances 0.000 description 2
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 2
- 201000010099 disease Diseases 0.000 description 2
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 2
- 230000001747 exhibiting effect Effects 0.000 description 2
- 210000001654 germ layer Anatomy 0.000 description 2
- 239000008103 glucose Substances 0.000 description 2
- 206010020871 hypertrophic cardiomyopathy Diseases 0.000 description 2
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 2
- 238000002955 isolation Methods 0.000 description 2
- 210000003716 mesoderm Anatomy 0.000 description 2
- 108020004999 messenger RNA Proteins 0.000 description 2
- 210000004457 myocytus nodalis Anatomy 0.000 description 2
- SAGZIBJAQGBRQA-UHFFFAOYSA-N n-(oxan-4-yl)-4-[4-(5-pyridin-2-yl-1h-pyrazol-4-yl)pyridin-2-yl]benzamide Chemical compound C=1C=C(C=2N=CC=C(C=2)C2=C(NN=C2)C=2N=CC=CC=2)C=CC=1C(=O)NC1CCOCC1 SAGZIBJAQGBRQA-UHFFFAOYSA-N 0.000 description 2
- 239000004633 polyglycolic acid Substances 0.000 description 2
- 229920002451 polyvinyl alcohol Polymers 0.000 description 2
- 235000019422 polyvinyl alcohol Nutrition 0.000 description 2
- 239000003755 preservative agent Substances 0.000 description 2
- 230000035755 proliferation Effects 0.000 description 2
- 230000001902 propagating effect Effects 0.000 description 2
- 230000008672 reprogramming Effects 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 229930002330 retinoic acid Natural products 0.000 description 2
- 230000019491 signal transduction Effects 0.000 description 2
- 230000022379 skeletal muscle tissue development Effects 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 230000002269 spontaneous effect Effects 0.000 description 2
- 238000010561 standard procedure Methods 0.000 description 2
- 235000000346 sugar Nutrition 0.000 description 2
- 229960001727 tretinoin Drugs 0.000 description 2
- OYHQOLUKZRVURQ-NTGFUMLPSA-N (9Z,12Z)-9,10,12,13-tetratritiooctadeca-9,12-dienoic acid Chemical compound C(CCCCCCC\C(=C(/C\C(=C(/CCCCC)\[3H])\[3H])\[3H])\[3H])(=O)O OYHQOLUKZRVURQ-NTGFUMLPSA-N 0.000 description 1
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 1
- JUHTXZGCTPDXRU-UHFFFAOYSA-N 1-[4-(1,3-benzodioxol-5-yl)-5-(6-methylpyridin-2-yl)-1h-imidazol-2-yl]bicyclo[2.2.2]octane-4-carboxamide Chemical compound CC1=CC=CC(C2=C(N=C(N2)C23CCC(CC2)(CC3)C(N)=O)C=2C=C3OCOC3=CC=2)=N1 JUHTXZGCTPDXRU-UHFFFAOYSA-N 0.000 description 1
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 1
- RHUJMHOIQBDFQR-UHFFFAOYSA-N 2-[[3-(2-methoxyphenyl)-4-oxo-6,7-dihydrothieno[3,2-d]pyrimidin-2-yl]sulfanyl]-n-(6-methyl-1,3-benzothiazol-2-yl)acetamide Chemical compound COC1=CC=CC=C1N1C(=O)C(SCC2)=C2N=C1SCC(=O)NC1=NC2=CC=C(C)C=C2S1 RHUJMHOIQBDFQR-UHFFFAOYSA-N 0.000 description 1
- CDOVNWNANFFLFJ-UHFFFAOYSA-N 4-[6-[4-(1-piperazinyl)phenyl]-3-pyrazolo[1,5-a]pyrimidinyl]quinoline Chemical compound C1CNCCN1C1=CC=C(C2=CN3N=CC(=C3N=C2)C=2C3=CC=CC=C3N=CC=2)C=C1 CDOVNWNANFFLFJ-UHFFFAOYSA-N 0.000 description 1
- KURYSXLJGKKDHT-UHFFFAOYSA-N 6-chloro-5-[4-(2-hydroxy-3-methoxyphenyl)phenyl]-3-(3-methoxyphenyl)-1h-pyrrolo[3,2-d]pyrimidine-2,4-dione Chemical compound COC1=CC=CC(N2C(C=3N(C=4C=CC(=CC=4)C=4C(=C(OC)C=CC=4)O)C(Cl)=CC=3NC2=O)=O)=C1 KURYSXLJGKKDHT-UHFFFAOYSA-N 0.000 description 1
- FHVDTGUDJYJELY-UHFFFAOYSA-N 6-{[2-carboxy-4,5-dihydroxy-6-(phosphanyloxy)oxan-3-yl]oxy}-4,5-dihydroxy-3-phosphanyloxane-2-carboxylic acid Chemical compound O1C(C(O)=O)C(P)C(O)C(O)C1OC1C(C(O)=O)OC(OP)C(O)C1O FHVDTGUDJYJELY-UHFFFAOYSA-N 0.000 description 1
- 101150030879 ALDH1A2 gene Proteins 0.000 description 1
- HJCMDXDYPOUFDY-WHFBIAKZSA-N Ala-Gln Chemical compound C[C@H](N)C(=O)N[C@H](C(O)=O)CCC(N)=O HJCMDXDYPOUFDY-WHFBIAKZSA-N 0.000 description 1
- 108010088751 Albumins Proteins 0.000 description 1
- 102000009027 Albumins Human genes 0.000 description 1
- 108091023037 Aptamer Proteins 0.000 description 1
- 208000031229 Cardiomyopathies Diseases 0.000 description 1
- 241000202252 Cerberus Species 0.000 description 1
- 102100025745 Cerberus Human genes 0.000 description 1
- 101710010675 Cerberus Proteins 0.000 description 1
- 108010035532 Collagen Proteins 0.000 description 1
- 102000008186 Collagen Human genes 0.000 description 1
- 206010056370 Congestive cardiomyopathy Diseases 0.000 description 1
- CKLJMWTZIZZHCS-UHFFFAOYSA-N D-OH-Asp Natural products OC(=O)C(N)CC(O)=O CKLJMWTZIZZHCS-UHFFFAOYSA-N 0.000 description 1
- 102100030074 Dickkopf-related protein 1 Human genes 0.000 description 1
- 101710099518 Dickkopf-related protein 1 Proteins 0.000 description 1
- 201000010046 Dilated cardiomyopathy Diseases 0.000 description 1
- 102100035716 Glycophorin-A Human genes 0.000 description 1
- 229920002683 Glycosaminoglycan Polymers 0.000 description 1
- 108010017080 Granulocyte Colony-Stimulating Factor Proteins 0.000 description 1
- 102000004269 Granulocyte Colony-Stimulating Factor Human genes 0.000 description 1
- 239000007995 HEPES buffer Substances 0.000 description 1
- 239000007756 Ham's F12 Nutrient Mixture Substances 0.000 description 1
- 206010019280 Heart failures Diseases 0.000 description 1
- 101001074244 Homo sapiens Glycophorin-A Proteins 0.000 description 1
- 101000840572 Homo sapiens Insulin-like growth factor-binding protein 4 Proteins 0.000 description 1
- 101000958741 Homo sapiens Myosin-6 Proteins 0.000 description 1
- 101001094700 Homo sapiens POU domain, class 5, transcription factor 1 Proteins 0.000 description 1
- 101000685824 Homo sapiens Probable RNA polymerase II nuclear localization protein SLC7A6OS Proteins 0.000 description 1
- 101000984042 Homo sapiens Protein lin-28 homolog A Proteins 0.000 description 1
- 101000713275 Homo sapiens Solute carrier family 22 member 3 Proteins 0.000 description 1
- 101000687905 Homo sapiens Transcription factor SOX-2 Proteins 0.000 description 1
- 102000008100 Human Serum Albumin Human genes 0.000 description 1
- 108091006905 Human Serum Albumin Proteins 0.000 description 1
- 108090001061 Insulin Proteins 0.000 description 1
- 102000004877 Insulin Human genes 0.000 description 1
- 102100029224 Insulin-like growth factor-binding protein 4 Human genes 0.000 description 1
- 102000000426 Integrin alpha6 Human genes 0.000 description 1
- 108010041100 Integrin alpha6 Proteins 0.000 description 1
- 239000007760 Iscove's Modified Dulbecco's Medium Substances 0.000 description 1
- 108700021430 Kruppel-Like Factor 4 Proteins 0.000 description 1
- CKLJMWTZIZZHCS-UWTATZPHSA-N L-Aspartic acid Natural products OC(=O)[C@H](N)CC(O)=O CKLJMWTZIZZHCS-UWTATZPHSA-N 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- 208000009525 Myocarditis Diseases 0.000 description 1
- 102000005604 Myosin Heavy Chains Human genes 0.000 description 1
- 102100038319 Myosin-6 Human genes 0.000 description 1
- WRKPZSMRWPJJDH-UHFFFAOYSA-N N-(6-methyl-1,3-benzothiazol-2-yl)-2-[(4-oxo-3-phenyl-6,7-dihydrothieno[3,2-d]pyrimidin-2-yl)thio]acetamide Chemical compound S1C2=CC(C)=CC=C2N=C1NC(=O)CSC1=NC=2CCSC=2C(=O)N1C1=CC=CC=C1 WRKPZSMRWPJJDH-UHFFFAOYSA-N 0.000 description 1
- MKYBYDHXWVHEJW-UHFFFAOYSA-N N-[1-oxo-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)propan-2-yl]-2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidine-5-carboxamide Chemical compound O=C(C(C)NC(=O)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F)N1CC2=C(CC1)NN=N2 MKYBYDHXWVHEJW-UHFFFAOYSA-N 0.000 description 1
- 102100035423 POU domain, class 5, transcription factor 1 Human genes 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 101710154115 Potassium voltage-gated channel subfamily A member 5 Proteins 0.000 description 1
- 102100023136 Probable RNA polymerase II nuclear localization protein SLC7A6OS Human genes 0.000 description 1
- 102100025460 Protein lin-28 homolog A Human genes 0.000 description 1
- 108010067787 Proteoglycans Proteins 0.000 description 1
- 239000012980 RPMI-1640 medium Substances 0.000 description 1
- 101100247004 Rattus norvegicus Qsox1 gene Proteins 0.000 description 1
- 102100040070 Retinal dehydrogenase 2 Human genes 0.000 description 1
- 101150086694 SLC22A3 gene Proteins 0.000 description 1
- BUGBHKTXTAQXES-UHFFFAOYSA-N Selenium Chemical compound [Se] BUGBHKTXTAQXES-UHFFFAOYSA-N 0.000 description 1
- 108700031126 Tetraspanins Proteins 0.000 description 1
- 102000043977 Tetraspanins Human genes 0.000 description 1
- 102100024270 Transcription factor SOX-2 Human genes 0.000 description 1
- 102000004903 Troponin Human genes 0.000 description 1
- 108090001027 Troponin Proteins 0.000 description 1
- 108010051583 Ventricular Myosins Proteins 0.000 description 1
- KLGQSVMIPOVQAX-UHFFFAOYSA-N XAV939 Chemical compound N=1C=2CCSCC=2C(O)=NC=1C1=CC=C(C(F)(F)F)C=C1 KLGQSVMIPOVQAX-UHFFFAOYSA-N 0.000 description 1
- 239000000556 agonist Substances 0.000 description 1
- 229960002648 alanylglutamine Drugs 0.000 description 1
- 229940072056 alginate Drugs 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- DTOSIQBPPRVQHS-PDBXOOCHSA-N alpha-linolenic acid Chemical compound CC\C=C/C\C=C/C\C=C/CCCCCCCC(O)=O DTOSIQBPPRVQHS-PDBXOOCHSA-N 0.000 description 1
- 235000020661 alpha-linolenic acid Nutrition 0.000 description 1
- 150000001413 amino acids Chemical group 0.000 description 1
- 230000003321 amplification Effects 0.000 description 1
- 230000000844 anti-bacterial effect Effects 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 235000006708 antioxidants Nutrition 0.000 description 1
- 108010054176 apotransferrin Proteins 0.000 description 1
- 229960005261 aspartic acid Drugs 0.000 description 1
- 239000003899 bactericide agent Substances 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 210000001185 bone marrow Anatomy 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 239000007853 buffer solution Substances 0.000 description 1
- 230000000747 cardiac effect Effects 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 230000021164 cell adhesion Effects 0.000 description 1
- 230000007910 cell fusion Effects 0.000 description 1
- 230000009087 cell motility Effects 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 239000002738 chelating agent Substances 0.000 description 1
- 235000012000 cholesterol Nutrition 0.000 description 1
- 229940107161 cholesterol Drugs 0.000 description 1
- 229920001436 collagen Polymers 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 210000000805 cytoplasm Anatomy 0.000 description 1
- 230000003111 delayed effect Effects 0.000 description 1
- 210000005258 dental pulp stem cell Anatomy 0.000 description 1
- 210000004207 dermis Anatomy 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- 239000002270 dispersing agent Substances 0.000 description 1
- 239000003937 drug carrier Substances 0.000 description 1
- 210000003981 ectoderm Anatomy 0.000 description 1
- 210000002257 embryonic structure Anatomy 0.000 description 1
- 210000001900 endoderm Anatomy 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- DEFVIWRASFVYLL-UHFFFAOYSA-N ethylene glycol bis(2-aminoethyl)tetraacetic acid Chemical compound OC(=O)CN(CC(O)=O)CCOCCOCCN(CC(O)=O)CC(O)=O DEFVIWRASFVYLL-UHFFFAOYSA-N 0.000 description 1
- 230000005284 excitation Effects 0.000 description 1
- 230000007717 exclusion Effects 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 239000004744 fabric Substances 0.000 description 1
- 210000004700 fetal blood Anatomy 0.000 description 1
- 230000001605 fetal effect Effects 0.000 description 1
- 238000007710 freezing Methods 0.000 description 1
- 230000008014 freezing Effects 0.000 description 1
- 239000012595 freezing medium Substances 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- 210000004602 germ cell Anatomy 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- 210000003780 hair follicle Anatomy 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 210000003958 hematopoietic stem cell Anatomy 0.000 description 1
- CHSDJDLAKKAWCI-UHFFFAOYSA-N hth-01-015 Chemical compound N1=C2N(C)C3=CC4=CC=CC=C4C=C3C(=O)N(C)C2=C(C)N=C1NC(=C1)C=NN1C1CCNCC1 CHSDJDLAKKAWCI-UHFFFAOYSA-N 0.000 description 1
- 210000005260 human cell Anatomy 0.000 description 1
- 210000004408 hybridoma Anatomy 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- HBDSHCUSXQATPO-BGBJRWHRSA-N indirubin-3'-monoxime Chemical compound O=C/1NC2=CC=CC=C2C\1=C\1/C(=N/O)/C2=CC=CC=C2N/1 HBDSHCUSXQATPO-BGBJRWHRSA-N 0.000 description 1
- 229940125396 insulin Drugs 0.000 description 1
- 102000006495 integrins Human genes 0.000 description 1
- 108010044426 integrins Proteins 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 239000007928 intraperitoneal injection Substances 0.000 description 1
- 238000010253 intravenous injection Methods 0.000 description 1
- ZGSXEXBYLJIOGF-BOPNQXPFSA-N iwr-1 Chemical compound C=1C=CC2=CC=CN=C2C=1NC(=O)C(C=C1)=CC=C1N1C(=O)[C@@H]2C(C=C3)CC3[C@@H]2C1=O ZGSXEXBYLJIOGF-BOPNQXPFSA-N 0.000 description 1
- 238000002350 laparotomy Methods 0.000 description 1
- 239000010410 layer Substances 0.000 description 1
- 229960004488 linolenic acid Drugs 0.000 description 1
- KQQKGWQCNNTQJW-UHFFFAOYSA-N linolenic acid Natural products CC=CCCC=CCC=CCCCCCCCC(O)=O KQQKGWQCNNTQJW-UHFFFAOYSA-N 0.000 description 1
- 108010082117 matrigel Proteins 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 210000002901 mesenchymal stem cell Anatomy 0.000 description 1
- 210000002200 mouth mucosa Anatomy 0.000 description 1
- 230000003551 muscarinic effect Effects 0.000 description 1
- 208000010125 myocardial infarction Diseases 0.000 description 1
- 208000031225 myocardial ischemia Diseases 0.000 description 1
- SDGJBAUIGHSMRI-UHFFFAOYSA-N n-[3-[5-chloro-2-[2-methoxy-4-(4-methylpiperazin-1-yl)anilino]pyrimidin-4-yl]oxyphenyl]propanamide Chemical compound CCC(=O)NC1=CC=CC(OC=2C(=CN=C(NC=3C(=CC(=CC=3)N3CCN(C)CC3)OC)N=2)Cl)=C1 SDGJBAUIGHSMRI-UHFFFAOYSA-N 0.000 description 1
- 210000001178 neural stem cell Anatomy 0.000 description 1
- 239000004745 nonwoven fabric Substances 0.000 description 1
- 230000007959 normoxia Effects 0.000 description 1
- 239000002773 nucleotide Substances 0.000 description 1
- 125000003729 nucleotide group Chemical group 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 210000004976 peripheral blood cell Anatomy 0.000 description 1
- 229960003243 phenformin Drugs 0.000 description 1
- ICFJFFQQTFMIBG-UHFFFAOYSA-N phenformin Chemical compound NC(=N)NC(=N)NCCC1=CC=CC=C1 ICFJFFQQTFMIBG-UHFFFAOYSA-N 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 229920000747 poly(lactic acid) Polymers 0.000 description 1
- 239000004626 polylactic acid Substances 0.000 description 1
- 229940117828 polylactic acid-polyglycolic acid copolymer Drugs 0.000 description 1
- 239000003761 preservation solution Substances 0.000 description 1
- 230000002062 proliferating effect Effects 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 238000002331 protein detection Methods 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 230000004043 responsiveness Effects 0.000 description 1
- 239000011435 rock Substances 0.000 description 1
- 229910052711 selenium Inorganic materials 0.000 description 1
- 239000011669 selenium Substances 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 239000002356 single layer Substances 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 210000001082 somatic cell Anatomy 0.000 description 1
- 210000001988 somatic stem cell Anatomy 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- 150000005846 sugar alcohols Chemical class 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 230000008685 targeting Effects 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- 238000013334 tissue model Methods 0.000 description 1
- 238000013518 transcription Methods 0.000 description 1
- 230000035897 transcription Effects 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 238000013519 translation Methods 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
- 239000002759 woven fabric Substances 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2896—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against molecules with a "CD"-designation, not provided for elsewhere
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/115—Aptamers, i.e. nucleic acids binding a target molecule specifically and with high affinity without hybridising therewith ; Nucleic acids binding to non-nucleic acids, e.g. aptamers
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0652—Cells of skeletal and connective tissues; Mesenchyme
- C12N5/0657—Cardiomyocytes; Heart cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/10—Cells modified by introduction of foreign genetic material
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/02—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving viable microorganisms
- C12Q1/04—Determining presence or kind of microorganism; Use of selective media for testing antibiotics or bacteriocides; Compositions containing a chemical indicator therefor
- C12Q1/06—Quantitative determination
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/569—Immunoassay; Biospecific binding assay; Materials therefor for microorganisms, e.g. protozoa, bacteria, viruses
- G01N33/56966—Animal cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2500/00—Specific components of cell culture medium
- C12N2500/05—Inorganic components
- C12N2500/10—Metals; Metal chelators
- C12N2500/20—Transition metals
- C12N2500/24—Iron; Fe chelators; Transferrin
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2500/00—Specific components of cell culture medium
- C12N2500/30—Organic components
- C12N2500/32—Amino acids
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/115—Basic fibroblast growth factor (bFGF, FGF-2)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/155—Bone morphogenic proteins [BMP]; Osteogenins; Osteogenic factor; Bone inducing factor
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/16—Activin; Inhibin; Mullerian inhibiting substance
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/165—Vascular endothelial growth factor [VEGF]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/50—Cell markers; Cell surface determinants
- C12N2501/599—Cell markers; Cell surface determinants with CD designations not provided for elsewhere
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2506/00—Differentiation of animal cells from one lineage to another; Differentiation of pluripotent cells
- C12N2506/45—Differentiation of animal cells from one lineage to another; Differentiation of pluripotent cells from artificially induced pluripotent stem cells
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/435—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans
- G01N2333/705—Assays involving receptors, cell surface antigens or cell surface determinants
- G01N2333/70596—Molecules with a "CD"-designation not provided for elsewhere in G01N2333/705
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- Biomedical Technology (AREA)
- Organic Chemistry (AREA)
- Genetics & Genomics (AREA)
- Biotechnology (AREA)
- Zoology (AREA)
- Immunology (AREA)
- Wood Science & Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Molecular Biology (AREA)
- Microbiology (AREA)
- Cell Biology (AREA)
- General Engineering & Computer Science (AREA)
- Biophysics (AREA)
- Physics & Mathematics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Hematology (AREA)
- Medicinal Chemistry (AREA)
- Urology & Nephrology (AREA)
- Analytical Chemistry (AREA)
- Rheumatology (AREA)
- Cardiology (AREA)
- Food Science & Technology (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Virology (AREA)
- Tropical Medicine & Parasitology (AREA)
- Toxicology (AREA)
- Plant Pathology (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Description
人工多能性幹細胞(iPSC)及び胚性幹細胞(ESC)等の幹細胞から心筋細胞を誘導し、心疾患のための再生医療に用いる試みがなされている。
心房筋細胞と心室筋細胞とは異なる機能を有する。幹細胞から誘導される心筋細胞を含む細胞集団には、心房筋細胞および心室筋細胞を含む複数種の心筋細胞が含まれ、未分化細胞等の非心筋細胞も含まれ得る。このため、幹細胞から心筋細胞を含む細胞集団を誘導し再生医療に適用するに際しては、治療の目的に応じて心房筋細胞または心室筋細胞のどちらか一方を細胞集団中において富化することが望ましい。
また、非特許文献2には、iPSCから誘導した心筋細胞を、CD235aおよびRALDH2をマーカーとして用いて、心室筋細胞と心房筋細胞とに分離する技術が記載されている。
[1] 幹細胞から誘導された、心筋細胞を含む細胞集団において、心房筋細胞または心室筋細胞を富化する方法であって、
前記細胞集団から、CD151の発現量を指標にして、心房筋細胞または心室筋細胞を回収する工程を含む、方法。
[2] 心房筋細胞を富化する、[1]の方法であって、
前記細胞集団からCD151低発現細胞を回収する工程を含む、方法。
[3] 心室筋細胞を富化する、[1]の方法であって、
前記細胞集団からCD151高発現細胞を回収する工程を含む、方法。
[4] 前記幹細胞が、人工多能性幹細胞である、[1]-[3]のいずれか1つに記載の方法。
[6] [2]の方法によって得られた、心房筋細胞が富化された細胞集団。
[7] [3]の方法によって得られた、心室筋細胞が富化された細胞集団。
[8] [5]-[7]のいずれか1つに記載の細胞集団を含む、医薬。
(A)前記幹細胞から心筋細胞を含む細胞集団を誘導する工程、および
(B)前記細胞集団から、CD151の発現量を指標にして、心房筋細胞または心室筋細胞を回収する工程、
を含む製造方法。
[10] 心房筋細胞を製造する、[9]の方法であって、
(A)心房筋細胞分化条件下で前記幹細胞から心筋細胞を含む細胞集団を誘導する工程、および
(B)前記細胞集団からCD151低発現細胞を回収する工程を含む、製造方法。
[11] 心室筋細胞を製造する、[9]の方法であって、
(A)心室筋細胞分化条件下で前記幹細胞から心筋細胞を含む細胞集団を誘導する工程、および
(B)前記細胞集団からCD151高発現細胞を回収する工程を含む、製造方法。
[12] 前記幹細胞が、人工多能性幹細胞である、[9]-[11]のいずれか1つに記載の方法。
[14] [10]の製造方法によって得られた、心房筋細胞。
[15] [11]の製造方法によって得られた、心室筋細胞。
[16] [9]-[11]のいずれか1つに記載の製造方法によって得られた、心房筋細胞または心室筋細胞を含む、医薬。
CD151検出プローブを含む、試薬。
[18] CD151検出プローブが、抗CD151抗体である、[17]の試薬。
[19] 幹細胞から誘導された、心筋細胞を含む細胞集団において、心房筋細胞または心室筋細胞を富化するための、CD151検出プローブの使用。
[20] 幹細胞から誘導された、心筋細胞を含む細胞集団において、心房筋細胞または心室筋細胞を富化するためのマーカーとしての、CD151の使用。
本発明において、「細胞集団(cell population)」とは、異なる種類の2以上の細胞の集合を意味する。「細胞亜集団(cell subpopulation)」は、細胞集団を構成する、同一または異なる細胞の集合であって、共通する性状を少なくとも1つ有する細胞の一群を意味する。
本発明においては、CD151は、幹細胞から誘導された、心筋細胞を含む細胞集団において、心房筋細胞または心室筋細胞を富化するためのマーカーとして使用される。
マーカータンパク質の検出は、当該マーカータンパク質に特異的な抗体を用いた免疫学的アッセイ、例えば、ELISA、免疫染色、フローサイトメトリーなどを利用して行うことができる。マーカータンパク質に特異的な抗体としては、マーカータンパク質における特定のアミノ酸配列またはマーカータンパク質に結合した特定の糖鎖等に結合する抗体を用いることができる。また、細胞内に発現し、細胞表面には現れないマーカータンパク質(例えば転写因子またはそのサブユニットなど)の場合は、当該マーカータンパク質とともにレポータータンパク質を発現させ、当該レポータータンパク質を検出することによって対象とするマーカータンパク質を検出できる。この方法は、適当な細胞表面マーカーが認められない場合に好ましく用いられ得る。マーカー遺伝子の検出は、当該分野で公知の核酸増幅方法および/または核酸検出方法、例えば、RT-PCR、マイクロアレイ、バイオチップおよびRNAseq等を利用して行うことができる。
「陽性(positive)」または「発現する」とは、タンパク質またはmRNAが当該分野で公知の手法による検出可能量で発現していることを意味する。タンパク質の検出は、抗体を用いた免疫学的アッセイ、例えば、ELISA、免疫染色、フローサイトメトリーを利用して行うことができる。また、細胞内に発現し、細胞表面には現れないタンパク質(例えば転写因子またはそのサブユニットなど)の場合は、当該タンパク質とともにレポータータンパク質を発現させ、当該レポータータンパク質を検出することによって対象とするタンパク質を検出できる。mRNAの検出は、例えば、RT-PCR、マイクロアレイ、バイオチップおよびRNAseq等の核酸増幅方法および/または核酸検出方法を利用して行うことができる。
「陰性(negative)」または「発現しない」とは、タンパク質または遺伝子の発現量が、上記のような公知手法の全てあるいはいずれかによる検出下限値未満であることを意味する。タンパク質または遺伝子の発現の検出下限値は、各手法により異なり得る。
「多能性(multipotency)」とは、複数の限定的な数の系統の細胞へと分化できる能力を意味する。例えば、間葉系幹細胞、造血幹細胞、神経幹細胞はmultipotentだが、pluripotentではない。
「維持培養(Sustain)」とは、所望の細胞集団をそれらの数を維持しながら培養することを意味する。細胞数の維持は、細胞が増殖することなく生存することにより達せられるものであっても、細胞の増殖による増数と死滅による減数とが拮抗することによって達せされるものであってもよい。細胞数の維持は、細胞の数が完全に同一に維持される必要はなく、本発明の目的に照らして細胞の数が実質的に同一に維持されればよい。
「拡大培養(Expand)」とは、所望の細胞集団を増殖させ、細胞数を増加させることを目的として培養することを意味する。細胞数の増加は、細胞の増殖による増数が死滅による減数を超えることによって達成されるものであればよく、細胞集団の全ての細胞が増殖することを要さない。細胞数の増加は、拡大培養の開始前に比して1.1倍、1.2倍、1.5倍、2倍、3倍、4倍、5倍、6倍、7倍、8倍、9倍、10倍、15倍、20倍、30倍、40倍、50倍、100倍、300倍、500倍、1000倍、3000倍、5000倍、10000倍、100000倍、1000000倍以上でありうる。
以下、本発明を実施するための好適な形態について説明する。なお、以下に説明する実施形態は、本発明の代表的な実施形態の一例を示したものであり、これにより本発明の範囲が狭く解釈されることはない。
本発明に係る心房筋細胞または心室筋細胞の富化方法は以下の工程を含む。
(1)心筋細胞を含む細胞集団から、CD151の発現量を指標にして、心房筋細胞または心室筋細胞を回収する工程。
(1-1)心筋細胞を含む細胞集団からCD151低発現細胞を回収する工程。
幹細胞から誘導された、心筋細胞を含む細胞集団において、CD151高発現によって特定される細胞亜集団には、CD151低発現によって特定される細胞亜集団に比して、より高い比率で心室筋細胞が含まれる。したがって、幹細胞から誘導された、心筋細胞を含む細胞集団からCD151高発現によって特定される細胞亜集団を除去すること、あるいは心筋細胞を含む細胞集団からCD151低発現によって特定される細胞亜集団を回収することで、細胞集団において心房筋細胞を富化することができる。
(1-2)心筋細胞を含む細胞集団からCD151高発現細胞を回収する工程。
幹細胞から誘導された、心筋細胞を含む細胞集団において、CD151高発現によって特定される細胞亜集団には、CD151低発現によって特定される細胞亜集団に比して、より高い比率で心室筋細胞が含まれる。したがって、幹細胞から誘導された、心筋細胞を含む細胞集団からCD151低発現によって特定される細胞亜集団を除去すること、あるいは心筋細胞を含む細胞集団からCD151高発現によって特定される細胞亜集団を回収することで、細胞集団において心室筋細胞を富化することができる。
細胞におけるCD151の発現レベルは、CD151に結合性を有するCD151検出プローブ(以下、単に「プローブ」とも称する)を用いて決定することができる。
プローブは、例えば、抗体および核酸(アプタマーなど)等であってよく、抗体であることが好ましい。
プローブは、光学的、電気的あるいは磁気的に検出可能な標識がなされていることが好ましい。この場合、細胞とプローブとを接触させ、CD151に結合したプローブの標識からの信号を光学的、電気的あるいは磁気的に検出することで、その信号強度に基づいて細胞におけるCD151の発現レベルを決定できる。
また、例えばプローブが抗体である場合には、該抗体に結合する標識2次抗体を用いて細胞におけるCD151の発現レベルを決定することもできる。
本発明は、上記プローブを含む、幹細胞から誘導された、心筋細胞を含む細胞集団において心房筋細胞または心室筋細胞を富化するための試薬をも提供する。
また、細胞におけるCD151の発現レベルは、幹細胞における発現レベルを基準値として設定し、該基準値以上の発現レベルを示す細胞を高発現、該基準値未満の発現レベルを示す細胞を低発現と決定することもできる。この場合の基準値としては、例えば幹細胞における発現レベルの最大値、平均値、中央値または最頻値であってよく、好ましくは最大値である。基準値は、目的とする細胞富化率に応じて適宜設定され得るものであり、例えば、幹細胞における発現レベルの最大値、平均値、中央値または最頻値(好ましくは最大値)よりも1%、2%、3%、4%、5%、10%、15%、20%、30%、40%、50%、60%、70%、80%、90%、100%あるいはそれ以上大きいまたは小さい値も設定し得る。
あるいは、細胞におけるCD151の発現レベルは、プローブと接触していない細胞(陰性コントロール)について、プローブと接触させた細胞と同様にして検出された信号強度を基準値として設定し、該基準値以上の信号強度を示す細胞を高発現、該基準値未満の信号強度を示す細胞を低発現と決定することもできる。基準値は、目的とする細胞富化率に応じて適宜設定され得るものであり、例えば、陰性コントロールの発現レベルの最大値、平均値、中央値または最頻値(好ましくは最大値)よりも1%、2%、3%、4%、5%、10%、15%、20%、30%、40%、50%、60%、70%、80%、90%、100%あるいはそれ以上大きいまたは小さい値も設定し得る。
本発明は、上記富化方法によって得られた、心房筋細胞が富化された細胞集団および心室筋細胞が富化された細胞集団をも提供する。
(1)30%再分極時の活動電位持続時間(APD30)と90%再分極時の活動電位持続時間(APD90)の比(APD30/90)が0.3以上であり、かつ、波形立ち上がりの最大速度(dv/dtmax)が10以上である活動電位波形を示す細胞を心室筋細胞と定義する。一方、APD30/90が0.3未満であり、かつ、dv/dtmaxが10以上である活動電位波形を示す細胞は心房筋細胞と定義する。この場合、dv/dtmaxが10未満、かつ自発活動電位周期が1s以上の活動電位波形を示す細胞は心室筋細胞および心房筋細胞のどちらにも分類されない未成熟な心筋細胞と定義される(Cell Stem Cell, 2017, 21, 179-194)。
(2)50%再分極時の活動電位持続時間(APD50)またはAPD90の値が有意に長い活動電位波形を示す細胞を心室筋細胞、有意に短い活動電位波形を示す細胞を心房筋細胞と定義する(JCI Insight, 2018;3(12):e99941、Eur. Heart J. 2017, 38, 292-301)。
(3)20%再分極時の活動電位持続時間(APD20)またはAPD50またはAPD90の値が有意に長く、活動電位プラトー相の振幅(APAPlat)が有意に大きな活動電位波形を示す細胞を心室筋細胞、APD20またはAPD50またはAPD90の値が有意に短く、APAPlatが有意に小さな活動電位波形を示す細胞を心房筋細胞と定義する(Stem Cell Reports. 2017 Dec 12; 9(6): 1765-1779)。
(4)APD20と80%再分極時の活動電位持続時間(APD80)の比(APD20/80)の値が有意に大きな活動電位波形を示す細胞を心室筋細胞、有意に小さな活動電位波形を示す細胞を心房筋細胞と定義する(JCI Insight, 2018;3(12):e99941)。
(5)APD90とAPD50の比(APD90/50)の値が有意に小さな活動電位波形を示す細胞を心室筋細胞、有意に大きな活動電位波形を示す細胞を心房筋細胞と定義する(Eur. Heart J., 2017, 38, 292-301、Eur. Heart J., 2011, 32, 952-962)。
(6)APD90/50が1.4未満となる活動電位波形を示す細胞を心室筋細胞と定義し、APD90/50が1.7よりも大きな活動電位波形を示す細胞を心房筋細胞と定義する。この場合、APD90/50が1.4以上1.7以下となる活動電位波形を示す細胞はペースメーカー細胞と定義される(Eur. Heart J., 2011, 32, 952-962)。
(7)20mV以内の膜電位変化を伴うプラトー相が50ms以上であり、dv/dtmaxが50よりも大きく、活動電位振幅(APA)が85 mVよりも大きく、かつAPD90/50が2.3未満である活動電位波形を示す細胞を心室筋細胞と定義する。同活動電位波形に対して、プラトー相を欠く点でのみ異なる活動電位波形を示す細胞を心房筋細胞、プラトー相を欠くのに加えてAPD90/50が2.3を超える点で異なる活動電位波形を示す細胞をペースメーカー細胞と定義する
(PNAS, 2017, E8372-E8381)。
なお、心房筋細胞心および心室筋細胞を含む心筋細胞は、少なくとも心筋トロポニン(cTNT), αMHC(α myosin heavy chain、MYH6)およびβMHC(MYH7)からなる群から選択される少なくとも一つのマーカーを発現している細胞を意味する。cTNT遺伝子は、ヒトの場合NCBIのaccession番号NM_000364が例示され、マウスの場合、NM_001130176が例示される。αMHC遺伝子は、ヒトの場合NCBIのaccession番号NM_002471が例示され、マウスの場合、NM_001164171が例示される。βMHC遺伝子は、ヒトの場合NCBIのaccession番号NM_000257が例示され、マウスの場合、NM_080728が例示される。
マーカータンパク質の検出は、当該マーカータンパク質に特異的な抗体を用いた免疫学的アッセイ、例えば、ELISA、免疫染色、フローサイトメトリーなどを利用して行うことができる。マーカー遺伝子の検出は、当該分野で公知の核酸増幅方法および/または核酸検出方法、例えば、RT-PCR、マイクロアレイ、バイオチップ等を利用して行うことができる。
本発明に係る幹細胞からの心房筋細胞または心室筋細胞の製造方法は、以下の工程を含む。
(A)前記幹細胞から心筋細胞を含む細胞集団を誘導する工程。
(B)前記細胞集団から、CD151の発現量を指標にして、心房筋細胞または心室筋細胞を回収する工程。
本発明に係る製造方法において心房筋細胞を製造する場合、工程(A)(B)は具体的には以下の工程(A-1)(B-1)である。
(A-1)心房筋細胞分化条件下で前記幹細胞から心筋細胞を含む細胞集団を誘導する工程。
(B-1)前記細胞集団からCD151低発現細胞を回収する工程。
一方、本発明に係る製造方法において心室筋細胞を製造する場合、工程(A)(B)は具体的には以下の工程(A-2)(B-2)である。
(A-2)心室筋細胞分化条件下で前記幹細胞から心筋細胞を含む細胞集団を誘導する工程、
(B-2)前記細胞集団からCD151高発現細胞を回収する工程。
工程(A)(A-1)(A-2)では、幹細胞から心筋細胞を含む細胞集団を誘導する。
「幹細胞(stem cell)」としては、例えば、多能性幹細胞(pluripotent stem cell)が挙げられる。
本発明において使用可能な「多能性幹細胞(pluripotent stem cell)」とは、生体の種々の異なった形態や機能を持つ組織や細胞に分化でき、3胚葉(内胚葉、中胚葉、外胚葉)のどの系統の細胞にも分化し得る能力を有する幹細胞を指す。それには、特に限定されないが、例えば、胚性幹細胞(ESC)、核移植により得られるクローン胚由来の胚性幹細胞、精子幹細胞、胚性生殖細胞、人工多能性幹細胞(本明細書中、「iPSC」と称することもある)などが挙げられる。また、本発明において使用可能な「多能性幹細胞(multipotent stem cell)」とは、複数の限定的な数の系統の細胞へと分化できる能力を有する幹細胞を指す。本発明において使用可能な「多能性幹細胞(multipotent stem cell)」としては、例えば、歯髄幹細胞、口腔粘膜由来幹細胞、毛包幹細胞、培養線維芽細胞や骨髄幹細胞由来の体性幹細胞などが挙げられる。好ましい多能性幹細胞(pluripotent stemcell)は、ESCおよびiPSCである。
このほか、公開されているすべての論文(例えば、Shi Y., Ding S., et al., Cell Stem Cell, (2008) Vol3, Issue 5,568-574;、Kim JB., Scholer HR., et al., Nature, (2008) 454, 646-650;Huangfu D., Melton, DA., et al., Nature Biotechnology, (2008) 26, No 7, 795-797)、あるいは特許(例えば、特開2008-307007号、特開2008-283972号、US2008-2336610、US2009-047263、WO2007-069666、WO2008-118220、WO2008-124133、WO2008-151058、WO2009-006930、WO2009-006997、WO2009-007852)に記載されている当該分野で公知の人工多能性幹細胞のいずれも用いることができる。
人工多能性幹細胞株としては、NIH、理研、京都大学等が樹立した各種iPSC株が利用可能である。例えば、ヒトiPSC株であれば、理研のHiPS-RIKEN-1A株、HiPS-RIKEN-2A株、HiPS-RIKEN-12A株、Nips-B2株等、京都大学の253G1株、201B7株、409B2株、454E2株、606A1株、610B1株、648A1株、1231A3株、1390D4株および1390C1株等が挙げられ、1390D4株および1390C1株がより好ましい。あるいは、京都大学やCellular Dynamics International等から提供される臨床グレードの細胞株並びにそれらの細胞株を用いて作製された研究用および臨床用の細胞株等を用いてもよい。
心房筋細胞分化条件は、従来公知(例えばEMBO Mol Med (2015)7:394-410参照)の条件を適用できる。例えば、iPSCから作成した胚葉体を、BMP4、アクチビンAおよびbFGFを含む基礎培地で2日間培養後、VEGF、Wnt阻害剤、TGF-β阻害剤およびレチノイン酸を含む基礎培地で3日間培養する。さらに、VEGFを含む基礎培地で培養を行うことにより、心房筋細胞を含む細胞集団を得ることができる。
分化誘導期間は、特に限定はされないが、例えば7-40日であり、目的に応じて例えば120日、90日、60日、30日、28日、21日、14日あるいは7日であってよい。
心室筋細胞分化条件は、従来公知(例えばCell Stem Cell. (2011) 8(2):228-40参照)の条件を適用できる。例えば、iPSCから作成した胚葉体を、BMP4、アクチビンAおよびbFGFを含む基礎培地で2日間培養後、VEGF、Wnt阻害剤、BMP4阻害剤およびTGF-β阻害剤を含む基礎培地で3日間培養する。さらに、VEGFを含む基礎培地で培養を行うことにより、心室筋細胞を含む細胞集団を得ることができる。
分化誘導期間は、特に限定はされないが、例えば7-40日であり、目的に応じて例えば120日、90日、60日、30日、28日、21日、14日あるいは7日であってよい。
CDM培地としては、特に限定されないが、例えば、Iscove's modified Dulbecco's medium(GEヘルスケア社製)から調製される培地が使用され得る。
基礎培地には、Ham's F-12 nutrient mixture、ヒト血清アルブミン等のアルブミン、polyvinylalcohol (PVA)、Deionized BSA、リノール酸、リノレン酸、コレステロール、インスリン、アポトランスフェリン、セレン、エタノールアミン、モノチオグリセロール、Protein-free hybridoma mixture II (PFHMII)、アスコルビン酸、L-alanyl-L-glutamineおよび/又は抗生物質等の通常の細胞培養に用いられる物質が添加され得る。
BMP4阻害剤には、例えばDorsomorphin(6-[4-(2-ピペリジン-1-イルエトキシ)フェニル]-3-ピリジン-4-イルピラゾロ[1,5-A]ピリミジン)、Indirubin-3'-oxime、Phenformin HCl、GSK621、WZ4003、HTH-01-015等を用いることができる。これらは、2以上を組み合わせて用いてもよい。
TGF-β阻害剤には、SB431542(4-[4-(1,3-benzodioxol-5-yl)-5-(2-pyridinyl)-1H-imidazol-2-yl]-benzamide)、A83-01(4-[4-(1,3-benzodioxol-5-yl)-5-(2-pyridinyl)-1H-imidazol-2-yl]-benzamide)、LDN193189(4-[6-[4-(1-Piperazinyl)phenyl]pyrazolo[1,5-a]pyrimidin-3-yl]-quinoline)、GW788388(4-[4-[3-(2-Pyridinyl)-1H-pyrazol-4-yl]-2-pyridinyl]-N-(tetrahydro-2H-pyran-4-yl)-benzamide)、SM16(4-[4-(1,3-Benzodioxol-5-yl)-5-(6-methyl-2-pyridinyl)-1H-imidazol-2-yl]-bicyclo[2.2.2]octane-1-carboxamide)、IN-1130(3-[[5-(6-Methyl-2-pyridinyl)-4-(6-quinoxalinyl)-1H-imidazol-2-yl]methyl]-benzamide)、GW6604(2-Phenyl-4-[3-(pyridin-2-yl)-1H-pyrazol-4-yl]pyridine)およびSB505124(2-[4-(1,3-Benzodioxol-5-yl)-2-(1,1-dimethylethyl)-1H-imidazol-5-yl]-6-methyl-pyridine)等が挙げられる。これらは、2以上を組み合わせて用いてもよい。
工程(B)(B-1)(B-2)では、得られた細胞集団から、CD151の発現量を指標にして、心房筋細胞または心室筋細胞を回収する。
本発明は、上記製造方法によって得られた、心房筋細胞および心室筋細胞が富化された細胞集団をも提供する。
本発明に係る細胞集団ならびに心房筋細胞および心室筋細胞は、これを含む心疾患治療用の細胞医薬、および該細胞医薬の投与による心疾患の治療方法に適用され得る。また、本発明は、前記細胞医薬の製造のための前記細胞集団ならびに心房筋細胞および心室筋細胞の使用、および心疾患の治療に用いるための前記細胞集団ならびに心房筋細胞および心室筋細胞をも提供する。
細胞医薬は、心筋梗塞、心不全、虚血性心疾患、心筋症、心筋炎、肥大型心筋症、拡張相肥大型心筋症、拡張型心筋症等の心疾患の再生医療に用いられ得る。
治療有効量とは、細胞を患者に投与した場合に、投与していない対照と比較して上記疾患に対して治療効果を得ることができる細胞の量である。具体的な治療有効量としては投与形態、投与方法、使用目的および患者の年齢、体重、症状等によって適宜設定され得る。ヒト(例えば成人)の1回の治療あたりの有効量は、例えば200,000~1,000,000個/kg体重である。
本発明は、本工程により得られる細胞集団ならびに/または心房筋細胞および/もしくは心室筋細胞を含む凍結ストックをも提供する。
凍結ストックは、得られた細胞集団ならびに/または心房筋細胞および/もしくは心室筋細胞を遠心分離により培地から分離し、凍結保存液中に懸濁して凍結することにより製造できる。凍結保存液には、従来細胞の凍結保存に用いられている試薬を用いればよい。例えば、Cryostem Freezing Medium(商品名)およびCELLBANKER(登録商標)などが市販されている。
凍結ストックは、例えば、心房筋細胞および心室筋細胞を構成要素とする組織モデル(人工心臓)の作製のために利用され得る。
心房筋細胞分化条件または心室筋細胞分化条件にて、iPSCから心筋細胞を含む細胞集団を誘導した。
iPSCには、レポータータンパク質としてTNNI1の遺伝子座にEmGFPを、TNNI3の遺伝子座にmCherryを挿入したダブルノックインヒトiPS細胞株(1390D4株)を用いた。
iPSCを低接着性の6ウェルプレートに播種し(2×106cells/1.5ml/well)、37℃、5%酸素条件下にて静置培養して、胚様体を形成させた(0日目)。培地には、L-グルタミン1%、トランスフェリン150μg/mL、アスコルビン酸50μg/mL、モノチオグリセロール4×10-4M、Rock阻害剤(Y-27632)10μM、BMP4 2ng/mLおよびMatrigel 0.5%を添加したStemPro-34 SFM (ThermoFisher)を用いた。
翌日(1日目)、細胞を播種した各ウェルに心房筋細胞誘導培地1を1.5ml/well添加し、37℃、5%酸素条件にてさらに2日間培養した。心房筋細胞誘導培地1には、L-グルタミン1%、トランスフェリン150μg/mL、アスコルビン酸50μg/mL、モノチオグリセロール4×10-4M、BMP4 4ng/ml、アクチビンA 8ng/ml、bFGF 10ng/mlを添加したStemPro-34 SFMを用いた。
続いて(3日目)、培地を心房筋細胞誘導培地2に交換し、37℃、5%酸素条件下で、3日間培養した。心房筋細胞誘導培地2には、L-グルタミン1%、トランスフェリン150μg/mL、アスコルビン酸50μg/mL、モノチオグリセロール4×10-4M、VEGF 10ng/mL、Wnt阻害剤(IWP-3)1μM、TGF-β阻害剤(SB431542)5.4 μMおよびレチノイン酸1μMを添加したStemPro-34 SFMを用いた。
翌日(1日目)、細胞播種した各ウェルに心室筋細胞誘導培地1を1.5ml/well添加し、37℃、5%酸素条件にてさらに2日間培養した。心室筋細胞誘導培地1には、L-グルタミン1%、トランスフェリン150μg/mL、アスコルビン酸50μg/mL、モノチオグリセロール4×10-4M、BMP4 18ng/ml、アクチビンA 12ng/ml、bFGF 10ng/mlを添加したStemPro-34 SFMを用いた。
続いて(3日目)、培地を心室筋細胞誘導培地2に交換し、37℃、5%酸素条件下で、3日間培養した。心室筋細胞誘導培地2には、L-グルタミン1%、トランスフェリン150μg/mL、アスコルビン酸50μg/mL、モノチオグリセロール4×10-4M、VEGF 10ng/mL、Wnt阻害剤(IWP-3)1μM、BMP4阻害剤(Dorsomorphin)0.6μMおよびTGF-β阻害剤(SB431542)5.4 μMを添加したStemPro-34 SFMを用いた。
心室筋細胞分化条件下または心房筋細胞分化条件下6日目に、心筋細胞誘導培地3に培地を交換し、37℃、5%酸素条件下で14日間培養し(20日目)、心室筋細胞または心房筋細胞を含む細胞集団を得た。心筋細胞誘導培地3には、L-グルタミン1%、トランスフェリン150μg/mL、アスコルビン酸50μg/mL、モノチオグリセロール4×10-4MおよびVEGF 5ng/mLを添加したStemPro-34 SFMを用いた。8、10、13、15、17日目には培地交換を行った。10日目の培地交換以降は通常酸素条件下で培養を行った。
培養20日目の、心室筋細胞または心房筋細胞を含む細胞集団を、単一の細胞(singlecell)に分散させ、細胞数を計測した。
細胞懸濁液に抗CD151抗体(BD)を添加し、4℃で30分間静置した。抗体を添加しないサンプルも調製し、ネガティブコントロールとした。
洗浄操作後、細胞懸濁液にAlexa(登録商標)647標識二次抗体を添加し、4℃で30分間静置した。
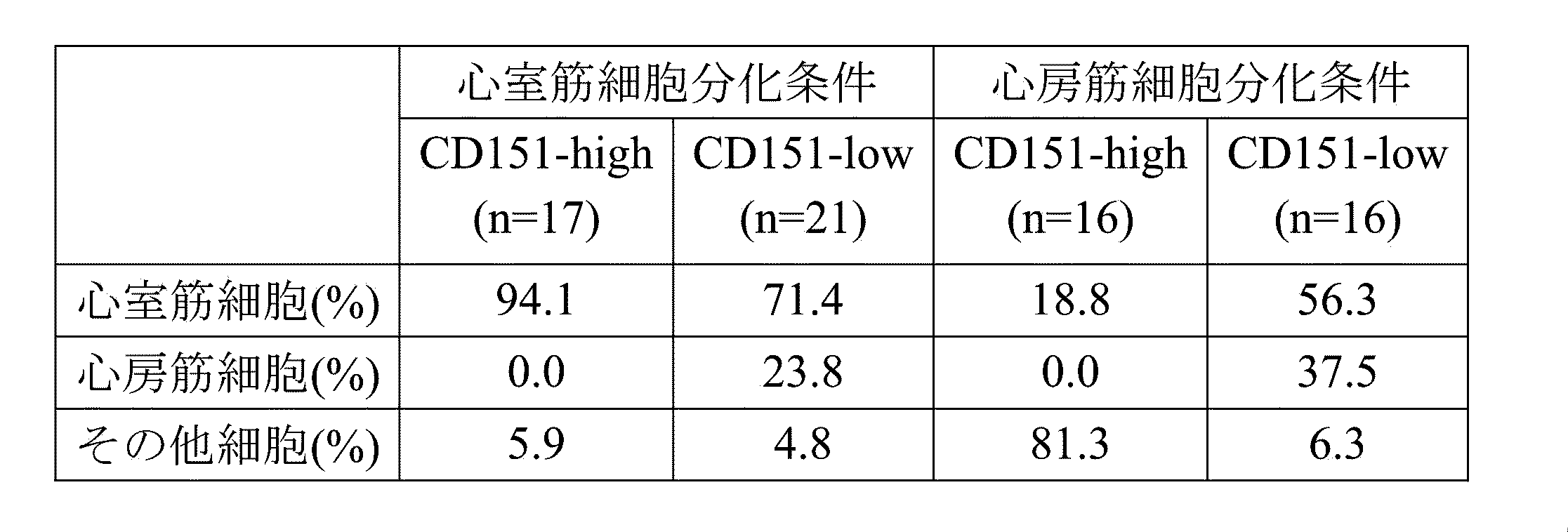
フローサイトメーター(BD FACSAria Fusionセルソーター)でEmGFP陽性細胞におけるCD151の発現を解析した。ネガティブコントロールの細胞の蛍光強度の最大値未満の蛍光強度を示す細胞亜集団を「CD151-low」、ネガティブコントロールより高い蛍光強度を示す細胞亜集団を「CD151-high」として、それぞれの細胞亜集団をソーティングした。フローサイトメーターのプロットを図2,3に、細胞亜集団の割合を表1に示す。
心室筋細胞分化条件および心房筋細胞分化条件でそれぞれ得られた「CD151-high」および「CD151-low」の細胞亜集団について、心房筋細胞および心室筋細胞の割合を電気生理学的手法を用いて決定した。
試験例2において心室筋細胞分化条件で得られた「CD151-high」および心房筋細胞分化条件で得られた「CD151-low」の細胞亜集団について、心房筋細胞マーカーおよび心室筋細胞マーカーの発現を解析した。
試験例2において心室筋細胞分化条件で得られた「CD151-high」および心房筋細胞分化条件で得られた「CD151-low」の細胞亜集団について、心房特異的チャネルの阻害剤である4-アミノピリジンおよび活性化剤であるカルバコールに対する応答を解析した。
4‐アミノピリジンの添加により、心房筋分化条件で得られた「CD151-low」の細胞亜集団では活動電位持続時間(APD)の延長が確認された。一方、心室筋分化条件で得られた「CD151-high」の細胞亜集団ではAPDの延長はみられなかった(図5(A)参照)。
また、カルバコールの添加により、心房筋分化条件で得られた「CD151-low」の細胞亜集団ではAPDの短縮が確認された。一方、心室筋分化条件で得られた「CD151-high」の細胞亜集団ではAPDの変化はみられなかった(図5(B)参照)。
以上の薬剤応答より、心房筋分化条件で得られた「CD151-low」の細胞亜集団は心房筋細胞であり、心室筋分化条件で得られた「CD151-high」の細胞亜集団は心室筋細胞であることが確認された。
Claims (5)
- 幹細胞から誘導された、心筋細胞を含む細胞集団において、心房筋細胞または心室筋細胞を富化する方法であって、
前記細胞集団から、CD151の発現量を指標にして、心房筋細胞または心室筋細胞を回収する工程を含む、方法。 - 前記幹細胞が、人工多能性幹細胞である、請求項1記載の方法。
- 幹細胞から心房筋細胞または心室筋細胞を製造する方法であって、
(A)前記幹細胞から心筋細胞を含む細胞集団を誘導する工程、および
(B)前記細胞集団から、CD151の発現量を指標にして、心房筋細胞または心室筋細胞を回収する工程、
を含む製造方法。 - 幹細胞から誘導された、心筋細胞を含む細胞集団において、心房筋細胞または心室筋細胞を富化するための試薬であって、
CD151検出プローブを含む、試薬。 - 幹細胞から誘導された、心筋細胞を含む細胞集団において、心房筋細胞または心室筋細胞を富化するための、CD151検出プローブの使用。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2019150593 | 2019-08-20 | ||
| JP2019150593 | 2019-08-20 | ||
| JP2020059409 | 2020-03-30 | ||
| JP2020059409 | 2020-03-30 | ||
| PCT/JP2020/031194 WO2021033699A1 (ja) | 2019-08-20 | 2020-08-19 | 心筋細胞の富化方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2021033699A1 JPWO2021033699A1 (ja) | 2021-02-25 |
| JP7541748B2 true JP7541748B2 (ja) | 2024-08-29 |
Family
ID=74661148
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021540957A Active JP7541748B2 (ja) | 2019-08-20 | 2020-08-19 | 心筋細胞の富化方法 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US20220298482A1 (ja) |
| EP (1) | EP4019549A4 (ja) |
| JP (1) | JP7541748B2 (ja) |
| CN (1) | CN114269900A (ja) |
| AU (1) | AU2020332643A1 (ja) |
| CA (1) | CA3151819A1 (ja) |
| IL (1) | IL290657A (ja) |
| WO (1) | WO2021033699A1 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2024029617A1 (ja) * | 2022-08-05 | 2024-02-08 | 国立大学法人京都大学 | 心筋の製造方法 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2005100548A1 (ja) | 2004-03-30 | 2005-10-27 | Kyoto University | 精巣細胞由来多能性幹細胞の製造方法 |
| JP2013531497A (ja) | 2010-06-13 | 2013-08-08 | インスティチュート・オブ・バイオフィジックス,チャイニーズ・アカデミー・オブ・サイエンシズ | 幹細胞から心筋細胞を調製するための方法および組成物ならびにその使用 |
| JP2015527886A (ja) | 2012-07-23 | 2015-09-24 | 中国科学院生物物理研究所 | 多能性幹細胞の心室心筋細胞へのインビトロでの分化を誘導するための方法 |
| JP2016518853A (ja) | 2013-05-17 | 2016-06-30 | ザ リサーチ ファウンデイション フォー ザ ステイト ユニバーシティー オブ ニューヨーク | ヒト誘導多能性幹細胞から生成された心筋細胞における内向き整流の電子的発現 |
Family Cites Families (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| PL1610642T3 (pl) | 2004-04-10 | 2007-01-31 | Henkel Kgaa | Wałek do włosów |
| US8048999B2 (en) | 2005-12-13 | 2011-11-01 | Kyoto University | Nuclear reprogramming factor |
| US8278104B2 (en) | 2005-12-13 | 2012-10-02 | Kyoto University | Induced pluripotent stem cells produced with Oct3/4, Klf4 and Sox2 |
| US7661738B2 (en) | 2006-11-28 | 2010-02-16 | Veritainer Corporation | Radiation detection unit for mounting a radiation sensor to a container crane |
| CA2684878A1 (en) * | 2007-01-09 | 2008-07-17 | Lead Pharma Cel Models Ip B.V. | Provision of new cardiomyocyte progenitor cells and cardiomyocytes derived therefrom |
| JP2010523117A (ja) | 2007-04-07 | 2010-07-15 | ホワイトヘッド・インスティテュート・フォー・バイオメディカル・リサーチ | 体細胞の再プログラミング |
| JP2010528622A (ja) | 2007-05-30 | 2010-08-26 | ザ ジェネラル ホスピタル コーポレイション | 体細胞から多能性細胞を生成する方法 |
| JP2008307007A (ja) | 2007-06-15 | 2008-12-25 | Bayer Schering Pharma Ag | 出生後のヒト組織由来未分化幹細胞から誘導したヒト多能性幹細胞 |
| CN101748096B (zh) * | 2008-12-17 | 2013-03-13 | 北京汉氏联合生物技术有限公司 | 亚全能干细胞、其制备方法及其用途 |
| US10913929B2 (en) * | 2009-10-13 | 2021-02-09 | Stemcell Technologies Inc. | Method of differentiating stem cells |
| JP7089484B2 (ja) * | 2016-06-01 | 2022-06-22 | ミルテニイ ビオテック ベー.ファー. ウント コー.カーゲー | ヒト多能性幹細胞由来の心筋細胞および心筋細胞サブポピュレーションの生成、同定ならびに単離のための方法 |
| CN111133099B (zh) * | 2017-08-23 | 2023-12-01 | 普罗赛拉治疗公司 | 神经纤毛蛋白-1(nrp1)作为细胞表面标志物用于分离人心脏心室祖细胞的用途 |
| CN108410802A (zh) * | 2018-03-09 | 2018-08-17 | 云南洛宇生物科技有限公司 | 一种大鼠心房肌细胞培养方法 |
| WO2019189545A1 (ja) * | 2018-03-30 | 2019-10-03 | 国立大学法人京都大学 | 細胞の製造方法 |
-
2020
- 2020-08-19 CA CA3151819A patent/CA3151819A1/en active Pending
- 2020-08-19 US US17/636,561 patent/US20220298482A1/en active Pending
- 2020-08-19 CN CN202080057254.0A patent/CN114269900A/zh active Pending
- 2020-08-19 EP EP20853941.1A patent/EP4019549A4/en active Pending
- 2020-08-19 WO PCT/JP2020/031194 patent/WO2021033699A1/ja unknown
- 2020-08-19 AU AU2020332643A patent/AU2020332643A1/en active Pending
- 2020-08-19 JP JP2021540957A patent/JP7541748B2/ja active Active
-
2022
- 2022-02-16 IL IL290657A patent/IL290657A/en unknown
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2005100548A1 (ja) | 2004-03-30 | 2005-10-27 | Kyoto University | 精巣細胞由来多能性幹細胞の製造方法 |
| JP2013531497A (ja) | 2010-06-13 | 2013-08-08 | インスティチュート・オブ・バイオフィジックス,チャイニーズ・アカデミー・オブ・サイエンシズ | 幹細胞から心筋細胞を調製するための方法および組成物ならびにその使用 |
| JP2015527886A (ja) | 2012-07-23 | 2015-09-24 | 中国科学院生物物理研究所 | 多能性幹細胞の心室心筋細胞へのインビトロでの分化を誘導するための方法 |
| JP2016518853A (ja) | 2013-05-17 | 2016-06-30 | ザ リサーチ ファウンデイション フォー ザ ステイト ユニバーシティー オブ ニューヨーク | ヒト誘導多能性幹細胞から生成された心筋細胞における内向き整流の電子的発現 |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2021033699A1 (ja) | 2021-02-25 |
| EP4019549A4 (en) | 2023-08-16 |
| US20220298482A1 (en) | 2022-09-22 |
| EP4019549A1 (en) | 2022-06-29 |
| CN114269900A (zh) | 2022-04-01 |
| CA3151819A1 (en) | 2021-02-25 |
| IL290657A (en) | 2022-04-01 |
| JPWO2021033699A1 (ja) | 2021-02-25 |
| AU2020332643A1 (en) | 2022-03-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7161775B2 (ja) | 中間中胚葉細胞から腎前駆細胞への分化誘導方法、および多能性幹細胞から腎前駆細胞への分化誘導方法 | |
| JP6461787B2 (ja) | 肺胞上皮前駆細胞の誘導方法 | |
| CN106459922B (zh) | Cd82阳性心肌前体细胞 | |
| WO2016143803A1 (ja) | 肺胞上皮細胞の分化誘導法 | |
| JP6830893B2 (ja) | 腎前駆細胞を製造する方法 | |
| US20180094245A1 (en) | Methods for cardiac fibroblast differentiation of human pluripotent stem cells | |
| JPWO2007010858A1 (ja) | 骨格筋組織由来の単一細胞よりクローン化した多能性幹細胞 | |
| JPWO2017188458A1 (ja) | 骨格筋前駆細胞及び骨格筋細胞の製造方法 | |
| CN105339489A (zh) | 多能干细胞向多能肾前体分化的方法 | |
| WO2013063305A2 (en) | Directed cardiomyocyte differentiation of stem cells | |
| JP7330466B2 (ja) | 細胞の培養方法 | |
| US20210332329A1 (en) | Novel renal progenitor cell marker and method for concentrating renal progenitor cells using same | |
| JP6780197B2 (ja) | 新規成熟心筋細胞マーカー | |
| JP7541748B2 (ja) | 心筋細胞の富化方法 | |
| JP2017108705A (ja) | 心筋細胞の製造方法 | |
| KR20120035801A (ko) | 인간 배아줄기세포 유래 심근세포의 배양 및 정제 방법 | |
| WO2020250913A1 (ja) | 腎間質細胞の製造方法 | |
| WO2019070021A1 (ja) | iPS細胞由来の遺伝的多様性を有するT細胞集団の製造方法 | |
| US20170240861A1 (en) | Human pluripotent stem cell derived endocardial endothelium | |
| WO2024029617A1 (ja) | 心筋の製造方法 | |
| WO2020090903A1 (ja) | 中内胚葉系への分化抵抗性が解除された多能性幹細胞の作製方法 | |
| WO2023286772A1 (ja) | 心筋細胞の製造方法 | |
| JP7508045B2 (ja) | 細胞の検出方法 | |
| WO2024079149A1 (en) | Methods for producing sinoatrial node subpopulations |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20230526 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240423 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240614 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20240716 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20240809 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7541748 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |