JP7167299B2 - 硫黄-炭素複合体、この製造方法、これを含むリチウム二次電池用正極及びリチウム二次電池 - Google Patents
硫黄-炭素複合体、この製造方法、これを含むリチウム二次電池用正極及びリチウム二次電池 Download PDFInfo
- Publication number
- JP7167299B2 JP7167299B2 JP2021502687A JP2021502687A JP7167299B2 JP 7167299 B2 JP7167299 B2 JP 7167299B2 JP 2021502687 A JP2021502687 A JP 2021502687A JP 2021502687 A JP2021502687 A JP 2021502687A JP 7167299 B2 JP7167299 B2 JP 7167299B2
- Authority
- JP
- Japan
- Prior art keywords
- sulfur
- carbon composite
- carbon
- carbon material
- positive electrode
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- GJEAMHAFPYZYDE-UHFFFAOYSA-N [C].[S] Chemical compound [C].[S] GJEAMHAFPYZYDE-UHFFFAOYSA-N 0.000 title claims description 106
- 239000002131 composite material Substances 0.000 title claims description 87
- 229910052744 lithium Inorganic materials 0.000 title claims description 35
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 title claims description 34
- 238000004519 manufacturing process Methods 0.000 title claims description 15
- 239000003575 carbonaceous material Substances 0.000 claims description 113
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 claims description 94
- 125000000524 functional group Chemical group 0.000 claims description 89
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 claims description 81
- 239000011593 sulfur Substances 0.000 claims description 75
- 229910052717 sulfur Inorganic materials 0.000 claims description 75
- 239000002041 carbon nanotube Substances 0.000 claims description 51
- 229910021393 carbon nanotube Inorganic materials 0.000 claims description 51
- 238000010438 heat treatment Methods 0.000 claims description 33
- 239000011148 porous material Substances 0.000 claims description 25
- JDZCKJOXGCMJGS-UHFFFAOYSA-N [Li].[S] Chemical compound [Li].[S] JDZCKJOXGCMJGS-UHFFFAOYSA-N 0.000 claims description 18
- 239000003792 electrolyte Substances 0.000 claims description 13
- 238000002411 thermogravimetry Methods 0.000 claims description 13
- 238000000034 method Methods 0.000 claims description 12
- 230000004580 weight loss Effects 0.000 claims description 11
- 239000002253 acid Substances 0.000 claims description 9
- 238000003841 Raman measurement Methods 0.000 claims description 8
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 claims description 4
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims description 4
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 4
- 239000011259 mixed solution Substances 0.000 claims description 3
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 claims description 2
- 229910017604 nitric acid Inorganic materials 0.000 claims description 2
- 230000000052 comparative effect Effects 0.000 description 31
- -1 etc. Inorganic materials 0.000 description 20
- 229910002804 graphite Inorganic materials 0.000 description 16
- 239000010439 graphite Substances 0.000 description 16
- 239000007774 positive electrode material Substances 0.000 description 16
- 239000011230 binding agent Substances 0.000 description 15
- 239000004020 conductor Substances 0.000 description 11
- 239000000203 mixture Substances 0.000 description 10
- 238000006243 chemical reaction Methods 0.000 description 9
- 239000002002 slurry Substances 0.000 description 9
- HBBGRARXTFLTSG-UHFFFAOYSA-N Lithium ion Chemical compound [Li+] HBBGRARXTFLTSG-UHFFFAOYSA-N 0.000 description 8
- 229910052799 carbon Inorganic materials 0.000 description 8
- 229910001416 lithium ion Inorganic materials 0.000 description 8
- 239000002245 particle Substances 0.000 description 8
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 7
- 239000011248 coating agent Substances 0.000 description 7
- 238000000576 coating method Methods 0.000 description 7
- 238000005087 graphitization Methods 0.000 description 7
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 6
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 6
- 229910052782 aluminium Inorganic materials 0.000 description 6
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 6
- 229910003002 lithium salt Inorganic materials 0.000 description 6
- 159000000002 lithium salts Chemical class 0.000 description 6
- 239000000463 material Substances 0.000 description 6
- 239000012528 membrane Substances 0.000 description 6
- 238000000926 separation method Methods 0.000 description 6
- 229910001220 stainless steel Inorganic materials 0.000 description 6
- 239000010935 stainless steel Substances 0.000 description 6
- 239000006229 carbon black Substances 0.000 description 5
- 239000007773 negative electrode material Substances 0.000 description 5
- 239000007784 solid electrolyte Substances 0.000 description 5
- 239000002904 solvent Substances 0.000 description 5
- 239000000126 substance Substances 0.000 description 5
- 239000004698 Polyethylene Substances 0.000 description 4
- 239000010949 copper Substances 0.000 description 4
- 230000007423 decrease Effects 0.000 description 4
- 239000003960 organic solvent Substances 0.000 description 4
- 229920000573 polyethylene Polymers 0.000 description 4
- 230000008569 process Effects 0.000 description 4
- 230000009257 reactivity Effects 0.000 description 4
- 238000006722 reduction reaction Methods 0.000 description 4
- 238000009210 therapy by ultrasound Methods 0.000 description 4
- WNXJIVFYUVYPPR-UHFFFAOYSA-N 1,3-dioxolane Chemical compound C1COCO1 WNXJIVFYUVYPPR-UHFFFAOYSA-N 0.000 description 3
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 3
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- 239000002033 PVDF binder Substances 0.000 description 3
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 3
- 239000012300 argon atmosphere Substances 0.000 description 3
- 229910021383 artificial graphite Inorganic materials 0.000 description 3
- 230000008859 change Effects 0.000 description 3
- 238000013329 compounding Methods 0.000 description 3
- 229910052802 copper Inorganic materials 0.000 description 3
- 230000000694 effects Effects 0.000 description 3
- 238000011156 evaluation Methods 0.000 description 3
- 239000011888 foil Substances 0.000 description 3
- 229910052751 metal Inorganic materials 0.000 description 3
- 239000002184 metal Substances 0.000 description 3
- 238000002156 mixing Methods 0.000 description 3
- 229910021382 natural graphite Inorganic materials 0.000 description 3
- 229910052759 nickel Inorganic materials 0.000 description 3
- 238000007254 oxidation reaction Methods 0.000 description 3
- 229920000642 polymer Polymers 0.000 description 3
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 3
- YEJRWHAVMIAJKC-UHFFFAOYSA-N 4-Butyrolactone Chemical compound O=C1CCCO1 YEJRWHAVMIAJKC-UHFFFAOYSA-N 0.000 description 2
- SBLRHMKNNHXPHG-UHFFFAOYSA-N 4-fluoro-1,3-dioxolan-2-one Chemical compound FC1COC(=O)O1 SBLRHMKNNHXPHG-UHFFFAOYSA-N 0.000 description 2
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 2
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 2
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 description 2
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 2
- ZHNUHDYFZUAESO-UHFFFAOYSA-N Formamide Chemical compound NC=O ZHNUHDYFZUAESO-UHFFFAOYSA-N 0.000 description 2
- 229910000733 Li alloy Inorganic materials 0.000 description 2
- 229910019142 PO4 Inorganic materials 0.000 description 2
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 2
- 239000004743 Polypropylene Substances 0.000 description 2
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 2
- KAESVJOAVNADME-UHFFFAOYSA-N Pyrrole Chemical class C=1C=CNC=1 KAESVJOAVNADME-UHFFFAOYSA-N 0.000 description 2
- 229910004283 SiO 4 Inorganic materials 0.000 description 2
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 2
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 2
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 description 2
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 2
- MCMNRKCIXSYSNV-UHFFFAOYSA-N Zirconium dioxide Chemical compound O=[Zr]=O MCMNRKCIXSYSNV-UHFFFAOYSA-N 0.000 description 2
- 239000006230 acetylene black Substances 0.000 description 2
- 239000011149 active material Substances 0.000 description 2
- 229910003481 amorphous carbon Inorganic materials 0.000 description 2
- 239000011575 calcium Substances 0.000 description 2
- 239000006182 cathode active material Substances 0.000 description 2
- 239000006231 channel black Substances 0.000 description 2
- 150000001875 compounds Chemical class 0.000 description 2
- 238000009831 deintercalation Methods 0.000 description 2
- SBZXBUIDTXKZTM-UHFFFAOYSA-N diglyme Chemical compound COCCOCCOC SBZXBUIDTXKZTM-UHFFFAOYSA-N 0.000 description 2
- 229920001971 elastomer Polymers 0.000 description 2
- 238000003487 electrochemical reaction Methods 0.000 description 2
- FKRCODPIKNYEAC-UHFFFAOYSA-N ethyl propionate Chemical compound CCOC(=O)CC FKRCODPIKNYEAC-UHFFFAOYSA-N 0.000 description 2
- LYCAIKOWRPUZTN-UHFFFAOYSA-N ethylene glycol Natural products OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 2
- 230000001747 exhibiting effect Effects 0.000 description 2
- 239000006260 foam Substances 0.000 description 2
- 239000006232 furnace black Substances 0.000 description 2
- 229910021389 graphene Inorganic materials 0.000 description 2
- 229910003480 inorganic solid Inorganic materials 0.000 description 2
- 238000009830 intercalation Methods 0.000 description 2
- 239000006233 lamp black Substances 0.000 description 2
- 239000011244 liquid electrolyte Substances 0.000 description 2
- 239000001989 lithium alloy Substances 0.000 description 2
- AMXOYNBUYSYVKV-UHFFFAOYSA-M lithium bromide Chemical compound [Li+].[Br-] AMXOYNBUYSYVKV-UHFFFAOYSA-M 0.000 description 2
- KWGKDLIKAYFUFQ-UHFFFAOYSA-M lithium chloride Chemical compound [Li+].[Cl-] KWGKDLIKAYFUFQ-UHFFFAOYSA-M 0.000 description 2
- 238000011068 loading method Methods 0.000 description 2
- 239000011777 magnesium Substances 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- TZIHFWKZFHZASV-UHFFFAOYSA-N methyl formate Chemical compound COC=O TZIHFWKZFHZASV-UHFFFAOYSA-N 0.000 description 2
- 239000002048 multi walled nanotube Substances 0.000 description 2
- 239000011356 non-aqueous organic solvent Substances 0.000 description 2
- 239000004745 nonwoven fabric Substances 0.000 description 2
- 230000003647 oxidation Effects 0.000 description 2
- 239000010452 phosphate Substances 0.000 description 2
- 229920000728 polyester Polymers 0.000 description 2
- 229920000098 polyolefin Polymers 0.000 description 2
- 229920001155 polypropylene Polymers 0.000 description 2
- 229920001343 polytetrafluoroethylene Polymers 0.000 description 2
- 239000004810 polytetrafluoroethylene Substances 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 239000011347 resin Substances 0.000 description 2
- 229920005989 resin Polymers 0.000 description 2
- 239000005060 rubber Substances 0.000 description 2
- 238000007086 side reaction Methods 0.000 description 2
- 229910052710 silicon Inorganic materials 0.000 description 2
- 239000010703 silicon Substances 0.000 description 2
- 229910052709 silver Inorganic materials 0.000 description 2
- 239000004332 silver Substances 0.000 description 2
- 239000002109 single walled nanotube Substances 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 238000004528 spin coating Methods 0.000 description 2
- 229920003048 styrene butadiene rubber Polymers 0.000 description 2
- VZGDMQKNWNREIO-UHFFFAOYSA-N tetrachloromethane Chemical compound ClC(Cl)(Cl)Cl VZGDMQKNWNREIO-UHFFFAOYSA-N 0.000 description 2
- 239000006234 thermal black Substances 0.000 description 2
- 229910052719 titanium Inorganic materials 0.000 description 2
- 239000010936 titanium Substances 0.000 description 2
- QDZRBIRIPNZRSG-UHFFFAOYSA-N titanium nitrate Chemical compound [O-][N+](=O)O[Ti](O[N+]([O-])=O)(O[N+]([O-])=O)O[N+]([O-])=O QDZRBIRIPNZRSG-UHFFFAOYSA-N 0.000 description 2
- 125000001889 triflyl group Chemical group FC(F)(F)S(*)(=O)=O 0.000 description 2
- PYOKUURKVVELLB-UHFFFAOYSA-N trimethyl orthoformate Chemical compound COC(OC)OC PYOKUURKVVELLB-UHFFFAOYSA-N 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- MIZLGWKEZAPEFJ-UHFFFAOYSA-N 1,1,2-trifluoroethene Chemical compound FC=C(F)F MIZLGWKEZAPEFJ-UHFFFAOYSA-N 0.000 description 1
- LZDKZFUFMNSQCJ-UHFFFAOYSA-N 1,2-diethoxyethane Chemical compound CCOCCOCC LZDKZFUFMNSQCJ-UHFFFAOYSA-N 0.000 description 1
- XNWFRZJHXBZDAG-UHFFFAOYSA-N 2-METHOXYETHANOL Chemical class COCCO XNWFRZJHXBZDAG-UHFFFAOYSA-N 0.000 description 1
- ROGIWVXWXZRRMZ-UHFFFAOYSA-N 2-methylbuta-1,3-diene;styrene Chemical compound CC(=C)C=C.C=CC1=CC=CC=C1 ROGIWVXWXZRRMZ-UHFFFAOYSA-N 0.000 description 1
- JWUJQDFVADABEY-UHFFFAOYSA-N 2-methyltetrahydrofuran Chemical compound CC1CCCO1 JWUJQDFVADABEY-UHFFFAOYSA-N 0.000 description 1
- PPDFQRAASCRJAH-UHFFFAOYSA-N 2-methylthiolane 1,1-dioxide Chemical compound CC1CCCS1(=O)=O PPDFQRAASCRJAH-UHFFFAOYSA-N 0.000 description 1
- LECKFEZRJJNBNI-UHFFFAOYSA-N 4-fluoro-5-methyl-1,3-dioxolan-2-one Chemical compound CC1OC(=O)OC1F LECKFEZRJJNBNI-UHFFFAOYSA-N 0.000 description 1
- XMWRBQBLMFGWIX-UHFFFAOYSA-N C60 fullerene Chemical compound C12=C3C(C4=C56)=C7C8=C5C5=C9C%10=C6C6=C4C1=C1C4=C6C6=C%10C%10=C9C9=C%11C5=C8C5=C8C7=C3C3=C7C2=C1C1=C2C4=C6C4=C%10C6=C9C9=C%11C5=C5C8=C3C3=C7C1=C1C2=C4C6=C2C9=C5C3=C12 XMWRBQBLMFGWIX-UHFFFAOYSA-N 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 229920000049 Carbon (fiber) Polymers 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 1
- 229910000925 Cd alloy Inorganic materials 0.000 description 1
- PIICEJLVQHRZGT-UHFFFAOYSA-N Ethylenediamine Chemical compound NCCN PIICEJLVQHRZGT-UHFFFAOYSA-N 0.000 description 1
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 229910012722 Li3N-LiI-LiOH Inorganic materials 0.000 description 1
- 229910012716 Li3N-LiI—LiOH Inorganic materials 0.000 description 1
- 229910012734 Li3N—LiI—LiOH Inorganic materials 0.000 description 1
- 229910013043 Li3PO4-Li2S-SiS2 Inorganic materials 0.000 description 1
- 229910013035 Li3PO4-Li2S—SiS2 Inorganic materials 0.000 description 1
- 229910012810 Li3PO4—Li2S-SiS2 Inorganic materials 0.000 description 1
- 229910012797 Li3PO4—Li2S—SiS2 Inorganic materials 0.000 description 1
- 229910003253 LiB10Cl10 Inorganic materials 0.000 description 1
- 229910010941 LiFSI Inorganic materials 0.000 description 1
- 229910010857 LiI—LiOH Inorganic materials 0.000 description 1
- 229910001290 LiPF6 Inorganic materials 0.000 description 1
- 229910012573 LiSiO Inorganic materials 0.000 description 1
- 229910012346 LiSiO4-LiI-LiOH Inorganic materials 0.000 description 1
- 229910012345 LiSiO4-LiI—LiOH Inorganic materials 0.000 description 1
- 229910012348 LiSiO4—LiI—LiOH Inorganic materials 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- 229920000914 Metallic fiber Polymers 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 239000004642 Polyimide Substances 0.000 description 1
- 229920000265 Polyparaphenylene Polymers 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 1
- 238000001069 Raman spectroscopy Methods 0.000 description 1
- BLRPTPMANUNPDV-UHFFFAOYSA-N Silane Chemical compound [SiH4] BLRPTPMANUNPDV-UHFFFAOYSA-N 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- UCKMPCXJQFINFW-UHFFFAOYSA-N Sulphide Chemical compound [S-2] UCKMPCXJQFINFW-UHFFFAOYSA-N 0.000 description 1
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical compound OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 1
- BEKPOUATRPPTLV-UHFFFAOYSA-N [Li].BCl Chemical compound [Li].BCl BEKPOUATRPPTLV-UHFFFAOYSA-N 0.000 description 1
- KXKVLQRXCPHEJC-UHFFFAOYSA-N acetic acid trimethyl ester Natural products COC(C)=O KXKVLQRXCPHEJC-UHFFFAOYSA-N 0.000 description 1
- 238000013019 agitation Methods 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- 229910045601 alloy Inorganic materials 0.000 description 1
- 239000000956 alloy Substances 0.000 description 1
- VSCWAEJMTAWNJL-UHFFFAOYSA-K aluminium trichloride Chemical class Cl[Al](Cl)Cl VSCWAEJMTAWNJL-UHFFFAOYSA-K 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 238000000498 ball milling Methods 0.000 description 1
- 229910052788 barium Inorganic materials 0.000 description 1
- DSAJWYNOEDNPEQ-UHFFFAOYSA-N barium atom Chemical compound [Ba] DSAJWYNOEDNPEQ-UHFFFAOYSA-N 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 229910052790 beryllium Inorganic materials 0.000 description 1
- ATBAMAFKBVZNFJ-UHFFFAOYSA-N beryllium atom Chemical compound [Be] ATBAMAFKBVZNFJ-UHFFFAOYSA-N 0.000 description 1
- 229910052792 caesium Inorganic materials 0.000 description 1
- TVFDJXOCXUVLDH-UHFFFAOYSA-N caesium atom Chemical compound [Cs] TVFDJXOCXUVLDH-UHFFFAOYSA-N 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 150000001721 carbon Chemical class 0.000 description 1
- 229910002092 carbon dioxide Inorganic materials 0.000 description 1
- 239000001569 carbon dioxide Substances 0.000 description 1
- 239000004917 carbon fiber Substances 0.000 description 1
- 239000002717 carbon nanostructure Substances 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 239000000919 ceramic Substances 0.000 description 1
- 229910010293 ceramic material Inorganic materials 0.000 description 1
- 239000003610 charcoal Substances 0.000 description 1
- 239000011247 coating layer Substances 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 150000004292 cyclic ethers Chemical class 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 238000007607 die coating method Methods 0.000 description 1
- 150000004862 dioxolanes Chemical class 0.000 description 1
- 238000003618 dip coating Methods 0.000 description 1
- 238000007599 discharging Methods 0.000 description 1
- 238000010494 dissociation reaction Methods 0.000 description 1
- 230000005593 dissociations Effects 0.000 description 1
- 238000007606 doctor blade method Methods 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 239000007772 electrode material Substances 0.000 description 1
- 239000008151 electrolyte solution Substances 0.000 description 1
- 150000002170 ethers Chemical class 0.000 description 1
- JBTWLSYIZRCDFO-UHFFFAOYSA-N ethyl methyl carbonate Chemical compound CCOC(=O)OC JBTWLSYIZRCDFO-UHFFFAOYSA-N 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 229910052730 francium Inorganic materials 0.000 description 1
- KLMCZVJOEAUDNE-UHFFFAOYSA-N francium atom Chemical compound [Fr] KLMCZVJOEAUDNE-UHFFFAOYSA-N 0.000 description 1
- 229910003472 fullerene Inorganic materials 0.000 description 1
- BLBBMBKUUHYSMI-UHFFFAOYSA-N furan-2,3,4,5-tetrol Chemical compound OC=1OC(O)=C(O)C=1O BLBBMBKUUHYSMI-UHFFFAOYSA-N 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 239000003365 glass fiber Substances 0.000 description 1
- 230000005484 gravity Effects 0.000 description 1
- 238000007756 gravure coating Methods 0.000 description 1
- 150000004820 halides Chemical class 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 150000002367 halogens Chemical class 0.000 description 1
- 230000002209 hydrophobic effect Effects 0.000 description 1
- 239000001863 hydroxypropyl cellulose Substances 0.000 description 1
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 description 1
- YAMHXTCMCPHKLN-UHFFFAOYSA-N imidazolidin-2-one Chemical compound O=C1NCCN1 YAMHXTCMCPHKLN-UHFFFAOYSA-N 0.000 description 1
- 150000002461 imidazolidines Chemical class 0.000 description 1
- 238000005470 impregnation Methods 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 239000011810 insulating material Substances 0.000 description 1
- 239000012212 insulator Substances 0.000 description 1
- 229920003049 isoprene rubber Polymers 0.000 description 1
- 239000003273 ketjen black Substances 0.000 description 1
- 239000004816 latex Substances 0.000 description 1
- 229920000126 latex Polymers 0.000 description 1
- 239000010410 layer Substances 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 229910001547 lithium hexafluoroantimonate(V) Inorganic materials 0.000 description 1
- 229910001540 lithium hexafluoroarsenate(V) Inorganic materials 0.000 description 1
- HSZCZNFXUDYRKD-UHFFFAOYSA-M lithium iodide Inorganic materials [Li+].[I-] HSZCZNFXUDYRKD-UHFFFAOYSA-M 0.000 description 1
- MHCFAGZWMAWTNR-UHFFFAOYSA-M lithium perchlorate Chemical compound [Li+].[O-]Cl(=O)(=O)=O MHCFAGZWMAWTNR-UHFFFAOYSA-M 0.000 description 1
- 229910001486 lithium perchlorate Inorganic materials 0.000 description 1
- 229910001537 lithium tetrachloroaluminate Inorganic materials 0.000 description 1
- 229910001496 lithium tetrafluoroborate Inorganic materials 0.000 description 1
- HSFDLPWPRRSVSM-UHFFFAOYSA-M lithium;2,2,2-trifluoroacetate Chemical compound [Li+].[O-]C(=O)C(F)(F)F HSFDLPWPRRSVSM-UHFFFAOYSA-M 0.000 description 1
- VDVLPSWVDYJFRW-UHFFFAOYSA-N lithium;bis(fluorosulfonyl)azanide Chemical compound [Li+].FS(=O)(=O)[N-]S(F)(=O)=O VDVLPSWVDYJFRW-UHFFFAOYSA-N 0.000 description 1
- MCVFFRWZNYZUIJ-UHFFFAOYSA-M lithium;trifluoromethanesulfonate Chemical compound [Li+].[O-]S(=O)(=O)C(F)(F)F MCVFFRWZNYZUIJ-UHFFFAOYSA-M 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 230000014759 maintenance of location Effects 0.000 description 1
- 229910021645 metal ion Inorganic materials 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 150000004767 nitrides Chemical class 0.000 description 1
- 150000005181 nitrobenzenes Chemical class 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- LYGJENNIWJXYER-UHFFFAOYSA-N nitromethane Chemical compound C[N+]([O-])=O LYGJENNIWJXYER-UHFFFAOYSA-N 0.000 description 1
- 239000012811 non-conductive material Substances 0.000 description 1
- 239000011255 nonaqueous electrolyte Substances 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 229910052763 palladium Inorganic materials 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 229920001721 polyimide Polymers 0.000 description 1
- 229920001451 polypropylene glycol Polymers 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 239000005373 porous glass Substances 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- QQONPFPTGQHPMA-UHFFFAOYSA-N propylene Natural products CC=C QQONPFPTGQHPMA-UHFFFAOYSA-N 0.000 description 1
- RUOJZAUFBMNUDX-UHFFFAOYSA-N propylene carbonate Chemical class CC1COC(=O)O1 RUOJZAUFBMNUDX-UHFFFAOYSA-N 0.000 description 1
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 1
- 239000001008 quinone-imine dye Substances 0.000 description 1
- 229910052705 radium Inorganic materials 0.000 description 1
- HCWPIIXVSYCSAN-UHFFFAOYSA-N radium atom Chemical compound [Ra] HCWPIIXVSYCSAN-UHFFFAOYSA-N 0.000 description 1
- 239000004627 regenerated cellulose Substances 0.000 description 1
- 230000027756 respiratory electron transport chain Effects 0.000 description 1
- 238000007763 reverse roll coating Methods 0.000 description 1
- 229910052701 rubidium Inorganic materials 0.000 description 1
- IGLNJRXAVVLDKE-UHFFFAOYSA-N rubidium atom Chemical compound [Rb] IGLNJRXAVVLDKE-UHFFFAOYSA-N 0.000 description 1
- 229910000077 silane Inorganic materials 0.000 description 1
- 239000011856 silicon-based particle Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 238000001179 sorption measurement Methods 0.000 description 1
- 238000005507 spraying Methods 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 229910052712 strontium Inorganic materials 0.000 description 1
- CIOAGBVUUVVLOB-UHFFFAOYSA-N strontium atom Chemical compound [Sr] CIOAGBVUUVVLOB-UHFFFAOYSA-N 0.000 description 1
- 150000005846 sugar alcohols Polymers 0.000 description 1
- HXJUTPCZVOIRIF-UHFFFAOYSA-N sulfolane Chemical compound O=S1(=O)CCCC1 HXJUTPCZVOIRIF-UHFFFAOYSA-N 0.000 description 1
- 150000003464 sulfur compounds Chemical class 0.000 description 1
- 150000003467 sulfuric acid derivatives Chemical class 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- XOLBLPGZBRYERU-UHFFFAOYSA-N tin dioxide Chemical compound O=[Sn]=O XOLBLPGZBRYERU-UHFFFAOYSA-N 0.000 description 1
- 229910001887 tin oxide Inorganic materials 0.000 description 1
- BDZBKCUKTQZUTL-UHFFFAOYSA-N triethyl phosphite Chemical compound CCOP(OCC)OCC BDZBKCUKTQZUTL-UHFFFAOYSA-N 0.000 description 1
- 238000004736 wide-angle X-ray diffraction Methods 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B17/00—Sulfur; Compounds thereof
- C01B17/02—Preparation of sulfur; Purification
- C01B17/0243—Other after-treatment of sulfur
- C01B17/0248—Other after-treatment of sulfur of particulate sulfur
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/13—Electrodes for accumulators with non-aqueous electrolyte, e.g. for lithium-accumulators; Processes of manufacture thereof
- H01M4/133—Electrodes based on carbonaceous material, e.g. graphite-intercalation compounds or CFx
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/362—Composites
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B17/00—Sulfur; Compounds thereof
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B17/00—Sulfur; Compounds thereof
- C01B17/02—Preparation of sulfur; Purification
- C01B17/0243—Other after-treatment of sulfur
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B32/00—Carbon; Compounds thereof
- C01B32/15—Nano-sized carbon materials
- C01B32/158—Carbon nanotubes
- C01B32/168—After-treatment
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B32/00—Carbon; Compounds thereof
- C01B32/15—Nano-sized carbon materials
- C01B32/158—Carbon nanotubes
- C01B32/168—After-treatment
- C01B32/174—Derivatisation; Solubilisation; Dispersion in solvents
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
- H01M10/0525—Rocking-chair batteries, i.e. batteries with lithium insertion or intercalation in both electrodes; Lithium-ion batteries
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/13—Electrodes for accumulators with non-aqueous electrolyte, e.g. for lithium-accumulators; Processes of manufacture thereof
- H01M4/139—Processes of manufacture
- H01M4/1393—Processes of manufacture of electrodes based on carbonaceous material, e.g. graphite-intercalation compounds or CFx
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/362—Composites
- H01M4/364—Composites as mixtures
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/38—Selection of substances as active materials, active masses, active liquids of elements or alloys
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/58—Selection of substances as active materials, active masses, active liquids of inorganic compounds other than oxides or hydroxides, e.g. sulfides, selenides, tellurides, halogenides or LiCoFy; of polyanionic structures, e.g. phosphates, silicates or borates
- H01M4/581—Chalcogenides or intercalation compounds thereof
- H01M4/5815—Sulfides
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/62—Selection of inactive substances as ingredients for active masses, e.g. binders, fillers
- H01M4/624—Electric conductive fillers
- H01M4/625—Carbon or graphite
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M2004/026—Electrodes composed of, or comprising, active material characterised by the polarity
- H01M2004/028—Positive electrodes
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Materials Engineering (AREA)
- Inorganic Chemistry (AREA)
- Manufacturing & Machinery (AREA)
- Nanotechnology (AREA)
- Composite Materials (AREA)
- Battery Electrode And Active Subsutance (AREA)
- Carbon And Carbon Compounds (AREA)
Description
本発明は、多孔性炭素材;及び
前記多孔性炭素材の内部及び表面のうち、少なくとも一部に硫黄;を含む硫黄-炭素複合体であって、
前記硫黄-炭素複合体の比表面積は7ないし20m2/gで、気孔体積は0.1ないし0.3cm3/gである、硫黄-炭素複合体を提供する。
(b)前記官能基が取り除かれた多孔性炭素材を硫黄粉末と複合化して硫黄-炭素複合体を製造する段階;を含む硫黄-炭素複合体の製造方法を提供する。
前記正極は前記本発明の正極であることを特徴とするリチウム二次電池を提供する。
本発明は、多孔性炭素材;及び
前記多孔性炭素材の内部及び表面のうち、少なくとも一部に硫黄;を含む硫黄-炭素複合体であって、
前記硫黄-炭素複合体の比表面積は7ないし20m2/gで、気孔体積は0.1ないし0.3cm3/gである、硫黄-炭素複合体に関する。
本発明は、硫黄-炭素複合体の製造方法に係り、
(a)官能基で表面改質された多孔性炭素材を熱処理して官能基を取り除く段階;
(b)前記官能基が取り除かれた多孔性炭素材を硫黄粉末と複合化して硫黄-炭素複合体を製造する段階;を含む。
また、本発明は、上述した本発明の硫黄-炭素複合体を含むリチウム二次電池用正極に関する。
また、本発明は、正極;負極;前記正極と負極の間に介在される分離膜;及び電解液を含むリチウム二次電池に係り、前記正極は上述した本発明のリチウム二次電池用正極である。
実施例1.
酸で処理されたカーボンナノチューブ(CNano、FT6120)10gをアルゴン雰囲気で1時間パージング(purging)した。その後、10℃/minの昇温速度で850℃まで昇温させた後、3時間熱処理して官能基が取り除かれたカーボンナノチューブを製造した。
カーボンナノチューブ(SUSN、HCNTS10)を使用したことを除いては、前記実施例1と同様に実施してカーボンナノチューブの内部(気孔)及び表面に硫黄が担持された硫黄-炭素複合体を製造した(図3及び図4)。
親水性官能基で表面改質されたカーボンナノチューブ(CNano、FT6120)及び硫黄を25:75の重量比で混合した後、155℃の温度で35分間反応させてカーボンナノチューブの内部(気孔)及び表面に硫黄が担持された硫黄-炭素複合体を製造した。
親水性官能基で表面改質されたカーボンナノチューブ(SUSN、HCNTS10)を使用したことを除いては、前記比較例1と同様に実施してカーボンナノチューブの内部(気孔)及び表面に硫黄が担持された硫黄-炭素複合体を製造した。
酸で処理されたカーボンナノチューブ(SUSN、HCNTS10)10gをアルゴン雰囲気で1時間パージング(purging)した。その後、10℃/minの昇温速度で2000℃まで昇温させた後、3時間熱処理して官能基が取り除かれたカーボンナノチューブを製造した。
前記実施例1、実施例2、比較例1及び比較例2のカーボンナノチューブの熱重量分析(Thermogravimetric Analyzer、TGA)を実施した。0℃から900℃まで昇温し、この時の重量減少率を測定してカーボンナノチューブの官能基除去可否を確認した。
前記実施例2、比較例2及び比較例3のカーボンナノチューブのラマン(Raman)分析を実施して前記カーボンナノチューブのD/G比率(ratio)を測定した。
前記実施例1、実施例2及び比較例1、比較例2で製造した硫黄-炭素複合体の比表面積及び気孔体積をBelsorp社の窒素吸着設備を利用して測定し、結果を下記表1に示す。
HANTECH社の粉体抵抗測定機を利用して前記実施例1、実施例2及び比較例1、比較例2で製造した硫黄-炭素複合体の電気伝導率を測定した。
前記実施例1、実施例2及び比較例1、比較例2で製造した硫黄-炭素複合体を正極活物質にしてそれぞれのリチウム-硫黄電池(コインセル)を製造した。
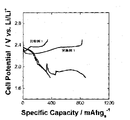
前記実施例1ないし2及び比較例1ないし2のリチウム-硫黄電池に対して、充・放電測定装置を用いて充・放電特性変化を試験した。得られた電池は、0.1C/0.1Cの充電/放電条件で初期容量を調べ、その結果を図12及び13に示す。
前記実施例1ないし2及び比較例1ないし2のリチウム-硫黄電池の寿命特性を評価した。
Claims (17)
- 多孔性炭素材;及び
前記多孔性炭素材の内部及び表面に担持された硫黄;を含む硫黄-炭素複合体であって、
前記硫黄-炭素複合体の比表面積は7ないし20m2/gで、気孔体積は0.1ないし0.3cm3/gであり、
前記多孔性炭素材が、カーボンナノチューブである、硫黄-炭素複合体。 - 前記多孔性炭素材は、その表面上に親水性官能基を有さないことを特徴とする請求項1に記載の硫黄-炭素複合体。
- 前記多孔性炭素材の熱重量分析結果、0℃から900℃まで昇温した時の重量減少率が1%以下で、ラマン測定時のD/Gの比率が0.8ないし1.5であることを特徴とする請求項2に記載の硫黄-炭素複合体。
- 前記硫黄-炭素複合体は、多孔性炭素材及び硫黄を1:1ないし1:9の重量比で含んでいることを特徴とする請求項1から3のいずれか一項に記載の硫黄-炭素複合体。
- 前記硫黄-炭素複合体の直径は0.1ないし20μmであることを特徴とする請求項1から4のいずれか一項に記載の硫黄-炭素複合体。
- (a)官能基で表面改質された多孔性炭素材を熱処理して官能基を取り除く段階;
(b)前記官能基が取り除かれた多孔性炭素材を硫黄粉末と複合化して硫黄-炭素複合体を製造する段階;を含み、
前記多孔性炭素材が、カーボンナノチューブであり、
前記官能基が、親水性官能基であり、
前記官能基が取り除かれた多孔性炭素材は、ラマン測定時のD/Gの比率が0.8ないし1.5である、硫黄-炭素複合体の製造方法。 - 前記(a)段階の熱処理は、5ないし20℃/minの速度で500ないし1000℃まで昇温させた後、1ないし5時間行うことを特徴とする請求項6に記載の硫黄-炭素複合体の製造方法。
- 前記(a)段階の官能基はヒドロキシ基またはカルボキシ基であることを特徴とする請求項6または7に記載の硫黄-炭素複合体の製造方法。
- 前記官能基で表面改質された多孔性炭素材は、多孔性炭素材を酸で処理して製造されたことを特徴とする請求項6から8のいずれか一項に記載の硫黄-炭素複合体の製造方法。
- 前記酸は、硝酸、硫酸及びこれらの混合溶液から選択される1種以上であることを特徴とする請求項9に記載の硫黄-炭素複合体の製造方法。
- 前記官能基が取り除かれた多孔性炭素材の熱重量分析結果、0℃から900℃まで昇温した時の重量減少率が1%以下であることを特徴とする請求項6から10のいずれか一項に記載の硫黄-炭素複合体の製造方法。
- 前記硫黄-炭素複合体の比表面積は7ないし20m2/gであることを特徴とする請求項6から11のいずれか一項に記載の硫黄-炭素複合体の製造方法。
- 前記硫黄-炭素複合体の気孔体積は0.1ないし0.3cm3/gであることを特徴とする請求項6から12のいずれか一項に記載の硫黄-炭素複合体の製造方法。
- 請求項1から5のいずれか一項に記載の硫黄-炭素複合体を含むリチウム二次電池用正極。
- 前記リチウム二次電池用正極はリチウム-硫黄電池用正極であることを特徴とする請求項14に記載のリチウム二次電池用正極。
- 正極;負極;前記正極と負極の間に介在される分離膜;及び電解液を含むリチウム二次電池であって、
前記正極は請求項14または15に記載の正極であることを特徴とするリチウム二次電池。 - 前記リチウム二次電池はリチウム-硫黄電池であることを特徴とする請求項16に記載のリチウム二次電池。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR20180112639 | 2018-09-20 | ||
| KR10-2018-0112639 | 2018-09-20 | ||
| KR10-2019-0109637 | 2019-09-04 | ||
| KR1020190109637A KR20200033736A (ko) | 2018-09-20 | 2019-09-04 | 황-탄소 복합체, 이의 제조방법, 이를 포함하는 리튬 이차전지용 양극 및 리튬 이차전지 |
| PCT/KR2019/011540 WO2020060084A1 (ko) | 2018-09-20 | 2019-09-06 | 황-탄소 복합체, 이의 제조방법, 이를 포함하는 리튬 이차전지용 양극 및 리튬 이차전지 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2021517110A JP2021517110A (ja) | 2021-07-15 |
| JP2021517110A5 JP2021517110A5 (ja) | 2021-08-26 |
| JP7167299B2 true JP7167299B2 (ja) | 2022-11-08 |
Family
ID=70003408
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021502687A Active JP7167299B2 (ja) | 2018-09-20 | 2019-09-06 | 硫黄-炭素複合体、この製造方法、これを含むリチウム二次電池用正極及びリチウム二次電池 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US20210036306A1 (ja) |
| EP (1) | EP3767715B1 (ja) |
| JP (1) | JP7167299B2 (ja) |
| KR (1) | KR20200033736A (ja) |
| CN (1) | CN112088453B (ja) |
| HU (1) | HUE064994T2 (ja) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20220100209A (ko) * | 2021-01-08 | 2022-07-15 | 주식회사 엘지에너지솔루션 | 황-탄소 복합체, 이의 제조방법, 및 이를 포함하는 리튬-황 전지 |
| WO2023210515A1 (ja) * | 2022-04-27 | 2023-11-02 | 日亜化学工業株式会社 | リチウム硫黄電池用炭素材料及びその製造方法 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2014118563A (ja) | 2012-12-18 | 2014-06-30 | Samsung Electro-Mechanics Co Ltd | 絶縁層組成物及びこれを用いる絶縁層を含む基板並びに基板製造方法 |
| CN106602063A (zh) | 2016-12-30 | 2017-04-26 | 浙江大学 | 一种石墨烯花的制备方法及其在锂硫电池中的应用 |
| JP2017119620A (ja) | 2015-12-24 | 2017-07-06 | 株式会社半導体エネルギー研究所 | 二次電池、酸化グラフェンおよびその作製方法 |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN102530926A (zh) * | 2010-12-10 | 2012-07-04 | 东丽纤维研究所(中国)有限公司 | 一种基于连二亚硫酸盐制备石墨烯的方法 |
| CN104094457B (zh) | 2011-09-30 | 2017-06-23 | 加州大学校务委员会 | 在高性能锂/硫电池中作为硫固定剂的氧化石墨烯 |
| DE102012209635A1 (de) * | 2012-06-08 | 2013-12-12 | Robert Bosch Gmbh | Verfahren zum Herstellen eines Polyacrylnitril-Schwefel-Kompositwerkstoffs |
| JP6011787B2 (ja) * | 2012-08-09 | 2016-10-19 | ソニー株式会社 | 電極材料及びその製造方法、並びに、リチウム−硫黄二次電池 |
| KR20180017796A (ko) * | 2016-08-11 | 2018-02-21 | 주식회사 엘지화학 | 황-탄소 복합체, 이의 제조방법 및 이를 포함하는 리튬-황 전지 |
| JP7118139B2 (ja) * | 2017-11-16 | 2022-08-15 | エルジー エナジー ソリューション リミテッド | 硫黄‐炭素複合体、その製造方法及びこれを含むリチウム二次電池 |
| KR102229453B1 (ko) * | 2017-11-24 | 2021-03-17 | 주식회사 엘지화학 | 황-탄소 복합체, 그의 제조방법 및 이를 포함하는 리튬 이차전지 |
-
2019
- 2019-09-04 KR KR1020190109637A patent/KR20200033736A/ko active Search and Examination
- 2019-09-06 JP JP2021502687A patent/JP7167299B2/ja active Active
- 2019-09-06 US US17/043,877 patent/US20210036306A1/en active Pending
- 2019-09-06 HU HUE19863294A patent/HUE064994T2/hu unknown
- 2019-09-06 CN CN201980030242.6A patent/CN112088453B/zh active Active
- 2019-09-06 EP EP19863294.5A patent/EP3767715B1/en active Active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2014118563A (ja) | 2012-12-18 | 2014-06-30 | Samsung Electro-Mechanics Co Ltd | 絶縁層組成物及びこれを用いる絶縁層を含む基板並びに基板製造方法 |
| JP2017119620A (ja) | 2015-12-24 | 2017-07-06 | 株式会社半導体エネルギー研究所 | 二次電池、酸化グラフェンおよびその作製方法 |
| CN106602063A (zh) | 2016-12-30 | 2017-04-26 | 浙江大学 | 一种石墨烯花的制备方法及其在锂硫电池中的应用 |
Non-Patent Citations (4)
| Title |
|---|
| Jing Gao et al.,Lithiated Nafion as polymer electrolyte for solid-state lithium sulfur batteries using carbon-sulfur composite cathode,Journal of Power Sources,2018年03月,vol.382,pp.179-189 |
| K.Balakumar and N.Kalaiselvi,High sulfur loaded carbon aerogel cathode for lithium-sulfur batteries,The Royal Society of Chemistry,2015年03月,vol.5,pp.34008-34018 |
| Kangke Jin et al.,Sulfur/Carbon Nanotube Composite Film as a Flexible Cathode for Lithium-Sulfur Batteries,THE JOURNAL OF PHYSICAL CHEMISTRY C,2013年,vol.117,pp.21112-21119 |
| Xin-Bing Cheng et al.,Aligned carbon nanotube/sulfur composite cathodes with high sulfur content for lithium-sulfur batteries,Nano Energy,2014年,vol.4,pp.65-72 |
Also Published As
| Publication number | Publication date |
|---|---|
| HUE064994T2 (hu) | 2024-04-28 |
| CN112088453A (zh) | 2020-12-15 |
| KR20200033736A (ko) | 2020-03-30 |
| CN112088453B (zh) | 2023-11-24 |
| US20210036306A1 (en) | 2021-02-04 |
| EP3767715B1 (en) | 2023-11-01 |
| JP2021517110A (ja) | 2021-07-15 |
| EP3767715A4 (en) | 2021-06-30 |
| EP3767715A1 (en) | 2021-01-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6732300B2 (ja) | 硫黄−炭素複合体、この製造方法及びこれを含むリチウム−硫黄電池 | |
| CN109314228B (zh) | 硫碳复合物及包含其的锂硫电池 | |
| JP7389100B2 (ja) | 酸化チタン-炭素ナノチューブ-硫黄(TiO2-x-CNT-S)複合体及びその製造方法 | |
| KR101990615B1 (ko) | 금속 나노입자를 포함하는 양극 활물질 및 양극, 이를 포함하는 리튬-황 전지 | |
| Shi et al. | Si nanoparticles adhering to a nitrogen-rich porous carbon framework and its application as a lithium-ion battery anode material | |
| CN112088451A (zh) | 包含二硫化钼的碳纳米结构体的制备方法、包含由其制备的包含二硫化钼的碳纳米结构体的锂二次电池用正极和包含所述锂二次电池用正极的锂二次电池 | |
| CN111066181B (zh) | 硫碳复合物、其制造方法和包含所述硫碳复合物的锂二次电池 | |
| WO2023241148A1 (zh) | 一种负极材料及包括该负极材料的负极片和电池 | |
| JP7128303B2 (ja) | 硫黄-炭素複合体、この製造方法及びこれを含むリチウム二次電池 | |
| US20240021803A1 (en) | Sulfur-carbon composite, preparation method therefor, and lithium secondary battery comprising same | |
| JP7167299B2 (ja) | 硫黄-炭素複合体、この製造方法、これを含むリチウム二次電池用正極及びリチウム二次電池 | |
| CN112335078B (zh) | 锂二次电池用正极活性材料 | |
| JP7174775B2 (ja) | 硫黄‐炭素複合体、この製造方法、これを含むリチウム‐硫黄電池用正極及びリチウム‐硫黄電池 | |
| JP2022530839A (ja) | 表面にリン酸陰イオンが吸着されたオキシ水酸化硝酸鉄、この製造方法、上記表面にリン酸陰イオンが吸着されたオキシ水酸化硝酸鉄を含むリチウム二次電池用正極及びこれを含むリチウム二次電池 | |
| JP7282116B2 (ja) | リン化鉄の製造方法、リン化鉄を含むリチウム二次電池用正極及びこれを備えたリチウム二次電池 | |
| CN114585588A (zh) | 多孔还原型氧化石墨烯、其制造方法、包含其的硫-碳复合材料和锂二次电池 | |
| JP7176110B2 (ja) | 熱膨張された還元グラフェンオキシド、この製造方法、これを含む硫黄-炭素複合体及びリチウム二次電池 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200930 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20200930 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20211004 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20211227 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A712 Effective date: 20211227 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20220509 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220727 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20221003 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20221026 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7167299 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |