JP6777576B2 - 窒化タンタルの製造方法 - Google Patents
窒化タンタルの製造方法 Download PDFInfo
- Publication number
- JP6777576B2 JP6777576B2 JP2017060801A JP2017060801A JP6777576B2 JP 6777576 B2 JP6777576 B2 JP 6777576B2 JP 2017060801 A JP2017060801 A JP 2017060801A JP 2017060801 A JP2017060801 A JP 2017060801A JP 6777576 B2 JP6777576 B2 JP 6777576B2
- Authority
- JP
- Japan
- Prior art keywords
- tantalum nitride
- tantalum
- nitriding
- tantalum oxide
- nitride
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Landscapes
- Catalysts (AREA)
Description
非特許文献1では、酸化タンタルをアンモニアで800℃で窒化反応させることにより、窒化タンタルを得ている。特許文献1では、酸化タンタルをアンモニア気流中、850℃で25時間窒化することで窒化タンタルを得て、光触媒に用いている。
特許文献2では、酸化タンタル水和物をアンモニアで750〜950℃で窒化反応させることにより、酸化タンタルの窒化反応により得られる窒化タンタルより高い光吸収率を有する窒化タンタルを得ている。
また、酸化タンタルの窒化反応において、酸素と水が存在すると、窒化タンタルが酸化され、酸化タンタルや酸窒化タンタルを生成する。酸化タンタル水和物の水分量から、水酸化タンタル(Ta(OH)5)であり、式(1)に示す窒化反応が起きる。酸化タンタルを原料としたときと同量の窒化タンタルを得るために、酸化タンタル水和物(水酸化タンタル)を原料したとき、式(2)と比較すると、酸化タンタルより酸素が多く、発生する水も多くなるため、窒化タンタルの酸化が起こりやすくなる。そのため、酸素含有量が多く、純度が低くなり、吸収波長の長波長側へのシフトは起こらないと考えられる。
3Ta2O5+10NH3→2Ta3N5+15H2O ・・・ 式(2)
〔1〕酸化タンタルを1400〜1850℃で焼成後、800〜950℃で、アンモニアガス下、アンモニアガス流量がTa2O51gあたり0.05〜0.8L/minで窒化することを特徴とする窒化タンタルの製造方法。
〔2〕加熱温度(℃)と加熱時間(hr)の積が10000〜25000になる時間、アンモニアガス下窒化する請求項1記載の製造方法。
〔3〕光吸収率が60%以上であり、620〜750nmの波長の可視光を吸収する窒化タンタル。
上記の反応により、反応容器中には高純度の窒化タンタルのみが残存するので回収が容易である。
本発明の窒化タンタルの吸収波長は、酸素含有量の低下及び純度の高度化とともに長波長側にシフトする傾向にあり、酸素含有量及び純度が高いことが好ましい。従って、窒化タンタルの純度は90%以上が好ましく、95%以上であるのがより好ましい。また、窒化タンタル中の酸素含有量は1質量%以下が好ましく、0.85質量%以下であるのがより好ましい。
酸化タンタル(三井金属鉱業(株)製、白色粉末)30gをアルミナボートに入れ、電気炉で1400℃で20時間焼成した。電気炉内の温度が室温程度(約25℃程度)になってから、アルミナボードを取り出し、焼成した酸化タンタルを回収した。
焼成した酸化タンタル5gをアルミナボートに入れ、アルミナ製の炉芯管内に置き、両端にガスフロー口とバルブの付いた栓をして、管状炉に設置した。アンモニアガス流量1L/min、850℃で20時間窒化反応を行った。窒化反応後、冷却し、室温程度(約25℃程度)になってから、アルミナボードを取り出し、窒化タンタルを回収した。
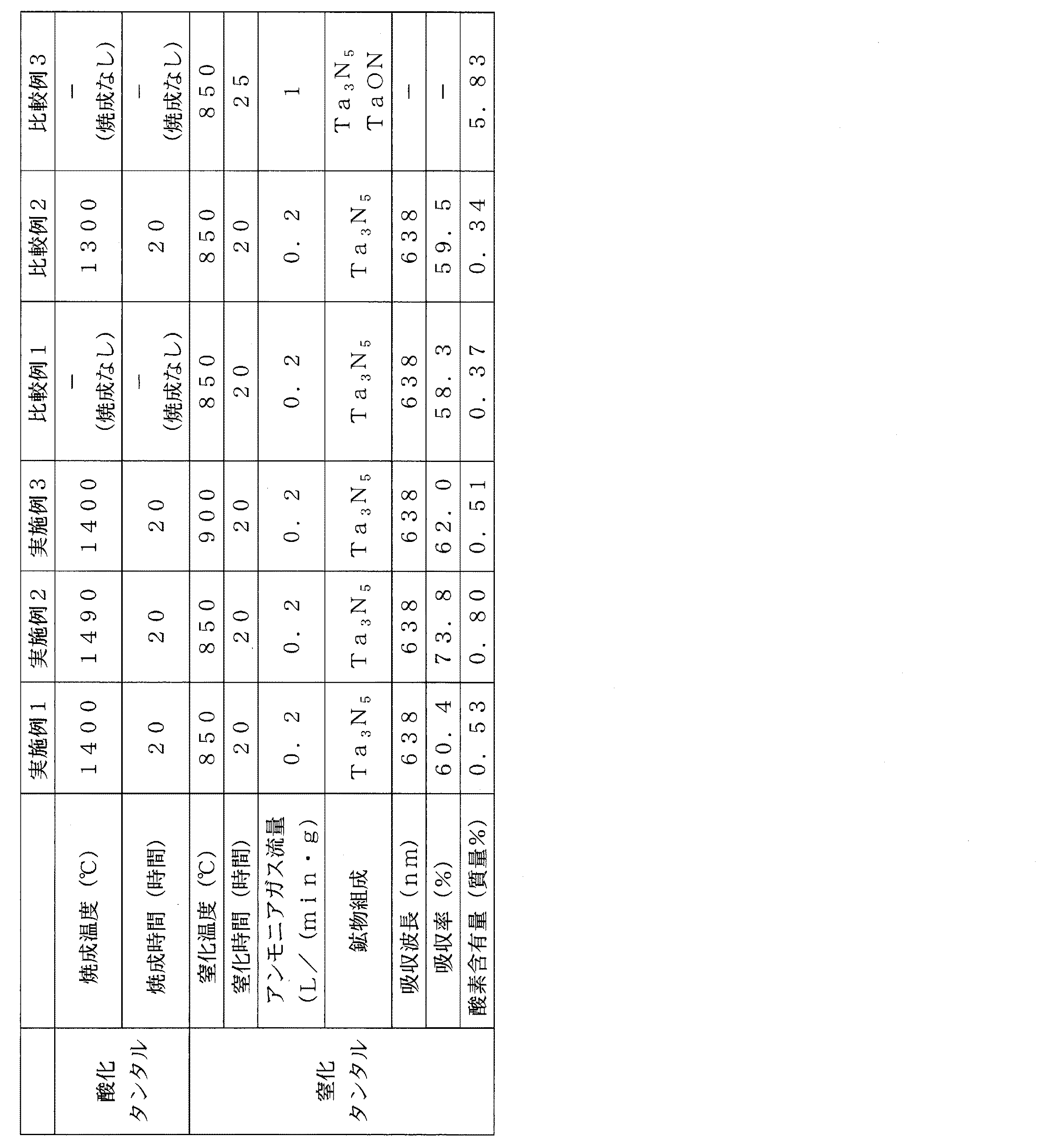
得られた窒化タンタルは、粉末X線回折(XRD)による鉱物組成の同定、紫外・可視分光光度計による吸収波長、吸収率の測定、窒素酸素同時分析計による酸素含有量の定量を行った。測定結果を表1に示す。
酸化タンタル30gの焼成温度を1490℃にした以外は、実施例1と同様に焼成、窒化反応を行った。得られた窒化タンタルも同様に分析を行った。測定結果を表1に示す。
実施例1で焼成した酸化タンタル5gを原料とし、窒化温度を900℃にした以外は、実施例1と同様に行った。得られた窒化タンタルも同様に分析を行った。測定結果を表1に示す。
焼成していない酸化タンタルを用いた以外、実施例1と同様に行った。得られた窒化タンタルも同様に分析を行った。測定結果を表1に示す。
酸化タンタル30gの焼成温度を1300℃にした以外は、実施例1と同様に焼成、窒化反応を行った。得られた窒化タンタルも同様に分析を行った。測定結果を表1に示す。
焼成していない酸化タンタル1gを入れ、アンモニアガスを1.0L/min雰囲気下で、反応温度850℃、25時間で窒化した。得られた合成物をXRDにより鉱物組成の同定を行ったところ、窒化タンタルと酸窒化タンタル(TaON)の混合相であり、酸素含有量は5.83質量%であった。窒化タンタルの単相が得られず酸素含有量も多かったため、紫外・可視分光光度計による吸収波長、吸収率の測定は行わなかった。
酸化タンタルの焼成温度が同じ実施例1と実施例3を比較すると、窒化温度の高い実施例3の方が吸収率が高くなることが確認できた。
実施例1〜3、比較例1〜2は、638nmと従来の窒化タンタルより長波長の吸収波長をもつ窒化タンタルである。
本発明の酸化タンタルを焼成した酸化タンタルを窒化タンタルの原料とすることにより、光吸収率が高く、本発明の窒化反応条件とすることにより吸収波長を長波長側へシフトすることができた。これより、本発明の窒化タンタルは、光触媒として有用であると考えられる。
Claims (3)
- 酸化タンタルを1400〜1850℃で焼成後、800〜950℃、アンモニアガス下、アンモニアガス流量がTa2O51gあたり0.05〜0.8L/minで窒化することを特徴とする窒化タンタルの製造方法。
- 加熱温度(℃)と加熱時間(hr)の積が10000〜25000になる時間、アンモニアガス下窒化する請求項1記載の製造方法。
- 光吸収率が60%以上で620〜680nmの吸収波長の可視光を吸収し、かつ酸素含有量が0.85質量%以下である窒化タンタル。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2017060801A JP6777576B2 (ja) | 2017-03-27 | 2017-03-27 | 窒化タンタルの製造方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2017060801A JP6777576B2 (ja) | 2017-03-27 | 2017-03-27 | 窒化タンタルの製造方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2018162188A JP2018162188A (ja) | 2018-10-18 |
| JP6777576B2 true JP6777576B2 (ja) | 2020-10-28 |
Family
ID=63860763
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017060801A Active JP6777576B2 (ja) | 2017-03-27 | 2017-03-27 | 窒化タンタルの製造方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP6777576B2 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPWO2023238387A1 (ja) * | 2022-06-10 | 2023-12-14 |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007022858A (ja) * | 2005-07-19 | 2007-02-01 | Univ Of Tokyo | 細孔構造を有する窒化物及びその製造方法 |
| JP6339046B2 (ja) * | 2015-06-12 | 2018-06-06 | 富士フイルム株式会社 | 光触媒、薄膜状光触媒の製造方法および可視光応答性光触媒デバイス |
-
2017
- 2017-03-27 JP JP2017060801A patent/JP6777576B2/ja active Active
Also Published As
| Publication number | Publication date |
|---|---|
| JP2018162188A (ja) | 2018-10-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Abu-Zied et al. | Pure and Ni-substituted Co3O4 spinel catalysts for direct N2O decomposition | |
| Xue et al. | Influence of additives on the γ-to-α transformation of alumina | |
| US11691882B2 (en) | Supported perovskite-oxide composites for enhanced low temperature thermochemical conversion of CO2 to CO | |
| CN101939099A (zh) | 低温水煤气轮换催化剂 | |
| WO2009021292A1 (en) | Titanate photocatalyst | |
| CN107552059B (zh) | 一种铁掺杂铈基固溶体烟气脱硝催化剂的制备方法 | |
| US12582967B2 (en) | Multi-cationic aluminate spinels | |
| JP6745164B2 (ja) | 窒化タンタル(Ta3N5)の製造方法 | |
| KR102132779B1 (ko) | 이산화탄소 흡착제, 그 제조 방법 및 이를 포함하는 이산화탄소 포집 모듈 | |
| JP4837651B2 (ja) | 酸化ニッケルの製造方法 | |
| JP6777576B2 (ja) | 窒化タンタルの製造方法 | |
| JP2017081812A (ja) | マンガン−ジルコニウム系複合酸化物及びその製造方法、並びにその用途 | |
| Drouet et al. | Synthesis and characterization of non-stoichiometric nickel–copper manganites | |
| EP3768640B1 (en) | Method for synthesis of gamma-aluminium oxide using plasma - modified aluminium and water reaction | |
| AU2003266780A1 (en) | A method for producing titanium oxide | |
| KR101728517B1 (ko) | 습식 혼합된 보헤마이트 슬러리를 이용한 질화알루미늄의 제조 방법 | |
| Chen et al. | Preparation of single-phase three-component alkaline earth oxide of (BaSrMg) O: a high capacity and thermally stable chemisorbent for oxygen separation | |
| Suino et al. | Thermal analysis and mechanism of α-Zn2SiO4: Mn2+ formation from zinc oxalate dihydrate under hydrothermal conditions | |
| JP6812910B2 (ja) | ペロブスカイト型構造を有するアルミン酸ランタン系化合物の製造方法 | |
| US20170121182A1 (en) | Calcination processes for preparing various types of alumina | |
| WO2015176166A1 (en) | Processes for decomposing aluminum chloride into alumina | |
| CN112569992B (zh) | 含沉淀型χ碳化铁组合物及其制备方法、催化剂和应用以及费托合成的方法 | |
| JP6815246B2 (ja) | 窒化タンタル粒子 | |
| CN104364199B (zh) | 钙铝石的制备方法 | |
| Bergadà et al. | Adsorption of carbon dioxide in several aged hydrotalcites and calcined hydrotalcites: Influence of microwave irradiation during the ageing step on their basic properties |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20190924 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20200624 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200721 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200902 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20201006 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20201008 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6777576 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |