JP6567425B2 - Cd3特異的結合ドメインによって引き起こされる潜在的有害事象を緩和するための抗白血球接着 - Google Patents
Cd3特異的結合ドメインによって引き起こされる潜在的有害事象を緩和するための抗白血球接着 Download PDFInfo
- Publication number
- JP6567425B2 JP6567425B2 JP2015556506A JP2015556506A JP6567425B2 JP 6567425 B2 JP6567425 B2 JP 6567425B2 JP 2015556506 A JP2015556506 A JP 2015556506A JP 2015556506 A JP2015556506 A JP 2015556506A JP 6567425 B2 JP6567425 B2 JP 6567425B2
- Authority
- JP
- Japan
- Prior art keywords
- cells
- cell
- endothelial
- amg
- blinatumomab
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 230000002411 adverse Effects 0.000 title claims description 47
- 230000009870 specific binding Effects 0.000 title description 33
- 210000001744 T-lymphocyte Anatomy 0.000 claims description 510
- 229960003008 blinatumomab Drugs 0.000 claims description 259
- 150000001875 compounds Chemical class 0.000 claims description 163
- 210000002889 endothelial cell Anatomy 0.000 claims description 142
- 210000004027 cell Anatomy 0.000 claims description 138
- 230000027455 binding Effects 0.000 claims description 136
- 238000011282 treatment Methods 0.000 claims description 92
- 238000000034 method Methods 0.000 claims description 66
- 210000003719 b-lymphocyte Anatomy 0.000 claims description 45
- 238000002560 therapeutic procedure Methods 0.000 claims description 36
- 229960004023 minocycline Drugs 0.000 claims description 32
- 210000005259 peripheral blood Anatomy 0.000 claims description 21
- 239000011886 peripheral blood Substances 0.000 claims description 21
- 239000000203 mixture Substances 0.000 claims description 19
- 230000000926 neurological effect Effects 0.000 claims description 12
- 239000003814 drug Substances 0.000 claims description 11
- 102100024222 B-lymphocyte antigen CD19 Human genes 0.000 claims description 9
- 210000004204 blood vessel Anatomy 0.000 claims description 8
- 210000004556 brain Anatomy 0.000 claims description 8
- 241000124008 Mammalia Species 0.000 claims description 7
- 210000004925 microvascular endothelial cell Anatomy 0.000 claims description 7
- 206010003591 Ataxia Diseases 0.000 claims description 6
- 206010010904 Convulsion Diseases 0.000 claims description 6
- 241000288906 Primates Species 0.000 claims description 6
- 239000003862 glucocorticoid Substances 0.000 claims description 6
- 208000024891 symptom Diseases 0.000 claims description 6
- 206010044565 Tremor Diseases 0.000 claims description 5
- 201000007201 aphasia Diseases 0.000 claims description 5
- 239000008194 pharmaceutical composition Substances 0.000 claims description 5
- 210000003606 umbilical vein Anatomy 0.000 claims description 5
- 208000028698 Cognitive impairment Diseases 0.000 claims description 4
- 230000002490 cerebral effect Effects 0.000 claims description 4
- 208000010877 cognitive disease Diseases 0.000 claims description 4
- 206010013887 Dysarthria Diseases 0.000 claims description 3
- 230000003416 augmentation Effects 0.000 claims description 2
- 238000004519 manufacturing process Methods 0.000 claims description 2
- 101000980825 Homo sapiens B-lymphocyte antigen CD19 Proteins 0.000 claims 8
- DYKFCLLONBREIL-KVUCHLLUSA-N minocycline Chemical compound C([C@H]1C2)C3=C(N(C)C)C=CC(O)=C3C(=O)C1=C(O)[C@@]1(O)[C@@H]2[C@H](N(C)C)C(O)=C(C(N)=O)C1=O DYKFCLLONBREIL-KVUCHLLUSA-N 0.000 claims 1
- 238000005096 rolling process Methods 0.000 description 148
- 102000017420 CD3 protein, epsilon/gamma/delta subunit Human genes 0.000 description 96
- 108050005493 CD3 protein, epsilon/gamma/delta subunit Proteins 0.000 description 96
- 102000016289 Cell Adhesion Molecules Human genes 0.000 description 88
- 108010067225 Cell Adhesion Molecules Proteins 0.000 description 88
- 229940043138 pentosan polysulfate Drugs 0.000 description 87
- 108010019670 Chimeric Antigen Receptors Proteins 0.000 description 52
- 230000000694 effects Effects 0.000 description 49
- 210000003169 central nervous system Anatomy 0.000 description 48
- 230000003511 endothelial effect Effects 0.000 description 40
- 238000001802 infusion Methods 0.000 description 40
- 238000002474 experimental method Methods 0.000 description 37
- 102100023472 P-selectin Human genes 0.000 description 36
- 230000014509 gene expression Effects 0.000 description 36
- 108010035766 P-Selectin Proteins 0.000 description 33
- FFTVPQUHLQBXQZ-KVUCHLLUSA-N (4s,4as,5ar,12ar)-4,7-bis(dimethylamino)-1,10,11,12a-tetrahydroxy-3,12-dioxo-4a,5,5a,6-tetrahydro-4h-tetracene-2-carboxamide Chemical compound C1C2=C(N(C)C)C=CC(O)=C2C(O)=C2[C@@H]1C[C@H]1[C@H](N(C)C)C(=O)C(C(N)=O)=C(O)[C@@]1(O)C2=O FFTVPQUHLQBXQZ-KVUCHLLUSA-N 0.000 description 32
- 230000007423 decrease Effects 0.000 description 26
- 210000000265 leukocyte Anatomy 0.000 description 26
- 108010064593 Intercellular Adhesion Molecule-1 Proteins 0.000 description 25
- 102000015271 Intercellular Adhesion Molecule-1 Human genes 0.000 description 25
- 230000007774 longterm Effects 0.000 description 24
- 206010028980 Neoplasm Diseases 0.000 description 22
- 108010000134 Vascular Cell Adhesion Molecule-1 Proteins 0.000 description 19
- 102100023543 Vascular cell adhesion protein 1 Human genes 0.000 description 19
- 230000008614 cellular interaction Effects 0.000 description 19
- 230000001965 increasing effect Effects 0.000 description 18
- 229960005027 natalizumab Drugs 0.000 description 17
- 230000002829 reductive effect Effects 0.000 description 17
- NTYJJOPFIAHURM-UHFFFAOYSA-N Histamine Chemical compound NCCC1=CN=CN1 NTYJJOPFIAHURM-UHFFFAOYSA-N 0.000 description 16
- 239000012980 RPMI-1640 medium Substances 0.000 description 16
- 230000021164 cell adhesion Effects 0.000 description 16
- 239000005557 antagonist Substances 0.000 description 15
- 201000011510 cancer Diseases 0.000 description 15
- 230000003993 interaction Effects 0.000 description 15
- 150000001413 amino acids Chemical group 0.000 description 14
- 239000000427 antigen Substances 0.000 description 14
- 102000036639 antigens Human genes 0.000 description 14
- 108091007433 antigens Proteins 0.000 description 14
- 230000000903 blocking effect Effects 0.000 description 14
- 239000012530 fluid Substances 0.000 description 14
- 102000006495 integrins Human genes 0.000 description 14
- 108010044426 integrins Proteins 0.000 description 14
- 238000001990 intravenous administration Methods 0.000 description 14
- 230000002265 prevention Effects 0.000 description 13
- 102100032912 CD44 antigen Human genes 0.000 description 12
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 12
- 101000868273 Homo sapiens CD44 antigen Proteins 0.000 description 12
- 102100022339 Integrin alpha-L Human genes 0.000 description 12
- 108010064548 Lymphocyte Function-Associated Antigen-1 Proteins 0.000 description 12
- 239000003446 ligand Substances 0.000 description 12
- 150000007523 nucleic acids Chemical class 0.000 description 12
- 230000009467 reduction Effects 0.000 description 12
- 238000010186 staining Methods 0.000 description 12
- 241000699666 Mus <mouse, genus> Species 0.000 description 11
- 208000028564 B-cell non-Hodgkin lymphoma Diseases 0.000 description 10
- 206010015866 Extravasation Diseases 0.000 description 10
- 230000001464 adherent effect Effects 0.000 description 10
- 230000036251 extravasation Effects 0.000 description 10
- 238000000386 microscopy Methods 0.000 description 10
- 102100022005 B-lymphocyte antigen CD20 Human genes 0.000 description 9
- 101000897405 Homo sapiens B-lymphocyte antigen CD20 Proteins 0.000 description 9
- 230000000181 anti-adherent effect Effects 0.000 description 9
- 229940079593 drug Drugs 0.000 description 9
- 210000001616 monocyte Anatomy 0.000 description 9
- 229920001184 polypeptide Polymers 0.000 description 9
- 102000004196 processed proteins & peptides Human genes 0.000 description 9
- 108090000765 processed proteins & peptides Proteins 0.000 description 9
- 239000000243 solution Substances 0.000 description 9
- 102100034925 P-selectin glycoprotein ligand 1 Human genes 0.000 description 8
- 102000003800 Selectins Human genes 0.000 description 8
- 108090000184 Selectins Proteins 0.000 description 8
- 238000003556 assay Methods 0.000 description 8
- 238000004113 cell culture Methods 0.000 description 8
- -1 etc.) Proteins 0.000 description 8
- 229960001340 histamine Drugs 0.000 description 8
- 230000023404 leukocyte cell-cell adhesion Effects 0.000 description 8
- 230000003211 malignant effect Effects 0.000 description 8
- 210000002966 serum Anatomy 0.000 description 8
- 230000026683 transduction Effects 0.000 description 8
- 238000010361 transduction Methods 0.000 description 8
- 241000282412 Homo Species 0.000 description 7
- 108060003951 Immunoglobulin Proteins 0.000 description 7
- 206010060860 Neurological symptom Diseases 0.000 description 7
- 102000018358 immunoglobulin Human genes 0.000 description 7
- 238000002347 injection Methods 0.000 description 7
- 239000007924 injection Substances 0.000 description 7
- 239000003550 marker Substances 0.000 description 7
- 108020004707 nucleic acids Proteins 0.000 description 7
- 102000039446 nucleic acids Human genes 0.000 description 7
- 238000001050 pharmacotherapy Methods 0.000 description 7
- 230000008569 process Effects 0.000 description 7
- 108090000623 proteins and genes Proteins 0.000 description 7
- 108010047041 Complementarity Determining Regions Proteins 0.000 description 6
- 102100023471 E-selectin Human genes 0.000 description 6
- 102100038591 Endothelial cell-selective adhesion molecule Human genes 0.000 description 6
- 101000882622 Homo sapiens Endothelial cell-selective adhesion molecule Proteins 0.000 description 6
- 101000873418 Homo sapiens P-selectin glycoprotein ligand 1 Proteins 0.000 description 6
- 101000946860 Homo sapiens T-cell surface glycoprotein CD3 epsilon chain Proteins 0.000 description 6
- 102100033467 L-selectin Human genes 0.000 description 6
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 6
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 6
- 102100035794 T-cell surface glycoprotein CD3 epsilon chain Human genes 0.000 description 6
- 210000004369 blood Anatomy 0.000 description 6
- 239000008280 blood Substances 0.000 description 6
- 239000000872 buffer Substances 0.000 description 6
- 239000003153 chemical reaction reagent Substances 0.000 description 6
- 210000003038 endothelium Anatomy 0.000 description 6
- 210000003989 endothelium vascular Anatomy 0.000 description 6
- 239000012634 fragment Substances 0.000 description 6
- 229940027941 immunoglobulin g Drugs 0.000 description 6
- 230000007246 mechanism Effects 0.000 description 6
- 239000002773 nucleotide Substances 0.000 description 6
- 125000003729 nucleotide group Chemical group 0.000 description 6
- 210000003819 peripheral blood mononuclear cell Anatomy 0.000 description 6
- 238000011533 pre-incubation Methods 0.000 description 6
- 150000003384 small molecules Chemical class 0.000 description 6
- 102000009076 src-Family Kinases Human genes 0.000 description 6
- 108010087686 src-Family Kinases Proteins 0.000 description 6
- 230000001052 transient effect Effects 0.000 description 6
- KIUKXJAPPMFGSW-DNGZLQJQSA-N (2S,3S,4S,5R,6R)-6-[(2S,3R,4R,5S,6R)-3-Acetamido-2-[(2S,3S,4R,5R,6R)-6-[(2R,3R,4R,5S,6R)-3-acetamido-2,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-2-carboxy-4,5-dihydroxyoxan-3-yl]oxy-5-hydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-3,4,5-trihydroxyoxane-2-carboxylic acid Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 KIUKXJAPPMFGSW-DNGZLQJQSA-N 0.000 description 5
- 208000024893 Acute lymphoblastic leukemia Diseases 0.000 description 5
- 208000014697 Acute lymphocytic leukaemia Diseases 0.000 description 5
- 102100038080 B-cell receptor CD22 Human genes 0.000 description 5
- 101000884305 Homo sapiens B-cell receptor CD22 Proteins 0.000 description 5
- 108010041012 Integrin alpha4 Proteins 0.000 description 5
- 108010064600 Intercellular Adhesion Molecule-3 Proteins 0.000 description 5
- 102100037872 Intercellular adhesion molecule 2 Human genes 0.000 description 5
- 101710148794 Intercellular adhesion molecule 2 Proteins 0.000 description 5
- 102100037871 Intercellular adhesion molecule 3 Human genes 0.000 description 5
- 206010025323 Lymphomas Diseases 0.000 description 5
- 208000006664 Precursor Cell Lymphoblastic Leukemia-Lymphoma Diseases 0.000 description 5
- 108091008874 T cell receptors Proteins 0.000 description 5
- 102000016266 T-Cell Antigen Receptors Human genes 0.000 description 5
- 239000006285 cell suspension Substances 0.000 description 5
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 5
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 5
- 229920002674 hyaluronan Polymers 0.000 description 5
- 229960003160 hyaluronic acid Drugs 0.000 description 5
- 230000006872 improvement Effects 0.000 description 5
- 238000011534 incubation Methods 0.000 description 5
- 239000003112 inhibitor Substances 0.000 description 5
- 230000000977 initiatory effect Effects 0.000 description 5
- 108010021315 integrin beta7 Proteins 0.000 description 5
- 238000002955 isolation Methods 0.000 description 5
- 229940043355 kinase inhibitor Drugs 0.000 description 5
- 230000036210 malignancy Effects 0.000 description 5
- 238000007431 microscopic evaluation Methods 0.000 description 5
- 230000001575 pathological effect Effects 0.000 description 5
- 230000010412 perfusion Effects 0.000 description 5
- 239000003757 phosphotransferase inhibitor Substances 0.000 description 5
- 102000004169 proteins and genes Human genes 0.000 description 5
- 230000001225 therapeutic effect Effects 0.000 description 5
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 4
- 108010083359 Antigen Receptors Proteins 0.000 description 4
- 102000006306 Antigen Receptors Human genes 0.000 description 4
- 208000010839 B-cell chronic lymphocytic leukemia Diseases 0.000 description 4
- 108010024212 E-Selectin Proteins 0.000 description 4
- 108010008212 Integrin alpha4beta1 Proteins 0.000 description 4
- 108010092694 L-Selectin Proteins 0.000 description 4
- 208000036110 Neuroinflammatory disease Diseases 0.000 description 4
- 108091028043 Nucleic acid sequence Proteins 0.000 description 4
- 102100024616 Platelet endothelial cell adhesion molecule Human genes 0.000 description 4
- 208000006011 Stroke Diseases 0.000 description 4
- 230000004913 activation Effects 0.000 description 4
- 238000013459 approach Methods 0.000 description 4
- 150000001719 carbohydrate derivatives Chemical class 0.000 description 4
- 239000002738 chelating agent Substances 0.000 description 4
- 238000002651 drug therapy Methods 0.000 description 4
- JYGXADMDTFJGBT-VWUMJDOOSA-N hydrocortisone Chemical compound O=C1CC[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 JYGXADMDTFJGBT-VWUMJDOOSA-N 0.000 description 4
- 238000003125 immunofluorescent labeling Methods 0.000 description 4
- 230000010534 mechanism of action Effects 0.000 description 4
- 230000001404 mediated effect Effects 0.000 description 4
- 239000013642 negative control Substances 0.000 description 4
- 230000003959 neuroinflammation Effects 0.000 description 4
- 208000017426 precursor B-cell acute lymphoblastic leukemia Diseases 0.000 description 4
- 238000012552 review Methods 0.000 description 4
- 229960004641 rituximab Drugs 0.000 description 4
- 239000002412 selectin antagonist Substances 0.000 description 4
- 239000013589 supplement Substances 0.000 description 4
- 238000012360 testing method Methods 0.000 description 4
- 238000013518 transcription Methods 0.000 description 4
- 230000035897 transcription Effects 0.000 description 4
- 238000013519 translation Methods 0.000 description 4
- 238000005406 washing Methods 0.000 description 4
- 102000008186 Collagen Human genes 0.000 description 3
- 108010035532 Collagen Proteins 0.000 description 3
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical group OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 3
- 102100025137 Early activation antigen CD69 Human genes 0.000 description 3
- 102000006354 HLA-DR Antigens Human genes 0.000 description 3
- 108010058597 HLA-DR Antigens Proteins 0.000 description 3
- 101000934374 Homo sapiens Early activation antigen CD69 Proteins 0.000 description 3
- 101000994375 Homo sapiens Integrin alpha-4 Proteins 0.000 description 3
- 101001057504 Homo sapiens Interferon-stimulated gene 20 kDa protein Proteins 0.000 description 3
- 101001055144 Homo sapiens Interleukin-2 receptor subunit alpha Proteins 0.000 description 3
- 101000622137 Homo sapiens P-selectin Proteins 0.000 description 3
- 101000622304 Homo sapiens Vascular cell adhesion protein 1 Proteins 0.000 description 3
- 102100032818 Integrin alpha-4 Human genes 0.000 description 3
- 102100027268 Interferon-stimulated gene 20 kDa protein Human genes 0.000 description 3
- 102000019298 Lipocalin Human genes 0.000 description 3
- 108050006654 Lipocalin Proteins 0.000 description 3
- 208000031422 Lymphocytic Chronic B-Cell Leukemia Diseases 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 239000004098 Tetracycline Substances 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 230000001588 bifunctional effect Effects 0.000 description 3
- 230000020411 cell activation Effects 0.000 description 3
- 208000032852 chronic lymphocytic leukemia Diseases 0.000 description 3
- 229920001436 collagen Polymers 0.000 description 3
- 229940124301 concurrent medication Drugs 0.000 description 3
- 230000003247 decreasing effect Effects 0.000 description 3
- 238000011161 development Methods 0.000 description 3
- 208000035475 disorder Diseases 0.000 description 3
- 238000000684 flow cytometry Methods 0.000 description 3
- 102000037865 fusion proteins Human genes 0.000 description 3
- 108020001507 fusion proteins Proteins 0.000 description 3
- 238000000338 in vitro Methods 0.000 description 3
- 230000002401 inhibitory effect Effects 0.000 description 3
- 210000004088 microvessel Anatomy 0.000 description 3
- 230000000116 mitigating effect Effects 0.000 description 3
- 230000009149 molecular binding Effects 0.000 description 3
- 102000005962 receptors Human genes 0.000 description 3
- 108020003175 receptors Proteins 0.000 description 3
- 235000019364 tetracycline Nutrition 0.000 description 3
- 150000003522 tetracyclines Chemical class 0.000 description 3
- 230000002792 vascular Effects 0.000 description 3
- 238000005303 weighing Methods 0.000 description 3
- HKZAAJSTFUZYTO-LURJTMIESA-N (2s)-2-[[2-[[2-[[2-[(2-aminoacetyl)amino]acetyl]amino]acetyl]amino]acetyl]amino]-3-hydroxypropanoic acid Chemical compound NCC(=O)NCC(=O)NCC(=O)NCC(=O)N[C@@H](CO)C(O)=O HKZAAJSTFUZYTO-LURJTMIESA-N 0.000 description 2
- NFGXHKASABOEEW-UHFFFAOYSA-N 1-methylethyl 11-methoxy-3,7,11-trimethyl-2,4-dodecadienoate Chemical compound COC(C)(C)CCCC(C)CC=CC(C)=CC(=O)OC(C)C NFGXHKASABOEEW-UHFFFAOYSA-N 0.000 description 2
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 2
- 208000000044 Amnesia Diseases 0.000 description 2
- 102100034608 Angiopoietin-2 Human genes 0.000 description 2
- 108010048036 Angiopoietin-2 Proteins 0.000 description 2
- 241000283707 Capra Species 0.000 description 2
- 108091007741 Chimeric antigen receptor T cells Proteins 0.000 description 2
- 229920002567 Chondroitin Polymers 0.000 description 2
- SRBFZHDQGSBBOR-IOVATXLUSA-N D-xylopyranose Chemical compound O[C@@H]1COC(O)[C@H](O)[C@H]1O SRBFZHDQGSBBOR-IOVATXLUSA-N 0.000 description 2
- 102000008946 Fibrinogen Human genes 0.000 description 2
- 108010049003 Fibrinogen Proteins 0.000 description 2
- 102000016359 Fibronectins Human genes 0.000 description 2
- 108010067306 Fibronectins Proteins 0.000 description 2
- 108010010803 Gelatin Proteins 0.000 description 2
- 239000007995 HEPES buffer Substances 0.000 description 2
- 208000004547 Hallucinations Diseases 0.000 description 2
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical class OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 2
- 101100383038 Homo sapiens CD19 gene Proteins 0.000 description 2
- 101000622123 Homo sapiens E-selectin Proteins 0.000 description 2
- 101001018097 Homo sapiens L-selectin Proteins 0.000 description 2
- 108010021625 Immunoglobulin Fragments Proteins 0.000 description 2
- 102000008394 Immunoglobulin Fragments Human genes 0.000 description 2
- 208000005615 Interstitial Cystitis Diseases 0.000 description 2
- 241000283283 Orcinus orca Species 0.000 description 2
- 241000283973 Oryctolagus cuniculus Species 0.000 description 2
- 101710137390 P-selectin glycoprotein ligand 1 Proteins 0.000 description 2
- 108010069381 Platelet Endothelial Cell Adhesion Molecule-1 Proteins 0.000 description 2
- 101710121440 Proteinase-activated receptor 1 Proteins 0.000 description 2
- 238000012228 RNA interference-mediated gene silencing Methods 0.000 description 2
- 241000700159 Rattus Species 0.000 description 2
- 102100028904 Serine/threonine-protein kinase MARK2 Human genes 0.000 description 2
- 238000000692 Student's t-test Methods 0.000 description 2
- 230000006044 T cell activation Effects 0.000 description 2
- 108090000631 Trypsin Proteins 0.000 description 2
- 102000004142 Trypsin Human genes 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 239000003855 balanced salt solution Substances 0.000 description 2
- 229960002685 biotin Drugs 0.000 description 2
- 235000020958 biotin Nutrition 0.000 description 2
- 239000011616 biotin Substances 0.000 description 2
- 239000002981 blocking agent Substances 0.000 description 2
- 210000005098 blood-cerebrospinal fluid barrier Anatomy 0.000 description 2
- 239000011575 calcium Substances 0.000 description 2
- 230000006727 cell loss Effects 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 238000012512 characterization method Methods 0.000 description 2
- DLGJWSVWTWEWBJ-HGGSSLSASA-N chondroitin Chemical compound CC(O)=N[C@@H]1[C@H](O)O[C@H](CO)[C@H](O)[C@@H]1OC1[C@H](O)[C@H](O)C=C(C(O)=O)O1 DLGJWSVWTWEWBJ-HGGSSLSASA-N 0.000 description 2
- 239000011248 coating agent Substances 0.000 description 2
- 238000000576 coating method Methods 0.000 description 2
- 230000000875 corresponding effect Effects 0.000 description 2
- 210000001151 cytotoxic T lymphocyte Anatomy 0.000 description 2
- 230000001472 cytotoxic effect Effects 0.000 description 2
- 238000007405 data analysis Methods 0.000 description 2
- 230000001627 detrimental effect Effects 0.000 description 2
- 230000008034 disappearance Effects 0.000 description 2
- 201000010099 disease Diseases 0.000 description 2
- 208000002173 dizziness Diseases 0.000 description 2
- 229960000284 efalizumab Drugs 0.000 description 2
- 230000008029 eradication Effects 0.000 description 2
- 229950004912 etrolizumab Drugs 0.000 description 2
- 229940012952 fibrinogen Drugs 0.000 description 2
- 201000003444 follicular lymphoma Diseases 0.000 description 2
- 230000006870 function Effects 0.000 description 2
- 239000007789 gas Substances 0.000 description 2
- 229920000159 gelatin Polymers 0.000 description 2
- 239000008273 gelatin Substances 0.000 description 2
- 235000019322 gelatine Nutrition 0.000 description 2
- 235000011852 gelatine desserts Nutrition 0.000 description 2
- 230000009368 gene silencing by RNA Effects 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- 229960000890 hydrocortisone Drugs 0.000 description 2
- 230000001939 inductive effect Effects 0.000 description 2
- 230000002452 interceptive effect Effects 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 210000002418 meninge Anatomy 0.000 description 2
- 238000013508 migration Methods 0.000 description 2
- 230000005012 migration Effects 0.000 description 2
- 230000003278 mimic effect Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 210000005087 mononuclear cell Anatomy 0.000 description 2
- 201000006417 multiple sclerosis Diseases 0.000 description 2
- 238000006386 neutralization reaction Methods 0.000 description 2
- 238000001543 one-way ANOVA Methods 0.000 description 2
- 230000003285 pharmacodynamic effect Effects 0.000 description 2
- 230000001766 physiological effect Effects 0.000 description 2
- 230000002035 prolonged effect Effects 0.000 description 2
- AAEVYOVXGOFMJO-UHFFFAOYSA-N prometryn Chemical compound CSC1=NC(NC(C)C)=NC(NC(C)C)=N1 AAEVYOVXGOFMJO-UHFFFAOYSA-N 0.000 description 2
- 238000001959 radiotherapy Methods 0.000 description 2
- 238000011084 recovery Methods 0.000 description 2
- 230000002441 reversible effect Effects 0.000 description 2
- 230000008054 signal transmission Effects 0.000 description 2
- DAEPDZWVDSPTHF-UHFFFAOYSA-M sodium pyruvate Chemical compound [Na+].CC(=O)C([O-])=O DAEPDZWVDSPTHF-UHFFFAOYSA-M 0.000 description 2
- 125000006850 spacer group Chemical group 0.000 description 2
- 208000027765 speech disease Diseases 0.000 description 2
- 230000003068 static effect Effects 0.000 description 2
- 238000011476 stem cell transplantation Methods 0.000 description 2
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 2
- 230000002459 sustained effect Effects 0.000 description 2
- 238000012353 t test Methods 0.000 description 2
- 229960002180 tetracycline Drugs 0.000 description 2
- 229930101283 tetracycline Natural products 0.000 description 2
- 229940124597 therapeutic agent Drugs 0.000 description 2
- 210000001519 tissue Anatomy 0.000 description 2
- 230000001960 triggered effect Effects 0.000 description 2
- 239000012588 trypsin Substances 0.000 description 2
- 229920001221 xylan Polymers 0.000 description 2
- KEQGZUUPPQEDPF-UHFFFAOYSA-N 1,3-dichloro-5,5-dimethylimidazolidine-2,4-dione Chemical compound CC1(C)N(Cl)C(=O)N(Cl)C1=O KEQGZUUPPQEDPF-UHFFFAOYSA-N 0.000 description 1
- FUFLCEKSBBHCMO-UHFFFAOYSA-N 11-dehydrocorticosterone Natural products O=C1CCC2(C)C3C(=O)CC(C)(C(CC4)C(=O)CO)C4C3CCC2=C1 FUFLCEKSBBHCMO-UHFFFAOYSA-N 0.000 description 1
- FWBHETKCLVMNFS-UHFFFAOYSA-N 4',6-Diamino-2-phenylindol Chemical compound C1=CC(C(=N)N)=CC=C1C1=CC2=CC=C(C(N)=N)C=C2N1 FWBHETKCLVMNFS-UHFFFAOYSA-N 0.000 description 1
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 1
- SQDAZGGFXASXDW-UHFFFAOYSA-N 5-bromo-2-(trifluoromethoxy)pyridine Chemical compound FC(F)(F)OC1=CC=C(Br)C=N1 SQDAZGGFXASXDW-UHFFFAOYSA-N 0.000 description 1
- 102100036775 Afadin Human genes 0.000 description 1
- 102100022704 Amyloid-beta precursor protein Human genes 0.000 description 1
- 102000008102 Ankyrins Human genes 0.000 description 1
- 108010049777 Ankyrins Proteins 0.000 description 1
- 108020005098 Anticodon Proteins 0.000 description 1
- 206010003062 Apraxia Diseases 0.000 description 1
- BSYNRYMUTXBXSQ-UHFFFAOYSA-N Aspirin Chemical compound CC(=O)OC1=CC=CC=C1C(O)=O BSYNRYMUTXBXSQ-UHFFFAOYSA-N 0.000 description 1
- 108090001008 Avidin Proteins 0.000 description 1
- 208000012639 Balance disease Diseases 0.000 description 1
- 101000984722 Bos taurus Pancreatic trypsin inhibitor Proteins 0.000 description 1
- 208000014644 Brain disease Diseases 0.000 description 1
- 238000011357 CAR T-cell therapy Methods 0.000 description 1
- 229940122953 CD44 antagonist Drugs 0.000 description 1
- 108010021064 CTLA-4 Antigen Proteins 0.000 description 1
- 229940045513 CTLA4 antagonist Drugs 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 241000282832 Camelidae Species 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- 241001631457 Cannula Species 0.000 description 1
- 229940123097 Cell adhesion molecule antagonist Drugs 0.000 description 1
- 108010012236 Chemokines Proteins 0.000 description 1
- 102000019034 Chemokines Human genes 0.000 description 1
- 229920001287 Chondroitin sulfate Polymers 0.000 description 1
- 108020004705 Codon Proteins 0.000 description 1
- 206010010301 Confusion and disorientation Diseases 0.000 description 1
- MFYSYFVPBJMHGN-ZPOLXVRWSA-N Cortisone Chemical compound O=C1CC[C@]2(C)[C@H]3C(=O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 MFYSYFVPBJMHGN-ZPOLXVRWSA-N 0.000 description 1
- MFYSYFVPBJMHGN-UHFFFAOYSA-N Cortisone Natural products O=C1CCC2(C)C3C(=O)CC(C)(C(CC4)(O)C(=O)CO)C4C3CCC2=C1 MFYSYFVPBJMHGN-UHFFFAOYSA-N 0.000 description 1
- CMSMOCZEIVJLDB-UHFFFAOYSA-N Cyclophosphamide Chemical compound ClCCN(CCCl)P1(=O)NCCCO1 CMSMOCZEIVJLDB-UHFFFAOYSA-N 0.000 description 1
- 108090000695 Cytokines Proteins 0.000 description 1
- 102000004127 Cytokines Human genes 0.000 description 1
- 102100039498 Cytotoxic T-lymphocyte protein 4 Human genes 0.000 description 1
- 241000196324 Embryophyta Species 0.000 description 1
- 208000032274 Encephalopathy Diseases 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- 101000998556 Escherichia coli Colicin-E7 immunity protein Proteins 0.000 description 1
- 240000000731 Fagus sylvatica Species 0.000 description 1
- 235000010099 Fagus sylvatica Nutrition 0.000 description 1
- 238000012413 Fluorescence activated cell sorting analysis Methods 0.000 description 1
- 108090000079 Glucocorticoid Receptors Proteins 0.000 description 1
- 102100033417 Glucocorticoid receptor Human genes 0.000 description 1
- 229920002683 Glycosaminoglycan Polymers 0.000 description 1
- 206010019233 Headaches Diseases 0.000 description 1
- 101000823051 Homo sapiens Amyloid-beta precursor protein Proteins 0.000 description 1
- 101000599852 Homo sapiens Intercellular adhesion molecule 1 Proteins 0.000 description 1
- 108010054477 Immunoglobulin Fab Fragments Proteins 0.000 description 1
- 102000001706 Immunoglobulin Fab Fragments Human genes 0.000 description 1
- 102000012214 Immunoproteins Human genes 0.000 description 1
- 108010036650 Immunoproteins Proteins 0.000 description 1
- 229940123038 Integrin antagonist Drugs 0.000 description 1
- 208000032382 Ischaemic stroke Diseases 0.000 description 1
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 1
- 229930182816 L-glutamine Natural products 0.000 description 1
- 206010025327 Lymphopenia Diseases 0.000 description 1
- 208000026139 Memory disease Diseases 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- FQISKWAFAHGMGT-SGJOWKDISA-M Methylprednisolone sodium succinate Chemical compound [Na+].C([C@@]12C)=CC(=O)C=C1[C@@H](C)C[C@@H]1[C@@H]2[C@@H](O)C[C@]2(C)[C@@](O)(C(=O)COC(=O)CCC([O-])=O)CC[C@H]21 FQISKWAFAHGMGT-SGJOWKDISA-M 0.000 description 1
- 241000699670 Mus sp. Species 0.000 description 1
- 101710160107 Outer membrane protein A Proteins 0.000 description 1
- 102000000470 PDZ domains Human genes 0.000 description 1
- 108050008994 PDZ domains Proteins 0.000 description 1
- 208000002193 Pain Diseases 0.000 description 1
- 229930040373 Paraformaldehyde Natural products 0.000 description 1
- 229930182555 Penicillin Natural products 0.000 description 1
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 1
- 208000007660 Residual Neoplasm Diseases 0.000 description 1
- 229940123578 Selectin antagonist Drugs 0.000 description 1
- 108010003723 Single-Domain Antibodies Proteins 0.000 description 1
- 239000004809 Teflon Substances 0.000 description 1
- 229920006362 Teflon® Polymers 0.000 description 1
- 102100036407 Thioredoxin Human genes 0.000 description 1
- 108090000190 Thrombin Proteins 0.000 description 1
- 108020004566 Transfer RNA Proteins 0.000 description 1
- 208000027418 Wounds and injury Diseases 0.000 description 1
- 230000005856 abnormality Effects 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 230000001070 adhesive effect Effects 0.000 description 1
- VREFGVBLTWBCJP-UHFFFAOYSA-N alprazolam Chemical compound C12=CC(Cl)=CC=C2N2C(C)=NN=C2CN=C1C1=CC=CC=C1 VREFGVBLTWBCJP-UHFFFAOYSA-N 0.000 description 1
- 230000001668 ameliorated effect Effects 0.000 description 1
- 125000000539 amino acid group Chemical group 0.000 description 1
- DZHSAHHDTRWUTF-SIQRNXPUSA-N amyloid-beta polypeptide 42 Chemical compound C([C@@H](C(=O)N[C@@H](C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@H](C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCCCN)C(=O)NCC(=O)N[C@@H](C)C(=O)N[C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](C(C)C)C(=O)NCC(=O)NCC(=O)N[C@@H](C(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(O)=O)[C@@H](C)CC)C(C)C)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@@H](NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)CNC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)CC(O)=O)C(C)C)C(C)C)C1=CC=CC=C1 DZHSAHHDTRWUTF-SIQRNXPUSA-N 0.000 description 1
- 238000011230 antibody-based therapy Methods 0.000 description 1
- 230000009831 antigen interaction Effects 0.000 description 1
- PYMYPHUHKUWMLA-UHFFFAOYSA-N arabinose Natural products OCC(O)C(O)C(O)C=O PYMYPHUHKUWMLA-UHFFFAOYSA-N 0.000 description 1
- 229960002707 bendamustine Drugs 0.000 description 1
- YTKUWDBFDASYHO-UHFFFAOYSA-N bendamustine Chemical compound ClCCN(CCCl)C1=CC=C2N(C)C(CCCC(O)=O)=NC2=C1 YTKUWDBFDASYHO-UHFFFAOYSA-N 0.000 description 1
- SRBFZHDQGSBBOR-UHFFFAOYSA-N beta-D-Pyranose-Lyxose Natural products OC1COC(O)C(O)C1O SRBFZHDQGSBBOR-UHFFFAOYSA-N 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 239000000090 biomarker Substances 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 230000017531 blood circulation Effects 0.000 description 1
- 238000004820 blood count Methods 0.000 description 1
- 210000001185 bone marrow Anatomy 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 150000001768 cations Chemical class 0.000 description 1
- 239000006143 cell culture medium Substances 0.000 description 1
- 230000010261 cell growth Effects 0.000 description 1
- 210000000170 cell membrane Anatomy 0.000 description 1
- 230000003833 cell viability Effects 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 230000005754 cellular signaling Effects 0.000 description 1
- 208000015114 central nervous system disease Diseases 0.000 description 1
- 210000001638 cerebellum Anatomy 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- JCKYGMPEJWAADB-UHFFFAOYSA-N chlorambucil Chemical compound OC(=O)CCCC1=CC=C(N(CCCl)CCCl)C=C1 JCKYGMPEJWAADB-UHFFFAOYSA-N 0.000 description 1
- XTHPWXDJESJLNJ-UHFFFAOYSA-N chlorosulfonic acid Substances OS(Cl)(=O)=O XTHPWXDJESJLNJ-UHFFFAOYSA-N 0.000 description 1
- 229940059329 chondroitin sulfate Drugs 0.000 description 1
- 230000004087 circulation Effects 0.000 description 1
- 238000002648 combination therapy Methods 0.000 description 1
- 239000012141 concentrate Substances 0.000 description 1
- 238000012790 confirmation Methods 0.000 description 1
- 230000036461 convulsion Effects 0.000 description 1
- 238000012937 correction Methods 0.000 description 1
- 230000002596 correlated effect Effects 0.000 description 1
- 229960004544 cortisone Drugs 0.000 description 1
- 238000012258 culturing Methods 0.000 description 1
- 229960004397 cyclophosphamide Drugs 0.000 description 1
- 206010052015 cytokine release syndrome Diseases 0.000 description 1
- 230000009089 cytolysis Effects 0.000 description 1
- 230000001461 cytolytic effect Effects 0.000 description 1
- 238000007822 cytometric assay Methods 0.000 description 1
- 210000000805 cytoplasm Anatomy 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 230000034994 death Effects 0.000 description 1
- MSJQCBORNZDNDU-UHFFFAOYSA-D decasodium 3-methoxy-6-[2-(6-methoxy-4,5-disulfonatooxyoxan-3-yl)oxy-5-[5-(5-methoxy-3,4-disulfonatooxyoxan-2-yl)oxy-3,4-disulfonatooxyoxan-2-yl]oxy-4-sulfonatooxyoxan-3-yl]oxy-4,5-disulfonatooxyoxane-2-carboxylate Chemical compound [Na+].[Na+].[Na+].[Na+].[Na+].[Na+].[Na+].[Na+].[Na+].[Na+].COC1COC(OC2COC(OC3COC(OC4COC(OC)C(OS([O-])(=O)=O)C4OS([O-])(=O)=O)C(OC4OC(C(OC)C(OS([O-])(=O)=O)C4OS([O-])(=O)=O)C([O-])=O)C3OS([O-])(=O)=O)C(OS([O-])(=O)=O)C2OS([O-])(=O)=O)C(OS([O-])(=O)=O)C1OS([O-])(=O)=O MSJQCBORNZDNDU-UHFFFAOYSA-D 0.000 description 1
- 230000003111 delayed effect Effects 0.000 description 1
- 238000000432 density-gradient centrifugation Methods 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 229960003957 dexamethasone Drugs 0.000 description 1
- UREBDLICKHMUKA-CXSFZGCWSA-N dexamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-CXSFZGCWSA-N 0.000 description 1
- 230000001206 effect on leukocytes Effects 0.000 description 1
- 229940043249 elmiron Drugs 0.000 description 1
- 230000008497 endothelial barrier function Effects 0.000 description 1
- 230000008556 epithelial cell proliferation Effects 0.000 description 1
- 210000003743 erythrocyte Anatomy 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 229930003935 flavonoid Natural products 0.000 description 1
- 150000002215 flavonoids Chemical class 0.000 description 1
- 235000017173 flavonoids Nutrition 0.000 description 1
- 229960002714 fluticasone Drugs 0.000 description 1
- MGNNYOODZCAHBA-GQKYHHCASA-N fluticasone Chemical compound C1([C@@H](F)C2)=CC(=O)C=C[C@]1(C)[C@]1(F)[C@@H]2[C@@H]2C[C@@H](C)[C@@](C(=O)SCF)(O)[C@@]2(C)C[C@@H]1O MGNNYOODZCAHBA-GQKYHHCASA-N 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 210000003714 granulocyte Anatomy 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- 231100000869 headache Toxicity 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 230000002489 hematologic effect Effects 0.000 description 1
- 229920000669 heparin Polymers 0.000 description 1
- 229960002897 heparin Drugs 0.000 description 1
- 239000002628 heparin derivative Substances 0.000 description 1
- 102000043559 human ICAM1 Human genes 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-M hydrogensulfate Chemical compound OS([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-M 0.000 description 1
- 230000001900 immune effect Effects 0.000 description 1
- 238000010166 immunofluorescence Methods 0.000 description 1
- 229940072221 immunoglobulins Drugs 0.000 description 1
- 238000000099 in vitro assay Methods 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 230000002779 inactivation Effects 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 210000004969 inflammatory cell Anatomy 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 208000014674 injury Diseases 0.000 description 1
- 238000003780 insertion Methods 0.000 description 1
- 230000037431 insertion Effects 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 230000002427 irreversible effect Effects 0.000 description 1
- 231100000518 lethal Toxicity 0.000 description 1
- 230000001665 lethal effect Effects 0.000 description 1
- 208000032839 leukemia Diseases 0.000 description 1
- 229940063725 leukeran Drugs 0.000 description 1
- 229960005381 lifitegrast Drugs 0.000 description 1
- JFOZKMSJYSPYLN-QHCPKHFHSA-N lifitegrast Chemical compound CS(=O)(=O)C1=CC=CC(C[C@H](NC(=O)C=2C(=C3CCN(CC3=CC=2Cl)C(=O)C=2C=C3OC=CC3=CC=2)Cl)C(O)=O)=C1 JFOZKMSJYSPYLN-QHCPKHFHSA-N 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 230000033001 locomotion Effects 0.000 description 1
- 231100000863 loss of memory Toxicity 0.000 description 1
- 231100000897 loss of orientation Toxicity 0.000 description 1
- 210000001165 lymph node Anatomy 0.000 description 1
- 210000004698 lymphocyte Anatomy 0.000 description 1
- 231100001023 lymphopenia Toxicity 0.000 description 1
- 239000012139 lysis buffer Substances 0.000 description 1
- 210000004962 mammalian cell Anatomy 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 230000006984 memory degeneration Effects 0.000 description 1
- 208000023060 memory loss Diseases 0.000 description 1
- MMHHPKCJJIFLBQ-QFIPXVFZSA-N methyl (2s)-2-[(2,6-dichlorobenzoyl)amino]-3-[4-[6-(dimethylamino)-1-methyl-2,4-dioxoquinazolin-3-yl]phenyl]propanoate Chemical compound N([C@@H](CC=1C=CC(=CC=1)N1C(C2=CC(=CC=C2N(C)C1=O)N(C)C)=O)C(=O)OC)C(=O)C1=C(Cl)C=CC=C1Cl MMHHPKCJJIFLBQ-QFIPXVFZSA-N 0.000 description 1
- 229960004584 methylprednisolone Drugs 0.000 description 1
- 229940110254 minocin Drugs 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- 230000036225 muscular coordination Effects 0.000 description 1
- 210000000822 natural killer cell Anatomy 0.000 description 1
- 230000010807 negative regulation of binding Effects 0.000 description 1
- 210000005036 nerve Anatomy 0.000 description 1
- 230000002314 neuroinflammatory effect Effects 0.000 description 1
- 239000004090 neuroprotective agent Substances 0.000 description 1
- 210000000440 neutrophil Anatomy 0.000 description 1
- 230000009965 odorless effect Effects 0.000 description 1
- 238000011275 oncology therapy Methods 0.000 description 1
- 229940126701 oral medication Drugs 0.000 description 1
- 229920002866 paraformaldehyde Polymers 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 229940049954 penicillin Drugs 0.000 description 1
- 210000004976 peripheral blood cell Anatomy 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- 208000024335 physical disease Diseases 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 229960005205 prednisolone Drugs 0.000 description 1
- OIGNJSKKLXVSLS-VWUMJDOOSA-N prednisolone Chemical compound O=C1C=C[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 OIGNJSKKLXVSLS-VWUMJDOOSA-N 0.000 description 1
- 229960004618 prednisone Drugs 0.000 description 1
- XOFYZVNMUHMLCC-ZPOLXVRWSA-N prednisone Chemical compound O=C1C=C[C@]2(C)[C@H]3C(=O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 XOFYZVNMUHMLCC-ZPOLXVRWSA-N 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 230000006798 recombination Effects 0.000 description 1
- 238000005215 recombination Methods 0.000 description 1
- 208000037922 refractory disease Diseases 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- BPRHUIZQVSMCRT-VEUZHWNKSA-N rosuvastatin Chemical compound CC(C)C1=NC(N(C)S(C)(=O)=O)=NC(C=2C=CC(F)=CC=2)=C1\C=C\[C@@H](O)C[C@@H](O)CC(O)=O BPRHUIZQVSMCRT-VEUZHWNKSA-N 0.000 description 1
- 229960000672 rosuvastatin Drugs 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 239000002795 scorpion venom Substances 0.000 description 1
- 238000002864 sequence alignment Methods 0.000 description 1
- 230000011664 signaling Effects 0.000 description 1
- 229940054269 sodium pyruvate Drugs 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 238000011255 standard chemotherapy Methods 0.000 description 1
- 238000011272 standard treatment Methods 0.000 description 1
- 238000007619 statistical method Methods 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 229960005322 streptomycin Drugs 0.000 description 1
- 230000001180 sulfating effect Effects 0.000 description 1
- 230000019635 sulfation Effects 0.000 description 1
- 238000005670 sulfation reaction Methods 0.000 description 1
- YBBRCQOCSYXUOC-UHFFFAOYSA-N sulfuryl dichloride Chemical compound ClS(Cl)(=O)=O YBBRCQOCSYXUOC-UHFFFAOYSA-N 0.000 description 1
- 210000000225 synapse Anatomy 0.000 description 1
- 229940037128 systemic glucocorticoids Drugs 0.000 description 1
- 229940040944 tetracyclines Drugs 0.000 description 1
- 108060008226 thioredoxin Proteins 0.000 description 1
- 229940094937 thioredoxin Drugs 0.000 description 1
- 229960004072 thrombin Drugs 0.000 description 1
- 230000036964 tight binding Effects 0.000 description 1
- 239000003053 toxin Substances 0.000 description 1
- 231100000765 toxin Toxicity 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 238000011277 treatment modality Methods 0.000 description 1
- 229960005294 triamcinolone Drugs 0.000 description 1
- GFNANZIMVAIWHM-OBYCQNJPSA-N triamcinolone Chemical compound O=C1C=C[C@]2(C)[C@@]3(F)[C@@H](O)C[C@](C)([C@@]([C@H](O)C4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 GFNANZIMVAIWHM-OBYCQNJPSA-N 0.000 description 1
- 210000004881 tumor cell Anatomy 0.000 description 1
- 229940079023 tysabri Drugs 0.000 description 1
- 230000003827 upregulation Effects 0.000 description 1
- 239000013598 vector Substances 0.000 description 1
- 210000000264 venule Anatomy 0.000 description 1
- 230000035899 viability Effects 0.000 description 1
- 239000011782 vitamin Substances 0.000 description 1
- 229940088594 vitamin Drugs 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
- 150000004823 xylans Chemical class 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2809—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against the T-cell receptor (TcR)-CD3 complex
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/095—Sulfur, selenium, or tellurium compounds, e.g. thiols
- A61K31/10—Sulfides; Sulfoxides; Sulfones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/65—Tetracyclines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/715—Polysaccharides, i.e. having more than five saccharide radicals attached to each other by glycosidic linkages; Derivatives thereof, e.g. ethers, esters
- A61K31/737—Sulfated polysaccharides, e.g. chondroitin sulfate, dermatan sulfate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39533—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals
- A61K39/3955—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals against proteinaceous materials, e.g. enzymes, hormones, lymphokines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P39/00—General protective or antinoxious agents
- A61P39/02—Antidotes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5008—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2500/00—Screening for compounds of potential therapeutic value
- G01N2500/04—Screening involving studying the effect of compounds C directly on molecule A (e.g. C are potential ligands for a receptor A, or potential substrates for an enzyme A)
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Immunology (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Epidemiology (AREA)
- Molecular Biology (AREA)
- Biomedical Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Biochemistry (AREA)
- Neurosurgery (AREA)
- Neurology (AREA)
- Genetics & Genomics (AREA)
- Biophysics (AREA)
- Urology & Nephrology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Hematology (AREA)
- Microbiology (AREA)
- Toxicology (AREA)
- Dermatology (AREA)
- Pathology (AREA)
- Analytical Chemistry (AREA)
- Cell Biology (AREA)
- Endocrinology (AREA)
- Physics & Mathematics (AREA)
- General Physics & Mathematics (AREA)
- Food Science & Technology (AREA)
- Tropical Medicine & Parasitology (AREA)
- Mycology (AREA)
- Biotechnology (AREA)
Description
本発明は本質的に、患者における標的細胞に対するT細胞の再指向化を含む治療によって引き起こされる臨床的有害事象を予防する、および/または改善する、および/または処置する方法において使用するための、哺乳動物T細胞の哺乳動物内皮細胞への結合を減少させるかまたは阻害する化合物に関する。標的細胞に対するT細胞の再指向化を含む治療によって引き起こされる臨床的有害事象を有するかまたはそのリスクがある患者を処置する方法もまた企図される。さらに、本発明は、これらの化合物のいずれかまたはそれらの組み合わせ、CD3特異的結合ドメインまたはキメラ抗原受容体 (CAR) をコードする核酸、および該化合物または該組み合わせが、標的細胞に対するT細胞の再指向化を含む治療によって引き起こされる臨床的有害事象の予防または改善のために使用されることを示す封入されたラベルまたは添付文書を含むキットに関する。
2012年に、B細胞悪性腫瘍は、米国で新たに診断された癌のおよそ5%を占めた。急性リンパ性白血病 (ALL)、慢性リンパ性白血病 (CLL)、およびB細胞非ホジキンリンパ腫 (B-NHL) の年齢調整発生率はそれぞれ、1.6人、4.2人、および16.5人/男女100,000人/年であった(Howlader N, Noone AM, Krapcho M, Neyman N, Aminou R, Altekruse SF, Kosary CL, Ruhl J, Tatalovich Z, Cho H, Mariotto A, Eisner MP, Lewis DR, Chen HS, Feuer EJ, Cronin KA (eds). SEER Cancer Statistics Review, 1975-2009 (Vintage 2009 Populations), National Cancer Institute. Bethesda, MD、http://seer.cancer.gov/csr/1975_2009_pops09/、2011年11月SEERデータ提出に基づく、2012年にSEERウェブサイトに掲示された(非特許文献1))。繰り返される集中的な標準治療にもかかわらず、B細胞悪性腫瘍は、治療に対して不応性となるかまたは治療後に再発する可能性があり、治癒できないままである場合が多い。したがって、これらの患者集団における転帰を改善するための革新的な処置様式に対する高い医学的必要性が存在する。
(a) T細胞接着分子に結合することができ、
(b) T細胞接着分子の結合部位を遮断することができ、および/または
(c) T細胞接着分子の発現を阻害するかまたは減少させ、
かつ、患者における標的細胞に対するT細胞の再指向化を含む治療によって引き起こされる臨床的有害事象を予防する、および/または改善する、および/または処置する方法において使用するための、哺乳動物T細胞の哺乳動物内皮細胞への結合を減少させるかまたは阻害する化合物である。
(a) 内皮接着分子に結合することができ、
(b) 内皮接着分子の結合部位を遮断することができ、および/または
(c) 内皮接着分子の発現を阻害するかまたは減少させ、
かつ、患者における標的細胞に対するT細胞の再指向化を含む治療によって引き起こされる臨床的有害事象を予防する、および/または改善する、および/または処置する方法において使用するための、哺乳動物T細胞の哺乳動物内皮細胞への結合を減少させるかまたは阻害する化合物である。
(a) 該化合物を哺乳動物T細胞、哺乳動物内皮細胞、T細胞接着分子、および/または内皮接着分子と接触させること;ならびに
(b) 該化合物が、
(i) 哺乳動物T細胞の哺乳動物内皮細胞への結合を減少させるかもしくは阻害するかどうか;
(ii) T細胞接着分子に結合することができるかどうか、
(iii) T細胞接着分子の結合部位を遮断することができるかどうか、
(iv) T細胞接着分子の発現を阻害するかもしくは減少させるかどうか、
(v) 内皮接着分子に結合することができるかどうか、
(vi) 内皮接着分子の結合部位を遮断することができるかどうか、および/または
(vii) 内皮接着分子の発現を阻害するかもしくは減少させるかどうか、
を評価すること
を含む方法を提供する。
[本発明1001]
患者における標的細胞に対するT細胞の再指向化を含む治療によって引き起こされる臨床的有害事象を予防する、および/または改善する、および/または処置する方法において使用するための、哺乳動物T細胞の哺乳動物内皮細胞への結合を減少させるかまたは阻害する化合物。
[本発明1002]
患者における標的細胞に対するT細胞の再指向化を含む治療によって引き起こされる臨床的有害事象を予防する、および/または改善する、および/または処置する方法において使用するための、
(a) T細胞接着分子に結合することができ、
(b) T細胞接着分子の結合部位を遮断することができ、および/または
(c) T細胞接着分子の発現を阻害するかまたは減少させ、
かつ哺乳動物T細胞の哺乳動物内皮細胞への結合を減少させるかまたは阻害する化合物。
[本発明1003]
患者における標的細胞に対するT細胞の再指向化を含む治療によって引き起こされる臨床的有害事象を予防する、および/または改善する、および/または処置する方法において使用するための、
(a) 内皮接着分子に結合することができ、
(b) 内皮接着分子の結合部位を遮断することができ、および/または
(c) 内皮接着分子の発現を阻害するかまたは減少させ、
かつ哺乳動物T細胞の哺乳動物内皮細胞への結合を減少させるかまたは阻害する化合物。
[本発明1004]
患者における標的細胞に対するT細胞の再指向化を含む治療によって引き起こされる臨床的有害事象を予防する、および/または改善する、および/または処置する方法において使用するための化合物を同定する方法であって、
(a) 該化合物を哺乳動物T細胞、哺乳動物内皮細胞、T細胞接着分子、および/または内皮接着分子と接触させること;ならびに
(b) 該化合物が、
(i) 哺乳動物T細胞の哺乳動物内皮細胞への結合を減少させるかもしくは阻害するかどうか、
(ii) T細胞接着分子に結合することができるかどうか、
(iii) T細胞接着分子の結合部位を遮断することができるかどうか、
(iv) T細胞接着分子の発現を阻害するかもしくは減少させるかどうか、
(v) 内皮接着分子に結合することができるかどうか、
(vi) 内皮接着分子の結合部位を遮断することができるかどうか、および/または
(vii) 内皮接着分子の発現を阻害するかもしくは減少させるかどうか
を評価すること
を含む方法。
[本発明1005]
患者における標的細胞に対するT細胞の再指向化を含む治療が、CD3結合ドメインを含む、本発明1001〜1004のいずれかの使用のための化合物。
[本発明1006]
患者における標的細胞に対するT細胞の再指向化を含む治療が、キメラ抗原受容体 (CAR) を有する遺伝子操作されたT細胞を含む、本発明1001〜1005のいずれかの使用のための化合物。
[本発明1007]
患者における標的細胞に対するT細胞の再指向化を含む治療の最初の投薬、再曝露、および/または増加の前に/と同時に投与される、本発明1001〜1006のいずれかの使用のための化合物。
[本発明1008]
CD3結合ドメインと共に、前記本発明のいずれかにおいて定義または同定された化合物を含むキット。
[本発明1009]
キメラ抗原受容体 (CAR) をコードする核酸と共に、前記本発明のいずれかにおいて定義または同定された化合物を含むキット。
[本発明1010]
CD3結合ドメインと共に、前記本発明のいずれかにおいて定義または同定された化合物を含む薬学的組成物。
[本発明1011]
患者が、前記本発明のいずれかにおいて定義された化合物を含む治療に供される、患者における標的細胞に対するT細胞の再指向化の方法において使用するためのCD3結合ドメイン。
[本発明1012]
患者が、前記本発明のいずれかにおいて定義された化合物を含む治療に供される、患者における標的細胞に対するT細胞の再指向化の方法において使用するための、キメラ抗原受容体 (CAR) をコードする核酸。
[本発明1013]
臨床的有害事象が神経学的有害事象を含む、前記本発明のいずれかのもの。
[本発明1014]
神経学的有害事象が、(i) 失見当識/錯乱および/または喚語困難/失語症を含む認知障害、(ii) 発作、(iii) 運動性振戦、運動失調、構音障害、および筆記困難を含む、一部は (i) または (ii) の任意の前駆期として観察される小脳症状のうちの1つまたは複数である、前記本発明のいずれかのもの。
[本発明1015]
CD3結合ドメインが二重特異性単鎖抗体である、前記本発明のいずれかのもの。
[本発明1016]
二重特異性単鎖抗体がCD19 x CD3二重特異性単鎖抗体である、前記本発明のいずれかのもの。
[本発明1017]
キメラ抗原受容体 (CAR) がCD19結合ドメインを含む、前記本発明のいずれかのもの。
[本発明1018]
CD19 x CD3二重特異性単鎖抗体がMT103/AMG103である、前記本発明のいずれかのもの。
[本発明1019]
患者が、B/T細胞比が1:5未満であること、またはB細胞数が約50個未満のB細胞/μl末梢血であることを特徴とする、前記本発明のいずれかのもの。
[本発明1020]
化合物がPPS、ミノサイクリン、またはナタリズマブである、前記本発明のいずれかのもの。
[本発明1021]
患者における標的細胞に対するT細胞の再指向化を含む治療によって引き起こされる臨床的有害事象を予防する、改善する、および/または処置するための方法であって、前記本発明のいずれかにおいて定義された化合物の治療有効量を投与することを含む、方法。
[本発明1022]
哺乳動物T細胞が再指向化哺乳動物T細胞である、前記本発明のいずれかのもの。
[本発明1023]
哺乳動物内皮細胞が大血管または毛細血管から単離される、前記本発明のいずれかのもの。
[本発明1024]
ヒト臍帯静脈内皮細胞 (HUVEC) またはヒト脳微小血管内皮細胞 (HBMEC) より選択される、本発明1023の哺乳動物内皮細胞。
[本発明1025]
T細胞接着分子が、インテグリン(α4-インテグリン;αL-β2-インテグリン、αL-インテグリン、β7-インテグリンなど)、セレクチン(L-セレクチンなど)、CD44、CD162、および/またはSrcファミリーキナーゼより選択される、前記本発明のいずれかの化合物。
[本発明1026]
内皮接着分子が、セレクチン(E-セレクチンまたはP-セレクチンなど);細胞接着分子CAM(ICAM-1、MAdCAM、VCAM-1など)、および/またはPAR-1より選択される、前記本発明のいずれかの化合物。
[本発明1027]
患者が哺乳動物、好ましくは霊長類、最も好ましくはヒトである、前記本発明のいずれかのもの。
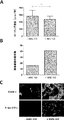
B-NHL (Bargou et al. Science. 2008; 321:974-7) およびB-前駆体ALL (Topp et al. J Clin Oncol. 2011; 29:2493-8) の両方において、ブリナツモマブの安全性および有効性を評価する様々な臨床試験が行われた。B-NHLでは、0.005 mg/m2/日ほどの低い用量を4週間にわたって持続静脈内 (civ) 注入により投与すると、末梢血中のBリンパ腫細胞が完全かつ持続的に除去された。0.015 mg/m2/日という用量レベルにおいて、部分寛解および完全寛解が最初に観察され、0.06 mg/m2/日という用量レベルで処置されたB-NHL患者の大部分が、実質的な腫瘍の退縮を経験した。ブリナツモマブはまた、この適応症において骨髄および肝臓から悪性B細胞を排除した。B-前駆体ALLでは、微小残存病変および再発性または難治性疾患の両方を有する患者は、0.015 mg/m2/日という用量レベルで4週間にわたってciv注入により処置された場合に、血液学的完全寛解を達成した。これらの試験により、一般的に二重特異性単鎖抗体形式の、および特にブリナツモマブの治療可能性が高いという概念の臨床的証明が確立され、そのさらなる開発がB-NHL、ALL、およびCLLにおいて検証された。B-NHLおよびB-前駆体ALLにおけるこれらの試験を通して、いくつかの薬力学的マーカーが評価された。選択された一般的特徴を以下に記載する:T細胞動力学は、用量レベルまたは循環B細胞の存在にかかわらず、非常に際立ったプロファイルを示した。それは、注入の開始後および任意の用量ステップ後の迅速な再分布によって特徴付けられ、すなわち最初の6〜12時間以内に循環T細胞は即座に消失し、それに続いて次の2〜7日間の間に再出現し、ここで初期の高いB細胞数はT細胞再出現の減速した動力学と相関した(図1A)。この過程は、絶対的血清濃度というよりは、むしろブリナツモマブの任意の顕著な用量変化によって誘発されるようであった。加えて、T細胞上のLFA-1に対する可溶性ICAM-1-Fc融合タンパク質の結合を解析することにより、T細胞接着性を処置第1週目を通して測定した。LFA-1高次構造は、注入の開始前の低親和性状態から、注入の開始後および任意の用量ステップ後の中等度の親和性状態に移行した;ICAM-1に対する結合親和性の増加は48時間以内にピークに達し、その後5日以内にベースラインに戻った(図1B)。この知見はT細胞再分布と一致し、再分布過程におけるブリナツモマブ誘導性の内皮に対するT細胞接着の概念を支持した。
本明細書で用いられる場合、「1つの (a)」、「1つの (an)」、および「その」という単数形は、文脈上明白に別の意味を示していない限り、複数の指示対象も含むことに留意しなければならない。したがって、例えば、「1つの試薬」への言及は、そのような種々の試薬の1つまたは複数を含み、「その方法」への言及は、本明細書に記載される方法に対して修正または置換され得る、当業者に公知の等価な段階および方法への言及を含む。
(a) T細胞接着分子に結合することができる、
(b) T細胞接着分子の結合部位を遮断することができる、および/または
(c) T細胞接着分子の発現を阻害するかまたは減少させる、
ことを特徴とする。
(a) 内皮接着分子に結合することができる、
(b) 内皮接着分子の結合部位を遮断することができる、および/または
(c) 内皮接着分子の発現を阻害するかまたは減少させる、
ことを特徴とする。
(a) 該化合物を哺乳動物T細胞、哺乳動物内皮細胞、T細胞接着分子、および/または内皮接着分子と接触させること;ならびに
(b) 該化合物が、
(i) 哺乳動物T細胞の哺乳動物内皮細胞への結合を減少させるかもしくは阻害するかどうか、
(ii) T細胞接着分子に結合することができるかどうか、
(iii) T細胞接着分子の結合部位を遮断することができるかどうか、
(iv) T細胞接着分子の発現を阻害するかもしくは減少させるかどうか、
(v) 内皮接着分子に結合することができるかどうか、
(vi) 内皮接着分子の結合部位を遮断することができるかどうか、および/または
(vii) 内皮接着分子の発現を阻害するかもしくは減少させるかどうか、
を評価すること
を含む方法に関する。
・血管外移動アッセイ(Rohnelt, Hoch et al. 1997、Ding, Xiong et al. 2000)
・固定化接着分子を用いる接着アッセイ(Gerli, Gresele et al. 2001、Valignat, Theodoly et al. 2013)
・静止条件下で内皮細胞およびT細胞を用いる接着アッセイ (Mobley and Shimizu 2001)
・フローサイトメトリーアッセイにおけるT細胞上の接着分子に対するそのような化合物の妨害 (Bucolo, Maltese et al. 2008)
Ding, Z., K. Xiong and T. B. Issekutz (2000). 「Regulation of chemokine-induced transendothelial migration of T lymphocytes by endothelial activation: differential effects on naive and memory T cells.」 J Leukoc Biol 67(6): 825-833.
Gerli, R., P. Gresele, O. Bistoni, C. Paolucci, L. Lanfrancone, S. Fiorucci, C. Muscat and V. Costantini (2001). 「Salicylates inhibit T cell adhesion on endothelium under nonstatic conditions: induction of L-selectin shedding by a tyrosine kinase-dependent mechanism.」 J Immunol 166(2): 832-840.
Mobley, J. L. and Y. Shimizu (2001). 「Measurement of cellular adhesion under static conditions.」 Curr Protoc Immunol Chapter 7: Unit 7 28.
Rohnelt, R. K., G. Hoch, Y. Reiss and B. Engelhardt (1997). 「Immunosurveillance modelled in vitro: naive and memory T cells spontaneously migrate across unstimulated microvascular endothelium.」 Int Immunol 9(3): 435-450.
Valignat, M. P., O. Theodoly, A. Gucciardi, N. Hogg and A. C. Lellouch (2013). 「T lymphocytes orient against the direction of fluid flow during LFA-1-mediated migration.」 Biophvs J 104(2): 322-331.
(b) VH(CD19)-VL(CD19)-VH(CD3)-VL(CD3)、
(c) VL(CD19)-VH(CD19)-VL(CD3)-VH(CD3)、
(d) VH(CD19)-VL(CD19)-VL(CD3)-VH(CD3)
(e) VL(CD3)-VH(CD3)-VH(CD19)-VL(CD19)
(f) VH(CD3)-VL(CD3)-VH(CD19)-VL(CD19)
(g) VL(CD3)-VH(CD3)-VL(CD19)-VH(CD19)、または
(h) VH(CD3)-VL(CD3)-VL(CD19)-VH(CD19)
などの他のドメイン配置のCD19xCD3二重特異性単鎖抗体を用いて実施することができることもまた想定される。
(a) SEQ ID NO: 24
、より好ましくはSEQ ID NO: 11
のCD3 CDR-H1、SEQ ID NO: 12
のCD3 CDR-H2、およびSEQ ID NO: 13
のCD3 CDR-H3として示される重鎖の抗CD3 CDR;ならびに/または、
(b) SEQ ID NO: 14
のCD3 CDR-L1、SEQ ID NO: 15
のCD3 CDR-L2、およびSEQ ID NO: 16
のCD3 CDR-L3として示される軽鎖の抗CD3 CDR;ならびに/または、
(c) SEQ ID NO: 25
、より好ましくはSEQ ID NO: 17
のCD19 CDR-H1、SEQ ID NO: 18
のCD19 CDR-H2、およびSEQ ID NO: 19
のCD19 CDR-H3として示される重鎖の抗CD19 CDR;ならびに/または、
(d) SEQ ID NO: 20
のCD19 CDR-L1、SEQ ID NO: 21
のCD19 CDR-L2、およびSEQ ID NO: 22
のCD19 CDR-L3として示さる軽鎖の抗CD19 CDR
を含む。
(a) SEQ ID NO: 3に示されるCD19可変重鎖(ヌクレオチド配列はSEQ ID NO: 4に示される)、および/または
(b) SEQ ID NO: 5に示されるCD19可変軽鎖(ヌクレオチド配列はSEQ ID NO: 6に示される)、および/または
(c) SEQ ID NO: 7に示されるCD3可変重鎖(ヌクレオチド配列はSEQ ID NO: 8に示される)、および/または
(d) SEQ ID NO: 9に示されるCD3可変軽鎖(ヌクレオチド配列はSEQ ID NO: 10に示される)
を含むことが好ましい。
(a) SEQ ID NO: 1に示されるアミノ酸配列、
(b) SEQ ID NO: 2に示される核酸配列によってコードされるアミノ酸配列、
(c) (b) の核酸配列と少なくとも70%、80%、90%、95%、または99%の同一性を有する核酸配列によってコードされるアミノ酸配列であって、CD3およびCD19に特異的に結合することができるアミノ酸配列、ならびに
(d) (b) のヌクレオチド配列に対して遺伝暗号の結果として縮重している核酸配列によってコードされるアミノ酸配列であって、CD3およびCD19に特異的に結合することができるアミノ酸配列、
からなる群より選択されるアミノ酸配列を含むこともまた好ましい。
(a) ヒト患者における悪性のCD19陽性細胞、好ましくはリンパ球、さらにより好ましくはB細胞を処置するため、および/もしくは
(b) ヒト患者にCD19xCD3二重特異性単鎖抗体を投与するための
方法に関し、この場合、抗接着特性を有する化合物は、該CD19xCD3二重特異性単鎖抗体によって引き起こされるCNS AEの予防または改善のために、該CD19xCD3二重特異性単鎖抗体によるヒト患者の処置の前に、それと同時に、またはその後に投与されるべきである。
新たに単離されたヒトT細胞の表面上のCD3、CD4、CD8、CD11a、CD49d、CD162 (PSGL-1)、CD69、CD25、およびHLA-DRの発現を、フローサイトメトリーにより決定した。CD3陽性細胞は、3回の独立した測定の全イベントに占める平均比率 ± SDとして表される。CD4、CD8、CD11a、CD49d、CD162、CD69、CD25、およびHLA-DR陽性細胞は、3回の独立した測定のCD3陽性細胞に占める平均比率 ± SDとして表される。
ブリナツモマブとPPSの同時薬物療法の投与計画
第1相臨床試験において、3名の患者を5μg/m2/日の初期用量のブリナツモマブで1週間処置し、その後60μg/m2/日まで用量を増加して、さらに3〜7週間処置した。併用PPSは、ブリナツモマブの注入開始および用量増加の3時間 ± 30分前に100 mgボーラスiv注入として投与し、その後ブリナツモマブの注入開始および用量増加後の48時間にわたり300 mg/日で灌流した。
患者109-036は、コーカサス人男性、62歳、体重96.8 kg、伸長178 cmであり、濾胞性リンパ腫グレードI/IIを示した。以前の治療は、CHOP(02/12〜03/04)、Dexa BEAM (03/05)、シクロホスファミド (03/08)、および放射線療法と、その後の自己幹細胞移植 (03/08) を含んだ。該患者は、ブリナツモマブのciv注入の57日後に完全寛解 (CR) を達成した。この患者は、B:T細胞比が低いためにCNS AEを発症するリスクが高かったが(PCT/EP2010/066207を参照されたい)、CNS AEに起因する処置の中断は必要なかった。
患者109-040は、コーカサス人男性、51歳、体重94.0 kg、伸長180 cmであり、リンパ形質細胞性 (Lymphoplasmocytic) リンパ腫(モルブス・ワルデンストレーム (Morbus Waldenstrom))を示した。以前の治療は、CVP(04/12〜05/03)、Leukeran(05/10〜05/12)、リツキシマブ(06/05〜06/07)、R-CHOP(06/07〜06/10)、Dexa BEAM (06/10)、BEAM (06/12)、および放射線療法と、その後の自己幹細胞移植 (06/12) を含んだ。さらなる事前の治療は、リツキシマブ + ベンダムスチン(09/04〜09/12)およびリツキシマブ(09/04〜09/12)を含んだ。該患者は、ブリナツモマブのciv注入の30日後に安定疾患 (SD) を達成した。この患者は、B:T細胞比が低いためにCNS AEを発症するリスクが高かったが(PCT/EP2010/066207を参照されたい)、CNS AEに起因する処置の中断は必要なかった。
患者109-042は、コーカサス人女性、49歳、体重92.0 kg、伸長169 cmであり、濾胞性リンパ腫グレードI/IIを示した。以前の治療は、R-CHOP(09/11〜10/02)およびリツキシマブ(10/03〜10/04)を含んだ。該患者は、ブリナツモマブのciv注入の56日後に完全寛解 (CR) を達成した。この患者は、B:T細胞比が低いためにCNS AEを発症するリスクが高かったが(PCT/EP2010/066207を参照されたい)、CNS AEに起因する処置の中断は必要なかった。
内皮細胞の培養
ヒト脳微小血管内皮細胞 (HBMEC)(#1000、Sciencell Research Laboratories)またはヒト臍帯静脈内皮細胞 (HUVEC)(#C-12200、Promocell)を、内皮細胞モデルとして使用した。凍結保存された継代1代目のHBMEC(> 5x105個細胞/ml)を、最初に、製造業者の説明書に従って、フィブロネクチンコーティングされたNunclon処理75 cm2細胞培養フラスコ(#156499、Nunc)で、Heraeus Cytoperm 2 (Thermo Scientific) 内で37℃および5% CO2にて培養した。HBMECの継代培養は、HEPES緩衝平衡塩類溶液(#C-40000、Promocell)、トリプシン-EDTA溶液 (0.04% / 0.03%)(#C-41000、Promocell)、およびトリプシン中和溶液(TNS、#C-41100、Promocell)からなるDetach Kit(#C-41200、Promocell)を用いて行った。簡潔に説明すると、HBMEC層から培地を吸引し、細胞を2 mlのHEPES緩衝平衡塩類溶液で洗浄した。2 mlのトリプシン-EDTA溶液を添加して、室温で1〜5分間置くことにより、HBMECをフラスコの底から剥離した。トリプシン-EDTA溶液の不活化は、2 mlのトリプシン中和溶液を細胞懸濁液に添加することによって行った。細胞をHeraeus Megafuge 40 (Thermo Scientific) で300 gにて4分間遠心分離し、ゼラチンコーティングされた75 cm2細胞培養フラスコ(#L7230、Biochrom)当たり5x105個細胞という細胞密度で播種した。ローリングおよび接着実験のためのHBMECは、Nu-Serum IV (10%)(#355505、BD Biosciences)、透析済みFBS (10%)(#SZ0115、Biochrom)、MEM-ビタミン (1 %)(#K0373、Biochrom)、L-グルタミン (1 %)(#K0283、Biochrom)、ピルビン酸ナトリウム (1 %)(#L0473、Biochrom)、ヘパリン (10 U/ml)(#L6510、Biochrom)、および上皮細胞増殖因子ECGS (30μg/ml)(#02-102、Millipore)を補充したRPMI 1640培地(#FG1215、Biochrom)中で培養した。HUVECの培養は、ゼラチンコーティングされた75 cm2細胞培養フラスコを用いて、透析済みFBS (10%)(#SZ0115、Biochrom)を補充した内皮細胞増殖培地(#C-22010、Promocell)中で行った。HUVECの継代培養はDetach Kit(#C-40000、Promocell)を用いて行い、細胞は75 cm2細胞培養フラスコ当たり4.0〜7.5x105個細胞という細胞密度で播種した。
血液からのヒトPBMCの単離は、他所に記載されているように、改良密度勾配遠心分離によって行った。簡潔に説明すると、新たに採取しヘパリン処理した15〜20 mlの血液を、Biocoll(#L6115、Biochrom)含有Leukosepチューブ(#227290、Greiner bio-one)に移し、Hettich Rotanta 460 RS Type 5606 (Hettich Laborapparate) で1066 gにて15分間遠心分離した。血漿画分を除去した後、PBMC含有相を新しいチューブに移し、FACS緩衝液(D-PBS #L1820、5% FBS #SO115、Biochrom)で2回洗浄した。溶解緩衝液(8.29 g/l NH4Cl、1.00 g/l KHC03、0.037 g/l EDTA)を用いて、赤血球溶解を室温で5分間行った。それに続く非標識 (untouched) T細胞の精製には、ヒトPan T細胞単離キットII(#130-091-156、Miltenyi Biotec)を製造業者の説明書に従って使用した。
単離されたT細胞を、フローサイトメトリーにより、接着分子および活性化マーカーの表面発現について特徴付けた。FACS染色および洗浄の手順は、冷FACS緩衝液(5% FBSを含むD-PBS)中で4℃で行った。表面に露出した接着分子を解析するため、3x105個のT細胞を、100μlのFACS緩衝液中で、抗CD11a-APC (1:10)(#550852、BD Biosciences)、抗CD49d-PE (1:10)(#560972、BD Biosciences)、および抗CD162-PerCP-eFluor710 (1:20)(#46-1629、eBioscience)で染色した。T細胞の活性化の可能性は、3x105個のT細胞を、抗CD69-PE (1:40)(#555531、BD Biosciences)、抗CD25-APC (1:40)(#340907、BD Biosciences)、および抗HLA-DR-FITC (1:40)(#555811、BD Biosciences)で染色することによりモニターした。さらに、T細胞亜集団を特徴付けるために、抗CD3-V450 (1:40)(#560365、BD Biosciences)、抗CD4-APC-Cy7 (1:40)(#341115、BD Biosciences)、および抗CD8-V500 (1:40)(#560774、BD Biosciences)を両方の染色に含めた。3x105個のT細胞のDAPI (1 μg/ml)(#A1001.0010、Applichem)による別々の染色により、細胞生存度のモニタリングを可能にした。30分間の染色後に、細胞をFACS緩衝液で2回洗浄した。染色された試料をFACSCanto II装置 (BD Biosciences) でのFACS解析に供し、FACSDivaソフトウェア (BD Biosciences) を用いて統計解析を行った。10,000イベントを記録し、CD4、CD8、CD11a、CD49d、CD162、CD69、CD25、およびHLA-DR陽性細胞を、CD3陽性細胞に占める割合として表した。
流動条件下での内皮細胞の培養のため、ならびに内皮細胞上でヒトT細胞の接着およびローリングアッセイを行うために、ibidi Pump System(#10902、ibidi)を使用した。このシステムはibidi Pump(#10905、ibidi)およびibidi Fluidic Unit(#10903、ibidi)からなり、これらは既定のチャネル高を有する付属のスライド内で培地の一方向流動を生じるように共に働く。このシステムは、ibidi Pump Controlソフトウェア(#10908、ノート型パソコン + ソフトウェア、ibidi)によって制御される。流動条件下でHBMECまたはHUVECを培養するために、HBMECまたはHUVECを、製造業者の説明書に従って、2.5x106個細胞/mlの細胞密度でそれぞれマイクロスライドI 0.4 Luer Collagen IV(#80172、ibidi)またはマイクロスライドI 0.4 Luer ibiTreat(#80176、ibidi)に播種し、灌流セット「黄色/緑色」(#10964、ibidi)を用いて、それぞれ5または10 dyn/cm2の壁剪断応力下で48時間培養した。単一の流体ユニットを用いて2枚以上のマイクロスライドI 0.4 Luerを培養するために、最大4枚までのマイクロスライドをマイクロスライド用のSerial Connector(#10830、ibidi)と互いに接続した。
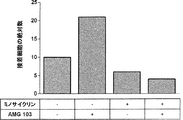
AMG 103媒介性の接着作用をさらに妨害するために、ローリングおよび接着実験の前に、T細胞を、抗白血球接着を潜在的に媒介する化合物と共にプレインキュベートした。よって、Tysabri(ナタリズマブ、20 mg/ml溶液、Elan Pharma International Ltd.)またはMinocin(ミノサイクリン、100 mg/バイアル、Triax Pharmaceuticals)をT細胞懸濁液に添加し、37℃でインキュベートした。
上記のような新たに単離したヒトT細胞および流動培養したHBMECまたはHUVECを用いて、既定の流体力学的流動条件下での実験を行い、倒立顕微鏡Ti-E(#MEA53100、Nikon)、デジタルカメラOrca Flash 2.8(#C-11440-10C、Hamamatsu)、NIS-Elements ARソフトウェア バージョン3.22.00および4.10.03(#MQS31200および#MQS31100、Nikon)、ibidi Pump System(#10902、ibidi)、細胞培養インキュベーターGalaxy 14S(#C014S-120-0000、Eppendorf)、Heating System 8(#10925、ibidi)、ならびにC02ガスインキュベーションユニットI(#10920、ibidi)からなる顕微鏡システムを用いて解析した。顕微鏡Ti-Eには、同焦点変動の補正を可能にするTI-ND6-PFS Perfect Focus System(#MEP59390、Nikon)を装備した。ローリングおよび接着実験は、10 x対物レンズ(CF1 PlanFluor DL-10 X位相、#MRH20101、Nikon)でモニターした。Heating System 8およびC02ガスインキュベーションユニットIは、任意の実験の少なくとも3時間前に作動させ、ステージトップインキュベーターを37℃および5% CO2になるよう予め温めた。RPMI 1640培地(#FG1215、Biochrom)もまた、37℃および5% CO2で予め温めた。ローリングおよび接着実験のため、流動培養したHBMECを伴うマイクロスライドI 0.4 Collagen IV、または流動培養したHUVECを伴うマイクロスライドI 0.4 ibiTreatを灌流セットから外し、PPS (200μg/ml) を含むかまたはPPSを含まない予め温めたRPMI 1640培地でリンスし、顕微鏡下のステージトップインキュベーターのマイクロスライド差し込み口に設置した。6x106個の新たに単離されたヒトT細胞を、PC Vチューブ(#347759、Nunc)中で300 gにて4分間遠心分離した。T細胞を、PPS (200μg/ml) を含むかまたはPPSを含まないRPMI 1640培地中に、最終T細胞密度が1x106個細胞/mlとなるように再懸濁した。これらの細胞は、AMG 103 (10 ng/ml) を細胞懸濁液に添加するかもしくは添加せずにローリング実験に直接使用するか、またはPC Vチューブ中でAMG 103の存在下もしくは非存在下において37℃で45分間プレインキュベートした。このように調製されたT細胞懸濁液を、流体ユニットおよびマイクロスライドの両方に接続した灌流セット「白色」(#10963、ibidi)に満たした。1 dyn/cm2の剪断応力におけるHBMECまたはHUVEC上でのT細胞のローリングおよび接着実験について、2つの異なる設定を適用した:
1. 45秒間の内皮細胞上でのT細胞のローリング(短期条件)
2. 45〜120分間の内皮細胞上でのT細胞のローリング(長期条件、流体ユニットを細胞培養インキュベーター内に配置)
順にNIS-Elementsソフトウェア3.22.00によって制御されるデジタルカメラOrca Flash 2.8を用いて画像を取得することにより、内皮細胞とのT細胞相互作用をモニターした。個々の時点について微速度撮影の45秒の獲得(遅延なし)を行い、結果として1920x1440の解像度で最大45フレーム/秒を得た。このように記録された45秒間の画像シーケンスを、NIS-Elements AR 4.10.03の自動追跡モジュールに供するか、またはNIS-Elements AR 3.22.00を用いた手動追跡に供した。作成された追跡データをMicrosoft Excelにエクスポートし、各追跡対象の平均進行方位 (heading)、平均速度、および経路長などのパラメータにフィルターをかけることによって、さらに解析した。その後、フィルター処理した全細胞の平均ローリング速度 ± 標準偏差を算出した。手動追跡を用いた場合には、10〜40個のT細胞を選択し、手動で追跡し、平均ローリング速度 ± 標準偏差を決定した。
流動条件下におけるHBMECまたはHUVEC上でのT細胞のローリングおよび接着後、150μlの4%パラホルムアルデヒド溶液(#P-6148、Sigma-Aldrich)を用いて、内皮細胞を4℃で30分間固定した。マイクロスライドを150μlのD-PBSでリンスし、免疫蛍光染色に供した。HBMECを最初に、150μlのアビジンブロッキング試薬(#PHA-70871、試薬1、Dianova)で室温にて10分間ブロッキングし、150μlのD-PBSで洗浄し、その後150μlのビオチンブロッキング試薬(#PHA-70871、試薬2、Dianova)と共にインキュベートした。その後の染色手順はすべて、5% FBSを含む150μlのD-PBS中で室温にて暗下で行い、洗浄段階は150μlのD-PBS中で行った。マイクロスライドを5μg/mlポリクローナルウサギ抗ヒトVCAM-1(#106777、abcam)と共に1時間インキュベートした。洗浄後、20μg/mlヤギ抗ウサギIgG-DyLight350を添加して1時間おき、その後洗浄し、15μg/mlマウス抗ヒトP-セレクチンIgG1(#BBA30、R&D Systems)と共に2時間インキュベートした。洗浄後、ヤギ抗マウスIgG-Alexa488 (1:100)(#A10680、Invitrogen)を添加して1時間おいた。ICAM-1染色は、10 μg/mlポリクローナルウサギ抗ヒトICAM-1ビオチン(#AB7815、abcam)を用いて1時間行い、その後洗浄し、ストレプトアビジン-Cy3 (1:100)(#016-160-084、Dianova)と共に1時間インキュベートした。PFA固定HUVEC上のICAM-1およびP-セレクチンの細胞表面染色は、HBMECについて記載される通りに行った。最後に、HBMECまたはHUVECを、UV光、およびPH-2位相モジュール(#MEH41200、Nikon)を備えたCFI Plan Apochromat DM 20 x λ対物レンズ(#MRD30205、Nikon)を用いる顕微鏡解析に供した。VCAM-1染色はCFL EPI-FL Filter Block UV-2A(#MBE41200、Nikon)でモニターし、P-セレクチン染色はCFL EPI-FL Filter Block GFP-B(#MBE44740、Nikon)でモニターし、ICAM-1染色は、EPI-FL Filter Block Cy3(#MXU96213、Nikon)でモニターした。画像取得は、NIS-Elementsソフトウェアを用いて行った。
いくつのグループのデータを比較するのかに応じて、独立t検定、またはチューキーの事後検定と組み合わせた一元配置ANOVAを用いて、Prism (GraphPad Software) で統計学的有意性を解析した。P値 < 0.05を統計学的に有意と見なした。
ヒトでの使用のためのブリナツモマブ処置との静脈内PPS同時薬物療法の投与スケジュール
患者は、ブリナツモマブの注入開始および任意の用量ステップの3時間 ± 30分前に、PPSの100 mgボーラス注入を受ける。ボーラス注入の直後から、PPSの静脈内投与をperfusorにより300 mg/日で72時間にわたって継続する。
患者は、ブリナツモマブの注入開始および任意の用量ステップの7日前に開始して、1日当たり300 mg(例えば、3x100 mg)を3回として、900 mg PPSの経口投与を毎日受ける。900 mg PPSの毎日の経口投与は、ブリナツモマブの注入開始および任意の用量ステップ後の72時間にわたって継続する。
患者は、ブリナツモマブの注入開始および任意の用量ステップの48時間、24時間、および3時間 ± 30分前、ならびに24時間、48時間、および72時間後に、短期静脈内注入により10 mg/kgミノサイクリンを受ける。
患者は、ブリナツモマブの注入開始および任意の用量ステップの48時間、24時間、および3時間 ± 30分前、ならびに24時間、48時間、および72時間後に、700 mgミノサイクリンの経口投与を1日に1回受ける。
患者は、ブリナツモマブの注入開始および任意の用量ステップの24時間前に、短期静脈内注入により300 mgナタリズマブを受ける。
組換えタンパク質のコーティング
組換えタンパク質(rhICAM-1 #ADP4-050、rhVCAM-1 #ADP5-050、またはrhP-セレクチン #ADP3-050、R&D Systems)を、製造業者の説明書に従ってddH20中に溶解した。ローリング実験の前に、組換えタンパク質を、Ca2+およびMg2+を含むダルベッコPBS(#L1815、Biochrom)で希釈し、マイクロスライドVI 0.4 Luer ibiTreat(#80606、ibidi)上に4℃で一晩コーティングした。使用前に、スライドをダルベッコPBSで3回洗浄し、記載がある場合には、PBS中の20% FBS(#10270、Gibco)で室温にて2時間ブロッキングした。ブロッキング溶液を、補充物を含まないRPMI 1640培地(#FG1215、Biochrom)と交換した。
血液からのヒト末梢血単核細胞 (PBMC) およびT細胞の単離および特徴付けは、実施例2(p.48、1〜31)に記載された通りに行った。
AMG 103誘導性の接着効果を妨害するため、T細胞を、T細胞受容体複合体からのシグナル伝達を特異的に遮断するSrcキナーゼ阻害剤と共にプレインキュベートした。この目的のために、阻害剤PP2(#529576、Merck、15μΜ)またはその媒体対照DMSO(#D2650、Sigma-Aldrich)をT細胞懸濁液(RPMI 1640培地中の1x106個細胞/ml)に添加し、次いで37℃および5% CO2で40分間インキュベートしてから、10 ng/mlブリナツモマブ (AMG 103) を添加した(t = 0分)。
上記のような新たに単離したヒトT細胞またはJurkat E6.1 T細胞、および様々な組換えタンパク質をコーティングしたマイクロスライドVI 0.4 Luer ibiTreat(#80606、ibidi)を用いて、既定の流体力学的流動条件下での実験を行った。アッセイ設定は、実施例2(p. 49、23〜37)に詳細に記載された。T細胞ローリング実験は、1.1 dyn/cm2の剪断応力で行った。組換えタンパク質とのT細胞相互作用を上記のように記録し、実施例2(p. 50、23〜30)に詳細に記載された通りにデータを解析した。
いくつのグループのデータを比較するのかに応じて、独立t検定、またはチューキーの事後検定と組み合わせた一元配置ANOVAを用いて、Prism (GraphPad Software) で統計学的有意性を解析した。P値 < 0.05を統計学的に有意と見なした。値はすべて、平均値 ± SDとして示す。
Claims (12)
- 患者における、標的細胞に対するT細胞の再指向化を含む治療によって引き起こされる臨床的有害事象を予防する、および/または改善する、および/または処置する方法において使用するための組成物であって、該治療がCD19 x CD3二重特異性単鎖抗体を使用するものであり、該CD19 x CD3二重特異性単鎖抗体がMT103であり、該組成物が、哺乳動物T細胞の哺乳動物内皮細胞への結合を減少させるかまたは阻害する非グルココルチコイド系化合物を含み、非グルココルチコイド系化合物がPPSまたはミノサイクリンである、前記組成物。
- 組成物が、患者における、標的細胞に対するT細胞の再指向化を含む治療の最初の投薬、再曝露、および/または増加の前に/と同時に投与するためのものであり、該治療がCD19 x CD3二重特異性単鎖抗体を使用するものであり、該CD19 x CD3二重特異性単鎖抗体がMT103である、請求項1記載の組成物。
- 臨床的有害事象が神経学的有害事象を含む、請求項1または2に記載の組成物。
- 神経学的有害事象が、(i) 失見当識/錯乱および/または喚語困難/失語症を含む認知障害、(ii) 発作、(iii) 運動性振戦、運動失調、構音障害、および筆記困難を含む、一部は (i) または (ii) の任意の前駆期として観察される小脳症状のうちの1つまたは複数である、請求項3に記載の組成物。
- 患者が、B/T細胞比が1:5未満であること、またはB細胞数が約50個未満のB細胞/μl末梢血であることを特徴とする、請求項1〜4のいずれか一項に記載の組成物。
- 哺乳動物T細胞が再指向化哺乳動物T細胞である、請求項1〜5のいずれか一項に記載の組成物。
- 哺乳動物内皮細胞が大血管または毛細血管から単離される、請求項1〜6のいずれか一項に記載の組成物。
- 哺乳動物内皮細胞がヒト臍帯静脈内皮細胞 (HUVEC) またはヒト脳微小血管内皮細胞 (HBMEC) より選択される、請求項1〜7のいずれか一項に記載の組成物。
- 患者が哺乳動物、好ましくは霊長類、最も好ましくはヒトである、請求項1〜8のいずれか一項に記載の組成物。
- 患者における、標的細胞に対するT細胞の再指向化を含む治療によって引き起こされる臨床的有害事象を予防する、および/または改善する、および/または処置する方法において使用するための、MT103と共に請求項1〜9のいずれか一項に記載の組成物を含むキットであって、該治療がCD19 x CD3二重特異性単鎖抗体を使用するものであり、該CD19 x CD3二重特異性単鎖抗体がMT103である、キット。
- MT103をさらに含む薬学的組成物である、請求項1〜9のいずれか一項に記載の組成物。
- 患者における、標的細胞に対するT細胞の再指向化を含む治療によって引き起こされる臨床的有害事象を予防する、改善する、および/または処置するための医薬の製造における、請求項1〜9のいずれか一項に記載の組成物の使用であって、該治療がCD19 x CD3二重特異性単鎖抗体を使用するものであり、該CD19 x CD3二重特異性単鎖抗体がMT103である、使用。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2019098999A JP6933684B2 (ja) | 2013-02-08 | 2019-05-28 | Cd3特異的結合ドメインによって引き起こされる潜在的有害事象を緩和するための抗白血球接着 |
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201361762718P | 2013-02-08 | 2013-02-08 | |
| US61/762,718 | 2013-02-08 | ||
| US201361811526P | 2013-04-12 | 2013-04-12 | |
| US61/811,526 | 2013-04-12 | ||
| PCT/EP2014/052406 WO2014122251A2 (en) | 2013-02-08 | 2014-02-07 | Anti-leukocyte adhesion for the mitigation of potential adverse events caused by cd3-specific binding domains |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019098999A Division JP6933684B2 (ja) | 2013-02-08 | 2019-05-28 | Cd3特異的結合ドメインによって引き起こされる潜在的有害事象を緩和するための抗白血球接着 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2016514090A JP2016514090A (ja) | 2016-05-19 |
| JP6567425B2 true JP6567425B2 (ja) | 2019-08-28 |
Family
ID=50231117
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015556506A Active JP6567425B2 (ja) | 2013-02-08 | 2014-02-07 | Cd3特異的結合ドメインによって引き起こされる潜在的有害事象を緩和するための抗白血球接着 |
| JP2019098999A Active JP6933684B2 (ja) | 2013-02-08 | 2019-05-28 | Cd3特異的結合ドメインによって引き起こされる潜在的有害事象を緩和するための抗白血球接着 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019098999A Active JP6933684B2 (ja) | 2013-02-08 | 2019-05-28 | Cd3特異的結合ドメインによって引き起こされる潜在的有害事象を緩和するための抗白血球接着 |
Country Status (13)
| Country | Link |
|---|---|
| US (2) | US9688760B2 (ja) |
| EP (2) | EP3760210A1 (ja) |
| JP (2) | JP6567425B2 (ja) |
| AR (1) | AR094740A1 (ja) |
| AU (2) | AU2014214020B2 (ja) |
| CA (1) | CA2898032C (ja) |
| ES (1) | ES2811764T3 (ja) |
| HK (1) | HK1216996A1 (ja) |
| JO (1) | JO3529B1 (ja) |
| MX (2) | MX2019012421A (ja) |
| TW (2) | TW201929865A (ja) |
| UY (1) | UY35313A (ja) |
| WO (1) | WO2014122251A2 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2019178142A (ja) * | 2013-02-08 | 2019-10-17 | アムゲン リサーチ (ミュンヘン) ゲーエムベーハーAMGEN Research(Munich)GmbH | Cd3特異的結合ドメインによって引き起こされる潜在的有害事象を緩和するための抗白血球接着 |
Families Citing this family (50)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN107303387A (zh) * | 2011-04-28 | 2017-10-31 | 安进研发(慕尼黑)股份有限公司 | 用于给处于潜在不良反应的风险的患者施用CD19xCD3双特异性抗体的给药方案 |
| CN107586340B (zh) | 2011-08-23 | 2022-01-21 | 罗切格利卡特公司 | 对t细胞活化性抗原和肿瘤抗原特异性的双特异性抗体及使用方法 |
| JP6444874B2 (ja) | 2012-10-08 | 2018-12-26 | ロシュ グリクアート アーゲー | 2つのFabフラグメントを含むFc不含抗体および使用方法 |
| US9486475B2 (en) * | 2013-02-08 | 2016-11-08 | Amgen Research (Munich) Gmbh | PPS for the prevention of potential adverse effects caused by CD3 specific binding domains |
| RU2015140915A (ru) | 2013-02-26 | 2017-04-03 | Роше Гликарт Аг | Биспецифические антигенсвязывающие молекулы, активирующие т-клетки |
| WO2014131712A1 (en) | 2013-02-26 | 2014-09-04 | Roche Glycart Ag | Bispecific t cell activating antigen binding molecules |
| US10101247B2 (en) * | 2013-07-19 | 2018-10-16 | Rarecyte, Inc. | Solution and method for adhering suspension components to a substrate |
| TWI747385B (zh) | 2013-12-17 | 2021-11-21 | 美商建南德克公司 | 抗cd3抗體及使用方法 |
| LT3531133T (lt) | 2014-05-30 | 2023-11-10 | Amgen Research (Munich) Gmbh | Ūminės b pirmtakų limfoblastinės leukemijos pacientų rizikos stratifikacija |
| LT3177643T (lt) | 2014-08-04 | 2019-08-12 | F. Hoffmann-La Roche Ag | T ląstelę aktyvinantį antigeną surišančios bispecifinės molekulės |
| BR112017004802A2 (pt) | 2014-09-12 | 2017-12-12 | Genentech Inc | anticorpos anti-cll-1 e imunoconjugados |
| WO2016079050A1 (en) | 2014-11-20 | 2016-05-26 | F. Hoffmann-La Roche Ag | Combination therapy of t cell activating bispecific antigen binding molecules cd3 abd folate receptor 1 (folr1) and pd-1 axis binding antagonists |
| CN107849132B (zh) | 2015-06-16 | 2022-03-08 | 豪夫迈·罗氏有限公司 | 人源化的和亲和力成熟的针对FcRH5的抗体和使用方法 |
| CN107847568B (zh) | 2015-06-16 | 2022-12-20 | 豪夫迈·罗氏有限公司 | 抗cll-1抗体和使用方法 |
| US11890301B2 (en) * | 2015-08-28 | 2024-02-06 | The Trustees Of The University Of Pennsylvania | Methods and compositions for cells expressing a chimeric intracellular signaling molecule |
| CN109824778B (zh) * | 2015-09-18 | 2022-07-19 | 上海科济制药有限公司 | 抗cd19全人抗体以及靶向cd19的免疫效应细胞 |
| AR106188A1 (es) | 2015-10-01 | 2017-12-20 | Hoffmann La Roche | Anticuerpos anti-cd19 humano humanizados y métodos de utilización |
| AR106201A1 (es) | 2015-10-02 | 2017-12-20 | Hoffmann La Roche | Moléculas biespecíficas de unión a antígeno activadoras de células t |
| US10101248B1 (en) * | 2015-12-02 | 2018-10-16 | Rarecyte, Inc. | Solution and method for adhering suspension components to a substrate |
| WO2017097723A2 (en) | 2015-12-09 | 2017-06-15 | F. Hoffmann-La Roche Ag | Treatment method |
| KR20180097615A (ko) | 2016-01-08 | 2018-08-31 | 에프. 호프만-라 로슈 아게 | Pd-1 축 결합 길항물질 및 항-cea/항-cd3 이중특이성 항체를 사용하는 cea-양성 암의 치료 방법 |
| DK3433280T5 (da) | 2016-03-22 | 2024-09-16 | F Hoffmann La Roche Ag | Protease-aktiverede T-celle-bispecifikke molekyler |
| JP6225321B1 (ja) * | 2016-08-31 | 2017-11-08 | 王子ホールディングス株式会社 | ポリ硫酸ペントサンの製造方法 |
| US11286272B2 (en) | 2016-08-31 | 2022-03-29 | Oji Holdings Corporation | Production method for acidic xylooligosaccharide, and acidic xylooligosaccharide |
| US10882918B2 (en) | 2016-09-30 | 2021-01-05 | Hoffmann-La Roche Inc. | Bispecific T cell activating antigen binding molecules |
| AU2017361081A1 (en) | 2016-11-15 | 2019-05-23 | Genentech, Inc. | Dosing for treatment with anti-CD20/anti-CD3 bispecific antibodies |
| EP3579870A4 (en) | 2017-02-07 | 2020-12-30 | Seattle Children's Hospital (DBA Seattle Children's Research Institute) | PHOSPHOLIPID ETHER (PLE) T CAR-LYMPHOCYTE TUMOR (CTCT) TARGETING AGENTS |
| JP6281659B1 (ja) | 2017-02-28 | 2018-02-21 | 王子ホールディングス株式会社 | ポリ硫酸ペントサン、医薬組成物及び抗凝固剤 |
| JP7178355B2 (ja) | 2017-02-28 | 2022-11-25 | エンドサイト・インコーポレイテッド | Car t細胞療法のための組成物および方法 |
| KR20240059648A (ko) | 2017-04-19 | 2024-05-07 | 더 보드 오브 리젠츠 오브 더 유니버시티 오브 텍사스 시스템 | 조작된 항원 수용체를 발현하는 면역 세포 |
| JP6555431B2 (ja) | 2017-05-31 | 2019-08-07 | 王子ホールディングス株式会社 | 保湿外用剤 |
| MX2020002726A (es) | 2017-09-12 | 2020-07-20 | Oji Holdings Corp | Polisulfato de pentosan y metodo para producir polisulfato de pentosan. |
| KR20200055037A (ko) | 2017-09-19 | 2020-05-20 | 메사추세츠 인스티튜트 오브 테크놀로지 | 키메라 항원 수용체 t 세포 요법을 위한 조성물 및 그의 용도 |
| MX2020006605A (es) | 2017-12-20 | 2020-09-10 | Oji Holdings Corp | Polisulfato de pentosano y medicamento que contiene polisulfato de pentosano. |
| US11779602B2 (en) | 2018-01-22 | 2023-10-10 | Endocyte, Inc. | Methods of use for CAR T cells |
| MX2020008289A (es) | 2018-02-08 | 2020-09-25 | Genentech Inc | Moleculas biespecificas de union al antigeno y metodos de uso. |
| CN112771071A (zh) | 2018-09-28 | 2021-05-07 | 麻省理工学院 | 胶原蛋白定位的免疫调节分子及其方法 |
| US11434291B2 (en) | 2019-05-14 | 2022-09-06 | Provention Bio, Inc. | Methods and compositions for preventing type 1 diabetes |
| WO2020263399A1 (en) | 2019-06-26 | 2020-12-30 | Massachusetts Institute Of Technology | Immunomodulatory fusion protein-metal hydroxide complexes and methods thereof |
| WO2021061648A1 (en) | 2019-09-23 | 2021-04-01 | Massachusetts Institute Of Technology | Methods and compositions for stimulation of endogenous t cell responses |
| AR120741A1 (es) | 2019-12-13 | 2022-03-16 | Genentech Inc | Anticuerpos anti-ly6g6d y métodos de uso |
| US11896619B2 (en) | 2020-03-10 | 2024-02-13 | Massachusetts Institute Of Technology | Compositions and methods for immunotherapy of NPM1c-positive cancer |
| BR112022018105A2 (pt) | 2020-03-10 | 2022-11-22 | Massachusetts Inst Technology | Métodos para gerar células nk tipo-memória modificadas e composições das mesmas |
| US20210338833A1 (en) | 2020-05-01 | 2021-11-04 | Massachusetts Institute Of Technology | Chimeric antigen receptor-targeting ligands and uses thereof |
| WO2021221783A1 (en) | 2020-05-01 | 2021-11-04 | Massachusetts Institute Of Technology | Methods for identifying chimeric antigen receptor-targeting ligands and uses thereof |
| MX2022015872A (es) | 2020-06-11 | 2023-05-16 | Provention Bio Inc | Metodos y composiciones para prevenir diabetes tipo 1. |
| TWI811703B (zh) | 2020-06-19 | 2023-08-11 | 瑞士商赫孚孟拉羅股份公司 | 與cd3及cd19結合之抗體 |
| CN112521513B (zh) * | 2020-12-15 | 2021-08-24 | 青岛西凯生物技术有限公司 | 一种靶向cd19的嵌合抗原受体(car)及其应用 |
| CN113637087A (zh) * | 2021-07-09 | 2021-11-12 | 上海易慕峰生物科技有限公司 | 一种提高细胞免疫疗法安全性的嵌合受体和细胞 |
| WO2023081715A1 (en) | 2021-11-03 | 2023-05-11 | Viracta Therapeutics, Inc. | Combination of car t-cell therapy with btk inhibitors and methods of use thereof |
Family Cites Families (28)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2689848A (en) | 1951-02-06 | 1954-09-21 | Wander Ag Dr A | Salts of sulfuric acid esters of xylan |
| DE3853515T3 (de) | 1987-05-21 | 2005-08-25 | Micromet Ag | Multifunktionelle proteine mit vorbestimmter zielsetzung. |
| US5605938A (en) | 1991-05-31 | 1997-02-25 | Gliatech, Inc. | Methods and compositions for inhibition of cell invasion and fibrosis using dextran sulfate |
| ES2112431T3 (es) | 1992-08-21 | 1998-04-01 | Genentech Inc | Procedimiento para el tratamiento de un trastorno mediado por lfa-1. |
| WO1999054440A1 (en) | 1998-04-21 | 1999-10-28 | Micromet Gesellschaft Für Biomedizinische Forschung Mbh | CD19xCD3 SPECIFIC POLYPEPTIDES AND USES THEREOF |
| US7635472B2 (en) | 2003-05-31 | 2009-12-22 | Micromet Ag | Pharmaceutical compositions comprising bispecific anti-cd3, anti-cd19 antibody constructs for the treatment of b-cell related disorders |
| CA2478458A1 (en) | 2004-08-20 | 2006-02-20 | Michael Panzara | Treatment of pediatric multiple sclerosis |
| WO2007068354A1 (en) | 2005-12-16 | 2007-06-21 | Micromet Ag | Means and methods for the treatment of tumorous diseases |
| PT2016102E (pt) | 2006-05-03 | 2012-05-15 | Us Gov Health & Human Serv | Recetores de célula t quimérica e materiais relacionados e métodos de uso |
| EP2815764A1 (en) * | 2006-06-14 | 2014-12-24 | Macrogenics, Inc. | Methods for the treatment of autoimmune disorders using monoclonal antibodies with reduced toxicity |
| WO2008107906A1 (en) | 2007-03-06 | 2008-09-12 | Alembic Limited | Process for the preparation of pentosan polysulfate or salts thereof |
| US20100183615A1 (en) | 2007-04-03 | 2010-07-22 | Micromet Ag | Cross-species-specific bispecific binders |
| TR201816277T4 (tr) | 2007-04-03 | 2018-11-21 | Amgen Res Munich Gmbh | Çapraz-tür-spesifik bağlama alanı. |
| RS58217B1 (sr) * | 2007-04-03 | 2019-03-29 | Amgen Res Munich Gmbh | Interspecijski specifičan vezujući domen |
| AU2008276451A1 (en) * | 2007-07-17 | 2009-01-22 | Zalicus Inc. | Treatments of B-cell proliferative disorders |
| AU2008276455A1 (en) * | 2007-07-17 | 2009-01-22 | Zalicus Inc. | Combinations for the treatment of B-cell proliferative disorders |
| CA2733706A1 (en) | 2007-08-10 | 2009-02-19 | Y's Therapeutics Co., Ltd. | Modulation of immune responses by administration of roxithromycin or its derivative |
| US8026343B2 (en) * | 2008-08-08 | 2011-09-27 | Dinona Inc. | Antibody modulating the differentiation and function of dendritic cells via binding intercellular adhesion molecule-1 and use thereof |
| ME02485B (me) * | 2008-10-01 | 2017-02-20 | Amgen Res Munich Gmbh | Bispecifično jednolančano protutijelo psmaxcd3 s međuvrsnom specifičnošću |
| CN102711822A (zh) * | 2009-10-27 | 2012-10-03 | 米克罗麦特股份公司 | 用于施用CD19xCD3双特异性抗体的给药方案 |
| ES2563439T5 (es) * | 2010-10-27 | 2022-02-04 | Amgen Res Munich Gmbh | Medios y métodos para tratar LDCBG |
| ES2627538T3 (es) * | 2010-11-10 | 2017-07-28 | Amgen Research (Munich) Gmbh | Prevención de los efectos adversos causados por dominios de unión específica a CD3 |
| CA2824997C (en) * | 2011-01-18 | 2023-01-17 | The Trustees Of The University Of Pennsylvania | Compositions and methods for treating cancer |
| CN107303387A (zh) * | 2011-04-28 | 2017-10-31 | 安进研发(慕尼黑)股份有限公司 | 用于给处于潜在不良反应的风险的患者施用CD19xCD3双特异性抗体的给药方案 |
| US9682143B2 (en) * | 2012-08-14 | 2017-06-20 | Ibc Pharmaceuticals, Inc. | Combination therapy for inducing immune response to disease |
| CN102875685B (zh) | 2012-09-29 | 2013-12-25 | 郑骏年 | 嵌合抗原受体hFⅦL-CD8-OX40-CD3ζ及其用途 |
| JO3529B1 (ar) * | 2013-02-08 | 2020-07-05 | Amgen Res Munich Gmbh | مضاد التصاق خلايا الدم البيض من أجل التخفيف من الاثار السلبية الممكنة الناتجة عن مجالات ارتباط cd3- المحدد |
| US9486475B2 (en) * | 2013-02-08 | 2016-11-08 | Amgen Research (Munich) Gmbh | PPS for the prevention of potential adverse effects caused by CD3 specific binding domains |
-
2014
- 2014-02-06 JO JOP/2014/0028A patent/JO3529B1/ar active
- 2014-02-07 ES ES14707953T patent/ES2811764T3/es active Active
- 2014-02-07 AU AU2014214020A patent/AU2014214020B2/en active Active
- 2014-02-07 EP EP20182831.6A patent/EP3760210A1/en not_active Withdrawn
- 2014-02-07 MX MX2019012421A patent/MX2019012421A/es unknown
- 2014-02-07 CA CA2898032A patent/CA2898032C/en active Active
- 2014-02-07 TW TW107140068A patent/TW201929865A/zh unknown
- 2014-02-07 AR ARP140100416A patent/AR094740A1/es unknown
- 2014-02-07 WO PCT/EP2014/052406 patent/WO2014122251A2/en active Application Filing
- 2014-02-07 TW TW103104162A patent/TWI704920B/zh active
- 2014-02-07 MX MX2015009922A patent/MX368842B/es active IP Right Grant
- 2014-02-07 UY UY0001035313A patent/UY35313A/es unknown
- 2014-02-07 JP JP2015556506A patent/JP6567425B2/ja active Active
- 2014-02-07 EP EP14707953.7A patent/EP2953630B1/en active Active
- 2014-02-08 US US14/176,091 patent/US9688760B2/en active Active
-
2016
- 2016-05-03 HK HK16105015.2A patent/HK1216996A1/zh unknown
-
2017
- 2017-05-24 US US15/604,341 patent/US11084876B2/en active Active
-
2019
- 2019-02-07 AU AU2019200841A patent/AU2019200841B2/en active Active
- 2019-05-28 JP JP2019098999A patent/JP6933684B2/ja active Active
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2019178142A (ja) * | 2013-02-08 | 2019-10-17 | アムゲン リサーチ (ミュンヘン) ゲーエムベーハーAMGEN Research(Munich)GmbH | Cd3特異的結合ドメインによって引き起こされる潜在的有害事象を緩和するための抗白血球接着 |
Also Published As
| Publication number | Publication date |
|---|---|
| AU2019200841A1 (en) | 2019-02-28 |
| AU2019200841B2 (en) | 2020-08-13 |
| ES2811764T3 (es) | 2021-03-15 |
| UY35313A (es) | 2014-08-29 |
| US9688760B2 (en) | 2017-06-27 |
| WO2014122251A2 (en) | 2014-08-14 |
| US20140227272A1 (en) | 2014-08-14 |
| AR094740A1 (es) | 2015-08-26 |
| HK1216996A1 (zh) | 2016-12-16 |
| EP2953630B1 (en) | 2020-07-01 |
| JP2016514090A (ja) | 2016-05-19 |
| MX2015009922A (es) | 2015-09-25 |
| EP3760210A1 (en) | 2021-01-06 |
| MX2019012421A (es) | 2022-10-13 |
| AU2014214020B2 (en) | 2018-11-15 |
| WO2014122251A3 (en) | 2014-10-02 |
| AU2014214020A1 (en) | 2015-07-30 |
| CA2898032C (en) | 2021-06-15 |
| TW201442714A (zh) | 2014-11-16 |
| TWI704920B (zh) | 2020-09-21 |
| JP2019178142A (ja) | 2019-10-17 |
| US11084876B2 (en) | 2021-08-10 |
| JO3529B1 (ar) | 2020-07-05 |
| CA2898032A1 (en) | 2014-08-14 |
| EP2953630A2 (en) | 2015-12-16 |
| JP6933684B2 (ja) | 2021-09-08 |
| US20170327581A1 (en) | 2017-11-16 |
| MX368842B (es) | 2019-10-18 |
| TW201929865A (zh) | 2019-08-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6933684B2 (ja) | Cd3特異的結合ドメインによって引き起こされる潜在的有害事象を緩和するための抗白血球接着 | |
| US11579142B2 (en) | Dosage regimen for administering a CD19xCD3 bispecific antibody to patients at risk for potential adverse effects | |
| JP7523084B2 (ja) | 抗ガレクチン-9抗体及びその使用 | |
| JP6709215B2 (ja) | 抗tim−3抗体 | |
| US10662243B2 (en) | Dosage regimen for administering a CD19XCD3 bispecific antibody | |
| JP2019517773A (ja) | 抗lag−3抗体 | |
| JP2022115879A (ja) | Cd39と結合する抗体及びその使用 | |
| WO2019152574A1 (en) | Methods for treating cancer or infection using a combination of an anti-pd-1 antibody, an anti-lag3 antibody, and an anti-tigit antibody | |
| JP2019519208A (ja) | 抗ctla−4抗体 | |
| JP2018508475A (ja) | 抗pd−l1抗体 | |
| US20220275091A1 (en) | Combination of tim-4 antagonist and pd-1 antagonist and methods of use | |
| JP2019513400A (ja) | エクスビボのbite活性化t細胞 | |
| KR20220005627A (ko) | 면역반응의 조절을 위한 방법 및 항체 | |
| EP3774903A1 (en) | Anti-cd27 antibodies and uses thereof | |
| AU2018315432A1 (en) | CD96-binding agents as immunomodulators | |
| WO2015136468A1 (en) | Combination treatment for multiple sclerosis | |
| US20230125234A1 (en) | Anti cd44-ctla4 bispecific antibodies | |
| WO2023163956A2 (en) | Kir3dl3 inhibitors and immune cell activating agents |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160202 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20170124 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20170830 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20171122 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20180122 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180216 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20180516 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20180814 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20181011 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20190130 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190528 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20190529 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190621 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20190624 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20190729 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20190731 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6567425 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |