JP6156246B2 - 固体電解質−電極複合体の製造方法 - Google Patents
固体電解質−電極複合体の製造方法 Download PDFInfo
- Publication number
- JP6156246B2 JP6156246B2 JP2014089841A JP2014089841A JP6156246B2 JP 6156246 B2 JP6156246 B2 JP 6156246B2 JP 2014089841 A JP2014089841 A JP 2014089841A JP 2014089841 A JP2014089841 A JP 2014089841A JP 6156246 B2 JP6156246 B2 JP 6156246B2
- Authority
- JP
- Japan
- Prior art keywords
- solid electrolyte
- reduction
- hydrogen
- layer
- cathode
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/30—Hydrogen technology
- Y02E60/50—Fuel cells
Landscapes
- Conductive Materials (AREA)
- Secondary Cells (AREA)
- Fuel Cell (AREA)
Description
初めに、本実施形態の概要を説明する。本実施形態は、水素吸蔵装置として機能する固体電解質−電極複合体(固体電解質の両側に電極を設けた複合体:以下「複合体」と略す)において、電極と固体電解質との密着性を向上させることを目的とする。この複合体に対し、密着性を向上させたい電極を陰極として、固体電解質を構成する金属元素の還元電位を超える電圧を印加する。電圧印加によって固体電解質の還元反応が起こり、還元析出した金属が電極となじみ、密着性が向上する。
以下、本実施形態の詳細を説明する。図1は、複合体20aの概略断面図である。複合体20aは、上記の複合体の一形態である。複合体20aは、陽極30と、固体電解質膜40と、還元防止層50と、犠牲還元層60と、密着層70と、陰極80とを備える。
図2は、水素吸蔵装置20の製造手順を示す工程図である。まず、複合体20aを製造する(工程P11)。工程P11については、「C−1:複合体20aの製造手順」で詳細を説明する。次に、製造した複合体20aをチャンバ内にセットし(工程P12)、チャンバ内を真空引きする(工程P13)。続いて、チャンバ内に水素を封入する(工程P14)。その後、目標温度に達するまで、複合体を加熱および保持する(工程P15)。そして、温度を維持しながら、陰電圧を所定時間、印加する(工程P16)。この一連の手順によって、犠牲還元層60が還元されて陰極80との密着性が向上することによって、水素吸蔵装置20が製造される。つまり、複合体20aが、高圧の水素を吸蔵できる水素吸蔵装置20として機能するようになる。工程P14〜工程P16の諸条件については、後述する実施例、比較例と共に説明する。
本実施形態における複合体20aの製造手順の概要は次の通りである。(1)陰極80を形成、(2)ジルコニウムの薄い層を形成して密着層70を形成、(3)固体電解質膜40の初期において高い雰囲気ガス圧で製膜して犠牲還元層60を形成、(4)雰囲気ガス圧を小さくして還元防止層50を形成、(5)雰囲気ガス圧を中程度として固体電解質膜40の主要部分を形成。なお、この手順においては、アルゴン雰囲気ガスの圧力の制御を実施しなかった。アルゴン雰囲気ガスの圧力を制御する場合の製造手順は、後述する(E−7)。
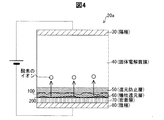
図3,4,5を用いて、工程P16における反応の概要を説明する。水素を含む雰囲気中において、陽極30及び陰極80に電位差を生じさせること(工程P16)によって、図3に示されるように、犠牲還元層60に還元生成物100が生じる。還元生成物100は、Bサイトの金属由来が析出したものであり、具体的には遊離した酸化ジルコニウム(ZrO2)や価数の低い酸化ジルコニウム(ZrO)が主である。還元生成物100は、成長する性質を持つ。但し、還元防止層50に達すると、還元が止まり、還元生成物100の成長も止まる。このように還元生成物100が非常に薄い層の段階で還元生成物100の成長が停止するため、固体電解質膜40の破壊は防止される。
ガラス基板上に、陰極80としてパラジウム陰極(厚さ200nm)、固体電解質膜40としてバリウムジルコネート(厚さ1000nm)、陽極30としてパラジウム陽極(厚さ10nm)を積層した複合体20aを製作した(工程P11)。
工程P15において、複合体20aを水素ガス中で270℃に加熱し、工程P16において、陽極30と陰極80との電位差を2Vに設定して、水素吸蔵装置20を製造した。この条件下においては、吸蔵された水素の圧力で固体電解質膜40が剥離、飛散してしまった。2Vでは還元反応が起こらないからだと考えられる。
工程P15において、複合体20aを水素ガス中で270℃に加熱し、工程P16において、陽極30と陰極80との電位差を15Vに設定して、水素吸蔵装置20を製造した。この場合は、絶縁破壊が起こり、スパークして固体電解質膜40が破壊してしまった。比較例2では、固体電解質膜40の厚みは1μmであった。よって、固体電解質膜40中の電界強度は、15MV/m以下に抑えることが好ましいことがわかる。
工程P16において、陽極30と陰極80との電位差を10Vに設定した。この場合、20min間の電圧印加後、過剰な還元反応によって固体電解質膜40が破壊し、白濁が生じた。この現象は、還元防止層50も還元されたことによると考えられる。
工程P14を実行せず、工程P16において、水素ガスのない雰囲気(真空)で電圧を印加して、水素吸蔵装置20を製造した。この場合、細かい気泡上に陽極30が剥離する現象が起きた。これは、還元によって生じた酸素が、陽極30でガスとして発生し、陽極30を押し剥がしたからと考えられる。
工程P14において封入する水素の分圧、並びに、工程P16における所定時間および温度の関係を変化させて、水素吸蔵装置20を製造した。(a)150℃の場合、時間は1hour、水素分圧は100kPaで充分な気泡抑制効果が得られた。(b)270℃の場合、時間は4〜6min、水素分圧は1kPaで充分な気泡抑制効果が得られた。(c)500℃の場合、時間は1min、水素分圧は10Paで充分な気泡抑制効果が得られた。
複合体20aの製造時においてアルゴン雰囲気ガスの圧力を制御して、水素吸蔵装置20を製造した。「C−1:複合体20aの製造手順(工程P11)」として既に説明した製造手順を一部、変更して複合体20aを製造した。変更点は、次の通りである。製造手順の(3)において、アルゴン雰囲気ガスの圧力を0.9Paに設定し、50nmの犠牲還元層60を陰極80上に形成した。製造手順の(4)において、アルゴン雰囲気ガスの圧力を0.3Paに下げて、50nmの還元防止層50を形成した。製造手順の(5)において、アルゴン雰囲気ガスの圧力を0.67Paに設定し、1000nmの固体電解質膜40を形成した。この後、陽極30を形成して、複合体20aを完成させた。
陽極30、固体電解質膜40及び陰極80が積層した構造を有する複合体21a(図7)を用いて、水素吸蔵装置21を製造した。つまり、還元防止層50、犠牲還元層60及び密着層70を廃止した水素吸蔵装置を製造した。
複合体21aを用いて、工程P14において10kPa(0.01MPa)の窒素を封入し、付きのように条件を順番に変更しながら工程P15,工程P16を繰り返した。(1)190℃ 3.8V 1min、(2)215℃ 3.7V 1min、(3)245℃ 3.7V 1min、(4)260℃ 3.8V 2min。この後、(5)水素同位体ガスの分圧を10kPa(0.01MPa)とし、275℃ 3.7V 1minに変更した。このように、(1)〜(5)で合計6min電圧を印加した。
複合体21aを用い、工程P14において10kPaの水素同位体を封入し、工程P15において270℃に加熱し、工程P16において3〜4Vを30sec印加した。実施例4に比べて印加時間が短いのは、印加の最初から水素同位体雰囲気だったので、陰極80が急激に水素同位体を吸蔵し、短時間でも充分に吸蔵されるからである。部分的に剥離が生じたが、剥がれずに残った部位では良好な吸蔵ができたと考えられる。なお、陰極80に小穴の発生が見られた。
複合体21aを用い、工程P15において260℃に加熱し、工程P16において3〜4Vを1min印加した。実施例6では、極めて高圧の吸蔵が実現されたことが、以下の現象から推測される。陰極80に発生した小穴は、非常に高密度になった。また、開放電圧の測定時に、陰極80の一部がガラス基板から剥離して飛ぶ現象が発生した。この現象は、開放電圧の測定時に印加電圧がほぼゼロになることにより、高圧(GPaオーダー)の水素が発生したため、ガラス基板と陰極80の界面がこの圧力に耐えられなくなったからだと考えられる。つまり、この現象は、固体電解質膜40は剥離しておらず、この圧力に耐えていることを示唆している。
本発明は、本明細書の実施形態や実施例、変形例に限られるものではなく、その趣旨を逸脱しない範囲において種々の構成で実現できる。例えば、発明の概要の欄に記載した各形態中の技術的特徴に対応する実施形態、実施例、変形例中の技術的特徴は、先述の課題の一部又は全部を解決するために、あるいは、先述の効果の一部又は全部を達成するために、適宜、差し替えや、組み合わせを行うことができる。その技術的特徴が本明細書中に必須なものとして説明されていなければ、適宜、削除できる。例えば、以下のものが例示される。
密着層を廃止した場合、陰極をジルコニウムで構成してもよい。このようにすれば、密着層を廃止しつつ、密着層がある場合と同等の密着性を得ることができる。ジルコニウムによる陰極を採用する場合、陰極の厚さを1〜100nm、より好ましくは3〜50nmに設定すると、陰極の水素透過性を向上させることができる。
固体電解質は、バリウムジルコネートでなくても、その他の種類、例えばバリウムとセリウムとによるものでもよい。
陰極として使用する部位でなくてもよく、例えば陽極に使用する部位であっても、この構造を適用し、さらにその製造段階において負の電圧を印加する処理を実施して密着を向上させた後に陽極として使用に供するという応用に対しても適用できる。
密着層、犠牲還元層、還元防止層、及び高い陰電位を掛ける処理、及びこの処理時に水素ガスを添加することの5つ全てを備えることが必要である訳ではなく、このうちの1つ又は複数の組み合わせだけであっても充分に効果を発揮し得るものである。例えば、犠牲還元層と還元防止層との一方を廃止しても良い。この場合でも、やはり密着性の向上の効果がある。但し、良好な密着が得られる条件と過剰な還元が起きて構造が破壊する条件との間が狭くなるので、適宜、実験によって数値を定めるのが好ましい。
陰極と陽極との両方に本発明を適用できる。
20a…固体電解質−電極複合体
21…水素吸蔵装置
21a…固体電解質−電極複合体
30…陽極
40…固体電解質膜
50…還元防止層
60…犠牲還元層
70…密着層
80…陰極
100…還元生成物
200…強還元物
Claims (3)
- AB1−XCXO3(0≦X≦0.3)からなるペロブスカイト構造を持つ固体電解質の両側に電極が配置される固体電解質−電極複合体の製造方法であって、
130℃以上500℃以下の温度条件かつ水素ガスの存在する雰囲気で、前記ペロブスカイト構造におけるBサイトの金属が還元されるように前記両側の電極間に電圧を印加し、前記両側の電極の少なくとも一方と前記固体電解質との間に前記Bサイトの金属由来の層を析出させる、製造方法。 - 前記電圧の印加を、水素ガスの分圧が10Pa以上100kPa以下の雰囲気において実施する請求項1に記載の製造方法。
- 前記両側の電極の少なくとも一方が水素を吸蔵可能である、請求項1又は請求項2に記載の製造方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2014089841A JP6156246B2 (ja) | 2014-04-24 | 2014-04-24 | 固体電解質−電極複合体の製造方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2014089841A JP6156246B2 (ja) | 2014-04-24 | 2014-04-24 | 固体電解質−電極複合体の製造方法 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2015211484A JP2015211484A (ja) | 2015-11-24 |
| JP2015211484A5 JP2015211484A5 (ja) | 2016-07-14 |
| JP6156246B2 true JP6156246B2 (ja) | 2017-07-05 |
Family
ID=54613341
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014089841A Active JP6156246B2 (ja) | 2014-04-24 | 2014-04-24 | 固体電解質−電極複合体の製造方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP6156246B2 (ja) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB201611953D0 (en) * | 2016-07-08 | 2016-08-24 | Univ Court Of The Univ Of St Andrews The | Method |
| US10840543B2 (en) * | 2017-03-31 | 2020-11-17 | The Regents Of The University Of Michigan | System and method for the formation of facile lithium metal anode interface with a solid state electrolyte |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH08278278A (ja) * | 1995-04-03 | 1996-10-22 | Tokyo Yogyo Co Ltd | 水素センサプローブ及びその製造方法 |
| JP3274356B2 (ja) * | 1996-05-13 | 2002-04-15 | 株式会社日本製鋼所 | 水素吸蔵合金を用いた発電方法および装置 |
| JP2005033960A (ja) * | 2003-07-10 | 2005-02-03 | Toyota Motor Corp | 熱電変換水素電池 |
| JP5061456B2 (ja) * | 2005-12-14 | 2012-10-31 | トヨタ自動車株式会社 | 燃料電池の製造方法 |
| JP2015059224A (ja) * | 2013-09-17 | 2015-03-30 | トヨタ自動車株式会社 | 水素吸蔵装置 |
-
2014
- 2014-04-24 JP JP2014089841A patent/JP6156246B2/ja active Active
Also Published As
| Publication number | Publication date |
|---|---|
| JP2015211484A (ja) | 2015-11-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Achour et al. | Role of nitrogen doping at the surface of titanium nitride thin films towards capacitive charge storage enhancement | |
| JP5807218B2 (ja) | 光電極およびその製造方法、光電気化学セルおよびそれを用いたエネルギーシステム、並びに水素生成方法 | |
| CN113249683B (zh) | 高导电耐蚀长寿命max相固溶复合涂层、其制法与应用 | |
| JP2008023404A (ja) | 水素透過構造体及び燃料電池 | |
| JP6156246B2 (ja) | 固体電解質−電極複合体の製造方法 | |
| JP2015134699A (ja) | 酸化物膜およびプロトン伝導デバイス | |
| JP6600300B2 (ja) | 固体電解質用多重層配置構成 | |
| JP4992522B2 (ja) | コンデンサ用電極箔及びそれを用いたコンデンサ | |
| CN106129172B (zh) | 一种可调节电荷密度的晶硅太阳能电池表面钝化方法 | |
| JP2016026987A (ja) | プロトン伝導性酸化物 | |
| JP4665866B2 (ja) | バルブ金属複合電極箔の製造方法 | |
| JP2008130514A (ja) | 電解質膜の成膜方法および燃料電池の製造方法 | |
| JP6911812B2 (ja) | 陽極酸化装置、陽極酸化方法及び陽極酸化装置の陰極の製造方法 | |
| JP2006314925A (ja) | 水素透過膜およびそれを備えた燃料電池 | |
| JP2006286537A (ja) | 水素透過構造体、及びその製造方法 | |
| KR101447023B1 (ko) | 다공성 복합체 박막의 제조방법 및 전극용 다공성 복합체 박막 | |
| KR20200037000A (ko) | 2차원 물질의 전기적 특성 회복 및 산화 안정성 개선 방법 | |
| JP2015059224A (ja) | 水素吸蔵装置 | |
| TW201605102A (zh) | 氫排出膜 | |
| TW201812811A (zh) | 電解電容器 | |
| US3491000A (en) | Method of producing vanadium dioxide thin films | |
| JP5138876B2 (ja) | 酸化物プロトン導電性膜及びそれを含む水素透過構造体 | |
| WO2015194471A1 (ja) | 水素排出膜 | |
| JP2007117810A (ja) | 水素透過膜、及びそれを用いた燃料電池 | |
| JP2004016971A (ja) | 酸素透過体 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160525 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20160525 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20170426 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20170509 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20170522 |
|
| R151 | Written notification of patent or utility model registration |
Ref document number: 6156246 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R151 |