JP6008024B2 - オリビン型リチウム遷移金属酸化物の製造方法 - Google Patents
オリビン型リチウム遷移金属酸化物の製造方法 Download PDFInfo
- Publication number
- JP6008024B2 JP6008024B2 JP2015137194A JP2015137194A JP6008024B2 JP 6008024 B2 JP6008024 B2 JP 6008024B2 JP 2015137194 A JP2015137194 A JP 2015137194A JP 2015137194 A JP2015137194 A JP 2015137194A JP 6008024 B2 JP6008024 B2 JP 6008024B2
- Authority
- JP
- Japan
- Prior art keywords
- metal oxide
- transition metal
- type lithium
- olivine
- lithium transition
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Description
すなわち、結晶へのリチウムの挿入及び脱離がスムーズで良好な充放電特性を有する正極活物質とするため、オリビン型リチウム鉄酸化物の粒子径を小さくすることでLiイオンの拡散速度を上げることができる。
特許文献2に開示されるオリビン型リチウム鉄酸化物の製造方法は、焼成時における粒子成長を抑制して粒子径を小さくするため、オリビン型リチウム鉄酸化物の原料とは別に界面活性剤を添加している。この界面活性剤は、正極活物質の前駆体を液中に微小な粒子(ミセル)として分散させるので、オリビン型リチウム鉄酸化物の粒子径を小さくすることができる。このような界面活性剤として特許文献2に開示されるものとしては、例えば、イソオクチルフェノール(Isooctylphenol)とエチレンオキサイド(Ethylene Oxide)とからなるオクタポール(Octapole、商品名、三洋化成工業株式会社製)といったような材料が挙げられている。
平均二次粒子径が2μm以上15μm以下でかつ粉体の見かけ密度が、0.5g/cm3以上1.7g/cm3以下である二次粒子からなり、前記二次粒子を構成する一次粒子が80nm以下の結晶子径を有し、放電容量が100mAh/g以上であることを特徴とする。
(a)リン酸源と、(b)リチウム源と、(c)炭素源と、(d)鉄源または前記金属元素M1、M2の酸化物、リン酸化物もしくは水酸化物と、(e)溶媒と、(f)分散剤とを含有するスラリーを調整する工程と、
前記スラリーに含まれる粒子を粉砕処理する工程と、
前記粉砕処理したスラリーを噴霧乾燥して前駆体とする工程と、
前記前駆体を不活性雰囲気または還元雰囲気のもとで熱処理する工程と、を有し、
前記分散剤として、それぞれ平均分子量が20000以上40000以下であるポリカルボン酸ナトリウム及びポリカルボン酸アンモニウムからなる群から選択された少なくとも一種であるポリカルボン酸塩を用いることを特徴とする。
また、本発明に係るオリビン型リチウム遷移金属酸化物の製造方法によれば、リチウムの結晶への挿入及び脱離がスムーズで高い放電容量を有するオリビン型リチウム遷移金属酸化物を作製することができる。
本発明者らは、鋭意研究を重ねた結果、原材料を含むスラリーを調整する工程と、そのスラリーに含まれる粒子を粉砕して乾燥することで前駆体を作製する工程と、その前駆体を不活性雰囲気または還元雰囲気のもとで熱処理する工程とを含むオリビン型リチウム遷移金属酸化物の製造方法において、スラリーを調整する工程で、特定の範囲の分子量に調整された特定の種類の分散剤(高分子型)を含有させてスラリーを調整することにより、高い放電容量を有する正極活物質を製造できることを見出して、本発明を完成させた。
本発明に係るオリビン型リチウム遷移金属酸化物の原料は、リン酸源と、リチウム源と、炭素源と、鉄源またはMo、Mg、Zr、Mn、Ti、Co、Ni、Al、Ce、Crからなる群より選択された少なくとも一種の金属元素の酸化物、リン酸化物もしくは水酸化物を含む原料である。
本発明の方法で使用可能な鉄源として、例えばリン酸鉄、硫酸鉄、塩化鉄、シュウ酸鉄等が挙げられる。このうち、リン酸鉄はリン酸源としてもはたらく。
尚、平均分子量が20000以上40000以下の範囲としたのは、以下のような本発明者等が得た知見に基づく。
また、分散剤は、スラリーに含まれる原料に対して1重量%以上10重量%以下の割合で添加することが好ましい。
スラリーに含まれる上述の原料は、原料によって粒径や粒度分布が異なる粒子状の原料として供給されるので、原料粒子を目的の特性が得られるように細かく粉砕して混合する。
混合粉砕の方法として、湿式粉砕混合又は乾式粉砕混合のいずれの方法を選択してもよい。湿式粉砕混合とは、粉砕する目的物を分散媒(例えば、水)に入れ1mm前後のメディアを使用しローラー台で回すことによる粉砕方法であり、乾式粉砕混合より細かく粉砕できることができる利点がある。
原料粒子が混合粉砕されたスラリーを、シャワー状に噴霧してこの噴霧されたスラリーに熱風を吹きつけることにより乾燥する(噴霧乾燥)。これにより、一次粒子の集合体である二次粒子(ほぼ球形)を前駆体として作製する。
本工程では、前駆体を不活性雰囲気または還元雰囲気の下で焼成する。不活性雰囲気または還元雰囲気は、窒素あるいは、水素またはアンモニアを含む還元雰囲気であることが好ましく、水素および窒素を含む雰囲気であることが、より好ましい。焼成温度は、500℃以上800℃以下が好ましく、より好ましくは、600℃以上700℃以下である。
本発明において、オリビン型リチウム遷移金属酸化物の組成は、Lix(Fe1−yM1y)1−zM2zPO4(式中x、y、zは、0.9<x<1.3、0≦y≦1、0≦z<0.3であり、M1は、Mn、CoおよびNiからなる群より選択された少なくとも1種の金属元素であり、M2は、Mo、Mg、Zr、Ti、Al、Ce、Cr、Mn、CoおよびNiからなる群より選択された少なくとも1種の金属元素である。)である。
本明細書におけるオリビン型リチウム遷移金属酸化物の物性は、以下の方法によって測定したものである。
結晶子径は、特定の回折角(面)のピーク高さと半価幅(FWHM:Full Width Half Maximum)より、いわゆるシェラー(Scherrer)の式を用いて、不均一歪みはないとの仮定のもとに結晶子の平均的なサイズを求める。
放電容量は、定電流放電を行ったときに10時間で放電終了となる電流(0.1C)で放電したときの値である。
粉体密度(見かけ密度)は、粉末を一定容積の容器内に入る粉末の量を測定し、単位体積当たりの重量を測定することで算出する。
本発明において、ポリカルボン酸塩の平均分子量とは、ゲルパーミテーションクロマトグラフィー(GPC)によるポリエチレングリコール(PEG)換算重量平均分子量のことである。
リン酸化物としてMn3(PO4)2:167.9g(Mnとして1.42mol)と、リン酸源ともなるリチウム源としてリン酸リチウム(Li3PO4):60.0g(Liとして1.49mol)と、炭素源としてショ糖:25.4g(1gのMnに対して0.325g)と、分散媒として純水1700mlと、分散剤として平均分子量が20000〜30000のポリカルボン酸アンモニウム3.9g(2重量%)と、を混合しスラリーとする。そのスラリーを容量が5000mlのボールミルにいれ、アルミナボールを用いて、40時間粉砕処理して微細化する。
リン酸化物としてMn3(PO4)2:167.9g(Mnとして1.42mol)と、リチウム源としてリン酸リチウム(Li3PO4):60.0g(Liとして1.49mol)と、炭素源としてショ糖:25.4g(1gのMnに対して0.325g)と、分散媒として純水1700mlと、分散剤として平均分子量が30000〜40000のポリカルボン酸アンモニウム3.9g(2重量%)と、を混合しスラリーとする。そのスラリーを容量が5000mlのボールミルにいれ、アルミナボールを用いて、40時間粉砕処理して微細化する。
得られた焼成物の相同定を、X線回折装置を用いて行った。X線としては、CuKα線(波長:λ=1.54nm)を用いて分析した結果、オリビン型リチウム遷移金属酸化物が確認され、また不純物のピークは見られなかった。得られた焼成物は、組成がLiMnPO4、結晶子径が422Å(42.2nm)、炭素含有量が2.8重量%、平均二次粒子径が6.2μmであった。放電容量が105mAh/gであった。粉体密度が、0.74g/cm3であった。
リン酸化物としてMn3(PO4)2:167.9g(Mnとして1.42mol)と、リチウム源としてリン酸リチウム(Li3PO4):60.0g(Liとして1.49mol)と、炭素源としてショ糖:25.4g(1gのMnに対し0.325g)と、分散媒として純水1700mlと、分散剤として分子量が20000〜30000のポリカルボン酸ナトリウム3.9g(2重量%)と、を混合しスラリーとする。そのスラリーを容量が5000mlのボールミルにいれ、アルミナボールを用いて、40時間粉砕処理して微細化する。
リン酸化物としてMn3(PO4)2:167.9g(Mnとして1.42mol)と、リチウム源としてリン酸リチウム(Li3PO4):60.0g(Liとして1.49mol)と、炭素源としてショ糖:25.4g(1gのMnに対して0.325g)と、分散媒として純水1700mlと、分散剤として分子量が30000〜40000のポリカルボン酸ナトリウム3.9g(2重量%)と、を混合しスラリーとする。そのスラリーを容量が5000mlのボールミルにいれ、アルミナボールを用いて、40時間粉砕処理して微細化する。
分散剤を添加しない他は、実施例1と同様に、焼成物を得る。
得られた焼成物の相同定を、X線回折装置を用いて行った。X線としては、CuKα線(波長:λ=1.54nm)を用いて分析した結果、オリビン型リチウム遷移金属酸化物が確認され、また不純物のピークは見られなかった。得られた焼成物は、組成がLiMnPO4、結晶子径が432Å(43.2nm)、炭素含有量が2.6重量%、平均二次粒子径が4.8μmであった。放電容量が92mAh/gであった。粉体密度が、0.55g/cm3であった。
リン酸化物としてMn3(PO4)2:167.9g(Mnとして1.42mol)と、リチウム源としてリン酸リチウム(Li3PO4):60.0g(Liとして1.49mol)と、炭素源としてショ糖:25.4g(1gのMnに対して0.325g)と、分散媒として純水1700mlと、分散剤として分子量が20000以下のポリカルボン酸アンモニウム3.9g(2重量%)とを混合しスラリーとする。そのスラリーを容量が5000mlのボールミルにいれ、アルミナボールを用いて、40時間粉砕処理して微細化する。
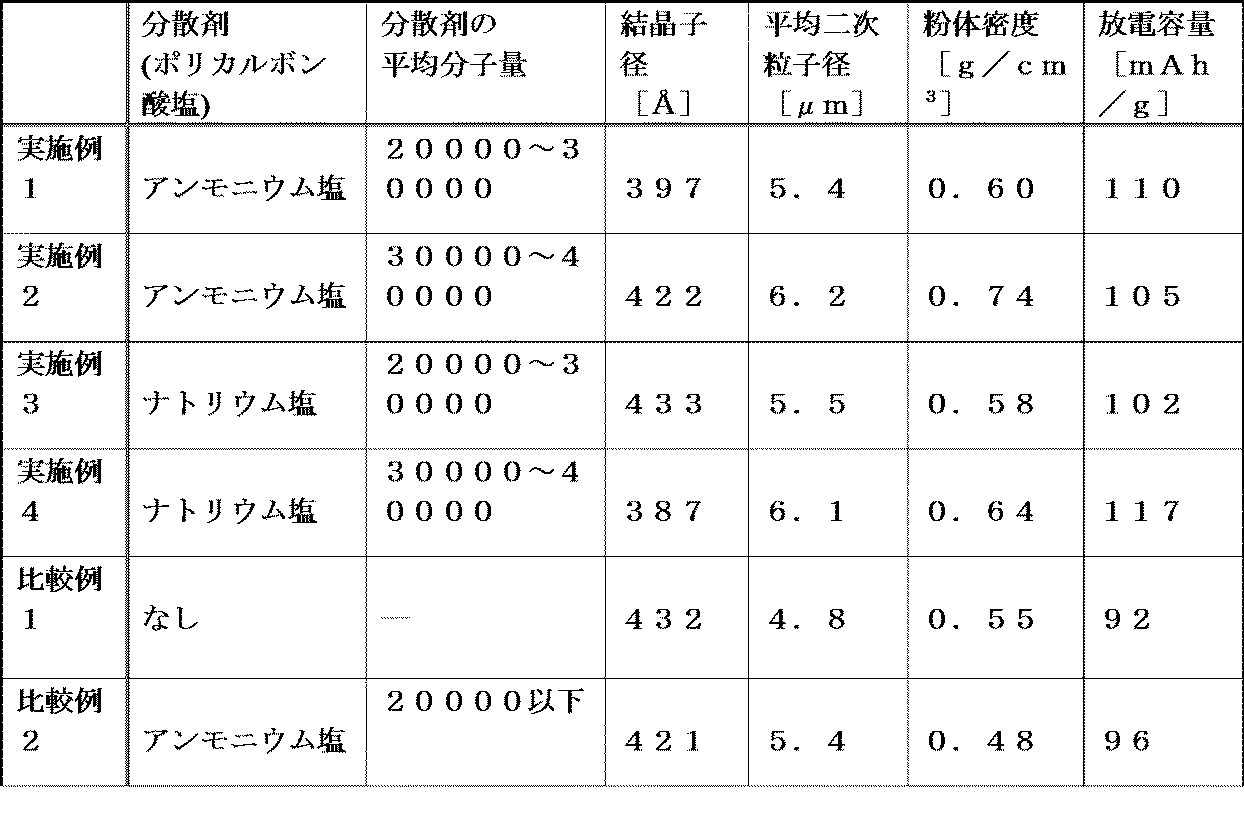
以下の[表1]は、実施例1から4および比較例1から2についての測定結果を示す。
態様1:
組成がLix(Fe1−yM1y)1−zM2zPO4(式中x、y、zは、0.9<x<1.3、0≦y≦1、0≦z<0.3であり、M1は、Mn、CoおよびNiからなる群より選択された少なくとも1種の金属元素であり、M2は、Mo、Mg、Zr、Ti、Al、CeおよびCrからなる群より選択された少なくとも1種の金属元素である。)であるオリビン型リチウム遷移金属酸化物であって、
平均二次粒子径が2μm以上15μm以下であり、粉体の見かけ密度が、0.5g/cm3以上1.7g/cm3以下であり、かつ、前記二次粒子を構成する一次粒子が80nm以下の結晶子径を有し、放電容量が100mAh/g以上であることを特徴とするオリビン型リチウム遷移金属酸化物。
態様2:
組成がLix(Fe1−yM1y)1−zM2zPO4(式中x、y、zは、0.9<x<1.3、0≦y≦1、0≦z<0.3であり、M1は、Mn、CoおよびNiからなる群より選択された少なくとも1種の金属元素であり、M2は、Mo、Mg、Zr、Ti、Al、CeおよびCrからなる群より選択された少なくとも1種の金属元素である。)であるオリビン型リチウム遷移金属酸化物の製造方法において、
(a)リン酸源と、(b)リチウム源と、(c)炭素源と、(d)鉄源または前記金属元素M1、M2の酸化物、リン酸化物もしくは水酸化物と、(e)溶媒と、(f)分散剤とを含有するスラリーを調整する工程と、
前記スラリーに含まれる粒子を粉砕処理する工程と、
前記粉砕処理したスラリーを噴霧乾燥して前駆体とする工程と、
前記前駆体を不活性雰囲気または還元雰囲気のもとで熱処理する工程と、を有し、
前記分散剤として、それぞれ平均分子量が20000以上40000以下であるポリカルボン酸ナトリウム及びポリカルボン酸アンモニウムからなる群から選択された少なくとも一種であるポリカルボン酸塩を用いることを特徴とするオリビン型リチウム遷移金属酸化物の製造方法。
態様3:
前記ポリカルボン酸塩は、平均分子量が20000以上30000以下のポリカルボン酸アンモニウムである態様2に記載のオリビン型リチウム遷移金属酸化物の製造方法。
態様4:
前記ポリカルボン酸塩は、平均分子量が30000以上40000以下のポリカルボン酸ナトリウムである態様2に記載のオリビン型リチウム遷移金属酸化物の製造方法。
態様5:
前記熱処理の温度は、500℃以上800℃以下である態様2〜4のうちのいずれか1つに記載のオリビン型リチウム遷移金属酸化物の製造方法。
態様6:
前記分散剤が、前記スラリーに含まれる原料に対して1重量%以上10重量%以下の割合で添加される態様2〜5のうちのいずれか1つに記載のオリビン型リチウム遷移金属酸化物の製造方法。
Claims (5)
- 組成がLiMnPO4であるオリビン型リチウム遷移金属酸化物の製造方法において、
(a)リン酸源と、(b)リチウム源と、(c)炭素源と、(d)Mnの酸化物、リン酸化物もしくは水酸化物と、(e)溶媒と、(f)分散剤とを含有するスラリーを調整する工程と、
前記スラリーに含まれる粒子を粉砕処理する工程と、
前記粉砕処理したスラリーを噴霧乾燥して前駆体とする工程と、
前記前駆体を不活性雰囲気または還元雰囲気のもとで熱処理する工程と、を有し、
前記分散剤として、それぞれ平均分子量が20000以上40000以下であるポリカルボン酸ナトリウム及びポリカルボン酸アンモニウムからなる群から選択された少なくとも一種であるポリカルボン酸塩を用いることを特徴とするオリビン型リチウム遷移金属酸化物の製造方法。 - 前記ポリカルボン酸塩は、平均分子量が20000以上30000以下のポリカルボン酸アンモニウムである請求項1に記載のオリビン型リチウム遷移金属酸化物の製造方法。
- 前記ポリカルボン酸塩は、平均分子量が30000以上40000以下のポリカルボン酸ナトリウムである請求項1に記載のオリビン型リチウム遷移金属酸化物の製造方法。
- 前記熱処理の温度は、500℃以上800℃以下である請求項1〜3のうちのいずれか1つに記載のオリビン型リチウム遷移金属酸化物の製造方法。
- 前記分散剤が、前記スラリーに含まれる原料に対して1重量%以上10重量%以下の割合で添加される請求項1〜4のうちのいずれか1つに記載のオリビン型リチウム遷移金属酸化物の製造方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015137194A JP6008024B2 (ja) | 2011-06-28 | 2015-07-08 | オリビン型リチウム遷移金属酸化物の製造方法 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011143318 | 2011-06-28 | ||
| JP2011143318 | 2011-06-28 | ||
| JP2015137194A JP6008024B2 (ja) | 2011-06-28 | 2015-07-08 | オリビン型リチウム遷移金属酸化物の製造方法 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011240834A Division JP2013032257A (ja) | 2011-06-28 | 2011-11-02 | オリビン型リチウム遷移金属酸化物及びその製造方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2015212224A JP2015212224A (ja) | 2015-11-26 |
| JP6008024B2 true JP6008024B2 (ja) | 2016-10-19 |
Family
ID=47788474
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011240834A Pending JP2013032257A (ja) | 2011-06-28 | 2011-11-02 | オリビン型リチウム遷移金属酸化物及びその製造方法 |
| JP2015137194A Active JP6008024B2 (ja) | 2011-06-28 | 2015-07-08 | オリビン型リチウム遷移金属酸化物の製造方法 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011240834A Pending JP2013032257A (ja) | 2011-06-28 | 2011-11-02 | オリビン型リチウム遷移金属酸化物及びその製造方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (2) | JP2013032257A (ja) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| TW201351763A (zh) * | 2012-05-10 | 2013-12-16 | Toyo Ink Sc Holdings Co Ltd | 鋰二次電池正極用造粒粒子及其製造方法、混合材油墨及鋰二次電池 |
| EP2778127A1 (en) * | 2013-03-15 | 2014-09-17 | Clariant International Ltd. | Lithium transition metal phosphate secondary agglomerates and process for its manufacture |
| EP2778126A1 (en) * | 2013-03-15 | 2014-09-17 | Clariant International Ltd. | Lithium transition metal phosphate secondary agglomerates and process for its manufacture |
| JP6205895B2 (ja) * | 2013-06-26 | 2017-10-04 | 日亜化学工業株式会社 | オリビン型ケイ酸遷移金属リチウム化合物およびその製造方法 |
| KR102145248B1 (ko) * | 2015-03-31 | 2020-08-18 | 도레이 카부시키가이샤 | 인산망간리튬 나노 입자 및 그의 제조 방법, 탄소 피복 인산망간리튬 나노 입자, 탄소 피복 인산망간리튬 나노 입자 조립체, 리튬 이온 전지 |
| WO2018029745A1 (ja) * | 2016-08-08 | 2018-02-15 | 東レ株式会社 | リン酸マンガンリチウムナノ粒子およびその製造方法、炭素被覆リン酸マンガンリチウムナノ粒子、炭素被覆リン酸マンガンリチウムナノ粒子造粒体、リチウムイオン電池 |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP4058680B2 (ja) * | 2002-08-13 | 2008-03-12 | ソニー株式会社 | 正極活物質の製造方法及び非水電解質二次電池の製造方法 |
| JP4656653B2 (ja) * | 2003-10-27 | 2011-03-23 | 三井造船株式会社 | 二次電池用正極材料、二次電池用正極材料の製造方法、および二次電池 |
| JP5293936B2 (ja) * | 2007-05-21 | 2013-09-18 | 戸田工業株式会社 | 非水電解質二次電池用オリビン型複合酸化物及びその製造方法、並びに二次電池 |
| JP5372476B2 (ja) * | 2007-12-25 | 2013-12-18 | 花王株式会社 | リチウム電池正極用複合材料の製造方法 |
| CN101980956A (zh) * | 2008-03-31 | 2011-02-23 | 户田工业株式会社 | 磷酸铁锂颗粒粉末的制造方法、橄榄石型结构的磷酸铁锂颗粒粉末、使用该磷酸铁锂颗粒粉末的正极材料片和非水溶剂类二次电池 |
| JP2009302044A (ja) * | 2008-05-14 | 2009-12-24 | Tokyo Institute Of Technology | 無機物粒子の製造方法、及びそれを用いた二次電池正極並びに二次電池 |
| JP5213534B2 (ja) * | 2008-06-17 | 2013-06-19 | 三洋電機株式会社 | 非水電解質二次電池及びその製造方法 |
| CN102186768B (zh) * | 2008-10-22 | 2013-08-21 | 株式会社Lg化学 | 具有橄榄石结构的锂铁磷酸盐及其制备方法 |
| JP5436896B2 (ja) * | 2009-03-17 | 2014-03-05 | 日本化学工業株式会社 | リチウムリン系複合酸化物炭素複合体、その製造方法、リチウム二次電池用正極活物質及びリチウム二次電池 |
| TW201124337A (en) * | 2009-09-09 | 2011-07-16 | Toda Kogyo Corp | Ferric phosphate hydrate particle powder and process for production thereof, olivine-type lithium iron phosphate particle powder and process for production thereof, and non-aqueous electrolyte secondary battery |
| CN103079998B (zh) * | 2010-08-18 | 2016-06-08 | 株式会社村田制作所 | 磷酸铁的制造方法、磷酸铁锂、电极活性物质及二次电池 |
| JP2012204150A (ja) * | 2011-03-25 | 2012-10-22 | Sumitomo Osaka Cement Co Ltd | 電極活物質の製造方法と電極活物質及び電極並びに電池 |
-
2011
- 2011-11-02 JP JP2011240834A patent/JP2013032257A/ja active Pending
-
2015
- 2015-07-08 JP JP2015137194A patent/JP6008024B2/ja active Active
Also Published As
| Publication number | Publication date |
|---|---|
| JP2015212224A (ja) | 2015-11-26 |
| JP2013032257A (ja) | 2013-02-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6008024B2 (ja) | オリビン型リチウム遷移金属酸化物の製造方法 | |
| Pan et al. | Hydrothermal synthesis of well-dispersed LiMnPO4 plates for lithium ion batteries cathode | |
| EP2471132B1 (en) | Mixed metal olivine electrode materials for lithium ion batteries having improved specific capacity and energy density | |
| TWI448420B (zh) | 鋰離子電池之磷酸亞鐵前驅物、使用其製備之磷酸鋰鐵粉末、及其製作方法 | |
| EP2203948B1 (en) | Positive electrode active material, lithium secondary battery, and manufacture methods therefore | |
| ES2957469T3 (es) | Materiales de cátodo de LMFP con rendimiento electroquímico mejorado | |
| KR101589294B1 (ko) | 리튬 이차 전지용 양극 활물질, 이의 제조 방법, 및 이를 포함하는 리튬 이차 전지 | |
| CN103303892A (zh) | 制备结晶的LiFePO4粉末的方法 | |
| JP2019040854A (ja) | リチウム電池のカソードに用いるためのリン酸マンガン鉄リチウム系粒子、これを含有するリン酸マンガン鉄リチウム系粉末材料、およびその粉末材料を製造する方法 | |
| US20170092937A1 (en) | Electrode material for lithium-ion rechargeable battery, method for manufacturing electrode material for lithium-ion rechargeable battery, electrode for lithium-ion rechargeable battery, and lithium-ion rechargeable battery | |
| US20210395104A1 (en) | A method of preparing an electrode material for lithium-ion batteries | |
| JP5804422B2 (ja) | 二次電池正極活物質の製造方法 | |
| JP5842792B2 (ja) | 二次電池正極活物質前駆体の製造方法 | |
| JP5765644B2 (ja) | リチウムイオン電池用の高電圧ナノ複合体カソード(4.9v)の調製のための方法 | |
| JP5636772B2 (ja) | オリビン型リチウム遷移金属複合酸化物及びその製造方法 | |
| JP5811695B2 (ja) | オリビン型リチウム遷移金属酸化物およびその製造方法 | |
| JP2012229147A (ja) | オリビン型リチウム遷移金属酸化物及びその製造方法 | |
| Nwachukwu et al. | Research progress in solid-state synthesized LiMnPO4 cathode material for Li-ion battery applications | |
| JP2012204079A (ja) | オリビン型リチウム遷移金属酸化物及びその製造方法 | |
| JP5831296B2 (ja) | オリビン型リチウム遷移金属酸化物およびその製造方法 | |
| JP6394391B2 (ja) | ポリアニオン系正極活物質複合体粒子の製造方法 | |
| JP6205895B2 (ja) | オリビン型ケイ酸遷移金属リチウム化合物およびその製造方法 | |
| KR101437886B1 (ko) | 리튬이차전지용 캐쏘드 활물질 나노복합체, 그 제조방법 및 이를 포함하는 리튬이차전지 | |
| Shivamurthy et al. | Formation of the Secondary Phase Domain by Multi-Cation Substitution for the Superior Electrochemical Performance of Spinel Cathodes for High-Voltage Li-Ion Batteries | |
| TWI493779B (zh) | 具有改良式比電容與能量密度之鋰離子電池用的混合金屬橄欖石電極材料 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20160216 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20160425 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20160517 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160614 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20160816 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20160829 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6008024 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |