JP5259193B2 - 加圧下にある用量計量型吸入器用の金属イオン封鎖剤を含む薬用エーロゾル配合物 - Google Patents
加圧下にある用量計量型吸入器用の金属イオン封鎖剤を含む薬用エーロゾル配合物 Download PDFInfo
- Publication number
- JP5259193B2 JP5259193B2 JP2007556521A JP2007556521A JP5259193B2 JP 5259193 B2 JP5259193 B2 JP 5259193B2 JP 2007556521 A JP2007556521 A JP 2007556521A JP 2007556521 A JP2007556521 A JP 2007556521A JP 5259193 B2 JP5259193 B2 JP 5259193B2
- Authority
- JP
- Japan
- Prior art keywords
- formulation
- active ingredient
- dose
- phosphoric acid
- sulfuric acid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/10—Dispersions; Emulsions
- A61K9/12—Aerosols; Foams
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/007—Pulmonary tract; Aromatherapy
- A61K9/0073—Sprays or powders for inhalation; Aerolised or nebulised preparations generated by other means than thermal energy
- A61K9/008—Sprays or powders for inhalation; Aerolised or nebulised preparations generated by other means than thermal energy comprising drug dissolved or suspended in liquid propellant for inhalation via a pressurized metered dose inhaler [MDI]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4704—2-Quinolinones, e.g. carbostyril
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/57—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids substituted in position 17 beta by a chain of two carbon atoms, e.g. pregnane or progesterone
- A61K31/573—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids substituted in position 17 beta by a chain of two carbon atoms, e.g. pregnane or progesterone substituted in position 21, e.g. cortisone, dexamethasone, prednisone or aldosterone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/58—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids containing heterocyclic rings, e.g. danazol, stanozolol, pancuronium or digitogenin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/02—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/08—Bronchodilators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/02—Drugs for disorders of the nervous system for peripheral neuropathies
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pulmonology (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Otolaryngology (AREA)
- Inorganic Chemistry (AREA)
- Dispersion Chemistry (AREA)
- Neurosurgery (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
- Containers And Packaging Bodies Having A Special Means To Remove Contents (AREA)
Description
R3、R4、R5及びR6は各々独立に、水素、ヒドロキシ、直鎖又は分枝鎖C1−C4アルキル、1個もしくはそれ以上のハロゲン原子及び/又はヒドロキシ基で置換された直鎖又は分枝鎖C1−C4アルキル、ハロゲン、直鎖又は分枝鎖C1−C4アルコキシであり、
R7は、水素、ヒドロキシ、直鎖又は分枝鎖C1−C4アルキル、直鎖又は分枝鎖C1−C4アルコキシであり、そして
R8およびR9は、独立に、水素、C1−C4アルキルであるか、あるいは共同してビニレン(−CH=CH−)基またはエチレン(−CH2CH2−)基を形成する。あるいは、その鏡像体、塩及び溶媒和物である。
R1がメチルであり、R4がメトキシであり、R2、R3、R5、R6、R8、R9が水素であり、R7がヒドロキシであり、そしてn=1である(ホルモテロール)、並びにR1がメチルであり、R4がメトキシであり、R2、R3、R5、R6が水素であり、R7がヒドロキシであり、R8およびR9が共同してビニレン(−CH=CH−)基を形成していて、そしてn=1である、すなわち8−ヒドロキシ−5−[(1R)−1−ヒドロキシ−2−[[(1R)−2−(4−メトキシフェニル)−1−メチルエチル]アミノ]エチル]−2(1H)−キノリノンである、その塩酸塩も実験コードTA2005およびCHF4226として報告されている。
(a)一種もしくはそれ以上の活性成分を、任意に更なる活性成分または賦形剤または適切な量の低揮発成分を含む、一種もしくはそれ以上の補助溶媒に添加する工程、
(b)吸入器に該溶液を充填する工程、
(c)予め決めた量のリン酸または硫酸を添加する工程、
(d)ヒドロフルオロアルカン(HFA)を含む噴射剤を添加する工程、そして
(e)弁を圧着して、ガスを供給する工程。
一作動当り表示用量200μgのブデソニドを投与するための配合物を製造し、そして50μlの計量室がある計量弁を備えたアルマイト製キャニスタに充填した。
一作動当り表示用量1μgの活性成分を投与するために、8−ヒドロキシ−5−[(1R)−1−ヒドロキシ−2−[[(1R)−2−(4−メトキシフェニル)−1−メチルエチル]アミノ]エチル]−2(1H)−キノリノン塩酸塩(TA2005)の配合物を、下記の配合で製造した。
成分 量
単位当り 表示用量
────────────────────────────────────
mg % μg
TA2005 0.15 0.0016質量/容量 1
エタノール 1650 15質量 −
H2SO4 0.075M 0.2−0.6 0.18−0.54質量 −
HFA134aを加えた9.72mlとした
──────────────────────────────────
40℃、直立した缶で1ヶ月保存後の回収率
────────────────────────────────────
硫酸(0.075M) 回収率(t=0) 回収率(t=1ヶ月)
mg 質量% mcg mcg %
────────────────────────────────────
0.2 0.0018 153 151 98
0.4 0.0036 153 153 100
0.6 0.0054 155 153 98
────────────────────────────────────
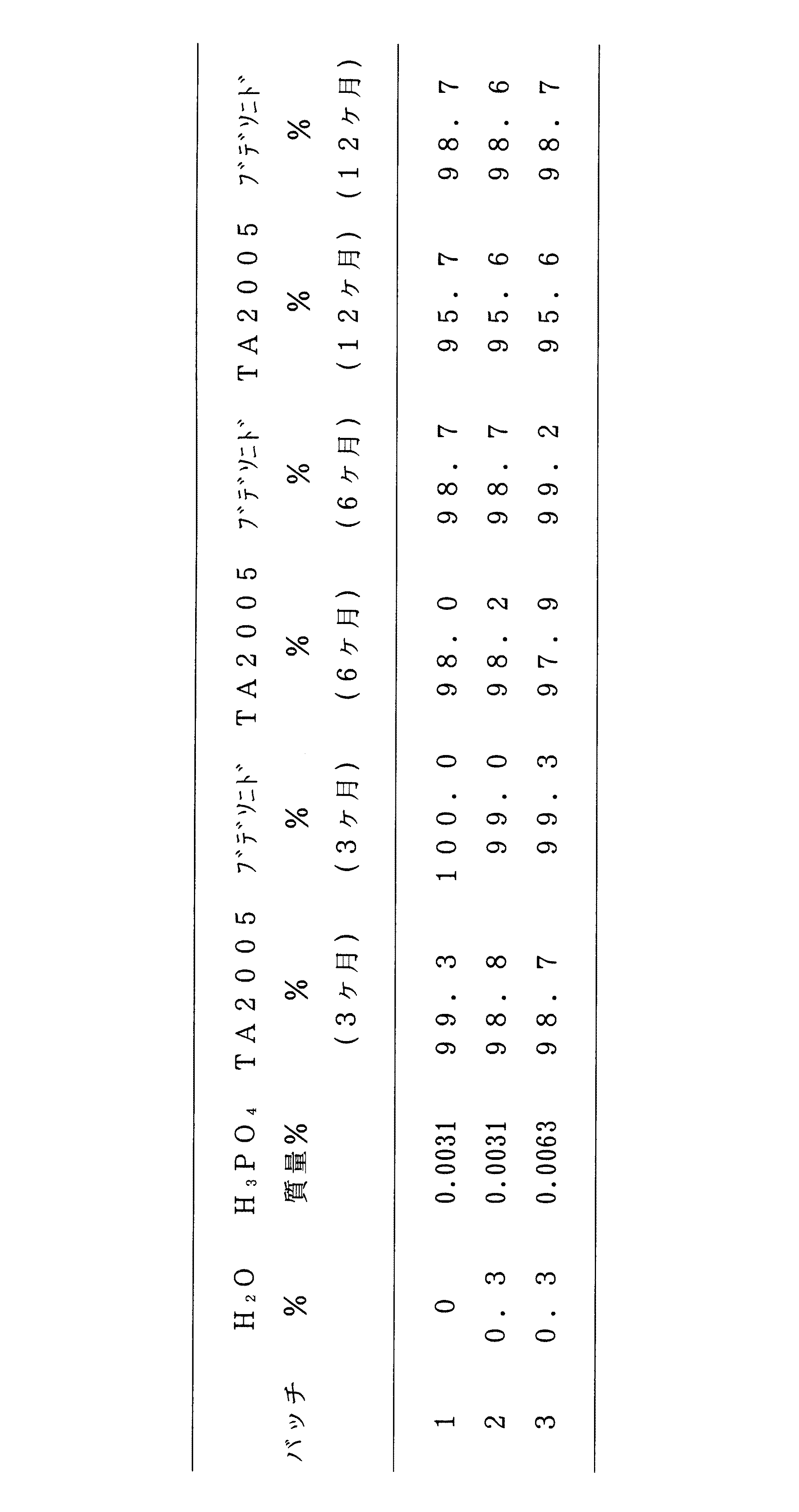
TA2005およそ0.30mg、およびブデソニド(「Bud」)およそ30mgを一緒にし、リン酸(15M)と水の量を変えて、HFA噴射剤/エタノール溶液を3バッチ分配合した。配合物を、ハロブチル又はブチルゴム(ブチル)弁を備えたテフロン被覆アルミニウム製キャニスタに入れた。キャニスタを、25℃、相対湿度60%で、倒立にした配置で最大12ヶ月間保存した。期間の様々な時点で安定性の研究を行った。下記の表に、詳細な結果を報告する。
Claims (18)
- 活性成分、液化HFA噴射剤、エタノール、並びにリン酸および硫酸からなる群より選ばれる金属イオン封鎖剤を含むエーロゾル配合物であって、該活性成分が、ブデソニド、フルニソリド、トリアムシノロンアセトニド、デキサメタゾン、およびベータメタゾン17バレレートから選ばれる20−ケトステロイドであって、該活性成分の化学安定性が改善されたエーロゾル配合物、ただし該エーロゾル配合物は、β 2 アゴニストを含有しない。
- 活性成分、液化HFA噴射剤、エタノール、並びにリン酸および硫酸からなる群より選ばれる金属イオン封鎖剤を含むエーロゾル配合物であって、該活性成分が、ブデソニド、フルニソリド、トリアムシノロンアセトニド、デキサメタゾン、およびベータメタゾン17バレレートから選ばれる20−ケトステロイドであって、該活性成分の化学安定性が改善されたエーロゾル配合物、ただし該エーロゾル配合物は、β 2 アゴニストを含む他の活性成分を含有しない。
- 活性成分、液化HFA噴射剤、エタノール、並びにリン酸および硫酸からなる群より選ばれる金属イオン封鎖剤を含むエーロゾル配合物であって、該活性成分が、ブデソニド、フルニソリド、トリアムシノロンアセトニド、デキサメタゾン、およびベータメタゾン17バレレートから選ばれる20−ケトステロイドのみであって、該活性成分の化学安定性が改善されたエーロゾル配合物。
- 該液化HFA噴射剤が、HFA134a、HFA227およびそれらの混合物からなる群より選ばれる少なくとも一種の成分である請求項1乃至3のうちのいずれか一項に記載の配合物。
- 該リン酸が、配合物の全質量に基づき0.0004乃至0.040質量/質量%の15Mリン酸と同等の量で存在する請求項1乃至4のうちのいずれか一項に記載の配合物。
- 該硫酸が、配合物の全質量に基づき0.0005乃至0.02質量/質量%の0.075M硫酸と同等の量で存在する請求項1乃至4のうちのいずれか一項に記載の配合物。
- 見掛pHが2.5から5.5までの間にある請求項1乃至6のうちのいずれか一項に記載の配合物。
- エタノールが、6乃至30質量/容量%の量で存在する請求項1乃至7のうちのいずれか一項に記載の配合物。
- エタノールが、6乃至25質量/容量%の量で存在する請求項1乃至8のうちのいずれか一項に記載の配合物。
- 該配合物が、活性成分が完全に溶解した溶液の状態にある請求項1乃至9のうちのいずれか一項に記載の配合物。
- 活性成分が懸濁状態にある請求項1乃至9のうちのいずれか一項に記載の配合物。
- 20−ケトステロイドがブデソニドである請求項1に記載の配合物。
- 活性成分の化学安定性を改善するための、請求項1乃至12のうちのいずれか一項に記載の配合物における、リン酸および硫酸から選ばれる金属イオン封鎖剤の使用。
- 請求項1乃至12のうちのいずれか一項に記載の配合物を含む加圧下にある用量計量型吸入器。
- 吸入器の金属内面の一部又は全部が、ステンレス鋼またはアルマイトであるか、または不活性有機被膜で内張りされている請求項14に記載の加圧下にある用量計量型吸入器。
- エポキシ−フェノール樹脂、ペルフルオロアルコキシアルカン類、ペルフルオロアルコキシアルキレン類、ペルフルオロアルキレン類、ポリエーテルスルホン類、フッ素化−エチレン−プロピレンとポリエーテルスルホンの混合物、およびそれらの混合物からなる群より選ばれる不活性有機被膜で内張りされている請求項15に記載の加圧下にある用量計量型吸入器。
- 活性成分が、6ヶ月後に95%又はそれより高いパーセント回収率を示す請求項15もしくは16に記載の加圧下にある用量計量型吸入器。
- 活性成分が、12ヶ月後に95%又はそれより高いパーセント回収率を示す請求項15もしくは16に記載の加圧下にある用量計量型吸入器。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP05004233.2 | 2005-02-25 | ||
| EP05004233 | 2005-02-25 | ||
| PCT/EP2006/001287 WO2006089656A2 (en) | 2005-02-25 | 2006-02-13 | Pharmaceutical aerosol formulations for pressurized metered dose inhalers comprising a sequestering agent |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2008537729A JP2008537729A (ja) | 2008-09-25 |
| JP2008537729A5 JP2008537729A5 (ja) | 2009-04-02 |
| JP5259193B2 true JP5259193B2 (ja) | 2013-08-07 |
Family
ID=36490097
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007556521A Expired - Fee Related JP5259193B2 (ja) | 2005-02-25 | 2006-02-13 | 加圧下にある用量計量型吸入器用の金属イオン封鎖剤を含む薬用エーロゾル配合物 |
Country Status (22)
| Country | Link |
|---|---|
| US (1) | US8877164B2 (ja) |
| EP (1) | EP1850831B1 (ja) |
| JP (1) | JP5259193B2 (ja) |
| KR (1) | KR101313959B1 (ja) |
| CN (1) | CN101119706B (ja) |
| AR (2) | AR054230A1 (ja) |
| AU (1) | AU2006218177B2 (ja) |
| BR (1) | BRPI0607990A2 (ja) |
| CA (1) | CA2594127C (ja) |
| EA (1) | EA013405B1 (ja) |
| GE (1) | GEP20105040B (ja) |
| IL (1) | IL184449A0 (ja) |
| MA (1) | MA29333B1 (ja) |
| MX (1) | MX2007010396A (ja) |
| NO (1) | NO20074854L (ja) |
| NZ (1) | NZ556376A (ja) |
| PE (1) | PE20061011A1 (ja) |
| SG (1) | SG159550A1 (ja) |
| TN (1) | TNSN07289A1 (ja) |
| UA (1) | UA92732C2 (ja) |
| WO (1) | WO2006089656A2 (ja) |
| ZA (1) | ZA200706870B (ja) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1950075A (zh) * | 2004-05-13 | 2007-04-18 | 奇斯药制品公司 | 化学稳定性改善的医用气溶胶制剂产品 |
| GB201200525D0 (en) * | 2011-12-19 | 2012-02-29 | Teva Branded Pharmaceutical Prod R & D Inc | An inhalable medicament |
| RU2519653C1 (ru) * | 2013-02-27 | 2014-06-20 | Шолекс Девелопмент Гмбх, | Аэрозольный препарат на основе ипратропия бромида для лечения заболеваний органов дыхания |
| US10034866B2 (en) * | 2014-06-19 | 2018-07-31 | Teva Branded Pharmaceutical Products R&D, Inc. | Inhalable medicament comprising tiotropium |
| US11642372B2 (en) | 2020-05-01 | 2023-05-09 | Tygrus, LLC | Therapeutic material with low pH and low toxicity active against at least one pathogen for addressing patients with respiratory illnesses |
| US12042514B2 (en) | 2020-05-01 | 2024-07-23 | Tygrus, LLC | Therapeutic material with low pH and low toxicity active against at least one pathogen for addressing patients with respiratory illnesses |
| US11826382B2 (en) | 2020-05-01 | 2023-11-28 | Tygrus, LLC | Therapeutic material with low pH and low toxicity active against at least one pathogen for addressing patients with respiratory illnesses |
Family Cites Families (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ZA939195B (en) * | 1992-12-09 | 1995-06-08 | Boehringer Ingelheim Pharma | Stabilized medicinal aerosol solution formulations |
| WO1994013262A1 (en) * | 1992-12-09 | 1994-06-23 | Boehringer Ingelheim Pharmaceuticals, Inc. | Stabilized medicinal aerosol solution formulations |
| DE69424181T2 (de) | 1993-12-20 | 2000-10-19 | Minnesota Mining And Mfg. Co., Saint Paul | Flunisolide aerosolformulierungen |
| BR9608721A (pt) * | 1995-06-07 | 1999-10-13 | Rhone Poulenc Rorer Pharma | Composição farmacêutica, e, processo para tratar inflamação |
| IL122752A (en) * | 1995-06-27 | 2001-07-24 | Boehringer Ingelheim Kg | Stable preparations for creating propellant-free sprays |
| DZ2947A1 (fr) * | 1998-11-25 | 2004-03-15 | Chiesi Farma Spa | Inhalateur à compteur de dose sous pression. |
| US6315985B1 (en) * | 1999-06-18 | 2001-11-13 | 3M Innovative Properties Company | C-17/21 OH 20-ketosteroid solution aerosol products with enhanced chemical stability |
| IT1313553B1 (it) * | 1999-07-23 | 2002-09-09 | Chiesi Farma Spa | Formulazioni ottimizzate costituite da soluzioni di steroidi dasomministrare per inalazione. |
| AU2001257621A1 (en) * | 2000-05-17 | 2001-11-26 | Chrysalis Technologies, Incorporated | Stabilized budesonide solution and method for making same |
| AU5070100A (en) * | 2000-05-22 | 2001-12-03 | Chiesi Farma Spa | Stable pharmaceutical solution formulations for pressurised metered dose inhalers |
| SI3494995T1 (sl) * | 2002-03-01 | 2020-08-31 | Chiesi Farmaceutici S.P.A. | Superfina formulacija formoterola |
| US7417051B2 (en) * | 2002-04-12 | 2008-08-26 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Medicaments comprising betamimetics and a novel anticholinergic |
| ES2248767T3 (es) | 2002-04-12 | 2006-03-16 | BOEHRINGER INGELHEIM PHARMA GMBH & CO.KG | Medicamento que contiene beta-mimeticos y un nuevo anticolinergico. |
| DE10230769A1 (de) | 2002-07-09 | 2004-01-22 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Neue Arzneimittelkompositionen auf der Basis neuer Anticholinergika und PDE-IV-Inhibitoren |
| US20040058950A1 (en) * | 2002-07-09 | 2004-03-25 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Pharmaceutical compositions based on anticholinergics and PDE-IV inhibitors |
| DE10237739A1 (de) | 2002-08-17 | 2004-02-26 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Inhalative Arzneimittel enthaltend ein neues Anticholinergikum in Kombination mit Corticosteroiden und Betamimetika |
| AU2003291634A1 (en) * | 2002-10-08 | 2004-05-04 | Sepracor Inc. | Fatty acid modified forms of glucocorticoids and their use as anti-inflammatory |
| EP1595531A1 (en) * | 2004-05-13 | 2005-11-16 | CHIESI FARMACEUTICI S.p.A. | Stable pharmaceutical solution formulations for pressurized metered dose inhalers |
-
2006
- 2006-02-13 MX MX2007010396A patent/MX2007010396A/es active IP Right Grant
- 2006-02-13 KR KR1020077016131A patent/KR101313959B1/ko not_active Expired - Fee Related
- 2006-02-13 CN CN2006800047251A patent/CN101119706B/zh not_active Expired - Fee Related
- 2006-02-13 EP EP06706899.9A patent/EP1850831B1/en not_active Expired - Lifetime
- 2006-02-13 WO PCT/EP2006/001287 patent/WO2006089656A2/en not_active Ceased
- 2006-02-13 EA EA200701805A patent/EA013405B1/ru not_active IP Right Cessation
- 2006-02-13 JP JP2007556521A patent/JP5259193B2/ja not_active Expired - Fee Related
- 2006-02-13 CA CA2594127A patent/CA2594127C/en not_active Expired - Fee Related
- 2006-02-13 SG SG201000998-3A patent/SG159550A1/en unknown
- 2006-02-13 AU AU2006218177A patent/AU2006218177B2/en not_active Ceased
- 2006-02-13 UA UAA200707949A patent/UA92732C2/ru unknown
- 2006-02-13 GE GEAP200610279A patent/GEP20105040B/en unknown
- 2006-02-13 BR BRPI0607990-3A patent/BRPI0607990A2/pt not_active IP Right Cessation
- 2006-02-13 NZ NZ556376A patent/NZ556376A/en not_active IP Right Cessation
- 2006-02-17 PE PE2006000199A patent/PE20061011A1/es not_active Application Discontinuation
- 2006-02-23 AR AR20060100670A patent/AR054230A1/es not_active Application Discontinuation
- 2006-02-24 US US11/361,562 patent/US8877164B2/en not_active Expired - Fee Related
-
2007
- 2007-07-05 IL IL184449A patent/IL184449A0/en unknown
- 2007-07-24 TN TNP2007000289A patent/TNSN07289A1/en unknown
- 2007-08-16 ZA ZA200706870A patent/ZA200706870B/xx unknown
- 2007-09-11 MA MA30220A patent/MA29333B1/fr unknown
- 2007-09-24 NO NO20074854A patent/NO20074854L/no not_active Application Discontinuation
-
2015
- 2015-04-06 AR ARP150101030A patent/AR099963A2/es unknown
Also Published As
| Publication number | Publication date |
|---|---|
| ZA200706870B (en) | 2008-11-26 |
| MX2007010396A (es) | 2007-10-19 |
| GEP20105040B (en) | 2010-07-12 |
| AU2006218177B2 (en) | 2012-04-12 |
| WO2006089656A3 (en) | 2006-12-21 |
| EP1850831B1 (en) | 2015-12-02 |
| AR099963A2 (es) | 2016-08-31 |
| IL184449A0 (en) | 2007-10-31 |
| CN101119706B (zh) | 2013-04-17 |
| NZ556376A (en) | 2010-01-29 |
| NO20074854L (no) | 2007-09-24 |
| EA200701805A1 (ru) | 2008-02-28 |
| HK1116337A1 (en) | 2008-12-19 |
| TNSN07289A1 (en) | 2008-12-31 |
| CA2594127A1 (en) | 2006-08-31 |
| MA29333B1 (fr) | 2008-03-03 |
| UA92732C2 (ru) | 2010-12-10 |
| WO2006089656A2 (en) | 2006-08-31 |
| EA013405B1 (ru) | 2010-04-30 |
| AU2006218177A1 (en) | 2006-08-31 |
| EP1850831A2 (en) | 2007-11-07 |
| BRPI0607990A2 (pt) | 2009-10-27 |
| KR20070107002A (ko) | 2007-11-06 |
| SG159550A1 (en) | 2010-03-30 |
| US8877164B2 (en) | 2014-11-04 |
| AR054230A1 (es) | 2007-06-13 |
| CN101119706A (zh) | 2008-02-06 |
| US20060193785A1 (en) | 2006-08-31 |
| JP2008537729A (ja) | 2008-09-25 |
| KR101313959B1 (ko) | 2013-10-02 |
| CA2594127C (en) | 2013-10-15 |
| PE20061011A1 (es) | 2006-12-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP1787639B1 (en) | Stable pharmaceutical solution formulations for pressurised metered dose inhalers | |
| JP4777560B2 (ja) | 増強された化学安定性を有するステロイド溶液エアゾール製品 | |
| US7381402B2 (en) | Stable pharmaceutical solution formulations for pressurized metered dose inhalers | |
| JP5259193B2 (ja) | 加圧下にある用量計量型吸入器用の金属イオン封鎖剤を含む薬用エーロゾル配合物 | |
| IL301617A (en) | A pharmaceutical formulation for pressurised metered dose inhaler | |
| US20070025920A1 (en) | Stable Pharmaceutical Solution Formulations for Pressurized Metered Dose Inhalers | |
| HK1116337B (en) | Pharmaceutical aerosol formulations for pressurized metered dose inhalers comprising a sequestering agent | |
| JP5409594B2 (ja) | 加圧式定量吸入器のための安定な製薬学的溶液製剤 | |
| KR20250016250A (ko) | 가압 정량 흡입기를 위한 약제학적 제제 | |
| EA048425B1 (ru) | Фармацевтический состав для дозирующего аэрозольного ингалятора | |
| HK1103280B (en) | Stable pharmaceutical solution formulations for pressurized metered dose inhalers | |
| MXPA06009584A (en) | Stable pharmaceutical solution formulations for pressurized metered dose inhalers | |
| PL203675B1 (pl) | Trwa le preparaty roztworów farmaceutycznych do inhalatorów z ci snieniowo dozowan a dawk a | |
| KR20060136446A (ko) | 압축화 계량된 도스흡입용 안정된 약제용액 제제 | |
| RS50233B (sr) | Stabilne farmaceutske formulacije rastvora za inhalatore odmerene doze pod pritiskom |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20090210 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20090210 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20111220 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20120319 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20120327 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20120515 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20120522 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120620 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20120831 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20121228 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20130311 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20130416 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20130424 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20160502 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| LAPS | Cancellation because of no payment of annual fees |