JP5121385B2 - 燃料電池システム - Google Patents
燃料電池システム Download PDFInfo
- Publication number
- JP5121385B2 JP5121385B2 JP2007266904A JP2007266904A JP5121385B2 JP 5121385 B2 JP5121385 B2 JP 5121385B2 JP 2007266904 A JP2007266904 A JP 2007266904A JP 2007266904 A JP2007266904 A JP 2007266904A JP 5121385 B2 JP5121385 B2 JP 5121385B2
- Authority
- JP
- Japan
- Prior art keywords
- hydrazine
- group
- resin
- immobilization
- aqueous
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/22—Fuel cells in which the fuel is based on materials comprising carbon or oxygen or hydrogen and other elements; Fuel cells in which the fuel is based on materials comprising only elements other than carbon, oxygen or hydrogen
- H01M8/222—Fuel cells in which the fuel is based on compounds containing nitrogen, e.g. hydrazine, ammonia
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/04—Auxiliary arrangements, e.g. for control of pressure or for circulation of fluids
- H01M8/04082—Arrangements for control of reactant parameters, e.g. pressure or concentration
- H01M8/04186—Arrangements for control of reactant parameters, e.g. pressure or concentration of liquid-charged or electrolyte-charged reactants
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/04—Auxiliary arrangements, e.g. for control of pressure or for circulation of fluids
- H01M8/04082—Arrangements for control of reactant parameters, e.g. pressure or concentration
- H01M8/04201—Reactant storage and supply, e.g. means for feeding, pipes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/04—Auxiliary arrangements, e.g. for control of pressure or for circulation of fluids
- H01M8/04298—Processes for controlling fuel cells or fuel cell systems
- H01M8/04313—Processes for controlling fuel cells or fuel cell systems characterised by the detection or assessment of variables; characterised by the detection or assessment of failure or abnormal function
- H01M8/0438—Pressure; Ambient pressure; Flow
- H01M8/04388—Pressure; Ambient pressure; Flow of anode reactants at the inlet or inside the fuel cell
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/04—Auxiliary arrangements, e.g. for control of pressure or for circulation of fluids
- H01M8/04298—Processes for controlling fuel cells or fuel cell systems
- H01M8/04313—Processes for controlling fuel cells or fuel cell systems characterised by the detection or assessment of variables; characterised by the detection or assessment of failure or abnormal function
- H01M8/0444—Concentration; Density
- H01M8/04447—Concentration; Density of anode reactants at the inlet or inside the fuel cell
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/04—Auxiliary arrangements, e.g. for control of pressure or for circulation of fluids
- H01M8/04298—Processes for controlling fuel cells or fuel cell systems
- H01M8/04694—Processes for controlling fuel cells or fuel cell systems characterised by variables to be controlled
- H01M8/04791—Concentration; Density
- H01M8/04798—Concentration; Density of fuel cell reactants
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/30—Hydrogen technology
- Y02E60/50—Fuel cells
Description
特許文献1および特許文献2の燃料電池では、燃料側電極で窒素のみが生成され、直接メタノール型燃料電池のように、炭酸ガスの生成がなく、実質的なゼロエミッションを実現することができる。
また、燃料電池は、燃料の残量を把握する方法などを含めて、システムとして効率的かつ経済的に構築する必要がある。
本発明の目的は、ヒドラジンを燃料とする燃料電池において、ヒドラジンを安全に利用することができながら、効率的かつ経済的なシステムとして構築することのできる、燃料電池システムを提供することにある。
また、本発明の燃料電池システムでは、検知部で検知されるヒドラジンの供給量と予め定める理論供給量とによって、固定化部に固定化されているヒドラジンの量を、検出部で検出することができる。検出部の検出により固定化されているヒドラジンの残量を検知することができるため、固定化部にヒドラジンの残量測定の機器を設けることを不要とすることができる。その結果、燃料電池システムを、効率的かつ経済的なシステムとして構築することができる。
図1は、本発明の燃料電池システムの一実施形態を示す概略構成図である。
図1において、燃料電池システムS1は、ヒドラジンが燃料として供給される燃料電池1と、ヒドラジンを固定化する固定化部2と、ヒドラジンを固定化部2へ供給するヒドラジン供給部3と、水系脱離液を固定化部2へ供給する脱離液供給部4と、固定化部2から燃料電池1へヒドラジンを燃料として供給する燃料供給部5と、固定化部2に固定化されているヒドラジンの量を検知する検出部6とを備えている。
(A)固定化部
固定化部2は、ケーシング7と、ケーシング7内に収容される固定化部材8とを備えている。
ケーシング7内には、攪拌機9が設けられている。攪拌機9によって、ケーシング7内に供給されるヒドラジンや水系脱離液が適宜攪拌される。
固定化部材8は、ケーシング7内に収容されている。固定化部材8は、ヒドラジンを固定化および脱離する合成樹脂(以下、固定化樹脂という。)からなり、ヒドラジンを脱離可能に固定化するヒドラジン固定基を有している。
そして、ヒドラジン固定基にヒドラジンが脱離可能に固定化されると、ヒドラジン脱離基が形成される。
また、固定化樹脂は、ヒドラジンが親水性であることから、親水性が付与されていることが好適である。固定化樹脂に親水性を付与するには、例えば、ポリオキシエチレンなどの親水性ユニットを主鎖に導入するか、あるいは、主鎖から枝分れする側鎖に、例えば、水酸基、カルボキシル基、スルホン酸基、リン酸基、アミド基、第4級アンモニウム基などの親水性基を導入する。
(1)炭化水素系固定化樹脂
炭化水素系固定化樹脂は、ヒドラジン固定基含有ビニルモノマーを単独重合させるか、あるいは、ヒドラジン固定基含有ビニルモノマーと、そのヒドラジン固定基含有ビニルモノマーと共重合可能な共重合ビニルモノマーとを共重合させることにより、得ることができる。
(1−1)炭化水素系固定化樹脂の合成
ヒドラジン固定基含有ビニルモノマーは、ヒドラジン固定基とビニル基とを併有するモノマーであって、例えば、アクロレイン、メチルビニルケトン、エチルビニルケトン、ヘキシルビニルケトン、p−アセチルメチルスチレン、p−アセチルスチレン、アクリル酸メチル、p−クロルメチルスチレン、o−アセチルメチルビニルアルコール、o−アセチルメチルアリルアルコール、N−アセチルメチルビニルピリジンなどが挙げられる。これらヒドラジン固定基含有ビニルモノマーは、単独使用または2種以上併用することができる。
親水性ビニルモノマーは、例えば、カルボキシル基、スルホン酸基、リン酸基などのイオン性解離基とビニル基とを併有するモノマーであって、例えば、アクリル酸、メタクリル酸、マレイン酸、イタコン酸、ケイ皮酸、フマル酸、マレイン酸モノアルキルエステル、イタコン酸モノアルキルエステル、スチレンスルホン酸、アリルスルフォコハク酸、2−アクリルアミド−2−メチルプロパンスルホン酸、アシッドホスホオキシエチルメタクリレート、3−クロロ−2−アシッドホスホオキシプロピルメタクリレートなどが挙げられる。これら親水性ビニルモノマーは、単独使用または2種以上併用することができる。
架橋性ビニルモノマーは、複数のビニル基を有するモノマーであって、例えば、ジビニルベンゼン、N,N´−メチレンビス(メタ)アクリルアミド、エチレングリコールジ(メタ)アクリレート、ポリエチレングリコールジ(メタ)アクリレート、プロピレングリコールジ(メタ)アクリレート、グリセリン(ジまたはトリ)アクリレート、トリメチロールプロパントリアクリレート、ネオペンチルグリコールジ(メタ)メタクリレート、トリアリルアミン、トリアリルシアヌレート、トリアリルイソシアヌレート、テトラアリロキシエタン、ペンタエリスリトールトリアリルエーテルなどが挙げられる。これら架橋性ビニルモノマーは、単独使用または2種以上併用することができる。
ヒドラジン固定基含有ビニルモノマーに対する共重合ビニルモノマーの配合割合は、ヒドラジンの供給量や要求物性などにより、適宜選択されるが、例えば、ヒドラジン固定基含有ビニルモノマーの固定基に対して、共重合ビニルモノマーが、当量比で、例えば、1:0.01〜100、好ましくは、1:0.1〜10、さらに好ましくは、1:0.5〜2である。より具体的には、ヒドラジン固定基含有ビニルモノマーの固定基に対して、親水性ビニルモノマーが、当量比で、例えば、1:0.01〜100、好ましくは、1:0.1〜10、さらに好ましくは、1:0.5〜2である。また、ヒドラジン固定基含有ビニルモノマーと親水性ビニルモノマーの合計100重量部に対して、架橋性ビニルモノマーが、例えば、0.1〜100重量部、好ましくは、1〜10重量部である。
ラジカル重合開始剤は、特に制限されず、例えば、2,2′−アゾビス−(2,4−ジメチルバレロニトリル)、2,2′−アゾビスイソブチロニトリル、1,1′−アゾビス(シクロヘキサン−1−カルボニトリル)、2,2′−アゾビス−4−メトキシ−2,4−ジメチルバレロニトリル、アゾビスイソブチロニトリル、2,2´−アゾビス(2−アミジノプロパン)などのアゾ系重合開始剤、例えば、ベンゾイルパーオキサイド、メチルエチルケトンペルオキサイド、ジイソプロピルペルオキシカーボネート、クメンヒドロペルオキサイド、t−ブチルヒドロペルオキサイド、ジ−t−ブチルペルオキサイド、ジクミルペルオキサイド、2,4−ジクロロベンゾイルペルオキサイド、ラウロイルペルオキサイド、2,2−ビス−(4,4−t−ブチルペルオキシシクロヘキシル)プロパン、トリス−(t−ブチルペルオキシ)トリアジンなどのパーオキサイド系重合開始剤、例えば、過硫酸カリウム、過硫酸アンモニウムなどの過硫酸塩、例えば、過酸化水素と還元剤(アスコルビン酸など)とを組合せるレドックス系開始剤などが挙げられる。
(1−2)炭化水素系固定化樹脂に対するヒドラジンの固定化
炭化水素系固定化樹脂にヒドラジンを固定化するには、例えば、炭化水素系固定化樹脂の固定化基(ケトン基)に対して、適当量(好ましくは当量以上)のヒドラジンを原料供給ライン13(後述)から供給し、ヒータ11で、例えば、室温〜100℃に温め、攪拌機9で、例えば、10分〜48時間攪拌する。すると、固定化基(ケトン基)にヒドラジンが固定化される。
(1−3)炭化水素系固定化樹脂からのヒドラジンの脱離
炭化水素系固定化樹脂からヒドラジンを脱離させるには、例えば、ケーシング7内に、脱離液供給部4から水系脱離液を供給する。すると、炭化水素系固定化樹脂が、水系脱離液によって分散され、炭化水素系固定化樹脂からヒドラジンが脱離される。
(2)ポリアクリルアミド系固定化樹脂
ポリアクリルアミド系固定化樹脂は、アクリルアミドのラジカル重合により得ることができる。
(2−1)ポリアクリルアミド系固定化樹脂の合成
ポリアクリルアミド系固定化樹脂は、アクリルアミドを水に配合して、アクリルアミド水溶液を調製した後、そのアクリルアミド水溶液にラジカル重合開始剤を添加して、アクリルアミドをラジカル重合させることにより、合成することができる。
(2−2)ポリアクリルアミド系固定化樹脂に対するヒドラジンの固定化
ポリアクリルアミド系固定化樹脂にヒドラジンを固定化するには、ポリアクリルアミド系固定化樹脂の固定化基(アミド基)に対して、適当量(好ましくは当量以上)のヒドラジンを原料供給ライン13(後述)から供給し、上記と同様に攪拌する。すると、固定化基(アミド基)にヒドラジンが固定化されて、ポリアクリル酸ヒドラジッドが得られる。
(2−3)ポリアクリルアミド系固定化樹脂からのヒドラジンの脱離
ポリアクリルアミド系固定化樹脂からヒドラジンを脱離させるには、例えば、ケーシング7内に、脱離液供給部4から水系脱離液を供給する。すると、ポリアクリルアミド系固定化樹脂が、水系脱離液によって分散され、ポリアクリルアミド系固定化樹脂からヒドラジンが脱離される。
(3)ポリ(メタ)アクリレート系固定化樹脂
ポリ(メタ)アクリレート系固定化樹脂は、まず、(メタ)アクリル酸エステルをラジカル重合することにより、得ることができる。
(3−1)ポリ(メタ)アクリレート系固定化樹脂の合成
ポリ(メタ)アクリレート系固定化樹脂は、(メタ)アクリル酸エステルにラジカル重合開始剤を添加して、重合させることによって得ることができる。得られたポリ(メタ)アクリレート系固定化樹脂は、微粉砕して、ケーシング7内に収容する。
(3−2)ポリ(メタ)アクリレート系固定化樹脂に対するヒドラジンの固定化
ポリ(メタ)アクリレート系固定化樹脂にヒドラジンを固定化するには、ポリ(メタ)アクリレート系固定化樹脂の固定化基(エステル基)に対して、当量以上のヒドラジンを原料供給ライン13(後述)から供給し、上記と同様に攪拌する。すると、固定化基(エステル基)にヒドラジンが固定化されて、ポリアクリル酸ヒドラジッドが得られる。
(3−3)ポリ(メタ)アクリレート系固定化樹脂からのヒドラジンの脱離
ポリ(メタ)アクリレート系固定化樹脂からヒドラジンを脱離させるには、例えば、ケーシング7内に、脱離液供給部4から水系脱離液を供給する。すると、ポリ(メタ)アクリレート系固定化樹脂が、水系脱離液によって分散され、ポリ(メタ)アクリレート系固定化樹脂からヒドラジンが脱離される。
(4)ポリビニルアルコール系固定化樹脂
ポリビニルアルコール系固定化樹脂は、ヒドラジン固定基含有ビニルモノマーと、酢酸ビニルとを共重合させることにより、ヒドラジン固定基含有ポリ酢酸ビニル共重合体を合成し、次いで、これをケン化することにより、得ることができる。
(4−1)ポリビニルアルコール系固定化樹脂の合成
ヒドラジン固定基含有ビニルモノマーは、ヒドラジン固定基とビニル基とを併有するモノマーであって、例えば、メチルビニルケトン、エチルビニルケトンなどのアルキルまたはアリールビニルケトン、p−アセチルメチレンオキシスチレン、p−アセチルエチレンオキシスチレンなどのp−アセチルアルキレンオキシスチレン、p−クロルメチルスチレンなどが挙げられる。これらヒドラジン固定基含有ビニルモノマーは、単独使用または2種以上併用することができる。
ラジカル重合は、特に制限されず、上記と同様の方法により実施することができる。また、例えば、ラジカル重合開始剤として、アゾ系重合開始剤やパーオキサイド系重合開始剤が用いられる。
その後、ヒドラジン固定基含有ポリ酢酸ビニルを、溶媒(例えば、アルコール類)に配合した後、アルカリ(例えば、NaOH水溶液、KOH水溶液など)を添加して、ケン化し、再度、水中に沈殿させ、これを単離および乾燥して、ポリビニルアルコール系固定化樹脂を得る。
(4−2)ポリビニルアルコール系固定化樹脂に対するヒドラジンの固定化
ポリビニルアルコール系固定化樹脂に、ヒドラジンを固定化するには、ポリビニルアルコール系固定化樹脂の固定化基(ケトン基、ハロゲノ基、ホルミル基、アミド基、エステル基など)に対して、適当量(好ましくは当量以上)のヒドラジンを原料供給ライン13(後述)から供給して、上記と同様に攪拌する。すると、固定化基(ケトン基、ハロゲノ基、ホルミル基、アミド基、エステル基など)にヒドラジンが固定化される。
(4−3)ポリビニルアルコール系固定化樹脂からのヒドラジンの脱離
ポリビニルアルコール系固定化樹脂からヒドラジンを脱離させるには、例えば、ケーシング7内に、脱離液供給部4から水系脱離液を供給する。すると、ポリビニルアルコール系固定化樹脂が、水系脱離液によって分散され、ポリビニルアルコール系固定化樹脂からヒドラジンが脱離される。
(5)ポリエステル系固定化樹脂
ポリエステル系固定化樹脂は、まず、ヒドラジン固定基含有多価アルコールと多塩基酸とを縮合重合させることにより、得ることができる。また、多価アルコールとヒドラジン固定基含有多塩基酸とを縮合重合させることにより、得ることもできる。さらに、ヒドラジン固定基含有多価アルコール(および必要により多価アルコール)と、ヒドラジン固定基含有多塩基酸(必要により多塩基酸)とを縮合重合させることにより、得ることもできる。
(5−1)ポリエステル系固定化樹脂の合成
ヒドラジン固定基含有多価アルコールは、ヒドラジン固定基と少なくとも2つの水酸基とを併有する多価アルコールであって、例えば、アセチルエチルエチレングリコールなどが挙げられる。また、必要により、例えば、エチレングリコール、プロピレングリコール、ブチレングリコール、ネオペンチルグリコールなどの多価アルコールを併用することもできる。
そして、ポリエステル系固定化樹脂は、ヒドラジン固定基含有多価アルコール(および必要により多価アルコール)と多塩基酸とを配合して、縮合重合することにより、得ることができる。
(5−2)ポリエステル系固定化樹脂に対するヒドラジンの固定化
ポリエステル系固定化樹脂にヒドラジンを固定化するには、ポリエステル系固定化樹脂の固定化基(ケトン基、ハロゲノ基、ホルミル基、アミド基、エステル基など)に対して、適当量(好ましくは当量以上)のヒドラジンを原料供給ライン13から供給して、上記と同様に攪拌する。すると、固定化基(ケトン基、ハロゲノ基、ホルミル基、アミド基、エステル基など)にヒドラジンが固定化される。
(5−3)ポリエステル系固定化樹脂からのヒドラジンの脱離
ポリエステル系固定化樹脂からヒドラジンを脱離させるには、例えば、ケーシング7内に、脱離液供給部4から水系脱離液を供給する。すると、ポリエステル系固定化樹脂が、水系脱離液によって分散され、ポリエステル系固定化樹脂からヒドラジンが脱離される。
(6)ポリアミド系固定化樹脂
ポリアミド系固定化樹脂は、多価アミンおよび多塩基酸(但し、多価アミンおよび多塩基酸の少なくとも一方にヒドラジン固定基が含まれていることが必要である。)の重合により、得ることができる。
(6−1)ポリアミド系固定化樹脂の合成
脂肪族多価アミンとしては、少なくとも2個のアミノ基を有し、例えば、エチレンジアミン、ヘキサメチレンジアミン、シクロヘキサンジアミンなどが挙げられる。
脂肪族多塩基酸は、少なくとも2つのカルボン酸を有し、例えば、アジピン酸、スペリン酸、アゼライン酸、セバシン酸、ドデカン二酸、ヘキサヒドロテレフタル酸、ヘキサヒドロイソフタル酸などが挙げられる。
多価アミンと多塩基酸との重合は、これらをほぼ当量で配合して、必要により、不活性ガス雰囲気下、減圧して、反応させる。反応温度は、例えば、30〜400℃、好ましくは、70〜300℃の範囲である。
ポリアミド系固定化樹脂は、そのまま使用することができるが、さらに、ポリアミド系固定化樹脂を適宜の溶媒(例えば、N−メチルピロリドン)に溶解した後、ハロゲノメチル基に対して当量以上のアセトンを添加し、さらに、アルカリ(例えば、NaOH水溶液、KOH水溶液など)を添加して攪拌することにより、ハロゲノメチル基をアセチルエチル基に変換することもできる。
(6−2)ポリアミド系固定化樹脂に対するヒドラジンの固定化
ポリアミド系固定化樹脂にヒドラジンを固定化するには、ポリアミド系固定化樹脂の固定化基(ケトン基、ハロゲノメチル基など)に対して、当量以上のヒドラジンを原料供給ライン13から供給して、上記と同様に攪拌する。すると、固定化基(ケトン基、ハロゲノメチル基など)にヒドラジンが固定化される。
(6−3)ポリアミド系固定化樹脂のヒドラジンの脱離およびヒドラジンの供給
ポリアミド系固定化樹脂からヒドラジンを脱離させるには、例えば、ケーシング7内に、脱離液供給部4から水系脱離液を供給する。すると、ポリアミド系固定化樹脂が、水系脱離液によって分散され、ポリアミド系固定化樹脂からヒドラジンが脱離される。
(7)ポリエーテル系固定化樹脂
ポリエーテル系固定化樹脂は、フェノール誘導体を、銅触媒および塩基の存在下で重合させることにより芳香環含有ポリエーテルを合成し、次いで、芳香環含有ポリエーテルの芳香環をハロゲノメチル化することにより、得ることができる。
(7−1)ポリエーテル系固定化樹脂の合成
フェノール誘導体としては、例えば、2,6−ジメチルフェノール、2,6−ジフェニルフェノールなどが挙げられる。
ポリエーテル系固定化樹脂は、そのまま使用することができるが、さらに、ポリエーテル系固定化樹脂を適宜の溶媒(例えば、クロロホルム)に溶解した後、ハロゲノメチル基に対して当量以上のアセトンを添加し、さらにアルカリ(例えば、NaOH水溶液、KOH水溶液など)を添加して攪拌して、ハロゲノメチル基を、例えば、アセチルエチル基に変換することもできる。さらに、モノクロルアセトン、モノクロルメチルアルキルケトン、モノクロルメチルアリルケトン、モノクロルメチルアラルキルケトンなどを反応させ、アセチルメチル基などのケトン基含有側鎖を導入することもできる。
(7−2)ポリエーテル系固定化樹脂に対するヒドラジンの固定化
ポリエーテル系固定化樹脂の固定化基(ケトン基、ハロゲノメチル基など)に対して、適当量(好ましくは当量以上)のヒドラジンを原料供給ライン13から供給して、上記と同様に攪拌する。すると、固定化基(ケトン基、ハロゲノメチル基など)にヒドラジンが固定化される。
(7−3)ポリエーテル系固定化樹脂のヒドラジンの脱離およびヒドラジンの供給
ポリエーテル系固定化樹脂からヒドラジンを脱離させるには、例えば、ケーシング7内に、脱離液供給部4から水系脱離液を供給する。すると、ポリエーテル系固定化樹脂が、水系脱離液によって分散され、ポリエーテル系固定化樹脂からヒドラジンが脱離される。
(8)ポリエーテルケトン系固定化樹脂
ポリエーテルケトン系固定化樹脂は、ジハロゲノベンゾフェノンとジフェノールとをアルカリ存在下に重合させることにより、得ることができる。
(8−1)ポリエーテルケトン系固定化樹脂の合成
ジハロゲノベンゾフェノンとしては、例えば、4,4′−ジハロベンゾフェノン、2,4′−ジハロベンゾフェノン、ビス−1,4−(4−ハロベンゾイル)ベンゼン、ビス−1,3−(4−ハロベンゾイル)ベンゼン、ビス−4,4′−(4−ハロベンゾイル)ビフェニル、ビス−4,4′−(4−ハロベンゾイル)ジフェニルエーテルなどが挙げられる。
アルカリとしては、アルカリ金属の炭酸塩、アルカリ土類金属の炭酸塩、アルカリ金属の重炭酸塩、アルカリ土類金属の炭酸塩、アルカリ金属の水酸化物などが挙げられる。
なお、ジハロゲノベンゾフェノンとジフェノールとの配合割合は、ほぼ当量でよく、また、重合には、公知の触媒および溶媒が添加される。また、反応温度は、例えば、10〜300℃、好ましくは、50〜200℃の範囲である。
溶媒としては、例えば、ジメチルスルホン、ジエチルスルホン、スルフォランなどの脂肪族スルホン類、例えば、ジフェニルスルホン、ジトリルスルホン、メチルフェニルスルホン、ジベンゾチオフェンオキサイド、フェノキサチンジオキシド、4ーフェニルスルフォニルビフェニルなどの芳香族スルホン類、例えば、ベンゾフェノン、イソフタロフェノン、テレフタロフェノン、4ーベンゾイルジフェニルエーテル、フルオレノン、キサントン、チオキサントンなどの芳香族ケトン類などが挙げられる。
(8−2)ポリエーテルケトン系固定化樹脂に対するヒドラジンの固定化
ポリエーテルケトン系固定化樹脂に、ヒドラジンを固定化するには、ポリエーテルケトン系固定化樹脂の固定化基(ケトン基、ハロゲノメチル基など)に対して、適当量(好ましくは当量以上)のヒドラジンを原料供給ライン13から供給して、上記と同様に攪拌する。すると、固定化基(ケトン基、ハロゲノメチル基など)にヒドラジンが固定化される。
(8−3)ポリエーテルケトン系固定化樹脂のヒドラジンの脱離
ポリエーテルケトン系固定化樹脂からヒドラジンを脱離させるには、例えば、ケーシング7内に、脱離液供給部4から水系脱離液を供給する。すると、ポリエーテルケトン系固定化樹脂が、水系脱離液によって分散され、ポリエーテルケトン系固定化樹脂からヒドラジンが脱離される。
(9)ポリチオエーテル系固定化樹脂
ポリチオエーテル系固定化樹脂は、ジハロゲノベンゼンと、硫化ナトリウムとを反応させることにより芳香環含有ポリチオエーテルを合成し、次いで、芳香環含有ポリチオエーテルの芳香環をハロゲノメチル化することにより、得ることができる。
(9−1)ポリチオエーテル系固定化樹脂の合成
ジクロロベンゼンとしては、例えば、p−ジクロロベンゼンなどが挙げられる。
ポリチオエーテル系固定化樹脂は、そのまま使用することができるが、さらに、ポリチオエーテル系固定化樹脂を適宜の溶媒(例えば、ジメチルスルホキシド)に溶解した後、ハロゲノメチル基に対して当量以上のアセトン、メチルアルキルケトン、メチルアリルケトンまたはメチルアラルキルケトンを添加し、さらにアルカリ(例えば、NaOH水溶液、KOH水溶液など)を添加して攪拌し、ハロゲノメチル基を、例えば、アセチルエチル基に変換することもできる。
(9−2)ポリチオエーテル系固定化樹脂に対するヒドラジンの固定化
ポリチオエーテル系固定化樹脂に、ヒドラジンを固定化するには、ポリチオエーテル系固定化樹脂の固定化基(ケトン基、ハロゲノメチル基など)に対して、適当量(好ましくは当量以上)のヒドラジンを原料供給ライン13から供給して、上記と同様に攪拌する。すると、固定化基(ケトン基、ハロゲノメチル基など)にヒドラジンが固定化される。
(9−3)ポリチオエーテル系固定化樹脂のヒドラジンの脱離
ポリチオエーテル系固定化樹脂からヒドラジンを脱離させるには、例えば、ケーシング7内に、脱離液供給部4から水系脱離液を供給する。すると、ポリチオエーテル系固定化樹脂が、水系脱離液によって分散され、ポリエーテルケトン系固定化樹脂からヒドラジンが脱離される。
(B)ヒドラジン供給部
ヒドラジン供給部3は、ヒドラジンを貯留するヒドラジン貯留槽12と、ヒドラジン貯留槽12からケーシング7へヒドラジンを供給する原料供給ライン13とを備えている。
ヒドラジンには、水加ヒドラジン(ヒドラジンヒドラート)および無水ヒドラジンのいずれも含まれる。
(C)脱離液供給部
脱離液供給部4は、水系脱離液を貯留する脱離液貯留槽15と、脱離液貯留槽15からケーシング7へ水系脱離液を供給する脱離液供給ライン16とを備えている。
水系脱離液は、固定化部材8に固定化されているヒドラジンを脱離させるための水または水溶液であり、上記したように、例えば、水、例えば、NaOH水溶液、KOH水溶液などのアルカリ水溶液などが挙げられる。
(D)燃料供給部
燃料供給部5は、上記と同様の材料から形成され、ケーシング7と燃料電池1とを接続する燃料供給ライン18を備えている。燃料供給部5の途中には、燃料側開閉弁19が設けられている。
ヒドラジンセンサ22は、燃料供給ライン18内に配置され、例えば、燃料供給ライン18を流れるヒドラジン水溶液(後述)の流量(ヒドラジン流量)およびヒドラジン水溶液(後述)に含まれるヒドラジンの濃度(ヒドラジン濃度)を検知して、それらの値を電気信号として制御部30(後述)へ入力する。ヒドラジンセンサ22としては、例えば、赤外分光法によりヒドラジンの赤外吸光度を測定するIRセンサ(赤外線センサ)など、公知の濃度センサを適用することができる。
(E)燃料電池
燃料電池1は、ヒドラジンを燃料とする燃料電池であれば、特に制限されず、例えば、固体高分子膜型燃料電池であって、例えば、国際公開パンフレットWO2003/056649(特許文献2参照)に記載されている燃料電池が挙げられる。
そして、ヒドラジンは、水系脱離液(水またはアルカリ水溶液)とともに、燃料供給ライン18から燃料電池1の燃料側電極へ流入される。また、酸素側電極には、酸素(空気)が流入される。すると、下記式の反応が生じて、起電力が発生する。
その後、上記反応により生成した窒素、および、水(水系脱離液がアルカリを含有する場合には、水にはアルカリが含まれる)が、排水として排出される。
(F)検出部
検出部6は、固定化部2に固定化されているヒドラジンの量を検出するための制御部30と、検出されたヒドラジンの量を表示するためのインジケータ24とを備えている。
制御部30は、ヒドラジンセンサ22から入力されたヒドラジン流量とヒドラジン濃度とを元に、理論供給値を参照して、固定化部材8に固定化されているヒドラジンの量を検出する。そして、検出したヒドラジンの量をインジケータ24に表示する。
なお、燃料電池システムS1において、原料供給ライン13、脱離液供給ライン16、および、燃料供給ライン18には、そのレイアウトにもよるが、重力輸送が困難な場合などには、適宜、公知の送液ポンプが設けられる。
II.作用効果
次に、この実施形態の燃料電池システムS1の作用効果について詳述する。
次いで、脱離液側開閉弁17を、燃料電池1の運転条件に対応するように、一定時間、一定開度で開放することにより、脱離液貯留槽15から、水系脱離液を所定流量で、脱離液供給ライン16を介してケーシング7へ供給する。すると、ケーシング7内では、固定化樹脂の種類に対応した脱離条件(例えば、脱離温度など)によって、ヒドラジンが固定化部材8から脱離される。
ヒドラジン水溶液を燃料電池1に供給するときには、燃料供給ライン18を流れるヒドラジン水溶液の流量(ヒドラジン流量)およびヒドラジン水溶液に含まれるヒドラジンの濃度(ヒドラジン濃度)が、ヒドラジンセンサ22で検知され、それらの値(実測値)が電気信号として制御部30に入力される。
また、燃料電池システムS1では、ヒドラジンセンサ22で検知される実測値と、予め制御部30に記憶された理論供給値とにより、固定化部材8に固定化されているヒドラジンの量を検出することができる。制御部30の検出により固定化されているヒドラジンの残量を検知することができるため、ケーシング7にヒドラジンの残量測定の機器を設けることを不要とすることができる。さらに、ヒドラジン濃度を、ケーシング7よりも濃度ムラの生じにくい燃料供給ライン18で測定(検知)するので、効率的にヒドラジンの残量検知を行なうことができる。その結果、燃料電池システムS1を、効率的かつ経済的なシステムとして構築することができる。
(車載する実施形態)
図2は、図1に示す実施形態の燃料電池システムS1を、車両に搭載したときの概略説明図である。なお、図2において、上記と同様の部材には、同一の符号を付し、その説明を省略する。
この場合、ヒドラジン貯留槽12は、原料補給ステーションに装備される。車両において、固定化部2で固定化されているヒドラジンがエンプティ状態となったときには、原料補給ステーションにおいて、ヒドラジン貯留槽12からのヒドラジンが、供給口36から原料供給ライン13へ注入される。
また、ケーシング7は、車両35の前後方向中央に配置されている。また、脱離液貯留槽15は、ケーシング7の上方に配置されている。
燃料電池システムS1が車載される場合には、例えば、停車時(発電停止時)に、原料補給ステーションでヒドラジンを補給して、ヒドラジンを固定化部材8に固定化しておき、走行時(発電時)に、脱離液貯留槽15から水系脱離液をケーシング7に供給して、ヒドラジンを脱離させ、燃料電池1へ供給する。
例えば、上述の実施形態では、理論供給値を、ヒドラジンが最大量で固定化されている固定化部材8に対して、水系脱離液を所定流量で供給してヒドラジンを脱離させる条件において、水系脱離液の供給流量と同じ流量で水系脱離液とともに燃料電池1に供給されるヒドラジンの濃度、と定義したが、上記条件にヒドラジンを固定化部材8から脱離させるときの温度(ヒドラジン脱離温度)を加えた条件において、水系脱離液の供給流量と同じ流量で燃料電池1に供給されるヒドラジンの濃度、と定義してもよい。
具体例1(炭化水素系アミド架橋固定化樹脂(固定基:ケトン基))
1)炭化水素系アミド架橋固定化樹脂の合成
メチルビニルケトン20g、p−スチレンスルホン酸Na59g、架橋剤としてメチレンビスアクリルアミド2.3g、イオン交換水79gを均一に混合して重合水溶液を作製し、重合槽に投入した。重合水溶液に窒素ガスを導入して、重合水溶液中の溶存酸素量を0.2ppmにし、また、溶液温度を5℃にした。
得られた含水ゲル状重合体を、ミートチョッパーを用いて小片に粉砕し、得られた小片含水ゲル重合体を、通気熱風乾燥機(井上金属工業社製)を用いて、供給風温120℃、風速1.5m/秒の条件下で70分間通気乾燥して、水分含量が約4%の乾燥物を得た。
この親水性固定化樹脂の吸収倍率は、9倍であった。なお、吸収倍率は、250メッシュのナイロン網で作製したティーバッグ(縦20cm、横10cm)に親水性固定化樹脂1gを入れ、生理食塩水(NaCl濃度0.90%のイオン交換水溶液)中に60分間浸漬した後、15分間吊るして水切りしてから、余剰水を取り除き、遠心脱水後の増加質量を測定することにより求めた。
2)炭化水素系アミド架橋固定化樹脂に対するヒドラジンの固定化
上記1)で得られた親水性固定化樹脂に、その樹脂2g中に含有するケトン基の2倍のモル数のヒドラジンを含有する100%ヒドラジンヒドラートを添加して、60分間攪拌反応させることにより、親水性固定化樹脂にヒドラジンを固定化し、これによって、親水性固定化樹脂を得た。
3)炭化水素系アミド架橋固定化樹脂のヒドラジンの脱離
3−1)アルカリによる脱離
上記2)で得られた親水性固定化樹脂0.8gを、1N−KOH水溶液に室温で分散して、攪拌した。1N−KOH水溶液中のヒドラジンを、HPLCで定量した結果、72.1%であった。
3−2)再固定化
上記3−1)でヒドラジンを脱離した親水性固定化樹脂に、その樹脂0.6g中に含有するケトン基の2倍のモル数のヒドラジンを含有する100%ヒドラジンヒドラートを添加して、60分間攪拌反応させることにより、親水性固定化樹脂にヒドラジンを固定化し、これによって、再度、親水性固定化樹脂を得た。
3−3)水による脱離
上記2)で得られた親水性固定化樹脂0.8gを、水に室温で分散して、攪拌した。水中のヒドラジンを、HPLCで定量した結果、固定化されているヒドラジンの72.8%の脱離を確認した。これは、最初のケトン基に対するヒドラジンの変換率として、78.8%に相当する。
具体例2(炭化水素系アミド架橋固定化貯蔵樹脂(固定基:ケトン基))
1)炭化水素系アミド架橋固定化樹脂に対するヒドラジンの固定化
具体例1の1)で得られた親水性固定化樹脂に、その樹脂に含有するケトン基と等モル数のヒドラジンを添加し、具体例1の2)と同様の操作を行った。その結果、濾液のイソプロピルアルコール中のヒドラジン量が13.9%であった。つまり、固定化されたヒドラジンは、86.1%であった。これは、樹脂の最初のケトン基を基準とすると、86.1%のヒドラジン吸着率に相当する。
2)炭化水素系アミド架橋固定化貯蔵樹脂のヒドラジンの脱離
上記1)で得られた親水性固定化貯蔵樹脂0.8gを、1N−KOH水溶液に室温で分散して、攪拌した。1N−KOH水溶液中のヒドラジンを、HPLCで定量した結果、18.8%であった。これは、最初のケトン基を基準とすると、21.8%のヒドラジンの脱離に相当する。
具体例3(炭化水素系エーテル架橋固定化樹脂)
1)炭化水素系エーテル架橋固定化樹脂の合成
N,N´−メチレンビスアクリルアミドに代替して、ペンタエリスリトールトリアリルエーテルを用いた以外は、具体例1の1)と同様の操作により、親水性固定化樹脂(炭化水素系エーテル架橋固定化樹脂)を得た。
2)炭化水素系エーテル架橋固定化樹脂に対するヒドラジンの固定化
上記1)で得られた親水性固定化樹脂に、その樹脂2g中に含有するケトン基と等モル数のヒドラジンを含有する100%ヒドラジンヒドラートを添加して、60分間攪拌反応させることにより、親水性固定化樹脂にヒドラジンを固定化し、これによって、親水性固定化樹脂を得た。
3)炭化水素系エーテル架橋固定化樹脂のヒドラジンの脱離
上記2)で得られた親水性固定化樹脂0.8gを、1N−KOH水溶液に室温で60分間、分散して、攪拌した。その後、メタノール40mlを添加して、親水性固定化樹脂をゲル化させた後、濾過分離して、濾液のアルコール溶液中のヒドラジンを、HPLCで定量した結果、固定化されているヒドラジンの19.4%の脱離を確認した。これは、最初のケトン基に対するヒドラジンの変換率として、22.3%に相当する。
具体例4(炭化水素系アミド架橋固定化樹脂(固定基:アルデヒド基))
アクロレイン16g、p−スチレンスルホン酸Na59g、架橋剤としてメチレンビスアクリルアミド2.3g、イオン交換水79gを均一に混合して重合水溶液を作製し、重合槽に投入した。重合水溶液に窒素ガスを導入して、重合水溶液中の溶存酸素量を0.2ppmにし、また、溶液温度を5℃にした。
具体例5(アクリルアミド系固定化樹脂)
アクリルアミド10gと水25.9mlとを混合してアクリルアミド水溶液を調製し、そのアクリルアミド水溶液に35%過酸化水素4.1gを加えて、85〜90℃で16時間攪拌した。反応液を10倍量のメタノール中に注入し、析出した白色沈殿物を濾過して分離した。その後、乾燥してポリアクリルアミドを得た(平均分子量:22,000)。
具体例6(ビニルアルコール系固定化樹脂)
500mlの三つ口フラスコに、攪拌機、コンデンサーおよび温度計を装備し、酢酸ビニル86gと、p−アセチルメチレンオキシスチレン152gと、メタノール50mlを仕込み、攪拌しながら湯浴温度を60〜63℃に上昇させた。
次いで、メタノールを滴下しながら加熱を継続し、未反応のモノマーを留去した。重合物を含む溶液を、大量の水の中に注入して重合物を沈殿させた。沈殿物を濾過して希釈メタノールおよび水で洗浄し、固形物をメタノールに溶解して、その溶液に1N−KOH溶液を滴下して、十分に攪拌してケン化し、酢酸カリウムとして除去した。ケン化された重合物を含む溶液を、大量の氷水に注入して重合物(固形物)を単離した。
具体例7(ポリエステル系固定化樹脂)
精留塔を備えた500mlの三つ口フラスコに、テレフタル酸75.5g、アセチルエチルエチレングリコール101.6g、チタン酸テトラ−n−ブチルエステル0.075g、ブチルヒドロキシスズオキシド0.03gを仕込んだ。
具体例8(ポリアミド系固定化樹脂−1)
窒素導入管および減圧用コックが装備された試験管中で、4,4´−ジアミノジフェニルメタン9.91gと、セバチン酸10.62gとを仕込み、その混合物を窒素気流下285℃に加熱して溶融させた。次に、反応系を1.33kPa程度に減圧し、1時間反応させた後、再び窒素気流下常圧で室温まで冷却した。その後、試験管を破壊し、得られたポリアミドを粉砕機で粉砕した。粉砕された粉末をN−メチルピロリドンに溶解させ、水で洗浄した。この溶液を、多量のメタノールに投入すると縮合物の粉末が析出した。この縮合物をN−メチルピロリドンに溶解して、縮合物と2倍等量のモル数のホルマリンと塩酸を添加して、5時間攪拌反応した(これにより、4,4´−ジアミノジフェニルメタンに対し2つのクロルメチルが導入された。)この反応物を多量のメタノールに投入して、クロルメチル化された縮合物の粉末を得た。
具体例9(ポリアミド系固定化樹脂−2)
具体例8と同様の操作により、クロルメチル化された縮合物の粉末を得た。その後、この縮合物のクロルメチル基と等モル数の60%ヒドラジンヒドラートを添加して、2時間攪拌し、メタノールに投入して、ヒドラジノメチル基を有する沈殿物(ポリアミド系固定化樹脂)を得た。この沈殿物を、ヨード滴定法で定量すると、理論計算量の76.8%に相当するヒドラジノ基が確認された。
具体例10(ポリエーテル系固定化樹脂−1)
攪拌機、酸素導入管、温度計を備えた500mlの三つ口フラスコを30℃の水浴中に置き、これに、ニトロベンゼン200ml、ピリジン70ml、塩化第一銅1gを加えた。激しく攪拌しながら酸素を吹き込み、2,6−ジメチルフェノール15gを加えた。温度が33℃に上昇し、反応混合物が粘性を帯びるようになった。さらに、反応を12分間継続した後、クロロホルム100mlで希釈し、濃塩酸3mlを含むメタノール1.1lに投入した。析出した縮合物を濾別し、メタノール250ml、濃塩酸10mlを含むメタノール250ml、メタノール250mlの順で洗浄した。さらに、縮合物をクロロホルム500mlに溶解し、濃塩酸3mlを含むメタノール1.2l中に投入して、再沈殿させた。得られた縮合物をメタノール洗浄後、110℃3時間減圧乾燥した。これにより、ポリフェニレンエーテルを得た。収率は91%であり、平均分子量は28000であった。
この固体を濾別して、メタノールで洗浄した後、減圧下乾燥した。この固形物をクロロホルムに溶解して高分子中の芳香環の4倍モル数のアセトンと苛性ソーダを加えて、2時間攪拌した。反応液に大量のメタノールに投入して、高分子の芳香環にアセチルエチル基が導入された固形物を得た。これを濾別した後、減圧下乾燥した。この固形物に、上記反応の理論量に相当する60%ヒドラジンヒドラートを添加して3時間攪拌し、その後、メタノールで洗浄して濾過し、濾別された固形物を減圧乾燥することにより、ポリエーテル系固定化樹脂を得た。濾液のメタノール中のヒドラジンをヨード滴定した結果、固定化されているヒドラジンは、51.5%であることが確認された。
具体例11(ポリエーテル系固定化樹脂−2)
具体例10と同様の操作により、クロルメチル化された固体(高分子)を得た。その後、この高分子の芳香環の4倍モル等量の60%ヒドラジンヒドラートを添加して、3時間攪拌し、メタノールに投入して、ヒドラジノメチル基を有する沈殿物(ポリエーテル系固定化樹脂)を得た。この沈殿物を、ヨード滴定法で定量すると、理論計算量の68.6%に相当するヒドラジノ基が確認された。
具体例12(ポリエーテルケトン系固定化樹脂)
攪拌機、窒素導入管および排出管を備えた1lのステンレス製反応管に、4,4´−ジクロロベンゾフェノン125g、微粉末炭酸ナトリウム59.2g、触媒としてシリカ(アエロジル)10g、塩化第二銅0.27gおよび溶媒としてジフェニルスルホン300gを加えた。
具体例13(ポリチオエーテル系固定化樹脂−1)
攪拌機を装備する内容積2Lのオートクレーブに、N−メチルピロリドン480g、硫化ナトリウム2.7gを仕込み、攪拌下加熱して、内温が120℃に到達するまで脱水した。79.3gの主として水からなる留出液が留去した。この際、0.069モルの硫化ナトリウムが硫化水素に分解して、消失した。
具体例14(ポリチオエーテル系固定化樹脂−2)
具体例13と同様の操作により、クロルメチル化された固形物を得た。その後、この固形物を、ジメチルスルホキシドに溶解し、固形物のクロルメチル基と等モル数の60%ヒドラジンヒドラートを添加して、5時間攪拌し、メタノールに投入して、ヒドラジノメチル基を有する沈殿物(ポリチオエーテル系固定化樹脂)を得た。この沈殿物を、HPLCで定量すると、理論計算量の58.5%に相当するヒドラジノ基が確認された。
具体例15(アクリルアミド系固定化樹脂から脱離されたヒドラジンを燃料とする燃料電池の燃料側電極の活性測定)
1)試験溶液および標準液の調製
具体例5で得られたポリアクリル酸ヒドラジッド2gに1N−KOHを38g添加して、ポリアクリル酸ヒドラジッドの5重量%1N−KOH水溶液を調製し、70℃で30分間加熱溶解した後、室温まで冷却して、試験溶液とした。
2)燃料側電極の活性測定
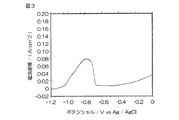
電気化学アナライザ(BAS株式会社製)を用い、LSV(リニアスイープボルタンメトリー)により、燃料側電極の活性を、以下の測定条件で測定した。結果を図3に示す。
活性測定条件:
試験溶液: 5重量%ポリアクリル酸ヒドラジッド/1N−KOH水溶液
燃料側電極 Co(コバルト)電極(BAS株式会社製)
参照電極 Ag/AgCl(銀−塩化銀)電極(BAS株式会社製)
対極 Pt(白金)電極(BAS株式会社製)
溶液温度 30℃
走査範囲 走査速度
前処理 −1.6〜0.6V 前処理 0.1V/s
ブランク測定 −1.6〜0V ブランク測定 0.02V/s
活性測定 −1.6〜0V 活性測定 0.02V/s
なお、各測定前にAr(アルゴン)ガスによるバブリングを行なった。
2 固定化部
4 脱離液供給部
6 検出部
7 ケーシング
8 固定化部材
9 攪拌機
10 フィルタ
11 ヒータ
15 脱離液貯留槽
16 脱離液供給ライン
17 脱離液側開閉弁
22 ヒドラジンセンサ
24 インジケータ
30 制御部
Claims (1)
- ヒドラジンを固定化または脱離する固定化部と、
前記固定化部で固定化されているヒドラジンを脱離させるための水系脱離液を、前記固定化部へ供給する脱離液供給部と、
前記固定化部において脱離されたヒドラジンが、燃料として供給される燃料電池と、
ヒドラジン水溶液の流量およびヒドラジン水溶液の濃度を検知するための検知部と、
予め定める前記燃料電池に供給されるヒドラジンの下記理論供給量と、前記検知部で検知されるヒドラジン水溶液の流量およびヒドラジン水溶液の濃度とに基づき、前記固定化部に固定化されているヒドラジンの量を検出する検出部と
を備えていることを特徴とする、燃料電池システム。
理論供給値:ヒドラジンが最大量で固定化されている前記固定化部に対して、水系脱離液を所定流量で供給してヒドラジンを脱離させる条件において、水系脱離液の供給流量と同じ流量で水系脱離液とともに前記燃料電池に供給されるヒドラジンの濃度
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2007266904A JP5121385B2 (ja) | 2007-10-12 | 2007-10-12 | 燃料電池システム |
| PCT/JP2008/065966 WO2009047956A1 (ja) | 2007-10-12 | 2008-09-04 | 燃料電池システム |
| EP08837141.4A EP2207231B1 (en) | 2007-10-12 | 2008-09-04 | Fuel cell system |
| US12/734,048 US8557476B2 (en) | 2007-10-12 | 2008-09-04 | Fuel cell system |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2007266904A JP5121385B2 (ja) | 2007-10-12 | 2007-10-12 | 燃料電池システム |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2009099272A JP2009099272A (ja) | 2009-05-07 |
| JP5121385B2 true JP5121385B2 (ja) | 2013-01-16 |
Family
ID=40549102
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2007266904A Expired - Fee Related JP5121385B2 (ja) | 2007-10-12 | 2007-10-12 | 燃料電池システム |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US8557476B2 (ja) |
| EP (1) | EP2207231B1 (ja) |
| JP (1) | JP5121385B2 (ja) |
| WO (1) | WO2009047956A1 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN109021222B (zh) * | 2017-06-12 | 2020-07-14 | 廊坊恺建化工有限公司 | 高保塌型聚醚单体的制作方法 |
Family Cites Families (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3542597A (en) * | 1967-12-04 | 1970-11-24 | Monsanto Res Corp | Fuel cell with automatic means for feeding reactant and method |
| US3592694A (en) * | 1968-09-16 | 1971-07-13 | Us Navy | Hydrazine fuel cell control system |
| JPS58186170A (ja) * | 1982-04-23 | 1983-10-31 | Hitachi Ltd | 液体燃料電池 |
| DE3582716D1 (de) | 1984-10-31 | 1991-06-06 | Hitachi Ltd | Fluessigbrennstoffzelle. |
| JP2001213605A (ja) | 2000-01-28 | 2001-08-07 | Honda Motor Co Ltd | 水素を燃料とする機器への水素供給システム |
| JP4700161B2 (ja) * | 2000-03-17 | 2011-06-15 | 本田技研工業株式会社 | 燃料電池運転システムにおける水素貯蔵合金再生装置 |
| US6834623B2 (en) * | 2001-08-07 | 2004-12-28 | Christopher T. Cheng | Portable hydrogen generation using metal emulsions |
| US20050095465A1 (en) | 2001-12-27 | 2005-05-05 | Hirohisa Tanaka | Fuel cell |
| CN1302021C (zh) | 2001-12-27 | 2007-02-28 | 三洋化成工业株式会社 | 非水系吸收体及其用途 |
| JP3862166B2 (ja) * | 2002-10-01 | 2006-12-27 | 三洋化成工業株式会社 | 燃料電池用燃料貯蔵物及び燃料電池 |
| JP2005158335A (ja) * | 2003-11-21 | 2005-06-16 | Denso Corp | 燃料電池システム |
| WO2005062410A1 (ja) | 2003-12-18 | 2005-07-07 | Kurita Water Industries Ltd. | 燃料電池用燃料及び燃料電池並びにその応用 |
| JP4806905B2 (ja) * | 2004-07-14 | 2011-11-02 | 栗田工業株式会社 | 燃料電池用燃料組成物中の燃料物質の存在量検知方法 |
| US7329470B2 (en) * | 2004-05-26 | 2008-02-12 | Societe Bic | Apparatus and method for in situ production of fuel for a fuel cell |
| JP2006079838A (ja) * | 2004-09-07 | 2006-03-23 | Konica Minolta Holdings Inc | 燃料電池用燃料およびこれを用いた燃料電池 |
| JP2006156086A (ja) * | 2004-11-29 | 2006-06-15 | Konica Minolta Holdings Inc | シート状燃料電池用燃料及びそれを製造する方法並びに燃料電池発電システム |
| JP4371374B2 (ja) | 2005-01-26 | 2009-11-25 | 古河電気工業株式会社 | 燃料電池用燃料カートリッジ |
| JP4993867B2 (ja) | 2005-03-07 | 2012-08-08 | ダイハツ工業株式会社 | 燃料電池 |
| US7897292B2 (en) * | 2005-05-18 | 2011-03-01 | Lilliputian Systems, Inc. | Fuel cell apparatus and methods |
| WO2008007650A1 (fr) * | 2006-07-14 | 2008-01-17 | Otsuka Chemical Co., Ltd. | résine d'accumulation de l'hydrazine |
| EP2043185B1 (en) * | 2006-07-14 | 2013-09-04 | Otsuka Chemical Co., Ltd. | Hydrazine supply device, fuel cell system utilizing the same, vehicle carrying the fuel cell system, and method of supplying hydrazine |
-
2007
- 2007-10-12 JP JP2007266904A patent/JP5121385B2/ja not_active Expired - Fee Related
-
2008
- 2008-09-04 US US12/734,048 patent/US8557476B2/en not_active Expired - Fee Related
- 2008-09-04 EP EP08837141.4A patent/EP2207231B1/en not_active Not-in-force
- 2008-09-04 WO PCT/JP2008/065966 patent/WO2009047956A1/ja active Application Filing
Also Published As
| Publication number | Publication date |
|---|---|
| US20100233583A1 (en) | 2010-09-16 |
| WO2009047956A1 (ja) | 2009-04-16 |
| EP2207231B1 (en) | 2013-06-19 |
| EP2207231A4 (en) | 2012-03-14 |
| US8557476B2 (en) | 2013-10-15 |
| JP2009099272A (ja) | 2009-05-07 |
| EP2207231A1 (en) | 2010-07-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5249029B2 (ja) | ヒドラジン供給装置、それを用いた燃料電池システムおよびその燃料電池システムを搭載した車両、ならびにヒドラジン供給方法 | |
| JP5398261B2 (ja) | ヒドラジンの貯蔵方法 | |
| Yin et al. | Synthesis and properties of highly sulfonated proton conducting polyimides from bis (3-sulfopropoxy) benzidine diamines | |
| JP5112796B2 (ja) | 燃料電池システム | |
| Zhang et al. | Novel fluoropolymer anion exchange membranes for alkaline direct methanol fuel cells | |
| Wang et al. | Sulfonated aromatic polyamides containing nitrile groups as proton exchange fuel cell membranes | |
| TWI373877B (en) | Fuel cell system | |
| JP5121385B2 (ja) | 燃料電池システム | |
| JP2008159462A (ja) | 燃料電池装置 | |
| Kang et al. | Properties and morphology study of proton exchange membranes fabricated from the pendant sulfonated poly (arylene ether ketone) copolymers composed of hydrophobic and hydrophilic multi-blocks for fuel cell | |
| Xu et al. | Novel piperidinium-functionalized crosslinked anion exchange membrane with flexible spacers for water electrolysis | |
| JP2009099273A (ja) | 燃料電池システム | |
| Ayaz et al. | Preparation of poly (arylene ether ketone) based anion exchange membrane with pendant pyrimidinium and pyridazinium cation derivatives for alkaline fuel cell | |
| JP5150178B2 (ja) | 燃料電池システム | |
| CN107346828B (zh) | 燃料电池的进气处理系统 | |
| JP2009070695A (ja) | 燃料電池システム | |
| EP2412051B1 (en) | Ion exchange filter for fuel cell system | |
| JP2007302717A (ja) | スルホン化芳香族ポリイミド、電解質膜及び燃料電池用固体電解質、並びに燃料電池 | |
| Potrekar et al. | Polybenzimidazoles tethered with N‐phenyl 1, 2, 4‐triazole units as polymer electrolytes for fuel cells | |
| JP4851072B2 (ja) | 燃料電池用電解質膜および燃料電池 | |
| WO2006048942A1 (ja) | ニトリル型疎水性ブロックを有するスルホン化ポリマーおよび固体高分子電解質 | |
| US8808931B2 (en) | Ion exchange filter for fuel cell system | |
| Chen et al. | Direct synthesis of sulfonated poly (phthalazinone ether) for proton exchange membrane via N–C coupling reaction | |
| JP2008034204A (ja) | 燃料電池装置 | |
| CN103974933B (zh) | 含硫的氟化和磺化芳族烷烃单体 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20100611 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20120807 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120926 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20121016 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20121023 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20151102 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| LAPS | Cancellation because of no payment of annual fees |