JP4838514B2 - 低粘度液体剤形 - Google Patents
低粘度液体剤形 Download PDFInfo
- Publication number
- JP4838514B2 JP4838514B2 JP2004570751A JP2004570751A JP4838514B2 JP 4838514 B2 JP4838514 B2 JP 4838514B2 JP 2004570751 A JP2004570751 A JP 2004570751A JP 2004570751 A JP2004570751 A JP 2004570751A JP 4838514 B2 JP4838514 B2 JP 4838514B2
- Authority
- JP
- Japan
- Prior art keywords
- chloride
- dosage form
- active substance
- bromide
- liquid dosage
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0087—Galenical forms not covered by A61K9/02 - A61K9/7023
- A61K9/0095—Drinks; Beverages; Syrups; Compositions for reconstitution thereof, e.g. powders or tablets to be dispersed in a glass of water; Veterinary drenches
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/57—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids substituted in position 17 beta by a chain of two carbon atoms, e.g. pregnane or progesterone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/20—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing sulfur, e.g. dimethyl sulfoxide [DMSO], docusate, sodium lauryl sulfate or aminosulfonic acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/32—Macromolecular compounds obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. carbomers, poly(meth)acrylates, or polyvinyl pyrrolidone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/36—Polysaccharides; Derivatives thereof, e.g. gums, starch, alginate, dextrin, hyaluronic acid, chitosan, inulin, agar or pectin
- A61K47/38—Cellulose; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/141—Intimate drug-carrier mixtures characterised by the carrier, e.g. ordered mixtures, adsorbates, solid solutions, eutectica, co-dried, co-solubilised, co-kneaded, co-milled, co-ground products, co-precipitates, co-evaporates, co-extrudates, co-melts; Drug nanoparticles with adsorbed surface modifiers
- A61K9/145—Intimate drug-carrier mixtures characterised by the carrier, e.g. ordered mixtures, adsorbates, solid solutions, eutectica, co-dried, co-solubilised, co-kneaded, co-milled, co-ground products, co-precipitates, co-evaporates, co-extrudates, co-melts; Drug nanoparticles with adsorbed surface modifiers with organic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/141—Intimate drug-carrier mixtures characterised by the carrier, e.g. ordered mixtures, adsorbates, solid solutions, eutectica, co-dried, co-solubilised, co-kneaded, co-milled, co-ground products, co-precipitates, co-evaporates, co-extrudates, co-melts; Drug nanoparticles with adsorbed surface modifiers
- A61K9/146—Intimate drug-carrier mixtures characterised by the carrier, e.g. ordered mixtures, adsorbates, solid solutions, eutectica, co-dried, co-solubilised, co-kneaded, co-milled, co-ground products, co-precipitates, co-evaporates, co-extrudates, co-melts; Drug nanoparticles with adsorbed surface modifiers with organic macromolecular compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
Description
本発明は、ナノ微粒子活性物質を含む低粘度液体剤形に関する。
本出願は、2003年4月14日に提出された「メゲストロルのナノ微粒子製剤」に関する米国実用新案出願番号不明および2002年12月3日に提出された米国特許出願第60/430,438号の利益を主張する。
A.液体剤形に関する背景
治療および診断に関する液体剤形は、様々な治療および投与経路において有用である。液体剤形は飲み込むことができない、または嚥下困難な患者にとって特に有用である。そのような患者には、幼児、小児、老人、何人かの精神医学患者、および経腸栄養を必要とする患者が含まれる。
固体を錠剤に調製すると、大きく、飲み込むことが難しい錠剤となりうる。そのような固体剤形は、粘度が低い液体に再調製することが望ましいであろう。そのような再調製された剤形は、幼児、小児、および高齢者のような、錠剤を飲み込むことが困難な患者集団にとって特に有用となるであろう。
これまでに提案されている水に難溶性の活性物質を調製する問題に対する一つの解決策は、参照として本明細書に特に組み入れられる、米国特許第5,145,684号(第'684号の特許)に記述されるように、サブミクロンの大きさの範囲の活性物質粒子を提供することである。そのような粒子は、粒子間の誘引力により認識できるほどに綿状沈殿または凝集しない。第'684号の特許は、低い粘度を有する液体剤形を教示していない。
本発明は、ナノ微粒子活性物質を含む、高用量をローディングすることができる低粘度液体剤形に向けられる。本発明の低粘度液体剤形は:(1)少なくとも一つの活性物質の粒子を(2)少なくとも一つの表面安定化剤と共に、および(3)好ましくは少なくとも一つの薬学的に許容される担体または賦形剤を含む。活性物質粒子は、有効平均粒子径が約2ミクロン未満であり、液体剤形の粘度は、ずり速度は0.1(1/s)で約2000 mPa・s未満である。本発明の他の態様において、液体剤形は、水の粘度に近い粘度、すなわち粘度1 mPa・sを有する。
本発明は、低い粘度を有するナノ微粒子活性物質の液体剤形に関する。活性物質に応じて、本発明の液体剤形は、高濃度の活性物質を必要とする剤形(液体または固体)において水に難溶性の活性物質のための剤形として特に有用となる可能性がある。水に難溶性の活性物質は、循環中に吸収される前に消化管から排泄される傾向がある。
本発明の液体剤形は、ナノ微粒子活性物質の安定な分散液を含む。安定な分散液は、均一性および一貫した流動学挙動を維持しながら大量の固体のローディングを可能にする。分散液の場合、安定性は、本発明の粒子がブラウン運動によって支配されることを意味するが、慣性および重力は、同じ活性物質の通常の液体剤形の場合のように、より大きい粒子の浮遊液の挙動に対してより大きい効果を有する。
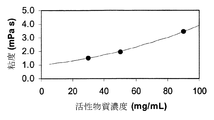
本発明は、低い粘度を有する液体剤形を提供する。粘度は、濃度および温度依存的である。典型的に、より高い濃度によってより高い粘度が得られるが、温度がより高ければ粘度はより低くなる。本明細書において定義される粘度は、約20℃で行った測定を指す。(20℃での水の粘度は1 mPa・sである)。本発明は、異なる温度で測定した同等の粘度を含む。
本発明の低粘度液体剤形には、「薬物」、「活性成分」、「治療物質」、または「診断物質」とも呼ばれる少なくとも一つの活性物質が含まれる。活性物質は、薬剤、または造影剤もしくは他の任意のタイプの診断材料のような診断薬となりうる。治療または診断薬は、個々の結晶相、半結晶相、アモルファス相、半アモルファス相、またはその混合物として存在する。
本発明において用いることができる有用な表面安定化剤には、既知の有機および無機薬学的賦形剤が含まれるがこれらに限定されない。そのような化合物には、様々なポリマー、低分子量オリゴマー、天然物、および界面活性剤が含まれる。表面安定化剤には、非イオン性、陰イオン性、陽イオン性、および両イオン性界面活性剤が含まれる。
(i)R1〜R4のいずれもCH3ではない;
(ii)R1〜R4の一つはCH3である;
(iii)R1〜R4の三つはCH3である;
(iv)R1〜R4の全てがCH3である;
(v)R1〜R4の二つがCH3であって、R1〜R4の一つがC6H5CH2であって、R1〜R4の一つが、炭素原子7個またはそれ未満のアルキル鎖である;
(vi)R1〜R4の二つがCH3であって、R1〜R4の一つがC6H5CH2であって、R1〜R4の一つが、炭素原子19個またはそれより多いアルキル鎖である;
(vii)R1〜R4の二つがCH3であって、R1〜R4の一つがC6H5(CH2)nであって、n>1である;
(viii)R1〜R4の二つがCH3であって、R1〜R4の一つがC6H5CH2であって、R1〜R4の一つが、少なくとも一つのヘテロ原子を含む;
(ix)R1〜R4の二つがCH3であって、R1〜R4の一つがC6H5CH2であって、R1〜R4の一つが、少なくとも一つのハロゲンを含む;
(x)R1〜R4の二つがCH3であって、R1〜R4の一つがC6H5CH2であって、R1〜R4の一つが、少なくとも一つの環状断片を含む;
(xi)R1〜R4の二つがCH3であって、R1〜R4の一つがフェニル環である;または
(xii)R1〜R4の二つがCH3であって、R1〜R4の二つが純粋に脂肪族の断片である。
本発明に従う薬学的組成物はまた、一つまたはそれ以上の結合剤、充填剤、潤滑剤、懸濁剤、甘味料、着香料、保存剤、緩衝液、湿潤剤、崩壊剤、発泡剤、および他の賦形剤を含んでもよい。そのような賦形剤は当技術分野で既知である。
本発明の液体剤形は、約2ミクロン(すなわち、2000 nm)未満の有効平均粒子径を有するナノ微粒子活性物質を含む。本発明の他の態様において、活性物質は、光散乱法、顕微鏡、または他の適当な方法によって測定した場合に、有効平均粒子径約1900 nm未満、約1800 nm未満、約1700 nm未満、約1600 nm未満、約1500 nm未満、約1400 nm未満、約1300 nm未満、約1200 nm未満、約1100 nm未満、約1000 nm未満、約900 nm未満、約800 nm未満、約700 nm未満、約600 nm未満、約500 nm未満、約400 nm未満、約300 nm未満、約250 nm未満、約200 nm未満、約150 nm未満、約100 nm未満、約75 nm未満、または約50 nm未満を有しうる。
一つまたはそれ以上の活性物質および一つまたはそれ以上の表面安定化剤の相対量は大きく変化しうる。個々の化合物の最適な量は、例えば選択した特定の活性物質、親水性親油性バランス(HLB)、融点、および表面安定化剤の水溶液の表面張力、所定の化合物が組成物の粘度を増加させることができるか否か等に依存しうる。
本発明はまた、活性物質の通常の固体または液体剤形を改善する方法を含む。
本発明の液体剤形に存在する一つまたはそれ以上のナノ微粒子活性物質は、例えば、粉砕、ホモジナイゼーション、または沈殿技術を用いて作製することができる。ナノ微粒子活性物質を作製する例としての方法は、第'684号の特許に記述されている。ナノ微粒子活性物質組成物を作成する方法はまた、その全てが特に参照として本明細書に組み入れられる、「Method of Grinding Pharmaceutical Substances」に関する米国特許第5,518,187号、「Continuous Method of Grinding Pharmaceutical Substances」に関する米国特許第5,718,388号、「Method of Grinding Pharmaceutical Substances」に関する米国特許第5,862,999号、「Co-Microprecipitation of Nanoparticulate Pharmaceutical Agents with Crystal Growth Modifiers.」に関する米国特許第5,665,331号、「Co-Microprecipitation of Nanoparticulate Pharmaceutical Agents with Crystal Growth Modifiers.」に関する米国特許第5,662,883号、「Microprecipitation of Nanoparticulate Pharmaceutical Agents.」に関する米国特許第5,560,932号、「Process of Preparing X-Ray Contrast Compositions Containing Nanoparticles.」に関する米国特許第5,543,133号、「Method of Preparing Stable Drug Nanoparticles」に関する米国特許第5,534,270号、「Process of Preparing Therapeutic Compositions Containing Nanoparticles.」に関する米国特許第5,510,118号、および「Method of Preparing Nanoparticle Compositions Containing Charged Phospholipids to Reduce Aggregation」に関する米国特許第5,470,583号に記述されている。
ナノ微粒子活性物質粒子の分散液を得るために活性物質を粉砕することは、活性物質が難溶性である液体分散培地に活性物質の粒子を分散させた後に、活性物質の粒子径を所望の有効平均粒子径まで減少させるために、粉砕媒体の存在下で機械的手段を適用することを含む。分散媒体は、例えば水、ヒマワリ油、エタノール、t-ブタノール、グリセリン、ポリエチレングリコール(PEG)、ヘキサン、またはグリコールとなりうる。好ましい分散媒体は水である。
本発明の液体剤形に存在する一つまたはそれ以上のナノ微粒子活性物質を調製するもう一つの方法は、微小沈殿による。これは、如何なる微量の毒性溶媒または可溶化重金属不純物も含まない、一つまたはそれ以上の表面安定化剤および一つまたはそれ以上のコロイド安定性増強表面活性物質の存在下で、難溶性の活性物質の安定な分散液を調製する方法である。そのような方法は、例えば以下を含む:(1)適した溶媒に活性物質を溶解する段階;(2)段階(1)からの調製物を少なくとも一つの表面安定化剤を含む溶液に加える段階;および(3)適当な非溶媒を用いて段階(2)からの製剤を沈殿させる段階。方法の後に、存在すれば任意の形成された塩を透析またはディアフィルトレーションによって除去すること、および通常の手段によって分散液の濃縮を行うことができる。得られたナノ微粒子分散液を全ての液体剤形において用いることができる。
ナノ微粒子活性物質を調製する例としてのホモジナイゼーション法は、「Process of Preparing Therapeutic Compositions Containing Nanoparticles.」に関する米国特許第5,510,118号に記述される。そのような方法は、活性物質が難溶性である液体分散媒体に活性物質の粒子を分散させる段階の後に、活性物質の粒子径を所望の有効平均粒子径まで減少させるために、分散液にホモジナイゼーションを行う段階を含む。活性物質粒子は、少なくとも一つの表面安定化剤の存在下で大きさを減少させることができる。または活性物質を摩耗の前後いずれかに一つまたはそれ以上の表面安定化剤に接触させることができる。希釈剤のような他の化合物を、サイズ減少プロセスの前、あいだ、または後に活性物質/表面安定化剤組成物に加えることができる。分散液は連続的またはバッチ毎に製造することができる。得られたナノ微粒子分散液を全ての液体投与製剤において用いることができる。
本発明の液体剤形は、経口、直腸内、点眼、非経口(例えば、静脈内、筋肉内、または皮下)、槽内、肺内、膣内、腹腔内、局所(例えば、軟膏または滴剤)が含まれるがこれらに限定されない任意の通常の方法によって、または口腔内もしくは鼻腔内スプレーとして被験者に投与することができる。本明細書において用いられるように、「被験者」という用語は、動物、好ましくはヒトまたはヒト以外を含む哺乳類を意味するために用いられる。「患者」および「被験者」という用語は互換的に用いてもよい。
本実施例の目的は、同じ活性物質である酢酸メゲストロルの通常の液体剤形と比較して、本発明の液体剤形の特徴である改善された粘度を証明するためであった。
本実施例の目的は、同じ活性成分であるナプロキセンの通常の液体剤形と比較した場合に本発明の液体剤形の改善された粘度特徴を示すことであった。
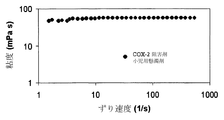
本実施例の目的は、同じ活性物質、すなわちCOX-2阻害剤であるコンパウンドAの通常の液体剤形と比較して、本発明の液体剤形の改善された粘度特徴を証明することであった。
Claims (20)
- 剤形の粘度がずり速度0.1(1/s)で2000 mPa・s未満である、以下を含む低粘度液体剤形:
(a)有効平均粒子径が2ミクロン未満である、少なくとも一つの活性物質の粒子であって、該活性物質が、酢酸メゲストロルである、粒子;
(b)該活性物質の粒子の表面に会合した少なくとも一つの表面安定化剤であって、該表面安定化剤は分子間クロスリンクを含まない;および
(c)少なくとも一つの薬学的に許容される賦形剤、担体、またはその組み合わせ。 - (a)ずり速度0.1(1/s)において、粘度が、2000 mPa・sから1 mPa・sである、請求項1記載の剤形。
- (b)剤形の粘度が、活性物質1mlあたりほぼ同じ濃度において同じ活性物質の標準的な通常の液体剤形の粘度の1/10未満である、請求項1または2記載の剤形。
- (c)剤形の粘度が、活性物質1mlあたりほぼ同じ濃度において同じ活性物質の標準的な通常の液体剤形の粘度の90%未満である、請求項1または2記載の剤形。
- 活性物質の濃度が、同じ活性物質からの標準的な通常の液体剤形の活性物質の濃度に等しいまたはそれより大きい、請求項1〜4のいずれかに記載の剤形。
- (a)経口、肺内、直腸内、点眼、結腸内、非経口、槽内、静脈内、膣内、腹腔内、局所、口腔内、鼻腔内、および局所投与からなる群より選択される投与のために調製され、かつ/または
(b)徐放性投与、即時融解投与、およびエアロゾル投与からなる群より選択される剤形での投与に適した、
請求項1〜5のいずれか一項に記載の剤形。 - 活性物質の有効平均粒子径が、1900 nm未満である、請求項1〜6のいずれか一項に記載の剤形。
- 活性物質粒子の少なくとも70%が有効平均粒子径より小さい粒子径を有する、請求項1〜7のいずれか一項に記載の剤形。
- 活性物質が水溶性または水に難溶性である、請求項1〜8のいずれか一項に記載の剤形。
- 活性物質が、結晶粒子、半結晶粒子、アモルファス粒子、またはその混合物の形である、請求項1〜9のいずれか一項に記載の剤形。
- (a)活性物質が、他の賦形剤を含まない少なくとも一つの活性物質と少なくとも一つの表面安定化剤との合計総重量に基づいて、重量で99.5%〜0.001%の量で存在し、かつ/または
(b)少なくとも一つの表面安定化剤が、他の賦形剤を含まない、少なくとも一つの活性物質と少なくとも一つの表面安定化剤との合計総乾燥重量に基づいて、重量で0.5%〜99.999%の量で存在する、
請求項1〜10のいずれか一項に記載の剤形。 - 少なくとも二つの表面安定化剤を含む、請求項1〜11のいずれか一項に記載の剤形。
- 少なくとも一つの表面安定化剤が、陰イオン性表面安定化剤、陽イオン性表面安定化剤、イオン性表面安定化剤、および両イオン性表面安定化剤からなる群より選択される、請求項1〜12のいずれか一項に記載の剤形。
- 少なくとも一つの表面安定化剤が、塩化セチルピリジニウム、ゼラチン、カゼイン、ホスファチド、デキストラン、グリセロール、アカシアゴム、コレステロール、トラガカント、ステアリン酸、塩化ベンザルコニウム、ステアリン酸カルシウム、モノステアリン酸グリセロール、セトステアリルアルコール、セトマクロゴール乳化ロウ、ソルビタンエステル、ポリオキシエチレンアルキルエーテル、ポリオキシエチレンヒマシ油誘導体、ポリオキシエチレンソルビタン脂肪酸エステル、ポリエチレングリコール、臭化ドデシルトリメチルアンモニウム、ステアリン酸ポリオキシエチレン、コロイド状二酸化ケイ素、ホスフェート、ドデシル硫酸ナトリウム、カルボキシメチルセルロースカルシウム、ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、カルボキシメチルセルロースナトリウム、メチルセルロース、ヒドロキシエチルセルロース、フタル酸ヒドロキシプロピルメチルセルロース、非結晶セルロース、ケイ酸アルミニウムマグネシウム、トリエタノールアミン、ポリビニルアルコール、ポリビニルピロリドン、エチレンオキサイドおよびホルムアルデヒドとの4-(1,1,3,3-テトラメチルブチル)-フェノールポリマー、ポロキサマー、ポロキサミン、荷電リン脂質、ジオクチルスルホスクシネート、スルホコハク酸ナトリウムのジアルキルエステル、ラウリル硫酸ナトリウム、アルキルアリールポリエーテルスルホネート、ステアリン酸ショ糖とジステアリン酸ショ糖の混合物、p-イソノニルフェノキシポリ-(グリシドール)、デカノイル-N-メチルグルカミド、n-デシルβ-D-グルコピラノシド、n-デシルβ-D-マルトピラノシド、n-ドデシルβ-D-グルコピラノシド、n-ドデシルβ-D-マルトシド、ヘプタノイル-N-メチルグルカミド、n-ヘプチル-β-D-グルコピラノシド、n-ヘプチルβ-D-チオグルコシド、n-ヘキシルβ-D-グルコピラノシド、ノナノイル-N-メチルグルカミド、n-ノイルβ-D-グルコピラノシド、オクタノイル-N-メチルグルカミド、n-オクチル-β-D-グルコピラノシド、オクチルβ-D-チオグルコピラノシド、ライソザイム、PEG-誘導体化リン脂質、PEG誘導体化コレステロール、PEG-誘導体化コレステロール誘導体、PEG-誘導体化ビタミンA、PEG-誘導体化ビタミンE、酢酸ビニルとビニルピロリドンとのランダムコポリマー、陽イオンポリマー、陽イオンバイオポリマー、陽イオン多糖類、陽イオンセルロース誘導体、陽イオンアルギン酸塩、陽イオン非ポリマー化合物、陽イオンリン脂質、両イオン性安定化剤、ポリ-n-メチルピリジニウム、塩化アンスリュル(anthryul)ピリジニウム、キトサン、ポリリジン、ポリビニルイミダゾール、ポリブレン、ポリメチルメタクリレートトリメチルアンモニウムブロミドブロミド(PMMTMABr)、ヘキシルデシルトリメチルアンモニウムブロミド(HDMAB)、ポリビニルピロリドン-2-ジメチルアミノエチルメタクリレートジメチルスルフェート、1,2ジパルミトイル-sn-グリセロ-3-ホスホエタノールアミン-N-[アミノ(ポリエチレングリコール)2000](ナトリウム塩)、ポリ(2-メタクリルオキシエチルトリメチルアンモニウムブロミド)、ポロキサミン、ライソザイム、アルギン酸、カラゲニン、POLYOX、陽イオン脂質、スルホニウム、ホスホニウム、四級アンモニウム化合物、塩化ステアリルトリメチルアンモニウム、臭化ベンジル-ジ(2-クロロエチル)エチルアンモニウム、塩化ココナッツトリメチルアンモニウム、臭化ココナッツトリメチルアンモニウム、塩化ココナッツメチルジヒドロキシエチルアンモニウム、臭化ココナッツメチルジヒドロキシエチルアンモニウム、塩化デシルトリエチルアンモニウム、塩化デシルジメチルヒドロキシエチルアンモニウム、臭化デシルジメチルヒドロキシエチルアンモニウム、塩化C12-15ジメチルヒドロキシエチルアンモニウム、臭化C12-15ジメチルヒドロキシエチルアンモニウム、塩化ココナッツジメチルヒドロキシエチルアンモニウム、臭化ココナッツジメチルヒドロキシエチルアンモニウム、ミリスチルトリメチルアンモニウムメチルスルフェート、塩化ラウリルジメチルベンジルアンモニウム、臭化ラウリルジメチルベンジルアンモニウム、塩化ラウリルジメチル(エテノキシ)4アンモニウム、臭化ラウリルジメチル(エテノキシ)4アンモニウム、塩化N-アルキル(C12-18)ジメチルベンジルアンモニウム、塩化N-アルキル(C14-18)ジメチルベンジルアンモニウム、塩化N-テトラデシルジメチルベンジルアンモニウム一水和物、塩化ジメチルジデシルアンモニウム、塩化N-アルキルおよび(C12-14)ジメチル1-ナフチルメチルアンモニウム、ハロゲン化トリメチルアンモニウム、アルキル-トリメチルアンモニウム塩、ジアルキル-ジメチルアンモニウム塩、塩化ラウリルトリメチルアンモニウム、エトキシル化アルキルアミドアルキルジアルキルアンモニウム塩、エトキシル化トリアルキルアンモニウム塩、塩化ジアルキルベンゼンジアルキルアンモニウム、塩化N-ジデシルジメチルアンモニウム、N-テトラデシルジメチルベンジルアンモニウム、塩化物一水和物、塩化N-アルキル(C12-14)ジメチル1-ナフチルメチルアンモニウム、塩化ドデシルジメチルベンジルアンモニウム、塩化ジアルキルベンゼンアルキルアンモニウム、塩化ラウリルトリメチルアンモニウム、塩化アルキルベンジルメチルアンモニウム、臭化アルキルベンジルジメチルアンモニウム、臭化C12、C15、C17トリメチルアンモニウム、塩化ドデシルベンジルトリエチルアンモニウム、塩化ポリジアルキルジメチルアンモニウム(DADMAC)、塩化ジメチルアンモニウム、ハロゲン化アルキルジメチルアンモニウム、塩化トリセチルメチルアンモニウム、臭化デシルトリメチルアンモニウム、臭化ドデシルトリエチルアンモニウム、臭化テトラデシルトリメチルアンモニウム、塩化メチルトリオクチルアンモニウム、POLYQUAT 10(商標)、臭化テトラブチルアンモニウム、臭化ベンジルトリメチルアンモニウム、コリンエステル、塩化ベンザルコニウム、塩化ステアラルコニウム化合物、臭化セチルピリジニウム、塩化セチルピリジニウム、四級ポリオキシエチルアルキルアミンのハロゲン塩、MIRAPOL(商標)、ALKAQUAT(商標)、アルキルピリジニウム塩、アミン、プロトン化四級アクリルアミド、メチル化四級ポリマー、陽イオングアー、塩化ベンザルコニウム、カルボニウム化合物、ホスホニウム化合物、オキソニウム化合物、ハロニウム化合物、陽イオン有機金属化合物、四級リン化合物、ピリジニウム化合物、アニリニウム化合物、アンモニウム化合物、ヒドロキシアンモニウム化合物、一級アンモニウム化合物、二級アンモニウム化合物、三級アンモニウム化合物、塩化ベヘナルコニウム、塩化ベンゼトニウム、塩化セチルピリジニウム、塩化ベヘントリモニウム、塩化ラウラルコニウム、塩化セタルコニウム、臭化セトリモニウム、塩化セトリモニウム、フッ化水素セチルアミン、塩化クロロアリルメテナミン(クアテルニウム-15)、塩化ジステアリルジモニウム(クアテルニウム-5)、塩化ドデシルジメチルエチルベンジルアンモニウム(クアテルニウム-14)、クアテルニウム-22、クアテルニウム-26、クアテルニウム-18ヘクトライト、塩酸ジメチルアミノエチルクロリド、塩酸システイン、ジエタノールアンモニウムPOE(10)オレチルエーテルホスフェート、ジエタノールアンモニウムPOE(3)オレイルエーテルホスフェート、塩化タロウアルコニウム、ジメチルジオクタデシルアンモニウムベントナイト、塩化ステアラルコニウム、臭化ドミフェン、安息香酸デナトニウム、塩化ミリスタルコニウム、塩化ラウルトリモニウム、エチレンジアミン二塩酸、塩酸グアニジン、塩酸ピリドキシン、塩酸イオフェタミン、塩酸メグルミン、塩化メチルベンゼトニウム、臭化ミルトリモニウム、塩化オレイルトリモニウム、ポリクアテルニウム-1、塩酸プロカイン、ココベタイン、ステアラルコニウムベントナイト、ステアラルコニウムヘクトナイト、ステアリルトリヒドロキシエチルプロピレンジアミンジヒドロフルオリド、塩酸タロウトリモニウム、および臭化ヘキサデシルトリメチルアンモニウムからなる群より選択される、請求項1〜13のいずれか一項記載の剤形。
- アミンが、アルキルアミン、ジアルキルアミン、アルカノールアミン、ポリエチレンポリアミン、N,N-ジアルキルアミノアルキルアクリレート、ビニルピリジン、アミン塩、ラウリル酢酸アミン、ステアリル酢酸アミン、アルキルピリジニウム塩、アルキルイミダゾリウム塩、アミンオキシド、およびイミドアゾリニウム塩からなる群より選択される、請求項14記載の剤形。
- 剤形が生体接着剤である、請求項1〜15のいずれか一項記載の剤形。
- 薬物を製造するための、請求項1〜16のいずれか一項記載の剤形の使用。
- 薬物が、HIV消耗、癌の消耗、偏頭痛、カヘキシア、食欲不振、去勢、および経口避妊薬からなる群より選択される状態を治療するのに有用である、請求項17記載の使用。
- 以下を含む、活性物質の通常の固体剤形または液体剤形を改善する方法であって、該活性物質が、酢酸メゲストロルである、方法:
(a)用量の均一性の不良、低い用量ローディングまたは用量ローディングの不良、大きい大きさ、生物学的利用率の不良、遅い活性の発現、血液および腫瘍における不良な活性物質保持、有意な絶食時変動、高い粘度、まずい味、砂のような感じ、濃化剤の存在、経口、静脈内、皮下、または筋肉内注射に関する動作特性不良、有機溶媒の存在、極端なpHの存在、高い投与容量、非経口投与の適格性不良、ならびに濾過滅菌できないことからなる群より選択される、少なくとも一つの望ましくない特性を有する活性物質の通常の固体剤形または液体剤形を同定する段階;および
(b)剤形の粘度がずり速度0.1(1/s)で2000 mPa・s未満である、以下を含む低粘度液体剤形に活性物質を調製する段階:
(i)有効平均粒子径が2ミクロン未満である、少なくとも一つの活性物質の粒子;
(ii)該活性物質の粒子の表面に会合した少なくとも一つの表面安定化剤であって、該表面安定化剤は分子間クロスリンクを含まない;および
(iii)少なくとも一つの薬学的に許容される賦形剤、担体、またはその組み合わせ。 - 少なくとも一つの活性物質の粒子を、活性物質のナノ微粒子組成物を提供するために十分な時間および条件で、少なくとも一つの表面安定化剤および少なくとも一つの薬学的に許容される賦形剤、担体、またはその組み合わせと接触させることを含み、該活性物質が、酢酸メゲストロルである、液体剤形を作製する方法であって、
(a)活性物質の粒子の有効平均粒子径が2ミクロン未満であり、該活性物質の粒子はその表面に表面安定化剤が会合し、該表面安定化剤は分子間クロスリンクを含まず、および
(b)液体剤形の粘度がずり速度0.1(1/s)で2000 mPa・s未満である、方法。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US43034802P | 2002-12-03 | 2002-12-03 | |
| US60/430,348 | 2002-12-03 | ||
| US10/412,669 US7101576B2 (en) | 2002-04-12 | 2003-04-14 | Nanoparticulate megestrol formulations |
| US10/412,669 | 2003-04-14 | ||
| PCT/US2003/012660 WO2004050059A1 (en) | 2002-12-03 | 2003-04-23 | Low viscosity liquid dosage forms |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011160522A Division JP2011251989A (ja) | 2002-12-03 | 2011-07-22 | 低粘度液体剤形 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2006510726A JP2006510726A (ja) | 2006-03-30 |
| JP2006510726A5 JP2006510726A5 (ja) | 2010-09-16 |
| JP4838514B2 true JP4838514B2 (ja) | 2011-12-14 |
Family
ID=32474388
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2004570751A Expired - Fee Related JP4838514B2 (ja) | 2002-12-03 | 2003-04-23 | 低粘度液体剤形 |
| JP2011160522A Pending JP2011251989A (ja) | 2002-12-03 | 2011-07-22 | 低粘度液体剤形 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011160522A Pending JP2011251989A (ja) | 2002-12-03 | 2011-07-22 | 低粘度液体剤形 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US7101576B2 (ja) |
| EP (2) | EP1613276A1 (ja) |
| JP (2) | JP4838514B2 (ja) |
| AU (1) | AU2003231071A1 (ja) |
| CA (1) | CA2508301A1 (ja) |
| WO (1) | WO2004050059A1 (ja) |
Families Citing this family (75)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6565885B1 (en) * | 1997-09-29 | 2003-05-20 | Inhale Therapeutic Systems, Inc. | Methods of spray drying pharmaceutical compositions |
| US20060165606A1 (en) * | 1997-09-29 | 2006-07-27 | Nektar Therapeutics | Pulmonary delivery particles comprising water insoluble or crystalline active agents |
| US20080113025A1 (en) * | 1998-11-02 | 2008-05-15 | Elan Pharma International Limited | Compositions comprising nanoparticulate naproxen and controlled release hydrocodone |
| US8404217B2 (en) | 2000-05-10 | 2013-03-26 | Novartis Ag | Formulation for pulmonary administration of antifungal agents, and associated methods of manufacture and use |
| US7871598B1 (en) | 2000-05-10 | 2011-01-18 | Novartis Ag | Stable metal ion-lipid powdered pharmaceutical compositions for drug delivery and methods of use |
| AU6124601A (en) | 2000-05-10 | 2001-11-20 | Alliance Pharmaceutical Corporation | Phospholipid-based powders for drug delivery |
| JP2005514393A (ja) | 2001-12-19 | 2005-05-19 | ネクター セラピューティクス | アミノグリコシドの肺への供給 |
| CA2475092C (en) | 2002-02-04 | 2012-05-01 | Christian F. Wertz | Nanoparticulate compositions having lysozyme as a surface stabilizer |
| ES2380318T3 (es) * | 2002-04-12 | 2012-05-10 | Alkermes Pharma Ireland Limited | Formulaciones nanoparticulares de megestrol |
| US20040105889A1 (en) * | 2002-12-03 | 2004-06-03 | Elan Pharma International Limited | Low viscosity liquid dosage forms |
| US9101540B2 (en) | 2002-04-12 | 2015-08-11 | Alkermes Pharma Ireland Limited | Nanoparticulate megestrol formulations |
| US20100226989A1 (en) * | 2002-04-12 | 2010-09-09 | Elan Pharma International, Limited | Nanoparticulate megestrol formulations |
| DE60332044D1 (de) * | 2003-01-13 | 2010-05-20 | Procter & Gamble | Zusammensetzungen zur vorbeugung und behandlung von erkältung und influenza-ähnlichen erscheinungen enthaltend ausgewählte mukadhäsive polymere |
| US20040253319A1 (en) * | 2003-06-11 | 2004-12-16 | Shrirang Netke | Pharmaceutical compositions and method for alleviating side-effects of estrogen replacement therapy |
| SI1669074T1 (sl) | 2004-12-01 | 2010-10-29 | Par Pharmaceuticals Inc | Uporaba megestrol acetata za izboljšanje delovanja srca in zdravljenje srčnega popuščanja |
| JP2008524239A (ja) * | 2004-12-15 | 2008-07-10 | エラン ファーマ インターナショナル リミティド | ナノ粒子のタクロリムス製剤 |
| US20120269886A1 (en) | 2004-12-22 | 2012-10-25 | Nitto Denko Corporation | Therapeutic agent for pulmonary fibrosis |
| DK1842557T3 (da) | 2004-12-22 | 2013-12-02 | Nitto Denko Corp | Lægemiddelbærer og lægemiddelbærerkit til inhibition af fibrose |
| EP1835890A2 (en) * | 2005-01-06 | 2007-09-26 | Elan Pharma International Limited | Nanoparticulate candesartan formulations |
| US20080254114A1 (en) * | 2005-03-03 | 2008-10-16 | Elan Corporation Plc | Controlled Release Compositions Comprising Heterocyclic Amide Derivative Nanoparticles |
| BRPI0607537A2 (pt) | 2005-04-12 | 2009-09-15 | Elan Pharma Int Ltd | formulações de derivado de quinazolina nanoparticulado |
| EP1901728A2 (en) * | 2005-06-03 | 2008-03-26 | Elan Pharma International Limited | Nanoparticulate acetaminophen formulations |
| KR20080016625A (ko) | 2005-06-10 | 2008-02-21 | 도날드 이. 스코트 | 손목 터널 증후군, 산 역류, 건선, 연골 결절, 섬유근육통및 당뇨병과 관련된 증상을 경감 또는 억제하기 위한 국소조성물 및 방법 |
| AU2006262144A1 (en) * | 2005-06-22 | 2007-01-04 | Elan Pharma International, Limited | Nanoparticulate megestrol formulations |
| PL1749531T3 (pl) * | 2005-08-03 | 2016-01-29 | Par Pharmaceuticals Inc | Zastosowanie doustnej zawiesiny zawierającej octan megestrolu do leczenia astmy oskrzelowej |
| US9572886B2 (en) | 2005-12-22 | 2017-02-21 | Nitto Denko Corporation | Agent for treating myelofibrosis |
| EP1991270A4 (en) * | 2005-12-22 | 2009-12-02 | Anaborex Inc | COMPOSITIONS AND METHODS FOR THE PREVENTION AND TREATMENT OF CACHEXIA |
| US20070196498A1 (en) * | 2006-02-22 | 2007-08-23 | Sherman Bernard C | Megestrol acetate suspension |
| CL2007001847A1 (es) * | 2006-06-23 | 2008-02-08 | Tibotec Pharm Ltd | Composicion farmaceutica intramuscular o subcutanea que comprende tmc278 (rilpivirina); proceso para preparar la composicion; y uso para el tratamiento o prevencion de infeccion por vih. |
| JP5508003B2 (ja) | 2006-06-30 | 2014-05-28 | アイスイティカ ピーティーワイ リミテッド | ナノ粒子状の形態における生物学的に活性な化合物の調製のための方法 |
| WO2008008733A2 (en) * | 2006-07-10 | 2008-01-17 | Elan Pharma International Ltd. | Nanoparticulate sorafenib formulations |
| WO2008027571A2 (en) * | 2006-08-30 | 2008-03-06 | Liquidia Technologies, Inc. | Nanoparticles having functional additives for self and directed assembly and methods of fabricating same |
| JP2010510988A (ja) * | 2006-11-28 | 2010-04-08 | マリナス ファーマシューティカルズ | ナノ粒子製剤とその製造方法およびその利用 |
| DE102006057904A1 (de) * | 2006-12-08 | 2008-06-12 | Dow Wolff Cellulosics Gmbh | Herstellung von Cellulose-Nanopartikeln |
| CA2578647A1 (en) * | 2007-02-15 | 2008-08-15 | University Of Saskatchewan | Reducing post-operative adhesion formation with intraperitoneal glutamine |
| GB0704718D0 (en) * | 2007-03-12 | 2007-04-18 | Prendergast Patrick T | Compounds and methods for preventing and treating mucositis |
| NZ598881A (en) | 2007-03-29 | 2013-11-29 | Abbvie Inc | Crystalline anti-human il-12 antibodies |
| TWI407971B (zh) | 2007-03-30 | 2013-09-11 | Nitto Denko Corp | Cancer cells and tumor-related fibroblasts |
| US8653052B2 (en) * | 2007-04-24 | 2014-02-18 | Acacia Pharma Limited | Drug combination and its use in the treatment of muscle loss |
| WO2009036368A2 (en) | 2007-09-14 | 2009-03-19 | Nitto Denko Corporation | Drug carriers |
| US20100261682A1 (en) * | 2007-09-17 | 2010-10-14 | Bioneris Ab | Method and Means for the Treatment of Cachexia |
| AU2008303129B2 (en) * | 2007-09-25 | 2013-08-01 | Formulex Pharma Innovations Ltd. | Compositions comprising lipophilic active compounds and method for their preparation |
| WO2009056256A1 (en) * | 2007-11-02 | 2009-05-07 | Par Pharmaceuticals, Inc. | Use of megestrol acetate having improved solubility for the treatment of cancer cachexia |
| US8883146B2 (en) | 2007-11-30 | 2014-11-11 | Abbvie Inc. | Protein formulations and methods of making same |
| KR100958138B1 (ko) * | 2008-01-10 | 2010-05-18 | 박성순 | 안정성이 우수한 초산메게스트롤 약학 조성물 및 그제조방법 |
| US20100055246A1 (en) * | 2008-08-28 | 2010-03-04 | Dong June Ahn | Nutrition delivery capsules for functional foods |
| US20100055187A1 (en) * | 2008-08-28 | 2010-03-04 | Dong June Ahn | Nanovitamin synthesis |
| BRPI1014272A2 (pt) | 2009-04-24 | 2016-10-18 | Iceutica Pty Ltd | nova formulação de diclofenac |
| KR20150058563A (ko) | 2009-04-24 | 2015-05-28 | 아이슈티카 피티와이 리미티드 | 신규 멜록시캄 제제 |
| AU2010239081C1 (en) | 2009-04-24 | 2014-11-06 | Iceutica Pty Ltd | A novel formulation of indomethacin |
| AU2010254180B2 (en) | 2009-05-27 | 2015-08-27 | Alkermes Pharma Ireland Limited | Reduction of flake-like aggregation in nanoparticulate active agent compositions |
| TR200904500A2 (tr) | 2009-06-10 | 2009-10-21 | Öner Levent | Ezetimib nanokristallerinin hazırlanması için yöntem ve farmasötik formülasyonları. |
| AU2010331187B2 (en) * | 2009-12-18 | 2015-04-30 | Kaneka Corporation | Liquid food composition |
| JP5636211B2 (ja) * | 2010-05-31 | 2014-12-03 | 株式会社 日立産業制御ソリューションズ | 異物検査装置および異物検査方法 |
| CN103476250A (zh) | 2010-08-18 | 2013-12-25 | 德玛医药 | 改善未达最佳给药的化合物包括取代的己糖醇比如卫康醇与二乙酰二脱水卫矛醇的治疗效果的组合物和方法 |
| EP2726066B1 (en) | 2011-06-28 | 2021-03-31 | Neos Therapeutics, LP | Dosage forms of amphetamine for oral administration |
| EP3795145A3 (en) | 2011-08-17 | 2021-06-09 | Dennis M. Brown | Compositions and methods to improve the therapeutic benefit of suboptimally administered chemical compounds including substituted hexitols such as dibromodulcitol |
| WO2013074526A2 (en) | 2011-11-15 | 2013-05-23 | Byocoat Enterprises, Inc. | Antimicrobial compositions and methods of use thereof |
| US9562015B2 (en) | 2011-11-17 | 2017-02-07 | The Regents Of The University Of Colorado, A Body | Methods and compositions for enhanced drug delivery to the eye and extended delivery formulations |
| MX367614B (es) | 2012-01-20 | 2019-08-28 | Del Mar Pharmaceuticals | Uso de hexitoles sustituidos que incluyen dianhidrogalactitol y analogos para tratar enfermedad neoplasica y celulas madre de cancer que incluyen glioblastoma multiforme y meduloblastoma. |
| WO2013133903A1 (en) * | 2012-03-05 | 2013-09-12 | Aerodesigns, Inc. | Particles for aerosolizing apparatus |
| US20150087687A1 (en) | 2012-03-23 | 2015-03-26 | Dennis Brown | Compositions and methods to improve the therapeutic benefit of indirubin and analogs thereof, including meisoindigo |
| US20130316001A1 (en) * | 2012-05-03 | 2013-11-28 | Kala Pharmaceuticals, Inc. | Particles, compositions and methods for ophthalmic and/or other applications |
| WO2013169600A1 (en) | 2012-05-09 | 2013-11-14 | Delmar Pharmaceuticals | Veterinary use of dianhydrogalactitol, diacetyldianhydrogalactitol, and dibromodulcitol to treat malignancies |
| CN104797267A (zh) | 2012-06-26 | 2015-07-22 | 德玛医药 | 使用卫康醇、二乙酰二脱水卫矛醇、二溴卫矛醇或类似物或其衍生物治疗具有基因多型性或ahi1失调或突变患者的抗酪氨酸激酶抑制剂的恶性肿瘤的方法 |
| US9125911B2 (en) | 2013-03-14 | 2015-09-08 | Quadex Pharmaceuticals, Llc | Combined systemic and topical treatment of disordered tissues |
| US9549930B2 (en) | 2013-03-14 | 2017-01-24 | Quadex Pharmaceuticals, Llc | Combined systemic and topical treatment of disordered and/or prodromal stage tissue |
| US9463180B2 (en) | 2013-03-14 | 2016-10-11 | Quadex Pharmaceuticals, Llc | Treatment of molluscum contagiosum |
| CN105764501A (zh) | 2013-07-26 | 2016-07-13 | 现代化制药公司 | 改善比生群治疗效益的组合物 |
| WO2015013772A1 (en) * | 2013-08-01 | 2015-02-05 | Monash University | Compositions and preparation methods of low melting ionic salts of poorly- water soluble drugs |
| AU2015240465B2 (en) | 2014-04-04 | 2020-02-27 | Del Mar Pharmaceuticals | Use of dianhydrogalactitol and analogs or derivatives thereof to treat non-small-cell carcinoma of the lung and ovarian cancer |
| US9526734B2 (en) | 2014-06-09 | 2016-12-27 | Iceutica Pty Ltd. | Formulation of meloxicam |
| WO2016162229A1 (en) | 2015-04-10 | 2016-10-13 | Capsugel Belgium N.V. | Abiraterone acetate lipid formulations |
| US10716774B1 (en) | 2018-01-05 | 2020-07-21 | Yale Pharmaceuticals LLC | Pharmaceutical compositions containing isotretinoin with improved dissolution profile and enhanced stability |
| CN115316401A (zh) * | 2022-07-27 | 2022-11-11 | 黑龙江实创农业技术开发有限责任公司 | 一种应用于植株促生长的粒子能量制剂及制备方法 |
Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH04295420A (ja) * | 1991-01-25 | 1992-10-20 | Sterling Winthrop Inc | 表面変性薬物微小粒子 |
| JPH06199658A (ja) * | 1992-12-15 | 1994-07-19 | Sterling Winthrop Inc | ナノ粒子を含む組成物及びその製造方法 |
| JPH07165562A (ja) * | 1992-07-01 | 1995-06-27 | Sterling Winthrop Inc | 表面を修飾された抗癌性ナノ粒子 |
| WO1997010814A1 (en) * | 1995-09-18 | 1997-03-27 | Vesifact Ag | Propofol nanodispersions |
| WO2001012229A1 (en) * | 1999-08-17 | 2001-02-22 | Ivax-Cr A.S. | Pharmaceutical compositions for oral and topical administration |
| JP2001316274A (ja) * | 2000-05-08 | 2001-11-13 | Asahi Kasei Corp | 経管栄養剤およびその製造方法 |
| WO2001091750A1 (en) * | 2000-05-26 | 2001-12-06 | Pharmacia Corporation | Use of a celecoxib composition for fast pain relief |
| WO2001097779A2 (en) * | 2000-06-16 | 2001-12-27 | Rtp Pharma Inc. | Improved injectable dispersions of propofol |
| JP2002540080A (ja) * | 1999-03-19 | 2002-11-26 | パーカー ヒューズ インスティテュート | ゲルミクロ乳濁液製剤 |
Family Cites Families (77)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4826689A (en) | 1984-05-21 | 1989-05-02 | University Of Rochester | Method for making uniformly sized particles from water-insoluble organic compounds |
| US4783484A (en) | 1984-10-05 | 1988-11-08 | University Of Rochester | Particulate composition and use thereof as antimicrobial agent |
| HUT50044A (en) * | 1988-04-12 | 1989-12-28 | Bristol Myers Co | Process for producing pharmaceutical composition comprising megestrol acetate as active ingredient |
| IT1227626B (it) | 1988-11-28 | 1991-04-23 | Vectorpharma Int | Farmaci supportati aventi velocita' di dissoluzione aumentata e procedimento per la loro preparazione |
| US5552160A (en) | 1991-01-25 | 1996-09-03 | Nanosystems L.L.C. | Surface modified NSAID nanoparticles |
| AU642066B2 (en) | 1991-01-25 | 1993-10-07 | Nanosystems L.L.C. | X-ray contrast compositions useful in medical imaging |
| US5338732A (en) | 1991-06-18 | 1994-08-16 | Bristol-Myers Squibb Company | Megestrol acetate formulation |
| AU2317592A (en) | 1991-07-05 | 1993-02-11 | University Of Rochester | Ultrasmall non-aggregated porous particles entrapping gas-bubbles |
| AU660852B2 (en) | 1992-11-25 | 1995-07-06 | Elan Pharma International Limited | Method of grinding pharmaceutical substances |
| US5349957A (en) | 1992-12-02 | 1994-09-27 | Sterling Winthrop Inc. | Preparation and magnetic properties of very small magnetite-dextran particles |
| US5298262A (en) | 1992-12-04 | 1994-03-29 | Sterling Winthrop Inc. | Use of ionic cloud point modifiers to prevent particle aggregation during sterilization |
| US5346702A (en) | 1992-12-04 | 1994-09-13 | Sterling Winthrop Inc. | Use of non-ionic cloud point modifiers to minimize nanoparticle aggregation during sterilization |
| US5302401A (en) | 1992-12-09 | 1994-04-12 | Sterling Winthrop Inc. | Method to reduce particle size growth during lyophilization |
| US5340564A (en) | 1992-12-10 | 1994-08-23 | Sterling Winthrop Inc. | Formulations comprising olin 10-G to prevent particle aggregation and increase stability |
| US5336507A (en) | 1992-12-11 | 1994-08-09 | Sterling Winthrop Inc. | Use of charged phospholipids to reduce nanoparticle aggregation |
| US5352459A (en) | 1992-12-16 | 1994-10-04 | Sterling Winthrop Inc. | Use of purified surface modifiers to prevent particle aggregation during sterilization |
| US5401492A (en) | 1992-12-17 | 1995-03-28 | Sterling Winthrop, Inc. | Water insoluble non-magnetic manganese particles as magnetic resonance contract enhancement agents |
| US5326552A (en) | 1992-12-17 | 1994-07-05 | Sterling Winthrop Inc. | Formulations for nanoparticulate x-ray blood pool contrast agents using high molecular weight nonionic surfactants |
| US5264610A (en) | 1993-03-29 | 1993-11-23 | Sterling Winthrop Inc. | Iodinated aromatic propanedioates |
| WO1995011039A1 (de) | 1993-10-22 | 1995-04-27 | Hexal Pharma Gmbh | Pharmazeutische zusammensetzung mit cyclosporin a und alpha-tocopherol |
| US5605889A (en) * | 1994-04-29 | 1997-02-25 | Pfizer Inc. | Method of administering azithromycin |
| TW384224B (en) | 1994-05-25 | 2000-03-11 | Nano Sys Llc | Method of preparing submicron particles of a therapeutic or diagnostic agent |
| US5718388A (en) | 1994-05-25 | 1998-02-17 | Eastman Kodak | Continuous method of grinding pharmaceutical substances |
| US5525328A (en) | 1994-06-24 | 1996-06-11 | Nanosystems L.L.C. | Nanoparticulate diagnostic diatrizoxy ester X-ray contrast agents for blood pool and lymphatic system imaging |
| US5587143A (en) | 1994-06-28 | 1996-12-24 | Nanosystems L.L.C. | Butylene oxide-ethylene oxide block copolymer surfactants as stabilizer coatings for nanoparticle compositions |
| US5466440A (en) | 1994-12-30 | 1995-11-14 | Eastman Kodak Company | Formulations of oral gastrointestinal diagnostic X-ray contrast agents in combination with pharmaceutically acceptable clays |
| US5628981A (en) | 1994-12-30 | 1997-05-13 | Nano Systems L.L.C. | Formulations of oral gastrointestinal diagnostic x-ray contrast agents and oral gastrointestinal therapeutic agents |
| US5585108A (en) | 1994-12-30 | 1996-12-17 | Nanosystems L.L.C. | Formulations of oral gastrointestinal therapeutic agents in combination with pharmaceutically acceptable clays |
| US5560932A (en) | 1995-01-10 | 1996-10-01 | Nano Systems L.L.C. | Microprecipitation of nanoparticulate pharmaceutical agents |
| US5662883A (en) | 1995-01-10 | 1997-09-02 | Nanosystems L.L.C. | Microprecipitation of micro-nanoparticulate pharmaceutical agents |
| US5665331A (en) | 1995-01-10 | 1997-09-09 | Nanosystems L.L.C. | Co-microprecipitation of nanoparticulate pharmaceutical agents with crystal growth modifiers |
| US5569448A (en) | 1995-01-24 | 1996-10-29 | Nano Systems L.L.C. | Sulfated nonionic block copolymer surfactants as stabilizer coatings for nanoparticle compositions |
| US5571536A (en) | 1995-02-06 | 1996-11-05 | Nano Systems L.L.C. | Formulations of compounds as nanoparticulate dispersions in digestible oils or fatty acids |
| US5560931A (en) | 1995-02-14 | 1996-10-01 | Nawosystems L.L.C. | Formulations of compounds as nanoparticulate dispersions in digestible oils or fatty acids |
| US5534270A (en) | 1995-02-09 | 1996-07-09 | Nanosystems Llc | Method of preparing stable drug nanoparticles |
| US5622938A (en) | 1995-02-09 | 1997-04-22 | Nano Systems L.L.C. | Sugar base surfactant for nanocrystals |
| US5593657A (en) | 1995-02-09 | 1997-01-14 | Nanosystems L.L.C. | Barium salt formulations stabilized by non-ionic and anionic stabilizers |
| US5518738A (en) | 1995-02-09 | 1996-05-21 | Nanosystem L.L.C. | Nanoparticulate nsaid compositions |
| US5500204A (en) | 1995-02-10 | 1996-03-19 | Eastman Kodak Company | Nanoparticulate diagnostic dimers as x-ray contrast agents for blood pool and lymphatic system imaging |
| US5591456A (en) | 1995-02-10 | 1997-01-07 | Nanosystems L.L.C. | Milled naproxen with hydroxypropyl cellulose as a dispersion stabilizer |
| US5573783A (en) | 1995-02-13 | 1996-11-12 | Nano Systems L.L.C. | Redispersible nanoparticulate film matrices with protective overcoats |
| US5543133A (en) | 1995-02-14 | 1996-08-06 | Nanosystems L.L.C. | Process of preparing x-ray contrast compositions containing nanoparticles |
| US5510118A (en) | 1995-02-14 | 1996-04-23 | Nanosystems Llc | Process for preparing therapeutic compositions containing nanoparticles |
| US5580579A (en) | 1995-02-15 | 1996-12-03 | Nano Systems L.L.C. | Site-specific adhesion within the GI tract using nanoparticles stabilized by high molecular weight, linear poly (ethylene oxide) polymers |
| WO1996025918A1 (en) | 1995-02-24 | 1996-08-29 | Nanosystems L.L.C. | Aerosols containing nanoparticle dispersions |
| US5718919A (en) | 1995-02-24 | 1998-02-17 | Nanosystems L.L.C. | Nanoparticles containing the R(-)enantiomer of ibuprofen |
| US5747001A (en) | 1995-02-24 | 1998-05-05 | Nanosystems, L.L.C. | Aerosols containing beclomethazone nanoparticle dispersions |
| US5565188A (en) | 1995-02-24 | 1996-10-15 | Nanosystems L.L.C. | Polyalkylene block copolymers as surface modifiers for nanoparticles |
| US5472683A (en) | 1995-03-09 | 1995-12-05 | Eastman Kodak Company | Nanoparticulate diagnostic mixed carbamic anhydrides as X-ray contrast agents for blood pool and lymphatic system imaging |
| US5643552A (en) | 1995-03-09 | 1997-07-01 | Nanosystems L.L.C. | Nanoparticulate diagnostic mixed carbonic anhydrides as x-ray contrast agents for blood pool and lymphatic system imaging |
| US5573749A (en) | 1995-03-09 | 1996-11-12 | Nano Systems L.L.C. | Nanoparticulate diagnostic mixed carboxylic anhydrides as X-ray contrast agents for blood pool and lymphatic system imaging |
| US5521218A (en) | 1995-05-15 | 1996-05-28 | Nanosystems L.L.C. | Nanoparticulate iodipamide derivatives for use as x-ray contrast agents |
| US5573750A (en) | 1995-05-22 | 1996-11-12 | Nanosystems L.L.C. | Diagnostic imaging x-ray contrast agents |
| US5834025A (en) | 1995-09-29 | 1998-11-10 | Nanosystems L.L.C. | Reduction of intravenously administered nanoparticulate-formulation-induced adverse physiological reactions |
| US6458373B1 (en) | 1997-01-07 | 2002-10-01 | Sonus Pharmaceuticals, Inc. | Emulsion vehicle for poorly soluble drugs |
| WO1998035666A1 (en) | 1997-02-13 | 1998-08-20 | Nanosystems Llc | Formulations of nanoparticle naproxen tablets |
| US6045829A (en) | 1997-02-13 | 2000-04-04 | Elan Pharma International Limited | Nanocrystalline formulations of human immunodeficiency virus (HIV) protease inhibitors using cellulosic surface stabilizers |
| GB9718568D0 (en) | 1997-09-03 | 1997-11-05 | Chauvin Pharmaceuticals Limite | Compositions |
| US5891845A (en) | 1997-11-21 | 1999-04-06 | Fuisz Technologies Ltd. | Drug delivery systems utilizing liquid crystal structures |
| FR2775435B1 (fr) * | 1998-02-27 | 2000-05-26 | Bioalliance Pharma | Nanoparticules comprenant au moins un polymere et au moins un compose apte a complexer un ou plusieurs principes actifs |
| US6028065A (en) | 1998-04-20 | 2000-02-22 | Pharmaceutical Resources, Inc. | Flocculated suspension of megestrol acetate |
| US6268356B1 (en) | 1998-04-20 | 2001-07-31 | Pharmaceutical Resources, Inc. | Flocculated suspension of megestrol acetate |
| US6153225A (en) | 1998-08-13 | 2000-11-28 | Elan Pharma International Limited | Injectable formulations of nanoparticulate naproxen |
| US6165506A (en) | 1998-09-04 | 2000-12-26 | Elan Pharma International Ltd. | Solid dose form of nanoparticulate naproxen |
| US8293277B2 (en) | 1998-10-01 | 2012-10-23 | Alkermes Pharma Ireland Limited | Controlled-release nanoparticulate compositions |
| US6375986B1 (en) | 2000-09-21 | 2002-04-23 | Elan Pharma International Ltd. | Solid dose nanoparticulate compositions comprising a synergistic combination of a polymeric surface stabilizer and dioctyl sodium sulfosuccinate |
| US6428814B1 (en) | 1999-10-08 | 2002-08-06 | Elan Pharma International Ltd. | Bioadhesive nanoparticulate compositions having cationic surface stabilizers |
| US6270806B1 (en) | 1999-03-03 | 2001-08-07 | Elan Pharma International Limited | Use of peg-derivatized lipids as surface stabilizers for nanoparticulate compositions |
| US6267989B1 (en) | 1999-03-08 | 2001-07-31 | Klan Pharma International Ltd. | Methods for preventing crystal growth and particle aggregation in nanoparticulate compositions |
| WO2000072973A1 (en) | 1999-06-01 | 2000-12-07 | Elan Pharma International Ltd. | Small-scale mill and method thereof |
| US6656504B1 (en) * | 1999-09-09 | 2003-12-02 | Elan Pharma International Ltd. | Nanoparticulate compositions comprising amorphous cyclosporine and methods of making and using such compositions |
| US6316029B1 (en) | 2000-05-18 | 2001-11-13 | Flak Pharma International, Ltd. | Rapidly disintegrating solid oral dosage form |
| US6656505B2 (en) | 2000-07-21 | 2003-12-02 | Alpharma Uspd Inc. | Method for forming an aqueous flocculated suspension |
| US20020028794A1 (en) | 2000-07-21 | 2002-03-07 | Brubaker Greg Allen | Megestrol acetate suspension |
| AU2001297844A1 (en) * | 2000-11-20 | 2002-12-03 | Elan Pharma International Ltd. | Nanoparticulate compositions comprising a drug and copolymers of vinyl pyrrolidone and vimyl acetate as surface stabilizers |
| CA2449490C (en) | 2001-06-05 | 2010-10-05 | Elan Pharma International Limited | System and method for milling materials |
| US9101540B2 (en) | 2002-04-12 | 2015-08-11 | Alkermes Pharma Ireland Limited | Nanoparticulate megestrol formulations |
-
2003
- 2003-04-14 US US10/412,669 patent/US7101576B2/en not_active Expired - Lifetime
- 2003-04-23 AU AU2003231071A patent/AU2003231071A1/en not_active Abandoned
- 2003-04-23 JP JP2004570751A patent/JP4838514B2/ja not_active Expired - Fee Related
- 2003-04-23 WO PCT/US2003/012660 patent/WO2004050059A1/en active Application Filing
- 2003-04-23 CA CA002508301A patent/CA2508301A1/en not_active Abandoned
- 2003-04-23 EP EP03724196A patent/EP1613276A1/en not_active Ceased
- 2003-04-23 EP EP10011267A patent/EP2263651A3/en not_active Withdrawn
-
2011
- 2011-07-22 JP JP2011160522A patent/JP2011251989A/ja active Pending
Patent Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH04295420A (ja) * | 1991-01-25 | 1992-10-20 | Sterling Winthrop Inc | 表面変性薬物微小粒子 |
| JPH07165562A (ja) * | 1992-07-01 | 1995-06-27 | Sterling Winthrop Inc | 表面を修飾された抗癌性ナノ粒子 |
| JPH06199658A (ja) * | 1992-12-15 | 1994-07-19 | Sterling Winthrop Inc | ナノ粒子を含む組成物及びその製造方法 |
| WO1997010814A1 (en) * | 1995-09-18 | 1997-03-27 | Vesifact Ag | Propofol nanodispersions |
| JP2002540080A (ja) * | 1999-03-19 | 2002-11-26 | パーカー ヒューズ インスティテュート | ゲルミクロ乳濁液製剤 |
| WO2001012229A1 (en) * | 1999-08-17 | 2001-02-22 | Ivax-Cr A.S. | Pharmaceutical compositions for oral and topical administration |
| JP2001316274A (ja) * | 2000-05-08 | 2001-11-13 | Asahi Kasei Corp | 経管栄養剤およびその製造方法 |
| WO2001091750A1 (en) * | 2000-05-26 | 2001-12-06 | Pharmacia Corporation | Use of a celecoxib composition for fast pain relief |
| WO2001097779A2 (en) * | 2000-06-16 | 2001-12-27 | Rtp Pharma Inc. | Improved injectable dispersions of propofol |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2011251989A (ja) | 2011-12-15 |
| EP1613276A1 (en) | 2006-01-11 |
| AU2003231071A1 (en) | 2004-06-23 |
| EP2263651A3 (en) | 2011-09-14 |
| JP2006510726A (ja) | 2006-03-30 |
| EP2263651A2 (en) | 2010-12-22 |
| WO2004050059A1 (en) | 2004-06-17 |
| US20030219490A1 (en) | 2003-11-27 |
| US7101576B2 (en) | 2006-09-05 |
| CA2508301A1 (en) | 2004-06-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4838514B2 (ja) | 低粘度液体剤形 | |
| US9101549B2 (en) | Nanoparticulate megestrol formulations | |
| US20130251805A1 (en) | Low viscosity liquid dosage forms | |
| JP4776229B2 (ja) | 安定なナノ粒子活性物質の液体投与組成物 | |
| JP4611641B2 (ja) | Mapキナーゼ阻害剤のナノ粒子組成物 | |
| US20070098805A1 (en) | Methods of making and using novel griseofulvin compositions | |
| KR20080017065A (ko) | 나노입자형 아세트아미노펜 제제 | |
| JP2013136621A (ja) | ナノ粒子アリピプラゾール製剤 | |
| JP2005529911A (ja) | ナノ粒子ナイスタチン製剤 | |
| JP2010248220A (ja) | ナノ粒子メゲストロール製剤 | |
| JP2008546796A (ja) | ナノ微粒子メゲストロール製剤 | |
| US20120087955A1 (en) | Nanoparticulate megestrol formulations | |
| EP1935407A1 (en) | Low viscosity liquid dosage forms |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20060407 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20060407 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20091221 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20100318 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20100326 |
|
| A524 | Written submission of copy of amendment under article 19 pct |
Free format text: JAPANESE INTERMEDIATE CODE: A524 Effective date: 20100618 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20110323 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110722 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110811 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20110817 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20110907 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20110930 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20141007 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| LAPS | Cancellation because of no payment of annual fees |