JP4579246B2 - 乳癌を診断する方法 - Google Patents
乳癌を診断する方法 Download PDFInfo
- Publication number
- JP4579246B2 JP4579246B2 JP2006527766A JP2006527766A JP4579246B2 JP 4579246 B2 JP4579246 B2 JP 4579246B2 JP 2006527766 A JP2006527766 A JP 2006527766A JP 2006527766 A JP2006527766 A JP 2006527766A JP 4579246 B2 JP4579246 B2 JP 4579246B2
- Authority
- JP
- Japan
- Prior art keywords
- breast cancer
- cells
- protein
- brc
- gene
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
- C12Q1/6883—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material
- C12Q1/6886—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material for cancer
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/04—Antineoplastic agents specific for metastasis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/46—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
- C07K14/47—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals
- C07K14/4701—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals not used
- C07K14/4702—Regulators; Modulating activity
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/575—Immunoassay; Biospecific binding assay; Materials therefor for cancer
- G01N33/57515—Immunoassay; Biospecific binding assay; Materials therefor for cancer of the breast
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/112—Disease subtyping, staging or classification
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/118—Prognosis of disease development
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/136—Screening for pharmacological compounds
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/156—Polymorphic or mutational markers
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/158—Expression markers
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2500/00—Screening for compounds of potential therapeutic value
- G01N2500/04—Screening involving studying the effect of compounds C directly on molecule A (e.g. C are potential ligands for a receptor A, or potential substrates for an enzyme A)
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Immunology (AREA)
- General Health & Medical Sciences (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Molecular Biology (AREA)
- Zoology (AREA)
- Biochemistry (AREA)
- Analytical Chemistry (AREA)
- Medicinal Chemistry (AREA)
- Genetics & Genomics (AREA)
- Pathology (AREA)
- Microbiology (AREA)
- Urology & Nephrology (AREA)
- Hematology (AREA)
- Biomedical Technology (AREA)
- Wood Science & Technology (AREA)
- Physics & Mathematics (AREA)
- Biophysics (AREA)
- Biotechnology (AREA)
- Oncology (AREA)
- Toxicology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Gastroenterology & Hepatology (AREA)
- General Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Cell Biology (AREA)
- Pharmacology & Pharmacy (AREA)
- Hospice & Palliative Care (AREA)
- Food Science & Technology (AREA)
- General Physics & Mathematics (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Description
本発明は、乳癌を診断する方法に関する。
乳癌は、多数の遺伝子における非常に多くの遺伝的および後成的な変化を特徴とする複合的な疾患である(Katherine N. N., Richard W. and Barbara L. W.「Breast Cancer genetics:What we know and what we need.」Nat Med, 7(5):552-556, 2001)。これらの異常が乳房腫瘍形成の原因であるのか否かはほとんど分かっていないが、これは異型乳管過形成、非浸潤性乳管癌(DCIS)および浸潤性乳管癌(IDC)の諸段階を含む、正常細胞の形質転換と大枠では同一視しうる多段階過程によって起こることが報告されている。乳癌発生の諸段階は他の組織におけるものと類似しているが、乳癌を引き起こす正確な分子的機序は依然として不明である。いずれにしても、原発性乳癌の発生、その進行およびその転移をもたらす分子的要因が、本疾患の早期診断、治療および予防のためのより良いツールの開発にとって有益な標的となることは容易に理解できる。
本発明は、アッセイした乳癌症例のそれぞれ49例中38例、73例中30例、および49例中28例で発現が有意に上方制御されていた以下の3つの遺伝子の発見に関する:A5657(SEQ ID NO:1)、これはユビキチン結合酵素に類似したHSPC150タンパク質(SEQ ID NO:2)をコードする;B9769(SEQ ID NO:3)、これは仮説上のタンパク質BC016861(SEQ ID NO:4)をコードする;およびC7965(SEQ ID NO:5)、これはLOC90557(SEQ ID NO:6)として指定される。その後の半定量的RT-PCRおよびノーザンブロット分析により、A5657、B9769、およびC7965が、臨床的な乳癌試料および乳癌細胞株では、乳管細胞および正常乳房を含む正常ヒト組織と比較して有意に過剰発現されることが確かめられた。特に、B9769はERα陽性乳癌細胞株において高発現された。免疫細胞化学染色により、乳癌細胞株T47D細胞において、外因性A5657、B9769、およびC7965はそれぞれ細胞質および/または核装置、細胞質、および細胞小器官のそれぞれに局在した。特に、外因性B9769は、COS7細胞およびT47D細胞において中間径フィラメント網に観察された。さらに、A5657タンパク質がユビキチンと相互作用することが免疫沈降結合アッセイによって示され、このことはA5657タンパク質がE2ユビキチン酵素活性を有する可能性を示唆する。低分子干渉RNA(siRNA)による乳癌細胞の処理は、A5657、B9769、およびC7965の発現を効果的に阻害し、乳癌の細胞/腫瘍成長をそれぞれ抑制した。加えて、この3種の遺伝子はいずれも、NIH3T3細胞で一過性に過剰発現させた場合にMTTアッセイにおける細胞増殖を劇的に促進することが見いだされ、このことからこれらが細胞の成長増殖に重要な役割を果たすことが示唆された。これらの所見は、A5657、B9769、およびC7965の過剰発現が乳房腫瘍形成に関与する可能性があり、かつ乳癌患者に対する特異的治療法のための有望な戦略となる可能性があることを示唆する。
本明細書で用いる「1つの(a)」、「1つの(an)」および「その(the)」という用語は、別に特記する場合を除き、「少なくとも1つの」を意味する。
本発明は、乳癌の大多数において、対応する非癌性乳房上皮と比較して発現が顕著に亢進している新規ヒト遺伝子A5657およびB9769を提供する。単離されたA5657遺伝子は、928ヌクレオチドを含むcDNA配列である、SEQ ID NO:1に記載されたポリヌクレオチド配列を含む。特に、A5657は7つのエクソンからなり、ゲノム中では染色体1q32.1上に約10.3kbの範囲にわたって存在する。このcDNA転写物は最終的には、ユビキチン結合酵素に類似したHSPC150タンパク質という197アミノ酸のポリペプチドをコードする。単離されたB9769遺伝子は、1472ヌクレオチドを含むcDNA配列である、SEQ ID NO:3に記載されたポリヌクレオチドを含む。特に、B9769は8つのエクソンからなり、ゲノム中では染色体2q21.2上に約5.7kbの範囲にわたって存在する。そのORFはエクソン1で始まり、エクソン8で終わる。最終的には、このcDNA転写物は378アミノ酸のポリペプチドをコードする。
本発明は、本発明のポリペプチドと結合する抗体をさらに提供する。本発明の抗体は、モノクローナル抗体またはポリクローナル抗体などの任意の形態で用いることができ、これにはウサギなどの動物を本発明のポリペプチドで免疫することによって得られる抗血清、すべてのクラスのポリクローナル抗体およびモノクローナル抗体、ヒト抗体、ならびに遺伝子組換えによって作製されたヒト化抗体が含まれる。
本発明の文脈において、BRCは、被験細胞集団(すなわち、患者由来の生物学的試料)からの1つまたは複数のBRC核酸の発現レベルを測定することによって診断される。好ましくは被験細胞集団は、上皮細胞、例えば、乳房組織から得られた細胞を含む。遺伝子発現を、血液または他の体液(尿など)から測定することもできる。他の生物学的試料をタンパク質レベルの測定のために用いることもできる。例えば、診断しようとする対象から得た血液または血清中のタンパク質レベルを、イムノアッセイまたは従来の生物学的アッセイによって測定することができる。
BRC関連遺伝子の発現またはその遺伝子産物の活性を阻害する物質は、BRCに関連して上方制御される遺伝子を発現する被験細胞集団を被験物質と接触させた後に、BRC関連遺伝子の発現レベルまたは活性を決定することによって同定することができる。物質の存在下、BRC関連遺伝子の発現レベルまたはその遺伝子産物の活性レベルが正常対照レベルと比較して(または被験物質の非存在下における発現レベルもしくは活性レベルと比較して)低下していることにより、その物質がBRC関連遺伝子の阻害物質であってBRCを阻害するのに有用であることが示される。
本明細書で同定された、差次的に発現されるBRC関連遺伝子は、BRCの治療の経過をモニターすることも可能にする。この方法では、BRCに対する治療を受けようとする対象から被験細胞集団を得る。必要に応じて、治療前、治療中、および/または治療後といった種々の時点で被験細胞集団を対象から入手する。続いて、細胞集団におけるBRC関連遺伝子の1つまたは複数の発現を決定し、BRCの状態が判明している細胞を含む参照細胞集団と比較する。本発明の文脈において、参照細胞は、関心対象の治療を受けていない必要がある。
個体における遺伝的構成の差によって、個体が様々な薬剤を代謝する相対的能力に差が起こりうる。対象において代謝されて抗BRC物質として作用する物質は、対象の細胞において、癌性状態に特徴的な遺伝子発現パターンから非癌性状態に特徴的な遺伝子発現パターンへの変化を誘導することによって顕在化しうる。したがって、物質が対象において適したBRC阻害物質であるか否かを決定するために、本明細書に開示される発現差のあるBRC関連遺伝子によって、選択された対象からの被験細胞集団において、治療効果があるまたは予防効果があると推定されるBRC阻害物質が適切かどうかを調べることができる。
本明細書に開示した、差次的に発現されるBRC関連遺伝子を、BRCを治療するための候補治療剤を同定するのに用いることもできる。本発明の方法は、候補治療剤が、BRC状態に特徴的なBRC関連遺伝子A5657、B9769、およびC7965のうち1つまたは複数の発現プロファイルを、非BRC状態に特徴的な遺伝子発現パターンへと変換させうるか否かを判定することを目的に、候補治療剤をスクリーニングすることを含む。
a)被験化合物を、A5657、B9769、およびC7965によってコードされるポリペプチドに接触させる段階;
b)ポリペプチドと被験化合物との結合活性を検出する段階;および
c)ポリペプチドと結合する被験化合物を選択する段階。
a)候補化合物を、A5657、B9769、およびC7965からなる群より選択される1つまたは複数のマーカー遺伝子を発現する細胞に接触させる段階;および
b)1つまたは複数のマーカー遺伝子の発現レベルを候補化合物の非存在下で検出される発現レベルと比較して低下させる候補化合物を選択する段階。
マーカー遺伝子を発現する細胞には、例えば、BRCから樹立された細胞株が含まれる;このような細胞は本発明の上記のスクリーニングに用いることができる。
a)被験化合物を、BRC関連遺伝子A5657、B9769、およびC7965からなる群より選択されるポリヌクレオチドによってコードされるポリペプチドに接触させる段階;
b)段階(a)のポリペプチドの生物学的活性を検出する段階;および
c)ポリペプチドの生物学的活性を被験化合物の非存在下で検出される生物学的活性と比較して抑制する化合物を選択する段階。
a)候補化合物を、BRC関連遺伝子A5657、B9769、およびC7965からなる群より選択される1つまたは複数のマーカー遺伝子の転写調節領域とその転写調節領域の制御下で発現されるレポーター遺伝子とを含むベクターが導入された細胞に接触させる段階;
b)該レポーター遺伝子の発現レベルまたは活性を測定する段階;ならびに
c)該レポーター遺伝子の発現レベルまたは活性を候補化合物の非存在下で検出される発現レベルまたは活性と比較して低下させる候補化合物を選択する段階。
本発明はまた、BRCを有する対象の予後を評価する方法であって、被験細胞集団における1つまたは複数のBRC関連遺伝子の発現を、ある範囲の疾患病期にわたる患者から得られた参照細胞集団におけるBRC関連遺伝子A5657、B9769、およびC7965の発現と比較する段階を含む方法も提供する。被験細胞集団および参照細胞集団における1つもしくは複数のBRC関連遺伝子の遺伝子発現を比較することにより、または対象から得られた被験細胞集団の経時的な遺伝子発現のパターンを比較することにより、対象の予後を評価することができる。
本発明にはまた、BRC検出試薬、例えばBRC核酸の一部と相補的なオリゴヌクレオチド配列のような、一つまたは複数のBRC核酸に特異的に結合する核酸か、BRC核酸にコードされる一つまたは複数のタンパク質に結合する抗体が含まれる。検出試薬は、キットの形で共に包装されていてもよい。例えば検出試薬、例えば核酸または抗体(固相マトリクスに結合させるか、またはそれらをマトリクスに結合させるための試薬とは別に包装される)、対照試薬(陽性および/または陰性)、ならびに/または検出標識は、異なる容器に包装されていてもよい。アッセイを行うための説明書(例えば、書面、テープ、VCR、CD-ROM等)がキットに含まれていてもよい。キットのアッセイフォーマットは、当技術分野でいずれも既知であるノーザンハイブリダイゼーションまたはサンドイッチELISAであってもよい。
本発明にはまた、一つまたは複数の核酸を含む核酸基質アレイも含まれる。アレイ上の核酸は、BRC関連遺伝子A5657、B9769、およびC7965によって示される一つまたは複数の核酸配列に特異的に対応する。BRC関連遺伝子A5657、B9769、およびC7965によって表される核酸の2つまたはそれ以上の発現レベルは、アレイに結合する核酸を検出することによって同定されうる。
本発明はさらに、上方制御されるBRC関連遺伝子A5657、B9769、およびC7965のうちの1つまたは複数の発現(またはその遺伝子産物の活性)を低下させることにより、対象におけるBRCの症状を治療または軽減するための方法も提供する。適した治療用化合物を、BRCに罹患している対象またはBRC発症のリスク(もしくはそれに対する感受性)を有する対象に対して、予防的または治療的に投与することができる。このような対象は、標準的な臨床的方法を用いて、またはBRC関連遺伝子A5657、B9769、およびC7965のうちの1つまたは複数の異常な発現レベルもしくはその遺伝子産物の異常な活性を検出することにより、同定することができる。本発明の文脈において、適した治療薬には、例えば、細胞周期調節、細胞増殖、およびプロテインキナーゼ活性の阻害物質が含まれる。
上記のように、BRC関連遺伝子A5657、B9769、およびC7965のヌクレオチド配列に対応するアンチセンス核酸は、遺伝子の発現レベルを低下させるために用いることができる。乳癌において上方制御されるBRC関連遺伝子A5657、B9769、およびC7965に対応するアンチセンス核酸は、乳癌の治療のために有用である。具体的には、本発明のアンチセンス核酸は、BRC関連遺伝子A5657、B9769、およびC7965またはそれらに対応するmRNAと結合することによって作用し、それによって遺伝子の転写または翻訳を阻害し、mRNAの分解を促進し、および/またはBRC関連遺伝子A5657、B9769、およびC7965によってコードされるタンパク質の発現を阻害し、それらによってタンパク質の機能を阻害することができる。本明細書で用いる「アンチセンス核酸」という用語には、標的配列に対して完全に相補的なヌクレオチドと、アンチセンス核酸が標的配列と特異的にハイブリダイズしうるという条件付きで、1つまたは複数のヌクレオチドにミスマッチがあるヌクレオチドとの両方が含まれる。例えば、本発明のアンチセンス核酸には、少なくとも15個の連続したヌクレオチドの範囲にわたって少なくとも70%またはそれ以上、好ましくは少なくとも80%またはそれ以上、より好ましくは少なくとも90%またはそれ以上、さらにより好ましくは少なくとも95%またはそれ以上の相同性を有するポリヌクレオチドが含まれる。相同性の決定には当技術分野で知られたアルゴリズムを用いうる。
CCC、CCACC、またはCCACACC:Jacque, J. M.Triques,K. and Stevenson, M (2002) 「Modulation of HIV-1 replication by RNA interference.」Nature, Vol. 418:435-438。
UUCG:Lee, N.S., Dohjima, T., Bauer, G., Li, H., Li, M.-J., Ehsani, A., Salvaterra, P. and Rossi, J. (2002) 「Expression of small interfering RNAs targeted against HIV-1 rev transcripts in human cells.」Nature Biotechnology 20:500-505。Fruscoloni, P., Zamboni, M. and Tocchini-Valentini, G. P. (2003) 「Exonucleolytic degradation of double-stranded RNA by an activity in Xenopus laevis germinal vesicles.」Proc. Natl. Acad. Sci. USA 100(4):1639-1644。
UUCAAGAGA:Dykxhoorn, D. M., Novina, C. D. and Sharp, P. A. (2002) 「Killing the messenger:Short RNAs that silence gene expression.」Nature Reviews Molecular Cell Biology 4:457-467。
A5657-siRNAに対して:
caucgcaacuguguugacc-[b]-ggucaacacaguugcgaug(SEQ ID NO:28の標的配列に対して);および
ugccagacaguggacagag-[b]-cucuguccacugucuggca(SEQ ID NO:29の標的配列に対して)。
B9769-siRNAに対して:
gccugcaguuccugcagca-[b]-ugcugcaggaacugcaggc(SEQ ID NO:30の標的配列に対して);
gcuuccagucugucaaguc-[b]-gacuugacagacuggaagc(SEQ ID NO:31の標的配列に対して);および
agcagaggccucuaaugca-[b]-ugcauuagaggccucugcu(SEQ ID NO:32の標的配列に対して)。
C7965-siRNAに対して:
acugcuccucucagcuucc-[b]-ggaagcugagaggagcagu(SEQ ID NO:33の標的配列に対して);および
guacgcuuacuggcaucaa-[b]-uugaugccaguaagcguac(SEQ ID NO:34の標的配列に対して)。
1.対象となる転写物のAUG開始コドンから始めて、AAジヌクレオチド配列を求めて下流にスキャンする。潜在的なsiRNA標的部位として、各AAおよび3'隣接ヌクレオチド19個の出現を記録する。Tuschlらは、5'および3'非翻訳領域(UTR)および開始コドン近傍(75塩基以内)の領域が、調節タンパク質結合部位により富んでいる可能性があることから、これらに対してsiRNAを設計しないことを推奨している。UTR-結合タンパク質および/または翻訳開始複合体は、siRNAエンドヌクレアーゼ複合体の結合を妨害しうる。
2.潜在的な標的部位をヒトゲノムデータベースと比較して、他のコード配列と有意な相同性を有する如何なる標的配列も検討から除外する。相同性検索は、NCBIサーバー、www.ncbi.nlm.nih.gov/BLAST/において認められうるBLASTを用いて行うことができる。
3.合成のために適格な標的配列を選択する。アンビオンでは、好ましくは、評価すべき遺伝子の長さに沿っていくつかの標的配列を選択することができる。
または、BRCにおいて過剰発現された遺伝子(例えば、A5657、B9769、またはC7965)の一つまたは複数の遺伝子産物の機能は、遺伝子産物に結合する化合物、さもなければ遺伝子産物の機能を阻害する化合物を投与することによって阻害されうる。例えば、化合物は、過剰発現された遺伝子産物または複数の遺伝子産物に結合する抗体であってもよい。
本発明はまた、BRC関連遺伝子A5657、B9769、およびC7965からなる群より選択される核酸にコードされるポリペプチド、該ポリペプチドの免疫学的活性断片、またはポリペプチドもしくはその断片をコードするポリヌクレオチドを含むワクチンを対象に投与する段階を含む、対象における乳癌を治療または予防する方法にも関する。ポリペプチドの投与は、対象において抗腫瘍免疫を誘導する。抗腫瘍免疫を誘導するために、BRC関連遺伝子A5657、B9769、およびC7965からなる群より選択される核酸にコードされるポリペプチド、該ポリペプチドの免疫学的活性断片、または該ポリペプチドもしくはその断片をコードするポリヌクレオチドを、治療または予防が必要な患者に投与する。ポリペプチドまたはその免疫学的活性断片はBRCに対するワクチンとして有用である。場合によっては、タンパク質またはその断片は、T細胞受容体(TCR)に結合した形で投与してもよく、またはマクロファージ、樹状細胞(DC)、もしくはB-細胞のような抗原提示細胞(APC)によって提示された形で投与してもよい。DCの強い抗原提示能のため、APCの中では、DCを用いることが最も好ましい。
−腫瘍に対する細胞障害性リンパ球の誘導、
−腫瘍を認識する抗体の誘導、および
−抗腫瘍サイトカイン産生の誘導。
本発明の文脈において、適切な薬学的製剤には、経口、直腸内、鼻腔内、局所(口腔内および舌下を含む)、膣内、もしくは非経口(筋肉内、皮下、および静脈内を含む)投与に適した製剤、または吸入もしくは吹入による投与に適した製剤が含まれる。好ましくは、投与は静脈内である。製剤は任意で用量単位ごとに個別に包装される。
疾病状態、例えば、BRCにおいて差次的に発現される遺伝子を同定するために、罹患組織(例えば、BRC由来の上皮細胞)および正常組織から入手した組織を評価した。アッセイは以下の通りに行った。
癌研究会附属病院乳腺外科部門(Department of Breast Surgery、Cancer Institute Hospital、東京、日本)で治療を受けた81例の患者(非浸潤性乳管癌12例および浸潤性乳管癌69例、2cm〜5cm(T2)、年齢の中央値45歳、21〜68歳の範囲)から、インフォームドコンセントを伴って原発性乳癌を入手した(表2)このことに関しては全ての患者からインフォームドコンセントを得た。臨床情報を診療記録から入手し、かつそれぞれの腫瘍を病理学者が病理組織学的なサブタイプおよびグレードに従って診断した。腫瘍組織を用いて腫瘍の種類を評価した(世界保健機構(World Health Organization)の分類および日本癌学会の分類による)。臨床病期はJBCSのTNM分類に従って判断した。リンパ節陽性症例とリンパ節陰性症例との間に有意差は観察されなかった。血管侵入性増殖および広範囲にわたるリンパ球浸潤の存在は病理学者が判定した。エストロゲン受容体(ER)およびプロゲステロン受容体(PgR)の発現はEIAにより判定した(13fmol/mgタンパク質未満であればER陰性、BML)。閉経前乳癌患者15例または閉経後患者12例からの正常乳管細胞の混合物をそれぞれ正常対照として用いた。試料はすべて直ちに凍結し、-80℃で保存した。
腫瘍に関する臨床情報および病理学的情報は表2に詳述されている。試料はTissueTek OCT媒質(Sakura)中に包埋した後に使用時まで-80℃で保存した。凍結標本をクリオスタットで連続的に切片化して8μmの切片とし、分析する領域を規定するためにヘマトキシリンおよびエオシンで染色した。癌細胞と非癌細胞の交差汚染を避けるために、EZ Cut LMM System(SL Microtest GmbH)を製造元のプロトコールにいくつかの修正を加えて用いることによって、これら2つの集団を調製した。貯蔵工程および組織採取の間の影響を最小化するために、癌組織を同じ手順によって慎重に取り扱った。RNAの質を調べるために、各症例の残りの組織から抽出した全RNAを変性アガロースゲル中で電気泳動し、リボソームRNAバンドの存在によってそれらの質を確認した。
ヒト乳癌細胞株HBC4、HBC5、MDA-MB-231、BSY-1は、Yamori博士(財団法人癌研究会(The Japanese Foundation of Cancer Research)、東京)より寄贈いただき、MCF7、T47D、SKBR3、HCC1937、MDA-MB-435S、YMB1、HBL100、COS7、NIH3T3はATCCから入手した。細胞はすべて適切な培地中で培養した;すなわち、RPMI-1640(Sigma、St. Louis、MO)をHBC4、HBC5、SKBR3、T47D、YMB1、およびHCC1937(2mM L-グルタミンを添加)に対して用い;ダルベッコ変法イーグル培地(Invitrogen、Carlsbad、CA)をHBL100、COS7、NIH3T3に対して用い;0.1mM必須アミノ酸(Roche)、1mMピルビン酸ナトリウム(Roche)、0.01mg/mlインスリン(Sigma)を加えたEMEM(Sigma)をMCF7に対して用い;L-15(Roche)をMDA-MB-231およびMDA-MB-435Sに対して用いた。それぞれの培地には、10%ウシ胎仔血清(Cansera)および1%抗生物質/抗真菌物質溶液(Sigma)を補充した。MDA-MB-231細胞およびMDA-MB-435S細胞は、CO2を含まない加湿空気雰囲気中で37℃に保った。他の細胞株は、5% CO2を含む加湿空気雰囲気中で37℃に保った。
レーザーで捕捉した細胞の各集団から、全RNAを350μlのRLT可溶化バッファー(QIAGEN)中に抽出した。抽出したRNAを、30単位のDNase I(QIAGEN)により室温で30分間処理した。70℃において10分間失活させた後に、製造元の推奨に従ってRNeasy Mini Kit(QIAGEN)を用い、RNAを精製した。DNase Iで処理したRNAすべてを、Ampliscribe T7転写キット(Epicentre Technologies)を用いた、T7に基づく増幅に供した。2回の増幅により、各試料に関して28.8〜329.4μgの増幅RNA(aRNA)が得られ、一方、15例の閉経前患者または12例の閉経後患者からの正常試料からのRNAを増幅した場合には、それぞれ合計2240.2μgおよび2023.8μgが得られた。それぞれの癌性乳管細胞および非癌性乳管細胞からのaRNAの2.5μgアリコートを、それぞれCy5-dCTPおよびCy3-dCTP(Amersham Biosciences)の存在下で逆転写させた。
National Center for Biotechnology Information(NCBI)のUniGeneデータベース(ビルド番号131)から選択した23,040種のcDNAを含む「ゲノムワイド」cDNAマイクロアレイシステムを確立した。cDNAマイクロアレイスライドの製作については別稿に記載されている(Ono K, Tanaka T, Tsunoda T, Kitahara O, Kihara C, Okamoto A, Ochiai K, Katagiri T and Nakamura Y.「Identification by cDNA Microarray of Genes Involved in Ovarian Carcinogenesis.」Cancer Res., 60, 5007-11, 2000)。手短に述べると、種々のヒト臓器から単離したポリ(A)+RNAを鋳型として用いる逆転写PCRによってcDNAを増幅した;アンプリコンの長さは反復配列またはポリ(A)配列を含まずに200〜1100bpの範囲とした。Lucidea Array Spotter(Amersham Biosciences)を用いて、PCR産物を7型スライドガラス(Amersham Bioscience)上に2箇所ずつスポットした;4,608種または9,216種の遺伝子を単一のスライド上に2箇所ずつスポットした。それぞれ同じ52種類のハウスキーピング遺伝子および2種類の陰性対照遺伝子もスポットした、3種類の異なるスライドのセット(合計23,040種の遺伝子)を調製した。
ハイブリダイゼーションおよび洗浄は、すべての工程をAutomated Slide Processor(Amersham Biosciences)により行った点を除き、以前に記載されたプロトコールに従って行った(Giuliani, N. et al., V.「Human myeloma cells stimulate the receptor activator of nuclear factor-kappa B ligand (RANKL) in T lymphocytes:a potential role in multiple myeloma bone disease.」Blood, 100:4615-4621, 2002)。各ハイブリダイゼーションシグナルの強度を、ArrayVisionコンピュータプログラム(Amersham Biosciences)により測定光度を算出し、バックグラウンド強度を差し引いた。52種のハウスキーピング遺伝子からの平均化シグナルを用いて、意味のあるCy5/Cy3比が得られるように、各標的スポットに対するCy5(腫瘍)およびCy3(対照)の蛍光強度を調整した。低いシグナル強度に由来するデータは信頼性が低いため、各スライド上のカットオフ値を以前の記載のように決定し(Ono K. et al.,「Identification by cDNA microarray of genes involved in ovarian carcinogenesis.」Cancer Res., 60, 5007-11, 2000)、Cy3色素およびCy5色素の両方でカットオフ値よりも低いシグナル強度が得られた場合には、その遺伝子を以降の分析から除外した(Saito-Hisaminato, A., Katagiri, T., Kakiuchi, S., Nakamura, T., Tsunoda, T. and Nakamura, Y.「Genome-wide profiling of gene expression in 29 normal human tissues with a cDNA microarray.」DNA Res, 9:35-45, 2002)。他の遺伝子に関しては、各試料の生データを用いてCy5/Cy3比を算出した。
全RNAの抽出および増幅を上記の通りに行った。乳癌細胞および正常乳管細胞から増幅されたRNAのアリコートを、それぞれCy5-dCTPおよびCy3-dCTP(Amersham Biosciences、Buckinghamshire、UK)を用いる逆転写によって標識した。ハイブリダイゼーション、洗浄、および検出は上記の通りに行った。乳癌において通例的に上方制御される遺伝子を検出するために、マイクロアレイ上の23,040種の遺伝子の全体的な発現パターンをスクリーニングし、i)81例の乳癌症例すべて、ii)69例の浸潤性乳管癌、iii)31例の高分化型病変、iv)14例の中程度分化型病変、またはv)24例の低分化型病変のそれぞれに50%を上回って存在する、発現比が3.0を上回る遺伝子を選択した。腫瘍細胞で上方制御されるように思われた合計102種の遺伝子のうち、以下の施設内識別番号、A5657、B9769、およびC7965を有する3つを、情報的価値のある乳癌症例の50%超において発現比が3.0を上回っていたことから、さらなる検討のために選択した。
上述した上方制御される3つの遺伝子、A5657、B9769、およびC7965を選択し、半定量的RT-PCR実験を適用することによってそれらの発現レベルを試験した。詳細には、上記の通りに全RNAを抽出し、増幅した上で逆転写した。定量的内部対照としてグリセルアルデヒド-3-リン酸デヒドロゲナーゼ(GAPDH)をモニターすることにより、その後のPCR増幅のための各一本鎖cDNAの適切な希釈物を調製した。PCRプライマー配列は以下である。
GAPDHに対して
5'-CGACCACTTTGTCAAGCTCA-3'(SEQ ID NO:7)および
5'-GGTTGAGCACAGGGTACTTTATT-3'(SEQ ID NO:8);
A5657に対して
5'-CAAATATTAGGTGGAGCCAACAC-3'(SEQ ID NO:9)および
5'-TAGATCACCTTGGCAAAGAACAC-3'(SEQ ID NO:10);
B9769に対して
5'-ACCTCAAGTCCCTCCTGGAA-3'(SEQ ID NO:11)および
5'-TCAGTTTCAACAGGTAAGGCGAT-3'(SEQ ID NO:12);
C7965に対して
5'-AGAGCCATAGAAACTGCTCCTCT-3'(SEQ ID NO:13)および
5'-CATAACTGCATAGACAGCACGTC-3'(SEQ ID NO:14)。
すべての乳癌細胞株から、RNeasyキット(QIAGEN)を製造元の使用説明書に従って用いて全RNAを抽出した。DNase I(ニッポンジーン、大阪、日本)で処理した後に、mRNA精製キット(Amersham Biosciences)を製造元の使用説明書に従って用いてmRNAを単離した。各mRNAの1μgアリコートを、正常成人の乳房(Biochain)、肺、心臓、肝臓、腎臓、骨髄(BD, Clontech, Palo Alto, CA)から単離したポリA(+)RNAとともに1%変性アガロースゲル上で分離し、かつナイロン膜に転写した(乳癌ノーザンブロット)。乳癌ノーザンブロットおよびヒト多組織ノーザンブロット(Clontech, Palo Alto, CA)を、RT-PCRによって調製したA5657、B9769、およびC7965の[α32P]-dCTP標識PCR産物とハイブリダイズさせた(下記参照)。プレハイブリダイゼーション、ハイブリダイゼーション、および洗浄は供給元の推奨に従って行った。ブロットのオートラジオグラフィーは増感スクリーンを用いて-80℃で14日間行った。A5657(541bp)、B9769(499bp)、およびC7965(238bp)に対する特異的プローブは、半定量的RT-PCRの項に述べたプライマーセットを用いてPCRにより調製した。
A5657に対して
5'-CAAATATTAGGTGGAGCCAACAC-3'(SEQ ID NO:9)および
5'-TAGATCACCTTGGCAAAGAACAC-3'(SEQ ID NO:10);
B9769に対して
5'-ACCTCAAGTCCCTCCTGGAA-3'(SEQ ID NO:11)および
5'-TCAGTTTCAACAGGTAAGGCGAT-3'(SEQ ID NO:12);
C7965に対して
5'-GGGAAGAGAAGTCCCGAGTC-3'(SEQ ID NO:15)および
5'-TCCTTATTCTGAATTTCCAGAATC-3'(SEQ ID NO:16)。
C7965転写物の完全長を検出するために、Marathon cDNA増幅キット(BD, CLONTECH)を製造元の使用説明書に従って用いて5'RACEを行った。逆方向プライマー(5'-CAAGCAGTCCTACCAGGGTTCGGAAGCTGA-3')(SEQ ID NO:17)を用い、乳癌細胞株MCF7から調製したcDNAを鋳型として用いて1回目のPCRを行ったところ、多数の産物バンドが検出された。1回目の5'RACE-PCRは以下の条件下で行った:最初の変性を94℃で1分間;94℃で30秒間、68℃で2分間を35サイクル;その後に最終伸長を68℃で7分間。1回目のPCR産物を希釈した後に、ネステッドリバースプライマー(5'-CCAGGGTTCGGAAGCTGAGAGGAGCAGTTT-3')(SEQ ID NO:18)を用いたNested PCRにより、強い産物バンドが検出された。Nested-PCRは以下の条件下で行った:最初の変性を94℃で1分間;94℃で30秒間、72℃で2分間を2サイクル、および94℃で30秒間、70℃で2分間を2サイクル、94℃で30秒間、68℃で2分間を15サイクル;その後に最終伸長を68℃で7分間。配列は、Gel抽出キット(Qiagen)およびTOPO TAクローニングキット(Invitrogen)を製造元の使用説明書に従って用いて同定した。
A5657 cDNA、B9769 cDNA、およびC7965 cDNAの全コード配列を、以下のプライマーとともにKOD-Plus DNAポリメラーゼ(東洋紡、大阪、日本)を用いてPCRにより増幅した。
A5657フォワードプライマー;5'-CCGGAATTCATGCAGAGAGCTTCACGTCTG-3'(SEQ ID NO:19)および
A5657リバースプライマー;5'-CCGCTCGAGAACATCAGGATGAAATTTCTTTTC-3'(SEQ ID NO:20)、
B9769フォワードプライマー;5'-CCGGAATTCATGAGCGGTGCGGGGGTGGCG-3'(SEQ ID NO:21)および
B9769リバースプライマー;5'-CCGCTCGAGAAGCACTGAGCGATGCAGGCG-3'(SEQ ID NO:22)、ならびに
C7965フォワードプライマー;5'-CCGGAATTCATGGACGCAGAGCTGGCAGAGGTGCG-3'(SEQ ID NO:23)および
C7965リバースプライマー;5'-CCGCTCGAGGTTGTTCTCCTCTGCACAAAG-3' (SEQ ID NO:24)。
これらのPCR産物を、それぞれpCAGGS-3xFLAGnおよびpCAGGSnHA、pcDNA3.1(+)-Myc/His(Invitrogen)発現ベクター中のEcoRI部位およびXhoI部位に挿入した。ユビキチン結合アッセイに関しては、HA-ユビキチン発現ベクター(pcdef3-HA-RPS27A)を、Kohei Miyazono博士(財団法人癌研究会癌研究所(The Cancer Institute of Japanese Foundation for Cancer Research))から寄贈いただいた。これらの構築物(pCAGGS-A5657-HA、pcDNA3.1-A5657-Myc/His、pCAGGS-3xFLAG-A5657、およびpcdef3-HA-RPS27A(Ub80a))をDNAシークエンシングによって確認した。細胞増殖促進アッセイに関して、変異型H-ras(G12K)の全コード配列はMotoko Unoki博士によって構築された。
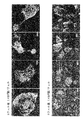
A5657、B9769、およびC7965タンパク質の細胞内局在を調べるために、A5657およびB9769に関してT47D細胞を5×104個/ウェルで播くとともに、B9769およびC7965に関してCOS7細胞を1×104(低密度)および1×105(高密度)で播いた。24時間後に、FuGENE 6トランスフェクション試薬(Roche)を製造元の使用説明書に従って用いて、T47D細胞に対してそれぞれ1μgのpCAGGS-A5657-HAを細胞に一過性にトランスフェクトした。続いて、細胞を4%パラホルムアルデヒドを含むPBSにより15分間固定し、0.1%Triton X-100を含むPBSを4℃で2.5分間用いて透過化処理した。引き続いて、非特異的なハイブリダイゼーションをブロックするために、細胞を3%BSAを含むPBSにより4℃で12時間覆った。次に、A5657-HAをトランスフェクトしたT47D細胞を、1:1000希釈したマウス抗HA抗体(SANTA CRUZ)または1:1000希釈したマウス抗myc抗体(Sigma)のそれぞれとインキュベートした。PBSで洗浄した後に、両方のトランスフェクト細胞を、1:5000希釈したAlexa594結合抗マウス二次抗体(Molecular Probe)によって染色した。さらに、B9769タンパク質と他の細胞骨格タンパク質との間で細胞内局在を比較した。1μgのpcDNA3.1(+)-B9769-myc-hisによるトランスフェクション後に、細胞を、1:1000希釈したウサギ抗myc抗体(SANTACRUZ)または1:500希釈したマウス抗βチューブリン抗体(SIGMA)とともにインキュベートした。PBSで洗浄した後に、トランスフェクトしたT47D細胞を、1:5000希釈したAlexa488結合抗ウサギ二次抗体(Molecular Probe)、Alexa594結合抗マウス二次抗体(Molecular Probe)、1:50希釈したAlexa594結合ファロイジンによって染色した。さらに、低密度または高密度の細胞におけるB9769の細胞内局在を調べるために、COS7細胞に対して1μgのpCAGGSn3F-B9769-HAをトランスフェクトし、上記と同じ手順を用いて免疫細胞化学染色を行った。トランスフェクトした細胞を、1:1000希釈したマウス抗HA抗体(SANTACRUZ)とともにインキュベートした。PBSで洗浄した後に、COS7細胞を、1:5000希釈したAlexa594結合抗マウス二次抗体(Molecular Probe)によって染色した。核は4',6'-ジアミジン-2'-フェニルインドール二塩酸(DAPI)で対比染色した。さらに、低密度または高密度の細胞におけるC7965の細胞内局在を調べるために、COS7細胞に対して1μgのpcDNA3.1(+)-C7965-Myc/Hisをトランスフェクトし、上記と同じ手順を用いて免疫細胞化学染色を行った。トランスフェクトした細胞を、1:1000希釈したマウス抗myc抗体(SANTACRUZ)とともにインキュベートした。PBSで洗浄した後に、COS7細胞を、1:5000希釈したAlexa594結合抗マウス二次抗体(Molecular Probe)によって染色した。核は4',6'-ジアミジン-2'-フェニルインドール二塩酸(DAPI)で対比染色した。蛍光画像はTCS SP2AOBS顕微鏡(Leica、東京、日本)を用いて取得した。
ベクターに基づくRNAiシステムを、文献に記載されているpsiU6BX siRNA発現ベクターを用いて確立した(Shimokawa T., Furukawa Y., Sakai M., Li M., Miwa N., Lin Y. M. Nakamura Y.「Involvement of the FGF18 Gene in Colorectal Carcinogenesis, as a Novel Downstream Target of the β-Catenin/T-Cell Factor Complex63.」Cancer Res., 63, 6116-20, 2003)。A5657(psiU6BX-A5657)、B9769(psiU6BX-B9769)およびC7965(psiU6BX-C7965)に対するsiRNA発現ベクターは、psiU6BXベクターのBbsI部位への二本鎖オリゴヌクレオチドのクローニングによって調製した。対照プラスミドpsiU6BX-EGFPは、二本鎖オリゴヌクレオチド、5'-CACCGAAGCAGCACGACTTCTTCTTCAAGAGAGAAGAAGTCGTGCTGCTTC-3'(SEQ ID NO:25)および5'-AAAAGAAGCAGCACGACTTCTTCTCTCTTGAAGAAGAAGTCGTGCTGCTTC-3'(SEQ ID NO:26)を、psiU6BX3.0ベクターのBbsI部位にクローニングすることによって調製した。
ヒト乳癌細胞株T47Dを10cm培養皿(1×106個/枚)にプレーティングし、FuGENE6試薬を供給元の推奨(Roche)に従って用いて、psiU6BX-EGFP(陰性対照として)、psiU6BX-A5657、psiU6BX-B9769およびpsiU6BX-C7965をトランスフェクトした。トランスフェクションから7日目の時点で細胞から全RNAを抽出し、上記のようにA5657、B9769、およびC7965ならびにGAPDHに対して特異的なプライマーを用いて半定量的RT-PCRによりsiRNAのノックダウン作用を確認した。さらに、T47D細胞株を用いたsiRNAを発現するトランスフェクタントを、0.7mg/mlネオマイシンを含む選択培地中で28日間増殖させた。4%パラホルムアルデヒドで固定した後に、コロニー形成を評価するためにトランスフェクト細胞をギムザ液で染色した。細胞の生存度の定量のためにMTTアッセイを行った。ネオマイシンを含む培地中で7日間培養した後に、MTT溶液(臭化3-(4,5-ジメチルチアゾール-2-イル)-2,5-ジフェニルテトラゾリウム)(Sigma)を濃度0.5mg/mlで添加した。37℃で2.5時間インキュベートした後に、酸-SDS(0.01N HCl/10% SDS)を添加した;紺青色の結晶を溶解するためにこの懸濁液を激しく混合し、37℃で一晩インキュベートした。570nmでの吸光度をMicroplate Reader 550(BioRad)を用いて測定した。
NIH3T3細胞を150mm培養皿当たり3×106個で播いた。24時間後に、16μgのpcDNA3.1(+)-Myc/His(Invitrogen)を陰性対照として、pcDNA3.1(+)-A5657-Myc/His、pcDNA3.1(+)-B9769-Myc/His、pcDNA3.1(+)-C7965-Myc/HisまたはpcDNA3.1(+)-H-Ras-変異型-Myc/Hisを陽性対照として、それぞれFuGENE 6(Roche)を用いてNIH3T3細胞に一過性にトランスフェクトした。次に、トランスフェクションから24時間後にNIH3T3細胞を1ウェル当たり2×104個で再び播いた。MTTアッセイは再播種から1日、2日、4日、および6日後に以前の記載の通りに行った。
COS7細胞を1ウェル当たり5×105個で播いた。24時間後に、1μgのFLAG標識A5657および0.1μgのHA標識ユビキチン発現ベクター(Ub80a-HA)による同時トランスフェクションを、FuGENE6(Roche)を用いてCOS7細胞に行った。HA標識ユビキチン発現ベクターは、ImamuraらおよびEbisawaらに従って構築した(Imamura et al., Nature 389/6651, 622-6, 1997 「Smad6 inhibits signalling by the TGF-beta super family.」;Ebisawa et al., J Biol Chem. 20:276/16, 12477-80, 2001 「Smurf1 interacts with transforming growth factor-beta type I receptor through Smad7 and induces receptor degradation.」)。トランスフェクションから24時間後に細胞に5μMプロテアソーム阻害剤MG132または5μM DMSOを添加し、その6時間後に細胞を1.0%NP40バッファー(1.0% NP40、50mM Tris-HCl(pH 8.0)、150mM NaClおよび完全プロテアーゼ阻害剤カクテル)1ml中で溶解させた。この細胞溶解液を、マウスモノクローナル抗FLAG-M2抗体またはマウス抗HA抗体を結合させたアガロースによって免疫沈降させた。可溶化バッファーによる洗浄を6回行った後に、結合性タンパク質をFlag-M2またはHAペプチド(SIGMA)によって溶出させた。免疫沈降物を、ウサギ抗HAポリクローナル抗体またはウサギ抗Flagポリクローナル抗体を用いてウエスタンブロットにて分析した。試料バッファー中の可溶性タンパク質を12%SDS-ポリアクリルアミドゲルにローディングし、ニトロセルロース膜(Hybond ECLO)に転写した。0.05% Tween 20を含むTris緩衝生理食塩水(TBST)にBlockAce粉末(雪印、東京、日本)を溶解させたものによって膜をブロックし、各抗体とともに室温で1時間インキュベートした。続いてブロットをHRP結合二次抗体(Amersharm Biosciences)とハイブリダイズさせ、ECL法(Amersham Biosciences)を用いて検出した。
乳癌細胞で上方制御される遺伝子としてのA5657、B9769、およびC7965の同定
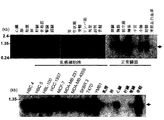
81例の乳癌患者からの癌細胞の遺伝子発現プロファイルを、23,040種のヒト遺伝子を提示したcDNAマイクロアレイを用いて解析したところ、乳癌細胞で通例的に上方制御されている102種の遺伝子が同定された。これらの上方制御される遺伝子の中から、ユビキチン結合酵素(Genbankアクセッション番号NM_014176)に類似したHSPC150タンパク質を指定する施設内コードA5657の遺伝子(SEQ ID NO:1)、仮説上のタンパク質BC016861(Genbankアクセッション番号NM_138770)を指定するB9769の遺伝子(SEQ ID NO:3)、および、ESTに対応するC7965の遺伝子(SEQ ID NO:5)を選択した。マイクロアレイ上での遺伝子A5657、B9769、およびC7965の発現は、正常乳管細胞と比較して、乳癌細胞のそれぞれ49例中38例、73例中30例、および49例中28例で有意に亢進していた。本発明者らが焦点としたこれらの上方制御される遺伝子の発現を確かめるために、乳癌細胞と正常ヒト組織(正常乳房細胞を含む)との間でのそれらの発現を比較するための半定量的RT-PCR分析を行った。第1に、A5657は、12例の臨床的な乳癌試料中9例(低分化型)で、正常乳管細胞および他のいくつかの正常組織と比較して発現の亢進が認められ、6種類の乳癌細胞株のすべてにおいても同様に過剰発現されることが見いだされた(図1a)。次に、B9769は、12例の臨床的な乳癌試料中6例(低分化型)で正常乳管細胞と比較して発現の亢進が認められ、20種類の乳癌細胞株中4種類で過剰発現されることが見いだされた(図1b)。最後に、C7965は、12例の臨床的な乳癌試料中7例(高分化型)で正常乳管細胞と比較して発現の亢進が認められ、20種類の乳癌細胞株中15種類で過剰発現されることが判明した(図1c)。
A5657、B9769、およびC7965の全cDNA配列を得るために、乳癌細胞株およびT47Dから調製したcDNAを鋳型として用い、RT-PCRを行った。A5657は、ユビキチン結合酵素に類似したHSPC150タンパク質を指定する7つのエクソンからなり、ゲノム中では染色体1q32.1上に約10.3kbの範囲にわたって存在する。A5657の完全長cDNA配列は928ヌクレオチドを含んでいた。オープンリーディングフレーム(ORF)はエクソン2で始まり、エクソン7で終わる。最終的に、この転写物は197アミノ酸をコードする。
A5657、B9769、およびC7965の特性をさらに検討するために、これらの遺伝子産物の細胞内局在を哺乳動物細胞で調べた。まず、本発明者らが、A5657タンパク質を発現するプラスミド(pCAGGS-A5657-HA)をT47D細胞に一過性にトランスフェクトした場合には、免疫細胞化学染色により、トランスフェクトしたT47D細胞全体のうち約80%では外因性A5657が細胞質中に局在し、細胞の残りの約20%では核に局在することが判明した(図3a)。
A5657、B9769、およびC7965の増殖促進上の役割を評価するために、A5657、B9769、およびC7965の過剰発現が示されている乳癌細胞株T47Dにおける内因性A5657、B9769、およびC7965の発現を、哺乳動物ベクターに基づくRNA干渉(RNAi)法(材料および方法の項を参照)によってノックダウンした(図4、5、および6)。A5657、B9769、およびC7965の発現レベルを半定量的RT-PCR実験によって調べた。図4、5、および6に示されているように、A5657(si2およびsi3)、B9769(si1およびsi2、si4)およびC7965(si1およびsi3)に対して特異的なsiRNAは、各遺伝子の発現を対照siRNA構築物(psiU6BX-EGFP)と比較して有意に抑制した。A5657、B9769、およびC7965に対して特異的なsiRNAによる細胞増殖阻害を確認するために、コロニー形成アッセイおよびMTTアッセイをそれぞれ行った。その結果、A5657(si2およびsi3)(図4b、c)、B9769(si1、およびsi2、si4)(図5b、c)およびC7965(si1およびsi3)(図6b、c)の構築物導入によってT47D細胞の増殖は抑制され、これは発現低下に関する上記の結果に一致した。それぞれの結果は3回の独立した実験によって確認された。このため、これらの所見は、A5657、B9769、およびC7965が乳癌の細胞増殖において重要な機能を有することを示唆している。
細胞増殖調節におけるA5657、B9769、およびC7965の役割についてさらに検討するために、A5657、B9769、C7965、H-ras変異体(陽性対照として)または擬似物(Mock)(陰性対照として)を発現するプラスミドのそれぞれをNIH3T3細胞に一過性にトランスフェクトし、その後にMTTアッセイを行った(図7)。トランスフェクションから6日後に、A5657(図7a)、B9769(図7b)、およびC7965(図7c)の過剰発現ならびにH-ras変異体の過剰発現は、対照プラスミド(擬似ベクター)をトランスフェクトしたNIH3T3細胞と比較して細胞増殖の有意な増大(3倍を上回る)をもたらし、このことから、A5657、B9769、およびC7965が細胞増殖に役割を果たす可能性が示唆された。これらの結果は2回の独立した実験によって確認された。
A5657の機能をさらに詳細に探るために、A5657を発現するプラスミドをトランスフェクトしたCOS7細胞からの全細胞溶解液を用いるウエスタンブロット分析を行った。その結果、予想される分子量を示すバンドに加えて、より移動性の遅いバンドが1本のみ余剰に観察され(図8;左図、全細胞溶解液中)、翻訳後修飾によって生じた可能性が示唆された。SMARTプログラムにより、A5657によってコードされる197アミノ酸がUBCcドメイン(ユビキチン結合酵素E2、触媒ドメイン相同体)(5〜152残基)を含むことが予想され、このことからA5657がE2ユビキチン酵素活性を有する可能性が示唆された。この余剰なバンドがモノユビキチン化によって生じたものか否かを調べるために、FLAG標識A5657およびHA標識ユビキチンを発現するように設計されたプラスミドDNA(それぞれA5657-FLAGおよびUB80a-HA)を、COS7細胞に同時トランスフェクトした。A5657を抗FLAG抗体を用いて免疫沈降させたところ、沈降物は抗HA抗体で検出可能であった。余剰な移動性の遅いバンドが1本観察され、このことからA5657がユビキチンと結合することが示された(図8)。さらに、免疫沈降を抗HA抗体を用いて行い、その後に抗FLAGを用いてウエスタンブロット分析を行ったところ、移動性の遅い余剰なバンドがこの場合も観察された(図8)。プロテアソーム阻害剤MG132による処理はこの結合に影響を及ぼさなかった。この所見は、A5657タンパク質がモノユビキチン化を介したE2ユビキチン酵素活性を有することを強く示唆する。
本明細書では、ゲノムワイドcDNAマイクロアレイを利用した乳癌の正確な発現プロファイルにより、正常ヒト組織と比較して乳癌細胞で有意に過剰発現される新規遺伝子A5657、B9769、およびC7965を単離した。
レーザービームを用いた切除法(laser-capture dissection)とゲノム全体のcDNAマイクロアレイとの組み合わせによって得られた、本明細書に記載の乳癌の遺伝子発現解析によって、癌の予防および治療の標的となる特異的遺伝子が同定された。これらの発現差のある遺伝子サブセットの発現に基づいて、本発明は、乳癌を同定または検出するための分子診断マーカーを提供する。
Claims (32)
- 患者から採取された乳癌細胞を含むことが疑われる組織試料におけるHSPC150タンパク質をコードする遺伝子の発現のレベルを決定する段階を含む、組織試料中の乳癌細胞を検出する方法であって、該試料の発現レベルが該遺伝子の正常対照レベルと比較して上昇していることにより、該組織試料中の乳癌細胞が検出される、方法。
- 試料の発現レベルが正常対照レベルを少なくとも10%上回る、請求項1記載の方法。
- 乳癌がIDCである、請求項1記載の方法。
- 試料の発現レベルが正常対照レベルを少なくとも10%上回る、請求項3記載の方法。
- 複数の乳癌関連遺伝子の発現レベルを決定する段階をさらに含む、請求項1記載の方法。
- 遺伝子発現レベルが、以下からなる群より選択される方法によって決定される、請求項1記載の方法:
(a)HSPC150タンパク質をコードする遺伝子のmRNAの検出、
(b)HSPC150タンパク質の検出、および
(c)HSPC150タンパク質の生物学的活性の検出。 - 検出がDNAアレイ上で行われる、請求項6記載の方法。
- 患者由来の組織試料が乳房組織を含む、請求項1記載の方法。
- 乳房組織が上皮細胞を含む、請求項8記載の方法。
- 患者由来の組織試料が乳癌細胞を含む、請求項1記載の方法。
- 患者由来の組織試料が乳癌細胞からの上皮細胞を含む、請求項1記載の方法。
- 以下の段階を含む、乳癌を治療または予防するための化合物をスクリーニングする方法:
a)被験化合物を、HSPC150タンパク質に接触させる段階;
b)ポリペプチドと被験化合物との結合活性を検出する段階;および
c)ポリペプチドと結合する被験化合物を選択する段階。 - 以下の段階を含む、乳癌を治療または予防するための化合物をスクリーニングする方法:
a)候補化合物を、HSPC150タンパク質をコードする遺伝子を発現する細胞に接触させる段階;および
b)該遺伝子の発現レベルを候補化合物の非存在下で検出される発現レベルと比較して低下させる候補化合物を選択する段階。 - 細胞が乳癌細胞を含む、請求項13記載の方法。
- 以下の段階を含む、乳癌を治療または予防するための化合物をスクリーニングする方法:
a)被験化合物を、HSPC150タンパク質に接触させる段階;
b)段階(a)のHSPC150タンパク質の生物学的活性を検出する段階;および
c)該タンパク質の生物学的活性を被験化合物の非存在下で検出される該タンパク質の生物学的活性と比較して抑制する被験化合物を選択する段階。 - 以下の段階を含む、乳癌を治療または予防するための化合物をスクリーニングする方法:
a)候補化合物を、HSPC150タンパク質をコードする遺伝子の転写調節領域とその転写調節領域の制御下で発現されるレポーター遺伝子とを含むベクターが導入された細胞に接触させる段階;
b)該レポーター遺伝子の発現レベルまたは活性を測定する段階;および
c)該レポーター遺伝子の発現レベルまたは活性を候補化合物の非存在下で検出される発現レベルまたは活性と比較して低下させる候補化合物を選択する段階。 - 乳癌がIDCであり、以下の段階を含む、請求項12記載の方法:
a)被験化合物を、HSPC150タンパク質に接触させる段階;
b)HSPC150タンパク質と被験化合物との結合活性を検出する段階;および
c)HSPC150タンパク質と結合する被験化合物を選択する段階。 - 乳癌がIDCであり、以下の段階を含む、請求項13記載の方法:
a)候補化合物を、HSPC150タンパク質をコードする遺伝子を発現する細胞に接触させる段階;および
b)該遺伝子の発現レベルを候補化合物の非存在下で検出される発現レベルと比較して低下させる候補化合物を選択する段階。 - 細胞がIDC細胞を含む、請求項18記載の方法。
- 乳癌がIDCであり、以下の段階を含む、請求項15記載の方法:
a)被験化合物を、HSPC150タンパク質に接触させる段階;
b)段階(a)のHSPC150タンパク質の生物学的活性を検出する段階;および
c)該タンパク質の生物学的活性を被験化合物の非存在下で検出される該タンパク質の生物学的活性と比較して抑制する被験化合物を選択する段階。 - 乳癌がIDCであり、以下の段階を含む、請求項16記載の方法:
a)候補化合物を、HSPC150タンパク質をコードする遺伝子の転写調節領域とその転写調節領域の制御下で発現されるレポーター遺伝子とを含むベクターが導入された細胞に接触させる段階;
b)該レポーター遺伝子の発現レベルまたは活性を測定する段階;および
c)該レポーター遺伝子の発現レベルまたは活性を候補化合物の非存在下で検出される発現レベルまたは活性と比較して低下させる候補化合物を選択する段階。 - HSPC150タンパク質をコードする遺伝子に特異的に結合する核酸またはHSPC150タンパク質と特異的に結合する抗体を含む乳癌の検出用キット。
- HSPC150タンパク質をコードする遺伝子のコード配列に対して相補的なヌクレオチド配列を含む、HSPC150タンパク質をコードする遺伝子を発現する乳癌細胞の増殖抑制に用いるためのアンチセンス組成物。
- HSPC150タンパク質をコードする遺伝子の発現を低下させるsiRNAを含む、HSPC150タンパク質をコードする遺伝子を発現する乳癌細胞の増殖抑制に用いるための組成物。
- siRNAの標的配列が、SEQ ID NO:28および29のヌクレオチド配列からなる群より選択されるヌクレオチド配列からなる請求項24記載の組成物。
- 乳癌がIDCである請求項23記載の組成物。
- 乳癌がIDCである、請求項24記載の組成物。
- siRNAの標的配列が、SEQ ID NO:28または29のヌクレオチド配列からなる、請求項27記載の組成物。
- HSPC150タンパク質をコードする遺伝子に対するアンチセンスポリヌクレオチドまたは低分子干渉RNAの薬学的有効量を含む、HSPC150タンパク質をコードする遺伝子を発現する乳癌を治療するための組成物。
- siRNAの標的配列が、SEQ ID NO:28および29のヌクレオチド配列からなる群より選択されるヌクレオチド配列からなる、請求項29記載の組成物。
- 乳癌がIDCである、請求項29記載の組成物。
- siRNAの標的配列が、SEQ ID NO:28または29のヌクレオチド配列からなる、請求項31記載の組成物。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US50557103P | 2003-09-24 | 2003-09-24 | |
| PCT/JP2004/011741 WO2005029067A2 (en) | 2003-09-24 | 2004-08-10 | Method of diagnosing breast cancer |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2007506424A JP2007506424A (ja) | 2007-03-22 |
| JP4579246B2 true JP4579246B2 (ja) | 2010-11-10 |
Family
ID=34375580
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006527766A Expired - Fee Related JP4579246B2 (ja) | 2003-09-24 | 2004-08-10 | 乳癌を診断する方法 |
| JP2006527773A Expired - Fee Related JP4620670B2 (ja) | 2003-09-24 | 2004-09-24 | 乳癌を診断する方法 |
| JP2007237927A Withdrawn JP2008092949A (ja) | 2003-09-24 | 2007-09-13 | 乳癌を診断する方法 |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006527773A Expired - Fee Related JP4620670B2 (ja) | 2003-09-24 | 2004-09-24 | 乳癌を診断する方法 |
| JP2007237927A Withdrawn JP2008092949A (ja) | 2003-09-24 | 2007-09-13 | 乳癌を診断する方法 |
Country Status (9)
| Country | Link |
|---|---|
| US (3) | US7531300B2 (ja) |
| EP (2) | EP1668354A2 (ja) |
| JP (3) | JP4579246B2 (ja) |
| CN (2) | CN1898563B (ja) |
| AT (1) | ATE508202T1 (ja) |
| DE (1) | DE602004032556D1 (ja) |
| ES (1) | ES2365732T3 (ja) |
| TW (2) | TW200512298A (ja) |
| WO (2) | WO2005029067A2 (ja) |
Families Citing this family (89)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2005054510A2 (en) * | 2003-12-05 | 2005-06-16 | Erasmus Mc | Predicting response and outcome of metastatic breast cancer anti-estrogen therapy |
| FR2875512B1 (fr) * | 2004-09-17 | 2011-02-04 | Diagnogene S A | Biopuce de diagnostic du caractere metastatique ou localise d'une tumeur mammaire, procede et kit d'utilisation |
| EP1854473A1 (en) * | 2005-03-03 | 2007-11-14 | Takeda Pharmaceutical Company Limited | Preventive/therapeutic agent for cancer |
| JP4746048B2 (ja) * | 2005-03-11 | 2011-08-10 | オンコセラピー・サイエンス株式会社 | 抗gfra1抗体のエフェクター機能を用いて細胞を障害する方法 |
| CN101273145A (zh) * | 2005-07-28 | 2008-09-24 | 肿瘤疗法科学股份有限公司 | 癌症相关基因rasgef1a |
| WO2007013670A2 (en) | 2005-07-29 | 2007-02-01 | Oncotherapy Science, Inc. | Gene galnt6 as breast cancer marker and small interfering rnas directed against gene galnt6 |
| JP2007037421A (ja) * | 2005-08-01 | 2007-02-15 | Osaka Univ | 大腸癌リンパ節転移の有無を予測するための遺伝子セット |
| US7662580B2 (en) | 2005-11-10 | 2010-02-16 | Aurelium Biopharma Inc. | Tissue diagnostics for breast cancer |
| WO2007061770A2 (en) * | 2005-11-17 | 2007-05-31 | University Of Maryland | Method and system for analysis of time-series molecular quantities |
| CA2641410A1 (en) * | 2006-02-03 | 2007-08-09 | Messengerscape Co., Ltd. | Genes for prognosis of cancer |
| US8138167B2 (en) | 2006-02-10 | 2012-03-20 | Oncotherapy Science, Inc. | Methods for treating lung cancers |
| US20080108065A1 (en) * | 2006-04-28 | 2008-05-08 | Indra Poola | Systems and diagnostic methods for breast cancer using mmp-1 markers |
| CA2660438A1 (en) | 2006-08-10 | 2008-02-14 | Oncotherapy Science, Inc. | Genes and polypeptides relating to breast cancers |
| WO2008037700A2 (en) * | 2006-09-27 | 2008-04-03 | Siemens Healthcare Diagnostics Gmbh | Methods for breast cancer prognosis |
| WO2008093427A1 (ja) * | 2007-02-01 | 2008-08-07 | Oriental Yeast Co., Ltd. | 乳癌細胞の検出方法 |
| EP2118663B1 (en) * | 2007-02-15 | 2014-04-02 | Universita' Degli Studi di Torino | Regulation of expression of pi3kb protein in tumors |
| TW200908998A (en) * | 2007-06-27 | 2009-03-01 | Oncotherapy Science Inc | Compositions and methods of treating cancer |
| MX2010002001A (es) | 2007-08-20 | 2010-03-11 | Oncotherapy Science Inc | Peptido cdca1 y agente farmaceutico que comprende elmismo. |
| JP5555952B2 (ja) * | 2007-08-20 | 2014-07-23 | オンコセラピー・サイエンス株式会社 | Foxm1ペプチドおよびこれを含む薬剤 |
| GB2467467C (en) * | 2007-10-04 | 2013-03-20 | A Star Agency For Science Technology And Res | TAZ/WWTR1 for diagnosis and treatment of cancer |
| WO2009064933A2 (en) * | 2007-11-13 | 2009-05-22 | Ikonisys, Inc. | Detection of circulating tumor cells in peripheral blood with an automated scanning fluorescence microscope |
| US9195796B2 (en) * | 2008-01-11 | 2015-11-24 | H. Lee Moffitt Cancer Center And Research Institute, Inc. | Malignancy-risk signature from histologically normal breast tissue |
| WO2009116860A1 (en) * | 2008-03-17 | 2009-09-24 | Vereniging Het Nederlands Kanker Instituut | Markers providing prognosis of metastasis among cancer patients |
| TWI526219B (zh) | 2008-06-19 | 2016-03-21 | 腫瘤療法 科學股份有限公司 | Cdca1抗原決定位胜肽及含此胜肽的疫苗 |
| TW201008574A (en) | 2008-08-19 | 2010-03-01 | Oncotherapy Science Inc | INHBB epitope peptides and vaccines containing the same |
| US20100055705A1 (en) * | 2008-08-29 | 2010-03-04 | Wilson Gerald M | Compositions and methods for diagnosing and treating cancer |
| TWI469791B (zh) | 2009-02-18 | 2015-01-21 | Oncotherapy Science Inc | Foxm1胜肽以及含此胜肽之疫苗 |
| KR101174369B1 (ko) | 2009-05-01 | 2012-08-16 | 한국생명공학연구원 | 유방암 진단용 바이오마커 및 유방암 진단제 |
| WO2010138826A1 (en) * | 2009-05-29 | 2010-12-02 | University Of Utah Research Foundation | Methods and compositions related to cellular assays |
| US20110217701A1 (en) * | 2010-03-03 | 2011-09-08 | Carter Scott L | Prognostic Marker for Endometrial Carcinoma |
| RU2012148125A (ru) * | 2010-04-13 | 2014-05-20 | Дзе Трастиз Оф Коламбия Юниверсити Ин Дзе Сити Оф Нью Йорк | Биомаркеры на основе мультиракового ассоциированного с инвазией механизма |
| EP2426216A1 (en) * | 2010-09-01 | 2012-03-07 | Institut Gustave Roussy (IGR) | Prognostic and/or predictive biomarkers and biological applications thereof |
| DK3091085T3 (da) | 2010-10-06 | 2019-05-06 | Inst Catalana Recerca Estudis Avancats | Fremgangsmåde til at designe en terapi mod brystcancermetastase |
| US9139881B2 (en) | 2010-10-26 | 2015-09-22 | Yamaguchi University | Method for assessing breast cancer susceptibility |
| WO2012066093A1 (en) * | 2010-11-19 | 2012-05-24 | Santaris Pharma A/S | Compounds for the modulation of pdz-binding kinase (pbk) expression |
| CA2823334A1 (en) * | 2010-12-29 | 2012-07-05 | Expression Pathology, Inc. | Protein biomarkers of recurrent breast cancer |
| CN102312002A (zh) * | 2011-09-20 | 2012-01-11 | 李艳 | 一种快速检测BRCA1基因mRNA表达量的试剂盒 |
| EP2771464B1 (en) | 2011-10-27 | 2018-03-21 | Yeda Research and Development Co. Ltd. | Methods of treating cancer |
| CN104066746B (zh) * | 2011-10-28 | 2017-12-05 | 肿瘤疗法科学股份有限公司 | Topk肽及包含它们的疫苗 |
| EP2650682A1 (en) | 2012-04-09 | 2013-10-16 | Fundació Privada Institut de Recerca Biomèdica | Method for the prognosis and treatment of cancer metastasis |
| RU2619739C2 (ru) * | 2012-05-30 | 2017-05-17 | Федеральное государственное бюджетное учреждение "Российский научный центр рентгенорадиологии" Министерства здравоохранения российской федерации (ФГБУ "РНЦРР" Минздрава России) | Способ диагностики и прогноза при гиперпролиферативных заболеваниях молочной железы |
| JP6255593B2 (ja) | 2012-07-10 | 2018-01-10 | オンコセラピー・サイエンス株式会社 | Th1細胞のCDCA1エピトープペプチドおよびこれを含有するワクチン |
| RU2663350C2 (ru) | 2012-09-11 | 2018-08-03 | Онкотерапи Сайенс, Инк. | Пептиды ube2t и содержащие их вакцины |
| US11306360B2 (en) * | 2012-12-26 | 2022-04-19 | Koninklijke Philips N.V. | Assessment of cellular signaling pathway activity using linear combination(s) of target gene expressions |
| TWI658049B (zh) | 2013-03-12 | 2019-05-01 | 腫瘤療法 科學股份有限公司 | Kntc2胜肽及含此胜肽之疫苗 |
| JP6550045B2 (ja) * | 2013-10-09 | 2019-07-24 | フンダシオ、インスティトゥト、デ、レセルカ、ビオメディカ(イエレベ、バルセロナ)Fundacio Institut De Recerca Biomedica (Irb Barcelona) | 乳がんに由来する骨の転移がんの予後診断および処置のための方法 |
| CA2942721A1 (en) * | 2014-03-14 | 2015-09-17 | Czerniecki, Brian J. | Methods for monitoring cd4+ t-helper type 1 response in cancer and immune restoration |
| KR20170040315A (ko) | 2014-08-04 | 2017-04-12 | 온코세라피 사이언스 가부시키가이샤 | Cdca1-유래 펩티드 및 이를 포함하는 백신 |
| US10311681B2 (en) | 2015-08-19 | 2019-06-04 | Mark A. Litman | Electronic table game platform with secondary random event displays |
| US10380834B2 (en) | 2015-07-22 | 2019-08-13 | Mark A. Litman | Replaceable flexible electronic table top with display function for gaming tables |
| BR112018005581A2 (ja) | 2015-10-08 | 2018-10-16 | Oncotherapy Science, Inc. | The vaccine containing FOXM1 origin peptide and it |
| US11609427B2 (en) | 2015-10-16 | 2023-03-21 | Ostendo Technologies, Inc. | Dual-mode augmented/virtual reality (AR/VR) near-eye wearable displays |
| US11106273B2 (en) * | 2015-10-30 | 2021-08-31 | Ostendo Technologies, Inc. | System and methods for on-body gestural interfaces and projection displays |
| KR102541256B1 (ko) | 2015-11-30 | 2023-06-12 | (주)아모레퍼시픽 | Lipa 억제를 통한 흑색종 예방 또는 치료제, 및 그 스크리닝 방법 |
| KR102475128B1 (ko) | 2015-11-30 | 2022-12-07 | (주)아모레퍼시픽 | Entpd4 억제를 통한 흑색종 예방 또는 치료제, 및 그 스크리닝 방법 |
| US10345594B2 (en) | 2015-12-18 | 2019-07-09 | Ostendo Technologies, Inc. | Systems and methods for augmented near-eye wearable displays |
| US10578882B2 (en) | 2015-12-28 | 2020-03-03 | Ostendo Technologies, Inc. | Non-telecentric emissive micro-pixel array light modulators and methods of fabrication thereof |
| US10353203B2 (en) | 2016-04-05 | 2019-07-16 | Ostendo Technologies, Inc. | Augmented/virtual reality near-eye displays with edge imaging lens comprising a plurality of display devices |
| US10453431B2 (en) | 2016-04-28 | 2019-10-22 | Ostendo Technologies, Inc. | Integrated near-far light field display systems |
| US10522106B2 (en) | 2016-05-05 | 2019-12-31 | Ostendo Technologies, Inc. | Methods and apparatus for active transparency modulation |
| PT3458610T (pt) | 2016-05-25 | 2021-06-29 | Inbiomotion Sl | Tratamento terapêutico de cancro da mama baseado no estado de c-maf |
| PT3466978T (pt) * | 2016-06-03 | 2021-05-07 | Univ Kyushu Nat Univ Corp | Proteína de fusão para melhorar a expressão proteica de arnm alvo |
| CN110352256B (zh) | 2016-10-19 | 2023-01-10 | 捷迪资源有限责任公司 | 用具有硫代羰基官能团的试剂浸出金属硫化物的工艺 |
| WO2018102552A1 (en) | 2016-11-30 | 2018-06-07 | Case Western Reserve University | Combinations of 15-pgdh inhibitors with corcosteroids and/or tnf inhibitors and uses thereof |
| US11718589B2 (en) | 2017-02-06 | 2023-08-08 | Case Western Reserve University | Compositions and methods of modulating short-chain dehydrogenase |
| KR102091747B1 (ko) * | 2017-11-15 | 2020-03-20 | 주식회사 프로탄바이오 | 유방암 진단용 바이오마커 및 이의 용도 |
| WO2019102380A1 (en) | 2017-11-22 | 2019-05-31 | Inbiomotion S.L. | Therapeutic treatment of breast cancer based on c-maf |
| CN108441559B (zh) * | 2018-02-27 | 2021-01-05 | 海门善准生物科技有限公司 | 一种免疫相关基因群作为标志物在制备评估高增殖性乳腺癌远处转移风险的产品中的应用 |
| TW202023581A (zh) | 2018-08-02 | 2020-07-01 | 日商腫瘤療法 科學股份有限公司 | 來自cdca1的胜肽及含有此的疫苗 |
| US12331320B2 (en) | 2018-10-10 | 2025-06-17 | The Research Foundation For The State University Of New York | Genome edited cancer cell vaccines |
| CN109234384A (zh) * | 2018-10-31 | 2019-01-18 | 中国医学科学院阜外医院 | Hmgcl作为诊断标志物和治疗靶点在致密化不全型心肌病的应用 |
| EP3874062A4 (en) * | 2018-11-04 | 2022-08-24 | PFS Genomics, Inc. | METHODS AND GENOMIC CLASSIFIERS FOR PRODICTING BREAST CANCER AND PREDICTING THE BENEFITS OF ADJUVANT RADIATION THERAPY |
| KR102921276B1 (ko) | 2018-11-21 | 2026-02-03 | 케이스 웨스턴 리저브 유니버시티 | 단쇄 데히드로게나아제 활성을 조절하는 조성물 및 방법 |
| CN109811059B (zh) * | 2019-03-31 | 2021-10-19 | 青岛泱深生物医药有限公司 | 生物标志物uggt1在宫颈疾病中的应用 |
| EP4185862A4 (en) * | 2020-09-14 | 2024-12-25 | Duke University | COMPOSITIONS AND METHODS FOR THE DIAGNOSIS AND TREATMENT OF DYSTONIA |
| WO2022056622A1 (en) | 2020-09-18 | 2022-03-24 | The University Of British Columbia | Extracting base metals using a wetting agent and a thiocarbonyl functional group reagent |
| CN113025720B (zh) * | 2021-04-28 | 2022-12-27 | 深圳市人民医院 | 一种用于检测原发性乳腺弥漫性大b细胞淋巴瘤的标志物及其试剂盒和应用 |
| CN113466447B (zh) * | 2021-05-28 | 2024-03-08 | 天津市肿瘤医院(天津医科大学肿瘤医院) | 诊断胰腺癌预后的肿瘤标志物bzw1及检测试剂盒 |
| CN114931665B (zh) * | 2021-12-14 | 2024-09-27 | 广州医科大学 | 六型胶原α2亚基在神经修复产品中的应用 |
| CN114561358B (zh) * | 2022-03-09 | 2023-10-03 | 广州源井生物科技有限公司 | 一种提高细胞慢病毒感染率的增强感染培养基及方法 |
| CN114561470B (zh) * | 2022-03-19 | 2024-03-01 | 新乡医学院 | 三阴性乳腺癌分子标志物及其应用 |
| CN115616214B (zh) * | 2022-09-20 | 2026-03-03 | 湖南中医药大学 | Sox10抗体的应用、试剂盒 |
| US12340627B2 (en) | 2022-09-26 | 2025-06-24 | Pison Technology, Inc. | System and methods for gesture inference using computer vision |
| US12366923B2 (en) | 2022-09-26 | 2025-07-22 | Pison Technology, Inc. | Systems and methods for gesture inference using ML model selection |
| US12366920B2 (en) | 2022-09-26 | 2025-07-22 | Pison Technology, Inc. | Systems and methods for gesture inference using transformations |
| US12502110B2 (en) | 2023-10-24 | 2025-12-23 | Pison Technology, Inc. | Systems and methods for determining physiological state based on surface biopotentials |
| CN118243927A (zh) * | 2024-04-29 | 2024-06-25 | 东莞市石碣医院 | eIF3b作为乳腺癌耐药检测靶点的应用 |
| CN119007982A (zh) * | 2024-07-26 | 2024-11-22 | 大连医科大学附属第二医院 | 基于肿瘤浸润边缘e-tls预测非小细胞肺癌预后的方法和设备 |
| CN119955854B (zh) * | 2025-01-20 | 2025-09-09 | 中国人民解放军军事科学院军事医学研究院 | 一种侏儒症小鼠模型的构建方法及应用 |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5744101A (en) | 1989-06-07 | 1998-04-28 | Affymax Technologies N.V. | Photolabile nucleoside protecting groups |
| CA2242340A1 (en) * | 1996-01-11 | 1997-07-17 | Corixa Corporation | Compositions and methods for the treatment and diagnosis of breast cancer |
| US5968747A (en) * | 1997-12-12 | 1999-10-19 | Incyte Pharmaceuticals, Inc. | Ubiquitin-like conjugating protein |
| EP1343886A2 (en) * | 2000-07-11 | 2003-09-17 | Corixa Corporation | Compositions and methods for the therapy and diagnosis of lung cancer |
| AU2001296448A1 (en) | 2000-10-03 | 2002-04-15 | Curagen Corporation | Tumor marker and methods of use |
| US20030157544A1 (en) * | 2000-10-30 | 2003-08-21 | Eos Biotechnology, Inc. | Novel methods of diagnosing breast cancer, compositions, and methods of screening for breast cancer modulators |
| US20030104418A1 (en) * | 2001-04-27 | 2003-06-05 | Chao Zhang | Diagnostic markers for breast cancer |
| US7189507B2 (en) * | 2001-06-18 | 2007-03-13 | Pdl Biopharma, Inc. | Methods of diagnosis of ovarian cancer, compositions and methods of screening for modulators of ovarian cancer |
| US20060194199A1 (en) | 2002-09-30 | 2006-08-31 | Oncotherapy Science, Inc. | Method for diagnosing testicular seminomas |
| EP2295601A1 (en) | 2005-02-10 | 2011-03-16 | Oncotherapy Science, Inc. | Method of diagnosing bladder cancer |
| CA2660438A1 (en) | 2006-08-10 | 2008-02-14 | Oncotherapy Science, Inc. | Genes and polypeptides relating to breast cancers |
| TW200908998A (en) * | 2007-06-27 | 2009-03-01 | Oncotherapy Science Inc | Compositions and methods of treating cancer |
-
2004
- 2004-08-10 WO PCT/JP2004/011741 patent/WO2005029067A2/en not_active Ceased
- 2004-08-10 JP JP2006527766A patent/JP4579246B2/ja not_active Expired - Fee Related
- 2004-08-10 CN CN2004800347098A patent/CN1898563B/zh not_active Expired - Fee Related
- 2004-08-10 EP EP04771702A patent/EP1668354A2/en not_active Withdrawn
- 2004-08-10 TW TW093123896A patent/TW200512298A/zh unknown
- 2004-09-22 TW TW093128694A patent/TW200521243A/zh unknown
- 2004-09-24 EP EP04773526A patent/EP1668156B9/en not_active Expired - Lifetime
- 2004-09-24 DE DE602004032556T patent/DE602004032556D1/de not_active Expired - Lifetime
- 2004-09-24 CN CN2004800347011A patent/CN1890381B/zh not_active Expired - Fee Related
- 2004-09-24 US US10/573,297 patent/US7531300B2/en not_active Expired - Fee Related
- 2004-09-24 WO PCT/JP2004/014438 patent/WO2005028676A2/en not_active Ceased
- 2004-09-24 AT AT04773526T patent/ATE508202T1/de not_active IP Right Cessation
- 2004-09-24 ES ES04773526T patent/ES2365732T3/es not_active Expired - Lifetime
- 2004-09-24 JP JP2006527773A patent/JP4620670B2/ja not_active Expired - Fee Related
-
2007
- 2007-09-13 JP JP2007237927A patent/JP2008092949A/ja not_active Withdrawn
-
2009
- 2009-04-01 US US12/416,900 patent/US8044193B2/en not_active Expired - Fee Related
-
2011
- 2011-09-21 US US13/238,273 patent/US20120010090A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| WO2005029067A2 (en) | 2005-03-31 |
| CN1898563B (zh) | 2011-11-23 |
| JP2007506424A (ja) | 2007-03-22 |
| US8044193B2 (en) | 2011-10-25 |
| TW200521243A (en) | 2005-07-01 |
| JP4620670B2 (ja) | 2011-01-26 |
| JP2007506426A (ja) | 2007-03-22 |
| ATE508202T1 (de) | 2011-05-15 |
| WO2005029067A3 (en) | 2005-08-18 |
| WO2005028676A2 (en) | 2005-03-31 |
| ES2365732T3 (es) | 2011-10-10 |
| EP1668156B9 (en) | 2012-02-22 |
| WO2005028676A3 (en) | 2005-09-15 |
| US20070269432A1 (en) | 2007-11-22 |
| US20120010090A1 (en) | 2012-01-12 |
| JP2008092949A (ja) | 2008-04-24 |
| EP1668156A2 (en) | 2006-06-14 |
| EP1668156B1 (en) | 2011-05-04 |
| CN1890381B (zh) | 2011-06-22 |
| US7531300B2 (en) | 2009-05-12 |
| CN1898563A (zh) | 2007-01-17 |
| TW200512298A (en) | 2005-04-01 |
| US20090286856A1 (en) | 2009-11-19 |
| DE602004032556D1 (ja) | 2011-06-16 |
| EP1668354A2 (en) | 2006-06-14 |
| CN1890381A (zh) | 2007-01-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4579246B2 (ja) | 乳癌を診断する方法 | |
| JP5109131B2 (ja) | 膀胱癌を診断する方法 | |
| JP2007506425A (ja) | 肝細胞癌を診断する方法 | |
| JP2006500946A (ja) | 精巣精上皮腫の診断方法 | |
| US8029981B2 (en) | Hypoxia-inducible protein 2 (HIG2), a diagnostic marker for clear cell renal cell carcinoma | |
| JP2009502112A (ja) | 腎細胞癌を診断および処置するための方法 | |
| US20070202109A1 (en) | Method Of Diagnosing Breast Cancer | |
| EP1786925B1 (en) | Genes and polypeptides relating to breast cancers | |
| EP1907859B1 (en) | Genes and polypeptides relating to prostate cancers | |
| EP1910570B1 (en) | Gene and polypeptide relating to breast cancer | |
| JP2007522791A (ja) | 結腸直腸癌を診断する方法 | |
| JP2009505631A (ja) | 癌関連遺伝子rasgef1a | |
| EP1727831A1 (en) | Genes and polypeptides relating to prostate cancers |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20070803 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20100517 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100707 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20100802 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20100825 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130903 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130903 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130903 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130903 Year of fee payment: 3 |
|
| LAPS | Cancellation because of no payment of annual fees |