JP4295826B2 - 前立腺特異的膜抗原の細胞外ドメインに対して特異的なモノクローナル抗体 - Google Patents
前立腺特異的膜抗原の細胞外ドメインに対して特異的なモノクローナル抗体 Download PDFInfo
- Publication number
- JP4295826B2 JP4295826B2 JP53466797A JP53466797A JP4295826B2 JP 4295826 B2 JP4295826 B2 JP 4295826B2 JP 53466797 A JP53466797 A JP 53466797A JP 53466797 A JP53466797 A JP 53466797A JP 4295826 B2 JP4295826 B2 JP 4295826B2
- Authority
- JP
- Japan
- Prior art keywords
- psma
- antibody
- hybridoma
- monoclonal antibody
- accession number
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/08—Drugs for disorders of the urinary system of the prostate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/34—Identification of a linear epitope shorter than 20 amino acid residues or of a conformational epitope defined by amino acid residues
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2799/00—Uses of viruses
- C12N2799/02—Uses of viruses as vector
- C12N2799/021—Uses of viruses as vector for the expression of a heterologous nucleic acid
- C12N2799/026—Uses of viruses as vector for the expression of a heterologous nucleic acid where the vector is derived from a baculovirus
Description
1.発明の分野
本発明は、前立腺特異的膜抗原(PSMA)の細胞外ドメインに結合するモノクローナル抗体、該抗体を生産するハイブリドーマ細胞系、並びにそのような抗体を癌の診断および治療に使用する方法に関する。特に本発明は、PSMAのカルボキシ末端領域の一部と実質的に相同である合成ペプチドに対して産生され、前立腺癌患者の腫瘍細胞表面上および血清中で発現するPSMAと反応するモノクローナル抗体に関する。さらに本発明は、前立腺癌の膜調製物に対して産生され、やはり細胞表面上で発現するPSMAと反応する2つのモノクローナル抗体に関する。本発明はまた、上記抗体により検出されるPSMAの新規のタンパク質変異型(PSM’)に関する。
2.発明の背景
前立腺癌は男性における癌による死亡原因の第2位を占める。実際、前立腺癌はアメリカ人男性において診断される最も一般的な皮膚以外に関わる癌である。高齢男性の人口の増加および前立腺癌に対する認識の広がりによる早期診断の結果、前立腺癌と診断される男性の数は着実に増加している(Parkerら、1997、CA Cancer J.for Clin.47:5-28)。1997年には334,500人を越える男性が前立腺癌と診断され、この病気によりおよそ41,800人が死亡すると予測された。男性が一生のうちに前立腺癌に罹る危険性は、白人では5人中約1人、アフリカ系アメリカ人では6人中1人である。高い危険性を有するグループは、家系に前立腺癌患者もしくはアフリカ系アメリカ人がいるグループに代表される。前立腺癌と診断された男性のうちの3分の2以上が一生のうちにこの病気が原因で死亡する(Wingoら、1996、CA Cancer J.for Clin.46:113-25)。また、前立腺癌で死亡していない患者の多くが、疼痛、出血、および尿路閉鎖などの症状を緩和するための継続的な治療を必要とする。つまり、前立腺癌はまた、苦痛および健康維持にかかる出費上昇の主な原因でもある(Catalona、1994、New Eng.J.Med.331:996-1004)。
PSMAは、前立腺組織で発現する分子量120kDaのタンパク質であり、従来7E11-C5と称されるモノクローナル抗体との反応性によって同定されていた(Horoszewiczら、1987、Anticancer Res.7:927-935;米国特許第5,162,504号)。PSMAは、精製された形態で入手でき(Wrightら、1990、Antibody Immunoconjugates and Radio Pharmaceuticals 3:要約193)、トランスフェリン受容体(Israeliら、1994、Cancer Res.54:1807-1811)およびNAALADase活性(Carterら、1996、Proc.Natl.Acad.Sci.U.S.A.93:749-753)と配列同一性を有するII型膜貫通タンパク質として特徴づけられる。さらに重要なことに、PSMAは前立腺癌においてより多く発現し、またこれらの患者の血清においても高い量のPSMAが検出される(Horoszewiczら、1987、同上;Rochonら、1994、Prostate 25:219-223;Murphyら、1995、Prostate 26:164-168;およびMurphyら、1995、Anticancer Res.15:1473-1479)。PSMAをコードするcDNAがクローニングされ(Israeliら、1993、Cancer Res.53:227-230)、このcDNAは、2つの選択的にスプライシングされたmRNA種、即ち、PSMAをコードする2,653ヌクレオチドを含むmRNA種、およびPSM’と称される2,387ヌクレオチドを含む第2のmRNA種を産生する(Suら、1995、Cancer Res.55:1441-1443)。本発明以前には、PSM’タンパク質産物は一度も検出されなかったために、PSM’がタンパク質産物をコードするのかそれとも単に未翻訳mRNA種として存在するだけなのか知られていなかった。
Carterらによる最近の報告(1996、Proc.Natl.Acad.Sci.U.S.A.、93:749-753)は、PSMAcDNAの一部に相当する1428塩基と、タンパク質N-アセチル化α結合酸性ジペプチダーゼ(NAALADase)のcDNA配列との間に高い同一性があることを示している。NAALADaseは、神経ペプチドN-アセチルアスパルチルグルタミン酸に対する酵素活性を有し、グルタミン酸とN-アセチルアスパラギン酸を生成する。この報告によれば、PSMAタンパク質固有のNAALADase活性は実証されているが、PSMAの触媒部分は同定されていない。NAALADase活性は、PSMAを発現したLNCaP細胞において認められたが、PSMAを発現しないPC3細胞においては認められなかった。PSMAcDNAをPC3細胞にトランスフェクトすることにより、これらの細胞にNAALADase活性およびPSMAの存在が生じた。
PSMAおよびPSM’のcDNAの違いは、ヌクレオチド#1〜171またはアミノ酸#1〜57を含む膜貫通、細胞内コード領域の欠損である。PSMAはII型膜タンパク質とされており、II型膜タンパク質の機能的触媒ドメインは分子のC-末端細胞外領域にあることが知られている(DeVriesら、1995、J.Biol.Chem.、270:8712-8722)。
良性の過形成または前立腺癌を患う患者の前立腺組織よりも正常な前立腺組織においてより多くのPSM’mRNAが認められた(Suら、1995、同上)。逆に、PSMA mRNAは、前立腺癌を患っていない患者よりも前立腺癌を患っている患者においてより高いレベルで認められた(Suら、1995、同上)。この観察された違いは、先に記載されたPSMAの血清タンパク質量と一致している(Horoszewiczら、1987、同上;Rochonら、1994、同上;Murphyら、1995、同上;およびMurphyら、1995、同上)。これに関連して、前立腺癌患者の血清中のPSMAの上昇量は、病気の進行対緩解に相関しており、予後マーカーとして用い得る(Murphyら、1995、同上)。
モノクローナル抗体7E11-C5によって認識されるエピトープは、PSMAの細胞内N-末端領域の最初の6個のアミノ酸にマッピングされた(Troyerら、1995、Urol.Oncol.1:29-37)(図1)。7E11-C5を用いた電子免疫細胞化学によって、この抗体に対するエピトープは細胞質と、特に原形質膜の内葉に局在化していた(Troyerら、1994、Proc.Am.Assoc.Cancer Res.35:283、要約1688)。さらに、モノクローナル抗体7E11-C5は、in vitro検査において、固定および透過した細胞のみを染色し(Horoszewiczら、1987、同上)。この結果、PSMAのN-末端または細胞内ドメインへの7E11-C5エピトープのマッピングと一致する。おそらく壊死および/またはアポトーシスを通じてそのエピトープを露呈すると考えられる前立腺癌をin vivoで検出するのに7E11-C5が有用であるのに対し、PSMAの細胞外ドメインに特異的なモノクローナル抗体は、癌細胞表面上のPSMAをより効率的に検出することを可能にする。また、PSM’はPSMAの細胞内ドメインを欠くために、モノクローナル抗体7E11-C5はPSM’のmRNA転写体の配列に基づいてPSM’を認識しない。
本節または本願のその他の全ての節における全参考文献を引用または列挙することにより、それらの参考文献が本発明の先行技術にあたると認めるものではない。
3.発明の要旨
本発明は、PSMAの細胞外ドメインに特異的なモノクローナル抗体、該抗体を生産するハイブリドーマ細胞系、該抗体を前立腺癌の診断および治療に使用する方法、並びにそのような抗体により認識されるPSM’として知られるPSMAの変異型タンパク質に関する。
本発明の一部は、出願人がPSMAの細胞外ドメインを認識する3つのモノクローナル抗体を発見したことに基づいている。抗体のうちの1つは、アミノ酸配列ESKVDPSK(配列番号1)を有するPSMAのC-末端ペプチドでマウスを免疫することにより産生した。この抗体は、前立腺癌患者の腫瘍細胞溶解物および血清中のPSMAおよびPSM’タンパク質と反応する。また、この抗体は、無傷の腫瘍生細胞を染色し、PSMAまたはPSM’タンパク質の細胞外ドメインに対する特異性が認識された。この抗体はまた、ヒト精液中のPSM’も検出し、このヒト精液中のPSM’はNAALADase活性を示す。2つの他のモノクローナル抗体は、前立腺癌の膜調製物に対して産生した。これらの抗体もまた、イムノアフィニティー精製により単離された天然PSMAおよび組換えDNA技術により生産された組換えPSMAを含むPSMAおよびPSM’の細胞外ドメインと反応する。これらの抗体は、PSMAの細胞内ドメインに対する抗体と組み合わせて、二部位捕捉アッセイにおいて検査サンプル中のPSMAの存在を検出するのに有用となる。さらに、本明細書において開示する3つの抗体全てが、検査サンプル中のPSM’の存在を検出するための二部位捕捉アッセイにおいて使用され得る。
本発明は、広範にわたる様々な使用を包含するものであり、以下に限定されないが、患者における前立腺癌の検出または病期分類のためのイムノアッセイを開発および使用すること、一次および/または転移前立腺癌をin vivoで画像化すること、細胞障害剤または化学療法剤に結合した抗体を使用する等抗体を治療に使用すること、並びに、抗体断片、キメラ抗体、ヒト化抗体、または二価抗体を構築および使用することを含む。
【図面の簡単な説明】
図1 PSMAおよびPSM’抗原の推定アミノ酸配列(配列番号2)(Israeliら、1994、Cancer Res.54:1807-1811)。PSM’ mRNAは、初めの57個のアミノ酸(一行目のアミノ酸配列)をコードするPSMAの5’末端を含まないためアミノ酸58から開始すると考えられる。しかし、本発明以前は、PSM’はタンパク質形態で同定されたことはなかった。下線領域は推定される膜貫通ドメインであり、太字領域(アミノ酸#716〜723)はモノクローナル抗体開発のために選択されたペプチドである。
図2モノクローナル抗体3F5.4G6(一次ハイブリドーマ3F5から誘導されたサブクローン)、およびPSMAに対応する分子量120kDaのLNCaP溶解物中に存在するタンパク質とその反応性の実例。HRP-抗IgG二次抗体を用いてウェスタンブロットを発色した。1列目は7E11-C5でプローブしたLNCaP溶解物、2列目は3F5.4G6でプローブしてLNCaP溶解物である。
図3モノクローナル抗体3F5.4G6(3列目および4列目)、並びに対照として7E11-C5(1列目および2列目)を用いた、前立腺癌患者(D2病期)の血清中のPSMAのウェスタンブロットによる実例。
図4モノクローナル抗体7E11-C5(1列目)および3F5.4G6(2列目)を使用し、HRP-抗IgM二次抗体を用いて発色したLNCaP溶解物のウェスタンブロットアッセイ。7E11-C5および3F5.4G6の両方が分子量120kDaのタンパク質を認識した。さらに、3F5.4G6はまた、PSM’のタンパク質形態と予測されるものに対応する分子量105〜110kDaのタンパク質も認識した。PSM’中に7E11-C5モノクローナル抗体のエピトープは認められなかったため、7E11-C5はPSM’を認識しなかったことに留意すべきである。抗体3F5.4G6は、PSMAおよびPSM’の細胞外ドメインに対応するタンパク質のC-末端部分(アミノ酸#716〜723)を認識する。
図5モノクローナル抗体7E11-C5および3F5.4G6が同じタンパク質を認識したが、3F5.4G6がさらにPSM’に対応するタンパク質を認識した実例。LNCaP溶解物をまず7E11-C5モノクローナル抗体で免疫沈降し、免疫沈降した物質をSDSゲル上で分離し、ウェスタンブロットアッセイにおいて7E11-C5(1〜4列目)もしくは3F5.4G6(5〜8列目)モノクローナル抗体のいずれかでプローブした。1列目および5列目は粗LNCaP溶解物;2列目および6列目は予め濁りを除いたLNCaP溶解物;3列目および7列目は7E11-C5モノクローナル抗体で免疫沈降した物質;そして4列目および8列目は先に免疫沈降したLNCaP溶解物中に残留したタンパク質であった。抗体7E11-C5は120kDaのタンパク質を免疫沈降し(3列目)、このタンパク質はまた3F5.4G6によっても認識された(7列目)。しかし、7E11-C5免疫沈降後、7E11-C5によって免疫沈降されなかった(4列目)第2のタンパク質は3F5.4G6によって認識され(8列目)、このタンパク質はPSM’に相当していた。つまり、7E11-C5はPSM’を認識しない。
図6モノクローナル抗体7E11-C5および3F5.4G6が同じ120kDaタンパク質を認識した実例。LNCaP溶解物由来のPSMAをモノクローナル抗体3F5.4G6で免疫沈降し、免疫沈降物中のタンパク質をSDSゲル上で分離し、Immobilon Pに転写し、ウェスタンブロットにおいてモノクローナル抗体7E11-C5でプローブした。1列目は7E11-C5でプローブしたLNCaP溶解物対照、2列目は3F5.4G6免疫沈降物である。
図7Aおよび7B PSMAの細胞外ドメインへの抗体結合を示した、3F5.4G6モノクロナール抗体によるLNCaP生細胞の認識についてのFACS分析の実例。図7Aは一次抗体のない対照を表し、図7BはFACS分析前に100μg/mlの3F5.4G6と共にインキュベートしたLNCaP細胞を表す。右方向へのシフトはLNCaP生細胞に対する抗体の結合を示す。
図8精液から単離、精製したPSM’とモノクローナル抗体3F5.4G6との反応性の実例。1列目はLNCaP溶解物、そして2列目は精液から精製したPSM’である。SDSポリアクリルアミドゲル上でタンパク質を分離し、Immobilon P紙に転写し、ウェスタンブロット法によりモノクローナル抗体3F5.4G6でプローブした。精液から精製した2列目に該当するタンパク質は分子量が90kDaであり、おそらく分子量105〜110kDaのグリコシル化されていないまたは部分的にグリコシル化されたPSM’産物と考えられる。
図9天然PSMAおよび3つのPSMA断片とモノクローナル抗体3D7-1.1および4E10-1.14との反応性の実例。マイクロタイター96ウェルプレートを天然PSMAかまたはPSMAの3つの細胞発現されたポリペプチド断片の内の1つで被覆し、ELISAにおいてハイブリドーマ上清と反応させた。3つの検査抗体の全てが天然PSMAと同等の結合を示したのに対して、3D7-1.1および4E10-1.14はPSMAの細胞外ドメイン中のエピトープに対応する断片と強く反応した。
図10モノクローナル抗体3D7-1.1を用いたPSMAのウェスタンブロット分析。1列目はLNCaP溶解物、2列目はPC-3溶解物、3列目はイムノアフィニティーによって精製されたPSMAである。
図11全長バキュロウィルスで発現されたPSMAのウェスタンブロット分析。組換えPSMAをSDS-PAGEゲル上で電気泳動し、エレクトロブロッティングし、種々の抗体調製物でプローブした。1列目はブランク;2列目は対照培地(20%FCS含有RPMI 1640);3列目は3D7-1.1モノクローナル抗体;4列目は3D7-1.2モノクローナル抗体;5列目は3D7-1.3モノクローナル抗体;6列目は3D7-1.7モノクローナル抗体;7列目は3D7-2.7モノクローナル抗体;8列目は4E10(親)モノクローナル抗体;9列目は4E10-1.3モノクローナル抗体;10列目は4E10-1.14モノクローナル抗体;11列目はブランク;12列目はブランク;13列目は7E11-C5モノクローナル抗体である。
図12A〜DPSMAの細胞外ドメインとの抗体結合を例示した、3D7-1.1および4E10-1.14モノクローナル抗体によるLNCaP生細胞の認識についてのFACS分析による実例。図12Aは4E10-1.14と共にインキュベートしたLNCaP細胞を示す。図12Bは4E10-1.14と共にインキュベートしたPC-3細胞を示す。図12Cは3D7-1.1と共にインキュベートしたLNCaP細胞を示す。図12Dは3D7-1.1と共にインキュベートしたPC-3細胞を示す。図12Aおよび12Cにおける右へのシフトのパターンの違いは、2つの抗体がPSMAの異なるエピトープを認識しうることを示している。
図13PSMAのエピトープを区別するために2つのモノクローナル抗体を用いた二部位捕捉ELISAによるPSMAの検出。連続希釈したイムノアフィニティ精製PSMAを7E11-C5で被覆された96ウェルプレートに加え、3D7-1.1または4E10-1.14上清と共にインキュベートすることによって検出した。マイクロプレートリーダーで405nmの吸収を測定した。
は3D7-1.1、
は4E10-1.14を表す。
図143D7-1.1および4E10-1.14モノクローナル抗体を用いた二部位捕捉ELISAによる、種々の生物学的サンプル中のPSMAの検出。
図153D7-1.1および4E10-1.14モノクローナル抗体を用いた二部位捕捉ELISAによる、正常なヒト血清で連続希釈したイムノアフィニティー精製PSMAの検出。
図16代替の二部位捕捉ELISAによるPSMAの検出。連続希釈したイムノアフィニティー精製PSMAを3D7-1.1で被覆された96ウェルプレートに加え、ビオチニル化7E11-C5(40μg/ml)次いで西洋ワサビペルオキシダーゼ結合ストレプトアビジンと共にインキュベートすることにより検出した。マイクロプレートリーダで405nmの吸収を測定した。7E11-C5をE-Z結合ビオチニル化キット(Pierce)を用いて製造元の使用説明書に従ってビオチニル化した。
図17LNCaP細胞溶解物、および4E10-1.14ハイブリドーマ由来の組織培養上清を用いてプローブした半精製PSMA断片(バキュロウィルス発現系で1.9kbインサートとして発現された全長PSMAのアミノ酸134〜750に対応する)の種々の画分のウェスタンブロット分析。1.9kb構築物(PSMAのアミノ酸134〜750)に由来するタンパク質産物の同定を矢印で示す。
1列目はマーカー;2列目はLNCaP細胞粗溶解物;3列目はウィルスペレット(即ち、1.9kb PSMA断片を発現するバキュロウィルスに感染させた100,000×gペレットの溶解SF9細胞);4列目は1.9kb PSMA断片を発現するバキュロウィルスに感染させた溶解SF9細胞由来の100,000×g上清画分;5列目はNi-NTAマトリックスを通過させた後の4列目に示す画分の素通り分;6列目はNi-NTAマトリックスの0.5M NaCl溶出;7列目はNi-NTAマトリックスの1Mイミダゾール(pH7.6)溶出;8列目はNi-NTAマトリックスを通過させた後の4列目に示す画分の素通り分;9列目はNi-NTAマトリックスの0.5M NaCl溶出;そして10列目はNi-NTAマトリックスの1Mイミダゾール(pH7.6)溶出を示す。また、2列目において、LNCaP細胞で発現された天然全長PSMAと4E10-1.14モノクローナル抗体との反応性にもふれておく。
図18関連性のないインサート、またはPSMAの一部(全長PSMAのアミノ酸134〜750)をコードする1.9kbインサートのいずれかを含むバキュロウィルスに感染させたSF9細胞の粗溶解物を抗体7E11-C5でプローブしたウェスタンブロット。1、2列目はMWマーカー;3列目は関連性のないウィルスで感染させたSF9細胞溶解物;4列目はSF9細胞溶解物;そして5列目はウィルスに感染させたSF9溶解物を含む1.9kb PSMAインサートである。SF9細胞またはいずれかのウィルスに感染させたいずれのタンパク質産物でも7E11-C5陽性バンドが観察されなかったことにふれておく。
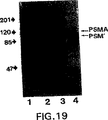
図19モノクローナル抗体3D7-1.1を用いてプローブした、LNCaP細胞、ヒト精液、およびヒト血清から得たPSMAおよびPSM’のウェスタンブロット。1列目はLNCaP細胞溶解物;2列目は7E11-C5イムノアフィニティー精製されたLNCaP細胞由来PSMA;3列目はヒト精液;そして4列目はヒト男性血清。PSMAおよびPSM’の位置を示している。
5. 発明の詳細な説明
本発明は、PSMAの細胞外ドメインに特異的なモノクローナル抗体、そのような抗体の使用方法、およびそのような抗体により同定される末端切断型タンパク質変異体であるPSM’に関する。本明細書に記載の特定の手順および方法は、マウスを免疫するためのC末端ペプチドまたはPSMA発現性腫瘍膜調製物を用いて例示されるが、それらは本発明の実施を説明するためのものにすぎない。類似の手順および技法が、タンパク質、ペプチド、細胞表面抗原および粗製膜調製物の形態のPSMAに対して免疫された種々の動物宿主に対して同じように適用可能である。
5.1 ハイブリドーマ細胞系および抗体産生
第6節(後記)の実施例による特定の実施態様では、PSMAのC末端領域から誘導される合成ペプチドを免疫原として用いた。その結果、3F5.4G6と命名された1つの抗体が、PSMAの細胞外ドメインに結合しており、これは生きている前立腺癌細胞の細胞表面上および前立腺癌患者の血清中に露出していることが示される。さらに、第7節(後記)の第2の実施例では、PSMA発現性腫瘍膜調製物を用いて動物を免疫した後で、PSMAの細胞外ドメインに対する2つのモノクロナール抗体を産生させることが示されている。これに関連して、PSMAの細胞外ドメインに特異的なモノクローナル抗体を産生するために動物宿主内で免疫応答を生起させる免疫原としては、PSMAを発現するLNCaPのような癌細胞、PSMAコード配列でトランスフェクトした宿主細胞、精製PSMA、PSM’またはPSMA細胞外ドメインペプチドが使用可能である。
抗体を産生する可能性のある体細胞、特にBリンパ球は、B細胞ミエローマ系との融合に好適である。分裂中の形質芽球期(dividing plasmablast stage)にある抗体産生細胞が優先的に融合する。体細胞は、抗原感作動物のリンパ節、脾臓および末梢血から得ることが可能であり、選択されるリンパ細胞は、特定の融合系における経験に基づく有用性に大きく依存する。一次感作または超免疫された動物が、抗体産生リンパ球の供給源として使用できる。マウス・リンパ球は、以下に記載するマウスミエローマ系との安定な融合を高比率でもたらす。それらの中でも、BALB/cマウスが好ましい。しかし、他のマウス系統、ウサギ、ハムスター、ヒツジおよびカエルもまた、抗体産生細胞を調製するための宿主として使用可能である。Godingにより概説されているように(Monoclonal Antibodies: Principles and Practice,第2版、60〜61頁、Orlando,Fla,Academic Press,1986)、ラット・リンパ球を使用すると幾つかの利点がもたらされることがある。
あるいは、抗体の産生能を有するヒト体細胞(特に、Bリンパ球)が、ミエローマ細胞系との融合に好適である。個体の生検した脾臓、扁桃またはリンパ節からのBリンパ球が使用可能であるが、さらに容易に入手可能な末梢血Bリンパ球が好ましい。このリンパ球は、前立腺癌種と診断された患者から誘導され得る。さらに、ヒトB細胞は、エプスタイン−バーウイルス(Epstein-Barr virus)により直接不死化してもよい(Coleら,1995,Monoclonal Antibodies and Cancer Therapy,Alan R.Liss,Inc.77〜96頁)。
ハイブリドーマ産生融合法での使用に適するミエローマ細胞系は、好ましくは、非抗体産生性であり、高い融合効率を有し、かつ所望のハイブリドーマの増殖を維持する特定の選択培地で該細胞系を増殖不能にする酵素欠損体である。本発明の融合細胞ハイブリッドの産生に使用可能なそのようなミエローマ細胞系の例としては、P3-X63/Ag8、X63-Ag8.653、NS1/1.Ag4.1、Sp210-Ag14、FO、NSO/U、MPC-11、MPC11-X45-GTG1.7、S194/5XX0 Bul(これらは全てマウス由来);R210.RCY3、Y3-Ag1.2.3.、IR983Fおよび4B210(ラット由来);ならびにU-266、GM1500-GRG2、LICR-LON-HMy2、UC729-6(これらは全てヒト由来)が挙げられる(Goding,Monoclonal Antibodies: Principles and Practice,第2版,65〜66頁,Orlando,Fla,Academic Press,1986;Campbell,Monoclonal Antibody Technology,Laboratory Techniques in Biochemistry and Molecular Biology第13巻,BurdenおよびVon Knippenberg編,75〜83頁,Amsterdam,Elseview,1984)。
抗体産生脾臓またはリンパ節細胞とミエローマ細胞とのハイブリッドの作製方法は、一般に、細胞膜の融合を促進する(化学的または電気的)作用因子(agent)の存在下で体細胞とミエローマ細胞とを各々2:1の比率(但し、この比率は約20:1〜約1:1の間で変えることが可能である)で混合することを含む。この融合手法で用いられる体細胞およびミエローマ細胞の供給源としては、同じ種の動物を用いることが好ましい場合が多い。融合方法は、KohlerおよびMilstein(1975,Nature 256: 495-497; 1976,Eur.J.Immunol.6: 511-519)ならびにGefterら(1977,Somatic Cell Genet.3: 231-236)により記載されている。それらの研究者が用いた融合促進剤は、それぞれセンダイウイルスおよびポリエチレングリコール(PEG)であった。Godingが概説している融合方法(1986,Monoclonal Antibodies: Principles and Practice,第2版,71〜74頁,Orlando,Fla,Academic Press)は上記の融合方法ならびに電気的に誘導される融合を包含しており、これもまた本発明のモノクロナール抗体の作製に好適である。
融合手順により、一般に、生存可能なハイブリッドが非常に低い頻度(約1×10-6〜1×10-8個の体細胞)で作製される。生存可能なハイブリッドはこのように低頻度で得られるので、融合細胞ハイブリッドを残りの未融合細胞(特に、未融合ミエローマ細胞)から選別する手段を有することが必須である。さらに、所望の抗体産生ハイブリドーマを他の残りの融合細胞ハイブリッドから検出する手段も必要である。
一般に、融合細胞は、選択培地、例えば、ヒポキサンチン、アミノプテリンおよびチミジンを含有するHAT培地で培養する。HAT培地は、ハイブリッド細胞の増殖(proliferation)を可能にし、通常は無限に分裂し続ける未融合ミエローマ細胞の増殖(growth)を阻止する。アミノプテリンは、テトラヒドロ葉酸塩の生成を阻害することによりプリンおよびピリミジンのde novo合成を遮断する。チミジンの添加によりピリミジン合成の遮断が回避され、一方、ヒポキサンチンが培地に含まれることにより阻害された細胞がヌクレオチド再利用経路を用いてプリンを合成するようになる。用いられるミエローマ細胞は、ヒポキサンチンホスホリボシルトランスフェラーゼ(HPRT)が欠如しており、そのためにその再利用経路を利用できない変異体である。生存ハイブリッドでは、Bリンパ球は、この酵素を産生するための遺伝情報を提供する。Bリンパ球自体は培養下で有限の寿命(約2週間)を有するので、HAT培地で増殖できる細胞だけが、ミエローマ細胞と脾臓細胞とから形成されるハイブリッドである。
上記ハイブリッドにより分泌される抗体のスクリーニングを容易にするために、そして個々のハイブリッドが他のものよりも過剰増殖しないようにするために、融合したミエローマおよびBリンパ球の混合物をHAT培地に希釈し、マイクロタイタープレートの複数のウエル中で培養する。2〜3週間で、ハイブリッドクローンが顕微鏡観察下で見えるようになったら、ハイブリッドクローンを含有する個々のウエルの上清液を、特定の抗体についてアッセイする。このアッセイは、高感度で、簡易で、かつ迅速なものでなければならない。アッセイ技術としては、ラジオイムノアッセイ、酵素免疫アッセイ、細胞障害性アッセイ、プラークアッセイ、ドット免疫結合(dot immunobinding)アッセイなどが挙げられる。
所望の融合細胞ハイブリッドを選択し個々の抗体産生細胞系にクローニングしたら、各細胞系は、2つの標準的な方法のいずれかにより増殖させてもよい。ハイブリドーマのサンプルは、最初の融合のための体細胞およびミエローマ細胞を供給するのに用いた種類の組織適合性動物に注射することができる。注射した動物は、融合細胞ハイブリッドにより産生される特定のモノクローナル抗体を分泌する腫瘍を生ずる。この動物の体液(例えば、血清または腹水)を抜き取ることにより、高濃度のモノクローナル抗体が得られる。あるいはまた、個々の細胞系を、実験室用培養容器内でin vitroで増殖させることも可能である。この培養培地も単一の特定のモノクローナル抗体を高濃度で含有しており、これはデカンテーション、濾過または遠心分離により採取できる。
モノクローナル抗体または抗原結合領域の少なくとも一部を有する該モノクローナル抗体の精製断片[例えば、Fv、F(ab’)2、Fab断片](HarlowおよびLane,1988,Antibody,Cold Spring Harber)、一本鎖抗体(米国特許第4,946,778号)、キメラまたはヒト化抗体(Morrisonら、1984,Proc.Natl.Acad.Sci.USA 81:6851;Newubergerら、1984,Nature,81:6851)および相補性決定領域(CDR)は、慣用の手法により調製可能である。これらの抗体または断片の精製は、例えば、硫酸アンモニウムまたは硫酸ナトリウムにより沈殿させた後で、食塩水への透析、イオン交換クロマトグラフィー、アフィニティまたはイムノアフィニティクロマトグラフィー、ならびにゲル濾過、ゾーン電気泳動などを行う、当業者に公知の種々の方法により達成できる(Goding、Monoclonal Antibodies:Principles and Practice,第2版、104〜126頁、Orlando,Fla,Academic Press参照)。
5.2 モノクローナル抗体およびPSM’の特性決定
第5.1節(前記)に概略的に説明した技術および第6節および第7節(後記)で説明する技術を用いて、PSMAの細胞外ドメインの特異的なモノクローナル抗体の産生に基づいて、3つのハイブリドーマ細胞系を選択した。本発明は、35F.4G6、3D7-1.1および4E10-1.14抗体、ならびに、PSMAおよびPSM’の細胞外ドメインに特異的に結合する他のモノクローナル抗体を包含するものであり、特に、酵素免疫アッセイ、放射線免疫アッセイまたは他の任意の競合結合免疫アッセイで評価された際に、上記3つの抗体のうちの任意の1つ以上の抗体がPSMAに結合するのを競合的に阻害する全ての抗体を含む。
抗体3F5.4G6は、前立腺癌細胞溶解物中および前立腺癌細胞の細胞表面上ならびに前立腺癌患者から得た血清中に発現されるPSMAに特異的に結合するIgMのイソ型抗体である。さらに、3F5.4G6はPSM’にも特異的に結合する。3F5.4G6反応性PSMAエピトープは細胞外でC末端であり、細胞の細胞質で膜結合している7E11-C5により認識されるもの(Horoszewiczら、Anticancer Res.7:927-936)とは異なる。抗体3D7-1.1および4E10-1.14もまたIgM抗体であり、前立腺癌細胞溶解物中および細胞表面上で発現されるPSMAに結合する。これらの抗体は、原発性前立腺癌および転移性腫瘍(例えば、前立腺癌の骨への転移)の双方を検出するのに使用可能である。
抗体応答が生じる際に、抗体産生細胞はまず最初にIgMイソ型を分泌し、これは最終的にIgGにスイッチされる。そのようなクラススイッチ事象は、同じ抗原特異性が保持されるような定常領域遺伝子のDNA再編成により生じるものである。異なる抗体のイソ型は、異なるエフェクター機能を有する。例えば、IgMおよびIgG4以外の全てのIgGサブクラスは、抗原結合の際に補体を固定する。これに対して、IgEはアレルギー反応において肥満細胞に結合してヒスタミンの放出を誘発する。
ハイブリドーマ細胞系も、長期培養の間にクラススイッチ変異体を産生する。特に、IgMからIgGまたはIgG1からIgG2nへとスイッチするモノクローナル抗体はプロテインAに対する高い親和性に基づいて選択されて、これにより、それら抗体の精製が促進される。任意のクラススイッチ変異体を特定の所望のエフェクター機能について選択することができる(Spiraら、1985,Hybridoma Technology in the Biosciences and Medicine,Springer編、77〜88頁,Plenum Press,NY; HarlowおよびLane,1988 Antibodies,Cold Spring Harbor Laboratory)。例示した抗体の場合、それらはIgMのイソ型なので、同じ抗原特異生を有するIgG変異体を選択することも望ましく、これは、in vitroまたはin vivoにおける特定の目的にはさらに有用である場合がある。本発明は、3F5.4G6、3D7-1.1および4E10-1.14を含む本発明のモノクローナル抗体のIgG変異体を包含する。
第6節および第7節(後記)では、例示の抗体が120kDaの分子量のタンパク質を認識することが示されている。特に、3F5.4G6はまた、前立腺腫瘍細胞溶解物中の105〜110kDaの分子量のタンパク質を認識する。この120kDaのタンパク質は抗体7E11-C5によっても認識されるが、その低分子量の方のタンパク質は抗体3F5.4G6、3D7-1.1および4E10-1.14によってのみ検出される。したがって、その105〜110kDaのタンパク質は、PSM’として知られるmRNAの産物を提示する。しかしながら、本発明以前には、PSM’タンパク質はいっさい報告されておらず、それは未翻訳のmRNAであると考えられていた。PSM’のアミノ酸配列は、そのRNA配列から推定されるように、PSMAの細胞質領域および膜貫通領域が欠如していると予想されるので、7E11-C5が、その細胞内エピトープに対する特異性のために、この産物と反応しないであろうことは確実である。これに対して、PSMAの細胞ドメンに特異的な抗体3F5.4G6、3D7-1.1および4E10-1.14はPSM’も認識する。
5.3 PSMA特異的モノクローナル抗体のコード配列
本発明の別の実施態様では、例示のハイブリドーマ細胞系を用いて、抗原結合部位または抗体変異体を含む組成物を製造することが可能であり、該抗体変異体は、ネズミの可変領域または超可変領域をヒトの定常領域もしくは定常および可変フレームワーク領域と組合せたもの、すなわち、キメラまたはヒト化抗体、ならびに患者の抗体由来の抗原結合CDRのみをヒト・フレームワーク領域と結合させて保持するヒト化抗体である(Waldmann,1991,Science 252:1657,1662,特に1658-59、ならびにそこに引用されている文献を参照)。ネズミ抗体の結合特異性を保持しているそのようなキメラまたはヒト化抗体は、本発明による診断、予防または治療の用途のためにin vivoで投与した場合、低下した免疫原性を有すると予想される。
さらに別の実施態様では、本発明は、再編成された活性化免疫グロブリン遺伝子をコードするDNAまたはmRNAの供給源としてハイブリドーマ細胞系を使用することを包含するものであり、この免疫グロブリン遺伝子は単離し、公知の組換えDNA技術によりクローニングし、そしてPSMAの細胞外ドメインに特異的な抗原結合断片の作製のために他の細胞へ移送することが可能である。本発明のハイブリドーマ細胞系の再編成DNAの単離または該ハイブリドーマ細胞系のmRNAからのcDNAの調製により、イントロンを含まない配列が得られる可能性がある。
説明のために(しかし限定しようとするものではないが)、以下のようにして免疫発現ライブラリーを作製し、PSMAおよびPSM’に対する抗体結合断片をスクリーニングすることができる(Huseら,1989,Sci.246:1275-1281;Mullinaxら,1990,Proc.Natl.Acad.Sci.USA 87:8045-8099参照)。全RNAが精製でき(例えば、市販のキットを用いることによる)、軽(L)鎖のためのオリゴ(dT)プライマーおよび重(H)鎖のための特定のプライマーを用いて逆転写酵素を用いてcDNAに変換できる。免疫グロブリンH鎖およびL鎖の配列のポリメラーゼ連鎖反応(PCR)増幅は、プライマー対の組を用いて別々に行われる。上流プライマーはリーダーの部分的に保存された配列および/またはVHもしくはVLのフレームワーク領域にハイブリダイズするように設計でき、下流プライマーは定常ドメイン配列にハイブリダイズするように設計できる。そのようなプライマーは、完全長L鎖を維持し、IgGのFdに対応しH−Lジスルフィド結合を保存しているH鎖を付与するであろう。PCR増幅したLおよびH DNA断片を次いで消化し、それぞれHおよびL鎖ベクターに連結する。そのようなベクターはpelBリーダー配列、リボソーム結合部位および終止コドンを含有する。大腸菌(E.coli)中での発現に適切なλファージベクターは、市販のベクター(ImmunoZAP L、ImmunoZAP H;Stratacyte,La Jolla,Ca)から調製できる。連結した組換えファージDNAをin vitroパッケージング抽出物(in vitro packaging extract)と共にバクテリオファージに組み込み、大腸菌を感染させるのに用いる。このようにして作製された免疫発現ライブラリーを、PSMA、PSM’またはそれらの特定のペプチドを用いて抗原結合断片についてスクリーニングする。陽性のクローンは、Mullinaxら(前掲)により記載されているようにしてスクリーニングおよび同定できる
5.4 PSMA細胞外ドメイン特異的抗体および抗体組成物の使用
本明細書に記載する特定の手法および方法は、本発明のモノクローナル抗体を用いて例示されるが、それらは本発明を実施するための説明にしかすぎない。本発明による以下に記載の手法および方法では、抗原結合領域の少なくとも一部を有するモノクローナル抗体の精製断片(例えば、Fv、F(ab’)2、Fab断片)、一本鎖抗体、キメラまたはヒト化抗体またはCDRが使用できる。
5.4.1 免疫組織学的および免疫細胞学的適用
本発明のモノクローナル抗体は、組織学的および細胞学的検体中の前立腺癌腫瘍細胞の検出、特に正常組織および非悪性腫瘍からの悪性腫瘍を識別するのに使用することができる。組織検体は該抗体により染色可能であり、それらの結合は、ペルオキシダーゼ、フルオロセイン、アルカリホスファターゼなどの標識に結合した二次抗体により検出し得る。
さらに、免疫蛍光法で本発明のモノクローナル抗体を用いて、ヒト組織、細胞および体液の検体を調べることができる。典型的なプロトコールでは、凍結した非固定化組織生検サンプルのクリオスタット切片を含むスライドガラスまたは細胞学的スミアを風乾し、ホルマリンまたはアセトンで固定し、モノクローナル抗体調製物と共に給湿チャンバー内で室温にてインキュベートする。
次に、そのスライドガラスを洗浄し、上記モノクローナル抗体に対する抗体の調製物と共にさらにインキュベートする。この抗体は、使用するモノクローナル抗体がマウス脾臓リンパ球とマウスミエローマ細胞系との融合物に由来する場合には、通常は或る特定のタイプの抗-マウス免疫グロブリンである。この抗-マウス免疫グロブリンは、特定の波長で蛍光発光する化合物(例えば、ローダミンまたはフルオロセインイソチオシアナート)でタグ付けする。次いで、サンプル中の染色パターンおよび強度を蛍光顕微鏡により測定し、場合によっては写真に記録する。
さらに別の実施態様として、本発明のモノクローナル抗体を用いて組織検体または剥脱細胞(すなわち、前立腺腫瘍の吸引生検から得られる単一細胞調製物)を試験するために、コンピューターで画質向上させた(computer enhanced)蛍光画像分析またはフローサイトメトリーを用いることができる。本発明のモノクローナル抗体は、コンピューターで画質向上させた蛍光画像アナライザーによる、またはフローサイトメーターを用いる生きている腫瘍細胞(すなわち、前立腺腫瘍の吸引生検から得られる単一細胞調製物)の定量に特に有用である。そのようなアッセイにおいて抗体3F5.4G6、および4E10-1.14を用いることは、良性の前立腺腫瘍と悪性の前立腺腫瘍とを区別するのに有用である。何故ならば、該モノクローナル抗体が結合するPSMAは、悪性腫瘍により増大した量で発現されるからである。さらに、PSMA陽性細胞集団の割合は、それ単独で、もしくはこれらの細胞のDNA倍数性の測定と共に、疾患の進行の初期の指標を提供することにより、非常に有用な予後の情報を提供し得る。
さらに別の実施態様では、本発明のモノクローナル抗体は、他の既知の前立腺抗体と組合せて使用して、前立腺癌腫の悪性表現型に関するさらなる情報を提供することができる。
5.4.2 免疫血清学的適用
本発明のモノクローナル抗体は、その使用を、認識される特異的抗原決定基の存在についてヒト生物学的体液のスクリーニングへも広げることができる。患者から集めた生物学的体液のin vitro免疫血清学的評価によって、非侵襲的に癌を診断することができる。例示として、前立腺液、精液、全血、血清あるいは尿のようなヒト体液を患者から採取し、標準的なラジオイムノアッセイまたは酵素結合(enzyme-linked)イムノアッセイ、競合的結合酵素結合イムノアッセイ、ドットブロットあるいはウェスタンブロット、または当業界で公知の他の測定法において、PSMAおよびPSM’の細胞外ドメインに特異的なモノクローナル抗体を用い、サンプル液中の放出された抗原または細胞膜に結合した抗原として、特異的エピトープについてアッセイすることができる。
さらに、PSMAおよびPSM’上の重複していないエピトープに対するモノクローナル抗体を使用することによって、より感度の高いPSMAまたはPSM’タンパク質の診断アッセイを開発することができる。7E11-C5、3F5.4G6、3D7-1.1または4E10-1.14のようなPSMAの反対末端に特異的な抗体は、特に、このようなアッセイに使用するのに適している。この点に関し、一つの抗体は生物学的液体中のPSMAまたはPSM’を捕捉する基質に固定させておいてもよく、もう1つの抗体を使用して抗体結合抗原を検出する。また、PSMAおよびPSM’の発現は前立腺癌および正常前立腺組織のそれぞれにおいて増大するので、これら二つの形態を識別する抗体を使用して、処置後の腫瘍の退行対進行をモニターするさらに精確な方法を提供してもよい。3F5.4G6、3D7-1.1および4E10-1.14は両方の形態を認識するが、7E11-C5のほうはPSMAだけと結合するので、患者における各形態の正確なレベルを測定するのにこれらの抗体を共同して使ってもよい。そうすれば、腫瘍負荷(tumor burden)とその量とを相関させることができる。例えば、7E11-C5は、二サイト捕捉アッセイのアンカー抗体として使用することができ、他の三つの抗体のいずれか一つをPSMA定量用の検出抗体として使用することができる。一方、同様な二サイト捕捉アッセイに、この三つのPSMA細胞外ドメイン特異的抗体の中の2つの任意の組合せを使用して、全PSM’+PSMA濃度を特異的に測定することもできる。全PSM’+PSMA濃度から単純にPSMAを差し引けば、PSM’を具体的に定量することができる。
組織および体液中の細胞外ドメインのPSMAおよびPSM’をモノクローナル抗体によって検出することに加えて、NAALADase酵素活性測定を利用して、組織および/または体液中の細胞外ドメインのPSMAおよび/またはPSM’を定量することができる。
例えば、ホモジネートした組織を界面活性剤で可溶化し、遠心分離により不溶性物質をペレット化し、残留上清中のNAALADase活性を測定することによって、組織レベルを測定することができる。同様にして、まず遠心分離により細胞性物質をペレット化し、上清についてNAALADase活性の典型的なエンザイムアッセイを行うことによって、体液中のNAALADase活性を測定することもできる。
抗体結合の特異性を利用するNAALADaseアッセイプロトコールもまた適用することができる。例えば、7E11-C5、3F5.4G6、3D7-1.1または4E10-1.14抗体のいずれかを塗布した固体表面は、NAALADaseエンザイムアッセイを用いる検出用のPSMAまたはPSM’を捕捉するのに使用することができるであろう。従ってこれは、細胞外ドメイン特異的抗体がPSMAおよびPSM’の両方に結合するが7E11-C5はPSMAだけに結合するのであれば、所与の検体中の全長PSMAタンパク質およびPSM’を示差的に検出し定量するのに使うことができる。
グルタミン酸デヒドロゲナーゼの反応特性を利用して、さらに簡便なNAALADaseエンザイムアッセイを適用することもできる(Frieden,1959,J.Biol.Chem.,234: 2891)。このアッセイ法では、NAALADase酵素の反応生成物はグルタミン酸である。これは、N-アセチルアスパラギン酸とグルタミン酸を生ずるN-アセチルアスパルチルグルタミン酸の酵素触媒分解から誘導される。NSA(P)+を必要とする工程において、グルタミン酸は、グルタミン酸デヒドロゲナーゼによって触媒される反応で、2-オキソグルタル酸とNAD(P)Hを生ずる。この反応の進行は、NAD(P)+からNAD(P)Hへの変換による340nmの吸収変化によって容易かつ簡便に測定することができる。こうして、固定化した捕捉抗体を用いる固相フォーマットに適用可能なNAALADase活性のアッセイを改良することができる。このようにして、NAD+またはNAD(P)+の添加前および添加後の340nmにおける吸収変化に基づき、マイクロプレートリーダーにおいて、多重アッセイを同時に実施することができる。これは固相アッセイだけに限定されるものではない。何故ならば、このタイプのNAALADaseアッセイを用いて、例えば、血清のような溶液アッセイも可能だからである。
本発明のモノクローナル抗体またはその断片を含有するキットは、上記の免疫組織学的、免疫細胞学的および免疫血清学的方法による、in vitro診断、予後および/または前立腺癌のモニター用に誂えることができる。キット成分は、水性媒体か、または凍結乾燥形式にパッケージすることができる。酵素や放射性金属イオンのような標識部分が付いたコンジュゲートの形でモノクローナル抗体(またはその断片)を上記キットに使用する場合、そのようなコンジュゲートの成分は、完全にコンジュゲートした形か、中間体の形、またはキット使用者によりコンジュゲートされる別々の部分として供給することができる。
キットは、試験管やバイアル、フラスコ、瓶、注射器などの、一またはそれ以上の容器手段または容器セット手段をコンパクトに収容するようにコンパートメント化したキャリアを含んでもよい。上記容器手段または容器セット手段の第一のものは、モノクローナル抗体(またはその断片)あるいはPSMAまたはPSM’を含んでいてもよい。第二の容器手段または容器セット手段は、第一抗体(またはその断片)PSMAまたはPSM’と結合することができる標識またはリンカー標識中間体を含んでいてもよい。
5.4.3 in vivoでの診断、予防および治療への使用
本発明のモノクローナル抗体またはその断片は、in vivoでの前立腺癌細胞のターゲッティングに特に有用である。これらは、検出およびモニター用の腫瘍局在化ならびに原発性前立腺癌および転移の治療に使用することができる。これらをin vivoで適用するには、精製モノクローナル抗体または、Fv、F(ab’)2、Fab断片のような抗原結合領域の少なくとも一部をもつモノクローナル抗体の精製断片(HarlowおよびLane,1988,Antibody,Cold Spding Harbor)、単一鎖抗体(米国特許第4,946,778号)、キメラ抗体またはヒト化抗体(Morrison et al.,1984,Proc.Natl.Acad.Sci.USA 81: 6851; Newuberger et al.,1984,Nature,81: 6851)、相補性決定領域(CDR)等を使用することが望ましい。上記抗体またはその断片の精製は、当業者に公知の様々な方法によって行うことができ、そのような公知方法としては、硫酸アンモニウムまたは硫酸ナトリウムにより沈澱させた後で生理食塩水に対する透析、イオン交換クロマトグラフィ、アフィニティあるいは免疫アフィニティクロマトグラフィ、ならびにゲル濾過、ゾーン電気泳動などがある(Goding,Monoclonal Antibodies: Principles and Practice,第2版、104-126頁、Orlando,Fla,Academic Press参照)。
in vivoでの前立腺癌の検出および/またはモニターに使用するには、精製モノクローナル抗体は、コンジュゲートまたは複合体の投与および局在化(loca;lization)後、特定の組織または臓器の画像化を可能にするリポーター群(a reporter group)として役立つ化合物に、直接またはリンカーを介して共有結合させることができる。種々の異なるタイプの物質をリポーター群として役立てることができ、そのような物質には、放射線不透過性染料、放射性金属および非金属同位元素、蛍光原性化合物、発蛍光性化合物、陽電子発生性同位元素、非常磁性金属などがある。
前立腺癌のin vivo治療での使用の場合、精製モノクローナル抗体を単独で、あるいは、上記コンジュゲートの投与および局在化後、悪性細胞または組織を死滅および/または増殖抑制する化合物に、直接またはリンカーを介して共有結合させて、使用することができる。抗体をそれ自体で使用する場合、抗体は、補体の固定化または抗体依存細胞の細胞障害性によって腫瘍破壊を媒介してもよい。あるいは、前記抗体は、相乗的な治療効果を与えるために化学療法剤と併用投与することもできる(BaslyaおよびMendelsohn,1994,Breast Cancer Res.and Treatment,29: 127-138)。治療の目的で、放射性金属および非金属同位元素、化学療法剤、毒素などを含む、種々の異なるタイプの物質を該抗体と直接コンジュゲートすることができる(VitettaおよびUhr,1985,Annu.Rev.Immunol.,3: 197)。
別の態様によれば、前立腺癌のin vivo治療のために、本発明のモノクローナル抗体は、二官能性または二重特異的抗体、すなわち、前立腺特異的膜抗原の細胞外ドメインに対して特異的な抗原結合領域および殺腫瘍活性または腫瘍抑制活性をもつエフェクター細胞に特異的な抗原結合領域をもつ抗体の形に改変することができる。二重特異的抗体の二つの抗原結合領域は化学的に結合されているか、または二重特異的抗体を産生するように遺伝子工学的に操作された細胞によって発現することができる(一般に、Fanger et al.,1995,Drug News & Perspec.,8(3): 133-137参照)。殺腫瘍活性を有する適切なエフェクター細胞としては、細胞障害性T細胞(主としてCD8+細胞)、ナチュラルキラー細胞などを例示することができるが、これらには限定されない。本発明による二重特異的抗体の有効量を、前立腺癌患者に投与すると、この二重特異的抗体は、PSMAをもつ原発性または転移性腫瘍の部位に局在化後、悪性細胞を死滅させるか、および/またはその増殖を阻害する。
検出、モニターおよび/または治療に有用な、本発明の抗体(またはその断片)の抗体コンジュゲートの作製方法は、米国特許第4,671,958号、4,741,900号および4,867,973号に記載されている。
上記のタイプの物質のいずれかとコンジュゲートしたモノクローナル抗体(またはその断片)を含む、そのようなin vivo腫瘍局在化および治療法と共に用いるためのキットは以下のように作ることができる。キットの成分は、水性媒体か、または凍結乾燥形態にパッケージすることができる。このモノクローナル抗体(またはその断片)を上記キットの中で放射性金属イオンや治療剤部分のような標識または治療部分が結合したコンジュゲートの形でに使用する場合、そのようなコンジュゲートの成分は、完全にコンジュゲートした形態、中間体の形態、またはキットの使用者がコンジュゲートを生成する別々の部分として供給することができる。
6. 実施例:PSMAペプチドに対するモノクローナル抗体の産生
6.1 材料と方法
6.1.1 免疫用ペプチドの調製
PierceRockford,IL)のEDC方法を用いて、PSMAペプチド#716〜723(NH2-ESKVDPSK-)を、キャリアとしてキーホールリンペットヘモシアニン(KLH)と共役結合させた。このペプチド-KLH複合体を、1mg/mlのムラミルジペプチド(MDP、Pierce,Rockford,IL)を含有する不完全フロインドアジュバント(シグマ社、ミズーリ州セントルイス)に最終濃度250μg/mlで乳化した。乳化抗原調製物を4℃で保存した。
6.1.2 免疫
0.1mlの乳化ペプチドキャリア-複合体を6週間にわたって14日毎に皮下注して、雌のBALB/cマウスを免疫した。マウスから採血し、その血清を抗ペプチド抗体の存在について調べるペプチド特異的ラジオイムノアッセイ(RIA)にて試験した。1:1,000またはそれ以上の力価で抗ペプチド抗体が陽性と出たマウスを融合プロトコルのドナーとして使用した。融合3日前に、生理食塩水に溶かしたペプチド-KLH複合体50μgを腹腔内に投与してマウスを免疫した。
6.1.3 細胞融合
同じペプチド-KLH複合体による最終免疫した3日後に、BALB/cマウスの脾臓を無菌的に摘出し、単一細胞懸濁液を作った。浸透ショックにより赤血球を溶解し、残ったリンパ球をRPMI-1640培地に懸濁させた。脾臓細胞を10:1の割合でP3X63Ag8U.1(X63)ミエローマ細胞(CRL 1597、ATCC、Rockville,MD)と混合した(脾臓細胞100 x 106:X63ミエローマ細胞10 x 106)。X63細胞に対する脾臓細胞の融合はGalfreおよびMilsteinの方法によって行った(1981,Methods in Enzymology,Vol.73,Immunochemical Techniques,Part B)。細胞培養培地(RPMI-1640-20%ウシ胎児血清)中アミノプテリンのインクルージョンによってハイブリドーマ細胞を選択した。
6.1.4 一次ハイブリドーマのスクリーニング
各ハイブリドーマ培養液から細胞培養上清50μlを取り、ペプチド特異的抗体が存在するかどうかをペプチド特異的RIAによって試験した。簡単に説明すると、ウシ血清アルブミン(BSA)と共役結合させたペプチドを50μg/mlを予め塗布した96ウェルプロバインド(Pro-Bind)プレート(ファルコン社)のウェルに前記上清を加える。4℃で一夜インキュベーションした後、プレートをPBS-0.1% BSAで4回洗浄する。ウサギ抗マウスIgMとIgG(ICN)の1:500希釈液50μlを各ウェルに加え、プレートを室温で1時間インキュベーションする。プレートを上記のように4回洗浄し、各ウェルに125I-プロテインAを50μl加える。プレートを室温で1時間インキュベーションし、上記のように4回洗浄する。プレートをオートラドフィルム(コダック、X-OMAT)に一夜曝露して現像する。陽性のウェルを選択し、さらなる試験を行うために細胞を細胞培地に広げた。
6.1.5 ウェスタンブロットスクリーニング
広げた陽性のウェルから上清を得、これを抗PSMA抗体についてウェスタンブロットアッセイで試験した。PSMAを発現する前立腺腫瘍であるLNCaP腫瘍細胞系(CRL 1740、ATCC、Rockville,MD)の溶解物を90分間175ボルトのSDSポリアクリルアミドゲルにかける。電気泳動タンパク質をイモビロン(Immobilon)-P(商標)メンブランに対してエレクトロブロッティングし、そのメンブランを、トリス緩衝生理食塩水中5%のBLOTTOで一夜インキュベーションすることによりブロックした。メンブランをバイオラッド(Bio-Rad)マルチスクリーン装置(バイオラッド社)に置き、ハイブリドーマ上清約650μlをそれぞれのレーンにピペットで加えた。メンブランを室温で90分間インキュベーションし、ブロットをトリス緩衝生理食塩水-0.5% Tween-20(TBS-T)で5回洗浄した。洗浄したブロットを、ペルオキシダーゼ標識ヤギ抗マウスIgG(Kirkegaard and Perry Laboratories,Gaithersburg,MD)の1:5,000希釈液と共に室温で1時間インキュベーションした。このブロットを上記のように5回洗浄し、2mlのLumiGLO(商標)化学発光基質(KPL,Gaithersburg,MD)と共に1分間インキュベーションした。このブロットをオートラドフィルムに曝露し現像した。陽性のハイブリドーマウェル(抗PSMA反応性)を同定し、さらなる発育(development)用として選択した。
6.1.6 限界希釈クローニング
上記のウェスタンブロットアッセイにおいてPSMAに対する反応性によって同定した陽性一次ハイブリドーマウェルを限界希釈法によりクローニングした。クローニングした細胞を、フィーダー細胞集団としての相乗的な胸腺細胞を含有する完全細胞培地の1mlにつき1個となるよう調整する。細胞懸濁液を96ウェルプレートのウェルに加えて200μlずつのアリコートを作る。7〜10日間培養した後、細胞のコロニーが見えてくる。単一コロニーを含むウェルを取り、その細胞を24ウェルプレートに広げる(1.5ml培養液)。クローン細胞の上清を得て、上記ウェスタンブロットアッセイにより抗PSMA抗体について試験を行う。陽性クローンを拡大増殖(expand)し液体窒素で凍結する。
6.1.7 腹水液の発生と抗体精製
10 x 106のハイブリドーマ細胞を注入する7〜8日前に、プリスタン0.4mlを腹腔内注射することによりBALB/cマウスを初回抗原刺激を行った。モノクローナル抗体を含有する腹水液を一定時間毎に抜き取って4℃で保存する。ピアース社(Rockford,IL)のImmunoPureTM IgM精製キットを用いて、腹水液からモノクローナル抗体を精製した。
6.1.8 PSMAの免疫沈降
約10 x 106のLNCaP腫瘍細胞を、4℃で30分間、1mlのNP-40細胞融解緩衝液(150mM NaCl、1% NP-40、50mM Tris)と共にインキュベーションした。細胞溶解物を12,000rpmで遠心分離し、得られた上清を正常マウス血清50μlと共に30分間インキュベーションした後で抗マウスIgMアガロースビーズの20%懸濁液60μlを添加することによって予め澄明にした(precleared)。4℃で1時間インキュベーションを行った後、この調製物を遠心分離してビーズを除き、得られた上清を3F5.4G6モノクローナル抗体と反応させた。3F5.4G6モノクローナル抗体の量を変えて(2.5、5および10μg)3個の複製細胞溶解物(replicate lysate)に加え、4℃で1時間インキュベーションした。抗マウスIgMアガロースビーズ(シグマ社)の10%懸濁液100μlを加え、細胞溶解物をさらに1時間4℃でインキュベーションした。12,000rpmで溶解物を遠心分離して、アガロースビーズをNP-40細胞融解緩衝液で3回洗浄する。電気泳動サンプル緩衝液30μlを該sビーズに加え、95℃で10分間加熱する。1,200rpmでビーズを簡単に遠心分離して、サンプル緩衝液をSDSポリアクリルアミドゲルに流した。電気泳動後、サンプルを上記のようにエレクトロブロッティングに付し、リポート抗体としてPSMA特異的モノクローナル抗体7E11-C5を使用してウェスタンブロットを行った。
6.1.9 フローサイトメトリーによる分析
まず細胞を燐酸緩衝化生理食塩水(PBS)で濯いだ。Versene(0.2g EDTA.4Na/L)溶液(75cm2フラスコにつき2ml)を加えた。Versene溶液の大部分は、室温で5分間インキュベーションする前にアスピレーションにより除去した。PBSを加えて、ピペッティングにより細胞を移した(dislodge)。細胞をPBSで2回洗浄した後計数した。50万個〜100万個の細胞を、50μlの一次抗体と共に30分間氷上でインキュベーションした後、PBSで2回洗浄した。次いで細胞を、50μlのFITC標識二次抗体(7E11-C5に対するヤギ抗マウスIgGまたは4G6に対するヤギ抗マウスIgG)と共に30分間氷上でインキュベーションした。過剰の二次抗体をPBSで細胞を洗い流す。フローサイトメーター(FACScan,Becton Dickinson,San Jose,CA)を使って蛍光を分析した。その前散乱プロファイルおよび横散乱プロファイルに基づいて分析した細胞集団から細胞破片を除いた。
6.1.10 ウェスタンブロットによる血清分析
血清サンプルを細胞融解緩衝液(1%トリトンX-100、50mM HEPES、10%グリセロール、15mM MgCl2、1mM AEBSF、1mM EGTA)で1:7に希釈した。LNCaP溶解物を溶解緩衝液で1:35に希釈した。次いで希釈したサンプルをサンプル緩衝液(SDS還元緩衝液)と2:3の割合で合せた。サンプル(20μl)を8.5%のSDS-PAGE(Bio-Rad Protein Assayを用いて測定した場合、最終タンパク質濃度93mg/サンプル)にかけ、分離したタンパク質を90ボルトで1時間、PVDFメンブラン上にブロットした。次いでメンブランを5%ミルク-TBS中で一夜ブロックした。翌日、TBS-T中1時間メンブランを3μg/mlの7E11-C5抗体でプローブし、TBS-T中で5分間5回洗浄し、TBS-T中30分間167ng/mlのヒツジ抗マウス西洋ワサビペルオキシダーゼ標識二次抗体でプローブした。再びメンブランをそれぞれTBS-T中各5分間5回洗浄し、化学発光基質キット(Kirkegaard & Perry Laboratories,Inc.,Gaithersburg,MD)(Rochon et al.,1994,The Prostate 25: 219-223)を用いて、メンブランを展開(develop)した。
X線フィルムを曝露することによりブロットを可視化し、約120kDのタンパク質バンドを見えるようにした。ブロット像をマイクロテックスキャンメーカーIIHRスキャナーでスキャンし、「公共領域の国立衛生研究所(NIH)画像プログラム(Wayne Rasbandが米国立衛生研究所で書いたもので、zippy.nimh.nih.govから作者不明のftpによりインターメットから、またはNTIS,5285 Port Royal Rd.,Springfield,VA22161,part number PB93-504868からのフロッピーディスクで入手可能)を使うマッキントッシュクアドラ(Macintosh Quadra)605コンピューターで行う分析」によって、バンド強度を測定した。全患者サンプルを、健常者の正常ドナーサンプルおよび、標準対照として同じウェスタンブロットから、高いPSMAをもつ前立腺癌患者サンプルに対して評価した。
6.1.11 PSM’酵素活性の検出
妊娠試験のためのWHOガイドラインに従って報酬を支払ったドナーからヒト精液100mlを採取した。10,000rpmで30分間遠心分離して細胞物質をペレット化し、上清を注意深く除いて、2回取り替えたpH7.6の20mM Tris緩衝液に対して一夜透析した。透析液を再び10,000rpmで遠心分離し、予めpH7.6の20mM Tris緩衝液で洗浄しておいたDEAEセファクリルカラムに流した。次いでこのカラムを再び500mlの同じ緩衝液で洗浄し、pH7.6で20mM〜200mMのTris緩衝液勾配を適用したタンパク質を分離した。5mlの画分を集めた。モノクローナル抗体7E11-C5を使って、各画分におけるPSMAの存在をウェスタンドットブロットにより測定した。7E11-C反応性タンパク質バンドを含有する画分をプールし、70%硫酸アンモニウムを用いて沈澱させた。沈澱したタンパク質を10,000rpmで30分間遠心分離してペレット化した後、200mMのTris緩衝液、pH7.6、1リットルの再懸濁させた。次いで、溶解したタンパク質を、2回取り替えたpH7.6の20mM Tris緩衝液に対して一夜透析した。透析物を次いで予め洗浄しておいたセファクリルカラムに流してタンパク質を溶出し、3mlの画分を集めた。モノクローナル抗体3F5.4G6を使って、溶出タンパク質についてウェスタンドットブロットを行った。画分88-96が陽性であり、これら画分のそれぞれは、SDSポリアクリルアミドゲル電気泳動により、その純度について試験した。
6.2. 結果
PSMAの細胞外ドメインに対するモノクローナル抗体を生成するために、このタンパク質のいくつかの領域をそれらの相対親水性に関してHopp & Woods法(1983,Mol.Immunol.20:483-489)に基づいて分析した。
以下の表1は、試験した数種類のペプチドの相対親水性を示す。特に、PSMAのC末端領域中のアミノ酸残基番号716-723に対応するESKVDPSK(Glu-Ser-Lys-Val-Asp-Pro-Ser-Lys)(配列番号1)の配列をもつペプチドを合成した。さらに、細胞外ドメインに対する抗体を産生するために、表1に示した細胞外ドメインの他の部分や全細胞外ドメインそのものも使用できるだろう。これとは対照的に、残基#44-58および#196-213に対応する2つのアミノ酸ペプチドは、天然PSMAと結合しない抗ペプチド抗体応答をもたらした。
免疫を行う前に、最初に担体としてのKLHにペプチドESKVDPSK(配列番号1)を結合させた。次に、マウスをこの結合体で免疫し、同じ結合体を用いて週1回の間隔で追加免疫した。検出可能な抗ペプチド血清力価を示した動物の脾臓を摘出し、ミエローマ細胞に融合させた。
抗原としてペプチド結合BSAを用いて結合アッセイにより初期スクリーニングを実施いた。個々のハイブリドーマ培養物から細胞培養上清50μlを分離し、ペプチド特異的ラジオイムノアッセイでペプチド特異的抗体の存在について試験した。簡単に述べると、ウシ血清アルブミン(BSA)に結合させたペプチドを予めコーティングしておいた96ウェルのPro-Bindプレートのウェルに上清を添加した。4℃で一夜インキュベーションした後、プレートをPBSで洗った。1:500の希釈度のウサギ抗マウスIgMおよびIgG 50μlを各ウェルに添加し、プレートを室温で1時間インキュベートした。その後プレートを4回洗浄し、125I標識プロテインAを各ウェルに添加した。プレートを室温で1時間インキュベートし、上記のように4回洗浄した。プレートをオートラッドフィルムに一夜露光して現像した。陽性のウェルを選択し、以後の試験のために細胞を培地中で増やした。同定された陽性ウェルのうち、3F5と称する一つのハイブリドーマをウエスタンブロットアッセイでさらに試験したところ、その分泌抗体はLNCaP溶解物中に含まれるPSMAと反応することがわかった。LNCaP細胞をHoroszewiczら(1983,Cancer Res.43:1809-1818)が記載したとおりに培養し、細胞溶解物をRochonら(1994,Prostate 25:219-223)が記載したとおりに調製した。3F5ハイブリドーマ細胞を限界希釈法によりクローニングし、細胞数を増やし、ウエスタンブロットアッセイで再試験した。3F5.4G6と称する抗体のサブクローンはLNCaP溶解物中の分子量120kDaのタンパク質と反応した(図2)。この抗体はIgMとしてアイソタイピングされた。3F5.4G6のアイソタイプの決定には、Boehringer Mannheimから得られた、マウスモノクローナル抗体のアイソタイピング用のISOStripを用いた。モノクローナル抗体をPBSで1:100に希釈し、希釈サンプル(150μl)をこのキットと共に供給された展開チューブに添加し、室温で30秒インキュベートした後しばらく攪拌した。次いでチューブの中にアイソタイプストリップを挿入し、5分間展開した。このストリップのラムダまたはカッパセクションおよびクラスまたはサブクラスセクションの一つに青色のバンドが出現した。モノクローナル抗体3F5.4G6はIgMアイソタイプであると同定された。
さらに、モノクローナル抗体3F5.4G6は、対照としてモノクローナル抗体7E11-C5を用いて、ステージD2の進行中の前立腺癌患者から採取した血清に対して試験した(図3)。両抗体とも約120kDa分子量のバンドを同定した(図3)。3F5.4G6モノクローナル抗体を用いるLNCaP細胞の追加のウエスタンブロットアッセイを、IgMに特異的な二次抗体を用いて行った(図4)。モノクローナル抗体7E11-C5は約120kDaの単一バンド(すなわち、PSMA)を認識したが、3F5.4G6は同様の分子量バンドだけでなく約105-110kDaのバンドも認識した。このバンドはPSM’の想定されたタンパク質形態に一致しており、PSMAとPSM’の両方の細胞外ドメインを特異的に認識する抗体の有用性を示す。
7E11-C5と前立腺癌患者の血清中の120kDaのタンパク質との反応性は抗体特異的であり、一般的な血清タンパク質と二次抗体との非特異的な反応性によるものでなかった。ウエスタンブロットアッセイでは、血清サンプル由来の分離したタンパク質を含むImmobilon P紙を、7E11-C5モノクローナル抗体+HRPに結合させた二次抗体と、またはHRPに結合させた二次抗体のみに反応させた。フィルムを1分間露光し、また、二次抗体と血清中の120kDaのタンパク質との非反応性を実証するために45分にわたり過度に露光した。さらに、この二次抗体を3F5.4G6と共に使用して同抗原を検出した。したがって、3F5.4G6モノクローナル抗体はPSMAとPSM’に特異的であった。
図5から、7E11-C5により同定されたタンパク質はモノクローナル抗体3F5.4G6によっても認識されたことが裏づけられる。さらに、モノクローナル抗体3F5.4G6は、モノクローナル抗体7E11-C5により検出されない105-110kDaのタンパク質をも認識した。この比較的速く泳動するタンパク質はPSM’に相当する。溶解物を最初に7E11-C5で沈殿させ、残りのタンパク質を7E11-C5と反応させたとき、この抗体はどのようなタンパク質も検出しなかった(レーン4)。これに対して、7E11-C5で前処理した溶解物を3F5.4G6と反応させたときには、この抗体は約110kDaのタンパク質を検出した。図6は、3F5.4G6により免疫沈降された120kDaタンパク質(すなわち、PSMA)が7E11-C5によっても認識されたことを示す。
図7AおよびBは、FACS分析でモノクローナル抗体3F5.4G6が生存LNCaP細胞を認識したことを示しており、これにより3F5.4G6はPSMAの細胞外ドメインを認識することが確認される。PSMAの細胞外ドメインを認識する抗体は前立腺癌における診断および/または治療ツールとして特に有用である。
ヒト精液をPSMA特異的抗体と反応させて、酵素活性についてアッセイした。図8は、レーン2のモノクローナル抗体3F5.4G6により認識されたタンパク質はおよその分子量が90kDaであることを示す。PSM’はLNCaP溶解物中で105-110kDaの分子量をもつことがわかったが、精液中の90kDaタンパク質はPSM’の非グリコシル化または部分グリコシル化産物であるらしかった。PSM’はいくつかのグリコシル化部位を含むので、この低い分子量は精液中のグリコシダーゼ活性の結果であった。PSMAがこの精製調製物中に存在しないことは、3F5.4G6がLNCaP細胞の溶解物中に存在する分子量120kDaのタンパク質(すなわち、PSMA)を認識した(レーン1)が、レーン2ではこの分子量のタンパク質を認識しなかったという事実から明らかである。さらに、抗体7E11-C5は精液中の90kDaバンドを認識しなかった。
その後、モノクローナル抗体3F5.4G6により認識されたPSM’のこの精製調製物をNAALADase活性についてアッセイした。LNCaP溶解物から調製した高速上清を陽性対照として用いた。3F5.4G6モノクローナル抗体と陽性に反応するタンパク質であって、それがPSM’であることと一致するタンパク質は、Robinsonら(1987,J.Biol.Chem.262:14498-14506)により記載されたアッセイを行ったところ、16.9nmol/min./mgタンパク質の固有のNAALADase活性を含んでいた。
7. 実施例:PSMA含有腫瘍細胞膜調製物に対するモノクローナル抗体の産生
7.1 材料と方法
7.1.1 免疫
2枚の150mmプレートからLNCaP膜を調製するにあたり、versene溶液中に細胞を分離し、遠心して細胞をペレットとした。細胞ペレットに蒸留水を添加し、Dounce型ホモジナイザーを用いて細胞をホモジナイズした。ホモジナイズした懸濁液を30,000×gで遠心し、ペレット化した膜画分を免疫用に用いた。
完全フロイントアジュバントで乳化したLNCaP前立腺癌細胞膜調製物を用いて成熟雌BALB/cマウスを4回、腹腔内投与により免疫した。細胞融合を行う5日前に、イムノアフィニティーで精製したPSMA(PBS中)50μgを用いてマウスを追加免疫した。細胞融合は上記の第6.1.3節に記載のとおり行った。
7.1.2 一次ハイブリドーマのスクリーニング
固相ELISA法をベースとするアッセイ法によりPSMA特異的抗体の検出を行った。イムノアフィニティーで精製したPSMA、バキュロウイルスで発現させた完全長のPSMA、あるいは細菌で発現させたPSMA断片をMaxi-Sorp(NuncImmuno)96ウェルプレート上にコートし、4℃で一晩インキュベートした。プレートをPBS-0.2% Tween-20で洗い、残存したサイトを5% BSA溶液を用い1時間室温でブロックした。ハイブリドーマ培養物からの上清50μlをPSMAをコートしたウェルに添加し、そのプレートを室温で2時間インキュベートした。プレートを上述の方法で洗い、1:600希釈したウサギ抗マウスIgG及びウサギ抗マウスIgMを50μl各ウェルに添加した。室温で1時間インキュベートした後、プレートを上述の方法で洗い。1:400希釈のHRPを結合させたProtein-A 50μlを各ウェルに添加した。室温で1時間インキュベートした後、プレートを上述の方法で洗い、100μlのABTS(2,2’-アジノ-ビス(3-エチルベンズチアゾリン)-6-スルホン酸150mgを0.1Mのクエン酸500ml,pH4.35中に含有する)/過酸化水素(10mlのABTS溶液あたり10μlの30%H2O2を含有)色原体/基質溶液を各ウェルに添加した。プレートをマイクロプレートリーダーで読みとり、OD405を測定した。OD値がバックグラウンド値より0.05高い値を示した上清を産生するハイブリドーマを限界希釈法でクローン化し、それ以後の分析に用いた。
PSMAの固相への捕捉のために上述のアッセイ法を次のように改変した:40μg/mlの7E11-C5抗PSMAモノクローナル抗体溶液(0.1M NaHCO3結合緩衝液pH8.2中)50μlを、Maxi-Sorpプレートのウェルに添加し、4℃で一晩付着させた。プレートを上述の方法で洗い、ブロックした。階段希釈したイムノアフィニティー精製PSMA 50μlを、7E11-C5をコートしたウェルに添加し、室温で2時間インキュベートした。十分に洗った後、3D7-1.1あるいは4E10-1.14ハイブリドーマクローンから得た50μlの無希釈の組織培養上清をウェルに添加し、プレートを室温で90分間インキュベートした。上述の方法で洗った後、ウェルを1:1000希釈のペルオキシダーゼを結合させたヤギ抗マウスIgM 50μlと反応させ、室温で1時間インキュベートした。十分洗った後、ABTS/H2O2を100μl各ウェルに添加し、プレートをマイクロプレートリーダーで上述の方法で読み取った。
7.1.3 PSMAのイムノアフィニティーによる精製
パックされたLNCaP細胞16mlを、5倍容量の25mM Tris-HCl,pH7.4、150mM NaCl、1% NP-40中でPotter-Elvehjem型ホモジナイザーを2往復させてホモジナイズした後、4℃で一晩攪拌した。抽出液を100,000×gで1時間遠心し、さらにペレットから初回同様に再抽出を行った。上清をあわせ、冷室で一晩7E11-C5-Immunobeads(Pierce)(3-5ml樹脂ベッド容積)と混合した。ビーズを遠心し、ホモジナイズ用緩衝液で十分洗い、カラムに注入した。ビーズを再度1%NP-40含有のホモジナイズ用緩衝液で洗った後、1%Triton-X-100R含有の緩衝液で再度洗った。洗浄後のビーズを100mMのグリシン緩衝液pH2.5、150mM NaCl、1% Triton X-100Rで溶出し、2ml画分を集めた。タンパク質の溶出はOD280でモニターした。
タンパク質を含有する画分をSDS-PAGゲルで銀染色及びウエスタンブロッティング法を用いて分析した。典型的な調製物においては、ウエスタンブロッティング法で7E11-C5反応性の120kDaのタンパク質のバンドは60-80%の純度であった。パックされた細胞16mlからのおよその収率は、PSMAタンパク質1mgであった。PSMA調製物中の界面活性剤は、溶液をExtractigelカラム(Pierce)に通すことによって除去した。
7.1.4 フローサイトメトリー分析
PSMAの外部つまり細胞外にあるエピトープに対するモノクローナル抗体の認識能をフローサイトメトリーで評価した。LNCaP(PSMA発現)及びPC-3細胞(PSMA非発現)を組織培養フラスコから新たに採取し、単細胞懸濁液を調製した。約100万個の細胞を、3D7-1.1あるいは4E10-1.14ハイブリドーマクローンから得た無希釈組織培養上清1ml中に再懸濁し、氷上で2時間インキュベートした。細胞をPBS-0.1% BSA,0.01%アジ化ナトリウムで2回洗い、1:100希釈のFITCを結合させたウサギ抗マウスIgM 100μl中に再懸濁し、氷上でさらに30分間インキュベートした。細胞を上述の方法で2回洗い、500μlの洗浄用緩衝液に再懸濁し、蛍光染色をFACSCalibur(Becton-Dickinson)を用い、CellQuest acquisitionソフトウエアで分析した。
7.1.5 ウエスタンブロット分析
3D7-1.1及び4E10-1.14ハイブリドーマクローンから得た組織培養上清のPSMA反応性をウエスタンブロット分析で調べた。ウエスタンブロット分析はPelletierとBoyntonのプロトコール(1994,J.Cell.Physiol.158:427-434)に従って行った。その概略は次のとおりである。LNCaP細胞及びPC-3細胞から得た溶解物、イムノアフィニティー精製PSMA、あるいはバキュロウイルス発現完全長PSMAを8.5% SDS-PAGEゲル上で電気泳動させ、分離したタンパク質をPVDF膜上に90ボルトで1時間電気的にブロッティングした。その膜を5% BLOTTO中で一晩ブロックし、適切なクローンから得た無希釈組織培養上清20mlと90分間インキュベートした。上清を除去し、ブロットをTBS-0.5% Tween-20(TBS-T)で5回洗い、1:5000希釈のペルオキシダーゼを結合させたヤギ抗マウスIgM二次抗体(Jackson)と室温で1時間反応させた。その膜をTBS-Tで5回洗い、Chemiluminescent Substrate Kit(KPL)を用いて展開し、X線フィルム(Kodak)に露光させることによって可視化した。
7.1.6 バキュロウイルス発現系を用いた組換えPSMAの調製
PSMAの完全長コード配列(Israeliら,1993,Cancer Res.53:227-230)を含むインサートを、Lambda pDR2ヒトライブラリー(Clonetech)からその遺伝子配列に特異的なプローブを用いてクローン化した。インサートはこのベクターからSmaI及びSspI消化によって切り出し、トランスファーベクターpAcHLT-C(Pharmingen)中に、製造者の説明書に従ってクローン化した。このトランスファーベクターとBacPAK6直線化ウイルスDNA(Clonetech)の同時トランスフェクションは製造者の説明書に従って行い、その結果、Ni-NTAカラムとの結合によってタンパク質単離に用いうるポリヒスチジンテールをタンパク質のN末端に持つ完全長PSMAタンパク質をコードするウイルスが得られた。PSMAタンパク質を産生させるために、プラーク精製した組換えバキュロウイルス粒子を単離、増幅し、5% FBS(Hyclone)を補給したSFM II培地(Gibco-BRI)の存在下でSf9細胞に、感染の多重度を約1:2として感染させた。48時間インキュベーションした後、感染細胞を採取し、1%CHAPSで溶解し、Ni-NTA-アガロース(Quiagen)を通し、製造者の説明書に従ってイミダゾールで溶出させることにより回収した。最終産物を1LのPBSに対して3回透析した。
7.2 結果
PSMA含有前立腺癌細胞膜に対するモノクローナル抗体を作製した。LNCaP細胞からイムノアフィニティー精製した天然PSMA、及びアミノ酸配列の1-175、134-437、438-750の領域に対応する細菌で発現させたPSMAの断片を用いて固相イムノアッセイで、2種のハイブリドーマクローン、3D7-1.1及び4E10-1.14を選択した。天然PSMAとの結合性において、3D7-1.1及び4E10-1.14ハイブリドーマクローンから得た上清は7E11-C5抗体と比肩しうるものであった(図9)。バックグラウンドのBSAに対する非特異的結合は基本的には3種の抗体調製物とも同様であった。
エピトープとの結合の特異性を調べると、7E11-C5モノクローナル抗体は、PSMのN末端で細胞内ドメインに対応するアミノ酸断片1-175に結合した。3D7-1.1及び4E10-1.14はこの断片に対して中等度の結合しか示さなかったが、これら2種のモノクローナル抗体はPSMAのアミノ酸断片134-437(この断片はPSMAの細胞外ドメインの一部である)に最も強い結合性を示した。この断片はPSM’の一部であるので、これらの抗体はPSM’とも反応する。
さらに、3D7-1.1ハイブリドーマクローンから得た上清について、LNCaP細胞及びPC-3細胞の溶解物、及びイムノアフィニティー精製PSMAに対してのウエスタンブロット分析を行った。図10は3D7-1.1ハイブリドーマクローンがLNCaP細胞(レーン1)に存在する120kDaバンドとは反応するが、PC-3細胞(レーン2)とは反応しないことを示している。レーン1及び2のどちらも、おそらく二次抗体試薬の非特異的結合のためと思われる反応性を示している。イムノアフィニティー精製PSMAを含むレーン3は3D7-1.1モノクローナル抗体と反応させたとき120kDaに主要なバンドを示している。同様なウエスタンブロットデータが、ブロットの非特異的バックグラウンドは3D7-1.1の場合よりはるかに大きいとはいえ、4E10-1.14クローンの上清でも得られている。このように、3D7-1.1及び4E10-1.14のどちらも、LNCaP細胞に存在する120kDaバンド及びイムノアフィニティー精製PSMAと反応する。
バキュロウイルスで発現させた完全長のPSMAをSDS-PAGEゲル上で電気泳動し、PVDF膜に電気的にブロッティングした。ブロットをMuni-Protean II Milti-Screen装置(Bio-Rad)に挿入し、各種の抗体調製物と反応させ、ウエスタンブロットとして発現させた。図11は3D7-1.1及び4E10-1.14モノクローナル抗体が、7E11-C5モノクローナル抗体が結合するのと同じバンドに対応するタンパク質のバンドと反応したことを示している。
LNCaP細胞及びPC-3細胞を3D7-1.1及び4E10-1.14ハイブリドーマクローンから得た上清で染色し、フローサイトメトリーで分析した。2種の抗体のどちらも非同定のLNCaP生細胞を染色したが、PC-3細胞は染色しなかった(図12A-D)。これらの結果から、2種の抗体がPSMA分子の細胞外ドメインのエピトープと反応することを確認した。さらに、LNCaP染色において、3D7-1.1で見られたショルダーと比較して、4E10-1.14モノクローナル抗体では明らかなシフトが認められたが、これは2種の抗体がPSMA分子の特定の領域の異なるエピトープを認識することを示唆している。
PSMAのための二部位捕捉ELISA(two-site capture ELISA)を、7E11-C5モノクローナル抗体をPSMA捕捉試薬として、3D7-1.1及び4E10-1.14モノクローナル抗体をレポーターあるいは検出抗体として用いて開発した。これらの抗体はPSMA分子の異なるエピトープを認識するため(7E11-C5はN末端の6個のアミノ酸と反応し、3D7-1.1及び4E10-1.14は134-475アミノ酸領域内の一つの配列と反応する)、二部位捕捉アッセイにおいては効果的な組み合わせとなる。イムノアフィニティー精製PSMAを階段希釈したものを試験抗原として用いたとき、3D7-1.1と4E10-1.14のどちらの上清も、7E11-C5をコートした96ウェルプレート上での捕捉後、PSMAを検出し得た(図13)。さらに、LNCaP細胞及び精液から精製したPSMA及びバキュロウイルスで発現させた完全長PSMAの粗調製物を試験した(図14)。PSMA対照抗原、精液、及びバキュロウイルスPSMA調製物では有意に大きいOD405値が得られた。精製PSMAを正常ヒト女性の血清で希釈し、サンプルを二部位捕捉アッセイで調べると、上記と同じ抗体がPSMAを検出した(図15)。PSMAの異なる部分に対するモノクローナル抗体を用いて開発した二部位捕捉アッセイは多様なソースから抗原特異的な様式でPSMAを検出した。
PSMA用の二部位捕捉ELISAとしてもう一つ別の方法を3D7-1.1モノクローナル抗体をPSMA捕捉試薬として、7E11-C5モノクローナル抗体をレポーター又は検出試薬として開発した。階段希釈したイムノアフィニティー精製PSMAを試験抗原として用い、3D7-1.1をコートしたプレートで捕捉させ、ビオチン化した7E11-C5モノクローナル抗体を用いて検出した。結果は図16に示す。
図16は3D7-1.1や4E10-1.14などのPSMAの細胞外ドメインと特異的に結合するモノクローナル抗体が、PSMAの二部位捕捉ELISAに有用であることを示している。
PSMAの捕捉に3D7-1.1が有用であることは、PSMAタンパク質の細胞外ドメインのみに依存したもう一つ別のイムノアッセイが使用しうることを示している。そのような2種の細胞外ドメイン特異的抗体を捕捉及び検出に用いるアッセイは、PSM’のエピトープのタンパク質内での位置からみてPSM’を検出しうるであろう。7E11-C5を捕捉又は検出のどちらかに用いたアッセイはどんなものでも特異的にPSM’を除外する。PSM’に特異的なアッセイの1例としては、3D7-1.1又はPSMAの細胞外ドメインに特異的なモノクローナル抗体のうちの1種の抗体をPSMA及びPSM’の捕捉に用いて平行試験を行うものが挙げられる。それに引き続き、4E10-1.14をPSMAとPSM’を合計したものの検出に用い、7E11-C5をPSMAのみの検出に用いることにより、PSM’の量は単純な引き算によって得られる。このデータからPSM’とPSMAの比率が求められ、それはSuら(Cancer Res.55:1141-1443,1995)の観点によれば診断に用いうるものとなろう。
SuはPSMAをコードする転写物が前立腺癌患者で選択的によく検出される(正常男性と比べて)ことを示しているが、SuらはPSMA転写物がこれらの患者の体内で実際にタンパク質に翻訳されているかどうかは示していない。さらに、SuはPSM’タンパク質を検出してはいないが、PSM’をコードする転写物が正常男性に選択的によく検出される(前立腺癌患者に比べて)ことを示している。本発明者らは、本出願において、PSMAタンパク質が前立腺癌患者の体の組織及び/又は体液中で(正常男性と比べ)増加していること、及びPSM’タンパク質が正常男性の体の組織及び/又は体液中で(前立腺癌患者と比べ)増加していることを示している。従って、本発明によれば、PSM’のPSMAに対する比は、前立腺癌患者の臨床的評価にあたって、診断上及び/又は予後判定での有用性を有することとなるであろう。
完全長PSMAのアミノ酸34-750に対応するPSMA断片を、バキュロウイルス発現系で1.9kbのインサートとして発現させた。バキュロウイルスで発現させたPSMA断片は、その断片のN末端からPSMA細胞外ドメインのさらに76アミノ酸が欠失していることを除けば、PSM’(完全長PSMAの残基58-750に対応している)と非常に類似している。各種のバキュロウイルス発現させた半精製PSMA断片及びLNCaP細胞溶解物のウエスタンブロット分析を4E10-1.14モノクローナル抗体をプローブとして用いて行った。結果を図17に示す。
1.9kbのPSMA断片(すなわち完全長PSMAのアミノ酸134-750)をコードするインサートあるいは無関係のインサートのどちらかを含むバキュロウイルスを感染させたSF9細胞の粗溶解物のウエスタンブロット分析を、7E11-C5モノクローナル抗体をプローブとして行った。結果を図18に示す。
図17は、PSMAの細胞外ドメインに特異的な4E10-1.14などの抗体が、PSM’に非常に類似したバキュロウイルス発現タンパク質にも結合しうることを示している。これに対して図18は、7E11-C5モノクローナル抗体はそのエピトープ特異性の故にそのような性質を有していないことを示している(図18に示すようにバキュロウイルス発現PSMA断片と7E11-C5との陰性の反応性に注目されたい)。バキュロウイルス発現PSMA断片は、N末端から追加の76アミノ酸(その全てが細胞外ドメインにある)が欠失していることを除けばPSM’(完全長PSMAのアミノ酸58-750に対応)と同一である。3D7-1.1及び4E10-1.14のエピトープ特異性は、PSM’及びPSMAの134-750アミノ酸断片(図9参照)のいずれにも含まれる細胞外ドメインの領域にマップされるので、これらの抗体が双方とも天然のPSM’と結合する固有の特性を持っているであろうと考えられ、これは7E11-C5には無いものである。
LNCaP細胞由来のPSMA、及びPSMAを含むことが知られたヒト血清及び精液のウエスタンブロットのプローブとして3D7-1.1モノクローナル抗体を用いた。結果を図19に示す。
約120kDaに移動するPSMAに対応するバンドが全画分に存在した。さらに、抗体3D7-1.1で現出させた場合には、血清及び精液中に、2番目に速く移動する分子量90から100Kdのバンドが認められた。この速く移動するバンドは血清を7E11-C5抗体を用いた場合のウエスタンブロットには認められなかった(Holmesら,The Prostate,Supple.7:25-29(1996)参照)。この速く移動する、3D7-1.1と反応するタンパク質のバンドはおそらく体液中に存在するPSM’であろう。
8. 細胞系の寄託
次のハイブリドーマ細胞系は1996年3月12日、及び1997年3月11日にAmerican Type Culture Collection,12301 Parklawn Drive,Rockville,Maryland 20852,U.S.A.に寄託され、下記の受託番号の指定を受けた。
ハイブリドーマ ATCC受託番号
3F5.4G6 HB12060
3D7-1.1 HB12309
4E10-1.14 HB12310
本発明は、本発明の個々の態様の説明を意図して例示した実施態様に示される範囲に限定されるものではない。事実、ここに示し、記述した事柄に加えて本発明に種々の改変を加えることは、上記の詳細な説明及び添付図面から当業者であれば自明なことであろう。そのような改変は本発明の特許請求の範囲に包含されるものとする。
本明細書中に引用された全ての公表文献は参照としてその全文を本明細書中に組み込むこととする。
Claims (29)
- 生細胞の表面に発現された天然の前立腺特異的膜抗原(PSMA)の細胞外ドメインに結合する抗原結合領域を有するモノクローナル抗体であって、該抗体が、アミノ酸配列ESKVDPSK(配列番号1)に結合するモノクローナル抗体、ならびにATCC受託番号HB12060を有するハイブリドーマ3F5.4G6、ATCC受託番号HB12309を有するハイブリドーマ3D7-1.1、およびATCC受託番号HB12310を有するハイブリドーマ4E10-1.14により産生されたモノクローナル抗体からなる群から選択される、モノクローナル抗体。
- PSMAの細胞外ドメインが図1(配列番号2)に示した残基番号44から750までのアミノ酸配列を含んでなる、請求項1に記載の抗体。
- ATCC受託番号HB12060、HB12309、またはHB12310を有するハイブリドーマ細胞系。
- 検体を生細胞の表面に発現された天然のPSMAの細胞外ドメインに結合する抗原結合領域を有するモノクローナル抗体と接触させ、該抗体に結合したPSMAを検出することを含んでなる、生物学的検体中のPSMAの存在を検出する方法であって、該抗体が、アミノ酸配列ESKVDPSK(配列番号1)に結合するモノクローナル抗体、ならびにATCC受託番号HB12060を有するハイブリドーマ3F5.4G6、ATCC受託番号HB12309を有するハイブリドーマ3D7-1.1、およびATCC受託番号HB12310を有するハイブリドーマ4E10-1.14により産生されたモノクローナル抗体からなる群から選択される、方法。
- 前記検体が体液、生検材料、尿、または尿中の細胞である、請求項4に記載の方法。
- 前記体液が全血、血清、または精液である、請求項5に記載の方法。
- 前記抗体に結合したPSMAの検出を、PSMAに特異的な二次抗体により行う、請求項4に記載の方法。
- 前記抗体に結合したPSMAの検出を、PSMAの酵素活性により行う、請求項4に記載の方法。
- 前記酵素活性がNAALADaseの活性である、請求項8に記載の方法。
- NAALADase活性がNAD(P)Hの増加により検出される、請求項9に記載の方法。
- 細胞のサンプルを生細胞の表面に発現された天然のPSMAの細胞外ドメインに結合する抗原結合領域を有するモノクローナル抗体と接触させ、該抗体に結合したPSMAを検出することを含んでなる、癌細胞により発現されたPSMAの存在を検出する方法であって、該抗体が、アミノ酸配列ESKVDPSK(配列番号1)に結合するモノクローナル抗体、ならびにATCC受託番号HB12060を有するハイブリドーマ3F5.4G6、ATCC受託番号HB12309を有するハイブリドーマ3D7-1.1、およびATCC受託番号HB12310を有するハイブリドーマ4E10-1.14により産生されたモノクローナル抗体からなる群から選択される、方法。
- 前記抗体がラジオアイソトープに結合されている、請求項11に記載の方法。
- ATCC受託番号HB12060を有するハイブリドーマ3F5.4G6、ATCC受託番号HB12309を有するハイブリドーマ3D7-1.1、またはATCC受託番号HB12310を有するハイブリドーマ4E10-1.14により産生されるモノクローナル抗体の抗原結合部位をコードする単離されたヌクレオチド配列を含む核酸。
- 検体を生細胞の表面に発現された天然のPSMAの細胞外ドメインに結合する抗原結合領域を有するモノクローナル抗体と接触させ、該抗体に結合したPSM’を検出することを含んでなる、生物学的検体中のPSM’タンパク質の存在を検出する方法であって、該抗体が、アミノ酸配列ESKVDPSK(配列番号1)に結合するモノクローナル抗体、ならびにATCC受託番号HB12060を有するハイブリドーマ3F5.4G6、ATCC受託番号HB12309を有するハイブリドーマ3D7-1.1、およびATCC受託番号HB12310を有するハイブリドーマ4E10-1.14により産生されたモノクローナル抗体からなる群から選択される、方法。
- 前記検体が体液、生検材料、尿、または尿中の細胞である、請求項14に記載の方法。
- 前記体液が全血、血清、または精液である、請求項15に記載の方法。
- 前記抗体に結合したPSM’の検出を、PSM’に特異的な二次抗体により行う、請求項14に記載の方法。
- 前記抗体に結合したPSM’の検出を酵素活性により行う、請求項17に記載の方法。
- 前記酵素活性がNAALADaseの活性である、請求項18に記載の方法。
- NAALADase活性がNAD(P)Hの増加により検出される、請求項19に記載の方法。
- 前立腺癌を治療するための医薬の製造における、生細胞の表面に発現された天然の前立腺特異的膜抗原の細胞外ドメインに結合する抗原結合領域を有するモノクローナル抗体の使用であって、該抗体が、アミノ酸配列ESKVDPSK(配列番号1)に結合するモノクローナル抗体、ならびにATCC受託番号HB12060を有するハイブリドーマ3F5.4G6、ATCC受託番号HB12309を有するハイブリドーマ3D7-1.1、およびATCC受託番号HB12310を有するハイブリドーマ4E10-1.14により産生されたモノクローナル抗体からなる群から選択される、使用。
- 前記抗体が薬剤と結合している、請求項21に記載の使用。
- 前記抗体がトキシンと結合している、請求項21に記載の使用。
- 前記抗体がラジオアイソトープと結合している、請求項21に記載の使用。
- 前記のモノクローナル抗体が二重特異的抗体であり、殺腫瘍または腫瘍抑制活性を有するエフェクター細胞に対して特異的な抗原結合領域をさらに含む、請求項21に記載の使用。
- 請求項1または2に記載のモノクローナル抗体またはその結合性断片を含んでなる、前立腺癌を診断、予後判定またはモニターするためのキット。
- 前記抗体またはその断片が水性媒体中にまたは凍結乾燥形態でパッケージされている、請求項26に記載のキット。
- PSMAに特異的な二次抗体をさらに含む、請求項26に記載のキット。
- グルタミン酸デヒドロゲナーゼをさらに含む、請求項26に記載のキット。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US62139996A | 1996-03-25 | 1996-03-25 | |
| US08/621,399 | 1996-03-25 | ||
| PCT/US1997/005214 WO1997035616A1 (en) | 1996-03-25 | 1997-03-25 | Monoclonal antibodies specific for the extracellular domain of prostate specific membrane antigen |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2001503601A JP2001503601A (ja) | 2001-03-21 |
| JP2001503601A5 JP2001503601A5 (ja) | 2004-12-02 |
| JP4295826B2 true JP4295826B2 (ja) | 2009-07-15 |
Family
ID=24490004
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP53466797A Expired - Lifetime JP4295826B2 (ja) | 1996-03-25 | 1997-03-25 | 前立腺特異的膜抗原の細胞外ドメインに対して特異的なモノクローナル抗体 |
Country Status (10)
| Country | Link |
|---|---|
| EP (1) | EP0914155B1 (ja) |
| JP (1) | JP4295826B2 (ja) |
| AT (1) | ATE318147T1 (ja) |
| AU (1) | AU725583B2 (ja) |
| CA (1) | CA2250141C (ja) |
| DE (1) | DE69735294T2 (ja) |
| DK (1) | DK0914155T3 (ja) |
| ES (1) | ES2260788T3 (ja) |
| IL (1) | IL126314A (ja) |
| WO (1) | WO1997035616A1 (ja) |
Families Citing this family (53)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7070782B1 (en) | 1992-11-05 | 2006-07-04 | Sloan-Kettering Institute For Cancer Research | Prostate-specific membrane antigen |
| US6953668B1 (en) | 1992-11-05 | 2005-10-11 | Sloan-Kettering Institute For Cancer Research | Prostate-specific membrane antigen |
| US7105159B1 (en) | 1992-11-05 | 2006-09-12 | Sloan-Kettering Institute For Cancer Research | Antibodies to prostate-specific membrane antigen |
| US6569432B1 (en) | 1995-02-24 | 2003-05-27 | Sloan-Kettering Institute For Cancer Research | Prostate-specific membrane antigen and uses thereof |
| DE69635801T2 (de) | 1995-02-24 | 2006-11-02 | Sloan-Kettering Institute For Cancer Research | Prostataspezifisches membranes antigen und seine anwendungen |
| US6150508A (en) * | 1996-03-25 | 2000-11-21 | Northwest Biotherapeutics, Inc. | Monoclonal antibodies specific for the extracellular domain of prostate-specific membrane antigen |
| US6962981B1 (en) | 1996-03-25 | 2005-11-08 | Medarex, Inc. | Monoclonal antibodies specific for the extracellular domain of prostate-specific membrane antigen |
| US7381407B1 (en) | 1996-03-25 | 2008-06-03 | Medarex, Inc. | Monoclonal antibodies specific for the extracellular domain of prostate-specific membrane antigen |
| US6136311A (en) | 1996-05-06 | 2000-10-24 | Cornell Research Foundation, Inc. | Treatment and diagnosis of cancer |
| US6107090A (en) | 1996-05-06 | 2000-08-22 | Cornell Research Foundation, Inc. | Treatment and diagnosis of prostate cancer with antibodies to extracellur PSMA domains |
| US6207805B1 (en) | 1997-07-18 | 2001-03-27 | University Of Iowa Research Foundation | Prostate cell surface antigen-specific antibodies |
| GB2328871A (en) * | 1997-09-05 | 1999-03-10 | Merck & Co Inc | Compositions for inhibiting platelet aggregation |
| WO1999043710A1 (en) * | 1998-02-26 | 1999-09-02 | Beckman Coulter, Inc. | Prostate-specific membrane antigens and methods of making and using |
| ES2329851T3 (es) * | 1998-06-01 | 2009-12-01 | Agensys, Inc. | Nuevos antigenos transmembranables expresados en canceres humano y utilizacion de los mismos. |
| US20030035798A1 (en) * | 2000-08-16 | 2003-02-20 | Fang Fang | Humanized antibodies |
| SE9900495D0 (sv) * | 1999-02-12 | 1999-02-12 | Pharmatrix Ab | Vaccine composition |
| WO2000050457A1 (en) * | 1999-02-22 | 2000-08-31 | Beckman Coulter, Inc. | Prostate-specific membrane antigens and methods of making and using |
| KR100733933B1 (ko) * | 1999-07-29 | 2007-07-03 | 메다렉스, 인코포레이티드 | 전립선 특이적 막 항원에 대한 인간 모노클로날 항체 |
| EP1710256A1 (en) * | 1999-07-29 | 2006-10-11 | Medarex, Inc. | Human monoclonal antibodies to prostate specific membrane antigen |
| FR2797743B1 (fr) * | 1999-08-23 | 2003-08-08 | Urogene | Lignee cellulaire prostatique et son utilisation pour l'obtention d'une tumeur prostatique etablie chez l'animal |
| US6653129B1 (en) * | 1999-09-13 | 2003-11-25 | The Regents Of The University Of Colorado | Method for isolation of cells from a solution |
| JP4838436B2 (ja) * | 2001-04-04 | 2011-12-14 | 積水メディカル株式会社 | 抗ヒト肝性トリグリセリドリパーゼ抗体 |
| EP1392360B1 (en) | 2001-06-01 | 2011-11-30 | Cornell Research Foundation, Inc. | Modified antibodies to prostate-specific membrane antigen and uses thereof |
| IL159422A0 (en) | 2001-09-20 | 2004-06-01 | Cornell Res Foundation Inc | Methods and compositions for treating or preventing skin disorders using binding agents specific for prostate-specific membrane antigen |
| AU2002356844C1 (en) | 2001-10-23 | 2010-03-04 | Amgen Fremont Inc. | PSMA antibodies and protein multimers |
| US20040161776A1 (en) * | 2001-10-23 | 2004-08-19 | Maddon Paul J. | PSMA formulations and uses thereof |
| US20050215472A1 (en) | 2001-10-23 | 2005-09-29 | Psma Development Company, Llc | PSMA formulations and uses thereof |
| ES2314272T3 (es) | 2003-01-10 | 2009-03-16 | Millennium Pharmaceuticals, Inc. | Metodos para el diagnostico y el tratamiento del cancer. |
| MX2007009935A (es) | 2005-02-18 | 2007-10-10 | Medarex Inc | Anticuerpos monoclonales que carecen de residuos fucosilo contra antigeno membranal especifico de prostata (psma). |
| EP1726650A1 (en) * | 2005-05-27 | 2006-11-29 | Universitätsklinikum Freiburg | Monoclonal antibodies and single chain antibody fragments against cell-surface prostate specific membrane antigen |
| EP1934261B1 (en) | 2005-09-26 | 2014-10-29 | Medarex, L.L.C. | Human monoclonal antibodies to cd70 |
| EP1996716B1 (en) | 2006-03-20 | 2011-05-11 | The Regents of the University of California | Engineered anti-prostate stem cell antigen (psca) antibodies for cancer targeting |
| JP6126773B2 (ja) | 2007-09-04 | 2017-05-10 | ザ リージェンツ オブ ザ ユニバーシティ オブ カリフォルニア | 癌のターゲッティングおよび検出のための高親和性抗前立腺幹細胞抗原(psca)抗体 |
| US8569006B2 (en) | 2008-02-29 | 2013-10-29 | Imec | Cell-enzyme based biosensors |
| EP2727606A3 (en) | 2008-09-08 | 2015-09-23 | Psma Development Company, L.L.C. | Compounds for killing psma-expressing, taxane-resistant cancer cells |
| WO2010096486A1 (en) | 2009-02-17 | 2010-08-26 | Cornell Research Foundation, Inc. | Methods and kits for diagnosis of cancer and prediction of therapeutic value |
| CA2782333C (en) | 2009-12-02 | 2019-06-04 | Imaginab, Inc. | J591 minibodies and cys-diabodies for targeting human prostate specific membrane antigen (psma) and methods for their use |
| WO2012143499A2 (de) | 2011-04-21 | 2012-10-26 | Bayer Intellectual Property Gmbh | Neue binder-wirkstoff konjugate (adcs) und ihre verwendung |
| SG194510A1 (en) | 2011-04-22 | 2013-12-30 | Emergent Product Dev Seattle | Prostate-specific membrane antigen binding proteins and related compositionsand methods |
| SG11201604758PA (en) | 2013-12-23 | 2016-07-28 | Bayer Pharma AG | Antibody drug conjugates (adcs) with kinesin spindel protein (ksp) |
| MX2017017172A (es) | 2015-06-22 | 2018-02-23 | Bayer Pharma AG | Conjugados de ligador-principio activo (adcs) y conjugados de ligador-profarmaco (apdcs) con grupos enzimaticamente escindibles. |
| JOP20160154B1 (ar) * | 2015-07-31 | 2021-08-17 | Regeneron Pharma | أجسام ضادة مضاد لل psma، وجزيئات رابطة لمستضد ثنائي النوعية الذي يربط psma و cd3، واستخداماتها |
| NZ739721A (en) | 2015-08-07 | 2019-09-27 | Imaginab Inc | Antigen binding constructs to target molecules |
| EP3352760A4 (en) | 2015-09-21 | 2019-03-06 | Aptevo Research and Development LLC | CD3 BINDING POLYPEPTIDES |
| WO2017060322A2 (en) | 2015-10-10 | 2017-04-13 | Bayer Pharma Aktiengesellschaft | Ptefb-inhibitor-adc |
| SG11201808167VA (en) | 2016-03-24 | 2018-10-30 | Bayer Pharma AG | Prodrugs of cytotoxic active agents having enzymatically cleavable groups |
| JP7022707B2 (ja) | 2016-06-15 | 2022-02-18 | バイエル・ファルマ・アクティエンゲゼルシャフト | Ksp阻害剤および抗cd123抗体を含む特異的抗体-薬物-コンジュゲート(adc) |
| CA3047522A1 (en) | 2016-12-21 | 2018-06-28 | Bayer Pharma Aktiengesellschaft | Specific antibody drug conjugates (adcs) having ksp inhibitors |
| WO2018114578A1 (de) | 2016-12-21 | 2018-06-28 | Bayer Pharma Aktiengesellschaft | Binder-wirkstoff-konjugate (adcs) mit enzymatisch spaltbaren gruppen |
| CN110312533B (zh) | 2016-12-21 | 2023-11-03 | 拜耳公司 | 具有酶促可裂解的基团的细胞毒性活性剂的前药 |
| AU2019231205A1 (en) | 2018-03-06 | 2020-09-24 | The Trustees Of The University Of Pennsylvania | Prostate-specific membrane antigen cars and methods of use thereof |
| US20220185910A1 (en) * | 2018-06-18 | 2022-06-16 | Eureka Therapeutics, Inc. | Constructs targeting prostate-specific membrane antigen (psma) and uses thereof |
| CN112533956A (zh) | 2018-07-31 | 2021-03-19 | 海德堡医药研究有限责任公司 | 针对psma的人源化抗体 |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1757694A3 (en) * | 1992-11-05 | 2008-02-27 | Sloan Kettering Institute For Cancer Research | Prostate-specific membrane antigen |
| US5541087A (en) * | 1994-09-14 | 1996-07-30 | Fuji Immunopharmaceuticals Corporation | Expression and export technology of proteins as immunofusins |
| DE69635801T2 (de) * | 1995-02-24 | 2006-11-02 | Sloan-Kettering Institute For Cancer Research | Prostataspezifisches membranes antigen und seine anwendungen |
-
1997
- 1997-03-25 IL IL12631497A patent/IL126314A/xx not_active IP Right Cessation
- 1997-03-25 DE DE69735294T patent/DE69735294T2/de not_active Revoked
- 1997-03-25 EP EP97917121A patent/EP0914155B1/en not_active Revoked
- 1997-03-25 CA CA002250141A patent/CA2250141C/en not_active Expired - Lifetime
- 1997-03-25 JP JP53466797A patent/JP4295826B2/ja not_active Expired - Lifetime
- 1997-03-25 WO PCT/US1997/005214 patent/WO1997035616A1/en active IP Right Grant
- 1997-03-25 AT AT97917121T patent/ATE318147T1/de not_active IP Right Cessation
- 1997-03-25 AU AU25552/97A patent/AU725583B2/en not_active Expired
- 1997-03-25 ES ES97917121T patent/ES2260788T3/es not_active Expired - Lifetime
- 1997-03-25 DK DK97917121T patent/DK0914155T3/da active
Also Published As
| Publication number | Publication date |
|---|---|
| ATE318147T1 (de) | 2006-03-15 |
| DE69735294D1 (de) | 2006-04-27 |
| DK0914155T3 (da) | 2006-06-26 |
| EP0914155A4 (en) | 2001-05-16 |
| AU2555297A (en) | 1997-10-17 |
| CA2250141C (en) | 2008-07-29 |
| WO1997035616A1 (en) | 1997-10-02 |
| ES2260788T3 (es) | 2006-11-01 |
| DE69735294T2 (de) | 2006-09-21 |
| IL126314A (en) | 2003-07-31 |
| EP0914155B1 (en) | 2006-02-22 |
| CA2250141A1 (en) | 1997-10-02 |
| AU725583B2 (en) | 2000-10-12 |
| EP0914155A1 (en) | 1999-05-12 |
| IL126314A0 (en) | 1999-05-09 |
| JP2001503601A (ja) | 2001-03-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4295826B2 (ja) | 前立腺特異的膜抗原の細胞外ドメインに対して特異的なモノクローナル抗体 | |
| JP4229591B2 (ja) | 前立腺特異的膜抗原の細胞外ドメインに対して特異的なモノクローナル抗体 | |
| US7201900B2 (en) | Monoclonal antibodies specific for the extracellular domain of prostate-specific membrane antigen | |
| US7476513B2 (en) | Monoclonal antibody specific for the extracellular domain of prostate specific membrane antigen | |
| AU733544B2 (en) | Treatment and diagnosis of cancer | |
| JP5328155B2 (ja) | Adam−9モジュレータ | |
| EP2913673B1 (en) | Diagnosis of ovarian carcinoma | |
| JP4813661B2 (ja) | 癌を診断するための方法および組成物 | |
| US20030031673A1 (en) | Treatment and diagnosis of cancer | |
| WO1998003873A9 (en) | Treatment and diagnosis of cancer | |
| US20030082188A1 (en) | Treatment of prostate cancer by inhibitors of NCAM2 | |
| US5879898A (en) | Antibodies specific for peptide corresponding to CD44 exon 6, and use of these antibodies for diagnosis of tumors | |
| KR100249294B1 (ko) | 사람 mdr1 다중약물 내성 유전자 생성물에 대한 단클론성 항체, 및 그것의 사용방법 | |
| JPH08506801A (ja) | Cd44エキソン6に対応するペプチド、そのペプチドに特異的な抗体、および、腫瘍診断にそれらの抗体を使用する方法 | |
| EP0906576B1 (en) | Prostate cancer specific antibodies for immunodetection and immunotherapy | |
| US20110104675A1 (en) | Methods and Compositions for Diagnosing Carcinomas |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20040325 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20040325 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20040514 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20070306 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20070606 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20080507 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080805 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20081127 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20081202 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20090212 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20090324 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20090413 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120417 Year of fee payment: 3 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20120417 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130417 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130417 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20140417 Year of fee payment: 5 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313111 |
|
| R360 | Written notification for declining of transfer of rights |
Free format text: JAPANESE INTERMEDIATE CODE: R360 |
|
| R360 | Written notification for declining of transfer of rights |
Free format text: JAPANESE INTERMEDIATE CODE: R360 |
|
| R371 | Transfer withdrawn |
Free format text: JAPANESE INTERMEDIATE CODE: R371 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313111 |
|
| S531 | Written request for registration of change of domicile |
Free format text: JAPANESE INTERMEDIATE CODE: R313531 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313111 |
|
| R360 | Written notification for declining of transfer of rights |
Free format text: JAPANESE INTERMEDIATE CODE: R360 |
|
| R360 | Written notification for declining of transfer of rights |
Free format text: JAPANESE INTERMEDIATE CODE: R360 |
|
| R371 | Transfer withdrawn |
Free format text: JAPANESE INTERMEDIATE CODE: R371 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313111 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| EXPY | Cancellation because of completion of term |