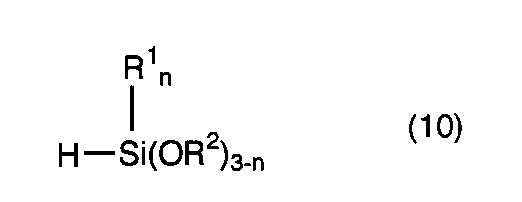JP3819087B2 - 新規シランカップリング剤 - Google Patents
新規シランカップリング剤 Download PDFInfo
- Publication number
- JP3819087B2 JP3819087B2 JP29493396A JP29493396A JP3819087B2 JP 3819087 B2 JP3819087 B2 JP 3819087B2 JP 29493396 A JP29493396 A JP 29493396A JP 29493396 A JP29493396 A JP 29493396A JP 3819087 B2 JP3819087 B2 JP 3819087B2
- Authority
- JP
- Japan
- Prior art keywords
- group
- compound
- epoxy
- silane coupling
- present
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
- 239000006087 Silane Coupling Agent Substances 0.000 title description 9
- 150000001875 compounds Chemical class 0.000 claims description 59
- 125000004432 carbon atom Chemical group C* 0.000 claims description 10
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 10
- 125000001183 hydrocarbyl group Chemical group 0.000 claims description 8
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 6
- 125000000816 ethylene group Chemical group [H]C([H])([*:1])C([H])([H])[*:2] 0.000 claims description 5
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 4
- 229910052757 nitrogen Inorganic materials 0.000 claims description 3
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 3
- 125000004430 oxygen atom Chemical group O* 0.000 claims description 3
- 229910052717 sulfur Inorganic materials 0.000 claims description 3
- 125000004434 sulfur atom Chemical group 0.000 claims description 3
- 125000004122 cyclic group Chemical group 0.000 claims 2
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 16
- 125000003700 epoxy group Chemical group 0.000 description 14
- 125000006091 1,3-dioxolane group Chemical group 0.000 description 13
- 125000003342 alkenyl group Chemical group 0.000 description 13
- 125000005370 alkoxysilyl group Chemical group 0.000 description 11
- 238000000034 method Methods 0.000 description 11
- 239000000126 substance Substances 0.000 description 11
- 150000002576 ketones Chemical class 0.000 description 10
- 239000004593 Epoxy Substances 0.000 description 9
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 6
- 239000002841 Lewis acid Substances 0.000 description 6
- WTEOIRVLGSZEPR-UHFFFAOYSA-N boron trifluoride Chemical compound FB(F)F WTEOIRVLGSZEPR-UHFFFAOYSA-N 0.000 description 6
- 150000007517 lewis acids Chemical class 0.000 description 6
- -1 tertiary amine compound Chemical class 0.000 description 6
- 239000000654 additive Substances 0.000 description 5
- ZWAJLVLEBYIOTI-UHFFFAOYSA-N cyclohexene oxide Chemical group C1CCCC2OC21 ZWAJLVLEBYIOTI-UHFFFAOYSA-N 0.000 description 5
- 238000006116 polymerization reaction Methods 0.000 description 5
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical group C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 4
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 4
- 239000003377 acid catalyst Substances 0.000 description 4
- 239000000853 adhesive Substances 0.000 description 4
- 230000001070 adhesive effect Effects 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 229910015900 BF3 Inorganic materials 0.000 description 3
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 3
- 230000000996 additive effect Effects 0.000 description 3
- 150000001299 aldehydes Chemical class 0.000 description 3
- ZTQSAGDEMFDKMZ-UHFFFAOYSA-N butyric aldehyde Natural products CCCC=O ZTQSAGDEMFDKMZ-UHFFFAOYSA-N 0.000 description 3
- 239000003054 catalyst Substances 0.000 description 3
- 238000004821 distillation Methods 0.000 description 3
- 239000000203 mixture Substances 0.000 description 3
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical group [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 3
- 239000013615 primer Substances 0.000 description 3
- 239000002987 primer (paints) Substances 0.000 description 3
- 239000000565 sealant Substances 0.000 description 3
- 238000003786 synthesis reaction Methods 0.000 description 3
- WNXJIVFYUVYPPR-UHFFFAOYSA-N 1,3-dioxolane Chemical group C1COCO1 WNXJIVFYUVYPPR-UHFFFAOYSA-N 0.000 description 2
- ZWEHNKRNPOVVGH-UHFFFAOYSA-N 2-Butanone Chemical compound CCC(C)=O ZWEHNKRNPOVVGH-UHFFFAOYSA-N 0.000 description 2
- QQZOPKMRPOGIEB-UHFFFAOYSA-N 2-Oxohexane Chemical compound CCCCC(C)=O QQZOPKMRPOGIEB-UHFFFAOYSA-N 0.000 description 2
- HCFAJYNVAYBARA-UHFFFAOYSA-N 4-heptanone Chemical compound CCCC(=O)CCC HCFAJYNVAYBARA-UHFFFAOYSA-N 0.000 description 2
- NBBJYMSMWIIQGU-UHFFFAOYSA-N Propionic aldehyde Chemical compound CCC=O NBBJYMSMWIIQGU-UHFFFAOYSA-N 0.000 description 2
- BLRPTPMANUNPDV-UHFFFAOYSA-N Silane Chemical compound [SiH4] BLRPTPMANUNPDV-UHFFFAOYSA-N 0.000 description 2
- 125000002723 alicyclic group Chemical group 0.000 description 2
- 125000002947 alkylene group Chemical group 0.000 description 2
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 2
- 125000003118 aryl group Chemical group 0.000 description 2
- HUMNYLRZRPPJDN-UHFFFAOYSA-N benzaldehyde Chemical compound O=CC1=CC=CC=C1 HUMNYLRZRPPJDN-UHFFFAOYSA-N 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 238000009835 boiling Methods 0.000 description 2
- 238000001816 cooling Methods 0.000 description 2
- ORTQZVOHEJQUHG-UHFFFAOYSA-L copper(II) chloride Chemical compound Cl[Cu]Cl ORTQZVOHEJQUHG-UHFFFAOYSA-L 0.000 description 2
- JHIVVAPYMSGYDF-UHFFFAOYSA-N cyclohexanone Chemical compound O=C1CCCCC1 JHIVVAPYMSGYDF-UHFFFAOYSA-N 0.000 description 2
- BGTOWKSIORTVQH-UHFFFAOYSA-N cyclopentanone Chemical compound O=C1CCCC1 BGTOWKSIORTVQH-UHFFFAOYSA-N 0.000 description 2
- GYZLOYUZLJXAJU-UHFFFAOYSA-N diglycidyl ether Chemical compound C1OC1COCC1CO1 GYZLOYUZLJXAJU-UHFFFAOYSA-N 0.000 description 2
- 239000003822 epoxy resin Substances 0.000 description 2
- JARKCYVAAOWBJS-UHFFFAOYSA-N hexanal Chemical compound CCCCCC=O JARKCYVAAOWBJS-UHFFFAOYSA-N 0.000 description 2
- 229910052739 hydrogen Inorganic materials 0.000 description 2
- 239000001257 hydrogen Substances 0.000 description 2
- XNLICIUVMPYHGG-UHFFFAOYSA-N pentan-2-one Chemical compound CCCC(C)=O XNLICIUVMPYHGG-UHFFFAOYSA-N 0.000 description 2
- FDPIMTJIUBPUKL-UHFFFAOYSA-N pentan-3-one Chemical compound CCC(=O)CC FDPIMTJIUBPUKL-UHFFFAOYSA-N 0.000 description 2
- HGBOYTHUEUWSSQ-UHFFFAOYSA-N pentanal Chemical compound CCCCC=O HGBOYTHUEUWSSQ-UHFFFAOYSA-N 0.000 description 2
- 229920000647 polyepoxide Polymers 0.000 description 2
- 229910000077 silane Inorganic materials 0.000 description 2
- JIAARYAFYJHUJI-UHFFFAOYSA-L zinc dichloride Chemical compound [Cl-].[Cl-].[Zn+2] JIAARYAFYJHUJI-UHFFFAOYSA-L 0.000 description 2
- NAWXUBYGYWOOIX-SFHVURJKSA-N (2s)-2-[[4-[2-(2,4-diaminoquinazolin-6-yl)ethyl]benzoyl]amino]-4-methylidenepentanedioic acid Chemical compound C1=CC2=NC(N)=NC(N)=C2C=C1CCC1=CC=C(C(=O)N[C@@H](CC(=C)C(O)=O)C(O)=O)C=C1 NAWXUBYGYWOOIX-SFHVURJKSA-N 0.000 description 1
- SYBYTAAJFKOIEJ-UHFFFAOYSA-N 3-Methylbutan-2-one Chemical compound CC(C)C(C)=O SYBYTAAJFKOIEJ-UHFFFAOYSA-N 0.000 description 1
- 125000005917 3-methylpentyl group Chemical group 0.000 description 1
- GJEZBVHHZQAEDB-UHFFFAOYSA-N 6-oxabicyclo[3.1.0]hexane Chemical group C1CCC2OC21 GJEZBVHHZQAEDB-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- 229910021577 Iron(II) chloride Inorganic materials 0.000 description 1
- NTIZESTWPVYFNL-UHFFFAOYSA-N Methyl isobutyl ketone Chemical compound CC(C)CC(C)=O NTIZESTWPVYFNL-UHFFFAOYSA-N 0.000 description 1
- UIHCLUNTQKBZGK-UHFFFAOYSA-N Methyl isobutyl ketone Natural products CCC(C)C(C)=O UIHCLUNTQKBZGK-UHFFFAOYSA-N 0.000 description 1
- 229910021627 Tin(IV) chloride Inorganic materials 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 125000000217 alkyl group Chemical group 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 238000003763 carbonization Methods 0.000 description 1
- 229960003280 cupric chloride Drugs 0.000 description 1
- 125000000753 cycloalkyl group Chemical group 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 150000002118 epoxides Chemical group 0.000 description 1
- 125000001033 ether group Chemical group 0.000 description 1
- 238000005755 formation reaction Methods 0.000 description 1
- FXHGMKSSBGDXIY-UHFFFAOYSA-N heptanal Chemical compound CCCCCCC=O FXHGMKSSBGDXIY-UHFFFAOYSA-N 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- NMCUIPGRVMDVDB-UHFFFAOYSA-L iron dichloride Chemical compound Cl[Fe]Cl NMCUIPGRVMDVDB-UHFFFAOYSA-L 0.000 description 1
- 238000005907 ketalization reaction Methods 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- VNKYTQGIUYNRMY-UHFFFAOYSA-N methoxypropane Chemical group CCCOC VNKYTQGIUYNRMY-UHFFFAOYSA-N 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- QNGNSVIICDLXHT-UHFFFAOYSA-N para-ethylbenzaldehyde Natural products CCC1=CC=C(C=O)C=C1 QNGNSVIICDLXHT-UHFFFAOYSA-N 0.000 description 1
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 1
- PJGSXYOJTGTZAV-UHFFFAOYSA-N pinacolone Chemical compound CC(=O)C(C)(C)C PJGSXYOJTGTZAV-UHFFFAOYSA-N 0.000 description 1
- 229910052697 platinum Inorganic materials 0.000 description 1
- 238000007142 ring opening reaction Methods 0.000 description 1
- 238000007086 side reaction Methods 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 238000001308 synthesis method Methods 0.000 description 1
- HPGGPRDJHPYFRM-UHFFFAOYSA-J tin(iv) chloride Chemical compound Cl[Sn](Cl)(Cl)Cl HPGGPRDJHPYFRM-UHFFFAOYSA-J 0.000 description 1
- 235000005074 zinc chloride Nutrition 0.000 description 1
- 239000011592 zinc chloride Substances 0.000 description 1
Images
Landscapes
- Compositions Of Macromolecular Compounds (AREA)
Description
【発明の属する技術分野】
本発明は、1,3−ジオキソラン環とアルコキシシリル基を有する新規化合物に関するものである。詳しくは、接着剤、シーラントおよびプライマーの添加剤として利用されるシランカップリング剤として有用な1,3−ジオキソラン環とアルコキシシリル基を有する新規化合物に関するものである。
【0002】
【従来の技術】
従来、接着性発現のために種々のシランカップリング剤が使用されている。その中でも、エポキシ基含有シランカップリング剤は、接着剤、シーラントおよびプライマーの添加剤として幅広く利用されている。しかし、グリシジルエーテルタイプのエポキシ基含有シランカップリング剤は、やはり接着剤等の添加剤として用いられる3級アミン化合物存在下ではエポキシ基が重合するため、貯蔵安定性に劣るという問題点がある。また、脂環式エポキシ基含有シランカップリング剤は、接着性が低く使用できる範囲が限定される等の問題点がある。
【0003】
【発明が解決しようとする課題】
本発明は、上記従来技術の持つ問題点を省みて成されたものであり、その目的は、共存する添加剤の種類に係わらず貯蔵安定性に優れ、また、接着性にも優れ、幅広い用途に使用可能なシランカップリング剤として有用な新規化合物を提供しようとするものである。
【0004】
【課題を解決するための手段】
本発明は、1分子中に1,3−ジオキソラン環とアルコキシシリル基を有する化合物を提供するものである。
【0005】
本発明は、下記(1)〜(5)を提供する。
(1)下記式(13)で表される化合物。
【化1】
(式中、R 1 、R 2 は、同一であっても異なっていてもよく、それぞれ独立に、メチル基またはエチル基である。R 3 、R 4 は、同一であっても異なっていてもよく、それぞれ独立に、水素基または炭素数1〜6の炭化水素基であり、もしくは、R 3 とR 4 が環状に結合した基であってもよい。nは0〜2の整数である。Aは、2価の炭化水素基であり、酸素原子、硫黄原子、窒素原子を含んでもよい。)
(2)前記Aが、エチレン基である上記(1)に記載の化合物。
(3)前記R 2 、前記R 3 および前記R 4 がメチル基であり、nが0であり、前記Aがエチレン基である上記(1)に記載の化合物。
(4)下記式(2)で表される化合物。
【化2】
(式中、R 1 、R 2 は、同一であっても異なっていてもよく、それぞれ独立に、メチル基またはエチル基である。R 3 、R 4 は、同一であっても異なっていてもよく、それぞれ独立に、炭素数1〜6の炭化水素基であり、もしくは、R 3 とR 4 が環状に結合した基であってもよい。nは0〜2の整数である。)
(5)前記R 2 、前記R 3 および前記R 4 がメチル基であり、nが0である上記(4)に記載の化合物。
【0006】
【発明の実施の形態】
以下、本発明についてさらに詳細に説明する。
本発明の新規化合物は、1分子中に1,3−ジオキソラン環とアルコキシシリル基を各々1個以上有する構造であれば特に限定はされない。例えば、下記一般式で表わされる。
【0007】
【化3】
【0008】
上記式中、Aは、2価の炭化水素基、例えば2価の脂肪族基、2価の芳香族基、またはこれらの組み合わせであってもよく、また、炭素、水素に加えてその他の原子、例えば酸素原子、硫黄原子、窒素原子等を含んでもよい。Aの好ましい例としては、炭素数2〜6のアルキレン基、例えばエチレン基、3−メチル−ペンチル基;炭素数4〜8のアルキレンエーテル基、例えばメチルプロピルエーテル基;炭素数5〜10の炭化水素エステル基等が挙げられる。
【0009】
上記本発明の新規化合物の好ましい態様として、下記式(1)および(2)により示される化合物を示すことができる。
【0010】
【化4】
【0011】
ここでR1 、R2 は、同一であっても異なっていてもよく、それぞれ独立に、メチル基またはエチル基である。
nは0、1、または2であり、好ましくは0または1である。
R3 、R4 は同一であっても異なっていてもよく、それぞれ独立に、水素基または炭素数1〜6の炭化水素基である。具体的には、炭素数1〜6の直鎖状もしくは分岐鎖を有するアルキル基、例えばメチル基、エチル基、n−プロピル基等;炭素数6〜12のアリール基、例えばフェニル基等;炭素数4〜7のシクロアルキル基、例えばR3 とR4 が結合するシクロペンチル基、シクロヘキシル基等が挙げられる。
【0012】
上記式(1)および(2)で表される化合物の好ましい例として、上記式(1)、(2)の各々について下記式(3)、(4)で表される化合物を示すことができる。
【0013】
【化5】
【0014】
本発明の1分子中に1,3−ジオキソラン環とアルコキシシリル基を有する新規化合物は以下の2つの方法により合成することができる。
方法1:エポキシ基含有アルコキシシラン化合物とケトンまたはアルデヒドを酸触媒存在下に反応させる。
方法2:アルケニル基含有エポキシ化合物とケトンを反応させジオキソラン環を合成した後、Si−H基を含有するアルコキシシラン化合物を反応させる。
【0015】
方法1におけるエポキシ基含有アルコキシシラン化合物としては、エチレンオキシド基や、トリシクロデセンオキシド基、シクロペンテンオキシド基、シクロヘキセンオキシド基等の環式脂肪族エポキシ基と、アルコキシシラン基とを各々1個以上有する化合物を用いることができる。また、アルコキシシラン基含有エポキシ樹脂を用いることもできる。特に、前記式(1)、(2)で示される本発明の新規化合物の合成には、エチレンオキシド基とアルコキシシラン基、シクロヘキセンオキシド基とアルコキシシラン基を各々分子末端に有する化合物、例えば下記式(5)、(6)により示されるエポキシ基含有アルコキシシラン化合物等の市販品を各々好適に用いることができる。
【0016】
【化6】
【0017】
また、方法1におけるケトンとしては、アセトン、2−ブタノン、2−ペンタノン、3−メチル−2−ブタノン、3−ペンタノン、2−ヘキサノン、4−メチル−2−ペンタノン、4−ヘプタノン、3,3−ジメチル−2−ブタノン、シクロペンタノン、シクロヘキサノン等が例示される。この中でもアセトン、2−ブタノンが好ましい。
アルデヒドとしては、プロピオンアルデヒド、n−ブチルアルデヒド、n−バレルアルデヒド、カプロアルデヒド、ヘプタアルデヒド、フェニルアルデヒド、ベンズアルデヒド等が例示される。
【0018】
酸触媒としては、燐酸、硫酸や、塩化鉄(II)、塩化錫(IV)、塩化亜鉛、三フッ化ホウ素エーテルコンプレックス等のルイス酸等を用いることができ、これらの中でも、ルイス酸を好適に用いることができる。
【0019】
方法1においては、上記エポキシ基含有アルコキシシラン化合物と上記ケトンまたは上記アルデヒドを、上記酸触媒の存在下に反応させることにより本発明の1分子中に1,3−ジオキソラン環とアルコキシシリル基を有する化合物を合成することができるが、好ましい態様として、酸触媒としてルイス酸を用いることができる。しかし、エポキシ基のルイス酸による開環反応、ケトンとの1,3−ジオキソラン環の生成反応には、ルイス酸によるエポキシ化合物の重合反応が副反応として起こりうるので問題となるが、ケトンをエポキシ基の好ましくは1.5〜10倍当量、より好ましくは2〜7倍当量使用し、ルイス酸を好ましくは0.05〜5重量%、より好ましくは0.5〜3重量%添加し、反応温度を好ましくは40℃以下、より好ましくは30℃以下で反応させると、重合反応を抑えることができるので好ましい。しかし、この反応においても、重合反応が起こりうるため、減圧蒸留を行って目的の本発明の化合物を単離することができる。
【0020】
方法2に用いる前記アルケニル基含有エポキシ化合物としては、エチレンオキシド基、シクロヘキセンオキシド基等の環式脂肪族エポキシ基等のエポキシ基と、アルケニル基とを各々1個以上有する化合物を用いることができ、また、アルケニル基含有エポキシ樹脂を用いることもできる。特に、前記式(1)により示される本発明の新規化合物合成には、エチレンオキシド基とアルケニル基を有する化合物、例えば下記式(7)、前記式(2)により示される本発明の新規化合物合成には、シクロヘキセンオキシド基とアルケニル基を有する化合物、例えば下記式(8)、(9)より示されるアルケニル基含有エポキシ化合物等の市販品を各々好適に用いることができる。
【0021】
【化7】
【0022】
方法2において用いるケトンは、方法1で例示したケトンを用いることができる。
Si−H基を含有するアルコキシシラン化合物としては、下記式(10)に示されるアルコキシシラン化合物を用いることができる。式中、R1 、R2 は、前記式(1)、(2)におけるR1 、R2 と同義である。
【0023】
【化8】
【0024】
方法2においては、まず、公知の合成方法、例えば特開昭52−95669号公報に記載の方法等を利用して、前記アルケニル基含有エポキシ化合物と前記ケトンとからアルケニル基含有1,3−ジオキソラン化合物を合成することができる。すなわち、前記アルケニル基含有エポキシ化合物のエポキシ基に対して65%燐酸もしくは濃硫酸を等モル、さらに前記ケトンを10〜20倍モル加える。この合成反応を通じて、アルケニル基の重合反応を禁止するため、さらに塩化第二銅等の重合禁止剤を前記アルケニル基含有エポキシ化合物に対して0.05〜0.1重量%加える。このようにして得られた混合物を、60℃で2時間撹拌して反応を行うことにより、エポキシド環もしくはシクロヘキセンオキシド環とケトンの間でケタール化を行ない1,3−ジオキソラン環を合成する。
ついで前記Si−H基を含有するアルコキシシラン化合物を、該ジオキソラン化合物中のアルケニル基と該アルコキシシラン化合物のケイ素に結合した水素原子とが等モル、もしくはアルコキシシラン化合物が若干過剰になるよう、白金やクロロ白金酸等の白金族金属含有化合物等の触媒の存在下、混合することにより本発明の1分子中に1,3−ジオキソラン環とアルコキシシリル基を有する化合物を合成することができる。白金等の触媒の添加量は、上記ジオキソラン化合物と上記アルコキシシラン化合物の間の反応を促進するに十分な量があればよく、用いる触媒に応じて適量を定めればよい。
【0025】
【実施例】
以下に、本発明をさらに具体的に説明するが、本発明はこれらに限られるものではない。
【0026】
(実施例1)
三口フラスコにアセトン100g、およびエポキシシラン(A−187、日本ユニカー社製)100gをいれ、氷冷した。ついで、三フッ化ホウ素エーテルコンプレックス(BF3 ・OEt2 )2gを25gのアセトンに溶かし、三口フラスコにゆっくり滴下した。反応温度は上昇するが、30℃以上に上昇しないようにした。滴下終了後、1時間氷冷下で攪拌した。アセトン留去後、減圧蒸留し、1分子中に1,3−ジオキソラン環とアルコキシシリル基を有する化合物を合成した。沸点は115℃/0.1mmHgであった。収率は52%であった。得られた化合物の構造を、NMRにて確認した。NMRチャートを図1に示す。
化学構造式は下記式(11)で示される。
【0027】
【化9】
【0028】
(実施例2)
三口フラスコにアセトン100g、およびエポキシシラン(A−186、日本ユニカー社製)100gをいれ、氷冷した。ついで、三フッ化ホウ素エーテルコンプレックス(BF3 ・OEt2 )0.2gを25gのアセトンに溶かし、三口フラスコにゆっくり滴下した。反応温度は上昇するが、30℃以上に上昇しないようにした。滴下終了後、1時間氷冷下で攪拌した。アセトン留去後、減圧蒸留し、1分子中に1,3−ジオキソラン環とアルコキシシリル基を有する化合物を合成した。沸点は135℃/0.1mmHgであった。収率は48%であった。得られた化合物の構造を、NMRにて確認した。NMRチャートを図2に示す。
化学構造式は下記式(12)で示される。
【0029】
【化10】
【0030】
【発明の効果】
本発明の新規化合物は、分子内にグリシジルエーテルタイプのエポキシ基を有さないので、3級アミン化合物存在下でも重合することがなく、貯蔵中安定である。また、脂環式エポキシ基含有シランカップリング剤のように接着性が低いために用途が限定されることもない。このため、本発明の新規化合物は、3級アミン化合物存在下でも安定で、プライマー、シーラント、接着剤の添加剤等の幅広い用途に使用可能なシランカップリング剤として有用である。
【図面の簡単な説明】
【図1】 式(11)で表される1分子中に1,3−ジオキソラン環とアルコキシシリル基を有する化合物のNMRチャートを示す図である。
【図2】 式(12)で表される1分子中に1,3−ジオキソラン環とアルコキシシリル基を有する化合物のNMRチャートを示す図である。
Claims (5)
- 前記Aが、エチレン基である請求項1に記載の化合物。
- 前記R 2 、前記R 3 および前記R 4 がメチル基であり、nが0であり、前記Aがエチレン基である請求項1に記載の化合物。
- 前記R 2 、前記R 3 および前記R 4 がメチル基であり、nが0である請求項4に記載の化合物。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP29493396A JP3819087B2 (ja) | 1996-11-07 | 1996-11-07 | 新規シランカップリング剤 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP29493396A JP3819087B2 (ja) | 1996-11-07 | 1996-11-07 | 新規シランカップリング剤 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPH10139787A JPH10139787A (ja) | 1998-05-26 |
| JP3819087B2 true JP3819087B2 (ja) | 2006-09-06 |
Family
ID=17814161
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP29493396A Expired - Lifetime JP3819087B2 (ja) | 1996-11-07 | 1996-11-07 | 新規シランカップリング剤 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP3819087B2 (ja) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002088238A (ja) * | 2000-09-12 | 2002-03-27 | Sumitomo Bakelite Co Ltd | 熱可塑性エラストマー組成物 |
| JP4605018B2 (ja) * | 2004-02-16 | 2011-01-05 | 東亞合成株式会社 | 有機ケイ素化合物の製造方法並びにジオールを有する有機ケイ素樹脂及びその製造方法 |
-
1996
- 1996-11-07 JP JP29493396A patent/JP3819087B2/ja not_active Expired - Lifetime
Also Published As
| Publication number | Publication date |
|---|---|
| JPH10139787A (ja) | 1998-05-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN110997649B (zh) | 制备硫代碳酸酯的方法 | |
| US5200543A (en) | Siloxane compounds | |
| US6303729B1 (en) | Process for preparing partially added cyclic organohydrogensiloxane | |
| US4788268A (en) | Method for preparation of epoxysilicone compounds and allyl-terminated silicone compounds | |
| JP6365445B2 (ja) | アミノアルキルアルコキシジシロキサン化合物及びその製造方法 | |
| JP3427742B2 (ja) | 硬化性樹脂組成物及び接着剤 | |
| US5010202A (en) | Novel silicon-organic compounds, containing an oxazolidine group | |
| JP4948813B2 (ja) | ケチミン構造含有アルコキシシランの製造方法 | |
| EP0578462A2 (en) | Polyepoxysilanes | |
| JP3819087B2 (ja) | 新規シランカップリング剤 | |
| JP2016204287A (ja) | 加水分解性シリル基含有環状オルガノハイドロジェンシロキサン | |
| US4469881A (en) | [2-(p-t-Butylphenyl)ethyl]silanes and method of making the same | |
| JP2011251936A (ja) | ウレイドシラン化合物 | |
| US3787452A (en) | Epoxysilanes | |
| KR102320689B1 (ko) | 알콕시알킬기를 갖는 이소시아눌산유도체 및 그 제조방법 | |
| US7402648B2 (en) | Method for producing cyclic organic silicon compound and organic silicon resin having alcoholic hydroxyl group | |
| JPH10139777A (ja) | 新規潜在性硬化剤およびその製造法 | |
| JP5062231B2 (ja) | アルコール性水酸基を有する有機ケイ素樹脂及びその製造方法 | |
| KR20160065814A (ko) | 인 함유 화합물 및 그것을 함유하는 경화성 에폭시 수지 조성물 | |
| EP1233020B1 (en) | Fluorinated organosilicon compounds | |
| EP0488681A1 (en) | N, N-dialkylaminoalkyl-N', N'-dialkylaminodimethylsilane | |
| JP6583050B2 (ja) | オルガノポリシロキサンの製造方法 | |
| JP7823771B2 (ja) | アミノアルキルアルコキシジシロキサン化合物およびアミノアルキルアルコキシオリゴシロキサン化合物を含む組成物ならびにその製造方法 | |
| JP3193740B2 (ja) | 有機ケイ素化合物及びその製造方法 | |
| JP2751568B2 (ja) | シラン化合物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20060314 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20060511 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20060606 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20060614 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20090623 Year of fee payment: 3 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20100623 Year of fee payment: 4 |