JP2012509067A - フラビウイルスに対する免疫反応を引き起こす抗原及びその使用方法 - Google Patents
フラビウイルスに対する免疫反応を引き起こす抗原及びその使用方法 Download PDFInfo
- Publication number
- JP2012509067A JP2012509067A JP2011536584A JP2011536584A JP2012509067A JP 2012509067 A JP2012509067 A JP 2012509067A JP 2011536584 A JP2011536584 A JP 2011536584A JP 2011536584 A JP2011536584 A JP 2011536584A JP 2012509067 A JP2012509067 A JP 2012509067A
- Authority
- JP
- Japan
- Prior art keywords
- diii
- vaccine
- sequence
- seq
- nucleic acid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/005—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from viruses
- C07K14/08—RNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/12—Viral antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/04—Immunostimulants
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/005—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from viruses
- C07K14/08—RNA viruses
- C07K14/18—Togaviridae; Flaviviridae
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/51—Medicinal preparations containing antigens or antibodies comprising whole cells, viruses or DNA/RNA
- A61K2039/53—DNA (RNA) vaccination
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55511—Organic adjuvants
- A61K2039/55522—Cytokines; Lymphokines; Interferons
- A61K2039/55527—Interleukins
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2770/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssRNA viruses positive-sense
- C12N2770/00011—Details
- C12N2770/24011—Flaviviridae
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2770/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssRNA viruses positive-sense
- C12N2770/00011—Details
- C12N2770/24011—Flaviviridae
- C12N2770/24111—Flavivirus, e.g. yellow fever virus, dengue, JEV
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2770/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssRNA viruses positive-sense
- C12N2770/00011—Details
- C12N2770/24011—Flaviviridae
- C12N2770/24111—Flavivirus, e.g. yellow fever virus, dengue, JEV
- C12N2770/24134—Use of virus or viral component as vaccine, e.g. live-attenuated or inactivated virus, VLP, viral protein
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Abstract
Description
本明細書で使用するヌクレオチドおよびアミノ酸の配列相同性は、FASTA、BLASTおよびGapped BLAST(Altschul et al.,Nuc.Acids Res.,1997,25,3389、これは、参照によりこの全体が本明細書に組み込まれる)ならびにPAUP*4.ObIO software(D.L.Swofford,Sinauer Associates,Massachusetts)を用いて決定してもよい。簡潔に述べると、Basic Local Alignment Search Toolを表すBLASTアルゴリズムは、配列類似度の決定に適している(Altschul et al.,J.MoI.Biol.,1990,215,403−410、これは、参照によりこの全体が本明細書に組み込まれる)。BLAST解析を行うソフトウェアは、全米バイオテクノロジー情報センター(http://www.ncbi.nlm.nih.gov)を通じて公表されている。BLASTアルゴリズムにより提供される類似度の1つの測定は、2つのヌクレオチド配列間の一致が偶然生じる確率の指標を与える最小合計確率(smallest sum probability(P(N))である。例えば、試験核酸と他の核酸の比較における最小合計確率が約1未満、好ましくは約0.1未満、より好ましくは約0.01未満、および最も好ましくは約0.001未満である場合、核酸配列は別の核酸配列と類似するとみなされる。「類似度のパーセンテージ」を、PAUP*4.ObIO software(D.L.Swofford,Sinauer Associates,Massachusetts)を用いて計算することができる。コンセンサス配列の平均類似度を、系統樹の全配列と比較して計算する。
本発明の態様は、タンパク質EのコンセンサスDIII領域をコードする単離した核酸配列を含む。これらの核酸配列は以下のヌクレオチド配列を含み得る:(a)配列番号12、13、もしくは14;(b)配列番号9、10、もしくは11のアミノ酸配列をコードするヌクレオチド配列;または(c)(a)もしくは(b)の相補体。本発明の別の態様は、本明細書に記載の単離した核酸配列を含む遺伝子構築物である。いくつかの実施形態において、遺伝子構築物は、コザック配列GGT ACC GCC ACC(配列番号15)および/またはIgGもしくはIgEの一部、好ましくはIgE、より好ましくは配列番号8の配列を有するIgEから選択されるリーダー配列を含み得る。
本明細書に記載のポリペプチド/抗原は、1つまたは複数のフラビウイルス血清型、特にウエストナイルウイルスおよび日本脳炎ウイルスの様々な血清型に対する免疫反応を哺乳類において引き起こすことができる抗原である。本抗原は、1つまたは複数の流行株に対する免疫反応を含む、1つまたは複数のフラビウイルス血清型に対する免疫反応を哺乳類において引き起こすことができる。本抗原は、抗フラビウイルス免疫反応が誘導され得る免疫原として特に効果的にさせるエピトープを含み得る。
本発明の態様は、宿主に複数のWNVおよびJEV血清型に対する免疫反応を引き起こすことのできるDNAワクチンであり、このワクチンは以下を含む:(a)本明細書に記載の単離した核酸配列を含むコード配列に作用可能に連結されたプロモーターを含む遺伝子構築物;および(b)薬学的に許容可能な賦形剤;ここで、この遺伝子構築物は、免疫反応を引き起こすことに効果的な量で、宿主細胞にタンパク質E抗原のコンセンサスDIII領域を発現することができる。
DIII抗原をコードする核酸を含み得る遺伝子構築物を本明細書で提供する。遺伝子構築物は、DIII抗原をコードする核酸、好ましくはDNAプラスミドを含む染色体外で機能する分子として細胞内に存在し得る。DIII抗原をコードする核酸含む遺伝子構築物は、セントロメア、テロマーを含む直鎖状の小染色体であり得る。本遺伝子構築物は、組換えアデノウイルス、組換えアデノウイルス関連ウイルスおよび組換えワクシニアを含む組換えウイルスベクターのゲノムの一部でもあり得る。本遺伝子構築物は、弱毒化した、生きている微生物内の遺伝物質の一部、または細胞内に居住する組換え微生物ベクターの一部であり得る。本遺伝子構築物は、DIII核酸の遺伝子発現の調節要素を含み得る。これらの調節要素は、プロモーター、エンハンサー、開始コドン、終止コドン、またはポリアデニル化シグナルであり得る。エンハンサーは、大抵、標的タンパク質または免疫調節タンパク質をコードする配列の遺伝子発現に必要とされる。これらの要素は、所望のタンパク質をコードする配列と作用可能に連結され得、これらの調節要素は、それらが投与される固体において機能し得る。
本発明の態様には、宿主に複数のフラビウイルス血清型に対する免疫反応を引き起こすための以下を含む方法がある:(a)本明細書に記載のワクチンを宿主の組織に送達するステップ;および(b)ワクチンの遺伝子構築物を宿主へ侵入させることに効果的なエネルギーパルスを送達する電気穿孔装置を用いて、組織の細胞を電気穿孔するステップ。
HeLaおよびRD細胞を、アメリカ合衆国培養細胞系統保存機関(Manassas,VA)から得た。加熱不活性化した10%ウシ胎仔血清、ペニシリンG(100U/ml)、ストレプトマイシン(100μg/ml)を補充したDMEM培地で、37℃、5%CO2で細胞を培養した。
HeLa細胞を用いて、間接的免疫蛍光アッセイを行った。細胞を2つのチャンバースライドに蒔き、一晩成長させ、その後トランスフェクションにそれらの細胞を用いた。FuGENE 6トランスフェクション試薬(Roche)を用いて、それらの細胞をワクチン構築物またはpVAX(1mg/ウェル)でトランスフェクトした。トランスフェクション36時間後、常温で20分間、細胞をメタノールで固定し、PBSで穏やかに洗浄した。それらの細胞を、90分間、ワクチン接種したマウスの抗マウス血清とインキュベートし、再び洗浄した。その後、45分間、その試料をFITC結合2次抗体(Sigma− Aldrich)とインキュベートした。与えられたフィールドで利用できる全細胞数を示すために、核内容物を対比染色するための2次抗体の溶液に40,6−ジアミド−2−フェニルインドール塩酸塩(Sigma−Aldrich)を加えた。蛍光顕微鏡(Media Cybernetics,Silver Spring,MD)のPhase 3 Pro programを用いて画像を得た。
全ての値を、各実験群の3つの試料から計算された平均値±平均値の標準誤差(SEM)として表す。必要に応じて、統計学的差異を両側ペア・スチューデントt-検定(Two−tailed、paired Student’s t Test)によって評価し、各実験群について特定のp値を得た。通常通り、示したデータは、2通りまたは3通り行った少なくとも3つの独立した実験を代表する。
JEVおよびWNV E DIIIコンセンサス配列を生成するために、標本抽出バイアスを避けるため、GeneBank(NCBI)から約15個の異なる配列を異なる地理的領域から収集し、MegAlign(DNASTAR,Madison,WI)を用いて整列させた。IgEリーダー配列を得られたコンセンサス配列のアミノ末端に加え、2つのストップコドンを翻訳領域の末端に加えた。KpnlおよびPstl部位をそれぞれ5’末端および3’末端に結合させた。GeneOptimizer(GENEART, Regensburg,Germany)を用いて、完全配列をコドン最適化およびRNA最適化した。その後、コドン最適化合成配列を、本明細書記載のpVAXl発現ベクター(Invitrogen)にクローニングした。
天然のIL−15は2つの別のリーダーペプチドを含み、それらはIL−15の翻訳の調節に関わるだけでなく、その細胞内移動を指示する。標準的な長い(48アミノ酸)シグナルペプチドはIL−15の全ての分泌型と関連し、一方、短い21個のアミノ酸のシグナルペプチドを含むIL−15は、分泌されずむしろ細胞内に貯蔵される(1〜4)。最適化ヒトIL−15のプラスミド型(pIL15 ECRO)の設計は、タンパク質発現を増加させるために発明者らの実験室で設計され、LSPを「最適化」IgEリーダーと置換することを必要とする(5、6)。さらに、コドン使用頻度を、ヒト遺伝子のコドンバイアスに適合させ、高いCAI値(非最適化:0.66;最適化:0.98)を得た。ヒトおよびマウスの遺伝子は73%の相同性を共有するので、マウスモデルを用いてインビボでpIL15 ECROを利用した。設計および合成のために、可能であれば、非常に高い(>80%)または非常に低い(<30%)GC含有量の領域を避けるようにコドンを選択した。この点において、野生型IL15遺伝子は高頻度にレアコドンを使用し、かつGC含量が非常に低く(35%)、迅速なmRNAの代謝回転を促進することが見出された。従って、mRNAの半減期を延ばすために、GC含量を増加させた(57%)。最適化の工程の間、以下のシス作用性配列モチーフを避けた:内部のTATAボックス、Chi部位およびリボソーム進入部位、ATリッチまたはGCリッチ配列ストレッチ、ARE、INS(登録商標)、CRS配列要素、反復配列およびRNA2次構造、(潜在性の)スプライス供与および受容部位ならびに枝分かれ部位。解析後、3つのネガティブにシス作用するモチーフを特定し、除去した。遺伝子の最終設計は、野生型LSP型を置換したIgEリーダーを有するヒトIL15の成熟型と100%一致した。合成の高度に最適化したヒトIL15遺伝子を、Geneart社(Germany)の合成オリゴヌクレオチドから構築した。コザック配列を導入し、翻訳開始を増加させ、2つのストップコドンを加えて効率的な翻訳終止を確実にした。EcoRIおよびXhol制限酵素認識部位を用いて、その断片をpVAXlにクローニングした。最終構築物を配列決定により検証し、100%一致することが判明した。トランスフェクション1日前に、DlO培地(DMEM、20%FBS、1%抗生物質)で増殖させた7.0×105のHeLaまたはRD細胞を、60mm培養皿(Falcon)上に蒔いた。
配列決定により挿入断片配列確認後のワクチン接種試験への適用の前に、DIIIワクチン構築物を、適切な分子量を有する遺伝子産物を発現するそれらの能力について検証した。インビトロ翻訳/転写システム(Promega,Madison,WI)を用いることによって、35S標識放射性タンパク質産物をこれらの構築物から生成し、免疫沈降し、SDS−PAGEにより分離した。これらのプラスミドは、翻訳領域の予想された長さに相当する約16.5kDaの質量の遺伝子産物を生成した(図1D)。細胞内でのそれらの発現中に、適切なmRNA転写産物の存在をRT−PCRにより確認するために、空ベクターまたはDIII領域構築物を運ぶpVAXlのいずれか一方でRD細胞をトランスフェクトした。個々のDIII構築物を発現するトランスフェクトした細胞において、約420塩基対を有するcDNAの存在を、DIII構築物でトランスフェクトした細胞からのみ観察した。模擬トランスフェクトした細胞から対応するシグナルが観察されなかったことが、このアッセイの特異異性を確かにする(図1E)。これらの結果は共に、JEV、WNVおよびJE/WNV DIII構築物を検証し、それゆえに、これらの構築物についてさらに免疫化試験を行った。
IL15の局在パターンを確認するために、HeLa細胞をこれらのIL15構築物のそれぞれでトランスフェクトし、モノクローナル抗IL15抗体を用いて免疫蛍光解析を行った。予想通り、IL15SSPは核領域内で保持され、IL15 LSPおよびIL15 ECROの両方は、細胞質の局在パターンを示した(図2A)。次に、RD細胞内でトランスフェクションアッセイを行い、機能的IL15を発現し、分泌するそれらの能力に対するIL15構築物の効率を比較した。特異的ELISA解析によって測定した時、タンパク質産物および分泌の(天然IL−15より87倍高い、IL−15−LSP構築物より5.7倍高い)実質的増加が、ヒト最適化構築物IL15 ECROから観察されたことをデータは示した(33)(図2B、C)。pIL15 ECRO構築物は、発明者らが以前に報告した、IL15を発現する全プラスミドよりもIL15を発現し、分泌することに非常に効率的であることをこれらのデータは明確に示す。
予想された分子量を有する遺伝子産物を生成する構築物の能力を、ワクチン接種試験に使用する前に確認した。pVAXl骨格の中のT7プロモーターを利用することによって、TNT T7 インビトロ/翻訳キット(Promega,Madison,WI)を使用して、メーカーの手順書に従い、35Sメチオニン標識タンパク質試料を生成した。これらの放射性標識タンパク質試料を、抗WNV Eまたは抗JEV E抗体により免疫沈降し、免疫沈降した複合体を15%SDS−PAGEゲル(BioRad)で電気泳動を行った。このゲルを、リン酸エンハンサー溶液(Amersham)を用いて固定し、真空乾燥機(Biorad)を用いて乾燥させた。オートラジオグラフィーを行い、取り込まれた35S標識遺伝子産物を検出した。
DIIIコード領域を、Kpnl/Pstlによる消化によりそれらのpVAX骨格から除去した。除去した断片をゲル精製し、その後Kpnl/Pstlで消化したpQE−30に結合させた。結合産物をJM 109細胞に形質転換し、50μg/mlのアンピシリンを含むLB寒天培地に蒔いた。37℃で一晩コロニーを形成させた。グリセロールストックを、個々のコロニーから調製した。タンパク質発現のために、50μg/mlのアンピシリンを含む6ミリリットルのLB培養液を含む16x150mmの試験管にグリセロールストックの3μl分を加えた。タンパク質試料の精製を行う標準手順書に従って、得られた細菌ペレットを処理し、溶解物をNiカラムに通過させた。得られた精製タンパク質試料を、ELISAおよびB細胞増殖ELISpotアッセイのコーティング用抗原として使用する。
DIIIコード断片を細菌発現ベクターにサブクローニングし、このタンパク質断片を本明細書記載のNiキレートカラムを用いて精製した。図3に、異なる精製ステップのDIII断片の精製量について記載する。DIIIを発現する細菌細胞の粗溶解物を含むレーンは、IPTGによる誘導がなくても、DIII断片の発現量が非常に顕著であることを示した。全粗試料のレーンに存在する試料のラダーと比較すると、16kDaの質量に相当する明確な単一バンドが250mMのイミダゾールを含む溶出画分から観察され、DIII発現断片の高レベルな純度を示した。20mMの濃度のイミダゾールは、Niキレート基質からHisタグ付きDIII試料を遊離させるのに不十分であった。従って、溶出緩衝液におけるイミダゾールの選択は、ヒスチジン標識タンパク質の溶出には非常に特異的であった。本試験のコーティング用抗原として次に適用するために精製画分の濃度を決定した際、精製画分を透析し、アリコートで保存した。
メスの6〜8週齢のC57BL/6マウスをジャクソン研究所から購入した。6〜8週齢のメスのBALB/cマウス(Charles River,Wilmington,MA)の大腿四頭筋に、隔週の間隔で各10μgのDNAを3回注射し、電気穿孔した。DNAの免疫化について、マウスを各5匹のマウス群に分離し、それぞれpIL15 ECROおよびpVAX(対照群)またはpIL15 ECROおよびpJEV DIII、pIL15 ECROおよびpJE/WNV DIII、pIL15 ECROおよびpWNV DIII、ならびにpIL15 ECROおよびpJEV DIII+pWNV DIIIを用いて電気穿孔することにより免疫化した。
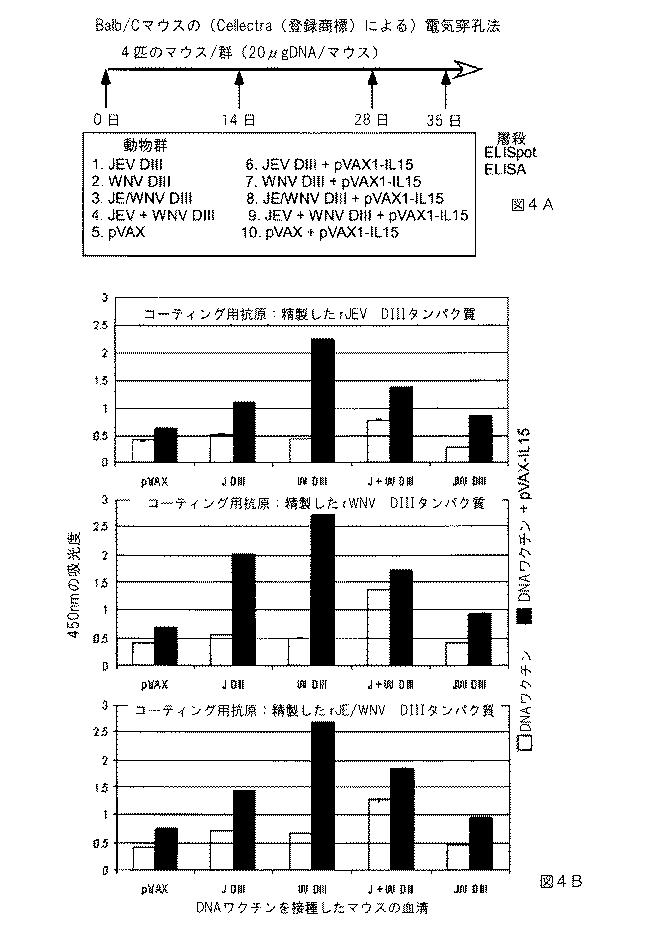
DNAワクチンの送達のためのインビボ電気穿孔法(IVE)をコンセンサス抗原と組み合わせ、合成DNA抗原に対する潜在的な免疫反応を引き起こした。pIL15 ECROの存在下または非存在下で、Balb/cマウスを個々のワクチン候補の各々で免疫化し、電気穿孔した(図4A)。3回目の追加免疫1週間後に得たDNAワクチン接種マウスの血清試料を、JEVおよびWNVに対するそれぞれの抗体の存在について、ELISAによりアッセイした。全ワクチン接種マウスはDIII領域に対する抗体を産生した。全DNAワクチン接種マウスの血清を、全3つの抗原:JEV DIII、WNV DIIIおよびJE/WNV DIIIに対して個々に評価した。
DIIIタンパク質懸濁液を解凍し、試験管をボルテックスして、細かいタンパク質微粒子に懸濁した。再懸濁したタンパク質試料の少量のアリコートをTU(62mM Tris−HCl/8M尿素、pH8.0)緩衝液に溶解し、10μg/ml溶液を生成した。希釈したタンパク質試料の100μl(1μg)分量を、Pierce HisGrabの銅で被覆した高結合能プレートのウェルに入れ、4℃で一晩インキュベートした。次の日、プレートをPBST(PBS、0.05%Tween 20)で洗浄し、PBST中に存在する3%BSAで1時間ブロックし、37℃で1時間、免疫化および天然マウスの段階希釈した血清とインキュベートした。1:10000の希釈で、ヤギ抗マウスIgG−HRP(Research Diagnostics,NJ)を用いて、結合したIgGを検出した。色素原基質溶液テトラメチルベンジン(TMB;R&D Systems)の付加により、結合した酵素を検出し、バイオテック社のEL312e Bio−Kineticsリーダーの450nmにおいて読み取った。全血清試料を2通りで試験した。
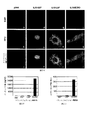
DNAワクチン接種したマウスの血清も試験し、それが、これらのワクチン構築物でトランスフェクトした細胞内で発現したDIII抗原と結合することができるか否かを確かめた。この目的のために、3つのDIIIをコードするpVAX発現構築物でHeLa細胞を一過的にトランスフェクトし、トランスフェクション36時間後、免疫蛍光解析のために細胞を固定した(上記方法を参照)。これらの細胞を最初に適切な血清試料とインキュベートし、その後、FITC結合抗マウス2次抗体とインキュベートした。与えられたフィールドで利用可能な全細胞数を知るために、DAPIを用いてこれらの細胞の核内容物を対比染色した。DNAワクチン接種したマウスの抗DIII血清は、WNV DIII(図5A)およびJEV DIII(図5B)を発現したトランスフェクト細胞のみを染色した。その染色パターンは、フラビウイルス Eの原型発現の染色パターンに似ていた(35)。最も重要なことに、DIII発現細胞は、主に細胞質局在パターンを明らかにした。抗DIII血清は、非トランスフェクトHeLa細胞またはpVAX1トランスフェクトHeLa細胞のいずれにおいてもいかなる顕著な染色も示さなかった。
3回目の免疫化の1週間後にマウスを屠殺し、各マウスの脾臓を摘出し、RPMI 1640を含む15mlコニカル試験管(各実験群に対して1つの試験管)に貯蔵した。滅菌組織培養フードの中で、各実験群の貯蔵した脾臓をペトリ皿に置き、Stomacherブレンダー(Brinkmann Instruments,Inc)を用いて滅菌袋の中で粉砕した。これらの脾細胞を洗浄し、沈殿させた(1200rpm);5〜10分間、このペレットをACK溶解緩衝液(Biosource)で処理し、その後、洗浄し、沈殿させ(1200rpm)、残っているいかなる脾臓の臓器の基質をも除去するために、70μm細胞濾過器に通過させた。これらの脾細胞を、RPMI 1640で2回洗浄し、RlO培地(10%FBSを含むRPMI 1640)で再懸濁し、血球計を用いて数を数えた(細胞生存率を、トリパンブルー染色を用いて決定する)。
ELISpot96ウェルプレート(Millipore)をlOOμl(2μg/ml)の精製タンパク質でコーティングし、4℃で一晩インキュベートした。別々のプレートに各コーティング用抗原を使用した。次の日、プレートを洗浄し、2時間、1%BSAでブロックした。免疫化マウスの25万個の脾細胞を各ウェルに加え、37℃、5%CO2で、5〜6時間、RPMI 1640存在下で刺激した(陰性対照)。インキュベーション後、これらの細胞を洗浄し、ビオチン化抗マウス抗体(R&D Systems)と共に4℃で一晩、インキュベートした。これらのプレートを洗浄し、ストレプトアビジン−アルカリホスファターゼ(R&D Systems)を各ウェルに加えて、常温で2時間、インキュベートした。このプレートを再び洗浄し、5−ブロモ−4−クロロ−3’−インドリルリン酸P−トルイジン塩およびニトロブルー塩化テトラゾリウム(色原体色試薬;R&D Systems)を各ウェルに加えた。その後、プレートを蒸留水でリンスし、常温で乾燥させた。自動化ELISPOTリーダー(Cellular Technology Limited)によりスポットを数えた。結果を抗原特異的抗体分泌細胞数(ASCs)として表す。
B細胞ELISPOT技術は、適切な抗原による刺激後、抗体分泌プラズマ細胞の中にB−記憶細胞のインビトロ分化を誘導することにより、抗原特異的記憶B細胞の定量化を可能にする。IL15アジュバンドによって誘導される免疫反応の質をさらに評価するため、B−記憶反応をマウスにおいて評価した。「方法」の欄で記載したように、マウスの脾臓を準備し、DIIIタンパク質に対する抗体を産生することができるB細胞の発生頻度を測定した。興味深いことに、ELISpotアッセイの結果は、上記のDIII抗体のELISAデータと一致する。DIIIDNAワクチンのみを投与した群よりも、IL15で共刺激したマウスにおいて、DIII特異的マウス抗体分泌細胞の高い発生頻度を観察した(図6)。この群が最も高レベルの抗体分泌細胞を示したことを証明したので、IL15が、pWNV DIIIワクチンに対する抗体分泌細胞応答を明確に高めたこともこのアッセイは示唆した。最も重要なことに、この群の動物の血清を用いたELISAデータにおいて観察されたように、WNV DIII+IL15の群のB細胞は全3つの抗原と結合するができた。この群とは別に、JEV DIII+IL15は、JEV DIIIのみを投与したマウスより、B−細胞応答量の増加を示した。キメラJE/WNV DIIIワクチン接種マウスのELISAの結果と一致して、この群のマウスのB細胞は、JEV DIIIまたはWNV DIIIのワクチン接種マウスだけでなく、キメラ抗原のみを投与した群と結合しなかった。総合すると、ELISA試験によって決定されたDIII特異的抗体の力価に相当する高い親和性の抗原特異的B細胞の活性化を、ELISpotの結果は示した。
Claims (20)
- タンパク質EのコンセンサスDIII領域をコードする単離した核酸であって:
(a)配列番号12、13、もしくは14;
(b)配列番号9、10、もしくは11のアミノ酸配列をコードする核酸配列;または
(c)(a)もしくは(b)の相補体
を含む核酸。 - 前記核酸が、配列番号12、配列番号13、または配列番号14である、請求項1に記載の単離した核酸配列。
- 請求項1の単離した核酸配列を含む遺伝子構築物。
- 配列番号15のコザック配列をさらに含む、請求項3に記載の遺伝子構築物。
- IgGまたはIgEの一部から選択されるリーダー配列をさらに含む、請求項3または4に記載の遺伝子構築物。
- 前記リーダー配列が配列番号8の核酸配列を含む、請求項5に記載の遺伝子構築物。
- アミノ酸配列を含むポリペプチドであって:
(a)配列番号9、10もしくは11;または
(b)(a)の断片
を含むポリペプチド。 - 前記ポリペプチドが、IgGまたはIgEの一部から選択されるN−末端リーダーアミノ酸配列をさらに含む、請求項7に記載のポリペプチド。
- 前記N−末端リーダーアミノ酸配列が配列番号7の配列を含む、請求項8に記載のポリペプチド。
- 宿主に複数のWNVおよびJEV血清型に対する免疫反応を起こすことができるDNAワクチンであって、前記ワクチンは:
(a)請求項1に記載の核酸を含むコード配列と作用可能に連結したプロモーターを含む遺伝子構築物;および
(b)薬学的に許容可能な賦形剤、
を含み、
ここで前記遺伝子構築物は、宿主の細胞に免疫反応を引き起こすのに効果的な量で、タンパク質E抗原のコンセンサスDIII領域を発現することができるワクチン。 - 前記遺伝子構築物が、前記コード配列の3’末端の後にポリアデニル化配列をさらに含む、請求項10に記載のワクチン。
- 前記遺伝子構築物がコドン最適化される、請求項10に記載のワクチン。
- 前記薬学的に許容可能な賦形剤がアジュバンドである、請求項10に記載のワクチン。
- 前記アジュバントが、IL−2、IL−15、IL−28およびRANTESからなる群から選択される、請求項13に記載のワクチン。
- 前記薬学的に許容可能な賦形剤がトランスフェクション促進剤である、請求項14に記載のワクチン。
- 宿主に複数のフラビウイルス血清型に対する免疫反応を引き起こす方法であって:
(a)宿主の組織に請求項10に記載のワクチンを送達するステップ;および
(b)前記細胞に前記ワクチンの遺伝子構築物を侵入させることに効果的なエネルギーパルスを送達する電気穿孔装置を用いて、組織の細胞を電気穿孔するステップ
を含む方法。 - ステップ(a)が皮内、皮下、または筋肉の組織に前記ワクチンを注射するステップを含む、請求項16に記載の方法。
- 事前に設定した電流に等しい定電流でエネルギーパルスを前記組織に送達するために、前記電流を事前設定する、請求項16に記載の方法。
- 前記電気穿孔ステップが:
(a)電気穿孔された細胞においてインピーダンスを測定するステップ;
(b)電気穿孔された細胞において定電流を維持するために、前記測定されたインピーダンスに対してエネルギーパルスのエネルギーレベルを調節するステップ;
をさらに含み、
ここで、前記測定ステップおよび調節するステップは、エネルギーパルスの存続期間内に生じる請求項16に記載の方法。 - 前記電気穿孔ステップが、分散的パターンで前記エネルギーパルスを送達するパルスシーケンスパターンに従って、複数の電極に前記エネルギーパルスを送達するステップを含む、請求項16に記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US11553508P | 2008-11-17 | 2008-11-17 | |
| US61/115,535 | 2008-11-17 | ||
| PCT/US2009/064726 WO2010057159A2 (en) | 2008-11-17 | 2009-11-17 | Antigens that elicit immune response against flavivirus and methods of using same |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2012509067A true JP2012509067A (ja) | 2012-04-19 |
| JP5763541B2 JP5763541B2 (ja) | 2015-08-12 |
Family
ID=42170795
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011536584A Expired - Fee Related JP5763541B2 (ja) | 2008-11-17 | 2009-11-17 | フラビウイルスに対する免疫反応を引き起こす抗原及びその使用方法 |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US8961994B2 (ja) |
| EP (1) | EP2358733B1 (ja) |
| JP (1) | JP5763541B2 (ja) |
| KR (1) | KR101667069B1 (ja) |
| CN (2) | CN102292345B (ja) |
| AU (1) | AU2009313714B2 (ja) |
| BR (1) | BRPI0921359A2 (ja) |
| CA (2) | CA3001374A1 (ja) |
| WO (1) | WO2010057159A2 (ja) |
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2015530410A (ja) * | 2012-09-19 | 2015-10-15 | ザ トラスティーズ オブ ザ ユニバーシティ オブ ペンシルバニア | B型肝炎ウイルスコアタンパク質および表面抗原タンパク質をコードする核酸分子ならびにそれを含むワクチン |
| JP2016515126A (ja) * | 2013-03-15 | 2016-05-26 | ザ トラスティーズ オブ ザ ユニバーシティ オブ ペンシルバニア | ボツリヌス菌の各血清型の重鎖を使用する1価または多価のボツリヌス神経毒素ワクチン |
| JP2019006787A (ja) * | 2012-04-12 | 2019-01-17 | ザ トラスティーズ オブ ザ ユニバーシティ オブ ペンシルバニア | フィロウイルスコンセンサス抗原、核酸構築物、およびそれから作製されるワクチン、ならびにその使用方法 |
| JP2019506175A (ja) * | 2016-02-25 | 2019-03-07 | ザ トラスティーズ オブ ザ ユニバーシティ オブ ペンシルバニア | ジカウイルスに対する新規のワクチン |
| JP2019533993A (ja) * | 2016-09-19 | 2019-11-28 | ザ トラスティーズ オブ ザ ユニバーシティ オブ ペンシルバニア | ジカウイルスに対する新規ワクチンとジカウイルスに対する使用に向けたdna抗体構築物との組み合わせ |
| JP7256024B2 (ja) | 2013-03-15 | 2023-04-11 | ザ トラスティーズ オブ ザ ユニバーシティ オブ ペンシルバニア | ガンワクチン及びそれを用いた治療方法 |
Families Citing this family (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ES2718846T3 (es) * | 2010-11-12 | 2019-07-04 | Univ Pennsylvania | Antígenos de próstata consenso, molécula de ácido nucleico que los codifica y la vacuna y usos que los comprenden |
| PL2672992T3 (pl) | 2011-02-11 | 2020-11-02 | The Trustees Of The University Of Pennsylvania | Cząsteczka kwasu nukleinowego kodująca białko rdzeniowe wirusa zapalenia wątroby typu B i szczepionka je zawierająca |
| JP6567824B2 (ja) * | 2011-10-12 | 2019-08-28 | ザ トラスティーズ オブ ザ ユニバーシティ オブ ペンシルバニア | ヒトパピローマウイルスのワクチンおよびその使用方法 |
| CA2858884A1 (en) | 2011-12-12 | 2013-06-20 | The Trustees Of The University Of Pennsylvania | Proteins comprising mrsa pbp2a and fragments thereof, nucleic acids encoding the same, and compositions and their use to prevent and treat mrsa infections |
| EP3586870A1 (en) | 2013-03-12 | 2020-01-01 | The Trustees Of The University Of Pennsylvania | Improved vaccines for human papilloma virus and methods for using the same |
| ITRM20130458A1 (it) | 2013-08-05 | 2015-02-05 | Internat Ct For Genetic En Gineering And | Vaccino genetico anti-dengue virus basato sugli ectodomini della proteina envelope |
| US11022611B2 (en) * | 2016-05-03 | 2021-06-01 | Nirmidas Biotech, Inc. | Methods and systems for diagnosis and treatment of viral infections |
| JP6795468B2 (ja) * | 2017-07-14 | 2020-12-02 | ザ トラスティーズ オブ ザ ユニバーシティ オブ ペンシルバニア | ヒトパピローマウイルスのワクチンおよびその使用方法 |
| US11549125B2 (en) * | 2017-08-09 | 2023-01-10 | The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Closed-ended, linear, duplex adenoassociated virus DNA, and uses thereof |
| JP7075130B2 (ja) * | 2019-10-25 | 2022-05-25 | ザ トラスティーズ オブ ザ ユニバーシティ オブ ペンシルバニア | ヒトパピローマウイルスのワクチンおよびその使用方法 |
| CN114573668B (zh) * | 2020-11-30 | 2023-06-02 | 中国人民解放军军事科学院军事医学研究院 | 一种乙脑病毒样颗粒及其制备方法 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004510440A (ja) * | 2000-10-04 | 2004-04-08 | ザ・トラスティーズ・オブ・ザ・ユニバーシティ・オブ・ペンシルバニア | 高発現可能遺伝子 |
| WO2007052165A2 (en) * | 2005-10-17 | 2007-05-10 | Institut Pasteur | A lentiviral vector-based vaccine |
| WO2008048632A1 (en) * | 2006-10-17 | 2008-04-24 | Vgx Pharmaceuticals, Inc. | Electroporation devices and methods of using same for electroporation of cells in mammals |
Family Cites Families (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ATE302854T1 (de) | 1993-01-26 | 2005-09-15 | Univ Pennsylvania | Zusammensetzungen und verfahren zur verabreichung von genetischem material |
| US5593972A (en) | 1993-01-26 | 1997-01-14 | The Wistar Institute | Genetic immunization |
| US5962428A (en) | 1995-03-30 | 1999-10-05 | Apollon, Inc. | Compositions and methods for delivery of genetic material |
| AU743546B2 (en) * | 1998-10-05 | 2002-01-31 | Research Foundation For Microbial Diseases Of Osaka University, The | Enhanced immunogen for inactivated vaccine for infection with Japanese encephalitis viruses and process for producing the same |
| JP3543326B2 (ja) | 2001-08-30 | 2004-07-14 | ソニー株式会社 | 情報処理装置および方法、情報処理システム、情報配信装置、記録媒体、並びにプログラム |
| US8209006B2 (en) | 2002-03-07 | 2012-06-26 | Vgx Pharmaceuticals, Inc. | Constant current electroporation device and methods of use |
| US7245963B2 (en) | 2002-03-07 | 2007-07-17 | Advisys, Inc. | Electrode assembly for constant-current electroporation and use |
| AU2003295366B2 (en) | 2002-11-04 | 2011-11-24 | Advisys, Inc. | Synthetic muscle promoters with activities exceeding naturally occurring regulatory sequences in cardiac cells |
| CA2567324C (en) | 2003-05-30 | 2012-01-03 | Advisys, Inc. | Devices and methods for biomaterial production |
| US7060280B2 (en) * | 2003-06-11 | 2006-06-13 | Academia Sinica | Immunization against flavivirus |
| EA015907B1 (ru) * | 2004-10-20 | 2011-12-30 | Санофи Пастер Байолоджикс Ко. | Рекомбинантный флавивирус и его применение |
| AU2005320001B2 (en) * | 2004-12-24 | 2011-05-19 | The Research Foundation For Microbial Diseases Of Osaka University | Attenuated chimeric flavivirus bearing attenuated Japanese encephalitis virus gene as backbone |
| US20080044808A1 (en) | 2006-08-15 | 2008-02-21 | Qian-Li Song | West nile virus antigen and assay |
| CN101096680A (zh) * | 2007-05-31 | 2008-01-02 | 中国人民解放军军事医学科学院基础医学研究所 | 一种dna疫苗真核表达载体及其在制备基因疫苗中的应用 |
| TWI445547B (zh) * | 2007-06-08 | 2014-07-21 | Nat Health Research Institutes | 登革熱病毒胜肽疫苗及其製備與使用方法 |
| CA2702971C (en) * | 2007-11-14 | 2023-03-14 | Vgx Pharmaceuticals, Llc | Antibody production elicited by a dna vaccine delivered by electroporation |
-
2009
- 2009-11-17 US US13/129,599 patent/US8961994B2/en not_active Expired - Fee Related
- 2009-11-17 CA CA3001374A patent/CA3001374A1/en not_active Abandoned
- 2009-11-17 WO PCT/US2009/064726 patent/WO2010057159A2/en active Application Filing
- 2009-11-17 CN CN200980145447.5A patent/CN102292345B/zh not_active Expired - Fee Related
- 2009-11-17 JP JP2011536584A patent/JP5763541B2/ja not_active Expired - Fee Related
- 2009-11-17 CN CN201510712955.4A patent/CN105400798A/zh active Pending
- 2009-11-17 EP EP09826953.3A patent/EP2358733B1/en not_active Not-in-force
- 2009-11-17 KR KR1020117013778A patent/KR101667069B1/ko active IP Right Grant
- 2009-11-17 BR BRPI0921359-7A patent/BRPI0921359A2/pt not_active Application Discontinuation
- 2009-11-17 AU AU2009313714A patent/AU2009313714B2/en not_active Ceased
- 2009-11-17 CA CA2740598A patent/CA2740598C/en not_active Expired - Fee Related
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004510440A (ja) * | 2000-10-04 | 2004-04-08 | ザ・トラスティーズ・オブ・ザ・ユニバーシティ・オブ・ペンシルバニア | 高発現可能遺伝子 |
| WO2007052165A2 (en) * | 2005-10-17 | 2007-05-10 | Institut Pasteur | A lentiviral vector-based vaccine |
| WO2008048632A1 (en) * | 2006-10-17 | 2008-04-24 | Vgx Pharmaceuticals, Inc. | Electroporation devices and methods of using same for electroporation of cells in mammals |
Non-Patent Citations (4)
| Title |
|---|
| JPN6014018073; The Journal of Immunology vol.178, 2007, p.2699-2705 * |
| JPN6014018074; Vaccine vol.26, 2008, p.153-157 * |
| JPN6014018075; The Journal of Immunology vol.175, 2005, p.112-123 * |
| JPN6014018077; Nucleic Acids Research vol.15, no.20, 1987, p.8125-8148 * |
Cited By (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2019006787A (ja) * | 2012-04-12 | 2019-01-17 | ザ トラスティーズ オブ ザ ユニバーシティ オブ ペンシルバニア | フィロウイルスコンセンサス抗原、核酸構築物、およびそれから作製されるワクチン、ならびにその使用方法 |
| JP7164353B2 (ja) | 2012-04-12 | 2022-11-01 | ザ トラスティーズ オブ ザ ユニバーシティ オブ ペンシルバニア | フィロウイルスコンセンサス抗原、核酸構築物、およびそれから作製されるワクチン、ならびにその使用方法 |
| JP2015530410A (ja) * | 2012-09-19 | 2015-10-15 | ザ トラスティーズ オブ ザ ユニバーシティ オブ ペンシルバニア | B型肝炎ウイルスコアタンパク質および表面抗原タンパク質をコードする核酸分子ならびにそれを含むワクチン |
| JP2019163286A (ja) * | 2012-09-19 | 2019-09-26 | ザ トラスティーズ オブ ザ ユニバーシティ オブ ペンシルバニア | B型肝炎ウイルスコアタンパク質および表面抗原タンパク質をコードする核酸分子ならびにそれを含むワクチン |
| JP7050310B2 (ja) | 2012-09-19 | 2022-04-08 | ザ トラスティーズ オブ ザ ユニバーシティ オブ ペンシルバニア | B型肝炎ウイルスコアタンパク質および表面抗原タンパク質をコードする核酸分子ならびにそれを含むワクチン |
| JP2016515126A (ja) * | 2013-03-15 | 2016-05-26 | ザ トラスティーズ オブ ザ ユニバーシティ オブ ペンシルバニア | ボツリヌス菌の各血清型の重鎖を使用する1価または多価のボツリヌス神経毒素ワクチン |
| JP7256024B2 (ja) | 2013-03-15 | 2023-04-11 | ザ トラスティーズ オブ ザ ユニバーシティ オブ ペンシルバニア | ガンワクチン及びそれを用いた治療方法 |
| JP2019506175A (ja) * | 2016-02-25 | 2019-03-07 | ザ トラスティーズ オブ ザ ユニバーシティ オブ ペンシルバニア | ジカウイルスに対する新規のワクチン |
| JP7012365B2 (ja) | 2016-02-25 | 2022-03-04 | ザ トラスティーズ オブ ザ ユニバーシティ オブ ペンシルバニア | ジカウイルスに対する新規のワクチン |
| JP2019533993A (ja) * | 2016-09-19 | 2019-11-28 | ザ トラスティーズ オブ ザ ユニバーシティ オブ ペンシルバニア | ジカウイルスに対する新規ワクチンとジカウイルスに対する使用に向けたdna抗体構築物との組み合わせ |
Also Published As
| Publication number | Publication date |
|---|---|
| CN102292345B (zh) | 2015-12-02 |
| JP5763541B2 (ja) | 2015-08-12 |
| EP2358733A4 (en) | 2013-01-23 |
| BRPI0921359A2 (pt) | 2015-08-25 |
| KR20110086610A (ko) | 2011-07-28 |
| KR101667069B1 (ko) | 2016-10-17 |
| US8961994B2 (en) | 2015-02-24 |
| CA2740598A1 (en) | 2010-05-20 |
| EP2358733B1 (en) | 2015-07-08 |
| US20110262394A1 (en) | 2011-10-27 |
| CN102292345A (zh) | 2011-12-21 |
| EP2358733A2 (en) | 2011-08-24 |
| CN105400798A (zh) | 2016-03-16 |
| CA2740598C (en) | 2018-05-22 |
| WO2010057159A3 (en) | 2010-07-08 |
| WO2010057159A2 (en) | 2010-05-20 |
| AU2009313714A1 (en) | 2010-05-20 |
| AU2009313714B2 (en) | 2016-05-19 |
| CA3001374A1 (en) | 2010-05-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5763541B2 (ja) | フラビウイルスに対する免疫反応を引き起こす抗原及びその使用方法 | |
| JP7142427B2 (ja) | コンセンサス前立腺抗原、それをコードする核酸分子、ならびにそれを含むワクチンおよび用途 | |
| JP6195943B2 (ja) | インフルエンザウイルスの複数のサブタイプに対する新規ワクチン | |
| KR20100103677A (ko) | 뎅기 바이러스 다중 서브타입에 대항하는 신규한 백신 | |
| JP7123800B2 (ja) | がんのワクチン及びそれを用いた処置の方法 | |
| AU2020203908B2 (en) | Consensus prostate antigens nucleic acid molecule encoding the same and vaccine and uses comprising the same | |
| KR20100100868A (ko) | 전기천공에 의해 전달되는 dna 백신에 의해 유도되는 항체의 생산 방법 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20121109 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140513 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20140813 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20140820 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20141112 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20150512 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20150611 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5763541 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |