JP2012106948A - 分岐オキサアルキル鎖を有している化合物およびその利用 - Google Patents
分岐オキサアルキル鎖を有している化合物およびその利用 Download PDFInfo
- Publication number
- JP2012106948A JP2012106948A JP2010256887A JP2010256887A JP2012106948A JP 2012106948 A JP2012106948 A JP 2012106948A JP 2010256887 A JP2010256887 A JP 2010256887A JP 2010256887 A JP2010256887 A JP 2010256887A JP 2012106948 A JP2012106948 A JP 2012106948A
- Authority
- JP
- Japan
- Prior art keywords
- compound
- chain
- oxaalkyl
- synthesis example
- abbreviation
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Landscapes
- Lubricants (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
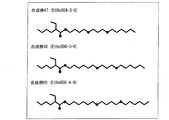
【解決手段】本発明に係る化合物は、分子中に、少なくとも1つの側鎖を有しているオキサアルキル鎖を有している。
【選択図】図1
Description
であり、R1〜R4のうち少なくとも1つは、置換基である。)。
本発明に係る化合物(以下、「本発明の化合物」ともいう。)は、分子中に、少なくとも1つの側鎖を有しているオキサアルキル鎖を有している化合物である。
であり、R1〜R4のうち少なくとも1つは、置換基である。)」とも言換え可能である。
H−(CH2)a−O−(CH2)b−O−(CH2)c−H … (2)
(一般式(1)中、a〜cはそれぞれ独立して1以上の整数である。)
で表す場合、エーテル酸素原子(−O−)で区切られるアルキレン基の数、すなわち、上記一般式(2)における整数a〜cは、目的に応じて適宜設定することができ、それぞれ独立して偶数であっても奇数であってもよい。
本発明に係る化合物の製造方法は特に限定されるものではなく、従来公知の方法を用いて好適に製造することができる。
本発明に係る化合物は、同じ分子量の直鎖アルキル鎖を有する化合物または直鎖オキサアルキル鎖を有する化合物と比較して、低融点または低ガラス転移点で、且つ低動粘度であるので、本発明に係る化合物または当該化合物を含有している組成物は、例えば、潤滑剤、可塑剤、界面活性剤、液晶分子、エラストマー、合成樹脂、粘着剤等として好適に用いることができる。なお、上記「本発明に係る化合物」については、上記「(1)本発明に係る化合物」の項で説明したとおりであるので、ここでは説明は省略する。
本発明に係る潤滑剤は、本発明に係る化合物を含有していれば、本発明に係る化合物を含有していない以外は同じ組成の潤滑剤と比較して、低融点または低ガラス転移点で、且つ低動粘度の組成物となり得る。このため、潤滑剤における本発明に係る化合物の含有量は特に限定されるものではないが、実用的な観点でいえば、潤滑剤の総重量に対して、20重量%以上であることが好ましく、50重量%以上であることがより好ましい。
本発明に係る潤滑剤は、潤滑剤の本発明の化合物を基油として配合することによって製造することができる。
本発明に係る化合物は、直鎖アルキル鎖を有する化合物および/または直鎖オキサアルキル鎖を有する化合物を含有している組成物(以下、「改質対象組成物」と称する)と混合することによって、当該改質対象組成物の融点またはガラス転移点、および動粘度を顕著に低下させることができる。従って、本発明に係る化合物は、「融点またはガラス転移点および動粘度低下剤」と読み替えることもできる。なお、本明細書において、上記「融点またはガラス転移点および動粘度低下剤」とは、「融点またはガラス転移点および動粘度を低下させるための組成物」を意図している。なお、本明細書では、融点を低下させるだけでなく、融点を消失させることも含めて、「融点を低下させる」と表現している。
合成例を以下に示す。
<モノオキサアルカノール>
〔合成例1:H−(CH2)6−O−(CH2)3−OH(略称:6−3OH)の製造〕
H−(CH2)6−Cl(174.8g)と、HO−(CH2)3−OH(430.2g)とを、50%水酸化ナトリウム水溶液(136.5g)中で、TBAH(23.4g)存在下、85℃、21時間反応させることにより、H−(CH2)6−O−(CH2)3−OHを製造した。
H−(CH2)6−Cl(166g)と、HO−(CH2)4−OH(381.3g)とを、50%水酸化ナトリウム水溶液(127.0g)中で、TBAH(46.8g)存在下、80℃、22時間反応させることにより、H−(CH2)6−O−(CH2)4−OHを製造した。
〔合成例3:H−(CH2)4−O−(CH2)2−Cl(略称:4−2Cl)の製造〕
窒素気流下で、H−(CH2)4−O−(CH2)2−OH(177.3g)と、ピリジン(177.8g)との溶液に塩化チオニル(267.8g)を滴下し、80℃で3時間反応させることにより、H−(CH2)4−O−(CH2)2−Cl(4−2Cl)を製造した。
窒素気流下で、H−(CH2)6−O−(CH2)2−OH(198.9g)と、ピリジン(157.5g)との溶液に塩化チオニル(222.8g)を滴下し、80℃で2時間反応させることにより、H−(CH2)6−O−(CH2)2−Clを製造した。
窒素気流下で、合成例1で得られたH−(CH2)6−O−(CH2)3−OH(167.2g)と、ピリジン(115.5g)との溶液に塩化チオニル(173.7g)を滴下し、80℃で2時間反応させることにより、H−(CH2)6−O−(CH2)3−Clを製造した。
H−(CH2)6−O−H(124.2g)と、Cl−(CH2)4−Cl(465.7g)とを、50%水酸化ナトリウム水溶液(119.1g)中で、TBAH(43.3g)存在下、82℃、22時間反応させることにより、H−(CH2)6−O−(CH2)4−Clを製造した。
H−(CH2)6−OH(74.5g)と、Cl−(CH2)6−Cl(460.2g)とを、50%水酸化ナトリウム水溶液(69.8g)中で、TBAH(22.8g)存在下、85℃、24時間反応させることにより、H−(CH2)6−O−(CH2)6−Clを製造した。
H−(CH2)8−OH(100.3g)と、Cl−(CH2)4−Cl(170.7g)とを、50%水酸化ナトリウム水溶液(78.2g)中で、TBAH(52.7g)存在下、85℃、24時間反応させることにより、H−(CH2)8−O−(CH2)4−Clを製造した。
〔合成例9:H−(CH2)4−O−(CH2)2−O−(CH2)4−OH(略称:4−2−4OH)の製造〕
合成例3で得られたH−(CH2)4−O−(CH2)2−Cl(略称:4−2Cl、116.0g)と、HO−(CH2)4−OH(305.8g)とを、50%水酸化ナトリウム水溶液(85.2g)中で、TBAH(24.7g)存在下、80℃、23時間反応させることにより、H−(CH2)4−O−(CH2)2−O−(CH2)4−OHを製造した。
合成例4で得られたH−(CH2)6−O−(CH2)2−Cl(略称:6−2Cl、172g)と、HO−(CH2)6−OH(372.4g)とを、50%水酸化ナトリウム水溶液(102.9g)中で、TBAH(36.5g)存在下、84℃、22時間反応させることにより、H−(CH2)6−O−(CH2)2−O−(CH2)6−OHを製造した。
合成例5で得られたH−(CH2)6−O−(CH2)3−Cl(略称:6−3Cl、66.5g)と、HO(CH2)4OH(100.6g)とを、50%水酸化ナトリウム水溶液(35.7g)中で、TBAH(6.3g)存在下、90℃、24時間反応させることにより、H−(CH2)6−O−(CH2)3−O−(CH2)4−OHを製造した。
合成例5で得られたH−(CH2)6−O−(CH2)3−Cl(略称:6−3Cl、67.4g)と、HO−(CH2)6−OH(98g)とを、50%水酸化ナトリウム水溶液(27.2g)中で、TBAH(7.5g)存在下、83℃、24時間反応させることにより、H−(CH2)6−O−(CH2)3−O−(CH2)6−OHを製造した。
合成例6で得られたH−(CH2)6−O−(CH2)4−Cl(略称:6−4Cl、51.2g)と、HO−(CH2)6−OH(92.6g)とを、50%水酸化ナトリウム水溶液(24.9g)中で、TBAH(9.9g)存在下、80℃、21時間反応させることにより、H−(CH2)6−O−(CH2)4−O−(CH2)6−OHを製造した。
合成例8で得られたH−(CH2)8−O−(CH2)4−Cl(略称:8−4Cl、47.2g)と、HO(CH2)4OH(65.4g)とを、50%水酸化ナトリウム水溶液(24.5g)中で、TBAH(4.2g)存在下、90℃、24時間反応させることにより、H−(CH2)8−O−(CH2)4−O−(CH2)4−OHを製造した。
〔合成例15:H−(CH2)6−O−(CH2)2−O−(CH2)4−Cl(略称:6−2−4Cl)の製造〕
H−(CH2)6−O−(CH2)2−O−H(183.1g)と、Cl−(CH2)4−Cl(563.3g)とを、50%水酸化ナトリウム水溶液(124.2g)中で、TBAH(21.1g)存在下、90℃、24時間反応させることにより、H−(CH2)6−O−(CH2)2−O−(CH2)4−Clを製造した。
H−(CH2)6−O−(CH2)2−O−H(157.9g)と、Cl−(CH2)6−Cl(353.2g)とを、50%水酸化ナトリウム水溶液(106.2g)中で、TBAH(25.5g)存在下、82℃、18時間反応させることにより、H−(CH2)6−O−(CH2)2−O−(CH2)6−Clを製造した。
H−(CH2)6−O−(CH2)3−O−H(51.9g)と、Cl−(CH2)4−Cl(159.4g)とを、50%水酸化ナトリウム水溶液(32.8g)中で、TBAH(5.6g)存在下、90℃、23時間反応させることにより、H−(CH2)6−O−(CH2)3−O−(CH2)4−Clを製造した。
〔合成例18:H−(CH2)6−O−(CH2)2−Br(略称:6−2Br)の製造〕
窒素気流下で、H−(CH2)6−O−(CH2)2−O−H(49.2g)にPBr3(30.9g)を滴下し、120℃で2時間反応させることにより、H−(CH2)6−O−(CH2)2−Brを製造した。
窒素気流下で、H−(CH2)6−O−(CH2)2−O−H(107g)にPBr3(60.4g)を滴下し、120℃で2時間反応させることにより、H−(CH2)6−O−(CH2)4−Brを製造した。
窒素気流下で、H−(CH2)6−O−(CH2)2−O−(CH2)2−O−H(57.7g)にPBr3(37.1g)を滴下し、120℃で2時間反応させることにより、H−(CH2)6−O−(CH2)2−O−(CH2)2−Brを製造した。
〔合成例21:H−(CH2)6−O−(CH2)5−CO−O−H(略称:6−6OOH)の製造〕
窒素気流下で、99%エタノール(235.4g)と、Na(16.3g)とを反応させ、更にマロン酸ジエチル(125.6g)を反応させ、40℃で、合成例19で得られたH−(CH2)6−O−(CH2)4−Br(略称:6−4Br)(144.7g)を滴下し、50℃で24時間反応させた。
窒素気流下で、99%エタノール(138g)と、Na(10.5g)とを反応させ、更にマロン酸ジエチル(75.2g)を反応させ、40℃で、合成例20で得られたH−(CH2)6−O−(CH2)2−O−(CH2)2−Br(略称:6−2−2Br、105.5g)を滴下し、50℃で21時間反応させた。
〔合成例23:H−(CH2)6−O−CH2−C(CH3)2−CH2−O−H(略称:6−PrMe2OH)の製造〕
H−(CH2)6−Cl(32.9g)と、H−O−CH2−C(CH3)2−CH2−O−H(105.3g)とを、50%水酸化ナトリウム水溶液(28g)中で、TBAH(8.6g)存在下、90℃、24時間反応させることにより、H−(CH2)6−O−CH2−C(CH3)2−CH2−O−H(略称:6−PrMe2OH)を製造した。
H−(CH2)12−Br(100.6g)と、H−O−CH2−C(CH3)2−CH2−O−H(160g)とを、50%水酸化ナトリウム水溶液(41.9g)中で、TBAH(14.1g)存在下、90℃、13時間反応させることにより、H−(CH2)12−O−CH2−C(CH3)2−CH2−O−H(略称:12−PrMe2OH)を製造した。
<直鎖対称ジエーテル>
〔比較合成例1:H−(CH2)12−O−(CH2)3−O−(CH2)12−H(略称:3(O12)2)の製造〕
H−(CH2)12−Cl(76.7g)と、H−O−(CH2)3−O−H(9.3g)とを、50%水酸化ナトリウム水溶液(30.8g)、TBAH(8.4g)存在下、90℃、48時間反応させることにより、H−(CH2)12−O−(CH2)3−O−(CH2)12−Hを製造した。
合成例8で得られたH−(CH2)8−O−(CH2)4−Cl(略称:8−4Cl、74.8g)と、H−O−(CH2)3−O−H(11.3g)とを、50%水酸化ナトリウム水溶液(30.8g)、TBAH(7.7g)存在下、90℃、24時間反応させた後、50%水酸化ナトリウム水溶液を少量添加し、さらに24.5時間反応させることにより、H−(CH2)8−O−(CH2)4−O−(CH2)3−O−(CH2)4−O−(CH2)8−Hを製造した。
合成例7で得られたH−(CH2)6−O−(CH2)6−Cl(略称:6−6Cl、81.6g)と、H−O−(CH2)3−O−H(9.2g)とを、50%水酸化ナトリウム水溶液(34.0g)、TBAH(7.8g)存在下、90℃、24時間反応させた後、50%水酸化ナトリウム水溶液を少量添加し、さらに24.5時間反応させることにより、H−(CH2)6−O−(CH2)6−O−(CH2)3−O−(CH2)6−O−(CH2)6−Hを製造した。
合成例15で得られたH−(CH2)6−O−(CH2)2−O−(CH2)4−Cl(略称:6−2−4Cl、47.0g)と、H−O−(CH2)3−O−H(6.0g)とを、50%水酸化ナトリウム水溶液(22.1g)、TBAH(5.1g)存在下、90℃、24時間反応させた後、50%水酸化ナトリウム水溶液を少量添加し、さらに24時間反応させることによりH−(CH2)6−O−(CH2)2−O−(CH2)4−O−(CH2)3−O−(CH2)4−O−(CH2)2−O−(CH2)6−Hを製造した。
合成例16で得られたH−(CH2)6−O−(CH2)2−O−(CH2)6−Cl(43.7g)と、H−O−(CH2)3−O−H(4.1g)とを、50%水酸化ナトリウム水溶液(16g)、ジエチレングリコールジメチルエーテル(8.3g)中で、TBAH(3.8g)存在下、90℃、48時間反応させることにより、H−(CH2)6−O−(CH2)2−O−(CH2)6−O−(CH2)3−O−(CH2)6−O−(CH2)2−O−(CH2)6−Hを製造した。
〔比較合成例6:H−(CH2)6−O−(CH2)2−O−(CH2)3−CO−O−(CH2)4−O−(CH2)2−O−(CH2)6−H(略称:6−2−4OO4−2−6)の製造〕
合成例22で得られたH−(CH2)6−O−(CH2)2−O−(CH2)3−CO−O−H(7.7g)と、H−(CH2)6−O−(CH2)2−O−(CH2)4−O−H(6.8g)とを、酸触媒H2SO4(0.16ml)と共に、80℃、4時間減圧下で反応させることにより、H−(CH2)6−O−(CH2)2−O−(CH2)3−CO−O−(CH2)4−O−(CH2)2−O−(CH2)6−Hを製造した。
〔比較合成例7:H−(CH2)7−CO−O−(CH2)6−O−(CH2)4−O−(CH2)6−H(略称:8OO6−4−6)の製造〕
H−(CH2)7−CO−O−H(3.8g)と、H−(CH2)6−O−(CH2)4−O−(CH2)6−O−H(5.3g)とを、酸触媒H2SO4(0.1ml)と共に、80℃、4時間減圧下で反応させることにより、H−(CH2)7−CO−O−(CH2)6−O−(CH2)4−O−(CH2)6−Hを製造した。
合成例22で得られたH−(CH2)6−O−(CH2)2−O−(CH2)3−CO−O−H(7.6g)と、H−(CH2)12−O−H(8.4g)とを、酸触媒H2SO4(0.18ml)と共に、80℃、4時間減圧下で反応させることにより、H−(CH2)6−O−(CH2)2−O−(CH2)3−CO−O−(CH2)12−Hを製造した。
合成例22で得られたH−(CH2)6−O−(CH2)2−O−(CH2)3−CO−O−H(8.9g)と、H−(CH2)6−O−(CH2)6−O−H(6.3g)とを、酸触媒H2SO4(0.16ml)と共に、80℃、4時間減圧下で反応させることにより、H−(CH2)6−O−(CH2)2−O−(CH2)3−CO−O−(CH2)6−O−(CH2)6−Hを製造した。
〔合成例25:H−(CH2)12−O−CH2−CH(CH3)−CH2−O−(CH2)12−H(略称:PrMe(O12)2)の製造〕
H−(CH2)12−Cl(44.8g)と、H−O−CH2−CH(CH3)−CH2−O−H(6.3g)とを、50%水酸化ナトリウム水溶液(12.8g)中で、TBAH(1.9g)存在下、85℃、51時間反応させることにより、H−(CH2)12−O−CH2−CH(CH3)−CH2−O−(CH2)12−Hを製造した。
合成例8で得られたH−(CH2)8−O−(CH2)4−Cl(48.9g)と、H−O−CH2−CH(CH3)−CH2−O−H(6.0g)とを、50%水酸化ナトリウム水溶液(12.4g)中で、TBAH(1.6g)存在下、85℃、48時間反応させることにより、H−(CH2)8−O−(CH2)4−O−CH2−CH(CH3)−CH2−O−(CH2)4−O−(CH2)8−Hを製造した。
合成例7で得られたH−(CH2)6−O−(CH2)6−Cl(49.5g)と、H−O−CH2−CH(CH3)−CH2−O−H(5.7g)とを、50%水酸化ナトリウム水溶液(11.9g)中で、TBAH(1.9g)存在下、85℃、48時間反応させることにより、H−(CH2)6−O−(CH2)6−O−CH2−CH(CH3)−CH2−O−(CH2)6−O−(CH2)6−Hを製造した。
合成例15で得られたH−(CH2)6−O−(CH2)2−O−(CH2)4−Cl(50g)と、H−O−CH2−CH(CH3)−CH2−O−H(5.2g)とを、50%水酸化ナトリウム水溶液(14.9g)中で、TBAH(4.2g)存在下、90℃、48時間反応させることにより、H−(CH2)6−O−(CH2)2−O−(CH2)4−O−CH2−CH(CH3)−CH2−O−(CH2)4−O−(CH2)2−O−(CH2)6−Hを製造した。
合成例16で得られたH−(CH2)6−O−(CH2)2−O−(CH2)6−Cl(41.9g)と、H−O−CH2−CH(CH3)−CH2−O−H(6.5g)とを、50%水酸化ナトリウム水溶液(10.2g)中で、TBAH(1.4g)存在下、85℃、47時間反応させることにより、H−(CH2)6−O−(CH2)2−O−(CH2)6−O−CH2−CH(CH3)−CH2−O−(CH2)6−O−(CH2)2−O−(CH2)6−Hを製造した。
H−(CH2)12−Cl(32.5g)と、H−O−CH2−C(CH3)2−CH2−O−H(5.3g)とを、50%水酸化ナトリウム水溶液(22.5g)およびジエチレングリコールジメチルエーテル(17.3g)中で、TBAH(1.9g)存在下、80℃、24時間反応させることにより、H−(CH2)12−O−CH2−C(CH3)2−CH2−O−(CH2)12−Hを製造した。
合成例8で得られたH−(CH2)8−O−(CH2)4−Cl(67.2g)と、H−O−CH2−C(CH3)2−CH2−O−H(10.4g)とを、50%水酸化ナトリウム水溶液(30.5g)およびジエチレングリコールジメチルエーテル(9.9g)中で、TBAH(7.1g)存在下、90℃で24時間反応させた後50%水酸化ナトリウム水溶液を少量添加し、さらに24時間反応させることにより、H−(CH2)8−O−(CH2)4−O−CH2−C(CH3)2−CH2−O−(CH2)4−O−(CH2)8−Hを製造した。
合成例7で得られたH−(CH2)6−O−(CH2)6−Cl(79.5g)と、H−O−CH2−C(CH3)2−CH2−O−H(10.5g)とを、50%水酸化ナトリウム水溶液(24.4g)およびジエチレングリコールジメチルエーテル(11.7g)中で、TBAH(7.0g)存在下、90℃で5時間反応させた後50%水酸化ナトリウム水溶液を少量添加し、さらに16時間反応後に50%水酸化ナトリウム水溶液を少量添加し、引き続き13時間反応させることにより、H−(CH2)6−O−(CH2)6−O−CH2−C(CH3)2−CH2−O−(CH2)6−O−(CH2)6−Hを製造した。
H−(CH2)4−O−(CH2)2−O−(CH2)4−Cl(21.0g)と、H−O−CH2−C(CH3)2−CH2−O−H(3.5g)とを、50%水酸化ナトリウム水溶液(8.0g)およびジエチレングリコールジメチルエーテル(6.4g)中で、TBAH(1.2g)存在下、80℃で24時間反応させることにより、H−(CH2)4−O−(CH2)2−O−(CH2)4−O−CH2−C(CH3)2−CH2−O−(CH2)4−O−(CH2)2−O−(CH2)4−Hを製造した。
合成例15で得られたH−(CH2)6−O−(CH2)2−O−(CH2)4−Cl(122.1g)と、H−O−CH2−C(CH3)2−CH2−O−H(19.9g)とを、50%水酸化ナトリウム水溶液(47.5g)、ジエチレングリコールジメチルエーテル(26.2g)中で、TBAH(13.9g)存在下、90℃、50時間反応させることにより、H−(CH2)6−O−(CH2)2−O−(CH2)4−O−CH2−C(CH3)2−CH2−O−(CH2)4−O−(CH2)2−O−(CH2)6−Hを製造した。
合成例17で得られたH−(CH2)6−O−(CH2)3−O−(CH2)4−Cl(99%24g)と、H−O−CH2−C(CH3)2−CH2−O−H(3.3g)とを、50%水酸化ナトリウム水溶液(7.8g)、ジエチレングリコールジメチルエーテル(5.8g)中で、TBAH(2g)存在下、90℃、48時間反応させることにより、H−(CH2)6−O−(CH2)3−O−(CH2)4−O−CH2−C(CH3)2−CH2−O−(CH2)4−O−(CH2)3−O−(CH2)6−Hを製造した。
合成例16で得られたH−(CH2)6−O−(CH2)2−O−(CH2)6−Cl(101.0g)と、H−O−CH2−C(CH3)2−CH2−O−H(12.5g)とを、50%水酸化ナトリウム水溶液(36.2g)およびジエチレングリコールジメチルエーテル(18.4g)中で、TBAH(8.5g)存在下、90℃で24時間反応させた後50%水酸化ナトリウム水溶液を少量添加し、さらに24時間反応させることにより、H−(CH2)6−O−(CH2)2−O−(CH2)6−O−CH2−C(CH3)2−CH2−O−(CH2)6−O−(CH2)2−O−(CH2)6−Hを製造した。
H−(CH2)6−O−(CH2)3−O−(CH2)6−Cl(85%、48g)と、H−O−CH2−C(CH3)2−CH2−O−H(5.3g)とを、50%水酸化ナトリウム水溶液(11.3g)、ジエチレングリコールジメチルエーテル(7.2g)中で、TBAH(3.6g)存在下、90℃、48時間反応させることにより、H−(CH2)6−O−(CH2)3−O−(CH2)6−O−CH2−C(CH3)2−CH2−O−(CH2)6−O−(CH2)3−O−(CH2)6−Hを製造した。
合成例15で得られたH−(CH2)6−O−(CH2)2−O−(CH2)4−Cl(93%、42.3g)と、H−O−CH2−C(C2H5)2−CH2−O−H(7.3g)とを、50%水酸化ナトリウム水溶液(14.2g)、ジエチレングリコールジメチルエーテル(9.7g)中で、TBAH(3.8g)存在下、90℃、48時間反応させることにより、H−(CH2)6−O−(CH2)2−O−(CH2)4−O−CH2−C(C2H5)2−CH2−O−(CH2)4−O−(CH2)2−O−(CH2)6−Hを製造した。
〔合成例39:H−(CH2)14−O−CH2−CH(C2H5)−(CH2)4−H(略称:EtHxO14)の製造〕
H−(CH2)14−Cl(13.6g)と、H−(CH2)4−CH(C2H5)−CH2−O−H(7.5g)とを、50%水酸化ナトリウム水溶液(6.5g)中で、TBAH(0.9g)存在下、90℃、24時間反応させることにより、H−(CH2)14−O−CH2−CH(C2H5)−(CH2)4−Hを製造した。
合成例8で得られたH−(CH2)8−O−(CH2)4−Cl(11.4g)と、H−(CH2)4−CH(C2H5)−CH2−O−H(6.5g)とを、50%水酸化ナトリウム水溶液(5.2g)中で、TBAH(0.9g)存在下、90℃、24時間反応させることにより、H−(CH2)8−O−(CH2)4−O−CH2−CH(C2H5)−(CH2)4−Hを製造した。
合成例15で得られたH−(CH2)6−O−(CH2)2−O−(CH2)4−Cl(97%、13.3g)と、H−(CH2)4−CH(C2H5)−CH2−O−H(8.1g)とを、50%水酸化ナトリウム水溶液(6.1g)中で、TBAH(1.7g)存在下、90℃、24時間反応させることにより、H−(CH2)6−O−(CH2)2−O−(CH2)4−O−CH2−CH(C2H5)−(CH2)4−Hを製造した。
〔合成例42:H−(CH2)6−O−(CH2)2−O−(CH2)3−CO−O−CH2−C(CH3)2−CH2−O−(CH2)6−H(略称:6−2−4OOPrMe2O6)の製造〕
合成例23で得られたH−(CH2)6−O−CH2−C(CH3)2−CH2−O−H(6−3Me2OH)(6.2g)と、合成例22で得られたH−(CH2)6−O−(CH2)2−O−(CH2)3−CO−O−H(10.8g)とを、酸触媒H2SO4(0.18ml)と共に、80℃、4時間減圧下で反応させることにより、H−(CH2)6−O−(CH2)2−O−(CH2)3−CO−O−CH2−C(CH3)2−CH2−O−(CH2)6−Hを製造した。
合成例24で得られたH−(CH2)12−O−CH2−C(CH3)2−CH2−O−H(略称:12−3Me2OH、6.5g)と、H−(CH2)11−CO−O−H(6.0g)とを、酸触媒H2SO4(0.13ml)と共に、80℃、2時間減圧下で反応させることにより、H−(CH2)11−CO−O−CH2−C(CH3)2−CH2−O−(CH2)12−Hを製造した。
合成例22で得られたH−(CH2)6−O−(CH2)2−O−(CH2)3−CO−O−H(7.6g)と、H−(CH2)12−O−CH2−CH(CH3)2−CH2−O−H(6.4g)とを、酸触媒H2SO4(0.13ml)と共に、80℃、7時間減圧下で反応させることにより、H−(CH2)6−O−(CH2)2−O−(CH2)3−CO−O−CH2−CH(CH3)2−CH2−O−OC−(CH2)11−Hを製造した。
H−(CH2)4−CH(C2H5)−CH2−O−H(7.8g)と、合成例22で得られたH−(CH2)6−O(CH2)2−O−(CH2)3−CO−O−H(9.8g)とを、酸触媒H2SO4(0.16ml)と共に、80℃、2時間減圧下で反応させることにより、H−(CH2)6−O(CH2)2−O−(CH2)3−CO−O−CH2−CH(C2H5)−(CH2)4−Hを製造した。
H−(CH2)6−O−(CH2)2−O−(CH2)4−O−H(90%、6.9g)と、H−(CH2)4−CH(C2H5)−CO−O−H(5.2g)とを、酸触媒H2SO4(0.16ml)と共に、80℃、4時間減圧下で反応させることにより、H−(CH2)4−CH(C2H5)−CO−O−(CH2)4−O−(CH2)2−O−(CH2)6−Hを製造した。
合成例11で得られたH−(CH2)6−O−(CH2)3−O−(CH2)4−OH(12.6g)と、H(CH2)4CH(C2H5)COOH(7.4g)とを、酸触媒H2SO4(0.3ml)と共に、80℃、4時間減圧下で反応させることにより、H−(CH2)4−CH(C2H5)−CO−O−(CH2)4−O−(CH2)3−O−(CH2)6−Hを製造した。
合成例14で得られたH−(CH2)8−O−(CH2)4−O−(CH2)4−OH(8g)と、H(CH2)4CH(C2H5)COOH(4.4g)とを、酸触媒H2SO4(0.2ml)と共に、80℃、4時間減圧下で反応させることにより、H−(CH2)4−CH(C2H5)−CO−O−(CH2)4−O−(CH2)4−O−(CH2)8−Hを製造した。
合成例12で得られたH−(CH2)6−O−(CH2)3−O−(CH2)6−OH(15.3g)と、H(CH2)4CH(C2H5)COOH(7.8g)とを、酸触媒H2SO4(0.3ml)と共に、80℃、6時間30分減圧下で反応させることにより、H−(CH2)4−CH(C2H5)−CO−O−(CH2)6−O−(CH2)3−O−(CH2)6−Hを製造した。
合成例13で得られたH−(CH2)6−O−(CH2)4−O−(CH2)6−OH(略称:6−4−6OH、13.6g)と、H−(CH2)4−CH(C2H5)−COOH(8.2g)とを、酸触媒H2SO4(0.2ml)と共に、減圧下80℃、4時間減圧下で反応させることにより、H−(CH2)4−CH(C2H5)−CO−O−(CH2)6−O−(CH2)4−O−(CH2)6−Hを製造した。
〔合成例51:H−(CH2)11−CO−O−CH2−C(CH3)2−CH2−O−CO−(CH2)11−H(略称:(12OO)2PrMe2)の製造〕
H−(CH2)11−CO−O−H(7.6g)と、H−O−CH2−CH(CH3)2−CH2−O−H(8.4g)とを、酸触媒H2SO4(0.18ml)と共に、80℃、4時間減圧下で反応させることにより、H−(CH2)11−CO−O−CH2−C(CH3)2−CH2−O−CO−(CH2)11−Hを製造した。
合成例21で得られたH−(CH2)6−O−(CH2)5−CO−O−H(8.7g)と、H−O−CH2−CH(CH3)2−CH2−O−H(1.7g)とを、酸触媒H2SO4(0.2ml)と共に、80℃、4時間減圧下で反応させることにより、H−(CH2)6−O−(CH2)5−CO−O−CH2−C(CH3)2−CH2−O−CO−(CH2)5−O−(CH2)6−Hを製造した。
合成例22で得られたH−(CH2)6−O−(CH2)2−O−(CH2)3−CO−O−H(10g)と、H−O−CH2−CH(CH3)2−CH2−O−H(1.5g)とを、酸触媒H2SO4(0.08ml)と共に、80℃、4時間減圧下で反応させることにより、H−(CH2)6−O−(CH2)2−O−(CH2)3−CO−O−CH2−CH(CH3)2−CH2−O−OC−(CH2)3−O−(CH2)2−O−(CH2)6−Hを製造した。
〔合成例54:H−(CH2)6−O−(CH2)2−O−(CH2)3−CO−O−CH2−C(−CH2−O−OC−(CH2)3−O−(CH2)2−O−(CH2)6−H)2−(CH2)2−H(略称:(6−2−4OO)3PrEt)の製造〕
合成例22で得られたH−(CH2)6−O−(CH2)2−O−(CH2)3−CO−O−H(14.8g)と、トリメチロールプロパン(1.5g)とを、酸触媒H2SO4(0.33ml)と共に、80℃、4時間減圧下で反応させることにより、H−(CH2)6−O−(CH2)2−O−(CH2)3−CO−O−CH2−C(−CH2−O−OC−(CH2)3−O−(CH2)2−O−(CH2)6−H)2−(CH2)2−Hを製造した。
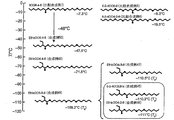
得られた化合物の融点およびガラス転移点は、DSC(島津社製、DSC−50)を用いて測定した。
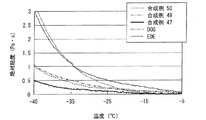
実施例1で合成した化合物を代表して、合成例47、49および50の化合物の物性を測定した。
化合物の融点およびガラス転移点は、DSC(島津社製、DSC−50)を用いて測定した。
Claims (6)
- 分子中に、少なくとも1つの側鎖を有しているオキサアルキル鎖を有していることを特徴とする、化合物。
- 上記側鎖は、アルキル基、オキサアルキル基、ハロゲン基およびシリコーン基からなる群から選択されることを特徴とする、請求項1に記載の化合物。
- 上記置換基は、アルキル基、オキサアルキル基、ハロゲン基およびシリコーン基からなる群から選択されることを特徴とする、請求項2に記載の化合物。
- 上記オキサアルキル鎖は、分子中に、少なくとも1つのエステル結合をさらに有していることを特徴とする、請求項1〜4の何れか1項に記載の化合物。
- 請求項1〜5の何れか1項に記載の化合物を含有していることを特徴とする、潤滑剤。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2010256887A JP5760218B2 (ja) | 2010-11-17 | 2010-11-17 | 分岐オキサアルキル鎖を有している化合物およびその利用 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2010256887A JP5760218B2 (ja) | 2010-11-17 | 2010-11-17 | 分岐オキサアルキル鎖を有している化合物およびその利用 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2012106948A true JP2012106948A (ja) | 2012-06-07 |
| JP5760218B2 JP5760218B2 (ja) | 2015-08-05 |
Family
ID=46493005
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010256887A Expired - Fee Related JP5760218B2 (ja) | 2010-11-17 | 2010-11-17 | 分岐オキサアルキル鎖を有している化合物およびその利用 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP5760218B2 (ja) |
Cited By (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013082900A (ja) * | 2011-09-30 | 2013-05-09 | Balbis:Kk | 軸受用潤滑剤組成物 |
| WO2015040937A1 (ja) * | 2013-09-20 | 2015-03-26 | 株式会社Moresco | 含エーテルモノエステル化合物およびその利用 |
| JP2015057453A (ja) * | 2012-12-27 | 2015-03-26 | 出光興産株式会社 | ジアルキルエーテル |
| JP2015199934A (ja) * | 2014-03-31 | 2015-11-12 | ウシオケミックス株式会社 | 潤滑性化合物及びそれを含む潤滑剤組成物 |
| JP2016074816A (ja) * | 2014-10-06 | 2016-05-12 | 株式会社バルビス | 潤滑油基油及び潤滑油組成物 |
| WO2017175522A1 (ja) * | 2016-04-05 | 2017-10-12 | 株式会社Moresco | オキサ酸化合物 |
| JP2018062632A (ja) * | 2016-10-14 | 2018-04-19 | 国立大学法人広島大学 | 潤滑油用基油及び潤滑油 |
| JP2019056080A (ja) * | 2017-09-22 | 2019-04-11 | 日本電産株式会社 | 流体動圧軸受用潤滑油、流体動圧軸受及びスピンドルモータ |
| CN113563598A (zh) * | 2021-08-04 | 2021-10-29 | 宁波锋成先进能源材料研究院有限公司 | 一种双亲超支化聚合物及其制备方法和应用 |
Citations (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2599803A (en) * | 1948-11-01 | 1952-06-10 | Shell Dev | Lubricating composition |
| US2936856A (en) * | 1957-02-01 | 1960-05-17 | Pure Oil Co | 2-ethylhexyl 6-(2-ethylhexoxy) hexanoate |
| JPH08311472A (ja) * | 1996-06-17 | 1996-11-26 | Nippon Oil Co Ltd | 非塩素系フロン冷媒用冷凍機油 |
| JPH0987223A (ja) * | 1995-05-17 | 1997-03-31 | Kao Corp | 新規エーテル化合物及びその製造方法 |
| JPH09255616A (ja) * | 1996-03-26 | 1997-09-30 | Kao Corp | エーテルカルボン酸誘導体の製造方法 |
| JPH09316017A (ja) * | 1996-05-23 | 1997-12-09 | Kao Corp | エーテル化合物の製造法 |
| JPH10109951A (ja) * | 1996-10-03 | 1998-04-28 | Kao Corp | エーテル化合物の製造方法 |
| JPH10251181A (ja) * | 1997-03-11 | 1998-09-22 | Kao Corp | エーテル化合物の製造方法 |
| JP2001107066A (ja) * | 1999-10-08 | 2001-04-17 | New Japan Chem Co Ltd | 冷凍機用潤滑油 |
| JP2004203889A (ja) * | 1994-05-20 | 2004-07-22 | Minnesota Mining & Mfg Co <3M> | ω−ヒドロフルオロアルキルエーテル類、その前駆物質のカルボン酸類と誘導体およびそれらの製造方法と用途 |
| JP2007056276A (ja) * | 2006-12-04 | 2007-03-08 | Idemitsu Kosan Co Ltd | 潤滑油基油 |
| JP2010053052A (ja) * | 2008-08-26 | 2010-03-11 | Fujifilm Corp | 多価エステル化合物の製造方法 |
| JP2010150228A (ja) * | 2008-03-28 | 2010-07-08 | Fujifilm Corp | 化合物 |
| WO2010085545A1 (en) * | 2009-01-26 | 2010-07-29 | Chemtura Corporation | Production of polyol ester lubricants for refrigeration systems |
| JP2010254678A (ja) * | 2009-03-30 | 2010-11-11 | Fujifilm Corp | パーフルオロクロロエーテル溶媒を含有する液体組成物 |
| JP2012056873A (ja) * | 2010-09-08 | 2012-03-22 | Moresco Corp | 2塩基酸エステル化合物および該化合物を含む潤滑油基油組成物 |
-
2010
- 2010-11-17 JP JP2010256887A patent/JP5760218B2/ja not_active Expired - Fee Related
Patent Citations (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2599803A (en) * | 1948-11-01 | 1952-06-10 | Shell Dev | Lubricating composition |
| US2936856A (en) * | 1957-02-01 | 1960-05-17 | Pure Oil Co | 2-ethylhexyl 6-(2-ethylhexoxy) hexanoate |
| JP2004203889A (ja) * | 1994-05-20 | 2004-07-22 | Minnesota Mining & Mfg Co <3M> | ω−ヒドロフルオロアルキルエーテル類、その前駆物質のカルボン酸類と誘導体およびそれらの製造方法と用途 |
| JPH0987223A (ja) * | 1995-05-17 | 1997-03-31 | Kao Corp | 新規エーテル化合物及びその製造方法 |
| JPH09255616A (ja) * | 1996-03-26 | 1997-09-30 | Kao Corp | エーテルカルボン酸誘導体の製造方法 |
| JPH09316017A (ja) * | 1996-05-23 | 1997-12-09 | Kao Corp | エーテル化合物の製造法 |
| JPH08311472A (ja) * | 1996-06-17 | 1996-11-26 | Nippon Oil Co Ltd | 非塩素系フロン冷媒用冷凍機油 |
| JPH10109951A (ja) * | 1996-10-03 | 1998-04-28 | Kao Corp | エーテル化合物の製造方法 |
| JPH10251181A (ja) * | 1997-03-11 | 1998-09-22 | Kao Corp | エーテル化合物の製造方法 |
| JP2001107066A (ja) * | 1999-10-08 | 2001-04-17 | New Japan Chem Co Ltd | 冷凍機用潤滑油 |
| JP2007056276A (ja) * | 2006-12-04 | 2007-03-08 | Idemitsu Kosan Co Ltd | 潤滑油基油 |
| JP2010150228A (ja) * | 2008-03-28 | 2010-07-08 | Fujifilm Corp | 化合物 |
| JP2010053052A (ja) * | 2008-08-26 | 2010-03-11 | Fujifilm Corp | 多価エステル化合物の製造方法 |
| WO2010085545A1 (en) * | 2009-01-26 | 2010-07-29 | Chemtura Corporation | Production of polyol ester lubricants for refrigeration systems |
| JP2010254678A (ja) * | 2009-03-30 | 2010-11-11 | Fujifilm Corp | パーフルオロクロロエーテル溶媒を含有する液体組成物 |
| JP2012056873A (ja) * | 2010-09-08 | 2012-03-22 | Moresco Corp | 2塩基酸エステル化合物および該化合物を含む潤滑油基油組成物 |
Non-Patent Citations (1)
| Title |
|---|
| "Study of the reaction of methyl methacrylate with C5-10 aliphatic alcohols", AZERBAIDZHANSKII KHIMICHESKII ZHURNAL, JPN6014030118, 1983, pages 65 - 8, ISSN: 0002883820 * |
Cited By (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013082900A (ja) * | 2011-09-30 | 2013-05-09 | Balbis:Kk | 軸受用潤滑剤組成物 |
| US9365789B2 (en) | 2012-12-27 | 2016-06-14 | Idemitsu Kosan Co., Ltd. | Dialkyl ether, and lubricant base oil and lubricating oil composition containing the same |
| JP2015057453A (ja) * | 2012-12-27 | 2015-03-26 | 出光興産株式会社 | ジアルキルエーテル |
| JP5994133B2 (ja) * | 2013-09-20 | 2016-09-21 | 株式会社Moresco | 含エーテルモノエステル化合物およびその利用 |
| JP2016216498A (ja) * | 2013-09-20 | 2016-12-22 | 株式会社Moresco | 含エーテルモノエステル化合物およびその利用 |
| US10077229B2 (en) | 2013-09-20 | 2018-09-18 | Moresco Corporation | Ether-containing monoester compound and use thereof |
| CN105579431B (zh) * | 2013-09-20 | 2018-05-04 | 株式会社Moresco | 含有醚的单酯化合物及其利用 |
| CN105579431A (zh) * | 2013-09-20 | 2016-05-11 | 株式会社Moresco | 含有醚的单酯化合物及其利用 |
| WO2015040937A1 (ja) * | 2013-09-20 | 2015-03-26 | 株式会社Moresco | 含エーテルモノエステル化合物およびその利用 |
| JP2016130316A (ja) * | 2014-03-31 | 2016-07-21 | ウシオケミックス株式会社 | 潤滑性化合物及びそれを含む潤滑剤組成物 |
| JP2015199934A (ja) * | 2014-03-31 | 2015-11-12 | ウシオケミックス株式会社 | 潤滑性化合物及びそれを含む潤滑剤組成物 |
| JP2016074816A (ja) * | 2014-10-06 | 2016-05-12 | 株式会社バルビス | 潤滑油基油及び潤滑油組成物 |
| WO2017175522A1 (ja) * | 2016-04-05 | 2017-10-12 | 株式会社Moresco | オキサ酸化合物 |
| JPWO2017175522A1 (ja) * | 2016-04-05 | 2019-02-14 | 株式会社Moresco | オキサ酸化合物 |
| US11021430B2 (en) | 2016-04-05 | 2021-06-01 | Moresco Corporation | Oxa acid compound |
| JP2018062632A (ja) * | 2016-10-14 | 2018-04-19 | 国立大学法人広島大学 | 潤滑油用基油及び潤滑油 |
| JP2019056080A (ja) * | 2017-09-22 | 2019-04-11 | 日本電産株式会社 | 流体動圧軸受用潤滑油、流体動圧軸受及びスピンドルモータ |
| CN113563598A (zh) * | 2021-08-04 | 2021-10-29 | 宁波锋成先进能源材料研究院有限公司 | 一种双亲超支化聚合物及其制备方法和应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP5760218B2 (ja) | 2015-08-05 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5760218B2 (ja) | 分岐オキサアルキル鎖を有している化合物およびその利用 | |
| CN104145009B (zh) | 冷冻机用工作流体组合物 | |
| CN104169405B (zh) | 冷冻机用工作流体组合物 | |
| JP2005105232A (ja) | 液晶ポリエステル樹脂 | |
| CN104160005A (zh) | 冷冻机用工作流体组合物 | |
| CN102712862B (zh) | 用于制冷系统的润滑剂 | |
| CN107523374A (zh) | 压缩式冷冻机用润滑油组合物 | |
| KR20110090924A (ko) | 냉장 시스템용 윤활제 | |
| WO1996006839A1 (en) | Synthetic lubricating oil | |
| CN103620004A (zh) | 压缩式冷冻机用润滑油组合物 | |
| JPWO2015125940A1 (ja) | フラーレン誘導体、フッ素樹脂組成物および潤滑剤 | |
| WO1990015122A1 (en) | Refrigerant composition | |
| CN108138067A (zh) | 冷冻机油、冷冻机用组合物、冷冻机和冷冻机油的选择方法 | |
| JP2015199934A (ja) | 潤滑性化合物及びそれを含む潤滑剤組成物 | |
| WO2015025929A1 (ja) | パーフルオロ(ポリ)エーテル基含有二官能化合物、パーフルオロ(ポリ)エーテル基含有二官能化合物を含む組成物およびこれらの製造方法 | |
| JP2008031149A (ja) | 新規ジカルボン酸ジエステル化合物、化学物質改質剤及びその利用 | |
| WO2009142085A1 (ja) | 含フッ素ポリエーテル化合物およびその製造方法 | |
| CN110088252A (zh) | 润滑油基础油、含有该润滑油基础油的润滑油组合物及其制造方法 | |
| JP2025004192A (ja) | 化合物 | |
| WO2017126578A1 (ja) | 冷媒r32用の冷凍機油およびこれを含む組成物 | |
| WO2017188151A1 (ja) | 冷凍機油、及び冷凍機用組成物 | |
| JPH04314797A (ja) | エステル組成物 | |
| JP2020128516A (ja) | グリース基油、および該グリース基油を含有するグリース組成物 | |
| JPH061970A (ja) | 冷凍機作動流体用組成物 | |
| JP2010242027A (ja) | 硬化性含フッ素ポリエーテル組成物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20130620 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20130620 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140826 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20150203 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150324 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20150414 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20150430 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5760218 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |