JP2010526068A - エリスロポエチン補完または置換 - Google Patents
エリスロポエチン補完または置換 Download PDFInfo
- Publication number
- JP2010526068A JP2010526068A JP2010506314A JP2010506314A JP2010526068A JP 2010526068 A JP2010526068 A JP 2010526068A JP 2010506314 A JP2010506314 A JP 2010506314A JP 2010506314 A JP2010506314 A JP 2010506314A JP 2010526068 A JP2010526068 A JP 2010526068A
- Authority
- JP
- Japan
- Prior art keywords
- itpp
- composition
- inositol
- erythropoietin
- tripyrophosphate
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- OXCMYAYHXIHQOA-UHFFFAOYSA-N potassium;[2-butyl-5-chloro-3-[[4-[2-(1,2,4-triaza-3-azanidacyclopenta-1,4-dien-5-yl)phenyl]phenyl]methyl]imidazol-4-yl]methanol Chemical compound [K+].CCCCC1=NC(Cl)=C(CO)N1CC1=CC=C(C=2C(=CC=CC=2)C2=N[N-]N=N2)C=C1 OXCMYAYHXIHQOA-UHFFFAOYSA-N 0.000 title claims abstract description 59
- 102000003951 Erythropoietin Human genes 0.000 title claims abstract description 56
- 108090000394 Erythropoietin Proteins 0.000 title claims abstract description 56
- 229940105423 erythropoietin Drugs 0.000 title claims abstract description 56
- 210000003743 erythrocyte Anatomy 0.000 claims abstract description 116
- 239000000203 mixture Substances 0.000 claims abstract description 111
- 238000000034 method Methods 0.000 claims abstract description 99
- 108010054147 Hemoglobins Proteins 0.000 claims abstract description 71
- 102000001554 Hemoglobins Human genes 0.000 claims abstract description 71
- 208000007502 anemia Diseases 0.000 claims abstract description 44
- 210000004369 blood Anatomy 0.000 claims abstract description 39
- 239000008280 blood Substances 0.000 claims abstract description 39
- 238000011282 treatment Methods 0.000 claims abstract description 32
- CDAISMWEOUEBRE-UHFFFAOYSA-N scyllo-inosotol Natural products OC1C(O)C(O)C(O)C(O)C1O CDAISMWEOUEBRE-UHFFFAOYSA-N 0.000 claims abstract description 26
- CDAISMWEOUEBRE-GPIVLXJGSA-N inositol Chemical compound O[C@H]1[C@H](O)[C@@H](O)[C@H](O)[C@H](O)[C@@H]1O CDAISMWEOUEBRE-GPIVLXJGSA-N 0.000 claims abstract description 25
- 150000003839 salts Chemical class 0.000 claims abstract description 24
- 206010021143 Hypoxia Diseases 0.000 claims abstract description 23
- 229960000367 inositol Drugs 0.000 claims abstract description 22
- 238000006213 oxygenation reaction Methods 0.000 claims abstract description 20
- 230000007954 hypoxia Effects 0.000 claims abstract description 17
- SQUHHTBVTRBESD-UHFFFAOYSA-N Hexa-Ac-myo-Inositol Natural products CC(=O)OC1C(OC(C)=O)C(OC(C)=O)C(OC(C)=O)C(OC(C)=O)C1OC(C)=O SQUHHTBVTRBESD-UHFFFAOYSA-N 0.000 claims abstract description 10
- 239000002253 acid Substances 0.000 claims abstract description 10
- 230000001771 impaired effect Effects 0.000 claims abstract description 7
- 230000004217 heart function Effects 0.000 claims abstract description 4
- 230000004199 lung function Effects 0.000 claims abstract 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 claims description 84
- 239000001301 oxygen Substances 0.000 claims description 84
- 229910052760 oxygen Inorganic materials 0.000 claims description 84
- 241001465754 Metazoa Species 0.000 claims description 37
- 208000024891 symptom Diseases 0.000 claims description 16
- 238000004820 blood count Methods 0.000 claims description 13
- HEDKSUBRULAYNO-UHFFFAOYSA-N myo-inositol trispyrophosphate Chemical compound C12OP(O)(=O)OP(O)(=O)OC2C2OP(O)(=O)OP(O)(=O)OC2C2C1OP(O)(=O)OP(O)(=O)O2 HEDKSUBRULAYNO-UHFFFAOYSA-N 0.000 claims description 13
- 238000004519 manufacturing process Methods 0.000 claims description 12
- 230000010437 erythropoiesis Effects 0.000 claims description 9
- 238000005534 hematocrit Methods 0.000 claims description 9
- 239000008194 pharmaceutical composition Substances 0.000 claims description 9
- 230000002829 reductive effect Effects 0.000 claims description 9
- 241000282412 Homo Species 0.000 claims description 8
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 7
- 230000009467 reduction Effects 0.000 claims description 7
- WHSPSJSZAIAJJD-UHFFFAOYSA-N [Na].[Na].[Na].[Na].[Ca] Chemical compound [Na].[Na].[Na].[Na].[Ca] WHSPSJSZAIAJJD-UHFFFAOYSA-N 0.000 claims description 6
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 6
- 239000003937 drug carrier Substances 0.000 claims description 5
- 150000004001 inositols Chemical class 0.000 claims description 5
- 230000000740 bleeding effect Effects 0.000 claims description 4
- 201000010099 disease Diseases 0.000 claims description 4
- 238000011269 treatment regimen Methods 0.000 claims description 4
- 230000004087 circulation Effects 0.000 claims description 3
- 208000035475 disorder Diseases 0.000 claims description 3
- 230000001737 promoting effect Effects 0.000 claims description 3
- 230000000287 tissue oxygenation Effects 0.000 claims description 3
- 208000022559 Inflammatory bowel disease Diseases 0.000 claims description 2
- 238000001631 haemodialysis Methods 0.000 claims description 2
- 230000000322 hemodialysis Effects 0.000 claims description 2
- 208000037581 Persistent Infection Diseases 0.000 claims 1
- 206010040047 Sepsis Diseases 0.000 claims 1
- 238000002512 chemotherapy Methods 0.000 abstract description 9
- 210000004072 lung Anatomy 0.000 abstract description 7
- 208000032467 Aplastic anaemia Diseases 0.000 abstract description 4
- 201000003793 Myelodysplastic syndrome Diseases 0.000 abstract description 4
- 208000005107 Premature Birth Diseases 0.000 abstract description 2
- 206010036590 Premature baby Diseases 0.000 abstract description 2
- 208000015181 infectious disease Diseases 0.000 abstract description 2
- 241000699670 Mus sp. Species 0.000 description 35
- IMQLKJBTEOYOSI-UHFFFAOYSA-N Phytic acid Natural products OP(O)(=O)OC1C(OP(O)(O)=O)C(OP(O)(O)=O)C(OP(O)(O)=O)C(OP(O)(O)=O)C1OP(O)(O)=O IMQLKJBTEOYOSI-UHFFFAOYSA-N 0.000 description 27
- 238000009472 formulation Methods 0.000 description 25
- 150000001875 compounds Chemical class 0.000 description 24
- IMQLKJBTEOYOSI-GPIVLXJGSA-N Inositol-hexakisphosphate Chemical compound OP(O)(=O)O[C@H]1[C@H](OP(O)(O)=O)[C@@H](OP(O)(O)=O)[C@H](OP(O)(O)=O)[C@H](OP(O)(O)=O)[C@@H]1OP(O)(O)=O IMQLKJBTEOYOSI-GPIVLXJGSA-N 0.000 description 23
- 229940068041 phytic acid Drugs 0.000 description 23
- 230000000694 effects Effects 0.000 description 22
- 238000002347 injection Methods 0.000 description 22
- 239000007924 injection Substances 0.000 description 22
- 239000000243 solution Substances 0.000 description 22
- 230000037396 body weight Effects 0.000 description 16
- 230000036961 partial effect Effects 0.000 description 16
- 210000001519 tissue Anatomy 0.000 description 16
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 15
- 239000011575 calcium Substances 0.000 description 14
- 159000000007 calcium salts Chemical class 0.000 description 14
- 230000007423 decrease Effects 0.000 description 14
- 239000003814 drug Substances 0.000 description 13
- 210000004027 cell Anatomy 0.000 description 11
- 229940079593 drug Drugs 0.000 description 11
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 10
- 239000007864 aqueous solution Substances 0.000 description 10
- 229920000642 polymer Polymers 0.000 description 10
- 239000011734 sodium Substances 0.000 description 10
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 9
- 239000004480 active ingredient Substances 0.000 description 9
- 230000027455 binding Effects 0.000 description 8
- 210000000601 blood cell Anatomy 0.000 description 8
- 239000004615 ingredient Substances 0.000 description 8
- 230000003204 osmotic effect Effects 0.000 description 8
- 239000000651 prodrug Substances 0.000 description 8
- 229940002612 prodrug Drugs 0.000 description 8
- 229920006395 saturated elastomer Polymers 0.000 description 8
- 241000894007 species Species 0.000 description 8
- 239000000725 suspension Substances 0.000 description 8
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical group [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 7
- 241000699666 Mus <mouse, genus> Species 0.000 description 7
- 229910052791 calcium Inorganic materials 0.000 description 7
- 239000007788 liquid Substances 0.000 description 7
- 239000000843 powder Substances 0.000 description 7
- 239000003826 tablet Substances 0.000 description 7
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 6
- 206010028980 Neoplasm Diseases 0.000 description 6
- 239000012637 allosteric effector Substances 0.000 description 6
- 210000001185 bone marrow Anatomy 0.000 description 6
- 201000011510 cancer Diseases 0.000 description 6
- 239000003795 chemical substances by application Substances 0.000 description 6
- 238000010494 dissociation reaction Methods 0.000 description 6
- 230000005593 dissociations Effects 0.000 description 6
- 239000012636 effector Substances 0.000 description 6
- 150000002500 ions Chemical class 0.000 description 6
- 210000003205 muscle Anatomy 0.000 description 6
- 108090000623 proteins and genes Proteins 0.000 description 6
- 229910052708 sodium Inorganic materials 0.000 description 6
- XOHUEYCVLUUEJJ-UHFFFAOYSA-I 2,3-Diphosphoglycerate Chemical compound [O-]P(=O)([O-])OC(C(=O)[O-])COP([O-])([O-])=O XOHUEYCVLUUEJJ-UHFFFAOYSA-I 0.000 description 5
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 5
- 239000001569 carbon dioxide Substances 0.000 description 5
- 229910002092 carbon dioxide Inorganic materials 0.000 description 5
- XPPKVPWEQAFLFU-UHFFFAOYSA-N diphosphoric acid Chemical compound OP(O)(=O)OP(O)(O)=O XPPKVPWEQAFLFU-UHFFFAOYSA-N 0.000 description 5
- 210000000265 leukocyte Anatomy 0.000 description 5
- 150000002632 lipids Chemical class 0.000 description 5
- 230000008569 process Effects 0.000 description 5
- 102000004169 proteins and genes Human genes 0.000 description 5
- 239000000126 substance Substances 0.000 description 5
- 108010064719 Oxyhemoglobins Proteins 0.000 description 4
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 4
- 150000007513 acids Chemical class 0.000 description 4
- 229920002988 biodegradable polymer Polymers 0.000 description 4
- 239000004621 biodegradable polymer Substances 0.000 description 4
- AXCZMVOFGPJBDE-UHFFFAOYSA-L calcium dihydroxide Chemical compound [OH-].[OH-].[Ca+2] AXCZMVOFGPJBDE-UHFFFAOYSA-L 0.000 description 4
- 239000000920 calcium hydroxide Substances 0.000 description 4
- 229910001861 calcium hydroxide Inorganic materials 0.000 description 4
- 239000002775 capsule Substances 0.000 description 4
- 239000000969 carrier Substances 0.000 description 4
- 230000002354 daily effect Effects 0.000 description 4
- 239000003085 diluting agent Substances 0.000 description 4
- 235000011180 diphosphates Nutrition 0.000 description 4
- 238000004520 electroporation Methods 0.000 description 4
- 239000008187 granular material Substances 0.000 description 4
- 150000003278 haem Chemical class 0.000 description 4
- 230000001146 hypoxic effect Effects 0.000 description 4
- 238000001727 in vivo Methods 0.000 description 4
- 238000010348 incorporation Methods 0.000 description 4
- 238000007912 intraperitoneal administration Methods 0.000 description 4
- 238000010253 intravenous injection Methods 0.000 description 4
- 239000002502 liposome Substances 0.000 description 4
- 230000004048 modification Effects 0.000 description 4
- 238000012986 modification Methods 0.000 description 4
- 229910052700 potassium Inorganic materials 0.000 description 4
- 239000011591 potassium Substances 0.000 description 4
- 238000002360 preparation method Methods 0.000 description 4
- 230000002265 prevention Effects 0.000 description 4
- 229940048084 pyrophosphate Drugs 0.000 description 4
- 210000001995 reticulocyte Anatomy 0.000 description 4
- 208000007056 sickle cell anemia Diseases 0.000 description 4
- -1 tritium ions Chemical class 0.000 description 4
- MYMOFIZGZYHOMD-UHFFFAOYSA-N Dioxygen Chemical compound O=O MYMOFIZGZYHOMD-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 239000013543 active substance Substances 0.000 description 3
- 239000002671 adjuvant Substances 0.000 description 3
- 230000002411 adverse Effects 0.000 description 3
- 150000001450 anions Chemical class 0.000 description 3
- 238000003556 assay Methods 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 210000001772 blood platelet Anatomy 0.000 description 3
- 150000001767 cationic compounds Chemical class 0.000 description 3
- 210000000170 cell membrane Anatomy 0.000 description 3
- 239000006071 cream Substances 0.000 description 3
- 230000009089 cytolysis Effects 0.000 description 3
- 238000000502 dialysis Methods 0.000 description 3
- 210000003617 erythrocyte membrane Anatomy 0.000 description 3
- 239000000499 gel Substances 0.000 description 3
- 210000003714 granulocyte Anatomy 0.000 description 3
- 229910052739 hydrogen Inorganic materials 0.000 description 3
- 238000011534 incubation Methods 0.000 description 3
- 229910001411 inorganic cation Inorganic materials 0.000 description 3
- 238000001990 intravenous administration Methods 0.000 description 3
- 229910052742 iron Inorganic materials 0.000 description 3
- 210000002540 macrophage Anatomy 0.000 description 3
- 231100000252 nontoxic Toxicity 0.000 description 3
- 230000003000 nontoxic effect Effects 0.000 description 3
- 150000002894 organic compounds Chemical class 0.000 description 3
- 239000002245 particle Substances 0.000 description 3
- 239000006072 paste Substances 0.000 description 3
- 102000004196 processed proteins & peptides Human genes 0.000 description 3
- 108090000765 processed proteins & peptides Proteins 0.000 description 3
- 239000000047 product Substances 0.000 description 3
- 159000000000 sodium salts Chemical class 0.000 description 3
- 239000007921 spray Substances 0.000 description 3
- 238000013268 sustained release Methods 0.000 description 3
- 239000012730 sustained-release form Substances 0.000 description 3
- 230000000699 topical effect Effects 0.000 description 3
- 231100000331 toxic Toxicity 0.000 description 3
- 230000002588 toxic effect Effects 0.000 description 3
- 210000003462 vein Anatomy 0.000 description 3
- XOHUEYCVLUUEJJ-UHFFFAOYSA-N 2,3-Bisphosphoglyceric acid Chemical group OP(=O)(O)OC(C(=O)O)COP(O)(O)=O XOHUEYCVLUUEJJ-UHFFFAOYSA-N 0.000 description 2
- 241000220479 Acacia Species 0.000 description 2
- 206010002660 Anoxia Diseases 0.000 description 2
- 241000976983 Anoxia Species 0.000 description 2
- 208000022305 Double heterozygous sickling disease Diseases 0.000 description 2
- AOJJSUZBOXZQNB-TZSSRYMLSA-N Doxorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 AOJJSUZBOXZQNB-TZSSRYMLSA-N 0.000 description 2
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 2
- 208000034502 Haemoglobin C disease Diseases 0.000 description 2
- 206010018910 Haemolysis Diseases 0.000 description 2
- 208000009336 Hemoglobin SC Disease Diseases 0.000 description 2
- 238000012404 In vitro experiment Methods 0.000 description 2
- 235000010643 Leucaena leucocephala Nutrition 0.000 description 2
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 2
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 2
- 241000124008 Mammalia Species 0.000 description 2
- 102000036675 Myoglobin Human genes 0.000 description 2
- 108010062374 Myoglobin Proteins 0.000 description 2
- SVYKKECYCPFKGB-UHFFFAOYSA-N N,N-dimethylcyclohexylamine Chemical compound CN(C)C1CCCCC1 SVYKKECYCPFKGB-UHFFFAOYSA-N 0.000 description 2
- 229920000388 Polyphosphate Polymers 0.000 description 2
- 241000700159 Rattus Species 0.000 description 2
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 2
- 229930006000 Sucrose Natural products 0.000 description 2
- 241000282887 Suidae Species 0.000 description 2
- 230000003281 allosteric effect Effects 0.000 description 2
- 201000006288 alpha thalassemia Diseases 0.000 description 2
- 230000007953 anoxia Effects 0.000 description 2
- 238000013459 approach Methods 0.000 description 2
- 229910052788 barium Inorganic materials 0.000 description 2
- DSAJWYNOEDNPEQ-UHFFFAOYSA-N barium atom Chemical compound [Ba] DSAJWYNOEDNPEQ-UHFFFAOYSA-N 0.000 description 2
- 230000009286 beneficial effect Effects 0.000 description 2
- 229910052790 beryllium Inorganic materials 0.000 description 2
- ATBAMAFKBVZNFJ-UHFFFAOYSA-N beryllium atom Chemical compound [Be] ATBAMAFKBVZNFJ-UHFFFAOYSA-N 0.000 description 2
- 208000005980 beta thalassemia Diseases 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- OWMVSZAMULFTJU-UHFFFAOYSA-N bis-tris Chemical compound OCCN(CCO)C(CO)(CO)CO OWMVSZAMULFTJU-UHFFFAOYSA-N 0.000 description 2
- 230000017531 blood circulation Effects 0.000 description 2
- 206010006451 bronchitis Diseases 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 238000006243 chemical reaction Methods 0.000 description 2
- 230000035602 clotting Effects 0.000 description 2
- 230000006835 compression Effects 0.000 description 2
- 238000007906 compression Methods 0.000 description 2
- 235000009508 confectionery Nutrition 0.000 description 2
- HSOHBWMXECKEKV-UHFFFAOYSA-N cyclooctanamine Chemical compound NC1CCCCCCC1 HSOHBWMXECKEKV-UHFFFAOYSA-N 0.000 description 2
- 230000002950 deficient Effects 0.000 description 2
- 238000010790 dilution Methods 0.000 description 2
- 239000012895 dilution Substances 0.000 description 2
- 239000002552 dosage form Substances 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 239000000796 flavoring agent Substances 0.000 description 2
- 239000012530 fluid Substances 0.000 description 2
- 239000006260 foam Substances 0.000 description 2
- 230000037406 food intake Effects 0.000 description 2
- 230000006870 function Effects 0.000 description 2
- 210000002216 heart Anatomy 0.000 description 2
- 108010047477 hemoglobin P Proteins 0.000 description 2
- 230000008588 hemolysis Effects 0.000 description 2
- 239000001257 hydrogen Substances 0.000 description 2
- 239000007943 implant Substances 0.000 description 2
- 239000012535 impurity Substances 0.000 description 2
- 238000011081 inoculation Methods 0.000 description 2
- 230000003993 interaction Effects 0.000 description 2
- 238000007918 intramuscular administration Methods 0.000 description 2
- 239000007928 intraperitoneal injection Substances 0.000 description 2
- 229910052744 lithium Inorganic materials 0.000 description 2
- 239000006166 lysate Substances 0.000 description 2
- 230000002934 lysing effect Effects 0.000 description 2
- 229910052749 magnesium Inorganic materials 0.000 description 2
- 239000011777 magnesium Substances 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 239000012528 membrane Substances 0.000 description 2
- 239000002324 mouth wash Substances 0.000 description 2
- 210000000663 muscle cell Anatomy 0.000 description 2
- 239000002105 nanoparticle Substances 0.000 description 2
- 239000007923 nasal drop Substances 0.000 description 2
- 229940100662 nasal drops Drugs 0.000 description 2
- 229910052757 nitrogen Inorganic materials 0.000 description 2
- IJGRMHOSHXDMSA-UHFFFAOYSA-N nitrogen Substances N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 2
- 239000002674 ointment Substances 0.000 description 2
- 150000002892 organic cations Chemical class 0.000 description 2
- 230000002093 peripheral effect Effects 0.000 description 2
- 230000035699 permeability Effects 0.000 description 2
- 239000002831 pharmacologic agent Substances 0.000 description 2
- 206010035653 pneumoconiosis Diseases 0.000 description 2
- 229920000447 polyanionic polymer Polymers 0.000 description 2
- 229920001184 polypeptide Polymers 0.000 description 2
- 239000001205 polyphosphate Substances 0.000 description 2
- 235000011176 polyphosphates Nutrition 0.000 description 2
- 230000002685 pulmonary effect Effects 0.000 description 2
- 230000009325 pulmonary function Effects 0.000 description 2
- 230000001105 regulatory effect Effects 0.000 description 2
- 229910052701 rubidium Inorganic materials 0.000 description 2
- IGLNJRXAVVLDKE-UHFFFAOYSA-N rubidium atom Chemical compound [Rb] IGLNJRXAVVLDKE-UHFFFAOYSA-N 0.000 description 2
- 210000002966 serum Anatomy 0.000 description 2
- 239000011780 sodium chloride Substances 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- 229910052712 strontium Inorganic materials 0.000 description 2
- CIOAGBVUUVVLOB-UHFFFAOYSA-N strontium atom Chemical compound [Sr] CIOAGBVUUVVLOB-UHFFFAOYSA-N 0.000 description 2
- 238000007920 subcutaneous administration Methods 0.000 description 2
- 239000005720 sucrose Substances 0.000 description 2
- RWSOTUBLDIXVET-UHFFFAOYSA-O sulfonium Chemical compound [SH3+] RWSOTUBLDIXVET-UHFFFAOYSA-O 0.000 description 2
- 239000000829 suppository Substances 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- 238000011200 topical administration Methods 0.000 description 2
- SBYHFKPVCBCYGV-UHFFFAOYSA-O 1-azoniabicyclo[2.2.2]octane Chemical compound C1CC2CC[NH+]1CC2 SBYHFKPVCBCYGV-UHFFFAOYSA-O 0.000 description 1
- INGWEZCOABYORO-UHFFFAOYSA-N 2-(furan-2-yl)-7-methyl-1h-1,8-naphthyridin-4-one Chemical compound N=1C2=NC(C)=CC=C2C(O)=CC=1C1=CC=CO1 INGWEZCOABYORO-UHFFFAOYSA-N 0.000 description 1
- 208000010543 22q11.2 deletion syndrome Diseases 0.000 description 1
- WOVKYSAHUYNSMH-RRKCRQDMSA-N 5-bromodeoxyuridine Chemical class C1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C(Br)=C1 WOVKYSAHUYNSMH-RRKCRQDMSA-N 0.000 description 1
- ZKHQWZAMYRWXGA-KQYNXXCUSA-J ATP(4-) Chemical compound C1=NC=2C(N)=NC=NC=2N1[C@@H]1O[C@H](COP([O-])(=O)OP([O-])(=O)OP([O-])([O-])=O)[C@@H](O)[C@H]1O ZKHQWZAMYRWXGA-KQYNXXCUSA-J 0.000 description 1
- 208000031261 Acute myeloid leukaemia Diseases 0.000 description 1
- ZKHQWZAMYRWXGA-UHFFFAOYSA-N Adenosine triphosphate Natural products C1=NC=2C(N)=NC=NC=2N1C1OC(COP(O)(=O)OP(O)(=O)OP(O)(O)=O)C(O)C1O ZKHQWZAMYRWXGA-UHFFFAOYSA-N 0.000 description 1
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 1
- 208000006820 Arthralgia Diseases 0.000 description 1
- 241000416162 Astragalus gummifer Species 0.000 description 1
- 102000004506 Blood Proteins Human genes 0.000 description 1
- 108010017384 Blood Proteins Proteins 0.000 description 1
- 206010006458 Bronchitis chronic Diseases 0.000 description 1
- UXVMQQNJUSDDNG-UHFFFAOYSA-L Calcium chloride Chemical compound [Cl-].[Cl-].[Ca+2] UXVMQQNJUSDDNG-UHFFFAOYSA-L 0.000 description 1
- UNMYWSMUMWPJLR-UHFFFAOYSA-L Calcium iodide Chemical compound [Ca+2].[I-].[I-] UNMYWSMUMWPJLR-UHFFFAOYSA-L 0.000 description 1
- 208000006545 Chronic Obstructive Pulmonary Disease Diseases 0.000 description 1
- 241000938605 Crocodylia Species 0.000 description 1
- VMQMZMRVKUZKQL-UHFFFAOYSA-N Cu+ Chemical compound [Cu+] VMQMZMRVKUZKQL-UHFFFAOYSA-N 0.000 description 1
- JPVYNHNXODAKFH-UHFFFAOYSA-N Cu2+ Chemical compound [Cu+2] JPVYNHNXODAKFH-UHFFFAOYSA-N 0.000 description 1
- 108020004414 DNA Proteins 0.000 description 1
- 108010019673 Darbepoetin alfa Proteins 0.000 description 1
- 201000004624 Dermatitis Diseases 0.000 description 1
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 description 1
- 208000000398 DiGeorge Syndrome Diseases 0.000 description 1
- 206010014561 Emphysema Diseases 0.000 description 1
- 108010074604 Epoetin Alfa Proteins 0.000 description 1
- CWYNVVGOOAEACU-UHFFFAOYSA-N Fe2+ Chemical compound [Fe+2] CWYNVVGOOAEACU-UHFFFAOYSA-N 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 102000003886 Glycoproteins Human genes 0.000 description 1
- 108090000288 Glycoproteins Proteins 0.000 description 1
- 102000008015 Hemeproteins Human genes 0.000 description 1
- 108010089792 Hemeproteins Proteins 0.000 description 1
- 108091005880 Hemoglobin F Proteins 0.000 description 1
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- 206010020772 Hypertension Diseases 0.000 description 1
- 208000001953 Hypotension Diseases 0.000 description 1
- 206010022004 Influenza like illness Diseases 0.000 description 1
- PIWKPBJCKXDKJR-UHFFFAOYSA-N Isoflurane Chemical compound FC(F)OC(Cl)C(F)(F)F PIWKPBJCKXDKJR-UHFFFAOYSA-N 0.000 description 1
- 239000000232 Lipid Bilayer Substances 0.000 description 1
- WAEMQWOKJMHJLA-UHFFFAOYSA-N Manganese(2+) Chemical compound [Mn+2] WAEMQWOKJMHJLA-UHFFFAOYSA-N 0.000 description 1
- 208000033761 Myelogenous Chronic BCR-ABL Positive Leukemia Diseases 0.000 description 1
- 208000033776 Myeloid Acute Leukemia Diseases 0.000 description 1
- 206010058116 Nephrogenic anaemia Diseases 0.000 description 1
- GLUUGHFHXGJENI-UHFFFAOYSA-N Piperazine Chemical class C1CNCCN1 GLUUGHFHXGJENI-UHFFFAOYSA-N 0.000 description 1
- NQRYJNQNLNOLGT-UHFFFAOYSA-O Piperidinium(1+) Chemical compound C1CC[NH2+]CC1 NQRYJNQNLNOLGT-UHFFFAOYSA-O 0.000 description 1
- 206010035664 Pneumonia Diseases 0.000 description 1
- 241000288906 Primates Species 0.000 description 1
- 206010036805 Progressive massive fibrosis Diseases 0.000 description 1
- 208000003251 Pruritus Diseases 0.000 description 1
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical class C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 1
- KAESVJOAVNADME-UHFFFAOYSA-N Pyrrole Chemical compound C=1C=CNC=1 KAESVJOAVNADME-UHFFFAOYSA-N 0.000 description 1
- 108020004511 Recombinant DNA Proteins 0.000 description 1
- 208000001647 Renal Insufficiency Diseases 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- 206010040880 Skin irritation Diseases 0.000 description 1
- 208000007536 Thrombosis Diseases 0.000 description 1
- 229920001615 Tragacanth Polymers 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- PTFCDOFLOPIGGS-UHFFFAOYSA-N Zinc dication Chemical compound [Zn+2] PTFCDOFLOPIGGS-UHFFFAOYSA-N 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 230000001154 acute effect Effects 0.000 description 1
- 239000000443 aerosol Substances 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 208000010123 anthracosis Diseases 0.000 description 1
- 230000000567 anti-anemic effect Effects 0.000 description 1
- 239000003173 antianemic agent Substances 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 239000012736 aqueous medium Substances 0.000 description 1
- 239000007900 aqueous suspension Substances 0.000 description 1
- 229940115115 aranesp Drugs 0.000 description 1
- 238000000149 argon plasma sintering Methods 0.000 description 1
- 210000001367 artery Anatomy 0.000 description 1
- 208000010668 atopic eczema Diseases 0.000 description 1
- 239000000022 bacteriostatic agent Substances 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 230000000975 bioactive effect Effects 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 230000036770 blood supply Effects 0.000 description 1
- 210000004204 blood vessel Anatomy 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 229910052792 caesium Inorganic materials 0.000 description 1
- TVFDJXOCXUVLDH-UHFFFAOYSA-N caesium atom Chemical compound [Cs] TVFDJXOCXUVLDH-UHFFFAOYSA-N 0.000 description 1
- 229910001622 calcium bromide Inorganic materials 0.000 description 1
- 239000001110 calcium chloride Substances 0.000 description 1
- 229910001628 calcium chloride Inorganic materials 0.000 description 1
- WGEFECGEFUFIQW-UHFFFAOYSA-L calcium dibromide Chemical compound [Ca+2].[Br-].[Br-] WGEFECGEFUFIQW-UHFFFAOYSA-L 0.000 description 1
- WUKWITHWXAAZEY-UHFFFAOYSA-L calcium difluoride Chemical compound [F-].[F-].[Ca+2] WUKWITHWXAAZEY-UHFFFAOYSA-L 0.000 description 1
- 229910001634 calcium fluoride Inorganic materials 0.000 description 1
- 229940046413 calcium iodide Drugs 0.000 description 1
- 229910001640 calcium iodide Inorganic materials 0.000 description 1
- KXDHJXZQYSOELW-UHFFFAOYSA-N carbonic acid monoamide Natural products NC(O)=O KXDHJXZQYSOELW-UHFFFAOYSA-N 0.000 description 1
- 238000006555 catalytic reaction Methods 0.000 description 1
- 125000002091 cationic group Chemical group 0.000 description 1
- 150000001768 cations Chemical class 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 230000005779 cell damage Effects 0.000 description 1
- 208000037887 cell injury Diseases 0.000 description 1
- 239000006285 cell suspension Substances 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 159000000006 cesium salts Chemical class 0.000 description 1
- 239000013626 chemical specie Substances 0.000 description 1
- 208000007451 chronic bronchitis Diseases 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 208000020832 chronic kidney disease Diseases 0.000 description 1
- CDAISMWEOUEBRE-JMVOWJSSSA-N cis-inositol Chemical class O[C@@H]1[C@H](O)[C@H](O)[C@H](O)[C@H](O)[C@@H]1O CDAISMWEOUEBRE-JMVOWJSSSA-N 0.000 description 1
- 238000003776 cleavage reaction Methods 0.000 description 1
- 229940110456 cocoa butter Drugs 0.000 description 1
- 235000019868 cocoa butter Nutrition 0.000 description 1
- 230000000536 complexating effect Effects 0.000 description 1
- 239000007891 compressed tablet Substances 0.000 description 1
- 238000013270 controlled release Methods 0.000 description 1
- 230000009146 cooperative binding Effects 0.000 description 1
- 150000003983 crown ethers Chemical class 0.000 description 1
- 239000002739 cryptand Substances 0.000 description 1
- VXVVUHQULXCUPF-UHFFFAOYSA-N cycloheptanamine Chemical class NC1CCCCCC1 VXVVUHQULXCUPF-UHFFFAOYSA-N 0.000 description 1
- VXVVUHQULXCUPF-UHFFFAOYSA-O cycloheptylazanium Chemical compound [NH3+]C1CCCCCC1 VXVVUHQULXCUPF-UHFFFAOYSA-O 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 230000034994 death Effects 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 239000008367 deionised water Substances 0.000 description 1
- 229910021641 deionized water Inorganic materials 0.000 description 1
- 108010002255 deoxyhemoglobin Proteins 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 229910052805 deuterium Inorganic materials 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- 206010012601 diabetes mellitus Diseases 0.000 description 1
- 239000000539 dimer Substances 0.000 description 1
- 229910001882 dioxygen Inorganic materials 0.000 description 1
- 208000037765 diseases and disorders Diseases 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 208000002173 dizziness Diseases 0.000 description 1
- 230000003828 downregulation Effects 0.000 description 1
- 229960004679 doxorubicin Drugs 0.000 description 1
- 230000035622 drinking Effects 0.000 description 1
- 239000006196 drop Substances 0.000 description 1
- 239000000428 dust Substances 0.000 description 1
- 230000002526 effect on cardiovascular system Effects 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 238000005538 encapsulation Methods 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 230000002255 enzymatic effect Effects 0.000 description 1
- CDAISMWEOUEBRE-NIPYSYMMSA-N epi-inositol Chemical compound O[C@H]1[C@H](O)[C@@H](O)[C@@H](O)[C@@H](O)[C@H]1O CDAISMWEOUEBRE-NIPYSYMMSA-N 0.000 description 1
- 229940089118 epogen Drugs 0.000 description 1
- 229940125367 erythropoiesis stimulating agent Drugs 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 230000003203 everyday effect Effects 0.000 description 1
- 210000003754 fetus Anatomy 0.000 description 1
- 235000019634 flavors Nutrition 0.000 description 1
- 239000007850 fluorescent dye Substances 0.000 description 1
- 238000001215 fluorescent labelling Methods 0.000 description 1
- 235000013355 food flavoring agent Nutrition 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 102000018146 globin Human genes 0.000 description 1
- 108060003196 globin Proteins 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 235000011187 glycerol Nutrition 0.000 description 1
- 239000003102 growth factor Substances 0.000 description 1
- 230000003394 haemopoietic effect Effects 0.000 description 1
- 230000003862 health status Effects 0.000 description 1
- 210000003709 heart valve Anatomy 0.000 description 1
- 229960002897 heparin Drugs 0.000 description 1
- 229920000669 heparin Polymers 0.000 description 1
- GLUUGHFHXGJENI-UHFFFAOYSA-O hydron piperazine Chemical compound [H+].C1CNCCN1 GLUUGHFHXGJENI-UHFFFAOYSA-O 0.000 description 1
- 230000036543 hypotension Effects 0.000 description 1
- 239000000815 hypotonic solution Substances 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 239000003701 inert diluent Substances 0.000 description 1
- 208000014674 injury Diseases 0.000 description 1
- 150000002484 inorganic compounds Chemical class 0.000 description 1
- 229910010272 inorganic material Inorganic materials 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 238000005342 ion exchange Methods 0.000 description 1
- 229920000554 ionomer Polymers 0.000 description 1
- 229960002725 isoflurane Drugs 0.000 description 1
- 230000007803 itching Effects 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- 201000006370 kidney failure Diseases 0.000 description 1
- 208000032839 leukemia Diseases 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 150000002678 macrocyclic compounds Chemical class 0.000 description 1
- 229920002521 macromolecule Polymers 0.000 description 1
- 210000004962 mammalian cell Anatomy 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 238000010297 mechanical methods and process Methods 0.000 description 1
- 230000005226 mechanical processes and functions Effects 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 230000010534 mechanism of action Effects 0.000 description 1
- 108020004999 messenger RNA Proteins 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 230000004060 metabolic process Effects 0.000 description 1
- 239000002207 metabolite Substances 0.000 description 1
- VUZPPFZMUPKLLV-UHFFFAOYSA-N methane;hydrate Chemical compound C.O VUZPPFZMUPKLLV-UHFFFAOYSA-N 0.000 description 1
- 238000000386 microscopy Methods 0.000 description 1
- 239000003595 mist Substances 0.000 description 1
- 210000003470 mitochondria Anatomy 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 238000000465 moulding Methods 0.000 description 1
- 201000006417 multiple sclerosis Diseases 0.000 description 1
- 210000004165 myocardium Anatomy 0.000 description 1
- 201000000977 neonatal anemia Diseases 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 231100000957 no side effect Toxicity 0.000 description 1
- 231100000956 nontoxicity Toxicity 0.000 description 1
- 238000010606 normalization Methods 0.000 description 1
- 239000007764 o/w emulsion Substances 0.000 description 1
- 229940100688 oral solution Drugs 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 210000003463 organelle Anatomy 0.000 description 1
- 150000004024 organic sulfonium compounds Chemical class 0.000 description 1
- 125000002524 organometallic group Chemical group 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 231100000915 pathological change Toxicity 0.000 description 1
- 230000036285 pathological change Effects 0.000 description 1
- 239000008055 phosphate buffer solution Substances 0.000 description 1
- 230000001766 physiological effect Effects 0.000 description 1
- 230000035790 physiological processes and functions Effects 0.000 description 1
- 239000006187 pill Substances 0.000 description 1
- 239000000902 placebo Substances 0.000 description 1
- 229940068196 placebo Drugs 0.000 description 1
- 210000002826 placenta Anatomy 0.000 description 1
- 239000003058 plasma substitute Substances 0.000 description 1
- 229920001467 poly(styrenesulfonates) Polymers 0.000 description 1
- 230000002028 premature Effects 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 238000004393 prognosis Methods 0.000 description 1
- 230000005180 public health Effects 0.000 description 1
- JUJWROOIHBZHMG-UHFFFAOYSA-O pyridinium Chemical compound C1=CC=[NH+]C=C1 JUJWROOIHBZHMG-UHFFFAOYSA-O 0.000 description 1
- 229940005657 pyrophosphoric acid Drugs 0.000 description 1
- 238000000163 radioactive labelling Methods 0.000 description 1
- 230000008929 regeneration Effects 0.000 description 1
- 238000011069 regeneration method Methods 0.000 description 1
- 238000009256 replacement therapy Methods 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 238000002390 rotary evaporation Methods 0.000 description 1
- YGSDEFSMJLZEOE-UHFFFAOYSA-M salicylate Chemical compound OC1=CC=CC=C1C([O-])=O YGSDEFSMJLZEOE-UHFFFAOYSA-M 0.000 description 1
- 229960001860 salicylate Drugs 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- 208000018316 severe headache Diseases 0.000 description 1
- 238000007493 shaping process Methods 0.000 description 1
- 210000002027 skeletal muscle Anatomy 0.000 description 1
- 230000036556 skin irritation Effects 0.000 description 1
- 231100000475 skin irritation Toxicity 0.000 description 1
- 229910001415 sodium ion Inorganic materials 0.000 description 1
- 235000019832 sodium triphosphate Nutrition 0.000 description 1
- 230000001954 sterilising effect Effects 0.000 description 1
- 238000004659 sterilization and disinfection Methods 0.000 description 1
- 239000000021 stimulant Substances 0.000 description 1
- 239000013589 supplement Substances 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 230000002459 sustained effect Effects 0.000 description 1
- 230000009747 swallowing Effects 0.000 description 1
- 230000008961 swelling Effects 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 238000009210 therapy by ultrasound Methods 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- 229940104230 thymidine Drugs 0.000 description 1
- KJAMZCVTJDTESW-UHFFFAOYSA-N tiracizine Chemical compound C1CC2=CC=CC=C2N(C(=O)CN(C)C)C2=CC(NC(=O)OCC)=CC=C21 KJAMZCVTJDTESW-UHFFFAOYSA-N 0.000 description 1
- 235000010487 tragacanth Nutrition 0.000 description 1
- 239000000196 tragacanth Substances 0.000 description 1
- 229940116362 tragacanth Drugs 0.000 description 1
- 230000002103 transcriptional effect Effects 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 238000002054 transplantation Methods 0.000 description 1
- 230000008733 trauma Effects 0.000 description 1
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 1
- WCZKTXKOKMXREO-UHFFFAOYSA-N triethylsulfanium Chemical compound CC[S+](CC)CC WCZKTXKOKMXREO-UHFFFAOYSA-N 0.000 description 1
- UNXRWKVEANCORM-UHFFFAOYSA-I triphosphate(5-) Chemical compound [O-]P([O-])(=O)OP([O-])(=O)OP([O-])([O-])=O UNXRWKVEANCORM-UHFFFAOYSA-I 0.000 description 1
- 229910052722 tritium Inorganic materials 0.000 description 1
- 230000004614 tumor growth Effects 0.000 description 1
- 210000004291 uterus Anatomy 0.000 description 1
- 210000005166 vasculature Anatomy 0.000 description 1
- 239000007762 w/o emulsion Substances 0.000 description 1
- 239000002699 waste material Substances 0.000 description 1
- 239000008215 water for injection Substances 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/66—Phosphorus compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/66—Phosphorus compounds
- A61K31/661—Phosphorus acids or esters thereof not having P—C bonds, e.g. fosfosal, dichlorvos, malathion or mevinphos
- A61K31/6615—Compounds having two or more esterified phosphorus acid groups, e.g. inositol triphosphate, phytic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/14—Blood; Artificial blood
- A61K35/15—Cells of the myeloid line, e.g. granulocytes, basophils, eosinophils, neutrophils, leucocytes, monocytes, macrophages or mast cells; Myeloid precursor cells; Antigen-presenting cells, e.g. dendritic cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/18—Growth factors; Growth regulators
- A61K38/1816—Erythropoietin [EPO]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/18—Antivirals for RNA viruses for HIV
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/06—Antianaemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/08—Plasma substitutes; Perfusion solutions; Dialytics or haemodialytics; Drugs for electrolytic or acid-base disorders, e.g. hypovolemic shock
Abstract
本発明は、貧血および低酸素症の治療時に、最大で90%のエリスロポエチン使用に代えられる方法および組成物を提供するものである。この方法では、酸や塩の形態のイノシトール−トリピロリン酸(ITPP)異性体を用いてヘモグロビンのP50値をシフトさせ、これによって赤血球数が少ないときですら血液による酸素化の速度と効率を改善するものである。この新たな方法の適応症としては、感染、化学療法、早産、高度変化、機能低下した肺または心臓の機能、再生不良性貧血、骨髄異形成症候群に関連する貧血、他の原因に起因する貧血および低酸素症があげられる。
Description
関連出願の相互参照
本出願は、2007年5月1日に出願された米国仮特許出願第60/927,059号(その全体を本明細書に援用する)の優先権の利益を主張するものである。
本出願は、2007年5月1日に出願された米国仮特許出願第60/927,059号(その全体を本明細書に援用する)の優先権の利益を主張するものである。
本発明は、化合物イノシトール−トリピロリン酸(ITPP)を使用して貧血を治療するための組成物および方法に関する。ITPPは、赤血球の細胞膜を通過して赤血球に含まれるヘモグロビンの酸素親和性を低下させる機能を有する、ヘモグロビンのアロステリックエフェクターのひとつである。本発明はさらに、赤血球を正常な酸素化状態に戻すための薬剤としてITPPを用いることにも関する。本発明はさらに、貧血および関連する他の症状の治療時に、エリスロポエチンに代えてITPPを用いることにも関する。
成人の血液量は約5〜6リットルであり、このうち約半分を細胞が占めている。その大半は赤血球(RBC、erythrocyte)であるが、白血球(leukocyte)や血小板も含まれる。血液の液体部分である血漿は、その約90%が水であり、10%がさまざまな溶質である。これらの溶質としては、血漿タンパク質、有機代謝産物、老廃物ならびに無機化合物があげられる。
RBCの主な機能は、肺から他の組織に酸素を運び、組織から肺へと二酸化炭素を運んで体外に排出することにある。水溶液に対する酸素の溶解性には限度があるため、血漿とともに運ばれる酸素の量はごくわずかである。血液によって運搬される酸素の大半が、赤血球中のヘモグロビンと結合した状態で運ばれる。哺乳類の赤血球にはヘモグロビンが約35重量%含まれる。核やミトコンドリア、他の細胞内小器官などは含まれず、赤血球自体の代謝に酸素は不要である。
ヘモグロビンは、分子量が約64500ダルトンのタンパク質であり、RBCだけに存在する。ヘモグロビンには4本のポリペプチド鎖と4個のヘム補欠分子族が含まれ、このうち鉄原子は二価鉄の状態で結合されている。正常なグロビンすなわちヘモグロビン分子のタンパク質部分は、2本のα鎖と2本のβ鎖からなり、その各々が1個のヘム基を含む特徴的な折り畳みの三次構造を有する。この4本のポリペプチド鎖が互いに結合してほぼ正四面体の配位をとり、ヘモグロビンの特徴的な四次構造をなす。ヘム基はいずれも、二原子酸素の分子1個と可逆的に結合してオキシヘモグロビンを形成できる。酸素が放出されると、この複合体が還元されてデオキシヘモグロビンになる。ヘモグロビンの4つの構成単位は、酸素が加わることでα−β二量体内での引力が緩和される形で酸素と協働的に相互作用し、4番目の酸素分子は1番目の酸素分子と比べて300倍の親和性でタンパク質と結合する。これとは対照的に、心臓や骨格筋での酸素の運搬を担うヘムタンパク質であるミオグロビンは、ヘモグロビン四量体を解離した個々のユニットのように機能するため、挙動が直接的である。
組織への酸素の送達は、血流量、赤血球数、赤血球中のヘモグロビン濃度、ヘモグロビンの酸素親和性を含むがこれに限定されるものではない、いくつかの要因に左右され、特定の種では、酸素親和性の高い/低い赤血球内ヘモグロビンのモル比に左右される。一方ヘモグロビンの酸素親和性は、さらに4つの要因すなわち、(1)酸素分圧、(2)pH、(3)ヘモグロビン中の2,3−ジホスホグリセリン酸(DPG)濃度、(4)二酸化炭素濃度に左右される。肺では、100mmHgの酸素分圧下で、循環しているヘモグロビンの約98%が酸素飽和状態となる。これは血液の酸素運搬能力そのものに相当する。完全に酸素化されると、哺乳類の全血100mlあたり約21mlの気体酸素を運搬できる。
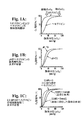
酸素分圧がヘモグロビンの酸素結合親和性に及ぼす影響については、ヘモグロビンの酸素飽和曲線から最もよく分かる。図1Aを参照されたい。このS字状曲線は、ヘモグロビン分子溶液が一定範囲の気体酸素分圧と平衡状態にあるときに、酸素分子が占めるヘム部位の割合をプロットしたものである。最初の酸素分子が結合すると、まだ酸素と結合されていない残りのヘモグロビン部位の酸素親和性が実際に高くなる。酸素分圧が高くなると、結合親和性は、それぞれのヘモグロビンが4個の酸素分子で完全に飽和された水平状態に近づくことになる。
ヘモグロビンによる酸素の可逆性結合には、以下に示す式に基づくプロトンの放出を伴う。図1Bに示すように、pHが上昇すると平衡が右に寄り、一定の分圧でさらに多くの酸素がヘモグロビンに結合される。pHが低下すると、酸素の結合量も減少する。血液中でpHを下げるプロトンの出所となるものとしては、二酸化炭素と水との触媒反応によって形成される炭酸ならびに、ヘモグロビンのαアミン基が運搬対象となる二酸化炭素を結合したときに形成されるカルバミン酸(−NH−C(=O)−O−H)があげられる。
肺の気腔内では、酸素分圧が約90〜100mmHgであり、pHも血液の通常のpHより高い(最大7.6)。この圧力とpHになると、ヘモグロビンは酸素飽和度約98%すなわち、ほぼ最大限に飽和した状態に近くなる。これとは対照的に、抹消組織の内部毛細血管における酸素分圧は、わずか約25〜40mmHgしかなく、そこでのpHもほぼ中性(約7.2〜7.3)である。筋肉の細胞では酸素の消費量が多く、局所的に酸素濃度が低下するため、筋肉での酸素放出が望まれる。このため、筋肉の毛細血管を流れる血液は、結合している酸素の約4分の1を、ほぼ飽和状態にある赤血球のヘモグロビンから血漿へ、さらには筋肉細胞へと放出する。ヘモグロビンが筋肉を出る頃には飽和度はわずか75%程度であり、したがって、肺と末梢組織との間を循環する際、静脈血のヘモグロビンでは、酸素飽和度が約65〜97%の間を行き来することになる。このように、pHと酸素分圧は、酸素の放出に相乗的に影響するのである。
ヘモグロビンの酸素化の調節にあたって重要なもうひとつの要因に、アロステリックエフェクターとしての2,3−ジホスホグリセリン酸(DPG)がある。DPGは、哺乳類の赤血球におけるヘモグロビンの通常の生理エフェクターである。DPGには、赤血球のDPG濃度が高くなればなるほど、ヘモグロビンの酸素親和性が低くなるという反比例的な作用がある(図1C参照)。
組織への酸素の送達量が慢性的に少ない個体では、通常の赤血球DPG濃度が個体群の標準値よりも高い。たとえば、高地では酸素分圧が比較的低いため、これに合わせて組織での酸素分圧も低くなる。正常な被験者が、ある地点から標高の高い地点まで移動すると、数時間もすれば赤血球のDPG濃度が上昇し、それまでよりも多くのDPGが結合されてヘモグロビンの酸素親和性は一気に下がる。結果として、組織を流れるRBCからの酸素の放出が一層容易になる(図1C)。赤血球のDPG濃度の上昇は、低酸素症に陥った患者でも生じる。繰り返すが、この調節は、肺のヘモグロビンでの酸素化が少ないことを補うものである。被験者が標高の高いところから標高の低いところへと移れば、これとは逆の変化が生じる。
正常な血液のヘモグロビンには、相当な量のDPGが含まれる。DPGが「除去」されたヘモグロビンは、それまでよりもかなり高い酸素親和性を示す。すなわち、その酸素が組織に放出される速度が落ちることになる。DPGが増えると、ヘモグロビンの酸素結合親和性は低下する。ヒトの場合、生後約6か月までは、2,3−BPGとは弱く結合するだけで、DPGを除去した成人のヘモグロビン(HbA)のような挙動を呈する、一種のヘモグロビンであるHbFが認められる。このHbFの特性のおかげで、子宮内では胎盤を通して母体から胎児に酸素が容易に運ばれるのであるが、かなり早産で生まれた乳児にとっては、この特性が故の問題を抱えることになる。子宮の外では、十分な酸素放出を促す上で、DPGなどの生理学的アロステリックエフェクターがヘモグロビンにあることが極めて重要だからである。
リン酸化イノシトールは、鳥類や爬虫類の赤血球において、哺乳動物でのDPGと同じ役割を果たす。イノシトール六リン酸(IHP)は、哺乳類の赤血球膜を通過できないが、DPGの結合部位で哺乳類の赤血球ヘモグロビンと結合して、そのアロステリックコンホメーションを変更することができる。また、IHPは、ヘモグロビンに対する親和性がDPGの1000倍で、DPGよりもはるかに影響力が大きい(R.E.Benesch et al.,Biochemistry,16:2594〜2597(1977))上に、pH7.4、37℃でヘモグロビンのP50を最大で96.4mmHgの値まで上昇させる(J.Biol.Chem.,250:7093〜7098(1975))。
哺乳類のRBCで酸素の放出量を増すことから、貧血の症状を治療する上でヘモグロビンのアロステリックエフェクターに注目が集まっている。これらのエフェクターを赤血球に封入するための方策として、赤血球の浸透圧パルス(膨化)および再構成、制御溶解および再封、リポソーム、エレクトロポレーションがあげられる。
以下の参考文献には、IHPを封入したリポソームとの相互作用による赤血球へのポリリン酸の取り込みについて記載している。Gersonde,et al.,“Modification of the Oxygen Affinity of Intracellular Haemoglobin by Incorporation of Polyphosphates into Intact Red Blood Cells and Enhanced O2 Release in the Capillary System”,Biblthca.Haemat.,No.46,pp.81〜92(1980);Gersonde,et al.,“Enhancement of the O2 Release Capacity and of the Bohr−Effect of Human Red Blood Cells after Incorporation of Inositol Hexaphosphate by Fusion with Effector−Containing Lipid Vesicles”,Origins of Cooperative Binding of Hemoglobin(1982);Weiner,“Right Shifting of Hb−O2 Dissociation in Viable Red Cells by Liposomal Technique,”Biology of the Cell,Vol.47,(1983)。
また、Nicolauらに付与された米国特許第4192869号明細書、同第4321259号明細書、同第4473563号明細書には、流体を含む脂質小胞を赤血球膜と融合させ、その内容物を赤血球に入れる方法が記載されている。この方法では、IHPなどのアロステリックエフェクターを赤血球内に運ぶことが可能になるが、赤血球内ではIHPのほうがDPGより結合定数が大きいため、ヘモグロビン結合部位でIHPがDPGと置換される。
リポソームによる手法では、IHPで飽和させたリン酸緩衝溶液を用いて脂質小胞の混合物を懸濁させ、これに超音波処理または注入処理をほどこして、さらに遠心処理する。上側の懸濁液にはIHPを含有する小さな脂質小胞が含まれるため、これを回収する。回収した懸濁液と一緒に赤血球をインキュベートすれば、IHP含有脂質小胞を細胞膜に融合させ、その内容物を赤血球の中に入れることができる。こうして変性させた赤血球を洗浄し、血漿に加えて生成物を得る。残念なことに、赤血球に取り込まれたIHPの濃度の再現性が低く、処理後に赤血球の大幅な溶血も起こる。また、この手法は、商業規模で使用するには冗長で複雑すぎるものである。
これらの欠点を解決するためのひとつの試みとして、赤血球を溶解して再封する方法が用いられている。Nicolau,et al.,“Incorporation of Allosteric Effectors of Hemoglobin in Red Blood Cells.Physiologic Effects,”Biblthca.Haemat.,No.51,pp.92〜107,(1985)を参照されたい。Roparsらに付与された関連の米国特許第4752586号明細書および同第4652449号明細書にも、赤血球とリポソームとの相互作用を回避する、赤血球の制御溶解および再封によって、生物活性を有する物質をヒトまたは動物の赤血球に封入する手法が記載されている。この手法の特徴は、浸透圧パルスに近い手法を用いる持続血液透析において最もよく表れている。具体的には、少なくとも1つの透析要素の第1コンパートメントに赤血球の水性懸濁液を連続的に供給する一方で、この透析要素の第2コンパートメントには赤血球懸濁液よりも浸透圧の低い水溶液を入れておく。低張液は赤血球を溶解させる。次に、その溶解物を、赤血球に取り込む予定の生物活性物質と接触させる。溶解物の浸透圧および/または膠質浸透圧を高めて赤血球膜を再封し、再封後の赤血球の懸濁液を回収する。
Goodrichらに付与された米国特許第4874690号明細書および同第5043261号明細書には、赤血球の凍結乾燥と再構成について関連する手法が開示されている。この再構成の段階で、IHPをはじめとするさまざまなポリアニオンを加える。これらの特許に開示されたプロセスで処理した赤血球は、活性が影響を受けないと言われている。おそらく、再構成の際に取り込まれたIHPによってヘモグロビンの活性が維持されるのであろう。
Francoらに付与された米国特許第4478824号明細書および同第4931276号明細書には、上記に匹敵する方法である「浸透圧パルス法」ならびに赤血球を効果的に溶解および再封することで、IHPをはじめとする非イオン性の作用剤を哺乳類の赤血球に効率よく導入するための装置が開示されている。この方法では、すみやかに拡散して赤血球に出入りする化合物を含有する溶液に、濃縮赤血球を懸濁させてインキュベートする。このときの化合物の濃度は、赤血球が高張になるように化合物を赤血球内に拡散させるのに十分な濃度である。次に、導入対象となる少なくとも1種の所望の作用剤の存在下、この赤血球溶液を原則として等張の水性媒質で希釈して、水を赤血球内に拡散させ、赤血球を膨化して外側の細胞膜の透過性を高め、膜貫通イオン勾配を形成する。膜の透過性は、所望の作用剤を赤血球に運んで、最初の化合物を赤血球外に拡散させるのに十分な時間だけ、高い状態に維持される。
浸透圧パルス法の実施にあたって使用できるポリアニオンとしては、ピロリン酸塩、トリポリリン酸塩、リン酸化イノシトール、2,3−ジホスホグリセリン酸(DPG)、アデノシン三リン酸、ヘパリン、ポリカルボン酸(いずれも水溶性であり、かつ赤血球の外側の脂質二重層膜を破壊しない)が挙げられる。残念なことに、浸透圧パルス法には、封入率の低さ、不完全な再封、細胞内容物の喪失、これに伴う細胞寿命の縮小をはじめとするいくつかの欠点がある。この手法は冗長であり、複雑で自動化には向かないため、商業的にはほとんど成功していない。
生物活性物質を細胞内に封入するためのもうひとつの方法にエレクトロポレーションがある。エレクトロポレーションは、Mouneimne,et al.,“Stable rightward shifts of the oxyhemoglobin dissociation curve induced by encapsulation of inositol hexaphosphate in red blood cells using electroporation,”FEBS,275(1,2):117〜120(1990)に記載されているように、赤血球にIHPを封入する例をはじめとして、さまざまな細胞のタイプでの異質分子の封入に用いられている。また、米国特許第5612207号明細書も参照されたい。現行のエレクトロポレーション方法は、商業規模で使用するには非実用的である。
貧血を治療するためのもうひとつの方法に、腎臓で極めて低濃度で自然に産生される糖タンパク質であるエリスロポエチン(EPO)の投与がある。エリスロポエチンは、哺乳類の細胞培養における組換えDNA技術を用いて商業規模でも生成され、骨髄での赤血球の形成を促進する。2種類の形態でのEPOの商品名には、エポエチンであるEpogen(登録商標)、Eprex(登録商標)、NeoRecormon(登録商標)と、ダルベポエチンであって同様に作用するAranesp(登録商標)がある。EPOは、疾患または障害それ自体として、腎不全などの別の疾患の症候として、癌関連の貧血として、癌治療の副作用としてなど、いくつかの原因による貧血の治療に用いられる。たとえば、Martindale:The Complete Drug Reference(第33版).Sweetman et al.Pharmaceutical Press,2002;British National Formulary(第50版),British Medical Association and Royal Pharmaceutical Society of Great Britain,September 2005を参照されたい。EPOの使用は、HIV、炎症性腸疾患、敗血症発症(septic episodes)といった貧血関連(慢性)感染のある患者ならびに、再生不良性貧血および骨髄異形成症候群の患者にとって、特に将来性のあるものである。
EPOは一般に、化学療法によって骨髄での血球の生成量が減少し、そのためヘモグロビン濃度が低くなりすぎてしまった癌患者の輸血の代用品として用いられており、鉄分の錠剤や注射が追加されることもある。赤血球の濃度は、この化合物の投与後2〜3週間は上昇の兆しを見せない。必要があれば毎日、あるいは3週間に1回といった少ない頻度で、EPOを皮下注射する。注射は通常、化学療法のコースを終えてから1か月を経過するまで、あるいは患者に貧血が認められなくなるまで継続される。EPOの用量は適応症によって異なるが、たとえば、多くの癌患者および腎性貧血患者では、体重で300I.U./kg/週以上、糖尿病患者では100〜180I.U./kg/週の範囲であり、小児の場合は、いくつかの適応症で50I.U./kg/週である。
一般的な副作用として、特に治療開始時に、関節痛、脱力感、眩暈、疲労感などのインフルエンザのような症候が認められる。ひどい頭痛を訴える患者も数名いる。高血圧も起こり得る。注射部位での皮膚刺激や痒みを伴う湿疹も起こり得る。また、EPOの使用は、ヘモグロビン濃度を13.0g/dlよりも高い濃度まで高める目的で用いた場合に、有害な心血管合併症のリスク増加と関連している。Drueke TB,Locatelli F,Clyne N,et al.,“Normalization of hemoglobin level in patients with chronic kidney disease and anemia,”N.Eng.J.Med.,355(20):2071〜2084(2006)。EPOの恩恵に関するいくつかの試験で、この化合物が実際に腫瘍の成長を容易にするのではないかと示唆されている。また、EPOが血塊形成(血栓症)のリスクを高めるのではないかという危惧もある。
2007年3月、米国食品医薬品局から、前月の医師に対するクリニカルアラート(clinical alert)に続いて、エリスロポエチンに関する公衆衛生勧告が発表された。FDAでは、これらの設定での生活の質の改善または輸血の必要性を裏付ける臨床的な根拠を欠くことを理由に、化学療法を受けている癌患者または化学療法の治療終了後の癌患者にエポエチンおよびダルベポエチンなどの赤血球新生(erythropoeisis)−刺激剤を使用する際に注意をすることを勧めている。同じく2007年3月、これらの薬剤の安全性に関する新たな「ブラックボックス」警告に製薬業者らが合意し、造血性成長因子の安全性についての議会による調査の結果、製造業者らは、医師に対するこれらの薬剤のリベートプログラムを保留とし、同時にこれを患者に販売することも保留にするよう求められた。
よって、赤血球の酸素化を回復できる、実質的に無毒の組成物および方法に継続的な需要がある。特に、赤血球のP50値を右に大きくシフトできる、単純かつ好ましくは経口で容易に投与される組成物に継続的な需要がある。
あらゆるタイプの貧血の治療において、イノシトール−トリピロリン酸(ITPP)を含む組成物を、エリスロポエチンの大規模置換に使用できることが発見されている。本発明の方法では、ITPPを用いることで、赤血球数が少ない状態ですら正常な酸素化を保証する。化学療法によって赤血球新生(新しい赤血球の生成)が減速または中断された場合、その治療をITPP療法と組み合わせると、従来技術で用いられている従来の用量の10%という少ない量のエリスロポエチンを用いて血球の生成を復活させることが可能である。よって、本発明は、ITPPをEPOとを組み合わせて使用または平行使用、EPOとITPPとを交互に使用、EPOに代えてITPPを使用して、あらゆるタイプの貧血および低酸素症を治療することができる組成物および方法を提供するものである。特定の実施形態では、本発明は、貧血またはそうでなければ低酸素状態のヒトおよび動物を、最大で90%の処方されたエリスロポエチンをITPP投与に代える方法を提供するものである。
本発明は、貧血および他の低酸素症状を治療する際に効果的なイノシトール−トリピロリン酸(ITPP)アニオンを含む組成物を提供する。本発明の組成物およびその用途には、実質的に無毒であり、巻き添え的な赤血球の損傷を生じたとしてもごくわずかであり、基本的に副作用がなく、酸素化をすみやかに改善でき、従来技術の組成物より一層容易に投与される。本発明の組成物および方法はまた、経済的と作動的の両方で商業規模での使用にしたがっている。特定の実施形態では、ITPP組成物が患者に優しい剤形で提供される。
また、本発明は、体内と体外での血液供給での両方で、ITPPによる赤血球への調節された酸素送達を増すための方法を提供するものである。いくつかの実施形態では、本発明は、機能低下した生理学的機能に関連する貧血または低酸素症を治療するための組成物および方法を提供するものである。特定の実施形態では、本発明は、機能低下した肺機能、機能低下した心臓機能、血行不良、大量出血、赤血球の生成または不十分な生成ならびに、不十分に酸素化しているヘモグロビンのタイプの低酸素による影響を防止または軽減するための組成物および方法を提供するものである。
以下の仮説に拘泥することを意図するものではないが、ITPPの有効性が、O2張力を最大で正常な組織のレベル(すなわち分圧≧約40mmHg)まで引き上げて、低酸素組織への赤血球のO2送達能と関連していると思われる。ITPPの作用機序は、ヘモグロビンの酸素親和性のアロステリックな調節によって、酸素の放出を促進するものであると思われる。
本発明の目的は、ITPPを有効用量で用いて、貧血および他の症状のあるヒトおよび動物において正常な酸素化を回復するための実質的に無毒の組成物および方法を提供することにある。
本発明の別の目的は、ITPPを有効用量で用いて、赤血球およびヘモグロビンによる酸素送達を促進するための組成物および方法を提供する。
本発明のさらに他の目的は、ITPPを有効用量で代用して、エリスロポエチンを交換するための組成物および方法を提供することにある。
本発明のさらなる目的は、標準酸素解離曲線上で、赤血球のP50値の大幅な右シフトを引き起こし得る有効用量で、ITPPを使用して、好ましくは経口で、単純かつ容易に投与される組成物を提供することにある。
本発明の上記および他の目的、特性、利点は、開示された実施形態の以下の詳細な説明の概説を読めば明らかになろう。
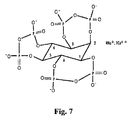
本発明で有用な組成物としては、イノシトール−トリピロリン酸(ITPP)の酸および塩があげられる。ITPPは、本明細書ではアニオンとして認識される。用語「イノシトールトリピロリン酸」は、イノシトール六リン酸トリピロリン酸としても知られており、ピロリン酸塩の内側の環が3つあるイノシトール六リン酸を示す。本明細書では、ITPPと対をなす種を対イオンと呼び、ITPPと対イオンとの組み合わせを酸または塩と呼ぶ。本発明は、純粋にイオン性の対に限定されるものではない。特に、対になったイオンが、対の2つの成分間でのある程度の共有結合特性または配位結合特性の証拠となることが多いことは、従来技術において周知である。本発明の組成物のITPPの酸および塩は、1タイプの対イオンを含むものであってもよいし、混合対イオンを含むものであってもよく、任意に、ITPPが1つであるアニオンの混合物を含有してもよい。この組成物は、任意に、対イオンのキレート化または複合化可能なクラウンエーテル、クリプタンド、他の種を含むものであってもよい。組成物も同様に、任意に、水素結合または他の分子引力によってITPPを複合化可能な酸性大員環または他の種を含むものであってもよい。ITPPの酸および塩の製造方法については、Nicolauらに付与された米国特許第7084115号明細書に記載されており、その内容全体を本明細書に援用する。本発明での使用が企図される対イオンとしては、
プロトンならびに、そのジュウテリウムおよびトリチウムの対応するイオンをはじめとするカチオン水素種;
リチウム、ナトリウム、カリウム、ルビジウム、セシウム、銅(I)の一価無機カチオン
ベリリウム、マグネシウム、カルシウム、ストロンチウム、バリウム、マンガン(II)、亜鉛(II)、銅(II)、鉄(II)をはじめとする二価無機カチオン;
鉄(III)をはじめとする多価無機カチオン;
アンモニウム、シクロヘプチルアンモニウム、シクロオクチルアンモニウム、N,N−ジメチルシクロヘキシルアンモニウム、他の有機アンモニウムカチオンをはじめとする四級窒素種;
トリエチルスルホニウムおよび他の有機スルホニウム化合物をはじめとするスルホニウム種;
ピリジニウム、ピペリジニウム、ピペラジニウム、キヌクリジニウム、ピロリウム、トリピペラジニウム、他の有機カチオンをはじめとする有機カチオン;
オリゴマー、ポリマー、ペプチド、タンパク質、正に荷電したアイオノマーならびに、ポリマーの側基、鎖末端および/または骨格に、スルホニウム、四級窒素および/または荷電した有機金属種を有する他の高分子(macromolecular)種をはじめとするポリマーカチオンが挙げられるが、これに限定されるものではない。
プロトンならびに、そのジュウテリウムおよびトリチウムの対応するイオンをはじめとするカチオン水素種;
リチウム、ナトリウム、カリウム、ルビジウム、セシウム、銅(I)の一価無機カチオン
ベリリウム、マグネシウム、カルシウム、ストロンチウム、バリウム、マンガン(II)、亜鉛(II)、銅(II)、鉄(II)をはじめとする二価無機カチオン;
鉄(III)をはじめとする多価無機カチオン;
アンモニウム、シクロヘプチルアンモニウム、シクロオクチルアンモニウム、N,N−ジメチルシクロヘキシルアンモニウム、他の有機アンモニウムカチオンをはじめとする四級窒素種;
トリエチルスルホニウムおよび他の有機スルホニウム化合物をはじめとするスルホニウム種;
ピリジニウム、ピペリジニウム、ピペラジニウム、キヌクリジニウム、ピロリウム、トリピペラジニウム、他の有機カチオンをはじめとする有機カチオン;
オリゴマー、ポリマー、ペプチド、タンパク質、正に荷電したアイオノマーならびに、ポリマーの側基、鎖末端および/または骨格に、スルホニウム、四級窒素および/または荷電した有機金属種を有する他の高分子(macromolecular)種をはじめとするポリマーカチオンが挙げられるが、これに限定されるものではない。
本発明で用いるITPPに特に好ましい異性体としては、cis−1,2,3,5−trans−4,6−シクロヘキサンヘキソールである、myo−イノシトールがあげられる。しかしながら、本発明はこのように限定されるものではない。よって、本発明は、天然に発生するscyllo−、chiro−、muco−、neo−イノシトール異性体それぞれのトリピロリン酸ならびに、allo、epi−およびcis−イノシトール異性体のトリピロリン酸を含むITPPでのイノシトール異性体の使用を企図するものである。
エステルの酵素開裂またはトリルスルホニル基などの脱離基の移動などによって、プロドラッグからITPPを生体内(in vivo)にて形成できることが企図される。このようにして生成されたITPPを用いて血球酸素経済を促進することも本発明の範囲に入ると想定される。
「貧血」という用語は、本明細書で使用する場合、体内で作られる赤血球の数が酸素を運ぶのに不十分であるか、周囲環境で酸素を効率よく運ぶことのできないタイプのヘモグロビンが体内で作られている症状を示す。第1のタイプの貧血の例として、化学療法が原因で骨髄での血球生成が減少または停止することによる貧血ならびに、再生不良性貧血および骨髄異形成症候群に関連する貧血があげられる。後者のタイプの貧血の例としては、鎌状赤血球貧血、ヘモグロビンSC疾患、ヘモグロビンC疾患、α−サラセミアおよびβ−サラセミア、早産後の新生児貧血、これと類似の症状があげられる。
「低酸素症」または「無酸素症」という用語は、本明細書では、患者の体の組織が医学的に不十分な濃度の酸素しか得ていない症状と同義に用いられる。「低酸素症」および「無酸素症」という用語は、本明細書で使用する場合、貧血症状と同時に生じることが多いが、同一の外延を持つものではない。
ITPPは、貧血、低酸素症および他の関連または関係のあるイベントおよび症状の制御にあたって有用であり、本発明は、治療の有効性の評価に用いられるタイプのアッセイに限定されるものではない。本明細書で使用する場合、貧血関連または関係イベントまたは症状の制御は、貧血と関係している場合があるまたは貧血と関係していると思われ、本発明の組成物の投与によって生じる任意のタイプの要因、症状、活性、インジケータ、化学種または化合物の組み合わせ、mRNA、レセプター、マーカー、メディエータ、タンパク質、転写活性などの定性的または定量的な変化で実証される制御を示す。このような他のアッセイとしては、組織培養プレートでの細胞数の計数;代謝アッセイによる細胞数の評価;DNAへの放射性標識(3H−チミジンなど)または蛍光標識または免疫反応性(BrdUなど)ヌクレオチドの取り込みがあげられる。
本明細書では、エリスロポエチン治療計画(treatment regimen)を、患者自身の自然なエリスロポエチン生成を実質的に補うことを想定した薬用量レベルと頻度でエリスロポエチンの投与が小胞される治療の治療過程と定義する。本明細書にて定義する場合、エリスロポエチンは、天然由来、製造されたもの、あるいは組換え遺伝子源由来であるか否かを問わず、エポエチンおよびダルベポエチンなどの赤血球新生−刺激剤を示す。エリスロポエチン治療計画の低減は、患者が過去に受けていたまたは処方されていたよりも少ない用量およびまたは少ない頻度の投与を示す。本明細書にて定義する場合、エリスロポエチン治療計画の低減という表現は、2006年末までに患者の世話や臨床研究において同じ目的で一般に報告されているよりも少ない用量およびまたは少ない頻度の投与を使用することも示す。
エリスロポエチンの置換とは、本明細書にて定義する場合、エリスロポエチン治療計画の低減によって失われる現行または予測の酸素化能の全体または一部を補償するために他の治療薬と併用してエリスロポエチン治療計画を低減することを示す。現行または予測の酸素化能とは、患者における組織酸素化の標的効率を示す。酸素化能の全体または一部の補償とは、エリスロポエチン治療計画の低減によって失われる既存の酸素化能または望まれる酸素化能の好ましくは少なくとも5%を置換するようITPP組成物を使用することを示す。より好ましくは、補償によって失われた酸素化能の少なくとも25%が置換される。なお一層好ましくは、少なくとも50%が置換され、さらにより好ましくは少なくとも75%が置換され;より一層好ましくは少なくとも90%が置換され;さらにより一層好ましくは、現行(既存)または予測(望まれる)酸素化能に対するITPPの補償によって、エリスロポエチン治療計画の低減によって失われた能力の少なくとも100%が置換される。
本明細書にて定義する場合、2種類の組成物を交互に投与するとは、特定の時点で一方の組成物だけに起因する治療有効量の活性物質が患者の体内に含まれると推定されるように投与のタイミングを決めることを示す。本明細書にて定義する場合、2種類の組成物の平行投与とは、同じ結果を得るのに2種類の組成物を組み合わせて1つの製剤にしてあるか否か、あるいは組成物または上記の任意の組み合わせを、間隔をあけて別々に投与するか否かを問わず、通常は特定の時点で両方の組成物からの治療有効量の活性物質が患者の体内に含まれると推定されるように投与することを示す。
本明細書にて定義する場合、PO2という用語は、気体状または組織での酸素分圧を示す。本明細書にて定義する場合、P50値は、ヘモグロビンの利用可能な酸素結合部位が酸素分子で50%占められているときの気体状または組織での酸素の平衡分圧を示す。本明細書にて定義する場合、P50値の右シフトとは、ヘモグロビンが転換前よりも高い酸素分圧で一層容易に酸素を放出する転換を示す。言葉を変えると、P50値の右シフトとは、本明細書では、PO2濃度が変わらないままでのヘモグロビンのO2親和性の低下を示す。
実質的に少ない赤血球数とは、本明細書にて定義する場合、その個体群について医学的に健康な正常範囲よりも低いとみなされる赤血球数を示す。同様に、低ヘマトクリット値とは、本明細書にて定義する場合、その個体群について医学的に健康な正常範囲よりも低いとみなされるヘマトクリット値を示す。
労作能(effort capacity)とは、本明細書にて定義する場合、貧血または低酸素症の問題とは関係なく患者がその個人の性別、身長、体重、健康状態に適した肉体作業を行う能力の目安である。労作能は、患者の赤血球による組織酸素化が十分であるか否かを判断する間接的な目安でもある。
赤血球新生とは、本明細書にて定義する場合、一般には骨髄での赤血球の生成および再生を示す。赤血球新生の減速または中断とは、本明細書では、赤血球新生の自然な、疾患によるまたは化学的に誘導された速度低下または停止が発生する現象を示す。本明細書にて定義する場合、赤血球新生の再開または復活とは、エリスロポエチンなどのエリスロポエチン的な物質を使用して、患者の自然な赤血球新生を加速または再び開始させることを示す。
経口投与の場合、ITPPは、毒性がほとんどないかまったくない状態で抗貧血活性を呈する。P50値(ヘモグロビンの50%飽和でのP50)のシフトで測定して、myo−ITPPがヘモグロビンのO2−親和性の低減を誘導する能力を試験した。高めのPO2への観察されたシフトは、マウスヘモグロビンでは最大250%、マウス全血では最大40%であった。シフトがin vivoにてRBCおよびヘマトクリット値の減少と同時に起こったことから、この所見は特に印象的であった。このような血液希釈は、体内の酸素需要が効率的に満たされている場合のRBC生成の下方制御の診断基準となるため、多くの状況で正のインジケータとして認識される。被験動物での労作能がITPP投与後に最大100%増すことから、別の裏付けが得られた。これは、動いている筋肉に対して、その筋肉だけに酸素が効率的に送達されたことを示すものであった。マウスとブタのいずれにおいても、ITPPの結果からその治療面での潜在性が大きく裏付けられた。血流に不具合がある際にITPPによって赤血球による酸素送達を規則的に促進可能だということが理由である。
本発明の化合物だけでなく、本発明の医薬組成物も、本明細書にて示す1つまたは複数の疾患または症状を治療する上で価値のある1つまたは複数の薬理作用物質を含むものであってもよいし、あるいは、このような1つまたは複数の薬理作用物質を同時にまたは逐次的に共投与してもよい。特に、本発明は、エリスロポエチン組成物の平行、交互または代用使用を含むITPP組成物を投与することを含む。
当業者であれば、Remington’s Pharmaceutical Sciences第17版などの標準的なテキストを参照して、どのようにして製剤を製造し、どのようにしてこれを投与できるかを判断することができよう。
本発明の別の態様では、本発明によるITPPの化合物またはそのプロドラッグを、貧血または低酸素症に関連する症状の予防または治療用の薬剤の調製に使用する用途が得られる。本発明のさらに別の態様では、貧血または低酸素症に関連する症状を予防または治療する方法であって、このような予防または治療が必要な患者に、本発明による有効量のITPP化合物またはそのプロドラッグを、本明細書にて記載するようにして投与することを含む方法が得られる。前記症状の予防または治療には、前記症状の改善も含まれることは理解されたい。
本発明のさらに別の態様では、薬学的に許容されるキャリア、希釈剤、アジュバントまたは賦形剤と一緒に、本発明によるITPPの化合物またはそのプロドラッグを含む医薬組成物が得られる。この医薬組成物を、貧血または他の低酸素症と関連する症状の予防または治療に使用してもよい。
「有効量」とは、本明細書で用いる場合、治療的または予防的な有効量を意味する。このような量は、当業者であれば、治療対照となる症状や投与経路、他の関連する要因を考慮して容易に判断できるものである。このような当業者は、好適な用量、モード、投与頻度を容易に判断することができる。「個体」とは、本出願で用いる場合、特定の症状の治療が必要であり得る動物を示す。「個体」には、ヒト、他の霊長類、家庭のペット、家畜、齧歯類、他の哺乳動物ならびに、一般に獣医が治療できる他の動物が含まれる。
上述した組成物は、周知の技法を用いて生理学的に許容可能な製剤として提供可能であり、これらの製剤を標準的な経路で投与することができる。通常、局所、経口、直腸、腹腔内または非経口(静脈内、皮下または筋肉内)経路で組み合わせを投与してもよい。また、組み合わせを任意にポリマーに取り込んで、徐放を可能にしたり、たとえば治療対象となる場所への送達が容易になるよう腔または血管内など送達が望ましい場所のそばにポリマーを移植したりしてもよい。この組成物の薬用量は、治療対象となる症状、使用する個々の誘導体のほか、患者の体重や症状、化合物の投与経路などの他の臨床因子に左右される。しかしながら、経口投与であれば、推奨薬用量は0.00001から10g/kg/日の範囲である。経口投与の薬用量は、0.5から2.0g/kg/日の範囲あるいは、約0.5から約1.5g/kg/日の範囲である。別の実施形態では、経口投与の薬用量は約0.80から1.0g/kg/日の範囲あるいは、約0.9から1.1g/kg/日の範囲である。
また、本発明は、ITPPによる赤血球への酸素の調節送達を増加するための方法も提供するものである。本発明の特定の実施形態では、ITPPを経口投与すなわち内服させることで、貧血患者の赤血球の正常な酸素化を回復する。もうひとつの実施形態では、貧血あるいは低酸素であるか、その可能性がある患者への輸血前に、ITPPを用いて血液試料を処理する。本発明の別の実施形態では、患者への輸血前に酸素放出能を改善する前に、ITPPを用いて血液試料を前処理する。さらに別の実施形態では、臨界酸素化レベルが得られる閾値量のRBCを提供しつつ、特に希少な血液型の場合に保存RBCを保護するために、輸血前にITPPを用いて血液試料の酸素経済を改善する。さらにもうひとつの実施形態では、透析時にITPPを用いて血液試料を処理し、その酸素放出能を改善する。
他の一実施形態では、本発明は、処方されたエリスロポエチンの最大で90%をITPP投与に置換することで、貧血症状のあるヒトおよび動物を治療する方法を提供するものである。
他の一実施形態では、本発明は、ヒトまたは動物における機能低下した肺機能による影響を軽減するための組成物および方法を提供するものである。特定の例としての実施形態では、本発明は、肺炎、急性または慢性の気管支炎、気腫、塵肺、炭坑作業員塵肺症、慢性閉塞性肺疾患、進行性塊状線維症、多発性硬化症、溺水、有毒蒸気の吸入、界面活性剤の吸入、油性物質の吸入、ディジョージ症候群の場合などの不十分な肺血管系、肺機能が衰える他の症状に羅患した患者の損傷を軽減し、快適さと「予後」を改善する方法を提供するものである。
さらに他の一実施形態では、本発明は、機能低下した心臓機能による影響を防止または軽減するための組成物および方法を提供するものである。特定の実施形態では、これには、心臓の弁が漏れやすい患者、1本または複数本の閉塞動脈またはほとんど閉塞した動脈のある患者、外科手術の過程で心臓が停止または交換された患者などを含む。
さらに別の実施形態では、本発明は、血行不良に関連する低酸素症による影響を防止または軽減するための組成物および方法を提供するものである。この実施形態の適応症の例としては、糖尿病、低血圧などがあげられる。
さらに別の実施形態では、本発明は、大量出血による影響を防止または軽減するための組成物および方法を提供するものである。この実施形態の適応症の例としては、外傷、内出血、臓器移植、外科合併症、遺伝的または薬剤関連の血塊形成不能などの患者での使用があげられる。
他の実施形態では、本発明は、赤血球の生成不全または生成が不十分であることに関連する疾患および障害による影響を防止または軽減するための組成物および方法を提供するものである。適応症の例としては、再生不良性貧血および骨髄異形成症候群などの貧血ならびに、急性骨髄性白血病、慢性白血病などの白血病などがあげられる。別の実施形態の例としては、骨髄の補充または置き換えが必要な他の適応症で使用することがあげられる。
さらに別の実施形態では、本発明は、不十分に酸素化しているヘモグロビンタイプを有する患者の赤血球の酸素放出能の改善に用いられる組成物および方法を提供するものである。これらの実施形態は、血液中に相当量のヘモグロビンFを有する早産児ならびに、鎌状赤血球貧血、ヘモグロビンC症、ヘモグロビンSC症、α−サラセミアおよびβ−サラセミアなどのヘモグロビン障害のある患者に使用することを含む。
本発明による製剤は、錠剤、カプセル、薬用キャンデー、カプセル(cachet)、溶液、懸濁液、エマルション、粉末、エアロゾル、坐薬、スプレー、トローチ、軟膏、クリーム、ペースト、フォーム、ゲル、タンポン、ペッサリー、顆粒剤、大丸薬、洗口液または経皮パッチの形で投与可能である。
この製剤は、経口、直腸、経鼻、吸入、局所(皮膚、経皮、頬側および舌下を含む)、膣内、非経口(皮下、筋肉内、静脈内、腹腔内、皮内、眼内、気管内,および硬膜外を含む)または吸入投与に適したものを含む。この製剤を適宜、単位剤形の形で提供してもよいし、従来の製薬技法で提供してもよい。このような技法は、活性成分と医薬キャリアまたは賦形剤とを会合させるステップを含む。通常、製剤は、活性成分および液体キャリアまたは微粉砕した固体キャリアまたはその両方と均一かつ密に会合させ、必要があれば、製品を成形して調製される。
また、ITPPの化合物または薬剤またはそのプロドラッグからなるインプラントまたは他の装置も本発明によって企図される。この場合、薬剤またはプロドラッグは、徐放用に生物分解可能なポリマーまたは生物分解されないポリマーに入れて作られる。生物分解されないポリマーは、物理的または機械的なプロセスで薬剤を制御しながら放出し、ポリマー自身が分解されることはない。生物分解可能なポリマーは、体内の自然なプロセスによって徐々に加水分解または可溶化するよう設計され、混合された薬剤またはプロドラッグが徐々に放出されるようになっている。薬剤またはプロドラッグは、ポリマーに化学的に結合されていてもよいし、混合物によってポリマーに取り込まれていてもよい。生物分解可能なポリマーと生物分解されないポリマーの両方ならびに、徐放用に薬剤をポリマーに取り込むプロセスは、当業者間で周知である。このようなポリマーの例は、Brem et al.,J.Neurosurg.74:441〜446(1991)(その全体を本明細書に援用する)などの多くの参考文献に見られる。これらのインプラントまたは装置については、たとえば骨髄から新たな血球が放出される部位の近くまたは肺組織の近くなど、所望の場所に移植可能である。
経口投与に適した本発明の製剤は、各々があらかじめ定められた量の活性成分を含む、カプセル、カプセル(cachet)または錠剤などの独立した単位で提供してもよく、粉末または顆粒剤として、水性の液体または非水性の液体中の溶液または懸濁液として、あるいは水中油滴型エマルションまたは油中水滴型エマルションなどとして提供してもよいものである。
錠剤は、任意に1つまたは複数の補助成分を用いて圧縮または成形によって製造できるものである。圧縮錠剤については、好適な装置にて、粉末または顆粒剤などの自由流動形態で、任意にバインダー、潤滑剤、不活性希釈剤、保存剤、界面活性または分散助剤などと混合して、活性成分を圧縮して調製してもよい。湿製錠については、好適な装置にて、不活性液体希釈剤で湿らせた粉末化合物の混合物を成形して製造してもよい。任意に、錠剤にコーティングをほどこしたり線を入れたりしてもよいし、活性成分の徐放(slow release)または徐放(controlled release)が得られるように処方してもよい。
口中での局所投与に適した製剤としては、通常はスクロースおよびアカシアまたはトラガントなどの香味ベースに成分を含む薬用キャンデー;ゼラチンおよびグリセリン、あるいはスクロースおよびアカシアなどの不活性ベースに活性成分を含むトローチ;投与対象となる成分を好適な液体キャリア中に含む洗口液があげられる。
皮膚への局所投与に適した製剤は、投与対象となる成分を薬学的に許容されるキャリア中に含む軟膏、クリーム、ゲル、ペーストとして提供できるものである。好ましい局所供給系は、投与対象となる成分を含む経皮パッチである。
直腸投与用の製剤は、たとえば、ココアバターおよび/またはサリチル酸塩を含む公的なベースを用いた坐薬として提供できるものである。
キャリアが固体である場合の経鼻投与に適した製剤は、嗅ぎ薬が取り込まれるような方法すなわち、鼻に近づけて保持した粉末の容器からの経鼻経路でのすみやかな吸入によって投与される、粒度が20から500ミクロンなどの範囲にある粗粉末を含む。たとえば、点鼻薬または経鼻滴など、投与用のキャリアが液体である場合の好適な製剤は、活性成分の水溶液または油性溶液を含む。
膣内投与に適した製剤は、活性成分に加えて、適切であることが従来技術において周知のキャリアなどの成分も含むペッサリー、タンポン、クリーム、ゲル、ペースト、フォームまたはスプレー製剤として提供できるものである。
吸入に適した製剤は、活性成分に加えて、適切であることが従来技術において周知のキャリアなどの成分も含むミスト、ダスト、粉末またはスプレー製剤として提供できるものである。
非経口投与に適した製剤としては、抗酸化剤、緩衝液、静菌薬ならびに、製剤を意図したレシピエントの血液と等張にする溶質を含むものであってもよい水性および非水性の滅菌注射溶液;懸濁剤および増粘剤を含むものであってもよい水性および非水性の滅菌懸濁液があげられる。この製剤は、単位用量または多用量の容器、たとえば、封止したアンプルやバイアルで提供できるものであり、使用の直前に注射用水などの滅菌液キャリアを加えるだけでよいフリーズドライ(凍結乾燥)させた状態で保管しておくことができる。上述したような種類の滅菌粉末、顆粒剤および錠剤から、即座に注射溶液および懸濁液を調製することができる。
本発明の一部として企図される製剤は、全体を本明細書に援用する米国特許出願第10/392403号明細書(公開番号2004/0033267号)に開示されている方法で製造されるナノ粒子製剤を含む。ナノ粒子を形成することで、本明細書で開示した組成物のバイオアベイラビリティが高まることが分かっている。好ましくは、本発明の化合物の粒子の有効平均粒度が、光散乱法、顕微鏡または当業者間で周知の他の適当な方法で測定した場合に、約2ミクロン未満、約1900nm未満、約1800nm未満、約1700nm未満、約1600nm未満、約1500nm未満、約1400nm未満、約1300nm未満、約1200nm未満、約1100nm未満、約1000nm未満、約900nm未満、約800nm未満、約700nm未満、約600nm未満、約500nm未満、約400nm未満、約300nm未満、約250nm未満、約200nm未満、約150nm未満、約100nm未満、約75nm未満または約50nm未満である。
好ましい単位処方剤は、投与される成分の1日用量または単位、本明細書にて上述した1日の分割用量(daily sub−dose)、あるいはその適当な一部を含むものである。
特に上述した成分に加えて、本発明の製剤は、目的の製剤のタイプを考慮して、従来技術における他の作用剤を含むものであってもよく、たとえば、経口投与に適したものなどに、製剤の味をよくして嚥下しやすくするための香味剤や他の作用剤を含むようにしてもよいことは理解されたい。
試験管内(in vitro)での実験で、ITPPを脱イオン水に溶解させ、pHをpH7に調整し、全血を用いるインキュベーション用に、ブドウ糖でITPP溶液のオスモル濃度を270〜297mOsMに調節した。ヘモグロビンとITPPの混合物を、混合直後にHEMOX分析器(PD Marketing、London)で測定した。赤血球を37℃で1時間、ITPPと一緒にインキュベートした。インキュベーション後、赤血球をBis−Tris緩衝液(pH=7.0)で3回洗浄した後、P50測定に用いた。
ITPPを経口投与して生体内で実施する実験では、20g/Lの濃度(=27mM、pH7.0)でITPPを飲用(脱イオンではない)水に溶解し、自由に飲めるようにしておいた。循環RBCのP50値の有意なシフトが観察された。
以下の実施例は本発明を示すものであるが、これを限定するものではない。よって、実施例は、修正を加えることができ、それでもなお本発明の主旨および範囲内に包含されるという理解のもとに提供されるものである。
実施例1
トリピロリン酸塩の経口投与
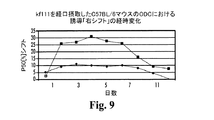
12匹のC57BL/6マウスが4日間にわたってITPPを飲んだ(約25ml/24時間)。7匹の対照マウスが純水(3匹)を飲み、ITPPと同じ濃度およびpHのIHP溶液(ピロリン酸塩の内側の環のないイノシトール六リン酸)を飲んだ(4匹)。純水、IHP−水またはITPP−水を与えたときの摂取した流体の量は同じであったことから、ITPP−またはIHP−溶液がマウスに拒絶されなかったことが分かる。P50値を測定するために、0日目(処理開始前)、1日目、2日目、4日目、6日目、7日目、8日目、10日目、11日目および12日目に12匹のC57BL/6マウスの尾静脈から血液を採取した。この処理に苦しんだC57BL/6マウスはいないように見えた。ITPPの経口適用によって、マウスのP50に有意な右シフト(最大31%)が生じた。
トリピロリン酸塩の経口投与
12匹のC57BL/6マウスが4日間にわたってITPPを飲んだ(約25ml/24時間)。7匹の対照マウスが純水(3匹)を飲み、ITPPと同じ濃度およびpHのIHP溶液(ピロリン酸塩の内側の環のないイノシトール六リン酸)を飲んだ(4匹)。純水、IHP−水またはITPP−水を与えたときの摂取した流体の量は同じであったことから、ITPP−またはIHP−溶液がマウスに拒絶されなかったことが分かる。P50値を測定するために、0日目(処理開始前)、1日目、2日目、4日目、6日目、7日目、8日目、10日目、11日目および12日目に12匹のC57BL/6マウスの尾静脈から血液を採取した。この処理に苦しんだC57BL/6マウスはいないように見えた。ITPPの経口適用によって、マウスのP50に有意な右シフト(最大31%)が生じた。
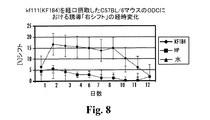
12匹のマウスを12日間にわたって観察し、循環RBCのP50値をほぼ毎日測定した。ITPPを摂取したマウスで誘導されたODC(オキシヘモグロビン解離曲線)P50(最大31%)の右シフトの経時変化ならびに、IHPの水溶液または純水を摂取した対照動物ではシフトがまったくないことを、図9に示す。個体ごとの差こそあれ、ITPPの水溶液を摂取したすべてのマウスで循環RBCのP50値のシフトがあるように見える。ITPPの水溶液を摂取したマウスで誘導されたP50シフトの個体ごとの差を図8に示す。
実施例2
ITPP処理マウスと対照マウスの血球数
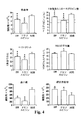
処理マウスと対照マウスの血球数(および血清エリスロポエチン量)の差を評価するために、ITPPまたはIHPの水溶液(4日間)または水のみを摂取したマウスの血液を、0日目、7日目および11日目に採取した。2つの主な観察がなされた。1)ITPPを摂取したマウスのRBC数が大幅に減少し、2)異なる群のマウスの血液の白血球数(顆粒球、マクロファージなど)には大きな差はなかった。ODCがシフトしたマウスのRBC数を対照との比較で表1に示す。
ITPP処理マウスと対照マウスの血球数
処理マウスと対照マウスの血球数(および血清エリスロポエチン量)の差を評価するために、ITPPまたはIHPの水溶液(4日間)または水のみを摂取したマウスの血液を、0日目、7日目および11日目に採取した。2つの主な観察がなされた。1)ITPPを摂取したマウスのRBC数が大幅に減少し、2)異なる群のマウスの血液の白血球数(顆粒球、マクロファージなど)には大きな差はなかった。ODCがシフトしたマウスのRBC数を対照との比較で表1に示す。
ITPPを与えた9匹のマウスの値と、水だけを与えた2匹のマウスの値、IHP/水を与えた1匹のマウスの値を示す。他のマウスの血液量は血球数の判断には不十分であった。(0日目に、マウスのRBC数は8.9〜11.8×106細胞/mm3であった)。これらのデータから、以下の結論が得られた。
・ITPPを27mMの濃度で経口投与すると、マウスの循環RBCではP50値に有意な右シフトが生じる。ITPPのip接種後の観察結果では接種後2時間でP50シフトが見られるのに比して、最大シフトに達するまでに約48時間のタイムラグが発生する。
・ITPPの経口投与開始後2日目と4日目の間に最大P50シフトに達する。
・4日目に摂取をやめると、12日以内にP50値が対照値(0日目に測定)に戻る。
・ITPP摂取がRBC数に大きく影響している。
しかしながら、in vitroではRBCの溶解が起こらないため、RBCの溶血については無視してもよい。
・ITPPを27mMの濃度で経口投与すると、マウスの循環RBCではP50値に有意な右シフトが生じる。ITPPのip接種後の観察結果では接種後2時間でP50シフトが見られるのに比して、最大シフトに達するまでに約48時間のタイムラグが発生する。
・ITPPの経口投与開始後2日目と4日目の間に最大P50シフトに達する。
・4日目に摂取をやめると、12日以内にP50値が対照値(0日目に測定)に戻る。
・ITPP摂取がRBC数に大きく影響している。
しかしながら、in vitroではRBCの溶解が起こらないため、RBCの溶血については無視してもよい。
ITPP(27mM)の適度な濃度ですら、マウスにおける循環RBCのODCをシフトさせるには経口投与が効果的であるように見える。
実施例3
正常な仔ブタへのITPPの静脈内注射
8週齢の正常な仔ブタ(体重17kg)1頭でin vivo実験を実施した。ITPPの注射時に、5%イソフルラン、0.7L/分のN2Oおよび2.0L/分のO2で仔ブタを20〜30分間麻酔するか、耳の静脈から血液を採取した。27gのITPP/100mlの水(注射容量:63ml、pH6.5、17gのITPP=体重1kgあたり1gを含有)という濃度で静脈内注射した化合物は、少なくとも10分間かけて仔ブタの耳の静脈に注射すれば、この動物にとって有害ではない。静脈内注射後2週間の期間に得られたブタの血液のP50値を図10に対照との比較で示す。
正常な仔ブタへのITPPの静脈内注射
8週齢の正常な仔ブタ(体重17kg)1頭でin vivo実験を実施した。ITPPの注射時に、5%イソフルラン、0.7L/分のN2Oおよび2.0L/分のO2で仔ブタを20〜30分間麻酔するか、耳の静脈から血液を採取した。27gのITPP/100mlの水(注射容量:63ml、pH6.5、17gのITPP=体重1kgあたり1gを含有)という濃度で静脈内注射した化合物は、少なくとも10分間かけて仔ブタの耳の静脈に注射すれば、この動物にとって有害ではない。静脈内注射後2週間の期間に得られたブタの血液のP50値を図10に対照との比較で示す。
実施例4
ITPP処理仔ブタの血球数
処理仔ブタと未処理仔ブタの血球数の差を評価するために、ITPP(体重1kgあたり1g)を与えた2匹の仔ブタの血液を、注射前、2時間後、注射後14日間の期間にわたって毎日採取した。以下の結論が導き出された。
・ヘマトクリットおよびRBC数のわずかな減少が注射後1日目に観察された。
・注射後最初の3日間に採取した血液試料で網状赤血球個体群の減少傾向(1.4%から0.5%)が観察された。
・注射をした動物で注射後5〜14日目に採取した血液試料で網状赤血球数の増加が計測された(14日目に最大3.0%)。
・ここでも、白血球(顆粒球、マクロファージ、血小板など)などの他の細胞数に大きな差は検出されなかった。
ITPP処理仔ブタの血球数
処理仔ブタと未処理仔ブタの血球数の差を評価するために、ITPP(体重1kgあたり1g)を与えた2匹の仔ブタの血液を、注射前、2時間後、注射後14日間の期間にわたって毎日採取した。以下の結論が導き出された。
・ヘマトクリットおよびRBC数のわずかな減少が注射後1日目に観察された。
・注射後最初の3日間に採取した血液試料で網状赤血球個体群の減少傾向(1.4%から0.5%)が観察された。
・注射をした動物で注射後5〜14日目に採取した血液試料で網状赤血球数の増加が計測された(14日目に最大3.0%)。
・ここでも、白血球(顆粒球、マクロファージ、血小板など)などの他の細胞数に大きな差は検出されなかった。
実施例5
仔ブタおよびマウスの用量効果曲線
体重1kgあたり1gのITPPを静脈内注射したところ、ブタのRBCでP50値の有意な右シフトが発生した(最大20%)。ほぼ飽和したITPP溶液、pH6.7を2頭の仔ブタ(いずれも体重約18kg)に20分間かけて(27gのITPP/100ml=体重1kgあたり1.5g)静脈内注射した。
仔ブタおよびマウスの用量効果曲線
体重1kgあたり1gのITPPを静脈内注射したところ、ブタのRBCでP50値の有意な右シフトが発生した(最大20%)。ほぼ飽和したITPP溶液、pH6.7を2頭の仔ブタ(いずれも体重約18kg)に20分間かけて(27gのITPP/100ml=体重1kgあたり1.5g)静脈内注射した。
どちらの仔ブタも注射が完了する前に死んだ(その時点で動物には体重1kgあたり<1.3g=70〜80mlの飽和ITPP溶液を注射していた)。
血球数ならびに、血清中のナトリウム、カリウムおよびカルシウムの量を調べるために、死んだ動物の心臓から血液を採取した。血球の数についてはいずれも(ヘマトクリット、白血球など)半分になった。カリウムおよびカルシウムの量はそのままで、一方ナトリウムは二倍になった(注射前:120〜140mmol/L;注射後:245mmol/L)。明らかに、ITPP(6Na+/分子)の形の大量のナトリウムが動物の死を引き起こしたのであろう。(ゆっくりと注射すれば)動物に有害な影響を及ぼさずに体重1kgあたり最大1gのITPPを静脈内注射できるように見える。用量効果曲線を図10Bに示す。これらの結果から、以下の結論が導き出された。
・ITPPは、体重1kgあたり1gの濃度でゆっくりと静脈内投与すれば(溶液の容量100mlを少なくとも10分間))仔ブタにとって有害ではなかった。体重1kgあたり1.2gのITPP(あるいはこれよりも多く)を静脈内注射後に2匹の仔ブタが死んだ後、2匹目の仔ブタにもITPPを1g/kgの濃度で注射した。処理後の仔ブタは喉が渇いていた。
・ITPPの静脈内注射量が増えると、動物を殺すことになった。
・P50値の有意な右シフト(最大20%)を発生させるには、体重1kgあたり1gのITPPの注射が必要である。
・この量のITPPを、この濃度で与えたブタでは、ゆっくりと注射をすれば血球数に病理学的な変化は何ら認められなかった。
・体重1kgあたり1gのITPPを与えた仔ブタでは、ヘマトクリットの減少が観察された。
・処理した仔ブタの血液の白血球数(顆粒球、マクロファージ、血小板など)には、大きな差は検出できなかった。
・注射後24時間から72時間の間に網状赤血球数がわずかに減少した(1.5%から0.5%)。アロステリックエフェクターの注射後3日目から開始して、網状赤血球の数は14日間の期間に約3%増加した。
・ITPPは、体重1kgあたり1gの濃度でゆっくりと静脈内投与すれば(溶液の容量100mlを少なくとも10分間))仔ブタにとって有害ではなかった。体重1kgあたり1.2gのITPP(あるいはこれよりも多く)を静脈内注射後に2匹の仔ブタが死んだ後、2匹目の仔ブタにもITPPを1g/kgの濃度で注射した。処理後の仔ブタは喉が渇いていた。
・ITPPの静脈内注射量が増えると、動物を殺すことになった。
・P50値の有意な右シフト(最大20%)を発生させるには、体重1kgあたり1gのITPPの注射が必要である。
・この量のITPPを、この濃度で与えたブタでは、ゆっくりと注射をすれば血球数に病理学的な変化は何ら認められなかった。
・体重1kgあたり1gのITPPを与えた仔ブタでは、ヘマトクリットの減少が観察された。
・処理した仔ブタの血液の白血球数(顆粒球、マクロファージ、血小板など)には、大きな差は検出できなかった。
・注射後24時間から72時間の間に網状赤血球数がわずかに減少した(1.5%から0.5%)。アロステリックエフェクターの注射後3日目から開始して、網状赤血球の数は14日間の期間に約3%増加した。
C57BL/6−マウスでのITPPの腹腔内(ip)注射についても用量効果曲線を得た。10匹のマウスに45〜120mmの30mM ITPP溶液を腹腔内注射した。この薬用量は、体重1kgあたり0.17〜0.88gに相当する。6匹のマウスに生理食塩溶液を注射した。ITPPを注射したマウスのデータ値で観察された平均および標準偏差を図11に示す。
実施例6
ヒト、マウス、ブタの全血で実施した試験管内実験
3つの種すなわち、ヒト、マウス、ブタでの全血におけるP50シフトのエフェクターとしてのコレステロイル誘導体(ここではkf96と表示)と一緒にITPP(いずれも60mM)を試験した。通常どおり、化合物溶液のpHを約7.0に調整し、両方の溶液のオスモル濃度を求めた(325〜373mOsM)上で、エフェクターで処理し、1:1比の全血容量でインキュベートした。インキュベーション後、血球をBis−Tris緩衝液で3回洗浄した。RBCの溶解は観察されなかった。エフェクターによって誘導した全血のP50値の概要を表2にあげておく。
ヒト、マウス、ブタの全血で実施した試験管内実験
3つの種すなわち、ヒト、マウス、ブタでの全血におけるP50シフトのエフェクターとしてのコレステロイル誘導体(ここではkf96と表示)と一緒にITPP(いずれも60mM)を試験した。通常どおり、化合物溶液のpHを約7.0に調整し、両方の溶液のオスモル濃度を求めた(325〜373mOsM)上で、エフェクターで処理し、1:1比の全血容量でインキュベートした。インキュベーション後、血球をBis−Tris緩衝液で3回洗浄した。RBCの溶解は観察されなかった。エフェクターによって誘導した全血のP50値の概要を表2にあげておく。
すべての血液試料で、Hb−O2解離曲線の強い右シフトが観察された。ITPPで観察されたシフト(最大40%)は、kf96(27%)の場合よりもさらに強かった。ITPPは120mMの濃度でもマウスにとっては十分許容できるものである。
実施例7
エフェクターITPPを腹腔内注射することによる影響の調査
45、60、120および150mMのITPP溶液を注射後2時間および1日の時点で採取したC57B1/6マウスの血液のP50シフトを、報告したようにして測定した。各試料のP50値を表3にあげておく。ITPPは150mMの濃度でも十分に許容できるものであった。いずれの動物も死なず、化合物に苦しんでいるようにも見えなかった。表3に示すように、どの濃度でもP50のシフトが認められた。
エフェクターITPPを腹腔内注射することによる影響の調査
45、60、120および150mMのITPP溶液を注射後2時間および1日の時点で採取したC57B1/6マウスの血液のP50シフトを、報告したようにして測定した。各試料のP50値を表3にあげておく。ITPPは150mMの濃度でも十分に許容できるものであった。いずれの動物も死なず、化合物に苦しんでいるようにも見えなかった。表3に示すように、どの濃度でもP50のシフトが認められた。
実施例8
P50シフト[%]と赤血球(erythrocyte)個体群の関係
報告した予備データに基づいて、RBC数とそのP50値のシフトとの間に反比例の関係が存在するように見える(図1参照)。ITPPの摂取12日後にΔP50が0%になると、RBC数の基底値が回復する。ヘマトクリットは、60mMのITPP溶液200μlの腹腔内注射6日後に、0日目(ITPP投与前)の40%から32%に落ちる。
P50シフト[%]と赤血球(erythrocyte)個体群の関係
報告した予備データに基づいて、RBC数とそのP50値のシフトとの間に反比例の関係が存在するように見える(図1参照)。ITPPの摂取12日後にΔP50が0%になると、RBC数の基底値が回復する。ヘマトクリットは、60mMのITPP溶液200μlの腹腔内注射6日後に、0日目(ITPP投与前)の40%から32%に落ちる。
循環赤血球におけるヘモグロビンのP50がシフトすると、赤血球数およびヘマトクリットが小さくなる。これは、生物での通常の酸素化に必要な赤血球が少なくなるからである。よって、多くの場合は血液希釈が良好な作用である。
図3に示すように、血球数がP50に影響されることから、貧血の治療でエリスロポエチンに代えてITPPを使用してもよいことの別の証明となる。
実施例9
労作能の増大
ITPPを投与することで、正常な動物の労作能が最大100%まで大きくなる場合がある。これは、動いている筋肉に、より多くの酸素を送達できるからである。図6に示すように、プラシーボにはマウスの労作能試験を実施したメートル距離にほとんど影響しないが、体重1kgあたり50gの用量のITPPでは、顕著な改善が認められ、体重1kgあたり400gでは基線値に対して労作能が約70%改善された。
労作能の増大
ITPPを投与することで、正常な動物の労作能が最大100%まで大きくなる場合がある。これは、動いている筋肉に、より多くの酸素を送達できるからである。図6に示すように、プラシーボにはマウスの労作能試験を実施したメートル距離にほとんど影響しないが、体重1kgあたり50gの用量のITPPでは、顕著な改善が認められ、体重1kgあたり400gでは基線値に対して労作能が約70%改善された。
実施例10
myo−イノシトール1,6:2,3:4,5−トリピロリン酸のカルシウム塩の調製
K.C.Fylaktakidou,J.M.Lehn,R.Greferath and C.Nicolau,Bioorganic & Medicinal Chemistry Letters,2005,75,1605〜1608(その内容全体を本明細書に援用する)に記載されているようにして、myo−イノシトール六リン酸(IHP)からmyo−イノシトールトリピロリン酸の六ナトリウム塩および六ピリジニウム塩(ITPP−NaおよびITPP−py)を得る。myo−イノシトールトリピロリン酸の他の塩についても、Fylaktakidouらの参考文献に従って生成できる。また、L.F.Johnson and M.E.Tate,Can.J.Chem.,1969,47,63(フィチンの説明についてその内容全体を本明細書に援用する)も参照のこと。また、Nicolauらの米国特許第7,084,115号明細書(2006年8月1日)に記載されたITPP酸および塩の合成も参照のこと。
myo−イノシトール1,6:2,3:4,5−トリピロリン酸のカルシウム塩の調製
K.C.Fylaktakidou,J.M.Lehn,R.Greferath and C.Nicolau,Bioorganic & Medicinal Chemistry Letters,2005,75,1605〜1608(その内容全体を本明細書に援用する)に記載されているようにして、myo−イノシトール六リン酸(IHP)からmyo−イノシトールトリピロリン酸の六ナトリウム塩および六ピリジニウム塩(ITPP−NaおよびITPP−py)を得る。myo−イノシトールトリピロリン酸の他の塩についても、Fylaktakidouらの参考文献に従って生成できる。また、L.F.Johnson and M.E.Tate,Can.J.Chem.,1969,47,63(フィチンの説明についてその内容全体を本明細書に援用する)も参照のこと。また、Nicolauらの米国特許第7,084,115号明細書(2006年8月1日)に記載されたITPP酸および塩の合成も参照のこと。
上記の化合物から他の化合物を生成することもできる。たとえば、ITPP−pyの水溶液をイオン交換Dowex H+カラムに通すと、myo−イノシトールトリピロリン酸の対応する過プロトン化(perprotonated)形態(すなわちITPP−H)の溶液が得られる。
ITPP−Hを3当量の水酸化カルシウム(ピロリン酸塩基1つあたり1当量)で処理すると、トリカルシウム塩ITPP−Caが得られ、ロータリーエバポレータ(すなわちrotovap)を使うなどして減圧下で水溶液を蒸発させて、これを単離することができる。
あるいは、ITPP−Naの水溶液と一緒に等モル量のCaCl2を加えてITPP−Caを生成することも可能である。得られる混合物がITPP−Caとなり、そこには不純物としてNaClが含まれる。ITPPのカルシウム/ナトリウム混合塩が有益であることが見いだされている。ITPPの純粋なカルシウム塩は、比較的不溶性であることが分かっており、かたや純粋なナトリウム塩は比較的毒性が高いことが判明した。
したがって、好ましい実施形態では、本発明は、任意に、イノシトールトリピロリン酸がmyo−イノシトール1,6:2,3:4,5トリピロリン酸であるイノシトールトリピロリン酸のカルシウム塩に関する。myo−イノシトールトリピロリン酸のリチウム、ベリリウム、マグネシウム、カリウム、ストロンチウム、バリウム、ルビジウムおよびセシウム塩などのmyo−イノシトールトリピロリン酸の他の塩を生成することも可能であり、これらも本発明の範囲内であることが企図される。これらの塩をmyo−イノシトールトリピロリン酸のカルシウム塩と併用することも可能である。あるいは、これらの塩の混合物を生成することや、myo−イノシトールトリピロリン酸のカルシウム塩なしで使用することも可能である。
もうひとつの実施形態では、本発明は、イノシトールトリピロリン酸のカルシウム塩と、その薬学的に許容されるアジュバント、希釈剤、キャリアまたは賦形剤を含む医薬組成物に関する。この医薬組成物では、イノシトールトリピロリン酸は、任意にmyo−イノシトール1,6:2,3:4,5トリピロリン酸である。別の実施形態では、本発明の組成物は、任意にmyo−イノシトールトリピロリン酸のナトリウム塩を、好ましくはITPP分子1つあたり4つのNa+イオンと1つのCa++イオンの比で含むものであってもよい。また、ピリジニウム塩、N,N−ジメチルシクロヘキシルアンモニウム塩、シクロヘプチルアンモニウム塩、シクロオクチルアンモニウム塩、ピペラジニウム塩およびトリピペラジニウム塩を含むが、これに限定されるものではない、他のmyo−イノシトールトリピロリン酸塩をmyo−イノシトールトリピロリン酸のカルシウム塩との関連で使用してもよいことが企図され、よってこれも本発明の範囲内である。
一実施形態では、上記の組成物がmyo−イノシトール1,6:2,3:4,5トリピロリン酸を含む。この組成物は、貧血を治療する薬用量で任意に調製される。
一実施形態では、本発明の組成物は、1日あたり約0.5〜1.5g/kg、任意に約0.9〜1.1g/kgが有効量で送達されるように、薬用量のmyo−イノシトール1,6:2,3:4,5トリピロリン酸(この化合物のカルシウム塩など)を送達する上述した任意の方法で調製される。
他の実施形態では、本発明は、カルシウム塩含有有機化合物を、myo−イノシトールトリピロリン酸の過プロトン化形態に加えることを含む、myo−イノシトール1,6:2,3:4,5トリピロリン酸カルシウム塩の製造方法に関する。一実施形態では、カルシウム塩含有有機化合物が、水酸化カルシウム、塩化カルシウム、臭化カルシウム、ヨウ化カルシウム、フッ化カルシウムのうちの1つまたは複数である。一実施形態では、この方法は、過プロトン化myo−イノシトールトリピロリン酸化合物の量に対して少なくとも3対1の比でカルシウム含有有機化合物を加えることを含む。したがって、一実施形態では、この方法は、過プロトン化myo−イノシトールトリピロリン酸化合物の量に対して少なくとも3対1の比で水酸化カルシウムを加えることを含む。
もうひとつの実施形態では、本発明は、薬学的に許容される量の上述したいずれかの組成物を個体に投与することを含む、貧血を治療するための方法であって、1日あたり約0.9〜1.1g/kgあるいは約0.5〜1.5g/kgの薬用量の量で組成物中の活性成分(すなわちITPP)を個体に投与する方法に関する。
別の実施形態では、本発明は、ヘモグロビンP50レベルを高めの酸素分圧値にシフトする方法であって、有効量のmyo−イノシトール1,6:2,3:4,5トリピロリン酸のカルシウム塩を単独あるいは上述したITPPの塩のうちの1つとの組み合わせで個体に投与することを含む、方法に関するものである。この方法では、myo−イノシトール1,6:2,3:4,5トリピロリン酸のカルシウム塩は、任意に組成物の一部として投与され、この組成物は任意に、アジュバント、希釈剤、キャリアまたは賦形剤のうちの1つまたは複数を含有する。この組成物におけるmyo−イノシトール1,6:2,3:4,5トリピロリン酸のカルシウム塩は、1日あたり約0.9〜1.1g/kgの薬用量あるいは、約0.5〜1.5g/kgの薬用量で投与される。あるいは、他のITPP塩をITPP−Caと併用し、ITPPの合計の薬用量(すべての塩形態を基準にし、対イオンの式量は含まない)を、1日あたり約0.5〜1.5g/kgの薬用量で送達してもよいし、あるいは1日あたり約0.9〜1.1g/kgの薬用量で送達してもよい。
他の実施形態では、本発明の組成物を使用して、ITPPのカルシウム塩などの有効量のITPP塩を送達することにより、貧血を治療することができる。
実施例11
一カルシウム四ナトリウム−myo−イノシトール−1.6:2,3:4,5−トリピロリン酸の調製
1当量の水酸化カルシウムと4当量の水酸化ナトリウムでmyo−イノシトール−1,6:2,3:4,5−トリピロリン酸−Hを処理し、ITPPの一カルシウム四ナトリウム塩組成物すなわち、ITPP−Ca1Na4を得た。次に、ロータリーエバポレータ(すなわちrotovap)を使うなどして減圧下で水溶液を蒸発させて、これを単離する。
一カルシウム四ナトリウム−myo−イノシトール−1.6:2,3:4,5−トリピロリン酸の調製
1当量の水酸化カルシウムと4当量の水酸化ナトリウムでmyo−イノシトール−1,6:2,3:4,5−トリピロリン酸−Hを処理し、ITPPの一カルシウム四ナトリウム塩組成物すなわち、ITPP−Ca1Na4を得た。次に、ロータリーエバポレータ(すなわちrotovap)を使うなどして減圧下で水溶液を蒸発させて、これを単離する。
あるいは、ITPP−Hの水溶液と一緒に等モル量のCaCl2と4当量の塩化ナトリウムを加えて、ITPP−Ca1Na4組成物を生成した。得られる混合物には、HClが不純物として含まれているが、これは回転蒸発で除去可能である。
ITPPのカルシウム/ナトリウム混合塩が有益であることが見いだされた。ITPPの純粋なカルシウム塩は、比較的不溶性であることが分かっており、かたや純粋なナトリウム塩は比較的毒性が高いことが判明した。
実施例12
エリスロポエチンに対する置き換え療法としてのITPP
一例において、患者の潜在的な赤血球新生能を持続または復活させて化学療法による治療の悪影響を防止または軽減できるように、化学療法誘導貧血の治療のために1週間につき患者の体重1kgあたり300I.U.を投与することを含むエリスロポエチン治療計画を、30I.U./kg/週に落とす。エリスロポエチン治療計画の低減に合わせて、一カルシウム四ナトリウム−myo−イノシトール−1,6:2,3:4,5−トリピロリン酸を経口溶液として1日あたりITPPの薬用量0.9〜1.1g/kgで患者に投与する。
エリスロポエチンに対する置き換え療法としてのITPP
一例において、患者の潜在的な赤血球新生能を持続または復活させて化学療法による治療の悪影響を防止または軽減できるように、化学療法誘導貧血の治療のために1週間につき患者の体重1kgあたり300I.U.を投与することを含むエリスロポエチン治療計画を、30I.U./kg/週に落とす。エリスロポエチン治療計画の低減に合わせて、一カルシウム四ナトリウム−myo−イノシトール−1,6:2,3:4,5−トリピロリン酸を経口溶液として1日あたりITPPの薬用量0.9〜1.1g/kgで患者に投与する。
以上、特定の組成物、検出方法、活性ソース、有効性の提案などに関して本発明を説明してきたが、本発明をこのような例示的な実施形態または機序で限定することは意図していない旨ならびに、添付の特許請求の範囲に記載した本発明の範囲または主旨を逸脱することなく修正をほどこし得る旨は、当業者であれば明らかであろう。このような自明の修正および変更をいずれも、添付の特許請求の範囲に記載の本発明の範囲に含むことを意図している。任意の実施形態の上述した1つまたは複数の要素のいずれも、他の実施形態の1つまたは複数の要素と組み合わせられることを理解されたい。さらに、範囲について言及した部分では、その範囲に含まれる実数がすべて、企図される端点であることを理解されたい。たとえば、0.9〜1.1g/kgの範囲がある場合、この範囲に含まれる実数値(たとえば、0.954〜1.052g/kg)はすべて、仮に明示的には言及していなかったとしても本発明の範囲の一部として企図される。本明細書に引用した参考文献はいずれも、その内容全体が本明細書に援用される。
Claims (36)
- ヒトまたは動物に、有効量のイノシトール−トリピロリン酸(ITPP)を含む組成物を投与することを含む、ヒトまたは動物における赤血球による組織酸素化を促進するための方法。
- 前記ITPP組成物がエリスロポエチンをさらに含む、請求項1に記載の方法。
- 前記ITPP組成物が、エリスロポエチン治療計画との組み合わせで用いられる、請求項1に記載の方法。
- 前記ITPP組成物が、エリスロポエチンを含む第2の組成物と交互に投与される、請求項1に記載の方法。
- 前記ITPP組成物が、エリスロポエチンを含む第2の組成物と平行して投与される、請求項1に記載の方法。
- 任意の順序または同時に、
a)薬用量または投与頻度を減らすことで、前記ヒトまたは動物に投与されるエリスロポエチンの量を最大90%減少させ、
b)前記エリスロポエチンの薬用量の減少によって失われた、現行または予測酸素化能を補償するよう計算した薬用量で、前記ITPP組成物を投与する、
請求項3に記載の方法。 - 前記イノシトール−トリピロリン酸が酸または塩として用いられる、請求項1に記載の方法。
- 前記ITPP組成物におけるイノシトールの異性体が、イノシトールのmyo−、scyllo−、chiro−、muco−、neo、allo−、epi−、cis−異性体からなる群から選択される、請求項1に記載の方法。
- 前記ITPP組成物が、一カルシウム四ナトリウムmyo−イノシトール−1,6:2,3:4,5−トリピロリン酸を含む、請求項1に記載の方法。
- 前記方法が、循環赤血球におけるヘモグロビンのP50値を右にシフトさせるのに用いられる、請求項1に記載の方法。
- 前記方法が、実質的に低赤血球数で正常な酸素化を達成するのに用いられる、請求項1に記載の方法。
- 前記方法が、低ヘマトクリット値で正常な酸素化を達成するのに用いられる、請求項1に記載の方法。
- 前記方法が、前記ヒトまたは動物の労作能を高めるのに用いられる、請求項1に記載の方法。
- 前記ITPP組成物での治療が、前記ヒトまたは動物への投与対象となる赤血球の酸素運搬能を高めるのに用いられ、前記ヒトまたは動物の体外での血液透析または他の赤血球処理時に前記治療を実施する、請求項1に記載の方法。
- ヒトまたは動物に、有効量のイノシトール−トリピロリン酸(ITPP)を含む組成物を投与することを含む、ヒトまたは動物における貧血または低酸素症を治療するための方法。
- 前記ITPP組成物がエリスロポエチンをさらに含む、請求項15に記載の方法。
- 前記ITPP組成物がエリスロポエチン治療計画との組み合わせで用いられる、請求項15に記載の方法。
- 前記方法が、HIV、炎症性腸疾患、敗血症エピソードまたは別の慢性感染と関連した貧血の治療に用いられる、請求項15に記載の方法。
- 前記方法を血液の輸血と併用して貧血または低酸素症を治療する、請求項15に記載の方法。
- 前記方法が、機能低下した肺の機能、機能低下した心臓の機能、血行不良、大量出血、不十分に酸素化しているヘモグロビンタイプあるいは、赤血球の喪失または不十分な生成に関連した疾患または障害に羅患したヒトまたは動物における低酸素症を防止または軽減するのに用いられる、請求項15に記載の方法。
- 前記イノシトール−トリピロリン酸が酸または塩として用いられる、請求項15に記載の方法。
- 前記ITPP組成物におけるイノシトールの異性体が、イノシトールのmyo−、scyllo−、chiro−、muco−、neo、allo−、epi−、cis−異性体からなる群から選択される、請求項15に記載の方法。
- 前記ITPP組成物が、一カルシウム四ナトリウムmyo−イノシトール−1,6:2,3:4,5−トリピロリン酸を含む、請求項15に記載の方法。
- ヒトまたは動物に、有効量のイノシトール−トリピロリン酸(ITPP)を含む組成物を投与することを含む、ヒトまたは動物において赤血球新生を生成するための方法。
- 前記ITPP組成物がエリスロポエチンをさらに含む、請求項24に記載の方法。
- 前記ITPP組成物がエリスロポエチン治療計画との組み合わせで用いられる、請求項24に記載の方法。
- 前記ITPP組成物がエリスロポエチンを含む第2の組成物と交互に投与される、請求項24に記載の方法。
- 前記ITPP組成物がエリスロポエチンを含む第2の組成物と平行して投与される、請求項24に記載の方法。
- 任意の順序または同時に、
a)薬用量およびまたは投与頻度を減らすことで、前記ヒトまたは動物に投与されるエリスロポエチンの量を最大90%減少させ、
b)前記エリスロポエチンの薬用量の減少によって失われた、現行または予測酸素化能を補償するよう計算した薬用量で、前記ITPP組成物を投与する、請求項26に記載の方法。 - 前記イノシトール−トリピロリン酸が酸または塩として用いられる、請求項24に記載の方法。
- 前記ITPP組成物におけるイノシトールの異性体が、イノシトールのmyo−、scyllo−、chiro−、muco−、neo、allo−、epi−、cis−異性体からなる群から選択される、請求項24に記載の方法。
- 前記ITPP組成物が、一カルシウム四ナトリウムmyo−イノシトール−1,6:2,3:4,5−トリピロリン酸を含む、請求項24に記載の方法。
- イノシトール−トリピロリン酸(ITPP)と、医薬キャリアまたは賦形剤とを、1日用量、1日の分割用量またはその適当な一部での投与時に有効量で含む、ヒトまたは動物における貧血または低酸素症を治療するための医薬組成物。
- 前記ITPPが、一カルシウム四ナトリウムmyo−イノシトール−1,6:2,3:4,5−トリピロリン酸である、請求項33に記載の医薬組成物。
- イノシトール−トリピロリン酸(ITPP)と、医薬キャリアまたは賦形剤とを、1日用量、1日の分割用量またはその適当な一部での投与時に有効量で含む、ヒトまたは動物における赤血球新生を生成するための医薬組成物。
- 前記ITPPが、一カルシウム四ナトリウムmyo−イノシトール−1,6:2,3:4,5−トリピロリン酸である、請求項35に記載の医薬組成物。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US92705907P | 2007-05-01 | 2007-05-01 | |
| PCT/US2008/005603 WO2008134082A1 (en) | 2007-05-01 | 2008-05-01 | Erythropoietin complementation or replacement |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010526068A true JP2010526068A (ja) | 2010-07-29 |
| JP2010526068A5 JP2010526068A5 (ja) | 2012-07-12 |
Family
ID=39926016
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2010506314A Pending JP2010526068A (ja) | 2007-05-01 | 2008-05-01 | エリスロポエチン補完または置換 |
Country Status (7)
| Country | Link |
|---|---|
| US (2) | US20080312138A1 (ja) |
| EP (1) | EP2152085A4 (ja) |
| JP (1) | JP2010526068A (ja) |
| CN (1) | CN101784193A (ja) |
| AU (1) | AU2008246061A1 (ja) |
| CA (1) | CA2688233A1 (ja) |
| WO (1) | WO2008134082A1 (ja) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20130266668A1 (en) * | 2010-12-01 | 2013-10-10 | Virginia Commonwealth University | Use of hemoglobin effectors to increase the bioavailability of therapeutic gases |
| CA2907175C (en) | 2013-03-15 | 2022-11-08 | M. Alphabet 3, L.L.C. | Methods and compositions for enhancing oxygen levels in tissues |
| WO2015138916A1 (en) * | 2014-03-14 | 2015-09-17 | Yves Claude Nicolau | Myo-inositol trispyrophoshate as an anti-diabetic agent |
| CN111714504A (zh) * | 2020-06-08 | 2020-09-29 | 广州新民培林医药科技有限公司 | Itpp在制备预防和/或治疗缺血缺氧损伤及肺损伤的药物中的应用 |
Family Cites Families (76)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4192869A (en) * | 1977-09-06 | 1980-03-11 | Studiengesellschaft Kohle Mbh. | Controlled improvement of the O2 release by intact erythrocytes with lipid vesicles |
| DE2740053A1 (de) * | 1977-09-06 | 1979-05-03 | Klaus Prof Dr Med Gersonde | Verwendung von allosterischen effektoren mit hilfe von lipidvesikeln ueber eine irreversible inkorporierung zwecks verbesserter o tief 2 -entladung des haemoglobins in erythrozyten |
| JPS5828878B2 (ja) * | 1980-08-20 | 1983-06-18 | 三金工業株式会社 | 環状ピロ燐酸エステル誘導体 |
| US4473496A (en) * | 1981-09-14 | 1984-09-25 | The United States Of America As Represented By The Secretary Of The Army | Intramolecularly crosslinked hemoglobin |
| FR2529463B1 (fr) * | 1982-07-05 | 1986-01-10 | Centre Nat Rech Scient | Procede et dispositif pour l'encapsulation dans les erythrocytes d'au moins une substance a activite biologique, notamment des effecteurs allosteriques de l'hemoglobine et erythrocytes ainsi obtenus |
| US4478824A (en) * | 1983-08-08 | 1984-10-23 | Franco Robert S | Method for altering red blood cell function and survival |
| GB8328917D0 (en) * | 1983-10-28 | 1983-11-30 | Fisons Plc | Blood substitute |
| SE465305B (sv) * | 1986-04-16 | 1991-08-26 | Perstorp Ab | Anvaendning av inositolfosfat foer framstaellning av ett laekemedel |
| US5023248A (en) * | 1984-10-23 | 1991-06-11 | Perstorp Ab | Method of treating diabetes with inositol triphosphate |
| US5545632A (en) * | 1984-10-23 | 1996-08-13 | Perstorp Ab | Method of treating retroviral disease |
| US5015634A (en) * | 1986-04-16 | 1991-05-14 | Perstorp Ab | Method of treating tissue damage with inositol triphosphate |
| SE465951B (sv) * | 1984-10-23 | 1991-11-25 | Perstorp Ab | Isomer av inositoltrifosfat foeretraedesvis i saltform foer anvaendning som terapeutiskt eller profylaktiskt medel samt kompositioner daerav |
| US5330979A (en) * | 1984-10-23 | 1994-07-19 | Perstorp Ab | Method of treating renal disorders with inositoltriphosphate |
| US5407924A (en) * | 1984-10-23 | 1995-04-18 | Perstorp Ab | Method of treating pain using inositol triphosphate |
| US4887995A (en) * | 1985-01-22 | 1989-12-19 | University Of Pittsburgh | Method of treating sickle cell anemia |
| US5292913A (en) * | 1986-03-11 | 1994-03-08 | Mitsui Toatsu Chemicals, Incorporated | Myoinositol derivatives and preparation process thereof |
| EP0262227B1 (en) * | 1986-03-11 | 1993-01-20 | MITSUI TOATSU CHEMICALS, Inc. | Process for the preparation of myoinositol derivatives |
| US4731473A (en) * | 1986-04-04 | 1988-03-15 | Merck & Co., Inc. | Compounds useful in treating sickle cell anemia |
| US4731381A (en) * | 1986-04-04 | 1988-03-15 | Merck & Co., Inc. | Method of treating a person for sickle cell anemia |
| US4699926A (en) * | 1986-04-04 | 1987-10-13 | Merck & Co., Inc. | Compounds useful in treating sickle cell anemia |
| US4751244A (en) * | 1986-04-04 | 1988-06-14 | Merck & Co., Inc. | Compounds useful in treating sickle cell anemia |
| US5057507A (en) * | 1986-04-16 | 1991-10-15 | Perstorp Ab | Method of alleviating bone damage with inositoltriphosphate |
| US5135923A (en) * | 1986-04-16 | 1992-08-04 | Perstorp Ab | Method of treating cardiovascular diseases |
| US5274161A (en) * | 1986-11-26 | 1993-12-28 | Perstorp Ab | Derivatives of cyclohexane |
| US4847082A (en) * | 1987-01-21 | 1989-07-11 | Robert Sabin | Method of treatment of Alzheimer's disease using phytic acid |
| US4873355A (en) * | 1987-05-29 | 1989-10-10 | E. I. Du Pont De Nemours And Company | Process for regioselectively preparing phosphorylated inositols and other cyclitols |
| US4924023A (en) * | 1987-05-29 | 1990-05-08 | E. I. Du Pont De Nemours And Company | Phosphorylated inositols |
| US4931276A (en) * | 1987-10-30 | 1990-06-05 | Franco Robert S | Method for introducing desired agents into red blood cells |
| US4826675A (en) * | 1988-02-17 | 1989-05-02 | Colgate-Palmolive Company | Anticalculus oral composition |
| US5043261A (en) * | 1989-04-10 | 1991-08-27 | Cryopharm Corporation | Lyophilized and reconstituted red blood cell and hemosome compositions |
| US5082833A (en) * | 1988-06-30 | 1992-01-21 | Shamsuddin Abulkalam M | Reduction of cell proliferation and enhancement of nk-cell activity |
| US4874690A (en) * | 1988-08-26 | 1989-10-17 | Cryopharm Corporation | Lyophilization of red blood cells |
| US5264605A (en) * | 1989-06-28 | 1993-11-23 | Mitsui Toatsu Chemicals, Incorporated | Myoinsitol derivatives, process for preparing same, phosphorylating agent, and its utilization |
| US5151539A (en) * | 1989-07-03 | 1992-09-29 | Akzo America Inc. | Formation of tetraarylpyrophosphate |
| WO1991004258A1 (en) * | 1989-09-22 | 1991-04-04 | Mitsui Toatsu Chemicals, Incorporated | Inositol derivative and production thereof |
| JPH03115290A (ja) * | 1989-09-28 | 1991-05-16 | Yokohama Rubber Co Ltd:The | 1d―ミオイノシトール―1―リン酸の合成法 |
| US5173426A (en) * | 1989-10-06 | 1992-12-22 | Yale University | DNAs encoding genetically engineered low oxygen affinity mutants of human hemoglobin |
| US5210263A (en) * | 1990-05-15 | 1993-05-11 | University Of Pittsburgh | Inositol phosphate analogs and methods for their use |
| US5295944A (en) * | 1991-05-14 | 1994-03-22 | Dana-Farber Cancer Institute | Method for treating a tumor with ionizing radiation |
| US5260472A (en) * | 1992-01-29 | 1993-11-09 | The Board Of Governors For Higher Education State Of Rhode Island And Providence Plantations | Efficient chemoenzymatic synthesis of D-myo-inositol 1,4,5-triphosphate, D-myo-inositol 1,3,4-triphosphate, and D-myo-inositol 1,3,4,5-tetraphosphate |
| US5296466A (en) * | 1992-02-19 | 1994-03-22 | Board Of Regents, The University Of Texas System | Inhibition of nitric oxide-mediated hypotension and septic shock with iron-containing hemoprotein |
| US5344393A (en) * | 1992-02-28 | 1994-09-06 | Alliance Pharmaceutical Corp. | Use of synthetic oxygen carriers to facilitate oxygen delivery |
| US5260287A (en) * | 1992-05-11 | 1993-11-09 | Board Of Regents, The University Of Texas System | Polyphosphorylated organic compounds: compositions useful in protecting biological tissues |
| EP0690671B1 (en) * | 1993-03-23 | 2004-08-04 | Cbr Laboratories, Inc. | Method and apparatus for encapsulation of biologically-active substances in cells |
| US5866548A (en) * | 1993-04-09 | 1999-02-02 | The Regents Of The University Of California | Caged membrane-permeant inositol phosphates |
| US5827837A (en) * | 1993-08-20 | 1998-10-27 | The Regents Of The University Of California | Polyanion anti-inflammatory agents |
| SE502989C2 (sv) * | 1993-11-22 | 1996-03-04 | Perstorp Ab | Användning av en inositoltrisfosfatester för beredning av läkemedel |
| SE503122C2 (sv) * | 1993-11-22 | 1996-03-25 | Perstorp Ab | Användning av en inositoltrisfosfatester för behandling av inflammatoriska tillstånd |
| US6074605A (en) * | 1995-03-10 | 2000-06-13 | Entremed, Inc. | Flow electroporation chamber and method |
| US5720921A (en) * | 1995-03-10 | 1998-02-24 | Entremed, Inc. | Flow electroporation chamber and method |
| US5626884A (en) * | 1995-08-18 | 1997-05-06 | Lockett; Curtis G. | Treatment of sickle cell disease |
| US6949517B1 (en) * | 1996-06-24 | 2005-09-27 | Matti Siren | Method of treating inflammatory, tissue repair and infectious conditions |
| US5880099A (en) * | 1996-09-20 | 1999-03-09 | The Regents Of The University Of California | Inositol polyphosphates and methods of using same |
| US5977078A (en) * | 1996-09-20 | 1999-11-02 | The Regents Of The Univesity Of California | Inositol polyphosphate derivatives and methods of using same |
| DE19649350A1 (de) * | 1996-11-28 | 1998-06-04 | Hoechst Ag | Inositolglykane mit insulinartiger Wirkung |
| US6096916A (en) * | 1997-05-23 | 2000-08-01 | Nutrimed Biotech | Synthesis of D-3 phosphorylated phosphoinositides and analogues |
| US6187335B1 (en) * | 1997-12-31 | 2001-02-13 | Orasomal Technologies, Inc. | Polymerizable fatty acids, phospholipids and polymerized liposomes therefrom |
| US7410941B1 (en) * | 1999-04-13 | 2008-08-12 | The Kenneth S. Warren Institute, Inc. | Methods for treatment of neurodegenerative conditions by peripherally administered erythropoietin |
| EP1272201B1 (de) * | 2000-04-12 | 2004-11-24 | Bitop Aktiengesellschaft Für Biotechnische Optimierung | Verwendung von kompatiblen soluten als substanzen mit radikalfangenden eigenschaften |
| US7084126B1 (en) * | 2000-05-01 | 2006-08-01 | Healthpartners Research Foundation | Methods and compositions for enhancing cellular function through protection of tissue components |
| WO2002010177A1 (en) * | 2000-08-01 | 2002-02-07 | Gmp Companies, Inc. | Ammonium salts of inositol hexaphosphate and uses thereof |
| WO2002009723A2 (en) * | 2000-08-01 | 2002-02-07 | Gmp Companies, Inc. | Ammonium salts of hemoglobin allosteric effectors, and uses thereof |
| US7453006B2 (en) * | 2000-11-21 | 2008-11-18 | Inologic, Inc. | Inositol derivatives for increasing chloride secretion and inhibiting inflammation |
| WO2002070009A1 (fr) * | 2001-02-27 | 2002-09-12 | Yasuda, Yoshiko | Medicaments preventifs/curatifs pour cicatrices hypertrophiques, cheloides et maladies arthritiques chroniques |
| AU2002254234A1 (en) * | 2001-03-14 | 2002-09-24 | Centocor, Inc. | Chronic obstructive pulmonary disease-related immunglobulin derived proteins, compositions, methods and uses |
| US20050020542A1 (en) * | 2001-09-20 | 2005-01-27 | Alexis Traynor-Kaplan | Method of modulating sodium ion absorption in epithelial cells |
| WO2003092700A1 (en) * | 2002-04-29 | 2003-11-13 | Gmp Oxycell, Inc. | Inositol pyrophosphates, and methods of use thereof |
| AU2003239973A1 (en) * | 2002-06-14 | 2004-01-19 | Gmp Oxycell, Inc. | Sterols bearing pendant allosteric effectors of hemoglobin, and uses thereof |
| US20050176627A1 (en) * | 2002-09-09 | 2005-08-11 | Anthony Cerami | Long acting erythropoietins that maintain tissue protective activity of endogenous erythropoietin |
| WO2004087721A1 (en) * | 2003-03-27 | 2004-10-14 | Inologic, Inc. | Camphanylidene and phenylalkyl inositol polyphosphate compounds, compositions, and methods of their use |
| ES2232302B1 (es) * | 2003-11-07 | 2006-08-01 | Universitat De Les Illes Balears | Myo-inositol hexafosfato para uso topico. |
| US20060258626A1 (en) * | 2004-07-06 | 2006-11-16 | Claude Nicolau | Use of inositol-tripyrophosphate in treating tumors and diseases |
| US20070135389A1 (en) * | 2004-07-06 | 2007-06-14 | Claude Nicolau | Tumor eradication by inositol-tripyrophosphate |
| US20060106000A1 (en) * | 2004-07-06 | 2006-05-18 | Claude Nicolau | Use of inositol-tripyrophosphate in treating tumors and diseases |
| DK1863495T3 (en) * | 2005-03-18 | 2015-04-20 | Normoxys Inc | CALCIUM AND SODIUM SALT OF MYO-INOSITOL 1.6: 2,3: 4,5 TRIPYROPHOSPHATE FOR CANCER TREATMENT |
| CA2674048A1 (en) * | 2006-12-29 | 2008-07-10 | Normoxys, Inc. | Cyclitols and their derivatives and their therapeutic applications |
-
2008
- 2008-05-01 JP JP2010506314A patent/JP2010526068A/ja active Pending
- 2008-05-01 WO PCT/US2008/005603 patent/WO2008134082A1/en active Application Filing
- 2008-05-01 AU AU2008246061A patent/AU2008246061A1/en not_active Abandoned
- 2008-05-01 CN CN200880020187A patent/CN101784193A/zh active Pending
- 2008-05-01 CA CA002688233A patent/CA2688233A1/en not_active Abandoned
- 2008-05-01 EP EP08767476A patent/EP2152085A4/en not_active Withdrawn
- 2008-05-01 US US12/150,946 patent/US20080312138A1/en not_active Abandoned
-
2011
- 2011-07-05 US US13/176,513 patent/US20110294732A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| US20080312138A1 (en) | 2008-12-18 |
| WO2008134082A1 (en) | 2008-11-06 |
| EP2152085A4 (en) | 2012-05-23 |
| AU2008246061A8 (en) | 2010-01-14 |
| CN101784193A (zh) | 2010-07-21 |
| AU2008246061A1 (en) | 2008-11-06 |
| EP2152085A1 (en) | 2010-02-17 |
| US20110294732A1 (en) | 2011-12-01 |
| CA2688233A1 (en) | 2008-11-06 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5028405B2 (ja) | ヘモグロビンのアロステリックエフェクターとしてのミオイノシトール1,6:2,3:4,5トリピロリン酸のカルシウム塩 | |
| EP1503768B1 (en) | Inositol pyrophosphates, and use thereof | |
| KR102223080B1 (ko) | 하나 이상의 약제학적 관심 물질이 로딩된 적혈구를 제조하는 방법 및 이렇게 하여 수득된 적혈구 | |
| US20170027966A1 (en) | Tumor eradication by inositol-tripyrophosphate | |
| US5631271A (en) | Methods and preparations for the treatment and prophylaxis of metabolic disturbances | |
| JP5112876B2 (ja) | 還元型グルタチオン経口投与のためのリポソーム処方物 | |
| WO1993008812A1 (en) | Reconstituted platelet membrane vesicles | |
| US20120035137A1 (en) | Use of inositol-tripyrophosphate in treating tumors and diseases | |
| JPS62265232A (ja) | 脂質置換治療法 | |
| US6610702B2 (en) | Ammonium salts of inositol hexaphosphate, and uses thereof | |
| US20110294732A1 (en) | Erythropoletin complementation or replacement | |
| EP1223942A2 (en) | Agents for the enhanced oxygen delivery in mammals | |
| WO1980001456A1 (en) | Pharmaceutical composition and process for the preparation thereof | |
| US20120003161A1 (en) | Use of inositol-tripyrophosphate in treating tumors and diseases | |
| KR20210148078A (ko) | 조직 관류 증가에 사용하기 위한 이노시톨 포스페이트 화합물 | |
| KR20060038387A (ko) | 화학요법을 받고 있는 암 환자를 치료하는 방법 | |
| RU2514004C1 (ru) | Способ получения комплексного препарата с иммунометаболической и антгельминтной активностью | |
| US20040072801A1 (en) | Sterols bearing pendant allosteric effectors of hemoglobin, and uses thereof | |
| CN114514034A (zh) | 稳定的血红蛋白组合物及其药物制剂 | |
| Toffelmire et al. | Plasma exchange in thrombotic thrombocytopenic purpura. | |
| CN103816119A (zh) | 制备维生素k1乳剂的方法和维生素k1乳剂 | |
| Zumbühl et al. | Cytotoxic effect of unilamellar detergent dialysis liposomes on Trypanosoma brucei and Trypanosoma congolense bloodstream forms in vitro | |
| JPWO2020092523A5 (ja) |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20110428 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110428 |
|
| A072 | Dismissal of procedure [no reply to invitation to correct request for examination] |
Free format text: JAPANESE INTERMEDIATE CODE: A073 Effective date: 20120911 |