JP2010513567A - プロテインキナーゼの阻害剤として有用なアミノピリミジン - Google Patents
プロテインキナーゼの阻害剤として有用なアミノピリミジン Download PDFInfo
- Publication number
- JP2010513567A JP2010513567A JP2009543169A JP2009543169A JP2010513567A JP 2010513567 A JP2010513567 A JP 2010513567A JP 2009543169 A JP2009543169 A JP 2009543169A JP 2009543169 A JP2009543169 A JP 2009543169A JP 2010513567 A JP2010513567 A JP 2010513567A
- Authority
- JP
- Japan
- Prior art keywords
- ring
- aliphatic
- disease
- con
- compound according
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing three or more hetero rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
- A61P19/10—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease for osteoporosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/18—Antipsychotics, i.e. neuroleptics; Drugs for mania or schizophrenia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/24—Antidepressants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/18—Antivirals for RNA viruses for HIV
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/04—Immunostimulants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/12—Antidiuretics, e.g. drugs for diabetes insipidus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
Landscapes
- Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Medicinal Chemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Neurology (AREA)
- Immunology (AREA)
- Neurosurgery (AREA)
- Biomedical Technology (AREA)
- Diabetes (AREA)
- Physical Education & Sports Medicine (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Rheumatology (AREA)
- Hematology (AREA)
- Psychiatry (AREA)
- Pulmonology (AREA)
- Virology (AREA)
- Pain & Pain Management (AREA)
- Obesity (AREA)
- Psychology (AREA)
- Endocrinology (AREA)
- Communicable Diseases (AREA)
- Hospice & Palliative Care (AREA)
- Heart & Thoracic Surgery (AREA)
- Cardiology (AREA)
- Emergency Medicine (AREA)
- Oncology (AREA)
- Molecular Biology (AREA)
- Transplantation (AREA)
- Tropical Medicine & Parasitology (AREA)
Abstract
Description
本発明は、プロテインキナーゼの阻害剤として有用な化合物に関する。また、本発明は、本発明の化合物を含む、薬学的に受容可能な組成物、および該組成物をさまざまな疾患の治療に用いる方法も提供する。また、本発明は、本発明の化合物を調製する工程も提供する。
グリコーゲンシンターゼキナーゼ−3(GSK−3)は、それぞれ異なった遺伝子によってコードされるαイソフォームおよびβイソフォームで構成されるセリン/スレオニンプロテインキナーゼである[Coghlanら、Chemistry & Biology 2000、7、793−803;ならびにKimおよびKimmel、Curr.Opinion Genetics Dev.、2000 10、508−514]。GSK−3は、糖尿病、アルツハイマー病、中枢神経系疾患(例えば、双極性疾患、統合失調症、脳卒中、ハンチントン病、およびその他の神経変性疾患)、白血球減少症、ならびに心筋細胞肥大などを含む、さまざまな疾患、障害、および症状と関連付けられている[特許文献1および特許文献2;ならびにHaqら、J.Cell Biol.2000、151、117−130]。これらの疾患、障害、および症状は、GSK−3が関与するある種の細胞シグナル伝達経路の異常な作用と関連している。GSK−3は、多くの調節タンパク質をリン酸化し、その活性を調節することが分かっている。これらのタンパク質には、グリコーゲン合成に必要な律速酵素であるグリコーゲンシンターゼ、微小管結合タンパク質タウ、遺伝子転写因子β−カテニン、翻訳開始因子e1F2B、ならびに、ATPクエン酸リアーゼ、アキシン、熱ショック因子−1、c−Jun、c−myc、c−myb、CREB、およびCEPBαが挙げられる。細胞の代謝、増殖、分化、および成長の数多くの態様において、これらの多様なタンパク質標的は、GSK−3に関係していることを示す。
本発明は、以下の化学式Iの化合物を提供する。
本発明は、以下の化学式Iの化合物、またはその薬学的に受容可能な塩を提供する。
環Dは、4〜7員の単環式環または8〜10員の二環式環であって、該環は、ヘテロシクリル環または炭素環から選択され、そして該ヘテロシクリル環は、窒素、酸素、または硫黄から選択される、1〜4個の環へテロ原子を有し、環Dの各置換可能な環炭素は、独立してオキソまたは−R5で置換され、そして任意の置換可能な環窒素は、−R4で独立して置換され;
Xは、硫黄、酸素、またはNR2’であり;
Yは、窒素またはCR2であり;
Z1およびZ2は、それぞれ独立してNまたはCR9である;ただし、Z1またはZ2の少なくとも一つはNであり;
RXは、−T1−R3であり;
RYは、−T2−R10であり;
R2およびR2’は、−Rまたは−T3−W−R6から独立して選択されるか;あるいは、R2およびR2’は、それらの間に介在する原子と一緒に、窒素、酸素、または硫黄から選択される0〜3個の環へテロ原子を有する、縮合した5〜8員の不飽和型または部分不飽和型の環を形成する;ただし、R2およびR2’によって形成された該縮合環上の置換可能な炭素はそれぞれ、ハロ、オキソ、−CN、−NO2、−R7、または−V−R6で置換され;また、R2およびR2’によって形成された該環上の置換可能な窒素はR4で置換され;
T、T1、T3はそれぞれ、独立して結合またはC1〜4アルキリデン鎖であり;
T2は、独立して結合またはC1〜4アルキリデン鎖であるが、該アルキリデン鎖のうち、最大3個のメチレン単位が、任意に、−O−、−C(=O)−、−S(O)−、−S(O)2−、−S−、または−N(R4)−によって置換され;
R3は、−R、−ハロ、−OR、−C(=O)R、−CO2R、−COCOR、−COCH2COR、−NO2、−CN、−S(O)R、−S(O)2R、−SR、−N(R4)2、−CON(R7)2、−SO2N(R7)2、−OC(=0)R、−N(R7)COR、−N(R7)CO2R”、−N(R4)N(R4)2、−C(=NH)N(R4)2、−C(=NH)−OR、−N(R7)CON(R7)2、−N(R7)SO2N(R7)2、−N(R4)SO2R、または−OC(=O)N(R7)2から選択され;
R4は、−R7、−COR7、−CO2(任意に置換されたC1〜6脂肪族)、−CON(R7)2、またはSO2R7からそれぞれ独立して選択されるか;または、同一の窒素上にある2つのR4が一緒になって3〜8員のヘテロシクリル環またはヘテロアリール環を形成し;
R5は、−R、ハロ、−OR、−C(=O)R、−CO2R、−COCOR、−NO2、−CN、−S(O)R、−SO2R、−SR、−N(R4)2、−CON(R4)2、−SO2N(R4)2、−OC(=O)R、−N(R4)COR、−N(R4)CO2R”、−N(R4)N(R4)2、−C=NN(R4)2、−C=N−OR、−N(R4)CON(R4)2、−N(R4)SO2N(R4)2、−N(R4)SO2R、または−OC(=O)N(R4)2からそれぞれ独立して選択され;
Vは、−O−、−S−、−SO−、−SO2−、−N(R6)SO2−、−SO2N(R6)−、−N(R6)−、−CO−、−CO2−、−N(R6)CO−、−N(R6)C(O)O−、−N(R6)CON(R6)−、−N(R6)SO2N(R6)−、−N(R6)N(R6)−、−C(O)N(R6)−、−OC(O)N(R6)−、−C(R6)2O−、−C(R6)2S−、−C(R6)2SO−、−C(R6)2SO2−、−C(R6)2SO2N(R6)−、−C(R6)2N(R6)−、−C(R6)2N(R6)C(O)−、−C(R6)2N(R6)C(O)O−、−C(R6)=NN(R6)−、−C(R6)=N−O−、−C(R6)2N(R6)N(R6)−、−C(R6)2N(R6)SO2N(R6)−、または−C(R6)2N(R6)CON(R6)−であり;
Wは、−C(R6)2O−、−C(R6)2S−、−C(R6)2SO−、−C(R6)2SO2−、−C(R6)2SO2N(R6)−、−C(R6)2N(R6)−、−CO−、−CO2−、−C(R6)20C(O)−、−C(R6)2OC(O)N(R6)−、−C(R6)2N(R6)CO−、−C(R6)2N(R6)C(O)O−、−C(R6)=NN(R6)−、−C(R6)=N−O−、−C(R6)2N(R6)N(R6)−、−C(R6)2N(R6)SO2N(R6)−、−C(R6)2N(R6)CON(R6)−、または−CON(R6)−であり;
R6はそれぞれ独立して、水素、または0〜3個のJ6で任意に置換されているC1〜4脂肪族基から選択されるか;または、同一の窒素原子上の2つのR6基が、その窒素原子と一緒になって、4〜6員のヘテロシクリル環またはヘテロアリール環であって、0〜4個のJ6によって任意に置換されているヘテロシクリル環またはヘテロアリール環を形成し;
R7はそれぞれ独立して、水素またはR”から選択されるか;または、同一の窒素上の2つのR7が該窒素と一緒になって、4〜8員のヘテロシクリル環またはヘテロアリール環であって、0〜4個のJ7によって任意に置換されているヘテロシクリル環またはヘテロアリール環を形成し;
R9はそれぞれ、−R’、−ハロ、−OR’、−C(=O)R’、−CO2R’、−COCOR’、COCH2COR’、−NO2、−CN、−S(O)R’、−S(O)2R’、−SR’、−N(R’)2、−CON(R’)2、−SO2N(R’)2、−OC(=O)R’、−N(R’)COR’、−N(R’)CO2(C1〜6脂肪族)、−N(R’)N(R’)2、−N(R’)CON(R’)2、−N(R’)SO2N(R’)2、−N(R’)SO2R’、−OC(=O)N(R’)2、=NN(R’)2、=N−OR’、または=Oであり;
R10はそれぞれ、O、NR11、およびSから選択される1〜2個のヘテロ原子を含む4員ヘテロシクリル環であって;R10はそれぞれ、0〜3個のJの存在によって任意に置換され;
R11はそれぞれ、−R7、−COR7、−CO2(任意に置換されたC1〜6脂肪族)、−CON(R7)2、または−SO2R7であり;
Rはそれぞれ独立して、水素、またはC1〜6脂肪族基、C6〜10アリール基、5〜10個の環原子を有するヘテロアリール環、もしくは4〜10個の環原子を有するヘテロシクリル環から選択される、任意で置換された基から選択され;各Rが、任意で0〜5個のR9でそれぞれ任意に置換され;
R’はそれぞれ独立して、水素、または任意に0〜4個のJ’によって置換されているC1〜6脂肪族基であるか;あるいは、2つのR’が、共に結合している原子とともに、3〜6員のカルボシクリルまたはヘテロシクリルであって、0〜4個のJ’によって任意に置換されているカルボシクリルまたはヘテロシクリルを形成し;
R”はそれぞれ独立して、0〜4個のJ”で任意に置換されているC1〜6脂肪族基であり;
J’およびJ”はそれぞれ独立して、NH2、NH(C1〜4脂肪族)、N(C1〜4脂肪族)2、ハロゲン、C1〜4脂肪族、OH、O(C1〜4脂肪族)、NO2、CN、CO2H、CO2(C1〜4脂肪族)、O(ハロC1〜4脂肪族)、またはハロC1〜4脂肪族であり;
J、J6、およびJ8はそれぞれ独立して、−ハロ、−OR、オキソ、C1〜6脂肪族、−C(=O)R、−CO2R、−COCOR、COCH2COR、−NO2、−CN、−S(O)R、−S(O)2R、−SR、−N(R4)2、−CON(R7)2、−SO2N(R7)2、−OC(=O)R、−N(R7)COR、−N(R7)CO2(C1〜6脂肪族)、−N(R4)N(R4)2、=NN(R4)2、=N−OR、−N(R7)CON(R7)2、−N(R7)SO2N(R7)2、−N(R4)SO2R、または−OC(=O)N(R7)2であり;
J7はそれぞれ独立して、−ハロ、−OR、オキソ、C1〜6脂肪族、−C(=O)R、−CO2R、−COCOR、COCH2COR、−NO2、−CN、−S(O)R、−S(O)2R、−SR、−N(R12)2、−CON(R12)2、−SO2N(R12)2、−OC(=O)R、−N(R12)COR、−N(R12)CO2(C1〜6脂肪族)、−N(R12)N(R12)2、=NN(R12)2、=N−OR、−N(R12)CON(R12)2、−N(R12)SO2N(R12)2、−N(R12)SO2R、または−OC(=O)N(R12)2であるか;あるいは、同一原子上または異なる原子上にある、2つのJ基、2つのJ6基、2つのJ7基、または2つのJ8基が、共に結合している原子とともに、O、N、またはSから選択される、0〜2個のヘテロ原子を有する、3〜8員の飽和型、部分飽和型、または非飽和型の環を形成し;
R12は独立して、水素またはR”から選択されるか;あるいは、同一の窒素上にある2つのR12が、その窒素原子と一緒になって、4〜8員のヘテロシクリル環またはヘテロアリール環であって、0〜4個のJ”によって任意に置換されているヘテロシクリル環またはヘテロアリール環を形成している。
LiHMDS リチウムヘキサメチルジシラジド
DCM ジクロロメタン
EtOAc 酢酸エチル
DMSO ジメチルスルホキシド
ATP アデノシン三リン酸
DTT ジチオスレイトール
NMR 核磁気共鳴法
HPLC 高速液体クロマトグラフィー法
LCMS 液体クロマトグラフィー質量分析法
TLC 薄層クロマトグラフィー法
Rt 保持時間。
環Dは、4〜7員の単環式環または8〜10員の二環式環であって、該環は、ヘテロシクリル環または炭素環から選択され、そして該ヘテロシクリル環は、窒素、酸素、または硫黄から選択される、1〜4個の環へテロ原子を有し、環Dの各置換可能な環炭素は、独立してオキソまたは−R5で置換され、そして任意の置換可能な環窒素は、−R4で独立して置換され;
Xは、硫黄、酸素、またはNR2’であり;
Yは、窒素またはCR2であり;
Z1およびZ2は、それぞれ独立してNまたはCR9である;ただし、Z1またはZ2の少なくとも一つはNであり;
RXは、−T1−R3であり;
RYは、−T2−R10であり;
R2およびR2’は、−Rまたは−T3−W−R6から独立して選択されるか;あるいは、R2およびR2’は、それらの間に介在する原子と一緒に、窒素、酸素、または硫黄から選択される0〜3個の環へテロ原子を有する、縮合した5〜8員の不飽和型または部分不飽和型の環を形成する;ただし、R2およびR2’によって形成された該縮合環上の置換可能な炭素はそれぞれ、ハロ、オキソ、−CN、−NO2、−R7、または−V−R6で置換され;また、R2およびR2’によって形成された該環上の置換可能な窒素はR4で置換され;
T、T1、T3はそれぞれ、独立して結合またはC1〜4アルキリデン鎖であり;
T2は、独立して結合またはC1〜4アルキリデン鎖であるが、該アルキリデン鎖のうち、最大3個のメチレン単位が、−O−、−C(=O)−、−S(O)−、−S(O)2−、−S−、または−N(R4)−によって任意に置換され;
R3は、−R、−ハロ、−OR、−C(=O)R、−CO2R、−COCOR、−COCH2COR、−NO2、−CN、−S(O)R、−S(O)2R、−SR、−N(R4)2、−CON(R7)2、−SO2N(R7)2、−OC(=0)R、−N(R7)COR、−N(R7)CO2R”、−N(R4)N(R4)2、−C(=NH)N(R4)2、−C(=NH)−OR、−N(R7)CON(R7)2、−N(R7)SO2N(R7)2、−N(R4)SO2R、または−OC(=O)N(R7)2から選択され;
R4は、−R7、−COR7、−CO2(任意に置換されたC1〜6脂肪族)、−CON(R7)2、またはSO2R7からそれぞれ独立して選択されるか;または、同一の窒素上にある2つのR4が一緒になって3〜8員のヘテロシクリル環またはヘテロアリール環を形成し;
R5は、−R、ハロ、−OR、−C(=O)R、−CO2R、−COCOR、−NO2、−CN、−S(O)R、−SO2R、−SR、−N(R4)2、−CON(R4)2、−SO2N(R4)2、−OC(=O)R、−N(R4)COR、−N(R4)CO2R”、−N(R4)N(R4)2、−C=NN(R4)2、−C=N−OR、−N(R4)CON(R4)2、−N(R4)SO2N(R4)2、−N(R4)SO2R、または−OC(=O)N(R4)2からそれぞれ独立して選択され;
Vは、−O−、−S−、−SO−、−SO2−、−N(R6)SO2−、−SO2N(R6)−、−N(R6)−、−CO−、−CO2−、−N(R6)CO−、−N(R6)C(O)O−、−N(R6)CON(R6)−、−N(R6)SO2N(R6)−、−N(R6)N(R6)−、−C(O)N(R6)−、−OC(O)N(R6)−、−C(R6)2O−、−C(R6)2S−、−C(R6)2SO−、−C(R6)2SO2−、−C(R6)2SO2N(R6)−、−C(R6)2N(R6)−、−C(R6)2N(R6)C(O)−、−C(R6)2N(R6)C(O)O−、−C(R6)=NN(R6)−、−C(R6)=N−O−、−C(R6)2N(R6)N(R6)−、−C(R6)2N(R6)SO2N(R6)−、または−C(R6)2N(R6)CON(R6)−であり;
Wは、−C(R6)2O−、−C(R6)2S−、−C(R6)2SO−、−C(R6)2SO2−、−C(R6)2SO2N(R6)−、−C(R6)2N(R6)−、−CO−、−CO2−、−C(R6)20C(O)−、−C(R6)2OC(O)N(R6)−、−C(R6)2N(R6)CO−、−C(R6)2N(R6)C(O)O−、−C(R6)=NN(R6)−、−C(R6)=N−O−、−C(R6)2N(R6)N(R6)−、−C(R6)2N(R6)SO2N(R6)−、−C(R6)2N(R6)CON(R6)−、または−CON(R6)−であり;
R6はそれぞれ独立して、水素、または0〜3個のJ6で任意に置換されているC1〜4脂肪族基から選択されるか;または、同一の窒素原子上の2つのR6基が、その窒素原子と一緒になって、4〜6員のヘテロシクリル環またはヘテロアリール環であって、0〜4個のJ6によって任意に置換されているヘテロシクリル環またはヘテロアリール環を形成し;
R7はそれぞれ独立して、水素またはR”から選択されるか;または、同一の窒素上の2つのR7が該窒素と一緒になって、4〜8員のヘテロシクリル環またはヘテロアリール環であって、0〜4個のJ7によって任意に置換されているヘテロシクリル環またはヘテロアリール環を形成し;
R9はそれぞれ、−R’、−ハロ、−OR’、−C(=O)R’、−CO2R’、−COCOR’、COCH2COR’、−NO2、−CN、−S(O)R’、−S(O)2R’、−SR’、−N(R’)2、−CON(R’)2、−SO2N(R’)2、−OC(=O)R’、−N(R’)COR’、−N(R’)CO2(C1〜6脂肪族)、−N(R’)N(R’)2、=N(R’)CON(R’)2、−N(R’)SO2N(R’)2、−N(R’)SO2R’、−OC(=O)N(R’)2、=NN(R’)2、=N−OR’、または=Oであり;
R10はそれぞれ、O、NR11、およびSから選択される1〜2個のヘテロ原子を含む4員ヘテロシクリル環であって;R10はそれぞれ、0〜3個のJの存在によって任意に置換され;
R11はそれぞれ、−R7、−COR7、−CO2(任意に置換されたC1〜6脂肪族)、−CON(R7)2、または−SO2R7であり;
Rはそれぞれ独立して、水素、またはC1〜6脂肪族基、C6〜10アリール基、5〜10個の環原子を有するヘテロアリール環、もしくは4〜10個の環原子を有するヘテロシクリル環から選択される、任意で置換された基から選択され;各Rが、任意で0〜5個のR9でそれぞれ任意に置換され;
R’はそれぞれ独立して、水素、または0〜4個のJ’によって任意に置換されているC1〜6脂肪族基であるか;あるいは、2つのR’が、ともに結合している原子とともに、3〜6員のカルボシクリルまたはヘテロシクリルであって、0〜4個のJ’によって任意に置換されているカルボシクリルまたはヘテロシクリルを形成し;
R”はそれぞれ独立して、0〜4個のJ”で任意に置換されているC1〜6脂肪族基であり;
J’およびJ”はそれぞれ独立して、NH2、NH(C1〜4脂肪族)、N(C1〜4脂肪族)2、ハロゲン、C1〜4脂肪族、OH、O(C1〜4脂肪族)、NO2、CN、CO2H、CO2(C1〜4脂肪族)、O(ハロC1〜4脂肪族)、またはハロC1〜4脂肪族であり;
J、J6、J7およびJ8はそれぞれ独立して、−ハロ、−OR、オキソ、C1〜6脂肪族、−C(=O)R、−CO2R、−COCOR、COCH2COR、−NO2、−CN、−S(O)R、−S(O)2R、−SR、−N(R4)2、−CON(R7)2、−SO2N(R7)2、−OC(=O)R、−N(R7)COR、−N(R7)CO2(C1〜6脂肪族)、−N(R4)N(R4)2、=NN(R4)2、=N−OR、−N(R7)CON(R7)2、−N(R7)SO2N(R7)2、−N(R4)SO2R、または−OC(=O)N(R7)2であるか;あるいは、同一原子上または異なる原子上にある、2つのJ基、2つのJ6基、2つのJ7基、または2つのJ8基が、共に結合している原子とともに、O、N、またはSから選択される、0〜2個のヘテロ原子を有する、3〜8員の飽和型、部分飽和型、、または非飽和型の環を形成する。
本発明の化合物は、通常、以下の一般的な手順に記載した方法などの方法によって調製することができ、その後に調製例を示す。別段の記載がない限り、以下の手順ですべての変数は、本明細書で定義されている通りである。
カラム:ACE C8カラム、4.6×150mm
勾配:0〜100%の60:40のアセトニトリル+メタノール(20mMのトリスリン酸塩)
流量:1.5mL/分
検出限界:225nm。
塩化水素ガスを、MeOH(33ml)およびEt2O(150ml)の混合液中のシクロヘキサンカルボニトリル溶液(60g、550ml)に0℃で撹拌しながら吹き込んだ。1時間の吹き込みの後、フラスコを冷蔵庫に移し、一晩放置した。そして、RMをEt2Oで希釈し、生成した固体を濾過した。この粗固体をエタノール(400mL)およびエタノール(100mL)中の2Nのアンモニアの混合液に溶解した。アンモニアガスをこの懸濁液に1時間吹き込んでから、反応混合液を冷蔵庫に移して一晩放置した。この反応混合液を濾過し、粘着性のある固体をメタノールで洗浄してフラスコに流し込んだ。この混合液を真空中で濃縮し、Et2Oを添加して固体を濾過した。この固体をメタノールに再溶解し、固体が析出し始めるまで濃縮し、その段階でEt2Oを添加した。そして、この固体を濾過し、一晩高真空中に置いたところ、表題の化合物が固体として得られた(87.8g、98%)。1H NMR:(DMSO)1.00−1.88(10H,m),2.35−2.57(1H,m),8.86(1H,s),9.02(1H,s)。
中間体2
エタノール中のナトリウム・エトキシド溶液[予め、エタノール(200mL)にナトリウム(2.12g、92.2mmol)を溶解して調製しておいたもの]を、常温で撹拌しながら、マロン酸ジエチル(6.1mL、40.2mmol)で処理した。そして、室温で撹拌しながら、エタノール(100mL)中の塩酸シクロヘキサンカルボキシミドアミド溶液(5g、31mmol)を滴加した。添加が完了したところで、反応混合液を還流しながら8時間加熱し一晩放置した。この反応混合液を真空中で濃縮し、水を加え、2NのHClを用いてpHをpH7〜8に調整した。生成して得られた固体を濾過し、ジエチルエーテルで洗浄したところ、表題の化合物が固体として得られた(5.53g、93%)。MS(ES+)m/e=195。1H NMR:(DMSO)1.09−1.81(10H,m),2.40−2.53(1H,m),5.09(1H,s),11.61(2H,brs)。
中間体3
2−シクロヘキシルピリミジン−4,6−ジオール(5.53g、28.5mmol)および塩化ホスホリル(70mL、751mmol)を含む混合液を還流しながら3時間加熱した後、室温に冷却し、真空中で濃縮した。次に、生成した半固体を冷水、sNaHCO3で処理し、Et2Oで抽出し、乾燥させ(Na2SO4)、真空中で濃縮した。得られた残留物をカラムクロマトグラフィー(EtOAc/石油、1/9で溶離)によって精製したところ、表題の化合物が油状物として得られた(5.74g、87%)。MS(ES+)m/e=231。1H NMR:(DMSO)1.15−2.00(10H,m),2.70−2.84(1H,m),7.86(1H,s)。
中間体4
4,6−ジクロロ−2−シクロヘキシルピリミジン(505mg、2.19mmol)、5−フルオロ−1H−ピラゾロ[3,4−b]ピリジン−3−アミン(400mg、2.63mmol)、およびTHF(20mL)を含む混合液を−60℃に冷却し、THF中のリチウムビス(トリメチルシリル)アミドの1Mの溶液(5.46mL、5.46mmol)を滴加して処理した。そして、この反応混合液を1時間で0℃に温めてから、水を加えた。この反応混合液を水とEtOAcに分配し、飽和NaCl溶液で洗浄し、乾燥させ(Na2SO4)、真空中で濃縮した。得られた残留物をカラムクロマトグラフィー(MeOH/DCM、5/95で溶離)によって精製したところ、表題の化合物が固体として得られた(380mg、50%)。MS(ES+)m/e=347。1H NMR:(DMSO)1.10−1.96(10H,m),2.56−2.69(1H,m),7.65(1H,brs),8.27−8.39(1H,m),8.58(1H,s),10.72(1H,s),13.34(1H,s)。
実施例1
N−(6−クロロ−2−シクロヘキシルピリミジン−4−イル)−5−フルオロ−1H−ピラゾロ[3,4−b]ピリジン−3−アミン(78mg、0.22mmol)、N,N−ジイソプロピルエチルアミン(158μL、0.91mmol)、アゼチジン(45μL、0.67mmol)、およびn−ブタノール(6mL)を含む混合液をマイクロ波照射により125℃にて20分間加熱した。この反応混合液を室温に冷却し、得られた固体を濾過し、この固体をEt2O、sNH4ClおよびEt2Oで洗浄した。得られた固体を風乾したところ、表題の化合物が白色の固体として得られた(48mg、58%)。MS(ES+)m/e=368。1H NMR:(DMSO)1.08−1.92(10H,m),2.26−2.58(3H,m),3.89−4.06(4H,m),6.50(1H,brs),8.32−8.62(2H,m),9.79(1H,s),13.03(1H,s)。
以下の化合物を、化合物I−1を調製するために用いた方法に従って調製した。
5−フルオロ−1H−ピラゾロ[3,4−b]ピリジン−3−アミン(5a)の合成についての全体の合成手順を下記に示す。
2―クロロ―5−フルオロニコチン酸(6a)
N2雰囲気下で丸底フラスコに、脱気DMF(270mL)、Pd(OAc)2(0.05当量、2.7g、11.9mmol)、PPh3(0.1当量、6.2g、23.8mmol)、および脱気Et3N(6当量、200mL、1428.6mmol)を加えた。この混合液を20分間撹拌してから、HCOOH(3当量、28mL、714.3mmol)を加え、続いて5分後に2,6−ジクロロ−5−フルオロニコチン酸(50g、238.1mmol)を加え、この混合液を50℃で撹拌した。この反応の後、後処理後の(worked−up)アリコートの分析を行った(1H NMR)。出発物質を使い切ったところで(24時間)、この反応液を0℃に冷却し、水(500mL)を加えた。20分後に、反応液を、水で洗浄したセライトパッドで濾過した。この反応液を30%のNaOH水溶液でpH9に塩基性化し、EtOAcで洗浄した(2×)。HCl(12N)を徐々に添加してpH1とし、この溶液をNaClで飽和させた。この混合液をEtOAcで抽出した(3×)。有機抽出物を合わせたものをブラインで洗浄し、乾燥させ(Na2SO4)、減圧下で濃縮すると、それ以上の精製を行うことなしに、次の段階で使用される37g(88%)の薄茶色の固体が得られた。1H NMR(DMSO−d6,300MHz):δ8.16(dd,1H);8.58(d,1H)。
2―クロロ―5−フルオロニコチンアミド(3a)
DCM中の2−クロロ−5−フルオロニコチン酸6a(50g、285mmol)およびDMF(2mL、28mmol)の溶液(400mL)に、0℃にてオキサリルクロリド(64mL、741mmol)を滴加した。この反応混合液を室温で一晩撹拌し、真空中で濃縮した。得られた黄色の液体を1,4−ジオキサン(600mL)に溶解し、0℃にて冷却し、NH3(g)をこの溶液に30分間吹き込んだ。この混合液を室温で一晩撹拌した。得られた混合液を濾過し、濾液を濃縮したところ、化合物3aが薄茶色の固体として得られた(44g、89%)。1H NMR(DMSO−d6,300MHz):δ7.84(s,1H),7.96(dd,1H),8.09(s,1H),8.49(d,1H)。
2―クロロ―5−フルオロニコチノニトリル−(4a)
DCM中の粗化合物3a(65g、372.4mmol)およびEt3N(114mL、819.2mmol)の懸濁液(700mL)を0℃に冷却し、TFAA(57mL、409.6mmol)を滴加した。得られた黄色の溶液を0℃で90分間撹拌し、DCMで希釈し、NaHCO3飽和水溶液およびブラインで洗浄し、乾燥させた(Na2SO4)。この混合液を濾過し、濃縮した。残留物をクーゲルロール(Kugel Rohl)蒸留(〜70℃/1ミリバール)したところ、50g(86%)の化合物4aが褐色の固体として得られた。また、化合物4aは、カラムクロマトグラフィー(SiO2、ヘプタン:EtOAc 8:1)によって精製することもできる。1H NMR(CDCl3,300MHz):δ7.78(dd,1H);8.49(d,1H)。
5−フルオロ−1H−ピラゾロ[3,4−b]ピリジン−3−アミン(5a)
1−ブタノール中の化合物4a(50g、321.7mmol)の溶液(1L)に、ヒドラジン一水和物(150mL、3.2mol)を添加し、この混合液を4時間還流した。この混合液を室温に冷却してから濃縮した。沈殿物をフィルター上で水(2×)およびEt2O(2×)で連続して洗浄し、真空中で一晩乾燥させると、化合物5aが黄色の固体として得られた(44g、88%)。1HNMR(DMSO−d6,300MHz):δ5.53(s,2H);7.94(dd,1H);8.35(dd,1H);12.02(s,1H)。
実施例3:GSK−3阻害アッセイ:
本発明の化合物を、標準的な共役酵素系(Foxら、Protein Sci.1998,7,2249)を用いて、GSK−3β(AA 1−420)の活性を阻害できるかについてスクリーニングした。反応は、100mMのHEPES(pH7.5)、10mMのMgCl2、25mMのNaCl、300μMのNADH、1mMのDTT、および1.5%DMSOを含む溶液中で行った。このアッセイにおける基質の最終濃度は、ATP(Sigma Chemicals,St Louis,MO)が20μM、およびペプチド(American Peptide,Sunnyvale,CA)が300μMであった。反応を、30℃および20nMのGSK−3βで行った。共役酵素系の成分の最終濃度は、ホスホエノールピルビン酸塩が2.5mM、NADHが300μM、ピルビン酸キナーゼが30μg/ml、また乳酸脱水素酵素が10μg/mlであった。
Claims (41)
- 以下の化学式I:
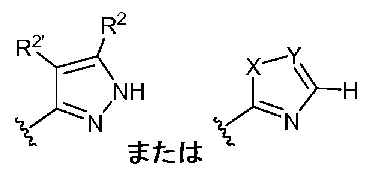
式中、Htは、
環Dは、4〜7員の単環式環または8〜10員の二環式環であって、該環は、ヘテロシクリル環または炭素環から選択され、そして該ヘテロシクリル環は、窒素、酸素、または硫黄から選択される、1〜4個の環へテロ原子を有し、環Dの各置換可能な環炭素は、独立してオキソまたは−R5で置換され、そして任意の置換可能な環窒素は、−R4で独立して置換され;
Xは、硫黄、酸素、またはNR2’であり;
Yは、窒素またはCR2であり;
Z1およびZ2は、それぞれ独立してNまたはCR9である;ただし、Z1またはZ2の少なくとも一つはNであり;
RXは、T1−R3であり;
RYは、T2−R10であり;
R2およびR2’は、−Rまたは−T3−W−R6から独立して選択されるか;あるいは、R2およびR2’は、それらの間に介在する原子と一緒に、窒素、酸素、または硫黄から選択される0〜3個の環へテロ原子を有する、縮合した5〜8員の不飽和型または部分不飽和型の環を形成し;ここで、R2およびR2’によって形成された該縮合環上の置換可能な炭素はそれぞれ、ハロ、オキソ、−CN、−NO2、−R7、または−V−R6で置換され;また、R2およびR2’によって形成された該環上の置換可能な窒素はR4で置換され; T、T1、T3はそれぞれ、独立して結合またはC1〜4アルキリデン鎖であり;
T2は、独立して結合またはC1〜4アルキリデン鎖であり、ここで該アルキリデン鎖の最大3個のメチレン単位が、任意に、−O−、−C(=O)−、−S(O)−、−S(O)2−、−S−、または−N(R4)−によって置換され;
R3は、−R、−ハロ、−OR、−C(=O)R、−CO2R、−COCOR、−COCH2COR、−NO2、−CN、−S(O)R、−S(O)2R、−SR、−N(R4)2、−CON(R7)2、−SO2N(R7)2、−OC(=O)R、−N(R7)COR、−N(R7)CO2R”、−N(R4)N(R4)2、−C(=NH)N(R4)2、−C(=NH)−OR、−N(R7)CON(R7)2、−N(R7)SO2N(R7)2、−N(R4)SO2R、または−OC(=O)N(R7)2から選択され;
R4は、−R7、−COR7、−CO2(任意に置換されたC1〜6脂肪族)、−CON(R7)2、または−SO2R7からそれぞれ独立して選択されるか;または、同一の窒素上にある2つのR4は、一緒になって3〜8員のヘテロシクリル環またはヘテロアリール環を形成し;
R5は、−R、ハロ、−OR、−C(=O)R、−CO2R、−COCOR、−NO2、−CN、−S(O)R、−SO2R、−SR、−N(R4)2、−CON(R4)2、−SO2N(R4)2、−OC(=O)R、−N(R4)COR、−N(R4)CO2R”、−N(R4)N(R4)2、−C=NN(R4)2、−C=N−OR、−N(R4)CON(R4)2、−N(R4)SO2N(R4)2、−N(R4)SO2R、または−OC(=O)N(R4)2からそれぞれ独立して選択され;
Vは、−O−、−S−、−SO−、−SO2−、−N(R6)SO2−、−SO2N(R6)−、−N(R6)−、−CO−、−CO2−、−N(R6)CO−、−N(R6)C(O)O−、−N(R6)CON(R6)−、−N(R6)SO2N(R6)−、−N(R6)N(R6)−、−C(O)N(R6)−、−OC(O)N(R6)−、−C(R6)2O−、−C(R6)2S−、−C(R6)2SO−、−C(R6)2SO2−、−C(R6)2SO2N(R6)−、−C(R6)2N(R6)−、−C(R6)2N(R6)C(O)−、−C(R6)2N(R6)C(O)O−、−C(R6)=NN(R6)−、−C(R6)=N−O−、−C(R6)2N(R6)N(R6)−、−C(R6)2N(R6)SO2N(R6)−、または−C(R6)2N(R6)CON(R6)−であり;
Wは、−C(R6)2O−、−C(R6)2S−、−C(R6)2SO−、−C(R6)2SO2−、−C(R6)2SO2N(R6)−、−C(R6)2N(R6)−、−CO−、−CO2−、−C(R6)2OC(O)−、−C(R6)2OC(O)N(R6)−、−C(R6)2N(R6)CO−、−C(R6)2N(R6)C(O)O−、−C(R6)=NN(R6)−、−C(R6)=N−O−、−C(R6)2N(R6)N(R6)−、−C(R6)2N(R6)SO2N(R6)−、−C(R6)2N(R6)CON(R6)−、または−CON(R6)−であり;
R6はそれぞれ独立して、水素、または0〜3個のJ6で任意に置換されているC1〜4脂肪族基から選択されるか;または、同一の窒素原子上の2つのR6基が、該窒素原子と一緒になって、4〜6員のヘテロシクリル環またはヘテロアリール環を形成し、該ヘテロシクリル環またはヘテロアリール環は、0〜4個のJ6によって任意に置換され;
R7はそれぞれ独立して、水素またはR”から選択されるか;または、同一の窒素上の2つのR7が該窒素と一緒になって、4〜8員のヘテロシクリル環またはヘテロアリール環を形成し、該ヘテロシクリル環またはヘテロアリール環は、0〜4個のJ7によって任意に置換され;
R9はそれぞれ、−R’、−ハロ、−OR’、−C(=O)R’、−CO2R’、−COCOR’、COCH2COR’、−NO2、−CN、−S(O)R’、−S(O)2R’、−SR’、−N(R’)2、−CON(R’)2、−SO2N(R’)2、−OC(=O)R’、−N(R’)COR’、−N(R’)CO2(C1〜6脂肪族)、−N(R’)N(R’)2、−N(R’)CON(R’)2、−N(R’)SO2N(R’)2、−N(R’)SO2R’、−OC(=O)N(R’)2、=NN(R’)2、=N−OR’、または=Oであり;
R10はそれぞれ、O、NR11、またはSから選択される1〜2個のヘテロ原子を含む4員ヘテロシクリル環であって;R10はそれぞれ、0〜3個のJの存在によって任意に置換され;
R11はそれぞれ、−R7、−COR7、−CO2(任意に置換されたC1〜6脂肪族)、−CON(R7)2、または−SO2R7であり;
Rはそれぞれ独立して、水素、またはC1〜6脂肪族基、C6〜10アリール基、5〜10個の環原子を有するヘテロアリール環、あるいは4〜10個の環原子を有するヘテロシクリル環から選択される、任意に置換された基から選択され;各Rは、任意で0〜5個のR9でそれぞれ任意に置換され;
R’はそれぞれ独立して、水素、または任意に0〜4個のJ’によって置換されているC1〜6脂肪族基であるか;あるいは、2つのR’は、それらが結合している原子と一緒になって、3〜6員のカルボシクリルまたはヘテロシクリルを形成し、該カルボシクリルまたはヘテロシクリルは、0〜4個のJ’で任意に置換され;
R”はそれぞれ独立して、0〜4個のJ”で任意に置換されているC1〜6脂肪族基であり;
J’およびJ”はそれぞれ独立して、NH2、NH(C1〜4脂肪族)、N(C1〜4脂肪族)2、ハロゲン、C1〜4脂肪族、OH、O(C1〜4脂肪族)、NO2、CN、CO2H、CO2(C1〜4脂肪族)、O(ハロC1〜4脂肪族)、またはハロC1〜4脂肪族であり;
J、J6、およびJ8はそれぞれ独立して、−ハロ、−OR、オキソ、C1〜6脂肪族、−C(=O)R、−CO2R、−COCOR、COCH2COR、−NO2、−CN、−S(O)R、−S(O)2R、−SR、−N(R4)2、−CON(R7)2、−SO2N(R7)2、−OC(=O)R、−N(R7)COR、−N(R7)CO2(C1〜6脂肪族)、−N(R4)N(R4)2、=NN(R4)2、=N−OR、−N(R7)CON(R7)2、−N(R7)SO2N(R7)2、−N(R4)SO2R、または−OC(=O)N(R7)2であり;
J7はそれぞれ独立して、−ハロ、−OR、オキソ、C1〜6脂肪族、−C(=O)R、−CO2R、−COCOR、COCH2COR、−NO2、−CN、−S(O)R、−S(O)2R、−SR、−N(R12)2、−CON(R12)2、−SO2N(R12)2、−OC(=O)R、−N(R12)COR、−N(R12)CO2(C1〜6脂肪族)、−N(R12)N(R12)2、=NN(R12)2、=N−OR、−N(R12)CON(R12)2、−N(R12)SO2N(R12)2、−N(R12)SO2R、または−OC(=O)N(R12)2であるか;あるいは、
同一原子上または異なる原子上にある、2つのJ基、2つのJ6基、2つのJ7基、または2つのJ8基は、それらが結合している原子と一緒になって、O、N、またはSから選択される、0〜2個のヘテロ原子を有する、3〜8員の飽和型、部分飽和型、、または非飽和型の環を形成し;
R12は独立して、水素またはR”から選択されるか;あるいは、同一の窒素上にある2つのR12は、その窒素原子と一緒になって、4〜8員のヘテロシクリル環またはヘテロアリール環を形成し、該ヘテロシクリル環またはヘテロアリール環は0〜4個のJ”によって任意に置換される、化合物。 - XがNである、請求項3記載の化合物。
- YがNである、請求項4記載の化合物。
- YがCR2である、請求項4記載の化合物。
- XがSであり、YがCR2である、請求項3記載の化合物。
- Z1およびZ2がどちらも窒素である、請求項1から7のいずれか一項記載の化合物。
- Z1が窒素であり、かつZ2がCHである、請求項1から7のいずれか一項記載の化合物。
- Z1がCR9であり、かつZ2が窒素である、請求項1から7のいずれか一項記載の化合物。
- R2’が水素またはメチルである、請求項8から10のいずれか一項記載の化合物。
- R2’が水素である、請求項11記載の化合物。
- R2が、T3−W−R6またはRであり;Wは、−C(R6)2O−、−C(R6)2N(R6)−、−CO−、−CO2−、−C(R6)2OC(O)−、−C(R6)2N(R6)CO−、−C(R6)2N(R6)C(O)O−、または−CON(R6)−であって、かつRが、C1〜6脂肪族またはフェニルから選択される、任意に置換されている基である、請求項11または12記載の化合物。
- R2が水素であるか、または、アリール、ヘテロアリール、もしくはC1〜6脂肪族基から選択される置換型もしくは非置換型の基である、請求項11または12記載の化合物。
- R2が水素であるか、または、アリール、もしくはC1〜6脂肪族基から選択される置換型もしくは非置換型の基である、請求項14記載の化合物。
- R2およびR2’が、それらの間にある原子と一緒になって、置換型または非置換型のベンゾ、ピリド、ピリミド、または部分不飽和型の6員炭素環を形成している、請求項1から10のいずれか一項記載の化合物。
- R2およびR2’が、それらの間にある介在原子と一緒になって、置換型または非置換型のベンゾ環またはピリド環を形成している、請求項16記載の化合物。
- 前記ベンゾ環またはピリド環が、1〜2個のハロ置換基で置換されている、請求項17記載の化合物。
- RXは水素、C1〜4脂肪族、またはハロである、請求項8から18のいずれか一項記載の化合物。
- RXが、水素、メチル、エチル、シクロプロピル、またはイソプロピルである、請求項19記載の化合物。
- RXが水素である、請求項20記載の化合物。
- RYがT2−R10であり、T2が結合である、請求項8から21のいずれか一項記載の化合物。
- R10が、任意に置換されているアゼチジンである、請求項23記載の化合物。
- 環Dが、ピペリジニル、ピペラジニル、ピロリジニル、モルホリニル、1,2,3,4−テトラヒドロイソキノリニル、1,2,3,4−テトラヒドロキノリニル、2,3−ジヒドロ−1H−イソインドリル、2,3−ジヒドロ−1H−インドリル、またはイソキノリニルから選択される、任意に置換されている環である、請求項8から26のいずれか一項記載の化合物。
- 環Dが、任意に置換されたテロラヒドロナフチル、ベンゾジオキシニル、インダニル、インドリニル、またはイソキノリニルである、請求項8から26のいずれか一項記載の化合物。
- 環Dが、シクロヘキシルである、請求項8から26のいずれか一項記載の化合物。
- 請求項1から30のいずれか一項記載の化合物、および薬学的に受容可能な担体、アジュバント、またはビヒクルを含む、組成物。
- 化学療法剤もしくは抗増殖剤、抗炎症剤、免疫調節剤もしくは免疫抑制剤、神経栄養因子、心血管系疾患を治療するための薬剤、糖尿病を治療するための薬剤、または免疫不全障害を治療するための薬剤から選択される治療薬をさらに含む、請求項31記載の組成物。
- 生体外の生物学的サンプルまたはインビトロの生物学的サンプル中のGSK−3活性を、請求項1から30のいずれか一項記載の化合物によって阻害する方法。
- 糖尿病、アルツハイマー病、ハンチントン病、パーキンソン病、AIDS関連認知症、双極性障害、萎縮性側索硬化症(ALS、ルー・ゲーリック病)、多発性硬化症(MS)、統合失調症、白血球減少症、心筋細胞肥大、脳卒中、または関節リウマチから選択される疾患または症状を治療するか、またはその重症度を低下させる方法であって、請求項1から30のいずれか一項記載の化合物を患者に投与する工程を含む、方法。
- 前記疾患が脳卒中である、請求項34記載の方法。
- 前記疾患が糖尿病である、請求項34記載の方法。
- 前記疾患が統合失調症である、請求項34記載の方法。
- 前記疾患が双極性障害である、請求項34記載の方法。
- 糖尿病を治療するための薬剤、アルツハイマー病を治療するための薬剤、ハンチントン病を治療するための薬剤、パーキンソン病を治療するための薬剤、AIDS関連認知症を治療するための薬剤、双極性障害を治療するための薬剤、萎縮性側索硬化症(ALS、ルー・ゲーリック病)を治療するための薬剤、多発性硬化症(MS)を治療するための薬剤、統合失調症を治療するための薬剤、白血球減少症を治療するための薬剤、心筋細胞肥大を治療するための薬剤、脳卒中を治療するための薬剤、または関節リウマチを治療するための薬剤から選択される追加的な治療剤を患者に投与するさらなる工程を含む、請求項34記載の方法であって、
a)該追加的な治療剤が、治療されている疾患に適し、かつ、
b)該追加的な治療剤が、前記組成物と一緒に単回投薬形態で投与されるか、または前記組成物とは別に、頻回投薬形態の一部として投与される、方法。 - 請求項1から30のいずれか一項記載の化合物を患者に投与する工程を含む、白血球減少症、糖尿病、脳卒中回復、または骨粗鬆症から選択される疾患または症状を治療するか、またはその重症度を低下させる方法。
- 白血球減少症を治療するための薬剤、糖尿病を治療するための薬剤、脳卒中回復を治療するための薬剤、または骨粗鬆症を治療するための薬剤から選択される追加的な治療剤を患者に投与するさらなる工程を含む、請求項40記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US87572906P | 2006-12-19 | 2006-12-19 | |
| US95302707P | 2007-07-31 | 2007-07-31 | |
| PCT/US2007/088058 WO2008077086A1 (en) | 2006-12-19 | 2007-12-19 | Aminopyrimidines useful as inhibitors of protein kinases |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010513567A true JP2010513567A (ja) | 2010-04-30 |
| JP2010513567A5 JP2010513567A5 (ja) | 2011-01-13 |
Family
ID=39226891
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2009543169A Pending JP2010513567A (ja) | 2006-12-19 | 2007-12-19 | プロテインキナーゼの阻害剤として有用なアミノピリミジン |
Country Status (11)
| Country | Link |
|---|---|
| US (2) | US8426425B2 (ja) |
| EP (1) | EP2099787B1 (ja) |
| JP (1) | JP2010513567A (ja) |
| AT (1) | ATE474835T1 (ja) |
| AU (1) | AU2007333650A1 (ja) |
| CA (1) | CA2673353A1 (ja) |
| DE (1) | DE602007007985D1 (ja) |
| ES (1) | ES2347721T3 (ja) |
| MX (1) | MX2009006690A (ja) |
| NZ (1) | NZ577768A (ja) |
| WO (1) | WO2008077086A1 (ja) |
Families Citing this family (28)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ATE327991T1 (de) | 2000-09-15 | 2006-06-15 | Vertex Pharma | Pyrazolverbindungen als protein-kinasehemmer |
| US6660731B2 (en) | 2000-09-15 | 2003-12-09 | Vertex Pharmaceuticals Incorporated | Pyrazole compounds useful as protein kinase inhibitors |
| NZ526473A (en) | 2000-12-21 | 2005-06-24 | Vertex Pharma | Pyrazole compounds useful as protein kinase inhibitors |
| MY141867A (en) | 2002-06-20 | 2010-07-16 | Vertex Pharma | Substituted pyrimidines useful as protein kinase inhibitors |
| US7601718B2 (en) | 2003-02-06 | 2009-10-13 | Vertex Pharmaceuticals Incorporated | Compositions useful as inhibitors of protein kinases |
| MX2008005818A (es) | 2005-11-03 | 2008-10-15 | Vertex Pharma | Aminopirimidinas utiles como inhibidores de cinasa. |
| KR20090071662A (ko) | 2006-10-21 | 2009-07-01 | 애보트 게엠베하 운트 콤파니 카게 | 헤테로사이클릭 화합물 및 글리코겐 신타제 키나제 3 억제제로서의 이의 용도 |
| DE602007004750D1 (de) | 2006-11-02 | 2010-03-25 | Vertex Pharma | Als inhibitoren von proteinkinasen geeignete aminopyridine und aminopyrimidine |
| JP2010513567A (ja) | 2006-12-19 | 2010-04-30 | バーテックス ファーマシューティカルズ インコーポレイテッド | プロテインキナーゼの阻害剤として有用なアミノピリミジン |
| CA2679884A1 (en) | 2007-03-09 | 2008-09-18 | Vertex Pharmaceuticals Incorporated | Aminopyrimidines useful as inhibitors of protein kinases |
| EP2137183B1 (en) | 2007-03-09 | 2011-09-28 | Vertex Pharmaceuticals Incorporated | Aminopyrimidines useful as inhibitors of protein kinases |
| EP2134709A1 (en) | 2007-03-09 | 2009-12-23 | Vertex Pharmaceuticals, Inc. | Aminopyridines useful as inhibitors of protein kinases |
| WO2008128009A2 (en) | 2007-04-13 | 2008-10-23 | Vertex Pharmaceuticals Incorporated | Aminopyrimidines useful as kinase inhibitors |
| WO2008137619A2 (en) | 2007-05-02 | 2008-11-13 | Vertex Pharmaceuticals Incorporated | Thiazoles and pyrazoles useful as kinase inhibitors |
| CN101801959A (zh) | 2007-05-02 | 2010-08-11 | 沃泰克斯药物股份有限公司 | 可用作激酶抑制剂的氨基嘧啶类化合物 |
| ES2400104T3 (es) * | 2007-07-31 | 2013-04-05 | Vertex Pharmaceuticals Incorporated | Proceso para preparación de 5-fluoro-1H-pirazolo[3,4-b]piridin-3-amina y derivados de la misma |
| CN101768111B (zh) * | 2009-01-07 | 2012-12-26 | 上海开拓者化学研究管理有限公司 | 一种2-氯-5-氟吡啶-3-甲酸的制备方法 |
| US9266855B2 (en) | 2010-09-27 | 2016-02-23 | AbbVie Deutschland GmbH & Co. KG | Heterocyclic compounds and their use as glycogen synthase kinase-3 inhibitors |
| US9090592B2 (en) | 2010-12-30 | 2015-07-28 | AbbVie Deutschland GmbH & Co. KG | Heterocyclic compounds and their use as glycogen synthase kinase-3 inhibitors |
| LT2841428T (lt) | 2012-04-24 | 2018-12-10 | Vertex Pharmaceuticals Incorporated | Dnr-pk inhibitoriai |
| SI2970218T1 (sl) | 2013-03-12 | 2019-04-30 | Vertex Pharmaceuticals Inc. | DNA-PK inhibitorji |
| KR20160058889A (ko) * | 2013-09-22 | 2016-05-25 | 칼리토르 사이언시즈, 엘엘씨 | 치환된 아미노피리미딘 화합물 및 이용 방법 |
| PL3057953T3 (pl) | 2013-10-17 | 2019-01-31 | Vertex Pharmaceuticals Incorporated | Kokryształy (S)-N-metylo-8-(1-((2'-metylo-[4,5'-bipirymidyn]-6-ylo)amino)propan-2-ylo)chinolino-4-karboksyamidu i ich deuterowane pochodne jako inhibitory DNA-PK |
| PT3089971T (pt) | 2014-01-01 | 2020-09-03 | Medivation Tech Llc | Compostos e métodos de utilização |
| CA2945263A1 (en) | 2014-04-09 | 2015-10-15 | Christopher Rudd | Use of gsk-3 inhibitors or activators which modulate pd-1 or t-bet expression to modulate t cell immunity |
| HK1252425A1 (zh) | 2015-06-05 | 2019-05-24 | Vertex Pharmaceuticals Incorporated | 用於治疗脱髓鞘疾病的三唑类药物 |
| CA3038657A1 (en) | 2016-09-27 | 2018-04-05 | Vertex Pharmaceuticals Incorporated | Method for treating cancer using a combination of dna-damaging agents and dna-pk inhibitors |
| WO2018106641A1 (en) * | 2016-12-06 | 2018-06-14 | Vertex Pharmaceuticals Incorporated | Pyrazoles for the treatment of demyelinating diseases |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004509113A (ja) * | 2000-09-15 | 2004-03-25 | バーテックス ファーマシューティカルズ インコーポレイテッド | プロテインキナーゼインヒビターとして有用なピラゾール化合物 |
| JP2009515992A (ja) * | 2005-11-16 | 2009-04-16 | バーテックス ファーマシューティカルズ インコーポレイテッド | キナーゼ阻害剤として有用なアミノピリミジン |
| JP2010509231A (ja) * | 2006-11-02 | 2010-03-25 | バーテックス ファーマシューティカルズ インコーポレイテッド | プロテインキナーゼの阻害剤として有用なアミノピリジンおよびアミノピリミジン |
Family Cites Families (71)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3133081A (en) | 1964-05-12 | J-aminoindazole derivatives | ||
| US3935183A (en) | 1970-01-26 | 1976-01-27 | Imperial Chemical Industries Limited | Indazole-azo phenyl compounds |
| BE754242A (fr) | 1970-07-15 | 1971-02-01 | Geigy Ag J R | Diamino-s-triazines et dinitro-s-triazines |
| US3998951A (en) | 1974-03-13 | 1976-12-21 | Fmc Corporation | Substituted 2-arylquinazolines as fungicides |
| DE2458965C3 (de) | 1974-12-13 | 1979-10-11 | Bayer Ag, 5090 Leverkusen | 3-Amino-indazol-N-carbonsäure-Derivate, Verfahren zu ihrer Herstellung sowie sie enthaltende Arzneimittel |
| MA18829A1 (fr) | 1979-05-18 | 1980-12-31 | Ciba Geigy Ag | Derives de la pyrimidine,procedes pour leur preparation,compositions pharmaceutiques contenant ces composes et leur utilisation therapeutique |
| DOP1981004033A (es) | 1980-12-23 | 1990-12-29 | Ciba Geigy Ag | Procedimiento para proteger plantas de cultivo de la accion fitotoxica de herbicidas. |
| SE8102193L (sv) | 1981-04-06 | 1982-10-07 | Pharmacia Ab | Terapeutiskt aktiv organisk forening och dess anvendning |
| SE8102194L (sv) | 1981-04-06 | 1982-10-07 | Pharmacia Ab | Terapeutiskt aktiv organisk forening och farmaceutisk beredning innehallande denna |
| JPS58124773A (ja) | 1982-01-20 | 1983-07-25 | Mitsui Toatsu Chem Inc | 5−メチルチオピリミジン誘導体とその製造法と農園芸用殺菌剤 |
| DE3725638A1 (de) | 1987-08-03 | 1989-02-16 | Bayer Ag | Neue aryloxy (bzw. thio)aminopyrimidine |
| US5710158A (en) | 1991-05-10 | 1998-01-20 | Rhone-Poulenc Rorer Pharmaceuticals Inc. | Aryl and heteroaryl quinazoline compounds which inhibit EGF and/or PDGF receptor tyrosine kinase |
| AU700964B2 (en) | 1994-11-10 | 1999-01-14 | Cor Therapeutics, Inc. | Pharmaceutical pyrazole compositions useful as inhibitors of protein kinases |
| IL117659A (en) | 1995-04-13 | 2000-12-06 | Dainippon Pharmaceutical Co | Substituted 2-phenyl pyrimidino amino acetamide derivative process for preparing the same and a pharmaceutical composition containing same |
| US6716575B2 (en) | 1995-12-18 | 2004-04-06 | Sugen, Inc. | Diagnosis and treatment of AUR1 and/or AUR2 related disorders |
| GB9619284D0 (en) | 1996-09-16 | 1996-10-30 | Celltech Therapeutics Ltd | Chemical compounds |
| US6267952B1 (en) | 1998-01-09 | 2001-07-31 | Geltex Pharmaceuticals, Inc. | Lipase inhibiting polymers |
| JP2000026421A (ja) | 1998-01-29 | 2000-01-25 | Kumiai Chem Ind Co Ltd | ジアリ―ルスルフィド誘導体及び有害生物防除剤 |
| IL137922A0 (en) | 1998-02-17 | 2001-10-31 | Tularik Inc | Anti-viral pyrimidine derivatives |
| WO2000011003A1 (en) | 1998-08-21 | 2000-03-02 | Du Pont Pharmaceuticals Company | ISOXAZOLO[4,5-d]PYRIMIDINES AS CRF ANTAGONISTS |
| US6184226B1 (en) | 1998-08-28 | 2001-02-06 | Scios Inc. | Quinazoline derivatives as inhibitors of P-38 α |
| GB9828511D0 (en) | 1998-12-24 | 1999-02-17 | Zeneca Ltd | Chemical compounds |
| GB9914258D0 (en) | 1999-06-18 | 1999-08-18 | Celltech Therapeutics Ltd | Chemical compounds |
| US20020065270A1 (en) | 1999-12-28 | 2002-05-30 | Moriarty Kevin Joseph | N-heterocyclic inhibitors of TNF-alpha expression |
| CA2369504C (en) | 2000-02-05 | 2009-01-06 | Vertex Pharmaceuticals Incorporated | Pyrazole compositions useful as inhibitors of erk |
| CN1429222A (zh) | 2000-02-17 | 2003-07-09 | 安姆根有限公司 | 激酶抑制剂 |
| GB0004887D0 (en) | 2000-03-01 | 2000-04-19 | Astrazeneca Uk Ltd | Chemical compounds |
| WO2002000649A1 (en) | 2000-06-28 | 2002-01-03 | Astrazeneca Ab | Substituted quinazoline derivatives and their use as inhibitors |
| US6610677B2 (en) | 2000-09-15 | 2003-08-26 | Vertex Pharmaceuticals Incorporated | Pyrazole compounds useful as protein kinase inhibitors |
| IL154710A0 (en) | 2000-09-15 | 2003-10-31 | Vertex Pharma | Isoxazole derivatives and pharmaceutical compositions containing the same |
| US6660731B2 (en) | 2000-09-15 | 2003-12-09 | Vertex Pharmaceuticals Incorporated | Pyrazole compounds useful as protein kinase inhibitors |
| US6613776B2 (en) | 2000-09-15 | 2003-09-02 | Vertex Pharmaceuticals Incorporated | Pyrazole compounds useful as protein kinase inhibitors |
| US7473691B2 (en) | 2000-09-15 | 2009-01-06 | Vertex Pharmaceuticals Incorporated | Pyrazole compounds useful as protein kinase inhibitors |
| DE10061863A1 (de) | 2000-12-12 | 2002-06-13 | Basf Ag | Verfahren zur Herstellung von Triethylendiamin (TEDA) |
| US6716851B2 (en) | 2000-12-12 | 2004-04-06 | Cytovia, Inc. | Substituted 2-aryl-4-arylaminopyrimidines and analogs as activators or caspases and inducers of apoptosis and the use thereof |
| NZ526473A (en) | 2000-12-21 | 2005-06-24 | Vertex Pharma | Pyrazole compounds useful as protein kinase inhibitors |
| MY130778A (en) | 2001-02-09 | 2007-07-31 | Vertex Pharma | Heterocyclic inhibitiors of erk2 and uses thereof |
| US6949544B2 (en) | 2001-03-29 | 2005-09-27 | Vertex Pharmaceuticals Incorporated | Inhibitors of c-Jun N-terminal kinases (JNK) and other protein kinases |
| JP2004535381A (ja) | 2001-04-13 | 2004-11-25 | バーテックス ファーマシューティカルズ インコーポレイテッド | c−JunN末端キナーゼ(JNK)および他のプロテインキナーゼのインヒビター |
| EP1383771A1 (en) | 2001-04-20 | 2004-01-28 | Vertex Pharmaceuticals Incorporated | 9-deazaguanine derivatives as inhibitors of gsk-3 |
| CA2446864C (en) | 2001-05-16 | 2011-02-15 | Vertex Pharmaceuticals Incorporated | Inhibitors of src and other protein kinases |
| EP1399440B1 (en) | 2001-06-15 | 2009-06-03 | Vertex Pharmaceuticals Incorporated | 5-(2-aminopyrimidin-4-yl)benzisoxazoles as protein kinase inhibitors |
| CA2452603A1 (en) | 2001-07-03 | 2003-01-16 | Vertex Pharmaceuticals Incorporated | Isoxazolyl-pyrimidines as inhibitors of src and lck protein kinases |
| US6698980B2 (en) * | 2001-07-30 | 2004-03-02 | Stewart Mining Products Inc. | Rock stabilizing apparatus and method |
| EP1474147B1 (en) | 2001-12-07 | 2010-05-05 | Vertex Pharmaceuticals Incorporated | Pyrimidine-based compounds useful as gsk-3 inhibitors |
| US6846928B2 (en) | 2002-03-15 | 2005-01-25 | Vertex Pharmaceuticals Incorporated | Compositions useful as inhibitors of protein kinases |
| US7863282B2 (en) | 2003-03-14 | 2011-01-04 | Vertex Pharmaceuticals Incorporated | Compositions useful as inhibitors of protein kinases |
| US20040009981A1 (en) | 2002-03-15 | 2004-01-15 | David Bebbington | Compositions useful as inhibitors of protein kinases |
| AU2003220299A1 (en) | 2002-03-15 | 2003-09-29 | Vertex Pharmaceuticals, Inc. | Azinylaminoazoles as inhibitors of protein kinases |
| EP1485381B8 (en) | 2002-03-15 | 2010-05-12 | Vertex Pharmaceuticals Incorporated | Azolylaminoazine as inhibitors of protein kinases |
| US20030207873A1 (en) | 2002-04-10 | 2003-11-06 | Edmund Harrington | Inhibitors of Src and other protein kinases |
| WO2003091246A1 (en) | 2002-04-26 | 2003-11-06 | Vertex Pharmaceuticals Incorporated | Pyrrole derivatives as inhibitors of erk2 and uses thereof |
| MY141867A (en) | 2002-06-20 | 2010-07-16 | Vertex Pharma | Substituted pyrimidines useful as protein kinase inhibitors |
| US7361665B2 (en) | 2002-07-09 | 2008-04-22 | Vertex Pharmaceuticals Incorporated | Inhibitors of c-Jun N-terminal kinases (JNK) and other protein kinases |
| BR0313176A (pt) | 2002-08-02 | 2005-06-14 | Vertex Pharma | Composições de pirazol úteis como inibidores de gsk-3 |
| KR20060123164A (ko) | 2003-10-17 | 2006-12-01 | 아스트라제네카 아베 | 암 치료에 사용하기 위한 4-(피라졸-3-일아미노)피리미딘유도체 |
| EP1917259B1 (en) | 2005-08-18 | 2012-01-25 | Vertex Pharmaceuticals Incorporated | Pyrazine kinase inhibitors |
| WO2007023382A2 (en) | 2005-08-25 | 2007-03-01 | Pfizer Inc. | Pyrimidine amino pyrazole compounds, potent kinase inhibitors |
| EP1928456B1 (en) | 2005-09-30 | 2015-04-22 | Miikana Therapeutics, Inc. | Substituted pyrazole compounds |
| MX2008005818A (es) | 2005-11-03 | 2008-10-15 | Vertex Pharma | Aminopirimidinas utiles como inhibidores de cinasa. |
| JP2010513567A (ja) | 2006-12-19 | 2010-04-30 | バーテックス ファーマシューティカルズ インコーポレイテッド | プロテインキナーゼの阻害剤として有用なアミノピリミジン |
| EP2137183B1 (en) | 2007-03-09 | 2011-09-28 | Vertex Pharmaceuticals Incorporated | Aminopyrimidines useful as inhibitors of protein kinases |
| CA2679884A1 (en) | 2007-03-09 | 2008-09-18 | Vertex Pharmaceuticals Incorporated | Aminopyrimidines useful as inhibitors of protein kinases |
| EP2134709A1 (en) | 2007-03-09 | 2009-12-23 | Vertex Pharmaceuticals, Inc. | Aminopyridines useful as inhibitors of protein kinases |
| EP2142537A2 (en) | 2007-03-20 | 2010-01-13 | Vertex Pharmaceuticals Incorporated | Aminopyrimidines useful as kinase inhibitors |
| WO2008131103A2 (en) | 2007-04-17 | 2008-10-30 | Vertex Pharmaceuticals Incorporated | Drug discovery methods for aurora kinase inhibitors |
| MX2009011811A (es) | 2007-05-02 | 2010-01-14 | Vertex Pharma | Aminopirimidinas utiles como inhibidores de cinasa. |
| CN101801959A (zh) | 2007-05-02 | 2010-08-11 | 沃泰克斯药物股份有限公司 | 可用作激酶抑制剂的氨基嘧啶类化合物 |
| WO2008137619A2 (en) | 2007-05-02 | 2008-11-13 | Vertex Pharmaceuticals Incorporated | Thiazoles and pyrazoles useful as kinase inhibitors |
| AU2008257044A1 (en) | 2007-05-24 | 2008-12-04 | Vertex Pharmaceuticals Incorporated | Thiazoles and pyrazoles useful as kinase inhibitors |
| SG10201504084QA (en) | 2009-03-20 | 2015-06-29 | Vertex Pharma | Process for making modulators of cystic fibrosis transmembrane conductance regulator |
-
2007
- 2007-12-19 JP JP2009543169A patent/JP2010513567A/ja active Pending
- 2007-12-19 DE DE602007007985T patent/DE602007007985D1/de active Active
- 2007-12-19 CA CA002673353A patent/CA2673353A1/en not_active Abandoned
- 2007-12-19 AU AU2007333650A patent/AU2007333650A1/en not_active Abandoned
- 2007-12-19 MX MX2009006690A patent/MX2009006690A/es active IP Right Grant
- 2007-12-19 AT AT07855256T patent/ATE474835T1/de active
- 2007-12-19 NZ NZ577768A patent/NZ577768A/en not_active IP Right Cessation
- 2007-12-19 EP EP07855256A patent/EP2099787B1/en active Active
- 2007-12-19 ES ES07855256T patent/ES2347721T3/es active Active
- 2007-12-19 WO PCT/US2007/088058 patent/WO2008077086A1/en not_active Ceased
-
2009
- 2009-06-17 US US12/486,235 patent/US8426425B2/en not_active Expired - Fee Related
-
2013
- 2013-03-13 US US13/798,875 patent/US20140256703A1/en not_active Abandoned
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004509113A (ja) * | 2000-09-15 | 2004-03-25 | バーテックス ファーマシューティカルズ インコーポレイテッド | プロテインキナーゼインヒビターとして有用なピラゾール化合物 |
| JP2004525075A (ja) * | 2000-09-15 | 2004-08-19 | バーテックス ファーマシューティカルズ インコーポレイテッド | プロテインキナーゼインヒビターとして有用なピラゾール化合物 |
| JP2009515992A (ja) * | 2005-11-16 | 2009-04-16 | バーテックス ファーマシューティカルズ インコーポレイテッド | キナーゼ阻害剤として有用なアミノピリミジン |
| JP2010509231A (ja) * | 2006-11-02 | 2010-03-25 | バーテックス ファーマシューティカルズ インコーポレイテッド | プロテインキナーゼの阻害剤として有用なアミノピリジンおよびアミノピリミジン |
Also Published As
| Publication number | Publication date |
|---|---|
| NZ577768A (en) | 2012-01-12 |
| EP2099787B1 (en) | 2010-07-21 |
| ES2347721T3 (es) | 2010-11-03 |
| US20100022507A1 (en) | 2010-01-28 |
| WO2008077086A1 (en) | 2008-06-26 |
| ATE474835T1 (de) | 2010-08-15 |
| MX2009006690A (es) | 2009-07-31 |
| US20140256703A1 (en) | 2014-09-11 |
| EP2099787A1 (en) | 2009-09-16 |
| US8426425B2 (en) | 2013-04-23 |
| AU2007333650A1 (en) | 2008-06-26 |
| DE602007007985D1 (de) | 2010-09-02 |
| CA2673353A1 (en) | 2008-06-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5520057B2 (ja) | 蛋白キナーゼの阻害剤として有用なアミノピリミジン | |
| JP2010513567A (ja) | プロテインキナーゼの阻害剤として有用なアミノピリミジン | |
| EP2086965B1 (en) | Aminopyridines and aminopyrimidines useful as inhibitors of protein kinases | |
| US8735593B2 (en) | Aminopyridines useful as inhibitors of protein kinases | |
| CN101589036A (zh) | 可用作蛋白激酶抑制剂的氨基嘧啶 | |
| HK1139667A (en) | Aminopyrimidines useful as inhibitors of protein kinases | |
| HK1133877A (en) | Aminopyridines and aminopyrimidines useful as inhibitors of protein kinases | |
| HK1137014A (en) | Aminopyrimidines useful as inhibitors of protein kinases | |
| HK1138579A (en) | Aminopyridines useful as inhibitors of protein kinases |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20101119 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20101119 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20121130 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20130227 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20130306 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20130329 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20130405 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20140124 |