JP2010100593A - 新規なカルバゾール系誘導体、それよりなるホスト材料およびそれを含む有機エレクトロルミネッセンス素子 - Google Patents
新規なカルバゾール系誘導体、それよりなるホスト材料およびそれを含む有機エレクトロルミネッセンス素子 Download PDFInfo
- Publication number
- JP2010100593A JP2010100593A JP2008275694A JP2008275694A JP2010100593A JP 2010100593 A JP2010100593 A JP 2010100593A JP 2008275694 A JP2008275694 A JP 2008275694A JP 2008275694 A JP2008275694 A JP 2008275694A JP 2010100593 A JP2010100593 A JP 2010100593A
- Authority
- JP
- Japan
- Prior art keywords
- layer
- group
- carbon atoms
- light emitting
- transport layer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- UFWIBTONFRDIAS-UHFFFAOYSA-N c1cc2ccccc2cc1 Chemical compound c1cc2ccccc2cc1 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 description 13
- 0 **(c(ccc(-c1cc(*)cc(*)c1)c1)c1-c1c2)c1ccc2-c1cc(*)cc(*N)c1 Chemical compound **(c(ccc(-c1cc(*)cc(*)c1)c1)c1-c1c2)c1ccc2-c1cc(*)cc(*N)c1 0.000 description 7
- JUJWROOIHBZHMG-UHFFFAOYSA-N c1ccncc1 Chemical compound c1ccncc1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 4
- QVEYCDLEISDMDG-UHFFFAOYSA-N C1C=C(C=CC=C2)C2=CC1 Chemical compound C1C=C(C=CC=C2)C2=CC1 QVEYCDLEISDMDG-UHFFFAOYSA-N 0.000 description 1
- NJIYKMKVNGSWBM-IJDSZTBYSA-N CC/C=C\C=C/C1=[N](C)(C)=C(C)C=CC=C1 Chemical compound CC/C=C\C=C/C1=[N](C)(C)=C(C)C=CC=C1 NJIYKMKVNGSWBM-IJDSZTBYSA-N 0.000 description 1
- JAPSNDNXJYQZGU-RINMHUMESA-N CC1(C)C(c(cc2)cc(c3cc(/C(/C=C)=C/C=C\C)ccc33)c2[n]3-c2cnccc2)=CC=CCC1 Chemical compound CC1(C)C(c(cc2)cc(c3cc(/C(/C=C)=C/C=C\C)ccc33)c2[n]3-c2cnccc2)=CC=CCC1 JAPSNDNXJYQZGU-RINMHUMESA-N 0.000 description 1
- XOHDQYUWRPLNOJ-UHFFFAOYSA-N C[n]1c(C=CC(C(C=C)=C)=C=C2)c2c2c1ccc(C1=CC=CCC1)c2 Chemical compound C[n]1c(C=CC(C(C=C)=C)=C=C2)c2c2c1ccc(C1=CC=CCC1)c2 XOHDQYUWRPLNOJ-UHFFFAOYSA-N 0.000 description 1
- FNKCOUREFBNNHG-UHFFFAOYSA-N Clc1cc(Br)cc(Br)c1 Chemical compound Clc1cc(Br)cc(Br)c1 FNKCOUREFBNNHG-UHFFFAOYSA-N 0.000 description 1
Images
Landscapes
- Electroluminescent Light Sources (AREA)
- Indole Compounds (AREA)
Abstract
【解決手段】下記一般式(1)
(式中、Ar1は、炭素数6〜20の置換基を有することもあるアリール基および炭素数6〜20の置換基を有することもあるヘテロアリール基よりなる群からそれぞれ独立して選ばれた基、またAr2〜Ar5は、炭素数6〜20の置換基を有することもあるアリール基、R1およびR2は、水素および炭素数1〜6の直鎖または分枝のアルキル基よりなる群からそれぞれ独立して選ばれた基であり、mおよびnは、それぞれ0または1〜3の整数である)で示されるカルバゾール系誘導体。
【選択図】なし
Description
特に青色リン光材料については、エネルギーギャップが大きいために、ワイドギャップ化されたホスト材料が必要になってくる。現在これらリン光材料には、従来から使用されているホスト材料のmCP〔1,3−ジ(カルバゾール−9−イル)ベンゼン〕やCDBP〔2,2′−ジメチル−4,4′−ジ(カルバゾール−9−イル)−1,1′−ビフェニル〕等が使用されている。しかしながら効率的には十分ではなく高効率化には新規なワイドギャップなホスト材料の開発が必要である。
含む有機エレクトロルミネッセンス素子を提供する点にある。
本発明の第2は、下記一般式(2)
本発明の第3は、請求項1または2記載のカルバゾール系誘導体よりなるホスト材料に関する。
本発明の第4は、請求項1または2記載のカルバゾール系誘導体を用いた有機エレクトロルミネッセンス素子に関する。
本発明の第5は、請求項1または2記載のカルバゾール系誘導体とリン光材料とを含む発光層を有する有機エレクトロルミネッセンス素子に関する。
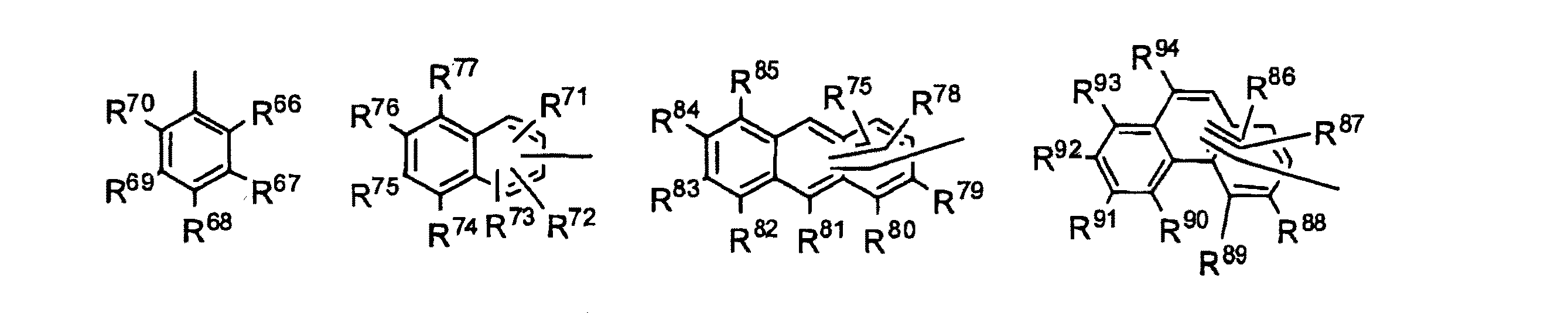
なお前記式中Ar1の例としては、下記のものを挙げることができる。
なおR1〜R94は、水素もしくは炭素数1〜6の直鎖あるいは分枝のアルキル基を示す。
R98とR99は、水素、炭素数1〜6の直鎖または分岐のアルキル基およびこれらが結合して環を形成した基からそれぞれ独立して選ばれた基であり、X1〜X5はハロゲンである。
反応式中の、Pd cat.はパラジウム触媒の、P cat.はリン触媒の、Base solutionは塩基性水溶液の、solventは有機溶媒のそれぞれ略称である。
用いる有機溶媒としては、反応基質のハロゲン化物とホウ酸化合物を溶かす溶媒なら特に問題ないが、例示すれば芳香族炭化水素系溶媒とアルコール系溶媒の混合溶媒もしくはエーテル系溶媒を挙げることができる。混合溶媒は任意の混合比で使用することができるが、一般には芳香族炭化水素系溶媒3部に対してアルコール系溶媒1部を混ぜたものを使用することが好ましい。芳香族炭化水素系溶媒としては、トルエン、キシレン、エチルベンゼン、トリメチルベンゼンなどが例示できる。アルコール系溶媒としては、メタノール、エタノール、プロパノール、ブタノールなどを例示することができる。エーテル系溶媒としては、テトラヒドロフラン、1,4−ジオキサンなどの環状エーテル、メチルセロソルブ、エチルセロソルブ、エチレングリコールジメチルエーテル、エチレングリコールジエチルエーテルなどの脂肪族エーテルなどが例示できる。本反応では、芳香族炭化水素系とアルコール系の混合溶媒が好ましく、特に好ましい組み合わせは、トルエンとエタノールの混合溶媒である。
2Mの塩基性溶液として使用できる塩基としては、アルカリあるいはアルカリ土類金属を含有するものであれば、特に限定されるものではない。例えば、水酸化リチウム、水酸化ナトリウム、水酸化カリウム、水酸化セシウム、水酸化ベリリウム、水酸化マグネシウム、水酸化カルシウムのような水酸化物、炭酸リチウム、炭酸ナトリウム、炭酸カリウム、炭酸セシウム、炭酸ベリリウム、炭酸マグネシウム、炭酸カルシウムのような炭酸塩、炭酸水素リチウム、炭酸水素ナトリウム、炭酸水素カリウム、炭酸水素セシウム、炭酸水素ベリリウム、炭酸水素マグネシウム、炭酸水素カルシウムのような重炭酸塩、あるいはこれらの金属を含むアルコラートや酢酸塩等の有機塩基を挙げることができる。本反応では、反応速度の関係から炭酸塩を用いることが好ましく、より好ましくは炭酸カリウムである。
パラジウム触媒は、ハロゲン化合物とホウ酸化合物とのカップリング反応であるためPd(0)のものが使用できる。その他のパラジウム触媒としては、テトラキス(トリフェニルホスフィン)パラジウム〔Pd(PPh3)4〕やトリス(ジベンジリデンアセトン)ジパラジウム〔Pd2(dba)3〕やパラジウムジベンジリデンアセトンなどが挙げられる。好ましくは、テトラキス(トリフェニルホスフィン)パラジウムを挙げることができる。
ハロゲン化物と反応するホウ酸化合物については、ホウ酸もしくはホウ酸エステルが使用できる。ホウ酸エステルについては、メチルエステルやエチルエステルなどを挙げることができる。またホウ素を含む環状エステル構造をもつ下記一般式
で示される(A)のような4,4,5,5−テトラメチル−1,3,2−ジオキサボロランや(B)のような5,5−ジメチル−1,3,2−ジオキサボリナンも使用することができる。
反応で使用する塩基については、前述の第1反応で使用される塩基を例示することができる。そのなかで好ましいものとしては、酢酸塩であり、より好ましくは反応時間の関係より酢酸カリウムである。
この反応で使用するパラジウム触媒としては、Pd(0)を示すものが使用できる。具体的には、有機配位子とパラジウムとの錯体が例示できる。好ましくはテトラキス(トリフェニルホスフィン)パラジウムやトリス(ジベンジリデンアセトン)ジパラジウムであり、より好ましくはジベンジリデンアセトンジパラジウムである。
またパラジウムを活性化するために添加するリン触媒としては、第3アルキルホスフィンを使用することができる。例えば、トリメチルホスフィン、トリエチルホスフィン、トリ〔n−(iso−)プロピル〕ホスフィン、トリ〔n−(iso−,tert−)ブチル〕ホスフィンのような脂肪族のものやトリシクロヘキシルホスフィン(PCy3)のような脂環式のものを挙げることができる。用いるパラジウム化合物との相性から、リン触媒としては脂環式のトリシクロヘキシルホスフィンが好ましい。
なお、例示化合物は、左右対称のもののみを示したが、左右対称の方が合成が容易ではあるが、左右非対称の化合物であってもよいことは勿論である。例えば〔化15〕の1番目の化合物における左側のトリアリール基の部分は1番目の化合物と同一であるが、右側のトリアリール基の部分は〔化15〕の2番目の化合物の対応するトリアリール基に置きかえた化合物であってもよい。
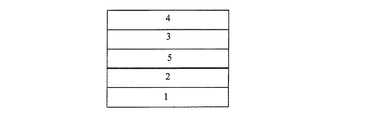
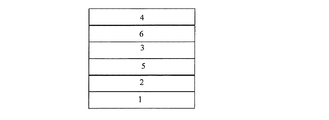
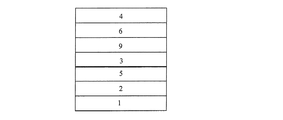
本発明の有機EL素子は、陽極と陰極間に複数層の有機化合物を積層した素子であり、発光層のホスト材料として本発明のカルバゾール系誘導体を含有する。発光層は、発光材料とホスト材料から構成される。多層型の有機EL素子の構成例としては、例えば陽極(例えばITO)/ホール輸送層/発光層/電子輸送層/陰極、ITO/ホール輸送層/発光層/電子輸送層/電子注入層/陰極、ITO/ホール輸送層/発光層/ホールブロック層/電子輸送層/陰極、ITO/ホール輸送層/発光層/ホールブロック層/電子輸送層/電子注入層/陰極、ITO/ホール注入層(正孔注入層)/ホール輸送層/発光層/ホールブロック層/電子輸送層/電子注入層/陰極等の多層構成で積層したものが挙げられる。また、必要に応じて陰極上に封止層を有していても良い。
ホール注入材料としては、下記化学式に示されるPEDOT−PSS(ポリマー混合物)やDNTPDを挙げることができる。
従って本発明のカルバゾール系誘導体は、工業的に極めて重要なものである。
(1)5′−クロロ−(1,1′;3′,1″)ターフェニル〔5′−Chloro−(1,1′;3′,1″)terphenyl〕(TPCl)の合成
(2)4,4,5,5−テトラメチル−2(1,1′;3′,1″)ターフェニル−5′−イル−(1,3,2)ジオキサボロラン〔4,4,5,5−Tetramethyl−2−(1,1′;3′,1″)terphenyl−5′−yl−(1,3,2)dioxaborolane〕(TPDOB)の合成
(3)3,6−ビス(3,5−ターフェニル)−9−フェニルカルバゾール〔3,6−Bis(3,5−terphenyl)−9−phenylcarbazole〕(CzTP)の合成
1H−NMR(400MHz,CDCl3):δ8.52(d,J=1.4Hz,2H)、7.93(d,J=1.8Hz,4H)、7.80−7.74(m,12H)、7.66−7.64(m,4H)、7.54−7.47(m,11H)、7.41−7.37(m,4H)ppm;MS:m/z700〔M〕+;Anal.Calcd for C54H37N(元素分析の計算値):C,92.67;H,5.33;N,2.00%.Found(元素分析の実測置):C,92.73;H,5.27;N,1.95%.
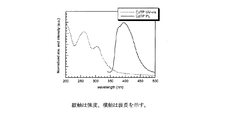
実施例1のCzTPのTG−DTA(Thermo Gravimetry−Differential Thermal Analyzer示差熱−熱重量同時測定計)、DSC(Differential Scanning Calorimeter 示差走査熱量計)を測定し、熱特性を評価した。また、紫外可視吸収スペクトル、発光スペクトルおよびイオン化ポテンシャルを測定し電気化学特性を評価した。CzTPの紫外線吸収スペクトル(UV)、フォトルミネッセンス(PL)スペクトルをそれぞれ図4に示す。
熱特性と電気化学特性について表1にまとめる。
Td5 :5%重量減少温度
Tg :ガラス転移温度
Tm :融点
Ip :イオン化ポテンシャル
Eg :エネルギーギャップ
Ea :エレクトロアフィニティ(電子親和力)
n.d.:検出されず
Tg(ガラス転移温度)については、DSC中にサンプルを加え、溶融されたものを急冷し、2〜3回繰返すとガラス点を示すカーブがチャート上に現れるので、そのカーブを接線で結び、その交点の温度をTgとして採用する。
Tm(融点)は、同じくDSCにサンプルを加え、昇温させていくと吸熱カーブが現れるのでその極大のところの温度を読んで、その温度をTmとする。
Td5(5%重量減少温度)は、TG−DTAにサンプルを加え、加熱していくとサンプルが熱によって分解し、重量が減少しだす。その減少が開始し5%重量減少したところの温度を読んでその点をTd5とする。
エネルギーギャップ(Eg)については、蒸着機で作成した薄膜を紫外−可視吸光度計で薄膜の吸収曲線を測定する。その薄膜の短波長側の立ち上がりのところに接線を引き、求まった交点の波長W(nm)を次の式に代入し目的の値を求める。それによって得た値がEgになる。
Eg=1240÷W
例えば接線を引いて求めた値W(nm)が470nmだったとしたらこの時のEgの値は
Eg=1240÷470=2.63(eV)
と言うことになる。
IP(イオン化ポテンシャル)はイオン化ポテンシャル測定装置(例えば理研計器AC−3)を使用して測定し、測定するサンプルがイオン化を開始したところの電圧(eV)の値を読む。
Ea(電子親和力)は、IpからEgを引いた値である。
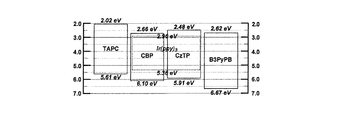
実施例1で得られたCzTPをホストに、Ir(ppy)3をドーパントに、それぞれ用いた緑色リン光素子の評価を行った。比較するホスト材料としてはCBPを用いた。また、ホール輸送材料にはTAPC、電子輸送材料にはB3PyPBを用いた。用いた材料のエネルギーダイアグラムを図5に示す。
<有機EL素子の構成>
比較例1:〔ITO/TPDPES:10wt%TBPAH(20nm)(ホール注入層)/TAPC(30nm)(ホール輸送層)/CBP:8wt% Ir(ppy)3(10nm)(発光層)/B3PyPB(50nm)(電子輸送層)/LiF(0.5nm)(電子注入層)/Al(100nm)〕
実施例2:〔ITO/TPDPES:10wt%TBPAH(20nm)(ホール注入層)/TAPC(30nm)(ホール輸送層)/CzTP:8wt% Ir(ppy)3(10nm)(発光層)/B3PyPB(50nm)(電子輸送層)/LiF(0.5nm)(電子注入層)/Al(100nm)〕
なお、TPDPES、TBPAH、TAPC、Ir(ppy)3、B3PyPB、CBPの化学式を下記に示す。
各素子の
電流密度−電圧特性を図6に、
輝度 −電圧特性を図7に、
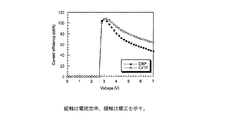
視感効率−電圧特性を図8に、
電流効率−電圧特性を図9に、
外部量子効率−輝度特性を図10に、
ELスペクトルを図11に、
それぞれ示す。また、得られた素子特性を上記表2にまとめた。
その結果、発光開始電圧である1cd/m2の電圧はCBP(2.66V)<CzTP(2.83V)の順で高くなった。
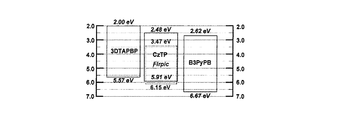
実施例1で得られたCzTPをホストとして用いた青色リン光素子の評価を行った。ホストの比較材料としてはmCPを用いた。また、ホール輸送材料には3DTAPBP、電子輸送材料にはB3PyPBを用いた。用いた材料のエネルギーダイアグラムを図12に示す。
<有機EL素子の構成>
比較例2:〔ITO/TPDPES:10wt%TBPAH(20nm)(ホール注入層)/3DTAPBP(20nm)(ホール輸送層)/mCP:11wt% FIrpic(10nm)(発光層)/B3PyPB(50nm)(電子輸送層)/LiF(0.5nm)(電子注入層)/Al(100nm)〕
実施例3:〔ITO/TPDPES:10wt%TBPAH(20nm)(ホール注入層)/3DTAPBP(20nm)(ホール輸送層)/CzTP:11wt% FIrpic(10nm)(発光層)/B3PyPB(50nm)(電子輸送層)/LiF(0.5nm)(電子注入層)/Al(100nm)〕
なお、3DTAPBP、mCP、FIrpicの化学式を下記2示す。
電流密度−電圧特性を図13に、
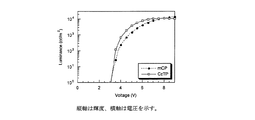
輝度 −電圧特性を図14に、
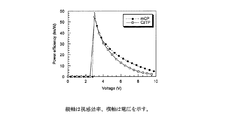
視感効率−電圧特性を図15に、
電流効率−電圧特性を図16に、
視感効率−輝度特性を図17に
外部量子効率−輝度特性を図18に、
ELスペクトルを図19に、
それぞれ示す。また、得られた素子特性を上記表3にまとめた。
実施例1で得られたCzTPをホスト材料として用いた青色リン光素子を作成した。その結果、発光開始電圧(1cd/m2)の電圧はCzTP(3.00V)<mCP(3.04V)の順で高く、電流密度−電圧特性も同じ序列であった。反対に輝度−電圧特性はCzTP>mCPの順であった。このことから、CzTPのキャリアバランスが高いことが示唆される。実際、外部量子効率−輝度特性を見ると量子収率が高くなっている。また、CzTPを用いた場合にmCPよりも低電圧駆動することから視感効率はCzTPが高くなった。なお、キャリアバランスというのは、ホールと電子の注入と再結合のバランスである。同じ数づつ注入されて、同じ数づつ再結合されている素子ほどキャリアバランスが高い。
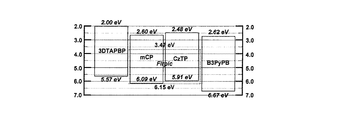
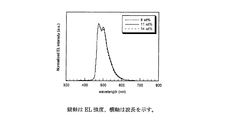
実施例3のデバイス評価で効率の高かったホスト材料CzTPを用いて素子の最適化を行った。素子構造はHTL(ホール輸送層)/EML(発光層)/ETL(電子輸送層)=20/10/50nm(EML:CzTP:8,11,14wt% FIrpic)とした。用いた材料のエネルギーダイアグラムを図20に示す。
<有機EL素子の構成>
実施例4:〔ITO/TPDPES:10wt%TBPAH(20nm)(ホール注入層)/3DTAPBP(20nm)(ホール輸送層)/CzTP:11wt% FIrpic(10nm)(発光層)/B3PyPB(50nm)(電子輸送層)/LiF(0.5nm)(電子注入層)/Al(100nm)〕
実施例5:〔ITO/TPDPES:10wt%TBPAH(20nm)(ホール注入層)/3DTAPBP(20nm)(ホール輸送層)/CzTP:14wt% FIrpic(10nm)(発光層)/B3PyPB(50nm)(電子輸送層)/LiF(0.5nm)(電子注入層)/Al(100nm)〕
実施例6:〔ITO/TPDPES:10wt%TBPAH(20nm)(ホール注入層)/3DTAPBP(20nm)(ホール輸送層)/CzTP: 8wt% FIrpic (10nm)(発光層)/B3PyPB(50nm)(電子輸送層)/LiF(0.5nm)(電子注入層)/Al(100nm)〕
Q.E.:外部量子効率
各素子の
電流密度−電圧特性を図21に、
輝度 −電圧特性を図22に、
視感効率−電圧特性を図23に、
電流効率−電圧特性を図24に、
外部量子効率−輝度特性を図25に、
ELスペクトルを図26に、
それぞれ示す。また、得られた素子特性を上記表4にまとめた。
その結果、11wt%時に視感効率が最大となり、100cd/m2時の視感効率は42.6lm/Wとなった。
以上の結果からホストからの励起3重項レベルのエネルギーがドーパントのFIrpic11wt%の時、最も失活しにくい濃度であるためホストのエネルギーが効率よくドーパントに渡り発光したため視感効率が良かったものと考察される。
2 陽極(ITO)
3 発光層
4 陰極
5 正孔(ホール)輸送層
6 電子輸送層
7 正孔(ホール)注入層
8 電子注入層
9 正孔(ホール)ブロック層
Claims (5)
- 請求項1または2記載のカルバゾール系誘導体よりなるホスト材料。
- 請求項1または2記載のカルバゾール系誘導体を用いた有機エレクトロルミネッセンス素子。
- 請求項1または2記載のカルバゾール系誘導体とリン光材料とを含む発光層を有する有機エレクトロルミネッセンス素子。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008275694A JP5674266B2 (ja) | 2008-10-27 | 2008-10-27 | 新規なカルバゾール系誘導体、それよりなるホスト材料およびそれを含む有機エレクトロルミネッセンス素子 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008275694A JP5674266B2 (ja) | 2008-10-27 | 2008-10-27 | 新規なカルバゾール系誘導体、それよりなるホスト材料およびそれを含む有機エレクトロルミネッセンス素子 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2010100593A true JP2010100593A (ja) | 2010-05-06 |
| JP5674266B2 JP5674266B2 (ja) | 2015-02-25 |
Family
ID=42291576
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008275694A Active JP5674266B2 (ja) | 2008-10-27 | 2008-10-27 | 新規なカルバゾール系誘導体、それよりなるホスト材料およびそれを含む有機エレクトロルミネッセンス素子 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP5674266B2 (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010173940A (ja) * | 2009-01-27 | 2010-08-12 | Chemiprokasei Kaisha Ltd | 新規なカルバゾール系誘導体、それよりなる電子輸送材料、ホスト材料およびそれを含む有機エレクトロルミネッセンス素子 |
| EP2433929A1 (en) * | 2010-09-27 | 2012-03-28 | Semiconductor Energy Laboratory Co, Ltd. | Organic Compound, Light-Emitting Element, Light-Emitting Device, Electronic Device, and Lighting Device |
| US9263682B2 (en) | 2010-08-06 | 2016-02-16 | Ricoh Company, Ltd. | Light emitting device and display unit |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2006199679A (ja) * | 2004-12-24 | 2006-08-03 | Pioneer Electronic Corp | 有機化合物、電荷輸送材料および有機電界発光素子 |
| JP2006306783A (ja) * | 2005-04-28 | 2006-11-09 | Jsr Corp | トリアジン化合物および有機エレクトロルミネッセンス素子用組成物並びに有機エレクトロルミネッセンス素子 |
| JP2007169268A (ja) * | 2005-11-22 | 2007-07-05 | Mitsubishi Chemicals Corp | 有機化合物、電荷輸送材料、電荷輸送材料組成物および有機電界発光素子 |
| JP2007302624A (ja) * | 2006-05-12 | 2007-11-22 | Mitsubishi Chemicals Corp | 有機化合物、電荷輸送材料、有機電界発光素子用組成物および有機電界発光素子 |
-
2008
- 2008-10-27 JP JP2008275694A patent/JP5674266B2/ja active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2006199679A (ja) * | 2004-12-24 | 2006-08-03 | Pioneer Electronic Corp | 有機化合物、電荷輸送材料および有機電界発光素子 |
| JP2006306783A (ja) * | 2005-04-28 | 2006-11-09 | Jsr Corp | トリアジン化合物および有機エレクトロルミネッセンス素子用組成物並びに有機エレクトロルミネッセンス素子 |
| JP2007169268A (ja) * | 2005-11-22 | 2007-07-05 | Mitsubishi Chemicals Corp | 有機化合物、電荷輸送材料、電荷輸送材料組成物および有機電界発光素子 |
| JP2007302624A (ja) * | 2006-05-12 | 2007-11-22 | Mitsubishi Chemicals Corp | 有機化合物、電荷輸送材料、有機電界発光素子用組成物および有機電界発光素子 |
Cited By (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010173940A (ja) * | 2009-01-27 | 2010-08-12 | Chemiprokasei Kaisha Ltd | 新規なカルバゾール系誘導体、それよりなる電子輸送材料、ホスト材料およびそれを含む有機エレクトロルミネッセンス素子 |
| US9263682B2 (en) | 2010-08-06 | 2016-02-16 | Ricoh Company, Ltd. | Light emitting device and display unit |
| TWI415922B (zh) * | 2010-09-27 | 2013-11-21 | Semiconductor Energy Lab | 咔唑化合物 |
| JP2017038063A (ja) * | 2010-09-27 | 2017-02-16 | 株式会社半導体エネルギー研究所 | 発光素子、発光装置、照明装置、電子機器 |
| JP2012092087A (ja) * | 2010-09-27 | 2012-05-17 | Semiconductor Energy Lab Co Ltd | 有機化合物、発光素子、発光装置、電子機器及び照明装置 |
| US8614334B2 (en) | 2010-09-27 | 2013-12-24 | Semiconductor Energy Laboratory Co., Ltd. | Organic compound, light-emitting element, light-emitting device, electronic device, and lighting device |
| CN102964291B (zh) * | 2010-09-27 | 2014-01-01 | 株式会社半导体能源研究所 | 有机化合物、发光元件、发光器件、电子器件和照明器件 |
| US9040720B2 (en) | 2010-09-27 | 2015-05-26 | Semiconductor Energy Laboratory Co., Ltd. | Organic compound, light-emitting element, light-emitting device, electronic device, and lighting device |
| EP2433929A1 (en) * | 2010-09-27 | 2012-03-28 | Semiconductor Energy Laboratory Co, Ltd. | Organic Compound, Light-Emitting Element, Light-Emitting Device, Electronic Device, and Lighting Device |
| CN102964291A (zh) * | 2010-09-27 | 2013-03-13 | 株式会社半导体能源研究所 | 有机化合物、发光元件、发光器件、电子器件和照明器件 |
| US9614164B2 (en) | 2010-09-27 | 2017-04-04 | Semiconductor Energy Laboratory Co., Ltd. | Organic compound, light-emitting element, light-emitting device, electronic device, and lighting device |
| US20170162798A1 (en) | 2010-09-27 | 2017-06-08 | Semiconductor Energy Laboratory Co., Ltd. | Organic compound, light-emitting element, light-emitting device, electronic device, and lighting device |
| JP2017193572A (ja) * | 2010-09-27 | 2017-10-26 | 株式会社半導体エネルギー研究所 | 化合物 |
| JP2018117152A (ja) * | 2010-09-27 | 2018-07-26 | 株式会社半導体エネルギー研究所 | 発光素子、発光装置、照明装置、電子機器 |
| US10263195B2 (en) | 2010-09-27 | 2019-04-16 | Semiconductor Energy Laboratory Co., Ltd. | Organic compound, light-emitting element, light-emitting device, electronic device, and lighting device |
| US10497880B2 (en) | 2010-09-27 | 2019-12-03 | Semiconductor Energy Laboratory Co., Ltd. | Organic compound, light-emitting element, light-emitting device, electronic device, and lighting device |
Also Published As
| Publication number | Publication date |
|---|---|
| JP5674266B2 (ja) | 2015-02-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5063992B2 (ja) | 新規なジ(ピリジルフェニル)誘導体、それよりなる電子輸送材料およびそれを含む有機エレクトロルミネッセンス素子 | |
| JP5207760B2 (ja) | 新規なピリミジン系またはトリアジン系誘導体、それよりなる電子輸送材料およびそれを含む有機エレクトロルミネッセンス素子 | |
| JP4878819B2 (ja) | 新規なトリアジン誘導体およびそれを含む有機エレクトロルミネッセンス素子 | |
| KR101663527B1 (ko) | 신규한 유기발광화합물 및 이를 포함하는 유기전계발광소자 | |
| JP5495578B2 (ja) | 新規なトリアリールホスフィンオキシド誘導体、それよりなるホスト材料およびそれを含む有機エレクトロルミネッセンス素子 | |
| JP5783749B2 (ja) | エキシマー特性を有する1,8−アリール置換ナフタレン誘導体及びこれを用いた有機el素子 | |
| JP2008120696A (ja) | 新規なトリピリジルフェニル誘導体、それよりなる電子輸送材料およびそれを含む有機エレクトロルミネッセンス素子 | |
| JP5201956B2 (ja) | 新規なジ(ピリジルフェニル)誘導体、それよりなる電子輸送材料およびそれを含む有機エレクトロルミネッセンス素子 | |
| JP5727237B2 (ja) | 新規なビカルバゾリル誘導体、それよりなるホスト材料およびそれを用いた有機エレクトロルミネッセンス素子 | |
| JP5220429B2 (ja) | 新規なジピレン誘導体、それよりなる電子輸送材料、発光材料およびそれを含む有機エレクトロルミネッセンス素子 | |
| JP5481076B2 (ja) | 新規な9,10−ジフェニルアントラセン誘導体、それよりなるホール輸送材料、発光材料およびそれを用いた有機エレクトロルミネッセンス素子 | |
| JP5476034B2 (ja) | 新規なトリアリールアミン化合物、それよりなるホール輸送材料およびそれを用いた有機エレクトロルミネッセンス素子 | |
| JP2008106015A (ja) | 新規なフェナントロリン誘導体、そのリチウム錯体、それを用いた電子輸送材料、電子注入材料および有機el素子 | |
| JP5349889B2 (ja) | 新規なターフェニル誘導体、それよりなる電子輸送材料およびそれを含む有機エレクトロルミネッセンス素子 | |
| JP5371312B2 (ja) | 新規なジカルバゾリルフェニル誘導体、それを用いたホスト材料および有機エレクトロルミネッセンス素子 | |
| JP4960045B2 (ja) | 新規なビフェニル中心骨格を有するヘテロアリール系化合物およびそれを含む有機エレクトロルミネッセンス素子 | |
| JP5086608B2 (ja) | 新規なジ(フェナントロリン)誘導体、それよりなる電子輸送材料およびそれを含む有機エレクトロルミネッセンス素子 | |
| JP2010090084A (ja) | 新規なビス(カルバゾリルフェニル)誘導体、それを用いたホスト材料および有機エレクトロルミネッセンス素子 | |
| JP2010013421A (ja) | 新規なビス(ジカルバゾリルフェニル)誘導体、それを用いたホスト材料および有機エレクトロルミネッセンス素子 | |
| JP5674266B2 (ja) | 新規なカルバゾール系誘導体、それよりなるホスト材料およびそれを含む有機エレクトロルミネッセンス素子 | |
| JP2010248112A (ja) | 芳香族炭化水素化合物、それよりなるホスト材料、それを用いた有機エレクトロルミネッセンス素子 | |
| JP2012167028A (ja) | 置換フェニルピリジンイリジウム錯体、該錯体よりなる発光材料及び該錯体を用いた有機el素子 | |
| JP5798754B2 (ja) | 新規な置換ジフェニルカルバゾール誘導体、該誘導体よりなるホスト材料及び該誘導体を含む有機エレクトロルミネッセンス素子 | |
| JP5492424B2 (ja) | 有機ラジカル化合物、それを用いた有機デバイス | |
| JP5427423B2 (ja) | 新規なカルバゾール系誘導体、それよりなる電子輸送材料、ホスト材料およびそれを含む有機エレクトロルミネッセンス素子 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100517 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20110920 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20130709 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20130711 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130909 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140311 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140508 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20141216 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20141222 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5674266 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |