JP2009521276A - 植え込み型集積回路 - Google Patents
植え込み型集積回路 Download PDFInfo
- Publication number
- JP2009521276A JP2009521276A JP2008547586A JP2008547586A JP2009521276A JP 2009521276 A JP2009521276 A JP 2009521276A JP 2008547586 A JP2008547586 A JP 2008547586A JP 2008547586 A JP2008547586 A JP 2008547586A JP 2009521276 A JP2009521276 A JP 2009521276A
- Authority
- JP
- Japan
- Prior art keywords
- integrated circuit
- circuit
- lead
- voltage
- implantable
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
- 238000000034 method Methods 0.000 claims abstract description 81
- 239000012636 effector Substances 0.000 claims abstract description 58
- 238000004891 communication Methods 0.000 claims abstract description 36
- 238000004146 energy storage Methods 0.000 claims abstract description 21
- 238000000605 extraction Methods 0.000 claims abstract description 13
- 238000011084 recovery Methods 0.000 claims description 29
- 230000000747 cardiac effect Effects 0.000 claims description 27
- 230000000670 limiting effect Effects 0.000 claims description 22
- 230000002792 vascular Effects 0.000 claims description 19
- 230000000638 stimulation Effects 0.000 claims description 10
- 230000005540 biological transmission Effects 0.000 claims description 6
- 230000008878 coupling Effects 0.000 claims description 6
- 238000010168 coupling process Methods 0.000 claims description 6
- 238000005859 coupling reaction Methods 0.000 claims description 6
- 230000003213 activating effect Effects 0.000 claims description 3
- 230000000712 assembly Effects 0.000 claims description 3
- 238000000429 assembly Methods 0.000 claims description 3
- 238000013480 data collection Methods 0.000 claims description 3
- 230000006870 function Effects 0.000 abstract description 113
- 238000009125 cardiac resynchronization therapy Methods 0.000 abstract description 13
- 230000007774 longterm Effects 0.000 abstract description 4
- 239000003990 capacitor Substances 0.000 description 325
- 239000010410 layer Substances 0.000 description 107
- 210000001519 tissue Anatomy 0.000 description 46
- 238000001514 detection method Methods 0.000 description 43
- 238000010586 diagram Methods 0.000 description 43
- 230000000903 blocking effect Effects 0.000 description 31
- 239000000463 material Substances 0.000 description 25
- 238000013461 design Methods 0.000 description 24
- 230000008901 benefit Effects 0.000 description 23
- 230000015556 catabolic process Effects 0.000 description 23
- 238000013459 approach Methods 0.000 description 22
- 230000006378 damage Effects 0.000 description 20
- 230000007246 mechanism Effects 0.000 description 19
- 230000002861 ventricular Effects 0.000 description 18
- 239000004020 conductor Substances 0.000 description 17
- 210000005003 heart tissue Anatomy 0.000 description 17
- 239000000758 substrate Substances 0.000 description 17
- 238000004519 manufacturing process Methods 0.000 description 16
- 230000002441 reversible effect Effects 0.000 description 14
- 239000012212 insulator Substances 0.000 description 13
- 230000008569 process Effects 0.000 description 13
- 239000007772 electrode material Substances 0.000 description 12
- 230000001965 increasing effect Effects 0.000 description 11
- 239000011148 porous material Substances 0.000 description 11
- 102100034274 Diamine acetyltransferase 1 Human genes 0.000 description 10
- 101000641077 Homo sapiens Diamine acetyltransferase 1 Proteins 0.000 description 10
- 101000713305 Homo sapiens Sodium-coupled neutral amino acid transporter 1 Proteins 0.000 description 10
- 238000012544 monitoring process Methods 0.000 description 10
- 230000015572 biosynthetic process Effects 0.000 description 9
- 239000012530 fluid Substances 0.000 description 9
- 230000002107 myocardial effect Effects 0.000 description 9
- 230000004044 response Effects 0.000 description 9
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 8
- 238000003860 storage Methods 0.000 description 8
- 101000640813 Homo sapiens Sodium-coupled neutral amino acid transporter 2 Proteins 0.000 description 7
- 101000716973 Homo sapiens Thialysine N-epsilon-acetyltransferase Proteins 0.000 description 7
- 102100020926 Thialysine N-epsilon-acetyltransferase Human genes 0.000 description 7
- 230000008859 change Effects 0.000 description 7
- 230000002829 reductive effect Effects 0.000 description 7
- 230000008672 reprogramming Effects 0.000 description 7
- 230000000451 tissue damage Effects 0.000 description 7
- 231100000827 tissue damage Toxicity 0.000 description 7
- 210000003462 vein Anatomy 0.000 description 7
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 6
- 230000004913 activation Effects 0.000 description 6
- 230000000694 effects Effects 0.000 description 6
- 208000014674 injury Diseases 0.000 description 6
- 230000007257 malfunction Effects 0.000 description 6
- 238000010248 power generation Methods 0.000 description 6
- 238000012545 processing Methods 0.000 description 6
- 210000005245 right atrium Anatomy 0.000 description 6
- 238000007600 charging Methods 0.000 description 5
- 210000000038 chest Anatomy 0.000 description 5
- HWLDNSXPUQTBOD-UHFFFAOYSA-N platinum-iridium alloy Chemical compound [Ir].[Pt] HWLDNSXPUQTBOD-UHFFFAOYSA-N 0.000 description 5
- 230000035939 shock Effects 0.000 description 5
- 239000003826 tablet Substances 0.000 description 5
- 238000002054 transplantation Methods 0.000 description 5
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 4
- 208000027418 Wounds and injury Diseases 0.000 description 4
- 238000009825 accumulation Methods 0.000 description 4
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 4
- 230000002457 bidirectional effect Effects 0.000 description 4
- 239000008280 blood Substances 0.000 description 4
- 210000004369 blood Anatomy 0.000 description 4
- 238000000541 cathodic arc deposition Methods 0.000 description 4
- 238000000151 deposition Methods 0.000 description 4
- 230000005684 electric field Effects 0.000 description 4
- 238000005516 engineering process Methods 0.000 description 4
- 238000002847 impedance measurement Methods 0.000 description 4
- 230000001788 irregular Effects 0.000 description 4
- 229910052751 metal Inorganic materials 0.000 description 4
- 239000002184 metal Substances 0.000 description 4
- 229910052760 oxygen Inorganic materials 0.000 description 4
- 239000001301 oxygen Substances 0.000 description 4
- 239000011241 protective layer Substances 0.000 description 4
- 230000000717 retained effect Effects 0.000 description 4
- 210000005241 right ventricle Anatomy 0.000 description 4
- 230000000630 rising effect Effects 0.000 description 4
- 238000005070 sampling Methods 0.000 description 4
- 239000004065 semiconductor Substances 0.000 description 4
- 229910052710 silicon Inorganic materials 0.000 description 4
- 239000010703 silicon Substances 0.000 description 4
- 238000012546 transfer Methods 0.000 description 4
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 4
- 238000002679 ablation Methods 0.000 description 3
- 210000001124 body fluid Anatomy 0.000 description 3
- 239000010839 body fluid Substances 0.000 description 3
- 229910002092 carbon dioxide Inorganic materials 0.000 description 3
- 239000001569 carbon dioxide Substances 0.000 description 3
- 150000001875 compounds Chemical class 0.000 description 3
- 210000003748 coronary sinus Anatomy 0.000 description 3
- 238000011161 development Methods 0.000 description 3
- 230000018109 developmental process Effects 0.000 description 3
- 201000010099 disease Diseases 0.000 description 3
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 3
- 238000005538 encapsulation Methods 0.000 description 3
- 238000002474 experimental method Methods 0.000 description 3
- 239000000284 extract Substances 0.000 description 3
- 210000004051 gastric juice Anatomy 0.000 description 3
- 230000036541 health Effects 0.000 description 3
- 230000000004 hemodynamic effect Effects 0.000 description 3
- 238000002513 implantation Methods 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- 230000033001 locomotion Effects 0.000 description 3
- 239000002071 nanotube Substances 0.000 description 3
- 230000001830 phrenic effect Effects 0.000 description 3
- 239000000523 sample Substances 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 238000001356 surgical procedure Methods 0.000 description 3
- 238000002560 therapeutic procedure Methods 0.000 description 3
- 230000008733 trauma Effects 0.000 description 3
- 210000002620 vena cava superior Anatomy 0.000 description 3
- TVZRAEYQIKYCPH-UHFFFAOYSA-N 3-(trimethylsilyl)propane-1-sulfonic acid Chemical compound C[Si](C)(C)CCCS(O)(=O)=O TVZRAEYQIKYCPH-UHFFFAOYSA-N 0.000 description 2
- 208000033988 Device pacing issue Diseases 0.000 description 2
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 2
- 241000124008 Mammalia Species 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- 241000283973 Oryctolagus cuniculus Species 0.000 description 2
- 206010067171 Regurgitation Diseases 0.000 description 2
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 2
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 2
- 239000013543 active substance Substances 0.000 description 2
- 230000009286 beneficial effect Effects 0.000 description 2
- 230000017531 blood circulation Effects 0.000 description 2
- 230000008468 bone growth Effects 0.000 description 2
- -1 carbon nitrides Chemical class 0.000 description 2
- 239000000969 carrier Substances 0.000 description 2
- 238000006243 chemical reaction Methods 0.000 description 2
- 238000005520 cutting process Methods 0.000 description 2
- 230000008021 deposition Effects 0.000 description 2
- 230000001066 destructive effect Effects 0.000 description 2
- 239000003989 dielectric material Substances 0.000 description 2
- 238000007599 discharging Methods 0.000 description 2
- 238000012377 drug delivery Methods 0.000 description 2
- 230000002526 effect on cardiovascular system Effects 0.000 description 2
- 230000002708 enhancing effect Effects 0.000 description 2
- 238000005530 etching Methods 0.000 description 2
- 230000001771 impaired effect Effects 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- 238000002955 isolation Methods 0.000 description 2
- WABPQHHGFIMREM-NOHWODKXSA-N lead-200 Chemical compound [200Pb] WABPQHHGFIMREM-NOHWODKXSA-N 0.000 description 2
- 238000007726 management method Methods 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 239000012528 membrane Substances 0.000 description 2
- 210000005036 nerve Anatomy 0.000 description 2
- 230000003071 parasitic effect Effects 0.000 description 2
- 230000002085 persistent effect Effects 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 230000005855 radiation Effects 0.000 description 2
- 230000035882 stress Effects 0.000 description 2
- 210000001321 subclavian vein Anatomy 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- 239000010936 titanium Substances 0.000 description 2
- 229910052719 titanium Inorganic materials 0.000 description 2
- 239000004408 titanium dioxide Substances 0.000 description 2
- OGIDPMRJRNCKJF-UHFFFAOYSA-N titanium oxide Inorganic materials [Ti]=O OGIDPMRJRNCKJF-UHFFFAOYSA-N 0.000 description 2
- 230000007704 transition Effects 0.000 description 2
- 230000000472 traumatic effect Effects 0.000 description 2
- 208000003663 ventricular fibrillation Diseases 0.000 description 2
- SJHPCNCNNSSLPL-UHFFFAOYSA-N 4-(ethoxymethylene)-2-phenyloxazol-5-one Chemical compound O1C(=O)C(=COCC)N=C1C1=CC=CC=C1 SJHPCNCNNSSLPL-UHFFFAOYSA-N 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 241000700198 Cavia Species 0.000 description 1
- 241000282693 Cercopithecidae Species 0.000 description 1
- 206010014405 Electrocution Diseases 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 101000809257 Homo sapiens Ubiquitin carboxyl-terminal hydrolase 4 Proteins 0.000 description 1
- 101100252165 Mus musculus Rnd2 gene Proteins 0.000 description 1
- 241000699670 Mus sp. Species 0.000 description 1
- 206010030924 Optic ischaemic neuropathy Diseases 0.000 description 1
- 241000282579 Pan Species 0.000 description 1
- 229910002673 PdOx Inorganic materials 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 241000288906 Primates Species 0.000 description 1
- 229910002842 PtOx Inorganic materials 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- 229910010282 TiON Inorganic materials 0.000 description 1
- 102100038463 Ubiquitin carboxyl-terminal hydrolase 4 Human genes 0.000 description 1
- MOGAEUYCQKROMC-UHFFFAOYSA-N [Ir].[Pt].[Ir].[Pt] Chemical compound [Ir].[Pt].[Ir].[Pt] MOGAEUYCQKROMC-UHFFFAOYSA-N 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 239000000853 adhesive Substances 0.000 description 1
- 230000001070 adhesive effect Effects 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 239000000956 alloy Substances 0.000 description 1
- 229910045601 alloy Inorganic materials 0.000 description 1
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 210000001367 artery Anatomy 0.000 description 1
- 230000006399 behavior Effects 0.000 description 1
- 230000036772 blood pressure Effects 0.000 description 1
- 210000004204 blood vessel Anatomy 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 239000002041 carbon nanotube Substances 0.000 description 1
- 229910021393 carbon nanotube Inorganic materials 0.000 description 1
- 229920002301 cellulose acetate Polymers 0.000 description 1
- 230000005591 charge neutralization Effects 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 210000003109 clavicle Anatomy 0.000 description 1
- 229920001940 conductive polymer Polymers 0.000 description 1
- 230000001186 cumulative effect Effects 0.000 description 1
- 230000009849 deactivation Effects 0.000 description 1
- 230000007423 decrease Effects 0.000 description 1
- 230000007547 defect Effects 0.000 description 1
- 230000001934 delay Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 230000009977 dual effect Effects 0.000 description 1
- 238000004870 electrical engineering Methods 0.000 description 1
- 238000004070 electrodeposition Methods 0.000 description 1
- 229940124645 emergency medicine Drugs 0.000 description 1
- 230000003628 erosive effect Effects 0.000 description 1
- 230000002169 extracardiac Effects 0.000 description 1
- 238000002594 fluoroscopy Methods 0.000 description 1
- 230000002496 gastric effect Effects 0.000 description 1
- 230000012010 growth Effects 0.000 description 1
- 239000003324 growth hormone secretagogue Substances 0.000 description 1
- 230000004217 heart function Effects 0.000 description 1
- 210000001308 heart ventricle Anatomy 0.000 description 1
- 238000005534 hematocrit Methods 0.000 description 1
- 239000007943 implant Substances 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 239000011810 insulating material Substances 0.000 description 1
- 229910052742 iron Inorganic materials 0.000 description 1
- VRIVJOXICYMTAG-IYEMJOQQSA-L iron(ii) gluconate Chemical compound [Fe+2].OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C([O-])=O.OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C([O-])=O VRIVJOXICYMTAG-IYEMJOQQSA-L 0.000 description 1
- 210000005240 left ventricle Anatomy 0.000 description 1
- 238000000691 measurement method Methods 0.000 description 1
- 230000028161 membrane depolarization Effects 0.000 description 1
- 150000001247 metal acetylides Chemical class 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- 238000004377 microelectronic Methods 0.000 description 1
- 239000000203 mixture Substances 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 230000007383 nerve stimulation Effects 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 150000004767 nitrides Chemical class 0.000 description 1
- 238000010899 nucleation Methods 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 238000013021 overheating Methods 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- BPUBBGLMJRNUCC-UHFFFAOYSA-N oxygen(2-);tantalum(5+) Chemical compound [O-2].[O-2].[O-2].[O-2].[O-2].[Ta+5].[Ta+5] BPUBBGLMJRNUCC-UHFFFAOYSA-N 0.000 description 1
- 238000004806 packaging method and process Methods 0.000 description 1
- 244000045947 parasite Species 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 210000002976 pectoralis muscle Anatomy 0.000 description 1
- 238000007747 plating Methods 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 230000008439 repair process Effects 0.000 description 1
- 238000002271 resection Methods 0.000 description 1
- 238000009436 residential construction Methods 0.000 description 1
- 230000002207 retinal effect Effects 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 230000033764 rhythmic process Effects 0.000 description 1
- 238000007789 sealing Methods 0.000 description 1
- 238000002633 shock therapy Methods 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- 235000012239 silicon dioxide Nutrition 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 239000007921 spray Substances 0.000 description 1
- 210000002784 stomach Anatomy 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 229910052715 tantalum Inorganic materials 0.000 description 1
- GUVRBAGPIYLISA-UHFFFAOYSA-N tantalum atom Chemical compound [Ta] GUVRBAGPIYLISA-UHFFFAOYSA-N 0.000 description 1
- 229910001936 tantalum oxide Inorganic materials 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 238000003325 tomography Methods 0.000 description 1
- 230000001052 transient effect Effects 0.000 description 1
- 210000000591 tricuspid valve Anatomy 0.000 description 1
- 210000000596 ventricular septum Anatomy 0.000 description 1
- 238000012800 visualization Methods 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N1/00—Electrotherapy; Circuits therefor
- A61N1/02—Details
- A61N1/04—Electrodes
- A61N1/05—Electrodes for implantation or insertion into the body, e.g. heart electrode
- A61N1/056—Transvascular endocardial electrode systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/24—Detecting, measuring or recording bioelectric or biomagnetic signals of the body or parts thereof
- A61B5/25—Bioelectric electrodes therefor
- A61B5/279—Bioelectric electrodes therefor specially adapted for particular uses
- A61B5/28—Bioelectric electrodes therefor specially adapted for particular uses for electrocardiography [ECG]
- A61B5/283—Invasive
- A61B5/287—Holders for multiple electrodes, e.g. electrode catheters for electrophysiological study [EPS]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N1/00—Electrotherapy; Circuits therefor
- A61N1/02—Details
- A61N1/025—Digital circuitry features of electrotherapy devices, e.g. memory, clocks, processors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N1/00—Electrotherapy; Circuits therefor
- A61N1/18—Applying electric currents by contact electrodes
- A61N1/32—Applying electric currents by contact electrodes alternating or intermittent currents
- A61N1/36—Applying electric currents by contact electrodes alternating or intermittent currents for stimulation
- A61N1/362—Heart stimulators
- A61N1/365—Heart stimulators controlled by a physiological parameter, e.g. heart potential
- A61N1/368—Heart stimulators controlled by a physiological parameter, e.g. heart potential comprising more than one electrode co-operating with different heart regions
- A61N1/3686—Heart stimulators controlled by a physiological parameter, e.g. heart potential comprising more than one electrode co-operating with different heart regions configured for selecting the electrode configuration on a lead
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N1/00—Electrotherapy; Circuits therefor
- A61N1/18—Applying electric currents by contact electrodes
- A61N1/32—Applying electric currents by contact electrodes alternating or intermittent currents
- A61N1/36—Applying electric currents by contact electrodes alternating or intermittent currents for stimulation
- A61N1/372—Arrangements in connection with the implantation of stimulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N1/00—Electrotherapy; Circuits therefor
- A61N1/18—Applying electric currents by contact electrodes
- A61N1/32—Applying electric currents by contact electrodes alternating or intermittent currents
- A61N1/36—Applying electric currents by contact electrodes alternating or intermittent currents for stimulation
- A61N1/362—Heart stimulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N1/00—Electrotherapy; Circuits therefor
- A61N1/18—Applying electric currents by contact electrodes
- A61N1/32—Applying electric currents by contact electrodes alternating or intermittent currents
- A61N1/36—Applying electric currents by contact electrodes alternating or intermittent currents for stimulation
- A61N1/372—Arrangements in connection with the implantation of stimulators
- A61N1/37205—Microstimulators, e.g. implantable through a cannula
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N1/00—Electrotherapy; Circuits therefor
- A61N1/18—Applying electric currents by contact electrodes
- A61N1/32—Applying electric currents by contact electrodes alternating or intermittent currents
- A61N1/36—Applying electric currents by contact electrodes alternating or intermittent currents for stimulation
- A61N1/372—Arrangements in connection with the implantation of stimulators
- A61N1/37211—Means for communicating with stimulators
- A61N1/37252—Details of algorithms or data aspects of communication system, e.g. handshaking, transmitting specific data or segmenting data
- A61N1/37276—Details of algorithms or data aspects of communication system, e.g. handshaking, transmitting specific data or segmenting data characterised by means for reducing power consumption during telemetry
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N1/00—Electrotherapy; Circuits therefor
- A61N1/18—Applying electric currents by contact electrodes
- A61N1/32—Applying electric currents by contact electrodes alternating or intermittent currents
- A61N1/36—Applying electric currents by contact electrodes alternating or intermittent currents for stimulation
- A61N1/372—Arrangements in connection with the implantation of stimulators
- A61N1/37211—Means for communicating with stimulators
- A61N1/37252—Details of algorithms or data aspects of communication system, e.g. handshaking, transmitting specific data or segmenting data
- A61N1/37288—Communication to several implantable medical devices within one patient
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61N—ELECTROTHERAPY; MAGNETOTHERAPY; RADIATION THERAPY; ULTRASOUND THERAPY
- A61N1/00—Electrotherapy; Circuits therefor
- A61N1/18—Applying electric currents by contact electrodes
- A61N1/32—Applying electric currents by contact electrodes alternating or intermittent currents
- A61N1/36—Applying electric currents by contact electrodes alternating or intermittent currents for stimulation
- A61N1/372—Arrangements in connection with the implantation of stimulators
- A61N1/375—Constructional arrangements, e.g. casings
- A61N1/3756—Casings with electrodes thereon, e.g. leadless stimulators
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Heart & Thoracic Surgery (AREA)
- Public Health (AREA)
- Cardiology (AREA)
- Veterinary Medicine (AREA)
- Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Radiology & Medical Imaging (AREA)
- Physiology (AREA)
- Biophysics (AREA)
- Vascular Medicine (AREA)
- Physics & Mathematics (AREA)
- Pathology (AREA)
- Medical Informatics (AREA)
- Molecular Biology (AREA)
- Surgery (AREA)
- Electrotherapy Devices (AREA)
Abstract
Description
米国特許法第119条(e)にしたがい、本出願は以下の出願日に対する優先件を主張し、これら出願の開示は本明細書において参照により引用される:米国仮特許出願第60/753,863号(出願日2005年12月22日);米国仮特許出願第60/753,598号(出願日2005年12月22日);米国仮特許出願第60/763,478号(出願日2006年1月30日);米国仮特許出願第60/773,699号(出願日2006年2月14日);米国仮特許出願第60/745,272号(出願日2006年4月20日);米国仮特許出願第60/805,060号(出願日2006年6月16日);米国仮特許出願第60/820,065号(出願日2006年7月21日);米国仮特許出願第60/820,588号(出願日2006年7月27日);米国仮特許出願第60/829,828号(出願日2006年10月17日);および、米国仮特許出願第60/868,041号(出願日2006年11月30日)。
本発明の実施形態は、植え込み型集積回路を提供する。植え込み型とは、回路が例えば約1週間以上、約4週間以上、約6ヶ月以上、約1年以上、例えば約5年以上の間、体内に見出される高塩分、高湿度環境を含む生理環境中に存在する場合に機能を保持するように構成されていることを意味する。特定の実施形態では、植え込み型回路は、約10年から約50年以上にわたる期間を含む、約1年から約80年以上、例えば約5年から約70年以上にわたる期間生理学的部位に植え込まれている場合に機能を保持するように構成されている。
一実施形態では、集積回路は、例えば該回路が多電極リード(MEL)のようなリード上の電極アセンブリに用いられる場合に、デフォルトモードで動作可能となるように構成されている。そのような実施形態では、回路は、最初に電極に電源を投入して電極を構成することなく、回路およびそれに連結されたアセンブリがデフォルトモードで動作することを可能にするデフォルトモード機能ブロックを含む。従って、これらの実施形態では、当該の集積回路によって提供される装置構成は、当該の集積回路に電力を供給することなく動作する。
本発明のさらに別の態様では、各サテライト上の制御装置が電荷平衡化動作を促進し、それにより電極の寿命を大幅に伸ばしている。そのように、本発明の実施形態は、集積回路が実質的に電荷を平衡化させた刺激パルスを送信することを可能にする機能ブロックを含む。
さらに、本発明の実施形態は、電極を駆動するために用いられる同一の2本のバスワイヤを用いて、異なるサテライトによって検出された信号を多重化して別個のデータ収集システムに送ることができる多重化システムを提供する。実施形態は、ペースメーカと関連する導線に隣接しかつそれらの間で電気的に連結して物理的に植え込み可能なモジュラー回路を含む。
特定の実施形態では、集積回路は、該回路が存在するシステム内の故障した回路またはワイヤを電気的に隔離するように構成された故障回復機能ブロックをさらに含む。本発明は、1つ以上のサテライトまたはバスワイヤの一部が故障した場合に植え込み型の医療装置またはシステムを選択された故障から保護するため、例えばMELシステムを保護するための故障回復機構も提供する。
本発明は、不注意による組織損傷を回避するための回路内の過電流保護機能と回路の過電圧保護機能の両方を提供する回路構成のための戦略を提供する。特定の実施形態では、集積回路は、限流機能ブロックをさらに含む。特定の実施形態では、集積回路は、電圧クランプ機能ブロックをさらに含む。本発明のさらに別の実施形態は、過電圧保護および過電流保護を提供する。これらの保護回路構成は、患者の組織が高電圧または大電流の電気パルスを受ける除細動工程中の途絶のない動作およびMELの保護を確実なものとする。
さらに、本発明は、制御装置をそのチップサイズに縮小し、MELの柔軟性を高め、かつMELの広範な用途を促進することを可能にする新規なオンチップコンデンサ設計およびオフチップコンデンサ設計を提供する。本発明の実施形態の集積回路は、そのような構成要素を可能にするための機能ブロックを含む。
特定の実施形態では、集積回路は、スリープ機能ブロックをさらに含む。このスリープ機能ブロックは、例えば遠隔制御装置から送信することができるようなスリープ信号に応答し、そのような信号の受信と同時に、例えば「スリープ中」の部分が電力を消費しないように、回路の特定の部分の電源を切る。特定の実施形態では、集積回路は、ウェイクアップ信号に応答する、例えば符号化されたウェイクアップ信号のようなウェイクアップ信号によってアクティブとなるウェイクアップ機能ブロックをさらに含み、そのような信号の受信と同時に、電源が切られていた回路の部分をオンとする。
上に概要を述べたように、本発明の集積回路は、いくつかの異なる所望の機能的能力を提供する追加の構成要素を含むかまたはそれらに連結することができる。関心のある追加機能には、デフォルトモード動作、例えば電荷平衡化動作用の阻止コンデンサを用いることによる電荷平衡化動作、フォールトトレラント動作、過電圧・過電流保護、オフチップキャパシタンスおよびオンチップキャパシタンス、DCRおよびウェイクアップ動作が含まれる。関心のあるこれらの異なる機能の各々を、ここで、全体として、かつ各図面の観点からさらに詳細に説明する。
本発明の実施形態は、デフォルトモードで動作可能な多電極リード(MEL)のサテライトユニットのような、植え込み型装置を提供する。そのような装置は、集積回路を含んでおり、該集積回路は、それが電源投入に続いて構成データを受信するか否かを問わず、電源投入と同時に動作するように構成されている。例えば、本発明のペースメーカリードは、それがペースメーカ缶から電極構成信号を受信するか否かに関係なく、それがペースメーカ缶に連結された後に、デフォルトモードで動作することができる。
MELは、より正確で効果的な心臓再同期療法を促進する同時ペーシングおよび同時信号監視を可能にする。しかしながら、あらゆる心臓ペーシング刺激の生成は、生体組織内での電荷の蓄積を引き起こす。蓄積された電荷がかなり逃げるまで、電気的活動の検出が困難となる可能性がある。さらに、電極上の不平衡な電荷蓄積によって電極の腐食が加速され、それによりMELの寿命が大幅に縮まる可能性がある。この電荷蓄積の問題は、同一の電極がペーシングと検出の両方に用いられる場合に特に顕著となる。蓄積された電荷に起因する電位が心臓の鼓動に起因するそれよりも有意に大きい限り、信頼できる検出は依然として困難なままとなる。
V(S1)−V(vlow_logic_s1)<10V (式1)
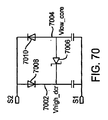
さらに、PMOSトランジスタ1518は、S2の電圧がS1の電圧よりも高いときのツェナーダイオード1520および1522を通る電流漏れを防止する。PMOSトランジスタ1518は、S2の電圧がS1の電圧を下回った場合にのみオンとされる。従って、S2の電圧がS1の電圧よりも高くある限り、コンデンサ1502内に貯蔵された電荷を保持することができる。
V(S1)−V(v2)<5V (式2)
さらに、全ペーシング工程中、S2の電圧はS1の電圧を10Vより大きく上回らないと仮定する:
V(S2)−V(S1)<10V (式3)
式2と式3をまとめると、次式となる:
V(S2)−V(v2)<15V (式4)
v2は実質的にvlow_logic_s2と同じであるので、次式が得られる:
V(S2)−V(vlow_logic_s2)<15V (式5)
S2とS1との間の最大ペーシング電圧は10Vを越えないので、図9と併せた説明を参照すると、次式が得られる:
V(vhigh_logic_s1)−V(S1)<10V (式6)
さらに、コンデンサ906が5Vを越えて充電されるのを防止するツェナーダイオード920のため、次の条件も真である:
V(vhigh_logic_s2)−V(S2)<5V (式7)
式5と式7をまとめると、次式となる:
V(vhigh_logic_s2)−V(vlow_logic_s2)<20V (式8)
これにより、スイッチ1532内のトランジスタが約20Vより大きい電圧スイッチングを受けるのが防止される。
同様に、式1と式6をまとめると、次式となる:
V(vhigh_logic_s1)−V(vlow_logic_s1)<20V (式9)
従って、式8および式9によれば、vhigh_logic_s2およびvlow_logic_s2、またはvhigh_logic_s1およびvlow_logic_s1を受けるすべての素子が、20Vより大きい電圧の振れを受けるのを防止される。
上に述べたように、MELの信頼性がありかつ堅調な動作は、ペーシング工程中の電荷平衡化動作に依存する。米国特許第4,903,700号には、ペースメーカ内の電荷の平衡を達成する手法が記載されている。一般的なペースメーカは、出力回路内に結合コンデンサを含む。コンデンサを通る正味の電流フローはゼロでなければならないので、AC結合を行うことにより、生体組織に正味の荷電が送達されることはないことが保証される。出力コンデンサは、通常、パルシング回路の一部である。電荷は、コンデンサ上に貯蔵され、次いで、刺激が必要な場合に、リードを介して素早く送達される。次いで、送達された電荷は、生体組織内の電荷が逃げるまで、コンデンサを経由して反対方向に流れる。
主題の回路の実施形態は、例えば以下に説明する多重化機能を提供する。ペースメーカの性能および能力においては多くの向上が見られるが、現在利用可能なペースメーカには欠点がないわけではない。多くの患者が、限定された数より多い電極またはセンサに接続して通信することはできない植え込み型ペースメーカを有する。特に、ペーシング用であろうと検出用であろうと、あるいはそれらの両方であろうと、多数のエフェクタが用いられる場合、多重化能力を有するペースメーカであっても、エフェクタの動作特性の変更もしくはエフェクタの起動または動作停止は、ペースメーカの再プログラミングの複雑さを増大させる。
現在のペースメーカ技術は、ヒトの心臓の血管および心室内に植え込まれたリードを有する。これらの装置のうちの1つに故障が生じた場合、装置の除去は、外傷性となるおそれがある。長期の植え込み後、リードが身体に付着し、リードを手術によって除去する場合、外傷のリスクが著しい。
図31に、予備ワイヤ3101を有する植え込み型装置を示す。図31では、電流は、ペースメーカ缶3100から、S1リード3102を通り、サテライト(例えばサテライト3104)を経由してS2リード3103上に戻り、缶3100に帰還する。図31に、開路3106のラベルが付けられた、リード3102内に生成された開路を示す。
心臓用装置の場合、除細動治療に必要となることがある内部高電圧ショックまたは外部高電圧ショックの場合における患者に対する傷害電流による不慮の組織損傷を回避するために、過電流保護は、回路における重要な構成要素である。過電圧の影響からの保護も、装置の利点を保持するにあたって有用となろう。しかしながら、現在利用可能な過電流および/または過電圧保護戦略は、高度に小型化された医療装置には適切ではない。
本発明の一実施形態は、除細動中は異なるサテライト上の電極を隔離し、電極が通常ペーシングに用いられているときは生じる電圧降下を最小限とする回路を提供する。図54に、本発明の一実施形態による、トランジスタを用いて電極をバスワイヤから隔離する構成を図解した略回路図を示す。
大きいエネルギー貯蔵を必要とする集積回路上に用いることができるコンデンサ、またはバイパスコンデンサを必要とする集積回路が必要である。集積回路チップ上にキャパシタンスを備えるために現在採用されている方法の1つは、コンデンサをシリコン自体の上に統合する方法である。本発明の実施形態は、両方とも引用によりそれらの全体が本明細書に組み込まれる、2005年12月22に出願された係属中の国際出願PCT/US2005/046811号「Implantable Addressable Segmented Electrodes」、および2005年12月22に出願された係属中の国際出願PCT/US2005/046815号「Implantable Hermetically Sealed Structures」に関連する。
Q=C・V
ここで、
Qは電荷
Cはキャパシタンス
Vはコンデンサ上に貯蔵される電圧
である。
図56Eに、第2の導電層5609の追加を示す。第2の導電層5609の追加によって、統合型オフチップコンデンサの第2の板が備えられる。この追加によって、装置のコンデンサ構成要素が完了する。
大きなエネルギー貯蔵を必要とする集積回路、またはバイパスコンデンサを必要とする集積回路が必要である。集積回路チップ上にキャパシタンスを備えるために現在用いられている方法の1つは、コンデンサをシリコン自体の上に統合する方法である。
ε0は真空の誘電率
εr用いられる絶縁体の比誘電率
Cは得られるキャパシタンス
である。
充電量は、次式によって定義される。
Q=C・V
ここで、
Qは電荷
Cはキャパシタンス
Vはコンデンサ上に貯蔵される電圧
である。
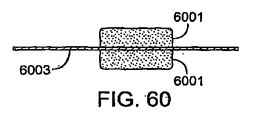
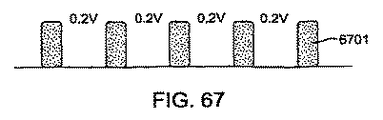
酸化することができる金属も、電極材料6101に適している。チタニウムは、陰極アークによってその純粋な形で堆積させ、キャパシタンスを提供することができる。酸化チタンの表面は、植え込み型オンチップコンデンサに対する保護層となる。酸化層は、植え込み型オンチップコンデンサのドレインを減らし、電極6101を保護する。保護層も、事偶発的な放電からさらに保護する。タンタルは、陰極アークによって堆積させ、次に酸化させることができる別の材料である。酸化チタンおよび酸化タンタルは、陰極アーク堆積法によって堆積させることができる。
別の実施形態では、本発明による植え込み型オンチップコンデンサは、イオン流体を充填した膜内に封入することができる。これは、植え込み型オンチップコンデンサが体液の必要なくして動作することを可能にする。そのような膜の利用は、体液が存在しない場合、または存在にムラがある場合に有用となろう。
本発明による制御回路のいくつかの実施形態では、制御回路は、2本のワイヤ、S1およびS2のみを介して制御装置に取り付けられている。同一の2本のバスワイヤにいくつかの制御回路を並列に取り付けてもよい。各制御回路は、その後、1つ以上のエフェクタを制御することができる。制御回路は、エフェクタを、S1、S2、に連結されるように設定するか、または中立の高インピーダンス状態に設定する。次いで、S1またはS2を通じて、接続された各エフェクタに信号を送信してもよく、エフェクタから信号を受信してもよい。2本だけのワイヤですべての通信、電力供給、エフェクタを往復する信号を処理するため、任意の所与の時刻に、様々な信号がバスワイヤS1およびS2上に存在する。存在する可能性がある他の信号と混同しない方法で制御装置に正確にコマンドを送達するデータ符号化スキームを提供する。これを達成し、同時に、クロックを取得し、かつ同一の信号から電力を生成する、効率的な符号化スキームおよび復号回路を提供する。
植え込み型装置を設計する際の1つの課題は、それらの電力消費を可能な限り制限することである。植え込み型装置の電池を交換または再充電するという標準的な手法は、危険を伴いかつ費用のかかるものであり、電池を交換するために外科的手技を必要とすることが多い。一実施形態では、本発明による回路は、特定のブロックが必要とされないときにそれらの電源を切るスリープモードを含むことによって、電力消費を大幅に減らす。追加の実施形態では、通常の通信中にスリープコマンドを送信することができる。この手法では、回路は、特定のブロックの電源を切るように命じられる。
本発明の実施形態は、電極サテライト構造体のような電極アセンブリをさらに含み、該構造体は、例えば上に考察した回路を含んだ集積回路制御装置、および少なくとも1つの電極素子を含む。従って、サテライト構造体は、該サテライト構造体がアドレス指定可能となるように、例えばIC(例えば、支持体の内側にあるIC)の形態の制御回路を含む。特定の実施形態では、この構造物は、例えばそれが分割電極構造体である場合、4つ以上の電極素子を含む、例えば3つ以上の電極素子など、2つ以上の電極素子を含む。
本発明の実施形態は、例えば上に述べたような1つ以上の電極サテライト構造体を含む医学的搬送体も含む。関心のある搬送体には、限定するものではないが、脈管リード構造体が含まれる。そのような構造体は、一般に、植え込み可能な寸法を有しており、生理学的に適合性を有する材料から製造される。脈管リードに関しては、種々の異なるリード構成を採用することができ、特定の実施形態における脈管リードは、近位端および遠位端を有する細長い管状、例えば円筒状の構造体である。近位端は、例えば「缶」または類似の装置内に存在する制御装置に接続するためのコネクタ要素、例えばIS−1コネクタを含むことができる。リードは、1つ以上の導体要素、例えばワイヤ等を格納するために、例えばガイドワイヤと共に用いるための1つ以上の管腔を含むことができる。遠位端は、所望に応じた種々の異なる特徴、例えば固定手段等を含むことができる。
本発明の実施形態は、植え込み型パルス発生器をさらに含む。植え込み型パルス発生器は、電源および電気刺激制御要素を含むハウジングと、各々が適切なコネクタ、例えばIS−1コネクタを介してハウジング内の制御要素に連結された1つ以上の上述の脈管リード、例えば2つ以上の脈管リードとを含む。特定の実施形態では、植え込み型パルス発生器は、心臓血管用途、例えばペーシング用途、心臓再同期療法用途等に用いられるものである。従って、特定の実施形態では、制御要素は、例えば該制御要素のプロセッサのコンピュータ可読媒体上に記録された適切な制御アルゴリズムを有することによって、パルス発生器がペースメーカとして動作するようパルス発生器を作動させるように構成されている。
植え込み型パルス発生器のような、上述の1つ以上の装置を含むシステムも提供する。本発明のシステムは、信号を送信および/または受信するように構成されたトランシーバを含む上述のIPG装置のような第1の植え込み型医療装置と、信号を送信および/または受信するように構成されたトランシーバを備える第2の装置との両方を含む、被術者、例えばヒトの体内で情報を通信するためのシステムと見なすことができる。第2の装置は、使用中、身体の内部にある装置であっても、身体の表面にある装置であっても、身体から離れている装置であってもよい。
本明細書に記載した主題の回路、構造体および装置は、任意の有利なプロトコルを用いる製造することができる。
例えば上に再度考察した主題の回路を例えば含む、回路ならびに/または植え込み型医療装置およびシステムまたはシステムの構成要素含むキットも提供する。特定の実施形態では、キットは、例えばペースメーカ缶の形の少なくとも1つの制御装置をさらに含む。
Claims (70)
- 植え込み型集積回路であって、該集積回路は、
電力抽出機能ブロックと、
エネルギー貯蔵機能ブロックと、
通信機能ブロックと、
装置構成機能ブロックと
を備え、該機能ブロックはすべて、管腔内に納まる大きさを有する支持体上の単一の集積回路内に存在する、植え込み型集積回路 - 使用中前記回路によって用いられる前記電力抽出の機能、前記エネルギー貯蔵の機能、前記通信の機能および前記装置構成の機能の実質的にすべてが、該単一の集積回路によって提供される、請求項1に記載の集積回路。
- 統合された防食膜をさらに備える、請求項1に記載の集積回路。
- 前記統合された防食膜は、平坦な堆積された防食膜である、請求項3に記載の集積回路。
- 前記集積回路によって提供される装置構成は、該集積回路に電力を印加することなく動作可能である、請求項1に記載の集積回路。
- 前記回路の電源投入と同時に、1つの電源端子を1つ以上のエフェクタ電極に接続するデフォルト構成が該集積回路内に設定される、請求項1に記載の集積回路。
- 前記通信機能ブロックは、約15kHzよりも高い周波数の交流を用いる、請求項1に記載の集積回路。
- 前記装置構成機能ブロックは、1つ以上のエフェクタを制御するように構成されている、請求項1に記載の集積回路。
- 前記集積回路は、前記エフェクタを介した組織の刺激を可能にする機能ブロックをさらに備える、請求項8に記載の集積回路。
- 前記集積回路は、組織から該集積回路への低電圧伝送を可能にする機能ブロックをさらに備える、請求項8に記載の集積回路。
- 前記集積回路は、実質的に電荷を平衡化させた刺激パルスの伝送を行う、請求項9に記載の集積回路。
- 前記装置構成ブロックは、電源端子と1つ以上エフェクタとの間にスイッチングブロックを備える、請求項8に記載の集積回路。
- 前記スイッチングブロックは、各エフェクタと電源端子との間に、各々が2つのトランジスタからなるスイッチング素子を備える、請求項12に記載の集積回路。
- 前記2つのトランジスタは、他のすべての回路から電気的に隔離された共通のバルクを共有する、請求項13に記載の集積回路。
- 前記2つのトランジスタは、電気的に接続されたゲートを備える、請求項14に記載の集積回路。
- 前記2つのトランジスタは、接続されたソースを備える、請求項15に記載の集積回路。
- 前記共通のバルクは、共通のソース端子に電気的に接続されている、請求項14に記載の集積回路。
- 前記ゲートに印加される制御電圧は、前記電源端子上の電圧を基準とする、請求項15に記載の集積回路。
- スリープ機能ブロックをさらに備える、請求項1に記載の集積回路。
- ウェイクアップ機能ブロックをさらに備える、請求項19に記載の集積回路。
- 前記ウェイクアップ機能ブロックは、符号化された信号によって起動されるように設定されている、請求項20に記載の集積回路。
- 限流機能ブロックをさらに備える、請求項1に記載の集積回路。
- 電圧クランプ機能ブロックをさらに備える、請求項1に記載の集積回路。
- 故障回復機能ブロックをさらに備える、請求項1に記載の集積回路。
- 前記故障回復機能ブロックは、故障した回路またはワイヤを電気的に隔離するように設定されている、請求項24に記載の集積回路。
- 前記管腔内に納まる大きさを有する支持体は、約0.05mm2から約5mm2にわたる最大表面積を有する、請求項1に記載の集積回路。
- 前記集積回路は、約100μW以下の平均消費電力を有するように構成されている、請求項1に記載の集積回路。
- 前記集積回路は、その構成状態を保持しながら約1nA以下の平均電流引き込み量を有するように構成されている、請求項1に記載の集積回路。
- 前記集積回路は、前記装置の前記構成状態が変更されている場合は、約1μAから約100μAにわたる平均電流引き込み量を有するように構成されている、請求項1に記載の集積回路。
- 前記集積回路は、データクロック回復モジュールをさらに備える、請求項1に記載の集積回路。
- 前記集積回路は、多電極サテライトを動作させるように構成されている、請求項1に記載の集積回路。
- 前記回路は、第1および第2の導電性パス連結要素をさらに備える、請求項1に記載の集積回路。
- 前記集積回路は、前記連結要素を介して第1および第2の導電性パスに接続されている、請求項32に記載の集積回路。
- 前記集積回路は、少なくとも1つのエフェクタにさらに接続されている、請求項33に記載の集積回路。
- 前記集積回路は、2つ以上のエフェクタに連結されている、請求項34に記載の集積回路。
- 前記2つ以上のエフェクタは、電極である、請求項35に記載の集積回路。
- 前記集積回路は、分割電極構造体内に存在する、請求項36に記載の集積回路。
- 前記分割電極構造体は、リード内に存在する、請求項37に記載の集積回路。
- 前記リードは、多重リードである、請求項38に記載の集積回路。
- (a)(i) 電力抽出機能ブロックと、
(ii) エネルギー貯蔵機能ブロックと、
(iii) 通信機能ブロックと、
(iv) 装置構成機能ブロックと
を備え、該機能ブロックはすべて管腔内に納まる大きさを有する支持体上の単一の集積回路内に存在する集積回路と、
(b) 該集積回路に連結された少なくとも1つのエフェクタと
を備える、植え込み型エフェクタユニット。 - 前記エフェクタユニットは、前記集積回路に連結された2つ以上のエフェクタを備える、請求項40に記載の植え込み型エフェクタユニット。
- 前記2つ以上のエフェクタは、電極である、請求項41に記載の植え込み型エフェクタユニット。
- 前記2つ以上の電極は、分割電極である、請求項42に記載の植え込み型エフェクタユニット。
- 前記ユニットは、リード上に存在する、請求項40に記載の植え込み型エフェクタユニット。
- 前記リードは、多重リードである、請求項44に記載の植え込み型エフェクタユニット。
- (a)(i) 電力抽出機能ブロックと、
(ii) エネルギー貯蔵機能ブロックと、
(iii) 通信機能ブロックと、
(iv) 装置構成機能ブロックと
を備え、該機能ブロックはすべて管腔内に納まる大きさを有する支持体上の単一の集積回路内に存在する集積回路と、
(b)該集積回路に連結された少なくとも1つの2つの電極と
を備える植え込み型電極アセンブリ。 - 前記電極アセンブリは、分割電極アセンブリである、請求項46に記載の植え込み型電極アセンブリ。
- 前記分割電極アセンブリは、4つの電極を備える、請求項47に記載の植え込み型電極アセンブリ。
- 前記電極アセンブリは、リード上に存在する、請求項46に記載の植え込み型電極アセンブリ。
- 前記リードは、多重リードである、請求項49に記載の植え込み型電極アセンブリ。
- 近位端および遠位端と、
請求項46に記載の少なくとも1つの電極アセンブリと
を備える、細長い可撓性構造体。 - 前記構造体は、脈管リードである、請求項51に記載の細長い可撓性構造体。
- 前記脈管リードは、請求項46に記載の2つ以上の電極アセンブリを備える、請求項52に記載の細長い可撓性構造体。
- 前記脈管リードは、多重脈管リードである、請求項53に記載の細長い可撓性構造体。
- 前記多重リードは、3本以下のワイヤを有する、請求項54に記載の細長い可撓性構造体。
- 前記脈管リードは、2本のみのワイヤを含む、請求項55に記載の細長い可撓性構造体。
- 前記脈管リードは、1本のみのワイヤを含む、請求項55に記載の細長い可撓性構造体。
- 前記脈管リードは、前記近位端にIS−1コネクタを含む、請求項51に記載の細長い可撓性構造体。
- (a)電源と、電気刺激制御要素とを備えるハウジングと、
(b)請求項51から請求項58のいずれか一項に記載の脈管リードと
を備える、植え込み型パルス発生器。 - 前記発生器は、2つ以上の請求項51から請求項58に記載の脈管リードを備える、請求項59に記載の植え込み型パルス発生器。
- 前記2つ以上の脈管リードに連結されたマルチプレクサであって、該マルチプレクサは、一組のサテライトを選択して遠隔データ収集装置に連結するように設定されている、マルチプレクサと、
該マルチプレクサおよび該遠隔データ収集装置に連結された導電性パスと
を備える、請求項60に記載の植え込み型パルス発生器。 - 前記マルチプレクサは、各選択されたサテライトと関連付けられた前記電極の状態を保持するように設定されている、請求項61に記載の植え込み型パルス発生器。
- 前記制御要素は、前記植え込み型パルス発生器をペースメーカとして動作させるように設定されている、請求項59に記載の植え込み型パルス発生器。
- 前記制御要素は、心臓再同期を達成するのに十分な形で前記植え込み型パルス発生器を動作させるように設定されている、請求項59に記載の植え込み型パルス発生器。
- (a)請求項59から請求項64のいずれか一項に記載の第1の植え込み型パルス発生器と、
(b)該植え込み型パルス発生器と通信するように構成された第2の装置と
を備える、システム。 - 前記第2の装置は、植え込み型医療装置である、請求項65に記載のシステム。
- 請求項59から請求項64のいずれか一項に記載の植え込み型パルス発生器を被術者の体内に植え込む工程と、
該植え込まれたパルス発生器を使用する工程と
を含む、方法。 - 前記使用する工程は、前記パルス発生器の前記電極のうちの少なくとも1つを起動して、前記被術者に電気エネルギーを送達する工程を含む、請求項67に記載の方法。
- 前記方法は、前記パルス発生器の前記電極のいずれを起動すべきかを決定する工程をさらに含む、請求項68に記載の方法。
- (a) 電源と、電気刺激制御要素とを備えるハウジングと、
(b) 請求項51から請求項58のいずれか一項に記載の脈管リードと
を備える、キット。
Applications Claiming Priority (11)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US75386305P | 2005-12-22 | 2005-12-22 | |
| US75359805P | 2005-12-22 | 2005-12-22 | |
| US76347806P | 2006-01-30 | 2006-01-30 | |
| US77369906P | 2006-02-14 | 2006-02-14 | |
| US74527206P | 2006-04-20 | 2006-04-20 | |
| US80506006P | 2006-06-16 | 2006-06-16 | |
| US82006506P | 2006-07-21 | 2006-07-21 | |
| US82058806P | 2006-07-27 | 2006-07-27 | |
| US82982806P | 2006-10-17 | 2006-10-17 | |
| US86804106P | 2006-11-30 | 2006-11-30 | |
| PCT/US2006/048944 WO2007075974A2 (en) | 2005-12-22 | 2006-12-22 | Implantable integrated circuit |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012120680A Division JP2012157747A (ja) | 2005-12-22 | 2012-05-28 | 植え込み型集積回路 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2009521276A true JP2009521276A (ja) | 2009-06-04 |
| JP2009521276A5 JP2009521276A5 (ja) | 2010-01-14 |
Family
ID=38218648
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2008547586A Ceased JP2009521276A (ja) | 2005-12-22 | 2006-12-22 | 植え込み型集積回路 |
| JP2012120680A Pending JP2012157747A (ja) | 2005-12-22 | 2012-05-28 | 植え込み型集積回路 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012120680A Pending JP2012157747A (ja) | 2005-12-22 | 2012-05-28 | 植え込み型集積回路 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US20100204766A1 (ja) |
| EP (1) | EP1968693A4 (ja) |
| JP (2) | JP2009521276A (ja) |
| WO (1) | WO2007075974A2 (ja) |
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2011524788A (ja) * | 2008-06-19 | 2011-09-08 | カーディアック ペースメイカーズ, インコーポレイテッド | 血管インターベンションカテーテルと一体化されたペースメーカー |
| US8457738B2 (en) | 2008-06-19 | 2013-06-04 | Cardiac Pacemakers, Inc. | Pacing catheter for access to multiple vessels |
| JP2015000350A (ja) * | 2013-06-17 | 2015-01-05 | バイオセンス・ウエブスター・(イスラエル)・リミテッドBiosense Webster (Israel), Ltd. | 多重バイポーラサンプリング |
| US9037235B2 (en) | 2008-06-19 | 2015-05-19 | Cardiac Pacemakers, Inc. | Pacing catheter with expandable distal end |
| JP2016508835A (ja) * | 2013-03-05 | 2016-03-24 | ザ チャールズ スターク ドレイパー ラボラトリー インク | 補助刺激記録制御ユニットを備えた分散神経調節システム |
| JP2016198686A (ja) * | 2012-04-06 | 2016-12-01 | ボストン サイエンティフィック ニューロモデュレイション コーポレイション | 電流分配回路を用いた埋め込み型神経刺激装置の正しい動作の検証 |
Families Citing this family (151)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU2003296956A1 (en) | 2002-12-11 | 2004-06-30 | Proteus Biomedical, Inc. | Monitoring and treating hemodynamic parameters |
| US7925329B2 (en) | 2004-10-08 | 2011-04-12 | Proteus Biomedical, Inc. | Implantable doppler tomography system |
| JP4747856B2 (ja) * | 2006-01-25 | 2011-08-17 | 株式会社デンソー | 乗員保護装置の起動システム |
| CA2676119C (en) | 2007-01-29 | 2021-01-19 | Simon Fraser University | Transvascular nerve stimulation apparatus and methods |
| US8127618B1 (en) | 2007-05-18 | 2012-03-06 | Pacesetter, Inc. | Implantable micro-electromechanical system sensor |
| EP2069005A4 (en) * | 2007-08-31 | 2010-12-15 | Proteus Biomedical Inc | SELF-RELATED COMMUNICATION IN IMPLANTABLE DEVICES |
| WO2009080785A1 (en) * | 2007-12-21 | 2009-07-02 | Neurodan A/S | Treatment of pelvic disorders by electrical nerve stimulation |
| DE102008007542A1 (de) * | 2008-02-05 | 2009-08-27 | Biotronik Crm Patent Ag | Multipolare Elektrodenleitung |
| US8473069B2 (en) | 2008-02-28 | 2013-06-25 | Proteus Digital Health, Inc. | Integrated circuit implementation and fault control system, device, and method |
| EP2110156B1 (de) * | 2008-04-14 | 2016-11-02 | Biotronik CRM Patent AG | Feldentkopplungs-Element zur Verwendung mit einer implantierbaren Leitung und implantierbares medizinisches Gerät |
| JP2012508622A (ja) * | 2008-11-13 | 2012-04-12 | プロテウス バイオメディカル インコーポレイテッド | 充電式刺激リード、システム、および方法 |
| WO2010057051A2 (en) * | 2008-11-13 | 2010-05-20 | Proteus Biomedical, Inc. | Implantable microstimulators |
| WO2010056438A2 (en) | 2008-11-13 | 2010-05-20 | Proteus Biomedical, Inc. | Shielded stimulation and sensing system and method |
| EP2352553A4 (en) * | 2008-11-13 | 2012-10-31 | Proteus Digital Health Inc | REGULATOR AND STIMULATOR SYSTEM, DEVICE AND METHOD |
| JP2012510343A (ja) | 2008-12-02 | 2012-05-10 | プロテウス バイオメディカル インコーポレイテッド | 電気断層撮影における最適な駆動周波数の選択 |
| US20120035684A1 (en) * | 2009-02-09 | 2012-02-09 | Todd Thompson | Multiplexed, Multi-Electrode Neurostimulation Devices with Integrated Circuits Having Integrated Electrodes |
| US20110082530A1 (en) * | 2009-04-02 | 2011-04-07 | Mark Zdeblick | Method and Apparatus for Implantable Lead |
| US8412347B2 (en) | 2009-04-29 | 2013-04-02 | Proteus Digital Health, Inc. | Methods and apparatus for leads for implantable devices |
| EP2424616A4 (en) * | 2009-04-30 | 2012-10-10 | Proteus Digital Health Inc | IMPLANTABLE DEVICE AND SYSTEM AND METHOD FOR MEASURING PHYSIOLOGICAL PARAMETERS |
| US9211410B2 (en) * | 2009-05-01 | 2015-12-15 | Setpoint Medical Corporation | Extremely low duty-cycle activation of the cholinergic anti-inflammatory pathway to treat chronic inflammation |
| WO2011011736A2 (en) * | 2009-07-23 | 2011-01-27 | Proteus Biomedical, Inc. | Solid-state thin film capacitor |
| TW201117849A (en) * | 2009-11-30 | 2011-06-01 | Unimed Invest Inc | Implantable pulsed-radiofrequency micro-stimulation system |
| AU2011292039B2 (en) * | 2010-08-17 | 2013-11-28 | Boston Scientific Neuromodulation Corporation | Telemetry-based wake up of an implantable medical device in a therapeutic network |
| WO2012033923A2 (en) * | 2010-09-08 | 2012-03-15 | Proteus Biomedical, Inc. | Maintaining high pace rate charge balance |
| US8768453B2 (en) | 2010-10-13 | 2014-07-01 | Boston Scientific Neuromodulation Corporation | Monitoring electrode voltages in an implantable medical device system having daisy-chained electrode-driver integrated circuits |
| US9061140B2 (en) * | 2010-10-13 | 2015-06-23 | Boston Scientific Neuromodulation Corporation | Sample and hold circuitry for monitoring voltages in an implantable neurostimulator |
| US8718770B2 (en) | 2010-10-21 | 2014-05-06 | Medtronic, Inc. | Capture threshold measurement for selection of pacing vector |
| US8688223B2 (en) | 2010-10-26 | 2014-04-01 | John D. Wahlstrand | Implantable medical device impedance measurement module for communication with one or more lead-borne devices |
| EP2637733A4 (en) * | 2010-11-11 | 2014-05-21 | Univ Iowa Res Found | REMOTELY CONTROLLED AND / OR LATERALLY SUPPORTED DEVICES FOR THE DIRECT STIMULATION OF SPINAL CORD |
| US10071240B2 (en) | 2010-11-11 | 2018-09-11 | University Of Iowa Research Foundation | Floating electrodes that engage and accommodate movement of the spinal cord |
| US20120123496A1 (en) * | 2010-11-12 | 2012-05-17 | Medtronic, Inc. | Connectivity detection and type identification of an implanted lead for an implantable medical device |
| FR2973709B1 (fr) * | 2011-04-06 | 2013-04-26 | Cema Com | Dispositif electro-stimulateur optimise |
| US8515545B2 (en) * | 2011-04-29 | 2013-08-20 | Greatbatch Ltd. | Current steering neurostimulator device with unidirectional current sources |
| US8355784B2 (en) | 2011-05-13 | 2013-01-15 | Medtronic, Inc. | Dynamic representation of multipolar leads in a programmer interface |
| US9101767B2 (en) | 2011-05-18 | 2015-08-11 | Greatbatch Ltd. | Measuring load impedance with active stimulation pulses in an implanted pulse generator |
| US8571667B2 (en) | 2011-07-01 | 2013-10-29 | Greatbatch Ltd. | Active current control using the enclosure of an implanted pulse generator |
| US8945146B2 (en) | 2011-10-24 | 2015-02-03 | Medtronic, Inc. | Delivery system assemblies and associated methods for implantable medical devices |
| WO2013061272A1 (en) | 2011-10-28 | 2013-05-02 | Koninklijke Philips Electronics N.V. | Data communication with interventional instruments |
| US10123717B2 (en) | 2011-11-10 | 2018-11-13 | Neuropace, Inc. | Multimodal brain sensing lead |
| US8721587B2 (en) * | 2011-11-17 | 2014-05-13 | Medtronic, Inc. | Delivery system assemblies and associated methods for implantable medical devices |
| US9216293B2 (en) | 2011-11-17 | 2015-12-22 | Medtronic, Inc. | Delivery system assemblies for implantable medical devices |
| EP2809386A4 (en) | 2012-01-30 | 2015-12-09 | Univ Iowa Res Found | SYSTEM FOR FIXING AN ELECTRODE ARRAY AT THE BACKMARK FOR THE TREATMENT OF BACK PAIN |
| JP6196634B2 (ja) | 2012-01-30 | 2017-09-13 | ユニバーシティー オブ アイオワ リサーチ ファンデーション | 高周波電気刺激を脊髄に直接適用することによる背痛の管理 |
| EP4070850A1 (en) | 2012-03-05 | 2022-10-12 | Lungpacer Medical Inc. | Transvascular nerve stimulation apparatus and methods |
| US9556860B2 (en) * | 2012-04-27 | 2017-01-31 | Medtronic, Inc. | Implantable infusion device having selective voltage boost circuit with charge pump circuit for generating control signals using first and second profiles |
| US8666511B2 (en) * | 2012-07-30 | 2014-03-04 | Medtronic, Inc. | Magnetic resonance imaging compatible medical electrical lead and method of making the same |
| US20150265833A1 (en) | 2013-06-21 | 2015-09-24 | Simon Fraser University | Transvascular diaphragm pacing systems and methods of use |
| EP3760276B1 (en) | 2013-11-22 | 2023-08-30 | Lungpacer Medical Inc. | Apparatus for assisted breathing by transvascular nerve stimulation |
| EP3092034B1 (en) | 2014-01-10 | 2019-10-30 | Cardiac Pacemakers, Inc. | Systems for detecting cardiac arrhythmias |
| CN106102830B (zh) | 2014-01-10 | 2019-07-16 | 心脏起搏器股份公司 | 用于改进医疗装置之间的通信的方法和系统 |
| AU2015208640B2 (en) | 2014-01-21 | 2020-02-20 | Lungpacer Medical Inc. | Systems and related methods for optimization of multi-electrode nerve pacing |
| KR101473443B1 (ko) * | 2014-02-07 | 2014-12-18 | (주)와이브레인 | 전기자극 시스템 |
| US9635147B2 (en) | 2014-07-09 | 2017-04-25 | The Regents Of The University Of Michigan | Protocol for an electronic device to receive a data packet from an external device |
| WO2016028799A1 (en) * | 2014-08-22 | 2016-02-25 | Cardiac Pacemakers, Inc. | Leadless cardiac pacemaker having a sensor with a lower power mode |
| EP3185952B1 (en) | 2014-08-28 | 2018-07-25 | Cardiac Pacemakers, Inc. | Implantable cardiac rhythm system and an associated method for triggering a blanking period through a second device |
| CN107206240B (zh) | 2015-02-06 | 2021-01-22 | 心脏起搏器股份公司 | 用于治疗心律不齐的系统和方法 |
| WO2016126968A1 (en) | 2015-02-06 | 2016-08-11 | Cardiac Pacemakers, Inc. | Systems and methods for safe delivery of electrical stimulation therapy |
| WO2016130477A2 (en) | 2015-02-09 | 2016-08-18 | Cardiac Pacemakers, Inc. | Implantable medical device with radiopaque id tag |
| CN107530002B (zh) | 2015-03-04 | 2021-04-30 | 心脏起搏器股份公司 | 用于治疗心律失常的系统和方法 |
| JP6515195B2 (ja) | 2015-03-18 | 2019-05-15 | カーディアック ペースメイカーズ, インコーポレイテッド | 植込み型医療装置及び医療システム |
| US10050700B2 (en) | 2015-03-18 | 2018-08-14 | Cardiac Pacemakers, Inc. | Communications in a medical device system with temporal optimization |
| WO2017031347A1 (en) | 2015-08-20 | 2017-02-23 | Cardiac Pacemakers, Inc. | Systems and methods for communication between medical devices |
| WO2017031221A1 (en) | 2015-08-20 | 2017-02-23 | Cardiac Pacemakers, Inc. | Systems and methods for communication between medical devices |
| US9968787B2 (en) | 2015-08-27 | 2018-05-15 | Cardiac Pacemakers, Inc. | Spatial configuration of a motion sensor in an implantable medical device |
| US9956414B2 (en) | 2015-08-27 | 2018-05-01 | Cardiac Pacemakers, Inc. | Temporal configuration of a motion sensor in an implantable medical device |
| US10226631B2 (en) | 2015-08-28 | 2019-03-12 | Cardiac Pacemakers, Inc. | Systems and methods for infarct detection |
| US10159842B2 (en) | 2015-08-28 | 2018-12-25 | Cardiac Pacemakers, Inc. | System and method for detecting tamponade |
| CN108136189B (zh) | 2015-08-28 | 2021-10-15 | 心脏起搏器股份公司 | 用于行为响应信号检测和治疗递送的系统 |
| US10092760B2 (en) | 2015-09-11 | 2018-10-09 | Cardiac Pacemakers, Inc. | Arrhythmia detection and confirmation |
| CN108136185B (zh) | 2015-10-08 | 2021-08-31 | 心脏起搏器股份公司 | 用于调整可植入医疗装置中的起搏速率的装置和方法 |
| EP3389775B1 (en) | 2015-12-17 | 2019-09-25 | Cardiac Pacemakers, Inc. | Conducted communication in a medical device system |
| US10905886B2 (en) | 2015-12-28 | 2021-02-02 | Cardiac Pacemakers, Inc. | Implantable medical device for deployment across the atrioventricular septum |
| WO2017127548A1 (en) | 2016-01-19 | 2017-07-27 | Cardiac Pacemakers, Inc. | Devices for wirelessly recharging a rechargeable battery of an implantable medical device |
| US11471681B2 (en) | 2016-01-20 | 2022-10-18 | Setpoint Medical Corporation | Batteryless implantable microstimulators |
| EP3411113B1 (en) | 2016-02-04 | 2019-11-27 | Cardiac Pacemakers, Inc. | Delivery system with force sensor for leadless cardiac device |
| US10485979B2 (en) * | 2016-02-22 | 2019-11-26 | The Charles Stark Draper Laboratory, Inc. | Integrated power delivery, communication, and health monitoring system for implantable electrode |
| KR102273650B1 (ko) * | 2016-02-22 | 2021-07-07 | 한국전자통신연구원 | 생체 자극 및 생체 신호 측정 겸용 회로 |
| WO2017173275A1 (en) | 2016-03-31 | 2017-10-05 | Cardiac Pacemakers, Inc. | Implantable medical device with rechargeable battery |
| FR3050050B1 (fr) * | 2016-04-11 | 2021-10-15 | Univ De Lille 1 | Neurone artificiel |
| US10328272B2 (en) | 2016-05-10 | 2019-06-25 | Cardiac Pacemakers, Inc. | Retrievability for implantable medical devices |
| US10668294B2 (en) | 2016-05-10 | 2020-06-02 | Cardiac Pacemakers, Inc. | Leadless cardiac pacemaker configured for over the wire delivery |
| EP3474945B1 (en) | 2016-06-27 | 2022-12-28 | Cardiac Pacemakers, Inc. | Cardiac therapy system using subcutaneously sensed p-waves for resynchronization pacing management |
| US20220118261A1 (en) * | 2020-10-20 | 2022-04-21 | Wesley Robert Pedersen | Curled shaft temporary pacing lead |
| WO2018009569A1 (en) | 2016-07-06 | 2018-01-11 | Cardiac Pacemakers, Inc. | Method and system for determining an atrial contraction timing fiducial in a leadless cardiac pacemaker system |
| WO2018009392A1 (en) | 2016-07-07 | 2018-01-11 | Cardiac Pacemakers, Inc. | Leadless pacemaker using pressure measurements for pacing capture verification |
| EP3487579B1 (en) | 2016-07-20 | 2020-11-25 | Cardiac Pacemakers, Inc. | System for utilizing an atrial contraction timing fiducial in a leadless cardiac pacemaker system |
| EP3500342B1 (en) | 2016-08-19 | 2020-05-13 | Cardiac Pacemakers, Inc. | Trans-septal implantable medical device |
| WO2018039322A1 (en) | 2016-08-24 | 2018-03-01 | Cardiac Pacemakers, Inc. | Cardiac resynchronization using fusion promotion for timing management |
| CN109640809B (zh) | 2016-08-24 | 2021-08-17 | 心脏起搏器股份公司 | 使用p波到起搏定时的集成式多装置心脏再同步治疗 |
| US10758737B2 (en) | 2016-09-21 | 2020-09-01 | Cardiac Pacemakers, Inc. | Using sensor data from an intracardially implanted medical device to influence operation of an extracardially implantable cardioverter |
| WO2018057626A1 (en) | 2016-09-21 | 2018-03-29 | Cardiac Pacemakers, Inc. | Implantable cardiac monitor |
| EP3515553B1 (en) | 2016-09-21 | 2020-08-26 | Cardiac Pacemakers, Inc. | Leadless stimulation device with a housing that houses internal components of the leadless stimulation device and functions as the battery case and a terminal of an internal battery |
| US10413733B2 (en) | 2016-10-27 | 2019-09-17 | Cardiac Pacemakers, Inc. | Implantable medical device with gyroscope |
| WO2018081225A1 (en) | 2016-10-27 | 2018-05-03 | Cardiac Pacemakers, Inc. | Implantable medical device delivery system with integrated sensor |
| WO2018081275A1 (en) | 2016-10-27 | 2018-05-03 | Cardiac Pacemakers, Inc. | Multi-device cardiac resynchronization therapy with timing enhancements |
| US10561330B2 (en) | 2016-10-27 | 2020-02-18 | Cardiac Pacemakers, Inc. | Implantable medical device having a sense channel with performance adjustment |
| JP7038115B2 (ja) | 2016-10-27 | 2022-03-17 | カーディアック ペースメイカーズ, インコーポレイテッド | 圧力センサを備えた植込み型医療装置 |
| WO2018081237A1 (en) | 2016-10-27 | 2018-05-03 | Cardiac Pacemakers, Inc. | Use of a separate device in managing the pace pulse energy of a cardiac pacemaker |
| EP3532158B1 (en) | 2016-10-31 | 2022-12-14 | Cardiac Pacemakers, Inc. | Systems for activity level pacing |
| EP3532157B1 (en) | 2016-10-31 | 2020-08-26 | Cardiac Pacemakers, Inc. | Systems for activity level pacing |
| US10583301B2 (en) | 2016-11-08 | 2020-03-10 | Cardiac Pacemakers, Inc. | Implantable medical device for atrial deployment |
| CN109952129B (zh) | 2016-11-09 | 2024-02-20 | 心脏起搏器股份公司 | 为心脏起搏设备设定心脏起搏脉冲参数的系统、设备和方法 |
| CN109982746B (zh) | 2016-11-21 | 2023-04-04 | 心脏起搏器股份公司 | 提供心脏再同步治疗的无引线心脏起搏器 |
| US10639486B2 (en) | 2016-11-21 | 2020-05-05 | Cardiac Pacemakers, Inc. | Implantable medical device with recharge coil |
| WO2018094344A2 (en) | 2016-11-21 | 2018-05-24 | Cardiac Pacemakers, Inc | Leadless cardiac pacemaker with multimode communication |
| WO2018094342A1 (en) | 2016-11-21 | 2018-05-24 | Cardiac Pacemakers, Inc | Implantable medical device with a magnetically permeable housing and an inductive coil disposed about the housing |
| US10881869B2 (en) | 2016-11-21 | 2021-01-05 | Cardiac Pacemakers, Inc. | Wireless re-charge of an implantable medical device |
| US11207532B2 (en) | 2017-01-04 | 2021-12-28 | Cardiac Pacemakers, Inc. | Dynamic sensing updates using postural input in a multiple device cardiac rhythm management system |
| WO2018140797A1 (en) | 2017-01-26 | 2018-08-02 | Cardiac Pacemakers, Inc. | Leadless implantable device with detachable fixation |
| WO2018140617A1 (en) | 2017-01-26 | 2018-08-02 | Cardiac Pacemakers, Inc. | Intra-body device communication with redundant message transmission |
| EP3573709A1 (en) | 2017-01-26 | 2019-12-04 | Cardiac Pacemakers, Inc. | Leadless device with overmolded components |
| US11524169B2 (en) | 2017-02-06 | 2022-12-13 | Medtronic, Inc. | Charge balanced cardiac pacing from high voltage circuitry of an extra-cardiovascular implantable cardioverter defibrillator system |
| CN110740779B (zh) | 2017-04-03 | 2024-03-08 | 心脏起搏器股份公司 | 具有基于感测到的心率的起搏脉冲能量调节的心脏起搏器 |
| US10905872B2 (en) | 2017-04-03 | 2021-02-02 | Cardiac Pacemakers, Inc. | Implantable medical device with a movable electrode biased toward an extended position |
| US10293164B2 (en) | 2017-05-26 | 2019-05-21 | Lungpacer Medical Inc. | Apparatus and methods for assisted breathing by transvascular nerve stimulation |
| EP4374910A3 (en) | 2017-06-30 | 2024-08-14 | Lungpacer Medical Inc. | System for prevention, moderation, and/or treatment of cognitive injury |
| US10195429B1 (en) | 2017-08-02 | 2019-02-05 | Lungpacer Medical Inc. | Systems and methods for intravascular catheter positioning and/or nerve stimulation |
| US10940308B2 (en) | 2017-08-04 | 2021-03-09 | Lungpacer Medical Inc. | Systems and methods for trans-esophageal sympathetic ganglion recruitment |
| EP3668592B1 (en) | 2017-08-18 | 2021-11-17 | Cardiac Pacemakers, Inc. | Implantable medical device with pressure sensor |
| WO2019036568A1 (en) | 2017-08-18 | 2019-02-21 | Cardiac Pacemakers, Inc. | IMPLANTABLE MEDICAL DEVICE COMPRISING A FLOW CONCENTRATOR AND A RECEPTION COIL PROVIDED AROUND THE FLOW CONCENTRATOR |
| CN111107899B (zh) | 2017-09-20 | 2024-04-02 | 心脏起搏器股份公司 | 具有多种操作模式的可植入医疗装置 |
| US11185703B2 (en) | 2017-11-07 | 2021-11-30 | Cardiac Pacemakers, Inc. | Leadless cardiac pacemaker for bundle of his pacing |
| CN111417433B (zh) | 2017-12-01 | 2024-04-30 | 心脏起搏器股份公司 | 从心室植入的无引线心脏起搏器检测心室充盈期间心房收缩定时基准的方法和系统 |
| CN111432874A (zh) | 2017-12-01 | 2020-07-17 | 心脏起搏器股份公司 | 从心室植入的无引线心脏起搏器检测搜索窗口内心房收缩定时基准的方法和系统 |
| WO2019108482A1 (en) | 2017-12-01 | 2019-06-06 | Cardiac Pacemakers, Inc. | Methods and systems for detecting atrial contraction timing fiducials and determining a cardiac interval from a ventricularly implanted leadless cardiac pacemaker |
| EP3717060B1 (en) | 2017-12-01 | 2022-10-05 | Cardiac Pacemakers, Inc. | Leadless cardiac pacemaker with reversionary behavior |
| US20190175908A1 (en) | 2017-12-11 | 2019-06-13 | Lungpacer Medical Inc. | Systems and methods for strengthening a respiratory muscle |
| US11529523B2 (en) | 2018-01-04 | 2022-12-20 | Cardiac Pacemakers, Inc. | Handheld bridge device for providing a communication bridge between an implanted medical device and a smartphone |
| WO2019136148A1 (en) | 2018-01-04 | 2019-07-11 | Cardiac Pacemakers, Inc. | Dual chamber pacing without beat-to-beat communication |
| US11058880B2 (en) | 2018-03-23 | 2021-07-13 | Medtronic, Inc. | VFA cardiac therapy for tachycardia |
| CN111886046A (zh) | 2018-03-23 | 2020-11-03 | 美敦力公司 | Av同步vfa心脏治疗 |
| JP2021518192A (ja) | 2018-03-23 | 2021-08-02 | メドトロニック,インコーポレイテッド | VfA心臓再同期治療 |
| US11351381B2 (en) | 2018-05-18 | 2022-06-07 | Washington University | Systems and methods for stimulating sympathetic nervous system |
| CN112469468A (zh) * | 2018-09-12 | 2021-03-09 | 科利耳有限公司 | 安全关键电子设备锁 |
| US11372093B2 (en) * | 2018-09-14 | 2022-06-28 | Fujifilm Sonosite, Inc. | Automated fault detection and correction in an ultrasound imaging system |
| WO2020065582A1 (en) | 2018-09-26 | 2020-04-02 | Medtronic, Inc. | Capture in ventricle-from-atrium cardiac therapy |
| EP3877043A4 (en) | 2018-11-08 | 2022-08-24 | Lungpacer Medical Inc. | STIMULATION SYSTEM AND ASSOCIATED USER INTERFACES |
| US11951313B2 (en) | 2018-11-17 | 2024-04-09 | Medtronic, Inc. | VFA delivery systems and methods |
| US11679265B2 (en) | 2019-02-14 | 2023-06-20 | Medtronic, Inc. | Lead-in-lead systems and methods for cardiac therapy |
| US11697025B2 (en) | 2019-03-29 | 2023-07-11 | Medtronic, Inc. | Cardiac conduction system capture |
| US11213676B2 (en) | 2019-04-01 | 2022-01-04 | Medtronic, Inc. | Delivery systems for VfA cardiac therapy |
| US11712188B2 (en) | 2019-05-07 | 2023-08-01 | Medtronic, Inc. | Posterior left bundle branch engagement |
| US11357979B2 (en) | 2019-05-16 | 2022-06-14 | Lungpacer Medical Inc. | Systems and methods for sensing and stimulation |
| US11771900B2 (en) | 2019-06-12 | 2023-10-03 | Lungpacer Medical Inc. | Circuitry for medical stimulation systems |
| US11305127B2 (en) | 2019-08-26 | 2022-04-19 | Medtronic Inc. | VfA delivery and implant region detection |
| US11813466B2 (en) | 2020-01-27 | 2023-11-14 | Medtronic, Inc. | Atrioventricular nodal stimulation |
| US20230046820A1 (en) * | 2020-02-10 | 2023-02-16 | Nanovision Biosciences, Inc. | Apparatuses and methods for wirelessly powered charge-balanced electrical stimulation |
| US11911168B2 (en) | 2020-04-03 | 2024-02-27 | Medtronic, Inc. | Cardiac conduction system therapy benefit determination |
| US20220023621A1 (en) * | 2020-07-27 | 2022-01-27 | Medtronic, Inc. | Implantable medical lead |
| US11813464B2 (en) | 2020-07-31 | 2023-11-14 | Medtronic, Inc. | Cardiac conduction system evaluation |
| CN112947500B (zh) * | 2021-02-10 | 2022-05-20 | 复旦大学 | 一种水下航行器水流监测系统 |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS63132459A (ja) * | 1986-11-25 | 1988-06-04 | Hitachi Ltd | 容量内蔵半導体パツケ−ジ |
| JPH09199374A (ja) * | 1995-11-13 | 1997-07-31 | Shinko Electric Ind Co Ltd | 薄膜コンデンサ、これを搭載した半導体装置用パッケージおよび半導体装置 |
| JPH1041437A (ja) * | 1996-07-26 | 1998-02-13 | Fuji Electric Co Ltd | 樹脂モールド型半導体装置 |
| JP2001516980A (ja) * | 1997-09-12 | 2001-10-02 | アルフレッド イー マン ファウンデーション フォア サイエンティフィック リサーチ | 埋設可能なセンサに用いる低電力電流・周波数変換回路 |
| JP2001517056A (ja) * | 1997-09-12 | 2001-10-02 | アルフレッド イー マン ファウンデーション フォア サイエンティフィック リサーチ | 低電力整流回路 |
| JP2002043468A (ja) * | 2000-07-27 | 2002-02-08 | Fujitsu Ltd | 表裏導通基板及びその製造方法 |
| JP2004533302A (ja) * | 2001-06-14 | 2004-11-04 | アルフレッド イー マン ファウンデイション フォー サイエンティフィック リサーチ | 埋込可能型デバイス用密封給電 |
Family Cites Families (103)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB1598791A (en) * | 1977-03-10 | 1981-09-23 | Needle Industries Ltd | Plug and socket connectors |
| US4902273A (en) * | 1984-02-21 | 1990-02-20 | Choy Daniel S J | Heart assist device |
| US5004275A (en) * | 1986-03-14 | 1991-04-02 | International Clamp Company | Clamp |
| US5005613A (en) * | 1986-09-26 | 1991-04-09 | The Goodyear Tire & Rubber Company | Light weight flexible coaxial vapor recovery hose |
| US4815472A (en) * | 1987-06-01 | 1989-03-28 | The Regents Of The University Of Michigan | Multipoint pressure-sensing catheter system |
| US5113868A (en) * | 1987-06-01 | 1992-05-19 | The Regents Of The University Of Michigan | Ultraminiature pressure sensor with addressable read-out circuit |
| CA1327838C (fr) * | 1988-06-13 | 1994-03-15 | Fred Zacouto | Dispositif implantable de protection contre les affections liees a la coagulation sanguine |
| US5176619A (en) * | 1989-05-05 | 1993-01-05 | Jacob Segalowitz | Heart-assist balloon pump with segmented ventricular balloon |
| US5209238A (en) * | 1989-08-17 | 1993-05-11 | Sundhar Shaam P | Electronic ovulation monitor |
| US5188106A (en) * | 1991-03-08 | 1993-02-23 | Telectronics Pacing Systems, Inc. | Method and apparatus for chronically monitoring the hemodynamic state of a patient using doppler ultrasound |
| IT1245814B (it) * | 1991-05-21 | 1994-10-18 | Sorin Biomedica Spa | Dispositivo cardiostimolatore del tipo rate responsive |
| US5267564A (en) * | 1991-06-14 | 1993-12-07 | Siemens Pacesetter, Inc. | Pacemaker lead for sensing a physiologic parameter of the body |
| US5213098A (en) * | 1991-07-26 | 1993-05-25 | Medtronic, Inc. | Post-extrasystolic potentiation stimulation with physiologic sensor feedback |
| DK0541338T3 (da) * | 1991-11-04 | 1996-12-02 | Cardiac Pacemakers Inc | Implanterbar indretning til overvågning og stimulering af hjertet til diagnose og terapi |
| US5419767A (en) * | 1992-01-07 | 1995-05-30 | Thapliyal And Eggers Partners | Methods and apparatus for advancing catheters through severely occluded body lumens |
| US5313020A (en) * | 1992-05-29 | 1994-05-17 | Western Atlas International, Inc. | Electrical cable |
| US5285744A (en) * | 1992-09-04 | 1994-02-15 | Vapor Systems Technologies, Inc. | Coaxial hose assembly |
| US5662108A (en) * | 1992-09-23 | 1997-09-02 | Endocardial Solutions, Inc. | Electrophysiology mapping system |
| US5706809A (en) * | 1993-01-29 | 1998-01-13 | Cardima, Inc. | Method and system for using multiple intravascular sensing devices to detect electrical activity |
| NL9300670A (nl) * | 1993-04-20 | 1994-11-16 | Cordis Europ | Catheter met elektrisch goed geleidende draadversterking. |
| US5411532A (en) * | 1993-06-04 | 1995-05-02 | Pacesetter, Inc. | Cardiac pacemaker having integrated pacing lead and oxygen sensor |
| US5628777A (en) * | 1993-07-14 | 1997-05-13 | Pacesetter, Inc. | Implantable leads incorporating cardiac wall acceleration sensors and method of fabrication |
| US5391199A (en) * | 1993-07-20 | 1995-02-21 | Biosense, Inc. | Apparatus and method for treating cardiac arrhythmias |
| US5411537A (en) * | 1993-10-29 | 1995-05-02 | Intermedics, Inc. | Rechargeable biomedical battery powered devices with recharging and control system therefor |
| US5810802A (en) * | 1994-08-08 | 1998-09-22 | E.P. Technologies, Inc. | Systems and methods for controlling tissue ablation using multiple temperature sensing elements |
| US6015429A (en) * | 1994-09-08 | 2000-01-18 | Gore Enterprise Holdings, Inc. | Procedures for introducing stents and stent-grafts |
| BR9509372A (pt) * | 1994-10-19 | 1998-11-03 | Avery Dennison Corp | Sistema de fixação de fralda descartável usando abas do tipo de ramificação soldada |
| US5487752A (en) * | 1994-11-15 | 1996-01-30 | Cardiac Pacemakers, Inc. | Automated programmable stimulating device to optimize pacing parameters and method |
| US5563762A (en) * | 1994-11-28 | 1996-10-08 | Northern Telecom Limited | Capacitor for an integrated circuit and method of formation thereof, and a method of adding on-chip capacitors to an integrated circuit |
| US5593430A (en) * | 1995-01-27 | 1997-01-14 | Pacesetter, Inc. | Bus system for interconnecting an implantable medical device with a plurality of sensors |
| US5743267A (en) * | 1995-10-19 | 1998-04-28 | Telecom Medical, Inc. | System and method to monitor the heart of a patient |
| JP2825074B2 (ja) * | 1995-10-25 | 1998-11-18 | 日本電気株式会社 | 半導体装置の製造方法 |
| US5713937A (en) * | 1995-11-07 | 1998-02-03 | Pacesetter, Inc. | Pacemaker programmer menu with selectable real or simulated implant data graphics |
| US6363279B1 (en) * | 1996-01-08 | 2002-03-26 | Impulse Dynamics N.V. | Electrical muscle controller |
| WO1997029802A2 (en) * | 1996-02-20 | 1997-08-21 | Advanced Bionics Corporation | Improved implantable microstimulator and systems employing the same |
| US6033398A (en) * | 1996-03-05 | 2000-03-07 | Vnus Medical Technologies, Inc. | Method and apparatus for treating venous insufficiency using directionally applied energy |
| US5755759A (en) * | 1996-03-14 | 1998-05-26 | Eic Laboratories, Inc. | Biomedical device with a protective overlayer |
| AU714617B2 (en) * | 1996-04-04 | 2000-01-06 | Medtronic, Inc. | Living tissue stimulation and recording techniques |
| US5720768A (en) * | 1996-05-22 | 1998-02-24 | Sulzer Intermedics Inc. | Dual chamber pacing with interchamber delay |
| SE9603573D0 (sv) * | 1996-09-30 | 1996-09-30 | Pacesetter Ab | Implantable medecal device |
| US5902248A (en) * | 1996-11-06 | 1999-05-11 | Millar Instruments, Inc. | Reduced size catheter tip measurement device |
| US5902234A (en) * | 1997-04-10 | 1999-05-11 | Webb; Nicholas J. | Medical communication system for ambulatory home-care patients |
| US5873849A (en) * | 1997-04-24 | 1999-02-23 | Ichor Medical Systems, Inc. | Electrodes and electrode arrays for generating electroporation inducing electrical fields |
| US6032699A (en) * | 1997-05-19 | 2000-03-07 | Furon Company | Fluid delivery pipe with leak detection |
| US5999848A (en) * | 1997-09-12 | 1999-12-07 | Alfred E. Mann Foundation | Daisy chainable sensors and stimulators for implantation in living tissue |
| US6016449A (en) * | 1997-10-27 | 2000-01-18 | Neuropace, Inc. | System for treatment of neurological disorders |
| SE9801238D0 (sv) * | 1998-04-08 | 1998-04-08 | Siemens Elema Ab | Apparatus and method for locating electrically active sites within an animal |
| US6223080B1 (en) * | 1998-04-29 | 2001-04-24 | Medtronic, Inc. | Power consumption reduction in medical devices employing multiple digital signal processors and different supply voltages |
| US6024704A (en) * | 1998-04-30 | 2000-02-15 | Medtronic, Inc | Implantable medical device for sensing absolute blood pressure and barometric pressure |
| US6042580A (en) * | 1998-05-05 | 2000-03-28 | Cardiac Pacemakers, Inc. | Electrode having composition-matched, common-lead thermocouple wire for providing multiple temperature-sensitive junctions |
| US6015386A (en) * | 1998-05-07 | 2000-01-18 | Bpm Devices, Inc. | System including an implantable device and methods of use for determining blood pressure and other blood parameters of a living being |
| US6044297A (en) * | 1998-09-25 | 2000-03-28 | Medtronic, Inc. | Posture and device orientation and calibration for implantable medical devices |
| US6044298A (en) * | 1998-10-13 | 2000-03-28 | Cardiac Pacemakers, Inc. | Optimization of pacing parameters based on measurement of integrated acoustic noise |
| US6026324A (en) * | 1998-10-13 | 2000-02-15 | Cardiac Pacemakers, Inc. | Extraction of hemodynamic pulse pressure from fluid and myocardial accelerations |
| US6370431B1 (en) * | 1998-10-26 | 2002-04-09 | Medtronic, Inc. | Pacemaker system for preventing ventricular tachycardia |
| US6206835B1 (en) * | 1999-03-24 | 2001-03-27 | The B. F. Goodrich Company | Remotely interrogated diagnostic implant device with electrically passive sensor |
| US6171252B1 (en) * | 1999-04-29 | 2001-01-09 | Medtronic, Inc. | Pressure sensor with increased sensitivity for use with an implantable medical device |
| US20010025192A1 (en) * | 1999-04-29 | 2001-09-27 | Medtronic, Inc. | Single and multi-polar implantable lead for sacral nerve electrical stimulation |
| US6692834B1 (en) * | 1999-06-28 | 2004-02-17 | Medtronic, Inc. | Method for coating implantable devices |
| US6360123B1 (en) * | 1999-08-24 | 2002-03-19 | Impulse Dynamics N.V. | Apparatus and method for determining a mechanical property of an organ or body cavity by impedance determination |
| US6197677B1 (en) * | 1999-11-01 | 2001-03-06 | United Microelectronics Corp. | Method of depositing a silicon oxide layer on a semiconductor wafer |
| JP2002006601A (ja) * | 2000-06-23 | 2002-01-11 | Canon Inc | 現像剤補給容器及び画像形成装置 |
| US6764446B2 (en) * | 2000-10-16 | 2004-07-20 | Remon Medical Technologies Ltd | Implantable pressure sensors and methods for making and using them |
| US6501992B1 (en) * | 2000-10-17 | 2002-12-31 | Medtronic, Inc. | Radiopaque marking of lead electrode zone in a continuous conductor construction |
| US20010000187A1 (en) * | 2000-10-23 | 2001-04-05 | Case Western Reserve University | Functional neuromuscular stimulation system |
| US7481759B2 (en) * | 2001-08-03 | 2009-01-27 | Cardiac Pacemakers, Inc. | Systems and methods for treatment of coronary artery disease |
| US6907297B2 (en) * | 2001-09-28 | 2005-06-14 | Ethicon, Inc. | Expandable intracardiac return electrode and method of use |
| US6934583B2 (en) * | 2001-10-22 | 2005-08-23 | Pacesetter, Inc. | Implantable lead and method for stimulating the vagus nerve |
| US7286878B2 (en) * | 2001-11-09 | 2007-10-23 | Medtronic, Inc. | Multiplexed electrode array extension |
| US6993384B2 (en) * | 2001-12-04 | 2006-01-31 | Advanced Bionics Corporation | Apparatus and method for determining the relative position and orientation of neurostimulation leads |
| US20040039417A1 (en) * | 2002-04-16 | 2004-02-26 | Medtronic, Inc. | Electrical stimulation and thrombolytic therapy |
| US7184840B2 (en) * | 2002-04-22 | 2007-02-27 | Medtronic, Inc. | Implantable lead with isolated contact coupling |
| NZ519153A (en) * | 2002-05-23 | 2004-09-24 | David Stanley Hoyle | Agricultural spreader having an inclinometer means and a microprocessor for controlling the supply rate of the fertiliser |
| JP2004024551A (ja) * | 2002-06-26 | 2004-01-29 | Renesas Technology Corp | センサシステム用半導体装置 |
| AU2003296956A1 (en) * | 2002-12-11 | 2004-06-30 | Proteus Biomedical, Inc. | Monitoring and treating hemodynamic parameters |
| US20060035147A1 (en) * | 2003-01-15 | 2006-02-16 | Quallion Llc | Battery |
| EP1585575A4 (en) * | 2003-01-24 | 2011-02-09 | Proteus Biomedical Inc | METHODS AND DEVICES FOR ENHANCING HEART RATE REGULATION |
| JP4528766B2 (ja) * | 2003-01-24 | 2010-08-18 | プロテウス バイオメディカル インコーポレイテッド | 遠隔血行力学的モニタリングのためのシステム |
| US7204798B2 (en) * | 2003-01-24 | 2007-04-17 | Proteus Biomedical, Inc. | Methods and systems for measuring cardiac parameters |
| US6885889B2 (en) * | 2003-02-28 | 2005-04-26 | Medtronic, Inc. | Method and apparatus for optimizing cardiac resynchronization therapy based on left ventricular acceleration |
| US8368150B2 (en) * | 2003-03-17 | 2013-02-05 | Megica Corporation | High performance IC chip having discrete decoupling capacitors attached to its IC surface |
| US6994676B2 (en) * | 2003-04-30 | 2006-02-07 | Medtronic, Inc | Method and apparatus for assessing ventricular contractile status |
| US7291105B2 (en) * | 2003-07-10 | 2007-11-06 | Paracor Medical, Inc. | Self-anchoring cardiac harness |
| US7092759B2 (en) * | 2003-07-30 | 2006-08-15 | Medtronic, Inc. | Method of optimizing cardiac resynchronization therapy using sensor signals of septal wall motion |
| US7174218B1 (en) * | 2003-08-12 | 2007-02-06 | Advanced Bionics Corporation | Lead extension system for use with a microstimulator |
| US8489196B2 (en) * | 2003-10-03 | 2013-07-16 | Medtronic, Inc. | System, apparatus and method for interacting with a targeted tissue of a patient |
| US7184833B2 (en) * | 2003-10-07 | 2007-02-27 | Medtronic, Inc. | Multiple pacing output channels |
| US20060004424A1 (en) * | 2004-06-04 | 2006-01-05 | University Of Southern California | Charge-metered biomedical stimulator |
| US7214189B2 (en) * | 2004-09-02 | 2007-05-08 | Proteus Biomedical, Inc. | Methods and apparatus for tissue activation and monitoring |
| FR2875071B1 (fr) * | 2004-09-03 | 2006-11-24 | Inst Nat Rech Inf Automat | Dispositif de repartition de courant entre des cathodes d'une electrode multipolaire, notamment d'un implant |
| US20080058656A1 (en) * | 2004-10-08 | 2008-03-06 | Costello Benedict J | Electric tomography |
| US7200437B1 (en) * | 2004-10-13 | 2007-04-03 | Pacesetter, Inc. | Tissue contact for satellite cardiac pacemaker |
| US20070198066A1 (en) * | 2005-11-03 | 2007-08-23 | Greenberg Robert J | Method and apparatus for visual neural stimulation |
| TWI330354B (en) * | 2006-07-07 | 2010-09-11 | Chimei Innolux Corp | Pulse light-adjusting circuit |
| US20080097566A1 (en) * | 2006-07-13 | 2008-04-24 | Olivier Colliou | Focused segmented electrode |
| US20080039916A1 (en) * | 2006-08-08 | 2008-02-14 | Olivier Colliou | Distally distributed multi-electrode lead |
| US8874214B2 (en) * | 2006-08-28 | 2014-10-28 | Cardiac Pacemakers, Inc. | Implantable pulse generator with a stacked capacitor, battery, and electronics |
| US7892675B1 (en) * | 2006-12-06 | 2011-02-22 | Quallion Llc | Electrochemical device having ultrasonic weld attaching weld material to electrode tab |
| US20090024184A1 (en) * | 2007-07-17 | 2009-01-22 | Nurotron Biotechnology, Inc. | Cochlear implant utilizing multiple-resolution current sources and flexible data encoding |
| US8326418B2 (en) * | 2007-08-20 | 2012-12-04 | Medtronic, Inc. | Evaluating therapeutic stimulation electrode configurations based on physiological responses |
| WO2009025816A1 (en) * | 2007-08-20 | 2009-02-26 | Medtronic, Inc. | Electrode configurations for directional leads |
| JP2010540073A (ja) * | 2007-09-27 | 2010-12-24 | カーディアック ペースメイカーズ, インコーポレイテッド | 電気刺激コンデンサを伴う埋込型リード線 |
| US8032218B2 (en) * | 2008-07-31 | 2011-10-04 | Pacesetter, Inc. | Implantable cardiac device with satellite refresh |
-
2006
- 2006-12-22 JP JP2008547586A patent/JP2009521276A/ja not_active Ceased
- 2006-12-22 EP EP06847996A patent/EP1968693A4/en not_active Withdrawn
- 2006-12-22 WO PCT/US2006/048944 patent/WO2007075974A2/en active Application Filing
- 2006-12-22 US US12/097,959 patent/US20100204766A1/en not_active Abandoned
-
2012
- 2012-05-28 JP JP2012120680A patent/JP2012157747A/ja active Pending
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS63132459A (ja) * | 1986-11-25 | 1988-06-04 | Hitachi Ltd | 容量内蔵半導体パツケ−ジ |
| JPH09199374A (ja) * | 1995-11-13 | 1997-07-31 | Shinko Electric Ind Co Ltd | 薄膜コンデンサ、これを搭載した半導体装置用パッケージおよび半導体装置 |
| JPH1041437A (ja) * | 1996-07-26 | 1998-02-13 | Fuji Electric Co Ltd | 樹脂モールド型半導体装置 |
| JP2001516980A (ja) * | 1997-09-12 | 2001-10-02 | アルフレッド イー マン ファウンデーション フォア サイエンティフィック リサーチ | 埋設可能なセンサに用いる低電力電流・周波数変換回路 |
| JP2001517056A (ja) * | 1997-09-12 | 2001-10-02 | アルフレッド イー マン ファウンデーション フォア サイエンティフィック リサーチ | 低電力整流回路 |
| JP2002043468A (ja) * | 2000-07-27 | 2002-02-08 | Fujitsu Ltd | 表裏導通基板及びその製造方法 |
| JP2004533302A (ja) * | 2001-06-14 | 2004-11-04 | アルフレッド イー マン ファウンデイション フォー サイエンティフィック リサーチ | 埋込可能型デバイス用密封給電 |
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2011524788A (ja) * | 2008-06-19 | 2011-09-08 | カーディアック ペースメイカーズ, インコーポレイテッド | 血管インターベンションカテーテルと一体化されたペースメーカー |
| US8457738B2 (en) | 2008-06-19 | 2013-06-04 | Cardiac Pacemakers, Inc. | Pacing catheter for access to multiple vessels |
| US9037235B2 (en) | 2008-06-19 | 2015-05-19 | Cardiac Pacemakers, Inc. | Pacing catheter with expandable distal end |
| JP2016198686A (ja) * | 2012-04-06 | 2016-12-01 | ボストン サイエンティフィック ニューロモデュレイション コーポレイション | 電流分配回路を用いた埋め込み型神経刺激装置の正しい動作の検証 |
| JP2016508835A (ja) * | 2013-03-05 | 2016-03-24 | ザ チャールズ スターク ドレイパー ラボラトリー インク | 補助刺激記録制御ユニットを備えた分散神経調節システム |
| JP2015000350A (ja) * | 2013-06-17 | 2015-01-05 | バイオセンス・ウエブスター・(イスラエル)・リミテッドBiosense Webster (Israel), Ltd. | 多重バイポーラサンプリング |
Also Published As
| Publication number | Publication date |
|---|---|
| EP1968693A2 (en) | 2008-09-17 |
| JP2012157747A (ja) | 2012-08-23 |
| EP1968693A4 (en) | 2011-04-27 |
| US20100204766A1 (en) | 2010-08-12 |
| WO2007075974A2 (en) | 2007-07-05 |
| WO2007075974A3 (en) | 2008-12-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2012157747A (ja) | 植え込み型集積回路 | |
| US10806932B2 (en) | Implantable medical device | |
| US8473069B2 (en) | Integrated circuit implementation and fault control system, device, and method | |
| US11724104B2 (en) | Epicardial lead design | |
| US8187161B2 (en) | Self-referencing communication in implantable devices | |
| JP5224579B2 (ja) | 能動埋め込み型医用装置用多重化電極の可制御切り替え回路 | |
| US7236821B2 (en) | Chronically-implanted device for sensing and therapy | |
| US10905886B2 (en) | Implantable medical device for deployment across the atrioventricular septum | |
| US20030149456A1 (en) | Multi-electrode cardiac lead adapter with multiplexer | |
| US8406898B2 (en) | Implantable lead with an electrostimulation capacitor | |
| US8412347B2 (en) | Methods and apparatus for leads for implantable devices | |
| US10675476B2 (en) | Internal thoracic vein placement of a transmitter electrode for leadless stimulation of the heart | |
| CN107206243A (zh) | 用于治疗心律不齐的系统和方法 | |
| WO2012054102A1 (en) | Detection of heart rhythm using an accelerometer | |
| US20220379128A1 (en) | Self-sufficient cardiac pacemaker | |
| US20050075672A1 (en) | Cardiac Stimulation Apparatus With Multiple Input Sense Amplifiers |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20091027 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20091027 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20101018 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20111129 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20120105 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20120113 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20120528 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20121128 |
|
| A045 | Written measure of dismissal of application [lapsed due to lack of payment] |
Free format text: JAPANESE INTERMEDIATE CODE: A045 Effective date: 20130322 |