JP2007196661A - 光学記録媒体及びアザシアニン色素 - Google Patents
光学記録媒体及びアザシアニン色素 Download PDFInfo
- Publication number
- JP2007196661A JP2007196661A JP2006174427A JP2006174427A JP2007196661A JP 2007196661 A JP2007196661 A JP 2007196661A JP 2006174427 A JP2006174427 A JP 2006174427A JP 2006174427 A JP2006174427 A JP 2006174427A JP 2007196661 A JP2007196661 A JP 2007196661A
- Authority
- JP
- Japan
- Prior art keywords
- group
- ring
- layer
- recording medium
- optical recording
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
- 0 CC(*1C)C(C=CCC2C)=C2N1NC=CC(C1(C)C)=[N+](C)C2(C)C1=CC=CC2 Chemical compound CC(*1C)C(C=CCC2C)=C2N1NC=CC(C1(C)C)=[N+](C)C2(C)C1=CC=CC2 0.000 description 1
- RQRMJTIEPRRUCE-YPKPFQOOSA-L CN(C(C(/N=N\c(cc(cc1)[N+]([O-])=O)c1[O-])=C(N1C)[O-])=O)C1=O Chemical compound CN(C(C(/N=N\c(cc(cc1)[N+]([O-])=O)c1[O-])=C(N1C)[O-])=O)C1=O RQRMJTIEPRRUCE-YPKPFQOOSA-L 0.000 description 1
Images
Classifications
-
- G—PHYSICS
- G11—INFORMATION STORAGE
- G11B—INFORMATION STORAGE BASED ON RELATIVE MOVEMENT BETWEEN RECORD CARRIER AND TRANSDUCER
- G11B7/00—Recording or reproducing by optical means, e.g. recording using a thermal beam of optical radiation by modifying optical properties or the physical structure, reproducing using an optical beam at lower power by sensing optical properties; Record carriers therefor
- G11B7/24—Record carriers characterised by shape, structure or physical properties, or by the selection of the material
- G11B7/241—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material
- G11B7/242—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material of recording layers
- G11B7/244—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material of recording layers comprising organic materials only
- G11B7/246—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material of recording layers comprising organic materials only containing dyes
- G11B7/247—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material of recording layers comprising organic materials only containing dyes methine or polymethine dyes
- G11B7/2472—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material of recording layers comprising organic materials only containing dyes methine or polymethine dyes cyanine
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/02—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom condensed with one carbocyclic ring
- C07D209/04—Indoles; Hydrogenated indoles
- C07D209/10—Indoles; Hydrogenated indoles with substituted hydrocarbon radicals attached to carbon atoms of the hetero ring
- C07D209/14—Radicals substituted by nitrogen atoms, not forming part of a nitro radical
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/56—Ring systems containing three or more rings
- C07D209/58—[b]- or [c]-condensed
- C07D209/60—Naphtho [b] pyrroles; Hydrogenated naphtho [b] pyrroles
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/56—Ring systems containing three or more rings
- C07D209/96—Spiro-condensed ring systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/12—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B23/00—Methine or polymethine dyes, e.g. cyanine dyes
- C09B23/10—The polymethine chain containing an even number of >CH- groups
- C09B23/105—The polymethine chain containing an even number of >CH- groups two >CH- groups
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B23/00—Methine or polymethine dyes, e.g. cyanine dyes
- C09B23/16—Methine or polymethine dyes, e.g. cyanine dyes the polymethine chain containing hetero atoms
- C09B23/162—Methine or polymethine dyes, e.g. cyanine dyes the polymethine chain containing hetero atoms only nitrogen atoms
- C09B23/164—Methine or polymethine dyes, e.g. cyanine dyes the polymethine chain containing hetero atoms only nitrogen atoms containing one nitrogen atom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B69/00—Dyes not provided for by a single group of this subclass
- C09B69/02—Dyestuff salts, e.g. salts of acid dyes with basic dyes
- C09B69/04—Dyestuff salts, e.g. salts of acid dyes with basic dyes of anionic dyes with nitrogen containing compounds
- C09B69/045—Dyestuff salts, e.g. salts of acid dyes with basic dyes of anionic dyes with nitrogen containing compounds of anionic azo dyes
-
- G—PHYSICS
- G11—INFORMATION STORAGE
- G11B—INFORMATION STORAGE BASED ON RELATIVE MOVEMENT BETWEEN RECORD CARRIER AND TRANSDUCER
- G11B7/00—Recording or reproducing by optical means, e.g. recording using a thermal beam of optical radiation by modifying optical properties or the physical structure, reproducing using an optical beam at lower power by sensing optical properties; Record carriers therefor
- G11B7/24—Record carriers characterised by shape, structure or physical properties, or by the selection of the material
- G11B7/241—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material
- G11B7/242—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material of recording layers
- G11B7/244—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material of recording layers comprising organic materials only
- G11B7/246—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material of recording layers comprising organic materials only containing dyes
- G11B7/2467—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material of recording layers comprising organic materials only containing dyes azo-dyes
-
- G—PHYSICS
- G11—INFORMATION STORAGE
- G11B—INFORMATION STORAGE BASED ON RELATIVE MOVEMENT BETWEEN RECORD CARRIER AND TRANSDUCER
- G11B7/00—Recording or reproducing by optical means, e.g. recording using a thermal beam of optical radiation by modifying optical properties or the physical structure, reproducing using an optical beam at lower power by sensing optical properties; Record carriers therefor
- G11B7/24—Record carriers characterised by shape, structure or physical properties, or by the selection of the material
- G11B7/241—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material
- G11B7/242—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material of recording layers
- G11B7/244—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material of recording layers comprising organic materials only
- G11B7/249—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material of recording layers comprising organic materials only containing organometallic compounds
- G11B7/2495—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material of recording layers comprising organic materials only containing organometallic compounds as anions
-
- G—PHYSICS
- G11—INFORMATION STORAGE
- G11B—INFORMATION STORAGE BASED ON RELATIVE MOVEMENT BETWEEN RECORD CARRIER AND TRANSDUCER
- G11B7/00—Recording or reproducing by optical means, e.g. recording using a thermal beam of optical radiation by modifying optical properties or the physical structure, reproducing using an optical beam at lower power by sensing optical properties; Record carriers therefor
- G11B7/24—Record carriers characterised by shape, structure or physical properties, or by the selection of the material
- G11B7/241—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material
- G11B7/242—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material of recording layers
- G11B7/244—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material of recording layers comprising organic materials only
- G11B7/246—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material of recording layers comprising organic materials only containing dyes
- G11B2007/24612—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material of recording layers comprising organic materials only containing dyes two or more dyes in one layer
-
- G—PHYSICS
- G11—INFORMATION STORAGE
- G11B—INFORMATION STORAGE BASED ON RELATIVE MOVEMENT BETWEEN RECORD CARRIER AND TRANSDUCER
- G11B7/00—Recording or reproducing by optical means, e.g. recording using a thermal beam of optical radiation by modifying optical properties or the physical structure, reproducing using an optical beam at lower power by sensing optical properties; Record carriers therefor
- G11B7/24—Record carriers characterised by shape, structure or physical properties, or by the selection of the material
- G11B7/241—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material
- G11B7/252—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material of layers other than recording layers
- G11B7/253—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material of layers other than recording layers of substrates
- G11B7/2533—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material of layers other than recording layers of substrates comprising resins
- G11B7/2534—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material of layers other than recording layers of substrates comprising resins polycarbonates [PC]
-
- G—PHYSICS
- G11—INFORMATION STORAGE
- G11B—INFORMATION STORAGE BASED ON RELATIVE MOVEMENT BETWEEN RECORD CARRIER AND TRANSDUCER
- G11B7/00—Recording or reproducing by optical means, e.g. recording using a thermal beam of optical radiation by modifying optical properties or the physical structure, reproducing using an optical beam at lower power by sensing optical properties; Record carriers therefor
- G11B7/24—Record carriers characterised by shape, structure or physical properties, or by the selection of the material
- G11B7/241—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material
- G11B7/252—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material of layers other than recording layers
- G11B7/254—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material of layers other than recording layers of protective topcoat layers
- G11B7/2542—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material of layers other than recording layers of protective topcoat layers consisting essentially of organic resins
-
- G—PHYSICS
- G11—INFORMATION STORAGE
- G11B—INFORMATION STORAGE BASED ON RELATIVE MOVEMENT BETWEEN RECORD CARRIER AND TRANSDUCER
- G11B7/00—Recording or reproducing by optical means, e.g. recording using a thermal beam of optical radiation by modifying optical properties or the physical structure, reproducing using an optical beam at lower power by sensing optical properties; Record carriers therefor
- G11B7/24—Record carriers characterised by shape, structure or physical properties, or by the selection of the material
- G11B7/241—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material
- G11B7/252—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material of layers other than recording layers
- G11B7/258—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material of layers other than recording layers of reflective layers
- G11B7/259—Record carriers characterised by shape, structure or physical properties, or by the selection of the material characterised by the selection of the material of layers other than recording layers of reflective layers based on silver
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Optical Record Carriers And Manufacture Thereof (AREA)
- Thermal Transfer Or Thermal Recording In General (AREA)
Abstract
Description
本発明は光学記録媒体及びアザシアニン色素に関し、より詳しくは、青色レーザーに対応が可能な耐光性に優れた光学記録媒体と、その光学記録媒体の記録層に好適に用いられるアザシアニン色素に関する。
現在、CD−R/RW(compact disc - recordable / rewritable)、DVD−R/RW(digital video disc - recordable / rewritable)、MO(magneto - optic)ディスク等の各種光学記録媒体は、大容量の情報を記憶でき、ランダムアクセスが容易であるために、コンピュータ等の情報処理装置における外部記憶装置として広く認知され普及している。これらの中で、CD−RやDVD−Rに代表される、有機色素化合物が含有される記録層を設けた有機色素系光学記録媒体は、低コストで且つ製造も容易であるという点で、優位性を有するものと考えられている。
一方、取り扱われる情報量の増大により、媒体の記録密度を高めることが望まれ、近年、開発が著しい青色レーザー光等の発振波長の短いレーザー光を用いた高密度の記録再生可能な光学記録媒体が提唱されつつある。
かかる青色レーザー光等の発振波長の短いレーザー光を用いた光学記録媒体に関しては、いくつかの報告例がある。しかしながら、記録装置や記録条件の統一がなされていない状況が続いており、望ましい光学記録媒体の像が見えにくいのが現状である。
かかる状況下において、例えば、下記特許文献1〜4には、波長405〜430nm程度の発信波長が短いレーザー光により情報の記録・再生が可能な光学記録媒体の記録層用の有機色素が示されている。
しかしながら、特許文献1〜2に記載されたような従来の青色レーザー用等の短波長用有機色素は、現在開発されている半導体レーザー、即ち、波長405nm近傍のレーザー光の吸収が少ない、或いは、有機溶媒への溶解性があまりよくない等の課題がある。特に、従来の短波長用有機色素は、その構造上、吸収波長の調整が容易ではなく、このため、それらの有機色素を記録層に含む光学記録媒体は、十分な記録感度が得られにくいなどの課題があった。
また、特許文献3〜4に記載された青色レーザー用等の短波長用有機色素は、従来のCD−RやDVD−Rと呼ばれる光学記録媒体と同様の記録メカニズム、すなわちHigh to Low記録を志向している。High to Low記録とは、未記録時の反射率が記録時に比べて高い記録方法であり、未記録部分の戻り光が多い材料が優れた記録材料とされている。しかしながら、現在開発されている青色半導体レーザーを用いた記録方法、例えばHD(High Definition)DVD−RやBD(Blu-ray Disc)−Rなどにおいては、High to Low記録の実用化は困難であるという課題がある。
本発明は上述の課題に鑑みてなされたもので、その目的は、青色レーザー等の短波長の光によって高密度の光情報の記録・再生が可能な光学記録媒体を提供するとともに、この光学記録媒体に好適に用いられる新規な色素を提供することに存する。
また、本発明のもう一つの目的は、従来と異なる記録メカニズムであるLow to High記録によって高密度の光情報の記録・再生が可能な光学記録媒体を提供するとともに、この光学記録媒体に好適に用いられる新規な色素を提供することに存する。なお、「Low to High記録」とは、未記録時よりも記録時の反射率が高い記録方法であり、当該記録方法においては、未記録時の反射率を低くすることが望ましい。
また、本発明のもう一つの目的は、従来と異なる記録メカニズムであるLow to High記録によって高密度の光情報の記録・再生が可能な光学記録媒体を提供するとともに、この光学記録媒体に好適に用いられる新規な色素を提供することに存する。なお、「Low to High記録」とは、未記録時よりも記録時の反射率が高い記録方法であり、当該記録方法においては、未記録時の反射率を低くすることが望ましい。
本発明者らは鋭意検討の結果、特定の構造を有するアザシアニン色素を光学記録媒体の記録層に用いることにより、青色レーザー等の短波長の光によって高密度の光情報の記録・再生が可能となり、特にLow to High記録による新たな光学記録媒体の実用化が可能となることを見出し、本発明を完成させた。
即ち、本発明の要旨は、基板と、前記基板上に設けられ、光が照射されることにより情報の記録又は再生が可能な記録層とを少なくとも有し、該記録層が、下記一般式[I]で示されるアザシアニン色素を含有することを特徴とする、光学記録媒体に存する(請求項1)。
(一般式[I]中、
R1及びR2はそれぞれ独立して、水素原子、又は、置換されていてもよい炭素数1〜4の直鎖若しくは分岐のアルキル基を表わす。また、R1及びR2が互いに結合して、環を形成していてもよい。
R3は、水素原子、又は、炭化水素基を表わす。また、R3が炭化水素基である場合、R3を介して2以上の一般式[I]の化合物が架橋されていてもよい。
R4は、水素原子、又は、炭素数1〜4の直鎖又は分岐のアルキル基を表わす。
R5は、置換されていてもよい芳香環基、又は、置換されていてもよい不飽和複素環基を表わす。また、R5を介して2以上の一般式[I]の化合物が結合されていてもよい。
但し、R4とR5とは互いに結合して、環構造を形成していてもよい。
X-は、対アニオンを表わす。
Aで示されるベンゼン環は、置換されていてもよい。)
R1及びR2はそれぞれ独立して、水素原子、又は、置換されていてもよい炭素数1〜4の直鎖若しくは分岐のアルキル基を表わす。また、R1及びR2が互いに結合して、環を形成していてもよい。
R3は、水素原子、又は、炭化水素基を表わす。また、R3が炭化水素基である場合、R3を介して2以上の一般式[I]の化合物が架橋されていてもよい。
R4は、水素原子、又は、炭素数1〜4の直鎖又は分岐のアルキル基を表わす。
R5は、置換されていてもよい芳香環基、又は、置換されていてもよい不飽和複素環基を表わす。また、R5を介して2以上の一般式[I]の化合物が結合されていてもよい。
但し、R4とR5とは互いに結合して、環構造を形成していてもよい。
X-は、対アニオンを表わす。
Aで示されるベンゼン環は、置換されていてもよい。)
ここで、上記一般式[I]中、R4が水素原子であり、R5が置換されていてもよいフェニル基であることが好ましい(請求項2)。
また、上記一般式[I]中、R4が水素原子であり、R5が置換されていてもよい5員又は6員の不飽和複素環基であることも好ましい(請求項3)。
また、上記一般式[I]中、R4とR5とが互いに結合して、5員又は6員の飽和炭化水素環又は飽和複素環を形成していることも好ましい(請求項4)。
また、R5がフェニル基の場合、置換基を有さないことが好ましい(請求項5)。
また、一般式[I]中、X-が下記一般式[II]で表わされるアゾ系金属錯体の陰イオンであることが好ましい(請求項6)。
(一般式[II]中、環C及び環Dは、各々独立に、芳香族環又は複素環を表わす。但し、環C及び環Dのうち少なくとも一方の環は複素環である。Y及びZは、各々独立に、活性水素を有する基を表わす。Mは、3価の金属元素を表わす。)
また、該記録層が、波長350nm〜530nmのレーザー光により情報の記録又は再生が行なわれるものであることが好ましい(請求項7)。
本発明の光学記録媒体及び本発明のアザシアニン色素によれば、青色レーザー等の短波長の光によって高密度の光情報の記録・再生が可能である。また、従来と異なる記録メカニズムであるLow to High記録によって高密度の光情報の記録・再生が可能である。
以下、本発明の実施の形態について詳細に説明するが、本発明は以下の説明に限定されるものではなく、その要旨の範囲内において種々に変更して実施することができる。
本発明の光学記録媒体は、基板と、前記基板上に設けられ、光が照射されることにより情報の記録又は再生が可能な記録層とを有し、前記記録層が、後述の一般式[I]で示されるアザシアニン色素を含有するものである。以下の記載では説明の便宜上、まずは本発明の光学記録媒体の記録層に含有されるアザシアニン色素について説明し、続いて本発明の光学記録媒体の説明に移るものとする。
[I.アザシアニン色素]
本発明の光学記録媒体は、その記録層に、下記一般式[I]で表わされるアザシアニン色素を含有する(以下適宜「式[I]のアザシアニン色素」と略称する。)。式[I]のアザシアニン色素は、波長350nm〜530nmの青色光領域に適度の吸収を有するため、青色レーザー光による記録に適し、実用に耐え得る耐光性を有する色素化合物である。
本発明の光学記録媒体は、その記録層に、下記一般式[I]で表わされるアザシアニン色素を含有する(以下適宜「式[I]のアザシアニン色素」と略称する。)。式[I]のアザシアニン色素は、波長350nm〜530nmの青色光領域に適度の吸収を有するため、青色レーザー光による記録に適し、実用に耐え得る耐光性を有する色素化合物である。
(一般式[I]中、
R1及びR2はそれぞれ独立して、水素原子、又は、炭素数1〜4の直鎖若しくは分岐のアルキル基を表わす。また、R1及びR2が互いに結合して、環を形成していてもよい。
R3は、水素原子、又は、炭化水素基を表わす。また、R3が炭化水素基である場合、R3を介して2以上の一般式[I]の化合物が架橋されていてもよい。
R4は、水素原子、又は、炭素数1〜4の直鎖又は分岐のアルキル基を表わす。
R5は、置換されていてもよい芳香環基、又は、置換されていてもよい不飽和複素環基を表わす。また、R5を介して2以上の一般式[I]の化合物が結合されていてもよい。
但し、R4とR5とは互いに結合して、環構造を形成していてもよい。
X-は、対アニオンを表わす。
Aで示されるベンゼン環は、置換されていてもよい。)
R1及びR2はそれぞれ独立して、水素原子、又は、炭素数1〜4の直鎖若しくは分岐のアルキル基を表わす。また、R1及びR2が互いに結合して、環を形成していてもよい。
R3は、水素原子、又は、炭化水素基を表わす。また、R3が炭化水素基である場合、R3を介して2以上の一般式[I]の化合物が架橋されていてもよい。
R4は、水素原子、又は、炭素数1〜4の直鎖又は分岐のアルキル基を表わす。
R5は、置換されていてもよい芳香環基、又は、置換されていてもよい不飽和複素環基を表わす。また、R5を介して2以上の一般式[I]の化合物が結合されていてもよい。
但し、R4とR5とは互いに結合して、環構造を形成していてもよい。
X-は、対アニオンを表わす。
Aで示されるベンゼン環は、置換されていてもよい。)
以下、前記一般式[I]におけるR1〜R5の各々について説明する。
なお、R1〜R5の説明において「置換されていてもよい」と言う場合、その置換基には、特に断りのある場合を除き、水酸基やスルホン酸基等の水溶性基は原則として含まれないものとする。これは、色素化合物が光学記録媒体の記録層に含有され得るためには、まず、有機溶媒に対してある程度の溶解性を有することが必要とされるからである。更に、そのような記録層が、ある程度の耐水性を有する安定な膜であることが、光ディスクの実用上、必要とされるからである。
なお、R1〜R5の説明において「置換されていてもよい」と言う場合、その置換基には、特に断りのある場合を除き、水酸基やスルホン酸基等の水溶性基は原則として含まれないものとする。これは、色素化合物が光学記録媒体の記録層に含有され得るためには、まず、有機溶媒に対してある程度の溶解性を有することが必要とされるからである。更に、そのような記録層が、ある程度の耐水性を有する安定な膜であることが、光ディスクの実用上、必要とされるからである。
前記一般式[I]中、R1及びR2はそれぞれ独立して、水素原子、又は、置換されていてもよい炭素数1〜4の直鎖若しくは分岐のアルキル基を表わす。また、R1とR2とが結合して環を形成していてもよい。炭素数1〜4の直鎖若しくは分岐のアルキル基としては、例えば、メチル基、エチル基、プロピル基、イソプロピル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基などが挙げられる。
R1又はR2が炭素数1〜4の直鎖若しくは分岐のアルキル基の場合、置換基としては、例えば、アズレン環、キノリン環、シクロプロパン環、シクロブタン環、シクロペンタン環、シクロヘキサン環、シクロヘキセン環、ナフタレン環、チオフェン環、ベンゼン環、ピペリジン環、ピリジン環、ピロリジン環、ピロール環、フラン環などの飽和又は不飽和の環状基や、ハロゲン原子(フッ素原子、塩素原子、臭素原子等)などが挙げられる。これらの中でも、ベンゼン環、ナフタレン環が置換基として好ましく、また、R1又はR2としては、炭素数1又は2のアルキル基にベンゼン環が結合したものが特に好ましい。
R1とR2とが結合して環を形成する場合の環としては、例えば、シクロブタン環、シクロペンタン環、シクロヘキサン環、シクロヘキセン環、シクロヘプタン環などの飽和又は不飽和の環状構造を形成する。
R1とR2とが結合して環を形成する場合の環としては、例えば、シクロブタン環、シクロペンタン環、シクロヘキサン環、シクロヘキセン環、シクロヘプタン環などの飽和又は不飽和の環状構造を形成する。
R1又はR2が環状の置換基を有する場合の環、および、R1とR2が結合して環を形成する場合の環には、一又は複数の置換基を有していてもよい。その場合の置換基としては、例えば、メチル基、エチル基、プロピル基、イソプロピル基、イソプロペニル基、1−プロペニル基、2−プロペニル基、2−プロピニル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、2−ブテニル基、1,3−ブタジエニル基、ペンチル基、イソペンチル基、ネオペンチル基、tert−ペンチル基、1−メチルペンチル基、2−メチルペンチル基、2−ペンテン−4−イニル基等の脂肪族炭化水素基、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロヘキセニル基などの脂環式炭化水素基、フェニル基、o−トリル基、m−トリル基、p−トリル基、キシリル基、メシチル基、o−クメニル基、m−クメニル基、p−クメニル基、ビフェニリル基などの芳香族炭化水素基、フルオロ基、クロロ基、ブロモ基、ヨード基などのハロゲン基、更には、それらの組み合わせによる置換基が挙げられる。
前記一般式[I]中、R3は、水素原子、又は、炭化水素基を表わす。R3が炭化水素基である場合、置換されていてもよい炭素数1〜6の直鎖若しくは分岐のアルキル基が好ましい。
また、R3が炭化水素基である場合、R3を介して2以上の一般式[I]の化合物が架橋されていてもよい。2以上の一般式[I]の化合物をR3を介して架橋する場合におけるR3としては、炭素数1〜6の直鎖若しくは分岐のアルキル基のほか、これより炭素数の多いアルキル基やフェニレン基等も用いることができる。
また、R3が炭化水素基である場合、R3を介して2以上の一般式[I]の化合物が架橋されていてもよい。2以上の一般式[I]の化合物をR3を介して架橋する場合におけるR3としては、炭素数1〜6の直鎖若しくは分岐のアルキル基のほか、これより炭素数の多いアルキル基やフェニレン基等も用いることができる。
尚、R1〜R3がアルキル基の場合に有していてもよい置換基としては、本発明の趣旨に反するものでない限り特に制限されないが、ハロゲン原子(フッ素原子、塩素原子、臭素原子等)、アルコキシ基(メトキシ基、エトキシ基等)、アルキルアミノ基(ジメチルアミノ基、ジエチルアミノ基等)、アリール基(フェニル基、ナフチル基等)などが挙げられる。ハロゲン原子はハロゲン系溶媒との親和性向上、アルコキシ基やアルキルアミノ基等の極性基は極性溶媒の溶媒和向上、アリール基は立体障害による色素分子同士の会合抑制により、何れも溶媒への溶解性向上が期待できるためである。
前記一般式[I]中、R4は、水素原子、又は、炭素数1〜4の直鎖又は分岐のアルキル基を表わす。中でも、水素原子であることが好ましい。
前記一般式[I]中、R5は、置換されていてもよい芳香環基、又は、置換されていてもよい不飽和複素環基を表わす。なお、本明細書において「芳香環基」及び「複素環基」とは、それぞれ、芳香環及び複素環から水素原子を一つ除いて得られる基をいうものとする。
得られる色素の有機溶媒への溶解性を向上させる観点からは、R5は、不飽和複素環基であることが好ましい。
R5が不飽和複素環基の場合、環の員数は5員又は6員が好ましい。4員以下の環状構造は一般に不安定で、7員以上の環状構造は合成が煩雑となるからである。
R5が不飽和複素環基の場合、環の員数は5員又は6員が好ましい。4員以下の環状構造は一般に不安定で、7員以上の環状構造は合成が煩雑となるからである。
R5が芳香環基の場合、具体的にはフェニル基が好ましい。
芳香環基や不飽和複素環基の場合は、アルキル基等の場合に比較して、得られる色素の光吸収が長波長となり、青色レーザーの発振波長である405nmの吸収が大きくなる。
芳香環基や不飽和複素環基の場合は、アルキル基等の場合に比較して、得られる色素の光吸収が長波長となり、青色レーザーの発振波長である405nmの吸収が大きくなる。
R5が不飽和複素環基の場合、その種類は特に制限されないが、ヘテロ原子として窒素原子、酸素原子、硫黄原子等を含有する複素環基が挙げられる。例えば、R5が、以下の式で表わされる不飽和複素環基の場合には、吸収の波長を調節することが可能となるので好ましい。
R5が芳香環基又は不飽和複素環基の場合、これらは置換基を有していてもよい。置換基としては、本発明の趣旨に反するものでない限り特に制限されないが、好ましい例としては、炭素数1〜8の直鎖又は分岐のアルキル基、フッ化アルキル基、アルコキシ基、アルキルチオ基等が挙げられる。何故ならば、これらの基の場合には、塗布溶媒に対する溶解性が向上し、薄膜での結晶化も起こり難いからである。中でも、炭素数1〜5の直鎖又は分岐のアルキル基、−CF3、−OCF3、−SCF3、−SC2F5、−OCH3、−O−(iso−C3H7)等が特に好ましい。
また、R5が芳香環基又は不飽和複素環基の場合、これらは更に縮合環を有していてもよい。縮合環の種類は本発明の趣旨に反するものでない限り特に制限されないが、5員又は6員の芳香環又は複素環が好ましい。また、この縮合環が上記例示の置換基を有していてもよい。
また、R5を介して2以上の一般式[I]の化合物が結合されていてもよい。
また、R5を介して2以上の一般式[I]の化合物が結合されていてもよい。
また、R4とR5とは互いに結合して、環構造を形成していてもよい。かかる環構造を形成することにより結晶化が抑制され、有機溶媒への溶解性が得られる場合があるので好ましい。環構造の種類は特に制限されないが、環の員数は5員又は6員が好ましい。4員以下の環状構造は一般に不安定で、7員以上の環状構造は合成が煩雑となるからである。また、R4とR5とが結合する窒素原子以外の環骨格原子は、全て炭素原子であってもよく、ヘテロ原子として窒素原子、酸素原子、硫黄原子等を含有していてもよい。
R4とR5とが環構造を形成する場合、この環構造は置換基を有していてもよい。置換基の種類は特に制限されないが、例としては、R5が芳香環基又は複素環基の場合に有していてもよい置換基として先に例示した各種の置換基が挙げられる。
また、R4とR5とが環構造を形成する場合、この環構造は更に縮合環を有していてもよい。縮合環の種類は特に制限されないが、例としては、R5が芳香環基又は複素環基の場合に有していてもよい縮合環として先に例示した各種の縮合環が挙げられる。更には、この縮合環が上記例示の置換基を有していてもよい。
また、R4とR5とが環構造を形成する場合、この環構造を介して2以上の一般式[I]の化合物が結合されていてもよい。
また、R4とR5とが環構造を形成する場合、この環構造を介して2以上の一般式[I]の化合物が結合されていてもよい。
前記一般式[I]中、Aで示されるベンゼン環は、置換されていてもよい。その場合の置換基としては、Cl、Br等のハロゲン原子、炭素数1〜4の直鎖又は分岐のアルキル基、アセチルアミノ基、炭素数1〜4のアルコキシ基等が挙げられる。ベンゼン環Aは、更に縮合環を有していてもよい。縮合環の種類は特に制限されないが、ベンゼン環が好ましい。
前記一般式[I]中、X-は、対アニオンを表わす。1価のアニオンであれば特に限定されないが、使用しやすいものとしては、I-、Cl-、Br-、BF4 -、PF6 -、SbF6 -、CH3SO3 -、
等が挙げられる。
また、X-としては、陰電荷を有する金属錯体を好適に用いることが出来る。個々の金属錯体としては、例えば、アセチルアセトナートキレート系、アゾ系、サリチルアルデヒドオキシム系、ジインモニウム系、ジチオール系、ジピロメテン系、スクアリリウム系、チオカテコールキレート系、チオビスフェノレートキレート系、ビスジチオ−α−ジケトンキレート系、ビスフェニレンジチオール系、ホルマザン系の遷移金属キレートなどが挙げられる。これらのうち、耐光性及び溶剤に対する溶解性の点で、アゾ金属錯体が好ましい。上記例示等の金属錯体における遷移元素としては、例えば、バナジウム、ニオブ、タンタル、クロム、モリブデン、タングステン、マンガン、テクネチウム、レニウム、鉄、ルテニウム、オスミウム、コバルト、ロジウム、イリジウム、ニッケル、パラジウム、白金、銅、銀、金、亜鉛、カドミウム、水銀などが挙げられる。これらのうち、経済性及び生体に対する影響の点で、バナジウム、マンガン、コバルト、銅が好ましい。
X-として好ましいアゾ金属錯体の陰イオンとしては、下記一般式[II]で表わされるアゾ系金属錯体の陰イオンが挙げられる。
一般式[II]中、環C及び環Dは、各々独立に、芳香族環又は複素環を表わす。但し、環C及び環Dのうち少なくとも一方の環は複素環である。Y及びZは、各々独立に、活性水素を有する基を表わす。Mは、3価の金属元素を表わす。Y及びZの活性水素が脱離してアゾ系配位子が−2の電荷を有し、このアゾ系配位子2個と+3の電荷の金属原子1個から全体で−1の電荷の金属錯体が形成される。
前記一般式[II]中、C及びDで表わされる環は、芳香族環又は不飽和若しくは飽和の複素環であり、Y及びZ以外の置換基を更に有していてもよい。C及びDで表わされる環の種類は特に限定されないが、例えば、ベンゼン、ナフタレン等の芳香族環;ピリジン、ピリミジン、チオフェン等の不飽和複素環;メルドラム酸、バルビツール酸、ピリドン等の飽和複素環;などが挙げられる。
前記一般式[II]中、Y及びZで表わされる基は、活性水素を有する基であり、プロトンが脱離して陰電荷を有するものであればよい。Y及びZで表わされる基の種類は特に限定されないが、例えば、カルボン酸、スルホン酸、アミノ基、水酸基、アミド基、ボロン酸、リン酸などが挙げられる。また、環内に基が含まれていてもよい。
前記一般式[II]中、Mで表わされる元素は、3価の金属元素である。アゾ系配位子の有する基Y、Z及びアゾ結合の窒素原子の一つが金属に配位すると仮定すれば、1個の金属元素に3配座の配位子を2個有する金属錯体が、6配座で安定化すると考えられる。そのため、−2の配位子が2個と、+3の金属が1個とからなるアゾ系金属錯体は、最も安定であり、且つ、一般式[I]で表わされるアザシアニン色素と等モルで対になることができるので好ましい。
上記一般式[II]で表わされるアゾ系金属錯体の陰イオンの中でも好ましいものとしては、例えば、下記一般式[II−1]〜[II−4]で表わされるアゾ金属錯体の陰イオンが挙げられる。
上記一般式[II−1]〜[II−4]において、Mは、周期律表の第5〜12族に属する遷移元素を表わす。
上記一般式[II−1]〜[II−4]におけるR11、R12、R14〜R17、R19〜R22、R25及びR26は、炭化水素基を表わす。同一分子内におけるこれらの炭化水素基は、互いに同一であってもよく、異なっていてもよい。個々の炭化水素基の種類は特に制限されず、脂肪族炭化水素基でも脂環式炭化水素基でもよい。脂肪族炭化水素基の例としては、炭素数1〜6の直鎖状又は分枝鎖状の脂肪族炭化水素基、例えば、メチル基、エチル基、プロピル基、イソプロピル基、イソプロペニル基、1−プロペニル基、2−プロペニル基、2−プロピニル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、2−ブテニル基、1,3−ブタジエニル基、ペンチル基、イソペンチル基、ネオペンチル基、tert−ペンチル基、1−メチルペンチル基、2−メチルペンチル基、2−ペンテン−4−イニル基等が挙げられる。脂環式炭化水素基の例としては、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロヘキセニル基等が挙げられる。斯かる炭化水素基は、その一又は複数の水素原子が、例えば、フッ素原子、塩素原子、臭素原子等のハロゲン原子によって置換されていてもよい。上記一般式[II−1]〜[II−4]のアゾ系金属錯体陰イオンを有する式[I]のアザシアニン色素は、溶剤の種類にもよるが、通常はR11、R12、R14〜R17、R19〜R22、R25及びR26の炭素数が多くなるほど、溶剤に対する溶解性が増大する。
上記一般式[II−1]、[II−3]、[II−4]におけるR10、R13、R18、R23、R24及びR27は、水素原子又は置換基を表わす。同一分子内におけるこれらの置換基は、互いに同一であってもよく、異なっていてもよい。個々の置換基の例としては、例えば、メチル基、エチル基、プロピル基、イソプロピル基、イソプロペニル基、1−プロペニル基、2−プロペニル基、2−プロピニル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、2−ブテニル基、1,3−ブタジエニル基、ペンチル基、イソペンチル基、ネオペンチル基、tert−ペンチル基、1−メチルペンチル基、2−メチルペンチル基、2−ペンテン−4−イニル基等の脂肪族炭化水素基;シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロヘキセニル基等の脂環式炭化水素基;フェニル基、o−トリル基、m−トリル基、p−トリル基、キシリル基、メシチル基、o−クメニル基、m−クメニル基、p−クメニル基、ビフェニリル基等の芳香族炭化水素基;メトキシ基、エトキシ基、プロポキシ基、イソプロポキシ基、ブトキシ基、イソブトキシ基、sec−ブトキシ基、tert−ブトキシ基、ペンチルオキシ基、フェノキシ基等のエーテル基;メトキシカルボニル基、エトキシカルボニル基、プロポキシカルボニル基、アセトキシ基、ベンゾイルオキシ基等のエステル基、ジメチルアミノ基、ジエチルアミノ基、ジプロピルアミノ基、ジイソプロピルアミノ基、ジブチルアミノ基、ジペンチルアミノ基等のアミノ基;フッ素原子、塩素原子、臭素原子、ヨウ素原子等のハロゲン原子;ヒドロキシ基、カルボキシ基、シアノ基、ニトロ基等;更には前記例示置換基が複数結合してなる置換基などが挙げられる。
なお、上記一般式[II−1]、[II−2]で表わされるアゾ金属錯体の陰イオンにおいて、二つのニトロ基が結合する位置は、アゾ基に対してオルト位、メタ位、パラ位の何れであっても構わないが、合成上の観点からはメタ位であることが好ましい。
上記式[I]のアザシアニン色素は、置換基の導入が可能な部位が多く、また、その置換基の電子吸引性或いは電子供与性などの効果が、π電子系の共役により伝わりやすいため、波長の調整が容易であるという特徴を有する。たとえば、R5が芳香環基又は複素環基の場合に有する置換基や、R4とR5とが環構造を形成する場合に有する置換基を適切に選択することにより、およそ350nm〜450nmまで吸収極大の波長を変えることが可能である。従って、記録光波長に大きな吸収を持たせることが可能であり、その結果、記録感度が向上するのである。
式[I]のアザシアニン色素の好ましい例としては、下記の構造式(1)〜(3)、(5)、(6)、(8)〜(16)、(20)〜(37)で示される化合物が挙げられる(なお、以下の記載では、各構造式で示される化合物を、その構造式の番号を付して「例示化合物(1)」等のように略称する場合がある。)。但し、以下の化合物はあくまでも例示であって、本発明の光記録媒体に使用可能な式[I]のアザシアニン色素はこれらに限定される訳ではない。
なお、上記例示化合物(13)のように、R5としてチアゾール環基を有する化合物は、溶解性の向上が期待されるという理由で好ましい。
また、例示化合物(8)のように、R5として、複素環にベンゼン環が縮合した基を有する化合物は、親水性が低下するので色素としての安定性が増す(加水分解性が低下する)という利点がある。
また、例示化合物(8)のように、R5として、複素環にベンゼン環が縮合した基を有する化合物は、親水性が低下するので色素としての安定性が増す(加水分解性が低下する)という利点がある。
以上の例示化合物(1)〜(3)、(5)、(6)、(8)〜(16)、(20)〜(37)の中でも、光学記録媒体の記録層に用いた場合に上述の効果がより顕著に得られるという観点から、例示化合物(1)〜(3)、(6)、(15)及び(20)〜(23)が好ましい。また、例示化合物(24)〜(30)も好ましい。
特に、例示化合物(27)及び(28)に代表される、下記式(i)で表わされるアザシアニン色素(これらを適宜「本発明のアザシアニン色素」という。)は、新規な構造の色素化合物であり、且つ、光学記録媒体の記録層に用いた場合に上述の効果がとりわけ顕著に得られるという観点から、極めて好ましい。
なお、上記式[I]のアザシアニン色素の合成方法は、特に制限されるものではないが、例えば、2−(1,3,3−トリメチルインドリン−2−イリデン)アセトアルデヒド{2-(1,3,3-Trimethylindolin-2-ylidene)acetaldehyde}とアミン化合物を酢酸中で加熱し、反応混合物を水中に放出した後に塩析する方法(K. Venkataraman, The Chemistry of Synthetic Dyes Volume II, 1952, Academic Press, pp.1175等参照)により合成することができる。
[II.光学記録媒体]
本発明の光学記録媒体は、基板と、前記基板上に設けられ、光が照射されることにより情報の記録又は再生が可能な記録層とを少なくとも有し、前記記録層が、上記一般式[I]のアザシアニン色素を含有するものである。必要に応じて、更に、下引き層、反射層、保護層など、基板及び記録層以外の層を有していてもよい。
本発明の光学記録媒体は、基板と、前記基板上に設けられ、光が照射されることにより情報の記録又は再生が可能な記録層とを少なくとも有し、前記記録層が、上記一般式[I]のアザシアニン色素を含有するものである。必要に応じて、更に、下引き層、反射層、保護層など、基板及び記録層以外の層を有していてもよい。
以下、本発明の光学記録媒体について、実施形態を挙げて具体的に説明するが、以下の実施形態はあくまでも説明のために挙げるものであって、本発明は以下の実施形態に制限されず、本発明の趣旨に反しない限り自由に変形して実施することが可能である。
まず、本発明の第1実施形態について説明する。図1(a)は、本発明の第1実施形態に係る光記録媒体の層構成の一例を模式的に表わす部分断面図である。図1(a)に示される光学記録媒体10は、光透過性材料からなる基板1と、基板1上に設けられた記録層2と、記録層2上に積層された反射層3及び保護層4とが順番に積層された構造を有している。光学記録媒体10は、基板1側から照射されるレーザー光Lにより、情報の記録・再生が行われる。
なお、説明の便宜上、光学記録媒体10において、保護層4が存在する側を上方、基板1が存在する側を下方とし、これらの方向に対応する各層の各面を、それぞれ各層の上面及び下面とする。
基板1の材料としては、基本的に記録光及び再生光の波長において透明な材料であれば、様々な材料を使用することができる。具体的には、例えば、アクリル系樹脂、メタクリル系樹脂、ポリカーボネート樹脂、ポリオレフィン系樹脂(特に、非晶質ポリオレフィン)、ポリエステル系樹脂、ポリスチレン樹脂、エポキシ樹脂等の樹脂;ガラス等が挙げられる。また、ガラス上に光硬化性樹脂等の放射線硬化性樹脂からなる樹脂層を設けた構造の基板を用いることもできる。中でも、高生産性、コスト、耐吸湿性等の観点からは、射出成型法にて使用されるポリカーボネート樹脂、耐薬品性及び耐吸湿性等の観点からは、非晶質ポリオレフィンが好ましい。更に、高速応答等の観点からは、ガラスが好ましい。
樹脂製の基板1を使用した場合、又は、記録層と接する側(上側)に樹脂層を設けた基板1を使用した場合には、上面に、記録再生光の案内溝やピットを形成してもよい。案内溝の形状としては、光学記録媒体10の中心を基準とした同心円状の形状やスパイラル状の形状が挙げられる。スパイラル状の案内溝を形成する場合には、溝ピッチが0.2〜1.2μm程度であることが好ましい。
記録層2は、基板1の上側に直接、又は必要に応じて基板1上に設けた下引き層等の上側に形成される層であって、上記式[I]のアザシアニン色素を含有する。式[I]のアザシアニン色素は、いずれか一種を単独で使用してもよく、二種以上を任意の組み合わせ及び比率で併用してもよい。
更に、記録層2には、式[I]のアザシアニン色素に加え、必要に応じて他系統の色素を併用することもできる。他系統の色素としては、主として記録用レーザー光の発振波長域に適度な吸収を有するものであればよく、特に制限されない。また、CD−R等に使用され、770〜830nmの波長帯域中に発振波長を有する近赤外レーザー光を用いた記録・再生に適する色素や、DVD−R等に使用され、620〜690nmの波長帯域中に発振波長を有する赤色レーザー光を用いた記録・再生に適する色素等を、式[I]のアザシアニン色素と併用して記録層2に含有させることにより、異なる波長帯域に属する複数種のレーザー光を用いた記録・再生に対応する光学記録媒体10を製造することもできる。また、上記CD−R用或いはDVD−R用の色素の中で耐光性が良好なものを選び、式[I]のアザシアニン色素と併用することにより、耐光性を更に向上させることが可能となる。
式[I]のアザシアニン色素以外の他系統の色素としては、含金属アゾ系色素、ベンゾフェノン系色素、フタロシアニン系色素、ナフタロシアニン系色素、シアニン系色素、アゾ系色素、スクアリリウム系色素、含金属インドアニリン系色素、トリアリールメタン系色素、メロシアニン系色素、アズレニウム系色素、ナフトキノン系色素、アントラキノン系色素、インドフェノール系色素、キサンテン系色素、オキサジン系色素、ピリリウム系色素等が挙げられる。
また、記録層2には、式[I]のアザシアニン色素に加えて、安定性や耐光性の向上のために、一重項酸素クエンチャーとして遷移金属キレート化合物(例えば、アセチルアセトナートキレート、ビスフェニルジチオール、サリチルアルデヒドオキシム、ビスジチオ−α−ジケトン等)等を含有させたり、記録感度の向上のために、金属系化合物等の記録感度向上剤を含有させたりしてもよい。ここで、金属系化合物とは、遷移金属等の金属が原子、イオン、クラスター等の形で化合物に含まれるものを言い、例えばエチレンジアミン系錯体、アゾメチン系錯体、フェニルヒドロキシアミン系錯体、フェナントロリン系錯体、ジヒドロキシアゾベンゼン系錯体、ジオキシム系錯体、ニトロソアミノフェノール系錯体、ピリジルトリアジン系錯体、アセチルアセトナート系錯体、メタロセン系錯体、ポルフィリン系錯体のような有機金属化合物が挙げられる。金属原子としては特に限定されないが、遷移金属であることが好ましい。
更に、必要に応じてバインダー、レベリング剤、消泡剤等を併用することもできる。好ましいバインダーとしては、ポリビニルアルコール、ポリビニルピロリドン、ニトロセルロース、酢酸セルロース、ケトン系樹脂、アクリル系樹脂、ポリスチレン系樹脂、ウレタン系樹脂、ポリビニルブチラール、ポリカーボネート、ポリオレフィン等が挙げられる。これらは何れか一種を単独で用いてもよく、二種以上を任意の組み合わせ及び比率で併用してもよい。
記録層2の成膜方法としては、真空蒸着法、スパッタリング法、ドクターブレード法、キャスト法、スピンコート法、浸漬法等、一般に行なわれている様々な薄膜形成法が挙げられる。量産性やコストの観点からは、スピンコート法が好ましく、均一な厚みの記録層2が得られるという観点からは、塗布法よりも真空蒸着法等の方が好ましい。スピンコート法による成膜の場合、回転数は500〜15000rpmが好ましい。また、場合によっては、スピンコートの後に、加熱する、溶媒蒸気にあてる等の処理を施してもよい。
ドクターブレード法、キャスト法、スピンコート法、浸漬法等の塗布法により記録層2を形成する場合に、式[I]のアザシアニン色素を溶解させて基板1に塗布するために使用する塗布溶媒は、基板1を侵食しない溶媒であれば特に限定されない。具体的には、例えばジアセトンアルコール、3−ヒドロキシ−3−メチル−2−ブタノン等のケトンアルコール系溶媒;メチルセロソルブ、エチルセロソルブ等のセロソルブ系溶媒;n−ヘキサン、n−オクタン等の鎖状炭化水素系溶媒;シクロヘキサン、メチルシクロヘキサン、エチルシクロヘキサン、ジメチルシクロヘキサン、n−ブチルシクロヘキサン、tert−ブチルシクロヘキサン、シクロオクタン等の環状炭化水素系溶媒;テトラフルオロプロパノール、オクタフルオロペンタノール、ヘキサフルオロブタノール等のパーフルオロアルキルアルコール系溶媒;乳酸メチル、乳酸エチル、2−ヒドロキシイソ酪酸メチル等のヒドロキシカルボン酸エステル系溶媒等が挙げられる。これらは何れか一種を単独で用いてもよく、二種以上を任意の組み合わせ及び比率で併用してもよい。
真空蒸着法を用いる場合には、例えば、式[I]のアザシアニン色素と、必要に応じて他の色素や各種添加剤等の記録層成分とを、真空容器内に設置されたるつぼに入れ、この真空容器内を適当な真空ポンプで10-2〜10-5Pa程度にまで排気した後、るつぼを加熱して記録層成分を蒸発させ、るつぼと向き合って置かれた基板上に蒸着させることによって、記録層2を形成する。
記録層2の膜厚は、記録方法等により適した膜厚が異なる為、特に限定するものではないが、記録を可能とするためにはある程度の膜厚が必要とされるため、通常、少なくとも1nm以上であり、好ましくは5nm以上である。但し、あまり厚すぎても記録が良好に行なえなくなる場合があるので、通常300nm以下、好ましくは200nm以下、より好ましくは100nm以下である。
反射層3は、記録層2の上に形成されている。反射層3の膜厚は、好ましくは50nm〜300nmである。反射層3の材料としては、再生光の波長において十分高い反射率を有する材料、例えば、Au、Al、Ag、Cu、Ti、Cr、Ni、Pt、Ta、Pd等の金属を、単独或いは合金にして用いることができる。これらの中でもAu、Al、Agは反射率が高く、反射層3の材料として適している。また、これらの金属を主成分とした上で、加えて他の材料を含有させてもよい。ここで「主成分」とは、含有率が50重量%以上のものをいう。主成分以外の他の材料としては、例えば、Mg、Se、Hf、V、Nb、Ru、W、Mn、Re、Fe、Co、Rh、Ir、Cu、Zn、Cd、Ga、In、Si、Ge、Te、Pb、Po、Sn、Bi、Ta、Ti、Pt、Pd、Nd等の金属及び半金属を挙げることができる。中でもAgを主成分とするものは、コストが安い点、高反射率が出やすい点、後述する印刷受容層を設けた場合に地色が白く美しいものが得られる点等から、特に好ましい。例えば、AgにAu、Pd、Pt、Cu、及びNdから選ばれる一種以上を0.1原子%〜5原子%程度含有させた合金は、高反射率、高耐久性、高感度且つ低コストであり好ましい。具体的には、例えば、AgPdCu合金、AgCuAu合金、AgCuAuNd合金、AgCuNd合金等である。金属以外の材料としては、低屈折率薄膜と高屈折率薄膜を交互に積み重ねて多層膜を形成し、これを反射層3として用いることも可能である。
反射層3を形成する方法としては、例えば、スパッタリング法、イオンプレーティング法、化学蒸着法、真空蒸着法等が挙げられる。また、基板1の上や反射層3の下に、反射率の向上、記録特性の改善、密着性の向上等のために、公知の無機系又は有機系の中間層、接着層を設けることもできる。
保護層4は、反射層3の上に形成される。保護層4の材料は、反射層3を外力から保護するものであれば、特に限定されない。有機物質の材料としては、熱可塑性樹脂、熱硬化性樹脂、電子線硬化性樹脂、紫外線(以下適宜「UV」という。)硬化性樹脂等を挙げることができる。また、無機物質としては、酸化ケイ素、窒化ケイ素、フッ化マグネシウム(MgF2)、酸化スズ(SnO2)等が挙げられる。
熱可塑性樹脂、熱硬化性樹脂等を用いる場合は、適当な溶剤に溶解して調製した塗布液を反射層3の上に塗布して乾燥させれば、保護層4を形成することができる。UV硬化性樹脂を用いる場合は、そのまま反射層3の上に塗布するか、又は適当な溶剤に溶解して調製した塗布液を反射層3の上に塗布し、UV光を照射して硬化させることによって、保護層4を形成することができる。UV硬化性樹脂としては、例えば、ウレタンアクリレート、エポキシアクリレート、ポリエステルアクリレート等のアクリレート系樹脂を用いることができる。これらの材料は、単独で用いても、複数種を混合して用いてもよい。また、保護層は、単層として形成しても、多層として形成してもよい。
保護層4の形成方法としては、記録層2と同様に、スピンコート法やキャスト法等の塗布法や、スパッタリング法や化学蒸着法等の方法が用いられるが、中でもスピンコート法が好ましい。保護層4の膜厚は、その保護機能を果たすためにはある程度の厚みが必要とされるため、通常0.1μm以上であり、好ましくは3μm以上である。但し、あまり厚すぎると、効果が変わらないだけでなく保護層4の形成に時間がかかったりコストが高くなる場合があるので、通常100μm以下であり、好ましくは30μm以下である。
以上、光学記録媒体10の層構造として、基板、記録層、反射層、保護層をこの順に積層して成る構造を例に採って説明したが、この他の層構造を採っても構わない。
例えば、上例の層構造における保護層4の上面に、又は上例の層構造から保護層4を省略して反射層3の上面に、更に別の基板1を貼り合わせてもよい。この際の基板1は、何ら層を設けていない基板そのものであってもよく、貼り合わせ面又はその反対面に反射層3等任意の層を有するものでもよい。また、同じく上例の層構造を有する光学記録媒体10や、上例の層構造から保護層4を省略した光学記録媒体10を、それぞれの保護層4及び/又は反射層3の上面を相互に対向させて2枚貼り合わせてもよい。
次に、本発明の第2実施形態について説明する。図1(b)は、本発明の第2実施形態に係る光記録媒体の層構成の一例を模式的に表わす部分断面図である。図1(b)中、図1(a)と共通する要素については同じ符号を付し、説明を省略する。図1(b)に示される光学記録媒体20は、光透過性材料からなる基板1と、基板1上に設けられた反射層3と、反射層3上に積層された記録層2及び保護被膜5とが順番に積層された構造を有している。光学記録媒体20は、保護被膜5側から照射されるレーザー光Lにより、情報の記録・再生が行われる。
保護被膜5は、フィルム又はシート状のものを接着剤によって貼り合わせてもよく、また、前述の保護層4と同様の材料を用い、成膜用の塗液を塗布し硬化又は乾燥することにより形成してもよい。保護被膜5の厚さは、その保護機能を果たすためにはある程度の厚さが必要とされるため、一般に0.1μm以上であり、好ましくは3μm以上である。但し、あまり厚すぎると、効果が変わらないだけでなく、保護被膜5の形成に時間がかかったり、コストが高くなる場合があるので、通常300μm以下であり、好ましくは200μm以下である。
尚、記録層2及び反射層3等の各層は、通常は第1実施形態の光学記録媒体10と同様のものが用い得る。但し、第2実施形態においては、基板1は透明である必要はなく、従って、前述の材料以外にも、不透明な樹脂、セラミック、金属(合金を含む)等が用いられる。このような層構成においても、上記各層間には、本発明の特性を損なわない限り、必要に応じて任意の層を有してよい。
ところで、光学記録媒体10,20の記録密度を上げるための一つの手段として、対物レンズの開口数を上げることがある。これにより情報記録面に集光される光スポットを微小化できる。しかしながら、対物レンズの開口数を上げると、記録・再生を行うためにレーザー光を照射した際に、光学記録媒体10,20の反り等に起因する光スポットの収差が大きくなりやすいため、良好な記録再生信号が安定して得られない場合がある。
このような収差は、レーザー光が透過する透明基板や保護被膜の膜厚が厚いほど大きくなりやすいので、収差を小さくするためには基板や保護被膜をできるだけ薄くするのが好ましい。ただし、通常、基板1は光学記録媒体10,20の強度を確保するためにある程度の厚みを要するので、この場合、第2実施形態の光学記録媒体20の構造(基板1、反射層3、記録層2、保護被膜5なる基本的層構成の光学記録媒体20)を採用するのが好ましい。第1実施形態の光学記録媒体10の基板1を薄くするのに比べると、第2実施形態の光学記録媒体20の保護被膜5は薄くしやすいため、好ましくは第2実施形態の光学記録媒体20を用いる。
但し、第1実施形態の光学記録媒体10の構造(基板1、記録層2、反射層3、保護層4からなる基本的層構成の光学記録媒体10)であっても、記録・再生用レーザー光が通過する透明な基板1の厚さを50〜300μm程度にまで薄くすることにより、収差を小さくして使用できるようになる。
また、他の各層の形成後に、記録・再生レーザー光の入射面(通常は、基板1の下面)に、表面の保護やゴミ等の付着防止の目的で、紫外線硬化樹脂層や無機系薄膜等を成膜形成してもよく、記録・再生レーザー光の入射面ではない面(通常は、反射層3や保護層4の上面)に、インクジェット、感熱転写等の各種プリンタ、或いは各種筆記具を用いて記入や印刷が可能な印刷受容層を設けてもよい。
本実施の形態が適用される光学記録媒体10,20において、情報の記録・再生のために使用するレーザー光は、高密度記録を実現する観点から波長が短いほど好ましいが、特に波長350〜530nmのレーザー光が好ましい。かかるレーザー光の代表例として、中心波長405nm、410nm、515nmのレーザー光が挙げられる。
波長350〜530nmのレーザー光は、波長405nm、410nmの青色又は515nmの青緑色の高出力半導体レーザー光を使用することによって得られる。また、その他にも例えば(a)基本発振波長が740〜960nmの連続発振可能な半導体レーザー光、及び(b)半導体レーザー光によって励起される基本発振波長740〜960nmの連続発振可能な固体レーザー光の何れかの発振レーザー光を、第二高調波発生(Second-Harmonic Generation:SHG)素子により波長変換することによっても得られる。
尚、SHG素子としては、反転対称性を欠くピエゾ素子であればいかなるものでもよいが、KDP(KH2PO4)、ADP(NH4H2PO4)、BNN(Ba2NaNb5O15)、KN(KNbO3)、LBO(LiB3O5)、化合物半導体等が好ましい。第二高調波の具体例として、基本発振波長が860nmの半導体レーザー光の場合には、その基本発振波長の倍波である430nm、また、半導体レーザー光励起の固体レーザー光の場合には、CrドープしたLiSrAlF6結晶(基本発振波長860nm)からの倍波の430nm等が挙げられる。
本発明の各実施の形態に係る光学記録媒体10,20に情報の記録を行なう際には、記録層2に対して(通常は、基板1側から基板1を透過させ)、通常0.4〜0.6μm程度に集束したレーザー光を照射する。記録層2のレーザー光が照射された部分は、レーザー光のエネルギーを吸収することによって分解、発熱、溶解等の熱的変形を起こすため、光学的特性が変化する。
一方、記録層2に記録された情報の再生を行なう際には、同じく記録層2に対して(通常は、記録時と同じ方向から)、よりエネルギーの低いレーザー光を照射する。記録層2において、光学的特性の変化が起きた部分(すなわち、情報が記録された部分)の反射率と、変化が起きていない部分の反射率との差を読み取ることにより、情報の再生が行なわれる。
次に、本発明の第3実施形態として、複数の記録層を有する光記録媒体及びその製造方法について説明する。
図7(a)〜(f)は、本発明の第3実施形態に係る2層型光記録媒体の製造方法を説明する図である。先ず、図7(a)に示すように、表面に溝及びランド、プリピットが形成された第1の基板201を、スタンパを用いた射出成形法等により作製する。次に、少なくとも有機色素を溶媒に溶解させた塗布液を第1の基板201の凹凸を有する側の表面にスピンコート等により塗布し、塗布液に使用した溶媒を除去するために加熱(アニール)して第1の記録層202を成膜する。第1の記録層202を成膜した後、Ag合金等をスパッタまたは蒸着することにより、第1の記録層202上に、スパッタ法等により半透明な第1の反射層203を成膜する。
図7(a)〜(f)は、本発明の第3実施形態に係る2層型光記録媒体の製造方法を説明する図である。先ず、図7(a)に示すように、表面に溝及びランド、プリピットが形成された第1の基板201を、スタンパを用いた射出成形法等により作製する。次に、少なくとも有機色素を溶媒に溶解させた塗布液を第1の基板201の凹凸を有する側の表面にスピンコート等により塗布し、塗布液に使用した溶媒を除去するために加熱(アニール)して第1の記録層202を成膜する。第1の記録層202を成膜した後、Ag合金等をスパッタまたは蒸着することにより、第1の記録層202上に、スパッタ法等により半透明な第1の反射層203を成膜する。
続いて、図7(b)に示すように、第1の反射層203の表面全体に紫外線硬化性樹脂層204aをスピンコート等により塗布して形成し、さらに、図7(c)に示すように、紫外線硬化性樹脂層204aをスピンコート等により塗布した後、樹脂スタンパ210を載置し、紫外線硬化性樹脂層204aに凹凸を転写する。このとき、紫外線硬化性樹脂層204aの膜厚が所定範囲になるように調節しつつ行なう。そして、この状態で樹脂スタンパ210側から紫外線を照射する等して紫外線硬化性樹脂層204aを硬化させ、十分硬化したところで樹脂スタンパ210を剥離し、表面に凹凸を有する中間層204を形成する。
尚、樹脂スタンパ210は、中間層204となるべき樹脂に対して十分な剥離性を有していれば良く、成形性が良く、形状安定性が良いことが望ましい。生産性及びコストの観点から、望ましくは、樹脂スタンパ210は複数回の転写に使用可能であるのが望ましい。また、使用後のリサイクルが可能であることが望ましい。また、樹脂スタンパ210の材料としては、例えばアクリル系樹脂、メタクリル系樹脂、ポリカーボネート樹脂、ポリオレフィン系樹脂(特に非晶質ポリオレフィン)、ポリエステル系樹脂、ポリスチレン樹脂、エポキシ樹脂等が挙げられる。これらの中でも、成形性等の高生産性、コスト、低吸湿性、形状安定性等の点から非晶質ポリオレフィンが好ましい。
続いて、図7(d)に示すように、有機色素を溶媒に溶解させた塗布液をスピンコート等により中間層204表面に塗布し、塗布液に使用した溶媒を除去するために加熱(アニール)して第2の記録層205を成膜する。
そして、図7(e)示すように、Ag合金等をスパッタ、蒸着することにより第2の記録層205上に第2の反射層206を成膜する。その後、図7(f)に示すように、ポリカーボネートを射出成形して得られた第2の基板208としての鏡面基板を、接着層207を介して第2の反射層206に貼り合わせて光記録媒体の製造が完了する。
以上、本発明の第3実施形態に係る光記録媒体及びその製造方法について説明したが、本実施の形態は上記の態様に限定されるものではなく、種々変形することができる。例えば、光記録媒体が3つ以上の複数の記録層を有していてもよい。また、各層間や最外層として必要に応じて他の層を設けてもよい。基板入射型光ディスクに限られず、少なくとも基板/反射層/第2の記録層/バッファー層/中間層/半透明反射膜/第1の記録層/保護層からなる積層構造を有し、保護層側(即ち、膜面側)からレーザー光を照射して情報の記録・再生を行なう膜面入射型光ディスクにおいても適用できる。
多層媒体に用いられる色素として好適な要件としては、単層媒体に用いられる色素よりも記録感度が良いことが挙げられる。なぜならば各層に情報を記録する際に、記録する目的以外の層にも光が吸収、透過する現象が必ず生じるためである。この意味でも、本願のアザシアニン色素は従来と比較して良好な記録感度を持つことから、より好ましいと考えられる。
以下、本発明について実施例を用いて更に詳細に説明するが、本発明はその要旨を超えない限り、以下の実施例に限定されるものではない。
[I.色素の合成及び評価]
〔実施例1〕
2−(1,3,3−トリメチルインドリン−2−イリデン)アセトアルデヒド{2-(1,3,3-Trimethylindolin-2-ylidene)acetaldehyde}2g及び4−アミノペンタフルオロエチルチオフェノール(4-Aminopentafluoroethylthiophenol)2.43gを酢酸10gに分散させ、80℃で6時間攪拌した。反応混合物を放冷後、水200ml中に放出し、ヨウ化ナトリウム約1gを加えて結晶を析出させた。得られた結晶を濾別し、アセトン100mlを加えて溶解させ、濾過によって不溶物を除去した後、アセトンを減圧留去した。得られた結晶をジイソプロピルエーテルで2回、イソプロピルアルコールで2回洗浄し、上述の例示化合物(1)2.93gを黄色結晶として得た。
〔実施例1〕
2−(1,3,3−トリメチルインドリン−2−イリデン)アセトアルデヒド{2-(1,3,3-Trimethylindolin-2-ylidene)acetaldehyde}2g及び4−アミノペンタフルオロエチルチオフェノール(4-Aminopentafluoroethylthiophenol)2.43gを酢酸10gに分散させ、80℃で6時間攪拌した。反応混合物を放冷後、水200ml中に放出し、ヨウ化ナトリウム約1gを加えて結晶を析出させた。得られた結晶を濾別し、アセトン100mlを加えて溶解させ、濾過によって不溶物を除去した後、アセトンを減圧留去した。得られた結晶をジイソプロピルエーテルで2回、イソプロピルアルコールで2回洗浄し、上述の例示化合物(1)2.93gを黄色結晶として得た。
得られた例示化合物(1)について、クロロホルム中での吸光度を測定したところ、最大吸収波長(λmax)は427nm、モル吸光係数は5.2×104であった。
また、得られた例示化合物(1)を1重量%の濃度となるようにオクタフルオロペンタノールに溶解させ、不溶物を濾過して除去し、色素溶液を調製した。得られた色素溶液を直径120mm、厚さ1.2mmの射出成形型ポリカーボネート樹脂基板上に滴下し、スピナー法により塗布(500rpm)した後、100℃で30分間乾燥することにより、色素塗布膜を形成した。この塗布膜の吸光度を測定したところ、最大吸収波長(λmax)は419nmであった。吸収スペクトルを図2に示す。
〔実施例2〕
2−(1,3,3−トリメチルインドリン−2−イリデン)アセトアルデヒド{2-(1,3,3-Trimethylindolin-2-ylidene)acetaldehyde}2gと3,4−(メチレンジオキシ)アニリン{3.4-(Methylenedioxy)aniline}1.37gとを酢酸10gに分散させ、80℃で2時間攪拌した。反応混合物を放冷後、水200ml中に放出し、ヨウ化ナトリウム約1gを加えて結晶を析出させた。得られた結晶を濾別し、アセトン100mlに溶解させて不溶物を濾過により除いたのち、アセトンを減圧留去した。得られた結晶をジイソプロピルエーテル50mlで洗浄し、上述の例示化合物(2)1.32gを得た。
2−(1,3,3−トリメチルインドリン−2−イリデン)アセトアルデヒド{2-(1,3,3-Trimethylindolin-2-ylidene)acetaldehyde}2gと3,4−(メチレンジオキシ)アニリン{3.4-(Methylenedioxy)aniline}1.37gとを酢酸10gに分散させ、80℃で2時間攪拌した。反応混合物を放冷後、水200ml中に放出し、ヨウ化ナトリウム約1gを加えて結晶を析出させた。得られた結晶を濾別し、アセトン100mlに溶解させて不溶物を濾過により除いたのち、アセトンを減圧留去した。得られた結晶をジイソプロピルエーテル50mlで洗浄し、上述の例示化合物(2)1.32gを得た。
得られた例示化合物(2)について、クロロホルム中での吸光度を測定したところ、最大吸収波長(λmax)は437nm、モル吸光係数は3.9×104であった。
また、得られた例示化合物(2)を用いて、実施例1と同様の手順でポリカーボネート樹脂基板上に色素塗布膜を形成し、この塗布膜の吸光度を測定したところ、最大吸収波長(λmax)は435.5nmであった。吸収スペクトルを図3に示す。
〔実施例3〕
2−(1,3,3−トリメチルインドリン−2−イリデン)アセトアルデヒド{2-(1,3,3-Trimethylindolin-2-ylidene)acetaldehyde}2gと3−アミノ−5−ターシャリーブチルイソオキサゾール(3-Amino-5-tert-butylisoxazole)1.40gとを酢酸10gに分散させ、50〜60℃で5時間攪拌した。反応混合物を放冷後、水100ml中に放出し、ヘキサフルオロりん酸アンモニウム(NH4PF6)数gを加えて結晶を析出させた。得られた結晶を濾別し、水100ml中で10分間攪拌した後、再び濾過し得られた固体を乾燥することにより、上述の例示化合物(15)2.79gを黄色の結晶として得た。
2−(1,3,3−トリメチルインドリン−2−イリデン)アセトアルデヒド{2-(1,3,3-Trimethylindolin-2-ylidene)acetaldehyde}2gと3−アミノ−5−ターシャリーブチルイソオキサゾール(3-Amino-5-tert-butylisoxazole)1.40gとを酢酸10gに分散させ、50〜60℃で5時間攪拌した。反応混合物を放冷後、水100ml中に放出し、ヘキサフルオロりん酸アンモニウム(NH4PF6)数gを加えて結晶を析出させた。得られた結晶を濾別し、水100ml中で10分間攪拌した後、再び濾過し得られた固体を乾燥することにより、上述の例示化合物(15)2.79gを黄色の結晶として得た。
得られた例示化合物(15)について、クロロホルム中での吸光度を測定したところ、最大吸収波長(λmax)は395.5nm、モル吸光係数は4.2×104であった。
[比較例1]
下記構造式(A)で示される色素を用いて、実施例1と同様の手順でポリカーボネート樹脂基板上に色素塗布膜を形成し、この塗布膜の吸光度を測定した。得られた吸収スペクトルを図4に示す。吸収ピークは500nmよりも長波長(539nm)に存在し、400nm付近の吸収は極めて小さく、405nmレーザーを使用する本発明の目的にはそぐわないものであった。
下記構造式(A)で示される色素を用いて、実施例1と同様の手順でポリカーボネート樹脂基板上に色素塗布膜を形成し、この塗布膜の吸光度を測定した。得られた吸収スペクトルを図4に示す。吸収ピークは500nmよりも長波長(539nm)に存在し、400nm付近の吸収は極めて小さく、405nmレーザーを使用する本発明の目的にはそぐわないものであった。
[比較例2]
下記構造式(B)で示される色素について、実施例1とほぼ同様の条件で実施例1で使用したポリカーボネート基板上に塗布した。塗布膜は結晶化して透明なものが得られず、本発明の目的にそぐわないものであった。
下記構造式(B)で示される色素について、実施例1とほぼ同様の条件で実施例1で使用したポリカーボネート基板上に塗布した。塗布膜は結晶化して透明なものが得られず、本発明の目的にそぐわないものであった。
〔実施例4〜9〕
2−(1,3,3−トリメチルインドリン−2−イリデン)アセトアルデヒドと反応させるアミン化合物の種類を変更した他は、実施例1と基本的に同様の手法により、上記式[I]のアザシアニン色素に該当する色素化合物を製造した(実施例4〜9)。
下記表1に、実施例1〜9で得られた色素化合物における、上記式[I]の基R5の構造及び対アニオンX-の構造を示す。下記表1において、「Pr(i)」はi−プロピル基を表わし、「t−Bu」はt−ブチル基を表わしている。なお、実施例1〜9で得られた何れの色素化合物においても、上記式[I]の基R1〜R3はメチル基であり、基R4は水素原子である。また、実施例1〜9で得られた色素化合物が上述の例示化合物(1)〜(19)の何れに該当するかを、下記表1に例示化合物の番号で示している。
2−(1,3,3−トリメチルインドリン−2−イリデン)アセトアルデヒドと反応させるアミン化合物の種類を変更した他は、実施例1と基本的に同様の手法により、上記式[I]のアザシアニン色素に該当する色素化合物を製造した(実施例4〜9)。
下記表1に、実施例1〜9で得られた色素化合物における、上記式[I]の基R5の構造及び対アニオンX-の構造を示す。下記表1において、「Pr(i)」はi−プロピル基を表わし、「t−Bu」はt−ブチル基を表わしている。なお、実施例1〜9で得られた何れの色素化合物においても、上記式[I]の基R1〜R3はメチル基であり、基R4は水素原子である。また、実施例1〜9で得られた色素化合物が上述の例示化合物(1)〜(19)の何れに該当するかを、下記表1に例示化合物の番号で示している。
また、実施例4〜9で得られた色素化合物の各々についても、実施例1と同様の手法により、クロロホルム中における最大吸収波長(λmax)、塗布膜の最大吸収波長(λmax)及びクロロホルム中におけるモル吸光係数を測定した。
〔評価〕
下記表1に、実施例1〜9で得られた色素化合物の、クロロホルム中における最大吸収波長(表中「λsol」の欄)、塗布膜の最大吸収波長(表中「λfilm」の欄)及びクロロホルム中におけるモル吸光係数(表中「ε」の欄)を示す。
下記表1に、実施例1〜9で得られた色素化合物の、クロロホルム中における最大吸収波長(表中「λsol」の欄)、塗布膜の最大吸収波長(表中「λfilm」の欄)及びクロロホルム中におけるモル吸光係数(表中「ε」の欄)を示す。
[II.光学記録媒体の作製及び評価]
上述の実施例1及び2において作製した色素塗布膜上に、必要に応じてスパッタリング法にてAg等を成膜して反射層を形成し、更にUV硬化樹脂をスピンコート等にて塗布・UV照射により硬化させて保護層を形成することにより、光学記録媒体とすることができる。この光学記録媒体は、色素塗布膜の最大吸収波長(λmax)の値より、例えば中心波長405nmの半導体レーザー光による記録再生が可能である。即ち、実施例1及び2において合成した例示化合物(1)及び(2)(本発明のアザシアニン色素)は、青色レーザー光の記録に対して有効な構造の化合物であることが分かる。
上述の実施例1及び2において作製した色素塗布膜上に、必要に応じてスパッタリング法にてAg等を成膜して反射層を形成し、更にUV硬化樹脂をスピンコート等にて塗布・UV照射により硬化させて保護層を形成することにより、光学記録媒体とすることができる。この光学記録媒体は、色素塗布膜の最大吸収波長(λmax)の値より、例えば中心波長405nmの半導体レーザー光による記録再生が可能である。即ち、実施例1及び2において合成した例示化合物(1)及び(2)(本発明のアザシアニン色素)は、青色レーザー光の記録に対して有効な構造の化合物であることが分かる。
そこで、実施例2において合成した例示化合物(2)を用いて、以下の手順により光学記録媒体を作製した。
実施例2において合成した例示化合物(2)を、1.4重量%の濃度となるようにオクタフルオロペンタノールに溶解させ、不溶物を濾過することにより色素溶液を調製した。溶解液をトラックピッチ400nm、溝幅200nm、溝深さ70nmの溝を持つ直径120mm、厚さ0.6mmの射出成型ポリカーボネート樹脂基板に滴下し、スピナー法により塗布した。なお、塗布は、回転数600rpmから4900rpmへ25秒かけて回転数を上げ、4900rpmで5秒間保持することによって行なった。更に、100℃で30分間乾燥することにより、記録層を形成した。次いで、この記録層の上に、スパッタリング法にて銀合金を100nmの厚さで成膜し、反射層を形成した。その後、UV硬化性樹脂からなる保護コート剤をスピナー法により塗布し、UV光を照射して厚さ5μmの保護層を形成させた。更に、遅延硬化型接着剤を用いて、保護層のある面に、厚さ0.6mmのポリカーボネート製基板を接着して、評価用の光学記録媒体を調製した。
実施例2において合成した例示化合物(2)を、1.4重量%の濃度となるようにオクタフルオロペンタノールに溶解させ、不溶物を濾過することにより色素溶液を調製した。溶解液をトラックピッチ400nm、溝幅200nm、溝深さ70nmの溝を持つ直径120mm、厚さ0.6mmの射出成型ポリカーボネート樹脂基板に滴下し、スピナー法により塗布した。なお、塗布は、回転数600rpmから4900rpmへ25秒かけて回転数を上げ、4900rpmで5秒間保持することによって行なった。更に、100℃で30分間乾燥することにより、記録層を形成した。次いで、この記録層の上に、スパッタリング法にて銀合金を100nmの厚さで成膜し、反射層を形成した。その後、UV硬化性樹脂からなる保護コート剤をスピナー法により塗布し、UV光を照射して厚さ5μmの保護層を形成させた。更に、遅延硬化型接着剤を用いて、保護層のある面に、厚さ0.6mmのポリカーボネート製基板を接着して、評価用の光学記録媒体を調製した。
得られた評価用の光学記録媒体を線速度6.61m/secで回転させながら、波長405nm(対物レンズの開口数NA=0.65)のレーザー光で、8Tマーク/8Tスペースの単一周波数信号を溝上に記録した。なお、Tは、周波数65MHzに対応する基準クロック周期である。記録パルスストラテジーとして、分割パルス数はマーク長をnTとして(n−1)、先頭記録パルス幅2T、後続記録パルス幅0.6T、バイアスパワー1.5mW、再生パワー0.4mW、記録パワーを可変とした。その結果、7mWで変調度51%の信号を記録することができた。変調度は、パルスストラテジー等記録条件の最適化によって、より大きくなると考えられる。
以上より、短波長レーザーで本発明の色素を用いて情報の記録が可能であることを示したが、これに加えて更に厳しい条件、すなわち高密度光ディスク用色素として要求される特性を満足することを確認するため、HD DVD−R規格に基づいた評価を実施した。
〔実施例A〕
厚さ0.6mm、トラックピッチ0.4μm、溝幅260nm、溝深さ60nmのポリカーボネート製の基板上に、上述の例示化合物(27)をTFP(2,2,3,3−テトラフルオロ−1−プロパノール)に対し1.0重量%の濃度となるように混合した溶液をスピンコート法で塗布し、70℃で25分乾燥させることにより、記録層を設けた。なお、空気をリファレンスとして測定した470nmでの吸光度は0.32であった。その後、この記録層の上に、スパッタリングにより厚さ120nmのAgBi0.2Nd0.5反射膜を設けた。更に、この反射層の上に、紫外線硬化樹脂(ソニーケミカル社製SK7100)を用いて、0.6mm厚のポリカーボネート製の裏板を接着して、光学記録媒体を作製した(実施例Aの光学記録媒体)。
厚さ0.6mm、トラックピッチ0.4μm、溝幅260nm、溝深さ60nmのポリカーボネート製の基板上に、上述の例示化合物(27)をTFP(2,2,3,3−テトラフルオロ−1−プロパノール)に対し1.0重量%の濃度となるように混合した溶液をスピンコート法で塗布し、70℃で25分乾燥させることにより、記録層を設けた。なお、空気をリファレンスとして測定した470nmでの吸光度は0.32であった。その後、この記録層の上に、スパッタリングにより厚さ120nmのAgBi0.2Nd0.5反射膜を設けた。更に、この反射層の上に、紫外線硬化樹脂(ソニーケミカル社製SK7100)を用いて、0.6mm厚のポリカーボネート製の裏板を接着して、光学記録媒体を作製した(実施例Aの光学記録媒体)。
得られた実施例Aの光学記録媒体に対し、レーザー波長405nm、NA(開口数)0.65のテスター(パルステック社製ODU−1000)を用い、線速度6.61m/s、最短マーク長204nmで記録を行なった。記録及び再生は、DVDフォーラムにより定められたHD DVD−R規格Ver1.0に準拠した方式で、同規格にあるPRSNR(Partial Response SNR)の評価を行なった。
その結果、記録メカニズムはLow To High型であり、最適記録パワーは6.4mWであった。得られたPRSNRを図5に示す。図5から明らかなように、実施例Aの光学記録媒体のPRSNRは34.0と、規格の15を大きく上回る結果であった。
〔実施例B〕
色素として上述の例示化合物(28)を使用した以外は、実施例Aと同様の条件で光学記録媒体を作製し(実施例Bの光学記録媒体)、同様の条件で評価を行なった。
色素として上述の例示化合物(28)を使用した以外は、実施例Aと同様の条件で光学記録媒体を作製し(実施例Bの光学記録媒体)、同様の条件で評価を行なった。
この結果、記録メカニズムはLow To High型であり、最適記録パワーは6.2mWであった。得られたPRSNRを図5に示す。図5から明らかなように、実施例Bの光学記録媒体のPRSNRは26.0と、規格の15を大きく上回る結果であった。
〔実施例C〕
色素として上述の例示化合物(29)を使用した以外は、実施例Aと同様の条件で光学記録媒体を作製し(実施例Cの光学記録媒体)、同様の条件で評価を行なった。
色素として上述の例示化合物(29)を使用した以外は、実施例Aと同様の条件で光学記録媒体を作製し(実施例Cの光学記録媒体)、同様の条件で評価を行なった。
この結果、記録メカニズムはLow To High型であり、最適記録パワーは6.8mWであった。得られたPRSNRを図5に示す。図5から明らかなように、実施例Cの光学記録媒体のPRSNRは28.0と、規格の15を大きく上回る結果であった。
〔実施例D〕
色素として上述の例示化合物(30)を使用した以外は、実施例Aと同様の条件で光学記録媒体を作製し(実施例Dの光学記録媒体)、同様の条件で評価を行なった。
色素として上述の例示化合物(30)を使用した以外は、実施例Aと同様の条件で光学記録媒体を作製し(実施例Dの光学記録媒体)、同様の条件で評価を行なった。
この結果、記録メカニズムはLow To High型であり、最適記録パワーは7.2mWであった。得られたPRSNRを図5に示す。図5から明らかなように、実施例Dの光学記録媒体のPRSNRは30.0と、規格の15を大きく上回る結果であった。
〔実施例E〕
色素として上述の例示化合物(31)を使用した以外は、実施例Aと同様の条件で光学記録媒体を作製し(実施例Eの光学記録媒体)、同様の条件で評価を行なった。
色素として上述の例示化合物(31)を使用した以外は、実施例Aと同様の条件で光学記録媒体を作製し(実施例Eの光学記録媒体)、同様の条件で評価を行なった。
この結果、記録メカニズムはLow To High型であり、最適記録パワーは6.8mWであった。得られたPRSNRを図5に示す。図5から明らかなように、実施例Eの光学記録媒体のPRSNRは26.0と、規格の15を大きく上回る結果であった。
〔実施例F〕
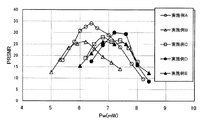
実施例Aと同一の色素、すなわち例示化合物(27)を用いて2層媒体を作製し、Layer 0、Layer 1それぞれの記録層の記録特性を評価した。ここで、Layer 0は「第1の記録層」(レーザー入射に近い側の記録層)を意味し、Layer 1は「第2の記録層」(レーザー入射に遠い側の記録層)を意味する。また、「第1の反射層」(半透明な反射層)としてAgBi1.0合金を20nmの膜厚で形成し、「第2の反射層」としてAgを120nmの膜厚で形成し、中間層として紫外線硬化性樹脂を25μmの膜厚で形成した。使用した基板のトラックピッチは0.4μm、溝深さはLayer 0:60nm、Layer 1:65nm、溝幅は両者とも260nmであり、また470nmでの吸光度は Layer 0:0.315、Layer 1:0.345とした。
実施例Aと同一の色素、すなわち例示化合物(27)を用いて2層媒体を作製し、Layer 0、Layer 1それぞれの記録層の記録特性を評価した。ここで、Layer 0は「第1の記録層」(レーザー入射に近い側の記録層)を意味し、Layer 1は「第2の記録層」(レーザー入射に遠い側の記録層)を意味する。また、「第1の反射層」(半透明な反射層)としてAgBi1.0合金を20nmの膜厚で形成し、「第2の反射層」としてAgを120nmの膜厚で形成し、中間層として紫外線硬化性樹脂を25μmの膜厚で形成した。使用した基板のトラックピッチは0.4μm、溝深さはLayer 0:60nm、Layer 1:65nm、溝幅は両者とも260nmであり、また470nmでの吸光度は Layer 0:0.315、Layer 1:0.345とした。
記録条件は単層媒体と同一であり、レーザー波長405nm、NA(開口数)0.65のテスター(パルステック社製ODU-1000)を用い、線速度6.61m/s、最短マーク長204nmでランダムパターン記録を行なった。記録、再生はDVDフォーラムにより定められたHDDVD−R規格Ver1.0に準拠した方式で行ない、同規格にあるPRSNR(Partial Response SNR)の評価を行なった。
評価の結果、記録メカニズムはLayer 0、Layer 1ともにLow To High型であった。得られたPRSNRを図6に示す。図6から明らかなように、Layer 0の最適記録パワーは9.4mW、PRNSRは25.1であり、Layer 1の最適記録パワーは12.5mW、PRNSRは24.0であった。PRSNRの値は、Layer 0、Layer 1ともに規格の15.0を大きく上回る良好な結果であり、2層媒体に必要な記録特性を十分に確保できた。
本発明の適用分野は特に制限されないが、青色レーザー光等の発振波長の短いレーザー光を用いて記録・再生を行なう光学記録媒体の分野において、好適に利用することが可能である。
1 基板
2 記録層
3 反射層
4 保護層
5 保護被膜
10,20 光学記録媒体
L レーザー光
201 第1の基板
202 第1の記録層
203 第1の反射層
204 中間層
204a 紫外線硬化性樹脂層
205 第2の記録層
206 第2の反射層
207 接着層
208 第2の基板(鏡面基板)
210 樹脂スタンパ
2 記録層
3 反射層
4 保護層
5 保護被膜
10,20 光学記録媒体
L レーザー光
201 第1の基板
202 第1の記録層
203 第1の反射層
204 中間層
204a 紫外線硬化性樹脂層
205 第2の記録層
206 第2の反射層
207 接着層
208 第2の基板(鏡面基板)
210 樹脂スタンパ
Claims (8)
- 基板と、前記基板上に設けられ、光が照射されることにより情報の記録又は再生が可能な記録層とを少なくとも有し、
該記録層が、下記一般式[I]で示されるアザシアニン色素を含有する
ことを特徴とする、光学記録媒体。
R1及びR2はそれぞれ独立して、水素原子、又は、置換されていてもよい炭素数1〜4の直鎖若しくは分岐のアルキル基を表わす。また、R1及びR2が互いに結合して、環を形成していてもよい。
R3は、水素原子、又は、炭化水素基を表わす。また、R3が炭化水素基である場合、R3を介して2以上の一般式[I]の化合物が架橋されていてもよい。
R4は、水素原子、又は、炭素数1〜4の直鎖又は分岐のアルキル基を表わす。
R5は、置換されていてもよい芳香環基、又は、置換されていてもよい不飽和複素環基を表わす。また、R5を介して2以上の一般式[I]の化合物が結合されていてもよい。
但し、R4とR5とは互いに結合して、環構造を形成していてもよい。
X-は、対アニオンを表わす。
Aで示されるベンゼン環は、置換されていてもよい。) - 上記一般式[I]中、R4が水素原子であり、R5が置換されていてもよいフェニル基である
ことを特徴とする、請求項1記載の光学記録媒体。 - 上記一般式[I]中、R4が水素原子であり、R5が置換されていてもよい5員又は6員の不飽和複素環基である
ことを特徴とする、請求項1記載の光学記録媒体。 - 上記一般式[I]中、R4とR5とが互いに結合して、5員又は6員の飽和炭化水素環又は飽和複素環を形成している
ことを特徴とする、請求項1記載の光学記録媒体。 - R5のフェニル基が、置換基を有さない
ことを特徴とする、請求項2記載の光学記録媒体。 - 該記録層が、波長350nm〜530nmのレーザー光により情報の記録又は再生が行なわれるものである
ことを特徴とする、請求項1〜6の何れか一項に記載の光学記録媒体。
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2006174427A JP2007196661A (ja) | 2005-12-27 | 2006-06-23 | 光学記録媒体及びアザシアニン色素 |
| PCT/JP2006/326031 WO2007074861A1 (ja) | 2005-12-27 | 2006-12-27 | 光学記録媒体及びアザシアニン色素 |
| EP06843413A EP1967378A1 (en) | 2005-12-27 | 2006-12-27 | Optical recording medium and azacyanine dye |
| US12/159,223 US20100173114A1 (en) | 2005-12-27 | 2006-12-27 | Optical recording medium and azacyanine dye |
| TW095149146A TW200737177A (en) | 2005-12-27 | 2006-12-27 | Optical recording medium and azacyanine dye |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2005375871 | 2005-12-27 | ||
| JP2006174427A JP2007196661A (ja) | 2005-12-27 | 2006-06-23 | 光学記録媒体及びアザシアニン色素 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2007196661A true JP2007196661A (ja) | 2007-08-09 |
Family
ID=38218083
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006174427A Withdrawn JP2007196661A (ja) | 2005-12-27 | 2006-06-23 | 光学記録媒体及びアザシアニン色素 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20100173114A1 (ja) |
| EP (1) | EP1967378A1 (ja) |
| JP (1) | JP2007196661A (ja) |
| TW (1) | TW200737177A (ja) |
| WO (1) | WO2007074861A1 (ja) |
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010010970A1 (ja) | 2008-07-25 | 2010-01-28 | 太陽誘電株式会社 | 光情報記録媒体用色素及び光情報記録媒体 |
| JP2010143184A (ja) * | 2008-12-22 | 2010-07-01 | Taiyo Yuden Co Ltd | 光情報記録媒体用色素及び光情報記録媒体 |
| WO2011086794A1 (ja) * | 2010-01-18 | 2011-07-21 | 太陽誘電株式会社 | 光情報記録媒体用色素及びそれを用いた光情報記録媒体 |
| US8715805B2 (en) | 2012-01-24 | 2014-05-06 | Taiyo Yuden Co., Ltd. | Optical recording medium |
| US8747984B2 (en) | 2012-01-24 | 2014-06-10 | Taiyo Yuden Co., Ltd. | Optical recording medium |
| US8747983B2 (en) | 2012-01-24 | 2014-06-10 | Taiyo Yuden Co., Ltd. | Optical recording medium |
| JP2015189767A (ja) * | 2014-03-27 | 2015-11-02 | 日本化薬株式会社 | メチン化合物 |
| JP2015189768A (ja) * | 2014-03-27 | 2015-11-02 | 日本化薬株式会社 | メチン化合物 |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2007007748A1 (ja) | 2005-07-14 | 2007-01-18 | Mitsubishi Kagaku Media Co., Ltd. | 光学記録媒体、光記録材料および金属錯体化合物 |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2699120B2 (ja) * | 1989-12-22 | 1998-01-19 | 富士写真フイルム株式会社 | 情報記録媒体および光情報記録方法 |
| JPH04201482A (ja) * | 1990-11-30 | 1992-07-22 | Fuji Photo Film Co Ltd | 情報記録媒体および光情報記録方法 |
| JP4754698B2 (ja) * | 2000-02-10 | 2011-08-24 | 株式会社林原生物化学研究所 | シアニン色素 |
| JP2001301333A (ja) * | 2000-02-16 | 2001-10-31 | Fuji Photo Film Co Ltd | 情報記録媒体および記録方法 |
| EP1132901A3 (en) * | 2000-02-16 | 2001-11-28 | Fuji Photo Film Co., Ltd. | Information recording medium and recording method |
| JP2002229195A (ja) * | 2001-02-01 | 2002-08-14 | Fuji Photo Film Co Ltd | 光重合性組成物及びそれを用いた記録材料 |
| JP3708094B2 (ja) * | 2003-08-07 | 2005-10-19 | 旭電化工業株式会社 | シアニン化合物、光学記録材料及び光学記録媒体 |
| TWI261605B (en) * | 2004-06-30 | 2006-09-11 | Ind Tech Res Inst | Dye compositon of the optical recording medium |
| JP4721682B2 (ja) * | 2004-09-27 | 2011-07-13 | 株式会社Adeka | 複素環化合物及び光学記録材料 |
| JP4688480B2 (ja) * | 2004-11-25 | 2011-05-25 | 株式会社Adeka | シアニン化合物、該化合物を用いた光学記録材料、及び光学記録媒体 |
| TW200702396A (en) * | 2005-04-07 | 2007-01-16 | Clariant Int Ltd | Basic yellow dyes as dye component for optical data recording media |
-
2006
- 2006-06-23 JP JP2006174427A patent/JP2007196661A/ja not_active Withdrawn
- 2006-12-27 WO PCT/JP2006/326031 patent/WO2007074861A1/ja active Application Filing
- 2006-12-27 TW TW095149146A patent/TW200737177A/zh unknown
- 2006-12-27 US US12/159,223 patent/US20100173114A1/en not_active Abandoned
- 2006-12-27 EP EP06843413A patent/EP1967378A1/en not_active Withdrawn
Cited By (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| TWI427630B (zh) * | 2008-07-25 | 2014-02-21 | Taiyo Yuden Kk | Optical information recording media with color and optical information recording media |
| JP2010033639A (ja) * | 2008-07-25 | 2010-02-12 | Taiyo Yuden Co Ltd | 光情報記録媒体用色素及び光情報記録媒体 |
| WO2010010970A1 (ja) | 2008-07-25 | 2010-01-28 | 太陽誘電株式会社 | 光情報記録媒体用色素及び光情報記録媒体 |
| JP2010143184A (ja) * | 2008-12-22 | 2010-07-01 | Taiyo Yuden Co Ltd | 光情報記録媒体用色素及び光情報記録媒体 |
| WO2010073971A1 (ja) | 2008-12-22 | 2010-07-01 | 太陽誘電株式会社 | 光情報記録媒体用色素及び光情報記録媒体 |
| US9135941B2 (en) | 2008-12-22 | 2015-09-15 | Taiyo Yuden Co., Ltd. | Dye for optical information recording medium and optical information recording medium |
| KR101235104B1 (ko) | 2008-12-22 | 2013-02-20 | 다이요 유덴 가부시키가이샤 | 광 정보 기록 매체용 색소 및 광 정보 기록 매체 |
| JP5205521B2 (ja) * | 2010-01-18 | 2013-06-05 | 太陽誘電株式会社 | 光情報記録媒体用色素及びそれを用いた光情報記録媒体 |
| WO2011086794A1 (ja) * | 2010-01-18 | 2011-07-21 | 太陽誘電株式会社 | 光情報記録媒体用色素及びそれを用いた光情報記録媒体 |
| US8715805B2 (en) | 2012-01-24 | 2014-05-06 | Taiyo Yuden Co., Ltd. | Optical recording medium |
| US8747984B2 (en) | 2012-01-24 | 2014-06-10 | Taiyo Yuden Co., Ltd. | Optical recording medium |
| US8747983B2 (en) | 2012-01-24 | 2014-06-10 | Taiyo Yuden Co., Ltd. | Optical recording medium |
| JP2015189767A (ja) * | 2014-03-27 | 2015-11-02 | 日本化薬株式会社 | メチン化合物 |
| JP2015189768A (ja) * | 2014-03-27 | 2015-11-02 | 日本化薬株式会社 | メチン化合物 |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2007074861A1 (ja) | 2007-07-05 |
| US20100173114A1 (en) | 2010-07-08 |
| EP1967378A1 (en) | 2008-09-10 |
| TW200737177A (en) | 2007-10-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4818000B2 (ja) | 光学記録媒体および金属錯体化合物。 | |
| JP2007196661A (ja) | 光学記録媒体及びアザシアニン色素 | |
| JPH11334205A (ja) | 光学記録媒体 | |
| JP2008195915A (ja) | ヒドラジドキレート錯体化合物および該化合物を用いた光学記録媒体およびその記録方法 | |
| JP4750504B2 (ja) | 光記録媒体及びアゾ系金属キレート色素添加剤 | |
| JP4961789B2 (ja) | 光学記録媒体及びその記録層形成用色素 | |
| EP1449890A1 (en) | Squarylium-metal chelate compounds and optical recording media | |
| JP3876970B2 (ja) | 光学記録媒体の記録層形成用色素、及びそれを用いた光学記録媒体、その光学記録媒体の記録方法 | |
| JP5352986B2 (ja) | 金属錯体化合物、光学記録媒体及び光記録材料 | |
| JP4120340B2 (ja) | 光学記録媒体および光学記録方法 | |
| JP2008239973A (ja) | シアニン色素及び光学記録媒体 | |
| JP3960276B2 (ja) | 光学記録媒体および光学記録方法 | |
| WO2011102348A1 (ja) | ヒドラジドキレート錯体化合物およびこれを用いた光学記録媒体 | |
| CN101346243A (zh) | 光学记录介质和氮杂菁色素 | |
| JP2003019867A (ja) | 光記録媒体 | |
| WO2010041691A1 (ja) | スクアリリウム化合物の金属錯体を含有する光記録媒体 | |
| JP2005305839A (ja) | 光記録材料及び光記録媒体 | |
| JP2011057881A (ja) | シアニン色素及び光学記録媒体 | |
| JP2000343825A (ja) | 光学記録媒体 | |
| JP2002002110A (ja) | 光学記録媒体 | |
| JP2010194870A (ja) | 光学記録媒体の記録層形成用色素および該色素を用いた光学記録媒体およびその記録方法 | |
| JP2009114345A (ja) | 金属錯体化合物、光学記録媒体、光記録材料及び色素 | |
| JP2003178489A (ja) | 情報記録媒体 | |
| JP2005305835A (ja) | 光記録材料及び光記録媒体 | |
| JPH10273484A (ja) | 金属キレートアゾメチン化合物及びこれを用いた光学的記録媒体 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20090216 |
|
| A761 | Written withdrawal of application |
Free format text: JAPANESE INTERMEDIATE CODE: A761 Effective date: 20100805 |