JP2005298822A - 共重合性ポリアルキレングリコールマクロモノマー並びにそれらの製造法及び使用法 - Google Patents
共重合性ポリアルキレングリコールマクロモノマー並びにそれらの製造法及び使用法 Download PDFInfo
- Publication number
- JP2005298822A JP2005298822A JP2005110021A JP2005110021A JP2005298822A JP 2005298822 A JP2005298822 A JP 2005298822A JP 2005110021 A JP2005110021 A JP 2005110021A JP 2005110021 A JP2005110021 A JP 2005110021A JP 2005298822 A JP2005298822 A JP 2005298822A
- Authority
- JP
- Japan
- Prior art keywords
- compound
- formula
- alkylene
- aqueous dispersion
- polymerization
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
- 238000000034 method Methods 0.000 title claims description 10
- 229920001515 polyalkylene glycol Polymers 0.000 title abstract description 20
- 238000004519 manufacturing process Methods 0.000 title description 6
- 229920000642 polymer Polymers 0.000 claims abstract description 9
- 238000006116 polymerization reaction Methods 0.000 claims abstract description 8
- 150000003254 radicals Chemical class 0.000 claims abstract description 7
- 125000000217 alkyl group Chemical group 0.000 claims abstract description 6
- 125000003118 aryl group Chemical group 0.000 claims abstract description 3
- 239000004815 dispersion polymer Substances 0.000 claims abstract description 3
- 150000001875 compounds Chemical class 0.000 claims description 28
- 239000006185 dispersion Substances 0.000 claims description 14
- 125000003545 alkoxy group Chemical group 0.000 claims description 13
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 10
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 claims description 9
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 claims description 6
- 229920003009 polyurethane dispersion Polymers 0.000 claims description 5
- 238000010526 radical polymerization reaction Methods 0.000 claims description 4
- ZJCCRDAZUWHFQH-UHFFFAOYSA-N Trimethylolpropane Chemical compound CCC(CO)(CO)CO ZJCCRDAZUWHFQH-UHFFFAOYSA-N 0.000 claims description 3
- 125000002947 alkylene group Chemical group 0.000 claims description 3
- 239000000839 emulsion Substances 0.000 claims description 3
- 238000007720 emulsion polymerization reaction Methods 0.000 claims description 3
- 239000003999 initiator Substances 0.000 claims description 3
- 238000002156 mixing Methods 0.000 claims description 3
- 238000010557 suspension polymerization reaction Methods 0.000 claims description 3
- 150000001336 alkenes Chemical class 0.000 claims description 2
- 125000004430 oxygen atom Chemical group O* 0.000 claims description 2
- 230000006641 stabilisation Effects 0.000 claims description 2
- 238000011105 stabilization Methods 0.000 claims description 2
- 239000000654 additive Substances 0.000 claims 1
- 230000000996 additive effect Effects 0.000 claims 1
- JRZJOMJEPLMPRA-UHFFFAOYSA-N olefin Natural products CCCCCCCC=C JRZJOMJEPLMPRA-UHFFFAOYSA-N 0.000 claims 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 abstract description 13
- 230000007062 hydrolysis Effects 0.000 abstract description 8
- 238000006460 hydrolysis reaction Methods 0.000 abstract description 8
- 150000002148 esters Chemical class 0.000 abstract description 6
- 229920002635 polyurethane Polymers 0.000 abstract description 4
- 239000004814 polyurethane Substances 0.000 abstract description 4
- 238000004132 cross linking Methods 0.000 abstract description 3
- 238000002360 preparation method Methods 0.000 abstract description 3
- 229920001577 copolymer Polymers 0.000 abstract description 2
- GYLZSBPASSUYIS-UHFFFAOYSA-N tert-butyl n-benzyl-n-prop-1-en-2-ylcarbamate Chemical compound CC(C)(C)OC(=O)N(C(=C)C)CC1=CC=CC=C1 GYLZSBPASSUYIS-UHFFFAOYSA-N 0.000 abstract description 2
- WNXJIVFYUVYPPR-UHFFFAOYSA-N 1,3-dioxolane Chemical compound C1COCO1 WNXJIVFYUVYPPR-UHFFFAOYSA-N 0.000 abstract 1
- 150000001732 carboxylic acid derivatives Chemical class 0.000 abstract 1
- 125000000532 dioxanyl group Chemical group 0.000 abstract 1
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 16
- 238000003860 storage Methods 0.000 description 12
- -1 α-methylstyryl group Chemical group 0.000 description 12
- 238000005160 1H NMR spectroscopy Methods 0.000 description 9
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 8
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 8
- 229920013747 hydroxypolyethylene Polymers 0.000 description 8
- 229910052740 iodine Inorganic materials 0.000 description 8
- 239000011630 iodine Substances 0.000 description 8
- 238000006243 chemical reaction Methods 0.000 description 7
- 239000000203 mixture Substances 0.000 description 7
- CERQOIWHTDAKMF-UHFFFAOYSA-N Methacrylic acid Chemical compound CC(=C)C(O)=O CERQOIWHTDAKMF-UHFFFAOYSA-N 0.000 description 6
- SMZOUWXMTYCWNB-UHFFFAOYSA-N 2-(2-methoxy-5-methylphenyl)ethanamine Chemical compound COC1=CC=C(C)C=C1CCN SMZOUWXMTYCWNB-UHFFFAOYSA-N 0.000 description 5
- NIXOWILDQLNWCW-UHFFFAOYSA-N 2-Propenoic acid Natural products OC(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 5
- 239000002202 Polyethylene glycol Substances 0.000 description 5
- 125000004036 acetal group Chemical group 0.000 description 5
- 238000007334 copolymerization reaction Methods 0.000 description 5
- 125000000524 functional group Chemical group 0.000 description 5
- 229920001223 polyethylene glycol Polymers 0.000 description 5
- 239000003381 stabilizer Substances 0.000 description 5
- ZVEMLYIXBCTVOF-UHFFFAOYSA-N 1-(2-isocyanatopropan-2-yl)-3-prop-1-en-2-ylbenzene Chemical compound CC(=C)C1=CC=CC(C(C)(C)N=C=O)=C1 ZVEMLYIXBCTVOF-UHFFFAOYSA-N 0.000 description 4
- 0 CCC(CC1)*C1C(C)CC1CC(C)CC1 Chemical compound CCC(CC1)*C1C(C)CC1CC(C)CC1 0.000 description 4
- 150000003863 ammonium salts Chemical class 0.000 description 4
- 239000011734 sodium Substances 0.000 description 4
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 229910052783 alkali metal Inorganic materials 0.000 description 3
- 150000001735 carboxylic acids Chemical class 0.000 description 3
- MTHSVFCYNBDYFN-UHFFFAOYSA-N diethylene glycol Chemical compound OCCOCCO MTHSVFCYNBDYFN-UHFFFAOYSA-N 0.000 description 3
- 239000000178 monomer Substances 0.000 description 3
- 239000000047 product Substances 0.000 description 3
- 229910052708 sodium Inorganic materials 0.000 description 3
- OAOABCKPVCUNKO-UHFFFAOYSA-N 8-methyl Nonanoic acid Chemical compound CC(C)CCCCCCC(O)=O OAOABCKPVCUNKO-UHFFFAOYSA-N 0.000 description 2
- KAKZBPTYRLMSJV-UHFFFAOYSA-N Butadiene Chemical compound C=CC=C KAKZBPTYRLMSJV-UHFFFAOYSA-N 0.000 description 2
- JOYRKODLDBILNP-UHFFFAOYSA-N Ethyl urethane Chemical compound CCOC(N)=O JOYRKODLDBILNP-UHFFFAOYSA-N 0.000 description 2
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical compound C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 2
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- GOOHAUXETOMSMM-UHFFFAOYSA-N Propylene oxide Chemical compound CC1CO1 GOOHAUXETOMSMM-UHFFFAOYSA-N 0.000 description 2
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical compound C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 description 2
- QYKIQEUNHZKYBP-UHFFFAOYSA-N Vinyl ether Chemical compound C=COC=C QYKIQEUNHZKYBP-UHFFFAOYSA-N 0.000 description 2
- DHKHKXVYLBGOIT-UHFFFAOYSA-N acetaldehyde Diethyl Acetal Natural products CCOC(C)OCC DHKHKXVYLBGOIT-UHFFFAOYSA-N 0.000 description 2
- 125000002777 acetyl group Chemical class [H]C([H])([H])C(*)=O 0.000 description 2
- 150000001340 alkali metals Chemical class 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 150000001733 carboxylic acid esters Chemical class 0.000 description 2
- 150000005690 diesters Chemical class 0.000 description 2
- LQZZUXJYWNFBMV-UHFFFAOYSA-N dodecan-1-ol Chemical compound CCCCCCCCCCCCO LQZZUXJYWNFBMV-UHFFFAOYSA-N 0.000 description 2
- HNRMPXKDFBEGFZ-UHFFFAOYSA-N ethyl trimethyl methane Natural products CCC(C)(C)C HNRMPXKDFBEGFZ-UHFFFAOYSA-N 0.000 description 2
- 125000003976 glyceryl group Chemical group [H]C([*])([H])C(O[H])([H])C(O[H])([H])[H] 0.000 description 2
- 150000002334 glycols Chemical class 0.000 description 2
- 229910052938 sodium sulfate Inorganic materials 0.000 description 2
- 235000011152 sodium sulphate Nutrition 0.000 description 2
- 150000005691 triesters Chemical class 0.000 description 2
- 229920002554 vinyl polymer Polymers 0.000 description 2
- JHPBZFOKBAGZBL-UHFFFAOYSA-N (3-hydroxy-2,2,4-trimethylpentyl) 2-methylprop-2-enoate Chemical group CC(C)C(O)C(C)(C)COC(=O)C(C)=C JHPBZFOKBAGZBL-UHFFFAOYSA-N 0.000 description 1
- BQCIDUSAKPWEOX-UHFFFAOYSA-N 1,1-Difluoroethene Chemical compound FC(F)=C BQCIDUSAKPWEOX-UHFFFAOYSA-N 0.000 description 1
- VXNZUUAINFGPBY-UHFFFAOYSA-N 1-Butene Chemical compound CCC=C VXNZUUAINFGPBY-UHFFFAOYSA-N 0.000 description 1
- JAHNSTQSQJOJLO-UHFFFAOYSA-N 2-(3-fluorophenyl)-1h-imidazole Chemical compound FC1=CC=CC(C=2NC=CN=2)=C1 JAHNSTQSQJOJLO-UHFFFAOYSA-N 0.000 description 1
- OEPOKWHJYJXUGD-UHFFFAOYSA-N 2-(3-phenylmethoxyphenyl)-1,3-thiazole-4-carbaldehyde Chemical compound O=CC1=CSC(C=2C=C(OCC=3C=CC=CC=3)C=CC=2)=N1 OEPOKWHJYJXUGD-UHFFFAOYSA-N 0.000 description 1
- DPBJAVGHACCNRL-UHFFFAOYSA-N 2-(dimethylamino)ethyl prop-2-enoate Chemical compound CN(C)CCOC(=O)C=C DPBJAVGHACCNRL-UHFFFAOYSA-N 0.000 description 1
- GOXQRTZXKQZDDN-UHFFFAOYSA-N 2-Ethylhexyl acrylate Chemical compound CCCCC(CC)COC(=O)C=C GOXQRTZXKQZDDN-UHFFFAOYSA-N 0.000 description 1
- XHZPRMZZQOIPDS-UHFFFAOYSA-N 2-Methyl-2-[(1-oxo-2-propenyl)amino]-1-propanesulfonic acid Chemical compound OS(=O)(=O)CC(C)(C)NC(=O)C=C XHZPRMZZQOIPDS-UHFFFAOYSA-N 0.000 description 1
- OMIGHNLMNHATMP-UHFFFAOYSA-N 2-hydroxyethyl prop-2-enoate Chemical compound OCCOC(=O)C=C OMIGHNLMNHATMP-UHFFFAOYSA-N 0.000 description 1
- CFVWNXQPGQOHRJ-UHFFFAOYSA-N 2-methylpropyl prop-2-enoate Chemical compound CC(C)COC(=O)C=C CFVWNXQPGQOHRJ-UHFFFAOYSA-N 0.000 description 1
- YFLAJEAQOBRXIK-UHFFFAOYSA-N 2-prop-2-enoyloxyethylphosphonic acid Chemical compound OP(O)(=O)CCOC(=O)C=C YFLAJEAQOBRXIK-UHFFFAOYSA-N 0.000 description 1
- XZOYHFBNQHPJRQ-UHFFFAOYSA-N 7-methyloctanoic acid Chemical compound CC(C)CCCCCC(O)=O XZOYHFBNQHPJRQ-UHFFFAOYSA-N 0.000 description 1
- NLHHRLWOUZZQLW-UHFFFAOYSA-N Acrylonitrile Chemical compound C=CC#N NLHHRLWOUZZQLW-UHFFFAOYSA-N 0.000 description 1
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 1
- IMROMDMJAWUWLK-UHFFFAOYSA-N Ethenol Chemical compound OC=C IMROMDMJAWUWLK-UHFFFAOYSA-N 0.000 description 1
- JIGUQPWFLRLWPJ-UHFFFAOYSA-N Ethyl acrylate Chemical compound CCOC(=O)C=C JIGUQPWFLRLWPJ-UHFFFAOYSA-N 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 239000004721 Polyphenylene oxide Substances 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 1
- PJANXHGTPQOBST-VAWYXSNFSA-N Stilbene Natural products C=1C=CC=CC=1/C=C/C1=CC=CC=C1 PJANXHGTPQOBST-VAWYXSNFSA-N 0.000 description 1
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 1
- XTXRWKRVRITETP-UHFFFAOYSA-N Vinyl acetate Chemical compound CC(=O)OC=C XTXRWKRVRITETP-UHFFFAOYSA-N 0.000 description 1
- BZHJMEDXRYGGRV-UHFFFAOYSA-N Vinyl chloride Chemical compound ClC=C BZHJMEDXRYGGRV-UHFFFAOYSA-N 0.000 description 1
- 239000003513 alkali Substances 0.000 description 1
- 125000005210 alkyl ammonium group Chemical group 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- BFNBIHQBYMNNAN-UHFFFAOYSA-N ammonium sulfate Chemical compound N.N.OS(O)(=O)=O BFNBIHQBYMNNAN-UHFFFAOYSA-N 0.000 description 1
- 229910052921 ammonium sulfate Inorganic materials 0.000 description 1
- 235000011130 ammonium sulphate Nutrition 0.000 description 1
- 125000000129 anionic group Chemical group 0.000 description 1
- 239000003945 anionic surfactant Substances 0.000 description 1
- 238000012653 anionic ring-opening polymerization Methods 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 229920001400 block copolymer Polymers 0.000 description 1
- IAQRGUVFOMOMEM-UHFFFAOYSA-N butene Natural products CC=CC IAQRGUVFOMOMEM-UHFFFAOYSA-N 0.000 description 1
- CQEYYJKEWSMYFG-UHFFFAOYSA-N butyl acrylate Chemical compound CCCCOC(=O)C=C CQEYYJKEWSMYFG-UHFFFAOYSA-N 0.000 description 1
- 239000003054 catalyst Substances 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- YACLQRRMGMJLJV-UHFFFAOYSA-N chloroprene Chemical compound ClC(=C)C=C YACLQRRMGMJLJV-UHFFFAOYSA-N 0.000 description 1
- 238000003776 cleavage reaction Methods 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- PYBNTRWJKQJDRE-UHFFFAOYSA-L dodecanoate;tin(2+) Chemical compound [Sn+2].CCCCCCCCCCCC([O-])=O.CCCCCCCCCCCC([O-])=O PYBNTRWJKQJDRE-UHFFFAOYSA-L 0.000 description 1
- GVGUFUZHNYFZLC-UHFFFAOYSA-N dodecyl benzenesulfonate;sodium Chemical compound [Na].CCCCCCCCCCCCOS(=O)(=O)C1=CC=CC=C1 GVGUFUZHNYFZLC-UHFFFAOYSA-N 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- UIWXSTHGICQLQT-UHFFFAOYSA-N ethenyl propanoate Chemical compound CCC(=O)OC=C UIWXSTHGICQLQT-UHFFFAOYSA-N 0.000 description 1
- 125000003827 glycol group Chemical group 0.000 description 1
- LNMQRPPRQDGUDR-UHFFFAOYSA-N hexyl prop-2-enoate Chemical compound CCCCCCOC(=O)C=C LNMQRPPRQDGUDR-UHFFFAOYSA-N 0.000 description 1
- 229920001519 homopolymer Polymers 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- 230000003301 hydrolyzing effect Effects 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 239000012948 isocyanate Substances 0.000 description 1
- 150000002513 isocyanates Chemical class 0.000 description 1
- LVHBHZANLOWSRM-UHFFFAOYSA-N methylenebutanedioic acid Natural products OC(=O)CC(=C)C(O)=O LVHBHZANLOWSRM-UHFFFAOYSA-N 0.000 description 1
- PNLUGRYDUHRLOF-UHFFFAOYSA-N n-ethenyl-n-methylacetamide Chemical compound C=CN(C)C(C)=O PNLUGRYDUHRLOF-UHFFFAOYSA-N 0.000 description 1
- SWPMNMYLORDLJE-UHFFFAOYSA-N n-ethylprop-2-enamide Chemical compound CCNC(=O)C=C SWPMNMYLORDLJE-UHFFFAOYSA-N 0.000 description 1
- WDFKEEALECCKTJ-UHFFFAOYSA-N n-propylprop-2-enamide Chemical compound CCCNC(=O)C=C WDFKEEALECCKTJ-UHFFFAOYSA-N 0.000 description 1
- 150000002825 nitriles Chemical class 0.000 description 1
- 239000012299 nitrogen atmosphere Substances 0.000 description 1
- 150000002924 oxiranes Chemical class 0.000 description 1
- YWAKXRMUMFPDSH-UHFFFAOYSA-N pentene Chemical compound CCCC=C YWAKXRMUMFPDSH-UHFFFAOYSA-N 0.000 description 1
- PNJWIWWMYCMZRO-UHFFFAOYSA-N pent‐4‐en‐2‐one Natural products CC(=O)CC=C PNJWIWWMYCMZRO-UHFFFAOYSA-N 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 150000003009 phosphonic acids Chemical class 0.000 description 1
- 238000006068 polycondensation reaction Methods 0.000 description 1
- 229920000570 polyether Polymers 0.000 description 1
- 239000003505 polymerization initiator Substances 0.000 description 1
- 229920005862 polyol Polymers 0.000 description 1
- 150000003077 polyols Chemical class 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- UIIIBRHUICCMAI-UHFFFAOYSA-N prop-2-ene-1-sulfonic acid Chemical compound OS(=O)(=O)CC=C UIIIBRHUICCMAI-UHFFFAOYSA-N 0.000 description 1
- 125000002572 propoxy group Chemical group [*]OC([H])([H])C(C([H])([H])[H])([H])[H] 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- 229940080264 sodium dodecylbenzenesulfonate Drugs 0.000 description 1
- RNVYQYLELCKWAN-UHFFFAOYSA-N solketal Chemical compound CC1(C)OCC(CO)O1 RNVYQYLELCKWAN-UHFFFAOYSA-N 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 230000000087 stabilizing effect Effects 0.000 description 1
- PJANXHGTPQOBST-UHFFFAOYSA-N stilbene Chemical compound C=1C=CC=CC=1C=CC1=CC=CC=C1 PJANXHGTPQOBST-UHFFFAOYSA-N 0.000 description 1
- 235000021286 stilbenes Nutrition 0.000 description 1
- 150000003460 sulfonic acids Chemical class 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- DVKJHBMWWAPEIU-UHFFFAOYSA-N toluene 2,4-diisocyanate Chemical compound CC1=CC=C(N=C=O)C=C1N=C=O DVKJHBMWWAPEIU-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F2/00—Processes of polymerisation
- C08F2/04—Polymerisation in solution
- C08F2/10—Aqueous solvent
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F212/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by an aromatic carbocyclic ring
- C08F212/02—Monomers containing only one unsaturated aliphatic radical
- C08F212/04—Monomers containing only one unsaturated aliphatic radical containing one ring
- C08F212/14—Monomers containing only one unsaturated aliphatic radical containing one ring substituted by heteroatoms or groups containing heteroatoms
- C08F212/26—Nitrogen
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08J—WORKING-UP; GENERAL PROCESSES OF COMPOUNDING; AFTER-TREATMENT NOT COVERED BY SUBCLASSES C08B, C08C, C08F, C08G or C08H
- C08J3/00—Processes of treating or compounding macromolecular substances
- C08J3/02—Making solutions, dispersions, lattices or gels by other methods than by solution, emulsion or suspension polymerisation techniques
- C08J3/03—Making solutions, dispersions, lattices or gels by other methods than by solution, emulsion or suspension polymerisation techniques in aqueous media
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Organic Chemistry (AREA)
- Dispersion Chemistry (AREA)
- Macromonomer-Based Addition Polymer (AREA)
- Polyethers (AREA)
- Polymerisation Methods In General (AREA)
- Polyurethanes Or Polyureas (AREA)
- Paints Or Removers (AREA)
Abstract
【課題】 不飽和カルボン酸のα−アルコキシポリアルキレングリコールエステルと比較して加水分解に対してかなり安定しており、十分に良好な共重合性を有し、かつ必要に応じて、遊離基共重合の前に付加ポリマー、例えばポリウレタン中に配合可能な、遊離基共重合性ポリアルキレングリコールマクロモノマーの提供。
【解決手段】 α−アルコキシもしくはα−ジヒドロキシ基を有するΩ−(ジメチルイソプロペニルベンジルウレタン)ポリアルキレングリコール(式1)の製造法、並びにポリマーの分散及び架橋のために加水分解安定性マクロモノマーとしてそれらを使用する。
[式中、AはC2〜C4アルキレンであり、mは5〜900の数であり、そしてRは、C1〜C20アルキル、C6〜C18アリール、またはジオキソラン環あるいはジオキサン環を含む基、または2個の水酸基を含む基]
【選択図】なし
【解決手段】 α−アルコキシもしくはα−ジヒドロキシ基を有するΩ−(ジメチルイソプロペニルベンジルウレタン)ポリアルキレングリコール(式1)の製造法、並びにポリマーの分散及び架橋のために加水分解安定性マクロモノマーとしてそれらを使用する。
[式中、AはC2〜C4アルキレンであり、mは5〜900の数であり、そしてRは、C1〜C20アルキル、C6〜C18アリール、またはジオキソラン環あるいはジオキサン環を含む基、または2個の水酸基を含む基]
【選択図】なし
Description
本発明は、α−アルコキシもしくはα−ジヒドロキシ基を有するΩ−(ジメチルイソプロペニルベンジルウレタン)ポリアルキレングリコール、並びにポリマーを分散、架橋させるための加水分解安定性のマクロモノマーとしてそれらを使用する方法に関する。
ポリアルキレングリコールは、通常は、以下の反応式に従って、開始剤としてアルコールを用いて、エポキシド(エチレンオキシド、プロピレンオキシド、ブチレンオキシド)のアニオン性開環重合によって製造される(Ullmann Encyclopedia of Industrial Chemistry 5. ed VCH, ISBN 3-527-20100-9参照)。R'−OHがメタノールの場合は、α−メトキシ−Ω−ヒドロキシポリアルキレングリコールが生成する。
ポリアルキレングリコールマクロモノマーは、そのポリエーテル鎖の他に、反応性の共重合性末端二重結合を含むポリアルキレングリコールである。これらは、多くの用途を有する、ポリアルキレングリコール側鎖を持つ所謂櫛状ポリマー(comb polymers)の製造に重要である。末端二重結合を有するこれらのポリアルキレングリコールマクロモノマーを製造するためには、WO00/012577によると、α−アルコキシ−Ω−ヒドロキシポリアルキレングリコールを、アクリル酸、メタクリル酸もしくは他の不飽和カルボン酸とのエステル化によって、対応するα−アルコキシポリアルキレングリコールエステルに転化する。これを、次いで他のモノマーと共重合させることができる。
この場合の欠点の一つは、α−アルコキシポリアルキレングリコールエステルマクロモノマーと、これの共重合の際に生ずる櫛状ポリマーが、双方とも、貯蔵中にエステルを加水分解して、α−アルコキシポリアルキレングリコール側鎖を解裂する傾向があることである。更に、アクリル酸及びメタクリル酸のα−アルコキシポリアルキレングリコールエステルはホモ重合する傾向があり、そのため、これらのエステルの製造及び貯蔵は困難であり、重合開始剤の存在下でしか可能ではない。
遊離基共重合性ポリアルキレングリコールマクロモノマーは、水性ポリウレタン分散液の製造及び次の架橋のためにも非常に重要である。しかし、この目的のためには、ポリアルキレングリコールマクロモノマーは、遊離基共重合性不飽和基の他に、ポリウレタン分散液中への配合を可能にする少なくとも一つの遊離のヒドロキシル基または第一アミノ基を含まなければならない。
それゆえ、本発明の課題の一つは、不飽和カルボン酸のα−アルコキシポリアルキレングリコールエステルと比較して加水分解に対してかなり安定しており、十分に良好な共重合性を有し、かつ必要に応じて、遊離基共重合の前に付加ポリマー、例えばポリウレタン中に配合可能な、遊離基共重合性ポリアルキレングリコールマクロモノマーを提供することであった。
それゆえ、本発明は、次式1
[式中、
Aは、C2〜C4アルキレンであり、
mは、5〜900の整数であり、そして
Rは、C1〜C20アルキル、C6〜C18アリール、または*で示した原子価を介して式1中のアルコキシ基(A−O)の末端酸素原子に結合している次式2a、2b、2c、3a、3bもしくは3cの基であり、
Aは、C2〜C4アルキレンであり、
mは、5〜900の整数であり、そして
Rは、C1〜C20アルキル、C6〜C18アリール、または*で示した原子価を介して式1中のアルコキシ基(A−O)の末端酸素原子に結合している次式2a、2b、2c、3a、3bもしくは3cの基であり、
そしてAは、C3−またはC4−アルキレンのみからはならない]
で表される化合物を提供する。
で表される化合物を提供する。
更に本発明は、水中のオレフィン性不飽和化合物を式1の化合物と混合し、そして遊離基開始剤を加えることによって重合を開始させることによって、式1の化合物の存在下にオレフィン性不飽和化合物を遊離基重合することにより製造することができる水性分散液も提供する。
更に本発明は、水中のオレフィン性不飽和化合物を式1の化合物と遊離基重合することによって水性ポリマー分散液を製造するために、式1の化合物を使用する方法も提供する。同様に、式1の化合物は、乳化重合及び懸濁重合においてエマルションの安定化のために使用することができる。特に好ましくは、式1の化合物は、ポリウレタン分散液の製造に使用される。
(A−O)mで表されるアルコキシ鎖においては、アルコキシ単位の合計数は好ましくは5〜300、特に8〜300である。このアルコキシ鎖は、ホモポリマーであるか、または異なるアルコキシ単位の交互ブロックを有するブロックポリマー鎖であることができる。またこれは、アルコキシ単位のランダムシーケンスを有する鎖であることもできる。前記アルコキシ単位は、好ましくは、エトキシ単位のみであるか、またはエトキシ単位とプロポキシ単位の混合物のいずれかである。
好ましい態様の一つでは、−(A−O)m−Rは、次式のアルコキシ鎖である。
[式中、
aは、0〜300、好ましくは0〜80の数であり、
bは、5〜300、好ましくは5〜200の数である]
更に別の好ましい態様の一つでは、−(A−O)m−は、8〜300個のエトキシ単位を有するエトキシ基である。
aは、0〜300、好ましくは0〜80の数であり、
bは、5〜300、好ましくは5〜200の数である]
更に別の好ましい態様の一つでは、−(A−O)m−は、8〜300個のエトキシ単位を有するエトキシ基である。
更に別の好ましい態様の一つでは、Rは、式2a、2b、3aまたは3bのグリセロールケタールまたはトリメチロールプロパンケタール/アセタール基である。
全ての態様の共通の特徴は、好ましくは基(A−O)の少なくとも50モル%、特に60〜100モル%が、エトキシ基であることである。
本発明の好ましい主題は、式2a、2b及び3a、3bに従う基Rを有する式1の化合物からケタールもしくはアセタール基の加水分解解裂によって生ずる次式4及び5の化合物である。記号A及びmは、式1について記載したものと同じ意味を有する。
式1、4及び5で表される化合物は、以下に重合性マクロモノマーとも称する。
前記重合性マクロモノマーの製造法及び本発明による分散液の典型的な用途は、以下により詳しく説明し、かつ例に基づいて例示する。
前記重合性マクロモノマーは、α位置にアルコキシもしくはグリセリルケタール/アセタールまたはトリメチルプロパンケタール/アセタール基を含むΩ−モノヒドロキシ官能性ポリアルキレングリコールから、ウレタンの生成に関して従来公知の触媒の存在下にα,α−ジメチルメタ−イソプロペニルベンジルイソシアネート(式6)との化学量論的な反応によって製造される。式4及び5のジオール官能性マクロモノマーの場合には、ウレタン生成段階の後に、追加的に、α−位置グリセリルケタール/アセタールもしくはトリメチロールプロパンケタール/アセタール基からのケタール/アセタール基を加水分解により解裂させる。この際、この工程は、ウレタン結合の解裂を伴うことなく行われる。
曇り点によって定義される重合性マクロモノマーの水中への溶解度、並びにそれらの親水化及び分散効果の程度は、アルキレンオキシド単位の比率及び数、好ましくはプロピレンオキシドに対するエチレンオキシドの比率及び数によって調節することができる。
本発明のマクロモノマーは、それら自体はホモ重合可能ではない。なぜならば、Ω位置α−メチルスチリル基は、アクリル酸もしくはメタクリル酸エステル基とは対照的に、ホモ重合性ではないからである(B. Vollmert, Grundriss der Makromolekularen Chemie [高分子化学の概要] volume I p. 55参照)。それゆえ、本発明のマクロモノマーは、貯蔵安定性である。
該重合性マクロモノマーとオレフィン性不飽和コモノマーとの遊離基開始共重合により、本発明のコポリマー分散液が生成される。該マクロモノマーと重合することができる適当なモノマーは、例えば次のものである。
− ビニルモノマー、例えばビニルアルコールのカルボン酸エステル、例えば、酢酸ビニル、プロピオン酸ビニル、イソノナン酸のビニルエーテルもしくはイソデカン酸のビニルエーテル、スチレン、及びスチルベン、
− オレフィン性不飽和カルボン酸エステル、例えばアクリル酸エチル、アクリル酸n−ブチル、アクリル酸イソブチル、アクリル酸ヘキシル、アクリル酸2−エチルヘキシル、アクリル酸ヒドロキシエチル、及び対応するメタクリル酸エステル、
− オレフィン性不飽和カルボン酸、例えばアクリル酸、メタクリル酸及びイタコン酸、並びにそれらのナトリウム、カリウム及びアンモニウム塩、
− オレフィン性不飽和スルホン酸及びホスホン酸並びにそれらのアルカリ金属塩及びアンモニウム塩、例えばアクリルアミドメチルプロパンスルホン酸並びにそれのアルカリ金属またはアンモニウム、アルキルアンモニウムもしくはヒドロキシアルキルアンモニウム塩、アリルスルホン酸及びそれのアルカリ金属またはアンモニウム塩、アクリロイルオキシエチルホスホン酸並びにそれのアンモニウムまたはアルカリ金属塩、並びに対応するメタクリル酸誘導体、
− オレフィン性不飽和アミン、アンモニウム塩、ニトリル及びアミド、例えばジメチルアミノエチルアクリレート、アクリロイルオキシエチルトリメチルアンモニウムハライド、アクリロニトリル、N−メタクリルアミド、N−エチルアクリルアミド、N−プロピルアクリルアミド、及び対応するメタクリル酸誘導体及びビニルメチルアセトアミド、
− オレフィン、例えばエチレン、プロピレン及びブテン、ペンテン、1,3−ブタジエン、及びクロロプレン、
− ビニルハライド、例えば塩化ビニル、塩化ビニリデン及びフッ化ビニリデン。
− ビニルモノマー、例えばビニルアルコールのカルボン酸エステル、例えば、酢酸ビニル、プロピオン酸ビニル、イソノナン酸のビニルエーテルもしくはイソデカン酸のビニルエーテル、スチレン、及びスチルベン、
− オレフィン性不飽和カルボン酸エステル、例えばアクリル酸エチル、アクリル酸n−ブチル、アクリル酸イソブチル、アクリル酸ヘキシル、アクリル酸2−エチルヘキシル、アクリル酸ヒドロキシエチル、及び対応するメタクリル酸エステル、
− オレフィン性不飽和カルボン酸、例えばアクリル酸、メタクリル酸及びイタコン酸、並びにそれらのナトリウム、カリウム及びアンモニウム塩、
− オレフィン性不飽和スルホン酸及びホスホン酸並びにそれらのアルカリ金属塩及びアンモニウム塩、例えばアクリルアミドメチルプロパンスルホン酸並びにそれのアルカリ金属またはアンモニウム、アルキルアンモニウムもしくはヒドロキシアルキルアンモニウム塩、アリルスルホン酸及びそれのアルカリ金属またはアンモニウム塩、アクリロイルオキシエチルホスホン酸並びにそれのアンモニウムまたはアルカリ金属塩、並びに対応するメタクリル酸誘導体、
− オレフィン性不飽和アミン、アンモニウム塩、ニトリル及びアミド、例えばジメチルアミノエチルアクリレート、アクリロイルオキシエチルトリメチルアンモニウムハライド、アクリロニトリル、N−メタクリルアミド、N−エチルアクリルアミド、N−プロピルアクリルアミド、及び対応するメタクリル酸誘導体及びビニルメチルアセトアミド、
− オレフィン、例えばエチレン、プロピレン及びブテン、ペンテン、1,3−ブタジエン、及びクロロプレン、
− ビニルハライド、例えば塩化ビニル、塩化ビニリデン及びフッ化ビニリデン。
式4及び5のジオール官能性マクロモノマーの場合は、上記の共重合は、ポリウレタンに該マクロモノマーを混入してから、式4及び5のマクロモノマーをイソシアネート(例えば、トルエンジイソシアネート)及び、必要に応じて、ポリウレタンの製造に慣用の他のポリオールと重縮合することによって行うこともできる。
更に本発明は、式1、4及び5の上に定義したマクロモノマーをポリマー分散液の安定化に使用する方法にも関する。
この目的に関しては、式1、4及び5の化合物は、懸濁もしくは乳化重合にまたは水性ポリウレタン分散液の製造に乳化剤としてそれら単独で使用されるか、あるいは従来公知のアニオン性及び/または非イオン性界面活性剤との混合物として使用される。
慣用のアニオン性界面活性剤は、アルキル硫酸ナトリウム、ドデシルベンゼンスルホン酸ナトリウム、アルキルスルホン酸ナトリウム、アルキルポリエチレングリコールエーテル硫酸ナトリウムもしくはアンモニウム、アルキルフェノールポリエチレングリコールエーテル硫酸ナトリウムもしくはアンモニウム、及びアルキルポリエチレングリコールエーテルリン酸モノ−、ジ−もしくはトリエステル及びこれらの混合物、並びにアルキルフェノールポリエチレングリコールエーテルリン酸モノ−、ジ−もしくはトリエステル及びこれらの混合物である。
本発明のマクロモノマーは、上記の他のコモノマーとの共重合の前と後のいずれにおいても、加水分解に対して非常に安定している。なぜならば、アクリル酸及びメタクリル酸に基づくマクロモノマーとは対照的に、共重合性α−メチルスチリル基がウレタン結合を介してポリアルコキシ鎖に結合しているからである。これは、一方では、水溶液として本発明のマクロモノマーを貯蔵することを可能にし、また他方では、本発明のマクロモノマーから製造されたポリマー分散液は、高められた温度において水の存在下でさえも安定しており、ポリアルコキシ側鎖を解裂しない。
以下の例は、本発明をより詳しく例示するものである。
例1
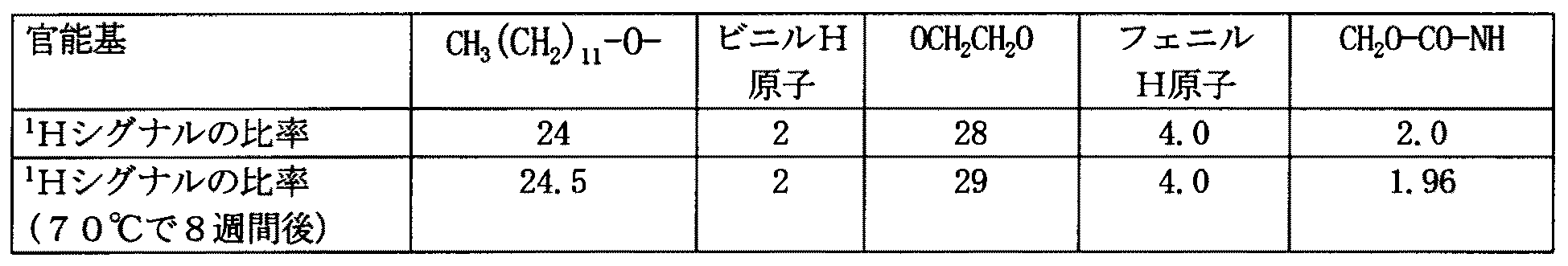
商業的に入手可能な500g/モルの分子量を有するα−メトキシ−Ω−ヒドロキシポリエチレングリコール(ヒドロキシル価:113mgKOH/g)250gを、減圧下に80℃で1時間乾燥する。次いで、窒素雰囲気下に、ジラウリン酸錫0.25g及びα,α−ジメチルメタ−イソプロペニルベンジルイソシアネート100.6gを加え、そしてこの混合物を120℃の温度で5時間攪拌した。80℃に冷却した後、水7gを加え、そしてこの混合物を更に1時間攪拌した。次いで、このサンプルをロータリーエバポレーターで減圧下に乾燥した。DIN53240に従い測定したヒドロキシル価は、反応後には2.3mgKOH/gに減少した。Kaufmann(DGF C−V11b法)によるヨウ素価は34.1gヨウ素/100gであった。H原子の比率を、1H−NMRによって測定した。このサンプルを、安定化剤を加えずに、70℃で8週間貯蔵した後に再び試験した。マクロモノマーの重合も加水分解も確認されなかった。
商業的に入手可能な500g/モルの分子量を有するα−メトキシ−Ω−ヒドロキシポリエチレングリコール(ヒドロキシル価:113mgKOH/g)250gを、減圧下に80℃で1時間乾燥する。次いで、窒素雰囲気下に、ジラウリン酸錫0.25g及びα,α−ジメチルメタ−イソプロペニルベンジルイソシアネート100.6gを加え、そしてこの混合物を120℃の温度で5時間攪拌した。80℃に冷却した後、水7gを加え、そしてこの混合物を更に1時間攪拌した。次いで、このサンプルをロータリーエバポレーターで減圧下に乾燥した。DIN53240に従い測定したヒドロキシル価は、反応後には2.3mgKOH/gに減少した。Kaufmann(DGF C−V11b法)によるヨウ素価は34.1gヨウ素/100gであった。H原子の比率を、1H−NMRによって測定した。このサンプルを、安定化剤を加えずに、70℃で8週間貯蔵した後に再び試験した。マクロモノマーの重合も加水分解も確認されなかった。
1H−NMRによって測定した貯蔵の前と後の官能基の比率を表1に示す。
例2
α−メトキシ−Ω−ヒドロキシポリエチレングリコールの代わりに、510g/モルの分子量を有するα−ドデシル−Ω−ヒドロキシポリエチレングリコール(ドデシルアルコールエトキシレート)(ヒドロキシル価:110mgKOH/g)を使用したことを除き、例1と同様に行った。反応の結果、ヒドロキシル価は2mgKOH/gまで減少した。このサンプルを、1H−NMRによって試験した。このサンプルを、安定化剤を加えずに70℃で8週間貯蔵した後に再び試験した。マクロモノマーの重合も、加水分解も確認されなかった。1H−NMRによって測定した官能基の比率を表2に示す。
α−メトキシ−Ω−ヒドロキシポリエチレングリコールの代わりに、510g/モルの分子量を有するα−ドデシル−Ω−ヒドロキシポリエチレングリコール(ドデシルアルコールエトキシレート)(ヒドロキシル価:110mgKOH/g)を使用したことを除き、例1と同様に行った。反応の結果、ヒドロキシル価は2mgKOH/gまで減少した。このサンプルを、1H−NMRによって試験した。このサンプルを、安定化剤を加えずに70℃で8週間貯蔵した後に再び試験した。マクロモノマーの重合も、加水分解も確認されなかった。1H−NMRによって測定した官能基の比率を表2に示す。
例3
500g/モルの分子量を有する商業的に入手可能なα−メトキシ−Ω−ヒドロキシポリエチレングリコールの代わりに、4796g/モルの分子量を有する商業的に入手可能なα−メトキシ−Ω−ヒドロキシポリエチレングリコール(ヒドロキシル価:11.7mgKOH/g)287.6gを使用し、かつα,α−ジメチルメタ−イソプロペニルベンジルイソシアネートの量を12.1gに減少して当モル量の使用としたことを除き、例1と同様に行った。このサンプルを1H−NMRによって分析した。反応後のヒドロキシル価は1.5mgKOH/gであった。ヨウ素価は、5.3gヨウ素/100gであった。
500g/モルの分子量を有する商業的に入手可能なα−メトキシ−Ω−ヒドロキシポリエチレングリコールの代わりに、4796g/モルの分子量を有する商業的に入手可能なα−メトキシ−Ω−ヒドロキシポリエチレングリコール(ヒドロキシル価:11.7mgKOH/g)287.6gを使用し、かつα,α−ジメチルメタ−イソプロペニルベンジルイソシアネートの量を12.1gに減少して当モル量の使用としたことを除き、例1と同様に行った。このサンプルを1H−NMRによって分析した。反応後のヒドロキシル価は1.5mgKOH/gであった。ヨウ素価は、5.3gヨウ素/100gであった。
このサンプルを、安定化剤を加えずに70℃で8週間貯蔵した後に再び試験した。マクロモノマーの重合も、加水分解も確認されなかった。
1H−HMRによって測定した貯蔵前と後の官能基の比率を表3に示す。
例4
500g/モルの分子量を有する商業的に入手可能なα−メトキシ−Ω−ヒドロキシポリエチレングリコールの代わりに、1396g/モルの分子量及び以下の構造、すなわち:
CH3-O-(CH2CHCH3-O)5- (CH2CH2O)25OH
を有するα−メトキシ−Ω−ヒドロキシポリプロピレングリコール−ポリエチレングリコールブロックコポリマー(ヒドロキシル価: 40.2mgKOH/g)279.1gを使用し、かつα,α−ジメチルメタ−イソプロペニルベンジルイソシアネートの量を40.24gに調節して当モル量の使用としたことを除き、例1と同様に行った。このサンプルを、1H−NMRで分析した。反応後のヒドロキシル価は1.9mgKOH/gであり、ヨウ素価は14.8gヨウ素/100gであった。これは、二重結合当たり1709g/モルの分子量の相当する。この生成物は、水中で28℃の曇り点を有する。
500g/モルの分子量を有する商業的に入手可能なα−メトキシ−Ω−ヒドロキシポリエチレングリコールの代わりに、1396g/モルの分子量及び以下の構造、すなわち:
CH3-O-(CH2CHCH3-O)5- (CH2CH2O)25OH
を有するα−メトキシ−Ω−ヒドロキシポリプロピレングリコール−ポリエチレングリコールブロックコポリマー(ヒドロキシル価: 40.2mgKOH/g)279.1gを使用し、かつα,α−ジメチルメタ−イソプロペニルベンジルイソシアネートの量を40.24gに調節して当モル量の使用としたことを除き、例1と同様に行った。このサンプルを、1H−NMRで分析した。反応後のヒドロキシル価は1.9mgKOH/gであり、ヨウ素価は14.8gヨウ素/100gであった。これは、二重結合当たり1709g/モルの分子量の相当する。この生成物は、水中で28℃の曇り点を有する。
前記サンプルを、安定化剤を加えずに、70℃で8週間貯蔵した後に再び試験した。マクロモノマーの重合も、加水分解も確認されなかった。
1H−NMRで測定した貯蔵の前と後の官能基の比率を表4に示す。
例5
500g/モルの分子量を有する商業的に入手可能なα−メトキシ−Ω−ヒドロキシポリエチレングリコールの代わりに、1345g/モルの分子量及び以下の構造、すなわち
500g/モルの分子量を有する商業的に入手可能なα−メトキシ−Ω−ヒドロキシポリエチレングリコールの代わりに、1345g/モルの分子量及び以下の構造、すなわち
[式中、n=27]
を有するα−(1,2−O−イソプロピリデングリセロール)−Ω−ヒドロキシポリエチレングリコール(ヒドロキシル価: 41.7mgKOH/g)336.25gを使用し、そしてα,α−ジメチルメタ−イソプロペニルベンジルイソシアネートの量を50.25gに調節して当モル量の使用としたことを除き、例1と同様に行った。このサンプルを、1H−NMRで分析した。反応後のヒドロキシル価は2.1mgKOH/gであった。
を有するα−(1,2−O−イソプロピリデングリセロール)−Ω−ヒドロキシポリエチレングリコール(ヒドロキシル価: 41.7mgKOH/g)336.25gを使用し、そしてα,α−ジメチルメタ−イソプロペニルベンジルイソシアネートの量を50.25gに調節して当モル量の使用としたことを除き、例1と同様に行った。このサンプルを、1H−NMRで分析した。反応後のヒドロキシル価は2.1mgKOH/gであった。
このサンプルを、安定化剤を添加せずに70℃で8週間貯蔵した後に再び試験した。マクロモノマーの重合も、加水分解も確認されなかった。
1H−NMRで測定した貯蔵の前と後の官能基の比率を表5に示す。
例6
ケタールの解裂:
例6の反応生成物100gを、水35g及びリン酸2gで溶解し、そして2時間80℃で攪拌した。次いでこの混合物を減圧下に脱水し、そして得られた生成物を希水酸化ナトリウム溶液でpH6〜7に中和し、再び減圧下に脱水し、そして濾過した。
ケタールの解裂:
例6の反応生成物100gを、水35g及びリン酸2gで溶解し、そして2時間80℃で攪拌した。次いでこの混合物を減圧下に脱水し、そして得られた生成物を希水酸化ナトリウム溶液でpH6〜7に中和し、再び減圧下に脱水し、そして濾過した。
得られた生成物は、以下の構造、すなわち
[n=23]
に一致し、86mgKOH/gのOH価及び17.4gヨウ素/100gのヨウ素価を有した。
に一致し、86mgKOH/gのOH価及び17.4gヨウ素/100gのヨウ素価を有した。
Claims (15)
- −(A−O)m−単位の少なくとも50モル%がエトキシ単位である、請求項1〜3のいずれか一つの化合物。
- 水中のオレフィン性不飽和化合物を、式1、4もしくは5の化合物と混合し、そして遊離基開始剤を加えて重合を開始させることによって、前記式1、4もしくは5の化合物の存在下にオレフィン性不飽和化合物の遊離基重合により製造可能な水性分散液。
- 式1、4もしくは5の化合物が水中で少なくとも20℃の曇り点を有する、請求項5の水性分散液。
- RがC1〜C20アルキルである、請求項5または6の水性分散液。
- Rがグリセロールもしくはトリメチロールプロパンのケタールである、請求項5または6の水性分散液。
- −(A−O)m−が、エトキシ基を少なくとも50モル%の割合で含む混合アルコキシ基である、請求項5〜9のいずれか一つの水性分散液。
- −(A−O)m−が、8〜240個のエトキシ単位を有するエトキシ鎖である、請求項5〜9のいずれか一つの水性分散液。
- 水中のオレフィン性不飽和化合物を式1、4もしくは5の化合物と遊離基重合することによって水性ポリマー分散液を製造するために、式1の化合物を使用する方法。
- 乳化重合もしくは懸濁重合においてエマルション安定化のための添加剤として、請求項1、4もしくは5の化合物を使用する方法。
- 水性ポリウレタン分散液を製造するために、式1、4もしくは5の化合物を使用する方法。
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102004017097A DE102004017097A1 (de) | 2004-04-07 | 2004-04-07 | Copolymerisierbare Polyalkylenglykol-Makromonomere, deren Herstellung und Verwendung |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2005298822A true JP2005298822A (ja) | 2005-10-27 |
Family
ID=34895505
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2005110021A Withdrawn JP2005298822A (ja) | 2004-04-07 | 2005-04-06 | 共重合性ポリアルキレングリコールマクロモノマー並びにそれらの製造法及び使用法 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US7514501B2 (ja) |
| EP (1) | EP1584631B1 (ja) |
| JP (1) | JP2005298822A (ja) |
| CN (1) | CN1680300A (ja) |
| DE (2) | DE102004017097A1 (ja) |
| ES (1) | ES2314507T3 (ja) |
| PT (1) | PT1584631E (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010275551A (ja) * | 2009-05-27 | 2010-12-09 | Bayer Materialscience Ag | 放出の少ない軟質ポリウレタンフォームの製造方法 |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1954140B1 (en) | 2005-11-22 | 2013-05-29 | Segetis, Inc. | Glycerol levulinate ketals and their use |
| BR112015012471B1 (pt) | 2012-11-29 | 2020-05-19 | Segetis Inc | cetais de carbóxi éster , métodos de fabricação e uso dos mesmos. |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU4387793A (en) * | 1992-05-29 | 1993-12-30 | Union Carbide Chemicals & Plastics Technology Corporation | Aqueous latexes containing macromonomeres |
| US5451641A (en) * | 1992-08-24 | 1995-09-19 | Rohm And Haas Company | Multi-stage polymer particles having a hydrophobically-modified, ionically-soluble stage |
| JP4003332B2 (ja) * | 1999-01-26 | 2007-11-07 | 東レ株式会社 | 眼用レンズ用モノマー、それを用いたポリマー、眼用レンズおよびコンタクトレンズ |
| FR2811674B1 (fr) * | 2000-07-17 | 2003-07-25 | Corning Sa | Resines et articles photochromiques; preparation; compositions precurseurs |
| WO2002081537A1 (de) * | 2001-04-06 | 2002-10-17 | Basf Aktiengesellschaft | Zellige polyisocyanat-polyadditionsprodukte |
| US6716898B2 (en) * | 2001-05-18 | 2004-04-06 | Eastman Chemical Company | Amber polyester compositions for packaging food and beverages |
| US6827759B2 (en) | 2001-08-03 | 2004-12-07 | Tosoh Smd, Inc. | Method for reducing the oxygen and oxide content in cobalt to produce cobalt sputtering targets |
| US7244784B2 (en) * | 2002-06-14 | 2007-07-17 | Rohm And Haas Company | Aqueous nanoparticle dispersions |
| DE10237195A1 (de) * | 2002-08-14 | 2004-02-26 | Bayer Ag | Wasserverdünnbare Polyester mit cyclischer Imid- und Isocyanuratstruktur |
| US6787589B2 (en) * | 2002-10-31 | 2004-09-07 | Eastman Chemical Company | Amber polyester compositions and container articles produced therefrom |
| US20040146674A1 (en) * | 2003-01-29 | 2004-07-29 | Howell Earl Edmondson | Acetaldehyde scavenging by addition of active scavengers to bottle closures |
| US7232478B2 (en) * | 2003-07-14 | 2007-06-19 | Enthone Inc. | Adhesion promotion in printed circuit boards |
| US7449440B2 (en) * | 2005-03-11 | 2008-11-11 | Rohm And Haas Company | Nonionic associative thickener containing vinyl addition polymer backbone |
-
2004
- 2004-04-07 DE DE102004017097A patent/DE102004017097A1/de not_active Withdrawn
-
2005
- 2005-03-11 CN CNA2005100545644A patent/CN1680300A/zh active Pending
- 2005-03-31 ES ES05007009T patent/ES2314507T3/es not_active Expired - Lifetime
- 2005-03-31 PT PT05007009T patent/PT1584631E/pt unknown
- 2005-03-31 DE DE502005005924T patent/DE502005005924D1/de not_active Expired - Lifetime
- 2005-03-31 EP EP05007009A patent/EP1584631B1/de not_active Expired - Lifetime
- 2005-04-06 JP JP2005110021A patent/JP2005298822A/ja not_active Withdrawn
- 2005-04-07 US US11/100,687 patent/US7514501B2/en not_active Expired - Fee Related
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010275551A (ja) * | 2009-05-27 | 2010-12-09 | Bayer Materialscience Ag | 放出の少ない軟質ポリウレタンフォームの製造方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| DE102004017097A1 (de) | 2005-11-10 |
| DE502005005924D1 (de) | 2008-12-24 |
| EP1584631B1 (de) | 2008-11-12 |
| EP1584631A1 (de) | 2005-10-12 |
| PT1584631E (pt) | 2008-12-31 |
| CN1680300A (zh) | 2005-10-12 |
| ES2314507T3 (es) | 2009-03-16 |
| US7514501B2 (en) | 2009-04-07 |
| US20050228125A1 (en) | 2005-10-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101991078B1 (ko) | 냉동-해동 안정한 에멀전 폴리머용 신규한 반응성 계면 활성제 및 그 코팅 | |
| US9777080B2 (en) | Dispersion stabilizer for suspension polymerization, and manufacturing method for vinyl resin | |
| US20050261457A1 (en) | Copolymers made of alkylene oxides and glycidyl ethers and use thereof as polymerisable emulsifiers | |
| CN106749777A (zh) | 水溶性疏水缔合共聚物 | |
| US4101490A (en) | Process for preparing aqueous emulsions of addition polymers with built-in emulsifier | |
| JP2001064332A (ja) | 水性ポリマー分散液、その製造法及び使用法 | |
| US7812114B2 (en) | Block copolymer by reacting alkylene oxide and glycidyl ether in presence of unsaturated monomer | |
| EP3205694A1 (en) | Carboxyl-group-containing polymer composition | |
| US8142681B2 (en) | Aqueous surfactant compositions with a low pour point | |
| JP2006505661A (ja) | スチレンオキシド含有コポリマー並びにそれの乳化剤及び分散剤としての使用 | |
| JP6857640B2 (ja) | 水分散体 | |
| JP5968679B2 (ja) | 乳化重合用反応性乳化剤 | |
| JP2005298822A (ja) | 共重合性ポリアルキレングリコールマクロモノマー並びにそれらの製造法及び使用法 | |
| JPH07228613A (ja) | 重合用乳化分散剤 | |
| JP5566645B2 (ja) | 泥水用分散剤 | |
| JP2006232947A (ja) | 乳化重合用乳化剤 | |
| CN109721720B (zh) | 一种酯类聚醚、其制备方法、在减水剂制备中的应用及由该酯类聚醚制得的减水剂 | |
| JP5722303B2 (ja) | 非イオン性界面活性剤のエマルジョン重合(iii)のための乳化剤としての使用 | |
| JPH0223562B2 (ja) | ||
| JP4782481B2 (ja) | 乳化重合用乳化剤 | |
| JP2006232946A (ja) | 乳化重合用乳化剤 | |
| JP4160438B2 (ja) | 新規硫酸エステル型界面活性剤 | |
| WO2013028950A1 (en) | Extended surfactant for emulsion polymerization | |
| JP2909343B2 (ja) | 界面活性剤組成物 | |
| JP6857639B2 (ja) | 水分散体 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A300 | Application deemed to be withdrawn because no request for examination was validly filed |
Free format text: JAPANESE INTERMEDIATE CODE: A300 Effective date: 20080701 |