JP2004203820A - 鉄キレート剤 - Google Patents
鉄キレート剤 Download PDFInfo
- Publication number
- JP2004203820A JP2004203820A JP2002376668A JP2002376668A JP2004203820A JP 2004203820 A JP2004203820 A JP 2004203820A JP 2002376668 A JP2002376668 A JP 2002376668A JP 2002376668 A JP2002376668 A JP 2002376668A JP 2004203820 A JP2004203820 A JP 2004203820A
- Authority
- JP
- Japan
- Prior art keywords
- group
- iron
- carbon atoms
- pyrazolin
- methyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Abstract
【課題】鉄が関与する疾病に対する広範囲な組織保護剤として応用できる鉄キレート剤を提供する。
【解決手段】式(I):
(式中、R1は、水素原子、アリール基、炭素数1〜5のアルキル基又は総炭素数3〜6のアルコキシカルボニルアルキル基を表し;R2は、水素原子、アリールオキシ基、アリールメルカプト基、炭素数1〜5のアルキル基又は炭素数1〜3のヒドロキシアルキル基を表し;あるいは、R1及びR2は、共同して炭素数3〜5のアルキレン基を表し;R3は、水素原子、アルキル基、シクロアルキル基、ヒドロキシアルキル基、ベンジル基、ナフチル基、フェニル基、アルキルアミノ基、ハロゲン原子、カルボキシル基、シアノ基、水酸基、ニトロ基、置換基で置換されたフェニル基等を表す。)で示されるピラゾロン誘導体若しくはその生理学的に許容される塩、又はそれらの水和物若しくは溶媒和物を有効成分として含む、鉄キレート剤。
【選択図】 なし
【解決手段】式(I):
(式中、R1は、水素原子、アリール基、炭素数1〜5のアルキル基又は総炭素数3〜6のアルコキシカルボニルアルキル基を表し;R2は、水素原子、アリールオキシ基、アリールメルカプト基、炭素数1〜5のアルキル基又は炭素数1〜3のヒドロキシアルキル基を表し;あるいは、R1及びR2は、共同して炭素数3〜5のアルキレン基を表し;R3は、水素原子、アルキル基、シクロアルキル基、ヒドロキシアルキル基、ベンジル基、ナフチル基、フェニル基、アルキルアミノ基、ハロゲン原子、カルボキシル基、シアノ基、水酸基、ニトロ基、置換基で置換されたフェニル基等を表す。)で示されるピラゾロン誘導体若しくはその生理学的に許容される塩、又はそれらの水和物若しくは溶媒和物を有効成分として含む、鉄キレート剤。
【選択図】 なし
Description
【0001】
【発明の属する技術分野】
本発明は、ピラゾロン誘導体若しくはその生理学的に許容される塩、又はそれらの水和物若しくは溶媒和物を有効成分として含む鉄キレート剤、並びに鉄と3−メチル−1−フェニル−2−ピラゾリン−5−オンとの1:6錯体に関する。
【0002】
【従来技術】
ヒトの体内には約4.5gの鉄が存在し、その約2/3は、ヘモグロビン鉄として酸素運搬に関与し、その他はミオグロビン、酵素の補欠分子族、鉄輸送タンパク(トランスフェリン、ラクトフェリン)、並びに鉄貯蔵タンパク(フェリチン、ヘモシデリン)として存在している。1日当たりの血清中における鉄のターンオーバーは35mgと考えられ、生体は鉄に対して能動的なシステムを有しているため、生体内では鉄欠乏症や鉄過剰症の発症が容易に起こり得る。
【0003】
酸化ストレスは、鉄、スーパーオキサイド又は過酸化物などのプロ−オキシダンツ(pro-oxidants)と抗酸化剤(antioxidant)との平衡状態の乱れにより起きる状態を言う。鉄が生体に対し酸化ストレスを与えるメカニズムは、以下のように考えられている。即ち、遊離状態の2価鉄は様々な反応を行い、強力な活性酸素種の生成を引き起こす。例えば、フェントン反応(Fenton reaction)と称されるヒドロキシルラジカル(・OH)を生成する反応(Fe2 + H2O2 → Fe3 + OH- +・OH)がある。ここで生じたヒドロキシルラジカル(・OH)は高い酸化能(Eo=+2.7V)を有し、生体中のほとんどの(高)分子と直ちに反応して障害を与える。特に脂質(H・CR3)とヒドロキシルラジカル(・OH)が反応すると、開始反応を経て脂質過酸化の連鎖反応を引き起こす。従って、ごく僅かなイニシエーター(initiator)(この場合、・OH)の発生が大きな生体障害を引き起こす元凶となる。
【0004】
一方、生体内には、多様な鉄キレーターが存在し、活性な遊離2価鉄を不活性な3価型に変換し、捕捉することにより、遊離2価鉄による組織障害を防止している。このような生体内鉄キレーターとして、フェリチン(Ferritin)及びヘモシダリン(Haemosiderin)が知られている。フェリチンは水溶性タンパク質で細胞質に主に分布し、ヘモシダリンは水不溶性タンパク質で、ライソゾーム内に局在している。フェリチンは20kDaの分子量からなるサブユニット24個からなり、フェリチン1分子で鉄原子を最高4500個捕捉できる。フェリチンによる鉄貯蔵機構は、2価鉄がフェリチンと接触するとフェリチンの金属結合部位(metal-binding site)に結合し、ここで鉄が2価から3価に酸化され、3価の形で貯蔵される。
【0005】
過剰に鉄を摂取した場合、最初にフェリチンに鉄が取り込まれ、その後フェリチンがライソゾーム内で消化された後、ヘモシダリンが鉄を取り込むことにより、遊離鉄による酸化ストレスを抑制している。フェリチンからの鉄の遊離は、3価鉄が2価鉄に還元されることにより起きる。キサンチンオキシダーゼやある種の還元酵素、それ以外では尿酸・アスコルビン酸・クエン酸・炭酸イオン・乳酸等の低分子化合物によって鉄が還元された後にフェリチンからの鉄の遊離が促進される。
【0006】
フェリチンやヘモシダリン以外にも、血漿中には効果的に遊離鉄を捕捉するトランスフェリンと呼ばれる一群のタンパク質があり、血漿中の遊離鉄をきわめて低い濃度に維持している。この中にはヒト血漿トランスフェリン、卵白オボトランスフェリン(ovotransferrin)、ラクトフェリン、メラノトランスフェリン、及びウテロフェリン等が含まれる。トランスフェリンと鉄との結合は、水素イオン濃度の影響を受けやすく、微酸性条件下では炭酸イオンが炭酸ガスとなり遊離するために、同時に鉄イオンもトランスフェリンから遊離してくる。更にこの酸による鉄イオンの遊離は鉄を還元しうる物質が共存する条件で加速される。
【0007】
トランスフェリンは肝臓で合成されて血漿中に放出され、遊離の鉄を捕捉する。通常、血漿中のトランスフェリンの鉄飽和率は50−60%程度であり、鉄との結合に対する予備能を有している。鉄と結合したトランスフェリンは細胞膜表面に存在するトランスフェリンレセプターを通って細胞内に入り、酸性条件下で鉄を遊離する。この鉄はDNA合成や鉄含有酵素の合成に用いられ、トランスフェリンは細胞外に放出されて再利用される。トランスフェリンに結合した鉄は過酸化水素刺激によるフェントン反応からのヒドロキシルラジカル(・OH)の生成には関与せず、生体を酸化ストレスから保護している。
【0008】
血漿中の鉄が過剰になる病態としては、ヘモクロマトーシス(hemochromatosis)、β−サラセミア(β−thalassaemia)、そして組織が障害を受けてトランスフェリンが処理出来ない量の鉄が放出されたとき(抗癌剤治療時、体外循環時、多臓器不全時の溶血)等が知られている。鉄が遊離鉄として血漿中に放出されると、血漿中には3価鉄を還元できる物質(アスコルビン酸、尿酸、グルタチオン、タンパク質のチオール基等)が多量に存在するため、2価鉄に還元される。2価鉄は様々な活性酸素種を生成し、直接生体高分子と反応したり、連鎖反応によって過酸化脂質を生成する元凶になる。このため、生体にはこの有害な2価鉄をより毒性の低い3価鉄に速やかに酸化するフェロキシダーゼ酵素(ferroxidase enzyme)であるカエルロプラスミン(caeruloplasmin)が存在している。
【0009】
一方、下記式(I):
【化3】
(式中、R1は水素原子、アリール、炭素数1〜5のアルキル又は総炭素数3〜6のアルコキシカルボニルアルキルを表し、R2は、水素原子、アリールオキシ、アリールメルカプト、炭素数1〜5のアルキル又は1〜3のヒドロキシアルキルを表し、あるいは、R1及びR2は、共同して炭素数3〜5のアルキレンを表し、R3は水素原子、炭素数1〜5のアルキル、炭素数5〜7のシクロアルキル、炭素数1〜3のヒドロキシアルキル、ベンジル、ナフチル又はフェニル、又は炭素数1〜5のアルコキシ、炭素数1〜3のヒドロキシアルキル、総炭素数2〜5のアルコキシカルボニル、炭素数1〜3のアルキルメルカプト、炭素数1〜4のアルキルアミノ、総炭素数2〜8のジアルキルアミノ、ハロゲン原子、トリフルオロメチル、カルボキシル、シアノ、水酸基、ニトロ、アミノ、及びアセトアミドからなる群から選ばれる同一若しくは異なる1〜3個の置換基で置換されたフェニルを表す。)で表されるピラゾロン誘導体については、医薬の用途として、脳機能正常化作用(特許文献1参照)、過酸化脂質生成抑制作用(特許文献2参照)、抗潰瘍作用(特許文献3参照)、及び血糖上昇抑制作用(特許文献4参照)等が知られている。
【0010】
また、上記式(I)の化合物のうち、3−メチル−1−フェニル−2−ピラゾリン−5−オンを有効成分とする製剤は、2001年6月以来、脳保護剤(一般名「エダラボン」、商品名「ラジカット」:三菱ウェルファーマ株式会社製造・販売)として上市されている。この「エダラボン」は、活性酸素に対して高い反応性を有することが報告されている(非特許文献1;非特許文献2参照)。このように、エダラボンは活性酸素をはじめとする種々のフリーラジカルを消去することで、細胞障害などを防ぐ働きをするフリーラジカルスカベンジャーである。しかしながら、これまでエダラボンが鉄キレート作用を有するか否かの検討については全く報告がない。
【0011】
【特許文献1】
特公平5−31523号公報
【特許文献2】
特公平5−35128号公報
【特許文献3】
特開平3−215425号公報
【特許文献4】
特開平3−215426号公報
【非特許文献1】
Kawai, H., et al., J. Phamacol. Exp. Ther., 281(2), 921, 1997
【非特許文献2】
Wu, TW. et al., Life Sci, 67(19), 2387, 2000
【0012】
【発明が解決しようとする課題】
本発明は、鉄が関与する疾病に対する広範囲な組織保護剤として応用できる鉄キレート剤を提供することを解決すべき課題とした。さらに本発明は、組織内に沈着した鉄に対して特に有効な高脂溶性の鉄キレート剤を提供することを解決すべき課題とした。さらに、本発明は、上記鉄キレート剤と鉄とが形成する新規鉄錯体を同定することを解決すべき課題とした。さらに本発明は、ヒトの体内において、体内に存在する鉄と反応して上記新規鉄錯体を形成せしめる化合物を含有する鉄過剰症の予防及び/又は治療のための医薬を提供することを解決すべき課題とした。
【0013】
【課題を解決するための手段】
本発明者は、上記課題を解決するために鋭意検討した結果、式(I)で示されるピラゾロン誘導体が鉄と6:1錯体を形成することを確認した。本発明はこの知見に基づいて完成したものである。
【0014】
即ち、本発明によれば、下記式(I):
【化4】
(式中、R1は、水素原子、アリール基、炭素数1〜5のアルキル基又は総炭素数3〜6のアルコキシカルボニルアルキル基を表し;R2は、水素原子、アリールオキシ基、アリールメルカプト基、炭素数1〜5のアルキル基又は炭素数1〜3のヒドロキシアルキル基を表し;あるいは、R1及びR2は、共同して炭素数3〜5のアルキレン基を表し;R3は、水素原子、炭素数1〜5のアルキル基、炭素数5〜7のシクロアルキル基、炭素数1〜3のヒドロキシアルキル基、ベンジル基、ナフチル基、フェニル基、又は炭素数1〜5のアルキル基、炭素数1〜5のアルコキシ基、炭素数1〜3のヒドロキシアルキル基、総炭素数2〜5のアルコキシカルボニル基、炭素数1〜3のアルキルメルカプト基、炭素数1〜4のアルキルアミノ基、総炭素数2〜8のジアルキルアミノ基、ハロゲン原子、トリフルオロメチル基、カルボキシル基、シアノ基、水酸基、ニトロ基、アミノ基及びアセトアミド基からなる群から選ばれる同一若しくは異なる1〜3個の置換基で置換されたフェニル基を表す。)
で示されるピラゾロン誘導体若しくはその生理学的に許容される塩、又はそれらの水和物若しくは溶媒和物を有効成分として含む、鉄キレート剤が提供され、この鉄キレート剤は鉄が関与する疾病に対する組織保護剤として用いることができる。
【0015】
好ましくは、式(I)で示されるピラゾロン誘導体は3−メチル−1−フェニル−2−ピラゾリン−5−オンである。
好ましくは、鉄と式(I)で示されるピラゾロン誘導体とが1:6錯体を形成する。
好ましくは、鉄は3価鉄である。
【0016】
本発明の別の側面によれば、鉄と下記式(I):
【化5】
(式中、R1は、水素原子、アリール基、炭素数1〜5のアルキル基又は総炭素数3〜6のアルコキシカルボニルアルキル基を表し;R2は、水素原子、アリールオキシ基、アリールメルカプト基、炭素数1〜5のアルキル基又は炭素数1〜3のヒドロキシアルキル基を表し;あるいは、R1及びR2は、共同して炭素数3〜5のアルキレン基を表し;R3は、水素原子、炭素数1〜5のアルキル基、炭素数5〜7のシクロアルキル基、炭素数1〜3のヒドロキシアルキル基、ベンジル基、ナフチル基、フェニル基、又は炭素数1〜5のアルキル基、炭素数1〜5のアルコキシ基、炭素数1〜3のヒドロキシアルキル基、総炭素数2〜5のアルコキシカルボニル基、炭素数1〜3のアルキルメルカプト基、炭素数1〜4のアルキルアミノ基、総炭素数2〜8のジアルキルアミノ基、ハロゲン原子、トリフルオロメチル基、カルボキシル基、シアノ基、水酸基、ニトロ基、アミノ基及びアセトアミド基からなる群から選ばれる同一若しくは異なる1〜3個の置換基で置換されたフェニル基を表す。)
で示されるピラゾロン誘導体との1:6錯体が提供される。
好ましくは、鉄と3−メチル−1−フェニル−2−ピラゾリン−5−オンとの1:6錯体が提供される。
本発明のさらに別の側面によれば、ヒトの体内において、体内に存在する鉄と反応して、鉄とピラゾロン誘導体との1:6錯体を形成せしめる化合物を含有する鉄過剰症の予防及び/又は治療のための医薬が提供される。ピラゾロン誘導体は好ましくは、3−メチル−1−フェニル−2−ピラゾリン−5−オンである。
【0017】
本発明のさらに別の側面によれば、上記式(I)で示されるピラゾロン誘導体若しくはその生理学的に許容される塩、又はそれらの水和物若しくは溶媒和物の予防及び/又は治療有効量をヒトを含む哺乳動物に投与する工程を含む、鉄をキレートする方法が提供される。
【0018】
本発明のさらに別の側面によれば、鉄キレート剤の製造のための上記式(I)で示されるピラゾロン誘導体若しくはその生理学的に許容される塩、又はそれらの水和物若しくは溶媒和物の使用が提供される。
【0019】
【発明の実施の形態】
以下、本発明の実施の形態について説明する。
本発明者らは、エダラボンがデフェロキサミンと同様に鉄イオンと結合することにより、遊離鉄による酸化ストレスの軽減に寄与しているのではないかと仮定した。脳組織には平均74μg/gタンパク質の濃度で非ヘム鉄が含まれており、部分的には淡蒼球、黒質、赤核に多く含まれている。また、脳の脂質過酸化速度は、そこに含まれている鉄の濃度に比例することが報告されている。脳卒中(stroke)のような虚血病変では、酸素の供給が絶たれるために、乳酸が蓄積し、脳虚血病変では局在的にpHが5.5〜6.5まで低下することが報告されている。これは、トランスフェリンからの鉄イオンの遊離を促進するのに十分な条件と言える。
【0020】
また、髄液は1.1μmol/lの鉄を含有し、このうち酸化還元反応に関与することのできる鉄は、0.55±0.27μmol/lと見積もられている。髄液中には血漿中の10倍という、高濃度のアスコルビン酸が含まれているために遊離鉄は2価鉄として存在する。さらに髄液中ではカエルロプラスミン活性は抑制されているため、脳−脊髄損傷時には、より生体障害性の高い2価鉄による酸化ストレス惹起が予想される。
【0021】
ヘムオキシダーゼ(Heme oxigenase)(HO)はヘム鉄をビリベルジン、鉄、一酸化炭素に分解する酵素であり、本質的なHO-2と、副次的なHO-1がある。ビリベルジンには抗酸化活性があるために、HOは抗酸化酵素と考えられてきた。しかし最近の知見によると脳障害時に1)HO-1はヘム鉄の分解に伴って鉄を遊離する、2)脳は元々HO-2活性が高いが、クモ膜下出血等の脳障害時にはHO-1の誘導が起きる、3)脳障害時にはNO産生が亢進する、4)HO-1の誘導が起きるとフェリチンの誘導も起きるが、これはNOによって阻害される、5)HO-2ノックアウト動物ではHO-1誘導と共に、酸化ストレスを与えることによる鉄の沈着が観察された、等のことが明らかとなってきた。
【0022】
本発明者らは、上記の知見より、組織保護剤の開発への新しいアプローチとして遊離鉄のキレート作用、及び鉄イオンによる脂質過酸化抑制効果を指標とすることを想到した。そこで本発明者らは、エダラボンの薬理活性は遊離鉄イオンを捕捉することによって脂質過酸化を含む酸化ストレスを軽減するものであると仮定し、エダラボンが鉄イオンと相互作用するかどうかを検討した。
【0023】
その結果、エダラボンは脂溶性(有機系)溶媒中で、鉄イオンと錯体を形成することが見いだされ、エタノール中での錯形成比はエダラボン:3価鉄=6:1であることが判明した。さらにまた、エダラボンはトランスフェリンと安定に結合している鉄には作用しない(鉄を引き抜かない)こと、エダラボンは3価鉄を2価鉄に還元しないことが判明した。
【0024】
本発明による鉄キレート剤は、本明細書に定義する式(I)で示されるピラゾロン誘導体若しくはその生理学的に許容される塩、又はそれらの水和物若しくは溶媒和物を含む。
【0025】
本発明で用いる式(I)で示される化合物は、互変異性により、以下の式(I')又は(I”)で示される構造をもとりうる。本明細書の式(I)には、便宜上、互変異性体のうちの1つを示したが、当業者には下記の互変異性体の存在は自明である。本発明の鉄キレート剤の有効成分としては、下記の式(I')又は(I”)で表される化合物若しくはその生理学的に許容される塩、又はそれらの水和物若しくは溶媒和物を用いてもよい。
【0026】
【化6】
【0027】
式(I)において、R1の定義におけるアリール基は単環性又は多環性アリール基のいずれでもよい。例えば、フェニル基、ナフチル基などのほか、メチル基、ブチル基などのアルキル基、メトキシ基、ブトキシ基などのアルコキシ基、塩素原子などのハロゲン原子、又は水酸基等の置換基で置換されたフェニル基等が挙げられる。アリール部分を有する他の置換基(アリールオキシ基など)におけるアリール部分についても同様である。
【0028】
R1、R2及びR3の定義における炭素数1〜5のアルキル基は直鎖状、分枝鎖状のいずれでもよい。例えば、メチル基、エチル基、プロピル基、イソプロピル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、ペンチル基等が挙げられる。アルキル部分を有する他の置換基(アルコキシカルボニルアルキル基)におけるアルキル部分についても同様である。
【0029】
R1の定義における総炭素数3〜6のアルコキシカルボニルアルキル基としては、メトキシカルボニルメチル基、エトキシカルボニルメチル基、プロポキシカルボニルメチル基、メトキシカルボニルエチル基、メトキシカルボニルプロピル基等が挙げられる。
【0030】
R2の定義におけるアリールオキシ基としては、p−メチルフェノキシ基、p−メトキシフェノキシ基、p−クロロフェノキシ基、p−ヒドロキシフェノキシ基等が挙げられ、アリールメルカプト基としては、フェニルメルカプト基、p−メチルフェニルメルカプト基、p−メトキシフェニルメルカプト基、p−クロロフェニルメルカプト基、p−ヒドロキシフェニルメルカプト基等が挙げられる。
【0031】
R2及びR3の定義における炭素数1〜3のヒドロキシアルキル基としては、ヒドロキシメチル基、2−ヒドロキシエチル基、3−ヒドロキシプロピル基等が挙げられる。R3の定義における炭素数5〜7のシクロアルキル基としては、シクロペンチル基、シクロヘキシル基、シクロヘプチル基等が挙げられる。
【0032】
R3の定義において、フェニル基の置換基における炭素数1〜5のアルコキシ基としては、メトキシ基、エトキシ基、プロポキシ基、イソプロポキシ基、ブトキシ基、ペンチルオキシ基等が挙げられ、総炭素数2〜5のアルコキシカルボニル基としては、メトキシカルボニル基、エトキシカルボニル基、プロポキシカルボニル基、ブトキシカルボニル基等が挙げられ、炭素数1〜3のアルキルメルカプト基としては、メチルメルカプト基、エチルメルカプト基、プロピルメルカプト基等が挙げられ、炭素数1〜4のアルキルアミノ基としては、メチルアミノ基、エチルアミノ基、プロピルアミノ基、ブチルアミノ基等が挙げられ、総炭素数2〜8のジアルキルアミノ基としては、ジメチルアミノ基、ジエチルアミノ基、ジプロピルアミノ基、ジブチルアミノ基等が挙げられる。
【0033】
本発明の鉄キレート剤の有効成分として好適に用いられる化合物(I)として、例えば、以下に示す化合物が挙げられる。
3−メチル−1−フェニル−2−ピラゾリン−5−オン;
3−メチル−1−(2−メチルフェニル)−2−ピラゾリン−5−オン;
3−メチル−1−(3−メチルフェニル)−2−ピラゾリン−5−オン;
3−メチル−1−(4−メチルフェニル)−2−ピラゾリン−5−オン;
3−メチル−1−(3,4−ジメチルフェニル)−2−ピラゾリン−5−オン;
1−(4−エチルフェニル)−3−メチル−2−ピラゾリン−5−オン;
3−メチル−1−(4−プロピルフェニル)−2−ピラゾリン−5−オン;
1−(4−ブチルフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(3−トリフルオロメチルフェニル)−3−メチル−2−ピラゾリン−5−オン;
【0034】
1−(4−トリフルオロメチルフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(2−メトキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(3−メトキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−メトキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(3,4−ジメトキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−エトキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
3−メチル−1−(4−プロポキシフェニル)−2−ピラゾリン−5−オン;
1−(4−ブトキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(2−クロロフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(3−クロロフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−クロロフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(3,4−ジクロロフェニル)−3−メチル−2−ピラゾリン−5−オン;
【0035】
1−(4−ブロモフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−フルオロフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(3−クロロ−4−メチルフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(3−メチルメルカプトフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−メチルメルカプトフェニル)−3−メチル−2−ピラゾリン−5−オン;
4−(3−メチル−5−オキソ−2−ピラゾリン−1−イル)安息香酸;
1−(4−エトキシカルボニルフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−ニトロフェニル)−3−メチル−2−ピラゾリン−5−オン;
3−エチル−1−フェニル−2−ピラゾリン−5−オン;
1−フェニル−3−プロピル−2−ピラゾリン−5−オン;
【0036】
1,3−ジフェニル−2−ピラゾリン−5−オン;
3−フェニル−1−(p−トリル)−2−ピラゾリン−5−オン;
1−(4−メトキシフェニル)−3−フェニル−2−ピラゾリン−5−オン;
1−(4−クロロフェニル)−3−フェニル−2−ピラゾリン−5−オン;
3,4−ジメチル−1−フェニル−2−ピラゾリン−5−オン;
4−イソブチル−3−メチル−1−フェニル−2−ピラゾリン−5−オン;
4−(2−ヒドロキシエチル)−3−メチル−1−フェニル−2−ピラゾリン−5−オン;
3−メチル−4−フェノキシ−1−フェニル−2−ピラゾリン−5−オン;
3−メチル−4−フェニルメルカプト−1−フェニル−2−ピラゾリン−5−オン;
【0037】
3,3',4,5,6,7−ヘキサヒドロ−2−フェニル−2H−インダゾール−3−オン;
3−(エトキシカルボニルメチル)−1−フェニル−2−ピラゾリン−5−オン;
1−フェニル−2−ピラゾリン−5−オン;
3−メチル−2−ピラゾリン−5−オン;
1,3−ジメチル−2−ピラゾリン−5−オン;
1−エチル−3−メチル−2−ピラゾリン−5−オン;
1−ブチル−3−メチル−2−ピラゾリン−5−オン;
1−(2−ヒドロキエチル)−3−メチル−2−ピラゾリン−5−オン;
1−シクロヘキシル−3−メチル−2−ピラゾリン−5−オン;
1−ベンジル−3−メチル−2−ピラゾリン−5−オン;
【0038】
1−(α−ナフチル)−3−メチル−2−ピラゾリン−5−オン;
1−メチル−3−フェニル−2−ピラゾリン−5−オン;
3−メチル−1−(4−メチルフェニル)−2−ピラゾリン−5−オン;
1−(4−ブチルフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−メトキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−ブトキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−クロロフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−ヒドロキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(3,4−ジヒドロキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(2−ヒドロキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(3−ヒドロキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
【0039】
1−(4−ヒドロキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(3,4−ヒドロキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−ヒドロキシフェニル)−3−フェニル−2−ピラゾリン−5−オン;
1−(4−ヒドロキシメチルフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−アミノフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−メチルアミノフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−エチルアミノフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−ブチルアミノフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−ジメチルアミノフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(アセトアミドフェニル)−3−メチル−2−ピラゾリン−5−オン;及び
1−(4−シアノフェニル)−3−メチル−2−ピラゾリン−5−オン
【0040】
本発明の鉄キレート剤の有効成分としては、式(I)で表される遊離形態の化合物のほか、生理学的に許容される塩を用いてもよい。生理学的に許容される塩としては、塩酸、硫酸、臭化水素塩、リン酸等の鉱酸との塩;メタンスルホン酸、p−トルエンスルホン酸、ベンゼンスルホン酸、酢酸、グリコール酸、グルクロン酸、マレイン酸、フマル酸、シュウ酸、アスコルビン酸、クエン酸、サリチル酸、ニコチン酸、酒石酸等の有機酸との塩;ナトリウム、カリウム等のアルカリ金属との塩;マグネシウム、カルシウム等のアルカリ土類金属との塩;アンモニア、トリス(ヒドロキシメチル)アミノメタン、N,N−ビス(ヒドロキシエチル)ピペラジン、2−アミノ−2−メチル−1−プロパノール、エタノールアミン、N−メチルグルタミン、L−グルタミン等のアミンとの塩が挙げられる。また、グリシンなどのアミノ酸との塩を用いてもよい。
【0041】
本発明の鉄キレート剤の有効成分としては、上記式(I)で表される化合物若しくはその生理学的に許容される塩の水和物、又は上記式(I)で表される化合物若しくはその生理学的に許容される塩の溶媒和物を用いてもよい。溶媒和物を形成する有機溶媒の種類は特に限定されないが、例えば、メタノール、エタノール、エーテル、ジオキサン、テトラヒドロフランなどを例示することができる。また、上記式(I)で表される化合物は、置換基の種類により1以上の不斉炭素を有する場合があり、光学異性体又はジアステレオ異性体などの立体異性体が存在する場合がある。本発明の鉄キレート剤の有効成分としては、純粋な形態の立体異性体、立体異性体の任意の混合物、ラセミ体などを用いてもよい。
【0042】
式(I)で表される化合物はいずれも公知の化合物であり、特公平5−31523号公報などに記載された方法により当業者が容易に合成できる。
【0043】
本発明の鉄キレート剤は、鉄が関与する疾病に対する広範囲な組織保護剤として応用できる。すなわち、本発明の鉄キレート剤は、鉄の過剰の存在を防止することによって疾病の発症を防止する予防剤としての作用、及び/又は過剰に存在する鉄を正常な状態に回復させることによって疾病を治療する治療剤としての作用を有している。
【0044】
鉄が関与する疾病とは、鉄イオン(または鉄の沈着)が関与する全ての病態を包含する。例えば、加齢に伴って、血管壁にカルシウムが沈着することが知られているが、最近の研究では鉄も同様に沈着していくことが明らかにされた。さらには、アンジオテンシンII(AngiotensinII)によってHO-1が活性化され、組織(心臓、腎臓)に鉄が沈着することなどが報告されている。
さらに糖尿病と鉄過剰症との関係については、瀉血により生体内の鉄量を減少させると糖尿病患者の糖代謝が改善してインスリン使用量が減少できること、貧血治療で鉄を負荷すると、糖尿病性臓器障害が早期に起こったり悪化することが報告されているので、生体内の鉄増加が糖尿病を進展させ、鉄減少が糖尿病の悪化を予防できることが予測される。そこで、鉄キレート剤は糖尿病の進展や・慢性化防止あるいはこれに伴う循環障害(動脈硬化、脳梗塞、心筋梗塞)の予防に有効であると考えられる。
また、特に、本発明の鉄キレート剤は脂溶性の鉄キレート剤であるため、組織内に沈着した鉄に対するキレート剤として有用である。
【0045】
本発明の鉄キレート剤の投与経路は特に限定されず、経口的又は非経口的に投与することができる。非経口投与の投与経路も特に限定されず、静脈内、筋肉内、皮内、皮下に注射投与することができる。
【0046】
また、本発明の鉄キレート剤は、鉄が関与する疾病の発症に先立って予防的に投与しておくことができる。また、当該疾病を起こした患者に対しては、症状の悪化の防止ないしは症状の軽減などを目的として、本発明の鉄キレート剤を該患者に投与することができる。
【0047】
本発明の鉄キレート剤の投与量は特に限定されないが、通常は、有効成分である式(I)で示される化合物の重量として一般に経口投与の場合には一日あたり0.1〜1000mg/kg体重、好ましくは一日あたり0.5〜50mg/kg体重、であり、非経口投与の場合には一日あたり0.01〜100mg/kg体重、好ましくは0.1〜10mg/kg体重である。上記投与量は1日1回又は2〜3回に分けて投与するのが好ましく、年齢、病態、症状により適宜増減してもよい。
【0048】
本発明の鉄キレート剤としては、上記式(I)で表される化合物若しくはその生理学的に許容される塩、又はそれらの水和物若しくは溶媒和物をそのまま投与してもよいが、一般的には、有効成分である上記の物質と薬理学的及び製剤学的に許容される添加物を含む医薬組成物を調製して投与することが好ましい。
【0049】
薬理学的及び製剤学的に許容しうる添加物としては、例えば、賦形剤、崩壊剤ないし崩壊補助剤、結合剤、滑沢剤、コーティング剤、色素、希釈剤、基剤、溶解剤ないし溶解補助剤、等張化剤、pH調節剤、安定化剤、噴射剤、及び粘着剤等を用いることができる。
【0050】
経口投与に適する医薬組成物には、添加物として、例えば、ブドウ糖、乳糖、D−マンニトール、デンプン、又は結晶セルロース等の賦形剤;カルボキシメチルセルロース、デンプン、又はカルボキシメチルセルロースカルシウム等の崩壊剤又は崩壊補助剤;ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、ポリビニルピロリドン、又はゼラチン等の結合剤;ステアリン酸マグネシウム又はタルク等の滑沢剤;ヒドロキシプロピルメチルセルロース、白糖、ポリエチレングリコール又は酸化チタン等のコーティング剤;ワセリン、流動パラフィン、ポリエチレングリコール、ゼラチン、カオリン、グリセリン、精製水、又はハードファット等の基剤を用いることができる。
【0051】
注射あるいは点滴用に適する医薬組成物には、注射用蒸留水、生理食塩水、プロピレングリコール等の水性あるいは用時溶解型注射剤を構成しうる溶解剤又は溶解補助剤;ブドウ糖、塩化ナトリウム、D−マンニトール、グリセリン等の等張化剤;無機酸、有機酸、無機塩基又は有機塩基等のpH調節剤等の添加物を用いることができる。
【0052】
本発明の鉄キレート剤の形態は特に限定されず、当業者に利用可能な種々の形態をとることができる。経口投与に適する医薬として、例えば、固体の製剤用添加物を用いて錠剤、散剤、顆粒剤、硬ゼラチンカプセル剤、坐剤、又はトローチ剤などを調製することができ、液状の製剤用添加物を用いてシロップ剤、乳剤、軟ゼラチンカプセル剤などを調製することができる。また、非経口投与に適する医薬として、注射剤、点滴剤、吸入剤、坐剤、経皮吸収剤、経粘膜吸収剤などを調製することができる。なお、上記の式(I)の化合物を有効成分とする脳保護剤(点滴剤)が、すでに臨床において使用されているので(一般名「エダラボン」、商品名「ラジカット」:三菱ウェルファーマ株式会社製造・販売)、本発明の鉄キレート剤において上記市販製剤をそのまま用いることができる。
【0053】
さらに本発明によれば、鉄と上記式(I)で示されるピラゾロン誘導体(特に好ましくは、3−メチル−1−フェニル−2−ピラゾリン−5−オン(エダラボン))との1:6錯体が提供される。鉄は好ましくは3価鉄である。
エダラボンは水に難溶性であるため、牛血清アルブミン(以下、BSAという。)を共存させることによって錯体を形成させることができる。例えば、10%BSA溶液に、3価鉄水溶液とエダラボン水溶液を添加することにより、鉄とエダラボンとの1:6錯体を形成することができる。3価鉄とエダラボンの溶液については水溶液の代わりにエタノール溶液などを用いることもできる。
【0054】
上記のようにして形成される鉄とエダラボンとの1:6錯体は、エダラボンの生理活性を評価の際あるいはエダラボンの生理活性を増強する物質のスクリーニングの際等に有用である。
【0055】
【実施例】
以下、本発明を実施例によりさらに具体的に説明するが、本発明は下記の実施例により限定されるものではない。
【0056】
合成例:3−メチル−1−フェニル−2−ピラゾリン−5−オン(以下、エダラボンと称す)の合成
エタノール50ml中にアセト酢酸エチル13.0g及びフェニルヒドラジン10.8gを加え、3時間還流攪拌した。反応液を放冷後、析出した結晶をろ取し、エタノールより再結晶して、表題の化合物11.3gを無色結晶として得た。
収率 67%
融点 127.5〜128.5℃
【0057】
実施例1:エダラボンによる3価鉄還元活性の検討
エダラボンがヒドロキシルラジカル(・OH)と相互作用するということは、エダラボンとヒドロキシルラジカル(・OH)はそれぞれ還元剤、酸化剤として相互作用していることを意味する。そこで、エダラボンに3価鉄を2価鉄に還元する能力があるか否かを確認するために、酸素電極による酸素吸収実験を行った。これは、もし3価鉄がエダラボンによって2価鉄に還元されると、溶存酸素を次式に従って消費する現象が確認できると考えたからである。
4Fe2+ + 4H+ + O2 → 4Fe3+ + 2H2O
【0058】
20mMのエダラボンを含む緩衝液(0.1M HEPES(丸善(株)化学便覧、基礎編改訂3版、II−355, 1998), pH 7.4,37℃)に0.2mMの3価鉄もしくは2価鉄を図1の矢印に示す位置で添加した。結果を図1に示す。
その結果、鉄イオンに比して100倍濃いエダラボンを添加したにもかかわらず、3価鉄の還元による酸素吸収の促進は見られなかった。このことより、エダラボンは3価鉄を2価鉄に還元する能力は乏しいと考えた。
【0059】
実施例2:エダラボンによるトランスフェリンからの鉄の遊離
トランスフェリンは血漿中での鉄貯蔵に関与しており、遊離鉄が関与する様々な酸化ストレスから生体を防御している。そこで、エダラボンがこのトランスフェリンと相互作用するか否かについて、分光光度計でトランスフェリンの吸光度の変化をモニタリングすることにより検討した。
【0060】
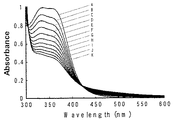
緩衝液(0.1M HEPES,pH 7.4,37℃)を用いて調製した0.1mMのトランスフェリン(A)と0.1mMのエダラボン(B)を混合し、直後と(C)、60分後に(D)吸光度を測定した。結果を図2に示す。
トランスフェリンは鉄と結合することにより、465nm近傍に特徴的な吸収スペクトルを呈する(A)。このスペクトルはエダラボンが共存しても変化しなかったことから、エダラボンと鉄との結合は、トランスフェリンと鉄の結合よりも弱い可能性が示唆された。
【0061】
実施例3:エダラボンと3価鉄の相互作用の検討
次に、エダラボンと3価鉄の相互作用について検討した。エダラボンは水に難溶性であるため、以下の実験はBSA(Serologicals Corporationより購入)を共存させて行った。最初に、極性溶媒(水)中でエダラボンが3価鉄と錯体を形成しているか否かをESR(電子スピン共鳴)にて検証した。
【0062】
(条件)
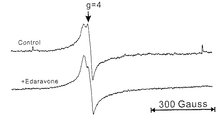
Control:10%BSA溶液に、0.6mM3価鉄を添加し、液体窒素温度でESRを測定した。測定条件は1600±500ガウス(gauss)。
+Edaravone:10%BSA溶液に、0.6mM3価鉄と3.0mMエダラボンを添加し、液体窒素温度でESRを測定。測定条件は1600±500ガウス。
【0063】
結果を図3に示す。この結果より、エダラボンを添加すると明らかに非ヘム鉄領域(g=4)のESRスペクトルが変化したことから、3価鉄とエダラボンが何らかの相互作用をしている可能性が示唆された。但し、エダラボンの添加による、ESRスペクトルの変化は小さかった。これは、鉄とアルブミンによる錯体と、鉄とエダラボンによる錯体のESRスペクトルが似ているためと思われた。
【0064】
実施例4:エダラボンと3価鉄の錯体形成比の検討
モル比法を用いて、エダラボンと三価鉄の錯形成時の構成比を検討した。
エタノールに溶解した0.25mMのエダラボンを、同じくエタノールに溶かした2.5mMの3価鉄に累積添加し、吸収スペクトルを測定した。結果を図4に示す。図中Aは2.5mM3価鉄の吸収スペクトルを示す。これにエダラボンを0.25mMづつ添加していくと、吸収スペクトルはB→Kと変化した。
【0065】
次に、最も吸光度の変化が大きかった337nmの吸光度変化を縦軸に、そして横軸にエダラボン/3価鉄の値をとってグラフを作成した(図5)。その結果、エダラボン:3価鉄の比が6:1の所に変曲点が見いだせた。このことからエダラボンと3価鉄は非プロトン溶媒中で錯体を形成していることが推測された。
【0066】
さらにこの点を詳細に検討する目的で、エタノール中でのエダラボン−3価鉄のESRスペクトルを液体窒素温度で測定した。
0.7mM3価鉄のエタノール溶液(A)に、エダラボンのエタノール溶液を0.7mMづつ追加((B)→(K))したときのESRスペクトルを図6に示す。測定条件は2500±2500ガウス。
【0067】
非プロトン溶媒系で、3価鉄とエダラボンの比率を変えながらESRスペクトルを測定したところ、ハイスピン(High-spin)鉄のg=6のシグナルが、エダラボンが追加されるに従って減弱した。逆に非ヘム鉄(g=4)のESRシグナルの増大が観察された。
【0068】
次に、これらを使ってそれぞれのESRシグナル強度と混合比の関係を調べると、図7に示すグラフが得られた。
(条件)
上のグラフ:g=6の部分のスペクトル強度と、エダラボン/3価鉄の比
下のグラフ:g=4の部分のスペクトル強度と、エダラボン/3価鉄の比
共にエダラボン/三価鉄の比が6の所で変曲点を迎えていることが示された。
【0069】
【発明の効果】
本発明の鉄キレート剤は、鉄が関与する疾病に対する広範囲な組織保護剤として応用できる。特に本発明の鉄キレート剤は高脂溶性の鉄キレート剤であるため、組織内に沈着した鉄に対して特に有効である。
【図面の簡単な説明】
【図1】図1は、エダラボンによる3価鉄還元活性の測定結果を示す。
【図2】図2は、エダラボンによるトランスフェリンからの鉄の遊離の測定結果を示す。
【図3】図3は、極性溶媒(水)中でエダラボンが3価鉄と錯体を形成しているか否かをESR(電子スピン共鳴法)にて検証した結果を示す。
【図4】図4は、エタノールに溶解した0.25mMのエダラボンを、同じくエタノールに溶かした2.5mMの3価鉄に累積添加し、吸収スペクトルを測定した結果を示す。
【図5】図5は、図4の結果に基づいて337nmの吸光度変化を縦軸に、そして横軸にエダラボン/3価鉄の値をとって作成したグラフを示す。
【図6】図6は、0.7mM3価鉄のエタノール溶液(A)に、エダラボンのエタノール溶液を0.7mMづつ追加((B)→(K))したときのESRスペクトルを示す。
【図7】図7は、図6の結果に基づいて、それぞれのESRシグナル強度と混合比の関係を調べたグラフを示す。
【発明の属する技術分野】
本発明は、ピラゾロン誘導体若しくはその生理学的に許容される塩、又はそれらの水和物若しくは溶媒和物を有効成分として含む鉄キレート剤、並びに鉄と3−メチル−1−フェニル−2−ピラゾリン−5−オンとの1:6錯体に関する。
【0002】
【従来技術】
ヒトの体内には約4.5gの鉄が存在し、その約2/3は、ヘモグロビン鉄として酸素運搬に関与し、その他はミオグロビン、酵素の補欠分子族、鉄輸送タンパク(トランスフェリン、ラクトフェリン)、並びに鉄貯蔵タンパク(フェリチン、ヘモシデリン)として存在している。1日当たりの血清中における鉄のターンオーバーは35mgと考えられ、生体は鉄に対して能動的なシステムを有しているため、生体内では鉄欠乏症や鉄過剰症の発症が容易に起こり得る。
【0003】
酸化ストレスは、鉄、スーパーオキサイド又は過酸化物などのプロ−オキシダンツ(pro-oxidants)と抗酸化剤(antioxidant)との平衡状態の乱れにより起きる状態を言う。鉄が生体に対し酸化ストレスを与えるメカニズムは、以下のように考えられている。即ち、遊離状態の2価鉄は様々な反応を行い、強力な活性酸素種の生成を引き起こす。例えば、フェントン反応(Fenton reaction)と称されるヒドロキシルラジカル(・OH)を生成する反応(Fe2 + H2O2 → Fe3 + OH- +・OH)がある。ここで生じたヒドロキシルラジカル(・OH)は高い酸化能(Eo=+2.7V)を有し、生体中のほとんどの(高)分子と直ちに反応して障害を与える。特に脂質(H・CR3)とヒドロキシルラジカル(・OH)が反応すると、開始反応を経て脂質過酸化の連鎖反応を引き起こす。従って、ごく僅かなイニシエーター(initiator)(この場合、・OH)の発生が大きな生体障害を引き起こす元凶となる。
【0004】
一方、生体内には、多様な鉄キレーターが存在し、活性な遊離2価鉄を不活性な3価型に変換し、捕捉することにより、遊離2価鉄による組織障害を防止している。このような生体内鉄キレーターとして、フェリチン(Ferritin)及びヘモシダリン(Haemosiderin)が知られている。フェリチンは水溶性タンパク質で細胞質に主に分布し、ヘモシダリンは水不溶性タンパク質で、ライソゾーム内に局在している。フェリチンは20kDaの分子量からなるサブユニット24個からなり、フェリチン1分子で鉄原子を最高4500個捕捉できる。フェリチンによる鉄貯蔵機構は、2価鉄がフェリチンと接触するとフェリチンの金属結合部位(metal-binding site)に結合し、ここで鉄が2価から3価に酸化され、3価の形で貯蔵される。
【0005】
過剰に鉄を摂取した場合、最初にフェリチンに鉄が取り込まれ、その後フェリチンがライソゾーム内で消化された後、ヘモシダリンが鉄を取り込むことにより、遊離鉄による酸化ストレスを抑制している。フェリチンからの鉄の遊離は、3価鉄が2価鉄に還元されることにより起きる。キサンチンオキシダーゼやある種の還元酵素、それ以外では尿酸・アスコルビン酸・クエン酸・炭酸イオン・乳酸等の低分子化合物によって鉄が還元された後にフェリチンからの鉄の遊離が促進される。
【0006】
フェリチンやヘモシダリン以外にも、血漿中には効果的に遊離鉄を捕捉するトランスフェリンと呼ばれる一群のタンパク質があり、血漿中の遊離鉄をきわめて低い濃度に維持している。この中にはヒト血漿トランスフェリン、卵白オボトランスフェリン(ovotransferrin)、ラクトフェリン、メラノトランスフェリン、及びウテロフェリン等が含まれる。トランスフェリンと鉄との結合は、水素イオン濃度の影響を受けやすく、微酸性条件下では炭酸イオンが炭酸ガスとなり遊離するために、同時に鉄イオンもトランスフェリンから遊離してくる。更にこの酸による鉄イオンの遊離は鉄を還元しうる物質が共存する条件で加速される。
【0007】
トランスフェリンは肝臓で合成されて血漿中に放出され、遊離の鉄を捕捉する。通常、血漿中のトランスフェリンの鉄飽和率は50−60%程度であり、鉄との結合に対する予備能を有している。鉄と結合したトランスフェリンは細胞膜表面に存在するトランスフェリンレセプターを通って細胞内に入り、酸性条件下で鉄を遊離する。この鉄はDNA合成や鉄含有酵素の合成に用いられ、トランスフェリンは細胞外に放出されて再利用される。トランスフェリンに結合した鉄は過酸化水素刺激によるフェントン反応からのヒドロキシルラジカル(・OH)の生成には関与せず、生体を酸化ストレスから保護している。
【0008】
血漿中の鉄が過剰になる病態としては、ヘモクロマトーシス(hemochromatosis)、β−サラセミア(β−thalassaemia)、そして組織が障害を受けてトランスフェリンが処理出来ない量の鉄が放出されたとき(抗癌剤治療時、体外循環時、多臓器不全時の溶血)等が知られている。鉄が遊離鉄として血漿中に放出されると、血漿中には3価鉄を還元できる物質(アスコルビン酸、尿酸、グルタチオン、タンパク質のチオール基等)が多量に存在するため、2価鉄に還元される。2価鉄は様々な活性酸素種を生成し、直接生体高分子と反応したり、連鎖反応によって過酸化脂質を生成する元凶になる。このため、生体にはこの有害な2価鉄をより毒性の低い3価鉄に速やかに酸化するフェロキシダーゼ酵素(ferroxidase enzyme)であるカエルロプラスミン(caeruloplasmin)が存在している。
【0009】
一方、下記式(I):
【化3】
(式中、R1は水素原子、アリール、炭素数1〜5のアルキル又は総炭素数3〜6のアルコキシカルボニルアルキルを表し、R2は、水素原子、アリールオキシ、アリールメルカプト、炭素数1〜5のアルキル又は1〜3のヒドロキシアルキルを表し、あるいは、R1及びR2は、共同して炭素数3〜5のアルキレンを表し、R3は水素原子、炭素数1〜5のアルキル、炭素数5〜7のシクロアルキル、炭素数1〜3のヒドロキシアルキル、ベンジル、ナフチル又はフェニル、又は炭素数1〜5のアルコキシ、炭素数1〜3のヒドロキシアルキル、総炭素数2〜5のアルコキシカルボニル、炭素数1〜3のアルキルメルカプト、炭素数1〜4のアルキルアミノ、総炭素数2〜8のジアルキルアミノ、ハロゲン原子、トリフルオロメチル、カルボキシル、シアノ、水酸基、ニトロ、アミノ、及びアセトアミドからなる群から選ばれる同一若しくは異なる1〜3個の置換基で置換されたフェニルを表す。)で表されるピラゾロン誘導体については、医薬の用途として、脳機能正常化作用(特許文献1参照)、過酸化脂質生成抑制作用(特許文献2参照)、抗潰瘍作用(特許文献3参照)、及び血糖上昇抑制作用(特許文献4参照)等が知られている。
【0010】
また、上記式(I)の化合物のうち、3−メチル−1−フェニル−2−ピラゾリン−5−オンを有効成分とする製剤は、2001年6月以来、脳保護剤(一般名「エダラボン」、商品名「ラジカット」:三菱ウェルファーマ株式会社製造・販売)として上市されている。この「エダラボン」は、活性酸素に対して高い反応性を有することが報告されている(非特許文献1;非特許文献2参照)。このように、エダラボンは活性酸素をはじめとする種々のフリーラジカルを消去することで、細胞障害などを防ぐ働きをするフリーラジカルスカベンジャーである。しかしながら、これまでエダラボンが鉄キレート作用を有するか否かの検討については全く報告がない。
【0011】
【特許文献1】
特公平5−31523号公報
【特許文献2】
特公平5−35128号公報
【特許文献3】
特開平3−215425号公報
【特許文献4】
特開平3−215426号公報
【非特許文献1】
Kawai, H., et al., J. Phamacol. Exp. Ther., 281(2), 921, 1997
【非特許文献2】
Wu, TW. et al., Life Sci, 67(19), 2387, 2000
【0012】
【発明が解決しようとする課題】
本発明は、鉄が関与する疾病に対する広範囲な組織保護剤として応用できる鉄キレート剤を提供することを解決すべき課題とした。さらに本発明は、組織内に沈着した鉄に対して特に有効な高脂溶性の鉄キレート剤を提供することを解決すべき課題とした。さらに、本発明は、上記鉄キレート剤と鉄とが形成する新規鉄錯体を同定することを解決すべき課題とした。さらに本発明は、ヒトの体内において、体内に存在する鉄と反応して上記新規鉄錯体を形成せしめる化合物を含有する鉄過剰症の予防及び/又は治療のための医薬を提供することを解決すべき課題とした。
【0013】
【課題を解決するための手段】
本発明者は、上記課題を解決するために鋭意検討した結果、式(I)で示されるピラゾロン誘導体が鉄と6:1錯体を形成することを確認した。本発明はこの知見に基づいて完成したものである。
【0014】
即ち、本発明によれば、下記式(I):
【化4】
(式中、R1は、水素原子、アリール基、炭素数1〜5のアルキル基又は総炭素数3〜6のアルコキシカルボニルアルキル基を表し;R2は、水素原子、アリールオキシ基、アリールメルカプト基、炭素数1〜5のアルキル基又は炭素数1〜3のヒドロキシアルキル基を表し;あるいは、R1及びR2は、共同して炭素数3〜5のアルキレン基を表し;R3は、水素原子、炭素数1〜5のアルキル基、炭素数5〜7のシクロアルキル基、炭素数1〜3のヒドロキシアルキル基、ベンジル基、ナフチル基、フェニル基、又は炭素数1〜5のアルキル基、炭素数1〜5のアルコキシ基、炭素数1〜3のヒドロキシアルキル基、総炭素数2〜5のアルコキシカルボニル基、炭素数1〜3のアルキルメルカプト基、炭素数1〜4のアルキルアミノ基、総炭素数2〜8のジアルキルアミノ基、ハロゲン原子、トリフルオロメチル基、カルボキシル基、シアノ基、水酸基、ニトロ基、アミノ基及びアセトアミド基からなる群から選ばれる同一若しくは異なる1〜3個の置換基で置換されたフェニル基を表す。)
で示されるピラゾロン誘導体若しくはその生理学的に許容される塩、又はそれらの水和物若しくは溶媒和物を有効成分として含む、鉄キレート剤が提供され、この鉄キレート剤は鉄が関与する疾病に対する組織保護剤として用いることができる。
【0015】
好ましくは、式(I)で示されるピラゾロン誘導体は3−メチル−1−フェニル−2−ピラゾリン−5−オンである。
好ましくは、鉄と式(I)で示されるピラゾロン誘導体とが1:6錯体を形成する。
好ましくは、鉄は3価鉄である。
【0016】
本発明の別の側面によれば、鉄と下記式(I):
【化5】
(式中、R1は、水素原子、アリール基、炭素数1〜5のアルキル基又は総炭素数3〜6のアルコキシカルボニルアルキル基を表し;R2は、水素原子、アリールオキシ基、アリールメルカプト基、炭素数1〜5のアルキル基又は炭素数1〜3のヒドロキシアルキル基を表し;あるいは、R1及びR2は、共同して炭素数3〜5のアルキレン基を表し;R3は、水素原子、炭素数1〜5のアルキル基、炭素数5〜7のシクロアルキル基、炭素数1〜3のヒドロキシアルキル基、ベンジル基、ナフチル基、フェニル基、又は炭素数1〜5のアルキル基、炭素数1〜5のアルコキシ基、炭素数1〜3のヒドロキシアルキル基、総炭素数2〜5のアルコキシカルボニル基、炭素数1〜3のアルキルメルカプト基、炭素数1〜4のアルキルアミノ基、総炭素数2〜8のジアルキルアミノ基、ハロゲン原子、トリフルオロメチル基、カルボキシル基、シアノ基、水酸基、ニトロ基、アミノ基及びアセトアミド基からなる群から選ばれる同一若しくは異なる1〜3個の置換基で置換されたフェニル基を表す。)
で示されるピラゾロン誘導体との1:6錯体が提供される。
好ましくは、鉄と3−メチル−1−フェニル−2−ピラゾリン−5−オンとの1:6錯体が提供される。
本発明のさらに別の側面によれば、ヒトの体内において、体内に存在する鉄と反応して、鉄とピラゾロン誘導体との1:6錯体を形成せしめる化合物を含有する鉄過剰症の予防及び/又は治療のための医薬が提供される。ピラゾロン誘導体は好ましくは、3−メチル−1−フェニル−2−ピラゾリン−5−オンである。
【0017】
本発明のさらに別の側面によれば、上記式(I)で示されるピラゾロン誘導体若しくはその生理学的に許容される塩、又はそれらの水和物若しくは溶媒和物の予防及び/又は治療有効量をヒトを含む哺乳動物に投与する工程を含む、鉄をキレートする方法が提供される。
【0018】
本発明のさらに別の側面によれば、鉄キレート剤の製造のための上記式(I)で示されるピラゾロン誘導体若しくはその生理学的に許容される塩、又はそれらの水和物若しくは溶媒和物の使用が提供される。
【0019】
【発明の実施の形態】
以下、本発明の実施の形態について説明する。
本発明者らは、エダラボンがデフェロキサミンと同様に鉄イオンと結合することにより、遊離鉄による酸化ストレスの軽減に寄与しているのではないかと仮定した。脳組織には平均74μg/gタンパク質の濃度で非ヘム鉄が含まれており、部分的には淡蒼球、黒質、赤核に多く含まれている。また、脳の脂質過酸化速度は、そこに含まれている鉄の濃度に比例することが報告されている。脳卒中(stroke)のような虚血病変では、酸素の供給が絶たれるために、乳酸が蓄積し、脳虚血病変では局在的にpHが5.5〜6.5まで低下することが報告されている。これは、トランスフェリンからの鉄イオンの遊離を促進するのに十分な条件と言える。
【0020】
また、髄液は1.1μmol/lの鉄を含有し、このうち酸化還元反応に関与することのできる鉄は、0.55±0.27μmol/lと見積もられている。髄液中には血漿中の10倍という、高濃度のアスコルビン酸が含まれているために遊離鉄は2価鉄として存在する。さらに髄液中ではカエルロプラスミン活性は抑制されているため、脳−脊髄損傷時には、より生体障害性の高い2価鉄による酸化ストレス惹起が予想される。
【0021】
ヘムオキシダーゼ(Heme oxigenase)(HO)はヘム鉄をビリベルジン、鉄、一酸化炭素に分解する酵素であり、本質的なHO-2と、副次的なHO-1がある。ビリベルジンには抗酸化活性があるために、HOは抗酸化酵素と考えられてきた。しかし最近の知見によると脳障害時に1)HO-1はヘム鉄の分解に伴って鉄を遊離する、2)脳は元々HO-2活性が高いが、クモ膜下出血等の脳障害時にはHO-1の誘導が起きる、3)脳障害時にはNO産生が亢進する、4)HO-1の誘導が起きるとフェリチンの誘導も起きるが、これはNOによって阻害される、5)HO-2ノックアウト動物ではHO-1誘導と共に、酸化ストレスを与えることによる鉄の沈着が観察された、等のことが明らかとなってきた。
【0022】
本発明者らは、上記の知見より、組織保護剤の開発への新しいアプローチとして遊離鉄のキレート作用、及び鉄イオンによる脂質過酸化抑制効果を指標とすることを想到した。そこで本発明者らは、エダラボンの薬理活性は遊離鉄イオンを捕捉することによって脂質過酸化を含む酸化ストレスを軽減するものであると仮定し、エダラボンが鉄イオンと相互作用するかどうかを検討した。
【0023】
その結果、エダラボンは脂溶性(有機系)溶媒中で、鉄イオンと錯体を形成することが見いだされ、エタノール中での錯形成比はエダラボン:3価鉄=6:1であることが判明した。さらにまた、エダラボンはトランスフェリンと安定に結合している鉄には作用しない(鉄を引き抜かない)こと、エダラボンは3価鉄を2価鉄に還元しないことが判明した。
【0024】
本発明による鉄キレート剤は、本明細書に定義する式(I)で示されるピラゾロン誘導体若しくはその生理学的に許容される塩、又はそれらの水和物若しくは溶媒和物を含む。
【0025】
本発明で用いる式(I)で示される化合物は、互変異性により、以下の式(I')又は(I”)で示される構造をもとりうる。本明細書の式(I)には、便宜上、互変異性体のうちの1つを示したが、当業者には下記の互変異性体の存在は自明である。本発明の鉄キレート剤の有効成分としては、下記の式(I')又は(I”)で表される化合物若しくはその生理学的に許容される塩、又はそれらの水和物若しくは溶媒和物を用いてもよい。
【0026】
【化6】
【0027】
式(I)において、R1の定義におけるアリール基は単環性又は多環性アリール基のいずれでもよい。例えば、フェニル基、ナフチル基などのほか、メチル基、ブチル基などのアルキル基、メトキシ基、ブトキシ基などのアルコキシ基、塩素原子などのハロゲン原子、又は水酸基等の置換基で置換されたフェニル基等が挙げられる。アリール部分を有する他の置換基(アリールオキシ基など)におけるアリール部分についても同様である。
【0028】
R1、R2及びR3の定義における炭素数1〜5のアルキル基は直鎖状、分枝鎖状のいずれでもよい。例えば、メチル基、エチル基、プロピル基、イソプロピル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、ペンチル基等が挙げられる。アルキル部分を有する他の置換基(アルコキシカルボニルアルキル基)におけるアルキル部分についても同様である。
【0029】
R1の定義における総炭素数3〜6のアルコキシカルボニルアルキル基としては、メトキシカルボニルメチル基、エトキシカルボニルメチル基、プロポキシカルボニルメチル基、メトキシカルボニルエチル基、メトキシカルボニルプロピル基等が挙げられる。
【0030】
R2の定義におけるアリールオキシ基としては、p−メチルフェノキシ基、p−メトキシフェノキシ基、p−クロロフェノキシ基、p−ヒドロキシフェノキシ基等が挙げられ、アリールメルカプト基としては、フェニルメルカプト基、p−メチルフェニルメルカプト基、p−メトキシフェニルメルカプト基、p−クロロフェニルメルカプト基、p−ヒドロキシフェニルメルカプト基等が挙げられる。
【0031】
R2及びR3の定義における炭素数1〜3のヒドロキシアルキル基としては、ヒドロキシメチル基、2−ヒドロキシエチル基、3−ヒドロキシプロピル基等が挙げられる。R3の定義における炭素数5〜7のシクロアルキル基としては、シクロペンチル基、シクロヘキシル基、シクロヘプチル基等が挙げられる。
【0032】
R3の定義において、フェニル基の置換基における炭素数1〜5のアルコキシ基としては、メトキシ基、エトキシ基、プロポキシ基、イソプロポキシ基、ブトキシ基、ペンチルオキシ基等が挙げられ、総炭素数2〜5のアルコキシカルボニル基としては、メトキシカルボニル基、エトキシカルボニル基、プロポキシカルボニル基、ブトキシカルボニル基等が挙げられ、炭素数1〜3のアルキルメルカプト基としては、メチルメルカプト基、エチルメルカプト基、プロピルメルカプト基等が挙げられ、炭素数1〜4のアルキルアミノ基としては、メチルアミノ基、エチルアミノ基、プロピルアミノ基、ブチルアミノ基等が挙げられ、総炭素数2〜8のジアルキルアミノ基としては、ジメチルアミノ基、ジエチルアミノ基、ジプロピルアミノ基、ジブチルアミノ基等が挙げられる。
【0033】
本発明の鉄キレート剤の有効成分として好適に用いられる化合物(I)として、例えば、以下に示す化合物が挙げられる。
3−メチル−1−フェニル−2−ピラゾリン−5−オン;
3−メチル−1−(2−メチルフェニル)−2−ピラゾリン−5−オン;
3−メチル−1−(3−メチルフェニル)−2−ピラゾリン−5−オン;
3−メチル−1−(4−メチルフェニル)−2−ピラゾリン−5−オン;
3−メチル−1−(3,4−ジメチルフェニル)−2−ピラゾリン−5−オン;
1−(4−エチルフェニル)−3−メチル−2−ピラゾリン−5−オン;
3−メチル−1−(4−プロピルフェニル)−2−ピラゾリン−5−オン;
1−(4−ブチルフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(3−トリフルオロメチルフェニル)−3−メチル−2−ピラゾリン−5−オン;
【0034】
1−(4−トリフルオロメチルフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(2−メトキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(3−メトキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−メトキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(3,4−ジメトキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−エトキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
3−メチル−1−(4−プロポキシフェニル)−2−ピラゾリン−5−オン;
1−(4−ブトキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(2−クロロフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(3−クロロフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−クロロフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(3,4−ジクロロフェニル)−3−メチル−2−ピラゾリン−5−オン;
【0035】
1−(4−ブロモフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−フルオロフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(3−クロロ−4−メチルフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(3−メチルメルカプトフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−メチルメルカプトフェニル)−3−メチル−2−ピラゾリン−5−オン;
4−(3−メチル−5−オキソ−2−ピラゾリン−1−イル)安息香酸;
1−(4−エトキシカルボニルフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−ニトロフェニル)−3−メチル−2−ピラゾリン−5−オン;
3−エチル−1−フェニル−2−ピラゾリン−5−オン;
1−フェニル−3−プロピル−2−ピラゾリン−5−オン;
【0036】
1,3−ジフェニル−2−ピラゾリン−5−オン;
3−フェニル−1−(p−トリル)−2−ピラゾリン−5−オン;
1−(4−メトキシフェニル)−3−フェニル−2−ピラゾリン−5−オン;
1−(4−クロロフェニル)−3−フェニル−2−ピラゾリン−5−オン;
3,4−ジメチル−1−フェニル−2−ピラゾリン−5−オン;
4−イソブチル−3−メチル−1−フェニル−2−ピラゾリン−5−オン;
4−(2−ヒドロキシエチル)−3−メチル−1−フェニル−2−ピラゾリン−5−オン;
3−メチル−4−フェノキシ−1−フェニル−2−ピラゾリン−5−オン;
3−メチル−4−フェニルメルカプト−1−フェニル−2−ピラゾリン−5−オン;
【0037】
3,3',4,5,6,7−ヘキサヒドロ−2−フェニル−2H−インダゾール−3−オン;
3−(エトキシカルボニルメチル)−1−フェニル−2−ピラゾリン−5−オン;
1−フェニル−2−ピラゾリン−5−オン;
3−メチル−2−ピラゾリン−5−オン;
1,3−ジメチル−2−ピラゾリン−5−オン;
1−エチル−3−メチル−2−ピラゾリン−5−オン;
1−ブチル−3−メチル−2−ピラゾリン−5−オン;
1−(2−ヒドロキエチル)−3−メチル−2−ピラゾリン−5−オン;
1−シクロヘキシル−3−メチル−2−ピラゾリン−5−オン;
1−ベンジル−3−メチル−2−ピラゾリン−5−オン;
【0038】
1−(α−ナフチル)−3−メチル−2−ピラゾリン−5−オン;
1−メチル−3−フェニル−2−ピラゾリン−5−オン;
3−メチル−1−(4−メチルフェニル)−2−ピラゾリン−5−オン;
1−(4−ブチルフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−メトキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−ブトキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−クロロフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−ヒドロキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(3,4−ジヒドロキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(2−ヒドロキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(3−ヒドロキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
【0039】
1−(4−ヒドロキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(3,4−ヒドロキシフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−ヒドロキシフェニル)−3−フェニル−2−ピラゾリン−5−オン;
1−(4−ヒドロキシメチルフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−アミノフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−メチルアミノフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−エチルアミノフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−ブチルアミノフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(4−ジメチルアミノフェニル)−3−メチル−2−ピラゾリン−5−オン;
1−(アセトアミドフェニル)−3−メチル−2−ピラゾリン−5−オン;及び
1−(4−シアノフェニル)−3−メチル−2−ピラゾリン−5−オン
【0040】
本発明の鉄キレート剤の有効成分としては、式(I)で表される遊離形態の化合物のほか、生理学的に許容される塩を用いてもよい。生理学的に許容される塩としては、塩酸、硫酸、臭化水素塩、リン酸等の鉱酸との塩;メタンスルホン酸、p−トルエンスルホン酸、ベンゼンスルホン酸、酢酸、グリコール酸、グルクロン酸、マレイン酸、フマル酸、シュウ酸、アスコルビン酸、クエン酸、サリチル酸、ニコチン酸、酒石酸等の有機酸との塩;ナトリウム、カリウム等のアルカリ金属との塩;マグネシウム、カルシウム等のアルカリ土類金属との塩;アンモニア、トリス(ヒドロキシメチル)アミノメタン、N,N−ビス(ヒドロキシエチル)ピペラジン、2−アミノ−2−メチル−1−プロパノール、エタノールアミン、N−メチルグルタミン、L−グルタミン等のアミンとの塩が挙げられる。また、グリシンなどのアミノ酸との塩を用いてもよい。
【0041】
本発明の鉄キレート剤の有効成分としては、上記式(I)で表される化合物若しくはその生理学的に許容される塩の水和物、又は上記式(I)で表される化合物若しくはその生理学的に許容される塩の溶媒和物を用いてもよい。溶媒和物を形成する有機溶媒の種類は特に限定されないが、例えば、メタノール、エタノール、エーテル、ジオキサン、テトラヒドロフランなどを例示することができる。また、上記式(I)で表される化合物は、置換基の種類により1以上の不斉炭素を有する場合があり、光学異性体又はジアステレオ異性体などの立体異性体が存在する場合がある。本発明の鉄キレート剤の有効成分としては、純粋な形態の立体異性体、立体異性体の任意の混合物、ラセミ体などを用いてもよい。
【0042】
式(I)で表される化合物はいずれも公知の化合物であり、特公平5−31523号公報などに記載された方法により当業者が容易に合成できる。
【0043】
本発明の鉄キレート剤は、鉄が関与する疾病に対する広範囲な組織保護剤として応用できる。すなわち、本発明の鉄キレート剤は、鉄の過剰の存在を防止することによって疾病の発症を防止する予防剤としての作用、及び/又は過剰に存在する鉄を正常な状態に回復させることによって疾病を治療する治療剤としての作用を有している。
【0044】
鉄が関与する疾病とは、鉄イオン(または鉄の沈着)が関与する全ての病態を包含する。例えば、加齢に伴って、血管壁にカルシウムが沈着することが知られているが、最近の研究では鉄も同様に沈着していくことが明らかにされた。さらには、アンジオテンシンII(AngiotensinII)によってHO-1が活性化され、組織(心臓、腎臓)に鉄が沈着することなどが報告されている。
さらに糖尿病と鉄過剰症との関係については、瀉血により生体内の鉄量を減少させると糖尿病患者の糖代謝が改善してインスリン使用量が減少できること、貧血治療で鉄を負荷すると、糖尿病性臓器障害が早期に起こったり悪化することが報告されているので、生体内の鉄増加が糖尿病を進展させ、鉄減少が糖尿病の悪化を予防できることが予測される。そこで、鉄キレート剤は糖尿病の進展や・慢性化防止あるいはこれに伴う循環障害(動脈硬化、脳梗塞、心筋梗塞)の予防に有効であると考えられる。
また、特に、本発明の鉄キレート剤は脂溶性の鉄キレート剤であるため、組織内に沈着した鉄に対するキレート剤として有用である。
【0045】
本発明の鉄キレート剤の投与経路は特に限定されず、経口的又は非経口的に投与することができる。非経口投与の投与経路も特に限定されず、静脈内、筋肉内、皮内、皮下に注射投与することができる。
【0046】
また、本発明の鉄キレート剤は、鉄が関与する疾病の発症に先立って予防的に投与しておくことができる。また、当該疾病を起こした患者に対しては、症状の悪化の防止ないしは症状の軽減などを目的として、本発明の鉄キレート剤を該患者に投与することができる。
【0047】
本発明の鉄キレート剤の投与量は特に限定されないが、通常は、有効成分である式(I)で示される化合物の重量として一般に経口投与の場合には一日あたり0.1〜1000mg/kg体重、好ましくは一日あたり0.5〜50mg/kg体重、であり、非経口投与の場合には一日あたり0.01〜100mg/kg体重、好ましくは0.1〜10mg/kg体重である。上記投与量は1日1回又は2〜3回に分けて投与するのが好ましく、年齢、病態、症状により適宜増減してもよい。
【0048】
本発明の鉄キレート剤としては、上記式(I)で表される化合物若しくはその生理学的に許容される塩、又はそれらの水和物若しくは溶媒和物をそのまま投与してもよいが、一般的には、有効成分である上記の物質と薬理学的及び製剤学的に許容される添加物を含む医薬組成物を調製して投与することが好ましい。
【0049】
薬理学的及び製剤学的に許容しうる添加物としては、例えば、賦形剤、崩壊剤ないし崩壊補助剤、結合剤、滑沢剤、コーティング剤、色素、希釈剤、基剤、溶解剤ないし溶解補助剤、等張化剤、pH調節剤、安定化剤、噴射剤、及び粘着剤等を用いることができる。
【0050】
経口投与に適する医薬組成物には、添加物として、例えば、ブドウ糖、乳糖、D−マンニトール、デンプン、又は結晶セルロース等の賦形剤;カルボキシメチルセルロース、デンプン、又はカルボキシメチルセルロースカルシウム等の崩壊剤又は崩壊補助剤;ヒドロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース、ポリビニルピロリドン、又はゼラチン等の結合剤;ステアリン酸マグネシウム又はタルク等の滑沢剤;ヒドロキシプロピルメチルセルロース、白糖、ポリエチレングリコール又は酸化チタン等のコーティング剤;ワセリン、流動パラフィン、ポリエチレングリコール、ゼラチン、カオリン、グリセリン、精製水、又はハードファット等の基剤を用いることができる。
【0051】
注射あるいは点滴用に適する医薬組成物には、注射用蒸留水、生理食塩水、プロピレングリコール等の水性あるいは用時溶解型注射剤を構成しうる溶解剤又は溶解補助剤;ブドウ糖、塩化ナトリウム、D−マンニトール、グリセリン等の等張化剤;無機酸、有機酸、無機塩基又は有機塩基等のpH調節剤等の添加物を用いることができる。
【0052】
本発明の鉄キレート剤の形態は特に限定されず、当業者に利用可能な種々の形態をとることができる。経口投与に適する医薬として、例えば、固体の製剤用添加物を用いて錠剤、散剤、顆粒剤、硬ゼラチンカプセル剤、坐剤、又はトローチ剤などを調製することができ、液状の製剤用添加物を用いてシロップ剤、乳剤、軟ゼラチンカプセル剤などを調製することができる。また、非経口投与に適する医薬として、注射剤、点滴剤、吸入剤、坐剤、経皮吸収剤、経粘膜吸収剤などを調製することができる。なお、上記の式(I)の化合物を有効成分とする脳保護剤(点滴剤)が、すでに臨床において使用されているので(一般名「エダラボン」、商品名「ラジカット」:三菱ウェルファーマ株式会社製造・販売)、本発明の鉄キレート剤において上記市販製剤をそのまま用いることができる。
【0053】
さらに本発明によれば、鉄と上記式(I)で示されるピラゾロン誘導体(特に好ましくは、3−メチル−1−フェニル−2−ピラゾリン−5−オン(エダラボン))との1:6錯体が提供される。鉄は好ましくは3価鉄である。
エダラボンは水に難溶性であるため、牛血清アルブミン(以下、BSAという。)を共存させることによって錯体を形成させることができる。例えば、10%BSA溶液に、3価鉄水溶液とエダラボン水溶液を添加することにより、鉄とエダラボンとの1:6錯体を形成することができる。3価鉄とエダラボンの溶液については水溶液の代わりにエタノール溶液などを用いることもできる。
【0054】
上記のようにして形成される鉄とエダラボンとの1:6錯体は、エダラボンの生理活性を評価の際あるいはエダラボンの生理活性を増強する物質のスクリーニングの際等に有用である。
【0055】
【実施例】
以下、本発明を実施例によりさらに具体的に説明するが、本発明は下記の実施例により限定されるものではない。
【0056】
合成例:3−メチル−1−フェニル−2−ピラゾリン−5−オン(以下、エダラボンと称す)の合成
エタノール50ml中にアセト酢酸エチル13.0g及びフェニルヒドラジン10.8gを加え、3時間還流攪拌した。反応液を放冷後、析出した結晶をろ取し、エタノールより再結晶して、表題の化合物11.3gを無色結晶として得た。
収率 67%
融点 127.5〜128.5℃
【0057】
実施例1:エダラボンによる3価鉄還元活性の検討
エダラボンがヒドロキシルラジカル(・OH)と相互作用するということは、エダラボンとヒドロキシルラジカル(・OH)はそれぞれ還元剤、酸化剤として相互作用していることを意味する。そこで、エダラボンに3価鉄を2価鉄に還元する能力があるか否かを確認するために、酸素電極による酸素吸収実験を行った。これは、もし3価鉄がエダラボンによって2価鉄に還元されると、溶存酸素を次式に従って消費する現象が確認できると考えたからである。
4Fe2+ + 4H+ + O2 → 4Fe3+ + 2H2O
【0058】
20mMのエダラボンを含む緩衝液(0.1M HEPES(丸善(株)化学便覧、基礎編改訂3版、II−355, 1998), pH 7.4,37℃)に0.2mMの3価鉄もしくは2価鉄を図1の矢印に示す位置で添加した。結果を図1に示す。
その結果、鉄イオンに比して100倍濃いエダラボンを添加したにもかかわらず、3価鉄の還元による酸素吸収の促進は見られなかった。このことより、エダラボンは3価鉄を2価鉄に還元する能力は乏しいと考えた。
【0059】
実施例2:エダラボンによるトランスフェリンからの鉄の遊離
トランスフェリンは血漿中での鉄貯蔵に関与しており、遊離鉄が関与する様々な酸化ストレスから生体を防御している。そこで、エダラボンがこのトランスフェリンと相互作用するか否かについて、分光光度計でトランスフェリンの吸光度の変化をモニタリングすることにより検討した。
【0060】
緩衝液(0.1M HEPES,pH 7.4,37℃)を用いて調製した0.1mMのトランスフェリン(A)と0.1mMのエダラボン(B)を混合し、直後と(C)、60分後に(D)吸光度を測定した。結果を図2に示す。
トランスフェリンは鉄と結合することにより、465nm近傍に特徴的な吸収スペクトルを呈する(A)。このスペクトルはエダラボンが共存しても変化しなかったことから、エダラボンと鉄との結合は、トランスフェリンと鉄の結合よりも弱い可能性が示唆された。
【0061】
実施例3:エダラボンと3価鉄の相互作用の検討
次に、エダラボンと3価鉄の相互作用について検討した。エダラボンは水に難溶性であるため、以下の実験はBSA(Serologicals Corporationより購入)を共存させて行った。最初に、極性溶媒(水)中でエダラボンが3価鉄と錯体を形成しているか否かをESR(電子スピン共鳴)にて検証した。
【0062】
(条件)
Control:10%BSA溶液に、0.6mM3価鉄を添加し、液体窒素温度でESRを測定した。測定条件は1600±500ガウス(gauss)。
+Edaravone:10%BSA溶液に、0.6mM3価鉄と3.0mMエダラボンを添加し、液体窒素温度でESRを測定。測定条件は1600±500ガウス。
【0063】
結果を図3に示す。この結果より、エダラボンを添加すると明らかに非ヘム鉄領域(g=4)のESRスペクトルが変化したことから、3価鉄とエダラボンが何らかの相互作用をしている可能性が示唆された。但し、エダラボンの添加による、ESRスペクトルの変化は小さかった。これは、鉄とアルブミンによる錯体と、鉄とエダラボンによる錯体のESRスペクトルが似ているためと思われた。
【0064】
実施例4:エダラボンと3価鉄の錯体形成比の検討
モル比法を用いて、エダラボンと三価鉄の錯形成時の構成比を検討した。
エタノールに溶解した0.25mMのエダラボンを、同じくエタノールに溶かした2.5mMの3価鉄に累積添加し、吸収スペクトルを測定した。結果を図4に示す。図中Aは2.5mM3価鉄の吸収スペクトルを示す。これにエダラボンを0.25mMづつ添加していくと、吸収スペクトルはB→Kと変化した。
【0065】
次に、最も吸光度の変化が大きかった337nmの吸光度変化を縦軸に、そして横軸にエダラボン/3価鉄の値をとってグラフを作成した(図5)。その結果、エダラボン:3価鉄の比が6:1の所に変曲点が見いだせた。このことからエダラボンと3価鉄は非プロトン溶媒中で錯体を形成していることが推測された。
【0066】
さらにこの点を詳細に検討する目的で、エタノール中でのエダラボン−3価鉄のESRスペクトルを液体窒素温度で測定した。
0.7mM3価鉄のエタノール溶液(A)に、エダラボンのエタノール溶液を0.7mMづつ追加((B)→(K))したときのESRスペクトルを図6に示す。測定条件は2500±2500ガウス。
【0067】
非プロトン溶媒系で、3価鉄とエダラボンの比率を変えながらESRスペクトルを測定したところ、ハイスピン(High-spin)鉄のg=6のシグナルが、エダラボンが追加されるに従って減弱した。逆に非ヘム鉄(g=4)のESRシグナルの増大が観察された。
【0068】
次に、これらを使ってそれぞれのESRシグナル強度と混合比の関係を調べると、図7に示すグラフが得られた。
(条件)
上のグラフ:g=6の部分のスペクトル強度と、エダラボン/3価鉄の比
下のグラフ:g=4の部分のスペクトル強度と、エダラボン/3価鉄の比
共にエダラボン/三価鉄の比が6の所で変曲点を迎えていることが示された。
【0069】
【発明の効果】
本発明の鉄キレート剤は、鉄が関与する疾病に対する広範囲な組織保護剤として応用できる。特に本発明の鉄キレート剤は高脂溶性の鉄キレート剤であるため、組織内に沈着した鉄に対して特に有効である。
【図面の簡単な説明】
【図1】図1は、エダラボンによる3価鉄還元活性の測定結果を示す。
【図2】図2は、エダラボンによるトランスフェリンからの鉄の遊離の測定結果を示す。
【図3】図3は、極性溶媒(水)中でエダラボンが3価鉄と錯体を形成しているか否かをESR(電子スピン共鳴法)にて検証した結果を示す。
【図4】図4は、エタノールに溶解した0.25mMのエダラボンを、同じくエタノールに溶かした2.5mMの3価鉄に累積添加し、吸収スペクトルを測定した結果を示す。
【図5】図5は、図4の結果に基づいて337nmの吸光度変化を縦軸に、そして横軸にエダラボン/3価鉄の値をとって作成したグラフを示す。
【図6】図6は、0.7mM3価鉄のエタノール溶液(A)に、エダラボンのエタノール溶液を0.7mMづつ追加((B)→(K))したときのESRスペクトルを示す。
【図7】図7は、図6の結果に基づいて、それぞれのESRシグナル強度と混合比の関係を調べたグラフを示す。
Claims (8)
- 下記式(I):
で示されるピラゾロン誘導体若しくはその生理学的に許容される塩、又はそれらの水和物若しくは溶媒和物を有効成分として含む、鉄キレート剤。 - 式(I)で示されるピラゾロン誘導体が3−メチル−1−フェニル−2−ピラゾリン−5−オンである請求項1に記載の鉄キレート剤。
- 鉄と式(I)で示されるピラゾロン誘導体とが1:6錯体を形成する、請求項1又は2に記載の鉄キレート剤。
- 鉄が3価鉄である、請求項1から3の何れかに記載の鉄キレート剤。
- 鉄が関与する疾病に対する組織保護剤として用いる請求項1から4の何れかに記載の鉄キレート剤。
- 鉄と下記式(I):
で示されるピラゾロン誘導体との1:6錯体。 - 鉄と3−メチル−1−フェニル−2−ピラゾリン−5−オンとの1:6錯体。
- ヒトの体内において、体内に存在する鉄と反応して請求項6又は7記載の1:6錯体を形成せしめる化合物を含有する鉄過剰症の予防及び/又は治療のための医薬。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002376668A JP2004203820A (ja) | 2002-12-26 | 2002-12-26 | 鉄キレート剤 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002376668A JP2004203820A (ja) | 2002-12-26 | 2002-12-26 | 鉄キレート剤 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2004203820A true JP2004203820A (ja) | 2004-07-22 |
Family
ID=32814072
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2002376668A Pending JP2004203820A (ja) | 2002-12-26 | 2002-12-26 | 鉄キレート剤 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2004203820A (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010032489A1 (ja) | 2008-09-22 | 2010-03-25 | 国立大学法人旭川医科大学 | 鉄キレート剤及びその製造方法、並びに鉄イオンの定量・捕捉方法 |
| WO2012096183A1 (ja) | 2011-01-14 | 2012-07-19 | 株式会社ダステック | 高分子鉄キレート剤 |
| CN103319409A (zh) * | 2013-07-12 | 2013-09-25 | 四川省惠达药业有限公司 | 一种依达拉奉化合物、其药物组合物及其制备方法 |
-
2002
- 2002-12-26 JP JP2002376668A patent/JP2004203820A/ja active Pending
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010032489A1 (ja) | 2008-09-22 | 2010-03-25 | 国立大学法人旭川医科大学 | 鉄キレート剤及びその製造方法、並びに鉄イオンの定量・捕捉方法 |
| US8623661B2 (en) | 2008-09-22 | 2014-01-07 | National University Corporation Asahikawa Medical College | Iron chelating agent, method for producing same, method for determining amount of iron ions and method for trapping iron ions |
| WO2012096183A1 (ja) | 2011-01-14 | 2012-07-19 | 株式会社ダステック | 高分子鉄キレート剤 |
| US9796605B2 (en) | 2011-01-14 | 2017-10-24 | Disease Adsorption System Technologies Co., Ltd. | Polymeric iron chelating agent |
| CN103319409A (zh) * | 2013-07-12 | 2013-09-25 | 四川省惠达药业有限公司 | 一种依达拉奉化合物、其药物组合物及其制备方法 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CA2555457C (en) | A novel therapeutic agent for amyotrophic lateral sclerosis (als) or diseases caused by als | |
| JP6116591B2 (ja) | 多発性嚢胞腎の予防及び/又は治療薬 | |
| JP5081890B2 (ja) | 抗血栓薬とピラゾロン誘導体との組み合わせ薬剤 | |
| US11382895B2 (en) | Methods for treating injury associated with exposure to an alkylating species | |
| US20210403434A1 (en) | Metabolically stable 5-hmf derivatives for the treatment of hypoxia | |
| JPWO2003024446A1 (ja) | 酸化ストレス抑制剤および酸化ストレスの測定方法 | |
| JP2004203820A (ja) | 鉄キレート剤 | |
| JP5469707B2 (ja) | 脳梗塞に関連する脳血管障害の治療に有用なピラゾロン化合物 | |
| BG63803B1 (bg) | Фармацевтичен състав за профилактика и лечение надиабетични усложнения | |
| JP5259970B2 (ja) | 薬物依存症治療剤 | |
| JP2003081830A (ja) | 酸化ストレス抑制剤 | |
| US20060135588A1 (en) | Preventive and/or therapeutic drugs for inflammatory intestinal diseases | |
| US7312239B2 (en) | Medicament for prevention and/or therapy of arterial wall disorder | |
| KR20080015123A (ko) | 피라졸론 유도체를 포함하는 의약 | |
| JP2004123700A (ja) | パーオキシナイトライト消去剤 | |
| JP2004115508A (ja) | 熱傷皮膚組織の機能改善のための医薬 | |
| JP2003083977A (ja) | 酸化ストレスの測定方法 | |
| JP2004137252A (ja) | 細胞障害マーカー抑制剤 | |
| JP2006096664A (ja) | 肝繊維化抑制剤 | |
| JP2021028335A (ja) | 糖尿病性腎症の治療薬または予防薬 | |
| JP2004002381A (ja) | エンドトキシン血症に起因する肝障害の予防及び/又は治療のための医薬 | |
| JP2006182677A (ja) | 尿細管間質障害の治療及び/又は予防剤 | |
| JP2005089456A (ja) | ミトコンドリア脳筋症の治療及び/又は予防剤 | |
| WO2003064395A1 (fr) | Agents preventifs et therapeutiques destines a lutter contre des maladies neurodegeneratives | |
| JP2004115511A (ja) | ピラゾロン誘導体を有効成分とするナトリウム・カルシウム交換系阻害剤 |