ES2882855T3 - Inmunomodulación por inhibidores de IAP - Google Patents
Inmunomodulación por inhibidores de IAP Download PDFInfo
- Publication number
- ES2882855T3 ES2882855T3 ES13178264T ES13178264T ES2882855T3 ES 2882855 T3 ES2882855 T3 ES 2882855T3 ES 13178264 T ES13178264 T ES 13178264T ES 13178264 T ES13178264 T ES 13178264T ES 2882855 T3 ES2882855 T3 ES 2882855T3
- Authority
- ES
- Spain
- Prior art keywords
- antigen
- alkyl
- iap inhibitor
- fluoro
- ethyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 0 CC(*(C)*)*(*C(*)C(CCNC)=*C)=O Chemical compound CC(*(C)*)*(*C(*)C(CCNC)=*C)=O 0.000 description 6
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4427—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems
- A61K31/4439—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems containing a five-membered ring with nitrogen as a ring hetero atom, e.g. omeprazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/42—Oxazoles
- A61K31/421—1,3-Oxazoles, e.g. pemoline, trimethadione
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/425—Thiazoles
- A61K31/427—Thiazoles not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/506—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/0005—Vertebrate antigens
- A61K39/0011—Cancer antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/39—Medicinal preparations containing antigens or antibodies characterised by the immunostimulating additives, e.g. chemical adjuvants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/10—Antimycotics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P33/00—Antiparasitic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P33/00—Antiparasitic agents
- A61P33/02—Antiprotozoals, e.g. for leishmaniasis, trichomoniasis, toxoplasmosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/04—Immunostimulants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55511—Organic adjuvants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/80—Vaccine for a specifically defined cancer
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0634—Cells from the blood or the immune system
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Medicinal Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Epidemiology (AREA)
- Immunology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Oncology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Mycology (AREA)
- Microbiology (AREA)
- Communicable Diseases (AREA)
- Tropical Medicine & Parasitology (AREA)
- Virology (AREA)
- Transplantation (AREA)
- Hematology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
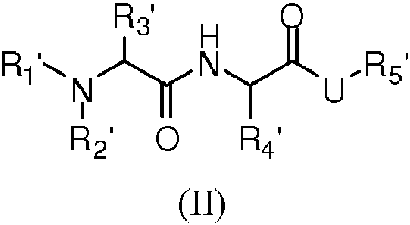
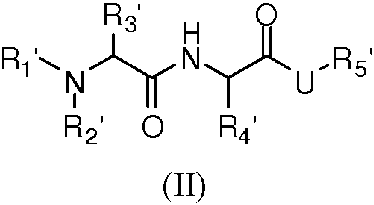
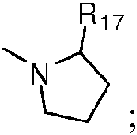
Una composición farmacéutica que comprende un vehículo farmacéuticamente aceptable, una cantidad inmunogénica de un antígeno y un adyuvante que comprende un inhibidor de IAP, en el que el antígeno comprende un antígeno presente en una célula de cáncer; una célula cancerosa; un fragmento de célula cancerosa; un antígeno tumoral; α-galcer; anti-CD3; anti-CD28; anti-IgM; anti-CD40; un patógeno, un patógeno atenuado o una porción del mismo; y el inhibidor de IAP es un compuesto de Fórmula II **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en el que R1' es H; R2' es alquilo C1-C4; R3' es alquilo C1-C4; R4' es cicloalquilo C3-C10; R5' es H o alquilo C1-C10; U es **(Ver fórmula)** R17 es Ar1-D-Ar2; D es CO, O o N(Rx); Rx es H o alquilo C1-7; y Ar1 y Ar2 son arilo o heteroarilo sustituido o no sustituido.
Description
DESCRIPCIÓN
Inmunomodulación por inhibidores de IAP
Antecedentes de la invención
La inmunización es el proceso de administrar material antigénico (por ejemplo, una vacuna) para producir o aumentar artificialmente una respuesta inmune. Un problema que se encuentra con frecuencia es que muchos antígenos usados para la inmunización no son lo suficientemente inmunogénicos para generar un título de anticuerpos suficiente para proporcionar protección contra futuros desafíos. Los antígenos débiles también pueden ser deficientes para inducir inmunidad mediada por células. Para fortalecer la respuesta inmune humoral y/o celular a un antígeno, es común administrar un antígeno junto con un adyuvante. Un adyuvante es una sustancia que mejora la respuesta inmune a un antígeno. La administración de un adyuvante con un antígeno puede hacer que un individuo responda a un antígeno que de otro modo no respondería en ausencia del adyuvante. Los adyuvantes comúnmente usados incluyen adyuvante de Freund, hemocianina de lapa californiana (KLH) y factor estimulante de colonias de granulocitos-macrófagos (GM-CSF). A pesar de las propiedades mejoradoras de la inmunidad de los adyuvantes conocidos, estos adyuvantes siguen siendo insuficientes para inducir una respuesta inmunitaria en un sujeto contra muchos antígenos clínicamente importantes, por ejemplo, antígenos asociados a tumores.
Por consiguiente, existe la necesidad de nuevas composiciones adyuvantes.
El documento WO2008057172 se refiere a métodos para predecir qué pacientes responderán a un compuesto inhibidor de IAP que comprende: a) administrar un compuesto inhibidor de IAP (inhibidor de la apoptosis) a un paciente, y b) medir los niveles de TNF-a o IL-8. El documento WO2008016893 se refiere a compuestos para el tratamiento de enfermedades proliferativas que dependen de la unión de la proteína Smac (segundo activador mitocondrial de caspasas) a las IAP. El documento WO2008109057 se refiere a métodos de tratamiento de neoplasias que comprenden la combinación de un inhibidor del receptor del factor de crecimiento con un compuesto que inhibe la unión de la proteína Smac a las IAP, y uno o más agentes farmacéuticamente activos. Los documentos US20050234042A y WO2008067280 se refieren a compuestos que inhiben la unión de la proteína Smac a las IAP. El documento WO2008014236 se refiere a antagonistas de IAP. El documento FR2610934A se refiere a tetrapéptidos, su preparación y composiciones farmacéuticas que los contienen. El documento US2005197403 se refiere a miméticos del péptido dimérico Smac. El documento WO2006091972 se refiere a imitaciones moleculares de Smac. El documento WO2005077969 se refiere a inhibidores de serina proteasa.
Sumario de la invención
La presente invención se describe en las reivindicaciones adjuntas y se refiere a adyuvantes que poseen propiedades inmunogénicas mejoradas. Estos adyuvantes inmunes son capaces de mejorar ampliamente la activación de las células inmunes. En al menos una realización, la presente invención se refiere al descubrimiento inesperado de que los inhibidores de la familia de la proteína IAP (inhibidora de apoptosis) funcionan como potentes adyuvantes inmunes capaces de mejorar señales de activación fisiológicamente relevantes en diversos linajes de células inmunes. Por consiguiente, la invención presenta, en un primer aspecto, una composición farmacéutica que comprende un vehículo farmacéuticamente aceptable, una cantidad inmunogénica de un antígeno y un adyuvante que comprende un inhibidor de IAP, en el que el antígeno comprende un antígeno presente en una célula de cáncer; una célula cancerosa; un fragmento de célula cancerosa; un antígeno tumoral; a-galcer; anti-CD3; anti-CD28; anti-IgM; anti-CD40; un patógeno, un patógeno atenuado o una porción del mismo; y el inhibidor de IAP es un compuesto de Fórmula II
o una sal farmacéuticamente aceptable del mismo, en el que
R1' es H;
R2 ' es alquilo C1-C4 ;
R3 ' es alquilo C1-C4 ;
R4 ' es cicloalquilo C3-C10;
R5 ' es H o alquilo C1-C10;
U es
R17 es Ari-D-Ar2 ;
D es CO, O o N(Rx);
Rx es H o alquilo C1-7; y
Ari y Ar2 son arilo sustituido o no sustituido o heteroarilo.
En un segundo aspecto, la invención presenta un kit que comprende:
(a) una composición farmacéutica de acuerdo con el primer aspecto de la invención;
(b) un material de empaquetamiento que encierra dicha composición farmacéutica; y
(c) instrucciones de uso de dicha composición farmacéutica.
En un tercer aspecto, la invención presenta una vacuna que comprende una cantidad inmunogénica de un antígeno y un adyuvante que comprende un inhibidor de IAP, en el que el antígeno comprende un antígeno presente en una célula de cáncer; una célula cancerosa; un fragmento de célula cancerosa; un antígeno tumoral; a-galcer; anti-CD3; anti-CD28; anti-IgM; anti-CD40; un patógeno, un patógeno atenuado o una porción del mismo; y el inhibidor de IAP es un compuesto de Fórmula II
o una sal farmacéuticamente aceptable del mismo, en el que
R1' es H;
R2' es alquilo C1-C4 ;
R3' es alquilo C1-C4 ;
R4' es cicloalquilo C3-C10;
R5' es H o alquilo C1-C10;
U es
R17 es An-D-Ar2 ;
D es CO, O o N(Rx);
Rx es H o alquilo C1-7; y
Ar1 y Ar2 son arilo sustituido o no sustituido o heteroarilo.
En un cuarto aspecto, la invención presenta una cantidad inmunogénica de un antígeno y una cantidad inmunogénica de un inhibidor de IAP para su uso en la mejora de la respuesta inmunitaria de un sujeto a un antígeno, en el que el antígeno comprende un antígeno presente en un célula de cáncer; una célula cancerosa; un fragmento de célula cancerosa; un antígeno tumoral; a-galcer; anti-CD3; anti-CD28; anti-IgM; anti-CD40; un patógeno, un patógeno atenuado o una porción del mismo; y el inhibidor de IAP es un compuesto de Fórmula (II)
o una sal farmacéuticamente aceptable del mismo, en el que
R1' es H;
R2' es alquilo C1-C4 ;
R3' es alquilo C1-C4 ;
R4' es cicloalquilo C3-C10;
R5' es H o alquilo C1-C10;
U es
R17 es Ari-D-Ar2 ;
D es CO, O o N(Rx);
Rx es H o alquilo C1-7; y
Ar1 y Ar2 son arilo sustituido o no sustituido o heteroarilo.
En un quinto aspecto, la invención presenta una cantidad terapéuticamente eficaz de un inhibidor de IAP y una cantidad inmunogénica de un antígeno para uso en el tratamiento de un cáncer en un sujeto, en el que dicho inhibidor de IAP y dicho antígeno mejoran la respuesta inmune del sujeto al cáncer, y en el que el antígeno comprende un antígeno presente en una célula de cáncer; una célula cancerosa; un fragmento de célula cancerosa; un an tígeno tumoral; agalcer; anti-CD3; anti-CD28; anti-IgM; anti-CD40; un patógeno, un patógeno atenuado o una porción del mismo; y el inhibidor de IAP es un compuesto de Fórmula (II)
o una sal farmacéuticamente aceptable del mismo, en el que
R1' es H;
R2 ' es alquilo C1-C4 ;
R3 ' es alquilo C1-C4 ;
R4 ' es cicloalquilo C3-C10;
R5 ' es H o alquilo C1-C10;
U es
R17 es Ar1-D-Ar2 ;
D es CO, O o N(Rx);
Rx es H o alquilo C1-7; y
Ar1 y Ar2 son arilo sustituido o no sustituido o heteroarilo.
En un sexto aspecto, la invención presenta una cantidad terapéuticamente eficaz de un inhibidor de IAP y una cantidad inmunogénica de un antígeno, para uso en el tratamiento o la prevención de una infección causada por un agente infeccioso, en el que dicho inhibidor de IAP y dicho antígeno mejoran la respuesta inmune del sujeto al agente infeccioso, en el que el inhibidor de IAP es un compuesto de Fórmula (II)
o una sal farmacéuticamente aceptable del mismo, en el que
R1' es H;
R2 ' es alquilo C1-C4 ;
R3 ' es alquilo C1-C4 ;
R4 ' es cicloalquilo C3-C10;
R5 ' es H o alquilo C1-C10;
U es
R17 es Ar1-D-Ar2 ;
D es CO, O o N(Rx);
Rx es H o alquilo C1-7; y
Ar1 y Ar2 son arilo sustituido o no sustituido o heteroarilo
En un séptimo aspecto, la invención presenta un inhibidor de IAP para uso en la mejora de la actividad inmunitaria de una célula inmunitaria activada en un sujeto, en el que el inhibidor de IAP es un compuesto de Fórmula (II).
o una sal farmacéuticamente aceptable del mismo, en el que
Ri' es H;
R2 ' es alquilo C1-C4 ;
R3 ' es alquilo C1-C4 ;
R4 ' es cicloalquilo C3-C10;
R5 ' es H o alquilo C1-C10;
U es
R17 es Ar1-D-Ar2 ;
D es CO, O o N(Rx);
Rx es H o alquilo C1-7 ; y
Ar1 y Ar2 son arilo sustituido o no sustituido o heteroarilo
En un octavo aspecto, la invención presenta una cantidad terapéuticamente eficaz de un inhibidor de IAP y una cantidad inmunogénica de un antígeno para uso en la activación de una célula inmunitaria contra el antígeno en un sujeto, en el que el inhibidor de IAP es un compuesto de Fórmula ( II)
o una sal farmacéuticamente aceptable del mismo, en el que
R1' es H;
R2 ' es alquilo C1-C4 ;
R3 ' es alquilo C1-C4 ;
R4 ' es cicloalquilo C3-C10;
R5 ' es H o alquilo C1-C10;
U es
R17 es Ar1-D-Ar2 ;
D es CO, O o N(Rx);
Rx es H o alquilo C1-7; y
Ar1 y Ar2 son arilo sustituido o no sustituido o heteroarilo.
En un noveno aspecto, la invención presenta el uso ex vivo de una cantidad terapéuticamente eficaz de un inhibidor de IAP y una cantidad inmunogénica de un antígeno para activar una célula inmunitaria contra el antígeno, en el que el inhibidor de IAP es un compuesto de Fórmula (II )
o una sal farmacéuticamente aceptable del mismo, en el que
R1' es H;
R2 ' es alquilo C1-C4;
R3 ' es alquilo C1-C4;
R4 ' es cicloalquilo C3-C10;
R5 ' es H o alquilo C1-C10;
U es
R17 es Ari-D-Ar2 ;
D es CO, O o N (Rx);
Rx es H o alquilo C1-7; y
Ar1 y Ar2 son arilo sustituido o no sustituido o heteroarilo.
Breve descripción de los dibujos
La Figura 1 representa datos que indican que el desarrollo de células NKT en cultivo de órganos tímicos fetales (FTOC) está bloqueado por el tratamiento con inhibidores de IAP.
La Figura 2 representa datos que indican que la inhibición de los miembros de la familia de IAP no sensibiliza las células T CD4+ maduras a la apoptosis.
La Figura 3 representa datos que indican que la inhibición de los miembros de la familia de IAP mejoran la secreción de citocinas a partir de células T activadas.
La Figura 4 representa datos que indican que la secreción de citocinas mejorada de las células T activadas causada por la inhibición de los miembros de la familia de IAP es independiente de las células NKT.
La Figura 5 representa datos que indican que la producción de citocinas a partir de células T CD8 + activadas aumenta mediante la inhibición de IAP.
La Figura 6 representa datos que indican que las células T CD4+ humanas responden a los inhibidores de IAP. La Figura 7 representa datos que indican que la inhibición de los miembros de la familia de IAP durante la activación de las células T conduce a una señalización mejorada a través de las rutas de JNK y NF-kB.
La Figura 8 representa datos que indican que los inhibidores de IAP mejoran ampliamente la activación de las células inmunes.
La Figura 9 representa datos que indican que la inhibición de los miembros de la familia de IAP mejora la aloreactividad.
La Figura 10 representa datos que indican que la inhibición de IAP se invierte rápidamente en células T alorreactivas estimuladas nuevamente.
La Figura 11 representa datos que indican que la sobreexpresión de la proteína de unión a SMAC, MLIAP, en células T CD4+ conduce a una menor producción de IL-2 después de la estimulación.
La Figura 12 representa datos que indican que las células T con inactivación (KO) de XIAP son resistentes al tratamiento con mimético de SMAC.
La Figura 13 representa datos que indican que los inhibidores de IAP mejoran la activación inmune in vivo y mejoran la inmunidad protectora después de la vacunación.
Descripción detallada de la invención
La presente invención se basa, al menos en parte, en el sorprendente descubrimiento de que los inhibidores de IAP funcionan como potentes adyuvantes inmunes capaces de mejorar señales de activación fisiológicamente relevantes en diversos linajes de células inmunes. Estos compuestos no alteraron la función de las células inmunes en reposo, pero mejoraron la activación de las células inmunes en el contexto de la estimulación. Esta activación se evidencia, por ejemplo, por una mayor expansión y producción de citocinas. Esta propiedad de los inhibidores de IAP posiciona a estos compuestos como agentes ideales para la promoción de la inmunidad, con numerosas aplicaciones clínicas.
Varios aspectos de la invención se describen con más detalle en las siguientes subsecciones. A menos que se defina lo contrario, todos los términos técnicos y científicos usados en este documento tienen el mismo significado que el que entiende comúnmente un experto en la técnica a la que pertenece esta invención. En caso de conflicto, prevalecerá la presente memoria descriptiva, incluidas las definiciones. Aunque se pueden usar métodos y materiales similares o equivalentes a los descritos en el presente documento en la práctica de la invención, a continuación se describen ejemplos de métodos y materiales adecuados. Los materiales, métodos y ejemplos descritos en este documento son solo ilustrativos.
I. Inhibidores de IAP
La apoptosis, un proceso de muerte celular programada, está estrechamente orquestada por una serie de eventos moleculares. Los principales efectores de la muerte celular apoptótica son las caspasas, una familia de cisteína proteasas que escinden preferentemente los péptidos diana adyacentes a los residuos de aspartato. En una célula no apoptótica, las caspasas se retienen en un estado inactivo. Un estímulo proapoptótico desencadena la activación de una cascada de caspasas jerárquica, lo que conduce a la escisión proteolítica de proteínas celulares esenciales y, en última instancia, a la muerte celular.
La activación de las caspasas está estrictamente controlada por varios factores celulares. Los miembros de la familia de proteínas IAP (inhibidora de la apoptosis) se unen directamente a las caspasas y esta unión suprime la actividad de las caspasas. La unión a caspasas está mediada por los dominios IAP BIR (repetición de IAP de baculovirus), que son esenciales para la actividad antiapoptótica de las IAP. La familia de IAP contiene los miembros prototípicos de la familia XIAP, cIAP-1 y cIAP-2, y también incluye, por ejemplo, NAIP (proteína inhibidora de la apoptosis neuronal), ML-IAP (IAP de melanoma), ILP-2 (proteína similar a IAP 2) y Op-IAP (una IAP baculoviral).
Se han identificado varios factores que median adicionalmente en la vía apoptótica suprimiendo la actividad de las IAP. Los más destacados son Smac (segundo activador mitocondrial de caspasas) y el ortólogo DIABLO de Smac murino (proteína de unión IAP directa con pI bajo), que se localizan en las mitocondrias y se liberan en el citosol en respuesta a estímulos apoptóticos. Smac/DIABLO inhibe la actividad de las proteínas IAP uniéndose directamente a las IAP y evitando la interacción de las IAP con las caspasas. El descubrimiento de que los miembros de la familia de IAP se sobreexpresan en numerosos tipos de cáncer llevó a los investigadores a plantear la hipótesis de que los inhibidores de IAP pueden tener importancia clínica como agentes anticancerosos al promover la señalización proapoptótica en las células cancerosas. La presente invención se basa, al menos en parte, en el descubrimiento inesperado de que los inhibidores de IAP son además útiles como adyuvantes inmunes capaces de mejorar una respuesta inmunitaria.
Se han desarrollado numerosos inhibidores de IAP que incluyen miméticos de Smac que también interactúan con las IAP e inhiben su actividad. Por consiguiente, un "inhibidor de IAP" se refiere a cualquier compuesto que inhiba la actividad de un miembro de la familia de IAP. Dichos compuestos pueden incluir, por ejemplo, moléculas pequeñas, polipéptidos (es decir, péptidos miméticos de Smac), moléculas de interferencia de ARN dirigidas a proteínas iA p (por ejemplo, ARNip o ARN antisentido) y anticuerpos anti-IAP.
En realizaciones particulares, un inhibidor de IAP de la divulgación es un compuesto de Fórmula I:
y sales, enantiómeros, estereoisómeros, rotámeros, tautómeros, diastereómeros o racematos farmacéuticamente aceptables de los mismos;
en el que
R1 es H, alquilo C1-C4 , alquenilo C2-C4 , alquinilo C2-C4 o cicloalquilo C3-C10, en el que R4 puede estar sustituido o no sustituido;
R2 es H, alquilo C1-C4 , alquenilo C2-C4 , alquinilo C2-C4 , cicloalquilo C3-C10, en el que R2 puede estar sustituido o no sustituido;
R3 es H, CF3 , C2 F5 , alquilo C1-C4 , alquenilo C2-C4 , alquinilo C2-C4 , CH2-Z, o
R2 y R3, junto con el átomo de nitrógeno al que están unidos, forman un anillo heterocíclico,
en el que los grupos alquilo, alquenilo, alquinilo o anillo heteroarilo pueden estar sustituidos o no sustituidos;
Z es H, OH, F, Cl, CH3 , CH2C CH2 F o CH2OH;
R4 es alquilo C1-10, alquenilo C1-10, alquinilo C1-10, cicloalquilo C3-C10, en el que los grupos alquilo C1-10 o cicloalquilo están sustituidos o no sustituidos;
A es heteroarilo que puede estar sustituido o no sustituido;
D es alquileno C1-C7 o alquenileno C2-C9 , C(O), O, NR7 , S(O)r, C(O)-alquilo C1-C10, O-alquilo C1-C10, S(O)r-alquilo C1-C10, C(O)-arilalquilo C0-C10, O-arilalquilo C0-C10 o S(O)r-arilalquilo C0-C10,
en el que los grupos alquilo y arilo pueden estar sustituidos o no sustituidos;
r es 0 , 1 o 2 ;
A 1 es un arilo sustituido o no sustituido o heteroarilo sustituido o no sustituido, en el que los sustituyentes en el arilo y el heteroarilo son halo, alquilo, alcoxi inferior, NR5R6 , CN, NO2 o SRs;
cada Q es independientemente H, alquilo C1-C10, alcoxi C1-C10, aril-alcoxi C1-C10, OH, O-alquilo C1-C10, (CH2)0-6-cicloalquilo C3-C7 , arilo, aril-alquilo C1-C10, O- arilo (CH2)0-6, heteroarilo (CH2)1-6, heteroarilo, O- heteroarilo(CH2)1-6, -OR11, C(O)Rn, -C(O)N(R11)( R12), N(R11)(R12), SR11, S(O)Rn, S(O)2Rn, S(O)2-N(Rn)(R12), o NRn-S(O)2-(R12), en los que alquilo, cicloalquilo y arilo están sustituidos o no sustituidos;
n es 0, 1, 2 o 3, 4, 5, 6 o 7;
R11 y R12 son independientemente H, alquilo C1-C10, (CH2)0-6-cicloalquilo C3-C7 , (CH2)0-6-(CH)0-1(arilo)1-2, C(O)-alquilo C1-C10, -C(O)-(CH2)1-6-cicloalquilo C3-C7 , -C(O)-O-(CH2)0-6-arilo, -C(O)-(CH2)0-6-O-fluorenilo, C(O)-NH-(CH2)0-6-arilo, C(O)-(CH2)0-6-arilo, C(O)-(CH2)1-6-heteroarilo, -C(S)-alquilo C1-C10, -C(S)-(CH2)1-6-cicloalquilo C3-C7 , -C(S)-O-(CH2)0-6-arilo, -C(S)-(CH2)0-6-O-fluorenilo, C(S)-NH-(CH2)0-6-arilo, -C(S)-(CH2)0-6-arilo o C(S)-(CH2)1-6-heteroarilo C(O)R15, C(O)NR15R16, C(O)OR15, S(O)mR15, S(O)mNR15R16, m = 1 o 2 , c (s )R15, C(S)NR15R16, C(S)OR15, en los que alquilo, cicloalquilo y arilo están sustituidos o no sustituidos; o R11 y R12 son un sustituyente que facilita el transporte de la molécula a través de la membrana celular, o
R11 y R12 junto con el átomo de nitrógeno forman heteroarilo
en el que
los sustituyentes alquilo de R11 y R12 pueden estar sustituidos o no sustituidos por uno o más sustituyentes seleccionados entre alquilo C1-C10, halógeno, OH, O-alquilo C1-C6 , -S-alquilo C1-C6 , CF3 o NR15R16;
los sustituyentes cicloalquilo sustituidos de R11 y R12 están sustituidos por uno o más sustituyentes seleccionados de un alqueno C2-C10; alquilo C1-C6 ; halógeno; OH; O-alquilo C1-C6 ; S-alquilo C1-C6 , CF3 ; o NR15R16 y
heteroarilo sustituido o arilo sustituido de R11 y R12 están sustituidos con uno o más sustituyentes seleccionados entre halógeno, hidroxilo, alquilo C1-C4 , alcoxi C1-C4 , nitro, CNO-C(O)-alquilo C1-C4 y C(O)-O-alquilo C1-C4 ;
R5 , R6 y R7 son independientemente hidrógeno, alquilo inferior, arilo, aril alquilo inferior, cicloalquilo o cicloalquil alquilo inferior, C(O)R15, S(O)R15, C(O)OR15, C(O)NR15R16; y
los sustituyentes en los grupos R1, R2 , R3 , R4 , Q y A y A 1 son independientemente halo, hidroxi, alquilo inferior, alquenilo inferior, alquinilo inferior, alcanoilo inferior, alcoxi inferior, arilo, aril alquilo inferior, amino, amino alquilo inferior, dialquilamino inferior, alcanoílo inferior, amino alcoxi inferior, nitro, ciano, ciano alquilo inferior, carboxi, carboalcoxi inferior, alcanoílo inferior, ariloilo, arilalcanoilo inferior, carbamoilo, N-mono- o N,N-dialquil carbamoilo inferior, éster ácido alquil carbámico inferior, amidino, guanidina, ureido, mercapto, sulfo, alquiltio inferior, sulfoamino, sulfonamida, benzosulfonamida, sulfonato, sulfanil alquilo inferior, arilsulfonamida, arilsulfonato sustituido con halógeno, alquilsulfinilo inferior, arilsulfinilo; aril-alquilsulfinilo inferior, alquilarilsulfinilo inferior, alquilsulfonilo inferior, arilsulfonilo, aril-alquilsulfonilo inferior, aril alquil inferior, alquilarilsulfonilo inferior, halógeno-alquil mercapto inferior-, halógeno-alquilsulfonilo inferior,
fosfono (-P(=O)(OH)2), hidroxi-alcoxi inferior fosforilo o di-alcoxifosforilo inferior, (R9)NC(O)-NR10R13, éster de ácido carbámico de alquilo inferior o carbamatos o -NR8R14,
en los que
Rg y R14 pueden ser iguales o diferentes y son independientemente H o alquilo inferior, o
R8 y R14, junto con el átomo de N, forman un anillo heterocíclico de 3 a 8 miembros que contiene heteroátomos de nitrógeno en el anillo y pueden contener opcionalmente uno o dos heteroátomos adicionales en el anillo seleccionados entre nitrógeno, oxígeno y azufre, en el que el anillo heterocíclico puede estar sin sustituir o sustituido con alquilo inferior, halo, alquenilo inferior, alquinilo inferior, hidroxi, alcoxi inferior, nitro, amino, alquilo inferior, amino, dialquil amino inferior, ciano, carboxi, carboalcoxi inferior, formilo, alcanoilo inferior, oxo, carbamoilo, N-inferior o N,N-dialquilcarbamoilo inferior, mercapto o alquiltio inferior;
R9 , R10 y R13 son independientemente hidrógeno, alquilo inferior, alquilo inferior sustituido con halógeno, arilo, aril alquilo inferior, arilo sustituido con halógeno, aril alquilo inferior sustituido con halógeno,
R15 y R16 son independientemente hidrógeno, alquilo inferior, arilo, aril alquilo inferior, cicloalquilo o cicloalquil alquilo inferior, y
heteroarilo es un anillo heterocíclico monocíclico de 5 a 7 miembros que contiene de 1 a 4 heteroátomos en el anillo seleccionados entre N, O y S o un sistema de anillo condensado de 8 a 12 miembros que incluye un anillo heterocíclico monocíclico de 5 a 7 miembros que contiene 1 ,2 o 3 heteroátomos en el anillo seleccionados entre N, O y S, en los que el heteroarilo está sustituido o no sustituido.
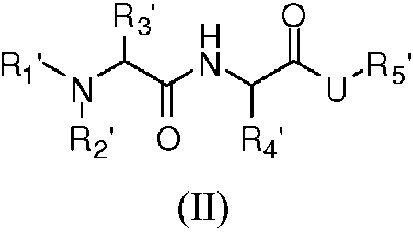
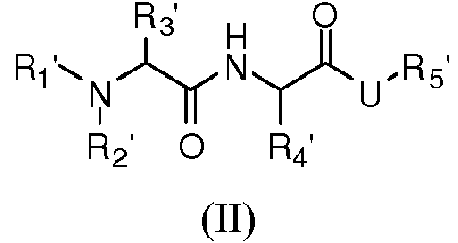
En otra realización, el inhibidor de IAP es un compuesto de Fórmula II:
y sales farmacéuticamente aceptables del mismo, en el que
R1' es H;
R2 ' es alquilo C1-C4 ;
R3 ' es alquilo C1-C4 ;
R4 ' es cicloalquilo C3-C10;
R5 ' es H o alquilo C1-C10;
y U es
R17 es An-D-Ar2 ;
en el que An y Ar2 son arilo o heteroarilo sustituidos o no sustituidos; y
D es -CO-; u -O-; o D es -N(Rx)- en el que Rx es H o alquilo C1-7.
Los inhibidores de IAP y los métodos para su elaboración se divulgan en los documentos WO 2005/097791 y WO 2008/016893.
Como se usa en este documento, el término "alquilo" se refiere a una fracción de hidrocarburo ramificado o no ramificado completamente saturado. Preferiblemente, el alquilo comprende de 1 a 20 átomos de carbono, más preferiblemente de 1 a 16 átomos de carbono, de 1 a 10 átomos de carbono, de 1 a 7 átomos de carbono o de 1 a 4 átomos de carbono. Los ejemplos representativos de alquilo incluyen, pero no se limitan a, metilo, etilo, n-propilo, isopropilo, n-butilo, sec-butilo, iso-butilo, terc-butilo, n-pentilo, isopentilo, neopentilo, n-hexilo, 3-metilhexilo, 2,2-dimetilpentilo, 2,3-dimetilpentilo, n-heptilo, n-octilo, n-nonilo, n-decilo y similares. Además, la expresión "alquilo Cx-Cy", en la que x es 1-5 e y es 2-10 indica un grupo alquilo particular (de cadena lineal o ramificada) de un intervalo particular de carbonos. Por ejemplo, la expresión alquilo C1-C4 incluye, pero no se limita a, metilo, etilo, propilo, butilo, isopropilo, terc-butilo e isobutilo.
El término "alquenilo", solo o en combinación, se refiere a un residuo de hidrocarburo de cadena lineal, cíclico o ramificado que comprende al menos un enlace olefínico y el número indicado de átomos de carbono. Los grupos alquenilo preferidos tienen hasta 8 , preferiblemente hasta 6 , particularmente preferido hasta 4 átomos de carbono. Ejemplos de grupos alquenilo son etenilo, 1-propenilo, 2-propenilo, isopropenilo, 1 -butenilo, 2-butenilo, 3-butenilo, isobutenilo, 1 -ciclohexenilo, 1 -ciclopentenilo.
El término "alquinilo" incluye grupos alifáticos insaturados de longitud análoga a los alquilos descritos anteriormente, pero que contienen al menos un triple enlace.
Por ejemplo, el término "alquinilo" incluye grupos alquinilo de cadena lineal (por ejemplo, etinilo, propinilo, butinilo, pentinilo, hexinilo, heptinilo, octinilo, noninilo, decinilo, etc.), grupos alquinilo de cadena ramificada y grupos alquinilo sustituidos con cicloalquilo o cicloalquenilo. El término alquinilo incluye además grupos alquinilo que incluyen átomos de oxígeno, nitrógeno, azufre o fósforo que reemplazan uno o más carbonos de la cadena hidrocarbonada. En determinadas realizaciones, un grupo alquinilo de cadena lineal o de cadena ramificada tiene 6 o menos átomos de carbono en su estructura (por ejemplo, C2-C6 para cadena lineal, C3-C6 para cadena ramificada). El término C2-C6 incluye grupos alquinilo que contienen de 2 a 6 átomos de carbono.
Como se usa en este documento, el término "cicloalquilo" se refiere a grupos hidrocarbonados monocíclicos, bicíclicos o tricíclicos saturados o insaturados de 3-12 átomos de carbono, preferiblemente 3-9, o 3-7 átomos de carbono. Los ejemplos grupos hidrocarbonados monocíclicos ejemplares incluyen, pero no se limitan a, ciclopropilo, ciclobutilo, ciclopentilo, ciclopentenilo, ciclohexilo y ciclohexenilo y similares. Ejemplos de grupos hidrocarbonados bicíclicos incluyen bornilo, indilo, hexahidroindilo, tetrahidronaftilo, decahidronaftilo, biciclo[2.1.1 ]hexilo, biciclo[2.2.1 ]heptilo, biciclo[2.2.1]heptenilo, 6 ,6 -dimetilbicicl [3.1.1 ]heptilo, 2,6,6-trimetilbiciclo[3.1.1]heptilo, biciclo[2.2.2]octilo y similares. Ejemplos de grupos hidrocarbonados tricíclicos incluyen adamantilo y similares.
El término "cicloalquenilo" se refiere a un grupo hidrocarbonado cíclico parcialmente insaturado que contiene de 1 a 3 anillos y de 4 a 8 carbonos por anillo. Los ejemplos de grupos incluyen ciclobutenilo, ciclopentenilo y ciclohexenilo. El término "cicloalquenilo" también incluye grupos bicíclicos y tricíclicos en los que al menos uno de los anillos es un anillo que contiene carbono parcialmente insaturado y el segundo o tercer anillo puede ser carbocíclico o heterocíclico, siempre que el punto de unión sea al grupo cicloalquenilo.
"Alcoxi" se refiere a aquellos grupos alquilo, que tienen de 1 a 10 átomos de carbono, unidos al resto de la molécula a través de un átomo de oxígeno. Se prefieren los grupos alcoxi con 1-8 átomos de carbono. La porción alquilo de un alcoxi puede ser lineal, cíclica o ramificada, o una combinación de los mismos. Los ejemplos de grupos alcoxi incluyen metoxi, etoxi, isopropoxi, butoxi, ciclopentiloxi y similares. Un grupo alcoxi también se puede representar por la siguiente fórmula: -ORi, en el que Ri es la "porción alquilo" de un grupo alcoxi.
El término "heteroalquilo", por sí mismo o en combinación con otro término, significa, a menos que se indique lo contrario, una cadena lineal o ramificada estable, o combinaciones de las mismas, que consisten en el número indicado de átomos de carbono y de uno a cinco heteroátomos, más preferiblemente de uno a tres heteroátomos, seleccionados
del grupo que consiste en O, N, Si y S, y en el que los átomos de nitrógeno y azufre pueden opcionalmente estar oxidados y el heteroátomo de nitrógeno opcionalmente puede estar cuaternizado. El grupo heteroalquilo está unido al resto de la molécula a través de un átomo de carbono o un heteroátomo.
El término "alquilcarbonilo" se refiere a un grupo que tiene la fórmula-C(O)-Rii, en la que Rii es un grupo alquilo como se definió anteriormente y en la que el número total de átomos de carbono se refiere a las fracciones alquilo y carbonilo combinadas. Se puede unir un grupo "alquilcarbonilo" al resto de la molécula mediante un grupo alquilo (es decir, -alquil-C(O)-Rii).
El término "alcoxicarbonilo" se refiere a un grupo que tiene la fórmula -C(C)ORiii, en la que Riii es un grupo alquilo como se definió anteriormente y en el que el número total de átomos de carbono se refiere a las fracciones alquilo y carbonilo combinadas. Un grupo "alcoxicarbonilo" se puede unir al resto de la molécula mediante un grupo alquilo (es decir, -alquil-C(O)O-Riii).
El término "heteroalquilcarbonilo" se refiere a un grupo que tiene la fórmula -C(O)Riv, en la que Riv es un grupo heteroalquilo como se definió anteriormente y en la que el número total de átomos de carbono se refiere a las fracciones alquilo y carbonilo combinadas. Un grupo "heteroalquilcarbonilo" se puede unir al resto de la molécula mediante un grupo alquilo o heteroalquilo (es decir, -alquil-CCO)O-Riv o -heteroalquil-C(O)O-Riv).
El término "arilo" incluye sistemas de anillos de hidrocarbonados aromáticos monocíclicos o multicíclicos, por ejemplo, tricíclicos, bicíclicos, que consisten solo en hidrógeno y carbono y que contienen de seis a diecinueve átomos de carbono, o de seis a diez átomos de carbono, en los que los sistemas de anillos pueden estar parcialmente saturado. Los grupos arilo incluyen, pero no se limitan a, grupos tales como fenilo, tolilo, xililo, antrilo, naftilo y fenantrilo. Los grupos arilo también se pueden fusionar o formar puentes con anillos alicíclicos o heterocíclicos que no son aromáticos para formar un policiclo (por ejemplo, tetralina).
El término "heteroarilo", como se usa en este documento, representa un anillo monocíclico o bicíclico estable de hasta 7 átomos en cada anillo, en el que al menos un anillo es aromático y contiene de 1 a 4 heteroátomos seleccionados del grupo que consiste en O, N y S. Los grupos heteroarilo dentro del alcance de esta definición incluyen, pero no se limitan a: acridinilo, carbazolilo, cinolinilo, quinoxalinilo, pirrazolilo, indolilo, benzotriazolilo, furanilo, tienilo, benzotienilo, benzofuranilo, quinolinilo, isoquinolinilo, oxazolilo, isoxazolilo, indolilo, pirazinilo, piridazinilo, piridinilo, pirimidinilo, pirrolilo, tetrahidroquinolina. Al igual que con la definición de heterociclo a continuación, también se entiende que "heteroarilo" incluye el derivado de N-óxido de cualquier heteroarilo que contiene nitrógeno. En los casos en los que el sustituyente heteroarilo es bicíclico y un anillo no es aromático o no contiene heteroátomos, se entiende que la unión se realiza mediante el anillo aromático o mediante el anillo que contiene heteroátomos, respectivamente.
El término "heterociclo" o "heterociclilo" se refiere a grupos heterocíclicos no aromáticos de cinco a diez miembros, completamente saturados o parcialmente insaturados que contienen al menos un heteroátomo tal como O, S o N. Los ejemplos más frecuentes son piperidinilo, morfolinilo, piperazinilo, pirrolidinilo o pirazinilo. La unión de un sustituyente heterociclilo puede ocurrir mediante un átomo de carbono o mediante un heteroátomo.
Además, los grupos alquilo, alquenilo, cicloalquilo, cicloalquenilo, alcoxi, arilo, heteroarilo y heterociclo descritos anteriormente pueden estar "sin sustituir" o "sustituidos". El término "sustituido" pretende describir fracciones que tienen sustituyentes que reemplazan un hidrógeno en uno o más átomos, por ejemplo, C, O o N, de una molécula. Dichos sustituyentes pueden incluir independientemente, por ejemplo, uno o más de los siguientes: grupos alquilo lineal o ramificado (preferiblemente C1-C5), cicloalquilo (preferiblemente C3-C8), alcoxi (preferiblemente C1-C6), tioalquilo (preferiblemente C1-C6), alquenilo (preferiblemente C2-C6), alquinilo (preferiblemente C2-C6), heterocíclico, carbocíclico, arilo (por ejemplo, fenilo), ariloxi (por ejemplo, fenoxi), aralquilo (por ejemplo, bencilo), ariloxialquilo (por ejemplo, feniloxialquilo), arilacetamidoilo, alquilarilo, heteroaralquilo, alquilcarbonilo y arilcarbonilo u otros tales como acilo, heteroarilcarbonilo o grupo heteroarilo, grupo (CR'R")0-3NR'R" (por ejemplo, -NH2), (CR'R")0-3CN (por ejemplo, -CN),-NO2 , halógeno (por ejemplo, -F, -Cl, -Br o -I), (Cr 'R")0-3C (halógeno)3 (por ejemplo,-CF3), (CR'R")0-3CH (halógeno)2 , (CR'R")0-3CH2 (halógeno), (CR'R")0-3CONR'R", (CR'R")0-3(CNH)NR'R", (CR'R")0-3S(O)1-2NR'R", (CR'R")0-3CHO, (CR'R")0-3O(CR'R")0-3H, (CR'R")0-3S(O)0-3R' (por ejemplo, -SO3 H, -OSO3 H), (CR'R")0-3O(CR'R")0-3H (por ejemplo, -CH2OCH3 y -OCH3 ), (CR'R")0-3S(CR'R")0-3H (por ejemplo, -SH y -SCH3 ), (CR'R")0-3OH (por ejemplo, -OH), (Cr 'R")0-3COR', (CR'R")0-3(fenilo sustituido o no sustituido), (Cr 'R")0-3 (cicloalquilo C3-C8), (CR'R")0-3CO2R' (por ejemplo, -CO2H), o (CR'R")0-3OR', o la cadena lateral de cualquier aminoácido de origen natural; en los que R' y R'' son cada uno independientemente hidrógeno, un grupo alquilo C1-C5, alquenilo C2-C5, alquinilo C2-C5 o arilo.
El término "amina" o "amino" debe entenderse que se aplica ampliamente tanto a una molécula, como a una fracción o grupo funcional, como se entiende generalmente en la técnica, y puede ser primario, secundario o terciario. El término "amina" o "amino" incluye compuestos en los que un átomo de nitrógeno está unido covalentemente a al menos un carbono, hidrógeno o heteroátomo. Los términos incluyen, por ejemplo, pero no se limitan a, "alquil amino", "arilamino", "diarilamino", "alquilarilamino", "alquilaminoarilo", "arilaminoalquilo", "alcaminoalquilo", "amida", "amido", y "aminocarbonilo". El término "alquilamino" comprende grupos y compuestos en los que el nitrógeno está unido a al menos un grupo alquilo adicional. El término "dialquil amino" incluye grupos en los que el átomo de nitrógeno está unido a al menos dos grupos alquilo adicionales. El término "arilamino" y "diarilamino" incluye grupos en los que el
nitrógeno está unido a al menos uno o dos grupos arilo, respectivamente. El término "alquilarilamino", "alquilaminoarilo" o "arilaminoalquilo" se refiere a un grupo amino que está unido a al menos un grupo alquilo y al menos un grupo arilo. El término "alcaminoalquilo" se refiere a un grupo alquilo, alquenilo o alquinilo unido a un átomo de nitrógeno que también está unido a un grupo alquilo.
El término "amida", "amido" o "aminocarbonilo" incluye compuestos o restos que contienen un átomo de nitrógeno que está unido al carbono de un grupo carbonilo o tiocarbonilo. El término incluye grupos "alcaminocarbonilo" o "alquilaminocarbonilo" que incluyen grupos alquilo, alquenilo, arilo o alquinilo unidos a un grupo amino unido a un grupo carbonilo. Incluye grupos arilaminocarbonilo y arilcarbonilamino que incluyen fracciones arilo o heteroarilo unidas a un grupo amino que está unido al carbono de un grupo carbonilo o tiocarbonilo. Los términos "alquilaminocarbonilo", "alquenilaminocarbonilo", "alquinilaminocarbonilo", "arilaminocarbonilo", "alquilcarbonilamino", "alquenilcarbonilamino", "alquinilcarbonilamino" y "arilcarbonilamino" se incluyen en el término "amida". Las amidas también incluyen grupos urea (aminocarbonilamino) y carbamatos (oxicarbonilamino).
En una realización particular de la invención, el término "amina" o "amino" se refiere a sustituyentes de las fórmulas N (R8)R9, CH2 N(R8)R9 y CH(CH3)N(R8)R9, en las que R8 y R9 se seleccionan cada una, independientemente, del grupo que consiste en H y (alquilo C1-C4)0-1G, en el que G se selecciona del grupo que consiste en COOH, H, PO3 H, SO3 H, Br, Cl, F, O-alquilo C1-4, S-alquilo C1-4, arilo, C(O)O-alquilo C1-C6 , C(O)-alquil-C1-C4-COOH, C(O)alquilo C1-C4 y C(O)-arilo.
Se observará que las estructuras de algunos de los compuestos de esta divulgación incluyen átomos de carbono asimétricos. En consecuencia, debe entenderse que los isómeros que surgen de tal asimetría (por ejemplo, todos los enantiómeros y diastereómeros) están incluidos dentro del alcance de esta invención. Dichos isómeros se pueden obtener en forma sustancialmente pura mediante técnicas de separación clásicas y mediante síntesis controlada estereoquímicamente. Además, las estructuras y otros compuestos y fracciones discutidos en esta solicitud también incluyen todos sus tautómeros. Los compuestos descritos en el presente documento se pueden obtener mediante estrategias de síntesis reconocidas en la técnica.
En una realización preferida, el inhibidor de IAP es LBW 242 (N-[1-ciclohexil-2-oxo-2-(6-fenetil-octahidro-pirrolo[2,3-c] piridin-1-il)-etil]-2-metilamino-propionamida):
Los siguientes representan compuestos que pueden usarse como inhibidores de IAP en la presente solicitud:
continuación
II. Propiedades inmunomoduladoras de los inhibidores de IAP
Para provocar una respuesta inmune en un sujeto, es común administrar un estímulo inmune, un inmunógeno o un antígeno en combinación con un adyuvante inmune. Un adyuvante es una sustancia que mejora una respuesta inmune a un estímulo inmune, inmunógeno o antígeno. De acuerdo con la presente invención, los inhibidores de IAP, incluidos los miméticos de Smac, son potentes adyuvantes inmunitarios. Los inhibidores de IAP son capaces de mejorar las señales de activación fisiológicamente relevantes en diversos linajes de células inmunes. Los inhibidores de IAP no alteran la función de las células inmunes en reposo, pero mejoran la activación de las células inmunes en el contexto de la estimulación. La activación de las células inmunes se evidencia, por ejemplo, por una mayor expansión, producción de citocinas y alteraciones en la expresión de los marcadores de la superficie celular. Los tipos de células que responden a los inhibidores de IAP incluyen, entre otros, células dendríticas, células B, células T (por ejemplo, Células T CD4+, células T CD8+ y células NKT), células NK y macrófagos, células plasmáticas e hibridomas.
El término "sujeto", como se usa en el presente documento, pretende incluir animales que son capaces de padecer o estar afectados por una enfermedad o trastorno, tal como cáncer, o que necesitan mejorar su respuesta inmune. Los ejemplos de sujetos incluyen mamíferos, por ejemplo, humanos, ratones, conejos, ratas, perros, vacas, caballos, cerdos, ovejas, cabras, gatos, burros y animales transgénicos no humanos. En ciertas realizaciones, el sujeto es un ser humano, por ejemplo, un ser humano que padece, corre el riesgo de padecer o es potencialmente capaz de padecer una enfermedad o trastorno, tal como cáncer, o que necesita mejorar su respuesta inmune.
El alcance de las señales inmunes potenciadas por los inhibidores de IAP excede el de los adyuvantes actualmente conocidos. Además, los inhibidores de IAP pueden estimular linajes más diversos de células inmunes que los adyuvantes actualmente conocidos. Estas propiedades posicionan a los inhibidores de IAP como agentes ideales para la promoción de la inmunidad. Al amplificar las señales inmunitarias débiles, los inhibidores de IAP pueden funcionar como adyuvantes de vacunas y, además, pueden usarse para mejorar la inmunidad a infecciones crónicas o tumores. Los inhibidores de IAP también son útiles en ciertas enfermedades autoinmunes en las que la estimulación inmunológica acelera la resolución de la enfermedad. En una realización particular, el inhibidor de iA p es un compuesto de Fórmula I o Fórmula II, tal como LBW 242 (N-[1-ciclohexil-2-oxo-2-(6-fenetil-octahidro-pirrolo[2,3-c] piridin-1 -il)-etil]-2-metilamino-propionamida). Las aplicaciones terapéuticas adicionales de los inhibidores de IAP se describen con mayor detalle a continuación.
III. Composiciones y métodos terapéuticos
(A) Adyuvantes y vacunas
Las propiedades inmunomoduladoras de los inhibidores de IAP hacen que los inhibidores de IAP sean adyuvantes ideales. Por consiguiente, la presente divulgación presenta un adyuvante inmunitario que comprende un inhibidor de IAP. Dichos adyuvantes inmunes se pueden administrar a un sujeto solos o en combinación con un antígeno o inmunógeno. El antígeno o inmunógeno puede ser una vacuna o un componente de una vacuna. La divulgación presenta además composiciones farmacéuticas que contienen un antígeno y un inhibidor de IAP. Además, la divulgación presenta vacunas que contienen un antígeno y un inhibidor de IAP.
La cantidad de un inhibidor de IAP proporcionada en tales composiciones farmacéuticas y/o vacunas, o administrada en combinación con un antígeno, es típicamente una cantidad mejoradora del sistema inmunológico. Una "cantidad mejoradora del sistema inmunológico" de un inhibidor de IAP como se usa en este documento se refiere a cualquier cantidad de un inhibidor de IAP capaz de estimular o mejorar cualquier indicador de respuesta inmunitaria. En ejemplos de realizaciones, la cantidad mejoradora de la inmunidad de un inhibidor de IAP es terapéuticamente eficaz para tratar o prevenir una enfermedad. La mejora de una respuesta inmune, como se usa en este documento, se refiere a la mejora de una respuesta inmune en relación con el nivel de respuesta inmune que ocurriría en ausencia de un inhibidor de IAP de la divulgación.
La cantidad de antígeno proporcionada en tales composiciones farmacéuticas y/o vacunas, o administrada en combinación con un inhibidor de IAP, es preferiblemente una cantidad inmunogénica. El antígeno puede ser inmunogénico cuando se administra solo, o puede ser inmunogénico solo cuando se administra en combinación con un adyuvante, por ejemplo, un inhibidor de iA p . La cantidad de antígeno es típicamente una cantidad que induce una respuesta inmune en un sujeto sin efectos secundarios adversos significativos. La cantidad de un antígeno que es inmunogénico cuando se administra solo puede reducirse cuando se administra en combinación con un adyuvante inmunológico de la divulgación, o cuando se administra como un componente de una composición farmacéutica o vacuna de la invención. Es deseable reducir la cantidad de antígeno requerida para estimular una respuesta inmune en un sujeto, ya que reduce la probabilidad de efectos secundarios no deseados asociados con algunos antígenos actualmente en uso.
Como se usa en este documento, el término "antígeno" se refiere a cualquier molécula o composición capaz de estimular o mejorar cualquier indicador de respuesta inmune. Los indicadores de una respuesta inmune incluyen, pero no se limitan a, cualquiera de las siguientes actividades inmunes: producción de citocinas, producción de anticuerpos, activación de células inmunes, expansión de células inmunes, proliferación de células inmunes, citotoxicidad mediada por células inmunes y alteraciones en la expresión de marcadores de superficie de células inmunes. El término "antígeno" se usa indistintamente con el término "inmunógeno". Una "cantidad inmunogénica" de un antígeno como se usa en este documento se refiere a cualquier cantidad de un antígeno capaz de estimular o mejorar cualquier indicador de respuesta inmune.
La estimulación o mejora de una respuesta inmune se puede determinar usando cualquier método adecuado conocido en la técnica, incluyendo, pero no limitado a detectar cambios en la producción de citocinas, producción de anticuerpos, activación de células inmunes, expansión de células inmunes, citotoxicidad mediada por células inmunes y alteraciones en la expresión de marcadores de superficie de células inmunes. Las células inmunes capaces de una respuesta inmunitaria incluyen, pero no se limitan a, células dendríticas, células B, células T (por ejemplo, células T CD4+, células T CD8 + y células NKT), células NK, macrófagos, células plasmáticas e hibridomas.
El término "vacuna", como se usa en este documento, se refiere ampliamente a cualquier preparación de material antigénico usado para inducir inmunidad.
(B) Métodos para mejorar una respuesta inmune
La presente divulgación proporciona un método para mejorar una respuesta inmune en un sujeto administrando al sujeto un inhibidor de IAP. Dicha respuesta inmune está mediada típicamente por uno o más tipos de células inmunes, incluidas, entre otras, células dendríticas, células B, células T (por ejemplo, células T CD4+, células T CD8 + y células NKT), células NK, macrófagos, células plasmáticas e hibridomas. Este método puede implicar la selección de un sujeto que necesite una respuesta inmune mejorada. Un sujeto seleccionado para este método de mejorar una respuesta inmune puede ser un sujeto que exhibe un nivel bajo de respuesta inmune a un antígeno, por ejemplo, un antígeno tumoral o un antígeno viral.
La presente divulgación proporciona además un método para mejorar una respuesta inmune de un sujeto a un antígeno administrando al sujeto un antígeno en combinación con un inhibidor de IAP. En una realización particular, el inhibidor de IAP es un compuesto de Fórmula I o Fórmula II, tal como LBW 242 (N-[1-ciclohexil-2-oxo-2-(6-fenetiloctahidro-pirrolo[2,3-c]piridin-1-il)-etil]-2-metilaminopropionamida). El antígeno puede ser inmunogénico cuando se administra solo, o puede ser inmunogénico solo cuando se administra en combinación con un adyuvante, por ejemplo, un inhibidor de IAP. Dicha respuesta inmune está mediada típicamente por uno o más tipos de células inmunes, incluidas, entre otras, células dendríticas, células B, células T (por ejemplo, células T CD4+, células T CD8 + y células NKT), células NK, macrófagos, células plasmáticas e hibridomas. El antígeno y el inhibidor de IAP pueden administrarse en composiciones separadas o pueden ser componentes de una única composición. En el caso de que el antígeno y el inhibidor de IAP se administren como composiciones separadas, las composiciones pueden administrarse simultánea o secuencialmente. El antígeno y/o el inhibidor de IAP se pueden administrar como dosis única o como dosis múltiples.
Los antígenos adecuados para su uso en la práctica de la invención incluyen, pero no se limitan a, antígenos de mamíferos, antígenos de plantas, antígenos tumorales, antígenos microbianos, antígenos virales y antígenos fúngicos. Estos antígenos pueden aislarse o purificarse de otro modo, o pueden estar presentes en una mezcla de otros compuestos. Los antígenos adecuados incluyen, por ejemplo, proteínas de mamíferos, proteínas vegetales, proteínas tumorales, proteínas microbianas, proteínas virales y proteínas fúngicas. Los antígenos adecuados también incluyen células o fragmentos de células vivas, atenuadas o muertas, incluidas células tumorales, células microbianas, células infectadas con un virus y células fúngicas. Los antígenos adecuados adicionales incluyen moléculas de ácido nucleico (por ejemplo, ADN, ARN, etc.) capaces de inducir una respuesta inmune.
(C) Métodos de tratamiento del cáncer
El término "tratado", "tratar' o "tratamiento" incluye la disminución o alivio de al menos un síntoma asociado con la afección que se está tratando. Por ejemplo, el tratamiento puede ser la disminución de uno o varios síntomas de un trastorno o la erradicación completa de un trastorno, tal como el cáncer.
La respuesta del sistema inmunológico a las células cancerosas y los antígenos tumorales es generalmente baja, lo que hace que la vacunación sea un enfoque problemático en el tratamiento del cáncer. La potencia y el alcance de las señales inmunes mejoradas por los inhibidores de IAP (por ejemplo, compuestos de Fórmula I o Fórmula II) hacen que los inhibidores de IAP (y adyuvantes, composiciones y vacunas que los comprenden) sean particularmente útiles para mejorar la respuesta inmunitaria al cáncer. Las vacunas contra el cáncer que contienen o coadministradas con inhibidores de IAP son, por lo tanto, ventajosas para tratar y/o prevenir el cáncer. En consecuencia, la divulgación proporciona métodos para tratar o reducir los síntomas del cáncer en un sujeto, administrando a un sujeto que tiene cáncer una cantidad terapéuticamente eficaz de un inhibidor de IAP y un antígeno, en el que el inhibidor de IAP y el antígeno mejoran la respuesta inmune del sujeto al cáncer de tal manera que se trate el cáncer. La divulgación proporciona además métodos para prevenir el cáncer en un sujeto, administrando a un sujeto con riesgo de desarrollar un cáncer una cantidad terapéuticamente eficaz de un inhibidor de IAP y un antígeno, de manera que se mejore la respuesta inmune del sujeto al antígeno, y de manera que se previene el desarrollo de cáncer en el sujeto. El antígeno puede ser inmunogénico cuando se administra solo, o puede ser inmunogénico solo cuando se administra en combinación con un adyuvante, por ejemplo, un inhibidor de IAP. Dicha respuesta inmune está mediada típicamente por uno o más tipos de células inmunes, incluidas, entre otras, células dendríticas, células B, células T (por ejemplo, células T CD4+, células T CD8 + y células NKT), células NK, macrófagos, células plasmáticas e hibridomas. El antígeno y el inhibidor de IAP pueden administrarse en composiciones separadas o pueden ser componentes de una única composición. En el caso de que el antígeno y el inhibidor de IAP se administren como composiciones separadas, las composiciones pueden administrarse simultánea o secuencialmente. El antígeno y/o el inhibidor de IAP se pueden administrar como dosis única o como dosis múltiples.
Los antígenos adecuados para su uso en los métodos anteriores para tratar o reducir los síntomas del cáncer en un sujeto incluyen cualquier antígeno asociado con el cáncer del sujeto. Tal antígeno puede estar presente en células cancerosas y ausente en células no cancerosas. Alternativamente, dicho antígeno puede estar presente a niveles elevados en las células cancerosas en relación con las células no cancerosas. Los antígenos expresados
diferencialmente se pueden identificar usando cualquier técnica adecuada conocida en la técnica, que incluye, entre otros, transferencia Northern, transferencia Western, RT-PCR cuantitativa, hibridación in situ, análisis de micromatrices de oligonucleótidos, análisis de matrices de anticuerpos, presentación diferencial, hibridación sustractiva y análisis en serie de la expresión génica (SAGE). En un ejemplo de realización, el antígeno es un antígeno de superficie celular. El antígeno puede ser un antígeno que se sabe que se expresa diferencialmente en células cancerosas con respecto a células no cancerosas. Alternativamente, el antígeno puede identificarse mediante la comparación de una célula cancerosa o una muestra celular obtenida del sujeto que tiene cáncer con una célula normal o una muestra celular obtenida de un sujeto. Los antígenos pueden aislarse o bien purificarse, o pueden estar presentes como componentes de una mezcla.
Los antígenos adecuados también incluyen células cancerosas vivas, muertas o atenuadas o fragmentos de células cancerosas. Las células cancerosas pueden irradiarse o tratarse de otro modo antes de su uso como antígeno de manera que no sean capaces de proliferar. Las células también pueden romperse, cortarse, sonicarse o lisarse antes de su uso como antígeno. En una realización preferida, las células cancerosas utilizadas como antígeno son células autólogas obtenidas de un sujeto al que se administrará el antígeno de acuerdo con los métodos descritos en el presente documento. En otra realización, las células cancerosas utilizadas como antígeno son células alogénicas.
Los antígenos adecuados para uso en los métodos anteriores para prevenir el cáncer en un sujeto incluyen cualquier antígeno que se sabe que está presente con frecuencia en un tipo particular de célula cancerosa y que está ausente de las células no cancerosas, o cualquier antígeno que se sabe que está presente con frecuencia a niveles elevados en las células cancerosas con respecto a las células no cancerosas. Dichos antígenos incluyen, entre otros, mucina-1 (MUC-1), antígeno prostático específico (PSA), antígeno carcinoembrionario (CEA), fosfatasa ácida prostática (PAP) y miembros de la familia de genes del antígeno del melanoma (MAGE). Se sabe que la infección por ciertos virus aumenta la probabilidad de que un sujeto desarrolle cáncer. Los antígenos asociados con dichos virus también son adecuados para su uso en los métodos anteriores para prevenir el cáncer. Dichos antígenos pueden aislarse o purificarse de otro modo, o pueden incluir todas o una parte de las partículas virales vivas, muertas o atenuadas. Los virus asociados con el aumento de la susceptibilidad de un sujeto al cáncer incluyen, entre otros, virus del papiloma humano (VPH), hepatitis B, hepatitis C, virus del herpes, virus de Epstein-Barr, virus linfotrópico de células T humanas y VIH-1. La mejora de la respuesta inmune de un sujeto a los antígenos anteriores permite al sujeto resistir el desafío posterior con un virus o célula cancerosa que contiene el antígeno y, por consiguiente, evita que el sujeto desarrolle un cáncer.
Se conocen en la técnica métodos adecuados para evaluar la mejora de una respuesta inmune, incluida una respuesta inmune a un cáncer. Dichos métodos incluyen, entre otros, título de anticuerpos, medición de la producción de citocinas, ensayo de dilución limitante, ELISA (para medir la producción de citocinas), ensayos de tetrámeros, inmunofenotipificación usando, por ejemplo, el ensayo FastImmuneMR (BD Biosciences, Franklin Lakes, NJ ) y ensayos de puntos inmunoabsorbentes ligados a enzimas (ELISPOT). Los criterios de valoración clínicos útiles para medir la respuesta al tratamiento del cáncer también se conocen en la técnica e incluyen, pero no se limitan a, la reducción del volumen del tumor, la supervivencia global, la supervivencia libre de enfermedad y el tiempo hasta la progresión de la enfermedad.
Debido a que los inhibidores de IAP de la divulgación mejoran ampliamente la respuesta inmune, los métodos anteriores son útiles para tratar un amplio espectro de tumores, incluidos todos los tumores sólidos y neoplasias malignas hematológicas. Los ejemplos de tales tumores incluyen, pero no se limitan a, leucemias, linfomas, mielomas, carcinomas, carcinomas metastásicos, sarcomas, adenomas, cánceres del sistema nervioso y cánceres genitourinarios. En ejemplos de realizaciones, los métodos anteriores son útiles en el tratamiento de leucemia linfoblástica aguda pediátrica y adulta, leucemia mieloide aguda, carcinoma adrenocortical, cánceres relacionados con el SIDA, cáncer anal, cáncer de apéndice, astrocitoma, carcinoma de células basales, cáncer de vías biliares, cáncer de vejiga, cáncer de hueso, osteosarcoma, histiocitoma fibroso, cáncer de cerebro, glioma de tronco encefálico, astrocitoma cerebeloso, glioma maligno, ependimoma, meduloblastoma, tumores neuroectodérmicos primitivos supratentoriales, glioma hipotalámico, cáncer de mama, cáncer de mama masculino, adenomas bronquiales, linfoma de Burkitt, tumor carcinoide, carcinoma de origen desconocido, linfoma del sistema nervioso central, astrocitoma cerebeloso, glioma maligno, cáncer de cuello uterino, cánceres infantiles, leucemia linfocítica crónica, leucemia mielógena crónica, trastornos mieloproliferativos crónicos, cáncer colorrectal, linfoma cutáneo de células T, cáncer de endometrio, ependimoma, cáncer de esófago, tumores de la familia Ewing, tumor extracraneal de células germinales, tumor extragonadal de células germinales, cáncer de vías biliares extrahepáticas, melanoma intraocular, retinoblastoma, cáncer de vesícula biliar, cáncer gástrico, tumor del estroma gastrointestinal, tumor extracraneal de células germinales, tumor extragonadal de células germinales, tumor ovárico de células germinales, tumor trofoblástico gestacional, glioma, leucemia de células pilosas, cáncer de cabeza y cuello, cáncer hepatocelular, linfoma de Hodgkin, linfoma no Hodgkin, cáncer de hipofaringe, glioma hipotalámico y de las vías visuales, melanoma intraocular, tumores de células de los islotes, sarcoma de Kaposi, cáncer de riñón, cáncer de células renales, cáncer de laringe, cáncer de labio y cavidad oral, cáncer de pulmón de células pequeñas, cáncer de pulmón de células no pequeñas, linfoma primario del sistema nervioso central, macroglobulinemia de Waldenstrom, histiocitoma fibroso maligno, meduloblastoma, melanoma, carcinoma de células de Merkel, mesotelioma maligno, cáncer escamoso de cuello, síndrome de neoplasia endocrina múltiple, mieloma múltiple, micosis fungoide, síndromes mielodisplásicos, trastornos mieloproliferativos, trastornos mieloproliferativos crónicos, cáncer de cavidad nasal y de seno paranasal, cáncer de
nasofaringe, neuroblastoma, cáncer de orofaringe, cáncer de ovario, cáncer de páncreas, cáncer de paratiroides, cáncer de pene, cáncer de faringe, feocromocitoma, pineoblastoma y tumores neuroectodérmicos primitivos supratentoriales, cáncer de pituitaria, neoplasias de células plasmáticas, blastoma pleuropulmonar, cáncer de próstata, cáncer de recto, rabdomiosarcoma, cáncer de glándulas salivales, sarcoma de tejidos blandos, sarcoma uterino, síndrome de Sezary, cáncer de piel no melanoma, cáncer de intestino delgado, carcinoma de células escamosas, cáncer escamoso de cuello, tumores neuroectodérmicos primitivos supratentoriales, cáncer testicular, cáncer de garganta, timoma y carcinoma tímico, cáncer de tiroides, cáncer de células de transición, tumores trofoblásticos, cáncer de uretra, cáncer de útero, sarcoma de útero, cáncer de vagina, cáncer de vulva y tumor de Wilms.
También se proporcionan métodos para tratar el cáncer ex vivo. De acuerdo con estos métodos, se aísla una población de células inmunes de un sujeto que tiene cáncer, y las células inmunes se estimulan con un antígeno y una cantidad terapéuticamente eficaz de un inhibidor de IAP, de modo que las células inmunes se activan contra el antígeno. A continuación, las células inmunes se devuelven al sujeto. A continuación, dichas células inmunes mejoran la respuesta inmunitaria de un sujeto contra el cáncer del sujeto. Los antígenos adecuados para los métodos de tratamiento, prevención o reducción de los síntomas del cáncer en un sujeto como se describió anteriormente son igualmente adecuados para los métodos de tratamiento del cáncer ex vivo. Varios protocolos de tratamiento experimental conocidos en la técnica implican la activación y expansión ex vivo de células T específicas de antígeno y la transferencia adoptiva de estas células a receptores para proporcionar células T específicas de antígeno contra el tumor de un receptor (véase, por ejemplo, Greenberg, R. y Riddell, S. (1999) Science 285: 546-551). Estos métodos también pueden usarse para activar respuestas de células T contra agentes infecciosos, incluidos agentes infecciosos que aumentan la probabilidad de que un sujeto desarrolle cáncer, como se describe en el presente documento. La activación ex vivo en presencia de un inhibidor de IAP de la divulgación puede aumentar la frecuencia y actividad de las células T transferidas adoptivamente. También se contempla el uso de inhibidores de IAP para mejorar la maduración de células dendríticas durante la producción de una vacuna de células dendríticas.
(D) Métodos para tratar o prevenir enfermedades infecciosas
La potencia y el alcance de las señales inmunes potenciadas por los inhibidores de IAP (por ejemplo, compuestos de Fórmula I o Fórmula II) hacen que los inhibidores de IAP (y adyuvantes, composiciones y vacunas que comprenden los mismos) sean particularmente útiles para mejorar la respuesta inmune de un sujeto a un agente infeccioso. Los inhibidores de IAP se pueden incorporar o administrar en combinación con vacunas, mejorando la inmunogenicidad del antígeno de la vacuna. Por lo tanto, las vacunas que contienen o se administran en combinación con inhibidores de IAP son útiles para prevenir la infección causada por un agente infeccioso, y son además útiles en el tratamiento de tales infecciones si se administran después de que ha ocurrido la infección. Por consiguiente, la divulgación presenta métodos para tratar una infección causada por un agente infeccioso, mediante la administración a un sujeto de una cantidad terapéuticamente eficaz de un inhibidor de IAP y un antígeno, en el que el inhibidor de IAP y el antígeno mejoran la respuesta inmune del sujeto al agente infeccioso, de modo que se trate la infección. La divulgación también presenta métodos para prevenir una infección causada por un agente infeccioso, mediante la administración a un sujeto de una cantidad terapéuticamente eficaz de un inhibidor de IAP y un antígeno, en el que el inhibidor de IAP y el antígeno mejoran la respuesta inmune del sujeto al agente infeccioso, de manera que se prevenga la infección. Dicha respuesta inmunitaria está mediada típicamente por uno o más tipos de células inmunes, que incluyen, entre otros, células dendríticas, células B, células T (por ejemplo, células T c D4+, células T CD8+ y células NKT), células NK, macrófagos, y células plasmáticas. El antígeno y el inhibidor de IAP pueden administrarse en composiciones separadas o pueden ser componentes de una única composición. En el caso de que el antígeno y el inhibidor de IAP se administren como composiciones separadas, las composiciones pueden administrarse simultánea o secuencialmente. El antígeno y/o el inhibidor de IAP se pueden administrar como dosis única o como dosis múltiples.
Las enfermedades infecciosas que se pueden tratar o prevenir usando los métodos anteriores incluyen, pero no se limitan a, enfermedades infecciosas causadas por agentes infecciosos tales como bacterias, virus, protozoos, hongos y parásitos. Los antígenos adecuados incluyen cualquier antígeno asociado con un agente infeccioso. Los antígenos pueden aislarse o bien purificarse, o pueden estar presentes como componentes de una mezcla. Los antígenos adecuados también incluyen partículas de agentes infecciosos completas, vivas, muertas o atenuadas, por ejemplo, células bacterianas, virus, protozoos, hongos o parásitos, o fragmentos de los mismos. Estos agentes infecciosos pueden irradiarse o bien tratarse antes de su uso como antígeno de modo que sean incompetentes para la proliferación, incompetentes para la replicación o bien incapaces de producir una infección activa. Los agentes infecciosos también pueden romperse, cortarse, someterse a ultrasonidos o lisarse antes de su uso como antígeno.
Los métodos adecuados para evaluar la mejora de una respuesta inmune a un antígeno son conocidos en la técnica e incluyen, por ejemplo, título de anticuerpo, ensayo de dilución limitante, ELISA (para medir la producción de citocinas), ensayos de tetrámeros, inmunofenotipificación usando, por ejemplo, el ensayo FastImmuneMR (BD Biosciences, Franklin Lakes, NJ) y los ensayos de puntos inmunoabsorbentes ligados a enzimas (ELISPOT). Los criterios de valoración clínicos útiles para medir la respuesta al tratamiento de un agente infeccioso también se conocen en la técnica e incluyen, pero no se limitan a, reducción del título bacteriano, reducción del título viral y mejora de los síntomas asociados con una enfermedad infecciosa.
(E) Métodos para mejorar la proliferación de células inmunes y/o la secreción de citocinas
La activación inmune induce la proliferación y expansión de linajes de células inmunes. Al mejorar la activación de las células inmunes, los inhibidores de IAP de la divulgación (por ejemplo, compuestos de Fórmula I o Fórmula II) aumentan la proliferación y expansión de una amplia gama de células inmunes, incluidas, entre otras, células dendríticas, células B, células T (por ejemplo, células T CD4+, células T CD8 + y células NKT), células NK y macrófagos. Por consiguiente, la divulgación presenta métodos para mejorar la proliferación de células inmunes poniendo en contacto una población celular que incluye una célula inmunitaria con un inhibidor de IAP. En una realización preferida, las células se ponen en contacto con estímulos de activación inmunitaria adicionales en combinación con un inhibidor de IAP para mejorar la proliferación de células inmunes. En esta realización, las células que se ponen en contacto con un inhibidor de IAP y los estímulos de activación inmunitaria adicionales demuestran una mayor expansión de la que tendrían de otra manera cuando se contactan con estímulos de activación inmunitaria en ausencia de un inhibidor de IAP. Los estímulos que inician la activación inmune son conocidos en la técnica e incluyen, pero no se limitan a, a-galcer, anti-CD3, anti-CD28, anti-IgM y anti-CD40. Se describen estímulos inmunes adicionales en, por ejemplo, Advanced Methods in Cellular Immunology, Fernandez-Botran et al., CRC; Spi Edition (26 de mayo de 2 0 0 0 ).
La activación inmunitaria también induce la expresión y secreción de citocinas en las células inmunes. Al mejorar la activación de las células inmunes, los inhibidores de IAP de la divulgación aumentan la producción y secreción de citocinas en las células inmunes. Dichas citocinas incluyen, entre otras, IFN-y, IFN-a, IL-2, IL-4, IL-6 , IL-8 , IL-10, IL-12, TNFa, TNFp, TGFp y GM-CSF. Por consiguiente, la divulgación presenta métodos para mejorar la producción de citocinas poniendo en contacto una población celular que incluye una célula inmune con un inhibidor de IAP. En una realización preferida, las células se ponen en contacto con estímulos de activación inmunitaria adicionales en combinación con un inhibidor de IAP para mejorar la producción de citocinas. En esta realización, las células que se ponen en contacto con un inhibidor de IAP y los estímulos de activación inmunitaria adicionales demuestran una mayor producción de citocinas de lo que lo harían de otro modo cuando se contactan con estímulos de activación inmunitaria en ausencia de un inhibidor de IAP. Los estímulos que inician la activación inmune se conocen en la técnica e incluyen, pero no se limitan a, a-galcer, anti-CD3, anti-CD28, anti-IgM, y anti-CD40. Se describen estímulos inmunes adicionales en, por ejemplo, Advanced Methods in Cellular Immunology, Femandez-Botran et al., CRC; SPI Edition (26 de mayo de 2 0 0 0 ), como se indicó anteriormente.
(F) Métodos para mejorar la producción de anticuerpos
Muchos antígenos comercialmente importantes son poco inmunogénicos, y tradicionalmente ha sido difícil obtener anticuerpos que reconozcan tales antígenos. La capacidad de los inhibidores de IAP de la divulgación para funcionar como potentes adyuvantes inmunitarios hace que los inhibidores de IAP sean particularmente adecuados para mejorar la eficacia de la producción de anticuerpos policlonales y/o monoclonales. Los inhibidores de IAP son especialmente útiles para producir anticuerpos que reconocen antígenos poco inmunogénicos. Por consiguiente, la divulgación presenta métodos para mejorar la producción de anticuerpos inmunizando a un mamífero con un antígeno y un inhibidor de IAP. Los métodos conocidos en la técnica útiles para aislar anticuerpos monoclonales y/o policlonales después de la inmunización son adecuados para poner en práctica la invención. Se produce un mayor número de hibridomas que reconocen el antígeno cuando se aíslan anticuerpos monoclonales de animales inmunizados con un antígeno y un inhibidor de IAP que el que se produciría de otro modo cuando se aíslan anticuerpos monoclonales de animales inmunizados con antígeno solo. Asimismo, la reactividad de los anticuerpos policlonales aislados del antisuero de animales inmunizados con un antígeno y un inhibidor de IAP es mayor que la de los anticuerpos policlonales aislados del antisuero de animales inmunizados con antígeno solo. Por consiguiente, el uso de un inhibidor de IAP para mejorar la producción de anticuerpos monoclonales y/o policlonales puede mejorar la eficiencia de la producción de anticuerpos en los sectores comerciales. Tras el aislamiento de un hibridoma que produce un anticuerpo de interés, la producción de anticuerpos puede mejorarse poniendo en contacto el hibridoma con un inhibidor de IAP. Por consiguiente, los inhibidores de IAP son útiles para aumentar la producción de anticuerpos monoclonales a partir de hibridomas. En una realización particular, el inhibidor de IAP es un compuesto de Fórmula I o Fórmula II, tal como LBW 242 (N[1-ciclohexil-2-oxo-2-(6-fenetil-octahidro-pirrolo[2,3-c]piridin-1-il)-etil]-2-metilamino-propionamida).
(G) Formulaciones y métodos de administración
Composiciones farmacéuticas
La presente invención también proporciona composiciones farmacéuticas. Dichas composiciones comprenden un adyuvante que comprende un compuesto inhibidor de IAP de Fórmula II, un vehículo farmacéuticamente aceptable y una cantidad inmunogénica de un antígeno que comprende un antígeno presente en una célula de cáncer, una célula cancerosa, un fragmento de célula cancerosa, un antígeno tumoral, a-galcer, anti-CD3, anti-CD28, anti-IgM, anti-CD40, un patógeno, un patógeno atenuado o una porción del mismo. Los vehículos farmacéuticamente aceptables adecuados incluyen, pero no se limitan a, solución salina, solución salina tamponada, dextrosa, agua, glicerol, etanol y combinaciones de los mismos. El portador y la composición pueden ser estériles. La formulación debe adaptarse al modo de administración.
La frase "portador farmacéuticamente aceptable" es reconocida en la técnica e incluye un material, composición o vehículo farmacéuticamente aceptable, adecuado para administrar compuestos de la presente divulgación a mamíferos. Los portadores pueden incluir un relleno líquido sólido, diluyente, excipiente, disolvente o material de
encapsulación, implicados en el porte o transporte del agente objetivo desde un órgano, o parte del cuerpo, a otro órgano o parte del cuerpo. Cada portador debe ser "aceptable" en el sentido de ser compatible con los demás ingredientes de la formulación y no perjudicial para el sujeto. Algunos ejemplos de materiales que pueden servir como portadores farmacéuticamente aceptables incluyen: azúcares, tales como lactosa, glucosa, dextrosa y sacarosa; almidones, tales como almidón de maíz y almidón de patata; celulosa y sus derivados, tales como carboximetilcelulosa de sodio, etilcelulosa, metilcelulosa y acetato de celulosa; tragacanto en polvo; malta; gelatina; talco; excipientes, tal como manteca de cacao y ceras para supositorios; aceites, tales como aceite de cacahuete, aceite de semilla de algodón, aceite de cártamo, aceite de sésamo, aceite de oliva, aceite de maíz, aceite de ricino, tetraglicol y aceite de soja; glicoles, tales como propilenglicol; polioles, tales como glicerina, sorbitol, manitol y polietilenglicol; ésteres, tales como oleato de etilo, ésteres de polietilenglicol y laurato de etilo; agar; agentes tamponadores, tales como hidróxido de magnesio, hidróxido de sodio, hidróxido de potasio, carbonatos, trietanolamina, acetatos, lactatos, citrato de potasio e hidróxido de aluminio; ácido algínico; agua libre de pirógenos; solución salina isotónica; solución de Ringer; alcohol etílico; soluciones tampón de fosfato; y otras sustancias compatibles no tóxicas empleadas en formulaciones farmacéuticas.
También pueden estar presentes en las composiciones agentes humectantes, emulsionantes y lubricantes, tales como lauril sulfato de sodio y estearato de magnesio, así como agentes colorantes, agentes de liberación, agentes de recubrimiento, agentes edulcorantes, saborizantes y perfumantes, conservantes y antioxidantes.
Los ejemplos de antioxidantes farmacéuticamente aceptables incluyen: antioxidantes solubles en agua, tales como ácido ascórbico, clorhidrato de cisteína, bisulfato de sodio, metabisulfito de sodio, sulfito de sodio y similares; antioxidantes solubles en aceite, tales como palmitato de ascorbilo, hidroxianisol butilado (BHA), hidroxitolueno butilado (BHT), lecitina, galato de propilo, a-tocoferol y derivados tales como vitamina E tocoferol y similares; y agentes quelantes de metales, tales como ácido cítrico, ácido etilendiaminotetraacético (EDTA), sorbitol, ácido tartárico, ácido fosfórico, citrato de sodio y similares.
Los vehículos farmacéuticamente aceptables adecuados incluyen pero no se limitan a agua, soluciones salinas (por ejemplo, NaCl), alcoholes, goma arábiga, aceites vegetales, alcoholes bencílicos, polietilenglicoles, gelatina, carbohidratos tales como lactosa, amilosa o almidón, ciclodextrina, estearato de magnesio, talco, ácido silícico, parafina viscosa, aceite de perfume, ésteres de ácidos grasos, hidroximetilcelulosa, polivinilpirrolidona, etc. Las preparaciones farmacéuticas se pueden esterilizar y, si se desea, mezclar con agentes auxiliares, por ejemplo, lubricantes, conservantes, estabilizadores, agentes humectantes, emulsionantes, sales para influir en la presión osmótica, tampones, sustancias colorantes, saborizantes y/o aromáticas y similares que no reaccionen perjudicialmente con los compuestos activos. Los vehículos farmacéuticamente aceptables también pueden incluir un agente de ajuste de la tonicidad tal como dextrosa, glicerina, manitol y cloruro de sodio.
La composición, si se desea, también puede contener cantidades menores de agentes humectantes o emulsionantes, o agentes tamponadores del pH. La composición puede ser una solución líquida, suspensión, emulsión, tableta, píldora, cápsula, formulación de liberación sostenida o polvo. La composición se puede formular como supositorio, con aglutinantes y vehículos tradicionales como los triglicéridos. La formulación oral puede incluir vehículos estándar tales como grados farmacéuticos de manitol, lactosa, almidón, estearato de magnesio, polivinilpirrolidona, sacarina de sodio, celulosa, carbonato de magnesio, etc.
La composición se puede formular de acuerdo con los procedimientos de rutina como una composición farmacéutica adaptada para la administración oral, subcutánea o intravenosa a seres humanos. Normalmente, las composiciones para administración subcutánea o intravenosa son soluciones en tampón acuoso isotónico estéril. Cuando sea necesario, la composición también puede incluir un agente solubilizante y un anestésico local para aliviar el dolor en el lugar de la inyección. Generalmente, los ingredientes se suministran por separado o mezclados juntos en forma de dosificación unitaria, por ejemplo, como un polvo liofilizado seco o concentrado libre de agua en un recipiente herméticamente cerrado tal como una ampolla o sobre que indica la cantidad de agente activo. Cuando la composición deba administrarse por infusión, se puede dispensar con una botella de infusión que contenga agua de calidad farmacéutica estéril, solución salina o dextrosa/agua. Cuando la composición se administra mediante inyección, se puede proporcionar una ampolla de agua estéril para inyección o solución salina para que los ingredientes se puedan mezclar antes de la administración.
Las formulaciones de la presente invención incluyen aquellas adecuadas para administración subcutánea, intravenosa, oral, nasal, tópica, de membranas mucosas, transdérmica, bucal, sublingual, rectal, vaginal y/o parenteral. Las formulaciones se pueden presentar convenientemente en forma de dosificación unitaria y se pueden preparar mediante cualquier método bien conocido en la técnica de la farmacia. La cantidad de ingrediente activo que se puede combinar con un material portador para producir una única forma de dosificación será generalmente la cantidad del compuesto que produce un efecto terapéutico. Generalmente, de un cien por ciento, esta cantidad variará de aproximadamente un 1 por ciento a aproximadamente un 99 por ciento de ingrediente activo, preferiblemente de aproximadamente un 5 por ciento a aproximadamente un 70 por ciento, lo más preferiblemente de aproximadamente un 10 por ciento a aproximadamente un 30 por ciento.
Los métodos para preparar estas formulaciones o composiciones incluyen la etapa de asociar un compuesto de la presente divulgación con el vehículo y, opcionalmente, uno o más ingredientes accesorios. En general, las formulaciones se preparan asociando uniforme e íntimamente un compuesto de la presente divulgación con vehículos líquidos, o vehículos sólidos finamente divididos, o ambos, y luego, si es necesario, dando forma al producto.
Las formulaciones de la invención adecuadas para la administración oral pueden estar en forma de cápsulas, cápsulas lisas, píldoras, tabletas, pastillas (usando una base saborizada, usualmente sacarosa y goma arábiga o tragacanto), polvos, gránulos o como una solución o un suspensión en un líquido acuoso o no acuoso, o como una emulsión líquida de aceite en agua o agua en aceite, o como un elixir o jarabe, o como pastillas (usando una base inerte, tal como gelatina y glicerina, o sacarosa y goma arábiga) y/o como enjuagues bucales y similares, cada uno de los cuales contiene una cantidad predeterminada de un compuesto de la presente divulgación como ingrediente activo. Un compuesto de la presente divulgación también se puede administrar como un bolo, electuario o pasta.
En las formas de dosificación sólidas de la invención para administración oral (cápsulas, tabletas, píldoras, grageas, polvos, gránulos y similares), el ingrediente activo se mezcla con uno o más vehículos farmacéuticamente aceptables, tales como citrato de sodio o fosfato dicálcico y/o cualquiera de los siguientes: rellenos o extensores, tales como almidones, lactosa, sacarosa, glucosa, manitol y/o ácido silícico; aglutinantes, tales como por ejemplo carboximetilcelulosa, alginatos, gelatina, polivinilpirrolidona, sacarosa y/o goma arábiga; humectantes, tales como glicerol; agentes desintegrantes, tales como agar-agar, carbonato de calcio, almidón de patata o tapioca, ácido algínico, ciertos silicatos y carbonato de sodio; agentes retardadores de la solución, tal como parafina; aceleradores de la absorción, tales como compuestos de amonio cuaternario; agentes humectantes, tales como, por ejemplo, alcohol cetílico y monoestearato de glicerol; absorbentes, tales como caolín y arcilla bentonita; lubricantes, tales como talco, estearato de calcio, estearato de magnesio, polietilenglicoles sólidos, lauril sulfato de sodio y mezclas de los mismos; y agentes colorantes. En el caso de cápsulas, tabletas y píldoras, las composiciones farmacéuticas también pueden comprender agentes tamponantes. También se pueden emplear composiciones sólidas de un tipo similar tales como rellenos en cápsulas de gelatina rellenas blandas y duras usando excipientes tales como lactosa o azúcares de la leche, así como polietilenglicoles de alto peso molecular y similares.
Se puede preparar una tableta por compresión o moldeo, opcionalmente con uno o más ingredientes accesorios. Las tabletas comprimidas se pueden preparar usando aglutinante (por ejemplo, gelatina o hidroxipropilmetilcelulosa), lubricante, diluyente inerte, conservante, desintegrante (por ejemplo, glicolato de almidón sódico o carboximetilcelulosa de sodio entrecruzada), agente tensoactivo o dispersante. Las tabletas moldeadas se pueden preparar moldeando en una máquina adecuada una mezcla del compuesto en polvo humedecido con un diluyente líquido inerte.
Las tabletas y otras formas de dosificación sólidas de las composiciones farmacéuticas de la presente invención, tales como grageas, cápsulas, píldoras y gránulos, se pueden marcar o preparar opcionalmente con recubrimientos y capas, tales como recubrimientos entéricos y otros recubrimientos bien conocidos en la técnica de formulación farmacéutica. También se pueden formular para proporcionar una liberación lenta o controlada del ingrediente activo en ellos usando, por ejemplo, hidroxipropilmetilcelulosa en proporciones variables para proporcionar el perfil de liberación deseado, otras matrices poliméricas, liposomas y/o microesferas. Pueden esterilizarse, por ejemplo, mediante filtración a través de un filtro de retención de bacterias o incorporando agentes esterilizantes en forma de composiciones sólidas estériles que se pueden disolver en agua estéril o algún otro medio inyectable estéril inmediatamente antes de su uso. Estas composiciones también pueden contener opcionalmente agentes opacificantes y pueden ser de una composición que liberen el ingrediente o ingredientes activos solo, o preferentemente, en una cierta porción del tracto gastrointestinal, opcionalmente, de manera retardada. Los ejemplos de composiciones de inclusión que pueden usarse incluyen sustancias poliméricas y ceras. El ingrediente activo también puede estar en forma microencapsulada, si es apropiado, con uno o más de los excipientes descritos anteriormente.
Las formas de dosificación líquidas para la administración oral de los compuestos de la divulgación incluyen emulsiones, microemulsiones, soluciones, suspensiones, jarabes y elixires farmacéuticamente aceptables. Además del ingrediente activo, las formas de dosificación líquidas pueden contener un diluyente inerte comúnmente utilizado en la técnica, tal como, por ejemplo, agua u otros disolventes, agentes solubilizantes y emulsionantes, como alcohol etílico, alcohol isopropílico, carbonato de etilo, acetato de etilo, alcohol bencílico, benzoato de bencilo, propilenglicol, 1,3-butilenglicol, aceites (en particular, aceites de semilla de algodón, maní, maíz, germen, oliva, ricino y sésamo), glicerol, alcohol tetrahidrofurílico, polietilenglicoles y ésteres de ácidos grasos de sorbitán y mezclas de los mismos.
Además de los diluyentes inertes, las composiciones orales también pueden incluir adyuvantes tales como agentes humectantes, agentes emulsionantes y de suspensión, agentes edulcorantes, saborizantes, colorantes, perfumantes y conservantes.
Las suspensiones, además de los compuestos activos, pueden contener agentes de suspensión como, por ejemplo, alcoholes isoestearílicos etoxilados, ésteres de polioxietilensorbitol y sorbitán, celulosa microcristalina, metahidróxido de aluminio, bentonita, agar-agar y tragacanto, y mezclas de los mismos.
Las formulaciones de las composiciones farmacéuticas de la invención para administración rectal o vaginal se pueden presentar como un supositorio, que se puede preparar mezclando uno o más compuestos de la divulgación con uno o más excipientes o vehículos no irritantes adecuados que comprenden, por ejemplo, manteca de cacao, polietilenglicol, una cera para supositorios o un salicilato, y que es sólida a temperatura ambiente, pero líquida a temperatura corporal y, por lo tanto, se derretirá en el recto o en la cavidad vaginal y liberará el compuesto activo.
Las formulaciones de la presente invención que son adecuadas para la administración vaginal también incluyen pesarios, tampones, cremas, geles, pastas, espumas o formulaciones en aerosol que contienen los vehículos que se sabe que son apropiados en la técnica.
Las formas de dosificación para la administración tópica o transdérmica de un compuesto de esta divulgación incluyen polvos, aerosoles, ungüentos, pastas, cremas, lociones, geles, soluciones, parches e inhalantes. El compuesto activo se puede mezclar en condiciones estériles con un vehículo farmacéuticamente aceptable y con cualquier conservante, tampón o propulsor que pueda ser necesario.
Los ungüentos, pastas, cremas y geles pueden contener, además de un compuesto activo de esta divulgación, excipientes, tales como grasas animales y vegetales, aceites, ceras, parafinas, almidón, tragacanto, derivados de celulosa, polietilenglicoles, siliconas, bentonitas, ácido silícico, talco y óxido de zinc, o mezclas de los mismos.
Los polvos y aerosoles pueden contener, además de un compuesto de esta divulgación, excipientes tales como lactosa, talco, ácido silícico, hidróxido de aluminio, silicatos de calcio y polvo de poliamida, o mezclas de estas sustancias. Los aerosoles pueden contener además propulsores habituales, tales como clorofluorohidrocarburos e hidrocarburos volátiles no sustituidos, tales como butano y propano.
Los parches transdérmicos tienen la ventaja añadida de proporcionar un suministro controlado de un compuesto de la presente divulgación al cuerpo. Estas formas de dosificación se pueden preparar disolviendo o dispersando el compuesto en el medio apropiado. También se pueden usar potenciadores de la absorción para aumentar el flujo del compuesto a través de la piel. La velocidad de dicho flujo se puede controlar proporcionando una membrana de control de la velocidad o dispersando el compuesto activo en una matriz de polímero o gel.
Las formulaciones oftálmicas, pomadas oculares, polvos, soluciones y similares también se contemplan dentro del alcance de esta invención.
Las composiciones farmacéuticas de esta invención adecuadas para administración parenteral comprenden uno o más compuestos de la divulgación en combinación con una o más soluciones, dispersiones, suspensiones o emulsiones acuosas o no acuosas isotónicas estériles farmacéuticamente aceptables, o polvos estériles que pueden reconstituirse en forma de soluciones o dispersiones estériles inyectables justo antes de su uso, que pueden contener antioxidantes, tampones, bacteriostáticos, solutos que hacen que la formulación sea isotónica con la sangre del receptor pretendido o agentes de suspensión o espesantes.
Los ejemplos de vehículos acuosos y no acuosos adecuados que se pueden emplear en las composiciones farmacéuticas de la invención incluyen agua, etanol, polioles (tales como glicerol, propilenglicol, polietilenglicol y similares) y mezclas adecuadas de los mismos, aceites vegetales, tales como el aceite de oliva, y ésteres orgánicos inyectables, tales como el oleato de etilo. Se puede mantener la fluidez adecuada, por ejemplo, mediante el uso de materiales de recubrimiento, tales como lecitina, mediante el mantenimiento del tamaño de partícula requerido en el caso de dispersiones, y mediante el uso de tensioactivos.
Estas composiciones también pueden contener adyuvantes tales como conservantes, agentes humectantes, agentes emulsionantes y agentes dispersantes. La prevención de la acción de microorganismos se puede asegurar mediante la inclusión de diversos agentes antibacterianos y antifúngicos, por ejemplo, parabeno, clorobutanol, ácido fenolsórbico y similares. También puede ser deseable incluir agentes isotónicos, tales como azúcares, cloruro de sodio y similares en las composiciones. Además, la absorción prolongada de la forma farmacéutica inyectable puede producirse mediante la inclusión de agentes que retrasan la absorción tales como monoestearato de aluminio y gelatina.
En algunos casos, para prolongar el efecto de un fármaco, es deseable ralentizar la absorción del fármaco por inyección subcutánea o intramuscular. Esto se puede lograr mediante el uso de una suspensión líquida de material cristalino o amorfo que tiene escasa solubilidad en agua. La velocidad de absorción del fármaco depende entonces de su velocidad de disolución que, a su vez, puede depender del tamaño del cristal y de la forma cristalina. Alternativamente, la absorción retardada de una forma de fármaco administrada por vía parenteral se logra disolviendo o suspendiendo el fármaco en un vehículo oleoso.
Las formas de depósito inyectables se preparan formando matrices microencapsuladas de los compuestos objetivo en polímeros biodegradables tales como polilactida-poliglicólido. Dependiendo de la relación de fármaco a polímero y de la naturaleza del polímero particular empleado, se puede controlar la velocidad de liberación del fármaco. Ejemplos de otros polímeros biodegradables incluyen poli(ortoésteres) y poli(anhídridos). Las formulaciones inyectables de
depósito también se preparan atrapando el fármaco en liposomas o microemulsiones que son compatibles con el tejido 52789-0corporal.
Kits
Ventajosamente, la presente invención también proporciona kits para que los utilice un consumidor para tratar o prevenir enfermedades. Los kits comprenden a) una composición farmacéutica de la invención, b) un material de empaque que incluye la composición farmacéutica de la invención, y c) instrucciones que describen un método de uso de la composición farmacéutica para tratar o prevenir una enfermedad específica. En ejemplos de realizaciones, las instrucciones describen un método de uso de la composición farmacéutica para mejorar una respuesta inmune. En otro ejemplo de realización, las instrucciones describen un método de uso de la composición farmacéutica para tratar o prevenir el cáncer. En otro ejemplo de realización ejemplar, las instrucciones describen un método para mejorar la actividad inmunitaria de una célula inmune. Los kits de la invención pueden contener además un antígeno para administrar o bien utilizar junto con la composición farmacéutica.
Un "kit" como se usa en la presente solicitud incluye un recipiente para contener las formas de dosificación unitarias separadas, tal como una botella dividida o un empaque de papel de aluminio dividido. El recipiente puede tener cualquier forma convencional o forma conocida en la técnica, que está hecho de un material farmacéuticamente aceptable, por ejemplo, una caja de papel o cartón, una botella o frasco de vidrio o plástico, una bolsa resellable (por ejemplo, para contener una "recarga" de tabletas para colocarlas en un recipiente diferente), o un blíster eon dosis individuales para presionar fuera del empaque de acuerdo con un programa terapéutico. El recipiente empleado puede depender de la forma de dosificación exacta involucrada, por ejemplo, una caja de cartón convencional no se usaría generalmente para contener una suspensión líquida. Es factible que se pueda usar más de un recipiente juntos en un solo empaque para comercializar una única forma de dosificación. Por ejemplo, las tabletas pueden estar contenidas en una botella que a su vez está contenida dentro de una caja.
Un ejemplo de un kit de este tipo es el denominado blíster. Los envases tipo blíster son bien conocidos en la industria del envasado y se utilizan ampliamente para el empaque de formas farmacéuticas de dosificación unitaria (tabletas, cápsulas y similares). Los empaques tipo blíster consisten generalmente en una lámina de material relativamente rígido recubierto con una lámina de material plástico preferiblemente transparente. Durante el proceso de empaque, se forman huecos en la lámina de plástico. Los huecos tienen el tamaño y la forma de tabletas o cápsulas individuales que se van a empacar o pueden tener el tamaño y la forma para acomodar múltiples tabletas y/o cápsulas que se van a empacar. A continuación, las tabletas o cápsulas se colocan en los huecos en consecuencia y la lámina de material relativamente rígido se sella contra la lámina de plástico en la cara de la lámina que es opuesta a la dirección en la que se formaron los huecos. Como resultado, las tabletas o cápsulas se sellan individualmente o se sellan colectivamente, según se desee, en los huecos entre la lámina de plástico y la otra lámina. Preferiblemente, la resistencia de la lámina es tal que las tabletas o cápsulas se pueden extraer del blíster manualmente aplicando presión sobre los huecos con lo que se forma una abertura en la lámina en el lugar del hueco. A continuación, la tableta o cápsula se puede extraer a través de dicha abertura.
Puede ser deseable proporcionar una información escrita, en la que la ayuda escrita para la memoria es del tipo que contiene información y/o instrucciones para el médico, el farmacéutico o el sujeto, por ejemplo, en forma de números junto a las tabletas o cápsulas por lo que los números corresponden a los días del régimen en que deben ingerirse las tabletas o cápsulas así especificados o una ficha que contenga el mismo tipo de información. Otro ejemplo de tal ayuda para la memoria es un calendario impreso en la tarjeta, por ejemplo, como sigue "primera semana, lunes, martes", ... etc. ... "segunda semana, lunes, martes, ..." etc. Otras variaciones de ayudas para la memoria serán evidentes. Una "dosis diaria" puede ser una sola tableta o cápsula o varias tabletas o cápsulas para tomar en un día determinado.
Otra realización específica de un kit es un dispensador diseñado para dispensar las dosis diarias de una en una. Preferiblemente, el dispensador está equipado con una ayuda para la memoria, para facilitar aún más el cumplimiento del régimen. Un ejemplo de tal ayuda para la memoria es un contador mecánico, que indica el número de dosis diarias que se han dispensado. Otro ejemplo de este tipo de ayuda para la memoria es una memoria de microchip alimentada por batería junto con una lectura de cristal líquido o una señal de recordatorio audible que, por ejemplo, lee la fecha en que se tomó la última dosis diaria y/o le recuerda a uno cuándo debe tomarse la siguiente dosis.
Esta invención se ilustra adicionalmente mediante los siguientes ejemplos, que no deben interpretarse como limitantes.
Ejemplos
Los ejemplos indicados con * están fuera del alcance de la invención.
Ejemplo 1: El desarrollo de células NKT en cultivo de órganos tímicos fetales (FTOC) se bloquea mediante el tratamiento con inhibidores de IAP
Con el fin de investigar el papel de los miembros de la familia de IAP en el desarrollo de células NKT, se obtuvieron miméticos farmacológicos del segundo activador mitocondrial de la apoptosis (SMAC) del inhibidor de IAP endógeno. Se utilizaron tres inhibidores químicamente distintos para la mayoría de los experimentos. Uno de tales inhibidores, LBW-242, es un potente inhibidor de los miembros de la familia de IAP que se une al dominio BIR de XIAP en concentraciones submicromolares (IC50 = 280 nM). Se utilizó LBW-242 para la mayoría de las réplicas experimentales.
Se estudió el desarrollo de células NKT usando cultivos de órganos tímicos fetales (FTOC). Se cultivaron embriones de 16,5 días embrionarios de ratones C57BL/6 en presencia de tres inhibidores de IAP distintos, un compuesto de control o un vehículo (PBS). Después de 14 días, los cultivos se recolectaron y analizaron mediante citometría de flujo. Como se muestra en la Figura 1, el desarrollo de células NKT en cultivo de órganos tímicos fetales (FTOC) se bloquea mediante el tratamiento con inhibidores de IAP. La Figura 1A representa una cuantificación de poblaciones tímicas en FTOC tratadas durante 14 días con inhibidores de IAP (miméticos de SMAC). Como se indica en la Figura 1A, el tratamiento de FTOC con inhibidores de IAP condujo a una disminución moderada de las células T CD4+, sin un efecto constante sobre el tamaño del cultivo o sobre las células T CD8 + y doble positivas. En múltiples experimentos, la inhibición de los miembros de la familia de IAP durante el cultivo de FTOC previno completamente el desarrollo de células NKT de una manera dependiente de la dosis, como se muestra en las Figuras 1B-D. La Figura 1B representa el desarrollo de un solo timocito positivo en el día 14 en función de la concentración de LBW-242. La Figura 1C presenta el análisis de citometría de flujo de las FTOC del día 14 utilizando tetrámeros de CD1d cargados con a-galcer y anti-CD3. El tratamiento utilizado para cada cultivo se escribe encima de la gráfica correspondiente. Los datos son representativos de cuatro experimentos independientes. La Figura 1D presenta una cuantificación del desarrollo de células NKT de varios experimentos independientes que utilizan inhibidores de IAP. La Figura 1E representa el porcentaje de células NKT recuperadas de las FTOC del día 14 en función de la dosis de LBW-242. La inhibición de los miembros de la familia de IAP no tuvo un efecto consistente sobre la expresión de CD1d, o sobre el desarrollo de células T positivas para FOXP3 o células T y§. Como se usa en la Figura 1, mimético 3 de SMAC es LBW-242; los miméticos 1 y 2 de SMAC son compuestos inhibidores de IAP adicionales con mayor potencia que LBW-242. Se usaron LBW-242 y el compuesto de control a 500 nM. Se utilizaron los miméticos 1 y 2 de Sm Ac a 100 nM. Se utilizaron para todos los cultivos embriones de C57BL/6 embrionario 16,5 días.
* Ejemplo 2: La inhibición de los miembros de la familia de IAP no sensibiliza a las células T CD4+ maduras a la apoptosis
Se evaluó el papel de los miembros de la familia de IAP en la supervivencia de las células NKT maduras. Se activaron células T c D4+ derivadas del bazo de ratones BALB/c con anti-CD3 y anti-CD28 durante 24 horas y luego se analizaron mediante citometría de flujo. Como se muestra en la Figura 2, la inhibición de los miembros de la familia de IAP no sensibiliza a las células T CD4+ maduras a la apoptosis. Se estimularon 2 x 106 células T CD4+ esplénicas de BALB/c con anti-CD3 y anti-CD28 en RPMI. Después de 24 horas, las células viables se cuantificaron mediante exclusión con azul de tripáno y los recuentos de células resultantes se representan en la Figura 2A. Las células apoptóticas se cuantificaron en los cultivos de la Figura 2A usando citometría de flujo con anexina V y 7-AAD (los resultados se muestran en la Figura 2B). Tanto LBW-242 como el compuesto de control se usaron a 500 nM. El tratamiento de células T CD4+ con inhibidores de IAP no alteró el número total de células T ni contribuyó a la apoptosis, como se muestra en las Figuras 2A-B. Las células NKT se identificaron en los cultivos de la Figura 2A usando tetrámeros de CD1d cargados con anti-CD3 y a-galcer. Las células NKT todavía eran detectables en cultivo a frecuencias normales, como se muestra en la Figura 2C. En ausencia de estimulación, la inhibición de los miembros de la familia de IAP tampoco tuvo un efecto discernible sobre la apoptosis.
Ejemplo 3: La inhibición de los miembros de la familia de IAP mejora la secreción de citocinas de las células T activadas
Para determinar las consecuencias funcionales de la inhibición de IAP en células NKT, se estimularon células de bazo de ratones BALB/c con el agonista específico de células NKT a-galactosilceramida (a-galcer). Sorprendentemente, las células de bazo estimuladas con a-galcer tratadas con inhibidores de IAP mostraron un aumento de la secreción tanto de IFN-y (interferón y) como de IL-2 (interleucina-2), como se muestra en las Figuras 3A-B. Se cultivaron 5 x 105 células de bazo de BALB/c de tres ratones separados en RPMI con a-galcer en presencia de LBW-242 o un compuesto de control. Después de 48 horas, se midieron los niveles de citocinas en los sobrenadantes del cultivo mediante ELISA y los resultados se muestran en la Figura 3A (IFNy) y la Figura 3B (IL-2). Se observó un efecto similar dependiente de la dosis sobre la producción de IL-2 en células T c D4+ no fraccionadas de BALB/c o C57BL/6 estimuladas con anti-CD3 y anti-CD28, como se muestra en las Figuras 3C-D. Se cultivaron 105 células T CD4+ esplénicas de ratones BALB/c en RPMI con anti-CD3 y anti-CD28 o control de isotipo durante 48 horas en presencia de LBW-242 o un compuesto de control. Los niveles de IL-2 se midieron en el sobrenadante del cultivo mediante ELISA, como se muestra en la Figura 3C. En la Figura 3D se representa una curva de respuesta a la dosis para LBW-242 usando las condiciones descritas en la Figura 3C. Se usaron LBW-242 y el compuesto de control a 500 nM. No se observaron efectos de la inhibición de IAP en ausencia de estimulación. Es importante destacar que el tratamiento con mimético de SMAC de las células T CD4+ condujo a una mayor producción de citocinas incluso en presencia del inhibidor de pan-caspasa ZVAD-FMK, lo que indica que el efecto observado no es el resultado de la liberación de la inhibición de la caspasa.
Debido a que el efecto observado de la inhibición de IAP en las células T todavía podría depender de alteraciones en la función de las células NKT, se evaluaron las consecuencias de la inhibición de IAP en ratones C57BL/6 con inactivación de CD1d deficientes en células NKT. La estimulación de las células T CD4+ con inactivación de CD1d con anti-CD3 y anti-CD28 en presencia de inhibidores de IAP condujo a una producción de IL-2 que era indistinguible de la de los animales WT, lo que indica que la secreción mejorada de citocinas de las células T activadas causada por la inhibición de los miembros de la familia IAP es independiente de las células NKT (Figura 4). Se cultivaron células T CD4+ de bazos de ratones tipo silvestre (WT) y C57BL/6 con inactivación (KO) de CD1d se cultivaron en RPMI con anti-CD3 y anti-CD28 o durante 48 horas en presencia de LBW-242, M2 o un compuesto de control. Los niveles de IL-2 se midieron en el sobrenadante del cultivo mediante ELISA, como se indica en la Figura 4. El efecto de la inhibición de IAP no se limitó a las células T CD4+, ya que las células T CD8+ produjeron de manera similar un exceso de IFN-Y e IL-2 después de la estimulación en presencia de inhibidores de IAP (Figura 5). Se cultivaron células T CD8+ de ratones C57BL/6 en RPMI con anti-CD3 y anti-CD28 o durante 48 horas en presencia de LBW-242 o un compuesto de control. Los niveles de citocinas se midieron en el sobrenadante del cultivo mediante ELISA. Como se muestra en la Figura 5, la producción de citocinas a partir de células T CD8+ activadas aumenta mediante la inhibición de IAP.
Ejemplo 4: Las células T CD4+ humanas responden a los inhibidores de IAP
La mayoría de los miembros de la familia de IAP están altamente conservados entre el ratón y humano, lo que sugiere que las observaciones anteriores en el ratón también pueden aplicarse a células humanas activadas. Para abordar esta posibilidad, se purificaron células T CD4+ de la sangre periférica de varios voluntarios sanos y se estimularon con anti-CD3 y anti-CD28 en presencia de inhibidores de IAP. Como se observó en el ratón, la inhibición de los miembros de la familia de IAP condujo a un aumento dependiente de la dosis en la secreción de IL-2 de las células T CD4+ activadas; también como se observó en el ratón, la inhibición de IAP no tuvo efecto aparente sobre las células en reposo (Figuras 6A-B). Se purificaron 105 células T CD4+ de la sangre periférica de un donante sano y se estimularon durante 48 horas con anti-CD3 y anti-CD28, o un anticuerpo de control de isotipo en presencia de inhibidores de IAP (M2, M3 y M4) o un compuesto de control (M1). La IL-2 se midió mediante ELISA, como se indica en la Figura 6A. Se utilizaron M1 y M4 (LBW-242) a 500 nM. Se usaron M2 y M3 a 100 nM. La Figura 6B presenta una curva de respuesta a la dosis para LBW-242 usando células T CD4+ de un donante diferente y la configuración descrita para la Figura 6A.
El bloqueo farmacológico de calcineurina con ciclosporina pudo bloquear la producción mejorada de IL-2 asociada con la inhibición de IAP. Por el contrario, la inhibición de la vía de Akt con rapamicina fue capaz de reducir la producción total de IL-2, pero no evitó el aumento de la producción de IL-2 durante la inhibición de IAP (Figura 6C). Se estimularon células T CD4+ humanas en presencia de inhibidores de IAP o un compuesto de control con sirolimus (rapamicina) o ciclosporina, y los niveles de IL-2 resultantes se muestran en la Figura 6C.
* Ejemplo 5: la inhibición de los miembros de la familia de IAP durante la activación de las células T conduce a una señalización mejorada a través de las vías de JNK y NF-kB
Para investigar el mecanismo que une la inhibición de IAP con la producción mejorada de citocinas dependiente de la activación, se evaluó mediante transferencia Western el efecto de la inhibición de IAP sobre la fosforilación de JNK y la degradación de IkB en células T CD4+ estimuladas. Tanto las vías de JNK como de NF-kB se activaron más rápidamente en las células T inhibidas por IAP, como se muestra en la Figura 7. Se estimularon cultivos replicados de 2 x 106 células T CD4+ durante los períodos de tiempo indicados con anti-CD3 y anti-CD28 en presencia de LBW-242 500 nM o un compuesto de control (LCV-843). Las réplicas se combinaron y los lisados celulares se analizaron mediante transferencia Western para las proteínas indicadas. Se utilizó PDI como control de carga. Aunque se ha informado que cIAP2 es una ubiquitina ligasa para bcl-10, la inhibición de IAP no condujo a un cambio detectable en los niveles de bcl-10 en células T activadas. No se observaron cambios en la fosforilación de JNK y la degradación de IkB en las células T tratadas con inhibidores de IAP en ausencia de estimulación.
* Ejemplo 6: Los inhibidores de IAP mejoran ampliamente la activación de las células inmunes
Debido a que las rutas de JNK y NF-kB juegan papeles importantes en la señalización secuencia abajo de una amplia gama de receptores inmunes, se analizó el efecto de los inhibidores de IAP en varias poblaciones inmunes adicionales. Las células B inhibidas por IAP estimuladas con anti-IgM y anti-CD40 produjeron más IL-6 en comparación con las células de control, como se muestra en la Figura 8A. Se cultivaron 2 x 106 células B con anti-IgM y anti-CD40 durante 96 horas en presencia de LBW-242 o un compuesto de control. La IL-6 se midió en el sobrenadante del cultivo mediante ELISA. Además, las células dendríticas (DC) derivadas de la médula ósea parcialmente activadas (es decir, por ruptura de grupos) produjeron un aumento de p40 de IL-12 después de la inhibición de IAP; este efecto también se observó en las CD inhibidas por IAP estimuladas con LPS o CpG (Figura 8B). Se cultivaron 4 x 104 células dendríticas derivadas de médula ósea parcialmente activadas con los estímulos indicados en la Figura 8B durante 24 horas en presencia de LBW-242 o un compuesto de control. Se midió p40 en los sobrenadantes de cultivo mediante ELISA. Para ambos experimentos representados en la Figura 8, se usaron LBW-242 y el compuesto de control a 500 nM. También se encontró que los macrófagos peritoneales tratados con LPS secretan más IL-6 cuando se tratan conjuntamente con inhibidores de IAP.
* Ejemplo 7: La inhibición de los miembros de la familia IAP mejora la alorreactividad
Dada la amplia capacidad de la inhibición de IAP para mejorar la activación de células inmunes, se examinó el efecto de los inhibidores de IAP sobre una respuesta alotípica. Se cultivaron 4 x 105 células de bazo de ratones BALB/c con 8 x 105 células de bazo C57BL/6 irradiadas en presencia de LBW-242 o un compuesto de control (LCV-843). Después de seis días, se recogieron los cultivos y se analizó la producción de citocinas y la proliferación de células del bazo. Los cultivos tratados con LBW-242 mostraron una secreción de IFN-y significativamente mejorada; sin embargo, los niveles de IL-2 se redujeron significativamente, como se ilustra en la Figura 9A. Las citocinas se midieron en los sobrenadantes celulares mediante ELISA. Tanto LBW-242 como el compuesto de control se usaron a 500 nM. Al final de los cultivos descritos en la Figura 9A, se contaron las células viables totales mediante exclusión con azul de tripáno y se identificaron los subconjuntos de células inmunes mediante citometría de flujo utilizando los marcadores indicados en la Figura 9B. Dado que los cultivos descritos en la Figura 9A también exhibieron una proliferación significativa de células T CD4 (Figura 9B), la disminución de IL-2 probablemente se deba al consumo de la citocina. Se produjo una proliferación sustancial de células B en cultivos inhibidos por IAP (Figura 9B).
Los efectos potenciadores de la activación de la inhibición de IAP se invirtieron fácilmente; en las células T alorreactivas, las estimulaciones secundarias con anti-CD3 en ausencia de inhibidores condujeron a respuestas equivalentes independientemente de las condiciones de cultivo previas (Figura 10). Las células estimuladas en una reacción de linfocitos mixtos de seis días se recuperaron y se volvieron a estimular con anti-CD3 durante 48 horas. Las citocinas se midieron en los sobrenadantes de cultivo mediante ELISA. Las etiquetas de muestra indicadas en la Figura 10 se refieren al tratamiento utilizado durante la estimulación primaria.
* Ejemplo 8: La sobreexpresión de la proteína de unión MLIAP a SMAC en las células T CD4+ conduce a una disminución de la producción de IL-2 después de la estimulación.
También se examinó si la sobreexpresión de ML-IAP, una proteína endógena de unión de SMAC, podría alterar la respuesta de las células T a los estímulos de activación. Las células T de BALB/c transgénicas para m L-IAP secretaron niveles reducidos de IL-2 en respuesta a la estimulación anti-CD3 y anti-CD28, y este efecto podría modularse mediante la inhibición de IAP, como se muestra en la Figura 11. Se cultivaron 105 células T CD4+ de ratones BALB/c WT o MLIAP transgénicos (IAP) en RPMI con anti-CD3 y anti-CD28 durante 48 horas en presencia de LBW-242 o un compuesto de control. Los niveles de IL-2 se midieron en el sobrenadante del cultivo mediante ELISA.
* Ejemplo 9: Las células T con inactivación (KO) de XIAP son resistentes al tratamiento con mimético de SMAC
Para establecer la especificidad del efecto dependiente de IAP sobre la activación de células T, se activaron células T de ratones deficientes en XIAP en presencia de LBW-242 o el compuesto de control LCV-843. Al inicio del estudio, las células T deficientes en XIAP secretaron IL-2 y niveles comparables a los de los animales WT; sin embargo, las células deficientes en XIAP fueron resistentes al tratamiento con mimético de SMAC, mostrando solo un pequeño aumento en la secreción de citocinas tras el tratamiento con LBW-242 (Figura 12). Como se muestra en la Figura 12A, se cultivaron 105 células T CD4+ de ratones C57BL/6 WT o con KO de XIAP en RPMI con anti-CD3 y anti-CD28 durante 48 horas en presencia de LBW-242 o el compuesto de control LCV-843. Los niveles de IL-2 se midieron en el sobrenadante del cultivo mediante ELISA. La Figura 12B representa la proporción de IL-2 producida a partir de células T CD4+ estimuladas en presencia de LBW-242 en comparación con LCV-843. Estos resultados indican que XIAP juega un papel importante en la sensibilización de las células T al tratamiento con mimético de SMAC.
* Ejemplo 10: Los inhibidores de IAP mejoran la activación inmune y mejoran la inmunidad protectora después de la vacunación in vivo
Para examinar el efecto de los inhibidores de IAP sobre la activación inmunitaria in vivo, se administró LBW-242 a ratones en combinación con una vacuna antes de la exposición posterior. Se administraron células de melanoma de ratón B16 irradiadas (vacuna) a ratones los días -14 y -7 con o sin una única dosis oral de LBW-242 (150 mg/kg). Se implantaron células tumorales B16 vivas en los ratones el día 0 (exposición). El volumen tumoral se midió a los 7, 10, 13 y 16 días después del implante de células vivas. Como se muestra en la Figura 13, los ratones que recibieron el inhibidor de IAP LBW-242 en combinación con la vacuna B16 tuvieron una carga tumoral reducida después de la exposición con células B16 vivas, en comparación con los ratones que recibieron LBW-242 o la vacuna B16 sola. Estos datos indican que la administración de un inhibidor de IAP en combinación con un antígeno mejora la activación inmunitaria, aumentando la inmunidad protectora.
* Ejemplo 11: Síntesis de los inhibidores de IAP de la divulgación
A continuación, se describe un procedimiento de síntesis para BPN 242 (N-[1-ciclohexil-2-oxo-2-(6-fenetil-octahidropirrolo[2,3-c]piridin-1-il)-etil]-2-metilamino-propionamida).
Pueden usarse procedimientos de síntesis análogos para preparar los otros inhibidores de IAP de la divulgación.
But-3-enil-((S)-1-fenil-etil)-amina (A): A una solución de S-(-)-1-feniletilamina (15,75 g, 130 mmol) en 150 ml de DMF a 0 °C se le añade K2CO3 (53,9 g, 390 mmol) en pequeñas porciones. Después de agitar a 0 °C durante 10 min, se añade gota a gota 4-bromobuteno (13,5 g, 100 mmol) seguido de NaI (58,5 g, 390 mmol) en pequeñas porciones. La mezcla de reacción, una suspensión blanca, se calienta a 95 °C y se agita durante la noche/16 h. La solución se enfría a TA y se diluye con 200 ml de éter y se lava con 3 x 100 ml de agua. La capa orgánica se seca sobre Na2SO4 y se concentra. El producto crudo se purifica por destilación (65-70 °C bajo alto vacío) para producir un líquido incoloro (13,5 g, 76,7%).
Éster etílico del ácido [But-3-enil-((S)-1-fenil-etil)-amino]-acético (B): A una solución de But-3-enil-((S)-1-feniletil)amina (6,37 g, 36,4 mmol) en 150 ml de DMF a 0 °C, se le añade K2CO3 (10,0 g, 72,8 mmol) en pequeñas porciones. Después de agitar a 0 °C durante 10 min, se añade lentamente bromoacetato de etilo (8,35 g, 54,6 mmol). La mezcla de reacción, una suspensión blanca, se agita a temperatura ambiente durante la noche/16 horas. La solución se diluye con 200 ml de éter y se lava con 3 x 100 ml de agua. El producto crudo se purifica mediante cromatografía (hexano/ChhCh: 50/50) para dar un líquido pálido (8,5 g, 94,5%).
Éster etílico del ácido (2S,3R)-3-but-3-enil-1-(S)-1-fenil-etil)-pirrolidin-2-carboxílico (C): A una solución de diisopropilamina (3,6 g, 35,7 mmol) en THF (80 ml) a -40 °C se le añade BuLi (14,28 ml, 35,7 mmol, 2,5 M en hexano) lentamente. La solución se calienta a 0 °C y se agita durante 30 min para formar una solución de LDA. La solución de LDA se enfría a -70 °C y se añade a una solución de éster etílico del ácido [But-3-enil-(S)-1-fenil-etil)-amino]-acético (7,8 g, 29,8 mmol) en t Hf (80 ml) lentamente a -70 °C. La solución de reacción de color amarillento claro se agita a-20 °C durante 30 min para convertirse en una solución de color amarillo intenso y luego se enfría a -70 °C. A la solución se le añade ZnBr2 (16,76 g, 74,5 mmol) en éter (50 ml) gota a gota a -70 °C. Después de agitar a TA durante 1,5 horas, la solución de la reacción se enfría a 0 °C y se le añade una solución de CuCN (3,47 g, 38,74 mmol) y LiCl (3,29 g, 77,48 mmol) en THF (80 ml) lentamente. Después de agitar a 0 °C durante 10 min, se añade bromuro de alilo (7,26 g,
60 mmol) gota a gota a la solución de la reacción y se calienta muy lentamente a temperatura ambiente. Después de agitar durante la noche a temperatura ambiente, la reacción se inactiva mediante la adición de 60 ml de NH4Cl saturado y se extrae con 3 X 150 ml de éter. Las capas orgánicas combinadas se concentran. El producto crudo se purifica mediante cromatografía (hexano/EtOAc: 85/15) para producir un líquido incoloro (7,4 g, 82,6%) (El ZnBr2 se seca a 150 °C a alto vacío durante 1 hora antes de su uso).
Éster etílico del ácido (2S,3R)-1-((2E,4Z)-(S)-1)-2-Dimetil-hexa-2,4-dienil)-3-(3-oxo-propil)pirrolidina-2-carboxílico (D): se disuelve en éster etílico del ácido (2S, 3R)-3-But-3-enil-1-((S)-1-fenil-etil)-pirrolidin-2-carboxílico (1,0 g, 3,32 mmol) EtOH (10 ml) con HCl (0,5 ml, 37%) y se enfría a -70 °C. Se burbujea gas ozono a través de la solución durante unos 10 minutos o hasta que la solución se vuelve de un color azul muy claro. El gas nitrógeno se burbujea a través de la solución durante 15 minutos para eliminar el exceso de ozono en la solución. A la solución fría se le añade polvo de Zn (0,43 g, 6,6 mmol) y HCl (0,5 ml, 37%) y se agita a temperatura ambiente durante 20 min. Después de la filtración, la solución se diluye con 50 ml de CH2Cl2 y se lava con NaHCO3 saturado (10 ml) y 2 x 20 ml de agua. Después de secar y concentrar, se obtiene un líquido incoloro (1,0 g) sin purificación adicional para la reacción de la siguiente etapa.
Éster etílico del ácido (2S,3R)-3-(3-fenetilamino-propil)-1-((S)-1-fenil-etil)-pirrolidin-2-carboxílico (E): A una solución de éster etílico del ácido 2S,3R)-1-((2E,4Z)-(S)-1,2-dimetil-hexa-2,4-dienil)-3-(3-oxo-propil) pinolidina-2-carboxílico (1 g, crudo) en EtOH (10 ml) se agrega fenetilamina (0,44 g, 3,65 mmol) a temperatura ambiente. Después de agitar a temperatura ambiente durante 30 min, se añade NaBHaCN (0,3 g, 4,87 mmol) en una porción. Después de agitar a temperatura ambiente durante 1,5 horas, la solución de reacción se diluye con 50 ml de éter y se lava con 20 ml de salmuera. La capa de éter se concentra y el producto crudo se purifica por cromatografía (CH2Ch/MeOH: 97/3) para dar un líquido pálido (405 mg, 30,0%).
(3aS,57aS)-6-Fenetil-1-((S)-1-fenil-etil)-octahidro-pirrolo[2,3-c]piridin-7-ona (F): se disuelve éster etílico del ácido (2S,3R)-3-(3-fenetilamino-propil)-1-(S)-1-fenil-etil)-pirrolidin-2-carboxílico (340 mg, 0,83 mmol) en 20 ml de MeOH/KOH/H2O (10 ml/5 g/5 ml). Después de agitar a 80 °C durante 2 horas, la solución se enfría a 0 °C y se neutraliza mediante la adición de HCl (37%) a pH = 5. Después de la concentración, el producto crudo se disuelve en 1 ml de CH2Cl2 y se filtra a través de un tapón corto de gel de sílice y se eluye con CH2Ch/MeOH (93/7) para dar un sólido vítreo pálido (250 mg, 78,9%) como el ácido.
A una solución (0,05 - 0,1 M) de ácido (1 equivalente) en DMF a temperatura ambiente se añade diisopropiletilamina (5 equivalentes). Después de agitar a temperatura ambiente durante 20 min, se añade una solución (0,05 ~ 0,1 M) de HOBT (1,2 equivalentes) y HBTU (1,2 equivalentes) en DMF a la mezcla de reacción y se continúa agitando durante 1.5 h (o se controla mediante TLC). La solución de reacción se diluye con éter (1 x 5 ~ 10 veces por volumen de la solución) y se lava con agua (dos veces x 3 por volumen de la solución). La solución orgánica combinada se concentra. El producto crudo se diluye con CH2Cl2 y se seca sobre Na2SO4 y se purifica por cromatografía (CH2Ch/MeOH: 97/3) para producir un producto puro (70-95% de rendimiento).
Procedimiento para el compuesto F usando 2-hidroxil piridina: se agita una solución de éster metílico de ácido (2S, 3R)-3-(2-fenetilamino-etil)-1-(S)-1-fenil-etil)-pirrolidin-2 carboxílico (400 mg, 1,05 mmol) y 2-hidroxilpiridina (100 mg, 1.05 mmol) en THF (10 ml) a 40 °C durante 24 h. La reacción se diluye con 50 ml de éter y se lava con 2 x 120 ml de agua. Después se secó y se concentró para dar un líquido pálido (350 mg) sin purificación adicional para la siguiente etapa de reacción.
(3aR,8aS)-7-fenetil-1-((S)-1-fenil-etil)-decahidro-pirrolo[2,3-c]azepina (G): a una solución (0,02 M) de lactama (1 equivalente) en THF a -20 °C se le añade lentamente una solución (0,02 M) de LiAlH4 (2 equivalentes) en THF. Después de agitar temperatura ambiente durante 1,5 horas, la solución se diluye con éter (1 x 5 veces por volumen de la solución) y se lava con agua (dos veces 2 veces por volumen de la solución), se seca y se concentra. El producto bruto se purifica mediante cromatografía (CH2Ch/MeOH: 97/3) para dar el producto (rendimiento 70-90%).
(3aR,8aS)-7-fenetil-decahidro-pirrolo[2,3-c]azepina (H): se agita vigorosamente una solución/suspensión de reactivo (<1 g) y Pd al 10% sobre carbono (20% en peso) en MeOH (10 ml, con 2 gotas de ácido acético) en un matraz redondo de 1000 ml a temperatura ambiente bajo gas hidrógeno (a presión atmosférica) en un balón durante 4-8 horas. Después de desgasificar mediante vacío doméstico durante 10 min, la mezcla de reacción se filtra para remover el catalizador y se concentra. El producto crudo se diluye con CH2Ch/H2O (8/2, cantidad razonable) y se neutraliza con NH4OH al 10% a pH = 7 - 8. Después se secó y se concentró para dar el producto (80% de rendimiento cuantitativo) sin purificación para la siguiente etapa de reacción.
LBW 242: Preparado a partir del compuesto H usando el esquema que se describe a continuación:
Compuesto (7): a una solución de 6 en diclorometano (25 ml) se le añade secuencialmente diisopropiletilamina (4,17 ml, 24 mmol), t-Boc-L-ciclohexilglicina (1,54 g, 6 mmol) y una solución de HOBt/HBTU 0,45 M en Dm F (16 ml, 7,19 mmol). La mezcla se agita durante la noche a temperatura ambiente, luego se diluye con EtOAc (200 ml) y se lava secuencialmente con ácido cítrico acuoso 1 M (50 ml), agua (50 ml), NaHCO3 acuoso saturado (50 ml) y salmuera (2 x 50 ml). La capa orgánica se seca y se concentra al vacío. El residuo se purifica mediante cromatografía ultrarrápida (gel de sílice; Hexano/EtOAc 1: 9) para proporcionar un aceite amarillo. El aceite amarillo se disuelve en diclorometano (20 ml), se agrega TFA (10 ml) y la mezcla se agita a temperatura ambiente durante 3 h. La mezcla se concentra y el residuo se disuelve en diclorometano (100 ml) y se neutraliza con bicarbonato de sodio saturado. La solución se extrae con diclorometano (3 x 50 ml). Los extractos orgánicos se combinan, secan y concentran al vacío para proporcionar 1,75 g (79% dos etapas) del compuesto del título que se usa en la siguiente etapa sin purificación o caracterización adicional.
LBW 242: A una solución de 7 (1,75 g, 4,74 mmol) en diclorometano (25 ml) se le añade secuencialmente diisopropiletilamina (3,30 ml, 19 mmol), t-Boc-N-metil-L-alanina (0,97 g, 4,74 mmol) y una solución de HOBt/HBTU 0,45 M en DMF (13 ml, 5,691 mmol). La mezcla se agita durante la noche a temperatura ambiente. La mezcla se diluye con EtOAc (200 ml) y se lava secuencialmente con ácido cítrico 1 M (50 ml), agua (50 ml), NaHCO3 acuoso saturado (50 ml), salmuera (2 x 50 ml). La capa orgánica se seca y se concentra al vacío. El residuo se disuelve en diclorometano (20 ml), se agrega TFA (10 ml) y la mezcla se agita a temperatura ambiente durante 3 horas. La mezcla se concentra y el residuo se disuelve en diclorometano (100 ml) y se neutraliza con bicarbonato de sodio saturado. La solución se extrae con diclorometano (3 x 50 ml). Los extractos orgánicos se combinan, se secan y se concentran al vacío. El residuo se purifica por Hp Lc (gel de sílice C-18, CH3CN/H2O al 20% en TFA al 0,5%) para proporcionar g (36% dos etapas) del compuesto del título como sal de TFA.
El alcance de la invención está definido por las reivindicaciones. Cualquier referencia en la descripción a los métodos de tratamiento se refiere a los compuestos, composiciones farmacéuticas y medicamentos de la presente invención para su uso en un método de tratamiento del cuerpo humano (o animal) mediante terapia.
Claims (24)
1. Una composición farmacéutica que comprende un vehículo farmacéuticamente aceptable, una cantidad inmunogénica de un antígeno y un adyuvante que comprende un inhibidor de IAP, en el que el antígeno comprende un antígeno presente en una célula de cáncer; una célula cancerosa; un fragmento de célula cancerosa; un antígeno tumoral; a-galcer; anti-CD3; anti-CD28; anti-IgM; anti-CD40; un patógeno, un patógeno atenuado o una porción del mismo; y el inhibidor de IAP es un compuesto de Fórmula II
o una sal farmacéuticamente aceptable del mismo, en el que
R1' es H;
R2 ' es alquilo C1-C4 ;
R3 ' es alquilo C1-C4 ;
R4 ' es cicloalquilo C3-C10;
R5 ' es H o alquilo C1-C10;
U es
R17 es Ar1-D-Ar2 ;
D es CO, O o N(Rx);
Rx es H o alquilo C1-7; y
Ar1 y Ar2 son arilo o heteroarilo sustituido o no sustituido.
2. La composición farmacéutica de la reivindicación 1, en la que el inhibidor de IAP se selecciona del grupo que consiste en:
(S)-N-((S)-1-Ciclohexil-2-{(S)-2-[4-(4-fluoro-benzoil)-tiazol-2-il]-pirrolidin-1-il}-2-oxo-etil)-2-metilamino-propionamida; (S)-N-[(S)-Ciclohexil-(etil-{(S)-1-[5-(4-fluoro-benzoil)-piridin-3-il]-propil}-carbamoil)-metil]-2-metilamino-propionamida; (S)-N-((S)-1-Ciclohexil-2-{(S)-2-[5-(4-fluoro-fenoxi)-piridin-3-il}-pirrolidin-1-il}-2-oxo-etil)-2-metilamino-propionamida; (S)-N-((S)-1-Ciclohexil-2-{(S)-2-[4-(4-fluoro-fenoxi)-piridin-2-il]-pirrolidin-1-il}-2-oxo-etil)-2-metilamino-propionamida; (S)-N-[(S)-Ciclohexil-2-((S)-2-{5-fluoro-2-[(4-fluoro-fenil)-metil-amino]-piridm-4-il}-pirrolidin-1-il)-2-oxo-etil]-2-metilamino-propionamida;
(S)-N-((S)-1-Ciclohexil-2-{(S)-2-[4-(4-fluoro-benzoil)-5-metil-tiazo-1-2-il]-pirrolidin-1-il}-2-oxo-eti-l)-2-metilaminopropionamida;
(S)-N-{(S)-2-[(S)-2-(4-Benzoil-5-metil-oxazol-2-il)-pirrolidin-1-il]-1-ciclohexil-2-oxo-etil}-2-metilamino-propionamida; (S)-N-((S)-1-Ciclohexil-2-{(S)-2-[4-(4-fluoro-benzoil)-5-metil-oxazol-2-il]-pirrolidin-1-il}-2-oxo-etil)-2-metilaminopropionamida;
(S)-N-((S)-1-Ciclohexil-2-{(S)-2-[4-(4-fluoro-benzoil)-5-metil-tiazol-2-il]-pirrolidin-1-il}-2-oxo-etil)-2-metilaminopropionamida;
(S)-N-{(S)-2-[(S)-2-(4-Benzoil-oxazol-2-il)-pirrolidin-1-il]-1-ciclohexil-2-oxo-etil}-2-metilamino-propionamida;
(S)-N-((S)-1-Ciclohexil-2-{(S)-2-[4-(2,4-difluoro-benzoil)-tiazol-2-il]-pirrolidin-1-il}-2-oxo-etil)-2-metilaminopropionamida;
(S)-N-((S)-1-Ciclohexil-2-{(S)-2-[4-(1 H-indole-2-carbonil)-tiazol-2-il]-pirrolidin-1-il}-2-oxo-etil)-2-metilaminopropionamida;
(S)-N-((S)-1-Ciclohexil-2-{(S)-2-[2-(4-fluoro-fenoxi)-piridin-4-il]-pirrolidin-1-il}-2-oxo-etil)-2-metilamino-propionamida; (S)-N-[(S)-1-((S)-2-{2-[(4-Fluoro-fenil)-metil-amino]-piridin-4-il}-pirrolidin-1-carbonil)-2-metil-propil]-2-metilaminopropionamida;
(S)-N-((S)-1-Ciclohexil-2-{(S)-2-[2-(4-fluoro-benzoil)-piridin-4-il]-pirrolidin-1-il}-2-oxo-etil)-2-metilamino-propionamida; (s )-N-((s )-1 -Ciclohexil-2-{(S)-2-[2-(S-fluoro-piridin-2-ilamino)-piridin-4-il]-pirrolidin-1 -il}-2-oxo-etil)-2-metilaminopropionamida;
(S)-N-[(S)-1-Ciclohexil-2-((S)-2-{3-fluoro-2-[(4-fluoro-fenil)-metil-amino]-piridin-4-il}-pirrolidin-1-il)-2-oxo-etil]-2-metilamino-propionamida;
(S)-N-((S)-1-Ciclohexil-2-{(S)-2-[3-fluoro-2-(4-fluoro-benzoil)-piridin-4-il]-pirrolidin-1-il}-2-oxo-etil)-2-metilaminopropionamida;
(S)-N-[(S)-2-((S)-2-{2-Amino-6-[N-(4-fluoro-fenil)-hidrazino]-piridin-4-il}-pirrolidin-1-il)-1-ciclohexil-2-oxo-etil]-2-metilamino-propionamida;
(S)-N-{(S)-1-Ciclohexil-2-oxo-2-[(S)-2-(4-fenoxi-piridin-2-il)-pirrolidin-1-il]-etil}-2-metilamino-propionamida;
(S)-N-((S)-1-Ciclohexil-2-{(S)-2-[6-(4-fluoro-fenoxi)-2-metil-pirimidin-4-il]-pirrolidin-1-il}-2-oxo-etil)-2-metilaminopropionamida;
(S)-N-((S)-1-Ciclohexil-2-{(S)-2-[4-(4-fluoro-benzoil)-piridin-2-il]-pirrolidin-1-il}-2-oxo-etil)-2-metilamino-propionamida; (S)-N-((S)-1-Ciclohexil-2-{(S)-2-[6-(4-fluoro-benzoil)-2-metil-pirimidin-4-il]-pirrolidin-1-il}-2-oxo-etil)-2-metilaminopropionamida;
(S)-N-[(S)-1-Ciclohexil-2-((S)-2-{5-[(4-fluoro-fenil)-metil-amino]-piridin-3-il}-pirrolidin-1-il)-2-oxo-etil]-2-metilaminopropionamida;
(S)-N-[(S)-1-Ciclohexil-2-((S)-2-{4-[(4-fluoro-fenil)-metil-amino]-piridin-2-il}-pirrolidin-1-il)-2-oxo-etil]-2-metilaminopropionamida;
(S)-N-[(S)-1-Ciclohexil-2-((S)-2-{6-[(4-fluoro-fenil)-metil-amino]-2-metil-pirimidin-4-il}-pirrolidin-1-il)-2-oxo-etil]-2-metilamino-propionamida;
(S)-N-((S)-1-{(S)-2-[6-(4-Fluoro-benzoil)-2-metil-pirimidin-4-il]-pirrolidin-1-carbonil}-2-metil-propil)-2-metilaminopropionamida;
(S)-N-((S)-1-{(S)-2-[6-(4-Fluoro-benzoil)-2-metil-pirimidin-4-il]-pirrolidin-1-carbonil}-2-metil-propil)-2-metilaminopropionamida;
(S)-N-[(S)-1-((S)-2-{6-[(4-Fluoro-fenil)-metil-amino]-2-metil-pirimidin-4-il}-pirrolidin-l-carbonil)-2-metil-propil]-2-metilamino-propionamida;
(S)-N-((S)-1-Ciclohexil-2-{(S)-2-[6-(4-fluoro-fenilamino)-2-metil-pirimidin-4-il]-pirrolidin-1-il}-2-oxo-etil)-2-metilaminopropionamida; y
(S)-N-((S)-1-{(S)-2-[6-(4-Fluoro-fenilamino)-2-metil-pirimidin-4-il]-pirrolidin-1-carbonil}-2-metil-propil)-2-metilaminopropionamida;
o una sal farmacéuticamente aceptable de las mismas.
3. La composición farmacéutica de la reivindicación 2, en la que el inhibidor de IAP es (S)-N-((S)-1-ciclohexil-2-{(S)-2-[4-(4-fluoro-benzoil)-tiazol-2-il]-pirrolidin-1-il}-2-oxo-etil)-2-metilamino-propionamida, o una sal farmacéuticamente aceptable de la misma.
4. La composición farmacéutica de la reivindicación 1 o 2, en la que el antígeno comprende un antígeno presente en una célula de cáncer; una célula cancerosa; un fragmento de células cancerosas; o un antígeno tumoral.
5. La composición farmacéutica de la reivindicación 3, en la que el antígeno comprende un antígeno presente en una célula de cáncer; una célula cancerosa; un fragmento de células cancerosas; o un antígeno tumoral.
6. La composición farmacéutica de la reivindicación 4 o 5, en la que la célula cancerosa es una célula autóloga.
7. La composición farmacéutica de la reivindicación 4 o 5, en la que la célula cancerosa es una célula alogénica.
8. La composición farmacéutica de cualquiera de las reivindicaciones 4-7, en la que la célula cancerosa es incapaz de proliferar.
9. La composición farmacéutica de cualquiera de las reivindicaciones 1 a 5, en la que el antígeno es mucina-1, antígeno prostático específico, antígeno carcinoembrionario, fosfatasa ácida prostática o MAGE.
10. La composición farmacéutica de una cualquiera de las reivindicaciones 1 a 3, en la que el antígeno es un patógeno, un patógeno atenuado o una porción del mismo.
11. La composición farmacéutica de una cualquiera de las reivindicaciones 1 a 3, en la que el antígeno es a-galcer, anti-CD3, anti-CD28, anti-IgM o anti-CD40.
12. Un kit que comprende: (a) una composición farmacéutica que comprende un vehículo farmacéuticamente aceptable, una cantidad inmunogénica de un antígeno y un adyuvante que comprende un inhibidor de IAP, en el que el antígeno comprende un antígeno presente en una célula de cáncer; una célula cancerosa; un fragmento de células cancerosas; un antígeno tumoral; a-galcer; anti-CD3; anti-CD28; anti-IgM; anti-CD40; un patógeno, un patógeno atenuado o una porción del mismo; y el inhibidor de IAP es un compuesto de Fórmula II
o una sal farmacéuticamente aceptable del mismo, en el que
R1' es H;
R2 ' es alquilo C1-C4 ;
R3' es alquilo C1-C4 ;
R4' es cicloalquilo C3-C10;
R5' es H o alquilo C1-C10;
U es
R17 es Ar1-D-Ar2 ;
D es CO, O o N(Rx);
Rx es H o alquilo C1-7; y
Ar1 y Ar2 son arilo o heteroarilo sustituido o no sustituido
(b) un material de empaquetamiento que encierra dicha composición farmacéutica; y
(c) instrucciones de uso de dicha composición farmacéutica.
13. Una vacuna que comprende una cantidad inmunogénica de un antígeno y un adyuvante que comprende un inhibidor de IAP, en la que el antígeno comprende un antígeno presente en una célula de cáncer; una célula cancerosa; un fragmento de células cancerosas; un antígeno tumoral; a-galcer; anti-CD3; anti-CD28; anti-IgM; anti-CD40; un patógeno, un patógeno atenuado o una porción del mismo; y el inhibidor de IAP es un compuesto de Fórmula II
o una sal farmacéuticamente aceptable del mismo, en el que
R1’ es H;
R2’ es alquilo C1-C4 ;
R3’ es alquilo C1-C4 ;
R4’ es cicloalquilo C3-C10;
R5’ es H o alquilo C1-C10;
U es
R17 es Ar1-D-Ar2 ;
D es CO, O o N (Rx);
Rx es H o alquilo C1-7; y
Ar1 y Ar2 son arilo o heteroarilo sustituido o no sustituido.
14. Una cantidad inmunogénica de un antígeno y una cantidad mejoradora de la inmunidad de un inhibidor de IAP para su uso en la mejora de una respuesta inmunitaria de un sujeto a un antígeno, en el que el antígeno comprende un antígeno presente en una célula de cáncer; una célula cancerosa; un fragmento de célula cancerosa; un antígeno tumoral; a-galcer; anti-CD3; anti-CD28; anti-IgM; anti-CD40; un patógeno, un patógeno atenuado o una porción del mismo; y el inhibidor de IAP es un compuesto de Fórmula (II)
o una sal farmacéuticamente aceptable del mismo, en el que
R1' es H;
R2' es alquilo C1-C4 ;
R3' es alquilo C1-C4 ;
R4' es cicloalquilo C3-C10;
R5' es H o alquilo C1-C10;
U es
R17 es Ari-D-Ar2 ;
D es CO, O o N (Rx);
Rx es H o alquilo C1-7; y
Ar1 y Ar2 son arilo o heteroarilo sustituido o no sustituido.
15. Una cantidad terapéuticamente eficaz de un inhibidor de IAP y una cantidad inmunogénica de un antígeno para uso en el tratamiento de un cáncer en un sujeto, en el que dicho inhibidor de IAP y dicho antígeno mejoran la respuesta inmune del sujeto al cáncer, y en el que el antígeno comprende un antígeno presente en una célula de cáncer; una célula cancerosa; un fragmento de células cancerosas; un antígeno tumoral; a-galcer; anti-CD3; anti-CD28; anti-IgM; anti-CD40; un patógeno, un patógeno atenuado o una porción del mismo; y el inhibidor de IAP es un compuesto de Fórmula (II)
o una sal farmacéuticamente aceptable del mismo, en el que
R1' es H;
R2 ' es alquilo C1-C4 ;
R3 ' es alquilo C1-C4 ;
R4 ' es cicloalquilo C3-C10;
R5 ' es H o alquilo C1-C10;
U es
R17 es Ar1-D-Ar2 ;
D es CO, O o N (Rx);
Rx es H o alquilo C1-7; y
Ar1 y Ar2 son arilo o heteroarilo sustituido o no sustituido.
16. Una cantidad terapéuticamente eficaz de un inhibidor de IAP y una cantidad inmunogénica de un antígeno, para su uso en el tratamiento o prevención de una infección causada por un agente infeccioso, en el que dicho inhibidor de IAP y dicho antígeno mejoran la respuesta inmune del sujeto al agente infeccioso, en el que el inhibidor de IAP es un compuesto de Fórmula (II)
R1 ’ es H;
R2 ’ es alquilo C1-C4 ;
R3 ’ es alquilo C1-C4 ;
R4 ’ es cicloalquilo C3-C10;
R5 ’ es H o alquilo C1-C10;
U es
R17 es Ari-D-Ar2 ;
D es CO, O o N (Rx);
Rx es H o alquilo C1-7; y
Ar1 y Ar2 son arilo o heteroarilo sustituido o no sustituido.
17. Un inhibidor de IAP para su uso en la mejora de la actividad inmune de una célula inmunitaria activada en un sujeto, en el que el inhibidor de IAP es un compuesto de Fórmula (II).
o una sal farmacéuticamente aceptable del mismo, en el que
R1 ’ es H;
R2 ’ es alquilo C1-C4 ;
R3 ’ es alquilo C1-C4 ;
R4 ’ es cicloalquilo C3-C10;
R5 ’ es H o alquilo C1-C10;
U es
R17 es Ar1-D-Ar2 ;
D es CO, O o N (Rx);
Rx es H o alquilo C1-7; y
Ar1 y Ar2 son arilo o heteroarilo sustituido o no sustituido.
18. Un inhibidor de IAP para su uso de acuerdo con la reivindicación 17 junto con un estímulo de activación inmune.
19. Un inhibidor de IAP y un estímulo de activación inmune para uso de acuerdo con la reivindicación 18, en el que el estímulo de activación inmune se selecciona entre a-galcer, anti-CD3, anti-CD28, anti-IgM y anti-CD40.
20. Una cantidad terapéuticamente eficaz de un inhibidor de IAP y una cantidad inmunogénica de un antígeno para su uso en la activación de una célula inmune contra el antígeno en un sujeto, en el que el inhibidor de IAP es un compuesto de Fórmula (II).
o una sal farmacéuticamente aceptable del mismo, en el que
R1 ’ es H;
R2 ’ es alquilo C1-C4 ;
R3 ’ es alquilo C1-C4 ;
R4 ’ es cicloalquilo C3-C10;
R5 ’ es H o alquilo C1-C10;
U es
R17 es Ari-D-Ar2 ;
D es CO, O o N (Rx);
Rx es H o alquilo C1-7; y
Ar1 y Ar2 son arilo o heteroarilo sustituido o no sustituido.
21. Uso ex vivo de una cantidad terapéuticamente eficaz de un inhibidor de IAP y una cantidad inmunogénica de un antígeno para activar una célula inmune contra el antígeno, en el que el inhibidor de IAP es un compuesto de Fórmula (II)
o una sal farmacéuticamente aceptable del mismo, en el que
R1' es H;
R2 ' es alquilo C1-C4 ;
R3 ' es alquilo C1-C4 ;
R4 ' es cicloalquilo C3-C10;
R5 ' es H o alquilo C1-C10;
U es
R17 es Ar1-D-Ar2 ;
D es CO, O o N (Rx);
Rx es H o alquilo C1-7; y
Ar1 y Ar2 son arilo o heteroarilo sustituido o no sustituido.
22. Una composición farmacéutica que comprende un vehículo farmacéuticamente aceptable, una cantidad inmunogénica de un antígeno y un adyuvante que comprende un inhibidor de IAP de acuerdo con cualquiera de las reivindicaciones 1-11; un kit de acuerdo con la reivindicación 12; una vacuna que comprende una cantidad inmunogénica de un antígeno y un adyuvante que comprende un inhibidor de IAP de acuerdo con la reivindicación 13; una cantidad inmunogénica de un antígeno y una cantidad mejoradora de la inmunidad de un inhibidor de IAP para su uso de acuerdo con la reivindicación 14; una cantidad terapéuticamente eficaz de un inhibidor de IAP y una cantidad inmunogénica de un antígeno para su uso de acuerdo con una cualquiera de las reivindicaciones 15, 16 o 20; o un uso ex vivo de acuerdo con la reivindicación 21, en el que la cantidad inmunogénica del antígeno es inmunogénica solo cuando se administra en combinación con el inhibidor de IAP.
23. Una composición farmacéutica que comprende un vehículo farmacéuticamente aceptable; una cantidad inmunogénica de un antígeno y un adyuvante que comprende un inhibidor de IAP de acuerdo con la reivindicación 22; un kit de acuerdo con la reivindicación 22; una vacuna que comprende una cantidad inmunogénica de un antígeno y un adyuvante que comprende un inhibidor de IAP de acuerdo con la reivindicación 22; una cantidad inmunogénica de un antígeno y una cantidad mejoradora de la inmunidad de un inhibidor de IAP para su uso de acuerdo con la reivindicación 22; una cantidad terapéuticamente eficaz de un inhibidor de IAP y una cantidad inmunogénica de un antígeno para su uso de acuerdo con cualquiera de la reivindicación 22; o un uso ex vivo de acuerdo con la reivindicación 22, en el que el inhibidor de IAP es (S)-N-((S)-1-ciclohexil-2-{(S)-2-[4-(4-fluoro-benzoil)-tiazol-2-il]-pirrolidin-1-il}-2-oxo-etil)-2-metilamino-propionamida.
24. Una vacuna que comprende una cantidad inmunogénica de un antígeno y un adyuvante que comprende un inhibidor de IAP de acuerdo con la reivindicación 13; una cantidad inmunogénica de un antígeno y una cantidad mejoradora de la inmunidad de un inhibidor de IAP para uso de acuerdo con la reivindicación 14; una cantidad terapéuticamente eficaz de un inhibidor de IAP y una cantidad inmunogénica de un antígeno para uso de acuerdo con cualquiera de las reivindicaciones 15 o 20; un uso ex vivo de acuerdo con la reivindicación 21, o un kit de acuerdo con la reivindicación 12, en el que el antígeno comprende un antígeno presente en una célula de cáncer; una célula cancerosa; un fragmento de célula cancerosa; o un antígeno tumoral.
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US5394708P | 2008-05-16 | 2008-05-16 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2882855T3 true ES2882855T3 (es) | 2021-12-02 |
Family
ID=40823320
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES13178264T Active ES2882855T3 (es) | 2008-05-16 | 2009-05-14 | Inmunomodulación por inhibidores de IAP |
| ES09747530T Active ES2791957T3 (es) | 2008-05-16 | 2009-05-14 | Inmunomodulación mediante inhibidores de IAP |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES09747530T Active ES2791957T3 (es) | 2008-05-16 | 2009-05-14 | Inmunomodulación mediante inhibidores de IAP |
Country Status (17)
| Country | Link |
|---|---|
| US (4) | US9750729B2 (es) |
| EP (3) | EP2698158B1 (es) |
| JP (3) | JP5779091B2 (es) |
| KR (1) | KR20110022608A (es) |
| CN (1) | CN102099035A (es) |
| AU (1) | AU2009246347A1 (es) |
| BR (1) | BRPI0912692A2 (es) |
| CA (1) | CA2724720A1 (es) |
| CL (1) | CL2009001195A1 (es) |
| EA (1) | EA201071316A1 (es) |
| ES (2) | ES2882855T3 (es) |
| IL (1) | IL209203A0 (es) |
| MA (1) | MA32388B1 (es) |
| MX (1) | MX2010012231A (es) |
| TW (1) | TW201006834A (es) |
| WO (1) | WO2009140447A1 (es) |
| ZA (1) | ZA201008176B (es) |
Families Citing this family (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1883627B1 (en) | 2005-05-18 | 2018-04-18 | Pharmascience Inc. | Bir domain binding compounds |
| KR20080067357A (ko) | 2005-10-25 | 2008-07-18 | 에게라 쎄라퓨틱스 인코포레이티드 | Iap bir 도메인 결합 화합물 |
| CA2724720A1 (en) * | 2008-05-16 | 2009-11-19 | Novartis Ag | Immunomodulation by iap inhibitors |
| JP4995211B2 (ja) * | 2008-09-29 | 2012-08-08 | キヤノン株式会社 | 電子写真画像形成装置 |
| SG182724A1 (en) | 2010-02-12 | 2012-08-30 | Pharmascience Inc | Iap bir domain binding compounds |
| EP3013329B1 (en) * | 2013-06-25 | 2020-08-05 | The Walter and Eliza Hall Institute of Medical Research | Smac mimetics for the treatment of persistent intracellular hbv infection |
| US10441654B2 (en) | 2014-01-24 | 2019-10-15 | Children's Hospital Of Eastern Ontario Research Institute Inc. | SMC combination therapy for the treatment of cancer |
| JP2019514878A (ja) * | 2016-04-20 | 2019-06-06 | グラクソスミスクライン、インテレクチュアル、プロパティー、ディベロップメント、リミテッドGlaxosmithkline Intellectual Property Development Limited | Ripk2阻害剤を含むコンジュゲート |
| CN106496213B (zh) * | 2016-09-30 | 2019-08-20 | 东南大学 | Lcl161前药及其制备方法和应用 |
| WO2020027225A1 (ja) * | 2018-07-31 | 2020-02-06 | ファイメクス株式会社 | 複素環化合物 |
| CN113453678A (zh) | 2018-11-26 | 2021-09-28 | 德彪药业国际股份公司 | Hiv感染的联合治疗 |
| WO2021058794A1 (en) | 2019-09-25 | 2021-04-01 | Debiopharm International S.A. | Dosing regimens for treatment of patients with locally advanced squamous cell carcinoma |
Family Cites Families (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2610934B1 (fr) | 1987-02-13 | 1989-05-05 | Adir | Nouveaux derives peptidiques a structure polycyclique azotee, leur procede de preparation et les compositions pharmaceutiques qui les contiennent |
| US6133437A (en) * | 1997-02-13 | 2000-10-17 | Apoptogen, Inc. | Modulation of IAPs for the treatment of proliferative diseases |
| PT1618130E (pt) * | 2003-04-11 | 2013-07-04 | Survac Aps | Vacina terapêutica contra o cancro |
| EP1711515A2 (en) * | 2004-02-04 | 2006-10-18 | Vertex Pharmaceuticals Incorporated | Inhibitors of serine proteases, particularly hcv ns3-ns4a protease |
| US7309792B2 (en) * | 2004-03-01 | 2007-12-18 | Board Of Regents, The University Of Texas System | Dimeric small molecule potentiators of apoptosis |
| AU2005228950B2 (en) * | 2004-03-23 | 2012-02-02 | Genentech, Inc. | Azabicyclo-octane inhibitors of IAP |
| RS52545B (sr) * | 2004-04-07 | 2013-04-30 | Novartis Ag | Inhibitori protein apoptoze (iap) |
| KR100841811B1 (ko) | 2004-05-02 | 2008-06-26 | 가부시키가이샤 세가 | 게임 시스템, 게임 시스템의 제어 방법 및 컴퓨터 판독가능 기록 매체 |
| PL1851200T3 (pl) | 2005-02-25 | 2014-06-30 | Tetralogic Pharm Corp | Dimeryczne inhibitory IAP |
| ES2684120T3 (es) | 2005-12-20 | 2018-10-01 | Novartis Ag | Combinación de un inhibidor de IAP y un taxano |
| US20100056495A1 (en) * | 2006-07-24 | 2010-03-04 | Tetralogic Pharmaceuticals Corporation | Dimeric iap inhibitors |
| PE20110218A1 (es) * | 2006-08-02 | 2011-04-01 | Novartis Ag | DERIVADOS DE 2-OXO-ETIL-AMINO-PROPIONAMIDA-PIRROLIDIN-2-IL-SUSTITUIDOS COMO INHIBIDORES DEL ENLACE DE LA PROTEINA Smac AL INHIBIDOR DE LA PROTEINA DE APOPTOSIS |
| RU2009117701A (ru) * | 2006-10-12 | 2010-11-20 | Новартис АГ (CH) | Производные пирролидина в качестве ингибиторов iap |
| WO2008057172A2 (en) * | 2006-10-19 | 2008-05-15 | Novartis Ag | Organic compounds |
| PT2089024E (pt) * | 2006-11-28 | 2011-08-31 | Novartis Ag | Combinação de inibidores de iap e inibidores de flt3 |
| EP2126188A1 (en) | 2006-12-26 | 2009-12-02 | Arçelik Anonim Sirketi | A washer / dryer with output from humidity sensor selectively input to control unit |
| WO2008109057A1 (en) | 2007-03-02 | 2008-09-12 | Dana-Farber Cancer Institute, Inc. | Organic compounds and their uses |
| CA2724720A1 (en) * | 2008-05-16 | 2009-11-19 | Novartis Ag | Immunomodulation by iap inhibitors |
-
2009
- 2009-05-14 CA CA2724720A patent/CA2724720A1/en not_active Abandoned
- 2009-05-14 CN CN2009801276872A patent/CN102099035A/zh active Pending
- 2009-05-14 BR BRPI0912692A patent/BRPI0912692A2/pt not_active IP Right Cessation
- 2009-05-14 EP EP13178264.1A patent/EP2698158B1/en active Active
- 2009-05-14 EP EP09747530.5A patent/EP2296650B1/en active Active
- 2009-05-14 US US12/992,631 patent/US9750729B2/en active Active
- 2009-05-14 JP JP2011509678A patent/JP5779091B2/ja active Active
- 2009-05-14 MX MX2010012231A patent/MX2010012231A/es not_active Application Discontinuation
- 2009-05-14 AU AU2009246347A patent/AU2009246347A1/en not_active Abandoned
- 2009-05-14 EA EA201071316A patent/EA201071316A1/ru unknown
- 2009-05-14 KR KR1020107028375A patent/KR20110022608A/ko not_active Withdrawn
- 2009-05-14 EP EP20159523.8A patent/EP3701947A1/en active Pending
- 2009-05-14 WO PCT/US2009/043874 patent/WO2009140447A1/en not_active Ceased
- 2009-05-14 ES ES13178264T patent/ES2882855T3/es active Active
- 2009-05-14 ES ES09747530T patent/ES2791957T3/es active Active
- 2009-05-15 CL CL2009001195A patent/CL2009001195A1/es unknown
- 2009-05-15 TW TW098116299A patent/TW201006834A/zh unknown
-
2010
- 2010-11-09 IL IL209203A patent/IL209203A0/en unknown
- 2010-11-15 ZA ZA2010/08176A patent/ZA201008176B/en unknown
- 2010-12-08 MA MA33406A patent/MA32388B1/fr unknown
-
2015
- 2015-03-02 JP JP2015040113A patent/JP5986655B2/ja active Active
- 2015-12-03 JP JP2015236482A patent/JP6030739B2/ja active Active
-
2017
- 2017-08-14 US US15/675,987 patent/US10786491B2/en active Active
-
2020
- 2020-07-13 US US16/926,930 patent/US11382905B2/en active Active
-
2022
- 2022-06-06 US US17/832,911 patent/US20220296581A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| JP5779091B2 (ja) | 2015-09-16 |
| MA32388B1 (fr) | 2011-06-01 |
| TW201006834A (en) | 2010-02-16 |
| EP2698158A1 (en) | 2014-02-19 |
| EP2698158B1 (en) | 2021-06-30 |
| EP2296650A1 (en) | 2011-03-23 |
| US20170368047A1 (en) | 2017-12-28 |
| US9750729B2 (en) | 2017-09-05 |
| CA2724720A1 (en) | 2009-11-19 |
| US20110135691A1 (en) | 2011-06-09 |
| JP5986655B2 (ja) | 2016-09-06 |
| US20220296581A1 (en) | 2022-09-22 |
| EP2296650B1 (en) | 2020-05-06 |
| CN102099035A (zh) | 2011-06-15 |
| US11382905B2 (en) | 2022-07-12 |
| JP2015129170A (ja) | 2015-07-16 |
| KR20110022608A (ko) | 2011-03-07 |
| US20200345714A1 (en) | 2020-11-05 |
| JP6030739B2 (ja) | 2016-11-24 |
| JP2011524339A (ja) | 2011-09-01 |
| CL2009001195A1 (es) | 2010-06-11 |
| US10786491B2 (en) | 2020-09-29 |
| AU2009246347A1 (en) | 2009-11-19 |
| WO2009140447A1 (en) | 2009-11-19 |
| ES2791957T3 (es) | 2020-11-06 |
| MX2010012231A (es) | 2011-02-18 |
| JP2016094429A (ja) | 2016-05-26 |
| BRPI0912692A2 (pt) | 2017-03-21 |
| IL209203A0 (en) | 2011-01-31 |
| ZA201008176B (en) | 2011-08-31 |
| EA201071316A1 (ru) | 2011-06-30 |
| EP3701947A1 (en) | 2020-09-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2882855T3 (es) | Inmunomodulación por inhibidores de IAP | |
| ES3039485T3 (en) | Vaccine adjuvant formulation | |
| JP6769976B2 (ja) | ピリミジン化合物 | |
| ES2625944T3 (es) | Inhibidores de tirosina cinasa de Bruton | |
| ES2596180T3 (es) | Tratamiento de enfermedades mediadas por los linfocitos T | |
| ES2939836T3 (es) | Conjugados de moléculas de unión celular con agentes citotóxicos | |
| ES2800026T3 (es) | Tratamiento de enfermedades inmunitarias e inflamatorias | |
| ES2256955T3 (es) | Composicion que contiene alfa-glicosilceramids, para potenciar la inmunogenicidad. | |
| KR20240004476A (ko) | 암 치료를 위한 병용 요법 | |
| JP2019196380A (ja) | Mhc−iの発現を増加させるためのクルクフェノール化合物 | |
| AU2009248039A1 (en) | Multiple myeloma treatments | |
| CA3228242A1 (en) | Compositions and methods for reducing immune intolerance and treating autoimmune disorders | |
| KR20260018046A (ko) | 이전의 면역 관문 억제제 노출 이력이 있는 대상체의 암 치료 방법 | |
| TW202340142A (zh) | Gcl抑制劑 | |
| WO2019108788A1 (en) | Biguanide compositions and methods related thereto |