ES2760003T3 - Compuestos antiproliferativos y procedimientos de uso de los mismos - Google Patents
Compuestos antiproliferativos y procedimientos de uso de los mismos Download PDFInfo
- Publication number
- ES2760003T3 ES2760003T3 ES15739485T ES15739485T ES2760003T3 ES 2760003 T3 ES2760003 T3 ES 2760003T3 ES 15739485 T ES15739485 T ES 15739485T ES 15739485 T ES15739485 T ES 15739485T ES 2760003 T3 ES2760003 T3 ES 2760003T3
- Authority
- ES
- Spain
- Prior art keywords
- methyl
- oxoisoindolin
- dioxopiperidin
- difluoro
- acetamide
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 150000001875 compounds Chemical class 0.000 title claims abstract description 427
- 238000000034 method Methods 0.000 title claims description 122
- 230000001028 anti-proliverative effect Effects 0.000 title description 3
- 239000000203 mixture Substances 0.000 claims abstract description 259
- 125000000217 alkyl group Chemical group 0.000 claims abstract description 201
- 150000003839 salts Chemical class 0.000 claims abstract description 160
- 239000012453 solvate Substances 0.000 claims abstract description 143
- 229910052739 hydrogen Inorganic materials 0.000 claims abstract description 139
- 239000001257 hydrogen Substances 0.000 claims abstract description 139
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 claims abstract description 138
- 125000001188 haloalkyl group Chemical group 0.000 claims abstract description 132
- 239000013078 crystal Substances 0.000 claims abstract description 88
- 125000005843 halogen group Chemical group 0.000 claims abstract description 86
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims abstract description 73
- 125000002947 alkylene group Chemical group 0.000 claims abstract description 53
- 125000000623 heterocyclic group Chemical group 0.000 claims abstract description 48
- 125000002768 hydroxyalkyl group Chemical group 0.000 claims abstract description 46
- 229910052757 nitrogen Inorganic materials 0.000 claims abstract description 37
- 125000004450 alkenylene group Chemical group 0.000 claims abstract description 35
- 229910052760 oxygen Inorganic materials 0.000 claims abstract description 35
- 125000004433 nitrogen atom Chemical group N* 0.000 claims abstract description 34
- 229910052717 sulfur Inorganic materials 0.000 claims abstract description 33
- 125000001072 heteroaryl group Chemical group 0.000 claims abstract description 32
- 125000001424 substituent group Chemical group 0.000 claims abstract description 31
- 125000003118 aryl group Chemical group 0.000 claims abstract description 23
- 125000004183 alkoxy alkyl group Chemical group 0.000 claims abstract description 20
- 125000000753 cycloalkyl group Chemical group 0.000 claims abstract description 10
- 125000004043 oxo group Chemical group O=* 0.000 claims abstract description 8
- 125000003545 alkoxy group Chemical group 0.000 claims abstract description 7
- 125000004415 heterocyclylalkyl group Chemical group 0.000 claims abstract description 7
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims abstract description 7
- 206010028980 Neoplasm Diseases 0.000 claims description 160
- -1 chloro, methyl Chemical group 0.000 claims description 146
- 201000011510 cancer Diseases 0.000 claims description 83
- 238000011282 treatment Methods 0.000 claims description 62
- 208000031261 Acute myeloid leukaemia Diseases 0.000 claims description 52
- 208000033776 Myeloid Acute Leukemia Diseases 0.000 claims description 51
- 208000032839 leukemia Diseases 0.000 claims description 51
- 239000003814 drug Substances 0.000 claims description 46
- 239000013543 active substance Substances 0.000 claims description 31
- 238000002560 therapeutic procedure Methods 0.000 claims description 31
- 208000006664 Precursor Cell Lymphoblastic Leukemia-Lymphoma Diseases 0.000 claims description 27
- 208000024893 Acute lymphoblastic leukemia Diseases 0.000 claims description 26
- 208000014697 Acute lymphocytic leukaemia Diseases 0.000 claims description 25
- 239000003795 chemical substances by application Substances 0.000 claims description 24
- 230000000306 recurrent effect Effects 0.000 claims description 24
- DLFVBJFMPXGRIB-UHFFFAOYSA-N Acetamide Chemical compound CC(N)=O DLFVBJFMPXGRIB-UHFFFAOYSA-N 0.000 claims description 22
- 239000002246 antineoplastic agent Substances 0.000 claims description 22
- 208000032791 BCR-ABL1 positive chronic myelogenous leukemia Diseases 0.000 claims description 19
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 19
- 208000010833 Chronic myeloid leukaemia Diseases 0.000 claims description 16
- 208000033761 Myelogenous Chronic BCR-ABL Positive Leukemia Diseases 0.000 claims description 16
- 230000001225 therapeutic effect Effects 0.000 claims description 15
- 208000031422 Lymphocytic Chronic B-Cell Leukemia Diseases 0.000 claims description 13
- 102000004127 Cytokines Human genes 0.000 claims description 11
- 108090000695 Cytokines Proteins 0.000 claims description 11
- 238000011443 conventional therapy Methods 0.000 claims description 10
- 208000010839 B-cell chronic lymphocytic leukemia Diseases 0.000 claims description 9
- 125000001316 cycloalkyl alkyl group Chemical group 0.000 claims description 9
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 9
- 208000032852 chronic lymphocytic leukemia Diseases 0.000 claims description 8
- 125000001153 fluoro group Chemical group F* 0.000 claims description 7
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 claims description 6
- 125000004076 pyridyl group Chemical group 0.000 claims description 6
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 5
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 claims description 5
- 241000124008 Mammalia Species 0.000 claims description 4
- 239000000427 antigen Substances 0.000 claims description 4
- 102000036639 antigens Human genes 0.000 claims description 4
- 108091007433 antigens Proteins 0.000 claims description 4
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 claims description 4
- 229940111134 coxibs Drugs 0.000 claims description 4
- 239000003255 cyclooxygenase 2 inhibitor Substances 0.000 claims description 4
- 230000003319 supportive effect Effects 0.000 claims description 4
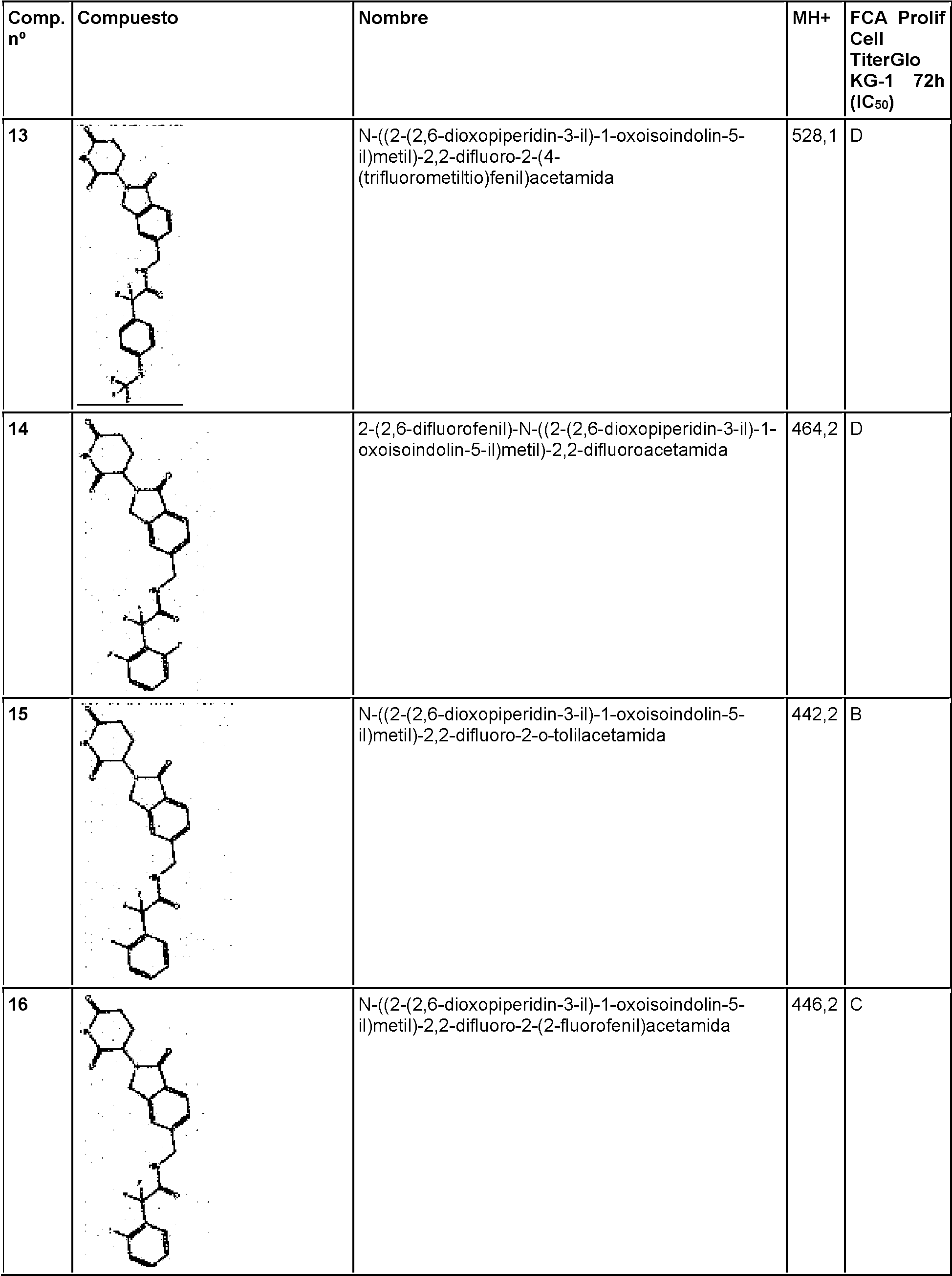
- AMQUQDRMUDITED-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(4-methoxyphenyl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC=C(C=C1)OC)(F)F)=O)=O)=O AMQUQDRMUDITED-UHFFFAOYSA-N 0.000 claims description 3
- 230000003115 biocidal effect Effects 0.000 claims description 3
- 239000003018 immunosuppressive agent Substances 0.000 claims description 3
- 229940125721 immunosuppressive agent Drugs 0.000 claims description 3
- PLAOBWJLOZVURK-UHFFFAOYSA-N 2-(1-benzyl-6-oxopyridin-3-yl)-N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoroacetamide Chemical compound FC(F)(C(=O)NCC1=CC2=C(C=C1)C(=O)N(C2)C1CCC(=O)NC1=O)C1=CN(CC2=CC=CC=C2)C(=O)C=C1 PLAOBWJLOZVURK-UHFFFAOYSA-N 0.000 claims description 2
- QQONSQRPXGBPLY-UHFFFAOYSA-N 2-(2,4-difluorophenyl)-N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoroacetamide Chemical compound FC1=C(C=CC(=C1)F)C(C(=O)NCC=1C=C2CN(C(C2=CC=1)=O)C1C(NC(CC1)=O)=O)(F)F QQONSQRPXGBPLY-UHFFFAOYSA-N 0.000 claims description 2
- PJGSJRDAOLRPTF-UHFFFAOYSA-N 2-(2,6-difluorophenyl)-N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoroacetamide Chemical compound FC1=C(C(=CC=C1)F)C(C(=O)NCC=1C=C2CN(C(C2=CC=1)=O)C1C(NC(CC1)=O)=O)(F)F PJGSJRDAOLRPTF-UHFFFAOYSA-N 0.000 claims description 2
- AIHKQMOGDSBXOL-UHFFFAOYSA-N 2-(2-aminopyrimidin-4-yl)-N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoroacetamide Chemical compound NC1=NC=CC(=N1)C(C(=O)NCC=1C=C2CN(C(C2=CC=1)=O)C1C(NC(CC1)=O)=O)(F)F AIHKQMOGDSBXOL-UHFFFAOYSA-N 0.000 claims description 2
- ZHBWCLQDPRTPKV-UHFFFAOYSA-N 2-(3,4-difluorophenyl)-N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoroacetamide Chemical compound FC=1C=C(C=CC=1F)C(C(=O)NCC=1C=C2CN(C(C2=CC=1)=O)C1C(NC(CC1)=O)=O)(F)F ZHBWCLQDPRTPKV-UHFFFAOYSA-N 0.000 claims description 2
- NYOULAILGSKVMS-UHFFFAOYSA-N 2-(3-chloro-4-methylphenyl)-N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoroacetamide Chemical compound ClC=1C=C(C=CC=1C)C(C(=O)NCC=1C=C2CN(C(C2=CC=1)=O)C1C(NC(CC1)=O)=O)(F)F NYOULAILGSKVMS-UHFFFAOYSA-N 0.000 claims description 2
- UXOHQYKAUVRSGR-UHFFFAOYSA-N 2-(4-bromophenyl)-N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoroacetamide Chemical compound BrC1=CC=C(C=C1)C(C(=O)NCC=1C=C2CN(C(C2=CC=1)=O)C1C(NC(CC1)=O)=O)(F)F UXOHQYKAUVRSGR-UHFFFAOYSA-N 0.000 claims description 2
- PBXOPAYJJVDLNM-UHFFFAOYSA-N 2-(4-tert-butylphenyl)-N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoroacetamide Chemical compound C(C)(C)(C)C1=CC=C(C=C1)C(C(=O)NCC=1C=C2CN(C(C2=CC=1)=O)C1C(NC(CC1)=O)=O)(F)F PBXOPAYJJVDLNM-UHFFFAOYSA-N 0.000 claims description 2
- KHOFGXWGIVOQDL-UHFFFAOYSA-N 2-(5-bromopyridin-2-yl)-N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoroacetamide Chemical compound BrC=1C=CC(=NC=1)C(C(=O)NCC=1C=C2CN(C(C2=CC=1)=O)C1C(NC(CC1)=O)=O)(F)F KHOFGXWGIVOQDL-UHFFFAOYSA-N 0.000 claims description 2
- GMHBAETVCYHAFR-UHFFFAOYSA-N 2-(5-tert-butylpyridin-2-yl)-N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoroacetamide Chemical compound C(C)(C)(C)C=1C=CC(=NC=1)C(C(=O)NCC=1C=C2CN(C(C2=CC=1)=O)C1C(NC(CC1)=O)=O)(F)F GMHBAETVCYHAFR-UHFFFAOYSA-N 0.000 claims description 2
- BZPFVYGZLNTSQB-UHFFFAOYSA-N 2-(trifluoromethoxy)acetamide Chemical compound NC(=O)COC(F)(F)F BZPFVYGZLNTSQB-UHFFFAOYSA-N 0.000 claims description 2
- IIEPAZNFJBYJHI-UHFFFAOYSA-N 2-[3-(dimethylamino)phenyl]-N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoroacetamide Chemical compound CN(C=1C=C(C=CC=1)C(C(=O)NCC=1C=C2CN(C(C2=CC=1)=O)C1C(NC(CC1)=O)=O)(F)F)C IIEPAZNFJBYJHI-UHFFFAOYSA-N 0.000 claims description 2
- ZTSSGBBTFIIQFW-UHFFFAOYSA-N 2-[3-[2-(4,4-difluoropiperidin-1-yl)ethoxy]phenyl]-N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoroacetamide Chemical compound FC1(CCN(CC1)CCOC=1C=C(C=CC=1)C(C(=O)NCC=1C=C2CN(C(C2=CC=1)=O)C1C(NC(CC1)=O)=O)(F)F)F ZTSSGBBTFIIQFW-UHFFFAOYSA-N 0.000 claims description 2
- VZXULRDQFRXODC-UHFFFAOYSA-N 2-[3-[2-(dimethylamino)ethoxy]phenyl]-N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoroacetamide Chemical compound CN(CCOC=1C=C(C=CC=1)C(C(=O)NCC=1C=C2CN(C(C2=CC=1)=O)C1C(NC(CC1)=O)=O)(F)F)C VZXULRDQFRXODC-UHFFFAOYSA-N 0.000 claims description 2
- FAAWXONVJKBBDX-UHFFFAOYSA-N 2-[3-bromo-4-(trifluoromethoxy)phenyl]-N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoroacetamide Chemical compound BrC=1C=C(C=CC=1OC(F)(F)F)C(C(=O)NCC=1C=C2CN(C(C2=CC=1)=O)C1C(NC(CC1)=O)=O)(F)F FAAWXONVJKBBDX-UHFFFAOYSA-N 0.000 claims description 2
- 108010002386 Interleukin-3 Proteins 0.000 claims description 2
- 102100039064 Interleukin-3 Human genes 0.000 claims description 2
- WOGJRNKJUQEEBB-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(1-methyl-6-oxopyridin-3-yl)acetamide Chemical compound CN1C=C(C=CC1=O)C(F)(F)C(=O)NCC1=CC2=C(C=C1)C(=O)N(C2)C1CCC(=O)NC1=O WOGJRNKJUQEEBB-UHFFFAOYSA-N 0.000 claims description 2
- VZKNLAMLJWIKET-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(2-fluoro-4-propan-2-yloxyphenyl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=C(C=C(C=C1)OC(C)C)F)(F)F)=O)=O)=O VZKNLAMLJWIKET-UHFFFAOYSA-N 0.000 claims description 2
- HWTTYVZOLNGISA-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(2-fluorophenyl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=C(C=CC=C1)F)(F)F)=O)=O)=O HWTTYVZOLNGISA-UHFFFAOYSA-N 0.000 claims description 2
- LYPGTEQCLOXQCX-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(2-methoxyphenyl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=C(C=CC=C1)OC)(F)F)=O)=O)=O LYPGTEQCLOXQCX-UHFFFAOYSA-N 0.000 claims description 2
- YSIRDUGLLWZOOG-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(2-methyl-4-propan-2-yloxyphenyl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=C(C=C(C=C1)OC(C)C)C)(F)F)=O)=O)=O YSIRDUGLLWZOOG-UHFFFAOYSA-N 0.000 claims description 2
- HEHFPFWQZAJOPM-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(2-methylphenyl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=C(C=CC=C1)C)(F)F)=O)=O)=O HEHFPFWQZAJOPM-UHFFFAOYSA-N 0.000 claims description 2
- WUFZNZYZAXHCPN-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(2-propan-2-yloxyphenyl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=C(C=CC=C1)OC(C)C)(F)F)=O)=O)=O WUFZNZYZAXHCPN-UHFFFAOYSA-N 0.000 claims description 2
- SOBWPOFPIRJNGF-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(3-fluoro-2-methylphenyl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=C(C(=CC=C1)F)C)(F)F)=O)=O)=O SOBWPOFPIRJNGF-UHFFFAOYSA-N 0.000 claims description 2
- NUFAWRNBHUWJFG-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(3-fluoro-4-propan-2-yloxyphenyl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC(=C(C=C1)OC(C)C)F)(F)F)=O)=O)=O NUFAWRNBHUWJFG-UHFFFAOYSA-N 0.000 claims description 2
- SBVXMVCDPWXTDN-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(3-fluorophenyl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC(=CC=C1)F)(F)F)=O)=O)=O SBVXMVCDPWXTDN-UHFFFAOYSA-N 0.000 claims description 2
- VMHLWRWULCOCNW-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(3-hydroxyphenyl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC(=CC=C1)O)(F)F)=O)=O)=O VMHLWRWULCOCNW-UHFFFAOYSA-N 0.000 claims description 2
- BFORLTWCVIRSQY-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(3-methyl-4-propan-2-yloxyphenyl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC(=C(C=C1)OC(C)C)C)(F)F)=O)=O)=O BFORLTWCVIRSQY-UHFFFAOYSA-N 0.000 claims description 2
- OKPHSMZSHNDXNN-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(3-methylphenyl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C=1C=C(C=CC=1)C)(F)F)=O)=O)=O OKPHSMZSHNDXNN-UHFFFAOYSA-N 0.000 claims description 2
- FLHSVDCZBFBMDD-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(3-methylpyridin-2-yl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=NC=CC=C1C)(F)F)=O)=O)=O FLHSVDCZBFBMDD-UHFFFAOYSA-N 0.000 claims description 2
- SKXBLDSEPZGVHM-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(3-methylsulfonylphenyl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC(=CC=C1)S(=O)(=O)C)(F)F)=O)=O)=O SKXBLDSEPZGVHM-UHFFFAOYSA-N 0.000 claims description 2
- FCUAFKOCULPWBR-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(3-piperidin-1-ylphenyl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC(=CC=C1)N1CCCCC1)(F)F)=O)=O)=O FCUAFKOCULPWBR-UHFFFAOYSA-N 0.000 claims description 2
- LEKLBINUIFRTJO-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(4-fluoro-2-methylphenyl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=C(C=C(C=C1)F)C)(F)F)=O)=O)=O LEKLBINUIFRTJO-UHFFFAOYSA-N 0.000 claims description 2
- PSIXNTKRSHRNNV-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(4-fluoro-2-propan-2-yloxyphenyl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=C(C=C(C=C1)F)OC(C)C)(F)F)=O)=O)=O PSIXNTKRSHRNNV-UHFFFAOYSA-N 0.000 claims description 2
- DOCFCULFTLNCRC-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(4-fluorophenyl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC=C(C=C1)F)(F)F)=O)=O)=O DOCFCULFTLNCRC-UHFFFAOYSA-N 0.000 claims description 2
- PWUTXKFALAYCGF-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(4-methylphenyl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC=C(C=C1)C)(F)F)=O)=O)=O PWUTXKFALAYCGF-UHFFFAOYSA-N 0.000 claims description 2
- YNEFVZUMWDLSFV-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(4-methylsulfonylphenyl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC=C(C=C1)S(=O)(=O)C)(F)F)=O)=O)=O YNEFVZUMWDLSFV-UHFFFAOYSA-N 0.000 claims description 2
- ZZKILESADYZFJV-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(4-propan-2-yloxyphenyl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC=C(C=C1)OC(C)C)(F)F)=O)=O)=O ZZKILESADYZFJV-UHFFFAOYSA-N 0.000 claims description 2
- RYKJGMYMKGWRQA-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(4-propan-2-ylphenyl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC=C(C=C1)C(C)C)(F)F)=O)=O)=O RYKJGMYMKGWRQA-UHFFFAOYSA-N 0.000 claims description 2
- QAXYIRJMJNSMJY-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(5-fluoropyridin-2-yl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=NC=C(C=C1)F)(F)F)=O)=O)=O QAXYIRJMJNSMJY-UHFFFAOYSA-N 0.000 claims description 2
- QAENVAZAYPDROH-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(5-methoxypyridin-2-yl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=NC=C(C=C1)OC)(F)F)=O)=O)=O QAENVAZAYPDROH-UHFFFAOYSA-N 0.000 claims description 2
- GRFBTHLLUKYPJX-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(5-methylpyridin-2-yl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=NC=C(C=C1)C)(F)F)=O)=O)=O GRFBTHLLUKYPJX-UHFFFAOYSA-N 0.000 claims description 2
- PRTMHZHJOHIYDF-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(5-propan-2-yloxypyridin-2-yl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=NC=C(C=C1)OC(C)C)(F)F)=O)=O)=O PRTMHZHJOHIYDF-UHFFFAOYSA-N 0.000 claims description 2
- HEVKLJWTQBESTQ-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(5-propan-2-ylpyridin-2-yl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=NC=C(C=C1)C(C)C)(F)F)=O)=O)=O HEVKLJWTQBESTQ-UHFFFAOYSA-N 0.000 claims description 2
- CGKVNGHZPREKHG-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[2-(2-hydroxyethoxy)phenyl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=C(C=CC=C1)OCCO)(F)F)=O)=O)=O CGKVNGHZPREKHG-UHFFFAOYSA-N 0.000 claims description 2
- TUTCXLAAKLEFBL-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[2-(2-methoxyethoxy)phenyl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=C(C=CC=C1)OCCOC)(F)F)=O)=O)=O TUTCXLAAKLEFBL-UHFFFAOYSA-N 0.000 claims description 2
- ZWODPKHPHXYYJQ-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[2-(methylamino)phenyl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=C(C=CC=C1)NC)(F)F)=O)=O)=O ZWODPKHPHXYYJQ-UHFFFAOYSA-N 0.000 claims description 2
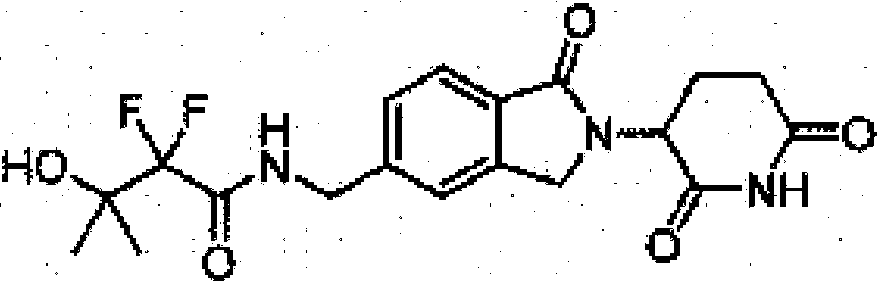
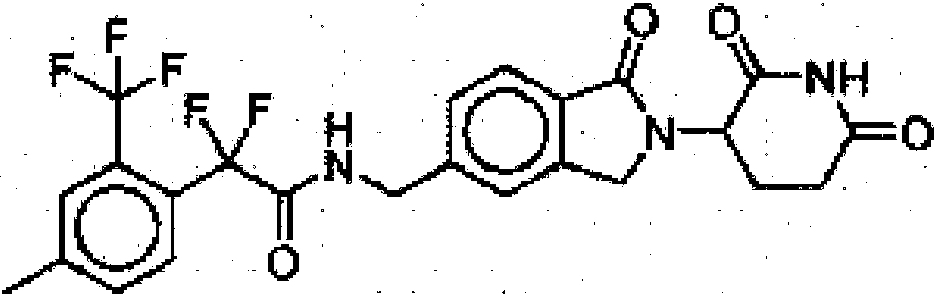
- FGUPOYDQMQRCLA-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[2-(trifluoromethyl)phenyl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=C(C=CC=C1)C(F)(F)F)(F)F)=O)=O)=O FGUPOYDQMQRCLA-UHFFFAOYSA-N 0.000 claims description 2
- JQBQFDRIJYALAO-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[2-fluoro-4-(trifluoromethoxy)phenyl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=C(C=C(C=C1)OC(F)(F)F)F)(F)F)=O)=O)=O JQBQFDRIJYALAO-UHFFFAOYSA-N 0.000 claims description 2
- RKIADEYYBGBGDM-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[2-methyl-4-(trifluoromethoxy)phenyl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=C(C=C(C=C1)OC(F)(F)F)C)(F)F)=O)=O)=O RKIADEYYBGBGDM-UHFFFAOYSA-N 0.000 claims description 2
- NBCDJJHARBDWLT-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[3-(2-hydroxyethoxy)phenyl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC(=CC=C1)OCCO)(F)F)=O)=O)=O NBCDJJHARBDWLT-UHFFFAOYSA-N 0.000 claims description 2
- IQVGIYKIPNVLDX-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[3-(2-hydroxyethyl)phenyl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC(=CC=C1)CCO)(F)F)=O)=O)=O IQVGIYKIPNVLDX-UHFFFAOYSA-N 0.000 claims description 2
- RJQYMGWMQORYNG-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[3-(2-methoxyethoxy)phenyl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC(=CC=C1)OCCOC)(F)F)=O)=O)=O RJQYMGWMQORYNG-UHFFFAOYSA-N 0.000 claims description 2
- YVTXDRLLWAJHRM-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[3-(2-methylsulfonylethoxy)phenyl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC(=CC=C1)OCCS(=O)(=O)C)(F)F)=O)=O)=O YVTXDRLLWAJHRM-UHFFFAOYSA-N 0.000 claims description 2
- DYXNCUJYFNQGQA-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[3-(2-piperidin-1-ylethoxy)phenyl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC(=CC=C1)OCCN1CCCCC1)(F)F)=O)=O)=O DYXNCUJYFNQGQA-UHFFFAOYSA-N 0.000 claims description 2
- MZMSBYKAFAQSSW-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[3-(2-propan-2-yloxyethoxy)phenyl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC(=CC=C1)OCCOC(C)C)(F)F)=O)=O)=O MZMSBYKAFAQSSW-UHFFFAOYSA-N 0.000 claims description 2
- GRWHSPLWEFAOFL-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[3-(3-methylsulfonylpropyl)phenyl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC(=CC=C1)CCCS(=O)(=O)C)(F)F)=O)=O)=O GRWHSPLWEFAOFL-UHFFFAOYSA-N 0.000 claims description 2
- HKQUNDIITVPWEA-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[3-(morpholin-4-ylmethyl)phenyl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC(=CC=C1)CN1CCOCC1)(F)F)=O)=O)=O HKQUNDIITVPWEA-UHFFFAOYSA-N 0.000 claims description 2
- LBHWADWDSWEHSU-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[3-(trifluoromethyl)pyridin-2-yl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=NC=CC=C1C(F)(F)F)(F)F)=O)=O)=O LBHWADWDSWEHSU-UHFFFAOYSA-N 0.000 claims description 2
- ISDGDBJEKQUMBM-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[3-[(4-methylpiperazin-1-yl)methyl]phenyl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC(=CC=C1)CN1CCN(CC1)C)(F)F)=O)=O)=O ISDGDBJEKQUMBM-UHFFFAOYSA-N 0.000 claims description 2
- KKTJMTHRCJXXOJ-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[3-[2-(2-methoxyethoxy)ethoxy]phenyl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC(=CC=C1)OCCOCCOC)(F)F)=O)=O)=O KKTJMTHRCJXXOJ-UHFFFAOYSA-N 0.000 claims description 2
- KQDJCLOQMKMRBG-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[3-methyl-4-(trifluoromethoxy)phenyl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC(=C(C=C1)OC(F)(F)F)C)(F)F)=O)=O)=O KQDJCLOQMKMRBG-UHFFFAOYSA-N 0.000 claims description 2
- VSEXZUHNKMCCHH-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[4-(2-fluoropropan-2-yl)phenyl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC=C(C=C1)C(C)(C)F)(F)F)=O)=O)=O VSEXZUHNKMCCHH-UHFFFAOYSA-N 0.000 claims description 2
- IDTPIHJNADCWNA-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[4-(2-methoxyethoxy)phenyl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC=C(C=C1)OCCOC)(F)F)=O)=O)=O IDTPIHJNADCWNA-UHFFFAOYSA-N 0.000 claims description 2
- UGVHSQJMBSIJLL-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[4-(4-fluorophenyl)phenyl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC=C(C=C1)C1=CC=C(C=C1)F)(F)F)=O)=O)=O UGVHSQJMBSIJLL-UHFFFAOYSA-N 0.000 claims description 2
- MWPYSDVUWHYHGA-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[4-(trifluoromethylsulfanyl)phenyl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC=C(C=C1)SC(F)(F)F)(F)F)=O)=O)=O MWPYSDVUWHYHGA-UHFFFAOYSA-N 0.000 claims description 2
- ZKWXXNYCHCSAHB-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[4-fluoro-2-(trifluoromethoxy)phenyl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=C(C=C(C=C1)F)OC(F)(F)F)(F)F)=O)=O)=O ZKWXXNYCHCSAHB-UHFFFAOYSA-N 0.000 claims description 2
- NCEREZDHAKLJND-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[4-fluoro-2-(trifluoromethyl)phenyl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=C(C=C(C=C1)F)C(F)(F)F)(F)F)=O)=O)=O NCEREZDHAKLJND-UHFFFAOYSA-N 0.000 claims description 2
- SORWFPATQRTPID-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[4-methoxy-2-(trifluoromethyl)phenyl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=C(C=C(C=C1)OC)C(F)(F)F)(F)F)=O)=O)=O SORWFPATQRTPID-UHFFFAOYSA-N 0.000 claims description 2
- GVBWAGDULNKFNC-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[4-methyl-2-(trifluoromethyl)phenyl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=C(C=C(C=C1)C)C(F)(F)F)(F)F)=O)=O)=O GVBWAGDULNKFNC-UHFFFAOYSA-N 0.000 claims description 2
- XWVHRSRMNFRKMT-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[4-propan-2-yloxy-2-(trifluoromethyl)phenyl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=C(C=C(C=C1)OC(C)C)C(F)(F)F)(F)F)=O)=O)=O XWVHRSRMNFRKMT-UHFFFAOYSA-N 0.000 claims description 2
- XGBDIBOYKIRRPQ-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-phenylacetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC=CC=C1)(F)F)=O)=O)=O XGBDIBOYKIRRPQ-UHFFFAOYSA-N 0.000 claims description 2
- JHHPGZRLZCXTNK-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-pyrimidin-4-ylacetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=NC=NC=C1)(F)F)=O)=O)=O JHHPGZRLZCXTNK-UHFFFAOYSA-N 0.000 claims description 2
- CMHLZILDAPBSQE-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2-(2-ethoxy-4-fluorophenyl)-2,2-difluoroacetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(F)(F)C1=C(C=C(C=C1)F)OCC)=O)=O)=O CMHLZILDAPBSQE-UHFFFAOYSA-N 0.000 claims description 2
- ULAJKCWEIRGQLH-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2-(2-ethoxy-5-fluorophenyl)-2,2-difluoroacetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(F)(F)C1=C(C=CC(=C1)F)OCC)=O)=O)=O ULAJKCWEIRGQLH-UHFFFAOYSA-N 0.000 claims description 2
- VMQQMXSTWSGBRB-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2-(2-ethoxy-6-fluorophenyl)-2,2-difluoroacetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(F)(F)C1=C(C=CC=C1F)OCC)=O)=O)=O VMQQMXSTWSGBRB-UHFFFAOYSA-N 0.000 claims description 2
- TWUZTYULRGTTHD-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2-(2-ethoxyphenyl)-2,2-difluoroacetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(F)(F)C1=C(C=CC=C1)OCC)=O)=O)=O TWUZTYULRGTTHD-UHFFFAOYSA-N 0.000 claims description 2
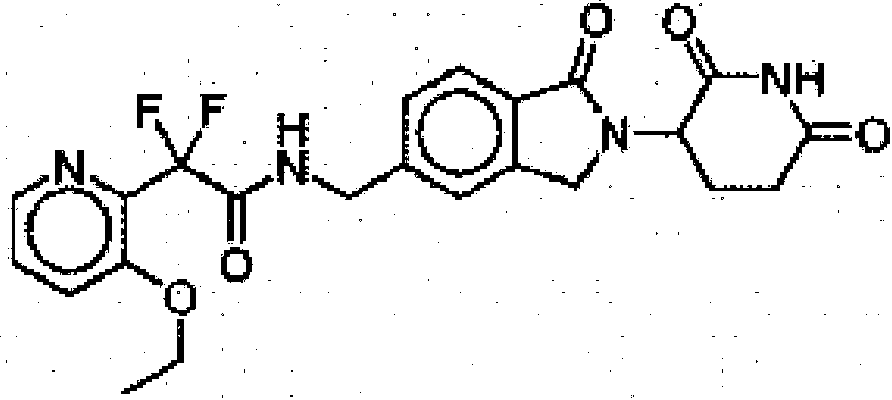
- PSZTVISAVWNYGJ-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2-(3-ethoxypyridin-2-yl)-2,2-difluoroacetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(F)(F)C1=NC=CC=C1OCC)=O)=O)=O PSZTVISAVWNYGJ-UHFFFAOYSA-N 0.000 claims description 2
- 239000003246 corticosteroid Substances 0.000 claims description 2
- XLONUSFDGBQNQO-UHFFFAOYSA-N 2-(3-chlorophenyl)-N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoroacetamide Chemical compound ClC=1C=C(C=CC=1)C(C(=O)NCC=1C=C2CN(C(C2=CC=1)=O)C1C(NC(CC1)=O)=O)(F)F XLONUSFDGBQNQO-UHFFFAOYSA-N 0.000 claims 1
- PWBHUSLMHZLGRN-UHFFFAOYSA-N 2-(4-chlorophenyl)-N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoroacetamide Chemical compound ClC1=CC=C(C=C1)C(C(=O)NCC=1C=C2CN(C(C2=CC=1)=O)C1C(NC(CC1)=O)=O)(F)F PWBHUSLMHZLGRN-UHFFFAOYSA-N 0.000 claims 1
- 239000002955 immunomodulating agent Substances 0.000 claims 1
- 230000002584 immunomodulator Effects 0.000 claims 1
- 229940121354 immunomodulator Drugs 0.000 claims 1
- 125000000325 methylidene group Chemical group [H]C([H])=* 0.000 claims 1
- 125000002950 monocyclic group Chemical group 0.000 abstract description 9
- 235000002639 sodium chloride Nutrition 0.000 description 158
- 150000002431 hydrogen Chemical group 0.000 description 67
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 49
- 201000010099 disease Diseases 0.000 description 36
- 210000004027 cell Anatomy 0.000 description 34
- 230000002354 daily effect Effects 0.000 description 34
- 239000004480 active ingredient Substances 0.000 description 33
- 238000009472 formulation Methods 0.000 description 30
- 229940079593 drug Drugs 0.000 description 29
- 239000000243 solution Substances 0.000 description 29
- 239000002552 dosage form Substances 0.000 description 28
- 206010025323 Lymphomas Diseases 0.000 description 27
- 230000000694 effects Effects 0.000 description 25
- 208000024891 symptom Diseases 0.000 description 25
- 210000003719 b-lymphocyte Anatomy 0.000 description 23
- 239000008194 pharmaceutical composition Substances 0.000 description 21
- 108090000623 proteins and genes Proteins 0.000 description 21
- 210000001744 T-lymphocyte Anatomy 0.000 description 20
- 235000018102 proteins Nutrition 0.000 description 20
- 102000004169 proteins and genes Human genes 0.000 description 20
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 20
- 206010035226 Plasma cell myeloma Diseases 0.000 description 19
- 230000001276 controlling effect Effects 0.000 description 19
- 125000001570 methylene group Chemical group [H]C([H])([*:1])[*:2] 0.000 description 19
- 239000000725 suspension Substances 0.000 description 19
- AOJJSUZBOXZQNB-TZSSRYMLSA-N Doxorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 AOJJSUZBOXZQNB-TZSSRYMLSA-N 0.000 description 18
- 229920001577 copolymer Polymers 0.000 description 18
- 230000002265 prevention Effects 0.000 description 16
- 102100039620 Granulocyte-macrophage colony-stimulating factor Human genes 0.000 description 15
- 238000002360 preparation method Methods 0.000 description 15
- 210000001519 tissue Anatomy 0.000 description 15
- 210000004881 tumor cell Anatomy 0.000 description 15
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 14
- 208000034578 Multiple myelomas Diseases 0.000 description 14
- NKANXQFJJICGDU-QPLCGJKRSA-N Tamoxifen Chemical compound C=1C=CC=CC=1C(/CC)=C(C=1C=CC(OCCN(C)C)=CC=1)/C1=CC=CC=C1 NKANXQFJJICGDU-QPLCGJKRSA-N 0.000 description 14
- 239000002775 capsule Substances 0.000 description 14
- 239000003112 inhibitor Substances 0.000 description 14
- 239000000126 substance Substances 0.000 description 14
- 108010017213 Granulocyte-Macrophage Colony-Stimulating Factor Proteins 0.000 description 13
- 230000002411 adverse Effects 0.000 description 13
- 238000013270 controlled release Methods 0.000 description 13
- 208000035475 disorder Diseases 0.000 description 13
- 239000003937 drug carrier Substances 0.000 description 13
- 239000000839 emulsion Substances 0.000 description 13
- 239000007788 liquid Substances 0.000 description 13
- 239000007787 solid Substances 0.000 description 13
- RCINICONZNJXQF-MZXODVADSA-N taxol Chemical compound O([C@@H]1[C@@]2(C[C@@H](C(C)=C(C2(C)C)[C@H](C([C@]2(C)[C@@H](O)C[C@H]3OC[C@]3([C@H]21)OC(C)=O)=O)OC(=O)C)OC(=O)[C@H](O)[C@@H](NC(=O)C=1C=CC=CC=1)C=1C=CC=CC=1)O)C(=O)C1=CC=CC=C1 RCINICONZNJXQF-MZXODVADSA-N 0.000 description 13
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 12
- 208000015914 Non-Hodgkin lymphomas Diseases 0.000 description 12
- 210000001185 bone marrow Anatomy 0.000 description 12
- SDUQYLNIPVEERB-QPPQHZFASA-N gemcitabine Chemical compound O=C1N=C(N)C=CN1[C@H]1C(F)(F)[C@H](O)[C@@H](CO)O1 SDUQYLNIPVEERB-QPPQHZFASA-N 0.000 description 12
- 238000001356 surgical procedure Methods 0.000 description 12
- 239000003826 tablet Substances 0.000 description 12
- CMSMOCZEIVJLDB-UHFFFAOYSA-N Cyclophosphamide Chemical compound ClCCN(CCCl)P1(=O)NCCCO1 CMSMOCZEIVJLDB-UHFFFAOYSA-N 0.000 description 11
- 229960004397 cyclophosphamide Drugs 0.000 description 11
- 239000000796 flavoring agent Substances 0.000 description 11
- 229960005277 gemcitabine Drugs 0.000 description 11
- GAGWJHPBXLXJQN-UORFTKCHSA-N Capecitabine Chemical compound C1=C(F)C(NC(=O)OCCCCC)=NC(=O)N1[C@H]1[C@H](O)[C@H](O)[C@@H](C)O1 GAGWJHPBXLXJQN-UORFTKCHSA-N 0.000 description 10
- VGGSQFUCUMXWEO-UHFFFAOYSA-N Ethene Chemical compound C=C VGGSQFUCUMXWEO-UHFFFAOYSA-N 0.000 description 10
- 239000005977 Ethylene Substances 0.000 description 10
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 10
- 210000004369 blood Anatomy 0.000 description 10
- 239000008280 blood Substances 0.000 description 10
- RZEKVGVHFLEQIL-UHFFFAOYSA-N celecoxib Chemical compound C1=CC(C)=CC=C1C1=CC(C(F)(F)F)=NN1C1=CC=C(S(N)(=O)=O)C=C1 RZEKVGVHFLEQIL-UHFFFAOYSA-N 0.000 description 10
- DQLATGHUWYMOKM-UHFFFAOYSA-L cisplatin Chemical compound N[Pt](N)(Cl)Cl DQLATGHUWYMOKM-UHFFFAOYSA-L 0.000 description 10
- 229960004316 cisplatin Drugs 0.000 description 10
- 239000002502 liposome Substances 0.000 description 10
- 238000004519 manufacturing process Methods 0.000 description 10
- 238000001959 radiotherapy Methods 0.000 description 10
- 239000002904 solvent Substances 0.000 description 10
- 229940124597 therapeutic agent Drugs 0.000 description 10
- 206010009944 Colon cancer Diseases 0.000 description 9
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 9
- 102100039619 Granulocyte colony-stimulating factor Human genes 0.000 description 9
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 9
- 108010002350 Interleukin-2 Proteins 0.000 description 9
- 102000000588 Interleukin-2 Human genes 0.000 description 9
- ZDZOTLJHXYCWBA-VCVYQWHSSA-N N-debenzoyl-N-(tert-butoxycarbonyl)-10-deacetyltaxol Chemical compound O([C@H]1[C@H]2[C@@](C([C@H](O)C3=C(C)[C@@H](OC(=O)[C@H](O)[C@@H](NC(=O)OC(C)(C)C)C=4C=CC=CC=4)C[C@]1(O)C3(C)C)=O)(C)[C@@H](O)C[C@H]1OC[C@]12OC(=O)C)C(=O)C1=CC=CC=C1 ZDZOTLJHXYCWBA-VCVYQWHSSA-N 0.000 description 9
- 229930012538 Paclitaxel Natural products 0.000 description 9
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 9
- 229930006000 Sucrose Natural products 0.000 description 9
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 9
- 229960004562 carboplatin Drugs 0.000 description 9
- YAYRGNWWLMLWJE-UHFFFAOYSA-L carboplatin Chemical compound O=C1O[Pt](N)(N)OC(=O)C11CCC1 YAYRGNWWLMLWJE-UHFFFAOYSA-L 0.000 description 9
- 239000000460 chlorine Substances 0.000 description 9
- 229910052801 chlorine Inorganic materials 0.000 description 9
- VJJPUSNTGOMMGY-MRVIYFEKSA-N etoposide Chemical compound COC1=C(O)C(OC)=CC([C@@H]2C3=CC=4OCOC=4C=C3[C@@H](O[C@H]3[C@@H]([C@@H](O)[C@@H]4O[C@H](C)OC[C@H]4O3)O)[C@@H]3[C@@H]2C(OC3)=O)=C1 VJJPUSNTGOMMGY-MRVIYFEKSA-N 0.000 description 9
- 210000004698 lymphocyte Anatomy 0.000 description 9
- 230000003211 malignant effect Effects 0.000 description 9
- 208000002154 non-small cell lung carcinoma Diseases 0.000 description 9
- 229960001592 paclitaxel Drugs 0.000 description 9
- 239000000843 powder Substances 0.000 description 9
- 239000011734 sodium Substances 0.000 description 9
- 229910052708 sodium Inorganic materials 0.000 description 9
- 229940083542 sodium Drugs 0.000 description 9
- 210000000130 stem cell Anatomy 0.000 description 9
- 239000005720 sucrose Substances 0.000 description 9
- 230000000699 topical effect Effects 0.000 description 9
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical class O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 8
- 208000001333 Colorectal Neoplasms Diseases 0.000 description 8
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 description 8
- 108010050904 Interferons Proteins 0.000 description 8
- 102000014150 Interferons Human genes 0.000 description 8
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Chemical class OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 8
- 239000004698 Polyethylene Substances 0.000 description 8
- 229910052799 carbon Inorganic materials 0.000 description 8
- 238000006243 chemical reaction Methods 0.000 description 8
- 238000002512 chemotherapy Methods 0.000 description 8
- 229910052805 deuterium Inorganic materials 0.000 description 8
- UREBDLICKHMUKA-CXSFZGCWSA-N dexamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-CXSFZGCWSA-N 0.000 description 8
- 229960003668 docetaxel Drugs 0.000 description 8
- 238000011156 evaluation Methods 0.000 description 8
- 229910052731 fluorine Inorganic materials 0.000 description 8
- 208000005017 glioblastoma Diseases 0.000 description 8
- 238000001727 in vivo Methods 0.000 description 8
- 239000007924 injection Substances 0.000 description 8
- 238000002347 injection Methods 0.000 description 8
- GURKHSYORGJETM-WAQYZQTGSA-N irinotecan hydrochloride (anhydrous) Chemical compound Cl.C1=C2C(CC)=C3CN(C(C4=C([C@@](C(=O)OC4)(O)CC)C=4)=O)C=4C3=NC2=CC=C1OC(=O)N(CC1)CCC1N1CCCCC1 GURKHSYORGJETM-WAQYZQTGSA-N 0.000 description 8
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 8
- 239000008101 lactose Chemical class 0.000 description 8
- 230000004060 metabolic process Effects 0.000 description 8
- 230000001394 metastastic effect Effects 0.000 description 8
- 206010061289 metastatic neoplasm Diseases 0.000 description 8
- 239000000546 pharmaceutical excipient Substances 0.000 description 8
- 229920000573 polyethylene Polymers 0.000 description 8
- GAGWJHPBXLXJQN-UHFFFAOYSA-N Capecitabine Natural products C1=C(F)C(NC(=O)OCCCCC)=NC(=O)N1C1C(O)C(O)C(C)O1 GAGWJHPBXLXJQN-UHFFFAOYSA-N 0.000 description 7
- 241001465754 Metazoa Species 0.000 description 7
- 208000000389 T-cell leukemia Diseases 0.000 description 7
- 208000028530 T-cell lymphoblastic leukemia/lymphoma Diseases 0.000 description 7
- 238000001815 biotherapy Methods 0.000 description 7
- 229910052794 bromium Inorganic materials 0.000 description 7
- 229960004117 capecitabine Drugs 0.000 description 7
- 229940127089 cytotoxic agent Drugs 0.000 description 7
- 239000003085 diluting agent Substances 0.000 description 7
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 7
- 235000019441 ethanol Nutrition 0.000 description 7
- 229960005420 etoposide Drugs 0.000 description 7
- 235000013355 food flavoring agent Nutrition 0.000 description 7
- 235000003599 food sweetener Nutrition 0.000 description 7
- 239000008176 lyophilized powder Substances 0.000 description 7
- 208000025113 myeloid leukemia Diseases 0.000 description 7
- 238000007911 parenteral administration Methods 0.000 description 7
- 230000000144 pharmacologic effect Effects 0.000 description 7
- 239000002953 phosphate buffered saline Substances 0.000 description 7
- 229920001223 polyethylene glycol Polymers 0.000 description 7
- 239000003765 sweetening agent Substances 0.000 description 7
- 239000006188 syrup Substances 0.000 description 7
- 235000020357 syrup Nutrition 0.000 description 7
- 229960001603 tamoxifen Drugs 0.000 description 7
- 208000029729 tumor suppressor gene on chromosome 11 Diseases 0.000 description 7
- 208000036762 Acute promyelocytic leukaemia Diseases 0.000 description 6
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 6
- 208000003174 Brain Neoplasms Diseases 0.000 description 6
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 6
- UHDGCWIWMRVCDJ-CCXZUQQUSA-N Cytarabine Chemical compound O=C1N=C(N)C=CN1[C@H]1[C@@H](O)[C@H](O)[C@@H](CO)O1 UHDGCWIWMRVCDJ-CCXZUQQUSA-N 0.000 description 6
- 206010018338 Glioma Diseases 0.000 description 6
- 108010017080 Granulocyte Colony-Stimulating Factor Proteins 0.000 description 6
- 206010060862 Prostate cancer Diseases 0.000 description 6
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 6
- 230000002159 abnormal effect Effects 0.000 description 6
- 239000002253 acid Substances 0.000 description 6
- 239000005557 antagonist Substances 0.000 description 6
- 229940041181 antineoplastic drug Drugs 0.000 description 6
- 238000000576 coating method Methods 0.000 description 6
- 239000003086 colorant Substances 0.000 description 6
- 229960003957 dexamethasone Drugs 0.000 description 6
- GIUYCYHIANZCFB-FJFJXFQQSA-N fludarabine phosphate Chemical compound C1=NC=2C(N)=NC(F)=NC=2N1[C@@H]1O[C@H](COP(O)(O)=O)[C@@H](O)[C@@H]1O GIUYCYHIANZCFB-FJFJXFQQSA-N 0.000 description 6
- 235000011187 glycerol Nutrition 0.000 description 6
- 239000008187 granular material Substances 0.000 description 6
- 238000001794 hormone therapy Methods 0.000 description 6
- 239000004615 ingredient Substances 0.000 description 6
- 229940079322 interferon Drugs 0.000 description 6
- 229960004768 irinotecan Drugs 0.000 description 6
- 230000000155 isotopic effect Effects 0.000 description 6
- 210000001165 lymph node Anatomy 0.000 description 6
- 239000000463 material Substances 0.000 description 6
- 230000007246 mechanism Effects 0.000 description 6
- 125000004312 morpholin-2-yl group Chemical group [H]N1C([H])([H])C([H])([H])OC([H])(*)C1([H])[H] 0.000 description 6
- 125000002757 morpholinyl group Chemical group 0.000 description 6
- 229960000435 oblimersen Drugs 0.000 description 6
- MIMNFCVQODTQDP-NDLVEFNKSA-N oblimersen Chemical compound O=C1NC(=O)C(C)=CN1[C@@H]1O[C@H](COP(S)(=O)O[C@@H]2[C@H](O[C@H](C2)N2C3=NC=NC(N)=C3N=C2)COP(O)(=S)O[C@@H]2[C@H](O[C@H](C2)N2C(N=C(N)C=C2)=O)COP(O)(=S)O[C@@H]2[C@H](O[C@H](C2)N2C(N=C(N)C=C2)=O)COP(O)(=S)O[C@@H]2[C@H](O[C@H](C2)N2C3=C(C(NC(N)=N3)=O)N=C2)COP(O)(=S)O[C@@H]2[C@H](O[C@H](C2)N2C(N=C(N)C=C2)=O)COP(O)(=S)O[C@@H]2[C@H](O[C@H](C2)N2C3=C(C(NC(N)=N3)=O)N=C2)COP(O)(=S)O[C@@H]2[C@H](O[C@H](C2)N2C(NC(=O)C(C)=C2)=O)COP(O)(=S)O[C@@H]2[C@H](O[C@H](C2)N2C3=C(C(NC(N)=N3)=O)N=C2)COP(O)(=S)O[C@@H]2[C@H](O[C@H](C2)N2C(N=C(N)C=C2)=O)COP(O)(=S)O[C@@H]2[C@H](O[C@H](C2)N2C3=C(C(NC(N)=N3)=O)N=C2)COP(O)(=S)O[C@@H]2[C@H](O[C@H](C2)N2C3=NC=NC(N)=C3N=C2)COP(O)(=S)O[C@@H]2[C@H](O[C@H](C2)N2C(N=C(N)C=C2)=O)COP(O)(=S)O[C@@H]2[C@H](O[C@H](C2)N2C(N=C(N)C=C2)=O)COP(O)(=S)O[C@@H]2[C@H](O[C@H](C2)N2C(N=C(N)C=C2)=O)COP(O)(=S)O[C@@H]2[C@H](O[C@H](C2)N2C(NC(=O)C(C)=C2)=O)COP(O)(=S)O[C@@H]2[C@H](O[C@H](C2)N2C(N=C(N)C=C2)=O)COP(O)(=S)O[C@@H]2[C@H](O[C@H](C2)N2C(NC(=O)C(C)=C2)=O)CO)[C@@H](O)C1 MIMNFCVQODTQDP-NDLVEFNKSA-N 0.000 description 6
- 239000006187 pill Substances 0.000 description 6
- 230000036470 plasma concentration Effects 0.000 description 6
- 229920000642 polymer Polymers 0.000 description 6
- 230000000069 prophylactic effect Effects 0.000 description 6
- 239000003981 vehicle Substances 0.000 description 6
- 206010000830 Acute leukaemia Diseases 0.000 description 5
- GHASVSINZRGABV-UHFFFAOYSA-N Fluorouracil Chemical compound FC1=CNC(=O)NC1=O GHASVSINZRGABV-UHFFFAOYSA-N 0.000 description 5
- 208000017604 Hodgkin disease Diseases 0.000 description 5
- 208000010747 Hodgkins lymphoma Diseases 0.000 description 5
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 5
- VSNHCAURESNICA-UHFFFAOYSA-N Hydroxyurea Chemical compound NC(=O)NO VSNHCAURESNICA-UHFFFAOYSA-N 0.000 description 5
- 108010047761 Interferon-alpha Proteins 0.000 description 5
- 102000006992 Interferon-alpha Human genes 0.000 description 5
- 239000002202 Polyethylene glycol Substances 0.000 description 5
- 208000000236 Prostatic Neoplasms Diseases 0.000 description 5
- 206010062237 Renal impairment Diseases 0.000 description 5
- BPEGJWRSRHCHSN-UHFFFAOYSA-N Temozolomide Chemical compound O=C1N(C)N=NC2=C(C(N)=O)N=CN21 BPEGJWRSRHCHSN-UHFFFAOYSA-N 0.000 description 5
- YZCKVEUIGOORGS-NJFSPNSNSA-N Tritium Chemical compound [3H] YZCKVEUIGOORGS-NJFSPNSNSA-N 0.000 description 5
- JXLYSJRDGCGARV-WWYNWVTFSA-N Vinblastine Natural products O=C(O[C@H]1[C@](O)(C(=O)OC)[C@@H]2N(C)c3c(cc(c(OC)c3)[C@]3(C(=O)OC)c4[nH]c5c(c4CCN4C[C@](O)(CC)C[C@H](C3)C4)cccc5)[C@@]32[C@H]2[C@@]1(CC)C=CCN2CC3)C JXLYSJRDGCGARV-WWYNWVTFSA-N 0.000 description 5
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 5
- 230000033115 angiogenesis Effects 0.000 description 5
- 239000003963 antioxidant agent Substances 0.000 description 5
- 235000006708 antioxidants Nutrition 0.000 description 5
- 230000008901 benefit Effects 0.000 description 5
- 239000000872 buffer Substances 0.000 description 5
- 125000004432 carbon atom Chemical group C* 0.000 description 5
- 229940047495 celebrex Drugs 0.000 description 5
- 229960000590 celecoxib Drugs 0.000 description 5
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Natural products OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 5
- 239000007891 compressed tablet Substances 0.000 description 5
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 5
- 230000002559 cytogenic effect Effects 0.000 description 5
- 230000007423 decrease Effects 0.000 description 5
- 239000008121 dextrose Substances 0.000 description 5
- 229960004679 doxorubicin Drugs 0.000 description 5
- 239000003995 emulsifying agent Substances 0.000 description 5
- 229960000390 fludarabine Drugs 0.000 description 5
- 201000003444 follicular lymphoma Diseases 0.000 description 5
- 239000000499 gel Substances 0.000 description 5
- 230000012010 growth Effects 0.000 description 5
- 230000003394 haemopoietic effect Effects 0.000 description 5
- 229910052736 halogen Inorganic materials 0.000 description 5
- 150000002367 halogens Chemical class 0.000 description 5
- 229960001330 hydroxycarbamide Drugs 0.000 description 5
- YLMAHDNUQAMNNX-UHFFFAOYSA-N imatinib methanesulfonate Chemical compound CS(O)(=O)=O.C1CN(C)CCN1CC1=CC=C(C(=O)NC=2C=C(NC=3N=C(C=CN=3)C=3C=NC=CC=3)C(C)=CC=2)C=C1 YLMAHDNUQAMNNX-UHFFFAOYSA-N 0.000 description 5
- 238000009169 immunotherapy Methods 0.000 description 5
- 238000000338 in vitro Methods 0.000 description 5
- 238000001802 infusion Methods 0.000 description 5
- 150000002605 large molecules Chemical class 0.000 description 5
- 229920002521 macromolecule Polymers 0.000 description 5
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical class [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 5
- 239000012528 membrane Substances 0.000 description 5
- 210000004379 membrane Anatomy 0.000 description 5
- 239000002207 metabolite Substances 0.000 description 5
- 201000000050 myeloid neoplasm Diseases 0.000 description 5
- 230000002093 peripheral effect Effects 0.000 description 5
- 125000003386 piperidinyl group Chemical group 0.000 description 5
- 125000005936 piperidyl group Chemical group 0.000 description 5
- 231100000857 poor renal function Toxicity 0.000 description 5
- OXCMYAYHXIHQOA-UHFFFAOYSA-N potassium;[2-butyl-5-chloro-3-[[4-[2-(1,2,4-triaza-3-azanidacyclopenta-1,4-dien-5-yl)phenyl]phenyl]methyl]imidazol-4-yl]methanol Chemical compound [K+].CCCCC1=NC(Cl)=C(CO)N1CC1=CC=C(C=2C(=CC=CC=2)C2=N[N-]N=N2)C=C1 OXCMYAYHXIHQOA-UHFFFAOYSA-N 0.000 description 5
- 239000003755 preservative agent Substances 0.000 description 5
- 150000003254 radicals Chemical class 0.000 description 5
- 239000006215 rectal suppository Substances 0.000 description 5
- 229960004641 rituximab Drugs 0.000 description 5
- 210000002784 stomach Anatomy 0.000 description 5
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 5
- 229910052722 tritium Inorganic materials 0.000 description 5
- 229960004528 vincristine Drugs 0.000 description 5
- OGWKCGZFUXNPDA-XQKSVPLYSA-N vincristine Chemical compound C([N@]1C[C@@H](C[C@]2(C(=O)OC)C=3C(=CC4=C([C@]56[C@H]([C@@]([C@H](OC(C)=O)[C@]7(CC)C=CCN([C@H]67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)C[C@@](C1)(O)CC)CC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-XQKSVPLYSA-N 0.000 description 5
- OGWKCGZFUXNPDA-UHFFFAOYSA-N vincristine Natural products C1C(CC)(O)CC(CC2(C(=O)OC)C=3C(=CC4=C(C56C(C(C(OC(C)=O)C7(CC)C=CCN(C67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)CN1CCC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-UHFFFAOYSA-N 0.000 description 5
- 239000000080 wetting agent Substances 0.000 description 5
- 108010011376 AMP-Activated Protein Kinases Proteins 0.000 description 4
- 102000014156 AMP-Activated Protein Kinases Human genes 0.000 description 4
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 4
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 4
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 4
- DLGOEMSEDOSKAD-UHFFFAOYSA-N Carmustine Chemical compound ClCCNC(=O)N(N=O)CCCl DLGOEMSEDOSKAD-UHFFFAOYSA-N 0.000 description 4
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 4
- 102000004190 Enzymes Human genes 0.000 description 4
- 108090000790 Enzymes Proteins 0.000 description 4
- 102100031939 Erythropoietin Human genes 0.000 description 4
- ZRALSGWEFCBTJO-UHFFFAOYSA-N Guanidine Chemical compound NC(N)=N ZRALSGWEFCBTJO-UHFFFAOYSA-N 0.000 description 4
- 208000021519 Hodgkin lymphoma Diseases 0.000 description 4
- 101001046870 Homo sapiens Hypoxia-inducible factor 1-alpha Proteins 0.000 description 4
- OAKJQQAXSVQMHS-UHFFFAOYSA-N Hydrazine Chemical compound NN OAKJQQAXSVQMHS-UHFFFAOYSA-N 0.000 description 4
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 4
- 102100022875 Hypoxia-inducible factor 1-alpha Human genes 0.000 description 4
- FBOZXECLQNJBKD-ZDUSSCGKSA-N L-methotrexate Chemical compound C=1N=C2N=C(N)N=C(N)C2=NC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 FBOZXECLQNJBKD-ZDUSSCGKSA-N 0.000 description 4
- 239000005517 L01XE01 - Imatinib Substances 0.000 description 4
- 108010000817 Leuprolide Proteins 0.000 description 4
- 206010052178 Lymphocytic lymphoma Diseases 0.000 description 4
- 206010033128 Ovarian cancer Diseases 0.000 description 4
- 206010061535 Ovarian neoplasm Diseases 0.000 description 4
- XYFCBTPGUUZFHI-UHFFFAOYSA-N Phosphine Chemical compound P XYFCBTPGUUZFHI-UHFFFAOYSA-N 0.000 description 4
- 206010039491 Sarcoma Diseases 0.000 description 4
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 4
- 229920002472 Starch Chemical class 0.000 description 4
- 102100040247 Tumor necrosis factor Human genes 0.000 description 4
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 4
- 230000009471 action Effects 0.000 description 4
- 230000001154 acute effect Effects 0.000 description 4
- 239000000443 aerosol Substances 0.000 description 4
- 230000006907 apoptotic process Effects 0.000 description 4
- 239000007864 aqueous solution Substances 0.000 description 4
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 4
- 239000011230 binding agent Substances 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- 210000004556 brain Anatomy 0.000 description 4
- DQXBYHZEEUGOBF-UHFFFAOYSA-N but-3-enoic acid;ethene Chemical compound C=C.OC(=O)CC=C DQXBYHZEEUGOBF-UHFFFAOYSA-N 0.000 description 4
- 125000003917 carbamoyl group Chemical group [H]N([H])C(*)=O 0.000 description 4
- 239000001768 carboxy methyl cellulose Substances 0.000 description 4
- 238000002648 combination therapy Methods 0.000 description 4
- 125000004122 cyclic group Chemical group 0.000 description 4
- 230000001351 cycling effect Effects 0.000 description 4
- 238000011161 development Methods 0.000 description 4
- 230000018109 developmental process Effects 0.000 description 4
- 230000004069 differentiation Effects 0.000 description 4
- 235000013870 dimethyl polysiloxane Nutrition 0.000 description 4
- 239000000975 dye Substances 0.000 description 4
- 229940088598 enzyme Drugs 0.000 description 4
- 150000002148 esters Chemical class 0.000 description 4
- 239000005038 ethylene vinyl acetate Substances 0.000 description 4
- 210000001508 eye Anatomy 0.000 description 4
- 235000019634 flavors Nutrition 0.000 description 4
- 229960002949 fluorouracil Drugs 0.000 description 4
- 239000008273 gelatin Substances 0.000 description 4
- 229920000159 gelatin Polymers 0.000 description 4
- 239000008103 glucose Substances 0.000 description 4
- 239000003102 growth factor Substances 0.000 description 4
- 206010073071 hepatocellular carcinoma Diseases 0.000 description 4
- 231100000844 hepatocellular carcinoma Toxicity 0.000 description 4
- 239000000017 hydrogel Substances 0.000 description 4
- 230000006872 improvement Effects 0.000 description 4
- 230000001965 increasing effect Effects 0.000 description 4
- 210000000936 intestine Anatomy 0.000 description 4
- 238000001990 intravenous administration Methods 0.000 description 4
- 210000000265 leukocyte Anatomy 0.000 description 4
- 229960004338 leuprorelin Drugs 0.000 description 4
- 230000007774 longterm Effects 0.000 description 4
- 239000000314 lubricant Substances 0.000 description 4
- 239000011159 matrix material Substances 0.000 description 4
- 229960000485 methotrexate Drugs 0.000 description 4
- 230000035772 mutation Effects 0.000 description 4
- 210000005170 neoplastic cell Anatomy 0.000 description 4
- 230000001613 neoplastic effect Effects 0.000 description 4
- 239000003921 oil Substances 0.000 description 4
- 239000006186 oral dosage form Substances 0.000 description 4
- 210000000056 organ Anatomy 0.000 description 4
- 239000001301 oxygen Substances 0.000 description 4
- 239000005022 packaging material Substances 0.000 description 4
- 238000004806 packaging method and process Methods 0.000 description 4
- 210000005259 peripheral blood Anatomy 0.000 description 4
- 239000011886 peripheral blood Substances 0.000 description 4
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 4
- 229920000435 poly(dimethylsiloxane) Polymers 0.000 description 4
- 229920001200 poly(ethylene-vinyl acetate) Polymers 0.000 description 4
- 229920000728 polyester Polymers 0.000 description 4
- 229920000139 polyethylene terephthalate Polymers 0.000 description 4
- 239000005020 polyethylene terephthalate Substances 0.000 description 4
- 239000002243 precursor Substances 0.000 description 4
- 210000001948 pro-b lymphocyte Anatomy 0.000 description 4
- 239000000047 product Substances 0.000 description 4
- 230000000750 progressive effect Effects 0.000 description 4
- 230000035755 proliferation Effects 0.000 description 4
- 229920002379 silicone rubber Polymers 0.000 description 4
- 239000011780 sodium chloride Substances 0.000 description 4
- 239000008107 starch Chemical class 0.000 description 4
- 235000019698 starch Nutrition 0.000 description 4
- 229940032147 starch Drugs 0.000 description 4
- 150000003431 steroids Chemical class 0.000 description 4
- 238000006467 substitution reaction Methods 0.000 description 4
- 239000000375 suspending agent Substances 0.000 description 4
- 238000013268 sustained release Methods 0.000 description 4
- 239000012730 sustained-release form Substances 0.000 description 4
- 230000009885 systemic effect Effects 0.000 description 4
- 229960004964 temozolomide Drugs 0.000 description 4
- ZMZDMBWJUHKJPS-UHFFFAOYSA-N thiocyanic acid Chemical compound SC#N ZMZDMBWJUHKJPS-UHFFFAOYSA-N 0.000 description 4
- UCFGDBYHRUNTLO-QHCPKHFHSA-N topotecan Chemical compound C1=C(O)C(CN(C)C)=C2C=C(CN3C4=CC5=C(C3=O)COC(=O)[C@]5(O)CC)C4=NC2=C1 UCFGDBYHRUNTLO-QHCPKHFHSA-N 0.000 description 4
- 229960000303 topotecan Drugs 0.000 description 4
- 238000002054 transplantation Methods 0.000 description 4
- 229960003048 vinblastine Drugs 0.000 description 4
- JXLYSJRDGCGARV-XQKSVPLYSA-N vincaleukoblastine Chemical compound C([C@@H](C[C@]1(C(=O)OC)C=2C(=CC3=C([C@]45[C@H]([C@@]([C@H](OC(C)=O)[C@]6(CC)C=CCN([C@H]56)CC4)(O)C(=O)OC)N3C)C=2)OC)C[C@@](C2)(O)CC)N2CCC2=C1NC1=CC=CC=C21 JXLYSJRDGCGARV-XQKSVPLYSA-N 0.000 description 4
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 4
- 229920002554 vinyl polymer Polymers 0.000 description 4
- FDKXTQMXEQVLRF-ZHACJKMWSA-N (E)-dacarbazine Chemical compound CN(C)\N=N\c1[nH]cnc1C(N)=O FDKXTQMXEQVLRF-ZHACJKMWSA-N 0.000 description 3
- HJTAZXHBEBIQQX-UHFFFAOYSA-N 1,5-bis(chloromethyl)naphthalene Chemical compound C1=CC=C2C(CCl)=CC=CC2=C1CCl HJTAZXHBEBIQQX-UHFFFAOYSA-N 0.000 description 3
- YBYIRNPNPLQARY-UHFFFAOYSA-N 1H-indene Natural products C1=CC=C2CC=CC2=C1 YBYIRNPNPLQARY-UHFFFAOYSA-N 0.000 description 3
- XBBVURRQGJPTHH-UHFFFAOYSA-N 2-hydroxyacetic acid;2-hydroxypropanoic acid Chemical compound OCC(O)=O.CC(O)C(O)=O XBBVURRQGJPTHH-UHFFFAOYSA-N 0.000 description 3
- 125000001255 4-fluorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C([H])=C1F 0.000 description 3
- VVIAGPKUTFNRDU-UHFFFAOYSA-N 6S-folinic acid Natural products C1NC=2NC(N)=NC(=O)C=2N(C=O)C1CNC1=CC=C(C(=O)NC(CCC(O)=O)C(O)=O)C=C1 VVIAGPKUTFNRDU-UHFFFAOYSA-N 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 3
- 241000416162 Astragalus gummifer Species 0.000 description 3
- WVDDGKGOMKODPV-UHFFFAOYSA-N Benzyl alcohol Chemical compound OCC1=CC=CC=C1 WVDDGKGOMKODPV-UHFFFAOYSA-N 0.000 description 3
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 3
- COVZYZSDYWQREU-UHFFFAOYSA-N Busulfan Chemical compound CS(=O)(=O)OCCCCOS(C)(=O)=O COVZYZSDYWQREU-UHFFFAOYSA-N 0.000 description 3
- 229920000623 Cellulose acetate phthalate Polymers 0.000 description 3
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 3
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical class OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 3
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 3
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 3
- 241000196324 Embryophyta Species 0.000 description 3
- 108010029961 Filgrastim Proteins 0.000 description 3
- 108010010803 Gelatin Proteins 0.000 description 3
- 201000010915 Glioblastoma multiforme Diseases 0.000 description 3
- 241000282412 Homo Species 0.000 description 3
- AVXURJPOCDRRFD-UHFFFAOYSA-N Hydroxylamine Chemical compound ON AVXURJPOCDRRFD-UHFFFAOYSA-N 0.000 description 3
- XDXDZDZNSLXDNA-TZNDIEGXSA-N Idarubicin Chemical compound C1[C@H](N)[C@H](O)[C@H](C)O[C@H]1O[C@@H]1C2=C(O)C(C(=O)C3=CC=CC=C3C3=O)=C3C(O)=C2C[C@@](O)(C(C)=O)C1 XDXDZDZNSLXDNA-TZNDIEGXSA-N 0.000 description 3
- 235000010643 Leucaena leucocephala Nutrition 0.000 description 3
- 240000007472 Leucaena leucocephala Species 0.000 description 3
- 229930195725 Mannitol Natural products 0.000 description 3
- NWIBSHFKIJFRCO-WUDYKRTCSA-N Mytomycin Chemical compound C1N2C(C(C(C)=C(N)C3=O)=O)=C3[C@@H](COC(N)=O)[C@@]2(OC)[C@@H]2[C@H]1N2 NWIBSHFKIJFRCO-WUDYKRTCSA-N 0.000 description 3
- 229910019142 PO4 Inorganic materials 0.000 description 3
- 208000033826 Promyelocytic Acute Leukemia Diseases 0.000 description 3
- OTKJDMGTUTTYMP-ROUUACIJSA-N Safingol ( L-threo-sphinganine) Chemical compound CCCCCCCCCCCCCCC[C@H](O)[C@@H](N)CO OTKJDMGTUTTYMP-ROUUACIJSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 208000021712 Soft tissue sarcoma Diseases 0.000 description 3
- FOCVUCIESVLUNU-UHFFFAOYSA-N Thiotepa Chemical compound C1CN1P(N1CC1)(=S)N1CC1 FOCVUCIESVLUNU-UHFFFAOYSA-N 0.000 description 3
- 229920001615 Tragacanth Polymers 0.000 description 3
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 3
- XTXRWKRVRITETP-UHFFFAOYSA-N Vinyl acetate Chemical compound CC(=O)OC=C XTXRWKRVRITETP-UHFFFAOYSA-N 0.000 description 3
- 150000001241 acetals Chemical class 0.000 description 3
- 239000011149 active material Substances 0.000 description 3
- 229940009456 adriamycin Drugs 0.000 description 3
- 230000032683 aging Effects 0.000 description 3
- 239000000556 agonist Substances 0.000 description 3
- 230000001093 anti-cancer Effects 0.000 description 3
- 239000004599 antimicrobial Substances 0.000 description 3
- GOLCXWYRSKYTSP-UHFFFAOYSA-N arsenic trioxide Inorganic materials O1[As]2O[As]1O2 GOLCXWYRSKYTSP-UHFFFAOYSA-N 0.000 description 3
- 229960002594 arsenic trioxide Drugs 0.000 description 3
- 235000010323 ascorbic acid Nutrition 0.000 description 3
- 125000004429 atom Chemical group 0.000 description 3
- 239000002585 base Substances 0.000 description 3
- 125000002619 bicyclic group Chemical group 0.000 description 3
- 210000000601 blood cell Anatomy 0.000 description 3
- 210000000988 bone and bone Anatomy 0.000 description 3
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 3
- 230000010261 cell growth Effects 0.000 description 3
- 230000004663 cell proliferation Effects 0.000 description 3
- 201000010989 colorectal carcinoma Diseases 0.000 description 3
- 238000007596 consolidation process Methods 0.000 description 3
- 229960003901 dacarbazine Drugs 0.000 description 3
- 230000034994 death Effects 0.000 description 3
- 231100000517 death Toxicity 0.000 description 3
- 239000003405 delayed action preparation Substances 0.000 description 3
- 238000003745 diagnosis Methods 0.000 description 3
- 230000002708 enhancing effect Effects 0.000 description 3
- 238000009505 enteric coating Methods 0.000 description 3
- 239000002702 enteric coating Substances 0.000 description 3
- FRPJXPJMRWBBIH-RBRWEJTLSA-N estramustine Chemical compound ClCCN(CCCl)C(=O)OC1=CC=C2[C@H]3CC[C@](C)([C@H](CC4)O)[C@@H]4[C@@H]3CCC2=C1 FRPJXPJMRWBBIH-RBRWEJTLSA-N 0.000 description 3
- IIUMCNJTGSMNRO-VVSKJQCTSA-L estramustine sodium phosphate Chemical compound [Na+].[Na+].ClCCN(CCCl)C(=O)OC1=CC=C2[C@H]3CC[C@](C)([C@H](CC4)OP([O-])([O-])=O)[C@@H]4[C@@H]3CCC2=C1 IIUMCNJTGSMNRO-VVSKJQCTSA-L 0.000 description 3
- 229940011871 estrogen Drugs 0.000 description 3
- 239000000262 estrogen Substances 0.000 description 3
- 230000029142 excretion Effects 0.000 description 3
- VVIAGPKUTFNRDU-ABLWVSNPSA-N folinic acid Chemical compound C1NC=2NC(N)=NC(=O)C=2N(C=O)C1CNC1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 VVIAGPKUTFNRDU-ABLWVSNPSA-N 0.000 description 3
- 235000008191 folinic acid Nutrition 0.000 description 3
- 239000011672 folinic acid Substances 0.000 description 3
- 235000019322 gelatine Nutrition 0.000 description 3
- 235000011852 gelatine desserts Nutrition 0.000 description 3
- 229940080856 gleevec Drugs 0.000 description 3
- 230000034659 glycolysis Effects 0.000 description 3
- 208000013210 hematogenous Diseases 0.000 description 3
- 201000005787 hematologic cancer Diseases 0.000 description 3
- 125000005842 heteroatom Chemical group 0.000 description 3
- 208000029824 high grade glioma Diseases 0.000 description 3
- 150000002430 hydrocarbons Chemical group 0.000 description 3
- 239000007943 implant Substances 0.000 description 3
- 230000001976 improved effect Effects 0.000 description 3
- 230000005764 inhibitory process Effects 0.000 description 3
- 239000000543 intermediate Substances 0.000 description 3
- 230000005445 isotope effect Effects 0.000 description 3
- 229940043355 kinase inhibitor Drugs 0.000 description 3
- 239000010410 layer Substances 0.000 description 3
- 230000003902 lesion Effects 0.000 description 3
- 229960001691 leucovorin Drugs 0.000 description 3
- GFIJNRVAKGFPGQ-LIJARHBVSA-N leuprolide Chemical compound CCNC(=O)[C@@H]1CCCN1C(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H]1NC(=O)CC1)CC1=CC=C(O)C=C1 GFIJNRVAKGFPGQ-LIJARHBVSA-N 0.000 description 3
- 150000002632 lipids Chemical class 0.000 description 3
- 210000004185 liver Anatomy 0.000 description 3
- 235000019359 magnesium stearate Nutrition 0.000 description 3
- 201000011614 malignant glioma Diseases 0.000 description 3
- 239000000594 mannitol Substances 0.000 description 3
- 235000010355 mannitol Nutrition 0.000 description 3
- 201000001441 melanoma Diseases 0.000 description 3
- SGDBTWWWUNNDEQ-LBPRGKRZSA-N melphalan Chemical compound OC(=O)[C@@H](N)CC1=CC=C(N(CCCl)CCCl)C=C1 SGDBTWWWUNNDEQ-LBPRGKRZSA-N 0.000 description 3
- 229960001924 melphalan Drugs 0.000 description 3
- 206010027191 meningioma Diseases 0.000 description 3
- 231100000252 nontoxic Toxicity 0.000 description 3
- 230000003000 nontoxic effect Effects 0.000 description 3
- 235000019198 oils Nutrition 0.000 description 3
- 238000011275 oncology therapy Methods 0.000 description 3
- 235000021317 phosphate Nutrition 0.000 description 3
- 239000003757 phosphotransferase inhibitor Substances 0.000 description 3
- 210000004180 plasmocyte Anatomy 0.000 description 3
- XOFYZVNMUHMLCC-ZPOLXVRWSA-N prednisone Chemical compound O=C1C=C[C@]2(C)[C@H]3C(=O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 XOFYZVNMUHMLCC-ZPOLXVRWSA-N 0.000 description 3
- 229960004618 prednisone Drugs 0.000 description 3
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 3
- 108090000765 processed proteins & peptides Proteins 0.000 description 3
- 238000004393 prognosis Methods 0.000 description 3
- 230000005855 radiation Effects 0.000 description 3
- 230000004044 response Effects 0.000 description 3
- CVHZOJJKTDOEJC-UHFFFAOYSA-N saccharin Chemical compound C1=CC=C2C(=O)NS(=O)(=O)C2=C1 CVHZOJJKTDOEJC-UHFFFAOYSA-N 0.000 description 3
- 108010038379 sargramostim Proteins 0.000 description 3
- 210000003491 skin Anatomy 0.000 description 3
- 150000003384 small molecules Chemical class 0.000 description 3
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 3
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 3
- 239000007909 solid dosage form Substances 0.000 description 3
- 239000000600 sorbitol Substances 0.000 description 3
- 235000010356 sorbitol Nutrition 0.000 description 3
- 229950006050 spiromustine Drugs 0.000 description 3
- 230000006641 stabilisation Effects 0.000 description 3
- 238000011105 stabilization Methods 0.000 description 3
- 238000011476 stem cell transplantation Methods 0.000 description 3
- 238000003860 storage Methods 0.000 description 3
- 235000000346 sugar Nutrition 0.000 description 3
- 230000002195 synergetic effect Effects 0.000 description 3
- 229960001196 thiotepa Drugs 0.000 description 3
- 238000011200 topical administration Methods 0.000 description 3
- 238000011269 treatment regimen Methods 0.000 description 3
- 150000003626 triacylglycerols Chemical class 0.000 description 3
- GBABOYUKABKIAF-GHYRFKGUSA-N vinorelbine Chemical compound C1N(CC=2C3=CC=CC=C3NC=22)CC(CC)=C[C@H]1C[C@]2(C(=O)OC)C1=CC([C@]23[C@H]([C@]([C@H](OC(C)=O)[C@]4(CC)C=CCN([C@H]34)CC2)(O)C(=O)OC)N2C)=C2C=C1OC GBABOYUKABKIAF-GHYRFKGUSA-N 0.000 description 3
- 229960002066 vinorelbine Drugs 0.000 description 3
- 239000001993 wax Substances 0.000 description 3
- 229940053867 xeloda Drugs 0.000 description 3
- HZSBSRAVNBUZRA-RQDPQJJXSA-J (1r,2r)-cyclohexane-1,2-diamine;tetrachloroplatinum(2+) Chemical compound Cl[Pt+2](Cl)(Cl)Cl.N[C@@H]1CCCC[C@H]1N HZSBSRAVNBUZRA-RQDPQJJXSA-J 0.000 description 2
- FELGMEQIXOGIFQ-CYBMUJFWSA-N (3r)-9-methyl-3-[(2-methylimidazol-1-yl)methyl]-2,3-dihydro-1h-carbazol-4-one Chemical compound CC1=NC=CN1C[C@@H]1C(=O)C(C=2C(=CC=CC=2)N2C)=C2CC1 FELGMEQIXOGIFQ-CYBMUJFWSA-N 0.000 description 2
- SWXOGPJRIDTIRL-DOUNNPEJSA-N (4r,7s,10s,13r,16s,19r)-10-(4-aminobutyl)-n-[(2s)-1-amino-3-(1h-indol-3-yl)-1-oxopropan-2-yl]-19-[[(2r)-2-amino-3-phenylpropanoyl]amino]-16-[(4-hydroxyphenyl)methyl]-13-(1h-indol-3-ylmethyl)-6,9,12,15,18-pentaoxo-7-propan-2-yl-1,2-dithia-5,8,11,14,17-pent Chemical compound C([C@H]1C(=O)N[C@H](CC=2C3=CC=CC=C3NC=2)C(=O)N[C@@H](CCCCN)C(=O)N[C@H](C(N[C@@H](CSSC[C@@H](C(=O)N1)NC(=O)[C@H](N)CC=1C=CC=CC=1)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(N)=O)=O)C(C)C)C1=CC=C(O)C=C1 SWXOGPJRIDTIRL-DOUNNPEJSA-N 0.000 description 2
- LKJPYSCBVHEWIU-KRWDZBQOSA-N (R)-bicalutamide Chemical compound C([C@@](O)(C)C(=O)NC=1C=C(C(C#N)=CC=1)C(F)(F)F)S(=O)(=O)C1=CC=C(F)C=C1 LKJPYSCBVHEWIU-KRWDZBQOSA-N 0.000 description 2
- GVJHHUAWPYXKBD-UHFFFAOYSA-N (±)-α-Tocopherol Chemical compound OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-UHFFFAOYSA-N 0.000 description 2
- ZORQXIQZAOLNGE-UHFFFAOYSA-N 1,1-difluorocyclohexane Chemical compound FC1(F)CCCCC1 ZORQXIQZAOLNGE-UHFFFAOYSA-N 0.000 description 2
- TZCPCKNHXULUIY-RGULYWFUSA-N 1,2-distearoyl-sn-glycero-3-phosphoserine Chemical compound CCCCCCCCCCCCCCCCCC(=O)OC[C@H](COP(O)(=O)OC[C@H](N)C(O)=O)OC(=O)CCCCCCCCCCCCCCCCC TZCPCKNHXULUIY-RGULYWFUSA-N 0.000 description 2
- FONKWHRXTPJODV-DNQXCXABSA-N 1,3-bis[2-[(8s)-8-(chloromethyl)-4-hydroxy-1-methyl-7,8-dihydro-3h-pyrrolo[3,2-e]indole-6-carbonyl]-1h-indol-5-yl]urea Chemical compound C1([C@H](CCl)CN2C(=O)C=3NC4=CC=C(C=C4C=3)NC(=O)NC=3C=C4C=C(NC4=CC=3)C(=O)N3C4=CC(O)=C5NC=C(C5=C4[C@H](CCl)C3)C)=C2C=C(O)C2=C1C(C)=CN2 FONKWHRXTPJODV-DNQXCXABSA-N 0.000 description 2
- WGIMXKDCVCTHGW-UHFFFAOYSA-N 2-(2-hydroxyethoxy)ethyl dodecanoate Chemical compound CCCCCCCCCCCC(=O)OCCOCCO WGIMXKDCVCTHGW-UHFFFAOYSA-N 0.000 description 2
- OEPOKWHJYJXUGD-UHFFFAOYSA-N 2-(3-phenylmethoxyphenyl)-1,3-thiazole-4-carbaldehyde Chemical compound O=CC1=CSC(C=2C=C(OCC=3C=CC=CC=3)C=CC=2)=N1 OEPOKWHJYJXUGD-UHFFFAOYSA-N 0.000 description 2
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 2
- FKOKUHFZNIUSLW-UHFFFAOYSA-N 2-Hydroxypropyl stearate Chemical compound CCCCCCCCCCCCCCCCCC(=O)OCC(C)O FKOKUHFZNIUSLW-UHFFFAOYSA-N 0.000 description 2
- QNKJFXARIMSDBR-UHFFFAOYSA-N 3-[2-[bis(2-chloroethyl)amino]ethyl]-1,3-diazaspiro[4.5]decane-2,4-dione Chemical compound O=C1N(CCN(CCCl)CCCl)C(=O)NC11CCCCC1 QNKJFXARIMSDBR-UHFFFAOYSA-N 0.000 description 2
- CLPFFLWZZBQMAO-UHFFFAOYSA-N 4-(5,6,7,8-tetrahydroimidazo[1,5-a]pyridin-5-yl)benzonitrile Chemical compound C1=CC(C#N)=CC=C1C1N2C=NC=C2CCC1 CLPFFLWZZBQMAO-UHFFFAOYSA-N 0.000 description 2
- AKJHMTWEGVYYSE-AIRMAKDCSA-N 4-HPR Chemical compound C=1C=C(O)C=CC=1NC(=O)/C=C(\C)/C=C/C=C(C)C=CC1=C(C)CCCC1(C)C AKJHMTWEGVYYSE-AIRMAKDCSA-N 0.000 description 2
- XAUDJQYHKZQPEU-KVQBGUIXSA-N 5-aza-2'-deoxycytidine Chemical compound O=C1N=C(N)N=CN1[C@@H]1O[C@H](CO)[C@@H](O)C1 XAUDJQYHKZQPEU-KVQBGUIXSA-N 0.000 description 2
- STQGQHZAVUOBTE-UHFFFAOYSA-N 7-Cyan-hept-2t-en-4,6-diinsaeure Natural products C1=2C(O)=C3C(=O)C=4C(OC)=CC=CC=4C(=O)C3=C(O)C=2CC(O)(C(C)=O)CC1OC1CC(N)C(O)C(C)O1 STQGQHZAVUOBTE-UHFFFAOYSA-N 0.000 description 2
- 208000030507 AIDS Diseases 0.000 description 2
- IKHGUXGNUITLKF-UHFFFAOYSA-N Acetaldehyde Chemical compound CC=O IKHGUXGNUITLKF-UHFFFAOYSA-N 0.000 description 2
- 108010012934 Albumin-Bound Paclitaxel Proteins 0.000 description 2
- 206010003571 Astrocytoma Diseases 0.000 description 2
- 229940122361 Bisphosphonate Drugs 0.000 description 2
- 206010006143 Brain stem glioma Diseases 0.000 description 2
- 239000004322 Butylated hydroxytoluene Substances 0.000 description 2
- NLZUEZXRPGMBCV-UHFFFAOYSA-N Butylhydroxytoluene Chemical compound CC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 NLZUEZXRPGMBCV-UHFFFAOYSA-N 0.000 description 2
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 2
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 2
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 2
- PTOAARAWEBMLNO-KVQBGUIXSA-N Cladribine Chemical compound C1=NC=2C(N)=NC(Cl)=NC=2N1[C@H]1C[C@H](O)[C@@H](CO)O1 PTOAARAWEBMLNO-KVQBGUIXSA-N 0.000 description 2
- 102000008186 Collagen Human genes 0.000 description 2
- 108010035532 Collagen Proteins 0.000 description 2
- 229920002785 Croscarmellose sodium Polymers 0.000 description 2
- 206010011686 Cutaneous vasculitis Diseases 0.000 description 2
- PQNNIEWMPIULRS-UHFFFAOYSA-N Cytostatin Natural products CC=CC=CC=CC(O)C(C)C(OP(O)(O)=O)CCC(C)C1OC(=O)C=CC1C PQNNIEWMPIULRS-UHFFFAOYSA-N 0.000 description 2
- ZQZFYGIXNQKOAV-OCEACIFDSA-N Droloxifene Chemical compound C=1C=CC=CC=1C(/CC)=C(C=1C=C(O)C=CC=1)\C1=CC=C(OCCN(C)C)C=C1 ZQZFYGIXNQKOAV-OCEACIFDSA-N 0.000 description 2
- 206010014950 Eosinophilia Diseases 0.000 description 2
- BRLQWZUYTZBJKN-UHFFFAOYSA-N Epichlorohydrin Chemical compound ClCC1CO1 BRLQWZUYTZBJKN-UHFFFAOYSA-N 0.000 description 2
- 208000031637 Erythroblastic Acute Leukemia Diseases 0.000 description 2
- 208000036566 Erythroleukaemia Diseases 0.000 description 2
- IMROMDMJAWUWLK-UHFFFAOYSA-N Ethenol Chemical compound OC=C IMROMDMJAWUWLK-UHFFFAOYSA-N 0.000 description 2
- JOYRKODLDBILNP-UHFFFAOYSA-N Ethyl urethane Chemical compound CCOC(N)=O JOYRKODLDBILNP-UHFFFAOYSA-N 0.000 description 2
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 2
- 108090000379 Fibroblast growth factor 2 Proteins 0.000 description 2
- ZWZWYGMENQVNFU-UHFFFAOYSA-N Glycerophosphorylserin Natural products OC(=O)C(N)COP(O)(=O)OCC(O)CO ZWZWYGMENQVNFU-UHFFFAOYSA-N 0.000 description 2
- 208000006050 Hemangiopericytoma Diseases 0.000 description 2
- 208000002250 Hematologic Neoplasms Diseases 0.000 description 2
- 244000043261 Hevea brasiliensis Species 0.000 description 2
- QIGBRXMKCJKVMJ-UHFFFAOYSA-N Hydroquinone Chemical compound OC1=CC=C(O)C=C1 QIGBRXMKCJKVMJ-UHFFFAOYSA-N 0.000 description 2
- XDXDZDZNSLXDNA-UHFFFAOYSA-N Idarubicin Natural products C1C(N)C(O)C(C)OC1OC1C2=C(O)C(C(=O)C3=CC=CC=C3C3=O)=C3C(O)=C2CC(O)(C(C)=O)C1 XDXDZDZNSLXDNA-UHFFFAOYSA-N 0.000 description 2
- 108010063738 Interleukins Proteins 0.000 description 2
- 102000015696 Interleukins Human genes 0.000 description 2
- 208000007766 Kaposi sarcoma Diseases 0.000 description 2
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 2
- 208000031671 Large B-Cell Diffuse Lymphoma Diseases 0.000 description 2
- 206010024305 Leukaemia monocytic Diseases 0.000 description 2
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 2
- 206010026673 Malignant Pleural Effusion Diseases 0.000 description 2
- 206010061269 Malignant peritoneal neoplasm Diseases 0.000 description 2
- 208000025205 Mantle-Cell Lymphoma Diseases 0.000 description 2
- 101710085938 Matrix protein Proteins 0.000 description 2
- 229930126263 Maytansine Natural products 0.000 description 2
- 101710127721 Membrane protein Proteins 0.000 description 2
- 206010027406 Mesothelioma Diseases 0.000 description 2
- 206010027476 Metastases Diseases 0.000 description 2
- 206010059282 Metastases to central nervous system Diseases 0.000 description 2
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 2
- 229930192392 Mitomycin Natural products 0.000 description 2
- CHJJGSNFBQVOTG-UHFFFAOYSA-N N-methyl-guanidine Natural products CNC(N)=N CHJJGSNFBQVOTG-UHFFFAOYSA-N 0.000 description 2
- 150000001204 N-oxides Chemical class 0.000 description 2
- LYPFDBRUNKHDGX-SOGSVHMOSA-N N1C2=CC=C1\C(=C1\C=CC(=N1)\C(=C1\C=C/C(/N1)=C(/C1=N/C(/CC1)=C2/C1=CC(O)=CC=C1)C1=CC(O)=CC=C1)\C1=CC(O)=CC=C1)C1=CC(O)=CC=C1 Chemical compound N1C2=CC=C1\C(=C1\C=CC(=N1)\C(=C1\C=C/C(/N1)=C(/C1=N/C(/CC1)=C2/C1=CC(O)=CC=C1)C1=CC(O)=CC=C1)\C1=CC(O)=CC=C1)C1=CC(O)=CC=C1 LYPFDBRUNKHDGX-SOGSVHMOSA-N 0.000 description 2
- 206010029260 Neuroblastoma Diseases 0.000 description 2
- 239000004677 Nylon Substances 0.000 description 2
- 108091034117 Oligonucleotide Proteins 0.000 description 2
- 102000035195 Peptidases Human genes 0.000 description 2
- 108091005804 Peptidases Proteins 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- GLUUGHFHXGJENI-UHFFFAOYSA-N Piperazine Chemical compound C1CNCCN1 GLUUGHFHXGJENI-UHFFFAOYSA-N 0.000 description 2
- 229920012485 Plasticized Polyvinyl chloride Polymers 0.000 description 2
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 2
- 239000005062 Polybutadiene Substances 0.000 description 2
- 229920002367 Polyisobutene Polymers 0.000 description 2
- HRHKSTOGXBBQCB-UHFFFAOYSA-N Porfiromycine Chemical compound O=C1C(N)=C(C)C(=O)C2=C1C(COC(N)=O)C1(OC)C3N(C)C3CN12 HRHKSTOGXBBQCB-UHFFFAOYSA-N 0.000 description 2
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 2
- HFVNWDWLWUCIHC-GUPDPFMOSA-N Prednimustine Chemical compound O=C([C@@]1(O)CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)[C@@H](O)C[C@@]21C)COC(=O)CCCC1=CC=C(N(CCCl)CCCl)C=C1 HFVNWDWLWUCIHC-GUPDPFMOSA-N 0.000 description 2
- RJKFOVLPORLFTN-LEKSSAKUSA-N Progesterone Chemical compound C1CC2=CC(=O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H](C(=O)C)[C@@]1(C)CC2 RJKFOVLPORLFTN-LEKSSAKUSA-N 0.000 description 2
- ZTHYODDOHIVTJV-UHFFFAOYSA-N Propyl gallate Chemical compound CCCOC(=O)C1=CC(O)=C(O)C(O)=C1 ZTHYODDOHIVTJV-UHFFFAOYSA-N 0.000 description 2
- 239000004365 Protease Substances 0.000 description 2
- 229940079156 Proteasome inhibitor Drugs 0.000 description 2
- 229940123924 Protein kinase C inhibitor Drugs 0.000 description 2
- 102100033810 RAC-alpha serine/threonine-protein kinase Human genes 0.000 description 2
- 208000006265 Renal cell carcinoma Diseases 0.000 description 2
- 239000008156 Ringer's lactate solution Substances 0.000 description 2
- 206010039710 Scleroderma Diseases 0.000 description 2
- 229920001800 Shellac Polymers 0.000 description 2
- 102000019259 Succinate Dehydrogenase Human genes 0.000 description 2
- 108010012901 Succinate Dehydrogenase Proteins 0.000 description 2
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 2
- 108010065917 TOR Serine-Threonine Kinases Proteins 0.000 description 2
- 102000013530 TOR Serine-Threonine Kinases Human genes 0.000 description 2
- 229940123237 Taxane Drugs 0.000 description 2
- ZMZDMBWJUHKJPS-UHFFFAOYSA-M Thiocyanate anion Chemical compound [S-]C#N ZMZDMBWJUHKJPS-UHFFFAOYSA-M 0.000 description 2
- 102000036693 Thrombopoietin Human genes 0.000 description 2
- 108010041111 Thrombopoietin Proteins 0.000 description 2
- 108091023040 Transcription factor Proteins 0.000 description 2
- 102000040945 Transcription factor Human genes 0.000 description 2
- 108010050144 Triptorelin Pamoate Proteins 0.000 description 2
- 102100031638 Tuberin Human genes 0.000 description 2
- 102000044209 Tumor Suppressor Genes Human genes 0.000 description 2
- 108700025716 Tumor Suppressor Genes Proteins 0.000 description 2
- 108010073929 Vascular Endothelial Growth Factor A Proteins 0.000 description 2
- 102000005789 Vascular Endothelial Growth Factors Human genes 0.000 description 2
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 description 2
- 240000008042 Zea mays Species 0.000 description 2
- 235000005824 Zea mays ssp. parviglumis Nutrition 0.000 description 2
- 235000002017 Zea mays subsp mays Nutrition 0.000 description 2
- PQNNIEWMPIULRS-SUTYWZMXSA-N [(8e,10e,12e)-7-hydroxy-6-methyl-2-(3-methyl-6-oxo-2,3-dihydropyran-2-yl)tetradeca-8,10,12-trien-5-yl] dihydrogen phosphate Chemical compound C\C=C\C=C\C=C\C(O)C(C)C(OP(O)(O)=O)CCC(C)C1OC(=O)C=CC1C PQNNIEWMPIULRS-SUTYWZMXSA-N 0.000 description 2
- QPWBZVAOCWJTFK-UHFFFAOYSA-L [2-(azanidylmethyl)-3-hydroxy-2-(hydroxymethyl)propyl]azanide;cyclobutane-1,1-dicarboxylate;platinum(4+) Chemical compound [Pt+4].[NH-]CC(C[NH-])(CO)CO.[O-]C(=O)C1(C([O-])=O)CCC1 QPWBZVAOCWJTFK-UHFFFAOYSA-L 0.000 description 2
- JLCPHMBAVCMARE-UHFFFAOYSA-N [3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-hydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methyl [5-(6-aminopurin-9-yl)-2-(hydroxymethyl)oxolan-3-yl] hydrogen phosphate Polymers Cc1cn(C2CC(OP(O)(=O)OCC3OC(CC3OP(O)(=O)OCC3OC(CC3O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c3nc(N)[nH]c4=O)C(COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3CO)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cc(C)c(=O)[nH]c3=O)n3cc(C)c(=O)[nH]c3=O)n3ccc(N)nc3=O)n3cc(C)c(=O)[nH]c3=O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)O2)c(=O)[nH]c1=O JLCPHMBAVCMARE-UHFFFAOYSA-N 0.000 description 2
- 229940028652 abraxane Drugs 0.000 description 2
- 238000010521 absorption reaction Methods 0.000 description 2
- 150000001242 acetic acid derivatives Chemical class 0.000 description 2
- 230000002378 acidificating effect Effects 0.000 description 2
- USZYSDMBJDPRIF-SVEJIMAYSA-N aclacinomycin A Chemical compound O([C@H]1[C@@H](O)C[C@@H](O[C@H]1C)O[C@H]1[C@H](C[C@@H](O[C@H]1C)O[C@H]1C[C@]([C@@H](C2=CC=3C(=O)C4=CC=CC(O)=C4C(=O)C=3C(O)=C21)C(=O)OC)(O)CC)N(C)C)[C@H]1CCC(=O)[C@H](C)O1 USZYSDMBJDPRIF-SVEJIMAYSA-N 0.000 description 2
- 229960004176 aclarubicin Drugs 0.000 description 2
- NIXOWILDQLNWCW-UHFFFAOYSA-N acrylic acid group Chemical group C(C=C)(=O)O NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 2
- RJURFGZVJUQBHK-UHFFFAOYSA-N actinomycin D Natural products CC1OC(=O)C(C(C)C)N(C)C(=O)CN(C)C(=O)C2CCCN2C(=O)C(C(C)C)NC(=O)C1NC(=O)C1=C(N)C(=O)C(C)=C2OC(C(C)=CC=C3C(=O)NC4C(=O)NC(C(N5CCCC5C(=O)N(C)CC(=O)N(C)C(C(C)C)C(=O)OC4C)=O)C(C)C)=C3N=C21 RJURFGZVJUQBHK-UHFFFAOYSA-N 0.000 description 2
- 230000004913 activation Effects 0.000 description 2
- 208000021841 acute erythroid leukemia Diseases 0.000 description 2
- 125000004442 acylamino group Chemical group 0.000 description 2
- 238000007792 addition Methods 0.000 description 2
- 239000000654 additive Substances 0.000 description 2
- 230000000996 additive effect Effects 0.000 description 2
- 229950004955 adozelesin Drugs 0.000 description 2
- BYRVKDUQDLJUBX-JJCDCTGGSA-N adozelesin Chemical compound C1=CC=C2OC(C(=O)NC=3C=C4C=C(NC4=CC=3)C(=O)N3C[C@H]4C[C@]44C5=C(C(C=C43)=O)NC=C5C)=CC2=C1 BYRVKDUQDLJUBX-JJCDCTGGSA-N 0.000 description 2
- 150000001299 aldehydes Chemical class 0.000 description 2
- 108700025316 aldesleukin Proteins 0.000 description 2
- 229960005310 aldesleukin Drugs 0.000 description 2
- 125000005262 alkoxyamine group Chemical group 0.000 description 2
- 125000003282 alkyl amino group Chemical group 0.000 description 2
- 229960000473 altretamine Drugs 0.000 description 2
- 150000001409 amidines Chemical class 0.000 description 2
- 229910021529 ammonia Inorganic materials 0.000 description 2
- 229960001220 amsacrine Drugs 0.000 description 2
- XCPGHVQEEXUHNC-UHFFFAOYSA-N amsacrine Chemical compound COC1=CC(NS(C)(=O)=O)=CC=C1NC1=C(C=CC=C2)C2=NC2=CC=CC=C12 XCPGHVQEEXUHNC-UHFFFAOYSA-N 0.000 description 2
- 206010002224 anaplastic astrocytoma Diseases 0.000 description 2
- 229960002932 anastrozole Drugs 0.000 description 2
- YBBLVLTVTVSKRW-UHFFFAOYSA-N anastrozole Chemical compound N#CC(C)(C)C1=CC(C(C)(C#N)C)=CC(CN2N=CN=C2)=C1 YBBLVLTVTVSKRW-UHFFFAOYSA-N 0.000 description 2
- 239000003098 androgen Substances 0.000 description 2
- 208000007502 anemia Diseases 0.000 description 2
- 239000004037 angiogenesis inhibitor Substances 0.000 description 2
- 230000002491 angiogenic effect Effects 0.000 description 2
- 229940069428 antacid Drugs 0.000 description 2
- 239000003159 antacid agent Substances 0.000 description 2
- 239000003242 anti bacterial agent Substances 0.000 description 2
- 229940088710 antibiotic agent Drugs 0.000 description 2
- 238000011319 anticancer therapy Methods 0.000 description 2
- 229940045985 antineoplastic platinum compound Drugs 0.000 description 2
- 238000013459 approach Methods 0.000 description 2
- 239000008135 aqueous vehicle Substances 0.000 description 2
- 239000008122 artificial sweetener Substances 0.000 description 2
- 239000011668 ascorbic acid Substances 0.000 description 2
- 229960005070 ascorbic acid Drugs 0.000 description 2
- 238000003556 assay Methods 0.000 description 2
- XFILPEOLDIKJHX-QYZOEREBSA-N batimastat Chemical compound C([C@@H](C(=O)NC)NC(=O)[C@H](CC(C)C)[C@H](CSC=1SC=CC=1)C(=O)NO)C1=CC=CC=C1 XFILPEOLDIKJHX-QYZOEREBSA-N 0.000 description 2
- 229950001858 batimastat Drugs 0.000 description 2
- 239000000440 bentonite Substances 0.000 description 2
- 235000012216 bentonite Nutrition 0.000 description 2
- 229910000278 bentonite Inorganic materials 0.000 description 2
- SVPXDRXYRYOSEX-UHFFFAOYSA-N bentoquatam Chemical compound O.O=[Si]=O.O=[Al]O[Al]=O SVPXDRXYRYOSEX-UHFFFAOYSA-N 0.000 description 2
- 125000003785 benzimidazolyl group Chemical group N1=C(NC2=C1C=CC=C2)* 0.000 description 2
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 2
- 229960000397 bevacizumab Drugs 0.000 description 2
- 229940087430 biaxin Drugs 0.000 description 2
- 229960000997 bicalutamide Drugs 0.000 description 2
- 230000004071 biological effect Effects 0.000 description 2
- 229950008548 bisantrene Drugs 0.000 description 2
- 150000004663 bisphosphonates Chemical class 0.000 description 2
- 229950006844 bizelesin Drugs 0.000 description 2
- 210000001124 body fluid Anatomy 0.000 description 2
- 239000010839 body fluid Substances 0.000 description 2
- 238000010322 bone marrow transplantation Methods 0.000 description 2
- 210000000481 breast Anatomy 0.000 description 2
- 229960002092 busulfan Drugs 0.000 description 2
- 229920005549 butyl rubber Polymers 0.000 description 2
- 235000010354 butylated hydroxytoluene Nutrition 0.000 description 2
- 229940095259 butylated hydroxytoluene Drugs 0.000 description 2
- 239000011575 calcium Substances 0.000 description 2
- 229910052791 calcium Inorganic materials 0.000 description 2
- BMLSTPRTEKLIPM-UHFFFAOYSA-I calcium;potassium;disodium;hydrogen carbonate;dichloride;dihydroxide;hydrate Chemical compound O.[OH-].[OH-].[Na+].[Na+].[Cl-].[Cl-].[K+].[Ca+2].OC([O-])=O BMLSTPRTEKLIPM-UHFFFAOYSA-I 0.000 description 2
- VSJKWCGYPAHWDS-FQEVSTJZSA-N camptothecin Chemical compound C1=CC=C2C=C(CN3C4=CC5=C(C3=O)COC(=O)[C@]5(O)CC)C4=NC2=C1 VSJKWCGYPAHWDS-FQEVSTJZSA-N 0.000 description 2
- 239000004202 carbamide Substances 0.000 description 2
- 150000001721 carbon Chemical group 0.000 description 2
- CREMABGTGYGIQB-UHFFFAOYSA-N carbon carbon Chemical compound C.C CREMABGTGYGIQB-UHFFFAOYSA-N 0.000 description 2
- 239000001569 carbon dioxide Substances 0.000 description 2
- 229910002092 carbon dioxide Inorganic materials 0.000 description 2
- 239000011203 carbon fibre reinforced carbon Substances 0.000 description 2
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 2
- 229960005243 carmustine Drugs 0.000 description 2
- 239000000969 carrier Substances 0.000 description 2
- BBZDXMBRAFTCAA-AREMUKBSSA-N carzelesin Chemical compound C1=2NC=C(C)C=2C([C@H](CCl)CN2C(=O)C=3NC4=CC=C(C=C4C=3)NC(=O)C3=CC4=CC=C(C=C4O3)N(CC)CC)=C2C=C1OC(=O)NC1=CC=CC=C1 BBZDXMBRAFTCAA-AREMUKBSSA-N 0.000 description 2
- 229950007509 carzelesin Drugs 0.000 description 2
- 150000001768 cations Chemical class 0.000 description 2
- 210000002421 cell wall Anatomy 0.000 description 2
- 230000019522 cellular metabolic process Effects 0.000 description 2
- 229920002678 cellulose Chemical class 0.000 description 2
- 239000001913 cellulose Chemical class 0.000 description 2
- 235000010980 cellulose Nutrition 0.000 description 2
- 229940081734 cellulose acetate phthalate Drugs 0.000 description 2
- 238000005119 centrifugation Methods 0.000 description 2
- 239000002738 chelating agent Substances 0.000 description 2
- OSASVXMJTNOKOY-UHFFFAOYSA-N chlorobutanol Chemical compound CC(C)(O)C(Cl)(Cl)Cl OSASVXMJTNOKOY-UHFFFAOYSA-N 0.000 description 2
- 210000000349 chromosome Anatomy 0.000 description 2
- 230000001684 chronic effect Effects 0.000 description 2
- 208000024207 chronic leukemia Diseases 0.000 description 2
- 150000001860 citric acid derivatives Chemical class 0.000 description 2
- 229960002436 cladribine Drugs 0.000 description 2
- AGOYDEPGAOXOCK-KCBOHYOISA-N clarithromycin Chemical compound O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H](O)[C@@H](C)C(=O)[C@H](C)C[C@](C)([C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)OC)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 AGOYDEPGAOXOCK-KCBOHYOISA-N 0.000 description 2
- 239000011248 coating agent Substances 0.000 description 2
- 229920001436 collagen Polymers 0.000 description 2
- 210000001072 colon Anatomy 0.000 description 2
- 208000029742 colonic neoplasm Diseases 0.000 description 2
- 235000005822 corn Nutrition 0.000 description 2
- 235000012343 cottonseed oil Nutrition 0.000 description 2
- 239000002385 cottonseed oil Substances 0.000 description 2
- ZYGHJZDHTFUPRJ-UHFFFAOYSA-N coumarin Chemical compound C1=CC=C2OC(=O)C=CC2=C1 ZYGHJZDHTFUPRJ-UHFFFAOYSA-N 0.000 description 2
- 239000006071 cream Substances 0.000 description 2
- 229960001681 croscarmellose sodium Drugs 0.000 description 2
- 235000010947 crosslinked sodium carboxy methyl cellulose Nutrition 0.000 description 2
- 208000035250 cutaneous malignant susceptibility to 1 melanoma Diseases 0.000 description 2
- XLJMAIOERFSOGZ-UHFFFAOYSA-M cyanate Chemical compound [O-]C#N XLJMAIOERFSOGZ-UHFFFAOYSA-M 0.000 description 2
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 2
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 2
- 229960000684 cytarabine Drugs 0.000 description 2
- STQGQHZAVUOBTE-VGBVRHCVSA-N daunorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(C)=O)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 STQGQHZAVUOBTE-VGBVRHCVSA-N 0.000 description 2
- 229940026692 decadron Drugs 0.000 description 2
- 229960003603 decitabine Drugs 0.000 description 2
- 230000002074 deregulated effect Effects 0.000 description 2
- 235000014113 dietary fatty acids Nutrition 0.000 description 2
- 206010012818 diffuse large B-cell lymphoma Diseases 0.000 description 2
- OTKJDMGTUTTYMP-UHFFFAOYSA-N dihydrosphingosine Natural products CCCCCCCCCCCCCCCC(O)C(N)CO OTKJDMGTUTTYMP-UHFFFAOYSA-N 0.000 description 2
- SWSQBOPZIKWTGO-UHFFFAOYSA-N dimethylaminoamidine Natural products CN(C)C(N)=N SWSQBOPZIKWTGO-UHFFFAOYSA-N 0.000 description 2
- BNIILDVGGAEEIG-UHFFFAOYSA-L disodium hydrogen phosphate Chemical compound [Na+].[Na+].OP([O-])([O-])=O BNIILDVGGAEEIG-UHFFFAOYSA-L 0.000 description 2
- 229910000397 disodium phosphate Inorganic materials 0.000 description 2
- 235000019800 disodium phosphate Nutrition 0.000 description 2
- 239000002270 dispersing agent Substances 0.000 description 2
- 239000006185 dispersion Substances 0.000 description 2
- 238000004090 dissolution Methods 0.000 description 2
- 238000009826 distribution Methods 0.000 description 2
- NOPFSRXAKWQILS-UHFFFAOYSA-N docosan-1-ol Chemical compound CCCCCCCCCCCCCCCCCCCCCCO NOPFSRXAKWQILS-UHFFFAOYSA-N 0.000 description 2
- 229940115080 doxil Drugs 0.000 description 2
- 229950004203 droloxifene Drugs 0.000 description 2
- 238000001035 drying Methods 0.000 description 2
- 235000013399 edible fruits Nutrition 0.000 description 2
- 229960001776 edrecolomab Drugs 0.000 description 2
- 229940000733 emcyt Drugs 0.000 description 2
- 150000002081 enamines Chemical class 0.000 description 2
- 238000006345 epimerization reaction Methods 0.000 description 2
- 229940082789 erbitux Drugs 0.000 description 2
- HCZKYJDFEPMADG-UHFFFAOYSA-N erythro-nordihydroguaiaretic acid Natural products C=1C=C(O)C(O)=CC=1CC(C)C(C)CC1=CC=C(O)C(O)=C1 HCZKYJDFEPMADG-UHFFFAOYSA-N 0.000 description 2
- 229960001842 estramustine Drugs 0.000 description 2
- 239000000328 estrogen antagonist Substances 0.000 description 2
- WCDWBPCFGJXFJZ-UHFFFAOYSA-N etanidazole Chemical compound OCCNC(=O)CN1C=CN=C1[N+]([O-])=O WCDWBPCFGJXFJZ-UHFFFAOYSA-N 0.000 description 2
- HQQADJVZYDDRJT-UHFFFAOYSA-N ethene;prop-1-ene Chemical group C=C.CC=C HQQADJVZYDDRJT-UHFFFAOYSA-N 0.000 description 2
- LIQODXNTTZAGID-OCBXBXKTSA-N etoposide phosphate Chemical compound COC1=C(OP(O)(O)=O)C(OC)=CC([C@@H]2C3=CC=4OCOC=4C=C3[C@@H](O[C@H]3[C@@H]([C@@H](O)[C@@H]4O[C@H](C)OC[C@H]4O3)O)[C@@H]3[C@@H]2C(OC3)=O)=C1 LIQODXNTTZAGID-OCBXBXKTSA-N 0.000 description 2
- 229960000752 etoposide phosphate Drugs 0.000 description 2
- 238000013213 extrapolation Methods 0.000 description 2
- 239000000194 fatty acid Substances 0.000 description 2
- 229930195729 fatty acid Natural products 0.000 description 2
- 150000004665 fatty acids Chemical class 0.000 description 2
- NMUSYJAQQFHJEW-ARQDHWQXSA-N fazarabine Chemical compound O=C1N=C(N)N=CN1[C@H]1[C@@H](O)[C@H](O)[C@@H](CO)O1 NMUSYJAQQFHJEW-ARQDHWQXSA-N 0.000 description 2
- 229950005096 fazarabine Drugs 0.000 description 2
- 229950003662 fenretinide Drugs 0.000 description 2
- 210000004700 fetal blood Anatomy 0.000 description 2
- 229960004177 filgrastim Drugs 0.000 description 2
- 239000007888 film coating Substances 0.000 description 2
- 238000009501 film coating Methods 0.000 description 2
- 238000009093 first-line therapy Methods 0.000 description 2
- 238000004108 freeze drying Methods 0.000 description 2
- 125000002541 furyl group Chemical group 0.000 description 2
- 230000004927 fusion Effects 0.000 description 2
- CHPZKNULDCNCBW-UHFFFAOYSA-N gallium nitrate Chemical compound [Ga+3].[O-][N+]([O-])=O.[O-][N+]([O-])=O.[O-][N+]([O-])=O CHPZKNULDCNCBW-UHFFFAOYSA-N 0.000 description 2
- 229960002963 ganciclovir Drugs 0.000 description 2
- IRSCQMHQWWYFCW-UHFFFAOYSA-N ganciclovir Chemical compound O=C1NC(N)=NC2=C1N=CN2COC(CO)CO IRSCQMHQWWYFCW-UHFFFAOYSA-N 0.000 description 2
- 239000007903 gelatin capsule Substances 0.000 description 2
- 229940084910 gliadel Drugs 0.000 description 2
- 230000004153 glucose metabolism Effects 0.000 description 2
- RWSXRVCMGQZWBV-WDSKDSINSA-N glutathione Chemical compound OC(=O)[C@@H](N)CCC(=O)N[C@@H](CS)C(=O)NCC(O)=O RWSXRVCMGQZWBV-WDSKDSINSA-N 0.000 description 2
- 208000024908 graft versus host disease Diseases 0.000 description 2
- 210000003128 head Anatomy 0.000 description 2
- 208000014829 head and neck neoplasm Diseases 0.000 description 2
- 230000036541 health Effects 0.000 description 2
- 208000024200 hematopoietic and lymphoid system neoplasm Diseases 0.000 description 2
- 229940022353 herceptin Drugs 0.000 description 2
- UUVWYPNAQBNQJQ-UHFFFAOYSA-N hexamethylmelamine Chemical compound CN(C)C1=NC(N(C)C)=NC(N(C)C)=N1 UUVWYPNAQBNQJQ-UHFFFAOYSA-N 0.000 description 2
- 150000007857 hydrazones Chemical class 0.000 description 2
- 229920001477 hydrophilic polymer Polymers 0.000 description 2
- 229960000908 idarubicin Drugs 0.000 description 2
- 229960003685 imatinib mesylate Drugs 0.000 description 2
- 125000002883 imidazolyl group Chemical group 0.000 description 2
- 150000003949 imides Chemical class 0.000 description 2
- 230000002519 immonomodulatory effect Effects 0.000 description 2
- 230000002779 inactivation Effects 0.000 description 2
- 208000015181 infectious disease Diseases 0.000 description 2
- 230000002401 inhibitory effect Effects 0.000 description 2
- 229940047124 interferons Drugs 0.000 description 2
- 229940047122 interleukins Drugs 0.000 description 2
- 238000007918 intramuscular administration Methods 0.000 description 2
- 230000009545 invasion Effects 0.000 description 2
- PNDPGZBMCMUPRI-UHFFFAOYSA-N iodine Chemical compound II PNDPGZBMCMUPRI-UHFFFAOYSA-N 0.000 description 2
- 229920000554 ionomer Polymers 0.000 description 2
- 239000012948 isocyanate Substances 0.000 description 2
- 150000002513 isocyanates Chemical class 0.000 description 2
- 150000002540 isothiocyanates Chemical class 0.000 description 2
- 239000007951 isotonicity adjuster Substances 0.000 description 2
- 125000000842 isoxazolyl group Chemical group 0.000 description 2
- 150000002576 ketones Chemical class 0.000 description 2
- 210000003734 kidney Anatomy 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 2
- 108010021336 lanreotide Proteins 0.000 description 2
- 229960003881 letrozole Drugs 0.000 description 2
- HPJKCIUCZWXJDR-UHFFFAOYSA-N letrozole Chemical compound C1=CC(C#N)=CC=C1C(N1N=CN=C1)C1=CC=C(C#N)C=C1 HPJKCIUCZWXJDR-UHFFFAOYSA-N 0.000 description 2
- 230000000670 limiting effect Effects 0.000 description 2
- 239000006193 liquid solution Substances 0.000 description 2
- 239000006194 liquid suspension Substances 0.000 description 2
- 239000003589 local anesthetic agent Substances 0.000 description 2
- 229960005015 local anesthetics Drugs 0.000 description 2
- 239000006210 lotion Substances 0.000 description 2
- 239000007937 lozenge Substances 0.000 description 2
- 210000004072 lung Anatomy 0.000 description 2
- 210000003563 lymphoid tissue Anatomy 0.000 description 2
- 229910052749 magnesium Inorganic materials 0.000 description 2
- 230000036210 malignancy Effects 0.000 description 2
- 208000006178 malignant mesothelioma Diseases 0.000 description 2
- 229960003951 masoprocol Drugs 0.000 description 2
- HCZKYJDFEPMADG-TXEJJXNPSA-N masoprocol Chemical compound C([C@H](C)[C@H](C)CC=1C=C(O)C(O)=CC=1)C1=CC=C(O)C(O)=C1 HCZKYJDFEPMADG-TXEJJXNPSA-N 0.000 description 2
- WKPWGQKGSOKKOO-RSFHAFMBSA-N maytansine Chemical compound CO[C@@H]([C@@]1(O)C[C@](OC(=O)N1)([C@H]([C@@H]1O[C@@]1(C)[C@@H](OC(=O)[C@H](C)N(C)C(C)=O)CC(=O)N1C)C)[H])\C=C\C=C(C)\CC2=CC(OC)=C(Cl)C1=C2 WKPWGQKGSOKKOO-RSFHAFMBSA-N 0.000 description 2
- 238000002844 melting Methods 0.000 description 2
- 230000008018 melting Effects 0.000 description 2
- LWYJUZBXGAFFLP-OCNCTQISSA-N menogaril Chemical compound O1[C@@]2(C)[C@H](O)[C@@H](N(C)C)[C@H](O)[C@@H]1OC1=C3C(=O)C(C=C4C[C@@](C)(O)C[C@H](C4=C4O)OC)=C4C(=O)C3=C(O)C=C12 LWYJUZBXGAFFLP-OCNCTQISSA-N 0.000 description 2
- 229950002676 menogaril Drugs 0.000 description 2
- 230000002503 metabolic effect Effects 0.000 description 2
- 230000009401 metastasis Effects 0.000 description 2
- 125000005397 methacrylic acid ester group Chemical group 0.000 description 2
- CSJDCSCTVDEHRN-UHFFFAOYSA-N methane;molecular oxygen Chemical compound C.O=O CSJDCSCTVDEHRN-UHFFFAOYSA-N 0.000 description 2
- 235000010270 methyl p-hydroxybenzoate Nutrition 0.000 description 2
- OSWPMRLSEDHDFF-UHFFFAOYSA-N methyl salicylate Chemical compound COC(=O)C1=CC=CC=C1O OSWPMRLSEDHDFF-UHFFFAOYSA-N 0.000 description 2
- 239000008108 microcrystalline cellulose Substances 0.000 description 2
- 229940016286 microcrystalline cellulose Drugs 0.000 description 2
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 2
- 239000004005 microsphere Substances 0.000 description 2
- 229960004857 mitomycin Drugs 0.000 description 2
- ZAHQPTJLOCWVPG-UHFFFAOYSA-N mitoxantrone dihydrochloride Chemical compound Cl.Cl.O=C1C2=C(O)C=CC(O)=C2C(=O)C2=C1C(NCCNCCO)=CC=C2NCCNCCO ZAHQPTJLOCWVPG-UHFFFAOYSA-N 0.000 description 2
- 201000006894 monocytic leukemia Diseases 0.000 description 2
- 230000000877 morphologic effect Effects 0.000 description 2
- 210000004877 mucosa Anatomy 0.000 description 2
- NJSMWLQOCQIOPE-OCHFTUDZSA-N n-[(e)-[10-[(e)-(4,5-dihydro-1h-imidazol-2-ylhydrazinylidene)methyl]anthracen-9-yl]methylideneamino]-4,5-dihydro-1h-imidazol-2-amine Chemical compound N1CCN=C1N\N=C\C(C1=CC=CC=C11)=C(C=CC=C2)C2=C1\C=N\NC1=NCCN1 NJSMWLQOCQIOPE-OCHFTUDZSA-N 0.000 description 2
- 125000001624 naphthyl group Chemical group 0.000 description 2
- 229920003052 natural elastomer Polymers 0.000 description 2
- 229920001194 natural rubber Polymers 0.000 description 2
- 230000007935 neutral effect Effects 0.000 description 2
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 2
- 229920001778 nylon Polymers 0.000 description 2
- 229960005343 ondansetron Drugs 0.000 description 2
- 239000007935 oral tablet Substances 0.000 description 2
- 229950008017 ormaplatin Drugs 0.000 description 2
- 230000003204 osmotic effect Effects 0.000 description 2
- 229960001756 oxaliplatin Drugs 0.000 description 2
- DWAFYCQODLXJNR-BNTLRKBRSA-L oxaliplatin Chemical compound O1C(=O)C(=O)O[Pt]11N[C@@H]2CCCC[C@H]2N1 DWAFYCQODLXJNR-BNTLRKBRSA-L 0.000 description 2
- 125000002971 oxazolyl group Chemical group 0.000 description 2
- 230000003647 oxidation Effects 0.000 description 2
- 238000007254 oxidation reaction Methods 0.000 description 2
- 150000002923 oximes Chemical class 0.000 description 2
- 210000000496 pancreas Anatomy 0.000 description 2
- 208000008443 pancreatic carcinoma Diseases 0.000 description 2
- 201000005163 papillary serous adenocarcinoma Diseases 0.000 description 2
- 239000002245 particle Substances 0.000 description 2
- 230000037361 pathway Effects 0.000 description 2
- VPAWVRUHMJVRHU-VGDKGRGNSA-N perfosfamide Chemical compound OO[C@@H]1CCO[P@@](=O)(N(CCCl)CCCl)N1 VPAWVRUHMJVRHU-VGDKGRGNSA-N 0.000 description 2
- 229950009351 perfosfamide Drugs 0.000 description 2
- 201000002524 peritoneal carcinoma Diseases 0.000 description 2
- 230000003285 pharmacodynamic effect Effects 0.000 description 2
- ZQBAKBUEJOMQEX-UHFFFAOYSA-N phenyl salicylate Chemical compound OC1=CC=CC=C1C(=O)OC1=CC=CC=C1 ZQBAKBUEJOMQEX-UHFFFAOYSA-N 0.000 description 2
- 210000004214 philadelphia chromosome Anatomy 0.000 description 2
- 239000010452 phosphate Substances 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 2
- WTJKGGKOPKCXLL-RRHRGVEJSA-N phosphatidylcholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCCCCCCC=CCCCCCCCC WTJKGGKOPKCXLL-RRHRGVEJSA-N 0.000 description 2
- UEZVMMHDMIWARA-UHFFFAOYSA-M phosphonate Chemical compound [O-]P(=O)=O UEZVMMHDMIWARA-UHFFFAOYSA-M 0.000 description 2
- 229910000073 phosphorus hydride Inorganic materials 0.000 description 2
- 230000004962 physiological condition Effects 0.000 description 2
- 125000004193 piperazinyl group Chemical group 0.000 description 2
- 229920003023 plastic Polymers 0.000 description 2
- 239000004033 plastic Substances 0.000 description 2
- 229910052697 platinum Inorganic materials 0.000 description 2
- 150000003058 platinum compounds Chemical class 0.000 description 2
- 229920001490 poly(butyl methacrylate) polymer Polymers 0.000 description 2
- 229920001084 poly(chloroprene) Polymers 0.000 description 2
- 229920000747 poly(lactic acid) Polymers 0.000 description 2
- 229920003229 poly(methyl methacrylate) Polymers 0.000 description 2
- 229920002857 polybutadiene Polymers 0.000 description 2
- 125000003367 polycyclic group Chemical group 0.000 description 2
- 229920001195 polyisoprene Polymers 0.000 description 2
- 239000004926 polymethyl methacrylate Substances 0.000 description 2
- 229920000259 polyoxyethylene lauryl ether Polymers 0.000 description 2
- 235000010482 polyoxyethylene sorbitan monooleate Nutrition 0.000 description 2
- 239000000244 polyoxyethylene sorbitan monooleate Substances 0.000 description 2
- 229920001296 polysiloxane Polymers 0.000 description 2
- 229920000136 polysorbate Polymers 0.000 description 2
- 229920000053 polysorbate 80 Polymers 0.000 description 2
- 229920002451 polyvinyl alcohol Polymers 0.000 description 2
- 229960004694 prednimustine Drugs 0.000 description 2
- CPTBDICYNRMXFX-UHFFFAOYSA-N procarbazine Chemical compound CNNCC1=CC=C(C(=O)NC(C)C)C=C1 CPTBDICYNRMXFX-UHFFFAOYSA-N 0.000 description 2
- 229960000624 procarbazine Drugs 0.000 description 2
- 102000004196 processed proteins & peptides Human genes 0.000 description 2
- QQONPFPTGQHPMA-UHFFFAOYSA-N propylene Natural products CC=C QQONPFPTGQHPMA-UHFFFAOYSA-N 0.000 description 2
- RUOJZAUFBMNUDX-UHFFFAOYSA-N propylene carbonate Chemical compound CC1COC(=O)O1 RUOJZAUFBMNUDX-UHFFFAOYSA-N 0.000 description 2
- 229940093625 propylene glycol monostearate Drugs 0.000 description 2
- 125000004805 propylene group Chemical group [H]C([H])([H])C([H])([*:1])C([H])([H])[*:2] 0.000 description 2
- QELSKZZBTMNZEB-UHFFFAOYSA-N propylparaben Chemical compound CCCOC(=O)C1=CC=C(O)C=C1 QELSKZZBTMNZEB-UHFFFAOYSA-N 0.000 description 2
- 210000002307 prostate Anatomy 0.000 description 2
- 239000003207 proteasome inhibitor Substances 0.000 description 2
- 239000003881 protein kinase C inhibitor Substances 0.000 description 2
- RXWNCPJZOCPEPQ-NVWDDTSBSA-N puromycin Chemical compound C1=CC(OC)=CC=C1C[C@H](N)C(=O)N[C@H]1[C@@H](O)[C@H](N2C3=NC=NC(=C3N=C2)N(C)C)O[C@@H]1CO RXWNCPJZOCPEPQ-NVWDDTSBSA-N 0.000 description 2
- BBEAQIROQSPTKN-UHFFFAOYSA-N pyrene Chemical compound C1=CC=C2C=CC3=CC=CC4=CC=C1C2=C43 BBEAQIROQSPTKN-UHFFFAOYSA-N 0.000 description 2
- 125000000714 pyrimidinyl group Chemical group 0.000 description 2
- 210000000664 rectum Anatomy 0.000 description 2
- 208000037922 refractory disease Diseases 0.000 description 2
- 208000015347 renal cell adenocarcinoma Diseases 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 229940081974 saccharin Drugs 0.000 description 2
- 235000019204 saccharin Nutrition 0.000 description 2
- 239000000901 saccharin and its Na,K and Ca salt Substances 0.000 description 2
- 229950008902 safingol Drugs 0.000 description 2
- CGFVUVWMYIHGHS-UHFFFAOYSA-N saintopin Chemical compound C1=C(O)C=C2C=C(C(=O)C=3C(=C(O)C=C(C=3)O)C3=O)C3=C(O)C2=C1O CGFVUVWMYIHGHS-UHFFFAOYSA-N 0.000 description 2
- 229960002530 sargramostim Drugs 0.000 description 2
- 229920006395 saturated elastomer Polymers 0.000 description 2
- 230000028327 secretion Effects 0.000 description 2
- FVLVBPDQNARYJU-UHFFFAOYSA-N semustine Chemical compound CC1CCC(NC(=O)N(CCCl)N=O)CC1 FVLVBPDQNARYJU-UHFFFAOYSA-N 0.000 description 2
- 230000035807 sensation Effects 0.000 description 2
- 235000019615 sensations Nutrition 0.000 description 2
- 239000004208 shellac Substances 0.000 description 2
- ZLGIYFNHBLSMPS-ATJNOEHPSA-N shellac Chemical compound OCCCCCC(O)C(O)CCCCCCCC(O)=O.C1C23[C@H](C(O)=O)CCC2[C@](C)(CO)[C@@H]1C(C(O)=O)=C[C@@H]3O ZLGIYFNHBLSMPS-ATJNOEHPSA-N 0.000 description 2
- 229940113147 shellac Drugs 0.000 description 2
- 235000013874 shellac Nutrition 0.000 description 2
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 2
- 235000017557 sodium bicarbonate Nutrition 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L sodium carbonate Substances [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- 239000001488 sodium phosphate Substances 0.000 description 2
- 235000011069 sorbitan monooleate Nutrition 0.000 description 2
- 239000001593 sorbitan monooleate Substances 0.000 description 2
- 229940035049 sorbitan monooleate Drugs 0.000 description 2
- PFNFFQXMRSDOHW-UHFFFAOYSA-N spermine Chemical compound NCCCNCCCCNCCCN PFNFFQXMRSDOHW-UHFFFAOYSA-N 0.000 description 2
- 238000011301 standard therapy Methods 0.000 description 2
- 239000008174 sterile solution Substances 0.000 description 2
- PVYJZLYGTZKPJE-UHFFFAOYSA-N streptonigrin Chemical compound C=1C=C2C(=O)C(OC)=C(N)C(=O)C2=NC=1C(C=1N)=NC(C(O)=O)=C(C)C=1C1=CC=C(OC)C(OC)=C1O PVYJZLYGTZKPJE-UHFFFAOYSA-N 0.000 description 2
- 238000007920 subcutaneous administration Methods 0.000 description 2
- 125000000547 substituted alkyl group Chemical group 0.000 description 2
- 229940124530 sulfonamide Drugs 0.000 description 2
- 150000003456 sulfonamides Chemical class 0.000 description 2
- 150000003457 sulfones Chemical class 0.000 description 2
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 description 2
- 239000011593 sulfur Substances 0.000 description 2
- MLKXDPUZXIRXEP-MFOYZWKCSA-N sulindac Chemical compound CC1=C(CC(O)=O)C2=CC(F)=CC=C2\C1=C/C1=CC=C(S(C)=O)C=C1 MLKXDPUZXIRXEP-MFOYZWKCSA-N 0.000 description 2
- 229960000894 sulindac Drugs 0.000 description 2
- 239000000829 suppository Substances 0.000 description 2
- 239000004094 surface-active agent Substances 0.000 description 2
- 230000004083 survival effect Effects 0.000 description 2
- 208000011580 syndromic disease Diseases 0.000 description 2
- 238000007910 systemic administration Methods 0.000 description 2
- 229940037128 systemic glucocorticoids Drugs 0.000 description 2
- 239000000454 talc Chemical class 0.000 description 2
- 229910052623 talc Inorganic materials 0.000 description 2
- 235000012222 talc Nutrition 0.000 description 2
- 230000008685 targeting Effects 0.000 description 2
- 229960001674 tegafur Drugs 0.000 description 2
- WFWLQNSHRPWKFK-ZCFIWIBFSA-N tegafur Chemical compound O=C1NC(=O)C(F)=CN1[C@@H]1OCCC1 WFWLQNSHRPWKFK-ZCFIWIBFSA-N 0.000 description 2
- 229960002197 temoporfin Drugs 0.000 description 2
- NRUKOCRGYNPUPR-QBPJDGROSA-N teniposide Chemical compound COC1=C(O)C(OC)=CC([C@@H]2C3=CC=4OCOC=4C=C3[C@@H](O[C@H]3[C@@H]([C@@H](O)[C@@H]4O[C@@H](OC[C@H]4O3)C=3SC=CC=3)O)[C@@H]3[C@@H]2C(OC3)=O)=C1 NRUKOCRGYNPUPR-QBPJDGROSA-N 0.000 description 2
- 229960001278 teniposide Drugs 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- 125000000335 thiazolyl group Chemical group 0.000 description 2
- 125000001544 thienyl group Chemical group 0.000 description 2
- 125000002813 thiocarbonyl group Chemical group *C(*)=S 0.000 description 2
- 150000003568 thioethers Chemical class 0.000 description 2
- 210000001541 thymus gland Anatomy 0.000 description 2
- 229960005267 tositumomab Drugs 0.000 description 2
- 231100000440 toxicity profile Toxicity 0.000 description 2
- 235000010487 tragacanth Nutrition 0.000 description 2
- 239000000196 tragacanth Substances 0.000 description 2
- 229940116362 tragacanth Drugs 0.000 description 2
- 230000009466 transformation Effects 0.000 description 2
- 230000007704 transition Effects 0.000 description 2
- 229960001099 trimetrexate Drugs 0.000 description 2
- NOYPYLRCIDNJJB-UHFFFAOYSA-N trimetrexate Chemical compound COC1=C(OC)C(OC)=CC(NCC=2C(=C3C(N)=NC(N)=NC3=CC=2)C)=C1 NOYPYLRCIDNJJB-UHFFFAOYSA-N 0.000 description 2
- VXKHXGOKWPXYNA-PGBVPBMZSA-N triptorelin Chemical compound C([C@@H](C(=O)N[C@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N1[C@@H](CCC1)C(=O)NCC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H]1NC(=O)CC1)C1=CC=C(O)C=C1 VXKHXGOKWPXYNA-PGBVPBMZSA-N 0.000 description 2
- 229960004824 triptorelin Drugs 0.000 description 2
- 229920011532 unplasticized polyvinyl chloride Polymers 0.000 description 2
- 210000002700 urine Anatomy 0.000 description 2
- 229960002730 vapreotide Drugs 0.000 description 2
- 108700029852 vapreotide Proteins 0.000 description 2
- 235000015112 vegetable and seed oil Nutrition 0.000 description 2
- 239000008158 vegetable oil Substances 0.000 description 2
- 229960003862 vemurafenib Drugs 0.000 description 2
- GPXBXXGIAQBQNI-UHFFFAOYSA-N vemurafenib Chemical compound CCCS(=O)(=O)NC1=CC=C(F)C(C(=O)C=2C3=CC(=CN=C3NC=2)C=2C=CC(Cl)=CC=2)=C1F GPXBXXGIAQBQNI-UHFFFAOYSA-N 0.000 description 2
- ZQFGRJWRSLZCSQ-ZSFNYQMMSA-N verteporfin Chemical compound C=1C([C@@]2([C@H](C(=O)OC)C(=CC=C22)C(=O)OC)C)=NC2=CC(C(=C2C=C)C)=NC2=CC(C(=C2CCC(O)=O)C)=NC2=CC2=NC=1C(C)=C2CCC(=O)OC ZQFGRJWRSLZCSQ-ZSFNYQMMSA-N 0.000 description 2
- 229960003895 verteporfin Drugs 0.000 description 2
- 229960001771 vorozole Drugs 0.000 description 2
- XLMPPFTZALNBFS-INIZCTEOSA-N vorozole Chemical compound C1([C@@H](C2=CC=C3N=NN(C3=C2)C)N2N=CN=C2)=CC=C(Cl)C=C1 XLMPPFTZALNBFS-INIZCTEOSA-N 0.000 description 2
- 239000008215 water for injection Substances 0.000 description 2
- 229950003017 zeniplatin Drugs 0.000 description 2
- XRASPMIURGNCCH-UHFFFAOYSA-N zoledronic acid Chemical compound OP(=O)(O)C(P(O)(O)=O)(O)CN1C=CN=C1 XRASPMIURGNCCH-UHFFFAOYSA-N 0.000 description 2
- 229960004276 zoledronic acid Drugs 0.000 description 2
- OPFTUNCRGUEPRZ-UHFFFAOYSA-N (+)-beta-Elemen Natural products CC(=C)C1CCC(C)(C=C)C(C(C)=C)C1 OPFTUNCRGUEPRZ-UHFFFAOYSA-N 0.000 description 1
- BMKDZUISNHGIBY-ZETCQYMHSA-N (+)-dexrazoxane Chemical compound C([C@H](C)N1CC(=O)NC(=O)C1)N1CC(=O)NC(=O)C1 BMKDZUISNHGIBY-ZETCQYMHSA-N 0.000 description 1
- OPFTUNCRGUEPRZ-QLFBSQMISA-N (-)-beta-elemene Chemical compound CC(=C)[C@@H]1CC[C@@](C)(C=C)[C@H](C(C)=C)C1 OPFTUNCRGUEPRZ-QLFBSQMISA-N 0.000 description 1
- GCPUVEMWOWMALU-HZMBPMFUSA-N (1s,3s)-1-hydroxy-8-methoxy-3-methyl-1,2,3,4-tetrahydrobenzo[a]anthracene-7,12-dione Chemical compound C1[C@H](C)C[C@H](O)C2=C1C=CC1=C2C(=O)C(C=CC=C2OC)=C2C1=O GCPUVEMWOWMALU-HZMBPMFUSA-N 0.000 description 1
- MXABZXILAJGOTL-AUYMZICSSA-N (2S)-N-[(2S)-1-[(2S)-1-[(2S,3S)-1-[(2S)-1-[2-[(2S)-1,3-dihydroxy-1-[(E)-1-hydroxy-1-[(2S,3S)-1-hydroxy-3-methyl-1-[[(2Z,6S,9S,12R)-5,8,11-trihydroxy-9-(2-methylpropyl)-6-propan-2-yl-1-thia-4,7,10-triazacyclotrideca-2,4,7,10-tetraen-12-yl]imino]pentan-2-yl]iminobut-2-en-2-yl]iminopropan-2-yl]imino-2-hydroxyethyl]imino-1,5-dihydroxy-5-iminopentan-2-yl]imino-1-hydroxy-3-methylpentan-2-yl]imino-1-hydroxy-3-methylbutan-2-yl]imino-1-hydroxy-3-phenylpropan-2-yl]-2-[[(2S)-2-[[(2S)-2-[[(Z)-2-[[(2S)-2-[[(Z)-2-[[(2S)-2-[[[(2S)-1-[(Z)-2-[[(2S)-2-(dimethylamino)-1-hydroxypropylidene]amino]but-2-enoyl]pyrrolidin-2-yl]-hydroxymethylidene]amino]-1-hydroxypropylidene]amino]-1-hydroxybut-2-enylidene]amino]-1-hydroxy-3-phenylpropylidene]amino]-1-hydroxybut-2-enylidene]amino]-1-hydroxy-3-methylbutylidene]amino]-1-hydroxypropylidene]amino]pentanediimidic acid Chemical compound CC[C@H](C)[C@H](\N=C(/O)[C@@H](\N=C(/O)[C@H](Cc1ccccc1)\N=C(/O)[C@H](CCC(O)=N)\N=C(/O)[C@H](C)\N=C(/O)[C@@H](\N=C(/O)\C(=C\C)\N=C(/O)[C@H](Cc1ccccc1)\N=C(/O)\C(=C\C)\N=C(/O)[C@H](C)\N=C(/O)[C@@H]1CCCN1C(=O)\C(=C\C)\N=C(/O)[C@H](C)N(C)C)C(C)C)C(C)C)C(\O)=N\[C@@H](CCC(O)=N)C(\O)=N\C\C(O)=N\[C@@H](CO)C(\O)=N\C(=C\C)\C(\O)=N\[C@@H]([C@@H](C)CC)C(\O)=N\[C@H]1CS\C=C/N=C(O)\[C@@H](\N=C(O)/[C@H](CC(C)C)\N=C1\O)C(C)C MXABZXILAJGOTL-AUYMZICSSA-N 0.000 description 1
- BUSGWUFLNHIBPT-XYBORKQMSA-N (2e,4e,6e)-7-[(1r,5r,6s)-3-[[(2e,4e)-5-cyclohexylpenta-2,4-dienoyl]amino]-5-hydroxy-2-oxo-7-oxabicyclo[4.1.0]hept-3-en-5-yl]hepta-2,4,6-trienoic acid Chemical compound C([C@]([C@H]1O[C@H]1C1=O)(O)/C=C/C=C/C=C/C(=O)O)=C1NC(=O)\C=C\C=C\C1CCCCC1 BUSGWUFLNHIBPT-XYBORKQMSA-N 0.000 description 1
- FKHUGQZRBPETJR-RXSRXONKSA-N (2r)-2-[[(4r)-4-[[(2s)-2-[[(2r)-2-[(3r,4r,5s,6r)-3-acetamido-2,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl]oxypropanoyl]amino]propanoyl]amino]-5-amino-5-oxopentanoyl]amino]-6-(octadecanoylamino)hexanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(=O)NCCCC[C@H](C(O)=O)NC(=O)CC[C@H](C(N)=O)NC(=O)[C@H](C)NC(=O)[C@@H](C)O[C@H]1[C@H](O)[C@@H](CO)OC(O)[C@@H]1NC(C)=O FKHUGQZRBPETJR-RXSRXONKSA-N 0.000 description 1
- SWTGJCNCBUCXSS-ISUZDFFFSA-N (2r)-3,4-dihydroxy-2-[(4s)-2-phenyl-1,3-dioxolan-4-yl]-2h-furan-5-one Chemical compound OC1=C(O)C(=O)O[C@@H]1[C@H]1OC(C=2C=CC=CC=2)OC1 SWTGJCNCBUCXSS-ISUZDFFFSA-N 0.000 description 1
- PAYBYKKERMGTSS-MNCSTQPFSA-N (2r,3r,3as,9ar)-7-fluoro-2-(hydroxymethyl)-6-imino-2,3,3a,9a-tetrahydrofuro[1,2][1,3]oxazolo[3,4-a]pyrimidin-3-ol Chemical compound N=C1C(F)=CN2[C@@H]3O[C@H](CO)[C@@H](O)[C@@H]3OC2=N1 PAYBYKKERMGTSS-MNCSTQPFSA-N 0.000 description 1
- NOENHWMKHNSHGX-IZOOSHNJSA-N (2s)-1-[(2s)-2-[[(2s)-2-[[(2r)-2-[[(2r)-2-[[(2s)-2-[[(2r)-2-[[(2s)-2-[[(2r)-2-acetamido-3-naphthalen-2-ylpropanoyl]amino]-3-(4-chlorophenyl)propanoyl]amino]-3-pyridin-3-ylpropanoyl]amino]-3-hydroxypropanoyl]amino]-3-(4-hydroxyphenyl)propanoyl]amino]-6-(ca Chemical compound C([C@H](C(=O)N[C@H](CCCCNC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCCNC(C)C)C(=O)N1[C@@H](CCC1)C(=O)N[C@H](C)C(N)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](CC=1C=NC=CC=1)NC(=O)[C@H](CC=1C=CC(Cl)=CC=1)NC(=O)[C@@H](CC=1C=C2C=CC=CC2=CC=1)NC(C)=O)C1=CC=C(O)C=C1 NOENHWMKHNSHGX-IZOOSHNJSA-N 0.000 description 1
- XDZGQQRZJDKPTG-HBNQUELISA-N (2s)-2-[(3s,6s)-6-[2-[(1r,2r,4as,8as)-1-hydroxy-2,4a,5,5,8a-pentamethyl-2,3,4,6,7,8-hexahydronaphthalen-1-yl]ethyl]-6-methyldioxan-3-yl]propanoic acid Chemical compound O1O[C@H]([C@H](C)C(O)=O)CC[C@@]1(C)CC[C@]1(O)[C@@]2(C)CCCC(C)(C)[C@]2(C)CC[C@H]1C XDZGQQRZJDKPTG-HBNQUELISA-N 0.000 description 1
- CUCSSYAUKKIDJV-FAXBSAIASA-N (2s)-2-[[(2r)-2-[[(2s)-2-[[(2r)-2-[[(2s)-2-amino-5-(diaminomethylideneamino)pentanoyl]amino]-3-(1h-indol-3-yl)propanoyl]-methylamino]-3-phenylpropanoyl]amino]-3-(1h-indol-3-yl)propanoyl]amino]-n-[(2s)-1-amino-4-methylsulfanyl-1-oxobutan-2-yl]-4-methylpent Chemical compound C([C@@H](C(=O)N[C@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(N)=O)N(C)C(=O)[C@@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@@H](N)CCCN=C(N)N)C1=CC=CC=C1 CUCSSYAUKKIDJV-FAXBSAIASA-N 0.000 description 1
- ZUQBAQVRAURMCL-DOMZBBRYSA-N (2s)-2-[[4-[2-[(6r)-2-amino-4-oxo-5,6,7,8-tetrahydro-1h-pyrido[2,3-d]pyrimidin-6-yl]ethyl]benzoyl]amino]pentanedioic acid Chemical compound C([C@@H]1CC=2C(=O)N=C(NC=2NC1)N)CC1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 ZUQBAQVRAURMCL-DOMZBBRYSA-N 0.000 description 1
- JRBXPUUAYKCCLQ-QMMMGPOBSA-N (2s)-2-amino-2-[3-hydroxy-4-(hydroxymethyl)phenyl]acetic acid Chemical compound OC(=O)[C@@H](N)C1=CC=C(CO)C(O)=C1 JRBXPUUAYKCCLQ-QMMMGPOBSA-N 0.000 description 1
- RPEPXOHTYVXVMA-CIUDSAMLSA-N (2s)-2-amino-5-[[(2s)-1-[[(1s)-1-carboxy-4-(3h-diazirin-3-yl)-4-oxobutyl]amino]-5-(3h-diazirin-3-yl)-1,5-dioxopentan-2-yl]amino]-5-oxopentanoic acid Chemical compound C([C@H](NC(=O)CC[C@H](N)C(O)=O)C(=O)N[C@@H](CCC(=O)C1N=N1)C(O)=O)CC(=O)C1N=N1 RPEPXOHTYVXVMA-CIUDSAMLSA-N 0.000 description 1
- XMQUEQJCYRFIQS-YFKPBYRVSA-N (2s)-2-amino-5-ethoxy-5-oxopentanoic acid Chemical compound CCOC(=O)CC[C@H](N)C(O)=O XMQUEQJCYRFIQS-YFKPBYRVSA-N 0.000 description 1
- HJNZCKLMRAOTMA-BRBGIFQRSA-N (2s)-n-[(2s)-1-[[(2s)-1-[[(2s)-1-[[(2s)-1-[[(2r)-1-[[(2s)-1-[[(2s)-5-(diaminomethylideneamino)-1-[(2s)-2-(ethylcarbamoyl)pyrrolidin-1-yl]-1-oxopentan-2-yl]amino]-4-methyl-1-oxopentan-2-yl]amino]-3-(2-methyl-1h-indol-3-yl)-1-oxopropan-2-yl]amino]-3-(4-hydr Chemical compound CCNC(=O)[C@@H]1CCCN1C(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H]1NC(=O)CC1)CC1=C(C)NC2=CC=CC=C12 HJNZCKLMRAOTMA-BRBGIFQRSA-N 0.000 description 1
- HWMMBHOXHRVLCU-QOUANJGESA-N (2s,4s,5s)-4-[(1e,3e,5e)-7-[(2r,6r)-6-[(2r,3s,4ar,12bs)-2,3,4a,8,12b-pentahydroxy-3-methyl-1,7,12-trioxo-2,4-dihydrobenzo[a]anthracen-9-yl]-2-methyloxan-3-yl]oxy-7-oxohepta-1,3,5-trienyl]-2,5-dimethyl-1,3-dioxolane-2-carboxylic acid Chemical compound C[C@@H]1O[C@](C)(C(O)=O)O[C@H]1\C=C\C=C\C=C\C(=O)OC1[C@@H](C)O[C@@H](C=2C(=C3C(=O)C4=C([C@]5(C(=O)[C@H](O)[C@@](C)(O)C[C@@]5(O)C=C4)O)C(=O)C3=CC=2)O)CC1 HWMMBHOXHRVLCU-QOUANJGESA-N 0.000 description 1
- NAALWFYYHHJEFQ-ZASNTINBSA-N (2s,5r,6r)-6-[[(2r)-2-[[6-[4-[bis(2-hydroxyethyl)sulfamoyl]phenyl]-2-oxo-1h-pyridine-3-carbonyl]amino]-2-(4-hydroxyphenyl)acetyl]amino]-3,3-dimethyl-7-oxo-4-thia-1-azabicyclo[3.2.0]heptane-2-carboxylic acid Chemical compound N([C@@H](C(=O)N[C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C=1C=CC(O)=CC=1)C(=O)C(C(N1)=O)=CC=C1C1=CC=C(S(=O)(=O)N(CCO)CCO)C=C1 NAALWFYYHHJEFQ-ZASNTINBSA-N 0.000 description 1
- TVIRNGFXQVMMGB-OFWIHYRESA-N (3s,6r,10r,13e,16s)-16-[(2r,3r,4s)-4-chloro-3-hydroxy-4-phenylbutan-2-yl]-10-[(3-chloro-4-methoxyphenyl)methyl]-6-methyl-3-(2-methylpropyl)-1,4-dioxa-8,11-diazacyclohexadec-13-ene-2,5,9,12-tetrone Chemical compound C1=C(Cl)C(OC)=CC=C1C[C@@H]1C(=O)NC[C@@H](C)C(=O)O[C@@H](CC(C)C)C(=O)O[C@H]([C@H](C)[C@@H](O)[C@@H](Cl)C=2C=CC=CC=2)C/C=C/C(=O)N1 TVIRNGFXQVMMGB-OFWIHYRESA-N 0.000 description 1
- IEFNEZUQHDYNRM-UHFFFAOYSA-L (4-azanidyl-2-methylbutyl)azanide;cyclobutane-1,1-dicarboxylate;platinum(4+) Chemical compound [Pt+4].[NH-]CC(C)CC[NH-].[O-]C(=O)C1(C([O-])=O)CCC1 IEFNEZUQHDYNRM-UHFFFAOYSA-L 0.000 description 1
- FRCJDPPXHQGEKS-BCHFMIIMSA-N (4S,5R)-N-[4-[(2,3-dihydroxybenzoyl)amino]butyl]-N-[3-[(2,3-dihydroxybenzoyl)amino]propyl]-2-(2-hydroxyphenyl)-5-methyl-4,5-dihydro-1,3-oxazole-4-carboxamide Chemical compound C[C@H]1OC(=N[C@@H]1C(=O)N(CCCCNC(=O)c1cccc(O)c1O)CCCNC(=O)c1cccc(O)c1O)c1ccccc1O FRCJDPPXHQGEKS-BCHFMIIMSA-N 0.000 description 1
- DEQANNDTNATYII-OULOTJBUSA-N (4r,7s,10s,13r,16s,19r)-10-(4-aminobutyl)-19-[[(2r)-2-amino-3-phenylpropanoyl]amino]-16-benzyl-n-[(2r,3r)-1,3-dihydroxybutan-2-yl]-7-[(1r)-1-hydroxyethyl]-13-(1h-indol-3-ylmethyl)-6,9,12,15,18-pentaoxo-1,2-dithia-5,8,11,14,17-pentazacycloicosane-4-carboxa Chemical compound C([C@@H](N)C(=O)N[C@H]1CSSC[C@H](NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CCCCN)NC(=O)[C@@H](CC=2C3=CC=CC=C3NC=2)NC(=O)[C@H](CC=2C=CC=CC=2)NC1=O)C(=O)N[C@H](CO)[C@H](O)C)C1=CC=CC=C1 DEQANNDTNATYII-OULOTJBUSA-N 0.000 description 1
- PUDHBTGHUJUUFI-SCTWWAJVSA-N (4r,7s,10s,13r,16s,19r)-10-(4-aminobutyl)-n-[(2s,3r)-1-amino-3-hydroxy-1-oxobutan-2-yl]-19-[[(2r)-2-amino-3-naphthalen-2-ylpropanoyl]amino]-16-[(4-hydroxyphenyl)methyl]-13-(1h-indol-3-ylmethyl)-6,9,12,15,18-pentaoxo-7-propan-2-yl-1,2-dithia-5,8,11,14,17-p Chemical compound C([C@H]1C(=O)N[C@H](CC=2C3=CC=CC=C3NC=2)C(=O)N[C@@H](CCCCN)C(=O)N[C@H](C(N[C@@H](CSSC[C@@H](C(=O)N1)NC(=O)[C@H](N)CC=1C=C2C=CC=CC2=CC=1)C(=O)N[C@@H]([C@@H](C)O)C(N)=O)=O)C(C)C)C1=CC=C(O)C=C1 PUDHBTGHUJUUFI-SCTWWAJVSA-N 0.000 description 1
- HLAKJNQXUARACO-ZDUSSCGKSA-N (5'r)-5'-hydroxy-2',5',7'-trimethylspiro[cyclopropane-1,6'-indene]-4'-one Chemical compound O=C([C@@]1(O)C)C2=CC(C)=CC2=C(C)C21CC2 HLAKJNQXUARACO-ZDUSSCGKSA-N 0.000 description 1
- WTSKMKRYHATLLL-UHFFFAOYSA-N (6-benzoyloxy-3-cyanopyridin-2-yl) 3-[3-(ethoxymethyl)-5-fluoro-2,6-dioxopyrimidine-1-carbonyl]benzoate Chemical compound O=C1N(COCC)C=C(F)C(=O)N1C(=O)C1=CC=CC(C(=O)OC=2C(=CC=C(OC(=O)C=3C=CC=CC=3)N=2)C#N)=C1 WTSKMKRYHATLLL-UHFFFAOYSA-N 0.000 description 1
- LKBBOPGQDRPCDS-YAOXHJNESA-N (7s,9r,10r)-7-[(2r,4s,5s,6s)-4-amino-5-hydroxy-6-methyloxan-2-yl]oxy-9-ethyl-4,6,9,10,11-pentahydroxy-8,10-dihydro-7h-tetracene-5,12-dione Chemical compound O([C@H]1C[C@]([C@@H](C2=C(O)C=3C(=O)C4=CC=CC(O)=C4C(=O)C=3C(O)=C21)O)(O)CC)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 LKBBOPGQDRPCDS-YAOXHJNESA-N 0.000 description 1
- MWWSFMDVAYGXBV-FGBSZODSSA-N (7s,9s)-7-[(2r,4s,5r,6s)-4-amino-5-hydroxy-6-methyloxan-2-yl]oxy-6,9,11-trihydroxy-9-(2-hydroxyacetyl)-4-methoxy-8,10-dihydro-7h-tetracene-5,12-dione;hydron;chloride Chemical compound Cl.O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@@H](O)[C@H](C)O1 MWWSFMDVAYGXBV-FGBSZODSSA-N 0.000 description 1
- GYPCWHHQAVLMKO-XXKQIVDLSA-N (7s,9s)-7-[(2r,4s,5s,6s)-4-amino-5-hydroxy-6-methyloxan-2-yl]oxy-6,9,11-trihydroxy-9-[(e)-n-[(1-hydroxy-2,2,6,6-tetramethylpiperidin-4-ylidene)amino]-c-methylcarbonimidoyl]-4-methoxy-8,10-dihydro-7h-tetracene-5,12-dione;hydrochloride Chemical group Cl.O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(\C)=N\N=C1CC(C)(C)N(O)C(C)(C)C1)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 GYPCWHHQAVLMKO-XXKQIVDLSA-N 0.000 description 1
- RCFNNLSZHVHCEK-YGCMNLPTSA-N (7s,9s)-7-[(2s,4r,6s)-4-amino-6-methyloxan-2-yl]oxy-6,9,11-trihydroxy-9-(2-hydroxyacetyl)-4-methoxy-8,10-dihydro-7h-tetracene-5,12-dione;hydrochloride Chemical compound Cl.O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)C[C@H](C)O1 RCFNNLSZHVHCEK-YGCMNLPTSA-N 0.000 description 1
- VNTHYLVDGVBPOU-QQYBVWGSSA-N (7s,9s)-9-acetyl-7-[(2r,4s,5s,6s)-4-amino-5-hydroxy-6-methyloxan-2-yl]oxy-6,9,11-trihydroxy-4-methoxy-8,10-dihydro-7h-tetracene-5,12-dione;2-hydroxypropane-1,2,3-tricarboxylic acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O.O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(C)=O)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 VNTHYLVDGVBPOU-QQYBVWGSSA-N 0.000 description 1
- FPVKHBSQESCIEP-UHFFFAOYSA-N (8S)-3-(2-deoxy-beta-D-erythro-pentofuranosyl)-3,6,7,8-tetrahydroimidazo[4,5-d][1,3]diazepin-8-ol Natural products C1C(O)C(CO)OC1N1C(NC=NCC2O)=C2N=C1 FPVKHBSQESCIEP-UHFFFAOYSA-N 0.000 description 1
- VHZXNQKVFDBFIK-NBBHSKLNSA-N (8r,9s,10r,13s,14s,16r)-16-fluoro-10,13-dimethyl-1,2,3,4,7,8,9,11,12,14,15,16-dodecahydrocyclopenta[a]phenanthren-17-one Chemical compound C1CCC[C@]2(C)[C@H]3CC[C@](C)(C([C@H](F)C4)=O)[C@@H]4[C@@H]3CC=C21 VHZXNQKVFDBFIK-NBBHSKLNSA-N 0.000 description 1
- IEXUMDBQLIVNHZ-YOUGDJEHSA-N (8s,11r,13r,14s,17s)-11-[4-(dimethylamino)phenyl]-17-hydroxy-17-(3-hydroxypropyl)-13-methyl-1,2,6,7,8,11,12,14,15,16-decahydrocyclopenta[a]phenanthren-3-one Chemical compound C1=CC(N(C)C)=CC=C1[C@@H]1C2=C3CCC(=O)C=C3CC[C@H]2[C@H](CC[C@]2(O)CCCO)[C@@]2(C)C1 IEXUMDBQLIVNHZ-YOUGDJEHSA-N 0.000 description 1
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 description 1
- MHFRGQHAERHWKZ-HHHXNRCGSA-N (R)-edelfosine Chemical compound CCCCCCCCCCCCCCCCCCOC[C@@H](OC)COP([O-])(=O)OCC[N+](C)(C)C MHFRGQHAERHWKZ-HHHXNRCGSA-N 0.000 description 1
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 1
- ICLYJLBTOGPLMC-KVVVOXFISA-N (z)-octadec-9-enoate;tris(2-hydroxyethyl)azanium Chemical compound OCCN(CCO)CCO.CCCCCCCC\C=C/CCCCCCCC(O)=O ICLYJLBTOGPLMC-KVVVOXFISA-N 0.000 description 1
- OJRZEKJECRTBPJ-NGAMADIESA-N (z,5s)-5-acetamido-1-diazonio-6-hydroxy-6-oxohex-1-en-2-olate Chemical compound CC(=O)N[C@H](C(O)=O)CC\C([O-])=C\[N+]#N OJRZEKJECRTBPJ-NGAMADIESA-N 0.000 description 1
- 125000006002 1,1-difluoroethyl group Chemical group 0.000 description 1
- UOAFGUOASVSLPK-UHFFFAOYSA-N 1-(2-chloroethyl)-3-(2,2-dimethylpropyl)-1-nitrosourea Chemical compound CC(C)(C)CNC(=O)N(N=O)CCCl UOAFGUOASVSLPK-UHFFFAOYSA-N 0.000 description 1
- YQYBWJPESSJLTK-HXFLIBJXSA-N 1-(2-chloroethyl)-3-[(2r,3s,4r,6s)-3-hydroxy-2-(hydroxymethyl)-6-methoxyoxan-4-yl]-1-nitrosourea Chemical compound CO[C@@H]1C[C@@H](NC(=O)N(CCCl)N=O)[C@H](O)[C@@H](CO)O1 YQYBWJPESSJLTK-HXFLIBJXSA-N 0.000 description 1
- RCLLNBVPCJDIPX-UHFFFAOYSA-N 1-(2-chloroethyl)-3-[2-(dimethylsulfamoyl)ethyl]-1-nitrosourea Chemical compound CN(C)S(=O)(=O)CCNC(=O)N(N=O)CCCl RCLLNBVPCJDIPX-UHFFFAOYSA-N 0.000 description 1
- JQJSFAJISYZPER-UHFFFAOYSA-N 1-(4-chlorophenyl)-3-(2,3-dihydro-1h-inden-5-ylsulfonyl)urea Chemical compound C1=CC(Cl)=CC=C1NC(=O)NS(=O)(=O)C1=CC=C(CCC2)C2=C1 JQJSFAJISYZPER-UHFFFAOYSA-N 0.000 description 1
- SNYUHPPZINRDSG-UHFFFAOYSA-N 1-(oxiran-2-ylmethyl)-4-[1-(oxiran-2-ylmethyl)piperidin-4-yl]piperidine Chemical compound C1CC(C2CCN(CC3OC3)CC2)CCN1CC1CO1 SNYUHPPZINRDSG-UHFFFAOYSA-N 0.000 description 1
- VXNZUUAINFGPBY-UHFFFAOYSA-N 1-Butene Chemical group CCC=C VXNZUUAINFGPBY-UHFFFAOYSA-N 0.000 description 1
- ZKFNOUUKULVDOB-UHFFFAOYSA-N 1-amino-1-phenylmethyl phosphonic acid Chemical compound OP(=O)(O)C(N)C1=CC=CC=C1 ZKFNOUUKULVDOB-UHFFFAOYSA-N 0.000 description 1
- IIZPXYDJLKNOIY-JXPKJXOSSA-N 1-palmitoyl-2-arachidonoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCC\C=C/C\C=C/C\C=C/C\C=C/CCCCC IIZPXYDJLKNOIY-JXPKJXOSSA-N 0.000 description 1
- CNQCTSLNJJVSAU-UHFFFAOYSA-N 132937-89-4 Chemical compound O.Cl.Cl.Cl.Cl.OCCNCCN1N=C2C3=CC=CC(O)=C3C(=O)C3=C2C1=CC=C3NCCNCCO.OCCNCCN1N=C2C3=CC=CC(O)=C3C(=O)C3=C2C1=CC=C3NCCNCCO CNQCTSLNJJVSAU-UHFFFAOYSA-N 0.000 description 1
- 101710175516 14 kDa zinc-binding protein Proteins 0.000 description 1
- 125000004206 2,2,2-trifluoroethyl group Chemical group [H]C([H])(*)C(F)(F)F 0.000 description 1
- 125000004778 2,2-difluoroethyl group Chemical group [H]C([H])(*)C([H])(F)F 0.000 description 1
- VKDGNNYJFSHYKD-UHFFFAOYSA-N 2,5-diamino-2-(difluoromethyl)pentanoic acid;hydron;chloride Chemical compound Cl.NCCCC(N)(C(F)F)C(O)=O VKDGNNYJFSHYKD-UHFFFAOYSA-N 0.000 description 1
- DQBFRGQHCCHNSG-UHFFFAOYSA-N 2-(2-aminopyrimidin-5-yl)-N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoroacetamide Chemical compound NC1=NC=C(C=N1)C(C(=O)NCC=1C=C2CN(C(C2=CC=1)=O)C1C(NC(CC1)=O)=O)(F)F DQBFRGQHCCHNSG-UHFFFAOYSA-N 0.000 description 1
- TXQPXJKRNHJWAX-UHFFFAOYSA-N 2-(3-aminopropylamino)ethylsulfanylphosphonic acid;trihydrate Chemical compound O.O.O.NCCCNCCSP(O)(O)=O TXQPXJKRNHJWAX-UHFFFAOYSA-N 0.000 description 1
- BLUVQMUHGZOMQM-UHFFFAOYSA-N 2-(5-cyclopropylpyridin-2-yl)-N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoroacetamide Chemical compound C1(CC1)C=1C=CC(=NC=1)C(C(=O)NCC=1C=C2CN(C(C2=CC=1)=O)C1C(NC(CC1)=O)=O)(F)F BLUVQMUHGZOMQM-UHFFFAOYSA-N 0.000 description 1
- XXCXSSMNJUZBQI-UHFFFAOYSA-N 2-[(3,4-dihydroxy-2-methylpentanoyl)amino]-3-hydroxy-2-methylpropanoic acid Chemical compound CC(O)C(O)C(C)C(=O)NC(C)(CO)C(O)=O XXCXSSMNJUZBQI-UHFFFAOYSA-N 0.000 description 1
- KPRFMAZESAKTEJ-UHFFFAOYSA-N 2-[1-amino-4-[2,5-dioxo-4-(1-phenylethyl)pyrrolidin-3-yl]-1-oxobutan-2-yl]-5-carbamoylheptanedioic acid;azane Chemical compound [NH4+].[NH4+].C=1C=CC=CC=1C(C)C1C(CCC(C(CCC(CC([O-])=O)C(N)=O)C([O-])=O)C(N)=O)C(=O)NC1=O KPRFMAZESAKTEJ-UHFFFAOYSA-N 0.000 description 1
- MHXVDXXARZCVRK-WCWDXBQESA-N 2-[2-[4-[(e)-3,3,3-trifluoro-1,2-diphenylprop-1-enyl]phenoxy]ethylamino]ethanol Chemical compound C1=CC(OCCNCCO)=CC=C1C(\C=1C=CC=CC=1)=C(C(F)(F)F)/C1=CC=CC=C1 MHXVDXXARZCVRK-WCWDXBQESA-N 0.000 description 1
- ZVAGBRFUYHSUHA-UHFFFAOYSA-N 2-[5-[(3,5-dimethyl-1h-pyrrol-2-yl)methylidene]-4-methoxypyrrol-2-ylidene]indole;methanesulfonic acid Chemical compound CS(O)(=O)=O.COC1=CC(=C2N=C3C=CC=CC3=C2)NC1=CC=1NC(C)=CC=1C ZVAGBRFUYHSUHA-UHFFFAOYSA-N 0.000 description 1
- HYHJFNXFVPGMBI-UHFFFAOYSA-N 2-[[2-chloroethyl(nitroso)carbamoyl]-methylamino]acetamide Chemical compound NC(=O)CN(C)C(=O)N(CCCl)N=O HYHJFNXFVPGMBI-UHFFFAOYSA-N 0.000 description 1
- QCXJFISCRQIYID-IAEPZHFASA-N 2-amino-1-n-[(3s,6s,7r,10s,16s)-3-[(2s)-butan-2-yl]-7,11,14-trimethyl-2,5,9,12,15-pentaoxo-10-propan-2-yl-8-oxa-1,4,11,14-tetrazabicyclo[14.3.0]nonadecan-6-yl]-4,6-dimethyl-3-oxo-9-n-[(3s,6s,7r,10s,16s)-7,11,14-trimethyl-2,5,9,12,15-pentaoxo-3,10-di(propa Chemical compound C[C@H]1OC(=O)[C@H](C(C)C)N(C)C(=O)CN(C)C(=O)[C@@H]2CCCN2C(=O)[C@H](C(C)C)NC(=O)[C@H]1NC(=O)C1=C(N=C2C(C(=O)N[C@@H]3C(=O)N[C@H](C(N4CCC[C@H]4C(=O)N(C)CC(=O)N(C)[C@@H](C(C)C)C(=O)O[C@@H]3C)=O)[C@@H](C)CC)=C(N)C(=O)C(C)=C2O2)C2=C(C)C=C1 QCXJFISCRQIYID-IAEPZHFASA-N 0.000 description 1
- VOXBZHOHGGBLCQ-UHFFFAOYSA-N 2-amino-3,7-dihydropurine-6-thione;hydrate Chemical compound O.N1C(N)=NC(=S)C2=C1N=CN2.N1C(N)=NC(=S)C2=C1N=CN2 VOXBZHOHGGBLCQ-UHFFFAOYSA-N 0.000 description 1
- VDCRFBBZFHHYGT-IOSLPCCCSA-N 2-amino-9-[(2r,3r,4s,5r)-3,4-dihydroxy-5-(hydroxymethyl)oxolan-2-yl]-7-prop-2-enyl-3h-purine-6,8-dione Chemical compound O=C1N(CC=C)C=2C(=O)NC(N)=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@H]1O VDCRFBBZFHHYGT-IOSLPCCCSA-N 0.000 description 1
- NIXVOFULDIFBLB-QVRNUERCSA-N 2-amino-9-[(2r,3r,4s,5r)-3,4-dihydroxy-5-(hydroxymethyl)oxolan-2-yl]purine-6-sulfinamide Chemical compound C12=NC(N)=NC(S(N)=O)=C2N=CN1[C@@H]1O[C@H](CO)[C@@H](O)[C@H]1O NIXVOFULDIFBLB-QVRNUERCSA-N 0.000 description 1
- CFWRDBDJAOHXSH-SECBINFHSA-N 2-azaniumylethyl [(2r)-2,3-diacetyloxypropyl] phosphate Chemical compound CC(=O)OC[C@@H](OC(C)=O)COP(O)(=O)OCCN CFWRDBDJAOHXSH-SECBINFHSA-N 0.000 description 1
- ZMLHBBXPXZXTSP-UHFFFAOYSA-N 2-fluoropropane Chemical group C[C](C)F ZMLHBBXPXZXTSP-UHFFFAOYSA-N 0.000 description 1
- ODJQKYXPKWQWNK-UHFFFAOYSA-N 3,3'-Thiobispropanoic acid Chemical compound OC(=O)CCSCCC(O)=O ODJQKYXPKWQWNK-UHFFFAOYSA-N 0.000 description 1
- NDMPLJNOPCLANR-UHFFFAOYSA-N 3,4-dihydroxy-15-(4-hydroxy-18-methoxycarbonyl-5,18-seco-ibogamin-18-yl)-16-methoxy-1-methyl-6,7-didehydro-aspidospermidine-3-carboxylic acid methyl ester Natural products C1C(CC)(O)CC(CC2(C(=O)OC)C=3C(=CC4=C(C56C(C(C(O)C7(CC)C=CCN(C67)CC5)(O)C(=O)OC)N4C)C=3)OC)CN1CCC1=C2NC2=CC=CC=C12 NDMPLJNOPCLANR-UHFFFAOYSA-N 0.000 description 1
- GRLUHXSUZYFZCW-UHFFFAOYSA-N 3-(8,8-diethyl-2-aza-8-germaspiro[4.5]decan-2-yl)-n,n-dimethylpropan-1-amine;dihydrochloride Chemical compound Cl.Cl.C1C[Ge](CC)(CC)CCC11CN(CCCN(C)C)CC1 GRLUHXSUZYFZCW-UHFFFAOYSA-N 0.000 description 1
- QGJZLNKBHJESQX-UHFFFAOYSA-N 3-Epi-Betulin-Saeure Natural products C1CC(O)C(C)(C)C2CCC3(C)C4(C)CCC5(C(O)=O)CCC(C(=C)C)C5C4CCC3C21C QGJZLNKBHJESQX-UHFFFAOYSA-N 0.000 description 1
- GTJXPMSTODOYNP-BTKVJIOYSA-N 3-[(e)-1-[4-[2-(dimethylamino)ethoxy]phenyl]-2-phenylbut-1-enyl]phenol;2-hydroxypropane-1,2,3-tricarboxylic acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O.C=1C=CC=CC=1C(/CC)=C(C=1C=C(O)C=CC=1)\C1=CC=C(OCCN(C)C)C=C1 GTJXPMSTODOYNP-BTKVJIOYSA-N 0.000 description 1
- WUIABRMSWOKTOF-OYALTWQYSA-N 3-[[2-[2-[2-[[(2s,3r)-2-[[(2s,3s,4r)-4-[[(2s,3r)-2-[[6-amino-2-[(1s)-3-amino-1-[[(2s)-2,3-diamino-3-oxopropyl]amino]-3-oxopropyl]-5-methylpyrimidine-4-carbonyl]amino]-3-[(2r,3s,4s,5s,6s)-3-[(2r,3s,4s,5r,6r)-4-carbamoyloxy-3,5-dihydroxy-6-(hydroxymethyl)ox Chemical compound OS([O-])(=O)=O.N([C@H](C(=O)N[C@H](C)[C@@H](O)[C@H](C)C(=O)N[C@@H]([C@H](O)C)C(=O)NCCC=1SC=C(N=1)C=1SC=C(N=1)C(=O)NCCC[S+](C)C)[C@@H](O[C@H]1[C@H]([C@@H](O)[C@H](O)[C@H](CO)O1)O[C@@H]1[C@H]([C@@H](OC(N)=O)[C@H](O)[C@@H](CO)O1)O)C=1NC=NC=1)C(=O)C1=NC([C@H](CC(N)=O)NC[C@H](N)C(N)=O)=NC(N)=C1C WUIABRMSWOKTOF-OYALTWQYSA-N 0.000 description 1
- MJKVTPMWOKAVMS-UHFFFAOYSA-N 3-hydroxy-1-benzopyran-2-one Chemical class C1=CC=C2OC(=O)C(O)=CC2=C1 MJKVTPMWOKAVMS-UHFFFAOYSA-N 0.000 description 1
- CLOUCVRNYSHRCF-UHFFFAOYSA-N 3beta-Hydroxy-20(29)-Lupen-3,27-oic acid Natural products C1CC(O)C(C)(C)C2CCC3(C)C4(C(O)=O)CCC5(C)CCC(C(=C)C)C5C4CCC3C21C CLOUCVRNYSHRCF-UHFFFAOYSA-N 0.000 description 1
- PDQGEKGUTOTUNV-TZSSRYMLSA-N 4'-deoxy-4'-iododoxorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@H](I)[C@H](C)O1 PDQGEKGUTOTUNV-TZSSRYMLSA-N 0.000 description 1
- AOJJSUZBOXZQNB-VTZDEGQISA-N 4'-epidoxorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@@H](O)[C@H](C)O1 AOJJSUZBOXZQNB-VTZDEGQISA-N 0.000 description 1
- LIETVYHJBSLSSW-UHFFFAOYSA-N 4,6,9-trihydroxy-8-methyl-3,4-dihydro-2h-anthracen-1-one Chemical compound OC1CCC(=O)C2=C1C=C1C=C(O)C=C(C)C1=C2O LIETVYHJBSLSSW-UHFFFAOYSA-N 0.000 description 1
- JARCFMKMOFFIGZ-UHFFFAOYSA-N 4,6-dioxo-n-phenyl-2-sulfanylidene-1,3-diazinane-5-carboxamide Chemical compound O=C1NC(=S)NC(=O)C1C(=O)NC1=CC=CC=C1 JARCFMKMOFFIGZ-UHFFFAOYSA-N 0.000 description 1
- ASNHGEVAWNWCRQ-UHFFFAOYSA-N 4-(hydroxymethyl)oxolane-2,3,4-triol Chemical compound OCC1(O)COC(O)C1O ASNHGEVAWNWCRQ-UHFFFAOYSA-N 0.000 description 1
- OUQPTBCOEKUHBH-LSDHQDQOSA-N 4-[2-[4-[(e)-2-(5,5,8,8-tetramethyl-6,7-dihydronaphthalen-2-yl)prop-1-enyl]phenoxy]ethyl]morpholine Chemical compound C=1C=C(C(CCC2(C)C)(C)C)C2=CC=1C(/C)=C/C(C=C1)=CC=C1OCCN1CCOCC1 OUQPTBCOEKUHBH-LSDHQDQOSA-N 0.000 description 1
- CTSNHMQGVWXIEG-UHFFFAOYSA-N 4-amino-n-(5-chloroquinoxalin-2-yl)benzenesulfonamide Chemical compound C1=CC(N)=CC=C1S(=O)(=O)NC1=CN=C(C(Cl)=CC=C2)C2=N1 CTSNHMQGVWXIEG-UHFFFAOYSA-N 0.000 description 1
- ALEVUYMOJKJJSA-UHFFFAOYSA-N 4-hydroxy-2-propylbenzoic acid Chemical compound CCCC1=CC(O)=CC=C1C(O)=O ALEVUYMOJKJJSA-UHFFFAOYSA-N 0.000 description 1
- SGOOQMRIPALTEL-UHFFFAOYSA-N 4-hydroxy-N,1-dimethyl-2-oxo-N-phenyl-3-quinolinecarboxamide Chemical compound OC=1C2=CC=CC=C2N(C)C(=O)C=1C(=O)N(C)C1=CC=CC=C1 SGOOQMRIPALTEL-UHFFFAOYSA-N 0.000 description 1
- NSUDGNLOXMLAEB-UHFFFAOYSA-N 5-(2-formyl-3-hydroxyphenoxy)pentanoic acid Chemical compound OC(=O)CCCCOC1=CC=CC(O)=C1C=O NSUDGNLOXMLAEB-UHFFFAOYSA-N 0.000 description 1
- PXLPCZJACKUXGP-UHFFFAOYSA-N 5-(3,4-dichlorophenyl)-6-ethylpyrimidine-2,4-diamine Chemical compound CCC1=NC(N)=NC(N)=C1C1=CC=C(Cl)C(Cl)=C1 PXLPCZJACKUXGP-UHFFFAOYSA-N 0.000 description 1
- IDPUKCWIGUEADI-UHFFFAOYSA-N 5-[bis(2-chloroethyl)amino]uracil Chemical compound ClCCN(CCCl)C1=CNC(=O)NC1=O IDPUKCWIGUEADI-UHFFFAOYSA-N 0.000 description 1
- PXRKCOCTEMYUEG-UHFFFAOYSA-N 5-aminoisoindole-1,3-dione Chemical compound NC1=CC=C2C(=O)NC(=O)C2=C1 PXRKCOCTEMYUEG-UHFFFAOYSA-N 0.000 description 1
- NMUSYJAQQFHJEW-KVTDHHQDSA-N 5-azacytidine Chemical compound O=C1N=C(N)N=CN1[C@H]1[C@H](O)[C@H](O)[C@@H](CO)O1 NMUSYJAQQFHJEW-KVTDHHQDSA-N 0.000 description 1
- DQOGWKZQQBYYMW-LQGIGNHCSA-N 5-methyl-6-[(3,4,5-trimethoxyanilino)methyl]quinazoline-2,4-diamine;(2s,3s,4s,5r,6s)-3,4,5,6-tetrahydroxyoxane-2-carboxylic acid Chemical compound O[C@H]1O[C@H](C(O)=O)[C@@H](O)[C@H](O)[C@H]1O.COC1=C(OC)C(OC)=CC(NCC=2C(=C3C(N)=NC(N)=NC3=CC=2)C)=C1 DQOGWKZQQBYYMW-LQGIGNHCSA-N 0.000 description 1
- PXBZKHOQHTVCSQ-QZTJIDSGSA-N 5-nitro-2-[(2r)-1-[2-[[(2r)-2-(5-nitro-1,3-dioxobenzo[de]isoquinolin-2-yl)propyl]amino]ethylamino]propan-2-yl]benzo[de]isoquinoline-1,3-dione Chemical compound [O-][N+](=O)C1=CC(C(N([C@@H](CNCCNC[C@@H](C)N2C(C=3C=C(C=C4C=CC=C(C=34)C2=O)[N+]([O-])=O)=O)C)C2=O)=O)=C3C2=CC=CC3=C1 PXBZKHOQHTVCSQ-QZTJIDSGSA-N 0.000 description 1
- ATCGGEJZONJOCL-UHFFFAOYSA-N 6-(2,5-dichlorophenyl)-1,3,5-triazine-2,4-diamine Chemical compound NC1=NC(N)=NC(C=2C(=CC=C(Cl)C=2)Cl)=N1 ATCGGEJZONJOCL-UHFFFAOYSA-N 0.000 description 1
- VJXSSYDSOJBUAV-UHFFFAOYSA-N 6-(2,5-dimethoxy-benzyl)-5-methyl-pyrido[2,3-d]pyrimidine-2,4-diamine Chemical compound COC1=CC=C(OC)C(CC=2C(=C3C(N)=NC(N)=NC3=NC=2)C)=C1 VJXSSYDSOJBUAV-UHFFFAOYSA-N 0.000 description 1
- WYWHKKSPHMUBEB-UHFFFAOYSA-N 6-Mercaptoguanine Natural products N1C(N)=NC(=S)C2=C1N=CN2 WYWHKKSPHMUBEB-UHFFFAOYSA-N 0.000 description 1
- OTSZCHORPMQCBZ-UHFFFAOYSA-N 6-[(3-chlorophenyl)-imidazol-1-ylmethyl]-1h-benzimidazole;hydron;chloride Chemical compound Cl.ClC1=CC=CC(C(C=2C=C3NC=NC3=CC=2)N2C=NC=C2)=C1 OTSZCHORPMQCBZ-UHFFFAOYSA-N 0.000 description 1
- LRHPCRBOMKRVOA-UHFFFAOYSA-N 6-[2-(2-hydroxyethylamino)ethyl]indeno[1,2-c]isoquinoline-5,11-dione Chemical compound C12=CC=CC=C2C(=O)N(CCNCCO)C2=C1C(=O)C1=CC=CC=C12 LRHPCRBOMKRVOA-UHFFFAOYSA-N 0.000 description 1
- KXBCLNRMQPRVTP-UHFFFAOYSA-N 6-amino-1,5-dihydroimidazo[4,5-c]pyridin-4-one Chemical compound O=C1NC(N)=CC2=C1N=CN2 KXBCLNRMQPRVTP-UHFFFAOYSA-N 0.000 description 1
- ZNTIXVYOBQDFFV-UHFFFAOYSA-N 6-amino-1,5-dihydroimidazo[4,5-c]pyridin-4-one;methanesulfonic acid Chemical compound CS(O)(=O)=O.O=C1NC(N)=CC2=C1N=CN2 ZNTIXVYOBQDFFV-UHFFFAOYSA-N 0.000 description 1
- XZIIFPSPUDAGJM-UHFFFAOYSA-N 6-chloro-2-n,2-n-diethylpyrimidine-2,4-diamine Chemical compound CCN(CC)C1=NC(N)=CC(Cl)=N1 XZIIFPSPUDAGJM-UHFFFAOYSA-N 0.000 description 1
- GOYNNCPGHOBFCK-UHFFFAOYSA-N 7-[4-(dimethylamino)-5-[(2,9-dimethyl-3-oxo-4,4a,5a,6,7,9,9a,10a-octahydrodipyrano[4,2-a:4',3'-e][1,4]dioxin-7-yl)oxy]-6-methyloxan-2-yl]oxy-9-ethyl-4,6,9,10,11-pentahydroxy-8,10-dihydro-7h-tetracene-5,12-dione Chemical compound O=C1C2=C(O)C=CC=C2C(=O)C2=C1C(O)=C1C(OC3OC(C)C(OC4OC(C)C5OC6OC(C)C(=O)CC6OC5C4)C(C3)N(C)C)CC(CC)(O)C(O)C1=C2O GOYNNCPGHOBFCK-UHFFFAOYSA-N 0.000 description 1
- KABRXLINDSPGDF-UHFFFAOYSA-N 7-bromoisoquinoline Chemical compound C1=CN=CC2=CC(Br)=CC=C21 KABRXLINDSPGDF-UHFFFAOYSA-N 0.000 description 1
- GOJJWDOZNKBUSR-UHFFFAOYSA-N 7-sulfamoyloxyheptyl sulfamate Chemical compound NS(=O)(=O)OCCCCCCCOS(N)(=O)=O GOJJWDOZNKBUSR-UHFFFAOYSA-N 0.000 description 1
- LPDLEICKXUVJHW-QJILNLRNSA-N 78nz2pmp25 Chemical compound OS(O)(=O)=O.O([C@]12[C@H](OC(C)=O)[C@]3(CC)C=CCN4CC[C@@]5([C@H]34)[C@H]1N(C)C1=C5C=C(C(=C1)OC)[C@]1(C(=O)OC)C3=C(C4=CC=CC=C4N3)CCN3C[C@H](C1)C[C@@](C3)(O)CC)C(=O)N(CCCl)C2=O LPDLEICKXUVJHW-QJILNLRNSA-N 0.000 description 1
- ZGXJTSGNIOSYLO-UHFFFAOYSA-N 88755TAZ87 Chemical compound NCC(=O)CCC(O)=O ZGXJTSGNIOSYLO-UHFFFAOYSA-N 0.000 description 1
- HPLNQCPCUACXLM-PGUFJCEWSA-N ABT-737 Chemical compound C([C@@H](CCN(C)C)NC=1C(=CC(=CC=1)S(=O)(=O)NC(=O)C=1C=CC(=CC=1)N1CCN(CC=2C(=CC=CC=2)C=2C=CC(Cl)=CC=2)CC1)[N+]([O-])=O)SC1=CC=CC=C1 HPLNQCPCUACXLM-PGUFJCEWSA-N 0.000 description 1
- 208000009746 Adult T-Cell Leukemia-Lymphoma Diseases 0.000 description 1
- 208000016683 Adult T-cell leukemia/lymphoma Diseases 0.000 description 1
- 229920001817 Agar Polymers 0.000 description 1
- 102100027211 Albumin Human genes 0.000 description 1
- 108010088751 Albumins Proteins 0.000 description 1
- 239000005995 Aluminium silicate Substances 0.000 description 1
- ITPDYQOUSLNIHG-UHFFFAOYSA-N Amiodarone hydrochloride Chemical compound [Cl-].CCCCC=1OC2=CC=CC=C2C=1C(=O)C1=CC(I)=C(OCC[NH+](CC)CC)C(I)=C1 ITPDYQOUSLNIHG-UHFFFAOYSA-N 0.000 description 1
- 206010073128 Anaplastic oligodendroglioma Diseases 0.000 description 1
- BOJKULTULYSRAS-OTESTREVSA-N Andrographolide Chemical compound C([C@H]1[C@]2(C)CC[C@@H](O)[C@]([C@H]2CCC1=C)(CO)C)\C=C1/[C@H](O)COC1=O BOJKULTULYSRAS-OTESTREVSA-N 0.000 description 1
- 108010074415 Angiogenic Proteins Proteins 0.000 description 1
- 102000008076 Angiogenic Proteins Human genes 0.000 description 1
- 102100022987 Angiogenin Human genes 0.000 description 1
- 108020000948 Antisense Oligonucleotides Proteins 0.000 description 1
- MJINRRBEMOLJAK-DCAQKATOSA-N Arg-Lys-Asp Chemical compound OC(=O)C[C@@H](C(O)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@@H](N)CCCN=C(N)N MJINRRBEMOLJAK-DCAQKATOSA-N 0.000 description 1
- DRCNRVYVCHHIJP-AQBORDMYSA-N Arg-Lys-Glu-Val-Tyr Chemical compound NC(N)=NCCC[C@H](N)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C(C)C)C(=O)N[C@H](C(O)=O)CC1=CC=C(O)C=C1 DRCNRVYVCHHIJP-AQBORDMYSA-N 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- BFYIZQONLCFLEV-DAELLWKTSA-N Aromasine Chemical compound O=C1C=C[C@]2(C)[C@H]3CC[C@](C)(C(CC4)=O)[C@@H]4[C@@H]3CC(=C)C2=C1 BFYIZQONLCFLEV-DAELLWKTSA-N 0.000 description 1
- 102000015790 Asparaginase Human genes 0.000 description 1
- 108010024976 Asparaginase Proteins 0.000 description 1
- 108700032558 Aspergillus restrictus MITF Proteins 0.000 description 1
- BSYNRYMUTXBXSQ-UHFFFAOYSA-N Aspirin Chemical compound CC(=O)OC1=CC=CC=C1C(O)=O BSYNRYMUTXBXSQ-UHFFFAOYSA-N 0.000 description 1
- 208000003950 B-cell lymphoma Diseases 0.000 description 1
- 208000032568 B-cell prolymphocytic leukaemia Diseases 0.000 description 1
- MLDQJTXFUGDVEO-UHFFFAOYSA-N BAY-43-9006 Chemical compound C1=NC(C(=O)NC)=CC(OC=2C=CC(NC(=O)NC=3C=C(C(Cl)=CC=3)C(F)(F)F)=CC=2)=C1 MLDQJTXFUGDVEO-UHFFFAOYSA-N 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- VGGGPCQERPFHOB-MCIONIFRSA-N Bestatin Chemical compound CC(C)C[C@H](C(O)=O)NC(=O)[C@@H](O)[C@H](N)CC1=CC=CC=C1 VGGGPCQERPFHOB-MCIONIFRSA-N 0.000 description 1
- ZETHHMPKDUSZQQ-UHFFFAOYSA-N Betulafolienepentol Natural products C1C=C(C)CCC(C(C)CCC=C(C)C)C2C(OC)OC(OC)C2=C1 ZETHHMPKDUSZQQ-UHFFFAOYSA-N 0.000 description 1
- DIZWSDNSTNAYHK-XGWVBXMLSA-N Betulinic acid Natural products CC(=C)[C@@H]1C[C@H]([C@H]2CC[C@]3(C)[C@H](CC[C@@H]4[C@@]5(C)CC[C@H](O)C(C)(C)[C@@H]5CC[C@@]34C)[C@@H]12)C(=O)O DIZWSDNSTNAYHK-XGWVBXMLSA-N 0.000 description 1
- 206010005003 Bladder cancer Diseases 0.000 description 1
- 108010006654 Bleomycin Proteins 0.000 description 1
- 208000010392 Bone Fractures Diseases 0.000 description 1
- 206010005949 Bone cancer Diseases 0.000 description 1
- 206010065553 Bone marrow failure Diseases 0.000 description 1
- 206010006002 Bone pain Diseases 0.000 description 1
- 101001042041 Bos taurus Isocitrate dehydrogenase [NAD] subunit beta, mitochondrial Proteins 0.000 description 1
- 244000056139 Brassica cretica Species 0.000 description 1
- 235000003351 Brassica cretica Nutrition 0.000 description 1
- 235000003343 Brassica rupestris Nutrition 0.000 description 1
- 206010006187 Breast cancer Diseases 0.000 description 1
- 206010055113 Breast cancer metastatic Diseases 0.000 description 1
- 208000026310 Breast neoplasm Diseases 0.000 description 1
- 208000011691 Burkitt lymphomas Diseases 0.000 description 1
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical class [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 1
- KLWPJMFMVPTNCC-UHFFFAOYSA-N Camptothecin Natural products CCC1(O)C(=O)OCC2=C1C=C3C4Nc5ccccc5C=C4CN3C2=O KLWPJMFMVPTNCC-UHFFFAOYSA-N 0.000 description 1
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 1
- 208000005623 Carcinogenesis Diseases 0.000 description 1
- 201000009030 Carcinoma Diseases 0.000 description 1
- 108010031425 Casein Kinases Proteins 0.000 description 1
- 102000005403 Casein Kinases Human genes 0.000 description 1
- JDVVGAQPNNXQDW-WCMLQCRESA-N Castanospermine Natural products O[C@H]1[C@@H](O)[C@H]2[C@@H](O)CCN2C[C@H]1O JDVVGAQPNNXQDW-WCMLQCRESA-N 0.000 description 1
- JDVVGAQPNNXQDW-TVNFTVLESA-N Castinospermine Chemical compound C1[C@H](O)[C@@H](O)[C@H](O)[C@H]2[C@@H](O)CCN21 JDVVGAQPNNXQDW-TVNFTVLESA-N 0.000 description 1
- 102000053642 Catalytic RNA Human genes 0.000 description 1
- 108090000994 Catalytic RNA Proteins 0.000 description 1
- JWBOIMRXGHLCPP-UHFFFAOYSA-N Chloditan Chemical compound C=1C=CC=C(Cl)C=1C(C(Cl)Cl)C1=CC=C(Cl)C=C1 JWBOIMRXGHLCPP-UHFFFAOYSA-N 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- 239000004709 Chlorinated polyethylene Substances 0.000 description 1
- 102000011022 Chorionic Gonadotropin Human genes 0.000 description 1
- 108010062540 Chorionic Gonadotropin Proteins 0.000 description 1
- 206010008805 Chromosomal abnormalities Diseases 0.000 description 1
- 208000031404 Chromosome Aberrations Diseases 0.000 description 1
- 241001340526 Chrysoclista linneella Species 0.000 description 1
- 206010052358 Colorectal cancer metastatic Diseases 0.000 description 1
- HVXBOLULGPECHP-WAYWQWQTSA-N Combretastatin A4 Chemical compound C1=C(O)C(OC)=CC=C1\C=C/C1=CC(OC)=C(OC)C(OC)=C1 HVXBOLULGPECHP-WAYWQWQTSA-N 0.000 description 1
- DFDTZECTHJFPHE-UHFFFAOYSA-N Crambescidin 816 Natural products C1CC=CC(CC)OC11NC(N23)=NC4(OC(C)CCC4)C(C(=O)OCCCCCCCCCCCCCCCC(=O)N(CCCN)CC(O)CCN)C3(O)CCC2C1 DFDTZECTHJFPHE-UHFFFAOYSA-N 0.000 description 1
- LUEYTMPPCOCKBX-KWYHTCOPSA-N Curacin A Chemical compound C=CC[C@H](OC)CC\C(C)=C\C=C\CC\C=C/[C@@H]1CSC([C@H]2[C@H](C2)C)=N1 LUEYTMPPCOCKBX-KWYHTCOPSA-N 0.000 description 1
- LUEYTMPPCOCKBX-UHFFFAOYSA-N Curacin A Natural products C=CCC(OC)CCC(C)=CC=CCCC=CC1CSC(C2C(C2)C)=N1 LUEYTMPPCOCKBX-UHFFFAOYSA-N 0.000 description 1
- 229920000858 Cyclodextrin Polymers 0.000 description 1
- 108010015742 Cytochrome P-450 Enzyme System Proteins 0.000 description 1
- 102000003849 Cytochrome P450 Human genes 0.000 description 1
- SPKNARKFCOPTSY-UHFFFAOYSA-N D-asperlin Natural products CC1OC1C1C(OC(C)=O)C=CC(=O)O1 SPKNARKFCOPTSY-UHFFFAOYSA-N 0.000 description 1
- 230000004543 DNA replication Effects 0.000 description 1
- 230000006820 DNA synthesis Effects 0.000 description 1
- 108010092160 Dactinomycin Proteins 0.000 description 1
- 108010019673 Darbepoetin alfa Proteins 0.000 description 1
- WEAHRLBPCANXCN-UHFFFAOYSA-N Daunomycin Natural products CCC1(O)CC(OC2CC(N)C(O)C(C)O2)c3cc4C(=O)c5c(OC)cccc5C(=O)c4c(O)c3C1 WEAHRLBPCANXCN-UHFFFAOYSA-N 0.000 description 1
- 206010051055 Deep vein thrombosis Diseases 0.000 description 1
- 108020005199 Dehydrogenases Proteins 0.000 description 1
- GJKXGJCSJWBJEZ-XRSSZCMZSA-N Deslorelin Chemical compound CCNC(=O)[C@@H]1CCCN1C(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H]1NC(=O)CC1)CC1=CNC2=CC=CC=C12 GJKXGJCSJWBJEZ-XRSSZCMZSA-N 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- 235000019739 Dicalciumphosphate Nutrition 0.000 description 1
- 101100520033 Dictyostelium discoideum pikC gene Proteins 0.000 description 1
- KYHUYMLIVQFXRI-SJPGYWQQSA-N Didemnin B Chemical compound CN([C@H](CC(C)C)C(=O)N[C@@H]1C(=O)N[C@@H]([C@H](CC(=O)O[C@H](C(=O)[C@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N2CCC[C@H]2C(=O)N(C)[C@@H](CC=2C=CC(OC)=CC=2)C(=O)O[C@@H]1C)C(C)C)O)[C@@H](C)CC)C(=O)[C@@H]1CCCN1C(=O)[C@H](C)O KYHUYMLIVQFXRI-SJPGYWQQSA-N 0.000 description 1
- HWMMBHOXHRVLCU-UHFFFAOYSA-N Dioxamycin Natural products CC1OC(C)(C(O)=O)OC1C=CC=CC=CC(=O)OC1C(C)OC(C=2C(=C3C(=O)C4=C(C5(C(=O)C(O)C(C)(O)CC5(O)C=C4)O)C(=O)C3=CC=2)O)CC1 HWMMBHOXHRVLCU-UHFFFAOYSA-N 0.000 description 1
- MWWSFMDVAYGXBV-RUELKSSGSA-N Doxorubicin hydrochloride Chemical compound Cl.O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 MWWSFMDVAYGXBV-RUELKSSGSA-N 0.000 description 1
- CYQFCXCEBYINGO-DLBZAZTESA-N Dronabinol Natural products C1=C(C)CC[C@H]2C(C)(C)OC3=CC(CCCCC)=CC(O)=C3[C@H]21 CYQFCXCEBYINGO-DLBZAZTESA-N 0.000 description 1
- 206010059866 Drug resistance Diseases 0.000 description 1
- VQNATVDKACXKTF-UHFFFAOYSA-N Duocarmycin SA Natural products COC1=C(OC)C(OC)=C2NC(C(=O)N3C4=CC(=O)C5=C(C64CC6C3)C=C(N5)C(=O)OC)=CC2=C1 VQNATVDKACXKTF-UHFFFAOYSA-N 0.000 description 1
- DYEFUKCXAQOFHX-UHFFFAOYSA-N Ebselen Chemical compound [se]1C2=CC=CC=C2C(=O)N1C1=CC=CC=C1 DYEFUKCXAQOFHX-UHFFFAOYSA-N 0.000 description 1
- 208000005189 Embolism Diseases 0.000 description 1
- 108010092408 Eosinophil Peroxidase Proteins 0.000 description 1
- HTIJFSOGRVMCQR-UHFFFAOYSA-N Epirubicin Natural products COc1cccc2C(=O)c3c(O)c4CC(O)(CC(OC5CC(N)C(=O)C(C)O5)c4c(O)c3C(=O)c12)C(=O)CO HTIJFSOGRVMCQR-UHFFFAOYSA-N 0.000 description 1
- 108010074604 Epoetin Alfa Proteins 0.000 description 1
- 102000003951 Erythropoietin Human genes 0.000 description 1
- 108090000394 Erythropoietin Proteins 0.000 description 1
- 108090000371 Esterases Proteins 0.000 description 1
- 229940102550 Estrogen receptor antagonist Drugs 0.000 description 1
- PIICEJLVQHRZGT-UHFFFAOYSA-N Ethylenediamine Chemical compound NCCN PIICEJLVQHRZGT-UHFFFAOYSA-N 0.000 description 1
- DBVJJBKOTRCVKF-UHFFFAOYSA-N Etidronic acid Chemical compound OP(=O)(O)C(O)(C)P(O)(O)=O DBVJJBKOTRCVKF-UHFFFAOYSA-N 0.000 description 1
- ITIONVBQFUNVJV-UHFFFAOYSA-N Etomidoline Chemical compound C12=CC=CC=C2C(=O)N(CC)C1NC(C=C1)=CC=C1OCCN1CCCCC1 ITIONVBQFUNVJV-UHFFFAOYSA-N 0.000 description 1
- 208000010201 Exanthema Diseases 0.000 description 1
- 108010037362 Extracellular Matrix Proteins Proteins 0.000 description 1
- 102000010834 Extracellular Matrix Proteins Human genes 0.000 description 1
- 201000001342 Fallopian tube cancer Diseases 0.000 description 1
- 208000013452 Fallopian tube neoplasm Diseases 0.000 description 1
- 102000018233 Fibroblast Growth Factor Human genes 0.000 description 1
- 108050007372 Fibroblast Growth Factor Proteins 0.000 description 1
- 102000003971 Fibroblast Growth Factor 1 Human genes 0.000 description 1
- 108090000386 Fibroblast Growth Factor 1 Proteins 0.000 description 1
- 102000003974 Fibroblast growth factor 2 Human genes 0.000 description 1
- 102100024785 Fibroblast growth factor 2 Human genes 0.000 description 1
- 206010068715 Fibrodysplasia ossificans progressiva Diseases 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- 208000004463 Follicular Adenocarcinoma Diseases 0.000 description 1
- 229930091371 Fructose Natural products 0.000 description 1
- 239000005715 Fructose Substances 0.000 description 1
- RFSUNEUAIZKAJO-ARQDHWQXSA-N Fructose Chemical compound OC[C@H]1O[C@](O)(CO)[C@@H](O)[C@@H]1O RFSUNEUAIZKAJO-ARQDHWQXSA-N 0.000 description 1
- 102100022629 Fructose-2,6-bisphosphatase Human genes 0.000 description 1
- 108010036781 Fumarate Hydratase Proteins 0.000 description 1
- 102100036160 Fumarate hydratase, mitochondrial Human genes 0.000 description 1
- 230000005526 G1 to G0 transition Effects 0.000 description 1
- 208000034951 Genetic Translocation Diseases 0.000 description 1
- 108010024636 Glutathione Proteins 0.000 description 1
- 102000004457 Granulocyte-Macrophage Colony-Stimulating Factor Human genes 0.000 description 1
- 101100340443 Halobacterium salinarum (strain ATCC 700922 / JCM 11081 / NRC-1) infB gene Proteins 0.000 description 1
- 108010054147 Hemoglobins Proteins 0.000 description 1
- 102000001554 Hemoglobins Human genes 0.000 description 1
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 1
- 229940122957 Histamine H2 receptor antagonist Drugs 0.000 description 1
- 101000823463 Homo sapiens Fructose-2,6-bisphosphatase Proteins 0.000 description 1
- 101000959820 Homo sapiens Interferon alpha-1/13 Proteins 0.000 description 1
- 101000960234 Homo sapiens Isocitrate dehydrogenase [NADP] cytoplasmic Proteins 0.000 description 1
- 101000599886 Homo sapiens Isocitrate dehydrogenase [NADP], mitochondrial Proteins 0.000 description 1
- 101000851976 Homo sapiens Nucleoside diphosphate phosphatase ENTPD5 Proteins 0.000 description 1
- 101000582950 Homo sapiens Platelet factor 4 Proteins 0.000 description 1
- 101000779418 Homo sapiens RAC-alpha serine/threonine-protein kinase Proteins 0.000 description 1
- 101000932478 Homo sapiens Receptor-type tyrosine-protein kinase FLT3 Proteins 0.000 description 1
- 101000628562 Homo sapiens Serine/threonine-protein kinase STK11 Proteins 0.000 description 1
- 101000795659 Homo sapiens Tuberin Proteins 0.000 description 1
- 101000611183 Homo sapiens Tumor necrosis factor Proteins 0.000 description 1
- 239000004354 Hydroxyethyl cellulose Substances 0.000 description 1
- 229920000663 Hydroxyethyl cellulose Polymers 0.000 description 1
- WOBHKFSMXKNTIM-UHFFFAOYSA-N Hydroxyethyl methacrylate Chemical compound CC(=C)C(=O)OCCO WOBHKFSMXKNTIM-UHFFFAOYSA-N 0.000 description 1
- 208000037147 Hypercalcaemia Diseases 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- MPBVHIBUJCELCL-UHFFFAOYSA-N Ibandronate Chemical compound CCCCCN(C)CCC(O)(P(O)(O)=O)P(O)(O)=O MPBVHIBUJCELCL-UHFFFAOYSA-N 0.000 description 1
- JJKOTMDDZAJTGQ-DQSJHHFOSA-N Idoxifene Chemical compound C=1C=CC=CC=1C(/CC)=C(C=1C=CC(OCCN2CCCC2)=CC=1)/C1=CC=C(I)C=C1 JJKOTMDDZAJTGQ-DQSJHHFOSA-N 0.000 description 1
- 206010062016 Immunosuppression Diseases 0.000 description 1
- 206010022004 Influenza like illness Diseases 0.000 description 1
- 108700022013 Insecta cecropin B Proteins 0.000 description 1
- 102100040018 Interferon alpha-2 Human genes 0.000 description 1
- 108010079944 Interferon-alpha2b Proteins 0.000 description 1
- 108010002352 Interleukin-1 Proteins 0.000 description 1
- 108090001005 Interleukin-6 Proteins 0.000 description 1
- 108010075869 Isocitrate Dehydrogenase Proteins 0.000 description 1
- 102000012011 Isocitrate Dehydrogenase Human genes 0.000 description 1
- 102100039905 Isocitrate dehydrogenase [NADP] cytoplasmic Human genes 0.000 description 1
- 102100037845 Isocitrate dehydrogenase [NADP], mitochondrial Human genes 0.000 description 1
- 102100020880 Kit ligand Human genes 0.000 description 1
- 101710177504 Kit ligand Proteins 0.000 description 1
- 108010043135 L-methionine gamma-lyase Proteins 0.000 description 1
- 239000005551 L01XE03 - Erlotinib Substances 0.000 description 1
- 239000002147 L01XE04 - Sunitinib Substances 0.000 description 1
- 239000005511 L01XE05 - Sorafenib Substances 0.000 description 1
- 239000002136 L01XE07 - Lapatinib Substances 0.000 description 1
- JVTAAEKCZFNVCJ-UHFFFAOYSA-M Lactate Chemical compound CC(O)C([O-])=O JVTAAEKCZFNVCJ-UHFFFAOYSA-M 0.000 description 1
- XNRVGTHNYCNCFF-UHFFFAOYSA-N Lapatinib ditosylate monohydrate Chemical compound O.CC1=CC=C(S(O)(=O)=O)C=C1.CC1=CC=C(S(O)(=O)=O)C=C1.O1C(CNCCS(=O)(=O)C)=CC=C1C1=CC=C(N=CN=C2NC=3C=C(Cl)C(OCC=4C=C(F)C=CC=4)=CC=3)C2=C1 XNRVGTHNYCNCFF-UHFFFAOYSA-N 0.000 description 1
- ZHTRILQJTPJGNK-FYBAATNNSA-N Leinamycin Chemical compound N([C@@H](C=1SC=C(N=1)\C=C/C=C/C(=O)[C@H](O)/C=C(C)/CC1)C)C(=O)C[C@@]21S(=O)SC(=O)[C@]2(C)O ZHTRILQJTPJGNK-FYBAATNNSA-N 0.000 description 1
- ZHTRILQJTPJGNK-UHFFFAOYSA-N Leinamycin Natural products C1CC(C)=CC(O)C(=O)C=CC=CC(N=2)=CSC=2C(C)NC(=O)CC21S(=O)SC(=O)C2(C)O ZHTRILQJTPJGNK-UHFFFAOYSA-N 0.000 description 1
- 208000018142 Leiomyosarcoma Diseases 0.000 description 1
- 108010062867 Lenograstim Proteins 0.000 description 1
- 229920001491 Lentinan Polymers 0.000 description 1
- LMVRPBWWHMVLPC-KBPJCXPTSA-N Leptolstatin Natural products CC(CC=CC(=CC(C)C(=O)C(C)C(O)C(C)CC(=CCO)C)C)C=C(C)/C=C/C1CC=CC(=O)O1 LMVRPBWWHMVLPC-KBPJCXPTSA-N 0.000 description 1
- HLFSDGLLUJUHTE-SNVBAGLBSA-N Levamisole Chemical compound C1([C@H]2CN3CCSC3=N2)=CC=CC=C1 HLFSDGLLUJUHTE-SNVBAGLBSA-N 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- GQYIWUVLTXOXAJ-UHFFFAOYSA-N Lomustine Chemical compound ClCCN(N=O)C(=O)NC1CCCCC1 GQYIWUVLTXOXAJ-UHFFFAOYSA-N 0.000 description 1
- 206010058467 Lung neoplasm malignant Diseases 0.000 description 1
- 241000195947 Lycopodium Species 0.000 description 1
- 206010025280 Lymphocytosis Diseases 0.000 description 1
- BLOFGONIVNXZME-UHFFFAOYSA-N Mannostatin A Natural products CSC1C(N)C(O)C(O)C1O BLOFGONIVNXZME-UHFFFAOYSA-N 0.000 description 1
- 102000004318 Matrilysin Human genes 0.000 description 1
- 108090000855 Matrilysin Proteins 0.000 description 1
- 208000037196 Medullary thyroid carcinoma Diseases 0.000 description 1
- 206010027193 Meningioma malignant Diseases 0.000 description 1
- 235000006679 Mentha X verticillata Nutrition 0.000 description 1
- 235000002899 Mentha suaveolens Nutrition 0.000 description 1
- 235000001636 Mentha x rotundifolia Nutrition 0.000 description 1
- 108700021154 Metallothionein 3 Proteins 0.000 description 1
- 102100028708 Metallothionein-3 Human genes 0.000 description 1
- 241000361919 Metaphire sieboldi Species 0.000 description 1
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 1
- 229920000881 Modified starch Polymers 0.000 description 1
- 102000010909 Monoamine Oxidase Human genes 0.000 description 1
- 108010062431 Monoamine oxidase Proteins 0.000 description 1
- 101710167839 Morphogenetic protein Proteins 0.000 description 1
- 229920000715 Mucilage Polymers 0.000 description 1
- 102100030173 Muellerian-inhibiting factor Human genes 0.000 description 1
- HFPXYDFQVINJBV-UHFFFAOYSA-N Mycaperoxide B Natural products O1OC(C(C)C(O)=O)CCC1(C)CCC1(O)C2(C)CCCC(C)(C)C2CCC1C HFPXYDFQVINJBV-UHFFFAOYSA-N 0.000 description 1
- USVMJSALORZVDV-SDBHATRESA-N N(6)-(Delta(2)-isopentenyl)adenosine Chemical compound C1=NC=2C(NCC=C(C)C)=NC=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@H]1O USVMJSALORZVDV-SDBHATRESA-N 0.000 description 1
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 1
- WUKZPHOXUVCQOR-UHFFFAOYSA-N N-(1-azabicyclo[2.2.2]octan-3-yl)-6-chloro-4-methyl-3-oxo-1,4-benzoxazine-8-carboxamide Chemical compound C1N(CC2)CCC2C1NC(=O)C1=CC(Cl)=CC2=C1OCC(=O)N2C WUKZPHOXUVCQOR-UHFFFAOYSA-N 0.000 description 1
- BNQSTAOJRULKNX-UHFFFAOYSA-N N-(6-acetamidohexyl)acetamide Chemical compound CC(=O)NCCCCCCNC(C)=O BNQSTAOJRULKNX-UHFFFAOYSA-N 0.000 description 1
- QJMCKEPOKRERLN-UHFFFAOYSA-N N-3,4-tridhydroxybenzamide Chemical compound ONC(=O)C1=CC=C(O)C(O)=C1 QJMCKEPOKRERLN-UHFFFAOYSA-N 0.000 description 1
- MCFVKSDETMRAJE-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(2-hydroxyphenyl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=C(C=CC=C1)O)(F)F)=O)=O)=O MCFVKSDETMRAJE-UHFFFAOYSA-N 0.000 description 1
- UOCBVEPOXDRRCU-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(3-morpholin-4-ylphenyl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=CC(=CC=C1)N1CCOCC1)(F)F)=O)=O)=O UOCBVEPOXDRRCU-UHFFFAOYSA-N 0.000 description 1
- PWANIHFJALMGQE-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-(4-fluorocyclohexyl)acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1CCC(CC1)F)(F)F)=O)=O)=O PWANIHFJALMGQE-UHFFFAOYSA-N 0.000 description 1
- FAHBFJBZVMRZPX-UHFFFAOYSA-N N-[[2-(2,6-dioxopiperidin-3-yl)-1-oxo-3H-isoindol-5-yl]methyl]-2,2-difluoro-2-[4-fluoro-2-(2,2,2-trifluoroethoxy)phenyl]acetamide Chemical compound O=C1NC(CCC1N1C(C2=CC=C(C=C2C1)CNC(C(C1=C(C=C(C=C1)F)OCC(F)(F)F)(F)F)=O)=O)=O FAHBFJBZVMRZPX-UHFFFAOYSA-N 0.000 description 1
- AXDLCFOOGCNDST-UHFFFAOYSA-N N-methyl-DL-tyrosine Natural products CNC(C(O)=O)CC1=CC=C(O)C=C1 AXDLCFOOGCNDST-UHFFFAOYSA-N 0.000 description 1
- 108010021717 Nafarelin Proteins 0.000 description 1
- 206010028813 Nausea Diseases 0.000 description 1
- 102400000058 Neuregulin-1 Human genes 0.000 description 1
- 108090000556 Neuregulin-1 Proteins 0.000 description 1
- BUSGWUFLNHIBPT-UHFFFAOYSA-N Nisamycin Natural products O=C1C2OC2C(C=CC=CC=CC(=O)O)(O)C=C1NC(=O)C=CC=CC1CCCCC1 BUSGWUFLNHIBPT-UHFFFAOYSA-N 0.000 description 1
- KYRVNWMVYQXFEU-UHFFFAOYSA-N Nocodazole Chemical compound C1=C2NC(NC(=O)OC)=NC2=CC=C1C(=O)C1=CC=CS1 KYRVNWMVYQXFEU-UHFFFAOYSA-N 0.000 description 1
- KGTDRFCXGRULNK-UHFFFAOYSA-N Nogalamycin Natural products COC1C(OC)(C)C(OC)C(C)OC1OC1C2=C(O)C(C(=O)C3=C(O)C=C4C5(C)OC(C(C(C5O)N(C)C)O)OC4=C3C3=O)=C3C=C2C(C(=O)OC)C(C)(O)C1 KGTDRFCXGRULNK-UHFFFAOYSA-N 0.000 description 1
- 102100036518 Nucleoside diphosphate phosphatase ENTPD5 Human genes 0.000 description 1
- UMDBGTRUNWFBPE-UHFFFAOYSA-N O.Cl.Cl.CNCCNc1ccc2c3c(nn2CCNCCO)c4c(O)ccc(O)c4C(=O)c13 Chemical compound O.Cl.Cl.CNCCNc1ccc2c3c(nn2CCNCCO)c4c(O)ccc(O)c4C(=O)c13 UMDBGTRUNWFBPE-UHFFFAOYSA-N 0.000 description 1
- 229960005524 O6-benzylguanine Drugs 0.000 description 1
- KRWMERLEINMZFT-UHFFFAOYSA-N O6-benzylguanine Chemical compound C=12NC=NC2=NC(N)=NC=1OCC1=CC=CC=C1 KRWMERLEINMZFT-UHFFFAOYSA-N 0.000 description 1
- 102000002491 Octamer Transcription Factor-1 Human genes 0.000 description 1
- 108010068098 Octamer Transcription Factor-1 Proteins 0.000 description 1
- 108010016076 Octreotide Proteins 0.000 description 1
- 201000010133 Oligodendroglioma Diseases 0.000 description 1
- VTAZRSXSBIHBMH-UHFFFAOYSA-N Ophiocordin Natural products OC1=CC(C(=O)O)=CC(O)=C1C(=O)C1=C(O)C=CC=C1C(=O)NC1C(OC(=O)C=2C=CC(O)=CC=2)CCCNC1 VTAZRSXSBIHBMH-UHFFFAOYSA-N 0.000 description 1
- LKBBOPGQDRPCDS-UHFFFAOYSA-N Oxaunomycin Natural products C12=C(O)C=3C(=O)C4=C(O)C=CC=C4C(=O)C=3C(O)=C2C(O)C(CC)(O)CC1OC1CC(N)C(O)C(C)O1 LKBBOPGQDRPCDS-UHFFFAOYSA-N 0.000 description 1
- 108090000854 Oxidoreductases Proteins 0.000 description 1
- 102000004316 Oxidoreductases Human genes 0.000 description 1
- 108091007960 PI3Ks Proteins 0.000 description 1
- 102000038030 PI3Ks Human genes 0.000 description 1
- 102000014160 PTEN Phosphohydrolase Human genes 0.000 description 1
- 108010011536 PTEN Phosphohydrolase Proteins 0.000 description 1
- 208000002193 Pain Diseases 0.000 description 1
- VYOQBYCIIJYKJA-UHFFFAOYSA-N Palauamine Natural products C1N2C(=O)C3=CC=CN3C3N=C(N)NC32C2C1C(CN)C(Cl)C12NC(N)=NC1O VYOQBYCIIJYKJA-UHFFFAOYSA-N 0.000 description 1
- 206010061902 Pancreatic neoplasm Diseases 0.000 description 1
- 206010033701 Papillary thyroid cancer Diseases 0.000 description 1
- FRCJDPPXHQGEKS-UHFFFAOYSA-N Parabactin Natural products CC1OC(=NC1C(=O)N(CCCCNC(=O)c1cccc(O)c1O)CCCNC(=O)c1cccc(O)c1O)c1ccccc1O FRCJDPPXHQGEKS-UHFFFAOYSA-N 0.000 description 1
- 102000015094 Paraproteins Human genes 0.000 description 1
- 108010064255 Paraproteins Proteins 0.000 description 1
- 235000019483 Peanut oil Nutrition 0.000 description 1
- 108010057150 Peplomycin Proteins 0.000 description 1
- 229940083963 Peptide antagonist Drugs 0.000 description 1
- 108090000608 Phosphoric Monoester Hydrolases Proteins 0.000 description 1
- 102000004160 Phosphoric Monoester Hydrolases Human genes 0.000 description 1
- 208000007452 Plasmacytoma Diseases 0.000 description 1
- 102000010752 Plasminogen Inactivators Human genes 0.000 description 1
- 108010077971 Plasminogen Inactivators Proteins 0.000 description 1
- 102100030304 Platelet factor 4 Human genes 0.000 description 1
- 229920002732 Polyanhydride Polymers 0.000 description 1
- 229920000954 Polyglycolide Polymers 0.000 description 1
- 206010036105 Polyneuropathy Diseases 0.000 description 1
- 229920001710 Polyorthoester Polymers 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- HCBIBCJNVBAKAB-UHFFFAOYSA-N Procaine hydrochloride Chemical compound Cl.CCN(CC)CCOC(=O)C1=CC=C(N)C=C1 HCBIBCJNVBAKAB-UHFFFAOYSA-N 0.000 description 1
- 208000035416 Prolymphocytic B-Cell Leukemia Diseases 0.000 description 1
- PICZCWCKOLHDOJ-UHFFFAOYSA-N Pseudoaxinellin Natural products N1C(=O)C2CCCN2C(=O)C(CC(N)=O)NC(=O)C(C(C)C)NC(=O)C2CCCN2C(=O)C(C(C)C)NC(=O)C(C(C)C)NC(=O)C1CC1=CC=CC=C1 PICZCWCKOLHDOJ-UHFFFAOYSA-N 0.000 description 1
- 208000010378 Pulmonary Embolism Diseases 0.000 description 1
- XESARGFCSKSFID-UHFFFAOYSA-N Pyrazofurin Natural products OC1=C(C(=O)N)NN=C1C1C(O)C(O)C(CO)O1 XESARGFCSKSFID-UHFFFAOYSA-N 0.000 description 1
- 206010037660 Pyrexia Diseases 0.000 description 1
- LCTONWCANYUPML-UHFFFAOYSA-M Pyruvate Chemical compound CC(=O)C([O-])=O LCTONWCANYUPML-UHFFFAOYSA-M 0.000 description 1
- 101710113459 RAC-alpha serine/threonine-protein kinase Proteins 0.000 description 1
- 102000003901 Ras GTPase-activating proteins Human genes 0.000 description 1
- 108090000231 Ras GTPase-activating proteins Proteins 0.000 description 1
- 229940078123 Ras inhibitor Drugs 0.000 description 1
- 102100020718 Receptor-type tyrosine-protein kinase FLT3 Human genes 0.000 description 1
- 206010038019 Rectal adenocarcinoma Diseases 0.000 description 1
- 108091007187 Reductases Proteins 0.000 description 1
- 208000001647 Renal Insufficiency Diseases 0.000 description 1
- GCPUVEMWOWMALU-UHFFFAOYSA-N Rubiginone B1 Natural products C1C(C)CC(O)C2=C1C=CC1=C2C(=O)C(C=CC=C2OC)=C2C1=O GCPUVEMWOWMALU-UHFFFAOYSA-N 0.000 description 1
- 101100450707 Schizosaccharomyces pombe (strain 972 / ATCC 24843) hif2 gene Proteins 0.000 description 1
- 102100026715 Serine/threonine-protein kinase STK11 Human genes 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- 208000000453 Skin Neoplasms Diseases 0.000 description 1
- 206010041067 Small cell lung cancer Diseases 0.000 description 1
- OCOKWVBYZHBHLU-UHFFFAOYSA-N Sobuzoxane Chemical compound C1C(=O)N(COC(=O)OCC(C)C)C(=O)CN1CCN1CC(=O)N(COC(=O)OCC(C)C)C(=O)C1 OCOKWVBYZHBHLU-UHFFFAOYSA-N 0.000 description 1
- DWAQJAXMDSEUJJ-UHFFFAOYSA-M Sodium bisulfite Chemical compound [Na+].OS([O-])=O DWAQJAXMDSEUJJ-UHFFFAOYSA-M 0.000 description 1
- UIRKNQLZZXALBI-MSVGPLKSSA-N Squalamine Chemical compound C([C@@H]1C[C@H]2O)[C@@H](NCCCNCCCCN)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H]([C@H](C)CC[C@H](C(C)C)OS(O)(=O)=O)[C@@]2(C)CC1 UIRKNQLZZXALBI-MSVGPLKSSA-N 0.000 description 1
- UIRKNQLZZXALBI-UHFFFAOYSA-N Squalamine Natural products OC1CC2CC(NCCCNCCCCN)CCC2(C)C2C1C1CCC(C(C)CCC(C(C)C)OS(O)(=O)=O)C1(C)CC2 UIRKNQLZZXALBI-UHFFFAOYSA-N 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- PCSMJKASWLYICJ-UHFFFAOYSA-N Succinic aldehyde Chemical compound O=CCCC=O PCSMJKASWLYICJ-UHFFFAOYSA-N 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- 206010042674 Swelling Diseases 0.000 description 1
- 206010042971 T-cell lymphoma Diseases 0.000 description 1
- 208000027585 T-cell non-Hodgkin lymphoma Diseases 0.000 description 1
- CYQFCXCEBYINGO-UHFFFAOYSA-N THC Natural products C1=C(C)CCC2C(C)(C)OC3=CC(CCCCC)=CC(O)=C3C21 CYQFCXCEBYINGO-UHFFFAOYSA-N 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- GUGOEEXESWIERI-UHFFFAOYSA-N Terfenadine Chemical compound C1=CC(C(C)(C)C)=CC=C1C(O)CCCN1CCC(C(O)(C=2C=CC=CC=2)C=2C=CC=CC=2)CC1 GUGOEEXESWIERI-UHFFFAOYSA-N 0.000 description 1
- WXZSUBHBYQYTNM-UHFFFAOYSA-N Tetrazomine Natural products C1=CC=2CC(N34)C(N5C)C(CO)CC5C4OCC3C=2C(OC)=C1NC(=O)C1NCCCC1O WXZSUBHBYQYTNM-UHFFFAOYSA-N 0.000 description 1
- 240000006474 Theobroma bicolor Species 0.000 description 1
- UPGGKUQISSWRJJ-XLTUSUNSSA-N Thiocoraline Chemical compound O=C([C@H]1CSSC[C@@H](N(C(=O)CNC2=O)C)C(=O)N(C)[C@@H](C(SC[C@@H](C(=O)NCC(=O)N1C)NC(=O)C=1C(=CC3=CC=CC=C3N=1)O)=O)CSC)N(C)[C@H](CSC)C(=O)SC[C@@H]2NC(=O)C1=NC2=CC=CC=C2C=C1O UPGGKUQISSWRJJ-XLTUSUNSSA-N 0.000 description 1
- 239000003490 Thiodipropionic acid Substances 0.000 description 1
- 102000011923 Thyrotropin Human genes 0.000 description 1
- 108010061174 Thyrotropin Proteins 0.000 description 1
- IVTVGDXNLFLDRM-HNNXBMFYSA-N Tomudex Chemical compound C=1C=C2NC(C)=NC(=O)C2=CC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)S1 IVTVGDXNLFLDRM-HNNXBMFYSA-N 0.000 description 1
- IWEQQRMGNVVKQW-OQKDUQJOSA-N Toremifene citrate Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O.C1=CC(OCCN(C)C)=CC=C1C(\C=1C=CC=CC=1)=C(\CCCl)C1=CC=CC=C1 IWEQQRMGNVVKQW-OQKDUQJOSA-N 0.000 description 1
- 208000032109 Transient ischaemic attack Diseases 0.000 description 1
- 108050009309 Tuberin Proteins 0.000 description 1
- 102000001742 Tumor Suppressor Proteins Human genes 0.000 description 1
- 108010040002 Tumor Suppressor Proteins Proteins 0.000 description 1
- VGQOVCHZGQWAOI-UHFFFAOYSA-N UNPD55612 Natural products N1C(O)C2CC(C=CC(N)=O)=CN2C(=O)C2=CC=C(C)C(O)=C12 VGQOVCHZGQWAOI-UHFFFAOYSA-N 0.000 description 1
- 208000007097 Urinary Bladder Neoplasms Diseases 0.000 description 1
- 102000003990 Urokinase-type plasminogen activator Human genes 0.000 description 1
- 108090000435 Urokinase-type plasminogen activator Proteins 0.000 description 1
- 108010003205 Vasoactive Intestinal Peptide Proteins 0.000 description 1
- 102400000015 Vasoactive intestinal peptide Human genes 0.000 description 1
- 206010047249 Venous thrombosis Diseases 0.000 description 1
- 229940122803 Vinca alkaloid Drugs 0.000 description 1
- BZHJMEDXRYGGRV-UHFFFAOYSA-N Vinyl chloride Chemical compound ClC=C BZHJMEDXRYGGRV-UHFFFAOYSA-N 0.000 description 1
- 241000700605 Viruses Species 0.000 description 1
- 229930003427 Vitamin E Natural products 0.000 description 1
- 208000033559 Waldenström macroglobulinemia Diseases 0.000 description 1
- TVXBFESIOXBWNM-UHFFFAOYSA-N Xylitol Natural products OCCC(O)C(O)C(O)CCO TVXBFESIOXBWNM-UHFFFAOYSA-N 0.000 description 1
- MHDDZDPNIDVLNK-ZGIWMXSJSA-N Zanoterone Chemical compound C1C2=NN(S(C)(=O)=O)C=C2C[C@]2(C)[C@H]3CC[C@](C)([C@](CC4)(O)C#C)[C@@H]4[C@@H]3CC[C@H]21 MHDDZDPNIDVLNK-ZGIWMXSJSA-N 0.000 description 1
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 1
- OGQICQVSFDPSEI-UHFFFAOYSA-N Zorac Chemical compound N1=CC(C(=O)OCC)=CC=C1C#CC1=CC=C(SCCC2(C)C)C2=C1 OGQICQVSFDPSEI-UHFFFAOYSA-N 0.000 description 1
- VUPBDWQPEOWRQP-RTUCOMKBSA-N [(2R,3S,4S,5R,6R)-2-[(2R,3S,4S,5S,6S)-2-[(1S,2S)-3-[[(2R,3S)-5-[[(2S,3R)-1-[[2-[4-[4-[[4-amino-6-[3-(4-aminobutylamino)propylamino]-6-oxohexyl]carbamoyl]-1,3-thiazol-2-yl]-1,3-thiazol-2-yl]-1-[(2S,3R,4R,5S,6S)-5-amino-3,4-dihydroxy-6-methyloxan-2-yl]oxy-2-hydroxyethyl]amino]-3-hydroxy-1-oxobutan-2-yl]amino]-3-hydroxy-5-oxopentan-2-yl]amino]-2-[[6-amino-2-[(1S)-3-amino-1-[[(2S)-2,3-diamino-3-oxopropyl]amino]-3-oxopropyl]-5-methylpyrimidine-4-carbonyl]amino]-1-(1H-imidazol-5-yl)-3-oxopropoxy]-4,5-dihydroxy-6-(hydroxymethyl)oxan-3-yl]oxy-3,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl] carbamate Chemical compound C[C@@H](O)[C@H](NC(=O)C[C@H](O)[C@@H](C)NC(=O)[C@@H](NC(=O)c1nc(nc(N)c1C)[C@H](CC(N)=O)NC[C@H](N)C(N)=O)[C@H](O[C@@H]1O[C@@H](CO)[C@@H](O)[C@H](O)[C@@H]1O[C@H]1O[C@H](CO)[C@@H](O)[C@H](OC(N)=O)[C@@H]1O)c1cnc[nH]1)C(=O)NC(O[C@@H]1O[C@@H](C)[C@@H](N)[C@@H](O)[C@H]1O)C(O)c1nc(cs1)-c1nc(cs1)C(=O)NCCCC(N)CC(=O)NCCCNCCCCN VUPBDWQPEOWRQP-RTUCOMKBSA-N 0.000 description 1
- SPKNARKFCOPTSY-XWPZMVOTSA-N [(2r,3s)-2-[(2s,3r)-3-methyloxiran-2-yl]-6-oxo-2,3-dihydropyran-3-yl] acetate Chemical compound C[C@H]1O[C@@H]1[C@H]1[C@@H](OC(C)=O)C=CC(=O)O1 SPKNARKFCOPTSY-XWPZMVOTSA-N 0.000 description 1
- ZHHIHQFAUZZMTG-BSVJBJGJSA-N [(2r,3s,4s,5r,6r)-2-[(2r,3s,4s,5s,6s)-2-[(1r,2s)-2-[[6-amino-2-[(1s)-3-amino-1-[[(2s)-2,3-diamino-3-oxopropyl]amino]-3-oxopropyl]-5-methylpyrimidine-4-carbonyl]amino]-3-[[(2r,3s,4s)-3-hydroxy-5-[[(2s,3r)-3-hydroxy-1-oxo-1-[2-[4-[4-[3-[[(1s)-1-phenylethyl] Chemical compound OS(O)(=O)=O.N([C@H](C(=O)N[C@H](C)[C@@H](O)[C@H](C)C(=O)N[C@@H]([C@H](O)C)C(=O)NCCC=1SC=C(N=1)C=1SC=C(N=1)C(=O)NCCCN[C@@H](C)C=1C=CC=CC=1)[C@@H](O[C@H]1[C@H]([C@@H](O)[C@H](O)[C@H](CO)O1)O[C@@H]1[C@H]([C@@H](OC(N)=O)[C@H](O)[C@@H](CO)O1)O)C=1NC=NC=1)C(=O)C1=NC([C@H](CC(N)=O)NC[C@H](N)C(N)=O)=NC(N)=C1C ZHHIHQFAUZZMTG-BSVJBJGJSA-N 0.000 description 1
- IVCRCPJOLWECJU-XQVQQVTHSA-N [(7r,8r,9s,10r,13s,14s,17s)-7,13-dimethyl-3-oxo-2,6,7,8,9,10,11,12,14,15,16,17-dodecahydro-1h-cyclopenta[a]phenanthren-17-yl] acetate Chemical compound C1C[C@]2(C)[C@@H](OC(C)=O)CC[C@H]2[C@@H]2[C@H](C)CC3=CC(=O)CC[C@@H]3[C@H]21 IVCRCPJOLWECJU-XQVQQVTHSA-N 0.000 description 1
- IFJUINDAXYAPTO-UUBSBJJBSA-N [(8r,9s,13s,14s,17s)-17-[2-[4-[4-[bis(2-chloroethyl)amino]phenyl]butanoyloxy]acetyl]oxy-13-methyl-6,7,8,9,11,12,14,15,16,17-decahydrocyclopenta[a]phenanthren-3-yl] benzoate Chemical compound C([C@@H]1[C@@H](C2=CC=3)CC[C@]4([C@H]1CC[C@@H]4OC(=O)COC(=O)CCCC=1C=CC(=CC=1)N(CCCl)CCCl)C)CC2=CC=3OC(=O)C1=CC=CC=C1 IFJUINDAXYAPTO-UUBSBJJBSA-N 0.000 description 1
- KMLCRELJHYKIIL-UHFFFAOYSA-N [1-(azanidylmethyl)cyclohexyl]methylazanide;platinum(2+);sulfuric acid Chemical compound [Pt+2].OS(O)(=O)=O.[NH-]CC1(C[NH-])CCCCC1 KMLCRELJHYKIIL-UHFFFAOYSA-N 0.000 description 1
- JJULHOZRTCDZOH-JGJFOBQESA-N [1-[[[(2r,3s,4s,5r)-5-(4-amino-2-oxopyrimidin-1-yl)-3,4-dihydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-hydroxyphosphoryl]oxy-3-octadecylsulfanylpropan-2-yl] hexadecanoate Chemical compound O[C@H]1[C@H](O)[C@@H](COP(O)(=O)OP(O)(=O)OCC(CSCCCCCCCCCCCCCCCCCC)OC(=O)CCCCCCCCCCCCCCC)O[C@H]1N1C(=O)N=C(N)C=C1 JJULHOZRTCDZOH-JGJFOBQESA-N 0.000 description 1
- XSMVECZRZBFTIZ-UHFFFAOYSA-M [2-(aminomethyl)cyclobutyl]methanamine;2-oxidopropanoate;platinum(4+) Chemical compound [Pt+4].CC([O-])C([O-])=O.NCC1CCC1CN XSMVECZRZBFTIZ-UHFFFAOYSA-M 0.000 description 1
- JURAJLFHWXNPHG-UHFFFAOYSA-N [acetyl(methylcarbamoyl)amino] n-methylcarbamate Chemical compound CNC(=O)ON(C(C)=O)C(=O)NC JURAJLFHWXNPHG-UHFFFAOYSA-N 0.000 description 1
- GZOSMCIZMLWJML-VJLLXTKPSA-N abiraterone Chemical compound C([C@H]1[C@H]2[C@@H]([C@]3(CC[C@H](O)CC3=CC2)C)CC[C@@]11C)C=C1C1=CC=CN=C1 GZOSMCIZMLWJML-VJLLXTKPSA-N 0.000 description 1
- 229960000853 abiraterone Drugs 0.000 description 1
- CWRYPZZKDGJXCA-UHFFFAOYSA-N acenaphthene Chemical compound C1=CC(CC2)=C3C2=CC=CC3=C1 CWRYPZZKDGJXCA-UHFFFAOYSA-N 0.000 description 1
- 125000004054 acenaphthylenyl group Chemical group C1(=CC2=CC=CC3=CC=CC1=C23)* 0.000 description 1
- DHKHKXVYLBGOIT-UHFFFAOYSA-N acetaldehyde Diethyl Acetal Natural products CCOC(C)OCC DHKHKXVYLBGOIT-UHFFFAOYSA-N 0.000 description 1
- IPBVNPXQWQGGJP-UHFFFAOYSA-N acetic acid phenyl ester Natural products CC(=O)OC1=CC=CC=C1 IPBVNPXQWQGGJP-UHFFFAOYSA-N 0.000 description 1
- RUGAHXUZHWYHNG-NLGNTGLNSA-N acetic acid;(4r,7s,10s,13r,16s,19r)-10-(4-aminobutyl)-n-[(2s,3r)-1-amino-3-hydroxy-1-oxobutan-2-yl]-19-[[(2r)-2-amino-3-naphthalen-2-ylpropanoyl]amino]-16-[(4-hydroxyphenyl)methyl]-13-(1h-indol-3-ylmethyl)-6,9,12,15,18-pentaoxo-7-propan-2-yl-1,2-dithia-5, Chemical compound CC(O)=O.CC(O)=O.CC(O)=O.CC(O)=O.CC(O)=O.C([C@H]1C(=O)N[C@H](CC=2C3=CC=CC=C3NC=2)C(=O)N[C@@H](CCCCN)C(=O)N[C@H](C(N[C@@H](CSSC[C@@H](C(=O)N1)NC(=O)[C@H](N)CC=1C=C2C=CC=CC2=CC=1)C(=O)N[C@@H]([C@@H](C)O)C(N)=O)=O)C(C)C)C1=CC=C(O)C=C1.C([C@H]1C(=O)N[C@H](CC=2C3=CC=CC=C3NC=2)C(=O)N[C@@H](CCCCN)C(=O)N[C@H](C(N[C@@H](CSSC[C@@H](C(=O)N1)NC(=O)[C@H](N)CC=1C=C2C=CC=CC2=CC=1)C(=O)N[C@@H]([C@@H](C)O)C(N)=O)=O)C(C)C)C1=CC=C(O)C=C1 RUGAHXUZHWYHNG-NLGNTGLNSA-N 0.000 description 1
- 229960001138 acetylsalicylic acid Drugs 0.000 description 1
- 239000003929 acidic solution Substances 0.000 description 1
- RJURFGZVJUQBHK-IIXSONLDSA-N actinomycin D Chemical compound C[C@H]1OC(=O)[C@H](C(C)C)N(C)C(=O)CN(C)C(=O)[C@@H]2CCCN2C(=O)[C@@H](C(C)C)NC(=O)[C@H]1NC(=O)C1=C(N)C(=O)C(C)=C2OC(C(C)=CC=C3C(=O)N[C@@H]4C(=O)N[C@@H](C(N5CCC[C@H]5C(=O)N(C)CC(=O)N(C)[C@@H](C(C)C)C(=O)O[C@@H]4C)=O)C(C)C)=C3N=C21 RJURFGZVJUQBHK-IIXSONLDSA-N 0.000 description 1
- 239000008186 active pharmaceutical agent Substances 0.000 description 1
- HLAKJNQXUARACO-UHFFFAOYSA-N acylfulvene Natural products CC1(O)C(=O)C2=CC(C)=CC2=C(C)C21CC2 HLAKJNQXUARACO-UHFFFAOYSA-N 0.000 description 1
- 125000005073 adamantyl group Chemical group C12(CC3CC(CC(C1)C3)C2)* 0.000 description 1
- 239000000853 adhesive Substances 0.000 description 1
- 239000002671 adjuvant Substances 0.000 description 1
- 201000005179 adrenal carcinoma Diseases 0.000 description 1
- 210000004100 adrenal gland Anatomy 0.000 description 1
- 201000005188 adrenal gland cancer Diseases 0.000 description 1
- 201000006966 adult T-cell leukemia Diseases 0.000 description 1
- 239000008272 agar Substances 0.000 description 1
- 235000010419 agar Nutrition 0.000 description 1
- 238000005054 agglomeration Methods 0.000 description 1
- 230000002776 aggregation Effects 0.000 description 1
- 230000001476 alcoholic effect Effects 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 235000010443 alginic acid Nutrition 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 229920000615 alginic acid Polymers 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 150000004781 alginic acids Chemical class 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 125000003342 alkenyl group Chemical group 0.000 description 1
- 150000003973 alkyl amines Chemical class 0.000 description 1
- 229940100198 alkylating agent Drugs 0.000 description 1
- 239000002168 alkylating agent Substances 0.000 description 1
- 125000000304 alkynyl group Chemical group 0.000 description 1
- SHGAZHPCJJPHSC-YCNIQYBTSA-N all-trans-retinoic acid Chemical compound OC(=O)\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C SHGAZHPCJJPHSC-YCNIQYBTSA-N 0.000 description 1
- 230000000735 allogeneic effect Effects 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 235000012211 aluminium silicate Nutrition 0.000 description 1
- 229950010949 ambamustine Drugs 0.000 description 1
- 229950004821 ambomycin Drugs 0.000 description 1
- 229960001097 amifostine Drugs 0.000 description 1
- 229940024606 amino acid Drugs 0.000 description 1
- 125000000539 amino acid group Chemical group 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- 229960002749 aminolevulinic acid Drugs 0.000 description 1
- 229960000510 ammonia Drugs 0.000 description 1
- 239000003708 ampul Substances 0.000 description 1
- 229960002550 amrubicin Drugs 0.000 description 1
- VJZITPJGSQKZMX-XDPRQOKASA-N amrubicin Chemical compound O([C@H]1C[C@](CC2=C(O)C=3C(=O)C4=CC=CC=C4C(=O)C=3C(O)=C21)(N)C(=O)C)[C@H]1C[C@H](O)[C@H](O)CO1 VJZITPJGSQKZMX-XDPRQOKASA-N 0.000 description 1
- 206010002022 amyloidosis Diseases 0.000 description 1
- 229960001694 anagrelide Drugs 0.000 description 1
- OTBXOEAOVRKTNQ-UHFFFAOYSA-N anagrelide Chemical compound N1=C2NC(=O)CN2CC2=C(Cl)C(Cl)=CC=C21 OTBXOEAOVRKTNQ-UHFFFAOYSA-N 0.000 description 1
- ASLUCFFROXVMFL-UHFFFAOYSA-N andrographolide Natural products CC1(CO)C(O)CCC2(C)C(CC=C3/C(O)OCC3=O)C(=C)CCC12 ASLUCFFROXVMFL-UHFFFAOYSA-N 0.000 description 1
- 229940121369 angiogenesis inhibitor Drugs 0.000 description 1
- 108010072788 angiogenin Proteins 0.000 description 1
- 108010070670 antarelix Proteins 0.000 description 1
- 125000002178 anthracenyl group Chemical group C1(=CC=CC2=CC3=CC=CC=C3C=C12)* 0.000 description 1
- 229940045799 anthracyclines and related substance Drugs 0.000 description 1
- VGQOVCHZGQWAOI-HYUHUPJXSA-N anthramycin Chemical compound N1[C@@H](O)[C@@H]2CC(\C=C\C(N)=O)=CN2C(=O)C2=CC=C(C)C(O)=C12 VGQOVCHZGQWAOI-HYUHUPJXSA-N 0.000 description 1
- 230000001458 anti-acid effect Effects 0.000 description 1
- 230000002280 anti-androgenic effect Effects 0.000 description 1
- 230000003474 anti-emetic effect Effects 0.000 description 1
- 229940046836 anti-estrogen Drugs 0.000 description 1
- 230000001833 anti-estrogenic effect Effects 0.000 description 1
- 230000001387 anti-histamine Effects 0.000 description 1
- 230000003110 anti-inflammatory effect Effects 0.000 description 1
- 230000000340 anti-metabolite Effects 0.000 description 1
- 229940044684 anti-microtubule agent Drugs 0.000 description 1
- 230000000259 anti-tumor effect Effects 0.000 description 1
- 239000000051 antiandrogen Substances 0.000 description 1
- 239000002111 antiemetic agent Substances 0.000 description 1
- 229940125683 antiemetic agent Drugs 0.000 description 1
- 239000000739 antihistaminic agent Substances 0.000 description 1
- 229940100197 antimetabolite Drugs 0.000 description 1
- 239000002256 antimetabolite Substances 0.000 description 1
- 229940045719 antineoplastic alkylating agent nitrosoureas Drugs 0.000 description 1
- 230000003078 antioxidant effect Effects 0.000 description 1
- 239000000074 antisense oligonucleotide Substances 0.000 description 1
- 238000012230 antisense oligonucleotides Methods 0.000 description 1
- IOASYARYEYRREA-LQAJYKIKSA-N aphidicolin glycinate Chemical compound C1[C@]23[C@]4(C)CC[C@H](O)[C@](C)(CO)[C@H]4CC[C@@H]3C[C@@H]1[C@@](COC(=O)CN)(O)CC2 IOASYARYEYRREA-LQAJYKIKSA-N 0.000 description 1
- 229940115115 aranesp Drugs 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 108010055530 arginyl-tryptophyl-N-methylphenylalanyl-tryptophyl-leucyl-methioninamide Proteins 0.000 description 1
- 239000003886 aromatase inhibitor Substances 0.000 description 1
- 229940046844 aromatase inhibitors Drugs 0.000 description 1
- 125000002102 aryl alkyloxo group Chemical group 0.000 description 1
- 125000004104 aryloxy group Chemical group 0.000 description 1
- 125000003289 ascorbyl group Chemical class [H]O[C@@]([H])(C([H])([H])O*)[C@@]1([H])OC(=O)C(O*)=C1O* 0.000 description 1
- 229960003272 asparaginase Drugs 0.000 description 1
- DCXYFEDJOCDNAF-UHFFFAOYSA-M asparaginate Chemical compound [O-]C(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-M 0.000 description 1
- 208000006673 asthma Diseases 0.000 description 1
- TWHSQQYCDVSBRK-UHFFFAOYSA-N asulacrine Chemical compound C12=CC=CC(C)=C2N=C2C(C(=O)NC)=CC=CC2=C1NC1=CC=C(NS(C)(=O)=O)C=C1OC TWHSQQYCDVSBRK-UHFFFAOYSA-N 0.000 description 1
- 229950011088 asulacrine Drugs 0.000 description 1
- PEPMWUSGRKINHX-TXTPUJOMSA-N atamestane Chemical compound C1C[C@@H]2[C@@]3(C)C(C)=CC(=O)C=C3CC[C@H]2[C@@H]2CCC(=O)[C@]21C PEPMWUSGRKINHX-TXTPUJOMSA-N 0.000 description 1
- 229950004810 atamestane Drugs 0.000 description 1
- 229950006933 atrimustine Drugs 0.000 description 1
- 229940120638 avastin Drugs 0.000 description 1
- 108010093161 axinastatin 1 Proteins 0.000 description 1
- PICZCWCKOLHDOJ-GHTSNYPWSA-N axinastatin 1 Chemical compound C([C@H]1C(=O)N[C@H](C(=O)N[C@H](C(=O)N2CCC[C@H]2C(=O)N[C@H](C(N[C@@H](CC(N)=O)C(=O)N2CCC[C@H]2C(=O)N1)=O)C(C)C)C(C)C)C(C)C)C1=CC=CC=C1 PICZCWCKOLHDOJ-GHTSNYPWSA-N 0.000 description 1
- 108010093000 axinastatin 2 Proteins 0.000 description 1
- OXNAATCTZCSVKR-AVGVIDKOSA-N axinastatin 2 Chemical compound C([C@H]1C(=O)N[C@H](C(=O)N[C@H](C(N2CCC[C@H]2C(=O)N[C@@H](C(=O)N[C@@H](CC(N)=O)C(=O)N2CCC[C@H]2C(=O)N1)C(C)C)=O)CC(C)C)C(C)C)C1=CC=CC=C1 OXNAATCTZCSVKR-AVGVIDKOSA-N 0.000 description 1
- UZCPCRPHNVHKKP-UHFFFAOYSA-N axinastatin 2 Natural products CC(C)CC1NC(=O)C2CCCN2C(=O)C(NC(=O)C(CC(=O)N)NC(=O)C3CCCN3C(=O)C(Cc4ccccc4)NC(=O)C(NC1=O)C(C)C)C(C)C UZCPCRPHNVHKKP-UHFFFAOYSA-N 0.000 description 1
- 108010092978 axinastatin 3 Proteins 0.000 description 1
- ANLDPEXRVVIABH-WUUSPZRJSA-N axinastatin 3 Chemical compound C([C@H]1C(=O)N[C@H](C(N[C@@H](CC(C)C)C(=O)N2CCC[C@H]2C(=O)N[C@@H](C(=O)N[C@@H](CC(N)=O)C(=O)N2CCC[C@H]2C(=O)N1)C(C)C)=O)[C@@H](C)CC)C1=CC=CC=C1 ANLDPEXRVVIABH-WUUSPZRJSA-N 0.000 description 1
- RTGMQVUKARGBNM-UHFFFAOYSA-N axinastatin 3 Natural products CCC(C)C1NC(=O)C(CC(C)C)NC(=O)C2CCCN2C(=O)C(NC(=O)C(CC(=O)N)NC(=O)C3CCCN3C(=O)C(Cc4ccccc4)NC1=O)C(C)C RTGMQVUKARGBNM-UHFFFAOYSA-N 0.000 description 1
- 229960002756 azacitidine Drugs 0.000 description 1
- OPWOOOGFNULJAQ-UHFFFAOYSA-L azane;cyclopentanamine;2-hydroxybutanedioate;platinum(2+) Chemical compound N.[Pt+2].NC1CCCC1.[O-]C(=O)C(O)CC([O-])=O OPWOOOGFNULJAQ-UHFFFAOYSA-L 0.000 description 1
- GRHLMSBCOPRFNA-UHFFFAOYSA-M azanide 2-oxidoacetate platinum(4+) Chemical compound N[Pt]1(N)OCC(=O)O1 GRHLMSBCOPRFNA-UHFFFAOYSA-M 0.000 description 1
- 229950005951 azasetron Drugs 0.000 description 1
- HRXVDDOKERXBEY-UHFFFAOYSA-N azatepa Chemical compound C1CN1P(=O)(N1CC1)N(CC)C1=NN=CS1 HRXVDDOKERXBEY-UHFFFAOYSA-N 0.000 description 1
- MIXLRUYCYZPSOQ-HXPMCKFVSA-N azatoxin Chemical compound COC1=C(O)C(OC)=CC([C@@H]2C3=C(C4=CC=CC=C4N3)C[C@@H]3N2C(OC3)=O)=C1 MIXLRUYCYZPSOQ-HXPMCKFVSA-N 0.000 description 1
- 125000002393 azetidinyl group Chemical group 0.000 description 1
- 229950004295 azotomycin Drugs 0.000 description 1
- 125000003828 azulenyl group Chemical group 0.000 description 1
- 150000004200 baccatin III derivatives Chemical class 0.000 description 1
- 230000003385 bacteriostatic effect Effects 0.000 description 1
- XYUFCXJZFZPEJD-PGRDOPGGSA-N balanol Chemical compound OC(=O)C1=CC=CC(O)=C1C(=O)C1=C(O)C=C(C(=O)O[C@H]2[C@H](CNCCC2)NC(=O)C=2C=CC(O)=CC=2)C=C1O XYUFCXJZFZPEJD-PGRDOPGGSA-N 0.000 description 1
- 229910052788 barium Inorganic materials 0.000 description 1
- DSAJWYNOEDNPEQ-UHFFFAOYSA-N barium atom Chemical compound [Ba] DSAJWYNOEDNPEQ-UHFFFAOYSA-N 0.000 description 1
- 229960000686 benzalkonium chloride Drugs 0.000 description 1
- 229960003872 benzethonium Drugs 0.000 description 1
- 229950005567 benzodepa Drugs 0.000 description 1
- 125000000499 benzofuranyl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- 229960004365 benzoic acid Drugs 0.000 description 1
- 125000004196 benzothienyl group Chemical group S1C(=CC2=C1C=CC=C2)* 0.000 description 1
- MMIMIFULGMZVPO-UHFFFAOYSA-N benzyl 3-bromo-2,6-dinitro-5-phenylmethoxybenzoate Chemical compound [O-][N+](=O)C1=C(C(=O)OCC=2C=CC=CC=2)C([N+](=O)[O-])=C(Br)C=C1OCC1=CC=CC=C1 MMIMIFULGMZVPO-UHFFFAOYSA-N 0.000 description 1
- 235000019445 benzyl alcohol Nutrition 0.000 description 1
- 229960004217 benzyl alcohol Drugs 0.000 description 1
- VFIUCBTYGKMLCM-UHFFFAOYSA-N benzyl n-[bis(aziridin-1-yl)phosphoryl]carbamate Chemical compound C=1C=CC=CC=1COC(=O)NP(=O)(N1CC1)N1CC1 VFIUCBTYGKMLCM-UHFFFAOYSA-N 0.000 description 1
- CADWTSSKOVRVJC-UHFFFAOYSA-N benzyl(dimethyl)azanium;chloride Chemical compound [Cl-].C[NH+](C)CC1=CC=CC=C1 CADWTSSKOVRVJC-UHFFFAOYSA-N 0.000 description 1
- 108010081355 beta 2-Microglobulin Proteins 0.000 description 1
- 102000015736 beta 2-Microglobulin Human genes 0.000 description 1
- QGJZLNKBHJESQX-FZFNOLFKSA-N betulinic acid Chemical compound C1C[C@H](O)C(C)(C)[C@@H]2CC[C@@]3(C)[C@]4(C)CC[C@@]5(C(O)=O)CC[C@@H](C(=C)C)[C@@H]5[C@H]4CC[C@@H]3[C@]21C QGJZLNKBHJESQX-FZFNOLFKSA-N 0.000 description 1
- GPRLTFBKWDERLU-UHFFFAOYSA-N bicyclo[2.2.2]octane Chemical compound C1CC2CCC1CC2 GPRLTFBKWDERLU-UHFFFAOYSA-N 0.000 description 1
- 238000010256 biochemical assay Methods 0.000 description 1
- 229920000249 biocompatible polymer Polymers 0.000 description 1
- 239000000090 biomarker Substances 0.000 description 1
- 230000008687 biosynthesis inhibition Effects 0.000 description 1
- 235000010290 biphenyl Nutrition 0.000 description 1
- 239000004305 biphenyl Substances 0.000 description 1
- QKSKPIVNLNLAAV-UHFFFAOYSA-N bis(2-chloroethyl) sulfide Chemical compound ClCCSCCCl QKSKPIVNLNLAAV-UHFFFAOYSA-N 0.000 description 1
- 229950002370 bisnafide Drugs 0.000 description 1
- NPSOIFAWYAHWOH-UHFFFAOYSA-N bistratene A Natural products O1C(CC(=O)C=CC)CCC(O2)(O)CC(C)C2CCCNC(=O)C(C)C2OC(CCC(C)C=C(C)C(C)O)CCCCC(C)C1CC(=O)NC2 NPSOIFAWYAHWOH-UHFFFAOYSA-N 0.000 description 1
- 229960004395 bleomycin sulfate Drugs 0.000 description 1
- 238000004820 blood count Methods 0.000 description 1
- 230000036765 blood level Effects 0.000 description 1
- 210000004204 blood vessel Anatomy 0.000 description 1
- 230000036760 body temperature Effects 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 238000010504 bond cleavage reaction Methods 0.000 description 1
- 238000006664 bond formation reaction Methods 0.000 description 1
- 201000008275 breast carcinoma Diseases 0.000 description 1
- PZOHOALJQOFNTB-UHFFFAOYSA-M brequinar sodium Chemical compound [Na+].N1=C2C=CC(F)=CC2=C(C([O-])=O)C(C)=C1C(C=C1)=CC=C1C1=CC=CC=C1F PZOHOALJQOFNTB-UHFFFAOYSA-M 0.000 description 1
- 150000004648 butanoic acid derivatives Chemical class 0.000 description 1
- 235000019282 butylated hydroxyanisole Nutrition 0.000 description 1
- 108700002839 cactinomycin Proteins 0.000 description 1
- 229950009908 cactinomycin Drugs 0.000 description 1
- LWQQLNNNIPYSNX-UROSTWAQSA-N calcipotriol Chemical compound C1([C@H](O)/C=C/[C@@H](C)[C@@H]2[C@]3(CCCC(/[C@@H]3CC2)=C\C=C\2C([C@@H](O)C[C@H](O)C/2)=C)C)CC1 LWQQLNNNIPYSNX-UROSTWAQSA-N 0.000 description 1
- 229960002882 calcipotriol Drugs 0.000 description 1
- 229960005084 calcitriol Drugs 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- CJZGTCYPCWQAJB-UHFFFAOYSA-L calcium stearate Chemical compound [Ca+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O CJZGTCYPCWQAJB-UHFFFAOYSA-L 0.000 description 1
- 235000013539 calcium stearate Nutrition 0.000 description 1
- 239000008116 calcium stearate Substances 0.000 description 1
- IVFYLRMMHVYGJH-PVPPCFLZSA-N calusterone Chemical compound C1C[C@]2(C)[C@](O)(C)CC[C@H]2[C@@H]2[C@@H](C)CC3=CC(=O)CC[C@]3(C)[C@H]21 IVFYLRMMHVYGJH-PVPPCFLZSA-N 0.000 description 1
- 229950009823 calusterone Drugs 0.000 description 1
- 229940127093 camptothecin Drugs 0.000 description 1
- 239000003560 cancer drug Substances 0.000 description 1
- 230000036952 cancer formation Effects 0.000 description 1
- 229940022399 cancer vaccine Drugs 0.000 description 1
- 238000009566 cancer vaccine Methods 0.000 description 1
- 239000007963 capsule composition Substances 0.000 description 1
- 229950009338 caracemide Drugs 0.000 description 1
- 229950005155 carbetimer Drugs 0.000 description 1
- 150000001720 carbohydrates Chemical group 0.000 description 1
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 1
- WNRZHQBJSXRYJK-UHFFFAOYSA-N carboxyamidotriazole Chemical compound NC1=C(C(=O)N)N=NN1CC(C=C1Cl)=CC(Cl)=C1C(=O)C1=CC=C(Cl)C=C1 WNRZHQBJSXRYJK-UHFFFAOYSA-N 0.000 description 1
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 1
- 231100000504 carcinogenesis Toxicity 0.000 description 1
- XREUEWVEMYWFFA-CSKJXFQVSA-N carminomycin Chemical compound C1[C@H](N)[C@H](O)[C@H](C)O[C@H]1O[C@@H]1C2=C(O)C(C(=O)C3=C(O)C=CC=C3C3=O)=C3C(O)=C2C[C@@](O)(C(C)=O)C1 XREUEWVEMYWFFA-CSKJXFQVSA-N 0.000 description 1
- 210000000845 cartilage Anatomy 0.000 description 1
- 229950001725 carubicin Drugs 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 229950010667 cedefingol Drugs 0.000 description 1
- 238000000423 cell based assay Methods 0.000 description 1
- 230000032823 cell division Effects 0.000 description 1
- 230000036755 cellular response Effects 0.000 description 1
- 201000007455 central nervous system cancer Diseases 0.000 description 1
- YMNCVRSYJBNGLD-KURKYZTESA-N cephalotaxine Chemical compound C([C@@]12C=C([C@H]([C@H]2C2=C3)O)OC)CCN1CCC2=CC1=C3OCO1 YMNCVRSYJBNGLD-KURKYZTESA-N 0.000 description 1
- 210000003679 cervix uteri Anatomy 0.000 description 1
- SBNPWPIBESPSIF-MHWMIDJBSA-N cetrorelix Chemical compound C([C@@H](C(=O)N[C@H](CCCNC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N1[C@@H](CCC1)C(=O)N[C@H](C)C(N)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](CC=1C=NC=CC=1)NC(=O)[C@@H](CC=1C=CC(Cl)=CC=1)NC(=O)[C@@H](CC=1C=C2C=CC=CC2=CC=1)NC(C)=O)C1=CC=C(O)C=C1 SBNPWPIBESPSIF-MHWMIDJBSA-N 0.000 description 1
- 108700008462 cetrorelix Proteins 0.000 description 1
- 229960003230 cetrorelix Drugs 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 230000009920 chelation Effects 0.000 description 1
- HZCWPKGYTCJSEB-UHFFFAOYSA-N chembl118841 Chemical compound C12=CC(OC)=CC=C2NC2=C([N+]([O-])=O)C=CC3=C2C1=NN3CCCN(C)C HZCWPKGYTCJSEB-UHFFFAOYSA-N 0.000 description 1
- OWSKEUBOCMEJMI-KPXOXKRLSA-N chembl2105946 Chemical compound [N-]=[N+]=CC(=O)CC[C@H](NC(=O)[C@@H](N)C)C(=O)N[C@H](CCC(=O)C=[N+]=[N-])C(O)=O OWSKEUBOCMEJMI-KPXOXKRLSA-N 0.000 description 1
- UKTAZPQNNNJVKR-KJGYPYNMSA-N chembl2368925 Chemical compound C1=CC=C2C(C(O[C@@H]3C[C@@H]4C[C@H]5C[C@@H](N4CC5=O)C3)=O)=CNC2=C1 UKTAZPQNNNJVKR-KJGYPYNMSA-N 0.000 description 1
- ZWVZORIKUNOTCS-OAQYLSRUSA-N chembl401930 Chemical compound C1([C@H](O)CNC2=C(C(NC=C2)=O)C=2NC=3C=C(C=C(C=3N=2)C)N2CCOCC2)=CC=CC(Cl)=C1 ZWVZORIKUNOTCS-OAQYLSRUSA-N 0.000 description 1
- DCKFXSZUWVWFEU-JECTWPLRSA-N chembl499423 Chemical compound O1[C@@H](CC)CCCC[C@]11NC(N23)=N[C@]4(O[C@H](C)CCC4)[C@@H](C(=O)OCCCCCCCCCCCCCCCC(=O)N(CCCN)C[C@@H](O)CCN)[C@@]3(O)CC[C@H]2C1 DCKFXSZUWVWFEU-JECTWPLRSA-N 0.000 description 1
- 210000000038 chest Anatomy 0.000 description 1
- 239000007910 chewable tablet Substances 0.000 description 1
- 229940112822 chewing gum Drugs 0.000 description 1
- 235000015218 chewing gum Nutrition 0.000 description 1
- 239000012069 chiral reagent Substances 0.000 description 1
- 229960004630 chlorambucil Drugs 0.000 description 1
- JCKYGMPEJWAADB-UHFFFAOYSA-N chlorambucil Chemical compound OC(=O)CCCC1=CC=C(N(CCCl)CCCl)C=C1 JCKYGMPEJWAADB-UHFFFAOYSA-N 0.000 description 1
- 150000004035 chlorins Chemical class 0.000 description 1
- 125000001309 chloro group Chemical group Cl* 0.000 description 1
- 229960004926 chlorobutanol Drugs 0.000 description 1
- 125000004218 chloromethyl group Chemical group [H]C([H])(Cl)* 0.000 description 1
- VDANGULDQQJODZ-UHFFFAOYSA-N chloroprocaine Chemical compound CCN(CC)CCOC(=O)C1=CC=C(N)C=C1Cl VDANGULDQQJODZ-UHFFFAOYSA-N 0.000 description 1
- 229960002023 chloroprocaine Drugs 0.000 description 1
- OEYIOHPDSNJKLS-UHFFFAOYSA-N choline Chemical compound C[N+](C)(C)CCO OEYIOHPDSNJKLS-UHFFFAOYSA-N 0.000 description 1
- 229960001231 choline Drugs 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- ARUGKOZUKWAXDS-SEWALLKFSA-N cicaprost Chemical compound C1\C(=C/COCC(O)=O)C[C@@H]2[C@@H](C#C[C@@H](O)[C@@H](C)CC#CCC)[C@H](O)C[C@@H]21 ARUGKOZUKWAXDS-SEWALLKFSA-N 0.000 description 1
- 229950000634 cicaprost Drugs 0.000 description 1
- 229950011359 cirolemycin Drugs 0.000 description 1
- 229960000928 clofarabine Drugs 0.000 description 1
- WDDPHFBMKLOVOX-AYQXTPAHSA-N clofarabine Chemical compound C1=NC=2C(N)=NC(Cl)=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@@H]1F WDDPHFBMKLOVOX-AYQXTPAHSA-N 0.000 description 1
- GKIRPKYJQBWNGO-OCEACIFDSA-N clomifene Chemical class C1=CC(OCCN(CC)CC)=CC=C1C(\C=1C=CC=CC=1)=C(\Cl)C1=CC=CC=C1 GKIRPKYJQBWNGO-OCEACIFDSA-N 0.000 description 1
- VNFPBHJOKIVQEB-UHFFFAOYSA-N clotrimazole Chemical compound ClC1=CC=CC=C1C(N1C=NC=C1)(C=1C=CC=CC=1)C1=CC=CC=C1 VNFPBHJOKIVQEB-UHFFFAOYSA-N 0.000 description 1
- 229960004022 clotrimazole Drugs 0.000 description 1
- 238000011260 co-administration Methods 0.000 description 1
- 229940110456 cocoa butter Drugs 0.000 description 1
- 235000019868 cocoa butter Nutrition 0.000 description 1
- 229940075614 colloidal silicon dioxide Drugs 0.000 description 1
- 201000010897 colon adenocarcinoma Diseases 0.000 description 1
- 238000004040 coloring Methods 0.000 description 1
- 238000011284 combination treatment Methods 0.000 description 1
- 229960005537 combretastatin A-4 Drugs 0.000 description 1
- HVXBOLULGPECHP-UHFFFAOYSA-N combretastatin A4 Natural products C1=C(O)C(OC)=CC=C1C=CC1=CC(OC)=C(OC)C(OC)=C1 HVXBOLULGPECHP-UHFFFAOYSA-N 0.000 description 1
- 150000004814 combretastatins Chemical class 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 238000007906 compression Methods 0.000 description 1
- 230000006835 compression Effects 0.000 description 1
- 235000005687 corn oil Nutrition 0.000 description 1
- 239000002285 corn oil Substances 0.000 description 1
- 239000006184 cosolvent Substances 0.000 description 1
- 235000001671 coumarin Nutrition 0.000 description 1
- 229960000956 coumarin Drugs 0.000 description 1
- 150000001896 cresols Chemical class 0.000 description 1
- PSNOPSMXOBPNNV-VVCTWANISA-N cryptophycin 1 Chemical class C1=C(Cl)C(OC)=CC=C1C[C@@H]1C(=O)NC[C@@H](C)C(=O)O[C@@H](CC(C)C)C(=O)O[C@H]([C@H](C)[C@@H]2[C@H](O2)C=2C=CC=CC=2)C/C=C/C(=O)N1 PSNOPSMXOBPNNV-VVCTWANISA-N 0.000 description 1
- 108010090203 cryptophycin 8 Proteins 0.000 description 1
- 229940097362 cyclodextrins Drugs 0.000 description 1
- MKNXBRLZBFVUPV-UHFFFAOYSA-L cyclopenta-1,3-diene;dichlorotitanium Chemical compound Cl[Ti]Cl.C=1C=C[CH-]C=1.C=1C=C[CH-]C=1 MKNXBRLZBFVUPV-UHFFFAOYSA-L 0.000 description 1
- 108010041566 cypemycin Proteins 0.000 description 1
- 208000031513 cyst Diseases 0.000 description 1
- 230000000093 cytochemical effect Effects 0.000 description 1
- 230000001461 cytolytic effect Effects 0.000 description 1
- 239000002254 cytotoxic agent Substances 0.000 description 1
- 231100000599 cytotoxic agent Toxicity 0.000 description 1
- YCWXIQRLONXJLF-PFFGJIDWSA-N d06307 Chemical compound OS(O)(=O)=O.C([C@]1([C@@H]2O1)CC)N(CCC=1C3=CC=CC=C3NC=11)C[C@H]2C[C@]1(C(=O)OC)C1=CC([C@]23[C@H]([C@@]([C@H](OC(C)=O)[C@]4(CC)C=CCN([C@H]34)CC2)(O)C(=O)OC)N2C)=C2C=C1OC.C([C@]1([C@@H]2O1)CC)N(CCC=1C3=CC=CC=C3NC=11)C[C@H]2C[C@]1(C(=O)OC)C1=CC([C@]23[C@H]([C@@]([C@H](OC(C)=O)[C@]4(CC)C=CCN([C@H]34)CC2)(O)C(=O)OC)N2C)=C2C=C1OC YCWXIQRLONXJLF-PFFGJIDWSA-N 0.000 description 1
- 229960000640 dactinomycin Drugs 0.000 description 1
- 229960000975 daunorubicin Drugs 0.000 description 1
- 229960003109 daunorubicin hydrochloride Drugs 0.000 description 1
- 229940041983 daunorubicin liposomal Drugs 0.000 description 1
- 125000004855 decalinyl group Chemical group C1(CCCC2CCCCC12)* 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 230000007812 deficiency Effects 0.000 description 1
- 230000006735 deficit Effects 0.000 description 1
- 230000003111 delayed effect Effects 0.000 description 1
- CYQFCXCEBYINGO-IAGOWNOFSA-N delta1-THC Chemical compound C1=C(C)CC[C@H]2C(C)(C)OC3=CC(CCCCC)=CC(O)=C3[C@@H]21 CYQFCXCEBYINGO-IAGOWNOFSA-N 0.000 description 1
- 239000005547 deoxyribonucleotide Substances 0.000 description 1
- 125000002637 deoxyribonucleotide group Chemical group 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 108700025485 deslorelin Proteins 0.000 description 1
- 229960005408 deslorelin Drugs 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- VPOCYEOOFRNHNL-RQDPQJJXSA-J dexormaplatin Chemical compound Cl[Pt](Cl)(Cl)Cl.N[C@@H]1CCCC[C@H]1N VPOCYEOOFRNHNL-RQDPQJJXSA-J 0.000 description 1
- 229950001640 dexormaplatin Drugs 0.000 description 1
- 229960000605 dexrazoxane Drugs 0.000 description 1
- 239000008355 dextrose injection Substances 0.000 description 1
- SGTNSNPWRIOYBX-HHHXNRCGSA-N dexverapamil Chemical compound C1=C(OC)C(OC)=CC=C1CCN(C)CCC[C@@](C#N)(C(C)C)C1=CC=C(OC)C(OC)=C1 SGTNSNPWRIOYBX-HHHXNRCGSA-N 0.000 description 1
- 229950005878 dexverapamil Drugs 0.000 description 1
- 229950010621 dezaguanine Drugs 0.000 description 1
- HEOKFDGOFROELJ-UHFFFAOYSA-N diacetal Natural products COc1ccc(C=C/c2cc(O)cc(OC3OC(COC(=O)c4cc(O)c(O)c(O)c4)C(O)C(O)C3O)c2)cc1O HEOKFDGOFROELJ-UHFFFAOYSA-N 0.000 description 1
- NEFBYIFKOOEVPA-UHFFFAOYSA-K dicalcium phosphate Chemical compound [Ca+2].[Ca+2].[O-]P([O-])([O-])=O NEFBYIFKOOEVPA-UHFFFAOYSA-K 0.000 description 1
- 229940038472 dicalcium phosphate Drugs 0.000 description 1
- 229910000390 dicalcium phosphate Inorganic materials 0.000 description 1
- KYHUYMLIVQFXRI-UHFFFAOYSA-N didemnin B Natural products CC1OC(=O)C(CC=2C=CC(OC)=CC=2)N(C)C(=O)C2CCCN2C(=O)C(CC(C)C)NC(=O)C(C)C(=O)C(C(C)C)OC(=O)CC(O)C(C(C)CC)NC(=O)C1NC(=O)C(CC(C)C)N(C)C(=O)C1CCCN1C(=O)C(C)O KYHUYMLIVQFXRI-UHFFFAOYSA-N 0.000 description 1
- 108010061297 didemnins Proteins 0.000 description 1
- ZBCBWPMODOFKDW-UHFFFAOYSA-N diethanolamine Chemical compound OCCNCCO ZBCBWPMODOFKDW-UHFFFAOYSA-N 0.000 description 1
- 229940043237 diethanolamine Drugs 0.000 description 1
- HPNMFZURTQLUMO-UHFFFAOYSA-N diethylamine Chemical compound CCNCC HPNMFZURTQLUMO-UHFFFAOYSA-N 0.000 description 1
- 230000029087 digestion Effects 0.000 description 1
- SBZXBUIDTXKZTM-UHFFFAOYSA-N diglyme Chemical compound COCCOCCOC SBZXBUIDTXKZTM-UHFFFAOYSA-N 0.000 description 1
- 150000004683 dihydrates Chemical class 0.000 description 1
- PZXJOHSZQAEJFE-UHFFFAOYSA-N dihydrobetulinic acid Natural products C1CC(O)C(C)(C)C2CCC3(C)C4(C)CCC5(C(O)=O)CCC(C(C)C)C5C4CCC3C21C PZXJOHSZQAEJFE-UHFFFAOYSA-N 0.000 description 1
- SIYLLGKDQZGJHK-UHFFFAOYSA-N dimethyl-(phenylmethyl)-[2-[2-[4-(2,4,4-trimethylpentan-2-yl)phenoxy]ethoxy]ethyl]ammonium Chemical compound C1=CC(C(C)(C)CC(C)(C)C)=CC=C1OCCOCC[N+](C)(C)CC1=CC=CC=C1 SIYLLGKDQZGJHK-UHFFFAOYSA-N 0.000 description 1
- 150000002016 disaccharides Chemical class 0.000 description 1
- 231100000676 disease causative agent Toxicity 0.000 description 1
- 208000037765 diseases and disorders Diseases 0.000 description 1
- SVJSWELRJWVPQD-KJWOGLQMSA-L disodium;(2s)-2-[[4-[2-[(6r)-2-amino-4-oxo-5,6,7,8-tetrahydro-1h-pyrido[2,3-d]pyrimidin-6-yl]ethyl]benzoyl]amino]pentanedioate Chemical compound [Na+].[Na+].C([C@@H]1CC=2C(=O)N=C(NC=2NC1)N)CC1=CC=C(C(=O)N[C@@H](CCC([O-])=O)C([O-])=O)C=C1 SVJSWELRJWVPQD-KJWOGLQMSA-L 0.000 description 1
- 239000007919 dispersible tablet Substances 0.000 description 1
- 208000009190 disseminated intravascular coagulation Diseases 0.000 description 1
- 239000012990 dithiocarbamate Substances 0.000 description 1
- 150000004659 dithiocarbamates Chemical class 0.000 description 1
- 239000002934 diuretic Substances 0.000 description 1
- 229940030606 diuretics Drugs 0.000 description 1
- VSJKWCGYPAHWDS-UHFFFAOYSA-N dl-camptothecin Natural products C1=CC=C2C=C(CN3C4=CC5=C(C3=O)COC(=O)C5(O)CC)C4=NC2=C1 VSJKWCGYPAHWDS-UHFFFAOYSA-N 0.000 description 1
- 239000003534 dna topoisomerase inhibitor Substances 0.000 description 1
- 229960000735 docosanol Drugs 0.000 description 1
- 229960003413 dolasetron Drugs 0.000 description 1
- 231100000371 dose-limiting toxicity Toxicity 0.000 description 1
- ZWAOHEXOSAUJHY-ZIYNGMLESA-N doxifluridine Chemical compound O[C@@H]1[C@H](O)[C@@H](C)O[C@H]1N1C(=O)NC(=O)C(F)=C1 ZWAOHEXOSAUJHY-ZIYNGMLESA-N 0.000 description 1
- 229950005454 doxifluridine Drugs 0.000 description 1
- 229960002918 doxorubicin hydrochloride Drugs 0.000 description 1
- 239000008298 dragée Substances 0.000 description 1
- NOTIQUSPUUHHEH-UXOVVSIBSA-N dromostanolone propionate Chemical compound C([C@@H]1CC2)C(=O)[C@H](C)C[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H](OC(=O)CC)[C@@]2(C)CC1 NOTIQUSPUUHHEH-UXOVVSIBSA-N 0.000 description 1
- 229960004242 dronabinol Drugs 0.000 description 1
- 229950004683 drostanolone propionate Drugs 0.000 description 1
- 238000001647 drug administration Methods 0.000 description 1
- 229940088679 drug related substance Drugs 0.000 description 1
- 238000002651 drug therapy Methods 0.000 description 1
- 229950005133 duazomycin Drugs 0.000 description 1
- 229930192837 duazomycin Natural products 0.000 description 1
- VQNATVDKACXKTF-XELLLNAOSA-N duocarmycin Chemical compound COC1=C(OC)C(OC)=C2NC(C(=O)N3C4=CC(=O)C5=C([C@@]64C[C@@H]6C3)C=C(N5)C(=O)OC)=CC2=C1 VQNATVDKACXKTF-XELLLNAOSA-N 0.000 description 1
- 229960005510 duocarmycin SA Drugs 0.000 description 1
- 238000010410 dusting Methods 0.000 description 1
- 229950005678 ecomustine Drugs 0.000 description 1
- FSIRXIHZBIXHKT-MHTVFEQDSA-N edatrexate Chemical compound C=1N=C2N=C(N)N=C(N)C2=NC=1CC(CC)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 FSIRXIHZBIXHKT-MHTVFEQDSA-N 0.000 description 1
- 229950006700 edatrexate Drugs 0.000 description 1
- 229950011461 edelfosine Drugs 0.000 description 1
- 230000002500 effect on skin Effects 0.000 description 1
- 229960002759 eflornithine Drugs 0.000 description 1
- VLCYCQAOQCDTCN-UHFFFAOYSA-N eflornithine Chemical compound NCCCC(N)(C(F)F)C(O)=O VLCYCQAOQCDTCN-UHFFFAOYSA-N 0.000 description 1
- 229960002046 eflornithine hydrochloride Drugs 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- MGQRRMONVLMKJL-KWJIQSIXSA-N elsamitrucin Chemical compound O1[C@H](C)[C@H](O)[C@H](OC)[C@@H](N)[C@H]1O[C@@H]1[C@](O)(C)[C@@H](O)[C@@H](C)O[C@H]1OC1=CC=CC2=C(O)C(C(O3)=O)=C4C5=C3C=CC(C)=C5C(=O)OC4=C12 MGQRRMONVLMKJL-KWJIQSIXSA-N 0.000 description 1
- 229950002339 elsamitrucin Drugs 0.000 description 1
- 239000002895 emetic Substances 0.000 description 1
- 229950005450 emitefur Drugs 0.000 description 1
- 238000005538 encapsulation Methods 0.000 description 1
- 210000004696 endometrium Anatomy 0.000 description 1
- JOZGNYDSEBIJDH-UHFFFAOYSA-N eniluracil Chemical compound O=C1NC=C(C#C)C(=O)N1 JOZGNYDSEBIJDH-UHFFFAOYSA-N 0.000 description 1
- 239000002662 enteric coated tablet Substances 0.000 description 1
- 229950004926 epipropidine Drugs 0.000 description 1
- 229960001904 epirubicin Drugs 0.000 description 1
- 229960003265 epirubicin hydrochloride Drugs 0.000 description 1
- 229940089118 epogen Drugs 0.000 description 1
- 229950001426 erbulozole Drugs 0.000 description 1
- KLEPCGBEXOCIGS-QPPBQGQZSA-N erbulozole Chemical compound C1=CC(NC(=O)OCC)=CC=C1SC[C@@H]1O[C@@](CN2C=NC=C2)(C=2C=CC(OC)=CC=2)OC1 KLEPCGBEXOCIGS-QPPBQGQZSA-N 0.000 description 1
- AAKJLRGGTJKAMG-UHFFFAOYSA-N erlotinib Chemical compound C=12C=C(OCCOC)C(OCCOC)=CC2=NC=NC=1NC1=CC=CC(C#C)=C1 AAKJLRGGTJKAMG-UHFFFAOYSA-N 0.000 description 1
- 229960001433 erlotinib Drugs 0.000 description 1
- 230000000925 erythroid effect Effects 0.000 description 1
- 229940105423 erythropoietin Drugs 0.000 description 1
- 210000003238 esophagus Anatomy 0.000 description 1
- 229960004750 estramustine phosphate Drugs 0.000 description 1
- ADFOJJHRTBFFOF-RBRWEJTLSA-N estramustine phosphate Chemical compound ClCCN(CCCl)C(=O)OC1=CC=C2[C@H]3CC[C@](C)([C@H](CC4)OP(O)(O)=O)[C@@H]4[C@@H]3CCC2=C1 ADFOJJHRTBFFOF-RBRWEJTLSA-N 0.000 description 1
- 229960001766 estramustine phosphate sodium Drugs 0.000 description 1
- CKHUMILJZKSHJU-UHFFFAOYSA-N ethane;tin Chemical compound CC[Sn] CKHUMILJZKSHJU-UHFFFAOYSA-N 0.000 description 1
- XPGDODOEEWLHOI-GSDHBNRESA-N ethyl (2s)-2-[[(2s)-2-[[(2s)-2-amino-3-(4-fluorophenyl)propanoyl]amino]-3-[3-[bis(2-chloroethyl)amino]phenyl]propanoyl]amino]-4-methylsulfanylbutanoate Chemical compound C([C@@H](C(=O)N[C@@H](CCSC)C(=O)OCC)NC(=O)[C@@H](N)CC=1C=CC(F)=CC=1)C1=CC=CC(N(CCCl)CCCl)=C1 XPGDODOEEWLHOI-GSDHBNRESA-N 0.000 description 1
- 229940009626 etidronate Drugs 0.000 description 1
- 230000003203 everyday effect Effects 0.000 description 1
- 201000005884 exanthem Diseases 0.000 description 1
- 229960000255 exemestane Drugs 0.000 description 1
- 208000021045 exocrine pancreatic carcinoma Diseases 0.000 description 1
- 238000013265 extended release Methods 0.000 description 1
- 210000002744 extracellular matrix Anatomy 0.000 description 1
- 229950011548 fadrozole Drugs 0.000 description 1
- 239000003925 fat Substances 0.000 description 1
- 235000019197 fats Nutrition 0.000 description 1
- 239000010685 fatty oil Substances 0.000 description 1
- 229940126864 fibroblast growth factor Drugs 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 239000007941 film coated tablet Substances 0.000 description 1
- DBEPLOCGEIEOCV-WSBQPABSSA-N finasteride Chemical compound N([C@@H]1CC2)C(=O)C=C[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H](C(=O)NC(C)(C)C)[C@@]2(C)CC1 DBEPLOCGEIEOCV-WSBQPABSSA-N 0.000 description 1
- 229960004039 finasteride Drugs 0.000 description 1
- 229960000961 floxuridine Drugs 0.000 description 1
- ODKNJVUHOIMIIZ-RRKCRQDMSA-N floxuridine Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C(F)=C1 ODKNJVUHOIMIIZ-RRKCRQDMSA-N 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- GVEPBJHOBDJJJI-UHFFFAOYSA-N fluoranthrene Natural products C1=CC(C2=CC=CC=C22)=C3C2=CC=CC3=C1 GVEPBJHOBDJJJI-UHFFFAOYSA-N 0.000 description 1
- RMBPEFMHABBEKP-UHFFFAOYSA-N fluorene Chemical compound C1=CC=C2C3=C[CH]C=CC3=CC2=C1 RMBPEFMHABBEKP-UHFFFAOYSA-N 0.000 description 1
- 125000003983 fluorenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3CC12)* 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 229950005682 flurocitabine Drugs 0.000 description 1
- 239000006260 foam Substances 0.000 description 1
- 239000011888 foil Substances 0.000 description 1
- 230000003325 follicular Effects 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- 229950004217 forfenimex Drugs 0.000 description 1
- 229960004421 formestane Drugs 0.000 description 1
- OSVMTWJCGUFAOD-KZQROQTASA-N formestane Chemical compound O=C1CC[C@]2(C)[C@H]3CC[C@](C)(C(CC4)=O)[C@@H]4[C@@H]3CCC2=C1O OSVMTWJCGUFAOD-KZQROQTASA-N 0.000 description 1
- UXTSQCOOUJTIAC-UHFFFAOYSA-N fosquidone Chemical compound C=1N2CC3=CC=CC=C3C(C)C2=C(C(C2=CC=C3)=O)C=1C(=O)C2=C3OP(O)(=O)OCC1=CC=CC=C1 UXTSQCOOUJTIAC-UHFFFAOYSA-N 0.000 description 1
- 229950005611 fosquidone Drugs 0.000 description 1
- VZCYOOQTPOCHFL-OWOJBTEDSA-L fumarate(2-) Chemical class [O-]C(=O)\C=C\C([O-])=O VZCYOOQTPOCHFL-OWOJBTEDSA-L 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 230000001408 fungistatic effect Effects 0.000 description 1
- 108020001507 fusion proteins Proteins 0.000 description 1
- 102000037865 fusion proteins Human genes 0.000 description 1
- 229940044658 gallium nitrate Drugs 0.000 description 1
- 229950004410 galocitabine Drugs 0.000 description 1
- WIGCFUFOHFEKBI-UHFFFAOYSA-N gamma-tocopherol Natural products CC(C)CCCC(C)CCCC(C)CCCC1CCC2C(C)C(O)C(C)C(C)C2O1 WIGCFUFOHFEKBI-UHFFFAOYSA-N 0.000 description 1
- GJNXBNATEDXMAK-PFLSVRRQSA-N ganirelix Chemical compound C([C@@H](C(=O)N[C@H](CCCCN=C(NCC)NCC)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCCN=C(NCC)NCC)C(=O)N1[C@@H](CCC1)C(=O)N[C@H](C)C(N)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](CC=1C=NC=CC=1)NC(=O)[C@@H](CC=1C=CC(Cl)=CC=1)NC(=O)[C@@H](CC=1C=C2C=CC=CC2=CC=1)NC(C)=O)C1=CC=C(O)C=C1 GJNXBNATEDXMAK-PFLSVRRQSA-N 0.000 description 1
- 108700032141 ganirelix Proteins 0.000 description 1
- 229960003794 ganirelix Drugs 0.000 description 1
- 210000001035 gastrointestinal tract Anatomy 0.000 description 1
- 239000002406 gelatinase inhibitor Substances 0.000 description 1
- 229960005144 gemcitabine hydrochloride Drugs 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 235000001727 glucose Nutrition 0.000 description 1
- 229960002989 glutamic acid Drugs 0.000 description 1
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 1
- 229960003180 glutathione Drugs 0.000 description 1
- 229960005150 glycerol Drugs 0.000 description 1
- 150000002334 glycols Chemical class 0.000 description 1
- 208000030316 grade III meningioma Diseases 0.000 description 1
- 210000003714 granulocyte Anatomy 0.000 description 1
- 229940093915 gynecological organic acid Drugs 0.000 description 1
- 201000009277 hairy cell leukemia Diseases 0.000 description 1
- 150000004820 halides Chemical class 0.000 description 1
- 230000003862 health status Effects 0.000 description 1
- 210000002216 heart Anatomy 0.000 description 1
- 210000003958 hematopoietic stem cell Anatomy 0.000 description 1
- 210000000777 hematopoietic system Anatomy 0.000 description 1
- 230000011132 hemopoiesis Effects 0.000 description 1
- 229960002897 heparin Drugs 0.000 description 1
- 229920000669 heparin Polymers 0.000 description 1
- 125000005844 heterocyclyloxy group Chemical group 0.000 description 1
- 230000003054 hormonal effect Effects 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 208000018821 hormone-resistant prostate carcinoma Diseases 0.000 description 1
- 229940084986 human chorionic gonadotropin Drugs 0.000 description 1
- 150000004677 hydrates Chemical class 0.000 description 1
- 150000003840 hydrochlorides Chemical class 0.000 description 1
- SOCGJDYHNGLZEC-UHFFFAOYSA-N hydron;n-methyl-n-[4-[(7-methyl-3h-imidazo[4,5-f]quinolin-9-yl)amino]phenyl]acetamide;chloride Chemical compound Cl.C1=CC(N(C(C)=O)C)=CC=C1NC1=CC(C)=NC2=CC=C(NC=N3)C3=C12 SOCGJDYHNGLZEC-UHFFFAOYSA-N 0.000 description 1
- 229920001600 hydrophobic polymer Polymers 0.000 description 1
- 229960004337 hydroquinone Drugs 0.000 description 1
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 1
- 235000019447 hydroxyethyl cellulose Nutrition 0.000 description 1
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 1
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 1
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 1
- UFVKGYZPFZQRLF-UHFFFAOYSA-N hydroxypropyl methyl cellulose Chemical compound OC1C(O)C(OC)OC(CO)C1OC1C(O)C(O)C(OC2C(C(O)C(OC3C(C(O)C(O)C(CO)O3)O)C(CO)O2)O)C(CO)O1 UFVKGYZPFZQRLF-UHFFFAOYSA-N 0.000 description 1
- 230000000148 hypercalcaemia Effects 0.000 description 1
- 208000030915 hypercalcemia disease Diseases 0.000 description 1
- MPGWGYQTRSNGDD-UHFFFAOYSA-N hypericin Chemical compound OC1=CC(O)=C(C2=O)C3=C1C1C(O)=CC(=O)C(C4=O)=C1C1=C3C3=C2C(O)=CC(C)=C3C2=C1C4=C(O)C=C2C MPGWGYQTRSNGDD-UHFFFAOYSA-N 0.000 description 1
- 229940005608 hypericin Drugs 0.000 description 1
- PHOKTTKFQUYZPI-UHFFFAOYSA-N hypericin Natural products Cc1cc(O)c2c3C(=O)C(=Cc4c(O)c5c(O)cc(O)c6c7C(=O)C(=Cc8c(C)c1c2c(c78)c(c34)c56)O)O PHOKTTKFQUYZPI-UHFFFAOYSA-N 0.000 description 1
- 239000007946 hypodermic tablet Substances 0.000 description 1
- 229960005236 ibandronic acid Drugs 0.000 description 1
- 229960001176 idarubicin hydrochloride Drugs 0.000 description 1
- 229950002248 idoxifene Drugs 0.000 description 1
- 229960001101 ifosfamide Drugs 0.000 description 1
- HOMGKSMUEGBAAB-UHFFFAOYSA-N ifosfamide Chemical compound ClCCNP1(=O)OCCCN1CCCl HOMGKSMUEGBAAB-UHFFFAOYSA-N 0.000 description 1
- NITYDPDXAAFEIT-DYVFJYSZSA-N ilomastat Chemical compound C1=CC=C2C(C[C@@H](C(=O)NC)NC(=O)[C@H](CC(C)C)CC(=O)NO)=CNC2=C1 NITYDPDXAAFEIT-DYVFJYSZSA-N 0.000 description 1
- 229960003696 ilomastat Drugs 0.000 description 1
- KTUFNOKKBVMGRW-UHFFFAOYSA-N imatinib Chemical compound C1CN(C)CCN1CC1=CC=C(C(=O)NC=2C=C(NC=3N=C(C=CN=3)C=3C=NC=CC=3)C(C)=CC=2)C=C1 KTUFNOKKBVMGRW-UHFFFAOYSA-N 0.000 description 1
- 229960002411 imatinib Drugs 0.000 description 1
- 229960002751 imiquimod Drugs 0.000 description 1
- DOUYETYNHWVLEO-UHFFFAOYSA-N imiquimod Chemical compound C1=CC=CC2=C3N(CC(C)C)C=NC3=C(N)N=C21 DOUYETYNHWVLEO-UHFFFAOYSA-N 0.000 description 1
- 230000005934 immune activation Effects 0.000 description 1
- 230000001900 immune effect Effects 0.000 description 1
- 230000036737 immune function Effects 0.000 description 1
- 230000028993 immune response Effects 0.000 description 1
- 230000037451 immune surveillance Effects 0.000 description 1
- 210000000987 immune system Anatomy 0.000 description 1
- 230000003308 immunostimulating effect Effects 0.000 description 1
- 230000001506 immunosuppresive effect Effects 0.000 description 1
- 238000002513 implantation Methods 0.000 description 1
- 238000000099 in vitro assay Methods 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 125000003454 indenyl group Chemical group C1(C=CC2=CC=CC=C12)* 0.000 description 1
- 208000015266 indolent plasma cell myeloma Diseases 0.000 description 1
- 125000001041 indolyl group Chemical group 0.000 description 1
- 239000000411 inducer Substances 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 210000004969 inflammatory cell Anatomy 0.000 description 1
- 208000027866 inflammatory disease Diseases 0.000 description 1
- 238000002664 inhalation therapy Methods 0.000 description 1
- 229910052500 inorganic mineral Inorganic materials 0.000 description 1
- 238000003780 insertion Methods 0.000 description 1
- 230000037431 insertion Effects 0.000 description 1
- 102000028416 insulin-like growth factor binding Human genes 0.000 description 1
- 108091022911 insulin-like growth factor binding Proteins 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 229950000038 interferon alfa Drugs 0.000 description 1
- 238000001361 intraarterial administration Methods 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- VBUWHHLIZKOSMS-RIWXPGAOSA-N invicorp Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(N)=O)C(O)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CCCCN)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](CCSC)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC=1NC=NC=1)C(C)C)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=C(O)C=C1 VBUWHHLIZKOSMS-RIWXPGAOSA-N 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 229950010897 iproplatin Drugs 0.000 description 1
- 229960000779 irinotecan hydrochloride Drugs 0.000 description 1
- 229950000855 iroplact Drugs 0.000 description 1
- 230000001788 irregular Effects 0.000 description 1
- 230000002262 irrigation Effects 0.000 description 1
- 238000003973 irrigation Methods 0.000 description 1
- 125000002183 isoquinolinyl group Chemical group C1(=NC=CC2=CC=CC=C12)* 0.000 description 1
- 239000000644 isotonic solution Substances 0.000 description 1
- RWXRJSRJIITQAK-ZSBIGDGJSA-N itasetron Chemical compound C12=CC=CC=C2NC(=O)N1C(=O)N[C@H](C1)C[C@H]2CC[C@@H]1N2C RWXRJSRJIITQAK-ZSBIGDGJSA-N 0.000 description 1
- 229950007654 itasetron Drugs 0.000 description 1
- GQWYWHOHRVVHAP-DHKPLNAMSA-N jaspamide Chemical compound C1([C@@H]2NC(=O)[C@@H](CC=3C4=CC=CC=C4NC=3Br)N(C)C(=O)[C@H](C)NC(=O)[C@@H](C)C/C(C)=C/[C@H](C)C[C@@H](OC(=O)C2)C)=CC=C(O)C=C1 GQWYWHOHRVVHAP-DHKPLNAMSA-N 0.000 description 1
- 108010052440 jasplakinolide Proteins 0.000 description 1
- GQWYWHOHRVVHAP-UHFFFAOYSA-N jasplakinolide Natural products C1C(=O)OC(C)CC(C)C=C(C)CC(C)C(=O)NC(C)C(=O)N(C)C(CC=2C3=CC=CC=C3NC=2Br)C(=O)NC1C1=CC=C(O)C=C1 GQWYWHOHRVVHAP-UHFFFAOYSA-N 0.000 description 1
- NLYAJNPCOHFWQQ-UHFFFAOYSA-N kaolin Chemical compound O.O.O=[Al]O[Si](=O)O[Si](=O)O[Al]=O NLYAJNPCOHFWQQ-UHFFFAOYSA-N 0.000 description 1
- 201000006370 kidney failure Diseases 0.000 description 1
- 150000003893 lactate salts Chemical class 0.000 description 1
- 235000014655 lactic acid Nutrition 0.000 description 1
- 239000004310 lactic acid Substances 0.000 description 1
- 229960002437 lanreotide Drugs 0.000 description 1
- 229960001739 lanreotide acetate Drugs 0.000 description 1
- 229960004891 lapatinib Drugs 0.000 description 1
- 235000010445 lecithin Nutrition 0.000 description 1
- 239000000787 lecithin Substances 0.000 description 1
- 229940067606 lecithin Drugs 0.000 description 1
- 201000010260 leiomyoma Diseases 0.000 description 1
- 229960002618 lenograstim Drugs 0.000 description 1
- 229940115286 lentinan Drugs 0.000 description 1
- 229940087875 leukine Drugs 0.000 description 1
- RGLRXNKKBLIBQS-XNHQSDQCSA-N leuprolide acetate Chemical compound CC(O)=O.CCNC(=O)[C@@H]1CCCN1C(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H]1NC(=O)CC1)CC1=CC=C(O)C=C1 RGLRXNKKBLIBQS-XNHQSDQCSA-N 0.000 description 1
- KDQAABAKXDWYSZ-SDCRJXSCSA-N leurosidine sulfate Chemical compound OS(O)(=O)=O.C([C@H](C[C@]1(C(=O)OC)C=2C(=CC3=C([C@]45[C@H]([C@@]([C@H](OC(C)=O)[C@]6(CC)C=CCN([C@H]56)CC4)(O)C(=O)OC)N3C)C=2)OC)C[C@](C2)(O)CC)N2CCC2=C1NC1=CC=CC=C21 KDQAABAKXDWYSZ-SDCRJXSCSA-N 0.000 description 1
- 229960001614 levamisole Drugs 0.000 description 1
- UGFHIPBXIWJXNA-UHFFFAOYSA-N liarozole Chemical compound ClC1=CC=CC(C(C=2C=C3NC=NC3=CC=2)N2C=NC=C2)=C1 UGFHIPBXIWJXNA-UHFFFAOYSA-N 0.000 description 1
- 229950007056 liarozole Drugs 0.000 description 1
- 239000008297 liquid dosage form Substances 0.000 description 1
- RBBBWKUBQVARPL-SWQMWMPHSA-N lissoclinamide 7 Chemical compound C([C@H]1C(=O)N2CCC[C@H]2C2=N[C@@H]([C@H](O2)C)C(=O)N[C@@H](C=2SC[C@H](N=2)C(=O)N[C@H](CC=2C=CC=CC=2)C=2SC[C@H](N=2)C(=O)N1)C(C)C)C1=CC=CC=C1 RBBBWKUBQVARPL-SWQMWMPHSA-N 0.000 description 1
- 108010020270 lissoclinamide 7 Proteins 0.000 description 1
- RBBBWKUBQVARPL-UHFFFAOYSA-N lissoclinamide 7 Natural products N1C(=O)C(N=2)CSC=2C(CC=2C=CC=CC=2)NC(=O)C(N=2)CSC=2C(C(C)C)NC(=O)C(C(O2)C)N=C2C2CCCN2C(=O)C1CC1=CC=CC=C1 RBBBWKUBQVARPL-UHFFFAOYSA-N 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- 201000007270 liver cancer Diseases 0.000 description 1
- 208000014018 liver neoplasm Diseases 0.000 description 1
- 229950008991 lobaplatin Drugs 0.000 description 1
- 229950000909 lometrexol Drugs 0.000 description 1
- 229960002247 lomustine Drugs 0.000 description 1
- 229960003538 lonidamine Drugs 0.000 description 1
- WDRYRZXSPDWGEB-UHFFFAOYSA-N lonidamine Chemical compound C12=CC=CC=C2C(C(=O)O)=NN1CC1=CC=C(Cl)C=C1Cl WDRYRZXSPDWGEB-UHFFFAOYSA-N 0.000 description 1
- YROQEQPFUCPDCP-UHFFFAOYSA-N losoxantrone Chemical compound OCCNCCN1N=C2C3=CC=CC(O)=C3C(=O)C3=C2C1=CC=C3NCCNCCO YROQEQPFUCPDCP-UHFFFAOYSA-N 0.000 description 1
- 229950008745 losoxantrone Drugs 0.000 description 1
- 229950005634 loxoribine Drugs 0.000 description 1
- 201000005202 lung cancer Diseases 0.000 description 1
- 208000020816 lung neoplasm Diseases 0.000 description 1
- RVFGKBWWUQOIOU-NDEPHWFRSA-N lurtotecan Chemical compound O=C([C@]1(O)CC)OCC(C(N2CC3=4)=O)=C1C=C2C3=NC1=CC=2OCCOC=2C=C1C=4CN1CCN(C)CC1 RVFGKBWWUQOIOU-NDEPHWFRSA-N 0.000 description 1
- 229950002654 lurtotecan Drugs 0.000 description 1
- 210000002751 lymph Anatomy 0.000 description 1
- 230000001926 lymphatic effect Effects 0.000 description 1
- 210000004324 lymphatic system Anatomy 0.000 description 1
- 201000011649 lymphoblastic lymphoma Diseases 0.000 description 1
- 230000000527 lymphocytic effect Effects 0.000 description 1
- 208000003747 lymphoid leukemia Diseases 0.000 description 1
- 210000005210 lymphoid organ Anatomy 0.000 description 1
- 230000007434 lytic lesion Effects 0.000 description 1
- 210000002540 macrophage Anatomy 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- ZLNQQNXFFQJAID-UHFFFAOYSA-L magnesium carbonate Chemical compound [Mg+2].[O-]C([O-])=O ZLNQQNXFFQJAID-UHFFFAOYSA-L 0.000 description 1
- 239000001095 magnesium carbonate Substances 0.000 description 1
- 229910000021 magnesium carbonate Inorganic materials 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 230000014759 maintenance of location Effects 0.000 description 1
- 239000001630 malic acid Substances 0.000 description 1
- 235000011090 malic acid Nutrition 0.000 description 1
- 150000004701 malic acid derivatives Chemical class 0.000 description 1
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 description 1
- 208000026037 malignant tumor of neck Diseases 0.000 description 1
- BLOFGONIVNXZME-YDMGZANHSA-N mannostatin A Chemical compound CS[C@@H]1[C@@H](N)[C@@H](O)[C@@H](O)[C@H]1O BLOFGONIVNXZME-YDMGZANHSA-N 0.000 description 1
- 229950008959 marimastat Drugs 0.000 description 1
- OCSMOTCMPXTDND-OUAUKWLOSA-N marimastat Chemical compound CNC(=O)[C@H](C(C)(C)C)NC(=O)[C@H](CC(C)C)[C@H](O)C(=O)NO OCSMOTCMPXTDND-OUAUKWLOSA-N 0.000 description 1
- 239000003771 matrix metalloproteinase inhibitor Substances 0.000 description 1
- 229940121386 matrix metalloproteinase inhibitor Drugs 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- QZIQJVCYUQZDIR-UHFFFAOYSA-N mechlorethamine hydrochloride Chemical compound Cl.ClCCN(C)CCCl QZIQJVCYUQZDIR-UHFFFAOYSA-N 0.000 description 1
- 229960002868 mechlorethamine hydrochloride Drugs 0.000 description 1
- 238000002483 medication Methods 0.000 description 1
- 208000023356 medullary thyroid gland carcinoma Diseases 0.000 description 1
- RQZAXGRLVPAYTJ-GQFGMJRRSA-N megestrol acetate Chemical compound C1=C(C)C2=CC(=O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@@](C(C)=O)(OC(=O)C)[C@@]1(C)CC2 RQZAXGRLVPAYTJ-GQFGMJRRSA-N 0.000 description 1
- 229960004296 megestrol acetate Drugs 0.000 description 1
- 229960003846 melengestrol acetate Drugs 0.000 description 1
- GLVAUDGFNGKCSF-UHFFFAOYSA-N mercaptopurine Chemical compound S=C1NC=NC2=C1NC=N2 GLVAUDGFNGKCSF-UHFFFAOYSA-N 0.000 description 1
- 229960001428 mercaptopurine Drugs 0.000 description 1
- HEBKCHPVOIAQTA-UHFFFAOYSA-N meso ribitol Natural products OCC(O)C(O)C(O)CO HEBKCHPVOIAQTA-UHFFFAOYSA-N 0.000 description 1
- 230000009988 metabolic benefit Effects 0.000 description 1
- 238000006241 metabolic reaction Methods 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 208000010658 metastatic prostate carcinoma Diseases 0.000 description 1
- 108700025096 meterelin Proteins 0.000 description 1
- KPQJSSLKKBKWEW-RKDOVGOJSA-N methanesulfonic acid;5-nitro-2-[(2r)-1-[2-[[(2r)-2-(5-nitro-1,3-dioxobenzo[de]isoquinolin-2-yl)propyl]amino]ethylamino]propan-2-yl]benzo[de]isoquinoline-1,3-dione Chemical compound CS(O)(=O)=O.CS(O)(=O)=O.[O-][N+](=O)C1=CC(C(N([C@@H](CNCCNC[C@@H](C)N2C(C=3C=C(C=C4C=CC=C(C=34)C2=O)[N+]([O-])=O)=O)C)C2=O)=O)=C3C2=CC=CC3=C1 KPQJSSLKKBKWEW-RKDOVGOJSA-N 0.000 description 1
- DASQOOZCTWOQPA-GXKRWWSZSA-L methotrexate disodium Chemical compound [Na+].[Na+].C=1N=C2N=C(N)N=C(N)C2=NC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC([O-])=O)C([O-])=O)C=C1 DASQOOZCTWOQPA-GXKRWWSZSA-L 0.000 description 1
- CYEXEOXALMJXDI-UHFFFAOYSA-N methyl 4-bromo-2-methylbenzoate Chemical compound COC(=O)C1=CC=C(Br)C=C1C CYEXEOXALMJXDI-UHFFFAOYSA-N 0.000 description 1
- 229920000609 methyl cellulose Polymers 0.000 description 1
- 239000004292 methyl p-hydroxybenzoate Substances 0.000 description 1
- 229960001047 methyl salicylate Drugs 0.000 description 1
- 235000010981 methylcellulose Nutrition 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- 229960002216 methylparaben Drugs 0.000 description 1
- TTWJBBZEZQICBI-UHFFFAOYSA-N metoclopramide Chemical compound CCN(CC)CCNC(=O)C1=CC(Cl)=C(N)C=C1OC TTWJBBZEZQICBI-UHFFFAOYSA-N 0.000 description 1
- 229960004503 metoclopramide Drugs 0.000 description 1
- VQJHOPSWBGJHQS-UHFFFAOYSA-N metoprine, methodichlorophen Chemical compound CC1=NC(N)=NC(N)=C1C1=CC=C(Cl)C(Cl)=C1 VQJHOPSWBGJHQS-UHFFFAOYSA-N 0.000 description 1
- QTFKTBRIGWJQQL-UHFFFAOYSA-N meturedepa Chemical compound C1C(C)(C)N1P(=O)(NC(=O)OCC)N1CC1(C)C QTFKTBRIGWJQQL-UHFFFAOYSA-N 0.000 description 1
- 229950009847 meturedepa Drugs 0.000 description 1
- HPNSFSBZBAHARI-UHFFFAOYSA-N micophenolic acid Natural products OC1=C(CC=C(C)CCC(O)=O)C(OC)=C(C)C2=C1C(=O)OC2 HPNSFSBZBAHARI-UHFFFAOYSA-N 0.000 description 1
- 239000003094 microcapsule Substances 0.000 description 1
- 239000011859 microparticle Substances 0.000 description 1
- BMGQWWVMWDBQGC-IIFHNQTCSA-N midostaurin Chemical class CN([C@H]1[C@H]([C@]2(C)O[C@@H](N3C4=CC=CC=C4C4=C5C(=O)NCC5=C5C6=CC=CC=C6N2C5=C43)C1)OC)C(=O)C1=CC=CC=C1 BMGQWWVMWDBQGC-IIFHNQTCSA-N 0.000 description 1
- VKHAHZOOUSRJNA-GCNJZUOMSA-N mifepristone Chemical compound C1([C@@H]2C3=C4CCC(=O)C=C4CC[C@H]3[C@@H]3CC[C@@]([C@]3(C2)C)(O)C#CC)=CC=C(N(C)C)C=C1 VKHAHZOOUSRJNA-GCNJZUOMSA-N 0.000 description 1
- 229960003248 mifepristone Drugs 0.000 description 1
- 229960003775 miltefosine Drugs 0.000 description 1
- PQLXHQMOHUQAKB-UHFFFAOYSA-N miltefosine Chemical compound CCCCCCCCCCCCCCCCOP([O-])(=O)OCC[N+](C)(C)C PQLXHQMOHUQAKB-UHFFFAOYSA-N 0.000 description 1
- 235000010755 mineral Nutrition 0.000 description 1
- 239000011707 mineral Substances 0.000 description 1
- 239000002480 mineral oil Substances 0.000 description 1
- 235000010446 mineral oil Nutrition 0.000 description 1
- 229950008541 mirimostim Drugs 0.000 description 1
- CFCUWKMKBJTWLW-BKHRDMLASA-N mithramycin Chemical compound O([C@@H]1C[C@@H](O[C@H](C)[C@H]1O)OC=1C=C2C=C3C[C@H]([C@@H](C(=O)C3=C(O)C2=C(O)C=1C)O[C@@H]1O[C@H](C)[C@@H](O)[C@H](O[C@@H]2O[C@H](C)[C@H](O)[C@H](O[C@@H]3O[C@H](C)[C@@H](O)[C@@](C)(O)C3)C2)C1)[C@H](OC)C(=O)[C@@H](O)[C@@H](C)O)[C@H]1C[C@@H](O)[C@H](O)[C@@H](C)O1 CFCUWKMKBJTWLW-BKHRDMLASA-N 0.000 description 1
- DRCJGCOYHLTVNR-ZUIZSQJWSA-N mitindomide Chemical compound C1=C[C@@H]2[C@@H]3[C@H]4C(=O)NC(=O)[C@H]4[C@@H]3[C@H]1[C@@H]1C(=O)NC(=O)[C@H]21 DRCJGCOYHLTVNR-ZUIZSQJWSA-N 0.000 description 1
- 229950001314 mitindomide Drugs 0.000 description 1
- 229950002137 mitocarcin Drugs 0.000 description 1
- 229950000911 mitogillin Drugs 0.000 description 1
- 229960003539 mitoguazone Drugs 0.000 description 1
- MXWHMTNPTTVWDM-NXOFHUPFSA-N mitoguazone Chemical compound NC(N)=N\N=C(/C)\C=N\N=C(N)N MXWHMTNPTTVWDM-NXOFHUPFSA-N 0.000 description 1
- VFKZTMPDYBFSTM-GUCUJZIJSA-N mitolactol Chemical compound BrC[C@H](O)[C@@H](O)[C@@H](O)[C@H](O)CBr VFKZTMPDYBFSTM-GUCUJZIJSA-N 0.000 description 1
- 229950010913 mitolactol Drugs 0.000 description 1
- 108010026677 mitomalcin Proteins 0.000 description 1
- 229950007612 mitomalcin Drugs 0.000 description 1
- 229950005715 mitosper Drugs 0.000 description 1
- 229960000350 mitotane Drugs 0.000 description 1
- 229960001156 mitoxantrone Drugs 0.000 description 1
- KKZJGLLVHKMTCM-UHFFFAOYSA-N mitoxantrone Chemical compound O=C1C2=C(O)C=CC(O)=C2C(=O)C2=C1C(NCCNCCO)=CC=C2NCCNCCO KKZJGLLVHKMTCM-UHFFFAOYSA-N 0.000 description 1
- 229960004169 mitoxantrone hydrochloride Drugs 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 229950008012 mofarotene Drugs 0.000 description 1
- VOWOEBADKMXUBU-UHFFFAOYSA-J molecular oxygen;tetrachlorite;hydrate Chemical compound O.O=O.[O-]Cl=O.[O-]Cl=O.[O-]Cl=O.[O-]Cl=O VOWOEBADKMXUBU-UHFFFAOYSA-J 0.000 description 1
- 108010032806 molgramostim Proteins 0.000 description 1
- 229960003063 molgramostim Drugs 0.000 description 1
- 150000004682 monohydrates Chemical class 0.000 description 1
- FOYWNSCCNCUEPU-UHFFFAOYSA-N mopidamol Chemical compound C12=NC(N(CCO)CCO)=NC=C2N=C(N(CCO)CCO)N=C1N1CCCCC1 FOYWNSCCNCUEPU-UHFFFAOYSA-N 0.000 description 1
- 229950010718 mopidamol Drugs 0.000 description 1
- AARXZCZYLAFQQU-UHFFFAOYSA-N motexafin gadolinium Chemical compound [Gd].CC(O)=O.CC(O)=O.C1=C([N-]2)C(CC)=C(CC)C2=CC(C(=C2C)CCCO)=NC2=CN=C2C=C(OCCOCCOCCOC)C(OCCOCCOCCOC)=CC2=NC=C2C(C)=C(CCCO)C1=N2 AARXZCZYLAFQQU-UHFFFAOYSA-N 0.000 description 1
- WIQKYZYFTAEWBF-UHFFFAOYSA-L motexafin lutetium hydrate Chemical compound O.[Lu+3].CC([O-])=O.CC([O-])=O.C1=C([N-]2)C(CC)=C(CC)C2=CC(C(=C2C)CCCO)=NC2=CN=C2C=C(OCCOCCOCCOC)C(OCCOCCOCCOC)=CC2=NC=C2C(C)=C(CCCO)C1=N2 WIQKYZYFTAEWBF-UHFFFAOYSA-L 0.000 description 1
- 238000000465 moulding Methods 0.000 description 1
- 210000000214 mouth Anatomy 0.000 description 1
- 210000004400 mucous membrane Anatomy 0.000 description 1
- 230000036457 multidrug resistance Effects 0.000 description 1
- 235000010460 mustard Nutrition 0.000 description 1
- 229960000951 mycophenolic acid Drugs 0.000 description 1
- HPNSFSBZBAHARI-RUDMXATFSA-N mycophenolic acid Chemical compound OC1=C(C\C=C(/C)CCC(O)=O)C(OC)=C(C)C2=C1C(=O)OC2 HPNSFSBZBAHARI-RUDMXATFSA-N 0.000 description 1
- 210000000066 myeloid cell Anatomy 0.000 description 1
- 208000010125 myocardial infarction Diseases 0.000 description 1
- CRJGESKKUOMBCT-PMACEKPBSA-N n-[(2s,3s)-1,3-dihydroxyoctadecan-2-yl]acetamide Chemical compound CCCCCCCCCCCCCCC[C@H](O)[C@H](CO)NC(C)=O CRJGESKKUOMBCT-PMACEKPBSA-N 0.000 description 1
- NKFHKYQGZDAKMX-PPRKPIOESA-N n-[(e)-1-[(2s,4s)-4-[(2r,4s,5s,6s)-4-amino-5-hydroxy-6-methyloxan-2-yl]oxy-2,5,12-trihydroxy-7-methoxy-6,11-dioxo-3,4-dihydro-1h-tetracen-2-yl]ethylideneamino]benzamide;hydrochloride Chemical compound Cl.O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(\C)=N\NC(=O)C=1C=CC=CC=1)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 NKFHKYQGZDAKMX-PPRKPIOESA-N 0.000 description 1
- TVYPSLDUBVTDIS-FUOMVGGVSA-N n-[1-[(2r,3r,4s,5r)-3,4-dihydroxy-5-methyloxolan-2-yl]-5-fluoro-2-oxopyrimidin-4-yl]-3,4,5-trimethoxybenzamide Chemical compound COC1=C(OC)C(OC)=CC(C(=O)NC=2C(=CN(C(=O)N=2)[C@H]2[C@@H]([C@H](O)[C@@H](C)O2)O)F)=C1 TVYPSLDUBVTDIS-FUOMVGGVSA-N 0.000 description 1
- LBWFXVZLPYTWQI-IPOVEDGCSA-N n-[2-(diethylamino)ethyl]-5-[(z)-(5-fluoro-2-oxo-1h-indol-3-ylidene)methyl]-2,4-dimethyl-1h-pyrrole-3-carboxamide;(2s)-2-hydroxybutanedioic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O.CCN(CC)CCNC(=O)C1=C(C)NC(\C=C/2C3=CC(F)=CC=C3NC\2=O)=C1C LBWFXVZLPYTWQI-IPOVEDGCSA-N 0.000 description 1
- ARKYUICTMUZVEW-UHFFFAOYSA-N n-[5-[[5-[(3-amino-3-iminopropyl)carbamoyl]-1-methylpyrrol-3-yl]carbamoyl]-1-methylpyrrol-3-yl]-4-[[4-[bis(2-chloroethyl)amino]benzoyl]amino]-1-methylpyrrole-2-carboxamide Chemical compound C1=C(C(=O)NCCC(N)=N)N(C)C=C1NC(=O)C1=CC(NC(=O)C=2N(C=C(NC(=O)C=3C=CC(=CC=3)N(CCCl)CCCl)C=2)C)=CN1C ARKYUICTMUZVEW-UHFFFAOYSA-N 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- RWHUEXWOYVBUCI-ITQXDASVSA-N nafarelin Chemical compound C([C@@H](C(=O)N[C@H](CC=1C=C2C=CC=CC2=CC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCN=C(N)N)C(=O)N1[C@@H](CCC1)C(=O)NCC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H]1NC(=O)CC1)C1=CC=C(O)C=C1 RWHUEXWOYVBUCI-ITQXDASVSA-N 0.000 description 1
- 229960002333 nafarelin Drugs 0.000 description 1
- UZHSEJADLWPNLE-GRGSLBFTSA-N naloxone Chemical compound O=C([C@@H]1O2)CC[C@@]3(O)[C@H]4CC5=CC=C(O)C2=C5[C@@]13CCN4CC=C UZHSEJADLWPNLE-GRGSLBFTSA-N 0.000 description 1
- 229960004127 naloxone Drugs 0.000 description 1
- 108010032539 nartograstim Proteins 0.000 description 1
- 229950010676 nartograstim Drugs 0.000 description 1
- 230000008693 nausea Effects 0.000 description 1
- 239000006199 nebulizer Substances 0.000 description 1
- 210000003739 neck Anatomy 0.000 description 1
- 229950007221 nedaplatin Drugs 0.000 description 1
- 230000009826 neoplastic cell growth Effects 0.000 description 1
- MQYXUWHLBZFQQO-UHFFFAOYSA-N nepehinol Natural products C1CC(O)C(C)(C)C2CCC3(C)C4(C)CCC5(C)CCC(C(=C)C)C5C4CCC3C21C MQYXUWHLBZFQQO-UHFFFAOYSA-N 0.000 description 1
- PUUSSSIBPPTKTP-UHFFFAOYSA-N neridronic acid Chemical compound NCCCCCC(O)(P(O)(O)=O)P(O)(O)=O PUUSSSIBPPTKTP-UHFFFAOYSA-N 0.000 description 1
- 229950010733 neridronic acid Drugs 0.000 description 1
- 229940029345 neupogen Drugs 0.000 description 1
- 201000011519 neuroendocrine tumor Diseases 0.000 description 1
- 208000004235 neutropenia Diseases 0.000 description 1
- XWXYUMMDTVBTOU-UHFFFAOYSA-N nilutamide Chemical compound O=C1C(C)(C)NC(=O)N1C1=CC=C([N+]([O-])=O)C(C(F)(F)F)=C1 XWXYUMMDTVBTOU-UHFFFAOYSA-N 0.000 description 1
- 229960002653 nilutamide Drugs 0.000 description 1
- 229940125745 nitric oxide modulator Drugs 0.000 description 1
- 229950006344 nocodazole Drugs 0.000 description 1
- KGTDRFCXGRULNK-JYOBTZKQSA-N nogalamycin Chemical compound CO[C@@H]1[C@@](OC)(C)[C@@H](OC)[C@H](C)O[C@H]1O[C@@H]1C2=C(O)C(C(=O)C3=C(O)C=C4[C@@]5(C)O[C@H]([C@H]([C@@H]([C@H]5O)N(C)C)O)OC4=C3C3=O)=C3C=C2[C@@H](C(=O)OC)[C@@](C)(O)C1 KGTDRFCXGRULNK-JYOBTZKQSA-N 0.000 description 1
- 229950009266 nogalamycin Drugs 0.000 description 1
- 125000006574 non-aromatic ring group Chemical group 0.000 description 1
- 239000002687 nonaqueous vehicle Substances 0.000 description 1
- 230000000683 nonmetastatic effect Effects 0.000 description 1
- 239000000346 nonvolatile oil Substances 0.000 description 1
- JFNLZVQOOSMTJK-KNVOCYPGSA-N norbornene Chemical compound C1[C@@H]2CC[C@H]1C=C2 JFNLZVQOOSMTJK-KNVOCYPGSA-N 0.000 description 1
- 210000004940 nucleus Anatomy 0.000 description 1
- NIHNNTQXNPWCJQ-UHFFFAOYSA-N o-biphenylenemethane Natural products C1=CC=C2CC3=CC=CC=C3C2=C1 NIHNNTQXNPWCJQ-UHFFFAOYSA-N 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 229960002700 octreotide Drugs 0.000 description 1
- 239000002674 ointment Substances 0.000 description 1
- 229940005619 omacetaxine Drugs 0.000 description 1
- 229950011093 onapristone Drugs 0.000 description 1
- 108091008820 oncogenic transcription factors Proteins 0.000 description 1
- 229940096978 oral tablet Drugs 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 230000008520 organization Effects 0.000 description 1
- 125000002524 organometallic group Chemical group 0.000 description 1
- ZLLOIFNEEWYATC-XMUHMHRVSA-N osaterone Chemical compound C1=C(Cl)C2=CC(=O)OC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@@](C(=O)C)(O)[C@@]1(C)CC2 ZLLOIFNEEWYATC-XMUHMHRVSA-N 0.000 description 1
- 229950006466 osaterone Drugs 0.000 description 1
- 210000002997 osteoclast Anatomy 0.000 description 1
- 229940043515 other immunoglobulins in atc Drugs 0.000 description 1
- 210000001672 ovary Anatomy 0.000 description 1
- 230000036542 oxidative stress Effects 0.000 description 1
- LXCFILQKKLGQFO-UHFFFAOYSA-N p-hydroxybenzoic acid methyl ester Natural products COC(=O)C1=CC=C(O)C=C1 LXCFILQKKLGQFO-UHFFFAOYSA-N 0.000 description 1
- 239000006179 pH buffering agent Substances 0.000 description 1
- VYOQBYCIIJYKJA-VORKOXQSSA-N palau'amine Chemical compound N([C@@]12[C@@H](Cl)[C@@H]([C@@H]3[C@@H]2[C@]24N=C(N)N[C@H]2N2C=CC=C2C(=O)N4C3)CN)C(N)=N[C@H]1O VYOQBYCIIJYKJA-VORKOXQSSA-N 0.000 description 1
- WRUUGTRCQOWXEG-UHFFFAOYSA-N pamidronate Chemical compound NCCC(O)(P(O)(O)=O)P(O)(O)=O WRUUGTRCQOWXEG-UHFFFAOYSA-N 0.000 description 1
- 229960003978 pamidronic acid Drugs 0.000 description 1
- 201000002528 pancreatic cancer Diseases 0.000 description 1
- 229960001972 panitumumab Drugs 0.000 description 1
- 206010033675 panniculitis Diseases 0.000 description 1
- 229950003440 panomifene Drugs 0.000 description 1
- 239000004031 partial agonist Substances 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 239000006072 paste Substances 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- LPHSYQSMAGVYNT-UHFFFAOYSA-N pazelliptine Chemical compound N1C2=CC=NC=C2C2=C1C(C)=C1C=CN=C(NCCCN(CC)CC)C1=C2 LPHSYQSMAGVYNT-UHFFFAOYSA-N 0.000 description 1
- 239000000312 peanut oil Substances 0.000 description 1
- 239000001814 pectin Substances 0.000 description 1
- 235000010987 pectin Nutrition 0.000 description 1
- 229920001277 pectin Polymers 0.000 description 1
- 229950006960 peliomycin Drugs 0.000 description 1
- VOKSWYLNZZRQPF-GDIGMMSISA-N pentazocine Chemical compound C1C2=CC=C(O)C=C2[C@@]2(C)[C@@H](C)[C@@H]1N(CC=C(C)C)CC2 VOKSWYLNZZRQPF-GDIGMMSISA-N 0.000 description 1
- 229960005301 pentazocine Drugs 0.000 description 1
- 229960003820 pentosan polysulfate sodium Drugs 0.000 description 1
- 229960002340 pentostatin Drugs 0.000 description 1
- FPVKHBSQESCIEP-JQCXWYLXSA-N pentostatin Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(N=CNC[C@H]2O)=C2N=C1 FPVKHBSQESCIEP-JQCXWYLXSA-N 0.000 description 1
- 229950003180 peplomycin Drugs 0.000 description 1
- 229940021222 peritoneal dialysis isotonic solution Drugs 0.000 description 1
- 230000002085 persistent effect Effects 0.000 description 1
- 229960002087 pertuzumab Drugs 0.000 description 1
- JGWRKYUXBBNENE-UHFFFAOYSA-N pexidartinib Chemical compound C1=NC(C(F)(F)F)=CC=C1CNC(N=C1)=CC=C1CC1=CNC2=NC=C(Cl)C=C12 JGWRKYUXBBNENE-UHFFFAOYSA-N 0.000 description 1
- 239000008177 pharmaceutical agent Substances 0.000 description 1
- 239000008024 pharmaceutical diluent Substances 0.000 description 1
- 239000011129 pharmaceutical packaging material Substances 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 239000002831 pharmacologic agent Substances 0.000 description 1
- 238000011422 pharmacological therapy Methods 0.000 description 1
- 210000003800 pharynx Anatomy 0.000 description 1
- 239000012071 phase Substances 0.000 description 1
- 150000002989 phenols Chemical class 0.000 description 1
- 229960000969 phenyl salicylate Drugs 0.000 description 1
- WVDDGKGOMKODPV-ZQBYOMGUSA-N phenyl(114C)methanol Chemical compound O[14CH2]C1=CC=CC=C1 WVDDGKGOMKODPV-ZQBYOMGUSA-N 0.000 description 1
- 229940049953 phenylacetate Drugs 0.000 description 1
- WLJVXDMOQOGPHL-UHFFFAOYSA-N phenylacetic acid Chemical compound OC(=O)CC1=CC=CC=C1 WLJVXDMOQOGPHL-UHFFFAOYSA-N 0.000 description 1
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N phenylbenzene Natural products C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 1
- 235000011007 phosphoric acid Nutrition 0.000 description 1
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 229940023488 pill Drugs 0.000 description 1
- 229960002139 pilocarpine hydrochloride Drugs 0.000 description 1
- RNAICSBVACLLGM-GNAZCLTHSA-N pilocarpine hydrochloride Chemical compound Cl.C1OC(=O)[C@@H](CC)[C@H]1CC1=CN=CN1C RNAICSBVACLLGM-GNAZCLTHSA-N 0.000 description 1
- 229960000952 pipobroman Drugs 0.000 description 1
- NJBFOOCLYDNZJN-UHFFFAOYSA-N pipobroman Chemical compound BrCCC(=O)N1CCN(C(=O)CCBr)CC1 NJBFOOCLYDNZJN-UHFFFAOYSA-N 0.000 description 1
- NUKCGLDCWQXYOQ-UHFFFAOYSA-N piposulfan Chemical compound CS(=O)(=O)OCCC(=O)N1CCN(C(=O)CCOS(C)(=O)=O)CC1 NUKCGLDCWQXYOQ-UHFFFAOYSA-N 0.000 description 1
- 229950001100 piposulfan Drugs 0.000 description 1
- XESARGFCSKSFID-FLLFQEBCSA-N pirazofurin Chemical compound OC1=C(C(=O)N)NN=C1[C@H]1[C@H](O)[C@H](O)[C@@H](CO)O1 XESARGFCSKSFID-FLLFQEBCSA-N 0.000 description 1
- 229950001030 piritrexim Drugs 0.000 description 1
- 230000003169 placental effect Effects 0.000 description 1
- 239000002797 plasminogen activator inhibitor Substances 0.000 description 1
- 229960003171 plicamycin Drugs 0.000 description 1
- 229950008499 plitidepsin Drugs 0.000 description 1
- 108010049948 plitidepsin Proteins 0.000 description 1
- UUSZLLQJYRSZIS-LXNNNBEUSA-N plitidepsin Chemical compound CN([C@H](CC(C)C)C(=O)N[C@@H]1C(=O)N[C@@H]([C@H](CC(=O)O[C@H](C(=O)[C@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N2CCC[C@H]2C(=O)N(C)[C@@H](CC=2C=CC(OC)=CC=2)C(=O)O[C@@H]1C)C(C)C)O)[C@@H](C)CC)C(=O)[C@@H]1CCCN1C(=O)C(C)=O UUSZLLQJYRSZIS-LXNNNBEUSA-N 0.000 description 1
- JKPDEYAOCSQBSZ-OEUJLIAZSA-N plomestane Chemical compound O=C1CC[C@]2(CC#C)[C@H]3CC[C@](C)(C(CC4)=O)[C@@H]4[C@@H]3CCC2=C1 JKPDEYAOCSQBSZ-OEUJLIAZSA-N 0.000 description 1
- 229950004541 plomestane Drugs 0.000 description 1
- 229920000768 polyamine Polymers 0.000 description 1
- 229940057838 polyethylene glycol 4000 Drugs 0.000 description 1
- 239000004633 polyglycolic acid Substances 0.000 description 1
- 239000004626 polylactic acid Substances 0.000 description 1
- 230000007824 polyneuropathy Effects 0.000 description 1
- 229920001451 polypropylene glycol Polymers 0.000 description 1
- 229940068968 polysorbate 80 Drugs 0.000 description 1
- 229920000915 polyvinyl chloride Polymers 0.000 description 1
- 239000004800 polyvinyl chloride Substances 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- LWIHDJKSTIGBAC-UHFFFAOYSA-K potassium phosphate Substances [K+].[K+].[K+].[O-]P([O-])([O-])=O LWIHDJKSTIGBAC-UHFFFAOYSA-K 0.000 description 1
- 229910000160 potassium phosphate Inorganic materials 0.000 description 1
- 235000011009 potassium phosphates Nutrition 0.000 description 1
- 229920001592 potato starch Polymers 0.000 description 1
- 230000001855 preneoplastic effect Effects 0.000 description 1
- 230000002335 preservative effect Effects 0.000 description 1
- 230000003449 preventive effect Effects 0.000 description 1
- 229960004919 procaine Drugs 0.000 description 1
- MFDFERRIHVXMIY-UHFFFAOYSA-N procaine Chemical compound CCN(CC)CCOC(=O)C1=CC=C(N)C=C1 MFDFERRIHVXMIY-UHFFFAOYSA-N 0.000 description 1
- 229960001309 procaine hydrochloride Drugs 0.000 description 1
- 229960001586 procarbazine hydrochloride Drugs 0.000 description 1
- 229940002612 prodrug Drugs 0.000 description 1
- 239000000651 prodrug Substances 0.000 description 1
- 239000000186 progesterone Substances 0.000 description 1
- 229960003387 progesterone Drugs 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- 210000004765 promyelocyte Anatomy 0.000 description 1
- 235000010388 propyl gallate Nutrition 0.000 description 1
- 239000000473 propyl gallate Substances 0.000 description 1
- 229940075579 propyl gallate Drugs 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 235000010232 propyl p-hydroxybenzoate Nutrition 0.000 description 1
- 239000004405 propyl p-hydroxybenzoate Substances 0.000 description 1
- 229960003415 propylparaben Drugs 0.000 description 1
- UQOQENZZLBSFKO-POPPZSFYSA-N prostaglandin J2 Chemical compound CCCCC[C@H](O)\C=C\[C@@H]1[C@@H](C\C=C/CCCC(O)=O)C=CC1=O UQOQENZZLBSFKO-POPPZSFYSA-N 0.000 description 1
- 125000006239 protecting group Chemical group 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 238000000159 protein binding assay Methods 0.000 description 1
- 239000003528 protein farnesyltransferase inhibitor Substances 0.000 description 1
- 239000003806 protein tyrosine phosphatase inhibitor Substances 0.000 description 1
- SSKVDVBQSWQEGJ-UHFFFAOYSA-N pseudohypericin Natural products C12=C(O)C=C(O)C(C(C=3C(O)=CC(O)=C4C=33)=O)=C2C3=C2C3=C4C(C)=CC(O)=C3C(=O)C3=C(O)C=C(O)C1=C32 SSKVDVBQSWQEGJ-UHFFFAOYSA-N 0.000 description 1
- 239000000784 purine nucleoside phosphorylase inhibitor Substances 0.000 description 1
- 229950010131 puromycin Drugs 0.000 description 1
- MKSVFGKWZLUTTO-FZFAUISWSA-N puromycin dihydrochloride Chemical compound Cl.Cl.C1=CC(OC)=CC=C1C[C@H](N)C(=O)N[C@H]1[C@@H](O)[C@H](N2C3=NC=NC(=C3N=C2)N(C)C)O[C@@H]1CO MKSVFGKWZLUTTO-FZFAUISWSA-N 0.000 description 1
- 125000004309 pyranyl group Chemical group O1C(C=CC=C1)* 0.000 description 1
- 125000003226 pyrazolyl group Chemical group 0.000 description 1
- 125000000719 pyrrolidinyl group Chemical group 0.000 description 1
- 125000000168 pyrrolyl group Chemical group 0.000 description 1
- 125000002943 quinolinyl group Chemical group N1=C(C=CC2=CC=CC=C12)* 0.000 description 1
- 125000004621 quinuclidinyl group Chemical group N12C(CC(CC1)CC2)* 0.000 description 1
- 230000002285 radioactive effect Effects 0.000 description 1
- 239000012217 radiopharmaceutical Substances 0.000 description 1
- 229940121896 radiopharmaceutical Drugs 0.000 description 1
- 230000002799 radiopharmaceutical effect Effects 0.000 description 1
- 229960004432 raltitrexed Drugs 0.000 description 1
- NTHPAPBPFQJABD-LLVKDONJSA-N ramosetron Chemical compound C12=CC=CC=C2N(C)C=C1C(=O)[C@H]1CC(NC=N2)=C2CC1 NTHPAPBPFQJABD-LLVKDONJSA-N 0.000 description 1
- 229950001588 ramosetron Drugs 0.000 description 1
- 206010037844 rash Diseases 0.000 description 1
- 229940044601 receptor agonist Drugs 0.000 description 1
- 239000000018 receptor agonist Substances 0.000 description 1
- 229940044551 receptor antagonist Drugs 0.000 description 1
- 239000002464 receptor antagonist Substances 0.000 description 1
- 102000005962 receptors Human genes 0.000 description 1
- 108020003175 receptors Proteins 0.000 description 1
- 229940100618 rectal suppository Drugs 0.000 description 1
- 201000001281 rectum adenocarcinoma Diseases 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- 230000028981 regulation of cellular metabolic process Effects 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 229940116176 remicade Drugs 0.000 description 1
- 210000002345 respiratory system Anatomy 0.000 description 1
- 229940100552 retinamide Drugs 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 229910052702 rhenium Inorganic materials 0.000 description 1
- WUAPFZMCVAUBPE-UHFFFAOYSA-N rhenium atom Chemical compound [Re] WUAPFZMCVAUBPE-UHFFFAOYSA-N 0.000 description 1
- 108091092562 ribozyme Proteins 0.000 description 1
- 229960003522 roquinimex Drugs 0.000 description 1
- 229960005399 satraplatin Drugs 0.000 description 1
- 190014017285 satraplatin Chemical compound 0.000 description 1
- 150000003335 secondary amines Chemical class 0.000 description 1
- 230000009758 senescence Effects 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 239000003352 sequestering agent Substances 0.000 description 1
- 230000021148 sequestering of metal ion Effects 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 239000008159 sesame oil Substances 0.000 description 1
- 235000011803 sesame oil Nutrition 0.000 description 1
- 230000019491 signal transduction Effects 0.000 description 1
- 230000011664 signaling Effects 0.000 description 1
- 208000000587 small cell lung carcinoma Diseases 0.000 description 1
- 229950010372 sobuzoxane Drugs 0.000 description 1
- WXMKPNITSTVMEF-UHFFFAOYSA-M sodium benzoate Chemical compound [Na+].[O-]C(=O)C1=CC=CC=C1 WXMKPNITSTVMEF-UHFFFAOYSA-M 0.000 description 1
- 239000004299 sodium benzoate Substances 0.000 description 1
- 235000010234 sodium benzoate Nutrition 0.000 description 1
- 229960003885 sodium benzoate Drugs 0.000 description 1
- WBHQBSYUUJJSRZ-UHFFFAOYSA-M sodium bisulfate Chemical compound [Na+].OS([O-])(=O)=O WBHQBSYUUJJSRZ-UHFFFAOYSA-M 0.000 description 1
- 229910000342 sodium bisulfate Inorganic materials 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- 239000008354 sodium chloride injection Substances 0.000 description 1
- 235000010267 sodium hydrogen sulphite Nutrition 0.000 description 1
- 229940006198 sodium phenylacetate Drugs 0.000 description 1
- 229910000162 sodium phosphate Inorganic materials 0.000 description 1
- 235000011008 sodium phosphates Nutrition 0.000 description 1
- 239000008109 sodium starch glycolate Substances 0.000 description 1
- 229920003109 sodium starch glycolate Polymers 0.000 description 1
- 229940079832 sodium starch glycolate Drugs 0.000 description 1
- QUCDWLYKDRVKMI-UHFFFAOYSA-M sodium;3,4-dimethylbenzenesulfonate Chemical compound [Na+].CC1=CC=C(S([O-])(=O)=O)C=C1C QUCDWLYKDRVKMI-UHFFFAOYSA-M 0.000 description 1
- 239000008137 solubility enhancer Substances 0.000 description 1
- 229960003787 sorafenib Drugs 0.000 description 1
- 229940035044 sorbitan monolaurate Drugs 0.000 description 1
- 229950009641 sparsomycin Drugs 0.000 description 1
- XKLZIVIOZDNKEQ-CLQLPEFOSA-N sparsomycin Chemical compound CSC[S@](=O)C[C@H](CO)NC(=O)\C=C\C1=C(C)NC(=O)NC1=O XKLZIVIOZDNKEQ-CLQLPEFOSA-N 0.000 description 1
- XKLZIVIOZDNKEQ-UHFFFAOYSA-N sparsomycin Natural products CSCS(=O)CC(CO)NC(=O)C=CC1=C(C)NC(=O)NC1=O XKLZIVIOZDNKEQ-UHFFFAOYSA-N 0.000 description 1
- 229940084106 spermaceti Drugs 0.000 description 1
- 239000012177 spermaceti Substances 0.000 description 1
- 229940063675 spermine Drugs 0.000 description 1
- YBZRLMLGUBIIDN-NZSGCTDASA-N spicamycin Chemical compound O1[C@@H](C(O)CO)[C@H](NC(=O)CNC(=O)CCCCCCCCCCCCC(C)C)[C@@H](O)[C@@H](O)[C@H]1NC1=NC=NC2=C1N=CN2 YBZRLMLGUBIIDN-NZSGCTDASA-N 0.000 description 1
- YBZRLMLGUBIIDN-UHFFFAOYSA-N spicamycin Natural products O1C(C(O)CO)C(NC(=O)CNC(=O)CCCCCCCCCCCCC(C)C)C(O)C(O)C1NC1=NC=NC2=C1NC=N2 YBZRLMLGUBIIDN-UHFFFAOYSA-N 0.000 description 1
- 229950004330 spiroplatin Drugs 0.000 description 1
- 210000000952 spleen Anatomy 0.000 description 1
- 206010062113 splenic marginal zone lymphoma Diseases 0.000 description 1
- 108010032486 splenopentin Proteins 0.000 description 1
- ICXJVZHDZFXYQC-UHFFFAOYSA-N spongistatin 1 Natural products OC1C(O2)(O)CC(O)C(C)C2CCCC=CC(O2)CC(O)CC2(O2)CC(OC)CC2CC(=O)C(C)C(OC(C)=O)C(C)C(=C)CC(O2)CC(C)(O)CC2(O2)CC(OC(C)=O)CC2CC(=O)OC2C(O)C(CC(=C)CC(O)C=CC(Cl)=C)OC1C2C ICXJVZHDZFXYQC-UHFFFAOYSA-N 0.000 description 1
- HAOCRCFHEPRQOY-JKTUOYIXSA-N spongistatin-1 Chemical compound C([C@@H]1C[C@@H](C[C@@]2(C[C@@H](O)C[C@@H](C2)\C=C/CCC[C@@H]2[C@H](C)[C@@H](O)C[C@](O2)(O)[C@H]2O)O1)OC)C(=O)[C@@H](C)[C@@H](OC(C)=O)[C@H](C)C(=C)C[C@H](O1)C[C@](C)(O)C[C@@]1(O1)C[C@@H](OC(C)=O)C[C@@H]1CC(=O)O[C@H]1[C@H](O)[C@@H](CC(=C)C(C)[C@H](O)\C=C\C(Cl)=C)O[C@@H]2[C@@H]1C HAOCRCFHEPRQOY-JKTUOYIXSA-N 0.000 description 1
- 239000007921 spray Substances 0.000 description 1
- 229950001248 squalamine Drugs 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 238000011255 standard chemotherapy Methods 0.000 description 1
- 238000011272 standard treatment Methods 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 238000011146 sterile filtration Methods 0.000 description 1
- 239000008223 sterile water Substances 0.000 description 1
- 230000004936 stimulating effect Effects 0.000 description 1
- 229960001052 streptozocin Drugs 0.000 description 1
- ZSJLQEPLLKMAKR-GKHCUFPYSA-N streptozocin Chemical compound O=NN(C)C(=O)N[C@H]1[C@@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O ZSJLQEPLLKMAKR-GKHCUFPYSA-N 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- 210000004304 subcutaneous tissue Anatomy 0.000 description 1
- 125000005415 substituted alkoxy group Chemical group 0.000 description 1
- 150000003890 succinate salts Chemical class 0.000 description 1
- 239000007940 sugar coated tablet Substances 0.000 description 1
- 238000009495 sugar coating Methods 0.000 description 1
- 150000003871 sulfonates Chemical class 0.000 description 1
- 125000005555 sulfoximide group Chemical group 0.000 description 1
- 125000004434 sulfur atom Chemical group 0.000 description 1
- 150000003467 sulfuric acid derivatives Chemical class 0.000 description 1
- 229950007841 sulofenur Drugs 0.000 description 1
- 239000013589 supplement Substances 0.000 description 1
- FIAFUQMPZJWCLV-UHFFFAOYSA-N suramin Chemical compound OS(=O)(=O)C1=CC(S(O)(=O)=O)=C2C(NC(=O)C3=CC=C(C(=C3)NC(=O)C=3C=C(NC(=O)NC=4C=C(C=CC=4)C(=O)NC=4C(=CC=C(C=4)C(=O)NC=4C5=C(C=C(C=C5C(=CC=4)S(O)(=O)=O)S(O)(=O)=O)S(O)(=O)=O)C)C=CC=3)C)=CC=C(S(O)(=O)=O)C2=C1 FIAFUQMPZJWCLV-UHFFFAOYSA-N 0.000 description 1
- 229960005314 suramin Drugs 0.000 description 1
- 230000002459 sustained effect Effects 0.000 description 1
- 229940034785 sutent Drugs 0.000 description 1
- 230000008961 swelling Effects 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 239000007916 tablet composition Substances 0.000 description 1
- VAZAPHZUAVEOMC-UHFFFAOYSA-N tacedinaline Chemical compound C1=CC(NC(=O)C)=CC=C1C(=O)NC1=CC=CC=C1N VAZAPHZUAVEOMC-UHFFFAOYSA-N 0.000 description 1
- 108700003774 talisomycin Proteins 0.000 description 1
- 229950002687 talisomycin Drugs 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- 150000003892 tartrate salts Chemical class 0.000 description 1
- 229950010168 tauromustine Drugs 0.000 description 1
- DKPFODGZWDEEBT-QFIAKTPHSA-N taxane Chemical class C([C@]1(C)CCC[C@@H](C)[C@H]1C1)C[C@H]2[C@H](C)CC[C@@H]1C2(C)C DKPFODGZWDEEBT-QFIAKTPHSA-N 0.000 description 1
- 229940063683 taxotere Drugs 0.000 description 1
- 229960000565 tazarotene Drugs 0.000 description 1
- 239000003277 telomerase inhibitor Substances 0.000 description 1
- 229940061353 temodar Drugs 0.000 description 1
- KKEYFWRCBNTPAC-UHFFFAOYSA-L terephthalate(2-) Chemical compound [O-]C(=O)C1=CC=C(C([O-])=O)C=C1 KKEYFWRCBNTPAC-UHFFFAOYSA-L 0.000 description 1
- 210000001550 testis Anatomy 0.000 description 1
- 229960005353 testolactone Drugs 0.000 description 1
- BPEWUONYVDABNZ-DZBHQSCQSA-N testolactone Chemical compound O=C1C=C[C@]2(C)[C@H]3CC[C@](C)(OC(=O)CC4)[C@@H]4[C@@H]3CCC2=C1 BPEWUONYVDABNZ-DZBHQSCQSA-N 0.000 description 1
- ZUHZGEOKBKGPSW-UHFFFAOYSA-N tetraglyme Chemical compound COCCOCCOCCOCCOC ZUHZGEOKBKGPSW-UHFFFAOYSA-N 0.000 description 1
- 150000004685 tetrahydrates Chemical class 0.000 description 1
- 125000003831 tetrazolyl group Chemical group 0.000 description 1
- WXZSUBHBYQYTNM-WMDJANBXSA-N tetrazomine Chemical compound C=1([C@@H]2CO[C@@H]3[C@H]4C[C@@H](CO)[C@H](N4C)[C@@H](N23)CC=1C=C1)C(OC)=C1NC(=O)C1NCCC[C@H]1O WXZSUBHBYQYTNM-WMDJANBXSA-N 0.000 description 1
- ZCTJIMXXSXQXRI-KYJUHHDHSA-N thalicarpine Chemical compound CN1CCC2=CC(OC)=C(OC)C3=C2[C@@H]1CC1=C3C=C(OC)C(OC2=C(C[C@H]3C4=CC(OC)=C(OC)C=C4CCN3C)C=C(C(=C2)OC)OC)=C1 ZCTJIMXXSXQXRI-KYJUHHDHSA-N 0.000 description 1
- 208000016595 therapy related acute myeloid leukemia and myelodysplastic syndrome Diseases 0.000 description 1
- 230000008719 thickening Effects 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- RTKIYNMVFMVABJ-UHFFFAOYSA-L thimerosal Chemical compound [Na+].CC[Hg]SC1=CC=CC=C1C([O-])=O RTKIYNMVFMVABJ-UHFFFAOYSA-L 0.000 description 1
- 229940033663 thimerosal Drugs 0.000 description 1
- 108010062880 thiocoraline Proteins 0.000 description 1
- UPGGKUQISSWRJJ-UHFFFAOYSA-N thiocoraline Natural products CN1C(=O)CNC(=O)C(NC(=O)C=2C(=CC3=CC=CC=C3N=2)O)CSC(=O)C(CSC)N(C)C(=O)C(N(C(=O)CNC2=O)C)CSSCC1C(=O)N(C)C(CSC)C(=O)SCC2NC(=O)C1=NC2=CC=CC=C2C=C1O UPGGKUQISSWRJJ-UHFFFAOYSA-N 0.000 description 1
- 235000019303 thiodipropionic acid Nutrition 0.000 description 1
- 125000003396 thiol group Chemical group [H]S* 0.000 description 1
- 210000000115 thoracic cavity Anatomy 0.000 description 1
- 206010043554 thrombocytopenia Diseases 0.000 description 1
- 108010013515 thymopoietin receptor Proteins 0.000 description 1
- 208000030901 thyroid gland follicular carcinoma Diseases 0.000 description 1
- 208000013818 thyroid gland medullary carcinoma Diseases 0.000 description 1
- 208000030045 thyroid gland papillary carcinoma Diseases 0.000 description 1
- YFTWHEBLORWGNI-UHFFFAOYSA-N tiamiprine Chemical compound CN1C=NC([N+]([O-])=O)=C1SC1=NC(N)=NC2=C1NC=N2 YFTWHEBLORWGNI-UHFFFAOYSA-N 0.000 description 1
- 229950011457 tiamiprine Drugs 0.000 description 1
- 229960003087 tioguanine Drugs 0.000 description 1
- 230000008467 tissue growth Effects 0.000 description 1
- 229940044693 topoisomerase inhibitor Drugs 0.000 description 1
- 229960005026 toremifene Drugs 0.000 description 1
- XFCLJVABOIYOMF-QPLCGJKRSA-N toremifene Chemical compound C1=CC(OCCN(C)C)=CC=C1C(\C=1C=CC=CC=1)=C(\CCCl)C1=CC=CC=C1 XFCLJVABOIYOMF-QPLCGJKRSA-N 0.000 description 1
- 229960004167 toremifene citrate Drugs 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 231100000583 toxicological profile Toxicity 0.000 description 1
- 230000037317 transdermal delivery Effects 0.000 description 1
- 201000010875 transient cerebral ischemia Diseases 0.000 description 1
- 229910052723 transition metal Inorganic materials 0.000 description 1
- 238000013519 translation Methods 0.000 description 1
- 230000005945 translocation Effects 0.000 description 1
- 229960000575 trastuzumab Drugs 0.000 description 1
- 229960001727 tretinoin Drugs 0.000 description 1
- ILJSQTXMGCGYMG-UHFFFAOYSA-N triacetic acid Chemical compound CC(=O)CC(=O)CC(O)=O ILJSQTXMGCGYMG-UHFFFAOYSA-N 0.000 description 1
- 125000001425 triazolyl group Chemical group 0.000 description 1
- 229940117013 triethanolamine oleate Drugs 0.000 description 1
- 125000000876 trifluoromethoxy group Chemical group FC(F)(F)O* 0.000 description 1
- YFNKIDBQEZZDLK-UHFFFAOYSA-N triglyme Chemical compound COCCOCCOCCOC YFNKIDBQEZZDLK-UHFFFAOYSA-N 0.000 description 1
- 150000004684 trihydrates Chemical class 0.000 description 1
- 229960000538 trimetrexate glucuronate Drugs 0.000 description 1
- 235000011178 triphosphate Nutrition 0.000 description 1
- 239000001226 triphosphate Substances 0.000 description 1
- UNXRWKVEANCORM-UHFFFAOYSA-N triphosphoric acid Chemical compound OP(O)(=O)OP(O)(=O)OP(O)(O)=O UNXRWKVEANCORM-UHFFFAOYSA-N 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- RYFMWSXOAZQYPI-UHFFFAOYSA-K trisodium phosphate Chemical compound [Na+].[Na+].[Na+].[O-]P([O-])([O-])=O RYFMWSXOAZQYPI-UHFFFAOYSA-K 0.000 description 1
- UIVFDCIXTSJXBB-ITGUQSILSA-N tropisetron Chemical compound C1=CC=C[C]2C(C(=O)O[C@H]3C[C@H]4CC[C@@H](C3)N4C)=CN=C21 UIVFDCIXTSJXBB-ITGUQSILSA-N 0.000 description 1
- 229960003688 tropisetron Drugs 0.000 description 1
- SZCZSKMCTGEJKI-UHFFFAOYSA-N tuberin Natural products COC1=CC=C(C=CNC=O)C=C1 SZCZSKMCTGEJKI-UHFFFAOYSA-N 0.000 description 1
- 230000004565 tumor cell growth Effects 0.000 description 1
- 239000000225 tumor suppressor protein Substances 0.000 description 1
- WMPQMBUXZHMEFZ-YJPJVVPASA-N turosteride Chemical compound CN([C@@H]1CC2)C(=O)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H](C(=O)N(C(C)C)C(=O)NC(C)C)[C@@]2(C)CC1 WMPQMBUXZHMEFZ-YJPJVVPASA-N 0.000 description 1
- 229950007816 turosteride Drugs 0.000 description 1
- 229940121358 tyrosine kinase inhibitor Drugs 0.000 description 1
- 239000005483 tyrosine kinase inhibitor Substances 0.000 description 1
- 229950009811 ubenimex Drugs 0.000 description 1
- 231100000402 unacceptable toxicity Toxicity 0.000 description 1
- 230000004222 uncontrolled growth Effects 0.000 description 1
- 229960001055 uracil mustard Drugs 0.000 description 1
- SPDZFJLQFWSJGA-UHFFFAOYSA-N uredepa Chemical compound C1CN1P(=O)(NC(=O)OCC)N1CC1 SPDZFJLQFWSJGA-UHFFFAOYSA-N 0.000 description 1
- 229950006929 uredepa Drugs 0.000 description 1
- AUFUWRKPQLGTGF-FMKGYKFTSA-N uridine triacetate Chemical compound CC(=O)O[C@@H]1[C@H](OC(C)=O)[C@@H](COC(=O)C)O[C@H]1N1C(=O)NC(=O)C=C1 AUFUWRKPQLGTGF-FMKGYKFTSA-N 0.000 description 1
- 210000003932 urinary bladder Anatomy 0.000 description 1
- 201000005112 urinary bladder cancer Diseases 0.000 description 1
- 229960005356 urokinase Drugs 0.000 description 1
- 208000037965 uterine sarcoma Diseases 0.000 description 1
- 210000004291 uterus Anatomy 0.000 description 1
- 229960005486 vaccine Drugs 0.000 description 1
- NQPDZGIKBAWPEJ-UHFFFAOYSA-M valerate Chemical class CCCCC([O-])=O NQPDZGIKBAWPEJ-UHFFFAOYSA-M 0.000 description 1
- 229950008261 velaresol Drugs 0.000 description 1
- XLQGICHHYYWYIU-UHFFFAOYSA-N veramine Natural products O1C2CC3C4CC=C5CC(O)CCC5(C)C4CC=C3C2(C)C(C)C21CCC(C)CN2 XLQGICHHYYWYIU-UHFFFAOYSA-N 0.000 description 1
- KDQAABAKXDWYSZ-PNYVAJAMSA-N vinblastine sulfate Chemical compound OS(O)(=O)=O.C([C@H](C[C@]1(C(=O)OC)C=2C(=CC3=C([C@]45[C@H]([C@@]([C@H](OC(C)=O)[C@]6(CC)C=CCN([C@H]56)CC4)(O)C(=O)OC)N3C)C=2)OC)C[C@@](C2)(O)CC)N2CCC2=C1NC1=CC=CC=C21 KDQAABAKXDWYSZ-PNYVAJAMSA-N 0.000 description 1
- 229960004982 vinblastine sulfate Drugs 0.000 description 1
- AQTQHPDCURKLKT-JKDPCDLQSA-N vincristine sulfate Chemical compound OS(O)(=O)=O.C([C@@H](C[C@]1(C(=O)OC)C=2C(=CC3=C([C@]45[C@H]([C@@]([C@H](OC(C)=O)[C@]6(CC)C=CCN([C@H]56)CC4)(O)C(=O)OC)N3C=O)C=2)OC)C[C@@](C2)(O)CC)N2CCC2=C1NC1=CC=CC=C21 AQTQHPDCURKLKT-JKDPCDLQSA-N 0.000 description 1
- 229960002110 vincristine sulfate Drugs 0.000 description 1
- UGGWPQSBPIFKDZ-KOTLKJBCSA-N vindesine Chemical compound C([C@@H](C[C@]1(C(=O)OC)C=2C(=CC3=C([C@]45[C@H]([C@@]([C@H](O)[C@]6(CC)C=CCN([C@H]56)CC4)(O)C(N)=O)N3C)C=2)OC)C[C@@](C2)(O)CC)N2CCC2=C1N=C1[C]2C=CC=C1 UGGWPQSBPIFKDZ-KOTLKJBCSA-N 0.000 description 1
- 229960004355 vindesine Drugs 0.000 description 1
- 229960005212 vindesine sulfate Drugs 0.000 description 1
- BCXOZISMDZTYHW-IFQBWSDRSA-N vinepidine sulfate Chemical compound OS(O)(=O)=O.C([C@H](C[C@]1(C(=O)OC)C=2C(=CC3=C([C@]45[C@H]([C@@]([C@H](OC(C)=O)[C@]6(CC)C=CCN([C@H]56)CC4)(O)C(=O)OC)N3C=O)C=2)OC)C[C@@H](C2)CC)N2CCC2=C1NC1=CC=CC=C21 BCXOZISMDZTYHW-IFQBWSDRSA-N 0.000 description 1
- 229960002166 vinorelbine tartrate Drugs 0.000 description 1
- GBABOYUKABKIAF-IWWDSPBFSA-N vinorelbinetartrate Chemical compound C1N(CC=2C3=CC=CC=C3NC=22)CC(CC)=C[C@H]1C[C@]2(C(=O)OC)C1=CC(C23[C@H]([C@@]([C@H](OC(C)=O)[C@]4(CC)C=CCN([C@H]34)CC2)(O)C(=O)OC)N2C)=C2C=C1OC GBABOYUKABKIAF-IWWDSPBFSA-N 0.000 description 1
- 238000012800 visualization Methods 0.000 description 1
- 235000019165 vitamin E Nutrition 0.000 description 1
- 239000011709 vitamin E Substances 0.000 description 1
- 229940046009 vitamin E Drugs 0.000 description 1
- 239000008136 water-miscible vehicle Substances 0.000 description 1
- 238000009736 wetting Methods 0.000 description 1
- DVPVGSLIUJPOCJ-XXRQFBABSA-N x1j761618a Chemical compound OS(O)(=O)=O.OS(O)(=O)=O.OS(O)(=O)=O.C([C@H](C[C@]1(C(=O)OC)C=2C(=CC3=C([C@]45[C@H]([C@@]([C@H](OC(=O)CN(C)C)[C@]6(CC)C=CCN([C@H]56)CC4)(O)C(=O)OC)N3C)C=2)OC)C[C@@](C2)(O)CC)N2CCC2=C1NC1=CC=CC=C21.C([C@H](C[C@]1(C(=O)OC)C=2C(=CC3=C([C@]45[C@H]([C@@]([C@H](OC(=O)CN(C)C)[C@]6(CC)C=CCN([C@H]56)CC4)(O)C(=O)OC)N3C)C=2)OC)C[C@@](C2)(O)CC)N2CCC2=C1NC1=CC=CC=C21 DVPVGSLIUJPOCJ-XXRQFBABSA-N 0.000 description 1
- 235000010447 xylitol Nutrition 0.000 description 1
- 239000000811 xylitol Substances 0.000 description 1
- HEBKCHPVOIAQTA-SCDXWVJYSA-N xylitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)CO HEBKCHPVOIAQTA-SCDXWVJYSA-N 0.000 description 1
- 229960002675 xylitol Drugs 0.000 description 1
- 229950005561 zanoterone Drugs 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
- 239000011701 zinc Substances 0.000 description 1
- 150000003952 β-lactams Chemical class 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
- A61K31/4523—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems
- A61K31/454—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems containing a five-membered ring with nitrogen as a ring hetero atom, e.g. pimozide, domperidone
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
- A61K31/4523—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems
- A61K31/4545—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems containing a six-membered ring with nitrogen as a ring hetero atom, e.g. pipamperone, anabasine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/496—Non-condensed piperazines containing further heterocyclic rings, e.g. rifampin, thiothixene or sparfloxacin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/50—Pyridazines; Hydrogenated pyridazines
- A61K31/501—Pyridazines; Hydrogenated pyridazines not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/506—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5377—1,4-Oxazines, e.g. morpholine not condensed and containing further heterocyclic rings, e.g. timolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B2200/00—Indexing scheme relating to specific properties of organic compounds
- C07B2200/13—Crystalline forms, e.g. polymorphs
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/02—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom condensed with one carbocyclic ring
- C07D209/04—Indoles; Hydrogenated indoles
- C07D209/30—Indoles; Hydrogenated indoles with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, directly attached to carbon atoms of the hetero ring
- C07D209/32—Oxygen atoms
- C07D209/34—Oxygen atoms in position 2
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Immunology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Oncology (AREA)
- Hematology (AREA)
- Communicable Diseases (AREA)
- Transplantation (AREA)
- Diabetes (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Indole Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
Abstract
Un compuesto de Fórmula I:**Fórmula** o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, donde: R1 es cicloalquilo monocíclico opcionalmente sustituido, arilo monocíclico opcionalmente sustituido, heteroarilo monocíclico opcionalmente sustituido o heterociclilo monocíclico opcionalmente sustituido; R2 y R3 son cada uno halo; donde los sustituyentes en R1, cuando están presentes, son de uno a tres grupos Q, donde cada Q es independientemente alquilo, halo, haloalquilo, oxo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, heterociclilo monocíclico opcionalmente sustituido, heterocicloalquilo monocíclico opcionalmente sustituido, arilo monocíclico opcionalmente sustituido, heteroarilo monocíclico opcionalmente sustituido, -R4OR5, -R4O-R4OR5, -R4N(R6)(R7), -R4SR5, -R4OR4N(R6)(R7), -R4OR4C(J)N(R6)(R7), - C(J)R9 o R4S(O)tR8; donde los sustituyentes en Q, cuando están presentes son de uno a tres grupos Qa, donde cada Qa es independientemente alquilo, halo, haloalquilo, alcoxialquilo, oxo, hidroxilo o alcoxi; cada R4 es independientemente alquileno, alquenileno o un enlace directo; cada R5 es independientemente hidrógeno, alquilo, haloalquilo, hidroxialquilo, alcoxialquilo, cicloalquilo monocíclico, arilo monocíclico, heteroarilo monocíclico, heterociclilo monocíclico o heterociclilalquilo monocíclico, donde los grupos alquilo, haloalquilo, hidroxialquilo, alcoxialquilo, cicloalquilo, arilo, heteroarilo, heterociclilo o heterociclilalquilo en R5 están cada uno independientemente opcionalmente sustituido con de uno a tres grupos Q1, donde cada Q1 es independientemente alquilo, haloalquilo o halo; R6 y R7 se seleccionan de la siguiente manera: i) R6 y R7 son cada uno independientemente hidrógeno o alquilo; o ii) R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un anillo heterociclilo o heteroarilo de 5 o 6 miembros, opcionalmente sustituido con uno o dos halo, alquilo o haloalquilo; R8 es alquilo, haloalquilo o hidroxialquilo; R9 es alquilo o arilo; J es O o S; y t es 1 o 2;
Description
DESCRIPCIÓN
Compuestos antiproliferativos y procedimientos de uso de los mismos
1. REFERENCIA A SOLICITUDES RELACIONADAS
2. CAMPO
En la presente memoria se proporcionan compuestos de la invención para su uso en procedimientos de tratamiento, prevención o control del cáncer. También se proporcionan composiciones farmacéuticas que comprenden los compuestos de la invención y usos de los compuestos y composiciones. En ciertas realizaciones, los procedimientos comprenden el tratamiento, la prevención o el control del cáncer, lo que incluye los tumores sólidos y los tumores transmitidos por vía hematógena usando los compuestos proporcionados en la presente memoria.
3. ANTECEDENTES
Patobiología del cáncer
El cáncer se caracteriza principalmente por un aumento en el número de células anómalas derivadas de un tejido normal determinado, la invasión de tejidos adyacentes por parte de esas células anómalas o la propagación por vía hematógena o linfática de células malignas a los ganglios linfáticos regionales y a sitios distantes (metástasis). Los datos clínicos y los estudios biológicos moleculares indican que el cáncer es un procedimiento de múltiples etapas que comienza con cambios preneoplásicos menores, que en determinadas circunstancias pueden evolucionar hasta una neoplasia. La lesión neoplásica puede evolucionar de manera clónica y desarrollar una capacidad creciente de invasión, crecimiento, metástasis y heterogeneidad, especialmente en condiciones en las que las células neoplásicas se escapan de la vigilancia inmunitaria del hospedador. Roitt, I., Brostoff, J y Kale, D., Immunology, 17,1-17,12 (3a ed., Mosby, St. Louis, Mo., 1993).
Existe una enorme variedad de cánceres que se describen detalladamente en la bibliografía médica. Los ejemplos incluyen cánceres de pulmón, colon, recto, próstata, mama, cerebro e intestino. La incidencia del cáncer continúa en aumento debido al envejecimiento de la población general, al desarrollo de nuevos cánceres y al crecimiento de las poblaciones propensas (por ejemplo, personas infectadas con SIDA o excesivamente expuestas a la luz solar). Por lo tanto, existe una gran demanda de composiciones y procedimientos nuevos que puedan usarse para tratar a los pacientes con cáncer.
Muchos tipos de cánceres están asociados con la formación de nuevos vasos sanguíneos, un procedimiento conocido como angiogénesis. Se han esclarecido varios de los mecanismos implicados en la angiogénesis inducida por tumores. El más directo de estos mecanismos es la secreción de citocinas con propiedades angiogénicas por parte de las células tumorales. Los ejemplos de estas citocinas incluyen el factor de crecimiento de fibroblastos ácido y básico (a,b-FGF), angiogenina, factor de crecimiento del endotelio vascular (VEGF) y TNF-a. De manera alternativa, las células tumorales pueden liberar péptidos angiogénicos a través de la producción de proteasas y la descomposición posterior de la matriz extracelular en la que se almacenan algunas citocinas (por ejemplo, b-FGF). La angiogénesis también puede inducirse indirectamente a través de la captación de células inflamatorias (particularmente, macrófagos) y su liberación posterior de citocinas angiogénicas (por ejemplo, TNF-a, b-FGF).
Linfoma hace referencia a cánceres que se originan en el sistema linfático. El linfoma se caracteriza por neoplasias malignas de los linfocitos, linfocitos B y linfocitos T (es decir, células B y células T). El linfoma comienza, por lo general, en los ganglios linfáticos o conjuntos de tejido linfático en órganos, lo que incluye, pero no se limita a, el estómago o el intestino. En algunos casos, el linfoma puede afectar a la médula y la sangre. El linfoma puede extenderse de un sitio a otras partes del cuerpo.
El tratamiento de diversas formas de linfomas se describe, por ejemplo, en la patente de EE.UU. 7.468.363. Dichos linfomas incluyen, pero no se limitan a, linfoma de Hodgkin, linfoma no hodgkiniano, linfoma cutáneo de linfocitos B, linfoma de linfocitos B activados, linfoma difuso de linfocitos B grandes (LDLBG), linfoma de células del manto (LCM), linfoma central folicular, linfoma transformado, linfoma linfocítico de diferenciación intermedia, linfoma linfocítico intermedio (LLI), linfoma linfocítico difuso con poca diferenciación (LPD), linfoma centrocítico, linfoma difuso de células pequeñas hendidas (LCPH), linfomas de linfocitos T periféricos (LLTP), linfoma de linfocitos T cutáneos y linfoma de la zona del manto y linfoma folicular de bajo grado.
El linfoma no hodgkiniano (LNH) es el quinto cáncer más común, tanto para hombres como para mujeres, en los Estados Unidos, con una estimación de 63.190 nuevos casos y 18.660 muertes en 2007. Jemal A, y col., CA Cancer
J Clin 2007; 57(1):43-66. La probabilidad de desarrollar LNH aumenta con la edad y la incidencia de LNH en los adultos mayores ha aumentado en forma constante en la última década, lo que genera preocupación dada la tendencia de envejecimiento de la población estadounidense. Id. Clarke CA, y col., Cancer2002; 94(7):2015-2023.
El linfoma difuso de linfocitos B grandes (LDLBG) representa aproximadamente un tercio de los linfomas no hodgkinianos. Si bien algunos pacientes con LDLBG se curan con quimioterapia tradicional, el resto fallece debido a la enfermedad. Los fármacos anticancerosos provocan un agotamiento rápido y persistente de los linfocitos, posiblemente mediante la inducción de apoptosis directa en los linfocitos T y B maduros. Véase K. Stahnke y col., Blood 2001, 98:3066-3073. Se ha demostrado que el recuento linfocitario absoluto (RLA) es un factor de pronóstico en el linfoma no Hodgkin folicular y los resultados recientes han sugerido que el RLA en el momento del diagnóstico es un factor de pronóstico importante en el linfoma difuso de linfocitos B grandes. Véase D. Kim y col., Journal of Clinical Oncology, 2007 ASCO Annual Meeting Proceedings Part I. Vol. 25, No. 18S (suplemento del 20 de junio), 2007:8082.
La leucemia se refiere a neoplasias malignas de los tejidos hematopoyéticos. Se describen diversas formas de leucemias, por ejemplo, en la patente de EE.UU. 7.393.862 y la solicitud de patente provisional de EE.UU. 60/380.842, presentada el 17 de mayo de 2002. Aunque se informa de que los virus causan varias formas de leucemia en los animales, las causas de la leucemia en los seres humanos son en gran medida desconocidas. The Merck Manual, 944-952 (17a ed. 1999). La transformación a malignidad generalmente ocurre en una sola célula a través de dos o más pasos con la posterior proliferación y expansión clonal. En algunas leucemias, se han identificado translocaciones cromosómicas específicas con una morfología celular leucémica constante y características clínicas especiales (por ejemplo, translocaciones de 9 y 22 en leucemia mielocítica crónica, y de 15 y 17 en leucemia promielocítica aguda). Las leucemias agudas son poblaciones celulares predominantemente indiferenciadas y las leucemias crónicas son formas celulares más maduras.
Las leucemias agudas se dividen en tipos linfoblásticos (LLA) y no linfoblásticos (LNLA). The Merck Manual, 946-949 (17a edición, 1999). Pueden subdividirse aún más por su aspecto morfológico y citoquímico según la clasificación franco-estadounidense-británica (FAB) o según su tipo y grado de diferenciación. El uso de anticuerpos monoclonales específicos de células B y T y antígeno mieloide son los más útiles para la clasificación. La LLA es predominantemente una enfermedad infantil que se establece mediante hallazgos de laboratorio y examen de médula ósea. La LNLA, también conocida como leucemia mielógena aguda o leucemia mieloblástica aguda (LMA), ocurre en todas las edades y es la leucemia aguda más común entre los adultos; es la forma generalmente asociada con la irradiación como agente causal.
Las leucemias crónicas se describen como linfocíticas (LLC) o mielocíticas (LMC). The Merck Manual, 949-952 (17a ed. 1999). La LLC se caracteriza por la aparición de linfocitos maduros en sangre, médula ósea y órganos linfoides. El sello distintivo de la LLC es la linfocitosis absoluta sostenida (> 5.000/pL) y un aumento de linfocitos en la médula ósea. La mayoría de los pacientes con LLC también tienen expansión clonal de linfocitos con características de células B. La LLC es una enfermedad de la edad mediana o avanzada. En la LMC, el rasgo característico es el predominio de las células granulocíticas de todas las etapas de diferenciación en sangre, médula ósea, hígado, bazo y otros órganos. En el paciente sintomático en el momento del diagnóstico, el recuento leucocitario total (RLT) suele ser de aproximadamente 200.000/pL, aunque puede llegar a 1.000.000/pL. La LMC es relativamente fácil de diagnosticar debido a la presencia del cromosoma Filadelfia.
Además de la categorización aguda y crónica, las neoplasias también se clasifican en función de las células que dan lugar a dicho trastorno en precursoras o periféricas. Véase, por ejemplo, la publicación de patente de EE.UU. n° 2008/0051379. Las neoplasias precursoras incluyen LLA y linfomas linfoblásticos y se presentan en los linfocitos antes de que se hayan diferenciado en células T o B. Las neoplasias periféricas son aquellas que ocurren en los linfocitos que se han diferenciado en células T o B. Dichas neoplasias periféricas incluyen, pero no se limitan a, LLC de células B, leucemia prolinfocítica de células B, linfoma linfoplasmocítico, linfoma de células del manto, linfoma folicular, linfoma de células B de la zona marginal extranodal del tejido linfoide asociado a la mucosa, linfoma de la zona marginal nodal, linfoma esplénico de la zona marginal, leucemia de células pilosas, plasmacitoma, linfoma difuso de células B grandes y linfoma de Burkitt. En más del 95% de los casos de LLC, la expansión clonal es de un linaje de células B. Véase Cancer: Principles & Practice of Oncology (3rd Edition) (1989) (pp. 1843-1847). En menos del 5% de los casos de LLC, las células tumorales tienen un fenotipo de células T. Sin embargo, a pesar de estas clasificaciones, el deterioro patológico de la hematopoyesis normal es el sello distintivo de todas las leucemias.
El mieloma múltiple (MM) es un cáncer de células plasmáticas en la médula ósea. Normalmente, las células plasmáticas producen anticuerpos y desempeñan un papel clave en la función inmunitaria. Sin embargo, el crecimiento descontrolado de estas células provoca dolor y fracturas óseas, anemia, infecciones y otras complicaciones. El mieloma múltiple es la segunda neoplasia hematológica más común, aunque las causas exactas del mieloma múltiple
siguen siendo desconocidas. El mieloma múltiple causa altos niveles de proteínas en la sangre, la orina y los órganos, incluidas, entre otras, la proteína M y otras inmunoglobulinas (anticuerpos), albúmina y beta-2-microglobulina. La proteína M, abreviatura de proteína monoclonal, también conocida como paraproteína, es una proteína particularmente anómala producida por las células plasmáticas del mieloma y se puede encontrar en la sangre u orina de casi todos los pacientes con mieloma múltiple.
Los síntomas esqueléticos, incluido el dolor óseo, se encuentran entre los síntomas clínicamente más significativos del mieloma múltiple. Las células plasmáticas malignas liberan factores estimulantes de osteoclastos (incluidos IL-1, IL-6 y TNF) que provocan que el calcio se filtre de los huesos y cause lesiones líticas; la hipercalcemia es otro síntoma. Los factores estimulantes de los osteoclastos, también conocidos como citocinas, pueden prevenir la apoptosis o muerte de las células de mieloma. El 50% de los pacientes tienen lesiones esqueléticas relacionadas con el mieloma detectables radiológicamente en el momento del diagnóstico. Otros síntomas clínicos comunes para el mieloma múltiple incluyen polineuropatía, anemia, hiperviscosidad, infecciones e insuficiencia renal.
Los tumores sólidos son masas anómalas de tejido que pueden contener, aunque generalmente no lo hacen, quistes o áreas líquidas. Los tumores sólidos pueden ser benignos (no cancerosos) o malignos (cancerosos). Los diferentes tipos de tumores sólidos se nombran por el tipo de células que los forman. Los ejemplos de tipos de tumores sólidos incluyen, pero no se limitan a, melanoma maligno, carcinoma suprarrenal, carcinoma de mama, cáncer de células renales, carcinoma de páncreas, carcinoma de pulmón no microcítico (CPNMC) y carcinoma primario desconocido. Los medicamentos comúnmente administrados a pacientes con varios tipos o estadios de tumores sólidos incluyen, pero no se limitan a, celebrex, etopósido, ciclofosfamida, docetaxel, apecitabina, IFN, tamoxifeno, IL-2, GM-CSF o una combinación de los mismos.
Si bien los pacientes que logran una remisión completa después de la terapia inicial tienen una buena posibilidad de curación, menos del 10% de los que no responden o recaen logran una cura o una respuesta que dura más de 3 años. Véase Cerny T, y col., Ann Oncol 2002; 13 Supl 4: 211-216.
Se sabe que el rituximab agota las células B normales del hospedador. Véase M. Aklilu y col., Annals of Oncology 15: 1109-1114, 2004. Los efectos inmunológicos a largo plazo del agotamiento de las células B con rituximab y las características del grupo de células B reconstituyentes en pacientes con linfoma no están bien definidos, a pesar del uso generalizado de esta terapia. Véase Jennifer H. Anolik y col., Clinical Immunology, vol. 122, número 2, febrero de 2007, páginas 139-145.
El enfoque para pacientes con enfermedad recidivante o refractaria se basa en gran medida en tratamientos experimentales seguidos de trasplante de células madre, que puede no ser apropiado para pacientes con un estado de bajo rendimiento o edad avanzada. Por lo tanto, existe una gran demanda de nuevos procedimientos que puedan usarse para tratar a pacientes con LNH.
El vínculo entre el cáncer y un metabolismo celular alterado ha sido bien establecido. Véase Cairns, RA, y col. Nature Rev., 2011, 11: 85-95. Comprender el metabolismo de las células tumorales y los cambios genéticos asociados al mismo puede conducir a la identificación de mejores procedimientos de tratamiento del cáncer. Id. Por ejemplo, la supervivencia y la proliferación de las células tumorales a través del aumento del metabolismo de la glucosa se ha relacionado con la vía PIK3, por lo que las mutaciones en los genes supresores de tumores como el PTEN activan el metabolismo de las células tumorales. Id. AKT1 (también conocido como PKB) estimula el metabolismo de la glucosa asociado con el crecimiento de células tumorales mediante diversas interacciones con PFKFB3, ENTPD5, mTOR y TSC2 (también conocido como tuberina). Id.
Los factores de transcripción HIF1 y HIF2 son en gran parte responsables de la respuesta celular en condiciones de bajo oxígeno a menudo asociadas con tumores. Id. Una vez activado, HIF1 promueve la capacidad de las células tumorales para llevar a cabo la glucólisis. Id. Por lo tanto, la inhibición de HIF1 puede ralentizar o revertir el metabolismo de las células tumorales. La activación de HIF1 se ha relacionado con PI3K, proteínas supresoras de tumores como VHL, succinato deshidrogenasa (SDH) y fumarato hidratasa. Id. El factor de transcripción oncogénico MYC también se ha relacionado con el metabolismo de las células tumorales, específicamente la glucólisis. Id. MYC también promueve la proliferación celular por vías metabólicas de glutamina. Id.
La proteína cinasa activada por AMP (AMPK) funciona como un punto de control metabólico que las células tumorales deben superar para proliferar. Id. Se han identificado varias mutaciones que suprimen la señalización de AMPK en las células tumorales. Véase Shackelford, D.B. & Shaw, R.J., Nature Rev. Cancer, 2009, 9: 563-575. STK11 ha sido identificado como un gen supresor de tumores relacionado con el papel de AMPK. Véase Cairns, RA, y col. Nature Rev., 2011, 11: 85-95.
El factor de transcripción p53, un supresortumoral, también tiene un papel importante en la regulación del metabolismo celular. Id. La pérdida de p53 en las células tumorales puede ser un contribuyente significativo a los cambios en el metabolismo de las células tumorales en la vía glucolítica. Id. El factor de transcripción OCT1, otra diana potencial para la quimioterapia, puede cooperar con p53 en la regulación del metabolismo de las células tumorales. Id.
El piruvato kinato M2 (PKM2) promueve cambios en el metabolismo celular que confieren ventajas metabólicas a las células cancerosas al favorecer la proliferación celular. Id. Por ejemplo, se ha descubierto que las células de cáncer de pulmón que expresan PKM2 sobre PKM1 tienen esta ventaja. Id. En la clínica, PKM2 ha sido identificado como sobreexpresado en varios tipos de cáncer. Id. Por lo tanto, PKM2 puede ser un biomarcador útil para la detección temprana de tumores.
Las mutaciones en las isocitrato deshidrogenasas IDH1 e IDH2 se han relacionado con la tumorigénesis, específicamente, en el glioblastoma y la leucemia mieloide aguda. Véase Mardis, ER y col., N. Engl. J. Med., 2009, 361:1058-1066; Parsons, DWy col., Science, 2008, 321:1807-1812.
La incidencia del cáncer continúa en aumento debido al envejecimiento de la población general, al desarrollo de nuevos cánceres y al crecimiento de las poblaciones propensas (por ejemplo, personas infectadas con SIDA o excesivamente expuestas a la luz solar). Por lo tanto, existe una gran demanda de nuevos procedimientos, tratamientos y composiciones que puedan usarse para tratar a pacientes con cáncer, lo que incluye, pero no se limita a, aquellos con linfoma, LNH, mieloma múltiple, LMA, leucemias y tumores sólidos.
Por consiguiente, los compuestos que pueden controlar y/o inhibir la angiogénesis no deseada o inhibir la producción de ciertas citocinas, incluido el TNF-a, pueden ser útiles en el tratamiento y prevención de diversas formas de cáncer.
Procedimientos para tratar el cáncer
La terapia actual contra el cáncer puede implicar cirugía, quimioterapia, terapia hormonal y/o tratamiento con radiación para erradicar las células neoplásicas en un paciente (véase, por ejemplo, Stockdale, 1998, Medicine, vol. 3, Rubenstein y Federman, eds., Capítulo 12, Sección IV). Recientemente, la terapia contra el cáncer podría implicar además una terapia biológica o inmunoterapia. Todos estos enfoques pueden plantear desventajas significativas para el paciente. La cirugía, por ejemplo, puede estar contraindicada debido al estado de salud de un paciente o puede ser inaceptable para el paciente. Además, es posible que la cirugía no extraiga completamente el tejido neoplásico. La terapia de radiación es eficaz únicamente cuando el tejido neoplásico presenta una mayor sensibilidad a la radiación que el tejido normal. La terapia de radiación también puede provocar a menudo efectos secundarios graves. No es común que la terapia hormonal se proporcione como un agente único. Si bien la terapia hormonal puede ser eficaz, no se usa frecuentemente para prevenir o retrasar la recurrencia del cáncer después de que otros tratamientos hayan extraído la mayor parte de las células cancerosas. Existe una cantidad limitada de inmunoterapias y terapias biológicas, y estas pueden producir efectos secundarios tales como erupciones o hinchazón, síntomas seudogripales, que incluyen fiebre, escalofríos y fatiga, problemas del tracto digestivo o reacciones alérgicas.
Con respecto a la quimioterapia, existe una variedad de agentes quimioterapéuticos disponibles para el tratamiento del cáncer. La mayor parte de los agentes quimioterapéuticos anticancerosos actúan mediante la inhibición de la síntesis del ADN, ya sea de forma directa o indirecta a través de la inhibición de la biosíntesis de los precursores de desoxirribonucleótidos trifosfato, para evitar la replicación del ADN y la división celular concomitante. Gilman y col., Goodman y Gilman's:The Pharmacological Basis of Therapeutics, 10a ed. (McGraw Hill, Nueva York).
A pesar de la disponibilidad de una variedad de agentes quimioterapéuticos, la quimioterapia tiene diversas desventajas. Stockdale, Medicine, vol. 3, Rubenstein y Federman, ed., cap. 12, sec. 10, 1998. Casi todos los agentes quimioterapéuticos son tóxicos y la quimioterapia causa efectos secundarios significativos y frecuentemente peligrosos que incluyen náuseas intensas, depresión de la médula ósea e inmunosupresión. De manera adicional, incluso con la administración de combinaciones de agentes quimioterapéuticos, varias células tumorales son resistentes o desarrollan resistencia a los agentes quimioterapéuticos. De hecho, esas células resistentes a los agentes quimioterapéuticos particulares usados en el protocolo de tratamiento frecuentemente demuestran ser resistentes a otros fármacos, incluso si esos agentes actúan mediante mecanismos diferentes a los de los fármacos usados en el tratamiento específico. Este fenómeno se denomina resistencia a múltiples fármacos. Debido a la resistencia a los fármacos, muchos cánceres demuestran ser refractarios a los protocolos estándar de tratamiento quimioterapéutico. Existe una necesidad importante de compuestos y procedimientos seguros y efectivos para tratar, prevenir y controlar el cáncer, incluidos los cánceres que son refractarios a los tratamientos estándar, tales como cirugía, radioterapia, quimioterapia y terapia hormonal, al tiempo que reducen o evitan toxicidades y/o efectos secundarios asociados con las terapias convencionales.
4. RESUMEN
La presente invención proporciona un compuesto de la fórmula I:
o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, donde:
R1 es cicloalquilo monocíclico opcionalmente sustituido, arilo monocíclico opcionalmente sustituido, heteroarilo monocíclico opcionalmente sustituido o heterociclilo monocíclico opcionalmente sustituido;
R2 y R3 son cada uno halo;
donde los sustituyentes en R1, cuando están presentes, son de uno a tres grupos Q, donde cada Q es independientemente alquilo, halo, haloalquilo, oxo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, heterociclilo monocíclico opcionalmente sustituido, heterociclilalquilo monocíclico opcionalmente sustituido, arilo monocíclico opcionalmente sustituido, heteroarilo monocíclico opcionalmente sustituido, -R4OR5, -R4O-R4OR5,-R4N(R6)(R7), -R4SR5, -R4OR4N(R6)(R7), -R4OR4C(J)N(R6)(R7), -C(J)R9 o R4S(O)tR8;
donde los sustituyentes en Q, cuando están presentes son de uno a tres grupos Qa, donde cada Qa es independientemente alquilo, halo, haloalquilo, alcoxialquilo, oxo, hidroxilo o alcoxi;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo, hidroxialquilo, alcoxialquilo, cicloalquilo monocíclico, arilo monocíclico, heteroarilo monocíclico, heterociclilo monocíclico o heterociclilalquilo monocíclico, donde los grupos alquilo, haloalquilo, hidroxialquilo, alcoxialquilo, cicloalquilo, arilo, heteroarilo, heterociclilo o heterociclilalquilo en R5 están cada uno independientemente opcionalmente sustituido con de uno a tres grupos Q1, donde cada Q1 es independientemente alquilo, haloalquilo o halo;
R6 y R7 se seleccionan de la siguiente manera:
i) R6 y R7 son cada uno independientemente hidrógeno o alquilo; o
ii) R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un anillo heterociclilo o heteroarilo de 5 o 6 miembros, opcionalmente sustituido con uno o dos halo, alquilo o haloalquilo;
R8 es alquilo, haloalquilo o hidroxialquilo;
R9 es alquilo o arilo;
J es O o S; y
t es 1 o 2;
En una realización, R1 es arilo monocíclico opcionalmente sustituido.
En una realización, el compuesto tiene la Fórmula II:
o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, donde:
R1 es cicloalquilo monocíclico opcionalmente sustituido, arilo monocíclico opcionalmente sustituido, heteroarilo monocíclico opcionalmente sustituido o heterociclilo monocíclico opcionalmente sustituido;
donde los sustituyentes en R1, cuando están presentes, son de uno a tres grupos Q, donde cada Q es independientemente alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, arilo monocíclico opcionalmente sustituido, -R4OR5, -R4SR5, -R4N(R6)(R7), R4OR4N(R6)(R7) o R4OR4C(J)N(R6)(R7);
J es O o S;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo o hidroxialquilo; y
R6 y R7 se seleccionan de la siguiente manera:
i) R6 y R7 son cada uno independientemente hidrógeno o alquilo; o
ii) R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un anillo heterociclilo o heteroarilo de 5 o 6 miembros, opcionalmente sustituido con uno o dos halo, alquilo o haloalquilo.
En una realización, R1 es arilo monocíclico opcionalmente sustituido; donde los sustituyentes en R1, cuando están presentes, son de uno a tres grupos Q, donde cada Q es independientemente alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, arilo monocíclico opcionalmente sustituido -R4OR5, -R4SR5, -R4N(R6)(R7), R4OR4N(R6)(R7) o R4OR4C(J)N(R6)(R7);
J es O o S;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo o hidroxialquilo; y
R6 y R7 se seleccionan de la siguiente manera:
i) R6 y R7 son cada uno independientemente hidrógeno o alquilo; o
ii) R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un anillo heterociclilo o heteroarilo de 5 o 6 miembros, opcionalmente sustituido con uno o dos halo, alquilo o haloalquilo.
En una realización, R1 es fenilo opcionalmente sustituido, ciclohexilo opcionalmente sustituido, piperidinilo opcionalmente sustituido o piridilo opcionalmente sustituido, donde los sustituyentes en R1, cuando están presentes, son de uno a tres grupos Q, donde cada Q es independientemente halo, alquilo, -R4OR5 o-R4N(R6)(R7); cada R4 es independientemente un enlace directo o alquileno; cada R5 es independientemente hidrógeno, alquilo o haloalquilo; y R6 y R7 se seleccionan de la siguiente manera:
i) R6 y R7 son cada uno independientemente hidrógeno o alquilo; o
ii) R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un anillo heterociclilo de 5 o 6 miembros.
En una realización R1 es fenilo opcionalmente sustituido, donde los sustituyentes en R1, cuando están presentes, son de uno a tres grupos Q, donde cada Q es independientemente flúor, cloro, metilo, tere butilo, -R4Or5, -R4SR5 o R4OR4C(J)N(R6)(R7); cada R4 es independientemente un enlace directo o metileno; cada R5 es independientemente hidrógeno, metilo, etilo o trifluorometilo; y R6 y R7 son cada uno independientemente hidrógeno o metilo.
En una realización, el compuesto tiene la fórmula III
o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, donde:
cada Q1 es independientemente alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, arilo monocíclico opcionalmente sustituido, -R4OR5, -R4SR5, -R4N(R6)(R7), R4OR4N(R6)(R7) o R4OR4C(J)N(R6)(R7);
J es O o S;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo o hidroxialquilo;
R6 y R7 se seleccionan de la siguiente manera:
i) R6 y R7 son cada uno independientemente hidrógeno o alquilo; o
ii) R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un anillo heterociclilo o heteroarilo de 5 o 6 miembros, opcionalmente sustituido con uno o dos halo, alquilo o haloalquilo; y
n es 0-3.
En una realización, el compuesto tiene la fórmula IV
o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, donde:
Q2 es hidrógeno, alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, arilo monocíclico opcionalmente sustituido, -R4OR5, -R4SR5, -R4N(R6)(R7), R4OR4N(R6)(R7) o R4OR4C(J)N(R6)(R7);
J es O o S;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo o hidroxialquilo; y
R6 y R7 son cada uno independientemente hidrógeno o alquilo.
En una realización, el compuesto tiene la fórmula V
o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, donde:
Q3 y Q4 son cada uno independientemente hidrógeno, alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, -R4OR5, -R4s R5, -R4N(R6)(R7), N(R6)(R7) o R4OR4C(J)N(R6)(R7);
J es O o S;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo o hidroxialquilo; y
R6 y R7 son cada uno independientemente hidrógeno o alquilo.
En una realización, el compuesto tiene la fórmula VI
o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, donde:
Q4 y Q5 son cada uno independientemente hidrógeno, alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, -R4OR5, -R4SR5, -R4N(R6)(R7), R4o R4N(R6)(R7) o R4OR4C(J)N(R6)(R7);
J es O o S;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo o hidroxialquilo; y
R6 y R7 se seleccionan de la siguiente manera:
i) R6 y R7 son cada uno independientemente hidrógeno o alquilo; o
ii) R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un anillo heterociclilo o heteroarilo de 5 o 6 miembros, opcionalmente sustituido con uno o dos halo, alquilo o haloalquilo.
En una realización, Q4 y Q5 son cada uno independientemente hidrógeno, halo, alquilo, -R4N(R6)(R7), o -R4OR5; R4 es un enlace directo o alquileno; R5 es hidrógeno, alquilo o haloalquilo; y R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un heterociclilo de 6 miembros.
En una realización, el compuesto tiene la fórmula VII
o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, donde:
Q5 es hidrógeno, alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, -R4OR5, -R4SR5, -R4N(R6)(R7), R4OR4N(R6)(R7) o R4OR4C(J)N(R6)(R7); J es O o S;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo o hidroxialquilo; y
R6 y R7 se seleccionan de la siguiente manera:
i) R6 y R7 son cada uno independientemente hidrógeno o alquilo; o
ii) R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un anillo heterociclilo o heteroarilo de 5 o 6 miembros, opcionalmente sustituido con uno o dos halo, alquilo o haloalquilo.
En una realización, Q5 es hidrógeno, halo, alquilo, -R4N(R6)(R7) o -R4OR5; R4es un enlace directo o alquileno; y R5 es hidrógeno, alquilo o haloalquilo; y R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un heterocicliclo de 6 miembros.
En una realización, el compuesto tiene la fórmula VIII
o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, donde:
Q2 y Q5 son cada uno independientemente hidrógeno, alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, -R4OR5, -R4SR5, -R4N(R6)(R7), R4o R4N(R6)(R7) o R4OR4C(J)N(R6)(R7);
J es O o S;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo o hidroxialquilo; y
R6 y R7 son cada uno independientemente hidrógeno o alquilo, o R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un heterociclilo de 6 miembros.
En una realización, Q2 y Q5 son cada uno independientemente hidrógeno, halo, alquilo, arilo monocíclico opcionalmente sustituido o -R4OR5; R4 es un enlace directo o alquileno; y R5 es hidrógeno, alquilo o haloalquilo. En una realización, el compuesto tiene la Fórmula IX:
o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, donde:
cada Q1 es independientemente alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido; cicloalquilalquilo monocíclico opcionalmente sustituido, heterociclilo monocíclico opcionalmente sustituido, -R4OR5, -R4O-R4OR5, -R4N(R6)(R7), -R4SR5, -R4OR4N(R6)(R7),-R4OR4C(J)N(R6)(R7), -C(J)R9 o R4S(O)tR8;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo, hidroxialquilo, alcoxialquilo, cicloalquilo monocíclico, arilo monocíclico, heteroarilo monocíclico, heterociclilo monocíclico o heterociclilalquilo monocíclico, donde los grupos alquilo, haloalquilo, hidroxialquilo, alcoxialquilo, cicloalquilo, arilo, heteroarilo, heterociclilo o heterociclilalquilo en R5 están cada uno independientemente opcionalmente sustituidos con de uno a tres grupos Q1 seleccionados de entre alquilo, haloalquilo o halo;
R6 y R7 son cada uno independientemente hidrógeno o alquilo.
R8 es alquilo, haloalquilo o hidroxialquilo;
R9 es alquilo o arilo;
J es O o S;
t es 1 o 2; y
n es 0-3.
En una realización, el compuesto se selecciona de entre
2-(3-cloro-4-metilfenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
2-(4-dorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-metoxifenil)acetamida;
2-(3-dorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluorofenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-p-tolilacetamida;
2-(3,4-didorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
2-(2-dorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(trifluorometil)fenil)acetamida;
2-(4-terc-butilfenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-fenilacetamida;
2-(3-doro-4-fluorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-(trifluorometiltio)fenil)acetamida;
2-(2,6-difluorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-o-tolilacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-fluorofenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2-(2-etoxifenil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(trifluorometoxi)acetamida;
2-(3-bromo-4-(trifluorometoxi)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida; 2-(3-doro-4-metoxifenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-m-tolilacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-isopropoxifenil)acetamida;
2-(3,4-difluorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-fluorofenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(trifluorometil)piridin-2-il)acetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-isopropilfenil)acetamida;
2-(2,4-didorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-metoxifenil)acetamida;
2-(4-cidopropilfenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
2-(4-doro-2-fluorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
2-(4-doro-3-fluorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-fluoro-2-metilfenil)acetamida;
2-(3-doro-2-metilfenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluoro-2-(trifluorometil)fenil)acetamida; 2-(4-doro-2-metilfenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluoro-2-metilfenil)acetamida;
2-(4-doro-2-(trifluorometil)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida; 2-cidohexil-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
2-(4-doro-2-(trifluorometoxi)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-metoxietoxi)fenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-hidroxietoxi)fenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-(2-metoxietoxi)fenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-hidroxietil)fenil)acetamida;
2-(3-(dimetilamino)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(piperidin-1-il)fenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-morfolinofenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluoro-2-isopropoxifenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(2,2,2-trifluoroetoxi)fenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2-(2-etoxi-4-fluorofenil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-isopropoxifenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-fluoro-4-isopropoxifenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(morfolinometil)fenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluoro-2-(2,2,2-trifluoroetoxi)fenil)acetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-isopropoxi-2-metilfenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-isopropoxi-3-metilfenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-fluoro-4-isopropoxifenil)acetamida;
2-(3-doro-4-isopropoxifenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-metil-4-(trifluorometoxi)fenil)acetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-fluoro-4-(trifluorometoxi)fenil)acetamida; 2-(5-doropiridin-2-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-fluoropiridin-2-il)acetamida;
2-(2,4-difluorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
2-(4-bromofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(2-metoxietoxi)fenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(1-hidroxicidohexil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(1-hidroxicidopentil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-metil-4-(trifluorometoxi)fenil)acetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2-(3-etoxipiridin-2-il)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-metilpiridin-2-il)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-metilpiridin-2-il)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2-(2-etoxi-6-fluorofenil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4'-fluorobifenil-4-il)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2-(2-etoxi-5-fluorofenil)-2,2-difluoroacetamida;
2-cidopentil-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
2-(3-doro-4-(trifluorometoxi)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-metoxi-2-(trifluorometil)fenil)acetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(2-hidroxietoxi)fenil)acetamida;
2-(4-doro-2-etoxifenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-hidroxifenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(metilamino)fenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-isopropoxi-2-(trifluorometil)fenil)acetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-metilcidohexil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-isopropoxietoxi)fenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-hidroxifenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-((4-metilpiperacin-1-il)metil)fenil)acetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-metil-2-(trifluorometil)fenil)acetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-(2-metoxietoxi)etoxi)fenil)acetamida; 2-(3-(2-(dimetilamino)etoxi)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-isopropilpiridin-2-il)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-(metilsulfonil)etoxi)fenil)acetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(3-(metilsulfonil)propil)fenil)acetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-(2-fluoropropan-2-il)fenil)acetamida;
2-(1-bencil-6-oxo-1,6-dihidropiridin-3-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-metoxipiridin-2-il)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridin-3-il)acetamida; 2-(5-terc-butilpiridin-2-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
2-(5-ciclopropilpiridin-2-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-isopropoxipiridin-2-il)acetamida;
2-(5-bromopiridin-2-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluoro-2-(trifluorometoxi)fenil)acetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluorociclohexil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-(metilsulfonil)fenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(metilsulfonil)fenil)acetamida;
2-(2-aminopirimidin-5-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-(trifluorometiltio)piridin-2-il)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-(metilamino)etoxi)fenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-3-il)acetamida;
2-(2-aminopirimidin-4-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(pirimidin-4-il)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-(piperidin-1-il)etoxi)fenil)acetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-morfolinoetoxi)fenil)acetamida;
2-(3-(2-(4,4-difluoropiperidin-1-il)etoxi)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-4-il)acetamida; y
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(4-metilpiperacin-1-il)fenil)acetamida; o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo.
La presente invención también proporciona un compuesto para su uso como medicamento.
La presente invención también proporciona un compuesto para su uso en un procedimiento de tratamiento del cáncer, que comprende la administración a un mamífero que tiene cáncer de una cantidad terapéuticamente efectiva del compuesto. En una realización, el cáncer es leucemia.
En otra realización, la leucemia es leucemia linfocítica crónica, leucemia mielocítica crónica, leucemia linfoblástica aguda o leucemia mieloide aguda.
En otra realización, la leucemia es leucemia mieloide aguda.
En otra realización, la leucemia es recidivante, refractaria o resistente a la terapia convencional.
En otra realización, el procedimiento comprende además la administración de una cantidad terapéuticamente efectiva de otro segundo agente activo o una terapia de cuidado de soporte.
En otra realización, el otro segundo agente activo es un anticuerpo terapéutico que se une específicamente a un antígeno canceroso, factor de crecimiento hematopoyético, citocina, agente anticanceroso, antibiótico, inhibidor de la cox-2, agente inmunomodulador, agente inmunosupresor, corticoesteroide o un mutante farmacológicamente activo o derivado del mismo.
En la presente memoria se proporcionan composiciones farmacéuticas de la invención que contienen los compuestos de la invención y su uso en el tratamiento del cáncer, lo que incluye tumores sólidos y tumores transmitidos por vía hematógena.
En una realización, el compuesto proporcionado en la presente memoria es un compuesto de fórmula I. En una realización, el compuesto proporcionado en la presente memoria es una sal farmacéuticamente aceptable del compuesto de fórmula I. En una realización, el compuesto proporcionado en la presente memoria es un solvato del compuesto de fórmula I. En una realización, el compuesto proporcionado en la presente memoria es un hidrato del compuesto de fórmula I. En una realización, el compuesto proporcionado en la presente memoria es una sal farmacéuticamente aceptable del compuesto de fórmula I.
También se proporcionan composiciones farmacéuticas formuladas para la administración por una ruta y medios apropiados que contienen concentraciones efectivas de uno o más de los compuestos proporcionados en la presente memoria, o un enantiómero o una mezcla de enantiómeros de los mismos, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, y que comprenden opcionalmente al menos un vehículo farmacéutico.
En una realización, las composiciones farmacéuticas proporcionan cantidades efectivas para el tratamiento del cáncer, que incluye tumores sólidos y tumores transmitidos por vía hematógena. En una realización, las composiciones farmacéuticas proporcionan cantidades efectivas para la prevención del cáncer, que incluye tumores sólidos y tumores transmitidos por vía hematógena. En una realización, las composiciones farmacéuticas proporcionan cantidades efectivas para la mejora del cáncer, que incluye tumores sólidos y tumores transmitidos por vía hematógena.
En la presente memoria también se proporcionan uno o más compuestos o composiciones proporcionados en la presente memoria, o un enantiómero o una mezcla de enantiómeros de los mismos, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables de los mismos en combinación con una terapia por ejemplo, otro agente farmacéutico con actividad contra el cáncer o sus síntomas para su uso en terapias combinadas. Los ejemplos de terapias dentro del alcance de los usos incluyen, pero no se limitan a, cirugía, quimioterapia, radioterapia, terapia hormonal, terapia biológica, inmunoterapia y combinaciones de las mismas.
Los compuestos o composiciones proporcionados en la presente memoria, o derivados farmacéuticamente aceptables de los mismos, pueden administrarse simultáneamente con, antes o después de la administración de una o más de las terapias anteriores. También se proporcionan composiciones farmacéuticas que contienen un compuesto que se proporciona en la presente memoria y uno o más de los agentes anteriores.
En ciertas realizaciones, se proporcionan en la presente memoria compuestos o composiciones de la invención para su uso en procedimientos de tratamiento, prevención o control del cáncer, que incluye tumores sólidos y tumores transmitidos por vía hematógena, o uno o más síntomas o causas de los mismos. En ciertas realizaciones, en la presente memoria se proporcionan compuestos o composiciones de la invención para su uso en procedimientos para prevenir el cáncer, que incluye tumores sólidos y tumores transmitidos por vía hematógena, o uno o más síntomas o causas de los mismos. En ciertas realizaciones, en la presente memoria se proporcionan compuestos o composiciones de la invención para mejorar el cáncer, que incluye tumores sólidos y tumores transmitidos por vía hematógena, o uno o más síntomas o causas de los mismos. En ciertas realizaciones, el tumor por vía hematógena es leucemia. En ciertas realizaciones, los procedimientos comprenden procedimientos para tratar diversas formas de leucemias tales como leucemia linfocítica crónica, leucemia mieloide crónica, leucemia linfocítica aguda, leucemia mieloide aguda y leucemia mieloblástica aguda. En ciertas realizaciones, los procedimientos comprenden procedimientos para prevenir diversas formas de leucemias tales como leucemia linfocítica crónica, leucemia mieloide crónica, leucemia linfocítica aguda, leucemia mieloide aguda y leucemia mieloblástica aguda. En ciertas realizaciones, los procedimientos comprenden procedimientos para controlar diversas formas de leucemias tales como leucemia linfocítica crónica, leucemia mieloide crónica, leucemia linfocítica aguda, leucemia mieloide aguda y leucemia mieloblástica aguda. En ciertas realizaciones, los procedimientos incluyen el tratamiento de leucemias que son recurrentes, refractarias o resistentes. En ciertas
realizaciones, los procedimientos incluyen la prevención de leucemias que son recurrentes, refractarias o resistentes. En ciertas realizaciones, los procedimientos incluyen el control de leucemias que son recurrentes, refractarias o resistentes. En una realización, los procedimientos comprenden procedimientos para tratar la leucemia mieloide aguda. En una realización, los procedimientos comprenden procedimientos para prevenir la leucemia mieloide aguda. En una realización, los procedimientos comprenden procedimientos para controlar la leucemia mieloide aguda. En ciertas realizaciones, se administran cantidades efectivas de los compuestos o composiciones que contienen concentraciones terapéuticamente efectivas de los compuestos a un individuo que muestra los síntomas de la enfermedad o trastorno a tratar. Las cantidades son efectivas para mejorar o eliminar uno o más síntomas de la enfermedad o el trastorno.
Además, se proporciona un paquete o kit farmacéutico que comprende uno o más recipientes llenos con uno o más de los ingredientes de las composiciones farmacéuticas de la invención. Opcionalmente, en asociación con dicho o dichos recipientes se puede incluir un aviso de la forma prescrita por un organismo gubernamental que regula la fabricación, el uso o la venta de productos farmacéuticos o biológicos, que refleje la aprobación por parte del organismo de la fabricación, el uso o la venta para administración en seres humanos. El paquete o kit se puede etiquetar con información con respecto al modo de administración, secuencia de administración de fármacos (por ejemplo, por separado, de forma secuencial o simultánea), o similares.
Estos y otros aspectos de la materia descrita en la presente memoria resultarán evidentes con referencia a la siguiente descripción detallada.
5. DESCRIPCIÓN DETALLADA DE LA INVENCIÓN
En la presente memoria se proporcionan compuestos de fórmula I. En la presente memoria se proporciona un enantiómero de compuestos de fórmula I. En la presente memoria se proporciona una mezcla de enantiómeros de compuestos de fórmula I. En la presente memoria se proporciona una sal farmacéuticamente aceptable de un compuesto de fórmula I. En la presente memoria se proporciona un solvato farmacéuticamente aceptable de un compuesto de fórmula I. En la presente memoria se proporciona un hidrato farmacéuticamente aceptable de un compuesto de fórmula I. En la presente memoria se proporciona un cocristal farmacéuticamente aceptable de un compuesto de fórmula I. En la presente memoria se proporciona un clartrato farmacéuticamente aceptable de un compuesto de fórmula I. En la presente memoria se proporciona un polimorfo farmacéuticamente aceptables de un compuesto de fórmula I. Además, se proporcionan composiciones de la invención, formas de dosificación y usos de las mismas en el tratamiento del cáncer, que incluye tumores sólidos, tumores transmitidos por vía hematógena. Además, se proporcionan composiciones de la invención, formas de dosificación y usos de las mismas para prevenir el cáncer, que incluye tumores sólidos y tumores transmitidos por vía hematógena. Se proporcionan además composiciones de la invención, formas de dosificación y usos de las mismas para mejorar el cáncer, que incluye tumores sólidos y tumores transmitidos por vía hematógena. Los compuestos, procedimientos y composiciones de la presente se describen en detalle en las secciones que se muestran a continuación.
A. Definiciones
A menos que se defina lo contrario, todos los términos técnicos y científicos usados en la presente memoria tienen el mismo significado que entiende comúnmente un experto en la materia. En el caso de que haya varias definiciones para un término en la presente memoria, prevalecerán las de esta sección a menos que se indique lo contrario. "Alquilo" se refiere a un grupo de cadena de hidrocarburo lineal o ramificado que consiste únicamente en átomos de carbono e hidrógeno, que no contiene insaturación, que tiene de uno a diez, uno a ocho, uno a seis o uno a cuatro átomos de carbono, y que está unido al resto de la molécula por un enlace simple, por ejemplo, metilo, etilo, n-propilo, 1 -metiletilo(Zso-propilo), n-butilo, n-pentilo, 1,1 -dimetiletilo(f-butilo), y similares.
"Alquileno" y "cadena de alquileno" se refieren a una cadena de hidrocarburos divalente lineal o ramificada que consiste únicamente en carbono e hidrógeno, que no contiene insaturación y que tiene de uno a ocho átomos de carbono, por ejemplo, metileno, etileno, propileno, n-butileno y similares. La cadena de alquileno se puede unir al resto de la molécula a través de dos carbonos cualesquiera dentro de la cadena.
"Alquenileno" o "cadena de alquenileno" se refiere a un radical divalente insaturado de cadena lineal o ramificada que consiste únicamente en átomos de carbono e hidrógeno, que tiene de dos a ocho átomos de carbono, donde la insaturación está presente solo como dobles enlaces y donde el doble enlace puede existir entre dos átomos de carbono en la cadena, por ejemplo, etenileno, prop-1-enileno, but-2-enileno y similares. La cadena de alquenileno se puede unir al resto de la molécula a través de dos carbonos cualesquiera dentro de la cadena.
"Alcoxi" se refiere al grupo que tiene la fórmula -OR donde R es alquilo o haloalquilo. Un “alcoxi opcionalmente sustituido” se refiere al grupo con la fórmula -OR, donde R es alquilo opcionalmente sustituido, tal como se define en la presente memoria.
"Amino" se refiere a un radical que tiene la fórmula -NR'R" donde R' y R" son cada uno independientemente hidrógeno, alquilo o haloalquilo. Un "amino opcionalmente sustituido" se refiere a un radical que tiene la fórmula -NR'R" donde uno o ambos de entre R' y R" son alquilo opcionalmente sustituido como se define en la presente memoria.
"Arilo" se refiere a un grupo de sistema de anillo carbocíclico, que incluye sistemas de anillo monocíclicos, bicíclicos, tricíclicos, tetracíclicos C6-C18, donde al menos uno de los anillos es aromático. El arilo puede ser totalmente aromático, cuyos ejemplos son fenilo, naftilo, antracenilo, acenaftilenilo, azulenilo, fluorenilo, indenilo y pirenilo. El arilo también puede contener un anillo aromático en combinación con un anillo no aromático, cuyos ejemplos son acenafteno, indeno y fluoreno.
"Cicloalquilo" se refiere a un grupo hidrocarburo monocíclico o bicíclico monovalente estable que consta únicamente de átomos de carbono e hidrógeno, que tiene de tres a diez átomos de carbono que está saturado, por ejemplo, ciclopropilo, ciclobutilo, ciclopentilo, ciclohexilo, decalinilo, norbomano, norborneno, adamantilo, biciclo [2,2,2] octano y similares.
"Halo", "halógeno" o "haluro" se refiere a F, Cl, Br o I.
"Haloalquilo" se refiere a un grupo alquilo, en ciertas realizaciones, grupo alquilo C1-6 donde uno o más de los átomos de hidrógeno están sustituidos por halógeno. Dichos grupos incluyen, pero no se limitan a, clorometilo, trifluorometilo 1-cloro-2-fluoroetilo, 2,2-difluoroetilo, 2-fluoropropilo, 2-fluoropropan-2-ilo, 2,2,2-trifluoroetilo, 1,1-difluoroetilo, 1,3-difluoro-2-metilpropilo, 2,2-difluorociclopropilo, (trifluorometil)ciclopropilo, 4,4-difluorociclohexilo y 2,2,2-trifluoro-1,1-dimetiletilo.
"Heterociclo" o "heterociclilo" se refiere a un radical de anillo no aromático estable de 3 a 15 miembros que consiste en átomos de carbono y de uno a cinco heteroátomos seleccionados de entre un grupo que consiste en nitrógeno, oxígeno y azufre. En una realización, el radical del sistema de anillo heterocíclico puede ser un sistema de anillo monocíclico, bicíclico, tricíclico o tetracíclico, que pueden incluir sistemas de anillos fusionados o en puente; y los átomos de nitrógeno o azufre en el radical del sistema de anillo heterocíclico pueden estar opcionalmente oxidados; el átomo de nitrógeno puede estar opcionalmente cuaternizado; y el radical de heterociclilo puede estar parcialmente o totalmente saturado. El sistema de anillo heterocíclico puede estar unido a la estructura principal en cualquier heteroátomo o átomo de carbono, lo que da como resultado la creación de un compuesto estable. Los ejemplos de radicales heterocíclicos incluyen morfolinilo, piperidinilo, piperacinilo, piranilo, pirrolidinilo, oxetanilo, azetidinilo, quinuclidinilo, octahidroquinolicinilo, decahidroquinolicinilo, azabiciclo[3,2,1]octanilo, azabiciclo[2,2,2]octanilo, isoindolinilo, indolinilo y otros.
"Heteroarilo" se refiere a un grupo heterociclilo como se definió anteriormente que es aromático. Los grupos heteroarilo incluyen, pero no se limitan a, grupos monociclilo, biciclilo y triciclilo, y se pueden unir a la estructura principal en cualquier heteroátomo o átomo de carbono, lo que da como resultado la creación de un compuesto estable. Los ejemplos de dichos grupos heteroarilo incluyen, pero no se limitan a: furanilo, imidazolilo, oxazolilo, isoxazolilo, pirimidinilo, piridinilo, piridacinilo, tiazolilo, tienilo, bencimidazolilo, imidazo[4,5-b]piridinilo, imidazo[1,2-a]piridinilo, imidazo[1,2-b]piridacinilo, imidazo[1,2-a]piracinilo y otros.
"IC50" se refiere a una cantidad, concentración o dosificación de un compuesto de prueba en particular que consigue una inhibición del 50% de una respuesta máxima, tal como crecimiento o proliferación celular, medida a través de cualquiera de los ensayos in vitro o basados en células descritos en la presente memoria.
Las sales farmacéuticamente aceptables incluyen, pero no se limitan a, sales de amina, tales como, pero sin limitarse a, A/,W-dibenciletilendiamina, cloroprocaína, colina, amoniaco, dietanolamina y otras hidroxialquilaminas, etilendiamina, W-metilglucamina, procaína, W-bencilfenetilamina, 1-para-clorobencil-2-pirrolidin-1'-ilmetil-bencimidazol, dietilamina y otras alquilaminas, piperacina y tris(hidroximetil)aminometano; sales de metales alcalinos, tales como, pero sin limitarse a, litio, potasio y sodio; sales de metales alcalinotérreos, tales como, pero sin limitarse a, bario, calcio y magnesio; sales de metales de transición, tales como, pero sin limitarse a, cinc; y otras sales metálicas, tales como, pero sin limitarse a, hidrogenofosfato de sodio y fosfato de disodio; y también incluye, pero no se limita a, sales de ácidos minerales, tales como, pero sin limitarse a, clorhidratos y sulfatos; y sales de ácidos orgánicos, tales como, pero sin limitarse a, acetatos, lactatos, malatos, tartratos, citratos, ascorbatos, succinatos, butiratos, valeratos, fumaratos y sulfonatos orgánicos.
Tal como se usa en la presente memoria y a menos que se indique lo contrario el término "hidrato" significa un compuesto proporcionado en la presente memoria o una sal del mismo, que incluye además una cantidad estequiométrica o no estequiométrica de agua unida por fuerzas intermoleculares no covalentes.
Tal como se usa en la presente memoria y a menos que se indique lo contrario el término "solvato" significa un solvato formado a partir de la asociación de una o más moléculas de disolvente a un compuesto proporcionado en la presente memoria. El término "solvato" incluye hidratos (por ejemplo, monohidrato, dihidrato, trihidrato, tetrahidrato y similares). A menos que se describa específicamente de otro modo en la memoria descriptiva, se entiende que la sustitución puede producirse en cualquier átomo del grupo alquilo, alquenilo, alquinilo, cicloalquilo, heterociclilo, arilo o heteroarilo. Cuando no se especifique el número de sustituyente determinado (por ejemplo, haloalquilo), puede haber uno o más sustituyentes presentes. Por ejemplo, “haloalquilo” puede incluir uno o más halógenos iguales o diferentes.
Cuando se dice que los grupos descritos en la presente memoria, con la excepción del grupo alquilo, están "sustituidos", pueden estar sustituidos con cualquier sustituyente o sustituyentes apropiados. Los ejemplos ilustrativos de sustituyentes son los que se encuentran en los compuestos y realizaciones de ejemplo descritos en la presente memoria, así como halógeno (cloro, yodo, bromo o fluoro); alquilo; hidroxilo; alcoxi; alcoxialquilo; amino; alquilamino; carboxi; nitro; ciano; tiol; tioéter; imina; imida; amidina; guanidina; enamina; aminocarbonilo; acilamino; fosfonato; fosfina; tiocarbonilo; sulfonilo; sulfona; sulfonamida; cetona; aldehído; éster; urea; uretano; oxima; hidroxilamina; alcoxiamina; aralcoxiamina; N-óxido; hidracina; hidracida; hidrazona; acida; isocianato; isotiocianato; cianato; tiocianato; oxígeno (=O); B(OH)2, O(alquil)aminocarbonilo; cicloalquilo, que puede ser monocíclico o policíclico fusionado o no fusionado (por ejemplo, ciclopropilo, ciclobutilo, ciclopentilo, o ciclohexilo), o un heterociclilo, que puede ser monocíclico o policíclico fusionado o no fusionado (por ejemplo, pirrolidilo, piperidilo, piperacinilo, morfolinilo o tiacinilo); arilo o heteroarilo monocíclico o policíclico fusionado o no fusionado (por ejemplo, fenilo, naftilo, pirrolilo, indolilo, furanilo, tiofenilo, imidazolilo, oxazolilo, isoxazolilo, tiazolilo, triazolilo, tetrazolilo, pirazolilo, piridinilo, quinolinilo, isoquinolinilo, acridinilo, piracinilo, piridacinilo, pirimidinilo, bencimidazolilo, benzotiofenilo o benzofuranilo) ariloxi; aralquiloxi; heterocicliloxi; y heterociclilalcoxi. En determinadas realizaciones, cuando se dice que los grupos alquilo descritos en la presente memoria están "sustituidos", pueden estar sustituidos con cualquier sustituyente o sustituyentes como los encontrados en los compuestos y realizaciones de ejemplo descritos en la presente memoria, así como halógeno (cloro, yodo, bromo o flúor); hidroxilo; alcoxi; alcoxialquilo; amino; alquilamino; carboxi; nitro; ciano; tiol; tioéter; imina; imida; amidina; guanidina; enamina; aminocarbonilo; acilamino; fosfonato; fosfina; tiocarbonilo; sulfonilo; sulfona; sulfonamida; cetona; aldehído; éster; urea; uretano; oxima; hidroxilamina; alcoxiamina; aralcoxiamina; N-óxido; hidracina; hidracida; hidrazona; acida; isocianato; isotiocianato; cianato; tiocianato; B(OH)2 u O(alquil)aminocarbonilo.
A menos que se indique específicamente de otro modo, si bien un compuesto puede adoptar formas tautoméricas, regioisoméricas y/o estereoisoméricas alternativas, se pretende que todos los isómeros alternativos se encuentren comprendidos dentro del alcance de la materia reivindicada. Por ejemplo, cuando un compuesto se describe con una de dos formas tautoméricas, se pretende que ambos tautómeros se encuentren comprendidos en la presente memoria. Por lo tanto, los compuestos proporcionados en la presente memoria pueden ser enantioméricamente puros, o pueden ser mezclas estereoisoméricas o diastereoisoméricas.
Debe entenderse que los compuestos proporcionados en la presente memoria pueden contener centros quirales. Dichos centros quirales pueden tener cualquiera de las configuraciones (R) o (S), o pueden ser una mezcla de las mismas. Debe entenderse que los centros quirales de los compuestos proporcionados en la presente memoria pueden experimentar epimerización in vivo. De este modo, un experto en la materia reconocerá que la administración de un compuesto en su forma (R) es equivalente, para los compuestos que experimentan epimerización in vivo, a la administración del compuesto en su forma (S).
Los isómeros (+) y (-), (R)- y (S)-, o (D)- y (L)- ópticamente activos se pueden preparar usando sintonas quirales o reactivos quirales o se pueden resolver mediante el uso de técnicas convencionales, tales como cromatografía o una fase estacionaria quiral.
En la descripción de la presente memoria, si existe alguna discrepancia entre un nombre químico y una estructura química, prevalece la estructura.
Tal como se usa en la presente memoria y a menos que se indique lo contrario, los términos "tratar", "tratando" y "tratamiento" se refieren a aliviar o reducir la gravedad de un síntoma asociado con la enfermedad o afección que se
está tratando.
El término "prevención" incluye la inhibición de un síntoma de la enfermedad o trastorno en particular. En algunas realizaciones, los pacientes con antecedentes familiares de cáncer, que incluye tumores sólidos y tumores transmitidos por vía hematógena, son candidatos para regímenes preventivos. En términos generales, el término "prevenir" se refiere a la administración del fármaco antes del inicio de los síntomas, particularmente para pacientes con riesgo de cáncer, que incluye tumores sólidos y tumores transmitidos por vía hematógena.
Tal como se usa en la presente memoria y a menos que se indique lo contrario el término "control" comprende la prevención de la recurrencia de la enfermedad o trastorno en particular en un paciente que lo ha padecido, prolongando el tiempo en que un paciente que ha padecido la enfermedad o trastorno se mantiene en remisión, reduciendo de las tasas de mortalidad de los pacientes y/o manteniendo de una reducción en la gravedad o la evitación de un síntoma asociado con la enfermedad o afección que se está tratando.
Tal como se usa en la presente memoria, "sujeto" es un animal, normalmente un mamífero, que incluye un ser humano, tal como un paciente humano.
Tal como se usa en la presente memoria, el término "tumor" se refiere a todo crecimiento y proliferación de células neoplásicas, ya sean malignas o benignas, y a todas las células y tejidos precancerosos y cancerosos. “Neoplásico”, tal como se usa en la presente memoria, se refiere a cualquier forma de crecimiento celular desregulado o no regulado, ya sea maligno o benigno, que provoca un crecimiento anómalo de tejido. Por lo tanto, las "células neoplásicas" incluyen las células malignas y benignas que presentan crecimiento celular desregulado o no regulado.
Tal como se usa en la presente memoria, "neoplasia maligna hematológica" se refiere a cáncer del sistema inmunitario y hematopoyético del organismo: la médula ósea y el tejido linfático. Dichos cánceres incluyen leucemias, linfomas (linfoma no hodgkiniano), enfermedad de Hodgkin (también denominada linfoma de Hodgkin) y mieloma.
La leucemia se refiere a neoplasias malignas de los tejidos hematopoyéticos. La leucemia incluye, pero no se limita a, leucemia linfocítica crónica, leucemia mielocítica crónica, leucemia linfoblástica aguda, leucemia mieloide aguda y leucemia mieloblástica aguda. La leucemia puede ser recidivante, refractaria o resistente a la terapia convencional. Tal como se usa en la presente memoria, "leucemia promielocítica" o "leucemia promielocítica aguda" se refiere a una neoplasia maligna de la médula ósea donde hay una deficiencia de células sanguíneas maduras en la línea de células mieloides y un exceso de células inmaduras llamadas promielocitos. Normalmente se caracteriza por un intercambio de las regiones de los cromosomas 15 y 17.
Tal como se usa en la presente memoria, "leucemia linfocítica aguda (LLA)", también conocida como "leucemia linfoblástica aguda", se refiere a una enfermedad maligna causada por el crecimiento y desarrollo anómalos de glóbulos blancos no granulares o linfocitos tempranos.
Tal como se usa en la presente memoria, "leucemia de linfocitos T" se refiere a una enfermedad en la que ciertas células del sistema linfoide llamadas linfocitos T o células T son malignas. Los linfocitos T son glóbulos blancos que pueden atacar normalmente a células infectadas por virus, células extrañas y células cancerosas y producen sustancias que regulan la respuesta inmunitaria.
El término "recidiva" se refiere a una situación en la que los pacientes que han tenido una remisión de la leucemia después de la terapia experimentan un retorno de las células de leucemia en la médula y una disminución de las células sanguíneas normales.
El término "refractario o resistente" se refiere a una circunstancia en la que los pacientes, incluso después de un tratamiento intensivo, tienen células residuales de leucemia en su médula.
Tal como se usa en la presente memoria, y a menos que se especifique lo contrario, los términos "cantidad terapéuticamente efectiva" y "cantidad efectiva" de un compuesto se refieren a una cantidad suficiente para proporcionar un beneficio terapéutico en el tratamiento, prevención y/o control de una enfermedad, para retrasar o minimizar uno o más síntomas asociados con la enfermedad o trastorno que se trata. Los términos "cantidad terapéuticamente efectiva" y "cantidad efectiva" pueden comprender una cantidad que mejora la terapia global, reduce o evita síntomas o causas de enfermedad o trastorno, o aumenta la eficacia terapéutica de otro agente terapéutico. Los términos "coadministración" y "en combinación con" incluyen la administración de dos agentes terapéuticos (por ejemplo, un compuesto proporcionado en la presente memoria y otro agente anticanceroso) de forma simultánea,
concurrente o secuencial sin límites de tiempo específicos. En una realización, los dos agentes están presentes en la célula o en el organismo del paciente al mismo tiempo o ejercen su efecto terapéutico o biológico al mismo tiempo. En una realización, los dos agentes terapéuticos se encuentran en la misma composición o forma de dosificación unitaria. En otra realización, los dos agentes terapéuticos se encuentran en composiciones o formas de dosificación unitarias diferentes.
El término "agente de cuidados de apoyo" se refiere a cualquier sustancia que trata, previene o controla un efecto adverso del tratamiento con el compuesto de Fórmula I.
El término "terapia biológica" se refiere a la administración de terapias biológicas tales como sangre del cordón umbilical, células madre, factores de crecimiento y similares.
El término "aproximadamente", tal como se usa en la presente memoria, a menos que se indique lo contrario, se refiere a un valor que no está más del 10% por encima o por debajo del valor que está siendo modificado por el término. Por ejemplo, el término "aproximadamente 10 mg/m2" significa un intervalo de 9 mg/m2 a 11 mg/m2.
"Agentes anticancerosos" se refiere a antimetabolitos (por ejemplo, 5-fluoro-uracilo, metotrexato, fludarabina), agentes antimicrotúbulos (por ejemplo, alcaloides de la vinca como vincristina, vinblastina; taxanos como paclitaxel, docetaxel), agentes de alquilación (por ejemplo, ciclofosfamida, melfalano, carmustina, nitrosoureas tales como biscloroetilnitrosurea e hidroxiurea), agentes de platino (por ejemplo, cisplatino, carboplatino, oxaliplatino, JM-216 o satraplatino, CI-973), antraciclinas (por ejemplo, doxorrubicina, daunorrubicina), antibióticos antitumorales (por ejemplo, mitomicina, idarrubicina, adriamicina, daunomicina), inhibidores de la topoisomerasa (por ejemplo, etopósido, camptotecinas), agentes antiangiogénicos (por ejemplo, Sutent® y Bevacizumab) o cualquier otro agente citotóxico (fosfato de estramustina, prednimustina), hormonas o agonistas hormonales, antagonistas, agonistas parciales o antagonistas parciales, inhibidores de cinasas y tratamiento por radiación.
Tal como se usan en la presente memoria, las abreviaturas para cualquier grupo protector, aminoácidos y otros compuestos, son, a menos que se indique de otro modo, según su uso común, abreviaturas reconocidas o la Comisión de Nomenclatura Bioquímica de la IUPAC-IUB (véase, Biochem. 1972, 11:942-944).
B. Compuestos
En la presente memoria se proporcionan compuestos de fórmula I.
o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, donde:
R1 es cicloalquilo monocíclico opcionalmente sustituido, arilo monocíclico opcionalmente sustituido, heteroarilo monocíclico opcionalmente sustituido o heterociclilo monocíclico opcionalmente sustituido;
R2 y R3 son cada uno halo;
donde los sustituyentes en R1, cuando están presentes, son de uno a tres grupos Q, donde cada Q es independientemente alquilo, halo, haloalquilo, oxo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, heterociclilo monocíclico opcionalmente sustituido, heterociclilalquilo monocíclico opcionalmente sustituido, arilo monocíclico opcionalmente sustituido, heteroarilo monocíclico
opcionalmente sustituido, -R4OR5, -R4O-R4OR5,-R4N(R6)(R7), -R4SR5, -R4OR4N(R6)(R7), -R4OR4C(J)N(R6)(R7), -C(J)R9 o R4S(O)tR8;
donde los sustituyentes en Q, cuando están presentes son de uno a tres grupos Qa, donde cada Qa es independientemente alquilo, halo, haloalquilo, alcoxialquilo, oxo, hidroxilo o alcoxi;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo, hidroxialquilo, alcoxialquilo, cicloalquilo monocíclico, arilo monocíclico, heteroarilo monocíclico, heterociclilo monocíclico o heterociclilalquilo monocíclico, donde los grupos alquilo, haloalquilo, hidroxialquilo, alcoxialquilo, cicloalquilo, arilo, heteroarilo, heterociclilo o heterociclilalquilo en R5 están cada uno independientemente opcionalmente sustituido con de uno a tres grupos Q1, donde cada Q1 es independientemente alquilo, haloalquilo o halo;
R6 y R7 se seleccionan de la siguiente manera:
i) R6 y R7 son cada uno independientemente hidrógeno o alquilo; o
ii) R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un anillo heterociclilo o heteroarilo de 5 o 6 miembros, opcionalmente sustituido con uno o dos halo, alquilo o haloalquilo;
R8 es alquilo, haloalquilo o hidroxialquilo;
R9 es alquilo o arilo;
J es O o S; y
t es 1 o 2;
En una realización, en la presente memoria se proporcionan compuestos de Fórmula II:
o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, donde:
R1 es cicloalquilo monocíclico opcionalmente sustituido, arilo monocíclico opcionalmente sustituido, heteroarilo monocíclico opcionalmente sustituido o heterociclilo monocíclico opcionalmente sustituido;
donde los sustituyentes en R1, cuando están presentes, son de uno a tres grupos Q, donde cada Q es independientemente alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, arilo monocíclico opcionalmente sustituido, -R4OR5, -R4SR5, -R4N(R6)(R7), R4OR4N(R6)(R7) o R4OR4C(J)N(R6)(R7);
J es O o S;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo o hidroxialquilo; y
R6 y R7 se seleccionan de la siguiente manera:
i) R6 y R7 son cada uno independientemente hidrógeno o alquilo; o
ii) R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un anillo heterociclilo o heteroarilo de 5 o 6 miembros, opcionalmente sustituido con uno o dos halo, alquilo o haloalquilo.
En una realización, los compuestos tienen Fórmula I o Fórmula II, donde R1 es arilo monocíclico opcionalmente sustituido; donde los sustituyentes en R1, cuando están presentes, son de uno a tres grupos Q, donde cada Q es independientemente alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, arilo monocíclico opcionalmente sustituido, -R4OR5, -R4SR5, -R4N(R6)(R7), R4OR4N(R6)(R7) o R4OR4C(J)N(R6)(R7); cada R4 es independientemente alquileno, alquenileno o un enlace directo; cada R5 es independientemente hidrógeno, alquilo, haloalquilo o hidroxialquilo; y R6 y R7 se seleccionan de la siguiente manera:
i) R6 y R7 son cada uno independientemente hidrógeno o alquilo; o
ii) R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un anillo heterociclilo o heteroarilo de 5 o 6 miembros, opcionalmente sustituido con uno o dos halo, alquilo o haloalquilo.
En una realización, los compuestos tienen Fórmula I o Fórmula II, donde R1 es arilo monocíclico opcionalmente sustituido, cicloalquilo monocíclico opcionalmente sustituido, heterociclilo monocíclico opcionalmente sustituido o heteroarilo monocíclico opcionalmente sustituido, donde los sustituyentes en R1, cuando están presentes, son de uno a tres grupos Q, donde cada Q es independientemente halo, alquilo, cicloalquilo monocíclico opcionalmente sustituido, arilo monocíclico opcionalmente sustituido, -R4OR5 o -R4N(R6)(R7); cada R4 es independientemente un enlace directo o alquileno; cada R5 es independientemente hidrógeno, alquilo o haloalquilo; y R6 y R7 se seleccionan de la siguiente manera:
i) R6 y R7 son cada uno independientemente hidrógeno o alquilo; o
ii) R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un anillo heterociclilo o heteroarilo de 5 o 6 miembros, opcionalmente sustituido con uno o dos halo, alquilo o haloalquilo.
En una realización, los compuestos tienen Fórmula I o Fórmula II, R1 es fenilo opcionalmente sustituido, ciclohexilo opcionalmente sustituido, piperidinilo opcionalmente sustituido o piridilo opcionalmente sustituido, donde los sustituyentes en R1, cuando están presentes, son de uno a tres grupos Q, donde cada Q es independientemente halo, alquilo, -R4OR5 o-R4N(R6)(R7); cada R4 es independientemente un enlace directo o alquileno; cada R5 es independientemente hidrógeno, alquilo o haloalquilo; y R6 y R7 se seleccionan de la siguiente manera:
i) R6 y R7 son cada uno independientemente hidrógeno o alquilo; o
ii) R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un anillo heterociclilo de 5 o 6 miembros. En una realización, los compuestos tienen Fórmula I o Fórmula II, donde R1 es fenilo opcionalmente sustituido, ciclohexilo opcionalmente sustituido, piperidinilo opcionalmente sustituido o piridilo opcionalmente sustituido, donde los sustituyentes en R1, cuando están presentes, son uno a tres grupos Q, donde cada Q es independientemente cloro, bromo, fluoro, metilo, isopropilo, tere butilo, trifluorometilo, metoxi, etoxi, isopropiloxi, metoxietoxi, isopropiloxietoxi, trifluorometoxi, metilamino, dimetilamino o piperidinilo.
En una realización, los compuestos tienen Fórmula I o Fórmula II, donde R1 es arilo monocíclico opcionalmente sustituido, donde los sustituyentes en R1, cuando están presentes, son uno a tres grupos Q, donde cada Q es independientemente halo, alquilo, -R4OR5, -R4SR5 o R4OR4C(O)N(R6)(R7); cada R4 es independientemente un enlace directo o alquileno; cada R5 es independientemente hidrógeno, alquilo o haloalquilo; y R6 y R7 son cada uno independientemente hidrógeno o alquilo.
En una realización, los compuestos tienen Fórmula I o Fórmula II, en donde R1 monocíclico es arilo monocíclico opcionalmente sustituido, donde los sustituyentes en R1, cuando están presentes, son de uno a tres grupos Q, donde cada Q es independientemente fluoro, cloro, metilo, -R4OR5, -R4N(R6)(R7), -R4SR5 o R4OR4C(O)N(R6)(R7); cada R4 es independientemente un enlace directo o metileno; cada R5 es independientemente hidrógeno, metilo, etilo o trifluorometilo; y R6 y R7 son cada uno independientemente hidrógeno o metilo.
En una realización, los compuestos tienen Fórmula I o Fórmula II, donde R1 es fenilo opcionalmente sustituido, donde los sustituyentes en R1, cuando están presentes, son de uno a tres grupos Q, donde cada Q es independientemente fluoro, cloro, metilo, tere butilo, -R4OR5, -R4N(R6)(R7), -R4SR5 o R4OR4C(O)N(R6)(R7); cada R4 es independientemente un enlace directo o metileno; cada R5 es independientemente hidrógeno, metilo, etilo o trifluorometilo; y R6 y R7 son
cada uno independientemente hidrógeno o metilo.
En una realización, en la presente memoria se proporcionan compuestos de Fórmula III:
o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, donde:
cada Q1 es independientemente alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, arilo monocíclico opcionalmente sustituido, -R4OR5, -R4SR5, -R4N(R6)(R7), R4OR4N(R6)(R7) o R4OR4C(J)N(R6)(R7);
J es O o S;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo o hidroxialquilo;
R6 y R7 se seleccionan de la siguiente manera:
i) R6 y R7 son cada uno independientemente hidrógeno o alquilo; o
ii) R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un anillo heterociclilo o heteroarilo de 5 o 6 miembros, opcionalmente sustituido con uno o dos halo, alquilo o haloalquilo; y
n es 0-3.
En una realización, en la presente memoria se proporcionan compuestos de Fórmula III o un enantiómero o una mezcla de enantiómeros de los mismos, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables de los mismos, donde:
cada Q1 es independientemente alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, arilo monocíclico opcionalmente sustituido, -R4OR5, -R4SR5, -R4N(R6)(R7);
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo o hidroxialquilo;
R6 y R7 se seleccionan de la siguiente manera:
i) R6 y R7 son cada uno independientemente hidrógeno o alquilo; o
ii) R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un anillo heterociclilo de 5 o 6 miembros. n es 0-3.
En una realización, los compuestos de la presente invención son de Fórmula III, donde cada Q1 es independientemente Br, Cl, F, metilo, isopropilo, t-butilo, isopropilo, ciclopropilo, -CF3, OH, -SCH3, -SCF3, -C(CH3)2F, -Oc H3, -OCF3, -OCH2CH3, -OCH(CH3)2, -OCH2CF3, -O(CH2)2OCH3, -O(CH2)2OCH(CH3)2, -O(CH2)2O(CH2)2OCH3, -NHCH3, -N(CH3)2, -O(CH2)2-morfolinilo, piperidilo, morfolinilo,-CH2-morfolinilo, -O(CH2)2-4,4-difluoro-1-piperidilo o p-fluorofenilo.
En una realización, en la presente memoria se proporcionan compuestos de Fórmula IV:
o un enantiómero o una mezcla de enantiómeros de los mismos, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables de los mismos, donde:
Q2 es hidrógeno, alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, arilo monocíclico opcionalmente sustituido, -R4OR5, -R4SR5, -R4N(R6)(R7), R4OR4N(R6)(R7) o R4OR4C(J)N(R6)(R7);
J es O o S;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo o hidroxialquilo; y
R6 y R7 son cada uno independientemente hidrógeno o alquilo.
En una realización, los compuestos de la presente invención son de Fórmula IV, donde Q2 es hidrógeno, halo, alquilo, arilo monocíclico opcionalmente sustituido, -R4OR5 o -R4N(R6)(R7); R4 es independientemente un enlace directo o alquileno; R5 es hidrógeno, alquilo o haloalquilo; y R6y R7 son cada uno independientemente hidrógeno o alquilo. En algunas realizaciones, Q2 es hidrógeno, Br, Cl, F, metilo, isopropilo, t-butilo, isopropilo, -OCH3, -SCH3, -C(CH3)2F, -OCH(CH3)2, -O(CH2)2OCH3 o p-fluorofenilo.
En una realización, en la presente memoria se proporcionan compuestos de Fórmula V:
o un enantiómero o una mezcla de enantiómeros de los mismos, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, donde:
Q3 y Q4 son cada uno independientemente hidrógeno, alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, -R4o R5,-R4SR5, -R4N(R6)(R7), R4o R4N(R6)(R7) o R4OR4C(J)N(R6)(R7);
J es O o S;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo o hidroxialquilo; y
R6 y R7 son cada uno independientemente hidrógeno o alquilo.
En una realización, los compuestos de la presente invención son de Fórmula V, donde Q4 y Q3 son cada uno independientemente hidrógeno, halo, alquilo, -R4OR5, o -R4N(R6)(R7); R4 es un enlace directo o alquileno; y R5 es hidrógeno, alquilo o haloalquilo; y R6 y R7 son cada uno independientemente hidrógeno o alquilo. En algunas de dichas realizaciones, Q4 y Q3 son cada uno independientemente hidrógeno, F, metilo,-CF3, OH, -OCF3, -OCH2CH3, OCH(CH3)2, -OCH2CF3 o -NHCH3.
En una realización, los compuestos de la presente invención son de Fórmula V, donde Q4 es hidrógeno, Q3 es hidrógeno, halo, alquilo, -R4N(R6)(R7) o -R4OR5; R4 es un enlace directo o alquileno; R5 es hidrógeno, alquilo o haloalquilo; y R6 y R7 son cada uno independientemente hidrógeno o alquilo.
En una realización, en la presente memoria se proporcionan compuestos de Fórmula VI:
o un enantiómero o una mezcla de enantiómeros de los mismos, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables de los mismos, donde:
Q4 y Q5 son cada uno independientemente hidrógeno, alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, -R4OR5, -R4SR5, -R4N(R6)(R7), R4o R4N(R6)(R7) o R4OR4C(J)N(R6)(R7);
J es O o S;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo o hidroxialquilo; y
R6 y R7 se seleccionan de la siguiente manera:
i) R6 y R7 son cada uno independientemente hidrógeno o alquilo; o
ii) R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un anillo heterociclilo o heteroarilo de 5 o 6 miembros, opcionalmente sustituido con uno o dos halo, alquilo o haloalquilo.
En una realización, los compuestos son de Fórmula VI, donde Q4 y Q5 son cada uno independientemente hidrógeno, halo, alquilo, -R4N(R6)(R7) o -R4OR5; R4 es un enlace directo o alquileno; R5 es hidrógeno, alquilo o haloalquilo; y R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un heterociclilo de 6 miembros. En algunas de dichas realizaciones, Q4 y Q5 son cada uno independientemente hidrógeno, F, Cl, OH, metilo, -CF3, -NHCH3, -N(CH3)2, -OCF3, -OCH2CH3, -OCH2CF3, -OCH(CH3)2, -O(CH2)2OCH3, -O(CH2)2OCH(CH3)2, -O(CH2)OCH2)2OCH3, O(CH2)2-morfolinilo, piperidilo, morfolinilo, -CH2-morfolinilo o -O(CH2)2 -4,4-difluoro-1 -piperidilo.
En una realización, en la presente memoria se proporcionan compuestos de Fórmula VII:
o un enantiómero o una mezcla de enantiómeros de los mismos, o una sal, solvato, hidrato, cocristal, clatrato o
polimorfo farmacéuticamente aceptables de los mismos, donde:
Q5 es hidrógeno, alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquMalquilo monocíclico opcionalmente sustituido, -R4OR5, -R4SR5, -R4N(R6)(R7), R4OR4N(R6)(R7) o R4OR4C(J)N(R6)(R7);
J es O o S;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo o hidroxialquilo; y
R6 y R7 se seleccionan de la siguiente manera:
i) R6 y R7 son cada uno independientemente hidrógeno o alquilo; o
ii) R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un anillo heterociclilo o heteroarilo de 5 o 6 miembros, opcionalmente sustituido con uno o dos halo, alquilo o haloalquilo.
En una realización, los compuestos de la presente memoria son de Fórmula VII, donde Q5 es hidrógeno, halo, alquilo, -R4N(R6)(R7) o -R4OR5; R4es un enlace directo o alquileno; y R5 es hidrógeno, alquilo o haloalquilo; y R6 y R7 junto con el átomo de nitrógeno son una forma sustituida de un heterociclilo de 6 miembros. En algunas de dichas realizaciones, Q5 es hidrógeno, F, Cl, metilo, piperidilo, morfolinilo, -CH2-morfolinilo, -N(CH3)2, -O(CH2)2OCH3, -O(CH2)2OCH(CH3)2, -O(CH2)2O(CH2)2OCH3, o -O(CH2)2-4,4-difluoro-1-piperidilo.
En una realización, en la presente memoria se proporcionan compuestos de Fórmula VIII:
o un enantiómero o una mezcla de enantiómeros de los mismos, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables de los mismos, donde:
Q2 y Q5 son cada uno independientemente hidrógeno, alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, -R4OR5, -R4SR5, -R4N(R6)(R7), R4o R4N(R6)(R7) o R4OR4C(J)N(R6)(R7);
J es O o S;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo o hidroxialquilo; y
R6 y R7 son cada uno independientemente hidrógeno o alquilo, o R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un heterociclilo de 6 miembros.
En una realización, los componentes son de Fórmula VIII, donde Q2 y Q5 son cada uno independientemente hidrógeno, halo, alquilo, arilo monocíclico opcionalmente sustituido o -R4OR5; R4 es un enlace directo o alquileno; y R5 es hidrógeno, alquilo o haloalquilo. En algunas de tales realizaciones, Q2 y Q5 son cada uno independientemente hidrógeno, F, Br, Cl, metilo, isopropilo, t-butilo, -C(CH3)2F, p-fluorofenilo, ciclopropilo, -N(CH3)2, -OCH3, -OCH(CH3)2, O(CH2)2OCH3, -O(CH2)2OCH(CH3)2, -O(CH2)2OCH3, -O(CH2)2O(CH2)2OCH3, -OCF3, -O(CH2)2-4,4-difluoro-1-piperidilo, -SCF3, morfolinilo, piperidilo o CH2-morfolinilo.
En una realización, en la presente memoria se proporcionan compuestos de Fórmula IX:
o un enantiómero o una mezcla de enantiómeros de los mismos, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables de los mismos, donde:
cada Q1 es independientemente alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido; cicloalquilalquilo monocíclico opcionalmente sustituido, heterociclilo monocíclico opcionalmente sustituido, -R4OR5, -R4O-R4OR5, -R4N(R6)(R7), -R4SR5, -R4OR4N(R6)(R7), -R4OR4C(J)N(R6)(R7), -C(J)R9 o R4S(O)tR8;
J es O o S;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo, hidroxialquilo, alcoxialquilo, cicloalquilo monocíclico, arilo monocíclico, heteroarilo monocíclico, heterociclilo monocíclico o heterociclilalquilo monocíclico, donde los grupos alquilo, haloalquilo, hidroxialquilo, alcoxialquilo, cicloalquilo, arilo, heteroarilo, heterociclilo o heterociclilalquilo en R5 están cada uno independientemente opcionalmente sustituidos con de uno a tres grupos Q seleccionados de entre alquilo, haloalquilo o halo;
R6 y R7 son cada uno independientemente hidrógeno o alquilo.
R8 es alquilo, haloalquilo o hidroxialquilo;
R9 es alquilo o arilo;
J es O o S;
t es 1 o 2; y
n es 0-3.
En una realización, los compuestos de la presente invención son de Fórmula IX, donde cada Q1 es independientemente halo, alquilo o haloalquilo. En algunas realizaciones, cadaQ1 es independientemente flúor, cloro, bromo, metilo, isopropilo, t-butilo, -CF3, -O-CH2CH3, -O-CH(CH3)2 o ciclopropilo.
En una realización, el compuesto proporcionado en la presente memoria se selecciona de entre el grupo que consiste en:
En una realización, el compuesto proporcionado en la presente memoria es un compuesto según la Tabla 1.
En la presente memoria se proporcionan también análogos enriquecidos isotópicamente de los compuestos proporcionados en la presente memoria. El enriquecimiento isotópico (por ejemplo, deuteración) de productos farmacéuticos para mejorar la farmacocinética ("PK"), la farmacodinámica ("PD") y los perfiles de toxicidad se ha demostrado previamente con algunas clases de medicamentos. Véase, por ejemplo, Lijinsky y col., Food Cosmet. Toxicol., 20:393 (1982); Lijinsky y col, J. Nat. Cancer Inst., 69:1127 (1982); Mangold y col., Mutation Res. 308:33 (1994); Gordon y col., Drug Metab. Dispos., 15:589 (1987); Zello y col., Metabolism, 43:487 (1994); Gately y col., J. Nucl. Med., 27:388 (1986); Wade D, Chem. Biol. Interact. 117:191 (1999).
Sin estar limitado por ninguna teoría en particular, el enriquecimiento isotópico de un fármaco puede usarse, por ejemplo, para (1) reducir o eliminar los metabolitos no deseados, (2) aumentar la vida media del fármaco precursor, (3) disminuir el número de dosis necesarias para lograr un efecto deseado, (4) disminuir la cantidad de una dosis necesaria para lograr un efecto deseado, (5) aumentar la formación de metabolitos activos, si se forma alguno y/o (6) disminuir la producción de metabolitos perjudiciales en tejidos específicos y/o crear un fármaco más efectivo y/o más seguro para la terapia de combinación, ya sea la terapia de combinación intencionada o no.
La sustitución de un átomo por uno de sus isótopos producirá frecuentemente un cambio en la velocidad de reacción de una reacción química. Este fenómeno se conoce como efecto isotópico cinético (“KIE”, por sus siglas en inglés). Por ejemplo, si se rompe un enlace C-H durante una etapa que determina la velocidad en una reacción química (es decir, la etapa con la mayor energía de estado de transición), la sustitución de un deuterio por ese hidrógeno provocará una disminución en la velocidad de reacción y el procedimiento se ralentizará. Este fenómeno se conoce como efecto isotópico cinético del deuterio (“DKIE”, por sus siglas en inglés). (Véase, por ejemplo, Fostery col., Adv. Drug Res., vol. 14, pp. 1-36 (1985); Kushner y col., Can. J. Physiol. Pharmacol., vol. 77, pág. 79-88 (1999)).
La magnitud del DKIE puede expresarse como la relación entre las velocidades de una reacción determinada en la que se rompe un enlace C-H, y la misma reacción en la que se sustituye deuterio por hidrógeno. El DKIE puede variar entre aproximadamente 1 (sin efecto isotópico) y números muy grandes, tales como 50 o más, lo que significa que la reacción puede ser cincuenta veces, o más, más lenta cuando se sustituye hidrógeno por deuterio. Sin limitarse a ninguna teoría particular, los valores de DKIE elevados pueden deberse en parte a un fenómeno conocido como efecto túnel, que es una consecuencia del principio de incertidumbre. El efecto túnel se atribuye a la masa pequeña de un átomo de hidrógeno, y ocurre debido a que los estados de transición que afectan a un protón a veces pueden formarse en ausencia de la energía de activación necesaria. Dado que el deuterio tiene más masa que el hidrógeno, estadísticamente tiene mucha menor probabilidad de experimentar este fenómeno.
El tritio ("T") es un isótopo radiactivo de hidrógeno, usado en investigación, reactores de fusión, generadores de neutrones y radiofármacos. El tritio es un átomo de hidrógeno que tiene 2 neutrones en el núcleo y tiene un peso
atómico cercano a 3. Se produce naturalmente en el ambiente en concentraciones muy bajas, encontrado más comúnmente como T2O. El tritio se descompone lentamente (semivida = 12,3 años) y emite una partícula beta de baja energía que no puede penetrar la capa externa de la piel humana. La exposición interna es el peligro principal asociado a este isótopo, y aún así debe ingerirse en grandes cantidades para que presente un riesgo significativo para la salud. En comparación con el deuterio, debe consumirse una menor cantidad de tritio antes de que alcance un nivel peligroso. La sustitución de hidrógeno por tritio (“T”) da como resultado un enlace aún más fuerte que el deuterio y proporciona efectos isotópicos numéricamente mayores.
De manera similar, la sustitución de isótopos por otros elementos, que incluyen, pero no se limitan a, 13C o 14C para el carbono, 33S, 34S o 36S para el azufre, 15N para el nitrógeno y 17O o 18O para el oxígeno, proporcionarán unos efectos isotópicos cinéticos similares.
El cuerpo animal expresa una variedad de enzimas con el propósito de eliminar sustancias extrañas, tales como agentes terapéuticos, de su sistema de circulación. Los ejemplos de dichas enzimas incluyen enzimas del citocromo P450 ("CYP"), esterasas, proteasas, reductasas, deshidrogenasas y monoaminooxidasas, para reaccionar con y convertir estas sustancias extrañas en metabolitos o productos intermedios más polares para la excreción renal. Algunas de las reacciones metabólicas más comunes de compuestos farmacéuticos implican la oxidación de un enlace carbono-hidrógeno (C-H) a un enlace pi carbono-oxígeno (C-O) o carbono-carbono (C-C). Los metabolitos resultantes pueden ser estables o inestables en condiciones fisiológicas, y pueden tener perfiles farmacocinéticos, farmacodinámicos y de toxicidad aguda y a largo plazo sustancialmente diferentes con respecto a los compuestos originales. Para muchos fármacos, dichas oxidaciones son rápidas. Como resultado, estos fármacos a menudo requieren la administración de dosis diarias múltiples o elevadas.
El enriquecimiento isotópico en determinadas posiciones de un compuesto proporcionado en la presente memoria puede producir un KIE detectable que afecta los perfiles farmacocinéticos, farmacológicos y/o toxicológicos de un compuesto proporcionado en la presente memoria en comparación con un compuesto similar que tiene una composición isotópica natural. En una realización, el enriquecimiento con deuterio se realiza en el sitio de escisión del enlace C-H durante el metabolismo.
C. Procedimientos de tratamiento y prevención
En una realización, en la presente memoria se proporciona un compuesto o una composición de la invención para su uso en un procedimiento de tratamiento y prevención de cáncer, donde el procedimiento comprende la administración a un paciente de un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo.
En otra realización, en la presente memoria se proporciona un compuesto o una composición de la invención para su uso en un procedimiento para controlar el cáncer, donde el procedimiento comprende la administración a un paciente de un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo.
En la presente memoria se proporcionan también compuestos o composiciones de la invención para su uso en procedimientos de tratamiento de pacientes que han sido tratados previamente para cáncer pero que no responden a terapias estándar, así como a aquellos que no han sido tratados previamente. La invención comprende también un compuesto o una composición de la invención para su uso en procedimientos de tratamiento de pacientes independientemente de la edad del paciente, aunque algunas enfermedades o trastornos son más comunes en ciertos grupos de edad. La invención comprende además un compuesto o una composición de la invención para su uso en procedimientos para tratar a pacientes que se han sometido a una cirugía en un intento de tratar la enfermedad o la afección en cuestión, así como a aquellos que no se han sometido a la misma. Debido a que los pacientes con cáncer presentan manifestaciones clínicas heterogéneas y resultados clínicos variables, el tratamiento que se administra a un paciente puede variar según su pronóstico. Los expertos en medicina podrán determinar fácilmente, sin experimentación innecesaria, los agentes secundarios específicos, los tipos de cirugía y los tipos de tratamiento estándar no basado en fármacos que se pueden usar de forma eficaz para tratar un paciente individual con cáncer. Tal como se usa en la presente memoria, el término "cáncer" incluye, pero no se limita a, tumores sólidos y tumores transmitidos por vía hematógena. El término "cáncer" se refiere a una enfermedad de los tejidos de la piel, órganos, sangre y vasos, que incluye, pero no se limita a, cánceres de vejiga, huesos, sangre, cerebro, mama, cuello del útero, tórax, colon, endometrio, esófago, ojo, cabeza, riñón, hígado, ganglios linfáticos, pulmón, boca, cuello, ovarios, páncreas, próstata, recto, estómago, testículos, garganta y útero. Los cánceres específicos incluyen, entre otros,
neoplasia maligna avanzada, amiloidosis, neuroblastoma, meningioma, hemangiopericitoma, metástasis cerebral múltiple, glioblastoma multiforme, glioblastoma, glioma del tronco encefálico, tumor cerebral maligno de pronóstico infausto, glioma maligno, glioma maligno recurrente, astrocitoma anaplásico, oligodendroglioma anaplásico, tumor neuroendocrino, adenocarcinoma rectal, cáncer colorrectal Dukes C y D, carcinoma colorrectal, carcinoma colorrectal irresecable, carcinoma hepatocelular metastásico, sarcoma de Kaposi, leucemia mieloblástica aguda cariotípica, linfoma de Hodgkin, linfoma no hodgkiniano, linfoma cutáneo de linfocitos T, linfoma cutáneo de linfocitos B, linfoma difuso de linfocitos B grandes, linfoma folicular de bajo grado, melanoma maligno, mesotelioma maligno, síndrome de mesotelioma de derrame pleural maligno, carcinoma peritoneal, carcinoma seroso papilar, sarcoma ginecológico, sarcoma de los tejidos blandos, esclerodermia, vasculitis cutánea, histiopatía de células de Langerhans, leiomiosarcoma, fibrodisplasia osificante progresiva, cáncer de próstata resistente a las hormonas, sarcoma de los tejidos blandos de alto riesgo resecado, carcinoma hepatocelular irresecable, macroglobulinemia de Waldenstrom, mieloma latente, mieloma indolente, cáncer de trompa de Falopio, cáncer de próstata independiente de andrógenos, cáncer de próstata no metastásico dependiente de andrógenos en estadio IV, cáncer de próstata insensible a las hormonas, cáncer de próstata insensible a la quimioterapia, carcinoma papilar de tiroides, carcinoma tiroideo folicular, carcinoma tiroideo medular y leiomioma.
En ciertas realizaciones, el cáncer es un tumor sólido. En ciertas realizaciones, el tumor sólido es metastásico. En ciertas realizaciones, el tumor sólido es resistente a los fármacos. En ciertas realizaciones, el tumor sólido es carcinoma hepatocelular, cáncer de próstata, cáncer de ovario o glioblastoma.
En ciertas realizaciones, el cáncer es un tumor transmitido por vía hematógena. En ciertas realizaciones, el tumor transmitido por vía hematógena es metastásico. En ciertas realizaciones, el tumor transmitido por vía hematógena es resistente a los fármacos. En ciertas realizaciones, el cánceres leucemia.
En una realización, los procedimientos proporcionados en la presente memoria comprenden un compuesto o una composición de la invención para su uso en el tratamiento, prevención o control de diversos tipos de leucemias tales como leucemia linfocítica crónica (LLC), leucemia mielocítica crónica (LMC), leucemia linfoblástica aguda (LLA), leucemia mieloide aguda (LMA) y leucemia mieloblástica aguda (LMA) mediante la administración de una cantidad terapéuticamente efectiva de un compuesto de fórmula I o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato farmacéuticamente aceptable, cocristal, clatrato o polimorfo del mismo.
En algunas realizaciones, los procedimientos comprenden el tratamiento, prevención o control de la leucemia aguda en un sujeto. En algunas realizaciones, la leucemia aguda es leucemia mieloide aguda (LMA), que incluye, pero no se limita a, LMA indiferenciada (M0), leucemia mieloblástica (M1), leucemia mieloblástica (M2), leucemia promielocítica (M3 o variante M3 [M3V]), leucemia mielomonocítica (M4 o variante M4 con eosinofilia [M4E]), leucemia monocítica (M5), eritroleucemia (M6 ) y leucemia megacarioblástica (M7). En una realización, la leucemia mieloide aguda es LMA no diferenciada (M0). En una realización, la leucemia mieloide aguda es leucemia mieloblástica (M1). En una realización, la leucemia mieloide aguda es leucemia mieloblástica (M2). En una realización, la leucemia mieloide aguda es leucemia promielocítica (M3 o variante M3 (M3V)). En una realización, la leucemia mieloide aguda es leucemia mielomonocítica (M4 o variante M4 con eosinofilia (M4E)). En una realización, la leucemia mieloide aguda es leucemia monocítica (M5). En una realización, la leucemia mieloide aguda es eritroleucemia (M6 ). En una realización, la leucemia mieloide aguda es leucemia megacarioblástica (M7). Por lo tanto, en algunas realizaciones, los procedimientos para tratar, prevenir o controlar la leucemia mieloide aguda en un sujeto comprenden la etapa de administrar al sujeto una cantidad de un compuesto proporcionado en la presente memoria o un enantiómero o una mezcla de enantiómeros del mismo, o una sal farmacéuticamente aceptable, solvato, hidrato, cocristal, clatrato o polimorfo del mismo efectiva para tratar, prevenir o controlar la leucemia mieloide aguda sola o en combinación. En algunas realizaciones, los procedimientos comprenden la etapa de administrar al sujeto un compuesto proporcionado en la presente memoria o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo en combinación con un segundo agente activo en cantidades efectivas para tratar, prevenir o controlar la leucemia mieloide aguda.
En algunas realizaciones, los procedimientos comprenden el tratamiento, prevención o control de la leucemia linfocítica aguda (LLA) en un sujeto. En algunas realizaciones, la leucemia linfocítica aguda incluye la leucemia que se origina en los blastos de la médula ósea (linfocitos B), el timo (linfocitos T) y los ganglios linfáticos. La leucemia linfocítica aguda se puede clasificar según el Esquema de Clasificación Morfológica Francés-Americano-Británico (FAB) como L1 - linfoblastos de apariencia madura (linfocitos T o pre-linfocitos B), L2 - linfoblastos inmaduros y pleomórficos (con varias formas) (linfocitos T o pre-linfocitos B) y L3 - linfoblastos (linfocitos B; células de Burkitt). En una realización, la leucemia linfocítica aguda se origina en los blastos de la médula ósea (linfocitos B). En una realización, la leucemia linfocítica aguda se origina en el timo (linfocitos T). En una realización, la leucemia linfocítica aguda se origina en los ganglios linfáticos. En una realización, la leucemia linfocítica aguda es de tipo L1, caracterizada por linfoblastos de apariencia madura (linfocitos T o pre-linfocitos B). En una realización, la leucemia linfocítica aguda es de tipo L2,
caracterizada por linfoblastos inmaduros y pleomórficos (con varias formas) (linfocitos T o pre-linfocitos B). En una realización, la leucemia linfocítica aguda es de tipo L3, caracterizada por linfoblastos (linfocitos B; células de Burkitt). En ciertas realizaciones, la leucemia linfocítica aguda es leucemia de linfocitos T. En una realización, la leucemia de linfocitos T es leucemia de linfocitos T periféricos. En otra realización, la leucemia de linfocitos T es leucemia linfoblástica de linfocitos T. En otra realización, la leucemia de linfocitos T es leucemia de linfocitos T cutáneos. En otra realización, la leucemia de linfocitos T es leucemia de linfocitos T adultos. Por lo tanto, en algunas realizaciones, los procedimientos para tratar, prevenir o controlar la leucemia mieloide aguda en un sujeto comprenden la etapa de administrar al sujeto una cantidad de un compuesto proporcionado en la presente memoria o un enantiómero o una mezcla de enantiómeros del mismo, o una sal farmacéuticamente aceptable, solvato, hidrato, cocristal, clatrato o polimorfo del mismo efectiva para tratar, prevenir o controlar la leucemia mieloide aguda sola o en combinación. En algunas realizaciones, los procedimientos comprenden la etapa de administrar al sujeto un compuesto proporcionado en la presente memoria o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo en combinación con un segundo agente activo en cantidades efectivas para tratar, prevenir o controlar la leucemia mieloide aguda.
En algunas realizaciones, los procedimientos comprenden el tratamiento, la prevención o el control de la leucemia mielógena crónica (LMC) en un sujeto. En algunas realizaciones, los procedimientos comprenden la etapa de administrar al sujeto una cantidad de un compuesto proporcionado en la presente memoria o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo en cantidades efectivas para tratar, prevenir o controlar la leucemia mieloide aguda. En algunas realizaciones, los procedimientos comprenden la etapa de administrar al sujeto un compuesto proporcionado en la presente memoria o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo en combinación con un segundo agente activo en cantidades efectivas para tratar, prevenir o controlar la leucemia mieloide crónica.
En algunas realizaciones, los procedimientos comprenden el tratamiento, la prevención o el control de la leucemia mielógena crónica (LMC) en un sujeto. En algunas realizaciones, los procedimientos comprenden la etapa de administrar al sujeto una cantidad de un compuesto proporcionado en la presente memoria o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo en cantidades efectivas para tratar, prevenir o controlar la leucemia linfocítica crónica. En algunas realizaciones, los procedimientos comprenden la etapa de administrar al sujeto un compuesto proporcionado en la presente memoria o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo en combinación con un segundo agente activo en cantidades efectivas para tratar, prevenir o controlar la leucemia linfocítica crónica.
En ciertas realizaciones, en la presente memoria se proporcionan compuestos o composiciones de la invención para su uso en procedimientos de tratamiento, prevención y/o control de enfermedades en pacientes con deterioro de la función renal. En ciertas realizaciones, en la presente memoria se proporcionan compuestos o composiciones de la invención para su uso en un procedimiento de tratamiento, prevención y/o control del cáncer en pacientes con deterioro de la función renal. En ciertas realizaciones, en la presente memoria se proporcionan compuestos o composiciones para su uso en métodos para proporcionar ajustes de dosis adecuados para pacientes con deterioro de la función renal debido a, pero sin limitarse a, enfermedad, envejecimiento u otros factores del paciente.
En ciertas realizaciones, en la presente memoria se proporcionan compuestos o composiciones de la invención para su uso en procedimientos de tratamiento, prevención y/o control de linfoma, incluido el linfoma no hodgkiniano. En algunas realizaciones, en la presente memoria se proporcionan compuestos o composiciones de la invención para su uso en procedimientos para el tratamiento o el control de linfoma no hodgkiniano (LNH) que incluye, pero no se limita a, linfoma difuso de linfocitos B grandes (LDLBG), mediante el uso de factores de pronóstico.
En ciertas realizaciones, en la presente memoria se proporcionan compuestos o composiciones de la invención para su uso en procedimientos de tratamiento, prevención y/o control de mieloma múltiple, lo que incluye mieloma múltiple recidivante/refractario en pacientes con deterioro de la función renal o un síntoma del mismo donde los procedimientos comprenden administrar una cantidad terapéuticamente efectiva del compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, estereoisómero, tautómero o mezclas racémicas farmacéuticamente aceptables del mismo a un paciente con mieloma múltiple recidivante/refractario con deterioro de la función renal
En ciertas realizaciones, una cantidad terapéutica o profilácticamente efectiva del compuesto es de aproximadamente 0,005 a aproximadamente 1.000 mg al día, de aproximadamente 0,01 a aproximadamente 500 mg al día, de aproximadamente 0,01 a aproximadamente 250 mg al día, de aproximadamente 0,01 a aproximadamente 100 mg al día, de aproximadamente 0,1 a aproximadamente 100 mg al día, de aproximadamente 0,5 a aproximadamente 100
mg al día, de aproximadamente 1 a aproximadamente 100 mg al día, de aproximadamente 0 ,01 a aproximadamente 50 mg al día, de aproximadamente 0,1 a aproximadamente 50 mg al día, de aproximadamente 0,5 a aproximadamente 50 mg al día, de aproximadamente 1 a aproximadamente 50 mg al día, de aproximadamente 0,02 a aproximadamente 25 mg al día, de aproximadamente 0,05 a aproximadamente 10 mg al día, de aproximadamente 0,05 a aproximadamente 5 mg al día, de aproximadamente 0,1 a aproximadamente 5 mg al día o de aproximadamente 0,5 a aproximadamente 5 mg al día.
En ciertas realizaciones, la cantidad terapéuticamente o profilácticamente eficaz es de aproximadamente 0,1, de aproximadamente 0,2, de aproximadamente 0,5, de aproximadamente 1, de aproximadamente 2, de aproximadamente 3, de aproximadamente 4, de aproximadamente 5, de aproximadamente 6 , de aproximadamente 7, de aproximadamente 8 , de aproximadamente 9, de aproximadamente 10, de aproximadamente 15, de aproximadamente 20, de aproximadamente 25, de aproximadamente 30, de aproximadamente 40, de aproximadamente 45, de aproximadamente 50, de aproximadamente 60, de aproximadamente 70, de aproximadamente 80, de aproximadamente 90, de aproximadamente 100, o de aproximadamente 150 mg al día. En algunas de dichas modalidades, la cantidad terapéuticamente o profilácticamente eficaz es de aproximadamente 2, alrededor de 3, de aproximadamente 4, de aproximadamente 5, de aproximadamente 6 o de aproximadamente 7 mg al día.
En una realización, el intervalo de dosis diaria recomendada del compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, para las condiciones descritas en la presente memoria se encuentra dentro del intervalo de aproximadamente 0,5 mg a aproximadamente 50 mg al día, preferentemente administrado como una dosis única una vez al día, o en dosis divididas a lo largo de un día. En algunas realizaciones, la dosis varía entre aproximadamente 1 mg y aproximadamente 50 mg al día. En otras realizaciones, la dosis varía entre aproximadamente 0,5 y aproximadamente 5 mg al día. Las dosis específicas por día incluyen 0,1, 0,2, 0,5, 1, 2, 3, 4, 5, 6 , 7, 8 , 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 4 4 , 4 5 , 46, 47, 48, 49 o 50 mg al día.
En una realización específica, la dosis inicial recomendada puede ser de 0,5, 1, 2, 3, 4, 5, 10, 15, 20, 25 o 50 mg al día. En otra realización, la dosis inicial recomendada puede ser de 0,5, 1, 2, 3, 4 o 5 mg al día. La dosis se puede aumentar a 15, 20, 25, 30, 35, 40, 45 y 50 mg/día. En una realización específica, una forma sólida del compuesto se puede administrar en una cantidad de alrededor 25 mg/día a pacientes con leucemia, que incluye LMA. En una realización en particular, una forma sólida del compuesto se puede administrar en una cantidad de aproximadamente 10 mg/día a pacientes con leucemia, que incluye LMA. En una realización en particular, el compuesto se puede administrar en una cantidad de aproximadamente 5 mg/día a pacientes con leucemia, que incluye LMA. En una realización en particular, el compuesto se puede administrar en una cantidad de aproximadamente 4 mg/día a pacientes con leucemia, que incluye LMA. En una realización en particular, el compuesto se puede administrar en una cantidad de aproximadamente 3 mg/día a pacientes con leucemia, que incluye LMA.
En ciertas realizaciones, la cantidad terapéutica o profilácticamente efectiva es de aproximadamente 0,001 a aproximadamente 100 mg/kg/día, de aproximadamente 0,01 a aproximadamente 50 mg/kg/día, de aproximadamente 0,01 a aproximadamente 25 mg/kg/día, de aproximadamente 0,01 a aproximadamente 10 mg/kg/día, de aproximadamente 0,01 a aproximadamente 9 mg/kg/día, de 0,01 a aproximadamente 8 mg/kg/día, de aproximadamente 0,01 a aproximadamente 7 mg/kg/día, de aproximadamente 0,01 a aproximadamente 6 mg/kg/día, de aproximadamente 0,01 a aproximadamente 5 mg/kg/día, de aproximadamente 0,01 a aproximadamente 4 mg/kg/día, de aproximadamente 0,01 a aproximadamente 3 mg/kg/día, de aproximadamente 0,01 a aproximadamente 2 mg/kg/día, de aproximadamente 0 ,01 a aproximadamente 1 mg/kg/día, o de aproximadamente 0 ,01 a aproximadamente 0,05 mg/kg/día.
La dosis administrada también se puede expresar en unidades diferentes a mg/kg/día. Por ejemplo, las dosis para administración parenteral se pueden expresar como mg/m2/día. Un experto en la materia sabría cómo convertir las dosis de mg/kg/día a mg/m2/día para proporcionar la altura o el peso de un sujeto o ambos (véase www.fda.gov/cder/cancer/animalframe.htm). Por ejemplo, una dosis de 1 mg/kg/día para un ser humano de 65 kg equivale aproximadamente a 38 mg/m2/día.
En ciertas realizaciones, la cantidad del compuesto administrado es suficiente para proporcionar una concentración plasmática del compuesto en estado estacionario, que varía de aproximadamente 0,001 a aproximadamente 500 pM, de aproximadamente 0,002 a aproximadamente 200 pM, de aproximadamente 0,005 a aproximadamente 100 pM, de aproximadamente 0,01 a aproximadamente 50 pM, de aproximadamente 1 a aproximadamente 50 pM, de aproximadamente 0,02 a aproximadamente 25 pM, de aproximadamente 0,05 a aproximadamente 20 pM, de aproximadamente 0,1 a aproximadamente 20 pM, de aproximadamente 0,5 a aproximadamente 20 pM o de
aproximadamente 1 a aproximadamente 20 pM.
En otras realizaciones, la cantidad de un compuesto administrada es suficiente para proporcionar una concentración en plasma del compuesto en estado estacionario, que varía de aproximadamente 5 a aproximadamente 100 nM, de aproximadamente 5 a aproximadamente 50 nM, de aproximadamente 10 a aproximadamente 100 nM, de aproximadamente 10 a aproximadamente 50 nM o de aproximadamente 50 a aproximadamente 100 nM.
Tal como se usa en la presente memoria, el término "concentración plasmática en estado estacionario" es la concentración alcanzada después de un período de administración de un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo. Una vez que se alcanza el estado estacionario, hay pequeños picos y depresiones en la curva en función del tiempo de la concentración en plasma del compuesto.
En ciertas realizaciones, la cantidad del compuesto administrado es suficiente para proporcionar una concentración plasmática máxima (concentración pico) del compuesto que varía de aproximadamente 0,001 a aproximadamente 500 pM, de aproximadamente 0,002 a aproximadamente 200 pM, de aproximadamente 0,005 a aproximadamente 100 pM, de aproximadamente 0,01 a aproximadamente 50 pM, de aproximadamente 1 a aproximadamente 50 pM, de aproximadamente 0,02 a aproximadamente 25 pM, de aproximadamente 0,05 a aproximadamente 20 pM, de aproximadamente 0 ,1 a aproximadamente 20 pM, de aproximadamente 0,5 a aproximadamente 20 pM o de aproximadamente 1 a aproximadamente 20 pM.
En ciertas realizaciones, la cantidad del compuesto administrado es suficiente para proporcionar una concentración plasmática mínima (concentración valle) del compuesto que varía de aproximadamente 0,001 a aproximadamente 500 pM, de aproximadamente 0,002 a aproximadamente 200 pM, de aproximadamente 0,005 a aproximadamente 100 pM, de aproximadamente 0,01 a aproximadamente 50 pM, de aproximadamente 1 a aproximadamente 50 pM, de aproximadamente 0,01 a aproximadamente 25 pM, de aproximadamente 0,01 a aproximadamente 20 pM, de aproximadamente 0,02 a aproximadamente 20 pM, de aproximadamente 0,02 a aproximadamente 20 pM o de aproximadamente 0,011 a aproximadamente 20 pM.
En ciertas realizaciones, la cantidad del compuesto administrada es suficiente para proporcionar un área bajo la curva (AUC) del compuesto en un intervalo de aproximadamente 100 a aproximadamente 100.000 ng*h/mL, de aproximadamente 1.000 a aproximadamente 50.000 ng*h/mL, de aproximadamente 5.000 a aproximadamente 25.000 ng*h/mL o de aproximadamente 5.000 a aproximadamente 10.000 ng*h/mL.
En ciertas realizaciones, el paciente para tratar no ha sido tratado con terapia anticancerosa antes de la administración del compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato farmacéuticamente aceptable, cocristal, clatrato o polimorfo del mismo. En ciertas realizaciones, el paciente para tratar ha sido tratado con terapia anticancerosa antes de la administración del compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal farmacéuticamente aceptable. clatrato o polimorfo del mismo. En ciertas realizaciones, el paciente para tratar ha desarrollado resistencia a los medicamentos para la terapia contra el cáncer.
En ciertas realizaciones, los procedimientos comprenden el tratamiento de un paciente independientemente de la edad del paciente, aunque algunas enfermedades o trastornos son más comunes en ciertos grupos de edad.
Dependiendo de la enfermedad para tratar y de la condición del sujeto, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo; o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, puede administrarse por vías de administración oral, parenteral (por ejemplo, intramuscular, intraperitoneal, intravenosa, IVC, inyección o infusión intracistemal, inyección subcutánea o implante), inhalación, nasal, vaginal, rectal, sublingual o tópica (por ejemplo, transdérmica o local). El compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo; o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo se puede formular, solo o en conjunto, en una unidad de dosificación adecuada con excipientes, soportes, adyuvantes y vehículos farmacéuticamente aceptables que sea adecuada para cada vía de administración.
En una realización, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo; o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra por vía oral. En otra realización, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo; o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra por vía parenteral. En otra realización más, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del
mismo; o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra por vía intravenosa.
El compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo; o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, puede administrarse como una dosis única tal como, por ejemplo, una inyección de bolo simple, o comprimidos o píldoras orales; o con el tiempo, tal como, por ejemplo, infusión continua a lo largo del tiempo o dosis de bolo divididas a lo largo del tiempo. El compuesto se puede administrar de forma repetida, si fuera necesario, por ejemplo, hasta que el paciente experimente la regresión o estabilización de la enfermedad, o hasta que el paciente experimente la evolución de la enfermedad o una toxicidad inaceptable. Por ejemplo, en el caso de tumores sólidos, la enfermedad estable generalmente significa que el diámetro perpendicular de las lesiones mensurables no aumentó el 25 % o más respecto a la última medida. Response Evaluation Criteria in Solid Tumors (RECIST) Guidelines, Journal ofthe National Cancer Institute 92(3):205-216 (2000). Se determina la estabilidad de la enfermedad o la ausencia de esta mediante procedimientos conocidos en la técnica, tales como la evaluación de los síntomas de un paciente, una exploración física, la visualización del tumor mediante rayos X, TAC, PET o RM, y otras modalidades de evaluación comúnmente aceptadas.
El compuesto de fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo; o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, puede administrarse una vez al día (QD), o dividirse en múltiples dosis diarias como dos veces al día (BID), tres veces al día (TID) y cuatro veces al día (QID). Además, la administración puede ser continua (es decir, diariamente durante días consecutivos o todos los días), intermitente, por ejemplo, en ciclos (es decir, que incluye días, semanas o meses de descanso sin fármacos). Tal como se usa en la presente memoria, el término "diario" pretende significar que un compuesto terapéutico, tal como el compuesto de Fórmula I, se administra una o más de una vez al día, por ejemplo, durante un período de tiempo. El término "continuo" pretende significar que un compuesto terapéutico, como el compuesto de Fórmula I, se administra diariamente durante un período ininterrumpido de al menos 10 días a 52 semanas. El término "intermitente" o "intermitentemente" tal como se usa en la presente memoria pretende significar detenerse y comenzar a intervalos regulares o irregulares. Por ejemplo, la administración intermitente de la forma sólida del compuesto de Fórmula I es la administración durante uno a seis días por semana, administración en ciclos (por ejemplo, la administración diaria durante dos a ocho semanas consecutivas, después de un período de descanso sin administración durante hasta una semana) o administración en días alternos. El término "cíclico" tal como se usa en la presente memoria pretende significar que un compuesto terapéutico, tal como el compuesto de Fórmula I, se administra diariamente o continuamente pero con un período de descanso. En algunas de dichas realizaciones, la administración es una vez al día durante dos a seis días, después un período de descanso sin administración durante cinco a siete días.
En algunas modalidades, la frecuencia de administración se encuentra en el intervalo de aproximadamente una dosis diaria a aproximadamente una dosis mensual. En ciertas realizaciones, la administración es una vez al día, dos veces al día, tres veces al día, cuatro veces al día, una vez cada dos días, dos veces por semana, una vez por semana, una vez cada dos semanas, una vez cada tres semanas o una vez cada cuatro semanas. En una realización, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo; o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra una vez al día. En otra realización, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo; o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra dos veces al día. En otra realización más, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo; o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra tres veces al día. En otra realización más, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo; o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra cuatro veces al día.
En ciertas realizaciones, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo; o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra una vez al día de un día a seis meses, de una semana a tres meses, de una semana a cuatro semanas, de una semana a tres semanas o de una semana a dos semanas. En ciertas realizaciones, el compuesto de Fórmula I, o una sal o solvato farmacéuticamente aceptable del mismo, se administra una vez al día durante una semana, dos semanas, tres semanas o cuatro semanas. En una realización, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo; o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra una vez al día durante 4 días. En una realización, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo; o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra una vez al día durante 5 días. En una realización, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo; o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra una vez al día durante 6 días. En una realización, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo; o una sal, solvato, hidrato,
cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra una vez al día durante una semana. En una realización, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo; 0 una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra una vez al día durante dos semanas. En otra realización más, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo; o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra una vez al día durante tres semanas. En otra realización más, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo; o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra una vez al día durante cuatro semanas.
C-1. Terapia combinada con un segundo agente activo
El compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo; o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, también se puede combinar o usar en combinación con otros agentes terapéuticos útiles en el tratamiento y/o prevención del cáncer descritos en la presente memoria.
En una realización, en la presente memoria se proporciona un compuesto o una composición de la invención para su uso en un procedimiento de tratamiento, prevención o control del cáncer donde el procedimiento comprende administrar a un paciente un compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo; o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo; en combinación con uno o más segundos agentes activos, y opcionalmente en combinación con radioterapia, transfusiones de sangre o cirugía. En la presente memoria se describen agentes activos secundarios (véase, por ejemplo, la sección 5.4).
Tal como se usa en la presente memoria, el término "en combinación" incluye el uso de más de una terapia (por ejemplo, uno o más agentes profilácticos y/o terapéuticos). Sin embargo, el uso de la expresión “en combinación” no limita el orden en el cual se administran las terapias (por ejemplo, los agentes profilácticos y/o terapéuticos) a un paciente con una enfermedad o trastorno. Una primera terapia (por ejemplo, un agente profiláctico o terapéutico tal como un compuesto proporcionado en la presente memoria, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato farmacéuticamente aceptable, cocristal, clatrato o polimorfo del mismo) pueden administrarse antes de (por ejemplo, 5 minutos, 15 minutos, 30 minutos, 45 minutos, 1 hora, 2 horas, 4 horas, 6 horas, 12 horas, 24 horas, 48 horas, 72 horas, 96 horas, 1 semana, 2 semanas, 3 semanas, 4 semanas, 5 semanas, 6 semanas, 8 semanas o 12 semanas antes), simultáneamente con o después de (por ejemplo, 5 minutos, 15 minutos, 30 minutos, 45 minutos, 1 hora, 2 horas, 4 horas, 6 horas, 12 horas, 24 horas, 48 horas, 72 horas, 96 horas, 1 semana, 2 semanas, 3 semanas, 4 semanas, 5 semanas, 6 semanas, 8 semanas o 12 semanas después) la administración de una segunda terapia (por ejemplo, un agente profiláctico o terapéutico) al sujeto. También se contempla en la presente memoria la terapia triple.
La administración del compuesto de Fórmula I y uno o más segundos agentes activos a un paciente puede ocurrir de forma simultánea o en secuencia por las mismas o diferentes vías de administración. La adecuación de una vía de administración particular empleada para un agente activo en particular dependerá del agente activo en sí (por ejemplo, si este puede administrarse por vía oral sin descomponerse antes de entrar en el torrente sanguíneo) y del cáncer que se trate.
La vía de administración del compuesto de Fórmula I es independiente de la vía de administración de una segunda terapia. En una realización, el compuesto de Fórmula I se administra por vía oral. En otra realización, el compuesto de Fórmula I se administra por vía intravenosa. Por tanto, según estas modalidades, el compuesto de Fórmula I se administra en forma oral o intravenosa, y la segunda terapia se puede administrar en forma oral, parenteral, intraperitoneal, intravenosa, intraarterial, transdérmica, sublingual, intramuscular, rectal, transbucal, intranasal, liposómica, mediante inhalación, vaginal, intraocular, mediante administración local por un catéter o stent, en forma subcutánea, intraadiposa, intraarticular, intratecal o en una forma de dosificación de liberación lenta. En una realización, el compuesto de Fórmula I y una segunda terapia se administran mediante el mismo modo de administración, oral o i.v. En otra realización, el compuesto de Fórmula I se administra por un modo de administración, por ejemplo, i.v., mientras que el segundo agente (un agente anticanceroso) se administra por otro modo de administración, por ejemplo, por vía oral.
En una realización, el segundo agente activo se administra por vía intravenosa o subcutánea y una o dos veces al día en una cantidad de aproximadamente 1 a aproximadamente 1.000 mg, de aproximadamente 5 a aproximadamente 500 mg, de aproximadamente 10 a aproximadamente 350 mg o de aproximadamente 50 a aproximadamente 200 mg. La cantidad específica del segundo agente activo dependerá del agente específico usado, el tipo de enfermedad que se está tratando o controlando, la gravedad y el estadio de la enfermedad y la cantidad del compuesto de Fórmula I
proporcionado en la presente memoria y cualquier agente activo adicional opcional administrado simultáneamente al paciente.
Uno o más segundos ingredientes activos o agentes pueden usarse junto con el compuesto de fórmula I en los procedimientos y composiciones proporcionados en la presente memoria. Los agentes activos secundarios pueden ser moléculas grandes (por ejemplo, proteínas) o moléculas pequeñas (por ejemplo, moléculas orgánicas, organometálicas o inorgánicas sintéticas).
Los ejemplos de agentes activos de moléculas grandes incluyen, pero no se limitan a, factores de crecimiento hematopoyéticos, citocinas y anticuerpos monoclonales y policlonales, particularmente, anticuerpos terapéuticos para antígenos de cáncer. Los agentes activos de moléculas grandes típicos son moléculas biológicas, tales como proteínas de origen natural o sintéticas o recombinantes. Las proteínas particularmente útiles en los métodos y las composiciones que se proporcionan en la presente memoria incluyen proteínas que estimulan la supervivencia y/o proliferación de las células precursoras hematopoyéticas y las células poyéticas inmunológicamente activas in vitro o in vivo. Otras proteínas útiles estimulan la división y la diferenciación de progenitoras eritroides comprometidas en células in vitro o in vivo. Las proteínas particulares incluyen, pero no se limitan a: interleucinas, tales como IL-2 (que incluye IL-II recombinante (“rIL2”) e IL-2 canaripox), IL-10, IL-12 e IL-18; interferones, tales como interferón alfa-2a, interferón alfa-2b, interferón alfa-n1, interferón alfa-n3, interferón beta-I a e interferón gamma-I b; GM-CF y GM-CSF; y EPO.
En ciertas realizaciones, GM-CSF, G-CSF, SCF o EPO se administra por vía subcutánea durante aproximadamente cinco días en un ciclo de cuatro o seis semanas en una cantidad que varía de aproximadamente 1 a aproximadamente 750 mg/m2/día, de aproximadamente 25 a aproximadamente 500 mg/m2/día, de aproximadamente 50 a aproximadamente 250 mg/m2/día o de aproximadamente 50 a aproximadamente 200 mg/m2/día. En ciertas realizaciones, GM-CSF puede administrarse en una cantidad de aproximadamente 60 a aproximadamente 500 mcg/m2 por vía intravenosa en 2 horas o de aproximadamente 5 a aproximadamente 12 mcg/m2/día por vía subcutánea. En ciertas realizaciones, se puede administrar G-CSF por vía subcutánea inicialmente en una cantidad de alrededor de 1 mcg/kg/día y se puede ajustar dependiendo del aumento del recuento de granulocitos totales. La dosis de mantenimiento de G-CSF se puede administrar en una cantidad de aproximadamente 300 mcg (en pacientes más pequeños) o 480 mcg de forma subcutánea. En ciertas realizaciones, se puede administrar EPO por vía subcutánea en una cantidad de 10.000 unidades 3 veces por semana.
Las proteínas particulares que pueden usarse en los procedimientos y las composiciones incluyen, pero no se limitan a: filgrastim, que se comercializa en los Estados Unidos con el nombre comercial Neupogen® (Amgen, Thousand Oaks, CA); sargramostim, que se comercializa en los Estados Unidos con el nombre comercial Leukine® (Immunex, Seattle, WA); y EPO recombinante, que se comercializa en los Estados Unidos con el nombre comercial Epogen® (Amgen, Thousand Oaks, CA).
Las formas recombinantes y mutadas de GM-CSF pueden prepararse tal como se describe en las patentes de EE.UU. n° 5.391.485; 5.393.870; y 5.229.496. Las formas recombinantes y mutadas de G-CSF se pueden preparar tal como se describe en las patentes de EE.UU. n° 4.810.643; 4.999.291; 5.528.823; y 5.580.755.
También se proporciona para su uso en combinación un compuesto proporcionado en la presente memoria o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo nativos, de origen natural y proteínas recombinantes. Además, se encuentran comprendidos los mutantes y derivados (por ejemplo, formas modificadas) de las proteínas de origen natural que presentan, in vivo, al menos parte de la actividad farmacológica de las proteínas en las que se basan. Los ejemplos de mutantes incluyen, pero no se limitan a, proteínas que tienen uno o más residuos de aminoácidos que difieren de los residuos correspondientes en las formas de origen natural de las proteínas. El término "mutantes" también comprende proteínas que carecen de los restos carbohidrato normalmente presentes en sus formas de origen natural (por ejemplo, formas no glucosiladas). Los ejemplos de derivados incluyen, pero no se limitan a, derivados pegilados y proteínas de fusión, tal como proteínas formadas mediante la fusión de IgG1 o IgG3 a la proteína o parte activa de la proteína de interés. Véase, por ejemplo, Penichet, M. L. y Morrison, S. L., J. Immunol. Methods 248:91-101 (2001).
Los anticuerpos que pueden usarse en combinación con un compuesto proporcionado en la presente memoria o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo incluyen anticuerpos monoclonales y policlonales. Los ejemplos de anticuerpos incluyen, pero no se limitan a, trastuzumab (Herceptin®), rituximab (Rituxan®), bevacizumab (Avastin™), pertuzumab (Omnitarg™), tositumomab (Bexxar®), edrecolomab (Panorex®) y G250. Los compuestos proporcionados en la presente memoria o un enantiómero o una mezcla de enantiómeros de los mismos, o una sal, solvato, hidrato,
cocristal, clatrato o polimorfo farmacéuticamente aceptables de los mismos también se pueden combinar o usar en combinación con anticuerpos anti-TNF-a y/o anticuerpos anti-EGFR, tales como, por ejemplo, Erbitux® o panitumumab.
Los agentes activos de moléculas grandes se pueden administrar en forma de vacunas anticancerosas. Por ejemplo, las vacunas que secretan o causan la secreción de citocinas tales como IL-2, G-CSF y GM-CSF pueden usarse en los procedimientos y las composiciones farmacéuticas que se proporcionan. Véase, por ejemplo, Emens, L. A., y col., Curr. Opinion Mol. Ther. 3(1):77-84 (2001).
Los segundos agentes activos que son moléculas pequeñas también se pueden usar para aliviar los efectos adversos asociados con la administración de un compuesto proporcionado en la presente memoria o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal farmacéuticamente aceptable, clatrato o polimorfo del mismo. Sin embargo, al igual que algunas moléculas grandes, se cree que muchas son capaces de proporcionar un efecto sinérgico cuando se administran (por ejemplo, antes, después o simultáneamente) con un compuesto proporcionado en la presente memoria o un enantiómero o una mezcla de enantiómeros del mismo, o una sal farmacéuticamente aceptable, solvato, hidrato, cocristal, clatrato o polimorfo del mismo. Los ejemplos de los segundos agentes activos de moléculas pequeñas incluyen, pero no se limitan a, agentes anticancerosos, antibióticos, agentes inmunosupresores y esteroides.
En ciertas realizaciones, el agente secundario es un inhibidor de HSP, un inhibidor de proteasoma, un inhibidor de FLT3 o un inhibidor de la cinasa TOR.
Los ejemplos de agentes anticancerosos que pueden usarse dentro de los procedimientos o las composiciones que se describen en la presente memoria incluyen, pero no se limitan a, acivicina; aclarrubicina; clorhidrato de acodazol; acronina; adozelesina; aldesleucina; altretamina; ambomicina; acetato de ametantrón; amsacrina; anastrozol; antramicina; asparaginasa; asperlina; azacitidina; azetepa; azotomicina; batimastat; benzodepa; bicalutamida; clorhidrato de bisantreno; dimesilato de bisnafida; bizelesina; sulfato de bleomicina; brequinar sódico; bropirimina; busulfán; cactinomicina; calusterona; caracemida; carbetimer; carboplatino; carmustina; clorhidrato de carubicina; carzelesina; cedefingol; celecoxib (inhibidor de COX-2); clorambucilo; cirolemicina; cisplatino; cladribina; clofarabina; crisnatol mesilato; ciclofosfamida; Ara-C; dacarbacina; dactinomicina; clorhidrato de daunorrubicina; decitabina; dexormaplatina; dezaguanina; mesilato de dezaguanina; diacicuona; docetaxel; doxorrubicina; clorhidrato de doxorrubicina; droloxifeno; citrato de droloxifeno; propionato de dromostanolona; duazomicina; edatrexato; clorhidrato de eflornitina; elsamitrucina; enloplatina; enpromato; epipropidina; clorhidrato de epirrubicina; erbulozol; clorhidrato de esorrubicina; estramustina; fosfato de estramustina sódica; etanidazol; etopósido; fosfato de etopósido; etoprina; clorhidrato de fadrozol; fazarabina; fenretinida; floxuridina; fosfato de fludarabina; fluorouracilo; flurocitabina; fosquidona; fostriecina sódica; gemcitabina; clorhidrato de gemcitabina; hidroxiurea; clorhidrato de idarrubicina; ifosfamida; ilmofosina; iproplatina; irinotecán; clorhidrato de irinotecán; acetato de lanreótido; letrozol; acetato de leuprolida; clorhidrato de liarozol; lometrexol sódico; lomustina; clorhidrato de losoxantrona; masoprocol; maitansina; clorhidrato de mecloretamina; acetato de megestrol; acetato de melengestrol; melfalán; menogaril; mercaptopurina; metotrexato; metotrexato sódico; metoprina; meturedepa; mitindomida; mitocarcina; mitocromina; mitogillina; mitomalcina; mitomicina; mitosper; mitotano; clorhidrato de mitoxantrona; ácido micofenólico; nocodazol; nogalamicina; omacetaxina; ormaplatina; oxisurano; paclitaxel; pegaspargasa; peliomicina; pentamustina; sulfato de peplomicina; perfosfamida; pipobromán; piposulfán; clorhidrato de piroxantrona; plicamicina; plomestano; porfímero sódico; porfiromicina; prednimustina; clorhidrato de procarbacina; puromicina; clorhidrato de puromicina; pirazofurina; riboprina; safingol; clorhidrato de safingol; semustina; simtrazeno; sorafenib; sparfosato sódico; sparsomicina; clorhidrato de espirogermanio; espiromustina; espiroplatina; estreptonigrina; estreptozocina; sulofenur; talisomicina; tecogalán sódico; taxotere; tegafur; clorhidrato de teloxantrona; temoporfina; tenipósido; teroxirona; testolactona; tiamiprina; tioguanina; tiotepa; tiazofurina; tirapazamina; citrato de toremifeno; acetato de trestolona; fosfato de triciribina; trimetrexato; glucuronato de trimetrexato; triptorelina; clorhidrato detubulozol; mostaza de uracilo; uredepa; vapreotida; verteporfina; sulfato de vinblastina; sulfato de vincristina; vindesina; sulfato de vindesina; sulfato de vinepidina; sulfato de vinglicinato; sulfato de vinleurosina; tartrato de vinorelbina; sulfato de vinrosidina; sulfato de vinzolidina; vorozol; zeniplatina; cinostatina; y clorhidrato de zorubicina.
Otros medicamentos anticancerosos que se incluirán dentro de los usos o composiciones incluyen, pero no se limitan a: 20-epi-1,25 dihidroxivitamina D3; 5-etiniluracilo; abiraterona; aclarrubicina; acilfulveno; adecipenol; adozelesina; aldesleucina; antagonistas ALL-TK; altretamina; ambamustina; amidox; amifostina; ácido aminolevulínico; amrubicina; amsacrina; anagrelida; anastrozol; andrografólido; inhibidores de la angiogénesis; antagonista D; antagonista G; antarelix; proteína-1 morfogenética antidorsalización; antiandrógeno, carcinoma prostático; antiestrógeno; antineoplastón; oligonucleótidos antisentido; glicinato de afidicolina; moduladores de genes de la apoptosis; reguladores de la apoptosis; ácido apurínico; ara-CDP-DL-PTBA; arginina desaminasa; asulacrina; atamestano; atrimustina; axinastatina 1; axinastatina 2; axinastatina 3; azasetrón; azatoxina; azatirosina; derivados de bacatina III; balanol; batimastat; antagonistas de BCR/ABL; benzoclorinas; benzoilstaurosporina; derivados de beta lactama; betaaletina; betaclamicina B; ácido betulínico; inhibidor de bFGF, bicalutamida; bisantreno; bisaciridinilespermina; bisnafida; bistrateno A; bizelesina; breflato; bropirimina; budotitano; butionina sulfoximina; calcipotriol; calfostina C; derivados de la camptotecina; capecitabina; carboxamida-amino-triazol; carboxiamidotriazol; CaRest M3; CARN 700; inhibidor derivado de cartílago, carzelesina; inhibidores de la caseína cinasa (ICOS); castanoespermina; cecropina B; cetrorelix; clorinas; cloroquinoxalina sulfonamida; cicaprost; cis-porfirina; cladribina; análogos de clomifeno; clotrimazol; colismicina A; colismicina B; combretastatina A4; análogo de combretastatina; conagenina; crambescidina 816; crisnatol; criptoficina 8; derivados de la criptoficina A; curacina A; ciclopentantraquinonas; cicloplatam; cipemicina; Ara-C ocfosfato; factor citolítico; citostatina; dacliximab; decitabina; deshidrodidemnina B; deslorelina; dexametasona; dexifosfamida; dexrazoxano; dexverapamilo; diacicuona; didemnina B; didox; dietilnorespermina; dihidro-5-azacitidina; dihidrotaxol, 9-; dioxamicina; difenil espiromustina; docetaxel; docosanol; dolasetrón; doxifluridina; doxorrubicina; droloxifeno; dronabinol; duocarmicina SA; ebseleno; ecomustina; edelfosina; edrecolomab; eflornitina; elemeno; emitefur; epirrubicina; epristerida; análogo de estramustina; agonistas de estrógenos; antagonistas de estrógenos; etanidazol; fosfato de etopósido; exemestano; fadrozol; fazarabina; fenretinida; filgrastim; finasterida; flavopiridol; flezelastina; fluasterona; fludarabina; clorhidrato de fluorodaunorunicina; forfenimex; formestano; fostriecina; fotemustina; gadolinio texafirina; nitrato de galio; galocitabina; ganirelix; inhibidores de la gelatinasa; gemcitabina; inhibidores de la glutationa; hepsulfam; heregulina; hexametileno bisacetamida; hipericina; ácido ibandrónico; idarrubicina; idoxifeno; idramantona; ilmofosina; ilomastat; imatinib (por ejemplo, Gleevec®); imiquimod; péptidos inmunoestimulantes; inhibidor del receptor del factor de crecimiento insulinoide-1, agonistas de interferón; interferones; interleucinas; iobenguano; yododoxorrubicina; ipomeanol, 4-; iroplact; irsogladina; isobengazol; isohomohalicondrina B; itasetrón; jasplakinolida; kahalalida F; triacetato de lamelarina-N; lanreótido; leinamicina; lenograstim; sulfato de lentinano; leptolstatina; letrozol; factor de inhibición de la leucemia; interferón alfa leucocitario; leuprolida+estrógeno+progesterona; leuprorelina; levamisol; liarozol; análogo de poliamina lineal; péptido de disacáridos lipófilo; compuestos de platino lipófilos; lissoclinamida 7; lobaplatina; lombricina; lometrexol; lonidamina; losoxantrona; loxoribina; lurtotecán; lutecio texafirina; lisofilina; péptidos líticos; maitansina; mannostatina A; marimastat; masoprocol; maspina; inhibidores de la matrilisina; inhibidores de la metaloproteinasa de matriz; menogaril; merbarona; meterelina; metioninasa; metoclopramida; inhibidor MIF, mifepristona; miltefosina; mirimostim; mitoguazona; mitolactol; análogos de mitomicina; mitonafida; factor de crecimiento de fibroblastos de mitotoxinasaporina; mitoxantrona; mofaroteno; molgramostim; Erbitux, gonadotropina coriónica humana; pared celular de A+miobacteria lipídica de monofosforilo sk; mopidamol; agente anticanceroso de mostaza; micaperóxido B; extracto de pared celular de micobacterias; miriaporona; N-acetildinalina; benzamidas sustituidas en N; nafarelina; nagrestip; naloxona+pentazocina; napavina; nafterpina; nartograstim; nedaplatina; nemorrubicina; ácido neridrónico; nilutamida; nisamicina; moduladores del óxido nítrico; antioxidante de nitróxido; nitrulina; oblimerseno (Genasense®); O6-bencilguanina; octreótido; okicenona; oligonucleótidos; onapristona; ondansetrón; ondansetrón; oracina; inductor de citocinas oral; ormaplatino; osaterona; oxaliplatino; oxaunomicina; paclitaxel; análogos del paclitaxel; derivados del paclitaxel; palauamina; palmitoilrizoxina; ácido pamidrónico; panaxitriol; panomifeno; parabactina; pazeliptina; pegaspargasa; peldesina; polisulfato de pentosán sódico; pentostatina; pentrozol; perflubrón; perfosfamida; alcohol perilílico; fenacinomicina; fenilacetato; inhibidores de la fosfatasa; picibanilo; clorhidrato de pilocarpina; pirarrubicina; piritrexim; placetina A; placetina B; inhibidor del activador de plasminógeno, complejo de platino; compuestos de platino; complejo de platino-triamina; porfímero sódico; porfiromicina; prednisona; propil bis-acridona; prostaglandina J2; inhibidores del proteasoma; modulador inmunológico basado en la proteína A; inhibidor de la proteína cinasa C, inhibidores de la proteína cinasa C, microalgas; inhibidores de la tirosina fosfatasa proteínica; inhibidores de la purina nucleósido fosforilasa; purpurinas; pirazoloacridina; conjugado de polioxietileno de hemoglobina piridoxilado; antagonistas raf; raltitrexed; ramosetrón; inhibidores ras farnesil proteína transferasa; inhibidores ras; inhibidor ras-GAP, reteliptina desmetilada; etidronato de renio Re 186; rizoxina; ribozimas; retinamida RII; rohitucina; romurtida; roquinimex; rubiginona B1; ruboxilo; safingol; saintopina; SarCNU; sarcofitol A; sargramostim; miméticos de Sdi 1; semustina; inhibidor derivado de la senescencia 1; oligonucleótidos de sentido directo; inhibidores de transducción de la señal; sizofirano; sobuzoxana; borocaptato de sodio; fenilacetato de sodio; solverol; proteína de unión a somatomedina; sonermina; ácido esparfósico; espicamicina D; espiromustina; esplenopentina; espongistatina 1; escualamina; estipiamida; inhibidores de la estromielisina; sulfinosina; antagonista del péptido intestinal vasoactivo superactivo; suradista; suramina; swainsonina; talimustina; metyoduro de tamoxifeno; tauromustina; tazaroteno; tecogalan sódico; tegafur; telurapirilio; inhibidores de la telomerasa; temoporfina; tenipósido; tetraclorodecaóxido; tetrazomina; taliblastina; tiocoralina; trombopoyetina; mimético de la trombopoyetina; timalfasina; agonista de receptor de la timopoyetina; timotrinano; hormona estimulante del tiroides; etiopurpurina de etil-estaño; tirapazamina; bicloruro de titanoceno; topsentina; toremifeno; inhibidores de traducción; tretinoina; triacetiluridina; triciribina; trimetrexato; triptorelina; tropisetrón; turosterida; inhibidores de la tirosina cinasa; tirfostinas; inhibidores UBC; ubenimex; factor inhibidor del crecimiento derivado del seno urogenital, antagonistas del receptor de la urocinasa; vapreótido; variolina B; velaresol; veramina; verdinas; verteporfina; vinorelbina; vinxaltina; vitaxina; vorozol; zanoterona; zeniplatina; zilascorb; y estimalámero de cinostatina.
Los agentes activos secundarios específicos particularmente útiles en los procedimientos y las composiciones incluyen, pero no se limitan a, rituximab, oblimerseno (Genasense®), remicade, docetaxel, celecoxib, melfalán,
dexametasona (Decadron®), esteroides, gemcitabina, cisplatino, temozolomida, etopósido, ciclofosfamida, temodar, carboplatino, procarbacina, gliadel, tamoxifeno, topotecán, metotrexato, Arisa®, taxol, taxotero, fluorouracilo, leucovorina, irinotecán, xeloda, CPT-11, interferón alfa, interferón alfa pegilado (por ejemplo, PEG INTRON-A), capecitabina, cisplatino, tiotepa, fludarabina, carboplatino, daunorrubicina liposómica, Ara-C, doxetaxol, pacilitaxel, vinblastina, IL-2, GM-CSF, dacarbacina, vinorrelbina, ácido zoledrónico, palmitronato, biaxin, busulfán, prednisona, bisfosfonato, trióxido de arsénico, vincristina, doxorrubicina (Doxil®), paclitaxel, ganciclovir, adriamicina, fosfato sódico de estramustina (Emcyt®), sulindac y etopósido.
En ciertas realizaciones de los usos proporcionados en la presente memoria, el uso de un segundo agente activo en combinación con un compuesto proporcionado en la presente memoria o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato farmacéuticamente aceptable o polimorfo del mismo puede modificarse o retrasarse durante o poco después de la administración de un compuesto proporcionado en la presente memoria o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo que considere apropiado el profesional experto en la materia. En ciertas realizaciones, los sujetos que reciben un compuesto proporcionado en la presente memoria o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo solo o en combinación con otras terapias pueden recibir cuidado de soporte incluyendo antieméticos, factores de crecimiento mieloide y transfusiones de plaquetas, cuando sea apropiado. En algunas realizaciones, a los sujetos que se les administra un compuesto proporcionado en la presente memoria o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo se les puede administrar un factor de crecimiento como un segundo agente activo según el juicio del profesional experto en la materia. En algunas realizaciones, un compuesto proporcionado en la presente memoria o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo se administra en combinación con eritropoyetina o darbepoyetina (Aranesp).
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra con gemcitabina y cisplatino a pacientes con cáncer de vejiga de células de transición metastásico o localmente avanzado.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra en combinación con un segundo ingrediente activo de la siguiente manera: temozolomida a pacientes pediátricos con tumores cerebrales recurrentes o progresivos o neuroblastoma recurrente; celecoxib, etopósido y ciclofosfamida para el cáncer del SNC recurrente o progresivo; temodar a pacientes con meningioma recurrente o progresivo, meningioma maligno, hemangiopericitoma, metástasis cerebrales múltiples, tumores cerebrales recidivados o multiformes de glioblastoma recién diagnosticados; irinotecán a pacientes con glioblastoma recurrente; carboplatino a pacientes pediátricos con glioma del tronco encefálico; procarbacina a pacientes pediátricos con gliomas malignos progresivos; ciclofosfamida a pacientes con tumores cerebrales malignos de pronóstico infausto, glioblastoma multiforme de diagnóstico reciente o recurrente; Gliadel® para gliomas malignos recurrentes de alto grado; temozolomida y tamoxifeno para el astrocitoma anaplásico; o topotecán para gliomas, glioblastoma, astrocitoma anaplásico u oligodendroglioma anaplásico.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra con metotrexato, ciclofosfamida, taxano, abraxano, lapatinib, herceptina, inhibidores de la aromatasa, moduladores selectivos de estrógenos, antagonistas de los receptores de estrógenos y/o PLX3397 (Plexxikon) a pacientes con cáncer de mama metastásico.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo del mismo farmacéuticamente aceptable, se administra con temozolomida a pacientes con tumores neuroendocrinos.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra con gemcitabina y cisplatino a pacientes con cáncer de cabeza o cuello recurrente o metastásico.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo
farmacéuticamente aceptables del mismo, se administra con gemcitabina y cisplatino a pacientes con cáncer de páncreas.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra a pacientes con cáncer de colon en combinación con ARISA®, avastatina, taxol y/o taxotero.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra con capecitabina y/o PLX4032 (Plexxikon) a pacientes con cáncer colorrectal refractario o a pacientes que fracasan en la terapia de primera línea o tienen un bajo rendimiento en el adenocarcinoma de colon o rectal.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra en combinación con fluorouracilo, leucovorina e irinotecán a pacientes con cáncer colorrectal Dukes C y D o a pacientes que han sido tratados previamente por cáncer colorrectal metastásico.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra a pacientes con cáncer colorrectal refractario en combinación con capecitabina, xeloda y/o CPT-11.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra con capecitabina e irinotecán a pacientes con cáncer colorrectal refractario o a pacientes con carcinoma colorrectal no resecable o metastásico.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra solo o en combinación con interferón alfa o capecitabina a pacientes con carcinoma hepatocelular no resecable o metastásico; o con cisplatino y tiotepa a pacientes con cáncer de hígado primario o metastásico.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra en combinación con interferón alfa pegilado a pacientes con sarcoma de Kaposi.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra en combinación con fludarabina, carboplatino y/o topotecán a pacientes con leucemia mieloide aguda refractaria o recidivante o de alto riesgo.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra en combinación con daunorrubicina liposómica, topotecán y/o citarabina a pacientes con leucemia mieloblástica aguda de cariotipo desfavorable.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra en combinación con gemcitabina, abraxano, erlotinib, geftinib y/o irinotecán a pacientes con cáncer de pulmón no microcítico.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra con gemcitabina y cisplatino a pacientes con cáncer de pulmón no microcítico.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra con doxetaxol a pacientes con cáncer de pulmón no microcítico que han sido tratados previamente con carbo/VP 16 y radioterapia.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra en combinación con carboplatino y/o taxotero, o en combinación con carboplatino, pacilitaxel y/o radioterapia torácica a pacientes con cáncer de pulmón no microcítico. En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra en combinación con taxotero a pacientes con cáncer de pulmón no microcítico en estadio IIIB o IV.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra en combinación con oblimerseno (Genasense®) a pacientes con cáncer de pulmón microcítico.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra en combinación con ABT-737 (Abbott Laboratories) y/u obatoclax (GX15-070) a pacientes con linfoma y otros cánceres hematológicos.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra solo o en combinación con un segundo ingrediente activo, tal como vinblastina o fludarabina, a pacientes con varios tipos de linfoma, que incluyen, pero no se limitan a, linfoma de Hodgkin, linfoma no hodgkiniano, linfoma cutáneo de linfocitos T, linfoma cutáneo de linfocitos B, linfoma difuso de linfocitos B grandes o linfoma folicular recidivante o refractario de bajo grado.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra en combinación con taxotero, IL-2, IFN, GM-CSF, PLX4032 (Plexxikon) y/o dacarbacina a pacientes con diversos tipos o estadios de melanoma.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra solo o en combinación con vinorelbina a pacientes con mesotelioma maligno o cáncer de pulmón no microcítico en estadio IIIB con implantes pleurales o síndrome de mesotelioma de derrame pleural maligno.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra a pacientes con varios tipos o estadios de mieloma múltiple en combinación con dexametasona, ácido zoledrónico, palmitronato, GM-CSf , biaxina, vinblastina, melfalán, busulfano, ciclofosfamida, IFN, palmidronato, prednisona, bisfosfonato, celecoxib, trióxido de arsénico, trióxido de arsénico, PEG INTRON-A, vincristina, o una combinación de los mismos.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo del mismo farmacéuticamente aceptable, se administra a pacientes con mieloma múltiple recidivante o refractario en combinación con doxorrubicina (Doxil®), vincristina y/o dexametasona (Decadron®).
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra a pacientes con varios tipos o estadios de cáncer de ovario, como carcinoma peritoneal, carcinoma seroso papilar, cáncer de ovario refractario o cáncer de ovario recurrente, en combinación con taxol, carboplatino, doxorrubicina, gemcitabina, cisplatino, xeloda, paclitaxel, dexametasona o una combinación de los mismos.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra a pacientes con varios tipos o estadios de cáncer de próstata, en combinación con xeloda, 5 FU/LV, gemcitabina, irinotecán más gemcitabina, ciclofosfamida, vincristina, dexametasona, GM-CSF, celecoxib, taxotero, ganciclovir, paclitaxel, adriamicina, docetaxel, estramustina, Emcyt, denderon o una combinación de los mismos.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra a pacientes con varios tipos o estadios de cáncer de células renales, en combinación con capecitabina, IFN, tamoxifeno, IL-2, GM-CSF, Celebrex® o una combinación de los mismos.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra a pacientes con varios tipos o estadios de cáncer de sarcoma ginecológico, de útero o de tejidos blandos en combinación con IFN, un inhibidor de la COX-2 como Celebrex® y/o sulindaco.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra a pacientes con varios tipos o estadios de tumores sólidos en combinación con celebrex, etopósido, ciclofosfamida, docetaxel, apecitabina, IFN, tamoxifeno, IL-2, GM-CSF, o una combinación de los mismos.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra a pacientes con esclerodermia o vasculitis cutánea en combinación con celebrex, etopósido, ciclofosfamida, docetaxel, apecitabina, IFN, tamoxifeno, IL-2, GM-CSF o una combinación de los mismos.
También se incluye en la presente memoria un compuesto o una composición de la invención para su uso en un procedimiento para aumentar la dosificación de un fármaco o agente anticanceroso que puede administrarse de manera segura y eficaz aun paciente, donde el procedimiento comprende administrar al paciente (por ejemplo, un ser humano) o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo. Los pacientes que pueden beneficiarse de este procedimiento son aquellos que sufren un efecto adverso relacionado con fármacos anticancerosos para el tratamiento de un cáncer específico de piel, tejido subcutáneo, ganglios linfáticos, cerebro, pulmones, hígado, huesos, intestino, colon, corazón, páncreas, glándulas suprarrenales, riñón, próstata, mama, colorrectal o combinaciones de los mismos. La administración de un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, alivia o reduce efectos que son tan graves que de otro modo limitarían la cantidad de fármaco anticanceroso.
En una realización, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra por vía oral y de forma diaria en una cantidad que varía de aproximadamente 0,1 a aproximadamente 150 mg, de aproximadamente 1 a aproximadamente 50 mg o de aproximadamente 2 a aproximadamente 25 mg, antes, durante o después de la aparición del efecto adverso asociado con la administración de un fármaco anticanceroso a un paciente. En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra en combinación con agentes específicos como heparina, aspirina, cumarina o G-CSF para evitar los efectos adversos asociados con los fármacos anticancerosos, como por ejemplo, neutropenia o trombocitopenia.
En una realización, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra a pacientes con enfermedades y trastornos asociados o caracterizados por angiogénesis no deseada en combinación con ingredientes activos adicionales, que incluyen, pero no se limitan a, fármacos anticancerosos, antiinflamatorios, antihistamínicos, antibióticos y esteroides.
En otra realización, en la presente memoria se incluye un compuesto o una composición de la invención para su uso en un procedimiento de tratamiento, prevención y/o control del cáncer, donde el procedimiento comprende administrar el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, junto con (por ejemplo, antes, durante o después) la terapia convencional que incluye, pero no se limita a, cirugía, inmunoterapia, terapia biológica, radioterapia u otra terapia no farmacológica usada actualmente para tratar, prevenir o controlar el cáncer. El uso combinado del compuesto que se proporciona en la presente memoria y una terapia convencional puede proporcionar un régimen de tratamiento único que es inesperadamente eficaz en determinados pacientes. Sin pretender limitarse a la teoría, se cree que el compuesto de Fórmula I puede proporcionar efectos sinérgicos o aditivos cuando se administra simultáneamente con terapias convencionales.
Tal como se expone en otra parte en la presente memoria, se incluye en la presente memoria un compuesto o una composición de la invención para su uso en un procedimiento para reducir, tratar y/o prevenir efectos adversos o no deseados asociados con la terapia convencional que incluye, pero no se limita a, cirugía, quimioterapia, radioterapia, terapia hormonal, terapia biológica e inmunoterapia. Un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, y otro ingrediente activo se puede administrar a un paciente antes, durante o después de la aparición del efecto adverso asociado con la terapia convencional.
En una realización, el compuesto de Fórmula I puede administrarse en una cantidad que varía de aproximadamente 0. 1 a aproximadamente 150 mg, de aproximadamente 1 a aproximadamente 25 mg o de aproximadamente 2 a aproximadamente 10 mg por vía oral y de forma diaria solo, o en combinación con un segundo agente activo descrito en la presente memoria (véase, por ejemplo, la sección 5,4), antes, durante o después del uso de terapia convencional.
En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula 1, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra con doxetaxol a pacientes con cáncer de pulmón no microcítico que han sido tratados previamente con carbo/VP 16 y radioterapia.
C-2. Uso con terapia de trasplante
El compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, proporcionados en la presente memoria, pueden usarse para reducir el riesgo de enfermedad de injerto contra el huésped (EICH). Por lo tanto, en la presente memoria se incluye un compuesto o una composición de la invención para su uso en un procedimiento de tratamiento, prevención y/o control del cáncer, que comprende la administración del compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal aceptable, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, junto con la terapia de trasplante.
Como conocen los expertos en la materia, el tratamiento del cáncer se basa frecuentemente en los estadios y el mecanismo de la enfermedad. Por ejemplo, a medida que se desarrolla la transformación leucémica inevitable en ciertos estadios del cáncer, puede ser necesario el trasplante de células madre de sangre periférica, la preparación de células madre hematopoyéticas o de médula ósea. El uso combinado del compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, proporcionados en la presente memoria y la terapia de trasplante proporciona una sinergia única e inesperada. En particular, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, muestra actividad inmunomoduladora que puede proporcionar efectos aditivos o sinérgicos cuando se administra simultáneamente con terapia de trasplante en pacientes con cáncer.
El compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, puede actuar en combinación con la terapia de trasplante reduciendo las complicaciones asociadas con el procedimiento invasivo de trasplante y el riesgo de EICH. En la presente memoria se incluye un compuesto o una composición de la invención para su uso en un procedimiento de tratamiento, prevención y/o control del cáncer donde el procedimiento comprende administrar a un paciente (por ejemplo, un ser humano) el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, antes, durante o después del trasplante de sangre del cordón umbilical, sangre placentaria, células madre de sangre periférica, preparación de células madre hematopoyéticas o médula ósea. Algunos ejemplos de células madre
adecuadas para su uso en los procedimientos proporcionados en la presente memoria se describen en la patente de EE.UU. n° 7.498.171.
En una realización, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra a pacientes con mieloma múltiple. antes, durante o después del trasplante de células progenitoras de sangre periférica autólogas. En una realización, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra a pacientes con LNH (por ejemplo, LDLBG) antes, durante o después del trasplante de células progenitoras de sangre periférica autólogas.
C-3. Terapia de ciclado
En ciertas realizaciones, los agentes profilácticos o terapéuticos que se proporcionan en la presente memoria se administran de forma cíclica a un paciente. La terapia de ciclado implica la administración de un agente activo durante un período de tiempo, seguido de un descanso durante un período de tiempo y la repetición de esta administración secuencial. La terapia de ciclado puede reducir el desarrollo de la resistencia a una o más terapias, evitar o reducir los efectos secundarios de una o más terapias y/o mejorar la eficacia del tratamiento.
Por consiguiente, en ciertas realizaciones, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, proporcionados en la presente memoria se administra diariamente en dosis únicas o divididas en un ciclo de cuatro a seis semanas con un período de descanso de aproximadamente una semana o dos semanas. El procedimiento de ciclado permite además aumentar la frecuencia, cantidad y extensión de los ciclos de dosificación. Por lo tanto, en la presente memoria en ciertas realizaciones se comprende la administración de un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, durante más ciclos que los típicos cuando se administra en solitario. En ciertas realizaciones, un compuesto proporcionado en la presente memoria, por ejemplo, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra durante un mayor número de ciclos que los que normalmente causarían toxicidad limitativa de la dosis en un paciente al que no se le está administrando además un segundo ingrediente activo.
En una realización, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, se administra de forma diaria y continua durante tres o cuatro semanas a una dosis de aproximadamente 0,1 a aproximadamente 150 mg/día seguido de un descanso de una o dos semanas.
En otra realización, el compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, y un segundo ingrediente activo, se administran por vía oral con la administración del compuesto de Fórmula I 30 a 60 minutos antes de un segundo ingrediente activo, durante un ciclo de cuatro a seis semanas. En ciertas realizaciones, la combinación del compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, y un segundo ingrediente activo se administran por infusión intravenosa durante aproximadamente 90 minutos en cada ciclo. En ciertas realizaciones, un ciclo comprende la administración de aproximadamente 0,1 a aproximadamente 150 mg/día del compuesto de Fórmula I, o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato farmacéuticamente aceptable, o polimorfo del mismo, y de aproximadamente 50 a aproximadamente 200 mg/m2/día de un segundo ingrediente activo diariamente durante tres a cuatro semanas y después una o dos semanas de descanso. En ciertas realizaciones, el número de ciclos durante los cuales se administra el tratamiento de combinación a un paciente varía de aproximadamente uno a aproximadamente 24 ciclos, de aproximadamente dos a aproximadamente 16 ciclos, o de aproximadamente cuatro a aproximadamente tres ciclos.
D. Población de pacientes
En ciertas realizaciones, el sujeto es un animal, preferentemente un mamífero, más preferentemente un primate no humano. En algunas realizaciones, el sujeto es un ser humano. El sujeto puede ser de sexo masculino o femenino. Los sujetos especialmente útiles para los procedimientos que se proporcionan en la presente memoria incluyen pacientes humanos con cáncer, por ejemplo, a los que se les ha diagnosticado leucemia, que incluye leucemia mieloide
aguda, leucemia linfocítica aguda, leucemia mielógena crónica y leucemia mielógena crónica. En ciertas realizaciones, al sujeto no se le ha diagnosticado leucemia promielocítica aguda.
En algunas modalidades, el sujeto tiene una población de blastos mayor de lo normal. En algunas realizaciones, el sujeto tiene una población de blastos de al menos el 10 %. En algunas realizaciones, el sujeto tiene una población de blastos de entre el 10 y el 15 %. En algunas realizaciones, el sujeto tiene una población de blastos de al menos el 15 %. En algunas modalidades, el sujeto tiene una población de blastos de entre el 15 y el 20%. En algunas realizaciones, el sujeto tiene una población de blastos de al menos el 20%. En algunas realizaciones, el sujeto tiene una población de blastos de aproximadamente el 10-15 %, aproximadamente el 15-20 % o aproximadamente el 20-25 %. En algunas realizaciones, el sujeto tiene una población de blastos menor del 10 %. En el contexto de los procedimientos que se describen en la presente memoria, los sujetos útiles que tienen una población de blastos menor que el 10 % incluyen los sujetos que, por cualquier motivo según el criterio del profesional experto en la materia, necesitan tratamiento con un compuesto que se proporciona en la presente memoria, solo o en combinación con un segundo agente activo.
En algunas realizaciones, el sujeto es tratado basándose en la puntuación del estado de rendimiento del sujeto del Eastern Cooperative Oncology Group (ECOG) en relación con la leucemia. El estado de rendimiento del ECOG se puede calificar en una escala de 0 a 5, donde 0 indica asintomático; 1 indica sintomático pero completamente ambulante; 2 indica sintomático y <50% en cama durante el día; 3 indica sintomático y >50 % en cama, pero no en cama permanentemente; 4 indica en cama permanentemente; y 5 indica muerte. En algunas realizaciones, el individuo presenta una puntuación del estado de rendimiento de ECOG de 0 o 1. En algunas realizaciones, el sujeto presenta una puntuación del estado de rendimiento de ECOG de 0. En algunas realizaciones, el sujeto presenta una puntuación del estado de rendimiento de ECOG de 1. En otras realizaciones, el sujeto presenta una puntuación del estado de rendimiento de ECOG de 2.
En ciertas realizaciones, los procedimientos comprenden el tratamiento de sujetos que no han sido tratados previamente para la leucemia. En algunas realizaciones, el sujeto no se ha sometido a trasplante de médula ósea alogénico. En algunas realizaciones, el sujeto no se ha sometido a un trasplante de células madre. En algunas realizaciones, el sujeto no ha recibido tratamiento con hidroxiurea. En algunas realizaciones, el sujeto no ha sido tratado con ningún producto de investigación para la leucemia. En algunas realizaciones, el sujeto no ha sido tratado con glucocorticoides sistémicos.
En otras realizaciones, los procedimientos comprenden tratar a sujetos que han sido tratados previamente o que se encuentran actualmente en tratamiento por leucemia. Por ejemplo, el sujeto puede haber sido tratado previamente o encontrarse actualmente sometido a un régimen de tratamiento estándar por leucemia. El sujeto puede haber sido tratado con cualquier régimen de tratamiento de leucemia estándar conocido por el profesional experto en la materia. En ciertas realizaciones, el sujeto ha sido tratado previamente con al menos un régimen de LMA de inducción/reinducción o consolidación. En algunas realizaciones, el sujeto se ha sometido a un trasplante autólogo de médula ósea o un trasplante de células madre como parte de un régimen de consolidación. En algunas realizaciones, el trasplante de células madre o médula ósea se produjo al menos 3 meses antes del tratamiento según los procedimientos que se proporcionan en la presente memoria. En algunas realizaciones, el sujeto se ha sometido a tratamiento con hidroxiurea. En algunas realizaciones, el tratamiento con hidroxiurea se produjo no más de 24 horas antes del tratamiento según los procedimientos que se proporcionan en la presente memoria. En algunas realizaciones, el sujeto se ha sometido a terapia de consolidación o inducción previa con citarabina (Ara-C). En algunas realizaciones, el sujeto se ha sometido a tratamiento con glucocorticoesteroides sistémicos. En algunas realizaciones, el tratamiento con glucocorticoesteroides sistémicos se produjo no más de 24 horas antes del tratamiento según los procedimientos que se describen en la presente memoria. En otras realizaciones, los procedimientos comprenden tratar a sujetos que han sido tratados previamente contra el cáncer, pero que no responden a terapias estándar.
También se incluyen compuestos o composiciones de la invención para su uso en procedimientos de tratamiento de sujetos que tienen leucemia recidivante o refractaria. En algunas realizaciones, al sujeto se le ha diagnosticado un subtipo de LMA recidivante o refractaria, tal como lo define la Organización Mundial de la Salud (OMS). La enfermedad recidivante o refractaria puede ser LMA de novo o LMA secundaria, por ejemplo, LMA relacionada con la terapia (LMA-t).
En algunas realizaciones, los compuestos o composiciones de la invención son para su uso en procedimientos para tratar leucemias resistentes a fármacos, tales como leucemia mielógena crónica (LMC). Por lo tanto, el tratamiento con el compuesto proporcionado en la presente memoria podría proporcionar una alternativa para pacientes que no responden a otros procedimientos de tratamiento. En algunas realizaciones, dichos procedimientos de tratamiento adicionales comprenden tratamiento con Gleevec® (mesilato de imatinib). En algunas realizaciones, en la presente memoria se proporcionan compuestos o composiciones de la invención para su uso en procedimientos de tratamiento de leucemia mielógena crónica positiva para cromosoma Filadelfia (LMC Ph+). En algunas realizaciones, en la
presente memoria se proporcionan procedimientos de tratamiento de leucemia mielógena crónica positiva para el cromosoma Filadelfia (LMC Ph+) resistente con Gleevec® (mesilato de imatinib).
También se incluyen compuestos o composiciones de la invención para su uso en procedimientos de tratamiento de un sujeto independientemente de la edad del sujeto, aunque algunas enfermedades o trastornos son más comunes en ciertos grupos de edad. En algunas realizaciones, el sujeto tiene al menos 18 años. En algunas realizaciones, el sujeto tiene más de 18, 25, 35, 40, 45, 50, 55, 60, 65 o 70 años. En otras realizaciones, el sujeto tiene menos de 65 años. En algunas realizaciones, el sujeto tiene menos de 18 años. En algunas realizaciones, el sujeto tiene menos de 18, 15, 12, 10, 9, 8 o 7 años.
En algunas realizaciones, los procedimientos pueden ser útiles en sujetos con al menos 50 años, si bien sujetos menores también se podrían beneficiar con el procedimiento. En otras realizaciones, los sujetos tienen al menos 55, al menos 60, al menos 65 y al menos 70 años de edad. En otra realización, los sujetos tienen citogenética adversa. “Citogenética adversa” se define como cualquier cariotipo no diploide, o mayor o igual a 3 anomalías cromosómicas. En otra realización, los sujetos tienen al menos 60 años y tienen citogenética adversa. En otra realización, los sujetos tienen 60-65 años y tienen citogenética adversa. En otra realización, los sujetos tienen 65-70 años y tienen citogenética adversa.
En ciertas realizaciones, el sujeto tratado no tiene antecedentes de infarto de miocardio dentro de los tres meses de tratamiento según los usos que se proporcionan en la presente memoria. En algunas realizaciones, el sujeto no tiene antecedentes de accidente cerebrovascular o ataque isquémico transitorio dentro de los tres meses de tratamiento según los usos que se proporcionan en la presente memoria. En algunas realizaciones, el sujeto no ha sufrido ningún evento tromboembólico, lo que incluye trombosis venosa profunda o embolia pulmonar, dentro de los 28 días de tratamiento según los usos que se proporcionan en la presente memoria. En otras realizaciones, el sujeto no ha experimentado o no está experimentando coagulación intravascular diseminada descontrolada.
Debido a que los sujetos con cáncer presentan manifestaciones clínicas heterogéneas y resultados clínicos variables, el tratamiento que se administra a un paciente puede variar dependiendo de su pronóstico. Los expertos en medicina podrán determinar fácilmente, sin experimentación innecesaria, los agentes secundarios específicos, los tipos de cirugía y los tipos de tratamiento estándar no farmacológico que se pueden usar de forma efectiva para tratar a un sujeto individual con cáncer.
Se observará que en la presente memoria se contemplan todas las combinaciones adecuadas de los compuestos que se proporcionan en la presente memoria con uno o más de los compuestos mencionados anteriormente y, opcionalmente, una o más sustancias farmacológicamente activas.
E. Formulación de composiciones farmacéuticas
Las composiciones farmacéuticas que se proporcionan en la presente memoria contienen cantidades terapéuticamente efectivas de uno o más de los compuestos que se proporcionan en la presente memoria y un soporte, diluyente o excipiente farmacéuticamente aceptable.
Los compuestos pueden formularse en preparaciones farmacéuticas adecuadas tales como soluciones, suspensiones, comprimidos, comprimidos dispersables, píldoras, cápsulas, polvos, formulaciones de liberación sostenida o elixires, para administración oral o en soluciones o suspensiones estériles para administración oftálmica o parenteral, así como preparación de parches transdérmicos e inhaladores de polvo seco. Normalmente, los compuestos descritos anteriormente se formulan en composiciones farmacéuticas usando técnicas y procedimientos bien conocidos en la técnica (véase, por ejemplo, Ansel Introduction to Pharmaceutical Dosage Forms, séptima edición 1999).
En las composiciones, las concentraciones efectivas de uno o más compuestos o sales farmacéuticamente aceptables se mezclan con un soporte o vehículo farmacéutico adecuado. En ciertas realizaciones, las concentraciones de los compuestos en las composiciones son efectivas para suministrar una cantidad, tras la administración, que trata, previene o mejora uno o más síntomas y/o la evolución del cáncer, que incluye tumores sólidos y tumores transmitidos por vía hematógena.
Normalmente, las composiciones se formulan para administración de una única dosificación. Para formular una composición, la fracción en peso del compuesto se disuelve, suspende, dispersa o mezcla de otra forma en un vehículo seleccionado a una concentración eficaz de forma tal que la afección tratada se mejore o se alivie. Los vehículos o soportes farmacéuticos adecuados para la administración de la forma sólida del compuesto que se proporciona en la presente memoria incluyen cualquiera de dichos soportes considerados adecuados por los expertos en la materia para el modo de administración en particular.
Además, los compuestos pueden formularse como el único ingrediente farmacéuticamente activo en la composición o pueden combinarse con otros ingredientes activos. Las suspensiones liposómicas, incluso liposomas dirigidos a tejidos, tales como liposomas dirigidos a tumores, también pueden ser adecuadas como soportes farmacéuticamente aceptables. Estos pueden prepararse según procedimientos conocidos por los expertos en la materia. Por ejemplo, las formulaciones de liposomas pueden prepararse como se conoce en la técnica. Brevemente, los liposomas tales como las vesículas multilaminares (VML) se pueden formar secando fosfatidilcolina de huevo y fosfatidilserina cerebral (fracción molar 7:3) en el interior de un matraz. Se agrega una solución del compuesto que se proporciona en la presente memoria en solución salina con tampón de fosfato que carece de cationes divalentes (PBS) y el matraz se agita hasta la dispersión de la película lipídica. Se lavan las vesículas resultantes para eliminar el compuesto no encapsulado, se sedimentan por centrifugación y a continuación se resuspenden en PBS.
El compuesto activo se incluye en el soporte farmacéuticamente aceptable en una cantidad suficiente para ejercer un efecto terapéuticamente útil en ausencia de efectos secundarios indeseables en el paciente tratado. La concentración terapéuticamente efectiva se puede determinar empíricamente probando los compuestos en los sistemas in vitro e in vivo descritos en la presente memoria y a continuación extrapolando a partir de los mismos las dosis para seres humanos.
La concentración del compuesto activo en la composición farmacéutica dependerá de las velocidades de absorción, distribución tisular, inactivación y excreción del compuesto activo, de las características fisicoquímicas del compuesto, del programa de dosificación y de la cantidad administrada, así como de otros factores conocidos por los expertos en la materia. Por ejemplo, la cantidad que se suministra es suficiente para mejorar uno o más de los síntomas del cáncer, que incluye tumores sólidos y tumores transmitidos por vía hematógena.
En ciertas realizaciones, una dosificación terapéuticamente eficaz debe producir una concentración de ingrediente activo en suero de aproximadamente 0,1 ng/mL a aproximadamente 50-100 pg/mL. En una realización, las composiciones farmacéuticas proporcionan una dosificación de aproximadamente 0,001 mg a aproximadamente 2.000 mg del compuesto por kilogramo de peso corporal al día. Se preparan formas de dosificación farmacéutica unitaria para proporcionar de aproximadamente 1 mg a aproximadamente 1.000 mg y, en ciertas realizaciones, de aproximadamente 10 a aproximadamente 500 mg del ingrediente activo esencial o una combinación de ingredientes esenciales por forma de dosificación unitaria.
El ingrediente activo puede administrarse de una vez, o puede dividirse en una cantidad de dosis más pequeñas que se administrarán en intervalos de tiempo. Debe entenderse que la dosificación precisa y la duración del tratamiento varían en función de la enfermedad que se trata y podrían determinarse de forma empírica mediante protocolos de evaluación conocidos o mediante extrapolación de datos de evaluaciones in vivo o in vitro. Debe observarse que también podrán variar las concentraciones y los valores de dosificación en función de la gravedad de la afección que se desea mejorar. Debe entenderse además que para cualquier sujeto en particular se deben ajustar las pautas de dosificación específicas en el transcurso del tiempo según la necesidad individual y el criterio profesional de la persona que administra o supervisa la administración de las composiciones, y que los intervalos de concentración que se establecen en la presente memoria se indican únicamente a modo de ejemplo y no se pretende que limiten el alcance o la puesta en práctica de las composiciones reivindicadas.
Por lo tanto, las concentraciones o cantidades efectivas de uno o más de los compuestos descritos en la presente memoria o las sales farmacéuticamente aceptables de los mismos se mezclan con un soporte o vehículo farmacéutico adecuado para administración sistémica, tópica o local con el fin de formar composiciones farmacéuticas. Los compuestos se incluyen en una cantidad efectiva para mejora de uno o más síntomas, o para tratamiento, retraso de la evolución o prevención. La concentración del compuesto activo en la composición dependerá de las velocidades de absorción, distribución en los tejidos, inactivación y excreción del compuesto activo, del programa de dosificación, de la cantidad administrada, de la formulación particular, así como de otros factores conocidos por los expertos en la materia.
Se pretende que las composiciones sean administradas por una vía adecuada, lo que incluye, pero no se limita a, vía oral, parenteral, rectal, tópica y local. Para la administración oral, se pueden formular cápsulas y comprimidos. Las composiciones están en forma líquida, semilíquida o sólida y están formuladas de manera adecuada para cada vía de administración.
Las soluciones o suspensiones usadas para aplicación parenteral, intradérmica, subcutánea o tópica pueden incluir cualquiera de los siguientes componentes: un diluyente estéril, tal como agua para inyección, solución salina, aceite fijo, polietilenglicol, glicerina, propilenglicol, dimetilacetamida u otro disolvente sintético; agentes antimicrobianos, tales como alcohol bencílico y metilparabenos; antioxidantes, tales como ácido ascórbico y bisulfito de sodio; agentes de
quelación, tales como ácido etilendiaminotetraacético (EDTA); tampones, tales como acetatos, citratos y fosfatos; y agentes para el ajuste de la tonicidad tales como cloruro de sodio o dextrosa. Las preparaciones parenterales pueden incluirse en ampollas, plumas, jeringas desechables o viales de dosis simples o múltiples hechos de vidrio, plástico u otro material adecuado.
En los casos en que los compuestos muestran una solubilidad insuficiente, pueden usarse procedimientos para solubilizar compuestos. Dichos procedimientos son conocidos para los expertos en la materia e incluyen, pero no se limitan a, el uso de codisolventes, tales como dimetilsulfóxido (DMSO), el uso de tensioactivos, tales como TWEEN®, o la disolución en bicarbonato de sodio acuoso.
Después de la mezcla o adición del o de los compuestos, la mezcla resultante puede ser una solución, suspensión, emulsión o similar. La forma de la mezcla resultante depende de una serie de factores, que incluyen el modo previsto de administración y la solubilidad del compuesto en el soporte o vehículo seleccionado. La concentración efectiva es suficiente para mejorar los síntomas de la enfermedad, trastorno o afección tratados y se puede determinar empíricamente.
Las composiciones farmacéuticas se proporcionan para administración a seres humanos y animales en formas de dosificación unitarias, tales como comprimidos, cápsulas, píldoras, polvos, gránulos, soluciones o suspensiones parenterales estériles y soluciones o suspensiones orales, y emulsiones de agua y aceite que contienen cantidades adecuadas. de los compuestos o sales farmacéuticamente aceptables de los mismos. Los compuestos farmacéutica y terapéuticamente activos y derivados de los mismos son formulados y administrados en formas de dosificación unitaria o formas de dosificación múltiple. Las formas de dosis unitarias tal como se usan en la presente memoria se refieren a unidades físicamente discretas adecuadas para sujetos humanos y animales y envasadas individualmente como se conoce en la técnica. Cada dosis unitaria contiene una cantidad predeterminada del compuesto terapéuticamente activo suficiente para producir el efecto terapéutico deseado, en asociación con el soporte, vehículo o diluyente farmacéutico requerido. Los ejemplos de formas de dosis unitarias incluyen ampollas y jeringas, y comprimidos o cápsulas envasados individualmente. Las formas de dosis unitarias se pueden administrar en fracciones o múltiplos de las mismas. Una forma de dosis múltiple es una pluralidad de formas de dosificación unitarias idénticas envasadas en un único recipiente que se administra en forma de dosis unitarias segregadas. Los ejemplos de formas de dosificación múltiples incluyen viales, frascos de comprimidos o cápsulas o botellas de pintas o galones. Por ende, la forma de dosis múltiple es un múltiplo de dosis unitarias que no están segregadas en el envasado.
También se pueden producir preparaciones de liberación sostenida. Los ejemplos adecuados de preparaciones de liberación sostenida incluyen matrices semipermeables de polímeros hidrofóbicos sólidos que contienen el compuesto que se proporciona en la presente memoria, y dichas matrices se encuentran en forma de artículos como, por ejemplo, películas o microcápsulas. Algunos ejemplos de las matrices de liberación sostenida incluyen parches de iontoforesis, poliésteres, hidrogeles (por ejemplo, poli(2 -hidroxietil-metacrilato) o poli(alcohol vinílico)), polilactidas, copolímeros de ácido L-glutámico y etil-L-glutamato, acetato de etilenvinilo no degradable, copolímeros degradables de ácido glicólicoácido láctico como LUPRON DEPOT™ (microesferas inyectables compuestas de copolímero de ácido glicólico-ácido láctico y acetato de leuprolida) y ácido poli-D-(-)-3-hidroxibutírico. Si bien los polímeros tales como acetato de etilenvinilo y ácido glicólico-ácido láctico permiten la liberación de moléculas durante más de 100 días, ciertos hidrogeles liberan proteínas durante períodos de tiempo más cortos. Cuando el compuesto encapsulado permanece en el organismo durante un tiempo prolongado, se puede desnaturalizar o agregar como resultado de la exposición a la humedad a 37°C, lo que da como resultado una pérdida de actividad biológica y posibles cambios en su estructura. Se pueden idear estrategias racionales para la estabilización dependiendo del mecanismo implicado. Por ejemplo, si se descubre que el mecanismo de aglomeración es la formación de enlace S-S intermolecular a través de intercambio tio-disulfuro, la estabilización se puede lograr modificando los residuos de sulfhidrilo, liofilizando a partir de soluciones ácidas, controlando el contenido de humedad, usando aditivos apropiados y desarrollando composiciones de matriz de polímero específicas.
Se pueden preparar formas de dosificación o composiciones que contienen ingrediente activo en el intervalo del 0,005% al 100% con el resto compuesto por un soporte no tóxico. Para la administración oral, una composición no tóxica farmacéuticamente aceptable se forma mediante la incorporación de cualquiera de los excipientes empleados normalmente, como, por ejemplo, calidades farmacéuticas de manitol, lactosa, almidón, estearato de magnesio, talco, derivados de celulosa, croscarmelosa de sodio, glucosa, sacarosa, carbonato de magnesio o sacarina sódica. Estas composiciones incluyen soluciones, suspensiones, comprimidos, cápsulas, polvos y formulaciones de liberación controlada, tales como, sin limitarse a, implantes y sistemas de administración microencapsulados y polímeros biodegradables, biocompatibles, como colágeno, acetato de etilenvinilo, polianhídridos, ácido poliglicólico, poliortoésteres, ácido poliláctico y otros. Los procedimientos para la preparación de estas composiciones son conocidos por los expertos en la materia. Las composiciones contempladas pueden contener de aproximadamente el 0,001% de ingrediente activo al 100%, en ciertas realizaciones, de aproximadamente el 0,185% o aproximadamente
el 75-95%.
Los compuestos activos o las sales farmacéuticamente aceptables pueden prepararse con soportes que protegen el compuesto contra la eliminación rápida del organismo, tales como formulaciones de liberación prolongada o recubrimientos.
Las composiciones pueden incluir otros compuestos activos para obtener combinaciones de propiedades deseadas. Los compuestos proporcionados en la presente memoria, o las sales farmacéuticamente aceptables de los mismos como se describe en la presente memoria, también se pueden administrar de forma conveniente para fines terapéuticos o profilácticos junto con otro agente farmacológico del que se sabe en la técnica general que es valioso para tratar una o más de las enfermedades o afecciones médicas mencionadas anteriormente, tales como enfermedades relacionadas con el estrés oxidativo. Debe entenderse que dicha terapia de combinación constituye un aspecto adicional de las composiciones y procedimientos de tratamiento proporcionados en la presente memoria. Las composiciones sin lactosa proporcionadas en la presente memoria pueden contener excipientes que son bien conocidos en la técnica y están recogidos, por ejemplo, en la farmacopea estadounidense (USP) SP (XXI)/NF (XVI). En general, las composiciones libres de lactosa contienen un ingrediente activo, un aglutinante/carga y un lubricante en cantidades farmacéuticamente compatibles y farmacéuticamente aceptables. Los ejemplos de formas de dosificación libres de lactosa contienen un ingrediente activo, celulosa microcristalina, almidón gelatinizado previamente y estearato de magnesio.
Además se incluyen composiciones farmacéuticas anhidras y formas de dosificación que contienen un compuesto proporcionado en la presente memoria. Por ejemplo, la adición de agua (por ejemplo, el 5%) es ampliamente aceptada en las técnicas farmacéuticas como un medio para simular el almacenamiento a largo plazo y determinar características tales como la vida media o la estabilidad de las formulaciones con el transcurso del tiempo. Véase por ejemplo Jens T. Carstensen, Drug Stability: Principles & Practice, 2d. Ed., Marcel Dekker, NY, NY, 1995, pp. 379-80. En efecto, el agua y el calor aceleran la descomposición de algunos compuestos. Por lo tanto, el efecto del agua sobre una formulación puede ser muy significativo debido a que comúnmente se encuentra humedad durante la fabricación, la manipulación, el envasado, el almacenamiento, el transporte y el uso de las formulaciones.
Las composiciones farmacéuticas y formas de dosificación anhidras pueden prepararse usando ingredientes anhidros o con bajo contenido en agua y condiciones de bajo contenido en agua o baja humedad. Las composiciones farmacéuticas y las formas de dosificación que comprenden lactosa y al menos un ingrediente activo que comprende una amina primaria o secundaria son anhidras si se espera el contacto considerable con la humedad y/o el contenido en agua durante la fabricación, el envasado y/o el almacenamiento.
Una composición farmacéutica anhidra debe prepararse y almacenarse de manera que se mantenga su naturaleza anhidra. Por consiguiente, las composiciones anhidras se envasan mediante el uso de materiales conocidos para impedir la exposición al agua de modo que puedan incluirse en kits de formulación adecuados. Los ejemplos de envases adecuados incluyen, pero no se limitan a, láminas cerradas herméticamente, plásticos, recipientes para dosis unitarias (por ejemplo, viales), blísteres y envases protectores.
E-1. Formas de dosificación oral
Las formas de dosificación farmacéutica oral son sólidas, en gel o líquidas. Las formas de dosificación sólidas son comprimidos, cápsulas, gránulos y polvos a granel. Los tipos de comprimidos orales incluyen píldoras masticables comprimidas y comprimidos que pueden poseer recubrimiento entérico, recubrimiento de azúcar o recubrimiento de película. Las cápsulas pueden ser cápsulas de gelatina blandas o duras, mientras que los gránulos y polvos pueden proporcionarse en forma efervescente o no efervescente con la combinación de otros ingredientes conocidos por los expertos en la materia.
En ciertas realizaciones, las formulaciones son formas de dosificación sólidas, como cápsulas o comprimidos. Los comprimidos, píldoras, cápsulas, pastillas y similares pueden contener cualquiera de los siguientes ingredientes o compuestos de una naturaleza similar: un aglutinante; un diluyente; un agente de desintegración; un lubricante; un deslizante; un agente edulcorante; y un agente aromatizante.
Los ejemplos de aglutinantes incluyen celulosa microcristalina, goma tragacanto, solución de glucosa, mucílago de acacia, solución de gelatina, sacarosa y pasta de almidón. Los lubricantes incluyen talco, almidón, estearato de magnesio o calcio, lycopodium y ácido esteárico. Los diluyentes incluyen, por ejemplo, lactosa, sacarosa, almidón, caolín, sal, manitol y fosfato de dicalcio. Los deslizantes incluyen, pero no se limitan a, dióxido de silicio coloidal. Los agentes de desintegración incluyen croscarmelosa de sodio, glicolato de almidón sódico, ácido algínico, almidón de
maíz, almidón de patata, bentonita, metilcelulosa, agar y carboximetilcelulosa. Los agentes colorantes incluyen, por ejemplo, cualquiera de los colorantes FD y C solubles en agua homologados aprobados, mezclas de los mismos; y colorantes FD y C insolubles en agua suspendidos en hidrato de alúmina. Los agentes edulcorantes incluyen sacarosa, lactosa, manitol y agentes edulcorantes artificiales como sacarina y cualquier serie de aromas secados por pulverización. Los agentes aromatizantes incluyen aromas naturales extraídos de plantas como frutas y mezclas sintéticas de compuestos que producen una sensación agradable, tales como, pero sin limitarse a, menta y salicilato de metilo. Los agentes humectantes incluyen monoestearato de propilenglicol, monooleato de sorbitano, monolaurato de dietilenglicol y lauril-éter de polioxietileno. Los recubrimientos eméticos incluyen ácidos grasos, grasas, ceras, goma laca, goma laca con amoníaco y ftalatos de acetato de celulosa. Los recubrimientos de películas incluyen hidroxietilcelulosa, carboximetilcelulosa de sodio, polietilenglicol 4000 y ftalato de acetato de celulosa.
Si se desea la administración oral, el compuesto podría proporcionarse en una composición que lo proteja del entorno ácido del estómago. Por ejemplo, la composición puede formularse en un recubrimiento entérico que mantiene su integridad en el estómago y libera el compuesto activo en el intestino. La composición también puede formularse en combinación con un antiácido u otro ingrediente similar.
Cuando la forma dosificación unitaria es una cápsula, puede contener, además del material del tipo anterior, un soporte líquido tal como un aceite graso. Además, las formas de dosificación unitarias pueden contener otros materiales diversos que modifican la forma física de la unidad de dosificación, por ejemplo, recubrimientos de azúcar u otros agentes entéricos. Los compuestos también se pueden administrar como un componente de un elixir, suspensión, jarabe, oblea, espolvoreo, goma de mascar o similares. Un jarabe puede contener, además de los compuestos activos, sacarosa como agente edulcorante y ciertos conservantes, tintes y colorantes y aromas.
Los materiales activos también se pueden mezclar con otros materiales activos que no afectan a la acción deseada, o con materiales que complementan la acción deseada, como antiácidos, bloqueadores de H2 y diuréticos. El ingrediente activo es un compuesto o una sal farmacéuticamente aceptable del mismo como se describe en la presente memoria. Se pueden incluir concentraciones mayores, de hasta aproximadamente el 98% en peso del ingrediente activo.
Los soportes farmacéuticamente aceptables incluidos en comprimidos son aglutinantes, lubricantes, diluyentes, agentes de desintegración, agentes colorantes, agentes aromatizantes y agentes humectantes. Los comprimidos con recubrimiento entérico, debido al recubrimiento entérico, resisten la acción del ácido del estómago y se disuelven o se desintegran en el intestino neutro o alcalino. Los comprimidos recubiertos con azúcar son pastillas comprimidas a las cuales se les han aplicado diferentes capas de sustancias farmacéuticamente aceptables. Los comprimidos recubiertos con una película son pastillas comprimidas que se han recubierto con un polímero u otro recubrimiento adecuado. Las pastillas comprimidas múltiples son pastillas comprimidas hechas por más de un ciclo de compresión usando las sustancias farmacéuticamente aceptables mencionadas anteriormente. Los agentes colorantes también pueden usarse en las formas de dosificación anteriores. Los agentes aromatizantes y edulcorantes se usan en pastillas comprimidas, recubiertas con azúcar, de compresión múltiple y masticables. Los agentes aromatizantes y edulcorantes son especialmente útiles en la formación de comprimidos y pastillas masticables.
Las formas de dosificación oral líquidas incluyen soluciones acuosas, emulsiones, suspensiones, soluciones y/o suspensiones rehidratadas a partir de gránulos no efervescentes y preparaciones efervescentes rehidratadas a partir de gránulos efervescentes. Las soluciones acuosas incluyen, por ejemplo, elixires y jarabes. Las emulsiones son de aceite en agua o de agua en aceite.
Los elixires son preparaciones transparentes, edulcoradas, hidroalcohólicas. Los soportes farmacéuticamente aceptables usados en elixires incluyen disolventes. Los jarabes son soluciones acuosas concentradas de un azúcar, por ejemplo, sacarosa, y pueden contener un conservante. Una emulsión es un sistema de dos fases en el cual un líquido se dispersa en forma de glóbulos pequeños a través de otro líquido. Los soportes farmacéuticamente aceptables usados en emulsiones son líquidos no acuosos, agentes emulsionantes y conservantes. Las suspensiones usan agentes de suspensión y conservantes farmacéuticamente aceptables. Las sustancias farmacéuticamente aceptables usadas en gránulos no efervescentes, para reconstituirse en una forma de dosificación oral líquida, incluyen diluyentes, edulcorantes y agentes humectantes. Las sustancias farmacéuticamente aceptables usadas en gránulos efervescentes, para reconstituirse en una forma de dosificación oral líquida, incluyen ácidos orgánicos y una fuente de dióxido de carbono. Los agentes colorantes y aromatizantes se usan en todas las formas de dosificación anteriores.
Los disolventes incluyen glicerina, sorbitol, alcohol etílico y jarabe. Los ejemplos de conservantes incluyen glicerina, metilo y propilparabeno, ácido benzoico, benzoato de sodio y alcohol. Los ejemplos de líquidos no acuosos usados en las emulsiones incluyen aceite mineral y aceite de semilla de algodón. Los ejemplos de agentes emulsionantes incluyen gelatina, acacia, tragacanto, bentonita y tensioactivos tales como monooleato de polioxietilensorbitano. Los
agentes de suspensión incluyen carboximetilcelulosa de sodio, pectina, tragacanto, Veegum y acacia. Los diluyentes incluyen lactosa y sacarosa. Los agentes edulcorantes incluyen sacarosa, jarabes, glicerina y agentes edulcorantes artificiales como sacarina. Los agentes humectantes incluyen monoestearato de propilenglicol, monooleato de sorbitano, monolaurato de dietilenglicol y lauril-éter de polioxietileno. Las adiciones orgánicas incluyen ácido cítrico y tartárico. Las fuentes de dióxido de carbono incluyen bicarbonato de sodio y carbonato de sodio. Los agentes colorantes incluyen cualquiera de los colorantes FD y C solubles en agua homologados y mezclas de los mismos. Los agentes aromatizantes incluyen aromas naturales extraídos de plantas tales como frutas y mezclas sintéticas de compuestos que producen una sensación de aroma placentera.
Para una forma de dosificación sólida, la solución o suspensión, por ejemplo en carbonato de propileno, aceites vegetales o triglicéridos, se encapsula en una cápsula de gelatina. Dichas soluciones, y la preparación y encapsulación de las mismas, se describen en las patentes de EE.UU. n° 4.328.245; 4.409.239; y 4.410.545. Para una forma de dosificación líquida, la solución, por ejemplo, en un polietilenglicol, se puede diluir con una cantidad suficiente de un soporte líquido farmacéuticamente aceptable, por ejemplo, agua, para medirse fácilmente para la administración.
Alternativamente, se pueden preparar formulaciones líquidas o semisólidas mediante disolución o dispersión del compuesto activo o sal en aceites vegetales, glicoles, triglicéridos, ésteres de propilenglicol (por ejemplo, carbonato de propileno) y otros soportes y encapsulando estas soluciones o suspensiones en cubiertas de cápsulas de gelatina dura o blanda. Otras formulaciones útiles incluyen, pero no se limitan a, aquellas que contienen un compuesto proporcionado en la presente memoria, un mono o poli-alquilenglicol dialquilado, que incluye, pero no se limita a, 1 ,2 -dimetoximetano, diglima, triglima, tetraglima, polietilenglicol-350-dimetiléter, polietilenglicol-550-dimetiléter, polietilenglicol-750-dimetiléter donde 350, 550 y 750 se refieren al peso molecular promedio aproximado del polietilenglicol y uno o más antioxidantes, como hidroxitolueno butilado (BHT), hidroxianisol butilado (BHA), galato de propilo, vitamina E, hidroquinona, hidroxicumarinas, etanolamina, lecitina, cefalina, ácido ascórbico, ácido málico, sorbitol, ácido fosfórico, ácido tiodipropiónico y sus ésteres y ditiocarbamatos.
Otras formulaciones incluyen, pero no se limitan a, soluciones alcohólicas acuosas que incluyen un acetal farmacéuticamente aceptable. Los alcoholes usados en estas formulaciones son cualquier disolvente miscible en agua farmacéuticamente aceptable que tiene uno o más grupos hidroxilo, que incluyen, pero no se limitan a, propilenglicol y etanol. Los acetales incluyen, pero no se limitan a, acetales di(alquilo inferior) de aldehídos de alquilo inferior como diacetal de acetaldehído.
En todas las realizaciones, las formulaciones de comprimidos y cápsulas pueden recubrirse como conocen los expertos en la materia con el fin de modificar o mantener la disolución del ingrediente activo. Así, por ejemplo, se pueden recubrir con un recubrimiento convencional de digestión entérica, como fenilsalicilato, ceras y ftalato acetato de celulosa.
E-2. Inyectables, soluciones y emulsiones
La administración parenteral, caracterizada generalmente por inyección, ya sea por vía subcutánea, intramuscular o intravenosa, también se contempla en la presente memoria. Los inyectables pueden prepararse en formas convencionales, ya sea como soluciones o suspensiones líquidas, formas sólidas adecuadas para solución o suspensión en líquido antes de la inyección, o como emulsiones. Los excipientes adecuados son, por ejemplo, agua, solución salina, dextrosa, glicerol o etanol. Además, si se desea, las composiciones farmacéuticas que se desea administrar también pueden contener cantidades menores de sustancias auxiliares no tóxicas, tales como agentes humectantes o emulsionantes, agentes amortiguadores del pH, estabilizantes, potenciadores de la solubilidad y similares como, por ejemplo, acetato de sodio, monolaurato de sorbitano, oleato de trietanolamina y ciclodextrinas. En la presente memoria también se contempla la implantación de un sistema de liberación lenta o liberación sostenida, de modo que se mantenga un nivel constante de dosificación. En resumen, un compuesto proporcionado en la presente se dispersa en una matriz interna sólida, por ejemplo, polimetilmetacrilato, polibutilmetacrilato, policloruro de vinilo plastificado o no plastificado, nailon plastificado, polietilentereftalato plastificado, goma natural, poliisopreno, poliisobutileno, polibutadieno, polietileno, copolímeros de etileno-vinilacetato, gomas de silicona, polidimetilsiloxanos, copolímeros de carbonato de silicona, polímeros hidrofílicos como hidrogeles de ésteres de ácido acrílico y metacrílico, colágeno, polialcohol vinílico reticulado y poliacetato de vinilo reticulado parcialmente hidrolizado, que está rodeado por una membrana polimérica exterior, por ejemplo, polietileno, polipropileno, copolímeros de etileno/propileno, copolímeros de etileno/acrilato de etilo, copolímeros de etileno/vinilacetato, gomas de silicona, polidimetilsiloxanos, goma de neopreno, polietileno clorado, policloruro de vinilo, copolímeros de cloruro de vinilo con acetato de vinilo, cloruro de vinilideno, etileno y propileno, tereftalato de polietileno ionómero, goma de butilo, gomas de epiclorhidrina, copolímero de etileno/alcohol vinílico, terc-polímero de etileno/acetato de vinilo/alcohol vinílico y copolímero de etileno/viniloxietanol, que es insoluble en los fluidos corporales. El compuesto se difunde a través de la membrana polimérica externa en una etapa de control de la velocidad de liberación. El porcentaje de compuesto activo contenido
en dichas composiciones parenterales depende en gran medida de la naturaleza específica del mismo, así como de la actividad del compuesto y de las necesidades del sujeto.
La administración parenteral de las composiciones incluye administraciones intravenosa, subcutánea e intramuscular. Las preparaciones para la administración parenteral incluyen soluciones estériles listas para inyección, productos estériles solubles en seco, como polvos liofilizados, listos para combinarse con un disolvente justo antes del uso, que incluye comprimidos hipodérmicos, suspensiones estériles listas para inyección, productos estériles insolubles secos listos para combinación con un vehículo justo antes del uso y emulsiones estériles. Las soluciones pueden ser acuosas o no acuosas.
Si se administran por vía intravenosa, los soportes adecuados incluyen solución salina fisiológica o solución salina con tampón de fosfato (PBS) y soluciones que contienen agentes espesantes y solubilizantes, tales como glucosa, polietilenglicol y polipropilenglicol y mezclas de los mismos.
Los soportes farmacéuticamente aceptables usados en preparaciones parenterales incluyen vehículos acuosos, vehículos no acuosos, agentes antimicrobianos, agentes isotónicos, tampones, antioxidantes, anestésicos locales, agentes de suspensión y dispersión, agentes emulsionantes, agentes secuestrantes o quelantes y otras sustancias farmacéuticamente aceptables.
Los ejemplos de vehículos acuosos incluyen inyección de cloruro de sodio, inyección de Ringer, inyección de dextrosa isotónica, inyección de agua estéril, dextrosa e inyección de Ringer de lactato. Los vehículos parenterales no acuosos incluyen aceites fijos de origen vegetal, aceite de semilla de algodón, aceite de maíz, aceite de sésamo y aceite de cacahuete. Los agentes antimicrobianos en concentraciones bacteriostáticas o fungistáticas se deben añadir a preparaciones parenterales envasadas en recipientes de varias dosis que incluyen fenoles o cresoles, mercuriales, alcohol bencílico, clorobutanol, ésteres de ácido metil y propil p-hidroxibenzoico, timerosal, cloruro de benzalconio y cloruro de bencetonio. Los agentes isotónicos incluyen cloruro de sodio y dextrosa. Los tampones incluyen fosfato y citrato. Los antioxidantes incluyen bisulfato de sodio. Los anestésicos locales incluyen clorhidrato de procaína. Los agentes de suspensión y dispersión incluyen carboximetilcelulosa de sodio, hidroxipropilmetilcelulosa y polivinilpirrolidona. Los agentes emulsionantes incluyen Polisorbato 80 (TWEEN® 80). Un agente secuestrante o quelante de iones metálicos incluye EDTA. Los soportes farmacéuticos también incluyen alcohol etílico, polietilenglicol y propilenglicol para vehículos miscibles con agua e hidróxido de sodio, ácido clorhídrico, ácido cítrico o ácido láctico para ajustar el pH.
La concentración del compuesto farmacéuticamente activo se ajusta de modo que una inyección proporcione una cantidad eficaz para producir el efecto farmacológico deseado. La dosis exacta depende de la edad, el peso y el estado del paciente o animal como se conoce en la técnica.
Las preparaciones parenterales de dosis unitaria se envasan en una ampolla, un vial o una jeringa con una aguja. Todas las preparaciones para administración parenteral deben ser estériles, como es conocido y practicado en la técnica.
De modo ilustrativo, la infusión intravenosa o intraarterial de una solución acuosa estéril que contiene un compuesto activo es un modo eficaz de administración. Otra realización es una solución o suspensión estéril acuosa u oleosa que contiene un material activo inyectado según sea necesario para producir el efecto farmacológico deseado.
Los inyectables están diseñados para administración local y sistémica. Normalmente, una dosificación terapéuticamente eficaz se formula para contener una concentración de al menos aproximadamente el 0,1% p/p a aproximadamente el 90% p/p o más, por ejemplo, más del 1% p/p del compuesto activo con respecto al o a los tejidos tratados. El ingrediente activo puede administrarse de una vez, o puede dividirse en una cantidad de dosis más pequeñas que se administrarán en intervalos de tiempo. Debe entenderse que la dosificación precisa y la duración del tratamiento varían en función de la enfermedad que se trata y podrían determinarse de forma empírica mediante protocolos de evaluación conocidos o mediante extrapolación de datos de evaluaciones in vivo o in vitro. Debe observarse que las concentraciones y los valores de dosificación también pueden variar con la edad del individuo tratado. Debe entenderse además que para cualquier sujeto en particular se deben ajustar las pautas de dosificación específicas en el transcurso del tiempo según la necesidad individual y el criterio profesional de la persona que administra o supervisa la administración de las composiciones, y que los intervalos de concentración que se establecen en la presente memoria se indican únicamente a modo de ejemplo y no se pretende que limiten el alcance o la puesta en práctica de las formulaciones reivindicadas.
El compuesto puede suspenderse en forma micronizada u otra forma adecuada o puede derivatizarse para producir un producto activo más soluble o para producir un profármaco. La forma de la mezcla resultante depende de una serie
de factores, que incluyen el modo previsto de administración y la solubilidad del compuesto en el soporte o vehículo seleccionado. La concentración efectiva es suficiente para mejorar los síntomas de la afección y se puede determinar empíricamente.
E-3. Polvos liofilizados
En la presente memoria también son de interés los polvos liofilizados, que se pueden reconstituir para su administración como soluciones, emulsiones u otras mezclas. También pueden reconstituirse y formularse como sólidos o geles.
El polvo liofilizado estéril se prepara disolviendo un compuesto proporcionado en la presente memoria, o una sal farmacéuticamente aceptable del mismo, en un disolvente adecuado. El disolvente puede contener un excipiente que mejora la estabilidad u otro componente farmacológico del polvo o solución reconstituida, preparada a partir del polvo. Los excipientes que pueden usarse incluyen, pero no se limitan a, dextrosa, sorbitol, fructosa, jarabe de maíz, xilitol, glicerina, glucosa, sacarosa u otro agente adecuado. El disolvente también puede contener un tampón, tal como citrato, fosfato de potasio o sodio u otro tampón conocido por los expertos en la materia, en una modalidad, con pH aproximadamente neutro. La filtración estéril posterior de la solución, seguida por liofilización en condiciones estándar, conocida por los expertos en la materia proporciona la formulación deseada. Generalmente, la solución resultante se dividirá en viales para la liofilización. Cada vial contiene una sola dosis (que incluye, pero no se limita a, 10-1.000 mg o 100-500 mg) o múltiples dosis del compuesto. El polvo liofilizado se puede almacenar en condiciones adecuadas, tales como aproximadamente 4°C a temperatura ambiente.
La reconstitución de este polvo liofilizado con agua para inyección proporciona una formulación para su uso en la administración parenteral. Para la reconstitución, se agrega aproximadamente 1-50 mg, aproximadamente 5-35 mg o aproximadamente 9-30 mg de polvo liofilizado por mL de agua u otro soporte adecuado. La cantidad exacta depende del compuesto seleccionado. Dicha cantidad se puede determinar empíricamente.
E-4. Administración tópica
Las mezclas tópicas se preparan tal como se describe para la administración local y sistémica. La mezcla resultante puede ser una solución, suspensión, emulsión o similar y se formula como cremas, geles, ungüentos, emulsiones, soluciones, elixires, lociones, suspensiones, tinturas, pastas, espumas, aerosoles, irrigaciones, nebulizaciones, supositorios, vendajes, parches dérmicos o cualquier otra formulación adecuada para administración tópica.
Los compuestos o sales farmacéuticamente aceptables de los mismos pueden formularse como aerosoles para aplicación tópica, tal como por inhalación (véanse, por ejemplo, las patentes de EE.UU. n° 4.044.126, 4.414.209 y 4.364.923, que describen aerosoles para la administración de un esteroide útil para el tratamiento de enfermedades inflamatorias, particularmente asma). Estas formulaciones para administración en el tracto respiratorio pueden estar en forma de aerosol o solución para un nebulizador, o como un polvo microfino para insuflación, en solitario o en combinación con un soporte inerte tal como lactosa. En tal caso, las partículas de la formulación tendrán diámetros menores que 50 micrómetros o menores que 10 micrómetros.
Los compuestos pueden formularse para aplicación local o tópica, tal como para aplicación tópica en la piel y las membranas mucosas, por ejemplo en el ojo, en forma de geles, cremas y lociones y para aplicación en el ojo o para aplicación intracisternal o intrarraquídea. La administración tópica se contempla para el suministro transdérmico y también para la administración en los ojos o la mucosa, o para terapias de inhalación. También se pueden administrar soluciones nasales del compuesto solo o en combinación con otros excipientes farmacéuticamente aceptables. Estas soluciones, en particular las previstas para uso oftálmico, se pueden formular como soluciones isotónicas al 0,01%-10%, con pH de aproximadamente 5-7, con sales adecuadas.
E-5. Composiciones para otras vías de administración
En la presente memoria se contemplan también otras vías de administración tales como aplicación tópica, parches transdérmicos y administración rectal.
Por ejemplo, las formas de dosificación farmacéuticas para administración rectal son supositorios rectales, cápsulas y comprimidos para un efecto sistémico. Los supositorios rectales que se usan en la presente memoria significan cuerpos sólidos para inserción en el recto que se derriten o ablandan a temperatura corporal liberando uno o más ingredientes farmacológica o terapéuticamente activos. Las sustancias farmacéuticamente aceptables usadas en los supositorios rectales son bases o vehículos y agentes para elevar el punto de fusión. Los ejemplos de bases incluyen
manteca de cacao (aceite de teobroma), glicerina-gelatina, carbocera (polioxietilenglicol) y mezclas adecuadas de mono, di y triglicéridos de ácidos grasos. Pueden usarse combinaciones de las diversas bases. Los agentes para elevar el punto de fusión de los supositorios incluyen espermaceti y cera. Los supositorios rectales pueden prepararse ya sea mediante el procedimiento comprimido o por moldeo. Un ejemplo de peso de un supositorio rectal es de aproximadamente 2 a 3 gramos.
Los comprimidos y cápsulas para administración rectal se fabrican mediante el uso de la misma sustancia farmacéuticamente aceptable y mediante los mismos procedimientos usados para las formulaciones para administración oral.
E-6. Composiciones de liberación sostenida
Los ingredientes activos proporcionados en la presente memoria pueden administrarse por medios de liberación controlada o por dispositivos de administración que son bien conocidos por los expertos en la materia. Los ejemplos incluyen, pero no se limitan a, los descritos en las patentes de EE.UU. n°: 3.845.770; 3.916.899; 3.536.809; 3.598.123; y 4.008.719, 5.674.533, 5.059.595, 5.591.767, 5.120.548, 5.073.543, 5.639.476, 5.354.556, 5.639.480, 5.733.566, 5.739.108, 5.891.474, 5.922.356, 5.972.891, 5.980.945, 5.993.855, 6.045.830, 6.087.324, 6.113.943, 6.197.350, 6.248.363, 6.264.970, 6.267.981, 6.376.461, 6.419.961, 6.589.548, 6.613.358, 6.699.500 y 6.740.634. Dichas formas de dosificación pueden usarse para proporcionar una liberación lenta o controlada de uno o más ingredientes activos usando, por ejemplo, hidropropilmetilcelulosa, otras matrices de polímero, geles, membranas permeables, sistemas osmóticos, recubrimientos con múltiples capas, micropartículas, liposomas, microesferas, o una combinación de los mismos para proporcionar el perfil de liberación deseado en proporciones variadas. Las formulaciones de liberación controlada adecuadas conocidas por los expertos en la materia, incluyendo las que se describen en la presente memoria, se pueden seleccionar fácilmente para su uso con los ingredientes activos.
Los productos farmacéuticos de liberación controlada tienen un fin común de mejorar la terapia de fármaco con respecto a lo logrado por sus alternativas no controladas. En una realización, el uso de una preparación de liberación controlada diseñada de manera óptima en el tratamiento médico se caracteriza por un uso mínimo de sustancia del fármaco para curar o controlar la afección en un mínimo de tiempo. En ciertas realizaciones, las ventajas de las formulaciones de liberación controlada incluyen la actividad prolongada del fármaco, la frecuencia de dosificación reducida y el cumplimiento mejorado por parte del paciente. De manera adicional, las formulaciones de liberación controlada pueden usarse para influir en el momento de inicio de la acción u otras características, tales como niveles en sangre del fármaco, y por lo tanto puede influir en la aparición de efectos secundarios (por ejemplo, adversos).
La mayoría de las formulaciones de liberación controlada están diseñadas para liberar inicialmente una cantidad de fármaco (ingrediente activo) que inmediatamente produce el efecto terapéutico deseado, y libera de forma gradual y continua otras cantidades de fármaco para mantener este nivel de efecto terapéutico o profiláctico durante un período de tiempo prolongado. Para mantener este nivel de fármaco constante en el organismo, el fármaco debe liberarse de la forma de dosificación a una velocidad que repondrá la cantidad de fármaco que se metaboliza y se excreta al exterior del cuerpo. La liberación controlada de un ingrediente activo se puede estimular por varias condiciones que incluyen, pero no se limitan a, pH, temperatura, enzimas, agua u otras condiciones o compuestos fisiológicos.
En ciertas realizaciones, el agente puede administrarse usando infusión intravenosa, una bomba osmótica implantable, un parche transdérmico, liposomas u otros modos de administración. En una modalidad, se puede usar una bomba (véase Sefton, CRC Crit. Ref. Biomed. Eng. 14:201 (1987); Buchwald y col., Surgery 88:507 (1980); Saudekycol., N. Engl. J. Med. 321:574 (1989). En otra realización, se pueden usar materiales poliméricos. En otra realización más, se puede colocar un sistema de liberación controlada cerca de la diana terapéutica, es decir, que requiere solo una fracción de la dosis sistémica (véase, por ejemplo, Goodson, Medical Applications of Controlled Release, vol. 2, pp.
115-138 (1984).
En algunas realizaciones, se introduce un dispositivo de liberación controlada en un sujeto cerca del sitio de activación inmunitaria inapropiada o un tumor. Se establecen otros sistemas de liberación controlada en la revisión de Langer (Science 249:1527-1533 (1990). El ingrediente activo se puede dispersar en una matriz interna sólida, por ejemplo, polimetilmetacrilato, polibutilmetacrilato, policloruro de vinilo plastificado o no plastificado, nailon plastificado, polietilentereftalato plastificado, goma natural, poliisopreno, poliisobutileno, polibutadieno, polietileno, copolímeros de etileno-vinilacetato, gomas de silicona, polidimetilsiloxanos, copolímeros de carbonato de silicona, polímeros hidrófilos como hidrogeles de ésteres de ácido acrílico y metacrílico, colágeno, polialcohol vinílico reticulado y poliacetato de vinilo reticulado parcialmente hidrolizado, que está rodeado por una membrana polimérica exterior, por ejemplo, polietileno, polipropileno, copolímeros de etileno/propileno, copolímeros de etileno/acrilato de etilo, copolímeros de etileno/vinilacetato, gomas de silicona, polidimetilsiloxanos, goma de neopreno, polietileno clorado, policloruro de vinilo, copolímeros de cloruro de vinilo con acetato de vinilo, cloruro de vinilideno, etileno y propileno, tereftalato de
polietileno ionómero, goma de butilo, gomas de epiclorhidrina, copolímero de etileno/alcohol vinílico, terc-polímero de etileno/acetato de vinilo/alcohol vinílico y copolímero de etileno/viniloxietanol, que es insoluble en los fluidos corporales. El ingrediente activo se difunde a continuación a través de la membrana polimérica externa en una etapa de control de la velocidad de liberación. El porcentaje de ingrediente activo contenido en dichas composiciones parenterales depende en gran medida de la naturaleza específica del mismo, así como de las necesidades del sujeto.
E-7. Formulaciones dirigidas
Los compuestos proporcionados en la presente memoria, o las sales farmacéuticamente aceptables de los mismos, también pueden formularse para dirigirse a un tejido, receptor u otra área particular del cuerpo del sujeto para tratar. Muchos de estos procedimientos de orientación son bien conocidos por los expertos en la materia. Se contempla que todos los compuestos y composiciones de la invención se usen en dichos procedimientos de direccionamiento. Para ejemplos no limitativos de procedimientos de direccionamiento, véanse, por ejemplo, las patentes de EE.UU. n° 6.316.652, 6.274.552, 6.271.359, 6.253.872, 6.139.865, 6.131.570, 6.120.751, 6.071.495, 6.060.082, 6.048.736, 6.039.975, 6.004.534, 5.985.307, 5.972.366, 5.900.252, 5.840.674, 5.759.542 y 5.709.874.
En una realización, las suspensiones liposómicas, que incluyen liposomas dirigidos a tejidos, como liposomas dirigidos a tumores, también pueden ser adecuadas como soportes farmacéuticamente aceptables. Estos pueden prepararse según procedimientos conocidos por los expertos en la materia. Por ejemplo, las formulaciones de liposomas se pueden preparar tal como se describe en la patente de EE.UU. n° 4.522.811. En resumen, los liposomas tales como las vesículas multilaminares (VML) se pueden formar mediante secado de fosfatidilcolina de huevo y fosfatidilserina cerebral (fracción molar de 7:3) en el interior de un matraz. Se agrega una solución del compuesto que se proporciona en la presente memoria en solución salina con tampón de fosfato que carece de cationes divalentes (PBS) y el matraz se agita hasta la dispersión de la película lipídica. Se lavan las vesículas resultantes para eliminar el compuesto no encapsulado, se sedimentan por centrifugación y a continuación se resuspenden en p Bs .
E-8. Artículos de fabricación
Los compuestos o sales farmacéuticamente aceptables pueden envasarse como artículos de fabricación que contienen material de envasado, un compuesto o una sal farmacéuticamente aceptable del mismo proporcionado en la presente memoria, que se usa para el tratamiento, prevención o mejora de uno o más síntomas o progresión del cáncer, que incluye tumores sólidos y tumores transmitidos por vía hematógena, y una etiqueta que indica que el compuesto o la sal farmacéuticamente aceptable del mismo se usa para el tratamiento, prevención o mejora de uno o más síntomas o progresión del cáncer, que incluye los tumores sólidos y los tumores transmitidos por vía hematógena. Los artículos de fabricación que se proporcionan en la presente contienen materiales de envasado. Los materiales de envasado para su uso en el envasado de productos farmacéuticos son bien conocidos por los expertos en la materia. Véanse, por ejemplo, las patentes de EE.UU. n° 5.323.907, 5.052.558 y 5.033.252. Algunos ejemplos de materiales de envase farmacéutico incluyen, pero no se limitan a, blísteres, frascos, tubos, inhaladores, bombas, bolsas, viales, recipientes, jeringas, plumas, frascos y cualquier material de envasado adecuado para una formulación seleccionada y un modo de administración y tratamiento deseados. Se contempla una amplia matriz de formulaciones de los compuestos y las composiciones que se proporcionan en la presente memoria.
F. Evaluación de la actividad de los compuestos
Se encuentran disponibles procedimientos fisiológicos, farmacológicos y bioquímicos estándar para analizar los compuestos con el fin de identificar si estos poseen la actividad antiproliferativa deseada.
Dichos ensayos incluyen, por ejemplo, ensayos bioquímicos tales como ensayos de unión, ensayos de incorporación de radiactividad, así como diversos ensayos basados en células.
G. Preparación de los compuestos
Los compuestos proporcionados en la presente memoria pueden prepararse mediante procedimientos conocidos por un experto en la materia y siguiendo procedimientos similares a los descritos en la sección de Ejemplos de la presente memoria y modificaciones de rutina de los mismos.
A continuación se ilustra un esquema de reacción de ejemplo para la preparación de compuestos.
6. EJEMPLOS
Ciertas realizaciones de la invención se ilustran mediante el siguiente ejemplo no limitativo.
Ejemplo 1
Síntesis de N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-metoxifenil)acetamida
4-bromo-2-metilbenzoato de metilo: Se combinó ácido 4-bromo-2-metilbenzoico (100 g, 465,02 mmol), ácido sulfúrico concentrado (52 mL) en metanol (1L) y se calentó hasta 65°C durante 18 horas. Se concentró la reacción y se diluyó el residuo con acetato de etilo (500 mL), se lavó con solución de bicarbonato de sodio saturada (150 mL), agua (200 mL) y salmuera (250 mL) y se secó sobre sulfato de sodio. Se concentró la fase orgánica a presión reducida y se secó adicionalmente al vacío para proporcionar 4-bromo-2-metilbenzoato de metilo (102 g, 445,27 mmol, 95% de rendimiento) como un líquido rojo. 1H RMN (400 MHz, Cloroformo-d-i) 87,78 (d, J=83 Hz, 1H), 7,45 - 7,30 (m, 2H), 3,88 (s, 3H), 2,57 (s, 3H).
Benzoato de metil-4-bromo-2-(bromometilo): Se combinó 4-bromo-2-metilbenzoato de metilo (102 g, 445,27 mmol), NBS (79,2 g, 445,27 mmol), Azo-isobutironitrilo (2,58 g, 16 mmol) en acetonitrilo (600 mL) y se sometió a reflujo a 85°C durante 18 horas. Se concentró la mezcla y al residuo se le agregó diclorometano (150 mL). El sólido resultante se retiró mediante filtración. Se concentró el filtrado y se purificó mediante cromatografía en columna ultrarrápida (EtOAc al 0-4% en hexanos). Las fracciones que contenían el producto se concentraron a presión reducida y se secaron adicionalmente a alto vacío para proporcionar benzoato de 4-bromo-2-(bromometil)metilo (100 g, 324,70 mmol, 72,9% de rendimiento) como un sólido blanquecino. 1H RMN (300 MHz, dimetilsulfóxido-cfó) 87,88 (d, J=2,2 Hz, 1H), 7,82 (dd, J=8,4, 2,1 Hz, 1H), 7,72 - 7,64 (m, 1H), 5,00 (s, 2H), 3,88 (s, 3H).
3-(5-bromo-1-oxoisoindolin-2-il) piperidina-2,6-diona: Se combinó benzoato de metil-4-bromo-2-(bromometilo) (100 g, 324,70 mmol), clorhidrato de 3-aminopiperidina-2,6-diona (53,2 g, 324,70 mmol), trietilamina (113,29 mL, 811,75 mmol), y dimetilformamida seca (400 mL) y se agitó a temperatura ambiente en atmósfera inerte durante 18 horas. Se enfrió la reacción a 5°C y se diluyó con agua (400 mL), ácido acético (115 mL), dietiléter (300 mL) con agitación continua a temperatura ambiente durante 2 horas. El sólido resultante se filtró con éter (100 mL) y se secó adicionalmente a alto vacío para proporcionar 3-(5-bromo-1-oxoisoindolin-2-il)piperidina-2,6-diona (46 g, 142,35 mmol, 43,8% de rendimiento) como un sólido azul claro. MS (ESI) m/z 325,0 [M 1]+.
2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-carbonitrilo: Se combinó 3-(5-bromo-1-oxoisoindolin-2-il)piperidina-2,6-diona (46 g, 142,35 mmol), 1,1'-bis(difenilfosfino)ferroceno (788 mg, 1,423 mmol), cianuro de cinc (25 g, 213,52
mmol), acetato de cinc (7,83 g, 42,7 mmol) y dimetilformamida seca (360 mL) y se desgasificaron antes de la adición de tris(dibencilideneacetona)dipaladio(0) (0,364 g, 0,398 mmol). Se evacuaron las mezclas y se reemplazó con argón 3 veces, a continuación se agitó a 120°C durante 20 h. La mezcla se enfrió hasta temperatura ambiente, se filtró y se purificó mediante cromatografía en columna en gel de sílice (metanol al 0-5% en diclorometano). Se combinaron fracciones que contenían producto y se extrajo el disolvente a presión reducida y a continuación se secó adicionalmente a alto vacío para proporcionar 2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolina-5-carbonitrilo (22 g, 81,78 mmol, 57,2% de rendimiento) como un sólido marrón. MS (ESI) m/z 268,0 [M-H+].
3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona: Se combinó 2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-carbonitrilo (10 g, 37,13 mmol), ácido metanosulfónico (2,6 mL, 40,85 mmol), paladio seco sobre carbono al 10% (4 g) y dimetilacetamida (320 mL) y se agitó en un recipiente de hidrogenación y se mantuvo a 50 Psi a 40°C durante 20 h. Se evacuó la atmósfera de hidrógeno y se filtró la mezcla a través de un lecho de celite, se lavó con agua (100 mL) y se concentró. Al residuo resultante se le agregó metanol-diclorometano al 1% que, tras el filtrado y el secado a alto vacío, proporcionó 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (5,6 g, 15,17 mmol, 40% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 272,0 [M-1].
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-metoxifenil)acetamida. A metanosulfonato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (,200 g, 0,541 mmol) en DMF (3 mL) se le agregó HATU (0,226 g, 0,596 mmol), ácido 2,2-difluoro-2-(4-fluorofenil)acético (0,109 g, 0,541 mmol) seguido por N-etil-N-isopropilpropan-2-amina (0,262 mL, 1,624 mmol). Se dejó agitara 25°C durante 16 h. Se añadieron 30 mL de agua y se filtró. Se enjuagó con EtOAc, se secó al vacío para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-metoxifenil)acetamida (0,080 g, 0,175 mmol, 32,3% de rendimiento) como un sólido blanco. 1H RMN (500 MHz, DMSO-cfe) 8 ppm 10,98 (s, 1 H) 9,57 (t, J=6,15 Hz, 1 H) 7,69 (d, J=7,88 Hz, 1 H) 7,48-7,57 (m, 2 H) 7,34-7,45 (m, 2 H) 7,07 (m, J=8,83 Hz, 2 H) 5,11 (dd, J=13,24, 5,36 Hz, 1 H) 4,38-4,50 (m, 3 H) 4,23-4,36 (m, 1 H) 3,81 (s, 3 H) 2,85-2,98 (m, 1 H) 2,56 - 2,68 (m, 1 H) 2,39 (dd, J=12,93, 4,73 Hz, 1 H) 1,95-2,07 (m, 1 H). MS (ESI) m/z 458,2 [M 1]+.
Ejemplo 2
Síntesis de 2-(3-clorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida
2-(3-clorofeml)-N-((2-(2,6-dioxopiperldm-3-M)-1-oxobomdoNn-5-N)metM)-2,2-difluoroacetamida. A metanosulfonato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (,200 g, 0,541 mmol) en DMF (3 mL) se le agregó HATU (0,226 g, 0,596 mmol), ácido 2-(3-clorofenil)-2,2-difluoroacético (0,112 g, 0,541 mmol) seguido por N-etil-N-isopropilpropan-2-amina (0,262 mL, 1,624 mmol). Se dejó agitar a 25°C durante 16 h. Se añadieron 30 mL de agua y se filtró. Se enjuagó con EtOAc, se secó al vacío para proporcionar 2-(3-clorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (,090 g, 0,195 mmol, 36,0% de rendimiento) como un sólido blanco.
1H RMN (500 MHz, DMSO-cfe) 8 ppm 10,98 (s, 1 H) 9,70 (t, J=5,99 Hz, 1 H) 7,53 - 7,71 (m, 5 H) 7,32 - 7,45 (m, 2 H) 5,11 (dd, J=13,40, 5,20 Hz, 1 H) 4,39-4,51 (m, 3 H) 4,25-4,38 (m, 1 H) 2,85-2,99 (m, 1 H) 2,55-2,68 (m, 1 H) 2,40 (dd, J=13,08, 4,57 Hz, 1 H) 1,95-2,05 (m, 1 H). MS (ESI) m/z 462,2 [M+1]+.
Ejemplo 3
Síntesis de N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluorofenil)acetamida
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluorofenil)acetamida. A metanosulfonato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (,200 g, 0,541 mmol) en DMF (3 mL) se le agregó HATU (0,226 g, 0,596 mmol), ácido 2,2-difluoro-2-(4-fluorofenil)acético (0,103 g, 0,541 mmol) seguido por N-etil-N-isopropilpropan-2-amina (0,262 mL, 1,624 mmol). Se dejó agitara 25°C durante 16 h. Se añadieron 30 mL de agua y se filtró. Se enjuagó el filtrado con EtOAc, se secó al vacío para obtener N-((2-(2,6-dioxopiperidin-3-il)-1 -oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluorofenil)acetamida (0,100 g, 0,225 mmol, 41,5% de rendimiento) como un sólido blanco. 1H RMN (500 MHz, DMSO-d6) 8 ppm 10,98 (br. s., 1 H) 9,66 (t, J=5,99 Hz, 1 H) 7,58 - 7,73 (m, 3 H) 7,29 - 7,47 (m, 4 H) 5,11 (dd, J=13,40, 5,20 Hz, 1 H) 4,38 -4,53 (m, 3 H) 4,24 -4,36 (m, 1 H) 2,81 - 3,00 (m, 1 H) 2,56 -2,67 (m, 1 H) 2,40 (qd, J=13,19, 4,57 Hz, 1 H) 1,91 -2,07 (m, 1 H).
Ejemplo 4
Síntesis de N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(p-tolilacetamida
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(p-tolil)acetamida. A metanosulfonato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (,200 g, 0,541 mmol) en DMF (3 mL) se le agregó HATU (0,226 g, 0,596 mmol), ácido 2,2-difluoro-2-(p-tolil)acético (0,101 g, 0,541 mmol) seguido por N-etil-N-isopropilpropan-2-amina (0,262 mL, 1,624 mmol). Se dejó agitar a 25°C durante 16 h. Se añadieron 30 mL de agua y se filtró. Se enjuagó con EtOAc, se secó al vacío para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(p-tolil)acetamida (,110 g, 0,249 mmol, 46,0% de rendimiento) como un sólido blanco. 1H RMN (500 MHz, DMSO-cfe) 8 ppm 10,98 (s, 1 H) 9,59 (t, J=6,15 Hz, 1 H) 7,68 (d, J=7,88 Hz, 1 H) 7,48 (d, J=8,20 Hz, 2 H) 7,26 - 7,43 (m, 4 H) 5,11 (dd, J=13,24, 5,04 Hz, 1 H) 4,37 - 4,50 (m, 3 H) 4,22-4,34 (m, 1 H) 2,84-2,99 (m, 1 H) 2,56-2,67 (m, 1 H) 2,31 - 2,45 (m, 4 H) 1,93-2,07 (m, 1 H). MS (ESI) m/z 442,2 [M+1]+.
Ejemplo 5
Síntesis de 2-(3,4-didorofeml)-N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdolm-5-M)metM)-2,2-difluoroacetamida 2-(3,4-did orofenM)-N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdoNn-5-N)metM)-2,2-difluoroacetamida. A metanosulfonato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (,200 g, 0,541 mmol) en DMF (3 mL) se le agregó HATU (0,226 g, 0,596 mmol), ácido 2-(3,4-diclorofenil)-2,2-difluoroacético (0,130 g, 0,541 mmol) seguido por N-etil-N-isopropilpropan-2-amina (0,262 mL, 1,624 mmol). Se dejó agitar a 25°C durante 16 h. Se añadieron 30 mL de agua y se filtró. Se enjuagó con EtOAc, se secó al vacío para proporcionar 2-(3,4-diclorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (,110 g, 0,222 mmol, 40,9% de rendimiento) como un sólido blanco. 1H RMN (500 MHz, DMSO-d6) 8 ppm 10,98 (s, 1 H) 9,71 (t, J=5,99 Hz, 1 H) 7,79 - 7,88 (m, 2 H) 7,69 (d, J=7,88 Hz, 1 H) 7,59 (dd, J=8,51, 2,21 Hz, 1 H) 7,43 (s, 1 H) 7,38 (d, J=7,88 Hz, 1 H) 5,11 (dd, J=13,08, 5,20 Hz, 1 H) 4,39 - 4,51 (m, 3 H) 4,26 - 4,37 (m, 1 H) 2,86 - 2,98 (m, 1 H) 2,61 (d, J=18,92 Hz, 1 H) 2,39 (dd, J=13,40, 4,89 Hz, 1 H) 1,95-2,06 (m, 1 H). MS (ESI) m/z 498,0[M+1]+.
Ejemplo 6
Síntesis de 2-(2-d orofenM)-N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdoNn-5-N)metM)-2,2-difluoroacetamida
2-(2-d orofeml)-N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdolm-5-M)metM)-2,2-difmoroacetamida. A metanosulfonato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (0,200 g, 0,541 mmol) en DMF (3 mL) se le agregó HATU (0,226 g, 0,596 mmol), ácido 2-(2-clorofenil)-2,2-difluoroacético (0,112 g, 0,541 mmol) seguido por N-etil-N-isopropilpropan-2-amina (0,262 mL, 1,624 mmol). Se dejó agitara 25°C durante 16 h. Se añadieron 30 mL de agua y se filtró. Se enjuagó con EtOAc, se secó al vacío para proporcionar 2-(2-clorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (,090 g, 0,195 mmol, 36,0% de rendimiento) como un sólido blanco.
1H RMN (500 MHz, DMSO-cfe) 8 ppm 10,98 (s, 1 H) 9,68 (t, J=6,31 Hz, 1 H) 7,68 - 7,79 (m, 2 H) 7,56 - 7,63 (m, 2 H) 7,49 - 7,56 (m, 2 H) 7,46 (d, J=7,88 Hz, 1 H) 5,12 (dd, J=13,24, 5,36 Hz, 1 H) 4,40 - 4,56 (m, 3 H) 4,27 - 4,38 (m, 1 H) 2,92 (ddd, J=17,50, 13,71, 5,36 Hz, 1 H) 2,61 (d, J=16,71 Hz, 1 H) 2,32 - 2,46 (m, 1 H) 1,94 - 2,10 (m, 1 H). MS (ESI) m/z 462,0 [M+1]+.
Ejemplo 7
Síntesis de 2-(4-d orofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida
2-(4-clorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoboindolin-5-il)metil)-2,2-difluoroacetamida. A metanosulfonato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (,200 g, 0,541 mmol) en DMF (3 mL) se le agregó HATU (0,226 g, 0,596 mmol), ácido 2-(4-clorofenil)-2,2-difluoroacético (0,112 g, 0,541 mmol) seguido por N-etil-N-isopropilpropan-2-amina (0,262 mL, 1,624 mmol). Se dejó agitar a 25°C durante 16 h. Se añadieron 30 mL de agua y se filtró. Se enjuagó con EtOAc, se secó al vacío para proporcionar 2-(4-clorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (,080 g, 0,173 mmol, 32,0% de rendimiento) como un sólido blanco.
1H RMN (500 MHz, DMSO-da) 5 ppm 10,98 (s, 1 H) 9,68 (t, J=6,15 Hz, 1 H) 7,69 (d, J=7,88 Hz, 1 H) 7,58 - 7,66 (m, 4 H) 7,33- 7,44 (m, 2 H) 5,11 (dd, J=13,24, 5,04 Hz, 1 H) 4,39 -4,50 (m, 3 H) 4,24-4,35 (m, 1 H) 2,85-2,98 (m, 1 H) 2,61 (dd, J=15,29, 2,05 Hz, 1 H) 2,39 (dd, J=12,93, 4,73 Hz, 1 H) 1,95-2,07 (m, 1 H). MS (ESI) m/z 462,0 [M+1]+.
Ejemplo 8
Síntesis de N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdolm-5-N)metM)-2,2-difluoro-2-(2-(trifluorometil)fenil)acetamida
N-((2-(2,6-diozopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(trifluorometil)fenil)acetamida. A metanosulfonato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (,200 g, 0,541 mmol) en DMF (3 mL) se le agregó HATU (0,226 g, 0,596 mmol), ácido 2,2-difluoro-2-(2-fluorofenil)acético (0,130 g, 0,541 mmol) seguido por N-etil-N-isopropilpropan-2-amina (0,262 mL, 1,624 mmol). Se dejó agitara 25°C durante 16 h. Se añadieron 30 mL de agua y se filtró. Se enjuagó con EtOAc, se secó al vacío para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1 -oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(trifluorometil)fenil)acetamida (,080 g, 0,161 mmol, 29,8% de rendimiento) como un sólido blanco. 1H RMN (500 MHz, DMSO-cfe) 5 ppm 10,98 (s, 1 H) 9,70 (t, J=6,15 Hz, 1 H) 7,66 - 7,81 (m, 3 H) 7,47 - 7,59 (m, 3 H) 7,44 (d, J=8,51 Hz, 1 H) 5,12 (dd, J=13,40, 5,20 Hz, 1 H) 4,40 - 4,54 (m, 3 H) 4,27 - 4,38 (m, 1 H) 2,85-3,00 (m, 1 H) 2,57 - 2,67 (m, 1 H) 2,35 - 2,45 (m, 1H) 1,94-2,07 (m, 1 H).
Ejemplo 9
Síntesis de 2-(4-(terc-butM)feml)-N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdolm-5-N)metM)-2,2-difluoroacetamida
2-(4-(terc-butil)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. A metanosulfonato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (0,200 g, 0,541 mmol) en DMF (3 mL) se le agregó HATU (0,226 g, 0,596 mmol), ácido 2-(4-(terc-butil)fenil)-2,2-difluoroacético (0,124 g, 0,541 mmol) seguido por N-etil-N-isopropilpropan-2-amina (0,262 mL, 1,624 mmol). Se dejó agitar a 25°C durante 16 h. Se añadieron 30 mL de agua y se filtró. Se enjuagó con EtOAc, se secó al vacío para proporcionar 2-(4-(terc-butil)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (0,095 g, 0,196 mmol, 36,3% de rendimiento) como un sólido blanco. 1H RMN (500 MHz, DMSO-cfe) 5 ppm 10,98 (s, 1 H) 9,61 (t, J=5,99 Hz, 1 H) 7,68 (d, J=7,88 Hz, 1 H) 7,49- 7,60 (m, 4 H) 7,33-7,44 (m, 2 H) 5,11 (dd, J=13,24, 5,04 Hz, 1 H) 4,37-4,50 (m, 3 H) 4,24 - 4,35 (m, 1 H) 2,86-2,98 (m, 1 H) 2,57 - 2,67 (m, 1 H) 2,38 (dd, J=13,40, 4,57 Hz, 1 H) 1,92-2,06 (m, 1 H) 1,22- 1,36 (m, 9 H). MS (ESI) m/z 484,0 [M+1]+.
Ejemplo 10
Síntesis de N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-fenilacetamida
A. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-fenilacetamida. Se colocó ácido mesílico de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (0,050 g, 0,135 mmol) en un vial con N,N-dimetilformamida (1,0 mL), ácido 2,2-difluoro-2-fenilacético (0,023 g, 0,135 mmol), diisopropiletilamina (0,071 mL, 0,406 mmol) y 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metilen]-1H-1,2,3-triazolo[4,5-b]piridinio (0,057 g, 0,149 mmol). Se agitó la mezcla de reacción a temperatura ambiente durante 18 h. Se recogió la mezcla de reacción en dimetilsulfóxido y se purificó usando HPLC semipreparatoria de fase inversa (acetonitrilo al 5-100% ácido fórmico al 0,1% en agua ácido fórmico al 0,1%, durante 20 min). Se combinaron las fracciones que contenían el producto deseado y se eliminaron los compuestos orgánicos volátiles a presión reducida para dar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-fenilacetamida (0,039 g, 0,091 mmol, 67,4% de rendimiento) como un sólido blanco. 1H RMN (400 MHz, DMSO-da) 811,00 (s, 1H), 9,67 (t, J = 6,25 Hz, 1H), 7,67 (d, J =7,81 Hz, 1H), 7,50-7,62 (m, 5H), 7,34-7,42 (m, 2H), 5,11 (dd, J = 5,08, 13,28 Hz, 1H), 4,38-4,47 (m, 3H), 4,24-4,31 (m, 1H), 2,86-2,97 (m, 1H), 2,55-2,64 (m, 1H), 2,32-2,45 (m, 1H), 1,99 (dtd, J = 2,34, 5,25, 12,55 Hz, 1H). MS (ESI) m/z 428,2 [M+1]+.
Ejemplo 11
Síntesis de 2-(3-doro-4-metNfenM)-N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdoMn-5-N)metM)-2,2-difluoroacetamida
A. 2-(3-cloro-4-metilfenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. Se colocó ácido mesílico de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (0,050 g, 0,135 mmol) en un vial con N,N-dimetilformamida (1,0 mL), ácido 2-(3-cloro-4-fluorofenil)-2,2-difluoroacético (0,030 g, 0,135 mmol), diisopropiletilamina (0,071 mL, 0,406 mmol) y 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metilen]-1H-1,2,3-triazolo[4,5-b]piridinio (0,057 g, 0,149 mmol). Se agitó la mezcla de reacción a temperatura ambiente durante 18 h. Se recogió la mezcla de reacción en dimetilsulfóxido y se purificó usando HPLC semipreparatoria de fase inversa (acetonitrilo al 5-100% ácido fórmico al 0,1% en agua ácido fórmico al 0,1%, durante 20 min). Se combinaron las fracciones que contenían el producto deseado y se eliminaron los compuestos orgánicos volátiles a presión reducida para dar 2-(3-cloro-4-fluorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida como un sólido blanco. 1H RMN (400 MHz, DMSO-d6) 811,01 (s, 1H), 9,72 (t, J=6,05 Hz, 1H), 7,81 (dd, J = 1,76, 7,23 Hz, 1H), 7,69 (d, J = 7,81 Hz, 1H), 7,58 - 7,65 (m, 2H), 7,43 (s, 1H), 7,35-7,39 (m, 1H), 5,11 (dd, J = 5,08, 13,28 Hz, 1H), 4,40-4,48 (m, 3H), 4,26-4,34 (m, 1H), 2,92 (ddd, J = 5,47, 13,77, 17,48 Hz, 1H), 2,56-2,64 (m, 1H), 2,31 - 2,45 (m, 1H), 1,95-2,04 (m, 1H). MS (ESI) m/z 480,0 [M+1]+.
Ejemplo 12
Síntesis de 2-(2,6-difluorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida
A. 2-(2,6-difluorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. Se colocó ácido mesílico de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (0,050 g, 0,135 mmol) en un vial con N,N-dimetilformamida (1,0 mL), ácido 2-(2,6-difluorofenil)-2,2-difluoroacético (0,028 g, 0,135 mmol), dMsopropiletilamina (0,071 mL, 0,406 mmol) y 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metilen]-1H-1,2,3-triazolo[4,5-b]piridinio (0,057 g, 0,149 mmol). Se agitó la mezcla de reacción a temperatura ambiente durante 18 h. Se recogió la mezcla de reacción en dimetilsulfóxido y se purificó usando HPLC semipreparatoria de fase inversa (acetonitrilo al 5-100% ácido fórmico al 0,1% en agua ácido fórmico al 0,1%, durante 20 min). Se combinaron las fracciones que contenían el producto deseado y se eliminaron los compuestos orgánicos volátiles a presión reducida para dar 2-(2,6-difluorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (0,039 g, 0,084 mmol, 62,2% de rendimiento) como un sólido blanco. 1H RMN (500 MHz, DMSo-d6) 8 10,98 (s, 1H), 9,73 (t, J = 5,99 Hz, 1H), 7,65 - 7,73 (m, 2H), 7,49 (s, 1H), 7,43 (d, J = 7,88 Hz, 1H), 7,27 (dd, J = 8,67, 9,62 Hz, 2H), 5,11 (dd, J = 5,20, 13,40 Hz, 1H), 4,50 (d, J = 5,99 Hz, 2H), 4,46 (d, J = 17,34 Hz, 1H), 4,29 - 4,35 (m, 1H), 2,91 (ddd, J = 5,36, 13,71, 17,50 Hz, 1H), 2,57 - 2,63 (m, 1H), 2,40 (qd, J = 4,57, 13,19 Hz, 1H), 2,01 (dtd, J = 2,36, 5,26, 12,65 Hz, 1H). MS (ESI) m/z 464,2 [M+1]+.
Ejemplo 13
Síntesis de 2-(5-doro-2-metoxifenM)-N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdoMn-5-N)metM)-2,2-difluoroacetamida
A. 2-(5-doro-2-metoxifenM)-N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdoNn-5-N)metM)-2,2-difluoroacetamida. Se colocó ácido mesílico de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (0,050 g, 0,135 mmol) en un vial con N,N-dimetilformamida (1,0 mL), ácido 2-(5,2-difluorofenil)-2,2-difluoroacético (0,032 g, 0,135 mmol), diisopropiletilamina (0,071 mL, 0,406 mmol) y 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metilen]-1H-1,2,3-triazolo[4,5-b]piridinio (0,057 g, 0,149 mmol). Se agitó la mezcla de reacción a temperatura ambiente durante 18 h. Se recogió la mezcla de reacción en dimetilsulfóxido y se purificó usando HPLC semipreparatoria de fase inversa (acetonitrilo al 5-100% ácido fórmico al 0,1% en agua ácido fórmico al 0,1%, durante 20 min). Se combinaron las fracciones que contenían el producto deseado y se eliminaron los compuestos orgánicos volátiles a presión reducida para dar 2-(5-cloro-2-metoxifenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (0,044 g, 0,089 mmol, 66,1% de rendimiento) como un sólido blanco. 1H RMN (500 MHz, DMSO-d6) 8 10,97 (s, 1H), 9,41 (t, J = 5,99 Hz, 1H), 7,73 (d, J = 7,88 Hz, 1H), 7,59 (dd, J = 2,84, 8,83 Hz, 1H), 7,53 (d, J = 2,52 Hz, 1H), 7,48 (s, 1H), 7,43 (d, J =7,57 Hz, 1H), 7,17 (d, J = 8,83 Hz, 1H), 5,11 (dd, J = 5,20, 13,40 Hz, 1H), 4,43-4,49 (m, 3H), 4,29 4,35 (m, 1H), 3,68 (s, 3H), 2,91 (ddd, J = 5,36, 13,71, 17,50 Hz, 1H), 2,57-2,63 (m, 1H), 2,40 (qd, J = 4,26, 13,08 Hz, 1H), 2,00 (dtd, J = 2,52, 5,32, 12,69 Hz, 1H). MS (ESI) m/z 492,2 [M+1]+.
Ejemplo 14
Síntesis de N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-fluoro-2-metoxifenil)acetamida
A. N-((2-(2,6-diozopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-fluoro-2-metoxifenil)acetamida. Se colocó ácido mesílico de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (0,050 g, 0,135 mmol) en un vial con N,N-dimetilformamida (1,0 mL), ácido 2,2-difluoro-2-(5-fluoro-2-metoxifenil)acético (0,030 g, 0,135 mmol), dMsopropiletilamina (0,071 mL, 0,406 mmol) y 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metilen]-1H-1,2,3-triazolo[4,5-b]piridinio (0,057 g, 0,149 mmol). Se agitó la mezcla de reacción a temperatura ambiente durante 18 h. Se recogió la mezcla de reacción en dimetilsulfóxido y se purificó usando HPLC semipreparatoria de fase inversa (acetonitrilo al 5-100% ácido fórmico al 0,1% en agua ácido fórmico al 0,1%, durante 20 min). Se combinaron las fracciones que contenían el producto deseado y se eliminaron los compuestos orgánicos volátiles a presión reducida para dar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-fluoro-2-metoxifenil)acetamida (0,043 g, 0,090 mmol, 6 6 ,8 % de rendimiento) como un sólido blanco. 1H RMN (500 MHz, DMSO-d6) 8 10,97 (s, 1H), 9,40 (t, J = 5,99 Hz, 1H), 7,73 (d, J = 7,57 Hz, 1H), 7,49 (s, 1H), 7,44 (d, J = 7,88 Hz, 1H), 7,36 - 7,41 (m, 2H), 7,13 -7,18 (m, 1H), 5,11 (dd, J = 5,20, 13,40 Hz, 1H), 4,43-4,50 (m, 3H), 4,29 - 4,35 (m, 1H), 3,65 (s, 3H), 2,92 (ddd, J = 5,52, 13,64, 17,42 Hz, 1H), 2,57-2,63 (m, 1H), 2,40 (qd, J = 4,10, 13,24 Hz, 1H), 2,01 (dtd, J = 2,21, 5,34, 12,65 Hz, 1H). MS (ESI) m/z 476,0 [M+1]+.
Ejemplo 15
Síntesis de N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(o-tolil)acetamida
A. N-((2-(2,6-dioxopipendm-3-M)-1-oxoisomdolm-5-M)metN)-2,2-difmoro-2-(o-tom)acetamida. Se colocó ácido mesílico de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (0,050 g, 0,135 mmol) en un vial con N,N-dimetilformamida (1,0 mL), ácido 2,2-difluoro-2-(o-tolil)acético (0,025 g, 0,135 mmol), diisopropiletilamina (0,071 mL, 0,406 mmol) y 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metilen]-1H-1,2,3-triazolo[4,5-b]piridinio (0,057 g, 0,149 mmol). Se agitó la mezcla de reacción a temperatura ambiente durante 18 h. Se recogió la mezcla de reacción en dimetilsulfóxido y se purificó usando HPLC semipreparatoria de fase inversa (acetonitrilo al 5-100% ácido fórmico al 0,1% en agua ácido fórmico al 0,1%, durante 20 min). Se combinaron las fracciones que contenían el producto deseado y se eliminaron los compuestos orgánicos volátiles a presión reducida para dar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(o-tolil)acetamida (0,038 g, 0,086 mmol, 63,6% de rendimiento) como un sólido blanco. 1H RMN (500 MHz, DMSO-d6) 8 10,97 (s, 1H), 9,59 (t, J = 5,99 Hz, 1H), 7,69 (d, J = 8,20 Hz, 1H), 7,50 - 7,53 (m, 1H), 7,39 - 7,46 (m, 3H), 7,28 - 7,34 (m, 2H), 5,10 (dd, J = 5,36, 13,24 Hz, 1H), 4,41 - 4,49 (m, 3H), 4,27 -4,33 (m, 1H), 2,87 - 2,95 (m, 1H), 2,57 - 2,63 (m, 1H), 2,39 (qd, J = 4,41, 13,24 Hz, 1H), 2,33 (s, 3H), 2,00 (dtd, J = 2,21, 5,32, 12,69 Hz, 1H). MS (ESI) m/z 442,2 [M+1]+.
Ejemplo 16
Síntesis de 2-(4-(2-(dimetilamino)-2-oxoetoxi)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida
A. 2-(4-(2-(dimetilamino)-2-oxoetoxi)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. Se colocó ácido mesílico de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (0,050 g, 0,135 mmol) en un vial con N,N-dimetilformamida (1,0 mL), ácido 2-(4-(2-(dimetilamino)-2-oxoetoxi)fenil)-2,2-difluoroacético (0,037 g, 0,135 mmol), diisopropiletilamina (0,071 mL, 0,406 mmol) y 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metilen]-1H-1,2,3-triazolo[4,5-b]piridinio (0,057 g, 0,149 mmol). Se agitó la mezcla de reacción a temperatura ambiente durante 18 h. Se recogió la mezcla de reacción en dimetilsulfóxido y se purificó usando HPLC semipreparatoria de fase inversa (acetonitrilo al 5-100% ácido fórmico al 0,1% en agua ácido fórmico al 0,1%, durante 20 min). Se combinaron las fracciones que contenían el producto deseado y se eliminaron los compuestos orgánicos volátiles a presión reducida para dar 2-(4-(2-(dimetilamino)-2-oxoetoxi)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (0,021 g, 0,040 mmol, 29,4% de rendimiento) como un sólido blanco.
1H RMN (500 MHz, DMSO-da) 8 10,97 (s, 1H), 9,56 (t, J = 6,15 Hz, 1H), 7,67 (dd, J = 0,63, 7,57 Hz, 1H), 7,46 - 7,50 (m, 2H), 7,35- 7,38 (m, 2H), 7,00- 7,04 (m, 2H), 5,10 (dd, J = 5,20, 13,40 Hz, 1H), 4,89 (s, 2H), 4,39-4,46 (m, 3H), 4,26 - 4,31 (m, 1H), 2,99 (s, 3H), 2,87 - 2,95 (m, 1H), 2,84 (s, 3H), 2,57 - 2,62 (m, 1H), 2,33 - 2,43 (m, 1H), 2,00 (dtd, J = 2,36, 5,18, 12,49 Hz, 1H). MS (ESI) m/z 529,2 [M+1]+.
Ejemplo 17
Síntesis de 2-(2,5-dimetoxifenM)-N-((2-(2,6-dioxopiperídm-3-M)-1-oxoisomdoNn-5-N)metM)-2,2-difluoroacetamida
A. 2-(2,5-dimetoxifenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. Se colocó ácido mesílico de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (0,050 g, 0,135 mmol) en un vial con N,N-dimetilformamida (1,0 mL), ácido 2-(2,5-difluorofenil)-2,2-difluoroacético (0,031 g, 0,135 mmol), diisopropiletilamina (0,071 mL, 0,406 mmol) y 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metilen]-1H-1,2,3-triazolo[4,5-b]piridinio (0,057 g, 0,149 mmol). Se agitó la mezcla de reacción a temperatura ambiente durante 18 h. Se recogió la mezcla de reacción en dimetilsulfóxido y se purificó usando HPLC semipreparatoria de fase inversa (acetonitrilo al 5-100% ácido fórmico al 0,1% en agua ácido fórmico al 0,1%, durante 20 min). Se combinaron las fracciones que contenían el producto deseado y se eliminaron los compuestos orgánicos volátiles a presión reducida para dar 2-(2,5-dimetoxifenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (0,043 g, 0,088 mmol, 65,2% de rendimiento) como un sólido blanco. 1H RMN (500 MHz, DMSO-d6) 8 10,97 (s, 1H), 9,33 (t, J = 5,99 Hz, 1H), 7,72 (d, J = 7,88 Hz, 1H), 7,49 (s, 1H), 7,42-7,46 (m, 1H), 7,04-7,10 (m, 3H), 5,11 (dd, J = 5,20, 13,40 Hz, 1H), 4,43-4,49 (m, 3H), 4,29-4,35 (m, 1H), 3,75 (s, 3H), 3,61 (s, 3H), 2,91 (ddd, J = 5,52, 13,56, 17,50 Hz, 1H), 2,57 - 2,64 (m, 1H), 2,40 (qd, J = 4,73, 13,24 Hz, 1H), 2,00 (dtd, J = 2,36, 5,30, 12,57 Hz, 1H). MS (ESI) m/z 488,2 [M+1]+.
Ejemplo 18
Síntesis de N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-fluorofenil)acetamida
A. N-((2-(2,6-dioxopiperldin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-fluorofenil)acetamida. Se colocó ácido mesílico de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (0,050 g, 0,135 mmol) en un vial con N,N-dimetilformamida (1,0 mL), ácido 2,2-difluoro-2-(2-fluorofenil)acético (0,026 g, 0,135 mmol), diisopropiletilamina (0,071 mL, 0,406 mmol) y 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metilen]-1H-1,2,3-triazolo[4,5-b]piridinio (0,057 g, 0,149 mmol). Se agitó la mezcla de reacción a temperatura ambiente durante 18 h. Se recogió la mezcla de reacción en dimetilsulfóxido y se purificó usando HPLC semipreparatoria de fase inversa (acetonitrilo al 5-100% ácido fórmico al 0,1% en agua ácido fórmico al 0,1%, durante 20 min). Se combinaron las fracciones que contenían el producto deseado y se eliminaron los compuestos orgánicos volátiles a presión reducida para dar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-fluorofenil)acetamida (0,030 g, 0,067 mmol, 49,8% de rendimiento) como un sólido blanco. 1H RMN (500 MHz, DMSO-da) 8 10,97 (s, 1H), 9,69 (t, J = 6,15 Hz, 1H), 7,70 (d, J = 8,20 Hz, 1H), 7,61 -7,67 (m, 2H), 7,47 (s, 1H), 7,40-7,44 (m, 1H), 7,34- 7,40 (m, 2H), 5,11 (dd, J = 5,20, 13,40 Hz, 1H), 4,50 (d, J = 6,31 Hz, 2H), 4,45 (d, J = 17,34 Hz, 1H), 4,29-4,34 (m, 1H), 2,91 (ddd, J = 5,52, 13,64, 17,42 Hz, 1H), 2,57-2,63 (m, 1H), 2,40 (qd, J = 4,73, 13,24 Hz, 1H), 2,01 (dtd, J = 2,36, 5,26, 12,65 Hz, 1H). MS (ESI) m/z 446,2 [M+1]+.
Ejemplo 19
Síntesis de N-((2-(2,6-dioxopiperldin-3-il)-1-oxoisoindolin-5-il)metil)-2-(2-etoxifenil)-2,2-difluoroacetamida
A. N-((2-(2,6-dioxopiperldin-3-il)-1-oxoisoindolin-5-il)metil)-2-(2-etoxifenil)-2,2-difluoroacetamida. Se colocó ácido mesílico de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (0,050 g, 0,135 mmol) en un vial con N,N-dimetilformamida (1,0 mL), ácido 2-(2-etoxifenil)-2,2-difluoroacético (0,029 g, 0,135 mmol), diisopropiletilamina (0,071 mL, 0,406 mmol) y 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metilen]-1H-1,2,3-triazolo[4,5-b]piridinio (0,057 g, 0,149 mmol). Se agitó la mezcla de reacción a temperatura ambiente durante 18 h. Se recogió la mezcla de reacción en dimetilsulfóxido y se purificó usando HPLC semipreparatoria de fase inversa (acetonitrilo al 5-100% ácido fórmico al 0,1% en agua ácido fórmico al 0,1%, durante 20 min). Se combinaron las fracciones que contenían el producto deseado y se eliminaron los compuestos orgánicos volátiles a presión reducida para dar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2-(2-etoxifenil)-2,2-difluoroacetamida (0,045 g, 0,095 mmol, 70,5% de rendimiento) como un sólido blanco. 1H RMN (500 MHz, DMSO-d6) 8 10,97 (s, 1H), 9,31 (t, J = 6,15 Hz, 1H), 7,70 (d, J = 7,88 Hz, 1H), 7,55 (dd, J = 1,58, 7,57 Hz, 1H), 7,47 - 7,52 (m, 2H), 7,45 (d, J = 8,51 Hz, 1H), 7,11 (d, J = 8,20Hz, 1H), 7,05 (td, J = 0,79, 7,49 Hz, 1H), 5,11 (dd, J = 5,20, 13,40 Hz, 1H), 4,42 -4,48 (m, 3H), 4,28 - 4,34 (m, 1H), 3,99 (q, J = 6,94 Hz, 2H), 2,87 - 2,96 (m, 1H), 2,57 - 2,63 (m, 1H), 2,40 (qd, J = 4,41, 13,24 Hz, 1H), 2,00 (dtd, J = 2,21, 5,08, 12,53 Hz, 1H), 1,13 (t, J = 6,94 Hz, 3H). MS (ESI) m/z 472,2 [M+1]+.
Ejemplo 20
Síntesis de N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(trifluorometoxi)fenil)acetamida
A. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(trifluorometoxi)fenil)acetamida.
Se colocó ácido mesílico de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (0,050 g, 0,135 mmol) en un vial con N,N-dimetilformamida (1,0 mL), ácido 2,2-difluoro-2-(2-(trifluorometoxi)fenil)acético (0,035 g, 0,135 mmol), dMsopropiletilamina (0,071 mL, 0,406 mmol) y 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metilen]-1H-1,2,3-triazolo[4,5-b]piridinio (0,057 g, 0,149 mmol). Se agitó la mezcla de reacción a temperatura ambiente durante 18 h. Se recogió la mezcla de reacción en dimetilsulfóxido y se purificó usando HPLC semipreparatoria de fase inversa (acetonitrilo al 5-100% ácido fórmico al 0,1% en agua ácido fórmico al 0,1%, durante 20 min). Se combinaron las fracciones que contenían el producto deseado y se eliminaron los compuestos orgánicos volátiles a presión reducida para dar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(trifluorometoxi)fenil)acetamida (0,047 g, 0,092 mmol, 67,9% de rendimiento) como un sólido blanco. 1H RMN (500 MHz, DMSO-d6) 8 10,97 (s, 1H), 9,69 (t, J = 5,83 Hz, 1H), 7,77 (dd, J = 1,58, 7,88 Hz, 1H), 7,68 - 7,74 (m, 2H), 7,48 - 7,56 (m, 3H), 7,43 (d, J = 7,88 Hz, 1H), 5,11 (dd, J = 5,04, 13,24 Hz, 1H), 4,49 (d, J = 6,31 Hz, 2H), 4,44 (d, J = 17,34 Hz, 1H), 4,28-4,33 (m, 1H), 2,91 (ddd, J = 5,36, 13,79, 17,42 Hz, 1H), 2,57 - 2,63 (m, 1H), 2,40 (qd, J = 4,26, 13,19 Hz, 1H), 2,00 (dtd, J = 2,36, 5,26, 12,65 Hz, 1H). MS (ESI) m/z 512,2 [M+1]+.
Ejemplo 21
Síntesis de 2-(3-bromo-4-(trifluorometoxi)fenil)-N-((2-(2,6-diozopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida
A. 2-(3-bromo-4-(trifluorometoxi)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. Se colocó ácido mesílico de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (0,050 g, 0,135 mmol) en un vial con N,N-dimetilformamida (1,0 mL), ácido 2-(3-bromo-4-(trifluorometoxi)fenil)-2,2-difluoroacético (0,045 g, 0,135 mmol), diisopropiletilamina (0,071 mL, 0,406 mmol) y 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metilen]-1H-1,2,3-triazolo[4,5-b]piridinio (0,057 g, 0,149 mmol). Se agitó la mezcla de reacción a temperatura ambiente durante 18 h. Se recogió la mezcla de reacción en dimetilsulfóxido y se purificó usando HPLC semipreparatoria de fase inversa (acetonitrilo al 5-100% ácido fórmico al 0,1% en agua ácido fórmico al 0,1%, durante 20 min). Se combinaron las fracciones que contenían el producto deseado y se eliminaron los compuestos orgánicos volátiles a presión reducida para dar 2-(3-bromo-4-(trifluorometoxi)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (0,048 g, 0,081 mmol, 60,1% de rendimiento) como un sólido blanco. 1H RMN (500 MHz, DMSO-d6) 8 10,99 (s, 1H), 9,75 (t, J = 6,15 Hz, 1H), 8,01 (d, J =1,89 Hz, 1H), 7,73 - 7,78 (m, 2H), 7,69 (d, J = 7,57 Hz, 1H), 7,45 (s, 1H), 7,38 (d, J = 7,88 Hz, 1H), 5,11 (dd, J =5,04, 13,24 Hz, 1H), 4,41 - 4,49 (m, 3H), 4,28 - 4,34 (m, 1H), 2,92 (ddd, J = 5,36, 13,71, 17,50 Hz, 1H), 2,58 - 2,64 (m, 1H), 2,39 (qd, J = 4,41, 13,24 Hz, 1H), 2,01 (dtd, J = 2,21, 5,20, 12,61 Hz, 1H). MS (ESI) m/z 592,0 [M 2]+.
Ejemplo 22
Síntesis de N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoropropanamida (ejemplo de referencia)
A. N-((2-(2,6-dioxopiperldin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoropropanamida. Se colocó ácido mesílico de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (0,050 g, 0,135 mmol) en un vial con N,N-dimetilformamida (1,0 mL), ácido 2,2-difluoropropanoico (0,015 g, 0,135 mmol), diisopropiletilamina (0,071 mL, 0,406 mmol) y 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metilen]-1H-1,2,3-triazolo[4,5-b]piridinio (0,057 g, 0,149 mmol). Se agitó la mezcla de reacción a temperatura ambiente durante 18 h. Se recogió la mezcla de reacción en dimetilsulfóxido y se purificó usando HPLC semipreparatoria de fase inversa (acetonitrilo al 5-100% ácido fórmico al 0,1% en agua ácido fórmico al 0,1%, durante 20 min). Se combinaron las fracciones que contenían el producto deseado y se eliminaron los compuestos orgánicos volátiles a presión reducida para dar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoropropanamida (0,016 g, 0,044 mmol, 32,4% de rendimiento) como un sólido blanco. 1H RMN (500 MHz, DMSO-da) 8 10,98 (s, 1H), 9,36 (t, J = 5,99 Hz, 1H), 7,71 (d, J =7,88 Hz, 1H), 7,49 (s, 1H), 7,42 (d, J = 7,88 Hz, 1H), 5,12 (dd, J = 5,20, 13,40 Hz, 1H), 4,43 - 4,49 (m, 3H), 4,30 - 4,35 (m, 1H), 2,92 (ddd, J = 5,52, 13,64, 17,42 Hz, 1H), 2,58-2,64 (m, 1H), 2,40 (qd, J = 4,57, 13,19 Hz, 1H), 2,01 (dtd, J = 2,21, 5,16, 12,69 Hz, 1H), 1,74- 1,84 (m, 3H). MS (ESI) m/z 366,2 [M+1]+.
Ejemplo 23
Síntesis de N-((2-(2,6-dioxopiperldin-3-il)-1-oxoisoindolin-5-il)metil)-2,2,3,3-tetrafluoropropanamida (ejemplo de referencia)
A. N-((2-(2,6-dioxopiperidin-3-il-1-oxoisoindolin-5-il)metil)-2,2,3,3-tetrafluoropropanamida. Se colocó ácido mesílico de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (0,050 g, 0,135 mmol) en un vial con N,N-dimetilformamida (1,0 mL), ácido 2,2,3,3-tetrafluoropropanoico (0,020 g, 0,135 mmol), diisopropiletilamina (0,071 mL, 0,406 mmol) y 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metilen]-1H-1,2,3-triazolo[4,5-b]piridinio (0,057 g, 0,149 mmol). Se agitó la mezcla de reacción a temperatura ambiente durante 18 h. Se recogió la mezcla de reacción en dimetilsulfóxido y se purificó usando HPLC semipreparatoria de fase inversa (acetonitrilo al 5-100% ácido fórmico al 0,1% en agua ácido fórmico al 0,1%, durante 20 min). Se combinaron las fracciones que contenían el producto deseado y se eliminaron los compuestos orgánicos volátiles a presión reducida para dar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2,3,3-tetrafluoropropanamida (0,013 g, 0,032 mmol, 23,93% de rendimiento) como un sólido blanco. 1H RMN (500 MHz, DMSO-d6) 8 10,97 (s, 1H), 9,92 (t, J = 5,99 Hz, 1H), 7,71 (d, J = 7,88 Hz, 1H), 7,47 (s, 1H), 7,41 (d, J = 7,88 Hz, 1H), 6,64-6,89 (m, 1H), 5,11 (dd, J =5,04, 13,24 Hz, 1H), 4,50 (d, J = 6,31 Hz, 2H), 4,46 (d, J = 17,34 Hz, 1H), 4,29-4,34 (m, 1H), 2,87 - 2,95 (m, 1H), 2,57 - 2,63 (m, 1H), 2,39 (qd, J = 4,73, 13,24 Hz, 1H), 2,00 (dtd, J = 2,21, 5,24, 12,53 Hz, 1H). MS (ESI) m/z 402,0[M+1]+.
Ejemplo 24
Síntesis de N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoropropanamida (ejemplo de referencia)
A. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluorobutanamida. Se colocó ácido mesílico de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (0,050 g, 0,135 mmol) en un vial con N,N-dimetilformamida (1,0 mL), ácido 2,2-difluorobutanoico (0,017 g, 0,135 mmol), diisopropiletilamina (0,071 mL, 0,406 mmol) y 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metilen]-1H-1,2,3-triazolo[4,5-b]piridinio (0,057 g, 0,149 mmol). Se agitó la mezcla de reacción a temperatura ambiente durante 18 h. Se recogió la mezcla de reacción en dimetilsulfóxido y se purificó usando HPLC semipreparatoria de fase inversa (acetonitrilo al 5-100% ácido fórmico al 0,1% en agua ácido fórmico al 0,1%, durante 20 min). Se combinaron las fracciones que contenían el producto deseado y se eliminaron los compuestos orgánicos volátiles a presión reducida para dar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoropropanamida (0,027 g, 0,071 mmol, 52,6% de rendimiento) como un sólido blanco.
1H RMN (500 MHz, DMSO-da) 8 10,97 (s, 1H), 9,37 (t, J =5,99 Hz, 1H), 7,70 (d, J = 7,88 Hz, 1H), 7,47(s, 1H), 7,41 (d, J = 7,88 Hz, 1H), 5,10 (dd, J = 5,20, 13,40 Hz, 1H), 4,42-4,48 (m, 3H), 4,28-4,34 (m, 1H), 2,91 (ddd, J = 5,36, 13,64, 17,58 Hz, 1H), 2,57-2,63 (m, 1H), 2,39 (qd, J = 4,57, 13,29 Hz, 1H), 1,97-2,14 (m, 3H), 0,92 (t, J = 7,41 Hz, 3H). MS (ESI) m/z 380,2 [M+1]+.
Ejemplo 25
Síntesis de N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-3-hidroxi-3-metilbutanamida (ejemplo de referencia)
A. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-3-hidroxi-3-metilbutanamida. Se colocó ácido mesílico de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (0,050 g, 0,135 mmol) en un vial con N,N-dimetilformamida (1,0 mL), ácido 2,2-difluoro-3-hidroxi-3-metilbutanoico (0,021 g, 0,135 mmol), diisopropiletilamina (0,071 mL, 0,406 mmol) y 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metilen]-1H-1,2,3-triazolo[4,5-b]piridinio (0,057 g, 0,149 mmol). Se agitó la mezcla de reacción a temperatura ambiente durante 18 h. Se recogió la mezcla de reacción en dimetilsulfóxido y se purificó usando HPLC semipreparatoria de fase inversa (acetonitrilo al 5-100% ácido fórmico al 0,1% en agua ácido fórmico al 0,1%, durante 20 min). Se combinaron las fracciones que contenían el producto deseado y se eliminaron los compuestos orgánicos volátiles a presión reducida para dar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-3-hidroxi-3-metilbutanamida (0,049 g, 0,120 mmol, 88 % de rendimiento) como un sólido blanco. 1H RMN (500 MHz, DMSO-d6) 8 10,97 (s, 1H), 9,07 (t, J = 5,99 Hz, 1H), 7,68 (d, J = 8,20 Hz, 1H), 7,50 (s, 1H), 7,43 (d, J =7,25 Hz, 1H), 5,46 (br. s., 1H), 5,10 (dd, J = 5,04, 13,24 Hz, 1H), 4,41 -4,46 (m, 3H), 4,27-4,33 (m, 1H), 2,86-2,96 (m, 1H), 2,57-2,63 (m, 1H), 2,39 (qd, J = 4,57, 13,19 Hz, 1H), 2,00 (dtd, J = 2,36, 5,26, 12,65 Hz, 1H), 1,24 (s, 6 H). MS (ESI) m/z 410,2 [M+1]+.
Ejemplo 26
2-(3-cloro-4-metilfenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida
A. 1-(3-cloro-4-metilfenil)etanona: A una solución agitada de 3-cloro-4-metilbenzonitrilo (3 g, 19,86 mmol) en benceno (25 mL) se añadió yoduro de metilmagnesio (6 , 6 mL, 19,86 mmol, 3 M en éter dietílico) a temperatura ambiente y se agitó a 80°C durante 8 h. A continuación se enfrió la mezcla de reacción a temperatura ambiente y se añadió ácido clorhídrico 6 N (25 mL) y se agitó a 80°C durante 6 h. Se enfrió la mezcla de reacción hasta temperatura ambiente y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 20 mL), salmuera (20 mL), se secaron sobre sulfato de sodio y se concentraron para proporcionar 1-(3-cloro-4
metilfenil)etanona (2 g, 11,90 mmol, 60% rendimiento) como un sólido blanquecino. 1H RMN (400 MHz, DMSO-d6) 8 7,93 (d, J =1,8 Hz, 1H), 7,82 (dd, J = 7,8, 1,8 Hz, 1H), 7,51 (dd, J = 7,7, 1,0 Hz, 1H), 2,57 (s, 3H), 2,40 (s, 3H).
B. 2-(3-cloro-4-metilfenil)-2-oxoacetato de etilo. A una solución agitada de 1-(3-cloro-4-metilfenil)etanona (500 mg, 2,97 mmol) en piridina (5 mL) se le añadió dióxido de selenio (660 mg, 5,95 mmol) y se agitó durante 12 h a 100°C. La mezcla de reacción se diluyó con diclorometano (20 mL) y se filtró a través de un lecho de Celite. Al filtrado se le añadió cloroformiato de etilo (2 mL) a 0°C y se agitó a temperatura ambiente durante 2 h. Se acidificó la mezcla de reacción con ácido clorhídrico acuoso 1 N (hasta pH 4) y se extrajo con acetato de etilo (3X 10 mL). Se lavaron las capas orgánicas combinadas con agua ( 2 X 5 mL), salmuera (5 mL), se secaron sobre sulfato de sodio y se concentraron para proporcionar 2-(3-cloro-4-metilfenil)-2-oxoacetato de etilo (300 mg, 1,32 mmol, 45%) como un líquido marrón. 1H RMN (300 MHz, DMSO-da) 8 7,99 (dd, J = 5,5, 1,7 Hz, 1H), 7,86 (dd, J = 7,9, 1,8 Hz, 1H), 7,59 (dd, J =11,6, 7,9 Hz, 1H), 4,42 (q, J =7,1 Hz, 2H), 2,44 (s, 3H), 1,33 (t, J = 7,1 Hz, 3H).
C.2-(3-cloro-4-metilfenil)-2,2-difluoroacetato de etilo. A 2-(3-cloro-4-metilfenil)-2-oxoacetato de etilo (300 mg, 1,32 mmol) se le añadió trifluoruro de dietilamino azufre (2 mL) y se agitó durante 12 h a temperatura ambiente. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8 ) y se extrajo con acetato de etilo (3x10 mL). Se lavaron las capas orgánicas combinadas con agua (2x5 mL), salmuera (10 mL), se secaron sobre sulfato de sodio y se concentraron para proporcionar 2-(3-cloro-4-metilfenil)-2,2-difluoroacetato de etilo (200 mg, 0,804 mmol, 61%) como un líquido marrón. 1H RMN (400 MHz, DMSO-d6) 8 7,63 - 7,52 (m, 2H), 7,47 (dd, J = 7,9, 1,9 Hz, 1H), 4,32 (q, J =7,1 Hz, 2H), 2,39 (s, 3H), 1,23 (t, J = 7,1 Hz, 4H).
D. Ácido 2-(3-cloro-4-metilfenil)-2,2-difluoroacético. A una solución fría (0°C) agitada de 2-(3-cloro-4-metilfenil)-2,2-difluoroacetato de etilo (200 mg, 0,806 mmol) en metanol/tetrahidrofurano/agua (10 mL, 1:1:1) se añadió hidróxido de litio monohidratado (169 mg, 4,03 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con ácido clorhídrico acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 15 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secaron sobre sulfato de sodio y se concentraron para proporcionar ácido 2-(3-cloro-4-metilfenil)-2,2-difluoroacético (150 mg, 0,68 mmol, 84% de rendimiento) como un semisólido marrón. 1H RMN (300 MHz, DMSO-d6) 8 7,61 - 7,50 (m, 2H), 7,45 (dd, J = 8,0, 1,8 Hz, 1H), 2,39 (s, 3H).
E.2-(3-cloro-4-metilfenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. A una solución fría (0°C) agitada de metanosulfonato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (200 mg, 0,619 mmol) en N, N-dimetilformamida (20 mL) se añadió ácido 2-(3-cloro-4-metilfenil)-2,2-difluoroacético (150 mg, 0,68 mmol) seguido de N,N-diisopropiletilamina (240 mg, 1,85 mmol), 3-óxido hexafluorofosfato de 1 [bis(dimetilamino)metilen]-1H-1,2,3-triazolo[4,5-b]piridinio (352 mg, 0,92 mmol) y se agitó a temperatura ambiente durante 12 h. Se diluyó la mezcla de reacción con agua (100 mL) y se extrajo con acetato de etilo (2X 10 mL) y se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secaron sobre sulfato de sodio y se concentraron al vacío. Se purificó el producto mediante una columna de fase inversa Reveleris C-18 usando acetonitrilo al 70% en ácido fórmico acuoso (0,1%) para dar2-(3-cloro-4-metilfenil)-N-((2-(2,6-dioxopiperidina-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (40 mg, 0,08 mmol, 14% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 476,18 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 8 10,98 (s, 1H), 9,66 (t, J = 6,0 Hz, 1H), 7,68 (d, J = 7,9 Hz, 1H), 7,61 -7,50 (m, 2H), 7,49 - 7,33 (m, 3H), 5,10 (dd, J = 13,3, 5,0 Hz, 1H), 4,51 - 4,12 (m, 4H), 2,98-2,83 (m, 1H), 2,65-2,55 (m, 1H), 2,46 - 2,27 (m, 4H), 2,06-1,93 (m, 1H).
Ejemplo 27
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-(trifluorometiltio)fenil)acetamida
A. 1-(4-(trifluorometiltio)fenil)etanona. En un matraz de fondo redondo agitado y evacuado se tomaron fosfato de potasio (19,38 g, 91,44 mmol), tamices moleculares (5 g, 4Á), azufre- 8 (2,92 g, 91,44 mmol), carbonato de plata (16,80 g, 60,96 mmol), ácido (4-acetilfenil)borónico (5 g, 30,48 mmol), tiocianato de cobre (1) (370 mg, 3,04 mmol) y 1,10-fenantrolina (1,09 g, 6,09). Se añadió trimetil(trifluorometil)silano (21,67 g, 152,43 mmol) en N,N-dimetilformamida seca
(50 mL) al matraz de fondo redondo y se agitó durante 12 h a temperatura ambiente. Se filtró la mezcla de reacción a través de un lecho de Celite, se añadió agua fría (20 mL) y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 10 mL), salmuera (10 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo resultante por cromatografía en columna (sílice 100-200) usando acetato de etilo al 10% en éter de petróleo para proporcionar 1-(4-(trifluorometiltio)fenil)etanona (2,8 g, 13,20 mmol, 45%) como un líquido amarillo claro. 1H RMN (400 MHz, CDCh) 8 8,03 - 7,89 (m, 2H), 7,75 (d, J = 7,9 Hz, 2H), 2,80 - 2,42 (m, 3H).
B. 2-oxo-2-(4-(trifluorometiltio)fenil)acetato de etilo. A una solución agitada de 1-(4-(trifluorometiltio)fenil)etanona (2,5 g, 11,79 mmol) en piridina (50 mL) se le añadió dióxido de selenio (2,61 g, 23,58 mmol) y se agitó durante 4 h a 100°C. Se diluyó la mezcla de reacción con diclorometano (50 mL) y se filtró a través de un lecho de Celite. Al filtrado se le añadió diclorometano (30 mL) seguido de cloroformiato de etilo (5 mL) a 0°C y se agitó durante 2 h. El pH de la mezcla de reacción se ajustó a pH-4 con ácido clorhídrico acuoso 1 N y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2X 10 mL), salmuera (10 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo resultante por cromatografía en columna (sílice 100-200) usando acetato de etilo al 10% en éter de petróleo para proporcionar 2-oxo-2-(4-(trifluorometiltio)fenil)acetato de etilo (2,0 g, 7,19 mmol, 62%) como un líquido. 1H RMN (400 MHz, CDCla) 8 8,12 - 8,04 (m, 2H), 7,84 - 7,72 (m, 2H), 4,61 - 4,33 (m, 2H), 1,49- 1,34 (m, 3H).
C. 2,2-difluoro-2-(4-(trifluorometiltio)fenil)acetato de etilo. A 2-oxo-2-(4-(trifluorometiltio)fenil)acetato de etilo (2,0 g, 7,19 mmol) se le añadió trifluoruro de dietilamino azufre (1,4 mL, 10,79 mmol) y se agitó durante 12 h a temperatura ambiente. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8 ) y se extrajo con acetato de etilo (3 x 50 mL). Se lavó la capa orgánica combinada con agua (2X 10 mL), salmuera (10 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(4-(trifluorometiltio)fenil)acetato de etilo (2,0 g, 6 , 66 mmol, 95%) como un líquido. 1H RMN (400 MHz, CDCh) 8 7,75 (d, J = 8,2 Hz, 2H),4,32 (q, J = 7,1 Hz, 2H), 1,32 (t, J =7,1 Hz, 3H).
D. Ácido 2,2-difluoro-2-(4-(trifluorometiltio)fenil)acético. A una solución fría agitada (0°C) de 2,2-difluoro-2-(4-(trifluorometiltio)fenil)acetato de etilo (1,5 g, 5,0 mmol) en metanol acuoso (10 mL, 80%) se le añadió hidróxido de sodio (0,4 g, 10,0 mmol) y se agitó a temperatura ambiente durante 6 h. Se concentró la mezcla de reacción y se neutralizó el residuo con ácido clorhídrico acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 20 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secaron sobre sulfato de sodio y se concentraron para proporcionar ácido 2,2-difluoro-2-(4-(trifluorometiltio)fenil)acético (1 g, 3,67 mmol, 73% de rendimiento) como un sólido marrón. MS (ESI) m/z 271,22 [M-1]+.
E. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-(trifluorometiltio)fenil)acetamida.
A una solución fría (0°C) agitada de metanosulfonato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (500 mg, 1,61 mmol) en N,N-dimetilformamida (20 mL) se añadió ácido 2,2-difluoro-2-(4-(trifluorometiltio)fenil)acético (520 mg, 1,94 mmol), N,N-diisopropiletilamina (0,86 mL, 4,8 mmol) seguido de 3-óxido hexafluorofosfato de 1 -[bis (dimetilamino)metileno]-1H-1,2,3-triazolo[4,5-b]piridinio (920 mg, 2,4 mmol) y se agitó a temperatura ambiente durante 12 h. Se diluyó la mezcla de reacción con agua (100 mL) y se filtró el sólido precipitado, se secó al vacío y se purificó mediante una columna de fase inversa Reveleris C-18 usando acetonitrilo al 70% en ácido fórmico acuoso (0,1%) para dar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-(trifluorometiltio)fenil)acetamida (60 mg, 0,11 mmol, 7% rendimiento) como un sólido blanquecino. Ms (ESI) m/z 528,07 [M+1]+. 1H r Mn (400 MHz, DMSO-d6) 8 10,98 (s, 1H), 9,76 (t, J = 6,1 Hz, 1H), 7,91 (d, J = 8,1 Hz, 2H), 7,81 -7,61 (m, 3H), 7,53-7,21 (m, 2H), 5,10 (dd, J = 13,4, 5,1 Hz, 1H) 4,57-4,10 (m, 4H), 2,85-2,93 (m, 1H), 2,72 - 2,56 (m, 1H), 2,42 - 2,26 (m, 1H), 2,10 -1,94 (m, 1H).
Ejemplo 28
2-(3-cloro-4-metilfenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida
A. 2-(3-cloro-4-metoxifenil)-2-oxoacetato de etilo. A una solución agitada de 1-(3-cloro-4-metoxifenil)etanona (2 g, 10,83 mmol) en piridina (15 mL) se añadió dióxido de selenio (3 g, 27,08 mmol) a temperatura ambiente. Se agitó la
mezcla de reacción a 100°C durante 16 h. Se filtró la mezcla de reacción a través de un lecho de Celite y se lavó con diclorometano (30 mL). Se añadió cloroformiato de etilo ( 6 mL) al filtrado a 0°C y se agitó a temperatura ambiente durante 4 h. Se inactivó la mezcla de reacción con agua con hielo y se extrajo con diclorometano (3 x 25 mL). Se lavaron las capas orgánicas combinadas con solución de clorhidrato 1 N (20 mL) y salmuera (20 mL), se secaron sobre sulfato de sodio, se filtraron y se concentraron para proporcionar 2-(3-cloro-4-metoxifenil)-2-oxoacetato de etilo (1,45 g, 5,98 mmol, 55% de rendimiento) como un líquido incoloro. MS (ESI) m/z 242,1 [M]+
B. 2-(3-cloro-4-metoxifenil)-2,2-difluoroacetato de etilo. Se añadió en porciones 2-(3-cloro-4-metoxifenil)-2-oxoacetato de etilo (1,45 g, 5,99 mmol) en trifluoruro de dietilamino azufre (2,35 mL) a 0°C y se agitó a temperatura ambiente durante 16 h. Se inactivó la mezcla de reacción con solución acuosa de bicarbonato de sodio y se extrajo con acetato de etilo (3 x 20 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secaron sobre sulfato de sodio, se filtraron y se concentraron. Se purificó el producto en bruto obtenido por cromatografía instantánea en columna (gel de sílice 100-200, acetato de etilo al 10% en éter de petróleo) para proporcionar 2-(3-cloro-4-metoxifenil)-2,2-difluoroacetato de etilo (1 g, 3,78 mmol, 63% de rendimiento) como un líquido incoloro. MS (ESI) m/z 264,1 [M]+
C. Ácido 2-(3-cloro-4-metoxifenil)-2,2-difluoroacético. A una solución agitada de 2-(3-cloro-4-metoxifenil)-2,2-difluoroacetato de etilo (1 g, 3,78 mmol) en tetrahidrofurano: etanol: agua (15 mL, 1:1:1) se le añadió hidróxido de litio monohidratado (480 mg, 11,36 mmol) y se agitó a temperatura ambiente durante 16 h. Se concentró la mezcla de reacción a presión reducida y se disolvió el residuo resultante en agua (20 mL) y se lavó con acetato de etilo (2X15 mL). Se acidificó la capa acuosa con solución de clorhidrato 1 N y se extrajo con acetato de etilo (3X15 mL). Se lavó la capa orgánica combinada con salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar ácido 2-(3-cloro-4-metoxifenil)-2,2-difluoroacético (550 mg, 2,32 mmol, 61% rendimiento) como compuesto semisólido. 1H RMN (300 MHz, DMSO-d6) 8 7,57 - 7,52 (m, 2H), 7,29 (d, J = 8,7 Hz, 1H), 3,92 (s, 3H).
D. 2-(3-cloro-4-metoxifenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. A una solución agitada de clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) en N, N-dimetilformamida seca ( 6 mL) se añadió ácido 2-(3-cloro-4-metoxifenil)-2,2-difluoroacético (252 mg, 1,07 mmol) seguido de 3-óxido hexafluorofosfato de 1-bis(dimetilamino)metileno]-1H-1,2,3-triazolo[4,5-b]piridinio (442 mg, 1,16 mmol) y diisopropiletilamina (375 mg, 2,91 mmol) a 0°C y se agitó a temperatura ambiente durante 16 h. Se concentró la mezcla de reacción a presión reducida y se disolvió el residuo obtenido en agua (15 mL) y se extrajo con acetato de etilo (3 X 15 mL). Se lavó la capa orgánica con salmuera (10 mL), se secó sobre sulfato de sodio anhidro, se filtró y se concentró. Se purificó el residuo resultante por cromatografía en columna Grace de fase inversa Reveleris C-18 (acetonitrilo al 45-55% en ácido fórmico acuoso al 0,1%) para proporcionar 2-(3-cloro-4-metoxifenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (58 mg, 11,7 mmol, 12% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 492,47 [M+1]+. 1H RMN (300 MHz, DMSO-d6 ) 8 10,98 (s, 1H), 9,62 (t, 1H), 7,68 (d, J = 7,8 Hz, 1H), 7,60 (d, J = 2,3 Hz, 1H), 7,53 (d, J = 8,7 Hz, 1H), 7,41 (s, 1H), 7,37 (d, J = 8,0 Hz, 1H), 7,29 (d, J = 8,7 Hz, 1H), 5,10 (dd, J = 13,2, 5,1 Hz, 1H), 4,45 (d, J = 5,4 Hz, 2H), 4,42 (d, J = 17,9 Hz, 1H), 4,28 (d, J = 17,9 Hz, 1H), 3,91 (s, 3H), 2,96 - 2,86 (m, 1H), 2,64 - 2,55 (m, 1H), 2,47 - 2,25 (m, 1H), 2,08 - 1,94 (m, 1H).
Ejemplo 29
N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdolm-5-il)metM)-2,2-difluoro-2-(m-tolil)acetamida
A. 2-oxo-2-m-tolilacetato de etilo. A una solución agitada de 1-m-toliletanona (3,0 g, 22,37 mmol) en piridina (50 mL) se le añadió dióxido de selenio (4,96 g, 44,74 mmol) y se agitó durante 16 h a 100°C. Se diluyó la mezcla de reacción con diclorometano (50 mL) y se filtró a través de un lecho de Celite. Al filtrado se le añadió cloroformiato de etilo ( 6 mL) a 0°C y se agitó durante 2 h. Se neutralizó la mezcla de reacción con ácido clorhídrico acuoso 1 N (hasta pH-4) y se extrajo con acetato de etilo (2 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 100 mL), salmuera (100 mL) y se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo resultante por cromatografía en columna (sílice 100 -2 00 ) usando acetato de etilo al 10 % en éter de petróleo para proporcionar 2 -oxo-2-m-tolilacetato de etilo (2,0 g, 10,41 mmol, 46,6%) como un líquido. GC-MS (ESI) m/z 192,2.
B. 2,2-difluoro-2-m-tolilacetato de etilo. Una solución agitada de 2-oxo-2-m-tolilacetato de etilo (2,0 g, 10,41 mmol) se hizo reaccionar con trifluoruro de dietilamino azufre (3,41 mL, 26,02 mmol) y se agitó durante 12 h a temperatura ambiente. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8 ) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secaron sobre sulfato de sodio y se concentraron para proporcionar 2,2-difluoro-2-m-tolilacetato de etilo (1,2 g, 5,60 mmol, 52,4%) como un líquido. GC-MS (ESI) m/z 214,1.
C. Ácido 2,2-difluoro-2-m-tolilacético. A una solución fría (0°C) agitada de acetato de 2,2-difluoro-2-m-tolilacetato de etilo (1,2 g, 7,47 mmol) en una mezcla de disolvente de tetrahidrofurano-metanol-agua (45 mL, 1:1:1), se añadió hidróxido de litio (1,85 g, 44,84 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con ácido clorhídrico acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 20 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secaron sobre sulfato de sodio y se concentraron para proporcionar ácido 2,2-difluoro-2-m-tolilacético (900 mg, 4,83 mmol, 86,5% de rendimiento) como un sólido marrón. MS (ESI) m/z 185,21 [M-1]-.
D. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(m-tolil)acetamida. A una solución agitada fría (0°C) de ácido 2,2-difluoro-2-m--tolilacético (216,6 mg, 0,970 mmol) en piridina (10 mL) se le añadió tricloruro de fósforo (0,3 mL, 2,912 mmol) y se agitó a 0°C-5°C durante 1 h. (300 mg, 2,40 mmol) se añadió a la mezcla de reacción a 0°C y se continuó agitando a temperatura ambiente durante 1 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8 ) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el producto en bruto por cromatografía en columna Grace de fase inversa Reveleris C-18 usando acetonitrilo al 45% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(m-tolil)acetamida (63 mg, 0,147 mmol, 14,7% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 442,25 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 8 10,98 (s, 1H), 9,61 (t, J = 6,1 Hz, 1H), 7,68 (d, J = 7,8 Hz, 1H), 7,48-7,32 (m, 6 H), 5,10 (dd, J =13,3, 5,0 Hz, 1H), 4,49 - 4,22 (m, 4H), 2,98-2,82 (m, 1H), 2,64 2,53 (m, 1H), 2,45 - 2,24 (m, 4H), 2,05 - 1,93 (m, 1H).
Ejemplo 30
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-isopropoxifenil)acetamida
A. 1-(4-isopropoxifenil)etanona. A una solución agitada de 1-(4-hidroxifenil)etanona (2,5 g, 18,38 mmol) en N,N-dimetilformamida se le añadió carbonato de potasio (6,34 g, 45,95 mmol) seguido de yoduro de isopropilo (4,59 g, 27,57 mmol) a 0°C y a continuación se calentó a 100°C durante 16 h. Se inactivó la mezcla de reacción con agua con hielo y se extrajo con acetato de etilo (3 x 25 mL). Se lavaron las capas orgánicas combinadas con salmuera (25 mL), se secaron sobre sulfato de sodio, se filtraron y se concentraron. Se purificó el compuesto en bruto obtenido por cromatografía en columna instantánea (gel de sílice 100-200, acetato de etilo al 20%/éter de petróleo) para proporcionar 1-(4-isopropoxifenil)etanona (2 g, 11,23 mmol, 61% de rendimiento) como un líquido. MS (ESI) m/z 179,13 [M+H]+
B. 2-(4-isopropoxifenil)-2-oxoacetato de etilo. A una solución agitada de 1-(4-isopropoxifenil)etanona (3 g, 16,85 mmol) en piridina (15 mL) se le añadió dióxido de selenio (4,67 g, 42,1 mmol) a temperatura ambiente y se agitó a 100°C durante 16 h. Se filtró la mezcla de reacción a través de un lecho de Celite y se lavó con diclorometano (30 mL). Se enfrió el filtrado a 0°C, se trató con cloroformiato de etilo ( 6 mL) y se agitó a temperatura ambiente durante 4 h. Se inactivó la mezcla de reacción con agua con hielo y se extrajo con diclorometano (3 x 30 mL). Se lavaron las capas orgánicas combinadas con solución de clorhidrato 1 N (30 mL), salmuera (30 mL), se secaron sobre sulfato de sodio, se filtraron y se concentraron para proporcionar 2-(4-isopropoxifenil)-2-oxoacetato de etilo (3 g, 12,76 mmol, 75% de rendimiento) como un líquido incoloro. MS (ESI) m/z 236,2 [M]+
C. 2,2-difluoro-2-(4-isopropoxifenil)acetato de etilo. A 2-(4-isopropoxifenil)-2-oxoacetato de etilo (3 g, 12,76 mmol) se le añadió trifluoruro de dietilamino azufre (4,9 mL) a 0°C y se agitó a temperatura ambiente durante 16 h. Se inactivó
la mezcla de reacción con solución acuosa de bicarbonato de sodio y se extrajo con acetato de etilo (3 x 30 mL). Se lavó la capa orgánica con salmuera (30 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto obtenido por cromatografía instantánea en columna (gel de sílice 100 -20 0 , acetato de etilo al 10%/éter de petróleo) para proporcionar acetato de 2,2-difluoro-2-(4-isopropoxifenil)etilo (2 g, 7,75 mmol, 61% de rendimiento) como un líquido incoloro. MS (ESI) m/z 258,2 [M+H]+.
D. Ácido 2,2-difluoro-2-(4-isopropoxifenil)acético. A una solución agitada de 2,2-difluoro-2-(4-isopropoxifenil)acetato de etilo (2 g, 7,75 mmol) en tetrahidrofurano: etanol: agua (20 mL, 1:1:1) se le añadió hidróxido de litio monohidratado (1,6 g, 38,75 mmol) y se agitó a temperatura ambiente durante 16 h. Se concentró la mezcla de reacción a presión reducida y se disolvió el residuo resultante en agua (20 mL) y se lavó con acetato de etilo (2 X 20 mL). Se acidificó la capa acuosa con solución de clorhidrato 1 N y se extrajo con acetato de etilo (3 X 20 mL). Se lavó la capa orgánica combinada con salmuera (20 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar ácido 2,2-difluoro-2-(4-isopropoxifenil)acético (1,2 g, 5,21 mmol, 67% de rendimiento) como compuesto semisólido. 1H RMN (300 MHz, DMSO-d6) 8 7,47 (d, J = 8,7 Hz, 2H), 7,03 (d, J =9 Hz, 2H), 4,71 -4,63 (m, 1H), 1,28 (d, J = 6 Hz, 6 H).
E. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-isopropoxifenil)acetamida. A una solución enfriada con hielo de ácido 2,2-difluoro-2-(4-isopropoxifenil)acético (267 mg, 1,16 mmol) en piridina ( 6 mL) se le añadió cloruro de fosforilo (0,27 mL, 2,91 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A continuación, se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) a la mezcla de reacción y se agitó a temperatura ambiente durante 30 minutos. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8 ) y se extrajo con acetato de etilo (3 X 15 mL). Se lavó la capa orgánica combinada con agua (15 mL) salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el residuo resultante por cromatografía en columna de fase inversa Reveleris C-18 (acetonitrilo al 45-55% en ácido fórmico acuoso al 0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1 -oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-isopropoxifenil)acetamida (27 mg, 0,05 mmol, 6 % de rendimiento) como un sólido blanquecino. MS (ESI) m/z 486,09 [M+1]+. 1H RMN (400 MHz, DMSO-d6) 8 10,98 (s, 1H), 9,56 (t, J = 6,3 Hz, 1H), 7,67 (d, J = 7,7 Hz, 1H), 7,48 (d, J = 8,4 Hz, 2H), 7,43 - 7,33 (m, 2H), 7,03 (d, J = 8,4 Hz, 2H), 5,10 (dd, J = 13,3, 5,2 Hz, 1H), 4,74 - 4,62 (m, 1H), 4,49 -4,27 (m, 4H), 3,02 - 2,83 (m, 1H), 2,69 - 2,58 (m, 1H), 2,39 - 2,28 (m, 1H), 2,05 - 1,95 (m, 1H), 1,27 (d, J = 6,0 Hz, 6 H).
Ejemplo 31
2-(3,4-difluorofenil)-N-((2-(2,6-dioxopiperldin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida
A. 2-(3,4-difluorofenil)-2-oxoacetato de etilo. A una solución agitada de 1-(3,4-difluorofenil)etanona (1 g, 6,4 mmol) en piridina (15 mL) se le añadió dióxido de selenio (1,7 g, 16,01 mmol) a temperatura ambiente. Se agitó la mezcla de reacción a 100°C durante 16 h. Se filtró la mezcla de reacción a través de un lecho de Celite y se lavó con diclorometano (30 mL). Se añadió cloroformiato de etilo (4 mL) al filtrado a 0°C y se agitó a temperatura ambiente durante 4 h. Se inactivó la mezcla de reacción con agua con hielo y se extrajo con diclorometano (3 x 25 mL). Se lavaron las capas orgánicas combinadas con solución de clorhidrato 1 N (20 mL) y salmuera (20 mL), se secaron sobre sulfato de sodio, se filtraron y se concentraron para proporcionar 2-(3,4-difluorofenil)-2-oxoacetato de etilo (750 mg, 3,50 mmol, 55% de rendimiento) como un líquido incoloro. MS (ESI) m/z 214,1 [M]+.
B. 2-(3,4-fluorofenil)-2,2-difluoroacetato de etilo. Se añadió 2-(3,4-difluorofenil)-2-oxoacetato de etilo (750 mg, 3,5 mmol) al trifluoruro de dietilamino azufre (1,37 mL) en atmósfera de nitrógeno a 0°C y se agitó a temperatura ambiente durante 16 h. Se inactivó la mezcla de reacción con solución acuosa de bicarbonato de sodio y se extrajo con acetato de etilo (3 x 20 mL). Se lavó la capa orgánica con salmuera (20 mL), se secó sobre sulfato de sodio anhidro, se filtró y se concentró. Se purificó el producto en bruto obtenido por cromatografía instantánea en columna (gel de sílice 100 200, acetato de etilo al 10% en éter de petróleo) para proporcionar 2-(3,4-difluorofenil)-2,2-difluoroacetato de etilo (520 g, 2,20 mmol, 63% de rendimiento) como un líquido incoloro. MS (ESI) m/z 236,1 [m ]+.
C. Ácido 2-(3,4-difluorofenil)-2,2-difluoroacético. A una solución agitada de 2-(3,4-difluorofenil)-2,2-difluoroacetato
de etilo (500 mg, 2,11 mmol) en tetrahidrofurano: etanol: agua (15 mL, 1: 1: 1) se le añadió hidróxido de litio monohidratado (267 mg, 6,35 mmol) y se agitó a temperatura ambiente durante 16 h. Se extrajeron los productos volátiles a presión reducida y se disolvió el producto en bruto obtenido en agua (15 mL) y se lavó con acetato de etilo (2X10 mL). Se acidificó la capa acuosa con solución de clorhidrato 1 N y se extrajo con acetato de etilo (3X15 mL). Se lavó la capa orgánica combinada con salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar ácido 2-(3,4-difluorofenil)-2,2-difluoroacético (300 mg, 1,44 mmol, 68 % de rendimiento) como compuesto semisólido. MS (ESI) m/z 208,1 [M]+.
D. 2-(3,4-difluorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. A una solución agitada de clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) en N,N-dimetilformamida seca ( 6 mL) se añadió ácido 2-(3,4-difluorofenil)-2,2-difluoroacético (222 mg, 1,07 mmol) seguido de 3-óxido hexafluorofosfato de 1-bis(dimetilamino)metileno]-1H-1,2,3-triazolo[4,5-b]piridinio (442 mg, 1,16 mmol) y diisopropiletilamina (0,5 mL, 2,91 mmol) a 0°C y se agitó a temperatura ambiente durante 16 h. Se concentró la mezcla de reacción a presión reducida y se disolvió el producto en bruto obtenido en agua (10 mL) y se extrajo con acetato de etilo (3 X 10 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secaron sobre sulfato de sodio anhidro, se filtraron y se concentraron. Se purificó el residuo resultante por cromatografía en columna Grace de fase inversa Reveleris C-18 (acetonitrilo al 45-55% en ácido fórmico acuoso al 0,1%) para proporcionar 2-(3,4-difluorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (75 mg, 0,16 mmol, 17% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 463,99 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 8 10,98 (s, 1H), 9,69 (t, J = 5,9 Hz, 1H), 7,72 - 7,62 (m, 2H), 7,61 (d, J = 8,4 Hz, 1H), 7,51 - 7,44 (m, 1H), 7,43 (s, 1H), 7,37 (d, J = 7,8 Hz, 1H), 5,10 (dd, J =13,3, 5,0 Hz, 1H),4,46(d, J =5,4 Hz, 2H), 4,43 (d, J =17,4 Hz, 1H), 4,29 (d, J =17,1 Hz, 1H), 2,98 - 2,87 (m, 1H), 2,65 - 2,56 (m, 1H), 2,45 - 2,29 (m, 1H), 2,08 - 1,90 (m, 1H).
Ejemplo 32
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-fluorofenil)acetamida
A. 2-(3-fluorofenil)-2-oxoacetato de etilo. A una solución agitada de 1-(3-fluorofenil)etanona (2 g, 14,48 mmol) en piridina (15 mL) se le añadió dióxido de selenio (4,01 g, 36,19 mmol) a temperatura ambiente. Se agitó la mezcla de reacción a 100°C durante 16 h. Se filtró la mezcla de reacción a través de un lecho de Celite y se lavó con diclorometano (30 mL). Se añadió cloroformiato de etilo ( 6 mL) al filtrado a 0°C y se agitó a temperatura ambiente durante 4 h. Se inactivó la mezcla de reacción con agua con hielo y se extrajo con diclorometano (3 x 25 mL). Se lavaron las capas orgánicas combinadas con solución de clorhidrato 1 N (20 mL) y salmuera (20 mL), se secaron sobre sulfato de sodio, se filtraron y se concentraron para proporcionar 2-(3-fluorofenil)-2-oxoacetato de etilo (1,5 g, 7,65 mmol, 53% de rendimiento) como un líquido incoloro. MS (ESI) m/z 196,1 [M]+.
B. 2,2-difluoro-2-(3-fluorofenil)acetato de etilo. Se añadió 2-(3-fluorofenil)-2-oxoacetato de etilo (1,5 g, 7,65 mmol) al trifluoruro de dietilamino azufre (3 mL) a 0°C y se agitó a temperatura ambiente durante 16 h. Se inactivó la mezcla de reacción con solución acuosa de bicarbonato de sodio y se extrajo con acetato de etilo (3 x 20 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secaron sobre sulfato de sodio anhidro, se filtraron y se concentraron. Se purificó el producto en bruto obtenido por cromatografía instantánea en columna (gel de sílice 100 200, acetato de etilo al 10% en éter de petróleo) para proporcionar 2,2-difluoro-2-(3-fluorofenil)acetato de etilo (850 mg, 3,89 mmol, 90% de rendimiento) como un líquido incoloro. MS (ESI) m/z 218,1 [M]+.
C. Ácido 2,2-difluoro-2-(3-fluorofenil)acético. A una solución agitada de 2,2-difluoro-2-(3-fluorofenil)acetato de etilo (850 mg, 3,89 mmol) en tetrahidrofurano: etanol: agua (15 mL, 1:1:1) se añadió hidróxido de litio monohidratado (491 mg, 11,69 mmol) y se agitó a temperatura ambiente durante 16 h. Se concentró la mezcla de reacción a presión reducida y se disolvió el producto en bruto en agua (15 mL) y se lavó con acetato de etilo (2X10 mL). Se acidificó la capa acuosa con solución de clorhidrato 1 N y se extrajo con acetato de etilo (3 X 15 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL) se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar ácido 2,2-difluoro-2-(3-fluorofenil)acético (500 mg, 2,63 mmol, 67% de rendimiento) como un compuesto semisólido. MS (ESI) m/z 190,1 [M]+.
D. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-fluorofenil)acetamida. A una solución agitada de clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (203 mg, 1,07 mmol) en N,N-dimetilformamida seca. ( 6 mL) se añadió ácido 2,2-difluoro-2-(3-fluorofenil)acético (300 mg, 0,97 mmol) seguido por 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metileno]-1H-1,2,3-triazolo[4,5-b]piridinio (442 mg, 1,16 mmol) y N,N-diisopropiletilamina (375 mg, 2,91 mmol) a 0°C y se agitó a temperatura ambiente durante 16 h. Se concentró la mezcla de reacción a presión reducida y se disolvió el producto en bruto obtenido en agua (10 mL) y se extrajo con acetato de etilo (3X 10 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el compuesto en bruto obtenido por cromatografía de columna en fase inversa Reveleris C-18 (acetonitrilo al 45-55% en ácido fórmico acuoso al 0,1% para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-fluorofenil)acetamida (45 mg, 0,1 mmol, 10% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 446,04 [M+1]+. 1H RMN (300 MHz, DMSO-da) 8 10,98 (s, 1H), 9,68 (t, J = 5,9 Hz, 1H), 7,67 (d, J = 8,1 Hz, 1H), 7,60 (dd, J = 13,5, 7,8 Hz, 1H), 7,47 - 7,41 (m, 4H), 7,36 (d, J = 8,1 Hz, 1H), 5,10 (dd, J = 13,3, 5,0 Hz, 1H), 4,46 (d, J = 5,7 Hz, 2H), 4,42 (d, J = 15,0 Hz, 1H), 4,28 (d, J = 17,4 Hz, 1H), 2,96-2,86 (m, 1H), 2,65 - 2,54 (m, 1H), 2,46 - 2,28 (m, 1H), 2,05 - 1,92 (m, 1H).
Ejemplo 33
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(trifluorometil)piridin-2-il)acetamida
A. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(trifluorometil)piridin-2-il)acetamida. Se colocó ácido mesílico de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (0,050 g, 0,135 mmol) en un vial con N,N-dimetilformamida (1,0 mL), ácido 2,2-difluoro-2-(3-(trifluorometil)piridin-2-il)acético (0,033 g, 0,135 mmol), diisopropiletilamina (0,071 mL, 0,406 mmol) y 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metileno]-1H-1,2,3-triazolo[4,5-b]piridinio (0,057 g, 0,149 mmol). Se agitó la mezcla de reacción a t.a. durante 18 h. Se recogió la mezcla de reacción en dimetilsulfóxido y se purificó usando HPLC semipreparatoria de fase inversa (acetonitrilo al 5-100% ácido fórmico al 0,1% en agua ácido fórmico al 0,1%, durante 20 min). Se combinaron fracciones que contenían el producto deseado y se eliminaron los productos orgánicos volátiles a presión reducida para dar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(trifluorometil)piridin-2-il)acetamida (0,033 g, 0,066 mmol, 49,1% de rendimiento) como un sólido blanco. 1H RMN (500 MHz, DMSO-d6) 8 10,98 (s, 1H), 9,59 (t, J = 6,15 Hz, 1H), 8,99 (d, J = 4,73 Hz, 1H), 8,47 (dd, J = 1,26, 8,20 Hz, 1H), 7,88 (dd, J = 4,73, 8,20 Hz, 1H), 7,74 (d, J = 7,57 Hz, 1H), 7,60 (s, 1H), 7,51 (dd, J = 0,63, 7,88 Hz, 1H), 5,12 (dd, J = 5,20, 13,40 Hz, 1H), 4,55 (d, J = 6,31 Hz, 2H), 4,49 (d, J =17,34 Hz, 1H),4,32-4,37 (m, 1H), 2,88-2,97 (m, 1H), 2,58-2,64 (m, 1H), 2,36-2,46 (m, 1H), 2,02 (dtd, J = 2,21, 5,16, 12,69 Hz, 1H). MS (ESI) m/z 497,4 [M+1]+.
Ejemplo 34
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)2,2-difluoro-2-(4-isopropilfenil)acetamida
A. 2-(4-isopropilfenil)-2-oxoacetato de etilo. A una solución agitada de 1-(4-isopropilfenil)etanona (2,0 g, 12,33 mmol) en piridina (25 mL) se añadió dióxido de selenio (3,42 g, 30,82 mmol) y se agitó durante 16 h a 100°C. Se diluyó la mezcla de reacción con diclorometano (50 mL) y se filtró a través de un lecho de Celite. Al filtrado se añadió
cloroformiato de etilo ( 6 mL) a 0°C y se agitó durante 2 h. Se diluyó la mezcla de reacción con agua (50 mL) y se extrajo con diclorometano (3 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-(4-isopropilfenil)-2-oxoacetato de etilo (2,0 g, 9,09 mmol, 74% de rendimiento). MS (ESI) m/z 221,29 [M+1]+.
B. 2,2-difluoro-2-(4-isopropilfenil)acetato de etilo. A 2-(4-isopropilfenil)-2-oxoacetato de etilo (1,0 g, 4,27 mmol) se añadió trifluoruro de dietilamino azufre (3 mL) a 0°C y se agitó a temperatura ambiente durante 16 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8 ) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 25 mL), salmuera (25 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(4-isopropilfenil)acetato de etilo (1,0 g, 4,13 mmol, 91% de rendimiento). GCMS (m/z) 242,2 [M]+.
C. Ácido 2,2-difluoro-2-(4-isopropilfenil)acético. A una solución agitada de 2,2-difluoro-2-(4-isopropilfenil)acetato de etilo (1,0 g, 4,13 mmol) en tetrahidrofurano:metanol:agua (30 mL, 1:1:1) se añadió hidróxido de litio ( 868 mg, 20,66 mmol) y se agitó a temperatura ambiente durante 4 h. Se concentró la mezcla de reacción y se neutralizó el residuo con bisulfato de potasio saturado (20 mL) y se extrajo con acetato de etilo (2 X 25 mL). Se lavaron las capas orgánicas combinadas con salmuera (25 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(4-isopropilfenil)acético (700 mg, 3,27 mmol, 79% de rendimiento) como un líquido marrón. MS (ESI) m/z 213,33 [M-1 ]+.
D. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-isopropilfenil)acetamida. A una solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(4-isopropilfenil)acético (200 mg, 0,93 mmol) en piridina (20 mL) se añadió cloruro de fosforilo (429 mg, 2,80 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A esta mezcla de reacción se añadió a continuación clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (290 mg, 0,93 mmol) y se agitó a temperatura ambiente durante 30 min. Se neutralizó la mezcla de reacción con bicarbonato de sodio saturado acuoso (hasta pH-8 ) y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 50-55% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-isopropilfenil)acetamida (85 mg, 0,18 mmol, 19% de rendimiento) como un solido amarillo claro. MS (ESI) m/z 470,21 [M+1]+. 1H RMN (300MHz, DMSO-d6) 8 10,99 (s, 1H), 9,60 (t, J=6,1 Hz, 1H), 7,67 (d, J=8,1 Hz, 1H), 7,57-7,47 (m, 2H), 7,45 - 7,30 (m, 4H), 5,10 (dd, J=5,1, 13,2 Hz, 1H), 4,48 - 4,22 (m, 4H), 3,02 - 2,84 (m, 2H), 2,74 - 2,54 (m, 1H), 2,46-2,30 (m, 1H), 2,05- 1,93 (m, 1H), 1,3-1,12 (m, 6 H).
Ejemplo 35
2-(2,4-diclorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida
A. 2-(2,4-diclorofenil)-2-oxoacetato de etilo. A una solución agitada de 1-(2,4-diclorofenil)etanona (3,0 g, 15,87 mmol) en piridina (20 mL) se añadió dióxido de selenio (3,5 g, 31,74 mmol) y se agitó a 100°C durante 16 h. Se diluyó la mezcla de reacción con diclorometano (30 mL) y se filtró a través de un lecho de Celite. Al filtrado se le añadió cloroformiato de etilo ( 6 mL) a 0°C y se agitó a temperatura ambiente durante 3 h. Se neutralizó la mezcla de reacción con ácido clorhídrico acuoso 1 N (hasta pH-4) y se extrajo con acetato de etilo (2 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-(2,4-diclorofenil)-2-oxoacetato de etilo (3,0 g, 12,19 mmol, 76% de rendimiento). 1H RMN cumple. 1H RMN (400MHz, DMSO-d6) 8 7,88 - 7,82 (m, 2H), 7,65 (d, J=8,4 Hz, 1H), 4,37 (q, J=7,0 Hz, 2H), 1,30 (t, J=7,0 Hz, 3H),
B.2-(2,4-diclorofenil)-2,2-difluoroacetato de etilo. Se agitó una solución de 2-(2,4-diclorofenil)-2-oxoacetato de etilo (1,0 g, 4,58 mmol) y trifluoruro de dietilamino azufre (3,7 g, 22,89 mmol) a temperatura ambiente durante 16 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8 ) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 30 mL), salmuera (30 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-(2,4-diclorofenil)-2,2-difluoroacetato de etilo (1,0 g, 3,73 mmol,
92% de rendimiento). GCMS (m/z) 268 [M]+.
C. Ácido 2-(2,4-diclorofenil)-2,2-difluoroacético. A una solución agitada de 2-(2,4-didorofenil)-2,2-difluoroacetato de etilo (1,0 g, 3,73 mmol) en mezcla de tetrahidrofurano:metanol:agua (30 mL, 1:1:1) se añadió hidróxido de litio monohidratado (940,2 mg, 22,38 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con ácido clorhídrico acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 50 mL). Se lavaron las capas orgánicas combinadas con salmuera ( 20 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2-(2,4-diclorofenil)-2,2-difluoroacético (800 mg, 3,33 mmol, 89% de rendimiento. MS (ESI) m/z 241 [M+2]+.
D. 2-(2,4-didorofenM)-N-((2-(2,6-dioxopiperidm-3-M)-1-ozolsomdoMn-5-M)metM)-2,2-difluoroacetamida. A una solución agitada en frío (0 °C) de ácido 2-(2,4-diclorofenil)-2,2-difluoroacético (279,6 mg, 1,165 mmol) en piridina ( 10 mL) se añadió cloruro de fosforilo (0,3 mL, 2,91 mmol) y se agitó a 0-5°C durante 30 min. A una mezcla de reacción se le añadió a continuación clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) y se agitó a temperatura ambiente durante 1 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8 ) y se extrajo con acetato de etilo (2 X 25 mL). Se lavaron las capas orgánicas combinadas con agua (25 mL), salmuera (25 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna Grace de fase inversa Reveleris C-18 usando acetonitrilo al 50-55% en ácido fórmico acuoso (0,1%) para proporcionar 2-(2,4-diclorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (60 mg, 0,12 mmol, 12% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 496,03 [M+1]+.
1H RMN (300MHz, DMSO-d6) 8 10,99 (m, 1H), 9,70 (t, J=6,3 Hz, 1H), 7,84 - 7,65 (m, 3H), 7,66 - 7,57 (d, J=8,4 Hz, 1H), 7,50 (s, 1H), 7,44 (d, J=80 Hz, 1H), 5,11 (dd, J=5,1, 13,2 Hz, 1H), 4,49 (brd, J=5,5 Hz, 2H), 4,43 (s, 1H), 4,34 (s, 1H), 4,28 (s, 1H), 2,99 - 2,84 (m, 1H), 2,60 - 2,57 (m, 1H), 2,44 - 2,31 (m, 1H), 2,05 - 1,94 (m, 1H).
Ejemplo 36
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-metoxifenil)acetamida
A. 2-(2-metoxifenil)-2-oxoacetato de etilo. A una solución agitada de 1-(2-metoxifenil)etanona (2,0 g, 13,32 mmol) en piridina (25 mL) se añadió dióxido de selenio (3,7 g, 33,29 mmol) y se agitó durante 16 h a 100°C. Se diluyó la mezcla de reacción con diclorometano (50 mL) y se filtró a través de un lecho de Celite. Al filtrado se le añadió cloroformiato de etilo ( 6 mL) a 0°C y se agitó durante 2 h. Se diluyó la mezcla de reacción con agua (30 mL) y se extrajo con acetato de etilo (3 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-(2-metoxifenil)-2-oxoacetato de etilo (2,0 g, 9,62 mmol, 72% de rendimiento). Gc Ms (m/z) 208,2 [M]+.
B. 2,2-difluoro-2-(2-metoxifenil)acetato de etilo. A 2-(2-metoxifenil)-2-oxoacetato de etilo (1,0 g, 4,81 mmol) se añadió trilfuoruro de dietilamino azufre (3 mL) a 0°C y se agitó a temperatura ambiente durante 16 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8 ) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 25 mL), salmuera (25 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(2-metoxifenil)acetato de etilo (1,0 g, 4,35 mmol, 90% de rendimiento). GCMS (m/z) 230,2 [M+].
C. Ácido 2,2-difluoro-2-(2-metoxifenil)acético. A una solución agitada de 2,2-difluoro-2-(2-metoxifenil)acetato de etilo (1,0 g, 4,35 mmol) en mezcla de tetrahidrofurano:metanol:agua (30 mL, 1:1:1) se añadió hidróxido de litio monohidratado (913 mg, 21,74 mmol) y se agitó a temperatura ambiente durante 4 h. Se concentró la mezcla de reacción y se neutralizó el residuo con bisulfato de potasio saturado (20 mL) y se extrajo con acetato de etilo (2 X 25 mL). Se lavaron las capas orgánicas combinadas con salmuera (25 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(2-metoxifenil)acético (700 mg, 3,46 mmol, 79% de rendimiento). MS (ESI) m/z 201,29 [M-1]+.
D. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-metoxifenil)acetamida. A una
solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(2-metoxifenil)acético (200 mg, 0,99 mmol) en piridina (20 mL) se añadió cloruro de fosforilo (454 mg, 0,99 mmol) gota a gota y se agitó a 0-5°C durante 1 h y a continuación se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (306 mg, 0,99 mmol) y se agitó a temperatura ambiente durante 30 min. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8 ) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 50-55% en ácido fórmico acuoso (0,1%) para dar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-metoxifenil)acetamida (80 mg, 0,17 mmol, 17% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 458,15 [M+1]+. 1H RMN (300MHz, DMSO-da) 8 10,99 (s, 1H), 9,37 (t, J=5,9 Hz, 1H), 7,73 (d, J=77 Hz, 1H), 7,59-7,41 (m, 4H), 7,17-7,03 (m, 2H), 5,11 (dd, J=5,0, 13,0 Hz, 1H), 4,53-4,26 (m, 4H), 3,66 (s, 3H), 3,01 -2,85(m, 1H), 2,74-2,54 (m, 1H), 2,45-2,29 (m, 1H), 2,09- 1,90 (m, 1H)
Ejemplo 37
2-(4-cidopropMfenM)-N-((2-(2,6-dioxopiperidm-3-M)-1-oxolsomdoMn-5-M)metM)-2,2-difluoroacetamida
A. 1-(4-ciclopropilfenil)etanona. A una solución agitada y desgasificada de 1-(4-bromofenil)etanona (1 g, 5,02 mmol) en agua: a 1,4-dioxano (1:10, 50 mL) se le añadió ácido ciclopropilborónico (519 mg, 6,02 mmol) seguido por fosfato de potasio (3,2 g, 15,07 mmol), complejo [1,1'-bis(difenilfosfino)ferroceno]dicloropaladio (II) diclorometano (205 mg, 0,25 mmol). Se desgasificó la mezcla de reacción durante 10 min y se calentó a 100°C durante 8 h. Se enfrió la mezcla de reacción a temperatura ambiente y se filtró a través del lecho de celite. Al filtrado se le añadió agua fría (50 mL) y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo resultante por cromatografía de columna (sílice 100-200) usando acetato de etilo en éter de petróleo al 20% para proporcionar 1-(4-ciclopropilfenil)etanona (700 mg, 4,37 mmol, 87% de rendimiento). GCMS (m/z) 160,2 [M]+.
B. 2-(4-ciclopropilfenil)-2-oxoacetato de etilo. A una solución agitada de 1-(4-ciclopropilfenil)etanona (700 mg, 4,37 mmol) en piridina (10 mL) se añadió dióxido de selenio (1,2 g, 10,93 mmol) y se agitó a 100°C durante 16 h. Se diluyó la mezcla de reacción con diclorometano (20 mL) y se filtró a través de un lecho de Celite. Al filtrado se le añadió cloroformiato de etilo (2 mL) a 0°C y se agitó a temperatura ambiente durante 3 h. Se neutralizó la mezcla de reacción con ácido clorhídrico acuoso 1 N (hasta pH-4) y se extrajo con acetato de etilo (2 X 60 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 30 mL), salmuera (30 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-(4-ciclopropilfenil)-2-oxoacetato de etilo (890 mg, 4,08 mmol, 93% de rendimiento). GCMS (m/z) 218,2 [M]+
C. 2-(4-ciclopropilfenil)-2,2-difluoroacetato de etilo. Se agitó una solución de 2-(4-ciclopropilfenil)-2-oxoacetato de etilo (890 mg, 4,08 mmol) ytrifluoruro de dietilamino azufre (3,7 g, 22,89 mmol) a temperatura ambiente durante 16 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8 ) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 30 mL), salmuera (30 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-(4-ciclopropilfenil)-2,2-difluoroacetato de etilo (920 mg, 3,83 mmol, 94% de rendimiento). GCMS (m/z) 240,2 [M]+
D. Ácido 2-(4-ciclopropilfenil)-2,2-difluoroacético. A una solución agitada de 2-(4-ciclopropilfenil)-2,2-difluoroacetato de etilo (920 mg, 3,83 mmol) en tetrahidrofurano-metanol-agua (30 mL, 1:1:1) se añadió hidróxido de litio monohidratado (483 mg, 11,49 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con ácido clorhídrico acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 50 mL). Se lavaron las capas orgánicas combinadas con salmuera ( 20 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2-(4-ciclopropilfenil)-2,2-difluoroacético (750 mg, 3,53 mmol, 92% de rendimiento). GCMS (m/z) 212,1 [M]+.
E. 2-(4-ciclopropMfenM)-N-((2-(2,6-dtoxopiperidm-3-M)-1-oxoisomdoMn-5-M)metM)-2,2-difluoroacetamida. A una solución agitada en frío (0°C) de ácido 2-(4-ciclopropilfenil)-2,2-difluoroacético (200 mg, 0,943 mmol) en piridina (10 mL) se añadió cloruro de fosforilo (0,4 mL, 2,830 mmol) y se agitó a 0-5°C durante 30 min. A esta mezcla de reacción se le añadió a continuación clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (359 mg, 1,16 mmol) y se agitó a temperatura ambiente durante 1 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8 ) y se extrajo con acetato de etilo (2 X 25 mL). Se lavaron las capas orgánicas combinadas con agua (25 mL), salmuera (25 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 40-45% en ácido fórmico acuoso (0,1%) para proporcionar 2-(4-ciclopropilfenil)-N-((2-(2,6-dioxopiperidin-3-M)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (90 mg, 0,192 mmol, 20,0% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 468,13 [M+1]+. 1H RMN (300MHz, DMSO-d6) 8 10,99 (s, 1H), 9,58 (t, J=5,9 Hz, 1H), 7,67 (d, J=8,1 Hz, 1H), 7,44 (d, J=8,1 Hz, 2H), 7,39-7,31 (m, 2H), 7,21 (d, J=8,1 Hz, 2H), 5,10(dd, J=5,1, 13,2 Hz, 1H), 4,49-4,21 (m, 4H), 3,00-2,81 (m, 1H), 2,67 - 2,56 (m, 1H), 2,45 - 2,29 (m, 1H), 2,07 - 1,92 (m, 2H), 1,04 - 0,97 (m, 2H), 0,55 - 0,77 (m, 2H).
Ejemplo 38
2-(4-cloro-2-fluorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroncetamida
A. 2-(4-cloro-2-fluorofenil)-2-oxoacetato de etilo. A una solución agitada de 1-(4-cloro-2-fluorofenil)etanona (2,0 g, 11,588 mmol) en piridina (30 mL) se añadió dióxido de selenio (2,57 g, 23,176 mmol) y se agitó durante 16 h a 100°C. Se diluyó la mezcla de reacción con diclorometano (30 mL) y se filtró a través de un lecho de Celite. Al filtrado se le añadió cloroformiato de etilo (4 mL) a 0°C y se agitó durante 2 h. A la mezcla de reacción se le añadió agua (30 mL) y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 20 mL), salmuera (20 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía de columna (sílice 100-200) usando acetato de etilo al 5-10% en éter de petróleo para proporcionar 2-(4-cloro-2-fluorofenil)-2-oxoacetato de etilo (1,71 g, 7,434 mmol, 64% de rendimiento) como un líquido incoloro. MS (ESI) m/z 230,1.
B. 2-(4-cloro-2-fluorofenil)-2,2-difluoroacetato de etilo. Se hizo reaccionar 2-(4-cloro-2-fluorofenil)-2-oxoacetato de etilo (1,71 g, 7,434 mmol) con trifluoruro de dietilamino azufre (2,45 mL, 18,585 mmol) y se agitó durante 12 h a temperatura ambiente. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8 ) y se extrajo con acetato de etilo (3x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2X10 mL), salmuera (10 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-(4-cloro-2-fluorofenil)-2,2-difluoroacetato de etilo (1,0 g, 4,087 mmol, 55% de rendimiento) como un líquido incoloro. MS (ESI) m/z 252,1.
C. Ácido 2-(4-cloro-2-fluorofenil)-2,2-difluoroacético. A una solución agitada en frío (0°C) de 2-(4-cloro-2-metilfenil)-2,2-difluoroacetato de etilo (1,0 g, 4,087 mmol) en mezcla de tetrahidrofurano:etanol:agua (30 mL, 1:1:1) se añadió hidróxido de litio monohidratado (0,85 g, 20,436 mmol) y se agitó a temperatura ambiente durante 6 h. Se concentró la mezcla de reacción y se neutralizó el residuo con ácido clorhídrico acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 20 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secó sobre sulfato de sodio y se concentró a ácido 2-(4-cloro-2-fluorofenil)-2,2-difluoroacético (550 mg, 2,455 mmol, 62% de rendimiento) como un sólido marrón. MS (ESI) m/z 224,0.
D. 2-(4-cloro-2-fluorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. A una solución agitada en frío (0°C) de ácido 2-(4-cloro-2-fluorofenil)-2,2-difluoroacético (217 mg, 0,968 mmol) en piridina se añadió oxicloruro de fósforo (0,27 mL, 2,906 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A esta mezcla de reacción se le añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,968 mmol) y se agitó a temperatura ambiente durante 30 min. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8 ) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 10 mL), salmuera ( 10 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 40-55% en ácido fórmico acuoso (0,1%) para dar 2-(4-cloro-2-fluorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2
difluoroacetamida (59 mg, 0,123 mmol, 12% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 480,07 [M+1]+.
1H RMN (300 MHz, DMSO-da) 8 10,99 (s, 1H), 9,74 (s, 1H), 7,69 (dd, J = 11,1, 7,8 Hz, 3H), 7,55-7,29 (m, 3H), 5,16 5,09 (dd, J = 5,1 Hz, 1H), 4,52-4,27 (m, 4H), 3,00-2,84 (m, 1H), 2,66-2,55 (m, 1H), 2,41-2,30 (m, 1H), 2,04-1,94 (m, 1H).
Ejemplo 39
2-(4-doro-3-fluorofeml)-N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdolm-5-M)metM)-2,2-difluoroacetamida
A. 2-(4-cloro-3-fluorofenil)-2-oxoacetato de etilo. A una solución agitada de 1-(4-doro-3-fluorofeml)etanona (2,0 g, 11,62 mmol) en piridina (20 mL) se añadió dióxido de selenio (2,5 g, 23,25 mmol) y se agitó a 100°C durante 16 h. Se diluyó la mezcla de reacción con diclorometano (30 mL) y se filtró a través de un lecho de Celite. Al filtrado se le añadió cloroformiato de etilo ( 6 mL) a 0°C y se agitó a temperatura ambiente durante 3 h. Se neutralizó la mezcla de reacción con ácido clorhídrico acuoso 1 N (hasta pH-4) y se extrajo con acetato de etilo (2 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-(4-cloro-3-fluorofenil)-2-oxoacetato de etilo (2,0 g, 8,69 mmol, 75% de rendimiento). GCMS (m/z) 230 [M]+.
B. 2-(4-cloro-3-fluorofenil)-2,2-difluoroacetato de etilo. Se agitó una solución de 2-(4-cloro-3-fluorofenil)-2-oxoacetato de etilo (1,0 g, 4,34 mmol) y trifluoruro de dietilamino azufre (3,7 g, 22,89 mmol) a temperatura ambiente durante 16 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8 ) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 30 mL), salmuera (30 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-(4-cloro-3-fluorofenil)-2,2-difluoroacetato de etilo (900 mg, 3,57 mmol, 82% de rendimiento). GCMS (m/z) 252,1 [M]+.
C. Ácido 2-(4-cloro-3-fluorofenil)-2,2-difluoroacético. A una solución agitada de 2-(4-cloro-3-fluorofenil)-2,2-difluoroacetato de etilo (800 mg, 3,17 mmol) en mezcla de tetrahidrofurano:metanol:agua (20 mL, 1:1:1) se añadió hidróxido de litio monohidratado (798 mg, 19,04 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con ácido clorhídrico acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 50 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2-(4-cloro-3-fluorofenil)-2,2-difluoroacético (600 mg, 2,67 mmol, 84% de rendimiento. MS (ESI) m/z 223,1 [M-1]+.
D. 2-(4-cloro-3-fluorofenil)-N-((2-(2,6-dioxopiperldin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. A una solución agitada en frío (0°C) de ácido 2-(4-cloro-3-fluorofenil)-2,2-difluoroacético (261 mg, 1,165 mmol) en piridina (10 mL) se añadió cloruro de fosforilo (0,3 mL, 2,91 mmol) y se agitó a 0-5°C durante 30 min. A una mezcla de reacción se le añadió a continuación clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) y se agitó a temperatura ambiente durante 1 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8 ) y se extrajo con acetato de etilo (2 X 25 mL). Se lavaron las capas orgánicas combinadas con agua (25 mL), salmuera (25 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía de columna Grace de fase inversa C-18 Reveleris usando acetonitrilo al 50-55% en ácido fórmico acuoso (0,1%) para proporcionar 2-(4-cloro-3-fluorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (50 mg, 0,10 mmol, 11% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 480,05 [M+1]+.
1H RMN (300MHz, DMSO-d6) 8 10,99 (s, 1H), 9,70 (brs, 1H), 7,81 (brt, J=7,9 Hz, 1H), 7,71 - 7,60 (m, 2H), 7,49-7,32 (m, 3H), 5,10 (brdd, J=5,1, 13,2 Hz, 1H), 4,49 - 4,38 (m, 3H), 4,34 - 4,25 (m, 1H), 2,99 - 2,83 (m, 1H), 2,63 - 2,56 (br s, 1H), 2,44 - 2,26 (m, 1H), 2,06 -1,94 (m, 1H).
Ejemplo 40
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-fluoro-2-metilfenil)acetamida
A. 1-(3-fluoro-2-metilfenil)etanona. A una solución agitada de 3-fluoro-2-metilbenzonitrilo (3 g, 22,22 mmol) en benceno (20 mL) se añadió yoduro de metilmagnesio (9,0 mL, 26,64 mmol, 3 M en éter dietílico) a 0°C y se agitó a 80°C durante 8 h. A continuación se enfrió la mezcla de reacción a temperatura ambiente, se añadió ácido clorhídrico 6 N (25 mL) y se agitó calentada a 80°C durante 8 h. Se enfrió la mezcla de reacción a temperatura ambiente y se extrajo con acetato de etilo (3 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 100 mL), salmuera (100 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 1-(3-fluoro-2-metilfenil)etanona (920 mg, 6,05 mmol, 27% de rendimiento). GCMS (m/z) 152,2 [M]+
B. 2-(3-fluoro-2-metilfenil)-2-oxoacetato de etilo. A una solución agitada de 1-(3-fluoro-2-metilfenil)etanona (900 mg, 5,91 mmol) en piridina (25 mL) se añadió dióxido de selenio (1,7 g, 14,79 mmol) y se agitó durante 12 h a 100°C. Se diluyó la mezcla de reacción con diclorometano (20 mL) y se filtró a través de un lecho de Celite. Al filtrado se le se añadió cloroformiato de etilo (3 mL) a 0°C y se agitó a temperatura ambiente durante 2 h. Se neutralizó la mezcla de reacción con ácido clorhídrico acuoso 1 N (hasta pH-4) y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar2-(3-fluoro-2-metilfenil)-2-oxoacetato de etilo (1,2 g, 5,71 mmol, 96%). GCMS (m/z) 210,2 [M]+
C. 2,2-difluoro-2-(3-fluoro-2-metilfenil)acetato de etilo. Se agitó una solución de 2-(3-fluoro-2-metilfenil)-2-oxoacetato de etilo (1,2 g, 5,71 mmol) ytrifluoruro de dietilamino azufre (4,3 g, 26,67 mmol) a temperatura ambiente durante 16 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8 ) y se extrajo con acetato de etilo (3 x 50 mL). Se lavó la capa orgánica combinada con agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(3-fluoro-2-metilfenil)acetato de etilo (1,0 g, 4,31 mmol, 76%) como un líquido marrón. Gc Ms (m/z) 232,2 [M]+
D. Ácido 2,2-difluoro-2-(3-fluoro-2-metilfenil)acético. A una solución agitada en frío (0°C) de 2,2-difluoro-2-(3-fluoro-2-metilfenil)acetato de etilo (1,0 g, 4,31 mmol) en metanol: tetrahidrofurano:agua (1:1:1, 30 mL) se añadió hidróxido de litio monohidratado (543 mg, 12,93 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con ácido clorhídrico acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 50 mL). Se lavaron las capas orgánicas combinadas con salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(3-fluoro-2-metilfenil)acético (800 mg, 3,92 mmol, 91% de rendimiento). GCMS (m/z) 204,1 [M]+
E. N-((2-(2,6-dioxopiperidin-3-il)-1-ozoisoindolin-5-il)metil)-2,2-difluoro-2-(3-fluoro-2-metilfenil)acetamida. A una solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(3-fluoro-2-metilfenil)acético (200 mg, 0,98 mmol) en piridina (10 mL) se añadió cloruro de fosforilo (0,3 mL, 2,94 mmol) gota a gota y se agitó a 0-5°C durante 30 min. A esta mezcla de reacción se le añadió a continuación clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (303 mg, 0,98 mmol) y se agitó a temperatura ambiente durante 1 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8 ) y se extrajo con acetato de etilo (2 X 25 mL). Se lavaron las capas orgánicas combinadas con agua (25 mL), salmuera (25 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 40-45% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-fluoro-2-metilfenil)acetamida (80 mg, 0,17 mmol, 18,0% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 460,10 [M+1]+. 1H RMN (300MHz, DMSO-d6) 8 10,98 (s, 1H), 9,68 (t, J=5,9 Hz, 1H), 7,70 (d, J=8,1 Hz, 1H), 7,49 - 7,31 (m, 5H), 5,10 (dd, J=4,8, 13,2 Hz, 1H), 4,52 - 4,22 (m, 4H), 3,00 - 2,82 (m, 1H), 2,67 - 2,54 (m, 1H), 2,46 - 2,30 (m, 1H), 2,21 (brs, 3H), 2,09- 1,92 (m, 1H).
Ejemplo 41
2-(3-doro-2-metilfenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida
A. 1-(3-cloro-2-metilfenil)etanona. A una solución agitada de 3-cloro-2-metilbenzonitrilo (2,0 g, 13,245 mmol) en benceno (30 mL) se añadió yoduro de metilmagnesio (3M) en solución de éter dietílico (5,3 mL, 15,89 mmol) a 0°C y se agitó durante 16 h a 75°C. Se trató la mezcla de reacción con solución de ácido clorhídrico acuoso 6 N (20 mL) a 0°C y se agitó durante 4 h a 75°C. Se inactivó la mezcla de reacción con agua (50 mL) y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 20 mL), salmuera (20 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo obtenido por cromatografía en columna (sílice 100-200) usando acetato de etilo al 5-8% en éter de petróleo para proporcionar 1-(4-cloro-2-metilfenil)etanona (1,4 g, 8,333 mmol, 63% de rendimiento) como un líquido incoloro. GCMS (ESI) m/z. 168,1.
B. 2-(3-cloro-2-metilfenil)-2-oxoacetato de etilo. A una solución agitada de 1-(4-cloro-2-metilfenil)etanona (1,4 g, 8,333 mmol) en piridina (30 mL) a 0°C, se añadió dióxido de selenio (1,85 g, 16,666 mmol) y se agitó durante 16 h a 100°C. Se diluyó la mezcla de reacción con diclorometano (30 mL) y se filtró a través de un lecho de Celite. Al filtrado se le añadió cloroformiato de etilo (3 mL) a 0°C y se agitó durante 2 h. Se inactivó la mezcla de reacción con agua y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 20 mL), salmuera (20 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna (sílice 100-200) usando acetato de etilo al 5-10% en éter de petróleo para dar 2-(3-cloro-2-metilfenil)-2-oxoacetato de etilo (1,1 g, 4,867 mmol, 58,5% de rendimiento) como un líquido incoloro. GCMS (ESI) m/z 226,1.
C. 2-(3-cloro-2-metilfenil)-2,2-difluoroacetato de etilo. Al 2-(3-cloro-2-metilfenil)-2-oxoacetato de etilo (1,1 g, 4,867 mmol) se le añadió trifluoruro de dietilamino azufre (1,6 mL, 12,168 mmol) y se agitó durante 12 h a temperatura ambiente. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8 ) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2X10 mL), salmuera (10 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-(3-cloro-2-metilfenil)-2,2-difluoroacetato de etilo (710 mg, 2,862 mmol, 58% de rendimiento) como un líquido incoloro. GCMS (ESI) m/z 248,1.
D. Ácido 2-(3-cloro-2-metilfenil)-2,2-difluoroacético. A una solución agitada en frío (0°C) de 2-(3-cloro-2-metilfenil)-2,2-difluoroacetato de etilo (710 mg, 2,862 mmol) en mezcla de tetrahidrofurano:etanol:agua (30 mL, 1:1:1) se añadió hidróxido de litio (0,6 g, 14,314 mmol) y se agitó a temperatura ambiente durante 6 h. Se concentró la mezcla de reacción y se neutralizó el residuo con ácido clorhídrico acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 30 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2-(3-cloro-2-metilfenil)-2,2-difluoroacético (382 g, 1,736 mmol, 60% de rendimiento) como un sólido. m S (ESI) m/z 219,17 [M-1]-.
E.2-(3-cloro-2-metilfenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. A una solución agitada en frío (0°C) de ácido 2-(3-cloro-2-metilfenil)-2,2-difluoroacético (213 mg, 0,968 mmol) en piridina se añadió oxicloruro de fósforo (0,27 mL, 2,906 mmol) gota a gota y se agitó a 0-5°C durante 1 h y a continuación se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,968 mmol) y se agitó a temperatura ambiente durante 30 min. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8 ) y se extrajo con acetato de etilo (3 x 50 mL). Se lavó la capa orgánica combinada con agua (2X10 mL), salmuera (10 mL) y se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 40-55% en ácido fórmico acuoso (0,1%) para proporcionar 2-(3-cloro-2-metilfenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (62 mg, 0,130 mmol, 13% de rendimiento) como un sólido blanco. MS (ESI) m/z 476,07 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 8 10,98 (s, 1H), 9,68 (s, 1H), 7,68 (dd, J = 15,3, 7,9 Hz, 2H), 7,55 (d, J = 7,3 Hz, 1H), 7,46 (s, 1H), 7,44 - 7,34 (m, 2H), 5,11 (dd, J = 13,3, 5,0 Hz, 1H), 4,52 - 4,27 (m, 4H), 3,00 - 2,84 (m, 1H), 2,66-2,55 (m, 1H), 2,43-2,30 (m, 4H), 2,04-1,94 (m, 1H).
Ejemplo 42
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluoro-2-
(trifluorometil)fenil)acetamida
A. 2,2-difluoro-2-(4-fluoro-2-(trifluorometil)fenil)acetato de etilo. A una solución agitada de 4-fluoro-1-yodo-2-(trifluorometil)benceno (500 mg, 1,72 mmol) en dimetilsulfóxido (5,2 mL) se añadió cobre (329 mg, 5,17 mmol) y 2-bromo-2,2-difluoroacetato de etilo (418 mg, 2,07 mmol) a temperatura ambiente y se agitó a 55°C durante 16 h. Se neutralizó la mezcla de reacción con solución de cloruro de amonio saturada acuosa y se extrajo con acetato de etilo (3 X 25 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 25 mL), salmuera (25 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(4-fluoro-2-(trifluorometil)fenil)acetato de etilo (300 mg, 1,05 mmol, 61%). 1H RMN (400 MHz, CDCla) 8 7,87 - 7,83 (m, 1H), 7,51 - 7,48 (m, 1H), 7,39 - 7,34 (m, 1H), 4,35 -4,30 (m, 2H), 1,30 (t, J =5,1 Hz, 3H).
B. Ácido 2,2-difluoro-2-(4-fluoro-2-(trifluorometil)fenil)acético. A una solución agitada de 2,2-difluoro-2-(4-fluoro-2-(trifluorometil)fenil)acetato de etilo (300 mg, 1,05 mmol) en mezcla de tetrahidrofurano:metanol:agua (15 mL, 1:1:1) se añadió hidróxido de litio (132 mg, 3,15 mmol) y se agitó a temperatura ambiente durante 4 h. Se concentró la mezcla de reacción y se neutralizó el residuo con bisulfato de potasio saturado (20 mL) y se extrajo con acetato de etilo (2 X 25 mL). Se lavaron las capas orgánicas combinadas con salmuera (25 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(4-fluoro-2-(trifluorometil)fenil)acético (220 mg, 0,85 mmol, 81% de rendimiento). MS (ESI) m/z 257,1[M-1]+.
C. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluoro-2-(trifluorometil)fenil)acetamida. A una solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(4-fluoro-2-(trifluorometil)fenil)acético (200 mg, 0,78 mmol) en piridina (20 mL) se añadió cloruro de fosforilo (356 mg, 2,32 mmol) gota a gota y se agitó a 0-5°C durante 1 h y a continuación se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (302 mg, 0,78 mmol) y se agitó a temperatura ambiente durante 30 min. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8 ) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 55-60% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluoro-2-(trifluorometil)fenil)acetamida (75 mg, 0,17 mmol, 21% de rendimiento) como un sólido blanco. MS (ESI) m/z 514,07 [M+1]+. 1H RMN (300MHz, DMSO-d6) 8 = 10,98 (s, 1H), 9,73- 9,62 (m, 1H), 7,96- 7,82 (m, 2H), 7,78-7,67 (m, 2H), 7,49- 7,37 (m, 2H), 5,11 (dd, J=4,8, 13,2 Hz, 1H), 4,53 4,26 (m, 4H), 3,00 - 2,82 (m, 1H), 2,77 - 2,54 (m, 1H), 2,44 - 2,23 (m, 1H), 2,08 - 1,93 (m, 1H)
Ejemplo 43
2-(4-cloro-2-metilfenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida
A. 1-(4-cloro-2-metilfenil)etanona. A una solución agitada de 4-cloro-2-metilbenzonitrilo (2,0 g, 13,193 mmol) en benceno (30 mL) se añadió yoduro de metilmagnesio (3M) en solución de éter dietílico (5,27 mL, 15,83 mmol) a 0°C y se agitó durante 16 h a 75°C. Se enfrió la mezcla de reacción a 0°C y se inactivó con solución de ácido clorhídrico 6 N (20 mL) y se siguió agitando a 75°C durante 4 h. Se inactivó la mezcla de reacción con agua y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 20 mL), salmuera (20 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo obtenido por cromatografía en columna (sílice 100-200)
usando acetato de etilo en éter de petróleo al 5-10% para proporcionar 1-(4-cloro-2-metilfenil)etanona (1,5 g, 8,928 mmol, 67% de rendimiento) como un líquido incoloro. GCMS (ESI) m/z 168,1.
B. 2-(4-cloro-2-metilfenil)-2-oxoacetato de etilo. A una solución agitada de 1-(4-cloro-2-metilfenil)etanona (1,5 g, 8,928 mmol) en piridina (30 mL) se añadió dióxido de selenio (2 g, 17,857 mmol) y se agitó durante 16 h a 100°C. Se enfrió la mezcla de reacción a temperatura ambiente, se diluyó con diclorometano (30 mL) y se filtró a través de un lecho de Celite. Al filtrado se añadió cloroformiato de etilo (3 mL) a 0°C y se agitó durante 2 h. Se inactivó la mezcla de reacción con agua y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 20 mL), salmuera (20 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo obtenido por cromatografía en columna (sílice 100-200) usando acetato de etilo en éter de petróleo al 5-10% para proporcionar 2-(4-cloro-2-metilfenil)-2-oxoacetato de etilo (1,1 g, 4,867 mmol, 54% de rendimiento) como un líquido incoloro. MS (ESI) m/z 226,2.
C. 2-(4-cloro-2-metilfenil)-2,2-difluoroacetato de etilo. A 2-(4-cloro-2-metilfenil)-2-oxoacetato de etilo (1,1 g, 4,867 mmol) se añadió trifluoruro dietilamino azufre (1,6 mL, 12,168 mmol) y se agitó durante 12 h a temperatura ambiente. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8 ) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2X10 mL), salmuera (10 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-(4-cloro-2-metilfenil)-2,2-difluoroacetato de etilo (692 mg, 2,790 mmol, 57% de rendimiento) como un líquido incoloro. GCMS (ESI) m/z 248,1.
D. Ácido 2-(4-cloro-2-metilfenil)-2,2-difluoroacético. A una solución agitada en frío (0°C) de 2-(4-cloro-2-metilfenil)-2,2-difluoroacetato de etilo (692 mg, 2,790 mmol) en mezcla de tetrahidrofurano:etanol:agua (30 mL, 1:1:1) se añadió hidróxido de litio (585 mg, 13,951 mmol) y se agitó a temperatura ambiente durante 6 h. Se concentró la mezcla de reacción y se neutralizó el residuo con ácido clorhídrico acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 20 mL). Se lavaron las capas orgánicas combinadas con salmuera ( 20 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2-(4-cloro-2-metilfenil)-2,2-difluoroacético (446 g, 2,027 mmol, 72% de rendimiento) como un líquido marrón. MS (ESI) m/z 219,29 [M-1]-.
E.2-(4-cloro-2-metilfenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. A una solución agitada en frío (0°C) de ácido 2-(4-cloro-2-metilfenil)-2,2-difluoroacético (213 mg, 0,968 mmol) en piridina se añadió oxicloruro de fósforo (0,27 mL, 2,906 mmol) gota a gota y se agitó a 0-5°C durante 1 h y a continuación se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,968 mmol) y se agitó a temperatura ambiente durante 30 min. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8 ) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 10 mL), salmuera (10 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo obtenido por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 40-60% en ácido fórmico acuoso (0,1%) para proporcionar 2-(4-cloro-2-metilfenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (90 mg, 0,189 mmol, 19,5% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 476,09 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 8 10,99 (s, 1H), 9,65 (t, J = 5,9 Hz, 1H), 7,70 (d, J = 7,8 Hz, 1H), 7,54 (d, J = 8,3 Hz, 1H), 7,50-7,31 (m, 4H), 5,11 (dd, J =13,2, 5,1 Hz, 1H), 4,52-4,25(m, 4H), 3,00-2,85(m, 1H), 2,65-2,55(m, 1H), 2,45-2,31 (m, 4H), 2,08 - 1,94 (m, 1H).
Ejemplo 44
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluoro-2-metilfenil)acetamida
A. 1-(4-fluoro-2-metilfenil)etanona. A una solución agitada de 4-fluoro-2-metilbenzonitrilo (2,0 g, 14,803 mmol) en benceno (30 mL) se añadió yoduro de metilmagnesio (3M) en solución de éter dietílico (5,92 mL, 17,764 mmol) a 0°C y se agitó durante 16 h a 75°C. Se enfrió la mezcla de reacción a 0°C y se inactivó con solución de ácido clorhídrico 6 N (20 mL) y se siguió agitando a 75°C durante 4 h. Se inactivó la mezcla de reacción con agua y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 20 mL), salmuera (20 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo obtenido por cromatografía en columna (sílice 100-200)
usando acetato de etilo en éter de petróleo al 5-10% para proporcionar 1-(4-fluoro-2-metilfenil)etanona (1,6 g, 10,526 mmol, 71% de rendimiento) como un líquido incoloro. GCMS (ESI) m/z 152,2.
B. 2-(4-fluoro-2-metilfenil)-2-ozoacetato de etilo. A una solución agitada de 1-(4-fluoro-2-metilfenil)etanona (1,6 g, 10,526 mmol) en piridina (30 mL) se añadió dióxido de selenio (2,3 g, 21,052 mmol) y se agitó durante 16 h a 100°C. Se enfrió la mezcla de reacción a temperatura ambiente, se diluyó con diclorometano (30 mL) y se filtró a través de un lecho de Celite. Al filtrado se le añadió cloroformiato de etilo (3,2 mL) a 0°C y se agitó durante 2 h. Se inactivó la mezcla de reacción con agua y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 20 mL), salmuera (20 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo obtenido por cromatografía en columna (sílice 100-200) usando acetato de etilo en éter de petróleo al 5-10% para proporcionar 2-(4-fluoro-2-metilfenil)-2-oxoacetato de etilo (1,37 g, 6,523 mmol, 62% de rendimiento) como un líquido incoloro. GCMS (ESI) m/z 210,1.
C.2,2-difluoro-2-(4-fluoro-2-metilfenil)acetato de etilo. A2-(4-cloro-2-metilfenil)-2-oxoacetato de etilo (1,37 g, 6,523 mmol) se añadió trifluoruro de dietilamino azufre (2,1 mL, 16,307 mmol) y se agitó durante 12 h a temperatura ambiente. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8 ) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 20 mL), salmuera (20 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(4-fluoro-2-metilfenil)acetato de etilo (860 mg, 3,706 mmol, 57% de rendimiento) como un líquido incoloro. GCMS (ESI) m/z 232,2.
D. Ácido 2,2-difluoro-2-(4-fluoro-2-metilfenil)acético. A una solución agitada en frío (0°C) de 2-(4-cloro-2-metilfenil)-2,2-difluoroacetato de etilo (860 mg, 3,706 mmol) en mezcla de tetrahidrofurano:etanol:agua (30 mL, 1:1:1) se añadió hidróxido de litio monohidratado (933 mg, 22,241 mmol) y se agitó a temperatura ambiente durante 6 h. Se concentró la mezcla de reacción y se neutralizó el residuo con ácido clorhídrico acuoso al 10% (10 mL) y se extrajo con acetato de etilo ( 2 X 20 mL). Se lavaron las capas orgánicas combinadas con salmuera ( 20 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(4-fluoro-2-metilfenil)acético (684 g, 2,948 mmol, 72% de rendimiento) como un líquido marrón. LCMS (ESI) m/z 203,37 [M-1]'ve.
E. N-((2-(2,6-dioxopiperidin-3-il)-1-oxosoindolin-5-il)metil)-2,2-difluoro-2-(4-fluoro-2-metilfenil)acetamida. A una solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(4-fluoro-2-metilfenil)acético (197 mg, 0,968 mmol) en piridina se añadió oxicloruro de fósforo (0,27 mL, 2,906 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A continuación se añadió a esta mezcla de reacción clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,968 mmol) y se agitó a temperatura ambiente durante 30 min. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8 ) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 10 mL), salmuera (10 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo obtenido por cromatografía en columna de fase inversa Reveleris C-18 usando acetonitrilo al 50-60% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluoro-2-metilfenil)acetamida (79 mg, 0,172 mmol, 18% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 460,10 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 8 10,99 (s, 1H), 9,63 (t, J = 6,0 Hz, 1H), 7,70 (d, J = 7,8 Hz, 1H), 7,56 (dd, J = 8,7, 5,8 Hz, 1H), 7,46 (s, 1H), 7,40 (d, J = 7,6 Hz, 1H), 7,25 - 7,11 (m, 2H), 5,11 (dd, J = 13,3, 5,0 Hz, 1H), 4,50 - 4,27 (m, 4H), 2,98-2,86 (m, 1H), 2,68 - 2,55 (m, 1H), 2,46-2,28 (m, 4H), 2,08-1,94 (m, 1H).
Ejemplo 45
2-(4-cloro-2-(trifluorometil)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida
A. 2-(4-cloro-2-(trifluorometilo)fenil)-2,2-difluoroacetato de etilo. A una solución agitada de 4-cloro-1-yodo-2-(trifluorometil)benceno (1,0 g, 3,26 mmol) en dimetilsulfóxido (15 mL) se añadió cobre (539 mg, 8,48 mmol) y 2-bromo-2,2-difluoroacetato de etilo (994 mg, 4,89 mmol) a temperatura ambiente y se agitó a 55°C durante 16 h. Se neutralizó la mezcla de reacción con solución de cloruro de amonio saturada acuosa y se extrajo con acetato de etilo (2 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 100 mL), salmuera (100 mL), se secó sobre sulfato
de sodio y se concentró para proporcionar 2-(4-cloro-2-(trifluorometil)fenil)-2,2-difluoroacetato de etilo (900 mg, 2,98 mmol, 91%). GCMS (m/z) 302,0 [M]+.
B. Ácido 2-(4-cloro-2-(trifluorometil)fenil)-2,2-difluoroacético. A una solución agitada de 2-(4-cloro-2-(trifluorometil)fenil)-2,2-difluoroacetato de etilo (900 mg, 2,98 mmol) en tetrahidrofurano:metanol:agua (15 mL, 1:1:1) se añadió hidróxido de litio (375 mg, 8,94 mmol) y se agitó a temperatura ambiente durante 4 h. Se concentró la mezcla de reacción y se neutralizó el residuo con hidrogenosulfato de potasio saturado (20 mL) y se extrajo con acetato de etilo (2 X 100 mL). Se lavaron las capas orgánicas combinadas con salmuera (100 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2-(4-cloro-2-(trifluorometil)fenil)-2,2-difluoroacético (700 mg, 2,55 mmol, 86 % de rendimiento). GCMS (m/z) 274,1 [M]+.
C. 2-(4-doro-2-(trifluorometN)fenM)-N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdoMn-5-N)metM)-2,2-difluoroacetamida. A una solución agitada en frío (0 °C) de ácido 2-(4-cloro-2-(trifluorometil)fenil)-2,2-difluoroacético (200 mg, 0,72 mmol) en piridina (10 mL) se añadió cloruro de fosforilo (336 mg, 2,18 mmol) gota a gota y se agitó a 0 5°C durante 1 h y a continuación se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (226 mg, 0,72 mmol) y se agitó a temperatura ambiente durante 1 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8 ) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 80-90% en ácido fórmico acuoso (0,1%) para proporcionar 2-(4-cloro-2-(trifluorometil)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (80 mg, 0,11 mmol, 21% de rendimiento) como un sólido blanquecino. LCMS (ESI) m/z 530,05 [M+1]+. 1H RMN (300MHz, DMSO-da) 8 10,98 (s, 1H), 9,70 (brt, J=5,9 Hz, 1H), 8,03 (s, 1H), 7,97 (brd, J=8,4 Hz, 1H), 7,85 (d, J=9 Hz, 1H), 7,70 (d, J=7,7 Hz, 1H), 7,47 (s, 1H), 7,41 (brd, J=7,7 Hz, 1H), 5,11 (brdd, J=4,8, 13,2 Hz, 1H), 4,53-4,25 (m, 4H), 3,01 -2,82 (m, 1H), 2,67-2,54 (m, 1H), 2,48-2,30 (m, 1H), 2,08- 1,94 (m, 1H)
Ejemplo 46
2-ciclohexil-N-((2-(2,6-dioxopiperidin-3-il)-1-ozoisoindolin-5-il)metil)-2,2-difluoroacetamida
A. 2-ciclohexil-2,2-difluoroacetato de etilo. Se añadió 2-ciclohexil-2-oxoacetato de etilo (1 g, 5,43 mmol) en trifluoruro de dietilamino azufre (2,5 mL) a 0°C y se agitó a temperatura ambiente durante 16 h. Se inactivó la mezcla de reacción con solución acuosa de bicarbonato de sodio y se extrajo con acetato de etilo (3 x 20 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secó sobre sulfato de sodio, se filtró y se evaporó el disolvente. Se purificó el producto en bruto obtenido por cromatografía en columna (gel de sílice 100-200, acetato de etilo en éter de petróleo al 10%) para proporcionar 2-ciclohexil-2,2-difluoroacetato de etilo (900 mg, 4,36 mmol, 80% de rendimiento) como un líquido incoloro. 1H RMN (300 MHz, CDCla) 4,32 (q, J = 6,9 Hz, 2H), 2,06-2,04 (m, 1H), 1,80 -1,60 (m, 6 H), 1,37- 1,30 (m, 4H), 1,26-1,19 (m, 3H).
B. Ácido 2-ciclohexil-2,2-difluoroacético. A una solución agitada de 2-ciclohexil-2,2-difluoroacetato de etilo (900 mg, 4,36 mmol) en mezcla detetrahidrofurano: etanol: agua (15 mL, 1:1:1), se añadió hidróxido de litio monohidratado (550 mg, 13,10 mmol) y se agitó a temperatura ambiente durante 16 h. Se evaporaron los productos volátiles a presión reducida y se disolvió el residuo resultante en agua (15 mL) y se lavó con acetato de etilo (2X15 mL). Se acidificó la capa acuosa con solución acuosa de clorhidrato 1 N y se extrajo con acetato de etilo (3 X 20 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secó sobre sulfato de sodio, se filtró y se evaporó el disolvente para proporcionar ácido 2-ciclohexil-2,2-difluoroacético (550 mg, 3,08 mmol, 70% de rendimiento) como un compuesto semisólido. MS (ESI) m/z 178 [M]+.
C. 2-ciclohexil-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. A una solución enfriada en hielo de ácido 2-ciclohexil-2,2-difluoroacético (207 mg, 1,16 mmol) en piridina ( 6 mL) se añadió oxicloruro de fósforo (0,27 mL, 2,9 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A continuación, se trató la mezcla de reacción con clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) y se agitó
a temperatura ambiente durante 2 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3X15 mL). Se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se evaporó el disolvente. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 (acetonitrilo al 50-55% en ácido fórmico acuoso al 0,1%) para proporcionar 2-ciclohexil-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (53 mg, 0,122 mmol, 12% de rendimiento) como un sólido blanco. MS (ESI) m/z 434,07 [M+1]+. 1H RMN (300 MHz, DMSO-da) 8 10,99 (s, 1H), 9,35 (t, J = 6,0Hz, 1H), 7,70 (d, J = 7,8 Hz, 1H), 7,47(s, 1H), 7,41 (d, J = 7,8 Hz, 1H), 5,11 (dd, J = 13,2, 5,4Hz, 1H), 4,45 (d, J =16,8 Hz, 1H), 4,44 (d, J = 6 , 6 Hz, 2H), 4,31 (d, J =17,7 Hz, 1H), 2,93-2,85 (m, 1H), 2,63 -2,56 (m, 1H), 2,45-2,36 (m, 1H), 2,10-1,97 (m, 2H), 1,74- 1,64 (m, 5H), 1,23- 1,08 (m, 5H).
Ejemplo 47
2-(4-cloro-2-(trifluorometoxi)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida
A. 4-cloro-1-yodo-2-(trifluorometoxi)benceno. A una solución de 4-cloro-2-(trifluorometoxi)anilina (2 g, 10,025 mmol) en ácido sulfúrico acuoso al 66 % (10 mL) se añadió una solución de nitrito de sodio (760 mg, 11,027 mmol) en agua (2 mL) a 0°C y se agitó a 0°C durante 20 min. A continuación se añadió una solución de urea (90 mg, 1,5 mmol) en agua (1 mL) a 0°C y se agitó a la misma temperatura durante 10 min. A continuación se añadió una solución de yoduro de potasio (3,49 g, 21,052 mmol) en agua (5 mL) a 0°C y se agitó a 50°C durante 2 h. A la mezcla de reacción se le añadió acetato de etilo (300 mL) y se lavó con agua (2X 100 mL), salmuera (100 mL) y se secó sobre sulfato de sodio, y se concentró. Se purificó el residuo resultante por cromatografía con gel de sílice gel (100-200) usando pentano como eluyente para proporcionar el 4-cloro-1-yodo-2-(trifluorometoxi)benceno (2,1 g, 6,52 mmol, 69% de rendimiento) como un jarabe incoloro. 1H RMN (400 MHz, CDCla) 8 (ppm) 7,79 (d, J= 88 Hz, 1H), 7,32-7,26 (m, 1H), 7,05 (dd, J=2,4, 8,3 Hz, 1H).
B. 2-(4-cloro-2-(trifluorometoxi)fenil)-2,2-difluoroacetato de etilo. A una solución agitada de 4-fluoro-1-yodo-2-(trifluorometil)benceno (2,1 g, 6,525 mmol) en dimetilsulfóxido (10 mL) se añadió polvo de cobre (1,03 g, 16,31 mmol) y 2-bromo-2,2-difluoroacetato de etilo (1,25 mL, 9,78 mmol) a temperatura ambiente y se agitó a 60°C durante 16 h. Se neutralizó la mezcla de reacción con solución de cloruro de amonio saturada acuosa y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (25 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en gel de sílice (100-200) usando éter dietílico en pentano al 5% como eluyente para proporcionar 2-(4-cloro-2-(trifluorometoxi)fenil)-2,2-difluoroacetato de etilo (1,8 g, 5,66 mmol, 87%). 1H RMN (300 MHz, CDCla) 8 (ppm) 7,70 (d, J=8,4 Hz, 1H), 7,44 - 7,32 (m, 2H), 4,34 (q, J=7,3 Hz, 2H), 1,32 (t, J=7,1 Hz, 3H).
C. Ácido 2-(4-cloro-2-(trifluorometoxi)fenil)-2,2-difluoroacético. A una solución agitada de 2-(4-cloro-2-(trifluorometoxi)fenil)-2,2-difluoroacetato (1,8 g, 6,14 mmol) en mezcla detetrahidrofurano:metanol:agua (15 mL, 1:1:1) se añadió hidróxido de litio monohidratado (774 mg, 18,42 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con bisulfato de potasio saturado (20 mL) y se extrajo con acetato de etilo (2 X 50 mL). Se lavaron las capas orgánicas combinadas con salmuera (25 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2-(4-cloro-2-(trifluorometoxi)fenil)-2,2-difluoroacético (1,2 g, 4,137 mmol, 73% de rendimiento). MS (ESI) m/z 289,14[M-1]+.
D. 2-(4-cloro-2-(trifluorometoxi)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoboindolin-5-il)metil)-2,2-difluoroacetamida. A una solución agitada en frío (0°C) clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) y ácido 2-(4-cloro-2-(trifluorometoxi)fenil)-2,2-difluoroacético (280 mg, 0,97 mmol) en N,N-dimetilformamida (10 mL) se añadió N,N-diisopropiletilamina (375 mg, 2,91 mmol) seguido por 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metileno]-1H-1,2,3-triazolo[4,5-b]piridinio (480 mg, 1.26 mmol) y se siguió
agitando a temperatura ambiente durante 16 h. Se diluyó la mezcla de reacción con agua (100 mL) y se filtró el sólido obtenido, se lavó con éter dietílico (20 mL), se secó y se purificó usando cromatografía en gel de sílice (metanol en cloroformo al 3%) para proporcionar 2-(4-cloro-2-(trifluorometoxi)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (70 mg, 0,128 mmol, 13% de rendimiento) como un sólido blanco. MS (ESI) m/z 545,97 (M+1)+. 1H RMN (300 MHz, DMSO-da) 8 (ppm) 10,95 (br s, 1H), 9,72 (brt, J=5,7 Hz, 1H), 7,79 (d, J=9,2 Hz, 1H), 7,71 - 7,61 (m, 3H), 7,46 (s, 1H), 7,41 (d, J=8,1 Hz, 1H), 5,10 (br dd, J=5,1, 13,2 Hz, 1H), 4,50 - 4,25 (m, 4H), 2,99 - 2,80 (m, 1H), 2,68 - 2,53 (m, 1H), 2,47 - 2,30 (m, 2H), 2,04 - 1,92 (m, 1H).
Ejemplo 48
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-metoxietoxi)fenil)acetamida
A. 1-yodo-3-(2-metoxietoxi)benceno. A una solución agitada de 3-yodofenol (2 g, 9,09 mmol) en N,N-dimetilformamida (20 mL) se añadió carbonato de potasio (3,13 g, 22,72 mmol) seguido por 1-bromo-2-metoxietano (1,51 g, 10,90 mmol) a TAy se agitó a 70°C durante 16 h. Se inactivó la mezcla de reacción con agua con hielo (30 mL) y se extrajo con acetato de etilo (3 X 20 mL). Se lavaron las capas orgánicas combinadas con agua (20 mL), salmuera (20 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto obtenido por cromatografía en columna (gel de sílice 100-200) usando acetato de etilo en éter de petróleo al 15% como eluyente para proporcionar 1-yodo-3-(2-metoxietoxi)benceno (1,3 g, 4,69 mmol, 52% de rendimiento) como un líquido incoloro. MS (ESI) m/z 279,04 [M+1]+.
B. 2,2-difluoro-2-(3-(2-metoxietoxi)fenil)acetato de etilo. A una solución agitada de 1-yodo-3-(2-metoxietoxi)benceno (1 g, 3,6 mmol) en dimetilsulfóxido (15 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (0,69 mL, 5,41 mmol) y cobre (0,59 g, 9,36 mmol) a 0°C y se agitó a 60°C durante 5 h. Se inactivó la mezcla de reacción con agua con hielo y se filtró a través de lecho de celite; se extrajo el filtrado con acetato de etilo (3 X 20 mL). Se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 2,2-difluoro-2-(3-(2-metoxietoxi)fenil)acetato de etilo (0,60 g, 2,19 mmol, 61%) como un líquido marrón. MS (ESI) m/z 274,1 [M]+.
C. Ácido 2,2-difluoro-2-(3-(2-metoxietoxi)fenil)acético. A una solución agitada en frío (0°C) de 2,2-difluoro-2-(3-(2-metoxietoxi)fenil)acetato de etilo (800 mg, 2,93 mmol) en mezcla de metanol: tetrahidrofurano:agua (15 mL, 1:1:1) se añadió hidróxido de litio monohidratado (370 mg, 8,79 mmol) y se agitó a temperatura ambiente durante 5 h. Se concentró la mezcla de reacción y se diluyó el producto en bruto obtenido con agua (10 mL) y se lavó con acetato de etilo (2X10 mL). Se acidificó la capa acuosa con ácido clorhídrico 2 N (10 mL) y se extrajo con acetato de etilo (3 X 15 mL). Se lavaron las capas orgánicas combinadas con salmuera (15 mL), se secó sobre sulfato de sodio, se filtró; se concentró el filtrado para proporcionar ácido 2,2-difluoro-2-(3-(2-metoxietoxi)fenil)acético (600 mg, 3,47 mmol, 83% de rendimiento) como un semisólido marrón. 1H RMN (300 m Hz , DMSO-d6 8 7,37 - 7,33 (m, 1H), 7,22 - 7,15 (m, 2H), 7,05 - 7,03 (m, 1H), 4,84 (brs, 1H), 4,14 (s, 3H), 3,86 - 3,77 (m, 4H).
D. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-metoxietoxi)fenil)acetamida. A una solución agitada en frío (0 °C) de ácido 2,2-difluoro-2-(3-(2-metoxietoxi)fenil)acético (285 mg, 1,16 mmol) en piridina (3 mL) se añadió cloruro de fosforilo (0,27 mL, 2,91 mmol) gota a gota y se agitó a 0-5°C durante 1 h y a continuación se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) y se agitó a temperatura ambiente durante 30 min. Se basificó la mezcla de reacción con bicarbonato de sodio saturado acuoso (hasta pH-8 ) y se extrajo con acetato de etilo (3X15 mL). Se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se secó sobre sulfato de sodio y se filtró y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 50-55% en ácido fórmico acuoso (0,1%) para producir N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-metoxietoxi)fenil)acetamida (48 mg, 0,09 mmol, 9% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 501,96 [M+1]+. 1H RMN (300 MHz, DMSO-de) 8 10,98 (s, 1H), 9,54 (t, J = 5,8 Hz, 1H), 7,67 (d, J = 8,1 Hz, 1H), 7,47-7,35 (m, 3H), 7,16-7,11 (m, 3H), 5,12(dd, J =13,2, 5,1 Hz, 1H), 4,45-4,27 (m, 4H), 4,11 (t, J = 4,2 Hz, 2H), 3,65 (t, J = 4,5 Hz, 2H), 3,30 (s, 3H), 2,91 - 2,80 (m, 1H), 2,63 - 2,57 (m, 1H), 2,44 - 2,36 (m, 1H), 2,08 - 2,05 (m, 1H).
Ejemplo 49
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-hidroxietoxi)fenil)acetamida
A. (2-bromoetoxi)(terc-butil)dimetilsilano. A una solución agitada de 2-bromoetanol (10 g, 80 mmol) en diclorometano (100 mL) se añadió ferc-butilclorodimetilsilano (14,5 g, 96,77 mmol) y imidazol (10 g, 161,2 mmol) a 0°C y se agitó a temperatura ambiente durante 12 h. Se inactivó la mezcla de reacción con solución de bicarbonato de sodio acuosa (40 mL) y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (40 mL), salmuera (40 mL), se secó sobre sulfato de sodio y se concentró para proporcionar (2-bromoetoxi)(tercbutil)dimetilsilano ( 8 g, 33,61 mmol, 42% de rendimiento) como un líquido incoloro.
B. Terc-butil(2-(3-yodofenoxi)etoxi)dimetilsilano. A una solución agitada de (2-bromoetoxi)(ferc-butil)dimetilsilano (5,19 g, 21,8 mmol) en N,N-dimetilformamida (20 mL) se añadió carbonato de potasio (6,27 g, 45,45 mmol), yoduro de tetrabutilamonio (1,34 g, 3,63 mmol) seguido por 3-yodofenol (4 g, 18,18 mmol) a TA y se agitó a 70°C durante 16 h. Se inactivó la mezcla de reacción con agua con hielo (20 mL) y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (40 mL), salmuera (40 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto obtenido por cromatografía en columna (gel de sílice 100-200, acetato de etilo en éter de petróleo al 15%) para proporcionar ferc-butil(2-(3-yodofenoxi)etoxi)dimetilsilano (3,5 g, 9,25 mmol, 43% de rendimiento) como un líquido incoloro. 1H RMN (300 MHz, CDCla) 8 7,28 - 7,26 (m, 2H), 6,98 (t, J = 8,4 Hz, 1H), 6,89 - 6 , 86 (m, 1H), 4,02 - 3,94 (m, 4H), 0,90 (s, 9H), 0,07 (s, 6 H).
C. 2,2-difluoro-2-(3-(2-hidroxietoxi)fenil)acetato de metilo. A una solución agitada de ferc-butil(2-(3-yodofenoxi)etoxi)dimetilsilano (1 g, 2,64 mmol) en dimetilsulfóxido (20 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (0,8 g, 3,97 mmol) y cobre (0,43 g, 6,87 mmol) a 0°C y se agitó a 60°C durante 5 h. Se inactivó la mezcla de reacción con agua con hielo y se filtró a través de un lecho de Celite. Se extrajo el filtrado con acetato de etilo (3 X 20 mL) y se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 2,2-difluoro-2-(3-(2-hidroxietoxi)fenil)acetato de metilo (0,2 g, 0,77 mmol, 29%) como un líquido marrón. m S (ESI) m/z 260,2 [M]+.
D. Ácido 2,2-difluoro-2-(3-(2-hidroxietoxi)fenil)acético. A una solución enfriada en hielo de 2,2-difluoro-2-(3-(2-hidroxietoxi)fenil)acetato de metilo (200 mg, 0,77 mmol) en mezcla de metanol: tetrahidrofurano:agua (15 mL, 1:1:1) se añadió hidróxido de litio monohidratado (97 mg, 2,31 mmol) y se agitó a temperatura ambiente durante 5 h. Se extrajeron los productos volátiles a presión reducida y se diluyó el residuo resultante con agua ( 6 mL) y se lavó con acetato de etilo ( 2 X 5 mL). Se acidificó la capa acuosa con ácido clorhídrico acuoso 2 N (5 mL) y se extrajo con acetato de etilo ( 3X5 mL). Se lavaron las capas orgánicas combinadas con salmuera (5 mL), se secó sobre sulfato de sodio, se concentró para proporcionar ácido 2,2-difluoro-2-(3-(2-hidroxietoxi)fenil)acético (150 mg, 0,65 mmol, 84% de rendimiento) como un semisólido marrón. 1H RMN (300 MHz, CDCla) 8 7,49 - 7,43 (m, 1H), 7,19 - 7,05 (m, 3H), 4,05 - 3,99 (m, 2H), 3,85 (brs, 1H), 3,73 - 3,70 (m, 2H).
E. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-hidroxietoxi)fenil)acetamida. A una solución enfriada en hielo de clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) y ácido 2,2-difluoro-2-(3-(2-hidroxietoxi)fenil)acético (225 mg, 0,97 mmol) en N,N-dimetilformamida (10 mL) se añadió N,N-diisopropiletilamina (0,52 mL, 2,91 mmol) seguido por 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metileno]-1H-1,2,3-triazolo[4,5-b]piridinio (479 mg, 1,26 mmol) y se agitó a temperatura ambiente durante 4 h. Se diluyó la mezcla de reacción con agua con hielo (15 mL) y se extrajo con acetato de etilo (3X15 mL). Se lavaron las capas orgánicas combinadas con salmuera (15 mL), se secó sobre sulfato de sodio, se filtró, se concentró y el producto en bruto obtenido se purificó por columna de fase inversa Reveleris C-18 (acetonitrilo al 50% en ácido fórmico acuoso al 0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-hidroxi etoxi)fenil)acetamida (61 mg, 0,16 mmol, 16% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 488,08 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 8 10,99 (s, 1H), 9,56 (s, 1H), 7,67 (d, J = 7,8 Hz, 1H), 7,47 -7,35 (m, 3H), 7,15-7,12(m, 3H), 5,10 (dd, J = 12,6, 4,5 Hz, 1H), 4,88 (t, J = 5,7 Hz, 1H), 4,45-4,27 (m, 4H), 4,11 (t, J = 4,8 Hz, 2H), 3,71 (q, J = 4,8 Hz, 2H), 2,91 - 2,87 (m, 1H), 2,62 - 2,56 (m, 1H), 2,41 - 2,35 (m, 1H), 2,02 - 1,97 (m, 1H).
Ejemplo 50
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-(2-metoxietoxi)fenil)acetamida
A. 1-yodo-4-(2-metoxietoxi)benceno. A una solución agitada de 4-yodofenol (2 g, 9,09 mmol) en N,N-dimetilformamida (25 mL) se añadió 1-bromo-2-metoxietano (1,5 g, 10,90 mmol), yoduro de tetrabutilamonio (670 mg, 1,818 mmol) y carbonato de potasio (3,13 g, 22,72 mmol) a TA y se agitó a 70°C durante 16 h. Se inactivó la mezcla de reacción con agua enfriada con hielo (40 mL) y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 10 mL), salmuera (10 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 1-yodo-4-(2-metoxietoxi)benceno (600 mg, 2,15 mmol, 24% de rendimiento) como un líquido incoloro. MS (ESI) m/z 277,9 [M+1]+.
B. 2,2-difluoro-2-(4-(2-metoxietoxi)fenil)acetato de etilo. Se hizo reaccionar una solución agitada de 1-yodo-4-(2-metoxietoxi)benceno (500 mg, 1,798 mmol) en dimetilsulfóxido (5 mL) con 2-bromo-2,2-difluoroacetato de etilo (0,34 mL, 2,69 mmol), cobre (297 mg, 4,67 mmol) y se agitó durante 12 h a 50°C. Se neutralizó la mezcla de reacción con solución de cloruro de amonio saturada acuosa y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua ( 2X10 mL), salmuera (10 mL), se secó sobre sulfato de sodio concentrado para proporcionar 2,2-difluoro-2-(4-(2-metoxietoxi)fenil)acetato de etilo (120 mg, 0,437 mmol, 24%) como un líquido marrón. GCMS (m/z) 274 [M]+
C. Ácido 2,2-difluoro-2-(4-(2-metoxietoxi)fenil)acético. A una solución agitada en frío (0°C) de 2,2-difluoro-2-(4-(2-metoxietoxi)fenil)acetato de etilo (1 g, 3,64 mmol) en mezcla de etanol/tetrahidrofurano/agua (15 mL, 1:1:1) se añadió hidróxido de litio monohidratado (460 mg, 10,94 mmol) y se agitó a temperatura ambiente durante 12 h. Se concentró la mezcla de reacción y se neutralizó el residuo con ácido clorhídrico acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 20 mL). Se lavó la capa orgánica combinada con salmuera (10 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(4-(2-metoxietoxi)fenil)acético (600 mg, 2,43 mmol, 66 % de rendimiento) como un semisólido marrón. El compuesto en bruto se usó sin purificación adicional para la etapa siguiente.
D. N-((2-(2,6-dioxopiperidin-3-il)-1-oxolsoindolin-5-il)metil)-2,2-difluoro-2-(4-(2-hidroxietoxi)fenil)acetamida. A una solución agitada en frío (0 °C) de ácido 2,2-difluoro-2-(4-(2-metoxietoxi)fenil)acético (573 mg, 2,33 mmol) en piridina se añadió oxicloruro de fósforo (0,54 mL, 5,82 mmol) gota a gota y se agitó a 0-5°C durante 1 h y a continuación se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (600 mg, 1,94 mmol) y se agitó a temperatura ambiente durante 30 min. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8 ) y se extrajo con acetato de etilo (3 x 50 mL). Se lavó la capa orgánica combinada con agua (2 X 20 mL), salmuera (20 mL) y se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 40-55% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-(2-metoxietoxi)fenil)acetamida (40 mg, 0,079 mmol, 4% de rendimiento) como un sólido blanco. MS (ESI) m/z 502,08 [M+1]+. 1H RMN (300MHz, DMSO-d6): 8 10,98 (s, 1H), 9,57 (brt, J=6,1 Hz, 1H), 7,68 (d, J=7,7 Hz, 1H), 7,50 (d, J=8 , 8 Hz, 2H), 7,42-7,32 (m, 2H), 7,07 (d, J=8 , 8 Hz, 2H), 5,10 (dd, J=13,2, 5,1 Hz, 1H), 4,44 -4,25 (m, 4H), 4,20-4,10 (m, 2H), 3,78-3,60 (m, 2H), 3,25 (s, 3H), 3,00-2,83 (m, 1H), 2,66-2,56 (m, 1H), 2,45-2,32 (m, 1H), 2,05-1,94 (m, 1H).
Ejemplo 51
N-((2-(2,6-dioxopiperldin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-hidroxietil)fenil)acetamida
A. 2-(3-yodofenil)etanol: A una solución agitada de ácido 2-(3-yodofenil)acético (1 g, 3,81 mmol) en tetrahidrofurano (20 mL) se añadió complejo de sulfuro de boranodimetilo (1 mL, 11,45 mmol) a 0°C y se agitó a temperatura ambiente durante 16 h. Se inactivó la mezcla de reacción con ácido clorhídrico 4 N (15 mL) y se extrajo con acetato de etilo (3 X 15 mL). Se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 2-(3-yodofenil)etanol (0,9 g, 3,63 mmol, 95% de rendimiento) como un líquido incoloro. 1H RMN (300 MHz, DMSO-da) 8 7,61 (s, 1H), 7,55 (d, J = 7,8 Hz, 1H), 7,25 (d, J = 7,8 Hz, 1H), 7,08 (dd, J = 7,8, 7,5 Hz, 1H), 3,59 (t, J = 6 , 6 Hz, 2H), 2,67 (t, J = 6,0 Hz, 2H).
B. Acetato de 3-yodofenilo. A una solución agitada de 2-(3-yodofenil)etanol (900 mg, 3,62 mmol) en piridina (15 mL) se añadió anhídrido acético (1,11 g, 10,88 mmol) a 0°C y se agitó a 80°C durante 2 h. Se inactivó la mezcla de reacción con clorhidrato acuoso 1 N (10 mL) a temperatura ambiente y se extrajo con acetato de etilo (3X15 mL). Se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se secó sobre sulfato de sodio y se concentró para proporcionar acetato de 3-yodofenetilo (700 mg, 2,41 mmol, 6 6 % de rendimiento) como un líquido incoloro. 1H RMN (400 MHz, DMSO-d6) 8 7,66 (s, 1H), 7,59 (d, J = 5,7 Hz, 1H), 7,28 (d, J = 6,5 Hz, 1H), 7,11 (dd, J = 8,0 Hz, 7,8 Hz, 1H), 4,20 (t, J = 6 , 8 Hz, 2H), 2,85 (t, J = 6 , 8 Hz, 2H), 1,97 (s, 3H).
C. 2-(3-(2-acetoxietil)fenil)-2,2-difluoroacetato de etilo. A una solución agitada de acetato de 3-yodofenetilo (1 g, 3,46 mmol) en dimetilsulfóxido (20 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (1,05 g, 5,19 mmol) seguido por polvo de cobre (0,57 g, 8,99 mmol) a temperatura ambiente y se agitó a 50°C durante 16 h. Se neutralizó la mezcla de reacción con solución de cloruro de amonio saturada acuosa y se extrajo con acetato de etilo ( 3X15 mL). Se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-(3-(2-acetoxietil)fenil)-2,2-difluoroacetato de etilo (550 mg, 1,92 mmol, 55%) como un sólido marrón. 1H RMN (400 MHz, DMSO-d6) 8 7,49 - 7,46 (m, 2H), 7,41 - 7,34 (m, 2H), 4,31 - 4,27 (m, 4H), 2,98 (t, J = 7,2 Hz, 2H), 2,03 (s, 3H), 1,31 (t, J = 6 , 8 Hz, 3H).
D. Ácido 2,2-difluoro-2-(3-(2-hidroxietil)fenil)acético. A una solución enfriada con hielo de 2-(3-(2-acetoxietil)fenil)-2,2-difluoroacetato de etilo (0,8 g, 2,77 mmol) en mezcla de etanol/tetrahidrofurano/agua (15 mL, 1:1:1) se añadió hidróxido de litio monohidratado (349 mg, 8,3 mmol) y se agitó a temperatura ambiente durante 16 h. Se extrajeron los productos volátiles y se diluyó el residuo con agua (10 mL), se lavó con acetato de etilo (2 X 10 mL). Se acidificó la capa acuosa con ácido clorhídrico acuoso 2 N (10 mL) y se extrajo con acetato de etilo (3X15 mL). Se lavaron las capas orgánicas combinadas con salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar ácido 2,2-difluoro-2-(3-(2-hidroxietil)fenil)acético (450 mg, 2,08 mmol, 75% de rendimiento) como un semisólido marrón. 1H RMN (300 MHz, DMSO-d6) 8 7,56 - 7,39 (m, 4H), 3,62 (t, J = 6 , 6 Hz, 2H), 2,78 (t, J = 6 , 6 Hz, 2H), 1,91 (s, 1H).
E. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-hidroxietil)fenil)acetamida. A una solución enfriada con hielo de clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) y ácido 2,2-difluoro-2-(3-(2-hidroxietil)fenil)acético (209 mg, 0,97 mmol) en N,N-dimetilformamida ( 10 mL) se añadió N,N-diisopropiletilamina (0,52 mL, 2,91 mmol) seguido por 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metileno]-1H-1,2,3-triazolo[4,5-b]piridinio (479 mg, 1,26 mmol) y se agitó a temperatura ambiente durante 16 h. Se diluyó la mezcla de reacción con agua (15 mL) y se extrajo con acetato de etilo (3 X 15 mL). Se lavaron las capas orgánicas combinadas con salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto obtenido con columna de fase inversa Reveleris C-18 (acetonitrilo al 50% en ácido fórmico acuoso al 0,1% para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-hidroxietil)fenil)acetamida (50 mg, 0,10 mmol, 11% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 472,11 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 8 10,98 (s, 1H), 9,61 (t, J = 6,3 Hz, 1H), 7,67 (d, J = 8,1 Hz, 1H), 7,43-7,41 (m, 5H), 7,36 (d, J = 8,1 Hz, 1H), 6,67 (t, J = 5,1 Hz, 1H), 5,10 (dd, J = 13,8, 5,1 Hz, 1H), 4,45 (d, J = 6,0 Hz, 2H), 4,43 (t, J = 15,3 Hz, 1H), 4,28 (d, J =17,7 Hz, 1H), 3,61 (q, J = 5,1 Hz, 2H), 2,96-2,83 (m, 1H), 2,75 (t, J = 6,9 Hz, 2H), 2,67 - 2,54 (m, 1H), 2,46 - 2,30 (m, 1H), 2,04 - 1,92 (m, 1H).
Ejemplo 52
2-(3-(dimetilamino)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida
A. 3-yodo-N,N-dimetilanilina. A una solución agitada de 3-yodoanilina (300 mg, 1,36 mmol) en etanol (10 mL) se añadió formaldehído (82 mg, 2,73 mmol), tamices moleculares (1 g) y ácido acético (2 mL) a 0°C, se agitó a temperatura ambiente durante 8 h. Se enfrió la mezcla de reacción a 0°C y se trató con cianoborohidruro de sodio (200 g, 2,73 mmol) y se agitó a temperatura ambiente durante 16 h. Se filtró la mezcla de reacción a través de un lecho de Celite y se diluyó el filtrado con agua (10 mL) y se basificó con solución de bicarbonato de sodio acuosa y se extrajo con acetato de etilo (3X10 mL). Se lavaron las capas orgánicas combinadas con agua (10 mL) y salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró a presión reducida para dar el compuesto en bruto. Se purificó el producto en bruto por cromatografía en columna en gel de sílice (acetato de etilo en éter de petróleo al 30%) para proporcionar 3-yodo-N,N-dimetilanilina (210 mg, 0,85 mmol, 74% de rendimiento) como un líquido. 1H RMN (300 MHz, CDCla) 8 7,03 - 6,89 (m, 3H), 6,67 - 6,64 (m, 1H), 2,92 (s, 6 H).
B. 2-(3-(dimetilamino)fenil)-2,2-difluoroacetato de etilo. A una solución agitada de 3-yodo-N,N-dimetilanilina (250 mg, 1,01 mmol) en dimetilsulfóxido (10 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (0,19 mL, 1,52 mmol) seguido por polvo de cobre (167 mg, 2,63 mmol) a TA y se agitó a 55°C durante 5 h. Se diluyó la mezcla de reacción con agua y se filtró a través de un lecho de Celite. Se basificó el filtrado con solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3X10 mL). Se lavaron las capas orgánicas combinadas con agua (10 mL), salmuera (10 mL), se secó sobre sulfato de sodio, se filtró, se concentró para proporcionar 2-(3-(dimetilamino)fenil)-2,2-difluoroacetato de etilo (80 mg, 6,99 mmol, 33%) como un líquido marrón. MS (ESI) m/z 243,2 [M]+
C. Ácido 2-(3-(dimetilamino)fenil)-2,2-difluoroacético. A una solución enfriada con hielo de 2-(3-(dimetilamino)fenil)-2,2-difluoroacetato de etilo (500 mg, 2,06 mmol) en mezcla de metanol/tetrahidrofurano/agua (15 mL, 1:1:1) se añadió hidróxido de litio monohidratado (260 mg, 6,17 mmol) y se agitó a temperatura ambiente durante 4 h. Se concentró la mezcla de reacción y se diluyó el residuo resultante con agua (10 mL) y se lavó con acetato de etilo (2X10 mL). Se acidificó la capa acuosa con bisulfato de potasio acuoso (10 mL) y se extrajo con acetato de etilo (3 X 10 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar ácido 2-(3-(dimetilamino)fenil)-2,2-difluoroacético (400 mg, 1,86 mmol, 91% de rendimiento) como un semisólido marrón 1H Rm N (300 MHz, DMSO-d6) 8 7,64 - 7,55 (m, 3H), 7,38 - 7,32 (m, 1H), 2,56 (s, 6 H).
D. 2-(3-(dimetilimino)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. A una solución enfriada en hielo de clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) y ácido 2-(3-(dimetilamino)fenil)-2,2-difluoroacético (208 mg, 0,97 mmol) en N,N-dimetilformamida (10 mL) se añadió N,N-diisopropiletilamina (0,52 mL, 2,91 mmol) seguido por 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metileno]-1H-1,2,3-triazolo[4,5-b]piridinio (479 mg, 1,26 mmol) y se agitó a temperatura ambiente durante 16 h. Se diluyó la mezcla de reacción con agua (15 mL) y se extrajo con acetato de etilo (3 X 15 mL). Se lavaron las capas orgánicas combinadas con salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto obtenido por columna de fase inversa Reveleris C-18 (acetonitrilo al 50% en ácido fórmico acuoso al 0,1%) para proporcionar 2-(3-(dimetilamino)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (63 mg, 0,13 mmol, 13% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 470,8 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 8 10,98 (s, 1H), 9,21 (t, J = 5,8 Hz, 1H), 7,72 (d, J = 7,8 Hz, 1H), 7,62 (d, J = 7,5 Hz, 1H), 7,57-7,48 (m, 4H), 7,32 (dd, J = 8,4, 6,9 Hz, 1H), 5,11 (dd, J = 13,2, 4,8 Hz, 1H), 4,48 (d, J = 6 , 6 Hz, 2H), 4,46 (d, J = 16,5 Hz, 1H), 4,32 (d, J = 17,4 Hz, 1H), 2,98-2,86 (m, 1H), 2,73 -2,57 (m, 1H), 2,51 -2,33 (m, 1H), 2,34 (s, 6 H), 2,07- 1,98 (m, 1H).
Ejemplo 53
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(piperldin-1-il)fenil)acetamida
A. 1-(3-yodofenil)piperidina. A una solución agitada de 3-yodoanilina (5 g, 22,83 mmol) en tolueno (50 mL) se añadió N,N-diisopropiletilamina (20 mL, 114,1 mmol) seguido por 1,5-dibromopentano (4,06 mL, 29,68 mmol) a 0°C y se agitó a 100°C durante 16 h. Se basificó la mezcla de reacción solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3 X 40 mL). Se lavaron las capas orgánicas combinadas con agua (40 mL), salmuera (40 mL), se secó sobre sulfato de sodio, se filtró; se concentró el filtrado. Se purificó el producto en bruto obtenido por cromatografía en columna instantánea (acetato de etilo en éter de petróleo al 25%) para proporcionar 1-(3-yodofenil)piperidina (2,8 g, 9,75 mmol, 43% de rendimiento) como un líquido incoloro. MS (ESI) m/z 287,90 [M+1]+.
B. Etilo 2,2-difluoro-2-(piperidin-1-il)fenil)acetato de etilo. A una solución agitada de 1-(3-yodofenil)piperidina (500 mg, 1,74 mmol) en dimetilsulfóxido (5 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (690 mg, 2,61 mmol) seguido por polvo de cobre (290 mg, 4,53 mmol) a temperatura ambiente y se agitó a 55°C durante 16 h. Se diluyó la mezcla de reacción con agua y se filtró a través de un lecho de Celite. Se extrajo el filtrado con acetato de etilo (3X10 mL) y se lavaron las capas orgánicas combinadas con agua (10 mL), salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto resultante por cromatografía en columna (acetato de etilo en éter de petróleo al 25%) para proporcionar 2,2-difluoro-2-(3-(piperidin-1-il)fenil)acetato de etilo (200 mg, 0,71 mmol, 41% de rendimiento) como un líquido incoloro. MS (ESI) m/z 283,2 [M]+.
C. Ácido 2,2-difluoro-2-(3-(piperidin-1-il)fenil)acético. A una solución agitada de 2,2-difluoro-2-(3-(piperidin-1 -il)fenil)acetato de etilo (250 mg, 0,88 mmol) en mezcla de tetrahidrofurano: metanol: agua (5 mL, 1:1:1) se añadió hidróxido de litio monohidratado (110 mg, 2,65 mmol) y se agitó a temperatura ambiente durante 16 h. Se concentró la mezcla de reacción a presión reducida y se disolvió el residuo obtenido en agua (10 mL) y se lavó con acetato de etilo (2X10 mL). Se acidificó la capa acuosa con bisulfato de potasio acuoso y se extrajo con acetato de etilo (3X10 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar ácido 2,2-difluoro-2-(3-(piperidin-1-il)fenil)acético (200 mg, 0,78 mmol, 88 % de rendimiento) como un compuesto semisólido. 1H Rm N (300 MHz, CDCh) 8 8,27 (d, J = 9,3 Hz, 1H), 7,89 (s, 1H), 7,70 (d, J = 7,5 Hz, 1H), 7,49 (dd, J =7,8 Hz, 7,6 Hz, 1H), 4,28 (brs, 1H), 3,49-3,39 (m, 4H), 2,12-2,08 (m, 4H), 1,69-1,65 (m, 2H).
D. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(piperldin-1-il)fenil)acetamida. A una solución enfriada con hielo de ácido 2,2-difluoro-2-(3-(piperidin-1-il)fenil)acético (206 mg, 0,81 mmol) en piridina ( 6 mL) se añadió oxicloruro de fósforo (371 mg, 2,43 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A continuación, se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (250 mg, 0,81 mmol) se añadió en la mezcla de reacción y se agitó a temperatura ambiente durante 2 h. Se basificó la mezcla de reacción con bicarbonato de sodio saturado acuoso y se extrajo con acetato de etilo (3X15 mL). Se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 (acetonitrilo al 50-55% en ácido fórmico acuoso al 0,1% para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(piperidin-1-il)fenil)acetamida (62 mg, 0,12 mmol, 15% de rendimiento) como un sólido blanco. MS (ESI) m/z 510,81 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 8 10,99 (s, 1H), 9,57 (t, J =5,7 Hz, 1H), 7,66 (d, J =7,5 Hz, 1H), 7,39 (s, 1H), 7,35 (d, J = 5,1 Hz, 1H), 7,30 (d, J = 8,1 Hz, 1H), 7,08 (d, J = 8,7 Hz, 1H), 7,00(s, 1H), 6,92 (d, J =7,5 Hz, 1H), 5,10 (dd, J =13,2, 4,8 Hz, 1H), 4,45 (d, J = 6,0 Hz, 2H), 4,41 (d, J = 17,7 Hz, 1H), 4,27 (d, J = 17,4 Hz, 1H), 3,31 - 3,11 (m, 4H), 2,98 -2,86 (m, 1H), 2,63 - 2,57 (m, 1H), 2,40 - 2,27 (m, 2H), 2,01 -1,97 (m, 1H), 1,57 - 1,54 (m, 5H).
Ejemplo 54
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-morfolinofenil)acetamida
A. Dimetanosulfonato de 2,2'-oxibis(etano-2,1-diilo). A una solución agitada de 2,2'-oxidietanol (2,0 g, 18,86 mmol) en diclorometano (20 mL) se añadió sulfonilcloruro de metano (2,1 g, 47,16 mmol), trietilamina (13 mL, 94,33 mmol) a 0°C y se agitó a temperatura ambiente durante 2 h. Se inactivó la mezcla de reacción con agua (100 mL) y se extrajo con diclorometano (2 X 100 mL). Se lavaron las capas orgánicas combinadas con salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar dimetanosulfonato de 2,2'-oxibis(etano-2,1-diilo) (4,0 g, 15,26 mmol, 81% de rendimiento). GC MS (m/z) 263,1.
B.4-(3-yodofenil)morfolina. A una solución agitada de 3-yodo anilina (1,0 g, 4,56 mmol) en tolueno (20 mL) se añadió dimetanosulfonato de 2,2'-oxibis(etano-2,1-diilo) (2,1 g, 9,13 mmol), diisopropiletilamina (4 mL, 22,82 mmol) y se agitó a reflujo durante 16 h. Se inactivó la mezcla de reacción con agua (100 mL) y se extrajo con acetato de etilo (2 X 100 mL). Se lavaron las capas orgánicas combinadas con salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para dar 4-(3-yodofenil)morfolina (1,2 g, 4,15 mmol, 91% de rendimiento). LCMS (ESI) m/z 290,16[M+1]+.
C. 2,2-difluoro-2-(3-morfolinofenil)acetato de etilo. A una solución agitada de 4-(3-yodofenil)morfolina (1,2 g, 4,15 mmol) en dimetilsulfóxido (50 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (0,6 mL, 4,98 mmol), cobre (686 mg, 10,79 mmol) y se agitó durante 6 h a 55°C. Se neutralizó la mezcla de reacción con solución de cloruro de amonio saturada acuosa y se extrajo con acetato de etilo (3 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(3-morfolinofenil)acetato de etilo (700 mg, 2,45 mmol, 59% de rendimiento). GC MS (m/z) 285,2.
D. Ácido 2,2-difluoro-2-(3-morfolinofenil)acético. A una solución agitada en frío (0°C) de 2,2-difluoro-2-(3-morfolinofenil)acetato de etilo (700 mg, 2,45 mmol) en tetrahidrofurano-metanol-agua (20 mL, 1:1:1) se añadió hidróxido de litio monohidratado (309 mg, 7,36 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con bisulfato de potasio acuoso al 10% (5 mL) y se extrajo con acetato de etilo (2 X 50 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(3-morfolinofenil)acético (550 mg, 2,14 mmol, 87% de rendimiento). LCMS (ESI) m/z 258,12[M+1]+.
E. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-morfolinofenil)acetamida. A una solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(3-morfolinofenil)acético (300 mg, 1,16 mmol) en piridina (5 mL) se añadió cloruro de fosforilo (0,4 mL, 3,50 mmol) y se agitó a 0-5°C durante 1 h. A esta mezcla de reacción se le añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (361 mg, 1,16 mmol) y se agitó a temperatura ambiente durante 1 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (2 X 25 mL). Se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 40-45% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-morfolinofenil)acetamida (80 mg, 0,15 mmol, 13% de rendimiento) como un sólido blanquecino. LCMS (ES1) m/z 512,95 [M+1]+. 1H RMN (400MHz, DMSO-d6) 8 = 10,98 (s, 1H), 9,58 (brt, J=6,1 Hz, 1H), 7,67 (d, J=7,8 Hz, 1H), 7,52 -7,31 (m, 2H), 7,11 (br d, J=8,3 Hz, 1H), 7,07-6,95 (m, 1H), 5,10 (dd, J=4,9, 13,2 Hz, 1H), 4,51 - 4,26 (m, 4H), 3,77 3,66 (m, 4H), 3,14-3,03 (m, 4H), 2,98-2,84 (m, 1H), 2,66-2,55 (m, 1H), 2,45-2,30 (m, 1H), 2,06- 1,94 (m, 1H)
Ejemplo 55
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluoro-2-isopropoxifenil)acetamida
A. 1-(4-fluoro-2-isopropoxiciclohexil)etanona. A una solución agitada de 1-(4-fluoro-2-hidroxifenil)etanona (3 g, 19,48 mmol) en N,N-dimetilformamida (15 mL) se añadió 2-bromopropano (5,94 g, 48,76 mmol) y carbonato de potasio (8,06 g 58,44 mmol) y se agitó durante 16 h a 90°C. Se diluyó la mezcla de reacción con acetato de etilo (30 mL) y se extrajo con acetato de etilo (2 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera
(50 mL) y se secó sobre sulfato de sodio y se concentró para proporcionar 1-(4-fluoro-2-isopropoxifenil)etanona (2,5 g, 12,75 mmol, 65% de rendimiento) como un líquido marrón. Ms (ESI) m/z 197,33 [M]+
B. 2-(4-fluoro-2-isopropoxifenil)-2-oxoacetato de etilo. A una solución agitada de 1-(4-fluoro-2-isopropoxifenil)etanona (2,0 g, 10,20 mmol) en piridina (15 mL) se añadió dióxido de selenio (2,83 g, 25,51 mmol) y se agitó durante 16 h a 100°C. Se diluyó la mezcla de reacción con diclorometano (30 mL) y se filtró a través de un lecho de Celite. Se trató el filtrado con cloroformiato de etilo (6 mL) a 0°C y se agitó a temperatura ambiente durante 3 h. Se neutralizó la mezcla de reacción con ácido clorhídrico acuoso 1 N (hasta pH-4) y se extrajo con acetato de etilo (2 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL) y se secó sobre sulfato de sodio y se concentró. Se purificó el producto en bruto con cromatografía en columna usando gel de sílice en malla 100-200 eluyendo acetato de etilo al 10% en hexanos para proporcionar 2-(4-fluoro-2-isopropoxifenil)-2-oxoacetato de etilo (800 g, 3,14 mmol, 32% de rendimiento) como un líquido marrón. MS (ESI) m/z 255,33 [M]+
C. 2,2-difluoro-2-(4-fluoro-2-isopropoxifenil)acetato de etilo. A una solución agitada de 2-(4-fluoro-2-isopropoxifenil)-2-oxoacetato de etilo (450 mg, 1,77 mmol) se añadió trifluoruro de dietilamino azufre (714 mg, 4,42 mmol) y se agitó a temperatura ambiente durante 16 h. Se basificó la mezcla de reacción con bicarbonato de sodio saturado acuoso a pH-8 y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 30 mL), salmuera (30 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(4-fluoro-2-isopropoxifenil)acetato de etilo (200 mg, 0,724 mmol, 40% de rendimiento) como un líquido marrón. GC-MS (ESI) m/z 276 [M]+
D. Ácido 2,2-difluoro-2-(4-fluoro-2-isopropoxifenil)acético. A una solución agitada de 2,2-difluoro-2-(4-fluoro-2-isopropoxifenil)acetato de etilo (350 mg, 1,26 mmol) en mezcla de tetrahidrofurano/metanol/agua (30 mL, 1:1:1) se añadió hidróxido de litio monohidratado (160 mg, 3,80 mmol) y se agitó a temperatura ambiente durante 4 h. Se concentró la mezcla de reacción; se neutralizó el residuo obtenido con ácido clorhídrico acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 50 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(4-fluoro-2-isopropoxifenil)acético (200 mg, 0,806 mmol, 63% de rendimiento) como un semisólido marrón. GC-MS (ESI) m/z 224,0 [M]+; 1H RMN (300 Mhz, CDCla) 8 ppm 7,62 (dd, J = 8,4, 2,1 Hz, 1H), 7,19 (brs, 1H), 6,72 (ddd, J = 10,8, 8,4, 2,1 Hz, 1H), 6,65 (brd, J =10,5 Hz, 1H), 4,58 (sep, J = 5,7 Hz, 1H), 1,33 (d, J = 6,3 Hz, 6H).
E. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluoro-2-isopropoxifenil)acetamida. A una solución enfriada con hielo de ácido 2,2-difluoro-2-(4-fluoro-2-isopropoxifenil)acético (289 mg, 1,165 mmol) en piridina (10 mL) se añadió POCh (446 mg, 2,91 mmol) y en agitación a 0-5°C durante 1 h. A continuación se trató la mezcla de reacción con clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,970 mmol) y se agitó a 0-30°C durante 1 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 10 mL), salmuera (10 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el producto en bruto por columna de fase inversa Reveleris C-18 (acetonitrilo al 45-55% en ácido fórmico acuoso al 0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluoro-2-isopropoxifenil)acetamida (35 mg, 0,069 mmol, 7% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 503,95 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 8 ppm 10,98 (s, 1 H), 9,32 (t, J =5,7 Hz, 1H), 7,70 (d, J =7,70 Hz, 1 H), 7,60-7,50 (m, 2H), 7,46 (brd, J = 7,7 Hz, 1 H), 7,08 (brd, J = 11,0 Hz, 1 H), 6,85 (dd, J = 8,7, 6,3 Hz, 1 H), 5,11 (dd, J =13,6, 4,77 Hz, 1 H), 4,68 (sep, J = 6,3 Hz, 1 H), 4,53-4,23 (m, 3 H), 3,00-2,81 (m, 1 H), 2,68-2,49 (m, 1H), 2,44-2,30 (m, 1 H), 2,07- 1,93 (m, 1 H), 1,11 (dd, J = 4,5 Hz, 0,2 Hz, 6H).
Ejemplo 56
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(2,2,2-trifluoroetoxi)fenil)acetamida
A. 1-yodo-2-(2,2,2-trifluoroetoxi)benceno. A una solución agitada de 2-yodofenol (2 g, 9,09 mmol) en N,N-dimetilformamida (30 mL) se añadió 1,1,1-trifluoro-2-yodoetano (1,34 mL, 13,63 mmol), seguido por carbonato de
potasio (3,76 g 2,72 mmol) y se agitó a 50°C durante 16 h. Se diluyó la mezcla de reacción con agua con hielo (40 mL) y se extrajo con acetato de etilo (3 X 40 mL). Se lavaron las capas orgánicas combinadas con agua (40 mL), salmuera (40 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 1-yodo-2-(2,2,2-trifluoroetoxi)benceno (1,6 g, 5,46 mmol, 58% de rendimiento) como un líquido incoloro. m S (ESI) m/z 302,0 [M]+.
B. 2,2-difluoro-2-(2-(2,2,2-trifluoroetoxi)fenil)acetato de etilo. A una solución agitada de 1-yodo-2-(2,2,2-trifluoroetoxi)benceno (1,5 g, 5,63 mmol) en dimetilsulfóxido (20 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (1,1 mL, 8,44 mmol) seguido por cobre (0,92 g, 14,63 mmol) a TA y se agitó a 55°C durante 6 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3 X 20 mL). Se lavaron las capas orgánicas combinadas con agua (20 mL), salmuera (20 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto obtenido por cromatografía en columna sobre gel de sílice (acetato de etilo en éter de petróleo al 20%) para proporcionar 2,2-difluoro-2-(2-(2,2,2-trifluoroetoxi)fenil)acetato de etilo (410 mg, 1,37 mmol, 24%) como un líquido incoloro. MS (ESI) m/z 298,1 [M]+.
C. Ácido 2,2-difluoro-2-(2-(2,2,2-trifluoroetoxi)fenil)acético. A una solución agitada de 2,2-difluoro-2-(2-(2,2,2-trifluoroetoxi)fenil)acetato de etilo (400 mg, 1,34 mmol) en tetrahidrofurano: metanol: agua (15 mL, 1:1:1) se añadió hidróxido de litio monohidratado (169 mg, 4,02 mmol) y se agitó a temperatura ambiente durante 4 h. Se extrajeron los productos volátiles a presión reducida y se disolvió el producto en bruto obtenido en agua (15 mL) y se lavó con acetato de etilo (2 X 10 mL). Se acidificó la capa acuosa con solución acuosa de clorhidrato 1 N y se extrajo con acetato de etilo (3 X 10 mL). Se lavaron las capas orgánicas combinadas con salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró el disolvente para proporcionar ácido 2,2-difluoro-2-(2-(2,2,2-trifluoroetoxi)fenil)acético (270 mg, 1 mmol, 59% de rendimiento) como un compuesto semisólido. 1H RMN (400 MHz, CDCh) 87,72 (d, J = 6,3 Hz, 1H), 7,51 (t, J =8,4 Hz, 1H), 7,19 (t, J = 7,8 Hz, 1H), 6,93 (d, J = 8,4 Hz, 1H), 6,68 (brs, 1 H), 4,38 (q, J = 8,1 Hz, 1H).
D. N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdolm-5-N)metM)-2,2-difluoro-2-(2-(2,2,2-trifluoroetoxi)fenil)acetamida. A una solución enfriada con hielo de ácido 2,2'-difluoro-2-(2-(2,2,2-trifluoroetoxi)fenil)acético (262 mg, 1,16 mmol) en piridina (6 mL) se añadió oxicloruro de fósforo (0,27 mL, 2,9 mmol) gota a gota y se agitó a 0-5°C durante 1 h y a continuación se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) y se agitó a temperatura ambiente durante 2 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3 X 15 mL). Se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 (acetonitrilo al 50-55% en ácido fórmico acuoso al 0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(2,2,2-trifluoroetoxi)fenil)acetamida (60 mg, 0,11 mmol, 11% de rendimiento) como un sólido blanco. MS (ESI) m/z 525,89 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 810,98 (s, 1H), 9,42 (t, J = 5,4 Hz, 1H), 7,70 (d, J= 7,5 Hz, 1H), 7,63-7,52 (m, 2H), 7,49 (s, 1H), 7,43 (d, J = 8,1 Hz, 1H), 7,26 (d, J =8,1 Hz, 1H),7,18 (dd, J = 7,7, 7,6 Hz, 1H), 5,11 (dd, J = 13,2, 4,8 Hz, 1H), 4,75 (q, J =8,7 Hz, 2H), 4,46 (d, J =17,1 Hz, 1H), 4,45 (d, J = 6,0 Hz, 2H), 4,31 (d, J =17,4 Hz, 1H), 2,92 - 2,86 (m, 1H), 2,63 - 2,57 (m, 1H), 2,42 - 2,37 (m, 1H), 2,02 - 1,98 (m, 1H).
Ejemplo 57
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2-(2-etoxi-4-fluorofenil)-2,2-difluoroacetamida
A. 1-(2-etoxi-4-fluorofenil)etanona. A una solución agitada de 1-(4-fluoro-2-hidroxifenil)etanona (3 g, 19,48 mmol) en N,N-dimetilformamida (15 mL) se añadió bromoetano (5,30 g, 48,76 mmol) carbonato de potasio (8,06 g 58,44 mmol) y se agitó durante 16 h a 100°C. Se diluyó la mezcla de reacción con acetato de etilo (30 mL) y se extrajo con acetato de etilo (2 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 1-(2-etoxi-4-fluorofenil)etanona (2,6 g, 14,28 mmol, 74% de rendimiento) como un líquido marrón. MS (ESI) m/z 183,17 [M]+
B. 2-(2-etoxi-4-fluorofenil)-2-oxoacetato de etilo. A una solución agitada de 1-(2-etoxi-4-fluorofenil)etanona (1,0 g, 5,49 mmol) en piridina (15 mL) se añadió dióxido de selenio (1,52 g, 13,73 mmol) y se agitó durante 16 h a 100°C. Se diluyó la mezcla de reacción con diclorometano (30 mL) y se filtró a través de un lecho de Celite. Al filtrado se le añadió cloroformiato de etilo (3 mL) a 0°C y se agitó a temperatura ambiente durante 3 h. Se neutralizó la mezcla de reacción con ácido clorhídrico acuoso 1 N (hasta pH-4) y se extrajo con acetato de etilo (2 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el producto en bruto con cromatografía en columna usando gel de sílice de malla 100-200 eluyendo acetato de etilo-éter de petróleo al 10% para proporcionar 2-(2-etoxi-4-fluorofenil)-2-oxoacetato de etilo (880 g, 3,66 mmol, 67% de rendimiento) como un líquido marrón. MS (ESI) m/z 241,14 [M]+
C. 2-(2-etoxi-4-fluorofenil)-2,2-difluoroacetato de etilo. A una solución agitada de 2-(2-etoxi-4-fluorofenil)-2-oxoacetato de etilo (800 mg, 3,33 mmol) se añadió trifluoruro de dietilamino azufre (1,34 g, 8,33 mmol) y se agitó durante 16 h a temperatura ambiente. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 30 mL), salmuera (30 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-(2-etoxi-4-fluorofenil)-2,2-difluoroacetato de etilo (450 mg, 1,71 mmol, 51% de rendimiento) como un líquido marrón. GC-MS (ESI) m/z 262 [M]+
D. Ácido 2-(2-etoxi-4-fluorofenil)-2,2-difluoroacético. A una solución agitada de 2-(2-etoxi-4-fluorofenil)-2,2-difluoroacetato de etilo (1 g, 3,81 mmol) en mezcla detetrahidrofurano/metanol/agua (30 mL, 1:1:1) se añadió hidróxido de litio monohidratado (480 mg, 11,45 mmol) y se agitó a temperatura ambiente durante 4 h. Se concentró la mezcla de reacción y se neutralizó el residuo con ácido clorhídrico acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 50 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2-(2-etoxi-4-fluorofenil)-2,2-difluoroacético (600 mg, 2,56 mmol, 67% de rendimiento) como un semisólido marrón. El compuesto en bruto se usó para la etapa siguiente sin purificación adicional.
E. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2-(2-etoxi-4-fluorofenil)-2,2-difluoroacetamida. A una solución agitada en frío (0°C) de ácido 2-(2-etoxi-4-fluorofenil)-2,2-difluoroacético (181 mg, 0,776 mmol) en piridina (10 mL) se añadió cloruro de fosforilo (294 mg, 1,93 mmol) y se agitó a 0°C-5°C durante 1 h. A esta mezcla de reacción se le añadió a continuación clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (200 mg, 0,647 mmol) a 0°C y se dejó calentar agitando a temperatura ambiente durante un periodo de 1 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2X10 mL), salmuera (10 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el producto en bruto por columna de fase inversa Reveleris C-18 usando acetonitrilo al 45-55% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2-(2-etoxi-4-fluorofenil)-2,2-difluoroacetamida (80 mg, 0,163 mmol, 25% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 489,95 [M+1]+. 1H RMN (300MHz, DMSO-d6) 810,98 (s, 1H), 9,35 (brt, J=5,8 Hz, 1H), 7,71 (d, J=7,7 Hz, 1H), 7,59 (dd, J=8,6, 6,8 Hz, 1H), 7,50 (s, 1H), 7,44 (d, J=7,7 Hz, 1H), 7,05 (br d, J=11,0 Hz, 1H), 6,88 (td, J=8,5, 2,4 Hz, 1H), 5,11 (dd, J=13,3, 5,3 Hz, 1H), 4,50-4,26 (m, 4H), 4,00 (q, J=6,9 Hz, 2H), 3,00-2,85 (m, 1H), 2,67-2,55 (m, 1H), 2,44-2,31 (m, 1H), 2,06-1,95 (m, 1H), 1,11 (t, J=6,9 Hz, 3H).
Ejemplo 58
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-isopropoxifenil)acetamida
A. 1-yodo-2-isopropoxibenceno. A una solución agitada de 2-yodofenol (2 g, 9,09 mmol) en N,N-dimetilformamida (20 mL) se añadió 2-bromopropano (3,38 mL, 36,3 mmol) seguido por carbonato de potasio (3,76 g, 27,27 mmol) y se agitó a 90°C durante 16 h. Se diluyó la mezcla de reacción con agua con hielo (25 mL) y se extrajo con acetato de etilo (3 X 20 mL). Se lavaron las capas orgánicas combinadas con agua (20 mL), salmuera (20 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 1-yodo-2-isopropoxibenceno (2,0 g, 7,63 mmol, 84% de rendimiento) como un líquido incoloro. MS (ESI) m/z 262,21 [M]+.
B. 2,2-difluoro-2-(2-isopropoxifenil)acetato de etilo. A una solución agitada de 1-yodo-2-isopropoxibenceno (2 g, 7,6 mmol) en dimetilsulfóxido (20 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (1,5 mL, 11,45 mmol) seguido por cobre (1,26 g, 19,84 mmol) a TA y se agitó a 55°C durante 6 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3 X 20 mL). Se lavaron las capas orgánicas combinadas con agua (20 mL), salmuera (20 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto obtenido por cromatografía instantánea (acetato de etilo en éter de petróleo al 20%) para proporcionar 2,2-difluoro-2-(2-isopropoxifenil)acetato de etilo (1,3 g, 5,03 mmol, 66%) como un líquido incoloro. MS (ESI) m/z 259,23 [M+1]+.
C. Ácido 2,2-difluoro-2-(2-isopropoxifenil)acético. A una solución agitada de 2,2-difluoro-2-(2-isopropoxifenil)acetato de etilo (1 g, 3,87 mmol) en tetrahidrofurano: metanol: agua (15 mL, 1:1:1) se añadió hidróxido de litio monohidratado (0,49 g, 11,62 mmol) y se agitó a temperatura ambiente durante 4 h. Se extrajeron los productos volátiles a presión reducida y se disolvió el producto en bruto obtenido en agua (15 mL), se lavó con acetato de etilo (2X10 mL). Se acidificó la capa acuosa con solución acuosa de clorhidrato 1 N y se extrajo con acetato de etilo (3 X 15 mL). Se lavaron las capas orgánicas combinadas con salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar ácido 2,2-difluoro-2-(2-isopropoxifenil)acético (600 mg, 2,60 mmol, 67% de rendimiento) como un compuesto semisólido. 1H RMN (300 MHz, CDCh) 88,75 (brs, 1H), 7,65 (d, J = 7,2 Hz, 1H), 7,44 (dd, J = 8,0, 7,6 Hz, 1H), 7,03 (dd, J = 8,0, 7,2 Hz, 1H), 6,94 (d, J = 8,4 Hz, 1H), 4,66 (Sep, J = 6,0 Hz, 1H), 1,32 (d, J = 6,0 Hz, 6H).
D. N-((2-(2,6-dioxopiperldin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-isopropoxifenil)acetamida. A una solución enfriada con hielo de ácido 2,2-difluoro-2-(2-isopropoxifenil)acético (267 mg, 1,16 mmol) en piridina (6 mL) se añadió oxicloruro de fósforo (0,27 mL, 2,9 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A continuación, se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) y se agitó a temperatura ambiente durante 2 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3X15 mL). Se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 (acetonitrilo al 50-55% en ácido fórmico acuoso al 0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-isopropoxifenil)acetamida (40 mg, 0,08 mmol, 8% de rendimiento) como un sólido blanco. MS (ESI) m/z 485,98 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 810,99 (s, 1H), 9,26 (t, J =5,8 Hz, 1H), 7,70 (d, J =7,8 Hz, 1H), 7,55-7,45 (m, 4H), 7,12 (d, J =8,4 Hz, 1H), 7,02 (dd, J = 7,2, 7,0 Hz, 1H), 5,11 (dd, J =13,2, 5,1 Hz, 1H), 4,46 (Sep, J = 6,0 Hz, 1H), 4,45 (d, J = 6,3 Hz, 2H), 4,44 (d, J =17,2, 1H), 4,31 (d, J =17,4 Hz, 1H), 2,98 - 2,86 (m, 1H), 2,57 - 2,49 (m, 1H), 2,43 - 2,30 (m, 1H), 2,04 - 1,94 (m, 1H), 1,13 (d, J = 6,0 Hz, 3H), 1,12 (d, J = 6,0 Hz, 3H).
Ejemplo 59
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-fluoro-4-isopropoxifenil)acetamida
A. 1-(2-fluoro-4-isopropoxifenil)etanona. A una solución agitada de 1-(2-fluoro-4-hidroxifenil)etanona (300 mg, 1,95 mmol) en N,N-dimetilformamida (3 mL) se añadió yoduro de isopropilo (397 mg, 2,33 mmol) seguido por carbonato de potasio (672 mg, 4,87 mmol) y se agitó a 90°C durante 16 h. Se diluyó la mezcla de reacción con agua con hielo (20 mL) y se extrajo con acetato de etilo (3 X 10 mL). Se lavaron las capas orgánicas combinadas con agua (10 mL), salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 1-(2-fluoro-4-isopropoxifenil)etanona (300 mg, 1,53 mmol, 79% de rendimiento) como un líquido incoloro. MS (ESI) m/z 197,2 [M+1]+.
B. 2-(2-fluoro-4-isopropoxifenil)-2-oxoacetato de etilo. A una solución agitada de 1-(2-fluoro-4-isopropoxifenil)etanona (300 mg, 1,63 mmol) en piridina (3 mL) se añadió dióxido de selenio (452 mg, 3,38 mmol) a temperatura ambiente. Se agitó la mezcla de reacción a 100°C durante 16 h. Se filtró la mezcla de reacción a través de un lecho de Celite y se lavó minuciosamente con diclorometano (10 mL). Se añadió cloroformiato de etilo (0,64 mL) al filtrado a 0°C y se agitó a temperatura ambiente durante 4 h. Se inactivó la mezcla de reacción con agua con hielo
y se extrajo con diclorometano (3X10 mL). Se lavaron las capas orgánicas combinadas con solución de clorhidrato 1 N (10 mL), salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 2-(2-fluoro-4-isopropoxifenil)-2-oxoacetato de etilo (200 mg, 0,787 mmol, 48% de rendimiento) como un líquido incoloro. MS (ESI) m/z 255,28 [M+1]+.
C. 2,2-difluoro-2-(2-fluoro-4-isopropoxifenil)acetato de etilo. Se añadió 2-(2-fluoro-4-isopropoxifenil)-2-oxoacetato de etilo (200 mg, 0,787 mmol) en trifluoruro de dietilamino azufre (0,4 mL) a 0°C y se agitó a temperatura ambiente durante 16 h. Se inactivó la mezcla de reacción con solución de bicarbonato de sodio acuosa y se extrajo con acetato de etilo (3X10 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secaron sobre sulfato de sodio anhidro, se filtraron y se concentraron. Se purificó el producto en bruto obtenido por cromatografía en columna instantánea (gel de sílice 100-200, acetato de etilo en éter de petróleo al 10%) para proporcionar 2,2-difluoro-2-(2-fluoro-4-isopropoxifenil)acetato de etilo (200 mg, 0,72 mmol, 92% de rendimiento) como un líquido incoloro. MS (ESI) m/z 276,1 [M+1]+.
D. Ácido 2,2-difluoro-2-(2-fluoro-4-isopropoxifenil)acético. A una solución agitada de 2,2-difluoro-2-(2-fluoro-4-isopropoxifenil)acetato de etilo (200 mg, 0,72 mmol) en mezcla de tetrahidrofurano: metanol: agua (10 mL, 1:1:1) se añadió hidróxido de litio monohidratado (91 mg, 2,17 mmol) y se agitó a temperatura ambiente durante 16 h. Se concentró la mezcla de reacción a presión reducida y se disolvió el residuo resultante en agua (10 mL) y se lavó con acetato de etilo (2X10 mL). Se acidificó la fase acuosa con solución acuosa de clorhidrato 1 N y se extrajo con acetato de etilo (3 X 10 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar ácido 2,2-difluoro-2-(2-fluoro-4-isopropoxifenil)acético (160 mg, 0,65 mmol, 89% de rendimiento) como un compuesto semisólido.
E. N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdoMn-5-M)metM)-2,2-difluoro-2-(2-fluoro-4-isopropoxifenil)acetamida. A una solución enfriada con hielo de ácido 2,2-difluoro-2-(2-fluoro-4-isopropoxifenil)acético (289 mg, 1,16 mmol) en piridina (9 mL) se añadió oxicloruro de fósforo (0,27 mL, 2,9 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A continuación, se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il) piperidina-2,6-diona (300 mg, 0,97 mmol) se añadió en la mezcla de reacción y se agitó a temperatura ambiente durante 1 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3X 15 mL). Se lavaron las capas orgánicas combinadas con salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto resultante por cromatografía de columna en fase inversa Reveleris C-18 (acetonitrilo al 50-55% en ácido fórmico acuoso al 0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-fluoro-4-isopropoxifenil)acetamida (60 mg, 0,12 mmol, 12% de rendimiento) como un sólido blanco. MS (ESI) m/z 503,99 [M+1]+. 1H RMN (400 MHz, DMSO-d6) 810,99 (s, 1H), 9,59 (d, J = 7,2 Hz, 1H), 7,70 (d, J = 7,6 Hz, 1H), 7,48 (dd, J = 8,8, 8,7 Hz, 1H), 7,47 (s, 1H), 7,41 (d, J = 8,0 Hz, 1H), 6,96 (dd, J = 13,2, 2,0 Hz, 1H), 6,87 (dd, J = 8,3, 2,0 Hz, 1H), 5,11 (dd, J = 13,2, 5,2 Hz, 1H), 4,71 (sep, J = 6,0 Hz, 1H), 4,48 (d, J = 6,4 Hz, 2H), 4,45 (d, J = 17,2 Hz, 1H), 4,31 (d, J = 18,0 Hz, 1H), 2,95 -2,87 (m, 1H), 2,62-2,58 (m, 1H), 2,41 - 2,37 (m, 1H), 2,02 - 1,99 (m, 1H), 1,28 (d, J = 5,6 Hz, 6H).
Ejemplo 60
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(morfolinometil)fenil)acetamida
A. 2,2-difluoro-2-(3-(morfolinometil)fenil)acetato de etilo. A una solución agitada de 2,2-difluoro-2-(3-formilfenil)acetato de etilo (1,2 g, 5,26 mmol) en etanol (25 mL) se añadió morfolina (0,91 g, 10,52 mmol), ácido acético (0,63 mL, 10,52 mmol) y se agitó a 0°C durante 1 h y a continuación se añadió cianoborohidruro de sodio (0,661 g, 10,52 mmol) y se agitó a temperatura ambiente durante 3 h. Se inactivó la mezcla de reacción con agua (50 mL) y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 20 mL), salmuera (30 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(3-(morfolinometil)fenil)acetato de etilo (0,8 g, 2,67 mmol, 51% de rendimiento) como un líquido marrón. LCMS (ESI) m/z 300,0.
B. Ácido 2,2-difluoro-2-(3-(morfolinometil)fenil)acético. A una solución agitada en frío (0°C) de 2,2-difluoro-2-(3(morfolinometil)fenil)acetato de etilo (0,8 g, 2,67 mmol) en mezcla de metanol/tetrahidrofurano/agua (15 mL, 1:1:1) se añadió hidróxido de litio monohidratado (337 mg, 8,02 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con bisulfato de potasio acuoso al 10% (20 mL) y se extrajo con acetato de etilo (2 X 40 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(3-(morfolinometil)fenil)acético (600 mg, 2,21 mmol, 82% de rendimiento) como un sólido marrón. LCMS (ESI) m/z 272.
C. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(morfolinometil)fenil)acetamida. A una solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(3-(morfolinometil)fenil)acético (290 mg, 1,06 mmol) y clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,970 mmol) en N,N-dimetilformamida (20 mL) se añadió N,N-diisopropiletilamina (0,6 mL, 3,33 mmol) seguido por 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metileno]- 1H-1,2,3-triazolo[4,5-b]piridinio (553,3 mg, 1,45 mmol) y se agitó a temperatura ambiente durante 4 h. Se diluyó la mezcla de reacción con agua (50 mL) y se extrajo con acetato de etilo (2 X 40 mL). Se lavaron las capas orgánicas combinadas con salmuera (30 mL), se secó sobre sulfato de sodio, se concentró y se secó al vacío. Se purificó el producto por columna de fase inversa Reveleris C-18 usando acetonitrilo al 40% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(morfolinometil)fenil)acetamida (40 mg, 0,06 mmol, 8% de rendimiento) como un sólido blanquecino. LCMS (ESI) m/z 526,7 [M+1]+. 1H RMN (300 MHz, TFA-d4) 8 = 8,03 - 7,92 (m, 2H), 7,83 (brs,1H), 7,72 (brs, 2H), 7,64 - 7,54 (m, 2H), 5,64-5,0 (m,1H), 4,80 (brs, 2H), 4,73 (br s,2H), 4,6 (br s,2H), 4,4(s,2H), 4,08 (t, J=11,7 Hz, 2H), 3,73 (d, J=11,7 Hz, 1H), 3,51 (d, J=12,1 Hz, 1H), 3,33- 3,04 (m, 2H), 2,92-2,61 (m, 1H), 2,53 (s, 1H).
Ejemplo 61
N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdoMn-5-M)metM)-2,2-difluoro-2-(4-fluoro-2-(2,2,2-trifluoroetoxi)fenil)acetamida
A. 1-(4-fluoro-2-(2,2,2-trifluoroetoxi)fenil)etanona. A una solución agitada de 1-(4-fluoro-2-hidroxifenil)etanona (1 g, 6,48 mmol) en N,N-dimetilformamida (20 mL) se añadió 1,1,1-trifluoro-2-yodoetano (0,64 mL, 6,48 mmol) seguido por carbonato de potasio (2,68 g, 19,46 mmol) y se agitó a 90°C durante 16 h. Se diluyó la mezcla de reacción con agua con hielo (30 mL) y se extrajo con acetato de etilo (3 X 20 mL). Se lavaron las capas orgánicas combinadas con agua (20 mL), salmuera (20 mL), se secó sobre sulfato de sodio, se filtró y se concentró el disolvente para proporcionar 1-(4-fluoro-2-(2,2,2-trifluoroetoxi)fenil)etanona (325 mg, 1,36 mmol, 20% de rendimiento) como un líquido incoloro. 1H RMN (400 MHz, CDCla) 87,90 (dd, J = 6,8, 6,8 Hz, 1H), 6,85 - 6,81 (m, 1H), 6,61 (dd, J = 2,0, 2,4 Hz, 1H), 4,42 - 4,38 (m, 2H), 2,61 (s, 3H).
B. 2-(4-fluoro-2-(2,2,2-trifluoroetoxi)fenil)-2-oxoacetato de etilo. A una solución agitada de 1-(4-fluoro-2-(2,2,2-trifluoroetoxi)fenil)etanona (320 mg, 1,35 mmol) en piridina (10 mL) se añadió dióxido de selenio (376 mg, 3,38 mmol) a temperatura ambiente. Se agitó la mezcla de reacción a 100°C durante 16 h. Se filtró la mezcla de reacción a través de lecho de celite y se lavó con diclorometano (10 mL). Se añadió cloroformiato de etilo(0,64 mL) al filtrado a 0°C y se agitó a temperatura ambiente durante 4 h. Se inactivó la mezcla de reacción con agua con hielo y se extrajo con diclorometano (3 X 10 mL). Se lavaron las capas orgánicas combinadas con en solución de clorhidrato (15 mL), salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 2-(4-fluoro-2-(2,2,2-trifluoroetoxi)fenil)-2-oxoacetato de etilo (300 mg, 1,02 mmol, 75% de rendimiento) como un líquido incoloro. 1H RMN (400 MHz, CDCla) 87,99 - 7,95 (m, 1H), 6,94 - 6,89 (m, 1H), 6,66 (dd, J = 2,4, 9,6 Hz, 1H), 4,42 - 4,35 (m, 4H), 1,38 (t, J = 7,6 Hz, 3H).
C. 2,2-difluoro-2-(4-fluoro-2-(2,2,2-trifluoroetoxi)fenil)acetato de etilo. Se añadió 2-(4-fluoro-2-(2,2,2-trifluoroetoxi)fenil)-2-oxoacetato de etilo (300 mg, 1,02 mmol) en trifluoruro de dietilamino azufre (DAST, 0,9 mL) a 0°C y se agitó a temperatura ambiente durante 16 h. Se inactivó la mezcla de reacción con solución de bicarbonato de sodio acuosa y se extrajo con acetato de etilo (3X10 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secaron sobre sulfato de sodio anhidro, se filtraron y se concentraron. Se purificó el producto en bruto obtenido por cromatografía en columna (gel de sílice 100-200, acetato de etilo en éter de petróleo al 10%) para
proporcionar 2,2-difluoro-2-(4-fluoro-2-(2,2,2-trifluoroetoxi)fenil)acetato de etilo (250 mg, 0,79 mmol, 77% de rendimiento) como un líquido incoloro. 1H RMN (300 MHz, CDCl3) 87,71 - 7,66 (m, 1H), 6,91 - 6,85 (m, 1H), 6,66 (d, J = 9,6 Hz, 1H), 4,39 - 4,28 (m, 4H), 1,33 (t, J = 4,2 Hz, 3H).
D. Ácido 2,2-difluoro-2-(4-fluoro-2-(2,2,2-trifluoroetoxi)fenil)acético. A una solución agitada de 2,2-difluoro-2-(4-fluoro-2-(2,2,2-trifluoroetoxi)fenil)acetato de etilo (390 mg, 1,23 mmol) en tetrahidrofurano: metanol: agua (12 mL, 1:1:1) se añadió hidróxido de litio monohidratado (155 mg, 3,70 mmol) y se agitó a temperatura ambiente durante 16 h. Se concentró la mezcla de reacción a presión reducida y se disolvió el producto en bruto obtenido en agua (10 mL) y se lavó con acetato de etilo (2X 10 mL). Se acidificó la capa acuosa con solución acuosa de clorhidrato 1 N y se extrajo con acetato de etilo (3X10 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró el disolvente para proporcionar ácido 2,2-difluoro-2-(4-fluoro-2-(2,2,2-trifluoroetoxi)fenil)acético (280 mg, 0,98 mmol, 79% de rendimiento) como un compuesto semisólido. 1H RMN (400 MHz, CDCla) 87,72 - 7,69 (m, 1H), 6,91 - 6,87 (m, 1H), 6,66 (d, J = 9,2 Hz, 1H), 6,57 (brs, 1H), 4,39 - 4,34 (m, 2H).
E. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluoro-2-(2,2,2-trifluoroetoxi)fenil)acetamida. A una solución enfriada con hielo de ácido 2,2-difluoro-2-(4-fluoro-2-(2,2,2-trifluoroetoxi)fenil)acético (280 mg, 0,97 mmol) en piridina (9 mL) se añadió oxicloruro de fósforo (0,27 mL, 2,9 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A continuación, se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) en la mezcla de reacción y se agitó a temperatura ambiente durante 1 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3X 15 mL). Se lavaron las capas orgánicas combinadas con salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 (acetonitrilo al 50-55% en 0,1% ácido fórmico acuoso) para dar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluoro-2-(2,2,2-trifluoroetoxi)fenil)acetamida (45 mg, 0,08 mmol, 8% de rendimiento) como un sólido blanco. MS (ESI) m/z 544,03 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 810,99 (s, 1H), 9,44 (t, J = 5,7 Hz, 1H), 7,70 (d, J = 7,8 Hz, 1H), 7,64 (dd, J = 9,0, 6,6 Hz, 1H), 8,49 (s, 1H), 7,42 (d, J = 8,1 Hz, 1H), 7,26 (dd, J = 11,1, 0,6 Hz, 1H), 7,02 (ddd, J =10,8, 8,7, 2,4 Hz, 1H), 5,11 (dd, J = 13,2, 5,1 Hz, 1H), 4,81 (q, J = 8,7 Hz, 2H), 4,45 (d, J = 7,2 Hz, 2H), 4,44 (d, J = 16,2 Hz, 1H), 4,31 (d, J = 17,1 Hz, 1H), 2,93-2,90 (m, 1H), 2,63 - 2,54 (m, 1H), 2,45 - 2,36 (m, 1H), 2,01 -1,98 (m, 1H).
Ejemplo 62
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil-2,2-difluoro-2-(4-isopropoxi-2-metilfenil)acetamida
A. 1-(4-Isopropoxi-2-metilfenil)etanona. A una solución agitada de 1-(4-hidroxi-2-metilfenil)etanona (2,0 g, 13,333 mmol) en N,N-dimetilformamida (20 mL) se añadió carbonato de potasio (5,5 g, 49,0 mmol) seguido por yoduro de isopropilo (2 mL, 20,0 mmol) y se agitó a 80°C durante 4 h. Se filtró la mezcla de reacción y agua (20 mL), se añadió y se extrajo con acetato de etilo (2 X 40 mL). Se lavaron las capas orgánicas combinadas con salmuera (30 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna (sílice 100 200) usando acetato de etilo en hexanos al 0-10% para proporcionar 1-(4-isopropoxi-2-metilfenil)etanona (1,58 g, 8,229 mmol, 62% de rendimiento). MS (ESI) m/z 193,48[M+1]+.
B. 2-(4-isopropoxi-2-metilfenil)-2-oxoacetato de etilo. A una solución agitada de 1-(4-isopropoxi-2-metilfenil)etanona (1,58 g, 8,229 mmol mmol) en piridina (30 mL) se añadió dióxido de selenio (1,82 g, 16,46 mmol) y se agitó durante 16 h a 100°C. Se diluyó la mezcla de reacción con diclorometano (40 mL) y se filtró a través de un lecho de Celite. Al filtrado se le añadió cloroformiato de etilo (3 mL) a 0°C y se agitó durante 2 h. Se neutralizó la mezcla de reacción con ácido clorhídrico acuoso 1 N (hasta pH-4) y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2X10 mL), salmuera (10 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo resultante por cromatografía en columna (sílice 100-200) usando acetato de etilo en éter de petróleo al 10% para proporcionar 2-(4-isopropoxi-2-metilfenil)-2-oxoacetato de etilo (1,0 g, 4,01 mmol, 49%) como un líquido incoloro. MS (ESI) m/z 251,40 [M+1]+.
C. 2,2-difluoro-2-(4-isopropoxi-2-metilfenil)acetato de etilo. Una solución agitada de 2-(4-isopropoxi-2-metilfenil)-2-oxoacetato (1,0 g, 4,01 mmol) de etilo se hizo reaccionar con trifluoruro de dietilamino azufre (1,32 mL, 10,025 mmol) y se agitó durante 12 h a temperatura ambiente. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavó la capa orgánica combinada con agua (2 X 10 mL), salmuera (10 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(4-isopropoxi-2-metilfenil)acetato de etilo (990 mg, 3,639 mmol, 91%) como un líquido. g C-MS (m/z) 272,2 [M]+.
D. Ácido 2,2-difluoro-2-(4-isopropoxi-2-metilfenil)acético. A una solución agitada en frío (0°C) de 2,2-difluoro-2-(4-isopropoxi-2-metilfenil)acetato de etilo (990 mg, 3,694 mmol) en mezcla de tetrahidrofurano: metanol:agua (1:1:1, 10 mL) se añadió hidróxido de litio (916 mg, 21,838 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con ácido clorhídrico acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 20 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(4-isopropoxi-2-metilfenil)acético (719 mg, 2,618 mmol, 81% de rendimiento) como un sólido marrón. 1H RMN (400 MHz, CdCís) 8 ppm 9,59 (br s, 1 H) 7,49 (d, J = 8,80 Hz, 1 H) 6,58-6,85 (m, 2 H) 4,41 -4,67 (m, 1 H) 2,41 (s, 3 H) 1,34 (m, 6H).
E. N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdolm-5-N)metN))-2,2-difluoro-2-(4-isopropoxi-2-metilfenil)acetamida. A una solución agitada de ácido 2,2-difluoro-2-(4-isopropoxi-2-metilfenil)acético (236 mg, 0,968 mmol) en piridina (25 mL) se añadió cloruro de fosforilo (0,3 mL, 2,16 mmol) gota a gota y se agitó a 0-5°C durante 1 h y a continuación se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,968 mmol) y se agitó a temperatura ambiente durante 1 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavó la capa orgánica combinada con agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna Grace de fase inversa Reveleris C-18 usando acetonitrilo al 40-50% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-isopropoxi-2-metilfenil)acetamida (79 mg, 0,158 mmol, 16% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 500,2329 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 8 ppm 10,98 (s, 1 H), 9,51 (brt, J=6,05 Hz, 1H), 7,69 (d, J=7,70 Hz, 1H), 7,51 -7,28 (m, 3H), 6,83 (s, 2H), 5,11 (br dd, J=13,20, 5,14 Hz, 1 H), 4,66 (dt, J= 12,10, 6,05 Hz, 1 H), 4,51 -4,25 (m, 4 H), 2,99 - 2,82 (m, 1H), 2,67 - 2,54 (m, 1 H), 2,46 - 2,30 (m, 1 H), 2,28 (s, 3 H), 2,07 - 1,95 (m, 1 H), 1,26 (m, 6H).
Ejemplo 63
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-isopropoxi-3-metilfenil)acetamida
A. 1-(4-Isopropoxi-3-metilfenil)etanona. A una solución agitada de 1-(4-hidroxi-3-metilfenil)etanona (3,0 g, 19,97 mmol) en N,N-dimetilformamida (20 mL) se añadió carbonato de potasio (8,3 g, 59,91 mmol), yoduro de isopropilo (4,0 g, 23,96 mmol) a temperatura ambiente y se agitó a 100°C durante 4 h. Se inactivó la mezcla de reacción con agua (150 mL) y se extrajo con acetato de etilo (2 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 100 mL), salmuera (100 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 1-(4-isopropoxi-3-metilfenil)etanona (3,2 g, 16,66 mmol, 84% de rendimiento). Lc Ms (ESI) m/z 193,3 [M+1]+.
B. 2-(4-isopropoxi-3-metilfenil)-2-oxoacetato de etilo. A una solución agitada de 1-(4-isopropoxi-3-metilfenil)etanona (3,2 g, 16,66 mmol) en piridina (15 mL) se añadió dióxido de selenio (4,6 g, 41,66 mmol) y se agitó a 100°C durante 16 h. Se diluyó la mezcla de reacción con diclorometano (30 mL) y se filtró a través de un lecho de Celite. Al filtrado se le añadió cloroformiato de etilo (9 mL) a 0°C y se agitó a temperatura ambiente durante 3 h. Se neutralizó la mezcla de reacción con ácido clorhídrico acuoso 1 N (hasta pH-4) y se extrajo con acetato de etilo (2 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-(4-isopropoxi-3-metilfenil)-2-oxoacetato de etilo (2,5 g, 10,0 mmol, 60% de rendimiento). LCMS (ESI) m/z 251,28 [M+1]+.
C. 2,2-difluoro-2-(4-isopropoxi-3-metilfenil)acetato de etilo. Una solución agitada de 2-(4-isopropoxi-3-metilfenil)
2- oxoacetato de etilo (500 mg, 2,00 mmol) se hizo reaccionar con trifluoruro de dietilamino azufre (2,5 g, 15,26 mmol) y se agitó a temperatura ambiente durante 16 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 30 mL), salmuera (30 mL) y se secó sobre sulfato de sodio y se concentró para dar 2,2-difluoro-2-(4-isopropoxi-3-metilfenil)acetato de etilo (450 mg, 1,65 mmol, 83% de rendimiento). GCMS (m/z) 272,2 [M]+.
D. Ácido 2,2-difluoro-2-(4-isopropoxi-3-metilfenil)acético. A una solución agitada de 2,2-difluoro-2-(4-isopropoxi-3- metilfenil)acetato de etilo (450 mg, 1,65 mmol) en tetrahidrofurano-metanol-agua (20 mL, 1:1:1) se añadió hidróxido de litio monohidratado (208 mg, 4,96 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con ácido clorhídrico al 10% (5 mL) y se extrajo con acetato de etilo (2 X 50 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secó sobre sulfato de sodio y se concentró para dar ácido 2,2-difluoro-2-(4-isopropoxi-3-metilfenil)acético (200 mg, 0,81 mmol, 50% de rendimiento). LCMS (ESI) m/z 243,34 [M-1]+.
E. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-isopropoxi-3-metilfenil)acetamida.
A una solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(4-isopropoxi-3-metilfenil)acético (200 mg, 0,81 mmol) en piridina (5 mL) se añadió cloruro de fosforilo (0,3 mL, 2,45 mmol) y se agitó a 0-5°C durante 1 h. A continuación se añadió clorhidrato de 3-(5-(amino metil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (253 mg, 0,81 mmol) y se agitó a temperatura ambiente durante 1 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (2 X 25 mL). Se lavaron las capas orgánicas combinadas con agua (25 mL), salmuera (25 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 40-45% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-isopropoxi-3-metilfenil)acetamida (90 mg, 0,18 mmol, 22,0% de rendimiento) como un sólido blanquecino. LCMS (ESI) m/z 500,57 [M+1]+. 1H RMN (400MHz, DMSO-d6) 8 = 10,98 (s, 1H), 9,52 (brt, J=6,1 Hz, 1H), 7,68 (d, J=7,8 Hz, 1H), 7,44 - 7,26 (m, 2H), 7,06 (d, J=8,3 Hz, 1H), 5,11 (dd, J=4,9, 13,2 Hz, 1H), 4,72-4,60 (m, 1H), 4,50-4,20 (m, 4H), 3,00-2,83 (m, 1H), 2,67-2,54 (m, 1H), 2,44-2,29 (m, 1H), 2,14 (s, 3H), 2,05 - 1,95 (m, 1H), 1,29 (d, J=6,4 Hz, 6H).
Ejemplo 64
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-fluoro-4-isopropoxifenil)acetamida
A. 1-(3-fluoro-4-isopropoxifenil)etanona. A una solución agitada de 1-(3-fluoro-4-hidroxifenil)etanona (3,0 g, 19,46 mmol) en N,N-dimetilformamida (20 mL) se añadió carbonato de potasio (8,0 g, 58,38 mmol), yoduro de isopropilo (3,9 g, 23,35 mmol) a temperatura ambiente y se agitó a 100°C durante 4 h. Se inactivó la mezcla de reacción con agua (150 mL) y se extrajo con acetato de etilo (2 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 100 mL), salmuera (100 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 1-(3-fluoro-4-isopropoxifenil)etanona (3,1 g, 15,81 mmol, 81% de rendimiento). LCMS (ESI) m/z 197,3 [M+1]+.
B. 2-(3-fluoro-4-isopropoxifenil)-2-oxoacetato de etilo. A una solución agitada de 1-(3-fluoro-4-isopropoxifenil)etanona (3,1 g, 15,81 mmol) en piridina (15 mL) se añadió dióxido de selenio (4,6 g, 39,54 mmol) y se agitó a 100°C durante 16 h. Se diluyó la mezcla de reacción con diclorometano (30 mL) y se filtró a través de un lecho de Celite. Al filtrado se le añadió cloroformiato de etilo (9 mL) a 0°C y se agitó a temperatura ambiente durante 3 h. Se neutralizó la mezcla de reacción con ácido clorhídrico acuoso 1 N (hasta pH-4) y se extrajo con acetato de etilo (2 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-(3-fluoro-4-isopropoxifenil)-2-oxoacetato de etilo (2,5 g, 9,84 mmol, 62% de rendimiento). LCMS (ESI) m/z 255,28 [M+1]+.
C. 2,2-difluoro-2-(3-fluoro-4-isopropoxifenil)acetato de etilo. A una solución agitada de 2-(3-fluoro-4-isopropoxifenil)-2-oxoacetato de etilo (1,2 g, 4,72 mmol) se añadió clorhidrato de dietilamino azufre (3,1 g, 19,23 mmol) y se agitó a temperatura ambiente durante 16 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio saturado acuoso (hasta pH-8) y se extrajo con acetato de etilo (3 X 100 mL). Se lavaron las capas orgánicas combinadas con
agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(3-fluoro-4-isopropoxifenil)acetato de etilo (900 mg, 3,26 mmol, 69% de rendimiento). Gc Ms (m/z) 276,2 [M]+.
D. Ácido 2,2-difluoro-2-(3-fluoro-4-isopropoxifenil)acético. A una solución agitada de 2,2-difluoro-2-(3-fluoro-4-isopropoxifenil)acetato de etilo (900 mg, 3,26 mmol) en tetrahidrofurano-metanol-agua (20 mL, 1:1:1) se añadió hidróxido de litio monohidratado (410 mg, 9,78 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con ácido clorhídrico al 10% (5 mL) y se extrajo con acetato de etilo (2 X 50 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(3-fluoro-4-isopropoxifenil)acético (700 mg, 2,82 mmol, 87% de rendimiento). LCMS (ESI) m/z 247,52 [M-1]+.
E. N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdoMn-5-N)metM)-2,2-difluoro-2-(3-fluoro-4-isopropoxifenil)acetamida. A una solución agitada en frío (0°C) de acido 2,2-difluoro-2-(3-fluoro-4-isopropoxifenil)acético (300 mg, 1,20 mmol) en piridina (10 mL) se añadió cloruro de fosforilo (0,4 mL, 3,62 mmol) y se agitó a 0-5°C durante 1 h. A continuación se añadió clorhidrato de 3-(5-(amino metil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (374 mg, 1,20 mmol) y se agitó a temperatura ambiente durante 1 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (2 X 25 mL). Se lavaron las capas orgánicas combinadas con agua (25 mL), salmuera (25 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 35 40% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-fluoro-4-isopropoxifenil)acetamida (80 mg, 0,15 mmol, 13,0% de rendimiento) como un sólido blanquecino. LCMS (ESI) m/z 504,56 [M+1]+. 1H RMN (400MHz, DMSO-d6) 8 = 10,98 (s, 1H), 9,60 (brt, J=6,1 Hz, 1H), 7,68 (d, J=7,8 Hz, 1H), 7,45 - 7,26 (m, 5H), 5,10 (dd, J=5,1, 13,5 Hz, 1H), 4,73 (m, 1H), 4,50-4,23 (m, 4H), 2,98-2,85 (m, 1H), 2,67 - 2,55 (m, 1H), 2,45 - 2,30 (m, 1H), 2,04 - 1,95 (m, 1H), 1,30 (d, J=5,9 Hz, 6H).
Ejemplo 65
2-(3-cloro-4-isopropoxifenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida
A. 1-(3-cloro-4-isopropoxifenil)etanona. A una solución agitada de 1-(3-cloro-4-hidroxifenil)etanona (2,5 g, 14,62 mmol) en N,N-dimetilformamida (30 mL) se añadió 2-yodopropano (2,98 g, 17,54 mmol) seguido por carbonato de potasio (5,04 g, 36,55 mmol) y se agitó a 90°C durante 16 h. Se diluyó la mezcla de reacción con agua con hielo (40 mL) y se extrajo con acetato de etilo (3 X 30 mL). Se lavaron las capas orgánicas combinadas con agua (30 mL), salmuera (30 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 1-(3-cloro-4-isopropoxifenil)etanona (2,3 g, 10,84 mmol, 74% de rendimiento) como un líquido incoloro. MS (ESI) m/z 213,23 [M]+.
B. 2-(3-cloro-4-isopropoxifenil)-2-oxoacetato de etilo. A una solución agitada de 1-(3-cloro-4-isopropoxifenil)etanona (2 g, 8,26 mmol) en piridina (30 mL) se añadió dióxido de selenio (2,69 g, 24,79 mmol) a temperatura ambiente. Se agitó la mezcla de reacción a 100°C durante 16 h. Se filtró la mezcla de reacción a través de un lecho de Celite y se lavó con diclorometano (30 mL). Se añadió cloroformiato de etilo (6 mL) al filtrado a 0°C y se agitó a temperatura ambiente durante 4 h. Se inactivó la mezcla de reacción con agua con hielo y se extrajo con diclorometano (3 x 30 mL). Se lavaron las capas orgánicas combinadas con solución de clorhidrato 1 N (30 mL), salmuera (30 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 2-(3-cloro-4-isopropoxifenil)-2-oxoacetato de etilo (1,8 g, 6,66 mmol, 80% de rendimiento) como un líquido incoloro. 1H RMN (400 MHz, CDCla) 88,08 (d, J = 2,0 Hz, 1H), 7,92 (dd, J = 8,8, 2,8 Hz, 1H), 7,00 (d, J = 8,8 Hz, 1H), 4,71 (sep, J = 6,2 Hz, 1H), 4,44 (q, J = 6,8 Hz, 2H), 1,44 (d, J = 6,5 Hz, 6H), 1,38 (t, J = 7,2 Hz, 3H).
C. 2-(3-cloro-4-isopropoxifenil)-2,2-difluoroacetato de etilo. Se añadió trifluoruro de dietilamino azufre (1,47 mL) en 2-(3-cloro-4-isopropoxifenil)-2-oxoacetato de etilo (1 g, 3,7 mmol) a 0°C y se agitó a temperatura ambiente durante 16 h. Se inactivó la mezcla de reacción con solución de bicarbonato de sodio acuosa y se extrajo con acetato de etilo (3 X 15 mL). Se lavaron las capas orgánicas combinadas con salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto obtenido por cromatografía en columna (gel de sílice 100-200, acetato de etilo en éter de petróleo al 10%) para proporcionar 2-(3-cloro-4-isopropoxifenil)-2,2-difluoroacetato de etilo
(900 mg, 3,08 mmol, 89% de rendimiento) como un líquido incoloro. MS (ESI) m/z 293,1 [M+1]+.
D. Ácido 2-(3-cloro-4-isopropoxifenil)-2,2-difluoroacético. A una solución agitada de 2-(3-cloro-4-isopropoxifenil)-2,2-difluoroacetato de etilo (0,45 g, 1,54 mmol) en tetrahidrofurano:metanol: agua (15 mL, 1:1:1) se añadió hidróxido de litio monohidratado (195 mg, 4,54 mmol) y se agitó a temperatura ambiente durante 16 h. Se extrajeron los productos volátiles a presión reducida y se disolvió el residuo obtenido en agua (10 mL), se lavó con acetato de etilo (2X10 mL). Se acidificó la capa acuosa con solución de clorhidrato 1 N y se extrajo con acetato de etilo (3X10 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar ácido 2-(3-cloro-4-isopropoxifenil)-2,2-difluoroacético (300 mg, 1,13 mmol, 74% de rendimiento) como un compuesto semisólido. 1H RMN (400 MHz, CDCh) 88,41 (brs, 1H), 7,65 (d, J = 2,1 Hz, 1H), 7,47 (dd, J =8,7, 2,1 Hz, 1H), 6,97 (dd, J = 5,1, 8,7 Hz, 1H), 4,62 (sep, J = 5,7 Hz, 1H), 1,40 (d, J = 6,3 Hz, 6H). E. 2-(3-doro-4-isopropoxifenM)-N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdoNn-5-N)metM)-2,2-difluoroacetamida.
A una solución enfriada con hielo de ácido 2-(3-cloro-4-isopropoxifenil)-2,2-difluoroacético (235 mg, 0,89 mmol) en piridina (6 mL) se añadió oxicloruro de fósforo (0,23 mL, 2,43 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A continuación, se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (250 mg, 0,81 mmol) y se agitó a temperatura ambiente durante 2 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3X15 mL). Se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 (acetonitrilo al 50-55% en ácido fórmico acuoso al 0,1%) para dar 2-(3-cloro-4-isopropoxifenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (60 mg, 0,11 mmol, 14% de rendimiento) como un sólido blanco. MS (ESI) m/z 520,01 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 810,98 (s, 1H), 9,62 (t, J = 5,7 Hz, 1H), 7,68 (d, J =7,8 Hz, 1H), 7,59 (d, J = 2,4 Hz, 1H), 7,49 (dd, J = 8,7, 2,1 Hz, 1H), 7,41 (s, 1H), 7,37 (d, J =8,1 Hz, 1H), 7,31 (d, J =8,7 Hz, 1H), 5,11 (dd, J = 13,2, 5,4 Hz, 1H), 4,76 (sep, J = 6,3 Hz, 1H), 4,45 (d, J = 5,7 Hz, 2H), 4,42 (d, J =18,0 Hz, 1H), 4,28 (d, J = 17,7, 1H), 2,93 - 2,87 (m, 1H), 2,63 -2,57 (m, 1H), 2,40 - 2,30 (m, 1H), 2,04 - 1,94 (m, 1H), 1,31 (d, J = 5,7 Hz, 6H).
Ejemplo 66
N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdoNn-5-N)metM)-2,2-difluoro-2-(2-metN-4-(trifluorometoxi)fenil)acetamida
A. 2,2-difluoro-2-(2-metil-4-(trifluorometoxi)fenil)acetato de etilo. A una solución agitada de 1-yodo-2-metil-4-(trifluorometoxi)benceno (1,0 g, 3,31 mmol) en dimetilsulfóxido (13 mL) se añadió cobre (546 mg, 8,60 mmol) y 2-bromo-2,2-difluoroacetato de etilo (0,638 mL 4,96 mmol) a temperatura ambiente y se agitó a 55°C durante 2 h. Se neutralizó la mezcla de reacción con solución de cloruro de amonio saturado (50 mL) y se extrajo con acetato de etilo (2 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 100 mL), salmuera (100 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(2-metil-4-(trifluorometoxi)fenil)acetato de etilo (900 mg, 3,02 mmol, 91%). 1H RMN (400MHz, CDCla) 87,65-7,58 (d, 1H), 7,18-7,02 (m, 2H), 4,41 - 4,25 (m, 2H), 2,43 (s, 3H), 1,36 - 1,29 (m, 3H). (trazas de acetato de etilo indicadas junto con el producto en la 1H RMN)
B. Ácido 2,2-difluoro-2-(2-metil-4-(trifluorometoxi)fenil)acético. A una solución agitada de 2,2-difluoro-2-(2-metil-4-(trifluorometoxi)fenil)acetato de etilo (900 mg, 3,020 mmol) en mezcla de tetrahidrofurano:metanol:agua (30 mL, 1:1:1) se añadió hidróxido de litio monohidratado (634 mg, 15,106 mmol) y se agitó a temperatura ambiente durante 4 h. Se concentró la mezcla de reacción y se neutralizó el residuo con bisulfato de potasio saturado (25 mL) y se extrajo con acetato de etilo (2 X 50 mL). Se lavaron las capas orgánicas combinadas con salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(2-metil-4-(trifluorometoxi)fenil)acético (450 mg, 1,66 mmol, 55% de rendimiento). 1H RMN (400MHz, CDCla) 87,65-7,49 (d, J = 9,2 Hz, 1H), 7,20-7,16 (m, 2H), 2,18 (s, 3H).
C. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-metil-4-(trifluorometoxi)fenil)acetamida. A una solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(2-metil-4(trifluorometoxi)fenil)acético (261 mg, 0,968 mmol) en piridina se añadió cloruro de fosforilo (0,27 mL, 2,906 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A continuación se añadió a esta mezcla de reacción clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,968 mmol) y se agitó a temperatura ambiente durante 30 min. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2X10 mL), salmuera (10 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 40-60% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-metil-4-(trifluorometoxi)fenil)acetamida (60 mg, 0,114 mmol, 11% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 526,52 [m +1]+. 1H RMN (300 MHz, DMSO-d6) 810,99 (s, 1H), 9,65 (t, J = 5,9 Hz, 1H), 7,73 - 7,63 (m, 2H), 7,46 (s, 1H), 7,43 - 7,38 (d, J = 8,0 Hz, 1H), 7,38- 7,32 (m, 2H), 5,10 (dd, J =13,2, 5,1 Hz, 1H), 4,52-4,28 (m, 4H), 2,96-2,85 (m, 1H), 2,68-2,53 (m, 1H), 2,47 -2,31 (m, 4H), 2,08- 1,94 (m, 1H).
Ejemplo 67
N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdoNn-5-N)metM)-2,2-difluoro-2-(2-fluoro-4-(trifluorometoxi)fenil)acetamida
A. 2-fluoro-1-yodo-4-(trifluorometoxi)benceno. A una solución agitada de 1-bromo-2-fluoro-4-(trifluorometoxi)benceno (500 mg, 1,93 mmol) en 1,4-dioxano (10 mL) se añadió yoduro de sodio (579 mg, 3,86 mmol), yoduro de cobre (18 mg, 0,09 mmol) y frans-N,N'-dimetilciclohexano-1,2-diamina (30 mg, 0,11 mmol) a temperatura ambiente, a continuación se calentó a 110°C durante 16 h. Se inactivó la mezcla de reacción con agua (10 mL) y se extrajo con acetato de etilo (3X10 mL). Se lavaron las capas orgánicas combinadas con agua (10 mL), salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 2-fluoro-1-yodo-4-(trifluorometoxi)benceno (400 mg, 1,3 mmol, 68% de rendimiento) como un líquido marrón. 1H RMN (300 MHz, CDCh) 8 7,78 (dd, J = 8,4, 6,9 Hz, 1H), 6,98 (dd, J = 8,1, 1,5 Hz, 1H), 6,84 (d, J =8,3 Hz, 1H).
B. 2,2-difluoro-2-(2-fluoro-4-(trifluorometoxi)fenil)acetato de etilo. A una solución agitada de 2-fluoro-1-yodo-4-(trifluorometoxi)benceno (1 g, 3,27 mmol) en dimetilsulfóxido (20 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (0,6 mL, 4,9 mmol) seguido por cobre (0,54 g, 8,49 mmol) a TA y se agitó a 60°C durante 6 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3X15 mL). Se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. El producto en bruto obtenido se purificó por cromatografía instantánea (acetato de etilo en éter de petróleo al 20%) para proporcionar 2,2-difluoro-2-(2-fluoro-4-(trifluorometoxi)fenil)acetato de etilo (800 mg, 2,64 mmol, 81% de rendimiento) como un líquido incoloro. m S (ESI) m/z 302,1 [M]+.
C. Ácido 2,2-difluoro-2-(2-fluoro-4-(trifluorometoxi)fenil)acético. A una solución agitada de 2,2-difluoro-2-(2-fluoro-4-(trifluorometoxi)fenil)acetato de etilo (800 mg, 2,64 mmol) en mezcla detetrahidrofurano:metanol:agua (15 mL, 1:1:1) se añadió hidróxido de litio monohidratado (333 mg, 7,94 mmol) y se agitó a temperatura ambiente durante 4 h. Se extrajeron los productos volátiles a presión reducida y se disolvió el producto en bruto obtenido en agua (15 mL) y se lavó con acetato de etilo (2X10 mL). Se acidificó la capa acuosa con solución acuosa de clorhidrato 1 N y se extrajo con acetato de etilo (3 X 10 mL). Se lavaron las capas orgánicas combinadas con salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar ácido 2,2-difluoro-2-(2-fluoro-4-(trifluorometoxi)fenil)acético (450 mg, 1,64 mmol, 62% de rendimiento) como un compuesto semisólido. Ms (ESI) m/z 298,1 [M]+.1H r Mn (400 MHz, CDCla) 87,70 (dd, J =9,6 Hz, 1,6 Hz, 1H), 7,14 (d, J = 7,9 Hz, 1H), 7,06 (dd, J =7,8 Hz, 1,8 Hz, 1H), 5,02 (brs, 1H).
D. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-fluoro-4-(trifluorometoxi)fenil)acetamida. A una solución agitada enfriada con hielo de ácido 2,2-difluoro-2-(2-fluoro-4-(trifluorometoxi)fenil)acético (274 mg, 1,55 mmol) en piridina (6 mL) se añadió oxicloruro de fósforo (0,36 mL, 3,87 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A continuación, se trató la mezcla de reacción con clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (400 mg, 1,29 mmol) y se agitó a temperatura ambiente durante 2 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3X 15 mL). Se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se
secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 (acetonitrilo al 50-55% en ácido fórmico acuoso al 0,1% para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-fluoro-4-(trifluorometoxi)fenil)acetamida (60 mg, 0,11 mmol, 9% de rendimiento) como un sólido blanco. MS (ESl) m/z 529,6 [M+1]+. 1H RMN (300 MHz, DMSo-d6) 810,99 (s, 1H), 9,76 (t, J = 5,8 Hz, 1H), 7,82 (dd, J = 8,4, 8,3 Hz, 1H), 7,70 (d, J = 7,5 Hz, 1H), 7,63 (d, J =11,4 Hz, 1H), 7,48 (s, 1H), 7,43-7,40 (m, 2H), 5,11 (dd, J =12,9, 4,8 Hz, 1H), 4,50 (d, J = 6,3 Hz, 2H), 4,46 (t, J =17,7 Hz, 1H), 4,31 (d, J =17,4, 1H), 2,90-2,63 (m, 1H), 2,63-2,56 (m, 1H), 2,42-2,27 (m, 1H), 2,02- 1,98 (m, 1H).
Ejemplo 68
2-(5-doropiridm-2-M)-N-((2-(2,6-dioxopiperidm-3-N)-1-oxoisomdoNn-5-N)metM)-2,2-difluoroacetamida
A. 2-(5-cloropiridin-2-il)-2,2-difluoroacetato de etilo. A una solución agitada de 5-cloro-2-yodopiridina (1,0 g, 4,18 mmol) en dimetilsulfóxido (11 mL) se añadió cobre (690 mg, 10,86 mmol) y 2-bromo-2,2-difluoroacetato de etilo (1,01 g, 5,01 mmol) a temperatura ambiente y se agitó a 55°C durante 6 h. Se neutralizó la mezcla de reacción con solución de cloruro de amonio acuosa saturada y se extrajo con acetato de etilo (2 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-(5-cloropiridin-2-il)-2,2-difluoroacetato de etilo (700 mg, 2,98 mmol, 70%). GCMS (m/z) 235,1 [M]+.
B. Ácido 2-(5-doropiridm-2-M)-2,2-difluoroacético. A una solución agitada de 2-(5-cloropiridin-2-il)-2,2-difluoroacetato de etilo (800 mg, 3,40 mmol) en mezcla de tetrahidrofurano:metanol:agua (30 mL, 1:1:1) se añadió hidróxido de litio monohidratado (429 mg, 10,21 mmol) y se agitó a temperatura ambiente durante 4 h. Se concentró la mezcla de reacción y se neutralizó el residuo con bisulfato de potasio saturado (20 mL) y se extrajo con acetato de etilo (2 X 25 mL). Se lavaron las capas orgánicas combinadas con salmuera (25 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2-(5-cloropiridin-2-il)-2,2-difluoroacético (400 mg, 1,94 mmol, 57% de rendimiento). MS (ESl) m/z 208,30 [M+1]+.
C. 2-(5-cloropiridin-2-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. A una solución agitada en frío (0°C) de ácido 2-(5-cloropiridin-2-il)-2,2-difluoroacético (200 mg, 0,96 mmol) en piridina (20 mL) se añadió cloruro de fosforilo (443 mg, 2,89 mmol) gota a gota y se agitó a 0-5°C durante 30 min. A esta mezcla de reacción se añadió a continuación clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,96 mmol) y se agitó a temperatura ambiente durante 1 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 40-45% en ácido fórmico acuoso (0,1%) para proporcionar 2-(5-cloropiridin-2-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (65 mg, 0,14 mmol, 14% de rendimiento) como un sólido blanquecino. MS (ESl) m/z 462,69 [M+1]+. 1H RMN (300MHz, DMSO-d6) 8 = 10,99 (s, 1H), 9,69 (t, J=5,9 Hz, 1H), 8,81 (d, J=2,2 Hz, 1H), 8,19 (dd, J=2,6, 8,4 Hz, 1H), 7,85 (d, J=8,4 Hz, 1H), 7,72 (d, J=8,1 Hz, 1H), 7,50 (s, 1H), 7,44 (d, J=77 Hz, 1H), 5,11 (dd, J=5,0, 13,0 Hz, 1H), 4,56-4,27 (m, 4H), 3,00-2,84 (m, 1H), 2,74-2,55 (m, 1H), 2,45-2,22 (m, 1H), 2,09-1,91 (m, 1H).
Ejemplo 69
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-fluoropiridin-2-il)acetamida A. 5-fluoro-2-yodopiridina. A una solución agitada de 2-bromo-5-fluoropiridina (2,5 g, 14,2 mmol) en 1,4-dioxano (10 mL) se añadió yoduro de sodio (4,26 g, 28,4 mmol), yoduro de cobre (135 mg, 0,71 mmol) seguido por frans-N,N-dimetilcidohexano-1,2-diamina (0,24 mL, 1,56 mmol) a temperatura ambiente y se agitó a 110°C durante 16 h. Se inactivó la mezcla de reacción con agua (30 mL) y se extrajo con acetato de etilo (3 X 25 mL). Se lavaron las capas orgánicas combinadas con agua (25 mL), salmuera (25 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 5-fluoro-2-yodopiridina (2,2 g, 9,86 mmol, 71% de rendimiento) como un líquido marrón. LCMS (m/z) 224,3 [M+].
B. 2,2-difluoro-2-(5-fluoropiridin-2-il)acetato de etilo. A una solución agitada de 5-fluoro-2-yodopiridina (300 mg, 1,34 mmol) en dimetilsulfóxido (3,4 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (409 mg, 2,02 mmol) seguido por cobre (22 mg, 3,49 mmol) a TA y se agitó a 60°C durante 6 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3X10 mL). Se lavaron las capas orgánicas combinadas con agua (10 mL), salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto obtenido por cromatografía en columna sobre gel de sílice (acetato de etilo en éter de petróleo al 20%) para proporcionar 2,2-difluoro-2-(5-fluoropiridin-2-il)acetato de etilo (200 mg, 0,72 mmol, 54% de rendimiento) como un líquido incoloro. MS (ESI) m/z 278 [M]+.
C. Ácido 2,2-difluoro-2-(5-fluoropiridin-2-il)acético. A una solución agitada de 2,2-difluoro-2-(5-fluoropiridin-2-il)acetato de etilo (250 mg, 1,14 mmol) en mezcla de tetrahidrofurano:metanol:agua (10 mL, 1:1:1) se añadió hidróxido de litio monohidratado (144 mg, 3,42 mmol) y se agitó a temperatura ambiente durante 4 h. Se extrajeron los productos volátiles a presión reducida y se disolvió el producto en bruto obtenido en agua (10 mL), se lavó con acetato de etilo (2X10 mL). Se acidificó la capa acuosa con solución acuosa de clorhidrato 1 N y se extrajo con acetato de etilo (3 X 10 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar ácido 2,2-difluoro-2-(5-fluoropiridin-2-il)acético (150 mg, 0,78 mmol, 69% de rendimiento) como un compuesto semisólido. 1H RMN (400 MHz, CDCh) 88,56 (s, 1H), 8,37 (brs, 1H), 7,84 (dd, J = 8,8 Hz, 4,4 Hz, 1H), 7,64 (ddd, J =10,8 Hz, 8,8 Hz, 2,4 Hz, 1H).
D. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-fluoropiridin-2-il)acetamida. A una solución enfriada con hielo de ácido 2,2-difluoro-2-(5-fluoropiridin-2-il)acético (221 mg, 1,16 mmol) en piridina (6 mL) se añadió oxicloruro de fósforo (0,27 mL, 2,91 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A continuación, se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) y se agitó a temperatura ambiente durante 2 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3 X 15 mL). Se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 (acetonitrilo al 50-55% en ácido fórmico acuoso al 0,1% para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-fluoropiridin-2-il)acetamida (60 mg, 0,11 mmol, 14% de rendimiento) como un sólido blanco. MS (ESI) m/z 446,7 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 810,98 (s, 1H), 9,67 (t, J = 5,7 Hz, 1H), 8,76 (d, J = 2,4 Hz, 1H), 8,01 - 7,89 (m, 2H), 7,71 (d, J = 7,8 Hz, 1H), 7,52 (s, 1H), 7,45 (d, J = 8,1 Hz, 1H), 5,11 (dd, J = 13,5, 5,1 Hz, 1H), 4,50 (d, J =5,4 Hz, 2H), 4,47 (d, J = 17,4 Hz, 1H), 4,32 (d, J =17,1, 1H), 2,98-2,84 (m, 1H), 2,66-2,58 (m, 1H), 2,43-2,30 (m, 1H), 2,02- 1,94 (m, 1H).
Ejemplo 70
2-(2,4-difluorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida
A. 2-(2,4-difluorofenil)-2,2-difluoroacetato de etilo. A una solución agitada de 2,4-difluoro-1-yodobenceno (800 mg, 3,33 mmol) en dimetilsulfóxido (10 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (1,01 g, 4,99 mmol), cobre (550 mg, 8,65 mmol) y se agitó a 55°C durante 6 h. Se neutralizó la mezcla de reacción con solución de cloruro de amonio saturada acuosa y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-(2,4-difluorofenil)-2,2-difluoroacetato de etilo (400 mg, 1,69 mmol, 51%) como un líquido marrón. GCMS: 236,1 [M]+.
B. Ácido 2-(2,4-difluorofenil)-2,2-difluoroacético. A una solución agitada de 2-(2,4-difluorofenil)-2,2-difluoroacetato de etilo (400 mg, 1,69 mmol) en etanol: tetrahidrofurano: agua (10 mL, 1:1:1) se añadió hidróxido de litio (214 mg, 5,08 mmol) y se agitó a temperatura ambiente durante 4 h. Se concentró la mezcla de reacción y se neutralizó el residuo con hidrogenosulfato de potasio saturado (20 mL) y se extrajo con acetato de etilo (2 X 50 mL). Se lavó la capa orgánica combinada con salmuera (25 mL), se secó sobre sulfato de sodio y se concentró para dar ácido 2-(2,4-difluorofenil)-2,2-difluoroacético (250 mg, 1,20 mmol, 71% de rendimiento). MS (ESI) m/z 207,43 [M-1]+
C. 2-(2,4-difluorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. A una solución agitada (0°C) de clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) en N,N-dimetilformamida (10 mL) se añadió ácido 2-(2,4-difluorofenil)-2,2-difluoroacético (202 mg, 0,97 mmol) seguido por diisopropiletilamina (0,52 mL, 2,91 mmol), 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metileno]-1H-1,2,3-triazolo[4,5-b]piridinio (480 mg, 1,26 mmol) y se agitó a temperatura ambiente durante 16 h. Se diluyó la mezcla de reacción con agua (100 mL) y se filtró el sólido obtenido, se lavó con éter dietílico (20 mL), se secó y se purificó por cromatografía en columna (sílice 100-200) usando metanol al 4% en diclorometano como eluyente para proporcionar 2-(2,4-difluorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (60 mg, 0,129 mmol, 13% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 463,68 [M+1]+. 1H RMN (400 MHz, DMSO-d6) 8 = 10,98 (s, 1H), 9,72 (brt, J=5,9 Hz, 1H), 7,78 - 7,65 (m, 2H), 7,55 - 7,34 (m, 3H), 7,29 - 7,18 (m, 1H), 5,11 (br dd, J=5,1, 13,2 Hz, 1H), 4,56 - 4,16 (m, 4H), 3,08 - 2,80 (m, 1H), 2,75 - 2,59 (m, 1H), 2,44 - 2,32 (m, 1H), 2,06 - 1,92 (m, 1H).
Ejemplo 71
2-(4-bromofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida
A. 2-(4-bromofenil)-2,2-difluoroacetato de etilo. A una solución agitada de 1-bromo-4-yodobenceno (300 mg, 2,81 mmol) en dimetilsulfóxido (3 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (324 mg, 1,6 mmol) seguido por polvo de cobre (175 mg, 2,75 mmol) a temperatura ambiente y se agitó a 55°C durante 6 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio acuosa y se extrajo con acetato de etilo (3 X 10 mL). Se lavaron las capas orgánicas combinadas con agua (10 mL), salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto obtenido por cromatografía en columna sobre gel de sílice (acetato de etilo en éter de petróleo al 20%) para proporcionar 2-(4-bromofenil)-2,2-difluoroacetato de etilo (200 mg, 0,72 mmol, 25% de rendimiento) como un líquido incoloro. g Cm S (ESI) m/z 278,1 [M]+
B. Ácido 2-(4-bromofenil)-2,2-difluoroacético. A una solución agitada de 2-(4-bromofenil)-2,2-difluoroacetato de etilo (200 mg, 0,72 mmol) en mezcla de tetrahidrofurano: metanol: agua (15 mL, 1:1:1) se añadió hidróxido de litio monohidratado (90 mg, 2,15 mmol) y se agitó a temperatura ambiente durante 4 h. Se extrajeron los productos volátiles a presión reducida y se disolvió el residuo obtenido en agua (15 mL), se lavó con acetato de etilo (2X 10 mL). Se acidificó la capa acuosa con solución acuosa de clorhidrato 1 N y se extrajo con acetato de etilo (3 X 10 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró el disolvente para proporcionar ácido 2-(4-bromofenil)-2,2-difluoroacético (150 mg, 0,60 mmol, 84% de rendimiento) como un compuesto semisólido. MS (ESI) m/z 251,43 [M-H]+
C. 2-(4-bromofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. A una solución enfriada con hielo de ácido 2-(4-bromofenil)-2,2-difluoroacético (291 mg, 1,16 mmol) en piridina (6 mL) se añadió oxicloruro de fósforo (0,27 mL, 2,9 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A continuación, se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) en la mezcla de reacción y se agitó a temperatura ambiente durante 2 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3X15 mL). Se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 (acetonitrilo al 50-55% en ácido fórmico acuoso al 0,1%) para proporcionar 2-(4-bromofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (50 mg, 0,098 mmol, 10% de rendimiento) como un sólido blanco. MS (ESI) m/z 505,6 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 810,99 (s, 1H), 9,68 (t, J = 5,8 Hz, 1H), 7,77 (d, J = 8,4 Hz, 2H), 7,68 (d, J =7,8 Hz, 1H), 7,54 (d, J = 8,7 Hz, 2H), 7,39 (s, 1H), 7,36 (d, J = 8,1 Hz, 1H), 5,10 (dd, J = 13,2, 4,8 Hz, 1H), 4,45 (d, J = 6,0 Hz, 2H), 4,43 (d, J = 18,1 Hz,
1H), 4,28 (d, J =17,4 Hz, 1H), 2,96-2,86 (m, 1H), 2,63-2,49 (m, 1H), 2,41 -2,30 (m, 1H), 2,07- 1,94 (m, 1H).
Ejemplo 72
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(2-metoxietoxi)fenil)acetamida
A. 1-yodo-2-(2-metoxietoxi)benceno. A una solución agitada de 2-yodofenol (1 g, 4,54 mmol) en N,N-dimetilformamida (10 mL) se añadió carbonato de potasio (1,88 g, 13,64 mmol) seguido por yoduro de potasio (0,07 g, 0,45 mmol) y 1-bromo-2-metoxietano (0,46 mL, 4,99 mmol) a temperatura ambiente y se agitó a 70°C durante 16 h. Se inactivó la mezcla de reacción con agua (15 mL) y se extrajo con acetato de etilo (3X15 mL). Se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 1-yodo-2-(2-metoxietoxi)benceno (0,8 g, 2,87 mmol, 84% de rendimiento) como un líquido incoloro. GCMS (m/z) 278,1 [M+].
B. 2,2-difluoro-2-(2-(2-metoxietoxi)fenil)acetato de etilo. A una solución agitada de 1-yodo-2-(2-metoxietoxi)benceno (800 mg, 2,87 mmol) en dimetilsulfóxido (15 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (0,42 mL, 4,31 mmol) seguido por polvo de cobre (470 mg, 7,46 mmol) a TAy se agitó a 60°C durante 6 h. Se inactivó la mezcla de reacción con agua y se filtró a través de un lecho de Celite. Se basificó el filtrado con solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3 X 15 mL). Se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto obtenido por cromatografía en columna instantánea (acetato de etilo en éter de petróleo al 20%) para proporcionar 2,2-difluoro-2-(2-(2-metoxietoxi)fenil)acetato de etilo (460 mg, 1,37 mmol, 24% de rendimiento) como un líquido incoloro. MS (ESI) m/z 274,2 [M]+.
C. Ácido 2,2-difluoro-2-(2-(2-metoxietoxi)fenil)acético. A una solución agitada de 2,2-difluoro-2-(2-(2-metoxietoxi)fenil)acetato de etilo (450 mg, 1,64 mmol) en mezcla de tetrahidrofurano: metanol:agua (15 mL, 1:1:1) se añadió hidróxido de litio monohidratado (206 mg, 4,92 mmol) y se agitó a temperatura ambiente durante 4 h. Se extrajeron los productos volátiles a presión reducida y se disolvió el producto en bruto obtenido en agua (10 mL), se lavó con acetato de etilo (2X10 mL). Se acidificó la capa acuosa con solución acuosa de clorhidrato 1 N y se extrajo con acetato de etilo (3 X 10 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar ácido 2,2-difluoro-2-(2-(2-metoxietoxi)fenil)acético (290 mg, 1,17 mmol, 72% de rendimiento) como un compuesto semisólido. MS (ESI) m/z 247,28 [M+H]+.
D. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(2-metoxietoxi)fenil)acetamida. A una solución enfriada con hielo de ácido 2,2-difluoro-2-(2-(2-metoxietoxi)fenil)acético (262 mg, 1,07 mmol) en piridina (9 mL) se añadió oxicloruro de fósforo (0,27 mL, 2,9 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A continuación, se trató la mezcla de reacción con clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) y se agitó a temperatura ambiente durante 2 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3X15 mL). Se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró el disolvente. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 (acetonitrilo al 50-55% en ácido fórmico acuoso al 0,1% para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(2-metoxietoxi)fenil)acetamida (60 mg, 0,12 mmol, 12% de rendimiento) como un sólido blanco. MS (ESI) m/z 502,34 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 810,99 (s, 1H), 9,23 (t, J = 5,6 Hz, 1H), 7,71 (d, J = 8,1 Hz, 1H), 7,55 (dd, J =9,6, 1,5 Hz, 1H), 7,52 -7,48 (m, 2H), 7,45 (d, J =8,1 Hz, 1H), 7,15 (d, J =8,4 Hz, 1H), 7,07 (dd, J = 7,8, 7,2 Hz, 1H), 5,11 (dd, J = 13,5, 5,1 Hz, 1H), 4,47 (d, J = 6,3 Hz, 2H), 4,45 (d, J = 15,9 Hz, 1H), 4,31 (d, J = 17,4 Hz, 1H), 4,05 (t, J = 4,8 Hz, 2H), 3,45 (t, J =5,1 Hz, 2H), 3,24 (s, 3H), 2,96-2,86 (m, 1H), 2,66-2,57 (m, 1H), 2,45-2,30 (m, 1H), 2,04- 1,94 (m, 1H).
Ejemplo 73
N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdoMn-5-M)metM)-2,2-difluoro-2-(1-hidroxiddohexM)acetamida
A. N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdolm-5-M)metM)-2,2-difluoro-2-(1-hidroxiddohexM)acetamida. Se colocó 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona, ácido mesílico (0,050 g, 0,135 mmol) (0,050 g, 0,113 mmol) en un vial con ácido 2,2-difluoro-2-(1-hidroxicidohexN)acético (0,026 g, 0,135 mmol), diisopropiletilamina (0,071 mL, 0,406 mmol), 3-óxido hexafluorofosfonato de 1-[bis(dimetilamino)metileno]-1H-1,2,3-triazolo[4,5-b]piridinio (0,057 g, 0,149 mmol) y N,N-dimetilformamida (1,0 mL). Se agitó la mezcla de reacción a 40°C durante 18 h. Se recogió la mezcla de reacción en dimetilsulfóxido y se purificó usando HPLC semipreparatoria de fase inversa (acetonitrilo al 5-100% ácido fórmico al 0,1% en agua ácido fórmico al 0,1%, durante 20 min). Se combinaron fracciones que contenían el producto deseado y se extrajeron los compuestos orgánicos volátiles a presión reducida para dar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(1-hidroxiciclohexil)acetamida (0,041 g, 0,091 mmol, 67,4% de rendimiento) como un sólido blanco. 1H RMN (500 MHz, DMSO-da) 810,97 (s, 1H), 9,04 (t, J = 6,15 Hz, 1H), 7,68 (d, J = 7,88 Hz, 1H), 7,50 (s, 1H), 7,43 (d, J = 7,88 Hz, 1H), 5,19 (s, 1H), 5,10 (dd, J = 5,04, 13,24 Hz, 1H), 4,40 4,47 (m, 3H), 4,27-4,34 (m, 1H), 2,86-2,96 (m, 1H), 2,57-2,63 (m, 1H), 2,40 (qd, J = 4,57, 13,19 Hz, 1H), 2,00 (dtd, J = 2,05, 5,28, 12,61 Hz, 1H), 1,70 (d, J =12,30 Hz, 2H), 1,45 -1,61 (m, 5H), 1,34- 1,43 (m, 2H), 1,00-1,13 (m, 1H). MS (ESI) m/z 450,2 [M+1]+.
Ejemplo 74
N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdoMn-5-M)metM)-2,2-difluoro-2-(1-hidroxiddopentM)acetamida
A. N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdoMn-5-M)metM)-2,2-difluoro-2-(1-hidroxiddopentM)acetamida. Se colocó 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona, ácido mesílico (0,050 g, 0,135 mmol) (0,050 g, 0,113 mmol) en un vial con ácido 2,2-difluoro-2-(1-hidroxiciclopentil)acético (0,024 g, 0,135 mmol), diisopropiletilamina (0,071 mL, 0,406 mmol), 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metileno]-1H-1,2,3-triazolo[4,5-b]piridinio (0,057 g, 0,149 mmol) y N,N-dimetilformamida (1,0 mL). Se agitó la mezcla de reacción a 40°C durante 18 h. Se recogió la mezcla de reacción en dimetilsulfóxido y se purificó usando HPLC semipreparatoria de fase inversa (acetonitrilo al 5-100% ácido fórmico al 0,1% en agua ácido fórmico al 0,1%, durante 20 min). Se combinaron fracciones que contenían el producto deseado y se extrajeron los compuestos orgánicos volátiles a presión reducida para dar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(1-hidroxiciclopentil)acetamida (0,044 g, 0,101 mmol, 74,7% de rendimiento) como un sólido blanco. 1H RMN (500 MHz, DMSO-d6) 810,97 (s, 1H), 9,10 (t, J = 6,15 Hz, 1H), 7,68 (d, J = 7,57 Hz, 1H), 7,49 (s, 1H), 7,43 (d, J = 7,88 Hz, 1H), 5,35 (s, 1H), 5,10 (dd, J = 5,20, 13,40 Hz, 1H), 4,40 4,49 (m, 3H), 4,27 - 4,33 (m, 1H), 2,91 (ddd, J = 5,36, 13,79, 17,42 Hz, 1H), 2,57 - 2,63 (m, 1H), 2,39 (qd, J = 4,57, 13,29 Hz, 1H), 2,00 (dtd, J = 2,36, 5,26, 12,65 Hz, 1H), 1,88 - 1,96 (m, 2H), 1,62 - 1,76 (m, 4H), 1,52 - 1,60 (m, 2H). MS (ESI) m/z 436,2 [M+1]+.
Ejemplo 75
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-(difluoro-2-(3-metil-4-(trifluorometoxi)fenil)acetamida
A. 4-yodo-2-metil-1-(trifluorometoxi)benceno. A una solución agitada de 4-bromo-2-metil-1-(trifluorometoxi)benceno (1 g, 3,92 mmol) en 1,4-dioxano (10 mL) se añadió yoduro de sodio (1,17 g, 7,84 mmol), yoduro de cobre (37,3 mg, 0,19 mmol), trans-N,N'-dimetilciclohexano-1,2-diamina (61,3 mg, 0,43 mmol) a temperatura ambiente y se agitó a 110°C durante 16 h. Se inactivó la mezcla de reacción con agua (50 mL) y se extrajo con acetato de etilo (3 X 50 mL). Se lavó la capa orgánica combinada con agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 4-yodo-2-metil-1-(trifluorometoxi)benceno (1,0 g, 3,31 mmol, 84%) como un líquido marrón. GCMS (m/z) 302[M+].
B. 2,2-difluoro-2-(3-metil-4-(trifluorometoxi)fenil)acetato de etilo. Se hizo reaccionar una solución agitada de 4-yodo-2-metil-1-(trifluorometoxi)benceno (1,0 g, 3,31 mmol) en dimetilsulfóxido (10 mL) con 2-bromo-2,2-difluoroacetato de etilo (802 mm, 3,97 mmol), cobre (547 mg, 8,61 mmol) y se agitó a 55°C durante 6 h. Se neutralizó la mezcla de reacción con solución de cloruro de amonio saturada acuosa y se extrajo con acetato de etilo (3 X 50 mL). Se lavó la capa orgánica combinada con agua (2 X 50 mL), salmuera (50 mL) y se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(3-metil-4-(trifluorometoxi)fenil)acetato de etilo (700 mg, 2,35 mmol, 70%) como un líquido marrón. GCMS (m/z) 298,1[M]+.
C. Ácido 2,2-difluoro-2-(3-metil-4-(trifluorometoxi)fenil)acético. A una solución agitada de 2,2-difluoro-2-(3-metil-4-(trifluorometoxi)fenil)acetato de etilo (700 mg, 2,35 mmol) en etanol: tetrahidrofurano: agua (15 mL, 1:1:1) se añadió hidróxido de litio (296 mg, 7,05 mmol) y se agitó a temperatura ambiente durante 4 h. Se concentró la mezcla de reacción y se neutralizó el residuo con bisulfato de potasio saturado (20 mL) y se extrajo con acetato de etilo (2 X 25 mL). Se lavó la capa orgánica combinada con salmuera (25 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(3-metil-4-(trifluorometoxi)fenil)acético (400 mg, 1,48 mmol, 63% de rendimiento). MS (ESI) m/z 269,45 [M-1]+.
D. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-metil-4-(trifluorometoxi)fenil)acetamida. A una solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(3-metil-4-(trifluorometoxi)fenil)acético (200 mg, 0,74 mmol) en piridina (20 mL) se añadió cloruro de fosforilo (340 mg, 2,22 mmol) gota a gota y se agitó a 0-5°C durante 1 h y a continuación se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (229 mg, 0,74 mmol) y se agitó a temperatura ambiente durante 30 min. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavó la capa orgánica combinada con agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 40-50% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-metil-4-(trifluorometoxi)fenil)acetamida (80 mg, 0,15 mmol, 20% de rendimiento) como un sólido blanco. MS (ESI) m/z 526,26 [M+1]+. 1H RMN (400MHz, DMS)-d6) 8 = 10,98 (s, 1H), 9,68 (t, J=6,1 Hz, 1H), 7,68 (d, J=7,9 Hz, 1H), 7,62 (s, 1H), 7,57 - 7,47 (m, 2H), 7,42 (s, 1H), 7,37 (d, J=7,9 Hz, 1H), 5,10 (dd, J=5,2, 13,4 Hz, 1H), 4,49 - 4,25 (m, 4H), 2,98 - 2,85 (m, 1H), 2,69 - 2,55 (m, 1H), 2,44 - 2,34 (m, 1H), 2,33 (s, 3H), 2,05 - 1,94 (m, 1H).
Ejemplo 76
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2-(3-etoxipiridin-2-il)-2,2-difluoroacetamida
A. 3-etoxi-2-yodopiridina. A una solución agitada de 2-yodopiridin-3-ol (1 g, 4,52 mmol) en N,N-dimetilformamida (20 mL) se añadió carbonato de potasio (0,936 g, 6,78 mmol) a temperatura ambiente, y se agitó durante 10 min. A esta mezcla de reacción se le añadió yoduro de etilo (1,41 g, 9,04 mmol) a temperatura ambiente y se agitó durante 2 h a 80°C. Se inactivó la mezcla de reacción con agua (50 mL) y se extrajo con acetato de etilo (2 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 100 mL), salmuera (100 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna (gel de sílice 100-200) 100% hexano como eluyente para proporcionar 3-etoxi-2-yodopiridina (1 g, 4,0 mmol, 88,8% de rendimiento) como un líquido marrón. LCMS(ESI) m/z 251,1 [M]+.
B. 2-(3-etoxipiridin-2-il)-2,2-difluoroacetato de etilo. A una solución agitada de 3-etoxi-2-yodopiridina (1,0 g, 4,01 mmol) en dimetilsulfóxido (20 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (1,6 mL, 8,03 mmol), cobre (0,66 g, 10,44 mmol) y se agitó a 55°C durante 16 h. Se neutralizó la mezcla de reacción con solución de cloruro de amonio saturada acuosa y se extrajo con acetato de etilo (3 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 100 mL), salmuera (10 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-(3-etoxipiridin-2-il)-2,2-difluoroacetato de etilo (800 mg, 3,26 mmol, 81%) como un líquido marrón. Lc Ms (ESI) m/z 246,1 [M]+.
C. Ácido 2-(3-etoxipiridin-2-il)-2,2-difluoroacético. A una solución agitada en frío (0°C) de 2-(3-etoxipiridin-2-il)-2,2-difluoroacetato de etilo (800 mg, 3,26 mmol) en metanol: tetrahidrofurano:agua (9 mL, 1:1:1) se añadió hidróxido de litio monohidratado (410 mg, 9,78 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción, se neutralizó el residuo con bisulfato de potasio acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 50 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2-(3-etoxipiridin-2-il)-2,2-difluoroacético (500 mg, 2,13 mmol, 88% de rendimiento) como un semisólido marrón. Se llevó la mezcla de reacción a la etapa siguiente sin purificación adicional.
D. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2-(3-etoxipiridin-2-il)-2,2-difluoroacetamida. A una solución agitada en frío (0°C) de ácido 2-(3-etoxipiridin-2-il)-2,2-difluoroacético (252 mg, 1,16 mmol) en piridina (20 mL) se añadió cloruro de fosforilo (446,4 mg, 2,91 mmol) gota a gota y se agitó a 0-5°C durante 30 min. A esta mezcla de reacción se añadió a continuación clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) y se agitó a temperatura ambiente durante 2 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo resultante por cromatografía en columna Grace de fase inversa Reveleris C-18 usando acetonitrilo al 45-50% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-N)-1-oxoisoindoNn-5-N)metN)-2-(3-etoxipiridin-2-il)-2,2-difluoroacetamida (60 mg, 0,12 mmol, 13% de rendimiento) como un sólido blanquecino. LCMS (ESI) m/z 473,29 [M+1]+. 1H RMN (400MHz, DMSO-d6) 8 = 10,98 (s, 1H), 9,41 (br t, J=6,3 Hz, 1H), 8,22 (dd, J=1,1, 4,4 Hz, 1H), 7,72 (d, J=7,9 Hz, 1H), 7,66 - 7,61 (m, 1H), 7,59 - 7,53 (m, 2H), 7,48 (d, J=7,9 Hz, 1H), 5,12 (dd, J=5,6, 13,2 Hz, 1H), 4,53 - 4,27 (m, 4H), 4,08 (q, J=7,2, 2H), 2,99 - 2,86 (m, 1H), 2,70 - 2,56 (m, 1H), 2,47 - 2,32 (m, 1H), 2,05- 1,96 (m, 1H), 1,19 (t, J=72 Hz, 3H).
Ejemplo 77
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-metilpiridin-2-il)acetamida
A. 2,2-difluoro-2-(3-metilpiridin-2-il)acetato de etilo. A una solución agitada de 2-yodo-3-metilpiridina (0,7 g, 3,19 mmol) en dimetilsulfóxido (20 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (0,8 mL, 6,39 mmol), cobre (0,52 g, 8,29 mmol) y se agitó durante 16 h a 50°C. Se neutralizó la mezcla de reacción con solución de cloruro de amonio saturada acuosa y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2X 10 mL), salmuera (10 mL) y se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(3-metilpiridin-2-il)acetato de etilo (500 mg, 2,32 mmol, 73%) como un líquido marrón. GCMS (m/z) 215,2.
B. Ácido 2,2-difluoro-2-(3-metilpiridin-2-il)acético. A una solución agitada en frío (0°C) de 2,2-difluoro-2-(3-metilpiridin-2-il)acetato de etilo (500 mg, 2,32 mmol) en mezcla de metanol/tetrahidrofurano/agua (9 mL, 1:1:1) se
añadió hidróxido de litio monohidratado (327 mg, 6,97 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con bisulfato de potasio acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 30 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(3-metilpiridin-2-il)acético (400 mg, 2,13 mmol, 88% de rendimiento) como un semisólido marrón. MS (ESI) m/z 188,31.
C. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-metilpiridin-2-il)acetimida. A una solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(3-metilpiridin-2-il)acético (300 mg, 1,60 mmol) en piridina (20 mL) se añadió cloruro de fosforilo (735 mg, 4,80 mmol) gota a gota y se agitó a 0-5°C durante 30 min. A la mezcla de reacción se añadió a continuación clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (395 mg, 1,60 mmol) y se agitó a temperatura ambiente durante 2 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL) y se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 45-50% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-metilpiridin-2-il)acetamida (40 mg, 0,09 mmol, 7% de rendimiento) como un sólido blanquecino. MS (ESI) m/z443,30 [M+1]+. 1H RMN (300 MHz, DMSO-da) 810,99 (s, 1H), 9,45 (brt, J=6,1 Hz, 1H), 8,51 (br d, J=3,9 Hz, 1H), 7,84 (br d, J=7,8 Hz, 1H), 7,72 (d, J=7,8 Hz, 1H), 7,63 (s, 1H), 7,51 (br d, J=7,8 Hz, 2H), 5,19-5,03 (m, 1H), 4,58-4,28 (m, 4H), 2,92 - 2,85(m, 1H), 2,68-2,54 (m, 1H), 2,45-2,30 (m, 4H), 2,10-1,92 (m, 1H).
Ejemplo 78
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-metilpiridin-2-il)acetamida
A. 2-yodo-5-metilpiridina. A una solución agitada de 2-bromo-5-metilpiridina (2 g, 11,63 mmol) en 1,4-dioxano (30 mL) se añadió yoduro de sodio (3,4 g, 23,24 mmol), yoduro de cobre (110 mg, 0,58 mmol), trans-N,N'-dimetilciclohexano-1,2-diamina (180 mg, 1,26 mmol) a temperatura ambiente y se agitó a 110°C durante 16 h en tubo sellado. Se inactivó la mezcla de reacción con agua (30 mL) y se extrajo con acetato de etilo (3 X 30 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 20 mL), salmuera (20 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-yodo-5-metilpiridina (1,3 g, 5,93 mmol, 52% de rendimiento) como un líquido marrón.
1H RMN (300MHz, CDCla) 88,2 (s, 1H), 7,6-7,56 (d, J=8,1 Hz, 1H), 7,18-7,12 (m, 1H), 2,3-2,25(s, 1H).
B. 2,2-difluoro-2-(5-metilpiridin-2-il)acetato de etilo. A una solución agitada de 2-yodo-5-metilpiridina (1 g, 4,56 mmol) en dimetilsulfóxido (20 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (1,2 mL, 9,13 mmol), cobre (0,75 g, 11,85 mmol) y se agitó durante 16 h a 50°C. Se neutralizó la mezcla de reacción con solución de cloruro de amonio saturada acuosa y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 10 mL), salmuera (10 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(5-metilpiridin-2-il)acetato de etilo (600 mg, 2,72 mmol, 60%) como un líquido marrón. GCMS (m/z) 215,0
C. Ácido 2,2-difluoro-2-(5-metilpiridin-2-il)acético. A una solución agitada en frío (0°C) de 2,2-difluoro-2-(5-metilpiridin-2-il)acetato de etilo (500 mg, 2,32 mmol) en mezcla de metanol/tetrahidrofurano/agua (9 mL, 1:1:1) se añadió hidróxido de litio monohidratado (327 mg, 6,97 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con bisulfato de potasio acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 30 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(5-metilpiridin-2-il)acético (350 mg, 1,87 mmol, 87% de rendimiento) como un semisólido marrón. MS (ESI) m/z 188,39.
D. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-metilpiridin-2-il)acetamida. A una solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(5-metilpiridin-2-il)acético (180 mg, 0,97 mmol) en piridina (20 mL) se añadió cloruro de fosforilo (0,2 mL, 2,91 mmol) gota a gota y se agitó a 0-5°C durante 30 min. A esta mezcla de reacción se añadió a continuación clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) y se agitó a temperatura ambiente durante 2 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas
combinadas con agua (2 X 50 mL), salmuera (50 mL) y se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 45-50% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-metilpiridin-2-il)acetamida (64 mg, 0,14 mmol, 13% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 443,30 [M+1]+. 1H RMN (300 MHz, DMSO-da) 810,99 (s, 1H), 9,60 (brt, J=5,9 Hz, 1H), 8,55 (bs, 1H), 7,88 - 7,98 (m, 1H), 7,69-7,63 (t, J=86 Hz, 2H), 7,52 (s, 1H), 7,49 - 7,40 (m, 1H), 5,11 (dd, J=5,1, 13,5 Hz, 1H), 4,59 - 4,21 (m, 4H), 2,98 - 2,85 (m, 1H), 2,68 - 2,53 (m, 1H), 2,45 - 2,39 (m, 4H), 2,06 - 1,97 (m, 1H).
Ejemplo 79
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2-(2-etoxi-6-fluorofenil)-2,2-difluoroacetamida
A. 1-etoxi-3-fluoro-2-yodobenceno. A una solución agitada de 2-bromo-1-etoxi-3-fluorobenceno (1 g, 4,58 mmol) en 1,4-dioxano (30 mL) se añadió yoduro de sodio (1,37 g, 9,17 mmol), yoduro de cobre (43,6 mg, 0,22 mmol), trans-W,W-dimetilciclohexano-1,2-diamina (71,2 mg, 0,504 mmol) a temperatura ambiente y se agitó a 110°C durante 16 h en tubo sellado. Se inactivó la mezcla de reacción con agua (100 mL) y se extrajo con acetato de etilo (3 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 1-etoxi-3-fluoro-2-yodobenceno (1 g, 5,93 mmol, 52% de rendimiento) como un líquido marrón. Gc-MS (ESI) m/z 266.
B. 2-(2-etoxi-6-fluorofenil)-2,2-difluoroacetato de etilo. A una solución agitada de 1-etoxi-3-fluoro-2-yodobenceno (1 g, 3,17 mmol) en dimetilsulfóxido (20 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (1,53 g, 7,54 mmol), cobre (0,62 g, 9,80 mmol) y se agitó durante 16 h a 50°C. Se neutralizó la mezcla de reacción con solución de cloruro de amonio saturada acuosa y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 20 mL), salmuera (20 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-(2-etoxi-6-fluorofenil)-2,2-difluoroacetato de etilo (800 mg, 3,05 mmol, 81%) como un líquido marrón. GC-MS (ESI) m/z 262,2 C. Ácido 2-(2-etoxi-6-fluorofenil)-2,2-difluoroacético. A una solución agitada en frío (0°C) de ácido y se concentró para dar 2-(2-etoxi-6-fluorofenil)-2,2-difluoroacetato de etilo (500 mg, 2,32 mmol) en mezcla de etanol/tetrahidrofurano/agua (9 mL, 1:1:1) se añadió hidróxido de litio monohidratado (327 mg, 6,97 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con bisulfato de potasio acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 30 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2-(2-etoxi-6-fluorofenil)-2,2-difluoroacético (400 mg, 1,70 mmol, 56% de rendimiento) como un semisólido marrón. LCMS (ESI) m/z 233,4 [M-1]-.
D. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-metilpiridin-2-il)acetamida. A una solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(5-metilpiridin-2-il)acético (272 mg, 1,16 mmol) en piridina (20 mL) se añadió cloruro de fosforilo (0,3 mL, 2,91 mmol) gota a gota y se agitó a 0-5°C durante 30 min. A esta mezcla de reacción se añadió a continuación clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) y se agitó a temperatura ambiente durante 2 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL) y se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna Grace de fase inversa Reveleris C-18 usando acetonitrilo al 45-50% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-metilpiridin-2-il)acetamida (60 mg, 0,12 mmol, 12% de rendimiento) como un sólido blanquecino. LCMS (ESI) m/z 490,3 [M+1]+. 1H RMN (400MHz, DMSO-d6) 8 = 10,98 (s, 1H), 9,36 (brt, J=6,1 Hz, 1H), 7,71 (d, J=7,6 Hz, 1H), 7,54- 7,47 (m, 3H), 7,45 (d, J=7,6 Hz, 1H), 7,00-6,84 (m, 1H), 5,11 (br dd, J=5,0, 13,3 Hz, 1H), 4,52-4,27 (m, 4H), 3,99 (q, J=7,0 Hz, 1H), 3,04 - 2,82 (m, 1H), 2,71 - 2,54 (m, 1H), 2,46 - 2,28 (m, 1H), 2,04 - 1,94 (m, 1H), 1,14 (t, J=7,0 Hz, 1H).
Ejemplo 80
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4'-fluorobifenil-4-il)acetamida
A. 1-(4'-fluorobifenil-4-il)etanona. A una solución de 1-(4-bromofenil)etanona (2 g, 10,05 mmol) en tolueno/etanol ((10 mL, 2:1) se añadió ácido 4-fluorofenilborónico (1,68 g, 12,06 mmol) seguido por carbonato de potasio (3,46 g, 25,12 mmol) y se desgasificó durante 10 min. Se cargó adicionalmente la mezcla de reacción con tetraquis(trifenilfosfina)paladio(0) (1,16 mg, 1,005 mmol) y se desgasificó durante 10 min adicionales y se calentó a 80°C en un tubo sellado durante 6 h. Se enfrió la mezcla de reacción a temperatura ambiente, se filtró a través del lecho de celite. Se diluyó el filtrado con agua fría y se extrajo con acetato de etilo (3X10 mL). Se lavaron las capas orgánicas combinadas con agua (10 mL), salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el residuo obtenido por cromatografía en columna (gel de sílice 100-200, acetato de etilo en hexano al 30%) para proporcionar 1-(4'-fluorobifenil-4-il)etanona (1 g, 4,67 mmol, 48% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 215,27 [M+1]+.
B. 2-(4'-fluorobifenil-4-il)-2-oxoacetato de etilo. A una solución agitada de 1-(4'-fluorobifenil-4-il)etanona (1,5 g, 7,009 mmol) en piridina (10 mL) se añadió dióxido de selenio (1,94 g, 17,52 mmol) a temperatura ambiente. Se agitó la mezcla de reacción a 100°C durante 16 h. Se filtró la mezcla de reacción a través de lecho de celite y se lavó con diclorometano (15 mL). Se añadió cloroformiato de etilo (15 mL) se añadió al filtrado a 0°C y se agitó a temperatura ambiente durante 4 h. Se inactivó la mezcla de reacción con agua con hielo y se extrajo con diclorometano (3X10 mL). Se lavaron las capas orgánicas combinadas con clorhidrato 1 N (15 mL), salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 2-(4'-fluorobifenil-4-il)-2-oxoacetato de etilo (900 mg, 3,308 mmol, 47% de rendimiento) como un líquido incoloro. MS (ESI) m/z 273,51 [M+1]+.
C. 2,2-difluoro-2-(4'-fluorobifenil-4-il)acetato de etilo. Se añadió 2-(4'-fluorobifenil-4-il)-2-oxoacetato de etilo (1 g, 3,676 mmol) porciones en trifluoruro de dietilamino azufre (1,4 mL) a 0°C y se agitó a temperatura ambiente durante 16 h. Se inactivó la mezcla de reacción con bicarbonato de sodio acuoso y se extrajo con acetato de etilo (3X10 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secaron sobre sulfato de sodio anhidro, se filtraron y se concentraron. Se purificó el producto en bruto obtenido por cromatografía en columna [usando gel de sílice (100-200), acetato de etilo en éter de petróleo al 10%] para proporcionar 2,2-difluoro-2-(4'-fluorobifenil-4-il)acetato de etilo (800 mg, 2,72 mmol, 80% de rendimiento) como un líquido incoloro. GCMS (ESI) m/z 294 [M+1]+.
D. Ácido 2,2-difluoro-2-(4'-fluorobifenil-4-il)acético. A una solución agitada de 2,2-difluoro-2-(4'-fluorobifenil-4-il)acetato de etilo (900 mg, 3,06 mmol) en mezcla de tetrahidrofurano: metanol: agua (12 mL, 1:1:1) se añadió hidróxido de litio monohidratado (385 mg, 9,18 mmol) y se agitó a temperatura ambiente durante 4 h. Se concentró la mezcla de reacción a presión reducida y se disolvió el residuo obtenido en agua (10 mL), se lavó con acetato de etilo (2X10 mL). Se acidificó la fase acuosa con solución acuosa de clorhidrato 1 N y se extrajo con acetato de etilo (3X10 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar ácido 2,2-difluoro-2-(4'-fluorobifenil-4-il)acético (400 mg, 2,91 mmol, 44% de rendimiento) como un compuesto semisólido. El producto en bruto se usó en la siguiente etapa sin purificación.
E. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4'-fluorobifenil-4-il)acetamida. A una solución enfriada con hielo de ácido 2,2-difluoro-2-(4'-fluorobifenil-4-il)acético (266 mg, 1,16 mmol) en piridina (15 mL) se añadió oxicloruro de fósforo (445 mL, 2,91 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A continuación, se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) en la mezcla de reacción y se agitó a temperatura ambiente durante 1 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3X15 mL). Se lavaron las capas orgánicas combinadas con salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 (acetonitrilo al 50-55% en ácido fórmico acuoso al 0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4'-fluorobifenil-4-il)acetamida (60 mg, 0,114 mmol, 11% de rendimiento) como un sólido blanco. MS (ESI) m/z 522,46 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 8 ppm 10,98 (s, 1 H), 9,68 (t, J = 5,8 Hz, 1 H), 7,86 - 7,72 (m, 4H), 7,72 - 7,62 (m, 3H), 7,43
7,28 (m, 4H), 5,09 (dd, J = 13,2, 5,1 Hz, 1H), 4,47 (d, J = 5,7 Hz, 2H), 4,38 (d, J =17,1 Hz, 1H), 4,24 (d, J =17,1 Hz, 1H), 3,00 - 2,81 (m, 1H), 2,64 - 2,53 (m, 1H), 2,38 - 2,20 (m, 1H), 2,03- 1,90 (m, 1H).
Ejemplo 81
N-((2-(2,6-diozopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2-(2-etoxi-5-fluorofenil)-2,2-difluoroacetamida
A. 1-(2-etoxi-5-fluorofenil)etanona. A una solución agitada de 1-(5-fluoro-2-hidroxifenil)etanona (500 mg, 3,24 mmol) en N,N-dimetilformamida (15 mL) se añadió bromuro de etilo (607 mg, 3,89 mmol) seguido por carbonato de potasio (1,11 g, 8,10 mmol) y se agitó a 90°C durante 16 h. Se diluyó la mezcla de reacción con agua con hielo (15 mL) y se extrajo con acetato de etilo (3X10 mL). Se lavaron las capas orgánicas combinadas con agua (10 mL), salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 1-(2-etoxi-5-fluorofenil)etanona (350 mg, 1,36 mmol, 20% de rendimiento) como un líquido incoloro. MS (ESI) m/z 183,34 [M+1]+.
B. 2-(2-etoxi-5-fluorofenil)-2-oxoacetato de etilo. A una solución agitada de 1-(2-etoxi-5-fluorofenil)etanona (2 g, 10,99 mmol) en piridina (10 mL) se añadió dióxido de selenio (3,05 g, 27,47 mmol) a temperatura ambiente calentado a 100°C durante 16 h. Se filtró la mezcla de reacción a través de un lecho de Celite y se lavó con diclorometano (15 mL). Se añadieron 4 mL de cloroformiato de etilo se añadió al filtrado a 0°C y se agitó a temperatura ambiente durante 4 h. Se inactivó la mezcla de reacción con agua con hielo y se extrajo con diclorometano (3 x 30 mL). Se lavaron las capas orgánicas combinadas con solución de clorhidrato 1 N (30 mL), salmuera (30 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 2-(2-etoxi-5-fluorofenil)-2-oxoacetato de etilo (1,7 g, 7,08 mmol, 75% de rendimiento) como un líquido incoloro. Se usó sin purificación adicional en la etapa siguiente.
C. 2-(2-etoxi-5-fluorofenil)-2,2-difluoroacetato de etilo. Se añadió 2-(2-etoxi-5-fluorofenil)-2-oxoacetato de etilo (1 g, 4,16 mmol) en trifluoruro de dietilamino azufre (2 mL) a 0°C y se agitó a temperatura ambiente durante 16 h. Se inactivó la mezcla de reacción con solución de bicarbonato de sodio acuosa y se extrajo con acetato de etilo (3X10 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secaron sobre sulfato de sodio anhidro, se filtraron y se concentraron. Se purificó el producto en bruto obtenido por cromatografía en columna (gel de sílice 100-200, acetato de etilo en éter de petróleo al 10%) para proporcionar 2-(2-etoxi-5-fluorofenil)-2,2-difluoroacetato de etilo (800 mg, 3,05 mmol, 73% de rendimiento) como un líquido incoloro. Ms (ESI) m/z 262,2 [M]+.
D. Ácido 2-(2-etoxi-5-fluorofenil)-2,2-difluoroacético. A una solución agitada de 2-(2-etoxi-5-fluorofenil)-2,2-difluoroacetato de etilo (600 mg, 2,29 mmol) en mezcla de tetrahidrofurano: metanol: agua (12 mL, 1:1:1) se añadió hidróxido de litio monohidratado (288 mg, 6,87 mmol) y se agitó a temperatura ambiente durante 16 h. Se extrajeron los productos volátiles a presión reducida y se disolvió el residuo obtenido en agua (10 mL) y se lavó con acetato de etilo (2X10 mL). Se acidificó la capa acuosa con solución acuosa de clorhidrato 1 N y se extrajo con acetato de etilo (3 X 10 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró disolvente para proporcionar ácido 2-(2-etoxi-5-fluorofenil)-2,2-difluoroacético (310 mg, 1,32 mmol, 87% de rendimiento) como un compuesto semisólido. 1H RMN (400 MHz, CDCh) 87,38 (dd, J = 8,8, 3,2 Hz, 1H), 7,16 (ddd, J =11,2, 8,8, 3,2 Hz, 1H), 6,91 (dd, J = 9,2, 4,4 Hz, 1H), 4,08 (q, J = 7,2 Hz, 2H), 2,68 (brs, 1H), 1,39 (t, J = 6,8 Hz, 3H).
E. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2-(2-etoxi-5-fluorofenil)-2,2-difluoroacetamida. A una solución enfriada con hielo de ácido 2-(2-etoxi-5-fluorofenil)-2,2-difluoroacético (151 mg, 0,65 mmol) en piridina (9 mL) se añadió oxicloruro de fósforo (0,18 mL, 1,94 mmol) gota a gota y se agitó a 0 - 5°C durante 1 h. A continuación, se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (200 mg, 0,65 mmol) en la mezcla de reacción y se agitó a temperatura ambiente durante 1 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3X15 mL). Se lavaron las capas orgánicas combinadas con salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 (acetonitrilo al 50-55% en ácido fórmico acuoso al 0,1%) para dar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindotin-5-il)metil)-2-(2-etoxi-5-fluorofenil)-2,2-difluoroacetamida (55 mg, 0,11 mmol, 17% de rendimiento) como un sólido blanco. m S (ESI) m/z 490,1 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 810,98 (s, 1H), 9,38 (t, J =5,6 Hz, 1H), 7,70 (d, J =7,5 Hz, 1H), 7,50 (s, 1H), 7,44 (d, J =
8,4 Hz, 1H), 7,39 - 7,34 (m, 2H), 7,19-7,11 (m, 1H), 5,11 (dd, J = 13,2, 5,1 Hz, 1H), 4,47 (d, J = 6,6 Hz, 2H), 4,45 (d, J = 16,5 Hz, 1H), 4,31 (d, J = 17,7, 1H), 3,97 (q, J = 6,9 Hz, 2H), 2,96 - 2,85 (m, 1H), 2,67 - 2,55 (m, 1H), 2,45 - 2,30 (m, 1H), 2,04- 1,94 (m, 1H), 1,11 (t, J =7,2 Hz, 3H).
Ejemplo 82
2-ciclopentN-N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdolm-5-N)metM)-2,2-difluoroacetamida
A. 2,2-difluoro-2-(1-hidroxiciclopentil)acetato de etilo. A una solución agitada de ciclopentanona (1 g, 11,90 mmol) en tetrahidrofurano (20 mL) se le añadió cloruro de cerio (III) anhidro (0,06 g, 0,24 mmol) seguido por polvo de cinc activado (0,93 g, 14,28 mmol) y 2-bromo-2,2-difluoroacetato de etilo (2,01 mL, 15,47 mmol) a 0°C y se agitó a temperatura ambiente durante 16 h. Se diluyó la mezcla de reacción con agua (20 mL) y se extrajo con acetato de etilo (3 X 20 mL). Se lavaron las capas orgánicas combinadas con agua (20 mL), salmuera (20 mL), se secó sobre sulfato de sodio, se filtró y se concentró el disolvente y se purificó el producto en bruto obtenido por cromatografía en columna sobre gel de sílice (acetato de etilo en éter de petróleo al 30%) para proporcionar 2,2-difluoro-2-(1-hidroxiciclopentil)acetato de etilo (0,55 g, 2,40 mmol, 22% de rendimiento) como un líquido incoloro. 1H RMN (300 MHz, DMSO-d6) 65,48 (s, 1H), 4,27 (q, J = 6,9 Hz, 2H), 1,87 - 1,81 (m, 2H), 1,75 - 1,57 (m, 6H), 1,26 (t, J = 6,9 Hz, 3H).
B. 2-ciclopentenil-2,2-difluoroacetato de etilo. A una solución agitada de 2,2-difluoro-2-(1-hidroxiciclopentil)acetato de etilo (50 mg, 0,24 mmol) en piridina (1,7 mL) se añadió cloruro de tionilo (0,17 mL, 2,40 mmol) a 0°C y se agitó a temperatura ambiente durante 16 h. Se diluyó la mezcla de reacción con agua (4 mL) y se basificó con solución de bicarbonato de sodio acuosa y se extrajo con acetato de etilo (3X 4 mL). Se lavaron las capas orgánicas combinadas con agua (4 mL), salmuera (4 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto obtenido por cromatografía en columna sobre gel de sílice (acetato de etilo en éter de petróleo al 30%) para proporcionar 2-ciclopentenil-2,2-difluoroacetato de etilo (25 mg, 0,13 mmol, 45% de rendimiento) como un líquido incoloro. MS (ESI) m/z 190,1 [M]+.
C. 2-ciclopentil-2,2-difluoroacetato de etilo. A una solución agitada de 2-ciclopentenil-2,2-difluoroacetato de etilo (100 mg, 0,52 mmol) en acetato de etilo (10 mL) se le añadió una suspensión espesa de hidróxido de paladio al 10% (30 mg) en acetato de etilo bajo una corriente de nitrógeno y se agitó bajo una presión de balón de hidrógeno a temperatura ambiente durante 4 h. Se evacuó la atmósfera de hidrógeno y se filtró la mezcla de reacción a través de un lecho de Celite, se concentró el filtrado para proporcionar 2-ciclopentil-2,2-difluoroacetato de etilo (60 mg, 0,31 mmol, 59% de rendimiento) como un líquido incoloro. 1H RMN (300 MHz, CDCh) 64,32 (q, J = 7,2 Hz, 2H), 2,67 - 2,57 (m, 1H), 1,79 - 1,55 (m, 8H), 1,35 (t, J = 6,9 Hz, 3H).
D. Ácido 2-ciclopentil-2,2-difluoroacético. A una solución agitada de 2-ciclopentil-2,2-difluoroacetato de etilo (450 mg, 2,34 mmol) en mezcla de tetrahidrofurano: metanol: agua (15 mL, 1:1:1) se añadió hidróxido de litio monohidratado (295 mg, 7,03 mmol) y se agitó a temperatura ambiente durante 4 h. Se extrajeron los productos volátiles a presión reducida y se disolvió el residuo resultante en agua (10 mL) y se lavó con acetato de etilo (2X10 mL). Se acidificó la capa acuosa con solución acuosa de clorhidrato 1 N y se extrajo con acetato de etilo (3X10 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar ácido 2-ciclopentil-2,2-difluoroacético (280 mg, 1,70 mmol, 72% de rendimiento) como un compuesto semisólido. 1H RMN (300 MHz, DMSO-d6) 68,68 (brs, 1H), 2,69 - 2,59 (m, 1H), 1,84 - 1,59 (m, 8H).
E. 2-ciclopentil-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. A una solución enfriada con hielo de ácido 2-ciclopentil-2,2-difluoroacético (159 mg, 0,97 mmol) en piridina (9 mL) se añadió oxicloruro de fósforo (0,27 mL, 2,9 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A continuación, se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) en la mezcla de reacción y se agitó a temperatura ambiente durante 2 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3X 15 mL). Se lavaron las capas orgánicas combinadas con salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 (acetonitrilo al 50-55% en ácido fórmico acuoso al 0,1%) para proporcionar 2cidopentil-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (50 mg, 0,12 mmol, 12% de rendimiento) como un sólido blanco. MS (ESI) m/z 420,17 [M+1]+. 1H RMN (300 MHz, DMSO-da) 8 10,98 (s, 1H), 9,36 (t, J = 6,3 Hz, 1H), 7,70 (d, J =7,8 Hz, 1H), 7,47 (s, 1H), 7,40 (d, J = 8,1 Hz, 1H), 5,11 (dd, J =13,5, 5,1 Hz, 1H), 4,46 (d, J =17,1 Hz, 1H), 4,44 (d, J = 6,0 Hz, 2H), 4,31 (d, J = 17,7 Hz, 1H), 2,92-2,87 (m, 1H), 2,73-2,57 (m, 2H), 2,40 2,36 (m, 1H), 2,02 - 1,98 (m, 1H), 1,70 - 1,53 (m, 8 H).
Ejemplo 83
N-((2-(2,6-dioxopipendm-3-M)-1-oxoisomdolm-5-M)metM)-2,2-dlfluoro-2-(3-metil-4-(trifluorometoxi)fenil)acetamida
A. 2-cloro-4-yodo-1-(trifluorometoxi)benceno. A una solución agitada en frío (0°C) de ácido 3-cloro-4-(trifluorometoxi)anilina (2,5 g, 11,79 mmol) en H2SO4 acuoso (10 mL) se añadió nitrito de sodio (894 mg, 12,96 mmol), urea (106 mg, 1,768 mmol) y yoduro de potasio (4,1 g, 24,75 mmol) a 0°C y se agitó a 50°C durante 2 h. Se inactivó la mezcla de reacción con solución de bicarbonato de sodio acuosa (40 mL) y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2X10 mL), salmuera (10 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-cloro-4-yodo-1-(trifluorometoxi)benceno y producto en bruto (2 g, 6,23 mmol, 52% de rendimiento) como un líquido incoloro que se usó en la siguiente etapa sin purificación adicional.
B. 2-(3-cloro-4-(trifluorometoxi)fenil)-2,2-difluoroacetato de etilo. Se hizo reaccionar una solución agitada de 2-cloro-4-yodo-1-(trifluorometoxi)benceno (1,5 g, 4,56 mmol) en dimetilsulfóxido (12 mL) con 2-bromo-2,2-difluoroacetato de etilo (138 g 6,84 mmol), cobre (753 mg, 11,85 mmol) y se agitó durante 6 h a 55°C. Se neutralizó la mezcla de reacción con solución de cloruro de amonio saturada acuosa y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 10 mL), salmuera (10 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-(3-cloro-4-(trifluorometoxi)fenil)-2,2-difluoroacetato de etilo (1,1 g, 3,45 mmol, 78% de rendimiento) como un líquido marrón. MS (ESI) m/z 318 [M+1]+.
C. Ácido 2-(3-cloro-4-(trifluorometoxi)fenil)-2,2-difluoroacético. A una solución agitada en frío (0°C) de 2-(3-cloro-4-(trifluorometoxi)fenil)-2,2-difluoroacetato de etilo (2 g, 6,289 mmol) en mezcla de metanol/tetrahidrofurano/agua (10 mL, 1:1:1) se añadió hidróxido de litio monohidratado (792 mg, 18,86 mmol) y se agitó a temperatura ambiente durante 16 h. Se concentró la mezcla de reacción y se neutralizó el residuo con ácido clorhídrico acuoso al 10% (10 mL) en 1,4-dioxano y se extrajo con acetato de etilo (2 X 30 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2-(3-cloro-4-(trifluorometoxi)fenil)-2,2-difluoroacético y producto en bruto (800 mg, 2,75 mmol, 44% de rendimiento) como un semisólido marrón que se usó en la etapa siguiente sin purificación adicional.
D. 2-(3-cloro-4-(trifluorometoxi)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. A una solución agitada en frío (0°C) de clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (250 mg, 0,809 mmol) y ácido 2-(3-cloro-4-(trifluorometoxi)fenil)-2,2-difluoroacético (234 mg, 0,970 mmol) en N,N-dimetilformamida (10 mL) se añadió N,N-diisopropiletilamina (0,4 mL, 2,42 mmol) seguido por 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metileno]-1H-1,2,3-triazolo[4,5-b]piridinio (614 mg, 1,61 mmol) y se agitó a temperatura ambiente durante 16 h. Se diluyó la mezcla de reacción con agua (30 mL) y se extrajo con acetato de etilo (2 X 40 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secó sobre sulfato de sodio y se concentró y secó al vacío. Se purificó el producto por columna de fase inversa Reveleris C-18 usando acetonitrilo al 60% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(2-hidroxietoxi)fenil)acetamida (35 mg, 0,064 mmol, 8 % de rendimiento) como un sólido blanquecino. MS (ESI) m/z 546,26 [M+1]+. 1H RMN (300MHz, DMSO-de,) 8 10,98 (s, 1H), 9,75 (brt, J=59 Hz, 1H), 7,92-7,90 (m, 1H), 7,82 -7,64 (m, 3H), 7,47-7,34 (m, 2H), 5,10 (dd, J=13,2, 5,1 Hz, 1H), 4,51-4,24 (m, 4H), 2,99-2,84 (m, 1H), 2,67-2,55 (m, 1H), 2,45-2,25 (m, 1H), 2,05-1,93 (m, 1H).
Ejemplo 84
N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdoMn-5-M-metM)-2,2-difluoro-2-(4-metoxi-2-(trifluorometil)fenil)acetamida
A. 1-bromo-4-metoxi-2-(trifluorometil)benceno. A una solución agitada de 4-bromo-3-(trifluorometil)fenol (2 g, 8,29 mmol) en N,N-dimetilformamida (20 mL) se añadió en porciones hidruro de sodio (398 mg, 16,59 mmol) a 0°C, y se agitó durante 30 min a temperatura ambiente. A esta masa de reacción se le añadió yoduro de metilo (671 mg, 10,78 mmol) a 0°C y se agitó a temperatura ambiente durante 1 h. Se inactivó la mezcla de reacción con agua (50 mL) y se extrajo con acetato de etilo (2 X200 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 100 mL), salmuera (100 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna (gel de sílice 100-200) hexano al 100% como eluyente para proporcionar 1-bromo-4-metoxi-2-(trifluorometil)benceno (1,2 g, 4,72 mmol, 57% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 254,1 [M]+.
B. 1-yodo-4-metoxi-2-(difluorometil)benceno. A una solución agitada de 1-bromo-4-metoxi-2-(trifluorometil)benceno (1 g, 3,93 mmol) en 1,4-dioxano (10 mL) se añadió yoduro de sodio (1,76 g, 11,79 mmol), yoduro de cobre (150 mg, 0,786 mmol) seguido portrans-N,N'-dimetilciclohexano-1,2-diamina (168 mg, 1,18 mmol) a temperatura ambiente y se agitó a 110°C durante 2 h en microondas. Se inactivó la mezcla de reacción con agua (20 mL) y se extrajo con acetato de etilo (3 X 200 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 1-yodo-4-metoxi-2-(trifluorometil)benceno (800 g, 2,65 mmol, 68% de rendimiento) como un líquido marrón. MS (ESI) m/z 302,0 [M]+.
C. 2,2-difluoro-2-(4-metoxi-2-(trifluorometil)fenil)acetato de etilo. A una solución agitada de 1-yodo-4-metoxi-2-(trifluorometil)benceno (800 mg, 2,65 mmol) en dimetilsulfóxido (20 mL) se añadió 2-yodo-2,2-difluoroacetato de etilo (0,62 mL, 3,97 mmol), cobre (438 g, 6,89 mmol) y se agitó durante 16 h a temperatura ambiente. Se neutralizó la mezcla de reacción con solución de cloruro de amonio saturada acuosa y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 10 mL), salmuera (10 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(4-metoxi-2-(trifluorometil)fenil)acetato de etilo (600 mg, 2,01 mmol, 76%) como un líquido marrón. MS (ESI) m/z 298,1 [M]+.
D. Ácido 2,2-difluoro-2-(4-metoxi-2-(trifluorometil)fenil)acético. A una solución agitada en frío (0°C) de 2,2-difluoro-2-(4-metoxi-2-(trifluorometil)fenil)acetato de etilo (600 mg, 2,01 mmol) en metanol/tetrahidrofurano/agua (9 mL, 1:1:1) se añadió hidróxido de litio monohidratado (253 mg, 6,03 mmol) y se agitó a temperatura ambiente durante 4 h. Se concentró la mezcla de reacción y se neutralizó el residuo con bisulfato de potasio acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 30 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(4-metoxi-2-(trifluorometil)fenil)acético (450 mg, 1,66 mmol, 83% de rendimiento) como un semisólido marrón. MS (ESI) m/z 269,30 [M-1]+.
E. N-((2-(2,6-dioxopiperldm-3-M)-1-oxoisomdoMn-5-N)metM)-2,2-difluoro-2-(4-metoxi-2-(trifluorometil)fenil)acetamida. A una solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(4-metoxi-2-(trifluorometil)fenil)acético (314 mg, 1,16 mmol) en piridina (20 mL) se añadió cloruro de fosforilo (0,7 mL, 2,91 mmol) gota a gota y se agitó a 0-5°C durante 30 min. A esto se le añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) y se agitó a temperatura ambiente durante 1 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 50-55% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1 -oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-metoxi-2-(trifluorometil)fenil)acetamida (35 mg, 0,07 mmol, 7% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 526,21 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 8 ppm 10,97 (br s, 1 H), 9,59 (brt, J=5,87 Hz, 1 H), 7,81 -7,60 (m, 2 H), 7,56 -7,20 (m, 4 H), 5,11 (br dd, J=13,39, 4,95 Hz, 1 H), 4,56-4,14 (m, 4 H), 3,89 (s, 3 H), 3,02-2,85 (m, 1 H), 2,67-2,55 (m, 1 H), 2,46-2,30 (m, 1 H), 2,06- 1,94 (m, 1 H).
Ejemplo 85
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(2-hidroxietoxi)fenil)acetamida
A. (2-bromoetoxi)(terc-butil)dimetilsilano. A una solución agitada de 2-bromoetanol (10 g, 80 mmol) en diclorometano (100 mL) se añadió terc-butilclorodimetilsilano (14,5 g, 96,77 mmol) e imidazol (10 g, 161,2 mmol) a 0°C y se agitó a temperatura ambiente durante 16 h. Se inactivó la mezcla de reacción con solución de bicarbonato de sodio acuosa (40 mL) y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 10 mL), salmuera (10 mL), se secó sobre sulfato de sodio y se concentró para proporcionar (2-bromoetoxi)(terc-butil)dimetilsilano (8 g, 33,61 mmol, 42% de rendimiento) como un líquido incoloro.
B. 7erc-butN(2-(2-yodofenoxi)etoxi)dimetNsilma. A una solución agitada de 2-yodofenol (3 g, 13,6 mmol) en N,N-dimetilformamida (20 mL) se añadió (2-bromoetoxi)(terc-butil)dimetilsilano (3,89 g, 16,36 mmol), yoduro de terc-butilamonio (1 g 2,72 mmol) y carbonato de potasio (4,69 g 34 mmol) a 0°C y se agitó a 80°C durante 16 h. Se inactivó la mezcla de reacción con agua (40 mL) y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 10 mL), salmuera (10 mL), se secó sobre sulfato de sodio y se concentró para proporcionar terc-butil(2-(2-yodofenoxi)etoxi)dimetilsilano (2,5 g, 6,613 mmol, 49% de rendimiento) como un líquido incoloro.
C. 2,2-difluoro-2-(2-(2-hidroxietoxi)fenil)acetato de etilo. A una solución agitada de terc-butil(2-(2-yodofenoxi)etoxi)dimetilsilano (3 g, 7,936 mmol) en dimetilsulfóxido (20 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (2,41 g 11,90 mmol), polvo de cobre (1,3. g, 20,63 mmol) y se agitó a 50°C durante 6 h. Se neutralizó la mezcla de reacción con solución de cloruro de amonio saturada acuosa y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 10 mL), salmuera (10 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(2-(2-hidroxietoxi)fenil)acetato de etilo (900 mg, 3,406 mmol, 45%) como un líquido marrón.
D. Ácido 2,2-difluoro-2-(2-(2-hidroxietoxi)fenil)acético. A una solución enfriada con hielo de 2,2-difluoro-2-(2-(2-hidroxietoxi)fenil)acetato de etilo (1,2 g, 3,20 mmol) en mezcla de etanol/tetrahidrofurano/agua (15 mL, 1:1:1) se añadió hidróxido de litio monohidratado (404 mg, 9,62 mmol) y se agitó a temperatura ambiente durante 6 h. Se concentró la mezcla de reacción y se neutralizó el residuo resultante con ácido clorhídrico acuoso al 10% en 1,4-dioxano (10 mL) y se extrajo con acetato de etilo (2 X 30 mL). Se lavó la capa orgánica combinada con salmuera (10 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(2-(2-hidroxietoxi)fenil)acético (650 mg, 2,82 mmol, 65% de rendimiento) como un semisólido marrón. 1H RMN (300 m Hz , DMSO-d6) 87,68 (d, J = 7,2 Hz, 1H), 7,46 (dd, J = 8,1 Hz, 7,8 Hz, 1H), 7,09 (dd, J = 8,0, 7,8 Hz, 1H), 6,91 (d, J =8,4 Hz, 1H), 6,38 (brs, 1H), 4,12 (t, J = 5,4 Hz, 2H), 3,99 (t, J = 3,9 Hz, 2H).
E. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(2-hidroxietoxi)fenil)acetamida. A una solución enfriada con hielo de clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,970 mmol) y ácido 2,2-difluoro-2-(2-(2-hidroxietoxi)fenil)acético (225 mg, 0,970 mmol) en N,N-dimetilformamida (10 mL) se añadió N,N-diisopropiletilamina (0,5 mL, 2,91 mmol) seguido por 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metileno]-1H-1,2,3-triazolo[4,5-b]piridinio (737 mg, 1,94 mmol) y se agitó a temperatura ambiente durante 12 h. Se diluyó la mezcla de reacción con agua (30 mL) y se extrajo con acetato de etilo (2 X 40 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secó sobre sulfato de sodio y se concentró y secó al vacío. Se purificó el producto por columna de fase inversa Reveleris C-18 (acetonitrilo al 60% en ácido fórmico acuoso al 0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(2-hidroxietoxi)fenil)acetamida (40 mg, 0,082 mmol, 8% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 488,12. 1H RMN (300MHz, DMSO-d6): 8 = 10,98 (s, 1H), 9,29 (t, J = 5,7 Hz, 1H), 7,70 (d, J=7,7 Hz, 1H), 7,60 - 7,39 (m, 4H), 7,16 (brd, J = 8,1 Hz, 1H), 7,10-7,01 (m, 1H), 5,11 (dd, J =13,0, 5,0 Hz, 1H), 4,72 (t, J = 5,5 Hz, 1H), 4,51 -4,27 (m, 4H), 3,98 (t, J = 5,3 Hz, 1H), 3,60 (q, J = 5,3 Hz, 1H), 3,00 - 2,82 (m, 1H), 2,63 - 2,54 (m, 1H), 2,45 - 2,32 (m,
1H), 2,06- 1,94 (m, 1H).
Ejemplo 86
2-(4-cloro-2-etox¡feml)-W-((2-(2,6-d¡oxop¡per¡dm-3-M)-1-oxo¡somdolm-5-¡l)metM)-2,2-d¡fluoroacetam¡da
A. 1-(4-cloro-2-etox¡fen¡l)etanona. A una solución agitada de 1-(4-cloro-2-hidroxifenil)etanona (2 g, 11,76 mmol) en N,N-dimetilformamida (15 mL) se añadió yoduro de etilo(2,8 mL, 29,4 mmol) seguido por carbonato de potasio (4,87 g, 35,29 mmol) y se agitó a 90°C durante 16 h. Se diluyó la mezcla de reacción con agua con hielo (20 mL) y se extrajo con acetato de etilo (3 X 20 mL). Se lavaron las capas orgánicas combinadas con agua (20 mL), salmuera (20 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 1-(4-cloro-2-etoxifenil)etanona (1,7 g, 8,58 mmol, 73% de rendimiento) como un líquido incoloro. MS (ESI) m/z 199,41 [M+1]+.
B. 2-(4-cloro-2-etox¡fen¡l)-2-oxoacetato de et¡lo. A una solución agitada de 1-(4-cloro-2-etoxifenil)etanona (1,7 g, 8,58 mmol) en piridina (10 mL) se añadió dióxido de selenio (2,38 g, 21,46 mmol) a temperatura ambiente y se agitó a 100°C durante 16 h. Se filtró la mezcla de reacción a través de un lecho de Celite y se lavó con diclorometano (15 mL). Se añadió cloroformiato de etilo (3,4 mL) al filtrado a 0°C y se agitó a temperatura ambiente durante 4 h. Se inactivó la mezcla de reacción con agua con hielo y se extrajo con diclorometano (3 X 20 mL). Se lavaron las capas orgánicas combinadas con solución de clorhidrato 1 N (20 mL), salmuera (20 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 2-(4-cloro-2-etoxifenil)-2-oxoacetato de etilo (1,2 g, 4,68 mmol, 54% de rendimiento) como un líquido incoloro. MS (ESI) m/z 256,1 [M]+.
C. 2-(4-cloro-2-etox¡fen¡l)-2,2-d¡fluoroacetato de et¡lo. Se añadió 2-(4-cloro-2-etoxifenil)-2-oxoacetato de etilo (1 g, 3,9 mmol) en trifluoruro de dietilamino azufre (1,89 g, 11,72 mmol) a 0°C y se agitó a temperatura ambiente durante 16 h. Se inactivó la mezcla de reacción con solución de bicarbonato de sodio acuosa y se extrajo con acetato de etilo (3 X 15 mL). Se lavaron las capas orgánicas combinadas con salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto obtenido por cromatografía instantánea (gel de sílice 100-200, acetato de etilo en éter de petróleo al 10%) para proporcionar 2-(4-cloro-2-etoxifenil)-2,2-difluoroacetato de etilo (570 mg, 2,05 mmol, 52% de rendimiento) como un líquido incoloro. 1H RMN (400 MHz, CDCh) 87,56 (d, J = 8,4 Hz, 1H), 7,03 (dd, J = 8,4, 1,6 Hz, 1H), 6,91 (s, 1H), 4,31 (q, J = 7,6 Hz, 2H), 4,05 (q, J = 6,8 Hz, 2H), 1,37 (t, J = 7,2 Hz, 3H), 1,31 (t, J = 7,2 Hz, 3H).
D. Ác¡do 2-(4-cloro-2-etox¡fen¡l)-2,2-d¡fluoroacét¡co. A una solución agitada de 2-(4-cloro-2-etoxifenil)-2,2-difluoroacetato de etilo (470 mg, 1,69 mmol) en tetrahidrofurano: metanol: agua (12 mL, 1:1:1) se añadió hidróxido de litio monohidratado (213 mg, 5,07 mmol) y se agitó a temperatura ambiente durante 16 h. Se extrajeron los productos volátiles a presión reducida y se disolvió el producto en bruto obtenido en agua (10 mL) y se lavó con acetato de etilo (2X10 mL). Se acidificó la capa acuosa con solución acuosa de clorhidrato 1 N y se extrajo con acetato de etilo (3 X 10 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró el disolvente para proporcionar ácido 2-(4-cloro-2-etoxifenil)-2,2-difluoroacético (260 mg, 1,04 mmol, 61% de rendimiento) como un compuesto semisólido. 1H Rm N (300 MHz, CDCh) 87,58 (d, J = 8,7 Hz, 1H), 7,05 (d, J = 8,1 Hz, 1H), 6,94 (s, 1H), 4,09 (q, J =7,2 Hz, 2H), 1,39 (t, J = 6,9 Hz, 3H).
E.2-(4-cloro-2-etox¡fen¡l)-N-((2-(2,6-dloxoplperldln-3-¡l)-1-oxo¡so¡ndol¡n-5-¡l)met¡l)-2,2-d¡fluoroacetam¡da. A una solución enfriada con hielo de ácido 2-(4 cloro-2-etoxifenil)-2,2-difluoroacético (178 mg, 0,71 mmol) en piridina (9 mL) se añadió oxicloruro de fósforo (0,18 mL, 1,94 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A continuación, se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (200 mg, 0,64 mmol) en la mezcla de reacción y se agitó a temperatura ambiente durante 1 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3X15 mL). Se lavaron las capas orgánicas combinadas con salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 (acetonitrilo al 50-55% en ácido fórmico acuoso al 0,1%) para dar 2-(4-cloro-2-etoxifenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (58 mg, 0,11 mmol, 18% de rendimiento) como un sólido blanco. MS (ESI) m/z 506,1 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 8 10,98 (s, 1H), 9,38 (t, J = 5,6 Hz, 1H), 7,71 (d, J = 7,8 Hz, 1H), 7,56 (d, J = 8,1 Hz, 1H), 7,50 (s, 1H), 7,44 (d, J = 7,5
Hz, 1H), 7,22 (s, 1H), 7,12 (dd, J = 7,8, 1,8 Hz, 1H), 5,11 (dd, J = 13,2, 5,1 Hz, 1H), 4,46 (d, J = 17,2 Hz, 1H), 4,46 (d, J = 5,7 Hz, 2H), 4,31 (d, J =17,4, 1H), 4,03 (q, J = 6,9 Hz, 2H), 2,98 - 2,85 (m, 1H), 2,67 - 2,55 (m, 1H), 2,43 - 2,30 (m, 1H), 2,04- 1,93 (m, 1H), 1,11 (t, J = 6,9 Hz, 3H).
Ejemplo 87
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-hidroxifenil)acetamida
A. 1-yodo-2-(metoximetoxi)benceno. A una solución agitada de 2-yodofenol (3 g, 13,63 mmol) en diclorometano (30 mL) se añadió diisopropiletilamina (7,2 mL, 40,89 mmol) seguido por éter clorometilmetílico (1,63 g, 20,45 mmol) a 0°C y se agitó a temperatura ambiente durante 16 h. Se inactivó la mezcla de reacción con agua con hielo (30 mL) y se extrajo con diclorometano (3 X 30 mL). Se lavaron las capas orgánicas combinadas con agua (30 mL), salmuera (30 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto resultante por cromatografía en columna sobre gel de sílice (acetato de etilo en éter de petróleo al 20%) para proporcionar 1-yodo-2-(metoximetoxi)benceno (2,5 g, 9,61 mmol, 72% de rendimiento) como un líquido marrón. 1H RMN (400 MHz, CDCh) 8 7,78 (dd, J = 8,0, 1,6 Hz, 1H), 7,28 (ddd, J = 8,5, 7,4, 1,6 Hz, 1H), 7,07 (dd, J = 8,4, 1,6 Hz, 1H), 6,76 (ddd, J = 8,8, 7,2, 0,8 Hz, 1H), 5,24 (s, 2H), 3,52 (s, 3H).
B. 2,2-difluoro-2-(2-(metoximetoxi)fenil)acetato de etilo. A una solución agitada de 1-yodo-2-(metoximetoxi)benceno (3 g, 8,24 mmol) en dimetilsulfóxido (11,5 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (2,67 g, 13,18 mmol) seguido por polvo de cobre (1,31 g, 20,6 mmol) a 0°C y se agitó a 60°C durante 5 h. Se inactivó la mezcla de reacción con agua con hielo (30 mL) y se filtró a través de un lecho de Celite. Se extrajo el filtrado con acetato de etilo (3 X 30 mL) y se lavaron las capas orgánicas combinadas con agua (30 mL), salmuera (30 mL), se secó sobre sulfato de sodio, se filtró y se concentró. El producto en bruto obtenido se purificó por cromatografía instantánea (acetato de etilo en éter de petróleo al 20% para proporcionar 2,2-difluoro-2-(2-(metoximetoxi)fenil)acetato de etilo (1,3 g, 5,0 mmol, 62% de rendimiento) como un líquido incoloro. MS (ESI) m/z 260,2 [M]+.
C. Ácido 2,2-difluoro-2-(2-(metoximetoxi)fenil)acético. A una solución agitada de 2,2-difluoro-2-(2-(metoximetoxi)fenil)acetato de etilo (2 g, 7,69 mmol) en mezcla de metanol:tetrahidrofurano:agua (20 mL, 1:1:1) a 0°C se añadió hidróxido de litio monohidratado (970 mg, 23,07 mmol) y se agitó a temperatura ambiente durante 4 h. Se extrajeron los productos volátiles a presión reducida y se diluyó el producto en bruto obtenido con agua (20 mL) y se lavó con acetato de etilo (2 X 15 mL). Se acidificó la capa acuosa con solución de bisulfato de sodio acuosa y se extrajo con acetato de etilo (3 X 20 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar ácido 2,2-difluoro-2-(2-(metoximetoxi)fenil)acético (1,2 g, 4,87 mmol, 63% de rendimiento) como un semisólido marrón. MS (ESI) m/z 246,3 [M]+.
D. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-hidroxifenil)acetamida. A una solución enfriada con hielo de ácido 2,2-difluoro-2-(2-(metoximetoxi)fenil)acético (258 mg, 1,16 mmol) en piridina (9 mL) se añadió oxicloruro de fósforo (0,27 mL, 2,9 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A continuación, se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) en la mezcla de reacción y se agitó a temperatura ambiente durante 1 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3X15 mL). Se lavaron las capas orgánicas combinadas con salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 (acetonitrilo al 50-55% en ácido fórmico acuoso al 0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1 -oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-hidroxifenil)acetamida (33 mg, 0,07 mmol, 8% de rendimiento) como un sólido blanco. MS (ESI) m/z 444,35 [M+1]+.
1H RMN (300 MHz, DMSO-d6) 811,00 (s, 1H), 10,24 (bs, 1H), 9,38 (bs, 1H), 7,68 (d, J = 7,8 Hz, 1H), 7,51 (s, 1H), 7,47 - 7,44 (m, 2H), 7,34 (dd, J = 7,8, 7,5 Hz, 1H), 6,91 -6,87 (m, 2H), 5,11 (dd, J = 13,5, 5,1 Hz, 1H), 4,48 (d, J = 4,5 Hz, 2H), 4,46 (d, J = 18,0 Hz, 1H), 4,32 (d, J = 17,4 Hz, 1H), 2,96-2,86 (m, 1H), 2,58-2,49 (m, 1H), 2,42-2,27 (m, 1H), 2,07- 1,98 (m, 1H).
Ejemplo 88
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(metilamino)fenil)acetamida
A. 2-yodofenilcarbamato de bencilo. A una solución agitada de 2-yodoanilina (3 g, 13,69 mmol) en hidróxido de sodio acuoso 4 N (3 mL), agua (10 mL) se añadió cloroformiato de bencilo (2,79 g, 16,43 mmol) a 0°C y se agitó a temperatura ambiente durante 3 h. Se diluyó la mezcla de reacción con agua (30 mL) y se extrajo con acetato de etilo (3 X 30 mL). Se lavaron las capas orgánicas combinadas con agua (30 mL), salmuera (30 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-yodofenilcarbamato de bencilo (3 g, 8,49 mmol, 62% de rendimiento) como un líquido incoloro. 1H RMN (400 MHz, CDCla) 88,08 (d, J = 8,8 Hz, 1H), 7,76 (dd, J =11,8 Hz, 1,8 Hz, 1H), 7,48-7,32 (m, 6H), 7,02 (brs, 1H), 6,79 (ddd, J = 8,0, 7,7, 1,8 Hz, 1H), 5,23 (s, 2H).
B. 2-yodofenil(metil)carbamato de bencilo. A una solución agitada de 2-yodofenilcarbamato de bencilo (1,5 g, 4,24 mmol) en N,N-dimetilformamida (15 mL) se añadió carbonato de cesio (4,13 g, 12,72 mmol) seguido por yodometano (0,9 g, 6,37 mmol) a 0°C y se agitó a 60°C durante 5 h. Se diluyó la mezcla de reacción con agua (25 mL) y se extrajo con acetato de etilo (3 X 25 mL). Se lavaron las capas orgánicas combinadas con agua (25 mL), salmuera (25 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto obtenido por cromatografía en columna sobre gel de sílice usando acetato de etilo en éter de petróleo al 30% para proporcionar 2-yodofenil(metil)carbamato de bencilo (1,2 g, 3,26 mmol, 80% de rendimiento) como un líquido incoloro. Ms (ESI) m/z 368,01 [M+1]+
C. 2-(2-((benciloxicarbonil)(metil)amino)fenil)-2,2-difluoroacetato de etilo. A una solución agitada de 2-yodofenil(metil)carbamato de bencilo (1 g, 2,72 mmol) en dimetilsulfóxido (20 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (0,83 g, 4,08 mmol) seguido por cobre (0,45 g, 7,08 mmol) a 0°C y se agitó a 60°C durante 5 h. Se inactivó la mezcla de reacción con agua con hielo y se filtró a través de un lecho de Celite. Se extrajo el filtrado con acetato de etilo (3 X 15 mL) y se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto obtenido por cromatografía instantánea (acetato de etilo en éter de petróleo al 20% para proporcionar 2-(2-((benciloxicarbonil)(metil)amino)fenil)-2,2-difluoroacetato de etilo (0,72 g, 1,98 mmol, 73% de rendimiento) como un líquido incoloro. MS (ESI) m/z 363,1 [M]+.
D. Ácido 2-(2-((benciloxicarbonil)(metil)amino)fenil)-2,2-difluoroacético. A una solución agitada en frío (0°C) de 2-(2-((benciloxicarbonil)(metil)amino)fenil)-2,2-difluoroacetato de etilo (700 mg, 1,9 mmol) en mezcla de metanol: tetrahidrofurano: agua (15 mL, 1:1:1) se añadió hidróxido de litio monohidratado (242 mg, 5,78 mmol) y se agitó a temperatura ambiente durante 4 h. Se extrajeron los productos volátiles a presión reducida y se disolvió el residuo obtenido en agua (10 mL), se lavó con acetato de etilo (2 X 10 mL). Se acidificó la capa acuosa con solución de bisulfato de potasio acuoso y se extrajo con acetato de etilo (3X15 mL). Se lavaron las capas orgánicas combinadas con salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar ácido 2-(2-((benciloxicarbonil)(metil)amino)fenil)-2,2-difluoroacético (620 mg, 1,85 mmol, 97% de rendimiento) como un semisólido. MS (ESI) m/z 336,4 [M+1]+.
E. 2-(2-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metilamino)-1,1-difluoro-2-oxoetil)fenil(metil)carbamato de bencilo. A una solución enfriada con hielo de ácido 2-(2-((benciloxicarbonil)(metil)amino)fenil)-2,2-difluoroacético (325 mg, 0,97 mmol) en piridina (9 mL) se añadió oxicloruro de fósforo (0,27 mL, 2,9 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A continuación, se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) en la mezcla de reacción y se agitó a temperatura ambiente durante 2 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3X15 mL). Se lavaron las capas orgánicas combinadas con salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 (acetonitrilo al 50-55% en ácido fórmico acuoso al 0,1%) para proporcionar 2-(2-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metilamino)-1,1-difluoro-2-oxoetil)fenil(metil)carbamato de bencilo (150 mg, 0,25 mmol, 26% de rendimiento) como un sólido blanco. MS (ESI) m/z 591,62 [M+1]+.
F. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(metilamino)fenil)acetamida. A una
solución agitada de 2-(2-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metilamino)-1,1-difluoro-2-oxoetil)fenil(metil)carbamato de bencilo (0,1 g, 0,169 mmol) en metanol (15 mL) se añadió una suspensión espesa de hidróxido de paladio al 10% (10 mg) en metanol bajo corriente de nitrógeno y se agitó bajo presión de hidrógeno de 60 psi a temperatura ambiente durante 6 h. Se evacuó la atmósfera de hidrógeno y se filtró la mezcla de reacción a través de un lecho de Celite y se concentró el filtrado. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 (acetonitrilo al 50-55% en ácido fórmico acuoso al 0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(metilamino)fenil)acetamida (62 mg, 0,13 mmol, 80% de rendimiento) como un sólido blanco. MS (ESI) m/z 457,23 [M+H]+. 1H RMN (300 MHz, DIVISOR) 810,98 (s, 1H), 9,56 (t, J = 6,0 Hz, 1H), 7,67 (d, J = 8,7 Hz, 1H), 7,42 (s, 1H), 7,39 - 7,28 (m, 3H), 6,70 - 6,65 (m, 2H), 5,43 (q, J = 4,2 Hz, 1H), 5,10 (dd, J =13,5, 5,1 Hz, 1H), 4,47 (d, J = 6,0 Hz, 2H), 4,42 (d, J =17,9 Hz, 1H), 4,28 (d, J =17,1 Hz, 1H), 2,91 - 2,85 (m, 1H), 2,74 (d, J = 4,8 Hz, 3H), 2,62 - 2,50 (m, 1H), 2,43 - 2,34 (m, 1H), 2,01 -1,99 (m, 1H).
Ejemplo 89
N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdoNn-5-N)metM)-2,2-difluoro-2-(4-isopropoxi-2-(trifluorometil)fenil)acetamida
A. 1-bromo-4-isopropoxi-2-(trifluorometil)benceno. A una solución agitada de 4-bromo-3-(trifluorometil)fenol (5 g, 20,83 mmol) en N,N-dimetilformamida (20 mL) se añadió carbonato de potasio (8,6 g, 62,49 mmol) seguido por yoduro de isopropilo (3,1 mL, 31,24 mmol) y se agitó a 80°C durante 4 h. Se filtró la mezcla de reacción y se añadió agua (50 mL) y se extrajo con acetato de etilo (2 X 60 mL). Se lavaron las capas orgánicas combinadas con salmuera (50 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna (sílice 100-200) usando acetato de etilo en hexanos al 0-10% para proporcionar 1-bromo-4-isopropoxi-2-(trifluorometil)benceno (3,5 g, 12,41 mmol, 59% de rendimiento). LCMS (ESI) m/z 284,38 [M+2]+.
B. 1-yodo-4-isopropoxi-2-(trifluorometil)benceno. A una solución agitada de 1-bromo-4-isopropoxi-2-(trifluorometil)benceno (3,5 g, 12,41 mmol) en 1,4-dioxano (30 mL) se añadió yoduro de sodio (5,58 g, 37,23 mmol), yoduro de cobre (471 mg, 2,48 mmol), trans-N,N'-dimetilciclohexano-1,2-diamina (529 mg, 3,72 mmol) a temperatura ambiente y se agitó a 110°C durante 16 h en tubo sellado. Se inactivó la mezcla de reacción con agua (20 mL) y se extrajo con acetato de etilo (3 X 300 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 1-yodo-4-isopropoxi-2-(trifluorometil)benceno (3 g, 9,09 mmol, 73% de rendimiento) como un líquido marrón. MS (ESI) m/z 331,0 [M]+.
C. 2,2-difluoro-2-(2-metil-4-(trifluorometoxi)fenil)acetato de etilo. A una solución agitada de 1-yodo-4-isopropoxi-2-(trifluorometil)benceno (3 g, 9,09 mmol) en dimetilsulfóxido (25 mL) se añadió cobre (1,5 g, 23,63 mmol) y 2-ido-2,2-difluoroacetato de etilo (2,005 mL, 13,63 mmol) a temperatura ambiente y se agitó a 55°C durante 2 h. Se neutralizó la mezcla de reacción con solución de cloruro de amonio saturado (50 mL) y se extrajo con acetato de etilo (2 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 100 mL), salmuera (100 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(4-isopropoxi-2-(trifluorometil)fenil)acetato de etilo (2,5 g, 7,66 mmol, 84%). GCMS (ESI) m/z 326,2.
D. Ácido 2,2-difluoro-2-(4-isopropoxi-2-(trifluorometil)fenil)acético. A una solución agitada en frío (0°C) de 2,2 difluoro-2-(4-isopropoxi-2-(trifluorometil)fenil)acetato de etilo (2,5 g, 7,66 mmol) en tetrahidrofurano:metanol:agua (30 mL, 1:1:1) se añadió hidróxido de litio (1,6 g, 38,34 mmol) y se agitó a temperatura ambiente durante 6 h. Se concentró la mezcla de reacción y se neutralizó el residuo con ácido clorhídrico acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 20 mL). Se lavó la capa orgánica combinada con salmuera (20 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(4-isopropoxi-2-(trifluorometil)fenil)acético (1,8 g, 6,04 mmol, 78% de rendimiento) como un líquido marrón. Se llevó el producto en bruto a la etapa siguiente sin purificación adicional. E. N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdoNn-5-N)metM)-2,2-difluoro-2-(4-isopropoxi-2-(trifluorometil)fenil)acetamida. A una solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(4-isopropoxi-2-(trifluorometil)fenil)acético (380 mg, 1,165 mmol) en piridina se añadió POCh (0,27 mL, 2,91 mmol) gota a gota y se
agitó a 0-5°C durante 1 h ya continuación se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,968 mmol) y se continuó agitando a temperatura ambiente durante 30 min. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2X10 mL), salmuera (10 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 40-60% en ácido fórmico acuoso (0,1%) para dar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-isopropoxi-2-(trifluorometil)fenil)acetamida (48 mg, 0,086 mmol, 10% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 554,03 [M+1]+. 1H RMN (300 MHz, DMSO-da) 810,99 (s, 1H), 9,58 (t, J = 5,6 Hz, 1H), 7,73 - 7,64 (m, 2H), 7,47 (s, 1H), 7,41 (d, J = 7,6 Hz, 1H), 7,36 (d, J = 8,8 Hz, 1H), 7,32 - 7,28 (m, 1H), 5,11(dd, J = 13,2,5,1 Hz, 1H), 5,00-4,25 (m, 4H), 3,00 - 2,85 (m, 1H), 2,69 - 2,55 (m, 1H), 2,44 - 2,35 (m, J = 2,0 Hz, 1H), 2,05 - 1,95 (m, 1H), 1,35 - 1,25 (m, 6H).
Ejemplo 90
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-metilciclohexil)acetamida
A. 2,2-difluoro-2-(1-hidroxi-4-metilciclohexil)acetato de etilo. A una solución agitada de 4-metilciclohexanona (1 g, 8,92 mmol) en tetrahidrofurano (20 mL) se añadió una cantidad catalítica de cloruro de cerio (III) anhidro (0,22 g, 0,89 mmol), seguido por polvo de cinc activado (0,75 g, 11,6 mmol) y 2-bromo-2,2-difluoroacetato de etilo (1,13 mL, 11,6 mmol) a 0°C y se agitó a temperatura ambiente durante 16 h. Se diluyó la mezcla de reacción con agua (20 mL) y se extrajo con acetato de etilo (3X15 mL). Se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto obtenido por cromatografía en columna sobre gel de sílice (acetato de etilo en éter de petróleo al 30%) para proporcionar 2,2-difluoro-2-(1-hidroxi-4-metilciclohexil)acetato de etilo (0,9 g, 3,81 mmol, 41% de rendimiento) como un líquido incoloro. 1H RMN (400 MHz, DMSO-d6) 85,33 (d, J =13,2 Hz, 1H), 4,27 (q, J = 7,2 Hz, 2H), 2,37 (dt, J =13,3, 7,8 Hz, 1H), 2,18-2,13 (m, 1H), 1,94 - 1,86 (m, 1H), 1,78- 1,70 (m, 4H), 1,48- 1,39 (m, 2H), 1,26 (t, J =7,3 Hz, 3H), 0,91 (dt, J =18,8, 5,6 Hz, 3H).
B. 2,2-difluoro-2-(4-metilciclohex-1-enil)acetato de etilo. A una solución agitada de 2,2-difluoro-2-(1-hidroxi-4-metilciclohexil)acetato de etilo (1,8 g, 7,62 mmol) en piridina (18 mL), se añadió cloruro detionilo (9 mL, 76,27 mmol) a 0°C y se agitó a temperatura ambiente durante 16 h. Se diluyó la mezcla de reacción con agua (20 mL) y se basificó con solución de bicarbonato de sodio acuosa y se extrajo con acetato de etilo (3 X 20 mL). Se lavaron las capas orgánicas combinadas con agua (20 mL), salmuera (20 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto obtenido por cromatografía en columna sobre gel de sílice usando acetato de etilo en éter de petróleo al 20% para proporcionar 2,2-difluoro-2-(4-metilciclohex-1-enil)acetato de etilo (1 g, 4,23 mmol, 62% de rendimiento) como un líquido incoloro. MS (ESI) m/z 218,2 [M]+.
C. 2,2-difluoro-2-(4-metilciclohexil)acetato de etilo. A una solución agitada de 2,2-difluoro-2-(4-metilciclohex-1-enil)acetato de etilo (700 mg, 3,21 mmol) en acetato de etilo (15 mL) se añadió una suspensión espesa de hidróxido de paladio al 10% (200 mg) en acetato de etilo bajo corriente de nitrógeno y se agitó bajo presión de balón de hidrógeno a temperatura ambiente durante 4 h. Se evacuó la atmósfera de hidrógeno y se filtró la mezcla de reacción a través de un lecho de Celite, se concentró el filtrado para proporcionar 2,2-difluoro-2-(4-metilciclohexil)acetato de etilo (500 mg, 1,3 mmol, 37% de rendimiento) como un líquido incoloro. MS (ESI) m/z 220,2 [M]+.
D. Ácido 2,2-difluoro-2-(4-metilciclohexil)acético. A una solución agitada de 2,2-difluoro-2-(4-metilciclohexil)acetato de etilo (500 mg, 2,27 mmol) en mezcla de tetrahidrofurano: metanol: agua (15 mL, 1:1:1) se añadió hidróxido de litio monohidratado (286 mg, 6,81 mmol) y se agitó a temperatura ambiente durante 4 h. Se extrajeron los productos volátiles a presión reducida y se disolvió el residuo obtenido en agua (10 mL) y se lavó con acetato de etilo (2X10 mL). Se acidificó la capa acuosa con clorhidrato 1 N y se extrajo con acetato de etilo (3X10 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró el disolvente para proporcionar 2,2-difluoro-2-(4-metilciclohexil)acético (280 mg, 1,45 mmol, 64% de rendimiento) como un compuesto semisólido. 1H RMN (300 MHz, CDCla) 88,26 (brs, 1H), 2,04 - 2,02 (m, 1H), 1,85 -1,78 (m, 3H), 1,60 - 1,52 (m, 2H), 1,36 - 1,24 (m, 2H), 1,01 - 0,87 (m, 2H), 0,90 (d, J = 6,3 Hz, 3H).
E. N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdoNn-5-N)metM)-2,2-difluoro-2-(4-metNcid ohexM)acetamida. A una solución enfriada con hielo de ácido 2,2-difluoro-2-(4-metNcidohexN)acético (186 mg, 0,97 mmol) en piridina (9 mL) se añadió oxicloruro de fósforo (0,27 mL, 2,9 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A continuación, se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) en la mezcla de reacción y se agitó a temperatura ambiente durante 2 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3 X 15 mL). Se lavaron las capas orgánicas combinadas con salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 (acetonitrilo al 50-55% en ácido fórmico acuoso al 0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-metilciclohexil)acetamida (45 mg, 0,1 mmol, 10% de rendimiento) como un sólido blanco. MS (ESI) m/z 448,19 [M+1]+. 1H RMN (300 MHz, DMSO-da) 810,98 (s, 1H), 9,35 (t, J = 6,0 Hz, 1H), 7,70 (d, J =7,5 Hz, 1H), 7,47 (s, 1H), 7,41 (d, J =8,1 Hz, 1H), 5,11 (dd, J =13,2, 5,4 Hz, 1H), 4,45 (d, J =16,5 Hz, 1H), 4,44 (d, J = 6,6 Hz, 2H), 4,31 (d, J =17,4 Hz, 1H), 2,92-2,87 (m, 1H), 2,63-2,57 (m, 1H), 2,41 -2,36 (m, 1H), 2,02 - 1,98 (m, 2H), 1,68- 1,65 (m, 3H), 1,48- 1,42 (m, 3H), 1,24 -1,15 (m, 2H), 0,99 - 0,86 (m, 1H), 0,87 (dd, J = 6,9, 6,3 Hz, 3H).
Ejemplo 91
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-isopropoxietoxi)fenil)acetamida
A. 2,2-difluoro-2-(3-(2-isopropoxietoxi)fenil)acetato de etilo. A una solución agitada de 2,2-difluoro-2-(3-hidroxifenil)acetato de etilo (200 mg, 0,92 mmol) en tetrahidrofurano (10 mL) se añadió azodicarboxilato de diisopropilo (373 mg, 1,85 mmol) seguido por trifenilfosfina (485 mg, 1,85 mmol) y 2-isopropoxietanol (96,2 mg, 0,92 mmol) a 0°C y se agitó a temperatura ambiente durante 16 h. Se inactivó la mezcla de reacción con agua con hielo y se extrajo con acetato de etilo (3X 10 mL). Se lavaron las capas orgánicas combinadas con agua (10 mL), salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró. El producto en bruto obtenido se purificó por cromatografía instantánea (acetato de etilo en éter de petróleo al 20%) para proporcionar 2,2-difluoro-2-(3-(2-isopropoxietoxi)fenil)acetato de etilo (100 mg, 0,33 mmol, 36% de rendimiento) como un líquido incoloro. GCMS (ESI) m/z 302,6 [M]+.
B. Ácido 2,2-difluoro-2-(3-(2-isopropoxietoxi)fenil)acético. A una solución agitada en frío con hielo de 2,2-difluoro-2- (3-(2-isopropoxietoxi)fenil)acetato de etilo (210 mg, 0,69 mmol) en mezcla de metanol: tetrahidrofurano:agua (10 mL, 1:1:1) se añadió hidróxido de litio monohidratado (87 mg, 2,086 mmol) y se agitó a temperatura ambiente durante 4 h. Se extrajeron los productos volátiles a presión reducida y se disolvió el residuo obtenido en agua (10 mL), se lavó con acetato de etilo (2 X 6 mL). Se acidificó la capa acuosa con solución de bisulfato de potasio acuoso y se extrajo con acetato de etilo (3X 10 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar ácido 2,2-difluoro-2-(3-(2-isopropoxietoxi)fenil)acético (180 mg, 0,65 mmol, 95% de rendimiento) como un semisólido. 1H RMN (300 MHz, CDCla) 87,29 (dd, J = 8,2, 7,5 Hz, 1H), 7,18 (d, J =7,8 Hz, 1H), 7,11 (s, 1H), 6,99 (d, J =7,5 Hz, 1H), 4,11 (t, J =5,4 Hz, 2H), 3,82 (t, J = 5,1 Hz, 2H), 3,75 (sep, J = 6,0 Hz, 1H), 1,23 (d, J = 5,7 Hz, 6H).
C. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-isopropoxietoxi)fenil)acetamida. A una solución enfriada con hielo de ácido 2,2-difluoro-2-(3-(2-isopropoxietoxi)fenil)acético (221 mg, 0,81 mmol) en piridina (9 mL) se añadió oxicloruro de fósforo (371 mg, 2,47 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A continuación, se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (250 mg, 0,81 mmol) en la mezcla de reacción y se agitó a temperatura ambiente durante 1 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3X 15 mL). Se lavaron las capas orgánicas combinadas con salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 (acetonitrilo al 50-55% en ácido fórmico acuoso al 0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3- il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-isopropoxi etoxi)fenil)acetamida (62 mg, 0,116 mmol, 15% de rendimiento) como un sólido blanco. MS (ESI) m/z 529,9 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 810,98 (s, 1H), 9,60 (t, J = 6,0 Hz, 1H), 7,67 (d, J = 7,5 Hz, 1H), 7,45 (d, J = 8,1 Hz, 1H), 7,40 (s, 1H), 7,36 (d, J =7,5 Hz, 1H), 7,15-7,12 (m, 3H), 5,10 (dd, J = 13,5, 5,1 Hz, 1H), 4,45 (d, J = 5,7 Hz, 2H), 4,42 (d, J =18,0 Hz, 1H), 4,27 (d, J =17,4 Hz, 1H), 4,08 (t, J = 4,5 Hz, 2H), 3,69 (t, J = 4,8 Hz, 2H), 3,62 (sep, J = 5,7 Hz, 1H), 2,98 - 2,87 (m, 1H), 2,66 - 2,56 (m, 1H),
2,45 - 2,30 (m, 1H), 2,04 - 1,94 (m, 1H), 1,09 (d, J = 6,3 Hz, 6H).
Ejemplo 92
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-hidroxifenil)acetamida
A. 1-yodo-3-(metoximetoxi)benceno. A una solución agitada de 3-yodofenol (1 g, 4,54 mmol) en diclorometano (10 mL) se añadió N,N-diisopropiletilamina (2,4 mL, 13,63 mmol) seguido por éter clorometilmetílico (0,5 mL, 6,81 mmol) a 0°C y se agitó a temperatura ambiente durante 2 h. Se inactivó la mezcla de reacción con agua con hielo y se extrajo con diclorometano (2 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (50 mL), salmuera (50 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 1-yodo-3-(metoximetoxi)benceno (1,0 g, 3,78 mmol, 83% de rendimiento). GC MS (m/z) 264,0 [M]+.
B. 2,2-difluoro-2-(3-(metoximetoxi)fenil)acetato de etilo. A una solución agitada de 1-yodo-3-(metoximetoxi)benceno (800 mg, 3,03 mmol) en dimetilsulfóxido (10 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (738 mg, 3,97 mmol) seguido por cobre (501 mg, 7,88 mmol) y se agitó a 55°C durante 5 h. Se inactivó la mezcla de reacción con solución de cloruro de amonio acuosa y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (50 mL), salmuera (50 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 2,2-difluoro-2-(3-(metoximetoxi)fenil)acetato de etilo (700 mg, 2,69 mmol, 89% de rendimiento). GC MS (m/z) 260,2 [M]+.
C. Ácido 2,2-difluoro-2-(3-(metoximetoxi)fenil)acético. A una solución agitada de 2,2-difluoro-2-(3-(metoximetoxi)fenil)acetato de etilo (700 mg, 2,69 mmol) en mezcla de metanol-tetrahidrofurano-agua (15 mL, 1:1:1) se añadió hidróxido de litio monohidratado (339 mg, 8,07 mmol) y se agitó a temperatura ambiente durante 2 h. Se diluyó la mezcla de reacción con agua (50 mL) y se acidificó con solución de bisulfato de potasio acuoso y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con salmuera (50 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar ácido 2,2-difluoro-2-(3-(metoximetoxi)fenil)acético (400 mg, 1,72 mmol, 64% de rendimiento). LCMS (ESI) m/z 231,31 [M-1]-.
D. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(metoximetoxi)fenil)acetamida. A una solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(3-(metoximetoxi)fenil)acético (300 mg, 1,29 mmol) en piridina (5 mL) se añadió cloruro de fosforilo (0,4 mL, 3,87 mmol) gota a gota y se agitó a 0-5°C durante 1 h, y a continuación se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (400 mg, 1,29 mmol) y se agitó a temperatura ambiente durante 1 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 30 mL), salmuera (30 mL), se secó sobre sulfato de sodio y se concentró para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(metoximetoxi)fenil)acetamida (250 mg, 0,51 mmol, 40% de rendimiento). LCMS (ESI) m/z 488,39 [M+1]+.
E. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-hidroxifenil)acetamida. A una solución agitada en frío (0°C) de N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(metoximetoxi)fenil)acetamida (250 mg, 0,51 mmol) en 1,4-dioxano (5 mL) se añadió 1,4-dioxano. HCl (2,0 mL) gota a gota y se agitó a temperatura ambiente durante 1 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavó la capa orgánica combinada con agua (2 X 30 mL), salmuera (30 mL) y se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 45-50% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-hidroxifenil)acetamida (75 mg, 0,16 mmol, 33,0% de rendimiento) como un sólido blanquecino. LCMS (ESI) m/z 444,13 [M+1]+. 1H RMN (300MHz, dmso) 6 = 10,98 (s, 1H), 9,87 (s, 1H), 9,62 - 9,53 (m, 1H), 7,67 (d, J=7,7 Hz, 1H), 7,42 -7,27 (m, 4H), 7,02-6,68 (m, 3H), 5,10 (brdd, J=5,0, 13,4 Hz, 1H), 4,50-4,22 (m, 4H), 2,96-2,82 (m, 1H), 2,68-2,54
(m, 1H), 2,44 - 2,30 (m, 1H), 2,05 - 1,93 (m, 1H).
Ejemplo 93
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-((4-metilpiperacin-1-il)metil)fenil)acetamida
A. 2,2-difluoro-2-(3-formilfenil)acetato de etilo. A una solución agitada de 4-yodobenzaldehído (5 g, 21,55 mmol) en dimetilsulfóxido (50 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (6,0 mL, 43,11 mmol), cobre (4,0 g, 56,03 mmol) y se agitó durante 4 h a 55°C. Se neutralizó la mezcla de reacción con solución de cloruro de amonio saturada acuosa y se extrajo con acetato de etilo (3 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(3-formilfenil)acetato de etilo (3,5 g, 15,35 mmol, 71%). GC MS (m/z) 228,2.
B. 2,2-difluoro-2-(3-((4-metilpiperacin-1-il)metil)fenil)acetato de etilo. A una solución agitada de 2,2-difluoro-2-(3-formilfenil)acetato de etilo (1,0 g, 4,38 mmol) en etanol (25 mL) se añadió 1-metilpiperacina (878 mg, 8,77 mmol), ácido acético (526 mg, 8,77 mmol) y se agitó a 0°C durante 1 h. A esta mezcla de reacción se añadió a continuación cianoborohidruro de sodio (551 mg, 8,77 mmol) y se agitó a temperatura ambiente durante 3 h. Se inactivó la mezcla de reacción con agua (100 mL) y se extrajo con acetato de etilo (3 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 100 mL), salmuera (100 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(3-((4-metilpiperacin-1-il)metil)fenil)acetato de etilo (1,0 g, 3,20 mmol, 74% de rendimiento). LCMS (ESI) m/z 313,53 [M+1]+
C. Ácido 2,2-difluoro-2-(3-((4-metilpiperacin-1-il)metil)fenil)acético. A una solución agitada en frío (0°C) de 2,2-difluoro-2-(3-((4-metilpiperacin-1-il)metil)fenil)acetato de etilo (1,0 g, 3,20 mmol) en mezcla de tetrahidrofurano:metanol:agua (1:1:1, 30 mL) se añadió hidróxido de litio monohidratado (403 mg, 5,01 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con bisulfato de potasio acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 50 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secó sobre sulfato de sodio y se concentró para dar ácido 2,2-difluoro-2-(3-((4-metilpiperacin-1-il)metil)fenil)acético (750 mg, 2,64 mmol, 82% de rendimiento). lCm S (ESI) m/z 284,9[M+1]+.
D. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-((4-metilpiperacin-1-il)metil)fenil)acetamida. A una solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(3-((4-metilpiperacin-1-il)metil)fenil)acético (350 mg, 1,23 mmol) en piridina (5 mL) se añadió cloruro de fosforilo (0,3 mL, 3,69 mmol) y se agitó a 0-5°C durante 1 h. A continuación se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (381 mg, 1,23 mmol) y se agitó a temperatura ambiente durante 1 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (2 X 25 mL). Se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 45-50% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-((4-metilpiperacin-1-il)metil)fenil)acetamida (40 mg, 0,26 mmol, 6% de rendimiento) como un sólido amarillo claro. LCMS (ESI) m/z 540,40 [M+1]+. 1H RMN (300MHz, DMSO-d6) 810,99 (s, 1H), 9,67 (t, J=5,8 Hz, 1H), 7,87 (br s, 2H), 7,67 - 7,55 (m, 3H), 7,45 - 7,33 (m, 2H), 5,10 (dd, J=4,9, 13,3 Hz, 1H), 4,48 - 4,24 (m, 6H), 3,65 - 3,03 (m, 8H), 3,01 -2,82 (m, 4H), 2,66 - 2,54 (m, 1H), 2,48 - 2,30 (m, 1H), 2,29 -1,82 (m, 1H).
Ejemplo 94
N-((2-(2,6-dioxopiperidin-3-il)-1-oxolsoindolin-5-il)metil)-2,2-difluoro-2-(4-metil-2-(trfluorometil)fenil)acetamida
A. 1-yodo-4-metil-2-(trifluorometil)benceno. A una solución agitada de 1-bromo-4-metil-2-(trifluorometil)benceno (1,0 g, 4,18 mmol) en 1,4-dioxano (10 mL) se añadió yoduro de sodio (1,3 g, 8,36 mmol), yoduro de cobre (40 mg, 0,20 mmol), trans-N,N'-dimetilcidohexano-1,2-diamina (66 mg, 0,46 mmol) a temperatura ambiente y se agitó a 110°C durante 16 h en tubo sellado. Se inactivó la mezcla de reacción con agua (100 mL) y se extrajo con acetato de etilo (3 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para dar 1-yodo-4-metil-2-(trifluorometil)benceno (900 mg, 3,14 mmol, 75% de rendimiento). GCMS (m/z) 286.
B. 2,2-difluoro-2-(4-metM-2-(trifluorometM)feml)acetato de etilo. A una solución agitada de 1-yodo-4-metil-2-(trifluorometil)benceno (900 mg, 3,14 mmol) en dimetilsulfóxido (10 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (1,3 g, 6,29 mmol), cobre (520 mg, 8,18 mmol) y se agitó a 55°C durante 16 h. Se neutralizó la mezcla de reacción con solución de cloruro de amonio saturada acuosa y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(4-metil-2-(trifluorometil)fenil)acetato de etilo (800 mg, 2,83 mmol, 90%). GCMS (m/z) 282,1.
C. Ácido 2,2-difluoro-2-(4-metM-2-(trifluorometN)feml)acético. A una solución agitada en frío (0°C) de 2,2-difluoro-2-(4-metil-2-(trifluorometil)fenil)acetato de etilo (800 mg, 2,83 mmol) en tetrahidrofurano-metanol-agua (15 mL, 1:1:1) se añadió hidróxido de litio monohidratado (357 mg, 8,51 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con bisulfato de potasio acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 50 mL). Se lavaron las capas orgánicas combinadas con salmuera (30 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(4-metil-2-(trifluorometil)fenil)acético (400 mg, 1,57 mmol, 56% de rendimiento). LCMS (ESI) m/z 253,32 [M-1]-.
D. N-((2-{2,6-dioxopiperidm-3-M)-1-oxoisomdolm-5-N)metM)-2,2-difluoro-2-(4-metN-2-(trifluorometM)feml)acetamida. A una solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(4-metil-2-(trifluorometil)fenil)acético (400 mg, 1,57 mmol) en piridina (5 mL) se añadió cloruro de fosforilo (0,4 mL, 4,72 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A esta mezcla de reacción se le añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (487 mg, 1,57 mmol) y se agitó a temperatura ambiente durante 1 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 30 mL), salmuera (30 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 45-50% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-metil-2-(trifluorometil)fenil)acetamida (50 mg, 0,09 mmol, 6,0% de rendimiento) como un sólido blanquecino. LCMS (ESI) m/z 510,28 [M+1]+. 1H RMN (400MHz, DMSO-d6) 8 = 10,98 (s, 1H), 9,62 (brt, J=6,1 Hz, 1H), 7,78-7,60 (m, 4H), 7,75 (s, 1H), 7,41 (d, J=7,6 Hz, 1H), 5,11 (dd, J=5,1, 13,5 Hz, 1H), 4,51 -4,21 (m, 4H), 2,98-2,85 (m, 1H), 2,65-2,54 (m, 1H), 2,47-2,31 (m, 4H), 2,04- 1,96 (m, 1H).
Ejemplo 95
N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdoMn-5-N)metM)-2,2-difluoro-2-(3-(2-(2-metoxietoxi)etoxi)fenil)acetamida
A. 1-yodo-3-(metoximetoxi)benceno. A una solución agitada de 3-yodofenol (1 g, 4,54 mmol) en diclorometano (10 mL) se añadió N,N-diisopropiletilamina (2,4 mL, 13,63 mmol) seguido por éter clorometilmetílico (0,5 mL, 6,81 mmol)
a 0°C y se agitó a temperatura ambiente durante 2 h. Se inactivó la mezcla de reacción con agua con hielo y se extrajo con diclorometano (3X15 mL). Se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 1-yodo-3-(metoximetoxi)benceno (1,0 g, 3,78 mmol, 83% de rendimiento). MS (ESI) m/z 264,0 [M]+.
B. 2,2-difluoro-2-(3-(metoximetoxi)fenil)acetato de etilo. A una solución agitada de 1-yodo-3-(metoximetoxi)benceno (800 mg, 3,03 mmol) en dimetilsulfóxido (10 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (738 mg, 3,97 mmol) seguido por cobre (501 mg, 7,88 mmol) y se agitó a 55°C durante 5 h. Se inactivó la mezcla de reacción con solución de cloruro de amonio acuosa y se extrajo con acetato de etilo (3 X 15 mL). Se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 2,2-difluoro-2-(3-(metoximetoxi)fenil)acetato de etilo (700 mg, 2,69 mmol, 89% de rendimiento). MS (ESI) m/z 260,2 [M]+.
C. 2,2-difluoro-2-(3-hidroxifenil)acetato de etilo. A una solución enfriada con hielo de 2,2-difluoro-2-(3-(metoximetoxi)fenil)acetato de etilo (1 g, 3,84 mmol) en 1,4-dioxano (5 mL) se añadió 1,4-dioxanô HCl (5 mL) a 0°C y se agitó a temperatura ambiente durante 3 h. Se extrajeron los productos volátiles a presión reducida y se purificó el producto en bruto obtenido por cromatografía en columna (acetato de etilo en éter de petróleo al 20%) para proporcionar 2,2-difluoro-2-(3-hidroxifenil)acetato de etilo (0,7 g, 3,24 mmol, 84% de rendimiento) como un líquido incoloro. MS (ESI) m/z 216,1 [M]+.
D. 2,2-difluoro-2-(3-(2-(2-metoxietoxi)etoxi)fenil)acetato de etilo. A una solución agitada de 2,2-difluoro-2-(3-hidroxifenil)acetato de etilo (1 g, 4,63 mmol) en tetrahidrofurano (10 mL) se le añadieron en secuencia azodicarboxilato de diisopropilo (1,87 g, 9,26 mmol), trifenilfosfina (2,42 g, 9,26 mmol) y 2-(2-metoxietoxi)etanol (0,55 g, 4,63 mmol) a 0°C y se agitó a temperatura ambiente durante 16 h. Se inactivó la mezcla de reacción con agua con hielo y se extrajo con acetato de etilo (3X15 mL). Se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto obtenido por cromatografía en columna instantánea (acetato de etilo en éter de petróleo al 20%) para proporcionar 2,2-difluoro-2-(3-(2-(2-metoxietoxi)etoxi)fenil)acetato de etilo (0,5 g, 1,57 mmol, 34% de rendimiento) como un líquido incoloro. GCMS (ESI) m/z 318,6 [M]+.
E. Ácido 2,2-difluoro-2-(3-(2-(2-metoxietoxi)etoxi)fenil)acético. A una solución enfriada con hielo de 2,2-difluoro-2-(3-(2-(2-metoxietoxi)etoxi)fenil)acetato de etilo (500 mg, 1,57 mmol) en mezcla de metanol: tetrahidrofurano:agua (15 mL, 1:1:1) se añadió hidróxido de litio monohidratado (198 mg, 4,71 mmol) y se agitó a temperatura ambiente durante 4 h. Se extrajeron los productos volátiles a presión reducida y se disolvió el producto en bruto obtenido en agua (10 mL), se lavó con acetato de etilo (2 X 8 mL). A continuación, se acidificó la capa acuosa con solución de bisulfato de potasio acuoso y se extrajo con acetato de etilo (3X10 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar ácido 2,2-difluoro-2-(3-(2-(2-metoxietoxi)etoxi)fenil)acético (300 mg, 0,65 mmol, 84% de rendimiento) como un semisólido. MS (ESI) m/z 289,36 [M-1]+.
F. N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdolm-5-N)metM)-2,2-difluoro-2-(3-(2-(2-metoxietoxi)etoxi)fenil)acetamida. A una solución enfriada con hielo de ácido 2,2-difluoro-2-(3-(2-(2-metoxietoxi)etoxi)fenil)acético (375 mg, 1,29 mmol) en piridina (9 mL) se añadió oxicloruro de fósforo (593 mg, 3,88 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A continuación, se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (400 mg, 1,29 mmol) en la mezcla de reacción y se agitó a temperatura ambiente durante 2 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3X 15 mL). Se lavaron las capas orgánicas combinadas con salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 (acetonitrilo al 50-55% en ácido fórmico acuoso al 0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-(2-metoxietoxi)etoxi)fenil)acetamida (46 mg, 0,08 mmol, 7% de rendimiento) como un sólido blanco. MS (ESI) m/z 546,06 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 610,99 (bs, 1H), 9,60 (t, J = 6,3 Hz, 1H), 7,67 (d, J = 7,5 Hz, 1H), 7,44 (dd, J = 8,1, 7,8 Hz, 1H), 7,40 (s, 1H), 7,37 (d, J = 7,8 Hz, 1H), 7,16 7,12 (m, 3H), 5,10 (dd, J = 13,2, 5,1 Hz, 1H), 4,45 (d, J = 5,7 Hz, 2H), 4,41 (d, J =18,2 Hz, 1H), 4,27 (d, J =17,7 Hz, 1H), 4,11 (t, J = 4,2 Hz, 2H), 3,73 (t, J = 4,5 Hz, 2H), 3,58 (t, J = 4,5 Hz, 2H), 3,45 (t, J = 5,1 Hz, 2H), 3,24 (s, 3H), 2,98 - 2,83 (m, 1H), 2,67 - 2,53 (m, 1H), 2,44 - 2,30 (m, 1H), 2,05 - 1,94 (m, 1H).
Ejemplo 96
Clorhidrato de 2-(3-(2-(dimetilamino)etoxi)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxolsoindolin-5-il)metil)-2,2-difluoroacetamida
A. 2-(3-yodofenoxi)-N,N-dimetiletanamina. A una solución agitada de 3-yodofenol (2 g, 9,09 mmol) en acetona (20 mL) se añadió clorhidrato de 2-doro-N,N-dimetiletanamina (1,57 g, 10,90 mmol), carbonato de potasio (5,07 g, 36,36 mmol) y se agitó durante 16 h a 55°C. Se inactivó la mezcla de reacción con agua (50 mL) y se extrajo con acetato de etilo (2 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 100 mL), salmuera (100 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna (gel de sílice 100-200) hexano al 100% como eluyente para proporcionar 2-(3-yodofenoxi)-N,N-dimetiletanamina (1,5 g, 5,22 mmol, 57% de rendimiento) como un líquido marrón. MS (ESI) m/z 291[M]+.
B. 2-(3-(2-(dimetilamino)etoxi)fenil)-2,2-difluoroacetato de etilo. A una solución agitada de 2-(3-yodofenoxi)-N,N-dimetiletanamina (1,5 g, 5,22 mmol) en dimetilsulfóxido (20 mL) se le añadió 2-bromo-2,2-difluoroacetato de etilo (1,36 mL, 10,45 mmol) seguido por cobre (0,86 g, 13,58 mmol) y se agitó durante 16 h a 50°C. Se neutralizó la mezcla de reacción con solución de cloruro de amonio saturada y se extrajo con acetato de etilo (3 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 100 mL), salmuera (10 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-(3-(2-(dimetilamino)etoxi)fenil)-2,2-difluoroacetato de etilo (1,5 g del producto en bruto) como un líquido marrón. MS (ESI) m/z 288,4[M]+.
C. Ácido 2-(3-(2-(dimetilamino)etoxi)fenil)-2,2-difluoroacético. A una solución agitada en frío (0°C) de 2-(3-(2-(dimetilamino)etoxi)fenil)-2,2-difluoroacetato de etilo (1,0 g, 3,48 mmol) en metanol/tetrahidrofurano/agua (20 mL, 1:1:1) se añadió hidróxido de litio monohidratado (438,4 mg, 10,44 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con bisulfato de potasio acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 50 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2-(3-(2-(dimetilamino)etoxi)fenil)-2,2-difluoroacético (600 mg) como un semisólido marrón que se llevó a la etapa siguiente sin purificación adicional.
D. Clorhidrato de 2-(3-(2-(dimetilamino)etoxi)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. A una solución agitada en frío (0°C) de ácido 2-(3-etoxipiridin-2-il)-2,2-difluoroacético (252 mg, 1,16 mmol) en piridina (20 mL) se añadió cloruro de fosforilo (446,4 mg, 2,91 mmol) gota a gota y se agitó a 0-5°C durante 30 min y a continuación se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) y se agitó a temperatura ambiente durante 2 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 45-50% en ácido fórmico acuoso (0,1%) para proporcionar clorhidrato de 2-(3-(2-(dimetilamino)etoxi)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (50 mg, 0,07 mmol, 7,5% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 515,13 [M+1 1H RMN (400MHz, DMSO-d6) 8 ppm 10,99 (s, 1H), 10,31 (br s, 1H), 9,68 (brt, J=59 Hz, 1H), 7,68 (d, J=7,8 Hz, 1H), 7,50 (t, J=7,8 Hz, 1H), 7,43 - 7,33 (m, 3H), 7,26 - 7,13 (m, 3H), 5,11 (dd, J=4,9, 13,2 Hz, 1H), 4,50-4,34(m, 4H), 4,33-4,23(m, 2H), 3,00-2,87 (m, 1H), 2,83 - 2,70 (br s, 2H), 2,67-2,55 (m, 1H), 2,45 - 2,25 (m, 7H), 2,05 - 1,94 (m, 1H).
Ejemplo 97
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-isopropilpiridin-2-il)acetamida
A. 5-(prop-1-en-2-il)piridin-2-amina. A una solución agitada y desgasificada de 5-bromopiridin-2-amina (3,5 g, 20,34 mmol) en 1,4-dioxano:agua (1:1,40 mL) se añadió fosfato de potasio (12,94 g, 61,04 mmol), y se siguió desgasificando durante 10 min. A continuación, se añadió 4,4,5,5-tetrametil-2-(prop-1-en-2-il)-1,3,2-dioxaborolano (5,21 g, 30,51 mmol) seguido por [1,1'-bis(difenilfosfino)ferroceno]dicloropaladio(N) (1,47 mg, 2,014 mmol) se añadió, se desgasificó 10 min con agitación y se calentó a 100°C durante 2 h. Se enfrió la mezcla de reacción a temperatura ambiente, se filtró a través del lecho de celite. Al filtrado se le añadió agua fría y se extrajo con acetato de etilo (3 X 200 mL). Se lavaron las capas orgánicas con agua (2 X 100 mL), salmuera (100 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna sobre gel de sílice (malla 100-200) de acetato de etilo en éter de petróleo al 40% para proporcionar 5-(prop-1-en-2-il)piridin-2-amina (2,5 g, 18,65 mmol, 91% de rendimiento) como un sólido de color marrón. MS (ESI) m/z 135,18 [M+1]+.
B. 5-isopropilpiridin-2-amina. A una suspensión espesa de hidróxido de paladio al 20% (1 g) en acetato de etilo (50 mL) se añadió 5-(prop-1-en-2-il) piridin-2-amina (2,5 g, 18,65 mmol) y se agitó a temperatura ambiente durante 2 h bajo un balón de hidrógeno (1 atm). Se filtró la mezcla de reacción a través de un lecho de Celite, se secó sobre sulfato de sodio y se concentró para proporcionar la 5-isopropilpiridin-2-amina (2 g, 14,70 mmol, 79% de rendimiento) como un líquido marrón. MS (ESI) m/z 137,15 [M+1]+.
C. 2-bromo-5-isopropilpiridina. A una solución agitada en frío (0°C) de ácido 5-isopropilpiridin-2-amina (2 g, 14,70 mmol) en ácido bromhídrico acuoso al 47% (20 mL) se añadió una solución de nitrito de sodio (2,63 g, 38,23 mmol, en 5 mL de agua) y se agitó a la misma temperatura durante 30 min. A esta mezcla de reacción se añadió bromo (2,27 mL, 44,1 mmol) gota a gota a -5°C y se agitó a temperatura ambiente durante 4 h. Se neutralizó la mezcla de reacción con solución de hidróxido de sodio acuosa y se extrajo con diclorometano (2 X 50 mL). Se lavaron las capas orgánicas combinadas con solución de tiosulfato de sodio acuosa saturada (100 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-bromo-5-isopropilpiridina (1,8 g, 9,04 mmol, 62% de rendimiento) como un líquido de color marrón. m S (ESI) (m/z) 200,23 [M+1]+.
D.2-yodo-5-isopropilpiridina. A una solución agitada de 2-bromo-5-isopropilpiridina (1,8 g, 9,04 mmol) en acetonitrilo (20 mL) se añadió yoduro de potasio (3,75 g, 22,61 mmol) y cloruro de acetilo (1,42 g, 18,08 mmol) a temperatura ambiente y se agitó a 85°C durante 16 h. Se neutralizó la mezcla de reacción con solución de bicarbonato de sodio acuosa y se extrajo con diclorometano (2 X 50 mL). Se lavaron las capas orgánicas combinadas con solución de tiosulfato de sodio acuosa (100 mL) y salmuera (50 mL) y se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía de columna Silicagel (malla 100-200) usando acetato de etilo en éter de petróleo al 5% como eluyente para proporcionar 2-bromo-5-isopropilpiridina (850 mg, 3,44 mmol, 39% de rendimiento). MS (ESI) (m/z) 248,24 [M+1]+.
E. 2,2-difluoro-2-(5-isopropilpiridin-2-il)acetato de etilo. A una solución agitada de 2-yodo-5-isopropilpiridina (800 mg, 3,23 mmol) en dimetilsulfóxido (15 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (0,62 mL, 4,845 mmol) seguido por cobre (534 g, 8,39 mmol) y se agitó durante 16 h a 50°C. Se neutralizó la mezcla de reacción con solución de cloruro de amonio saturada acuosa y se extrajo con acetato de etilo (2 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(5-isopropilpiridin-2-il)acetato de etilo (650 mg, 2,67 mmol, 82%) como un líquido marrón. Ms (ESI) m/z 244,28 [M+1]+.
F. Ácido 2,2-difluoro-2-(5-isopropilpiridin-2-il)acético de etilo. A una solución agitada en frío (0°C) de 2,2-difluoro-2-(5-isopropilpiridin-2-il)acetato de etilo (600 mg, 2,46 mmol) en mezcla de metanol/tetrahidrofurano/agua (9 mL, 1:1:1) se añadió hidróxido de litio monohidratado (310 mg, 7,40 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con bisulfato de potasio acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 50 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(5-isopropilpiridin-2-il)acético de etilo (450 mg, 2,09 mmol, 85% de rendimiento) como un semisólido marrón. MS (ESI) m/z 216,30 [M-1]+.
G. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-Isopropilpiridin-2-il)acetamida. A una solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(5-isopropilpiridin-2-il)acético de etilo (333 mg, 1,54 mmol) en piridina (10 mL) se añadió cloruro de fosforilo (0,4 mL, 3,87 mmol) gota a gota y se agitó a 0-5°C durante 30 min. A esto se le añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (400 mg, 1,29 mmol) y se agitó a temperatura ambiente durante 2 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo resultante por cromatografía en columna usando 3-4% de metanol en diclorometano como eluyente para proporcionar W-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-isopropilpiridin-2-il)acetamida (65 mg, 0,138
mmol, 11% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 471,10 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 8 ppm 10,99 (s, 1 H), 9,61 (brt, J=6,05 Hz, 1 H), 8,62 (s, 1 H), 7,91 (dd, J=8,07, 1,83 Hz, 1 H), 7,71 (d, J=8,07 Hz, 2 H), 7,52 (s, 1 H), 7,46 (br d, J=7,70 Hz, 1 H), 5,11 (brdd, J= 13,57, 5,14 Hz, 1 H), 4,55-4,27 (m, 4 H), 3,10-3,00 (m, 1 H), 2,95 - 2,85 (m, 1 H), 2,75 - 2,67 - 2,54 (m, 1 H), 2,44 - 2,30 (m, 1 H), 2,07 - 1,93 (m, 1 H), 1,30 - 1,20 (m, 6 H).
Ejemplo 98
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-(metilsulfonil)etoxi)fenil)acetamida
A. (2-(3-yodofenoxi)etil)(metil)sulfano. A una solución agitada de 3-yodofenol (5 g, 22,72 mmol) en tetrahidrofurano (60 mL) se añadió azodicarboxilato de diisopropilo (8,9 mL, 45,45 mmol) seguido portrifenilfosfina (11,9 g, 45,45 mmol) y 2-(metiltio)etanol (1,97 mL, 22,72 mmol) a 0°C y se agitó a temperatura ambiente durante 3 h. Se inactivó la mezcla de reacción con agua con hielo (50 mL) y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (50 mL), salmuera (50 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto obtenido por cromatografía instantánea (acetato de etilo en éter de petróleo al 1%) para proporcionar (2-(3-yodofenoxi)etil)(metil)sulfano (2,5 g, 8,503 mmol, 37% de rendimiento) como un líquido incoloro. 1H RMN (300MHz, DMSO-d6) 8 (ppm) 7,33-7,24 (m, 1H), 7,04-6,95 (m, 1H), 6,90-6,83 (m, 1H), 4,12 (t, J=68 Hz, 1H), 2,87 (t, J=6,8 Hz, 1H), 2,21 (s, 1H).
B. 1-yodo-3-(2-(metilsulfonil)etoxi)benceno. A una solución agitada de (2-(3-yodofenoxi)etil)(metil)sulfano (2,5 g, 8,503 mmol) en diclorometano (25 mL) se añadió ácido m-cloroperbenzoico (4,4 g, 25,5 mmol) a 0°C y se agitó a temperatura ambiente durante 3 h. Se basificó la mezcla de reacción con NaHCO ac.3 (200 mL) y se extrajo con diclorometano (3 X 50 mL), se lavó con salmuera (50 mL) y se secó sobre sulfato de sodio, se concentró la fase orgánica. Se purificó el residuo obtenido por cromatografía en columna (sílice 100-200) usando acetato de etilo en hexanos al 5% para dar el 1-yodo-3-(2-(metilsulfonil)etoxi)benceno (1,2 g, 3,68 mmol, 43% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 349,26 [M+Na]+.
C. 2,2-difluoro-2-(3-(2-(metilsulfonil)etoxi)fenil)acetato de etilo. A una solución agitada de 1-yodo-3-(2-(metilsulfonil)etoxi)benceno (1,2 g, 3,68 mmol) en dimetilsulfóxido (12 mL) se añadió cobre (708 mg, 11,04 mmol) y 2-yodo-2,2-difluoroacetato de etilo (1,1 g, 4,42 mmol) a temperatura ambiente y se agitó a temperatura ambiente durante 16 h. A la mezcla de reacción se añadió solución de cloruro de amonio saturada acuosa (50 mL) y se extrajo con acetato de etilo (2 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 100 mL), salmuera (100 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(3-(2-(metilsulfonil)etoxi)fenil)acetato de etilo (720 mg, 2,23 mmol, 61% de rendimiento). MS (ESI) m/z 345,4 [M+Na]+.
D. Ácido 2,2-difluoro-2-(3-(2-(metilsulfonil)etoxi)fenil)acético. A una solución agitada de 2,2-difluoro-2-(3-(2-(metilsulfonil)etoxi)fenil)acetato de etilo (720 mg, 2,23 mmol) en 1,4-dioxano (30 mL) se añadió ácido clorhídrico acuoso 4 M (15 mL) a temperatura ambiente y se agitó a temperatura ambiente durante 16 h. Se extrajo la mezcla de reacción con acetato de etilo (3 X 50 mL), se lavó con salmuera (50 mL) y se secó sobre sulfato de sodio, se concentró la fase orgánica para dar el ácido 2,2-difluoro-2-(3-(2-(metilsulfonil)etoxi)fenil)acético (550 mg, 1,87 mmol, 84% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 293,21 [M+H]+.
E. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-(metilsulfonil)etoxi)fenil)acetamida. A una solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(3-(2-(metilsulfonil)etoxi)fenil)acético (250 mg, 0,85 mmol) en piridina (10 mL) se añadió cloruro de fosforilo (0,2 mL, 2,55 mmol) gota a gota y se agitó a 0°C durante 1 h y a continuación se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (394 mg, 1,02 mmol) y se agitó a temperatura ambiente durante 1 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 50-55% en ácido fórmico acuoso (0,1%) para dar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-(metilsulfonil)etoxi)fenil)acetamida (50 mg, 0,091
mmol, 11% de rendimiento) como un sólido blanco. MS (ESI) m/z 549,81 [M+1]+. 1H RMN (300MHz, DMSO-d6) 8 (ppm) 10,98 (s, 1H), 9,63 (brt, J=5,9 Hz, 1H), 7,68 (d, J=7,8 Hz, 1H), 7,52-7,44 (m, 1H), 7,41 -7,34 (m, 2H), 7,23-7,13 (m, 3H), 5,10 (dd, J=5,1, 13,5 Hz, 1H), 4,45 (br d, J=6,4 Hz, 2H), 4,40 - 4,22 (m, 4H), 3,64 (t, J=5,4 Hz, 1H), 2,97 - 2,84 (m, 1H), 2,63 - 2,57 (m, 1H), 2,44 - 2,33 (m, 1H), 2,04 - 1,95 (m, 1H).
Ejemplo 99
N-((2-(2,6-dioxopiperidm-3-M)-1-oxoisomdoMn-5-N)metM)-2,2-difluoro-2-(3-(3-(metilsulfonil)propil)fenil)acetamida
A. 2,2-difluoro-2-(3-formilfenil)acetato de etilo. A una solución agitada de 3-yodobenzaldehído (4 g, 17,24 mmol) en dimetilsulfóxido (20 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (5,25 g, 25,86 mmol) seguido por polvo de cobre (2,84 g, 44,82 mmol) a temperatura ambiente y se agitó a 60°C durante 5 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3 X 40 mL). Se lavaron las capas orgánicas combinadas con agua (40 mL), salmuera (40 mL), se secó sobre sulfato de sodio, se filtró y se concentró el disolvente y se purificó el producto en bruto obtenido por cromatografía en columna instantánea (acetato de etilo en éter de petróleo al 20%) para proporcionar 2,2-difluoro-2-(3-formilfenil)acetato de etilo (2,3 g, 8,27 mmol, 58%) como un líquido incoloro. MS (ESI) m/z 228,1 [M]+.
B. 2,2-difluoro-2-(3-vinilfenil)acetato de etilo. A una solución agitada de bromuro de metiltrifenilfosfonio (1,58 g, 4,4 mmol) en mezcla de tetrahidrofurano/éter dietílico (30 mL, 2:1), se añadió n-butil-litio (1 mL, 2,49 mmol) a -78°C y se agitó a la misma temperatura durante 30 min. A continuación, se añadió 2,2-difluoro-2-(3-formilfenil)acetato de etilo (0,5 g, 2,27 mmol) se añadió a la mezcla de reacción a -78°C y se agitó a 0°C durante 3 h. Se inactivó la mezcla de reacción con solución de cloruro de amonio saturada acuosa y se extrajo con acetato de etilo (3 X 20 mL). Se lavaron las capas orgánicas combinadas con agua (20 mL), salmuera (20 mL), se secó sobre sulfato de sodio, se filtró y se concentró el disolvente y se purificó el producto en bruto obtenido por cromatografía en columna (acetato de etilo en éter de petróleo al 20%) para proporcionar 2,2-difluoro-2-(3-vinilfenil)acetato de etilo (0,32 g, 1,41 mmol, 64% de rendimiento) como un líquido incoloro. 1H RMN (400 MHz, CDCla) 87,63 (s, 1H), 7,53 - 7,48 (m, 2H), 7,42 (d, J = 7,6 Hz, 1H), 6,73 (dd, J =17,6, 10,4 Hz, 1H), 5,81 (d, J =17,6 Hz, 1H), 5,33 (d, J =10,8 Hz, 1H), 4,30 (q, J =7,2 Hz, 2H), 1,31 (t, J = 7,2 Hz, 3H).
C. 3-(metilsulfonil)prop-1-eno. A una solución agitada de alil(metil)sulfano (5 g, 56,81 mmol) en diclorometano (50 mL) se añadió ácido meta-cloroperoxibenzoico (19,65 g, 113,63 mmol) a 0°C y se agitó a temperatura ambiente durante 16 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada y se extrajo con diclorometano (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (40 mL), salmuera (40 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto obtenido por cromatografía en columna instantánea (acetato de etilo en éter de petróleo al 20%) para proporcionar 3-(metilsulfonil)prop-1-eno (2,5 g, 20,83 mmol, 36% de rendimiento) como un sólido blanco. 1H RMN (400 MHz, CDCla) 85,98 (ddt, J =17,2, 14,8, 7,2 Hz, 1H), 5,48 (dd, J = 17,2, 1,2 Hz, 2H), 3,74 (d, J = 7,6 Hz, 2H), 2,88 (s, 3H).
D. 2,2-difluoro-2-(3-(3-(metilsulfonil)prop-1-enil)fenil)acetato de (E)-etilo. A una solución agitada de 2,2-difluoro-2-(3-vinilfenil)acetato de etilo (100 mg, 0,44 mmol) en diclorometano (10 mL) se añadió 3-(metilsulfonil)prop-1-eno (265 mg, 2,21 mmol) seguido por catalizador de generación II de Grubbs (19 mg, 0,02 mmol) a temperatura ambiente y se sometió a reflujo a 40°C durante 16 h. Se extrajeron los productos volátiles a presión reducida y se purificó el residuo obtenido por cromatografía en columna instantánea (acetato de etilo en éter de petróleo al 30%) para proporcionar 2,2-difluoro-2-(3-(3-(metilsulfonil)prop-1-enil)fenil)acetato de (E)-etilo (60 mg, 0,18 mmol, 42% de rendimiento) como un líquido incoloro. 1H RMN (300 MHz, CDCh) 87,64 (s, 1H), 7,59-7,42 (m, 3H), 6,76 (d, J =16,2 Hz, 1H), 6,41 -6,31 (m, 1H), 4,31 (q, J = 6,9 Hz, 2H), 3,91 (d, J =7,2 Hz, 2H), 2,92 (s, 3H), 1,31 (t, J = 6,9 Hz, 3H).
E. 2,2-difluoro-2-(3-(3-(metilsulfonil)propil)fenil)acetato de etilo. A una solución agitada de 2,2-difluoro-2-(3-(3-(metilsulfonil)prop-1-enil)fenil)acetato de (E)-etilo (220 mg, 0,69 mmol) en acetato de etilo (10 mL) se añadió una suspensión espesa de hidróxido de paladio al 10% (50 mg) en acetato de etilo bajo vapor de nitrógeno. Se agitó la mezcla de reacción bajo presión de balón de hidrógeno a temperatura ambiente durante 16 h. Se evacuó la atmósfera de hidrógeno y se filtró la mezcla de reacción a través de un lecho de Celite, se filtró y se concentró se purificó el
residuo obtenido por cromatografía en columna instantánea (acetato de etilo en éter de petróleo al 20%) para proporcionar 2,2-difluoro-2-(3-(3-(metilsulfonil)propil)fenil)acetato de etilo (120 mg, 0,37 mmol, 54% de rendimiento) como un líquido incoloro. 1H RMN (300 MHz, CDCla) 87,48 (d, J =7,8 Hz, 1H), 7,43 (s, 1H), 7,39 (d, J = 7,5 Hz, 1H), 7,32 (dd, J = 8,1, 7,9 Hz, 1H), 4,31 (q, J = 6,9 Hz, 2H), 2,99 (t, J = 7,5 Hz, 2H), 2,89 (s, 3H), 2,66 (t, J = 7,5 Hz, 2H), 2,23-2,15 (m, 2H), 1,32 (t, J = 6,9 Hz, 3H).
F. Ácido 2,2-difluoro-2-(3-(3-(metilsulfonil)propil)fenil)acético. A una solución agitada de 2,2-difluoro-2-(3-(3-(metilsulfonil)propil)fenil)acetato de etilo (150 mg, 0,47 mmol) en mezcla de tetrahidrofurano: metanol: agua (10 mL, 1:1:1) se añadió hidróxido de litio monohidratado (59 mg, 1,41 mmol) y se agitó a temperatura ambiente durante 4 h. Se extrajeron los productos volátiles a presión reducida y se disolvió el producto en bruto obtenido en agua (15 mL), se lavó con acetato de etilo (2X6 mL). Se acidificó la capa acuosa con solución acuosa de clorhidrato 1 N y se extrajo con acetato de etilo (3 X 8 mL). Se lavaron las capas orgánicas combinadas con salmuera (8 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar ácido 2,2-difluoro-2-(3-(3-(metilsulfonil)propil)fenil)acético (130 mg, 0,44 mmol, 94% de rendimiento) como un compuesto semisólido. 1H r Mn (300 MHz, DMSo-d6) 87,50 -7,41 (m, 4H), 3,32 (brs, 1H), 3,12 - 3,09 (m, 2H), 3,04 (s, 3H), 2,78 (t, J= 7,8 Hz, 2H), 2,04 - 1,96 (m, 2H).
G. N-((2-(2,6-dioxopiperidm-3-N)-1-oxoisomdoMn-5-N)metM)-2,2-difluoro-2-(3-(3-(metilsulfonil)propil)fenil)acetamida. A una solución enfriada con hielo de clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (180 mg, 0,58 mmol) y ácido 2,2-difluoro-2-(3-(3-(metilsulfonil)propil)fenil)acético (136 mg, 0,46 mmol) en N,N-dimetilformamida (10 mL) se añadió N,N-diisopropiletilamina (0,3 mL, 1,74 mmol) seguido por 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metileno]-1H-1,2,3-triazolo[4,5-b]piridinio (442 mg, 1,16 mmol) y se agitó a temperatura ambiente durante 4 h. Se diluyó la mezcla de reacción con agua (15 mL) y se extrajo con acetato de etilo (3X10 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto obtenido por columna de fase inversa Reveleris C-18 (acetonitrilo al 50% en ácido fórmico acuoso al 0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(3-(metilsulfonil)propil)fenil)acetamida (40 mg, 0,07 mmol, 12% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 472,11 [M+1]+. 1H RMN (300 m Hz , DMSO-d6) 810,98 (s, 1H), 9,63 (t, J = 5,6 Hz, 1H), 7,68 (d, J =7,8 Hz, 1H), 7,44-7,36 (m, 6H), 5,10 (dd, J =13,2, 5,1 Hz, 1H), 4,45 (d, J = 5,1 Hz, 2H), 4,42 (d, J =17,9 Hz, 1H), 4,28 (d, J =17,7, 1H), 3,11 (t, J = 8,1 Hz, 2H), 2,96 (s, 3H), 2,91 - 2,85 (m, 1H), 2,76 (t, J = 7,8 Hz, 2H), 2,67 - 2,55 (m, 1H), 2,45 - 2,30 (m, 1H), 2,06 - 1,92 (m, 3H).
Ejemplo 100
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-(2-fluoropropan-2-il)fenil)acetamida
A. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-(2-fluoropropan-2-il)fenil)acetamida. A una solución agitada en frío (0°C) de N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-(2-hidroxipropan-2-il)fenil)acetamida (170 mg, 0,35 mmol) en diclorometano (20 mL) se añadió trifluoruro de dietilamino azufre (0,06 mL, 0,52 mmol) y se agitó a temperatura ambiente durante 2 h. Se diluyó la mezcla de reacción con solución de bicarbonato de sodio saturada (20 mL) y se extrajo con acetato de etilo (2 X 25 mL). Se lavó la capa orgánica combinada con salmuera (20 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el producto por columna de fase inversa Reveleris C-18 usando acetonitrilo al 65% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-(2-fluoropropan-2-il)fenil)acetamida (70 mg, 0,16 mmol, 41% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 486,23 [M+1]+.
1H RMN (400 MHz, DMSO-d6) 810,98 (s, 1H), 9,65 (brt, J=6,1 Hz, 1H), 7,68 (d, J=7,8 Hz, 1H), 7,64 - 7,54 (m, 1H), 7,40-7,38 (m, 4H), 7,37 - 7,32 (d, J=8,3 Hz, 2H), 5,10 (brdd, J=5,1, 13,4 Hz, 1H), 4,54-4,38 (m, 3H), 4,31 -4,23 (m, 1H), 2,99 - 2,84 (m, 1H), 2,69 - 2,55 (m, 1H), 2,43 - 2,29 (m, 1H), 2,05 - 1,93 (m, 1H), 1,69 (s, 3H), 1,63 (s, 3H).
Ejemplo 101
2-(1-bencil-6-oxo-1,6-dihidropiridin-3-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-
difluoroacetamida
A. 1-bencil-5-yodopiridin-2(1H)-ona. A una solución agitada de 5-yodopiridin-2-ol (5 g, 22,62 mmol) en N,N-dimetilformamida seca (50 mL) se añadió carbonato de potasio (9,36 g, 67,86 mmol) seguido por bromuro de bencilo (2,95 mL, 24,88 mmol) a temperatura ambiente y se agitó a 70°C durante 4 h. Se inactivó la mezcla de reacción con agua (100 mL) y se extrajo con acetato de etilo (2 X 100 mL). Se lavaron las capas orgánicas combinadas con salmuera (50 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna (sílice 100-200) usando acetato de etilo al 30% en hexanos como eluyente para proporcionar 1 -bencil-5-yodopiridin-2(1H)-ona (4,5 g, 14,46 mmol, 64% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 311,98 [M+1]+.
B.5-acetil-1-bencilpiridin-2(1H)-ona. A una solución agitada de 1-bencil-5-yodopiridin-2(1H)-ona (1,2 g, 3,858 mmol) en N,N-dimetilformamida (12 mL) se añadió 1-(viniloxi)butano (1,93 g, 19,29 mmol) seguido por carbonato de potasio acuoso 3 M (2,4 mL, 11,57 mmol), se añadió Pd(OAc)2 (400 mg, 0,192 mmol) seguido por 1, 3-bis (difenilfosfino) propano (477 mg, 1,157 mmol) y se agitó a 80°C durante 3 h. Se enfrió la mezcla de reacción a temperatura ambiente y ácido clorhídrico acuoso 1 N (12 mL) se añadió y se agitó a 40°C durante 2 h. Se enfrió la mezcla de reacción a temperatura ambiente y agua (40 mL) se añadió y se extrajo con acetato de etilo (3 X 50 mL), se lavó con agua (2 X 50 mL), salmuera (50 mL) y se secó sobre sulfato de sodio, se concentró la fase orgánica. Se purificó el residuo obtenido por cromatografía en columna (sílice 100-200) usando acetato de etilo en hexanos al 30% para dar la 5-acetil-1-bencilpiridin-2(1H)-ona (700 mg, 3,08 mmol, 80% de rendimiento) como un jarabe amarillo. MS (ESI) m/z 228,24 [M+H]+.
C.2-(1-bencil-6-oxo-1,6-dihidropiridin-3-il)-2-oxoacetatode etilo. A una solución agitada de 5-acetil-1-bencilpiridin-2(1H)-ona (700 mg, 3,08 mmol) en piridina (7 mL) se añadió dióxido de selenio (855 mg, 7,709 mmol) y se agitó a 100°C durante 3 h. Se diluyó la mezcla de reacción con diclorometano (14 mL) y se filtró a través de lecho de celite. Al filtrado se le añadió cloroformiato de etilo (2,1 mL) a 0°C y se agitó a temperatura ambiente durante 16 h. Se neutralizó la mezcla de reacción con ácido clorhídrico acuoso 1 N (hasta pH-4) y se extrajo con acetato de etilo (2 X 50 mL). Se lavó la capa orgánica combinada con agua (2 X 50 mL), salmuera (50 mL) y se secó sobre sulfato de sodio y se concentró para dar 2-(1-bencil-6-oxo-1,6-dihidropiridin-3-il)-2-oxoacetato de etilo (500 mg, 1,75 mmol, 57% de rendimiento) como un jarabe amarillo. MS (ESI) m/z 286,12 [M+H]+.
D.2-(1-bencil-6-oxo-1,6-dihidropiridin-3-il)-2,2-difluoroacetato de etilo. A 2-(1-bencil-6-oxo-1,6-dihidropiridin-3-il)-2-oxoacetato de etilo (500 mg, 1,75 mmol) se añadió trifluoruro de dietilamino azufre (1,5 mL) a 0°C y se agitó a temperatura ambiente durante 16 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 25 mL), salmuera (25 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-(1-bencil-6-oxo-1,6-dihidropiridin-3-il)-2,2-difluoroacetato de etilo (450 mg, 1,46 mmol, 84% de rendimiento). MS (ESI) m/z 265,07 [M+1]+.
E. Ácido 2-(1-bencil-6-oxo-1,6-dihidropiridin-3-il)-2,2-difluoroacético. A una solución agitada de 2-(1-bencil-6-oxo-1,6-dihidropiridin-3-il)-2,2-difluoroacetato de etilo (400 mg, 1,302 mmol) en mezcla de tetrahidrofurano:metanol:agua (10 mL, 1:1:1) se añadió hidróxido de litio monohidratado (112 mg, 3,906 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con bisulfato de potasio saturado (20 mL) y se extrajo con acetato de etilo (2 X 25 mL). Se lavaron las capas orgánicas combinadas con salmuera (25 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2-(1-bencil-6-oxo-1,6-dihidropiridin-3-il)-2,2-difluoroacético (350 mg, 1,254 mmol, 96% de rendimiento). MS (ESI) m/z 280,32 [M+1]+.
F. 2-(1-bencil-6-oxo-1,6-dihidropiridin-3-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. A una solución agitada en frío (0°C) de ácido 2-(1-bencil-6-oxo-1,6-dihidropiridin-3-il)-2,2-difluoroacético (279 mg, 1,294 mmol) en piridina (10 mL) se añadió cloruro de fosforilo (0,36 mL, 3,894 mmol) gota a gota y se agitó a 0°C durante 1 h y a continuación se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (400 mg, 1,294 mmol) y se agitó a temperatura ambiente durante 1 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secaron sobre sulfato de sodio
y se concentraron. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 50-55% en ácido fórmico acuoso (0,1%) para proporcionar 2-(1 -bencil-6-oxo-1,6-dihidropiridin-3-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (80 mg, 0,148 mmol, 11% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 535,09 [M+1]+. 1H RMN (300MHz, DMSO-d6) 8 (ppm) 10,99 (s, 1H), 9,62 (brt, J=5,9 Hz, 1H), 8,18 (br s, 1H), 7,68 (d,>7,8 Hz, 1H), 7,56 (dd, J=2,7, 9,5 Hz, 1H), 7,44 (s, 1H), 7,40 -7,24 (m, 6H), 5,16 (s, 1H), 5,10 (brdd, J=4,9, 13,2 Hz, 1H), 4,46 (brd, J=59 Hz, 1H), 4,41 (br d, J=17,6 Hz, 1H), 4,27 (br d, J=17,6 Hz, 1H), 2,97-2,85 (m, 1H), 2,69-2,56 (m, 1H), 2,43-2,30 (m, 1H), 2,02- 1,98 (m, 1H).
Ejemplo 102
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-metoxipiridin-2-il)acetamida
A. 2-yodo-5-metoxipiridina. A una solución agitada de 2-bromo-5-metoxipiridina (2 g, 10,63 mmol) en 1,4-dioxano (20 mL) se añadió yoduro de sodio (3,3 g, 21,27 mmol), yoduro de cobre (100 mg, 0,53 mmol), trans-N,N'-dimetilciclohexano-1,2-diamina (150 mg, 1,16 mmol) a temperatura ambiente y se agitó a 110°C durante 16 h en tubo sellado. Se inactivó la mezcla de reacción con agua (20 mL) y se extrajo con acetato de etilo (3 X 20 mL). Se lavaron las capas orgánicas combinadas con agua ( 2 X 10 mL), salmuera (10 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-yodo-5-metoxipiridina (1,1 g, 4,46 mmol, 47% de rendimiento) como un líquido marrón. GCMS (m/z) 235,0 [M]+.
B. 2,2-difluoro-2-(5-metoxipiridin-2-il)acetato de etilo. A una solución agitada de 2-yodo-5-metoxipiridina (1 g, 4,32 mmol) en dimetilsulfóxido (20 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (1,1 mL, 8,65 mmol), cobre (0,73 g, 11,20 mmol) y se agitó durante 16 h a 50°C. Se neutralizó la mezcla de reacción con solución de cloruro de amonio saturada acuosa y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua ( 2X10 mL), salmuera (10 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(5-metoxipiridin-2-il)acetato de etilo (700 mg, 3,03 mmol, 71%) como un líquido marrón. GCMS (m/z) 231,1.
C. Ácido 2,2-difluoro-2-(5-metoxipiridin-2-il)acético. A una solución agitada en frío (0°C) de 2,2-difluoro-2-(5-metoxipiridin-2-il)acetato de etilo (600 mg, 2,59 mmol) en mezcla de etanol/tetrahidrofurano/agua (9 mL, 1:1:1) se añadió hidróxido de litio monohidratado (327 mg, 7,79 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con bisulfato de potasio acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 30 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(5-metoxipiridin-2-il)acético (450 mg, 2,21 mmol, 85% de rendimiento) como un semisólido marrón. MS (ESI) m/z 204,23 [M+1]+.
D. N-((2-(2,6-dioxopiperidin-3-il)-1-ozoisoindolin-5-il)metil)-2,2-difluoro-2-(5-metoxipiridin-2-il)acetamida. A una solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(5-metoxipiridin-2-il)acético (300 mg, 1,47 mmol) y clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (360 mg, 1,18 mmol) en N,N-dimetilformamida (20 mL) se añadió N,N-diisopropiletilamina (0,8 mL, 2,20 mmol) seguido por 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metileno]-1H-1,2,3-triazolo[4,5-b]piridinio (670 mg, 4,41 mmol) y se agitó a temperatura ambiente durante 16 h. Se diluyó la mezcla de reacción con agua (70 mL) y se extrajo con acetato de etilo (2 X 20 mL). Se lavaron las capas orgánicas combinadas con salmuera (30 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por columna de fase inversa Reveleris C-18 usando acetonitrilo al 57% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-metoxipiridin-2-il)acetamida (58 mg, 0,12 mmol, 8% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 459,20 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 810,99 (s, 1H), 9,61 -9,53 (m, 1H), 8,41 (brd, J=2,9 Hz, 1H), 7,72 (dd, J=8,3, 11,2 Hz, 2H), 7,57 (dd, J=2,9, 8,8 Hz, 1H), 7,52 (s, 1H), 7,45 (br d, J=8,3 Hz, 1H), 5,11 (br dd, J=4,9, 13,2 Hz, 1H), 4,53-4,27 (m, 4H), 3,89 (s, 3H) 2,98-2,85 (m, 1H), 2,69-2,56 (m, 1H), 2,44-2,31 (m, 1H), 2,06- 1,95 (m, 1H).
Ejemplo 103
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(1-metil-6-xo-1,6-dihidropiridin-3-
il)acetamida
A. 6-hidroxi-N-metoxi-N-metilnicotinamida. A una solución agitada de ácido 6-hidroxenicoténico (10 g, 45,24 mmol) en tetrahidrofurano (100 mL) se añadió EDC. HCl (13,01 g, 67,87 mmol), HOBT (10,39 g, 67,87 mmol), N,O-dimetilhidroxilamina HCl (5,29 g, 67,87 mmol), N,N-diisopropiletilamina (31,55 mL, 180,99 mmol) en secuencia y se agitó a temperatura ambiente durante 16 h. Se diluyó la mezcla de reacción con agua (100 mL) y se extrajo con acetato de etilo (3 X 500 mL). Se lavaron las capas orgánicas combinadas con salmuera (50 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna (sílice 100-200) usando metanol:diclorometano al 5% para proporcionar 6-hidroxi-N-metoxi-N-metilnicotinamida (8 g, 43,95 mmol, 96% de rendimiento). LCMS (ESI) m/z 183,0 [M+1]+.
B. N-metoxi-N,1-dimetil-6-oxo-1,6-dihidropiridina-3-carboxamida. A una solución agitada de 6-hidroxi-N-metoxi-N-metilnicotinamida (8 g, 43,95 mmol) en N,N-dimetilformamida se añadió yoduro de metilo (3,01 mL, 48,35 mmol), carbonato de potasio (18,19 g, 131,86 mmol) a temperatura ambiente y se agitó durante 3 h. Se diluyó la mezcla de reacción con agua (100 mL) y se extrajo con acetato de etilo (3 X 500 mL). Se lavaron las capas orgánicas combinadas con salmuera (50 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna (sílice 100-200) usando metanol:diclorometano al 4% para proporcionar N-metoxi-N,1-dimetil-6-oxo-1,6-dihidropiridina-3-carboxamida (6 g, 30,61 mmol, 69% de rendimiento). LCMS (ESI) m/z 197,29 [M+1]+.
C. 5-acetil-1-metilpiridin-2(1H)-ona. A una solución agitada de N-metoxi-N,1-dimetil-6-oxo-1,6-dihidropiridina-3-carboxamida (6 g, 30,61 mmol) en tetrahidrofurano seco (50 mL) se añadió metil-litio 1,6 M en éter dietílico (2,67 mL), a 0°C durante 3 h. Se inactivó la mezcla de reacción con solución de cloruro de amonio saturado y se extrajo con acetato de etilo (2 X 500 mL). Se lavaron las capas orgánicas combinadas con salmuera (50 mL), se secó sobre sulfato de sodio y se concentró Se purificó el residuo resultante por cromatografía en columna (sílice 100-200) usando metanol:diclorometano al 7-10% para proporcionar 5-acetil-1-metilpiridin-2(1H)-ona (4 g, 26,49 mmol, 86% de rendimiento). MS (ESI) m/z 152,14 [M+1]+.
D. 2-(1-metil-6-oxo-1,6-dihidropiridin-3-il)-2-oxoacetato de etilo. A una solución agitada de 5-acetil-1-metilpiridin-2(1H)-ona (4 g, 26,49 mmol) en piridina (50 mL) se añadió dióxido de selenio (7,35 g, 66,22 mmol) y se agitó durante 16 h a 100°C. Se diluyó la mezcla de reacción con diclorometano (50 mL) y se filtró a través de un lecho de Celite. Al filtrado se le añadió cloroformiato de etilo (12 mL) a 0°C y se agitó durante 2 h. A la mezcla de reacción resultante se le añadió agua (30 mL) y se extrajo con acetato de etilo (3 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 100 mL), salmuera (100 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna (sílice 100-200) usando 15-acetato de etilo en éter de petróleo al 20% para proporcionar2-(1-metil-6-oxo-1,6-dihidropiridin-3-il)-2-oxoacetato de etilo (2 g, 9,56 mmol, 36% de rendimiento). LCMS (ESI) m/z 210,29 [M+1]+.
E. 2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridin-3-il)acetato de etilo. A 2-(1-metil-6-oxo-1,6-dihidropiridin-3-il)-2-oxoacetato de etilo (2 g, 9,56 mmol) se le añadió trifluoruro de dietilamino azufre (3,2 mL, 23,92 mmol) y se agitó durante 12 h a temperatura ambiente. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 10 mL), salmuera (10 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridin-3-il)acetato de etilo (1 g, 4,32 mmol, 45%) como un líquido. LCMS (ESI) m/z 232,33 [M+1]+.
F. Ácido 2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridin-3-il)acético. A una solución agitada en frío (0°C) de 2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridin-3-il)acetato de etilo (1 g, 4,32 mmol) en mezcla de tetrahidrofurano:metanol:agua (30 mL, 1:1:1) se añadió hidróxido de litio (0,909 g, 21,64 mmol) y se agitó a temperatura ambiente durante 6 h. Se concentró la mezcla de reacción y se neutralizó el residuo con ácido clorhídrico acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X20 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridin-3-il)acético (500 g, 2,46 mmol, 56% de rendimiento) como un sólido blanquecino. LCMS (ESI) m/z 204,35
[M+1]+.
G. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridin-3-il)acetamida. A una solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(1 -metil-6-oxo-1,6-dihidropiridin-3-il)acético (196,6 mg, 0,968 mmol) en piridina se añadió cloruro de fosforilo (0,27 mL, 2,906 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A esta mezcla de reacción se le añadió clorhidrato de 3-(5-(aminometN)-1-oxoisoindoNn-2-il)piperidina-2,6-diona (300 mg, 0,968 mmol) y se agitó a temperatura ambiente durante 30 min. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua ( 2 X 10 mL), salmuera (10 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo resultante por cromatografía en columna Grace de fase inversa Reveleris C-18 usando acetonitrilo al 40-60% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1 -oxoisoindolin-5-il)metil)-2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridin-3-il)acetamida (60 mg, 0,131 mmol, 13% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 459,16 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 8 ppm 10,98 (s, 1 H), 9,58 (brt, J=5,85 Hz, 1 H), 8,05 (s, 1 H), 7,70 (d, J=7,68 Hz, 1 H), 7,58 - 7,35 (m, 3 H), 6,49 (d, J=9,50 Hz, 1 H), 5,11 (dd, J=13,16, 5,12 Hz, 1 H), 4,5-4,35 (m, 3 H), 4,35 -4,25 (d, 1H), 3,53 - 3,45 (s, 3H), 2,98-2,82 (m, 1 H), 2,67 - 2,52 (m, 1 H), 2,45 - 2,30 (m, 1 H), 2,05 - 1,95 (m, 1 H).
Ejemplo 104
2-(5-terc-butilpiridin-2-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida
A.5-bromopiridin-2-ilcarbamato de íerc-butilo. A una solución agitada en frío (0°C) de ácido 5-bromopiridin-2-amina (20 g, 116,30 mmol) en diclorometano (200 mL) se añadió trietilamina (34 mL, 255,87 mmol), dicarbonato de di-tercbutilo (35 mL, 151,19 mmol) seguido por 4-dimetilaminopiridina (1,4 g, 11,63 mmol) y se agitó a temperatura ambiente durante 2 h. Se inactivó la mezcla de reacción con agua y se extrajo con diclorometano (2 X 200 mL). Se lavaron las capas orgánicas combinadas con agua (200 mL), salmuera (200 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna con acetato de etilo en éter de petróleo al 5% como eluyente para proporcionar 5-bromopiridin-2-ilcarbamato de ferc-butilo (25,0 g, 91,91 mmol, 79% de rendimiento). LCMS (ESI) m/z 219,08 [M+1]+.
B. 5-terc-butilpiridin-2-ilcarbamato de íerc-butilo. A una solución agitada en frío (-78°C) de cianuro de cobre (33 g, 367,64 mmol) en tetrahidrofurano seco (1200 mL) se añadió cloruro de ferc-butilmagnesio (2,0 M en tetrahidrofurano) (362 mL, 735,29 mmol) lentamente y se agitó durante 1 h. A esta mezcla de reacción se le añadió 5-bromopiridin-2-ilcarbamato de ferc-butilo (25,0 g, 91,91 mmol) a -78°C, se agitó durante 2 h y se dejó en agitación a temperatura ambiente durante 16 h. Se inactivó la mezcla de reacción con solución de cloruro de amonio acuosa y se extrajo con acetato de etilo (3 X 200 mL). Se lavaron las capas orgánicas combinadas con agua (200 mL), salmuera (200 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna con el eluyente de acetato de etilo en éter de petróleo al 10% para proporcionar ferc-butil 5-ferc-butilpiridin-2-ilcarbamato (15,0 g, 60,00 mmol, 65% de rendimiento). LCMS (ESI) m/z 251,48 [M+1]+.
C.2-bromo-5-íerc-butilpiridina. A una solución agitada en frío (0°C) de 5-terc-butilpiridin-2-ilcarbamato de ferc-butilo (13,0 g, 52,00 mmol) en ácido bromhídrico acuoso (150 mL) se añadió nitrito de sodio (9,3 g, 135,2 mmol) lentamente y se agitó durante 15 min. A esta mezcla de reacción se le añadió bromo líquido (8,0 mL, 156,00 mmol) y se agitó a temperatura ambiente durante 4 h. Se inactivó la mezcla de reacción con solución de hidróxido de sodio acuosa y se extrajo con acetato de etilo (3 X 150 mL). Se lavaron las capas orgánicas combinadas con agua (100 mL), salmuera (100 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna con el eluyente de acetato de etilo en éter de petróleo al 5% para proporcionar 2-bromo-5-terc-butilpiridina (3,2 g, 15,02 mmol, 29% de rendimiento). LCMS (ESI) m/z 214,11 [M+1]+.
D. 5-íerc-butil-2-yodopiridina. A una solución agitada de 2-bromo-5-terc-butilpiridina (3,2 g, 15,02 mmol) en 1,4-dioxano (10 mL) se añadió yoduro de sodio (4,5 g, 30,04 mmol), yoduro de cobre (145 mg, 0,75 mmol), trans-N,N'dimetilcidohexano-1,2-diamina (235 mg, 1,65 mmol) a temperatura ambiente y se agitó a 100°C durante 16 h en tubo sellado. Se inactivó la mezcla de reacción con agua (100 mL) y se extrajo con acetato de etilo (3X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 5-terc-butil-2-yodopiridina (3,5 g, 13,40 mmol, 89% de rendimiento). GCMS (m/z) 261,0.
E. 2-(5-ferc-butilpiridm-2-il)-2,2-difluoroacetato de etilo. A una solución agitada de 5-terc-butil-2-yodopiridina (3,5 g, 13,40 mmol) en dimetilsulfóxido (30 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (5,4 g, 26,81 mmol) seguido por cobre (2,2 g, 34,86 mmol) y se agitó a 55°C durante 5 h. Se inactivó la mezcla de reacción con solución de cloruro de amonio acuosa y se extrajo con acetato de etilo (3 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (100 mL), salmuera (100 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 2-(5-tercbutilpiridin-2-il)-2,2-difluoroacetato de etilo (2,8 g, 10,89 mmol, 81% de rendimiento). LCMS (ESI) m/z 258,17 [M+1]+.
F. Ácido 2-(5-ferc-butilpiridm-2-il)-2,2-difluoroacético. A una solución agitada de 2-(5-terc-butilpiridin-2-il)-2,2-difluoroacetato de etilo (2,8 g, 10,89 mmol) en mezcla de metanol-tetrahidrofurano-agua (15 mL, 1:1:1) se añadió hidróxido de litio monohidratado (1,4 g, 32,68 mmol) y se agitó a temperatura ambiente durante 2 h. Se diluyó la mezcla de reacción con agua (50 mL) y se acidificó con solución de bisulfato de potasio acuoso y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con salmuera (50 mL), se secó sobre sulfato de sodio, se filtró se concentró para proporcionar ácido 2-(5-terc-butilpiridin-2-il)-2,2-difluoroacético (2,0 g, 8,73 mmol, 80% de rendimiento). LCMS (ESI) m/z 230,32 [M+1]+.
G. 2-(5-terc-butilpiridin-2-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. A una solución agitada en frío (0°C) de ácido 2-(5-terc-butilpiridin-2-il)-2,2-difluoroacético (2,0 g, 8,73 mmol (300 mg, 1,31 mmol) en piridina (5 mL) se añadió cloruro de fosforilo (0,4 mL, 3,87 mmol) gota a gota y se agitó a 0-5°C durante 1 h, y a continuación se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (404 mg, 1,31 mmol) y se agitó a temperatura ambiente durante 1 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 30 mL), salmuera (30 mL) y se secó sobre sulfato de sodio y se concentró para proporcionar 2-(5-tercbutilpiridin-2-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (75 mg, 0,15 mmol, 12% de rendimiento) como un sólido blanquecino. LCMS (ESI) m/z 485,17 [M+1]+. 1H RMN (400MHz, DMSO-d6) 8 = 10,98 (br s, 1H), 9,62 (brt, J=6,1 Hz, 1H), 8,78 (d, J=24 Hz, 1H), 8,02 (dd, J=2,4, 8,3 Hz, 1H), 7,71 (dd, J=2,2, 8,1 Hz, 1H), 7,52 (s, 1H), 7,46 (d, J=7,8 Hz, 1H), 5,11 (dd, J=4,9, 13,2 Hz, 1H), 4,53-4,28 (m, 4H), 2,99 - 2,84 (m, 1H), 2,69-2,55 (m, 1H), 2,45 - 2,30 (m, 1H), 2,06 - 1,94 (m, 1H), 1,35 (s, 9H).
Ejemplo 105
2-(5-ciclopropilpiridin-2-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida
A. 5-ciclopropilpiridin-2-amina. A una solución agitada y desgasificada de 5-bromopiridin-2-amina (5 g, 28,90 mmol) en mezcla de agua: tolueno 10% (100 mL) se añadió ácido ciclopropilborónico (3,73 g, 43,35 mmol) seguido por fosfato de potasio (12,25 g, 57,80 mmol), triciclohexilfosfina (794 mg, 2,89 mmol) y se siguió desgasificando durante 10 min. A continuación, se añadió acetato de paladio(II) (650 mg, 2,89 mmol), se desgasificó durante 10 min adicionales y se calentó a 110°C durante 3 h. Se enfrió la mezcla de reacción a temperatura ambiente y se filtró a través del lecho de celite. Al filtrado se le añadió agua fría (100 mL) y se extrajo con acetato de etilo (3 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 100 mL), salmuera (100 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 5-ciclopropilpiridin-2-amina (3,0 g, 22,39 mmol, 77% de rendimiento). GCMS (m/z) 134,1 [M]+.
B. 2-bromo-5-ciclopropilpiridina. A una solución agitada en frío (0°C) de 5-ciclopropilpiridin-2-amina (3,0 g, 22,39 mmol) en bromhídrico acuoso (25 mL) al 47% se le añadió una solución de nitrito de sodio (4,0 g, 58,21 mmol) y se agitó a la misma temperatura durante 30 min. A esta mezcla de reacción se le añadió a continuación bromo (10,75 g, 67,16 mmol) y se agitó a temperatura ambiente durante 2 h. Se vertió la mezcla de reacción en agua (100 mL) y se extrajo con acetato de etilo (3 X 100 mL). Se lavaron las capas orgánicas combinadas con salmuera (100 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna combinada,
usando 15-acetato de etilo en éter de petróleo al 20% para proporcionar 2-bromo-5-ciclopropilpiridina (1,2 g, 6,09 mmol, 27% de rendimiento). GCMS (m/z) 197,0 [M]+.
C. 5-ciclopropil-2-yodopiridina. A una solución agitada de 2-bromo-5-ciclopropilpiridina (1,2 g, 6,09 mmol) en 1,4 dioxano (25 mL) se añadió yoduro de sodio (1,83 g, 12,18 mmol), yoduro de cobre (58 mg, 0,30 mmol), trans-N,N'-dimetilciclohexano-1,2-diamina (95 mg, 0,67 mmol) a temperatura ambiente y se agitó a 110°C durante 16 h. Se inactivó la mezcla de reacción con agua (100 mL) y se extrajo con acetato de etilo (3 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 100 mL), salmuera (100 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 5-ciclopropil-2-yodopiridina (1,2 g, 4,90 mmol, 81%). GCMS (m/z) 245,0[M]+.
D. 2-(5-ciclopropilpiridin-2-il)-2,2-difluoroacetato de etilo. A una solución agitada de 5-ciclopropil-2-yodopiridina (1,2 g, 4,90 mmol) en dimetilsulfóxido (12 mL) se añadió cobre (809 mg, 12,73 mmol) y 2-bromo-2,2-difluoroacetato de etilo (1,48 g, 7,35 mmol) a temperatura ambiente y se agitó a 55°C durante 2 h. A la mezcla de reacción se añadió solución de cloruro de amonio saturada acuosa (50 mL) y se extrajo con acetato de etilo (2 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 100 mL), salmuera (100 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-(5-ciclopropilpiridin-2-il)-2,2-difluoroacetato de etilo (1,0 g, 4,15 mmol, 85%). 1H RMN (400MHz, CDCla) 88,44 (br s, 1H), 7,61(br s, 1H), 7,43 (d, J=8,0 Hz, 1H), 4,42 - 4,30 (m, 2H), 2,04 - 1,91 (m, 1H), 1,40 - 1,24 (m, 3H), 1,12 -1,09 (m, 2H), 0,84 - 0,77 (m, 2H).
E. Ácido 2-(5-ciclopropilpiridin-2-il)-2,2-difluoroacético. A una solución agitada de 2-(5-ciclopropilpiridin-2-il)-2,2-difluoroacetato de etilo (1,0 g, 4,15 mmol) en mezcla de tetrahidrofurano:metanol:agua (30 mL, 1:1:1) se añadió hidróxido de litio monohidratado (523 mg, 12,45 mmol) y se agitó a temperatura ambiente durante 4 h. Se concentró la mezcla de reacción y se neutralizó el residuo con bisulfato de potasio saturado (25 mL) y se extrajo con acetato de etilo (2 X 50 mL). Se lavaron las capas orgánicas combinadas con salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2-(5-ciclopropilpiridin-2-il)-2,2-difluoroacético (500 mg, 2,35 mmol, 50% de rendimiento). MS (ESI) m/z 214,3 [M-1]-ve.
F. 2-(5-ciclopropilpiridin-2-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. A una solución agitada en frío (0°C) de ácido 2-(5-ciclopropilpiridin-2-il)-2,2-difluoroacético (300 mg, 1,41 mmol) en piridina (20 mL) se añadió cloruro de fosforilo (646 mg, 4,22 mmol) gota a gota y se agitó a 0-5°C durante 30 min. A esta mezcla de reacción se añadió a continuación clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (435 mg, 1,41 mmol) y se agitó a temperatura ambiente durante 1 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio saturado acuoso (hasta pH-8) y se extrajo con acetato de etilo (2 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (100 mL), salmuera (100 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 60-65% en ácido fórmico acuoso (0,1%) para proporcionar 2-(5-ciclopropilpiridin-2-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (140 mg, 0,30 mmol, 21% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 469,06 [M+1]+. 1H RMN (400MHz, DMSO-d6) 810,99 (s, 1H), 9,58 (t, J=6,1 Hz, 1H), 8,53 (s, 1H), 7,71 (d, J=7,8 Hz, 1H), 7,66 - 7,60 (m, 2H), 7,51 (s, 1H), 7,46 (d, J=8,3 Hz, 1H), 5,11 (dd, J=4,9, 13,2 Hz, 1H), 4,56-4,28 (m, 4H), 3,08 - 2,85 (m, 1H), 2,67 - 2,56 (m, 1H), 2,45 - 2,32 (m, 1H), 2,10 - 1,96 (m, 2H), 1,13-1,03 (m, 2H), 0,89 -0,79 (m, 2H).
Ejemplo 106
N-((2-(2,6-diozopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-isopropoxipiridin-2-il)acetamida
A. 2-bromo-5-isopropoxipiridina. A una solución agitada de 6-bromopiridin-3-ol (2 g, 11,49 mmol) en N,N-dimetilformamida (20 mL) se añadió 2-yodopropano (1,4 mL, 13,79 mmol), carbonato de potasio (4,7 g, 34,47 mmol) y se agitó a 80°C durante 6 h. Se inactivó la mezcla de reacción con agua y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 20 mL), salmuera (20 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-bromo-5-isopropoxipiridina (1,4 g, 6,48 mmol, 58%) como un sólido amarillo claro. MS (ESI) m/z 216,20
B. 2-yodo-5-isopropoxipiridina. A una solución agitada de 2-bromo-5-isopropoxipiridina (1,4 g, 6,48 mmol) en 1,4-dioxano (30 mL) en un tubo sellado, se añadió yoduro de sodio (1,9 g, 12,96 mmol), yoduro de cobre (61 mg, 0,32 mmol), trans-N,N'-dimetilciclohexano-1,2-diamina (101 mg, 0,71 mmol) a temperatura ambiente y se agitó a 110°C durante 16 h. Se inactivó la mezcla de reacción con agua (30 mL) y se extrajo con acetato de etilo (3 X 30 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 20 mL), salmuera (20 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-yodo-5-isopropoxipiridina (1 g, 3,83 mmol, 58% de rendimiento) como un sólido marrón. GCm S (m/z) 263,0.
C.2,2-difluoro-2-(5-isopropoxipiridin-2-il)acetato de etilo. A una solución agitada de 2-yodo-5-isopropoxipiridina (1 g, 3,80 mmol) en dimetilsulfóxido (10 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (1 mL, 7,60 mmol), cobre (0,6 g, 10,09 mmol) y se agitó durante 16 h a 50°C. Se neutralizó la mezcla de reacción con solución de cloruro de amonio saturada acuosa y se extrajo con acetato de etilo (3 X 40 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 20 mL), salmuera (20 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(5-isopropoxipiridin-2-il)acetato de etilo (500 mg, 2,30 mmol, 60%) como un líquido marrón. MS (m/z) 259,1.
D. Ácido 2,2-difluoro-2-(5-isopropoxipiridin-2-il)acético. A una solución agitada en frío (0°C) de 2,2-difluoro-2-(5-isopropoxipiridin-2-il)acetato (500 mg, 2,32 mmol) en mezcla de metanol/tetrahidrofurano/agua (9 mL, 1:1:1) se añadió hidróxido de litio monohidratado (280 mg, 6,91 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con bisulfato de potasio acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 30 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio, se concentró para proporcionar ácido 2,2-difluoro-2-(5-isopropoxipiridin-2-il)acético (350 mg, 1,51 mmol, 79% de rendimiento) como un semisólido marrón. MS (ESI) m/z 232,24
E. N-((2-(2,6-dioxopiperldin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-isopropoxipiridin-2-il)acetamida. A una solución agitada en frío (0°C) de clorhidrato de 3-(6-((metilamino)metil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (400 mg, 1,29 mmol) y ácido 2,2-difluoro-2-(5-isopropoxipiridin-2-il)acético (300 mg, 1,29 mmol) en N,N-dimetilformamida (20 mL) se añadió N,N-diisopropiletilamina (0,7 mL, 3,86 mmol) seguido por 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metileno]-1H-1,2,3-triazolo[4,5-b]piridinio (735 mg, 1,93 mmol) y se agitó a temperatura ambiente durante 16 h. Se diluyó la mezcla de reacción con agua (70 mL) y se extrajo con acetato de etilo (2 X 40 mL). Se lavaron las capas orgánicas combinadas con salmuera (30 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por columna de fase inversa Reveleris C-18 usando acetonitrilo al 58% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-isopropoxi piridin-2-il)acetamida (70 mg, 0,14 mmol, 11% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 487,20 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 810,99 (s, 1H), 9,55 (brt, J=6,1 Hz, 1H), 8,36 (d, J=2,6 Hz, 1H), 7,76-7,66 (m, 2H), 7,60-7,50 (m, 2H), 7,45 (d, J=8,1 Hz, 1H), 5,11 (dd, J=4,8, 13,2 Hz, 1H), 4,80-4,75 (m, 1H), 4,65 - 4,26 (m, 4H), 3,02 - 2,83 (m, 1H), 2,75 - 2,54 (m, 1H), 2,46 - 2,305 (m, 1H), 2,06 - 1,94 (m, 1H), 1,31 (m, 6H).
Ejemplo 107
2-(5-bromopiridin-2-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida
A.2-(5-bromopiridin-2-il)-2,2-difluoroacetato de etilo. A una solución agitada de 5-bromo-2-yodopiridina (3 g, 10,56 mmol) en dimetilsulfóxido (20 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (3,13 g, 15,84 mmol) seguido por polvo de cobre (1,74 g, 27,46 mmol) a temperatura ambiente y se agitó a 55°C durante 6 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3 X 20 mL). Se lavaron las capas orgánicas combinadas con agua (20 mL), salmuera (20 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el producto en bruto obtenido por cromatografía en columna sobre gel de sílice (acetato de etilo en éter de petróleo al 20%) para proporcionar 2-(5-bromopiridin-2-il)-2,2-difluoroacetato de etilo (1,5 g, 5,35 mmol, 60%) como un líquido incoloro. MS (ESI) m/z 280,2 [M+1]+.
B. Ácido 2-(5-bromopiridin-2-il)-2,2-difluoroacético. A una solución agitada de 2-(5-bromopiridin-2-il)-2,2-difluoroacetato de etilo (1,5 g, 5,37 mmol) en mezcla de tetrahidrofurano: metanol:agua (15 mL, 1:1:1) se añadió hidróxido de litio monohidratado (677 mg, 16,13 mmol) y se agitó a temperatura ambiente durante 4 h. Se extrajeron los productos volátiles a presión reducida y se disolvió el producto en bruto resultante en agua (15 mL), se lavó con acetato de etilo ( 2X10 mL). Se acidificó la capa acuosa con solución acuosa de clorhidrato 1 N y se extrajo con acetato de etilo (3 X 15 mL). Se lavaron las capas orgánicas combinadas con salmuera (15 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2-(5-bromopiridin-2-il)-2,2-difluoroacético (900 mg, 3,57 mmol, 69% de rendimiento) como un compuesto semisólido. MS (ESI) m/z 252,2 [M+H]+.
C.2-(5-bromopiridin-2-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. A una solución en frío de ácido 2-(5-bromopiridin-2-il)-2,2-difluoroacético (243 mg, 0,97 mmol) en piridina (6 mL) se añadió oxicloruro de fósforo (1,8 mL, 2,9 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A continuación, se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) y se agitó a temperatura ambiente durante 2 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada y se extrajo con acetato de etilo (3X15 mL). Se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 (acetonitrilo al 50-55% en ácido fórmico acuoso al 0,1% (para proporcionar 2-(5-bromopiridin-2-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (33 mg, 0,065 mmol, 7% de rendimiento) como un sólido blanco. MS (ESI) m/z 507,8 [M+1]+. 1H RMN (400 MHz, DMSO-d6) 810,99 (s, 1H), 9,68 (t, J = 4,5 Hz, 1H), 8,89 (d, J =1,6 Hz, 1H), 8,31 (dd, J = 8,4, 2,4 Hz, 1H), 7,78 (d, J = 8,4 Hz, 1H), 7,72 (d, J = 8,0 Hz, 1H), 7,49 (s, 1H), 7,44 (d, J = 8,0 Hz, 1H), 5,11 (dd, J = 13,2, 5,2 Hz, 1H), 4,50 (d, J = 6,4 Hz, 2H), 4,46 (d, J = 17,9 Hz, 1H), 4,32 (d, J = 17,6 Hz, 1H), 2,95 - 2,87 (m, 1H), 2,66 - 2,55 (m, 1H), 2,45 - 2,30 (m, 1H), 2,05 - 1,96 (m, 1H).
Ejemplo 108
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluoro-2-(trifluorometoxi)fenil)acetamida
A. (2-fluoro-6-(trifluoroinetoxi)fenil)trimetilsilano. A una solución agitada en frío (-78°C) de 1-fluoro-3-(trifluorometoxi)benceno (2,0 g, 11,11 mmol) y TMEDA (1,3 mL, 11,11 mmol) en tetrahidrofurano seco (20 mL) se añadió sec-butil-litio (1,4 M en ciclohexano, 8 mL) y se agitó durante 2 h. A esta mezcla de reacción se le añadió cloruro de trimetilsililo (1,81 g, 16,66 mmol) a -78°C y se agitó durante 1 h a temperatura ambiente. Se inactivó la mezcla de reacción con solución de cloruro de amonio acuosa y se extrajo con éter dietílico (2 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar (2-fluoro-6-(trifluorometoxi)fenil)trimetilsilano (1,8 g, 7,14 mmol, 64% de rendimiento). 1H RMN (400MHz, CDCla) 8 (ppm) 7,35 (dt, J=6,6, 8,2 Hz, 1H), 7,05 - 7,00 (m, 1H), 6,92 (t, J=8,3 Hz, 1H), 0,41 - 0,33 (m, 9H).
B. (6-fluoro-3-yodo-2-(trifluorometoxi)fenil)trimetilsilano. A una solución agitada en frío (-78°C) de 2,2,6,6-tetrametilpiperidina (897 mg, 6,34 mmol) en tetrahidrofurano seco (20 mL) se añadió n-butil-litio (2,5 M en n-hexano, 2,5 mL, 6,34 mmol) lentamente, seguido por (2-fluoro-6-(trifluorometoxi)fenil)trimetilsilano (1,6 g, 6,34 mmol) en tetrahidrofurano (5 mL) y se agitó durante 2 h a la misma temperatura. Se añadió yodo (2,4 g, 9,52 mmol) en tetrahidrofurano seco (10 mL) a esta mezcla de reacción a -78°C y se dejó en agitación a 0°C durante 1 h. Se inactivó la mezcla de reacción con solución de cloruro de amonio acuosa y se extrajo con éter dietílico (2 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar (6-fluoro-3-yodo-2-(trifluorometoxi)fenil)trimetilsilano (2,0 g, 5,29 mmol, 84% de rendimiento). GCMS (m/z) 378,1.
C. 2,2-difluoro-2-(4-fluoro-2-(trifluorometoxi)fenil)acetato de etilo. A una solución agitada de (6-fluoro-3-yodo-2
(trifluorometoxi)fenil)trimetilsilano (2,0 g, 5,29 mmol) en dimetilsulfóxido (30 mL) en tubo sellado se añadió 2-bromo-2,2-difluoroacetato de etilo (2,1 g, 10,58 mmol) seguido por cobre (874 mg, 13,76 mmol) y se agitó a 55°C durante 16 h. Se inactivó la mezcla de reacción con solución de cloruro de amonio acuosa y se extrajo con acetato de etilo (3 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (100 mL), salmuera (50 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 2,2-difluoro-2-(4-fluoro-2-(trifluorometoxi)fenil)acetato de etilo (1,5 g, 4,96 mmol, 94% de rendimiento). GCMS (m/z) 302,1.
D. Ácido 2,2-difluoro-2-(4-fluoro-2-(trifluorometoxi)fenil)acético. A una solución agitada de 2,2-difluoro-2-(4-fluoro-2-(trifluorometoxi)fenil)acetato de etilo (1,5 g, 4,96 mmol) en mezcla de metanol: tetrahidrofurano:agua (15 mL, 1:1:1) se añadió hidróxido de litio monohidratado (1,4 g, 14,90 mmol) y se agitó a temperatura ambiente durante 2 h. Se diluyó la mezcla de reacción con agua (50 mL), se acidificó con solución de bisulfato de potasio acuosa y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con salmuera (50 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar ácido 2,2-difluoro-2-(4-fluoro-2-(trifluorometoxi)fenil)acético (1,0 g, 3,64 mmol, 73% de rendimiento). LCMS (ESI) m/z 273,26 [M-1]-.
E. N-((2-(2,6-dioxopiperldm-3-M)-1-oxoisomdoMn-5-M)metNo-2,2-difluoro-2-(4-fluoro-2-(trifluorometoxi)fenil)acetamida. A una solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(4-fluoro-2-(trifluorometoxi)fenil)acético (300 mg, 1,09 mmol) en piridina (5 mL) se añadió cloruro defosforilo (0,3 mL, 3,28 mmol) gota a gota y se agitó a 0-5°C durante 1 h. Se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (338 mg, 1,09 mmol) a esta mezcla de reacción y se agitó a temperatura ambiente durante 1 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 30 mL), salmuera (30 mL) y se secó sobre sulfato de sodio y se concentró para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1 -oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluoro-2-(trifluorometoxi)fenil)acetamida (37 mg, 0,06 mmol, 6% de rendimiento) como un sólido blanquecino. LCMS (ESI) m/z 530,07 [M+1]+. 1H RMN (300MHz, DMSO-d6) 8 (ppm) 10,98 (s, 1H), 9,78 (brt, J=5,9 Hz, 1H), 7,82 (t, J=8,6 Hz, 1H), 7,71 (d, J=8,1 Hz, 1H), 7,63 (brd, J=11,4 Hz, 1H), 7,51 -7,38 (m, 3H), 5,11 (br dd, J=5,1, 13,2 Hz, 1H), 4,56 - 4,40 (m, 3H), 4,31 (d, J=17,6 Hz, 1H), 3,00 - 2,83 (m, 1H), 2,66 - 2,54 (m, 1H), 2,44 - 2,30 (m, 1H), 2,08 - 1,93 (m, 1H).
Ejemplo 109
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluorociclohexil)acetamida
A. 8-fluoro-1,4-oxaspiro[4,5]dec-7-eno. A una solución agitada de 1,4-dioxaspiro[4,5]decan-8-ona (12 g, 76,92 mmol) en piridina (120 mL) se añadió trifluoruro de dietilamino azufre (37 g, 230 mmol) a 0°C y se agitó a temperatura ambiente durante 48 h. Se inactivó la mezcla de reacción con solución de bicarbonato de sodio acuosa y se extrajo con acetato de etilo (3 X 100 mL). Se lavaron las capas orgánicas combinadas con salmuera (100 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto obtenido por cromatografía en columna (gel de sílice 100-200, acetato de etilo en éter de petróleo al 10%) para proporcionar 8-fluoro-1,4-dioxaspiro[4,5]dec-7-eno (6,5 g, 41 mmol, 54% de rendimiento) como un líquido incoloro. MS (ESI) m/z 158,1 [M]+
B. 8-fluoro-1,4-dioxaspiro[4,5]decano. A una solución agitada de 8-fluoro-1,4-dioxaspiro[4,5]dec-7-eno (1 g, 3,53 mmol) en acetato de etilo (15 mL) se añadió una suspensión espesa de paladio al 10% sobre carbón (200 mg) en acetato de etilo bajo vapor de nitrógeno. Se agitó la mezcla de reacción a temperatura ambiente durante 4 h en atmósfera de hidrógeno. Se evacuó la atmósfera de hidrógeno y se filtró la mezcla de reacción a través de un lecho de Celite, se concentró el filtrado para proporcionar 8-fluoro-1,4-dioxaspiro[4,5]decano (500 mg, 1,3 mmol, 37% de rendimiento) como un líquido incoloro. MS (ESI) m/z 160,1 [M]+.
C. 4-fluorociclohexanona. A una solución agitada de 8-fluoro-1,4-dioxaspiro[4,5]decano (3,5 g, 21,87 mmol) en tetrahidrofurano (20 mL) se añadió 20 mL de ácido clorhídrico acuoso 4 N a 0°C y se agitó a temperatura ambiente durante 6 h. Se diluyó la mezcla de reacción con agua (10 mL) y se basificó con solución de bicarbonato de sodio acuosa y se extrajo con acetato de etilo (3 X 30 mL). Se lavaron las capas orgánicas combinadas con agua (30 mL), salmuera (30 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 4-fluorociclohexanona (1,2 g, 10,34
mmol, 48% de rendimiento) como un líquido incoloro. MS (ESI) m/z 116,1 [M]+
D. 2,2-difluoro-2-(4-fluoro-1-hidroxiciclohexil)acetato de etilo. A una solución agitada de 4-fluorociclohexanona (1,6 g, 13,7 mmol) en tetrahidrofurano (20 mL) se añadió cloruro de cerio (III) heptahidratado (340 mg 1,37 mmol) seguido por cinc (1,07 g, 16,55 mmol) y 2-bromo-2,2-difluoroacetato de etilo (3,35 g, 16,55 mmol) a 0°C y se agitó a temperatura ambiente durante 16 h. Se diluyó la mezcla de reacción con agua (20 mL) y se extrajo con acetato de etilo (3 X 20 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secaron sobre sulfato de sodio anhidro, se filtraron y se concentraron. Se purificó el producto en bruto obtenido por cromatografía instantánea (acetato de etilo en éter de petróleo al 30%) para proporcionar 2,2-difluoro-2-(4-fluoro-1-hidroxiciclohexil)acetato de etilo (1,1 g, 4,58 mmol, 34% de rendimiento) como un líquido incoloro. 1H RMN (300 MHz, DMSO-d6) 85,60 (s, 1H), 4,83 (dt, J = 49,2, 2,7 Hz, 1H), 4,29 (q, J = 7,2 Hz, 2H), 1,82 - 1,64 (m, 8H), 1,26 (t, J = 7,0 Hz, 3H).
E. 2,2-difluoro-2-(4-fluorociclohex-1-enil)acetato de etilo. A una solución agitada de 2,2-difluoro-2-(4-fluoro-1-hidroxiciclohexil)acetato de etilo (0,75 g, 3,12 mmol) en piridina (22,6 mL) se añadió cloruro de tionilo (3,72 g, 31,25 mmol) a 0°C y se agitó a temperatura ambiente durante 16 h. Se diluyó la mezcla de reacción con agua (10 mL), se basificó con solución de bicarbonato de sodio acuosa y se extrajo con acetato de etilo (3 X 15 mL). Se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto obtenido por cromatografía en columna sobre gel de sílice (acetato de etilo en éter de petróleo al 5%) para proporcionar 2,2-difluoro-2-(4-fluorociclohex-1-enil)acetato de etilo (0,3 g, 1,35 mmol, 43% de rendimiento) como un líquido incoloro. MS (ESI) m/z 221,9 [M]+.
F. 2,2-difluoro-2-(4-fluorociclohexil)acetato de etilo. A una solución agitada de 2,2-difluoro-2-(4-fluorociclohex-1-enil)acetato de etilo (200 mg, 0,9 mmol) en acetato de etilo (10 mL) se añadió una suspensión espesa de óxido de platino al 10% (20 mg) en acetato de etilo bajo corriente de nitrógeno. Se agitó la mezcla de reacción bajo una presión de hidrógeno de 60 psi a temperatura ambiente durante 16 h. Se evacuó la atmósfera de hidrógeno y se filtró la mezcla de reacción se filtró a través de un lecho de Celite, se filtró y se concentró para proporcionar 2,2-difluoro-2-(4-fluorociclohexil)acetato de etilo (100 mg, 0,44 mmol, 50% de rendimiento) como un líquido incoloro. 1H RMN (300 MHz, CDCla) 84,83 (dt, J = 49,2, 2,7 Hz, 1H), 4,34 (q, J = 7,2 Hz, 2H), 2,16 - 1,98 (m, 4H), 1,70 - 1,57 (m, 4H), 1,51 - 1,41 (m, 1H), 1,26 (t, J = 6,6 Hz, 3H).
G. Ácido 2,2-difluoro-2-(4-fluorociclohexil)acético. A una solución agitada de 2,2-difluoro-2-(4-fluorociclohexil)acetato de etilo (100 mg, 0,446 mmol) en mezcla de tetrahidrofurano: metanol: agua (6 mL, 1:1:1) se añadió hidróxido de litio monohidratado (56 mg, 1,34 mmol) y se agitó a temperatura ambiente durante 4 h. Se extrajeron los productos volátiles a presión reducida y se disolvió el producto en bruto obtenido en agua (5 mL), se lavó con acetato de etilo (2 X 5 mL). Se acidificó la capa acuosa con solución acuosa de clorhidrato 1 N y se extrajo con acetato de etilo (3 X 5 mL). Se lavaron las capas orgánicas combinadas con salmuera (5 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar ácido 2,2-difluoro-2-(4-fluorociclohexil)acético (50 mg, 0,255 mmol, 59% de rendimiento) como un compuesto semisólido. 1H RMN (300 MHz, CDCla) 84,82 (dt, J = 42,2, 6,6 Hz, 1H), 2,18-1,20 (m, 10H).
H. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluorociclobexil)acetamida. A una solución enfriada con hielo de ácido 2,2-difluoro-2-(4-fluorociclohexil)acético (190 mg, 0,97 mmol) en piridina (9 mL) se añadió oxicloruro de fósforo (445 mg, 2,91 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A continuación, se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona en la mezcla de reacción y se agitó a temperatura ambiente durante 2 h. Se basificó la mezcla de reacción con bicarbonato de sodio saturado acuoso y se extrajo con acetato de etilo (3X15 mL). Se lavaron las capas orgánicas combinadas con salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 (acetonitrilo al 50-55% en ácido fórmico acuoso al 0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluorociclohexil)acetamida (33 mg, 0,073 mmol, 7% de rendimiento) como un sólido blanco. MS (ESI) m/z 452,15 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 810,98 (s, 1H), 9,56 (t, J = 5,6 Hz, 1H), 7,70 (d, J =8,1 Hz, 1H), 7,47 (s, 1H), 7,41 (d, J = 8,1 Hz, 1H), 5,11 (dd, J =13,2, 5,4 Hz, 1H), 4,84 (d, J = 48,6 Hz, 1H), 4,45 (d, J =17,1 Hz, 1H), 4,44(d, J = 6,3 Hz, 2H), 4,31 (d, J = 17,4 Hz, 1H), 2,96-2,72 (m, 1H), 2,62 - 2,51 (m, 1H), 2,40 - 2,21 (m, 2H), 2,07 - 1,90 (m, 4H), 1,62 -1,41 (m, 6H).
Ejemplo 110
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-(metilsulfonil)fenil)acetamida
A. 1-yodo-4-(metilsulfonil)benceno. A una solución agitada de 1-bromo-4-(metilsulfonil)benceno (2 g, 8,506 mmol) en 1,4-dioxano (15 mL) se añadió yoduro de sodio (2,55 g, 17,01 mmol), yoduro de cobre (80 mg, 0,42 mmol), trans-N,N'-dimetilciclohexano-1,2-diamina (133 mg, 0,93 mmol) a temperatura ambiente y se agitó a 110°C durante 16 h en tubo sellado. Se inactivó la mezcla de reacción con agua (50 mL) y se extrajo con acetato de etilo (3 X 200 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 1-yodo-3-(metilsulfonil)benceno (1,8 g, 6,38 mmol, 75% de rendimiento) como un sólido marrón. LCMS (ESI) m/z 283,16 [M+H]+.
B. 2,2-difluoro-2-(4-(metilsulfonil)fenil)acetato de etilo. A una solución agitada de 1-yodo-4-(metilsulfonil)benceno (500 mg, 1,77 mmol) en dimetilsulfóxido (5 mL) se añadió 2-yodo-2,2-difluoroacetato de etilo (0,32 mL, 2,313 mmol), cobre (107 mg, 1,68 mmol) y se agitó durante 16 h a temperatura ambiente. Se neutralizó la mezcla de reacción con solución de cloruro de amonio saturada acuosa y se extrajo con acetato de etilo (2 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo resultante con gel de sílice (malla 100-200, acetato de etilo al 20% en hexanos) para proporcionar para proporcionar 2,2-difluoro-2-(4-(metilsulfonil)fenil)acetato de etilo (250 mg, 0,899 mmol, 50%) como un sólido blanquecino. MS (ESI) m/z 279,26 [M+1]+.
C. Ácido 2,2-difluoro-2-(4-(metilsulfonil)fenil)acético. A una solución agitada en frío (0°C) de 2,2-difluoro-2-(4-(metilsulfonil)fenil)acetato de etilo (250 mg, 0,899 mmol) en metanol/tetrahidrofurano/agua (6 mL, 1:1:1) se añadió hidróxido de litio monohidratado (75 mg, 0,798 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con bisulfato de potasio acuoso al 10% (10 mL) y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(4-(metilsulfonil)fenil)acético (180 mg, 0,72 mmol, 80% de rendimiento) como un sólido gomoso. MS (ESI) m/z 249,26 [M-1]+.
D. N-((2-(2,dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-(metilsulfonil)fenil)acetamida. A una solución agitada en frío (0°C) de ácido 22,2-difluoro-2-(4-(metilsulfonil)fenil)acético (194 mg, 0,776 mmol) en piridina (10 mL) se añadió cloruro de fosforilo (0,18 mL, 1,94 mmol) gota a gota y se agitó a 0-5°C durante 30 min. A esto se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (200 mg, 0,64 mmol) y se agitó a temperatura ambiente durante 2 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo resultante por cromatografía en columna Grace usando ACN al 52% en solución de ácido fórmico acuoso al 0,1% como eluyente para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1 -oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-(metilsulfonil)fenil)acetamida (70 mg, 0,138 mmol, 21% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 506,06 [M+1]+. 1H RMN (400MHz, DMSO-d6) 810,98 (s, 1H), 9,78 (brt, J=6,1 Hz, 1H), 8,11 (d, J=8,3 Hz, 2H), 7,88 (d, J=8,3 Hz, 2H), 7,69 (d, J=7,8 Hz, 1H), 7,42 - 7,34 (m, 2H), 5,10 (dd, J=4,9, 13,2 Hz, 1H), 4,53-4,37 (m, 3H), 4,28 (d, J=17,2 Hz, 1H), 3,29 (s, 3H), 2,98-2,87 (m, 1H), 2,68-2,55 (m, 1H), 2,46-2,31 (m, 1H), 2,06- 1,94 (m, 1H).
Ejemplo 111
N-(2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(metilsulfonil)fenil)acetamida A. 1-yodo-3-(metilsulfonil)benceno. A una solución agitada de 1-bromo-3-(metilsulfonil)benceno (1 g, 4,25 mmol) en 1,4-dioxano (15 mL) se añadió yoduro de sodio (1,92 g, 12,76 mmol), yoduro de cobre (81 mg, 0,425 mmol), trans-N,N'-dimetilcidohexano-1,2-diamina (90 mg, 0,63 mmol) a temperatura ambiente y se agitó a 110°C durante 16 h en tubo sellado. Se inactivó la mezcla de reacción con agua (50 mL) y se extrajo con acetato de etilo (3 X 200 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 1-yodo-3-(metilsulfonil)benceno (900 g, 3,19 mmol, 75% de rendimiento) como un sólido marrón. LCMS (ESI) m/z 282,85 [M+H]+.
B. 2,2-difluoro-2-(3-(metilsulfonil)fenil)acetato de etilo. A una solución agitada de 1-yodo-3-(metilsulfonil)benceno (900 mg, 3,19 mmol) en dimetilsulfóxido (15 mL) se añadió 2-yodo-2,2-difluoroacetato de etilo (0,56 mL, 4,147 mmol), cobre (527 mg, 8,29 mmol) y se agitó durante 16 h a temperatura ambiente. Se neutralizó la mezcla de reacción con solución de cloruro de amonio saturada acuosa y se extrajo con acetato de etilo (2 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo resultante con gel de sílice (malla 100-200, acetato de etilo en hexano al 12%) para proporcionar 2,2-difluoro-2-(3-(metilsulfonil)fenil)acetato de etilo (850 mg, 3,05 mmol, 95%) como un sólido blanquecino. MS (ESI) m/z 320,32 [M+1]+ (aducto ACN (+41))
C. Ácido 2,2-difluoro-2-(3-(metilsulfonil)fenil)acético. A una solución agitada en frío (0°C) de 2,2-difluoro-2-(3-(metilsulfonil)fenil)acetato de etilo (800 mg, 2,87 mmol) en metanol/tetrahidrofurano/agua (10 mL, 1:1:1) se añadió hidróxido de litio monohidratado (361 mg, 8,61 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con bisulfato de potasio acuoso al 10% (20 mL) y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas con salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(3-(metilsulfonil)fenil)acético (650 mg, 1,74 mmol, 70% de rendimiento) como un sólido gomoso. MS (ESI) m/z 251,07 [m +1]+.
D. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(metilsulfonil)fenil)acetamida. A una solución agitada en frío (0°C) de ácido 2 2,2-difluoro-2-(3-(metilsulfonil)fenil)acético (291 mg, 1,16 mmol) en piridina (10 mL) se añadió cloruro de fosforilo (0,27 mL, 2,91 mmol) gota a gota y se agitó a 0-5°C durante 30 min. A esta mezcla de reacción se añadió a continuación clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) y se agitó a temperatura ambiente durante 2 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo resultante por cromatografía en columna Grace usando el 52% de ACN-0,1% de ácido fórmico en agua como eluyente para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1 -oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(metilsulfonil)fenil)acetamida (72 mg, 0,142 mmol, 15% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 506,01 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 8 ppm 10,98 (s, 1H) 9,80 (brt, J=5,85 Hz, 1 H), 8,12 - 8,09 (m, 2 H), 7,96 (d, J=8,4 Hz, 1 H), 7,90 - 7,80 (m, 1 H), 7,67 (d, J=7,68 Hz, 1 H), 7,41 (s, 1 H), 7,36 (d, J=7,8 Hz, 1 H), 5,10 (dd, J=13,16, 5,12 Hz, 1 H), 4,54 - 4,20 (m, 4 H), 3,30 (d, J=8,04 Hz, 3 H), 3,01 - 2,79 (m, 1 H), 2,67 - 2,55 (m, 1 H), 2,47 -2,30 (m, 1 H), 2,06 - 1,92 (m, 1 H).
Ejemplo 112
2-(2-aminopirimidin-5-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetimida
A.2-(2-aminopirimidin-5-il)-2,2-difluoroacetato de etilo. Una solución agitada de 5-yodopirimidin-2-amina (1 g, 4,52 mmol) en dimetilsulfóxido (20 mL) se hizo reaccionar con 2-bromo-2,2-difluoroacetato de etilo (1,1 mL, 9,04 mmol), cobre (0,75 g, 11,76 mmol) y se agitó durante 16 h a 50°C. Se neutralizó la mezcla de reacción con solución de cloruro de amonio saturada acuosa y se extrajo con acetato de etilo (3 X 50 mL). Se lavó la capa orgánica combinada con agua (2X10 mL), salmuera (10 mL) y se secó sobre sulfato de sodio y se concentró para dar 2-(2-aminopirimidin-5-il)-2,2-difluoroacetato de etilo (600 mg, 2,76 mmol, 61%) como un líquido marrón. Gc Ms (m/z) 217,1.
B. Ácido 2-(2-aminopirimidin-5-il)-2,2-difluoroacético. A una solución agitada en frío (0°C) de 2-(2-aminopirimidin-5-il)-2,2-difluoroacetato de etilo (500 mg, 2,30 mmol) en etanol/tetrahidrofurano/agua (12 mL, 1:1:1) se añadió hidróxido de litio monohidratado (290 mg, 6,91 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con bisulfato de potasio acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 30 mL). Se lavó la capa orgánica combinada con salmuera (10 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2-(2-aminopirimidin-5-il)-2,2-difluoroacético (300 mg, 1,58 mmol, 69% de rendimiento) como un semisólido marrón. MS (ESI) m/z 190,22.[M+1]+.
C. 2-(2-aminopirimidin-5-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. A una solución agitada en frío (0°C) de ácido 2-(2-aminopirimidin-5-il)-2,2-difluoroacético (800 mg, 4,23 mmol) y clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (915 mg, 2,96 mmol) en N,N-dimetilformamida (30 mL) se añadió N,N-diisopropiletilamina (2,3 mL, 12,69 mmol) seguido por 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metileno]-1H-1,2,3-triazolo[4,5-b]piridinio (2,4 g, 6,34 mmol) y en agitación a temperatura ambiente durante 16 h. Se diluyó la mezcla de reacción con agua (70 mL) y se extrajo con acetato de etilo (2 X 20 mL) y se lavó la capa orgánica combinada con salmuera (30 mL), se secó sobre sulfato de sodio y se concentró y se secó al vacío. Se purificó el producto por columna de fase inversa Reveleris C-18 usando acetonitrilo al 40% en ácido fórmico acuoso (0,1%) para proporcionar 2-(2-aminopirimidin-5-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (45 mg, 1,01 mmol, 15% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 445,44 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 810,96 (s, 1H), 9,59 (br t, J=5,8 Hz, 1H), 8,36 (s, 2H), 7,67 (d, J=7,7 Hz, 1H), 7,43 (s, 1H), 7,37 (d, J=8,0 Hz, 1H), 7,26 (s, 2H), 5,10 (dd, J= 5,2, 13,4 Hz, 1H), 4,65-4,24 (m, 4H), 3,02-2,83 (m, 1H), 2,67-2,54 (m, 1H), 2,46-2,30 (m, 1H), 2,01 -1,95 (m, 1H).
Ejemplo 113
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-(trifluorometiltio)piridin-2-il)acetamida
A.6-bromopiridin-3-ilcarbamato de ferc-butilo. A una solución agitada de 6-bromopiridin-3-amina (7 g, 40,46 mmol) en diclorometano (70 mL) se añadió dicarbonato de di-ferc-butilo (10,58 mL, 48,55 mmol) seguido por 4-dimetilaminopiridina (0,99 g, 8,09 mmol), trietilamina (0,99 g, 8,09 mmol) a 0°C y se agitó a temperatura ambiente durante 6 h. Se diluyó la mezcla de reacción con agua (50 mL) y se extrajo con diclorometano (3 X 50 mL). Se lavaron las capas orgánicas combinadas con salmuera (50 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto obtenido por cromatografía en columna sobre gel de sílice (acetato de etilo en éter de petróleo al 5%) para proporcionar 6-bromopiridin-3-ilcarbamato de ferc-butilo (6 g, 22,05 mmol, 54% de rendimiento) como un líquido incoloro. MS (ESI) m/z 273,22 [M+1]+
B. 2-(5-(ferc-butoxicarbomlammo)piridm-2-M)-2,2-difluoroacetato de etilo. A una solución agitada de 6 bromopiridin-3-ilcarbamato de ferc-butilo (6 g, 16,08 mmol) en dimetilsulfóxido (40 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (4,89 mL, 24,12 mmol) seguido por polvo de cobre (2,65 g, 41,73 mmol) a temperatura ambiente y se agitó a 60°C durante 6 h. Se diluyó la mezcla de reacción con agua y se filtró a través de un lecho de Celite. Se extrajo el filtrado con acetato de etilo (3 X 50 mL) y se lavaron las capas orgánicas combinadas con salmuera (50 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto obtenido por cromatografía en columna sobre gel de sílice (acetato de etilo/éter de petróleo al 5%) para proporcionar 2-(5-(fercbutoxicarbonilamino)piridin-2-il)-2,2-difluoroacetato de etilo (4 g, 12,65 mmol, 57% de rendimiento) como un líquido incoloro. 1H RMN (300 MHz, CDCla) 88,42 (d, J = 2,1 Hz, 1H), 8,16 (d, J = 6,9 Hz, 1H), 7,66 (d, J =9,0 Hz, 1H), 6,67 (bs, 1H), 4,36 (q, J = 7,1 Hz, 2H), 1,53 (s, 9H), 1,32 (t, J = 7,2 Hz, 3H).
C. 2,2-difluoro-2-(5-tiocianatopiridin-2-il)acetato de etilo. Una solución agitada de 2-(5-(fercbutoxicarbonilamino)piridin-2-il)-2,2-difluoroacetato de etilo (4 g, 12,65 mmol) en HCl 6 N (80 mL) a 0°C y se agitó a temperatura ambiente durante 30 min. A continuación, se añadió nitrito de sodio (0,87 g, 12,65 mmol) a la mezcla de reacción seguido portiocianato de cobre(I) (0,77 g, 6,32 mmol), tiocianato de potasio (0,99 g, 8,09 mmol) a -5°C y se agitó a temperatura ambiente durante 1 h. Se vertió la mezcla de reacción en solución de bicarbonato de sodio acuosa
saturada y se extrajo con acetato de etilo (3 X 40 mL). Se lavaron las capas orgánicas combinadas con salmuera (40 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto obtenido por cromatografía en columna sobre gel de sílice (acetato de etilo al 5%/éter de petróleo) para proporcionar 2,2-difluoro-2-(5-tiocianatopiridin-2-il)acetato de etilo (0,7 g, 2,71 mmol, 21% de rendimiento) como un líquido incoloro. MS (ESI) m/z 259,23 [M+1]+
D. 2,2-difluoro-2-(5-(trifluorometiltio)piridin-2-il)acetato de etilo. A una solución agitada de 2,2-difluoro-2-(5-tiocianatopiridin-2-il)acetato de etilo (700 mg, 2,71 mmol) en tetrahidrofurano (10 mL) se añadió trifluorometiltrimetilsilano (770 mg, 5,42 mmol) seguido por fluoruro de tetra-n-butilamonio (1,08 mL, 1,08 mmol) a 0°C y se agitó a temperatura ambiente durante 16 h. Se inactivó la mezcla de reacción con solución de bicarbonato de sodio acuosa y se extrajo con acetato de etilo (3X10 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secaron sobre sulfato de sodio anhidro, se filtraron y se concentraron. Se purificó el producto en bruto obtenido por cromatografía en columna instantánea (gel de sílice 100-200, acetato de etilo/éter de petróleo al 2%) para proporcionar 2,2-difluoro-2-(5-(trifluorometiltio)piridin-2-il)acetato de etilo (170 mg, 0,56 mmol, 21% de rendimiento) como un líquido incoloro. MS (ESI) m/z 302,27 [M+1]+.
E. Ácido 2,2-difluoro-2-(5-(trifluorometiltio)piridin-2-il)acético. A una solución agitada de 2,2-difluoro-2-(5-(trifluorometiltio)piridin-2-il)acetato de etilo (170 mg, 0,56 mmol) en tetrahidrofurano: etanol: agua (5 mL, 1:1:1) se añadió hidróxido de litio monohidratado (71 mg, 1,69 mmol) y se agitó a temperatura ambiente durante 4 h. Se extrajeron los productos volátiles a presión reducida y se disolvió el producto en bruto obtenido en agua (5 mL) y se lavó con acetato de etilo (2 x 4 mL). Se acidificó la capa acuosa con solución de bisulfato de potasio acuosa y se extrajo con acetato de etilo (3 x 5 mL). Se lavaron las capas orgánicas combinadas con salmuera (5 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar ácido 2,2-difluoro-2-(5-(trifluorometiltio)piridin-2-il)acético (140 mg, 0,51 mmol, 91% de rendimiento) como un compuesto semisólido. MS (ESI) m/z 274,18 [M+1]+.
F. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-(trifluorometiltio)piridin-2-il)acetimida. A una solución enfriada con hielo de ácido 2,2-difluoro-2-(5-(trifluorometiltio)piridin-2-il)acético (220 mg, 0,81 mmol) en piridina (5 mL) se añadió oxicloruro de fósforo (371 mg, 2,42 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A continuación, se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (250 mg, 0,81 mmol) en la mezcla de reacción y se agitó a temperatura ambiente durante 1 h. Se neutralizó la mezcla de reacción con bicarbonato de sodio saturado acuoso y se extrajo con acetato de etilo (3X10 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 (acetonitrilo al 50-55%/ácido fórmico acuoso al 0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-(trifluorometiltio) piridina-2-il)acetamida (45 mg, 0,08 mmol, 10% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 529,03 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 810,99 (s, 1H), 9,77 (t, J = 5,4 Hz, 1H), 9,01 (s, 1H), 8,44 (dd, J = 7,8, 0,8 Hz, 1H), 7,98 (d, J = 8,4 Hz, 1H), 7,71 (d, J =7,5 Hz, 1H), 7,50 (s, 1H), 7,44 (d, J = 7,5 Hz, 1H), 5,11 (dd, J =12,9, 5,1 Hz, 1H), 4,51 (d, J = 6,3 Hz, 2H), 4,46 (d, J =17,9 Hz, 1H), 4,31 (d, J =17,6 Hz, 1H), 2,92-2,88 (m, 1H), 2,63 - 2,57 (m, 1H), 2,41 - 2,36 (m, 1H), 2,02 - 2,00 (m, 1H).
Ejemplo 114
Clorhidrato de N-((2-(2,6-dioxopiperidm-3-N)-1-oxoisomdolm-5-N)metM)-2,2-difluoro-2-(3-(2-(metilamino)etoxi)fenil)acetamida
A.2-(3-(2-(ferc-butoxicarboml(metM)ammo)etoxi)feml)-2,2-difluoroacetato de etilo. A una solución agitada de 2,2-difluoro-2-(3-hidroxifenil)acetato de etilo (2 g, 9,25 mmol) en tetrahidrofurano (20 mL) se añadió carbamato de tercbutil 2-hidroxietil(metilo)(2,43 g 13,88 mmol), azodicarboxilato de N,N-diisopropilo (1,87 g 9,25 mmol) seguido por trifenilfosfina (2,4 g, 9,25 mmol) a temperatura ambiente y se agitó a 50-55°C durante 16 h. La masa de reacción se concentró directamente. Se purificó el residuo resultante por cromatografía en columna (gel de sílice 100-200) acetato de etilo - hexanos al 30% como eluyente para proporcionar 2-(3-(2-(terc-butoxicarbonil(metil)amino)etoxi)fenil)-2,2-difluoroacetato de etilo (1 g, 4,0 mmol, 29% de rendimiento) como un líquido marrón. MS (ESI) m/z 274,2 [M-100]+.
B. Ácido 2-(3-(2-(íerc-butoxicarboml(metil)ammo)etoxi)feml)-2,2-difluoroacético. A una solución agitada en frío (0°C) de 2-(3-(2-(íerc-butoxicarbonil(metil)amino)etoxi)fenil)-2,2-difluoroacetato de etilo (1,0 g, 2,67 mmol) en Metanol/Tetrahidrofurano/agua (15 mL, 1:1:1) se añadió hidróxido de litio monohidratado (224,5 mg, 5,64 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con bisulfato de potasio acuoso al 10% (10 mL) y se extrajo con acetato de etilo (2 X 50 mL). Se lavó la capa orgánica combinada con salmuera (20 mL), se secó sobre sulfato de sodio y se concentró para dar ácido 2-(3-(2-(terc-butoxicarbonil (metil)amino)etoxi)fenil)-2,2-difluoroacético de etilo (600 mg, 1,73 mmol, 65% de rendimiento) como un semisólido marrón. MS (ESI) m/z 343,8 [M-1]+.
C. 2-(3-(2-((2-(2,6-dioxopiperidm-3-il)-1-oxoisomdolm-5-il)metilammo)-1,1-difluoro-2-oxoetil)fenoxi)etil(metil)carbamato de íerc-butilo. A una solución de ácido 2-(3-(2-(tercbutoxicarbonil(metil)amino)etoxi)fenil)-2,2-difluoroacético de etilo (447,8 mg, 1,44 mmol) en N,N-dimetilformamida (20 mL) se añadió clorhidrato de (3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (500 mg, 1,44 mmol) se añadió en subsecuencia diisopropiletilamina (561,8 mg, 4,34 mmol) y 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metileno]-1H-1,2,3-triazolo[4,5-b]piridinio (825,9 g, 2,17 mmol) a temperatura ambiente y se continuó con la reacción a temperatura ambiente durante 2 h. Se vertió la mezcla de reacción en agua enfriada con hielo (40 mL) para observar el sólido blanquecino. Se purificó el residuo resultante por cromatografía en columna de fase inversa Reveleris C-18 usando acetonitrilo al 45-50% en ácido fórmico acuoso (0,1%) para dar 2-(3-(2-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metilamino)-1,1-difluoro-2-oxoetil)fenoxi)etil(metil)carbamato de íerc-butilo (200 mg, 0,33 mmol, 20% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 501 [M-100]+ (masa Dc Boc).
D. Clorhidrato de N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-(metilamino)etoxi)fenil)acetamida. A 2-(3-(2-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metilamino)-1,1-difluoro-2-oxoetil)fenoxi)etil(metil)carbamato de íerc-butilo (160 mg, 0,26 mmol), se añadió ácido clorhídrico 4 M en dioxano (5 mL) y se agitó a temperatura ambiente durante 4 h. Se destiló la solución a presión reducida y se lavó con éter dietílico para proporcionar clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (60 mg, 0,11 mmol, 42% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 501,59 [M+1]+. 1H RMN (400MHz, DMSO-d6) 8 ppm 10,99 (s, 1H), 9,87 - 9,58 (m, 1H), 8,98 (br s, 2H), 7,68 (d, J=7,8 Hz, 1H), 7,53 - 7,46 (m, 1H), 7,44 - 7,40 (m, 1H), 7,39 - 7,34 (m, 1H), 7,46 - 7,32 (m, 1H), 7,24 - 7,16 (m, 3H), 5,11 (dd, J=5,1, 13,5 Hz, 1H), 4,48 - 4,39 (m, 3H), 4,33-4,24 (m, 3H), 3,40- 3,25 (m, 2H), 2,97-2,85 (m, 1H), 2,67-2,55 (m, 4H), 2,39 (dq, J=4,4, 13,2 Hz, 4H), 2,05 1,94 (m, 1H).
Ejemplo 115
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-3-il)acetamida
A. 2-(6-cloropiridacin-3-il)malonato de 1-íerc-butil 3-etilo. Se añadió gota a gota malonato de 1-íerc-butiletilo(26,6 mL, 140,54 mmol) a una suspensión de hidruro de sodio (12,9 g, 324,32 mmol) en dioxano a 10°C. Se agitó la reacción a 10°C durante 1 h y a continuación se dejó calentar a temperatura ambiente. A continuación se añadió 3,6-dicloropiridacina (20 g, 135,13 mmol) en porciones a la reacción a 25°C y se sometió a reflujo durante 2 h. Se diluyó la mezcla de reacción con agua fría con hielo (500 mL) y se extrajo con acetato de etilo (5 X 500 mL). Se lavaron las capas orgánicas combinadas con salmuera (50 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna (sílice 100-200) usando EtoAc:Hexeno al 6% para proporcionar 2-(6-cloropiridacin-3-il)malonato de 1 -terc-butil-3-etilo (16 g, 53,33 mmol, 39% de rendimiento). LCMS (ESI) m/z 301,31 [M+1]+.
B. 2-(6-cloropiridacin-3-il)-2-fluoromalonato de 1-íerc-butil 3-etilo. A una solución de 3-etil-2-(6-cloropiridacin-3-il)malonato de 1-íerc-butilo (16 g, 53,33 mmol) en tetrahidrofurano (200 mL) se añadió hidruro de sodio (2,31 g, 58,133 mmol) a 0°C y se agitó durante 15 min. Se añadió una solución turbia de SelectFluor (20,5 g, 58,13 mmol) en N,N-dimetilformamida seca (40 mL) gota a gota a 0°C durante un periodo de 20 min y a continuación se dejó en agitación
la reacción a temperatura ambiente durante 2 h. Se inactivó la reacción con cloruro de amonio (200 mL) y se extrajo con acetato de etilo (5 X 500 mL). Se lavaron las capas orgánicas combinadas con salmuera (50 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna (sílice 100-200) usando EtoAc:Hexeno al 5% para proporcionar 2-(6-cloropiridacin-3-il)-2-fluoromalonato de 1-ferc-butil-3-etilo (11 g, 34,59 mmol, 64% de rendimiento). LCMS (ESI) m/z 219,27 [M+1]+.
C. 2-(6-cloropiridacin-3-il)-2-fluoroacetato de etilo. Una solución de 2-(6-cloropiridacin-3-il)-2-fluoromalonato de 1-ferc-butil-3-etilo (11 g, 34,54 mmol) en mezcla de ácido trifluoroacético :diclorometano (1:1, 60 mL) se agitó a 25°C durante 2 h y a continuación se concentró hasta sequedad en un evaporador rotatorio. Se disolvió el residuo resultante en acetato de etilo (100 mL), se lavó con solución saturada de bicarbonato de sodio acuosa, se secó sobre sulfato de sodio y a continuación se concentró hasta sequedad para proporcionar 2-(6-cloropiridacin-3-il)-2-fluoroacetato de etilo (6 g, 27,52 mmol 79% de rendimiento), LCMS (ESI) m/z 219,06 [M+1]+. El material se llevó a la etapa siguiente sin purificación adicional.
D. 2-fluoro-2-(6-hidroxipiridacin-3-il)acetato de etilo. A una solución agitada de 2-(6-cloropiridacin-3-il)-2-fluoroacetato de etilo (6 g, 27,52 mmol) en ácido acético (20 mL) se añadió acetato de sodio (22,56 g, 275,52 mmol) y se agitó durante 16 h a 100°C. Se diluyó la mezcla de reacción con agua enfriada con hielo (500 mL) y se extrajo con acetato de etilo (5 X 500 mL). Se lavaron las capas orgánicas combinadas con salmuera (50 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna (sílice 100-200) usando acetato de etilo en hexanos al 30% para proporcionar 2-fluoro-2-(6-hidroxipiridacin-3-il)acetato de etilo (4 g, 20,00 mmol, 72% de rendimiento). LCMS (ESI) m/z 201,22 [M+1]+.
E. 2-fluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-3-il)acetato de etilo. A una solución agitada de 2-fluoro-2-(6-hidroxipiridacin-3-il)acetato de etilo (4 g, 20,00 mmol) en N,N-dimetilformamida (20 mL) se añadió yoduro de metilo (1,86 mL, 30,00 mmol), carbonato de potasio (8,28 g, 60,00 mmol) a temperatura ambiente y se agitó durante 3 h. Se diluyó la mezcla de reacción con agua (50 mL) y se extrajo con acetato de etilo (3 X 100 mL). Se lavaron las capas orgánicas combinadas con salmuera (50 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna (sílice 100-200) usando acetato de etilo en hexanos al 40% para proporcionar 2-fluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-3-il)acetato de etilo (3 g, 14,01 mmol, 70% de rendimiento). LCMS (ESI) m/z 215,66 [M+1]+.
F. 2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-3-il)acetato de etilo. A una solución de 2-fluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-3-il)acetato de etilo (3 g 14,01 mmol) en tetrahidrofurano seco (30 mL) se añadió hexametildisilacida de litio (14 mL, 16,82 mmol) gota a gota a -78°C y se agitó durante 15 minutos. A esto, se añadió una suspensión de SelectFluor (5,9 g, 16,8 mmol) en N,N-dimetilformamida seca (10 mL) gota a gota durante un periodo de 10 min. Tras completar la adición, se dejó calentar la reacción a temperatura ambiente durante un periodo de 30 min. Se inactivó la reacción con cloruro de amonio saturado (50 mL) y se destilaron las fracciones orgánicas. Se diluyó el residuo obtenido con agua enfriada con hielo (500 mL) y se extrajo con acetato de etilo (5 X 500 mL). Se lavaron las capas orgánicas combinadas con salmuera (50 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna Combi-Flash (sílice 100-200) usando acetato de etilo en hexanos al 42% para proporcionar 2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-3-il)acetato de etilo (1,2 g, 5,17 mmol, 36% de rendimiento). LCMS (ESI) m/z 233,33 [M+1]+.
G. Ácido 2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-3-il)acético. A una solución agitada en frío (0°C) de 2,2 difluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-3-il)acetato de etilo (1,2 g, 5,17 mmol) en mezcla de tetrahidrofurano:metanol:agua (30 mL, 1:1:1) se añadió hidróxido de litio monohidratado (1,08 g, 25,86 mmol) y se agitó a temperatura ambiente durante 6 h. Se concentró la mezcla de reacción y se neutralizó el residuo con ácido clorhídrico acuoso al 10% y se extrajo con acetato de etilo (2 X 50 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-3-il)acético (700 mg, 3,43 mmol, 66% de rendimiento) como un sólido blanquecino. LCMS (ESI) m/z 205,31 [M+1]+.
H. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-3-il)acetamida. A una solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-3-il)acético (197,6 mg, 0,968 mmol) en piridina se añadió cloruro de fosforilo (0,27 mL, 2,906 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A esta mezcla de reacción se le añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,968 mmol) y se siguió agitando a temperatura ambiente durante 30 min. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2X10 mL), salmuera (10 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 40-60% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)1- oxoisoindolin-5-il)metil)-2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-3-il)acetamida (70 mg, 0,152 mmol, 15% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 460,52 [M+1]+. 1H RMN (300MHz, DMSO-d6) 5 = 10,98 (s, 1H), 9,68 (brt, J=58 Hz, 1H), 7,79-7,69 (m, 2H), 7,51 (s, 1H), 7,45 (d, J=7,7 Hz, 1H), 7,12 (d, J=9,5 Hz, 1H), 5,11 (dd, J=4,9, 13,3 Hz, 1H), 4,58 - 4,27 (m, 4H), 3,66 (s, 3H), 2,99 - 2,83 (m, 1H), 2,67 - 2,56 (m, 1H), 2,45 - 2,29 (m, 1H), 2,08 - 1,93 (m, 1H).
Ejemplo 116
2- (2-aminopirimidin4-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetimida
A. 4-yodopirimidin-2-amina. A una solución enfriada con hielo de 4-cloropirimidin-2-amina (5 g, 38,5 mmol) en ácido clorhídrico (100 mL) se añadió yoduro de sodio (17,2 g, 115,7 mmol) a 0°C y se agitó a temperatura ambiente durante 2 h. Se inactivó la mezcla de reacción con cautela con solución de bicarbonato de sodio acuosa a 0°C y se extrajo con diclorometano (3 X 150 mL). Se lavaron las capas orgánicas combinadas agua (150 mL), salmuera (150 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 4-yodopirimidina-2-amina (1,55 g, 7,01 mmol, 18% de rendimiento) como un líquido incoloro. MS (ESI) m/z 222 [M+H]+.
B. 2-(2-aminopirimidin-4-il)-2,2-difluoroacetato de etilo. A una solución agitada de 4-yodopirimidina-2-amina (5 g, 22,60 mmol) en dimetilsulfóxido (10 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (4,53 mL, 33,92 mmol) seguido por polvo de cobre (3,7 g, 58,75 mmol) y se agitó a 50°C durante 4 h. Se neutralizó la mezcla de reacción con solución de cloruro de amonio saturada acuosa y se extrajo con acetato de etilo (3 X 150 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2-(2-aminopirimidin-4-il)-2,2-difluoroacetato de etilo (1,4 mg, 6,45 mmol, 28%) como un líquido marrón. Ms (ESI) m/z 218 [M+H]+.
C. Ácido 2-(2-aminopirimidin-4-il)-2,2-difluoroacético. A una solución agitada en frío (0°C) de 2-(2-aminopirimidin-4-il)-2,2-difluoroacetato de etilo (700 mg, 3,22 mmol) en tetrahidrofurano se añadió ácido clorhídrico 1 N y se agitó a temperatura ambiente durante 12 h. Se concentró la mezcla de reacción y se codestiló el residuo obtenido con tolueno para proporcionar ácido 2-(2-aminopirimidin-4-il)-2,2-difluoroacético (550 mg, 2,91 mmol, 82% de rendimiento) como un sólido blanco. MS (ESI) m/z 188 [M-H]+.
D. 2-(2-aminopirimidin-4-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. A una solución agitada en frío (0°C) de clorhidrato de 3-(6-((metilamino)metil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (683 mg, 2,21 mmol) y ácido 2-(2-aminopirimidin-4-il)-2,2-difluoroacético (500 mg, 2,21 mmol) en N,N-dimetilformamida (10 mL) se añadió N,N-diisopropiletilamina (1,15 mL, 6,63 mmol) seguido por 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metileno]-1H-1,2,3-triazolo[4,5-b]piridinio (1 g, 2,65 mmol) y se agitó a temperatura ambiente durante 16 h. Se diluyó la mezcla de reacción con agua (70 mL) y se extrajo con acetato de etilo (2 X 50 mL). Se lavaron las capas orgánicas combinadas con salmuera (30 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por columna de fase inversa Reveleris C-18 usando acetonitrilo al 58% en ácido fórmico acuoso (0,1%) para proporcionar 2-(2-aminopirimidin-4-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (52 mg, 11,6 mmol, 5% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 445,1 [M+H]+. 1H RMN (400 MHz, DMSO-d6) 510,99 (s, 1H), 9,57 (t, J = 6,0 Hz, 1H), 8,46 (d, J = 4,8 Hz, 1H), 7,71(d, J =8,0 Hz, 1H), 7,48 (s, 1H), 7,60 (d, J = 7,6 Hz, 1H), 7,07 (s, 1H), 6,86 (d, J = 4,8 Hz, 1H), 5,11 (dd, J =13,2,4,8 Hz, 1H), 4,48 (d, J = 5,2 Hz, 2H), 4,46 (d, J = 16,9 Hz, 1H), 4,31 (d, J =17,2 Hz, 1H), 2,93-2,89 (m, 1H), 2,67 - 2,58 (m, 1H), 2,40 - 2,33 (m, 1H), 2,01 -1,98 (m, 1H).
Ejemplo 117
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(pirimidin-4-il)acetamida
A. 2,2-difluoro-2-(2-(metiltio)pirimidin-4-il)acetato de etilo. A una solución agitada de 4-doro-2-(metiltio)pirimidina (5 g, 21,55 mmol) en dimetilsulfóxido (50 mL) se añadió 2-bromo-2,2-difluoroacetato de etilo (8 mL, 62,2 mmol) seguido por polvo de cobre (5,93 g, 93,4 mmol) a TA y se agitó a 60°C durante 6 h. Se basificó la mezcla de reacción con solución de bicarbonato de sodio saturada y se extrajo con acetato de etilo (3 X 20 mL). Se lavaron las capas orgánicas combinadas con agua (40 mL), salmuera (40 mL), se secó sobre sulfato de sodio, se filtró y se concentró el disolvente y se purificó el producto en bruto obtenido por cromatografía en columna sobre gel de sílice usando acetato de etilo en éter de petróleo al 20% para proporcionar 2,2-difluoro-2-(3-formilfenil)acetato de etilo (3 g, 12,00 mmol, 38%) como un líquido incoloro. MS (ESI) m/z 249,66 [M+1]+.
B. 2,2-difluoro-2-(pirimidin-4-il)acetato de etilo. Se añadió 2,2-difluoro-2-(2-(metiltio)pirimidin-4-il)acetato de etilo (2,8 g, 11,29 mmol) en tetrahidrofurano a trimetilsilano (5,3 mL) a 0°C y se añadió Pd/C al 10% (622 mg) y a continuación se agitó a temperatura ambiente durante 5 h. Se filtró la mezcla de reacción a través de lecho de celite. Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el producto en bruto obtenido por cromatografía en columna instantánea (gel de sílice 100-200, acetato de etilo en éter de petróleo al 10%) para proporcionar 2,2-difluoro-2-(pirimidin-4-il)acetato de etilo (800 mg, 3,96 mmol, 36% de rendimiento) como un líquido incoloro. MS (ESI) m/z 203,65 [M+1]+.
C. Ácido 2,2-difluoro-2-(pirimidin-4-il)acético. A una solución agitada de 2,2-difluoro-2-(pirimidin-4-il)acetato de etilo (1 g, 4,95 mmol) en tetrahidrofurano: etanol: agua (15 mL, 1:1:1) se añadió hidróxido de litio monohidratado (624 mg, 14,85 mmol) y se agitó a temperatura ambiente durante 16 h. Se extrajeron los productos volátiles a presión reducida y se disolvió el producto en bruto obtenido en agua (15 mL) y se lavó con acetato de etilo (2x10 mL). Se acidificó la capa acuosa con solución de clorhidrato 1 N y se extrajo con acetato de etilo ( 3x 15 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró en ácido 2,2-difluoro-2-(pirimidin-4-il)acético (800 mg, 4,59 mmol, 92% de rendimiento) como un compuesto semisólido. MS (ESI) m/z 175 [M+1]+.
D. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(pirimidin4-il)acetamida. A una solución enfriada con hielo de ácido 2,2-difluoro-2-(pirimidin-4-il)acético (203 mg, 1,16 mmol) en piridina (10 mL) se añadió oxicloruro de fósforo (0,27 mL, 2,91 mmol) gota a gota y se agitó a 0-5°C durante 1 h y a continuación se añadió clorhidrato de 3-(6-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,97 mmol) y se agitó a temperatura ambiente durante 30 min. Se neutralizó la mezcla de reacción con bicarbonato de sodio saturado acuoso y se extrajo con acetato de etilo (3X15 mL). Se lavaron las capas orgánicas combinadas con agua (15 mL), salmuera (15 mL), se secó sobre sulfato de sodio, se filtró y se concentró. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 (acetonitrilo al 50-55% en ácido fórmico acuoso al 0,1% para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(pirimidin-4-il)acetamida (55 mg, 0,12 mmol, 12% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 430,47 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 810,99 (s, 1H), 9,81 (t, J = 6,0 Hz, 1H), 9,41 (s, 1H), 9,12 (d, J = 5,1 Hz,1H) 7,95 (dd, J = 5,1, 1,5 Hz, 1H) 7,71 (d, J = 7,5 Hz,1H), 7,52(s, 1H),7,44 (d, J = 7,5 Hz, 1H), 5,11 (dd,J= 13,2, 5,1 Hz, 1H), 4,51 (d, J = 6,3 Hz, 2H), 4,47 (d, J =17,6 Hz, 1H), 4,32 (d, J =17,4 Hz, 1H) 2,96-2,88 (m, 1H), 2,63-2,57 (m, 1H), 2,43-2,38 (m, 1H), 2,07- 1,98 (m, 1H).
Ejemplo 118
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-(piperidin-1-il)etoxi)fenil)acetamida
A. 2,2-difluoro-2-(3-hidroxifenil)acetato de metilo. A una solución agitada de 2,2-difluoro-2-(3-(metoximetoxi)fenil)acetato de etilo (13,0 g, 49,98 mmol) en diclorometano (130 mL) se añadió ácido trifluoroacético (65 mL) a 0°C y se agitó a temperatura ambiente durante 5 h. Se inactivó la mezcla de reacción con agua (200 mL) y se extrajo con diclorometano (3 X 200 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 100 mL), salmuera (100 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(3-hidroxifenil)acetato de metilo (8,0 g, 37,03 mmol, 74% de rendimiento). GCMS (m/z) 216,1.
B. 1-(2-cloroetil)piperidina. A una solución agitada de 2-(piperidin-1-il)etanol (4,0 g, 30,95 mmol) en diclorometano (40 mL) se añadió cloruro de tionilo (7,0 mL, 92,87) a 0°C y se agitó a temperatura ambiente durante 3 h. Se inactivó la mezcla de reacción con agua (50 mL) y se extrajo con diclorometano (3 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 1- (2-cloroetil)piperidina (1,8 g, 12,24 mmol, 40% de rendimiento). GCMS (m/z) 147,1.
C. 2,2-difluoro-2-(3-(2-(piperidin-1-il)etoxi)fenil)acetato de etilo. A una solución agitada de 2,2-difluoro-2-(3-hidroxifenil)acetato de metilo (1,0 g, 4,62 mmol) en acetona (15 mL) se añadió 1-(2-cloroetil)piperidina (885 mg, 6,01 mmol), carbonato de potasio (1,9 g, 13,88 mmol) y se agitó a 55°C durante 4 h. Se filtró la mezcla de reacción con lecho de celite y se lavó con acetato de etilo (3 X 50 mL). Se secó el filtrado sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(3-(2-(piperidin-1-il)etoxi)fenil)acetato de etilo (1,4 g, 4,28 mmol, 93% de rendimiento). LCMS(ESI) m/z 328,0.
D. Ácido 2,2-difluoro-2-(3-(2-(piperidin-1-il)etoxi)fenil)acético. A una solución agitada en frío (0°C) de 2,2-difluoro-2- (3-(2-(piperidin-1-il)etoxi)fenil)acetato de etilo (1,4 g, 4,28 mmol) en mezcla de metanol-tetrahidrofurano-agua (20 mL, 1:1:1) se añadió hidróxido de litio monohidratado (539 mg, 12,84 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con bisulfato de potasio acuoso al 10% (20 mL) y se extrajo con acetato de etilo (2 X 40 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(3-(2-(piperidin-1-il)etoxi)fenil)acético (700 mg, 2,34 mmol, 55% de rendimiento). Lc Ms (ESI) m/z 300,0.
E. N-((2-(2,6-diozopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-(piperidin-1-il)etoxi)fenil)acetamida. A una solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(3-(2-(piperidin-1-il)etoxi)fenil)acético (300 mg, 1,00 mmol) y clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (310 mg, 1,00 mmol) en N,N-dimetilformamida (20 mL) se añadió N,N-diisopropiletilamina (389 mg, 3,01 mmol) seguido por 3-óxido de hexafluorofosfato de 1-[bis(dimetilamino)metileno]-1H-1,2,3-triazolo[4,5-b]piridinio (572 mg, 1,50 mmol) y se agitó a temperatura ambiente durante 4 h. Se diluyó la mezcla de reacción con agua (50 mL) y se extrajo con acetato de etilo (2 X 40 mL). Se lavaron las capas orgánicas combinadas con salmuera (30 mL), se secó sobre sulfato de sodio, se concentró y se secó al vacío. Se purificó el producto por columna de fase inversa Reveleris C-18 usando acetonitrilo al 40% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-(piperidin-1-il)etoxi)fenil)acetamida (56 mg, 0,09 mmol, 9% de rendimiento) como un sólido blanquecino. LCMS (ESI) m/z 555,23 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 8 (ppm) 10,99 (s, 1H), 9,66 (brt, J=5,9 Hz, 1H), 9,47 (br s, 1H), 7,68 (d, J=7,7 Hz, 1H), 7,51 (t, J=8,1 Hz, 1H), 7,42 (s, 1H), 7,36 (d, J=7,8 Hz, 1H), 7,27-7,12 (m, 3H), 5,11 (brdd, J=5,1, 13,2 Hz, 1H), 4,56-4,21 (m, 6H), 3,61 - 3,45 (m, 4H), 3,10-2,83 (m, 3H), 2,68 - 2,55 (m, 1H), 2,44 - 2,30 (m, 1H), 2,08 -1,91 (m, 1H), 1,90 - 1,60 (m, 5H), 1,50 - 1,30 (m, 1H).
Ejemplo 119
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-morfolinoetoxi)fenil)acetamida
A. 2,2-difluoro-2-(3-(2-morfolinoetoxi)fenil)acetato de etilo. A una solución agitada de 2,2-difluoro-2-(3-hidroxifenil)acetato de metilo (2,0 g, 9,25 mmol) en acetona (25 mL) se añadió ácido 4-(2-cloroetil)morfolino clorhídrico (2,23 g, 12,03 mmol), carbonato de potasio (3,83 g, 27,77 mmol) y se agitó a 55°C durante 16 h. Se inactivó la mezcla de reacción con agua (50 mL) y se extrajo con acetato de etilo (3 X 50 mL). Se lavaron las capas orgánicas combinadas
con agua (2 X 20 mL), salmuera (30 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2,2-difluoro-2-(3-(2-morfolinoetoxi)fenil)acetato de etilo (1,5 g, 4,55 mmol, 49% de rendimiento) como un líquido marrón. LCMS (ESI) m/z 330,0 [M+1]+.
B. Ácido 2,2-difluoro-2-(3-(2-morfolinoetoxi)fenil)acético. A una solución agitada en frío (0°C) de 2,2-difluoro-2-(3-(2-morfolinoetoxi)fenil)acetato de etilo (1,5 g, 4,55 mmol) en mezcla de metanol/tetrahidrofurano/agua (20 mL, 1:1:1) se añadió hidróxido de litio monohidratado (382 mg, 9,11 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se neutralizó el residuo con bisulfato de potasio acuoso al 10% (20 mL) y se extrajo con acetato de etilo (2 X 40 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(3-(morfolinoetoxi)fenil)acético (600 mg, 1,99 mmol, 44% de rendimiento) como un sólido marrón. LCMS (ESI) m/z 302,0 [M+1]+.
C. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-morfolinoetoxi)fenil)acetamida.
A una solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(3-(morfolinoetoxi)fenil)acético (513 mg, 1,66 mmol) y clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (500 mg, 1,66 mmol) en N,N-dimetilformamida (20 mL) se añadió N,N-diisopropiletilamina (643,8 mg, 4,98 mmol) seguido por 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metileno]-1H-1,2,3-triazolo[4,5-b]piridinio (946,4 mg, 2,49 mmol) y se agitó a temperatura ambiente durante 4 h. Se diluyó la mezcla de reacción con agua (50 mL) y se extrajo con acetato de etilo (2 X 40 mL). Se lavaron las capas orgánicas combinadas con salmuera (30 mL), se secó sobre sulfato de sodio, se concentró y se secó al vacío. Se purificó el producto por columna de fase inversa Reveleris C-18 usando acetonitrilo al 40% en ácido fórmico acuoso (0,1%) para proporcionar sal de clorhidrato de N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(morfolinoetoxi)fenil)acetamida (40 mg, 0,07 mmol, 4,4% de rendimiento) como un sólido blanquecino. LCMS (ESI) m/z 557,2 [M+1]+. 1H RMN (400MHz, DMSO-d6) 8 ppm 10,99 (s, 1H), 10,17 (brs, 1H), 9,66 (brt, J=6,1 Hz, 1H), 7,68 (d, J=7,8 Hz, 1H), 7,51 (t, J=8,1 Hz, 1H), 7,42 (s, 1H), 7,36 (d, J=7,8 Hz, 1H), 7,25-7,15 (m, 3H), 5,11 (dd, J=4,9, 13,2 Hz, 1H), 4,48-4,37 (m, 5H), 4,28 (d, J=17,2 Hz, 1H), 3,98 (br d, J=12,2 Hz, 2H), 3,73 (br t, J=11,7 Hz, 2H), 3,64 - 3,49 (m, 5H), 3,48 - 3,22 (m, 2H), 2,98 - 2,84 (m, 1H), 2,68 - 2,56 (m, 1H), 2,45 -2,31 (m, 1H), 2,05- 1,95 (m, 1H).
Ejemplo 120
2-(3-(2-(4,4-difluoropiperidin-1-il)etoxi)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida
A.2-(4,4-difluoropiperidin-1-il)acetato de etilo. A una solución agitada de hidrogenocloruro de 4,4-difluoropiperidina (2 g, 12,048 mmol) en tetrahidrofurano (45 mL) se añadió 2-bromoacetato de etilo (2,83 g, 18,07 mmol), trietilamina (6,51 mL, 48,19 mmol) seguido por yoduro de tetrabutilamonio (2,2 g, 6,024 mmol) a temperatura ambiente y se dejó en agitación a la misma temperatura durante 16 h. Se inactivó la reacción con agua con hielo y se extrajo con acetato de etilo (3 X 30 mL). Se lavaron las capas orgánicas combinadas con salmuera (30 mL), se secó sobre sulfato de sodio, y se concentró para proporcionar 2-(4,4-difluoropiperidin-1-il)acetato de etilo (1,5 g, 7,2 mmol, 60% de rendimiento) como un líquido incoloro. GCMS (ESI) m/z 207 [M]+.
B. 2-(4,4-difluoropiperidin-1-il)etanol: A una solución agitada de 2-(4,4-difluoropiperidin-1-il)acetato de etilo (2 g, 9,66 mmol) en tetrahidrofurano (15 mL) se añadió hidruro de litio-aluminio (9,6 mL, 19,32 mmol) a 0°C y se agitó a temperatura ambiente durante 3 h. Se enfrió la mezcla de reacción a 0°C y se inactivó con Celite/sulfato de sodio hidratado (4:1) y se agitó a temperatura ambiente durante 1 h. Se filtró la suspensión espesa blanca se filtró a través de un lecho de Celite y se lavó minuciosamente con diclorometano (60 mL). Se secó el filtrado sobre sulfato de sodio y se concentró para proporcionar 2-(4,4-difluoropiperidin-1-il)etanol (1 g, 6,06 mmol, 62% de rendimiento) como un líquido incoloro. 1H RMN (300 MHz, DMSO-d6) 84,45 (bs, 1H), 3,50 (t, J = 5,6 Hz, 2H), 2,54-2,43 (m, 6H), 2,00 - 1,87 (m, 4H).
C. Metanosulfonato de 2-(4,4-difluoropiperidin-1-il)etilo. A una solución de 2-(4,4-difluoropiperidin-1-il)etanol (1 g,
4,8 mmol) en tetrahidrofurano se añadió cloruro de sulfonilmetano (0,706 mL) a 0°C y se agitó a temperatura ambiente durante 1 h. Se inactivó la mezcla de reacción con solución de bicarbonato de sodio acuosa y se extrajo con acetato de etilo ( 3X10 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar metanosulfonato de 2-(4,4-difluoropiperidin-1-il)etilo (800 mg, 3,27 mmol, 54% de rendimiento) como un líquido incoloro. Se usó el compuesto en bruto en la etapa siguiente sin purificación adicional.
D. 7erc-butN(3-yodofenoxi)dimetMsNano. A una solución agitada de 3-yodofenol (5 g, 22,7 mmol) en N,N-dimetilformamida (15 mL, 1:1:1) se añadió sililcloruro de ferc-butildimetilo (8,2 mL, 27,24 mmol) a 0°C y se agitó a temperatura ambiente durante 16 h. Se vertió la mezcla de reacción en agua con hielo (15 mL) y se extrajo con acetato de etilo (2 x 10 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar ferc-butil(3-yodofenoxi)dimetilsilano (10 g, 17,96 mmol, 80% de rendimiento) como compuesto semisólido que se llevó a la siguiente etapa sin purificación adicional.
E. 2,2-difluoro-2-(3-hidroxifenil)acetato de etilo. A una solución agitada de ferc-butil(3-yodofenoxi)dimetilsilano (10 g, 22,33 mmol) en dimetilsulfóxido (75 mL) se añadió polvo de cobre (3,5 g, 55,82 mmol) seguido por 2-bromo-2,2-difluoroacetato de etilo (4,3 mL, 33,49 mmol) a temperatura ambiente y se agitó a 55°C durante 16 h. Se vertió la mezcla de reacción en agua (20 mL) y se filtró a través de un lecho de Celite. Se extrajo el filtrado con acetato de etilo (3 X 30 mL) y se lavaron las capas orgánicas combinadas con salmuera (30 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 2,2-difluoro-2-(3-hidroxifenil)acetato de etilo (3,5 g, 16,20 mmol, 54% de rendimiento) como un líquido incoloro. MS (ESI) m/z 215,34 [M-1]+.
F.2-(3-(2-(4,4-difluoropiperidin-1-il)etoxi)fenil)-2,2-difluoroacetato de etilo. A una solución agitada de 2,2-difluoro-2-(3-hidroxifenil)acetato de etilo (700 mg, 2,86 mmol) en tolueno (20 mL) se añadió metanosulfonato de 2-(4,4-difluoropiperidin-1 -il)etilo (619 mg, 2,86 mmol) seguido por carbonato de potasio (1,59 g, 11,47 mmol), yoduro de tetrabutilamonio (30 mg) a temperatura ambiente y se dejó en agitación a 110°C durante 16 h. Se vertió la mezcla de reacción en agua con hielo y se extrajo con acetato de etilo (3 X 30 mL). Se lavaron las capas orgánicas combinadas con salmuera (30 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar 2-(3-(2-(4,4-difluoropiperidin-1 -il)etoxi)fenil)-2,2-difluoroacetato de etilo (600 mg, 1,65 mmol, 60% de rendimiento) como un líquido incoloro. MS (ESI) m/z 364,14 [M+1]+.
G. Ácido 2-(3-(2-(4,4-difluoropiperidin-1-il)etoxi)fenil)-2,2-difluoroacético. A una solución agitada de 2-(3-(2-(4,4-difluoropiperidin-1 -il)etoxi)fenil)-2,2-difluoroacetato de etilo (1 g, 2,75 mmol) en tetrahidrofurano: metanol: agua (15 mL, 1:1:1) se añadió hidróxido de litio monohidratado (348 mg, 8,26 mmol) y se agitó a temperatura ambiente durante 3 h. Se extrajeron los productos volátiles a presión reducida y se disolvió el producto en bruto obtenido en agua (15 mL) y se lavó con acetato de etilo (2x10 mL). Se acidificó la capa acuosa con solución de clorhidrato 1 N y se extrajo con acetato de etilo (3x15 mL). Se lavaron las capas orgánicas combinadas con salmuera (10 mL), se secó sobre sulfato de sodio, se filtró y se concentró para proporcionar ácido 2-(3-(2-(4,4-difluoropiperidin-1-il)etoxi)fenil)-2,2-difluoroacético (800 mg, 2,38 mmol, 86% de rendimiento) como un compuesto semisólido. MS (ESI) m/z 334,04 [M]+.
H. 2-(3-(2-(4,4-difluoropiperidin-1-il)etoxi)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. A una solución agitada en frío (0°C) de clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (276 mg, 0,895 mmol) y ácido 2-(3-(2-(4,4-difluoropiperidin-1-il)etoxi)fenil)-2,2-difluoroacético (300 mg, 0,895 mmol) en N,N-dimetilformamida (10 mL) se añadió N,N-diisopropiletilamina (0,3 mL, 1,79 mmol) seguido por 3-óxido hexafluorofosfato de 1-[bis(dimetilamino)metileno]-1H-1,2,3-triazolo[4,5-b]piridinio (408 mg, 1,074 mmol) y se agitó a temperatura ambiente durante 2 h. Se diluyó la mezcla de reacción con agua (30 mL) y se extrajo con acetato de etilo (2 X 40 mL). Se lavaron las capas orgánicas combinadas con salmuera (20 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el compuesto en bruto por columna de fase inversa Reveleris C-18 (acetonitrilo al 60%/ácido fórmico acuoso al 0,1%) para proporcionar 2-(3-(2-(4,4-difluoropiperidin-1-il)etoxi)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida (45 mg, 0,076 mmol, 8% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 591,17. 1H RMN (400 MHz, DMSO-d6) 610,98 (s, 1H), 9,61 (t, J = 5,6 Hz, 1H), 7,67 (d, J =8,0 Hz, 1H), 7,44 (dd, J =8,0, 7,6 Hz, 1H), 7,40 (s, 1H), 7,36 (d, J =7,6 Hz, 1H), 7,16-7,11 (m, 3H), 5,10 (dd, J = 13,2, 5,6 Hz, 1H), 4,45 (d, J = 6,0 Hz, 2H), 4,42 (d, J =17,8 Hz, 1H), 4,28 (d, J = 17,2 Hz, 1H), 4,09 (t, J = 5,6 Hz, 2H), 2,95 - 2,87 (m, 1H), 2,78 (t, J = 5,6 Hz, 2H), 2,65 - 2,59 (m, 5H), 2,45 - 2,35 (m, 1H), 2,03 - 1,88 (m, 5H).
Ejemplo 121
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-4-il)acetamida
A. 4,5-dicloro-2-metilpiridacin-3(2H)-ona. A una solución agitada de 4,5-dicloropiridacin-3-ol (20 g, 0,121 mol) en N,N-dimetilformamida (100 mL) se añadió carbonato de potasio (42 g, 0,303 mol) seguido por yoduro de metilo (18,9 g, 0,133 mol) y se agitó a temperatura ambiente durante 2 h. Se filtró la mezcla de reacción, al filtrado se le añadió agua (100 mL) y se extrajo con acetato de etilo (3 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (100 mL), salmuera (100 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna (sílice 100-200) usando 10-acetato de etilo al 20% en hexanos para proporcionar 4,5-dicloro-2-metilpiridacin-3(2H)-ona (15 g, 0,0837 mol, 69% de rendimiento). MS (ESI) m/z 179,03 [M+1]+.
B. 5-yodo-2-metilpiridacin-3(2H)-ona. A 4,5-dicloro-2-metilpiridacin-3(2H)-ona (15 g, 83,79 mmol) se le añadió el 47% de ácido yodhídrico acuoso (185 mL) y se agitó durante 24 h a 140°C. A esta mezcla de reacción se le añadió tiosulfato de sodio saturado acuoso y se extrajo con acetato de etilo (3 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 50 mL), salmuera (50 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo resultante por cromatografía en columna (sílice 100-200) usando acetato de etilo en hexanos al 30-40% para proporcionar 5-yodo-2-metilpiridacin-3(2H)-ona (8,5 g, 36,016 mmol, 43% de rendimiento). MS (ESI) m/z 237,22 [M+1]+.
C.2-(1-metil-6-oxo-1,6-dihidropiridacin-4-il)malonatode 1-íerc-butN-3-etNo. A una suspensión de hidruro de sodio (2,07 g, 86,44 mmol) en 1,4-dioxano (85 mL) a 10°C se añadió gota a gota malonato de ferc-butiletilo (7 g, 37,45 mmol) y se dejó calentar a 25°C durante 1 h con agitación. A continuación se añadió 5-yodo-2-metilpiridacin-3(2H)-ona (8,5 g, 36,016 mmol) en porciones a 25°C y se sometió a reflujo durante 2 h. Se diluyó la mezcla de reacción con agua enfriada con hielo (100 mL) y se extrajo con acetato de etilo (3 X 100 mL). Se lavaron las capas orgánicas combinadas con agua (50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna (sílice 100-200) usando acetato de etilo en hexanos al 20-30% para proporcionar 2-(1-metil-6-oxo-1,6-dihidropiridacin-4-il)malonato de 1 -ferc-butil-3-etilo(7 g, 23,64 mmol, 65% de rendimiento). MS (ESI) m/z 296,97 [M+1]+.
D. 2-fluoro-2-(1-metil-6-ozo-1,6-dihidropiridacin-4-il)malonato de 1-íerc-butil 3-etilo. A una solución de 2-(6-cloropiridacin-3-il)malonato de 1-ferc-butilo-3-etilo (7 g, 23,64 mmol) en tetrahidrofurano (100 mL) a 0°C se añadió hidruro de sodio (1,2 g, 25,77 mmol). Se filtró la reacción durante 15 min. Se añadió una solución turbia de SelectFluor (9,12 g, 25,77 mmol) en N,N-dimetilformamida (20 mL seca) gota a gota a 0°C durante un periodo de 10 min y se dejó en agitación a temperatura ambiente durante 2 h. Se inactivó la reacción con cloruro de amonio (50 mL) y se extrajo con acetato de etilo (3 X 70 mL). Se lavaron las capas orgánicas combinadas con agua (50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna (sílice 100 200) usando acetato de etilo en hexanos al 25-35% para proporcionar 2-fluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-4-il)malonato de 1-ferc-butil 3-etilo (5 g, 15,92 mmol, 67% de rendimiento). LCMS (ESI) m/z 315,40 [M+1]+.
E. 2-fluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-4-il)acetato de etilo. Se agitó una solución de 2-fluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-4-il)malonato de 1-ferc-butil-3-etilo (5 g, 15,92 mmol) en 25 mL de ácido trifluoroacético/diclorometano (1:1) a temperatura ambiente durante 4 h. A esta mezcla de reacción se le añadió solución de bicarbonato de sodio saturada acuosa y se extrajo con acetato de etilo (3 X 70 mL). Se lavaron las capas orgánicas combinadas con agua (50 mL), salmuera (50 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna (sílice 100-200) usando acetato de etilo en hexanos al 25-35% para proporcionar 2-fluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-4-il)acetato de etilo (3 g, 32,71 mmol, 88% de rendimiento). LCMS (ESI) m/z 215,13 [M+1]+.
F. 2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-4-il)acetato de etilo. A una solución de 2-fluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-4-il)acetato de etilo (3 g, 32,71 mmol) en tetrahidrofurano seco (30 mL) se añadió hexametildisililacida de litio (16,8 mL, 39,25 mmol) gota a gota a -78°C durante un periodo de 10 min. Después de agitación durante 15 min a la misma temperatura, se añadió una solución de SelectFluor (5,9 g, 16,8 mmol) en N,N-dimetilformamida seca (10 mL) gota a gota durante 10 min. Tras completar la adición, se dejó calentar la reacción a temperatura ambiente durante 30 min con agitación y se inactivó con cloruro de amonio saturado (50 mL). Después de la evaporación de las fracciones orgánicas en el evaporador rotatorio, se diluyó la mezcla de reacción con agua
enfriada con hielo (50 mL) y se extrajo con acetato de etilo (5 X 50 mL). Se lavaron las capas orgánicas combinadas con agua (30 mL), salmuera (30 mL), se secó sobre sulfato de sodio y se concentró. Se purificó el residuo resultante por cromatografía en columna CombiFlash (sílice 100-200) usando acetato de etilo en hexanos al 20-30% para proporcionar 2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-4-il)acetato de etilo (1,2 g, 5,17 mmol, 36% de rendimiento). LCMS (ESI) m/z 233,39 [M+1]+.
G. Ácido 2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-4-il)acético. A una solución agitada en frío (0°C) de 2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-4-il)acetato de etilo (1,2 g, 5,17 mmol) en 1,4-dioxano (36 mL) se añadió solución de ácido clorhídrico acuosa 3 N (24 mL) a 5°C y se agitó a temperatura ambiente durante 16 h. Se diluyó la mezcla de reacción con agua (20 mL) y se extrajo con acetato de etilo (2 X 30 mL). Se lavaron las capas orgánicas combinadas con agua (20 mL), salmuera (20 mL), se secó sobre sulfato de sodio y se concentró para proporcionar ácido 2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-4-il)acético (700 mg, 3,43 mmol, 66% de rendimiento) como un sólido blanquecino. Lc MS (ESI) m/z 205,02 [M+1]+.
H. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-4-il)acetamida. A una solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-4-il)acético (197,6 mg, 0,968 mmol) en piridina se añadió cloruro de fosforilo (0,27 mL, 2,906 mmol) gota a gota y se agitó a 0-5°C durante 1 h. A continuación se añadió a esta mezcla de reacción clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (300 mg, 0,968 mmol) y se agitó a temperatura ambiente durante 30 min. Se neutralizó la mezcla de reacción con bicarbonato de sodio acuoso saturado (hasta pH-8) y se extrajo con acetato de etilo (3 x 50 mL). Se lavaron las capas orgánicas combinadas con agua (2X10 mL), salmuera (10 mL), se secaron sobre sulfato de sodio y se concentraron. Se purificó el residuo resultante por cromatografía de columna en fase inversa Reveleris C-18 usando acetonitrilo al 40-60% en ácido fórmico acuoso (0,1%) para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-4-il)acetamida (70 mg, 0,152 mmol, 15% de rendimiento) como un sólido blanquecino. MS (ESI) m/z 459,16 [M+1]+. 1H RMN (300 MHz, DMSO-d6) 8 ppm 10,98 (s, 1H) 9,80 (brt, J=5,66 Hz, 1H) 8,06 (d, J=2,19 Hz, 1H) 7,70 (d, J=7,68 Hz, 1 H) 7,47 (s, 1H) 7,40 (d, J=8,04 Hz, 1H) 7,15 (s, 1H) 5,11 (dd, J =13,16, 5,12 Hz, 1H) 4,55 - 4,23 (m, 4 H) 3,69 (s, 1 H) 3,01 -2,82 (m, 1H) 2,68 -2,45 (m, 1 H) 2,46 - 2,31 (m, 1 H) 2,06 - 1,93 (m, 1 H).
Ejemplo 121
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(4-metilpiperacin-1-il)fenil)acetamida
A. 2-(3-bromofenil)acetato de metilo. A una solución de ácido 2-(3-bromofenil)acético (25 g, 116,27 mmol) en diclorometano (60 mL) se añadió cloruro de oxalilo (20 mL, 232,25 mmol) seguido por N,N-dimetilformamida (1 mL) a 0°C y se agitó a temperatura ambiente durante 1 h. Se concentró la mezcla de reacción, a este residuo resultante se le añadió metanol (250 mL) y se agitó a temperatura ambiente durante 1 h. Se concentró la masa de reacción, se inactivó el residuo resultante con bicarbonato de sodio acuoso saturado (250 mL) y se extrajo con acetato de etilo (3 X 200 mL). Se lavaron las capas orgánicas combinadas con agua (2 X 100 mL), salmuera (200 mL), se secó sobre sulfato de sodio y se concentró 2-(3-bromofenil)acetato de metilo (20 g, 87,71 mmol, 76% de rendimiento) como un líquido incoloro. LCMS (ESI) m/z 270,29 [M+42]+. (aducto ACN).
B. 2-(3-(4-metilpiperacin-1-il)fenil)acetato de etilo. A una solución desgasificada de 2-(3-bromofenil)acetato de metilo (20 g, 87,71 mmol) en tolueno (250 mL) se añadió 1-metilpiperacina (10,52 g, 105,52 mmol), carbonato de cesio (40 g, 122,79 mmol) y se desgasificó durante 30 min. A esta mezcla de reacción se añadió a continuación 2,2'-bis(difenilfosfino)-1,1'-binaftaleno (818 mg, 1,31 mmol), acetato de paladio (II) (590 mg, 0,877 mmol) y se agitó a 110°C durante 16 h. Se filtró la mezcla de reacción a través de lecho de Celite, se concentró el filtrado, se diluyó con agua (300 mL) y se extrajo con acetato de etilo (3 X 200 mL). Se lavaron las capas orgánicas combinadas con agua (200 mL) y salmuera (150 mL), se secó sobre sulfato de sodio, se concentró la capa orgánica a presión reducida para dar el producto en bruto que se purificó por cromatografía en columna CombiFlash (sílice 100-200) usando metanol al 21-24% en diclorometano para proporcionar 2-(3-(4-metilpiperacin-1-il)fenil)acetato de etilo (4,0 g, 16,12 mmol, 19% de rendimiento) como un sólido de color marrón. LCMS (ESI) m/z 249,26[M+1]+.
C. 2,2-difluoro-2-(3-(4-metilpiperacin-1-il)fenil)acetato de etilo. A una solución de 2-(3-(4-metilpiperacin-1-il)fenil)acetato de etilo (4 g, 16,12 mmol) en tetrahidrofurano seco (80 mL) se añadió hexametildisilamida de litio (1 M en tetrahidrofurano) (24 mL, 24,18 mmol) gota a gota a -78°C y se agitó durante 15 min. A esto se añadió una solución de N-fluorodibencenosulfonimida (7,6 g, 24,18 mmol) en tetrahidrofurano seco (20 mL) gota a gota durante un periodo de 10 min. Tras completar la adición, se dejó calentar la reacción a temperatura ambiente durante un periodo de 30 min y se agitó durante 1 h a temperatura ambiente. Se inactivó la reacción con cloruro de amonio saturado (50 mL) diluido con agua enfriada con hielo (100 mL) y se extrajo con acetato de etilo (2 X 200 mL). Se lavaron las capas orgánicas combinadas con salmuera (100 mL), se secó sobre sulfato de sodio y se concentró para proporcionar 2,2 difluoro-2-(3-(4-metilpiperacin-1-il)fenil)acetato de etilo (2,2 g, 8,87 mmol) como un sólido de color marrón claro. LCMS (ESI) m/z 285,40 [M+1]+.
D. Ácido 2,2-difluoro-2-(3-(4-metilpiperacin-1-il)fenil)acético. A una solución agitada en frío (0°C) de 2,2-difluoro-2-(3-(4-metilpiperacin-1-il)fenil)acetato de etilo (2,0 g, 7,04 mmol) en mezcla de tetrahidrofurano:metanol:agua (1:1:1, 30 mL) se añadió hidróxido de litio monohidratado (504 mg, 21,12 mmol) y se agitó a temperatura ambiente durante 2 h. Se concentró la mezcla de reacción y se diluyó el residuo con agua (50 mL) y se lavó con éter dietílico (2 X 50 mL). Se neutralizó la capa acuosa con bisulfato de potasio acuoso al 10% (15 mL) y se puso la liofilización para dar ácido 2,2-difluoro-2-(3-(4-metilpiperacin-1-il)fenil)acético (1,2 g, 4,44 mmol). LCMS (ESI) m/z 270,11[M+1]+.
E. N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(4-metilpiperacin-1-il)fenil)acetamida. A una solución agitada en frío (0°C) de ácido 2,2-difluoro-2-(3-(4-metilpiperacin-1-il)fenil)acético (524 mg, 1,94 mmol) en piridina (10 mL) se añadió cloruro de fosforilo (0,45 mL, 4,83 mmol) a 0-5°C y se agitó a la misma temperatura durante 1 h. A continuación se añadió clorhidrato de 3-(5-(aminometil)-1-oxoisoindolin-2-il)piperidina-2,6-diona (500 mg, 1,61 mmol) y se agitó a temperatura ambiente durante 1 h. Se concentró la mezcla de reacción. Se purificó el residuo resultante por PREP-HPLc ((AtlantisT columna) usando acetonitrilo - 0,1% de bicarbonato de amonio en agua como eluyente). Después de que la liofilización LCMS indicara el 84% de m/z deseado, se observó el 16% de anillo abierto m/z, que se purificó adicionalmente mediante cromatografía en columna CombiFlash usando metanol al 6-7% en diclorometano para proporcionar N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-((4-metilpiperacin-1-il)metil)fenil)acetamida (35 mg, 0,067 mmol, 4% de rendimiento) como un sólido blanquecino. LCMS (ESI) m/z 526,39 [M+1]+. 1H RMN (300MHz, DMSO-d6) 6 = 11,00 (s, 1H), 9,59 (brt, J=6,1 Hz, 1H), 7,67 (d, J=7,7 Hz, 1H), 7,45 - 7,29 (m, 3H), 7,11 (br d, J=8,4 Hz, 1H), 7,04 (s, 1H), 6,97 (brd, J=7,7 Hz, 1H), 5,11 (brdd, J=5,1, 13,2 Hz, 1H), 4,53-4,34 (m, 3H), 4,33-4,21 (m, 1H), 3,42 - 3,26 (m, 4H), 3,14 (br s, 4H), 3,00-2,84 (m, 1H), 2,66-2,66 (m, 1H), 2,42-2,33 (brdd, J=4,2, 13,0 Hz, 1H), 2,27 (br s, 3H), 2,06 -1,92 (m, 1H).
Ejemplo 123
EFECTO DE LOS COMPUESTOS DE PRUEBA EN PROLIFERACIÓN DE CÉLULAS KG-1
Se evaluó la actividad antiproliferativa del compuesto de prueba en la línea celular KG-1 (American Type Culture Collection [ATCC]: número de catálogo ATCC® CCL-246™) 72 horas después del tratamiento. Se optimizó la densidad de sedimentación para KG-1 para garantizar la linealidad del ensayo en placas de 384 pocillos.
Se determinaron concentraciones crecientes del compuesto de prueba (0,5 nM a 10 pM) de una forma de dilución en serie de 10 puntos (3 veces de dilución) por duplicado mediante un dispensador acústico (EDC ATS-100) en una placa de 384 pocillos vacía. La concentración de dimetilsulfóxido (DMSO) se mantuvo constante para una concentración final de ensayo del 0,1% de DMSO. Antes de la prueba se cultivaron células KG-1 en medio RPMI-1640 (Roswell Park Memorial Institute - 1640) con FBS (suero bovino fetal: HyClone) al 10% y se amplió en matraces de cultivo para proporcionar cantidades suficientes de material de partida. A continuación se diluyeron las células en 5.000 células por pocillo, en un volumen de 50 pL y se añadieron directamente a las placas de 384 pocillos en las que se observó el compuesto. Se dejaron crecer las células durante 72 horas en CO2 al 5% a 37°C. En el momento en que comenzó la exposición de las células al compuesto (tü), se evaluó el número de células viables inicial mediante Cell Titer-Glo® Luminescent Cell Viability Assay en una relación 1 vol: 2 vol según las instrucciones del fabricante (Promega Corporation, Madison, WI) cuantificando el nivel de luminiscencia generado por adenosina-5'-trifosfato (ATP) presente en células viables. Después de 72 horas, se evaluó la viabilidad celular de las células t-tratadas por medio de Cell Titer-Glo® y se leyó la luminiscencia. En la Tabla 1 se proporcionan valores de IC50 para compuestos de ejemplo. En la Tabla 1, se proporcionan valores de IC50 del modo siguiente: A:< 0,01 pM; B:0,01 a 0,05 pM; C:> 0,05 pM a 0,1 pM; y D:> 0,1 pM a 10 pM.
Tabla 1
Los compuestos de la invención son para su uso en medicina.
Los compuestos de la invención son para su uso en los procedimientos de tratamiento proporcionados en la presente memoria.
Claims (25)
1. Un compuesto de Fórmula I:
o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, donde:
R1 es cicloalquilo monocíclico opcionalmente sustituido, arilo monocíclico opcionalmente sustituido, heteroarilo monocíclico opcionalmente sustituido o heterociclilo monocíclico opcionalmente sustituido;
R2 y R3 son cada uno halo;
donde los sustituyentes en R1, cuando están presentes, son de uno a tres grupos Q, donde cada Q es independientemente alquilo, halo, haloalquilo, oxo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, heterociclilo monocíclico opcionalmente sustituido, heterocicloalquilo monocíclico opcionalmente sustituido, arilo monocíclico opcionalmente sustituido, heteroarilo monocíclico opcionalmente sustituido, -R4OR5, -R4O-R4OR5, -R4N(R6)(R7), -R4SR5, -R4OR4N(R6)(R7), -R4OR4C(J)N(R6)(R7), -C(J)R9 o R4S(O)tR8;
donde los sustituyentes en Q, cuando están presentes son de uno a tres grupos Qa, donde cada Qa es independientemente alquilo, halo, haloalquilo, alcoxialquilo, oxo, hidroxilo o alcoxi;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo, hidroxialquilo, alcoxialquilo, cicloalquilo monocíclico, arilo monocíclico, heteroarilo monocíclico, heterociclilo monocíclico o heterociclilalquilo monocíclico, donde los grupos alquilo, haloalquilo, hidroxialquilo, alcoxialquilo, cicloalquilo, arilo, heteroarilo, heterociclilo o heterociclilalquilo en R5 están cada uno independientemente opcionalmente sustituido con de uno a tres grupos Q1, donde cada Q1 es independientemente alquilo, haloalquilo o halo;
R6 y R7 se seleccionan de la siguiente manera:
i) R6 y R7 son cada uno independientemente hidrógeno o alquilo; o
ii) R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un anillo heterociclilo o heteroarilo de 5 o 6 miembros, opcionalmente sustituido con uno o dos halo, alquilo o haloalquilo;
R8 es alquilo, haloalquilo o hidroxialquilo;
R9 es alquilo o arilo;
J es O o S; y
t es 1 o 2;
2. El compuesto según la reivindicación 1, donde R1 es arilo monocíclico opcionalmente sustituido.
3. El compuesto según la reivindicación 1 que tiene la Fórmula II:
o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, donde:
R1 es cicloalquilo monocíclico opcionalmente sustituido, arilo monocíclico opcionalmente sustituido, heteroarilo monocíclico opcionalmente sustituido o heterociclilo monocíclico opcionalmente sustituido;
donde los sustituyentes en R1, cuando están presentes, son de uno a tres grupos Q, donde cada Q es independientemente alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, arilo monocíclico opcionalmente sustituido, -R4OR5, -R4SR5, -R4N(R6)(R7), R4OR4N(R6)(R7) o R4OR4C(J)N(R6)(R7);
J es O o S;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo o hidroxialquilo; y
R6 y R7 se seleccionan de la siguiente manera:
i) R6 y R7 son cada uno independientemente hidrógeno o alquilo; o
ii) R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un anillo heterociclilo o heteroarilo de 5 o 6 miembros, opcionalmente sustituido con uno o dos halo, alquilo o haloalquilo.
4. El compuesto según la reivindicación 1, donde R1 es arilo monocíclico opcionalmente sustituido; donde los sustituyentes en R1, cuando están presentes, son de uno a tres grupos Q, donde cada Q es independientemente alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, arilo monocíclico opcionalmente sustituido, -R4OR5, -R4SR5, -R4N(R6)(R7), R4OR4N(R6)(R7) o R4OR4C(J)N(R6)(R7); J es O o S; cada R4 es independientemente alquileno, alquenileno o un enlace directo; cada R5 es independientemente hidrógeno, alquilo, haloalquilo o hidroxialquilo; y R6 y R7 se seleccionan del modo siguiente: i) R6 y R7 son cada uno independientemente hidrógeno o alquilo; o
ii) R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un anillo heterociclilo o heteroarilo de 5 o 6 miembros, opcionalmente sustituido con uno o dos halo, alquilo o haloalquilo.
5. El compuesto según la reivindicación 1, donde R1 es fenilo opcionalmente sustituido, ciclohexilo opcionalmente sustituido, piperinidilo opcionalmente sustituido, o piridilo opcionalmente sustituido, donde los sustituyentes en R1, cuando están presentes, son de uno a tres grupos Q, donde cada Q es independientemente halo, alquilo, -R4OR5 o -R4N(R6)(R7); cada R4 es independientemente un enlace directo o alquileno; cada R5 es independientemente hidrógeno, alquilo, o haloalquilo; y R6 y R7 se seleccionan del modo siguiente:
i) R6 y R7 son cada uno independientemente hidrógeno o alquilo; o
ii) R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un anillo heterociclilo de 5 o 6 miembros.
6. El compuesto según la reivindicación 1, donde R1 es fenilo opcionalmente sustituido, donde los sustituyentes en R1, cuando están presentes, son de uno a tres grupos Q, donde cada Q es independientemente fluoro, cloro, metilo, tere butilo, -R4Or5, -R4SR5 o R4OR4C(J)N(R6)(R7); cada R4 es independientemente un enlace directo o metileno; cada R5 es independientemente hidrógeno, metilo, etilo o trifluorometilo; y R6 y R7 son cada uno independientemente hidrógeno o metilo.
7. El compuesto según la reivindicación 1, donde el compuesto tiene la fórmula III
o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, donde:
cada Q1 es independientemente alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, arilo monocíclico opcionalmente sustituido, -R4OR5, -R4SR5, -R4N(R6)(R7), R4OR4N(R6)(R7) o R4OR4C(J)N(R6)(R7);
J es O o S;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo o hidroxialquilo;
R6 y R7 se seleccionan de la siguiente manera:
i) R6 y R7 son cada uno independientemente hidrógeno o alquilo; o
ii) R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un anillo heterociclilo o heteroarilo de 5 o 6 miembros, opcionalmente sustituido con uno o dos halo, alquilo o haloalquilo; y
n es 0-3.
8. El compuesto según la reivindicación 1, donde el compuesto tiene la fórmula IV
o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, donde:
Q2 es hidrógeno, alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, arilo monocíclico opcionalmente sustituido, -R4OR5, -R4SR5, -R4N(R6)(R7), R4OR4N(R6)(R7) o R4OR4C(J)N(R6)(R7);
J es O o S;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo o hidroxialquilo; y
R6 y R7 son cada uno independientemente hidrógeno o alquilo.
9. El compuesto según la reivindicación 1, donde el compuesto tiene la fórmula V
o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, donde:
Q3 y Q4 son cada uno independientemente hidrógeno, alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, -R4OR5, -R4SR5, -R4N(R6)(R7), R4o R4N(R6)(R7) o R4OR4C(J)N(R6)(R7);
J es O o S;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo o hidroxialquilo; y
R6 y R7 son cada uno independientemente hidrógeno o alquilo.
10. El compuesto según la reivindicación 1, donde el compuesto tiene la fórmula VI
o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, donde:
Q4 y Q5 son cada uno independientemente hidrógeno, alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, -R4OR5, -R4SR5, -R4N(R6)(R7), R4o R4N(R6)(R7) o R4OR4C(J)N(R6)(R7);
J es O o S;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo o hidroxialquilo; y
R6 y R7 se seleccionan de la siguiente manera:
i) R6 y R7 son cada uno independientemente hidrógeno o alquilo; o
ii) R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un anillo heterociclilo o heteroarilo de 5 o 6 miembros, opcionalmente sustituido con uno o dos halo, alquilo o haloalquilo.
11. El compuesto según la reivindicación 10, donde Q4 y Q5 son cada uno independientemente hidrógeno, halo, alquilo, -R4N(R6)(R7), o -R4OR5; R4 es un enlace directo o alquileno; R5 es hidrógeno, alquilo o haloalquilo; y R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un heterociclilo de 6 miembros.
12. El compuesto según la reivindicación 1, donde el compuesto tiene la fórmula VII
o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, donde:
Q5 es hidrógeno, alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, -R4OR5, -R4SR5, -R4N(R6)(R7), R4OR4N(R6)(R7) o R4OR4C(J)N(R6)(R7);
J es O o S;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo o hidroxialquilo; y
R6 y R7 se seleccionan de la siguiente manera:
i) R6 y R7 son cada uno independientemente hidrógeno o alquilo; o
ii) R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un anillo heterociclilo o heteroarilo de 5 o 6 miembros, opcionalmente sustituido con uno o dos halo, alquilo o haloalquilo.
13. El compuesto según la reivindicación 12, donde Q5 es hidrógeno, halo, alquilo, -R4N(R6)(R7) o -R4OR5; R4 es un enlace directo o alquileno; y R5 es hidrógeno, alquilo o haloalquilo; y R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un heterociclilo de 6 miembros.
14. El compuesto según la reivindicación 1, donde el compuesto tiene la fórmula VIII
o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, donde:
Q2 y Q5 son cada uno independientemente hidrógeno, alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido, cicloalquilalquilo monocíclico opcionalmente sustituido, -R4OR5, -R4SR5, -R4N(R6)(R7), R4o R4N(R6)(R7) o R4OR4C(J)N(R6)(R7);
J es O o S;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo o hidroxialquilo; y
R6 y R7 son cada uno independientemente hidrógeno o alquilo, o R6 y R7 junto con el átomo de nitrógeno donde están sustituidos forman un heterociclilo de 6 miembros.
15. El compuesto según la reivindicación 14, donde Q2 y Q5 son cada uno independientemente hidrógeno, halo, alquilo, arilo monocíclico opcionalmente sustituido, o -R4OR5; R4 es un enlace directo o alquileno; y R5 es hidrógeno, alquilo o haloalquil.
16. El compuesto según la reivindicación 1 que tiene la Fórmula IX:
o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo, donde:
cada Q1 es independientemente alquilo, halo, haloalquilo, cicloalquilo monocíclico opcionalmente sustituido; cicloalquilalquilo monocíclico opcionalmente sustituido, heterociclilo monocíclico opcionalmente sustituido, -R4OR5, -R4O-R4OR5, -R4N(R6)(R7), -R4SR5, -R4OR4N(R6)(R7), -R4OR4C(J)N(R6)(R7), -C(J)R9 o R4S(O)tR8;
cada R4 es independientemente alquileno, alquenileno o un enlace directo;
cada R5 es independientemente hidrógeno, alquilo, haloalquilo, hidroxialquilo, alcoxialquilo, cicloalquilo monocíclico, arilo monocíclico, heteroarilo monocíclico, heterociclilo monocíclico o heterociclilalquilo monocíclico, donde los grupos alquilo, haloalquilo, hidroxialquilo, alcoxialquilo, cicloalquilo, arilo, heteroarilo, heterociclilo o heterociclilalquilo en R5 están cada uno independientemente opcionalmente sustituidos con de uno a tres grupos Q1 seleccionados de entre alquilo, haloalquilo o halo;
R6 y R7 son cada uno independientemente hidrógeno o alquilo.
R8 es alquilo, haloalquilo o hidroxialquilo;
R9 es alquilo o arilo;
J es O o S;
t es 1 o 2; y
n es 0-3.
17. El compuesto de la reivindicación 1, donde el compuesto se selecciona de entre:
2-(3-cloro-4-metilfenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
2-(4-clorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-metoxifenil)acetamida;
2-(3-clorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluorofenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-p-tolilacetamida;
2-(3,4-didorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
2-(2-dorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(trifluorometil)fenil)acetamida;
2-(4-terc-butilfenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-fenilacetamida;
2-(3-doro-4-fluorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-(trifluorometiltio)fenil)acetamida;
2-(2,6-difluorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-o-tolilacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-fluorofenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2-(2-etoxifenil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(trifluorometoxi)acetamida;
2-(3-bromo-4-(trifluorometoxi)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida; 2-(3-doro-4-metoxifenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-m-tolilacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-isopropoxifenil)acetamida;
2-(3,4-difluorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-fluorofenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(trifluorometil)piridin-2-il)acetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-isopropilfenil)acetamida;
2-(2,4-didorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-metoxifenil)acetamida;
2-(4-cidopropilfenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
2-(4-doro-2-fluorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
2-(4-doro-3-fluorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-fluoro-2-metilfenil)acetamida;
2-(3-doro-2-metilfenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluoro-2-(trifluorometil)fenil)acetamida;
2-(4-doro-2-metilfenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluoro-2-metilfenil)acetamida;
2-(4-doro-2-(trifluorometil)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida; 2-cidohexil-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
2-(4-doro-2-(trifluorometoxi)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-metoxietoxi)fenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-hidroxietoxi)fenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-(2-metoxietoxi)fenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-hidroxietil)fenil)acetamida;
2-(3-(dimetilamino)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(piperidin-1-il)fenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-l-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-morfolinofenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluoro-2-isopropoxifenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(2,2,2-trifluoroetoxi)fenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2-(2-etoxi-4-fluorofenil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-isopropoxifenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-fluoro-4-isopropoxifenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(morfolinometil)fenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluoro-2-(2,2,2-trifluoroetoxi)fenil)acetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-isopropoxi-2-metilfenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-isopropoxi-3-metilfenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-fluoro-4-isopropoxifenil)acetamida;
2-(3-doro-4-isopropoxifenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-metil-4-(trifluorometoxi)fenil)acetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-fluoro-4-(trifluorometoxi)fenil)acetamida; 2-(5-doropiridin-2-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-fluoropiridin-2-il)acetamida;
2-(2,4-difluorofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
2-(4-bromofenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(2-metoxietoxi)fenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(1-hidroxicidohexil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(1-hidroxicidopentil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-metil-4-(trifluorometoxi)fenil)acetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2-(3-etoxipiridin-2-il)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-metilpiridin-2-il)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-metilpiridin-2-il)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2-(2-etoxi-6-fluorofenil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4'-fluorobifenil-4-il)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2-(2-etoxi-5-fluorofenil)-2,2-difluoroacetamida;
2-cidopentil-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
2-(3-doro-4-(trifluorometoxi)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-metoxi-2-(trifluorometil)fenil)acetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(2-hidroxietoxi)fenil)acetamida;
2-(4-doro-2-etoxifenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-hidroxifenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(2-(metilamino)fenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-isopropoxi-2-(trifluorometil)fenil)acetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-metilcidohexil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-isopropoxietoxi)fenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-hidroxifenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-((4-metilpiperacin-1-il)metil)fenil)acetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-metil-2-(trifluorometil)fenil)acetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-(2-metoxietoxi)etoxi)fenil)acetamida; 2-(3-(2-(dimetilamino)etoxi)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-isopropilpiridin-2-il)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-(metilsulfonil)etoxi)fenil)acetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(3-(metilsulfonil)propil)fenil)acetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-(2-fluoropropan-2-il)fenil)acetamida;
2-(1-bencil-6-oxo-1,6-dihidropiridin-3-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-metoxipiridin-2-il)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridin-3-il)acetamida;
2-(5-terc-butilpiridin-2-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
2-(5-cidopropilpiridin-2-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-isopropoxipiridin-2-il)acetamida;
2-(5-bromopiridin-2-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluoro-2-(trifluorometoxi)fenil)acetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-fluorocidohexil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(4-(metilsulfonil)fenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(metilsulfonil)fenil)acetamida;
2-(2-aminopirimidin-5-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(5-(trifluorometiltio)piridin-2-il)acetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-(metilamino)etoxi)fenil)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-3-il)acetamida;
2-(2-aminopirimidin-4-il)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(pirimidin-4-il)acetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-(piperidin-1-il)etoxi)fenil)acetamida; N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(2-morfolinoetoxi)fenil)acetamida;
2-(3-(2-(4,4-difluoropiperidin-1-il)etoxi)fenil)-N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida;
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(1-metil-6-oxo-1,6-dihidropiridacin-4-il)acetamida; y
N-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoro-2-(3-(4-metilpiperacin-1-il)fenil)acetamida; o un enantiómero o una mezcla de enantiómeros del mismo, o una sal, solvato, hidrato, cocristal, clatrato o polimorfo farmacéuticamente aceptables del mismo.
18. Un compuesto según una cualquiera de las reivindicaciones 1 a 17 para su uso como un medicamento.
19. Un compuesto según una cualquiera de las reivindicaciones 1 a 17 para su uso en un procedimiento de tratamiento del cáncer, donde el procedimiento comprende la administración a un mamífero que tiene cáncer de una cantidad terapéuticamente efectiva del compuesto.
20. El compuesto para su uso según la reivindicación 19, donde el cáncer es leucemia.
21. El compuesto para su uso según la reivindicación 20, donde la leucemia es leucemia linfocítica crónica, leucemia mielocítica crónica, leucemia linfoblástica aguda o leucemia mieloide aguda.
22. El compuesto para su uso según la reivindicación 20 o 21, donde la leucemia es una leucemia mieloide aguda.
23. El compuesto para su uso según una cualquiera de las reivindicaciones 20 a 22, donde la leucemia es recidivante, refractaria o resistente a la terapia convencional.
24. El compuesto para su uso según una cualquiera de las reivindicaciones 19 a 23, donde el procedimiento comprende además la administración de una cantidad terapéuticamente efectiva de otro segundo agente activo o una terapia de cuidados de soporte.
25. El compuesto para su uso según la reivindicación 24, donde el otro segundo agente activo es un anticuerpo terapéutico que se une específicamente a un antígeno del cáncer, factor de crecimiento hematopoyético, citocina, agente anticanceroso, antibiótico, inhibidor cox-2, agente inmunomodulador, agente inmunosupresor, corticoesteroide o un mutante o derivado farmacológicamente activo de los mismos.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201462023775P | 2014-07-11 | 2014-07-11 | |
| PCT/US2015/039926 WO2016007848A1 (en) | 2014-07-11 | 2015-07-10 | Antiproliferative compounds and methods of use thereof |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2760003T3 true ES2760003T3 (es) | 2020-05-12 |
Family
ID=53682892
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES19193334T Active ES2968308T3 (es) | 2014-07-11 | 2015-07-10 | Compuestos antiproliferativos y métodos de uso de los mismos |
| ES15739485T Active ES2760003T3 (es) | 2014-07-11 | 2015-07-10 | Compuestos antiproliferativos y procedimientos de uso de los mismos |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES19193334T Active ES2968308T3 (es) | 2014-07-11 | 2015-07-10 | Compuestos antiproliferativos y métodos de uso de los mismos |
Country Status (30)
| Country | Link |
|---|---|
| US (6) | US9499514B2 (es) |
| EP (2) | EP3166937B1 (es) |
| JP (3) | JP6779870B2 (es) |
| KR (1) | KR102477960B1 (es) |
| CN (2) | CN106660991B (es) |
| AR (1) | AR101189A1 (es) |
| AU (1) | AU2015287688B2 (es) |
| BR (1) | BR112017000550B1 (es) |
| CA (1) | CA2954784C (es) |
| CL (1) | CL2017000075A1 (es) |
| CO (1) | CO2017000223A2 (es) |
| CY (1) | CY1122340T1 (es) |
| DK (1) | DK3166937T3 (es) |
| EA (1) | EA033633B1 (es) |
| EC (1) | ECSP17002135A (es) |
| ES (2) | ES2968308T3 (es) |
| HR (1) | HRP20191821T1 (es) |
| HU (1) | HUE046000T2 (es) |
| IL (2) | IL276946B (es) |
| LT (1) | LT3166937T (es) |
| MX (2) | MX2017000408A (es) |
| PL (1) | PL3166937T3 (es) |
| PT (1) | PT3166937T (es) |
| RS (1) | RS59619B1 (es) |
| SA (1) | SA517380693B1 (es) |
| SG (2) | SG10202010780WA (es) |
| SI (1) | SI3166937T1 (es) |
| TW (1) | TWI660952B (es) |
| WO (1) | WO2016007848A1 (es) |
| ZA (1) | ZA201700217B (es) |
Families Citing this family (38)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9732154B2 (en) | 2014-02-28 | 2017-08-15 | Janssen Biotech, Inc. | Anti-CD38 antibodies for treatment of acute lymphoblastic leukemia |
| US9603927B2 (en) | 2014-02-28 | 2017-03-28 | Janssen Biotech, Inc. | Combination therapies with anti-CD38 antibodies |
| US9499514B2 (en) * | 2014-07-11 | 2016-11-22 | Celgene Corporation | Antiproliferative compounds and methods of use thereof |
| ES2890669T3 (es) | 2014-09-09 | 2022-01-21 | Janssen Biotech Inc | Terapias de combinación con anticuerpos anti-CD38 |
| EA037084B9 (ru) * | 2014-12-04 | 2021-08-05 | Янссен Байотек, Инк. | Антитела к cd38 для лечения острого миелолейкоза |
| KR102602754B1 (ko) | 2015-05-20 | 2023-11-14 | 얀센 바이오테크 인코포레이티드 | 경쇄 아밀로이드증 및 다른 cd38-양성 혈액학적 악성종양을 치료하기 위한 항-cd38 항체 |
| AU2016282674B2 (en) | 2015-06-22 | 2022-01-13 | Janssen Biotech, Inc. | Combination therapies for heme malignancies with anti-CD38 antibodies and survivin inhibitors |
| US20170044265A1 (en) | 2015-06-24 | 2017-02-16 | Janssen Biotech, Inc. | Immune Modulation and Treatment of Solid Tumors with Antibodies that Specifically Bind CD38 |
| US10781261B2 (en) | 2015-11-03 | 2020-09-22 | Janssen Biotech, Inc. | Subcutaneous formulations of anti-CD38 antibodies and their uses |
| US10385135B2 (en) | 2015-11-03 | 2019-08-20 | Janssen Biotech, Inc. | Subcutaneous formulations of anti-CD38 antibodies and their uses |
| US10648983B2 (en) | 2016-01-08 | 2020-05-12 | Celgene Corporation | Methods for treating cancer and the use of biomarkers as a predictor of clinical sensitivity to therapies |
| CN108601777B (zh) * | 2016-01-08 | 2021-08-03 | 细胞基因公司 | 2-(4-氯苯基)-n-((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)甲基)-2,2-二氟乙酰胺的制剂 |
| ES2957477T3 (es) * | 2016-01-08 | 2024-01-19 | Celgene Corp | Compuestos antiproliferativos para usar en el tratamiento de leucemia |
| EP3399981B1 (en) | 2016-01-08 | 2023-08-02 | Celgene Corporation | Solid forms of 2-(4-chlorophenyl)-n-((2-2,6-dioxopiperidin-3-yl)-1-oxoisoindolin-5-yl) methyl)-2,2-difluoroacetamide, and their pharmaceutical compositions and uses |
| MX2018015120A (es) | 2016-06-06 | 2019-04-15 | Celgene Corp | Tratamiento de una neoplasia maligna hematologica con 2-(4-clorofenil)-n-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin- 5-il)metil)-2,2-difluoroacetamida. |
| US11535603B1 (en) | 2016-09-30 | 2022-12-27 | Deuterx, Llc | Deuterium-enriched piperidinonyl-oxoisoindolinyl acetamides and methods of treating medical disorders using same |
| CN106928253A (zh) * | 2017-03-09 | 2017-07-07 | 武汉工程大学 | 一种唑啉草酯的制备方法 |
| SG11201913008TA (en) | 2017-06-30 | 2020-01-30 | Celgene Corp | Compositions and methods of use of 2-(4-chlorophenyl)-n-((2-(2,6-doxopiperidin-3-yl)-1-oxoisoindolin-5-yl) methyl) -2,2-difluoroacetamide |
| CA3079242A1 (en) | 2017-10-31 | 2019-05-09 | Janssen Biotech, Inc. | Methods of treating high risk multiple myeloma |
| CN107827721B (zh) * | 2017-11-17 | 2021-03-16 | 上海恩氟佳科技有限公司 | 一种合成4-氟环己酮的方法 |
| EP3735243A4 (en) * | 2018-01-02 | 2021-08-25 | Celgene Corporation | ISOTOPOLOGISTS OF 2- (4-CHLOROPHENYL) -N - ((2- (2,6-DIOXOPIPERIDIN-3-YL) -1-OXOISOINDOLIN-5-YL) METHYL) -2,2-DIFLUOROACETAMIDE |
| US11530219B2 (en) | 2018-06-29 | 2022-12-20 | Dana-Farber Cancer Institute, Inc. | Ligands to cereblon (CRBN) |
| SG11202106598QA (en) * | 2018-12-31 | 2021-07-29 | Celgene Corp | Compositions and methods of use of 2-(4-chlorophenyl)-n-((2-(2,6-dioxopiperidin-3-yl)-1-oxoisoindolin-5yl) methyl)-2,2-difluoroacetamide |
| EP3976595A4 (en) | 2019-05-31 | 2023-01-04 | Celgene Corporation | SUBSTITUTED 1-OXO-ISOINDOLINE-5-CARBOXAMIDE COMPOUNDS, COMPOSITIONS THEREOF AND METHODS OF TREATMENT THEREOF |
| WO2021091946A1 (en) * | 2019-11-05 | 2021-05-14 | Celgene Corporation | Combination therapy with 2-(4-chlorophenyl)-n-((2-(2,6-dioxopiperidin-3-yl)-1-oxoisoindolin-5-yl) methyl)-2,2-difluoroacetamide |
| GB201916600D0 (en) * | 2019-11-14 | 2020-01-01 | Syngenta Crop Protection Ag | 81991-gb-reg-org-nat-1 |
| KR20220103753A (ko) * | 2019-11-19 | 2022-07-22 | 브리스톨-마이어스 스큅 컴퍼니 | 헬리오스 단백질의 억제제로서 유용한 화합물 |
| MX2022006133A (es) | 2019-12-06 | 2022-06-17 | Celgene Corp | Procesos para preparar 2-(4-clorofenil)-n-((2-(2,6-dioxopiperidin- 3-il)-1-oxoisoindolin-5-il)metil)-2,2-difluoroacetamida. |
| WO2021198965A1 (en) * | 2020-03-31 | 2021-10-07 | Orum Therapeutics, Inc. | Neodegrader conjugates |
| EP4171550A1 (en) | 2020-06-25 | 2023-05-03 | Celgene Corporation | Methods for treating cancer with combination therapies |
| KR20230048373A (ko) * | 2020-08-03 | 2023-04-11 | 캡터 테라퓨틱스 에스.에이. | 저분자량 단백질 분해제 및 이의 응용 |
| WO2022152821A1 (en) | 2021-01-13 | 2022-07-21 | Monte Rosa Therapeutics Ag | Isoindolinone compounds |
| BR112023023076A2 (pt) * | 2021-05-06 | 2024-01-30 | Celgene Corp | Métodos de tratamento com n-((r)-1-(3-cloropiridin-2-il)-2,2,2-trifluoroetil)-2-((s)-2,6-dioxopiperidin-3-il)-1-oxoisoindolina-5-carboxamida |
| EP4091449A1 (en) * | 2021-05-19 | 2022-11-23 | Syngenta Crop Protection AG | Weed control method |
| MX2024002862A (es) * | 2021-09-08 | 2024-05-24 | Orum Therapeutics Inc | Enlazadores para usar en conjugados fármaco-anticuerpo. |
| WO2024027694A1 (zh) * | 2022-08-01 | 2024-02-08 | 苏州开拓药业股份有限公司 | 一种蛋白降解剂 |
| TW202423411A (zh) * | 2022-10-06 | 2024-06-16 | 南韓商歐倫醫療公司 | 新降解劑綴合物 |
| WO2024169913A1 (zh) * | 2023-02-15 | 2024-08-22 | 石药集团巨石生物制药有限公司 | 一种度胺类分子胶衍生物及其用途 |
Family Cites Families (75)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3536809A (en) | 1969-02-17 | 1970-10-27 | Alza Corp | Medication method |
| US3598123A (en) | 1969-04-01 | 1971-08-10 | Alza Corp | Bandage for administering drugs |
| US4044126A (en) | 1972-04-20 | 1977-08-23 | Allen & Hanburys Limited | Steroidal aerosol compositions and process for the preparation thereof |
| GB1429184A (en) | 1972-04-20 | 1976-03-24 | Allen & Hanburys Ltd | Physically anti-inflammatory steroids for use in aerosols |
| US3845770A (en) | 1972-06-05 | 1974-11-05 | Alza Corp | Osmatic dispensing device for releasing beneficial agent |
| US3916899A (en) | 1973-04-25 | 1975-11-04 | Alza Corp | Osmotic dispensing device with maximum and minimum sizes for the passageway |
| US4008719A (en) | 1976-02-02 | 1977-02-22 | Alza Corporation | Osmotic system having laminar arrangement for programming delivery of active agent |
| US4410545A (en) | 1981-02-13 | 1983-10-18 | Syntex (U.S.A.) Inc. | Carbonate diester solutions of PGE-type compounds |
| US4328245A (en) | 1981-02-13 | 1982-05-04 | Syntex (U.S.A.) Inc. | Carbonate diester solutions of PGE-type compounds |
| US4409239A (en) | 1982-01-21 | 1983-10-11 | Syntex (U.S.A.) Inc. | Propylene glycol diester solutions of PGE-type compounds |
| US4522811A (en) | 1982-07-08 | 1985-06-11 | Syntex (U.S.A.) Inc. | Serial injection of muramyldipeptides and liposomes enhances the anti-infective activity of muramyldipeptides |
| HU196714B (en) | 1984-10-04 | 1989-01-30 | Monsanto Co | Process for producing non-aqueous composition comprising somatotropin |
| IE58110B1 (en) | 1984-10-30 | 1993-07-14 | Elan Corp Plc | Controlled release powder and process for its preparation |
| US5391485A (en) | 1985-08-06 | 1995-02-21 | Immunex Corporation | DNAs encoding analog GM-CSF molecules displaying resistance to proteases which cleave at adjacent dibasic residues |
| US4810643A (en) | 1985-08-23 | 1989-03-07 | Kirin- Amgen Inc. | Production of pluripotent granulocyte colony-stimulating factor |
| JPS63500636A (ja) | 1985-08-23 | 1988-03-10 | 麒麟麦酒株式会社 | 多分化能性顆粒球コロニー刺激因子をコードするdna |
| US5033252A (en) | 1987-12-23 | 1991-07-23 | Entravision, Inc. | Method of packaging and sterilizing a pharmaceutical product |
| US5052558A (en) | 1987-12-23 | 1991-10-01 | Entravision, Inc. | Packaged pharmaceutical product |
| US5073543A (en) | 1988-07-21 | 1991-12-17 | G. D. Searle & Co. | Controlled release formulations of trophic factors in ganglioside-lipsome vehicle |
| IT1229203B (it) | 1989-03-22 | 1991-07-25 | Bioresearch Spa | Impiego di acido 5 metiltetraidrofolico, di acido 5 formiltetraidrofolico e dei loro sali farmaceuticamente accettabili per la preparazione di composizioni farmaceutiche in forma a rilascio controllato attive nella terapia dei disturbi mentali organici e composizioni farmaceutiche relative. |
| PH30995A (en) | 1989-07-07 | 1997-12-23 | Novartis Inc | Sustained release formulations of water soluble peptides. |
| US5120548A (en) | 1989-11-07 | 1992-06-09 | Merck & Co., Inc. | Swelling modulated polymeric drug delivery device |
| US5585112A (en) | 1989-12-22 | 1996-12-17 | Imarx Pharmaceutical Corp. | Method of preparing gas and gaseous precursor-filled microspheres |
| IT1246382B (it) | 1990-04-17 | 1994-11-18 | Eurand Int | Metodo per la cessione mirata e controllata di farmaci nell'intestino e particolarmente nel colon |
| US5733566A (en) | 1990-05-15 | 1998-03-31 | Alkermes Controlled Therapeutics Inc. Ii | Controlled release of antiparasitic agents in animals |
| US5543390A (en) | 1990-11-01 | 1996-08-06 | State Of Oregon, Acting By And Through The Oregon State Board Of Higher Education, Acting For And On Behalf Of The Oregon Health Sciences University | Covalent microparticle-drug conjugates for biological targeting |
| US5580578A (en) | 1992-01-27 | 1996-12-03 | Euro-Celtique, S.A. | Controlled release formulations coated with aqueous dispersions of acrylic polymers |
| US5323907A (en) | 1992-06-23 | 1994-06-28 | Multi-Comp, Inc. | Child resistant package assembly for dispensing pharmaceutical medications |
| TW333456B (en) | 1992-12-07 | 1998-06-11 | Takeda Pharm Ind Co Ltd | A pharmaceutical composition of sustained-release preparation the invention relates to a pharmaceutical composition of sustained-release preparation which comprises a physiologically active peptide. |
| US5360352A (en) | 1992-12-24 | 1994-11-01 | The Whitaker Corporation | Wire retainer for current mode coupler |
| US5591767A (en) | 1993-01-25 | 1997-01-07 | Pharmetrix Corporation | Liquid reservoir transdermal patch for the administration of ketorolac |
| US6274552B1 (en) | 1993-03-18 | 2001-08-14 | Cytimmune Sciences, Inc. | Composition and method for delivery of biologically-active factors |
| US5523092A (en) | 1993-04-14 | 1996-06-04 | Emory University | Device for local drug delivery and methods for using the same |
| US5985307A (en) | 1993-04-14 | 1999-11-16 | Emory University | Device and method for non-occlusive localized drug delivery |
| US6087324A (en) | 1993-06-24 | 2000-07-11 | Takeda Chemical Industries, Ltd. | Sustained-release preparation |
| US6004534A (en) | 1993-07-23 | 1999-12-21 | Massachusetts Institute Of Technology | Targeted polymerized liposomes for improved drug delivery |
| IT1270594B (it) | 1994-07-07 | 1997-05-07 | Recordati Chem Pharm | Composizione farmaceutica a rilascio controllato di moguisteina in sospensione liquida |
| US5759542A (en) | 1994-08-05 | 1998-06-02 | New England Deaconess Hospital Corporation | Compositions and methods for the delivery of drugs by platelets for the treatment of cardiovascular and other diseases |
| US5660854A (en) | 1994-11-28 | 1997-08-26 | Haynes; Duncan H | Drug releasing surgical implant or dressing material |
| US6316652B1 (en) | 1995-06-06 | 2001-11-13 | Kosta Steliou | Drug mitochondrial targeting agents |
| EP0835101B1 (en) | 1995-06-27 | 2004-06-09 | Takeda Chemical Industries, Ltd. | Method of producing sustained-release preparation |
| TW448055B (en) | 1995-09-04 | 2001-08-01 | Takeda Chemical Industries Ltd | Method of production of sustained-release preparation |
| JP2909418B2 (ja) | 1995-09-18 | 1999-06-23 | 株式会社資生堂 | 薬物の遅延放出型マイクロスフイア |
| US6039975A (en) | 1995-10-17 | 2000-03-21 | Hoffman-La Roche Inc. | Colon targeted delivery system |
| US5980945A (en) | 1996-01-16 | 1999-11-09 | Societe De Conseils De Recherches Et D'applications Scientifique S.A. | Sustained release drug formulations |
| TW345603B (en) | 1996-05-29 | 1998-11-21 | Gmundner Fertigteile Gmbh | A noise control device for tracks |
| US6264970B1 (en) | 1996-06-26 | 2001-07-24 | Takeda Chemical Industries, Ltd. | Sustained-release preparation |
| US6419961B1 (en) | 1996-08-29 | 2002-07-16 | Takeda Chemical Industries, Ltd. | Sustained release microcapsules of a bioactive substance and a biodegradable polymer |
| US6139865A (en) | 1996-10-01 | 2000-10-31 | Eurand America, Inc. | Taste-masked microcapsule compositions and methods of manufacture |
| CA2217134A1 (en) | 1996-10-09 | 1998-04-09 | Sumitomo Pharmaceuticals Co., Ltd. | Sustained release formulation |
| DK0839525T3 (da) | 1996-10-31 | 2004-11-29 | Takeda Pharmaceutical | Præparat med forlænget frigivelse |
| US6131570A (en) | 1998-06-30 | 2000-10-17 | Aradigm Corporation | Temperature controlling device for aerosol drug delivery |
| ATE233088T1 (de) | 1996-12-20 | 2003-03-15 | Takeda Chemical Industries Ltd | Verfahren zur herstellung einer zusammensetzung mit verzoegerter abgabe |
| US5891474A (en) | 1997-01-29 | 1999-04-06 | Poli Industria Chimica, S.P.A. | Time-specific controlled release dosage formulations and method of preparing same |
| US6120751A (en) | 1997-03-21 | 2000-09-19 | Imarx Pharmaceutical Corp. | Charged lipids and uses for the same |
| US6060082A (en) | 1997-04-18 | 2000-05-09 | Massachusetts Institute Of Technology | Polymerized liposomes targeted to M cells and useful for oral or mucosal drug delivery |
| PL341733A1 (en) | 1998-01-16 | 2001-05-07 | Takeda Chemical Industries Ltd | Prolonged release composition, method of obtaining same and application thereof |
| US6613358B2 (en) | 1998-03-18 | 2003-09-02 | Theodore W. Randolph | Sustained-release composition including amorphous polymer |
| US6048736A (en) | 1998-04-29 | 2000-04-11 | Kosak; Kenneth M. | Cyclodextrin polymers for carrying and releasing drugs |
| KR19990085365A (ko) | 1998-05-16 | 1999-12-06 | 허영섭 | 지속적으로 약물 조절방출이 가능한 생분해성 고분자 미립구 및그 제조방법 |
| US6248363B1 (en) | 1999-11-23 | 2001-06-19 | Lipocine, Inc. | Solid carriers for improved delivery of active ingredients in pharmaceutical compositions |
| US6271359B1 (en) | 1999-04-14 | 2001-08-07 | Musc Foundation For Research Development | Tissue-specific and pathogen-specific toxic agents and ribozymes |
| US7498171B2 (en) | 2002-04-12 | 2009-03-03 | Anthrogenesis Corporation | Modulation of stem and progenitor cell differentiation, assays, and uses thereof |
| US7968569B2 (en) | 2002-05-17 | 2011-06-28 | Celgene Corporation | Methods for treatment of multiple myeloma using 3-(4-amino-1-oxo-1,3-dihydro-isoindol-2-yl)-piperidine-2,6-dione |
| US7393862B2 (en) * | 2002-05-17 | 2008-07-01 | Celgene Corporation | Method using 3-(4-amino-1-oxo-1,3-dihydro-isoindol-2-yl)-piperidine-2,6-dione for treatment of certain leukemias |
| US20080051379A1 (en) | 2004-12-01 | 2008-02-28 | Trustees Of Boston University | Compositions and Methods for the Treatment of Peripheral B-Cell Neoplasms |
| MX2009001989A (es) * | 2006-08-30 | 2009-03-09 | Celgene Corp | Compuestos de isoindolina 5-substituidos. |
| US8877780B2 (en) * | 2006-08-30 | 2014-11-04 | Celgene Corporation | 5-substituted isoindoline compounds |
| WO2009085234A2 (en) * | 2007-12-20 | 2009-07-09 | Signal Pharmaceuticals, Inc. | Use of micro-rna as a biomarker of immunomodulatory drug activity |
| SG195613A1 (en) | 2008-10-29 | 2013-12-30 | Celgene Corp | Isoindoline compounds for use in the treatment of cancer |
| US9499514B2 (en) * | 2014-07-11 | 2016-11-22 | Celgene Corporation | Antiproliferative compounds and methods of use thereof |
| ES2957477T3 (es) | 2016-01-08 | 2024-01-19 | Celgene Corp | Compuestos antiproliferativos para usar en el tratamiento de leucemia |
| CN108601777B (zh) | 2016-01-08 | 2021-08-03 | 细胞基因公司 | 2-(4-氯苯基)-n-((2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉-5-基)甲基)-2,2-二氟乙酰胺的制剂 |
| EP3399981B1 (en) | 2016-01-08 | 2023-08-02 | Celgene Corporation | Solid forms of 2-(4-chlorophenyl)-n-((2-2,6-dioxopiperidin-3-yl)-1-oxoisoindolin-5-yl) methyl)-2,2-difluoroacetamide, and their pharmaceutical compositions and uses |
| MX2018015120A (es) | 2016-06-06 | 2019-04-15 | Celgene Corp | Tratamiento de una neoplasia maligna hematologica con 2-(4-clorofenil)-n-((2-(2,6-dioxopiperidin-3-il)-1-oxoisoindolin- 5-il)metil)-2,2-difluoroacetamida. |
-
2015
- 2015-07-09 US US14/795,837 patent/US9499514B2/en active Active
- 2015-07-10 DK DK15739485.9T patent/DK3166937T3/da active
- 2015-07-10 SG SG10202010780WA patent/SG10202010780WA/en unknown
- 2015-07-10 LT LT15739485T patent/LT3166937T/lt unknown
- 2015-07-10 KR KR1020177003826A patent/KR102477960B1/ko active IP Right Grant
- 2015-07-10 RS RS20191550A patent/RS59619B1/sr unknown
- 2015-07-10 MX MX2017000408A patent/MX2017000408A/es active IP Right Grant
- 2015-07-10 JP JP2017522462A patent/JP6779870B2/ja active Active
- 2015-07-10 EP EP15739485.9A patent/EP3166937B1/en active Active
- 2015-07-10 IL IL276946A patent/IL276946B/en unknown
- 2015-07-10 HU HUE15739485A patent/HUE046000T2/hu unknown
- 2015-07-10 AR ARP150102218A patent/AR101189A1/es unknown
- 2015-07-10 PL PL15739485T patent/PL3166937T3/pl unknown
- 2015-07-10 WO PCT/US2015/039926 patent/WO2016007848A1/en active Application Filing
- 2015-07-10 PT PT157394859T patent/PT3166937T/pt unknown
- 2015-07-10 CN CN201580048551.8A patent/CN106660991B/zh active Active
- 2015-07-10 ES ES19193334T patent/ES2968308T3/es active Active
- 2015-07-10 BR BR112017000550-6A patent/BR112017000550B1/pt active IP Right Grant
- 2015-07-10 SI SI201530944T patent/SI3166937T1/sl unknown
- 2015-07-10 CA CA2954784A patent/CA2954784C/en active Active
- 2015-07-10 AU AU2015287688A patent/AU2015287688B2/en active Active
- 2015-07-10 EA EA201790174A patent/EA033633B1/ru not_active IP Right Cessation
- 2015-07-10 CN CN202010096963.1A patent/CN111170991B/zh active Active
- 2015-07-10 SG SG11201700126RA patent/SG11201700126RA/en unknown
- 2015-07-10 ES ES15739485T patent/ES2760003T3/es active Active
- 2015-07-10 EP EP19193334.0A patent/EP3594211B1/en active Active
- 2015-07-13 TW TW104122680A patent/TWI660952B/zh active
-
2016
- 2016-09-23 US US15/275,045 patent/US9808451B2/en active Active
-
2017
- 2017-01-09 IL IL250008A patent/IL250008B/en active IP Right Grant
- 2017-01-09 SA SA517380693A patent/SA517380693B1/ar unknown
- 2017-01-10 MX MX2020007485A patent/MX2020007485A/es unknown
- 2017-01-10 ZA ZA2017/00217A patent/ZA201700217B/en unknown
- 2017-01-11 CO CONC2017/0000223A patent/CO2017000223A2/es unknown
- 2017-01-11 CL CL2017000075A patent/CL2017000075A1/es unknown
- 2017-01-12 EC ECIEPI20172135A patent/ECSP17002135A/es unknown
- 2017-10-02 US US15/723,065 patent/US9968596B2/en active Active
-
2018
- 2018-04-09 US US15/948,904 patent/US20180221361A1/en not_active Abandoned
-
2019
- 2019-06-10 US US16/436,819 patent/US11241423B2/en active Active
- 2019-10-07 HR HRP20191821TT patent/HRP20191821T1/hr unknown
- 2019-12-03 CY CY20191101269T patent/CY1122340T1/el unknown
-
2020
- 2020-10-14 JP JP2020173475A patent/JP2021011495A/ja active Pending
-
2021
- 2021-12-23 US US17/560,972 patent/US20220387413A1/en active Pending
-
2022
- 2022-10-26 JP JP2022171356A patent/JP2023011732A/ja active Pending
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2760003T3 (es) | Compuestos antiproliferativos y procedimientos de uso de los mismos | |
| US11560390B2 (en) | Compounds for the treatment of cancer and inflammatory disease | |
| US20230331693A1 (en) | Gspt1 compounds and methods of use of the novel compounds | |
| NZ765933B2 (en) | Antiproliferative compounds and methods of use thereof | |
| NZ728127B2 (en) | Antiproliferative compounds and methods of use thereof |