DE68907124T3 - Verfahren zum Stabilisieren von menschlichen Albuminlösungen und so erhaltene Lösung. - Google Patents
Verfahren zum Stabilisieren von menschlichen Albuminlösungen und so erhaltene Lösung. Download PDFInfo
- Publication number
- DE68907124T3 DE68907124T3 DE68907124T DE68907124T DE68907124T3 DE 68907124 T3 DE68907124 T3 DE 68907124T3 DE 68907124 T DE68907124 T DE 68907124T DE 68907124 T DE68907124 T DE 68907124T DE 68907124 T3 DE68907124 T3 DE 68907124T3
- Authority
- DE
- Germany
- Prior art keywords
- albumin
- solution
- sodium
- tween
- human albumin
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2/00—Disinfection or sterilisation of materials or objects, in general; Accessories therefor
- A61L2/02—Disinfection or sterilisation of materials or objects, in general; Accessories therefor using physical processes
- A61L2/04—Heat
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2103/00—Materials or objects being the target of disinfection or sterilisation
- A61L2103/05—Living organisms or biological materials
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Epidemiology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Pharmacology & Pharmacy (AREA)
- Medicinal Chemistry (AREA)
- Immunology (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Medicinal Preparation (AREA)
Description
- Die Erfindung betrifft ein Verfahren zum Stabilisieren von Human-Albuminlösungen zur therapeutischen Verwendung im Hinblick auf ihre Wärmebehandlung in einem Behälter, insbesondere im Endbehälter.
- Die Erfindung betrifft ebenfalls die durch das erfindungsgemäße Verfahren erhaltene Human-Albuminlösung.
- Bei der Herstellung von Human-Albuminlösungen ist das End-Pasteurisieren des Produkts bei 60°C über 10 Stunden ein obligatorischer Schritt. Dieser Schritt des Erwärmens ist Anfang der Jahre 1950 in den USA eingeführt worden, um den Hepatitis B-Virus zu inaktivieren, welcher möglicherweise trotz der verschiedenen Reinigungsschritte aufgrund der möglichen Kontamination des ersten biologischen Materials, im vorliegenden Fall zu dieser Zeit des menschlichen Bluts, im Endprodukt anwesend ist. Die Wirksamkeit dieses Pasteurisierens zum Ausschalten oder Vermindern des Risikos der Übertragung von Hepatitis B durch Albuminlösungen wurde zu Beginn bei gesunden Freiwilligen gezeigt. Studien, die beim Schimpansen durchgeführt wurden, haben anschließend gezeigt, daß das Hepatitis-Virus nicht-A nicht-B ebenfalls durch eine Behandlung von 10 Stunden bei 60°C inaktiviert wird. Diese Gegebenheiten waren der Gegenstand eines Übersichtartikels von GERETY und ARONSON (1). Seither haben verschiedene Studien in vitro mit Hilfe von Virus-Modellen gezeigt, daß das Pasteurisieren von Proteinlösungen über 10 Stunden bei 60°C als hinlänglich allgemeines Verfahren angesehen werden kann, um das Risiko einer Virus-Übertragung beim Empfänger zu vermindern, obwohl bestimmte Viren, wie das Parvovirus, gegen die thermische Inaktivierung resistenter als andere sind (2–3).
- Das Patent EP-A-0 050 061 sieht eine andere Lösung vor, welche bei Präparaten von Plasmaproteinen, z. B. Albumin, darin besteht, das Pasteurisieren durch Temperaturerhöhung zu vermeiden und im Gegensatz dazu durch die Wirkung von oberflächenaktiven Mitteln bei erhöhter Konzentration das Hepatitis-Virus zu inaktivieren und gegebenenfalls die Endotoxine auszuschalten. Diese Lösung bietet indessen nicht die Vorteile der Inaktivierung von Albuminpräparaten durch Wärme und erfordert, da das Präparat zur körperlichen Verabreichung bestimmt ist, darüber hinaus, daß die starken zur Inaktivierung verwendeten Konzentrationen an oberflächenaktivem Mittel entfernt werden.
- Das Patent EP-A-0 124 044 beschreibt ein Verfahren zum Pasteurisieren eines Proteins, wie z. B. des Fibronectins, in Gegenwart eines an das Fibronectin angepaßten stabilisierenden Mittels, wie z. B. Polyolen und insbesondere eines Disaccharids, zu dem es, mit dem Ziel, eine Beschädigung aufgrund der mechanischen Bewegung bei der industriellen Herstellung von Fibronectin während der thermischen Behandlung zu verhindern, ein oberflächenaktives Mittel und ein Chelat-bildendes oder Anti-Oxidations-Mittel hinzufügt. Die Gesamtheit des Verfahrens ist für Fibronectin und die Pasteurisierungsbehandlung in großem Volumen in industriellem Maßstab mit mechanischem Bewegen spezifisch.
- Heute schreiben sämtliche nationalen und internationalen Pharmakopöen das Pasteurisieren von Albuminlösungen bei 60°C über 10 Stunden vor, wobei dieses Pasteurisieren im allerletzten Stadium der Herstellung, nämlich im Endbehälter, im allgemeinen einem Fläschchen aus neutralem Glas, vorgenommen werden muß; siehe z. B. die Europäische Pharmakopöe, II. Auflage von 1984, die Pharmakopöe der USA, XXI. Auflage, und die japanische Pharmakopöe von 1986. Trotz der relativen Stabilität des Albumins gegen Wärme muß dieses mit Hilfe von geeigneten Stabilisatoren geschützt werden, um jegliche Gelbildung während des Pasteurisierens zu vermeiden. Die heute gleichsam generell verwendeten Stabilisatoren sind Natriumcaprylat und Natriumacetyltryptophanat, allein oder in Kombination. Speziell schreiben die Pharmakopöen der USA, XXI. Auflage, und von Japan 1986 Natriumacetyltryptophanat allein in einer Dosis von 0,16 Millimol pro Gramm Albumin oder auch die Mischung Natriumacetyltryptophanat/Natriumcaprylat jeweils in einer Dosis von 0,08 Millimol pro Gramm Albumin vor. Natriummandelat kann ebenfalls allein oder zusammen mit Natriumcaprylat verwendet werden (siehe die französische Pharmakopöe, VIII. Ausgabe von 1965).
- Die Stabilisatoren werden nach den Pharmakopöen der USA und von Japan in großem Überschuß bezüglich Albumin, nämlich 10 Moleküle Stabilisator auf 1 Molekül Albumin, hinzugefügt, und aufgrund ihrer besonderen Affinität zu Albumin sind sie in der Lage, es wirksam gegen eine direkte Denaturierung durch die Wärme zu schützen. In Abwesenheit dieser Stabilisatoren ist die Denaturierung des Albumins unvermeidlich und führt zu einer fortschreitenden Aggregation der Albuminmoleküle, was sich im Erscheinen einer Opaleszenz und dann in einer vollständigen Gelbildung der Lösung äußert.
- Wenn auch diese Opaleszenz und diese Gelbildung durch die Verwendung der vorstehend beschriebenen Stabilisatoren vermieden werden, ist es bekannt, daß nach dem Pasteurisieren eine gewisse Anzahl von Fläschchen mit Albumin bei einer visuellen Überprüfung feine flockige Teilchen oder Fädchen oder Häute in mehr oder weniger großer Anzahl aufweisen. Dieses Phänomen ist bei den Albuminpräparaten, die verdünnter sind, d. h. mit 4% oder 5% Proteinen, ausgeprägter als bei den Präparaten, die konzentrierter sind, d. h. mit 20% Proteinen.
- Abgesehen davon, daß das Feststellen dieser unlöslichen Teilchen die Verwerfung der betroffenen Fläschchen während der Endüberprüfung im Rahmen der Qualitätskontrolle verlangt, was sich in einem ökonomischen Verlust äußert, verrät das Erscheinen dieser Teilchen während des Pasteurisierens eine gewisse Denaturierung des Produkts, was Zweifel an seiner guten Verträglichkeit bei der eventuellen Verabreichung an den Menschen hinterlassen kann.
- Die Erfindung hat zum Ziel, diesen Nachteil abzustellen, indem sie ein Verfahren zur Stabilisierung von Human-Albuminlösungen im Hinblick auf ihre Wärmebehandlung in einem Behälter, insbesondere dem Endbehälter, vorschlägt, welches eine vollkommene Stabilisierung gestattet und zu einer mit dem normalen Gebrauch dieser Lösungen kompatiblen Human-Albuminlösung führt.
- Gegenstand der Erfindung ist ein Pasteurisations-Wärmebehandlungsverfahren einer Humanalbumin-Lösung mit einer Reinheit gemäß dem in Pharmacopée Européenne (2. Ausgabe von 1984 unter der Bezeichnung "Albumini humani solutio") oder dem Code of Federal Regulations (Ausgabe vom 1. April 1986 unter der Bezeichnung "Albumin (human)" und "Plasma protein fraction (human)") definierten Zustand, wobei diese in die endgültigen Fläschchen für die therapeutische Verwendung verteilt werden kann, in Gegenwart eines Stabilisierungsmittels, das an die Stabilisierung des Albumins während dessen Wärmebehandlung angepasst ist, dadurch gekennzeichnet, dass man die Wärmebehandlung in einem Behälter in Gegenwart eines oberflächenaktiven Mittels, ausgewählt aus Tween 80, Tween 20, Pluronic F68 und Laurat von Polyethylenglycol 600, und weiterhin des Stabilisierungsmittels, durchführt.
- Das im erfindungsgemäßen Verfahren verwendete oberflächenaktive Mittel spielt nicht die gleiche Rolle wie die gewöhnliche stabilisierende Formulierung und kann sich deshalb nicht an dessen Stelle setzen. Tatsächlich resultiert das Auftreten von Teilchen als Folge des Pasteurisierens nicht aus den gleichen Gründen, die ursprünglich in der Verwendung der gewöhnlichen Stabilisatoren liegen, wie es weiter unten erläutert wird, sondern aus Wechselwirkungen der Lösung mit der Wand des Behälters bei der thermischen Behandlung.
- Dieses Phänomen beobachtet man in Fläschchen aus klassischem neutralem Glas, z. B. Borsilikatglas vom Typ I, oder aus durch Behandlung mit Schwefeldioxid oder Ammoniumsulfat an der Oberfläche neutralisiertem Glas vom Typ II, wie sie in den Pharmakopöen Europas und der USA beschrieben sind (Société SAINT-GOBAIN DESJONQUERES), aber auch in Fläschchen aus Kunststoffmaterial, z. B. aus Polystyrol (Société CORNING). Dieses Phänomen läßt demnach wahrscheinlich denaturierende hydrophobe Wechselwirkungen zwischen dem Produkt und der Wand des Fläschchens mitspielen.
- Unter gewöhnlicher stabilisierender Mischung versteht man insbesondere Natriumcaprylat, Natriumacetyltryptophanat, Natriummandelat oder eine Mischung von zwei oder drei derselben.
- Erfindungsgemäß liegen die Konzentrationen vorteilhafterweise im Bereich zwischen 5 und 50 mg/l zu stabilisierende Lösung. Es genügt ungefähr 0,25 bis 1 Molekül eines geeigneten oberflächenaktiven Mittels auf 100 Moleküle Albumin jeweils in einer Lösung von 200 bis 50 g/l, um die Denaturierung und das Auftreten von unlöslichen Teilchen nach dem Pasteurisieren in Gegenwart der gewöhnlichen stabilisierenden Formulierung zu verhindern.
- Das bevorzugte oberflächenaktive Mittel ist Tween 80 mit einem mittleren Molekulargewicht von 1320 Dalton. Es muß bei einer Konzentration oberhalb von 5 mg/l und vorzugsweise zwischen 10 und 20 mg/l verwendet werden. Eine Konzentration von Tween 80 von 10 mg/l zu stabilisierende Lösung für eine Albuminlösung von 50 g/l entspricht 1 Molekül dieses Stabilisators auf 100 Moleküle Albumin.
- In einer speziellen Ausführungsform der Erfindung wird das oberflächenaktive Mittel in einem frühen Stadium der Herstellung des Albumins zugesetzt. In einem solchen Fall muß die anfängliche Konzentration des oberflächenaktiven Mittels so sein, daß der verbleibende Anteil des letzteren zum Zeitpunkt des Pasteurisierens ausreichend ist, um die gewünschte Schutzwirkung sicherzustellen.
- Bei den Lösungen von Human-Albumin, welche die Erfindung betrifft, handelt es sich insbesondere um alle Proteinlösungen, bei denen Albumin der Haupt-Proteinbestandteil ist, d. h. mehr als 80% der Gesamtheit der Proteine darstellt, und die zur klinischen Verwendung beim Menschen bestimmt sind. Sie sind insbesondere in der Europäischen Pharmakopöe, II. Auflage von 1984, unter der Bezeichnung "Albumini humani solutio" und im Code of Federal Regulations der USA, Ausgabe vom 1. April 1986, unter der Bezeichnung "Albumin (human)" und "Plasma protein fraction (human)" definiert.
- Das durch die Erfindung betroffene Human-Albumin wird insbesondere durch Extraktion und Reinigung gemäß jedem geeigneten Verfahren, ausgehend von einer menschlichen Albumin-Quelle oder auch von Kulturen tierischer, pflanzlicher Zellen, von Bakterien oder Hefen, die mit Hilfe gentechnischer Verfahren zum Produzieren von Human-Albumin transformiert worden sind, gewonnen. Unter den geeigneten Verfahren zur Extraktion und Reinigung von Human-Albumin kann man speziell die Fraktionierung von Plasma mit Hilfe von Alkohol, von COHN et al. (4) beschrieben, oder die Fraktionierung von Plazenta-Blut mit Hilfe von Alkohol und Zink, von TAYLOR et al. (5) beschrieben, oder die Fraktionierung von Plazenta-Blut mit Hilfe von Alkohol, Natriumcaprylat und Aluminiumgel, von LIAUTAUD et al. (6) beschrieben, oder die Fraktionierung von Plazenta-Blut mit Hilfe von Alkohol und durch Chromatographie, wie von TAYOT et al. (7) beschrieben, oder die Fraktionierung von Plasma durch Chromatographie, wie im US-Patent Nr. 4,675,384 beschrieben, aufführen.
- Die Erfindung wird nun mit Hilfe von nicht beschränkenden Beispielen beschrieben.
- BEISPIEL 1
- Man versuchte, die Stabilität einer Lösung von Albumin zu 50 g/l, erhalten durch Fraktionierung von Plazenta-Blut mit Hilfe von Alkohol und durch Chromatographie, wie von TAYOT et al. (4) beschrieben, zu verbessern. Das erhaltene Albumin weist eine Protein-Reinheit von 100% in der Analyse durch Elektrophorese auf Celluloseacetat und in der Zweidimensionalen Immunelektrophorese (Gegenwart eines einzigen Peaks) auf.
- Der Versuch bestand darin, die Mengen klassischer Stabilisatoren, Natriumcaprylat und Natriumacetyltryptophanat, im Verhältnis zu den durch die Pharmakopöe der USA vorgeschriebenen Mengen zu vergrößern, während man einen Natriumanteil von 145 mÄq/l und eine pH von 7,0 aufrechterhielt. Das Albumin wurde filtriert, dann in 100 ml-Fläschchen aus Glas vom Typ I verteilt und 10 Stunden bei 60°C im Wasserbad pasteurisiert. Die Fläschchen wurden vor und nach Pasteurisieren und spontanem Abkühlen an Luft überprüft. Kein Fläschchen wies vor dem Pasteurisieren sichtbare Teilchen auf.
- Man stellt fest (siehe Tabelle I), daß die klassischen Stabilisatoren trotz der stark vergrößerten Dosen es nicht zulassen, die Gegenwart von Teilchen in den pasteurisierten Fläschchen zu vermeiden. Diese Feststellung bestätigt die Tatsache, daß die durch die klassischen Stabilisatoren verhinderte Gelbildung und die Bildung von Teilchen zwei unabhängige physikalische Phänomene sind.
- BEISPIEL 2
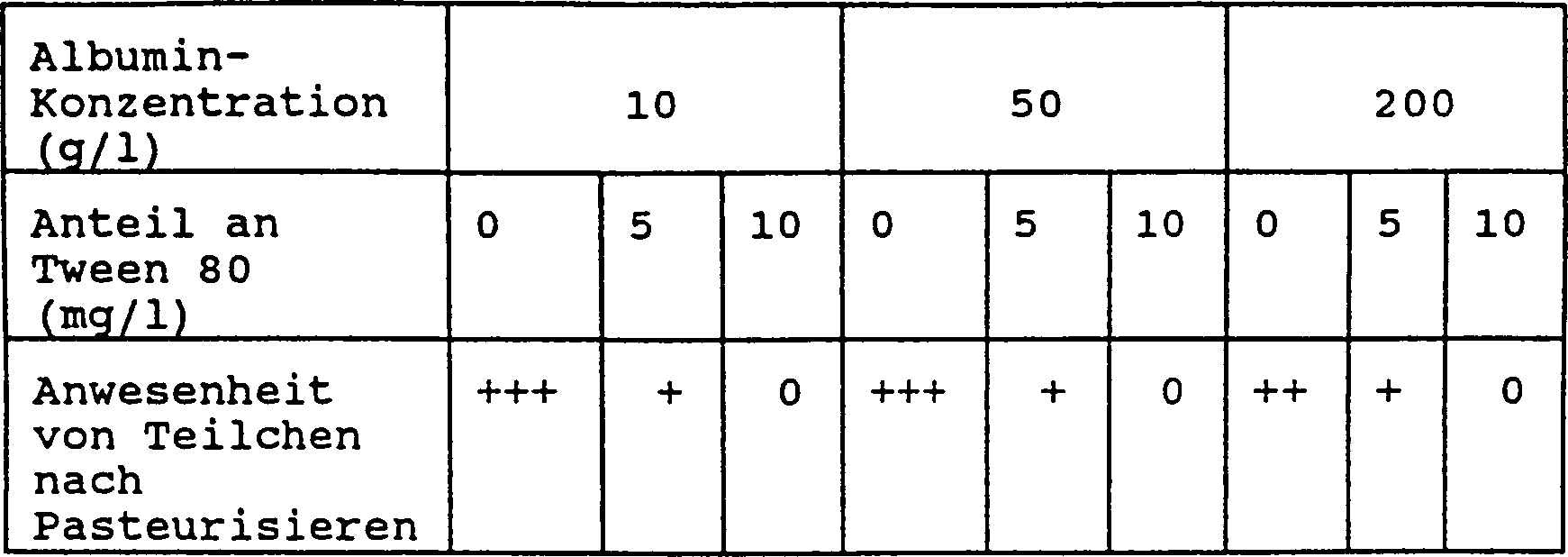
- Ausgehend von einem Plazenta-Albumin, hergestellt wie in Beispiel 1, stellte man Lösungen von Proteinen zu 200 g/l, 50 g/l und 10 g/l her, die mit einer Standard-Stabilisierungsformulierung, z. B., 0,08 mMol Natriumcaprylat/g Protein und 0,08 mMol Natriumacetyltryptophanat/g Protein, stabilisiert waren. Natrium wurde mit Natriumchlorid auf 145 mÄq/l eingestellt, und der pH wurde auf 7,0 eingestellt. Zu den Lösungen wurden anschließend 0 oder 5 oder 10 mg/l Tween 80 gegeben, dann wurden sie filtriert und in 100 ml-Fläschchen aus Glas vom Typ I verteilt, dann 10 Stunden bei 60°C im Wasserbad pasteurisiert. Kein Fläschchen wies vor dem Pasteurisieren sichtbare Teilchen auf.
- Man stellt fest (siehe Tabelle II), daß Tween 80 in der Dosis von 10 mg/l, wie groß auch die Albumin-Konzentration in der Lösung ist, vollständig die Bildung von sichtbaren Teilchen verhindert.
- BEISPIEL 3
- Man versuchte, die Stabilität einer Lösung von Albumin zu 50 g/l, erhalten durch Fraktionieren von Plasma nach dem Verfahren von LOHN, zu verbessern. Das Albumin wurde in lyophilisierter Form von der Gesellschaft HYLAND geliefert. Das Pulver wurde wieder in Lösung gegeben und auf 50 g/l Proteine eingestellt und mit einer Standard-Stabilisierungsformulierung, z. B. 0,08 mMol Natriumcaprylat/g Protein und 0,08 mMol Natriumacetyltryptophanat/g Protein, stabilisiert. Natrium wurde mit Natriumchlorid auf 145 mÄq/l eingestellt, und der pH wurde auf 7,0 eingestellt. Zu einem Teil dieser Lösung wurden 10 mg/l Tween 80 gegeben. Die beiden erhaltenen Lösungen wurden filtriert und in 100 ml-Fläschchen aus Glas vom Typ I verteilt, dann 10 Stunden bei 60°C im Wasserbad pasteurisiert. Kein Fläschchen wies vor dem Pasteurisieren sichtbare Teilchen auf.
- Man stellt fest, (siehe Tabelle III), daß Tween 80 in der Dosis von 10 mg/l vollständig die Bildung von sichtbaren Teilchen im Albumin von COHN zu 50 g/l, das 10 Stunden bei 60°C einem Pasteurisieren unterzogen wurde, verhindert.
Claims (7)
- Verfahren zum Stabilisieren von Human-Albuminlösungen zur therapeutischen Verwendung im Hinblick auf ihre Wärmebehandlung in einem Behälter, insbesondere im Endbehälter, mit Hilfe eines Stabilisierungsmittels, das an die Stabilisierung des Albumins während dessen Wärmebehandlung angepaßt ist, dadurch gekennzeichnet, daß man vor der Wärmebehandlung zusätzlich zu dem Stabilisierungsmittel ein oberflächenaktives Mittel, ausgewählt aus Tween 80, Tween 20, Pluronic F68 und Laurat von Polyethylenglykol 600, zusetzt.
- Verfahren nach Anspruch 1, dadurch gekennzeichnet, daß das oberflächenaktive Mittel in einer Konzentration von 5 bis 50 mg/l eingesetzt wird.
- Verfahren nach Anspruch 1, dadurch gekennzeichnet, daß das Tween 80 in einer Konzentration über 5 mg/l und insbesondere im Bereich von 10 bis 20 mg/l eingesetzt wird.
- Verfahren nach irgendeinem der Ansprüche 1 bis 3, dadurch gekennzeichnet, daß man zu der zu stabilisierenden Human-Albuminlösung die übliche stabilisierende Formulierung gibt, das Natrium mit Natriumchlorid auf 145 mÄq/l und den pH auf 7,0 einstellt, das oberflächenaktive Mittel hinzufügt, filtriert, dann die Lösung in Fläschchen verteilt und 10 Stunden bei 60°C pasteurisiert.
- Verfahren nach Anspruch 4, dadurch gekennzeichnet, daß sich die übliche stabilisierende Formulierung aus 0,08 mMol Natriumcaprylat und 0,08 mMol Natriumacetyltryptophanat pro Gramm Albumin zusammensetzt.
- Verfahren nach Anspruch 1, dadurch gekennzeichnet, daß man das oberflächenaktive Mittel in einem frühen Stadium der Herstellung des Albumins zusetzt.
- Human-Albuminlösung, erhalten durch das in einem der vorangehenden Ansprüche beschriebene Verfahren.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR8804936 | 1988-04-14 | ||
| FR8804936A FR2630115B1 (fr) | 1988-04-14 | 1988-04-14 | Procede de stabilisation des solutions d'albumine humaine et solution obtenue |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| DE68907124D1 DE68907124D1 (de) | 1993-07-22 |
| DE68907124T2 DE68907124T2 (de) | 1993-11-04 |
| DE68907124T3 true DE68907124T3 (de) | 2005-10-06 |
Family
ID=9365304
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE68907124T Expired - Lifetime DE68907124T3 (de) | 1988-04-14 | 1989-04-06 | Verfahren zum Stabilisieren von menschlichen Albuminlösungen und so erhaltene Lösung. |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US5118794A (de) |
| EP (1) | EP0341103B2 (de) |
| JP (1) | JP2970911B2 (de) |
| AT (1) | ATE90573T1 (de) |
| AU (1) | AU617451B2 (de) |
| CA (1) | CA1339440C (de) |
| DE (1) | DE68907124T3 (de) |
| ES (1) | ES2055120T5 (de) |
| FR (1) | FR2630115B1 (de) |
Families Citing this family (42)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5981485A (en) | 1997-07-14 | 1999-11-09 | Genentech, Inc. | Human growth hormone aqueous formulation |
| US4939176A (en) * | 1988-12-20 | 1990-07-03 | Miles Inc. | Viral inactivation process |
| AT402891B (de) * | 1991-06-20 | 1997-09-25 | Immuno Ag | Verfahren zur herstellung eines inaktivierten blutproduktes |
| AT399818B (de) * | 1992-04-24 | 1995-07-25 | Immuno Ag | Verfahren zur herstellung einer hochgereinigten virussicheren faktor viii-präparation |
| ES2154650T3 (es) * | 1992-10-02 | 2001-04-16 | Genetics Inst | Composicion que comprende una formulacion con factor de coagulacion viii, procedimiento para su preparacion y uso de un tensioactivo como estabilizador. |
| AU6653094A (en) * | 1992-12-16 | 1994-07-04 | Immuno Aktiengesellschaft | Process for preparing a virus-safe biological composition |
| DE69428521T2 (de) * | 1993-02-02 | 2002-05-23 | Xoma Technology Ltd | Arzneizusammensetzungen enthaltend ein bakterizides permeabilität erhöhendes protein und ein tensid |
| SE9301581D0 (sv) * | 1993-05-07 | 1993-05-07 | Kabi Pharmacia Ab | Protein formulation |
| DE4320294A1 (de) * | 1993-06-18 | 1994-12-22 | Immuno Ag | Verwendung von humanem Protein C zur Verhinderung und Behandlung von Thrombozytenablagerungen |
| JPH07126182A (ja) * | 1993-10-27 | 1995-05-16 | Green Cross Corp:The | 組換えヒト血清アルブミン製剤の滅菌方法 |
| US5932544A (en) * | 1994-05-31 | 1999-08-03 | Xoma Corporation | Bactericidal/permeability-increasing protein (BPI) compositions |
| USRE38827E1 (en) | 1994-07-27 | 2005-10-11 | 3M Innovative Properties Company | Adhesive sealant composition |
| US5583114A (en) | 1994-07-27 | 1996-12-10 | Minnesota Mining And Manufacturing Company | Adhesive sealant composition |
| AT403989B (de) * | 1996-09-16 | 1998-07-27 | Immuno Ag | Verfahren zur herstellung eines plasmaprotein-hältigen arzneimittels |
| JPH10251161A (ja) * | 1997-03-11 | 1998-09-22 | Green Cross Corp:The | 浮腫治療効果増強剤 |
| DE19830914C1 (de) * | 1998-07-10 | 1999-06-24 | Centeon Pharma Gmbh | Verfahren zur Herstellung einer Proteinlösung |
| DE19858188A1 (de) | 1998-12-17 | 2000-07-06 | Centeon Pharma Gmbh | Verfahren zum Auflösen von Albuminflocken in einer Flüssigkeit sowie Einrichtung zur Durchführung des Verfahrens |
| US7780967B2 (en) | 2000-02-08 | 2010-08-24 | Allergan, Inc. | Reduced toxicity Clostridial toxin pharmaceutical compositions |
| US20030118598A1 (en) * | 2000-02-08 | 2003-06-26 | Allergan, Inc. | Clostridial toxin pharmaceutical compositions |
| KR100753765B1 (ko) * | 2000-02-08 | 2007-08-31 | 알레간 인코포레이티드 | 보툴리눔 독소 약제학적 조성물 |
| US8632785B2 (en) * | 2000-02-08 | 2014-01-21 | Allergan, Inc. | Clostridial toxin pharmaceutical composition containing a gelatin fragment |
| US20060269575A1 (en) * | 2000-02-08 | 2006-11-30 | Allergan, Inc. | Botulinum toxin pharmaceutical compositions formulated with recombinant albumin |
| GB0305989D0 (en) * | 2003-03-15 | 2003-04-23 | Delta Biotechnology Ltd | Agent |
| ES2526913T3 (es) * | 2004-08-04 | 2015-01-16 | Ipsen Biopharm Limited | Composición farmacéutica que contiene neurotoxina 2 botulínica |
| ES2627627T3 (es) * | 2004-08-04 | 2017-07-28 | Ipsen Biopharm Limited | Composición farmacéutica que contiene neurotoxina botulínica A2 |
| JP2006045173A (ja) * | 2004-08-09 | 2006-02-16 | Hidetoshi Tsuchida | 表面修飾血清アルブミン−金属ポルフィリン複合体、およびそれを含有する酸素輸液 |
| JP2009520714A (ja) | 2005-12-22 | 2009-05-28 | ツェー・エス・エル・ベーリング・ゲー・エム・ベー・ハー | 低オクタノエート型ヒトアルブミン |
| TW200806315A (en) * | 2006-04-26 | 2008-02-01 | Wyeth Corp | Novel formulations which stabilize and inhibit precipitation of immunogenic compositions |
| JP4935242B2 (ja) * | 2006-08-24 | 2012-05-23 | ニプロ株式会社 | 脂肪酸を含有するs−ニトロソタンパク質とその製法 |
| BR112012030950B1 (pt) | 2010-06-04 | 2020-02-04 | Wyeth Llc | composição imunogênica multivalente, formulação, frasco, dispositivo de distribuição de vacinas pré-enchido, kit, e recipiente |
| JP2016028102A (ja) * | 2015-10-21 | 2016-02-25 | 株式会社スリー・ディー・マトリックス | タンパク質の凝集抑制剤 |
| CN106963942A (zh) * | 2016-01-13 | 2017-07-21 | 华北制药集团新药研究开发有限责任公司 | 重组人血白蛋白的液体制剂 |
| WO2017205588A1 (en) * | 2016-05-26 | 2017-11-30 | Zhuhai Beihai Biotech Co., Ltd. | Formulations of chlorambucil |
| CA3058234A1 (en) | 2017-03-16 | 2018-09-20 | Therapure Biopharma Inc. | Method for purification of albumin |
| US11739166B2 (en) | 2020-07-02 | 2023-08-29 | Davol Inc. | Reactive polysaccharide-based hemostatic agent |
| US12161777B2 (en) | 2020-07-02 | 2024-12-10 | Davol Inc. | Flowable hemostatic suspension |
| MX2023007767A (es) | 2020-12-28 | 2023-07-07 | Davol Inc | Materiales hemostaticos secos en polvo reactivos que comprenden una proteina y un agente de entrelazado a base de polietilenglicol modificado multifuncional. |
| CN114544926A (zh) * | 2021-12-02 | 2022-05-27 | 浙江鑫科医疗科技有限公司 | 一种血清蛋白稳定剂 |
| CH720224B1 (de) | 2023-08-18 | 2024-05-31 | Csl Behring Ag | Verfahren zur Sterilfiltration albuminhaltiger wässriger Lösungen |
| CN118652320B (zh) * | 2024-08-16 | 2024-11-05 | 通化安睿特生物制药股份有限公司 | 一种速溶重组人白蛋白冻干的制备方法及其应用 |
| CN118681001B (zh) * | 2024-08-19 | 2024-12-06 | 通化安睿特生物制药股份有限公司 | 一种含人白蛋白和葡萄糖的透析液及其制备方法 |
| CN119846228A (zh) * | 2025-01-08 | 2025-04-18 | 武汉生之源生物科技股份有限公司 | 一种变性缓冲液、类风湿因子试剂盒及其制备方法和应用 |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4315919A (en) * | 1980-10-06 | 1982-02-16 | Edward Shanbrom | Depyrogenation process |
| DE3173208D1 (en) * | 1980-10-06 | 1986-01-23 | Edward Shanbrom | Method of reducing undesirable activities of biological and pharmaceutical products |
| US4314997A (en) * | 1980-10-06 | 1982-02-09 | Edward Shanbrom | Purification of plasma protein products |
| CA1213827A (en) * | 1983-04-29 | 1986-11-12 | Ricardo H. Landaburu | Process for pasteurizing fibronectin |
| US4585654A (en) * | 1983-04-29 | 1986-04-29 | Armour Pharmaceutical Co. | Process for pasteurizing fibronectin |
| US4540573A (en) * | 1983-07-14 | 1985-09-10 | New York Blood Center, Inc. | Undenatured virus-free biologically active protein derivatives |
| EP0445108A1 (de) * | 1986-03-10 | 1991-09-11 | RUBINSTEIN, Alan I. | Verfahren zur behandlung von gammaglobulin |
-
1988
- 1988-04-14 FR FR8804936A patent/FR2630115B1/fr not_active Expired - Lifetime
-
1989
- 1989-04-06 AT AT89400947T patent/ATE90573T1/de not_active IP Right Cessation
- 1989-04-06 DE DE68907124T patent/DE68907124T3/de not_active Expired - Lifetime
- 1989-04-06 EP EP89400947A patent/EP0341103B2/de not_active Expired - Lifetime
- 1989-04-06 ES ES89400947T patent/ES2055120T5/es not_active Expired - Lifetime
- 1989-04-11 US US07/336,387 patent/US5118794A/en not_active Expired - Lifetime
- 1989-04-12 AU AU32756/89A patent/AU617451B2/en not_active Expired
- 1989-04-13 CA CA000596561A patent/CA1339440C/en not_active Expired - Fee Related
- 1989-04-14 JP JP1095049A patent/JP2970911B2/ja not_active Expired - Lifetime
Also Published As
| Publication number | Publication date |
|---|---|
| EP0341103B2 (de) | 2003-08-13 |
| DE68907124D1 (de) | 1993-07-22 |
| US5118794A (en) | 1992-06-02 |
| FR2630115A1 (fr) | 1989-10-20 |
| DE68907124T2 (de) | 1993-11-04 |
| CA1339440C (en) | 1997-09-02 |
| ES2055120T3 (es) | 1994-08-16 |
| JP2970911B2 (ja) | 1999-11-02 |
| ES2055120T5 (es) | 2004-04-16 |
| FR2630115B1 (fr) | 1994-10-28 |
| ATE90573T1 (de) | 1993-07-15 |
| AU3275689A (en) | 1989-10-19 |
| AU617451B2 (en) | 1991-11-28 |
| JPH01311027A (ja) | 1989-12-15 |
| EP0341103B1 (de) | 1993-06-16 |
| EP0341103A1 (de) | 1989-11-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE68907124T3 (de) | Verfahren zum Stabilisieren von menschlichen Albuminlösungen und so erhaltene Lösung. | |
| DE69329651T3 (de) | Wässrige arzneizusammensetzung, welche das menschliche wachstumshormon enthält | |
| DE2751717C2 (de) | ||
| DE3876600T2 (de) | Plasma- und rekombinationsproteinformulierungen in einem milieu hoher ionenstaerke. | |
| DE3520228C2 (de) | Wasserlösliche bioaktive Trockenfeststoffzusammensetzung, Verfahren zu ihrer Herstellung und sie enthaltende pharmazeutische Präparate | |
| DE69432179T3 (de) | Eine formulierung des gerinnungsfaktors viii | |
| DE69531204T2 (de) | Formulierungen fuer faktor ix | |
| DE69329795T2 (de) | Zusammensetzung, welche den koagulationsfaktor viii beinhaltet; verfahren zu deren herstellung und die benutzung eines oberflächenaktiven stoffes als stabilisator | |
| DE69333928T2 (de) | Verbesserte solubilisierung und stabilisierung des faktor viii-komplexes | |
| EP0352500B1 (de) | Verfahren zur Herstellung eines intravenös verabreichbaren polyklonalen immunoglobulin-Präparates mit hohemIgM-Gehalt. | |
| DE69821741T2 (de) | Immunoglobulin enthaltende zusammensetzung | |
| DE3927111C3 (de) | Verfahren zur Herstellung nicht modifizierter intravenös verabreichbarer IgM- und/oderIgA-haltiger Immunglobulinpräparate | |
| DE4111393A1 (de) | Stabilisierte faktor viii-praeparationen | |
| DE69630291T2 (de) | Proteinformulierung, die koajulationsfehler viii oder ix in einer saccharose wässriger lösung enthält | |
| DE10333317A1 (de) | Formulierung für Proteinarzneimittel ohne Zusatz von humanem Serumalbumin (HSA) | |
| EP0971958B1 (de) | Verfahren zur reinigung von faktor viii/vwf-komplex mittels kationenaustauscherchromatographie | |
| DE69029765T2 (de) | Stabilisierung von hochgereinigten Proteinen | |
| DE3786832T2 (de) | Verfahren zur Herstellung von Immunoglobulinzubereitungen für intravenöse Injektion. | |
| EP0722344B1 (de) | Verfahren zur virusinaktivierung in gegenwart eines polyethers und eines agens | |
| AT403989B (de) | Verfahren zur herstellung eines plasmaprotein-hältigen arzneimittels | |
| DE3888571T2 (de) | Stabilisierung von biologischen und pharmazeutischen Produkten während der Inaktivierung von viralen und bakteriellen Keimen. | |
| DE69632771T2 (de) | Menschliche therapeutische Albumin mit niedriger Aluminiumbindungsfähigkeit | |
| DE69303941T2 (de) | Verfahren zur Herstellung von hochreinem Fibrinogen | |
| AT405135B (de) | Präparation umfassend thiolgruppen-hältige proteine | |
| DE60226327T2 (de) | Reinigungsverfahren zur grossmassstabigen produktion von gc-globulin, damit erhaltenes produkt und dessen verwendung in medizin |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 8363 | Opposition against the patent | ||
| 8366 | Restricted maintained after opposition proceedings | ||
| 8327 | Change in the person/name/address of the patent owner |
Owner name: AVENTIS PASTEUR, LYON, FR |