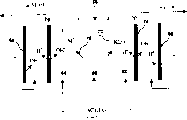CN1258598C - 用于纯化和回收葡萄糖酸衍生物的电渗析方法 - Google Patents
用于纯化和回收葡萄糖酸衍生物的电渗析方法 Download PDFInfo
- Publication number
- CN1258598C CN1258598C CNB998064831A CN99806483A CN1258598C CN 1258598 C CN1258598 C CN 1258598C CN B998064831 A CNB998064831 A CN B998064831A CN 99806483 A CN99806483 A CN 99806483A CN 1258598 C CN1258598 C CN 1258598C
- Authority
- CN
- China
- Prior art keywords
- acid derivatives
- gluconic acid
- klg
- electrodialysis
- spissated
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P7/00—Preparation of oxygen-containing organic compounds
- C12P7/40—Preparation of oxygen-containing organic compounds containing a carboxyl group including Peroxycarboxylic acids
- C12P7/58—Aldonic, ketoaldonic or saccharic acids
- C12P7/60—2-Ketogulonic acid
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D61/00—Processes of separation using semi-permeable membranes, e.g. dialysis, osmosis or ultrafiltration; Apparatus, accessories or auxiliary operations specially adapted therefor
- B01D61/42—Electrodialysis; Electro-osmosis ; Electro-ultrafiltration; Membrane capacitive deionization
- B01D61/44—Ion-selective electrodialysis
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D61/00—Processes of separation using semi-permeable membranes, e.g. dialysis, osmosis or ultrafiltration; Apparatus, accessories or auxiliary operations specially adapted therefor
- B01D61/42—Electrodialysis; Electro-osmosis ; Electro-ultrafiltration; Membrane capacitive deionization
- B01D61/44—Ion-selective electrodialysis
- B01D61/445—Ion-selective electrodialysis with bipolar membranes; Water splitting
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H7/00—Compounds containing non-saccharide radicals linked to saccharide radicals by a carbon-to-carbon bond
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P20/00—Technologies relating to chemical industry
- Y02P20/141—Feedstock
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Water Supply & Treatment (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Urology & Nephrology (AREA)
- Wood Science & Technology (AREA)
- Genetics & Genomics (AREA)
- General Health & Medical Sciences (AREA)
- Biotechnology (AREA)
- Biochemistry (AREA)
- Zoology (AREA)
- Microbiology (AREA)
- Molecular Biology (AREA)
- General Chemical & Material Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Engineering & Computer Science (AREA)
- Separation Using Semi-Permeable Membranes (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Water Treatment By Electricity Or Magnetism (AREA)
Abstract
一种用于纯化和浓缩葡萄糖酸衍生物,例如2-酮-L-古洛糖酸的方法,包括将至少包括葡萄糖酸衍生物和/或其盐的非活性的和/或酸化的发酵培养基或活体外反应器培养基加以电渗析,从而纯化和浓缩葡萄糖酸衍生物。
Description
技术领域
本发明一般涉及用于优选的最终产品的分离和纯化的电渗析方法,特别是涉及用于纯化和回收葡萄糖酸衍生物的电渗析方法,这样的葡萄糖酸衍生物例如,是源自发酵反应器和活体外反应器去除的溶液的2-酮-L-古洛糖酸。
本发明的背景技术
葡萄糖酸衍生物,即2-酮-L-古洛糖酸(以下简写为KLG),是包括抗坏血酸(维生素C)在内的重要化合物生产中的关键中间体。然而,在KLG至抗坏血酸的转化过程中,为了获得高产量,KLG必须进行只含有有限量杂质的高度纯化。
生产KLG简便的方法是通过发酵方法进行。然而,由于多数发酵肉汤通过添加碱性物质,保持在中性或接近中性的pH值,生产出KLG盐而不是KLG。而且,发酵肉汤也含有细胞、中性物质和其它无用的物质。这些附加的成分会阻碍后续的用于将KLG转化为抗坏血酸的化学过程,因此,KLG必须从肉汤分离。因此,应该理解,任何用于KLG的发酵方法必须与有效的回收和纯化方法结合。
US5747306公开了一种采用电渗析的分离方法。该活性发酵肉汤通过添加碱性物质,例如氢氧化钠、氢氧化钾或氨水保持在5至9之间的接近中性或碱性pH值范围内。该肉汤接着通过含有多重阳离子和阴离子交换膜的电渗析槽,其中KLG盐从肉汤中去除。含中性物质,例如确保微生物生存的营养素的活性发酵肉汤接着再循环进发酵系统用于再使用。然而,该电渗析方法产生的纯化KLG盐流,在转化至抗坏血酸过程中产量较低。
另外,通过采用活的和代谢的活性微生物将有机糖转换至KLG盐的现有技术方法是复杂的,且需要一直小心以保持用于微生物生长和/或代谢的发酵肉汤有活力和活性,以确保基质至KLG盐的满意转化。
为了克服在从发酵培养基回收KLG期间与KLG盐的高浓度有关的问题,US4990441公开了一种用硫酸酸化发酵培养基,从而导致该盐阳离子与硫酸根阴离子和质子化的KLG阴离子沉淀的方法。然而,应该注意到该培养基含有KLG盐也含有无机杂质,例如磷酸根和氯化物阴离子,在加入硫酸的情况下它们会转化成其对应的酸。结果,这些无机酸在例如蒸发结晶或直接干燥的KLG回收方法中被浓缩,且可以导致酸催化KLG降解。为了解决这个问题,现有技术将含KLG和其它杂质的培养基与阳离子和阴离子交换树脂接触以去除任何离子化杂质。但是,存在于发酵肉汤中的中性有机物包括简单和复杂的糖可以在该溶液pH值下未被电离,且由此该培养基通过阳离子和阴离子交换树脂而未被去除。同样地。纯化的KLG的回收由于培养基中的这些中性物质的存在而被限制。在KLG蒸发结晶期间中性糖被浓缩,导致母液粘度的增加。结果,多程结晶变得困难,且限制了KLG回收。另外,中性物质阻碍了作为回收的优选方法的直接干燥,该方法具有较低的资金投入和较高的KLG产量。
由此,需要用于葡萄糖酸衍生物,例如KLG浓缩和纯化的方法,该方法提供较高的KLG产量而无其盐,没有无机杂质和中性有机物的污染和/或不需要保持发酵培养基用于活的和活性的微生物培养基的生长和/或代谢。
本发明概要
对本发明来说,出现在说明书和权利要求书中的下述术语和措辞被定义为下述意思:
“葡萄糖酸衍生物”被定义为衍生于葡萄糖酸的有机酸,包括,但不仅限于2,4,酮-D-葡萄糖酸、2,5,二酮-D-葡萄糖酸、艾杜糖酸、2-酮-L-古洛糖酸(KLG)、香草酸和抗坏血酸。
“发酵反应器”被定义为标准的发酵反应器,其中有活的和活性的微生物或细胞,例如用于碳水化合物代谢的细菌。
“发酵培养基”是来源于标准发酵反应器的培养基或肉汤。
“活体外反应器”是这样一种反应器,其中酶是基本上无非生命、非活性和非代谢的细胞结构,酶附着于非生命、非活性和非代谢的细胞结构或酶固定在具有化学氧化能力的基质和/或化学还原基质或合成葡萄糖酸衍生物路径上的中间体上。
“活体外反应器培养基”是来源于活体外反应器的培养基或溶液,包括至少一种葡萄糖酸衍生物盐和辅酶。
“辅酶”是对酶起催化作用所需要的有机分子,例如烟酰胺、腺嘌呤二核甙酸、烟酰胺腺嘌呤二核甙酸磷酸酯和其混合物。
“中性物质”被定义为在溶液pH环境中基本上未电离的糖和/或化合物。
“非活性发酵培养基”指的是在发酵肉汤或培养基中的条件,例如pH,使得用于发酵方法的微生物不能在其中存活,且培养基或肉汤在无预处理的情况下,不能被再循环回发酵槽中再使用。
“非生命培养基”指的是从发酵反应器或活体外反应器,例如非活性发酵培养基或活体外反应器培养基,去除的培养基,其中不存在能够生长和/或代谢的活性细胞或活性微生物,其用于生产葡萄糖酸衍生物和/或其盐。
本发明的主要目的是提供一种新型的电渗析方法,用于浓缩和纯化来源于酸化的和/或非活性发酵培养基或活体外反应器培养基的葡萄糖酸衍生物。
本发明的另一个目的是提供一种电渗析纯化方法,该方法产生较高的KLG回收率,以及后续的较高的抗坏血酸产量,从而实现在抗坏血酸的生产中较低的资金投入和操作成本。
本发明进一步的目的是提供一种电渗析纯化方法,使得回收的产品不需酸催化降解,并且由于降低了母液的粘度,可以通过蒸发结晶回收方法来达到多路。
本发明再进一步的目的是提供一种电渗析纯化方法,浓缩最终产品至高纯度,例如KLG,可以采用KLG直接干燥以提供接近同样的定量回收。
本发明的又一个目的是提供一种电渗析纯化方法,回收昂贵的辅酶和/或酶,该辅酶和/或酶用于活体外反应器系统,该系统用于化学合成葡萄糖酸衍生物的盐,例如KLG。
通过包括下述步骤的电渗析纯化方法可以实现所有的上述目的:
a)提供一种无生命培养基,例如酸化的和/或非活性的发酵培养基或活体外反应器培养基包括至少一种葡萄糖酸衍生物和/或其盐;和
b)通过电渗析从无生命培养基去除葡萄糖酸衍生物,从而提供至少包括葡萄糖酸衍生物的浓缩液。
本发明另外的目的是提供用于制备纯化和浓缩的葡萄糖酸衍生物的方法,包括下述步骤:
a)提供一种酸化的和/或非活性的发酵培养基,至少包括葡萄糖酸衍生物、无机杂质和中性物质,其中葡萄糖酸衍生物基本上被质子化。
b)通过电渗析从酸化的和/或非活性的发酵培养基去除葡萄糖酸衍生物和无机杂质,从而提供至少包括葡萄糖酸衍生物和无机杂质的浓缩的酸化水溶液;
c)从浓缩的酸化的水溶液分离无机杂质,从而提供纯化的和浓缩的葡萄糖酸衍生物水溶液;和
d)从纯化和浓缩的水溶液回收葡萄糖酸衍生物。
从浓缩的、酸化水溶液分离无机杂质的步骤通过几种方法可以实现,这些方法包括但不仅限于电渗析和阴离子交换树脂。当酸化的和/或非活性的发酵培养基在游离酸结构中含大量的葡萄糖酸衍生物例如KLG时,本方法是特别有利的。
本发明还有另一个目的是提供制备高纯化和浓缩的KLG的方法,包括下述步骤:
a)提供至少包含KLG、无机杂质和中性物质的酸化的和/或非活性的发酵培养基;
b)通过电渗析从酸化的和/或非活性发酵培养基去除至少KLG和无机杂质,从而提供至少包括KLG和无机杂质的浓缩酸化水溶液,以及一种废液,其包含基本上耗尽了KLG的废酸化和/或非活性发酵培养基;和
c)通过电渗析从浓缩、酸化的水溶液分离无机杂质,从而提供纯化的和浓缩的KLG水溶液。
通过任何本领域公知的回收方法包括蒸发结晶或直接干燥,可以实现纯化的KLG的回收。
通过第一电渗析堆可以实现步骤(b)的电渗析方法,包括:
(i)在阳极液室的一个阳极,该阳极与阳极液流接触,在阴极液室的一个阴极,该阴极与阴极液流接触,且电渗析(以下简称ED)膜堆排列在阳极和阴极之间。ED膜堆包括至少一个进料室,至少一个浓缩室和交替的阴离子和阳离子交换膜,被散布在进料室和浓缩室之间。阴离子交换膜必须优选地输送KLG阴离子和无机阴离子以使酸化的发酵培养基中的中性物质排除。酸化的和/或非活性的发酵培养基被引入进料室,且含酸或盐的水溶液被引入浓缩室。对阳极和阴极施加充分的电压,使得质子或其它阳离子穿过阳离子交换膜迁移进浓缩室,而KLG阴离子和无机阴离子穿过阴离子交换膜输送进浓缩室,浓缩室中浓缩的酸化的水溶液被收集,其至少包括KLG和无机杂质。酸化的和/或非活性的发酵培养基将KLG耗尽,且从系统排除作为废液。
通过第二电渗析堆可以实现步骤(c)的电渗析方法,包括:
i)在阳极液室的一个阳极,该阳极与阳极液流接触,在阴极液室的一个阴极,该阴极与阴极液流接触,且ED膜堆排列在阳极和阴极之间。ED膜堆包括至少一个进料室,至少一个浓缩室和交替的阴离子和阳离子交换膜,被散布在进料室和浓缩室之间。阴离子交换膜必须优选地输送无机阴离子以使浓缩的、酸化的水溶液中的KLG阴离子被排除。浓缩的、酸化的水溶液被引入进料室,且含酸或盐的水溶液被引入浓缩室。对阳极和阴极施加充分的电压,使得质子或其它阳离子穿过阳离子交换膜迁移进浓缩室,而无机阴离子穿过阴离子交换膜输送进浓缩室。KLG遗留在进料液流中,从而提供纯化的和浓缩的KLG水溶液。
本发明的酸化的和/或非活性发酵培养基优选pH值小于4.5,更优选小于3.5,最优选小于2,其中葡萄糖酸衍生物、且特别是KLG基本上是质子化的。本文所用的“基本上被质子化”意思是葡萄糖酸衍生物至少80%被质子化,且优选超过90%被质子化。
在一个可选择的实施方案中,用于分离无机杂质的步骤(c)可以在上述方法的步骤(b)之前进行。
在第一电渗析堆中,KLG和无机杂质从酸化的和/或非活性的发酵培养基中去除,其中KLG阴离子,以及如果存在的无机阴离子被输送穿过阴离子交换膜。在这种情况下,该膜拒绝中性物质的通过。以下,该第一电渗析电池被简称为“KLG ED”。
在第二电渗析堆中,通过使用阴离子交换膜,无机杂质例如酸或盐从KLG分离,该交换膜对无机阴离子是选择透过性的,但它不能输送KLG阴离子。该阴离子交换膜必须对KLG阴离子的输送具有非常高的抵抗力,使得无机阴离子的输送具有最小限度的KLG损失。以下,该第二电渗析堆被简称为“脱盐ED”。脱盐ED指的是去除了无机酸以及无机盐。
发明人已经发现,如果辅酶在葡萄糖酸衍生物的化学合成中用作氧化还原辅因子,通过将该辅酶返还回活体外反应器可以被再使用,则活体外反应器提供一种生产KLG更有效和更经济的方法。使用在活体外反应器培养基中不具有生命和代谢活性的细胞或微生物的活体外反应器的优点是很多的,包括通过活细胞使用的可选择代谢路径被关闭。应该理解,基质的转化,例如,碳水化合物和/或中间体分子至优选的最终产品是预定的。因此,基质和/或中间体分子不会因被转化成不需要的副产品而被浪费。作为替代,采用最有效的转化路径,从而从基质或中间体分子生产出较高产量的优选的葡萄糖酸衍生物。
使用活体外反应器,若有细胞的话,该细胞含氧化还原酶是死亡的和/或不存在的,且严格地通过化学氧化还原反应转化成葡萄糖酸衍生物盐。然而,在葡萄糖酸衍生物的化学合成中用作氧化还原辅因子的辅酶在反应器培养基中是需要的,且这些辅酶的回收是必要的,这是由于更换的成本太高。考虑到这些,发明人发现采用电渗析的方法回收这些昂贵而有价值的辅酶用于再使用或循环回反应器容器。
由此可以理解,本发明还有另一个目的,就是公开一种制备高纯度和浓缩的KLG的方法,包括下述步骤:
a)提供一种至少包括葡萄糖酸衍生物阴离子、金属抗衡离子和辅酶的活体外反应器培养基;和
b)将活体外反应器培养基引入电渗析电池,该电池至少包括一个双极性膜,其中葡萄糖酸衍生物阴离子被质子化,且金属抗衡离子增加一个氢氧离子,从而提供至少包括葡萄糖酸衍生物的浓缩的水溶液和包括金属氢氧化物溶液的液流。另外,一个包括辅酶的分离液流也可以包括在该方法中。
在这个实施方案中,可以使用几种不同的双极性膜电渗析(ED)堆,包括两个或三个室的双极性膜电渗析堆。该两室堆包括在阳极液室的一个阳极,该阳极与阳极液流接触,在阴极液室的一个阴极,该阴极与阴极液流接触,且两室双极性膜ED堆排列在阳极和阴极之间。两室双极性膜ED堆包括至少一个阴离子交换膜,双极性膜位于阴离子交换膜的对面,且空出足够的空间来设置至少一个进料室和至少一个浓缩室,位于该电池不同端的阳极和阴极与提供通过该电池堆电流的电源连接。阴离子交换膜必须优选输送葡萄糖酸衍生物阴离子,例如KLG阴离子,和无机阴离子以使中性带电分子排除。至少含葡萄糖酸衍生物盐的活体外反应器培养基被引入进料室。水或葡萄糖酸衍生物或其盐的水溶液被引入浓缩室。对阳极和阴极之间施加足够大的电压以分离水,用以在双极性膜上形成质子和氢氧离子,且通过阴离子交换膜将葡萄糖酸衍生物阴离子输送进双极性膜ED堆的浓缩室。葡萄糖酸衍生物阴离子通过阴离子交换膜被输送,同时中性物质的通过被阻止。一旦通过添加形成在双极性膜的质子,葡萄糖酸衍生物阴离子被输送进浓缩或酸室,葡萄糖酸衍生物阴离子被转化成其酸的形式。通过添加形成在双极性膜的氢氧离子,在进料溶液中本来与葡萄糖酸衍生物阴离子结合的阳离子被转化成碱。最后效果是形成了浓缩的和纯化的葡萄糖酸衍生物,例如KLG和从KLG钠盐分解的碱,例如苛性钠。
在两室结构中,替换KLG阴离子的氢氧离子通过将CO2添加至进料溶液而被中和,使得进料室中的pH值保持在使剩余的KLG的碱催化分解不会发生的范围。结果,两室结构的产品是纯化的和浓缩的KLG溶液和含至少包括金属碳酸盐或碳酸氢盐、金属氢氧化物和辅酶中的一种或全部的溶液。
三室双极性膜ED堆包括排列在碱室和浓缩室之间的进料或稀释室;碱室通过阳离子交换膜与进料室分离;而浓缩室通过阴离子交换膜与进料室分离。这些三室单元通过双极性膜作为端部被限制住,双极性膜给碱室提供氢氧离子,给浓缩室提供质子。该三室双极性膜ED堆由至少排列在阳极和阴极之间的这些三室单元中的一组组成。在该三室结构中,氢氧离子被引入碱室,与来自进料室穿过阳离子交换膜迁移的阳离子结合。因此,向碱中添加缓冲剂例如CO2不是必需的,因为葡萄糖酸衍生物例如KLG的进料溶液通过阳离子膜从碱中分离。或者,如果在碱溶液中优选的最终产品是碳酸盐或碳酸氢盐,可以添加CO2。因此,三室结构的产品是在浓缩室中的纯化的和浓缩的KLG溶液,源自碱室的金属氢氧化物溶液和含至少一种辅酶的液流,该液流可以被收集和再使用或再循环回反应器容器。如果在进料溶液中含有任何中性物质,它们仍遗留在其中。
两室和三室结构这两者的共同之处是阴离子交换膜,该膜对葡萄糖酸衍生物阴离子的输送具有低的抵抗力,且对葡萄糖酸衍生物阴离子的输送比起在进料溶液中发现的任何中性物质的输送呈选择性。
生产的葡萄糖酸衍生物例如KLG的纯化溶液适合于通过进一步的加工,即通过蒸发结晶或其它回收技术,例如直接干燥包括喷雾干燥或薄膜干燥来回收。如果去除不想要的无机酸,可以期待较高的KLG回收,因为基于浓缩的KLG酸催化分解电位被去除。从KLG分离例如中性物质的有机杂质,使KLG的回收更高,因为在蒸发期间由于夹杂的中性物质的降低均可以造成粘度的增加。而且,通过ED,已经被纯化的KLG在后续转换成抗坏血酸的过程中可以被喷雾干燥而没有产量的损失。
附图简要说明
图1是用于将至少含有葡萄糖酸衍生物,且特别是KLG(KLGED)的酸化的和/或非活性的发酵培养基与培养基中的任何中性物质分离的ED膜电池的示意图。
图2是用于将无机杂质从至少包含葡萄糖酸衍生物,例如KLG的酸化的和/或非活性的发酵培养基分离的ED膜电池的示意图(脱盐ED)。
图3是用于从活性的或非活性的发酵培养基;或活体外反应器培养基浓缩和纯化葡萄糖酸衍生物、例如KLG的两室双极性膜ED电池的示意图(盐分解KLG ED)。
图4是用于从活性的或非活性的发酵培养基浓缩和纯化葡萄糖酸衍生物、且特别是KLG的三室双极性膜ED电池的示意图(盐分解KLGED)。
图5是用于从活体外反应器培养基浓缩和纯化葡萄糖酸衍生物、且特别是KLG的三室双极性膜ED电池的示意图(盐分解KLG ED)。
优选实施方案说明
在本发明的一个实施方案中,其中进料溶液是酸化的和/或非活性的发酵培养基,葡萄糖酸衍生物例如KLG和/或其盐可以通过在发酵方法中活的微生物代谢碳水化合物而制备。任何能够将碳水化合物转化成葡萄糖酸衍生物或其盐、且特别是2-酮-L-古洛糖酸或其盐的微生物可以用于本发明。
在浓缩和纯化葡萄糖酸衍生物例如KLG之前,发酵肉汤优选通过下述的任意一种或全部步骤预处理:(i)过滤或离心以去除任何微生物细胞和其它微粒;(ii)通过添加酸例如硫酸进行酸化,用以质子化KLG和使大多数阳离子沉淀,该大多数阳离子在发酵期间引入肉汤(用以保持确保微生物生存能力的可接受的pH值),从而提供非活性的和/或酸化的发酵培养基;(iii)碳处理以吸附色体和其它有机杂质;(iv)阳离子交换树脂,例如Amberlite IRC120、Amberlite 200C用以更完全地质子化任何遗留的KLG阴离子和/或以去除可溶的阳离子,例如钙;(v)阴离子交换树脂,例如Amberlite IRA 93,AmberliteIRA 94用以去除能够弄脏ED膜的无机或有机杂质;(vi)用聚合的吸附树脂处理以去除杂质;和(vii)通过脱盐ED去除无机酸或盐例如硫酸(见图2的说明)。另外,稳定的阴离子或阳离子交换树脂或其混合物可以加入进料溶液室中以提供加强的无机离子大量传输至膜表面(如果包括在进料溶液中)。
如果该溶液已经通过蒸发结晶进行了回收KLG的处理,则图1的电渗析电池可以用在结晶母液上以去除中性物质,且可以进一步地进行KLG的浓缩和回收。
酸化的和/或实质上非活性的发酵肉汤被引入如图1所示的电渗析堆。KLG ED方法和ED电池堆被用于至少从酸化的和/或非活性的发酵肉汤中去除KLG,同时在非活性的发酵肉汤中遗留中性物质。KLGED堆的组成包括用电解液清洗的一个阳极(2)和阴极(4)、包括至少排列在阳极和阴极之间的一个进料室(6)和一个浓缩室(8)的电渗析电池堆(5),至少一个进料室和浓缩室分别通过交替的阴离子和阳离子交换膜(10)和(12)被分离。
阳极(2)对电渗析条件是稳定的,且可以包括碳,例如石墨,铂、钯、铱、金、钌等贵金属或合金,贵金属或合金沉积在诸如钛或钽等电子管金属上。一般,阳极反应会是水的氧化,以产生氧和质子(反应式1)。
阳极(4)可以包括碳、贵金属和合金、镍、钢等。一般,阴极反应根据反应式2从水的还原产生氢和氢氧化物。
阳极和阴极用电解液清洗,且一般阳极电解液和阴极电解液溶液是惰性强酸、碱或盐溶液,例如硫酸、氢氧化钠或硫酸钠。
引入进料室(6)的是进料电解液溶液包括酸化的和/或非活性的发酵培养基,该培养基至少包括葡萄糖酸衍生物例如KLG。
引入如图1所示的浓缩室(8)的是最初包括去离子水的浓缩溶液,或KLG或其盐以足够的量溶于水的溶液,以提供溶液的导电性。
如图1所示的KLG ED电池堆进一步包括分离进料室和浓缩室的至少一个交替的阴离子(10)和阳离子(12)交换膜。该阳离子交换膜可以是弱酸性的(例如羧酸型)、中等酸性的(例如膦酸型),或强酸性的(磺酸阳离子交换基)。该阳离子膜对电渗析条件必须稳定,在葡萄糖酸衍生物溶液中对透析有较低的抵抗力,且可以包括全氟化膜例如DuPont Nafion或任何非全氟化阳离子交换膜例如NeoseptaCMX,这两者均可以市售得到。阴离子交换膜可以是强、适度的或弱碱性的,且一般包括季铵或叔铵基。阴离子交换膜也必须在该堆条件下稳定,且具有足够的开孔结构,使得葡萄糖酸衍生物阴离子的输送可以在适度的低电位下发生。而且,阴离子交换膜应基本上防止进料液流中的任何中性物质的输送。优选阴离子交换膜是Neosepta AFX。多数包含阴离子和阳离子交换膜的这些两室单元可以在电渗析堆中堆叠在一起,该电渗析堆至少具有一对位于外部的和相对的电池端的电极。
在势场的影响下,电压决定膜对数,且优选范围是0.1至10V/每对,阳离子将通过阳离子交换膜(12)朝着阴极(4)迁移,进入浓缩室(8)。葡萄糖酸衍生物阴离子,且特别是KLG阴离子将穿过阴离子交换膜(10)朝着阳极(2)迁移,进入浓缩室(8),形成浓缩液中的纯化的和浓缩的KLG溶液,且将中性物质遗留在进料溶液中。在该方式中,KLG几乎完全从进料溶液去除,以高达约3-4倍或更多的系数浓缩,且与任何中性物质分离。将KLG与中性物质在进料液流中分离的结果是可以通过直接干燥浓缩液进行KLG的回收。
存在的任何无机阴离子例如,氯离子、硫酸根离子或磷酸根离子优选超过葡萄糖酸衍生物阴离子的输送传送进浓缩液。在浓缩中,如果无机阴离子以酸存在,KLG ED浓缩液中的无机酸的增强可以启动质子回迁。通过下述任何方式可以防止回迁:(i)向浓缩液添加足够量的强碱例如氢氧化钠,以中和无机酸;(ii)从浓缩液的初馏分去除无机酸,由于无机酸的传送优于葡萄糖酸衍生物,因此该浓缩液几乎没有葡萄糖酸衍生物;(iii)用阴离子交换树脂从浓缩液去除强酸;和(iv)同时进行ED堆脱盐操作,以从浓缩液去除无机酸,与通过将浓缩液从KLG ED堆送进脱盐ED堆它们的增强几乎一样快速(如图2所示)。这四种技术均可以防止在浓缩液中强酸的增强和接下来的质子穿过阴离子交换膜回迁,否则可以导致电流效率的损失。作为进一步的好处是葡萄糖酸衍生物,例如KLG的酸催化分解在蒸发结晶或直接干燥期间被避免。
图1所示的KLG ED电池堆可以在单元电池电压从约0.1至约10V/每阴离子/阳离子交换膜对,和更优选从约0.5至约3V/每对的情况下操作。温度范围应在约5℃至约90℃之间,更优选从约20℃至约50℃。较高的温度可以导致一些膜和葡萄糖酸衍生物的降解,因此应予避免。该方法可以连续或间歇地运行。
用于将无机杂质从葡萄糖酸衍生物,特别是KLG的浓缩溶液中分离的一个优选方法如图2所示。该图显示出脱盐ED方法和用于从包括KLG或图1所示的电渗析电池产生的KLG浓缩液的酸化的和/或非活性的发酵培养基中分离无机酸或盐的ED膜电池堆中的膜结构。电渗析堆的组成包括用电解液清洗的阳极(20)和阴极(22),和一个至少具有排列在阳极和阴极之间的一个进料室(26)和一个浓缩室(28)的电渗析电池堆(24),其中进料室和浓缩室分别通过交替的阴离子(30)和阳离子(32)交换膜分离。
最初引入脱盐ED堆的浓缩室(28)的是去离子水或溶于水的无机酸或盐的溶液。引入进料室(26)的是进料电解液溶液,其中可以包括,非活性和/或酸化的发酵培养基;溶于水的优选的葡萄糖酸衍生物和/或该衍生物的盐的溶液;或从图1所示的电渗析电池获得的浓缩溶液,至少包括葡萄糖酸衍生物,例如KLG和无机杂质。
一般,进料溶液来源于显示出酸化的和/或非活性的发酵肉汤,且可以包括来源于无生命的微生物,例如细胞、中性物质、碱性阳离子和无机酸的碎屑中的任何一种或全部。对于进料溶液的预处理步骤可以包括下述的一种或全部:(i)过滤以去除细胞和其它微粒;(ii)通过添加用作对葡萄糖酸衍生物,例如KLG的盐质子化的合适的酸,例如硫酸进行酸化,且使大多数阳离子,例如硫酸钙沉淀(如果在酸化之前,KLG以钙盐的形式存在)并提供非活性和/或酸化的发酵培养基;(iii)碳处理以吸附色体和其它有机杂质;(iv)阳离子交换以对葡萄糖酸衍生物的盐更彻底地质子化和/或去除可溶钙;(v)阴离子交换以去除可以弄脏ED膜的的杂质;(vi)用聚合吸附树脂处理以去除杂质;(vii)蒸发结晶;和(viii)通过如图1所示的电渗析堆去除中性物质。另外,可以向进料电解液溶液室添加稳定的阴离子或阳离子交换树脂或其混合物,以提供增强的无机离子向膜表面的大量输送。
脱盐ED电池堆还包括至少一个交替阴离子(30)和阳离子(32)交换膜来将进料室和浓缩室分离。该阳离子交换膜可以是弱酸性的(例如羧酸交换基)、中等酸性的(例如膦酸型)或强酸性的(例如磺酸阳离子交换基)。该阳离子膜对用于电渗析电池的条件必须稳定,在溶液中对透析有较低的抵抗力,且可以包括全氟化膜例如DuPontNafion或任何非全氟化阳离子交换膜例如Neosepta CMX。阴离子交换膜可以是强、适度的或弱碱性的,且包括季铵或叔铵基。阴离子交换膜也必须稳定,且具有足够的闭孔结构使得无机阴离子例如氯离子或硫酸根离子通过该膜传送,同时对葡萄糖酸衍生物阴离子的传送基本上或全部阻止。而且,如果需要去除无机酸,阴离子交换膜应优选是低质子回迁型的,例如Asahi Glass Selemion AAV或Neosepta ACM。这种类型的膜通过防止质子从浓缩室至进料室回迁,将会改善该方法的电流效率。
或者,浓缩室中的无机酸可以与例如氢氧化钠的强碱中和,使得质子回迁被阻止。
许多这些包括阴离子和阳离子的膜的两室单元可以在电渗析堆中堆叠在一起,该电渗析堆至少具有一对位于外部端的电极。
在势场的影响下,阳离子将通过阳离子交换膜(32)朝着阴极(22)迁移,进入浓缩室(28)。无机阴离子将穿过阴离子交换膜(30)朝着阳极(20)迁移,进入浓缩室(28),形成无机酸或盐的溶液,且将纯化的葡萄糖酸衍生物溶液遗留在进料溶液中(如果原始的进料溶液是来源于图1所示的电渗析堆的浓缩液)。当无机阴离子耗尽时,电池电流会降到接近于零,因为葡萄糖酸衍生物阴离子遗留在进料液中,基本上防止了通过膜结构穿过阴离子交换膜的输送。
图2所示的脱盐ED电池堆,可以在单元电池电压从约0.1至约10V/每阴离子/阳离子交换膜对,和更优选从约0.5至约3V/每对的情况下操作。温度范围应在约5℃至约90℃之间,更优选从约20℃至约50℃。较高的操作温度可以导致膜和葡萄糖酸衍生物的降解。该方法可以连续或间歇地运行。
图3、4和5显示了所采用的盐分解KLG ED方法和两或三室双极性膜ED电池堆。在盐分解KLG ED方法中,葡萄糖酸衍生物,例如KLG的盐被转化成纯化的和浓缩的KLG。
如图3所示的两室电渗析堆的成分,包括用电解液清洗的阳极(40)和阴极(42),和一个至少具有排列在阳极和阴极之间的一个进料室(44)和一个浓缩室(46)的电渗析电池堆(43)。进料室和浓缩室通过阴离子交换膜(48)分离。双极性膜(50)位于阴离子交换膜的两侧。
引入两室双极性膜ED电池堆的进料室(44)的是进料电解液溶液,其中可以包括包含至少有葡萄糖酸衍生物盐和辅酶的活体外反应器培养基;至少包含葡萄糖酸衍生物盐的非活性发酵培养基;含该衍生物盐的溶液;或溶于水的KLG盐。应选择该衍生物的盐,使其基于碱的添加,不能形成不溶的沉淀物,否则,这些沉淀物会弄脏双极性膜或阳离子膜。合适的盐的典型例子包括碱金属盐,例如钠和钾或铵盐。
如果进料源自活性的或非活性的发酵培养基,对于该溶液的预处理步骤应包括上述的一种或全部预处理步骤:(i)过滤以去除细胞和其它微粒;(ii)碳处理以吸附色体和其它有机杂质;(iii)通过添加无机酸例如硫酸以使葡萄糖酸衍生物的盐质子化,并沉淀硫酸盐形式的金属抗衡离子给予发酵培养基酸化的和/或非活性;(iv)添加碱金属盐例如硫酸钠或碳酸钠,造成硫酸钙或碳酸钙沉淀,并形成适合于双极性膜ED堆的盐分解ED的葡萄糖酸衍生物的碱金属盐;(v)阳离子交换以去除二价金属,否则这些金属在与碱接触的情况下形成弄脏膜的沉淀物;(vi)阴离子交换以去除可以弄脏ED膜的的杂质;(vii)用聚合的吸附树脂处理以去除杂质;和(viii)通过脱盐ED(如图1所示)去除无机盐例如硫酸钠。
另外,可以向进料溶液室添加稳定的阴离子或阳离子交换树脂或其混合物,以提供增强的无机离子向膜表面的大量输送。
引入两室双极性膜ED电池堆的浓缩室(46)的是最初包括去离子水或浓缩的葡萄糖酸衍生物溶液,例如溶于水的KLG的浓缩溶液。
图3所示的两室双极性膜电渗析电池堆进一步包括阴离子交换膜(48)和至少一个双极性膜(50),其中阴离子交换膜将进料室和浓缩室分离。双极性膜由阴离子交换层和与其粘合的阳离子交换层,例如Neosepta BP-1或其他的组成。该膜将水分离形成低电位的氢氧离子和质子。该阴离子交换膜可以是强、适度的或弱碱性的,且包括季铵或叔铵基。阴离子交换膜必须在电渗析电池条件下稳定,且具有足够的开孔结构,使得葡萄糖酸衍生物阴离子的输送,可以在适度的低电位下发生。而且,阴离子交换膜应防止任何中性物质的输送。许多这些包括阴离子和双极性膜的两室单元可以在电渗析堆中堆叠在一起,该电渗析堆至少具有一对位于外部端的电极。
在势场的影响下,水将在双极性膜中被分离形成氢氧离子和质子。氢氧离子朝着阳极(40)迁移,进入两室双极性膜ED电池的进料室(44),其中它们将与金属阳离子,例如Na+结合,以形成例如氢氧化钠的碱。可以使用二氧化碳,因为它是发酵方法的副产品,也可以加入进料中,以中和氢氧化物使得进料pH值不会呈碱性,以避免葡萄糖酸衍生物的分解。质子将朝着阴极(42)迁移,进入浓缩室(46),其中它们将会与穿过阴离子膜(48)朝着阳极(40)迁移的葡萄糖酸衍生物的阴离子结合,从而形成纯化的、和浓缩的葡萄糖酸衍生物溶液,且将任何中性物质和/或辅酶遗留在进料溶液中。遗留的进料溶液的组合物依赖于培养基的原始类型,例如,活体外反应器培养基或酸化的和/或非活性的发酵培养基。葡萄糖酸衍生物,例如KLG可以几乎完全从进料溶液去除,以高达约3-4倍或更高的系数浓缩。KLG纯化的结果,可以通过直接喷雾干燥浓缩液实现后续的KLG回收。
图4和5所示的三室双极性膜ED堆(58),由排列在阳极(66)和阴极(68)之间的至少的三室单元组成。三室双极性膜ED堆包括排列在碱室(64)和浓缩室(62)之间的进料或稀释室(60);通过阳离子交换膜(70)碱室与进料室分离,通过阴离子交换膜(72)浓缩室(62)与进料室(60)分离。这些三室单元通过双极性膜(74)作为端部被限制住,该双极性膜浸于阳极电解液和阴极电解液清洗液流中,从而给碱室(64)提供氢氧离子,给浓缩室(62)提供质子。双极性和阴离子膜在上述的两室双极性膜ED电池堆的描述中被进一步描述。该阳离子交换膜可以是弱酸性的(例如羧酸型的)、中等酸性的(例如膦酸型)或强酸性的(磺酸阳离子交换基)。该阳离子交换膜对双极性膜ED堆的条件必须稳定,在葡萄糖酸衍生物溶液中对透析有较低的抵抗力,且可以包括全氟化膜例如DuPont Nafion或任何非全氟化阳离子交换膜例如Neosepta CMX。许多这些包括双极性、阳离子交换和阴离子交换的膜的三室单元可以在电渗析堆中堆叠在一起,该电渗析堆至少具有一对位于外部端的电极。
在势场的影响下,水将在双极性膜(74)中被分离形成氢氧离子和质子。如图4所示,如果进料溶液是酸化的和/或非活性的发酵培养基,氢氧根离子朝着阳极(66)迁移,进入三室双极性膜ED电池的碱室(64),其中它们将与穿过阳离子交换膜(70),从进料室(60)输送来的金属阳离子结合,以形成例如氢氧化钠的碱。质子将朝着阴极(68)迁移,进入浓缩室(62),其中它们将会与穿过阴离子膜(72)朝着阳极(66)迁移的葡萄糖酸衍生物的阴离子结合,从而形成纯化的、和浓缩的葡萄糖酸衍生物,例如KLG的溶液,且将任何中性物质遗留在进料溶液中。
引入三室双极性膜ED电池堆的进料室(60)的是进料电解液溶液,其中可以包括包含至少有葡萄糖酸衍生物盐和辅酶的活体外反应器培养基;至少包含葡萄糖酸衍生物盐的非活性发酵培养基;含该衍生物盐的溶液;或溶于水的KLG盐。应选择该衍生物的盐,使其基于碱的添加,不能形成不溶的沉淀物,否则,这些沉淀物会弄脏双极性膜或阳离子膜。合适的盐的典型例子包括碱金属盐,例如钠和钾或铵盐。
引入三室双极性膜ED电池堆的浓缩室(62)的是最初包括去离子水或浓缩的葡萄糖酸衍生物溶液,例如溶于水的KLG的浓缩溶液。去离子水和/或含NaOH或KOH的碱性水溶液可以被引入碱室(64)。
在图5所示的优选的实施方案中,进料溶液包括包含至少有葡萄糖酸衍生物盐和辅酶的活体外反应器培养基,其中有价值的辅酶遗留在进料溶液中,且可以取出再使用或再循环进活体外反应器。KLG几乎完全从进料溶液去除,以高达约3-4倍或更高的系数浓缩。
在两或三室的双极性膜ED堆中,如果在进料溶液中存在任何无机阴离子,它们可以优于葡萄糖酸衍生物阴离子输送进入浓缩室。该无机阴离子可以与形成于双极性膜的质子结合,导致浓缩液中无机酸的增加,和导致质子回迁,伴随着电流效率的损失。通过下述任何方式可以防止这种情况:(i)向浓缩液添加足够量的强碱例如氢氧化钠,以中和无机酸;(ii)从浓缩液的初馏分去除无机酸,由于无机酸的传送优于葡萄糖酸衍生物,因此该浓缩液几乎没有任何葡萄糖酸衍生物;(iii)同时进行ED堆脱盐操作,以从浓缩液去除无机酸,与通过将浓缩液从盐分解KLG ED堆送进脱盐ED堆它们的增加几乎一样快速;和(iv)用阴离子交换树脂从浓缩液去除强酸。这四种技术均可以防止在浓缩液中强酸的增加和质子穿过阴离子交换膜回迁的可能。作为进一步的好处,葡萄糖酸衍生物,特别是KLG的酸催化分解在蒸发结晶或喷雾干燥期间被避免。
另外,可以向进料溶液室添加稳定的阴离子或阳离子交换树脂或其混合物,以提供增加的无机离子向膜表面的大量输送(如果在进料溶液中含有)。
图3、4和5所示的盐分解ED电池堆,可以在单元电池电压从约0.1至约10V/每组膜,和更优选从约0.5至约5V/每组的情况下操作。温度范围应在约5℃至约90℃之间,更优选从约20℃至约50℃。较高的温度可以导致一些膜产生降解和产生葡萄糖酸衍生物的酸。该方法可以连续或间歇地运行。
在上述各实施方案中,进料溶液中的杂质可以弄脏膜,对性能造成损害。这些膜可以用不同的溶液就地清洗(在ED堆中)包括:(i)NaCL溶液;(ii)pH值是12的氯化钠溶液;(iii)硝酸或其他无机酸溶液;和(iv)添加有非离子或离子洗涤剂的溶液i、ii或iii。只要能有效地清洗必需的膜,而不使膜性能下降的其它洗涤溶液也是可用的。就地清洗(CIP)的步骤可以包括对洗涤溶液升温,只要该膜对温度稳定。CIP步骤也可以包括给ED膜堆通电流或电流回归;然而,双极性膜堆一般不能经受电流回归,因为这将损害双极性膜。
通过下述实施例,本发明将会被更清楚地认知和更好地理解。
实施例1
从KLG发酵肉汤去除无机酸
在脱盐ED的实施例中,使用图2所示的电渗析堆从非活性的和酸化的发酵肉汤中去除硫酸、盐酸和磷酸。KLG最初以钙盐的形式存在于肉汤中。该肉汤被微孔过滤去除细胞,且添加硫酸以质子化KLG盐,并造成硫酸钙沉淀。该酸化的肉汤接着被阳离子交换以完全去除钙。使用的电渗析电池是设置有用铂处理的钛阳极和阴极,SelemionAAV低质子回迁阴离子交换膜(Asahi Glass),和Neosepta CMX(Tokuyama)阳离子交换膜的Electrosynthesis Company ED-1 BP电池。各膜的面积是100cm2(5对),膜间距是0.75mm。该清洗溶液是0.2摩尔的硫酸。最初的酸室溶液是350ml水。
最初的进料溶液包含910ml的酸化的和非活性的发酵肉汤,肉汤中含91gl-1KLG,153ppm盐酸根、257ppm磷酸根、和5176ppm硫酸根,均以酸的形式存在。控制电池电压为1.6V/每膜对(11V总电池电压,假定结合3V的电极电势)和30℃的温度,进行实验。最终的进料含少于10ppm的盐酸根、34ppm的硫酸根和120ppm的磷酸根。总电荷通过量是2790库仑,对于去除盐的电流效率是76%。对该实验的电流密度范围是约13.5至约1.5mA cm-2,平均电流密度是6.5mAcm-2。只有1.2%的存在于进料的KLG通过输送进酸室被损失掉。
实施例2
来源于发酵肉汤的KLG的浓缩和纯化
在KLG ED方法的实施例中,以上述图1所示的类似的电渗析堆进行KLG的浓缩和纯化。所选择阴离子交换膜为Neosepta AFX,这是一种用来输送KLG阴离子的膜。进料溶液是非活性的和酸化的发酵培养基,进行如下预处理:发酵肉汤被微孔过滤以去除细胞,并加入硫酸以质子化KLG盐,并以硫酸盐的形式沉淀钙阳离子。剩余的钙接着通过阳离子交换被去除。
使用总共10膜对,提供1000cm2的膜面积。阳极电解液和阴极电解液是0.2摩尔的硫酸溶液。最初的浓缩液由来源于先前的KLG电渗析实验的300ml浓缩液组成。最初的进料溶液由3.5L的酸化的和非活性的发酵肉汤组成,肉汤中含142.4gl-1KLG。无机离子浓度是241mg l-1的Cl-、565mg l-1的PO4 3-、和1277mg l-1的SO4 2-。进料液进行上述的预处理。控制电池电压为2.7V/每膜对,或30V总电池电压和45℃的温度进行实验。输送进浓缩液的无机酸用50%的NaOH中和,用以防止质子回迁。213分钟之后,95.1%的KLG从进料液去除,并输送进浓缩液中,提供浓缩液中最终的KLG浓度是435.4gl-1。电流密度范围是约70.0至约8.4mA cm-2,平均电流密度是26.8mA cm-2。对于KLG输送的电流效率是67%。KLG通过ED浓缩近3倍。
表1显示出典型的ED运行的糖分析,其中KLG采用AFX阴离子交换膜被浓缩和纯化。95%的KLG被输送进浓缩液,但表中显示大多数的糖保留在进料液中。
表1:KLG肉汤的AFX ED期间糖的保留
| 成分 | 保留时间(分钟) | 最初进料液浓度g/L(总量g) | 最终进料液浓度g/L(总量g) | 保留在进料液的% |
| 麦芽糖 | 10.7 | 6.84(23.94) | 8.97(23.55) | 98 |
| 葡萄糖 | 12.3 | 1.97(6.90) | 2.29(6.01) | 87 |
| 果糖 | 13.4 | 1.61(5.64) | 1.73(4.54) | 80 |
ED总的条件:3.5L发酵肉汤,在2.7V/对膜,10对ED堆中进行电渗析。通过添加硫酸使硫酸钙沉淀,接着通过阳离子交换对肉汤预处理;95%的KLG被输送。
表2显示出通过ED提供的KLG回收和抗坏血酸(AsA)产量的改善。该表显示ED结合直接干燥提供了较好的抗坏血酸总收率,超过了其它任何回收方法。常规的结晶(方法B),当通过使用多次结晶,迫使达到较高的KLG回收(90%)时,却提供了从KLG转化至AsA较差的产率,且因此,得到较低的总收率。这是由于肉汤中中性物质的存在,导致了在多次结晶期间的粘度增加而造成的,其结果是使从结晶步骤中的KLG中分离出中性物质情况较差。该中性物质接着进入AsA的转化方法,它们导致了差的产率。发酵肉汤没有ED(方法C)的直接干燥受同样问题的困扰;肉汤中的中性物质污染了KLG,结果转化至AsA的产率和总产率较低。
表2:用ED的KLG回收和AsA产率的提高
| 步骤产率 | ||||||
| 回收方法 | CX | AX/阴离子ED | 方法A、B、C | 转化至AsA | 杂质情况 | 总产率 |
| ABC | 0.980.980.980.98 | 0.990.990.990.99 | 0.950.860.901.00 | 0.8660.9070.8300.774 | <1%的无机盐15%的有机酸1%的中性物质3%的无机盐0.5%的有机酸0.5%的中性物质1%的无机盐1%的有机酸8%的中性物质<1%的无机盐1%的有机酸16%的中性物质 | 0.800.760.720.75 |
回收方法A=微孔过滤器、用硫酸酸化、阳离子交换、SelemionAAV ED用于无机阴离子的去除,Neosepta AFX ED用于KLG的浓缩/纯化至95%的回收,直接干燥浓缩。
回收方法B=微孔过滤器、用硫酸酸化、阳离子交换、阴离子交换、结晶。
回收方法C=微孔过滤器、用硫酸酸化、阳离子交换、阴离子交换、肉汤直接干燥。
通过从KLG分离中性物质,ED减缓了这些问题。无机阴离子的ED也可以用来代替阴离子交换。ED浓缩液的直接干燥提供了高的KLG产品的产率,基本上没有中性物质。结果,转化至AsA的产率好,且总产率和经济性方面优于其它回收技术。此外,ED允许采用喷雾干燥代替结晶,大大节省了资金成本。
实施例3
在三室双极性膜电池堆中的盐分解KLG ED
从活体外反应器去除KLG钾盐,并引入如图5所示的三室双极性膜电池堆。该电渗析电池的进料溶液是活体外反应器培养基,包括815ml的含121.7g/L的KLG钾盐和0.5毫摩尔的烟酰胺腺嘌呤二核甙酸磷酸酯(NADP)的溶液。电渗析电池是设置有用铂处理的钛阳极和阴极、Neosepta BP-1的双极性膜、Neosepta AMX-SB的阴离子交换膜和Neosepta CMB(Tokuyama Soda)的阳离子交换膜的Electrosynthesis Company ED-1 BP电池。各膜的面积是100cm2(4组),膜间距是0.75mm。该清洗溶液是0.2摩尔的硫酸钾。最初的浓缩室和碱室各用200ml水填充。
控制电池电压为3.25V/膜对,或16V总电池电压和约30至约40℃的温度进行实验。95%以上的KLG从进料液去除,并输送进浓缩液,转化成酸形式,得到最终的KLG酸。只有1.5%的辅酶NADP被输送进浓缩液,和剩余物一起,存在于进料溶液中。电流密度范围是约30.0至约4.6mA cm-2,平均电流密度是23.9mA cm-2。用于形成KLG的电流效率是72%。
Claims (17)
1.一种用于制备纯化的和浓缩的葡萄糖酸衍生物的方法,其特征在于包括下述步骤:
a)提供一种pH值小于4.5的非活性发酵培养基,包括至少葡萄糖酸衍生物或其盐,葡萄糖酸衍生物选自由2,4,酮-D-葡萄糖酸、2,5,二酮-D-葡萄糖酸、艾杜糖酸、2-酮-L-古洛糖酸(KLG)、香草酸和抗坏血酸组成的组;和
b)通过电渗析从非活性发酵培养基去除葡萄糖酸衍生物,从而提供至少包括葡萄糖酸衍生物的浓缩的溶液,而其中具有中性物质的非活性发酵废液从该系统去除。
2.根据权利要求1的方法,其特征在于该非活性的发酵培养基[是非活性的发酵培养基,酸化]的pH值小于2.0。
3.根据权利要求1的方法,其特征在于该酸化的和非活性的发酵培养基,还包括与葡萄糖酸衍生物一起从非活性的发酵培养基去除的无机杂质。
4.根据权利要求3的方法,还包括通过电渗析从含葡萄糖酸衍生物的浓缩溶液中分离无机杂质。
5.一种用于制备纯化的和浓缩的葡萄糖酸衍生物的方法,其特征在于包括下述步骤:
a)提供一种pH值小于4.5,至少包括葡萄糖酸衍生物、无机杂质和中性物质的非活性的发酵培养基;该葡萄糖酸衍生物选自由2,4,酮-D-葡萄糖酸、2,5,二酮-D-葡萄糖酸、艾杜糖酸、2-酮-L-古洛糖酸(KLG)、香草酸和抗坏血酸组成的组;
b)通过电渗析从非活性的发酵培养基去除葡萄糖酸衍生物和无机杂质,从而提供至少包括葡萄糖酸衍生物和无机杂质的浓缩的酸化水溶液,且废液包含废非活性发酵废液,该发酵废液含未电离的中性物质,其实质上耗尽了葡萄糖酸衍生物;
c)从浓缩的酸化的水溶液分离无机杂质,从而提供纯化的和浓缩的葡萄糖酸衍生物水溶液;和
d)从纯化和浓缩的水溶液回收葡萄糖酸衍生物。
6.根据权利要求5的方法,其特征在于非活性发酵培养基的酸性pH值小于2.0。
7.根据权利要求5的方法,其特征在于通过电渗析从浓缩的酸化水溶液分离无机杂质的步骤。
8.根据权利要求7的方法,其特征在于电渗析是在一个电池中进行,该电池具有许多交替的阳离子交换膜和阴离子交换膜,它们之间空出足够的空间以提供至少一个进料和浓缩室,容器电池的不同端的阳极和阴极与电源连接,用以提供通过电渗析电池的电流。
9.根据权利要求7的方法,其特征在于通过直接干燥回收葡萄糖酸衍生物。
10.根据权利要求5的方法,其特征在于无机杂质是无机酸。
11.根据权利要求8的方法,其特征在于用于步骤(b)的阴离子交换膜基本上防止进料液流中的中性物质输送进浓缩室。
12.根据权利要求8的方法,其特征在于用于步骤(c)的阴离子交换膜具有足够的闭孔结构使得无机阴离子通过该膜传送,同时对葡萄糖酸衍生物阴离子的传送基本上或全部阻止。
13.一种用于制备高纯化和浓缩的葡萄糖酸衍生物的方法,其特征在于包括以下步骤:
a)提供一种至少包括葡萄糖酸衍生物阴离子、金属抗衡离子和辅酶的活体外反应器培养基,该葡萄糖酸衍生物选自由2,4,酮-D-葡萄糖酸、2,5,二酮-D-葡萄糖酸、艾杜糖酸、2-酮-L-古洛糖酸(KLG)、香草酸和抗坏血酸组成的组;和
b)将活体外反应器培养基引入电渗析电池,该电渗析电池包括至少一个交替的阴离子和阳离子交换膜,且空出足够的空间以提供其间的至少一个进料室,双极性膜和阳离子交换膜空出足够的空间以提供其间的至少一个碱室,双极性膜和阴离子交换膜空出足够的空间以提供其间的至少一个浓缩室,位于该电池不同端的阳极和阴极与提供通过该电池的电流的电源连接,其中葡萄糖酸衍生物阴离子被质子化,且金属抗衡离子增加氢氧离子,从而提供至少包括葡萄糖酸衍生物的浓缩的水溶液、包括至少金属氢氧化物溶液的液流和含中性物质的废液。
14.根据权利要求13的方法,其特征在于还包括向含有金属氢氧化物的进料室添加二氧化碳,从而形成溶液中的碳酸盐产品,该碳酸盐选自金属碳酸盐和金属碳酸氢盐组成的组。
15.根据权利要求13的方法,其特征在于还包括包含辅酶的液流。
16.根据权利要求13的方法,其特征在于还包括从浓缩水溶液回收葡萄糖酸衍生物。
17.一种用于制备高纯化和浓缩的葡萄糖酸衍生物的方法,其特征在于包括以下步骤:
a)提供一种至少包括葡萄糖酸衍生物盐、金属抗衡离子和辅酶的发酵溶液,该葡萄糖酸衍生物选自由2,4,酮-D-葡萄糖酸、2,5,二酮-D-葡萄糖酸、艾杜糖酸、2-酮-L-古洛糖酸(KLG)、香草酸和抗坏血酸组成的组;和
b)将发酵溶液引入电渗析电池,该电渗析电池包括至少一个交替的阴离子和阳离子交换膜,且空出足够的空间以提供其间的至少一个进料室,双极性膜和阳离子交换膜空出足够的空间以提供其间的至少一个碱室,双极性膜和阴离子交换膜空出足够的空间以提供其间的至少一个浓缩室,位于该电池不同端的阳极和阴极与提供通过该电池的电流的电源连接,其中葡萄糖酸衍生物阴离子被质子化,且金属抗衡离子增加氢氧离子,从而提供至少包括葡萄糖酸衍生物的浓缩的水溶液、包括至少金属氢氧化物溶液的液流和含未电离的中性物质的废液。
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US8679298P | 1998-05-26 | 1998-05-26 | |
| US60/086,792 | 1998-05-26 | ||
| US09/318,348 | 1999-05-25 | ||
| US09/318,348 US6187570B1 (en) | 1998-05-26 | 1999-05-25 | Electrodialysis methods for purification and recovery of gluconic acid derivatives |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN1302336A CN1302336A (zh) | 2001-07-04 |
| CN1258598C true CN1258598C (zh) | 2006-06-07 |
Family
ID=26775159
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CNB998064831A Expired - Fee Related CN1258598C (zh) | 1998-05-26 | 1999-05-26 | 用于纯化和回收葡萄糖酸衍生物的电渗析方法 |
Country Status (6)
| Country | Link |
|---|---|
| US (2) | US6187570B1 (zh) |
| EP (1) | EP1084264A4 (zh) |
| JP (1) | JP2003523164A (zh) |
| CN (1) | CN1258598C (zh) |
| CA (1) | CA2332323A1 (zh) |
| WO (1) | WO1999061647A1 (zh) |
Families Citing this family (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6187570B1 (en) * | 1998-05-26 | 2001-02-13 | The Electrosynthesis Company, Inc. | Electrodialysis methods for purification and recovery of gluconic acid derivatives |
| US6495013B2 (en) * | 2000-07-13 | 2002-12-17 | The Electrosynthesis Company, Inc. | Bipolar membrane electrodialysis of multivalent metal salts whose corresponding base is insoluble |
| US7238532B1 (en) * | 2001-06-01 | 2007-07-03 | David Michael Philbrook | Isothiazolone monitoring in aqueous systems |
| US6712946B2 (en) * | 2001-06-18 | 2004-03-30 | The Electrosynthesis Company, Inc. | Electrodialysis of multivalent metal salts |
| DE10149869A1 (de) * | 2001-10-10 | 2003-04-24 | Basf Ag | Verfahren zur Isolierung von Salzen von organischen Säuren aus einer Fermentationsbrühe und zur Freisetzung der organischen Säure |
| DE102004001187A1 (de) * | 2004-01-05 | 2005-08-04 | Basf Ag | Verfahren zur Herstellung von Keto-L-gulonsäuresprühgranulaten |
| CN100528304C (zh) * | 2004-03-17 | 2009-08-19 | Ge爱奥尼克斯公司 | 用于有机产物的生产线和处理 |
| US7630103B2 (en) * | 2005-03-16 | 2009-12-08 | Kabushiki Kaisha Toshiba | Image reading apparatus and image forming apparatus |
| WO2008100798A1 (en) | 2007-02-09 | 2008-08-21 | Primafuel, Inc. | Biodiesel production method and apparatus |
| US8137527B1 (en) | 2008-07-28 | 2012-03-20 | Primafuel, Inc. | Carbon dioxide isolation and generation |
| US9156002B2 (en) * | 2008-09-08 | 2015-10-13 | Carlsberg A/S | Process for controlling the pH and level of target ions of a liquid composition |
| AT513562A1 (de) | 2012-11-14 | 2014-05-15 | Annikki Gmbh | Verfahren zur Gewinnung von Zuckerderivaten |
| CN104313633B (zh) * | 2014-07-22 | 2016-09-07 | 宜宾丝丽雅集团有限公司 | 一种双极膜法制备葡萄糖酸的生产工艺 |
| CN104383813B (zh) * | 2014-11-04 | 2017-05-31 | 帝斯曼江山制药(江苏)有限公司 | 一种古龙酸发酵液的综合处理方法 |
| EP3464606A1 (de) | 2016-05-23 | 2019-04-10 | Annikki GmbH | Verfahren zur enzymatischen umwandlung von d-glucose in d-fructose via d-sorbitol |
| CN106349055B (zh) * | 2016-08-24 | 2017-12-01 | 山东福洋生物科技有限公司 | 一种葡萄糖酸钠母液的新型分离提取方法 |
| CN113441009B (zh) * | 2021-06-22 | 2022-07-22 | 黑龙江新和成生物科技有限公司 | 一种维生素c的双极膜酸化生产工艺及装置 |
Family Cites Families (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3619396A (en) * | 1969-01-29 | 1971-11-09 | Cpc International Inc | Enzymatic production of gluconic acid |
| US3964985A (en) | 1974-10-29 | 1976-06-22 | Ionics, Incorporated | Electrodialysis apparatus and process for ion modification |
| JPS5910796B2 (ja) | 1976-11-11 | 1984-03-12 | 塩野義製薬株式会社 | 2↓−ケト↓−l↓−グロン酸ナトリウム高純度結晶の採取方法 |
| DE3621781A1 (de) * | 1985-07-05 | 1987-01-15 | Takeda Chemical Industries Ltd | Verfahren zur reinigung von l-ascorbinsaeure |
| DE3542861A1 (de) * | 1985-12-04 | 1987-06-11 | Huels Chemische Werke Ag | Verfahren zur gewinnung von l-aepfelsaeure |
| JPS62146595A (ja) * | 1985-12-20 | 1987-06-30 | Daicel Chem Ind Ltd | 醗酵による有機酸の連続製造方法 |
| US5143834A (en) | 1986-06-11 | 1992-09-01 | Glassner David A | Process for the production and purification of succinic acid |
| US4885247A (en) | 1988-04-19 | 1989-12-05 | Michigan Biotechnology Institute | Recovery and purification of lactate salts from whole fermentation broth by electrodialysis |
| US5202476A (en) | 1988-04-29 | 1993-04-13 | Takeda Chemical Industries, Ltd. | Purification of 2-keto-L-gulonic acid |
| NL8801516A (nl) | 1988-06-14 | 1990-01-02 | Suiker Unie | Werkwijze voor de fermentatieve bereiding van organische zuren. |
| FR2636343B1 (zh) | 1988-09-13 | 1994-11-25 | Rhone Poulenc Sante | |
| US5282939A (en) * | 1988-09-20 | 1994-02-01 | Basf Aktiengesellschaft | Removal of salts by electrodialysis |
| US5464760A (en) | 1990-04-04 | 1995-11-07 | University Of Chicago | Fermentation and recovery process for lactic acid production |
| JP3134236B2 (ja) * | 1992-01-30 | 2001-02-13 | 株式会社林原生物化学研究所 | α−グリコシル−L−アスコルビン酸高含有物の製造方法とその製造のための分離システム |
| CN1048282C (zh) | 1993-07-09 | 2000-01-12 | 武田药品工业株式会社 | 生产2-酮-l-古洛糖酸的方法 |
| US5522995A (en) * | 1995-02-28 | 1996-06-04 | Cockrem; Michael C. M. | Process for recovering organic acids from aqueous salt solutions |
| US5681728A (en) * | 1995-06-07 | 1997-10-28 | Chronopol, Inc. | Method and apparatus for the recovery and purification of organic acids |
| DE59608956D1 (de) * | 1995-12-14 | 2002-05-02 | Hoffmann La Roche | Herstellung von Ascorbinsäure |
| CN1102073C (zh) * | 1997-06-30 | 2003-02-26 | 电合成公司 | 回收抗坏血酸的电化学方法 |
| US6187570B1 (en) * | 1998-05-26 | 2001-02-13 | The Electrosynthesis Company, Inc. | Electrodialysis methods for purification and recovery of gluconic acid derivatives |
-
1999
- 1999-05-25 US US09/318,348 patent/US6187570B1/en not_active Expired - Fee Related
- 1999-05-26 CA CA002332323A patent/CA2332323A1/en not_active Abandoned
- 1999-05-26 WO PCT/US1999/011671 patent/WO1999061647A1/en active Application Filing
- 1999-05-26 JP JP2000551029A patent/JP2003523164A/ja active Pending
- 1999-05-26 CN CNB998064831A patent/CN1258598C/zh not_active Expired - Fee Related
- 1999-05-26 EP EP99953361A patent/EP1084264A4/en not_active Withdrawn
-
2000
- 2000-11-28 US US09/724,443 patent/US6541228B1/en not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| WO1999061647A8 (en) | 2000-12-21 |
| CN1302336A (zh) | 2001-07-04 |
| US6187570B1 (en) | 2001-02-13 |
| EP1084264A4 (en) | 2005-11-23 |
| JP2003523164A (ja) | 2003-08-05 |
| WO1999061647A9 (en) | 2001-03-08 |
| WO1999061647A1 (en) | 1999-12-02 |
| CA2332323A1 (en) | 1999-12-02 |
| EP1084264A1 (en) | 2001-03-21 |
| US6541228B1 (en) | 2003-04-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN1258598C (zh) | 用于纯化和回收葡萄糖酸衍生物的电渗析方法 | |
| CN1102073C (zh) | 回收抗坏血酸的电化学方法 | |
| CN102753514B (zh) | 制备琥珀酸的方法 | |
| CN101195639B (zh) | 草甘膦母液处理方法 | |
| CN87103274A (zh) | 5-芳烷基-4-烷氧基-2(5h)-呋喃酮,中间产物及其制备方法以及作为药物的使用 | |
| US9057137B2 (en) | Method and device for carboxylic acid production | |
| EP3006407A1 (en) | Bioelectrochemical system having polyvalent ion removing function | |
| CN1516615A (zh) | 多价金属盐的电渗析 | |
| CN109097408A (zh) | 一种尼龙56盐的制备方法 | |
| CN1201710A (zh) | 盐的电渗析方法与装置 | |
| CN87102881A (zh) | 电渗析分离硫酸锌电解液中单价离子的方法 | |
| CN103922980A (zh) | 一种利用双极膜电渗析从蛋氨酸盐与碳酸盐的混合溶液中分离出蛋氨酸的方法 | |
| CN1247481A (zh) | 从废溶液中回收有机氢氧化物的方法 | |
| CN1293231C (zh) | 通过电渗析纯化氢氧化鎓 | |
| CN100528304C (zh) | 用于有机产物的生产线和处理 | |
| US4874700A (en) | Process for the production of L-malic acid | |
| CN1568299A (zh) | 从发酵液中分离有机酸盐和释放有机酸的方法 | |
| CN1048282C (zh) | 生产2-酮-l-古洛糖酸的方法 | |
| CN1108304A (zh) | 发酵制造乳酸的方法 | |
| JP2005270025A (ja) | 有機酸の精製方法 | |
| CN1172028C (zh) | 电解法制备次磷酸的方法 | |
| US20130081947A1 (en) | Bioprocess utilizing carbon dioxide and electrodeionization | |
| JP2820206B2 (ja) | ジペプチドエステルの精製方法 | |
| WO2024213736A1 (en) | Production of organic acid from monovalent acid salt via electrodialysis using a two-compartment electrodialysis unit | |
| WO2024213739A1 (en) | Production of organic acid from monovalent acid salt via electrodialysis using a three-compartment electrodialysis unit |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C14 | Grant of patent or utility model | ||
| GR01 | Patent grant | ||
| C19 | Lapse of patent right due to non-payment of the annual fee | ||
| CF01 | Termination of patent right due to non-payment of annual fee |