CN1245395C - 使用过氧化物制造环氧烷烃的方法 - Google Patents
使用过氧化物制造环氧烷烃的方法 Download PDFInfo
- Publication number
- CN1245395C CN1245395C CNB018148026A CN01814802A CN1245395C CN 1245395 C CN1245395 C CN 1245395C CN B018148026 A CNB018148026 A CN B018148026A CN 01814802 A CN01814802 A CN 01814802A CN 1245395 C CN1245395 C CN 1245395C
- Authority
- CN
- China
- Prior art keywords
- reactor
- superoxide
- epoxy alkane
- solvent
- alkene
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D301/00—Preparation of oxiranes
- C07D301/02—Synthesis of the oxirane ring
- C07D301/03—Synthesis of the oxirane ring by oxidation of unsaturated compounds, or of mixtures of unsaturated and saturated compounds
- C07D301/12—Synthesis of the oxirane ring by oxidation of unsaturated compounds, or of mixtures of unsaturated and saturated compounds with hydrogen peroxide or inorganic peroxides or peracids
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P20/00—Technologies relating to chemical industry
- Y02P20/50—Improvements relating to the production of bulk chemicals
- Y02P20/52—Improvements relating to the production of bulk chemicals using catalysts, e.g. selective catalysts
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Inorganic Chemistry (AREA)
- Epoxy Compounds (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Silver Salt Photography Or Processing Solution Therefor (AREA)
- Processes Of Treating Macromolecular Substances (AREA)
Abstract
在至少两个串联布置的各装有一部分催化剂的反应器中,在催化剂和溶剂存在下,通过烯烃和过氧化物的反应制造环氧烷烃的方法,按照该方法,只在第一反应器中加入过氧化物,后面的一个或几个反应器中不加入新鲜的过氧化物,而只是使用在来自前面反应器的介质中存在同时在前面反应器中未消耗的过氧化物。
Description
本发明涉及在催化剂和溶剂存在下,通过烯烃和过氧化物之间的反应制造环氧烷烃的方法。本发明特别涉及在含有TS-1的催化剂存在下,借助于过氧化氢使丙烯(或烯丙基氯)环氧化制造环氧丙烷(或环氧氯丙烷)的方法。
在TS-1存在下通过丙烯和过氧化氢之间的反应制造环氧丙烷的方法是已知的。比如在专利US-5849937中,在串联的多个反应器中实施了这样的方法。在此已知的方法中,串联的每个反应器都送入新鲜的过氧化氢。
本申请人发现,当每个反应器都送入新鲜过氧化氢时,不可能把使用的全部过氧化氢都转化掉,使之不形成大量的副产物,因此而具有最佳的产率。
本发明通过提供一个新方法来对此缺点进行了改善,此方法能够将加入的过氧化氢100%地转化,形成副产物的量很少,同时还不降低反应速度。
为此,本发明涉及在至少两个其中每个都装有部分催化剂的串联反应器中,在催化剂和溶剂存在下,通过烯烃和过氧化物之间的反应制造环氧烷烃的方法,按照该方法,在第一反应器中加入第一部分烯烃、溶剂和全部过氧化物,使第一部分烯烃进行环氧化反应,形成第一部分环氧烷烃,从此反应器中取出反应介质,该反应介质含有形成的第一部分环氧烷烃、溶剂和未消耗的过氧化物并任选含有未转化烯烃,把此反应介质加入到后面的反应器中,并加入另一部分烯烃,在这里借助于来自第一反应器中未消耗的过氧化物使另一部分烯烃环氧化,以形成另一部分环氧烷烃,以及回收此另一部分如此形成的环氧烷烃。
本发明的基本特征在于,仅在第一反应器中加入过氧化物。因此,在后面的一个或数个反应器中不再送入新鲜的过氧化物,而且只是使用来自前面反应器的介质中存在并在此前面反应器中没有消耗的过氧化物。一般在第一反应器中,与过氧化物一起还加入水。由于在后面的一个或数个反应器中不再加入过氧化物,这就使得能够消耗掉100%量的全部使用的过氧化物,而与使用同样总数量的过氧化物,但在每个反应器中都加入新鲜过氧化物的方法相比,同样不会降低反应速度。
在本发明的方法中,使用的装置包括至少两个串联放置并彼此连接的环氧化反应器,但不包括下述情况:在单一的反应器中相继配置至少两个反应区。因此这涉及到有区别的反应器。每个反应器都送入烯烃,但只在第一反应器中加入过氧化物和溶剂。每个反应器都装有一部分催化剂,而且此催化剂并不离开此反应器。当催化剂呈固定床形式的时候,一般用不着为了把此催化剂保持在反应器中而操心。在另外的情况下,催化剂呈颗粒的形状,由于液体的流动或者由于机械搅拌或者由于气体搅拌,使其中至少一部分是呈流态化的状态。当使用液体流的时候,建议在流化床之上设计一个分离区,使处于运动中的催化剂颗粒停止运动和/或在反应器出口处设计过滤器。
此装置明显可以包括两个以上的串联连接的反应器。在此情况下,在串联的第一反应器中送入烯烃、过氧化物和溶剂,而在后面的每个反应器中则送入烯烃和来自串联的前面反应器的介质。优选使用串联的3个反应器。
在本发明的方法中,一般在第一反应器中消耗掉在第一反应器中使用的过氧化物总量的至少50%。当在第一反应器中消耗掉至少70%时,会得到最好的产率。在第一反应器中更经常消耗掉最多99%的过氧化物,优选最多消耗掉85%。其余的过氧化物则在后面的一个或数个反应器中消耗掉。
在本发明的方法中,优选使用相同尺寸的几个反应器。这样使得能够当一个反应器中失活的催化剂要用新鲜的催化剂更换时,或者要进行再生时,切换反应器的操作而不干扰整个装置的操作(所谓的“循环(en carrousel)”操作)。
如在本申请人在与本专利申请同一天提交的题为“在颗粒状催化剂存在下制造环氧烷烃的方法”专利申请(其内容在此引做参考)中所述,按照本发明方法的第一种特别有利的实施方式包括,使用呈颗粒状的催化剂,其中至少一部分处于流态化的状态。在此情况下,建议设计一个过滤器,从第一反应器出来的介质要穿过此过滤器,然后进入后面的反应器中。这样的实施方式能够使催化剂在环氧化反应介质中得到均匀分布,能够得到良好的换热,因此使反应温度容易控制。
在本发明方法的第二种实施方式中,要使进入到后面反应器中的介质首先降压,然后再进入后一个反应器。当环氧化反应是在加压下进行,或者在气体化合物存在下进行时,这种实施方式是特别好的。如在本申请人的专利申请WO 99/48883中所述,此气体化合物可以是烯烃本身(比如丙烯),或者是加入到环氧化反应介质中携带环氧烷烃并从反应器排出的惰性气体。
在本发明方法的第三种实施方式中,让进入后面反应器的介质首先进行分离形成的环氧烷烃的处理,然后再进入后一个反应器。此种实施方式的目的是自从环氧烷烃形成时起,尽可能快地从环氧化反应介质中分离出环氧烷烃,以避免由于形成的环氧烷烃发生水解或醇解(当使用甲醇作为溶剂时发生甲醇解)而产生副产物。因此该实施方式的优点是得到更高的选择性。如在本申请人在与本专利申请同一天提交的题为“包括从反应介质中分离环氧烷烃的环氧烷烃制造方法”(其内容在此引做参考)中所述,此分离处理优选是蒸馏。
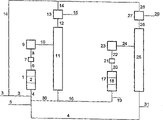
在图1上示意性说明的是按照本发明方法的一个优选实施方式。在此优选的方式中,第一反应器1装有一部分催化剂,优选是呈流化床2形式的催化剂。先经过管道3,然后经过管道4把第一部分烯烃送入反应器1中,而经过管道5然后经过管道4送入过氧化物、以及经过管道4送入来自在更后面叙述的装置另一部分的溶剂到反应器1中。在第一反应器中,在催化剂存在下,第一部分烯烃与过氧化物反应,生成第一部分环氧烷烃。从反应器1经过管道6排出的介质含有溶剂、第一部分环氧烷烃、未消耗的过氧化物和未转化的烯烃。此介质经过过滤器7,再经过管道8送入到容器9中,在这里此介质经受减压。然后此介质经过管道10被转移到蒸馏塔11中。在此蒸馏塔11的塔顶回收环氧烷烃和未转化烯烃的混合物。经过管道12把此混合物送到冷凝器13中,此冷凝器把环氧烷烃和未转化的烯烃分离。经过管道14、3和4,此未转化的烯烃循环到反应器1中。经过管道15,第一部分环氧烷烃作为最终产物被回收。在蒸馏塔11的塔底,回收含有溶剂、在反应器1中未消耗的过氧化物和任选含有一部分未转化烯烃的介质。此介质其中的一部分任选通过管道30循环到反应器1中,此介质通过管道16被输送到装有另一部分优选呈流化床状态的催化剂18的第二反应器17中。经过管道19把第二部分烯烃送入第二反应器17中。在此第二反应器17中,在催化剂18存在下,第二部分烯烃与来自第一反应器的未消耗过氧化物发生反应,形成第二部分环氧烷烃。在第二反应器17中的条件优选使得来自第一反应器的全部过氧化物都被消耗掉。此时经过管道20从反应器17排出的介质含有溶剂、第二部分环氧烷烃和未转化的烯烃。此介质通过过滤器21,经管道22送入容器23中,在这里它们经受减压。然后此反应介质经过管道24被送入到第二蒸馏塔25中。在此蒸馏塔25的塔顶,回收第二部分环氧烷烃和未转化烯烃的混合物。此混合物经过管道26被送入冷凝器27中,将环氧烷烃和未转化的烯烃分离。未转化的烯烃经过管道28、14、3和4被循环到反应器1中。而经过管道29把第二部分环氧烷烃作为最终产物而回收。在蒸馏塔25的塔底,回收溶剂,然后经过管道4将其循环到第一反应器1中,回收的水性流出物经过管道31被排掉。
在本发明的方法中使用的催化剂一般含有沸石作为活性元素,优选含有含钛沸石。所谓含钛沸石,指的是含有呈沸石类微孔晶体结构的二氧化硅的固体,而且其中有多个硅原子被钛原子替代。含钛沸石有利地具有ZSM-5、ZSM-11、ZSM-12、MCM-41和ZSM-48型晶体结构。它们还具有β-沸石型晶体结构,优选不含有铝。此类沸石的红外吸收带通常在大约950~960cm-1。人造沸石类(Silicalite)的含钛沸石是优选的。它们的通式相当于xTiO2(1-x)SiO2,其中x是0.0001~0.5,优选0.001~0.05的是性能良好的。此类已知名叫TS-1的材料具有与ZSM-5沸石相类似的微孔晶体沸石结构。
在本发明的方法中使用的催化剂,有利地如在本申请人的专利申请WO 99/28029中所述,呈通过挤塑得到的颗粒状,或者如在本申请人的专利申请WO 99/24164中所述,呈用喷雾的方法得到的颗粒状。这两个专利申请的内容在此都引做参考。
在本发明的方法中使用的溶剂可选自直链或支链的饱和脂肪醇,此醇类溶剂一般含有不超过10个碳原子,优选含有1~6个碳原子。作为例子可以举出甲醇和乙醇,优选是甲醇。
在第一反应器中溶剂的用量一般是在第一反应器中液体反应介质的至少25wt%,特别是至少40wt%,比如至少50wt%。此量通常不超过99wt%,特别不超过95wt%。
在本发明的方法中投入的烯烃和过氧化物用量的摩尔比一般至少是0.1,特别是至少0.2,优选至少是0.5。此摩尔比最经常不超过100,特别是不超过50,优选不超过25。
本发明的方法可以是连续的,也可以是间歇的。
在本发明的方法中,当连续地进行时,在第一反应器中使用的过氧化物的用量一般是:对于在第一反应器中每克催化剂,每小时至少为0.005mol,特别是至少0.01mol。过氧化物的用量一般小于或等于25mol,特别是小于或等于10mol。过氧化物的用量优选高于或等于0.03mol,而低于或等于2.5mol。
在本发明的方法中,使用的过氧化物有利地呈水溶液的形式。此水溶液一般含有至少2wt%的过氧化物,特别含有至少5wt%的过氧化物。它最经常含有最多90wt%的过氧化物,特别是含有最多70wt%的过氧化物。
烯烃和过氧化物的反应温度一般为10~125℃。在一个如在本申请人的专利申请EP 99/08703中叙述的有利的实施方案中,反应温度高于35℃,使得能够克服催化剂的逐渐失活。此温度可以高于或等于40℃,优选高于或等于45℃。此温度高于或等于50℃是特别优选的。反应温度优选低于100℃。
在本发明的方法中,烯烃和过氧化物之间的反应可以在大气压下进行。此反应还可以在压力下进行。此压力一般不超过40bar。实际上20bar的压力是很适当的。
在本发明的方法中可以使用的过氧化物是含有一个或多个过氧官能团(-OOH)的过氧化物,此官能团能够释放出活性氧并能够进行环氧化反应。无机过氧化物就能够给出很好的结果。过氧化氢和在环氧化反应条件下可以产生过氧化氢的过氧化物都是很适当的。过氧化氢是优选的。
当使用过氧化氢时,在本发明的方法中使用粗态的,即没有提纯的过氧化氢水溶液是有意义的。比如可以使用用基本上纯的水对来自至少一种烷基蒽氢醌氧化(被称为“AO自动氧化法”)得到的混合物进行简单萃取所得到的溶液,用不着以后的洗涤和/或提纯处理。此过氧化氢粗溶液一般含有0.001~10g/L以COT(总有机碳)表示的有机杂质。其金属阳离子(比如碱金属或碱土金属,如钠)和阴离子(比如磷酸根、硝酸根)的含量一般是0.01~10g/L。
在该方法的另外一个实施方案中,可以使用在甲醇存在下由氧和氢直接合成的过氧化氢溶液。
可以用本发明方法制备的环氧烷烃是含有用如下通式表示的基团的有机化合物:
此环氧烷烃一般含有2~10个碳原子,优选含有3~6个碳原子。可以用本发明的方法有利地制备的环氧烷烃是1,2-环氧丙烷和1,2-环氧-3-氯丙烷。环氧烷烃优选是1,2-环氧丙烷。
在本发明的方法中适合使用的烯烃一般含有2~10个碳原子,优选含有3~6个碳原子。丙烯、丁烯和烯丙基氯都是合适的。优选丙烯和烯丙基氯。特别优选丙烯。
在本发明的方法中控制液相的pH值可能是有意义的。正如在本申请人的专利申请WO 99/48882(其内容在本专利申请中引做参考)中所建议的,比如在烯烃和过氧化物进行反应时,通过在环氧化介质中添加碱(氢氧化钠)保持液相的pH值在4.8~6.5可能是有意义的。此碱可以加入到单一的反应器(比如第一反应器)中,或可以加入到多个反应器中。优选在每个反应器中都加入。
正如在本申请人的专利申请WO 99/08703(其内容在本专利申请中引做参考)中所叙述的,可以在如氯化钠的盐存在下进行烯烃和过氧化物之间的反应。此盐可以加入到单一的反应器(比如第一反应器)中,或可以加入到多个反应器中。优选在每个反应器中都加入。
可以有利地以在一种或多种烷烃中稀释的状态加入烯烃。比如在环氧化反应器中可以加入含有烯烃且还含有至少10vol%(特别是20vol%,比如至少30vol%)一种或几种烷烃的流体。比如,在丙烯的情况下,当把循环的未转化丙烯加入到反应器中时,它可以与至少10vol%的丙烷相混合。也可以涉及到没有完全提纯掉丙烷的丙烯源。
下面的实施例用来说明本发明,但不对其构成任何限制。
实施例1和实施例2使用Aspen技术公司的软件ASPEN PLUS,由基于叙述的实验和在文献中得到的液-汽平衡数据所确定的反应动力学参数进行了计算。
比较例1
在此比较例中,在串联的两个反应器中合成环氧丙烷,同时在一个精馏塔中对在第一反应器中形成的环氧丙烷进行中间分离。一半过氧化氢送入第一反应器,一半过氧化氢送入第二反应器。
把伴随着1100kmol/hr水的326.5kmol/hr的过氧化氢分成相同的两份,各含有163.25kmol/hr过氧化氢和550kmol/hr水,第一份与1500kmol/hr甲醇、250kmol/hr丙烯以及从精馏塔塔底循环的馏分在足够的压力下混合,使得在反应温度下全部丙烯都能够溶解。在70℃下把反应混合物连续地送入装有600kg催化剂的按照本方法的反应器中。用适当的冷却系统把反应器的温度保持在70℃。
把反应器的流出物引到具有50块理论塔板(包括冷凝器和蒸发器)的精馏塔中;将其送入到第10块理论塔板(从冷凝器算起)上;此塔在1.1bar(绝对)的压力(塔顶压力)下操作;塔顶温度保持在40℃(使馏出液部分汽化;摩尔回流比固定为1;馏出液的总流量固定为600kmol/hr。
从塔底放出的贫环氧丙烷的混合物被分成两份,第一份占混合物的90vol%,被循环到第一反应器的进料处;第二份占从精馏塔塔底得到的混合物的其余部分,与200kmol/hr的丙烯混合,在足够的压力下使得在反应温度下丙烯全部溶解,并连续地在70℃下加入到装有820kg催化剂的按照本方法的第二反应器中,用适当的冷却系统保持70℃的温度。
第二反应器的流出物含有24.5kmol/hr的未转化过氧化氢、209.4kmol/hr环氧丙烷和87.8kmol/hr的副产物(主要是甲氧基丙醇和丙二醇);此塔的馏出液含有56.2kmol/hr的环氧丙烷;对于92.4%的过氧化氢转化率,C3的收率达到64.1%。
实施例1
在此实施例中,在串联的两个反应器中合成环氧丙烷,同时对在第一反应器中形成的环氧丙烷进行中间分离。
把伴随着1100kmol/hr水的326.5kmol/hr的过氧化氢与1500kmol/hr甲醇、250kmol/hr丙烯以及从精馏塔塔底循环的馏分在足够的压力下混合,使得在反应温度下全部丙烯都能够溶解。在70℃下把反应混合物连续地送入装有600kg催化剂的按照本方法的反应器中。用适当的冷却系统把反应器的温度保持在70℃。
把反应器的流出物引到具有50块理论塔板(包括冷凝器和蒸发器)的精馏塔中;将其送入到第10块理论塔板(从冷凝器算起)上;此塔在1.1bar(绝对)的压力(塔顶压力)下操作;塔顶温度保持在40℃(使馏出液部分汽化;摩尔回流比固定为1;馏出液的总流量固定为600kmol/hr。
从塔底放出的贫环氧丙烷的混合物被分成两份,第一份占混合物的90vol%,被循环到第一反应器的进料处;第二份占从精馏塔塔底得到的混合物的其余部分,与200kmol/hr的丙烯混合,在足够的压力下使得在反应温度下丙烯全部溶解,并连续地在70℃下加入到装有820kg催化剂的按照本方法的第二反应器中,用适当的冷却系统保持70℃的温度。
第二反应器的流出物含有1.9kmol/hr的未转化过氧化氢、256.5kmol/hr环氧丙烷和62.2kmol/hr的副产物(主要是甲氧基丙醇和丙二醇);此塔的馏出液含有88.4kmol/hr的环氧丙烷;对于99.4%的过氧化氢转化率,C3的收率达到78.6%。
Claims (12)
1.在至少两个串联布置的各装有一部分催化剂的反应器中,在催化剂和溶剂存在下,通过烯烃和过氧化物的反应制造环氧烷烃的方法,按照该方法,在第一反应器中加入第一部分烯烃、溶剂和全部过氧化物,在此进行第一部分烯烃的环氧化反应,形成第一部分环氧烷烃,从此反应器中取出含有形成的第一部分环氧烷烃、溶剂、未消耗的过氧化物和任选含有未转化烯烃的介质,把此介质和另一部分烯烃加入到后一个反应器中,在那里借助于来自第一反应器的未消耗的过氧化物进行另一部分烯烃的环氧化反应,形成另一部分环氧烷烃,以及回收如此形成的另一部分环氧烷烃。
2.如权利要求1的方法,其中在第一反应器和第二反应器之间,被除去的溶剂是那样小以致于不必向第二反应器中加入溶剂。
3.如权利要求1的方法,使用串联的另外的第三个反应器。
4.如权利要求1~3中任何一项的方法,其中在第一反应器中使用的过氧化物总量的50~99%消耗在第一反应器中,其余部分消耗在后面的一个或几个反应器中。
5.如权利要求1~4中任何一项的方法,其中所有的反应器尺寸是一样的。
6.如权利要求1~5中任何一项的方法,其中在每个反应器中的催化剂呈颗粒状,其中至少一部分处于流态化的状态。
7.如权利要求6的方法,其中从第一反应器出来的介质经过一个过滤器,然后进入后一个反应器。
8.如权利要求1~7中任何一项的方法,其中进入后一个反应器的介质在加入到后一个反应器之前先要进行降压。
9.如权利要求1~8中任何一项的方法,其中进入后一个反应器的介质在加入到后一个反应器之前先要进行分离形成的环氧烷烃的处理。
10.如权利要求9的方法,其中的分离处理是蒸馏。
11.如权利要求1~10中任何一项的方法,其中的环氧烷烃是环氧氯丙烷,烯烃是烯丙基氯,过氧化物是过氧化氢,溶剂是甲醇而催化剂含有TS-1,其中TS-1相应于通式xTiO2(1-x)SiO2,其中x是0.0001~0.5。
12.如权利要求1~10中任何一项的方法,其中的环氧烷烃是环氧丙烷,烯烃是丙烯,过氧化物是过氧化氢,溶剂是甲醇而催化剂含有TS-1,其中TS-1相应于通式xTiO2(1-x)SiO2,其中x是0.0001~0.5。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR0008355 | 2000-06-28 | ||
| FR0008355A FR2810983B1 (fr) | 2000-06-28 | 2000-06-28 | Procede de fabrication d'oxiranne au moyen d'un compose peroxyde |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN1449392A CN1449392A (zh) | 2003-10-15 |
| CN1245395C true CN1245395C (zh) | 2006-03-15 |
Family
ID=8851835
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CNB018148026A Expired - Lifetime CN1245395C (zh) | 2000-06-28 | 2001-06-26 | 使用过氧化物制造环氧烷烃的方法 |
Country Status (15)
| Country | Link |
|---|---|
| US (2) | US6677467B2 (zh) |
| EP (1) | EP1299371B1 (zh) |
| JP (2) | JP5196696B2 (zh) |
| CN (1) | CN1245395C (zh) |
| AT (1) | ATE385495T1 (zh) |
| AU (1) | AU2001287559A1 (zh) |
| BR (1) | BR0111973B1 (zh) |
| CA (1) | CA2412546C (zh) |
| DE (1) | DE60132700T2 (zh) |
| ES (1) | ES2301560T3 (zh) |
| FR (1) | FR2810983B1 (zh) |
| MX (1) | MXPA02012665A (zh) |
| RU (1) | RU2256656C2 (zh) |
| WO (1) | WO2002000637A1 (zh) |
| ZA (1) | ZA200210159B (zh) |
Families Citing this family (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2846964B1 (fr) * | 2002-11-12 | 2006-07-21 | Procede de fabrication de 1,2-epoxy-3-chloropropane | |
| EP2103604A1 (de) * | 2008-03-17 | 2009-09-23 | Evonik Degussa GmbH | Verfahren zur Herstellung von Epichlorhydrin |
| EP2149569A1 (en) | 2008-08-01 | 2010-02-03 | Hexion Specialty Chemicals Research Belgium S.A. | Process for the manufacture of a 1,2-Epoxide |
| EP2149570A1 (en) * | 2008-08-01 | 2010-02-03 | Hexion Specialty Chemicals Research Belgium S.A. | Process for the manufacture of epichlorohydrin using hydrogen peroxide and a manganese komplex |
| US8859791B2 (en) * | 2010-10-11 | 2014-10-14 | China Petroleum & Chemical Corporation | Process for producing an alkylene oxide by olefin epoxidation |
| CN102442979B (zh) * | 2010-10-11 | 2014-10-08 | 中国石油化工股份有限公司 | 一种环氧丙烷的制备方法 |
| CN102442976B (zh) * | 2010-10-11 | 2014-01-15 | 中国石油化工股份有限公司 | 烯烃环氧化方法 |
| CN102442978B (zh) * | 2010-10-11 | 2014-01-15 | 中国石油化工股份有限公司 | 一种烯烃环氧化方法 |
| WO2012048530A1 (zh) | 2010-10-11 | 2012-04-19 | 中国石油化工股份有限公司 | 环氧丙烷粗产品的精制方法和环氧丙烷的制备方法 |
| EA201391089A1 (ru) | 2011-01-27 | 2014-06-30 | Солвей Са | Способ изготовления 1,2-эпокси-3-хлорпропана |
| EP2668173A1 (en) | 2011-01-27 | 2013-12-04 | Solvay SA | Process for the manufacture of 1,2-epoxy-3-chloropropane |
| WO2013012518A1 (en) * | 2011-06-23 | 2013-01-24 | Dow Technology Investments Llc | Production of oxidized olefins |
| CN103724299B (zh) * | 2013-12-12 | 2015-10-21 | 中石化上海工程有限公司 | 制备环氧丙烷的方法 |
| CN103641800B (zh) * | 2013-12-12 | 2016-08-17 | 中石化上海工程有限公司 | 环氧丙烷的生产方法 |
| CN105524019B (zh) * | 2014-09-29 | 2017-12-22 | 中国石油化工股份有限公司 | 一种氧化烯烃的制备方法 |
| CA3235908A1 (en) | 2021-12-22 | 2023-06-29 | Andrew WILLSON | Novel process for the production of hydrogen peroxide |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2137310C (en) * | 1993-12-20 | 2004-02-17 | John C. Jubin Jr. | Catalytic converter and method for highly exothermic reactions |
| BE1011539A3 (fr) * | 1997-11-07 | 1999-10-05 | Solvay | Procede de fabrication d'un compose organique. |
| GB2331071A (en) | 1997-11-11 | 1999-05-12 | Solvay | Manufacture of micro spherical zeolite containing catalyst particles |
| BE1011577A3 (fr) | 1997-11-27 | 1999-11-09 | Solvay | Catalyseur d'epoxydation, son utilisation et procede d'epoxydation en presence de catalyseur. |
| US5849937A (en) * | 1997-12-19 | 1998-12-15 | Arco Chemical Technology, L.P. | Epoxidation process using serially connected cascade of fixed bed reactors |
| BE1011851A3 (fr) | 1998-03-24 | 2000-02-01 | Solvay | Procede de fabrication d'un oxiranne. |
| BE1011852A3 (fr) * | 1998-03-24 | 2000-02-01 | Solvay | Procede de fabrication d'un oxiranne. |
| GB9812742D0 (en) * | 1998-06-12 | 1998-08-12 | Philips Electronics Nv | Active matrix electroluminescent display devices |
| DE19835907A1 (de) | 1998-08-07 | 2000-02-17 | Basf Ag | Verfahren zur Umsetzung einer organischen Verbindung mit einem Hydroperoxid |
| BE1012303A3 (fr) | 1998-11-20 | 2000-09-05 | Solvay | Procede de fabrication d'un oxiranne. |
-
2000
- 2000-06-28 FR FR0008355A patent/FR2810983B1/fr not_active Expired - Fee Related
-
2001
- 2001-06-26 US US10/311,308 patent/US6677467B2/en not_active Expired - Lifetime
- 2001-06-26 AT AT01967093T patent/ATE385495T1/de not_active IP Right Cessation
- 2001-06-26 DE DE60132700T patent/DE60132700T2/de not_active Expired - Lifetime
- 2001-06-26 RU RU2003102385/04A patent/RU2256656C2/ru active
- 2001-06-26 CN CNB018148026A patent/CN1245395C/zh not_active Expired - Lifetime
- 2001-06-26 ES ES01967093T patent/ES2301560T3/es not_active Expired - Lifetime
- 2001-06-26 BR BRPI0111973-7A patent/BR0111973B1/pt not_active IP Right Cessation
- 2001-06-26 MX MXPA02012665A patent/MXPA02012665A/es active IP Right Grant
- 2001-06-26 EP EP01967093A patent/EP1299371B1/fr not_active Revoked
- 2001-06-26 CA CA2412546A patent/CA2412546C/fr not_active Expired - Lifetime
- 2001-06-26 JP JP2002505385A patent/JP5196696B2/ja not_active Expired - Lifetime
- 2001-06-26 AU AU2001287559A patent/AU2001287559A1/en not_active Abandoned
- 2001-06-26 WO PCT/EP2001/007273 patent/WO2002000637A1/fr active IP Right Grant
-
2002
- 2002-12-13 ZA ZA200210159A patent/ZA200210159B/en unknown
-
2003
- 2003-08-29 US US10/650,730 patent/US6838571B2/en not_active Expired - Lifetime
-
2012
- 2012-12-10 JP JP2012269523A patent/JP2013079259A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| DE60132700T2 (de) | 2009-02-12 |
| BR0111973B1 (pt) | 2012-01-10 |
| CA2412546A1 (fr) | 2002-01-03 |
| FR2810983A1 (fr) | 2002-01-04 |
| US6677467B2 (en) | 2004-01-13 |
| JP5196696B2 (ja) | 2013-05-15 |
| ATE385495T1 (de) | 2008-02-15 |
| BR0111973A (pt) | 2003-07-01 |
| FR2810983B1 (fr) | 2004-05-21 |
| EP1299371B1 (fr) | 2008-02-06 |
| US6838571B2 (en) | 2005-01-04 |
| WO2002000637A1 (fr) | 2002-01-03 |
| DE60132700D1 (de) | 2008-03-20 |
| US20040039216A1 (en) | 2004-02-26 |
| MXPA02012665A (es) | 2003-05-14 |
| AU2001287559A1 (en) | 2002-01-08 |
| JP2013079259A (ja) | 2013-05-02 |
| ES2301560T3 (es) | 2008-07-01 |
| CA2412546C (fr) | 2011-02-01 |
| EP1299371A1 (fr) | 2003-04-09 |
| RU2256656C2 (ru) | 2005-07-20 |
| CN1449392A (zh) | 2003-10-15 |
| JP2004501908A (ja) | 2004-01-22 |
| US20030109726A1 (en) | 2003-06-12 |
| ZA200210159B (en) | 2004-03-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN1245395C (zh) | 使用过氧化物制造环氧烷烃的方法 | |
| CN1109883A (zh) | 制备环氧化物的集中方法 | |
| WO2009063487A2 (en) | An improved process for manufacture of epoxides, particularly epichlorohydrin | |
| CN100447138C (zh) | 烯烃的环氧化方法 | |
| JP2013049726A (ja) | 反応媒体からオキシランを分離する事を含むオキシランの製造方法 | |
| CN102137850A (zh) | 环氧丙烷方法 | |
| KR100830278B1 (ko) | 집적된 에폭사이드 제조방법 | |
| WO2001070710A1 (fr) | Procede de production d'oxyde de propylene | |
| CN1240693C (zh) | 环氧烷烃的制造方法 | |
| JPS6247172B2 (zh) | ||
| RU2019103844A (ru) | Способ получения этиленоксида | |
| KR20080081195A (ko) | 프로펜의 에폭시화 방법 | |
| CN1249042C (zh) | 烯烃直接环氧化的悬浮催化蒸馏工艺方法 | |
| WO2002088104A1 (fr) | Procede de fabrication d'oxyde de propylene | |
| RU2315760C2 (ru) | Способ получения стирола | |
| JP3969078B2 (ja) | ペンタシル型ゼオライトの製造方法およびε−カプロラクタムの製造方法 | |
| CN113968768B (zh) | 丙烯回收方法和设备以及环氧化反应产物分离方法和装置以及环氧化方法和环氧化系统 | |
| CN117700299A (zh) | 一种烯丙醇的制备方法 | |
| JP3213497B2 (ja) | メチルアミンの製造方法 | |
| JP2003081954A (ja) | プロピレンオキサイドの製造方法 | |
| JP2004525073A (ja) | オレフィンオキシドの連続製造方法 | |
| KR20220013700A (ko) | 비닐계 단량체의 제조방법 | |
| CN111606871A (zh) | 一种环氧氯丙烷的制备方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C14 | Grant of patent or utility model | ||
| GR01 | Patent grant | ||
| CX01 | Expiry of patent term | ||
| CX01 | Expiry of patent term |
Granted publication date: 20060315 |