CN1178973C - 官能化聚亚烷基亚胺的制备方法,含有它们的组合物及其应用 - Google Patents
官能化聚亚烷基亚胺的制备方法,含有它们的组合物及其应用 Download PDFInfo
- Publication number
- CN1178973C CN1178973C CNB018068014A CN01806801A CN1178973C CN 1178973 C CN1178973 C CN 1178973C CN B018068014 A CNB018068014 A CN B018068014A CN 01806801 A CN01806801 A CN 01806801A CN 1178973 C CN1178973 C CN 1178973C
- Authority
- CN
- China
- Prior art keywords
- preparation
- poly alkylene
- functionalized poly
- alkylene imine
- nucleic acid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 238000000034 method Methods 0.000 title claims abstract description 33
- 239000000203 mixture Substances 0.000 title claims abstract description 21
- 108020004707 nucleic acids Proteins 0.000 claims abstract description 43
- 102000039446 nucleic acids Human genes 0.000 claims abstract description 43
- 150000007523 nucleic acids Chemical class 0.000 claims abstract description 43
- VXUYXOFXAQZZMF-UHFFFAOYSA-N titanium(IV) isopropoxide Chemical compound CC(C)O[Ti](OC(C)C)(OC(C)C)OC(C)C VXUYXOFXAQZZMF-UHFFFAOYSA-N 0.000 claims abstract description 20
- 150000002373 hemiacetals Chemical class 0.000 claims abstract description 16
- 239000012279 sodium borohydride Substances 0.000 claims abstract description 8
- 229910000033 sodium borohydride Inorganic materials 0.000 claims abstract description 8
- 108090000623 proteins and genes Proteins 0.000 claims description 46
- 150000002466 imines Chemical class 0.000 claims description 32
- 238000002360 preparation method Methods 0.000 claims description 27
- 229920001281 polyalkylene Polymers 0.000 claims description 26
- 229920002873 Polyethylenimine Polymers 0.000 claims description 25
- 102000004169 proteins and genes Human genes 0.000 claims description 21
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 claims description 13
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 claims description 11
- GUBGYTABKSRVRQ-QUYVBRFLSA-N beta-maltose Chemical compound OC[C@H]1O[C@H](O[C@H]2[C@H](O)[C@@H](O)[C@H](O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@@H]1O GUBGYTABKSRVRQ-QUYVBRFLSA-N 0.000 claims description 11
- OWEGMIWEEQEYGQ-UHFFFAOYSA-N 100676-05-9 Natural products OC1C(O)C(O)C(CO)OC1OCC1C(O)C(O)C(O)C(OC2C(OC(O)C(O)C2O)CO)O1 OWEGMIWEEQEYGQ-UHFFFAOYSA-N 0.000 claims description 9
- GUBGYTABKSRVRQ-PICCSMPSSA-N Maltose Natural products O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@@H](CO)OC(O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-PICCSMPSSA-N 0.000 claims description 9
- 239000008101 lactose Substances 0.000 claims description 9
- 238000006243 chemical reaction Methods 0.000 claims description 8
- 108090000765 processed proteins & peptides Proteins 0.000 claims description 8
- 239000000126 substance Substances 0.000 claims description 8
- -1 polytrimethylene Polymers 0.000 claims description 7
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims description 6
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical group OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 claims description 6
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 6
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 5
- 239000003446 ligand Substances 0.000 claims description 5
- 239000002904 solvent Substances 0.000 claims description 5
- 210000001541 thymus gland Anatomy 0.000 claims description 5
- 108091034117 Oligonucleotide Proteins 0.000 claims description 4
- 230000001476 alcoholic effect Effects 0.000 claims description 4
- 239000003814 drug Substances 0.000 claims description 4
- 108010021625 Immunoglobulin Fragments Proteins 0.000 claims description 3
- 102000008394 Immunoglobulin Fragments Human genes 0.000 claims description 3
- 239000005556 hormone Substances 0.000 claims description 3
- 229940088597 hormone Drugs 0.000 claims description 3
- 239000002858 neurotransmitter agent Substances 0.000 claims description 3
- 101710186708 Agglutinin Proteins 0.000 claims description 2
- SHZGCJCMOBCMKK-UHFFFAOYSA-N D-mannomethylose Natural products CC1OC(O)C(O)C(O)C1O SHZGCJCMOBCMKK-UHFFFAOYSA-N 0.000 claims description 2
- PNNNRSAQSRJVSB-SLPGGIOYSA-N Fucose Natural products C[C@H](O)[C@@H](O)[C@H](O)[C@H](O)C=O PNNNRSAQSRJVSB-SLPGGIOYSA-N 0.000 claims description 2
- 102000009465 Growth Factor Receptors Human genes 0.000 claims description 2
- 108010009202 Growth Factor Receptors Proteins 0.000 claims description 2
- 101710146024 Horcolin Proteins 0.000 claims description 2
- SHZGCJCMOBCMKK-DHVFOXMCSA-N L-fucopyranose Chemical compound C[C@@H]1OC(O)[C@@H](O)[C@H](O)[C@@H]1O SHZGCJCMOBCMKK-DHVFOXMCSA-N 0.000 claims description 2
- 101710189395 Lectin Proteins 0.000 claims description 2
- 101710179758 Mannose-specific lectin Proteins 0.000 claims description 2
- 101710150763 Mannose-specific lectin 1 Proteins 0.000 claims description 2
- 101710150745 Mannose-specific lectin 2 Proteins 0.000 claims description 2
- 240000004808 Saccharomyces cerevisiae Species 0.000 claims description 2
- LPQOADBMXVRBNX-UHFFFAOYSA-N ac1ldcw0 Chemical compound Cl.C1CN(C)CCN1C1=C(F)C=C2C(=O)C(C(O)=O)=CN3CCSC1=C32 LPQOADBMXVRBNX-UHFFFAOYSA-N 0.000 claims description 2
- 239000000910 agglutinin Substances 0.000 claims description 2
- WQZGKKKJIJFFOK-PQMKYFCFSA-N alpha-D-mannose Chemical compound OC[C@H]1O[C@H](O)[C@@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-PQMKYFCFSA-N 0.000 claims description 2
- 102000003675 cytokine receptors Human genes 0.000 claims description 2
- 108010057085 cytokine receptors Proteins 0.000 claims description 2
- 150000002016 disaccharides Chemical class 0.000 claims description 2
- 229940014144 folate Drugs 0.000 claims description 2
- OVBPIULPVIDEAO-LBPRGKRZSA-N folic acid Chemical compound C=1N=C2NC(N)=NC(=O)C2=NC=1CNC1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 OVBPIULPVIDEAO-LBPRGKRZSA-N 0.000 claims description 2
- 235000019152 folic acid Nutrition 0.000 claims description 2
- 239000011724 folic acid Substances 0.000 claims description 2
- 102000006495 integrins Human genes 0.000 claims description 2
- 108010044426 integrins Proteins 0.000 claims description 2
- 150000002632 lipids Chemical class 0.000 claims description 2
- 229920001542 oligosaccharide Polymers 0.000 claims description 2
- 150000002482 oligosaccharides Chemical class 0.000 claims description 2
- 230000001105 regulatory effect Effects 0.000 claims description 2
- 150000004043 trisaccharides Chemical class 0.000 claims description 2
- 239000011782 vitamin Substances 0.000 claims description 2
- 235000013343 vitamin Nutrition 0.000 claims description 2
- 229940088594 vitamin Drugs 0.000 claims description 2
- 229930003231 vitamin Natural products 0.000 claims description 2
- 150000003722 vitamin derivatives Chemical class 0.000 claims description 2
- 238000009472 formulation Methods 0.000 abstract 1
- 210000004027 cell Anatomy 0.000 description 60
- 108020004414 DNA Proteins 0.000 description 17
- 239000000243 solution Substances 0.000 description 13
- GHMLBKRAJCXXBS-UHFFFAOYSA-N resorcinol Chemical compound OC1=CC=CC(O)=C1 GHMLBKRAJCXXBS-UHFFFAOYSA-N 0.000 description 12
- 238000001890 transfection Methods 0.000 description 12
- 239000013612 plasmid Substances 0.000 description 10
- 230000000694 effects Effects 0.000 description 9
- 239000011541 reaction mixture Substances 0.000 description 9
- 231100000419 toxicity Toxicity 0.000 description 9
- 230000001988 toxicity Effects 0.000 description 9
- 239000000047 product Substances 0.000 description 8
- 238000003756 stirring Methods 0.000 description 8
- NOWKCMXCCJGMRR-UHFFFAOYSA-N Aziridine Chemical compound C1CN1 NOWKCMXCCJGMRR-UHFFFAOYSA-N 0.000 description 6
- 238000000502 dialysis Methods 0.000 description 6
- 230000013595 glycosylation Effects 0.000 description 6
- 238000006206 glycosylation reaction Methods 0.000 description 6
- 210000001519 tissue Anatomy 0.000 description 6
- 238000012546 transfer Methods 0.000 description 6
- 125000003277 amino group Chemical group 0.000 description 5
- 238000002347 injection Methods 0.000 description 5
- 239000007924 injection Substances 0.000 description 5
- 108020004999 messenger RNA Proteins 0.000 description 5
- 108090000790 Enzymes Proteins 0.000 description 4
- 102000004190 Enzymes Human genes 0.000 description 4
- 241001465754 Metazoa Species 0.000 description 4
- 241000700605 Viruses Species 0.000 description 4
- 150000001298 alcohols Chemical class 0.000 description 4
- 125000000217 alkyl group Chemical group 0.000 description 4
- 239000000427 antigen Substances 0.000 description 4
- 108091007433 antigens Proteins 0.000 description 4
- 102000036639 antigens Human genes 0.000 description 4
- 229920006317 cationic polymer Polymers 0.000 description 4
- 201000010099 disease Diseases 0.000 description 4
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 4
- 125000003071 maltose group Chemical group 0.000 description 4
- 239000012299 nitrogen atmosphere Substances 0.000 description 4
- 229920000642 polymer Polymers 0.000 description 4
- 230000004083 survival effect Effects 0.000 description 4
- 206010028980 Neoplasm Diseases 0.000 description 3
- 108020004566 Transfer RNA Proteins 0.000 description 3
- 239000004615 ingredient Substances 0.000 description 3
- 210000000056 organ Anatomy 0.000 description 3
- 108020003175 receptors Proteins 0.000 description 3
- 102000005962 receptors Human genes 0.000 description 3
- 238000011160 research Methods 0.000 description 3
- 210000002966 serum Anatomy 0.000 description 3
- 239000013598 vector Substances 0.000 description 3
- 108020004635 Complementary DNA Proteins 0.000 description 2
- 102000001039 Dystrophin Human genes 0.000 description 2
- 108010069091 Dystrophin Proteins 0.000 description 2
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 2
- 108090001090 Lectins Proteins 0.000 description 2
- 102000004856 Lectins Human genes 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 150000001412 amines Chemical class 0.000 description 2
- 230000000692 anti-sense effect Effects 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 238000010804 cDNA synthesis Methods 0.000 description 2
- 244000309466 calf Species 0.000 description 2
- 239000000969 carrier Substances 0.000 description 2
- 125000002091 cationic group Chemical group 0.000 description 2
- 238000001311 chemical methods and process Methods 0.000 description 2
- 239000003795 chemical substances by application Substances 0.000 description 2
- 239000002299 complementary DNA Substances 0.000 description 2
- 125000000753 cycloalkyl group Chemical group 0.000 description 2
- 238000010586 diagram Methods 0.000 description 2
- 150000004985 diamines Chemical class 0.000 description 2
- 239000000975 dye Substances 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 239000012634 fragment Substances 0.000 description 2
- 125000000524 functional group Chemical group 0.000 description 2
- 230000002068 genetic effect Effects 0.000 description 2
- 230000028993 immune response Effects 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- 230000001939 inductive effect Effects 0.000 description 2
- 210000000936 intestine Anatomy 0.000 description 2
- 239000002523 lectin Substances 0.000 description 2
- 239000006166 lysate Substances 0.000 description 2
- 239000002609 medium Substances 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 210000004940 nucleus Anatomy 0.000 description 2
- 238000006068 polycondensation reaction Methods 0.000 description 2
- 238000006116 polymerization reaction Methods 0.000 description 2
- 239000000376 reactant Substances 0.000 description 2
- 210000000664 rectum Anatomy 0.000 description 2
- 239000013074 reference sample Substances 0.000 description 2
- 150000003384 small molecules Chemical class 0.000 description 2
- 229910052708 sodium Inorganic materials 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 210000002784 stomach Anatomy 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- 229960005486 vaccine Drugs 0.000 description 2
- 230000003612 virological effect Effects 0.000 description 2
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 1
- XQCZBXHVTFVIFE-UHFFFAOYSA-N 2-amino-4-hydroxypyrimidine Chemical compound NC1=NC=CC(O)=N1 XQCZBXHVTFVIFE-UHFFFAOYSA-N 0.000 description 1
- XMTQQYYKAHVGBJ-UHFFFAOYSA-N 3-(3,4-DICHLOROPHENYL)-1,1-DIMETHYLUREA Chemical compound CN(C)C(=O)NC1=CC=C(Cl)C(Cl)=C1 XMTQQYYKAHVGBJ-UHFFFAOYSA-N 0.000 description 1
- 102000007592 Apolipoproteins Human genes 0.000 description 1
- 108010071619 Apolipoproteins Proteins 0.000 description 1
- 102000013918 Apolipoproteins E Human genes 0.000 description 1
- 108010025628 Apolipoproteins E Proteins 0.000 description 1
- 108010002913 Asialoglycoproteins Proteins 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- 108090000715 Brain-derived neurotrophic factor Proteins 0.000 description 1
- 102000004219 Brain-derived neurotrophic factor Human genes 0.000 description 1
- 108090000994 Catalytic RNA Proteins 0.000 description 1
- 102000053642 Catalytic RNA Human genes 0.000 description 1
- 206010057248 Cell death Diseases 0.000 description 1
- 108010005939 Ciliary Neurotrophic Factor Proteins 0.000 description 1
- 102100031614 Ciliary neurotrophic factor Human genes 0.000 description 1
- 102100023804 Coagulation factor VII Human genes 0.000 description 1
- 108020004394 Complementary RNA Proteins 0.000 description 1
- 102000012605 Cystic Fibrosis Transmembrane Conductance Regulator Human genes 0.000 description 1
- 108010079245 Cystic Fibrosis Transmembrane Conductance Regulator Proteins 0.000 description 1
- 201000003883 Cystic fibrosis Diseases 0.000 description 1
- 206010011766 Cystic fibrosis pancreatic Diseases 0.000 description 1
- 241000701022 Cytomegalovirus Species 0.000 description 1
- 230000033616 DNA repair Effects 0.000 description 1
- ZNZYKNKBJPZETN-WELNAUFTSA-N Dialdehyde 11678 Chemical compound N1C2=CC=CC=C2C2=C1[C@H](C[C@H](/C(=C/O)C(=O)OC)[C@@H](C=C)C=O)NCC2 ZNZYKNKBJPZETN-WELNAUFTSA-N 0.000 description 1
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 1
- 241000196324 Embryophyta Species 0.000 description 1
- 102000004533 Endonucleases Human genes 0.000 description 1
- 108010042407 Endonucleases Proteins 0.000 description 1
- 241000206602 Eukaryota Species 0.000 description 1
- 108010023321 Factor VII Proteins 0.000 description 1
- 108090000386 Fibroblast Growth Factor 1 Proteins 0.000 description 1
- 102100031706 Fibroblast growth factor 1 Human genes 0.000 description 1
- 102100024785 Fibroblast growth factor 2 Human genes 0.000 description 1
- 108090000379 Fibroblast growth factor 2 Proteins 0.000 description 1
- 102000004038 Glia Maturation Factor Human genes 0.000 description 1
- 108090000495 Glia Maturation Factor Proteins 0.000 description 1
- 108010054147 Hemoglobins Proteins 0.000 description 1
- 241000700721 Hepatitis B virus Species 0.000 description 1
- 101000599951 Homo sapiens Insulin-like growth factor I Proteins 0.000 description 1
- 241000701044 Human gammaherpesvirus 4 Species 0.000 description 1
- 241000725303 Human immunodeficiency virus Species 0.000 description 1
- 108090000723 Insulin-Like Growth Factor I Proteins 0.000 description 1
- 102100037852 Insulin-like growth factor I Human genes 0.000 description 1
- 102000014150 Interferons Human genes 0.000 description 1
- 108010050904 Interferons Proteins 0.000 description 1
- 108060001084 Luciferase Proteins 0.000 description 1
- 239000005089 Luciferase Substances 0.000 description 1
- 101001055320 Myxine glutinosa Insulin-like growth factor Proteins 0.000 description 1
- 108010025020 Nerve Growth Factor Proteins 0.000 description 1
- 102000015336 Nerve Growth Factor Human genes 0.000 description 1
- 108090000742 Neurotrophin 3 Proteins 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 1
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 1
- 101100379247 Salmo trutta apoa1 gene Proteins 0.000 description 1
- 102000013275 Somatomedins Human genes 0.000 description 1
- 102100032889 Sortilin Human genes 0.000 description 1
- 102000006601 Thymidine Kinase Human genes 0.000 description 1
- 108020004440 Thymidine kinase Proteins 0.000 description 1
- 102000044209 Tumor Suppressor Genes Human genes 0.000 description 1
- 108700025716 Tumor Suppressor Genes Proteins 0.000 description 1
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 description 1
- 102000005789 Vascular Endothelial Growth Factors Human genes 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 238000012382 advanced drug delivery Methods 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 150000001299 aldehydes Chemical class 0.000 description 1
- NIGUVXFURDGQKZ-UQTBNESHSA-N alpha-Neup5Ac-(2->3)-beta-D-Galp-(1->4)-[alpha-L-Fucp-(1->3)]-beta-D-GlcpNAc Chemical compound O[C@H]1[C@H](O)[C@H](O)[C@H](C)O[C@H]1O[C@H]1[C@H](O[C@H]2[C@@H]([C@@H](O[C@]3(O[C@H]([C@H](NC(C)=O)[C@@H](O)C3)[C@H](O)[C@H](O)CO)C(O)=O)[C@@H](O)[C@@H](CO)O2)O)[C@@H](CO)O[C@@H](O)[C@@H]1NC(C)=O NIGUVXFURDGQKZ-UQTBNESHSA-N 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 230000000845 anti-microbial effect Effects 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- 229920005601 base polymer Polymers 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 239000003914 blood derivative Substances 0.000 description 1
- 210000000988 bone and bone Anatomy 0.000 description 1
- 229910000085 borane Inorganic materials 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 125000004432 carbon atom Chemical group C* 0.000 description 1
- 210000000845 cartilage Anatomy 0.000 description 1
- 230000001925 catabolic effect Effects 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 239000003184 complementary RNA Substances 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 230000001276 controlling effect Effects 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 230000009089 cytolysis Effects 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 238000009792 diffusion process Methods 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 230000009144 enzymatic modification Effects 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 229940012413 factor vii Drugs 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 238000007306 functionalization reaction Methods 0.000 description 1
- 210000004907 gland Anatomy 0.000 description 1
- 210000002216 heart Anatomy 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 210000003958 hematopoietic stem cell Anatomy 0.000 description 1
- 229920000140 heteropolymer Polymers 0.000 description 1
- 229920001519 homopolymer Polymers 0.000 description 1
- 238000009396 hybridization Methods 0.000 description 1
- 238000009169 immunotherapy Methods 0.000 description 1
- 230000002779 inactivation Effects 0.000 description 1
- 238000011081 inoculation Methods 0.000 description 1
- 229940079322 interferon Drugs 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 239000000644 isotonic solution Substances 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 210000005229 liver cell Anatomy 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- 210000002751 lymph Anatomy 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 230000004060 metabolic process Effects 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 210000004400 mucous membrane Anatomy 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- 230000001537 neural effect Effects 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 239000012454 non-polar solvent Substances 0.000 description 1
- 210000000633 nuclear envelope Anatomy 0.000 description 1
- 235000015097 nutrients Nutrition 0.000 description 1
- 235000003170 nutritional factors Nutrition 0.000 description 1
- 230000008520 organization Effects 0.000 description 1
- 210000001672 ovary Anatomy 0.000 description 1
- 210000000496 pancreas Anatomy 0.000 description 1
- 230000007170 pathology Effects 0.000 description 1
- 150000003014 phosphoric acid esters Chemical class 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 239000002994 raw material Substances 0.000 description 1
- 230000010076 replication Effects 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 108091092562 ribozyme Proteins 0.000 description 1
- 210000003491 skin Anatomy 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- BEOOHQFXGBMRKU-UHFFFAOYSA-N sodium cyanoborohydride Chemical compound [Na+].[B-]C#N BEOOHQFXGBMRKU-UHFFFAOYSA-N 0.000 description 1
- 239000012321 sodium triacetoxyborohydride Substances 0.000 description 1
- 210000000952 spleen Anatomy 0.000 description 1
- 230000004936 stimulating effect Effects 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 210000001550 testis Anatomy 0.000 description 1
- 230000005030 transcription termination Effects 0.000 description 1
- 230000009261 transgenic effect Effects 0.000 description 1
- UORVGPXVDQYIDP-UHFFFAOYSA-N trihydridoboron Substances B UORVGPXVDQYIDP-UHFFFAOYSA-N 0.000 description 1
- 210000004881 tumor cell Anatomy 0.000 description 1
- 210000003932 urinary bladder Anatomy 0.000 description 1
- 210000001215 vagina Anatomy 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G73/00—Macromolecular compounds obtained by reactions forming a linkage containing nitrogen with or without oxygen or carbon in the main chain of the macromolecule, not provided for in groups C08G12/00 - C08G71/00
- C08G73/02—Polyamines
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/87—Introduction of foreign genetic material using processes not otherwise provided for, e.g. co-transformation
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G73/00—Macromolecular compounds obtained by reactions forming a linkage containing nitrogen with or without oxygen or carbon in the main chain of the macromolecule, not provided for in groups C08G12/00 - C08G71/00
- C08G73/02—Polyamines
- C08G73/0206—Polyalkylene(poly)amines
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G73/00—Macromolecular compounds obtained by reactions forming a linkage containing nitrogen with or without oxygen or carbon in the main chain of the macromolecule, not provided for in groups C08G12/00 - C08G71/00
- C08G73/02—Polyamines
- C08G73/0206—Polyalkylene(poly)amines
- C08G73/0213—Preparatory process
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Genetics & Genomics (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Medicinal Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Polymers & Plastics (AREA)
- Biomedical Technology (AREA)
- Biotechnology (AREA)
- General Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Biophysics (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Microbiology (AREA)
- Plant Pathology (AREA)
- Molecular Biology (AREA)
- Physics & Mathematics (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Macromolecular Compounds Obtained By Forming Nitrogen-Containing Linkages In General (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Polymers With Sulfur, Phosphorus Or Metals In The Main Chain (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
本发明涉及一种官能化聚亚烷基亚胺的制备方法,该官能化聚亚烷基亚胺适用于有待转染到细胞中的核酸的配方。该方法在于在异丙醇钛(IV)和硼氢化钠存在下,用官能化半缩醛处理聚亚烷基亚胺。
Description
本发明涉及适用于有待转染到细胞中的核酸配方的官能化聚亚烷基亚胺的制备方法。
随着生物技术的发展,往细胞中有效转移核酸的可能性已变成许多生物技术应用的基本技术。可以涉及例如用于生产重组蛋白质、或在实验室中研究基因表达的调节作用、基因克隆选择,或涉及DNA任何其他处理方面核酸往离体细胞中的转移。还可以涉及例如用于制备疫苗、研究标记或治疗方法方面核酸往活体内细胞中的转移。还可以涉及在从生物体取出的细胞中转移基因,以便以后再使用这些基因,例如用于产生转基因动物。
目前用于往细胞中转移基因的最流行的方法是使用病毒载体。由于这些载体并未完全丧失危险性,所以人们曾提出其他几种基于应用合成载体的方法。这些合成载体具有两种基本功能:复合和密集待转染的核酸,促进核酸通过质粒膜并且任选地通过两种核膜。
于是曾提出多组合成载体。在这些载体中,阳离子聚合物如聚亚烷基亚胺是特别有意义的。事实上业已证明,特别是在活体内转染核酸时,这些阳离子聚合物是比较有效的,并且还具有比较低的毒性。还观察到,这些阳离子聚合物与核酸生成的配合物(也被称作《聚丛(polyplexes)》)在注射点外扩散得比较好(J.S.Remy等人《Advanced Drug Delivery Reviews》,30,1998,第85-95页)。
另外,迄今为止,重要的似乎是将能击中适当核酸的载体带到器官、组织、一类细胞或特别的细胞腔,因为重要的是能够保证转染的核酸与靶细胞有效地整合在一起,而不会非常不利地扩散到生物体的其余部分。希望达到的目的是避免核酸与除靶细胞外的细胞有任何非专一的作用。于是证明了,半乳糖基化聚亚乙基亚胺是一种质粒体离体转移到具有相应于半乳糖的细胞受体(凝集素)的细胞中的有效载体(Zanta等人,《Bioconj.Chem.》,8(2),1997,第839页;T.Bettinger等人,《Bioconj.Chem.》,1999)。
迄今为止,例如像半乳糖基化聚亚乙基亚胺之类聚合物是在氰基硼氢化钠存在下,通过低聚糖与聚亚乙基亚胺作用得到的。但是,这种反应物的缺陷是成本高,特别是毒性非常高。在相对地阳离子的最后产物中,可能残存氰离子的危险性使其完全不可能被用于药物。另外,对可供选择替代的制备方法的研究迄今为止仍然是徒劳的,因为聚亚烷基亚胺是聚合物-因此不是小分子-它们不溶于许多溶剂中,特别是不溶于非极性溶剂中。因此,不可能利用其中使用三乙酰氧基硼氢化钠的可供选择替代方法。此外,在含水硫酸中使用硼氢化钠和吡啶-硼烷混合物与这些阳离子聚合物不相容。因此,有必要研制一种与聚亚烷基亚胺类阳离子聚合物相容的不涉及在药学上可接受的反应物的选择替代方法。
于是曾发现在异丙醇钛(IV)和硼氢化钠存在下,通过用官能化半缩醛处理聚亚烷基亚胺,可能制备官能化的聚亚烷基亚胺。
这样一种方法的优点是能够在与聚亚烷基亚胺相容的溶剂如醇中实施,同时只涉及既不太贵、毒性也不大的反应剂。
Bhattacharyya等人在(《有机化学杂志》,1995,60,第4928-4929页);《Synlett》,1995,第1079-1080页;《J.Chem.Soc.,Perkin Trans.》1,1998,第2527-2531页中的不同文章,描述了用下述醛酮制备胺的方法:
式中R和R′彼此独立地代表氢原子、烷基、芳基或一起构成具有5、6或7节链的任选地含有杂原子的环烷基,R1和R2彼此独立地代表氢原子、任选地被羟基或酯取代的烷基,或R1和R2一起构成具有5或6节链的任选地含有杂原子的环烷基。但是,这样一种方法只是在使用相应酮或醛为原料制备小分子、特别是含有唯一胺官能团的非聚合分子领域中描述过。
根据本发明,原料聚亚烷基亚胺具有下述通式:
式中R代表氢原子或下述通式基团:
n是2~10的整数,
p和q是整数,其条件是p+q之和使得聚合物平均分子量是100-107Da。
应当理解在通式(I)中,n值和R基团可以在不同结构单元-NR-(CH2)n-与-(CH2)n-NH-之间发生变化。因此,通式(I)同时汇集了直链聚合物和支链聚合物以及均聚物和杂聚物。
优选地,n是2-5,优选的聚合物例如是聚亚乙基亚胺(PEI)或聚亚丙基亚胺(PPI)。另外,曾证明实施本发明的优选聚合物在转染中是特别有效的,这些聚合物的平均分子量为103-5×106。作为实例,可以列举平均分子量为50 000Da(PEI 50K)、25 000Da(PEI 25K)、22 000Da(PEI22K)的聚亚乙基亚胺,或800000Da(PPI 800K)聚亚丙基亚胺。
本发明中使用的聚亚烷基亚胺可以根据本领域技术人员已知的不同方法得到。例如可以在阴离子聚合(例如亚乙基亚胺聚合)条件下使用一种或多种相应单体采用化学方法、或通过还原由二酸或二胺缩聚作用得到的聚酰胺或通过还原由二醛与二胺缩聚作用得到的亚胺可以合成这些聚亚烷基亚胺。另外,许多聚亚烷基亚胺可从市场上得到,例如像PEI 25K、PEI 22K或PPI 800K。
按照本发明,《官能化聚亚烷基亚胺》应当被理解为靶元素以共价键方式与其连接的聚亚烷基亚胺类阳离子聚合物。这些靶元素能够使核酸转移朝向某些类型细胞、某些组织或某些所希望的细胞腔。靶元素与聚亚烷基亚胺之间的共价键是在上述反应条件下通过与官能化半缩醛,即其中一个取代基是上述靶元素的半缩醛反应得到的。
更确切地,按照本发明,官能化半缩醛应当被理解为具有下述通式的任何分子:
式中n等于0或1,R1、R2、R3和R4相同或不同,彼此独立地代表氢原子、与进行该反应相容的基团,或靶元素,条件是选自R1、R2、R3和R4的单独一个取代基是靶元素。
作为相容基团实例,可以列举羟基、具有1-4个碳原子的(C1~4)烷基或羟基(C1~4)烷基。
靶元素可以直接接枝在半缩醛上,或者通过双官能键分子(还被称作《连接剂》)被接枝。《连接剂》能将所述靶元素接枝在半缩醛上,即从化学观点来看不大可能进行的接枝,和/或能将所述靶元素远离半缩醛。关于双官能键分子,应当被理解为包括至少一个能够以共价键方式与靶元素相连的官能团和至少一个能够以共价键方式与半缩醛相连的官能团的分子。
按照本发明,靶元素应当被理解为任何能够使核酸转移定向的分子。这种靶元素可以是能够将DNA转移定向于某些类型细胞或某些所希望组织(肿瘤细胞、肝细胞、造血细胞等)的细胞外靶元素。还可以涉及能够将核酸转移定向于某些优选细胞腔(例如线粒体或细胞核)的细胞内靶元素。
在本发明范围内可使用的靶元素中,可以列举糖、肽、蛋白质、寡核苷酸、脂类、神经传递质、激素、维生素或它们的衍生物。优选地,例如涉及糖、肽或蛋白质像抗体或抗体片段、细胞受体的配位体或它们的片段、受体或受体片段。特别地,可能涉及生长因子受体、细胞因子受体、细胞凝集素类受体的配位体,或对如整联蛋白粘附蛋白质受体具有亲合性的RGD序列配位体。还可以列举转铁蛋白受体、HDL和LDL或叶酸盐转运蛋白。靶元素还可以是能够对准凝集素的糖,例如脱唾液酸糖蛋白或唾液酸化受体,像唾液酸化的路易斯寡糖(Sialyl Lewis X),或抗体Fab片段,或单链抗体(ScFv)。作为实例,所述糖可以选自单糖、二糖或三糖。例如可以涉及半乳糖、甘露糖、岩藻糖、鼠李糖、乳糖或麦芽糖。
一般地,在例如甲醇或乙醇的醇溶剂中,在温度100-30℃下进行该反应。优选地,在乙醇中在室温下,即在温度18-25℃下操作。
另外,一般地相对于每摩尔加入的聚合物使用25-100摩尔异丙醇钛(IV),更优选地,40-60摩尔异丙醇钛(IV)。
在反应混合物中还加入其量等于50-80摩尔%异丙醇钛(IV)用量的硼氢化钠。
用于实施本发明方法的官能化半缩醛的量取决于希望达到的接枝率。有利地,每摩尔聚合物使用6-100摩尔官能化半缩醛。
根据官能化半缩醛的用量,得到比率可以是1-20%,优选地是4-20%的官能化聚亚烷基亚胺。在利用糖作为靶元素的情况下,采用间苯二酚法可以精确地测定接枝在聚亚烷基亚胺上的糖百分数。这种方法在于用间苯二酚和硫酸处理预先渗析的官能化聚亚烷基亚胺,然后在90℃加热20分钟。在冷却后,测量在495nm处的吸收,并与参比试样(标准溶液)比较。渗析能够除去末接枝的靶元素,通过与参比试样比较进行的测量能够确定接枝靶元素的量。这种方法还是一种最准确表征所得到产物的方法,因为涉及聚合物,不可能如对通常小分子所进行的采用NMR(核磁共振)或采用质量测定表征它们。
本发明的方法对于制备能对准某些组织、某些类型细胞或某些特定细胞腔的转移核酸载体是特别有意义的,因为这种方法是一种既便宜、毒性又不大的可供选择替代的方法。另外,可以看出,用糖官能化的聚亚烷基亚胺对细胞的毒性小于非官能化的聚亚烷基亚胺。
官能化的聚亚烷基亚胺适用于在细胞中转染核酸。为此目的,官能化的聚亚烷基亚胺与一种或多种核酸混合,以便生成也被称作《聚丛》的配合物(这时可以说“多染”(polyfection),而不说转染)。为了达到最佳的转染效率,优选地选择官能化聚亚烷基亚胺与核酸的比例,以便生成的聚丛总体上呈中性或稍微呈阳性。一般地,选择所述的比例以便生成不沉淀、也不会过分增加所生成的聚丛阳离子性的阳性聚丛,否则这样也会增加毒性。所述比例因此应该根据具体情况决定。但是,一般选择所述比例以便官能化聚亚烷基亚胺的胺与核酸的磷酸酯的摩尔比是0.1-50,优选地是0.5-20。当然,本领域技术人员可以根据使用的官能化聚亚烷基亚胺、核酸、靶细胞、用药方式或根据所希望的应用(特别地待转染细胞类型),很容易修改和优化这个比例。
在上述聚丛中,核酸既是脱氧核糖核酸又是核糖核酸。可能涉及自然或人工序列,特别是基因组DNA(gDNA)、互补DNA(cDNA)、信使RNA(mRNA)、转移RNA(tRNA)、核蛋白体RNA(rRNA)、杂交序列或合成或半合成序列、修饰或未修饰寡核苷酸。这些核酸例如可以是人、动物、植物、细菌或病毒源的。它们可以采用本领域技术人员已知的任何技术、特别是采用库靶、化学合成或其中包括采用库靶所得到序列的化学或酶修饰在内的混合方法得到。它们可以通过化学方法修饰。
更特别地涉及脱氧核糖核酸,它们可以是单链或双链以及短链的寡核苷酸或更长序列。特别地,核酸有利地由例如质粒、载体、游离基因或表达盒构成。这些脱氧核糖核酸特别地可以在靶细胞中带有官能或非官能复制源,一个或多个标记基因,转录或复制调节序列,有治疗意义的基因,修饰或未修饰反义序列,或与其他细胞组分连接的区域。
优选地,该核酸包括一个或多个在调节序列控制下有治疗意义的基因,例如在靶细胞中一个或多个启动子和活性转录终止区。
按照本发明,有治疗意义的基因特别应当被理解为任何可编码具有治疗作用的蛋白质产品的基因。如此编码的蛋白质产品特别地可以是蛋白质或肽。这种蛋白质产品可以是对靶细胞均匀外生或内生的,即靶细胞没有任何病理时,通常可在这种细胞中表达的产品。在这种情况下,蛋白质表达例如能够克服在细胞中不充分表达或由于修饰失活或低活性蛋白质的表达,或能够过表达所述蛋白质。有治疗意义的基因还可以编码例如具有高稳定性或修饰活性的细胞蛋白质的突变体。蛋白质产品对靶细胞也可以是异源的。在这种情况下,表达的蛋白质例如可以补充或带来在该细胞中缺失的活性,这样能够使它抵抗疾病,或刺激免疫反应。
本发明的治疗产品中,作为实例可以列举酶、血液衍生物、激素、淋巴因子(例如白细胞介素、干扰素或TNF:FR 92/03120)、生长因子、神经传递质或它们的前体或合成酶、营养因子(例如BDNF、CNTF、NGF、IGF、GMF、aFGF、bFGF、VEGF、NT3、NT5或HARP/超营养蛋白)、阿朴脂蛋白(例如ApoAI、ApoAIV或ApoE:FR 93/05125)、肌营养不良蛋白或微肌营养不良蛋白(FR 91/11947)、与粘液粘稠病相关的CFTR蛋白质、肿瘤抑制基因(例如p53,Rb、Rap1A,DCC或k-rev:FR 93/04745)、凝结中相关因子的编码基因(例如因子VII、VIII、IX)、在DNA修复中涉及的基因、自杀基因(胸苷激酶、胞嘧啶脱氨酶)、血红蛋白基因或其他的蛋白质转运基因、新陈代谢或分解代射酶。
有治疗意义的核酸还可以是基因或反义序列,它们在靶细胞中的表达能够控制基因表达或细胞mRNA转录。根据在专利EP 140 308中描述的技术,这样一些序列例如可以在靶细胞中转录成细胞mRNA的互补RNA,并且因此可以阻断它们在蛋白质中翻译。治疗基因还包括核酶的编码序列,这些酶能够有选择地破坏靶RNA(EP 321 201)。
如上所述,核酸还可以包括一个或多个抗原肽的编码基因,这些基因能在人体或动物体内产生免疫反应。在这种特别实施方式中,本发明允许制造疫苗,或者应用于人或动物体内特别是抗微生物、病毒或癌的免疫治疗。特别地涉及Epstein Barr病毒、HIV病毒、乙型肝炎病毒(EP 185 573)、假-暴怒病毒、“多核体形成病毒”、其他病毒的特效抗原肽,或肿瘤的特效抗原肽(EP 259212)。
优选地,核酸还包括能表达有治疗意义的基因和/或在所希望细胞或器官中编码抗原肽的基因的序列。这些序列在感染细胞中能功能化时,可能涉及自然是对所考虑基因表达负责的序列。还可能涉及不同源的序列(负责其他蛋白质或合成蛋白质的表达)。特别地,可能涉及真核生物或病毒基因的启动子序列。例如,可能涉及来自希望感染的细胞的基因组的启动子序列。对此,可以列举例如E1A、MLP、CMV或RSV基因的启动子。另外,这些表达序列可以例如通过添加活化或复制序列进行修饰。还可能涉及诱导或阻抑型启动子。
为了例如通过局部、皮肤、口服、直肠、阴道、肠胃道外、鼻内、静脉内、肌肉内、皮下、眼内、经皮、气管内或腹膜内方式用药,可以配制如此生成的聚丛。优选地,生成的聚丛含有在药学上可接受的注射配方用、特别是在所希望器官部位直接注射用或局部用药(皮肤和/或粘膜上)载体。特别地涉及无菌等渗溶液或干组合物,特别是冻干组合物,根据灭菌水或生理血清的情况,它们还可以含有可注射溶质成分。注射使用的核酸剂量以及给药次数可以根据不同的参数、特别是根据用药方式、相关疾病、待表达基因或要求治疗时间进行修改。更特别地,有关用药方式,可能涉及直接注射到组织中如注射到肿瘤部位、或在循环途径中、或者培养物中细胞处理,接着通过注射或接枝进行活体再移植。在本发明范围内有关组织例如是肌肉、皮肤、脑、肺、肝脏、脾、骨髓、胸腺、心脏、淋巴、血、骨、软骨、胰腺、肾脏、膀胱、胃、肠、睾丸、卵巢、直肠、神经系统、眼、腺体或结缔组织。
含有上述聚丛的组合物可以用于往细胞中转移核酸。更确切地,所述组合物可以用于制备用于治疗疾病,特别是因缺乏蛋白质或核酸产品所造成的疾病的药物。
往细胞中转移核酸的方法在于进行下述步骤:
(1)制备含有上述聚丛的组合物,和
(2)让细胞与(1)中生成的组合物进行接触。
除了上述内容以外,本发明还包括由下述实施例和附图得出的其他特点和优点,这些实施例和附图应该认为用于说明本发明,而不限制其保护范围。
附图
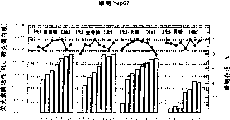
图1:柱状图代表对于电荷比(+/-)为3-28的糖基化聚亚烷基亚胺/DNA不同配方,在ECV304细胞中以RLU/微克蛋白质表示的荧光素酶活性(RLU:《相对光单位》)。
黑色连续曲线表示对于每个使用的配方[3a]、[3b]、[4a]和[4b],按照糖基化聚亚烷基亚胺与DNA之间电荷(+/-)比的细胞存活百分数。
图2:柱状图代表对于电荷比(+/-)为3-28的糖基化聚亚烷基亚胺/DNA不同配方,在HeLa细胞中以RLU/微克蛋白质表示的荧光素酶活性(RLU:《相对光单位》)。
黑色连续曲线表示对于每个使用的配方[3a]、[3b]、[4a]和[4b],按照糖基化聚亚烷基亚胺与DNA之间电荷(+/-)比的细胞存活百分数。
图3:柱状图代表对于电荷比(+/-)为3-28的糖基化聚亚烷基亚胺/DNA不同配方,在HepG2细胞中以RLU/微克蛋白质表示的荧光素酶活性(RLU:《相对光单位》)。
黑色连续曲线表示对于每个使用的配方[3a]、[3b]、[4a]和[4b],按照糖基化聚亚烷基亚胺与DNA之间电荷(+/-)比的细胞存活百分数。
图4:在往细胞中转移DNA的试验中使用的Pxl2774质粒示意图。
实施例
实施例1:制备PEI-4%麦芽糖[3a]
按照下述方式示意说明进行的反应:
0.02毫摩尔PEI 25KDa(500毫克,Aldrich公司)溶于20毫升无水乙醇中。然后添加0.7毫摩尔麦芽糖(252毫克),这样得到的溶液在氮气气氛下混合15分钟。再往反应混合物缓慢添加1毫摩尔异丙醇钛IV(0.3毫升),保持搅拌一夜。然后,添加0.75毫摩尔硼氢化钠(28.5毫克),再继续搅拌8小时。然后过滤反应混合物,并浓缩到10毫升。最后,得到的溶液渗析12小时(尺寸为12000的排斥膜)。产率是80%。
可采用上述间苯二酚法测定接枝麦芽糖残基百分数:23个麦芽糖残基接枝在PEI 25KDa上,相应于氨基基团接枝率为4%。
实施例2:制备PEI-12%麦芽糖[3b]
0.02毫摩尔PEI 25KDa(500毫克,Aldrich公司)溶于20毫升无水乙醇中。然后添加2毫摩尔麦芽糖(720毫克),这样得到的溶液在氮气气氛下混合15分钟。再往反应混合物缓慢添加2.7毫摩尔异丙醇钛IV(0.8毫升),保持搅拌一夜。然后,添加2毫摩尔硼氢化钠(76毫克),再继续搅拌8小时。然后过滤反应混合物,并浓缩到10毫升。最后,得到的溶液渗析12小时(尺寸为12000的排斥膜)。产率是80%。
可采用上述间苯二酚法测定接枝麦芽糖残基百分数:70个麦芽糖残基接枝在PEI 25KDa上,相应于氨基基团接枝率为12%。
实施例3:制备PEI-6%乳糖[4a]
按照下述方式示意说明进行的反应:
0.02毫摩尔PEI 25KDa(500毫克,Aldrich公司)溶于20毫升无水乙醇中。然后,添加1毫摩尔乳糖(360毫克),这样得到的溶液在氮气气氛下混合15分钟。再往反应混合物缓慢添加1.35毫摩尔异丙醇钛IV(0.4毫升),保持搅拌一夜。然后,添加1毫摩尔硼氢化钠(38毫克),再继续搅拌8小时。然后,过滤反应混合物,并浓缩到10毫升。最后,得到的溶液渗析12小时(尺寸为12000的排斥膜)。产率是80%。
可采用上述间苯二酚法测定接枝乳糖残基百分数:35个乳糖残基接枝在PEI 25KDa上,相应于氨基基团接枝率为6%。
实施例4:制备PEI-17%乳糖[4b]
0.02毫摩尔PEI 25KDa(500毫克,Aldrich公司)溶于20毫升无水乙醇中。然后添加3毫摩尔乳糖(1080毫克),这样得到的溶液在氮气气氛下混合15分钟。再往反应混合物缓慢添加4毫摩尔异丙醇钛IV(1.2毫升),保持搅拌一夜。然后,添加3毫摩尔硼氢化钠(114毫克),再继续搅拌8小时。然后,过滤反应混合物,并浓缩到10毫升。最后,得到的溶液渗析12小时(尺寸为12000的排斥膜)。产率是80%。
可采用上述间苯二酚法测定接枝乳糖残基百分数:99个乳糖残基接枝在PEI 25KDa上,相应于氨基基团接枝率为17%。
应用实施例:在不同细胞类型中,与PEI-4%和12%麦芽糖配合或与PEI-6%
和17%乳糖配合的质粒DNA离体转染
这个实施例说明上述合成的官能化聚亚烷基亚胺在细胞中转染DNA的能力。
使用的DNA是在浓度为80微克/毫升的150毫摩尔氯化钠混合物溶液中的pXL2774质粒。这种质粒含有在细胞肥大病毒的CMV启动子控制下编码荧光素酶的luc基因。其大小是4500碱基对。这种质粒示意图被展示于图4中。根据专利申请WO 97/35002中描述的方法纯化pXL2774质粒。
pXL2774质粒溶液与稀释在水中的官能化PEI溶液按照体积与体积混合可以制备聚丛,所述稀释浓度可按照所希望的电荷比而改变。
24井微板按照每个井60000HeLa细胞(ATCC)接种,稍后转染24小时。往每个井滴加50微升聚丛溶液。在无血清的情况下,在转染前2小时,该介质预先补加SVF(胎牛血清)。然后,这些细胞在37℃培养4小时。然后除去含有配合物的介质,用DMEM和10%胎牛血清混合物替换。然后,这些细胞再培养24小时。最后,这些细胞溶解,使用荧光素酶检测盒(Promega)和Dynex MLX光度计进行检测。另外,通过测量细胞的溶胞产物浓度评价聚丛毒性,其毒性可用相对于每微克溶胞产物蛋白质的酶活性表示。
这些结果列于图1、2和3中,这些结果说明对于不同DNA以及在3种不同细胞系中的电荷比而言,前面合成的不同官能化PEI的转染效率。
总体上看到,转移效率是相对高的,除非使用由高接枝率的PEI制成的聚丛(PEI-12%麦芽糖的效率低于PEI-4%麦芽糖的效率,PEI-17%乳糖的效率低于PEI-6%乳糖的效率)。因此,接枝率是一个按照所希望应用优化的重要参数。
另外,还观察到,用官能化半缩醛取代氨基基团可显著降低PEI诱导的对细胞的毒性,特别是在高DNA的电荷比情况下。事实上,对于转染DNA(未列出结果),细胞存活百分数(图1-3)远高于使用非官能化PEI所得到的百分数。
因此,这个实施例表明,采用本发明的可靠与廉价方法所得到的官能化聚亚烷基亚胺是在细胞中转染DNA的良好候选者。
Claims (21)
1、官能化聚亚烷基亚胺的制备方法,其特征在于在异丙醇钛(IV)和硼氢化钠存在下,在醇溶剂中,用官能化半缩醛处理聚亚烷基亚胺。
2、权利要求1的官能化聚亚烷基亚胺的制备方法,其特征在于所述醇溶剂是甲醇或乙醇。
3、权利要求1的官能化聚亚烷基亚胺的制备方法,其特征在于在温度10-30℃下进行操作。
4、权利要求1的官能化聚亚烷基亚胺的制备方法,其特征在于每摩尔聚亚烷基亚胺使用25-100摩尔异丙醇钛(IV)。
5、权利要求1的官能化聚亚烷基亚胺的制备方法,其特征在于硼氢化钠的用量等于异丙醇钛(IV)用量的50-80摩尔%。
6、权利要求1的官能化聚亚烷基亚胺的制备方法,其特征在于相对于每摩尔聚亚烷基亚胺使用6-100摩尔官能化半缩醛。
7、权利要求1的官能化聚亚烷基亚胺的制备方法,其特征在于起始的聚亚烷基亚胺具有下述通式:
式中R代表氢原子或下述通式的基团:
n是2-10的整数,
p和q是整数,其条件是p+q之和使得聚合物平均分子量是100-107Da。
8、权利要求7的官能化聚亚烷基亚胺的制备方法,其特征在于所述起始聚亚烷基亚胺是聚亚乙基亚胺或聚亚丙基亚胺。
9、权利要求8的官能化聚亚烷基亚胺的制备方法,其特征在于所述起始聚亚烷基亚胺选自平均分子量为50 000Da或25 000Da或22 000Da的聚亚乙基亚胺,或平均分子量为800 000 Da的聚亚丙基亚胺。
10、权利要求1的官能化聚亚烷基亚胺的制备方法,其特征在于官能化半缩醛具有下述通式:
式中n等于0或1,R1、R2、R3和R4相同或不同,彼此独立地代表氢原子、与进行该反应相容的基团或靶元素,条件是选自R1、R2、R3和R4的单独一个取代基是靶元素。
11、权利要求10的官能化聚亚烷基亚胺的制备方法,其特征在于,与进行所述反应相容的基团选自羟基、C1~4烷基或羟基C1-4烷基。
12、权利要求10的官能化聚亚烷基亚胺的制备方法,其特征在于所述靶元素选自糖、肽、蛋白质、寡核苷酸、脂类、神经传递质、激素、维生素或它们的衍生物。
13、权利要求12的官能化聚亚烷基亚胺的制备方法,其特征在于所述靶元素选自生长因子受体、细胞因子受体、细胞凝集素类受体的配位体,对如整联蛋白粘附蛋白质受体具有亲合性的RGD序列配位体、转铁蛋白受体、HDL、LDL、叶酸盐转运蛋白、唾液酸化的路易斯寡糖、抗体Fab片段、单链抗体ScFv、单糖、二糖或三糖。
14、权利要求13的官能化聚亚烷基亚胺的制备方法,其特征在于所述糖选自半乳糖、甘露糖、岩藻糖、鼠李糖、乳糖或麦芽糖。
15、权利要求1的官能化聚亚烷基亚胺的制备方法,其特征在于接枝在聚亚烷基亚胺上的官能化半缩醛百分数是1-20摩尔%。
16、含有至少一种根据权利要求1所述方法得到的官能化聚亚烷基亚胺和至少一种核酸的组合物。
17、权利要求16的组合物,其特征在于所述核酸是脱氧核糖核酸或核糖核酸。
18、权利要求17的组合物,其特征在于所述核酸包含一种或多种在调节序列控制下具有治疗意义的基因。
19、权利要求16的组合物在制备用于转染细胞的药物中的应用。
20、权利要求16的组合物在核酸往细胞中转移的应用。
21、往细胞中转移核酸的方法,该方法包括下述步骤:
(1)制备权利要求16限定的组合物,和
(2)让细胞与(1)中生成的组合物进行接触。
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR0002059A FR2805271B1 (fr) | 2000-02-18 | 2000-02-18 | Procede de preparation de polyalkylenimines fonctionnalises, compositions les contenant et leurs utilisations |
| FR00/02059 | 2000-02-18 | ||
| US20390700P | 2000-05-12 | 2000-05-12 | |
| US60/203,907 | 2000-05-12 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN1441820A CN1441820A (zh) | 2003-09-10 |
| CN1178973C true CN1178973C (zh) | 2004-12-08 |
Family
ID=26212187
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CNB018068014A Expired - Fee Related CN1178973C (zh) | 2000-02-18 | 2001-02-15 | 官能化聚亚烷基亚胺的制备方法,含有它们的组合物及其应用 |
Country Status (17)
| Country | Link |
|---|---|
| US (1) | US6825341B2 (zh) |
| EP (1) | EP1268609B1 (zh) |
| KR (1) | KR100751105B1 (zh) |
| CN (1) | CN1178973C (zh) |
| AT (1) | ATE326499T1 (zh) |
| AU (2) | AU2001235695B2 (zh) |
| CA (1) | CA2400666C (zh) |
| CY (1) | CY1105416T1 (zh) |
| DE (1) | DE60119711T2 (zh) |
| DK (1) | DK1268609T3 (zh) |
| ES (1) | ES2263589T3 (zh) |
| HU (1) | HU227264B1 (zh) |
| IL (2) | IL151289A0 (zh) |
| MX (1) | MXPA02007956A (zh) |
| NZ (1) | NZ521420A (zh) |
| PT (1) | PT1268609E (zh) |
| WO (1) | WO2001060890A2 (zh) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1317317C (zh) * | 2005-06-03 | 2007-05-23 | 中国科学院上海应用物理研究所 | 聚烯亚胺凝胶的光化学合成方法 |
Families Citing this family (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2476769A1 (en) * | 2002-02-22 | 2003-09-04 | Insert Therapeutics, Inc. | Carbohydrate-modified polymers, compositions and uses related thereto |
| JP2005248144A (ja) * | 2004-02-05 | 2005-09-15 | Nippon Shokubai Co Ltd | ポリアルキレンイミン系重合体、その製造方法およびその用途 |
| WO2007034586A1 (ja) * | 2005-09-22 | 2007-03-29 | Toto Ltd. | 光触媒性二酸化チタン微粒子、その分散液、およびその製造方法 |
| EP1834646B1 (en) * | 2005-10-26 | 2016-06-22 | Toto Ltd. | Ultrasonic cancer therapy accelerator and cytotoxic agent |
| FR2894984B1 (fr) * | 2005-12-20 | 2009-01-16 | Millipore Corp | Composition pour augmenter la permeabilite des parois microorganismes et procede de detection sur membrane desdits microorganismes. |
| EP2000150B1 (en) * | 2006-03-24 | 2016-07-13 | Toto Ltd. | Titanium oxide complex particle, dispersion solution of the particle, and process for production of the particle |
| GB0724253D0 (en) * | 2007-12-12 | 2008-01-30 | Fermentas Uab | Transfection reagent |
| US8252834B2 (en) | 2008-03-12 | 2012-08-28 | The Regents Of The University Of Michigan | Dendrimer conjugates |
| WO2010039861A2 (en) | 2008-09-30 | 2010-04-08 | The Regents Of The University Of Michigan | Dendrimer conjugates |
| WO2010054321A2 (en) | 2008-11-07 | 2010-05-14 | The Regents Of The University Of Michigan | Methods of treating autoimmune disorders and/or inflammatory disorders |
| GB0917792D0 (en) * | 2009-10-12 | 2009-11-25 | Fermentas Uab | Delivery agent |
| US9856456B2 (en) | 2009-10-12 | 2018-01-02 | Thermo Fisher Scientific Baltics Uab | Delivery agent |
| CN102917699A (zh) | 2009-10-13 | 2013-02-06 | 密执安大学评议会 | 树枝状聚合物组合物和合成方法 |
| US8912323B2 (en) | 2009-10-30 | 2014-12-16 | The Regents Of The University Of Michigan | Multifunctional small molecules |
| BR112012030453A2 (pt) * | 2010-05-31 | 2016-08-09 | Basf Se | processo para a preparação de polialquileno-poliaminas, polialquileno-poliamina, polietilenoimina, e , uso de polialquileno-poliaminas |
| KR101039701B1 (ko) * | 2010-11-29 | 2011-06-08 | 주식회사 유성엔지니어링 | 슬러지 수집장치 |
| CN102181053B (zh) * | 2011-02-25 | 2012-12-05 | 苏州大学 | 一种疏水基团修饰的聚乙烯亚胺衍生物及其应用 |
| IN2014CN03935A (zh) * | 2011-11-25 | 2015-09-04 | Basf Se | |
| US9402911B2 (en) | 2011-12-08 | 2016-08-02 | The Regents Of The University Of Michigan | Multifunctional small molecules |
| EP3910073B1 (en) | 2015-09-01 | 2024-03-06 | Eisai R&D Management Co., Ltd. | Splice variants associated with neomorphic sf3b1 mutants |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1162528C (zh) * | 1996-05-03 | 2004-08-18 | 普罗格特-甘布尔公司 | 棉料去污聚合物 |
| DE19726186A1 (de) * | 1997-06-20 | 1998-12-24 | Boehringer Ingelheim Int | Komplexe für den Transport von Nukleinsäure in höhere eukaryotische Zellen |
| DE19743135A1 (de) * | 1997-09-30 | 1999-04-01 | Hoechst Marion Roussel De Gmbh | Biologisch verträgliche niedermolekular Polyethylenimine |
| US5962400A (en) * | 1998-12-22 | 1999-10-05 | National Starch And Chemical Investment Holding Corporation | Amino acid copolymers having pendent polysaccharide moieties and uses thereof |
-
2001
- 2001-02-15 MX MXPA02007956A patent/MXPA02007956A/es active IP Right Grant
- 2001-02-15 KR KR1020027010751A patent/KR100751105B1/ko not_active IP Right Cessation
- 2001-02-15 PT PT01907819T patent/PT1268609E/pt unknown
- 2001-02-15 HU HU0300144A patent/HU227264B1/hu not_active IP Right Cessation
- 2001-02-15 NZ NZ521420A patent/NZ521420A/en not_active IP Right Cessation
- 2001-02-15 DK DK01907819T patent/DK1268609T3/da active
- 2001-02-15 CA CA2400666A patent/CA2400666C/fr not_active Expired - Fee Related
- 2001-02-15 AT AT01907819T patent/ATE326499T1/de active
- 2001-02-15 ES ES01907819T patent/ES2263589T3/es not_active Expired - Lifetime
- 2001-02-15 IL IL15128901A patent/IL151289A0/xx active IP Right Grant
- 2001-02-15 AU AU2001235695A patent/AU2001235695B2/en not_active Ceased
- 2001-02-15 WO PCT/FR2001/000460 patent/WO2001060890A2/fr active IP Right Grant
- 2001-02-15 AU AU3569501A patent/AU3569501A/xx active Pending
- 2001-02-15 EP EP01907819A patent/EP1268609B1/fr not_active Expired - Lifetime
- 2001-02-15 CN CNB018068014A patent/CN1178973C/zh not_active Expired - Fee Related
- 2001-02-15 DE DE60119711T patent/DE60119711T2/de not_active Expired - Lifetime
- 2001-02-16 US US09/783,981 patent/US6825341B2/en not_active Expired - Lifetime
-
2002
- 2002-08-15 IL IL151289A patent/IL151289A/en not_active IP Right Cessation
-
2006
- 2006-08-07 CY CY20061101103T patent/CY1105416T1/el unknown
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1317317C (zh) * | 2005-06-03 | 2007-05-23 | 中国科学院上海应用物理研究所 | 聚烯亚胺凝胶的光化学合成方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| US6825341B2 (en) | 2004-11-30 |
| IL151289A0 (en) | 2003-04-10 |
| EP1268609A2 (fr) | 2003-01-02 |
| KR100751105B1 (ko) | 2007-08-22 |
| KR20030009362A (ko) | 2003-01-29 |
| WO2001060890A2 (fr) | 2001-08-23 |
| ES2263589T3 (es) | 2006-12-16 |
| IL151289A (en) | 2007-03-08 |
| DE60119711D1 (de) | 2006-06-22 |
| ATE326499T1 (de) | 2006-06-15 |
| DK1268609T3 (da) | 2006-09-18 |
| HUP0300144A3 (en) | 2005-10-28 |
| US20010031498A1 (en) | 2001-10-18 |
| AU3569501A (en) | 2001-08-27 |
| PT1268609E (pt) | 2006-10-31 |
| AU2001235695B2 (en) | 2006-01-12 |
| HUP0300144A2 (en) | 2003-05-28 |
| MXPA02007956A (es) | 2004-09-10 |
| CY1105416T1 (el) | 2010-04-28 |
| CN1441820A (zh) | 2003-09-10 |
| CA2400666C (fr) | 2011-01-18 |
| DE60119711T2 (de) | 2007-02-22 |
| EP1268609B1 (fr) | 2006-05-17 |
| CA2400666A1 (fr) | 2001-08-23 |
| WO2001060890A3 (fr) | 2002-09-19 |
| HU227264B1 (en) | 2010-12-28 |
| NZ521420A (en) | 2006-01-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN1178973C (zh) | 官能化聚亚烷基亚胺的制备方法,含有它们的组合物及其应用 | |
| Zugates et al. | Rapid optimization of gene delivery by parallel end-modification of poly (β-amino ester) s | |
| US8258235B2 (en) | Biodegradable cationic polymers | |
| EP2007432B1 (en) | Biodegradable cationic polymers | |
| CN109288815B (zh) | 一种可实现肿瘤靶向投递核酸药物的多级递送纳米粒子的制备方法和应用 | |
| CN113413467A (zh) | 一种无载体mRNA递送方法 | |
| CN110403915B (zh) | Dna和聚合物的杂化核酸药物载体及其制备方法和应用 | |
| JP4827358B2 (ja) | 機能的ポリアルキレンイミンの製造方法、前記化合物を含む組成物及びその使用 | |
| CN113101376A (zh) | 一种可用于基因治疗的复合基因载体及其制备方法和应用 | |
| CN108531514B (zh) | 内源性超支化聚精胺阳离子基因载体及其制备方法与应用 | |
| JP3938954B2 (ja) | 新規なグラフト共重合体、それを用いた薬剤、及びそれを用いて薬物を特定細胞に取り込ませる方法 | |
| CN1317320C (zh) | 聚乙烯亚胺纳米凝胶及其应用 | |
| CN112245594B (zh) | 一种用于基因分子传递的非病毒纳米粒子及其制备方法与应用 | |
| CN113683780B (zh) | 具有穿膜活性和细胞核定位功能的抗血清、低细胞毒性的聚氨基酸类基因递送载体材料 | |
| WO2024140546A1 (zh) | 一种阳离子脂质化合物及制备方法和应用、mRNA递送系统 | |
| CN118755084A (zh) | 用于mRNA递送的聚合物、利用该聚合物的脂质/聚合物杂化纳米粒及其制备方法和应用 | |
| CN111184686A (zh) | 一种新型药载纳米水凝胶及其制备方法和应用 | |
| CN115429891A (zh) | 含氟高分子在mRNA胞内递送中的应用 | |
| CN115975182A (zh) | 一种氨基酸共聚物及其应用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C14 | Grant of patent or utility model | ||
| GR01 | Patent grant | ||
| CF01 | Termination of patent right due to non-payment of annual fee |
Granted publication date: 20041208 Termination date: 20180215 |
|
| CF01 | Termination of patent right due to non-payment of annual fee |