CN1135981C - 硫酸吗啡微粒、其制备方法和药物制剂 - Google Patents
硫酸吗啡微粒、其制备方法和药物制剂 Download PDFInfo
- Publication number
- CN1135981C CN1135981C CNB998030120A CN99803012A CN1135981C CN 1135981 C CN1135981 C CN 1135981C CN B998030120 A CNB998030120 A CN B998030120A CN 99803012 A CN99803012 A CN 99803012A CN 1135981 C CN1135981 C CN 1135981C
- Authority
- CN
- China
- Prior art keywords
- microgranule
- promptly
- morphine sulfate
- preparation
- coating
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
- GRVOTVYEFDAHCL-RTSZDRIGSA-N morphine sulfate pentahydrate Chemical compound O.O.O.O.O.OS(O)(=O)=O.O([C@H]1[C@H](C=C[C@H]23)O)C4=C5[C@@]12CCN(C)[C@@H]3CC5=CC=C4O.O([C@H]1[C@H](C=C[C@H]23)O)C4=C5[C@@]12CCN(C)[C@@H]3CC5=CC=C4O GRVOTVYEFDAHCL-RTSZDRIGSA-N 0.000 title claims abstract description 54
- 238000000034 method Methods 0.000 title claims abstract description 15
- 239000000825 pharmaceutical preparation Substances 0.000 title claims abstract description 14
- 239000004531 microgranule Substances 0.000 claims abstract description 53
- 229960004715 morphine sulfate Drugs 0.000 claims abstract description 46
- 238000002360 preparation method Methods 0.000 claims abstract description 33
- 239000011230 binding agent Substances 0.000 claims abstract description 26
- 239000000203 mixture Substances 0.000 claims abstract description 22
- 230000007935 neutral effect Effects 0.000 claims abstract description 22
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 claims abstract description 8
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 claims abstract description 8
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 claims abstract description 8
- UFVKGYZPFZQRLF-UHFFFAOYSA-N hydroxypropyl methyl cellulose Chemical compound OC1C(O)C(OC)OC(CO)C1OC1C(O)C(O)C(OC2C(C(O)C(OC3C(C(O)C(O)C(CO)O3)O)C(CO)O2)O)C(CO)O1 UFVKGYZPFZQRLF-UHFFFAOYSA-N 0.000 claims abstract description 8
- 238000000576 coating method Methods 0.000 claims description 54
- 239000011248 coating agent Substances 0.000 claims description 53
- 239000008187 granular material Substances 0.000 claims description 35
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 23
- 239000007900 aqueous suspension Substances 0.000 claims description 12
- 239000012530 fluid Substances 0.000 claims description 12
- 239000000314 lubricant Substances 0.000 claims description 10
- 239000000454 talc Substances 0.000 claims description 9
- 229910052623 talc Inorganic materials 0.000 claims description 9
- 235000012222 talc Nutrition 0.000 claims description 9
- 239000002245 particle Substances 0.000 claims description 8
- 238000003756 stirring Methods 0.000 claims description 6
- 239000004480 active ingredient Substances 0.000 claims description 4
- 239000000853 adhesive Substances 0.000 claims description 4
- 230000001070 adhesive effect Effects 0.000 claims description 4
- 238000005063 solubilization Methods 0.000 claims description 4
- 230000007928 solubilization Effects 0.000 claims description 4
- 238000004090 dissolution Methods 0.000 claims description 2
- 238000009472 formulation Methods 0.000 abstract description 6
- 239000012736 aqueous medium Substances 0.000 abstract 1
- 239000012729 immediate-release (IR) formulation Substances 0.000 abstract 1
- BQJCRHHNABKAKU-KBQPJGBKSA-N morphine Chemical compound O([C@H]1[C@H](C=C[C@H]23)O)C4=C5[C@@]12CCN(C)[C@@H]3CC5=CC=C4O BQJCRHHNABKAKU-KBQPJGBKSA-N 0.000 description 21
- 239000000725 suspension Substances 0.000 description 19
- 229960005181 morphine Drugs 0.000 description 13
- 239000007903 gelatin capsule Substances 0.000 description 11
- 239000000243 solution Substances 0.000 description 5
- RZVAJINKPMORJF-UHFFFAOYSA-N Acetaminophen Chemical compound CC(=O)NC1=CC=C(O)C=C1 RZVAJINKPMORJF-UHFFFAOYSA-N 0.000 description 4
- 239000000470 constituent Substances 0.000 description 4
- 229960005195 morphine hydrochloride Drugs 0.000 description 4
- XELXKCKNPPSFNN-BJWPBXOKSA-N morphine hydrochloride trihydrate Chemical compound O.O.O.Cl.O([C@H]1[C@H](C=C[C@H]23)O)C4=C5[C@@]12CCN(C)[C@@H]3CC5=CC=C4O XELXKCKNPPSFNN-BJWPBXOKSA-N 0.000 description 4
- -1 morphine sulfates Chemical class 0.000 description 3
- 230000036470 plasma concentration Effects 0.000 description 3
- 239000003826 tablet Substances 0.000 description 3
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 229910000831 Steel Inorganic materials 0.000 description 2
- 229930006000 Sucrose Natural products 0.000 description 2
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 2
- 238000004891 communication Methods 0.000 description 2
- 239000003085 diluting agent Substances 0.000 description 2
- 239000003814 drug Substances 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 210000001035 gastrointestinal tract Anatomy 0.000 description 2
- 238000012423 maintenance Methods 0.000 description 2
- 210000000440 neutrophil Anatomy 0.000 description 2
- 229960005489 paracetamol Drugs 0.000 description 2
- 210000002381 plasma Anatomy 0.000 description 2
- 229920000233 poly(alkylene oxides) Polymers 0.000 description 2
- 239000010959 steel Substances 0.000 description 2
- 239000005720 sucrose Substances 0.000 description 2
- 238000005550 wet granulation Methods 0.000 description 2
- WSVLPVUVIUVCRA-KPKNDVKVSA-N Alpha-lactose monohydrate Chemical compound O.O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O WSVLPVUVIUVCRA-KPKNDVKVSA-N 0.000 description 1
- 208000000094 Chronic Pain Diseases 0.000 description 1
- 206010013786 Dry skin Diseases 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 1
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 description 1
- 208000002193 Pain Diseases 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 230000002939 deleterious effect Effects 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- 230000036571 hydration Effects 0.000 description 1
- 238000006703 hydration reaction Methods 0.000 description 1
- 229910000041 hydrogen chloride Inorganic materials 0.000 description 1
- IXCSERBJSXMMFS-UHFFFAOYSA-N hydrogen chloride Substances Cl.Cl IXCSERBJSXMMFS-UHFFFAOYSA-N 0.000 description 1
- 239000001863 hydroxypropyl cellulose Substances 0.000 description 1
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 229940031703 low substituted hydroxypropyl cellulose Drugs 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 239000002207 metabolite Substances 0.000 description 1
- 239000011859 microparticle Substances 0.000 description 1
- 238000005457 optimization Methods 0.000 description 1
- 239000007935 oral tablet Substances 0.000 description 1
- 229940096978 oral tablet Drugs 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 229940098458 powder spray Drugs 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 230000006641 stabilisation Effects 0.000 description 1
- 238000011105 stabilization Methods 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 229910052717 sulfur Inorganic materials 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- 238000013268 sustained release Methods 0.000 description 1
- 239000012730 sustained-release form Substances 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 231100000816 toxic dose Toxicity 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/5073—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals having two or more different coatings optionally including drug-containing subcoatings
- A61K9/5078—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals having two or more different coatings optionally including drug-containing subcoatings with drug-free core
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/485—Morphinan derivatives, e.g. morphine, codeine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/04—Centrally acting analgesics, e.g. opioids
Landscapes
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Epidemiology (AREA)
- Emergency Medicine (AREA)
- Pain & Pain Management (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Biomedical Technology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
Abstract
本发明涉及新的、微粒形式的硫酸吗啡的即释口服制剂。每个微粒含有被由硫酸吗啡和粘合剂如羟丙甲基纤维素形成的混合物包衣的中性载体颗粒,该粘合剂占硫酸吗啡/粘合剂混合物的10至50%(重量)。本发明还涉及制备所述微粒的方法,该方法完全在含水介质中在中性载体颗粒上进行。本发明进一步涉及含本发明微粒的药物制剂。
Description
技术领域
本发明涉及新的即释硫酸吗啡口服配方。
此外,本发明涉及此配方的制备方法及含此配方的药物制剂。
背景技术
口服吗啡被视为用于慢性疼痛的治疗手段。
文献EP655240公开了含即释芯的缓释片剂,该芯中含扑热息痛和吗啡,当将其置于900ml 0.1N氯化氢溶液中时其中超过75%的扑热息痛在45分钟内释放。
文献US5445829公开了含即释颗粒和缓释颗粒混合物的制剂。此即释颗粒通过将粘合剂溶液喷雾到活性组份和惰性颗粒的混合物上制备。该即释颗粒含有粘合剂,其占硫酸吗啡/粘合剂混合物的4至8%。
文献US5026560公开了通过粉末喷雾得到的颗粒。这些颗粒由被活性组份和低取代羟丙基纤维素混合物包衣的中性芯构成。所用粘合剂是羟丙基纤维素水溶液。
文献WO95/31972公开了即释多颗粒口服制剂,其中含有微粒,该微粒由被活性组分、特别是硫酸吗啡和稀释剂如乳糖水合物混合物包衣的中性芯组成,其表观密度为0.4至0.9g/ml。文献WO95/31972指出将硫酸吗啡固定于中性芯之上需要加入稀释剂以便获得良好的结果。
文献WO96/00066公开了吗啡控制释放口服片剂。这些片剂通过连续压制两种组合物获得:首先是其通过将含硫酸吗啡、一种或多种聚亚烷基氧化物和聚乙烯吡咯烷酮的混合物湿法制粒获得的所谓“治疗”组合物,第二种是通过将含聚亚烷基氧化物、氯化钠和羟丙甲基纤维素的混合物湿法制粒获得的组合物。所得片剂含有被能够控制所述活性组分的释放速度的多孔半透膜包衣的活性组分组合物。
发明内容
本发明的目的是提供即释微粒形式的硫酸吗啡口服制剂。
在本申请中,“硫酸吗啡”指(5α,6α)-7,8-二脱氢-4,5-环氧-17-甲基-吗啡喃-3,6-二醇的任选地被水合的硫酸盐。
在本申请中,“即释”指某种活性组份(在此为硫酸吗啡)在机体内以在少于约4小时的时间内活性组份的血浆浓度为治疗有效的并低于毒性浓度的速度被提供。
本发明的微粒具有如下优点:
—通过这些颗粒在消化道中广泛分布的特性使治疗作用的分布最佳化,这导致活性组分更好地被吸收,
—避免消化道中出现高浓度活性组分区域,
—构成稳定制剂,
—构成具有相同药剂形式的缓释制剂的载体,
—能通过不使用任何有机溶剂的方法制备。
本发明的即释微粒的特征在于每个微粒含有被硫酸吗啡和药用粘合剂如羟丙甲基纤维素的混合物包衣的中性载体颗粒,有利地,所述粘合剂占硫酸吗啡/粘合剂混合物重量的10至50%。
粘合剂优选占硫酸吗啡/粘合剂混合物重量的15至40%。
该中性载体颗粒由蔗糖或蔗糖和淀粉例如以质量比3/1形成的混合物组成。该中性颗粒的直径优选为200至900微米,更优选为400至750微米。
这些微粒优选用保护性外层包衣,该层含有优选为羟丙甲基纤维素的成膜剂,及任选地存在的、选自药用润滑剂,特别是滑石的润滑剂。有利地,此润滑剂的用量占该粘合剂/润滑剂混合物重量的10至60%。
有利地,外层占包衣前微粒总重量的1至5%。
本发明的微粒中硫酸吗啡的含量优选为50至200mg/g。
本发明提供即释硫酸吗啡微粒,通过用桨以100转/分钟搅拌的方法溶解,其在37℃,在pH被缓冲至约等于7的水中的溶解特性如下:
—在30分钟后,超过70%重量的活性组分溶解,
—在60分钟后,超过90%重量的活性组分溶解。
本发明微粒的平均粒度为0.5至2mm。
本发明还涉及制备本发明即释硫酸吗啡微粒的方法,该方法全部在含水介质中进行。
本发明的方法有利地使用在中性载体颗粒上包衣的方法,该方法在穿孔平锅中或空气流化床中进行,或者通过制药工业中常用的任何其它技术制备微粒。
所述方法包括将硫酸吗啡和粘合剂的水混悬液置于中性载体颗粒上的步骤。此步骤包括通过将粘合剂溶解于水中并再将硫酸吗啡悬浮于所得溶液中、再将包衣混悬液喷雾到中性颗粒上制备包衣混悬液。
所述粘合剂选自药用粘合剂,特别是羟丙甲基纤维素。
将微粒任选地过筛并优选用成膜剂的水混悬液包衣。该混悬液通过将选自药用成膜剂、优选羟丙甲基纤维素的成膜剂溶解于水中获得。
任选地,将选自药用润滑剂的润滑剂悬浮于此保护性包衣溶液中,并优选以占所用成膜剂的干涂剂重量的15%至70%的比例使用滑石。
在被装于硬明胶胶囊、泡状包装或外壳中之前,被保护的微粒可以用滑石润滑和/或再次过筛。
本发明的另一个主题是含本发明微粒的药物制剂,其中颗粒任选地通过上述方法获得,其单位剂量的等效用量为1至100mg,优选5至60mg,更优选10至30mg硫酸吗啡。
本发明的制剂有利地以硬明胶胶囊和/或小药囊的形式存在,对于这些剂型,患者可以直接吞咽或与其食物混和。
下列实施例举例说明本发明,而不是对其范围进行限制。
附图说明
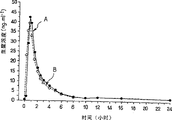
附图表示血浆中吗啡浓度的几何平均值随时间的变化,其数值测量于:
—以硬明胶胶囊的形式给药本发明微粒制剂的30位患者体内(曲线A);
—以先有技术盐酸吗啡可饮用制剂给药的30位患者体内(曲线B)。
具体实施方式
实施例1:在平锅中包衣
·制备活性包衣混悬液
所用起始物的质量比如下:
| 硫酸吗啡 | 18.7% |
| Pharmacoat 603 | 6.5% |
| 纯水 | 74.8% |
在不锈钢容器中制备该混悬液。将纯水倒入此容器中,然后搅拌。分批加入Pharmacoat 603(由Shin-Etsu公司制备)。
维持搅拌直到Pharmacoat 603彻底溶解为止。分批加入硫酸吗啡。
维持搅拌直到活性混悬液被充分均质化,然后进行包衣步骤。
·在中性载体颗粒上包衣活性硫酸吗啡混悬液
将Neutres 26载体颗粒(由NP-Pharm公司制备)置于旋转穿孔平锅中。在整个包衣阶段维持热气流通过微粒床层。通过将上述混悬液连续喷雾将硫酸吗啡包衣在Neutres 26上。
任选地将微粒过筛以便保证此批颗粒的粒径一致。包衣后,维持不热的气流通过微粒床以便让它们冷却至室温。
·制备保护性包衣混悬液
所用赋形剂的质量比如下:
| Pharmacoat 603 | 9.6% |
| 滑石 | 4.7% |
| 纯水 | 85.7% |
在不锈钢容器中制备该混悬液。将纯水倒入此容器中,然后搅拌。
分批加入Pharmacoat 603。维持搅拌直到Pharmacoat 603彻底溶解为止。分批加入滑石。
维持搅拌直到混悬液被充分均质化为止,然后进行保护性包衣步骤。
·硫酸吗啡微粒的保护性包衣
将要保护的微粒置于旋转穿孔平锅中。在整个保护性包衣阶段维持热空气流通过微粒床。通过将上述混悬液连续喷雾进行硫酸吗啡微粒的保护性包衣。在保护性包衣结束后,维持不热的空气流通过微粒床以便让它们冷却至室温。
任选地将微粒过筛以便保证此批颗粒的粒径均一。
最终制剂组成
| 量(%) | 量(g) | |
| 硫酸吗啡 | 15.0 | 157.5 |
| Neutres 26 | 75.3 | 787.1 |
| Pharmacoat 603 | 8.2 | 85.5 |
| 滑石 | 1.4 | 15.2 |
| 理论含量 | 150mg/g |
将颗粒溶解于水中
在37℃,在100转/分钟的桨式装置中将颗粒溶于500ml纯水。
在285和310nm读取紫外吸收值。
| 时间(分钟) | 作为时间的函数的释放量(%) |
| 5 | 61.2 |
| 10 | 88.4 |
| 15 | 91.8 |
| 20 | 93.0 |
| 25 | 93.5 |
| 30 | 93.5 |
| 35 | 93.5 |
| 40 | 93.6 |
| 45 | 93.8 |
| 50 | 93.7 |
| 55 | 93.5 |
| 60 | 93.4 |
实施例2:在空气流化床中包衣
·活性包衣混悬液按照实施例1制备。
·在中性载体颗粒上包衣活性硫酸吗啡混悬液
将Neutres 26载体颗粒置于空气流化床装置中。
通过将上述制备的混悬液连续喷雾在被热空气流流化的Neutres26上完成硫酸吗啡的包衣过程。将微粒团任选地过筛以便保证此批颗粒粒度一致。
·保护性包衣混悬液按照实施例1制备。
·硫酸吗啡微粒的保护性包衣
将要保护的微粒置于空气流化床装置中。
通过将如上制备的混悬液连续喷雾在被热空气流流化的硫酸吗啡颗粒上进行保护性包衣。
在保护性包衣结束时,将颗粒维持在热空气流中以便将它们干燥。将微粒任选地过筛以便保证此批颗粒粒度一致。
最终制剂组成
| 量(%) | 量(g) | |
| 硫酸吗啡 | 14.7 | 138.3 |
| Neutres 26 | 75.8 | 713.3 |
| Pharmacoat 603 | 8.0 | 75.8 |
| 滑石 | 1.4 | 13.6 |
| 理论含量 | 147mg/g |
将颗粒溶解于水中
如实施例1进行操作。
| 时间(分钟) | 作为时间的函数的释放量(%) |
| 5 | 65.60 |
| 10 | 83.83 |
| 15 | 90.71 |
| 20 | 93.71 |
| 25 | 94.69 |
| 30 | 94.87 |
| 35 | 94.95 |
| 40 | 94.95 |
| 45 | 94.99 |
| 50 | 95.04 |
| 55 | 94.99 |
| 60 | 94.99 |
实施例3:在空气流化床中包衣
按照实施例2操作,降低保护性包衣数量。
最终制剂组成
| 量(%) | 量(g) | |
| 硫酸吗啡 | 15.3 | 138.3 |
| Neutres 26 | 77.52 | 713.3 |
| Pharmacoat 603 | 6.73 | 61.9 |
| 滑石 | 0.73 | 6.7 |
| 理论含量 | 150mg/g |
将颗粒和30mg硬明胶胶囊溶解于水中
如实施例2操作。
| 时间(分钟) | 质量% | 硬明胶胶囊(总重量30mg)(质量%) |
| 5 | 67.18 | 87.84 |
| 10 | 83.57 | 97.83 |
| 15 | 90.07 | 102.55 |
| 20 | 92.85 | 104.77 |
| 25 | 93.58 | 105.44 |
| 30 | 93.80 | 105.48 |
| 35 | 93.84 | 105.28 |
| 40 | 93.80 | 105.33 |
| 45 | 93.88 | 105.38 |
| 50 | 93.92 | 105.38 |
| 55 | 93.84 | 105.43 |
| 60 | 93.83 | 105.38 |
实施例4:在平锅中包衣
按照实施例1制备活性包衣混悬液并且包衣中性载体颗粒。
按照实施例1,制备保护性包衣混悬液并对硫酸吗啡微粒进行保护性包衣,但是降低保护性包衣数量。
最终制剂组成
| 量(质量%) | 量(Kg) | |
| 硫酸吗啡 | 15.5 | 7.6 |
| Neutres 26 | 76.2 | 37.2 |
| Pharmacoat 603 | 6.9 | 3.4 |
| 滑石 | 1.2 | 0.6 |
| 理论含量 | 155.7mg/g |
将颗粒和硬明胶胶囊溶解于水中
如实施例1操作。
| 颗粒 | 硬明胶胶囊 | |||
| 总重30mg | 总重20mg | 总重10mg | ||
| 5 | 72.89% | 87.68% | 90.44% | 90.99% |
| 10 | 82.66% | 93.64% | 96.65% | 95.88% |
| 15 | 88.90% | 96.14% | 99.06% | 97.66% |
| 20 | 91.93% | 96.96% | 99.87% | 98.27% |
| 25 | 93.18% | 97.15% | 100.06% | 98.53% |
| 30 | 93.48% | 97.24% | 100.04% | 98.51% |
| 35 | 93.6 5% | 97.12% | 100.02% | 98.51% |
| 40 | 93.67% | 97.12% | 100.04% | 98.36% |
| 45 | 93.71% | 97.24% | 100.02% | 98.40% |
| 50 | 93.87% | 97.12% | 100.06% | 98.38% |
| 55 | 93.71% | 97.14% | 99.94% | 98.44% |
| 60 | 93.80% | 97.07% | 100.06% | 98.42% |
临床试验
用30mg硬明胶胶囊进行生物等值研究,用(A)标记形式为0.1%小药瓶的、可饮用吗啡盐酸盐口服制剂,用(B)标记每只含10ml溶液,即约7.6mg吗啡的小药瓶,而每个硬明胶胶囊含30mg微粒,即约22.5mg吗啡。
对30位给药A的患者和30位给药B的患者进行单盲试验随机研究。
采用高效液相色谱-质谱检测吗啡和6-葡糖醛酸苷酶-吗啡(活性代谢物)的血浆浓度。
观察到由含本发明微粒的硬明胶胶囊(A)得到的药物动力学参数与含溶解的吗啡盐酸盐的小药瓶(B)获得的参数具有可比性。
下表概括了与吗啡血浆浓度有关的结果:
| 参数 | 治疗 | 几何平均值 | 最小值/最大值 | A/B几何平均值比的90%置信区间 | 此区间的最佳点 |
| Cmax(ng.ml-1) | AB | 5045 | 27/9820/80 | 100-121 | 110 |
| AUC0-∞(ng.ml-1.h) | AB | 10194 | 57/16156/172 | 102-114 | 108 |
| 参数 | 治疗 | Cmax平均值 | 最小值/最大值 | A/B几何平均值差别的90%置信区间 | 此区间最佳点 |
| Tmax(h) | AB | 0.750.5 | 0.5/10.25/1 | 0.125-0.250 | 0.125 |
发现Cmax和AUC0-∞参数的A/B比例的最佳点及其共有置信区间在80-125%生物等效范围。
因此,就Cmax、AUC0-∞和Tmax而言,含本发明微粒的硬明胶胶囊与现有技术中可饮用的吗啡盐酸盐口服制剂是生物等效的。
附图中的曲线A和B表明作为时间的函数的血浆吗啡浓度的几何平均值的变化。
对6-葡糖醛酸苷酶-吗啡得到了类似的结果。
制剂A和B的耐受性是可比的,并且没有观察到任何有害的副作用。
Claims (28)
1.一种即释微粒,其特征在于每个微粒含有用由硫酸吗啡和药用粘合剂形成的混合物包衣的中性载体颗粒,所述粘合剂占硫酸吗啡/粘合剂混合物重量的15至40%。
2.权利要求1的即释微粒,其特征在于被该层含有成膜剂和可能存在的润滑剂的外保护层包衣。
3.权利要求2的即释微粒,其特征在于润滑剂占粘合剂/润滑剂混合物重量的10至60%。
4.权利要求2或3的即释微粒,其特征在于润滑剂是滑石。
5.权利要求2至4中任一项的即释微粒,其特征在于外层占包衣前微粒总重量的1至5%。
6.权利要求1中的即释微粒,其特征在于粘合剂和/或成膜剂是羟丙甲基纤维素。
7.权利要求1中的即释微粒,其特征在于硫酸吗啡含量为50至200mg/g。
8.权利要求1中的即释微粒,其特征在于通过用桨以100转/分钟搅拌的方法溶解,其在37℃,在pH被缓冲至约等于7的水中的溶解特性如下:
—在30分钟后,超过70%重量的活性组分溶解,
—在60分钟后,超过90%重量的活性组分溶解。
9.权利要求1中的即释微粒,其特征在于平均粒度为0.5至2mm。
10.权利要求1的即释微粒的制备方法,其特征在于全部在含水介质中进行,包括在平锅中或在空气流化床中将含有硫酸吗啡和粘合剂的水混悬液包衣到中性载体颗粒上的步骤。
11.权利要求2的即释微粒的制备方法,其特征在于全部在含水介质中进行,包括在平锅中或在空气流化床中将含有硫酸吗啡和粘合剂的水混悬液包衣到中性载体颗粒上的步骤。
12.权利要求3的即释微粒的制备方法,其特征在于全部在含水介质中进行,包括在平锅中或在空气流化床中将含有硫酸吗啡和粘合剂的水混悬液包衣到中性载体颗粒上的步骤。
13.权利要求4的即释微粒的制备方法,其特征在于全部在含水介质中进行,包括在平锅中或在空气流化床中将含有硫酸吗啡和粘合剂的水混悬液包衣到中性载体颗粒上的步骤。
14.权利要求5的即释微粒的制备方法,其特征在于全部在含水介质中进行,包括在平锅中或在空气流化床中将含有硫酸吗啡和粘合剂的水混悬液包衣到中性载体颗粒上的步骤。
15.权利要求6的即释微粒的制备方法,其特征在于全部在含水介质中进行,包括在平锅中或在空气流化床中将含有硫酸吗啡和粘合剂的水混悬液包衣到中性载体颗粒上的步骤。
16.权利要求7的即释微粒的制备方法,其特征在于全部在含水介质中进行,包括在平锅中或在空气流化床中将含有硫酸吗啡和粘合剂的水混悬液包衣到中性载体颗粒上的步骤。
17.权利要求8的即释微粒的制备方法,其特征在于全部在含水介质中进行,包括在平锅中或在空气流化床中将含有硫酸吗啡和粘合剂的水混悬液包衣到中性载体颗粒上的步骤。
18.权利要求9的即释微粒的制备方法,其特征在于全部在含水介质中进行,包括在平锅中或在空气流化床中将含有硫酸吗啡和粘合剂的水混悬液包衣到中性载体颗粒上的步骤。
19.权利要求10-18中任一项的方法,其特征在于将包衣步骤结束时获得的微粒用成膜剂如羟丙甲基纤维素的水混悬液包衣。
20.一种药物制剂,其特征在于含有权利要求1的即释微粒,其单位剂量的等效用量为1至100mg硫酸吗啡。
21.一种药物制剂,其特征在于含有权利要求2的即释微粒,其单位剂量的等效用量为1至100mg硫酸吗啡。
22.一种药物制剂,其特征在于含有权利要求3的即释微粒,其单位剂量的等效用量为1至100mg硫酸吗啡。
23.一种药物制剂,其特征在于含有权利要求4的即释微粒,其单位剂量的等效用量为1至100mg硫酸吗啡。
24.一种药物制剂,其特征在于含有权利要求5的即释微粒,其单位剂量的等效用量为1至100mg硫酸吗啡。
25.一种药物制剂,其特征在于含有权利要求6的即释微粒,其单位剂量的等效用量为1至100mg硫酸吗啡。
26.一种药物制剂,其特征在于含有权利要求7的即释微粒,其单位剂量的等效用量为1至100mg硫酸吗啡。
27.一种药物制剂,其特征在于含有权利要求8的即释微粒,其单位剂量的等效用量为1至100mg硫酸吗啡。
28.一种药物制剂,其特征在于含有权利要求9的即释微粒,其单位剂量的等效用量为1至100mg硫酸吗啡。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR98/01816 | 1998-02-16 | ||
| FR9801816A FR2774910B1 (fr) | 1998-02-16 | 1998-02-16 | Microgranules de sulfate de morphine, procede de fabrication et preparations pharmaceutiques |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN1291097A CN1291097A (zh) | 2001-04-11 |
| CN1135981C true CN1135981C (zh) | 2004-01-28 |
Family
ID=9522990
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CNB998030120A Expired - Lifetime CN1135981C (zh) | 1998-02-16 | 1999-02-15 | 硫酸吗啡微粒、其制备方法和药物制剂 |
Country Status (16)
| Country | Link |
|---|---|
| US (2) | US6482437B2 (zh) |
| EP (1) | EP1054672B1 (zh) |
| JP (1) | JP4447166B2 (zh) |
| CN (1) | CN1135981C (zh) |
| AU (1) | AU2429899A (zh) |
| BR (1) | BR9907908A (zh) |
| CA (1) | CA2320878C (zh) |
| CY (1) | CY1107559T1 (zh) |
| DE (1) | DE69934781T2 (zh) |
| DK (1) | DK1054672T3 (zh) |
| ES (1) | ES2277427T3 (zh) |
| FR (1) | FR2774910B1 (zh) |
| HK (1) | HK1036402A1 (zh) |
| NZ (1) | NZ506307A (zh) |
| PT (1) | PT1054672E (zh) |
| WO (1) | WO1999040918A1 (zh) |
Families Citing this family (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2790668B1 (fr) * | 1999-03-12 | 2002-07-26 | D B F | Granules contenant une substance vegetale et leur procede de preparation |
| WO2003024430A1 (en) | 2001-09-21 | 2003-03-27 | Egalet A/S | Morphine polymer release system |
| EP2957281A1 (en) | 2001-09-21 | 2015-12-23 | Egalet Ltd. | Polymer release system |
| DE602004031096D1 (de) | 2003-03-26 | 2011-03-03 | Egalet As | Morphin-system mit kontrollierter freisetzung |
| JP5171038B2 (ja) * | 2003-10-10 | 2013-03-27 | エティファルム | イチョウ・エキスを含む放出持続性の微小顆粒およびそのような顆粒の製造方法 |
| FR2883179B1 (fr) | 2005-03-18 | 2009-04-17 | Ethypharm Sa | Comprime enrobe |
| US20070190141A1 (en) * | 2006-02-16 | 2007-08-16 | Aaron Dely | Extended release opiate composition |
| US20070286900A1 (en) | 2006-06-09 | 2007-12-13 | Catherine Herry | Low dose tablets of opioid analgesics and preparation process |
| US20100233257A1 (en) * | 2006-06-09 | 2010-09-16 | Ethypharm | Low dose sublingual tablets of opioid analgesics and preparation process |
| CA2687192C (en) | 2007-06-04 | 2015-11-24 | Egalet A/S | Controlled release pharmaceutical compositions for prolonged effect |
| PL2197429T3 (pl) * | 2007-09-03 | 2016-09-30 | Kompozycje w postaci cząstek do dostarczania słabo rozpuszczalnych leków | |
| US9005660B2 (en) | 2009-02-06 | 2015-04-14 | Egalet Ltd. | Immediate release composition resistant to abuse by intake of alcohol |
| WO2010149169A2 (en) | 2009-06-24 | 2010-12-29 | Egalet A/S | Controlled release formulations |
| CA2877183A1 (en) | 2012-07-06 | 2014-01-09 | Egalet Ltd. | Abuse deterrent pharmaceutical compositions for controlled release |
| US9683448B2 (en) | 2013-03-18 | 2017-06-20 | Honeywell International Inc. | Low conductivity thermal barrier coating |
| US11479846B2 (en) | 2014-01-07 | 2022-10-25 | Honeywell International Inc. | Thermal barrier coatings for turbine engine components |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4135514A (en) * | 1974-12-23 | 1979-01-23 | Alza Corporation | Osmotic releasing system for administering ophthalmic drug to eye of animal |
| US4309996A (en) * | 1980-04-28 | 1982-01-12 | Alza Corporation | System with microporous releasing diffusor |
| US4673405A (en) * | 1983-03-04 | 1987-06-16 | Alza Corporation | Osmotic system with instant drug availability |
| US5026560A (en) * | 1987-01-29 | 1991-06-25 | Takeda Chemical Industries, Ltd. | Spherical granules having core and their production |
| DE3708856A1 (de) | 1987-03-18 | 1988-09-29 | Kajetan Leitner | Mit zaehnen versehene einpressmutter |
| US5202128A (en) * | 1989-01-06 | 1993-04-13 | F. H. Faulding & Co. Limited | Sustained release pharmaceutical composition |
| US5133974A (en) * | 1989-05-05 | 1992-07-28 | Kv Pharmaceutical Company | Extended release pharmaceutical formulations |
| US5580578A (en) * | 1992-01-27 | 1996-12-03 | Euro-Celtique, S.A. | Controlled release formulations coated with aqueous dispersions of acrylic polymers |
| US5478577A (en) * | 1993-11-23 | 1995-12-26 | Euroceltique, S.A. | Method of treating pain by administering 24 hour oral opioid formulations exhibiting rapid rate of initial rise of plasma drug level |
| US5891471A (en) * | 1993-11-23 | 1999-04-06 | Euro-Celtique, S.A. | Pharmaceutical multiparticulates |
| US5411745A (en) * | 1994-05-25 | 1995-05-02 | Euro-Celtique, S.A. | Powder-layered morphine sulfate formulations |
| US5582838A (en) * | 1994-12-22 | 1996-12-10 | Merck & Co., Inc. | Controlled release drug suspension delivery device |
| US6066339A (en) * | 1997-10-17 | 2000-05-23 | Elan Corporation, Plc | Oral morphine multiparticulate formulation |
-
1998
- 1998-02-16 FR FR9801816A patent/FR2774910B1/fr not_active Expired - Lifetime
-
1999
- 1999-02-15 JP JP2000531170A patent/JP4447166B2/ja not_active Expired - Lifetime
- 1999-02-15 CN CNB998030120A patent/CN1135981C/zh not_active Expired - Lifetime
- 1999-02-15 BR BR9907908-9A patent/BR9907908A/pt not_active Application Discontinuation
- 1999-02-15 ES ES99903752T patent/ES2277427T3/es not_active Expired - Lifetime
- 1999-02-15 WO PCT/FR1999/000326 patent/WO1999040918A1/fr active IP Right Grant
- 1999-02-15 DE DE69934781T patent/DE69934781T2/de not_active Expired - Lifetime
- 1999-02-15 CA CA002320878A patent/CA2320878C/fr not_active Expired - Lifetime
- 1999-02-15 NZ NZ506307A patent/NZ506307A/en not_active IP Right Cessation
- 1999-02-15 DK DK99903752T patent/DK1054672T3/da active
- 1999-02-15 EP EP99903752A patent/EP1054672B1/fr not_active Expired - Lifetime
- 1999-02-15 AU AU24298/99A patent/AU2429899A/en not_active Abandoned
- 1999-02-15 PT PT99903752T patent/PT1054672E/pt unknown
- 1999-02-16 US US09/250,393 patent/US6482437B2/en not_active Expired - Lifetime
-
2001
- 2001-10-11 HK HK01107153A patent/HK1036402A1/xx not_active IP Right Cessation
-
2002
- 2002-09-30 US US10/259,854 patent/US20030129244A1/en not_active Abandoned
-
2007
- 2007-02-20 CY CY20071100242T patent/CY1107559T1/el unknown
Also Published As
| Publication number | Publication date |
|---|---|
| CA2320878C (fr) | 2009-04-21 |
| US20030129244A1 (en) | 2003-07-10 |
| JP2002502877A (ja) | 2002-01-29 |
| FR2774910B1 (fr) | 2001-09-07 |
| NZ506307A (en) | 2003-11-28 |
| AU2429899A (en) | 1999-08-30 |
| DK1054672T3 (da) | 2007-04-10 |
| ES2277427T3 (es) | 2007-07-01 |
| JP4447166B2 (ja) | 2010-04-07 |
| CA2320878A1 (fr) | 1999-08-19 |
| CY1107559T1 (el) | 2013-03-13 |
| DE69934781T2 (de) | 2007-10-11 |
| PT1054672E (pt) | 2007-04-30 |
| EP1054672A1 (fr) | 2000-11-29 |
| US20020028246A1 (en) | 2002-03-07 |
| FR2774910A1 (fr) | 1999-08-20 |
| US6482437B2 (en) | 2002-11-19 |
| BR9907908A (pt) | 2002-04-30 |
| HK1036402A1 (en) | 2002-01-04 |
| WO1999040918A1 (fr) | 1999-08-19 |
| EP1054672B1 (fr) | 2007-01-10 |
| DE69934781D1 (de) | 2007-02-22 |
| CN1291097A (zh) | 2001-04-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN1135981C (zh) | 硫酸吗啡微粒、其制备方法和药物制剂 | |
| CN1040061C (zh) | 控释药物制剂的制备方法 | |
| CN1114405C (zh) | 胃保护性奥美拉唑微粒、其制备方法及药物制剂 | |
| CN1360499A (zh) | 含有非诺贝特的药物组合物及其制备方法 | |
| CN86106651A (zh) | 新的药物制剂 | |
| CN1249950A (zh) | 药学活性颗粒的制备 | |
| JPH09511767A (ja) | 新規な経口用の医薬使用形態 | |
| CN101094675A (zh) | [1,4]二氮杂庚因并[6,7,1-ij]喹啉衍生物制剂 | |
| JP2008007458A (ja) | レイヤリング用核粒子とその製造方法 | |
| CN1747723A (zh) | 含活性成分混合物的组合物及其制备方法 | |
| CN1744889A (zh) | 坦洛新的控释药物组合物 | |
| CN1525852A (zh) | 被掩味的包衣颗粒和粒状物 | |
| CN1161112C (zh) | 含氯雷他定和伪麻黄碱的药物胶囊组合物 | |
| CN1186014C (zh) | 程序化和随时间释放的多颗粒药物剂型及其制备方法 | |
| CN1882321A (zh) | 包含盐酸文拉法辛的小丸 | |
| CN1267089C (zh) | 硫酸吗啡微粒,其制备方法及含有该物质的组合物 | |
| CN106890161A (zh) | 一种左乙拉西坦缓释胶囊及其制备方法 | |
| CN1207681A (zh) | 含硫氮䓬酮活性成分的缓释微粒 | |
| CN1285738A (zh) | 卡维地洛的新的口服剂型 | |
| CN1823804A (zh) | 一种克拉霉素速释微丸及其制备方法 | |
| CN102133195A (zh) | 盐酸曲美他嗪的缓控释微丸及其制备方法 | |
| AU2009315449B2 (en) | Novel method for preparing granulates of active principles, and granulates obtained thereof | |
| CN101076318A (zh) | 造粒方法 | |
| CN1529587A (zh) | 含有粪便软化剂泊洛沙姆和包有肠溶衣的比沙可定颗粒的药物组合物 | |
| CN1634006A (zh) | 盐酸文拉法辛液体缓释制剂及其制备方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C14 | Grant of patent or utility model | ||
| GR01 | Patent grant | ||
| C56 | Change in the name or address of the patentee |
Owner name: ETHYPHARM COMPANY Free format text: FORMER NAME OR ADDRESS: ROOM #, AIDIKEAIDIFAMUYAOPINSHIYAN |
|
| CP01 | Change in the name or title of a patent holder |
Address after: Wudang, France Patentee after: Effalm S.A. Address before: Wudang, France Patentee before: Labortoires Des Produits Ethiques Ethypharm |
|
| CX01 | Expiry of patent term | ||
| CX01 | Expiry of patent term |
Granted publication date: 20040128 |