CN111196802A - 化合物、包含所述化合物的有机电子器件和包含所述有机电子器件的显示设备和照明设备 - Google Patents
化合物、包含所述化合物的有机电子器件和包含所述有机电子器件的显示设备和照明设备 Download PDFInfo
- Publication number
- CN111196802A CN111196802A CN201911117538.XA CN201911117538A CN111196802A CN 111196802 A CN111196802 A CN 111196802A CN 201911117538 A CN201911117538 A CN 201911117538A CN 111196802 A CN111196802 A CN 111196802A
- Authority
- CN
- China
- Prior art keywords
- group
- compound
- layer
- formula
- electronic device
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 150000001875 compounds Chemical class 0.000 title claims abstract description 154
- 230000000903 blocking effect Effects 0.000 claims description 48
- 125000003118 aryl group Chemical group 0.000 claims description 46
- 239000004065 semiconductor Substances 0.000 claims description 39
- 125000004429 atom Chemical group 0.000 claims description 31
- JEGZRTMZYUDVBF-UHFFFAOYSA-N Benz[a]acridine Chemical group C1=CC=C2C3=CC4=CC=CC=C4N=C3C=CC2=C1 JEGZRTMZYUDVBF-UHFFFAOYSA-N 0.000 claims description 16
- 229910052757 nitrogen Inorganic materials 0.000 claims description 15
- 229910052760 oxygen Inorganic materials 0.000 claims description 11
- 125000004432 carbon atom Chemical group C* 0.000 claims description 9
- 125000003968 arylidene group Chemical group [H]C(c)=* 0.000 claims description 8
- 125000005842 heteroatom Chemical group 0.000 claims description 8
- 229910052717 sulfur Inorganic materials 0.000 claims description 8
- 125000001424 substituent group Chemical group 0.000 claims description 7
- 125000000609 carbazolyl group Chemical class C1(=CC=CC=2C3=CC=CC=C3NC12)* 0.000 claims description 2
- 125000004986 diarylamino group Chemical class 0.000 claims description 2
- 229910052739 hydrogen Inorganic materials 0.000 claims description 2
- 238000002347 injection Methods 0.000 description 40
- 239000007924 injection Substances 0.000 description 40
- 238000000151 deposition Methods 0.000 description 32
- 239000000463 material Substances 0.000 description 32
- 239000000758 substrate Substances 0.000 description 31
- 230000005525 hole transport Effects 0.000 description 29
- 239000002019 doping agent Substances 0.000 description 28
- -1 benzacridine compound Chemical class 0.000 description 27
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 24
- 230000008021 deposition Effects 0.000 description 23
- 239000011248 coating agent Substances 0.000 description 16
- 238000000576 coating method Methods 0.000 description 16
- 229910052751 metal Inorganic materials 0.000 description 16
- 239000002184 metal Chemical class 0.000 description 16
- IMKMFBIYHXBKRX-UHFFFAOYSA-M lithium;quinoline-2-carboxylate Chemical compound [Li+].C1=CC=CC2=NC(C(=O)[O-])=CC=C21 IMKMFBIYHXBKRX-UHFFFAOYSA-M 0.000 description 15
- 150000003254 radicals Chemical group 0.000 description 15
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 14
- 239000007787 solid Substances 0.000 description 14
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 12
- 238000004770 highest occupied molecular orbital Methods 0.000 description 12
- 239000011777 magnesium Substances 0.000 description 11
- 229910052783 alkali metal Inorganic materials 0.000 description 10
- 239000000203 mixture Substances 0.000 description 10
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 9
- 238000000034 method Methods 0.000 description 9
- 239000002244 precipitate Substances 0.000 description 9
- 238000004528 spin coating Methods 0.000 description 9
- 238000001771 vacuum deposition Methods 0.000 description 9
- 125000001072 heteroaryl group Chemical group 0.000 description 8
- 229910052749 magnesium Inorganic materials 0.000 description 8
- 238000000967 suction filtration Methods 0.000 description 8
- 239000000654 additive Substances 0.000 description 7
- 150000001340 alkali metals Chemical class 0.000 description 7
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 7
- 125000000217 alkyl group Chemical group 0.000 description 7
- 239000011575 calcium Substances 0.000 description 7
- 230000000052 comparative effect Effects 0.000 description 7
- 238000004768 lowest unoccupied molecular orbital Methods 0.000 description 7
- 239000011159 matrix material Substances 0.000 description 7
- 229910052709 silver Inorganic materials 0.000 description 7
- 239000004332 silver Substances 0.000 description 7
- IXHWGNYCZPISET-UHFFFAOYSA-N 2-[4-(dicyanomethylidene)-2,3,5,6-tetrafluorocyclohexa-2,5-dien-1-ylidene]propanedinitrile Chemical compound FC1=C(F)C(=C(C#N)C#N)C(F)=C(F)C1=C(C#N)C#N IXHWGNYCZPISET-UHFFFAOYSA-N 0.000 description 6
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 6
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 6
- 229910052769 Ytterbium Inorganic materials 0.000 description 6
- 229910052791 calcium Inorganic materials 0.000 description 6
- 238000007639 printing Methods 0.000 description 6
- 239000000126 substance Substances 0.000 description 6
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 6
- 150000001342 alkaline earth metals Chemical class 0.000 description 5
- 150000004646 arylidenes Chemical group 0.000 description 5
- 238000005266 casting Methods 0.000 description 5
- 239000000306 component Substances 0.000 description 5
- 230000006866 deterioration Effects 0.000 description 5
- 238000001035 drying Methods 0.000 description 5
- 125000006575 electron-withdrawing group Chemical group 0.000 description 5
- 239000011521 glass Substances 0.000 description 5
- 150000002430 hydrocarbons Chemical group 0.000 description 5
- 229910052744 lithium Inorganic materials 0.000 description 5
- SKEDXQSRJSUMRP-UHFFFAOYSA-N lithium;quinolin-8-ol Chemical compound [Li].C1=CN=C2C(O)=CC=CC2=C1 SKEDXQSRJSUMRP-UHFFFAOYSA-N 0.000 description 5
- 238000000746 purification Methods 0.000 description 5
- 230000005855 radiation Effects 0.000 description 5
- 239000000725 suspension Substances 0.000 description 5
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 4
- 229910052693 Europium Inorganic materials 0.000 description 4
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 4
- 230000000996 additive effect Effects 0.000 description 4
- 229910052788 barium Inorganic materials 0.000 description 4
- 229910052792 caesium Inorganic materials 0.000 description 4
- 239000003795 chemical substances by application Substances 0.000 description 4
- 150000004696 coordination complex Chemical class 0.000 description 4
- 238000002330 electrospray ionisation mass spectrometry Methods 0.000 description 4
- 238000000295 emission spectrum Methods 0.000 description 4
- 125000001153 fluoro group Chemical group F* 0.000 description 4
- 238000004128 high performance liquid chromatography Methods 0.000 description 4
- 238000005286 illumination Methods 0.000 description 4
- 238000004519 manufacturing process Methods 0.000 description 4
- IBHBKWKFFTZAHE-UHFFFAOYSA-N n-[4-[4-(n-naphthalen-1-ylanilino)phenyl]phenyl]-n-phenylnaphthalen-1-amine Chemical compound C1=CC=CC=C1N(C=1C2=CC=CC=C2C=CC=1)C1=CC=C(C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C3=CC=CC=C3C=CC=2)C=C1 IBHBKWKFFTZAHE-UHFFFAOYSA-N 0.000 description 4
- 229920000767 polyaniline Polymers 0.000 description 4
- 229910052700 potassium Inorganic materials 0.000 description 4
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 4
- 229910052701 rubidium Inorganic materials 0.000 description 4
- 229910052708 sodium Inorganic materials 0.000 description 4
- 229910052712 strontium Inorganic materials 0.000 description 4
- VQGHOUODWALEFC-UHFFFAOYSA-N 2-phenylpyridine Chemical compound C1=CC=CC=C1C1=CC=CC=N1 VQGHOUODWALEFC-UHFFFAOYSA-N 0.000 description 3
- AWXGSYPUMWKTBR-UHFFFAOYSA-N 4-carbazol-9-yl-n,n-bis(4-carbazol-9-ylphenyl)aniline Chemical compound C12=CC=CC=C2C2=CC=CC=C2N1C1=CC=C(N(C=2C=CC(=CC=2)N2C3=CC=CC=C3C3=CC=CC=C32)C=2C=CC(=CC=2)N2C3=CC=CC=C3C3=CC=CC=C32)C=C1 AWXGSYPUMWKTBR-UHFFFAOYSA-N 0.000 description 3
- 101000837344 Homo sapiens T-cell leukemia translocation-altered gene protein Proteins 0.000 description 3
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 3
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 3
- 102100028692 T-cell leukemia translocation-altered gene protein Human genes 0.000 description 3
- 150000001339 alkali metal compounds Chemical class 0.000 description 3
- 150000004945 aromatic hydrocarbons Chemical group 0.000 description 3
- 229910052799 carbon Inorganic materials 0.000 description 3
- 238000001816 cooling Methods 0.000 description 3
- IOJUPLGTWVMSFF-UHFFFAOYSA-N cyclobenzothiazole Natural products C1=CC=C2SC=NC2=C1 IOJUPLGTWVMSFF-UHFFFAOYSA-N 0.000 description 3
- 239000000706 filtrate Substances 0.000 description 3
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 3
- 239000012299 nitrogen atmosphere Substances 0.000 description 3
- 150000002902 organometallic compounds Chemical class 0.000 description 3
- 229920003227 poly(N-vinyl carbazole) Polymers 0.000 description 3
- 229910052761 rare earth metal Inorganic materials 0.000 description 3
- 150000003839 salts Chemical class 0.000 description 3
- 239000000741 silica gel Substances 0.000 description 3
- 229910002027 silica gel Inorganic materials 0.000 description 3
- 229910052710 silicon Inorganic materials 0.000 description 3
- 238000000859 sublimation Methods 0.000 description 3
- 230000008022 sublimation Effects 0.000 description 3
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 description 3
- 239000010409 thin film Substances 0.000 description 3
- 238000005406 washing Methods 0.000 description 3
- CBLFIXRJCLJWKL-UHFFFAOYSA-N 13-[3-(9-phenylcarbazol-3-yl)carbazol-9-yl]-2-azapentacyclo[12.8.0.03,12.04,9.017,22]docosa-1,3(12),4,6,8,10,13,15,17,19,21-undecaene Chemical compound C1(=CC=CC=C1)N1C2=CC=CC=C2C=2C=C(C=CC1=2)C=1C=CC=2N(C3=CC=CC=C3C=2C=1)C1=C2C=CC3=C(C2=NC=2C4=C(C=CC1=2)C=CC=C4)C=CC=C3 CBLFIXRJCLJWKL-UHFFFAOYSA-N 0.000 description 2
- LCWRXYDLRLSHOR-UHFFFAOYSA-N 13-[4-(3,6-diphenylcarbazol-9-yl)phenyl]-2-azapentacyclo[12.8.0.03,12.04,9.017,22]docosa-1,3(12),4,6,8,10,13,15,17,19,21-undecaene Chemical compound C1(=CC=CC=C1)C=1C=CC=2N(C3=CC=C(C=C3C=2C=1)C1=CC=CC=C1)C1=CC=C(C=C1)C1=C2C=CC3=C(C2=NC=2C4=C(C=CC1=2)C=CC=C4)C=CC=C3 LCWRXYDLRLSHOR-UHFFFAOYSA-N 0.000 description 2
- OBAJPWYDYFEBTF-UHFFFAOYSA-N 2-tert-butyl-9,10-dinaphthalen-2-ylanthracene Chemical compound C1=CC=CC2=CC(C3=C4C=CC=CC4=C(C=4C=C5C=CC=CC5=CC=4)C4=CC=C(C=C43)C(C)(C)C)=CC=C21 OBAJPWYDYFEBTF-UHFFFAOYSA-N 0.000 description 2
- OGGKVJMNFFSDEV-UHFFFAOYSA-N 3-methyl-n-[4-[4-(n-(3-methylphenyl)anilino)phenyl]phenyl]-n-phenylaniline Chemical compound CC1=CC=CC(N(C=2C=CC=CC=2)C=2C=CC(=CC=2)C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C=C(C)C=CC=2)=C1 OGGKVJMNFFSDEV-UHFFFAOYSA-N 0.000 description 2
- MAGFQRLKWCCTQJ-UHFFFAOYSA-M 4-ethenylbenzenesulfonate Chemical compound [O-]S(=O)(=O)C1=CC=C(C=C)C=C1 MAGFQRLKWCCTQJ-UHFFFAOYSA-M 0.000 description 2
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 2
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 2
- 229910052684 Cerium Inorganic materials 0.000 description 2
- 229910052692 Dysprosium Inorganic materials 0.000 description 2
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 2
- QAZYOQWUSJVJAR-UHFFFAOYSA-N N-[3-(2-azapentacyclo[12.8.0.03,12.04,9.017,22]docosa-1,3(12),4,6,8,10,13,15,17,19,21-undecaen-13-yl)phenyl]-N-phenylnaphthalen-2-amine Chemical compound C1=CC=CC=2C=CC=3C(=C4C=CC5=C(C4=NC=3C=21)C=CC=C5)C=1C=C(C=CC=1)N(C1=CC2=CC=CC=C2C=C1)C1=CC=CC=C1 QAZYOQWUSJVJAR-UHFFFAOYSA-N 0.000 description 2
- UFWIBTONFRDIAS-UHFFFAOYSA-N Naphthalene Chemical compound C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 description 2
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical group CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 2
- 229920001609 Poly(3,4-ethylenedioxythiophene) Polymers 0.000 description 2
- SMWDFEZZVXVKRB-UHFFFAOYSA-N Quinoline Chemical compound N1=CC=CC2=CC=CC=C21 SMWDFEZZVXVKRB-UHFFFAOYSA-N 0.000 description 2
- 229910052772 Samarium Inorganic materials 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 229910052771 Terbium Inorganic materials 0.000 description 2
- 125000002252 acyl group Chemical group 0.000 description 2
- 239000003513 alkali Substances 0.000 description 2
- 150000001341 alkaline earth metal compounds Chemical class 0.000 description 2
- 229910052782 aluminium Inorganic materials 0.000 description 2
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 2
- MWPLVEDNUUSJAV-UHFFFAOYSA-N anthracene Chemical compound C1=CC=CC2=CC3=CC=CC=C3C=C21 MWPLVEDNUUSJAV-UHFFFAOYSA-N 0.000 description 2
- 150000001491 aromatic compounds Chemical class 0.000 description 2
- 125000000732 arylene group Chemical group 0.000 description 2
- 230000005540 biological transmission Effects 0.000 description 2
- 229910052796 boron Inorganic materials 0.000 description 2
- 150000001716 carbazoles Chemical class 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 230000000694 effects Effects 0.000 description 2
- 125000003983 fluorenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3CC12)* 0.000 description 2
- 239000010931 gold Substances 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- RBTKNAXYKSUFRK-UHFFFAOYSA-N heliogen blue Chemical compound [Cu].[N-]1C2=C(C=CC=C3)C3=C1N=C([N-]1)C3=CC=CC=C3C1=NC([N-]1)=C(C=CC=C3)C3=C1N=C([N-]1)C3=CC=CC=C3C1=N2 RBTKNAXYKSUFRK-UHFFFAOYSA-N 0.000 description 2
- 150000002391 heterocyclic compounds Chemical class 0.000 description 2
- 239000012535 impurity Substances 0.000 description 2
- 229910052746 lanthanum Inorganic materials 0.000 description 2
- XMGQYMWWDOXHJM-UHFFFAOYSA-N limonene Chemical compound CC(=C)C1CCC(C)=CC1 XMGQYMWWDOXHJM-UHFFFAOYSA-N 0.000 description 2
- 229910001092 metal group alloy Inorganic materials 0.000 description 2
- 150000002894 organic compounds Chemical class 0.000 description 2
- 125000005010 perfluoroalkyl group Chemical group 0.000 description 2
- YNPNZTXNASCQKK-UHFFFAOYSA-N phenanthrene Chemical compound C1=CC=C2C3=CC=CC=C3C=CC2=C1 YNPNZTXNASCQKK-UHFFFAOYSA-N 0.000 description 2
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 2
- IEQIEDJGQAUEQZ-UHFFFAOYSA-N phthalocyanine Chemical class N1C(N=C2C3=CC=CC=C3C(N=C3C4=CC=CC=C4C(=N4)N3)=N2)=C(C=CC=C2)C2=C1N=C1C2=CC=CC=C2C4=N1 IEQIEDJGQAUEQZ-UHFFFAOYSA-N 0.000 description 2
- 229920003023 plastic Polymers 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- 229910000027 potassium carbonate Inorganic materials 0.000 description 2
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 2
- 150000002910 rare earth metals Chemical class 0.000 description 2
- 239000011541 reaction mixture Substances 0.000 description 2
- 238000001953 recrystallisation Methods 0.000 description 2
- 125000006413 ring segment Chemical group 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- XOLBLPGZBRYERU-UHFFFAOYSA-N tin dioxide Chemical compound O=[Sn]=O XOLBLPGZBRYERU-UHFFFAOYSA-N 0.000 description 2
- 150000003623 transition metal compounds Chemical class 0.000 description 2
- TVIVIEFSHFOWTE-UHFFFAOYSA-K tri(quinolin-8-yloxy)alumane Chemical compound [Al+3].C1=CN=C2C([O-])=CC=CC2=C1.C1=CN=C2C([O-])=CC=CC2=C1.C1=CN=C2C([O-])=CC=CC2=C1 TVIVIEFSHFOWTE-UHFFFAOYSA-K 0.000 description 2
- 150000003918 triazines Chemical class 0.000 description 2
- MIOPJNTWMNEORI-GMSGAONNSA-N (S)-camphorsulfonic acid Chemical compound C1C[C@@]2(CS(O)(=O)=O)C(=O)C[C@@H]1C2(C)C MIOPJNTWMNEORI-GMSGAONNSA-N 0.000 description 1
- IWZZBBJTIUYDPZ-DVACKJPTSA-N (z)-4-hydroxypent-3-en-2-one;iridium;2-phenylpyridine Chemical compound [Ir].C\C(O)=C\C(C)=O.[C-]1=CC=CC=C1C1=CC=CC=N1.[C-]1=CC=CC=C1C1=CC=CC=N1 IWZZBBJTIUYDPZ-DVACKJPTSA-N 0.000 description 1
- JYEUMXHLPRZUAT-UHFFFAOYSA-N 1,2,3-triazine Chemical compound C1=CN=NN=C1 JYEUMXHLPRZUAT-UHFFFAOYSA-N 0.000 description 1
- ZKXGQPQAMRSBOL-UHFFFAOYSA-N 1,2,3-trifluoro-9h-fluorene Chemical compound C12=CC=CC=C2CC2=C1C=C(F)C(F)=C2F ZKXGQPQAMRSBOL-UHFFFAOYSA-N 0.000 description 1
- BCMCBBGGLRIHSE-UHFFFAOYSA-N 1,3-benzoxazole Chemical class C1=CC=C2OC=NC2=C1 BCMCBBGGLRIHSE-UHFFFAOYSA-N 0.000 description 1
- IYZMXHQDXZKNCY-UHFFFAOYSA-N 1-n,1-n-diphenyl-4-n,4-n-bis[4-(n-phenylanilino)phenyl]benzene-1,4-diamine Chemical compound C1=CC=CC=C1N(C=1C=CC(=CC=1)N(C=1C=CC(=CC=1)N(C=1C=CC=CC=1)C=1C=CC=CC=1)C=1C=CC(=CC=1)N(C=1C=CC=CC=1)C=1C=CC=CC=1)C1=CC=CC=C1 IYZMXHQDXZKNCY-UHFFFAOYSA-N 0.000 description 1
- XEZNGIUYQVAUSS-UHFFFAOYSA-N 18-crown-6 Chemical compound C1COCCOCCOCCOCCOCCO1 XEZNGIUYQVAUSS-UHFFFAOYSA-N 0.000 description 1
- BFTIPCRZWILUIY-UHFFFAOYSA-N 2,5,8,11-tetratert-butylperylene Chemical group CC(C)(C)C1=CC(C2=CC(C(C)(C)C)=CC=3C2=C2C=C(C=3)C(C)(C)C)=C3C2=CC(C(C)(C)C)=CC3=C1 BFTIPCRZWILUIY-UHFFFAOYSA-N 0.000 description 1
- XANIFASCQKHXRC-UHFFFAOYSA-N 2-(1,3-benzothiazol-2-yl)phenol zinc Chemical compound [Zn].Oc1ccccc1-c1nc2ccccc2s1.Oc1ccccc1-c1nc2ccccc2s1 XANIFASCQKHXRC-UHFFFAOYSA-N 0.000 description 1
- GEQBRULPNIVQPP-UHFFFAOYSA-N 2-[3,5-bis(1-phenylbenzimidazol-2-yl)phenyl]-1-phenylbenzimidazole Chemical compound C1=CC=CC=C1N1C2=CC=CC=C2N=C1C1=CC(C=2N(C3=CC=CC=C3N=2)C=2C=CC=CC=2)=CC(C=2N(C3=CC=CC=C3N=2)C=2C=CC=CC=2)=C1 GEQBRULPNIVQPP-UHFFFAOYSA-N 0.000 description 1
- RKVIAZWOECXCCM-UHFFFAOYSA-N 2-carbazol-9-yl-n,n-diphenylaniline Chemical compound C1=CC=CC=C1N(C=1C(=CC=CC=1)N1C2=CC=CC=C2C2=CC=CC=C21)C1=CC=CC=C1 RKVIAZWOECXCCM-UHFFFAOYSA-N 0.000 description 1
- BCHZICNRHXRCHY-UHFFFAOYSA-N 2h-oxazine Chemical class N1OC=CC=C1 BCHZICNRHXRCHY-UHFFFAOYSA-N 0.000 description 1
- PCMKGEAHIZDRFL-UHFFFAOYSA-N 3,6-diphenyl-9h-carbazole Chemical compound C1=CC=CC=C1C1=CC=C(NC=2C3=CC(=CC=2)C=2C=CC=CC=2)C3=C1 PCMKGEAHIZDRFL-UHFFFAOYSA-N 0.000 description 1
- DNTVTBIKSZRANH-UHFFFAOYSA-N 4-(4-aminophenyl)-3-(3-methylphenyl)aniline Chemical compound CC1=CC=CC(C=2C(=CC=C(N)C=2)C=2C=CC(N)=CC=2)=C1 DNTVTBIKSZRANH-UHFFFAOYSA-N 0.000 description 1
- RLPAWKJLZUFLCR-UHFFFAOYSA-N 4-(4-aminophenyl)-3-naphthalen-1-yl-n,n-diphenylaniline Chemical compound C1=CC(N)=CC=C1C1=CC=C(N(C=2C=CC=CC=2)C=2C=CC=CC=2)C=C1C1=CC=CC2=CC=CC=C12 RLPAWKJLZUFLCR-UHFFFAOYSA-N 0.000 description 1
- PUGLQYLNHVYWST-UHFFFAOYSA-N 4-[[2,3-bis[cyano-(4-cyano-2,3,5,6-tetrafluorophenyl)methylidene]cyclopropylidene]-cyanomethyl]-2,3,5,6-tetrafluorobenzonitrile Chemical compound FC1=C(C#N)C(F)=C(F)C(C(C#N)=C2C(C2=C(C#N)C=2C(=C(F)C(C#N)=C(F)C=2F)F)=C(C#N)C=2C(=C(F)C(C#N)=C(F)C=2F)F)=C1F PUGLQYLNHVYWST-UHFFFAOYSA-N 0.000 description 1
- OSQXTXTYKAEHQV-WXUKJITCSA-N 4-methyl-n-[4-[(e)-2-[4-[4-[(e)-2-[4-(4-methyl-n-(4-methylphenyl)anilino)phenyl]ethenyl]phenyl]phenyl]ethenyl]phenyl]-n-(4-methylphenyl)aniline Chemical compound C1=CC(C)=CC=C1N(C=1C=CC(\C=C\C=2C=CC(=CC=2)C=2C=CC(\C=C\C=3C=CC(=CC=3)N(C=3C=CC(C)=CC=3)C=3C=CC(C)=CC=3)=CC=2)=CC=1)C1=CC=C(C)C=C1 OSQXTXTYKAEHQV-WXUKJITCSA-N 0.000 description 1
- DIVZFUBWFAOMCW-UHFFFAOYSA-N 4-n-(3-methylphenyl)-1-n,1-n-bis[4-(n-(3-methylphenyl)anilino)phenyl]-4-n-phenylbenzene-1,4-diamine Chemical compound CC1=CC=CC(N(C=2C=CC=CC=2)C=2C=CC(=CC=2)N(C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C=C(C)C=CC=2)C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C=C(C)C=CC=2)=C1 DIVZFUBWFAOMCW-UHFFFAOYSA-N 0.000 description 1
- WDYVUKGVKRZQNM-UHFFFAOYSA-N 6-phosphonohexylphosphonic acid Chemical compound OP(O)(=O)CCCCCCP(O)(O)=O WDYVUKGVKRZQNM-UHFFFAOYSA-N 0.000 description 1
- VIZUPBYFLORCRA-UHFFFAOYSA-N 9,10-dinaphthalen-2-ylanthracene Chemical compound C12=CC=CC=C2C(C2=CC3=CC=CC=C3C=C2)=C(C=CC=C2)C2=C1C1=CC=C(C=CC=C2)C2=C1 VIZUPBYFLORCRA-UHFFFAOYSA-N 0.000 description 1
- GJWBRYKOJMOBHH-UHFFFAOYSA-N 9,9-dimethyl-n-[4-(9-phenylcarbazol-3-yl)phenyl]-n-(4-phenylphenyl)fluoren-2-amine Chemical compound C1=C2C(C)(C)C3=CC=CC=C3C2=CC=C1N(C=1C=CC(=CC=1)C=1C=C2C3=CC=CC=C3N(C=3C=CC=CC=3)C2=CC=1)C(C=C1)=CC=C1C1=CC=CC=C1 GJWBRYKOJMOBHH-UHFFFAOYSA-N 0.000 description 1
- XJQPGLAFAMHLCE-UHFFFAOYSA-N 9-[3-(2-azapentacyclo[12.8.0.03,12.04,9.017,22]docosa-1,3(12),4,6,8,10,13,15,17,19,21-undecaen-13-yl)phenyl]carbazole-3-carbonitrile Chemical compound C1=CC=CC=2C=CC=3C(=C4C=CC5=C(C4=NC=3C=21)C=CC=C5)C=1C=C(C=CC=1)N1C2=CC=CC=C2C=2C=C(C=CC1=2)C#N XJQPGLAFAMHLCE-UHFFFAOYSA-N 0.000 description 1
- VIJYEGDOKCKUOL-UHFFFAOYSA-N 9-phenylcarbazole Chemical compound C1=CC=CC=C1N1C2=CC=CC=C2C2=CC=CC=C21 VIJYEGDOKCKUOL-UHFFFAOYSA-N 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 238000004057 DFT-B3LYP calculation Methods 0.000 description 1
- 238000003775 Density Functional Theory Methods 0.000 description 1
- 229910021578 Iron(III) chloride Inorganic materials 0.000 description 1
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 1
- XBDYBAVJXHJMNQ-UHFFFAOYSA-N Tetrahydroanthracene Natural products C1=CC=C2C=C(CCCC3)C3=CC2=C1 XBDYBAVJXHJMNQ-UHFFFAOYSA-N 0.000 description 1
- YTPLMLYBLZKORZ-UHFFFAOYSA-N Thiophene Chemical class C=1C=CSC=1 YTPLMLYBLZKORZ-UHFFFAOYSA-N 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- 229910052770 Uranium Inorganic materials 0.000 description 1
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 1
- XLOMVQKBTHCTTD-UHFFFAOYSA-N Zinc monoxide Chemical compound [Zn]=O XLOMVQKBTHCTTD-UHFFFAOYSA-N 0.000 description 1
- CUJRVFIICFDLGR-UHFFFAOYSA-N acetylacetonate Chemical compound CC(=O)[CH-]C(C)=O CUJRVFIICFDLGR-UHFFFAOYSA-N 0.000 description 1
- 150000001335 aliphatic alkanes Chemical class 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 229910045601 alloy Inorganic materials 0.000 description 1
- 239000000956 alloy Substances 0.000 description 1
- JYMITAMFTJDTAE-UHFFFAOYSA-N aluminum zinc oxygen(2-) Chemical compound [O-2].[Al+3].[Zn+2] JYMITAMFTJDTAE-UHFFFAOYSA-N 0.000 description 1
- 239000010405 anode material Substances 0.000 description 1
- 125000005428 anthryl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C3C(*)=C([H])C([H])=C([H])C3=C([H])C2=C1[H] 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 125000006615 aromatic heterocyclic group Chemical group 0.000 description 1
- DSAJWYNOEDNPEQ-UHFFFAOYSA-N barium atom Chemical compound [Ba] DSAJWYNOEDNPEQ-UHFFFAOYSA-N 0.000 description 1
- QVQLCTNNEUAWMS-UHFFFAOYSA-N barium oxide Inorganic materials [Ba]=O QVQLCTNNEUAWMS-UHFFFAOYSA-N 0.000 description 1
- 239000002585 base Substances 0.000 description 1
- 150000001555 benzenes Chemical class 0.000 description 1
- LPTWEDZIPSKWDG-UHFFFAOYSA-N benzenesulfonic acid;dodecane Chemical compound OS(=O)(=O)C1=CC=CC=C1.CCCCCCCCCCCC LPTWEDZIPSKWDG-UHFFFAOYSA-N 0.000 description 1
- HFACYLZERDEVSX-UHFFFAOYSA-N benzidine Chemical class C1=CC(N)=CC=C1C1=CC=C(N)C=C1 HFACYLZERDEVSX-UHFFFAOYSA-N 0.000 description 1
- JYZIHLWOWKMNNX-UHFFFAOYSA-N benzimidazole Chemical compound C1=C[CH]C2=NC=NC2=C1 JYZIHLWOWKMNNX-UHFFFAOYSA-N 0.000 description 1
- 125000005605 benzo group Chemical group 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 235000010290 biphenyl Nutrition 0.000 description 1
- 239000004305 biphenyl Substances 0.000 description 1
- 150000004074 biphenyls Chemical class 0.000 description 1
- 150000001642 boronic acid derivatives Chemical class 0.000 description 1
- QARVLSVVCXYDNA-UHFFFAOYSA-N bromobenzene Chemical compound BrC1=CC=CC=C1 QARVLSVVCXYDNA-UHFFFAOYSA-N 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 238000004440 column chromatography Methods 0.000 description 1
- 229940125904 compound 1 Drugs 0.000 description 1
- 229940125898 compound 5 Drugs 0.000 description 1
- 125000006165 cyclic alkyl group Chemical group 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 229940043397 deconex Drugs 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 230000003111 delayed effect Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- BTVBCAKHMZHLFR-UHFFFAOYSA-N dibenz[c,h]acridine Chemical compound C1=CC=CC2=C(N=C3C4=CC=CC=C4C=CC3=C3)C3=CC=C21 BTVBCAKHMZHLFR-UHFFFAOYSA-N 0.000 description 1
- 238000009792 diffusion process Methods 0.000 description 1
- 229940060296 dodecylbenzenesulfonic acid Drugs 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 230000005281 excited state Effects 0.000 description 1
- 230000005669 field effect Effects 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 230000004907 flux Effects 0.000 description 1
- JVZRCNQLWOELDU-UHFFFAOYSA-N gamma-Phenylpyridine Natural products C1=CC=CC=C1C1=CC=NC=C1 JVZRCNQLWOELDU-UHFFFAOYSA-N 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 230000005283 ground state Effects 0.000 description 1
- 150000002357 guanidines Chemical class 0.000 description 1
- 125000001188 haloalkyl group Chemical group 0.000 description 1
- 150000008282 halocarbons Chemical group 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 125000005843 halogen group Chemical group 0.000 description 1
- 150000002367 halogens Chemical class 0.000 description 1
- 208000006359 hepatoblastoma Diseases 0.000 description 1
- 150000002390 heteroarenes Chemical class 0.000 description 1
- 229940058961 hydroxyquinoline derivative for amoebiasis and other protozoal diseases Drugs 0.000 description 1
- 150000002460 imidazoles Chemical class 0.000 description 1
- 229910052738 indium Inorganic materials 0.000 description 1
- AMGQUBHHOARCQH-UHFFFAOYSA-N indium;oxotin Chemical compound [In].[Sn]=O AMGQUBHHOARCQH-UHFFFAOYSA-N 0.000 description 1
- 238000000025 interference lithography Methods 0.000 description 1
- PNDPGZBMCMUPRI-UHFFFAOYSA-N iodine Chemical compound II PNDPGZBMCMUPRI-UHFFFAOYSA-N 0.000 description 1
- RBTARNINKXHZNM-UHFFFAOYSA-K iron trichloride Chemical compound Cl[Fe](Cl)Cl RBTARNINKXHZNM-UHFFFAOYSA-K 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 229940087305 limonene Drugs 0.000 description 1
- 235000001510 limonene Nutrition 0.000 description 1
- 150000002627 limonene derivatives Chemical class 0.000 description 1
- PWFLNWVNVSGEIS-UHFFFAOYSA-M lithium;2-diphenylphosphorylphenolate Chemical compound [Li+].[O-]C1=CC=CC=C1P(=O)(C=1C=CC=CC=1)C1=CC=CC=C1 PWFLNWVNVSGEIS-UHFFFAOYSA-M 0.000 description 1
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 1
- CSNNHWWHGAXBCP-UHFFFAOYSA-L magnesium sulphate Substances [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 125000002950 monocyclic group Chemical group 0.000 description 1
- BXFYXYKLIORMBI-UHFFFAOYSA-N n,n-diphenyl-4-[2-(2-phenylphenyl)ethenyl]aniline Chemical group C=1C=C(N(C=2C=CC=CC=2)C=2C=CC=CC=2)C=CC=1C=CC1=CC=CC=C1C1=CC=CC=C1 BXFYXYKLIORMBI-UHFFFAOYSA-N 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- 125000002560 nitrile group Chemical group 0.000 description 1
- 125000004433 nitrogen atom Chemical group N* 0.000 description 1
- 125000006574 non-aromatic ring group Chemical group 0.000 description 1
- 229940078552 o-xylene Drugs 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 230000005693 optoelectronics Effects 0.000 description 1
- 239000012074 organic phase Substances 0.000 description 1
- 238000013086 organic photovoltaic Methods 0.000 description 1
- WCPAKWJPBJAGKN-UHFFFAOYSA-N oxadiazole Chemical class C1=CON=N1 WCPAKWJPBJAGKN-UHFFFAOYSA-N 0.000 description 1
- 150000002916 oxazoles Chemical class 0.000 description 1
- NRNFFDZCBYOZJY-UHFFFAOYSA-N p-quinodimethane Chemical class C=C1C=CC(=C)C=C1 NRNFFDZCBYOZJY-UHFFFAOYSA-N 0.000 description 1
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 1
- 125000005003 perfluorobutyl group Chemical group FC(F)(F)C(F)(F)C(F)(F)C(F)(F)* 0.000 description 1
- 125000005004 perfluoroethyl group Chemical group FC(F)(F)C(F)(F)* 0.000 description 1
- 125000005062 perfluorophenyl group Chemical group FC1=C(C(=C(C(=C1F)F)F)F)* 0.000 description 1
- 125000005009 perfluoropropyl group Chemical group FC(C(C(F)(F)F)(F)F)(F)* 0.000 description 1
- 239000012071 phase Substances 0.000 description 1
- 150000005041 phenanthrolines Chemical class 0.000 description 1
- 125000005561 phenanthryl group Chemical group 0.000 description 1
- ISWSIDIOOBJBQZ-UHFFFAOYSA-M phenolate Chemical compound [O-]C1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-M 0.000 description 1
- 150000004707 phenolate Chemical class 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 125000003367 polycyclic group Chemical group 0.000 description 1
- VLRICFVOGGIMKK-UHFFFAOYSA-N pyrazol-1-yloxyboronic acid Chemical compound OB(O)ON1C=CC=N1 VLRICFVOGGIMKK-UHFFFAOYSA-N 0.000 description 1
- 150000003217 pyrazoles Chemical class 0.000 description 1
- 125000001725 pyrenyl group Chemical group 0.000 description 1
- 150000003230 pyrimidines Chemical class 0.000 description 1
- 238000010791 quenching Methods 0.000 description 1
- 230000000171 quenching effect Effects 0.000 description 1
- JWVCLYRUEFBMGU-UHFFFAOYSA-N quinazoline Chemical compound N1=CN=CC2=CC=CC=C21 JWVCLYRUEFBMGU-UHFFFAOYSA-N 0.000 description 1
- LISFMEBWQUVKPJ-UHFFFAOYSA-N quinolin-2-ol Chemical class C1=CC=C2NC(=O)C=CC2=C1 LISFMEBWQUVKPJ-UHFFFAOYSA-N 0.000 description 1
- 238000010992 reflux Methods 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 238000007789 sealing Methods 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 229910052711 selenium Inorganic materials 0.000 description 1
- 230000011664 signaling Effects 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 150000003384 small molecules Chemical class 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 238000010129 solution processing Methods 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 238000004544 sputter deposition Methods 0.000 description 1
- 125000005504 styryl group Chemical group 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 229940042055 systemic antimycotics triazole derivative Drugs 0.000 description 1
- 150000001911 terphenyls Chemical class 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- IFLREYGFSNHWGE-UHFFFAOYSA-N tetracene Chemical compound C1=CC=CC2=CC3=CC4=CC=CC=C4C=C3C=C21 IFLREYGFSNHWGE-UHFFFAOYSA-N 0.000 description 1
- PCCVSPMFGIFTHU-UHFFFAOYSA-N tetracyanoquinodimethane Chemical class N#CC(C#N)=C1C=CC(=C(C#N)C#N)C=C1 PCCVSPMFGIFTHU-UHFFFAOYSA-N 0.000 description 1
- 238000002207 thermal evaporation Methods 0.000 description 1
- 150000003557 thiazoles Chemical class 0.000 description 1
- 125000005259 triarylamine group Chemical group 0.000 description 1
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 1
- 125000001889 triflyl group Chemical group FC(F)(F)S(*)(=O)=O 0.000 description 1
- ODHXBMXNKOYIBV-UHFFFAOYSA-N triphenylamine Chemical compound C1=CC=CC=C1N(C=1C=CC=CC=1)C1=CC=CC=C1 ODHXBMXNKOYIBV-UHFFFAOYSA-N 0.000 description 1
- 150000003732 xanthenes Chemical class 0.000 description 1
- NAWDYIZEMPQZHO-UHFFFAOYSA-N ytterbium Chemical compound [Yb] NAWDYIZEMPQZHO-UHFFFAOYSA-N 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
- 239000011701 zinc Substances 0.000 description 1
- YVTHLONGBIQYBO-UHFFFAOYSA-N zinc indium(3+) oxygen(2-) Chemical compound [O--].[Zn++].[In+3] YVTHLONGBIQYBO-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/10—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D221/00—Heterocyclic compounds containing six-membered rings having one nitrogen atom as the only ring hetero atom, not provided for by groups C07D211/00 - C07D219/00
- C07D221/02—Heterocyclic compounds containing six-membered rings having one nitrogen atom as the only ring hetero atom, not provided for by groups C07D211/00 - C07D219/00 condensed with carbocyclic rings or ring systems
- C07D221/04—Ortho- or peri-condensed ring systems
- C07D221/18—Ring systems of four or more rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/10—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
- H10K85/636—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine comprising heteroaromatic hydrocarbons as substituents on the nitrogen atom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1007—Non-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/10—Triplet emission
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/30—Highest occupied molecular orbital [HOMO], lowest unoccupied molecular orbital [LUMO] or Fermi energy values
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
- H10K50/16—Electron transporting layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/18—Carrier blocking layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Optics & Photonics (AREA)
- Electroluminescent Light Sources (AREA)
Abstract
Description
技术领域
本发明涉及一种化合物和包含所述化合物的有机电子器件。本发明还涉及包含所述有机电子器件的显示设备或照明设备。
背景技术
作为自发光器件的有机发光二极管(OLED)具有广视角、出色的对比度、快速响应、高亮度、出色的驱动电压特性和色彩再现。典型的OLED包括阳极、空穴传输层(HTL)、发光层(EML)、电子传输层(ETL)和阴极,它们被顺序堆叠在基底上。就此而言,所述HTL、EML和ETL是基本上由有机和/或有机金属化合物形成的薄膜。
当向所述阳极和阴极施加电压时,从所述阳极注入的空穴通过所述HTL向所述EML移动,从所述阴极注入的电子通过所述ETL向所述EML移动。所述空穴和电子主要在所述EML中重合,以产生激子。当所述激子从激发态下降到基态时,发射光。空穴和电子的注入和流动应该是平衡的,使得具有上述结构的OLED具有出色的效率。
各种不同的有机发光二极管和包含它们的设备在本领域中是已知的。此外,在其一个或多个层中包含苯并吖啶化合物的相应OLED的使用,在本领域中是已知的。
然而,对于改进用于有机电子器件的相应化合物的电子性能,特别是提供适合于改进OLED的性能、特别是在相当电压下的工作寿命方面的性能的化合物,仍存在着需求。
因此,本发明的目的是提供克服了现有技术的缺点的用于有机电子器件的新的化合物,特别是适合于在工作寿命方面改进顶部发光OLED和底部发光OLED的性能的化合物。
发明内容
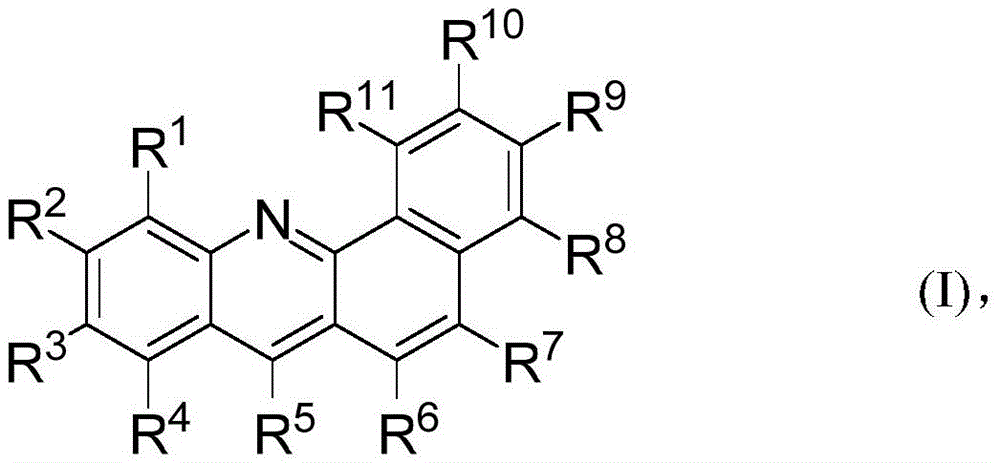
上述目的通过一种式(I)的化合物得以实现
其中所有的R1至R11,除了一个之外,都独立地选自H、D、F、取代或未取代的C1至C18烷基、取代或未取代的C6至C42芳基、取代或未取代的C3至C42杂芳基,并且相邻的基团R1至R11可以彼此连接以形成稠合环,
其中所述R1至R11中不选自上述基团的一个是基团G,其中
-所述基团G包含一个在其p-轨道中具有电子对的原子A;
-所述基团G包含连接到所述原子A的两个6元芳基环,其中所述两个6元芳基环中的每个分别通过单键连接到所述原子A,并且其中连接到所述原子A的所述两个6元芳基环可以通过单键彼此连接;
-所述基团G包含总共12至66个碳原子;
-所述基团G通过单键或通过C6至C18芳亚基连接到所述式(I)的化合物的苯并吖啶部分,其中所述C6至C18芳亚基是所述基团G的一部分;并且
-所述基团G是未取代的或者被一个或多个取代基取代,所述取代基独立地选自D、F、C1至C18烷基、C6至C42芳基、C6至C42杂芳基、(R12)2P=O、CN或G’,其中所述基团G’与所述基团G定义相同,区别在于所述基团G’不被连接到所述式(I)的化合物的苯并吖啶部分,而是通过单键或通过C6至C18芳亚基连接到所述基团G,其中所述C6至C18芳亚基是所述基团G’的一部分,前提是在所述基团G通过所述C6至C18芳亚基连接到所述式(I)的化合物的苯并吖啶部分的情况下,可以连接到所述C6至C18芳亚基的取代基只选自C1至C18烷基、C6至C42芳基、(R12)2P=O和CN;
其中在不是所述基团G的R1至R11中的至少一个被取代的情况下,相应的一个或多个取代基独立地选自D、F、C1至C18烷基、C6至C36芳基、C6至C42杂芳基、(R12)2P=O、CN;并且
其中R12独立地选自C1至C18烷基和C6至C24芳基。
本发明人令人吃惊地发现,上述化合物当用于有机电子器件例如OLED中的某些层时,适合于改进其性能,特别是在工作寿命方面。
所述p-轨道是非杂化轨道。
在连接到所述式(I)的化合物的苯并吖啶部分的基团G被其它基团G’取代的情况下,这个未直接连接到所述苯并吖啶部分的其它基团G’可不包含另一个基团G’作为其取代基。
根据本发明,所述基团G和基团G’,对于所述原子A、通过单键连接到所述原子A的所述两个6元芳基环和连接到所述原子A的其它基团,基本上是平面的。
所述两个6元芳基环可以包含选自碳和氮的环原子。在一个实施方式中,所述两个6元芳基环的环原子是碳。
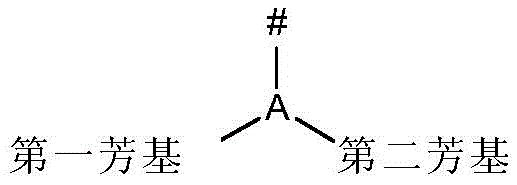
所述基团G可以包含下述结构单元
所述基团G可以在由“#”指示的位置处连接到所述式(I)的化合物的苯并吖啶部分。
在所述基团G中,特别是在上述结构单元中,所述两个6元芳基环可以通过单键彼此连接。
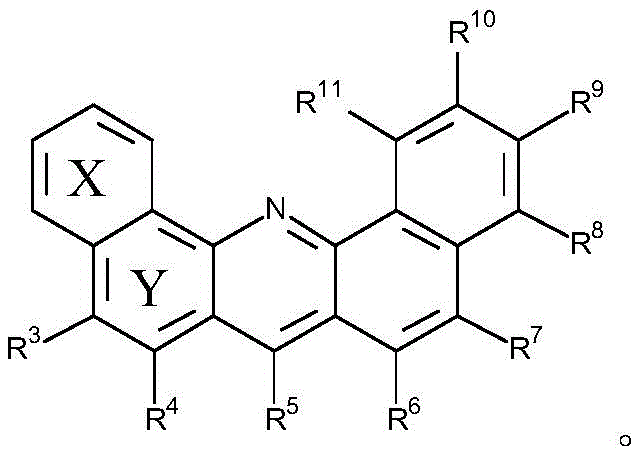
根据本发明,所述基团R1至R11中彼此相邻的两个(例如基团R1和R2)可一起形成稠合环。就此而言,稠合环是与所述两个相邻的Rn基团所键合的环一起形成稠合环体系的第二个环。通过这种方式,所述两个Rn基团所键合至的两个碳原子被彼此稠合的两个相邻环共有。参考其中R1和R2形成稠合环的实例,得到的结构可以如下所示,其中环X被稠合到共有两个碳原子的相邻环Y:
然而,必须指出,上述其中R1和R2一起形成6元芳族环(其是稠合环)的实施方式在本质上仅仅是示例性的,并且包括其它稠合环(例如5或7元环、非芳族环等)的形成。然而优选地,由两个相邻Rn基团形成的稠合环是如上所描绘的6元芳族环。
对于本发明的化合物来说,所述基团R1至R11中的恰好一个是本文中所定义的基团G。所有的其它基团R1至R11不同地选自上面提到的基团。
所述基团G包含一个在其p-轨道中具有电子对的原子A。所述原子A在其p-轨道中具有电子对这一事实,产生了对于所述原子A和直接连接到所述原子A的部分基本上是平面的化学结构,这意味着A到#、A到第一芳基和A到第二芳基的三个键位于仅仅几度(°)偏差结构内的同一分子平面中。所述偏差可以是10°或5°或<1°。
这将通过参考下述结构来示例:
在上述示例性结构中,正如根据本发明所要求的,所述原子A直接连接到两个6元芳基环(在上图中被标记为“第一芳基”和“第二芳基”)。在上述情形中,其中所述原子A是三价原子例如氮原子N,将所述第一芳基连接到原子A的键与将所述第二芳基连接到基团A的键之间的角度为约120°,例如110°至120°,或115°至120°,或119°至120°。对于#到所述原子A的键与A到所述第一芳基、相应的第二芳基的相应键来说,也是如此。
连接到所述原子A的所述两个6元芳基环可以不彼此连接,或者可以通过单键彼此连接。在第一种情况(不连接)下,相应的结构可以如上所描绘。
在所述两个6元芳基环通过单键彼此连接的情况下,所述基团G或G’可以包含下述结构:
所述基团G可以在键合位置“#”处通过单键或通过C6至C18芳亚基连接到所述式(I)的化合物的苯并吖啶部分
所述C6至C18芳亚基(如果存在的话)是所述基团G的一部分。也就是说,在所述基团G被取代的情况下,所述连接到基团G的取代基可以被连接到C6至C18芳亚基部分,所述C6至C18芳亚基部分将所述基团G连接到所述式(I)的化合物的苯并吖啶部分。
所述基团G只包含一个原子A。然而,在所述基团G被本文中所定义的另一个基团G’取代的情况下,所述通式(I)的化合物(而不是所述基团G)可包含另一个原子A。所述基团G’不可被连接到C6至C18芳亚基,所述C6至C18芳亚基作为所述基团G的一部分并将基团G连接到所述式(I)的化合物的苯并吖啶部分。
在所述式(I)的化合物中,所述基团G可以包含1至5个选自N、S和O的杂原子。通过这种方式,所述式(I)化合物的改进包含它的有机电子器件的工作寿命的能力被进一步提高。
在所述式(I)的化合物中,所述原子A可以选自N、S和O。通过这种方式,所述式(I)化合物的改进包含它的有机电子器件的工作寿命的能力被进一步提高。
在所述式(I)的化合物中,所述原子A可以是N。通过这种方式,所述式(I)化合物的改进包含它的有机电子器件的工作寿命的能力被进一步提高。
在所述式(I)的化合物中,所述基团G可以包含所述原子A和以二芳基氨基的形式或以咔唑基的形式连接到所述原子A的所述两个6元芳基环。通过这种方式,所述式(I)化合的物改进包含它的有机电子器件的工作寿命的能力被进一步提高。
在所述式(I)的化合物中,包含在所述式(I)的化合物中的芳族环的总数可以为6至21。通过这种方式,所述式(I)化合物的改进包含它的有机电子器件的工作寿命的能力被进一步提高。
在所述式(I)的化合物中,R1与R2、或R2与R3、或R3与R4可以一起形成芳基环。就此而言,上述成对的相邻基团Rn中只有一对形成稠合环。通过这种方式形成的稠合环是上文提到的稠合环。通过这种方式,所述式(I)化合物的改进包含它的有机电子器件的工作寿命的能力被进一步提高。
在一个实施方式中,R1与R2、或R3与R4可以形成稠合环。优选地,R1和R2可以形成稠合环。
在所述式(I)的化合物中,所述由R1与R2、或R2与R3、或R3与R4形成的稠合环可以是C6-芳基环。通过这种方式,所述式(I)化合物的改进包含它的有机电子器件的工作寿命的能力被进一步提高。
在所述式(I)的化合物中,所述基团G可以通过未取代的C6至C18芳亚基连接到所述式(I)的化合物的苯并吖啶部分。就此而言,将所述基团G连接到所述苯并吖啶部分的未取代的C6至C18芳亚基可以是苯亚基。通过这种方式,所述式(I)化合物的改进包含它的有机电子器件的工作寿命的能力被进一步提高。
在所述通式(I)的化合物中,R5或R10可以是所述基团G。换句话说,优选地所述基团G在R5或R10位置处被连接到所述式(I)的化合物的苯并吖啶部分。通过这种方式,所述通式(I)化合物的改进包含它的有机电子器件的工作寿命的能力被进一步提高。
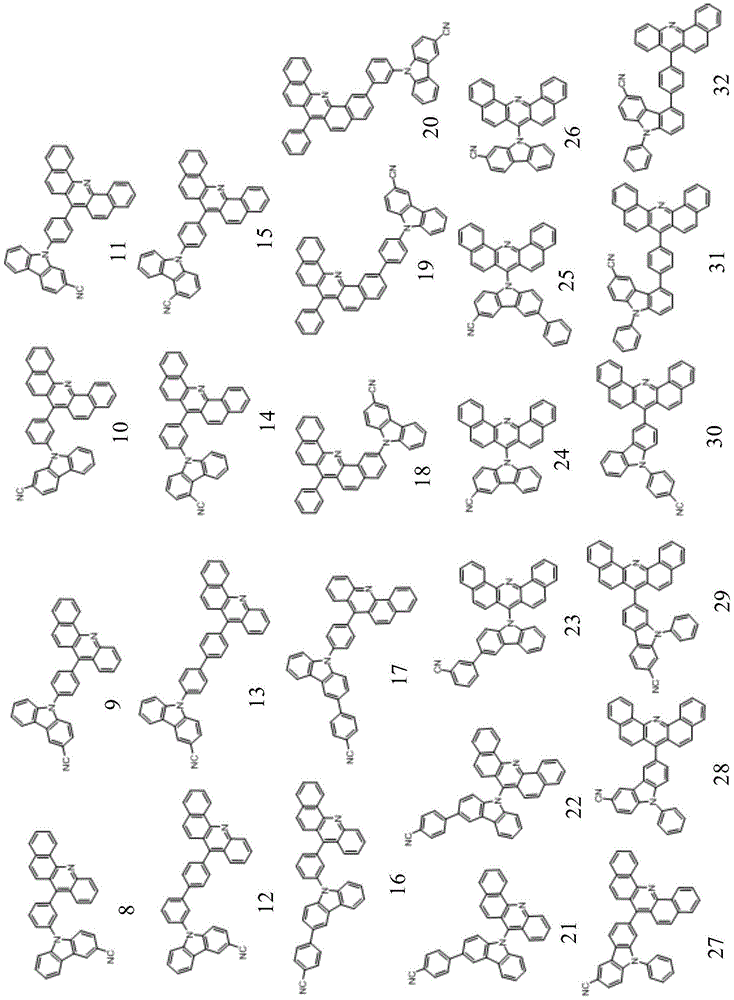
在一个非常优选的实施方式中,所述式(I)的化合物是选自下述化合物中的一种,
在一个实施方式中,所述式(I)的化合物具有低于3.89eV的能隙LUMO–HOMO。
所述目标还通过包含有机半导体层的有机电子器件得以实现,其中所述有机半导体层包含如本文中所描述的通式(I)的化合物。
所述有机电子器件还可以包含第一电极和第二电极,其中所述有机半导体层布置在所述第一电极与第二电极之间。
在所述有机电子器件中,所述有机半导体层可以是发光层。也就是说,根据本发明的一个实施方式,所述有机电子器件在其发光层中包含所述式(I)的化合物。
在另一个实施方式中,所述有机半导体层是空穴阻挡层。也就是说,在本发明的一个实施方式中,所述有机电子器件在其空穴阻挡层中包含所述式(I)的化合物。
就此而言,所述空穴阻挡层可以不包含掺杂剂或添加剂。
在另一个实施方式中,所述有机半导体层是电子传输层。也就是说,在这个实施方式中,所述有机电子器件在其电子传输层中包含所述式(I)的化合物。
就此而言,所述电子传输层还(除了所述式(I)的化合物之外)可以包含掺杂剂或添加剂。
就此而言,适合的添加剂或掺杂剂可以是n型添加剂或n型掺杂剂,例如LiQ、稀土元素金属、碱金属、碱土金属、硼酸盐(CAS 14728-62-2)、酚盐(例如CAS 1440864-50-5)、膦亚胺(例如CAS 51870-56-5)、胍类(例如CAS 1623748-16-2)、如US2009212280中所公开的金属络合物、US2007252140中公开的杂环化合物等。
在所述有机电子器件中,所述有机半导体层除了所述式(I)的化合物之外还可以包含至少一种第二化合物。就此而言,所述至少一种第二化合物可以是金属、金属盐、金属络合物、US2007252140中公开的杂环化合物、有机或金属有机发光体化合物或其混合物。所述金属络合物可以是有机碱金属络合物或US2009212280中公开的络合物。所述有机碱金属络合物可以是碱金属硼酸盐和/或酚盐和/或8-羟基喹啉锂。
所述目的还通过包含如本文中所定义的有机电子器件的显示设备得以实现。
所述目的还通过包含如本文中所定义的有机电子器件的照明设备得以实现。
本申请的实施例部分的结构是最优选的。
其它层
根据本发明,所述有机电子器件除了上面已经提到的层之外,还可以包含其它层。相应的层的示例性实施方式在下文中描述:
基底
所述基底可以是在电子器件例如有机发光二极管的制造中常用的任何基底。如果光穿过所述基底发射,则所述基底应该是透明或半透明材料,例如玻璃基底或透明塑料基底。如果光通过顶部表面发射,则所述基底可以是透明以及不透明材料两者,例如玻璃基底、塑料基底、金属基底或硅基底。
阳极
包含在本发明的有机电子器件中的第一电极或第二电极中的任一者可以是阳极。所述阳极可以通过沉积或溅射用于形成阳极的材料来形成。所述用于形成阳极的材料可以是高逸出功材料,以便促进空穴注入。所述阳极材料也可以选自低逸出功材料(即铝)。所述阳极可以是透明或反射电极。透明导电氧化物例如氧化锡铟(ITO)、氧化铟锌(IZO)、二氧化锡(SnO2)、氧化锌铝(AlZO)和氧化锌(ZnO),可用于形成所述阳极。所述阳极也可以使用金属、通常为银(Ag)、金(Au)或金属合金来形成。
空穴注入层
空穴注入层(HIL)可以通过真空沉积、旋涂、印刷、浇注、狭缝式涂布、Langmuir-Blodgett(LB)沉积等形成在所述阳极上。当所述HIL使用真空沉积来形成时,沉积条件可根据用于形成所述HIL的化合物以及所述HIL的所需结构和热学性质而变化。然而,一般来说,用于真空沉积的条件可以包括100℃至500℃的沉积温度、10-8至10-3托(1托等于133.322Pa)的压力和0.1至10nm/秒的沉积速率。
当所述HIL使用旋涂或印刷来形成时,涂布条件可根据用于形成所述HIL的化合物以及所述HIL的所需结构和热学性质而变化。例如,所述涂布条件可以包括约2000rpm至约5000rpm的涂布速度和约80℃至约200℃的热处理温度。在所述涂布进行后,热处理除去溶剂。
所述HIL可以由常用于形成HIL的任何化合物来形成。可用于形成所述HIL的化合物的实例包括酞菁化合物例如铜酞菁(CuPc)、4,4',4"-三(3-甲基苯基苯基氨基)三苯基胺(m-MTDATA)、TDATA、2T-NATA、聚苯胺/十二烷基苯磺酸(Pani/DBSA)、聚(3,4-乙叉二氧基噻吩)聚(4-苯乙烯磺酸酯)(PEDOT/PSS)、聚苯胺/樟脑磺酸(Pani/CSA)和聚苯胺/聚(4-苯乙烯磺酸酯)(PANI/PSS)。
所述HIL可以包含p型掺杂剂或由p型掺杂剂构成,并且所述p型掺杂剂可以选自四氟-四氰基醌二甲烷(F4TCNQ)、2,2'-(全氟代萘-2,6-二亚基)二丙二腈或2,2',2”-(环丙烷-1,2,3-三亚基)三(2-(对氰基四氟苯基)乙腈),但不限于此。所述HIL可以选自掺杂有p型掺杂剂的空穴传输基质化合物。已知的掺杂的空穴传输材料的典型实例是:HOMO能级约为-5.2eV的铜酞菁(CuPc),其掺杂有LUMO能级约为-5.2eV的四氟-四氰基醌二甲烷(F4TCNQ);掺杂有F4TCNQ的锌酞菁(ZnPc)(HOMO=-5.2eV);掺杂有F4TCNQ的α-NPD(N,N'-双(萘-1-基)-N,N'-双(苯基)-联苯胺);掺杂有2,2'-(全氟代萘-2,6-二亚基)二丙二腈的α-NPD。所述p型掺杂剂的浓度可以选自1至20重量%,更优选为3重量%至10重量%。
所述HIL的厚度可以在约1nm至约100nm,例如约1nm至约25nm的范围内。当所述HIL的厚度在这个范围内时,所述HIL可以具有出色的空穴注入特性而没有驱动电压的实质性劣化。
空穴传输层
空穴传输层(HTL)可以通过真空沉积、旋涂、狭缝式涂布、印刷、浇注、Langmuir-Blodgett(LB)沉积等形成在所述HIL上。当所述HTL通过真空沉积或旋涂来形成时,用于沉积和涂布的条件可以与用于形成所述HIL的条件相似。然而,用于真空或溶液沉积的条件可以根据用于形成所述HTL的化合物而变化。
所述HTL可以由常用于形成HTL的任何化合物形成。可以适合地使用的化合物公开在例如Yasuhiko Shirota和Hiroshi Kageyama,Chem.Rev.2007,107,953-1010中,并通过引用并入本文。可用于形成所述HTL的化合物的实例是:咔唑衍生物,例如N-苯基咔唑或聚乙烯基咔唑;联苯胺衍生物,例如N,N'-双(3-甲基苯基)-N,N'-二苯基-[1,1-联苯]-4,4'-二胺(TPD)或N,N'-二(萘-1-基)-N,N'-二苯基联苯胺(α-NPD);和基于三苯基胺的化合物,例如4,4',4"-三(N-咔唑基)三苯基胺(TCTA)。在这些化合物中,TCTA可以传输空穴并抑制激子扩散到EML中。
所述HTL的厚度可以在约5nm至约250nm、优选地约10nm至约200nm、更优选地约20nm至约190nm、更优选地约40nm至约180nm、更优选地约60nm至约170nm、更优选地约80nm至约160nm、更优选地约100nm至约160nm、更优选地约120nm至约140nm的范围内。
当所述HTL的厚度在这个范围内时,所述HTL可以具有出色的空穴传输特性而没有驱动电压的实质性劣化。
电子阻挡层
电子阻挡层(EBL)的功能是阻止电子从发光层转移到所述空穴传输层,并因此将电子禁闭到所述发光层。由此提高了效率、工作电压和/或寿命。通常,所述电子阻挡层包含三芳基胺化合物。所述三芳基胺化合物可以具有比所述空穴传输层的LUMO能级更接近真空能级的LUMO能级。所述电子阻挡层可以具有比所述空穴传输层的HOMO能级更远离真空能级的HOMO能级。所述电子阻挡层的厚度可以在2至20nm之间选择。
如果所述电子阻挡层具有高的三重态能级,则它也可以被描述为三重态控制层。
所述三重态控制层的功能是在使用绿色或蓝色磷光发光层的情况下减少三重态的淬灭。由此,可以实现从磷光发光层的更高效率的发光。所述三重态控制层选自三重态能级比相邻发光层中的磷光发光体的三重态能级更高的化合物。用于三重态控制层的适合的化合物、特别是三芳基胺化合物,描述在EP 2 722 908 A1中。
发光层(EML)
所述EML可以通过真空沉积、旋涂、狭缝式涂布、印刷、浇铸、LB沉积等形成在所述HTL上。当所述EML使用真空沉积或旋涂来形成时,用于沉积和涂布的条件可以与用于形成所述HIL的条件相似。然而,用于沉积和涂布的条件可以根据用于形成所述EML的化合物而变化。
所述发光层可以包含式(I)的化合物。
所述EML可以由主体材料与发光体掺杂剂的组合形成。所述EML可以包含单一主体材料或多种主体材料。所述EML可以包含单一发光体掺杂剂或多种发光体掺杂剂。所述主体材料的实例是Alq3、4,4'-N,N'-二咔唑-联苯(CBP)、聚(n-乙烯基咔唑)(PVK)、9,10-二(萘-2-基)蒽(ADN)、4,4',4”-三(咔唑-9-基)-三苯基胺(TCTA)、1,3,5-三(N-苯基苯并咪唑-2-基)苯(TPBI)、3-叔丁基-9,10-二-2-萘基蒽(TBADN)、二(苯乙烯基)芳亚基(DSA)、双(2-(2-羟基苯基)苯并噻唑)锌(Zn(BTZ)2)或式(I)的化合物。
在所述EML包含多种主体材料以形成主体混合物的情况下,所述主体材料的混合物中的每种主体材料的量可以在0.01至99.99重量份之间变化。
所述发光体掺杂剂可以是磷光或荧光发光体。由于它们较高的效率,磷光发光体和通过热激活延迟荧光(TADF)机制发光的发光体是优选的。所述发光体可以是小分子或聚合物。
红光发光体掺杂剂的实例是PtOEP、Ir(piq)3和Btp2lr(acac),但不限于此。这些化合物是磷光发光体,然而也可以使用红色荧光发光体掺杂剂。
绿色磷光发光体掺杂剂的实例是Ir(ppy)3(ppy=苯基吡啶)、Ir(ppy)2(acac)、Ir(mpyp)3。
蓝色磷光发光体掺杂剂的实例是F2Irpic、(F2ppy)2Ir(tmd)和Ir(dfppz)3以及三芴。4.4'-双(4-二苯基氨基苯乙烯基)联苯(DPAVBi)、2,5,8,11-四-叔丁基苝(TBPe)是蓝色荧光发光体掺杂剂的实例。
基于100重量份的主体或主体混合物,所述发光体掺杂剂的量可以在约0.01至约50重量份的范围内。或者,所述发光层可以由发光聚合物构成。所述EML可以具有约10nm至约100nm、例如约20nm至约60nm的厚度。当所述EML的厚度在这一范围内时,所述EML可以具有出色的发光,而没有驱动电压的实质性劣化。
空穴阻挡层(HBL)
可以将空穴阻挡层(HBL)通过使用真空沉积、旋涂、狭缝式涂布、印刷、浇铸、LB沉积等形成在所述EML上,以便阻止空穴扩散到所述ETL中。当所述EML包含磷光掺杂剂时,所述HBL也可以具有三重态激子阻挡功能。所述空穴阻挡层可以是本发明的有机半导体层,其包含由如上所定义的通式(I)表示的本发明的化合物,或者其由所述通式(I)表示的化合物构成。
所述HBL可以是包含所述式(I)的化合物的层(或多个层中的一个)。
所述HBL也可以称为辅助ETL或a-ETL。
当所述HBL使用真空沉积或旋涂来形成时,用于沉积和涂布的条件可以与用于形成所述HIL的条件类似。然而,用于沉积和涂布的条件可以根据用于形成所述HBL的化合物而变化。可以使用常用于形成HBL的任何化合物。用于形成所述HBL的化合物的实例包括二唑衍生物、三嗪衍生物、三唑衍生物和菲咯啉衍生物。
所述HBL可以具有约5nm至约100nm、例如约10nm至约30nm范围内的厚度。当所述HBL的厚度在这一范围内时,所述HBL可以具有出色的空穴阻挡性能,而没有驱动电压的实质性劣化。
电子传输层(ETL)
根据本发明的OLED可以包含电子传输层(ETL)。根据本发明,所述电子传输层可以是包含由如上所定义的通式(I)表示的本发明化合物的本发明有机半导体层。在一个实施方式中,所述ETL可以由式(I)的化合物构成。
根据多种不同实施方式,所述OLED可以包含电子传输层或电子传输层叠层结构,所述叠层结构包含至少一个第一电子传输层和至少一个第二电子传输层。
通过适合地调整所述ETL的特定层的能级,可以控制电子的注入和传输,并且可以高效地阻挡空穴。因此,所述OLED可以具有长寿命。
所述有机电子器件的电子传输层可以包含由如上所定义的通式(I)表示的化合物作为有机电子传输基质(ETM)材料。除了所述由通式(I)表示的化合物之外,所述电子传输层还可以包含本领域中已知的其它ETM材料。同样地,所述电子传输层可以包含所述由通式(I)表示的化合物作为唯一电子传输基质材料。在本发明的有机电子器件包含超过一个电子传输层的情况下,所述由通式(I)表示的化合物可以被包含在所述电子传输层中的仅仅一层中、在所述电子传输层中的超过一个层中、或在所述电子传输层中的所有层中。根据本发明,除了所述ETM材料之外,所述电子传输层还可以包含至少一种如本文中所定义的添加剂。
此外,所述电子传输层可以包含一种或多种n型掺杂剂。添加剂可以是n型掺杂剂。所述添加剂可以是碱金属、碱金属化合物、碱土金属、碱土金属化合物、过渡金属、过渡金属化合物或稀土元素金属。在另一个实施方式中,所述金属可以是选自Li、Na、K、Rb、Cs、Mg、Ca、Sr、Ba、La、Ce、Sm、Eu、Tb、Dy和Yb中的一种。在另一个实施方式中,所述n型掺杂剂可以是选自Cs、K、Rb、Mg、Na、Ca、Sr、Eu和Yb中的一种。在一个实施方式中,所述碱金属化合物可以是8-羟基喹啉锂(LiQ)、四(1H-吡唑-1-基)硼酸锂或2-(二苯基磷酰基)苯酚锂。适合用于ETM的化合物(其可以在除了由如上所定义的通式(I)表示的本发明的化合物之外使用)没有特别限制。在一个实施方式中,所述电子传输基质化合物由共价键合的原子构成。优选地,所述电子传输基质化合物包含至少6个、更优选地至少10个离域电子的共轭体系。在一个实施方式中,所述离域电子的共轭体系可以被包含在芳族或杂芳族结构部分中,正如在例如文献EP 1 970 371 A1或WO 2013/079217 A1中所公开的。
电子注入层(EIL)
可以促进电子从所述阴极的注入的任选的EIL,可以形成在所述ETL上,优选地直接形成在所述电子传输层上。用于形成所述EIL的材料的实例包括在本领域中已知的8-羟基喹啉锂(LiQ)、LiF、NaCl、CsF、Li2O、BaO、Ca、Ba、Yb、Mg。用于形成所述EIL的沉积和涂布条件与用于形成所述HIL的条件类似,但是所述沉积和涂布条件可以根据用于形成所述EIL的材料而变化。所述EIL可以是包含所述式(I)的化合物的有机半导体层。
所述EIL的厚度可以在约0.1nm至约10nm的范围内,例如在约0.5nm至约9nm的范围内。当所述EIL的厚度在这个范围内时,所述EIL可以具有令人满意的电子注入性能,而没有驱动电压的实质性劣化。
阴极
如果存在EIL的话,所述阴极被形成在所述EIL上。所述阴极可以由金属、合金、导电化合物或其混合物形成。所述阴极可以具有低逸出功。例如,所述阴极可以由锂(Li)、镁(Mg)、铝(Al)、铝(Al)-锂(Li)、钙(Ca)、钡(Ba)、镱(Yb)、镁(Mg)-铟(In)、镁(Mg)-银(Ag)等形成。或者,所述阴极可以由透明导电氧化物例如ITO或IZO形成。
所述阴极的厚度可以在约5nm至约1000nm的范围内,例如在约10nm至约100nm的范围内。当所述阴极的厚度在约5nm至约50nm的范围内时,所述阴极可以是透明或半透明的,即使其由金属或金属合金形成。
应该理解,所述阴极不是电子注入层或电子传输层的一部分。
电荷产生层
所述电荷产生层(CGL)可以包含p型和n型层。在所述p型层与n型层之间可以布置中间层。所述CGL可以包含所述由通式(I)表示的化合物。
通常,所述电荷产生层是联结n型电荷产生层(电子产生层)和空穴产生层的p-n结。所述p-n结的n侧产生电子并将它们注入到在朝向阳极的方向上与p-n结相邻的层中。类似地,所述p-n结的p侧产生空穴并将它们注入到在朝向阴极的方向上与p-n结相邻的层中。
电荷产生层可用于串联器件中,例如在两个电极之间包含两个或更多个发光层的串联OLED中。在包含两个发光层的串联OLED中,所述n型电荷产生层为布置在阳极附近的第一发光层提供电子,而所述空穴产生层向布置在所述第一发光层与阴极之间的第二发光层提供空穴。
适合用于所述空穴产生层的基质材料可以是常规用作空穴注入和/或空穴传输基质材料的材料。此外,用于所述空穴产生层的p型掺杂剂可以使用常规材料。例如,所述p型掺杂剂可以是选自四氟-7,7,8,8-四氰基醌二甲烷(F4-TCNQ)、四氰基醌二甲烷的衍生物、轴烯衍生物、碘、FeCl3、FeF3和SbCl5中的一种。此外,主体材料可以是选自N,N'-二(萘-1-基)-N,N-二苯基-联苯胺(NPB)、N,N'-二苯基-N,N'-双(3-甲基苯基)-1,1-联苯-4,4'-二胺(TPD)和N,N',N'-四萘基-联苯胺(TNB)中的一种。所述p型电荷产生层可以由CNHAT构成。
所述n型电荷产生层可以是包含所述式(I)的化合物的层。所述n型电荷产生层可以是纯净n型掺杂剂例如电正性金属的层,或者可以由掺杂有n型掺杂剂的有机基质材料构成。在一个实施方式中,所述n型掺杂剂可以是碱金属、碱金属化合物、碱土金属、碱土金属化合物、过渡金属、过渡金属化合物或稀土元素金属。在另一个实施方式中,所述金属可以是选自Li、Na、K、Rb、Cs、Mg、Ca、Sr、Ba、La、Ce、Sm、Eu、Tb、Dy和Yb中的一种。更具体来说,所述n型掺杂剂可以是选自Cs、K、Rb、Mg、Na、Ca、Sr、Eu和Yb中的一种。适合用于电子产生层的基质材料可以是常规作为基质材料用于电子注入或电子传输层的材料。所述基质材料可以是例如选自三嗪化合物、羟基喹啉衍生物如三(8-羟基喹啉)铝、苯并唑类衍生物和硅杂环戊熳衍生物中的一种。
所述空穴产生层布置成直接接触所述n型电荷产生层。
有机发光二极管(OLED)
根据本发明的有机电子器件可以是有机发光器件。
根据本发明的一个方面,提供了一种有机发光二极管(OLED),其包含:基底,形成在所述基底上的阳极,空穴注入层,空穴传输层,发光层,包含式(I)的化合物或由式(I)的化合物构成的有机半导体层,以及阴极。
根据本发明的另一方面,提供了一种OLED,其包含:基底,形成在所述基底上的阳极,空穴注入层,空穴传输层,电子阻挡层,发光层,空穴阻挡层,包含式(I)的化合物或由式(I)的化合物构成的有机半导体层,以及阴极。
根据本发明的另一方面,提供了一种OLED,其包含:基底,形成在所述基底上的阳极,空穴注入层,空穴传输层,电子阻挡层,发光层,空穴阻挡层,包含式(I)的化合物或由式(I)的化合物构成的有机半导体层,电子注入层,以及阴极。
根据本发明的多种不同实施方式,可以提供布置在上面提到的层之间、在所述基底上或在所述顶部电极上的OLED层。
根据一个方面,所述OLED可以包含下述层结构:基底,其与阳极相邻布置,所述阳极与第一空穴注入层相邻布置,所述第一空穴注入层与第一空穴传输层相邻布置,所述第一空穴传输层与第一电子阻挡层相邻布置,所述第一电子阻挡层与第一发光层相邻布置,所述第一发光层与第一电子传输层相邻布置,所述第一电子传输层与n型电荷产生层相邻布置,所述n型电荷产生层与空穴产生层相邻布置,所述空穴产生层与第二空穴传输层相邻布置,所述第二空穴传输层与第二电子阻挡层相邻布置,所述第二电子阻挡层与第二发光层相邻布置,在所述第二发光层与阴极之间布置任选的电子传输层和/或任选的电子注入层。
根据本发明的有机半导体层可以是发光层、空穴阻挡层、电子传输层、第一电子传输层、n型电荷产生层和/或第二电子传输层。
例如,根据图2的OLED(10)可以通过下述方法形成,其中
在基底(110)上,随后依次形成阳极(120)、空穴注入层(130)、空穴传输层(140)、电子阻挡层(145)、发光层(150)、空穴阻挡层(155)、电子传输层(160)、电子注入层(180)和阴极(190)。
有机电子器件
根据本发明的有机电子器件包含有机半导体层,所述有机半导体层含有根据式(I)的化合物或由式(I)的化合物构成。
根据一个实施方式的有机电子器件可以包括基底、阳极层、包含式(I)的化合物或由式(I)的化合物构成的有机半导体层以及阴极层。
根据一个实施方式的有机电子器件包含至少一个含有至少一种式(I)的化合物或由式(I)的化合物构成的有机半导体层、至少一个阳极层、至少一个阴极层和至少一个发光层,其中所述有机半导体层优选布置在所述发光层与阴极层之间。
根据本发明的有机发光二极管(OLED)可以包括阳极、空穴传输层(HTL)、发光层(EML)、包含至少一种式(I)的化合物的电子传输层(ETL)和阴极,它们被顺序堆叠在基底上。就此而言,所述HTL、EML和ETL是由有机化合物形成的薄膜。
根据一个实施方式的有机电子器件可以是发光器件、薄膜晶体管、电池组、显示设备或光伏电池,优选为发光器件。
根据本发明的一个方面,提供了一种制造有机电子器件的方法,所述方法使用:
-至少一个沉积源,优选地两个沉积源,更优选地至少三个沉积源。
可适合的用于沉积的方法包括:
-通过真空热蒸发的沉积;
-通过溶液加工的沉积,优选地所述加工选自旋涂、印刷、浇铸;和/或
-狭缝式涂布。
根据本发明的多种不同实施方式,提供了一种方法,其使用:
-第一沉积源来释放根据本发明的式(I)的化合物,和
-第二沉积源来释放金属、金属络合物、有机金属化合物、金属盐或碱金属或碱土金属络合物,或有机碱金属或碱土金属络合物,或8-羟基喹啉锂或碱金属硼酸盐;
所述方法包括形成所述有机半导体层的步骤,由此用于有机发光二极管(OLED):
-所述有机半导体层通过以下步骤来形成:从所述第一沉积源释放根据本发明的式(I)的化合物,并从所述第二沉积源释放金属、金属络合物、有机金属化合物、金属盐或碱金属或碱土金属络合物或者有机碱金属或碱土金属络合物或者8-羟基喹啉锂或碱金属硼酸盐。
根据本发明的多种不同实施方式,所述方法还可以包括在所述阳极上形成发光层,并在所述阳极与所述第一电子传输层之间形成至少一个层,所述至少一个层选自形成空穴注入层、形成空穴传输层或形成空穴阻挡层。
根据本发明的多种不同实施方式,所述方法还可以包括用于形成有机发光二极管(OLED)的步骤,其中:
-在基底上形成第一阳极,
-在所述第一阳极上形成发光层,
-在所述发光层上形成电子传输层叠层结构,任选地在所述发光层上形成空穴阻挡层并形成有机半导体层,
-最后形成阴极,
-在所述第一阳极与所述发光层之间依次形成任选的空穴注入层、空穴传输层和空穴阻挡层,
-在所述有机半导体层与所述阴极之间形成任选的电子注入层。
根据本发明的多种不同实施方式,所述方法还可以包括在所述有机半导体层上形成电子注入层。然而,根据本发明的OLED的多种不同实施方式,所述OLED可以不包含电子注入层。
根据多种不同实施方式,所述OLED可以具有下述层结构,其中所述层具有下述顺序:
阳极,空穴注入层,第一空穴传输层,第二空穴传输层,发光层,任选的空穴阻挡层,包含根据本发明的式(I)的化合物的有机半导体层,任选的电子注入层和阴极,或
阳极,空穴注入层,第一空穴传输层,第二空穴传输层,包含根据本发明的式(I)的化合物的有机半导体层,任选的空穴阻挡层,第一电子传输层,任选的电子注入层和阴极,或
阳极,空穴注入层,第一空穴传输层,第二空穴传输层,发光层,包含根据本发明的式(I)的化合物的有机半导体层,第一电子传输层,任选的电子注入层和阴极。
根据本发明的另一方面,提供了一种电子设备,其包含至少一个根据整个本申请中描述的任何实施方式的有机发光器件,优选地,所述电子设备包含在整个本申请中描述的实施方式之一中的有机发光二极管。更优选地,所述电子设备是显示设备。
在一个实施方式中,包含含有根据式(I)的化合物或由式(I)的化合物构成的有机半导体层的根据本发明的有机电子器件,还可以包含含有轴烯化合物和/或醌二甲烷化合物的层。
在一个实施方式中,所述轴烯化合物和/或醌二甲烷化合物可以被一个或多个卤素原子和/或一个或多个吸电子基团取代。吸电子基团可以选自腈基团、卤代烷基,可替选地选自全卤代烷基,可替选地选自全氟代烷基。吸电子基团的其它实例可以是酰基、磺酰基或磷酰基。
可替选地,酰基、磺酰基和/或磷酰基可以包含卤代和/或全卤代烃基。在一个实施方式中,所述全卤代烃基可以是全氟代烃基。全氟代烃基的实例可以是全氟代甲基、全氟代乙基、全氟代丙基、全氟代异丙基、全氟代丁基、全氟代苯基、全氟代甲苯基;包含卤代烃基的磺酰基的实例可以是三氟甲基磺酰基、五氟乙基磺酰基、五氟苯基磺酰基、七氟丙基磺酰基、九氟丁基磺酰基等。
在一个实施方式中,所述轴烯和/或醌二甲烷化合物可以被包含在空穴注入、空穴传输和/或空穴产生层中。
在一个实施方式中,所述轴烯化合物可以具有式(XX),和/或所述醌二甲烷化合物可以具有式(XXIa)或(XXIb):
其中R1、R2、R3、R4、R5、R6、R7、R8、R11、R12、R15、R16、R20、R21独立地选自上面提到的吸电子基团,并且R9、R10、R13、R14、R17、R18、R19、R22、R23和R24独立地选自H、卤素和上面提到的吸电子基团。
在下文中,参考实施例对实施方式进行更详细的说明。然而,本公开不限于下述实施例。现在将详细参考所述示例性方面。
本发明的详情和定义
术语“稠合环”在本文中用于指称一种结合状况,其中两个相邻的R1至R11例如R1与R2、或R2与R3、或R3与R4一起形成稠合到具有式(I)的结构的其余部分的环。
在本说明书中,当没有另外提供定义时,“烷基”可以是指脂族烃类基团。烷基可以是指没有任何双键或叁键的“饱和烷基”。当在本文中使用时,术语“烷基”将涵盖直链以及支链和环状的烷基。例如,C3-烷基可以选自正丙基和异丙基。同样地,C4-烷基涵盖了正丁基、仲丁基和叔丁基。同样地,C6-烷基涵盖正己基和环己基。
Cn中的下标数字n涉及相应的烷基、芳亚基、杂芳亚基或芳基中碳原子的总数。
当在本文中使用时,术语“芳基”或“芳亚基”将涵盖苯基(C6-芳基)、稠合的芳族化合物例如萘、蒽、菲、并四苯等。还涵盖联苯和寡聚苯或多聚苯,例如三联苯等。还将涵盖任何其它芳族烃类取代基例如芴基等。“芳亚基”和相应的“杂芳亚基”是指连接有另外两个部分的基团。在本说明书中,术语“芳基”或“芳亚基”可以是指包含至少一个芳族烃类部分的基团,并且所述芳族烃类部分的所有元素都可以具有形成共轭的p轨道,例如苯基、萘基、蒽基、菲基、芘基、芴基等。所述芳基或芳亚基可以包括单环或稠合环多环(即共有相邻的碳原子对的环)官能团。
当在本文中使用时,术语“杂芳基”是指其中至少一个碳原子被优选地选自N、O、S、B或Si的杂原子代替的芳基。
术语“杂芳基”可以是指具有至少一个杂原子的芳族杂环,并且所述杂芳族烃类部分的所有元素可以具有形成共轭的p-轨道。所述杂原子可以选自N、O、S、B、Si、P、Se,优选地选自N、O和S。杂芳亚基环可以包含至少1至3个杂原子。优选地,杂芳亚基环可以包含至少1至3个各自选自N、S和/或O的杂原子。
在本说明书中,单键是指直接键。
当在本文中使用时,术语“氟代”是指烃类基团,其中所述烃类基团中包含的至少一个氢原子被氟原子取代。其中所有氢原子都被氟原子取代的氟代基团被称为全氟代基团,并特别用术语“全氟代”指称。
根据本发明,如果一个基团中包含的氢原子之一被另一个基团代替,则该基团被另一个基团“取代”,其中所述另一个基团是取代基。
根据本发明,对于一个层在另外两个层之间而言,表述“之间”不排除可布置在所述一个层与所述另外两个层之一之间的其它层的存在。根据本发明,对于两个层彼此直接接触而言,表述“直接接触”意味着在那两个层之间没有布置其它层。一个层被沉积在另一个层顶部被视为与该层直接接触。
对于本发明的有机半导体层以及对于本发明的化合物而言,在实验部分中提到的化合物是最优选的。
本发明的有机电子器件可以是有机电致发光器件(OLED)、有机光伏器件(OPV)、照明设备或有机场效应晶体管(OFET)。照明设备可以是用于照明、辐射、发信号或投影的任何设备。它们被相应地分类为照明、辐射、信号和投影设备。照明设备通常由下述部分构成:光学辐射源,将辐射通量以所需方向传输到空间中的装置,以及将部件连接成单个设备并保护辐射源和光传输系统不受损坏和环境影响的外壳。
根据另一方面,根据本发明的有机电致发光器件可以包含超过一个发光层,优选地两个或三个发光层。包含超过一个发光层的OLED也被描述为串联OLED或堆叠OLED。
所述有机电致发光器件(OLED)可以是底部发光或顶部发光器件。
另一方面涉及一种包含至少一个有机电致发光器件(OLED)的设备。
包含有机发光二极管的设备是例如显示器或照明板。
在本发明中,下面将定义术语,除非在权利要求书中或本说明书中的别处给出不同的定义,否则将以这些定义为准。
在本说明书的上下文中,与基质材料相关的术语“不同”或“差异”意味着所述基质材料在它们的结构式上不同。
术语“OLED”和“有机发光二极管”被同时使用并具有相同含义。当在本文中使用时,术语“有机电致发光器件”可以包含有机发光二极管和有机发光晶体管(OLET)两者。
当在本文中使用时,“重量百分数”、“wt.-%”、“以重量计的百分数”、“重量%”、“重量份”及其变化形式是将组合物、组分、物质或试剂表示为相应的电子传输层的该组分、物质或试剂的重量除以所述相应电子传输层的总重量并乘以100。应该理解,相应的电子传输层和电子注入层的所有组分、物质和试剂的总重量百分数的量被选择成使其不超过100重量%。
当在本文中使用时,“体积百分数”、“vol.-%”、“以体积计的百分数”、“体积%”及其变化形式是将组合物、组分、物质或试剂表示为相应的电子传输层的该组分、物质或试剂的体积除以所述相应电子传输层的总体积并乘以100。应该理解,所述阴极层的所有组分、物质和试剂的总体积百分数的量被选择成使其不超过100体积%。
本文中的所有数值被假定用术语“约”修饰,不论是否明确指示。当在本文中使用时,术语“约”是指数值量可以发生的变化。不论是否用术语“约”修饰,权利要求都包括所述量的等同量。
应该指出,当在本说明书和权利要求书中使用时,单数形式“一个”、“一种”、“该”和“所述”包括复数指称物,除非上下文明确指明不是如此。
术语“没有”、“不含”、“不包括”不排除杂质。杂质对通过本发明所实现的目的而言没有技术效果。
在本说明书的上下文中,术语“基本上不发光”或“不发光”意味着所述化合物或层对来自于所述器件的可见发光光谱的贡献相对于所述可见发光光谱低于10%,优选地低于5%。所述可见发光光谱是波长为约≥380nm至约≤780nm的发光光谱。
优选地,包含所述式I的化合物的有机半导体层是基本上不发光或不发光的。
工作电压,也被称为U,在10毫安每平方厘米(mA/cm2)下以伏特(V)为单位测量。
每安培的坎德拉效率,也被称为cd/A效率,在10毫安每平方厘米(mA/cm2)下以坎德拉/安培为单位测量。
外量子效率,也被称为EQE,以百分数(%)为单位度量。
颜色空间通过坐标CIE-x和CIE-y(国际照明委员会(International Commissionon Illumination 1931)来描述。对于蓝色发光来说,CIE-y是特别重要的。更小的CIE-y表示更深的蓝色。
最高占据分子轨道,也被称为HOMO,和最低未占分子轨道,也被称为LUMO,以电子伏特(eV)为单位度量。
术语“OLED”、“有机发光二极管”、“有机发光器件”和“有机光电器件”被同时使用并具有相同含义。
术语“使用期限”和“寿命”被同时使用并具有相同含义。
所述阳极和阴极可以被描述为阳极/阴极或阳极电极/阴极电极或阳极层/阴极层。
室温,也被称为环境温度,是23℃。
附图说明
与附图结合,从下面示例性实施方式的描述,本发明的这些和/或其它方面和优点将变得明显并且更容易理解,在所述附图中:
图1是根据本发明的一个示例性实施方式的有机发光二极管(OLED)的示意性剖视图。
图2是根据本发明的一个示例性实施方式的OLED的示意性剖视图。
图3是根据本发明的一个示例性实施方式的包含电荷产生层的串联OLED的示意性剖视图。
具体实施方式
现在将详细参考本发明的示例性实施方式,其实例在附图中示出,其中相同的附图标记数字始终指相同的元件。为了解释本发明的多种情况,下面参考附图来描述所述示例性实施方式。
在本文中,当第一元件被称为是形成或布置在第二元件“上”时,所述第一元件可以被直接布置在所述第二元件上,或者可以在它们之间布置一个或多个其它元件。当第一元件被称为是“直接”形成或布置在第二元件“上”时,在它们之间不配置其它元件。
图1是根据本发明的一个示例性实施方式的有机发光二极管(OLED)100的示意性剖视图。OLED 100包括基底110、阳极120、空穴注入层(HIL)130、空穴传输层(HTL)140、发光层(EML)150、电子传输层(ETL)160。电子传输层(ETL)160形成在EML 150上。在电子传输层(ETL)160上布置电子注入层(EIL)180。阴极190被直接布置在电子注入层(EIL)180上。
代替单个电子传输层160,可以任选地使用电子传输层叠层结构(ETL)。
图2是根据本发明的另一个示例性实施方式的OLED 100的示意性剖视图。图2与图1的区别在于图2的OLED 100包含电子阻挡层(EBL)145和空穴阻挡层(HBL)155。
参考图2,OLED 100包括基底110、阳极120、空穴注入层(HIL)130、空穴传输层(HTL)140、电子阻挡层(EBL)145、发光层(EML)150、空穴阻挡层(HBL)155、电子传输层(ETL)160、电子注入层(EIL)180和阴极190。
优选地,所述包含式(I)的化合物或由式(I)的化合物构成的有机半导体层可以是EML、HBL或ETL。
图3是根据本发明的另一个示例性实施方式的串联OLED 200的示意性剖视图。图3与图2的区别在于图3的OLED 200还包含电荷产生层(CGL)和第二发光层(151)。
参考图3,OLED 200包括基底110、阳极120、第一空穴注入层(HIL)130、第一空穴传输层(HTL)140、第一电子阻挡层(EBL)145、第一发光层(EML)150、第一空穴阻挡层(HBL)155、第一电子传输层(ETL)160、n型电荷产生层(n型CGL)185、空穴产生层(p型电荷产生层、p型GCL)135、第二空穴传输层(HTL)141、第二电子阻挡层(EBL)146、第二发光层(EML)151、第二空穴阻挡层(EBL)156、第二电子传输层(ETL)161、第二电子注入层(EIL)181和阴极190。
优选地,所述包含式(I)的化合物或由式(I)的化合物构成的有机半导体层可以是所述第一EML、第一HBL、第一ETL、n型CGL和/或第二EML、第二HBL、第二ETL。
尽管在图1、图2和图3中未示出,但可以在阴极190上进一步形成密封层,以便密封OLED 100和200。此外,可以对其进行多种不同的其它修改。
在后文中,将参考下述实施例详细描述本发明的一个或多个示例性实施方式。然而,这些实施例不意欲限制本发明的所述一个或多个示例性实施方式的目的和范围。
实验部分
通过下述实施例进一步说明本发明,所述实施例仅仅是说明性而不是限制性的。
式(I)的化合物的合成
9-(3-(二苯并[c,h]吖啶-7-基)苯基)-9H-咔唑-3-甲腈(化合物5)
mmol)和K2CO3(15.9g,115mmol)。添加脱气的1,4-二烷/水(3:1,240mL)的混合物,并将所述反应混合物在氮气气氛下加热至95℃持续16h。在冷却至室温后,通过抽滤收集形成的沉淀物并将其用1,4-二烷、水和甲醇洗涤。将得到的固体溶解在热的二氯甲烷中,并通过硅胶垫过滤。在用另外的热的二氯甲烷清洗后,将滤液在减压下浓缩并添加正己烷。通过抽滤收集得到的沉淀物并用正己烷洗涤。在干燥后,得到19.2g(91%)浅黄色固体。HPLC/ESI-MS:100%,m/z=546([M+H]+)。
7-(4-(3,6-二苯基-9H-咔唑-9-基)苯基)二苯并[c,h]吖啶(化合物4)
7-(4-溴苯基)二苯并[c,h]吖啶(10g,23mmol)、3,6-二苯基-9H-咔唑(8.8g,27.6mmol)、K2CO3(9.5g,69mmol)、18-冠-6(1.2g,0.46mmol)和另外的脱气邻二甲苯(200mL)。将得到的反应混合物在氮气气氛下加热至回流48h。在冷却至10℃后,通过抽滤收集形成的沉淀物并将其用正己烷洗涤。将得到的固体溶解在氯仿中并用水萃取5次。用MgSO4干燥后,将有机相过滤,在减压下浓缩并添加正己烷。通过抽滤收集得到的沉淀物并用正己烷洗涤。进一步的纯化通过从甲苯中重结晶来实现。在干燥后,得到11.7g(76%)的浅黄色固体。最后的纯化通过升华来实现。HPLC/ESI-MS:99.6%,m/z=673([M+H]+)。
7-(9'-苯基-9H,9'H-[3,3'-联咔唑]-9-基)二苯并[c,h]吖啶(化合物6)
应混合物在110℃搅拌4小时。将反应用甲醇(100mL)淬灭,将形成的沉淀物过滤并用甲醇洗涤。将得到的固体溶解在氯仿/甲苯1/1(500mL)中,并通过硅胶垫过滤。在用另外的氯仿/甲苯1/1清洗后,将滤液在减压下浓缩,并将悬浮液在室温下搅拌过夜。通过抽滤收集得到的沉淀物并将其用甲苯洗涤。将粗品固体溶解在热THF中,缓慢添加乙醇,并将悬浮液在室温下搅拌过夜。通过抽滤收集得到的沉淀物并将其通过柱层析进一步纯化(用二氯甲烷/己烷1/3到最终的纯二氯甲烷来洗脱)。将固体溶解在热THF中,缓慢添加乙醇,并将悬浮液在室温下搅拌过夜,然后过滤固体。在干燥后,得到8.8g(52%)固体。最终的纯化通过升华来实现。HPLC/ESI-MS:100%,m/z=686([M+H]+)。
N-(3-(二苯并[c,h]吖啶-7-基)苯基)-N-苯基萘-2-胺(化合物7)
混合物在氮气气氛下加热至80℃持续5小时。在冷却至室温后,通过抽滤收集形成的沉淀物并将其用甲苯洗涤。将得到的固体在室温下在水中搅拌30分钟,然后将它过滤,用水洗涤并干燥。将粗品固体溶解在甲苯中,并通过硅胶垫过滤。在用另外的甲苯清洗后,将滤液在减压下浓缩,并将悬浮液在室温下搅拌过夜。通过抽滤收集得到的沉淀物并将其用正己烷洗涤。进一步的纯化通过从丙酮中重结晶来实现。最后,将固体溶解在热甲苯中,缓慢添加正己烷,并将悬浮液在室温下搅拌过夜,然后过滤出固体。在干燥后,得到8.5g(64%)固体。最终的纯化通过升华来实现。HPLC/ESI-MS:100%,m/z=573([M+H]+)。
制造OLED的程序
对于A型和B型顶部发光OLED器件(顶部发光器件)来说,将尺寸为150mm×150mm×0.7mm的玻璃基底用Deconex FPD 211的2%水溶液超声清洁7分钟,然后用纯水超声清洁5分钟,并在清洗旋干机中干燥15分钟。随后,在10-5至10-7mbar的压力下沉积100nm的Ag作为阳极。对于底部发光OLED器件即C型OLED器件来说,使用UV-臭氧清洁的ITO/玻璃基底代替玻璃基底。
然后,将HT-1和D-1以92:8的重量%比例真空共沉积在所述阳极上,以形成HIL。然后将HT-1真空沉积在所述HIL上,以形成HTL。然后将HT-2真空沉积在所述HTL上,以形成电子阻挡层(EBL)。
随后,通过将主体-1和发光体-1以97:3的重量%比例共沉积,在所述EBL上形成发光层。
然后,对于A型顶部发光OLED器件来说,将ET-1真空沉积在所述发光层上,以形成空穴阻挡层(HBL)。然后,通过将式(I)的化合物或比较化合物-1与喹啉锂(LiQ)以1:1的重量%比例共沉积,在所述空穴阻挡层上形成电子传输层。
对于B型顶部发光OLED器件来说,将式(I)的化合物真空沉积在所述发光层上,以形成空穴阻挡层。然后,通过将ET-2与喹啉锂(LiQ)以1:1的重量%比例共沉积,在所述空穴阻挡层上形成电子传输层。
然后,对于A型和B型顶部发光OLED器件两者来说,通过沉积Yb在所述电子传输层上形成电子注入层。
在所述阴极上形成N-([1,1'-联苯]-4-基)-9,9-二甲基-N-(4-(9-苯基-9H-咔唑-3-基)苯基)-9H-芴-2-胺的覆盖层。
对于底部发光OLED器件即C型OLED器件来说,将HT-1和D-1以97:3的重量%比例真空共沉积在所述ITO上,以形成HIL。然后将HT-1真空沉积在所述HIL上,以形成HTL。然后将HT-3真空沉积在所述HTL上,以形成电子阻挡层(EBL)。
随后,通过将主体-2:式(I)的化合物:发光体-2以49:49:2的重量%比例共沉积,来沉积发光层。
随后,将ET-1真空沉积在所述发光层上,以形成空穴阻挡层。然后,通过将ET-2与喹啉锂(LiQ)以1:1的重量%比例共沉积,在所述空穴阻挡层上形成电子传输层。
然后,通过沉积LiQ在所述电子传输层上形成电子注入层。
实施例
表1:在ETL、辅助ETL或EML中包含式1的化合物的有机电致发光器件的性能。
制备3种类型(A、B和C)的OLED器件,以便测试本发明的式(I)的化合物。所述OLED器件中层堆叠的详情在下文给出。斜线“/”将各个层分开。层厚度提供在方括号[…]中,以重量%计的混合比例提供在圆括号(…)中:
A型OLED器件:所述式(I)的化合物或比较化合物被包含在电子传输层中。层堆叠:银[100nm]/HT-1:D-1(92:8)[10nm]/HT-1[118nm]/HT-2[5nm]/主体-1:发光体-1(97:3)[20nm]/ET-1[5nm]/式(I)的化合物:LiQ或比较化合物:LiQ(1:1)[31nm]/Yb[2nm]/银[11nm]
B型OLED器件:所述式(I)的化合物被包含在空穴阻挡层中。层堆叠:银[100nm]/HT-1:D-1(92:8)[10nm]/HT-1[125nm]/HT-2[5nm]/主体-1:发光体-1(97:3)[20nm]/式(I)的化合物[5nm]/ET-2:LiQ(1:1)[31nm]/Yb[2nm]/银[11nm]
C型OLED器件:所述式(I)的化合物被包含在发光层中。层堆叠:ITO/HT-1:D-1(97:3)[10nm]/HT-1[144nm]/HT-3[70nm]/主体-2:式(I)的化合物:发光体-2(49:49:2)[40nm]/ET-1[5nm]/ET-2:LiQ(1:1)[31nm]/LiQ[2nm]/银[100nm]
发明的技术效果
在下面的表1中,示出了式(I)的化合物和比较化合物的材料性能。
在下面的表2中,示出了式(I)的化合物的偶极矩、HOMO能级和LUMO能级以及能隙LUMO–HOMO。式(I)的化合物具有低于3.89eV的能隙LUMO–HOMO。
在下面的表3中,示出了包含式(I)的化合物的OLED在30mA/cm2下的工作电压和寿命LT97(h)。
从表3明显看出,与比较例相比,所有实施例1至9在30mA/cm2下的工作寿命LT97(h)提高至少28%或更多。不受理论的限制,LT的提高可能是由于在OLED制造期间式(I)的化合物的降解减少导致的。
使用的化合物列表
表1:式(I)的化合物和比较化合物的性质
表2.通过DFT(B3LYP_Gaussian/6-31G*,气相)模拟的式(I)的化合物和比较化合物的偶极矩、HOMO和LUMO能级、能隙LUMO–HOMO
表3.包含式1的化合物和比较化合物的OLED器件
前述说明书和从属权利要求中公开的特征,可以单独地和以其任何组合作为用于以各种不同形式实现独立权利要求中所公开的方面的材料。
Claims (15)
1.一种式(I)的化合物
其中所有的R1至R11,除了一个之外,都独立地选自H、D、F、取代或未取代的C1至C18烷基、取代或未取代的C6至C42芳基、取代或未取代的C3至C42杂芳基,并且相邻的基团R1至R11可以彼此连接以形成稠合环,
其中R1至R11中不选自上述基团的一个是基团G,其中
-所述基团G包含一个在其p-轨道中具有电子对的原子A;
-所述基团G包含连接到所述原子A的两个6元芳基环,其中所述两个6元芳基环中的每个分别通过单键连接到所述原子A,并且其中连接到所述原子A的所述两个6元芳基环可以通过单键彼此连接;
-所述基团G包含总共12至66个碳原子;
-所述基团G通过单键或通过C6至C18芳亚基连接到所述式(I)的化合物的苯并吖啶部分,其中所述C6至C18芳亚基是所述基团G的一部分;并且
-所述基团G是未取代的或者被一个或多个取代基取代,所述取代基独立地选自D、F、C1至C18烷基、C6至C42芳基、C6至C42杂芳基、(R12)2P=O、CN或G’,其中所述基团G’与所述基团G定义相同,区别在于所述基团G’不被连接到所述式(I)的化合物的苯并吖啶部分,而是通过单键或通过C6至C18芳亚基连接到所述基团G,其中所述C6至C18芳亚基是所述基团G’的一部分,前提是在所述基团G通过所述C6至C18芳亚基连接到所述式(I)的化合物的苯并吖啶部分的情况下,可以连接到所述C6至C18芳亚基的取代基只选自C1至C18烷基、C6至C42芳基、(R12)2P=O和CN;
其中在不是所述基团G的R1至R11中的至少一个被取代的情况下,相应的一个或多个取代基独立地选自D、F、C1至C18烷基、C6至C36芳基、C6至C42杂芳基、(R12)2P=O、CN;并且
其中R12独立地选自C1至C18烷基和C6至C24芳基。
2.根据权利要求1所述的化合物,其中所述基团G包含1至5个选自N、S和O的杂原子。
3.根据权利要求1所述的化合物,其中所述原子A选自N、S和O。
4.根据权利要求1所述的化合物,其中所述基团G包含所述原子A和以二芳基氨基形式或以咔唑基形式连接到所述原子A的所述两个6元芳基环。
5.根据权利要求1所述的化合物,其中包含在所述式(I)的化合物中的芳族环的总数为6至21。
6.根据权利要求1所述的化合物,其中R1与R2、或R2与R3、或R3与R4连接以形成芳基环结构。
7.根据权利要求1所述的化合物,其中R5或R10是所述基团G。
8.一种有机电子器件,所述有机电子器件包含有机半导体层,其中所述有机半导体层包含根据前述权利要求中的任一项所述的式(I)的化合物。
9.根据权利要求8所述的有机电子器件,所述有机电子器件还包含第一电极和第二电极,其中所述有机半导体层布置在所述第一电极与所述第二电极之间。
10.根据权利要求8所述的有机电子器件,其中所述有机半导体层是发光层。
11.根据权利要求8所述的有机电子器件,其中所述有机半导体层是空穴阻挡层。
12.根据权利要求8所述的有机电子器件,其中所述有机半导体层是电子传输层。
13.根据权利要求8所述的有机电子器件,其中所述有机半导体层还包含至少一种不是式(I)的化合物的第二化合物。
14.一种显示设备,所述显示设备包含根据权利要求8所述的有机电子器件。
15.一种照明设备,所述照明设备包含根据权利要求8所述的有机电子器件。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP18206770.2A EP3653619A1 (en) | 2018-11-16 | 2018-11-16 | Compound, organic electronic device comprising the same, and display device and lighting device comprising the same |
| EP18206770.2 | 2018-11-16 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN111196802A true CN111196802A (zh) | 2020-05-26 |
Family
ID=64331933
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201911117538.XA Pending CN111196802A (zh) | 2018-11-16 | 2019-11-15 | 化合物、包含所述化合物的有机电子器件和包含所述有机电子器件的显示设备和照明设备 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US11539001B2 (zh) |
| EP (1) | EP3653619A1 (zh) |
| KR (1) | KR20200057657A (zh) |
| CN (1) | CN111196802A (zh) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN110183381A (zh) * | 2019-06-28 | 2019-08-30 | 上海天马有机发光显示技术有限公司 | 一种化合物、oled显示面板以及电子设备 |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3726599B1 (en) * | 2019-04-15 | 2022-03-23 | Novaled GmbH | Compound, organic semiconducting material comprising the same, organic electronic device comprising the same, and display device and lighting device comprising the same |
| CN114975839B (zh) * | 2022-07-26 | 2022-10-28 | 吉林奥来德光电材料股份有限公司 | 一种有机电致发光器件、有机电致发光装置及光电设备 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2011154131A1 (en) * | 2010-06-10 | 2011-12-15 | Novaled Ag | Electronic device comprising an organic semiconducting material |
| WO2015083948A1 (ko) * | 2013-12-03 | 2015-06-11 | 덕산네오룩스 주식회사 | 유기전기 소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| CN103539737B (zh) * | 2013-10-23 | 2017-03-08 | Tcl集团股份有限公司 | 一种氮杂菲并芴类衍生物、制备方法及电致荧光发光器件 |
| CN104672211B (zh) * | 2015-01-23 | 2017-11-17 | 固安鼎材科技有限公司 | 一种苯并吖啶衍生物、其制备方法及其应用 |
| CN107619391A (zh) * | 2016-07-13 | 2018-01-23 | 三星显示有限公司 | 杂环化合物和包括该杂环化合物的有机发光器件 |
Family Cites Families (25)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| TWI314947B (en) * | 2002-04-24 | 2009-09-21 | Eastman Kodak Compan | Organic light emitting diode devices with improved operational stability |
| DE102004010954A1 (de) | 2004-03-03 | 2005-10-06 | Novaled Gmbh | Verwendung eines Metallkomplexes als n-Dotand für ein organisches halbleitendes Matrixmaterial, organisches Halbleitermaterial und elektronisches Bauteil |
| US8415473B2 (en) * | 2004-10-29 | 2013-04-09 | Versitech Limited | Luminescent gold(III) compounds for organic light-emitting devices and their preparation |
| DE502006000749D1 (de) | 2006-03-21 | 2008-06-19 | Novaled Ag | Heterocyclisches Radikal oder Diradikal, deren Dimere, Oligomere, Polymere, Dispiroverbindungen und Polycyclen, deren Verwendung, organisches halbleitendes Material sowie elektronisches Bauelement |
| DE102007012794B3 (de) | 2007-03-16 | 2008-06-19 | Novaled Ag | Pyrido[3,2-h]chinazoline und/oder deren 5,6-Dihydroderivate, deren Herstellungsverfahren und diese enthaltendes dotiertes organisches Halbleitermaterial |
| EP3457451B1 (de) | 2007-04-30 | 2019-07-17 | Novaled GmbH | Die verwendung von oxokohlenstoff-, pseudooxokohlenstoff- und radialenverbindungen |
| CN104247070B (zh) * | 2011-11-30 | 2017-04-12 | 诺瓦尔德股份有限公司 | 显示器 |
| EP2722908A1 (en) | 2012-10-17 | 2014-04-23 | Novaled AG | Phosphorescent OLED and hole transporting materials for phosphorescent OLEDs |
| JP2014096418A (ja) | 2012-11-07 | 2014-05-22 | Idemitsu Kosan Co Ltd | 有機エレクトロルミネッセンス素子および電子機器 |
| KR101684979B1 (ko) | 2012-12-31 | 2016-12-09 | 제일모직 주식회사 | 유기광전자소자 및 이를 포함하는 표시장치 |
| KR101537500B1 (ko) | 2014-04-04 | 2015-07-20 | 주식회사 엘지화학 | 유기 발광 소자 |
| EP3093288A1 (en) | 2015-05-12 | 2016-11-16 | Novaled GmbH | Organic light-emitting diode comprising different matrix compounds in the first and second electron transport layer |
| KR101888934B1 (ko) | 2015-04-24 | 2018-08-16 | 삼성에스디아이 주식회사 | 유기 광전자 소자용 화합물, 유기 광전자 소자 및 표시장치 |
| US9859503B2 (en) | 2015-04-30 | 2018-01-02 | Samsung Display Co., Ltd. | Organic light-emitting device |
| KR101826427B1 (ko) * | 2015-06-05 | 2018-02-06 | 주식회사 엘지화학 | 이중 스피로형 유기 화합물 및 이를 포함하는 유기 전자 소자 |
| US10897014B2 (en) * | 2016-07-13 | 2021-01-19 | Samsung Display Co., Ltd. | Heterocyclic compound and organic light-emitting device including the same |
| EP3291319B1 (en) * | 2016-08-30 | 2019-01-23 | Novaled GmbH | Method for preparing an organic semiconductor layer |
| EP3312899B1 (en) * | 2016-10-24 | 2021-04-07 | Novaled GmbH | Electron transport layer stack for an organic light-emitting diode |
| EP3312896B1 (en) * | 2016-10-24 | 2021-03-31 | Novaled GmbH | Organic electroluminescent device comprising a redox-doped electron transport layer and an auxiliary electron transport layer |
| EP3369729B1 (en) * | 2017-03-02 | 2022-01-12 | Novaled GmbH | Fused 9-phenyl-acridine derivatives for use in an electronic device and display device |
| EP3425692B1 (en) * | 2017-07-07 | 2023-04-05 | Novaled GmbH | Organic electroluminescent device comprising an electron injection layer with zero-valent metal |
| EP3503242B1 (en) * | 2017-12-22 | 2021-08-25 | Novaled GmbH | Semiconducting material, a method for preparing the same and electronic device |
| EP3556753B1 (en) * | 2018-04-18 | 2023-10-11 | Novaled GmbH | Compound and organic semiconducting layer, organic electronic device, display device and lighting device comprising the same |
| EP3895227B1 (en) * | 2018-12-14 | 2023-10-11 | Novaled GmbH | Organic electroluminescent device and a solid composition for use therein |
| EP3683223B1 (en) * | 2019-01-17 | 2021-06-16 | Novaled GmbH | Compound and organic electronic device comprising the same |
-
2018
- 2018-11-16 EP EP18206770.2A patent/EP3653619A1/en active Pending
-
2019
- 2019-11-14 US US16/683,508 patent/US11539001B2/en active Active
- 2019-11-15 CN CN201911117538.XA patent/CN111196802A/zh active Pending
- 2019-11-15 KR KR1020190146916A patent/KR20200057657A/ko not_active Application Discontinuation
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2011154131A1 (en) * | 2010-06-10 | 2011-12-15 | Novaled Ag | Electronic device comprising an organic semiconducting material |
| CN103539737B (zh) * | 2013-10-23 | 2017-03-08 | Tcl集团股份有限公司 | 一种氮杂菲并芴类衍生物、制备方法及电致荧光发光器件 |
| WO2015083948A1 (ko) * | 2013-12-03 | 2015-06-11 | 덕산네오룩스 주식회사 | 유기전기 소자용 화합물, 이를 이용한 유기전기소자 및 그 전자 장치 |
| CN104672211B (zh) * | 2015-01-23 | 2017-11-17 | 固安鼎材科技有限公司 | 一种苯并吖啶衍生物、其制备方法及其应用 |
| CN107619391A (zh) * | 2016-07-13 | 2018-01-23 | 三星显示有限公司 | 杂环化合物和包括该杂环化合物的有机发光器件 |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN110183381A (zh) * | 2019-06-28 | 2019-08-30 | 上海天马有机发光显示技术有限公司 | 一种化合物、oled显示面板以及电子设备 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3653619A1 (en) | 2020-05-20 |
| US11539001B2 (en) | 2022-12-27 |
| US20200161565A1 (en) | 2020-05-21 |
| KR20200057657A (ko) | 2020-05-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN110462872B (zh) | 电子器件、所述电子器件的制备方法和包含所述电子器件的显示装置 | |
| CN107452896B (zh) | 包含有机半导体层的有机发光二极管 | |
| CN113228325B (zh) | 有机电致发光器件以及用于其中的固体组合物 | |
| EP3895226B1 (en) | Organic light emitting device and a compound for use therein | |
| CN116171059A (zh) | 包含有机半导体层的有机发光二极管 | |
| KR20180132848A (ko) | 유기 반도체 층을 포함하는 유기 발광 다이오드 | |
| CN115413374A (zh) | 有机发光二极管和包括其的装置 | |
| KR20190039014A (ko) | 전자 디바이스 및 이를 제조하는 방법 | |
| CN111770922A (zh) | 有机电子器件、包含有机电子器件的显示和照明装置 | |
| CN113228334A (zh) | 有机发光器件,其制造方法,以及用于其中的组合物 | |
| CN111788177A (zh) | 螺苯并蒽-芴衍生物以及它们在有机电子器件、显示和照明装置中的应用 | |
| US11539001B2 (en) | Compound, organic electronic device comprising the same, and display device and lighting device comprising the same | |
| CN115362571A (zh) | 有机发光二极管以及包含其的器件 | |
| CN113597420A (zh) | 化合物和包含该化合物的有机半导体层、有机电子器件和显示或照明装置 | |
| CN113490672A (zh) | 化合物和包含该化合物的有机电子器件 | |
| CN110911571A (zh) | 有机电子器件、有机半导体材料和硼烷化合物 | |
| CN113728454B (zh) | 化合物、包含所述化合物的有机半导体材料、包含所述材料的有机电子器件和包含所述有机电子器件的显示器件和照明器件 | |
| CN113728454A (zh) | 化合物、包含所述化合物的有机半导体材料、包含所述材料的有机电子器件和包含所述有机电子器件的显示器件和照明器件 | |
| CN115836599A (zh) | 化合物、所述化合物的中间体、所述化合物的制备方法、包含所述化合物的有机半导体材料、包含所述有机半导体材料的有机电子器件以及包含所述有机电子器件的显示器件和照明器件 | |
| CN117413634A (zh) | 有机电致发光器件和其中使用的化合物 | |
| CN117917206A (zh) | 有机发光二极管以及用于其中的化合物 | |
| CN118434821A (zh) | 有机发光二极管和包含其的装置 | |
| CN118303147A (zh) | 有机电子器件和化合物 | |
| CN118414894A (zh) | 有机发光二极管、其制备方法和包含其的器件 | |
| CN113874370A (zh) | 化合物和包含所述化合物的有机半导体层、有机电子器件和显示或照明装置 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination |