CN107011348B - 作为btk活性的抑制剂的杂芳基吡啶酮和氮杂-吡啶酮化合物 - Google Patents
作为btk活性的抑制剂的杂芳基吡啶酮和氮杂-吡啶酮化合物 Download PDFInfo
- Publication number
- CN107011348B CN107011348B CN201710227680.4A CN201710227680A CN107011348B CN 107011348 B CN107011348 B CN 107011348B CN 201710227680 A CN201710227680 A CN 201710227680A CN 107011348 B CN107011348 B CN 107011348B
- Authority
- CN
- China
- Prior art keywords
- cancer
- methyl
- pyridin
- oxo
- och
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/12—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains three hetero rings
- C07D487/14—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/496—Non-condensed piperazines containing further heterocyclic rings, e.g. rifampin, thiothixene
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/4965—Non-condensed pyrazines
- A61K31/497—Non-condensed pyrazines containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/4985—Pyrazines or piperazines ortho- or peri-condensed with heterocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/4995—Pyrazines or piperazines forming part of bridged ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/50—Pyridazines; Hydrogenated pyridazines
- A61K31/501—Pyridazines; Hydrogenated pyridazines not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/50—Pyridazines; Hydrogenated pyridazines
- A61K31/5025—Pyridazines; Hydrogenated pyridazines ortho- or peri-condensed with heterocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/506—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/53—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with three nitrogens as the only ring hetero atoms, e.g. chlorazanil, melamine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5377—1,4-Oxazines, e.g. morpholine not condensed and containing further heterocyclic rings, e.g. timolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5383—1,4-Oxazines, e.g. morpholine ortho- or peri-condensed with heterocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/14—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/12—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains three hetero rings
- C07D471/14—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/08—Bridged systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D495/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms
- C07D495/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D495/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D495/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms
- C07D495/12—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms in which the condensed system contains three hetero rings
- C07D495/14—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D498/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D498/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D498/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D513/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for in groups C07D463/00, C07D477/00 or C07D499/00 - C07D507/00
- C07D513/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for in groups C07D463/00, C07D477/00 or C07D499/00 - C07D507/00 in which the condensed system contains two hetero rings
- C07D513/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D519/00—Heterocyclic compounds containing more than one system of two or more relevant hetero rings condensed among themselves or condensed with a common carbocyclic ring system not provided for in groups C07D453/00 or C07D455/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic System
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/18—Compounds having one or more C—Si linkages as well as one or more C—O—Si linkages
- C07F7/1804—Compounds having Si-O-C linkages
Abstract
本申请提供式I的杂芳基吡啶酮和氮杂‑吡啶酮化合物,其中X1、X2和X3中的一个或两个为N,并且包括所述化合物的立体异构体、互变异构体和可药用盐,其用于抑制Btk激酶和用于治疗免疫障碍例如由Btk激酶介导的炎症。本申请披露用式I化合物体外、原位和体内诊断和治疗在哺乳动物细胞中的所述障碍或相关病理病症的方法。
Description
本发明申请是基于申请日为2012年11月02日,申请号为201280065965.8(国际申请号为PCT/US2012/063194),发明名称为“作为BTK活性的抑制剂的杂芳基吡啶酮和氮杂-吡啶酮化合物”的中国专利申请的分案申请。
相关申请的交叉参考
根据37 CFR§1.53(b)提交的该非临时申请根据35 USC§119(e)要求2011年11月3日提交的美国临时申请61/555,393的权益,将61/555,393全文并入本申请作为参考。
技术领域
本发明大体上涉及用于治疗由Bruton酪氨酸蛋白激酶(Bruton’s TyrosineKinase(Btk))介导的障碍的化合物,所述由Bruton酪氨酸蛋白激酶介导的障碍包括炎症、免疫疾病和癌症,并且更具体地涉及抑制Btk活性的化合物。本发明还涉及用所述化合物体外、原位和体内诊断或治疗哺乳动物细胞或相关病理病症的方法。
背景技术
蛋白激酶,人类酶中的最大家族,包括远远超过500种蛋白质。Bruton酪氨酸蛋白激酶(Btk)是酪氨酸激酶中Tec家族的成员,并且是早期B细胞发育以及成熟B细胞活化、信号转导和存活的调节剂。
B细胞通过B细胞受体(BCR)的信号转导可导致宽范围的生物结果,而这些结果反过来依赖于B细胞的发育阶段。BCR信号的大小和持续时间必须受到精确的调节。异常的BCR介导的信号转导可引起错误调节的(disregulated)B细胞活化和/或病原性自身抗体的形成,这导致多种自身免疫性和/或炎症性疾病。人类中Btk的突变导致与X相关的无γ球蛋白血症(X-linked agammaglobulinaemia(XLA))。这种疾病与受损的B细胞成熟、减少的免疫球蛋白产生、缺乏免疫力的T细胞依赖性免疫应答(compromised T-cell-independentimmune response)和应对BCR刺激时持续钙信号的显著衰减(marked attenuation of thesustained calcium sign upon BCR stimulation)相关。已经在缺乏Btk的小鼠模型中建立了有关Btk在变应性障碍和/或自身免疫性疾病和/或炎症性疾病中的作用的证据。例如,已经在系统性红斑狼疮(SLE)的标准鼠类临床前模型中显示出Btk的缺乏导致疾病进展的显著改善。此外,缺乏Btk的小鼠也对发展成胶原诱发的关节炎具有抵抗力,并且较不易患上葡萄球菌诱发的关节炎(Staphylococcus-induced arthritis)。大量证据支持了B细胞和体液免疫系统(humoral immune system)在自身免疫性和/或炎症性疾病的发病中的作用。发展成减少B细胞的基于蛋白质的疗法(如Rituxan)代表了治疗多种自身免疫性和/或炎症性疾病的重要途径。由于Btk在B细胞活化中的作用,Btk的抑制剂可用作B细胞介导的病原活性(如产生自身抗体)的抑制剂。Btk也在破骨细胞、肥大细胞和单核细胞中表达,并且已被证明对于这些细胞的机能是重要的。例如,小鼠中的Btk缺乏与受损的IgE介导的肥大细胞活化(TNF-α和其它炎症性细胞因子释放的显著减少)相关,并且人类中的Btk缺乏与大大降低的由活化的单核细胞引起的TNF-α产生相关。
由此,对Btk活性的抑制可用于治疗变应性障碍和/或自身免疫性和/或炎症性疾病,这些疾病包括但不限于SLE、类风湿性关节炎、多发性血管炎(multiple vasculitide)、特发性血小板减少性紫癜(idiopathic thrombocytopenic purpura(ITP))、重症肌无力、变应性鼻炎和哮喘(Di Paolo et al(2011)Nature Chem.Biol.7(1):41-50;Liu et al(2011)Jour.of Pharm.and Exper.Ther.338(1):154-163)。此外,Btk已被报道在细胞凋亡中发挥作用;因此,抑制Btk或许可用于癌症,以及治疗B-细胞淋巴瘤、白血病和其它血液恶性肿瘤。此外,鉴于Btk在破骨细胞功能中的作用,抑制Btk活性可用于治疗骨障碍例如骨质疏松。具体的Btk抑制剂已被以下文献报道:(Liu(2011)Drug Metab.and Disposition 39(10):1840-1849;US 7884108,WO 2010/056875;US 7405295;US 7393848;WO 2006/053121;US 7947835;US 2008/0139557;US 7838523;US 2008/0125417;US 2011/0118233;PCT/US2011/050034“PYRIDINONES/PYRAZINONES,METHOD OF MAKING,AND METHOD OF USETHEREOF”,2011年8月31日提交;PCT/US2011/050013“PYRIDAZINES,METHOD OF MAKING,ANDMETHOD OF USE THEREOF”,2011年8月31日提交;US Ser.No.13/102720“PYRIDONE ANDAZA-PYRIDONE COMPOUNDS AND METHODS OF USE”,2011年5月6日提交)。
发明内容
本发明大体上涉及具有Bruton酪氨酸蛋白激酶(Btk)调节活性的式I的杂芳基吡啶酮和氮杂-吡啶酮化合物。
式I化合物具有以下结构:
包括其立体异构体、互变异构体或可药用盐。各取代基如本申请下面所定义。
本发明一个方面为药物组合物,其包含式I化合物和可药用载体、助流剂、稀释剂或赋形剂。所述药物组合物可进一步包含第二治疗剂。
本发明另一个方面为制备药物组合物的方法,所述方法包括将式I化合物与可药用载体组合。
本发明包括治疗疾病或障碍的方法,所述方法包括向患有疾病或障碍的患者给药治疗有效量的式I化合物,所述疾病或障碍选自免疫障碍、癌症、心血管疾病、病毒感染、炎症、代谢/内分泌机能障碍和神经障碍,和由Bruton酪氨酸蛋白激酶介导的疾病或障碍。
本发明包括用于治疗由Bruton酪氨酸蛋白激酶介导的病症的试剂盒,包括:a)第一药物组合物,其包含式I化合物;和b)使用说明。
本发明包括用作药物并且用于治疗选自以下疾病或障碍的式I化合物:免疫障碍、癌症、心血管疾病、病毒感染、炎症、代谢/内分泌机能障碍和神经障碍和由Bruton酪氨酸蛋白激酶介导的疾病或障碍。
本发明包括式I化合物在制备药物中的用途,所述药物用于治疗免疫障碍、癌症、心血管疾病、病毒感染、炎症、代谢/内分泌机能障碍和神经障碍,并且其中所述药物调节Bruton酪氨酸蛋白激酶。
本发明包括制备式I化合物的方法。
附图说明
图1显示制备2-(4-(羟基甲基)-5-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮101,以2,2,2-三氯-1-(4,5,6,7-四氢-1H-吲哚-2-基)乙酮101a开始。
图2显示制备2-(4-(羟基甲基)-5-(1-甲基-5-(5-(4-甲基哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮102,以1-甲基-3-[5-(4-甲基-哌嗪-1-基)-吡啶-2-基氨基]-5-(4,4,5,5-四甲基-[1,3,2]二氧杂硼杂戊环-2-基)-1H-吡啶-2-酮102a开始。
图3显示制备2-(3-(羟基甲基)-4-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮103,以2-溴-4-氯吡啶-3-甲醛103a开始。
图4显示制备2-(3-(羟基甲基)-2-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-4-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮104,以4-溴-2-氯吡啶-3-甲醛104a开始。
图5显示制备4-羟基甲基-3-[1-甲基-5-({5-[4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]-5-{6-氧代-8-硫杂-5-氮杂三环-[7.4.0.02,7]十三碳-1(9),2(7)-二烯-5-基}吡啶105,以N-甲氧基-N-甲基-4,5,6,7-四氢苯并[b]噻吩-2-甲酰胺105a开始。
图6显示制备4-羟基甲基-3-[1-甲基-5-({5-[4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]-5-{4,4-二甲基-9-氧代-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-10-基}吡啶-4-甲醛106,以3,3-二甲基环戊酮106a开始。
图7显示制备10-[4-[1-甲基-5-({5-[4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]-4-(羟基甲基)吡啶-3-基]-4,4-二甲基-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-9-酮107,以(E)-3-(2-氯-4,4-二甲基环戊-1-烯基)丙烯酸乙酯107a开始。
图8显示制备2-(3-(羟基甲基)-4-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-4,4-二甲基-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-9-酮108,以4-氯-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-甲醛108a开始。
图9显示制备2-(3-(羟基甲基)-4-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-4,4-二甲基-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-9-酮109,以4-氯-2-{4,4-二甲基-9-氧代-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-10-基}吡啶-3-甲醛109a开始。
图10显示制备2-(3-(羟基甲基)-4-(1-甲基-5-(6-(4-甲基哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮110,以1-甲基-3-(6-(4-甲基哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮110a开始。
图11显示制备2-(3-(羟基甲基)-4-(1-甲基-5-(5-(吗啉-4-羰基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮111,以(6-氨基吡啶-3-基)(吗啉代)甲酮111a开始。
图12显示制备2-(4-(羟基甲基)-5-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-基)-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-1(2H)-酮112,以5,6,7,8-四氢吲嗪-2-羧酸甲酯112a开始。
图13显示制备2-(3-(羟基甲基)-4-(1-甲基-5-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮113,以(3-硝基-1H-吡唑-5-基)甲醇113a开始。
图14显示制备(R)-2-(4-(6-(4-(1,4-二甲基-3-氧代哌嗪-2-基)苯基氨基)-4-甲基-5-氧代-4,5-二氢吡嗪-2-基)-3-(羟基甲基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮114,以(R)-5-溴-3-(4-(1,4-二甲基-3-氧代哌嗪-2-基)苯基氨基)-1-甲基吡嗪-2(1H)-酮114a开始。
图15显示制备2-(3-(羟基甲基)-4-(1-甲基-5-(5-甲基-1H-吡唑-3-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮115,以5-溴-1-甲基-3-(5-甲基-1H-吡唑-3-基氨基)吡啶-2(1H)-酮115a开始。
图16显示制备4-羟基甲基-3-[1-甲基-5-({5-[4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]-5-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶116,以3-溴-5-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-4-甲醛116a开始。
图17显示制备2-(3-(羟基甲基)-4-(1-甲基-5-(5-(甲基磺酰基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢-吡嗪并[1,2-a]吲哚-1(2H)-酮117,以5-(甲基硫基)-2-硝基吡啶117a开始。
图18显示制备2-(4-(5-(5-环丙基-1H-吡唑-3-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-3-(羟基甲基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮118,以5-氨基-3-环丙基-1H-吡唑-1-羧酸叔丁酯118a开始。
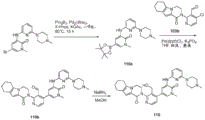
图19显示制备(S)-2-(3-(羟基甲基)-4-(1-甲基-5-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮119,以(S)-乙酸(4-(1-甲基-5-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯119a开始。
图20显示制备2-(4-(5-(5-(4-(2-羟基-2-甲基丙基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-3-(羟基甲基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮120,以5-溴-3-(5-(4-(2-羟基-2-甲基丙基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基吡啶-2(1H)-酮120a开始。
图21显示制备2-(3-(羟基甲基)-4-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-6,7,8,9-四氢吡嗪并[1,2-a]吲哚-1(2H)-酮121,以4-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-6,7,8,9-四氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛121a开始。
图22显示制备2-(4-(5-(5-((2S,5R)-2,5-二甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-3-(羟基甲基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮122,以(2R,5S)-2,5-二甲基-4-(6-硝基吡啶-3-基)哌嗪-1-羧酸叔丁酯122a开始。
图23显示制备2-(4-(5-(5-(4-(2-羟基乙基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-3-(羟基甲基)吡啶-2-基)-3,4,6,7,8,9-六氢-吡嗪并[1,2-a]吲哚-1(2H)-酮123,以(2-溴乙氧基)(叔丁基)二甲基硅烷123a开始。
图24显示制备3-羟基甲基-4-[1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基]-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶124,以4-氯-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-甲醛124a开始。
图25显示制备用于制备140的7,7-二氟-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮,自1H-吡咯-2-羧酸乙酯开始。
图26显示制备用于制备266的5-(氧杂环丁烷-3-基)-1H-吡唑-3-胺,自3-硝基-1H-吡唑开始。
示例性实施方案的详述
现将详细说明本发明某些实施方案即所附结构和化学式所显示的实施例。当本发明用所列举的实施方案描述时,应该理解的是,它们并非意在将本发明局限于那些实施方案。相反地,本发明旨在涵盖可包括在如权利要求书所定义的本发明范围内的所有变更、修改和等价形式。本领域技术人员会认识到与本申请描述的那些方法和物质类似或等价的多种方法和物质,这些方法和物质可用于实践本发明。本发明决不限于所述的方法和物质。如果一篇或多篇所引入的文献、专利和类似材料与本申请(包括但不限于所定义的术语、术语的用法、所述的技术等)不同或矛盾,以本申请为准。除非另有定义,本申请使用的所有科技术语具有与本发明所属领域的普通技术人员通常理解的含义相同的含义。下面描述了适当的方法和物质,但与本申请描述的那些方法和物质类似或等价的方法和物质可用于实践或测试本发明。将本申请提及的所有出版物、专利申请、专利和其它参考文献全文并入本申请作为参考。该申请中使用的命名基于IUPAC系统命名法,除非另有说明。
定义
当表明取代基的数目时,术语“一个或多个”是指范围为自一个取代基至最高可能数目的取代基,即用取代基替换一个氢至最高替换所有氢。术语“取代基”表示替代母体分子上的氢原子的一个原子或一组原子。术语“取代的”表示具有一个或多个取代基的特定基团。在任意基团可携带多个取代基并且提供了多种可能的取代基的情况下,所述取代基是经独立选择的并且不需要是相同的。术语“未取代的”是指所述特定基团不具有取代基。术语“任选取代的”是指所述特定基团是未取代的或被一个或多个取代基取代,所述取代基独立地选自可能取代基组。当表明取代基的数目时,术语“一个或多个”是指自一个取代基至最高可能数目的取代基,即用取代基替换一个氢至最高替换所有氢。
本申请使用的术语“烷基”是指一至十二个碳原子(C1-C12)的饱和直链或支链单价烃基,其中所述烷基可任选地独立地被一或多个下述取代基取代。在另一个实施方案中,烷基为一至八个碳原子(C1-C8),或一至六个碳原子(C1-C6)。烷基的实例包括但不限于甲基(Me,-CH3)、乙基(Et,-CH2CH3)、1-丙基(n-Pr、正丙基、-CH2CH2CH3)、2-丙基(i-Pr、异丙基、-CH(CH3)2)、1-丁基(n-Bu、正丁基、-CH2CH2CH2CH3)、2-甲基-1-丙基(i-Bu、异丁基、-CH2CH(CH3)2)、2-丁基(s-Bu、仲丁基、-CH(CH3)CH2CH3)、2-甲基-2-丙基(t-Bu、叔丁基、-C(CH3)3)、1-戊基(正戊基、-CH2CH2CH2CH2CH3)、2-戊基(-CH(CH3)CH2CH2CH3)、3-戊基(-CH(CH2CH3)2)、2-甲基-2-丁基(-C(CH3)2CH2CH3)、3-甲基-2-丁基(-CH(CH3)CH(CH3)2)、3-甲基-1-丁基(-CH2CH2CH(CH3)2)、2-甲基-1-丁基(-CH2CH(CH3)CH2CH3)、1-己基(-CH2CH2CH2CH2CH2CH3)、2-己基(-CH(CH3)CH2CH2CH2CH3)、3-己基(-CH(CH2CH3)(CH2CH2CH3))、2-甲基-2-戊基(-C(CH3)2CH2CH2CH3)、3-甲基-2-戊基(-CH(CH3)CH(CH3)CH2CH3)、4-甲基-2-戊基(-CH(CH3)CH2CH(CH3)2)、3-甲基-3-戊基(-C(CH3)(CH2CH3)2)、2-甲基-3-戊基(-CH(CH2CH3)CH(CH3)2)、2,3-二甲基-2-丁基(-C(CH3)2CH(CH3)2)、3,3-二甲基-2-丁基(-CH(CH3)C(CH3)3、1-庚基、1-辛基等。
本申请使用的术语“亚烷基”是指一至十二个碳原子(C1-C12)的饱和直链或支链二价烃基,其中所述亚烷基可任选地独立地被一个或多个下述取代基取代。在另一个实施方案中,亚烷基为一至八个碳原子(C1-C8)或一至六个碳原子(C1-C6)。亚烷基的实例包括但不限于亚甲基(-CH2-)、亚乙基(-CH2CH2-)、亚丙基(-CH2CH2CH2-)等。
术语“烯基”是指具有至少一个不饱和位点(即,碳-碳,sp2双键)的两至八个碳原子(C2-C8)的直链或支链单价烃基,其中所述烯基可任选地独立地被一个或多个本申请所述取代基取代,并且包括具有“顺式”和“反式”取向(或者可选择地“E”和“Z”取向)的基团。实例包括但不限于乙烯基或乙烯基(-CH=CH2),烯丙基(-CH2CH=CH2)等。
术语“亚烯基”是指具有至少一个不饱和位点(即,碳-碳,sp2双键)的两至八个碳原子(C2-C8)的直链或支链二价烃基,其中所述亚烯基可任选地独立地被一个或多个本申请所述取代基取代,并且包括具有“顺式”和“反式”取向(或者可选择地“E”和“Z”取向)的基团。实例包括但不限于亚乙烯基(-CH=CH-),亚烯丙基(-CH2CH=CH-)等。
术语“炔基”是指具有至少一个不饱和位点(即,碳-碳,sp三键)的两至八个碳原子(C2-C8)的直链或支链单价烃基,其中所述炔基可任选地独立地被一个或多个本申请所述取代基取代。实例包括但不限于乙炔基(-C≡CH)、丙炔基(炔丙基、-CH2C≡CH)等。
术语“亚炔基”是指具有至少一个不饱和位点(即,碳-碳,sp三键)的两至八个碳原子(C2-C8)的直链或支链二价烃基,其中所述炔基可任选地独立地被一个或多个本申请所述取代基取代。实例包括但不限于亚乙炔基(-C≡C-)、亚丙炔基(亚炔丙基、-CH2C≡C-)等。
术语“碳环”、“碳环基”、“碳环状环”和“环烷基”是指具有3至12个碳原子(C3-C12)(作为单环)或具有7至12个碳原子(作为二环)的单价非芳香性饱和或部分不饱和环。具有7至12个原子的二环碳环可排列为例如二环[4,5]、[5,5]、[5,6]或[6,6]系统,而具有9或10个环原子的二环碳环可排列为二环[5,6]或[6,6]系统或排列为桥接系统如二环[2.2.1]庚烷、二环[2.2.2]辛烷和二环[3.2.2]壬烷。螺部分也包括在本发明的范围内。单环碳环的实例包括但不限于环丙基、环丁基、环戊基、1-环戊-1-烯基、1-环戊-2-烯基、1-环戊-3-烯基、环己基、1-环己-1-烯基、1-环己-2-烯基、1-环己-3-烯基、环己二烯基、环庚基、环辛基、环壬基、环癸基、环十一烷基、环十二烷基等。碳环基任选地独立地被一个或多个本申请所述的取代基取代。
"芳基"表示通过由母体芳环系统中的单个碳原子除去一个氢原子而衍生的具有6-20个碳原子(C6-C20)的单价芳族烃基。在示例性结构中一些芳基被表示为"Ar"。芳基包括这样的二环基团,其含有与饱和环、部分不饱和环或芳族碳环稠合的芳环。典型的芳基包括但不限于由苯(苯基)、取代的苯、萘、蒽、联苯、茚、茚满、1,2-二氢萘、1,2,3,4-四氢萘等衍生的基团。芳基任选地独立地被一个或多个本申请所述的取代基取代。
“亚芳基”表示通过由母体芳环系统中的两个碳原子除去二个氢原子而衍生的具有6-20个碳原子(C6-C20)的二价芳族烃基。在示例性结构中一些亚芳基被表示为"Ar"。亚芳基包括这样的二环基团,其含有与饱和环、部分不饱和环或芳族碳环稠合的芳环。典型的亚芳基包括但不限于由苯(亚苯基)、取代的苯、萘、蒽、亚联苯、亚茚、亚茚满、1,2-二氢萘、1,2,3,4-四氢萘等衍生的基团。亚芳基任选地独立地被一个或多个本申请所述的取代基取代。
术语"杂环(heterocycle)"、"杂环基(heterocyclyl)"和"杂环(heterocyclicring)"在本申请中可交换使用且是指具有3至约20个环原子的饱和或部分不饱和(即在环中具有一个或多个双键和/或三键)碳环基团,其中至少一个环原子为选自氮、氧、磷和硫的杂原子,其余环原子为C,其中一个或多个环原子任选独立被一个或多个下述取代基取代。杂环可以是具有3至7个环成员(2至6个碳原子及1至4个选自N、O、P和S的杂原子)的单环或具有7至10个环成员(4至9个碳原子及1至6个选自N、O、P和S的杂原子)的二环,例如二环[4,5]、[5,5]、[5,6]或[6,6]系统。杂环参见Paquette,Leo A.;"Principles of ModernHeterocyclic Chemistry"(W.A.Benjamin,New York,1968)(特别是第1、3、4、6、7和9章);"The Chemistry of Heterocyclic Compounds,A series of Monographs"(John Wiley&Sons,New York,1950至今)(特别是第13、14、16、19和28卷);及J.Am.Chem.Soc.(1960)82:5566。"杂环基"还包括这样的基团,其中杂环基与饱和环、部分不饱和环、芳族碳环或芳族杂环稠合。杂环的实例包括但不限于吗啉-4-基、哌啶-1-基、哌嗪基、哌嗪-4-基-2-酮、哌嗪-4-基-3-酮、吡咯烷-1-基、硫吗啉-4-基、S-二氧代硫吗啉-4-基、氮杂环辛烷-1-基、氮杂环丁烷-1-基、八氢吡啶并[1,2-a]吡嗪-2-基、[1,4]二氮杂环庚烷-1-基、吡咯烷基、四氢呋喃基、二氢呋喃基、四氢噻吩基、四氢吡喃基、二氢吡喃基、四氢噻喃基、哌啶子基、吗啉代、硫吗啉代、硫杂氧杂环己基、哌嗪基、高哌嗪基、氮杂环丁烷基、氧杂环丁烷基、硫杂环丁烷基、高哌啶基、氧杂环庚烷基、硫杂环庚烷基、氧杂氮杂基、二氮杂基、硫杂氮杂基、2-吡咯啉基、3-吡咯啉基、二氢吲哚基、2H-吡喃基、4H-吡喃基、二氧杂环己烷基、1,3-二氧杂环戊烷基、吡唑啉基、二硫杂环己基、二硫杂环戊基、二氢吡喃基、二氢噻吩基、二氢呋喃基、吡唑烷基、咪唑啉基、咪唑烷基、3-氮杂二环[3.1.0]己烷基、3-氮杂二环[4.1.0]庚烷基、氮杂二环[2.2.2]己烷基、3H-吲哚基、喹嗪基和N-吡啶基脲。螺环基团也包括在该定义的范围内。其中环原子被氧代(=O)取代的杂环基的实例为嘧啶酮基和1,1-二氧代-硫吗啉基。本申请的杂环基任选地独立地被一个或多个本申请所述的取代基取代。
术语“杂芳基”是指作为5-、6-或7-元环的单价芳族基团及包括5-20个原子的稠环系统(其中至少一个环是芳族的),其含有一个或多个独立选自氮、氧和硫的杂原子。杂芳基的实例为吡啶基(包括例如2-羟基吡啶基)、咪唑基、咪唑并吡啶基、嘧啶基(包括例如4-羟基嘧啶基)、吡唑基、三唑基、吡嗪基、四唑基、呋喃基、噻吩基、异噁唑基、噻唑基、噁二唑基、噁唑基、异噻唑基、吡咯基、喹啉基、异喹啉基、四氢异喹啉基、吲哚基、苯并咪唑基、苯并呋喃基、噌啉基、吲唑基、吲嗪基、酞嗪基、哒嗪基、三嗪基、异吲哚基、蝶啶基、嘌呤基、噁二唑基、三唑基、噻二唑基、噻二唑基、呋咱基、苯并呋咱基、苯并噻吩基、苯并噻唑基、苯并噁唑基、喹唑啉基、喹喔啉基、二氮杂萘基和呋喃并吡啶基。
杂环基或杂芳基在适当连接的情况下可以是经碳连接的(碳联的)或经氮连接的(氮联的)。例如而非限制,经碳键合的杂环基或杂芳基在以下位置键合:吡啶的2、3、4、5或6位,哒嗪的3、4、5或6位,嘧啶的2、4、5或6位,吡嗪的2、3、5或6位,呋喃、四氢呋喃、噻吩、吡咯或四氢吡咯的2、3、4或5位,噁唑、咪唑或噻唑的2、4或5位,异噁唑、吡唑或异噻唑的3、4或5位,氮丙啶的2或3位,氮杂环丁烷的2、3或4位,喹啉的2、3、4、5、6、7或8位,或异喹啉的1、3、4、5、6、7或8位。
例如而非限制,经氮键合的杂环基或杂芳基在以下位置键合:氮丙啶、氮杂环丁烷、吡咯、吡咯烷、2-吡咯啉、3-吡咯啉、咪唑、咪唑烷、2-咪唑啉、3-咪唑啉、吡唑、吡唑啉、2-吡唑啉、3-吡唑啉、哌啶、哌嗪、吲哚、二氢吲哚或1H-吲唑的1位,异吲哚或异二氢吲哚的2位,吗啉的4位,和咔唑或β-咔啉的9位。
术语“治疗”是指治疗性处置,其中目的是减缓(减轻)不期望的生理学变化或障碍如关节炎或癌症的发展或扩散。出于本发明目的,有益的或所期望的临床结果包括但不限于缓解症状、减小病变程度、稳定(即不是恶化)病症、延迟或减缓疾病进展、改善或缓和病症及好转(部分好转或完全好转),无论这些结果是可检测的还是不可检测的。“治疗”还可表示与未接受治疗的预期存活相比延长的存活。需要治疗的那些对象包括已经患有所述病症或障碍的那些对象。
术语“治疗有效量”是指(i)治疗本申请描述的具体疾病、病症或障碍的本发明化合物的量,(ii)削弱、改善或消除本申请描述的具体疾病、病症或障碍的一种或多种症状的本发明化合物的量,或(iii)预防或延迟本申请描述的具体疾病、病症或障碍的一种或多种症状的发作的本发明化合物的量。在癌症的情况下,治疗有效量的药物可减少癌细胞数量;减小肿瘤尺寸;抑制(即在一定程度上减慢及优选为停止)癌细胞浸润到周围器官中;抑制(即在一定程度上减慢及优选为停止)肿瘤转移;在一定程度上抑制肿瘤生长;和/或在一定程度上缓解与癌症相关的一种或多种症状。如果药物可预防癌细胞的生长和/或杀死已有的癌细胞,则其可能是细胞生长抑制性的和/或细胞毒性的。对于癌症治疗,可例如通过评价疾病进展时间(TTP)和/或确定应答率(RR)来测量功效。
本申请使用的“炎症性障碍”可指其中过度或未调节的炎症应答导致过渡炎症症状、宿主组织受损或组织功能丧失的任意疾病、障碍或综合征。"炎症性障碍"也指由粒细胞内流和/或嗜中性粒细胞趋化性介导的病理状态。
本申请使用的“炎症”是指由组织损伤或破坏引起的局部保护性应答,其用于摧毁、稀释或阻隔(隔离物(sequester))有害物质(injurious agent)和受损组织。炎症明显与粒细胞内流和/或嗜中性粒细胞趋化性有关。以下原因可导致炎症:感染了病原性微生物和病毒,和非传染性方式例如心肌梗塞或中风后的创伤或再灌注、对外来抗体的免疫应答和自身免疫性应答。因此,用式I化合物治疗的炎性疾病涵盖与特异性防御体系的反应有关的障碍和与非特异性防御体系的反应有关的障碍。
“特异性防御体系”是指对特异性抗原的存在产生反应的免疫系统组分。由特异性防御体系应答引起的炎症的实例包括经典的对外来抗原的应答、自身免疫性疾病和由T-细胞介导的迟发型超敏反应。特异性防御体系炎症反应的进一步实例为慢性炎症性疾病、实体移植的组织和器官(例如肾脏移植和骨髓移植)的排斥和移植物抗宿主病(GVHD)。
本申请使用的术语“非特异性防御体系”是指由无免疫记忆能力的白细胞(例如,粒细胞和巨噬细胞)介导的炎性疾病。至少部分是由非特异性防御体系反应引起的炎症的实例包括与以下病症相关的炎症,所述病症为例如成人(急性)呼吸窘迫综合征(ARDS)或多发性器官损伤综合征(multiple organ injury syndrome);再灌注损伤;急性肾小球肾炎;反应性关节炎;具有急性炎症性成分的皮肤病;急性化脓性脑膜炎或其它中枢神经系统炎性疾病例如中风;热损伤;炎症性肠病;粒细胞输注相关综合征(granulocyte transfusionassociated syndromes);和细胞因子诱导的毒性。
本申请使用的“自身免疫性疾病”是指其中组织损伤与体液或细胞介导的对身体自身成分的应答相关的任意类型障碍。
本申请使用的“变态反应性疾病”是指由变态反应引起的任意症状、组织受损或组织功能丧失。本申请使用的“关节炎性疾病”是指以由于多种病因导致的关节炎症性损害为特征的任意疾病。本申请使用的“皮炎”是指以由多种病因导致的皮肤炎症为特征的一大类皮肤病中的任一种。本申请使用的"移植排斥"是指直接抗被移植组织例如器官或细胞(例如,骨髓)的任意免疫反应,特征在于被移植组织和周围组织功能的丧失、疼痛、肿胀、白细胞增多和血小板减少。本发明的治疗方法包括治疗与炎症细胞活化相关的障碍的方法。
“炎症细胞活化”是指在炎症细胞(包括但不限于单核细胞、巨噬细胞、T淋巴细胞、B淋巴细胞、粒细胞(即,多形核性白细胞例如嗜中性粒细胞、嗜碱性粒细胞和嗜酸性粒细胞)、肥大细胞、树状突细胞、朗氏细胞和内皮细胞)中由刺激物(包括但不限于细胞因子、抗原或自身抗体)诱导的增殖性细胞应答、可溶性介质(包括但不限于细胞因子、氧自由基、酶、类前列腺素或血管活性胺)的产生或细胞表面表达新的或增加数目的介质(包括但不限于主要组织相容性抗原或细胞粘附分子)。本领域技术人员应当理解的是,这些细胞中这些表型中的一种或其组合的活化可促成炎性疾病的发生、持续(perpetuation)或恶化。
术语“NSAID”为“非甾体抗炎药”的缩写,其为具有止痛、解热(降低高体温并缓解疼痛,但不破坏意识)和在较高剂量时具有抗炎作用(减少炎症)的治疗药物。术语“非甾体”用于将这些药物与甾体类药物区分开,所述甾体类药物的众多作用中包括类似的阻抑花生四烯酸(eicosanoid-depressing)、抗炎作用。作为止痛药,NSAID是独特的,因为它们是非麻醉性的。NSAID包括阿司匹林(aspirin)、布洛芬(ibuprofen)和萘普生(naproxen)。NSAID通常被指示用于存在疼痛和炎症时治疗急性或慢性病症。NSAID一般被指示用于缓解以下病症的症状:类风湿性关节炎、骨关节炎、炎症性关节炎(例如,强直性脊柱炎、牛皮癣性关节炎、莱特尔综合征(Reiter's syndrome)、急性痛风、痛经、转移性骨疼痛、头痛和偏头痛、术后痛、由于炎症和组织损伤引起的轻度至中度疼痛、发热、肠梗阻和肾绞痛。大多数NSAID用作酶即环氧合酶的非选择性抑制剂,抑制环氧合酶-1(COX-1)和环氧合酶-2(COX-2)同工酶。环氧合酶催化由花生四烯酸(本身是通过磷脂酶A2从细胞磷脂双层衍生的)形成前列腺素和血栓烷。在众多作用中,前列腺素包括在炎症过程中用作信使分子。COX-2抑制剂包括塞来考昔(celecoxib)、艾托考昔(etoricoxib)、罗美昔布(lumiracoxib)、帕瑞考昔(parecoxib)、罗非考昔(rofecoxib)、罗非考昔(rofecoxib)和伐地考昔(valdecoxib)。
术语“癌症(cancer)”是指哺乳动物中特征通常为未调节的细胞生长的生理条件或描述所述生理条件。“肿瘤”包含一种或多种癌细胞。癌症的实例包括但不限于癌(carcinoma)、淋巴瘤、母细胞瘤、肉瘤以及白血病(leukemia)或淋巴样恶性肿瘤(lymphoidmalignancy)。所述癌症的更具体的实例包括鳞状细胞癌(例如上皮鳞状细胞癌);肺癌,包括小细胞肺癌、非小细胞肺癌(“NSCLC")、肺腺癌(adenocarcinoma of the lung)和肺鳞状细胞癌(squamous carcinoma of the lung);腹膜癌;肝细胞癌;胃癌(gastric orstomach cancer),包括胃肠癌;胰腺癌;成胶质细胞瘤;子宫颈癌;卵巢癌;肝癌(livercancer);膀胱癌;肝细胞瘤(hepatoma);乳腺癌(breast cancer);结肠癌;直肠癌;结肠直肠癌;子宫内膜癌或子宫癌;唾液腺癌;肾脏癌(kidney cancer)或肾癌(renal cancer);前列腺癌;外阴癌(vulval cancer);甲状腺癌;肝脏癌(hepatic carcinoma);肛门癌;阴茎癌;以及头颈癌。
“血液恶性肿瘤(Hematological malignancies)”(英式英语拼法为"Haematological"malignancies)为影响血液、骨髓和淋巴结的癌症类型。由于这三种通过免疫系统密切关联,因此影响三者中一者的疾病通常也会影响其它两者:尽管淋巴瘤为淋巴结的疾病,但其经常扩散到骨髓,影响血液。血液恶性肿瘤为恶性新生物("癌症"),并且它们通常是由血液学和/或肿瘤学的专家治疗的。在一些癌症中,"血液学/肿瘤学"是内科学的单一亚种,但在其它癌症中,它们被认为是不同的科室(也有外科肿瘤学和放射肿瘤学)。并不是所有的血液障碍都是恶性的("癌症性的");还存在也由血液病专家治疗的其它血液病症。血液恶性肿瘤可源自两种主要的血液细胞谱系:骨髓细胞系和淋巴样细胞系。所述骨髓细胞系通常产生粒细胞、红细胞、血小板、巨噬细胞和肥大细胞;所述淋巴样细胞系产生B、T、NK和浆细胞。淋巴瘤、淋巴细胞白血病和骨髓瘤来自淋巴细胞系,而急性和慢性髓细胞性白血病、骨髓增生异常综合征和骨髓增生性疾病为骨髓源性的。白血病包括急性淋巴母细胞性白血病(ALL)、急性髓细胞性白血病(AML)、慢性淋巴细胞白血病(CLL)、慢性髓细胞性白血病(CML)、急性单核细胞性白血病(AMOL)和小淋巴细胞性淋巴瘤(SLL)。淋巴瘤包括何杰金氏淋巴瘤(全部四种亚型)和非-何杰金氏淋巴瘤(全部亚型)。
“化疗药物”是可用于治疗癌症的化合物,而与其作用机理无关。化疗药物的种类包括,但是不限于:烷化剂、抗代谢药、纺丝体毒植物生物碱(spindle poison plantalkaloids)、细胞毒性/抗肿瘤抗生素(cytotoxic/antitumor antibiotics)、拓扑异构酶抑制剂(topoisomerase inhibitors)、抗体、光敏性药物和激酶抑制剂。化疗药物包括在“靶向疗法”和常规化学疗法中使用的化合物。化疗药物的实例包括:厄洛替尼(erlotinib)(Genentech/OSI Pharm.)、多西他赛(docetaxel)(Sanofi-Aventis)、5-FU(氟尿嘧啶,5-氟尿嘧啶,CAS No.51-21-8)、吉西他滨(gemcitabine)(Lilly)、PD-0325901(CAS No.391210-10-9,Pfizer)、顺铂(cisplatin)(顺-二胺、二氯化铂(II)、CAS No.15663-27-1)、卡铂(carboplatin)(CASNo.41575-94-4)、紫杉醇(paclitaxel)(Bristol-Myers Squibb Oncology,Princeton,N.J.)、曲妥单抗(trastuzumab)(Genentech)、替莫唑胺(temozolomide)(4-甲基-5-氧代-2,3,4,6,8-五氮杂二环[4.3.0]壬-2,7,9-三烯-9-甲酰胺、CAS No.85622-93-1,Schering Plough)、他莫昔芬(tamoxifen)((Z)-2-[4-(1,2-二苯基丁-1-烯基)苯氧基]-N,N-二甲基-乙基胺,)、多柔比星(doxorubicin)Akti-1/2、HPPD和雷帕霉素(rapamycin)。
化疗药物的其它实例包括:奥沙利铂(oxaliplatin)(Sanofi)、硼替佐米(bortezomib)(Millennium Pharm.)、舒尼替尼(sutent)(SU11248,Pfizer)、来曲唑(letrozole)(Novartis)、甲磺酸伊马替尼(imatinib mesylate)(Novartis)、XL-518(MEK抑制剂,Exelixis,WO 2007/044515)、ARRY-886(MEK抑制剂,AZD6244,Array BioPharma,Astra Zeneca)、SF-1126(PI3K抑制剂,Semafore Pharmaceuticals)、BEZ-235(PI3K抑制剂,Novartis)、XL-147(PI3K抑制剂,Exelixis)、PTK787/ZK 222584(Novartis)、氟维司群(fulvestrant)(AstraZeneca)、甲酰四氢叶酸(leucovorin)(亚叶酸)、雷帕霉素(西罗莫司、Wyeth)、拉帕替尼(lapatinib)(GSK572016,GlaxoSmith Kline)、lonafarnib(SARASARTM,SCH 66336,Schering Plough)、索拉非尼(sorafenib)(BAY43-9006、Bayer Labs)、吉非替尼(gefitinib)(AstraZeneca)、伊立替康(irinotecan)(CPT-11,Pfizer)、tipifarnib(ZARNESTRATM,Johnson&Johnson)、ABRAXANETM(Cremophor-free)、紫杉醇的白蛋白工程化纳米微粒制剂(albumin-engineered nanoparticle formulations ofpaclitaxel)(American Pharmaceutical Partners,Schaumberg,Il)、凡德他尼(rINN,ZD6474,AstraZeneca)、chloranmbucil、AG1478、AG1571(SU 5271;Sugen)、temsirolimus(Wyeth)、pazopanib(GlaxoSmithKline)、canfosfamide(Telik)、塞替派(thiotepa)和环磷酰胺(cyclosphosphamide)();磺酸烷基酯(alkyl sulfonate)如白消安、英丙舒凡和哌泊舒凡(piposulfan);氮丙啶(aziridine)如benzodopa、卡波醌、meturedopa和uredopa;乙撑亚胺(ethylenimine)和甲基氨基吖啶(methylamelamine),包括六甲蜜胺、三亚胺嗪(triethylenemelamine)、三亚乙基磷酰胺(triethylenephosphoramide)、三亚乙基硫化磷酰胺(triethylenethiophosphoramide)和trimethylomelamine;番荔枝内酯(acetogenin)(尤其是布拉它辛(bullatacin)和布拉它辛酮(bullatacinone));喜树碱(包括合成性类似物托泊替康(topotecan));苔藓抑素(bryostatin);callystatin;CC-1065(包括其阿多来新(adozelesin)、卡折来新(carzelesin)和比折来新(bizelesin)合成性类似物);cryptophycins(特别是cryptophycin 1和cryptophycin 8);多拉司他汀(dolastatin);duocarmycin(包括合成性类似物KW-2189和CB1-TM1);艾榴塞洛素(eleutherobin);pancratistatin;sarcodictyin;spongistatin;氮芥如苯丁酸氮芥、萘氮芥、氯磷酰胺(chlorophosphamide)、雌莫司汀、异环磷酰胺、双氯乙基甲胺(mechlorethamine)、盐酸氧氮芥(mechlorethamine oxide hydrochloride)、美法仑、新氮芥(novembichin)、苯芥胆甾醇(phenesterine)、泼尼莫司汀(prednimustine)、曲磷胺(trofosfamide)、尿嘧啶氮芥(uracil mustard);硝基脲如卡莫司汀、氯脲菌素(chlorozotocin)、福莫司汀、洛莫司汀、尼莫司汀和雷莫司汀;抗生素如烯二炔(enediyne)抗生素(例如刺孢霉素(calicheamicin),刺孢霉素γ1I、刺孢霉素ωI1((Angew Chem.Intl.Ed.Engl.(1994)33:183-186));蒽环类抗生素(dynemicin),dynemicin A;二膦酸盐(bisphosphonate)如氯膦酸盐(clodronate);埃斯培拉霉素(esperamicin);以及新抑癌蛋白生色团(neocarzinostatin chromophore)和相关色蛋白烯二炔抗生素生色团(enediyneantibiotic chromophore)、aclacinomysin、放线菌素(actinomycin)、authramycin、偶氮丝氨酸(azaserine)、博来霉素、放线菌素C(cactinomycin)、carabicin、去甲柔红霉素(carminomycin)、嗜癌素(carzinophilin)、色霉素(chromomycin)、放线菌素D(dactinomycin)、柔红霉素(daunorubicin)、地托比星(detorubicin)、6-重氮基-5-氧代-L-正亮氨酸(6-diazo-5-oxo-L-norleucine)、吗啉代-多柔比星、氰基吗啉代-多柔比星、2-吡咯啉子基-多柔比星和去氧多柔比星)、表柔比星(epirubicin)、依索比星、伊达比星、奈莫柔比星(nemorubicin)、麻西罗霉素(marcellomycin)、丝裂霉素如丝裂霉素C、麦考酚酸(mycophenolic acid)、诺拉霉素(nogalamycin)、橄榄霉素(olivomycins)、培洛霉素(peplomycin)、泊非霉素(porfiromycin)、嘌罗霉素(puromycin)、三铁阿霉素(quelamycin)、罗多比星(rodorubicin)、链黑霉素(streptonigrin)、链佐星(streptozocin)、杀结核菌素(tubercidin)、乌苯美司(ubenimex)、净司他丁(zinostatin)、佐柔比星;抗代谢物如甲氨喋呤和5-氟尿嘧啶(5-FU);叶酸类似物如二甲叶酸(denopterin)、甲氨喋呤(methotrexate)、喋罗呤(pteropterin)、三甲曲沙(trimetrexate);嘌呤类似物如氟达拉滨(fludarabine)、6-巯嘌呤、硫咪嘌呤(thiamiprine)、硫鸟嘌呤(thioguanine);嘧啶类似物如安西他滨(ancitabine)、阿扎胞苷(azacytidine)、6-氮鸟苷(6-azauridine)、卡莫氟(carmofur)、阿糖胞苷(cytarabine)、二脱氧尿苷(dideoxyuridine)、去氧氟尿苷(doxifluridine)、伊诺他滨(enocitabine)、氟尿苷(floxuridine);雄激素如卡普睾酮(calusterone)、丙酸甲雄烷酮(dromostanolonepropionate)、环硫雄醇(epitiostanol)、美雄烷(mepitiostane)、睾内酯(testolactone);抗肾上腺素(anti-adrenal)如氨鲁米特(aminoglutethimide)、米托坦(mitotane)、曲洛司坦(trilostane);叶酸补充剂(folic acid replenisher)如亚叶酸(frolinic acid);醋葡醛内酯(aceglatone);醛磷酰胺糖苷(aldophosphamide glycoside);氨基乙酰丙酸(aminolevulinic acid);恩尿嘧啶(eniluracil);安吖啶(amsacrine);bestrabucil;比生群(bisantrene);伊达曲杀(edatraxate);地磷酰胺(defofamine);秋水仙胺(demecolcine);地吖醌(diaziquone);elfornithine;依利醋铵(elliptinium acetate);埃坡霉素(epothilone);依托格鲁(etoglucid);硝酸镓(gallium nitrate);羟基脲(hydroxyurea);香菇多糖(lentinan);氯尼达明(lonidainine);美登醇(maytansinoid)如美登素(maytansine)和安丝菌素(ansamitocin);米托胍腙(mitoguazone);米托蒽醌(mitoxantrone);mopidanmol;根瘤菌剂(nitraerine);喷司他丁(pentostatin);蛋氨氮芥(phenamet);吡柔比星(pirarubicin);洛索蒽醌(losoxantrone);鬼臼酸(podophyllinicacid);2-乙基肼;丙卡巴肼(procarbazine);多糖复合物(JHS Natural Products,Eugene,OR);雷佐生(razoxane);根霉素(rhizoxin);西佐喃(sizofiran);锗螺胺(spirogermanium);细交链孢菌酮酸(tenuazonic acid);三亚胺醌(triaziquone);2,2',2"-三氯三乙胺;单端孢菌毒素(trichothecene)(尤其是T-2毒素、verracurin A、杆孢菌素A和anguidine);乌拉坦;长春地辛;达卡巴嗪(dacarbazine);甘露莫司汀(mannomustine);二溴甘露醇(mitobronitol);二溴卫矛醇(mitolactol);哌泊溴烷(pipobroman);gacytosine;阿糖胞苷(arabinoside)(“Ara-C”);环磷酰胺;塞替派;6-硫代鸟嘌呤;巯嘌呤;甲氨喋呤;铂类似物如顺铂和卡铂;长春碱;依托泊苷(VP-16);异环磷酰胺;米托蒽醌;长春新碱;长春瑞滨诺消灵(novantrone);替尼泊苷(teniposide);伊达曲杀(edatrexate);柔红霉素;氨基喋呤(aminopterin);卡培他滨(capecitabine)(Roche);伊班膦酸盐(ibandronate);CPT-11;拓扑异构酶抑制剂RFS 2000;二氟甲基鸟氨酸(difluoromethylornithine、DMFO);类视黄醇(retinoid)如视黄酸(retinoic acid);以及上述任何物质的可药用盐、酸和衍生物。
以下物质也包括在“化疗药物”的定义中:(i)用于调节或抑制激素对肿瘤的作用的抗激素药物,如抗雌激素药物(anti-estrogen)和选择性雌激素受体调节剂(selectiveestrogen receptor modulator,SERM),包括例如他莫昔芬(包括枸橼酸他莫昔芬)、雷洛昔芬、屈洛昔芬、4-羟基他莫昔芬、曲沃昔芬(trioxifene)、雷洛西芬(keoxifene)、LY117018、奥那司酮(onapristone)和(枸橼酸托米芬(toremifine citrate));(ii)抑制芳香酶(调节肾上腺中雌激素产生)的芳香酶抑制剂,例如4(5)-咪唑、氨鲁米特、(醋酸甲地孕酮(megestrol acetate))、(依西美坦(exemestane);Pfizer)、formestanie、法倔唑(fadrozole)、(伏氯唑(vorozole))、(来曲唑;Novartis)和(阿那曲唑(anastrozole);AstraZeneca);(iii)抗雄激素药物(anti-androgen),如氟他胺(flutamide)、尼鲁米特(nilutamide)、比卡鲁胺(bicalutamide)、醋酸亮丙瑞林(leuprolide)和戈舍瑞林(goserelin)以及曲沙他滨(troxacitabine)(1,3-二氧戊环核苷胞嘧啶类似物);(iv)蛋白激酶抑制剂,例如MEK抑制剂(WO 2007/044515);(v)脂质激酶抑制剂;(vi)反义寡核苷酸,特别是抑制异常细胞增殖中所涉及的信号转导途径中的基因表达的那些反义寡核苷酸,例如PKC-α、Raf和H-Ras,如oblimersen(Genta Inc.);(vii)核酶如VEGF表达抑制剂(例如)和HER2表达抑制剂;(viii)疫苗如基因治疗疫苗,例如和rIL-2;拓扑异构酶1抑制剂如rmRH;(ix)抗血管生成药物如贝伐单抗(Genentech);以及上述任何物质的可药用盐、酸和衍生物。
还包括在“化疗药物”定义中的有治疗性抗体,比如阿仑珠单抗(alemtuzumab,Campath)、贝伐珠单抗(Genentech);西妥昔单抗(Imclone);帕木单抗(panitumumab,Amgen)、利妥昔单抗(Genentech/Biogen Idec)、培妥珠单抗(pertuzumab,2C4,Genentech)、曲妥单抗(Genentech)、托西莫单抗单抗(Bexxar,Corixia)和抗体药物轭合物奥吉妥珠单抗(gemtuzumab ozogamicin,Wyeth)。
具有作为化疗药物的治疗潜力而与本发明的Btk抑制剂联用的人源化单克隆抗体包括:阿仑珠单抗(alemtuzumab)、阿泊珠单抗(apolizumab)、阿塞珠单抗(aselizumab)、atlizumab、bapineuzumab、贝伐珠单抗(bevacizumab)、莫比伐珠单抗(bivatuzumabmertansine)、莫坎妥珠单抗(cantuzumab mertansine)、西利珠单抗(cedelizumab)、赛妥珠单抗(certolizumab pegol)、cidfusituzumab、cidtuzumab、达克珠单抗(daclizumab)、依库珠单抗(eculizumab)、依法珠单抗(efalizumab)、依帕珠单抗(epratuzumab)、厄利珠单抗(erlizumab)、泛维珠单抗(felvizumab)、芳妥珠单抗(fontolizumab)、奥吉妥珠单抗(gemtuzumab ozogamicin)、奥英妥珠单抗(inotuzumab ozogamicin)、ipilimumab、拉贝珠单抗(labetuzumab)、林妥珠单抗(lintuzumab)、马妥珠单抗(matuzumab)、美泊珠单抗(mepolizumab)、莫维珠单抗(motavizumab)、motovizumab、那他珠单抗(natalizumab)、尼妥珠单抗(nimotuzumab)、nolovizumab、numavizumab、ocrelizumab、奥马珠单抗(omalizumab)、帕利珠单抗(palivizumab)、帕考珠单抗(pascolizumab)、pecfusituzumab、pectuzumab、培妥珠单抗(pertuzumab)、培克珠单抗(pexelizumab)、ralivizumab、雷珠单抗(ranibizumab)、瑞利珠单抗(reslivizumab)、瑞利珠单抗(reslizumab)、resyvizumab、罗维珠单抗(rovelizumab)、卢利珠单抗(ruplizumab)、西罗珠单抗(sibrotuzumab)、西利珠单抗(siplizumab)、索土珠单抗(sontuzumab)、他珠单抗(tacatuzumab tetraxetan)、tadocizumab、他利珠单抗(talizumab)、特非珠单抗(tefibazumab)、托珠单抗(tocilizumab)、托利珠单抗(toralizumab)、曲司珠单抗(trastuzumab)、Tucotuzumab西莫白介素(tucotuzumab celmoleukin)、tucusituzumab、umavizumab、乌珠单抗(urtoxazumab)和维西珠单抗(visilizumab)。
“代谢物”是通过具体化合物或其盐在体内的代谢而产生的产物。可使用本领域已知的常规技术鉴定化合物的代谢物,并使用如本申请所述的试验确定它们的活性。所述产物可起因于例如所给药的化合物的氧化、还原、水解、酰胺化、脱酰胺化、酯化、脱酯化、酶法裂解等。因此,本发明包括本发明化合物的代谢物,包括由以下方法产生的化合物,所述方法包括使本发明式I化合物与哺乳动物接触足以产生其代谢产物的一段时间。
术语“包装说明书”是指通常包括在治疗产品的市售包装中的说明书,其含有关于适应症、用法、剂量、给药、禁忌症和/或注意事项的信息,这些信息涉及上述治疗产品的使用。
术语“手性”是指具有镜像配偶体(mirror image partner)不可重叠性质的分子,而术语“非手性”是指可与其镜像配偶体重叠的分子。
术语“立体异构体”是指具有相同化学组成但原子或基团在空间上的排列不同的化合物。
“非对映异构体”是指具有两个或更多手性中心并且其分子不互为镜像的立体异构体。非对映异构体具有不同的物理性质,如熔点、沸点、光谱性质和反应性。非对映异构体的混合物可通过高分辨分析操作如电泳和色谱来分离。
“对映异构体”是指互为不可重叠镜像的化合物的两种立体异构体。
本申请使用的立体化学定义和常规用语(convention)通常遵循S.P.Parker,Ed.,McGraw-Hill Dictionary of Chemical Terms(1984)McGraw-Hill Book Company,NewYork;and Eliel,E.and Wilen,S.、“Stereochemistry of Organic Compounds”,JohnWiley&Sons,Inc.,New York,1994。本发明化合物可含有不对称或手性中心,因此以不同立体异构形式存在。预期的是,本发明化合物的所有立体异构形式,包括但不限于非对映异构体、对映异构体和阻转异构体(atropisomers)及它们的混合物如外消旋混合物,形成了本发明的部分。许多有机化合物以光学活性形式存在,即它们具有旋转平面偏振光的平面的能力。在描述有光学活性的化合物时,使用前缀D和L或者R和S来表示分子关于其一个或多个手性中心的绝对构型。前缀d和l或者(+)和(-)用于指定平面偏振光由化合物引起的旋转的符号,其中(-)或l表示化合物是左旋的。前缀为(+)或d的化合物是右旋的。对于给定的化学结构而言,除了这些立体异构体互为镜像外,这些立体异构体是相同的。具体的立体异构体也可称为对映异构体,所述异构体的混合物通常称作对映异构混合物。对映异构体的50:50混合物称为外消旋混合物或外消旋体,当化学反应或方法中没有立体选择性或立体专一性时可出现这种情况。术语“外消旋混合物”和“外消旋体”是指两种对映异构物质的等摩尔混合物,其没有光学活性。对映异构体可通过手性分离方法从外消旋混合物中分离出来,所述手性分离方法为例如超临界流体色谱法(SFC)。在单独的对映异构体中,手性中心处的构型的归属描述在表1的示例性结构中,同时立体化学确定等待例如x射线晶体学数据。
术语“互变异构体”或“互变异构形式”是指可通过低能垒(low energy barrier)互相转化的不同能量的结构异构体。例如,质子互变异构体(proton tautomer)(也称为质子移变互变异构体(prototropic tautomer))包括通过质子迁移进行的互相转化,如酮-烯醇异构化和亚胺-烯胺异构化。价键互变异构体(valence tautomer)包括通过一些成键电子的重组进行的互相转化。
术语“可药用盐”表示不是生物学不期望的盐。可药用盐包括酸式加成盐和碱式加成盐。短语“可药用的”表明所述物质或组合物必须与制剂所包含的其它成分和/或用其治疗的哺乳动物是化学和/或毒理学相容的。
术语“可药用酸加成盐”表示与无机酸和有机酸形成的那些可药用盐,所述无机酸为例如盐酸、氢溴酸、硫酸、硝酸、碳酸、磷酸,和所述有机酸选自脂肪族类有机酸、环脂族类有机酸、芳族类有机酸、芳脂族类有机酸、杂环类有机酸、羧酸类有机酸和磺酸类有机酸例如甲酸、乙酸、丙酸、乙醇酸、葡糖酸、乳酸、丙酮酸、草酸、苹果酸、马来酸、丙二酸、琥珀酸、富马酸、酒石酸、柠檬酸、门冬氨酸、抗坏血酸、谷氨酸、邻氨基苯甲酸、苯甲酸、肉桂酸、扁桃酸、双羟萘酸、苯基乙酸、甲磺酸(“mesylate”)、乙磺酸、对甲苯磺酸和水杨酸。
术语“可药用碱加成盐”表示与有机碱或无机碱形成的那些可药用盐。可药用无机碱的实例包括钠盐、钾盐、铵盐、钙盐、镁盐、铁盐、锌盐、铜盐、锰盐和铝盐。衍生自可药用有机无毒碱的盐包括以下物质的盐:伯胺、仲胺和叔胺,取代的胺包括天然存在的取代的胺、环胺和碱性离子交换树脂,例如异丙胺、三甲基胺、二乙基胺、三乙胺、三丙基胺、乙醇胺、2-二乙基氨基乙醇、氨基丁三醇、二环己基胺、赖氨酸、精氨酸、组氨酸、咖啡因、普鲁卡因、海巴明(hydrabamine)、胆碱、甜菜碱、乙二胺、葡糖胺、甲基葡糖胺、可可碱、嘌呤、哌嗪、哌啶、N-乙基哌啶、氨基丁三醇(tromethamine)、N-甲基葡糖胺、多元胺树脂。
“溶剂化物”是指一种或多种溶剂分子与本发明化合物的缔合物(association)或络合物(complex)。形成溶剂化物的溶剂的实例包括但不限于水、异丙醇、乙醇、甲醇、DMSO、乙酸乙酯、乙酸和乙醇胺。
术语“EC50”为半数最大有效浓度,并且表示在体内获得具体作用最大值的50%所需的具体化合物的血浆浓度。
术语“Ki”为抑制常数并且表示具体抑制剂与受体的绝对亲和力。其是用竞争结合测定测量的并且等于在不存在竞争配体(例如,放射配体)的情况下,具体化合物占据所述受体的50%时的浓度。可将Ki值对数转化为pKi值(-log Ki),其中较高值表明指数级较大效力。
术语“IC50”为半数最大抑制浓度并且表示在体外实现对生物过程的50%抑制所需的具体化合物的浓度。可将IC50值对数转化为pIC50值(-log IC50),其中较高值表明指数级较大效力。所述IC50值不是绝对值,而是依赖于实验条件例如所使用的浓度,并且可用Cheng-Prusoff方程转化成绝对抑制常数(Ki)(Biochem.Pharmacol.(1973)22:3099)。可计算其它百分比抑制参数,例如IC70、IC90等。
术语“本发明化合物”和“式I化合物”包括式I化合物及其立体异构体、几何异构体、互变异构体、溶剂化物、代谢物和可药用盐和前药。
本申请提供的任意式或结构(包括式I化合物)也预期表示所述化合物的水合物、溶剂化物和多晶型和它们的混合物。
本申请给出的任意式或结构(包括式I化合物)也预期表示所述化合物的同位素标记形式和未标记形式。同位素标记的化合物具有本申请给出的式所描述的结构,不同的是一个或多个原子被具有所选原子质量或质量数的原子替换。可结合到本发明化合物中的同位素的实例包括氢、碳、氮、氧、磷、氟和氯的同位素,例如但不限于2H(氘D)、3H(氚)、11C、13C、14C、15N、18F、31P、32P、35S、36Cl和125I。各种同位素标记的本发明化合物例如其中结合了放射性同位素例如3H、13C和14C的那些化合物。所述同位素标记的化合物可用在代谢研究、反应动力性研究、检测或成像技术例如正电子发射断层扫描(PET)或单光子发射计算机断层成像(SPECT)(包括药物或底物组织分布测定)中,或用在放射活性治疗患者中。氘标记或氘取代的本发明化合物可具有改善的DMPK(药物代谢和药代动力学)性质,涉及分布、代谢和排泄(ADME)。用较重同位素例如氘取代可因较大代谢稳定性而得到一些治疗益处,例如体内半衰期延长或剂量需要量减少。18F标记的化合物可用于PET或SPECT研究。同位素标记的本发明化合物及其前药可大体上通过以下方式用实施例中披露的操作和下面描述的制备方法来制备,所述方式为用容易获得的同位素标记的试剂代替非同位素标记的试剂。此外,用较重同位素特别是氘(即,2H或D)取代可因较大代谢稳定性而得到一些治疗益处,例如体内半衰期延长或剂量需要量减少或治疗指数得到改善。应当理解的是,该上下文中的氘被认为是式化合物(I)中的取代基。所述较重同位素(特别是氘)的浓度可通过同位素富集因子(isotopic enrichment factor)定义。在本发明的化合物中,未被专门指定为特定同位素的原子是表示该原子的任意稳定同位素。除非另有说明,当将一处位置专门指定为"H"或"氢",该位置应被理解为具有天然丰度同位素组成的氢。因此,本在本发明化合物中,被专门指定为氘(D)的任意原子意欲表示氘。
杂芳基吡啶酮和氮杂-吡啶酮化合物
本发明提供式I的杂芳基吡啶酮和氮杂-吡啶酮化合物,包括式Ia-Ii及其药用制剂,其潜在用于治疗由Btk激酶介导的疾病、病症和/或障碍:
包括其立体异构体、互变异构体或可药用盐,其中:
X1为CR1或N;
X2为CR2或N;
X3为CR3或N;
其中X1、X2和X3中的一个或两个为N;
R1、R2和R3独立地选自H、F、Cl、-NH2、-NHCH3、-N(CH3)2、-OH、-OCH3、-OCH2CH3、-OCH2CH2OH和C1-C3烷基;
R4选自H、F、Cl、CN、-CH2OH、-CH(CH3)OH、-C(CH3)2OH、-CH(CF3)OH、-CH2F、-CHF2、-CH2CHF2、-CF3、-C(O)NH2、-C(O)NHCH3、-C(O)N(CH3)2、-NH2、-NHCH3、-N(CH3)2、-NHC(O)CH3、-OH、-OCH3、-OCH2CH3、-OCH2CH2OH、环丙基、环丙基甲基、1-羟基环丙基、咪唑基、吡唑基、3-羟基-氧杂环丁烷-3-基、氧杂环丁烷-3-基和氮杂环丁烷-1-基;
R5为任选取代的C6-C20芳基、C3-C12碳环基、C2-C20杂环基、C1-C20杂芳基、-(C6-C20芳基)-(C2-C20杂环基)、-(C1-C20杂芳基)-(C2-C20杂环基)、-(C1-C20杂芳基)-(C2-C20杂环基)-(C2-C20杂环基)、-(C1-C20杂芳基)-(C2-C20杂环基)-(C1-C6烷基)、-(C1-C20杂芳基)-(C1-C6烷基)、-(C2-C20杂环基)-(C1-C6烷基)、-(C2-C20杂环基)-(C3-C12碳环基)、-(C1-C20杂芳基)-(C3-C12碳环基)或-(C1-C20杂芳基)-C(=O)-(C2-C20杂环基);
R6为H、F、-CH3、-CH2CH3、-CH2CH2OH、-NH2或-OH;
R7选自以下结构:
其中波浪线表示连接位点;和
Y1和Y2独立地选自CH和N,其中Y1和Y2不都是N;
其中烷基、碳环基、杂环基、芳基和杂芳基被一个或多个独立选自以下的基团取代:F、Cl、Br、I、-CN、-CH3、-CH2CH3、-CH(CH3)2、-CH2CH(CH3)2、-CH2OH、-CH2OCH3、-CH2CH2OH、-C(CH3)2OH、-CH(OH)CH(CH3)2、-C(CH3)2CH2OH、-CH2CH2SO2CH3、-CH2OP(O)(OH)2、-CH2F、-CHF2、-CF3、-CH2CF3、-CH2CHF2、-CH(CH3)CN、-C(CH3)2CN、-CH2CN、-CO2H、-COCH3、-CO2CH3、-CO2C(CH3)3、-COCH(OH)CH3、-CONH2、-CONHCH3、-CON(CH3)2、-C(CH3)2CONH2、-NH2、-NHCH3、-N(CH3)2、-NHCOCH3、-N(CH3)COCH3、-NHS(O)2CH3、-N(CH3)C(CH3)2CONH2、-N(CH3)CH2CH2S(O)2CH3、-NO2、=O、-OH、-OCH3、-OCH2CH3、-OCH2CH2OCH3、-OCH2CH2OH、-OCH2CH2N(CH3)2、-OP(O)(OH)2、-S(O)2N(CH3)2、-SCH3、-S(O)2CH3、-S(O)3H、环丙基、氧杂环丁烷基、氮杂环丁烷基、(1-甲基氮杂环丁烷-3-基)氧基、N-甲基-N-氧杂环丁烷-3-基氨基、氮杂环丁烷-1-基甲基和吗啉代。
式I化合物的示例性实施方案包括式Ia-c化合物:
式I化合物的示例性实施方案包括式Id-i化合物:
式I化合物的示例性实施方案包括其中X1为N,X1为N,X1为N,X1和X3为N,X1和X2为N,或X2和X3为N的化合物,如式Ic-Ii所示。
式I化合物的示例性实施方案包括其中R5为任选取代的C1-C20杂芳基的化合物,所述杂芳基选自吡唑基、吡啶基、嘧啶基、5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基、5-乙酰基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基、6,7-二氢-4H-吡唑并[5,1-c][1,4]噁嗪-2-基和1-甲基-5-(5-(4-甲基哌嗪-1-基)吡啶-2-基。
式I化合物的示例性实施方案包括其中R5为-(C1-C20杂芳基)-(C2-C20杂环基)的化合物,其中杂芳基为任选取代的吡啶基,和杂环基为任选取代的哌嗪基。
式I化合物的示例性实施方案包括其中R5为苯基的化合物,所述苯基任选地被一个或多个选自F、Cl、-CH3、-S(O)2CH3、环丙基、氮杂环丁烷基、氧杂环丁烷基和吗啉代的基团取代。
式I化合物的示例性实施方案包括其中R5选自以下结构的化合物:
其中波浪线表示连接位点。
式I化合物的示例性实施方案包括其中R5为以下结构的化合物:
其中R8选自H、-CH3、-CH2OCH3、-CH2CH3、-CH(CH3)2、-CH2CH2OH、-CH2CH2OCH3、-CH2F、-CHF2、-CF3、-CH2CF3、-CH2CHF2、-CH(CH3)CN、-C(CH3)2CN、-CH2CN、-C(O)CH3、-C(O)CH2CH3、-C(O)CH(CH3)2、-NH2、-NHCH3、-N(CH3)2、-OH、-OCH3、-OCH2CH3、-OCH2CH2OH、环丙基和氧杂环丁烷基。
式I化合物的示例性实施方案包括其中R6为CH3的化合物。
式I化合物的示例性实施方案包括其中Y1为CH,和Y2为N,Y1为N和Y2为CH,Y1和Y2各自为CH,或Y1和Y2各自为CH,和R6为CH3的化合物。
式I化合物的示例性实施方案包括表1和2中的化合物。
本发明的式I化合物可含有不对称或手性中心,因此以不同立体异构形式存在。预期的是,本发明化合物的所有立体异构形式,包括但不限于非对映异构体、对映异构体和阻转异构体及它们的混合物如外消旋混合物,形成了本发明的部分。
此外,本发明包括所有非对映异构体,包括顺式-反式(几何)异构体和构象异构体。例如,若式I化合物含有双键或稠环,则其顺式和反式形式以及其混合物都包括在本发明的范围中。
在本申请所示的结构中,当未指定任何具体手性原子的立体化学时,则预期了所有立体异构体并且都包括在本发明的化合物中。当立体化学被表示具体构型的楔形实线(solid wedge)或虚线指定时,则所述立体异构体被如此指定和定义。
本发明化合物可以呈非溶剂化形式以及与药用溶剂如水、乙醇等形成的溶剂化形式存在,预期的是本发明包括溶剂化和非溶剂化形式。
本发明化合物可以按不同的互变异构形式存在,并且所有这些形式都包括在本发明的范围中。术语“互变异构体”或“互变异构形式”是指可通过低能垒互相转化的不同能量的结构异构体。例如,质子互变异构体(也称为质子移变互变异构体)包括通过质子迁移进行的互相转化,如酮-烯醇异构化和亚胺-烯胺异构化。价键互变异构体包括通过一些成键电子的重组进行的互相转化。
生物学评价
式I化合物作为酶活性(或其它生物活性)抑制剂的相对效力可通过以下方式来建立,所述方式为确定每种化合物抑制活性至预定义程度时的浓度,然后比较结果。通常,优选的是在生物化学测定中确定抑制50%活性的浓度,即50%抑制浓度或"IC50"。可使用本领域已知的常规技术来确定IC50值。大体上,可通过以下方式确定IC50,所述方式为在一定浓度范围的进行研究的抑制剂存在下,测量给定酶的活性。然后将通过实验获得的酶活性值对所使用的抑制剂浓度作图。将显示50%酶活性的抑制剂的浓度(与在缺少任意抑制剂情况下的活性相比较)设为IC50值。类似地,可通过活性的适当确定结果来定义其它抑制浓度。例如,在一些情况下可能期望确立90%抑制浓度即IC90,以此类推。
式I化合物是通过标准生物化学Btk激酶测定测试的(实施例901)。
可用于测试式I化合物的标准细胞Btk激酶测定的一般操作为Ramos Cell Btk测定(实施例902)。
标准细胞B-细胞增生测定可用于测试式I化合物,其中使用自Balb/c小鼠的脾纯化的B-细胞(实施例903)。
标准细胞T-细胞增生测定可用于测试式I化合物,其中使用自Balb/c小鼠的脾纯化的T-细胞(实施例904)。
可用式I化合物进行CD86抑制测定来测定其对B细胞活性的抑制,使用自8-16周龄Balb/c小鼠的脾纯化的全鼠脾细胞(实施例905)。
可用式I化合物进行B-ALL细胞存活测定来测量培养物中活B-ALL细胞的数目(实施例906)。
可用式I化合物进行CD69全血测定以确定化合物对人全血中由B淋巴细胞产生CD69的抑制,所述由B淋巴细胞产生CD69是被具有羊F(ab’)2抗人IgM的交联表面IgM激活的(实施例907)。CD69是牵涉淋巴细胞迁移和细胞因子分泌的II型C-型凝集素。CD69表达代表了最早可获得的白细胞活化指示剂之一,并且它的快速诱导是通过转录激活发生的(Vazquez et al(2009)Jour.of Immunology Published October 19,2009,doi:10.4049/jimmunol.0900839)。抗原受体刺激被选择性Btk抑制剂的浓度依赖性抑制诱导淋巴细胞激活标志物CD69的细胞表面表达(Honigberg et al(2010)Proc.Natl.Acad.Sci.107(29):13075-13080)。因此,选择性Btk抑制剂对CD69的抑制可能与一些B-细胞障碍的治疗性效力相关。示例性式I化合物的CD69Hu血液FACS IC70值呈现在表1和2中。
式I示例性化合物的细胞毒性或细胞生长抑制活性可通过以下方式来测量:在细胞培养介质中建立增生的哺乳动物肿瘤细胞系,添加式I化合物,将所述细胞培养约6小时至约5天;和测量细胞存活力(实施例908)。基于细胞的体外测定用于测量存活力,即增生(IC50),细胞毒性(EC50)和细胞凋亡的诱导(胱天蛋白酶激活)并且可用于预测抗血液恶性肿瘤和实体瘤的临床效力。
式I化合物与化疗剂的组合的体外效力可通过实施例908的细胞增生测定;荧光细胞存活力测定(从Promega Corp.,Madison,WI购得)来测量。该均相测定方法是基于鞘蛾目荧光素酶的重组表达(US 5583024;US 5674713;US 5700670)并且基于所存在的ATP(代谢活性细胞的指示物)的量确定培养物中活细胞的数目(Crouch etal(1993)J.Immunol.Meth.160:81-88;US 6602677)。所述测定是在96孔或384孔板式中进行的,使其顺从自动化高通量筛选(HTS)(Cree et al(1995)AntiCancerDrugs 6:398-404)。所述均相测量操作包括直接向在补充有血清的培养基中培养的细胞中添加单一试剂(Reagent)。不需要细胞洗涤、除去培养基和多移液步骤。在添加试剂并混合后,所述系统在10分钟内在384-孔板式中最低检测15个细胞/孔。
所述均相"添加-混合-测量"模式导致细胞溶解并生成与存在的ATP的量成比例的荧光信号。ATP的量与培养物中存在的细胞的数目成正比例。所述测定生成"辉光型"荧光信号,其是由荧光素酶反应产生的,其具有通常大于五小时的半衰期,依赖于所使用的细胞类型和培养基。活细胞以相对荧光单位(RLU)来表示。所述底物即甲虫荧光素(Beetle Luciferin)被重组萤火虫荧光素酶氧化性脱羧,伴随着ATP转化成AMP和生成光子。延长的半衰期导致不再需要使用试剂注射器并且提供以连续或分批模式加工多个板的灵活性。该细胞增生测定可用于各种多孔板式,例如96或384孔板式。数据可通过光度计或CCD相机成像设备来记录。所述荧光输出以随时间测量的相对光单元(RLU)来呈现。
式I示例性化合物和其与化疗剂的组合的抗增生效力是通过测定(实施例908)抗一些血液肿瘤细胞系来测定的。就所测试的化合物和组合建立EC50值。
制备并表征了表1和2中的示例性式I化合物,并且根据本发明的方法测试对Btk的抑制,并且具有以下结构和相应的名称(ChemDraw Ultra,版本9.0.1,和ChemBioDraw,版本11.0,CambridgeSoft Corp.,Cambridge MA)。在式I化合物或中间体存在不止一种名称时,以化学结构为准。
表1.
表2.
式I化合物的给药
可通过适于待处置的病症的途径给予式I化合物。合适的途径包括口服途径、胃肠外途径(包括皮下、肌肉内、静脉内、动脉内、皮内、鞘膜内和硬膜外途径)、经皮途径、直肠途径、经鼻途径、局部途径(包括口腔和舌下途径)、阴道途径、腹膜内途径、肺内途径和鼻内途径。对于局部免疫抑制处置,所述化合物可通过病灶内给药(intralesionaladministration)给予,包括灌注或者将移植物与抑制剂在移植之前相接触。应当理解的是,优选的途径可随着例如接受者的情况而改变。当式I化合物是经口给药时,其可与可药用载体或赋形剂配制为丸剂、胶囊、片剂等。当式I化合物是肠胃外给药时,其可与可药用的肠胃外媒介物配制,并且呈如下文详述的单位剂量可注射形式。
治疗人类患者的剂量可为约10毫克至约1000毫克的式I化合物。典型的剂量可为约100毫克至约300毫克化合物。剂量可每日一次(QID)、每日两次(BID)或更频繁给药,这取决于药物代谢动力学和药效学性质,包括具体化合物的吸收、分布、代谢和排泄。此外,毒性因素可能影响剂量和给药方案。当口服给药时,在指定时间期限内,丸剂、胶囊剂或片剂可每日服用,或以更低的频率服用。所述方案可重复多个治疗周期。
用式I化合物进行治疗的方法
本发明式I化合物用于治疗患有由异常细胞生长引起的疾病或病症的人或动物患者,因此,与Btk激酶相关的功能或行为例如免疫障碍、心血管疾病、病毒感染、炎症、代谢/内分泌障碍或神经障碍可用如下方法治疗,所述方法包括向所述患者给药如上定义的本发明化合物。也可通过以下方法制备患有癌症的人或动物患者,所述方法包括向所述患者给药如上定义的本发明化合物。所述患者的症状可因此得到好转或改善。
式I化合物可用于体外、原位和体内诊断或治疗处置动物细胞、有机体或相关病理性病症,例如全身性炎症和局部炎症、免疫-炎症性疾病如类风湿性关节炎、免疫抑制、器官移植排斥、变态反应、溃疡性结肠炎、克罗恩氏病、皮炎、哮喘、全身性红斑狼疮、舍格伦综合征、多发性硬化、硬皮病/全身性硬化症、特发性血小板减少性紫癜(ITP)、抗中性粒细胞胞质抗体(ANCA)血管炎、慢性阻塞性肺病(COPD)、牛皮癣和用于全身关节保护性作用。
本发明方法还包括治疗例如以下疾病:关节炎性疾病如类风湿性关节炎、单关节炎、骨关节炎、痛风性关节炎、脊椎炎;贝赫切特病;脓毒病、脓毒性休克、内毒素性休克、革兰氏阴性脓毒病、革兰氏阳性脓毒病和中毒性休克综合征;继发于败血症的多发性器官损伤综合征、创伤或出血;眼部障碍(ophthalmic disorder)例如变应性结膜炎、春季结膜炎、葡萄膜炎(uveitis)和甲状腺相关眼病(thyroid-associated ophthalmopathy);嗜酸细胞肉芽肿(eosinophilic granuloma);肺或呼吸疾病如哮喘、慢性支气管炎、变应性鼻炎、ARDS、慢性肺部炎症性疾病(例如,慢性阻塞性肺病)、硅肺病、肺结节病、胸膜炎(pleurisy)、肺泡炎(alveolitis)、血管炎、肺气肿(emphysema)、肺炎、支气管扩张和肺型氧中毒(pulmonary oxygen toxicity);心肌膜、脑或骨端的再灌注损伤;纤维化如囊性纤维化;瘢痕疙瘩形成或瘢痕组织形成;动脉粥样硬化;自身免疫性疾病如全身性红斑狼疮(SLE)、自身免疫性甲状腺炎、多发性硬化、一些形式的糖尿病和Reynaud综合征(Reynaud'ssyndrome);和移植排斥障碍如GVHD和同种异体移植物排斥;慢性肾小球肾炎;炎症性肠病如慢性炎症性肠病(CIBD)、克罗恩氏病、溃疡性结肠炎和坏死性小肠结肠炎;炎症性皮肤病如接触性皮炎、特应性皮炎、牛皮癣或或荨麻疹;由于感染引起的发热和肌痛;中枢或外周神经系统炎性疾病如脑膜炎、脑炎和由于小创伤引起的脑或脊髓损伤(brain or spinalcord injury due to minor trauma);斯耶格伦氏综合征(Sjogren’s syndrome);牵涉白细胞渗出的疾病(diseases involving leukocyte diapedesis);酒精性肝炎(alcoholichepatitis);细菌性肺炎(bacterial pneumonia);抗原-抗体复合物介导的疾病(antigen-antibody complexmediated disease);低血容量性休克(hypovolemic shock);I型糖尿病(Type I diabetes mellitus);急性和迟发型超敏反应(acute and delayedhypersensitivity);由于白细胞恶性增生和转移引起的病症(disease states due toleukocyte dyscrasia and metastasis);热损伤;粒细胞输注相关综合征(granulocytetransfusion-associated syndrome);和细胞因子诱导的毒性。
本发明方法还包括治疗癌症,所述癌症选自乳癌、卵巢癌、子宫颈癌、前列腺癌、睾丸癌、泌尿生殖道癌、食道癌、喉癌、成胶质细胞瘤、神经母细胞瘤、胃癌、皮肤癌、角化棘皮瘤、肺癌、表皮样癌、大细胞癌、非小细胞肺癌(NSCLC)、小细胞癌、肺腺癌、骨癌、结肠癌、腺瘤、胰腺癌、腺癌、甲状腺癌、滤泡性癌、未分化癌、乳头状癌、精原细胞瘤、黑色素瘤、肉瘤、膀胱癌、肝癌和胆道癌、肾癌、胰脏癌、骨髓障碍、淋巴瘤、毛细胞癌、口腔癌、鼻咽癌、咽癌、唇癌、舌癌、口癌、小肠癌、结肠-直肠癌、大肠癌、直肠癌、脑和中枢神经系统癌症、何杰金氏病、白血病、支气管癌、甲状腺癌、肝脏和肝内胆管癌、肝细胞癌、胃癌、神经胶质瘤/成胶质细胞瘤、子宫内膜癌、黑色素瘤、肾脏和肾盂癌、膀胱癌、子宫癌、子宫颈部癌(uterinecorpus)、多发性骨髓瘤、急性髓细胞性白血病、慢性髓细胞性白血病、淋巴细胞白血病、慢性淋巴样白血病(CLL)、髓细胞性白血病、口腔和咽癌、非何杰金淋巴瘤、黑色素瘤和绒毛状结肠腺瘤。
本发明方法可用于治疗经受或可经受再灌注损伤的受试者,所述再灌注损伤即由以下情况导致的损伤:组织或器官经受了一段时间缺血,然后再灌注。术语“局部缺血”是指由于动脉血流入受阻引起的局部组织缺血。短暂性局部缺血然后再灌注特征性地导致嗜中性粒细胞活化并在感染区转移渗过血管的内皮。经活化的嗜中性粒细胞的累积,随后导致产生反应性氧代谢产物,其破坏所牵涉的组织或器官的组分。该“再灌注损伤”现象通常与例如以下病症有关:血管性休克(包括全身缺血和局灶性缺血(global and focalischemia))、失血性休克(hemorrhagic shock)、心肌缺血(myocardial ischemia)或梗塞(infarction)、器官移植(organ transplantation)和脑血管痉挛(cerebral vasospasm)。举例而言,在心脏搭桥操作结束时或在心脏停搏过程中,当被阻止接受血液的心脏开始再灌注时就会发生再灌注损伤。预期的是,抑制Btk活性可导致所述情况中再灌注损伤量减少。
药物制剂
为了使用本发明化合物对哺乳动物(包括人)进行治疗性处置,通常根据标准药学实践将其配制为药物组合物。根据本发明的这一方面,其提供了药物组合物,其包含本发明化合物,以及结合有药用稀释剂或载体。
典型的制剂通过将本发明化合物与载体、稀释剂或赋形剂混合来制备。合适的载体、稀释剂和赋形剂是本领域技术人员公知的,并且包括以下物质,如碳水化合物、蜡、水溶性聚合物和/或水可溶胀聚合物(swellable polymer)、亲水性物质或疏水性物质、明胶、油、溶剂、水等。所用的具体载体、稀释剂或赋形剂将取决于应用本发明化合物的方式和目的。通常基于本领域技术人员认为给予哺乳动物安全的溶剂(GRAS)来选择溶剂。一般而言,安全溶剂为无毒性水性溶剂如水和可在水中溶解或混溶的其它无毒性溶剂。合适的水性溶剂包括水、乙醇、聚乙二醇(例如,PEG 400、PEG 300)等及其混合物。制剂还可包括以下物质中的一种或多种:缓冲剂、稳定剂、表面活性剂、润湿剂、润滑剂、乳化剂、助悬剂、防腐剂、抗氧化剂、遮光剂(opaquing agent)、助流剂、加工助剂(processing aid)、着色剂、增甜剂、芳香剂、矫味剂和提供药物(即本发明化合物或其药物组合物)的优质外观或辅助制造药物产品(即药物)的其它已知添加剂。
制剂可使用常规溶出和混合操作制备。例如,将散装的药品(即,本发明化合物或化合物的经稳定形式(例如,与环糊精衍生物或其它已知复合剂(complexation agent)的复合物))在一种或多种上述的赋形剂存在下溶于合适的溶剂中。通常将本发明化合物配制成以下药物剂型,所述药物剂型提供容易可控的药物剂量,且使患者能够依从所开出的方案。
根据用于给药药物的方法,用于施用的药物组合物(或制剂)可按多种方式包装。一般地,用于分配的物品(article)包括容器,容器内存放有适当形式的药物制剂。合适的容器是本领域技术人员公知的,并且包括以下物质,如瓶(塑料的和玻璃的)、小袋(sachet)、安瓿、塑料袋、金属圆筒等。容器还可包括防止不慎取得包装中的内含物的的防干扰装置(tamper-proof assemblage)。此外,在容器上具有描述容器中的内含物的标签。所述标签还可包括适当的注意事项。
可制备本发明化合物的药物制剂用于多种给药途径和类型。例如,具有期望纯度的式I化合物可任选与药用稀释剂、载体、赋形剂或稳定剂(Remington's PharmaceuticalSciences(1980)16th edition,Osol,A.Ed.)以冻干制剂、磨细的粉末剂或水溶液剂形式混合。配制可如下进行:在环境温度在适当的pH以及在适当的纯度,与生理学可接受的载体(即在采用的剂量和浓度下对接受者是无毒性的载体)混合。配制的pH主要取决于具体用途和化合物的浓度,但范围可为约3至约8。在pH为5的乙酸盐缓冲液中配制是合适的实施方案。
化合物通常可按固体组合物、冻干制剂或水性溶液剂形式储存。
按与良好医学实践一致的方式(即,量、浓度、时间表、过程、媒介物和给药途径)来配制、确定剂量和给药本发明的药物组合物。在此背景下考虑的因素包括所治疗的具体障碍、所治疗的具体哺乳动物、个体患者的临床情况、病症的起因、药物的递送位点、给药方法、给药的时间表和医学实践者已知的其它因素。所给药的化合物的“治疗有效量”将由这些考虑因素控制,并且是预防、改善或治疗过度增殖性病症所需的最小量。
作为通常的建议,每剂量肠胃外给药的初始药学有效量的抑制剂为约每日0.01-100毫克/kg,即约0.1至20毫克/kg患者体重,所使用的化合物的典型的最初范围为0.3至15毫克/kg/日。
可接受的稀释剂、载体、赋形剂和稳定剂在所用的剂量和浓度下对接受者是无毒性的,并且包括缓冲剂如磷酸盐、枸橼酸盐和其它有机酸;抗氧化剂,包括抗坏血酸和蛋氨酸(methionine);防腐剂(如十八烷基二甲基苄基氯化铵;氯化六甲双铵(hexamethoniumchloride);苯扎氯铵、苄索氯胺;苯酚、丁醇或苄醇;对羟基苯甲酸烷基酯,如对羟基苯甲酸甲酯或对羟基苯甲酸丙酯;儿茶酚;间苯二酚(resorcinol);环己醇;3-戊醇和间甲酚);低分子量(少于约10个残基)多肽;蛋白质,如血清白蛋白、明胶或免疫球蛋白;亲水性聚合物,如聚乙烯吡咯烷酮;氨基酸,如甘氨酸、谷氨酰胺、天冬酰胺、组氨酸、精氨酸或赖氨酸;单糖、二糖和其它碳水化合物,包括葡萄糖、甘露糖或糊精;螯合剂,如EDTA;糖如蔗糖、甘露醇、海藻糖或山梨醇;成盐的抗衡离子,如钠;金属络合物(例如,Zn-蛋白质络合物);和/或非离子型表面活性剂,如TWEENTM、PLURONICSTM或聚乙二醇(PEG)。活性药物成分还可包埋在通过例如凝聚技术或通过界面聚合制备的微胶囊中,例如在胶体药物递送系统(例如脂质体、白蛋白微球、微乳液、纳米颗粒和纳米胶囊(nanocapsules))中或在巨乳液(macroemulsion)中,分别为羟基甲基纤维素或明胶微胶囊和聚-(甲基丙烯酸甲酯)微胶囊。所述技术披露于Remington's Pharmaceutical Sciences 16th edition,Osol,A.Ed.(1980)中。
可制备式I化合物的缓释制剂。缓释制剂的合适实例包括含有式I化合物的固态疏水性聚合物的半渗透性基质,其中基质以成形的制品形式(例如薄膜或微胶囊)存在。缓释基质的实例包括聚酯、水凝胶(例如,聚(甲基丙烯酸2-羟基乙酯)或聚(乙烯醇))、聚交酯(US3773919)、L-谷氨酸和γ-乙基-L-谷氨酸的共聚物、非降解性乙烯-乙酸乙烯酯、降解性乳酸-羟乙酸共聚物如LUPRON DEPOTTM(由乳酸-羟乙酸共聚物和醋酸亮丙瑞林组成的可注射微球)和聚-D-(-)-3-羟基丁酸。
所述制剂包括适于本申请详述的给药途径的那些制剂。制剂可适宜地以单位剂量形式存在并可通过药学领域公知的任何方法制备。技术和制剂通常参见Remington'sPharmaceutical Sciences(Mack Publishing Co.,Easton,PA)。所述方法包括使活性成分与构成一种或多种助剂(accessory ingredient)的载体结合的步骤。通常,制剂如下制备:使活性成分与液态载体或微细粉碎的固态载体或与这两种载体同时均匀和紧密的结合,然后必要时,对产品进行成型。
适于口服给药的式I化合物的制剂可制备为离散的单位,如各自含有预定量的式I化合物的丸剂、胶囊剂、扁囊剂或片剂。压制片可如下制备:在合适的机器中对自由流动形式(如粉末或颗粒)的活性成分以及任选混合的粘合剂、润滑剂、惰性稀释剂、防腐剂、表面活性剂或分散剂进行压制。模制片可如下制备:在合适的机器中对用惰性液态稀释剂润湿的粉末状活性成分的混合物进行模制。可任选对片剂进行包衣或刻痕,并任选进行配制以提供活性成分从其中缓慢或控制释放。可制备片剂、含片(troche)、糖锭、水性混悬剂或油性混悬剂、可分散粉末剂或可分散颗粒剂、乳剂、硬胶囊剂或软胶囊剂例如明胶胶囊、糖浆剂或酏剂,以用于口服。预期用于口服的式I化合物的制剂可根据制备药物组合物的领域已知的任何方法制备,所述组合物可含有一种或多种试剂,包括增甜剂、矫味剂、着色剂和防腐剂,以提供适口的制剂。含有活性成分以及混合有适于制造片剂的无毒性生理学可接受的赋形剂的片剂是可接受的。这些赋形剂可以是,例如,惰性稀释剂,如碳酸钙或碳酸钠、乳糖、磷酸钙或磷酸钠;造粒剂和崩解剂(granulating and disintegrating agent),如玉米淀粉或海藻酸;粘合剂,如淀粉、明胶或阿拉伯胶;以及润滑剂,如硬脂酸镁、硬脂酸或滑石。片剂可以是未包衣的或可通过已知技术(包括微胶囊化)包衣,以延迟在胃肠道的崩解和吸收,由此在较长的时间提供持续的作用。例如,可采用延时物质,如单独的或与蜡结合的单硬脂酸甘油酯或二硬脂酸甘油酯。
对于治疗眼部或其它外部组织如嘴和皮肤而言,所述制剂优选应用为局部软膏剂(ointment)或乳膏剂(cream),其含有的活性成分的量为例如,0.075至20%w/w。当配制成软膏剂时,活性成分可与石蜡(paraffinic)或可与水混溶的软膏基质一起使用。可供选择地,活性成分可与水包油性乳膏基质一起配制成乳膏。如果期望的话,乳膏基质的水相可包括多元醇(即,具有两个或更多个羟基的醇),如丙二醇、丁-1,3-二醇、甘露醇、山梨醇、甘油和聚乙二醇(包括PEG 400)及这些醇的混合物。局部制剂可预期包括增强活性成分通过皮肤或其它作用区域吸收或渗透的化合物。所述皮肤渗透增强剂的实例包括二甲基亚砜和相关类似物。本发明乳剂的油相可由已知成分以已知方式构成。尽管所述相可仅包含乳化剂,但期望的是包括至少一种乳化剂与脂肪或油的混合物或至少一种乳化剂与脂肪和油两者的混合物。优选地,亲水性乳化剂与亲脂性乳化剂一起用作稳定剂。还优选的是,即包括油又包括脂肪。含有或不含有稳定剂的乳化剂构成了所谓的乳化蜡(emulsifying wax),所述蜡和油和脂肪一起构成了形成软膏制剂的油性分散相的所谓乳化软膏基质。适用于本发明制剂的乳化剂和乳化稳定剂包括60、80、十八醇/十六醇(cetostearylalcohol)、苄醇、肉豆蔻醇、单硬脂酸甘油酯和月桂基硫酸钠。
式I化合物的水性混悬剂含有活性物质以及混合有适于制备水性混悬剂的赋形剂。所述赋形剂包括助悬剂,如羧甲基纤维素钠、交联羧甲基纤维素、聚维酮、甲基纤维素、羟丙基甲基纤维素、海藻酸钠、聚乙烯吡咯烷酮、西黄蓍胶和阿拉伯胶,以及分散剂或润湿剂(dispersing or wetting agent),如天然存在的磷脂(例如,卵磷脂)、氧化烯与脂肪酸的缩合产物(例如,聚氧乙烯硬脂酸酯)、环氧乙烷与长链脂肪醇的缩合产物(例如,十七亚乙氧基十六醇(heptadeca ethyleneoxycetanol))、环氧乙烷与衍生自脂肪酸和己糖醇脱水物(hexitol anhydride)的偏酯的缩合产物(例如,聚氧乙烯脱水山梨糖醇单油酸酯(polyoxyethylene sorbitan monooleate))。水性混悬剂还可含有一种或多种防腐剂如对羟基苯甲酸乙酯或对羟基苯甲酸正丙酯、一种或多种着色剂、一种或多种矫味剂和一种或多种增甜剂如蔗糖或糖精。
式I化合物的药物组合物可呈无菌注射制剂,如无菌注射水性混悬剂或油性混悬液制剂形式存在。该混悬液可使用上文已提及的合适的分散剂或润湿剂和助悬剂根据本领域已知方法配制。无菌注射制剂还可以是于无毒性的肠胃外可接受的稀释剂或溶剂中的无菌注射溶液或混悬液,如于1,3-丁二醇中的溶液,或制备为冻干粉末。可使用的可接受媒介物和溶剂包括水、林格氏溶液(Ringer's solution)和等张氯化钠溶液。此外,无菌不挥发性油(sterile fixed oil)通常可用作溶剂或助悬介质。出于该目的,可采用任何温和的不挥发性油,包括合成性甘油一酯或甘油二酯。此外,脂肪酸如油酸同样可用于制备注射剂。
可与载体物质结合以产生单一剂量形式的活性成分的量将随着所治疗的宿主和具体的给药模式而变化。例如,意在对人类口服给药的定时释放制剂可含有约1至1000毫克活性物质,以及混合有适当和适宜量的载体物质,所述载体其可占总组合物的约5至约95%(重量:重量)。可制备药物组合物以提供给药时容易测量的量。例如,意在用于静脉输注的水溶液每毫升溶液可含有约3至500μg活性成分,从而实现以约30毫升/hr的速率输注合适体积。
适于肠胃外给药的制剂包括水性和非水性无菌注射溶液剂,其可含有抗氧化剂、缓冲剂、抑菌剂和使得制剂与预期接受者的血液等张的溶质;以及水性和非水性无菌混悬剂,其可包括助悬剂和增稠剂。
适于局部给药至眼部的制剂还包括滴眼剂,其中将活性成分溶于或悬浮于合适的载体(尤其是活性成分的含水溶剂)中。在所述制剂中存在的活性成分的浓度优选为约0.5至20%w/w,例如约0.5至10%w/w,例如约1.5%w/w。
适于在口内局部给药的制剂包括糖锭(lozenge),其含有于矫味基质(通常是蔗糖和阿拉伯胶或西黄蓍胶)中的活性成分;锭剂(pastille),其含有于惰性基质(如明胶和甘油,或蔗糖和阿拉伯胶)中的活性成分;以及漱口剂,其包含于液态载体中的活性成分。
适于直肠给药的制剂可呈现为栓剂形式,其具有合适基质(其包含例如可可脂或水杨酸酯(盐))。
适于肺内或经鼻给药的制剂具有例如为0.1至500微米的粒度(包括在0.1和500微米之间,增量为例如0.5、1、30微米、35微米等的粒度),其通过鼻道经快速吸入给药或通过口经吸入给药,以便到达肺泡囊(alveolar sacs)。合适的制剂包括活性成分的水性或油性溶液剂。适于气雾剂或干粉给药的制剂可根据常规方法制备,并可与其它治疗药物(如迄今用于治疗或预防下文所述的病症的化合物)一起递送。
适于阴道给药的制剂可呈现为阴道栓剂、棉塞(tampon)、乳膏剂、凝胶剂、糊剂、泡沫或喷雾制剂,这些制剂除了活性成分外还含有本领域已知为适当的载体。
制剂可包装在单位剂量或多剂量容器例如密封安瓿或小瓶中,并且可在冷冻干燥(冻干)条件下储存,在即将使用前仅需要加入无菌液态载体例如水,用于注射。即时注射溶液剂和混悬剂(Extemporaneous injection solutions and suspension)从前述种类的无菌粉末、颗粒和片剂制备。优选的单位剂量制剂是含有本申请上文所述的日剂量或单位日亚剂量(sub-dose)或其适当分数的活性成分的制剂。
本发明还提供了兽用组合物(veterinary composition),由此其含有上文定义的至少一种活性成分以及兽用载体。兽用载体是用于给药所述组合物目的的物质,并可为固态、液态或气态物质,这些物质在兽医领域要么是惰性的要么是可接受的,并且与活性成分相容。这些兽用组合可经肠胃外、口服或经任何其它期望的途径给药。
联用治疗
式I化合物可单独使用或与其它治疗药物联用,用来治疗本申请描述的疾病或病症,如炎症和过度增殖性病症(例如,癌症)。在某些实施方案中,式I化合物与具有抗炎或抗过度增殖性质或用于治疗炎症、免疫应答障碍或过度增殖性病症(例如,癌症)的额外的第二种化合物在药物组合制剂或给药方案中作为联用治疗组合。所述额外的治疗剂可为抗炎剂、免疫调节剂、化疗剂、细胞凋亡增强剂、亲神经因子、用于治疗心血管疾病的药物、用于治疗肝病的药物、抗病毒药物、用于治疗血液障碍的药物、用于治疗糖尿病的药物和用于治疗免疫缺陷障碍的药物。所述第二种治疗剂可为NSAID抗炎药物。所述第二种治疗剂可为化疗药物。药物组合制剂或给药方案的第二种化合物优选具有对式I化合物的补充活性,由此它们不彼此不利地影响。在组合中所述化合物的存在量适宜地为对于所预期的目的是有效的量。在一个实施方案中,本发明的组合物包含与治疗剂例如NSAID联用的式I化合物或其立体异构体、互变异构体、溶剂化物、代谢物或药用盐或前药。
联用治疗可作为同时或先后方案给药。当先后给药时,组合物可按两次或多次给药方式给药。联用给药包括使用分开的制剂或单一的药物制剂同时给药,和以任意顺序先后给药,其中优选的是存在两种(或所有)活性药物同时发挥其生物活性的一段时间。
任何上述同时给药药物的合适剂量是目前所用的剂量,并且由于新鉴定的药物和其它治疗药物或治疗的联用作用(协同),所述剂量可降低。
联用治疗可提供“协同(synergy)”及提供“协同作用(synergistic)”,即,当活性成分一起使用时实现的作用大于分开使用这些化合物导致的作用的总和。当活性成分:(1)在组合的单位剂量制剂中同时配制以及同时给药或递送时;(2)作为分开的制剂经交替或平行递送时;或(3)通过一些其它方案给药时,可达到协同作用。当在交替治疗中递送时,当化合物例如通过在分开的注射器中分开注射,通过分开的丸剂或胶囊剂或分开输注而先后给药或递送时,可达到协同作用。一般而言,在交替治疗期间,将有效剂量的各种活性成分先后(即顺次)给药,而在联用治疗中,将有效剂量的两种或多种活性成分一起给药。
在具体的治疗实施方案中,式I化合物或其立体异构体、互变异构体、溶剂化物、代谢物或药用盐或其前药,可与其它治疗药物、激素药物或抗体药物(例如本申请描述的药物)联用,或与外科治疗和放射治疗联用。本发明的联用治疗由此包括给药至少一种式I化合物或其立体异构体、互变异构体、溶剂化物、代谢物或药用盐或前药,以及使用至少一种其它癌症治疗方法。对式I化合物和其它药学活性的化疗药物的量和相关的给药时限进行选择,以便实现期望的联用治疗作用。
式I化合物的代谢物
本申请描述的式I的体内代谢产物也落入本发明的范围内。所述产物可以是由例如所给药化合物的氧化、还原、水解、酰胺化、脱酰胺化、酯化、脱脂化、酶法裂解等而引起的。因此,本发明包括式I化合物的代谢物,包括由以下方法产生的化合物,所述方法包括使本发明化合物与哺乳动物接触足以产生其代谢产物的一段时间。
代谢产物通常如下鉴定:制备本发明化合物的放射标记的(例如,14C或3H)同位素,将其以可检测的剂量(例如,大于约0.5毫克/kg)肠胃外给药至动物,如大鼠、小鼠、豚鼠、猴或给药至人,允许足够发生代谢的时间(通常约30秒至30小时),然后将其转化产物与尿、血样或其它生物样品中分离。这些产物容易分离,因为它们进行了标记(其它的通过使用能够与代谢物中存活的抗原表位结合的抗体来分离)。通过常规方式例如MS、LC/MS或NMR分析确定代谢物结构。一般而言,代谢物的分析以与本领域技术人员公知的常规药物代谢研究中相同的方式来完成。所述代谢产物,只要它们不是在体内另外存在的,就用于本发明化合物的治疗剂量的诊断测定。
制品
在本发明的另一实施方案中,其提供了含有用于治疗上文描述的疾病和病症的物质的制品和“试剂盒”。在一个实施方案中,所述试剂盒包含容器,所述容器包含式I化合物或其立体异构体、互变异构体、溶剂化物、代谢物或药用盐或前药。所述试剂盒还可包含附在容器上或容器中的标签或包装说明书。术语“包装说明书”用来指通常包括在治疗产品的市售包装中的说明书,其含有关于适应症、用法、剂量、给药、禁忌症和/或注意事项的信息,这些信息涉及所述治疗产品的使用。合适的容器包括,例如,瓶、小瓶、注射器、泡罩包装(blister pack)等。容器可从多种材料(如玻璃或塑料)形成。容器可装有有效治疗所述病症的式I的化合物或其制剂,并可具有无菌入口(例如,容器可为静脉注射溶液袋或具有可由皮下注射针头刺穿的塞子的小瓶)。组合物中的至少一种活性药物是式I化合物。标签或包装说明书指示所述组合物用于治疗选择的病症如癌症。此外,标签或包装说明书可指示待治疗的患者是患有病症如过度增殖性病症、神经变性、心脏肥大、疼痛、偏头痛或神经创伤性疾病或事件的患者。在一个实施方案中,标签或包装说明书指示包含式I化合物的组合物可用于治疗起因于异常细胞生长的病症。标签或包装说明书还可指示所述组合物可用于治疗其它病症。可供选择地或另外地,所述制品还可包含第二种容器,所述容器包含药用缓冲液,如抑菌性注射用水(BWFI)、磷酸盐缓冲生理盐水、林格氏溶液和葡萄糖溶液。试剂盒还可包括从商业和使用者角度看是期望的其它物质,包括其它缓冲液、稀释剂、滤器、针头和注射器。
试剂盒还可包含给药式I化合物以及第二种药物制剂(如果存在)的说明。例如,若试剂盒包含第一种组合物(含有式I化合物)和第二种药物制剂,则试剂盒还可包含将第一种和第二种药物组合物同时、先后或分开给予需要所述制剂的患者的说明。
在另一实施方案中,试剂盒适于递送固态口服形式的式I化合物,如片剂或胶囊剂。这样的试剂盒优选包括多个单位剂量。所述试剂盒可以包括针对预期用途为目的的剂量卡片。这样的试剂盒的一个实例是“泡罩包装”。泡罩包装在包装工业中是公知的,并且广泛用于包装药物单位剂量形式。如果期望的话,可提供记忆辅助装置(memory aid),其可呈例如数字、字母或其它标记形式,或具有日历插入物,所述记忆辅助装置指定在可对所述剂量进行给药的治疗时间表中的天数。
根据一实施方案,试剂盒可包含(a)在其中含有式I化合物的第一容器;以及任选地(b)在其中含有第二种药物制剂的第二容器,其中所述第二种药物制剂包含具有抗过度增殖活性的第二种化合物。可供选择地或另外地,所述试剂盒还可包含第三容器,其包含药用缓冲液,如抑菌性注射用水(BWFI)、磷酸盐缓冲生理盐水、林格氏溶液和右旋糖溶液。其还可包括从商用和使用者角度来看是期望的其它物质,包括其它缓冲液、稀释剂、滤器、针头和注射器。
在试剂盒包含式I和第二种治疗药物的组合物的某些其它实施方案中,所述试剂盒可包含用于容纳分开的组合物的容器,如分开的瓶或分开的箔包装(foil packet),然而,分开的组合物还可容纳在单一的未分开的容器中。典型地,试剂盒包含给药分开的组分的说明。当分开的组分优选以不同剂量形式(例如口服和肠胃外)给药时,当以不同剂量间隔给药时,或当对联用的单独组分进行滴定对开具处方的医师是期望之时,试剂盒形式是特别有益的。
式I化合物的制备
可通过包括与化学领域公知的那些方法类似的方法的合成路线合成式I化合物,特别是根据本申请所含的描述和在以下文献中针对杂环描述的那些方法合成式I化合物,所述文献为:Comprehensive Heterocyclic Chemistry II,Editors Katritzky andRees,Elsevier,1997,e.g.Volume 3;Liebigs Annalen der Chemie,(9):1910-16,(1985);Helvetica Chimica Acta,41:1052-60,(1958);Arzneimittel-Forschung,40(12):1328-31,(1990),将这些文献各自明确并入本申请作为参考。起始物质通常由商业来源获得,例如Aldrich Chemicals(Milwaukee,WI)或使用本领域技术人员公知的方法容易地制备(例如,通过以下文献中一般描述的方法来制备:Louis F.Fieser and MaryFieser,Reagents for Organic Synthesis,v.1-23,Wiley,N.Y.(1967-2006ed.),orBeilsteins Handbuch der organischen Chemie,4,Aufl.ed.Springer-Verlag,Berlin,(包括增刊)(也可通过Beilstein在线数据库获得))。
合成式I化合物中有用的合成化学性转化和保护基方法学(保护和脱保护)及必要试剂和中间体是本领域公知的并包括例如在以下文献中披露的那些,所述文献为R.Larock,Comprehensive Organic Transformations,VCH Publishers(1989);T.W.Greene and P.G.M.Wuts,Protective Groups in Organic Synthesis,3rd Ed.,JohnWiley and Sons(1999);和L.Paquette,ed.,Encyclopedia of Reagents for OrganicSynthesis,John Wiley和Sons(1995)及其随后版本。
式I的化合物可单独制备或作为包含至少2种,例如5至1,000种或10至100种化合物的化合物库来制备。式I的化合物库可通过本领域技术人员已知的操作,使用溶液相或固相化学,通过组合的“分裂和混合(split and mix)”途径来制备,或通过多平行合成(multiple parallel syntheses)来制备。因此,本发明另一个方面提供了含有至少2种化合物或其药用盐的化合物库。
附图和实施例提供了制备式I化合物的示例性方法。本领域技术人员理解的是,其它合成路线可用于合成式I化合物。尽管附图和实施例描述和讨论的是具体起始物质和试剂,但其它起始物质和试剂可容易地代替所述具体的起始物质和试剂以得到多种衍生物和/或反应条件。此外,可根据本说明书披露的内容用本领域技术人员公知的常规化学方法将通过所述方法制备的示例性化合物中的多个作进一步修饰。
在制备式I化合物中,可能有必要保护中间体的远端官能团(例如,伯胺或仲胺)。是否需要所述保护取决于远端官能团的性质和制备方法的条件。适当的氨基-保护基包括乙酰基、三氟乙酰基、叔丁氧羰基(BOC)、苄氧羰基(CBz)和9-芴基亚甲基氧基羰基(Fmoc)。本领域技术人员可容易地确定是否需要所述保护。对于保护基和它们用途的一般描述,参见T.W.Greene,Protective Groups in Organic Synthesis,John Wiley&Sons,New York,1991。
用于制备式I化合物的实验操作、中间体和试剂可在美国专利13/102720,“PYRIDONE AND AZA-PYRIDONE COMPOUNDS AND METHODS OF USE”(2011年5月6日提交)中找到,将其全文并入本申请作为参考。
图1-24描述了式I化合物101-124的示例性实施方案的合成,更充分地描述在实施例101-124中,并且可用于制备其它式I化合物。
一般制备性操作
一般操作:苏楚基偶联(Suzuki Coupling)
所述苏楚基型偶联反应用于形成碳-碳键,从而将式I化合物的环与中间体例如A-3相连(Suzuki(1991)Pure Appl.Chem.63:419-422;Miyaura and Suzuki(1979)Chem.Reviews 95(7):2457-2483;Suzuki(1999)J.Organometal.Chem.576:147-168)。苏楚基偶联为杂芳基卤化物例如B-2或B-4与硼酸例如A-1或A-2进行的钯介导的交叉偶联反应。例如,B-2可与约1.5当量的4,4,4',4',5,5,5',5'-八甲基-2,2'-二(1,3,2-二氧杂硼杂戊环)组合,并溶解在约3当量的碳酸钠(其为1M的水溶液)和等体积的乙腈中。添加催化量或更多量的低价钯试剂例如二(三苯基膦)二氯化钯(II)。在一些情况下,用醋酸钾代替碳酸钠以调节水层的pH。然后将反应混合物在微波反应器(Biotage AB,Uppsala,Sweden)中减压加热至约140-150℃,保持10-30分钟。将内容物用乙酸乙酯或另一种有机溶剂萃取。蒸发有机层后,可在硅胶上或通过反相HPLC来纯化硼酯A-1。取代基如所定义的那样,或为其受保护形式或前体。同样,可将溴化物中间体B-4硼化得到A-2。
B-2与A-2或A-1与B-4的苏楚基偶联得到式I化合物或中间体A-3。将硼酸酯(或酸)(1.5当量)A-1或A-2和钯催化剂例如二(三苯基膦)二氯化钯(II)(0.05eq)添加到卤代中间体(1eq)B-2或B-4于乙腈和1M碳酸钠水溶液(与乙腈等体积)中的混合物中。将反应混合物在微波中在约150℃加热约15分钟。LC/MS表明此时反应完成。向混合物中加入水,过滤析出的产物并通过HPLC纯化得到产物A-3。取代基R1’、R2’、R4’可为如本申请所定义的R1、R2、R4或其受保护形式或前体。
可在苏楚基偶联步骤中使用多种钯催化剂。各种低价Pd(II)和Pd(0)催化剂可用在苏楚基偶联反应中,包括PdCl2(PPh3)2、Pd(t-Bu)3、PdCl2dppf CH2Cl2、Pd(PPh3)4、Pd(OAc)/PPh3、Cl2Pd[(Pet3)]2、Pd(DIPHOS)2、Cl2Pd(Bipy)、[PdCl(Ph2PCH2PPh2)]2、Cl2Pd[P(邻甲苯基)3]2、Pd2(dba)3/P(邻甲苯基)3、Pd2(dba)/P(呋喃基)3、Cl2Pd[P(呋喃基)3]2、Cl2Pd(PMePh2)2、Cl2Pd[P(4-F-Ph)3]2、Cl2Pd[P(C6F6)3]2、Cl2Pd[P(2-COOH-Ph)(Ph)2]2、Cl2Pd[P(4-COOH-Ph)(Ph)2]2和包封的催化剂Pd EnCatTM 30、Pd EnCatTM TPP30和Pd(II)EnCatTMBINAP30(US 2004/0254066)。
一般操作:Buchwald反应(Buchwald reaction)
所述Buchwald反应用于氨化6-溴中间体B-1(Wolf和Buchwald(2004)Org.SynthColl.Vol.10:423;Paul et al(1994)Jour.Amer.Chem.Soc.116:5969-5970)。向卤代中间体B-1于DMF中的溶液中加入适当的胺R5-NH2(200mol%)、Cs2CO3(50mol%)、Pd2(dba)3(5mol%)和4,5-二(二苯基膦基)-9,9-二甲基呫吨(Xantphos,CAS Reg.No.161265-03-8,10mol%)。将反应混合物在微波反应器(Biotage AB,Uppsala,Sweden)中在约110℃减压加热约30分钟。真空浓缩所得溶液得到B-2。也可使用其它钯催化剂和膦配体。
N-杂芳基酰胺中间体B-4也可在Buchwald条件下用环状酰胺中间体(R7)例如3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮101e与杂芳基二溴化物B-3来制备。
分离方法
在制备式I化合物的方法中,将反应产物彼此分离和/或与原料分离可能是有益的。通过本领域常见技术将每步或多步中期望的产物分离和/或纯化为期望的同质性程度。通常所述分离涉及多相萃取、用溶剂或溶剂混合物结晶、蒸馏、升华或色谱法。色谱法可涉及多种方法,包括例如:反相和正相;尺寸排阻(size exclusion);离子交换;高、中和低压液相色谱方法和装置;小规模分析;模拟移动床(SMB)和制备性薄层或厚层色谱,以及小规模薄层和快速色谱技术。
另一类分离方法涉及用所选择的试剂处理混合物,从而与期望的产物、未反应的原料、反应副产物等结合或使得期望的产物、未反应的原料、反应副产物等分离。所述试剂包括吸附剂(adsorbent)或吸收剂(absorbent),如活性炭、分子筛、离子交换介质等。可供选择地,所述试剂可以是酸(在碱性物质的情况下),碱(在酸性物质的情况下),结合剂如抗体、结合蛋白,选择性螯合剂如冠醚,液/液离子交换试剂(LIX)等。对适当的分离方法的选择依赖于所涉及的物质的性质。例如,沸点和分子量(在蒸馏和升华中)、存在或不存在极性官能团(在色谱法中)、在酸性和碱性介质中物质的稳定性(在多相萃取中)等等。
可通过本领域技术人员公知的方法(如色谱法和/或分级结晶),基于非对映异构体的物理化学差别,将非对映异构混合物分离为其单独的非对映异构体。对映异构体可通过以下方式分离:通过使对映异构体混合物与适当的光学活性的化合物(例如,手性助剂如手性醇或Mosher酰氯(Mosher’s acid chloride))反应将其转化为非对映异构混合物,分离非对映异构体,然后将单独的非对映异构体转化(例如,水解)为相应的纯的对映异构体。此外,一些本发明化合物可以是阻转异构体(例如,取代的联芳(biaryl))并视为本发明的部分。对映异构体也可通过使用手性HPLC柱分离。
单一的立体异构体,例如,基本上不含其立体异构体的对映异构体,可通过以下方式获得:使用诸如形成非对映异构体的方法,用光学活性的拆分剂来拆分外消旋混合物(Eliel,E.and Wilen,S.“Stereochemistry of Organic Compounds,”John Wiley&Sons,Inc.,New York,1994;Lochmuller,C.H.,(1975)J.Chromatogr.,113(3):283-302)。本发明的手性化合物的外消旋混合物可通过任何合适的方法分开和离析,所述方法包括:(1)与手性化合物形成离子性非对映异构的盐,然后通过分级结晶或其它方法分离,(2)与手性衍生试剂形成非对映异构的化合物,分离所述非对映异构体,然后转化为纯的立体异构体,(3)在手性条件下直接分离基本上纯的或富集的立体异构体。参见:“Drug Stereochemistry,Analytical Methods and Pharmacology,”Irving W.Wainer,Ed.,Marcel Dekker,Inc.,New York(1993)。
在方法(1)的情况下,非对映异构的盐可通过以下方式形成:使对映异构纯的手性碱如马钱子碱(brucine)、奎宁、麻黄碱、番木鳖碱(strychnine)、α-甲基-β-苯基乙胺(安非他明)等与带有酸性官能团的不对称化合物如羧酸和磺酸反应。可通过分级结晶或离子色谱法诱导非对映异构体盐分离。对于氨基化合物的光学异构体的分离而言,加入手性羧酸或磺酸如樟脑磺酸、酒石酸、扁桃酸或乳酸可引起非对映异构体的盐的形成。
可供选择地,通过方法(2),使待拆分的底物与手性化合物的一种对映异构体反应,形成非对映异构对(E.and Wilen,S.“Stereochemistry of Organic Compounds”,JohnWiley&Sons,Inc.,1994,p.322)。非对映异构化合物可通过以下方式形成:使不对称化合物与对映异构纯的手性衍生试剂如薄荷基衍生物反应,接着分离非对映异构体,然后水解得到纯的或富集的对映异构体。确定光学纯度的方法涉及制备外消旋混合物的手性酯,如在碱的存在下制备薄荷基酯例如(-)氯甲酸薄荷基酯,或Mosher酯,乙酸α-甲氧基-α-(三氟甲基)苯基酯(Jacob III.J.Org.Chem.,(1982)47:4165),然后就两种阻转异构的对映异构体或非对映异构体的存在而分析1H NMR光谱。阻转异构化合物的稳定的非对映异构体可遵循分离阻转异构的萘基-异喹啉(WO96/15111)的方法通过正相和反相色谱分开和离析。通过方法(3),两种对映异构体的外消旋混合物可使用手性固定相通过色谱来分离(“ChiralLiquid Chromatography”(1989)W.J.Lough,Ed.、Chapman and Hall,New York;Okamoto,J.Chromatogr.,(1990)513:375-378)。富集的或纯化的对映异构体可通过用于区分带有不对称碳原子的其它手性分子的方法(如旋光性或圆二色性)来区分。
实施例
实施例101a 2,2,2-三氯-1-(4,5,6,7-四氢-1H-吲哚-2-基)乙酮101a
将配备有磁力搅拌子、冷凝器和氮气进气口的100-mL单颈圆底烧瓶用氮气吹洗并装入4,5,6,7-四氢-1H-吲哚(3.00g,24.8mmol)、三氯乙酰氯(13.5g,74.4mmol)和1,2-二氯乙烷(50mL)。将溶液在85℃搅拌2小时。之后,减压浓缩反应混合物得到100%收率(6.50g)的2,2,2-三氯-1-(4,5,6,7-四氢-1H-吲哚-2-基)乙酮101a,其为黑色半固体:1H NMR(500MHz,DMSO-d6)δ11.94(s,1H),7.05(s,1H),2.62(t,2H,J=6.0Hz),2.47(t,2H,J=6.0Hz),1.80(m,2H),1.65(m,2H);MS(ESI+)m/z 266.0(M+H)
实施例101b 4,5,6,7-四氢-1H-吲哚-2-羧酸乙酯101b
将配备有磁力搅拌子和氮气进气口的100-mL单颈圆底烧瓶用氮气吹洗并装入101a(6.50g,24.8mmol)、乙醇钠(17.0mg,0.25mmol)和乙醇(40mL)。将溶液在室温搅拌1小时。之后,减压浓缩反应混合物。将残余物通过柱色谱法来纯化得到100%收率(4.80g)的4,5,6,7-四氢-1H-吲哚-2-羧酸乙酯101b,其为棕色固体:mp 70–72℃;1H NMR(300MHz,CDCl3)δ9.08(s,1H),6.75(s,1H),4.25(q,2H,J=7.2Hz),2.65(t,2H,J=6.0Hz),2.56(t,2H,J=6.0Hz),1.85(m,4H),1.28(t,3H,J=7.2Hz);MS(ESI+)m/z 194.1(M+H)
实施例101c 1-(氰基甲基)-4,5,6,7-四氢-1H-吲哚-2-羧酸乙酯101c
将配备有磁力搅拌子和氮气进气口的125-mL单颈圆底烧瓶用氮气吹洗并装入101b(5.76g,29.8mmol)和DMF(50mL)。将溶液用冰浴冷却至0℃。加入NaH(60%分散于矿物油中,1.43g,35.8mmol)。将所得混合物在室温搅拌1小时。之后,加入溴乙腈(1.43g,35.8mmol)。将混合物在室温搅拌14小时。之后减压浓缩反应混合物,并将残余物在乙酸乙酯(150mL)和水(450mL)之间分配。分离出有机层,并将水层用乙酸乙酯(3×150mL)萃取。将合并的有机层用盐水洗涤,用硫酸钠干燥并减压浓缩。将残余物通过柱色谱法来纯化得到55%收率(3.80g)的1-(氰基甲基)-4,5,6,7-四氢-1H-吲哚-2-羧酸乙酯101c,其为黄色半固体:1H NMR(300MHz,CDCl3)δ6.66(s,1H),5.29(s,2H),4.28(q,2H,J=7.2Hz),2.62(t,2H,J=6.3Hz),2.49(t,2H,J=6.3Hz),1.92(m,2H),1.75(m,2H),1.33(t,3H,J=7.2Hz);MS(ESI+)m/z 233.1(M+H)
实施例101d 1-(2-氨基乙基)-4,5,6,7-四氢-1H-吲哚-2-羧酸乙酯101d
将200-mL帕尔反应瓶用氮气吹洗并装入10%钯/炭(50%水分,1.28g干重)、101c(3.00g、12.9mmol)、12%盐酸(6.5mL、25mmol)、乙酸乙酯(60mL)和乙醇(40mL)。将所述瓶连于帕尔氢化器,排空,充入氢气至压力为50psi并震摇6小时。之后,将氢气排空,并将氮气充入所述瓶中。加入硅藻土过滤剂(Imerys Minerals California,Inc.)521(4.0g),并将混合物用521垫过滤。将滤饼用乙醇(2X20mL)洗涤,并将合并的滤液减压浓缩至干。使残余物在乙酸乙酯(150mL)和10%碳酸钾水溶液(100mL)之间分配。分离出有机层,并将水层用乙酸乙酯(3X75mL)萃取。将合并的有机层用硫酸钠干燥并减压浓缩。将残余物用乙醇(5mL)研磨得到71%收率(1.71g)1-(2-氨基乙基)-4,5,6,7-四氢-1H-吲哚-2-羧酸乙酯101d,其为白色固体:mp 102–104℃;1H NMR(500MHz,DMSO-d6)δ6.61(s,1H),6.22(br,2H),4.15(m,4H),2.77(m,2H),2.59(t,2H,J=6.5Hz),2.42(t,2H,J=6.5Hz),1.70(m,2H),1.62(m,2H),1.23(t,3H,J=7.0Hz);MS(APCI+)m/z 237.2(M+H)
实施例101e 3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮101e
将配备有磁力搅拌子和氮气进气口的100-mL单颈圆底烧瓶用氮气吹洗并装入101d(1.80g,7.63mmol)、乙醇钠(1.55g,22.8mmol)和乙醇(50mL)。将混合物在55C搅拌5小时。之后,减压浓缩反应混合物,并将残余物在乙酸乙酯(200mL)和水(100mL)之间分配。分离出有机层,并将水层用乙酸乙酯(2×100mL)萃取。将合并的有机层用盐水洗涤,用硫酸钠干燥并减压浓缩。将残余物通过柱色谱法来纯化得到42%收率(605mg)的3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮101e,其为白色固体:mp 207–209℃;1H NMR(500MHz,DMSO-d6)δ7.41(s,1H),6.36(s,1H),3.84(t,2H,J=6.0Hz),3.42(m,2H),2.51(t,2H,J=6.0Hz),2.42(t,2H,J=6.0Hz),1.76(m,2H),1.65(m,2H);(APCI+)m/z 191.3(M+H)
实施例101f 3-溴-5-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-甲醛101f
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入101e(300mg,1.57mmol)、3,5-二溴吡啶-4-甲醛(2)(517mg,1.96mmol)、4,5-二(二苯基膦基)-9,9-二甲基呫吨(XantPhos,120mg,0.2mmol)、三(二亚苄基丙酮)二钯(0)(180mg,0.2mmol)、Cs2CO3(650mg,2mmol)和1,4-二噁烷(8mL)。在经过三轮真空/氩气吹洗后,将混合物在100℃加热6小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物通过快速柱色谱法(用DCM/MeOH(从40:1至20:1)洗脱)来纯化得到101f,其为浅黄色固体(350mg,40%)。MS:[M+H]+374。
实施例101g 4-(6-硝基吡啶-3-基)哌嗪-1-羧酸叔丁酯101g
在5-溴-2-硝基吡啶(30g,148mmol)DMSO(1L)溶液中加入K2CO3(40g,296mmol)和哌嗪-1-羧酸叔丁酯(28g,148mmol)。将混合物在65℃搅拌整夜。冷却下来后,将其倒入水(2L)中。收集析出的固体并真空干燥。然后将其通过快速柱色谱法进一步纯化(先后用20:1石油醚/乙酸乙酯和二氯甲烷洗脱)得到101g,其为黄色固体(17g,37%)。MS:[M+H]+309。
实施例101h 4-(6-氨基吡啶-3-基)哌嗪-1-羧酸叔丁酯101h
将500-mL烧瓶用氮气吹洗并装入4-(6-硝基吡啶-3-基)哌嗪-1-羧酸叔丁酯101g(3.1g,10mmol)、10%钯/炭(50%水分,1.0g)和乙醇(100mL)。将其排空,充入氢气,并在室温搅拌16小时。然后将氢气排空并将氮气充入瓶中。通过用垫过滤除去催化剂并减压浓缩滤液得到101h(2.7g,97%)。MS:[M+H]+279
实施例101i 4-(6-(5-溴-1-甲基-2-氧代-1,2-二氢吡啶-3-基氨基)吡啶-3-基)哌嗪-1-羧酸叔丁酯101i
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(50mL)、101h(1.3g,4.7mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(1.24g,4.7mmol)和碳酸铯(3.8g,12mmol)。使氮气鼓泡通过所得混合物30分钟后,加入XantPhos(272mg,0.47mmol)和三(二亚苄基丙酮)二钯(0)(430mg,0.47mmol),并将反应混合物回流加热3小时。之后,将反应混合物冷却至室温,在乙酸乙酯(100mL)和水(100mL)之间分配并过滤。分离出水层并用乙酸乙酯(50mL×2)萃取。合并有机层,用盐水(50mL)洗涤,并用硫酸钠干燥。过滤除去干燥剂并减压浓缩滤液。将残余物在快速柱上纯化(用50:1二氯甲烷/甲醇洗脱)得到101i(1.3g,59%)。MS:[M+H]+464。
实施例101j 5-溴-1-甲基-3-(5-(哌嗪-1-基)吡啶-2-基氨基)吡啶-2(1H)-酮101j
将101i(3.6g,7.8mmol)和4.0M HCl/二噁烷(10mL)的混合物在室温搅拌5小时。然后将其减压浓缩。将残余物用1.0M NaOH水溶液碱化并用二氯甲烷萃取。将合并的有机层用水洗涤并减压浓缩得到101j(2.46g,87%)。MS:[M+H]+364。
实施例101k 5-溴-1-甲基-3-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)吡啶-2(1H)-酮101k
将101j(2.75g,7.5mmol)、氧杂环丁烷-3-酮(1.6g、22.7mmol)、NaBH3CN(4.75g、22.5mmol)和氯化锌(3g,22.7mmol)于甲醇(125mL)中的混合物在50℃搅拌5小时。将混合物加至水中并用二氯甲烷萃取三次。减压浓缩有机层。将残余物通过柱色谱法(用25:1二氯甲烷/甲醇洗脱)来纯化得到101k(1.92g,61%)。MS:[M+H]+420。1H NMR(500MHz,DMSO)δ8.58(d,J=2.5,1H),8.55(s,1H),7.94(d,J=3,1H),7.54(d,J=2.5,1H),7.39(dd,J=3,1H),7.25(d,J=4,1H),4.56(t,J=6.5,2H),4.46(t,J=6.5,2H),3.50(s,3H),3.43(m,1H),3.01(m,4H),2.40(m,4H)。
实施例101l 1-甲基-3-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮101l
在配备有磁力搅拌子和回流冷凝器的500-mL单颈圆底烧瓶中装入101k(10.5g,25mmol)、Pin2B2(15.6g,2.5当量,62mmol)、Pd2(dba)3(1.14g,0.05当量,1.25mmol)、X-phos(1.16g,0.1当量,2.5mmol)、AcOK(7.35g,3当量,75mmol)和二噁烷(150mL)。在经历三轮真空/氩气吹洗后,将混合物加热至65℃,保持14小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物通过PE/EA=3/1(80mL)来洗涤得到101l,其为黄色固体(10.5g,94%)。MS:[M+H]+468。
实施例101m 3-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-5-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-甲醛101m
在密封管中装入101f(200mg,0.53mmol)、101l(250mg,0.53mmol)、PdCl2(dppf)(42mg,0.05mmol)、K3PO4(210mg,1.0mmol)和NaOAc(85mg,1.0mmol)于乙腈/H2O(8mL/1mL)中。在经历三轮真空/氩气吹洗后,将混合物在密封管中在100℃加热4小时。然后将其过滤并真空蒸发滤液。将残余物在反相Combi-flash上纯化(用20:1DCM/MeOH洗脱)得到101m(135mg,40%)。LCMS:[M+H]+635。
实施例101 2-(4-(羟基甲基)-5-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮101
将101m(135mg,0.21mmol)和NaBH4(20mg,0.5mmol)在MeOH(5mL)中的混合物在0℃搅拌0.5小时。将混合物用水淬灭并将残余物用EtOAc(5mLX2)萃取。将合并的EtOAc萃取物减压浓缩并将残余物通过反相制备性HPLC来纯化得到101(55mg,40%)。LCMS:[M+H]+637。1HNMR(500MHz,DMSO)δ8.58(s,1H),8.55(s,1H),8.49(s,1H),8.41(s,1H),7.86(d,J=3.0,1H),7.38-7.37(m,2H),7.25-7.23(m,1H),6.54(s,1H),5.16(t,J=3.0,1H),4.56-4.40(m,6H),4.19-4.12(m,3H),3.95(t,J=3.0,1H),3.60(s,3H),3.43-3.41(m,1H),3.06(s,4H),2.57-2.61(m,2H),2.45-2.48(m,6H),1.78-1.80(m,2H),1.69-1.70(m,2H)
实施例102a 1-甲基-3-[5-(4-甲基-哌嗪-1-基)-吡啶-2-基氨基]-5-(4,4,5,5-四甲基-[1,3,2]二氧杂硼杂戊环-2-基)-1H-吡啶-2-酮102a
将配备有磁力搅拌子和调温器的1-L单颈圆底烧瓶用氮气吹洗并装入根据US2009/0318448制备的5-溴-1-甲基-3-[5-(4-甲基哌嗪-1-基)-吡啶-2-基氨基]-1H-吡啶-2-酮(10.0g,0.027mol)、双(频哪醇合)二硼烷(bis(pinacolato)diboron)(8.06g,0.032mol)、乙酸钾(10.4g,0.11mol)和1,4-二噁烷(200mL)。在使氮气流流经所得悬浮液30分钟后,加入Pd(dppf)Cl2CH2Cl2(582mg,0.795mmol)。将所得反应混合物回流搅拌3小时。然后,将其冷却至室温,在水(400mL)和乙酸乙酯(600mL)之间分配并用垫过滤。萃取有机相,用硫酸钠干燥,过滤并浓缩。将残余物用乙醚(50mL)和己烷(250mL)的混合物研磨,并过滤悬浮液。在室温真空干燥滤饼得到27%收率(3.04g)的1-甲基-3-[5-(4-甲基-哌嗪-1-基)-吡啶-2-基氨基]-5-(4,4,5,5-四甲基-[1,3,2]二氧杂硼杂戊环-2-基)-1H-吡啶-2-酮102a,其为棕色固体。
实施例102b 3-(1-甲基-5-(5-(4-甲基哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-5-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-甲醛102b
在密封管中装入3-溴-5-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-甲醛101f(200mg,0.53mmol)、1-甲基-3-(5-(4-甲基哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮102a(225mg,0.53mmol)、PdCl2(dppf)(42mg,0.05mmol)、K3PO4(210mg,1mmol)和NaOAc(85mg,1mmol)于乙腈/H2O(8mL/1mL)中。在经历三轮真空/氩气吹洗后,将混合物在100℃加热4小时。然后将其过滤并真空蒸发滤液。将残余物在快速柱上纯化(用20:1DCM/MeOH洗脱)得到102b(135mg,43%)。LCMS:[M+H]+593。
实施例102 2-(4-(羟基甲基)-5-(1-甲基-5-(5-(4-甲基哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮102
将3-(1-甲基-5-(5-(4-甲基哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-5-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-甲醛102b(135mg,0.22mmol)和NaBH4(20mg,0.5mmol)于MeOH(5mL)中的混合物在0℃搅拌0.5小时。将混合物用水淬灭并将残余物用EtOAc(5mLX2)萃取。将合并的EtOAc萃取物减压浓缩并将残余物通过反相制备性HPLC来纯化得到102(18mg,20%)。LCMS:[M+H]+595。1H NMR(500MHz,DMSO)δ8.59(s,1H),8.55(s,1H),8.49(s,1H),8.45(s,1H),7.87(s,1H),7.37-7.38(m,2H),7.23-7.25(m,1H),6.54(s,1H),5.16(t,J=3.0,1H),4.40(s,2H),4.14-4.18(m,3H),3.93-3.95(m,1H),3.60(s,3H),3.09(s,4H),2.60-2.61(m,6H),2.48-2.34(m,5H),1.78-1.79(m,2H),1.69-1.70(m,2H)
实施例103a 2-溴-4-氯吡啶-3-甲醛103a
历时5分钟,向在-70℃冷却的2-溴-4-氯吡啶(1.6g,8.0mmol)于无水四氢呋喃(40mL)中的溶液中添加二异丙基氨基锂溶液(5.0mL,10.0mmol,2.0M)并在-70℃再搅拌1小时。历时3分钟加入无水DMF(1.3g)并将混合物再搅拌30分钟。然后将其用饱和NH4Cl(30mL)淬灭并用乙酸乙酯(20mL×3)萃取。将合并的有机层用无水Mg2SO4干燥,过滤并减压蒸发。将残余物通过硅胶柱色谱法(用石油醚/乙酸乙酯(20:1)洗脱)来纯化得到103a,其为黄色固体(900mg,48%)。1H NMR(500MHz,DMSO)δ10.21(s,1H),8.52(d,J=5.5Hz,1H),7.79(d,J=5.0Hz,1H)。
实施例103b 4-氯-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛103b
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入103a(800mg,3.5mmol)、3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮101e(665mg,3.5mmol)、三(二亚苄基丙酮)二钯(0)(320mg,0.35mmol)、XantPhos(400mg,0.7mmol)、Cs2CO3(2.3g,7.0mmol)和1,4-二噁烷(20mL)。在经历三轮真空/氩气吹洗后,将混合物在90℃加热5小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(80:1)洗脱)得到103b,其为黄色固体(1.2g,50%)。MS:[M+H]+330。
实施例103c 4-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛103c
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入103b(600mg,1.0mmol)、1-甲基-3-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮101l(468mg,1.0mmol)、Pd(dppf)Cl2(81mg,0.1mmol)、K3PO4.3H2O(678mg,3.0mmol)和四氢呋喃(20mL)。在经历三轮真空/氩气吹洗后,将混合物回流加热4小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(40:1)洗脱)得到103c,其为黄色固体(510mg,73%)。MS:[M+H]+635。
实施例103 2-(3-(羟基甲基)-4-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮103
在0℃,向103c(500mg,0.8mmol)于甲醇(50mL)中的溶液中添加硼氢化钠(91mg,2.4mmol)并再搅拌30分钟。然后将反应混合物用水(3mL)淬灭并浓缩。将残余物用反相制备性-HPLC来纯化得到103(224mg,45%)。LCMS:[M+H]+637.1H NMR(500MHz,DMSO)δ8.61(d,J=3.0,1H),8.48(d,J=6.0,1H),7.92(d,J=3.5,1H),7.81(d,J=3.0,1H),7.78(s,1H),7.38(d,J=6.0,1H),7.24-7.27(m,1H),6.88(s,1H),6.81(d,J=11.5,1H),5.01-5.04,(m,1H),4.60-4.71(m,5H),4.32-4.49(m,2H),3.83-4.15(m,3H),3.70(s,3H),3.53-3.59(m,1H),3.13-3.16(m,4H),2.55-2.61(m,4H),2.49-2.52(m,4H),1.78-1.90(m,4H)
实施例104a 4-溴-2-氯吡啶-3-甲醛104a
历时30分钟,向在-70℃冷却的4-溴-2-氯吡啶(12.0g,60.0mmol)于无水四氢呋喃(300mL)中的溶液中加入二异丙基氨基锂的溶液(30.0mL,60.0mmol,2.0M)并在-70℃再搅拌2小时。历时10分钟加入无水DMF(12.0g)并再搅拌30分钟。然后将其用饱和NaHCO3(200mL)淬灭,用乙酸乙酯(100mL×3)萃取。将合并的有机层用无水Mg2SO4来干燥,过滤并减压蒸发。将残余物通过硅胶柱色谱法来纯化(用石油醚/乙酸乙酯(20:1)洗脱)得到104a,其为黄色固体(4.0g,29%)。1H NMR(500MHz,DMSO)δ10.23(s,1H),8.44(d,J=5.5Hz,1H),7.94(d,J=5.5Hz,1H)。
实施例104b 2-氯-4-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛104b
向配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入104a(1.1g,5.0mmol)、3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮101e(477mg,2.5mmol)、三(二亚苄基丙酮)二钯(0)(230mg,0.25mmol)、XantPhos(430mg,0.75mmol)、Cs2CO3(1.6g,5.0mmol)和1,4-二噁烷(50mL)。在经历三轮真空/氩气吹洗后,将混合物在65℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(40:1)洗脱)得到104b,其为黄色固体(1.1g,80%)。MS:[M+H]+330。
实施例104c 2-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-4-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛104c
向配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入104b(658mg,1.0mmol)、1-甲基-3-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮101l(622mg,2.0mmol)、Pd(dppf)Cl2(65mg,0.08mmol)、K3PO4·3H2O(361mg,1.6mmol)和四氢呋喃(40mL)。在经历三轮真空/氩气吹洗后,将混合物回流加热4小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(40:1)洗脱)得到104c,其为黄色固体(400mg,63%)。MS:[M+H]+635。
实施例104 2-(3-(羟基甲基)-2-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-4-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮104
在0℃,向104c(360mg,0.6mmol)于甲醇(50mL)中的溶液中加入硼氢化钠(70mg,1.8mmol)并再搅拌30分钟。将反应混合物用水(2mL)淬灭并浓缩。将残余物用反相制备性-HPLC来纯化得到104(63mg,16%),其为灰白色固体。LCMS:[M+H]+637。1H NMR(500MHz,DMSO)δ8.70(d,J=3.0,1H),8.65(d,J=5.5,1H),8.34(s,1H),7.85(d,J=3.0,1H),7.60(d,J=2.5,1H),7.36-7.37(m,2H),7.22-7.23(m,1H),6.56(s,1H),5.12(t,J=5.5,1H),4.55-4.56(m,2H),4.43-4.45(m,4H),4.14-4.16(m,3H),3.93-3.95(m,1H),3.60(s,3H),3.43-3.44(m,1H),3.05-3.08(m,4H),2.61-2.63(m,2H),2.46-2.47(m,2H),2.36-2.39(m,4H),1.68-1.78(m,4H)。
实施例105a N-甲氧基-N-甲基-4,5,6,7-四氢苯并[b]噻吩-2-甲酰胺105a
将配备有磁力搅拌子的250-mL单颈圆底烧瓶用氮气吹洗,装入4,5,6,7-四氢苯并[b]噻吩-2-羧酸(3.00g,16.5mmol)、二氯甲烷(80mL)和DMF(60mg,0.825mmol)并冷却至0℃。向所得溶液中滴加草酰氯(2.31g,18.2mmol)。该添加结束后,将反应混合物温热至室温并搅拌2小时。之后,将反应混合物减压浓缩至干。将所得白色固体溶解在二氯甲烷(80mL)中并将溶液冷却至0℃。然后加入三乙胺(5.00g,49.5mmol)和N,O-二甲基羟基胺(1.61g,16.5mmol)。添加结束后,移去冷却浴,并将反应混合物在室温搅拌16小时。之后,使反应混合物在水(100mL)和乙酸乙酯(200mL)之间分配。分离各层,并将水相用乙酸乙酯(100mL)萃取。将合并的有机萃取物用水(100mL)洗涤,然后用盐水(100mL)洗涤并用硫酸钠干燥。过滤除去干燥剂,并减压蒸发溶剂。将所得残余物通过快速色谱法来纯化得到88%收率的105a(3.29gm),其为白色固体:mp 36–37℃;1H NMR(500MHz,CDCl3)δ7.79(s,1H),3.76(s,3H),3.34(s,3H),2.78(t,2H,J=6.0Hz),2.62(t,2H,J=6.0Hz),1.82(m,4H);MS(APCI+)m/z226.3(M+H)
实施例105b 3-氯-1-(4,5,6,7-四氢苯并[b]噻吩-2-基)丙烷-1-酮105b
将装备有磁力搅拌子的100-mL单颈圆底烧瓶用氮气吹洗并装入105a(2.70g,12.0mmol)和无水THF(45mL),将所述溶液用丙酮/冰浴冷却至-10℃。滴加1.0M乙烯基溴化镁的THF溶液(13.2mL,13.2mmol),并将所得反应混合物在0℃搅拌4小时。之后,使反应混合物在乙酸乙酯(100mL)和2M盐酸(40mL)之间分配。分离各层,并将水相用乙酸乙酯(40mL)萃取。将合并的有机萃取物用水(100mL)洗涤,然后用盐水(100mL)洗涤,用硫酸钠干燥,过滤并减压浓缩。将所得残余物溶解在二氯甲烷(30mL)中并加入2M氯化氢的乙醚溶液(15mL)。在室温搅拌1小时后,减压除去溶剂。通过柱色谱法纯化所得残余物得到29%收率(804mg)的105b,其为灰白色固体:mp 57–58℃;1H NMR(500MHz,CDCl3)δ7.41(s,1H),3.89(t,2H,J=7.0Hz),3.30(t,2H,J=7.0Hz),2.81(t,2H,J=6.0Hz),2.64(t,2H,J=6.0Hz),1.83(m,4H);MS(ECI+)m/z 229.1(M+H)
实施例105c 5,6,7,8-四氢-1H-苯并[b]环戊二烯并[d]噻吩-3(2H)-酮105c
向装备有磁力搅拌子的50-mL单颈圆底烧瓶中装入105b(800mg,3.51mmol)和98%硫酸(8mL)。在95℃搅拌16小时后,将反应混合物倒入冰(50g)中,并将所得悬浮液用乙酸乙酯(3×50mL)萃取。合并有机萃取物,用硫酸钠干燥,过滤并减压浓缩。将所得残余物通过快速色谱法来纯化得到105c,47%收率(320mg),其为灰白色固体:mp 75–76℃;1H NMR(500MHz,CDCl3)δ2.89(m,2H),2.87–2.83(m,4H),2.56(t,2H,J=6.5Hz),1.84(m,4H)
实施例105d 5,6,7,8-四氢-1H-苯并[b]环戊二烯并[d]噻吩-3(2H)-酮肟105d
在配备有机械搅拌器和氮气进气口的100-mL单颈圆底烧瓶中装入羟基胺盐酸盐(573mg,8.25mmol)和甲醇(10mL)。将混合物用冰浴冷却至0℃。加入乙酸钠(677mg,8.25mmol)。将混合物在0℃搅拌30分钟。之后,加入105c(319mg,1.65mmol),将反应混合物在室温搅拌16小时。之后,浓缩混合物,并将所得残余物用水(10mL)研磨。收集所得固体并在真空烘箱中在45℃干燥得到84%收率(287mg)的105d,其为灰白色固体:mp 173–174℃;1H NMR(500MHz,DMSO-d6)δ10.38(s,1H),2.97(m,2H),2.77–2.73(m,4H),2.47(m,2H),1.75(m,4H);MS(APCI+)m/z 208.3(M+H)
实施例105e 3,4,5,6,7,8-六氢苯并噻吩并[2,3-c]吡啶-1(2H)-酮105e
向配备有回流冷凝器、磁力搅拌子和氮气进气口的50-mL单颈圆底烧瓶中装入105d(285mg,1.38mmol)和聚磷酸(15g)。在80℃搅拌16小时后,将反应混合物冷却至室温,并加入水(30mL)。将所得混合物搅拌30分钟并过滤。将滤饼用水(20mL)洗涤并在真空烘箱中在45℃干燥得到75%收率(215mg)的105e,其为灰白色固体:mp 203℃分解;1H NMR(500MHz,CDCl3)δ5.62(s,1H),3.59(t,2H,J=7.0Hz),2.81(t,2H,J=6.0Hz),2.72(t,2H,J=7.0Hz),2.48(t,2H,J=6.0Hz),1.84(m,4H)。MS(APCI+)m/z 208.3(M+H)
实施例105f 3-溴-5-{6-氧代-8-硫杂-5-氮杂三环[7.4.0.02,7]十三碳-1(9),2(7)-二烯-5-基}吡啶-4-甲醛105f
向配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(15mL)、3,5-二溴吡啶-4-甲醛(400mg,1.5mmol)、8-硫杂-5-氮杂三环[7.4.0.02,7]十三碳-1(9),2(7)-二烯-6-酮105e(146mg,0.76mmol)和碳酸铯(176mg,1.5mmol)。加入Xantphos(40mg,0.08mmol)和Pd2(dba)3(70mg,0.08mmol),并将反应混合物在100℃加热5小时。之后,将反应混合物冷却至室温并过滤。减压浓缩滤液并将残余物在快速柱上纯化(用DCM:MeOH(20:1)洗脱)得到105f(200mg,70%)。MS:[M+H]+377.
实施例105g 3-[1-甲基-5-({5-[4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]-5-{6-氧代-8-硫杂-5-氮杂三环[7.4.0.02,7]十三碳-1(9),2(7)-二烯-5-基}吡啶-4-甲醛105g
在密封管中装入105f(200mg,0.53mmol)、1-甲基-3-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮101l(240mg,0.51mmol)、PdCl2(dppf)(42mg,0.05mmol)、K3PO4(230mg,1mmol)和NaOAc(80mg,1mmol)于CH3CN(5mL)和H2O(1.5mL)中。将体系排空并用氮气回填。将反应混合物在100℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物通过快速柱色谱法(用10:1的DCM/MeOH洗脱)来纯化得到105g,40%收率(138mg),其为浅黄色固体.MS:[M+H]+638。
实施例105 4-羟基甲基-3-[1-甲基-5-({5-[4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]-5-{6-氧代-8-硫杂-5-氮杂三环-[7.4.0.02 ,7]十三碳-1(9),2(7)-二烯-5-基}吡啶105
在0℃,向3-[1-甲基-5-({5-[4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]-5-{6-氧代-8-硫杂-5-氮杂三环[7.4.0.02,7]-十三碳-1(9),2(7)-二烯-5-基}吡啶-4-甲醛105g(130mg,0.20mmol)于甲醇(5mL)中的溶液中添加硼氢化钠(22mg,0.6mmol)并搅拌30分钟。将反应混合物用水(1.0mL)淬灭并浓缩。将残余物通过反相制备性-HPLC来纯化得到105(90mg,65%)。LCMS:[M+H]+:654.1H NMR(500MHz,DMSO)δ8.58(d,J=2.0,1H),8.56(s,1H),8.49(s,1H),8.41(s,1H),7.86(s,1H),7.36(m,2H),7.24-7.22(m,1H),5.14(t,J=3.0,1H),4.56-4.42(m,6H),4.08-3.90(m,2H),3.60(s,3H),3.43(d,J=3.5,1H),3.07(s,4H),2.89-2.79(m,4H),2.55-2.53(m,2H),2.39-2.37(m,4H),1.80-1.81(m,4H)
实施例106a 3,3-二甲基环戊酮106a
将配备有磁力搅拌子、加料漏斗和氮气进气口的1-L三颈圆底烧瓶用氮气吹洗并装入乙醚(200mL)和碘化亚铜(I)(54.46g,0.286mol)。将混合物冷却至0℃,历时1.5小时向反应混合物中滴加甲基锂(1.6M于乙醚中,357.5mL,0.572mol)并在0℃再搅拌2小时。之后,历时1.5小时滴加3-甲基环戊-2-烯酮(25g,0.260mol)于乙醚(150mL)中的溶液。然后将反应混合物在0℃搅拌2小时并倒入十水硫酸钠(300g)中。将所得混合物搅拌30分钟。之后,将混合物过滤并用乙醚(1000mL)洗涤。浓缩滤液并减压蒸馏得到70%收率(20.5g)的3,3-二甲基环戊酮106a,其为无色液体:bp 50–55℃(在10mmHg);1H NMR(300MHz,CDCl3)δ2.31(t,2H,J=7.8Hz),2.05(s,2H),1.79(t,2H,J=7.8Hz);MS(ESI+)m/z 113.3(M+H)
实施例106b 5,5-二甲基-5,6-二氢-4H-环戊二烯并[b]噻吩-2-羧酸乙酯106b
将配备有磁力搅拌子、回流冷凝器、加料漏斗和氮气进气口的500-mL三颈圆底烧瓶用氮气吹洗并装入DMF(9.49g,0.100mol)和二氯甲烷(100mL)。将反应混合物冷却至0℃并历时30分钟滴加三氯氧磷(14.1g,0.920mol)。该添加结束后,将反应混合物温热至室温并搅拌1小时。之后,历时1小时滴加106a(11.2g,0.100mol)于二氯甲烷(100mL)中的溶液。然后将反应混合物回流搅拌18小时。将反应混合物冷却至室温并倒入碎冰(400mL)和乙酸钠(100g,1.22mol)的混合物中。将所得混合物搅拌45分钟。之后,分离出水层并用二氯甲烷(2×500mL)萃取。然后将合并的有机层用水(2×200mL)洗涤,接着用盐水(200mL)洗涤并用硫酸钠干燥。然后过滤除去干燥剂,浓缩滤液得到粗制产物2-氯-4,4-二甲基环戊-1-烯甲醛,将其放置在配备有机械搅拌器、回流冷凝器和氮气进气口的500-mL三颈圆底烧瓶中。然后加入二氯甲烷(200mL)、2-巯基乙酸乙酯(11.0g,0.092mol)和三乙胺(30g,0.207mol)。然后将反应混合物回流搅拌6小时。之后,将反应混合物冷却至室温并浓缩成稠厚的橙色残余物。加入乙醇(200mL)和三乙胺(30.0g,0.207mol)并将反应混合物回流加热12小时。然后将反应混合物冷却至室温并减压浓缩,将所得残余物用乙醚(600mL)稀释。将所得混合物用1M盐酸(150mL)、盐水(100mL)洗涤,用硫酸钠干燥,过滤并减压浓缩。将所得残余物通过快速色谱法来纯化得到106b,34%收率(7.70g),其为无色液体:1H NMR(300MHz,CDCl3)δ7.48(s,1H),4.33(q,2H,J=7.2Hz),2.72(s,2H),2.56(s,2H),1.38(t,3H,J=1.8Hz),1.17(s,6H);MS(ESI+)m/z 225.1
实施例106c 5,5-二甲基-5,6-二氢-4H-环戊二烯并[b]噻吩-2-羧酸106c
在配备有磁力搅拌子和回流冷凝器的250-mL单颈圆底烧瓶器中,将106b(4.00g,17.8mmol)溶解在乙醇(50mL)中。加入THF(50mL),水(50mL)和氢氧化锂(854mg,35.6mmol),并将混合物在60℃搅拌4小时。之后,将反应混合物冷却至室温并用2M盐酸酸化至pH 1.5,然后用乙酸乙酯(2×200mL)萃取。合并有机层,先后用水(2×100mL)和盐水(100ml)洗涤并用硫酸钠干燥。然后通过过滤分离出干燥剂。在蒸发所得滤液后,得到106c,91%收率(3.2g),其为白色固体:mp 170–172℃;1H NMR(300MHz,CDCl3)δ12.77(s,1H),7.46(s,1H),2.71(s,2H),2.53(s,2H),1.20(s,6H);MS(ESI–)m/z 195.0
实施例106d 5,5-二甲基-5,6-二氢-4H-环戊二烯并[b]噻吩-2-羧酸106d
向配备有磁力搅拌子、回流冷凝器和安置在冷凝器上的鼓泡器的100-mL单颈圆底烧瓶中装入106c(2.30g,11.6mmol)、甲苯(25mL)、亚硫酰氯(4.09g,34.9mmol)和DMF(1drop)。将混合物回流加热1小时,然后在旋转蒸发仪上在45℃减压蒸发。将所得酰氯用二氯甲烷(20mL)稀释。
在单独的配备有磁力搅拌子的250-mL三颈圆底烧瓶中,氮气中,将N,O-二甲基羟基胺盐酸盐(2.26g,23.2mmol)和N,N-二异丙基乙基胺(2.97g,23.0mmol)溶解在无水二氯甲烷(20mL)中,将所述溶液在冰/水浴中冷却至0℃。加入所述酰氯溶液,并将反应混合物在室温搅拌18小时。将反应混合物用水(100mL)、10%柠檬酸水溶液(50mL)和饱和碳酸氢钠水溶液和水的1:1混合物(100mL)萃取。将有机层用硫酸钠干燥并在旋转蒸发仪上减压蒸发得到93%收率(2.60g)的106d,其为浅黄色固体:1H NMR(300MHz,CDCl3)δ7.66(s,1H),3.77(s,3H),3.35(s,3H),2.74(s,2H),2.58(s,2H),1.23(s,6H)
实施例106e 3-氯-1-(5,5-二甲基-5,6-二氢-4H-环戊二烯并[b]噻吩-2-基)丙烷-1-酮106e
将配备有磁力搅拌子的100-mL单颈圆底烧瓶用氮气吹洗并装入106d(2.41g,10.0mmol)和无水THF(20mL)。将所述溶液冷却至-70℃,在维持反应温度低于-60℃的情况下,加入1M乙烯基溴化镁/THF(11mL,11.0mmol)。将反应混合物在-13至-7℃搅拌2小时,然后历时30分钟温热至室温。将反应混合物再次冷却至-70℃,加入2M氯化氢的乙醚溶液(22.5ml,45mmol)。然后将反应混合物在冰箱中在-10℃贮存整夜。之后,在旋转蒸发仪上减压蒸发所述混合物,并使所得残余物在水(100mL)和乙醚(100mL)之间分配。将乙醚萃取物用硫酸钠干燥并在旋转蒸发仪上减压蒸发得到粗制106e(2.86g,118%),其为棕色油状物,具有约75%的纯度(通过NMR):1H NMR(300MHz,CDCl3)δ7.45(s,1H),3.89(t,2H,J=6.9Hz),3.30(t,2H,J=6.9Hz),2.75(s,2H),2.59(s,2H),1.24(s,6H)
实施例106f 6,6-二甲基-1,2,6,7-四氢二环戊二烯并[b,d]噻吩-3(5H)-酮106f
在配备有磁力搅拌子的100-mL单颈圆底烧瓶中装入粗制106e(2.86g,10.0mmol假定为定量收率)和98%硫酸。将反应混合物在90℃油浴中加热整夜。将反应混合物放在冰/丙酮浴中,一次性加入冷(5℃)的磷酸氢二钾(105g,0.603mol)于水(300mL)中的溶液。将所得混合物与乙酸乙酯(300mL)一起震摇并过滤。将滤饼用乙酸乙酯(100mL)洗涤。分离出滤液的乙酸乙酯层,用硫酸钠干燥并在旋转蒸发仪上减压蒸发。将所得残余物通过快速柱色谱法(硅胶,80:20己烷/乙酸乙酯)来纯化得到106f,两步的收率为37%(683mg),其为无定形棕色固体:mp 60–62℃;1H NMR(500MHz,CDCl3)δ2.92–2.87(m,4H),2.79(s,2H),2.53(s,2H),1.26(s,6H);LCMS(ESI+)m/z 207.0(M+H)
实施例106g 6,6-二甲基-1,2,6,7-四氢二环戊二烯并[b,d]噻吩-3(5H)-酮106g
在配备有磁力搅拌子和氮气进气口的250-mL单颈圆底烧瓶中装入羟基胺盐酸盐(688mg,9.90mmol)、乙酸钠(812mg,9.90mmol)和甲醇(10mL),并将所述混合物在室温搅拌30分钟。之后,在室温滴加106f(680mg,3.30mmol)的溶液,并将反应混合物在室温和氮气中搅拌14小时。由于反应不完全,加入羟基胺盐酸盐(1.15g,16.5mmol)和乙酸钠(1.35g,16.5mmol),并继续在室温搅拌58小时。之后,将混合物用二氯甲烷(150mL)和水(100mL)稀释并分离各层。将有机层用盐水(50mL)洗涤并用硫酸钠干燥。过滤除去干燥剂并浓缩滤液得到粗制106g,定量收率(730mg),其为黄色半固体,将其不经进一步纯化即用在下一步骤中:mp 122–124℃;主要异构体的1H NMR(500MHz,CDCl3)δ3.13–3.11(m,2H),2.85–2.83(m,2H),2.77(s,2H),2.49(s,2H),1.24(s,6H);MS(ESI+)m/z 222.0(M+H)
实施例106h 6,6-二甲基-3,4,6,7-四氢-5H-环戊二烯并[4,5]噻吩并[2,3-c]吡啶-1(2H)-酮106h
在配备有回流冷凝器、机械搅拌器和氮气进气口的100-mL三颈圆底烧瓶中装入106g(700mg,3.16mmol)和聚磷酸(25g)。将反应混合物在氮气中在80℃搅拌13小时。之后,将混合物冷却至0℃,并小心地滴加水(50mL),维持内部温度在10–45℃。将混合物用90:10二氯甲烷/甲醇(100mL)稀释并分离各层。将水层用90:10二氯甲烷/甲醇(50mL)萃取,并将合并的有机层用饱和碳酸氢钠水溶液(50mL)、盐水(150mL)洗涤并用硫酸钠干燥。通过过滤除去干燥剂。减压浓缩滤液,并将所得残余物通过快速柱色谱法(硅胶,95:5二氯甲烷/甲醇)来纯化得到6,6-二甲基-3,4,6,7-四氢-5H-环戊二烯并[4,5]噻吩并[2,3-c]吡啶-1(2H)-酮106h,90%收率(630mg),其为无定形灰白色固体:mp 205–207℃;1H NMR(500MHz,CDCl3)δ5.51(s,1H),3.60–3.56(m,2H),2.76–2.73(m,4H),2.49(s,2H),1.26(s,6H);MS(ESI+)m/z 222.0(M+H)
实施例106i 3-溴-5-{4,4-二甲基-9-氧代-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-10-基}吡啶-4-甲醛106i
向配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(15mL)、3,5-二溴吡啶-4-甲醛(400mg,1.5mmol)、4,4-二甲基-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-9-酮(106h)(170mg,0.76mmol)和碳酸铯(176mg,1.5mmol)。加入Xantphos(40mg,0.08mmol)和Pd2(dba)3(70mg,0.08mmol),并将反应混合物在100℃加热5小时。之后,将反应混合物冷却至室温并过滤。减压浓缩滤液并将残余物在快速柱上纯化(用DCM:MeOH(20:1)洗脱)得到106i(200mg,65%)。MS:[M+H]+405。
实施例106j 3-[1-甲基-5-({5-[4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]-5-{4,4-二甲基-9-氧代-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-10-基}吡啶-4-甲醛106j
在密封管中装入106i(200mg,0.50mmol)、1-甲基-3-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮101l(240mg,0.51mmol)、PdCl2(dppf)(42mg,0.05mmol)、K3PO4(230mg,1mmol)和NaOAc(80mg,1mmol)/CH3CN(5mL)和H2O(1.5mL)。将体系排空并用氮气回填。将反应混合物在100℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物通过快速柱色谱法(用10:1DCM/MeOH洗脱)来纯化得到106j(130mg,40%),其为浅黄色固体。MS:[M+H]+666。
实施例106 4-羟基甲基-3-[1-甲基-5-({5-[4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]-5-{4,4-二甲基-9-氧代-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-10-基}吡啶-4-甲醛106
在0℃,向106j(130mg,0.20mmol)于甲醇(5mL)中的溶液中加入硼氢化钠(22mg,0.6mmol)并搅拌30分钟。将反应混合物用水(1.0mL)淬灭并浓缩。将残余物通过反相制备性-HPLC来纯化得到106(60mg,45%),其为黄色固体。LCMS:[M+H]+:668.1H NMR(500MHz,DMSO)δ8.58(d,J=2.0,1H),8.56(s,1H),8.49(s,1H),8.41(s,1H),7.87(d,J=2.5,1H),7.38-7.36(m,2H),7.24-7.22(m,1H),5.15(t,J=5.0,1H),4.56-4.42(m,6H),4.08-4.04(m,2H),3.60(s,3H),3.43-3.42(m,1H),3.07-2.94(m,6H),2.55-2.53(m,4H),2.39-2.38(m,4H),1.23(s,6H)
实施例107a(E)-3-(2-氯-4,4-二甲基环戊-1-烯基)丙烯酸乙酯107a
下面的两个操作是自Organic Preparations and Procedures Int.,29(4):471-498改编的。在配备有磁力搅拌子和氮气进气口的500-mL单颈圆底烧瓶中装入2-氯-4,4-二甲基环戊-1-烯甲醛(38g,240mmol)/苯(240mL)。向所述溶液中加入乙氧基羰基亚甲基三苯基膦烷(84g,240mmol)。将所述混合物搅拌14小时。之后,蒸发溶剂并将残余物用己烷(2L)研磨以萃取产物使其与PPh3副产物分离。将有机层用硫酸钠干燥并真空浓缩。将残余物通过柱色谱法(使用100%己烷–1:1己烷/乙酸乙酯梯度)来纯化得到37%收率(20g)的(E)-3-(2-氯-4,4-二甲基环戊-1-烯基)丙烯酸乙酯107a。
实施例107b 5,5-二甲基-1,4,5,6-四氢环戊二烯并[b]吡咯-2-羧酸乙酯107b
在配备有磁力搅拌子和氮气进气口的250-mL单颈圆底烧瓶中装入107a(17g,74mmol)/DMSO(100mL)。向所述溶液中添加叠氮化钠(9.6g,150mmol)。然后将所述混合物加热至75℃并搅拌8小时。冷却至rt(室温)后,加入H2O(100mL)和CH2Cl2(200mL)并分离有机层。将水层用CH2Cl2(50mL)萃取。将合并的有机层用盐水洗涤,用硫酸钠干燥并真空浓缩。将残余物通过柱色谱法(使用100%己烷–1:1己烷/乙酸乙酯梯度)来纯化得到37%收率(5.7g)的107b.
实施例107c 1-(氰基甲基)-5,5-二甲基-1,4,5,6-四氢环戊二烯并[b]吡咯-2-羧酸乙酯107c
在配备有磁力搅拌子和氮气进气口的250-mL单颈圆底烧瓶中装入107b(6.2g,30mmol)/DMF(57mL)。向所述溶液中加入NaH(80%分散于矿物油中,1.26g,42.1mmol)。将所得混合物在室温搅拌90分钟。之后,加入溴乙腈(2.94mL,42mmol)。将混合物搅拌14小时。之后,加入水(100mL)和乙酸乙酯(200mL)并分离有机层。将水层用乙酸乙酯(2X50mL)萃取。将合并的有机层用盐水洗涤,用硫酸钠干燥并真空浓缩。将残余物通过柱色谱法来纯化得到95%收率(7g)的107c。
实施例107d 1-(2-氨基乙基)-5,5-二甲基-1,4,5,6-四氢环戊二烯并[b]吡咯-2-羧酸乙酯盐酸盐107d
将500-mL帕尔反应瓶用氮气吹洗并装入10%钯/炭(50%水分,2.0g干重)、107c(4.5g,18mmol)、12%盐酸(9.2mL,37mmol)、乙酸乙酯(80mL)和乙醇(52mL)。将所述瓶与帕尔氢化器连接,排空,充入氢气至压力为50psi并震摇6小时。之后,将氢气排空,并将氮气充入所述瓶中。加入521(10.0g),并将所述混合物用521垫过滤。将滤饼用乙醇(2×50mL)洗涤,并将合并的滤液减压浓缩至干。将粗制残余物1-(2-氨基乙基)-5,5-二甲基-1,4,5,6-四氢环戊二烯并[b]吡咯-2-羧酸乙酯盐酸盐107d不经进一步纯化即用于下一步骤。
实施例107e 4,4-二甲基-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-9-酮107e
将配备有磁力搅拌子和氮气进气口的100-mL单颈圆底烧瓶用氮气吹洗并装入粗制1-(2-氨基乙基)-5,5-二甲基-1,4,5,6-四氢环戊二烯并[b]吡咯-2-羧酸乙酯盐酸盐107d(~18mmol)、乙醇钠(6.2g,92mmol)和乙醇(120mL)。将混合物在55℃搅拌整夜。之后,减压浓缩反应混合物,并将残余物在乙酸乙酯(200mL)和水(100mL)之间分配。将所述溶液过滤。将固体用乙酸乙酯(15mL)洗涤得到850mg所需产物107e。分离出有机层,并将水层用乙酸乙酯(2×100mL)萃取。将合并的有机层用硫酸钠干燥并减压浓缩至近乎干燥。将所述溶液过滤并将固体(1.44g)用乙酸乙酯(15mL)洗涤。将合并的固体真空干燥得到61%收率(2.3g)的107e。
实施例107f 3-溴-5-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-甲醛107f
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中加入1,4-二噁烷(15mL)、3,5-二溴吡啶-4-甲醛(400mg,1.5mmol)、107e(155mg,0.76mmol)和碳酸铯(176mg,1.5mmol)。加入Xantphos(40mg,0.08mmol)和Pd2(dba)3(70mg,0.08mmol),并将反应混合物在100℃加热5小时。之后,将反应混合物冷却至室温并过滤。减压浓缩滤液。将残余物在快速柱上纯化(用DCM:MeOH(20:1)洗脱得到107f(200mg,70%)。MS:[M+H]+388。
实施例107g 5-[1-甲基-5-({5-[4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]-3-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02 ,6]-十二碳-2(6),7-二烯-10-基}吡啶-4-甲醛107g
在密封管中装入107f(200mg,0.51mmol)、1-甲基-3-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮101l(240mg,0.51mmol)、PdCl2(dppf)(42mg,0.05mmol)、K3PO4(230mg,1mmol)和NaOAc(80mg,1mmol)/CH3CN(5mL)和H2O(1.5mL)。将体系排空并用回填氮气。将反应混合物在100℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物通过快速柱色谱法(用10:1的DCM/MeOH洗脱)来纯化得到107g,35%收率(120mg),其为棕色固体。MS:[M+H]+649。
实施例107 10-[4-[1-甲基-5-({5-[4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]-4-(羟基甲基)吡啶-3-基]-4,4-二甲基-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-9-酮107
在0℃,向107g(120mg,0.18mmol)于甲醇(5mL)中的溶液中加入硼氢化钠(22mg,0.6mmol)并将混合物搅拌30分钟。将反应混合物用水(1.0mL)淬灭并浓缩。将残余物通过反相制备性-HPLC来纯化得到107(72mg,60%)。LCMS:[M+H]+:651。1H NMR(500MHz,CDCl3)δ8.65(s,1H),8.59(s,1H),8.49(s,1H),7.86(d,J=1.5,1H),7.36(m,2H),7.22(d,J=2.4,2H),6.52(s,1H),5.16(t,J=3.0,1H),4.56-4.44(m,6H),4.21-4.12(m,3H),3.92(m,1H),3.60(s,3H),3.43-3.42(m,1H),3.06(s,4H),2.57-2.38(m,8H),1.21(s,6H)
实施例108a 4-氯-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-甲醛108a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入2-溴-4-氯吡啶-3-甲醛103a(3.0g,13.6mmol)、4,4-二甲基-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-9-酮107e(1.84g,9.0mmol)、三(二亚苄基丙酮)二钯(0)(826mg,0.9mmol)、XantPhos(1.04mg,1.8mmol)、Cs2CO3(5.8g,18.0mmol)和1,4-二噁烷(40mL)。在经历三轮真空/氩气吹洗后,将混合物在90℃加热5小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物用乙酸乙酯重结晶得到108a,其为黄色固体(730mg,纯度:99%;收率:31.7%)。MS:[M+H]+344.0。
实施例108b 4-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02 ,6]-十二碳-2(6),7-二烯-10-基}吡啶-3-甲醛108b
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入4-氯-2-{4,4-二甲基-9-氧代-1,10-二氮杂-三环并[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-甲醛108a(350mg,1.02mmol)、1-甲基-3-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮101l(476mg,1.02mmol)、Pd(dppf)Cl2(83mg,0.10mmol)、K3PO4(526mg,3.06mmol)和四氢呋喃(20mL)。在经历三轮真空/氩气吹洗后,将混合物回流加热4小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(40:1)洗脱)得到108b,其为白色固体(400mg,61%)。MS:[M+H]+649.4。
实施例108 2-(3-(羟基甲基)-4-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-4,4-二甲基-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-9-酮108
在0℃,向4-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环-[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-甲醛108b(400mg,0.62mmol)于甲醇(30mL)中的溶液中加入硼氢化钠(70mg,1.86mmol)并搅拌30分钟。将反应混合物用水(1.0mL)淬灭并浓缩。将残余物通过反相制备性-HPLC来纯化得到108(170mg,42%)。LCMS:[M+H]+651.4.1H NMR(500MHz,CDCl3)δ8.63(d,J=2.0,1H),8.48(d,J=5.0,1H),7.92(d,J=2.5,1H),7.82(d,J=2.5,1H),7.78(s,1H),7.36(d,J=5.0,1H),7.27-7.25(m,1H),6.84(s,1H),6.81(d,J=9.5,1H),5.05(t,J=6.5,1H),4.72-4.64(m,5H),4.51-4.48(m,1H),4.34-4.32(m,1H),4.15(d,J=4.5,2H),3.87-3.84(m,1H),3.71(s,3H),3.59-3.54(m,1H),3.16-3.14(m,4H),2.58-2.50(m,8H),1.27(s,6H)
实施例109a 4-氯-2-{4,4-二甲基-9-氧代-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-10-基}吡啶-3-甲醛109a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入2-溴-4-氯吡啶-3-甲醛103a(660mg,3.0mmol)、4,4-二甲基-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-9-酮106h(665mg,3.0mmol)、三(二亚苄基丙酮)二钯(0)(270mg,0.3mmol)、XantPhos(340mg,0.6mmol)、Cs2CO3(2.0g,6.0mmol)和1,4-二噁烷(20mL)。在经历三轮真空/氩气吹洗后,将混合物在90℃加热5小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用二氯甲烷洗脱)来纯化得到109a,其为黄色固体(105mg,14%)。MS:[M+H]+361。
实施例109b 4-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-{4,4-二甲基-9-氧代-7-硫杂-10-氮杂三环[6.4.0.02,6]-十二碳-1(8),2(6)-二烯-10-基}吡啶-3-甲醛109b
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入109a(75mg,0.2mmol)、1-甲基-3-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮101l(94mg,0.2mmol)、Pd(dppf)Cl2(17mg,0.02mmol)、K3PO4.3H2O(140mg,0.6mmol)和四氢呋喃(10mL)。在经历三轮真空/氩气吹洗后,将混合物回流加热4小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(40:1)洗脱)来纯化得到109b,其为黄色固体(60mg,47%)。MS:[M+H]+666。
实施例109 2-(3-(羟基甲基)-4-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-4,4-二甲基-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-9-酮109
在0℃,向109b(60mg,0.1mmol)于甲醇(5mL)中的溶液中加入硼氢化钠(11mg,0.3mmol)并将混合物搅拌30分钟。将反应混合物用水(0.3mL)淬灭并浓缩。将残余物用反相制备性-HPLC来纯化得到109(14mg,24%),其为棕色固体。LCMS:[M+H]+668。1H NMR(500MHz,DMSO)δ8.60(d,J=2.5,1H),8.48(d,J=5.0,1H),8.42(s,1H),7.85(d,J=3.0,1H),7.44(d,J=2.0,1H),7.34-7.38(m,2H),7.23(d,J=9.0,1H),4.94(t,J=5.0,1H),4.55(t,J=7.0,2H),4.39-4.46(m,4H),4.14-4.19(m,1H),3.79-3.83(m,1H),3.59(s,3H),3.42-3.44(m,1H),3.00-3.07(m,5H),2.85-2.90(m,1H),2.76(s,2H),2.52-2.59(m,2H),2.36-2.39(m,4H),1.21(d,J=6.5,6H)
实施例110a 1-甲基-3-(6-(4-甲基哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮110a
在配备有磁力搅拌子和冷凝器的250-mL单颈圆底烧瓶中装入5-溴-1-甲基-3-(6-(4-甲基哌嗪-1-基)吡啶-2-基氨基)吡啶-2(1H)-酮(0.45g,1.08mmol),(PinB)2(1.37g,5.4mmol)、Pd2(dba)3(49mg,0.054mmol)、X-Phos(52mg0.11mmol)、KOAc(318mg,3.24mmol)、1,4-二噁烷20mL)。在经历三轮真空/氩气吹洗后,将反应混合物在60℃加热15小时。然后将其冷却至室温并过滤。减压浓缩滤液得到粗制110a,将其直接用在下一反应中。MS:[M+H]+426。
实施例110b 4-(1-甲基-5-(6-(4-甲基哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛110b
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入4-氯-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并-[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛103b(377mg,1.15mmol)、110a(320mg,0.78mmol)、Pd(dppf)Cl2(130mg,0.16mmol)、K3PO4.3H2O(52.9mg,0.23mmol)和四氢呋喃(20mL)。在经历三轮真空/氩气吹洗后,将混合物加热回流整夜,冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(40:1)洗脱)得到110b,其为黄色固体(351mg,76%)。MS:[M+H]+593。
实施例110 2-(3-(羟基甲基)-4-(1-甲基-5-(6-(4-甲基哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮110
在0℃,向110b(60mg,0.1mmol)于甲醇(50mL)中的溶液中加入硼氢化钠(11.5mg,0.3mmol)并将混合物再搅拌30分钟。将反应混合物用水(3mL)淬灭并浓缩。将残余物用反相制备性-HPLC来纯化得到110(26.2mg,49%)。LCMS:[M+H]+595。1H NMR(500MHz,CDCl3)δ8.69(d,J=1.5,1H),8.46(d,J=5.0,1H),7.97(s,1H),7.80(s,1H),7.41-7.37(m,1H),7.34(d,J=1.5,1H),6.89(s,1H),6.22(d,J=8.0,1H),6.15(d,J=8.5,1H),5.10(t,J=6.5,1H),4.66-4.64(m,1H),4.51-4.30(m,2H),4.15-4.12(m,2H),3.93-3.89(m,1H),3.71(s,3H),3.58-3.48(m,4H),2.61-2.56(m,7H),2.47-2.39(m,3H),1.91-1.87(m,2H),1.79-1.78(d,J=5.0,3H)
实施例111a(6-氨基吡啶-3-基)(吗啉代)甲酮111a
向吗啉(9.00g,103mmol)于EtOH(400mL)中的溶液中加入EDCI(10.0g,52.2mmol)、HOBt(7.00g 51.8mmol)和6-氨基吡啶-3-甲酸(6.00g,43.4mmol)。搅拌18小时后,过滤所得悬浮液。将固体用MeOH(100mL)和二氯甲烷(100mL)的混合物研磨,得到111a,其为白色固体(2.7g,30%)。LCMS:(M+H)+208
实施例111b 5-溴-1-甲基-3-(5-(吗啉-4-羰基)吡啶-2-基氨基)吡啶-2(1H)-酮111b
按照就合成101i所述的操作,中间体111a和3,5-二溴-1-甲基吡啶-2(1H)-酮反应得到111b,21%收率。LCMS:(M+H)+394.1H NMR(500MHz,MeOD)δ8.84(d,J=2.5,1H),8.42(d,J=2,1H),7.72(m,1H),7.42(d,J=2,1H),7.11(d,J=8.5,1H),3.72(m,8H),3.63(s,3H)。
实施例111c 1-甲基-3-(5-(吗啉-4-羰基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮111c
在配备有磁力搅拌子和冷凝器的250-mL单颈圆底烧瓶中装入111b(1.0g,0.25mmol)、X-phos(120mg,0.025mmol)、Pd2(dba)3(110g,0.0125mmol)、KOAc(750mg,0.75mmol)、4,4,4',4',5,5,5',5'-八甲基-2,2'-二(1,3,2-二氧杂硼杂戊环)(3.2g,1.25mmol)和1,4-二噁烷(50mL)。在经历三轮真空/氩气吹洗后,将反应混合物在100℃加热15小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物通过快速柱色谱法(用5:1石油醚/乙酸乙酯洗脱)来纯化得到111c,其为黄色固体(700mg,63%)。MS:[M+H]+441。
实施例111d 4-(1-甲基-5-(5-(吗啉-4-羰基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛111d
在配备有磁力搅拌子和冷凝器的250-mL单颈圆底烧瓶中装入111c(450mg,1.26mmol)、4-氯-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛103b(413mg,1.26mmol)、Pd(dppf)Cl2(102mg,0.126mmol)、K3PO4.3H2O(85mg,0.352mmol)和THF(10mL)。在经历三轮真空/氩气吹洗后,将反应混合物在100℃加热15小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物通过快速柱色谱法(用7:1石油醚/乙酸乙酯洗脱)来纯化得到111d,其为黄色固体(700mg,63%)。MS:[M+H]+608。
实施例111 2-(3-(羟基甲基)-4-(1-甲基-5-(5-(吗啉-4-羰基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮111
将111d(60mg,0.05mmol)、NaBH4(6.4mg,0.1mmol)和MeOH(5mL)的混合物在0℃搅拌30分钟。真空蒸发混合物并将残余物用EtOAc(10mLX2)萃取。将合并的EtOAc萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到111(27mg,44%)。LCMS:[M+H]+610。1HNMR(500MHz,DMSO)δ9.00(s,1H),8.78(d,J=2.0,1H),8.49(d,J=5,1H),8.26(d,J=2.0,1H),7.65-7.67(m,2H),7.60(d,J=2.5,1H),6.58(s,1H),4.96(t,J=5,1H),4.40-4.46(m,2H),4.11-4.24(m,3H),3.86-3.88(m,1H),3.56-3.62(m,8H),3.50(s,4H),2.62-2.63(m,2H),2.46-2.47(m,2H),1.67-1.80(m,4H)
实施例112a 5,6,7,8-四氢吲嗪-2-羧酸甲酯112a
将配备有磁力搅拌子和氮气进气口的500-mL圆底烧瓶用氮气吹洗并装入5,6,7,8-四氢吲嗪-2-羧酸(30.4g,184mmol)、DMF(1.00g,13.6mmol)和二氯甲烷(300mL)。将所述溶液用冰浴冷却至0℃。滴加草酰氯(28.0g,221mmol),历时30分钟将反应混合物温热至室温并搅拌5小时。之后,将所得溶液浓缩得到棕色固体。将该固体溶解在无水甲醇(400mL)中,将所述溶液冷却至0℃。将三乙胺(57g,552mmol)加至反应混合物中,并将其在室温再搅拌2小时。之后,将反应混合物减压浓缩至干。将残余物用二氯甲烷(300mL)稀释并用水(200mL)和饱和碳酸氢钠水溶液(200mL)洗涤。将有机层用硫酸钠干燥,过滤并减压浓缩。将所得残余物用己烷(200mL)研磨得到112a,58%收率(19.1g),其为白色固体:mp 72–74℃;1H NMR(300MHz,DMSO-d6)δ7.13(s,1H),6.23(s,1H),3.93(t,2H,J=6.0Hz),3.77(s,3H),2.75(t,2H,J=6.0Hz),1.93(m,2H),1.80(m,2H);(APCI+)m/z 180.1(M+H)
实施例112b 3-(氰基甲基)-5,6,7,8-四氢吲嗪-2-羧酸甲酯112b
向配备有加料漏斗、温度计的500-mL三颈圆底烧瓶中装入112a(6.70g,37.4mmol)、碘乙腈(12.5g,74.9mmol)、硫酸亚铁(II)七水合物(5.20g,18.7mmol)和二甲基亚砜(250mL)。在室温,在使用水浴的情况下,历时1小时向混合物中通过注射泵滴加过氧化氢(35%,18.2g,187mmol)。向所述反应混合物中逐份加入硫酸亚铁(II)七水合物(2至3当量)以保持温度在25℃至35℃之间,直到反应混合物的颜色为深红色。如果TLC显示反应不完全,则以相同方式加入更多的过氧化氢(2-3当量)和更多的硫酸亚铁(II)七水合物(1-2当量)直到反应结束。之后,将反应混合物在饱和碳酸氢钠溶液(200mL)和乙酸乙酯(400mL)之间分配。分离出有机层,并将水层用乙酸乙酯(2×100mL)萃取。将合并的有机层用饱和硫代硫酸钠溶液(50mL)洗涤,用硫酸钠干燥并减压浓缩。将残余物通过柱色谱法来纯化得到78%收率(6.40g)的112b,其为黄色油状物:1H NMR(500MHz,CDCl3)δ6.23(s,1H),4.23(s,2H),3.94(t,2H,J=6.5Hz),3.81(s,3H),2.74(t,2H,J=6.5Hz),2.00(m,2H),1.83(m,2H);(APCI+)m/z 219.3(M+H)
实施例112c 3-(2-氨基乙基)-5,6,7,8-四氢吲嗪-2-羧酸甲酯盐酸盐112c
在室温,在50psi氢气下,在乙醇和乙酸乙酯中和在盐酸存在下,将3-(氰基甲基)-5,6,7,8-四氢吲嗪-2-羧酸甲酯112b用氧化铂催化剂氢化得到112c(380mg,1.74mmol),将其直接用在下一步骤中。
实施例112d 3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-1(2H)-酮112d
将配备有磁力搅拌子和氮气进气口的100-mL单颈圆底烧瓶用氮气吹洗并装入3-(2-氨基乙基)-5,6,7,8-四氢吲嗪-2-羧酸甲酯盐酸盐112c(如上所述制备,估计为1.74mmol,假定为定量收率)、乙醇钠(354mg,5.22mmol)和乙醇(20mL)。将混合物在55℃搅拌5小时。之后,减压浓缩反应混合物,并将残余物在乙酸乙酯(200mL)和水(100mL)之间分配。分离出有机层,并将水层用乙酸乙酯(2×100mL)萃取。将合并的有机层用盐水洗涤,用硫酸钠干燥并减压浓缩。将残余物通过柱色谱法来纯化得到67%收率(220mg)的112d,其为白色固体:mp 195–197℃;1H NMR(500MHz,DMSO-d6)δ6.76(s,1H),5.89(s,1H),3.78(t,2H,J=6.5Hz),3.35(m,2H),2.66(m,4H),1.87(m,2H),1.72(m,2H);(APCI+)m/z 191.3(M+H)
实施例112e 3-溴-5-(1-氧代-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-4-甲醛112e
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶装入1,4-二噁烷(15mL)、3,5-二溴吡啶-4-甲醛(400mg,1.5mmol)、112d(142mg,0.76mmol)和碳酸铯(176mg,1.5mmol)。加入Xantphos(40mg,0.08mmol)和Pd2(dba)3(70mg,0.08mmol),并将反应混合物在100℃加热5小时。之后,将反应混合物冷却至室温并过滤。减压浓缩滤液并将残余物在快速柱上纯化(用DCM:MeOH(20:1)洗脱)得到112e(200mg,70%)。MS:[M+H]
实施例112f 3-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-5-(1-氧代-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-4-甲醛112f
在密封管中装入112e(200mg,0.53mmol)、1-甲基-3-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮101l(240mg,0.51mmol)、PdCl2(dppf)(42mg,0.05mmol)、K3PO4(230mg,1mmol)和NaOAc(80mg,1mmol)/CH3CN(5mL)和H2O(1.5mL)。将体系排空并用氮气回填。将反应混合物在100℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物通过快速柱色谱法(用10:1的DCM/MeOH洗脱)来纯化得到112f(138mg,40%),其为浅黄色固体。MS:[M+H]+635。
实施例112 2-(4-(羟基甲基)-5-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-基)-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-1(2H)-酮112
在0℃,将112f(130mg,0.20mmol)和NaBH4(20mg,0.5mmol)于MeOH(5mL)中的混合物搅拌0.5小时。将混合物用水淬灭并用EtOAc(5mLX2)萃取。将合并的EtOAc萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到112(48mg,34%)。LCMS:[M+H]+:637.1H NMR(500MHz,DMSO)δ8.58(s,1H),8.48(s,1H),8.45(s,1H),8.39(s,1H),7.86(d,J=2.4,1H),7.37-7.36(m,2H),7.23-7.21(m,1H),6.02(s,1H),5.02(s,1H),4.54(t,J=6.5,2H),4.45(t,J=5.5,2H),4.36-4.35(m,2H),4.00-3.79(m,4H),3.59(s,3H),3.43-3.41(m,1H),3.07-2.96(m,6H),2.70(t,J=6.0,2H),2.39-2.38(m,4H),1.92-1.90(m,2H),1.75-1.73(m,2H).
实施例113a(3-硝基-1H-吡唑-5-基)甲醇113a
将配备有机械搅拌器、加料漏斗和氮气进气口的3-L三颈圆底烧瓶用氮气吹洗并装入3-硝基吡唑-5-羧酸(28.0g,178mmol)和THF(420mL),用冰/丙酮浴冷却至–5℃。加入硼烷-THF复合物溶液(1.0M,535mL,535mmol),加入速度是维持内部反应温度低于5℃。加入结束后,移去冷却浴并将反应混合物在室温搅拌18小时。之后,将反应混合物用冰/丙酮浴冷却至–5℃,加入水(70mL)和4N盐酸(70mL)并将反应混合物回流搅拌1小时,目的是破坏硼烷与吡唑的复合物。将反应混合物冷却至室温并减压浓缩至体积为约30mL。加入乙酸乙酯(175mL)并将混合物搅拌15分钟。分离出水层并用乙酸乙酯(4×200mL)萃取。将合并的有机层用饱和碳酸氢钠水溶液(2×50mL)、盐水(50mL)洗涤并用硫酸钠干燥,过滤除去干燥剂,并减压浓缩滤液得到(3-硝基-1H-吡唑-5-基)甲醇113a,94%收率(24.0g),其为浅黄色固体:1H NMR(300MHz,DMSO-d6)δ13.90(br s,1H),6.87(s,1H),5.58(t,1H,J=5.4Hz),4.53(d,2H,J=5.1Hz);MS(ESI+)m/z 144.0(M+H)
实施例113b(1-(2-溴乙基)-3-硝基-1H-吡唑-5-基)甲醇113b
将配备有机械搅拌器和调温器的1-L三颈圆底烧瓶用氮气吹洗并装入113a(25.0g,175mmol)、DMF(250mL)和碳酸铯(70.0g,215mmol),在104℃加热5分钟。然后将反应混合物用冰/丙酮浴冷却至0℃并逐份加入二溴乙烷(329g,1.75mol)(无放热)。将反应混合物在0℃搅拌1小时,然后在室温搅拌4小时。之后,缓慢加入KH2PO4(40g)的水(400mL)溶液。将反应混合物在室温搅拌30分钟。加入乙酸乙酯(450mL),分离出水层并用乙酸乙酯(2×100mL)萃取。将合并的有机层用水(200mL)、盐水(200mL)洗涤,用硫酸钠干燥,并通过过滤除去干燥剂。减压浓缩滤液得到86%收率(37.5g)的粗制113b,其为橙色油状物:1H NMR(300MHz,CDCl3)δ6.85(s,1H),4.82(d,2H,J=5.4Hz),4.66(t,2H,J=6.3Hz),3.83(t,2H,J=6.3Hz);MS(ESI+)m/z 249.9(M+H)。
实施例113c 1-(2-溴乙基)-5-(溴甲基)-3-硝基-1H-吡唑113c
将配备有磁力搅拌子、氮气进气口和回流冷凝器的500-mL三颈圆底烧瓶用氮气吹洗并装入113b(37.0g,148mmol)和氯仿(160mL)。将反应混合物用冰/丙酮浴冷却至–5℃并逐份加入三溴化磷(40.0g,148mmol)。移去冷却浴并将反应混合物回流搅拌2小时。之后,将反应混合物冷却至–5℃并加入饱和碳酸氢钠水溶液(250mL)直到达到pH 8.5。将混合物用乙酸乙酯(3×150mL)萃取并将合并的有机层用饱和碳酸钠水溶液(2×50mL)、盐水(75mL)洗涤,用硫酸钠干燥,并通过过滤除去干燥剂。减压浓缩滤液得到黄色残余物,将其在轻微加热下溶解在二氯甲烷(60mL)中。加入己烷(约20mL)并且所述溶液变浑浊。加热混合物直到形成固体析出物,加入二氯甲烷(9mL)并且所述溶液变澄清。使所述溶液冷却至室温,4小时后,通过真空过滤收集所得晶体。将滤饼用冰冷却的二氯甲烷:己烷的1:2混合物(2×20mL)洗涤得到1-(2-溴乙基)-5-(溴甲基)-3-硝基-1H-吡唑(19.7g)。蒸发合并的滤液并再次进行所述操作得到额外9.70g 1-(2-溴乙基)-5-(溴-甲基)-3-硝基-1H-吡唑。合并所述固体并高真空干燥18小时得到57%收率(26.0g)的1-(2-溴乙基)-5-(溴甲基)-3-硝基-1H-吡唑113c,其为白色晶体:mp 95–97℃;1H NMR(300MHz,CDCl3)δ6.93(s,1H),4.63(t,2H,J=6.0Hz),4.54(s,2H),3.86(t,2H,J=6.0Hz)。
实施例113d 5-甲基-2-硝基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪113d
在配备有磁力搅拌子和氮气进气口的1-L单颈圆底烧瓶中装入THF(350mL)、113c(10.0g,32.2mmol)、2M甲胺的THF溶液(113mL,225mmol)并在室温搅拌72小时。之后,将反应混合物减压浓缩至干,并将所得固体与乙酸乙酯(75mL)和10%碳酸钾水溶液(75mL)的混合物一起搅拌。分离出水层并用乙酸乙酯(2×75mL)萃取。将合并的有机萃取物先后用10%碳酸钾水溶液(75mL)和盐水(50mL)洗涤并用硫酸钠干燥。过滤除去干燥剂,并减压浓缩滤液得到113d,97%收率(5.70g),其为黄色固体:1H NMR(300MHz,CDCl3)δ6.62(s,1H),4.28(t,2H,J=5.4Hz),3.67(s,2H),2.95(t,2H,J=5.4Hz),2.52(s,3H);MS(ESI+)m/z 183.0(M+H)
实施例113e 5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-胺113e
将500-mL帕尔反应瓶用氮气吹洗并装入10%钯/炭(50%水分,800mg干重)和113d(4.00g,2.20mmol)的乙醇(160mL)溶液。将所述瓶与帕尔氢化器相连,排空,充入氢气至压力为45psi并震摇2小时。之后,将氢气排空,并将氮气充入所述瓶中。加入521(1.0g),并将混合物用521垫过滤。将滤饼用乙醇(2×75mL)洗涤,并将合并的滤液减压浓缩至干得到99%收率的113e(3.31g),其为橙色固体:1H NMR(300MHz,CDCl3)δ5.34(s,1H),3.98(t,2H,J=5.4Hz),3.52(s,3H),2.84(t,2H,J=5.7Hz),2.45(s,3H);MS(ESI+)m/z 153.1(M+H)
实施例113f 5-溴-1-甲基-3-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)吡啶-2(1H)-酮113f
在配备有磁力搅拌子的密封管中装入113e(1.02g,6.7mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(2.15g,8.1mmol)、Pd2(dba)3(610mg,0.67mmol)、2,2-二(二苯基膦基)-1,1-联萘(775mg,1.34mmol)、碳酸铯(4.37g,13.6mmol)和1,4-二噁烷(30mL)。在经历三轮真空/氩气吹洗后,将混合物在110℃加热2小时。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(15:1,V/V)洗脱)来纯化得到113f(380mg,14%),其为白色固体。LCMS:[M+H]+338
实施例113g 2-(4-氯-3-(羟基甲基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮113g
在10℃,向4-氯-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛103b(1.0g,3.0mmol)于甲醇(50mL)中的溶液中加入硼氢化钠(380mg,9.0mmol)并将混合物再搅拌30分钟。将反应混合物用水(1mL)淬灭并浓缩。将残余物溶解在二氯甲烷(50mL)中并用水(10mL)洗涤。将有机相用无水Na2SO4干燥,过滤并减压蒸发得到113g,其为黄色固体(900mg,90%)。MS:[M+H]+332。
实施例113h乙酸(4-氯-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯113h
在室温搅拌的同时向113g(900mg,2.7mol)和三乙胺(900mg,9.0mol)于二氯甲烷(5mL)中的混合物中滴加乙酰氯(600mg,6.0mol),并再搅拌1小时。将反应混合物浓缩并通过硅胶柱色谱法来纯化(用二氯甲烷洗脱)得到113h,其为白色固体(950mg,94%)。MS:[M+H]+374。
实施例113i乙酸(2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-3-基)甲酯113i
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入113h(950mg,2.5mmol)、Pin2B2(1.6g,2.0当量,5mmol)、Pd2(dba)3(230mg,0.1当量,0.25mmol)、X-phos(232mg,0.2当量,0.5mmol)、AcOK(735mg,3当量,7.5mmol)和二噁烷(20mL)。在经历三轮真空/氩气吹洗后,将混合物加热至65℃,保持14小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物通过PE/EA=3/1(10mL)来洗涤得到113i,其为黄色固体(950mg,87%)。MS:[M+H]+383。
实施例113j乙酸(4-(1-甲基-5-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯113j
在配备有磁力搅拌子的密封管中装入113f(190mg,0.56mmol)、113i(215mg,0.56mmol)、Pd(dppf)Cl2(47mg,0.056mmol)、1.0M NaOAc(93mg,1.12mmol,2.0当量)、1.0MK3PO4(240mg,1.12mmol,2.0当量)和乙腈(3mL)。在经历三轮真空/氩气吹洗后,将混合物在110℃加热2小时。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(10:1,V/V)洗脱)来纯化得到113j(300mg,94%),其为棕色固体。LCMS:[M+H]+597
实施例113 2-(3-(羟基甲基)-4-(1-甲基-5-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮113
将113j(300mg,0.50mmol)和LiOH·H2O(120mg,2.50mmol)于iPrOH/THF(1:1,3mL)和H2O(1mL)中的混合物在30℃搅拌2小时。真空蒸发混合物并将残余物用EtOAc(10mLX2)萃取。将合并的EtOAc萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到113(91mg,32%),其为白色固体。LCMS:[M+H]+555.1H NMR(500MHz,CDCl3)δ8.47(d,J=5.0,1H),7.95(d,J=5.0,1H),7.72(d,J=2.0,1H),7.42(s,1H),7.35(d,J=5.0,1H),6.89(s,1H),5.69(s,1H),5.01-5.02(m,1H),4.61-4.62(m,1H),4.48-4.49(m,1H),4.32-4.33(m,1H),4.15-4.07(m,4H),3.86-3.87(m,1H),3.69(s,3H),3.60-3.59(m,2H),2.88(t,J=6.0,2H),2.61-2.56(m,4H),2.47(s,3H),1.89-1.90(m,2H),1.78-1.79(m,2H)
实施例114a(R)-5-溴-3-(4-(1,4-二甲基-3-氧代哌嗪-2-基)苯基氨基)-1-甲基吡嗪-2(1H)-酮114a
在配备有磁力搅拌子的密封管中装入(R)-3-(4-氨基苯基)-1,4-二甲基哌嗪-2-酮(1.08g,5mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(1.47g,5.5mmol)、二异丙基乙基胺(1.94g,15mmol)和iPrOH(20mL)。在经历三轮真空/氩气吹洗后,将混合物在110℃加热整夜。冷却至室温后,加入水(20mL)并将混合物用乙酸乙酯(50mLX2)萃取。分离出有机层,合并,用无水硫酸钠干燥并浓缩。将所得残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(10:1,V/V)洗脱)得到114a(1.8g,90%),其为红色固体。LCMS:[M+H]+406
实施例114b乙酸(R)-(4-(6-(4-(1,4-二甲基-3-氧代哌嗪-2-基)苯基氨基)-4-甲基-5-氧代-4,5-二氢吡嗪-2-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯114b
在配备有磁力搅拌子的密封管中装入114a(228mg,0.56mmol)、3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113i(215mg,0.56mmol)、Pd(dppf)Cl2(47mg,0.056mmol)、1.0M NaOAc(93mg,1.12mmol,2.0当量)、1.0M K3PO4(240mg,1.12mmol,2.0当量)和乙腈(3mL)。在经历三轮真空/氩气吹洗后,将混合物在110℃加热2小时。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(10:1,V/V)洗脱)来纯化得到114b(360mg,96%),其为棕色固体。LCMS:[M+H]+665。
实施例114(R)-2-(4-(6-(4-(1,4-二甲基-3-氧代哌嗪-2-基)苯基氨基)-4-甲基-5-氧代-4,5-二氢吡嗪-2-基)-3-(羟基甲基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮114
将114b(360mg,0.54mmol)和LiOH·H2O(138mg,2.76mmol)于iPrOH/THF(1:1,3mL)和H2O(1mL)中的混合物在30℃搅拌2小时。真空蒸发混合物并将残余物用EtOAc(10mLX2)萃取。将合并的EtOAc萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到114(72mg,21%),其为白色固体。LCMS:[M+H]+623.1H NMR(500MHz,CDCl3)δ8.53(d,J=4.5,1H),8.31(s,1H),8.10(s,1H),7.83-7.78(m,3H),7.36(d,J=8.0,2H),6.89(s,1H),5.12-5.14(m,1H),4.68-4.70(m,1H),4.49-4.53(m,1H),4.38-4.43(m,1H),4.15-4.06(m,2H),3.89-3.90(m,1H),3.72-3.73(m,2H),3.65(s,3H),3.21-3.22(m,1H),3.01-3.03(m,4H),2.71-2.56(m,5H),2.20(s,3H),1.90-1.92(m,2H),1.79-1.80(m,2H)
实施例115a 5-溴-1-甲基-3-(5-甲基-1H-吡唑-3-基氨基)吡啶-2(1H)-酮115a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(15mL)、5-甲基-1H-吡唑-3-胺(1g,10mmol)(1)、3,5-二溴-1-甲基吡啶-2(1H)-酮(4g,15mmol)(2)和碳酸铯(6.4g,20mmol)。加入Xantphos(400mg,0.8mmol)和Pd2(dba)3(700mg,0.8mmol)并将反应混合物在100℃加热5小时。之后,将反应混合物冷却至室温并过滤。减压浓缩滤液并将残余物在快速柱上纯化(用DCM:MeOH(20:1)洗脱)得到115a(1.0g,35%)。MS:[M+H]+283。
实施例115b 4-(1-甲基-5-(5-甲基-1H-吡唑-3-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛115b
在密封管中装入115a(280mg,1mmol)、3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113i(420mg,1.1mmol)、PdCl2(dppf)(41mg,0.056mmol)、K3PO4(100mg)和NaOAc(50mg)/CH3CN(10mL)+H2O(3mL)。将体系排空并用氮气回填。将反应混合物在100℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物通过快速柱色谱法(用10:1的DCM/MeOH洗脱)来纯化得到115b,35%收率(190mg),其为浅黄色固体。MS:[M+H]+542。
实施例115 2-(3-(羟基甲基)-4-(1-甲基-5-(5-甲基-1H-吡唑-3-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮115
在搅拌的同时,在100-mL单颈圆底烧瓶中装入115b(190mg,0.35mol)于THF/iPA/H2O(5mL/5mL/2mL)中和LiOH(85mg,3.5mmol)。将该混合物在50℃搅拌0.5小时。然后加入20mL H2O并将混合物用EA(30mLX3)萃取。将合并的有机层用Na2SO4干燥并浓缩得到黄色固体,将其进一步通过反相制备性-HPLC来纯化得到115,其为白色固体(48mg,30%收率)。LCMS:[M+H]+500。1H NMR(500MHz,CDCl3)δ8.44(d,J=6.0,1H),7.95(s,1H),7.69(s,1H),7.44(s,1H),7.30(d,J=6.0,2H),6.87(s,1H),5.74(s,1H),4.59-3.86(m,7H),3.69(s,3H),2.57-2.56(m,4H),2.25(s,3H)1.88-1.77(m,4H)
实施例116a 3-溴-5-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-4-甲醛116a
向配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(15mL)、3,5-二溴吡啶-4-甲醛(200mg,0.76mmol)、8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-6-酮191d(160mg,0.76mmol)和碳酸铯(176mg,1.5mmol)。加入碘化亚铜(CuI)(100mg,0.76mmol)和4,7-二甲氧基-1,10-菲咯啉(127mg,0.52mmol)并将反应混合物在100℃加热5小时。之后,将反应混合物冷却至室温并过滤。减压浓缩滤液并将残余物在快速柱上纯化(用EtOAC/PE(1:2)洗脱)得到116a(80mg,30%)。MS:[M+H]+390。
实施例116b 3-[1-甲基-5-({5-[4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]-5-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-4-甲醛116b
在密封管中装入116a(80mg,0.20mmol)、1-甲基-3-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮101l(96mg,0.20mmol)、PdCl2(dppf)(18mg,0.02mmol)、K3PO4(30mg)和NaOAc(20mg)/CH3CN(5mL)+H2O(1mL)。将体系排空并用氮气回填。将反应混合物在100℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物通过快速柱色谱法(用10:1的DCM/MeOH洗脱)来纯化得到116b,35%收率(46mg)。MS:[M+H]+651。
实施例116 4-羟基甲基-3-[1-甲基-5-({5-[4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]-5-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶116
在0℃,向116b(46mg,0.07mmol)于甲醇(4mL)中的溶液中加入硼氢化钠(20mg,0.7mmol)并搅拌30分钟。将反应混合物用水(1.0mL)淬灭并浓缩。将残余物通过反相制备性-HPLC来纯化得到116(12mg,28%),其为黄色固体。LCMS:[M+H]+653。1H NMR(500MHz,DMSO)δ8.60(s,1H),8.59(s,1H),8.56(d,J=2.0,1H),8.50(s,1H),8.44(s,1H),7.87(d,J=3.0,1H),7.38-7.36(m,2H),7.24-7.22(m,1H),4.90(m,1H),4.56-4.53(m,2H),4.46-4.44(m,4H),3.59(s,3H),3.44-3.42(m,1H),3.06(t,J=4.5,4H),2.94-2.93(m,2H),2.85-2.84(m,2H),2.38(t,J=4.0,4H),1.89-1.84(m,4H)
实施例117a 5-(甲基硫基)-2-硝基吡啶117a
在0℃,向5-氯-2-硝基吡啶(3g,18mmol)于MeOH(20mL)中的混合物中加入甲硫醇钠(1.4g,20mmol)并将混合物在20℃搅拌2小时。过滤所得悬浮液并用水洗涤,真空干燥得到粗制117a,其为黄色固体(2g,66%),将其不经纯化即用于下一步骤。MS:[M+H]+171。
实施例117b 5-(甲基磺酰基)-2-硝基吡啶117b
向117a(260mg,0.5mmol)于乙酸(15mL)中的混合物中加入H2O2(30%水溶液)(7.5mL),将反应混合物在25℃搅拌整夜。将反应溶液倒入水中并用EtOAC萃取,浓缩得到浅黄色液体,通过硅胶纯化(EtOAC/PE:1:3)得到117b(2g,86%)。MS:[M+H]+203.
实施例117c 5-(甲基磺酰基)吡啶-2-胺117c
将117b(2g,10mmol)、MeOH(10mL)、Pd/C(120mg)于甲醇(8mL)中的混合物在氢气(50Psi)中在25℃搅拌整夜。过滤除去Pd/C并减压浓缩滤液得到117c(1.7g,98%)。MS:[M+H]+173。
实施例117d 5-溴-1-甲基-3-(5-(甲基磺酰基)吡啶-2-基氨基)吡啶-2(1H)-酮117d
在配备有磁力搅拌子和回流冷凝器的250-mL单颈圆底烧瓶中装入1,4-二噁烷(15mL)、117c(1.7g,10mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(5.2g,20mmol)和碳酸铯(6.4g,20mmol)。加入Xantphos(300mg,0.8mmol)和Pd2(dba)3(500mg,0.8mmol)并将反应混合物在100℃加热5h(小时)。之后,将反应混合物冷却至室温。过滤除去混合物并减压浓缩滤液。将残余物在快速柱上纯化(用DCM:MeOH(20:1)洗脱)得到117d(1g,30%)。MS:[M+H]+358.
实施例117e乙酸(4-(1-甲基-5-(5-(甲基磺酰基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯117e
在密封管中装入117d(100mg,0.28mmol)、3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113i(115mg,0.3mmol)、PdCl2(dppf)(25mg,0.03mmol)、K3PO4(126mg,0.6mmol)和NaOAc(60mg,0.6mmol)于MeCN(8mL)和H2O(1mL)中。将体系排空并用氮气回填。将反应混合物在100℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物通过硅胶快速柱来纯化(用DCM:MeOH(20:1)洗脱)得到117e(100mg,40%)。MS:[M+H]+617.
实施例117 2-(3-(羟基甲基)-4-(1-甲基-5-(5-(甲基磺酰基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢-吡嗪并[1,2-a]吲哚-1(2H)-酮117
在搅拌的同时,在100-mL单颈圆底烧瓶中加入117e(100mg,0.2mol)于THF/iPA/H2O(5mL/5mL/2mL)和LiOH(50mg,2mmol)中。将该混合物在50℃搅拌0.5小时。然后加入20mLH2O并将混合物用EA(30mLX3)萃取。将合并的有机层用Na2SO4干燥并浓缩得到黄色固体,将其进一步通过反相制备性-HPLC来纯化得到117,其为白色固体(72mg,90%收率)。MS:[M+H]+575.1H NMR(500MHz,CDCl3)δ9.39(s,1H),8.84(d,J=2.0,1H),8.60(d,J=2.5,1H),8.50(d,J=2.5,1H),7.98(dd,J=2.5,4.0,1H),7.69(d,J=2.4,1H),7.49-7.47(d,J=9.0,1H),7.38-7.37(m,1H),6.58(s,1H),4.99(t,J=4.5,1H),4.47-4.39(m,2H),4.26-4.11(m,3H),3.88-3.86(m,1H),3.62(s,3H),3.19(s,3H),2.66-2.54(m,2H),2.48-2.46(m,2H),1.79-1.66(m,4H)
实施例118a 5-氨基-3-环丙基-1H-吡唑-1-羧酸叔丁酯118a
向3-环丙基-1H-吡唑-5-胺(0.25g,2mmol)和K2CO3(0.828g,6mmol)于THF(5mL)中的混合物中加入(Boc)2O(0.436g,2mmol)/THF(5mL)。将反应混合物在室温搅拌15小时。然后将其过滤并浓缩。将残余物通过快速柱来纯化(用6:1石油醚/乙酸乙酯洗脱)得到118a,其为白色固体(240mg,54%)。LCMS:(M-Boc)+124.
实施例118b 5-溴-3-(3-环丙基-1H-吡唑-5-基氨基)-1-甲基吡啶-2(1H)-酮118b
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶器中装入1,4-二噁烷(15mL)、118a(455mg,1.95mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(0.40g,1.5mmol)和碳酸铯(1.22g,3.75mmol)。使氮气鼓泡通过所得混合物30分钟后,加入XantPhos(87mg,0.15mmol)和三(二亚苄基丙酮)二钯(0)(70mg,0.075mmol),将反应混合物回流加热15小时。之后,将反应混合物冷却至室温,在乙酸乙酯(30mL)和水(30mL)之间分配。分离出水层并用乙酸乙酯(50mL×2)萃取。合并有机层,用盐水洗涤(50mL)并用硫酸钠干燥。过滤除去干燥剂并减压浓缩滤液。将残余物在快速柱上纯化(用50:1DCM/MeOH洗脱)得到118b,其为黄色固体(320mg,50%)。LCMS:(M+H)+309.1H NMR(500MHz,DMSO)δ11.85(s,1H),8.23(s,1H),8.02(d,J=2.5,1H),7.35(d,J=2.5,1H),5.77(d,J=2,1H),3.46(s,3H),1.83(m,1H),0.90(m,2H),0.64(m,2H)
实施例118c乙酸(4-(5-(5-环丙基-1H-吡唑-3-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯118c
在配备有磁力搅拌子的密封管中装入118b(310mg,1mmol)、3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113i(385mg,1mmol)、Pd(dppf)Cl2(80mg,0.1mmol)、K3PO4(424mg,2mmol)、NaOAc(165mg,2mmol)、CH3CN(15mL)和水(1mL)。在经历三轮真空/氩气吹洗后,将混合物在110℃加热3小时。将其真空蒸发。将残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(50:1,V/V)洗脱)得到118c(400mg,68%),其为黄色固体。LCMS:[M+H]+569
实施例118 2-(4-(5-(5-环丙基-1H-吡唑-3-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-3-(羟基甲基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮118
将118c(350mg,0.62mmol)和LiOH·H2O(260mg,6.2mmol)于iPrOH/THF(1:1,3mL)和H2O(1mL)中的混合物在30℃搅拌1小时。真空蒸发混合物并将残余物用EtOAc(10mLX2)萃取。将合并的EtOAc萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到118(200mg,54%),其为白色固体。LCMS:[M+H]+526.1H NMR(500MHz,DMSO)δ11.83(s,1H),8.48(d,J=5,1H),8.05(d,J=2,1H),8.03(s,1H),7.38(d,J=2,1H),7.31(d,J=5,1H),6.58(s,1H),5.81(d,J=2,1H),4.95(t,J=5,1H),4.49-4.51(m,1H),4.38-4.40(m,1H),4.19-4.21(m,3H),3.85-3.87(m,1H),3.58(s,3H),2.61-2.62(m,1H),2.56-2.57(m,1H),2.48-2.49(m,2H),1.81-1.82(m,3H),1.70-1.71(m,2H),0.88-0.89(m,2H),0.63-0.64(m,2H)
实施例119a(S)-乙酸(4-(1-甲基-5-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯119a
按照就所118c描述的操作,使乙酸(2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-3-基)甲酯113i(250mg)与(S)-5-溴-1-甲基-3-(3-甲基-5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)吡啶-2(1H)-酮130e(233mg)反应得到119a,其为黄色固体(230mg,62%)。LCMS:[M+H]+693
实施例119(S)-2-(3-(羟基甲基)-4-(1-甲基-5-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮119
按照就所118描述的操作,用LiOH·H2O/iPrOH/THF(1:1)和H2O使119a的乙酸酯水解,得到119,其为白色固体(184mg,85%)。LCMS:[M+H]+651.1H NMR(500MHz,CDCl3)δ8.65(d,J=2.5,1H),8.50(d,J=5.0,1H),7.99(s,1H),7.87(s,1H),7.84(d,J=2.0,1H),7.35(d,J=5.0,1H),7.33(d,J=7.0,1H),6.90(s,1H),6.83(d,J=9.0,1H),5.04-5.06(m,1H),4.62-4.73(m,5H),4.51(s,1H),4.32(s,1H),4.16(s,1H),4.11(s,1H),3.89(s,1H),3.72(s,3H),3.57(t,J=6.0,1H),3.48(s,1H),3.07-3.12(m,2H),2.53-2.63(m,7H),2.24(m,1H),1.88-1.93(m,2H),1.80(s,2H),0.99(d,J=6.5,3H).
实施例120a 5-溴-3-(5-(4-(2-羟基-2-甲基丙基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基吡啶-2(1H)-酮120a
在配备有磁力搅拌子的密封管中装入5-溴-1-甲基-3-(5-(哌嗪-1-基)吡啶-2-基氨基)吡啶-2(1H)-酮101j(500mg,1.37mmol)、2,2-二甲基环氧乙烷(990mg,13.7mmol)、Cs2CO3(1.3g,4.11mmol)和CH3CN(15mL)。在经历三轮真空/氩气吹洗后,将混合物在110℃加热15小时。然后将其过滤并真空蒸发滤液。将由此获得的粗制120a不经进一步纯化即用在下一步骤中(460mg,77%)。LCMS:[M+H]+437。
实施例120b乙酸(4-(5-(5-(4-(2-羟基-2-甲基丙基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯120b
按照就制备118c所描述的操作,使120a(435mg,1.0mmol)和3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113i(383mg,1mmol)反应得到120b(437mg,63%)。LCMS:[M+H]+696。
实施例120 2-(4-(5-(5-(4-(2-羟基-2-甲基丙基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-3-(羟基甲基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮120
按照就制备118所描述的操作,用LiOH·H2O/iPrOH/THF(1:1)和H2O使120b(70mg,0.1mmol)的乙酸酯水解,得到120(27mg,42%),其为灰色固体。LCMS:[M+H]+653。1H NMR(500MHz,DMSO-d6)δ8.61(d,J=3,1H),8.50(d,J=5,1H),8.41(s,1H),7.83(d,J=3,1H),7.46(d,J=2,1H),7.36(m,2H),7.24(d,J=9,1H),6.58(s,1H),4.95(m,1H),4.44(m,2H),4.24(m,2H),4.13(m,2H),3.87-3.88(m,1H),3.60(s,3H),3.03-3.05(m,4H),2.64-2.66(m,5H),2.61-2.63(m,1H),2.49-2.51(m,2H),2.24(s,2H),1.70-1.71(m,4H),1.10(s,6H)。
实施例121a 4-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-6,7,8,9-四氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛121a
在烧瓶中装入4-氯-2-(1-氧代-6,7,8,9-四氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛103b(88mg,0.27mmol)、1-甲基-3-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮101l(125mg,0.27mmol)、PdCl2(dppf)(18mg,0.02mmol)、K3PO4(30mg)于THF(5mL)和H2O(1mL)中。将体系排空并用氮气回填。将反应混合物回流4小时,然后冷却降至室温。然后将其过滤并减压浓缩滤液。将所得残余物通过快速柱色谱法(用10:1的DCM/MeOH洗脱)来纯化得到121a(90mg,56%),其为黄色固体。MS:[M+H]+633。
实施例121 2-(3-(羟基甲基)-4-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-6,7,8,9-四氢吡嗪并[1,2-a]吲哚-1(2H)-酮121
在0℃,向121a(76mg,0.12mmol)于甲醇(4mL)中的悬浮液中加入硼氢化钠(20mg,0.7mmol)并搅拌30分钟。将反应混合物用水(1.0mL)淬灭并浓缩。将残余物通过反相制备性-HPLC来纯化得到121(56mg,74%)。LCMS:[M+H]+635。1H NMR(500MHz,DMSO)δ8.66(d,J=2.0,1H),8.57(d,J=5.0,1H),7.93(d,J=3.0,1H),7.85(d,J=2.5,1H),7.80(s,1H),7.50(d,J=5.0,1H),7.24-7.27(m,1H),7.06(s,1H),6.97(d,J=6.0,1H),6.81(d,J=8.0,1H),6.67(d,J=6.0,1H),5.08(d,J=11.5,1H),4.67-4.72(m,4H),4.51(d,J=12.0,1H),4.35(t,J=12.0,1H),3.72(s,3H),3.57-3.59(m,1H),3.16-3.17(m,4H),2.70-2.74(m,4H),2.52-2.53(m,4H),1.94-1.95(m,2H),1.84-1.86(m,2H).
实施例122a(2R,5S)-2,5-二甲基-4-(6-硝基吡啶-3-基)哌嗪-1-羧酸叔丁酯122a
按照就化合物101g所描述的操作,使(2R,5S)-2,5-二甲基哌嗪-1-羧酸叔丁酯(1.5g,6.0mmol)与5-溴-2-硝基吡啶(1212mg,6.0mmol)反应得到122a,其为黄色固体(1500mg,75%)。LCMS:[M+H]+337
实施例122b(2R,5S)-4-(6-氨基吡啶-3-基)-2,5-二甲基哌嗪-1-羧酸叔丁酯122b
按照就化合物101h所描述的操作,使122a(1.5g,4.46mmol)反应得到122b,其为黄色固体(1130mg,83%)。LCMS:[M+H]+307
实施例122c(2R,5S)-4-(6-(5-溴-1-甲基-2-氧代-1,2-二氢吡啶-3-基氨基)吡啶-3-基)-2,5-二甲基哌嗪-1-羧酸叔丁酯122c
按照就化合物101i所描述的操作,使122b(766mg,2.50mmol)与3,5-二溴-1-甲基吡啶-2(1H)-酮(668mg,2.50mmol)反应得到122c,其为黄色固体(978mg,79%)。LCMS:[M+H]+492
实施例122d(2R,5S)-4-(6-(5-溴-1-甲基-2-氧代-1,2-二氢吡啶-3-基氨基)吡啶-3-基)-2,5-二甲基哌嗪-1-羧酸叔丁酯122d
按照就化合物101j所描述的操作,使122c(978mg,1.99mmol)反应得到122d,其为黄色固体(700mg,90%)。LCMS:[M+H]+392
实施例122e 5-溴-3-(5-((2S,5R)-2,5-二甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基吡啶-2(1H)-酮122e
按照就化合物101k所描述的操作,使122d(700mg,1.79mmol)反应得到122e,其为黄色固体(723mg,91%)。LCMS:[M+H]+448
实施例122f乙酸(4-(5-(5-((2S,5R)-2,5-二甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯122f
按照就化合物113j所描述的操作,使122e(723mg,1.62mmol)与3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113i(613mg,1.62mmol)反应得到122f,其为黄色固体(464mg,41%)。LCMS:[M+H]+707
实施例122 2-(4-(5-(5-((2S,5R)-2,5-二甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-3-(羟基甲基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮122
按照就化合物113所描述的操作,用氢氧化锂将122f(464mg,0.66mmol)水解得到122,其为白色固体(83mg,20%)。LCMS:[M+H]+665.1H NMR(500MHz,CDCl3)δ8.69(d,J=2.5,1H),8.51(d,J=5.0,1H),8.03(d,J=2.5,1H),7.88(s,1H),7.86(d,J=2.5,1H),7.38(d,J=5.0,2H),6.90(s,1H),6.82(d,J=9.0,1H),5.07(s,1H),4.77-4.72(m,2H),4.68-4.61(m,3H),4.52(s,1H),4.33(s,1H),4.17-4.11(m,2H),3.88(s,1H),3.76(s,1H),3.73(s,3H),3.19(s,1H),2.93-2.90(m,1H),2.73(s,2H),2.63-2.57(m,4H),2.48(s,1H),1.99-1.90(m,3H),1.80(s,2H),0.91(t,J=5.5,6H)
实施例123a(2-溴乙氧基)(叔丁基)二甲基硅烷123a
向2-溴乙醇(5.0g,40.3mmol)于DCM(20mL)中的溶液中加入叔丁基二甲基甲硅烷基氯化物(9.1g,60.5mmol),然后加入三乙胺(8.14g,80.6mmol)和4-二甲基氨基吡啶(49.2mg,0.4mmol)。将混合物在室温搅拌15小时并真空浓缩。使残余物在1N HCl和乙酸乙酯之间分配。将含水部分用乙酸乙酯萃取。将合并的有机部分用盐水洗涤,用硫酸钠干燥,过滤并真空浓缩得到黄色油状物,将其通过柱色谱法来纯化(用PE:EA(50:1)洗脱)得到123a,其为无色油状物(6.0g,62.4%)。LCMS:(M+H)+241。
实施例123b 5-溴-3-(5-(4-(2-(叔丁基二甲基甲硅烷基氧基)乙基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基吡啶-2(1H)-酮123b
在70℃,向123a(231mg,0.96mmol)于MeCN(40mL)中的悬浮液中加入5-溴-1-甲基-3-(5-(哌嗪-1-基)吡啶-2-基氨基)吡啶-2(1H)-酮101j(350mg,0.96mmol)。将反应混合物搅拌3天。然后将其过滤并减压浓缩滤液。将所得残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(30:1)洗脱)得到123b,其为黄色固体(452mg,90%)。MS:[M+H]+524.7。
实施例123c 5-溴-3-(5-(4-(2-羟基乙基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基吡啶-2(1H)-酮123c
在室温,向123b(300mg,0.57mmol)于MeOH(20mL)中的悬浮液中加入L(-)-樟脑磺酸(199mg,0.86mmol)。将反应混合物搅拌整夜。加入水(20mL)并将混合物用乙酸乙酯(50mLX2)萃取。将合并的有机层用无水硫酸钠来干燥并浓缩得到123c(325mg,95%),其为黄色固体。MS:[M+H]+408.7。
实施例123d乙酸(4-(5-(5-(4-(2-羟基乙基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯123d
在密封管中装入123c(200mg,0.49mmol)、3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸(113i)(188mg,0.49mmol)、Pd(dppf)Cl2(40mg,0.049mmol)、K3PO4(208mg,0.98mmol)、NaOAc(133mg,0.98mmol)、H2O(3mL)和MeCN(50mL)。将混合物在110°加热3小时。真空蒸发溶剂并将残余物通过硅胶色谱法来纯化(用30:1DCM/MeOH洗脱)得到123d(187mg,57%)。MS:[M+H]+667.7。
实施例123 2-(4-(5-(5-(4-(2-羟基乙基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-3-(羟基甲基)吡啶-2-基)-3,4,6,7,8,9-六氢-吡嗪并[1,2-a]吲哚-1(2H)-酮123
将123d(187mg,0.28mmol)和LiOH(235mg,5.6mmol)于iPrOH/THF(1:1,3.5mL)和H2O(0.5mL)中的混合物在35℃搅拌0.5小时。然后将其真空蒸发并将残余物用EtOAc(5mLX2)萃取。将合并的EtOAc萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到123(40mg,31%),其为黄色固体。MS:[M+H]+625.4.1H NMR(500MHz,CDCl3)δ8.63(d,J=2.5,1H),8.49(d,J=5.0,1H),7.92(d,J=2.5,1H),7.82(d,J=2.0,1H),7.78(s,1H),7.36(d,J=5.5,1H),7.27-7.25(m,1H),6.89(s,1H),6.81(d,J=9.5,1H),5.04-5.02(m,1H),4.62(d,J=10,1H),4.50-4.47(m,1H),4.34-4.29(m,1H),4.12-4.09(m,2H),3.89-3.85(m,1H),3.71-3.67(m,5H),3.15-3.12(m,4H),2.74-2.54(m,10H),1.92-1.87(m,2H),1.79-1.78(m,3H)
实施例124a 4-氯-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-甲醛124a
向2-溴-4-氯吡啶-3-甲醛103a(641mg,2.9mmol)和8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-6-酮191d(400mg,1.94mmol)于二噁烷(20mL)中的悬浮液中加入K2CO3(536mg,3.88mmol)、CuI(369mg,1.94mmol)和4,7-二甲氧基-1,10-菲咯啉(471mg,1.96mmol)。在使氮气鼓泡通过所得溶液30分钟后,将混合物在80℃搅拌16小时。使其冷却至室温并加至H2O(100mL)中。分离出水层并用乙酸乙酯(2×200mL)萃取。将合并的有机层用盐水(100mL)洗涤并用硫酸钠干燥。过滤除去干燥剂并减压浓缩滤液。将残余物在快速柱上纯化(用PE:EA(5:1)洗脱)得到124a(230mg,34%)。LCMS:[M+H]+346
实施例124b 4-[1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基]-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-甲醛124b
在圆底烧瓶中装入124a、1-甲基-3-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮101l(271mg,0.58mmol)、PdCl2(dppf)(50mg,0.06mmol)、K3PO4.3H2O(323mg,1.16mmol)、THF(15mL)和H2O(5mL)。在经历三轮真空/氩气吹洗后,将混合物在70℃加热2小时。然后将其过滤并真空蒸发滤液。将残余物在快速柱色谱上纯化(用1:3石油醚/乙酸乙酯洗脱)得到124b,其为黄色固体(200mg,53%)。LCMS:[M+H]+651
实施例124 3-羟基甲基-4-[1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基]-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶124
将4-[1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基]-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-甲醛124b(200mg,0.31mmol)、NaBH4(35mg,0.92mmol)和CH3OH(10mL)的混合物在25℃搅拌1小时。然后将混合物用CH2Cl2(10mLX2)萃取。将合并的CH2Cl2萃取物减压浓缩。将残余物用反相制备性-HPLC来纯化得到124(100mg,50%),其为黄色固体。LCMS:[M+H]+653.1H NMR(500MHz,DMSO)δ8.64(d,J=2.0Hz,1H),8.57(d,J=5.0Hz,1H),8.46-8.48(m,2H),7.88(d,J=3.0Hz,1H),7.54(d,J=5.0Hz,1H),7.48(d,J=2.5Hz,1H),7.37-7.39(m,1H),7.24(d,J=9.0Hz,1H),4.85-4.87(m,1H),4.55-4.57(m,2H),4.45-4.47(m,2H),3.67-4.39(m,2H),3.60(s,3H),3.42-3.45(m,1H),3.06-3.08(m,4H),2.95(s,2H),2.87(s,2H),2.38-2.40(m,4H),1.87-1.89(m,4H).
实施例125a(3-硝基-1H-吡唑-5-基)甲醇125a
将配备有机械搅拌器、加料漏斗和氮气进气口的3-L三颈圆底烧瓶用氮气吹洗并装入3-硝基吡唑-5-羧酸(28.0g,178mmol)和THF(420mL),用冰/丙酮浴冷却至–5℃。加入硼烷-THF复合物溶液(1.0M,535mL,535mmol),加入速度是维持内部反应温度低于5℃。添加结束后,移去冷却浴并将反应混合物在室温搅拌18小时。之后,将反应混合物用冰/丙酮浴冷却至–5℃,加入水(70mL)和4N盐酸(70mL)并将反应混合物回流搅拌1小时,目的是破坏硼烷与吡唑的复合物。将反应混合物冷却至室温并减压浓缩至体积为约30mL。加入乙酸乙酯(175mL)并将混合物搅拌15分钟。分离出水层并用乙酸乙酯(4×200mL)萃取。将合并的有机层用饱和碳酸氢钠水溶液(2×50mL)、盐水(50mL)洗涤并用硫酸钠干燥,过滤除去干燥剂,并减压浓缩滤液得到125a,94%收率(24.0g),其为浅黄色固体:1H NMR(300MHz,DMSO-d6)δ13.90(br s,1H),6.87(s,1H),5.58(t,1H,J=5.4Hz),4.53(d,2H,J=5.1Hz);MS(ESI+)m/z144.0(M+H)
实施例125b(1-(2-溴乙基)-3-硝基-1H-吡唑-5-基)甲醇125b
将配备有机械搅拌器和调温器的1-L三颈圆底烧瓶用氮气吹洗并装入125a(25.0g,175mmol)、DMF(250mL)和碳酸铯(70.0g,215mmol),在104℃加热5分钟。然后将反应混合物用冰/丙酮浴冷却至0℃并逐份加入二溴乙烷(329g,1.75mol)(无放热)。将反应混合物在0℃搅拌1小时,然后在室温搅拌4小时。之后,缓慢加入KH2PO4(40g)的水(400mL)溶液。将反应混合物在室温搅拌30分钟。加入乙酸乙酯(450mL),分离出水层并用乙酸乙酯(2×100mL)萃取。将合并的有机层用水(200mL)、盐水(200mL)洗涤,用硫酸钠干燥和通过过滤除去干燥剂。减压浓缩滤液得到86%收率(37.5g)的粗制125b,其为橙色油状物:1H NMR(300MHz,CDCl3)δ6.85(s,1H),4.82(d,2H,J=5.4Hz),4.66(t,2H,J=6.3Hz),3.83(t,2H,J=6.3Hz);MS(ESI+)m/z 249.9(M+H).
实施例125c 1-(2-溴乙基)-5-(溴甲基)-3-硝基-1H-吡唑125c
将配备有磁力搅拌子、氮气进气口和回流冷凝器的500-mL三颈圆底烧瓶用氮气吹洗并装入125b(37.0g,148mmol)和氯仿(160mL)。将反应混合物用冰/丙酮浴冷却至–5℃,并逐份加入三溴化磷(40.0g,148mmol)。移去冷却浴并将反应混合物回流搅拌2小时。之后,将反应混合物冷却至–5℃,加入饱和碳酸氢钠水溶液(250mL)直到pH达到8.5。将混合物用乙酸乙酯(3×150mL)萃取并将合并的有机层用饱和碳酸钠水溶液(2×50mL)、盐水(75mL)洗涤,用硫酸钠干燥并通过过滤除去干燥剂。减压浓缩滤液得到黄色残余物,将其在轻微加热下溶解在二氯甲烷(60mL)中。加入己烷(约20mL)并且所述溶液变浑浊。加热混合物直到形成固体析出物,加入二氯甲烷(9mL)并且所述溶液变澄清。使所述溶液冷却至室温,4小时后,通过真空过滤收集所得晶体。将滤饼用冰冷的二氯甲烷:己烷的1:2混合物(2×20mL)洗涤得到1-(2-溴乙基)-5-(溴甲基)-3-硝基-1H-吡唑(19.7g)。蒸发合并的滤液并再次进行所述操作得到额外9.70g 1-(2-溴乙基)-5-(溴-甲基)-3-硝基-1H-吡唑。合并所述固体并高真空干燥18小时得到57%收率(26.0g)的125c,其为白色晶体:mp 95–97℃;1H NMR(300MHz,CDCl3)δ6.93(s,1H),4.63(t,2H,J=6.0Hz),4.54(s,2H),3.86(t,2H,J=6.0Hz)。
实施例125d 2-硝基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪125d
在配备有磁力搅拌子的密封管中装入125c(4g,12.9mmol)0.5M氨的二噁烷溶液(200mL)。将所得混合物小心加热至50℃,过夜。之后,减压浓缩反应混合物并向残余物中加入H2O(50mL)和EtOAc(50mL)。分离出水层并用EtOAc(2×50mL)萃取。将合并的有机萃取物用盐水(100mL)洗涤并用硫酸钠干燥。将所得溶液减压浓缩得到100%收率(2.1g)的粗制125d。
实施例125e 1-(2-硝基-6,7-二氢吡唑并[1,5-a]吡嗪-5(4H)-基)乙酮125e
在200mL圆底烧瓶中装入125d(2.1g,12.9mmol)、三乙胺(5.5mL,38.7mmol)、乙酰氯(1.1mL,15.5mmol)和CH2Cl2(100mL)。将混合物在室温搅拌整夜。之后,减压浓缩反应混合物并向残余物中加入H2O(50mL)和EtOAc(50mL)。分离出水层并用EtOAc(2×50mL)萃取。将合并的有机萃取物用盐水(100mL)洗涤。将合并的水性萃取物用9:1CH2Cl2:MeOH(2X50mL)回提。将合并的有机物用硫酸钠干燥。将所得残余物通过柱色谱法来纯化(用CH2Cl2–9:1CH2Cl2:MeOH的梯度洗脱)得到84%收率(2.3g)的125e。
实施例125f 1-(2-氨基-6,7-二氢吡唑并[1,5-a]吡嗪-5(4H)-基)乙酮125f
在500-mL帕尔氢化瓶中装入125e(2.3g,10.9mmol)、10%钯/炭(50%水分,570mg干重)和乙醇(100mL)。将所述瓶排空,充入氢气至压力为50psi并在帕尔氢化装置上震摇2小时。通过用521垫过滤除去催化剂(用1:1CH2Cl2:MeOH(500mL)洗涤)。将所得溶液减压浓缩得到95%收率(1.9g)的粗制125f。
实施例125g 3-(5-乙酰基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-5-溴-1-甲基吡啶-2(1H)-酮125g
给密封管配备磁力搅拌子并装入125f(860mg,4.8mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(1.8g,6.7mmol)和碳酸铯(3.4g,10.5mmol)于1,4-二噁烷(67mL)中。在使氮气鼓泡通过所述溶液30分钟后,加入Xantphos(330mg,0.6mmol)和三(二亚苄基丙酮)二钯(0)(300mg,0.3mmol)并将反应混合物加热至100℃,保持16小时。之后,加入H2O(50mL)和EtOAc(50mL)。分离出水层并用EtOAc(2×50mL)萃取。将合并的有机萃取物用盐水(100mL)洗涤并用硫酸钠干燥。将所得残余物通过柱色谱法来纯化(用CH2Cl2-60:35:5CH2Cl2:Et2O:MeOH的梯度洗脱)得到41%收率的125g(720mg)。
实施例125h 5-溴-1-甲基-3-(4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)吡啶-2(1H)-酮125h
在具有磁力搅拌子和回流冷凝器的50mL圆底烧瓶中装入125g(250mg,0.7mmol)、NaOH水溶液(5N,6mL)和乙醇(6mL)。将混合物回流搅拌30分钟。之后,加入乙酸乙酯(5mL)和水(5mL)。将分离出的水层用乙酸乙酯(2X5mL)萃取。将合并的有机物用盐水(10mL)洗涤,用硫酸钠干燥,过滤并减压浓缩得到91%收率(200mg)的粗制125h。
实施例125i 5-溴-1-甲基-3-(5-(氧杂环丁烷-3-基)-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)吡啶-2(1H)-酮125i
化合物125i是用与合成101k相同的操作合成的,其中将5-溴-1-甲基-3-(4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)吡啶-2(1H)-酮(125h)(250mg,0.78mmol)与氧杂环丁烷-3-酮(600mg,8.3mmol)/甲醇(8mL)混合。加入氰基硼氢化钠(148mg,3mmol)和氯化锌(165mg,1.5mmol)/甲醇(8mL)并将反应混合物在48℃加热12小时。后处理并经快速柱色谱法(硅胶,60:35:5二氯甲烷/乙醚/甲醇)得到34%收率(100mg)的5-溴-1-甲基-3-(5-(氧杂环丁烷-3-基)-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)吡啶-2(1H)-酮(125i),其为浅绿色固体:MS(ESI+)m/z 382.1(M+H)。
实施例125j乙酸(4-(1-甲基-5-(5-(氧杂环丁烷-3-基)-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯125j
按照就化合物113j所描述的操作,使3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113i(200mg,0.52mmol)与125i(198mg,0.52mmol)反应得到125j,其为黄色固体(200mg,60%)。LCMS:[M+H]+639
实施例125 2-(3-(羟基甲基)-4-(1-甲基-5-(5-(氧杂环丁烷-3-基)-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮125
按照如实施例123中所述的操作,通过氢氧化锂水解125j(200mg 0.31mmol)得到125,其为白色固体(116mg,62%)。LCMS:[M+H]+597.1H NMR(500MHz,CDCl3)δ8.48(d,J=5.0,1H),7.95(d,J=2.0,1H),7.69(d,J=2.0,1H),7.43(s,1H),7.34(d,J=5.5,1H),6.89(s,1H),5.73(s,1H),5.02(t,J=6.5,1H),4.75(t,J=6.5,2H),4.67(t,J=6.5,2H),4.61-4.63(m,1H),4.50(s,1H),4.31-4.35(m,1H),4.10-4.16(m,4H),3.86-3.88(m,1H),3.74-3.79(m,1H),3.70(s,3H),3.56(d,J=4.5,2H),2.82(t,J=4.5,2H),2.50-2.62(m,4H),1.88-1.92(m,2H),1.78-1.82(m,2H)
实施例126a 3-溴-5-(1-氧代-6,7,8,9-四氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-甲醛126a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(15mL)、3,5-二溴吡啶-4-甲醛(604mg,2.28mmol)、6,7,8,9-四氢吡嗪并[1,2-a]吲哚-1(2H)-酮(142mg,0.76mmol)和碳酸铯(485mg,1.5mmol)。加入CuI(143mg,0.76mmol)和4,7-二甲氧基-1,10-菲咯啉(127mg,0.52mmol)并将反应混合物在100℃加热5小时。之后,将反应混合物冷却至室温。然后将其过滤并减压浓缩滤液。将残余物在快速柱上纯化(用EtOAC/PE(1:2)洗脱)得到126a(100mg,35%),其为黄色固体。MS:[M+H]+372。
实施例126b 3-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-5-(1-氧代-6,7,8,9-四氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-甲醛126b
在密封管中装入126a(100mg,0.27mmol)、1-甲基-3-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮101l(125mg,0.27mmol)、PdCl2(dppf)(18mg,0.02mmol)、K3PO4(30mg)和NaOAc(20mg)于CH3CN(5mL)和H2O(1mL)中。将体系排空并用氮气回填。将反应混合物在100℃加热2小时,然后冷却至室温。然后将其过滤并减压浓缩滤液。将所得残余物通过快速柱色谱法来纯化(用10:1的DCM/MeOH洗脱)得到126b(80mg,48%),其为黄色固体。MS:[M+H]+633。
实施例126 2-(4-(羟基甲基)-5-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-基)-6,7,8,9-四氢吡嗪并[1,2-a]吲哚-1(2H)-酮126
在0℃,向126b(76mg,0.12mmol)于甲醇(4mL)中的悬浮液中加入硼氢化钠(20mg,0.7mmol)并将混合物搅拌30分钟。将反应混合物用水(1.0mL)淬灭并浓缩。将残余物通过反相制备性-HPLC来纯化得到126(28mg,37%)。LCMS:[M+H]+635。1H NMR(500MHz,DMSO)δ8.61(d,J=2.5,1H),8.59(s,1H),8.50(s,1H),8.43(s,1H),7.86(d,J=3.0,1H),7.38-7.36(m,2H),7.27-7.22(m,2H),6.82-6.78(m,2H),5.18-5.11(m,1H),4.55(t,J=6.0,2H),4.45(t,J=6.0,2H),4.41-4.29(m,2H),3.60(s,3H),3.44-3.42(m,1H),3.06(t,J=4.5,4H),2.75-2.73(m,2H),2.62-2.60(m,2H),2.38(t,J=4.5,4H),1.86-1.75(m,4H).
实施例127a乙酸(4-(1-甲基-6-氧代-5-(5-(哌嗪-1-基)吡啶-2-基氨基)-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯127a
在装备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入5-溴-1-甲基-3-(5-(哌嗪-1-基)吡啶-2-基氨基)吡啶-2(1H)-酮101j(200mg,0.55mmol)、3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113i(210mg,0.55mmol)、Pd(dppf)Cl2(45mg,0.055mmol)、K3PO4(284mg,1.65mmol)和四氢呋喃(20mL)。在经历三轮真空/氩气吹洗后,将混合物回流加热5小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(33:1)洗脱)来纯化得到127a,其为棕色固体(200mg,58.3%).MS:[M+H]+623.7。
实施例127 2-(3-(羟基甲基)-4-(1-甲基-6-氧代-5-(5-(哌嗪-1-基)吡啶-2-基氨基)-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮127
将127a(190mg,0.31mmol)和LiOH(571mg,13.6mmol)于iPrOH/THF(1:1,3.5mL)和H2O(0.5mL)中的混合物在35℃搅拌0.5小时。然后将其真空蒸发并将残余物用EtOAc(5mLX2)萃取。将合并的EtOAc萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到127(50mg,26.9%)。MS:[M+H]+581.3.1H NMR(500MHz,CDCl3)δ8.63(d,J=2.0,1H),8.49(d,J=5.0,1H),7.91(d,J=3.5,1H),7.82(d,J=2.0,1H),7.77(s,1H),7.37(d,J=5.0,1H),7.20-7.25(m,1H),6.89(s,1H),6.81(d,J=9.0,1H),5.04-5.02(m,1H),4.64-4.61(m,1H),4.50(d,J=5.0,1H),4.34-4.31(m,1H),4.18-4.08(m,2H),3.89-3.86(m,1H),3.71(s,3H),3.05-3.06(m,8H),2.62-2.56(m,4H),1.92-1.88(m,2H),1.81-1.78(m,3H)
实施例128a 5-环丙基-2-硝基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪128a
将1-(2-溴乙基)-5-(溴甲基)-3-硝基-1H-吡唑113c(4g,12.9mmol)和环丙胺(7.35g,129mmol)于THF(40mL)中的混合物在30℃搅拌整夜。反应结束后,过滤混合物并将固体用THF(100mL)洗涤。减压浓缩滤液得到128a(2.68g,99%)。MS:[M+H]+209。
实施例128b 5-环丙基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-胺128b
将128a(2.68g,12.9mmol)、Fe(3.6g,64.4mmol)和NH4Cl(4.1g,77.4mmol)于乙醇(30mL)和水(5mL)中的混合物回流加热2小时。反应结束后,过滤混合物并将固体用乙醇(150mL)洗涤。真空蒸发滤液并将残余物用甲醇/二氯甲烷(1/7)萃取。将合并的萃取物用Na2SO4干燥并蒸发。将残余物在反相Combi-flash上纯化得到128b(1.8g,75%)。MS:[M+H]+179。
实施例128c 5-溴-3-(5-环丙基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-1-甲基吡啶-2(1H)-酮128c
将128b(1.39g,7.8mmol)、XantPhos(450mg,0.78mmol)、Pd2dba3(476mg,0.52mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(1.72g,6.5mmol)和Cs2CO3(6.3mg.19.5mmol)于1,4-二噁烷(30mL)中的混合物回流加热1小时。反应结束后,过滤混合物并将固体用甲醇(60mL)洗涤。真空蒸发滤液并将残余物在反相Combi-flash上纯化得到128c(0.84g,30%)。MS:[M+H]+364。
实施例128d乙酸(4-(5-(5-环丙基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢-吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯128d
按照如实施例113j中所述的操作,128c(230mg,0.6mmol)与3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113i(218mg,0.6mmol)反应得到128d,其为黄色固体(331mg,89%)。LCMS:[M+H]+623
实施例128 2-(4-(5-(5-环丙基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-3-(羟基甲基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮128
按照如实施例113中所述的操作,将128d(331mg,0.53mmol)用氢氧化锂水解得到128,其为白色固体(54mg,20%)。LCMS:[M+H]+581。1H NMR(500MHz,CDCl3)δ8.48(d,J=5.0,1H),7.93(d,J=2.0,1H),7.72(d,J=2.0,1H),7.40(s,1H),7.34(d,J=5.0,1H),6.90(s,1H),5.70(s,1H),5.03-5.02(m,1H),4.64-4.62(m,1H),4.52(s,1H),4.32(s,1H),4.16-4.03(m,4H),3.89-3.87(m,1H),3.80(s,2H),3.70(s,3H),3.12-3.10(m,2H),2.61-2.57(m,4H),1.90(d,J=5.5,3H),1.79(s,2H),0.56(d,J=6.0,2H),0.53(s,2H)
实施例129a 2-硝基-6,7-二氢-4H-吡唑并[5,1-c][1,4]噁嗪129a
向配备有磁力搅拌子和回流冷凝器的250-mL单颈圆底烧瓶中装入1-(2-溴乙基)-5-(溴甲基)-3-硝基-1H-吡唑113c(3.00g,9.59mmol)和4M氢溴酸水溶液(120mL),将所得混合物回流加热24小时。之后,减压浓缩反应混合物至约6mL体积并将残余物在2M氢氧化钠水溶液(40mL)中搅拌2小时。之后,加入二氯甲烷(40mL)并将混合物搅拌15分钟。分离出水层并用二氯甲烷(2×50mL)萃取。将合并的有机萃取物用盐水(100mL)洗涤并用硫酸钠干燥。过滤除去干燥剂并减压浓缩滤液得到62%收率(1.01g)的129a,其为白色固体:mp 110–112℃;1H NMR(300MHz,CDCl3)δ6.68(s,1H),4.87(s,2H),4.28(t,2H,J=5.4Hz),4.20(t,2H,J=5.1Hz);MS(ESI+)m/z 170.0(M+H).
实施例129b 6,7-二氢-4H-吡唑并[5,1-c][1,4]噁嗪-2-胺129b
将500-mL帕尔氢化瓶用氮气吹洗并装入129a(1.01g,5.92mmol)、10%钯/炭(50%水分,125mg干重)和乙醇(50mL)。将所述瓶排空,充入氢气至压力为25psi并在帕尔氢化装置上震摇2小时。然后将氢气排空并将氮气充入所述瓶中。通过用521垫过滤除去催化剂并减压浓缩滤液。将所得残余物通过柱色谱法来纯化(使用400cc硅胶和用3%甲醇/二氯甲烷洗脱)。收集含有129b的馏分,减压浓缩后得到73%收率(601mg)的129b,其为黄色固体:mp 74–76℃1H NMR(300MHz,CDCl3δ5.37(s,1H),4.72(s,2H),4.07(t,2H,J=5.1Hz),3.98(t,2H,J=5.1Hz),3.57(br s,2H);MS(ESI+)m/z 140.4(M+H)。
实施例129c 5-溴-3-(6,7-二氢-4H-吡唑并[5,1-c][1,4]噁嗪-2-基氨基)-1-甲基吡啶-2(1H)-酮129c
在配备有磁力搅拌子、回流冷凝器和氮气进气口的50-mL三颈圆底烧瓶中装入1,4-二噁烷(20mL)、129b(600mg,4.31mmol)、3,5-二溴-1-甲基吡啶–2(1H)-酮(1.44g,5.40mmol)和碳酸铯(3.08g,9.48mmol)。在使氮气鼓泡通过所得溶液30分钟后,加入Xantphos(300mg,0.52mmol)和三(二亚苄基丙酮)二钯(0)(320mg,0.35mmol),并将反应混合物回流加热2小时。之后,将反应混合物冷却至室温,在乙酸乙酯(75mL)和水(75mL)之间分配并过滤。分离出水层并用乙酸乙酯(2×25mL)萃取。合并有机层并用盐水(50mL)洗涤,用硫酸钠干燥。过滤除去干燥剂并减压浓缩滤液。将所得残余物通过柱色谱法来纯化(使用500cc硅胶和用1%甲醇/二氯甲烷洗脱)。收集含129c的馏分并且在减压浓缩后得到31%收率(433mg)的129c,其为绿色固体:mp 195–197℃;1H NMR(300MHz,CDCl3)δ7.92(d,1H,J=2.4Hz),7.44(s,1H),6.90(d,1H,J=2.4Hz),5.65(s,1H),4.80(s,2H),4.13(s,2H),3.61(s,5H);MS(ESI+)m/z 324.9(M+H)。
实施例129d乙酸(4-(5-(6,7-二氢-4H-吡唑并[5,1-c][1,4]噁嗪-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯129d
按照如实施例113j中所述的操作,3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113i(200mg,0.52mmol)与129c(170mg,0.52mmol)反应得到129d,其为黄色固体(185mg,61%)。LCMS:[M+H]+584
实施例129 2-(4-(5-(6,7-二氢-4H-吡唑并[5,1-c][1,4]噁嗪-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-3-(羟基甲基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮129
按照如实施例113中所述的操作,将129d(180mg 0.31mmol)用氢氧化锂水解得到129,其为白色固体(100mg,62%)。LCMS:[M+H]+542.1H NMR(500MHz,CDCl3)δ8.48(d,J=5.0,1H),7.98(d,J=2.0,1H),7.71(d,J=2.0,1H),7.46(s,1H),7.35(d,J=5.0,1H),6.89(s,1H),5.72(s,1H),5.03(d,J=6.5,1H),4.79(s,2H),4.61-4.64(m,1H),4.50(s,1H),4.31-4.35(m,1H),4.06-4.16(m,6H),3.86(s,1H),3.71(s,3H),2.56-2.62(m,4H),1.88-1.92(m,2H),1.80(m,2H)
实施例130a(3S)-3-甲基-4-(6-硝基吡啶-3-基)哌嗪-1-羧酸叔丁酯130a
按照就化合物101g所描述的操作,5-溴-2-硝基吡啶(10.5g,50mmol)与(3S)-3-甲基哌嗪-1-羧酸叔丁酯(10.0g,50mmol)反应得到130a,其为黄色固体(8.05g,50%)。LCMS:[M+H]+323
实施例130b(3S)-4-(6-氨基吡啶-3-基)-3-甲基哌嗪-1-羧酸叔丁酯130b
按照就化合物101h所描述的操作,氢化130a(5.8g)得到130b,其为棕色固体(4.9g,96%)。LCMS:[M+H]+293
实施例130c(3S)-4-(6-(5-溴-1-甲基-2-氧代-1,2-二氢吡啶-3-基氨基)吡啶-3-基)-3-甲基哌嗪-1-羧酸叔丁酯130c
按照就化合物101i所描述的操作,130b(4.0g)与3,5-二溴-1-甲基吡啶-2(1H)-酮(5.5g)反应得到130c,其为黄色固体(5.4g,83%)。LCMS:[M+H]+478
实施例130d(3S)-5-溴-1-甲基-3-(5-(2-甲基哌嗪-1-基)吡啶-2-基氨基)吡啶-2(1H)-酮130d
按照就化合物101j所描述的操作,酸水解130c(3.1g)的Boc基团得到130d,其为黄色固体(2.3g,95%)。LCMS:[M+H]+380。
实施例130e(3S)-5-溴-1-甲基-3-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)吡啶-2(1H)-酮130e
按照就化合物101k所描述的操作,用氧杂环丁烷-3-酮(0.4mL)将130d(2.35g)还原氨化得到130e,其为黄色固体(2.6g,98%)。LCMS:[M+H]+434.
实施例130f(3S)-1-甲基-3-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮130f
在配备有磁力搅拌子和回流冷凝器的100mL单颈圆底烧瓶中装入130e(1.0g,1.0当量,2.3mmol)、Pin2B2(1.46g,2.50当量,5.75mmol)、Pd2(dba)3(105mg,0.05当量,0.125mmol)、X-Phos(93mg,0.1当量,0.23mmol)、AcOK(676mg,3.0当量,6.9mmol)和二噁烷(50mL)。在经历三轮真空/氩气吹洗后,将混合物在90℃加热4小时,然后冷却至室温并过滤。减压浓缩滤液并将所得残余物用3:1PE/EA(80mL)洗涤得到130f,其为黄色固体(1.0g,90%)。MS:[M+H]+482。
实施例130g(3S)-4-[1-甲基-5-({5-[2-甲基4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-甲醛130g
在配备有磁力搅拌子和回流冷凝器的50mL单颈圆底烧瓶中装入130f(420mg,1.0当量,0.44mmol)、4-氯-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-甲醛108a(200mg,2当量,0.88mmol):
PdCl2(dppf)(36mg,0.1当量,0.044mmol)、K3PO4(279mg,3当量,1.32mmol)和THF(20mL)。在经历三轮真空/氩气吹洗后,将混合物回流加热5小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物用3:1PE/EA(80mL)洗涤得到130g(90mg,31%),其为黄色固体。MS:[M+H]+663。
实施例130(3S)-10-[4-[1-甲基-5-({5-[2-甲基4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]-3-(羟基甲基)吡啶-2-基]-4,4-二甲基-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-9-酮130
给50mL单颈圆底烧瓶配备磁力搅拌子并装入130g(90mg,1当量,0.11mmol)、LiOH(7.9mg,3当量,0.33mmol)、i-PrOH(3mL)、THF(3mL)和H2O(2mL)。将混合物在30℃搅拌2小时。然后将其过滤并浓缩。将残余物通过反相制备性-HPLC来纯化得到130(40mg,44%),其为黄色固体。LCMS:[M+H]+665.4.1H NMR(500MHz,CDCl3)δ8.65(d,J=2.0,1H),8.48(d,J=5.0,1H),7.96(d,J=2.0,1H),7.84-7.83(m,2H),7.36(d,J=5.0,1H),7.31(dd,J=3.0,9.0,1H),6.84(s,1H),6.81(d,J=9.0,1H),5.08-5.05(m,1H),4.71-4.61(m,5H),4.51-4.29(m,2H),4.16-4.15(m,2H),3.87-3.85(m,1H),3.72(s,3H),3.55-3.45(m,2H),3.06-3.08(m,2H),2.59-2.47(m,7H),2.22-2.17(m,1H),1.27(s,6H),0.98(d,J=6.5,3H).
实施例131a(S)-乙酸(4-(5-(5-(2-乙基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯131a
在配备有磁力搅拌子的密封管中装入(S)-5-溴-3-(5-(2-乙基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基吡啶-2(1H)-酮161e(269mg,0.60mmol):
113i(230mg,0.60mmol)、Pd(dppf)Cl2(25mg,0.03mmol)、NaOAc(98mg,1.2mmol)、K3PO4(254mg,1.2mmol)和乙腈(4mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热1小时。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(25:1,V/V)洗脱)得到131a(150mg,40%),其为棕色固体。LCMS:[M+H]+707
实施例131(S)-2-(4-(5-(5-(2-乙基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-3-(羟基甲基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮131
将131a(150mg,0.21mmol)和LiOH(50mg,2.1mmol)于iPrOH/THF(1:1,4mL)和H2O(1mL)中的混合物在30℃搅拌1小时。真空蒸发混合物并将残余物用EtOAc(10mLX2)萃取。将合并的EtOAc萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到131(26mg,25%),其为白色固体。LCMS:[M+H]+665。1H NMR(500MHz,CDCl3)δ8.64(d,J=2.0,1H),8.50(d,J=5.0,1H),7.93(d,J=2.5,1H),7.83(d,J=1.5,2H),7.38(d,J=5.0,1H),7.27(d,J=5.0,1H),6.90(s,1H),6.83(d,J=8.5,1H),4.73-4.64(m,5H),4.50(s,1H),4.33-4.31(m,1H),4.20-4.16(m,2H),3.88-3.86(m,1H),3.73(s,3H),3.53-3.51(m,1H),3.33(s,1H),3.13(t,J=5.0,2H),2.61-2.56(m,4H),2.45(d,J=4.0,2H),2.37(s,1H),1.91-1.79(m,7H),1.39-1.40(m,1H),0.83(t,J=7.0,3H).
实施例132a 6-氯-4-(6,7-二氢-4H-吡唑并[5,1-c][1,4]噁嗪-2-基氨基)-2-甲基哒嗪-3(2H)-酮132a
将6,7-二氢-4H-吡唑并[5,1-c][1,4]噁嗪-2-胺129b(0.8g,5.76mmol)、xantophos(360mg,0.623mmol)、Pd2dba3(384mg,0.42mmol)、4-溴-6-氯-2-甲基哒嗪-3(2H)-酮(1.28g,5.76mmol)和Cs2CO3(5.05g.17.3mmol)于1,4-二噁烷(40mL)中的混合物回流加热2小时。反应结束后,过滤混合物,并用MeOH(60mL)洗涤。真空蒸发滤液。将残余物在反相Combi-flash上纯化得到132a(1.3g,81%)。MS:[M+H]+282。
实施例132b乙酸(4-(5-(6,7-二氢-4H-吡唑并[5,1-c][1,4]噁嗪-2-基氨基)-1-甲基-6-氧代-1,6-二氢哒嗪-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯132b
按照就化合物131a所描述的操作,3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113i(200mg,0.52mmol)与132a(146mg,0.52mmol)反应得到132b,其为黄色固体(100mg,53%)。LCMS:[M+H]+585
实施例132 2-(4-(5-(6,7-二氢-4H-吡唑并[5,1-c][1,4]噁嗪-2-基氨基)-1-甲基-6-氧代-1,6-二氢哒嗪-3-基)-3-(羟基甲基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮132
按照就化合物131所描述的操作,用氢氧化锂水解132b(100mg 0.171mmol)得到132,其为白色固体(60mg,65%)。LCMS:[M+H]+543.1H NMR(500MHz,CDCl3)δ8.55(d,J=5.0,1H),8.01(s,1H),7.94(s,1H),7.43(d,J=5.5,1H),6.87(s,1H),5.97(s,1H),4.80(s,2H),4.58(s,3H),4.47(s,1H),4.15-1.14(m,2H),4.11(s,4H),3.90(s,4H),2.61-2.60(m,2H),2.57(t,J=6.5,2H),1.89-1.91(m,2H),1.79-1.80(m,2H)
实施例133a 6-氯-2-甲基-4-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)哒嗪-3(2H)-酮133a
在配备有回流冷凝器、磁力搅拌子和氮气进气口的250-mL三颈圆底烧瓶中装入4-溴-6-氯-2-甲基哒嗪-3(2H)-酮(1.90g,8.53mmol):
113e(1.18g,7.75mmol)和1,4-二噁烷(40mL)。将所述烧瓶用氮气吹洗并冷却至0℃。加入1M六甲基二硅基氨基锂的THF溶液(39mL,39.0mmol)。在使氮气鼓泡通过所得悬浮液30分钟后,加入Xantphos(381mg,0.659mmol)和三(二亚苄基丙酮)二钯(0)(355mg,0.388mmol),并将反应混合物回流加热2小时。之后,将混合物冷却至室温并用水(10mL)稀释。将所述溶液的pH用2N盐酸调整至7.6。分离出有机层,并将水层用乙酸乙酯(3×40mL)萃取。将合并的有机层用硫酸钠干燥并减压浓缩。将残余物通过硅胶柱色谱法来纯化得到76%收率(1.74g)的133a,其为灰白色固体:mp 184–186℃;1H NMR(300MHz,DMSO-d6)δ9.62(s,1H),7.72(s,1H),6.00(s,1H),4.04(t,2H,J=5.1Hz),3.65(s,3H),3.53(s,2H),2.82(t,2H,J=5.1Hz),2.37(s,3H);MS(ESI+)m/z 295.1(M+H)。
实施例133b乙酸(4-(1-甲基-5-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢哒嗪-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯133b
按照就化合物131a所描述的操作,以3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113i(200mg,0.52mmol)和132a(153mg,0.52mmol)开始得到132b,其为黄色固体(170mg,55%)。LCMS:[M+H]+598
实施例133 2-(3-(羟基甲基)-4-(1-甲基-5-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢哒嗪-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮133
用氢氧化锂水解133b(160mg 0.267mmol)得到133,其为白色固体(94mg,63%)。LCMS:[M+H]+556.1H NMR(500MHz,CDCl3)δ8.55(d,J=5.0,1H),7.98(s,1H),7.89(s,1H),7.43(d,J=5.0,1H),6.87(s,1H),5.94(s,1H),4.57(s,3H),4.47(s,1H),4.11-4.15(m,4H),3.89(s,3H),3.87(s,1H),3.61(d,J=4.0,2H),2.90(s,2H),2.61(d,J=4.0,2H),2.57(t,J=6.0,2H),2.49(s,3H),1.89-1.91(m,2H),1.79-.80(m,2H)
实施例134a 10-溴-1H,2H,3H,4H,6H,7H,8H,9H-吡嗪并[1,2-a]吲哚-1-酮134a
在250-mL 3-颈圆底烧瓶中放入1H,2H,3H,4H,6H,7H,8H,9H-吡嗪并[1,2-a]吲哚-1-酮101e(9.5g,49.94mmol,1.00当量)于N,N-二甲基甲酰胺(100mL)中的溶液,然后在0℃,分数份加入N-溴琥珀酰亚胺(9.8g,55.06mmol,1.10当量)。将所得溶液在室温搅拌2小时并用500mL水稀释。过滤出析出物并在真空烘箱中干燥得到9.5g(71%)of 119a,其为浅棕色固体。
实施例134b 10-氟-1H,2H,3H,4H,6H,7H,8H,9H-吡嗪并[1,2-a]吲哚-1-酮134b
在2-L 4-颈圆底烧瓶(用氮气吹洗并保持在氮气惰性气氛中)中放入134a(40g,148.62mmol,1.00当量)于四氢呋喃(200mL)中的溶液,然后在-78℃在搅拌的同时滴加n-BuLi(2.4M)(218mL,3.50当量)。将所得溶液在-40℃搅拌3小时。在-78℃和在搅拌的同时,向其中滴加N-氟苯磺酰亚胺(98.7g,313.33mmol,2.10当量)的四氢呋喃(200mL)溶液。将所得溶液在室温搅拌3小时,通过添加200mL水来淬灭并用3x500mL乙酸乙酯萃取。将合并的有机层用无水硫酸钠来干燥并真空浓缩。将粗制产物(30g)通过制备性-HPLC来纯化(所遵循的条件为:流动相,A:0.05%三氟乙酸/水;B:CH3CN;梯度:10%B-25%B)得到5.05g(16%)134b,其为白色固体。MS:[M+H]+209.1H NMR(300MHz,CDCl3)δ6.16(br,1H),3.90-3.86(m,2H),3.65-3.62(m,2H),2.53-2.47(m,4H),1.88-1.80(m,2H),1.77-1.72(m,2H).
实施例134c 4-氯-2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛134c
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(60mL),134b(500mg,2.4mmol):
2-溴-4-氯吡啶-3-甲醛103a(1.60g,7.2mmol)和乙酸钾(471mg,4.8mmol)。使氮气鼓泡通过所得混合物30分钟后,加入Xantphos(140mg,0.24mmol)和三(二亚苄基丙酮)二钯(0)(220mg,0.24mmol),并将反应混合物在80℃加热10小时。之后,将反应混合物冷却至室温,在乙酸乙酯(40mL)和水(40mL)之间分配并过滤。分离出水层并用乙酸乙酯(50mL×3)萃取。将合并的有机层用盐水(30mL)洗涤并用硫酸钠干燥。过滤除去干燥剂并减压浓缩滤液。将残余物在快速柱上纯化(用3:1PE/EA洗脱)得到134c(678mg,81%),其为黄色固体.MS:[M+H]+348.1H NMR(500MHz,DMSO-d6)δ9.87(s,1H),8.60(d,J=5.5,1H),7.56(d,J=5.5,1H),4.23-4.25(m,2H),4.13-4.15(m,2H),2.59(t,J=6.0,2H),2.41(t,J=6.0,2H),1.75-1.80(m,2H),1.66-1.70(m,2H)
实施例134d 2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)-4-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-甲醛134d
将134c(300mg,0.86mmol)、1-甲基-3-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮101l(403mg,0.86mmol)、CH3COONa(142mg,1.72mmol)、K3PO4(460mg,1.72mmol)、PdCl2(dppf)(71mg,0.086mmol)于CH3CN(25mL)和H2O(1mL)中的混合物在100℃加热3小时。反应后,将其蒸发并将残余物通过硅胶柱(用二氯甲烷/甲醇(30:1)洗脱)来纯化得到134d(312mg,收率55%),其为棕色固体。MS:(M+H)+653。
实施例134 10-氟-2-(3-(羟基甲基)-4-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮134
向134d(200mg,0.30mmol)于MeOH(20mL)中的溶液中加入NaBH4(40mg,0.9mmol)。将混合物在20℃搅拌2小时。反应后,将其蒸发并将残余物通过反相制备性-HPLC来纯化得到134(108mg,收率54%),其为黄色固体。MS:(M+H)+655。1H NMR(500MHz,DMSO-d6)δ8.61(d,J=2.0,1H),8.49(d,J=5.0,1H),8.43(s,1H),7.85(d,J=2.5,1H),7.45(d,J=1.5,1H),7.37-7.39(m,1H),7.35(d,J=5.0,1H),7.24(d,J=9.0,1H),4.99(s,1H),4.56(t,J=6.5,2H),4.40-4.47(m,4H),4.18-4.22(m,2H),4.05-4.09(m,1H),3.84-3.96(m,1H),3.60(s,3H),3.41-3.46(m,1H),3.07(s,4H),2.54-2.61(m,2H),2.39-2.42(m,6H),1.78(s,2H),1.69(s,2H)
实施例135a 1-甲基-3-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮135a
在配备有磁力搅拌子和冷凝器的100-mL单颈圆底烧瓶中装入化合物113h(1.0g,3mmol)、Pin2B2(3.8g,15mmol)、Pd(dppf)Cl2(137mg,0.15mmol)、X-phos(143mg,0.3mmol)、KOAc(88mg,9mmol)和1,4-二噁烷(50mL)。在经历三轮真空/氩气吹洗后,将反应混合物在60℃加热15小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物用石油醚洗涤得到135a,其为黄色固体(0.87g,75%)。MS:[M+H]+386
实施例135b 2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)-4-(1-甲基-5-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-甲醛135b
将135a(385mg,1mmol)、4-氯-2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛134c(347mg,1mmol)、K3PO4(424mg,2mmol)、NaOAc(164g,2mmol)和1,1’-二(二苯基膦基)二茂铁二氯化钯(II)(41mg,0.05mmol)于CH3CN(50ml)中的悬浮液在100℃和氢气囊条件下加热4小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将反应混合物冷却至室温并用DCM(50ml)和水(80mL)稀释。分离出水层并用DCM(3×50mL)萃取。将合并的有机层用Na2SO4干燥,过滤并浓缩。将黑色残余物通过硅胶柱色谱法来纯化(用DCM/MeOH(自80/1至30/1)洗脱)得到135b(285g,50%),其为黄色固体。MS:[M+H]+571
实施例135 10-氟-2-(3-(羟基甲基)-4-(1-甲基-5-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮135
在室温,向135b(280g,0.49mmol)于MeOH(50mL)中的溶液中加入NaBH4(56g,1.47mmol)。将反应混合物搅拌3小时后,LCMS表明反应结束。然后将混合物倒入H2O(50mL)中并用DCM(50mL×3)萃取。将合并的有机层用盐水(50mL)洗涤,用Na2SO4干燥,过滤并浓缩。将残余物通过反相制备性-HPLC来纯化得到135(187mg,67%),其为白色固体。MS:[M+H]+572.1H NMR(500MHz,CDCl3)δ8.47(d,J=5.5,1H),7.95(d,J=2.0,1H),7.70(d,J=2.0,1H),7.42(s,1H),7.35(d,J=5.5,1H),5.70(s,1H),4.96(t,J=7.0,1H),4.62(s,1H),4.45(s,1H),4.33(s,1H),4.07-4.12(m,4H),3.84(s,1H),3.70(s,3H),3.60(s,2H),2.88(t,J=5.5,2H),2.61(s,2H),2.57(s,2H),2.48(s,3H),1.86-1.90(m,2H),1.77(s,2H)
实施例136a(S)-2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)-4-(1-甲基-5-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-甲醛136a
在配备有磁力搅拌子和回流冷凝器的50mL单颈圆底烧瓶中加入(S)-1-甲基-3-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮130f(225mg,1.5当量,0.47mmol)、4-氯-2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛134c(150mg,1当量,0.43mmol):
PdCl2(dppf)(35mg,0.1当量,0.043mmol)、K3PO4(273mg,3当量,1.29mmol)和THF(20mL)。在经历三轮真空/氩气吹洗后,将混合物回流加热5小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物通过柱色谱法(使用DCM/EtOH(40:1))来纯化得到136a,其为黄色固体(100mg,34%)。MS:[M+H]+667.3。
实施例136(S)-10-氟-2-(3-(羟基甲基)-4-(1-甲基-5-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮136
在配备有磁力搅拌子的25mL单颈圆底烧瓶中装入136a(100mg,1.0当量,0.15mmol)、NaBH4(17mg,3.0当量,0.45mmol)和MeOH(10mL)。将混合物在室温搅拌1小时。将残余物通过反相制备性-HPLC来纯化得到136(64mg,64%)。LCMS:[M+H]+669.3。1H NMR(500MHz,CDCl3)δ8.64(d,J=2.0,1H),8.48(d,J=5.0,1H),7.96(d,J=2.5,1H),7.83-7.82(m,2H),7.36(d,J=5.0,1H),7.30(dd,J=2.5,9.0,1H),6.81(d,J=8.5,1H),4.99-4.96(m,1H),4.71-4.61(m,5H),4.45-3.83(m,5H),3.71(s,3H),3.54-3.45(m,2H),3.08-3.06(m,2H),2.56-2.47(m,7H),2.21-2.17(m,1H),1.89-1.76(m,4H),0.98(d,J=6.5,3H)
实施例137a(R)-乙酸(4-(1-甲基-5-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯137a
将(R)-5-溴-1-甲基-3-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)吡啶-2(1H)-酮151f(130f对映异构体的混合物)(283mg,0.65mmol):
3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113i(250mg,0.65mmol)、PdCl2(dppf)(53mg,0.065mmol)、NaOAc(107mg,1.3mmol)、K3PO4(347mg,1.3mmol)于乙腈(30mL)中的混合物在100℃加热3小时。真空蒸发溶剂并将残余物通过快速柱色谱法(用30:1DCM/MeOH洗脱)来纯化得到137a(216mg,48%),其为棕色固体。LCMS:[M+H]+693.4
实施例137(R)-2-(3-(羟基甲基)-4-(1-甲基-5-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮137
向137a(200mg,0.29mmol)于丙烷-2-醇(8mL)、四氢呋喃(8mL)和水(2.0mL)中的溶液中加入LiOH(690mg,29mmol)。将混合物在30℃搅拌2小时。然后将其蒸发并将残余物通过反相制备性-HPLC来纯化得到137(143mg,76%),其为白色固体。LCMS:(M+H)+651.4.1H NMR(500MHz,DMSO-d6)δ8.63(d,J=2.0,1H),8.49(d,J=5.0,1H),8.45(s,1H),7.84(d,J=2.5,1H),7.47(d,J=2.0,1H),7.37-7.39(m,1H),7.35(d,J=5.5,1H),7.25(d,J=9.5,1H),6.58(s,1H),4.95(t,J=4.0,1H),4.54-4.58(m,2H),4.40-4.49(m,4H),4.11-4.26(m,3H),3.86-3.88(m,1H),3.68(s,1H),3.61(s,3H),3.37-3.42(m,1H),3.08-3.11(m,1H),2.95(t,J=9.0,1H),2.62-2.67(m,1H),2.54-2.59(m,2H),2.48(t,J=6.0,2H),2.30-2.36(m,2H),2.19(t,J=8.0,1H),1.81(s,2H),1.68-1.72(m,2H),0.93(d,J=6.0,3H)
实施例138a 3-(1-甲基-5-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-5-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-甲醛138a
在100-mL单颈圆底烧瓶中装入3-溴-5-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-甲醛101f(298mg,0.7mmol)、1-甲基-3-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮135a(325mg,0.84mmol)、PdCl2(dppf)(30mg,0.035mmol)、K3PO4(300mg,1.4mmol)和NaOAc·3H2O(200mg,1.4mmol)/CH3CN(70mL)。将体系排空并用氩气回填。将反应混合物在100℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物通过快速柱色谱法(用25:1DCM/MeOH洗脱)来纯化得到138a(220mg,55%),其为浅黄色固体.MS:[M+H]+553.3。
实施例138 2-(4-(羟基甲基)-5-(1-甲基-5-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮138
将138a(200mg,0.36mmol)和NaBH4(50mg,1.2mmol)于MeOH(60mL)中的混合物在室温搅拌2小时。将混合物用水淬灭并用EtOAc(10mLX3)萃取。将合并的EtOAc萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到138(162mg,85%)。LCMS:[M+H]+:555.3.1HNMR(500MHz,CDCl3)δ8.64(s,1H),8.49(s,1H),7.97(d,J=2.5,1H),7.42(s,1H),7.33(d,J=2,1H),6.88(s,1H),5.68(s,1H),4.65-4.63(m,1H),4.57-4.55(m,1H),4.37(t,J=11,1H),4.20-4.16(m,3H),4.07-3.98(m,3H),3.70(s,3H),3.59(s,2H),2.87(t,J=5.5,2H),2.61-2.56(m,4H),2.48(s,3H),1.92-1.90(m,2H),1.80-1.79(m,2H)
实施例139a 4-氯-2-(1-氧代-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-3-甲醛139a
在配备有磁力搅拌子和回流冷凝器的250-mL单颈圆底烧瓶中装入1,4-二噁烷(50mL)、2-溴-4-氯吡啶-3-甲醛103a(1.4g,6.4mmol)、3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-1(2H)-酮112d(0.6g,3.2mmol)、Pd2(dba)3(293mg,0.32mmol)、XantPhos(370mg,0.64mmol)和碳酸钾(627mg,6.4mmol)。在经历三轮真空/氩气吹洗后,将混合物在80℃加热整夜。之后,将反应混合物冷却至室温。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用DCM/CH3OH(20:1,V/V)洗脱)来纯化得到139a(528mg,50%),其为黄色固体。MS:[M+H]+330.1H NMR(500MHz,CDCl3)δ10.09(s,1H),8.37(d,J=5.5,1H),7.16(d,J=5.5,1H),6.25(s,1H),4.29-4.32(m,2H),3.83-3.86(m,2H),2.96-2.99(m,2H),2.75-2.78(m,2H),2.00-2.07(m,2H),1.82-1.85(m,2H)
实施例139b 4-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-3-甲醛139b
在圆底烧瓶中装入139a(100mg,0.30mmol)、1-甲基-3-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮101l(140mg,0.30mmol)、PdCl2(dppf)(25mg,0.03mmol)、K3PO4.3H2O(160mg,0.60mmol)、NaOAc(59mg,0.60mmol)、乙腈(10mL)和H2O(5mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热3小时。然后将其过滤并真空蒸发滤液。将残余物在快速柱色谱上纯化(用1:3石油醚/乙酸乙酯洗脱)得到139b,其为黄色固体(95mg,50%)。LCMS:[M+H]+635
实施例139 2-(3-(羟基甲基)-4-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-1(2H)-酮139
将139b(95mg,0.15mmol),NaBH4(17mg,0.45)和CH3OH(10mL)的混合物在25℃搅拌1小时。将混合物用CH2Cl2(10mLX2)萃取。将合并的CH2Cl2萃取物减压浓缩。将残余物用反相制备性-HPLC来纯化得到139(60mg,63%)。LCMS:[M+H]+637。1H NMR(500MHz,DMSO-d6)δ8.63(d,J=2.0,1H),8.47(d,J=5.5,1H),8.42(s,1H),7.85(d,J=2.5,1H),7.49(d,J=2.0,1H),7.37-7.39(m,1H),7.30(d,J=5.0,1H),7.24(d,J=9.0,1H),6.05(s,1H),4.47-4.57(m,2H),4.41-4.47(m,2H),4.39-4.41(m,1H),4.33-4.35(m,1H),4.11-4.16(m,1H),3.93-3.96(m,1H),3.76-3.82(m,2H),3.59(s,3H),3.41-3.45(m,2H),3.06-3.08(m,4H),2.98-3.01(m,1H),2.92-2.95(m,1H),2.71-2.72(m,2H),2.36-2.39(m,4H),1.91-1.93(m,2H),1.72-1.78(m,2H)
实施例140a(S)-2-(7,7-二氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)-4-(1-甲基-5-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-甲醛140a
按照如实施例130g中所述的操作,(S)-1-甲基-3-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮130f与4-氯-2-(7,7-二氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛(170mg):
反应得到140a,其为黄色固体(200mg,60%)。LCMS:[M+H]+684.3。根据图25中的反应方案,从7,7-二氟-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮制备4-氯-2-(7,7-二氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛。
实施例140(S)-7,7-二氟-2-(3-(羟基甲基)-4-(1-甲基-5-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮140
按照如实施例130中所述的操作,用硼氢化钠还原140a(200mg)得到140,其为黄色固体(104mg,51%)。LCMS:[M+H]+686.3。1H NMR(500MHz,DMSO)δ8.62(d,J=2.0,1H),8.46-8.49(m,2H),7.83(d,J=3.0,1H),7.45(d,J=2.5,1H),7.35-7.38(m,2H),7.25(d,J=9.5,1H),6.64(s,1H),4.95-4.97(m,1H),4.54-4.57(m,2H),4.38-4.48(m,4H),4.15-4.27(m,3H),3.87-3.90(m,1H),3.67(s,1H),3.59(s,3H),3.26-3.39(m,3H),3.08-3.10(m,1H),2.92-2.96(m,1H),2.63-2.67(m,2H),2.52-2.55(m,1H),2.30-2.36(m,2H),2.18-2.24(m,3H),0.93(d,J=6.0,3H)
实施例141a 4-氯-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-甲醛141a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入2-溴-4-氯吡啶-3-甲醛103a(3.0g,13.6mmol)、4,4-二甲基-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-9-酮107e(1.84g,9.0mmol)、三(二亚苄基丙酮)二钯(0)(826mg,0.9mmol)、XantPhos(1.04mg,1.8mmol)、Cs2CO3(5.8g,18.0mmol)和1,4-二噁烷(40mL)。在经历三轮真空/氩气吹洗后,将混合物在90℃加热5小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物用乙酸乙酯重结晶得到141a,其为黄色固体(730mg,31.7%)。MS:[M+H]+344.0.
实施例141b 2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-[1-甲基-5-({5-甲基-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]吡啶-3-甲醛141b
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入141a(130mg,0.38mmol)、1-甲基-3-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮135a(146mg,0.38mmol)、Pd(dppf)Cl2(31mg,0.038mmol)、K3CO3(105mg,0.76mmol)和DMF(20mL)。在经历三轮真空/氩气吹洗后,将混合物在110℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(30:1)洗脱)得到141b,其为棕色固体(160mg,74.6%)。MS:[M+H]+567.3。
实施例141 2-[3'-羟基甲基-1-甲基-5-(5-甲基-4,5,6,7-四氢-吡唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基]-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮141
在室温,向141b(150mg,0.26mmol)于甲醇(10mL)中的溶液中加入硼氢化钠(29mg,0.78mmol),将所得混合物搅拌30分钟。将其用水(1.0mL)淬灭并浓缩。将残余物通过反相制备性-HPLC来纯化得到141(35mg,23.2%)。LCMS:[M+H]+569.3。1H NMR(500MHz,CDCl3)δ8.46(d,J=5.0,1H),7.94(d,J=2.5,1H),7.72(d,J=2.0,1H),7.41(s,1H),7.33(d,J=5.5,1H),6.83(s,1H),5.68(s,1H),5.03-5.00(m,1H),4.64-4.61(m,1H),4.51-4.48(m,1H),4.32-4.27(m,1H),4.21-4.09(m,4H),3.91-3.82(m,1H),3.69(s,3H),3.62-3.58(m,2H),2.87(t,J=2.5,2H),2.57(d,J=4.0,2H),2.54(s,2H),2.51(s,3H),1.27(s,6H)
实施例142a 5-溴-1-甲基-3-(嘧啶-4-基氨基)吡啶-2(1H)-酮142a
在配备有的磁力搅拌子和氮气进气口的100-mL单颈圆底烧瓶中装入3,5-二溴-1-甲基吡啶-2(1H)-酮(2.00g,21.0mmol)、2-氨基嘧啶(5.61g,21.0mmol)、碳酸铯(13.7g,42.1mmol)、DMF(5mL)和1,4-二噁烷(70mL)。在使氮气鼓泡通过所得悬浮液30分钟后,加入Xantphos(1.10g,1.89mmol)和三(二亚苄基丙酮)二钯(0)(963mg,1.05mmol)。使回流冷凝器与所述烧瓶相连并将反应混合物在100℃加热4小时。之后,将混合物冷却至室温并用90:10二氯甲烷/甲醇(150mL)和水(100mL)稀释,分离各层。将水层用90:10二氯甲烷/甲醇(50mL)萃取,将合并的有机层用盐水洗涤并用硫酸钠干燥。通过过滤除去干燥剂。减压浓缩滤液,并将所得残余物通过快速柱色谱法(硅胶,90:10二氯甲烷/甲醇)来纯化得到142a,58%收率(3.42g),其为无定形浅绿色固体:mp 217–219℃;1H NMR(500MHz,CDCl3)δ9.29(s,1H),8.77(s,1H),8.72(d,J=2.5Hz,1H),8.36(d,J=6.0Hz,1H),7.69(d,J=2.5Hz,1H),7.37(dd,J=5.5,1.0Hz,1H),3.53(s,3H);LCMS(ESI+)m/z 281.0(M+H).
实施例142b乙酸(4-(1-甲基-6-氧代-5-(嘧啶-4-基氨基)-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯142b
在配备有磁力搅拌子的密封管中装入142a(154.5mg,0.55mmol)、乙酸(2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-3-基)甲酯113i(252.5mg,0.55mmol)、Pd(dppf)Cl2(25.9mg,0.03135mmol)、NaOAc(108mg,1.1mmol)、K3PO4·3H2O(293mg,1.1mmol)、乙腈(6mL)和水(0.5mL)。在经历三轮真空/氩气吹洗后,将混合物在110℃加热2小时。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(15:1,V/V)洗脱)来纯化得到142b(117mg,30%),其为棕色固体。LCMS:[M+H]+540.2
实施例142 2-[3'-羟基甲基-1-甲基-6-氧代-5-(嘧啶-4-基氨基)-1,6-二氢-[3,4']联吡啶-2'-基]-3,4,6,7,8,9-六氢-2H-吡嗪并[1,2-a]吲哚-1-酮142
将142b(121.6mg,0.225mmol)和LiOH(100mg,4.2mmol)于iPrOH/THF(1:1,4mL)和H2O(1mL)中的混合物在35℃搅拌0.5小时。真空蒸发混合物并将残余物用EtOAc(20mLX3)萃取。将合并的EtOAc萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化。得到142(54mg,48.2%),其为浅黄色固体。LCMS:[M+H]+498.1。1H NMR(500MHz,DMSO-d6)δ9.23(s,1H),8.76(d,J=2.5,1H),8.65(s,1H),8.50(d,J=5.0,1H),8.31(d,J=6.0,1H),7.69(d,J=2.5,1H),7.37(d,J=5.0,1H),7.31-7.33(m,1H),6.58(s,1H),4.97(t,J=4.5,1H),4.39-4.43(m,2H),4.10-4.24(m,3H),3.87(d,J=12.0,1H),3.61(s,3H),2.57-2.64(m,2H),2.47(d,J=6,2H),1.79(d,J=4.0,2H),1.69(d,J=6.0,2H)
实施例143a 1-甲基-3-(嘧啶-4-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮143a
在配备有磁力搅拌子和冷凝器的250-mL单颈圆底烧瓶中装入5-溴-1-甲基-3-(嘧啶-4-基氨基)吡啶-2(1H)-酮142a(4.0g,14mmol)、X-phos(400mg,0.7mmol)、Pd2(dba)3(635mg,0.7mmol)、KOAc(7.3mg,28mmol)、4,4,4',4',5,5,5',5'-八甲基-2,2'-二(1,3,2-二氧杂硼杂戊环)(10.6g,42mmol)和1,4-二噁烷(100mL)。在经历三轮真空/氩气吹洗后,将反应混合物在60℃加热8小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物通过快速柱色谱法(用5:1石油醚/乙酸乙酯洗脱)来纯化得到143a,其为浅黄色固体(3.8mg,82%)。MS:[M+H]+329.5.
实施例143b 4-(1-甲基-5-(嘧啶-4-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-{4,4-二甲基-9-氧代-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-10-基}吡啶-3-甲醛143b
在配备有磁力搅拌子和冷凝器的250-mL单颈圆底烧瓶中装入143a(150mg,0.46mmol)、4-氯-2-{4,4-二甲基-9-氧代-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-10-基}吡啶-3-甲醛109a(164mg,0.46mmol):
Pd(dppf)Cl2(16mg,0.02mmol)、K3PO4.3H2O(223mg,0.92mmol)/CH3CN(5mL)+H2O(1mL)。在经历三轮真空/氩气吹洗后,将反应混合物在100℃加热3小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物通过快速柱色谱法(用20:1的DCM/MeOH洗脱)来纯化得到143b,其为黄色固体(110mg,48%)。MS:[M+H]+527。
实施例143 6-[3'-羟基甲基-1-甲基-6-氧代-5-(嘧啶-4-基氨基)-1,6-二氢-[3,4']联吡啶-2'-基]-2,2-二甲基-2,3,5,6-四氢-1H,4H-8-硫杂-6-氮杂-环戊二烯并[a]茚-7-酮143
将143b(110mg,0.2mmol)、NaBH4(30mg,0.8mmol)和MeOH(5mL)的混合物在25℃搅拌30分钟。真空蒸发混合物并将残余物用EtOAc(10mLX2)萃取。将合并的EtOAc萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到143(48mg,44%)。LCMS:[M+H]+529.1HNMR(500MHz,DMSO)δ9.23(s,1H),8.76(d,J=2.5,1H),8.65(s,1H),8.51-8.49(m,1H),8.31(m,1H),7.67(d,J=3.0,1H),7.38-7.37(m,1H),7.33-7.31(m,1H),5.02-5.01(m,1H),4.43(d,J=2.5,2H),4.18-4.15(m,1H),3.83-3.81(m,1H),3.61-3.59(m,3H),3.03-2.99(m,1H),2.91-2.89(m,1H),2.76(s,2H),2.60-2.53(m,2H),1.23-1.22(m,6H)
实施例144a 4-(1-甲基-5-(嘧啶-4-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-甲醛144a
在配备有磁力搅拌子和冷凝器的250-mL单颈圆底烧瓶中装入1-甲基-3-(嘧啶-4-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮143a(150mg,0.46mmol)、4-氯-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-甲醛108a(157mg,0.46mmol):
Pd(dppf)Cl2(16mg,0.02mmol)、K3PO4.3H2O(223mg,0.92mmol)/CH3CN(5mL)+H2O(1mL)。在经历三轮真空/氩气吹洗后,将反应混合物在100℃加热3小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物通过快速柱色谱法(用20:1的DCM/MeOH洗脱)来纯化得到144a,其为黄色固体(98mg,48%)。MS:[M+H]+510。
实施例144 2-[3'-羟基甲基-1-甲基-6-氧代-5-(嘧啶-4-基氨基)-1,6-二氢-[3,4']联吡啶-2'-基]-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并-[4,5]吡咯并[1,2-a]吡嗪-1-酮144
将144a(98mg,0.19mmol)、NaBH4(30mg,0.8mmol)和MeOH(5mL)的混合物在25℃搅拌30分钟。真空蒸发混合物并将残余物用EtOAc(10mLX2)萃取。将合并的EtOAc萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到144(25mg,42%)。LCMS:[M+H]+512.1HNMR(500MHz,DMSO)δ9.18(s,1H),8.76-8.74(m,1H),8.64(s,1H),8.50-8.47(m,1H),8.31-8.30(m,1H),7.68-7.69(m,1H),7.37-7.36(m,1H),7.33-7.31(m,1H),6.56(s,1H),5.07-5.04(m,1H),4.44-4.41(m,2H),4.23-4.18(m,3H),3.86-3.84(m,1H),3.61(s,3H),2.61-2.56(m,2H),2.42(s,2H),1.21-1.20(m,6H)
实施例145a(S)-4-(1-甲基-5-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-{4,4-二甲基-9-氧代-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-10-基}吡啶-3-甲醛145a
在配备有磁力搅拌子和回流冷凝器的50mL单颈圆底烧瓶中装入(S)-1-甲基-3-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮130f(160mg,1当量,0.33mmol)、4-氯-2-{4,4-二甲基-9-氧代-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-10-基}吡啶-3-甲醛109a(120mg,1当量,0.33mmol):
PdCl2(dppf)(27mg,0.1当量,0.033mmol)、K3PO4(140mg,2当量,0.66mmol)、NaOAc(54mg,2当量,0.66mmol)和CH3CN(20mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物通过柱色谱法(用DCM/EtOH(40/1)洗脱)来纯化得到145a,其为黄色固体(97mg,43%)。MS:[M+H]+680.3.
实施例145 6-{3'-羟基甲基-1-甲基-5-[5-((S)-2-甲基-4-氧杂环丁烷-3-基-哌嗪-1-基)-吡啶-2-基氨基]-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基}-2,2-二甲基-2,3,5,6-四氢-1H,4H-8-硫杂-6-氮杂-环戊二烯并[a]茚-7-酮145
在25mL配备有磁力搅拌子的单颈圆底烧瓶中装入145a(97mg,1.0当量,0.14mmol)、NaBH4(16mg,3.0当量,0.42mmol)和MeOH(10mL)。将混合物在室温搅拌1小时。将残余物通过反相制备性-HPLC来纯化得到145(61mg,63%)。LCMS:[M+H]+682.3.1H NMR(500MHz,CDCl3)δ8.65(d,J=2.5,1H),8.50(d,J=5.0,1H),7.97(d,J=2.5,1H),7.84(s,1H),7.80(d,J=2.5,1H),7.37(d,J=5.0,1H),7.30(dd,J=3.0,9.0,1H),6.81(d,J=9.0,1H),4.82-4.79(m,1H),4.71-4.61(m,5H),4.45-4.31(m,2H),3.85-3.80(m,1H),3.71(s,3H),3.54-3.46(m,2H),3.07(d,J=5.0,2H),2.98-2.93(m,2H),2.79(s,2H),2.60-2.46(m,5H),2.21-2.18(m,1H),1.28(s,6H),0.98(d,J=6.0,3H)
实施例146a 4-氯-2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛146a
向2-溴-4-氯吡啶-3-甲醛103a(1600mg,7.27mmol)、10-氟-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮(500mg,2.40mmol):
于二噁烷(50mL)中的溶液中加入KOAc(471mg,4.82mmol)、Pd2(dba)3(220mg,0.24mmol)和4,5-二(二苯基膦基)-9,9-二甲基-呫吨(140mg,0.24mmol)。在使氩气鼓泡通过所得溶液30分钟后,将所述混合物在80℃搅拌10小时。使其冷却至室温并加入H2O(100mL)。分离出水层并用乙酸乙酯(2×200mL)萃取。将合并的有机层用盐水(100mL)洗涤并用硫酸钠干燥。过滤除去干燥剂并减压浓缩滤液。将残余物在快速柱上纯化(用PE/EA(3:1)洗脱)得到146a,其为黄色固体(420mg,49%)。LCMS:[M+H]+348
实施例146b 2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)-4-(1-甲基-6-氧代-5-(嘧啶-4-基氨基)-1,6-二氢吡啶-3-基)吡啶-3-甲醛146b
在圆底烧瓶中装入146a(200mg,0.58mmol)、1-甲基-3-(嘧啶-4-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮143a(227mg,0.69mmol)、PdCl2(dppf)(47mg,0.06mmol)、K3PO4(244mg,1.15mmol)、NaOAc(94mg,1.15mmol)、乙腈(30mL)和H2O(3mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热3小时。然后将其过滤并真空蒸发滤液。将残余物在快速柱色谱法上纯化(用1:20甲醇/二氯甲烷洗脱)得到146b,其为红色固体(79mg,27%)。LCMS:[M+H]+514
实施例146 10-氟-2-(3-(羟基甲基)-4-(1-甲基-6-氧代-5-(嘧啶-4-基氨基)-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮146
将146b(79mg,0.15mmol)、NaBH4(22mg,0.60)和CH3OH(10mL)在25℃搅拌1小时。将混合物用CH2Cl2(10mLX2)萃取。将合并的CH2Cl2萃取物减压浓缩。将残余物用反相制备性-HPLC来纯化得到146(39mg,49%)。LCMS:[M+H]+516。1H NMR(500MHz,CDCl3)δ8.83(d,J=2.0,1H),8.78(s,1H),8.52(d,J=5.0,1H),8.35(d,J=5.5,1H),8.12(s,1H),8.03(d,J=2.0,1H),7.36(d,J=5.0,1H),6.76-6.77(m,1H),5.07(s,1H),4.65(d,J=9.5,1H),4.48(d,J=9.5,1H),4.29(d,J=1.5,1H),4.02-4.13(m,2H),3.79(d,J=6.5,1H),3.73(s,3H),2.52-2.58(m,4H),1.85-1.90(m,2H),1.77(d,J=5.0,2H)
实施例147a 4-氯-2-(1-氧代-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-3-甲醛147a
在配备有磁力搅拌子和回流冷凝器的250-mL单颈圆底烧瓶中装入1,4-二噁烷(50mL)、2-溴-4-氯吡啶-3-甲醛103a(1.4g,6.4mmol)、3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-1(2H)-酮112d(0.6g,3.2mmol)、Pd2(dba)3(293mg,0.32mmol)、XantPhos(370mg,0.64mmol)和乙酸钾(627mg,6.4mmol)。在经历三轮真空/氩气吹洗后,将混合物在80℃加热整夜。之后,将反应混合物冷却至室温。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法来纯化(用CH2Cl2/CH3OH(20:1,V/V)洗脱)得到147a(528mg,50%),其为黄色固体。MS:[M+H]+330.1H NMR(500MHz,CDCl3)δ10.09(s,1H),8.37(d,J=5.5,1H),7.16(d,J=5.5,1H),6.25(s,1H),4.29-4.32(m,2H),3.83-3.86(m,2H),2.96-2.99(m,2H),2.77-2.78(m,2H),2.00-2.07(m,2H),1.83-1.85(m,2H)
实施例147b 2-(3-甲酰基-4-(1-甲基-5-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-1(2H)-酮147b
在圆底烧瓶中装入4-氯-2-(1-氧代-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-3-甲醛147a(100mg,0.30mmol)、1-甲基-3-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮135a(116mg,0.30mmol)、PdCl2(dppf)(25mg,0.03mmol)、K3PO4.3H2O(160mg,0.60mmol)、NaOAc(59mg,0.60mmol)、乙腈(10mL)和H2O(5mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热3小时。然后将其过滤并真空蒸发滤液。将残余物在快速柱色谱上纯化(用1:3石油醚/乙酸乙酯洗脱)得到147b,其为黄色固体(100mg,60%)。LCMS:[M+H]+553
实施例147 2-(3-(羟基甲基)-4-(1-甲基-5-(5-甲基-4,5,6,7-四氢-吡唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-1(2H)-酮147
将147b(100mg,0.18mmol)、NaBH4(21mg,0.54)和CH3OH(10mL)的混合物在25℃搅拌1小时。将混合物用CH2Cl2(10mLX2)萃取。将合并的CH2Cl2萃取物减压浓缩。将残余物用反相制备性-HPLC来纯化得到147(60mg,60%)。LCMS:[M+H]+555。1H NMR(500MHz,DMSO)δ8.45(d,J=5.0,1H),8.19(s,1H),8.06(d,J=5.0,1H),7.41(d,J=2.0,1H),7.29(d,J=5.0,1H),6.04(s,1H),5.88(s,1H),4.92(s,1H),4.33-4.42(m,2H),4.11-4.16(m,1H),3.91-3.96(m,3H),3.77-3.82(m,2H),3.57(s,3H),3.45-3.48(m,2H),2.91-3.01(m,2H),2.71-2.79(m,4H),2.35(s,3H),1.90-1.92(m,2H),1.71-1.79(m,2H)
实施例148a 3-(2-溴-4-氯吡啶-3-基)氧杂环丁烷-3-醇148a
在-70℃,向2-溴-4-氯吡啶(14g,70mmol)于无水THF(200mL)中的溶液中滴加LDA(42.0mL,84.0mmol,2.0M)。在该温度搅拌0.5小时后,缓慢加入氧杂环丁烷-3-酮(6.6g,90mmol)于无水THF(40mL)中的溶液并将反应混合物在0℃再搅拌1小时。加入饱和NH4CI水溶液(50mL)和EA(200mL)。将混合物在水和乙酸乙酯之间分配。将水层用乙酸乙酯萃取。将合并的有机层用水和盐水洗涤。用无水硫酸镁干燥后,蒸发溶剂并将粗制物通过SGC(用洗脱DCM)来纯化得到148a,其为黄色固体(8.8g,45%)。MS:[M+H]+266.0。
实施例148b 2-(4-氯-3-(3-羟基氧杂环丁烷-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮148b
在配备有磁力搅拌子的100mL单颈圆底烧瓶中装入3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮101e(190mg,1.0mmol)、148a(795mg,3.0mmol)、CuI(95mg,0.5mmol)、DMEDA(88mg,1.0mmol)、KOAc(294mg,3.0mmol)和1,4-二噁烷(50ml)。将体系排空然后用氮气回填。将回流冷凝器与所述烧瓶相连并将反应混合物在85℃加热15小时。然后,将混合物冷却至室温并过滤。减压浓缩滤液并将所得残余物通过快速柱色谱法(用2:1石油醚/乙酸乙酯洗脱)来纯化得到148b,其为黄色固体(156mg,42%)。MS:[M+H]+374.2.
实施例148(S)-2-(3-(3-羟基氧杂环丁烷-3-基)-4-(1-甲基-5-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮148
在100-mL单颈圆底烧瓶中装入148b(100mg,0.3mmol)、(S)-1-甲基-3-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮130f(173mg,0.36mmol)、Pd(dppf)Cl2(15mg,0.015mmol)、K3PO4(130mg,0.6mmol)和NaOAc·3H2O(90mg,0.6mmol)于CH3CN(30mL)中。将体系排空并用氮气回填。将反应混合物在100℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物通过快速柱色谱法(用25:1DCM/MeOH洗脱)来纯化得到148(30mg,20%),其为浅黄色固体。MS:[M+H]+693.3.1H NMR(500MHz,CDCl3)δ8.69(d,J=2,1H),8.50(d,J=5,1H),8.01(d,J=2.5,1H),7.85(s,1H),7.67(s,1H),7.38-7.32(m,2H),6.89(s,1H),6.83(d,J=8.5,1H),6.67(s,1H),4.93(d,J=6,1H),4.71-4.63(m,6H),4.46(d,J=7.5,1H),4.24-4.18(m,2H),4.10-4.05(m,1H),3.90(d,J=12.5,1H),3.70(s,3H),3.55-3.46(m,2H),3.10(t,J=4.5,2H),2.63-2.48(m,7H),2.22(t,J=7.5,1H),1.92-1.88(m,2H),1.82-1.77(m,2H),1.02-1.00(m,3H)
实施例149a(S)-4-(1-甲基-5-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-3-甲醛149a
在配备有回流冷凝器的100-mL圆底烧瓶中装入4-氯-2-(1-氧代-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-3-甲醛139a(100mg,0.30mmol)、(S)-1-甲基-3-(5-(2-甲基-4-(氧杂环丁烷-3-基)-哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮191j(146mg,0.30mmol)、PdCl2(dppf)(25mg,0.030mmol)、K3PO4三水合物(160mg,0.60mmol)、乙酸钠(49mg,0.60mmol)、乙腈(20mL)和水(3mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热3小时。然后将其过滤并减压蒸发滤液。将残余物通过硅胶柱色谱法来纯化(用1:3石油醚/乙酸乙酯洗脱)得到149a,其为黄色固体(97mg,50%)。MS-ESI:[M+H]+649
实施例149 2-{3'-羟基甲基-1-甲基-5-[5-((S)-2-甲基-4-氧杂环丁烷-3-基-哌嗪-1-基)-吡啶-2-基氨基]-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基}-2,3,5,6,7,8-六氢-4H-2,4b-二氮杂-芴-1-酮149
将149a(97mg,0.15mmol)、NaBH4(17mg,0.45)和甲醇(10mL)的混合物在25℃搅拌1小时。然后将反应混合物用水(10mL)淬灭并减压浓缩。将残余物用二氯甲烷(2X10mL)萃取。将合并的二氯甲烷萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到149(62mg,63%)。MS-ESI:[M+H]+651.3。1H NMR(500MHz,DMSO-d6)δ8.63(s,1H),8.46(d,J=5.0Hz,1H),8.43(s,1H),7.83(d,J=3.0Hz,1H),7.48(d,J=2.0Hz,1H),7.38-7.36(m,1H),7.31(J=5.0Hz,1H),7.25-7.23(m,1H),6.04(s,1H),4.57-4.55(m,2H),4.48-4.46(m,1H),4.42-4.38(m,2H),4.35-4.33(m,1H),4.15-4.12(m,1H),3.96-3.94(m,1H),3.82-3.78(m,2H),3.69-3.67(m,1H),3.59(s,3H),3.41-3.38(m,2H),3.18-3.15(m,2H),3.00-2.95(m,3H),2.73-2.71(m,2H),2.30-2.28(m,2H),2.20-2.16(m,1H),1.93-1.89(m,3H),1.77-1.75(m,1H),0.93(d,J=6.5Hz,3H).
实施例150a 3-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-5-[1-甲基-5-({5-甲基-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]吡啶-4-甲醛150a
在配备有磁力搅拌子和回流冷凝器的25-mL单颈圆底烧瓶中装入3-溴-5-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-甲醛107f(233mg,0.60mmol)、1-甲基-3-({5-甲基-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基}氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)-1,2-二氢吡啶-2-酮135a(231mg,0.60mmol)、Pd(dppf)Cl2(49mg,0.060mmol)、乙酸钾(118mg,1.2mmol)、K3PO4三水合物(320mg,1.2mmol)、乙腈(12mL)和水(5滴)。在经历三轮真空/氩气吹洗后,将混合物在110℃加热2小时。然后将其过滤并减压蒸发滤液。将残余物通过硅胶柱色谱法(用30:1二氯甲烷/甲醇洗脱)来纯化得到150a(168mg,49%),其为固体。MS-ESI:[M+H]+567
实施例150 2-[4-羟基甲基-1'-甲基-5'-(5-甲基-4,5,6,7-四氢-吡唑并[1,5-a]吡嗪-2-基氨基)-6'-氧代-1',6'-二氢-[3,3']联吡啶-5-基]-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮150
在0℃,向150a(170mg,0.30mmol)于甲醇(10mL)中的溶液中加入硼氢化钠(68mg,1.8mmol)。将混合物在室温搅拌30分钟。将反应混合物用水(2mL)淬灭并浓缩。将残余物用反相制备性-HPLC来纯化得到150(42mg,25%),其为浅黄色固体。MS-ESI:[M+H]+569.1H NMR(500MHz,CDCl3)δ8.63(s,1H),8.48(s,1H),7.95(d,J=2.0Hz,1H),7.40(s,1H),7.32(d,J=2.5Hz,1H),6.82(s,1H),5.67(s,1H),4.63-4.55(m,2H),4.37-4.35(m 1H),4.22-4.18(m,3H),4.05-3.97(m,3H),3.69(s,3H),3.59-3.57(m,2H),2.86(t,J=6.0Hz,2H),2.56(s,2H),2.50(s,2H),2.46(s,3H),1.26(s,6H).
实施例151a(R)-3-甲基-4-(6-硝基吡啶-3-基)哌嗪-1-羧酸叔丁酯151a
在配备有磁力搅拌子和回流冷凝器的250-mL单颈圆底烧瓶中装入1,4-二噁烷(60mL)、5-溴-2-硝基吡啶(2.0g,10.0mmol)、(R)-3-甲基哌嗪-1-羧酸叔丁酯(2.0g,10.0mmol)和碳酸铯(6.5g,20mmol)。使氮气鼓泡通过所得混合物10分钟后,加入三(二亚苄基丙酮)二钯(0)(915mg,1.0mmol)和XantPhos(579mg,1.0mmol)。使所述体系经历三轮真空/氩气吹洗并在100℃加热15小时。之后,将反应混合物冷却至室温并过滤。将滤液在乙酸乙酯(100mL)和水(100mL)之间分配。分离出水层并用乙酸乙酯(3X50mL)萃取。将合并的有机层用盐水(100mL)洗涤并用硫酸钠干燥。过滤除去干燥剂并减压浓缩滤液。将残余物通过硅胶柱色谱法(用30:1二氯甲烷/甲醇洗脱)来纯化得到151a(1.6g,44%),其为黄色固体。MS-ESI:[M+H]+323.1H NMR(500MHz,DMSO-d6)δ8.21(d,J=3.5Hz,1H),8.18(d,J=9.0Hz,1H),7.45-7.43(m,1H),4.34-4.33(m,1H),3.92-3.99(m,1H),3.80(d,J=12.5Hz,2H),3.06-3.23(m,3H),1.43(s,9H),1.09(d,J=6.5Hz,3H).
实施例151b(R)-4-(6-氨基吡啶-3-基)-3-甲基哌嗪-1-羧酸叔丁酯151b
将250-mL烧瓶用氮气吹洗并装入151a(1.5g,4.6mmol)、10%钯/炭(50%水分,200mg)和甲醇(70mL)。将其排空,充入氢气并在室温搅拌10小时。然后将氢气排空并在所述烧瓶中充入氮气。通过用垫过滤除去催化剂,减压浓缩滤液得到151b(1.1g,81%),其为棕色固体。MS-ESI:[M+H]+293
实施例151c(R)-4-(6-(5-溴-1-甲基-2-氧代-1,2-二氢吡啶-3-基氨基)吡啶-3-基)-3-甲基哌嗪-1-羧酸叔丁酯151c
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(40mL)、151b(1.0g,3.4mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(2.7g,10.2mmol)和碳酸铯(2.2g,6.8mmol)。使氮气鼓泡通过所得混合物10分钟后,加入XantPhos(198mg,0.34mmol)和三(二亚苄基丙酮)二钯(0)(313mg,0.34mmol)。使反应混合物经历三轮真空/氩气吹洗并在100℃加热5小时。之后,将反应混合物冷却至室温并过滤。将滤液在乙酸乙酯(50mL)和水(50mL)之间分配。分离出水层并用乙酸乙酯(3X30mL)萃取。将合并的有机层用盐水(50mL)洗涤并用硫酸钠干燥。过滤除去干燥剂并减压浓缩滤液。将残余物通过硅胶柱色谱法来纯化(用30:1二氯甲烷/甲醇洗脱)得到151c,其为黄色固体(1.1g,63%)。MS-ESI:[M+H]+478.
实施例151d(R)-5-溴-1-甲基-3-(5-(2-甲基哌嗪-1-基)吡啶-2-基氨基)吡啶-2(1H)-酮151d
向151c(600mg,1.26mmol)于甲醇(20mL)中的混合物中加入HCl/二噁烷(4M,4mL)。将反应混合物在室温搅拌4小时。然后将其减压浓缩。将残余物用1M NaOH水溶液碱化并用二氯甲烷(3X30mL)萃取。将合并的有机层用盐水洗涤并减压浓缩得到151d(450mg,95%),其为黄色固体。MS-ESI:[M+H]+378.
实施例151e(R)-5-溴-1-甲基-3-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)吡啶-2(1H)-酮151f
将151d(40.0g,106mmol)、氧杂环丁烷-3-酮(11.4g,159mmol)、NaBH3CN(10.0g,159mmol)和氯化锌(21.3g,159mmol)于甲醇(700mL)中的混合物在50℃搅拌5小时。向所述混合物中加入水(50mL)并减压浓缩。将残余物用二氯甲烷(3X200mL)萃取并将合并的有机层减压浓缩。将残余物通过硅胶柱色谱法来纯化(用40:1二氯甲烷/甲醇洗脱)得到151e(35g,73%)。MS:[M+H]+434。
实施例151f(R)-1-甲基-3-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮151f
向151e(2.0g,4.60mmol)、4,4,4',4',5,5,5',5'-八甲基-2,2'-二(1,3,2-二氧杂硼杂戊环)(3.50g,13.80mmol)于二噁烷(50mL)中的溶液中加入PdCl2(dppf)(377.10mg,0.46mmol)和乙酸钾(2.70g,27.80mmol)。将混合物在10℃和在氩气中搅拌12小时。反应后,过滤混合物并减压蒸发滤液。将残余物通过硅胶柱色谱法(用15:1二氯甲烷/甲醇洗脱)来纯化得到151f(1.10g,49%),其为棕色固体.MS:[M+H]+482.3
实施例151g(R)-4-(1-甲基-5-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-6,7,8,9-四氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛151g
在配备有回流冷凝器的100-mL圆底烧瓶中装入4-氯-2-(1-氧代-6,7,8,9-四氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛103b(150mg,0.45mmol)、151f(331mg,0.69mmol)、PdCl2(dppf)(37mg,0.045mmol)、K3PO4(190mg,0.90mmol)、乙酸钠(74mg,0.90mmol)、乙腈(15mL)和水(1.5mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热3小时。然后将其过滤并减压蒸发滤液。将残余物用硅胶柱色谱法(用1:20甲醇/二氯甲烷洗脱)来纯化得到151g,其为红色固体(89mg,30%)。MS-ESI:[M+H]+647
实施例151 2-{3'-羟基甲基-1-甲基-5-[5-((R)-2-甲基-4-氧杂环丁烷-3-基-哌嗪-1-基)-吡啶-2-基氨基]-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基}-6,7,8,9-四氢-2H-吡嗪并[1,2-a]吲哚-1-酮151
将151g(89mg,0.14mmol)、NaBH4(22mg,0.60)和甲醇(10mL)的混合物在25℃搅拌1小时。将混合物用水淬灭(8mL)并减压浓缩。将残余物用二氯甲烷(2X10mL)萃取。将合并的二氯甲烷萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到151(35mg,39%)。MS-ESI:[M+H]+649.1H NMR(500MHz,CDCl3)δ8.65(d,J=2.0Hz,1H),8.55(d,J=5.0Hz,1H),8.46(s,1H),7.83(d,J=2.5Hz,1H),7.50-7.48(m,2H),7.38-7.36(m,1H),7.26-7.24(m,2H),6.83-6.80(m,2H),4.98(bs,1H),4.57-4.54(m,2H),4.48-4.33(m,4H),3.67-3.66(m,1H),3.60(s,3H),3.39-3.38(m,2H),3.09-3.08(m,1H),2.96-2.94(m,1H),2.76-2.74(m,2H),2.64-2.62(m,2H),2.36-2.31(m,2H),2.20-2.17(t,J=7.5Hz,1H),1.88-1.86(m,2H),1.75-1.74(m,2H),0.93(d,J=6.5Hz,3H).
实施例152a 8-(6-硝基吡啶-3-基)-3,8-二氮杂二环[3.2.1]辛烷-3-羧酸叔丁酯152a
在配备有磁力搅拌子和回流冷凝器的250-mL单颈圆底烧瓶中装入1,4-二噁烷(100mL)、5-溴-2-硝基吡啶(2.5g,12.4mmol)、3,8-二氮杂二环[3.2.1]辛烷-3-羧酸叔丁酯(869g,4.1mmol)、Pd2(dba)3(193mg,0.21mmol)、XantPhos(237mg,0.41mmol)和碳酸铯(2.7g,8.2mmol)。在经历三轮真空/氩气吹洗后,将混合物在110℃搅拌整夜。将反应混合物冷却至室温。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用3:1石油醚/乙酸乙酯洗脱)来纯化得到152a(2.63g,66.8%),其为黄色固体。MS-ESI:[M+H]+335.2.
实施例152b 8-(6-氨基吡啶-3-基)-3,8-二氮杂二环[3.2.1]辛烷-3-羧酸叔丁酯152b
将100-mL单颈圆底烧瓶用氮气吹洗并装入152a(2.5g,7.5mmol)、10%钯/炭(50%水分,250mg)和甲醇(40mL)。将所述混合物排空、充入氢气并在室温搅拌16小时。然后将氢气排空并将氮气充入所述烧瓶中。通过用垫过滤除去催化剂,减压浓缩滤液得到152b(1.51g,66%),其为无色油状物。MS-ESI:[M+H]+305.3
实施例152c 8-(6-(5-溴-1-甲基-2-氧代-1,2-二氢吡啶-3-基氨基)吡啶-3-基)-3,8-二氮杂二环[3.2.1]辛烷-3-羧酸叔丁酯152c
在配备有磁力搅拌子的密封管中装入152b(1.3g,4.3mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(1.2g,4.3mmol)、三(二亚苄基丙酮)二钯(0)(394mg,0.43mmol)、XantPhos(497mg,0.86mmol)、Cs2CO3(2.8g,8.6mmol)和1,4-二噁烷(15mL)。在经历三轮真空/氩气吹洗后,将混合物在120℃搅拌2小时。减压浓缩滤液并将残余物通过硅胶柱色谱法(用50:1二氯甲烷/甲醇洗脱)来纯化得到152c,其为黄色固体(900mg,43%)。MS-ESI:[M+H]+490.3。
实施例152d 3-(5-(3,8-二氮杂二环[3.2.1]辛烷-8-基)吡啶-2-基氨基)-5-溴-1-甲基-吡啶-2(1H)-酮152d
将152c(900mg,1.84mmol)和4.0M HCl/二噁烷(60mL)的混合物在室温搅拌5小时。然后将其减压浓缩得到粗制152d,其为黄色固体(700mg,98%),将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+390.3。
实施例152e 5-溴-1-甲基-3-(5-(3-(氧杂环丁烷-3-基)-3,8-二氮杂二环[3.2.1]辛烷-8-基)吡啶-2-基氨基)吡啶-2(1H)-酮152e
将152d(676mg,1.7mmol)、氧杂环丁烷-3-酮(251mg,3.5mmol)、NaBH3CN(274mg,4.4mmol)和氯化锌(592mg,4.4mmol)于甲醇(30mL)中的混合物在50℃搅拌5小时。加入水并将混合物减压浓缩。将残余物用二氯甲烷萃取三次。将合并的萃取物减压浓缩得到粗制152e,其为黄色固体(650mg,84%),将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+446.2.
实施例152f乙酸(4-(1-甲基-5-(5-(3-(氧杂环丁烷-3-基)-3,8-二氮杂二环[3.2.1]辛烷-8-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯152f
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入152e(300mg,0.67mmol)、3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113h(257mg,0.67mmol)、Pd(dppf)Cl2(55mg,0.067mmol)、K3PO4(284mg,1.34mmol)、乙酸钠(110mg,1.34mmol)、水(6滴)和乙腈(20mL)。在经历三轮真空/氩气吹洗后,将混合物回流搅拌3小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用30:1二氯甲烷/甲醇洗脱)来纯化得到152f,其为棕色固体(200mg,42%)。MS-ESI:[M+H]+705.4。
实施例152 2-{3'-羟基甲基-1-甲基-5-[5-((1S,5R)-3-氧杂环丁烷-3-基-3,8-二氮杂-二环[3.2.1]辛-8-基)-吡啶-2-基氨基]-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基}-3,4,6,7,8,9-六氢-2H-吡嗪并[1,2-a]吲哚-1-酮152
将152f(180mg,0.26mmol)和氢氧化锂(215mg,5.1mmol)于异丙醇/THF(1:1,4mL)和水(1mL)中的混合物在35℃搅拌1小时。真空蒸发混合物并将残余物用水和乙酸乙酯稀释。分离出水相并用乙酸乙酯(2X10mL)萃取。将合并的乙酸乙酯萃取物减压浓缩,将残余物通过反相制备性-HPLC来纯化得到152(12mg,71%),其为黄色固体。MS-ESI:[M+H]+663.3.1HNMR(500MHz,DMSO-d6)δ8.55(d,J=2.5Hz,1H),8.48(d,J=5.0Hz,1H),8.32(s,1H),7.80(d,J=2.5Hz,1H),7.43(d,J=2.0Hz,1H),7.33(d,J=5.0Hz,1H),7.25-7.23(m,1H),7.20(d,J=9.0Hz,1H),6.57(s,1H),4.96-4.94(m,1H),4.48-4.43(m,3H),4.39-4.37(m,3H),4.25-4.19(m,5H),3.85(d,J=11.5Hz,1H),3.59(s,3H),2.66-2.54(m,4H),2.40-2.36(m,3H),2.17(d,J=10.5Hz,2H),1.94-1.65(m,8H).
实施例153a 2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-[1-甲基-5-({5-[(2R)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]吡啶-3-甲醛153a
在配备有回流冷凝器的50-mL圆底烧瓶中装入4-氯-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-甲醛108a(105mg,0.30mmol)、1-甲基-3-({5-[(2R)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-5-(四甲基-1,3,2-二氧杂硼杂戊环-2-基)-1,2-二氢吡啶-2-酮151g(216mg,0.45mmol)、PdCl2(dppf)(25mg,0.030mmol)、K3PO4(126mg,0.60mmol)、乙酸钠(49mg,0.60mmol)、乙腈(15mL)和水(1.5mL)。在经历三轮真空/氩气吹洗后,将混合物在80℃加热2小时。然后将其过滤并减压蒸发滤液。将残余物通过硅胶柱色谱法(用1:20甲醇/二氯甲烷洗脱)来纯化得到153a,其为红色固体(82mg,41%)。MS-ESI:[M+H]+663
实施例153 2-{3'-羟基甲基-1-甲基-5-[5-((R)-2-甲基-4-氧杂环丁烷-3-基-哌嗪-1-基)-吡啶-2-基氨基]-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基}-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮153
将153a(82mg,0.12mmol)、NaBH4(22mg,0.60)和甲醇(10mL)的混合物在25℃搅拌1小时。然后将其用水(5mL)淬灭并减压浓缩。将残余物用二氯甲烷(2X10mL)萃取。将合并的二氯甲烷萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到153(22mg,28%)。MS-ESI:[M+H]+665.1H NMR(500MHz,CDCl3)δ8.65(d,J=2.0Hz,1H),8.48(d,J=5.0Hz,1H),7.96(s,1H),7.84(s,1H),7.83(s,1H),7.36(d,J=5.0Hz,1H),7.32-7.26(m,1H),6.84-6.80(m,2H),5.30(s,1H),4.71-4.32(m,7H),4.15(d,J=5.0Hz,2H),3.85(t,J=8.0Hz,1H),3.71(s,3H),3.57-3.43(m,2H),3.08-3.06(m,2H),2.57-2.48(m,7H),2.22-2.20(m,1H),1.27(s,6H),0.98(d,J=6.5Hz,3H).
实施例154a 4-[1-甲基-5-({5-[(2R)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-甲醛154a
在配备有回流冷凝器的100-mL圆底烧瓶中装入4-氯-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-甲醛124a(84mg,0.24mmol)、(R)-1-甲基-3-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮151g(173mg,0.36mmol)、PdCl2(dppf)(20mg,0.024mmol)、K3PO4(100mg,0.48mmol)、乙酸钠(40mg,0.48mmol)、乙腈(20mL)和水(2mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热3小时。然后将其过滤并减压蒸发滤液。将残余物通过硅胶柱色谱法(用1:20甲醇/二氯甲烷洗脱)来纯化得到154a,其为红色固体(112mg,70%)。MS-ESI:[M+H]+665
实施例154 3-{3'-羟基甲基-1-甲基-5-[5-((R)-2-甲基-4-氧杂环丁烷-3-基-哌嗪-1-基)-吡啶-2-基氨基]-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基}-6,7,8,9-四氢-3H-苯并[4,5]噻吩并[2,3-d]哒嗪-4-酮154
将154a(150mg,0.23mmol)、NaBH4(35mg,0.92)和甲醇(10mL)的混合物在室温搅拌1小时。然后将混合物用水(8mL)淬灭并减压浓缩。将残余物用二氯甲烷(2X10mL)萃取。将合并的二氯甲烷萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到154(29mg,19%)。MS-ESI:[M+H]+667.1H NMR(500MHz,DMSO-d6)δ8.64(d,J=2.5Hz,1H),8.56(d,J=5.0Hz,1H),8.49-8.47(m,2H),7.85(d,J=3.0Hz,1H),7.53(d,J=5.0Hz,1H),7.48(d,J=2.5Hz,1H),7.38-7.36(m,1H),7.24(d,J=8.5Hz,1H),4.85(t,J=9.5Hz,1H),4.57-4.54(m,2H),4.43-4.36(m,4H),3.69-3.68(m,1H),3.60(s,3H),3.40-3.36(m,1H),3.11-3.07(m,1H),2.97-2.86(m,6H),2.33-2.31(m,2H),2.16(t,J=8.5Hz,1H),1.89-1.86(m,4H),0.92(d,J=6.5Hz,3H).
实施例155a 3-(5-((2S,5R)-2,5-二甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮155a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入5-溴-3-(5-((2S,5R)-2,5-二甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基吡啶-2(1H)-酮122e(3.0g,6.70mmol)、Pin2B2(8442mg,33.5mmol)、Pd2(dba)3(311mg,0.34mmol)、X-phos(319mg,0.67mmol)、乙酸钾(1970mg,20.1mmol)和二噁烷(50mL)。在经历三轮真空/氩气吹洗后,将混合物在60℃加热16小时。然后将其冷却至室温并过滤。减压浓缩滤液。将所得残余物用8:1石油醚/乙酸乙酯(80mL)洗涤得到155a,其为黄色固体(3g,90%)。MS:[M+H]+496.4。
实施例155b 4-(5-(5-(2,5-二甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-3-甲醛155b
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入4-氯-2-(1-氧代-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-3-甲醛139a(133mg,0.40mmol)、155a(198mg,0.40mmol)、Pd(dppf)Cl2(17mg,0.020mmol)、K3PO4(254mg,1.2mmol)、乙酸钠(98mg,1.2mmol)、水(5滴)和乙腈(10mL)。在经历三轮真空/氩气吹洗后,将混合物回流加热3小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用30:1二氯甲烷/甲醇洗脱)来纯化得到155b,其为白色固体(80mg,30%)。MS-ESI:[M+H]+663.3。
实施例155 2-{5-[5-((2S,5R)-2,5-二甲基-4-氧杂环丁烷-3-基-哌嗪-1-基)-吡啶-2-基氨基]-3'-羟基甲基-1-甲基-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基}-2,3,5,6,7,8-六氢-4H-2,4b-二氮杂-芴-1-酮155
在0℃,向155b(80mg,0.12mmol)于甲醇(5mL)中的溶液中加入硼氢化钠(12mg,0.36mmol)。将反应混合物搅拌30分钟。然后将其用水(1mL)淬灭并减压浓缩。将残余物通过反相制备性-HPLC来纯化得到155(32mg,40%)。MS-ESI:[M+H]+665.3。1H NMR(500MHz,CDCl3)δ8.68(d,J=2.0Hz,1H),8.50(d,J=5.0Hz,1H),8.04(d,J=2.5Hz,1H),7.88(s,1H),7.86(d,J=2.5Hz,1H),7.37-7.33(m,2H),6.82(d,J=9.0Hz,1H),6.32(s,1H),5.02(d,J=13.0Hz,1H),4.78-4.71(m,2H),4.67-4.61(m,3H),4.44-4.39(m,1H),4.31-4.29(m,1H),3.96-3.91(m,1H),3.86-3.80(m,2H),3.78-3.75(m,1H),3.72(s,3H),3.21-3.19(m,1H),3.01-2.93(m,3H),2.85-2.83(m,2H),2.72(d,J=10.0Hz,2H),2.49-2.47(m,1H),2.05-2.03(m,2H),1.98-1.97
实施例156a 4-(5-(5-((2S,5R)-2,5-二甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛156a
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入3-(5-((2S,5R)-2,5-二甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮155a(171mg,0.35mmol)、4-氯-2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛134c(120mg,0.35mmol)、K3PO4(146mg,0.69mmol)、PdCl2(dppf)(28mg,0.035mmol)、乙酸钠(56mg,0.69mmol)、水(5滴)和乙腈(20mL)。在经历三轮真空/氩气吹洗后,将混合物在90℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用40/1二氯甲烷/甲醇洗脱)来纯化得到156a,其为黄色固体(60mg,25%)。MS-ESI:[M+H]+681.3
实施例156 2-{5-[5-((2S,5R)-2,5-二甲基-4-氧杂环丁烷-3-基-哌嗪-1-基)-吡啶-2-基氨基]-3'-羟基甲基-1-甲基-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基}-10-氟-3,4,6,7,8,9-六氢-2H-吡嗪并[1,2-a]吲哚-1-酮156
在配备有磁力搅拌子的50-mL圆底烧瓶中装入156a(60mg,0.088mmol)、NaBH4(17mg,0.44mmol)和甲醇(10mL)。将混合物在室温搅拌1小时。然后将其用水淬灭并减压浓缩。将残余物通过反相制备性-HPLC来纯化得到156(15mg,25%)。MS-ESI:[M+H]+683.5。1HNMR(500MHz,CDCl3)δ8.67(d,J=2.5Hz,1H),8.48(d,J=5.0Hz,1H),8.02(d,J=2.5Hz,1H),7.87(s,1H),7.84(d,J=2.0Hz,1H),7.37-7.35(m,2H),6.81(d,J=9.0Hz,1H),4.99-4.59(m,6H),4.45-4.32(m,2H),4.12-4.03(m,2H),3.85-3.73(m,2H),3.71(s,3H),3.19-3.16(m,1H),2.91-2.89(m,1H),2.75-2.69(m,2H),2.57-2.47(m,5H),1.97-1.76(m,5H),0.89-0.87(m,重叠,6H).
实施例157 2-{5'-[5-((2S,5R)-2,5-二甲基-4-氧杂环丁烷-3-基-哌嗪-1-基)-吡啶-2-基氨基]-4-羟基甲基-1'-甲基-6'-氧代-1',6'-二氢-[3,3']联吡啶-5-基}-3,4,6,7,8,9-六氢-2H-吡嗪并[1,2-a]吲哚-1-酮157
在配备有磁力搅拌子和回流冷凝器的25-mL单颈圆底烧瓶中装入3-溴-5-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2a]吲哚-2(1H)-基)吡啶-4-甲醛101f(200mg,0.54mmol)、3-(5-((2S,5R)-2,5-二甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮155a(267mg,0.54mmol)、Pd(dppf)Cl2(44mg,0.054mmol)、K3PO4(229mg,1.08mmol)、乙酸钠(89mg,1.08mmol)、水(0.2mL)和乙腈(10mL)。在经历三轮真空/氩气吹洗后,将混合物回流加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过反相制备性-HPLC来纯化得到157(35.5mg,11%),其为黄色固体。MS-ESI:[M+H]+665.4.1H NMR(500MHz,CDCl3)δ8.65-8.63(m,2H),8.50(s,1H),7.80(s,1H),7.87(s,1H),7.48-7.47(m,1H),7.36(d,J=7.5Hz,1H),6.88(s,1H),6.81(d,J=9.0Hz,1H),4.75-4.54(m,重叠,6H),4.37-4.13(m,重叠,4H),4.00-3.95(m,1H),3.74-3.73(m,1H),3.72(s,3H),3.19-3.15(m,1H),2.91-2.90(m,1H),2.74-2.44(m,重叠,7H),1.92-1.88(m,2H),1.81-1.79(m,2H),0.90-0.89(m,6H).
实施例158a 4-[5-({5-[(2S,5R)-2,5-二甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-甲醛158a
在配备有回流冷凝器的100-mL单颈圆底烧瓶中装入(4-氯-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-甲醛)108a(280mg,0.80mmol)、3-(5-((2S,5R)-2,5-二甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮155a(480mg,0.96mmol)、Pd(dppf)Cl2(33mg,0.040mmol)、K3PO4(339mg,1.6mmol)、乙酸钠·三水合物(218mg,1.6mmol)和乙腈(100mL)。将体系排空并用氮气回填。将反应混合物在100℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用25:1的二氯甲烷/甲醇洗脱)来纯化得到158a(300mg,54%),其为棕黄色固体。MS-ESI:[M+H]+677.3。
实施例158 2-{5-[5-((2S,5R)-2,5-二甲基-4-氧杂环丁烷-3-基-哌嗪-1-基)-吡啶-2-基氨基]-3'-羟基甲基-1-甲基-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基}-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮158
将158a(200mg,0.30mmol)和NaBH4(36mg,0.90mmol)于甲醇(30mL)中的混合物在30℃搅拌1小时。将混合物用水(5mL)淬灭并用乙酸乙酯(3X10mL)萃取。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到158(110mg,55%),其为白色固体。MS-ESI:[M+H]+679.4.1H NMR(500MHz,CDCl3)δ8.68(d,J=2.0Hz,1H),8.50(d,J=5.0Hz,1H),8.03(d,J=2.5Hz,1H),7.88(s,1H),7.87(d,J=2.0Hz,1H),7.37-7.36(m,2H),6.85(s,1H),6.81(d,J=3.5Hz,1H),5.07(t,J=7.0Hz,1H),4.77-4.71(m,2H),4.67-4.61(m,3H),4.53-4.51(m,1H),4.34-4.32(m,1H),4.16(d,J=5.5Hz,2H),3.88-3.86(m,1H),3.76(t,J=7.5Hz,1H),3.72(s,3H),3.20-3.17(m,1H),2.92(dd,J=3.0,11.5Hz,1H),2.76-2.70(m,2H),2.58(d,J=6.0Hz,2H),2.52(s,2H),2.49-2.46(m,1H),1.97-1.93(m,1H),1.28(s,6H),0.92-0.89(m,6H)。
实施例159a 4-[5-({5-[2,5-二甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基]-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-甲醛159a
在配备有回流冷凝器的100-mL圆底烧瓶中装入4-氯-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-甲醛124a(200mg,0.58mmol)、3-({5-[(2S,5R)-2,5-二甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)-1,2-二氢吡啶-2-酮155a(1.0g,2.0mmol)、PdCl2(dppf)(47mg,0.060mmol)、K3PO4(280mg,1.2mmol)、乙酸钠(95mg,1.2mmol)、乙腈(15mL)和水(1.5mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热3小时。然后将其过滤并减压蒸发滤液。将残余物用硅胶柱色谱法(用1:20甲醇/二氯甲烷洗脱)来纯化得到159a,其为红色固体(150mg,38%)。MS-ESI:[M+H]+679
实施例159 3-{5-[5-((2S,5R)-2,5-二甲基-4-氧杂环丁烷-3-基-哌嗪-1-基)-吡啶-2-基氨基]-3'-羟基甲基-1-甲基-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基}-6,7,8,9-四氢-3H-苯并[4,5]噻吩并[2,3-d]哒嗪-4-酮159
将159a(130mg,0.19mmol)、NaBH4(22mg,0.60)和甲醇(10mL)的混合物在25℃搅拌1小时。然后将混合物用水(8mL)淬灭并减压浓缩。将残余物用二氯甲烷(2X10mL)萃取。将合并的二氯甲烷萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到159(28mg,22%)。MS-ESI:[M+H]+681.1H NMR(500MHz,CDCl3)δ8.71(d,J=2.5Hz,1H),8.65(d,J=5.0Hz,1H),8.30(s,1H),8.04(s,1H),7.87(s,1H),7.70(d,J=2.0Hz,1H),7.55(d,J=5.0Hz,1H),7.37(d,J=9.0Hz,1H),6.81(d,J=9.0Hz,1H),4.67-4.61(m,2H),4.71-4.64(m,2H),4.44-4.42(m,2H),4.34-4.33(m,1H),3.83-3.76(m,1H),3.72(s,3H),3.20-3.16(m,1H),2.99-2.84(m,6H),2.79-2.71(m,2H),2.50-2.48(m,1H),2.02-1.98(m,4H),0.91(d,J=6.0Hz,6H).
实施例160a 4-(5-(5-((2S,5R)-2,5-二甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-6,7,8,9-四氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛160a
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入4-氯-2-(1-氧代-6,7,8,9-四氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛103b(150mg,1.0当量,0.46mmol)、3-(5-((2S,5R)-2,5-二甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮155a(228mg,0.46mmol)、K3PO4(195mg,0.92mmol)、PdCl2(dppf)(37mg,0.046mmol)、乙酸钠(75mg,0.92mmol)、水(8滴)和乙腈(20mL)。在经历三轮真空/氩气吹洗后,将混合物在80℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用40:1二氯甲烷/乙醇洗脱)来纯化得到160a,其为黄色固体(80mg,26%)。MS-ESI:[M+H]+661.4。
实施例160 2-{5-[5-((2S,5R)-2,5-二甲基-4-氧杂环丁烷-3-基-哌嗪-1-基)-吡啶-2-基氨基]-3'-羟基甲基-1-甲基-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基}-6,7,8,9-四氢-2H-吡嗪并[1,2-a]吲哚-1-酮160
在配备有磁力搅拌子的50-mL单颈圆底烧瓶中装入160a(80mg,0.12mmol)、NaBH4(23mg,0.60mmol)和甲醇(10mL)。将混合物在室温搅拌1小时。将其用水(1mL)淬灭并过滤。减压浓缩滤液并将残余物通过反相制备性-HPLC来纯化得到160(44mg,55%)。MS-ESI:[M+H]+663.3.1H NMR(500MHz,CDCl3)δ8.72-8.70(m,1H),8.57(d,J=5.0Hz,1H),8.03(d,J=2.5Hz,1H),7.89-7.87(m,2H),7.50(d,J=5.0Hz,1H),7.37-7.35(m,1H),7.06(s,1H),6.97(d,J=6.0Hz,1H),6.81(d,J=9.0Hz,1H),6.68(d,J=6.0Hz,1H),5.10-5.08(m,1H),4.76-4.32(m,6H),3.76-3.72(m,4H),3.20-3.17(m,1H),2.93-2.90(m,1H),2.76-2.69(m,6H),2.49-2.46(m,1H),1.97-1.94(m,3H),1.87-1.84(m,2H),0.89(t,J=6.5Hz,6H).
实施例161a(S)-3-乙基-4-(6-硝基吡啶-3-基)哌嗪-1-羧酸叔丁酯161a
在配备有磁力搅拌子和回流冷凝器的250-mL单颈圆底烧瓶中装入1,4-二噁烷(50mL)、5-溴-2-硝基吡啶(2.02g,10mmol)、(S)-3-乙基哌嗪-1-羧酸叔丁酯(2.14g,10.0mmol)、Pd2(dba)3(458mg,0.50mmol)、XantPhos(576mg,1.0mmol)和碳酸铯(6.52g,20mmol)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热整夜。之后,将反应混合物冷却至室温。然后将其过滤并减压蒸发滤液。将残余物通过硅胶柱色谱法(用3:1石油醚/乙酸乙酯洗脱)来纯化得到161a(700mg,22%),其为黄色固体。MS:[M+H]+336
实施例161b(S)-4-(6-氨基吡啶-3-基)-3-乙基哌嗪-1-羧酸叔丁酯161b
将100-mL单颈圆底烧瓶用氮气吹洗并装入161a(0.7g,2.08mmol)、10%钯/炭(50%水分,208mg)和甲醇(40mL)。将混合物排空,充入氢气并在室温搅拌6小时。然后将氢气排空并将氮气充入所述烧瓶中。通过用垫过滤除去催化剂,减压浓缩滤液得到161b(568mg,89%)。MS:[M+H]+306
实施例161c(S)-4-(6-(5-溴-1-甲基-2-氧代-1,2-二氢吡啶-3-基氨基)吡啶-3-基)-3-乙基哌嗪-1-羧酸叔丁酯161c
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(50mL)、161b(568mg,1.86mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(498mg,1.86mmol)、Pd2(dba)3(85mg,0.093mmol)、XantPhos(107mg,0.186mmol)和碳酸铯(1.198g,3.72mmol)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热6小时。然后将其过滤并减压蒸发滤液。将残余物通过硅胶柱色谱法(用100:1二氯甲烷/甲醇洗脱)来纯化得到161c(502mg,55%),其为黄色固体。MS:[M+H]+492。
实施例161d(S)-5-溴-3-(5-(2-乙基哌嗪-1-基)吡啶-2-基氨基)-1-甲基吡啶-2(1H)-酮161d
将161c(502mg,1.02mmol)、二氯甲烷(2mL)和4.0M HCl/二噁烷(4mL)的混合物在室温搅拌5小时。然后将其减压浓缩得到粗制161d,其为黄色固体(263mg,66%),将其不经进一步纯化即用于下一步骤。MS:[M+H]+392.
实施例161e(S)-5-溴-3-(5-(2-乙基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基吡啶-2(1H)-酮161e
将161d(263mg,0.67mmol)、氧杂环丁烷-3-酮(96mg,1.34mmol)、NaBH3CN 104mg,1.68mmol)和氯化锌(227mg,1.68mmol)于甲醇(10mL)中的混合物在50℃搅拌5小时。然后向反应混合物中加入水(10mL)。将所得混合物减压浓缩。将残余物用二氯甲烷萃取三次。将合并的有机层减压浓缩并将残余物通过硅胶柱色谱法(用50:1二氯甲烷/甲醇洗脱)来纯化得到161e(203mg,68%)。MS:[M+H]+448。
实施例161f(S)-3-(5-(2-乙基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮161f
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入161e(3219mg,7.20mmol)、Pin2B2(9072mg,36.0mmol)、Pd2(dba)3(329mg,0.36mmol)、X-phos(302mg,0.72mmol)、乙酸钾(2117mg,21.6mmol)和二噁烷(50mL)。在经历三轮真空/氩气吹洗后,将混合物在60℃加热16小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物用8:1石油醚/乙酸乙酯(80mL)洗涤得到161f,其为黄色固体(3.0g,84%)。MS:[M+H]+496.4.
实施例161g 4-(5-(5-(2-乙基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-3-甲醛161g
在配备有回流冷凝器的50-mL圆底烧瓶中装入161f(200mg,0.40mmol)、4-氯-2-(1-氧代-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-3-甲醛139a(132mg,0.40mmol)、三水合K3PO4(213mg,0.80mmol)、乙酸钠(66mg,0.80mmol)、1,1’-二(二苯基膦基)二茂铁二氯化钯(II)(16mg,0.020mmol)和乙腈(20mL)。在经历三轮真空/氮气吹洗后,将混合物在100℃和在氮气保护下加热2小时。通过LCMS分析反应混合物,显示完全转化成所期望的产物。将反应混合物冷却至室温并过滤。减压浓缩滤液。将残余物用二氯甲烷(50mL)和水(50mL)稀释。分离出水层并用二氯甲烷(3×20mL)萃取。将合并的有机层用Na2SO4干燥,过滤并减压浓缩。将黑色残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(80/1至30/1)洗脱)来纯化得到161g(150mg,57%),其为黄色固体。MS-ESI:[M+H]+663
实施例161 2-{5-[5-((S)-2-乙基-4-氧杂环丁烷-3-基-哌嗪-1-基)-吡啶-2-基氨基]-3'-羟基甲基-1-甲基-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基}-2,3,5,6,7,8-六氢-4H-2,4b-二氮杂-芴-1-酮161
在室温,向161g(120mg,0.18mmol)于甲醇(20mL)中的溶液中加入NaBH4(21mg,0.54mmol)。将反应混合物搅拌1小时后,LCMS表明反应完成。然后将混合物倒入水(20mL)中并减压浓缩。将残余物用二氯甲烷(3X40mL)萃取。将合并的有机层用盐水(20mL)洗涤,用Na2SO4干燥,过滤并浓缩。将残余固体通过制备性-HPLC来纯化得到161(97mg,81%),其为白色固体。MS-ESI:[M+H]+665。1H NMR(500MHz,CDCl3)δ8.63(s,1H),8.50(d,J=5.0Hz,1H),7.93(s,1H),7.84-7.82(m,2H),7.35(d,J=4.5Hz,1H),7.28(s,1H),6.82(d,J=9.0Hz,1H),6.32(s,1H),5.01-4.99(m,1H),4.73-4.64(m,5H),4.45-4.40(m,1H),4.30(t,J=12.0Hz,1H),3.94-3.91(m,1H),3.85-3.83(m,2H),3.72(s,3H),3.55-3.53(m,1H),3.34-3.32(m,1H),3.14-3.12(m,2H),3.04-2.92(m,2H),2.84-2.82(m,2H),2.59-2.57(m,1H),2.46-2.44(m,2H),2.38-2.36(m,1H),2.06-2.01(m,2H),1.90-1.86(m,2H),1.68-1.66(m,1H),1.43-1.39(m,1H),0.82(t,J=7.5Hz,3H).
实施例162a 5-溴-1-甲基-3-(吡嗪-2-基氨基)吡啶-2(1H)-酮162a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入吡嗪-2-胺(500mg,5.3mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(1335mg,5.3mmol)、Pd2(dba)3(229mg,0.25mmol)、XantPhos(289mg,0.50mmol)、碳酸铯(3.26g,10mmol)和1,4-二噁烷(50mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃搅拌2小时。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用50:1二氯甲烷/甲醇洗脱)来纯化得到162a(420mg,30%),其为黄色固体。MS-ESI:[M+H]+281.0。
实施例162b乙酸(4-(1-甲基-6-氧代-5-(吡嗪-2-基氨基)-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯162b
在配备有回流冷凝器的100-mL单颈圆底烧瓶中装入162a(170mg,0.61mmol)、3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113i(280mg,0.72mmol)、Pd(dppf)Cl2(30mg,0.037mmol)、K3PO4·三水合物(270mg,1.2mmol)、乙酸钠(180mg,1.2mmol)、乙腈(20mL)和水(0.5mL)。将体系排空并用氮气回填。将反应混合物在100℃搅拌2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用25:1的二氯甲烷/甲醇洗脱)来纯化得到162b(130mg,40%),其为棕黄色固体。MS-ESI:[M+H]+540.3
实施例162 2-[3'-羟基甲基-1-甲基-6-氧代-5-(吡嗪-2-基氨基)-1,6-二氢-[3,4']联吡啶-2'-基]-3,4,6,7,8,9-六氢-2H-吡嗪并[1,2-a]吲哚-1-酮162
将162b(110mg,0.20mmol)和氢氧化锂(84mg,2.0mmol)于异丙醇/THF(1:1,4mL)和水(1mL)中的混合物在30℃搅拌1小时。真空蒸发混合物并将残余物用水和乙酸乙酯稀释。分离出水相并用乙酸乙酯(2X10mL)萃取。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到162(85mg,85%),其为浅黄色固体。MS-ESI:[M+H]+498.3。1HNMR(500MHz,CHCl3)δ8.73(d,J=2.5Hz,1H),8.54(d,J=5Hz,1H),8.29(s,1H),8.15-8.14(m,2H),8.01(d,J=2.5Hz,1H),8.00(d,J=2.0Hz,1H),7.37(d,J=5Hz,1H),6.91(s,1H),4.66-4.65(m,1H),4.52-4.51(m,1H),4.32-4.31(m,1H),4.18-4.17(m,1H),4.14-4.12(m,1H),3.90-3.88(m,1H),3.75(s,3H),2.62-2.57(m,4H),1.92-1.88(m,3H),1.80-1.79(m,2H).
实施例163a 1-甲基-5-(5-(氧杂环丁烷-3-基)-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基硼酸163a
在配备有磁力搅拌子的100-mL圆底烧瓶中装入5-溴-1-甲基-3-(5-(氧杂环丁烷-3-基)-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)吡啶-2(1H)-酮125i(1.0g,2.64mmol)、4,4,4',4',5,5,5',5'-八甲基-2,2'-二(1,3,2-二氧杂硼杂戊环)(2.0g,7.92mmol)、PdCl2(dppf)(190mg,0.26mmol)、乙酸钾(776mg,7.92mmol)和二噁烷(40mL)。在向所述混合物中鼓泡氩气30分钟后,将回流冷凝器与所述烧瓶相连并将混合物在100℃和氩气中搅拌6小时。过滤所得混合物并减压蒸发滤液。将残余物通过反相Combiflash来纯化(用0.3%NH4HCO3水溶液/CH3CN洗脱)得到163a,其为白色固体(300mg,33%)。MS:[M+H]+346。
实施例163b 2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-(1-甲基-5-{[5-(氧杂环丁烷-3-基)-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基]氨基}-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-甲醛163b
在配备有回流冷凝器的100-mL单颈圆底烧瓶中装入(4-氯-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-甲醛)108a(280mg,0.81mmol)、163a(440mg,0.96mmol)、Pd(dppf)Cl2(40mg,0.049mmol)、K3PO4(360mg,1.6mmol)、乙酸钠三水合物(240mg,1.6mmol)、水(6滴)和乙腈(20mL)。将体系排空并用氮气回填。将反应混合物在100℃搅拌2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用25:1二氯甲烷/甲醇洗脱)来纯化得到163b(150mg,31%),其为棕黄色固体。MS-ESI:[M+H]+609.3
实施例163 2-[3'-羟基甲基-1-甲基-5-(5-氧杂环丁烷-3-基-4,5,6,7-四氢-吡唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基]-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮163
将163b(80mg,0.12mmol)和NaBH4(15mg,0.36mmol)于甲醇(5mL)中的混合物在30℃搅拌2小时。将混合物用水淬灭并减压浓缩。将残余物用乙酸乙酯(3X10mL)萃取。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到163(30mg,50%),其为深红色固体。MS-ESI:[M+H]+611.4.1H NMR(500MHz,CHCl3)δ8.48(d,J=5.5Hz,1H),7.96(d,J=2.5Hz,1H),7.70(d,J=2,1H),7.43(s,1H),7.34(d,J=5Hz,1H),6.8(s,1H),5.70(s,1H),5.03(t,J=6,1H),4.77-4.73(m,3H),4.68(t,J=6.5Hz,2H),4.51-4.50(m,1H),4.34-4.33(m,1H),4.23-4.16(m,2H),4.09(t,J=5.5Hz,2H),3.86-3.85(m,1H),3.79-3.74(m,1H),3.71(s,3H),3.56(d,J=4,2H),2.83(t,J=5.5Hz,2H),2.58(d,J=5.5Hz,2H),2.52(s,2H),1.28(s,6H).
实施例164a 2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-[5-({5-[(2S)-2-乙基-4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基]吡啶-3-甲醛164a
在配备有回流冷凝器的100-mL单颈圆底烧瓶中装入(4-氯-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-甲醛)108a(280mg,0.8mmol)、(S)-3-(5-(2-乙基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮161f(500mg,0.96mmol)、Pd(dppf)Cl2(33mg,0.040mmol)、K3PO4(360mg,1.6mmol)、乙酸钠三水合物(240mg,1.6mmol)和乙腈(100mL)。将体系排空并用氮气回填。将反应混合物在100℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用25:1二氯甲烷/甲醇洗脱)来纯化得到164a(320mg,60%),其为棕黄色固体。MS-ESI:[M+H]+677.3。
实施例164 2-{5-[5-((S)-2-乙基-4-氧杂环丁烷-3-基-哌嗪-1-基)-吡啶-2-基氨基]-3'-羟基甲基-1-甲基-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基}-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮164
将164a(200mg,0.30mmol)和NaBH4(36mg,0.90mmol)于甲醇(30mL)中的混合物在30℃搅拌2小时。将混合物用水淬灭并减压浓缩。将残余物用乙酸乙酯(3X10mL)萃取。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到164(140mg,72%),其为浅绿色固体。MS-ESI:[M+H]+679.3。1H NMR(500MHz,CDCl3)δ8.63(d,J=2.5Hz,1H),8.49(d,J=5.0Hz,1H),7.93(d,J=2.5Hz,1H),7.83(s,1H),7.82(s,1H),7.37(d,J=5.0Hz,1H),7.27(s,1H),6.85(s,1H),6.82(d,J=9.0Hz,1H),5.06(s,1H),4.71-4.61(m,5H),4.52-4.50(m,1H),4.34-4.32(m,1H),4.16(d,J=4.5Hz,2H),3.87-3.85(m,1H),3.72(s,3H),3.55-3.50(m,1H),3.33-3.30(m,1H),3.12(t,J=5.0Hz,2H),2.58-2.55(m,3H),2.52(s,2H),2.44(d,J=3.5Hz,2H),2.35(t,J=5.5Hz,1H),1.68-1.64(m,1H),1.42-1.37(m,1H),1.28(s,6H),0.82(t,J=7.5Hz,3H)。
实施例165a(S)-4-(5-(5-(2-乙基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-6,7,8,9-四氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛165a
在配备有回流冷凝器的50-mL烧瓶中装入4-氯-2-(1-氧代-6,7,8,9-四氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛103b(164mg,0.50mmol)、(S)-3-(5-(2-乙基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮161f(347mg,0.70mmol)、乙酸钾(137mg,1.4mmol)、1,1’-二(二苯基膦基)二茂铁二氯化钯(II)(29mg,0.035mmol)、水(5滴)和乙腈(20mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃和氩气中加热3小时。将反应混合物冷却至室温并过滤。减压浓缩滤液。将残余物用二氯甲烷(50mL)和水(50mL)稀释。分离出水层并用二氯甲烷(3×20mL)萃取。将合并的有机层用Na2SO4干燥,过滤并减压浓缩。将黑色残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(80/1至25/1)洗脱)来纯化得到165a(151mg,46%),其为黄色固体。MS-ESI:[M+H]+661
实施例165 2-{5-[5-((S)-2-乙基-4-氧杂环丁烷-3-基-哌嗪-1-基)-吡啶-2-基氨基]-3'-羟基甲基-1-甲基-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基}-6,7,8,9-四氢-2H-吡嗪并[1,2-a]吲哚-1-酮165
在室温,向165a(100mg,0.15mmol)于甲醇(10mL)中的溶液中加入NaBH4(34mg,0.90mmol)。在将反应混合物搅拌1小时后,LCMS表明反应完成。然后将混合物用水淬灭(8mL)并减压浓缩。将残余物用二氯甲烷(3X10mL)萃取。将合并的有机层用盐水(30mL)洗涤,用Na2SO4干燥,过滤并减压浓缩。将残余物通过反相制备性-HPLC来纯化得到165(35mg,35%),其为浅黄色固体。MS-ESI:[M+H]+663。1H NMR(500MHz,DMSO-d6)δ8.64(s,1H),8.57(d,J=5.0Hz,1H),8.44(s,1H),7.82(d,J=2.0Hz,1H),7.51-7.48(m,2H),7.35(dd,J=2.0Hz,9.0Hz,1H),7.27-7.23(m,2H),6.83-6.81(m,2H),4.97(bs,1H),4.59-4.55(m,2H),4.49-4.32(m,4H),3.61(s,3H),3.51-3.47(m,1H),3.42-3.37(m,1H),3.17-3.16(m,1H),3.01-2.98(m,1H),2.76-2.74(m,2H),2.63-2.61(m,3H),2.55-2.54(m,1H),2.19-2.16(m,1H),2.12-2.07(m,1H),1.90-1.85(m,2H),1.77-1.66(m,3H),1.27-1.25(m,1H),0.79(t,J=7.0Hz,3H).
实施例166a 2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)-4-(1-甲基-5-(5-(氧杂环丁烷-3-基)-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-甲醛166a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1-甲基-3-(5-(氧杂环丁烷-3-基)-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮163a(354mg,0.83mmol)、4-氯-2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛134c(289mg,0.83mmol)、PdCl2(dppf)(68mg,0.08mmol)、K3PO4(352mg,1.66mmol)、乙酸钠(136mg,1.66mmol)、乙腈(50mL)和水(3mL)。将体系排空并用氮气回填。将反应混合物在100℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用30:1二氯甲烷/甲醇洗脱)得到166a(305mg,60%),其为棕色固体。MS-ESI:[M+H]+:613.6.
实施例166 10-氟-2-[3'-羟基甲基-1-甲基-5-(5-氧杂环丁烷-3-基-4,5,6,7-四氢-吡唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基]-3,4,6,7,8,9-六氢-2H-吡嗪并[1,2-a]吲哚-1-酮166
在0℃,向166a(250mg,0.41mmol)于甲醇(20mL)中的悬浮液中加入硼氢化钠(47mg,1.23mmol)。将混合物搅拌30分钟。然后将其用水(2mL)淬灭并减压浓缩。将残余物通过反相制备性-HPLC来纯化得到166(20mg,6.6%)。MS-ESI:[M+H]+615.6.1H NMR(500MHz,CDCl3)δ8.46(d,J=5.0Hz,1H),7.94(d,J=3.0Hz,1H),7.66(d,J=2.0Hz,1H),7.43(s,1H),7.34(d,J=5.0Hz,1H),5.75(s,1H),4.95(t,J=6.5Hz,1H),4.76-4.74(m,2H),4.69-4.65-4.67(m,3H),4.46-4.44(m,1H),4.35-4.33(m,1H),4.10-4.08(m,4H),3.38-3.35(m,2H),3.69(s,3H),3.58-3.56(m,2H),2.842.82(m,2H),2.58-2.53(m,4H),1.89-1.84(m,2H),1.77-1.76(m,2H).
实施例167a 3-氯二环[2.2.1]庚-2-烯-2-甲醛167a
将配备有磁力搅拌子和回流冷凝器的250-mL三颈圆底烧瓶用氮气吹洗并装入无水1,2-二氯乙烷(24mL)和无水DMF(9.12g,125mmol)。将反应混合物冷却至0℃并历时5分钟加入三氯氧磷(15.3g,100mmol),同时维持反应温度在0-10℃之间。移去冷却浴并将反应混合物在室温搅拌30分钟。加入二环[2.2.1]庚烷-2-酮(5.50g,50.0mmol)于1,2-二氯乙烷(10mL)中的溶液并将所得混合物在80℃加热整夜。之后,将反应混合物倒入磷酸一氢钾(43.5g,250mmol)的水(200mL)溶液并搅拌15分钟。分离出有机层并减压浓缩。将残余物溶解在二氯甲烷(300mL)中并用水(2X50mL)洗涤。将二氯甲烷层用硫酸钠干燥,过滤并减压浓缩。将残余物通过硅胶柱色谱法(用1:100乙酸乙酯/石油醚洗脱)来纯化得到167a,其为黄色油状物(2.2g,28%)。MS:[M+H]+157.1H NMR(500MHz,CDCl3)δ9.80(s,1H),3.42-3.41(m,1H),3.08-3.07(m,1H),1.95-1.77(m,2H),1.68-1.66(m,1H),1.41-1.17(m,3H).
实施例167b(E)-3-(3-氯二环[2.2.1]庚-2-烯-2-基)丙烯酸乙酯167b
向167a(9.0g,57.7mmol)于二氯甲烷(250mL)中的溶液中加入2-(三苯基-λ5-亚膦烷基)乙酸乙酯(20g,57.7mmol)。将混合物在室温搅拌整夜。然后将其减压蒸发。将残余物通过硅胶柱色谱法(用1:100乙酸乙酯/石油醚洗脱)来纯化得到167b,其为黄色油状物(6.0g,46%)。MS:[M+H]+227.
实施例167c 3-氮杂三环[5.2.1.02,6]十碳-2(6),4-二烯-4-羧酸乙酯167c
向167b(5.0g,22mmol)于DMSO(30mL)中的溶液中加入NaN3(2.2g,33mmol)。将混合物在105℃加热6小时。在冷却降至室温后,向反应混合物中加入水(13mL)并将所得混合物用二氯甲烷(3X50mL)萃取。将合并的有机相用Na2SO4干燥并减压蒸干。将残余物通过硅胶柱色谱法来纯化(用20:1二氯甲烷/甲醇洗脱)得到167c,其为棕色固体(2.7g,60%)。MS:[M+H]+206.1H NMR(500MHz,CDCl3)δ11.51(s,1H),6.45(s,1H),4.16(q,J=6.5Hz,2H),3.26-3.24(m,2H),1.82-1.79(m,2H),1.74-1.72(m,2H),1.24(t,J=6.5Hz,3H),0.91-0.89(m,2H).
实施例167d 3-(氰基甲基)-3-氮杂三环[5.2.1.02,6]十碳-2(6),4-二烯-4-羧酸乙酯167d
在167c(3.0g,14.6mmol)于无水DMF(30mL)中的溶液中加入NaH(880mg,22mmol)。将混合物在室温搅拌30分钟。加入2-溴乙腈(3.5g,29.3mmol)并将所得混合物在65℃加热1小时。然后将其在室温搅拌整夜。反应后,加入水(30mL)并将所得混合物用乙酸乙酯(200mL×3)萃取。将合并的有机相减压蒸干。将残余物通过硅胶柱色谱法来纯化(用20:1二氯甲烷/甲醇洗脱)得到167d,其为棕色固体(2.6g,72%)。MS:[M+H]+245.
实施例167e 3-(2-氨基乙基)-3-氮杂三环[5.2.1.02,6]十碳-2(6),4-二烯-4-羧酸乙酯167e
将167d(4.0g,16mmol)和Raney Ni(400mg)于甲醇(60mL)中的悬浮液在帕尔装置中在50psi氢化整夜。将混合物用垫过滤并减压浓缩滤液。将残余物通过硅胶柱色谱法(用20:1二氯甲烷/甲醇洗脱)来纯化得到167e,其为黄色固体(2.0g,50%)。MS:[M+H]+249。
实施例167f 3,6-二氮杂四环[9.2.1.02,10.03,8]十四碳-2(10),8-二烯-7-酮167f
向167e(1.8g,7.2mmol)于乙醇(40mL)中的溶液中加入甲醇钠(2.5g,36mmol)。将混合物在65℃加热12小时。然后将其冷却至室温。将溶剂减压蒸干。将残余物通过硅胶柱色谱法(用20:1二氯甲烷/甲醇洗脱)来纯化得到外消旋体,其为棕色固体(800mg,53%),对其进行手性拆分得到167f和170a。MS:[M+H]+203。
实施例167g 4-氯-2-[(1S,11R)-7-氧代-3,6-二氮杂四环[9.2.1.02,10.03,8]十四碳-2(10),8-二烯-6-基]吡啶-3-甲醛167g
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(30mL)、167f(400mg,2.0mmol)、2-溴-4-氯吡啶-3-甲醛(1.30g,6.0mmol)和乙酸钾(390mg,4.0mmol)。使氮气鼓泡通过所得混合物30分钟后,加入Xantphos(110mg,0.20mmol)和三(二亚苄基丙酮)二钯(0)(180mg,0.20mmol)并将反应混合物在80℃加热10小时。然后将其冷却至室温并过滤。使滤液在乙酸乙酯(50mL)和水(30mL)之间分配。分离出水层并用乙酸乙酯(3X30mL)萃取。将合并的有机层用盐水(20mL)洗涤并用硫酸钠干燥。过滤除去干燥剂并减压浓缩滤液。将残余物用硅胶柱色谱法(用2:1石油醚/乙酸乙酯洗脱)来纯化得到167g(391mg,57%),其为黄色固体。MS-ESI:[M+H]+342.2
实施例167h 4-[1-甲基-5-({5-甲基-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]-2-[(1S,11R)-7-氧代-3,6-二氮杂四环[9.2.1.02,10.03 ,8]十四碳-2(10),8-二烯-6-基]吡啶-3-甲醛167h
在配备有回流冷凝器的100-mL圆底烧瓶中装入167g(150mg,0.44mmol)、1-甲基-3-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮135a(169mg,0.44mmol)、乙酸钠(72mg,0.88mmol)、K3PO4(234mg,0.88mmol)、PdCl2(dppf)(36mg,0.044mmol)、乙腈(20mL)和水(1mL)。在使氮气鼓泡通过所述混合物30分钟后,将其在氮气中在100℃加热3小时。将反应混合物冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用25:1二氯甲烷/甲醇洗脱)得到167h(132mg,53%),其为棕色固体。MS-ESI:[M+H]+565.3
实施例167 2-(3-(羟基甲基)-4-(1-甲基-5-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢-6,9-桥亚甲基吡嗪并[1,2-a]吲哚-1(2H)-酮167
向167h(120mg,0.21mmol)于甲醇(20mL)中的溶液中加入NaBH4(24mg,0.63mmol)。将混合物在20℃搅拌2小时。将反应混合物用水淬灭并减压浓缩。将残余物通过反相制备性-HPLC来纯化得到167(98mg,83%),其为黄色固体。MS-ESI:[M+H]+567.3.1H NMR(500MHz,DMSO-d6)δ8.48(d,J=5.0Hz,1H),8.19(s,1H),8.05(d,J=2.5Hz,1H),7.40(s,1H),7.32(d,J=5.0Hz,1H),6.53(d,J=5.5Hz,1H),5.89(s,1H),4.98(t,J=5.0Hz,1H),4.48-4.30(m,3H),4.27-4.22(m,2H),3.92-3.91(m,2H),3.86-3.84(m,1H),3.60(s,3H),3.52-3.33(m,3H),3.29(ps,1H),2.79-2.77(m,2H),2.35(s,3H),1.87-1.76(m,3H),1.60-1.59(m,1H),1.09-0.91(m,2H).
实施例168a 3-(6,7-二氢-4H-吡唑并[5,1-c][1,4]噁嗪-2-基氨基)-1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮168a
在配备有磁力搅拌子和回流冷凝器的250-mL圆底烧瓶中装入5-溴-3-(6,7-二氢-4H-吡唑并[5,1-c][1,4]噁嗪-2-基氨基)-1-甲基吡啶-2(1H)-酮129c(1.3g,4.0mmol)、双(频哪醇合)二硼烷(bis(pinacolato)diboron)(2.03g,8.0mmol)、PdCl2(dppf)(439mg,0.60mmol)、乙酸钾(784mg,8.0mmol)和1,4-二噁烷(60mL)的混合物。在使氮气鼓泡通过所述混合物30分钟后,将其回流加热15小时。反应结束后将混合物冷却至室温并过滤。将固体用乙酸乙酯(100mL)洗涤。将合并的滤液减压蒸发并将残余物通过硅胶柱色谱法(用30:1二氯甲烷/甲醇洗脱)来纯化得到168a(446mg,30%)。MS:[M+H]+373。
实施例168b 4-(1-甲基-5-(6,7-二氢-4H-吡唑并[5,1-c][1,4]噁嗪-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基)吡啶-3-甲醛168b
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入4-氯-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-甲醛108a(200mg,0.58mmol)、168a(433mg,1.16mmol)、PdCl2(dppf)(48mg,0.052mmol)、K3PO4(246mg,1.16mmol)、乙酸钠(96mg,1.16mmol)、乙腈(10mL)和水(0.5mL)。将体系排空并用氮气回填。将反应混合物在100℃搅拌2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用30:1二氯甲烷/甲醇洗脱)来纯化得到168b(250mg,78%),其为黄色固体。MS-ESI:[M+H]+554.6。
实施例168 2-[5-(6,7-二氢-4H-吡唑并[5,1-c][1,4]噁嗪-2-基氨基)-3'-羟基甲基-1-甲基-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基]-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮168
在0℃,向168b(200mg,0.36mmol)于甲醇(10mL)中的悬浮液中加入硼氢化钠(42mg,1.1mmol)。将反应混合物搅拌30分钟并用水(2mL)淬灭。然后将其减压浓缩并将残余物通过反相制备性-HPLC来纯化得到168(53mg,21%),其为黄色固体。MS-ESI:[M+H]+556.6。1H NMR(400MHz,CDCl3)δ8.46(d,J=5.2Hz,1H),7.97(d,J=2.4Hz,1H),7.71(d,J=2.0Hz,1H),7.45(s,1H),7.33(d,J=5.2Hz,1H),6.83(s,1H),5.71(s,1H),5.04-5.01(m,1H),4.78(s,2H),4.64-4.62(m,1H),4.49(d,J=2.8Hz,1H),4.32-4.28(m,1H),4.14(d,J=4.4Hz,2H),4.09-4.08(m,4H),3.87-3.83(m,1H),3.70(s,3H),2.56(d,J=2.8Hz,2H),2.50(s,2H),1.26(s,6H).
实施例169a 4-氯-2-{6-氧代-8-硫杂-5-氮杂三环[7.4.0.02,7]十三碳-1(9),2(7)-二烯-5-基}吡啶-3-甲醛169a
在配备有回流冷凝器的100-mL单颈圆底烧瓶中装入2-溴-4-氯吡啶-3-甲醛103a(1276mg,5.80mmol)、8-硫杂-5-氮杂三环[7.4.0.02,7}]十三碳-1(9),2(7)-二烯-6-酮105e(600mg,2.90mmol)、CuI(551mg,2.90mmol)、K2CO3(800mg,5.80mmol)、4,7-二甲氧基-1,10-菲咯啉(696mg,2.90mmol)和二噁烷(20mL)。在使氮气鼓泡通过所得溶液10分钟后,将混合物在95℃搅拌16小时。然后将其冷却至室温并过滤。向残余物中加入水(20mL)。分离出水层并用乙酸乙酯(3×20mL)萃取。将合并的有机层用盐水(50mL)洗涤并用硫酸钠干燥。过滤除去干燥剂并减压浓缩滤液。将残余物通过硅胶柱色谱法(用10:1石油醚/乙酸乙酯洗脱)来纯化得到169a(171mg,17%)。LCMS-ESI:[M+H]+347
实施例169b 4-[1-甲基-5-({5-[4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]-2-{6-氧代-8-硫杂-5-氮杂三环[7.4.0.02,7]十三碳-1(9),2(7)-二烯-5-基}吡啶-3-甲醛169b
在50-mL配备有回流冷凝器的单颈圆底烧瓶中装入169a(150mg,0.43mmol)、3-(5-(2-乙基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮101l(200mg,0.43mmol)、Pd2(dba)3(37mg,0.040mmol)、三环己基膦(120mg,0.43mmol)、Cs2CO3(281mg,0.86mmol)、二噁烷(10mL)和水(0.1mL)。在经历三轮真空/氩气吹洗后,将混合物在110℃加热4小时。然后将其过滤并减压蒸发滤液。将残余物通过硅胶柱色谱法(用1:3石油醚/乙酸乙酯洗脱)来纯化得到169b,其为黄色固体(45mg,16%)。LCMS-ESI:[M+H]+652
实施例169 2-{3'-羟基甲基-1-甲基-5-[5-(4-氧杂环丁烷-3-基-哌嗪-1-基)-吡啶-2-基氨基]-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基}-3,4,5,6,7,8-六氢-2H-苯并[4,5]噻吩并[2,3-c]吡啶-1-酮169
将169b(45mg,0.070mmol)、NaBH4(8mg,0.21)和甲醇(5mL)的混合物在室温搅拌1小时。将反应混合物用水(5mL)淬灭并减压浓缩。将残余物用二氯甲烷(2X10mL)萃取。将合并的二氯甲烷萃取物减压浓缩。将残余物用反相制备性-HPLC来纯化得到169(14mg,30%)。LCMS-ESI:[M+H]+654。1H NMR(500MHz,DMSO-d6)δ8.62(s,1H),8.50(d,J=2.0Hz,1H),8.43(s,1H),7.86(d,J=4.5Hz,1H),7.45(d,J=2.5Hz,1H),7.39-7.34(m,2H),7.25-7.22(m,1H),4.95-4.93(m,1H),4.57-4.55(m,2H),4.47-4.41(m,4H),4.19-4.17(m,1H),3.82-3.80(m,1H),3.60(s,3H),3.45-3.43(m,1H),3.32-3.30(m,1H),3.09-3.07(m,4H),3.01-2.90(m,1H),2.89-2.88(m,1H),2.80-2.79(m,2H),2.51-2.50(m,1H),2.40-2.38(m,4H),1.83-1.80(m,4H).
实施例170b 4-氯-2-[(1R,11S)-7-氧代-3,6-二氮杂四环[9.2.1.02,10.03,8]十四碳-2(10),8-二烯-6-基]吡啶-3-甲醛170b
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(30mL)、(1S,11R)-3,6-二氮杂四环[9.2.1.02,10.03,8]十四碳-2(10),8-二烯-7-酮170a(400mg,2.0mmol)、2-溴-4-氯吡啶-3-甲醛103a(1.30g,6.0mmol)和乙酸钾(390mg,4.0mmol)。使氮气鼓泡通过所得混合物30分钟后,加入Xantphos(110mg,0.20mmol)和三(二亚苄基丙酮)二钯(0)(180mg,0.20mmol),并将反应混合物在80℃加热10小时。之后,将反应混合物冷却至室温并过滤。使滤液在乙酸乙酯(50mL)和水(30mL)之间分配。分离出水层并用乙酸乙酯(3X30mL)萃取。将合并的有机层用盐水(20mL)洗涤并用硫酸钠干燥。过滤除去干燥剂并减压浓缩滤液。将残余物通过硅胶柱色谱法(用2:1石油醚/乙酸乙酯洗脱)来纯化得到170b(405mg,59%),其为黄色固体。MS-ESI:[M+H]+342.2
实施例170c 4-[1-甲基-5-({5-甲基-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]-2-[(1R,11S)-7-氧代-3,6-二氮杂四环[9.2.1.02,10.03 ,8]十四碳-2(10),8-二烯-6-基]吡啶-3-甲醛170c
在配备有回流冷凝器的100-mL圆底烧瓶中装入170b(150mg,0.44mmol)、1-甲基-3-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮135a(169mg,0.44mmol)、乙酸钠(72mg,0.88mmol)、K3PO4(234mg,0.88mmol)、Pd(dppf)Cl2(36mg,0.044mmol)、乙腈(20mL)和水(1mL)。在使氮气鼓泡通过反应混合物30分钟后,将其在100℃加热3小时。将反应混合物减压蒸发并将残余物通过硅胶柱色谱法(用25:1二氯甲烷/甲醇洗脱)来纯化得到170c(146mg,52%),其为棕色固体。MS-ESI:[M+H]+565.3
实施例170 2-(3-(羟基甲基)-4-(1-甲基-5-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢-6,9-桥亚甲基吡嗪并[1,2-a]吲哚-1(2H)-酮170
在170c(122mg,0.22mmol)于甲醇(20mL)中的溶液中加入NaBH4(24mg,0.64mmol)。将混合物在20℃搅拌2小时。将反应混合物减压蒸发并将残余物通过反相制备性-HPLC来纯化得到标题化合物(98mg,75%),其为白色固体。MS-ESI:[M+H]+567.3.1H NMR(500MHz,DMSO-d6)δ8.48(d,J=5.0Hz,1H),8.19(s,1H),8.05(d,J=2.5Hz,1H),7.40(s,1H),7.32(d,J=5.0Hz,1H),6.53(s,1H),5.89(s,1H),4.98(t,J=5.0Hz,1H),4.48-4.30(m,3H),4.27-4.22(m,2H),3.92-3.91(m,2H),3.86-3.84(m,1H),3.59(s,3H),3.49-3.47(m,3H),3.30-3.28(m,1H),2.79-2.77(m,2H),2.35(s,3H),1.87-1.76(m,3H),1.61-1.59(m,1H),1.09-0.88(m,2H).
实施例171a 4-[1-甲基-5-({5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]-2-[(1S,11R)-7-氧代-3,6-二氮杂四环[9.2.1.02,10.03,8]十四碳-2(10),8-二烯-6-基]吡啶-3-甲醛171a
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入乙腈(30mL)、4-氯-2-[(1S,11R)-7-氧代-3,6-二氮杂四环[9.2.1.02,10.03,8]十四碳-2(10),8-二烯-6-基]吡啶-3-甲醛167g(170mg,0.50mmol)、(S)-1-甲基-3-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮130f(336mg,0.70mmol)、水(3mL)和乙酸钾(147mg,1.5mmol)。在使氩气鼓泡通过所述悬浮液30分钟后,加入1,1’-二(二苯基膦基)二茂铁二氯化钯(II)(408mg,0.05mmol)。使体系经历三轮真空/氩气吹洗并在80℃加热3小时。然后将其冷却至室温并过滤。将固体用二氯甲烷(2X100ml)洗涤。将合并的滤液减压浓缩并将残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(50:1至30:1)洗脱)来纯化得到171a(95mg,29%),其为浅黄色固体。MS-ESI:[M+H]+661.3
实施例171(S)-2-(3-(羟基甲基)-4-(1-甲基-5-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢-6,9-桥亚甲基吡嗪并[1,2-a]吲哚-1(2H)-酮171
在室温,向171a(90mg,0.136mmol)于甲醇(10mL)中的溶液中加入NaBH4(26mg,0.7mmol)。在将反应混合物搅拌1小时后,LCMS表明反应完成。将其用水(30mL)淬灭并减压浓缩。将残余物用二氯甲烷(3X30mL)萃取。将合并的有机层用盐水(30mL)洗涤,用Na2SO4干燥,过滤并减压浓缩。将残余固体通过反相制备性-HPLC来纯化得到171(35mg,31.5%),其为浅黄色固体。MS-ESI:[M+H]+663.3。1H NMR(500MHz,DMSO-d6)δ8.62(s,1H),8.48(d,J=5.0Hz,1H),8.44(s,1H),7.83(d,J=2.5Hz,1H),7.47(s,1H),7.38(dd,J=2.5,9.0Hz 1H),7.34(d,J=5.0Hz,1H),7.24(d,J=9.5Hz,1H),6.51(s,1H),4.97(t,J=4.5Hz,1H),4.58-4.54(m,2H),4.50-4.37(m,4H),4.30-4.24(m,2H),3.86-3.84(m,1H),3.69-3.67(m,1H),3.60(s,3H),3.47(s,1H),3.42-3.37(m,1H),3.30(s,2H),3.10-3.07(m,1H),2.95-2.92(m,1H),2.36-2.29(m,3H),2.21-2.16(m,1H),1.88-1.754(m,3H),1.60-1.58(m,1H),1.08-1.05(m,1H),0.98-0.96(m,1H),0.93(d,J=6.0Hz,3H).
实施例172a 3-(1,2,4-三嗪-3-基氨基)-5-溴-1-甲基吡啶-2(1H)-酮172a
在配备有磁力搅拌子和回流冷凝器的500-mL单颈圆底烧瓶中装入1,4-二噁烷(100mL)、1,2,4-三嗪-3-胺(1.5g,15.6mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(4.2g,15.6mmol)、Pd2(dba)3(458mg,1.56mmol)、XantPhos(1.8g,3.12mmol)和碳酸铯(10g,31.2mmol)。在经历三轮真空/氩气吹洗后,将混合物在90℃搅拌2.5小时。之后,将反应混合物过滤并真空蒸发滤液。将所得残余物用乙酸乙酯重结晶得到172a,其为黄色固体(1.76g,40%)。MS-ESI:[M+H]+282。
实施例172b乙酸(4-(5-(1,2,4-三嗪-3-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯172b
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入172a(200mg,0.71mmol)、3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113i(272mg,0.71mmol)、Pd(dppf)Cl2(58mg,0.071mmol)、乙酸钠(193mg,1.42mmol)、K3PO4(321mg,1.42mmol)、水(0.5mL)和乙腈(10mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃搅拌3小时。之后,将反应混合物过滤并真空蒸发滤液。将所得残余物用乙酸乙酯重结晶得到172b,其为黄色固体(380mg,99%)。MS-ESI:[M+H]+541.2
实施例172 2-(4-(5-(1,2,4-三嗪-3-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-3-(羟基甲基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮172
将172b(350mg,0.65mmol)和氢氧化锂(273mg,6.5mmol)于异丙醇/THF(1:1,5mL)和水(0.5mL)中的混合物在36℃搅拌0.5小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物通过反相制备性-HPLC来洗涤得到172(90mg,28%)。MS-ESI:[M+H]+499.2.1H NMR(500MHz,CDCl3)δ8.77(d,J=2.5Hz,1H),8.72(d,J=2.0Hz,1H),8.67(s,1H),8.50(d,J=5.0Hz,1H),8.34(d,J=2.0Hz,1H),8.05(d,J=2.5Hz,1H),7.35(d,J=5.0Hz,1H),6.89(s,1H),5.10(t,J=6.5Hz,1H),4.65-4.51(m,2H),4.31-4.27(m,1H),4.16-4.08(m,2H),3.90-3.87(m,1H),3.75(s,3H),2.62-2.56(m,4H),1.92-1.87(m,2H),1.79-1.78(m,2H).
实施例173a 5-溴-3-(2,6-二甲基嘧啶-4-基氨基)-1-甲基吡啶-2(1H)-酮173a
在配备有磁力搅拌子和回流冷凝器的250-mL单颈圆底烧瓶中装入1,4-二噁烷(150mL)、2,6-二甲基嘧啶-4-胺(2.5g,20.3mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(5.4g,20.3mmol)、Pd2(dba)3(1.86mg,2.03mmol)、XantPhos(2.3g,4.06mmol)和碳酸铯(13.2g,40.6mmol)。在经历三轮真空/氩气吹洗后,将混合物在90℃加热2.5小时。之后,将反应混合物过滤并真空蒸发滤液。将所得残余物用乙酸乙酯重结晶得到173a,其为黄色固体(4.4g,40%)。MS-ESI:[M+H]+309.0.
实施例173b 3-(2,6-二甲基嘧啶-4-基氨基)-1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮173b
在配备有磁力搅拌子和回流冷凝器的单颈圆底烧瓶250-mL中装入173a(1.5g,4.9mmol)、Pin2B2(6.2g,24.5mmol)、Pd2(dba)3(449mg,0.49mmol)、X-phos(467mg,0.98mmol)、乙酸钾(1.4g,14.7mmol)和二噁烷(60mL)。在经历三轮真空/氩气吹洗后,将混合物在65℃加热16小时。将反应混合物过滤并真空蒸发滤液。将所得残余物用乙酸乙酯重结晶得到173b,其为浅灰色固体(1.2g,72%)。MS-ESI:[M+H]+357.2.
实施例173c 2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{5-[(2,6-二甲基嘧啶-4-基)氨基]-1-甲基-6-氧代-1,6-二氢吡啶-3-基}吡啶-3-甲醛173c
在配备有磁力搅拌子和回流冷凝器的100-mL圆底烧瓶中装入173b(250mg,0.70mmol)、4-氯-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-甲醛108a(240mg,0.70mmol)、Pd(dppf)Cl2(57mg,0.071mmol)、乙酸钠(19mg,1.4mmol)、K3PO4(316mg,1.4mmol)、水(0.5mL)和乙腈(15mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热3小时。之后,将反应混合物过滤并真空蒸发滤液。将所得残余物用乙酸乙酯重结晶得到173c,其为棕色固体(300mg,80%)。MS-ESI:[M+H]+538.3。
实施例173 2-[5-(2,6-二甲基-嘧啶-4-基氨基)-3'-羟基甲基-1-甲基-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基]-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮173
在0℃,向173c(290mg,0.54mmol)于甲醇(5mL)中的溶液中加入硼氢化钠(62mg,1.62mmol)。将反应混合物在室温搅拌20分钟并用水(1mL)淬灭。然后将其减压浓缩并将残余物通过反相制备性-HPLC来纯化得到173,其为白色固体(50mg,17%)。MS-ESI:[M+H]+540.3.1H NMR(500MHz,CDCl3)δ8.90(d,J=2.5Hz,1H),8.51(d,J=5.0Hz,1H),8.01(d,J=2.0Hz,1H),8.00(s,1H),7.35(d,J=5.5Hz,1H),6.85(s,1H),6.45(s,1H),5.16-5.13(m,1H),4.67-4.52(m,2H),4.33-4.29(m,1H),4.16(d,J=5.0Hz,2H),3.90-3.86(m,1H),3.72(s,3H),2.58-2.56(m,重叠,5H),2.51(s,2H),2.40(s,3H),2.02(s,6H).
实施例174a 4-[1-甲基-5-({5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]-2-[(1R,11S)-7-氧代-3,6-二氮杂四环[9.2.1.02,10.03,8]十四碳-2(10),8-二烯-6-基]吡啶-3-甲醛174a
在圆底烧瓶中装入4-氯-2-[(1R,11S)-7-氧代-3,6-二氮杂四环[9.2.1.02,10.03 ,8]十四碳-2(10),8-二烯-6-基]吡啶-3-甲醛170b(200mg,0.59mmol)、1-甲基-3-({5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)-1,2-二氢吡啶-2-酮191j(400mg,0.88mmol)、PdCl2(dppf)(50mg,0.06mmol)、三水合K3PO4(300mg,1.20mmol)、乙酸钠(100mg,1.20mmol)、乙腈(15mL)和水(1.5mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热3小时。然后将其过滤并减压蒸发滤液。将残余物用硅胶柱色谱法(用1:20甲醇/二氯甲烷洗脱)来纯化得到174a,其为红色固体(170mg,44%)。MS-ESI:[M+H]+661.3
实施例174(1R,11S)-6-[3-(羟基甲基)-4-[1-甲基-5-({5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]吡啶-2-基]-3,6-二氮杂四环[9.2.1.02,10.03,8]十四碳-2(10),8-二烯-7-酮174
将174a(150mg,0.23mmol)、NaBH4(34mg,0.90)和甲醇(10mL)的混合物在室温搅拌1小时。将混合物用水(30ml)淬灭并减压浓缩。将残余物用二氯甲烷(2X10mL)萃取。将合并的二氯甲烷萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到174(42mg,28%)。MS-ESI:[M+H]+663.3.1H NMR(500MHz,CDCl3)δ8.65(d,J=3.0Hz,1H),8.48(d,J=6.0Hz,1H),7.96(d,J=2.5Hz,1H),7.85-7.84(m,2H),7.36(d,J=6.5Hz,1H),7.32(dd,J=3.5,11.0Hz,1H),6.82-6.80(m,2H),5.16-5.06(m,1H),4.72-4.61(m,5H),4.08-4.05(m,1H),4.32-4.21(m,3H),3.88-3.85(m,1H),3.71(s,3H),3.54-3.50(m,2H),3.38-3.37(m,2H),3.08-3.06(m,2H),2.57-2.54(m,1H),2.48-2.45(m,2H),2.21-2.17(m,1H),1.93-1.91(m,3H),1.66-1.64(m,1H),1.14-1.08(m,2H),0.98(d,J=8.0Hz,3H).
实施例175a 4-氯-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-甲醛175a
在配备有磁力搅拌子和回流冷凝器的250-mL单颈圆底烧瓶中装入4-氯-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-甲醛124a(150mg,0.43mmol)、3-(5-(2-乙基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮161f(215mg,0.43mmol)、PdCl2(dppf)(33mg,0.040mmol)、K3PO4三水合物(202mg,0.86mmol)、乙酸钠(71mg,0.86mmol)、乙腈(10mL)和水(2mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热3小时。然后将其过滤并减压蒸发滤液。将残余物通过硅胶柱色谱法(用1:3石油醚/乙酸乙酯洗脱)来纯化得到175a,其为黄色固体(108mg,37%)。MS-ESI:[M+H]+679
实施例175 3-{5-[5-((S)-2-乙基-4-氧杂环丁烷-3-基-哌嗪-1-基)-吡啶-2-基氨基]-3'-羟基甲基-1-甲基-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基}-6,7,8,9-四氢-3H-苯并[4,5]噻吩并[2,3-d]哒嗪-4-酮175
将175a(200mg,0.16mmol)、NaBH4(18mg,0.48)和甲醇(8mL)的混合物在25℃搅拌1小时。将反应混合物用水(10mL)淬灭并减压蒸发。将残余物用二氯甲烷(2X10mL)萃取。将合并的二氯甲烷萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到175(55mg,50%)。MS-ESI:[M+H]+681.1H NMR(500MHz,DMSO-d6)8.61(d,J=2.0Hz,1H),8.57-8.56(m,1H),8.47(s,1H),8.43(s,1H),7.83(d,J=3.0Hz,1H),7.54-7.53(m,1H),7.47(d,J=2.0Hz,1H),7.35-7.32(m,1H),7.24-7.22(m,1H),4.85-4.83(m,1H),4.59-4.55(m,2H),4.47-4.44(m,1H),4.40-4.36(m,2H),3.60(s,3H),3.51-3.49(m,1H),3.40-3.38(m,1H),3.17-3.14(m,1H),3.00-2.95(m,3H),2.87-2.85(m,2H),2.66-2.60(m,1H),2.55-2.53(m,1H),2.18-2.15(m,1H),2.10-2.06(m,1H),1.89-1.86(m,4H),1.68-1.64(m,1H),1.28-1.25(m,2H),0.79(t,J=9.5Hz,3H).
实施例176a(S)-4-(1-甲基-5-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-6,7,8,9-四氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛176a
在圆底烧瓶中装入4-氯-2-(1-氧代-6,7,8,9-四氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛121a(180mg,0.55mmol)、(S)-1-甲基-3-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮191j(397mg,0.82mmol)、PdCl2(dppf)(45mg,0.06mmol)、K3PO4三水合物(286mg,1.10mmol)、乙酸钠(90mg,1.10mmol)、乙腈(15mL)和水(1.5mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热3小时。然后将其过滤并减压蒸发滤液。将残余物通过硅胶柱色谱法来纯化(用1:20甲醇/二氯甲烷洗脱)得到176a,其为红色固体(228mg,64%)。MS-ESI:[M+H]+647.3
实施例176(S)-2-(3-(羟基甲基)-4-(1-甲基-5-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-6,7,8,9-四氢吡嗪并[1,2-a]吲哚-1(2H)-酮176
将176a(200mg,0.31mmol)、NaBH4(47mg,1.20)和甲醇(10mL)的混合物在室温搅拌1小时。然后将反应混合物用水(10mL)淬灭并减压浓缩。将残余物用二氯甲烷(2X10mL)萃取。将合并的二氯甲烷萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到176(42mg,28%)。MS-ESI:[M+H]+649.3.1H NMR(500MHz,DMSO-d6)δ8.66(d,J=2.5Hz,1H),8.56(d,J=5.5Hz,1H),8.47(s,1H),7.84(d,J=2.5Hz,1H),7.50-7.48(m,2H),7.39-7.36(m,1H),7.26-7.24(m,2H),6.83-6.80(m,2H),4.57-4.54(m,2H),4.48-4.40(m,3H),4.35-4.33(m,1H),3.69-3.67(m,1H),3.60(s,3H),3.41-3.38(m,2H),3.11-3.08(m,1H),2.97-2.93(m,1H),2.76-2.74(m,2H),2.62-2.60(m,2H),2.52-2.51(m,1H),2.35-2.32(m,2H),2.19-2.17(m,1H),1.90-1.87(m,2H),1.77-1.75(m,2H),0.94(d,J=6.5Hz,3H).
实施例177a乙酸(4-(5-(5-乙基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯177a
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入5-溴-3-(5-乙基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-1-甲基吡啶-2(1H)-酮208c(300mg,0.85mmol)、3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113i(1.21g,3.16mmol)、PdCl2(dppf)(35mg,0.043mmol)、K3PO4(361mg,1.70mmol)、乙酸钠(140mg,1.70mmol)、乙腈(10mL)和水(0.5mL)。将体系排空并用氮气回填。将反应混合物在100℃搅拌2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用30:1二氯甲烷/甲醇洗脱)来纯化得到177a(365mg,60%),其为棕色油状物。MS-ESI:[M+H]+611
实施例177 2-(4-(5-(5-乙基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-3-(羟基甲基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮177
向177a(300mg,0.49mmol)于丙烷-2-醇(4mL)、四氢呋喃(4mL)和水(1mL)中的溶液中加入氢氧化锂(35mg,1.47mmol)。将混合物在室温搅拌0.5小时。将其蒸发并将残余物通过反相制备性-HPLC来纯化得到177(79mg,28%),其为白色固体。MS-ESI:[M+H]+569.1H NMR(500MHz,CDCl3)δ8.46(d,J=5.5Hz,1H),7.92(d,J=2.0Hz,1H),7.70(d,J=2.0Hz,1H),7.39(s,1H),7.33(d,J=5.5Hz,1H),6.88(s,1H),5.69(s,1H),4.99-4.97(m,1H),4.61-4.60(m,1H),4.48-4.46(m,1H),4.33-4.31(m,1H),4.14-4.06(m,4H),3.87-3.85(m,1H),3.69(s,3H),3.62(d,J=5.5Hz,2H),2.91(d,J=5.0Hz,2H),2.63-2.55(m,6H),1.91-1.87(m,2H),1.79-1.78(m,2H),1.17(t,J=7.5Hz,3H).
实施例178a 5-溴-1-甲基-3-(吡啶-2-基氨基)吡啶-2(1H)-酮178a
在配备有磁力搅拌子和回流冷凝器的250-mL单颈圆底烧瓶中装入1,4-二噁烷(60mL)、5-溴-2-硝基吡啶(8.0g,31.8mmol)、吡啶-2-胺(1.0g,10.6mmol)和碳酸铯(7.0g,21.2mmol)。使氮气鼓泡通过所得混合物30分钟后,加入XantPhos(616mg,1.0mmol)和三(二亚苄基丙酮)二钯(0)(973mg,1.0mmol)。使反应混合物经历三轮真空/氩气吹洗并在100℃加热12小时。之后,将反应混合物冷却至室温并过滤。使滤液在乙酸乙酯(100mL)和水(100mL)之间分配。分离出水层并用乙酸乙酯(3X150mL)萃取。将合并的有机层用盐水(50mL)洗涤并用硫酸钠干燥。过滤除去干燥剂并减压浓缩滤液。将残余物在硅胶柱上纯化(用30:1二氯甲烷/甲醇洗脱)得到178a(1.5g,51%),其为黄色固体。MS:[M+H]+280
实施例178b 1-甲基-3-(吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮178b
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入178a(1.06g,3.8mmol)、Pin2B2(4.8g,19.0mmol)、Pd2(dba)3(348mg,0.38mmol)、X-Phos(350mg,0.76mmol)、乙酸钾(1.12g,11.40mmol)和二噁烷(30mL)。在经历三轮真空/氩气吹洗后,将混合物在60℃加热6小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用3:1石油醚/乙酸乙酯洗脱)来纯化得到178b,其为黄色固体(1.2g,96%)。MS-ESI:[M+H]+328.2
实施例178c 4-{1-甲基-6-氧代-5-[(吡啶-2-基)氨基]吡啶-3-基}-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-甲醛178c
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入178b(131mg,0.40mmol)、4-氯-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-甲醛124a(138mg,0.40mmol)、Pd(dppf)Cl2(33mg,0.040mmol)、K3PO4(170mg,0.80mmol)、乙酸钠(66mg,0.80mmol)、水(6滴)和乙腈(10mL)。在经历三轮真空/氩气吹洗后,将混合物回流加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用30:1二氯甲烷/甲醇洗脱)来纯化得到178c,其为黄色固体(180mg,88%)。MS-ESI:[M+H]+511.2
实施例178 3-[3'-羟基甲基-1-甲基-6-氧代-5-(吡啶-2-基氨基)-1,6-二氢-[3,4']联吡啶-2'-基]-6,7,8,9-四氢-3H-苯并[4,5]噻吩并[2,3-d]哒嗪-4-酮178
在0℃,向178c(179mg,0.35mmol)于甲醇(6mL)中的溶液中加入硼氢化钠(39mg,1.05mmol)。将反应混合物搅拌30分钟并用水(1.0mL)淬灭。然后将其减压浓缩并将残余物通过反相制备性-HPLC来纯化得到178(100mg,56%)。MS-ESI:[M+H]+513.3.1H NMR(500MHz,CDCl3)δ8.81(s,1H),8.68(d,J=5.0Hz,1H),8.32(s,1H),8.27(d,J=4.0Hz,1H),7.94(bs,1H),7.76(d,J=1.5Hz,1H),7.58-7.56(m,2H),6.85-6.80(m,2H),4.47-4.45(m,2H),4.38-4.36(m,1H),3.74(s,3H),3.01-2.99(m,2H),2.89-2.87(m,2H),2.02-1.99(m,4H).
实施例179a 4-(1-甲基-5-(2-甲基嘧啶-4-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基)吡啶-3-甲醛179a
在配备有回流冷凝器的50-mL圆底烧瓶中装入1-甲基-3-(2-甲基嘧啶-4-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮213b(510mg,1.5mmol)、4-氯-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-甲醛108a(343mg,1.0mmol)、K3PO4(424mg,2.0mmol)、乙酸钠(272mg,2.0mmol)、1,1’-二(二苯基膦基)二茂铁二氯化钯(II)(40mg,0.044mmol)、乙腈(20mL)和水(0.5mL)。在使氮气鼓泡通过所述混合物30分钟后,将其在氮气保护下在100℃加热2小时。通过LCMS分析反应混合物,显示完全转化成所期望的产物。将反应混合物冷却至室温并过滤。减压浓缩滤液。将残余物用二氯甲烷(30mL)和水(30mL)稀释。分离出水层并用二氯甲烷(3×20mL)萃取。将合并的有机层用Na2SO4干燥,过滤并减压浓缩。将黑色残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(80/1至30/1)洗脱)来纯化得到179a(300mg,57%),其为黄色固体。MS-ESI:[M+H]+524
实施例179 2-[3'-羟基甲基-1-甲基-5-(2-甲基-嘧啶-4-基氨基)-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基]-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮179
在室温,向179a(262mg,0.50mmol)于甲醇/二氯甲烷(10/10mL)中的溶液中加入NaBH4(57mg,1.5mmol)。在将反应混合物搅拌1小时后,LCMS表明反应完成。然后将混合物减压浓缩。将残余物用水(5mL)和二氯甲烷(20mL)稀释。分离出水相并用二氯甲烷(3X10mL)萃取。将合并的有机层用盐水(30mL)洗涤,用Na2SO4干燥,过滤并减压浓缩。将残余固体通过反相制备性-HPLC来纯化得到179(180mg,69%),其为白色固体。MS-ESI:[M+H]+526.1H NMR(500MHz,CDCl3)δ8.93(d,J=2.0Hz,1H),8.53(d,J=5.5Hz,1H),8.28(d,J=5.5Hz,1H),8.07(s,1H),8.03(d,J=2.0Hz,1H),7.36(s,1H),6.86(s,1H),6.60(d,J=6.0Hz,1H),5.18-5.16(m,1H),4.70-4.67(m,1H),4.55-4.53(m,1H),4.33-4.31(m,1H),4.18-4.16(m,2H),3.91-3.90(m,1H),3.74(s,3H),2.60(s,3H),2.58(d,J=5.5Hz,2H),2.52(s,2H),1.28(s,6H).
实施例180a 5-溴-1-甲基-3-(6-甲基嘧啶-4-基氨基)吡啶-2(1H)-酮180a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入6-甲基嘧啶-4-胺(800mg,2.6mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(694mg,2.6mmol)、三(二亚苄基丙酮)二钯(0)(238mg,0.26mmol)、XantPhos(300mg,0.52mmol)、Cs2CO3(1.7g,5.2mmol)和1,4-二噁烷(30mL)。在经历三轮真空/氩气吹洗后,将混合物在90℃加热2.5小时。将混合物冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用50:1二氯甲烷/甲醇洗脱)来纯化得到180a,其为黄色固体(800mg,36%)。MS-ESI:[M+H]+295.1
实施例180b 1-甲基-3-(6-甲基嘧啶-4-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮180b
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入180a(1.0g,3.4mmol)、Pin2B2(4.3g,17mmol)、Pd2(dba)3(312mg,0.34mmol)、X-phos(324mg,0.68mmol)、乙酸钾(666mg,6.8mmol)和二噁烷(40mL)。在经历三轮真空/氩气吹洗后,将混合物在65℃加热14小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物用3:1石油醚/乙酸乙酯(80mL)洗涤得到180b,其为黄色固体(600mg,50%)。MS-ESI:[M+H]+343.2.
实施例180c 2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{1-甲基-5-[(6-甲基嘧啶-4-基)氨基]-6-氧代-1,6-二氢吡啶-3-基}吡啶-3-甲醛180c
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入180b(239mg,0.70mmol)、4-氯-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-甲醛108a(239mg 0.70mmol)、Pd(dppf)Cl2(57mg,0.070mmol)、乙酸钠(115mg,1.4mmol)、K3PO4(320mg,1.4mmol)、水(5mL)和乙腈(15mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热3小时。之后,将反应混合物过滤并减压浓缩滤液。将所得残余物通过硅胶柱色谱法(用40:1二氯甲烷/甲醇洗脱)来纯化得到180c,其为黄色固体(170mg,47%)。MS-ESI:[M+H]+524.2.
实施例180 2-[3'-羟基甲基-1-甲基-5-(6-甲基-嘧啶-4-基氨基)-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基]-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮180
在0℃,向180c的溶液中加入水(1mL)。然后将其减压浓缩并将残余物通过反相制备性-HPLC来纯化得到180(47mg,32%)。MS-ESI:[M+H]+526.2.1H NMR(500MHz,CDCl3)δ8.82(d,J=2.5Hz,1H),8.68(s,1H),8.51(d,J=2.5Hz,1H),8.02-8.00(m,2H),7.35(d,J=5.0Hz,1H),6.84(s,1H),6.62(s,1H),5.13(t,J=6.5Hz,1H),4.67-4.52(m,2H),4.29-4.15(m,3H),3.88-3.86(m,1H),3.72(s,3H),2.57(d,J=5.5Hz,2H),2.51(s,2H),2.43(s,3H),1.28(s,6H)。
实施例181a 4-[1-甲基-5-({5-甲基-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-甲醛181a
在配备有回流冷凝器的100-mL单颈圆底烧瓶中装入4-氯-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-甲醛124a(210mg,0.60mmol)、1-甲基-3-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮135a(346mg,0.90mmol)、Pd(dppf)Cl2(30mg,0.030mmol)、K3PO4(270mg,1.2mmol)、乙酸钠三水合物(180mg,1.2mmol)、水(6滴)和乙腈(40mL)。将体系排空并用氮气回填。将反应混合物在100℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用25:1二氯甲烷/甲醇洗脱)来纯化得到181a(300mg,88%),其为棕黄色固体。MS-ESI:[M+H]+569.3.
实施例181 3-[3'-羟基甲基-1-甲基-5-(5-甲基-4,5,6,7-四氢-吡唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基]-6,7,8,9-四氢-3H-苯并[4,5]噻吩并[2,3-d]哒嗪-4-酮181
将181a(300mg,0.50mmol)和NaBH4(60mg,1.5mmol)于甲醇(20mL)中的混合物在30℃搅拌1小时。将混合物用水淬灭并减压浓缩。将残余物用乙酸乙酯(3X10mL)萃取。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到181(100mg,35%)。MS-ESI:[M+H]+571.2.1H NMR(500MHz,CHCl3)δ8.64(d,J=5.0Hz,1H),8.30(s,1H),8.00(d,J=2.0Hz,1H),7.57(d,J=2.0Hz,1H),7.53(d,J=5.0Hz,1H),7.43(s,1H),5.70(s,1H),4.45-4.43(m,2H),4.32(bs,1H),4.11-4.09(m,2H),3.71(s,3H),3.63(s,2H),2.99-2.97(m,2H),2.93-2.91(m,2H),2.88-2.86(m,2H),2.50(s,3H),2.00-1.98(m,4H).
实施例182a 4-{1-甲基-6-氧代-5-[(嘧啶-4-基)氨基]-1,6-二氢吡啶-3-基}-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-甲醛182a
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入4-氯-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-甲醛124a(345mg,1.0mmol)、1-甲基-3-(嘧啶-4-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮143a(328mg,1.0mmol)、Pd(dppf)Cl2(82mg,0.10mmol)、乙酸钠(162mg,2.0mmol)、K3PO4(424mg,2.0mmol)和乙腈/水(20/1mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热3小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用40:1二氯甲烷/甲醇洗脱)来纯化得到182a,其为黄色固体(156mg,30%)。MS-ESI:[M+H]+512.1.
实施例182 3-[3'-羟基甲基-1-甲基-6-氧代-5-(嘧啶-4-基氨基)-1,6-二氢-[3,4']联吡啶-2'-基]-6,7,8,9-四氢-3H-苯并[4,5]噻吩并[2,3-d]哒嗪-4-酮182
在室温,向182a(140mg,0.27mmol)于甲醇(5mL)中的溶液中加入硼氢化钠(31mg,0.82mmol)。将反应混合物搅拌20分钟并用水(1mL)淬灭。然后将其减压浓缩并将残余物通过硅胶柱色谱法(用60:1二氯甲烷/甲醇洗脱)来纯化得到182,其为白色固体(60mg,43%)。MS-ESI:[M+H]+514.2.1H NMR(500MHz,CDCl3)δ8.89(d,J=2.5Hz,1H),8.82(s,1H),8.70(d,J=5.5Hz,1H),8.36(d,J=6.5Hz,1H),8.31(s,1H),8.20(s,1H),7.89(d,J=2.0Hz,1H),7.55(d,J=5.0Hz,1H),6.80(d,J=9.5Hz,1H),4.44-4.42(m,3H),3.75(s,3H),2.99-2.98(m,2H),2.88-2.87(m,2H),2.03-1.98(m,4H).
实施例183a 2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)-4-(1-甲基-6-氧代-5-(吡啶-2-基氨基)-1,6-二氢吡啶-3-基)吡啶-3-甲醛183a
在配备有回流冷凝器的100-mL烧瓶中装入4-氯-2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛134c(297mg,0.57mmol)、1-甲基-3-(吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮178b(186mg,0.57mmol)、乙酸钠(90mg,1.1mmol)、K3PO4(234mg,1.1mmol)、PdCl2(dppf)(50mg,0.057mmol)、乙腈(25mL)和水(1mL)。在使氮气鼓泡通过所述混合物30分钟后,将其在氮气中在100℃加热3小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用20:1二氯甲烷/甲醇洗脱)来纯化得到183a(178mg,61%),其为棕色固体。MS-ESI:[M+H]+513.3。
实施例183 10-氟-2-(3-(羟基甲基)-4-(1-甲基-6-氧代-5-(吡啶-2-基氨基)-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮183
将183a(160mg,0.31mmol)和NaBH4(59mg,1.55mmol)于甲醇(20mL)中的混合物在20℃搅拌2小时。然后将反应用水淬灭并减压蒸发。将残余物通过反相制备性-HPLC来纯化得到183(42mg,26%),其为灰白色固体。MS-ESI:[M+H]+515.3.1H NMR(500MHz,DMSO-d6)δ8.74(d,J=2.5Hz,1H),8.65(s,1H),8.50(d,J=5.0Hz,1H),8.18-8.17(m,1H),7.61-7.58(m,1H),7.53(d,J=2.0Hz,1H),7.36(d,J=5.0Hz,1H),7.31(d,J=8.5Hz,1H),6.81-6.79(m,1H),4.95(t,J=5.0Hz,1H),4.49-4.40(m,2H),4.22-4.14(m,2H),4.10-4.05(m,1H),3.87-3.85(m,1H),3.62(s,3H),2.64-2.60(m,1H),2.57-2.53(m,1H),2.43-2.41(m,2H),1.81-1.75(m,2H),1.71-1.67(m,2H).
实施例184a 1-甲基-3-(吡嗪-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮184a
在100-mL配备有磁力搅拌子和回流冷凝器的单颈圆底烧瓶中装入5-溴-1-甲基-3-(吡嗪-2-基氨基)吡啶-2(1H)-酮162a(600mg,2.1mmol)、Pin2B2(2540mg,10mmol)、Pd2(dba)3(100mg,0.11mmol)、X-phos(100mg,0.25mmol)、乙酸钾(600mg,6.1mmol)和二噁烷(30mL)。在经历三轮真空/氩气吹洗后,将混合物在65℃加热15小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物通过石油醚来洗涤得到184a,其为黄色固体(700mg,90%)。MS-ESI:[M+H]+329.4
实施例184b 2-{4,4-二甲基-9-氧代-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-10-基}-4-{1-甲基-6-氧代-5-[(吡嗪-2-基)氨基]-1,6-二氢吡啶-3-基}吡啶-3-甲醛184b
在25-mL配备有回流冷凝器的单颈圆底烧瓶中装入4-氯-2-{4,4-二甲基-9-氧代-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-10-基}吡啶-3-甲醛109a(100mg,0.30mmol)、184a(170mg,0.60mmol)、Pd(dppf)Cl2(12mg,0.015mmol)、K3PO4(130mg,0.60mmol)、乙酸钠三水合物(85mg,0.60mmol)、乙腈(10mL)和水(6滴)。将体系排空并用氮气回填。将反应混合物在100℃搅拌2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用25:1的二氯甲烷/甲醇洗脱)来纯化得到184b(80mg,54%),其为棕黄色固体。MS-ESI:[M+H]+527.2。
实施例184 6-[3'-羟基甲基-1-甲基-6-氧代-5-(吡嗪-2-基氨基)-1,6-二氢-[3,4']联吡啶-2'-基]-2,2-二甲基-2,3,5,6-四氢-1H,4H-8-硫杂-6-氮杂-环戊二烯并[a]茚-7-酮184
将184b(80mg,0.15mmol)和NaBH4(18mg,0.45mmol)于甲醇(5mL)中的混合物在30℃搅拌2小时。将混合物用水淬灭并减压浓缩。将残余物用乙酸乙酯(3X10mL)萃取。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到184(24mg,35%),其为白色固体。MS-ESI:[M+H]+529.3.1H NMR(500MHz,CHCl3)δ8.73(d,J=2.0Hz,1H),8.54(d,J=5.0Hz,1H),8.29(s,1H),8.14(d,J=8.0Hz,2H),8.02(s,1H),7.96(d,J=2.5Hz,1H),7.37(d,J=5.5Hz,1H),4.86-4.83(m,1H),4.71-4.68(m,1H),4.46-4.41(m,1H),4.32(t,J=11.0Hz,1H),3.85-3.81(m,1H),3.74(s,3H),2.99-2.94(m,2H),2.81(s,2H),2.61-2.51(m,2H),1.30(s,6H).
实施例185a 5-溴-3-(咪唑并[1,2-a]吡啶-7-基氨基)-1-甲基吡嗪-2(1H)-酮185a
在配备有回流冷凝器的100-mL圆底烧瓶中装入咪唑并[1,2-a]吡啶-7-胺(665mg,5.0mmol)、Cs2CO3(3.26g,10mmol)、3,5-二溴-1-甲基吡嗪-2(1H)-酮(1.86g,7.0mmol)、Xantphos(289mg,0.50mmol)、Pd2(dba)3(458mg,0.50mmol)和1,4-二噁烷(30mL)。在使氮气鼓泡通过所述混合物30分钟后,将其在氮气中在100℃加热16小时。通过LCMS分析反应混合物,结果显示存留非常少量的起始物质。将反应混合物冷却至室温并过滤。将滤液用二氯甲烷(60mL)和水(50mL)稀释。分离出水层并用二氯甲烷(3×20mL)萃取。将合并的有机层用Na2SO4干燥,过滤并减压浓缩。将黑色残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(60/1至30/1)洗脱)来纯化得到185a(700mg,44%),其为浅黄色固体。MS-ESI:[M+H]+320
实施例185b 6-(咪唑并[1,2-a]吡啶-7-基氨基)-4-甲基-5-氧代-4,5-二氢吡嗪-2-基硼酸185b
在配备有回流冷凝器的100-mL圆底烧瓶中装入185a(638mg,1.99mmol)、4,4,4',4',5,5,5',5'-八甲基-2,2'-二(1,3,2-二氧杂硼杂戊环)(Pin2B2,2.54mg,10mmol)、1,1’-二(二苯基膦基)二茂铁二氯化钯(II)(163mg,0.18mmol)、Cs2CO3(1.3g,3.98mmol)和1,4-二噁烷(20mL)。在使氮气鼓泡通过所述混合物30分钟后,将其在氮气中在80℃加热3小时。将反应混合物冷却至室温并过滤。将滤液用石油醚(150mL)和乙酸乙酯(15mL)稀释。将所得悬浮液在室温搅拌30分钟。过滤收集固体并通过硅胶柱色谱法进一步纯化(用二氯甲烷/甲醇(60/1至15/1)洗脱)得到185b(400mg,70%),其为灰白色固体。MS-ESI:[M+H]+286
实施例185c 2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-(6-{咪唑并[1,2-a]吡啶-7-基氨基}-4-甲基-5-氧代吡嗪-2-基)吡啶-3-甲醛185c
在配备有磁力搅拌子和回流冷凝器的100-mL圆底烧瓶中装入185b(400mg,1.40mmol)、4-氯-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-甲醛108a(192mg,0.56mmol)、乙酸钾(220mg,2.24mmol)、乙腈(20mL)和水(0.5mL)。在使氮气鼓泡通过所述悬浮液30分钟后,加入1,1’-二(二苯基膦基)二茂铁二氯化钯(II)(49mg,0.054mmol)。使体系经历三轮真空/氩气吹洗并在80℃加热3小时。然后将其冷却至室温并过滤。将固体用二氯甲烷(2X20mL)洗涤。将合并的滤液减压浓缩并将残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(40:1至10:1)洗脱)来纯化得到185c(90mg,29%),其为浅黄色固体。MS-ESI:[M+H]+549
实施例185 2-{3-羟基甲基-4-[6-(咪唑并[1,2-a]吡啶-7-基氨基)-4-甲基-5-氧代-4,5-二氢-吡嗪-2-基]-吡啶-2-基}-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮185
在室温,向185c(80mg,0.146mmol)于甲醇(5mL)中的溶液中加入NaBH4(34mg,0.90mmol)。在将反应混合物搅拌1小时后,LCMS表明反应完成。将反应混合物用水(3mL)淬灭并减压浓缩。将残余物用二氯甲烷(3X10mL)萃取。将合并的有机层用盐水(30mL)洗涤,用Na2SO4干燥,过滤并减压浓缩。将残余物通过反相制备性-HPLC来纯化得到185(49mg,61%),其为浅黄色固体。MS-ESI:[M+H]+551.1H NMR(500MHz,DMSO-d6)δ9.67(s,1H),8.57(d,J=10.5Hz,1H),8.51(s,1H),8.41(d,J=7.0Hz,1H),7.77(s,1H),7.75(s,1H),7.63(s,1H),7.46(d,J=6.0Hz,1H),7.42(s,1H),6.59(s,1H),5.04-5.02(m,1H),4.67-4.64(m,1H),4.519-4.481(m,1H),4.31-4.20(m,3H),3.88(d,J=7.0Hz,1H),3.58(s,3H),2.63-2.55(m,2H),2.44-2.42(m,2H),1.23(s,6H).
实施例186a 5-溴-1-甲基-3-(吡啶-3-基氨基)吡嗪-2(1H)-酮186a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入吡啶-3-胺(940mg,10mmol)、3,5-二溴-1-甲基吡嗪-2(1H)-酮(5.4g,20mmol)、异丙醇(50mL)和二-异丙基乙基胺(10mL)。将混合物回流加热5小时。反应结束后,将其冷却至室温。减压除去溶剂。将粗制物通过硅胶柱色谱法(用30:1二氯甲烷/甲醇洗脱)来纯化得到186a(1.4g,50%),其为黄色固体。MS-ESI:[M+H]+281.6.
实施例186b 4-甲基-5-氧代-6-(吡啶-3-基氨基)-4,5-二氢吡嗪-2-基硼酸186b
在配备有回流冷凝器的250-mL圆底烧瓶中装入186a(800mg,2.86mmol)、4,4,4',4',5,5,5',5'-八甲基-2,2'-二(1,3,2-二氧杂硼杂戊环)(2.18g,8.57mmol)、Pd(dppf)Cl2(204mg,0.28mmol)、乙酸钾(560mg,5.71mmol)和二噁烷(60mL)。在使氮气鼓泡通过所述混合物30分钟后,将其在氮气中在100℃搅拌3小时。将混合物冷却至室温并过滤。减压蒸发滤液。将残余固体用石油醚(2X30mL)洗涤得到186b(406mg,58%),其为棕色固体。MS-ESI:[M+H]+247.3.
实施例186c 2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)-4-(4-甲基-5-氧代-6-(吡啶-3-基氨基)-4,5-二氢吡嗪-2-基)吡啶-3-甲醛186c
在配备有回流冷凝器的50-mL圆底烧瓶中装入186b(127mg,0.52mmol)、4-氯-2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛134c(180mg,0.52mmol)、Na2CO3(110mg,1.04mmol)、PdCl2(dppf)(38mg,0.052mmol)、DMF(12mL)和水(1mL)。在使氮气鼓泡通过所述混合物30分钟后,将其在氮气中在50℃加热8小时。然后将反应混合物冷却至室温并减压浓缩。将残余物通过硅胶柱色谱法(用30:1二氯甲烷/甲醇洗脱)来纯化得到186c(132mg,49%),其为棕色固体。MS-ESI:[M+H]+514.3.
实施例186 10-氟-2-(3-(羟基甲基)-4-(4-甲基-5-氧代-6-(吡啶-3-基氨基)-4,5-二氢吡嗪-2-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮186
向186c(118mg,0.23mmol)于甲醇(15mL)中的溶液中加入NaBH4(27mg,0.70mmol)。将混合物在20℃搅拌2小时。将反应混合物用水淬灭并减压蒸发。将残余物通过反相制备性-HPLC来纯化得到186(33mg,28%),其为白色固体。MS-ESI:[M+H]+516.3。1H NMR(500MHz,DMSO-d6)δ9.78(s,1H),8.54(d,J=5.0Hz,1H),8.39-8.37(m,2H),8.06-8.04(m,2H),7.76(s,1H),7.59(d,J=5.5Hz,1H),4.97(t,J=5.0Hz,1H),4.68-4.65(m,1H),4.51-4.47(m,1H),4.25-4.19(m,2H),4.10-4.05(m,1H),3.91-3.88(m,1H),3.58(s,3H),2.66-2.60(m,1H),2.57-2.53(m,1H),2.44-2.42(m,2H),1.82-1.75(m,2H),1.71-1.67(m,2H).
实施例187a乙酸(4-(5-(5-(2,2-二甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯187a
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入5-溴-3-(5-(2,2-二甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基吡啶-2(1H)-酮190e(200mg,1.0当量,0.45mmol)、乙酸(2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-3-基)甲酯113i(345mg,2当量,0.90mmol)、PdCl2(dppf)(36mg,0.1当量,0.045mmol)、K3PO4(191mg,2当量,0.90mmol)、乙酸钠(74mg,2.0当量,0.90mmol)、乙腈(15mL)和水(0.1mL)。在经历三轮真空/氩气吹洗后,将混合物在90℃搅拌2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用50:1二氯甲烷/乙醇洗脱)来纯化得到187a(100mg,31%),其为黄色固体。MS-ESI:[M+H]+707.4.
实施例187 2-(4-(5-(5-(2,2-二甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-3-(羟基甲基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮187
在配备有磁力搅拌子的50-mL单颈圆底烧瓶中装入187a(100mg,1当量,0.14mmol)、氢氧化锂(54mg,10当量,1.4mmol)、异丙醇(3mL)、THF(3mL)和水(2mL)。将混合物在30℃搅拌1小时。然后将其过滤并减压浓缩滤液。将残余物通过反相制备性-HPLC来纯化得到187,其为白色固体(43mg,46%)。MS-ESI:[M+H]+665.3.1H NMR(500MHz,DMSO-d6)δ8.69(d,J=2.0Hz,1H),8.60(s,1H),8.48(d,J=5.0Hz,1H),7.93(d,J=2.0Hz,1H),7.51(d,J=1.5Hz,1H),7.42-7.40(m,1H),7.35(d,J=5.0Hz,1H),7.24(d,J=8.5Hz,1H),6.58(s,1H),4.98(brs,1H),4.54(t,J=6.0Hz,2H),4.46-4.38(m,4H),4.25-3.85(m,4H),3.60(s,3H),3.38-3.35(m,1H),3.03-2.54(m,4H),2.47(t,J=6.0Hz,2H),2.32-2.12(m,4H),1.79-1.67(m,4H),0.97(s,6H).
实施例188a乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{1-甲基-6-氧代-5-[(吡嗪-2-基)氨基]-1,6-二氢吡啶-3-基}吡啶-3-基)甲酯188a
在配备有回流冷凝器的50-mL单颈圆底烧瓶中装入5-溴-1-甲基-3-(吡嗪-2-基氨基)吡啶-2(1H)-酮162a(210mg,0.70mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(560mg,1.4mmol)、Pd(dppf)Cl2(70mg,0.035mmol)、K3PO4(320mg,1.4mmol)、乙酸钠三水合物(210mg,1.4mmol)、乙腈(10mL)和水(6滴)。将体系排空并用氮气回填。将反应混合物在100℃搅拌2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用25:1的二氯甲烷/甲醇洗脱)来纯化得到188a(150mg,40%),其为棕黄色固体。MS-ESI:[M+H]+554.2。
实施例188 2-[3'-羟基甲基-1-甲基-6-氧代-5-(吡嗪-2-基氨基)-1,6-二氢-[3,4']联吡啶-2'-基]-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮188
将188a(150mg,0.27mmol)和氢氧化锂(103mg,2.7mmol)于异丙醇/THF(5:3,8mL)和水(2mL)中的混合物在30℃搅拌1小时。真空蒸发混合物并将残余物用乙酸乙酯(2X20mL)萃取。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到188(40mg,35%),其为白色固体。MS-ESI:[M+H]+512.3.1H NMR(500MHz,CHCl3)δ8.73(d,J=2.0Hz,1H),8.53(d,J=5.0Hz,1H),8.29(s,1H),8.15-8.13(m,重叠,2H),8.02-8.00(m,2H),7.38(d,J=5.0Hz,1H),6.86(s,1H),5.12(s,1H),4.68-4.51(m,2H),4.33-4.29(m,1H),4.18(t,J=5.5Hz,2H),3.91-3.86(m,1H),3.75(s,3H),2.60-2.58(m,2H),2.53(s,2H),1.28(s,6H).
实施例189a 4-(吡嗪-2-基)哌嗪-1-羧酸叔丁酯189a
在500-mL配备有磁力搅拌子和回流冷凝器的单颈圆底烧瓶中装入DMSO(250mL)、哌嗪-1-羧酸叔丁酯(15.8g,85.0mmol)、2-氯吡嗪(9.7g,85.0mmol)和Cs2CO3(55.3g,170mmol)。将混合物在60℃加热3天。之后,将反应混合物冷却至室温。然后将其过滤并减压蒸发滤液。将残余物通过硅胶柱色谱法(用5:1石油醚/乙酸乙酯洗脱)来纯化得到189a(13.3g,60%),其为黄色固体。MS:[M+H]+265.3
实施例189b 4-(5-溴吡嗪-2-基)哌嗪-1-羧酸叔丁酯189b
在配备有磁力搅拌子和回流冷凝器的500-mL单颈圆底烧瓶中装入乙腈(150mL)、189a(3.0g,8.8mmol)和N-溴琥珀酰亚胺(1.56g,8.8mmol)。将混合物在室温搅拌整夜。然后将其减压浓缩并将残余物通过硅胶柱色谱法(用10:1石油醚/乙酸乙酯洗脱)来纯化得到189b,其为黄色固体(2.85g,73.4%)。MS:[M+H]+343.3。1H NMR(500MHz,(CD3)2CO)δ8.03(s,1H),7.94(s,1H),3.48-3.46(m,4H),3.42-3.40(m,4H),1.33(s,9H).
实施例189c 4-(5-(二苯基亚甲基氨基)吡嗪-2-基)哌嗪-1-羧酸叔丁酯189c
在配备有磁力搅拌子和回流冷凝器的250-mL单颈圆底烧瓶中装入189b(3.3g,9.6mmol)、二苯基甲亚胺(1.74g,9.6mmol)、二醋酸钯(440mg,0.48mmol)、(R)-(+)-2,2'-二(二苯基膦基)-1,1'-联萘(598mg,0.96mmol)、Cs2CO3(6.2g,19.2mmol)和1,4-二噁烷(80mL)。在经历三轮真空/氩气吹洗后,将混合物在115℃加热64小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用5:1石油醚/乙酸乙酯洗脱)来纯化得到189c,其为黄色固体(3.2g,75%)。MS:[M+H]+444.2.
实施例189d 4-(5-氨基吡嗪-2-基)哌嗪-1-羧酸叔丁酯189d
向189c(2.5g,5.6mmol)于甲醇(25mL)中的溶液中加入乙酸钠(0.56g,6.8mmol)和羟基胺盐酸盐(0.7g,10mmol)。将反应混合物搅拌0.5小时。然后将其减压浓缩并将残余物通过柱色谱法(用15:1二氯甲烷/甲醇洗脱)来纯化得到189d(1.3g,71%)。MS:[M+H]+280.3。
实施例189e 4-(5-(5-溴-1-甲基-2-氧代-1,2-二氢吡啶-3-基氨基)吡嗪-2-基)哌嗪-1-羧酸叔丁酯189e
将189d(1.1g,3.94mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(1.1g,3.94mmol)、二醋酸钯(45mg,0.20mmol)、(R)-(+)-2,2'-二(二苯基膦基)-1,1'-联萘(245mg,0.39mmol)和Cs2CO3(2.6g,7.9mmol)于1,4-二噁烷(150mL)中的混合物在120℃加热2小时。然后将其冷却至室温并减压浓缩。将残余物通过柱色谱法(用30:1二氯甲烷/甲醇洗脱)来纯化得到189e(900mg,54%)。MS:[M+H]+465.1。
实施例189f 5-溴-1-甲基-3-(5-(哌嗪-1-基)吡嗪-2-基氨基)吡啶-2(1H)-酮189f
将189e(1.0g,2.2mmol)和4.0M HCl/二噁烷(60mL)的混合物在室温搅拌5小时。然后将其减压浓缩得到粗制189f,其为黄色固体(760mg,98%),将其不经进一步纯化即用于下一步骤。MS:[M+H]+395.1.
实施例189g 5-溴-1-甲基-3-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡嗪-2-基氨基)吡啶-2(1H)-酮189g
将189f(740mg,2.0mmol)、氧杂环丁烷-3-酮(288mg,4.0mmol)、NaBH3CN(315mg,5.0mmol)和氯化锌(680mg,5.0mmol)于甲醇(60mL)中的混合物在50℃搅拌5小时。然后将其用水淬灭并减压浓缩。将残余物用二氯甲烷萃取三次。将合并的萃取物减压浓缩得到粗制189g,其为黄色固体(660mg,78%),将其不经进一步纯化即用于下一步骤。MS:[M+H]+423.1.
实施例189h乙酸(4-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡嗪-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯189h
在配备有回流冷凝器的50-mL圆底烧瓶中装入189g(180mg,0.43mmol)、3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113i(165mg,0.43mmol)、Pd(dppf)Cl2(35mg,0.043mmol)、乙酸钠(71mg,0.86mmol)、K3PO4(194mg,0.86mmol)、乙腈(10mL)和水(0.5mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热3小时。之后,将反应混合物过滤并减压浓缩滤液。将所得残余物通过硅胶柱色谱法(用40:1二氯甲烷/甲醇洗脱)来纯化得到189h,其为黄色固体(100mg,34%)。MS-ESI:[M+H]+680.3。
实施例189 2-(3-(羟基甲基)-4-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡嗪-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮189
在室温,向189h(90mg,0.13mmol)于异丙醇/THF(1:1,5mL)和水(0.5mL)中的混合物中加入氢氧化锂(126mg,2.9mmol)。将反应混合物在35℃搅拌0.5小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物通过反相制备性-HPLC来纯化得到189(60mg,71%),其为黄色固体。MS-ESI:[M+H]+638.3.1H NMR(500MHz,CDCl3)δ8.48(d,J=5.0Hz,1H),8.43(d,J=2.0Hz,1H),7.98(s,1H),7.82(d,J=1.5Hz,1H),7.80(s,1H),7.78(s,1H),7.33(d,J=5.0Hz,1H),6.89(s,1H),5.04-5.01(m,1H),4.72-4.50(m,6H),4.32-4.30(m,1H),4.15-4.09(m,2H),3.88-3.86(m,1H),3.72(s,3H),3.57-3.49(m,5H),2.61-2.43(m,8H),1.92-1.78(m,4H)。
实施例190a 3,3-二甲基-4-(6-硝基吡啶-3-基)哌嗪-1-羧酸叔丁酯190a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入5-溴-2-硝基吡啶(5.6g,28.0mmol)、3,3-二甲基-4-哌嗪-1-羧酸叔丁酯(3.0g,14.0mmol)、碳酸铯(9.1g,28mmol)和1,4-二噁烷(50mL)。在使氮气鼓泡通过所得溶液30分钟后,加入Binap(870mg,1.4mmol)和三(二亚苄基丙酮)-二钯(0)(1.2g,1.4mmol)。使反应混合物经历三轮真空/氩气吹洗并在120℃搅拌24小时。之后,将反应混合物冷却至室温,过滤并将滤液在乙酸乙酯(200mL)和水(50mL)之间分配。分离出水层并用乙酸乙酯(3×50mL)萃取。将合并的有机层用盐水洗涤(50mL)并用硫酸钠干燥。过滤除去干燥剂并减压浓缩滤液。将残余物通过硅胶柱色谱法(用5:1石油醚/乙酸乙酯洗脱)来纯化得到190a(1.27g,27%)。LCMS:[M+H]+337.2。
实施例190b 4-(6-氨基吡啶-3-基)-3,3-二甲基哌嗪-1-羧酸叔丁酯190b
将50-mL圆底烧瓶用氮气吹洗并装入3,3-二甲基-4-(6-硝基吡啶-3-基)哌嗪-1-羧酸叔丁酯190a(1100mg,3.2mmol)、10%钯/炭(10%水分,110mg)和甲醇(20mL)。然后将其排空,充入氢气并在室温搅拌5小时。将氢气排空并将氮气充入所述烧瓶中。通过用硅藻土过滤剂(Imerys Minerals California,Inc.)垫过滤除去催化剂并减压浓缩滤液得到190b(950mg,94%)。LCMS:[M+H]+307.3
实施例190c 4-(6-(5-溴-1-甲基-2-氧代-1,2-二氢吡啶-3-基氨基)吡啶-3-基)-3,3-二甲基哌嗪-1-羧酸叔丁酯190c
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入4-(6-氨基吡啶-3-基)-3,3-二甲基哌嗪-1-羧酸叔丁酯190b(950mg,3.1mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(1240mg,4.6mmol)、1,4-二噁烷(30mL)和碳酸铯(2015mg,6.2mmol)。在使氮气鼓泡通过所得溶液5分钟后,加入Xantphos(179mg,0.31mmol)和三(二亚苄基丙酮)二钯(0)(283mg,0.31mmol)。使反应混合物经历三轮真空/氩气吹洗并回流加热10小时。之后,将反应混合物冷却至室温并过滤。使滤液在乙酸乙酯(50mL)和水(10mL)之间分配。分离出水层并用乙酸乙酯(3×20mL)萃取。将合并的有机层用盐水(30mL)洗涤并用硫酸钠干燥。过滤除去干燥剂并减压浓缩滤液。将残余物通过硅胶柱色谱法(用4:1石油醚/乙酸乙酯洗脱)来纯化得到190c(1.21g,79%)。LCMS:[M+H]+492.1。
实施例190d 5-溴-3-(5-(2,2-二甲基哌嗪-1-基)吡啶-2-基氨基)-1-甲基吡啶-2(1H)-酮190d
向4-(6-(5-溴-1-甲基-2-氧代-1,2-二氢吡啶-3-基氨基)吡啶-3-基)-3,3-二甲基哌嗪-1-羧酸叔丁酯190c(1.19g,1.9mmol)于二氯甲烷(20mL)中的溶液中加入3M HCl/乙醚(15mL)。将反应混合物在室温搅拌4小时。然后将其减压浓缩得到190d(900mg,95%)。LCMS:[M+H]+392.1。
实施例190e 5-溴-3-(5-(2,2-二甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基吡啶-2(1H)-酮190e
将5-溴-3-(5-(2,2-二甲基哌嗪-1-基)吡啶-2-基氨基)-1-甲基-吡啶-2(1H)-酮190d(900mg,2.3mmol)、氧杂环丁烷-3-酮(497mg,6.9mmol)、NaBH3CN(435mg,6.9mmol)和氯化锌(311mg,2.3mmol)于甲醇(30mL)中的混合物在50℃搅拌4小时。然后将其减压浓缩。向残余物中加入水(10mL)并将混合物用氯仿(3X50mL)萃取。将合并的有机层减压浓缩。将残余物通过硅胶柱色谱法(用50:1二氯甲烷/甲醇洗脱)来纯化得到190e(800mg,78%)。LCMS:[M+H]+448.1。1H NMR(500MHz,CDCl3)δ8.65(d,J=2.0Hz,1H),8.11(d,J=2.5Hz,1H),7.85(s,1H),7.37-7.34(m,1H),6.96(d,J=2.5Hz,1H),6.72(d,J=8.5Hz,1H),4.69-4.61(m,4H),3.60(s,3H),3.50-3.14(m,3H),2.43-2.17(m,4H),1.06(s,6H)。
实施例190f 2-(4-氯-3-(羟基甲基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮190f
在10℃,向4-氯-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)-吡啶-3-甲醛103b(1.0g,3.0mmol)于甲醇(30mL)中的溶液中加入硼氢化钠(380mg,9.0mmol)。将反应混合物搅拌30分钟并用水(10mL)淬灭。然后将其减压浓缩并将残余物溶解在二氯甲烷(50mL)中。将混合物用水(10mL)洗涤,用无水Na2SO4干燥,过滤并减压蒸发得到190f,其为黄色固体(900mg,90%)。MS-ESI:[M+H]+332。
实施例190g乙酸(4-氯-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯190g
向2-(4-氯-3-(羟基甲基)吡啶-2-基)-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮190f(900mg,2.7mol)和三乙胺(900mg,9.0mol)于二氯甲烷(25mL)中的混合物中滴加乙酰氯(600mg,6.0mol)同时在室温搅拌。将反应混合物搅拌1小时并减压浓缩。将残余物通过硅胶柱色谱法(用二氯甲烷洗脱)来纯化得到190g,其为白色固体(950mg,94%)。MS-ESI:[M+H]+374。
实施例190h乙酸(4-氯-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯190h
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入乙酸(4-氯-2-(1-氧代-3,4,6,7,8,9-六氢-吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯190g(950mg,2.5mmol)、Pin2B2(4,4,4',4',5,5,5',5'-八甲基-2,2'-二(1,3,2-二氧杂硼杂戊环)(1.6g,2.0当量,5mmol)、Pd2(dba)3(230mg,0.1当量,0.25mmol)、X-phos(232mg,0.2当量,0.50mmol)、乙酸钾(735mg,3当量,7.5mmol)和二噁烷(20mL)。在经历三轮真空/氩气吹洗后,将混合物在65℃加热15小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物用3:1石油醚/乙酸乙酯洗涤得到190h,其为黄色固体(950mg,87%)。MS-ESI:[M+H]+383。
实施例190i乙酸(4-(5-(5-(2,2-二甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯190i
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入5-溴-3-(5-(2,2-二甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基吡啶-2(1H)-酮190e(200mg,1.0当量,0.45mmol)、乙酸(2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-3-基)甲酯190h(345mg,2当量,0.90mmol)、PdCl2(dppf)(36mg,0.1当量,0.045mmol)、K3PO4(191mg,2当量,0.90mmol)、乙酸钠(74mg,2.0当量,0.90mmol)、乙腈(15mL)和水(0.1mL)。在经历三轮真空/氩气吹洗后,将混合物在90℃搅拌2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用50:1二氯甲烷/乙醇洗脱)来纯化得到190i(100mg,31%),其为黄色固体。MS-ESI:[M+H]+707.4。
实施例190 2-[4-[5-[[5-[2,2-二甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]-2-吡啶基]氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1-酮190
在配备有磁力搅拌子的50-mL单颈圆底烧瓶中装入乙酸(4-(5-(5-(2,2-二甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯190i(100mg,1当量,0.14mmol)、氢氧化锂(54mg,10当量,1.4mmol)、异丙醇(3mL)、THF(3mL)和水(2mL)。将混合物在30℃搅拌1小时。然后将其过滤并减压浓缩滤液。将残余物通过反相制备性-HPLC来纯化得到190,其为白色固体(43mg,46%)。MS-ESI:[M+H]+665.3.1H NMR(500MHz,DMSO-d6)δ8.69(d,J=2.0Hz,1H),8.60(s,1H),8.48(d,J=5.0Hz,1H),7.93(d,J=2.0Hz,1H),7.51(d,J=1.5Hz,1H),7.42-7.40(m,1H),7.35(d,J=5.0Hz,1H),7.24(d,J=8.5Hz,1H),6.58(s,1H),4.98(brs,1H),4.54(t,J=6.0Hz,2H),4.46-4.38(m,4H),4.25-3.85(m,4H),3.60(s,3H),3.38-3.35(m,1H),3.03-2.54(m,4H),2.47(t,J=6.0Hz,2H),2.32-2.12(m,4H),1.79-1.67(m,4H),0.97(s,6H)
实施例191a N-叔丁基-4,5,6,7-四氢苯并[b]噻吩-2-甲酰胺191a
将4,5,6,7-四氢苯并[b]噻吩-2-羧酸(500g,2.75mol,1.0当量)和亚硫酰氯(655g,5.5mol,2.0当量)的混合物回流加热3小时。通过减压蒸馏除去过量亚硫酰氯。将残余物吸收在二氯甲烷(1.0L)中并在搅拌下加入叔丁基胺(402g,5.5mol,2.0当量)于二氯甲烷(500mL)中的溶液,同时使混合物的温度保持在低于10℃。将所得溶液在25℃搅拌16小时。减压除去大多数溶剂。将残余物在冰浴中冷却并在搅拌下缓慢引入2M KOH溶液以调节pH至11。过滤悬浮液并收集固体,用水洗涤三次并真空干燥得到191a,其为白色固体(580g,两步的收率为80%)。MS:[M+H]+238.1H NMR(500MHz,CDCl3)δ7.02(s,1H),5.77(s,1H),2.65(t,J=6.0Hz,1H),2.47(t,J=6.0Hz,1H),1.74-1.70(m,4H),1.35(s,9H).
实施例191c N-叔丁基-3-(二氮烯基甲基)-4,5,6,7-四氢苯并-[b]噻吩-2-甲酰胺191c
在-78℃和氩气保护下,将191a(100g,0.42mol,1.0当量)于THF(500mL)中的溶液缓慢加入正丁基锂(672mL,2.5M于THF中,1.68mol,4.0当量)中。将混合物搅拌2小时。向混合物中加入N,N-二甲基甲酰胺(306g,4.2mol,10.0当量),同时将温度维持在-78℃。再过2.0小时后,在-78℃,通过加入甲醇(500mL)将反应混合物淬灭。将其在室温搅拌0.50小时,原位得到191b。然后加入80%水合肼水溶液(131g,2.1mol)并将混合物在65℃回流整夜。减压除去有机溶剂。过滤残余物并将所得黄色固体用水洗涤。真空干燥固体得到191c,将其不经进一步纯化即用于下一步骤。MS:[M+H]+280。
实施例191d 8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-(9),2(7),3-三烯-6-酮191d
将N-叔丁基-3-(二氮烯基甲基)-4,5,6,7-四氢苯并[b]噻吩-2-甲酰胺191c(40g,144mmol)于H2SO4(30%水溶液,3L)中的混合物在105℃回流24小时。然后将其过滤并将滤液用二氯甲烷(3ⅹ1L)萃取。将合并的萃取物用Na2SO4干燥并减压蒸发。将残余物通过硅胶柱色谱法(用100:1二氯甲烷/甲醇洗脱)来纯化得到191d,其为白色固体(9.0g,31%)。MS:[M+H]+207.1H NMR(500MHz,CDCl3)δ8.15(s,1H),2.96-2.94(m,2H),2.86-2.84(m,2H),1.96-1.94(m,4H).
实施例191e(3S)-3-甲基-4-(6-硝基吡啶-3-基)哌嗪-1-羧酸叔丁酯191e
按照就化合物101g所描述的操作,以(3S)-3-甲基哌嗪-1-羧酸叔丁酯(10.0g,50mmol)和5-溴-2-硝基吡啶(10.5g,50mmol)开始得到191e,其为黄色固体(8.05g,50%)。MS-ESI:[M+H]+323
实施例191f(3S)-4-(6-氨基吡啶-3-基)-3-甲基哌嗪-1-羧酸叔丁酯191f
按照就化合物101h所描述的操作,以(3S)-3-甲基-4-(6-硝基吡啶-3-基)哌嗪-1-羧酸叔丁酯191e(5.8g,18mmol)开始得到191f,其为棕色固体(4.9g,93%)。MS-ESI:[M+H]+293
实施例191g(3S)-4-(6-(5-溴-1-甲基-2-氧代-1,2-二氢吡啶-3-基氨基)吡啶-3-基)-3-甲基哌嗪-1-羧酸叔丁酯191g
按照就化合物101i所描述的操作,以(3S)-3-甲基-4-(6-硝基吡啶-3-基)哌嗪-1-羧酸叔丁酯191f(4.0g,13.7mmol)和3,5-二溴-1-甲基吡啶-2(1H)-酮(5.5g,20.6mmol)开始得到191g,其为黄色固体(5.4g,83%)。MS-ESI:[M+H]+478
实施例191h(3S)-5-溴-1-甲基-3-(5-(2-甲基哌嗪-1-基)吡啶-2-基氨基)吡啶-2(1H)-酮191h
按照就化合物101j所描述的操作,以(3S)-4-(6-(5-溴-1-甲基-2-氧代-1,2-二氢吡啶-3-基氨基)吡啶-3-基)-3-甲基-哌嗪-1-羧酸叔丁酯191g(3.1g,6.5mmol)开始得到191h,其为黄色固体(2.3g,94%)。MS-ESI:[M+H]+378.
实施例191i(S)-5-溴-1-甲基-3-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)吡啶-2(1H)-酮191i
将(S)-5-溴-1-甲基-3-(5-(2-甲基哌嗪-1-基)吡啶-2-基氨基)吡啶-2(1H)-酮191h(40.0g,106mmol)、氧杂环丁烷-3-酮(11.4g,159mmol)、NaBH3CN(10.0g,159mmol)和氯化锌(21.3g,159mmol)于甲醇(700mL)中的混合物在50℃搅拌5小时。将混合物加至水(100mL)中并减压浓缩。将残余物用二氯甲烷(200mL×3)萃取。将合并的有机层减压浓缩并将残余物通过硅胶柱色谱法(用40:1二氯甲烷/甲醇洗脱)来纯化得到191i(35g,73%)。MS:[M+H]+434.
实施例191j(3S)-1-甲基-3-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)-吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮191j
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入(S)-4-(6-(5-溴-1-甲基-2-氧代-1,2-二氢吡啶-3-基氨基)吡啶-3-基)-3-甲基哌嗪-1-羧酸叔丁酯191i(1.0g,1.0当量,2.3mmol)、Pin2B2(1.46g,2.50当量,5.75mmol)、Pd2(dba)3(105mg,0.05当量,0.125mmol)、X-Phos(93mg,0.1当量,0.23mmol)、乙酸钾(676mg,3.0当量,6.9mmol)和二噁烷(50mL)。在经历三轮真空/氩气吹洗后,将混合物在90℃加热4小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物用3:1石油醚/乙酸乙酯(80mL)洗涤得到191j,其为黄色固体(1.0g,90%)。MS:[M+H]+482。
实施例191k 4-[1-甲基-5-({5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]-2-{6-氧代-8-硫杂-4,5-二氮杂-三环并[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-甲醛191k
在配备有回流冷凝器的50-mL圆底烧瓶中装入(S)-1-甲基-3-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮191j(168mg,0.35mmol)、4-氯-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-甲醛124a(121mg,0.35mmol)、K3PO4(148mg,0.70mmol)、1,1’-二(二苯基膦基)二茂铁二氯化钯(II)(13mg,0.0175mmol)、乙酸钠三水合物(95mg,0.70mmol)、水(6滴)和乙腈(10mL)。在使氮气鼓泡通过所述混合物30分钟后,将其在氮气保护下在100℃加热1小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将反应混合物冷却至室温并过滤。减压浓缩滤液。将残余物用二氯甲烷(30mL)和水(30mL)稀释。分离出水层并用二氯甲烷(3×20mL)萃取。将合并的有机层用Na2SO4干燥,过滤并减压浓缩。将黑色残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(80/1至30/1)洗脱)来纯化得到191k(118mg,51%),其为黄色固体。MS-ESI:[M+H]+665
实施例191 5-[3-(羟基甲基)-4-[1-甲基-5-({5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]吡啶-2-基]-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-6-酮191
在室温,向4-[1-甲基-5-({5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]-2-{6-氧代-8-硫杂-4,5-二氮杂三环-[7.4.0.02,7]-十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-甲醛191k(118mg,0.18mmol)于甲醇/二氯甲烷(10/10mL)中的溶液中加入NaBH4(21mg,0.54mmol)。在将反应混合物搅拌1小时后,LCMS表明反应完成。然后将混合物倒入水(20mL)中并减压浓缩。将残余物用二氯甲烷(20mL×3)萃取。将合并的有机层用盐水(30mL)洗涤,用Na2SO4干燥,过滤并减压浓缩。将残余固体通过反相制备性-HPLC来纯化得到191(71mg,60%),其为白色固体。MS-ESI:[M+H]+667。1H NMR(500MHz,DMSO-d6)δ8.64(d,J=2.5Hz,1H),8.58(d,J=5.0Hz,1H),8.48-8.46(m,2H),7.86(d,J=3.0Hz,1H),7.54(d,J=5.5Hz,1H),7.48(d,J=2.0Hz,1H),7.37(dd,J=3.0,9.0Hz,1H),7.25(d,J=9.5Hz,1H),4.86-4.85(m,1H),4.58-4.55(m,2H),4.48-4.46(m,2H),4.42-4.40(m,2H),3.65-3.64(m,1H),3.61(s,3H),3.41-3.99(m,1H),3.05-3.04(m,1H),2.97-2.95(m,3H),2.87-2.86(m,2H),2.52-2.51(m,1H),2.34-2.32(m,2H),2.21-2.20(m,1H),1.89-1.87(m,4H),0.94(d,J=6.0Hz,3H).
实施例192a 1-甲酰基-5,6,7,8-四氢吲嗪-2-羧酸甲酯192a
将配备有磁力搅拌子的100-mL圆底烧瓶用氮气吹洗并装入无水二氯乙烷(10mL)和无水DMF(0.7mL,9.0mmol)。将反应混合物冷却至0℃并历时2分钟加入三氯氧磷(0.7mL,7.3mmol),同时维持反应温度在0℃至10℃之间。移去冷却浴并将反应混合物在室温搅拌1小时。加入5,6,7,8-四氢吲嗪-2-羧酸甲酯112a(1.0g,5.6mmol)于乙腈(10mL)中的溶液并将混合物在室温再搅拌3小时。之后,将溶液减压浓缩并将油性残余物用饱和NaHCO3水溶液(20mL)吸收。将水层用乙酸乙酯(3X70mL)萃取。将合并的有机层用水(20mL)洗涤,用Na2SO4干燥并减压蒸发。将残余物通过硅胶柱色谱法(用1:1乙酸乙酯/石油醚洗脱)来纯化得到192a,其为白色固体(406mg,33%)。MS:(M+H)+208.3.1H NMR(500MHz,DMSO)δ10.29(s,1H),7.43(s,1H),3.99(t,J=6.0Hz,2H),3.76(s,3H),2.95(t,J=6.5Hz,2H),1.90-1.85(m,2H),1.78-1.74(m,2H).
实施例192b 7,8,9,10-四氢哒嗪并[4,5-a]吲嗪-4(3H)-酮192b
在100mL单颈圆底烧瓶中装入氢氧化肼(20mL)、1-甲酰基-5,6,7,8-四氢吲嗪-2-羧酸甲酯192a(2.5g,12.0mmol)。将反应混合物在100℃加热4小时。之后,将反应混合物冷却至室温并过滤得到192b,其为黄色固体(1.9g,83%)。MS:(M+H)+190.3。1H NMR(500MHz,DMSO)δ11.44(s,1H),8.03(s,1H),7.42(s,1H),4.18(t,J=6.0Hz,2H),2.96(t,J=6.5Hz,2H),1.98-1.93(m,2H),1.87-1.82(m,2H).
实施例192c 4-氯-2-(4-氧代-7,8,9,10-四氢哒嗪并[4,5-a]吲嗪-3(4H)-基)吡啶-3-甲醛192c
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(50mL)、碳酸钾(1.5g,10.6mmol)、7,8,9,10-四氢哒嗪并[4,5-a]吲嗪-4(3H)-酮192b(1.0g,5.3mmol)和2-溴-4-氯吡啶-3-甲醛(3.5g,15.9mmol)。使氮气鼓泡通过所得混合物30分钟后,加入溴化亚铜(I)(75.0mg,0.53mmol)和肌氨酸(47.0mg,0.53mmol)并将反应混合物在95℃加热12小时。之后,将反应混合物冷却至室温并过滤。使滤液在二氯甲烷(60mL)和水(40mL)之间分配。分离出水层并用二氯甲烷(3X70mL)萃取。将合并的有机层用盐水(30mL)洗涤并用硫酸钠干燥。过滤除去干燥剂并减压浓缩滤液。将残余物通过硅胶柱色谱法(用10:1乙酸乙酯/石油醚洗脱)来纯化得到192c,其为棕色固体(521mg,30%)。MS-ESI:[M+H]+329.2。
实施例192d(S)-4-(1-甲基-5-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(4-氧代-7,8,9,10-四氢哒嗪并[4,5-a]吲嗪-3(4H)-基)吡啶-3-甲醛192d
在配备有回流冷凝器的100-mL圆底烧瓶中装入4-氯-2-(4-氧代-7,8,9,10-四氢哒嗪并[4,5-a]吲嗪-3(4H)-基)吡啶-3-甲醛192c(196mg,0.60mmol)、(S)-1-甲基-3-(5-(2-甲基-4-(氧杂环丁烷-3-基)-哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮191j(290mg,0.60mmol)、乙酸钠(100mg,1.2mmol)、K3PO4(320mg,1.2mmol)、PdCl2(dppf)(50mg,0.060mmol)、乙腈(25mL)和水(1mL)。在使氮气鼓泡通过所述混合物30分钟后,将其在氮气保护下在100℃加热3小时。将反应混合物冷却至室温并减压蒸发。将残余物通过硅胶柱色谱法(用20:1二氯甲烷/甲醇洗脱)来纯化得到192d(173mg,44%),其为棕色固体。MS-ESI:[M+H]+648.4.
实施例192 3-[3-(羟基甲基)-4-[1-甲基-5-[[5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]-2-吡啶基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,8,9,10-四氢哒嗪并[4,5-a]吲嗪-4-酮192
向192d(160mg,0.25mmol)于MeOH(20mL)中的溶液中加入NaBH4(28mg,0.75mmol)。将混合物在20℃搅拌2小时并减压蒸发。将残余物通过反相制备性-HPLC来纯化得到192(97mg,60%),其为黄色固体。MS-ESI:[M+H]+650.4.1H NMR(500MHz,DMSO-d6)δ8.65(d,J=2.5Hz,1H),8.54(d,J=4.5Hz,1H),8.45(s,1H),8.25(s,1H),7.86(d,J=2.5Hz,1H),7.62(s,1H),7.51(d,J=2.5Hz,1H),7.47(d,J=5.0Hz,1H),7.38-7.36(m,1H),7.25(d,J=9.5Hz,1H),4.66(s,1H),4.57-4.54(m,2H),4.48-4.46(m,1H),4.43-4.41(m,1H),4.33(s,2H),4.25-4.21(m,2H),3.69-3.66(m,1H),3.60(s,3H),3.42-3.37(m,1H),3.11-3.07(m,1H),3.06-3.04(m,2H),2.97-2.92(m,1H),2.55-2.53(m,1H),2.35-2.29(m,2H),2.19-2.17(m,1H),2.04-1.96(m,2H),1.93-1.85(m,2H),0.93(d,J=6.5Hz,3H).
实施例193a 2-(羟基(吡啶-2-基)甲基)丙烯酸甲酯193a
在250-mL单颈圆底烧瓶中装入氯仿(100mL)、吡啶-2-甲醛(10.7g,0.10mol)、丙烯酸甲酯(8.60g,0.10mol)和1,4-二氮杂-二环[2.2.2]辛烷(0.560g,5.00mmol)。将反应混合物在室温搅拌48小时。之后,将反应混合物减压浓缩并将残余物通过硅胶柱色谱法(用3:1石油醚/乙酸乙酯洗脱)来纯化得到193a,其为深黄色油状物(11.6g,60%)。MS-ESI:(M+H)+194.2.1H NMR(500MHz,CDCl3)δ8.54(d,J=5.0Hz,1H),7.69-7.66(m,1H),7.42(d,J=8.0Hz,1H),7.22-7.20(m,1H),6.36(s,1H),5.97(s,1H),5.62(s,1H),4.85(s,1H),3.74(s,3H)。
实施例193b吲嗪-2-羧酸甲酯193b
在配备有磁力搅拌子和回流冷凝器的250-mL单颈圆底烧瓶中装入乙酸酐(80mL)和193a(6.68g,34.6mmol)。将反应混合物在氮气中回流加热4小时。之后,将反应混合物冷却至室温,倒在冰(100g)与碳酸氢钠饱和水溶液(200mL)的混合物上并搅拌1小时。将所得溶液用饱和碳酸氢钠水溶液中和并用二氯甲烷萃取(3×200mL)。将合并的有机萃取物用硫酸钠干燥并减压浓缩。将残余物通过硅胶柱色谱法(用10:1石油醚/乙酸乙酯(10:1)洗脱)来纯化得到193b,其为白色固体(2.1g,35%)。MS-ESI:(M+H)+176.2。1H NMR(500MHz,CDCl3)δ7.86-7.84(m,1H),7.79(d,J=1.0Hz,1H),7.36-7.34(m,1H),6.82(s,1H),6.70-6.66(m,1H),6.55-6.51(m,1H),3.88(s,3H).
实施例193c 5,6,7,8-四氢吲嗪-2-羧酸甲酯193c
将250-mL圆底烧瓶用氮气吹洗并装入193b(2.0g,11.4mmol)、10%钯/炭(50%水分,200mg)和甲醇(50mL)。将其排空,充入氢气并在5atm氢气条件下在室温搅拌8小时。然后将氢气排空并将氮气充入所述烧瓶中。通过用垫过滤除去催化剂并减压浓缩滤液得到193c,其为白色固体(1.1g,81%)。MS-ESI:[M+H]+180.3。1H NMR(500MHz,DMSO-d6)δ7.25(d,J=2.0Hz,1H),6.09(s,1H),3.93(t,J=6.0Hz,2H),3.66(s,3H),2.67(t,J=6.0Hz,2H),1.87-1.83(m,2H),1.75-1.70(m,2H).
实施例193d 3-甲酰基-5,6,7,8-四氢吲嗪-2-羧酸甲酯193d
将配备有磁力搅拌子的100-mL圆底烧瓶用氮气吹洗并装入无水二氯乙烷(20mL)和无水DMF(0.70mL,9.0mmol)。在0℃,历时2分钟向所述混合物加入三氯氧磷(0.70mL,7.3mmol),同时维持反应温度在0℃至10℃之间。移去冷却浴并将反应混合物在室温搅拌1小时。加入193c(1.0g,5.6mmol)于乙腈(10mL)中的溶液并将反应混合物在室温搅拌3小时。之后,将其减压浓缩。将油性残余物用饱和NaHCO3水溶液(20mL)吸收并用乙酸乙酯(3X50mL)萃取。将合并的有机层用水(50mL)洗涤,用Na2SO4干燥并减压蒸发。将残余物通过硅胶柱色谱法(用1:5乙酸乙酯/石油醚洗脱)来纯化得到193d,其为白色固体(703mg,58%)。MS-ESI:(M+H)+208.3.1H NMR(500MHz,DMSO-d6)δ10.14(s,1H),6.40(s,1H),4.27(t,J=6.0Hz,2H),3.78(s,3H),2.78(t,J=6.0Hz,2H),1.94-1.85(m,2H),1.78-1.69(m,2H).
实施例193e 6,7,8,9-四氢哒嗪并[4,5-b]吲嗪-1(2H)-酮193e
在配备有回流冷凝器的100-mL单颈圆底烧瓶中装入193d(600mg,2.9mmol)和水合肼(20mL)。将反应混合物在100℃加热4小时。之后,将反应混合物冷却至室温并过滤得到193e,其为黄色固体(413mg,75%)。MS-ESI:(M+H)+190.1.1H NMR(500MHz,DMSO-d6)δ12.17(s,1H),8.24(s,1H),6.33(s,1H),4.16(t,J=6.0Hz,2H),2.88(t,J=6.5Hz,2H),2.00-1.96(m,2H),1.84-1.79(m,2H).
实施例193f 4-氯-2-(1-氧代-6,7,8,9-四氢哒嗪并[4,5-b]吲嗪-2(1H)-基)吡啶-3-甲醛193f
在配备有回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(40mL),193e(800mg,3.6mmol)、2-溴-4-氯吡啶-3-甲醛(2.8g,12.6mmol)和碳酸钾(1.2g,8.4mmol)。使氮气鼓泡通过所得混合物30分钟后,加入碘化亚铜(I)(800mg,4.2mmol)和4,7-二甲氧基-1,10-菲咯啉(1.0g,4.2mmol)并将反应混合物在90℃加热12小时。之后,将反应混合物冷却至室温并过滤。使滤液在二氯甲烷(60mL)和水(40mL)之间分配。分离出水层并用二氯甲烷(3X40mL)萃取。将合并的有机层用盐水(30mL)洗涤并用硫酸钠干燥。过滤除去干燥剂并减压浓缩滤液。将残余物通过硅胶柱色谱法(用1:1乙酸乙酯/石油醚洗脱)来纯化得到193f,其为棕色固体(513mg,收率37%)。MS-ESI:[M+H]+329.1.
实施例193g(S)-4-(1-甲基-5-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)-吡啶-2-基-氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-6,7,8,9四氢-哒嗪并[4,5-b]吲嗪-2(1H)-基)吡啶-3-甲醛193g
在配备有回流冷凝器的100-mL圆底烧瓶中装入193f(200mg,0.61mmol)、191j(293mg,0.60mmol)、乙酸钠(98mg,1.2mmol)、K3PO4(254mg,1.2mmol)、PdCl2(dppf)(50mg,0.060mmol)、乙腈(25mL)和水(1mL)。在使氮气鼓泡通过所述混合物30分钟后,将其在100℃加热3小时。将混合物冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用25:1二氯甲烷/甲醇洗脱)来纯化得到193g(206mg,53%),其为棕色固体。MS-ESI:[M+H]+648.3。
实施例193 2-[3-(羟基甲基)-4-[1-甲基-5-[[5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]-2-吡啶基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-6,7,8,9-四氢哒嗪并[4,5-b]吲嗪-1-酮193
向193g(180mg,0.28mmol)于甲醇(20mL)中的溶液中加入NaBH4(32mg,0.84mmol)。将混合物在20℃搅拌2小时并用水淬灭。然后将其减压蒸发并将残余物通过反相制备性-HPLC来纯化得到193(140mg,78%),其为灰白色固体。MS-ESI:[M+H]+650.4。1H NMR(500MHz,DMSO-d6)δ8.67(d,J=2.0Hz,1H),8.55(d,J=5.5Hz,1H),8.47(s,1H),8.48(s,1H),7.85(d,J=2.5Hz,1H),7.52-7.50(m,2H),7.38-7.36(m,1H),7.25(d,J=8.5Hz,1H),6.49(s,1H),4.72(t,J=5.0Hz,1H),4.57-4.54(m,2H),4.47(t,J=6.0Hz,1H),4.41(t,J=6.0Hz,1H),4.33-4.29(m,2H),4.28-4.25(m,2H),3.71-3.65(m,1H),3.60(s,3H),3.41-3.77(m,1H),3.10-3.08(m,1H),2.98-2.90(m,3H),2.57-2.52(m,1H),2.35-2.30(m,2H),2.18-2.16(m,1H),2.06-2.0(m,2H),1.89-1.82(m,2H),0.93(d,J=6.0Hz,3H).
实施例194a 1-甲基-3-(吡嗪-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮194a
在配备有磁力搅拌子和回流冷凝器的250-mL单颈圆底烧瓶中装入5-溴-1-甲基-3-(吡嗪-2-基氨基)吡啶-2(1H)-酮142a(600mg,2.0mmol)、Pin2B2(2.54g,10mmol)、Pd2(dba)3(100mg,0.10mmol)、X-phos(100mg,0.20mmol)、乙酸钾(600mg,6.0mmol)和二噁烷(80mL)。在经历三轮真空/氩气吹洗后,将混合物在65℃加热16小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物用石油醚洗涤得到194a,其为黄色固体(粗制产物)(1.0g,LCMS纯度:70%)。MS-ESI:[M+H]+329.4.
实施例194b 4-{1-甲基-6-氧代-5-[(吡嗪-2-基)氨基]-1,6-二氢吡啶-3-基}-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-甲醛194b
在配备有回流冷凝器的100-mL单颈圆底烧瓶中装入4-氯-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-甲醛124a(345mg,1.0mmol)、194a(659mg,2.0mmol)、Pd(dppf)Cl2(50mg,0.050mmol)、K3PO4(450mg,2.0mmol)、乙酸钠三水合物(300mg,2.0mmol)、水(6滴)和乙腈(40mL)。将体系排空并用氮气回填。将反应混合物在100℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用25:1二氯甲烷/甲醇洗脱)来纯化得到194b(250mg,49%),其为棕黄色固体。MS-ESI:[M+H]+512.3。
实施例194 3-[3-(羟基甲基)-4-[1-甲基-6-氧代-5-(吡嗪-2-基氨基)-3-吡啶基]-2-吡啶基]-6,7,8,9-四氢苯并噻吩并[2,3-d]哒嗪-4-酮194
将194b(200mg,0.4mmol)和NaBH4(48mg,1.2mmol)于甲醇(20mL)中的混合物在30℃搅拌2小时。将混合物用水淬灭(5mL)并减压浓缩。将残余物用乙酸乙酯(3X10mL)萃取。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到194(60mg,30%),其为白色固体。MS-ESI:[M+H]+514.2。1H NMR(500MHz,CDCl3)δ8.78(d,J=2.0Hz,1H),8.69(d,J=5.0Hz,1H),8.31(s,1H),8.29(s,1H),8.17(s,1H),8.13(s,1H),8.04(d,J=2.5Hz,1H),7.83(d,J=2.5Hz,1H),7.56(d,J=5Hz,1H),4.44-4.37(m,3H),3.76(s,3H),3.01-2.99(m,2H),2.88-2.86(m,2H),2.01-1.96(m,4H).
实施例195a 4,5,6,7-四氢-1H-吲哚-2-羧酸乙酯195a
向3-(2-氯环己-1-烯基)丙烯酸乙酯(21.4g,100mmol)于DMSO(100mL)中的溶液中加入叠氮化钠(9.75g,150mmol)。将反应混合物在105℃加热4小时。冷却至室温后,将混合物倒入冰水中。过滤收集所得析出物得到195a(18.0g,93.3%)。MS-ESI:[M+H]+194。
实施例195b 1-(2,2-二乙氧基乙基)-4,5,6,7-四氢-1H-吲哚-2-羧酸乙酯195b
在0℃,向NaH(1.44g,60.2mmol)于N,N-二甲基甲酰胺(DMF)(30mL)中的悬浮液中缓慢加入195a(5.80g,30.1mmol)。将所得混合物在室温搅拌0.5小时,然后加入2-溴-1,1-二乙氧基乙烷(11.9g,60.2mmol)。将反应混合物在70℃加热30小时并用水(100mL)淬灭。然后将混合物用乙酸乙酯(3X100mL)萃取。将合并的有机相减压浓缩并将残余物用硅胶柱色谱法(用40:1石油醚/乙酸乙酯洗脱)来纯化得到195b(4.7g,51%)。MS-ESI:[M-EtOH+H]+264.1H NMR(500MHz,DMSO-d6)δ6.65(s,1H),4.59(t,J=5.0Hz,1H),4.17-4.16(m,4H),3.59-3.57(m,2H),3.27-3.26(m,2H),2.61(t,J=6.0Hz,2H),2.51(t,J=6.0Hz,2H),1.73-1.71(m,2H),1.63-1.61(m,2H),1.25(t,J=7.0Hz,3H),1.02(t,J=7.0Hz,6H).
实施例195c 1-(2,2-二乙氧基乙基)-4,5,6,7-四氢-1H-吲哚-2-羧酸195c
向195b(4.7g,15.2mmol)于乙醇(20mL)、四氢呋喃(20mL)和水(30mL)的混合溶剂中的混合物中加入氢氧化钠(3.0g,75.0mmol)。将反应混合物在75℃加热两天并减压浓缩。将残余物悬浮在水中并用稀柠檬酸水溶液中和。将混合物用乙酸乙酯(3X100mL)萃取并将合并的有机相减压浓缩得到195c(3.32g,78%)。MS-ESI:[M-EtOH+H]+236.
实施例195d 1-(2,2-二乙氧基乙基)-4,5,6,7-四氢-1H-吲哚-2-甲酰胺195d
向195c(2.8g,10.0mmol)于N,N-二甲基甲酰胺(30mL)中的混合物中加入O-(7-氮杂苯并三唑-1-基)-N,N,N′,N′-四甲基脲鎓六氟磷酸盐(HATU)(5.7g,15.0mmol)、Et3N(1.5g,15.0mmol)和DMAP(128mg,1.0mmol)。将反应混合物在室温搅拌整夜。加入饱和氢氧化铵(30mL)并将所得混合物进一步搅拌2小时。然后将其用水(100mL)稀释并用乙酸乙酯(3X100mL)萃取。将合并的有机相减压浓缩并将残余物通过硅胶柱色谱法(用石油醚/乙酸乙酯(6:1至3:1)洗脱)来纯化得到195d(2.7g,96%)。MS-ESI:[M-EtOH+H]+235.1H NMR(500MHz,DMSO)δ7.35(bs,1H),6.70(bs,1H),6.60(s,1H),4.60(t,J=5.5Hz,1H),4.18(d,J=4.0Hz,2H),3.57-3.56(m,2H),3.25(m,2H),2.57(t,J=6.0Hz,2H),2.40(t,J=6.0Hz,2H),1.71(t,J=5.0Hz,2H),1.64(t,J=5.0Hz,2H),1.01(t,J=7.0Hz,6H).
实施例195e 6,7,8,9-四氢吡嗪并[1,2-a]吲哚-1(2H)-酮195e
将195d(2.7g,9.6mmol)和乙酸(10mL)的混合物在110℃加热2小时。将混合物冷却至室温,用碳酸钠水溶液中和并用乙酸乙酯(3X30mL)萃取。将合并的有机相减压浓缩得到195e,其为黄色固体(1.6g,88%)。MS-ESI:[M+H]+189.3.1H NMR(500MHz,DMSO-d6)δ10.28(s,1H),7.02(d,J=5.5Hz,1H),6.63(s,1H),,6.52(pt,J=5.5Hz,1H),2.66(t,J=6.0Hz,2H),2.57(t,J=6.0Hz,2H),1.83-1.82(m,2H),1.73-1.72(m,2H).
实施例195f 4-氯-2-(1-氧代-6,7,8,9-四氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛195f
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(15mL)、2-溴-4-氯吡啶-3-甲醛103a(503mg,2.28mmol)、195e(142mg,0.76mmol)、碳酸铯(490mg,1.5mmol)、CuI(143mg,0.76mmol)和4,7-二甲氧基-1,10-菲咯啉(127mg,0.52mmol)。在经历三轮真空/氩气吹洗后,将混合物在80℃加热10小时。然后将其冷却至室温并过滤。将滤液用盐水洗涤并减压浓缩。将所得残余物用硅胶柱色谱法(用1:4乙酸乙酯/石油醚洗脱)来纯化得到195f(160mg,65%),其为黄色固体。MS-ESI:[M+H]+328。
实施例195g 2-(3-(甲酰基)-4-(1-甲基-5-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-6,7,8,9-四氢-吡嗪并[1,2-a]吲哚-1(2H)-酮195g
在配备有回流冷凝器的50-mL单颈圆底烧瓶中装入195f(130mg,0.40mmol)、1-甲基-3-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮135a(154mg,0.40mmol)、Pd(dppf)Cl2(29mg,0.040mmol)、K3PO4(170mg,0.80mmol)、乙酸钠(66mg,0.80mmol)、水(6滴)和乙腈(10mL)。在经历三轮真空/氩气吹洗后,将混合物回流加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用30:1二氯甲烷/甲醇洗脱)来纯化得到195g,其为黄色固体(120mg,54%)。MS-ESI:[M+H]+551.2
实施例195 2-[3-(羟基甲基)-4-[1-甲基-5-[(5-甲基-6,7-二氢-4H-吡唑并[1,5-a]吡嗪-2-基)氨基]-6-氧代-3-吡啶基]-2-吡啶基]-6,7,8,9-四氢吡嗪并[1,2-a]吲哚-1-酮195
在0℃,向195g(120mg,0.22mmol)于甲醇(5mL)中的溶液中加入硼氢化钠(25mg,0.66mmol)。将反应混合物搅拌30分钟。然后将其用水(1.0mL)淬灭并减压浓缩。将残余物通过反相制备性-HPLC来纯化得到195(70mg,58%)。MS-ESI:[M+H]+553.3。1H NMR(500MHz,CDCl3)δ8.56(d,J=5.0Hz,1H),7.99(d,J=2.0Hz,1H),7.75(d,J=2.0Hz,1H),7.49(d,J=4.5Hz,1H),7.43(s,1H),7.07(s,1H),6.97(d,J=6.0Hz,1H),6.67(d,J=6.0Hz,1H),5.70(s,1H),5.08-5.06(m,1H),4.51-4.49(m,1H),4.36-4.34(m,1H),4.14-4.05(m,2H),3.72(s,3H),3.62-3.60(m,2H),2.91-2.89(m,2H),2.75-2.70(m,4H),2.49(s,3H),1.97-1.95(m,2H),1.86-1.84(m,2H).
实施例196a 2-环丙基嘧啶-4-胺196a
将环丙基胍盐酸盐(1.0g,8.3mmol)溶解在乙醇(25mL)和三乙胺(1.26g,12.5mmol)中,然后加入2-氯丙烯腈(870mg,10mmol)。将所得橙黄色溶液回流1小时。将混合物冷却至室温并过滤。真空浓缩滤液并将残余物通过反相Combiflash来纯化得到196a(300mg,27%),其为浅棕色固体。MS-ESI:[M+H]+136
实施例196b 5-溴-3-(2-环丙基嘧啶-4-基氨基)-1-甲基吡啶-2(1H)-酮196b
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入196a(300mg,2.22mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(593mg,2.22mmol)和碳酸铯(1.45g,4.44mmol)。在使氮气鼓泡通过所述悬浮液30分钟后,加入Xantphos(127mg,0.22mmol)和三(二亚苄基丙酮)二钯(0)(100mg,0.11mmol)。使体系经历三轮真空/氩气吹洗并回流加热5小时。然后将其冷却至室温并过滤。将固体用二氯甲烷(2X50mL)洗涤。将合并的滤液减压浓缩并将残余物用乙腈(5mL)洗涤得到196b(420mg,59%),其为黄色固体。MS-ESI:[M+H]+321
实施例196c 3-(2-环丙基嘧啶-4-基氨基)-1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮196c
在配备有磁力搅拌子和冷凝器的100-mL单颈圆底烧瓶中装入196b(380mg,1.2mmol)、Pin2B2(1.5g,5.9mmol)、Pd2(dba)3(55mg,0.060mmol)、X-phos(57mg,0.060mmol)、乙酸钾(350mg,3.6mmol)和1,4-二噁烷(20mL)。使反应混合物经历三轮真空/氩气吹洗并在60℃加热15小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物用石油醚洗涤得到196c(410mg,94%),其为黄色固体,将其不经进一步纯化直接用于下一步骤。MS-ESI:[M+H]+369
实施例196d 4-{5-[(2-环丙基吡啶-4-基)氨基]-1-甲基-6-氧代-1,6-二氢吡啶-3-基}-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-甲醛196d
在备有回流冷凝器的50-mL圆底烧瓶配中装入196c(258mg,0.70mmol)、4-氯-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-甲醛108a(240mg,0.70mmol)、K3PO4(297mg,1.4mmol)、乙酸钠(190mg,1.4mmol)、1,1’-二(二苯基膦基)二茂铁二氯化钯(II)(29mg,0.035mmol)、乙腈(10mL)和水(0.5mL)。在使氮气鼓泡通过所述混合物30分钟后,将其在氮气保护下在100℃加热1小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将混合物冷却至室温并用二氯甲烷(20mL)和水(20mL)稀释。分离出水层并用二氯甲烷(3X20mL)萃取。将合并的有机层用Na2SO4干燥,过滤并减压浓缩。将黑色残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(80/1至30/1)洗脱)来纯化得到196d(220mg,57%),其为黄色固体。MS-ESI:[M+H]+549
实施例196 3-[4-[5-[(2-环丙基嘧啶-4-基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮196
在室温,向196d(200mg,0.36mmol)于甲醇/二氯甲烷(5/5mL)中的溶液中加入NaBH4(42mg,1.1mmol)。在将反应混合物搅拌1小时后,LCMS表明反应完成。将混合物减压浓缩并向残余物中加入水(10mL)。然后将其用二氯甲烷(20mL×3)萃取。将合并的有机层用盐水(30mL)洗涤,用Na2SO4干燥,过滤并减压浓缩。将残余物通过制备性HPLC来纯化得到196(135mg,68%),其为白色固体。MS-ESI:[M+H]+551.1H NMR(500MHz,CDCl3)δ8.84(d,J=2.5Hz,1H),8.53(d,J=5.0Hz,1H),8.22(d,J=6.0Hz,1H),8.13(d,J=1.5Hz,1H),8.01(s,1H),7.38(d,J=5.0Hz,1H),6.86(s,1H),6.52(d,J=6.0Hz,1H),5.22-5.19(m,1H),4.72-4.69(m,1H),4.56-4.54(m,1H),4.31(t,J=11.0Hz,1H),4.17(d,J=5.0Hz,2H),3.94-3.91(m,1H),3.74(s,3H),2.58(d,J=5.5Hz,2H),2.53(s,2H),2.18-2.13(m,1H),1.29(s,6H),1.16-1.13(m,1H),1.06-0.95(m,3H).
实施例197a 4-(5-硝基吡啶-2-基)哌嗪-1-羧酸叔丁酯197a
将2-溴-5-硝基吡啶(5.0g,24.6mmol)、哌嗪-1-羧酸叔丁酯(13.8g,74.2mmol)、乙腈(150mL)的混合物回流搅拌2.5小时。反应结束后,减压除去溶剂得到197a,其为黄色固体(4.1g,54%)。MS-ESI:[M+H]+309.
实施例197b 4-(5-氨基吡啶-2-基)哌嗪-1-羧酸叔丁酯197b
将250-mL圆底烧瓶用氮气吹洗并装入197a(4.0g,13.0mmol)、10%钯/炭(10%水分,500mg)和甲醇(130mL)。将所述烧瓶排空,充入氢气并在室温搅拌15小时。然后将氢气排空并向所述烧瓶中充入氮气。通过用垫过滤除去催化剂并减压浓缩滤液得到197b(3.3g,91%)。MS-ESI:[M+H]+279
实施例197c 4-(5-(6-溴-4-甲基-3-氧代-3,4-二氢吡嗪-2-基氨基)吡啶-2-基)哌嗪-1-羧酸叔丁酯197c
将197b(500mg,1.8mmol)、3,5-二溴-1-甲基吡嗪-2(1H)-酮(530mg,2.0mmol)、N-乙基-N-异丙基丙烷-2-胺(1.5mL,0.90mmol)和丙烷-2-醇(20mL)的混合物在100℃搅拌15小时。反应结束后,减压除去溶剂。得到197c,其为棕色固体(375mg,45%)。MS-ESI:[M+H]+465。
实施例197d 5-溴-1-甲基-3-(6-(哌嗪-1-基)吡啶-3-基氨基)-吡嗪-2(1H)-酮197d
向197c(500mg,1.08mmol)于二氯甲烷(10mL)中的溶液中加入4.0M HCl/二噁烷(10mL)。将反应混合物在室温搅拌5小时。然后将其减压浓缩得到197d(358mg,91%)。MS-ESI:[M+H]+365。
实施例197e 5-溴-1-甲基-3-(6-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-3-基氨基)吡嗪-2(1H)-酮197e
将197d(0.75g,2.1mmol)、氧杂环丁烷-3-酮(0.24mL,4.2mmol)、NaBH3CN(0.32g,5.1mmol)和氯化锌/乙醚(5.1mL,5.1mmol)于甲醇(30mL)中的混合物在50℃搅拌5小时。过滤除去固体并减压浓缩滤液。将残余物通过硅胶柱色谱法(用10:1二氯甲烷/甲醇洗脱)来纯化得到197e(550mg,64%)。MS-ESI:[M+H]+421。
实施例197f乙酸(4-(4-甲基-6-(6-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-3-基氨基)-5-氧代-4,5-二氢吡嗪-2-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯197f
在配备有回流冷凝器的圆底烧瓶中装入197e(200mg,0.48mmol)、3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113i(364mg,0.95mmol)、PdCl2(dppf)(40mg,0.049mmol)、K3PO43H2O(250mg,0.95mmol)、乙酸钠(80mg,0.95mmol)、乙腈(10mL)和水(0.5mL)。在经历三轮真空/氩气吹洗后,将混合物在80℃加热3小时。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用1:20甲醇/二氯甲烷洗脱)来纯化得到197f,其为红色固体(230mg,70%)。MS-ESI:[M+H]+680
实施例197 2-[3-(羟基甲基)-4-[4-甲基-6-[[6-[4-(氧杂环丁烷-3-基)哌嗪-1-基]-3-吡啶基]氨基]-5-氧代-吡嗪-2-基]-2-吡啶基]-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1-酮197
将197f(200mg,0.30mmol)和氢氧化锂(70mg,3.0mmol)于THF(9mL),异丙醇(6mL)和水(1mL)中的混合物在室温搅拌0.5小时。将混合物减压浓缩并用水(4mL)稀释。然后将其用二氯甲烷(2X10mL)萃取并将合并的二氯甲烷萃取物减压浓缩。将残余物用反相制备性-HPLC来纯化得到197(59mg,30%),其为黄色固体。MS-ESI:[M+H]+638.1H NMR(500MHz,DMSO-d6)δ9.30(s,1H),8.70(d,J=2.5Hz,1H),8.49(d,J=5.5Hz,1H),8.14-8.11(m,1H),7.59(s,1H),7.55(d,J=5.0Hz,1H),6.82(d,J=9.5Hz,1H),6.58(s,1H),4.93(t,J=5.5Hz,1H),4.60-4.54(m,3H),4.48-4.42(m,3H),4.26-4.08(m,3H),3.86(d,J=12.0Hz,1H),3.54(s,3H),3.44-3.40(m,重叠,5H),2.66-2.53(m,2H),2.46-2.47(m,2H),2.35-2.33(m,4H),1.80-1.68(m,4H).
实施例198a 4-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(4-氧代-7,8,9,10-四氢哒嗪并[4,5-a]吲嗪-3(4H)-基)吡啶-3-甲醛198a
在配备有回流冷凝器的50-mL圆底烧瓶中装入4-氯-2-(4-氧代-7,8,9,10-四氢哒嗪并[4,5-a]吲嗪-3(4H)-基)吡啶-3-甲醛192c(118mg,0.36mmol)、1-甲基-3-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基-氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮101l(171mg,0.36mmol)、Na2CO3(78mg,0.72mmol)、Pd(dppf)Cl2(30mg,0.036mmol)、DMF(10mL)和水(1mL)。在使氮气鼓泡通过所述混合物30分钟后,将其在氮气保护下在50℃加热10小时。然后将其冷却至室温并减压蒸发。将残余物通过硅胶柱色谱法(用20:1二氯甲烷/甲醇洗脱)来纯化得到198a(93mg,40%),其为棕色固体。MS-ESI:[M+H]+634.3。
实施例198 3-[3-(羟基甲基)-4-[1-甲基-5-[[5-[4-(氧杂环丁烷-3-基)哌嗪-1-基]-2-吡啶基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,8,9,10-四氢哒嗪并[4,5-a]吲嗪-4-酮198
向198a(80mg,0.13mmol)于甲醇(4mL)中的溶液中加入NaBH4(14mg,0.39mmol)。将混合物在20℃搅拌2小时。然后将其减压蒸发并将残余物通过反相制备性-HPLC来纯化得到198(38mg,43%),其为灰白色固体。MS-ESI:[M+H]+636.4。1H NMR(500MHz,DMSO-d6)δ8.65(d,J=2.0Hz,1H),8.54(d,J=5.0Hz,1H),8.44(s,1H),8.25(s,1H),7.88(d,J=2.5Hz,1H),7.62(s,1H),7.50(d,J=2.0Hz,1H),7.46(d,J=4.5Hz,1H),7.39-7.36(m,1H),7.25-7.23(m,1H),4.67(bs,1H),4.55(t,J=6.5Hz,2H),4.46(t,J=6.0Hz,2H),4.33-4.31(m,2H),4.26-4.20(m,2H),3.59(s,3H),3.46-3.41(m,1H),3.09-3.03(m,6H),2.39-2.37(m,4H),2.04-1.96(m,2H),1.93-1.86(m,2H).
实施例199a咪唑并[1,2-a]嘧啶-7-胺199a
向嘧啶-2,4-二胺(3.0g,0.027mol)于乙醇(90mL)和NaHCO3水溶液(2M,20mL)中的溶液中加入2-氯乙醛(4.3g,0.055mol)。将混合物在70℃搅拌整夜。TLC显示起始物质消失。减压除去溶剂并将残余物用乙酸乙酯(3X30mL)萃取。将合并的有机层减压浓缩并将残余物通过硅胶柱色谱法(用1:5石油醚/乙酸乙酯洗脱)来纯化得到199a,其为白色固体(2.2g,60%)。MS:[M+H]+135.1。
实施例199b 5-溴-3-(咪唑并[1,2-a]嘧啶-7-基氨基)-1-甲基吡啶-2(1H)-酮199b
在配备有磁力搅拌子和回流冷凝器的250-mL圆底烧瓶中装入199a(2.2g,16.4mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(8.77g,32.8mmol)、Pd2dba3(1.5g,1.64mmol)、Xantphos(1.88g,3.28mmol)、Cs2CO3(10.7g.32.8mmol)和1,4-二噁烷(150mL)。将体系排空,然后用氮气回填。然后将其回流加热3小时。反应结束后,过滤混合物并将固体用甲醇(60mL)洗涤。将合并的滤液减压蒸发并将残余物通过硅胶柱色谱法(用20:1二氯甲烷/甲醇洗脱)来纯化得到199b,其为浅绿色固体(1.63g,31%)。MS:[M+H]+320.1
实施例199c 10-[4-氯-3-(羟基甲基)吡啶-2-基]-4,4-二甲基-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-9-酮199c
在0℃,在配备有磁力搅拌子的250-mL单颈圆底烧瓶中装入4-氯-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-甲醛108a(9.0g,26.1mmol,1.0当量)、甲醇(50mL)、二氯甲烷(30mL)和NaBH4(5.95g,156.6mmol,5.0当量)。将反应混合物搅拌1小时。反应结束后,将反应混合物用水淬灭并减压浓缩。将残余物用二氯甲烷萃取。将合并的有机层用Na2SO4干燥并减压浓缩。将残余物通过硅胶柱色谱法(用1:4乙酸乙酯/石油醚洗脱)来纯化得到199c,其为白色固体(7.0g,77%)。MS-ESI:[M+H]+345.9.
实施例199d乙酸(4-氯-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环-[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-基)甲酯199d
在配备有磁力搅拌子的250-mL单颈圆底烧瓶中装入199c(7.0g,20.2mmol,1.0当量)、三乙胺(4.08g,40.4mmol,2.0当量)和THF(50mL)。向所述混合物中滴加乙酰氯(2.36g,30.3mmol,1.5当量)于THF(20mL)中的溶液。将反应混合物在室温搅拌一小时。反应结束后,将其用冰水淬灭并减压蒸发。将残余物用二氯甲烷萃取。将合并的有机层用Na2SO4干燥并减压浓缩。将所得残余物用1:8乙酸乙酯/石油醚洗涤得到199d,其为白色固体(5.9g,76%)。MS-ESI:[M+H]+388.3.
实施例199e{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e
在配备有磁力搅拌子和回流冷凝器的250-mL单颈圆底烧瓶中装入199d(4.5g,1.0当量,11.6mmol)、Pin2B2(7.38g,2.5当量,29.0mmol)、PdCl2(dppf)(473mg,0.05当量,0.58mmol)、x-phos(470mg,0.1当量,1.16mmol)、乙酸钾(3.41g,3.0当量,34.8mmol)和二噁烷(100mL)。在经历三轮真空/氩气吹洗后,将混合物在65℃加热4小时。然后将其冷却至室温并过滤。减压浓缩滤液得到粗制199e,其为棕红色液体(4.0g,纯度:65%)。MS-ESI:[M+H]+398.3.
实施例199f乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-[5-({咪唑并[1,2-a]嘧啶-7-基}氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基]吡啶-3-基)甲酯199f
在配备有回流冷凝器的100-mL单颈圆底烧瓶中装入199b(500mg,1.5mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(1200mg,3.0mmol)、Pd(dppf)Cl2(65mg,0.075mmol)、K3PO4(650mg,3.0mmol)、乙酸钠三水合物(420mg,3.0mmol)、水(6滴)和乙腈(20mL)。将体系排空并用氮气回填。将反应混合物在100℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用25:1二氯甲烷/甲醇洗脱)来纯化得到199f(240mg,40%),其为棕黄色固体。MS-ESI:[M+H]+593.4.
实施例199 3-[3-(羟基甲基)-4-[5-(咪唑并[1,2-a]嘧啶-7-基氨基)-1-甲基-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮199
将199f(180mg,0.30mmol)和氢氧化锂(130mg,3.0mmol)于异丙醇/THF(5:3,8mL)和水(2mL)中的混合物在30℃搅拌1小时。真空蒸发混合物并将残余物用水(3mL)稀释。然后将其用乙酸乙酯(2X10mL)萃取。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过制备性HPLC来纯化得到199(40mg,30%),其为白色固体。MS-ESI:[M+H]+551.3.1H NMR(500MHz,CHCl3)δ9.09(d,J=1.5Hz,1H),8.51(d,J=5.0Hz,1H),8.23(s,1H),8.13(d,J=7.0Hz,1H),7.93(d,J=2.0Hz,1H),7.45(s,1H),7.38(d,J=5.0Hz,1H),7.27(s,1H),6.84(s,1H),6.47(d,J=7.5Hz,1H),5.10(s,1H),4.67-4.50(m,2H),4.32-4.18(m,3H),3.93-3.88(m,1H),3.74(s,3H),2.60-2.58(m,2H),2.52(s,2H),1.28(s,6H).
实施例200a 4-(6-硝基吡啶-3-基)-5,6-二氢吡啶-1(2H)-羧酸叔丁酯200a
将5-溴-2-硝基吡啶(2.0g,9.7mmol)、4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)-5,6-二氢吡啶-1(2H)-羧酸叔丁酯(3.0g,9.7mmol)、Pd(dppf)Cl2(792mg,0.97mmol)、K3PO4.3H2O(5.2g,19.4mmol)和乙酸钠(1.59g,19.4mmol)于乙腈(100mL)和水(5mL)中的混合物排空,然后用氮气回填。将反应混合物在80℃加热6小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用1:5乙酸乙酯/石油醚洗脱)来纯化得到200a,其为黄色固体(2.2g,74%)。
实施例200b 4-(6-氨基吡啶-3-基)哌啶-1-羧酸叔丁酯200b
将500-mL圆底烧瓶用氮气吹洗并装入200a(2.5g,8.2mmol)、10%钯/炭(50%水分,300mg)和甲醇(80mL)。将所述烧瓶排空,充入氢气并在氢气中在室温搅拌12小时。然后将氢气排空并向所述烧瓶中充入氮气。通过用垫过滤除去催化剂,减压浓缩滤液得到200b(1.8g,78%),其为白色固体。MS-ESI:[M+H]+278.1
实施例200c 4-(6-(5-溴-1-甲基-2-氧代-1,2-二氢吡啶-3-基氨基)吡啶-3-基)-5,6-二氢吡啶-1(2H)-羧酸叔丁酯200c
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入200b(2.0g,7.2mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(1.9g,7.2mmol)、碳酸铯(4.7g,14.4mmol)和1,4-二噁烷(50mL)。使氮气鼓泡通过所得混合物30分钟后,加入Xantphos(418mg,0.72mmol)和三(二亚苄基丙酮)二钯(0)(661mg,0.72mmol)。使反应混合物经历三轮真空/氩气吹洗并在100℃加热6小时。之后,将反应混合物冷却至室温并过滤。使滤液在乙酸乙酯(120mL)和水(60mL)之间分配。分离出水层并用乙酸乙酯(3×80mL)萃取。将合并的有机层用盐水(30mL)洗涤并用硫酸钠干燥。过滤除去干燥剂并减压浓缩滤液。将残余物通过硅胶柱色谱法来纯化(用1:4乙酸乙酯/石油醚洗脱)得到200c(2.0g,61%),其为黄色固体。MS-ESI:[M+H]+463.2
实施例200d 5-溴-1-甲基-3-(5-(1,2,3,6-四氢吡啶-4-基)吡啶-2-基氨基)吡啶-2(1H)-酮200d
将200c(1.0g,2.3mmol)和4M HCl/二噁烷(10mL)的混合物在室温搅拌4小时。将混合物减压浓缩。将残余物用氢氧化钠水溶液碱化并用二氯甲烷萃取。将合并的有机层用水和盐水洗涤,用Na2SO4干燥并减压浓缩得到200d(650mg,84%),其为黄色固体。MS-ESI:[M+H]+363.0
实施例200e 5-溴-1-甲基-3-(5-(1-(氧杂环丁烷-3-基)-1,2,3,6-四氢吡啶-4-基)吡啶-2-基氨基)吡啶-2(1H)-酮200e
将200d(500mg,1.4mmol)、氧杂环丁烷-3-酮(298mg,4.2mmol)、NaBH3CN(261mg,4.2mmol)和1mol/L氯化锌/乙氧基乙烷(4mL,4.2mmol)于甲醇(20mL)中的混合物在50℃搅拌5小时。向反应混合物中加入水(20mL)并将所得混合物用二氯甲烷(3×50mL)萃取。将合并的有机层减压浓缩并将残余物通过硅胶柱色谱法(用10:1二氯甲烷/甲醇洗脱)来纯化得到200e(450mg,78%),其为黄色固体。MS-ESI:[M+H]+419.1
实施例200f乙酸(4-(1-甲基-5-(5-(1-(氧杂环丁烷-3-基)-1,2,3,6-四氢吡啶-4-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯200f
在配备有回流冷凝器的圆底烧瓶中装入200e(300mg,0.72mmol)、3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113i(414mg,1.08mmol)、PdCl2(dppf)(57mg,0.070mmol)、K3PO43H2O(560mg,2.16mmol)、乙酸钠(177mg,2.16mmol)、乙腈(10mL)和水(0.5mL)。在经历三轮真空/氩气吹洗后,将混合物在80℃加热3小时。然后将其过滤并真空蒸发滤液。将残余物用硅胶柱色谱法(用1:20甲醇/二氯甲烷洗脱)来纯化得到200f,其为红色固体(324mg,68%)。MS-ESI:[M+H]+676.2
实施例200 2-[3-(羟基甲基)-4-[1-甲基-5-[[5-[1-(氧杂环丁烷-3-基)-3,6-二氢-2H-吡啶-4-基]-2-吡啶基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1-酮200
将200f(260mg,0.39mmol)和氢氧化锂(92.4mg,3.85mmol)于THF(9mL)、异丙醇(6mL)和水(1mL)中的混合物在室温搅拌0.5小时。将混合物减压浓缩并用水(4mL)稀释。然后将其用二氯甲烷(2X10mL)萃取并将合并的二氯甲烷萃取物减压浓缩。将残余物用反相制备性-HPLC来纯化得到200(53.1mg,20%),其为黄色固体。MS-ESI:[M+H]+634.2。1H NMR(500MHz,DMSO-d6)δ8.76(d,J=1.5Hz,1H),8.74(s,1H),8.49(d,J=5.5Hz,1H),8.24(d,J=2.0Hz,1H),7.73-7.71(m,1H),7.54(d,J=2.5Hz,1H),7.36(d,J=5.0Hz,1H),7.30(d,J=8.5Hz,1H),6.58(s,1H),6.11(s,1H),4.97(s,1H),4.57(t,J=6.5Hz,2H),4.38-4.49(m,4H),4.08-4.26(m,3H),3.86(d,J=12.0Hz,1H),3.61(s,3H),3.54-3.45(m,1H),2.95(s,2H),2.68-2.54(m,2H),2.48-2.46(m,重叠,6H),1.83-1.75(m,2H),1.73-1.65(m,2H).
实施例201a 5-溴-3-(咪唑并[1,2-a]吡啶-7-基氨基)-1-甲基吡嗪-2(1H)-酮201a
在配备有回流冷凝器的100-mL圆底烧瓶中装入咪唑并[1,2-a]吡啶-7-胺(665mg,5.0mmol)、Cs2CO3(3.26g,10mmol)、3,5-二溴-1-甲基吡嗪-2(1H)-酮(1.86g,7.0mmol)、Xantphos(289mg,0.50mmol)、Pd2(dba)3(458mg,0.50mmol)和1,4-二噁烷(30mL)。在使氮气鼓泡通过所述混合物30分钟后,将其在氮气中在100℃加热16小时。通过LCMS分析反应混合物,结果显示剩余非常少的起始物质。将反应混合物冷却至室温并过滤。将滤液用二氯甲烷(60mL)和水(50mL)稀释。分离出水层并用二氯甲烷(3×20mL)萃取。将合并的有机层用Na2SO4干燥,过滤并减压浓缩。将黑色残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(60/1至30/1)洗脱)来纯化得到201a(700mg,44%),其为浅黄色固体。MS-ESI:[M+H]+320
实施例201b乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-[6-({咪唑并[1,2-a]吡啶-6-基}氨基)-4-甲基-5-氧代-4,5-二氢吡嗪-2-基]吡啶-3-基)甲酯201b
在配备有回流冷凝器的25-mL单颈圆底烧瓶中装入201a(64mg,0.20mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(160mg,0.40mmol)、Pd(dppf)Cl2(10mg,0.012mmol)、K3PO4(100mg,0.39mmol)、NaOAc·3H2O(60mg,0.44mmol)、水(6滴)和乙腈(5mL)。将体系排空并用氮气回填。将反应混合物在100℃搅拌2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用20:1二氯甲烷/甲醇洗脱)来纯化得到201b(40mg,34%),其为棕黄色固体。MS-ESI:[M+H]+593.2.
实施例201 3-[3-(羟基甲基)-4-[6-(咪唑并[1,2-a]吡啶-6-基氨基)-4-甲基-5-氧代-吡嗪-2-基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮201
将201b(40mg,0.067mmol)和氢氧化锂(25mg,0.60mmol)于异丙醇/THF(3:2,5mL)和水(1mL)中的混合物在30℃搅拌1小时。真空蒸发混合物并将残余物用乙酸乙酯(2X10mL)萃取。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到201(10mg,30%),其为白色固体。MS-ESI:[M+H]+551.3。1H NMR(500MHz,CHCl3)δ9.58(s,1H),8.58(d,J=5.0Hz,1H),8.18(s,1H),8.12(s,1H),7.73(d,J=5.0Hz,1H),7.63-7.61(m,2H),7.55(s,1H),7.13-7.11(m,1H),6.87(s,1H),5.19-5.17(m,1H),4.77-4.75(m,1H),4.57-4.42(m,2H),4.20-4.17(m,2H),3.92-3.90(m,1H),3.70(s,3H),2.60-2.53(m,4H),1.29(s,6H).
实施例202a 4-(1-甲基-5-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(4-氧代-7,8,9,10-四氢哒嗪并[4,5-a]吲嗪-3(4H)-基)吡啶-3-甲醛202a
在配备有回流冷凝器的100-mL圆底烧瓶中装入4-氯-2-(4-氧代-7,8,9,10-四氢哒嗪并[4,5-a]吲嗪-3(4H)-基)吡啶-3-甲醛192c(200mg,0.60mmol)、1-甲基-3-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮135a(230mg,0.60mmol)、乙酸钠(100mg,1.2mmol)、K3PO4(320mg,1.2mmol)、PdCl2(dppf)(50mg,0.060mmol)、乙腈(25mL)和水(1mL)。在使氮气鼓泡通过所述混合物30分钟后,将其在氮气保护下在100℃加热3小时。将反应混合物冷却至室温并减压蒸发。将残余物通过硅胶柱色谱法(用25:1二氯甲烷/甲醇洗脱)来纯化得到202a(205mg,62%),其为棕色固体。MS-ESI:[M+H]+552.3。
实施例202 3-[3-(羟基甲基)-4-[1-甲基-5-[(5-甲基-6,7-二氢-4H-吡唑并[1,5-a]吡嗪-2-基)氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,8,9,10-四氢哒嗪并[4,5-a]吲嗪-4-酮202
向202a(180mg,0.33mmol)于甲醇(25mL)中的溶液中加入NaBH4(37mg,0.99mmol)。将混合物在20℃搅拌2小时并用水淬灭。然后将其减压蒸发并将残余物通过反相制备性-HPLC来纯化得到202(120mg,66%),其为白色固体。MS-ESI:[M+H]+554.3。1H NMR(500MHz,DMSO-d6)δ8.53(d,J=5.0Hz,1H),8.25(s,1H),8.19(s,1H),8.07(d,J=2.0Hz,1H),7.61(s,1H),7.45(d,J=5.0Hz,1H),7.43(d,J=2.5Hz,1H),5.89(s,1H),4.65(t,J=5.0Hz,1H),4.34-4.32(m,2H),4.26-4.20(m,2H),3.93-3.91(m,2H),3.58(s,3H),3.49(s,2H),3.06-3.04(m,2H),2.79-2.77(m,2H),2.35(s,3H),2.04-1.96(m,2H),1.93-1.86(m,2H).
实施例203a 5-甲基-4,5,6,7-四氢噻唑并[5,4-c]吡啶-2-胺203a
将1-甲基-4-哌啶酮(11.3g,100mmol)于2-丙醇(80mL)中的溶液加热至50℃。向所述溶液中依次加入氰胺(4.2g,100mmol)于2-丙醇(25mL)中的溶液和硫粉(3.2g,100mmol)。加入催化量的吡咯烷(1.3mL)后,将所得混合物在50℃搅拌2小时。使反应混合物冷却至室温并搅拌整夜。然后将其在冰-水浴中冷却至10℃或低于10℃并在相同温度搅拌1小时。过滤收集析出的晶体并用2-丙醇(20mL)洗涤。真空干燥湿的晶体得到203a(10g,59%)。MS:[M+H]+170。1H NMR(500MHz,DMSO-d6)δ6.70(s,2H),3.31(s,2H),2.61(t,J=5.5Hz,2H),2.45(m,2H),2.33(s,3H).
实施例203b 5-溴-1-甲基-3-(5-甲基-4,5,6,7-四氢噻唑并[5,4-c]吡啶-2-基氨基)吡啶-2(1H)-酮203b
按照就191g描述的操作,以203a(4.0g,23.5mmol)和3,5-二溴-1-甲基吡啶-2(1H)-酮(3.0g,17.8mmol)开始得到203b,其为黄色固体(2.8g,44%)。MS:[M+H]+357。
实施例203c 10-[3-(乙酰氧基甲基)-4-[1-甲基-5-({5-甲基-4H,5H,6H,7H-[1,3]噻唑并[5,4-c]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]吡啶-2-基]-4,4-二甲基-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-9-酮203c
在配备有回流冷凝器的50-mL圆底烧瓶中装入203b(178mg,0.50mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(200mg,0.50mmol)、K3PO4(212mg,1.0mmol)、乙酸钠(82mg,1.0mmol)、1,1’-二(二苯基膦基)二茂铁-二氯化钯(II)(21mg,0.025mmol)、乙腈(10mL)和水(0.5mL)。在使氮气鼓泡通过所述混合物30分钟后,将其在氮气保护下在100℃加热1h。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将反应混合物冷却至室温并过滤。减压浓缩滤液并将残余物用二氯甲烷(20mL)和水(10mL)稀释。分离出水层并用二氯甲烷(2×20mL)萃取。将合并的有机层用Na2SO4干燥,过滤并减压浓缩。将黑色残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(80/1至30/1)洗脱)来纯化得到203c(135mg,43%),其为黄色固体。MS-ESI:[M+H]+584
实施例203 3-[3-(羟基甲基)-4-[1-甲基-5-[(5-甲基-6,7-二氢-4H-噻唑并[5,4-c]吡啶-2-基)氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮203
在室温,向203c(140g,0.22mmol)于THF/异丙醇/水(5/2/2mL)中的溶液中加入LiOH(54mg,2.2mmol)。在将反应混合物搅拌1小时后,LCMS表明反应完成。然后将混合物减压浓缩并用水(3mL)稀释。然后将其用二氯甲烷(3X10mL)萃取。将合并的有机层用盐水(30mL)洗涤,用Na2SO4干燥,过滤并减压浓缩。将残余物通过制备性HPLC来纯化得到203(85mg,66%),其为白色固体。MS-ESI:[M+H]+586。1H NMR(500MHz,CDCl3)δ8.50(d,J=5.5Hz,1H),8.37(d,J=2.0Hz,1H),8.32(s,1H),7.95(d,J=2.0Hz,1H),7.34(d,J=5.0Hz,1H),6.85(s,1H),5.11-5.09(m,1H),4.67-4.64(m,1H),4.52(bs,1H),4.30-4.28(m,1H),4.16(d,J=4.5Hz,2H),3.89-3.86(m,1H),3.72(s,3H),3.60(s,2H),2.84-2.81(m,4H),2.58(d,J=5.0Hz,2H),2.53(s,3H),2.52(s,2H),1.28(s,6H).
实施例204a 4-(1-甲基-5-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-6,7,8,9-四氢哒嗪并[4,5-b]吲嗪-2(1H)-基)吡啶-3-甲醛204a
在配备有回流冷凝器的100-mL圆底烧瓶中装入4-氯-2-(1-氧代-6,7,8,9-四氢哒嗪并[4,5-b]吲嗪-2(1H)-基)吡啶-3-甲醛193f(200mg,0.60mmol)、1-甲基-3-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮135a(230mg,0.60mmol)、乙酸钠(100mg,1.2mmol)、K3PO4(320mg,1.2mmol)、PdCl2(dppf)(50mg,0.060mmol)、乙腈(25mL)和水(1mL)。使氮气鼓泡通过所得混合物30分钟后,将混合物在100℃加热3小时。将反应混合物冷却至室温并减压浓缩。将残余物通过硅胶柱色谱法(用20:1二氯甲烷/甲醇洗脱)来纯化得到204a(185mg,55%),其为棕色固体。MS-ESI:[M+H]+552.3。
实施例204 2-[3-(羟基甲基)-4-[1-甲基-5-[(5-甲基-6,7-二氢-4H-吡唑并[1,5-a]吡嗪-2-基)氨基]-6-氧代-3-吡啶基]-2-吡啶基]-6,7,8,9-四氢哒嗪并[4,5-b]吲嗪-1-酮204
向204a(160mg,0.29mmol)于甲醇(20mL)中的溶液中加入NaBH4(33.0mg,0.87mmol)。将混合物在20℃搅拌2小时并用水淬灭。然后将其减压蒸发并将残余物通过反相制备性-HPLC来纯化得到204(120mg,75%),其为白色固体。MS-ESI:[M+H]+554.3.1H NMR(500MHz,DMSO-d6)δ8.55(d,J=5.0Hz,1H),8.46(s,1H),8.23(s,1H),8.09(d,J=2.5Hz,1H),7.49(d,J=5.0Hz,1H),7.40(d,J=2.0Hz,1H),6.49(s,1H),5.89(s,1H),4.73(bs,1H),4.30(s,2H),4.27-4.25(m,2H),3.93-3.91(m,2H),3.58(s,3H),3.49(s,2H),2.95-2.93(m,2H),2.78-2.76(m,2H),2.34(s,3H),2.04-1.99(m,2H),1.88-1.83(m,2H).
实施例205a 2-硝基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪205a
在配备有磁力搅拌子的250-mL单颈圆底烧瓶中装入1-(2-溴乙基)-5-(溴甲基)-3-硝基-1H-吡唑125c(3.0g,9.64mmol)/THF(35mL)和氨水(135mL,25-28%)。将混合物在氮气中在室温搅拌72小时。然后减压浓缩反应混合物并使所得残余物在乙酸乙酯(100mL)和水(100mL)之间分配。将水层用乙酸乙酯(2×50mL)萃取。将合并的有机层用10%碳酸钾(2×100mL)、盐水(200mL)洗涤,并用硫酸钠干燥。过滤除去干燥剂,并减压浓缩滤液得到205a,其为黄色固体(1.23g,76%)。MS:[M+H]+169。
实施例205b 2-硝基-6,7-二氢吡唑并[1,5-a]吡嗪-5(4H)-羧酸叔丁酯205b
向205a(504mg,3.0mmol)于THF(20mL)中的溶液中加入(Boc)2O(785mg,3.60mmol)和DMAP(74mg,0.60mmol)。将反应混合物在室温搅拌整夜。然后将其过滤并减压浓缩滤液。将所得残余物通过硅胶柱色谱法(用100:1二氯甲烷/甲醇洗脱)来纯化得到205b,其为白色固体(750mg,80%)。MS-ESI:[M+H]+269.3
实施例205c 2-氨基-6,7-二氢吡唑并[1,5-a]吡嗪-5(4H)-羧酸叔丁酯205c
将100-mL单颈圆底烧瓶用氮气吹洗并装入205b(0.75g,2.80mmol)、10%钯/炭(50%水分,280mg)和甲醇(30mL)。将混合物排空、充入氢气并在室温搅拌2小时。然后将氢气排空并将氮气充入所述烧瓶中。通过用垫过滤除去催化剂并减压浓缩滤液得到205c(524mg,79%)。MS-ESI:[M+H]+239.1
实施例205d 2-(5-溴-1-甲基-2-氧代-1,2-二氢吡啶-3-基氨基)-6,7-二氢吡唑并[1,5-a]吡嗪-5(4H)-羧酸叔丁酯205d
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入205c(524mg,2.2mmol)、Pd2(dba)3(201mg,0.22mmol)、XantPhos(254mg,0.44mmol)、碳酸铯(1434mg,4.4mmol)和1,4-二噁烷(20mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热4小时。之后,将反应混合物冷却至室温。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用50:1二氯甲烷/甲醇洗脱)来纯化得到205d(600mg,70%),其为黄色固体。MS-ESI:[M+H]+424.2
实施例205e 2-(5-(3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基)-1-甲基-2-氧代-1,2-二氢吡啶-3-基氨基)-6,7-二氢吡唑并[1,5-a]吡嗪-5(4H)-羧酸叔丁酯205e
在配备有磁力搅拌子的密封管中装入205d(213mg,0.50mmol)、3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113i(192mg,0.50mmol)、Pd(dppf)Cl2(41mg,0.050mmol)、乙酸钠(82mg,1.0mmol)、K3PO4(212mg,1.0mmol)、乙腈(10mL)和水(0.5mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热2小时。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用25:1二氯甲烷/甲醇洗脱)来纯化得到205e(280mg,82%),其为黄色固体。MS-ESI:[M+H]+683.3
实施例205f乙酸(4-(1-甲基-6-氧代-5-(4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯205f
将205e(280mg,0.41mmol)、4.0M HCl/二噁烷(4mL)和二氯甲烷(4mL)的混合物在室温搅拌2小时。然后将其减压浓缩得到205f,其为黄色固体(165mg,66%),将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+583.3.
实施例205 2-[3-(羟基甲基)-4-[1-甲基-6-氧代-5-(4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-3-吡啶基]-2-吡啶基]-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1-酮205
将205f(165mg,0.28mmol)和氢氧化锂(67mg,2.80mmol)于异丙醇/THF(1:1,4mL)和水(1mL)中的混合物在室温搅拌1小时。真空蒸发混合物并用水(4mL)稀释。然后将其用乙酸乙酯(10mLX2)萃取。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到205(70mg,46%),其为白色固体。MS-ESI:[M+H]+541.2.1H NMR(500MHz,CDCl3)δ8.48(d,J=5.0Hz,1H),7.96(d,J=2.0Hz,1H),7.72(d,J=2.0Hz,1H),7.43(s,1H),7.35(d,J=5.5Hz,1H),6.90(s,1H),5.70(s,1H),5.01(s,1H),4.64-4.61(m,1H),4.50(s,1H),4.34(s,1H),4.16-3.99(m,6H),3.89-3.87(m,1H),3.71(s,3H),3.30(t,J=5.5Hz,2H),2.63-2.57(m,4H),1.92-1.89(m,2H),1.80-1.78(m,3H).
实施例206a 3-碘氮杂环丁烷-1-羧酸叔丁酯206a
将3-羟基氮杂环丁烷-1-羧酸叔丁酯(3.5g,0.020mol)于甲苯(200mL)中的溶液用咪唑(4.08g,0.060mol)、三苯基膦(0.60g,0.040mol)和碘(7.62g,0.030mol)处理。将混合物在100℃加热1小时。然后将其冷却至室温并倒在饱和NaHCO3溶液(30mL)中。通过加入碘破坏过量的三苯基膦直到碘持续在有机层中显色。将混合物用5%Na2SO3溶液洗涤,用Na2SO4干燥并真空蒸发。将残余物通过硅胶柱色谱法来纯化得到206a(5.31g,93%)。MS-ESI:[M+H]+284。
实施例206b 3-(6-硝基吡啶-3-基氧基)氮杂环丁烷-1-羧酸叔丁酯206b
将206a(2.24g,7.9mmol)、6-硝基吡啶-3-醇(1.0g,7.2mmol)和Cs2CO3(2.6g,7.9mmol)于DMF(8mL)中的混合物在密封管中在125℃加热整夜。过滤固体并用乙酸乙酯(2X20mL)洗涤。将合并的滤液真空蒸发并将残余物在反相Combiflash上纯化得到206b(1.25g,59%)。MS-ESI:[M+H]+296.
实施例206c 3-(6-氨基吡啶-3-基氧基)氮杂环丁烷-1-羧酸叔丁酯206c
将100-mL帕尔氢化瓶用氮气吹洗并装入206b(1.07g,3.6mmol)、10%钯/炭(50%水分,0.30g)和甲醇(60mL)。将所述瓶排空,充入氢气至压力为25psi并在帕尔氢化装置上震摇2小时。然后将氢气排空并向所述瓶中充入氮气。通过用垫过滤除去催化剂并减压浓缩滤液得到206c(0.95g,99%)。MS-ESI:[M+H]+266.
实施例206d 3-(6-(5-溴-1-甲基-2-氧代-1,2-二氢吡啶-3-基氨基)吡啶-3-基氧基)氮杂环丁烷-1-羧酸叔丁酯206d
在配备有回流冷凝器的100-mL圆底烧瓶中装入206c(950mg,3.6mmol)、XantPhos(125mg,0.29mmol)、Pd2dba3(260mg,0.29mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(1.03g,3.9mmol)、Cs2CO3(1.8g,7.2mmol)和1,4-二噁烷(20mL)。将体系排空并用氮气回填。然后将其回流加热2小时。反应结束后,过滤混合物并用甲醇(100mL)洗涤。将合并的滤液真空蒸发并将残余物在反相Combiflash上纯化得到206d(1.46g,90%)。MS-ESI:[M+H]+451.
实施例206e 3-(5-(氮杂环丁烷-3-基氧基)吡啶-2-基氨基)-5-溴-1-甲基吡啶-2(1H)-酮盐酸盐206e
将206d(1.46g,3.2mmol)和HCl/1,4-二噁烷(3.2mL,4M,12.8mmol)于甲醇(20mL)中的混合物在80℃加热1小时。然后减压浓缩混合物得到206e(1.24g,99%)。MS-ESI:[M+H]+351。
实施例206f 5-溴-1-甲基-3-(5-(1-甲基氮杂环丁烷-3-基氧基)吡啶-2-基氨基)吡啶-2(1H)-酮206f
将206e(1.24g,3.2mmol)、37%甲醛水溶液(15mL,)、乙酸(1mL)和NaBH(OAc)3(1.36g,6.4mmol)于甲醇(10mL)中的混合物在室温搅拌4小时。真空蒸发溶剂并将残余物用乙酸乙酯(3X20mL)萃取。将合并的萃取物用硫酸钠干燥并减压浓缩。将残余物在反相Combiflash上纯化得到206f(940mg,80%)。MS-ESI:[M+H]+365.
实施例206g乙酸(4-(1-甲基-5-(5-(1-甲基氮杂环丁烷-3-基氧基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯206g
在配备有回流冷凝器的100-mL圆底烧瓶中装入206f(108mg,0.30mmol)、3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113i(115mg,0.30mmol)、Pd(dppf)Cl2(15mg,0.015mmol)、K3PO4(135mg,0.60mmol)、乙酸钠三水合物(90mg,0.60mmol)于乙腈(10mL)和水(0.5mL)中。将体系排空并用氮气回填。将反应混合物在100℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用25:1二氯甲烷/甲醇洗脱)来纯化得到206g(90mg,52%),其为棕黄色固体。MS-ESI:[M+H]+624.2。
实施例206 2-[3-(羟基甲基)-4-[1-甲基-5-[[5-(1-甲基氮杂环丁烷-3-基)氧基-2-吡啶基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1-酮206
将206g(93.6mg,0.15mmol)和氢氧化锂(65mg,1.5mmol)于THF/异丙醇(5:3,8mL)和水(2mL)中的混合物在30℃搅拌1小时。真空蒸发混合物并用水(3mL)稀释。然后将其用乙酸乙酯(2X10mL)萃取。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到206(35mg,42%),其为白色固体。MS-ESI:[M+H]+582.3。1H NMR(500MHz,CHCl3)δ8.62(d,J=1.5Hz,1H),8.51(d,J=5.0Hz,1H),7.86(d,J=2.0Hz,1H),7.84(s,1H),7.76(d,J=3.0Hz,1H),7.37(d,J=5.0Hz,1H),7.12-7.10(m,1H),6.90(s,1H),6.81-6.80(m,1H),5.07-5.04(m,1H),4.77(t,J=5.5Hz,1H),4.64-4.62(m,1H),4.52-4.50(m,1H),4.33-4.30(m,1H),4.16-4.10(m,2H),3.97-3.88(m,3H),3.72(s,3H),3.25-3.24(m,2H),2.63-2.57(m,4H),2.51(s,3H),1.93-1.91(m,2H),1.80-1.79(m,2H).
实施例207a乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-[1-甲基-5-({5-[(1-甲基氮杂环丁烷-3-基)氧基]吡啶-2-基}氨基)-6-氧代吡啶-3-基]吡啶-3-基)甲酯207a
在配备有回流冷凝器的50-mL单颈圆底烧瓶中装入5-溴-1-甲基-3-(5-(1-甲基氮杂环丁烷-3-基氧基)吡啶-2-基氨基)-吡啶-2(1H)-酮206f(108mg,0.40mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂-三环并[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(240mg,0.60mmol)、Pd(dppf)Cl2(20mg,0.02mmol)、K3PO4(180mg,0.80mmol)、乙酸钠三水合物(120mg,0.80mmol)、水(0.5mL)和乙腈(10mL)。将体系排空并用氮气回填。将反应混合物在100℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用10:1二氯甲烷/甲醇洗脱)来纯化得到207a(100mg,45%),其为棕黄色固体。LCMS-ESI:[M+H]+638.4.
实施例207 3-[3-(羟基甲基)-4-[1-甲基-5-[[5-(1-甲基氮杂环丁烷-3-基)氧基-2-吡啶基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮207
将207a(90mg,0.15mmol)和氢氧化锂(65mg,1.5mmol)于THF/异丙醇(5:3,8mL)和水(2mL)中的混合物在30℃搅拌1小时。将混合物减压蒸发并用水(4mL)稀释。然后将其用乙酸乙酯(2X20mL)萃取。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到207(30mg,38%),其为白色固体。LCMS:[M+H]+596.3。1H NMR(500MHz,CDCl3)δ8.61(d,J=2.0Hz,1H),8.51(d,J=5.0Hz,1H),7.86-7.83(m,2H),7.77(d,J=3.0Hz,1H),7.37(d,J=5.0Hz,1H),7.12-7.10(m,1H),6.85(s,1H),6.81(d,J=3.5Hz,1H),5.07-5.04(m,1H),4.74-4.64(m,2H),4.52-4.51(m,1H),4.34-4.32(m,1H),4.17-4.16(m,2H),3.88-3.87(m,3H),3.72(s,3H),3.17-3.16(m,2H),2.58(d,J=5.5Hz,2H),2.52(s,2H),2.45(s,3H),1.28(s,6H).
实施例208a 5-乙基-2-硝基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪208a
在配备有磁力搅拌子的150-mL单颈圆底烧瓶中装入甲醇(60mL)、2-硝基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪205a(1.5g,8.9mmol)、ZnCl2(2.43g,17.8mmol)、乙醛(784mg,17.8mmol)和NaBH3CN(1.12g,17.8mmol)。将混合物在室温搅拌2小时并减压浓缩。将残余物用硅胶柱色谱法(用40:1石油醚/乙酸乙酯洗脱)来纯化得到208a(1.4g,81%),其为黄色油状物。MS-ESI:[M+H]+197
实施例208b 5-乙基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-胺208b
将50-mL单颈圆底烧瓶用氮气吹洗并装入208a(1.4g,7.1mmol)、10%钯/炭(50%水分,208mg)、甲醇(30mL)和氢气。将混合物在氢气中在室温搅拌2小时。通过用垫过滤除去催化剂并减压浓缩滤液得到208b(1.0g,84%),其为黄色油状物。MS-ESI:[M+H]+167
实施例208c 5-溴-3-(5-乙基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-1-甲基吡啶-2(1H)-酮208c
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入208b(1.0g,6.0mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(1.6g,6.0mmol)、Pd2(dba)3(274mg,0.30mmol)、XantPhos(347mg,0.60mmol)、碳酸铯(3.9g,12.0mmol)和1,4-二噁烷(50mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃搅拌3小时。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用40:1二氯甲烷/甲醇洗脱)来纯化得到208c(630mg,29%),其为黄色固体。MS-ESI:[M+H]+352
实施例208d 3-(5-乙基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮208d
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(20mL)、208c(350mg.0.99mmol)、双(频哪醇合)二硼烷(1.31g,4.99mmol)、Pd2(dba)3(45mg,0.050mmol)、X-phos(58mg,0.10mmol)和乙酸钾(291mg,2.97mmol)。在使氮气鼓泡通过所述混合物30分钟后,将其在90℃加热3小时。然后将其过滤并真空蒸发滤液。将残余物用石油醚洗涤得到208d(120mg,30%),其为棕色固体。MS-ESI:[M+H]+400.2
实施例208e 4-(5-(5-乙基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢-吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-3-甲醛208e
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入208d(120mg,0.30mmol)、4-氯-2-(1-氧代-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-3-甲醛139a(99mg,0.30mmol)、PdCl2(dppf)(13mg,0.015mmol)、K3PO4(127mg,0.60mmol)、乙酸钠(49mg,0.60mmol)、乙腈(10mL)和水(0.5mL)。将体系排空并用氮气回填。将反应混合物在100℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用30:1二氯甲烷/甲醇洗脱)来纯化得到208e(95mg,56%),其为黄色固体。MS-ESI:[M+H]+567.2。
实施例208 2-[4-[5-[(5-乙基-6,7-二氢-4H-吡唑并[1,5-a]吡嗪-2-基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-1-酮208
在0℃,向208e(95mg,0.16mmol)于甲醇(10mL)中的混合物中加入硼氢化钠(19mg,0.50mmol)。将反应混合物搅拌30分钟并用水(2.0mL)淬灭。然后将其减压浓缩并将残余物通过反相制备性-HPLC来纯化得到208(8mg,9%),其为白色固体。MS-ESI:[M+H]+569.3.1HNMR(500MHz,CDCl3)δ8.46(d,J=5.0Hz,1H),7.92(d,J=2.0Hz,1H,7.70(d,J=2.0Hz,1H),7.40(s,1H),7.30(d,J=5.0Hz,1H),6.30(s,1H),5.71(s,1H),4.93-4.96(m,1H),4.63-4.61(m,1H),4.42-4.26(m,2H),4.09(s,2H),3.94-3.81(m,3H),3.69-3.68(m,重叠,5H),3.06-2.90(m,4H),2.81(d,J=3.0Hz,2H),2.66(d,J=3.5Hz,2H),2.04-2.00(m,2H),1.88-1.85(m,2H),1.20(t,J=7.5Hz,3H).
实施例209a 1-(2-硝基-6,7-二氢吡唑并[1,5-a]吡嗪-5(4H)-基)乙酮209a
向2-硝基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪205a(672mg,4.0mmol)于二氯甲烷(20mL)中的溶液中加入乙酰氯(936mg,12.0mmol)和K2CO3(1104mg,8.0mmol)。将混合物搅拌整夜。然后将其过滤并减压浓缩滤液。将所得残余物通过硅胶柱色谱法(用100:1二氯甲烷/甲醇洗脱)来纯化得到209a,其为白色固体(500mg,60%)。MS:[M+H]+211.2
实施例209b 1-(2-氨基-6,7-二氢吡唑并[1,5-a]吡嗪-5(4H)-基)乙酮209b
将50-mL单颈圆底烧瓶用氮气吹洗并装入209a(492mg,2.34mmol)、10%钯/炭(50%水分,234mg)和甲醇(20mL)。将混合物排空,充入氢气并在室温搅拌2小时。然后将氢气排空并将氮气充入所述烧瓶中。通过用垫过滤除去催化剂并减压浓缩滤液得到209b(380mg,80%)。MS:[M+H]+181.1
实施例209c 3-(5-乙酰基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-5-溴-1-甲基吡啶-2(1H)-酮209c
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入3,5-二溴-1-甲基吡啶-2(1H)-酮(481mg,1.8mmol)、209b(270mg,1.5mmol)、1,4-二噁烷(20mL)、Pd2(dba)3(137mg,0.15mmol)、XantPhos(173mg,0.30mmol)和碳酸铯(978mg,3.0mmol)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热6小时。之后,将反应混合物冷却至室温。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用50:1二氯甲烷/甲醇洗脱)来纯化得到209c(540mg,89%),其为黄色固体.MS:[M+H]+368.0
实施例209d 3-(5-乙酰基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮209d
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入209c(365mg,1.0mmol)、Pin2B2(1.26g,5.0mmol)、Pd2(dba)3(91mg,0.10mmol)、X-phos(92mg,0.20mmol)、AcOK(294mg,3.0mmol)和二噁烷(10mL)。在经历三轮真空/氩气吹洗后,将混合物在60℃加热16小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用50:1二氯甲烷/甲醇洗脱)来纯化得到209d,其为棕色固体(330mg,80%)。MS:[M+H]+414.2
实施例209e乙酸(4-(5-(5-乙酰基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯209e
在配备有磁力搅拌子的密封管中装入209d(185mg,0.50mmol)、乙酸(4-氯-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并-[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯113h(192mg,0.50mmol)、Pd(dppf)Cl2(41mg,0.050mmol)、乙酸钠(82mg,1.0mmol,)、K3PO4(212mg,1.0mmol)、水(0.5mL)和乙腈(10mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热2小时。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用25:1二氯甲烷/甲醇洗脱)来纯化得到209e(150mg,48%),其为黄色固体。MS-ESI:[M+H]+625.4
实施例209 2-[4-[5-[(5-乙酰基-6,7-二氢-4H-吡唑并[1,5-a]吡嗪-2-基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1-酮209
将209e(150mg,0.24mmol)和氢氧化锂(58mg,2.4mmol)于异丙醇/THF(1:1,4mL)和水(1mL)中的混合物在室温搅拌1小时。真空蒸发混合物并用水(4mL)稀释。然后将其用乙酸乙酯(2X10mL)萃取。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到209(75mg,53%),其为白色固体。MS-ESI:[M+H]+583.3.1H NMR(500MHz,T=80℃,DMSO-d6)δ8.44(d,J=8.5Hz,1H),7.93-7.90(m,2H),7.34(d,J=4.5Hz,1H),7.29(d,J=8.5Hz,1H),6.56(s,1H),5.98(s,1H),4.72-4.63(m,3H),4.45-4.43(m,2H),4.16-4.10(m,3H),3.99-3.86(m,重叠,5H),3.58(s,3H),2.62-2.57(m,2H),2.49-2.47(m,2H),2.08(s,3H),1.83-1.77(m,2H),1.72-1.68(m,2H).
实施例210a 4-氯-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环-[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-羧酸210a
向4-氯-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-甲醛108a(500mg,1.46mmol)、叔丁醇(20mL)和二氯甲烷(5mL)的混合物加入2-甲基-2-丁烯(3066mg,43.8mmol)。在-10℃,滴加NaClO2(263mg,2.92mmol)和NaH2PO4·2H2O(683mg,4.38mmol)的水溶液(8mL)并将反应混合物在-10℃搅拌整夜。将其减压浓缩并将残余物用乙酸乙酯(4×20mL)萃取。将合并的有机萃取物用MgSO4干燥并浓缩。将残余物用反相制备性-HPLC来纯化得到210a(315mg,60%),其为浅黄色固体。MS-ESI:[M+H]+360.1
实施例210b 2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-[1-甲基-5-({5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]吡啶-3-羧酸210b
在配备有回流冷凝器的25-mL圆底烧瓶中装入210a(400mg,1.1mmol)、(S)-1-甲基-3-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮191j(536mg,1.1mmol)、PdCl2(dppf)(81mg,0.11mmol)、K3PO4(466mg,2.2mmol)、乙酸钠(216mg,2.2mmol)、乙腈(10mL)和水(0.2mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热3小时。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用1:3石油醚/乙酸乙酯洗脱)来纯化得到210b,其为黄色固体(306mg,41%)。MS-ESI:[M+H]+679.3
实施例210 2-(7,7-二甲基-4-氧代-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-3-基)-4-[1-甲基-5-[[5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]-2-吡啶基]氨基]-6-氧代-3-吡啶基]吡啶-3-甲酰胺210
在25-mL圆底烧瓶中装入210b(300mg,0.44mmol)、三乙胺(1mL)、DMAP(5mg,0.040mmol)、HATU(250mg,0.66mmol)和DMF(10mL)。将混合物在室温搅拌0.5小时。然后缓慢加入37%氨水(15mL)并将反应混合物在室温再搅拌2.5小时。将混合物用20mL水处理并用二氯甲烷(3X20mL)萃取。将合并的有机萃取物减压浓缩并将残余物用反相制备性-HPLC纯化得到210(98mg,33%),其为黄色固体。MS-ESI:[M+H]+678.3.1H NMR(500MHz,DMSO)δ8.71(d,J=2.0Hz,1H),8.55(d,J=2.5Hz,1H),8.41(s,1H),7.84(d,J=3.0Hz,1H),7.61(s,1H),7.49(s,1H),7.45-7.42(m,2H),7.38-7.36(m,1H),7.24-7.22(m,1H),6.49(s,1H),4.57-4.54(m,2H),4.48-4.47(m,1H),4.43-4.40(m,1H),4.12-4.11(m,2H),4.04-4.00(m,2H),3.67-3.66(m,1H),3.57(s,3H),3.42-3.37(m,1H),3.10-3.08(m,1H),2.97-2.92(m,1H),2.55-2.53(m,3H),2.41(s,2H),2.36-2.29(m,2H),2.21-2.18(m,1H),1.21(s,6H),0.93(d,J=6.0Hz,3H)
实施例211 2-(7,7-二甲基-4-氧代-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-3-基)-N-甲基-4-[1-甲基-5-[[5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]-2-吡啶基]氨基]-6-氧代-3-吡啶基]吡啶-3-甲酰胺211
在圆底烧瓶中装入2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-[1-甲基-5-({5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]吡啶-3-羧酸210b(300mg,0.44mmol)、三乙胺(1mL)、DMAP(5mg,0.040mmol)、HATU(250mg,0.66mmol)和DMF(10mL)。将混合物在室温搅拌0.5小时。然后缓慢加入CH3NH2(27mg,0.88mmol)并将反应混合物在室温再搅拌2.5小时。将混合物用水(20mL)处理并用二氯甲烷(20mLX3)萃取。将合并的有机萃取物减压浓缩并将残余物用反相制备性-HPLC纯化得到211(106mg,35%),其为黄色固体。MS-ESI:[M+H]+692.5.1H NMR(500MHz,DMSO-d6)δ8.71(d,J=2.5Hz,1H),8.55(d,J=5.0Hz,1H),8.42(s,1H),8.11-8.08(m,1H),7.86(d,J=2.5Hz,1H),7.44-7.41(m,2H),7.38-7.35(m,1H),7.24-7.22(m,1H),6.48(s,1H),4.58-4.56(m,2H),4.48-4.46(m,1H),4.43-4.41(m,1H),4.08-4.07(m,2H),3.97-3.94(m,2H),3.66-3.65(m,1H),3.58(s,3H),3.41-3.39(m,1H),3.10-3.08(m,1H),2.97-2.93(m,1H),2.56(s,2H),2.53-2.48(m,重叠,4H),2.37-2.36(m,2H),2.35-2.31(m,2H),2.29-2.19(m,1H),1.21(s,6H),0.93(d,J=6.0Hz,3H).
实施例212a乙酸{4-[5-({5-乙酰基-4H,6H,7H-吡唑并[1,5-a]吡嗪-2-基}氨基)-1-甲基-6-氧代吡啶-3-基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]-十二碳-2(6),7-二烯-10-基}吡啶-3-基}甲酯212a
在配备有回流冷凝器的50-mL圆底烧瓶中装入3-(5-乙酰基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-5-溴-1-甲基吡啶-2(1H)-酮209c(185mg,0.50mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(200mg,0.50mmol)、Pd(dppf)Cl2(41mg,0.050mmol)、乙酸钠(82mg,1.0mmol)、K3PO4(212mg,1.0mmol)、水(0.5mL)和乙腈(10mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热2小时。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用25:1二氯甲烷/甲醇洗脱)来纯化得到212a(180mg,56%),其为黄色固体。MS-ESI:[M+H]+639.3
实施例212 3-[4-[5-[(5-乙酰基-6,7-二氢-4H-吡唑并[1,5-a]吡嗪-2-基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮212
将212a(180mg,0.28mmol)和氢氧化锂(67mg,2.8mmol)于异丙醇/THF(1:1,4mL)和水(1mL)中的混合物在30℃搅拌1小时。真空蒸发混合物并用水(4mL)稀释。然后将其用乙酸乙酯(2X10mL)萃取。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到212(70mg,42%),其为白色固体。MS-ESI:[M+H]+597.3.1H NMR(500MHz,T=80℃,DMSO-d6)δ8.47(d,J=8.0Hz,1H),7.95(d,J=4.0Hz,1H),7.92(s,1H),7.37(d,J=3.5Hz,1H),7.31(d,J=8.5Hz,1H),6.57(s,1H),6.00(s,1H),4.66(bs,2H),4.47(s,2H),4.20-4.18(m,3H),4.00-3.99(m,3H),3.92-3.88(m,3H),3.61(s,3H),2.59(s,2H),2.46(s,2H),2.11(s,3H),1.25(s,6H).
实施例213a 5-溴-1-甲基-3-(2-甲基嘧啶-4-基氨基)吡啶-2(1H)-酮213a
按照实施例196中描述的操作,使2-甲基嘧啶-4-胺(2.0g,18.3mmol)与3,5-二溴-1-甲基吡啶-2(1H)-酮(9.6g,36mmol)反应得到213a,其为黄色固体(2.3g,43.4%)。MS:[M+H]+295.1H NMR(500MHz,DMSO-d6)δ9.20(s,1H),8.78(s,1H),8.26(d,J=4.5Hz,1H),7.68(s,1H),7.18(d,J=4.5Hz,1H),3.59(s,3H),2.52(s,3H).
实施例213b 1-甲基-3-(2-甲基嘧啶-4-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮213b
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入双(频哪醇合)二硼烷(689mg,2.61mmol)、1,4-二噁烷(30mL)、213a(307mg,1.04mmol)、Pd2(dba)3(47mg,0.050mmol)、X-phos(48mg,0.10mmol)和乙酸钾(305mg,3.12mmol)。将混合物在65℃加热6小时。然后将其过滤并真空蒸发滤液得到213b(300mg,84%),其为棕色固体。MS:[M+H]+342.2
实施例213c 2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)-4-(1-甲基-5-(2-甲基嘧啶-4-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-甲醛213c
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入4-氯-2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛134c(150mg,0.43mmol)、213b(147mg 0.43mmol)、Pd(dppf)Cl2(35mg,0.043mmol)、乙酸钠(71mg,0.86mmol)、K3PO4(182mg,0.86mmol)、水(0.5mL)和乙腈(15mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热2.5小时。在冷却至室温后,过滤反应混合物。减压浓缩滤液并将残余物通过硅胶柱色谱法(用40:1二氯甲烷/甲醇洗脱)来纯化得到213c,其为黄色固体(130mg,57%)。MS-ESI:[M+H]+528.2。
实施例213 10-氟-2-[3-(羟基甲基)-4-[1-甲基-5-[(2-甲基嘧啶-4-基)氨基]-6-氧代-3-吡啶基]-2-吡啶基]-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1-酮213
在0℃,向213c(120mg,0.23mmol)于甲醇(10mL)中的溶液中加入硼氢化钠(26mg,0.69mmol)。将反应混合物搅拌20分钟并用水(10mL)淬灭。然后将其用二氯甲烷(3X20mL)萃取并将合并的有机层减压浓缩。将残余物通过反相制备性-HPLC来纯化得到213(62mg,44%),其为白色固体。MS-ESI:[M+H]+530.3.1H NMR(500MHz,DMSO-d6)δ9.11(s,1H),8.93(d,J=2.5Hz,1H),8.50(d,J=5.0Hz,1H),8.21(d,J=6.0Hz,1H),7.69(d,J=2.5Hz,1H),7.37(d,J=5.0Hz,1H),7.13(d,J=5.5Hz,1H),4.96(t,J=5.5Hz,1H),4.57-4.45(m,2H),4.23-4.18(m,2H),4.08-4.05(m,1H),3.90-3.87(m,1H),3.62(s,3H),2.64-2.56(m,2H),2.45(s,3H),2.43-2.42(m,2H),1.78-1.76(m,2H),1.72-1.66(m,2H).
实施例214a 3-溴-5-碘吡啶-2-醇214a
在配备有磁力搅拌子的100-mL单颈圆底烧瓶中装入乙腈(50mL)、三氟乙酸(10mL)、3-溴吡啶-2-醇(4.0g,11.56mmol)和N-碘琥珀酰亚胺(5.2g,11.56mmol)。将混合物在室温搅拌15小时。将混合物用水(100mL)稀释并过滤收集所得白色固体得到214a(6.6g,96%),其为白色固体。MS-ESI:[M+H]+300
实施例214b 3-溴-5-碘-1-甲基吡啶-2(1H)-酮214b
在配备有磁力搅拌子的100-mL单颈圆底烧瓶中装入DMF(50mL)、214a(6.0g,20.0mmol)、碘甲烷(4.26g,30.0mmol)和K2CO3(5.52g,40.0mmol)。将混合物在室温搅拌2小时并用水(200mL)稀释。过滤收集所得白色固体得到214b(5.97g,95%),其为白色固体。MS-ESI:[M+H]+314
实施例214c乙酸[4-(5-溴-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-基]甲酯214c
在配备有磁力搅拌子的100-mL单颈圆底烧瓶中装入214b(1.57g,5.0mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]-十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(1.98g,5.0mmol)、PdCl2(dppf)(205mg,0.25mmol)、K3PO4(2.12g,10.0mmol)、乙酸钠(820mg,10.0mmol)、乙腈(45mL)和水(1mL)。将体系排空并用氮气回填。将反应混合物在30℃搅拌3小时。然后将其过滤并减压浓缩滤液。将所得残余物通过硅胶柱色谱法(用30:1二氯甲烷/甲醇洗脱)来纯化得到214c(580mg,22%),其为白色固体。MS-ESI:[M+H]+539.2.1H NMR(500MHz,CDCl3)δ8.49(d,J=5.0Hz,1H),7.84(d,J=2.5Hz,1H),7.45(d,J=2.0Hz,1H),7.09(d,J=5.0Hz,1H),6.79(s,1H),5.15(s,2H),4.55-4.51(m,1H),4.27-4.25(m,1H),4.15-4.13(m,1H),4.06-4.04(m,1H),3.68(s,3H),2.58-2.56(m,2H),2.51(s,2H),1.86(s,3H),1.28(s,6H).
实施例214d乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-[1-甲基-6-氧代-5-({4H,6H,7H-吡喃并[4,3-d][1,3]噻唑-2-基}氨基)-1,6-二氢-吡啶-3-基]吡啶-3-基)甲酯214d
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入1,4-二噁烷(10mL)、214c(150mg,0.28mmol)、Pd2(dba)3(27mg,0.030mmol)、XantPhos(35mg,0.060mmol)和碳酸铯(183mg,0.56mmol)。在三轮真空/氩气冲洗后,将混合物在100℃加热10小时。之后,将反应混合物冷却至室温。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用50:1二氯甲烷/甲醇洗脱)来纯化得到214d(89mg,52%),其为黄色固体。MS-ESI:[M+H]+615.2
实施例214 3-[4-[5-(6,7-二氢-4H-吡喃并[4,3-d]噻唑-2-基氨基)-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮214
将214d(89mg,0.14mmol)、氢氧化锂(35mg,1.45mmol)和水/THF/异丙醇(3mL/5mL/5mL)的混合物在30℃搅拌2小时。然后将反应混合物减压浓缩并将残余物用二氯甲烷(2X10mL)萃取。将合并的二氯甲烷萃取物减压浓缩。将残余物用反相制备性-HPLC来纯化得到214(45mg,50%),其为黄色固体。MS-ESI:[M+H]+573.2.1H NMR(500MHz,DMSO-d6)δ10.01(s,1H),8.67(d,J=2.5Hz,1H),8.50(d,J=5.0Hz,1H),8.59(d,J=2.5Hz,1H),7.34(d,J=5.0Hz,1H),6.56(s,1H),4.96-4.94(m,1H),4.61(s,2H),4.46-4.43(m,2H),4.22-4.17(m,3H),3.89-3.87(m,3H),3.61(s,3H),2.62-2.57(m,4H),2.43(s,2H),1.22(s,6H).
实施例215a 3-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-5-{1-甲基-5-[(2-甲基嘧啶-4-基)氨基]-6-氧代-1,6-二氢吡啶-3-基}吡啶-4-甲醛215a
在密封管中装入3-溴-5-{4,4-二甲基-9-氧代-1,10-二氮杂三环-[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-吡啶-4-甲醛107f(210mg,0.54mmol)、1-甲基-3-(嘧啶-4-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2-酮213b(177mg,0.54mmol)、PdCl2(dppf)(42mg,0.050mmol)、K3PO4(210mg,1.0mmol)和乙酸钠(85mg,1.0mmol)、乙腈(8mL)和水(0.5mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热4小时。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法来纯化(用20:1二氯甲烷/甲醇洗脱)得到215a(150mg,53%)。MS-ESI:[M+H]+524.2.
实施例215 3-[4-(羟基甲基)-5-[1-甲基-5-[(2-甲基嘧啶-4-基)氨基]-6-氧代-3-吡啶基]-3-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮215
将215a(150mg,0.28mmol)和NaBH4(20mg,0.50mmol)于甲醇(5mL)中的混合物在25℃搅拌0.2小时。将混合物通过水(5mL)来淬灭并真空蒸发。将残余物用乙酸乙酯(3X10mL)萃取。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到215(80mg,53%)。MS-ESI:[M+H]+526.3.1H NMR(500MHz,DMSO-d6)δ9.09(s,1H),8.89(s,1H),8.56(s,1H),8.53(s,1H),8.20(d,J=4.0Hz,1H),7.61(s,1H),7.13(d,J=6.0Hz,1H),6.52(s,1H),5.19-5.18(m,1H),4.47-4.46(m,2H),4.23-4.20(m,3H),3.95-3.93(m,1H),3.62(s,3H),2.57(s,2H),2.42(s,3H),2.41(s,2H),1.21(s,6H).
实施例216a 1-甲基-3-(5-甲基-4,5,6,7-四氢噻唑并[5,4-c]吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮216a
将5-溴-1-甲基-3-(5-甲基-4,5,6,7-四氢噻唑并[5,4-c]吡啶-2-基氨基)吡啶-2(1H)-酮203b(997mg,2.8mmol)溶解在二噁烷(50mL)中,然后加入双(频哪醇合)二硼烷(3.0g,12.0mmol)、Pd2(dba)3(128mg,0.14mmol)、X-phos(134mg,0.28mmol)和乙酸钾(823mg,8.4mmol)。在经历三轮真空/氩气吹洗后,将混合物在65℃加热2小时。将混合物冷却至室温并过滤。减压浓缩滤液并将残余物用石油醚(2×10mL)洗涤得到216a,其为黄色固体(968mg,86%),将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+403.2
实施例216b 4-[1-甲基-5-({5-甲基-4H,6H,7H-[1,3]噻唑并[5,4-c]吡啶-2-基}氨基)-6-氧代吡啶-3-基]-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-甲醛216b
在配备有磁力搅拌子和回流冷凝器的圆底烧瓶中装入4-氯-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-甲醛124a(138mg,0.40mmol)、216a(240mg,0.60mmol)、PdCl2(dppf)(20mg,0.020mmol)、K3PO4(180mg,0.80mmol)、乙酸钠三水合物(120mg,0.80mmol)、水(6滴)和乙腈(15mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热2小时。然后,将其冷却至室温并过滤。减压蒸发滤液并将残余物通过硅胶柱色谱法(用25:1二氯甲烷/甲醇洗脱)来纯化得到216b,其为黄色固体(100mg,45%)。MS-ESI:[M+H]+586.2.
实施例216 3-[3-(羟基甲基)-4-[1-甲基-5-[(5-甲基-6,7-二氢-4H-噻唑并[5,4-c]吡啶-2-基)氨基]-6-氧代-3-吡啶基]-2-吡啶基]-6,7,8,9-四氢苯并噻吩并[2,3-d]哒嗪-4-酮216
向216b(100mg,0.15mmol)于甲醇(6mL)中的溶液中加入NaBH4(18mg,0.45mmol)。将反应混合物在30℃搅拌1小时并用盐水(10mL)淬灭。然后将其减压蒸发。将残余物用二氯甲烷(2X20mL)萃取并将合并的有机层减压浓缩。将所得残余物通过反相制备性-HPLC来纯化得到216,其为白色固体(40mg,40%)。MS-ESI:[M+H]+588.3。1H NMR(500MHz,CDCl3)δ8.68(d,J=5.0Hz,1H),8.43(d,J=2.0Hz,1H),8.31(s,1H),8.29(s,1H),7.79(d,J=2.5Hz,1H),7.55(d,J=5.0Hz,1H),4.43-4.39(m,3H),3.73(s,3H),3.57-3.55(m,2H),3.00-2.98(m,2H),2.88-2.86(m,2H),2.82-2.80(m,4H),2.50(s,3H),2.03-1.95(m,4H).
实施例217a乙酸(4-(5-溴-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯217a
在配备有磁力搅拌子的密封管中装入3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113i(766mg,2.0mmol)、3-溴-5-碘-1-甲基吡啶-2(1H)-酮214b(626mg,2.0mmol)、Pd(dppf)Cl2(164mg,0.20mmol)、乙酸钠(328mg,4.0mmol)、K3PO4(848mg,4.0mmol)、乙腈(10mL)和水(0.5mL)。在经历三轮真空/氩气吹洗后,将混合物在室温搅拌5小时。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用50:1二氯甲烷/甲醇洗脱)来纯化得到217a(700mg,67%),其为黄色固体。MS-ESI:[M+H]+525.2
实施例217b乙酸(4-(5-(1H-咪唑并[4,5-b]吡啶-5-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯217b
在配备有磁力搅拌子和回流冷凝器的25-mL单颈圆底烧瓶中装入217a(158mg,0.30mmol)、1H-咪唑并[4,5-b]吡啶-5-胺(80mg,0.60mmol)、Pd2(dba)3(27mg,0.030mmol)、XantPhos(35mg,0.061mmol)、碳酸铯(200mg,0.60mmol)和1,4-二噁烷(5mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃搅拌6小时。之后,将反应混合物冷却至室温。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用30:1二氯甲烷/甲醇洗脱)来纯化得到217b(40mg,23%),其为黄色固体。MS-ESI:[M+H]+579.4
实施例217 2-[3-(羟基甲基)-4-[5-(1H-咪唑并[4,5-b]吡啶-5-基氨基)-1-甲基-6-氧代-3-吡啶基]-2-吡啶基]-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1-酮217
将217b(40mg,0.070mmol)和氢氧化锂(26mg,0.70mmol)于异丙醇/THF(1:1,4mL)和水(1mL)中的混合物在室温搅拌1小时。真空蒸发混合物并将残余物用水和乙酸乙酯稀释。分离出水相并用乙酸乙酯(2X10mL)萃取。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到217(15mg,40%),其为白色固体。MS-ESI:[M+H]+537.3.1H NMR(500MHz,DMSO-d6)δ12.62(s,1H),8.91-8.64(m,2H),8.52(d,J=4.5Hz,1H),8.19-8.06(m,1H),7.89-7.79(m,1H),7.57-7.53(m,1H),7.43-7.40(m,1H),7.22(d,J=8.5Hz,1H),6.59(s,1H),5.06-4.96(m,1H),4.5-4.40(m,2H),4.26-4.11(m,3H),3.88-3.85(m,1H),3.62(s,3H),2.62-2.54(m,2H),2.50-2.48(m,2H),1.81-1.79(m,2H),1.71-1.67(m,2H).
实施例218a 5-溴-3-(1,5-二甲基-1H-吡唑-3-基氨基)-1-甲基吡啶-2(1H)-酮218a
在氮气下搅拌的同时,将5-溴-1-甲基-3-(5-甲基-1H-吡唑-3-基氨基)吡啶-2(1H)-酮(2.8g,9.9mmol)于无水DMF(10mL)中的溶液用60%NaH于矿物油(0.51g,13mmol)中的分散体来处理。沸腾后,将反应混合物再搅拌30分钟。之后,将反应混合物用碘甲烷(0.98g,7.0mmol)处理,并且在氮气中继续搅拌2小时。缓慢加入水(50mL)并过滤混合物。将滤液用乙酸乙酯(3X30mL)萃取。将合并的萃取物减压浓缩并将残余物通过快速柱色谱法(用3:1石油醚/乙酸乙酯洗脱)来纯化得到218a(0.70g,24%)。MS:[M+H]+297.
实施例218b乙酸(4-{5-[(1,5-二甲基-1H-吡唑-3-基)氨基]-1-甲基-6-氧代-1,6-二氢-吡啶-3-基}-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-基)甲酯218b
在配备有回流冷凝器的50-mL圆底烧瓶中装入218a(130mg,0.44mmol)、(3-(乙酰氧基甲基)-2-(7,7-二甲基-1-氧代-3,4,7,8-四氢-1H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-2(6H)-基)吡啶-4-基)硼酸199e(175mg,0.44mmol)、PdCl2(dppf)(36mg,0.044mmol)、K3PO4(343mg,1.32mmol)、乙酸钠(108mg,1.32mmol)、乙腈(10mL)和水(0.5mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热3小时。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用1:20甲醇/二氯甲烷洗脱)来纯化得到218b,其为红色固体(103mg,42%)。MS-ESI:[M+H]+570.2
实施例218 3-[4-[5-[(1,5-二甲基吡唑-3-基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮218
将218b(103mg,0.17mmol)、氢氧化锂(42mg,1.75mmol)、THF(3mL)、异丙醇(2mL)和水(1mL)的混合物在室温搅拌0.5小时。减压浓缩反应混合物并用水(4mL)稀释。然后将其用二氯甲烷(10mLX2)萃取并将合并的二氯甲烷萃取物减压浓缩。将残余物用反相制备性-HPLC来纯化得到218(29mg,48%),其为白色固体。MS-ESI:[M+H]+528.4.1H NMR(500MHz,DMSO-d6)δ8.48(d,J=5.0Hz,1H),8.04(s,1H),8.02(d,J=2.5Hz,1H),7.38(d,J=2.0Hz,1H),7.32(d,J=5.0Hz,1H),6.55(s,1H),5.89(s,1H),4.97(s,1H),4.48-4.39(m,2H),4.24-4.16(m,3H),3.86-3.84(m,1H),3.58(s,3H),3.57(s,3H),2.62-2.56(m,2H),2.42(s,2H),2.16(s,3H),1.22(s,6H).
实施例219a 3-(3-氨基苯基氨基)-5-溴-1-甲基吡嗪-2(1H)-酮219a
向3,5-二溴-1-甲基吡嗪-2(1H)-酮(536mg,2.0mmol)和苯-1,3-二胺(324mg,3.0mmol)于异丙醇(18mL)中的溶液中加入三乙胺(2.8mL)。将反应混合物在80℃搅拌整夜。然后将混合物减压蒸发得到219a(480mg,81%),其为白色固体。MS-ESI:[M+H]+295.0
实施例219b乙酸(4-{6-[(3-氨基苯基)氨基]-4-甲基-5-氧代-4,5-二氢吡嗪-2-基}-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-基)甲酯219b
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入219a(480mg,1.62mmol)、(3-(乙酰氧基甲基)-2-(7,7-二甲基-1-氧代-3,4,7,8-四氢-1H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-2(6H)-基)吡啶-4-基)硼酸199e(1.61g,4.05mmol)、Pd(dppf)Cl2(134mg,0.162mmol)、乙酸钾(318mg,3.24mmol)、K3PO4(706mg,3.24mmol)、乙腈(20mL)和水(8滴)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热2小时。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用20:1乙酸乙酯/甲醇洗脱)来纯化得到219b(354mg,38%),其为黄色固体。MS-ESI:[M+H]+568.3
实施例219 3-[4-[6-(3-氨基苯胺基)-4-甲基-5-氧代-吡嗪-2-基]-3-(羟基甲基)-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮219
将219b(283.5mg,0.50mmol)和氢氧化锂一水合物(630mg,15.0mmol)于异丙醇/THF(1:1,8mL)和水(2mL)中的混合物在35℃搅拌0.5小时。真空蒸发混合物并将残余物用水(3mL)稀释。然后将其用二氯甲烷(3X20mL)萃取。将合并的二氯甲烷萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到219(170mg,79%),其为浅黄色固体。MS-ESI:[M+H]+526.4.1H NMR(500MHz,DMSO-d6)δ8.85(s,1H),8.47(d,J=5.5Hz,1H),7.63(s,1H),7.56(s,1H),7.51(d,J=5.0Hz,1H),6.92-6.91(m,2H),6.57(s,1H),6.24-6.22(m,1H),5.13(s,2H),4.84-4.75(m,2H),4.49-4.46(m,1H),4.30-4.26(m,1H),4.20-4.19(m,2H),3.95-3.92(m,1H),3.56(s,3H),2.62-2.54(m,2H),2.43(s,2H),1.23(s,6H).
实施例220a(S)-2-氯-4-(1-甲基-5-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-甲醛220a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入(S)-1-甲基-3-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮191j(1.5g,1.0当量,3.11mmol)、4-溴-2-氯吡啶-3-甲醛104a(1.02g,1.5当量,4.67mmol)、PdCl2(dppf)(130mg,0.05当量,0.16mmol)、K3PO4(1.32g,2当量,6.22mmol)、乙酸钠(510mg,2.0当量,6.22mmol)、乙腈(35mL)和水(1.0mL)。在经历三轮真空/氩气吹洗后,将混合物在90℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用50:1二氯甲烷/乙醇洗脱)得到220a(1.1g,71%),其为黄色固体。MS-ESI:[M+H]+495.3。
实施例220b(S)-2-(3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)-4-(1-甲基-5-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-甲醛220b
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入220a(300mg,1.0当量,0.61mmol)、1,2,3,4,6,7,8,9-八氢吡嗪并[1,2-a]吲哚(128mg,1.2当量,0.73mmol)、Pd2(dba)3(55mg,0.1当量,0.060mmol)、X-Phos(30mg,0.1当量,0.060mmol)、Cs2CO3(390mg,2.0当量,1.22mmol)和二噁烷(15.0mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热16小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用40:1二氯甲烷/EtOH洗脱)来纯化得到220b(100mg,26%),其为黄色固体。MS-ESI:[M+H]+635.3。
实施例220 5-[2-(3,4,6,7,8,9-六氢-1H-吡嗪并[1,2-a]吲哚-2-基)-3-(羟基甲基)-4-吡啶基]-1-甲基-3-[[5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]-2-吡啶基]氨基]吡啶-2-酮220
在50-mL单颈圆底烧瓶中装入220b(100mg,1.0当量,0.15mmol)、NaBH4(30mg,5.0当量,0.75mmol)、甲醇(5mL)和二氯甲烷(5mL)。将混合物在0℃搅拌10分钟并用水(5mL)淬灭。然后将其过滤并减压浓缩滤液。将残余物通过反相制备性-HPLC来纯化得到标题化合物(10mg,10%)。MS-ESI:[M+H]+637.5.1H NMR(500MHz,DMSO-d6)δ8.61(d,J=2.0Hz,1H),8.44(s,1H),8.24(d,J=5.0Hz,1H),7.82(d,J=3.0Hz,1H),7.53(d,J=2.0Hz,1H),7.39-7.36(m,1H),7.24(d,J=9.0Hz,1H),6.99(d,J=5.0Hz,1H),5.55(s,1H),5.36-5.35(m,1H),4.57-4.54(m,2H),4.48-4.40(m,6H),3.92-3.90(m,2H),3.79-3.67(m,3H),3.59(s,3H),3.40-3.37(m,2H),3.09-3.07(m,1H),2.95-2.92(m,1H),2.55-2.51(m,2H),2.38-2.30(m,4H),2.17-2.16(m,1H),1.75-1.74(m,2H),1.68-1.65(m,2H),0.92(d,J=6.5Hz,3H).
实施例221a 3-[(6-氨基吡啶-2-基)氨基]-5-溴-1-甲基-1,2-二氢吡啶-2-酮221a
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入1,4-二噁烷(20mL)、3,5-二溴-1-甲基吡啶-2(1H)-酮(1.06g,4.0mmol)、吡啶-2,6-二胺(872mg,8.0mmol)、Pd2(dba)3(732mg,0.80mmol)、XantPhos(462.4mg,0.80mmol)和碳酸铯(2.6g,8.0mmol)。在经历三轮真空/氩气吹洗后,将混合物在110℃加热1小时。之后,将反应混合物冷却至室温。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用20:1乙酸乙酯/甲醇洗脱)来纯化得到221a(570mg,48%),其为白色固体。MS-ESI:[M+H]+295.0
实施例221b乙酸(4-{5-[(6-氨基吡啶-2-基)氨基]-1-甲基-6-氧代-1,6-二氢吡啶-3-基}-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-基)甲酯221b
在配备有磁力搅拌子和回流冷凝器的25-mL单颈圆底烧瓶中装入221a(354mg,1.2mmol)、(3-(乙酰氧基甲基)-2-(7,7-二甲基-1-氧代-3,4,7,8-四氢-1H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-2(6H)-基)吡啶-4-基)硼酸199e(1.20g,3.0mmol)、Pd(dppf)Cl2(99mg,0.12mmol)、乙酸钾(235mg,2.4mmol)、K3PO4(532mg,2.4mmol)、乙腈(12mL)和水(10滴)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热2小时。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用30:1乙酸乙酯/甲醇洗脱)来纯化得到221b(210mg,31%),其为黄色固体。MS-ESI:[M+H]+568.3
实施例221 3-[4-[5-[(6-氨基-2-吡啶基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮221
将221b(181mg,0.32mmol)和氢氧化锂一水合物(148mg,3.2mmol)于异丙醇/THF(1:1,6mL)和水(1.5mL)中的混合物在35℃搅拌0.5小时。将混合物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到221(82mg,49%),其为浅黄色固体。MS-ESI:[M+H]+526.3.1HNMR(500MHz,DMSO-d6)δ8.84(d,J=2.0Hz,1H),8.46(d,J=5.0Hz,1H),8.11(s,1H),7.54(d,J=2.0Hz,1H),7.38(d,J=5.0Hz,1H),7.23(d,J=8.0Hz,1H),6.57(s,1H),6.36(d,J=7.5Hz,1H),5.91(d,J=8.0Hz,1H),5.79(bs,2H),5.07(t,J=5.0Hz,1H),4.58-4.47(m,2H),4.27-4.20(m,3H),3.90(d,J=10.5Hz,1H),3.60(s,3H),2.62-2.57(m,2H),2.43(s,2H),1.22(s,6H).
实施例222a N-(5-氯-2-甲氧基吡啶-3-基)-2-甲基嘧啶-4-胺222a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(30mL)、3-溴-5-氯-2-甲氧基吡啶(865mg,3.9mmol)、2-甲基嘧啶-4-胺(327mg,3.0mmol)、Pd2(dba)3(275mg,0.30mmol)、XantPhos(173.4mg,0.30mmol)和碳酸铯(1.96g,6.0mmol)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热5小时。之后,将反应混合物冷却至室温。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用5:1乙酸乙酯/石油醚洗脱)来纯化得到222a(555mg,74%),其为白色固体。MS-ESI:[M+H]+251.0
实施例222b乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{6-甲氧基-5-[(2-甲基嘧啶-4-基)氨基]吡啶-3-基}吡啶-3-基)甲酯222b
在配备有磁力搅拌子的密封管中装入222a(550mg,2.2mmol)、(3-(乙酰氧基甲基)-2-(7,7-二甲基-1-氧代-3,4,7,8-四氢-1H-环戊二烯并[4,5]吡咯并-[1,2-a]吡嗪-2(6H)-基)吡啶-4-基)硼酸199e(2.18g,5.5mmol)、Pd2(dba)3(201mg,0.22mmol)、三环己基膦(84mg,0.30mmol)、Cs2CO3(1.43g,4.4mmol)、二噁烷(12mL)和水(1mL)。在经历三轮真空/氩气吹洗后,将混合物在110℃加热4小时。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用30:1乙酸乙酯/甲醇洗脱)来纯化得到222b(310mg,25%),其为黄色固体。MS-ESI:[M+H]+568.6
实施例222c 10-[3-(羟基甲基)-4-{6-甲氧基-5-[(2-甲基嘧啶-4-基)氨基]吡啶-3-基}吡啶-2-基]-4,4-二甲基-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-9-酮222c
将222b(283.5mg,0.50mmol)和氢氧化锂一水合物(630mg,15.0mmol)于异丙醇/THF(1:1,10mL)和水(2.5mL)中的混合物在35℃搅拌0.5小时。真空蒸发混合物并将残余物用水(3mL)稀释。然后将其用二氯甲烷(3X20mL)萃取。将合并的有机萃取物减压浓缩得到222c(240mg,92%),其为白色固体。MS-ESI:[M+H]+526.2
实施例222 3-[3-(羟基甲基)-4-[5-[(2-甲基嘧啶-4-基)氨基]-6-氧代-1H-吡啶-3-基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮222
向222c(226mg,0.43mmol)于二噁烷(8mL)中的溶液中加入浓HCl(1.1mL)。将反应混合物在100℃搅拌1小时。然后通过引入饱和NaHCO3水溶液将所述混合物调整至pH 7.0。将其用二氯甲烷(3X20mL)萃取并将合并的萃取物减压蒸发。将所得残余物通过反相制备性-HPLC来纯化得到222(30mg,14%),其为白色固体。MS-ESI:[M+H]+512.3.1H NMR(500MHz,DMSO-d6)δ12.24(s,1H),9.10(s,1H),8.96(d,J=2.0Hz,1H),8.50(d,J=5.0Hz,1H),8.22(d,J=6.5Hz,1H),7.50(d,J=2.0Hz,1H),7.40(d,J=5.0Hz,1H),7.13(d,J=6.0Hz,1H),6.57(s,1H),5.08-5.06(m,1H),4.50-4.42(m,2H),4.25-4.19(m,3H),3.87-3.85(m,1H),2.62-2.53(m,2H),2.45(s,3H),2.43(s,2H),1.23(s,3H),1.22(s,3H)
实施例223a 2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)-4-(1-甲基-5-(5-甲基-4,5,6,7-四氢噻唑并[5,4-c]吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-甲醛223a
在配备有回流冷凝器的50-mL圆底烧瓶中装入1-甲基-3-(5-甲基-4,5,6,7-四氢噻唑并[5,4-c]吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮216a(200mg,0.50mmol)、4-氯-2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛134c(174mg,0.50mmol)、K3PO4(212mg,1.0mmol)、乙酸钠(82mg,1.0mmol)、1,1’-二(二苯基膦基)二茂铁二氯化钯(II)(21mg,0.025mmol)和乙腈/水(15/1mL)。在使氮气鼓泡通过所述混合物30分钟后,将其在氮气保护下在100℃加热1小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将反应混合物冷却至室温并过滤。减压浓缩滤液。将残余物用二氯甲烷(50mL)和水(50mL)稀释。将水层用二氯甲烷(3X20mL)萃取。将合并的有机层用Na2SO4干燥,过滤并减压浓缩。将黑色残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(70/1至30/1)洗脱)来纯化得到223a(167mg,57%),其为黄色固体。MS-ESI:[M+H]+588.1
实施例223 10-氟-2-[3-(羟基甲基)-4-[1-甲基-5-[(5-甲基-6,7-二氢-4H-噻唑并[5,4-c]吡啶-2-基)氨基]-6-氧代-3-吡啶基]-2-吡啶基]-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1-酮223
将化合物223a(160mg,0.27mmol)溶解在甲醇(30mL)中,然后在0℃加入NaBH4(31mg,082mmol)。将反应混合物搅拌30分钟,然后用水(10mL)淬灭。将其减压浓缩并将残余物用二氯甲烷(3X30mL)萃取。将合并的有机相减压浓缩并将残余物通过反相制备性-HPLC来纯化得到223(56mg,35%),其为白色固体。MS-ESI:[M+H]+590.2.1H NMR(500MHz,DMSO-d6):δ9.92(s,1H),8.64(d,J=2.5Hz,1H),8.48(d,J=5.5Hz,1H),7.56(d,J=2.0Hz,1H),7.34(d,J=5.0Hz,1H),4.93(t,J=5.5Hz,1H),4.46-4.41(m,2H),4.19-4.17(m,2H),4.08-4.03(m,1H),3.88-3.85(m,1H),3.60(s,3H),3.42(s,2H),2.63-2.58(m,6H),2.41(s,3H),2.34(s,2H),1.78-1.76(m,2H),1.68-1.66(m,2H).
实施例224a(S)-4-(6-(6-氯-2-甲基-3-氧代-2,3-二氢哒嗪-4-基氨基)吡啶-3-基)-3-甲基哌嗪-1-羧酸叔丁酯224a
在配备有磁力搅拌子和回流冷凝器的250-mL单颈圆底烧瓶中装入(S)-4-(6-氨基吡啶-3-基)-3-甲基哌嗪-1-羧酸叔丁酯191f(2.5g,8.5mmol)、4-溴-6-氯-2-甲基哒嗪-3(2H)-酮(2.2g,10.0mmol)、XantPhos(240mg,0.40mmol)、三(二亚苄基丙酮)二钯(0)(360mg,0.40mmol)、Cs2CO3(5.5g,17mmol)和1,4-二噁烷(100mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热2.5小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(40:1至30:1)洗脱)来纯化得到224a,其为浅黄色固体(3.2g,86%)。MS-ESI:[M+H]+435.1。
实施例224b(S)-6-氯-2-甲基-4-(5-(2-甲基哌嗪-1-基)吡啶-2-基氨基)哒嗪-3(2H)-酮224b
将224a(3.0g,6.9mmol)和4.0M HCl/乙醇(20mL)的混合物在室温搅拌2小时。然后减压浓缩混合物得到粗制224b,其为黄色固体(2.5g,98%),将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+335.1.
实施例224c(S)-6-氯-2-甲基-4-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)哒嗪-3(2H)-酮224c
将224b(2.3g,6.8mmol)、氧杂环丁烷-3-酮(1.4g,20.0mmol)、NaBH3CN(620mg,10mmol)和氯化锌(1.36g,10mmol)于甲醇(20mL)中的混合物在50℃搅拌3小时。将混合物加至水(40mL)中并减压浓缩。将残余物用二氯甲烷萃取三次。将合并的有机层干燥并减压浓缩。将残余物通过硅胶柱色谱法(用50:1二氯甲烷/甲醇洗脱)来纯化得到224c(2.0g,75%)。MS-ESI:[M+H]+391.2.
实施例224d乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-[1-甲基-5-({5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢哒嗪-3-基]吡啶-3-基)甲酯224d
在配备有磁力搅拌子的密封管中装入224c(200mg,0.50mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(240mg,0.60mmol)、Pd(dppf)Cl2(18mg,0.025mmol)、乙酸钠(74mg,0.90mmol)、K3PO4(191mg,0.90mmol)和乙腈/水(6:1,3.5mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热1小时。然后将其冷却至室温并过滤。减压蒸发滤液并将残余物通过硅胶柱色谱法来纯化(用25:1二氯甲烷/甲醇洗脱)得到224d(180mg,51%),其为棕色固体。MS-ESI:[M+H]+708.3。
实施例224 3-[3-(羟基甲基)-4-[1-甲基-5-[[5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]-2-吡啶基]氨基]-6-氧代-哒嗪-3-基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮224
将224d(180mg,0.25mmol)和氢氧化锂(72mg,3.0mmol)于异丙醇/THF(5/3mL)和水(2mL)中的混合物在35℃搅拌0.2小时。将混合物减压蒸发并将残余物用乙酸乙酯(10mLX2)萃取。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过反相Combiflush来纯化(用0.3%NH4HCO3于水/乙腈中洗脱)得到224(54mg,33%),其为白色固体。MS-ESI:[M+H]+666.3.1HNMR(500MHz,DMSO-d6)δ9.29(s,1H),8.52(d,J=4.0Hz,1H),8.43(s,1H),7.91(s,1H),7.43-7.42(m,2H),7.40-7.39(m,1H),6.55(s,1H),4.77-4.75(m,1H),4.57-4.55(m,3H),4.48-4.47(m,1H),4.43-4.41(m,2H),4.28-4.26(m,1H),4.19-4.18(m,2H),3.88-3.86(m,2H),3.77(s,3H),3.38-3.37(m,1H),3.21-3.19(m,1H),2.98-2.96(m,1H),2.64-2.62(m,1H),2.58-2.56(m,2H),2.42-2.41(m,3H),2.26-2.25(m,1H),2.11-2.09(m,1H),1.21(s,6H),0.98(d,J=5.5Hz,3H).
实施例225a 6-氯-2-甲基-4-(2-甲基嘧啶-4-基氨基)哒嗪-3(2H)-酮225a
在配备有回流冷凝器的100-mL单颈圆底烧瓶中装入2-甲基嘧啶-4-胺(330mg,3.03mmol)、4-溴-6-氯-2-甲基哒嗪-3(2H)-酮(675mg,3.03mmol)、Pd2(dba)3(274mg,0.30mmol)、XantPhos(143mg,0.30mmol)、Cs2CO3(2960mg,9.09mmol)和二噁烷(40mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热整夜。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用1:20甲醇/二氯甲烷洗脱)来纯化得到225a,其为黄色固体(560mg,73%)。MS-ESI:[M+H]+252.1
实施例225b乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{1-甲基-5-[(2-甲基嘧啶-4-基)氨基]-6-氧代-1,6-二氢哒嗪-3-基}吡啶-3-基)甲酯225b
在配备有回流冷凝器的圆底烧瓶中装入225a(200mg,0.80mmol)、(3-(乙酰氧基甲基)-2-(7,7-二甲基-1-氧代-3,4,7,8-四氢-1H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-2(6H)-基)吡啶-4-基)硼酸199e(318mg,0.80mmol)、PdCl2(dppf)(65.3mg,0.080mmol)、K3PO4(624mg,2.4mmol)、乙酸钠(200mg,2.4mmol)、乙腈(10mL)和水(0.5mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热3小时。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用1:20甲醇/二氯甲烷洗脱)来纯化得到225b,其为红色固体(150mg,47%)。MS-ESI:[M+H]+569.3
实施例225 3-[3-(羟基甲基)-4-[1-甲基-5-[(2-甲基嘧啶-4-基)氨基]-6-氧代-哒嗪-3-基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮225
将225b(120mg,0.21mmol)、氢氧化锂(59mg,2.11mmol)、THF(6mL)、异丙醇(4mL)和水(2mL)的混合物在室温搅拌0.5小时。将混合物减压浓缩并用水(3mL)稀释。然后将其用二氯甲烷(2X10mL)萃取。将合并的二氯甲烷萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到225,其为白色固体(29mg,48%)。MS-ESI:[M+H]+527.3.1H NMR(500MHz,DMSO-d6)δ9.82(s,1H),8.88(s,1H),8.54(d,J=5.0Hz,1H),8.37(d,J=6.0Hz,1H),7.44(d,J=4.5Hz,1H),7.34(d,J=3.5Hz,1H),6.56(d,J=4.0Hz,1H),4.87(t,J=1.5Hz,1H),4.67(d,J=11.5Hz,1H),4.42(d,J=12.5Hz,1H),4.29-4.25(m,1H),4.20(bs,2H),3.93(d,J=9.5Hz,1H),3.81(s,3H),2.62-2.58(m,2H),2.50-2.49(m,在溶剂峰下面,2H),2.40(s,3H),1.22(s,6H).
实施例226a 6-氯-2-甲基-4-({5-[(吗啉-4-基)羰基]吡啶-2-基}氨基)-2,3-二氢哒嗪-3-酮226a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(40mL)、(6-氨基吡啶-3-基)(吗啉代)甲酮111a(2.07g,10.0mmol)、4-溴-6-氯-2-甲基哒嗪-3(2H)-酮(3.35g,15.0mmol)、Pd2(dba)3(915mg,1.0mmol)、XantPhos(578mg,1.0mmol)和碳酸铯(6.52g,20mmol)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热8小时。然后将其冷却至室温并过滤。将固体用二氯甲烷(2X20mL)洗涤。将合并的滤液用无水Na2SO4干燥并减压浓缩得到226a(2.45g,51%),其为黄色固体。MS:[M+H]+350.1
实施例226b乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-[1-甲基-5-({5-[(吗啉-4-基)羰基]吡啶-2-基}氨基)-6-氧代-1,6-二氢-哒嗪-3-基]吡啶-3-基)甲酯226b
在配备有磁力搅拌子的密封管中装入226a(279mg,0.80mmol)、乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-(四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-3-基)甲酯199e(1.53g,3.2mmol)、Pd2(dba)3(73.2mg,0.080mmol)、三环己基膦(44.6mg,0.16mmol)、碳酸铯(521.6mg,1.6mmol)、1,4-二噁烷(10mL)和水(8滴)。在经历三轮真空/氩气吹洗后,将混合物在110℃搅拌4小时。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用40:1乙酸乙酯/甲醇洗脱)来纯化得到226b,其为黄色固体(120mg,23%)。MS-ESI:[M+H]+667.3
实施例226 3-[3-(羟基甲基)-4-[1-甲基-5-[[5-(吗啉-4-羰基)-2-吡啶基]氨基]-6-氧代-哒嗪-3-基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮226
将226b(120mg,0.18mmol)和氢氧化锂一水合物(227mg,5.4mmol)于异丙醇/THF/水(3mL/3mL/2mL)中的混合物在35℃搅拌0.5小时。真空蒸发混合物并将残余物用二氯甲烷(3X10mL)萃取。将合并的二氯甲烷萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到226,其为白色固体(53mg,47%)。MS-ESI:[M+H]+625.3.1H NMR(500MHz,DMSO-d6)δ9.75(s,1H),8.64(s,1H),8.54(d,J=5.0Hz,1H),8.36(d,J=2.5Hz,1H),7.79-7.77(m,1H),7.59(d,J=8.5Hz,1H),7.43(d,J=5.0Hz,1H),6.56(s,1H),4.82(s,1H),4.60-4.57(m,1H),4.40-4.37(m,1H),4.27-4.25(m,1H),4.20-4.17(m,2H),3.91-3.88(m,1H),3.80(s,3H),3.60-3.45(m,重叠,8H),2.62-2.56(m,2H),2.42(s,2H),1.22(s,6H).
实施例227a乙酸{4-[1-甲基-5-({5-[(吗啉-4-基)羰基]吡啶-2-基}氨基)-6-氧代-1,6-二氢哒嗪-3-基]-2-{1-氧代-1H,2H,3H,4H,6H,7H,8H,9H-吡嗪并[1,2-a]吲哚-2-基}吡啶-3-基}甲酯227a
在配备有磁力搅拌子的密封管中装入6-氯-2-甲基-4-({5-[(吗啉-4-基)羰基]吡啶-2-基}氨基)-2,3-二氢哒嗪-3-酮226a(244mg,0.70mmol)、3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113i(558mg,1.5mmol)、Pd2(dba)3(64mg,0.070mmol)、三环己基膦(39mg,0.14mmol)、碳酸铯(456mg,1.4mmol)、1,4-二噁烷(7mL)和水(6滴)。在经历三轮真空/氩气吹洗后,将混合物在110℃搅拌4小时。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用40:1乙酸乙酯/甲醇洗脱)来纯化得到227a,其为黄色固体(290mg,63%)。MS-ESI:[M+H]+653.3
实施例227 2-[3-(羟基甲基)-4-[1-甲基-5-[[5-(吗啉-4-羰基)-2-吡啶基]氨基]-6-氧代-哒嗪-3-基]-2-吡啶基]-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1-酮227
将227a(131mg,0.20mmol)和氢氧化锂·1H2O(120mg,2.0mmol)于异丙醇/THF/水(4mL/4mL/2mL)中的混合物在35℃搅拌0.5小时。真空蒸发混合物并将残余物用二氯甲烷(3X10mL)萃取。将合并的二氯甲烷萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到227,其为白色固体(75mg,62%)。MS-ESI:[M+H]+611.2.1H NMR(500MHz,DMSO-d6)δ9.75(s,1H),8.64(s,1H),8.54(d,J=5.0Hz,1H),8.36(d,J=2.0Hz,1H),7.79-7.77(m,1H),7.59(d,J=8.5Hz,1H),7.43(d,J=5.0Hz,1H),6.58(s,1H),4.82(s,1H),4.60-4.57(m,1H),4.38-4.36(m,1H),4.29-4.19(m,2H),4.10-4.05(m,1H),3.93-3.90(m,1H),3.80(s,3H),3.60-3.50(m,重叠,8H),2.66-2.54(m,2H),2.48-2.46(m,2H),1.81-1.66(m,4H).
实施例228a(S)-乙酸(4-(1-甲基-5-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡嗪-2-基-氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯228a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入(S)-5-溴-1-甲基-3-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡嗪-2-基氨基)吡啶-2(1H)-酮(90mg,0.21mmol)191i、3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113i(80.4mg,0.21mmol)、Pd(dppf)Cl2(17.2mg,0.021mmol)、K3PO4(89mg,0.42mmol)、乙酸钠(57.1mg,0.42mmol)、水(0.5mL)和乙腈(30mL)。在经历三轮真空/氩气吹洗后,将混合物回流加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(50:1至30:1)洗脱)来纯化得到228a,其为棕色固体(60mg,42%)。MS-ESI:[M+H]+694.3.
实施例228 2-[3-(羟基甲基)-4-[1-甲基-5-[[5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]吡嗪-2-基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1-酮228
将228a(50mg,0.070mmol)和氢氧化锂(43mg,1.8mmol)于异丙醇/THF(1:1,4mL)和水(1mL)中的混合物在35℃搅拌30分钟。减压浓缩反应混合物并将残余物通过反相制备性-HPLC来纯化得到228(10mg,21%)。MS-ESI:[M+H]+652.3。1H NMR(500MHz,DMSO-d6)δ8.61(s,1H),8.48(d,J=4.5Hz,1H),8.39(s,1H),8.34(s,1H),7.84(s,1H),7.48(s,1H),7.34(d,J=5.0Hz,1H),6.58(s,1H),4.94(bs,1H),4.56-4.55(m,2H),4.49-4.47(m,1H),4.42-4.36(m,重叠,4H)4.25-4.17(m,2H),4.13-4.10(m,1H),3.86-3.76(m,2H),3.60(s,3H),3.39-3.37(m,1H),3.01-2.96(m,1H),2.78-2.76(m,1H),2.62-2.57(m,重叠,3H),2.50-2.47(m,2H),2.10-2.07(m,1H),1.94-1.90(m,1H),1.80-1.78(m,2H),1.70-1.69(m,2H),1.12(d,J=6.5Hz,3H).
实施例229a 2-乙基嘧啶-4-胺229a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入2-氯嘧啶-4-胺(2.60g,20.0mmol)、三乙基硼烷(20.0mL,1.0M于THF中,20.0mmol)、Pd(dppf)Cl2(816mg,1.0mmol)、K3PO4(13.0g,40.0mmol)、水(2mL)和四氢呋喃(50mL)。在经历三轮真空/氩气吹洗后,将混合物回流加热14小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用40:1二氯甲烷/甲醇洗脱)来纯化得到229a,其为黄色固体(600mg,24%)。MS-ESI:[M+H]+124.3
实施例229b 5-溴-3-(2-乙基嘧啶-4-基氨基)-1-甲基吡啶-2(1H)-酮229b
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入229a(246mg,2.0mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(534mg,2.0mmol)、Pd2(dba)3(182mg,0.20mmol)、XantPhos(231mg,0.40mmol)、Cs2CO3(1.30g,4.0mmol)和1,4-二噁烷(20mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热4小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用40:1二氯甲烷/甲醇洗脱)来纯化得到229b,其为灰白色固体(308mg,50%)。MS-ESI:[M+H]+309.1
实施例229c乙酸(2'-(7,7-二甲基-1-氧代-3,4,7,8-四氢-1H-环戊二烯并-[4,5]吡咯并[1,2-a]吡嗪-2(6H)-基)-5-((2-乙基嘧啶-4-基)氨基)-1-甲基-6-氧代-1,6-二氢-[3,4'-联吡啶]-3'-基)甲酯229c
在配备有回流冷凝器的100-mL圆底烧瓶中装入229b(277mg,0.90mmol)、(3-(乙酰氧基甲基)-2-(7,7-二甲基-1-氧代-3,4,7,8-四氢-1H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-2(6H)-基)吡啶-4-基)硼酸199e(358mg,0.90mmol)、Pd(dppf)Cl2(74mg,0.090mmol)、K3PO4(381mg,1.80mmol)、水(2mL)和四氢呋喃(20mL)。在经历三轮真空/氩气吹洗后,将混合物回流加热3小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用60:1二氯甲烷/甲醇洗脱)来纯化得到229c,其为白色固体(291mg,50%)。MS-ESI:[M+H]+582.4
实施例229 3-[4-[5-[(2-乙基嘧啶-4-基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮229
向229c(291mg,0.45mmol)于四氢呋喃(10mL)和水(2mL)中的溶液中加入氢氧化锂(48mg,2.0mmol)。将反应混合物在25℃搅拌1小时并减压浓缩。将残余物通过反相制备性-HPLC来纯化得到229(165mg,61%),其为黄色固体。MS-ESI:[M+H]+540.3.1H NMR(500MHz,DMSO-d6)δ9.12(s,1H),8.96(d,J=2.5Hz,1H),8.50(d,J=5.0Hz,1H),8.25(d,J=5.5Hz,1H),7.72(d,J=2.5Hz,1H),7.38(d,J=5.5Hz,1H),7.15(d,J=6.0Hz,1H),6.56(s,1H),5.00(t,J=5.5Hz,1H),4.55-4.44(m,2H),4.26-4.19(m,重叠,3H),3.88-3.86(m,1H),3.62(s,3H),2.74(q,J=7.5Hz,2H),2.59-2.54(m,2H),2.43(s,2H),1.22-1.20(m,重叠,9H).
实施例230a(S)-4-(5-溴吡嗪-2-基)-3-甲基哌嗪-1-羧酸叔丁酯230a
将(S)-3-甲基哌嗪-1-羧酸叔丁酯(6.0g,30mmol)和2,5-二溴吡嗪(14.1g,60mmol)的混合物在80℃搅拌15小时。然后将其冷却至室温并通过硅胶柱色谱法(用石油醚/乙酸乙酯(10:1至2:1)洗脱)来纯化得到230a,其为黄色固体(1.14g,19%)。MS:[M+H]+359.1.
实施例230b(S)-4-(5-(二苯基亚甲基氨基)吡嗪-2-基)-3-甲基哌嗪-1-羧酸叔丁酯230b
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入230a(2.6g,7.3mmol)、二苯基甲亚胺(1.3g,7.3mmol)、Pd2(dba)3(669mg,0.73mmol)、(R)-(+)-2,2'-二(二苯基膦基)-1,1'-联萘(968mg,1.46mmol)、Cs2CO3(4.7g,14.6mmol)和1,4-二噁烷(40mL)。在经历三轮真空/氩气吹洗后,将混合物在96℃加热3小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用石油醚/乙酸乙酯(10:1至3:1)洗脱)来纯化得到230b,其为红色油状物(3.3g,75%)。MS:[M+H]+458.3.
实施例230c(S)-4-(5-氨基吡嗪-2-基)-3-甲基哌嗪-1-羧酸叔丁酯230c
向230b(3.3g,7.2mmol)于甲醇(25mL)中的溶液中加入乙酸钠(708mg,8.6mmol)和羟基胺盐酸盐(907mg,8.6mmol)。将反应混合物搅拌0.5小时。然后将其真空浓缩。将残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(50:1至30:1)洗脱)来纯化得到230c,其为黄色油状物(1.35g,64%)。MS:[M+H]+294.3.
实施例230d(S)-4-(5-(5-溴-1-甲基-2-氧代-1,2-二氢吡啶-3-基氨基)吡嗪-2-基)-3-甲基哌嗪-1-羧酸叔丁酯230d
在配备有磁力搅拌子和回流冷凝器的250-mL单颈圆底烧瓶中装入230c(1.25g,4.3mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(3.4g,12.9mmol)、Pd2(dba)3(394mg,0.43mmol)、Xantphos(497mg,0.86mmol)、Cs2CO3(4.7g,14.6mmol)和1,4-二噁烷(80mL)。在经历三轮真空/氩气吹洗后,将混合物在90℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(50:1至30:1)洗脱)来纯化得到230d(1.9g,72%)。MS:[M+H]+481.2.
实施例230e(S)-5-溴-1-甲基-3-(5-(2-甲基哌嗪-1-基)吡嗪-2-基氨基)吡啶-2(1H)-酮230e
将230d(1.9g,3.97mmol)和三氟乙酸(4mL)的混合物在室温搅拌1小时。然后将其减压浓缩得到粗制230e(1.45g,97%),将其不经进一步纯化即用于下一步骤。MS:[M+H]+381.2。
实施例230f(S)-5-溴-1-甲基-3-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡嗪-2-基氨基)吡啶-2(1H)-酮230f
将230e(2.0g,5.3mmol)、氧杂环丁烷-3-酮(763mg,10.6mmol)、NaBH3CN(835mg,13.3mmol)和氯化锌(1.8g,13.3mmol)于甲醇(60mL)中的混合物在50℃搅拌30分钟。将混合物减压浓缩。向残余物中加入水并将所得混合物用二氯甲烷萃取三次。然后将合并的有机层减压浓缩并将残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(50:1至20:1)洗脱)来纯化得到230f,其为黄色油状物(1.6g,70%)。MS:[M+H]+437.2。
实施例230g 5-[4-氯-3-(羟基甲基)吡啶-2-基]-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-6-酮230g
将4-氯-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-甲醛124a(797mg,2.31mmol)、NaBH4(263mg,6.92mmol)和CH3OH(50mL)的混合物在室温搅拌1小时。将反应混合物用水(30mL)淬灭并减压浓缩。将残余物用二氯甲烷(2X30mL)萃取并将合并的二氯甲烷萃取物减压浓缩。将残余物通过硅胶色谱法(用5:1洗脱)来纯化得到230g(649mg,81%),其为黄色固体。MS-ESI:[M+H]+348.1。
实施例230h乙酸(4-氯-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-基)甲酯230h
在圆底烧瓶中装入230g(597mg,1.72mmol)、二氯甲烷(50mL)和三乙胺(5mL)。将所述溶液在0℃搅拌0.5小时并缓慢加入乙酰氯(135mg,1.72mmol)。将混合物在0℃再搅拌2.5小时。然后将其减压浓缩。将残余物通过硅胶柱色谱法(用9:1石油醚/乙酸乙酯洗脱)来纯化得到230h(602mg,90%),其为黄色固体。MS-ESI:[M+H]+390.1
实施例230i乙酸4-(二羟基硼烷基)-2-{6-氧代-8-硫杂-4,5-二氮杂三环-[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-基]甲酯230i
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入230h(595mg,1.53mmol)、Pin2B2(1.94g,7.65mmol)、PdCl2(dppf)(65mg,0.080mmol)、X-Phos(73mg,0.15mmol)、乙酸钾(304mg,3.1mmol)和二噁烷(50mL)。在经历三轮真空/氩气吹洗后,将混合物在65℃加热5小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物用石油醚洗涤得到230i(409mg,67%),其为黄色固体。MS-ESI:[M+H]+400.1
实施例230j乙酸{4-[1-甲基-5-({5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]吡嗪-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-基}甲酯230j
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入230f(100mg,0.23mmol)、230i(140mg,0.35mmol)、Pd(dppf)Cl2(19mg,0.023mmol)、乙酸钠(63mg,0.46mmol)、K3PO4(98mg,0.46mmol)、水(0.5mL)和乙腈(20mL)。在经历三轮真空/氩气吹洗后,将混合物在90℃加热3小时。冷却至室温后,过滤反应混合物。减压浓缩滤液并将残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(50:1至30:1)洗脱)来纯化得到230j,其为黄色固体(90mg,55%)。MS-ESI:[M+H]+710.2。
实施例230 3-[3-(羟基甲基)-4-[1-甲基-5-[[5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]吡嗪-2-基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-6,7,8,9-四氢苯并噻吩并[2,3-d]哒嗪-4-酮230
将230j(80mg,0.11mmol)和氢氧化锂(27mg,1.1mmol)于异丙醇/THF(1:1,10mL)和水(2mL)中的混合物在35℃搅拌0.5小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物通过反相制备性-HPLC来纯化得到230(34mg,45%)。MS-ESI:[M+H]+668.2.1HNMR(500MHz,DMSO-d6)δ8.64(s,1H),8.56(d,J=6.0Hz,1H),8.46(s,1H),8.40(d,J=2.5Hz,1H),8.34(d,J=1.5Hz,1H),7.85(s,1H),7.53(d,J=6.0Hz,1H),7.49(d,J=2.5Hz,1H),4.84(bs,1H),4.58-4.54(m,2H),4.50-4.47(m,1H),4.43-4.36(m,重叠,4H),3.78-3.75(m,1H),3.59(s,3H),3.39-3.35(m,1H),3.02-3.0(m,1H),2.98-2.95(m,2H),2.90-2.82(m,2H),2.78-2.76(m,1H),2.60-2.56(m,1H),2.10-2.09(m,1H),1.95-1.88(m,重叠,5H),1.10(d,J=8.0Hz,3H).
实施例231a 2-(4-氯-3-(羟基甲基)吡啶-2-基)-10-氟-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1(2H)-酮231a
将4-氯-2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛134c(800mg,2.31mmol)、NaBH4(263mg,6.92mmol)和甲醇(50mL)的混合物在0℃搅拌1小时。将反应混合物用水(30mL)淬灭并减压浓缩。将残余物用二氯甲烷(2X30mL)萃取并将合并的二氯甲烷萃取物减压浓缩。将残余物通过硅胶色谱法(用5:1石油醚/乙酸乙酯洗脱)来纯化得到231a(650mg,81%),其为黄色固体。MS-ESI:[M+H]+340.1
实施例231b乙酸(4-氯-2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯231b
在圆底烧瓶中装入231a(600mg,1.72mmol)、二氯甲烷(50mL)和三乙胺(5mL)。将所述溶液在0℃搅拌0.5小时并缓慢加入乙酰氯(135mg,1.72mmol)。将混合物在0℃再搅拌2.5小时。然后将其减压蒸发。将残余物通过硅胶柱色谱法(用9:1石油醚/乙酸乙酯洗脱)来纯化得到231b(605mg,90%),其为黄色固体。MS-ESI:[M+H]+392.1
实施例231c 3-(乙酰氧基甲基)-2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸231c
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入231b(600mg,1.53mmol)、Pin2B2(1.94g,7.65mmol)、PdCl2(dppf)(65mg,0.080mmol)、X-Phos(73mg,0.15mmol)、乙酸钾(304mg,3.1mmol)和二噁烷(30mL)。在经历三轮真空/氩气吹洗后,将混合物在65℃加热5小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物用石油醚洗涤得到231c(412mg,67%),其为黄色固体。MS-ESI:[M+H]+402.1
实施例231d乙酸(S)-(2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)-4-(1-甲基-5-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢哒嗪-3-基)吡啶-3-基)甲酯231d
在配备有回流冷凝器的圆底烧瓶中装入231c(200mg,0.50mmol)、(S)-6-氯-2-甲基-4-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)哒嗪-3(2H)-酮224c(195mg,0.50mmol)、PdCl2(dppf)(24mg,0.030mmol)、K3PO4(212mg,1.0mmol)、乙酸钠(98mg,1.0mmol)、乙腈(30mL)和水(3mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热2小时。然后将其冷却至室温并过滤。减压蒸发滤液。将残余物用硅胶柱色谱法(用1:3石油醚/乙酸乙酯洗脱)来纯化得到231d,其为黄色固体(213mg,60%)。MS-ESI:[M+H]+712.3
实施例231 10-氟-2-[3-(羟基甲基)-4-[1-甲基-5-[[5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]-2-吡啶基]氨基]-6-氧代-哒嗪-3-基]-2-吡啶基]-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1-酮231
将231d(150mg,0.21mmol)和氢氧化锂(51mg,2.1mmol)于异丙醇/THF(1:1,10mL)和水(3mL)中的混合物在室温搅拌1小时。将混合物减压蒸发并将残余物用乙酸乙酯(2X10mL)萃取。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到231(83mg,59%),其为黄色固体。MS-ESI:[M+H]+670.3.1H NMR(500MHz,DMSO-d6)δ9.29(s,1H),8.53(d,J=5.5Hz,1H),8.42(s,1H),7.91(s,1H),7.43-7.40(m,3H),4.76(bs,1H),4.60-4.54(m,3H),4.49-4.46(m,1H),4.43-4.37(m,2H),4.21-4.56(m,2H),4.07-4.03(m,1H),3.89-3.83(m,2H),3.78(s,3H),3.41-3.37(m,1H),3.22-3.19(m,1H),3.00-2.93(m,1H),2.65-2.60(m,2H),2.55-2.54(m,1H),2.43-2.39(m,3H),2.27-2.24(m,1H),2.12-2.07(m,1H),1.76-1.66(m,4H),0.97(d,J=9.0Hz,3H).
实施例232a 2-硝基-5-(1,2,3,6-四氢吡啶-4-基)吡啶232a
将4-(6-硝基吡啶-3-基)-5,6-二氢吡啶-1(2H)-羧酸叔丁酯200a(2.0g,6.6mmol)于HCl/二噁烷(20mL,4M)中的混合物在室温搅拌2小时。然后将其减压蒸发。将残余物用乙酸乙酯(3X7mL)洗涤得到232a,其为黄色固体(1.0g,74%)。MS-ESI:[M+H]+206.
实施例232b 5-(1-甲基-1,2,3,6-四氢吡啶-4-基)-2-硝基吡啶232b
向232a(1.2g,5.8mmol)于CH3OH(25mL)中的溶液中加入HCHO(1mL,35mmol)和乙酸(1mL),然后加入NaBHCN3(1.0g,12mmol)。将混合物在室温搅拌2小时。然后将其减压蒸发并将残余物通过反相Combiflush(用0.3%NH4HCO3于水/乙腈中洗脱)来纯化得到232b,其为黄色固体(1.0g,78%)。MS-ESI:[M+H]+220。
实施例232c 5-(1-甲基哌啶-4-基)吡啶-2-胺232c
将250-mL单颈圆底烧瓶用氮气吹洗并装入232b(2.0g,9.0mmol)、10%钯/炭(50%水分,200mg)和甲醇(40mL)。将所述烧瓶排空、充入氢气并在氢气中在室温搅拌12小时。然后将氢气排空并向所述烧瓶中充入氮气。通过用垫过滤除去催化剂,减压浓缩滤液得到232c(1.6g,92.5%),将其不经进一步纯化直接用于下一步骤。MS-ESI:[M+H]+192
实施例232d 5-溴-1-甲基-3-(5-(1-甲基哌啶-4-基)吡啶-2-基氨基)吡啶-2(1H)-酮232d
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入232c(1.5g,7.9mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(2.0g,7.9mmol)、碳酸铯(5.0g,16mmol)和1,4-二噁烷(50mL)。在使氮气鼓泡通过所得悬浮液30分钟后,加入XantPhos(455mg,0.79mmol)和三(二亚苄基丙酮)二钯(0)(718mg,0.79mmol)。使体系经历三轮真空/氩气吹洗并在100℃加热2小时。之后,将反应混合物冷却至室温并过滤。使滤液在乙酸乙酯(100mL)和水(100mL)之间分配。分离出水层并用乙酸乙酯(3X50mL)萃取。将合并的有机层用盐水(3X20mL)洗涤并用硫酸钠干燥。过滤除去干燥剂并减压浓缩滤液。将残余物通过硅胶柱色谱法(用1:3乙酸乙酯/石油醚洗脱)来纯化得到232d,其为棕色固体(1.5g,50%)。MS-ESI:[M+H]+377。
实施例232e乙酸(4-(1-乙基-5-(5-(1-甲基哌啶-4-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯232e
在配备有回流冷凝器的圆底烧瓶中装入232d(160mg,0.40mmol)、3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113i(191mg,0.50mmol)、Pd(dppf)Cl2(20mg,0.024mmol)、K3PO4(180mg,0.80mmol)、乙酸钠三水合物(120mg,0.80mmol)、水(0.5mL)和乙腈(10mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热2小时。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用25:1二氯甲烷/CH3OH洗脱)来纯化得到232e,其为黄色固体(180mg,55%)。MS-ESI:[M+H]+636.3
实施例232 2-[3-(羟基甲基)-4-[1-甲基-5-[[5-(1-甲基-4-哌啶基)-2-吡啶基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1-酮232
将232e(180mg,0.30mmol)和氢氧化锂(130mg,3.0mmol)于THF/异丙醇(6:3,9mL)和水(3mL)中的混合物在30℃搅拌1小时。将混合物减压蒸发并将残余物用乙酸乙酯(2X20mL)萃取。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到232(55mg,35%),其为白色固体。MS-ESI:[M+H]+594.3.1H NMR(500MHz,CDCl3)δ8.72(d,J=3.0Hz,1H),8.51(d,J=6.0Hz,1H),8.11(d,J=3.0Hz,1H),7.88(d,J=2.0Hz,1H),7.44-7.36(m,2H),6.90(s,1H),6.80-6.78(m,1H),5.08-5.04(m,1H),4.64-4.50(m,2H),4.34-4.29(m,1H),4.16-4.10(m,2H),3.91-3.87(m,1H),3.72(s,3H),3.03-3.00(m,2H),2.62-2.56(m,4H),2.46-2.42(m,1H),2.36(s,1H)2.13-2.07(m,2H),1.92-1.82(m,重叠,8H).
实施例233a 2-(5-溴-1-甲基-2-氧代-1,2-二氢吡啶-3-基氨基)-6,7-二氢噻唑并[5,4-c]吡啶-5(4H)-羧酸叔丁酯233a
在配备有回流冷凝器的100-mL圆底烧瓶中装入2-氨基-6,7-二氢噻唑并[5,4-c]吡啶-5(4H)-羧酸叔丁酯(600mg,2.35mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(942mg,3.53mmol)、Pd2(dba)3(214mg,0.235mmol)、Xantphos(270.5mg,0.47mmol)、Cs2CO3(1.53g,4.7mmol)和二噁烷(30mL)。在使氮气鼓泡通过所述混合物30分钟后,将其在氮气保护下在110℃加热12小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将混合物冷却至室温并过滤。减压浓缩滤液并将残余物用乙腈洗涤得到233a(600mg,54%),其为黄色固体。MS-ESI:[M+H]+441.1
实施例233b 2-[(5-{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}-1-甲基-2-氧代-1,2-二氢吡啶-3-基)氨基]-4H,5H,6H,7H-[1,3]噻唑并[5,4-c]吡啶-5-羧酸叔丁酯233b
在配备有回流冷凝器的50-mL圆底烧瓶中装入233a(300mg,0.68mmol)、(3-(乙酰氧基甲基)-2-(7,7-二甲基-1-氧代-3,4,7,8-四氢-1H-环戊二烯并[4,5]吡咯并-[1,2-a]吡嗪-2(6H)-基)吡啶-4-基)硼酸199e(1.8g,2.72mmol)、Pd(dppf)Cl2(27.7mg,0.034mmol)、K3PO4(288.3mg,1.36mmol)、乙酸钠(111.5mg,1.36mmol)、水(10滴)和乙腈(10mL)。在使氮气鼓泡通过所述混合物30分钟后,将其在氮气保护下在100℃加热1小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。过滤混合物并减压浓缩滤液,将残余物通过硅胶柱色谱法(用100:1二氯甲烷/甲醇洗脱)来纯化得到233b(220mg,45%),其为黄色固体。MS-ESI:[M+H]+714.3
实施例233c乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-[1-甲基-6-氧代-5-({4H,5H,6H,7H-[1,3]噻唑并[5,4-c]吡啶-2-基}氨基)-1,6-二氢吡啶-3-基]吡啶-3-基)甲酯233c
向233b(220mg,0.308mmol)于乙酸乙酯(5mL)中的溶液中加入HCl于乙酸乙酯中的溶液(0.123mL,2.5M,0.308mmol)。将混合物在室温搅拌1小时。然后将其减压浓缩得到233c(180mg,粗制),将其不经进一步纯化直接用于下一步骤。MS-ESI:[M+H]+614.3
实施例233 3-[3-(羟基甲基)-4-[1-甲基-6-氧代-5-(4,5,6,7-四氢噻唑并[5,4-c]吡啶-2-基氨基)-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮233
向233c(180mg,0.29mmol)于THF(3mL)和丙烷-2-醇(3mL)中的溶液中加入水(1mL)和氢氧化锂(14.0mg,0.58mmol)。将反应混合物在室温搅拌1小时。然后将其减压浓缩并将所得残余物通过反相制备性-HPLC来纯化得到233(28.6mg,17%),其为白色固体。MS-ESI:[M+H]+572.3.1H NMR(500MHz,DMSO-d6)δ9.85(s,1H),8.63(d,J=2.5Hz,1H),8.48(d,J=6.5Hz,1H),7.57(d,J=2.5Hz,1H),7.32(d,J=6.0Hz,1H),6.55(s,1H),4.95-4.92(m,1H),4.47-4.37(m,2H),4.25-4.18(m,3H),3.86-3.84(m,1H),3.71(s,2H),3.59(s,3H),2.92-2.90(m,2H),2.62-2.56(m,2H),2.50-2.39(m,5H),1.21(s,6H).
实施例235a乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-[1-甲基-5-({5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]吡嗪-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]吡啶-3-基)甲酯235a
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入(S)-5-溴-1-甲基-3-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡嗪-2-基氨基)吡啶-2(1H)-酮230f(200mg,0.46mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]-十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(366mg,0.92mmol)、Pd(dppf)Cl2(38mg,0.046mmol)、乙酸钠(126mg,0.92mmol)、K3PO4(196mg,0.92mmol)、水(0.5mL)和乙腈(10mL)。在经历三轮真空/氩气吹洗后,将混合物在65℃加热3小时。冷却至室温后,过滤反应混合物。减压浓缩滤液并将残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(50:1至30:1)洗脱)来纯化得到235a,其为棕色固体(100mg,31%)。MS-ESI:[M+H]+708.5.
实施例235 3-[3-(羟基甲基)-4-[1-甲基-5-[[5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]吡嗪-2-基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮235
将235a(90.0mg,0.13mmol)和氢氧化锂(36.4mg,3.25mmol)于异丙醇/THF(1:1,5mL)和水(1mL)中的混合物在35℃搅拌0.5小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物通过反相制备性-HPLC来纯化得到235(18.2mg,22%)。MS-ESI:[M+H]+666.3。1H NMR(500MHz,DMSO-d6)δ8.61(s,1H),8.48(d,J=4.5Hz,1H),8.39(d,J=1.5Hz,1H),8.34(s,1H),7.83(s,1H),7.47(d,J=2.0Hz,1H),7.33(d,J=5.0Hz,1H),6.56(s,1H),4.96(bs,1H),4.57-4.55(m,2H),4.49-4.47(m,1H),4.42-4.37(m,重叠,4H),4.22-4.18(m,重叠,3H),3.84-3.76(m,2H),3.60(s,3H),3.39-3.37(m,1H),3.02-2.81(m,1H),2.78-2.76(m,1H),2.62-2.56(m,3H),2.43-2.41(m,2H),2.10-2.07(m,1H),1.92-1.90(m,1H),1.22(s,6H),1.12(d,J=6.0Hz,3H).
实施例236a乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-(1-甲基-5-{[5-(1-甲基哌啶-4-基)吡啶-2-基]氨基}-6-氧代吡啶-3-基)吡啶-3-基)甲酯236a
在配备有回流冷凝器的50-mL圆底烧瓶中装入5-溴-1-甲基-3-(5-(1-甲基哌啶-4-基)吡啶-2-基氨基)吡啶-2(1H)-酮232d(160mg,0.40mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(240mg,0.60mmol)、Pd(dppf)Cl2(20mg,0.020mmol)、K3PO4(180mg,0.80mmol)、乙酸钠三水合物(120mg,0.80mmol)、水(0.5mL)和乙腈(10mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热2小时。然后将其过滤并减压蒸发滤液。将残余物在硅胶柱色谱上纯化(用25:1二氯甲烷/甲醇洗脱)得到236a,其为黄色固体(150mg,38%)。MS-ESI:[M+H]+650.3
实施例236 3-[3-(羟基甲基)-4-[1-甲基-5-[[5-(1-甲基-4-哌啶基)-2-吡啶基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮236
将236a(150mg,0.25mmol)和氢氧化锂(105mg,2.5mmol)于THF/异丙醇(6:3,9mL)和水(3mL)中的混合物在30℃搅拌1小时。真空蒸发混合物并将残余物用乙酸乙酯(2X20mL)萃取。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到236(40mg,30%),其为浅绿色固体。MS-ESI:[M+H]+608.3.1H NMR(500MHz,CDCl3)δ8.73(s,1H),8.52(d,J=4.0Hz,1H),8.13(s,1H),7.90-7.88(m,2H),7.45-7.37(m,2H),6.86-6.80(m,2H),5.11(bs,1H),4.67-4.65(m,1H),4.53-4.51(m,1H),4.35-4.33(m,1H),4.18(bs,2H),3.90-3.89(m,1H),3.73(s,3H),3.24-3.22(m,2H),2.59-2.50(m,,重叠,8H),2.36-2.32(m,2H),2.01-1.87(m,4H),1.29(s,6H).
实施例237a 2-{10-氟-1-氧代-1H,2H,3H,4H,6H,7H,8H,9H-吡啶并[3,4-b]吲嗪-2-基}-4-[1-甲基-5-({5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]吡啶-3-甲醛237a
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入4-氯-2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-3-甲醛134c(70mg,0.20mmol)、1-甲基-3-({5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-5-(四甲基-1,3,2-二氧杂硼杂戊环-2-基)-1,2-二氢吡啶-2-酮191j(192mg,0.40mmol)、Pd(dppf)Cl2(33mg,0.040mmol)、乙酸钾(39mg,0.40mmol)、K3PO4(87mg,0.40mmol)、乙腈(7mL)和水(6滴)。在经历三轮真空/氩气吹洗后,将混合物在95℃加热2小时。然后将其过滤并减压蒸发滤液。将残余物通过硅胶柱色谱法(用50:1乙酸乙酯/甲醇洗脱)来纯化得到237a(286mg,纯度:46%,收率:98%),其为固体。MS-ESI:[M+H]+667.3
实施例237 10-氟-2-[3-(羟基甲基)-4-[1-甲基-5-[[5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]-2-吡啶基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-1-酮237
在0℃,向237a(131mg,0.197mmol)于甲醇(7mL)中的溶液中加入硼氢化钠(59.8mg,1.57mmol)。将反应混合物在0-25℃搅拌1.5小时。然后将其用水(1.5mL)淬灭。将混合物减压蒸发并将残余物用二氯甲烷(3X30mL)萃取。将合并的二氯甲烷萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到237(36mg,28%),其为白色固体。MS-ESI:[M+H]+669.3.1H NMR(500MHz,CDCl3)δ8.66(d,J=1.5Hz,1H),8.51(d,J=5.0Hz,1H),7.99(s,1H),7.85(s,1H),7.83(d,J=2.0Hz,1H),7.36-7.32(m,2H),6.84(d,J=9.0Hz,1H),4.90-4.86(m,1H),4.73-4.65(m,5H),4.39-4.30(m,2H),3.90-3.77(m,3H),3.72(s,3H),3.56-3.48(m,2H),3.10-3.09(m,2H),2.98-2.92(m,2H),2.79-2.75(m,2H),2.59-2.57(m,1H),2.50-2.49(m,2H),2.22-2.21(s,1H),2.04-1.99(m,2H),1.88-1.84(m,2H),1.01(d,J=6.0Hz,3H).
实施例238a(E)-3-((叔丁基亚磺酰基亚氨基)甲基)-5,6,7,8-四氢吲嗪-2-羧酸甲酯238a
在配备有磁力搅拌子的500-mL单颈圆底烧瓶中装入3-甲酰基-5,6,7,8-四氢吲嗪-2-羧酸甲酯(10.0g,48.3mmol,1.0当量)、2-甲基丙烷-2-亚磺酰胺(11.7g,96.6mmol,2.0当量)、KHSO4(32.8g,241.5mmol,5当量)和二氯甲烷(250mL)。将混合物在室温搅拌10小时。然后将其过滤并将滤液减压浓缩。将所得残余物通过硅胶柱色谱法(用1:3乙酸乙酯/石油醚洗脱)来纯化得到238a(12.4g,83%),其为黄色固体。MS:[M+H]+311.3.
实施例238b 3-((1,1-二甲基乙基亚磺酰氨基)甲基)-5,6,7,8-四氢吲嗪-2-羧酸甲酯238b
在配备有磁力搅拌子的250-mL单颈圆底烧瓶中装入238a(4.0g,12.8mmol,1.0当量)、NaBH4(2.9g,76.9mmol,6.0当量)和甲醇(100mL)。将反应混合物在室温搅拌1小时。之后,向反应混合物中加入水(50mL)并将所得混合物减压浓缩。将残余物用二氯甲烷(3X50mL)萃取。将合并的有机层减压蒸发得到238b(3.9g,96%),将其不经进一步纯化直接用于下一步骤。MS:[M-C4H10NOS]+192.3.
实施例238c 3-(氨基甲基)-5,6,7,8-四氢吲嗪-2-羧酸甲酯238c
在配备有磁力搅拌子的100-mL单颈圆底烧瓶中装入238b(3.5g,11.2mmol)、饱和HCl/乙醚溶液(15mL)和二氯甲烷(15mL)。将混合物在室温搅拌4小时。反应结束后,向反应混合物中加入NaHCO3溶液(50mL)并将混合物用二氯甲烷(3X50mL)萃取。将合并的有机层加压蒸发得到238c(2.2g,94%),将其不经进一步纯化直接用于下一步骤。MS:[M-NH2]+192.1.1H NMR(500MHz,MeOD)δ6.28(s,1H),4.38(s,2H),4.03(t,J=6.5Hz,2H),3.84(s,3H),2.78(t,J=6.5Hz,2H),2.06-2.02(m,2H),1.87-1.82(m,2H).
实施例238d 2,3,5,6,7,8-六氢吡咯并[3,4-b]吲嗪-1-酮238d
在配备有磁力搅拌子的100-mL单颈圆底烧瓶中装入238c(1.3g,6.25mmol,1.0当量)和THF(20mL)。在-78℃,在所述溶液中加入六甲基二硅基氨基锂/THF(18.7mL,18.7mmol,3.0当量)。然后将其在室温搅拌2小时。反应结束后,加入饱和NH4Cl水溶液(30mL)并将混合物减压浓缩。将残余物用二氯甲烷(3X50mL)萃取并将合并的有机层加压蒸发。将所得残余物通过硅胶柱色谱法(用60:1二氯甲烷/甲醇洗脱)来纯化得到238d(585mg,53%),其为黄色固体。MS:[M+H]+177.3.1H NMR(500MHz,DMSO-d6)δ7.38(s,1H),5.82(s,1H),4.13(s,2H),3.86(t,J=6.5Hz,2H),2.73(t,J=6.5Hz,2H),191-1.88(m,2H),1.75-1.73(m,2H).
实施例238e 4-氯-2-(1-氧代-5,6,7,8-四氢-1H-吡咯并[3,4-b]吲嗪-2(3H)-基)吡啶-3-甲醛238e
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入238d(400mg,2.27mmol)、2-溴-4-氯吡啶-3-甲醛(1.50g,6.90mmol,3.0当量)、Pd2(dba)3(208mg,0.227mmol,0.1当量)、xantphos(131mg,0.227mmol,0.1当量)、Cs2CO3(1.50g,4.54mmol,2.0当量)和二噁烷(30mL)。使氮气鼓泡通过所得混合物30分钟后,将反应混合物在90℃搅拌16小时。反应完成后,将混合物冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用1:3乙酸乙酯/石油醚洗脱)来纯化得到238e(300mg,42%),其为浅黄色固体。MS-ESI:[M+H]+316.1.
实施例238f S)-4-(1-甲基-5-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基-氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-5,6,7,8-四氢-1H-吡咯并[3,4-b]吲嗪-2(3H)-基)吡啶-3-甲醛238f
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入238e(150mg,0.48mmol,1.0当量)、(S)-1-甲基-3-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮191j(459mg,0.95mmol,2.0当量)、Pd(dppf)Cl2(39mg,0.048mmol,0.1当量)、乙酸钠(78mg,0.95mmol,2.0当量)、K3PO4(202mg,0.95mmol,2.0当量)、乙腈(10mL)和水(1mL)。在经历三轮真空/氩气吹洗后,将混合物在85℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用40:1二氯甲烷/乙醇洗脱)来纯化得到238f(90mg,30%),其为黄色固体。MS-ESI:[M+H]+635.3.
实施例238 2-[3-(羟基甲基)-4-[1-甲基-5-[[5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]-2-吡啶基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-5,6,7,8-四氢-1H-吡咯并[3,4-b]吲嗪-3-酮238
在配备有磁力搅拌子的25-mL单颈圆底烧瓶中装入238f(90mg,1.0当量,0.14mmol)、NaBH4(23mg,5当量,0.60mmol)和甲醇(5mL)。将所得混合物在室温搅拌20分钟并用水淬灭。然后将其减压浓缩并将残余物通过反相制备性-HPLC来纯化得到238(60mg,66%),其为白色固体。MS-ESI:[M+H]+637.3.1H NMR(500MHz,CDCl3)δ8.69(d,J=1.5Hz,1H),8.47(d,J=5.0Hz,1H),7.99(d,J=2.5Hz,1H),7.93(d,J=2.0Hz,1H),7.86(s,1H),7.36-7.31(m,2H),6.83(d,J=9.0Hz,1H),6.15(s,1H),5.71(t,J=6.5Hz,1H),4.96(s,2H),4.72-4.63(m,4H),4.52-4.51(m,2H),3.97-3.95(m,2H),3.75(s,3H),3.55-3.53(m,1H),3.48-3.46(m,1H),3.10-3.08(m,2H),2.91-2.89(m,2H),2.58-2.56(m,1H),2.49-2.48(m,2H),2.23-2.19(m,1H),2.08-2.02(m,2H),1.93-1.89(m,2H),1.00(d,J=6.0Hz,3H).
实施例239a 3-(6-(5-溴-1-甲基-2-氧代-1,2-二氢吡啶-3-基氨基)吡啶-3-基)氮杂环丁烷-1-羧酸叔丁酯239a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(50mL)、3-(6-氨基吡啶-3-基)氮杂环丁烷-1-羧酸叔丁酯(1.8g,7.2mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(1.9g,7.2mmol)和碳酸铯(4.7g,14.4mmol)。在使氮气鼓泡通过所得悬浮液30分钟后,加入XantPhos(418mg,0.72mmol)和三(二亚苄基丙酮)二钯(0)(661mg,0.72mmol)。使反应混合物经历三轮真空/氩气吹洗并在105℃加热0.5小时。之后,将反应混合物冷却至室温并过滤。使滤液在乙酸乙酯(120mL)和水(60mL)之间分配。分离出水层并用乙酸乙酯(3X80mL)萃取。将合并的有机层用盐水(30mL)洗涤并用硫酸钠干燥。过滤除去干燥剂并减压浓缩滤液。将残余物通过硅胶柱色谱法(用1:4乙酸乙酯/石油醚洗脱)来纯化得到239a,其为黄色固体(3.06g,98%)。MS-ESI:[M+H]+435。
实施例239b 3-(5-(氮杂环丁烷-3-基)吡啶-2-基氨基)-5-溴-1-甲基吡啶-2(1H)-酮239b
将化合物239a(1.0g,2.3mmol)悬浮在4M HCl/二噁烷(10mL)中。将反应混合物在室温搅拌4小时。然后将其减压浓缩。将残余物用NaOH水溶液碱化并将所得混合物用二氯甲烷萃取。将合并的有机层用盐水洗涤并减压浓缩得到239b,其为黄色固体(650mg,84%)。MS-ESI:[M+H]+335。
实施例239c 5-溴-1-甲基-3-(5-(1-甲基氮杂环丁烷-3-基)吡啶-2-基氨基)吡啶-2(1H)-酮239c
将239b(469mg,1.4mmol)、37%甲醛水溶液(4.0g,50mmol)、NaBH3CN(261mg,4.2mmol)和1M氯化锌/乙氧基乙烷(4mL,4.2mmol)于甲醇(40mL)中的混合物在室温搅拌2小时。将混合物加至水(20mL)中并减压浓缩。将残余物用二氯甲烷(3X50mL)萃取。将合并的有机层减压浓缩并将残余物通过硅胶柱色谱法来纯化(用10:1二氯甲烷/甲醇洗脱)得到239c,其为黄色固体(300mg,83%)。MS-ESI:[M+H]+349.
实施例239d乙酸(4-(1-甲基-5-(4-(1-甲基氮杂环丁烷-3-基)苯基氨基)-6-氧代-1,6-二氢-吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯239d
在配备有磁力搅拌子和回流冷凝器的50-mL圆底烧瓶中装入239c(106mg,0.30mmol)、3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113i(115mg,0.30mmol)、Pd(dppf)Cl2(25mg,0.030mmol)、K3PO4(127mg,0.60mmol)、乙酸钠(49mg,0.60mmol)、水(1mL)和乙腈(10mL)。在经历三轮真空/氩气吹洗后,将混合物回流加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用15:1二氯甲烷/甲醇洗脱)来纯化得到239d,其为白色固体(100mg,49%)。MS-ESI:[M+H]+607.3
实施例239 2-[3-(羟基甲基)-4-[1-甲基-5-[[5-(1-甲基氮杂环丁烷-3-基)-2-吡啶基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1-酮239
向239d(100mg,0.16mmol)于丙烷-2-醇(2mL)、四氢呋喃(2mL)和水(1mL)中的溶液中加入氢氧化锂(38mg,1.60mmol)。将混合物在30℃搅拌2小时。然后将其减压蒸发并将残余物通过反相制备性-HPLC来纯化得到239(22.5mg,26%),其为白色固体。MS-ESI:[M+H]+566.4.1H NMR(500MHz,CDCl3)δ8.75(d,J=1.5Hz,1H),8.52(d,J=5.0Hz,1H),8.17(d,J=2.0Hz,1H),7.91-7.89(m,2H),7.59(d,J=8.5Hz,1H),7.38(d,J=5.0Hz,1H),6.91(s,1H),6.84(d,J=8.5Hz,1H),5.09-5.06(m,1H),4.66-4.64(m,1H),4.54-4.50(m,1H),4.36-4.33(m,1H),4.18-4.11(m,2H),3.92-3.88(m,1H),3.75-3.72(m,重叠,5H),3.63-3.58(m,1H),3.16-3.14(m,2H),2.64-2.58(m,4H),2.40(s,3H),1.93-1.90(m,2H),1.84-1.79(m,2H).
实施例240a乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-(1-甲基-5-{[5-(1-甲基氮杂环丁烷-3-基)吡啶-2-基]氨基}-6-氧代吡啶-3-基)吡啶-3-基)甲酯240
在配备有磁力搅拌子和回流冷凝器的50-mL圆底烧瓶中装入5-溴-1-甲基-3-(5-(1-甲基氮杂环丁烷-3-基)吡啶-2-基氨基)-吡啶-2(1H)-酮239c(106mg,0.30mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(119mg,0.30mmol)、Pd(dppf)Cl2(25mg,0.031mmol)、K3PO4(127mg,0.60mmol)、乙酸钠(49mg,0.60mmol)、水(0.5mL)和乙腈(10mL)。在经历三轮真空/氩气吹洗后,将混合物回流加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用15:1二氯甲烷/甲醇洗脱)来纯化得到240a,其为白色固体(80mg,48%)。MS-ESI:[M+H]+622.7
实施例240 3-[3-(羟基甲基)-4-[1-甲基-5-[[5-(1-甲基氮杂环丁烷-3-基)-2-吡啶基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮240
向240a(80mg,0.130mmol)于丙烷-2-醇(2mL)、四氢呋喃(2mL)和水(1mL)中的溶液中加入氢氧化锂(38mg,1.60mmol)。将混合物在30℃搅拌1小时。将反应混合物减压蒸发并将残余物通过反相制备性-HPLC来纯化得到240(24.3mg,33%),其为白色固体。MS-ESI:[M+H]+580.4.1H NMR(500MHz,CDCl3)δ8.76(d,J=2.0Hz,1H),8.52(d,J=5.0Hz,1H),8.17(d,J=2.0Hz,1H),7.92-7.90(m,2H),7.59(dd,J=1.5,8.5Hz,1H),7.38(d,J=5.0Hz,1H),6.87(s,1H),6.84(d,J=8.5Hz,1H),5.09-5.06(m,1H),4.68-4.66(m,1H),4.56-4.54(m,1H),4.37-4.35(m,1H),4.19-4.17(m,2H),3.90-3.88(m,1H),3.75-3.72(m,重叠,5H),3.64-3.62(m,1H),3.19-3.16(m,2H),2.60(d,J=5.0Hz,2H),2.54(s,2H),2.42(s,3H),1.30(s,6H).
实施例241a 2-{10-氟-1-氧代-1H,2H,3H,4H,6H,7H,8H,9H-吡啶并[3,4-b]吲嗪-2-基}-4-[1-甲基-5-({5-甲基-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]吡啶-3-甲醛241a
在配备有磁力搅拌子和回流冷凝器的25-mL单颈圆底烧瓶中装入4-氯-2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-3-甲醛134c(59.6mg,0.17mmol)、1-甲基-3-({5-甲基-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基}氨基)-5-(四甲基-1,3,2-二氧杂硼杂戊环-2-基)-1,2-二氢吡啶-2-酮135a(261.8mg,0.68mmol)、Pd(dppf)Cl2(25.0mg,0.030mmol)、Na2CO3(54.1mg,0.51mmol)、DMF(6mL)和水(0.75mL)。在经历三轮真空/氩气吹洗后,将混合物在70℃加热1小时。然后将其过滤并减压蒸发滤液。将残余物通过硅胶柱色谱法(用50:1二氯甲烷/甲醇洗脱)来纯化得到241a(100mg,纯度:54%,收率:56%),其为黄色固体。MS-ESI:[M+H]+571.3
实施例241 10-氟-2-[3-(羟基甲基)-4-[1-甲基-5-[(5-甲基-6,7-二氢-4H-吡唑并[1,5-a]吡嗪-2-基)氨基]-6-氧代-3-吡啶基]-2-吡啶基]-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-1-酮241
在0℃,向241a(54.0mg,0.095mmol)于甲醇(5mL)中的溶液中加入硼氢化钠(28.9mg,0.76mmol)。将反应混合物在0-25℃搅拌1.5小时。然后将其用水(5mL)淬灭。将混合物减压蒸发并将残余物用二氯甲烷(3X30mL)萃取。将合并的二氯甲烷萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到241(8.0mg,15%),其为白色固体。MS-ESI:[M+H]+573.3.1H NMR(500MHz,DMSO-d6)δ8.47(d,J=5.0Hz,1H),8.21(s,1H),8.06(d,J=2.0Hz,1H),7.40(d,J=2.0Hz,1H),7.31(d,J=5.0Hz,1H),5.88(s,1H),4.87-4.85(m,1H),4.44-4.35(m,2H),4.13-4.08(m,1H),3.92-3.89(m,3H),3.79-3.76(m,2H),3.58(s,3H),3.49(s,2H),2.99-2.94(m,2H),2.79-2.77(m,2H),2.66-2.64(m,2H),2.35(s,3H),1.90-1.78(m,2H),1.75-1.73(m,2H).
实施例242a 3-(1,5-二甲基-1H-吡唑-3-基氨基)-1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮242a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入5-溴-3-(1,5-二甲基-1H-吡唑-3-基氨基)-1-甲基吡啶-2(1H)-酮218a(800mg,2.69mmol,1.0当量)、4,4,4',4',5,5,5',5'-八甲基-2,2'-二(1,3,2-二氧杂硼杂戊环)(1.70g,6.73mmol,2.5当量)、Pd2(dba)3(123mg,0.13mmol,0.05当量)、X-Phos(128mg,0.27mmol,0.1当量)、乙酸钾(528mg,5.38mmol,2.0当量)和二噁烷(50mL)。在经历三轮真空/氩气吹洗后,将混合物在70℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用1:70甲醇/二氯甲烷洗脱)得到242a(740mg,79%),其为绿色固体。MS-ESI:[M+H]+345.3
实施例242b 4-(5-(1,5-二甲基-1H-吡唑-3-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-3-甲醛242b
在配备有磁力搅拌子和回流冷凝器的100mL单颈圆底烧瓶中装入242a(282mg,0.82mmol,1.5当量)、4-氯-2-(1-氧代-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-3-甲醛139a(180mg,0.55mmol,1.0当量)、Pd(dppf)Cl2(45mg,0.055mmol,0.1当量)、乙酸钠(90mg,1.25mmol,2.0当量)、K3PO4(232mg,1.25mmol,2.0当量)、乙腈(20mL)和水(1mL)。在经历三轮真空/氩气吹洗后,将混合物在90℃加热1小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用50:1二氯甲烷/甲醇洗脱)来纯化得到242b(150mg,48%),其为黄色固体。MS-ESI:[M+H]+512.3.
实施例242 2-[4-[5-[(1,5-二甲基吡唑-3-基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-1-酮242
在配备有磁力搅拌子的50-mL单颈圆底烧瓶中装入242b(150mg,0.29mmol,1.0当量)、NaBH4(55mg,1.46mmol,5.0当量)和甲醇(10mL)。将所得混合物在室温搅拌20分钟。然后将其过滤并减压浓缩滤液。将残余物通过反相制备性-HPLC来纯化得到242(100mg,66%),其为白色固体。MS-ESI:[M+H]+514.3.1H NMR(500MHz,DMSO-d6)δ8.47(d,J=5.5Hz,1H),8.04-8.03(m,2H),7.42(d,J=2.0Hz,1H),7.30(d,J=5.0Hz,1H),6.05(s,1H),5.90(s,1H),4.87-4.85(m,1H),4.43-4.35(m,2H),4.18-4.12(m,1H),3.98-3.93(m,1H),3.84-3.78(m,2H),3.59(s,3H),3.58(s,3H),3.06-2.92(m,2H),2.75-2.68(m,2H),2.18(s,3H),1.94-1.92(m,2H),1.79-1.73(m,2H).
实施例243a 4-(甲基磺酰基氧基)哌啶-1-羧酸叔丁酯243a
在0℃,向4-羟基哌啶-1-羧酸叔丁酯(14.0g,70.0mmol)于三乙胺(9.9g,98mmol)和二氯甲烷(100mL)中的溶液中滴加甲磺酰氯(11.2g,98.0mmol)。使反应混合物达到环境温度并搅拌1小时。将反应混合物用水(50mL)淬灭。分离出水层并用乙酸乙酯(2X50mL)萃取。将合并的有机层用盐水(50mL)洗涤,并用硫酸钠干燥。过滤除去干燥剂并减压浓缩滤液得到243a,将其不经进一步纯化即用于下一步骤(19.5g,100%)。MS-ESI:[M-t-Bu]+224.1
实施例243b 4-(4-硝基-1H-咪唑-1-基)哌啶-1-羧酸叔丁酯243b
在配备有磁力搅拌子和回流冷凝器的250-mL单颈圆底烧瓶器中装入243a(7.0g,25.1mmol)、DMF(120mL)、4-硝基-1H-咪唑(2.80g,25.1mmol)和K2CO3(6.9g,50.2mmol)。将混合物在120℃加热整夜。之后,将反应混合物冷却至室温并过滤。真空蒸发滤液。将残余物通过硅胶柱色谱法(用2:2:1乙酸乙酯/石油醚/二氯甲烷洗脱)来纯化得到243b(2.4g,32.4%),其为黄色固体。MS-ESI:[M+H]+297.3
实施例243c 4-(4-氨基-1H-咪唑-1-基)哌啶-1-羧酸叔丁酯243c
将100-mL单颈圆底烧瓶用氮气吹洗并装入243b(2.3g,7.8mmol)、10%钯/炭(10%水分,230mg)和乙醇(40mL)。将混合物排空、充入氢气并在室温搅拌3小时。然后将氢气排空并将氮气充入所述烧瓶中。通过用垫过滤除去催化剂,减压浓缩滤液得到243c(2.0g,95%)。MS-ESI:[M+H]+267.2.
实施例243d 4-(4-(5-溴-1-甲基-2-氧代-1,2-二氢吡啶-3-基氨基)-1H-咪唑-1-基)哌啶-1-羧酸叔丁酯243d
在配备有磁力搅拌子和回流冷凝器的250-mL单颈圆底烧瓶中装入243c(2.3g,8.6mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(2.3g,8.6mmol)、三-(二亚苄基丙酮)二钯(0)(789mg,0.86mmol)、XantPhos(994mg,1.72mmol)、Cs2CO3(5.6g,17.2mmol)和1,4-二噁烷(80mL)。在经历三轮真空/氩气吹洗后,将混合物在95℃加热4小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(50:1至20:1)洗脱)来纯化得到243d,其为黄色油状物固体(2.3g,59%)。MS-ESI:[M+H]+452.3。
实施例243e 5-溴-1-甲基-3-(1-(哌啶-4-基)-1H-咪唑-4-基氨基)吡啶-2(1H)-酮243e
将243d(2.2g,4.88mmol)和三氟乙酸(20mL)的混合物在室温搅拌1小时。然后将其减压浓缩得到粗制243e(1.5g,88%),将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+352.2
实施例243f 5-溴-1-甲基-3-(1-(1-(氧杂环丁烷-3-基)哌啶-4-基)-1H-咪唑-4-基氨基)吡啶-2(1H)-酮243f
在配备有磁力搅拌子和回流冷凝器的250-mL单颈圆底烧瓶中装入243e(2.2g,6.3mmol)、NaBH3CN(995mg,15.8mmol)、氧杂环丁烷-3-酮(907mg,12.6mmol)、氯化锌(2.1g,15.8mmol)和甲醇(60mL)。将反应混合物在50℃搅拌5小时并减压浓缩。向残余物中加入水并将所得混合物用二氯甲烷萃取三次。然后减压浓缩合并的有机层并将残余物通过硅胶柱色谱法(用1%三乙胺于甲醇中洗脱)来纯化。将含有所期望产物的馏分减压浓缩。向残余物中加入二氯甲烷并过滤所得悬浮液。减压浓缩滤液得到243f,其为黄色固体(800mg,62%)。MS-ESI:[M+H]+408.2
实施例243g乙酸(4-(1-甲基-5-(1-(1-(氧杂环丁烷-3-基)哌啶-4-基)-1H-咪唑-4-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯243g
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入243f(300mg,0.74mmol)、3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-4-基硼酸113i(567mg,1.48mmol)、Pd(dppf)Cl2(60.5mg,0.074mmol)、K3PO4(314mg,1.48mmol)、乙酸钠(201mg,1.48mmol)、水(0.5mL)和乙腈(10mL)。在经历三轮真空/氩气吹洗后,将混合物在90℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用含有0.5%三乙胺的1:1二氯甲烷/甲醇洗脱)来纯化得到243g,其为黄色固体(100mg,20%)。MS-ESI:[M+H]+667.4.
实施例243 2-[3-(羟基甲基)-4-[1-甲基-5-[[1-[1-(氧杂环丁烷-3-基)-4-哌啶基]咪唑-4-基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1-酮243
将243g(80mg,0.12mmol)和氢氧化锂(100mg,2.4mmol)于异丙醇/THF/水(2:2:1,8mL)中的混合物在35℃搅拌30分钟。然后减压浓缩反应混合物。向残余物中加入水并将所得混合物用二氯甲烷萃取三次。将合并的有机层减压浓缩并将所得残余物通过反相制备性-HPLC来纯化得到243(28.0mg,30%)。MS-ESI:[M+H]+625.4.1H NMR(500MHz,DMSO-d6)δ8.48(d,J=6.5Hz,1H),7.54(d,J=1.5Hz,1H),7.53(s,1H),7.45(d,J=3.0Hz,1H),7.35-7.34(m,2H),7.11(d,J=1.0Hz,1H),6.58(s,1H),5.14(bs,1H),4.54(t,J=7.5Hz,2H),4.43-4.40(m,4H),4.23-4.11(m,3H),3.99-3.96(m,1H),3.91-3.84(m,1H),3.59(s,3H),3.43-3.39(m,1H),2.77-2.76(m,2H),2.62-2.57(m,2H),2.47-2.46(m,2H),1.94-1.89(m,6H),1.79-1.78(m,2H),1.69-1.66(m,2H).
实施例244a 2-(4-氯-3-(羟基甲基)吡啶-2-基)-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-1(2H)-酮244a
在30℃,向4-氯-2-(1-氧代-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-3-甲醛139a(1.0g,3.0mmol)于甲醇(30mL)中的溶液中加入硼氢化钠(380mg,9.0mmol)。将反应混合物再搅拌1小时并用水(10mL)淬灭。然后将其减压浓缩并将残余物用二氯甲烷(3X20mL)萃取。将合并的有机萃取物用无水Na2SO4干燥,过滤并减压蒸发得到244a,其为黄色固体(920mg,92%)。MS-ESI:[M+H]+332.3
实施例244b乙酸(4-氯-2-(1-氧代-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-3-基)甲酯244b
向244a(900mg,2.7mmol)和三乙胺(810mg,8.1mmol)于二氯甲烷(30mL)中的混合物中滴加乙酰氯(630mg,8.1mmol)。将反应混合物在30℃搅拌1小时。然后将其减压浓缩并将残余物通过硅胶柱色谱法(用二氯甲烷洗脱)来纯化得到244b,其为白色固体(900mg,90%)。MS-ESI:[M+H]+374.2
实施例244c 3-(乙酰氧基甲基)-2-(1-氧代-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-4-基硼酸244c
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入244b(900mg,2.4mmol)、Pin2B2(3.05g,12mmol)、Pd(dppf)Cl2(98mg,0.12mmol)、X-phos(114mg,0.24mmol)、乙酸钾(720mg,7.2mmol)和二噁烷(20mL)。在经历三轮真空/氩气吹洗后,将混合物在65℃加热4小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物用5:1石油醚/乙酸乙酯(10mL)洗涤得到244c,其为黄色固体(1.0g,纯度:60%)。MS-ESI:[M+H]+384.1.
实施例244d乙酸(4-(1-甲基-5-(5-(1-甲基氮杂环丁烷-3-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-3-基)甲酯244d
在配备有回流冷凝器的50-mL圆底烧瓶中装入5-溴-1-甲基-3-(5-(1-甲基氮杂环丁烷-3-基)吡啶-2-基氨基)吡啶-2(1H)-酮239c(140mg,0.40mmol)、244c(230mg,0.60mmol)、Pd(dppf)Cl2(20mg,0.020mmol)、K3PO4(180mg,0.80mmol)、乙酸钠·3H2O(120mg,0.80mmol)、水(0.5mL)和乙腈(10mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热2小时。然后将其过滤并减压蒸发滤液。将残余物在硅胶柱色谱上纯化(用25:1二氯甲烷/甲醇洗脱)得到244d,其为黄色固体(90mg,43%)。MS-ESI:[M+H]+608.3
实施例244 2-[3-(羟基甲基)-4-[1-甲基-5-[[5-(1-甲基氮杂环丁烷-3-基)-2-吡啶基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-1-酮244
将244d(90mg,0.15mmol)和氢氧化锂(60mg,1.5mmol)于THF/异丙醇(5:3,8mL)和水(2mL)中的混合物在30℃搅拌1小时。真空蒸发混合物并将残余物用水(3mL)稀释。然后将其用乙酸乙酯(20mLX2)萃取。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到244(25mg,30%),其为白色固体。MS-ESI:[M+H]+566.4.1H NMR(500MHz,CDCl3)δ8.74(d,J=2.5Hz,1H),8.51(d,J=5.5Hz,1H),8.16(d,J=2.0Hz,1H),7.91(s,1H),7.87(d,J=2.0Hz,1H),7.59-7.57(m,1H),7.35(d,J=5.0Hz,1H),6.85-6.83(m,1H),6.33(s,1H),5.04-5.01(m,1H),4.67-4.65(m,1H),4.44-4.39(m,1H),4.33-4.29(m,1H),3.95-3.91(m,1H),3.86-3.83(m,2H),3.76-3.74(m,1H),3.73(s,3H),3.62-3.59(m,1H),3.16-3.13(m,2H),3.02-2.95(m,2H),2.84-2.83(m,2H),2.39(s,3H),2.05-2.02(m,2H),1.90-1.87(m,2H).
实施例245a 4-氯-2-(1-氧代-6,7,8,9-四氢吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-3-甲醛245a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入6,7,8,9-四氢吡啶并[3,4-b]吲嗪-1(2H)-酮112d(1.48g,7.9mmol,1.0当量)、2-溴-4-氯吡啶-3-甲醛(3.48g,15.8mmol,2.0当量)、CuI(1.50g,7.9mmol,1.0当量)、4,7-二甲氧基-1,10-菲咯啉(2.13g,7.9mmol,1.0当量)、K2CO3(2.18g,15.8mmol,2.0当量)和二噁烷(50mL)。将反应混合物在100℃搅拌24小时。反应结束后,过滤混合物并减压浓缩滤液。将残余物通过硅胶柱色谱法(用1:2乙酸乙酯/石油醚洗脱)来纯化得到245a(550mg,21%),其为浅黄色固体。MS-ESI:[M+H]+328.1.
实施例245b 4-氟-2-(1-甲基-5-(5-(4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-6-(1-氧代-5,6,7,8-四氢-1H-吡咯并[3,4-b]吲嗪-2(3H)-基)苯甲醛245b
在配备有回流冷凝器的50-mL单颈圆底烧瓶中装入245a(140mg,0.42mmol,1.0当量)、(S)-1-甲基-3-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮191i(308mg,0.63mmol,1.5当量)、Pd(dppf)Cl2(35mg,0.042mmol,0.1当量)、乙酸钠(70mg,0.84mmol,2.0当量)、K3PO4(175mg,0.84mmol,2.0当量)、乙腈(20mL)和水(1mL)。在经历三轮真空/氩气吹洗后,将混合物在90℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用40:1二氯甲烷/甲醇洗脱)来纯化得到245b(100mg,36%),其为黄色固体。MS-ESI:[M+H]+647.4.
实施例245(S)-2-(3-(羟基甲基)-4-(1-甲基-5-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-2-基)-6,7,8,9-四氢吡啶并[3,4-b]吲嗪-1(2H)-酮245
在配备有磁力搅拌子的50-mL单颈圆底烧瓶中装入245b(100mg,0.15mmol,1.0当量)、NaBH4(29mg,0.77mmol,5.0当量)和甲醇(10mL)。将所得混合物在室温搅拌20分钟。然后将其过滤并减压浓缩滤液。将残余物通过反相制备性-HPLC来纯化得到245(80mg,79%),其为白色固体。MS-ESI:[M+H]+649.3.1H NMR(500MHz,DMSO-d6)δ8.69-8.68(m,1H),8.57(d,J=5.0Hz,1H),8.46(s,1H),7.85(d,J=3.0Hz,1H),7.55(d,J=2.5Hz,1H),7.52(d,J=5.0Hz,1H),7.39-7.36(m,1H),7.26-7.24(m,2H),6.69(d,J=7.5Hz,1H),6.31(s,1H),4.97(bs,1H),4.58-4.54(m,2H),4.49-4.41(m,2H),4.34-4.27(m,2H),4.09-4.06(m,2H),3.69-3.68(m,1H),3.61(s,3H),3.41-3.39(m,1H),3.12-3.19(m,1H),2.97-2.93(m,1H),2.87(t,J=6.0Hz,2H),2.56-2.54(m,1H),2.37-2.30(m,2H),2.21-2.16(m,1H),2.03-1.98(m,2H),1.85-1.82(m,2H),0.94(d,J=5.5Hz,3H).
实施例246a 4-(5-(1,5-二甲基-1H-吡唑-3-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-6,7,8,9-四氢吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-3-甲醛246a
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入4-氯-2-(1-氧代-6,7,8,9-四氢吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-3-甲醛245a(130mg,0.39mmol,1.0当量)、3-(1,5-二甲基-1H-吡唑-3-基氨基)-1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮218a(600mg,1.75mmol,4.0当量)、Pd(dppf)Cl2(32mg,0.040mmol,0.1当量)、乙酸钠(64mg,0.78mmol,2.0当量)、K3PO4(165mg,0.78mmol,2.0当量)、乙腈(15mL)和水(1mL)。在经历三轮真空/氩气吹洗后,将混合物在90℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用50:1二氯甲烷/乙醇洗脱)来纯化得到246a(38mg,19%),其为黄色固体。MS-ESI:[M+H]+510.3.
实施例246 2-[4-[5-[(1,5-二甲基吡唑-3-基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-6,7,8,9-四氢吡啶并[3,4-b]吲嗪-1-酮246
在配备有磁力搅拌子的25-mL单颈圆底烧瓶中装入246a(38mg,0.074mmol,1.0当量)、NaBH4(29mg,0.37mmol,5.0当量)和甲醇(5mL)。将所得混合物在室温搅拌20分钟。然后将其过滤并浓缩滤液。将残余物通过反相制备性-HPLC来纯化得到标题化合物(18mg,48%),其为白色固体。MS-ESI:[M+H]+512.3.1H NMR(500MHz,CDCl3)δ8.58(d,J=5.0Hz,1H),7.98(d,J=2.5Hz,1H),7.78(d,J=2.5Hz,1H),7.52(d,J=5.0Hz,1H),7.37(s,1H),7.17(d,J=7.0Hz,1H),6.58-6.57(m,2H),5.74(s,1H),5.41-5.39(m,1H),4.42-4.32(m,2H),4.08(t,J=6.5Hz,2H),3.72(s,3H),3.70(s,3H),2.98(t,J=6.5Hz,2H),2.25(s,3H),2.13-2.09(m,2H),1.97-1.92(m,2H).
实施例247a乙酸{4-[5-({5-乙酰基-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基}氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基]-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02 ,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-基}甲酯247a
在配备有磁力搅拌子和回流冷凝器的25-mL单颈圆底烧瓶中装入3-(5-乙酰基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-5-溴-1-甲基吡啶-2(1H)-酮209c(183mg,0.50mmol)、{3-[(乙酰氧基)甲基]-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-4-基}硼酸230i(200mg,0.50mmol)、Pd(dppf)Cl2(37mg,0.05mmol)、K3PO4(212mg,1.0mmol)、乙酸钠(82mg,1.0mmol)、水(0.5mL)和乙腈(5mL)。在经历三轮真空/氩气吹洗后,将混合物在90℃加热1小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(50:1至20:1)洗脱)来纯化得到247a,其为黄色固体(100mg,31%)。MS-ESI:[M+H]+641.2.
实施例247 3-[4-[5-[(5-乙酰基-6,7-二氢-4H-吡唑并[1,5-a]吡嗪-2-基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-6,7,8,9-四氢苯并噻吩并[2,3-d]哒嗪-4-酮247
将乙酸{4-[5-({5-乙酰基-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基}氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基]-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-基}甲酯247a(100mg,0.16mmol)和氢氧化锂(96mg,4.0mmol)于异丙醇/THF/水(2:2:1,10mL)中的混合物在35℃搅拌30分钟。将混合物减压浓缩。向残余物中加入水(5mL)并将所得混合物用二氯甲烷萃取三次。然后减压浓缩合并的有机层并将所得残余物通过反相制备性-HPLC来纯化得到247(51mg,53%)。MS-ESI:[M+H]+599.3.1H NMR(500MHz,DMSO-d6,T=80℃)δ8.54-8.51(m,1H),8.38(d,J=3.0Hz,1H),7.93-7.91(m,2H),7.48(d,J=8.5Hz,1H),7.35(d,J=3.0Hz,1H),6.00(s,1H),4.64-4.62(m,2H),4.39(s,2H),3.98-3.95(m,2H),3.89-3.86(m,2H),3.58(s,3H),2.95-2.93(m,2H),2.87-2.84(m,2H),2.08(s,3H),1.89-1.87(m,4H).
实施例248a(R)-(6-氨基吡啶-3-基)(3-甲基吗啉代)甲酮248a
向(R)-3-甲基吗啉(2.02g,20mmol)于乙醇(25mL)中的溶液中加入1-乙基-3-(3-二甲基氨基丙基)碳二亚胺(EDCI)(3.33g,17.4mmol)、羟基苯并三唑(HOBt)(2.35g,17.4mmol)和6-氨基吡啶-3-甲酸(2.0g,14.5mmol)。在室温搅拌18小时后,过滤反应悬浮液并减压浓缩滤液。将残余物通过硅胶柱色谱法(用3:1乙酸乙酯/石油醚洗脱)来纯化得到248a,其为白色固体(1.6g,36%)。MS-ESI:[M+H]+222.3。
实施例248b 6-氯-2-甲基-4-[(5-{[(3R)-3-甲基吗啉-4-基]羰基}吡啶-2-基)氨基]-2,3-二氢哒嗪-3-酮248b
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(50mL)、248a(330mg,1.5mmol)、4-溴-6-氯-2-甲基哒嗪-3(2H)-酮(446mg,2.0mmol)、碳酸铯(978mg,3.0mmol)、Xantphos(88mg,0.15mmol)和三(二亚苄基丙酮)二钯(0)(68mg,0.075mmol)。使体系经历三轮真空/氩气吹洗并回流加热4小时。然后将其冷却至室温并过滤。将固体用二氯甲烷(3X30mL)洗涤并将合并的滤液减压浓缩。将残余物通过硅胶柱色谱法(用石油醚/乙酸乙酯(2:1至1:2)洗脱)来纯化得到248b(430mg,79%),其为黄色固体。MS-ESI:[M+H]+364.3
实施例248c乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{1-甲基-5-[(5-{[(3R)-3-甲基吗啉-4-基]羰基}吡啶-2-基)氨基]-6-氧代-1,6-二氢哒嗪-3-基}吡啶-3-基)甲酯248c
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入248b(364mg,1.0mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(596mg,1.5mmol)、K3PO4(424mg,2.0mmol)、1,1’-二(二苯基膦基)二茂铁二氯化钯(II)(73mg,0.10mmol)、乙酸钠(164mg,2.0mmol)、乙腈(10mL)和水(0.5mL)。在经历三轮真空/氩气吹洗后,将反应混合物在100℃加热2.5小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将反应混合物冷却至室温并过滤。减压浓缩滤液。将残余物用二氯甲烷(50mL)和水(50mL)稀释。分离出水层并用二氯甲烷(3×20mL)萃取。将合并的有机层用Na2SO4干燥并过滤。减压浓缩滤液并将黑色残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(80:1至50:1)洗脱)来纯化得到248c(250mg,37%),其为黄色油状物。MS-ESI:[M+H]+681.3
实施例248 3-[3-(羟基甲基)-4-[1-甲基-5-[[5-[(3R)-3-甲基吗啉-4-羰基]-2-吡啶基]氨基]-6-氧代-哒嗪-3-基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮248
在室温,向248c(250mg,0.37mmol)于THF/异丙醇/水(2.5/2/0.5mL)中的溶液中加入氢氧化锂(86mg,3.6mmol)。在将反应混合物搅拌3小时后,LCMS表明反应完成。然后将混合物倒入水(20mL)中并用二氯甲烷(3X20mL)萃取。将合并的有机层用盐水(30mL)洗涤,用Na2SO4干燥,过滤。减压浓缩滤液。将残余固体通过反相制备性-HPLC来纯化得到248(110mg,48%),其为白色固体。MS-ESI:[M+H]+639.3.1H NMR(500MHz,MeOD)δ8.85(s,1H),8.58(d,J=5.0Hz,1H),8.44(d,J=2.0Hz,1H),7.79(dd,J=2.5,8.5Hz,1H),7.57(d,J=5.0Hz,1H),7.32(d,J=8.5Hz,1H),6.74(s,1H),4.85-4.83(m,1H),4.66-4.64(m,1H),4.42-4.27(m,4H),4.02-3.88(m,over lap,6H),3.74-3.67(m,2H),3.56-3.46(m,2H),2.67-2.59(m,2H),2.51(s,2H),1.39(d,J=6.5Hz,3H),1.28(s,6H).
实施例249a(R)-5-溴-1-甲基-3-(5-(3-甲基吗啉-4-羰基)吡啶-2-基氨基)吡啶-2(1H)-酮249a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(15mL)、(R)-(6-氨基吡啶-3-基)(3-甲基吗啉代)甲酮248a(332mg,1.5mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(480mg,1.8mmol)和碳酸铯(978mg,3.0mmol)。在使氮气鼓泡通过所述悬浮液3分钟后,加入Xantphos(87mg,0.15mmol)和三(二亚苄基丙酮)二钯(0)(69mg,0.075mmol)。使体系经历三轮真空/氩气吹洗并回流加热2.5小时。然后将其冷却至室温并过滤。将固体用二氯甲烷(2X50mL)洗涤并将合并的滤液减压浓缩。将残余物通过硅胶柱色谱法(用石油醚/乙酸乙酯(2:1至1:2)洗脱)来纯化得到249a(430mg,70%),其为黄色固体。MS-ESI:[M+H]+407.3
实施例249b乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{1-甲基-5-[(5-{[(3R)-3-甲基吗啉-4-基]羰基}吡啶-2-基)氨基]-6-氧代-1,6-二氢吡啶-3-基}吡啶-3-基)甲酯249b
在配备有磁力搅拌子和回流冷凝器的25-mL单颈圆底烧瓶中装入249a(407mg,1.0mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(800mg,2.0mmol)、K3PO4(424mg,2.0mmol)、1,1’-二(二苯基膦基)二茂铁二氯化钯(II)(73mg,0.1mmol)、乙酸钠(164mg,2.0mmol)、乙腈(8mL)和水(0.2mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热1.5小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将反应混合物冷却至室温并减压浓缩。将残余物用二氯甲烷(20mL)和水(20mL)稀释。分离出水层并用二氯甲烷(20mL×3)萃取。将合并的有机层用Na2SO4干燥并过滤。减压浓缩滤液。将黑色残余物通过硅胶柱色谱法(用60:1二氯甲烷/甲醇洗脱)来纯化得到249b(200mg,29%),其为黄色固体。MS-ESI:[M+H]+680.1
实施例249 3-[3-(羟基甲基)-4-[1-甲基-5-[[5-[(3R)-3-甲基吗啉-4-羰基]-2-吡啶基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮249
在室温,向249b(204mg,0.30mmol)于THF/异丙醇/水(3/3/0.5mL)中的溶液中加入氢氧化锂(72mg,3mmol)。在将反应混合物搅拌3小时后,LCMS表明反应完成。将混合物减压浓缩并将残余物用水(10mL)稀释。然后将其用二氯甲烷(3X10mL)萃取。将合并的有机层用盐水(30mL)洗涤,用Na2SO4干燥并过滤。减压浓缩滤液。将残余物通过反相制备性-HPLC来纯化(A:1%NH4HCO3于水中,B:乙腈)得到249(85mg,44%),其为白色固体。MS-ESI:[M+H]+638.3.1H NMR(500MHz,MeOD)δ8.93(d,J=2.0Hz,1H),8.52(d,J=5.0Hz,1H),8.33(d,J=2.0Hz,1H),7.69(dd,J=2.0,6.5Hz,1H),7.61(d,J=2.0Hz,1H),7.48(d,J=5.0Hz,1H),7.13(d,J=8.5Hz,1H),6.74(s,1H),4.70(d,J=12.0Hz,1H),4.58(d,J=12.0Hz,1H),4.40-4.27(m,4H),3.99-3.89(m,3H),3.74(S,3H),3.55-3.46(m,重叠,4H),2.67-2.59(m,2H),2.51(s,2H),1.39(d,J=6.5Hz,3H),1.28(s,6H).
实施例250a 1-(5-(羟基甲基)-3-硝基-1H-吡唑-1-基)丙烷-2-醇250a
在配备有磁力搅拌子的100-mL单颈圆底烧瓶中装入(3-硝基-1H-吡唑-5-基)甲醇(0.57g,4.0mmol)、Cs2CO3(261mg,0.8mmol)和2-甲基环氧乙烷(20mL)。将混合物在30℃搅拌2天。将混合物冷却至室温并用二氯甲烷(100mL)稀释。过滤所得混合物并减压浓缩滤液。将残余物通过硅胶柱色谱法(用30:1二氯甲烷/甲醇洗脱)来纯化得到250a(0.40g,50%),其为白色固体。MS-ESI:[M+H]+202.3
实施例250b 1-(5-(溴甲基)-3-硝基-1H-吡唑-1-基)丙烷-2-醇250b
历时30分钟,向在0℃冷却的250a(4.0g,20.0mmol)于氯仿(100mL)中的溶液中加入POBr3(22.9g,80mmol)于氯仿(20mL)中的溶液,同时维持内部温度低于5℃。将反应混合物温热至50℃并在该温度搅拌3小时。然后将其冷却至0℃并用水淬灭。分离有机层并减压蒸发。将残余物通过硅胶柱色谱法(用30:1二氯甲烷/甲醇洗脱)来纯化得到250b(3.3g,62%),其为黄色固体。MS-ESI:[M+H]+264.1
实施例250c 1-(5-((甲基氨基)甲基)-3-硝基-1H-吡唑-1-基)丙烷-2-醇250c
向250b(3.0g,11.4mmol)于二氯甲烷(30mL)中的溶液中加入CH3NH2溶液(3.0g,34.2mmol,35%于水中)。将该反应混合物在室温搅拌1小时。然后分离出有机层,用Na2SO4干燥并过滤。减压浓缩滤液得到250c(1.9g,78%),其为黄色固体。MS-ESI:[M+H]+215.3
实施例250d 5,6-二甲基-2-硝基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪250d
历时30分钟,向在0℃冷却的250c(1.129g,5.27mmol)和三苯基膦(4.14g,15.8mmol)于无水THF(40mL)中的混合物中加入偶氮二羧酸二异丙酯(DIAD)(3.19g,15.8mmol)于THF(15mL)中的溶液,同时维持内部温度低于5℃。将反应混合物温热至30℃并在该温度搅拌5小时。然后将混合物用水(50mL)淬灭并减压浓缩。将残余物用二氯甲烷(3X80mL)萃取。将合并的有机层用Na2SO4干燥并过滤。减压浓缩滤液。将残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(80:1至30:1)洗脱)来纯化得到250d(0.83g,80%),其为黄色固体。MS-ESI:[M+H]+197.2
实施例250e 5,6-二甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-胺250e
向250d(550mg,2.8mmol)于甲醇(20mL)中的溶液中加入Raney Ni(约600mg)。向反应混合物中充入氢气(通过气囊)并在室温搅拌2小时。然后将其用塞过滤并减压浓缩滤液得到250e,其为黄色固体(400mg,86%),将其不经进一步纯化直接用于下一步骤。MS-ESI:[M+H]+167.3
实施例250f乙酸(4-(5-(5,6-二甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯250f
在配备有磁力搅拌子和回流冷凝器的50-mL圆底烧瓶中装入乙酸(4-(5-溴-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯217a(525mg,1.0mmol)、250e(166mg,1.0mmol)、碳酸铯(652mg,2.0mmol)和1,4-二噁烷(10mL)。在使氮气鼓泡通过所述悬浮液30分钟后,加入xantphos(116mg,0.20mmol)和三(二亚苄基丙酮)二钯(0)(92mg,0.10mmol)。使体系经历三轮真空/氩气吹洗并回流加热5小时。然后将其冷却至室温并过滤。将固体用二氯甲烷(2X30mL)洗涤并将合并的滤液减压浓缩。将残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(80:1至30:1)洗脱)来纯化得到250f(80mg,13%),其为黄色固体。MS-ESI:[M+H]+611.4
实施例250 2-[4-[5-[(5,6-二甲基-6,7-二氢-4H-吡唑并[1,5-a]吡嗪-2-基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1-酮250
向250f(75mg,0.123mmol)于THF/异丙醇/水(4/2/2mL)中的溶液中加入氢氧化锂(15mg,0.62mmol)。将混合物在30℃搅拌1小时。反应完成后,将混合物减压蒸发并将残余物通过反相制备性-HPLC来纯化得到250,其为白色固体(40mg,57%)。MS-ESI:[M+H]+569.3.1HNMR(500MHz,CDCl3)δ8.49(d,J=5.0Hz,1H),7.96(bs,1H),7.73(d,J=2.0Hz,1H),7.43(s,1H),7.36(d,J=5.0Hz,1H),6.91(s,1H),5.71(s,1H),5.03(t,J=3.5Hz,1H),4.65-4.62(m,1H),4.52-4.50(m,1H),4.35-4.33(m,1H),4.17-4.05(m,3H),3.91-3.88(m,2H),3.73-3.71(m,1H),3.71(s,3H),3.55-3.52(m,1H),2.90-2.87(m,1H),2.64-2.58(m,4H),2.43(s,3H),1.93-1.90(m,2H),1.81-1.80(m,2H),1.24(d,J=6.5Hz,3H).
实施例252a 5-溴-3-(1-乙基-5-甲基-1H-吡唑-3-基氨基)-1-甲基吡啶-2(1H)-酮252a
在100-mL圆底烧瓶中装入5-溴-1-甲基-3-(5-甲基-1H-吡唑-3-基氨基)吡啶-2(1H)-酮115a(800mg,2.83mmol)、溴乙烷(216mg,1.98mmol)、K2CO3(780mg,5.66mmol)和DMF(20mL)。将混合物在85℃加热整夜。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用1:20甲醇/二氯甲烷洗脱)来纯化得到252a,其为红色固体(298mg,37%)。MS-ESI:[M+H]+311.0.1H NMR(500MHz,DMSO-d6)δ8.28(s,1H),7.99(d,J=2.5Hz,1H),7.35(d,J=2.5Hz,1H),5.85(s,1H),3.98-3.94(m,2H),3.48(s,3H),2.19(s,3H),1.27(t,J=7.0Hz,3H).
实施例252b乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{5-[(1-乙基-5-甲基-1H-吡唑-3-基)氨基]-1-甲基-6-氧代-1,6-二氢吡啶-3-基}吡啶-3-基)甲酯252b
在配备有回流冷凝器的圆底烧瓶中装入252a(200mg,0.64mmol)、(3-(乙酰氧基甲基)-2-(7,7-二甲基-1-氧代-3,4,7,8-四氢-1H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-2(6H)-基)吡啶-4-基)硼酸199e(309mg,0.64mmol)、PdCl2(dppf)(52.5mg,0.060mmol)、K3PO4(333mg,1.29mmol)、乙酸钠(105mg,1.29mmol)、乙腈(10mL)和水(0.5mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热3小时。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用1:20甲醇/二氯甲烷洗脱)来纯化得到252b,其为黄色固体(120mg,27.6%)。MS-ESI:[M+H]+584.3
实施例252 3-[4-[5-[(1-乙基-5-甲基-吡唑-3-基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮252
将252b(120mg,0.21mmol)和氢氧化锂(23mg,0.82mmol)于THF(6mL),异丙醇(4mL)和水(2mL)中的混合物在室温搅拌0.5小时。然后将其减压浓缩并将残余物用水(5mL)稀释。将所得混合物用二氯甲烷(2X10mL)萃取。将合并的二氯甲烷萃取物减压浓缩。将残余物用反相制备性-HPLC来纯化得到252(52mg,47%),其为白色固体。MS-ESI:[M+H]+542.3.1H NMR(500MHz,DMSO-d6)δ9.06(d,J=5.5Hz,1H),8.09(s,1H),8.07(s,1H),7.41(s,1H),7.33(d,J=5.0Hz,1H),6.56(s,1H),5.88(s,1H),4.97(t,J=4.5Hz,1H),4.50-4.41(m,2H),4.24-4.19(m,3H),3.93-3.85(m,3H),3.59(s,3H),2.62-2.57(m,2H),2.43(s,2H),2.19(s,3H),1.27-1.23(m,重叠,9H).
实施例253a 4-溴-6-氯-2-((2-(三甲基甲硅烷基)乙氧基)甲基)哒嗪-3(2H)-酮253a
将配备有磁力搅拌子的500-mL单颈圆底烧瓶用氮气吹洗并装入无水DMF(150mL)和4-溴-6-氯-哒嗪-3(2H)-酮(10.0g,47.8mmol)。将反应混合物冷却至0℃并加入氢化钠。将反应混合物在0℃搅拌20分钟。之后,加入2-(三甲基甲硅烷基)乙氧基甲基氯化物(11.9g,71.6mmol)并移去冷却浴,将反应混合物在室温搅拌3小时。然后将反应用饱和碳酸氢钠水溶液(30mL)淬灭。将混合物用乙酸乙酯(2×300mL)萃取。将萃取物用硫酸钠干燥,过滤并减压浓缩。将所得残余物通过快速色谱法来纯化得到253a,56%收率(9.00g),其为黄色油状物:1H NMR(300MHz,CDCl3)δ8.02(s,1H),5.42(s,2H),3.79(t,2H,J=5.4Hz),0.96(t,2H,J=5.4Hz),0.01(s,9H).
实施例253b(S)-4-(6-(6-氯-3-氧代-2-((2-(三甲基甲硅烷基)乙氧基)-甲基)-2,3-二氢哒嗪-4-基氨基)吡啶-3-基)-3-甲基哌嗪-1-羧酸叔丁酯253b
在配备有回流冷凝器的50-mL圆底烧瓶中装入(S)-4-(6-氨基吡啶-3-基)-3-甲基哌嗪-1-羧酸叔丁酯191f(580mg,2.0mmol)、253a(1.36g,4.0mmol)、Pd2(dba)3(180mg,0.20mmol)、Xantphos(230mg,0.40mmol)、Cs2CO3(1.3g,4.0mmol)和二噁烷(20mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热2小时。然后将其冷却至室温并过滤。减压蒸发滤液并将残余物通过硅胶柱色谱法来纯化(用4:1石油醚/乙酸乙酯洗脱)得到253b(1.0g,91%),其为黄色固体。MS-ESI:[M+H]+551.2
实施例253c(S)-6-氯-4-(5-(2-甲基哌嗪-1-基)吡啶-2-基氨基)哒嗪-3(2H)-酮253c
在50-mL圆底烧瓶中装入253b(551mg,1.0mmol)、浓HCl(2mL)和甲醇(10mL)。将混合物在室温搅拌整夜。然后将其减压浓缩得到253c,将其不经进一步纯化直接用于下一步骤。MS-ESI:[M+H]+321.1
实施例253d(S)-6-氯-4-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)哒嗪-3(2H)-酮253d
在配备有磁力搅拌子的50-mL圆底烧瓶中装入253c(321mg,1.0mmol)、3-氧杂环丁酮(142mg,2.0mmol)、NaBH3CN(125mg,2.0mmol)、ZnCl2(272mg,2.0mmol)和甲醇(10mL)。将混合物在室温搅拌整夜并减压浓缩。向残余物中加入水(20mL)并将所得混合物用二氯甲烷(3X20mL)萃取。将合并的有机层减压浓缩并将残余物通过硅胶柱色谱法(用乙酸乙酯洗脱)来纯化得到253d(210mg,56%),其为黄色固体。MS-ESI:[M+H]+377.3.
实施例253e乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-[5-({5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢哒嗪-3-基]吡啶-3-基)甲酯253e
在配备有磁力搅拌子和回流冷凝器的25-mL单颈圆底烧瓶中装入253d(172mg,0.46mmol)、(3-(乙酰氧基甲基)-2-(7,7-二甲基-1-氧代-3,4,7,8-四氢-1H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-2(6H)-基)吡啶-4-基)硼酸199e(0.91g,2.29mmol)、Pd(dppf)Cl2(36mg,0.050mmol)、K3PO4(195mg,0.92mmol)、乙酸钠(75mg,0.050mmol)、水(0.5mL)和乙腈(10mL)。在经历三轮真空/氩气吹洗后,将混合物在90℃加热2小时。然后将其冷却至室温并过滤。减压蒸发滤液并将残余物通过硅胶柱色谱法(用20:1乙酸乙酯/甲醇洗脱)来纯化得到253e(100mg,31%),其为棕色固体。MS-ESI:[M+H]+694.3.
实施例253 3-[3-(羟基甲基)-4-[5-[[5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]-2-吡啶基]氨基]-6-氧代-1H-哒嗪-3-基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮253
在配备有磁力搅拌子的25-mL单颈圆底烧瓶中装入253e(92mg,0.13mmol)、氢氧化锂(16mg,0.65mmol)、THF(2mL)、异丙醇(2mL)和水(0.5mL)。将混合物在室温搅拌1小时。然后将其减压浓缩。向残余物中加入水(10mL)并将所得混合物用二氯甲烷(3X20mL)萃取。将合并的有机层减压浓缩并将残余物通过反相制备性-HPLC来纯化得到253(22mg,26%),其为白色固体。MS-ESI:[M+H]+652.2.1H NMR(500MHz,CDCl3)δ10.83(s,1H),8.61(s,1H),8.58(d,J=5.0Hz,1H),8.12(s,1H),8.05(d,J=2.5Hz,1H),7.45(d,J=5.0Hz,1H),7.32(dd,J=3.0Hz,5.5Hz,1H),7.00(d,J=3.5Hz,1H),6.84(s,1H),4.74-4.68(m,3H),4.65-4.58(m,3H),4.26-4.14(m,2H),3.99-3.96(m,1H),3.71-3.69(m,1H),3.55-3.53(m,1H),3.18-3.14(m,2H),2.64-2.59(m,3H),2.53-2.47(m,4H),2.40-2.33(m,2H),1.29(s,6H),1.09(d,J=7.0Hz,3H).
实施例254a 4-[5-({5-乙酰基-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基}氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基]-2-{4,4-二甲基-9-氧代-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-10-基}吡啶-3-甲醛254a
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入3-(5-乙酰基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基-氨基)-1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮209d(344mg,0.83mmol)、4-氯-2-{4,4-二甲基-9-氧代-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-10-基}吡啶-3-甲醛109a(202mg,0.56mmol)、Pd(dppf)Cl2(20mg,0.028mmol)、K3PO4(235mg,1.11mmol)、乙酸钠(91mg,1.11mmol)、水(0.5mL)和乙腈(10mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热1小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将混合物冷却降至室温并过滤。减压浓缩滤液得到254a(400mg,粗制),将其不经进一步纯化直接用于下一步骤。MS-ESI:[M+H]+612.3
实施例254 3-[4-[5-[(5-乙酰基-6,7-二氢-4H-吡唑并[1,5-a]吡嗪-2-基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]噻吩并[1,3-c]吡啶-4-酮254
向254a(98mg,0.16mmol)于甲醇和二氯甲烷中的溶液中加入NaBH4(13mg,0.33mmol)。将反应混合物在室温搅拌1小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将混合物用NH4Cl水溶液(5mL)淬灭并减压浓缩。将残余物用二氯甲烷(3X10mL)萃取。将合并的萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到254(53mg,54%),其为白色固体。MS-ESI:[M+H]+613.9.1H NMR(500MHz,DMSO-d6,T=80℃)δ8.45(d,J=8.5Hz,1H),7.93-7.92(m,2H),7.33(d,J=3.5Hz,1H),7.30(d,J=8.5Hz,1H),5.97(s,1H),4.67-4.63(m,3H),4.46-4.45(m,2H),3.97-3.93(m,2H),3.89-3.86(m,3H),3.56(s,3H),2.97-2.91(m,2H),2.53-2.55(m,2H),2.49-2.46(m,2H),2.08(s,3H),1.21(s,6H).
实施例255a 4-(5-(5-乙酰基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛255a
按照实施例246中描述的操作,以4-氯-2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛134c(200mg,0.575mmol)和3-(5-乙酰基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮209d(356mg,0.863mmol)开始,获得255a,其为红色油状物(320mg,93%)。MS-ESI:[M+H]+599.3
实施例255 2-[4-[5-[(5-乙酰基-6,7-二氢-4H-吡唑并[1,5-a]吡嗪-2-基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-10-氟-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1-酮255
按照实施例254中描述的操作,以255a(200mg,0.334mmol)开始获得255,其为白色固体(55.5mg,28%)。MS-ESI:[M+H]+601.3.1HNMR(500MHz,DMSO-d6,T=80℃)δ8.45(d,J=8.0Hz,1H),7.93(d,J=3.5Hz,2H),7.33(d,J=4.0Hz,1H),7.30(d,J=8.5Hz,1H),5.97(s,1H),4.70-4.63(m,3H),4.46(d,J=8.5Hz,2H),4.10-3.86(m,重叠,8H),3.58(s,3H),2.57-2.55(m,2H),2.43-2.39(m,2H),2.08(s,3H),1.79-1.67(m,4H).
实施例256a(S)-(6-氨基吡啶-3-基)(3-甲基吗啉代)甲酮256a
在室温,向(S)-3-甲基吗啉(1.5g,15.0mmol)于乙醇(20mL)中的溶液中加入EDCI(3.33g,17.4mmol)、HOBt(2.35g,17.4mmol)和6-氨基吡啶-3-甲酸(2.07g,15.0mmol)。搅拌18小时后,过滤所得悬浮液。将固体通过硅胶柱色谱法(用2:1石油醚/乙酸乙酯至纯乙酸乙酯洗脱)来纯化得到256a(1.0g,30%),其为白色固体。MS-ESI:222.3(M+H)+.
实施例256b(S)-5-溴-1-甲基-3-(5-(3-甲基吗啉-4-羰基吡啶-2-基氨基)吡啶-2(1H)-酮256b
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入1,4-二噁烷(10ml)、256a(111mg,0.50mmol)、4-溴-6-氯-2-甲基哒嗪-3(2H)-酮(134mg,0.60mmol)、碳酸铯(326mg,1.0mmol)、Xantphos(29mg,0.05mmol)和三(二亚苄基丙酮)二钯(0)(23mg,0.025mmol)。使体系经历三轮真空/氩气吹洗并在100℃加热5小时。然后将其冷却至室温并过滤。将固体用二氯甲烷(3X30mL)洗涤并将合并的滤液减压浓缩。将残余物通过硅胶柱色谱法(用石油醚/乙酸乙酯(2:1至1:2)洗脱)来纯化得到256b(140mg,77%),其为黄色固体。MS-ESI:[M+H]+364.3
实施例256c乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{1-甲基-5-[(5-{[(3S)-3-甲基吗啉-4-基]羰基}吡啶-2-基)氨基]-6-氧代-1,6-二氢哒嗪-3-基}吡啶-3-基)甲酯256c
在配备有磁力搅拌子和回流冷凝器的25-mL单颈圆底烧瓶中装入256b(140mg,0.38mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(159mg,0.40mmol)、K3PO4(85mg,0.40mmol)、乙酸钠(33mg,0.40mmol)、1,1’-二(二苯基膦基)二茂铁二氯化钯(II)(15mg,0.020mmol)、乙腈(10mL)和水(0.5mL)。使体系经历三轮真空/氩气吹洗并在100℃加热2.5小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将反应混合物冷却至室温并用二氯甲烷(30mL)和水(30mL)稀释。分离出水层并用二氯甲烷(3×20mL)萃取。将合并的有机层用Na2SO4干燥并过滤。减压浓缩滤液。将黑色残余物通过硅胶柱色谱法(用60:1二氯甲烷:/甲醇洗脱)来纯化得到256c(90mg,35%),其为黄色固体。MS-ESI:[M+H]+681.3
实施例256 3-[3-(羟基甲基)-4-[1-甲基-5-[[5-[(3S)-3-甲基吗啉-4-羰基]-2-吡啶基]氨基]-6-氧代-哒嗪-3-基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮256
在室温,向256c(90mg,0.13mmol)于THF/异丙醇/水(2.0/1/0.5ml)中的溶液中加入氢氧化锂(31mg,1.3mmol)。在将反应混合物搅拌3小时后,LCMS表明反应完成。然后将混合物倒入水(15mL)中并用二氯甲烷(3X10mL)萃取。将合并的有机层用盐水(30mL)洗涤,用Na2SO4干燥并过滤。减压浓缩滤液并将残余物通过反相制备性-HPLC来纯化得到256(40mg,48%),其为白色固体。MS-ESI:[M+H]+639.3.1H NMR(500MHz,MeOD)δ8.86(s,1H),8.58(d,J=5.0Hz,1H),8.44(d,J=2.0Hz,1H),7.79(dd,J=2.0,6.5Hz,1H),7.57(d,J=5.0Hz,1H),7.32(d,J=8.5Hz,1H),6.74(s,1H),4.85-4.82(m,1H),4.66-4.64(m,1H),4.42-4.27(m,4H),4.02-3.88(m,重叠,6H),3.74-3.67(m,2H),3.56-3.46(m,2H),2.67-2.59(m,2H),2.51(s,2H),1.39(d,J=7.0Hz,3H),1.28(s,6H).
实施例257(S)-5-溴-1-甲基-3-(5-(3-甲基吗啉-4-羰基)吡啶-2-基氨基)吡啶-2(1H)-酮257a
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入(S)-(6-氨基吡啶-3-基)(3-甲基吗啉代)甲酮(222mg,1.0mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(320mg,1.2mmol)、碳酸铯(652mg,2mmol)和1,4-二噁烷(10mL)。在使氮气鼓泡通过所述悬浮液10分钟后,加入Xantphos(58mg,0.10mmol)和三(二亚苄基丙酮)二钯(0)(46mg,0.050mmol)。使体系经历三轮真空/氩气吹洗并回流加热2.5小时。然后将其冷却至室温并过滤。将固体用二氯甲烷(2X30mL)洗涤并将合并的滤液减压浓缩。将残余物通过硅胶柱色谱法(用石油醚/乙酸乙酯(2:1至1:2)洗脱)来纯化得到257a(280mg,69%),其为黄色固体。MS-ESI:[M+H]+407.3
实施例257b乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{1-甲基-5-[(5-{[(3S)-3-甲基吗啉-4-基]羰基}吡啶-2-基)氨基]-6-氧代-1,6-二氢吡啶-3-基}吡啶-3-基)甲酯257b
在配备有磁力搅拌子和回流冷凝器的25-mL单颈圆底烧瓶中装入257a(203mg,0.50mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(640mg,1.6mmol)、K3PO4(212mg,1.0mmol)、1,1’-二(二苯基膦基)二茂铁二氯化钯(II)(18mg,0.025mmol)、乙酸钠(82mg,1.0mmol)、乙腈(10mL)和水(0.2mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热2.5小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将反应混合物冷却至室温并减压浓缩。将残余物用二氯甲烷(20mL)和水(20mL)稀释。分离出水层并用二氯甲烷(3X20mL)萃取。将合并的有机层用Na2SO4干燥并过滤。减压浓缩滤液。将黑色残余物通过硅胶柱色谱法(用60:1二氯甲烷/甲醇洗脱)来纯化得到257b(160mg,47%),其为黑色固体。MS-ESI:[M+H]+680.1
实施例257 3-[3-(羟基甲基)-4-[1-甲基-5-[[5-[(3S)-3-甲基吗啉-4-羰基]-2-吡啶基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮257
在室温,向257b(157mg,0.23mmol)于THF/异丙醇/水(2/2/0.5mL)中的溶液中加入氢氧化锂(55mg,2.3mmol)。在将反应混合物搅拌3小时后,LCMS表明反应完成。将混合物倒入水(15mL)中并用二氯甲烷(3X15mL)萃取。将合并的有机层用盐水(30mL)洗涤,用Na2SO4干燥并过滤。减压浓缩滤液。将残余固体通过反相制备性-HPLC来纯化(A:1‰NH4HCO3于水中;B:乙腈)得到257(52mg,35%),其为黄色固体。MS-ESI:[M+H]+668.3.1H NMR(500MHz,MeOD)δ8.94(d,J=2.0Hz,1H),8.53(d,J=5.0Hz,1H),8.33(d,J=2.0Hz,1H),7.69(dd,J=2.0,6.5Hz,1H),7.61(d,J=2.0Hz,1H),7.48(d,J=5.0Hz,1H),7.13(d,J=8.5Hz,1H),6.74(s,1H),4.70(d,J=12.0Hz,1H),4.58(d,J=12.0Hz,1H),4.41-4.27(m,4H),3.99-3.89(m,3H),3.74-3.66(m,重叠,5H),3.55-3.46(m,2H),2.67-2.59(m,2H),2.51(s,2H),1.39(d,J=6.5Hz,3H),1.28(s,6H).
实施例258a 6-氯-2-甲基-4-({5-[(吗啉-4-基)羰基]吡啶-2-基}氨基)-2,3-二氢哒嗪-3-酮258a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(40mL)、(6-氨基吡啶-3-基)(吗啉代)-甲酮(2.07g,10.0mmol)、4-溴-6-氯-2-甲基哒嗪-3(2H)-酮111a(3.35g,15.0mmol)、Pd2(dba)3(915mg,1.0mmol)、XantPhos(578mg,1.0mmol)和碳酸铯(6.52g,20mmol)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热8小时。然后将其冷却至室温并过滤。将固体用二氯甲烷(2X20mL)洗涤。将合并的滤液用无水Na2SO4干燥并减压浓缩得到258a(2.45g,51%),其为黄色固体。MS:[M+H]+350.1
实施例258b 1-甲基-5-(5-(吗啉-4-羰基)吡啶-2-基氨基)-6-氧代-1,6-二氢哒嗪-3-基硼酸258b
在配备有磁力搅拌子和回流冷凝器的250-mL单颈圆底烧瓶中装入258a(2.0g,5.73mmol,1.0当量)、4,4,4',4',5,5,5',5'-八甲基-2,2'-二(1,3,2-二氧杂硼杂戊环)(7.56g,28.6mmol,5.0当量)、Pd(dppf)Cl2(465mg,0.57mmol,0.1当量)、X-Phos(461mg,1.14mmol,0.2当量)、乙酸钾(1.11g,11.4mmol,2.0当量)和二噁烷(50mL)。在经历三轮真空/氩气吹洗后,将混合物在50℃加热6小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物用1:3乙酸乙酯/石油醚洗涤得到258b(1.70g,83%),其为黄色固体,将其不经进一步纯化即用于下一步骤。MS:[M+H]+360.1
实施例258c 4-氯-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-甲醛258c
在配备有回流冷凝器的100-mL圆底烧瓶中装入4-氯-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-甲醛124a(100mg,0.29mmol)、258b(128mg,0.36mmol)、PdCl2(dppf)(24mg,0.031mmol)、K3PO4(123mg,0.58mmol)、乙酸钠(57mg,0.58mmol)、乙腈(30mL)和水(3mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃搅拌3小时。然后将其过滤并真空蒸发滤液。将残余物用硅胶柱色谱法(用1:3石油醚/乙酸乙酯洗脱)来纯化得到258c,其为黄色固体(45mg,25%)。MS-ESI:[M+H]+625.2
实施例258 3-[3-(羟基甲基)-4-[1-甲基-5-[[5-(吗啉-4-羰基)-2-吡啶基]氨基]-6-氧代-哒嗪-3-基]-2-吡啶基]-6,7,8,9-四氢苯并噻吩并[2,3-d]哒嗪-4-酮258
将258c(45mg,0.071mmol)、NaBH4(8mg,0.21mmol)和甲醇(7mL)的混合物在室温搅拌2小时。将反应混合物用水(5mL)淬灭并减压浓缩。将残余物用二氯甲烷(2X10mL)萃取并将合并的二氯甲烷萃取物减压浓缩。将残余物通过反相制备性-HPLC来纯化得到258(24mg,53%),其为黄色固体。MS-ESI:[M+H]+627.2.1H NMR(500MHz,DMSO-d6)δ9.80(s,1H),8.68(s,1H),8.65(d,J=4.5Hz,1H),8.50(s,1H),8.39(d,J=2.0Hz,1H),7.80-7.78(m,1H),7.67(d,J=5.0Hz,1H),7.60(d,J=8.5Hz,1H),4.85(t,J=5.5Hz,1H),4.52-4.35(m,2H),3.82(s,3H),3.60-3.49(m,8H),2.95-2.93(m,2H),2.89-2.84(m,2H),1.94-1.83(m,4H).
实施例259a 2-{4,4-二甲基-9-氧代-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-10-基}-4-[1-甲基-5-({5-[(吗啉-4-基)羰基]吡啶-2-基}氨基)-6-氧代哒嗪-3-基]吡啶-3-甲醛259a
在配备有回流冷凝器的圆底烧瓶中装入4-氯-2-{4,4-二甲基-9-氧代-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-10-基}吡啶-3-甲醛109a(144mg,0.40mmol)、1-甲基-5-(5-(吗啉-4-羰基)吡啶-2-基氨基)-6-氧代-1,6-二氢哒嗪-3-基硼酸258a(215mg,0.60mmol)、PdCl2(dppf)(16mg,0.020mmol)、K3PO4三水合物(207mg,0.80mmol)、乙酸钠(66mg,0.80mmol)、乙腈(15mL)和水(1.5mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃搅拌2小时。然后将其过滤并真空蒸发滤液。将残余物用硅胶柱色谱法(用25:1二氯甲烷/甲醇洗脱)来纯化得到259a,其为黄色固体(80mg,30%)。MS-ESI:[M+H]+640.3。
实施例259 3-[3-(羟基甲基)-4-[1-甲基-5-[[5-(吗啉-4-羰基)-2-吡啶基]氨基]-6-氧代-哒嗪-3-基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]噻吩并[1,3-c]吡啶-4-酮259
将259a(80mg,0.12mmol)、NaBH4(14mg,0.36mmol)和甲醇(5mL)的混合物在室温搅拌1小时。然后将其用盐水(5mL)淬灭并减压蒸发。将残余物用二氯甲烷(2X10mL)萃取并将合并的二氯甲烷萃取物减压浓缩。将所得残余物通过反相制备性-HPLC来纯化得到259,其为白色固体(38mg,49%)。MS-ESI:[M+H]+642.8.1H NMR(500MHz,CDCl3)δ8.78(s,1H),8.61(d,J=5.0Hz,1H),8.44(d,J=2.5Hz,2H),7.80-7.77(m,1H),7.45(d,J=5.0Hz,1H),7.06-7.04(m,1H),4.65-4.59(m,2H),4.42(s,1H),4.30-4.27(m,1H),3.95(s,3H),3.90-3.87(m,1H),3.76-3.68(m,8H),3.04-2.92(m,2H),2.82-2.80(m,2H),2.59-2.54(m,2H),1.30(s,6H).
实施例260a乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{1-甲基-5-[(5-甲基-1H-吡唑-3-基)氨基]-6-氧代-1,6-二氢吡啶-3-基}吡啶-3-基)甲酯260a
在配备有回流冷凝器的圆底烧瓶中装入5-溴-1-甲基-3-(5-甲基-1H-吡唑-3-基氨基)吡啶-2(1H)-酮218a(201mg,0.71mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(282mg,0.71mmol)、Pd(dppf)Cl2(51mg,0.07mmol)、K3PO4(301mg,1.42mmol)、乙酸钠(116mg,1.42mmol)、乙腈(10mL)和水(0.2mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热3小时。然后将其过滤并减压蒸发滤液。将残余物通过硅胶柱色谱法(用1:20甲醇/二氯甲烷洗脱)来纯化得到260a,其为红色固体(150mg,38%)。MS-ESI:[M+H]+556.3
实施例260 3-[3-(羟基甲基)-4-[1-甲基-5-[(5-甲基-1H-吡唑-3-基)氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮260
将260a(150mg,0.27mmol)和氢氧化锂(13mg,0.54mmol)于THF(6mL),异丙醇(4mL)和水(2mL)中的混合物在室温搅拌0.5小时。将混合物减压浓缩并将残余物用水(5mL)稀释。然后将其用二氯甲烷(2X10mL)萃取并将合并的二氯甲烷萃取物减压浓缩。将残余物用反相制备性-HPLC来纯化得到260(28mg,20%),其为白色固体。MS-ESI:[M+H]+514.3.1H NMR(500MHz,DMSO-d6)δ11.76(s,1H),8.47(d,J=5.0Hz,1H),8.07-8.05(m,2H),7.38-7.31(m,2H),6.55(s,1H),5.88(s,1H),4.95-4.93(m,1H),4.48-4.39(m,2H),4.22-4.18(m,3H),3.83(d,J=5.5Hz,1H),3.58(s,3H),2.64-2.56(m,2H),2.36-2.34(m,2H),2.16(s,3H),1.22(s,6H).
实施例261a 4-{5-[(1,5-二甲基-1H-吡唑-3-基)氨基]-1-甲基-6-氧代-1,6-二氢吡啶-3-基}-2-{10-氟-1-氧代-1H,2H,3H,4H,6H,7H,8H,9H-吡啶并[3,4-b]吲嗪-2-基}吡啶-3-甲醛261a
在配备有磁力搅拌子和回流冷凝器的25-mL单颈圆底烧瓶中装入4-氯-2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-3-甲醛134c(97mg,0.28mmol)、3-[(1,5-二甲基-1H-吡唑-3-基)氨基]-1-甲基-5-(四甲基-1,3,2-二氧杂硼杂戊环-2-基)-1,2-二氢吡啶-2-酮218a(192.6mg,0.56mmol)、Pd2(dba)3(54.9mg,0.060mmol)、三(环己基)膦(50.2mg,0.18mmol)、Cs2CO3(182.6mg,0.56mmol)、二噁烷(8mL)和水(0.25mL)。在经历三轮真空/氩气吹洗后,将混合物在110℃搅拌2小时。然后将其过滤并真空蒸发滤液。将残余物通过硅胶柱色谱法(用35:1乙酸乙酯/甲醇洗脱)来纯化得到261a(90mg,61%),其为黑色固体。MS-ESI:[M+H]+530.2
实施例261 2-[4-[5-[(1,5-二甲基吡唑-3-基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-10-氟-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-1-酮261
在室温,向261a(90.0mg,0.17mmol)于甲醇(5mL)中的溶液中加入硼氢化钠(64.6mg,1.7mmol)。将反应混合物搅拌0.5小时。然后将其用水(2mL)淬灭并真空蒸发。将残余物用二氯甲烷(3X10mL)萃取。将合并的二氯甲烷萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到261(47.0mg,52%),其为白色固体。MS-ESI:[M+H]+532.3.1H NMR(500MHz,DMSO-d6)δ8.47(d,J=5.0Hz,1H),8.05(s,1H),8.03(d,J=2.5Hz,1H),7.39(d,J=2.5Hz,1H),7.31(d,J=5.0Hz,1H),5.89(s,1H),4.87-4.85(m,1H),4.45-4.36(m,2H),4.11-4.09(m,1H),3.93-3.91(m,1H),3.79-3.76(m,2H),3.59(s,3H),3.58(s,3H),3.00-2.94(m,2H),2.66-2.63(m,2H),2.18(s,3H),1.90-1.88(m,2H),1.78-1.73(m,2H)
实施例262a 5-溴-1-甲基-3-(5-甲基噁唑-2-基氨基)吡啶-2(1H)-酮262a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入5-甲基噁唑-2-胺(276mg,2.82mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(753mg,2.82mmol)、三-(二亚苄基丙酮)二钯(0)(256mg,0.28mmol)、XantPhos(324mg,0.56mmol)、Cs2CO3(1.8g,5.64mmol)和1,4-二噁烷(30mL)。在经历三轮真空/氩气吹洗后,将混合物在92℃加热3小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用100:1二氯甲烷/甲醇洗脱)来纯化得到262a,其为白色固体(702mg,88%)。MS-ESI:[M+H]+284.1.
实施例262b乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{1-甲基-5-[(5-甲基-1,3-噁唑-2-基)氨基]-6-氧代-1,6-二氢吡啶-3-基}吡啶-3-基)甲酯262b
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入262a(150mg,0.53mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(421mg,1.06mmol)、Pd(dppf)Cl2(37mg,0.050mmol)、K3PO4(225mg,1.06mmol)、乙酸钠(87mg,1.06mmol)、水(0.5mL)和乙腈(10mL)。在经历三轮真空/氩气吹洗后,将混合物在90℃加热1小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(50:1至30:1)洗脱)来纯化得到262b,其为黄色固体(100mg,34%)。MS-ESI:[M+H]+556.9.
实施例262 3-[3-(羟基甲基)-4-[1-甲基-5-[(5-甲基噁唑-2-基)氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮262
将262b(100mg,0.18mmol)和氢氧化锂(108mg,4.5mmol)于异丙醇/THF/水(4/4/2mL)中的混合物在35℃搅拌30分钟。将混合物减压浓缩。向残余物中加入水(5mL)并将所得混合物用二氯甲烷萃取三次。将合并的有机层减压浓缩并将所得残余物通过反相制备性-HPLC来纯化得到262,其为白色固体(21.0mg,23%)。MS-ESI:[M+H]+515.3.1H NMR(500MHz,DMSO-d6)δ9.19(s,1H),8.49(d,J=5.0Hz,1H),8.30(s,1H),7.60(d,J=1.0Hz,1H),7.32(d,J=4.5Hz,1H),6.62(s,1H),6.56(s,1H),4.96-4.94(m,1H),4.45-4.36(m,2H),4.24-4.14(m,3H),3.84(d,J=10.5Hz,1H),3.59(s,3H),2.62-2.56(m,2H),2.44-2.42(m,2H),2.22(s,3H),1.22(s,6H).
实施例263a 6-氯-2-甲基-4-(嘧啶-4-基氨基)哒嗪-3(2H)-酮263a
在配备有磁力搅拌子和回流冷凝器的250-mL单颈圆底烧瓶中装入1,4-二噁烷(150mL)、嘧啶-4-胺(1.7g,18.0mmol)、4-溴-6-氯-2-甲基哒嗪-3(2H)-酮(4.0g,18.0mmol)和碳酸铯(11.74g,36.0mmol)。在使氮气鼓泡通过所述悬浮液30分钟后,加入Xantphos(1.04g,1.8mmol)和三(二亚苄基丙酮)二钯(0)(823mg,0.9mmol)。使体系经历三轮真空/氩气吹洗并回流加热15小时。然后将其冷却至室温并过滤。将固体用二氯甲烷(2X50mL)洗涤。将合并的滤液浓缩并将残余物用乙腈(5mL)洗涤得到263a(2.99g,70%),其为黄色固体。MS:[M+H]+238
实施例263b 1-甲基-6-氧代-5-(嘧啶-4-基氨基)-1,6-二氢哒嗪-3-基-硼酸263b
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入263a(500mg,2.11mmol)、4,4,4',4',5,5,5',5'-八甲基-2,2'-二(1,3,2-二氧杂硼杂戊环)(2.68g,10.6mmol)、Pd(dppf)Cl2(170mg,0.20mmol)、X-phos(170mg,0.40mmol)、乙酸钾(410mg,4.21mmol)和二噁烷(30mL)。使体系经历三轮真空/氩气吹洗并在50℃搅拌6小时。LCMS表明263a完全被转化成263b。
实施例263c 2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)-4-(1-甲基-6-氧代-5-(嘧啶-4-基氨基)-1,6-二氢哒嗪-3-基)吡啶-3-甲醛263c
在室温,向263b的混合物中加入4-氯-2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛134c(300mg,0.90mmol)、Pd(dppf)Cl2(170mg,0.20mmol)、K3PO4(103mg,0.40mmol)和水(2mL)。使体系再次经历三轮真空/氩气吹洗并在80℃搅拌4小时。然后将反应混合物冷却至室温,用水(30mL)稀释并过滤。将滤液用二氯甲烷(2X30mL)萃取。将合并的二氯甲烷萃取物减压浓缩并将残余物通过硅胶柱色谱法(用二氯甲烷/甲醇(40:1至20:1)洗脱)来纯化得到263c,其为黄色固体(210mg,45%)。MS-ESI:[M+H]+515.3
实施例263 10-氟-2-[3-(羟基甲基)-4-[1-甲基-6-氧代-5-(嘧啶-4-基氨基)哒嗪-3-基]-2-吡啶基]-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1-酮263
在配备有磁力搅拌子的100-mL单颈圆底烧瓶中装入263c(100mg,0.19mmol)、NaBH4(30mg,0.78mmol)和甲醇(20mL)。将混合物在室温搅拌0.5小时。然后将其用水(30mL)稀释并减压浓缩。将残余物用二氯甲烷(2X30mL)萃取,将合并的二氯甲烷萃取物干燥并减压浓缩。将残余物用反相制备性-HPLC来纯化得到263,其为白色固体(67mg,68%)。MS-ESI:[M+H]+517.3.1H NMR(500MHz,DMSO-d6)δ9.93(s,1H),8.81(s,1H),8.67(s,1H),8.55(d,J=4.5Hz,1H),8.49(d,J=5.5Hz,1H),7.56(dd,J=1.0,6.0Hz,1H),7.43(d,J=5.0Hz,1H),4.83(t,J=5.5Hz,1H),4.62-4.58(m,1H),4.39-4.36(m,1H),4.25-4.19(m,2H),4.06-4.04(m,1H),3.92-3.90(m,1H),3.81(s,3H),2.64-2.54(m,2H),2.43-2.41(m 2H),1.781.76(m,2H),1.69-1.67(m,2H).
实施例264a 2-(4-氨基嘧啶-2-基)丙烷-2-醇264a
历时5分钟,向在-20℃冷却的4-氨基嘧啶-2-羧酸乙酯(840mg,5.0mmol)于无水四氢呋喃(50mL)中的溶液中加入甲基溴化镁的THF溶液(8.5mL,25.0mmol,3.0M)。将反应混合物在0℃再搅拌2小时。然后将其用饱和NH4Cl(20mL)淬灭并减压浓缩。将残余物用乙酸乙酯(5X40mL)萃取。将合并的有机层用无水Mg2SO4来干燥,过滤并减压蒸发。将残余物通过反相Combiflash来纯化得到264a,其为黄色固体(240mg,32%)MS-ESI:[M+H]+154.1
实施例264b 5-溴-3-(2-(2-羟基丙烷-2-基)嘧啶-4-基氨基)-1-甲基吡啶-2(1H)-酮264b
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入264a(300mg,2.0mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(800mg,3.0mmol)、Pd2(dba)3(182mg,0.20mmol)、XantPhos(231mg,0.40mmol)、Cs2CO3(1.30g,4.0mmol)和1,4-二噁烷(20mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热15小时。然后将其冷却至室温并过滤。减压浓缩滤液。将所得残余物通过硅胶柱色谱法来纯化(用40:1二氯甲烷/甲醇(40:1)洗脱)并进一步通过反相Combiflash来纯化得到264b,其为白色固体(200mg,30%)。MS-ESI:[M+H]+339.0
实施例264c乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-(5-{[2-(2-羟基丙烷-2-基)嘧啶-4-基]氨基}-1-甲基-6-氧代-1,6-二氢-吡啶-3-基)吡啶-3-基)甲酯264c
在配备有回流冷凝器的50-mL圆底烧瓶中装入264b(170mg,0.50mmol)、(3-(乙酰氧基甲基)-2-(7,7-二甲基-1-氧代-3,4,7,8-四氢-1H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-2(6H)-基)吡啶-4-基)硼酸199e(200mg,0.50mmol)、Pd(dppf)Cl2(40mg,0.050mmol)、K3PO4(212mg,1.0mmol)、水(0.5mL)和四氢呋喃(10mL)。在经历三轮真空/氩气吹洗后,将混合物回流加热6小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用40:1二氯甲烷/甲醇洗脱)得到264c,其为棕色固体(200mg,54%)。MS-ESI:[M+H]+612.3
实施例264 3-[3-(羟基甲基)-4-[5-[[2-(1-羟基-1-甲基-乙基)嘧啶-4-基]氨基]-1-甲基-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮264
向264c(170mg,0.27mmol)于四氢呋喃(10mL)和水(2mL)中的溶液中加入氢氧化锂(64mg,3.0mmol)。将反应混合物在35℃搅拌2小时。然后将其减压浓缩并将残余物通过反相制备性-HPLC来纯化得到264(86mg,46%),其为黄色固体。MS-ESI:[M+H]+570.1.1H NMR(500MHz,DMSO-d6)δ9.27(s,1H),8.94(d,J=2.0Hz,1H),8.50(d,J=5.0Hz,1H),8.33(d,J=6.0Hz,1H),7.76(d,J=2.5Hz,1H),7.41(d,J=5.0Hz,1H),7.22(d,J=5.5Hz,1H),6.56(s,1H),5.14(t,J=5.0Hz,1H),4.89(s,1H),4.48-4.42(m,2H),4.23-4.19(m,重叠,3H),3.85-3.84(m,1H),3.62(s,3H),2.67-2.56(m,2H),2.42(s,2H),1.42(s,3H),1.40(s,3H),1.21(s,重叠,6H).
实施例265a 1-(2-硝基-6,7-二氢吡唑并[1,5-a]吡嗪-5(4H)-基)丙烷-1-酮265a
向2-硝基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪209a(200mg,1.19mmol)于二氯甲烷(8mL)中的溶液中加入Et3N(240mg,2.38mmol)。搅拌5分钟后,加入丙酰氯(121mg,1.31mmol)于二氯甲烷(2mL)中的溶液并将反应混合物在室温搅拌1小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将混合物用水和盐水洗涤,用Na2SO4干燥并过滤。减压浓缩滤液得到265a(260mg,98%),其为白色固体,将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+225.0
实施例265b 1-(2-氨基-6,7-二氢吡唑并[1,5-a]吡嗪-5(4H)-基)丙烷-1-酮265b
向265a(260mg,1.16mmol)于甲醇(10mL)中的溶液中加入10%Pd/C(26mg)。将体系排空,然后重新填充H2。搅拌2小时后,通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。过滤混合物并减压浓缩滤液得到265b,其为黄色固体(225mg,99%)。MS-ESI:[M+H]+195.1
实施例265c 5-溴-1-甲基-3-(5-丙酰基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)吡啶-2(1H)-酮265c
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入265b(200mg,1.03mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(414mg,1.55mmol)、Pd2(dba)3(47mg,0.052mmol)、Xantphos(60mg,0.103mmol)、Cs2CO3(671.6mg,2.06mmol)和二噁烷(20mL)。在经历三轮真空/氩气吹洗后,将反应混合物在100℃加热3小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将反应混合物冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用80:1二氯甲烷/甲醇洗脱)得到265c(280mg,72%),其为白色固体。MS-ESI:[M+H]+380.2
实施例265d乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-[1-甲基-6-氧代-5-({5-丙酰基-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基}氨基)-1,6-二氢吡啶-3-基]吡啶-3-基)甲酯265d
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入265c(200mg,0.53mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(834mg,2.10mmol)、Pd(dppf)Cl2(19mg,0.0263mmol)、K3PO4(223mg,1.052mmol)、乙酸钠(86mg,1.052mmol)、乙腈(10mL)和水(5滴)。在经历三轮真空/氩气吹洗后,将反应混合物在100℃加热3小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将反应混合物冷却降至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用60:1二氯甲烷/甲醇洗脱)得到265d(100mg,29%),其为黄色油状物。MS-ESI:[M+H]+653.3
实施例265 3-[3-(羟基甲基)-4-[1-甲基-6-氧代-5-[(5-丙酰基-6,7-二氢-4H-吡唑并[1,5-a]吡嗪-2-基)氨基]-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮265
向265d(100mg,0.153mmol)于THF(3mL)、异丙醇(3mL)和水(5mL)中的溶液中加入氢氧化锂(37mg,1.53mmol)。将反应混合物在室温搅拌1小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将混合物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到265(50mg,54%),其为白色固体。MS-ESI:[M+H]+611.3.1H NMR(500MHz,DMSO-d6,T=80℃)δ8.45(d,J=8.5Hz,1H),7.93-7.90(m,2H),7.35(d,J=3.5Hz,1H),7.29(d,J=8.5Hz,1H),6.55(s,1H),5.98(s,1H),4.74-4.71(m,1H),4.65(s,2H),4.46-4.44(m,2H),4.18-4.16(m,2H),3.97-3.87(m,重叠,5H),3.58(s,3H),2.57-2.56(m,2H),2.49-2.37(m,4H),1.22(s,6H),1.03(t,J=12.0Hz,3H).
实施例266a 5-溴-1-甲基-3-((5-(氧杂环丁烷-3-基)-1H-吡唑-3-基)氨基)吡啶-2(1H)-酮266a
按照图26的反应方案制备了266a。
实施例266b乙酸(2'-(7,7-二甲基-1-氧代-3,4,7,8-四氢-1H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-2(6H)-基)-1-甲基-5-((5-(氧杂环丁烷-3-基)-1H-吡唑-3-基)氨基)-6-氧代-1,6-二氢-[3,4'-联吡啶]-3'-基)甲酯266b
在配备有磁力搅拌子和回流冷凝器的25-mL单颈圆底烧瓶中装入266a(33mg,0.10mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(60mg,0.15mmol)、Pd(dppf)Cl2(7mg,0.010mmol)、K3PO4(42mg,0.20mmol)、乙酸钠(16mg,0.20mmol)、乙腈(6mL)、水(0.1mL)。在经历三轮真空/氩气吹洗后,将混合物回流加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用30:1二氯甲烷/甲醇洗脱)得到266b,其为白色固体(17mg,28%)。MS-ESI:[M+H]+598.4
实施例266 3-[3-(羟基甲基)-4-[1-甲基-5-[[5-(氧杂环丁烷-3-基)-1H-吡唑-3-基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮266
将266b(15mg,0.025mmol)和氢氧化锂(6mg,0.25mmol)于异丙醇/THF(1:1,4mL)和水(1mL)中的混合物在30℃搅拌1小时。将混合物减压蒸发并将残余物用水(5mL)稀释。然后将其用乙酸乙酯(2X10mL)萃取。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到266(4.5mg,33%),其为白色固体。MS-ESI:[M+H]+556.3.1H NMR(500MHz,CDCl3)δ8.49(d,J=5.0Hz,1H),7.98(s,1H),7.68(s,1H),7.58(s,1H),7.33(d,J=5.0Hz,1H),6.86(s,1H),6.09(s,1H),5.07-5.04(m,2H),4.79-4.76(m,2H),4.68-4.66(m,1H),4.54-4.51(m,1H),4.37-4.34(m,1H),4.28-4.25(m,1H),4.18(d,J=5.5Hz,2H),3.89-3.87(m,1H),3.73(s,3H),2.59-2.57(m,2H),2.54-2.52(m,3H),1.29(s,6H).
实施例267a 5-溴-1-甲基-3-(5-甲基-1,3,4-噻二唑-2-基氨基)吡啶-2(1H)-酮267a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入5-甲基-1,3,4-噻二唑-2-胺(1.15g,10.0mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(4.00g,15.0mmol)、Pd2(dba)3(916mg,1.0mmol)、Xantphos(1.16g,2.0mmol)、Cs2CO3(6.52g,20.0mmol)和二噁烷(50mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热3小时。然后将其冷却至室温并过滤。减压蒸发滤液并将残余物通过硅胶柱色谱法来纯化(用20:1二氯甲烷/甲醇洗脱)得到267a(2.2g,73%),其为白色固体。MS-ESI:[M+H]+301.2
实施例267b乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{1-甲基-5-[(5-甲基-1,3,4-噻二唑-2-基)氨基]-6-氧代-1,6-二氢吡啶-3-基}吡啶-3-基)甲酯267b
在配备有回流冷凝器的50-mL圆底烧瓶中装入267a(150mg,0.50mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(640mg,1.5mmol)、PdCl2(dppf)(37mg,0.050mmol)、K3PO4(212mg,1.0mmol)、乙酸钠(82mg,1.0mmol)、乙腈(10mL)和水(0.2mL)。在经历三轮真空/氩气吹洗后,将混合物在90℃加热2小时。然后将其冷却至室温并过滤。减压蒸发滤液并将残余物通过硅胶柱色谱法来纯化(用50:1二氯甲烷/甲醇洗脱)得到267b(80mg,28%),其为黄色固体。MS-ESI:[M+H]+574.2
实施例267 3-[3-(羟基甲基)-4-[1-甲基-5-[(5-甲基-1,3,4-噻二唑-2-基)氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮267
在配备有磁力搅拌子的25-mL圆底烧瓶中加入267b(80mg,0.14mmol)、氢氧化锂(17mg,0.70mmol)、THF(2mL)、异丙醇(2mL)和水(0.5mL)。将混合物在室温搅拌1小时并减压浓缩。将残余物用水(5mL)稀释并用二氯甲烷(10mL×3)萃取,将合并的有机层减压浓缩。将残余物通过反相制备性-HPLC来纯化得到267(32mg,43%),其为白色固体。MS-ESI:[M+H]+532.3.1H NMR(500MHz,DMSO-d6)δ10.19(s,1H),8.57(d,J=3.0Hz,1H),8.49(d,J=6.0Hz,1H),7.63(d,J=3.0Hz,1H),7.32(d,J=6.0Hz,1H),6.56(s,1H),4.92(t,J=6.5Hz,1H),4.45-4.37(m,2H),4.22-4.17(m,3H),3.85-3.80(m,1H),3.60(s,3H),2.58-2.56(m,2H),2.52(s,3H),2.42(s,2H),1.17(s,6H).
实施例268a 1-甲基-4-硝基-1H-咪唑268a
向4-硝基-1H-咪唑(2.0g,17.7mmol)和K2CO3(3.67g,26.5mmol)于乙腈(20mL)中的混合物中滴加碘甲烷(1.3mL,3.0g,21.2mmol),同时在室温搅拌。将所得混合物在60℃搅拌整夜。然后将其减压蒸发并将残余物用水(20mL)稀释。将混合物用二氯甲烷(2X20mL)萃取。将合并的萃取物减压浓缩并将残余物通过硅胶柱色谱法来纯化(用100:1二氯甲烷/甲醇洗脱)得到268a,其为黄色固体(1.8g,82%)。MS-ESI:[M+H]+128.1.1H NMR(500MHz,DMSO-d6)δ8.37(s,1H),7.82(s,1H),3.76(s,3H).
实施例268b 1-甲基-1H-咪唑-4-胺268b
在100-mL圆底烧瓶中装入268a(1.6g,12.6mmol)、10%钯/炭(50%水分,160mg)和乙醇(15mL)。将所述烧瓶排空、充入氢气并在室温搅拌整夜。通过用垫过滤除去催化剂,减压浓缩滤液得到268b(1.2g,98%),其为黄色固体。MS-ESI:[M+H]+98.2
实施例268c 5-溴-1-甲基-3-(1-甲基-1H-咪唑-4-基氨基)吡啶-2(1H)-酮268c
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(50mL)、268b(1.1g,11.3mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(3.0g,11.3mmol)、Pd2(dba)3(1.0g,1.13mmol)、XantPhos(1.3g,2.26mmol)和碳酸铯(7.3g,22.6mmol)。在经历三轮真空/氩气吹洗后,将混合物在92℃加热4.5小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(100:1至50:1)洗脱)得到268c(2.4g,76%),其为黄色固体。MS-ESI:[M+H]+283.1
实施例268d乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{1-甲基-5-[(1-甲基-1H-咪唑-4-基)氨基]-6-氧代-1,6-二氢吡啶-3-基}吡啶-3-基)甲酯268d
在配备有回流冷凝器的50-mL圆底烧瓶中装入268c(150mg,0.53mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(80.4mg,0.21mmol)、Pd(dppf)Cl2(17.2mg,0.021mmol)、K3PO4(89mg,0.42mmol)、乙酸钠(57.1mg,0.42mmol)、水(0.2mL)和乙腈(10mL)。在经历三轮真空/氩气吹洗后,将混合物在90℃加热2.5小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(30:1至20:1)洗脱)得到268d(110mg,37.2%),其为棕色固体。MS-ESI:[M+H]+556.4.
实施例268 3-[3-(羟基甲基)-4-[1-甲基-5-[(1-甲基咪唑-4-基)氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮268
将268d(100mg,0.18mmol)和氢氧化锂(189mg,4.5mmol)于异丙醇/THF(1:1,4.0mL)和水(1.0mL)中的混合物在35℃搅拌30分钟。将混合物减压浓缩。向残余物中加入水(5mL)并将所得混合物用二氯甲烷(3X10mL)萃取。将合并的有机层减压浓缩并将所得残余物通过反相制备性-HPLC来纯化得到268(19.8mg,22%),其为黄色固体。MS-ESI:[M+H]+514.3.1H NMR(500MHz,DMSO-d6)δ8.47(d,J=5.5Hz,1H),7.57(s,1H),7.44(d,J=2.5Hz,1H),7.39(s,1H),7.36(d,J=2.5Hz,1H),7.34(d,J=5.0Hz,1H),6.95(s,1H),6.56(s,1H),5.12-5.10(m,1H),4.44-4.41(m,2H),4.22-4.18(m,3H),3.84-3.82(m,1H),3.60(s,3H),3.59(s,3H),2.59-2.56(m,2H),2.44-2.42(m,2H),1.22(s,6H).
实施例269a 2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-[1-甲基-5-({5-[(吗啉-4-基)羰基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]吡啶-3-甲醛269a
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入4-氯-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-甲醛108a(100mg,0.29mmol)、1-甲基-3-(5-(吗啉-4-羰基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮111c(192mg,0.44mmol)、Pd(dppf)Cl2(12mg,0.015mmol)、K3PO4(123mg,0.58mmol)、乙酸钠(47mg,0.58mmol)、乙腈(10mL)和水(5滴)。在经历三轮真空/氮气吹洗后,将混合物在100℃加热1小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法(二氯甲烷/甲醇40:1)来纯化得到269a(150mg,83%),其为棕色固体。MS-ESI:[M+H]+621.8
实施例269 3-[3-(羟基甲基)-4-[1-甲基-5-[[5-(吗啉-4-羰基)-2-吡啶基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮269
向269a(150mg,0.24mmol)于二氯甲烷(5mL)和甲醇(5mL)中的溶液中加入NaBH4(18.2mg,0.482mmol)。在室温搅拌1小时后,将混合物用NH4Cl水溶液(10mL)淬灭并减压浓缩。将残余物用二氯甲烷(3X20m)萃取。将合并的萃取物用盐水洗涤,用Na2SO4干燥,减压浓缩并通过反相制备性-HPLC来纯化得到269(114mg,76%),其为白色固体。MS-ESI:[M+H]+624.3.1H NMR(500MHz,DMSO-d6)δ9.00(s,1H),8.79(d,J=2.0Hz,1H),8.50(d,J=4.5Hz,1H),8.26(d,J=1.5Hz,1H),7.67(dd,J=2.0,9.0Hz,1H),7.61(d,J=1.5Hz,1H),7.38-7.36(m,2H),6.56(s,1H),5.00(s,1H),4.47-4.40(m,2H),4.25-4.19(m,3H),3.86-3.84(m,1H),3.62-3.60(重叠,m,4H),3.51(s,3H),3.52-3.50(m,4H),2.59-2.57(m,2H),2.43(s,2H),1.22(s,6H).
实施例270a N-[(吡嗪-2-基)氨基硫代羰基]氨基甲酸乙酯270a
在配备有磁力搅拌子的250-mL单颈圆底烧瓶中装入吡嗪-2-胺(7.6g,80.0mmol,1.0当量)、异硫氰酸乙氧羰酯(O-ethyl carbonisothiocyanatidate)(12.5g,95.4mmol,1.2当量)和二噁烷(150mL)。将反应混合物在室温搅拌24小时。反应完成后,将其减压浓缩至体积为约20mL并过滤所得悬浮液。收集固体并用乙酸乙酯(3×20mL)洗涤得到270a(14.0g,77%),其为白色固体。MS-ESI:[M+H]+227.3
实施例270b[1,2,4]三唑并[1,5-a]吡嗪-2-胺270b
在配备有磁力搅拌子和回流冷凝器的250-mL单颈圆底烧瓶中装入270a(6.00g,26.43mmol,1.0当量)、羟基胺盐酸盐(3.32g,47.52mmol,1.8当量)、DIPEA(12mL)、乙醇(40mL)和甲醇(40mL)。将反应混合物在65℃搅拌16小时。反应完成后,将其冷却至室温并减压浓缩至体积为约20mL。过滤收集所得悬浮液并将固体用60:1二氯甲烷/乙醇(50mL)洗涤得到270b(3.3g,92%),其为白色固体。MS-ESI:[M+H]+136.3.1H NMR(500MHz,DMSO-d6)δ8.84(d,J=1.0Hz,1H),8.70(dd,J=1.0,4.0Hz,1H),7.98(d,J=5.0Hz,1H),6.47(s,2H).
实施例270c[1,2,4]三唑并[1,5-a]吡嗪-2-基氨基甲酸叔丁酯270c
在配备有磁力搅拌子的250-mL单颈圆底烧瓶中装入270b(2.00g,14.8mmol,1.0当量)、Boc2O(3.87g,17.77mmol,1.2当量)和无水THF(60mL)。将体系排空并用氮气回填。将反应混合物冷却至-78℃,然后加入LHMDS(37.0mL,37.0mmol,2.5当量,1.0M于THF中)。将反应混合物在-78℃搅拌2小时后,将其用饱和NH4Cl水溶液(30mL)淬灭。将混合物减压浓缩并将残余物用二氯甲烷(3X50mL)萃取。将合并的有机层用硫酸钠干燥,过滤并减压浓缩。将所得残余物通过硅胶柱色谱法来纯化(用1:4乙酸乙酯/石油醚洗脱)得到270c(1.87g,53%),其为白色固体。MS-ESI:[M-t-Bu]+180.0.1H NMR(500MHz,DMSO-d6)δ10.31(s,1H),8.94(s,1H),8.72(d,J=3.5Hz,1H),7.95(d,J=4.0Hz,1H),1.25(s,9H).
实施例270d 5,6,7,8-四氢-[1,2,4]三唑并[1,5-a]吡嗪-2-基氨基甲酸叔丁酯270d
将100-mL圆底烧瓶用氮气吹洗并装入270c(1.0g,4.25mmol)、20%钯/炭(10%水分,200mg)和乙醇(40mL)。然后将其排空、充入氢气(25atm)并在60℃搅拌24小时。将氢气排空并将氮气充入所述烧瓶中。通过用垫过滤除去催化剂并减压浓缩滤液得到270d(700mg,68%)。MS-ESI:[M-t-Bu]+184.0
实施例270e 7-甲基-5,6,7,8-四氢-[1,2,4]三唑并[1,5-a]吡嗪-2-基-氨基甲酸叔丁酯270e
按照实施例191i中的操作,以270d(500mg,2.1mmol,1.0当量)、低聚甲醛(630mg,21.0mmol,10.0当量)、ZnCl2/乙醚(2.1mL,2.1mmol,1.0M)、NaBH3CN(390mg,6.3mmol,3.0当量)和甲醇(20mL)开始得到270e,其为黄色固体(500mg,94%)。MS-ESI:[M-tBu]+198.0.
实施例270f 7-甲基-5,6,7,8-四氢-[1,2,4]三唑并[1,5-a]吡嗪-2-胺270f
按照实施例131e中的操作,以270e(500mg,1.97mmol)开始,用酸进行Boc脱保护得到270f,其为黄色固体(200mg,66%)。MS-ESI:[M+H]+154.1.
实施例270g乙酸(4-(1-甲基-5-(7-甲基-5,6,7,8-四氢-[1,2,4]三唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯270g
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入270f(100mg,0.65mmol,1.7当量)、乙酸(4-(5-溴-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯217a(200mg,0.38mmol,1.0当量)、DMF(10mL)和碳酸铯(499mg,1.52mmol,4.0当量)。在使氮气鼓泡通过所得溶液10分钟后,加入Xantphos(44mg,0.076mmol,0.20当量)和三(二亚苄基丙酮)二钯(0)(35mg,0.038mmol,0.10当量)。使反应混合物经历三轮真空/氩气吹洗并在100℃加热16小时。之后,将反应混合物冷却至室温并过滤。使滤液在乙酸乙酯(50mL)和水(10mL)之间分配。分离出水层并用乙酸乙酯(3×20mL)萃取。将合并的有机层减压浓缩。将残余物在硅胶柱色谱上纯化(用50:1二氯甲烷/甲醇洗脱)得到270g(90mg,41%)。MS-ESI:[M+H]+598.3.
实施例270 2-[3-(羟基甲基)-4-[1-甲基-5-[(7-甲基-6,8-二氢-5H-[1,2,4]三唑并[1,5-a]吡嗪-2-基)氨基]-6-氧代-3-吡啶基]-2-吡啶基]-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1-酮270
按照实施例241的操作,以270g(90mg,0.15mmol)开始得到270,其为白色固体(47mg,56%)。MS-ESI:[M+H]+556.3.1H NMR(500MHz,DMSO-d6)δ8.50(d,J=5.0Hz,1H),8.03(d,J=2.5Hz,1H),7.83(s,1H),7.50(d,J=2.5Hz,1H),7.33(d,J=5.5Hz,1H),6.58(s,1H),4.93(t,J=5.5Hz,1H),4.44-4.38(m,2H),4.24-4.02(m,5H),3.88-3.85(m,1H),3.61-3.59(m,重叠,5H),2.87(t,J=5.5Hz,2H),2.64-2.58(m,2H),2.49-2.46(m,2H),2.40(s,3H),1.80-1.69(m,4H).
实施例271a(S)-4-(6-(5-氯-2-甲氧基吡啶-3-基氨基)吡啶-3-基)-3-甲基哌嗪-1-羧酸叔丁酯271a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(40mL)、(S)-4-(6-氨基吡啶-3-基)-3-甲基哌嗪-1-羧酸叔丁酯101h(2.04g,7.0mmol)、3-溴-5-氯-2-甲氧基吡啶(2.8g,12.6mmol)、Pd2(dba)3(640mg,0.70mmol)、XantPhos(404.6mg,0.70mmol)和碳酸铯(4.56g,14.0mmol)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热4小时。之后,将反应混合物冷却至室温。然后将其过滤并减压蒸发滤液。将残余物通过硅胶柱色谱法来纯化(用1:3乙酸乙酯/石油醚洗脱)得到271a(1.7g,57%),其为黄色固体。MS-ESI:[M+H]+434.2
实施例271b(3S)-4-(6-{[5-(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-3-(羟基甲基)吡啶-4-基)-2-甲氧基吡啶-3-基]氨基}吡啶-3-基)-3-甲基哌嗪-1-羧酸叔丁酯271b
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入271a(650mg,1.50mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(1.79g,4.5mmol)、Pd2(dba)3(137.2mg,0.15mmol)、P(cy)3(167.4mg,0.60mmol)、Cs2CO3(978mg,3.0mmol)、二噁烷(20mL)和水(0.5mL)。在经历三轮真空/氩气吹洗后,将混合物在110℃加热16小时。之后,将反应混合物冷却至室温。加入氢氧化锂一水合物(1.89g,45mmol)和水(2.0mL)。将所得混合物在45℃搅拌4小时。然后将其过滤并减压蒸发滤液。将残余物通过硅胶柱色谱法来纯化(用3:1乙酸乙酯/石油醚洗脱)得到271b(290mg,27%),其为黄色固体。MS-ESI:[M+H]+709.3
实施例271c 10-[3-(羟基甲基)-4-[5-({5-[(2S)-2-甲基哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]吡啶-2-基]-4,4-二甲基-1,10-二氮杂三环[6.4.0.02 ,6]十二碳-2(6),7-二烯-9-酮271c
将271b(286.6mg,0.40mmol)于二噁烷/HCl(30mL)中的溶液在50℃搅拌2小时。将其减压蒸发得到271c(450mg,粗制),其为黑色固体。MS-ESI:[M+H]+595.3
实施例271 3-[3-(羟基甲基)-4-[5-[[5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]-2-吡啶基]氨基]-6-氧代-1H-吡啶-3-基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮271
向271c(450mg,0.75mmol)于甲醇(10mL)中的溶液中加入氧杂环丁烷-3-酮(162mg,2.25mmol)、NaBH3CN(141.8mg,2.25mmol)和ZnCl2(306mg,2.25mmol)。将反应混合物在室温搅拌3小时。将混合物减压蒸发并将残余物用水(5mL)稀释。然后将其用二氯甲烷(3X10mL)萃取并将合并的二氯甲烷萃取物减压浓缩。将残余物通过反相制备性-HPLC来纯化得到271(23.0mg,两步的收率为8.8%),其为黄色固体。MS-ESI:[M+H]+651.3.1HNMR(500MHz,CDCl3)δ9.76(s,1H),8.74(d,J=2.0Hz,1H),8.53(d,J=5.0Hz,1H),7.99(d,J=3.0Hz,1H),7.84(s,1H),7.73(s,1H),7.41(d,J=4.5Hz,1H),7.35(dd,J=2.5Hz,8.5Hz,1H),6.87(s,1H),6.85(d,J=9.0Hz,1H),5.16-5.13(m,1H),4.72-4.69(m,5H),4.54-4.53(m,1H),4.36-4.35(m,1H),4.19-4.17(m,2H),3.89-3.87(m,1H),3.56-3.49(m,2H),3.11-3.09(m,2H),2.60-2.48(m,重叠,7H),2.24-2.21(m,1H),1.29(s,6H),1.02(d,J=6.0Hz,3H)
实施例272a 5-溴-1-甲基-3-(5-(1-(氧杂环丁烷-3-基)氮杂环丁烷-3-基)吡啶-2-基氨基)吡啶-2(1H)-酮272a
将3-(5-(氮杂环丁烷-3-基)吡啶-2-基氨基)-5-溴-1-甲基吡啶-2(1H)-酮239b(140mg,0.42mmol)、氧杂环丁烷-3-酮(91mg,1.26mmol)、NaBH3CN(78mg,1.26mmol)和氯化锌(171mg,1.26mmol)于甲醇(10mL)中的混合物在50℃搅拌2小时。将混合物减压浓缩,并向残余物中加入水(5mL)。然后将其用二氯甲烷(3X10mL)萃取。将合并的有机层减压浓缩。将残余物通过柱色谱法来纯化(用50:1二氯甲烷/甲醇洗脱)得到272a(145mg,85%)。MS-ESI:[M+H]+390.8
实施例272b乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-[1-甲基-5-({5-[1-(氧杂环丁烷-3-基)氮杂环丁烷-3-基]吡啶-2-基}氨基)-6-氧代吡啶-3-基]吡啶-3-基)甲酯272b
在配备有回流冷凝器的25-ml圆底烧瓶中装入272a(140mg,0.35mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂-三环并[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(140mg,0.35mmol)、Pd(dppf)Cl2(28mg,0.035mmol)、乙酸钠(58mg,0.70mmol,)、K3PO4(148mg,0.70mmol)、水(6滴)和乙腈(6mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热2小时。然后将其过滤并减压蒸发滤液。将残余物通过硅胶柱色谱法来纯化(用25:1二氯甲烷/甲醇洗脱)得到272b(114mg,46%),其为棕色固体。MS-ESI:[M+H]+664.4
实施例272 3-[3-(羟基甲基)-4-[1-甲基-5-[[5-[1-(氧杂环丁烷-3-基)氮杂环丁烷-3-基]-2-吡啶基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮272
将272b(114mg,0.17mmol)和氢氧化锂(41mg,1.7mmol)于异丙醇/THF(1:1,4mL)和水(1mL)中的混合物在30℃搅拌1小时。真空蒸发混合物并将残余物用水(5mL)稀释。然后将其用乙酸乙酯(3X10mL)萃取。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到272(52mg,50%),其为白色固体。MS-ESI:[M+H]+622.3.1H NMR(500MHz,CDCl3)δ8.77(d,J=2.0Hz,1H),8.52(d,J=5.0Hz,1H),8.19(d,J=1.5Hz,1H),7.94(s,1H),7.90(d,J=2.0Hz,1H),7.61(dd,J=2.0,8.5Hz,1H),7.38(d,J=5.0Hz,1H),6.86-6.84(m,2H),5.12-5.09(m,1H),4.77-4.74(m,2H),4.69-4.66(m,1H),4.61-4.59(m,2H),4.54(bs,1H),4.36-4.32(m,1H),4.19-4.17(m,2H),3.90-3.83(m,2H),3.80-3.77(m,2H),3.74(s,3H),3.71-3.68(m,1H),3.30-3.27(m,2H),2.60-2.59(m,2H),2.54(s,2H),1.30(s,6H).
实施例273a乙酸[4-(5-溴-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-基]甲酯273a
在配备有磁力搅拌子的100-mL单颈圆底烧瓶中装入3-溴-5-碘-1-甲基吡啶-2(1H)-酮214b(1.57g,5.0mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(1.98g,5.0mmol)、PdCl2(dppf)(205mg,0.25mmol)、K3PO4(2.12g,10.0mmol)、乙酸钠(820mg,10.0mmol)、乙腈(45mL)和水(1mL)。将体系排空并用氮气回填。将反应混合物在30℃搅拌3小时。然后将其过滤并减压浓缩滤液。将所得残余物通过硅胶柱色谱法来纯化(用30:1二氯甲烷/甲醇洗脱)得到273a(580mg,22%),其为白色固体。MS-ESI:[M+H]+539.2.1H NMR(500MHz,CDCl3)δ8.49(d,J=5.0Hz,1H),7.84(d,J=2.5Hz,1H),7.45(d,J=2.0Hz,1H),7.09(d,J=5.0Hz,1H),6.79(s,1H),5.15(s,2H),4.55-4.51(m,1H),4.27-4.25(m,1H),4.15-4.13(m,1H),4.06-4.04(m,1H),3.68(s,3H),2.58-2.56(m,2H),2.51(s,2H),1.86(s,3H),1.28(s,6H).
实施例273b乙酸(2'-(7,7-二甲基-1-氧代-3,4,7,8-四氢-1H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-2(6H)-基)-1-甲基-6-氧代-5-(吡啶-2-基氨基)-1,6-二氢-[3,4'-联吡啶]-3'-基)甲酯273b
在1-打兰小瓶中加入273a(40mg,0.074mmol)、2-氨基吡啶(1.2当量)、碳酸铯(1.5当量)、Xantphos(10mol%)和三(二亚苄基丙酮)二钯(0)(5mol%)于无水1,4-二噁烷(0.2M)中。然后将反应混合物在80℃搅拌3小时。冷却至室温后,将反应混合物用二氯甲烷(3mL)稀释并用水(2X3mL)洗涤。将有机层用硫酸镁干燥,过滤并真空浓缩。然后将粗制产物273b不经纯化即用于随后的步骤。
实施例273 3-[3-(羟基甲基)-4-[1-甲基-6-氧代-5-(2-吡啶基氨基)-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮273
在1打兰小瓶中加入273b(1当量)于THF和水的4:1混合物(1mL)中。然后向所述混合物中加入氢氧化锂(1.5当量)并将反应混合物在室温搅拌16小时。然后将反应混合物用二氯甲烷(3mL)稀释并用水(2X3mL)洗涤。收集有机层,用硫酸镁干燥,过滤并真空浓缩。将粗制物通过反相色谱法来纯化得到273。1H NMR(400MHz,DMSO-d6)δ8.73(d,J=2.4Hz,1H),8.62(s,1H),8.49(d,J=5.0Hz,1H),8.17(dd,J=5.1,1.9Hz,1H),7.62–7.56(m,1H),7.54(d,J=2.5Hz,1H),7.35(d,J=5.1Hz,1H),7.30(d,J=8.5Hz,1H),6.80(dd,J=7.0,5.1Hz,1H),6.56(s,1H),4.96–4.93(m,1H),4.48–4.39(m,2H),4.24–4.17(m,2H),3.89–3.84(m,1H),3.61(s,3H),2.58(d,J=8.0Hz,2H),2.43(s,3H),1.22(s,6H).
实施例274 3-[3-(羟基甲基)-4-[1-甲基-5-[(5-甲基吡嗪-2-基)氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮274
按照实施例273的操作,用2-氨基-5-甲基吡嗪代替2-氨基吡啶,制备274。1H NMR(400MHz,DMSO-d6)δ8.98(s,1H),8.68–8.58(m,2H),8.49(d,J=5.1Hz,1H),8.04(s,1H),7.58(d,J=2.4Hz,1H),7.34(d,J=5.1Hz,1H),6.56(s,1H),5.75(s,1H),4.93(t,J=5.2Hz,1H),4.47–4.37(m,2H),4.25–4.16(m,2H),3.88–3.82(m,1H),3.62(s,3H),2.57(d,J=8.0Hz,2H),2.43(s,2H),2.34(s,3H),1.22(s,6H).
实施例275 3-[4-[5-[(5-氟-2-吡啶基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮275
按照实施例273的操作,用2-氨基-5-氟吡啶代替2-氨基吡啶,制备275。1H NMR(400MHz,DMSO-d6)δ8.79(s,1H),8.65(d,J=2.4Hz,1H),8.49(d,J=5.1Hz,1H),8.14(d,J=3.1Hz,1H),7.58(td,J=8.7,3.1Hz,1H),7.54(d,J=2.4Hz,1H),7.40(dd,J=9.2,3.9Hz,1H),7.35(d,J=5.0Hz,1H),6.56(s,1H),4.98–4.91(m,1H),4.46–4.38(m,2H),4.23–4.16(m,2H),3.88–3.82(m,1H),3.61(s,3H),2.61–2.51(m,2H),2.43(s,2H),1.22(s,6H).
实施例276 6-[[5-[2-(7,7-二甲基-4-氧代-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-3-基)-3-(羟基甲基)-4-吡啶基]-1-甲基-2-氧代-3-吡啶基]氨基]吡啶-3-甲腈276
按照实施例273的操作,用2-氨基-5-氰基吡啶代替2-氨基吡啶,制备276。1H NMR(400MHz,DMSO-d6)δ9.38(s,1H),8.73(d,J=2.2Hz,1H),8.58(d,J=2.4Hz,1H),8.49(d,J=5.0Hz,1H),7.94(dd,J=9.0,2.4Hz,1H),7.68(d,J=2.4Hz,1H),7.44(d,J=8.9Hz,1H),7.36(d,J=5.2Hz,1H),6.56(s,1H),5.75(s,1H),4.97(t,J=5.3Hz,1H),4.46–4.38(m,2H),4.21(s,3H),3.84(s,1H),3.62(s,3H),2.58(d,J=8.1Hz,2H),2.45(s,2H),1.22(s,6H).
实施例277 3-[3-(羟基甲基)-4-[5-[(5-甲氧基-2-吡啶基)氨基]-1-甲基-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮277
按照实施例273的操作,用2-氨基-5-甲氧基吡啶代替2-氨基吡啶,制备277。1HNMR(400MHz,DMSO-d6)δ8.61(d,J=2.4Hz,1H),8.51–8.47(m,2H),7.91(d,J=2.4Hz,1H),7.48(d,J=2.4Hz,1H),7.34(d,J=5.0Hz,1H),7.33–7.29(m,2H),6.56(s,1H),4.94(t,J=5.3Hz,1H),4.47–4.38(m,2H),4.24–4.16(m,2H),3.87–3.83(m,1H),3.75(s,3H),3.60(s,3H),2.58(d,J=7.9Hz,2H),2.43(s,2H),1.22(s,6H).
实施例278 3-[4-[5-[(5-环丙基-2-吡啶基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮278
按照实施例273的操作,用2-氨基-5-环丙基吡啶代替2-氨基吡啶,制备278。1HNMR(400MHz,DMSO-d6)δ8.67(d,J=2.4Hz,1H),8.53–8.45(m,2H),8.01(d,J=2.5Hz,1H),7.50(d,J=2.4Hz,1H),7.34(d,J=5.0Hz,1H),7.28(dd,J=8.6,2.5Hz,1H),7.21(d,J=8.6Hz,1H),6.56(s,1H),4.96–4.92(m,1H),4.47–4.41(m,2H),4.24–4.16(m,2H),3.89–3.85(m,1H),3.60(s,3H),2.58(d,J=7.9Hz,2H),2.44(s,2H),1.86–1.77(m,1H),1.22(s,6H),0.93(t,J=8.0Hz,1H),0.90–0.85(m,1H),0.67–0.58(m,2H).
实施例279 3-[3-(羟基甲基)-4-[1-甲基-6-氧代-5-[[5-(三氟甲基)-2-吡啶基]氨基]-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮279
按照实施例273的操作,用2-氨基-5-三氟甲基吡啶代替2-氨基吡啶,制备279。1HNMR(400MHz,DMSO-d6)δ9.23(s,1H),8.80(d,J=2.4Hz,1H),8.54–8.46(m,2H),7.88(dd,J=8.7,2.6Hz,1H),7.66(d,J=2.3Hz,1H),7.48(d,J=8.8Hz,1H),7.37(d,J=5.1Hz,1H),6.56(s,1H),4.97(t,J=5.1Hz,1H),4.50–4.40(m,2H),4.26–4.16(m,2H),3.90–3.81(m,1H),3.62(s,3H),2.58(d,J=8.2Hz,2H),2.43(s,2H),1.22(s,6H).
实施例280 3-[3-(羟基甲基)-4-[1-甲基-5-[[1-甲基-5-(吗啉-4-羰基)吡唑-3-基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮280
按照实施例273的操作,用(3-氨基-1-甲基-1H-吡唑-5-基)(吗啉代)甲酮代替2-氨基吡啶,制备280。1H NMR(400MHz,DMSO-d6)δ8.48(d,J=5.0Hz,1H),8.27(s,1H),8.05(d,J=2.4Hz,1H),7.43(d,J=2.4Hz,1H),7.33(d,J=5.1Hz,1H),6.55(s,1H),6.30(s,2H),4.99–4.91(m,1H),4.48–4.39(m,2H),4.23–4.15(m,7H),3.89–3.82(m,2H),3.72(s,3H),3.59(s,3H),3.27(s,2H),2.58(d,J=7.5Hz,2H),2.43(s,2H),1.22(s,6H).
实施例281 3-[3-(羟基甲基)-4-[1-甲基-5-[(5-甲基-2-吡啶基)氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮281
按照实施例273的操作,用2-氨基-5-甲基吡啶代替2-氨基吡啶,制备281。1H NMR(400MHz,DMSO-d6)δ8.67(d,J=2.4Hz,1H),8.48(d,J=5.4Hz,2H),8.01(d,J=2.3Hz,1H),7.51(d,J=2.4Hz,1H),7.44(dd,J=8.5,2.4Hz,1H),7.34(d,J=5.1Hz,1H),7.21(d,J=8.5Hz,1H),6.56(s,1H),5.75(s,1H),4.93(t,J=5.4Hz,1H),4.46–4.36(m,2H),4.26–4.16(m,2H),3.86–3.80(m,1H),3.60(s,3H),2.58(d,J=7.8Hz,2H),2.43(s,2H),2.17(s,3H),1.22(s,6H).
实施例282a 3,3-二甲基环戊酮282a
历时30分钟,向冷却至0℃的CuI(81.0g,420mmol)于无水乙醚(500mL)中的悬浮液中加入甲基锂的乙醚溶液(430mL,860mmol,2.0M)。将混合物在0℃搅拌2小时。在0℃,历时1小时向上述混合物中滴加3-甲基环戊烯-2-烯酮(33.6g,350mmol)。将所得混合物在0℃再搅拌2小时。然后将其用饱和NH4Cl(300mL)淬灭并过滤。并将滤液用乙醚(2X200mL)萃取。将合并的有机层用无水Mg2SO4来干燥并过滤。减压蒸发滤液得到282a,其为无色油状物(28g,71%)。1H NMR(500MHz,DMSO-d6)δ2.31(t,J=8.0Hz,2H),2.05(s,2H),1.79(t,J=8.0Hz,2H),1.12(s,6H)。
实施例282b 2-氯-4,4-二甲基环戊-1-烯甲醛282b
历时10分钟,向冷却至0℃的DMF(18.3g,250mmol)于二氯甲烷(300mL)中的溶液中加入POCl3(40.5g,250mmol)。将混合物在20℃搅拌1小时。历时20分钟向上述混合物中滴加282a(28.0g,250mmol)。将所得混合物回流加热20小时。将反应混合物冷却至室温并倒入乙酸钠(60g)于冰-水(400g)中的溶液中。将混合物用二氯甲烷(2X300mL)萃取。将合并的有机层用水(2X200mL)洗涤,用无水Mg2SO4干燥并过滤。减压蒸发滤液得到282b,其为无色油状物(33.0g,粗制)。1H NMR(500MHz,DMSO-d6)δ9.99(s,1H),2.62(d,J=2.0Hz,2H),2.38(d,J=2.0Hz,2H),1.15(s,6H).
实施例282c 5,5-二甲基-5,6-二氢-4H-环戊二烯并[b]噻吩-2-羧酸乙酯282c
向282b(33.0g,粗制)于二氯甲烷(400mL)和三乙胺(60g,600mmol)中的溶液中加入2-巯基乙酸乙酯(19.2g,160mmol)。将反应混合物回流加热6小时。然后将其减压浓缩。将残余物溶解在乙醇(400mL)和三乙胺(60g,600mmol)中。将混合物回流加热12小时。将其再次减压浓缩并将残余物通过硅胶柱色谱法来纯化(用40:1石油醚/乙酸乙酯洗脱)得到282c,其为黄色固体(18.0g,两步的收率为32%)。MS-ESI:[M+H]+225.3。1H NMR(500MHz,DMSO-d6)δ7.49(s,1H),4.32(q,J=7.0Hz,2H),2.72(s,2H),2.56(s,2H),1.35(t,J=7.0Hz,3H),1.22(s,6H)。
实施例282d 5,5-二甲基-5,6-二氢-4H-环戊二烯并[b]噻吩-2-羧酸282d
向282c(16.0g,71.0mmol)于丙烷-2-醇(200mL)、四氢呋喃(200mL)和水(200mL)中的溶液中加入氢氧化锂(6.82g,284mmol)。将反应混合物在65℃加热5小时。减压除去有机溶剂。用盐酸(12M)将残余物的pH调整至1.0。过滤收集析出物并真空干燥得到282d(12.0g,86%),其为白色固体。MS-ESI:[M+H]+196.9
实施例282e N-叔丁基-5,5-二甲基-5,6-二氢-4H-环戊二烯并[b]噻吩-2-甲酰胺282e
将282d(12.0g,61.0mmol)于SOCl2(80mL)中的悬浮液在65℃加热2小时。减压浓缩反应混合物。将残余物用二氯甲烷(20mL)稀释,将其添加至2-甲基丙烷-2-胺(4.45g,61.0mmol)和三乙胺(18.0g,180mmol)于二氯甲烷(180mL)中的溶液中。将所得混合物搅拌16小时并用二氯甲烷(200mL)稀释。将其用水(3X50mL)洗涤,用无水Mg2SO4干燥,过滤并减压蒸发得到282e(15.0g,97%),其为黄色固体。MS-ESI:[M+H]+252.0
实施例282f N-叔丁基-3-甲酰基-5,5-二甲基-5,6-二氢-4H-环戊二烯并[b]噻吩-2-甲酰胺282f
历时5分钟,向在-70℃冷却的282e(1.5g,6.0mmol)于无水THF(60mL)中的溶液中加入正丁基锂的溶液(10.0mL,25mmol,2.5M于己烷中)。将其在-70℃搅拌6小时。历时5分钟加入DMF(1.3g,18.0mmol)并将所得混合物在室温搅拌整夜。然后将其用饱和NH4Cl(40mL)淬灭并减压浓缩。将残余物用乙酸乙酯(2X30mL)萃取。将合并的有机层用无水Mg2SO4来干燥并过滤。减压蒸发滤液得到282f,其为黄色固体(1.34g,80%)。MS-ESI:[M+H]+280.3
实施例282g N-叔丁基-3-(肼叉甲基)-5,5-二甲基-5,6-二氢-4H-环戊二烯并[b]噻吩-2-甲酰胺282g
历时5分钟,向85%肼水溶液(10mL)于THF(180mL)中的溶液中加入282f(5.6g,20.0mmol)/无水THF(20mL)。将其在20℃搅拌3小时。减压浓缩反应混合物得到282g,其为黑色固体(6.0g,收率:95%,纯度:95%)。MS-ESI:[M+H]+294.0
实施例282h 4,4-二甲基-7-硫杂-10,11-二氮杂三环[6.4.0.02,6]十二碳-1(8),2(6),11-三烯-9-酮282h
将282g(3.8g,13.0mmol)于30%H2SO4(100mL)中的溶液回流加热16小时。将反应混合物冷却至室温并用二氯甲烷(3X200mL)萃取。将合并的有机层减压浓缩并将残余物通过硅胶柱色谱法(用100:1二氯甲烷/甲醇洗脱)来纯化得到282h,其为黄色固体(1.72g,60%)。MS-ESI:[M+H]+221.0
实施例282i 4-氯-2-{4,4-二甲基-9-氧代-7-硫杂-10,11-二氮杂三环[6.4.0.02 ,6]十二碳-1(8),2(6),11-三烯-10-基}吡啶-3-甲醛282i
按照如实施例108a中所述的操作,以282h(330mg,1.5mmol)和2-溴-4-氯吡啶-3-甲醛(950mg,4.5mmol)开始得到282i,其为黄色固体(260mg,48%)。MS-ESI:[M+H]+359.9
实施例282j 2-{4,4-二甲基-9-氧代-7-硫杂-10,11-二氮杂三环[6.4.0.02,6]十二碳-1(8),2(6),11-三烯-10-基}-4-[1-甲基-5-({5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]吡啶-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]吡啶-3-甲醛282j
按照实施例191k的制备操作,以282i(216mg,0.60mmol)和(S)-1-甲基-3-(5-(2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基)吡啶-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮191j(482mg,0.90mmol)开始获得282jd,其为黄色固体(407mg,48%)。MS-ESI:[M+H]+678.8
实施例282 3-[3-(羟基甲基)-4-[1-甲基-5-[[5-[(2S)-2-甲基-4-(氧杂环丁烷-3-基)哌嗪-1-基]-2-吡啶基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-6,8-二氢环戊二烯并[3,4]噻吩并[1,3-d]哒嗪-4-酮282
按照实施例191中的操作,以282j(370mg,0.55mmol)开始获得282,其为黄色固体(64mg,17%)。MS-ESI:[M+H]+681.3.1H NMR(500MHz,DMSO-d6)δ8.63(d,J=2.0Hz,1H),8.56(d,J=5.0Hz,1H),8.46-8.45(m,2H),7.85(d,J=3.0Hz,1H),7.53(d,J=5.0Hz,1H),7.47(d,J=2.5Hz,1H),7.36(dd,J=3.0,9.0Hz,1H),7.24(d,J=9.0Hz,1H),4.85(t,J=5.0Hz,1H),4.57-4.54(m,2H),4.47(t,J=6.0Hz,1H),4.4-4.37(m,3H),3.68-3.67(m,1H),3.60(s,3H),3.40-3.38(m,1H),3.11-3.08(m,1H),2.96-2.90(m,3H),2.81-2.79(m,2H),2.56-2.53(m,1H),2.33-2.32(m,2H),2.19-2.16(m,1H),1.28(s,3H),1.27(s,3H),0.93(d,J=6.0Hz,3H).
实施例283a 5-溴-1-甲基-3-(5-甲基异噁唑-3-基氨基)吡啶-2(1H)-酮283a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入5-甲基异噁唑-3-胺(1.0g,10.2mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(4.09g,15.3mmol)、Pd2(dba)3(467mg,0.51mmol)、Xantphos(598mg,1.02mmol)、Cs2CO3(6.65g,20.4mmol)和二噁烷(50mL)。在经历三轮真空/氩气吹洗后,将反应混合物在100℃加热3小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将混合物趁热过滤。将滤液冷却降至室温并过滤收集所得析出物得到283a(1.6g,55%),其为黄色固体。MS-ESI:[M+H]+284.1
实施例283b乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{1-甲基-5-[(5-甲基-1,2-噁唑-3-基)氨基]-6-氧代-1,6-二氢吡啶-3-基}吡啶-3-基)甲酯283b
在配备有磁力搅拌子和回流冷凝器的50-mL圆底烧瓶中装入283a(150mg,0.53mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(834mg,2.1mmol)、Pd(dppf)Cl2(21mg,0.026mmol)、K3PO4(224mg,0.053mmol)、乙酸钠(87mg,1.1mmol)、乙腈(10mL)和水(5滴)。在经历三轮真空/氮气吹洗后,将混合物在100℃加热1小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物用乙腈洗涤得到283b(100mg,34%),其为白色固体。MS-ESI:[M+H]+557.3
实施例283 3-[3-(羟基甲基)-4-[1-甲基-5-[(5-甲基异噁唑-3-基)氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮283
向283b(90mg,0.162mmol)于THF(5mL)、异丙醇(5mL)和水(5mL)中的溶液中加入氢氧化锂(3.8mg,1.62mmol)。将反应混合物在室温搅拌1小时并减压浓缩。将残余物用二氯甲烷(20mL×3)萃取。将合并的有机层用盐水洗涤,用Na2SO4干燥,过滤并减压浓缩。将残余物通过反相制备性-HPLC来纯化得到283(65mg,78%),其为白色固体。MS-ESI:[M+H]+514.9.1HNMR(500MHz,DMSO-d6)δ8.98(s,1H),8.49(d,J=5.0Hz,1H),8.02(d,J=2.0Hz,1H),7.56(d,J=2.5Hz,1H),7.32(d,J=5.0Hz,1H),6.57(s,1H),6.25(s,1H),4.93(t,J=5.0Hz,1H),4.48-4.38(m,2H),4.25-4.19(m,3H),3.87-3.85(m,1H),3.60(s,3H),2.62-2.54(m,2H),2.43(s,2H),2.31(s,3H),1.22(s,6H).
实施例284a 2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)-4-(1-甲基-5-(5-(氧杂环丁烷-3-基)-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-甲醛284a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1-甲基-3-(5-(氧杂环丁烷-3-基)-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮163a(354mg,0.83mmol)、4-氯-2-(10-氟-1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-甲醛134c(289mg,0.83mmol)、PdCl2(dppf)(68mg,0.08mmol)、K3PO4(352mg,1.66mmol)、乙酸钠(136mg,1.66mmol)、乙腈(50mL)和水(3mL)。将体系排空并用氮气回填。将反应混合物在100℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用30:1二氯甲烷/甲醇洗脱)得到284a(305mg,60%),其为棕色固体。MS-ESI:[M+H]+:613.6.
实施例284 10-氟-2-[3-(羟基甲基)-4-[1-甲基-5-[[5-(氧杂环丁烷-3-基)-6,7-二氢-4H-吡唑并[1,5-a]吡嗪-2-基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-1-酮284
在0℃,向284a(250mg,0.41mmol)于甲醇(20mL)中的悬浮液中加入硼氢化钠(47mg,1.23mmol)。将混合物搅拌30分钟。然后将其用水(2mL)淬灭并减压浓缩。将残余物通过反相制备性-HPLC来纯化得到284(20mg,6.6%)。MS-ESI:[M+H]+615.6.1H NMR(500MHz,CDCl3)δ8.46(d,J=5.0Hz,1H),7.94(d,J=3.0Hz,1H),7.66(d,J=2.0Hz,1H),7.43(s,1H),7.34(d,J=5.0Hz,1H),5.75(s,1H),4.95(t,J=6.5Hz,1H),4.76-4.74(m,2H),4.69-4.65-4.67(m,3H),4.46-4.44(m,1H),4.35-4.33(m,1H),4.10-4.08(m,4H),3.38-3.35(m,2H),3.69(s,3H),3.58-3.56(m,2H),2.842.82(m,2H),2.58-2.53(m,4H),1.89-1.84(m,2H),1.77-1.76(m,2H).
实施例285a 4-硝基-1-(氧杂环丁烷-3-基)-1H-咪唑285a
在密封管中装入4-硝基-1H-咪唑(500mg,4.42mmol)、3-碘氧杂环丁烷(920mg,5.0mmol)、Cs2CO3(2.90g,8.84mmol)和二噁烷(12mL)。将密封管在120℃加热16小时。然后将其冷却至室温并过滤。减压蒸发滤液。将残余物通过硅胶柱色谱法来纯化(用30:1二氯甲烷/甲醇洗脱)得到285a,其为白色固体(250mg,33%)。MS-ESI:[M+H]+170.2.
实施例285b 1-(氧杂环丁烷-3-基)-1H-咪唑-4-胺285b
将25-mL单颈圆底烧瓶用氮气吹洗并装入285a(100mg,0.6mmol)、10%钯/炭(10%水分,10mg)和甲醇(10mL)。将所述烧瓶排空,充入氢气(通过囊)并在室温搅拌1小时。然后将氢气排空并向所述烧瓶中充入氮气。通过用垫过滤除去催化剂,减压浓缩滤液得到285b(70mg,85%)。MS-ESI:[M+H]+140.3。
实施例285c乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-(1-甲基-5-{[1-(氧杂环丁烷-3-基)-1H-咪唑-4-基]氨基}-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-基)甲酯285c
在配备有磁力搅拌子和回流冷凝器的25-mL圆底烧瓶中装入285b(40mg,0.28mmol)、乙酸[4-(5-溴-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-基]甲酯273a(150mg,0.28mmol)、Pd2(dba)3(15mg,0.015mmol)、XantPhos(18mg,0.03mmol)、碳酸铯(200mg,0.6mmol)和1,4-二噁烷(6mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用25:1二氯甲烷/甲醇洗脱)得到285c,其为黄色固体(80mg,47%)。MS-ESI:[M+H]+598.3.
实施例285 3-[3-(羟基甲基)-4-[1-甲基-5-[[1-(氧杂环丁烷-3-基)咪唑-4-基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮285
将285c(80mg,0.13mmol)和氢氧化锂·水(55mg,1.3mmol)于异丙醇/THF(3:2,5mL)和水(2mL)中的混合物在30℃搅拌1小时。将混合物减压蒸发并向残余物中加入水(5mL)。然后将其用二氯甲烷(3X10mL)萃取。将合并的二氯甲烷萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到285(36mg,50%),其为白色固体。MS-ESI:[M+H]+556.3.1HNMR(500MHz,CDCl3)δ8.48(d,J=5.0Hz,1H),7.53(d,J=2.0Hz,1H),7.47-7.45(m,2H),7.35-7.34(m,2H),7.28(s,1H),6.88(s,1H),5.27-5.19(m,2H),5.10-5.07(m,2H),4.94-4.91(m,2H),4.69-4.65(m,1H),4.52-4.44(m,2H),4.17-4.16(m,2H),3.87-3.84(m,1H),3.72(s,3H),2.59-2.58(m,2H),2.53(s,2H),1.29(s,6H).
实施例286a乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{1-甲基-5-[(1,2-噁唑-3-基)氨基]-6-氧代-1,6-二氢吡啶-3-基}吡啶-3-基)甲酯286a
在配备有回流冷凝器的25-mL圆底烧瓶中装入乙酸[4-(5-溴-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-基]甲酯273a(161g,0.30mmol)、异噁唑-3-胺(25mg,0.30mmol)、碳酸铯(196mg,0.60mmol)和1,4-二噁烷(10mL)。在使氮气鼓泡通过所述悬浮液10分钟后,加入三(二亚苄基丙酮)二钯(0)(14.0mg,0.015mmol)和xantphos(17mg,0.030mmol)。使体系经历三轮真空/氩气吹洗并回流加热5小时。然后将其冷却至室温并过滤。将固体用二氯甲烷(2X10mL)洗涤。将合并的有机滤液减压浓缩。将残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(80/1至30/1)洗脱)得到286a(96mg,59%),其为黄色固体。MS-ESI:[M+H]+542.8.
实施例286 3-[3-(羟基甲基)-4-[5-(异噁唑-3-基氨基)-1-甲基-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮286
向286a(96mg,0.18mmol)于THF/异丙醇/水(5/3/2mL)中的溶液中加入氢氧化锂(21mg,0.88mmol)。将混合物在室温搅拌1小时。反应完成后,减压蒸发混合物并将残余物通过反相制备性-HPLC来纯化得到286,其为白色固体(75mg,85%)。MS-ESI:[M+H]+501.3.1HNMR(500MHz,CDCl3)δ8.49(d,J=6.5Hz,1H),8.19(d,J=2.5Hz,1H),8.10(d,J=2.5Hz,1H),8.97(d,J=3.0Hz,1H),7.71(s,1H),7.37(d,J=6.5Hz,1H),6.85(s,1H),6.18(d,J=2.5Hz,1H),5.12-5.11(m,1H),4.66-4.64(m,1H),4.52-4.51(m,1H),4.29-4.27(m,1H),4.18-4.16(m,2H),3.87-3.86(m,1H),3.73(s,3H),2.59-2.57(m,2H),2.53-2.51(m,2H),1.28(s,6H).
实施例287a N-甲氧基-N-甲基-3-硝基-1H-吡唑-5-甲酰胺287a
在配备有磁力搅拌子的500-mL单颈圆底烧瓶中装入3-硝基-1H-吡唑-5-羧酸(15.7g,1.0当量,100mmol)、N,O-二甲基羟基胺盐酸盐(19.5g,2.0当量,200mmol)、HATU(76.0g,2.0当量,200mmol)、三乙胺(40.4g,4.0当量,400mmol)和二氯甲烷(300mL)。将反应混合物在室温搅拌整夜。减压除去溶剂。将所得残余物通过硅胶柱色谱法来纯化(用100:1二氯甲烷/甲醇洗脱)得到287a(16.0g,80%),其为白色固体。MS-ESI:[M+H]+201.1
实施例287b 3-氨基-N-甲氧基-N-甲基-1H-吡唑-5-甲酰胺287b
将250-mL单颈圆底烧瓶用氮气吹洗并装入287a(16.0g,1.0当量,80.0mmol)、10%钯/炭(50%水分,800mg)和甲醇(100mL)。将混合物排空、充入氢气并在氢气中在室温搅拌整夜。然后将氢气排空并将氮气充入所述烧瓶中。通过用垫过滤除去催化剂。减压浓缩滤液得到287b(11.0g,81%),其为白色固体。MS-ESI:[M+H]+171.1
实施例287c 3-(2,5-二甲基-1H-吡咯-1-基)-N-甲氧基-N-甲基-1H-吡唑-5-甲酰胺287c
在配备有磁力搅拌子和Dean-Stark阱的250-mL圆底烧瓶中装入287b(11.0g,1.0当量,64.7mmol)、己烷-2,5-二酮(11.1g,1.5当量,97.2mmol)、对甲苯磺酸一水合物(558mg,0.05当量,3.24mmol)和甲苯(100mL)。将反应混合物回流整夜。将所得混合物冷却至室温并减压浓缩。将所得残余物通过硅胶柱色谱法来纯化(用1:2石油醚/乙酸乙酯洗脱)得到287c(10.4g,65%),其为白色固体。MS-ESI:[M+H]+249.0
实施例287d 2-(3-(2,5-二甲基-1H-吡咯-1-基)-5-(甲氧基(甲基)氨基甲酰基)-1H-吡唑-1-基)乙基氨基甲酸叔丁酯287d
在配备有磁力搅拌子的250-mL圆底烧瓶中装入287c(10.4g,1.0当量,41.9mmol)、2-氯乙基氨基甲酸叔丁酯(37.7g,5.0当量,210.0mmol)、Na2CO3(22.3g,5.0当量,210.0mmol)和DMF(100mL)。将反应混合物在110℃搅拌整夜。冷却至室温后,将所得混合物倒入水(200mL)中并用乙酸乙酯(3X100mL)萃取。将合并的有机层减压浓缩。将所得残余物通过硅胶柱色谱法来纯化(用乙酸乙酯洗脱)得到287d(10.8g,66%),其为黄色油状物。MS-ESI:[M+H]+392.0
实施例287e 2-(5-乙酰基-3-(2,5-二甲基-1H-吡咯-1-基)-1H-吡唑-1-基)乙基氨基甲酸叔丁酯287e
氮气保护下,在配备有磁力搅拌子的250-mL圆底烧瓶中装入287d(7.82g,1.0当量,20.0mmol)和THF(100mL)。在-78℃,加入MeMgBr溶液(3.0M于乙醚中)(17mL,2.5当量,50.0mmol)。将混合物在室温搅拌3小时并用饱和NH4Cl溶液淬灭。然后将其减压浓缩并将残余物用乙酸乙酯(3X50mL)萃取。将合并的有机层减压蒸发。将残余物通过硅胶柱色谱法来纯化(用4:1石油醚/乙酸乙酯洗脱)得到287e,其为无色油状物(5.40g,78%)。MS-ESI:[M+H]+347.0.1H NMR(500MHz,CDCl3)δ6.57(s,1H),5.91(s,2H),4.93(bs,1H),4.71(t,J=5.5Hz,2H),3.62(t,J=5.5Hz,2H),2.57(s,3H),2.16(s,6H),1.28(s,9H).
实施例287f 2-(2,5-二甲基-1H-吡咯-1-基)-4-甲基-6,7-二氢吡唑并[1,5-a]吡嗪287f
在配备有磁力搅拌子的100-mL单颈圆底烧瓶中装入287e(5.40g,1.0当量,15.6mmol)、CF3COOH(10mL)和二氯甲烷(50mL)。将混合物在室温搅拌1小时并减压浓缩得到粗制287f,将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+229.1
实施例287g 2-(2,5-二甲基-1H-吡咯-1-基)-4-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪287g
在配备有磁力搅拌子的100-mL单颈圆底烧瓶中装入287f(3.56g,1.0当量,15.6mmol)、NaBH4(2.96g,5.0当量,78.0mmol)和甲醇(50mL)。将混合物在室温搅拌1小时并减压浓缩。使残余物在水(50mL)和二氯甲烷(50mL)之间分配。将水相用二氯甲烷(3X50mL)萃取。将合并的有机层减压浓缩。将残余物通过硅胶柱色谱法来纯化(用10:1二氯甲烷/甲醇洗脱)得到287g,其为无色油状物(1.54g,两步的收率为43%)。MS-ESI:[M+H]+231.3.1HNMR(500MHz,CDCl3)δ5.91(s,1H),5.86(s,2H),4.17-4.11(m,3H),3.51-3.48(m,1H),3.36-3.31(m,1H),2.13(s,6H),1.50(d,J=6.5Hz,3H).
实施例287h 2-(2,5-二甲基-1H-吡咯-1-基)-4,5-二甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪287h
在配备有磁力搅拌子的100-mL单颈圆底烧瓶中装入287g(1.54g,1.0当量,6.70mmol)、甲醛(37%于水中)(1.09g,2.0当量,13.4mmol)、NaBH3CN(2.11g,5.0当量,33.5mmol)、HOAc(3mL)和甲醇(30mL)。将混合物在室温搅拌1小时并减压浓缩。使残余物在水(50mL)和二氯甲烷(50mL)之间分配。将水相用二氯甲烷(3X50mL)萃取。将合并的有机层减压浓缩得到粗制287h,将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+245.0
实施例287i 4,5-二甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-胺287i
在配备有回流冷凝器的100-mL单颈圆底烧瓶中装入287h(1.63g,1.0当量,6.70mmol)、NH2OH·HCl(2.33g,5.0当量,33.5mmol)和乙醇(50mL)。将混合物回流2天。然后将其冷却至室温并减压浓缩。将残余物通过反相制备性-HPLC来纯化得到287i,其为黄色固体(211mg,19%)。MS-ESI:[M+H]+167.1.1H NMR(500MHz,CDCl3)δ5.36(s,1H),4.04-4.00(m,1H),3.94-3.92(m,1H),3.61(bs,2H),3.30(q,J=6.5Hz,1H),3.10-3.08(m,1H),2.81-2.75(m,1H),2.43(s,3H),1.38(d,J=6.5Hz,3H).
实施例287j乙酸(4-(5-(4,5-二甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯287j
在配备有磁力搅拌子和回流冷凝器的25-mL圆底烧瓶中装入287i(20mg,1.0当量,0.12mmol)、乙酸(4-(5-溴-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯273a(127mg,2.0当量,0.24mmol)、Pd2(dba)3(9.0mg,0.1当量,0.010mmol)、Xantphos(11mg,0.2当量,0.020mmol)、Cs2CO3(78mg,2.0当量,0.24mmol)和二噁烷(5mL)。在经历三轮真空/氮气吹洗后,将混合物在100℃搅拌2小时。然后将其冷却至室温并过滤。减压浓缩滤液。将所得残余物通过硅胶柱色谱法来纯化(用20:1二氯甲烷/甲醇洗脱)得到287j,其为棕色固体(60mg,82%)。MS-ESI:[M+H]+610.9
实施例287 2-[4-[5-[(4,5-二甲基-6,7-二氢-4H-吡唑并[1,5-a]吡嗪-2-基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1-酮287
在配备有磁力搅拌子的25-mL单颈圆底烧瓶中装入287j(60mg,1.0当量,0.098mmol)、氢氧化锂(12mg,5.0当量,0.49mmol)、异丙醇/THF(4/4mL)和水(1mL)。将混合物在室温搅拌1小时并减压浓缩。将残余物通过反相制备性-HPLC来纯化得到287,其为黄色固体(24mg,43%)。MS-ESI:[M+H]+568.9.1H NMR(500MHz,CDCl3)δ8.49(d,J=5.0Hz,1H),7.99(s,1H),7.72(d,J=2.0Hz,1H),7.44(s,1H),7.36(d,J=5.0Hz,1H),6.91(s,1H),5.74(s,1H),5.04-5.02(m,1H),4.64-4.62(m,1H),4.56-4.54(m,1H),4.39-4.37(m,1H),4.17-3.92(m,4H),3.86-3.84(m,1H),3.72(s,3H),3.45-3.37(m,1H),3.17-3.14(m,1H),2.89-2.81(m,1H),2.64-2.58(m,4H),2.48(s,3H),1.93-1.89(m,2H),1.81-1.80(m,2H),1.46(d,J=6.5Hz,3H).
实施例288a 1-甲基-3-(5-甲基异噁唑-3-基氨基)-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮288a
在配备有磁力搅拌子和回流冷凝器的50-mL圆底烧瓶中装入5-溴-1-甲基-3-(5-甲基异噁唑-3-基氨基)吡啶-2(1H)-酮283a(330mg,1.16mmol)、Pin2B2(442mg,1.74mmol)、Pd2(dba)3(53mg,0.058mmol)、X-Phos(55mg,0.116mmol)、乙酸钾(227mg,2.32mmol)和二噁烷(20mL)。在经历三轮真空/氮气吹洗后,将混合物在70℃加热2小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将其冷却至室温并过滤。减压浓缩滤液并将残余物用石油醚洗涤得到288a(300mg,78%),其为黄色固体。MS-ESI:[M+H]+332.3
实施例288b 2-{4,4-二甲基-9-氧代-7-硫杂-10,11-二氮杂三环[6.4.0.02,6]十二碳-1(8),2(6),11-三烯-10-基}-4-{1-甲基-5-[(5-甲基-1,2-噁唑-3-基)氨基]-6-氧代-1,6-二氢-吡啶-3-基}吡啶-3-甲醛288b
在配备有磁力搅拌子的50-mL圆底烧瓶中装入4-氯-2-{4,4-二甲基-9-氧代-7-硫杂-10,11-二氮杂三环[6.4.0.02,6]十二碳-1(8),2(6),11-三烯-10-基}吡啶-3-甲醛282i(72mg,0.20mmol)、288a(102mg,0.30mmol)、PdCl2(dppf)(16mg,0.020mmol)、K3PO4(85mg,0.40mmol)、乙酸钠(33mg,0.40mmol)、乙腈(10mL)和水(0.5mL)。在使氮气鼓泡到所述混合物10分钟后,将回流冷凝器连于所述烧瓶并将混合物在100℃加热1小时。然后将其冷却至室温并过滤。减压浓缩滤液得到288b,将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+529.3.
实施例288 3-[3-(羟基甲基)-4-[1-甲基-5-[(5-甲基异噁唑-3-基)氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-6,8-二氢环戊二烯并[3,4]噻吩并[1,3-d]哒嗪-4-酮288
将288a(82mg,0.16mmol)和NaBH4(18.1mg,0.48mmol)于甲醇(10mL)中的混合物在室温搅拌30分钟。将混合物用水(5mL)淬灭并减压蒸发。将残余物用二氯甲烷(3X10mL)萃取。将合并的萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到288(54mg,两步:34%),其为白色固体。MS-ESI:[M+H]+531.3.1H NMR(500MHz,DMSO-d6)δ9.0(s,1H),8.57(d,J=5.0Hz,1H),8.46(s,1H),8.00(d,J=1.5Hz,1H),7.57(d,J=2.0Hz,1H),7.51(d,J=5.0Hz,1H),6.25(s,1H),4.86(bs,1H),4.39(d,J=8.5Hz,2H),3.60(s,3H),2.91(s,2H),2.81(s,2H),2.31(s,3H),1.28(s,6H).
实施例289a 3-氨基-1H-吡唑-1-羧酸叔丁酯289a
向3-环丙基-1H-吡唑-5-胺(3.0g,36mmol)和三乙胺(7.6g,75mmol)于1,4-二噁烷(35mL)中的混合物中加入(Boc)2O(7.8g,36mmol)。将反应混合物在25℃搅拌2小时。然后将其减压浓缩。将残余物通过硅胶柱来纯化(用3:1石油醚/乙酸乙酯洗脱)得到289a,其为白色固体(3.4g,52%)。MS-ESI:[M+H]+184.1。
实施例289b 3-(1H-吡唑-3-基氨基)-5-溴-1-甲基吡啶-2(1H)-酮289b
在配备有磁力搅拌子和回流冷凝器的250-mL单颈圆底烧瓶中装入289a(2.2g,12mmol)、XantPhos(0.69g,1.2mmol)、Pd2(dba)3(1.1g,1.2mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(6.4g,24mmol)、Cs2CO3(15.6g,48mmol)和1,4-二噁烷(50mL)。使氮气鼓泡通过所得混合物10分钟后,将其在105℃加热15小时。将混合物冷却至室温并过滤。减压浓缩滤液,并将残余混合物用甲醇(8mL)洗涤得到289b,其为浅黄色固体(1.2g,37%).MS-ESI:[M+H]+269.1.
实施例289c乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{1-甲基-6-氧代-5-[(1H-吡唑-3-基)氨基]-1,6-二氢吡啶-3-基}吡啶-3-基)甲酯289c
在配备有磁力搅拌子和回流冷凝器的50-mL圆底烧瓶中装入289b(200mg,0.74mmol)、(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(360mg,0.90mmol)、PdCl2(dppf)(41mg,0.050mmol)、K3PO4(320mg,1.5mmol)、乙酸钠(123mg,1.5mmol)、乙腈(10mL)和水(0.2mL)。将体系排空然后用氮气回填。然后将其在90℃加热4小时。将混合物冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用10:1二氯甲烷/甲醇洗脱)得到289c,其为浅黄色固体(150mg,38%)。MS-ESI:[M+H]+542.3.
实施例289 3-[3-(羟基甲基)-4-[1-甲基-6-氧代-5-(1H-吡唑-3-基氨基)-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮289
将289c(150mg,0.28mmol)和氢氧化锂水合物(236mg,5.6mmol)于THF(4mL)、异丙醇(4mL)和水(2mL)中的混合物在40℃搅拌0.5小时。将混合物减压蒸发并用水(10mL)稀释。然后将其用乙酸乙酯(3X15mL)萃取。将合并的萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到289,其为浅黄色固体(25mg,18%)。MS-ESI:[M+H]+499.9.1H NMR(500MHz,DMSO-d6)δ12.07(s,1H),8.47(d,J=5.0Hz,1H),8.17(s,1H),8.08(s,1H),7.55-7.54(m,1H),7.40-7.39(m,1H),7.32(d,J=5.0Hz,1H),6.55(s,1H),6.12(s,1H),4.94-4.92(m,1H),4.48-4.47(m,1H),4.41-4.39(m,1H),4.23-4.17(m,3H),3.84-3.82(m,1H),3.59(s,3H),2.58-2.56(m,2H),2.50-2.42(m,2H),1.22(s,6H).
实施例290a 5-溴-1-甲基-3-(1-甲基-1H-吡唑-3-基氨基)吡啶-2(1H)-酮290a
在配备有磁力搅拌子和回流冷凝器的250-mL单颈圆底烧瓶中装入1,4-二噁烷(100mL)、1-甲基-1H-吡唑-3-胺(970mg,10.0mmol)、3,5-二溴-1-甲基吡啶-2-(1H)-酮(2.9g,11mmol)和碳酸铯(6.5g,20.0mmol)。在使氮气鼓泡通过所述悬浮液10分钟后,加入三(二亚苄基丙酮)二钯(0)(457mg,0.50mmol)和Xantphos(587mg,1.0mmol)。使体系经历三轮真空/氩气吹洗并回流加热2小时。然后将其冷却至室温并过滤。将固体用二氯甲烷(2X50mL)洗涤并浓缩合并的有机滤液。将残余物通过硅胶柱色谱法来纯化(用30:1二氯甲烷/甲醇洗脱)得到290a,其为黄色固体(900mg,32%)。MS-ESI:[M+H]+283.1
实施例290b乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{1-甲基-5-[(1-甲基-1H-吡唑-3-基)氨基]-6-氧代-1,6-二氢吡啶-3-基}吡啶-3-基)甲酯290b
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(595mg,1.5mmol)、290a(282mg,1.0mmol)、K3PO4(424mg,2.0mmol)、乙酸钠(164mg,2.0mmol)、1,1’-二(二苯基膦基)二茂铁二氯化钯(II)(82mg,0.1mmol)和乙腈/水(15/1mL)。在经历三轮真空/氮气吹洗后,将混合物在100℃加热1.5小时。将混合物冷却至室温并减压浓缩。使残余物在二氯甲烷(30mL)和水(30mL)之间分配。将水层用二氯甲烷(3X20mL)萃取。将合并的有机层用Na2SO4干燥,过滤并减压浓缩。将黑色残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(80/1至50/1)洗脱)得到290b(300mg,54%),其为黄色固体。MS-ESI:[M+H]+556.1
实施例290 3-[3-(羟基甲基)-4-[1-甲基-5-[(1-甲基吡唑-3-基)氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮290
向290b(139mg,0.25mmol)于THF(5mL)、丙烷-2-醇(5mL)和水(2mL)中的溶液中加入氢氧化锂(60mg,2.5mmol)。将反应混合物在室温搅拌2.5小时。然后将其减压浓缩。使残余物在二氯甲烷(20mL)和水(10mL)之间分配。将水层用二氯甲烷(3X10mL)萃取。将合并的萃取物用盐水洗涤,用Na2SO4干燥,过滤并减压浓缩。将残余物通过反相制备性-HPLC来纯化得到290(30mg,23%),其为白色固体。MS-ESI:[M+H]+514.3.1H NMR(500MHz,DMSO-d6)δ8.47(d,J=5.0Hz,1H),8.16(s,1H),8.03(d,J=2.5Hz,1H),7.48(d,J=2.0Hz,1H),7.39(d,J=1.5Hz,1H),7.33(d,J=5.0Hz,1H),6.55(s,1H),6.07(d,J=2.0Hz,1H),4.97(t,J=5.0Hz,1H),4.47-4.40(m,2H),4.24-4.18(m,3H),3.85-3.83(m,1H),3.70(s,3H),3.58(s,3H),2.58-2.56(m,2H),2.42(s,2H),1.22(s,6H).
实施例291a乙酸(4-{1-甲基-5-[(5-甲基-1,2-噁唑-3-基)氨基]-6-氧代-1,6-二氢吡啶-3-基}-2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}吡啶-3-基)甲酯291a
在配备有回流冷凝器的50-mL圆底烧瓶中装入乙酸(2-{6-氧代-8-硫杂-4,5-二氮杂三环[7.4.0.02,7]十三碳-1(9),2(7),3-三烯-5-基}-4-(四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-3-基)甲酯230i(150mg,0.31mmol)、5-溴-1-甲基-3-(5-甲基异噁唑-3-基氨基)吡啶-2(1H)-酮283a(88mg,0.31mmol)、PdCl2(dppf)(24mg,0.031mmol)、K3PO4(131mg,0.62mmol)、乙酸钠(61mg,0.62mmol)、水(0.2mL)和乙腈(10mL)。使体系经历三轮真空/氩气吹洗并在100℃搅拌3小时。将反应混合物冷却至室温并过滤。减压浓缩滤液。使残余物在二氯甲烷(20mL)和水(10mL)之间分配。分离有机层并将水层用二氯甲烷(2×20mL)萃取。将合并的有机层用Na2SO4干燥,过滤并减压浓缩。将黑色残余物通过硅胶柱色谱法来纯化(用30:1二氯甲烷/甲醇洗脱)得到291a(104mg,60%),其为黄色固体。MS-ESI:[M+H]+559.1
实施例291 3-[3-(羟基甲基)-4-[1-甲基-5-[(5-甲基异噁唑-3-基)氨基]-6-氧代-3-吡啶基]-2-吡啶基]-6,7,8,9-四氢苯并噻吩并[2,3-d]哒嗪-4-酮291
在室温,向291a(100mg,0.18mmol)于THF/异丙醇/水(10/5/5mL)中的溶液中加入氢氧化锂(43mg,1.8mmol)。在搅拌1小时后,MS表明反应完成。然后将混合物减压浓缩,并将残余物在水(10mL)和二氯甲烷(15mL)之间分配。将水相用二氯甲烷(3X10mL)萃取。将合并的有机层用盐水(30mL)洗涤,用Na2SO4干燥,过滤并减压浓缩。将残余物通过反相制备性-HPLC来纯化得到291(56mg,60%),其为白色固体。MS-ESI:[M+H]+517.2.1H NMR(500MHz,DMSO-d6)δ9.02(s,1H),8.58(d,J=5.0Hz,1H),8.48(s,1H),8.00(d,J=2.0Hz,1H),7.58(d,J=2.0Hz,1H),7.52(d,J=5.0Hz,1H),6.25(s,1H),4.87-4.85(m,1H),4.42-4.36(m,2H),3.61(s,3H),2.98-2.85(m,4H),2.32(s,3H),1.92-1.86(m,4H).
实施例292a 4-{5-[(1,5-二甲基-1H-吡唑-3-基)氨基]-1-甲基-6-氧代-1,6-二氢-吡啶-3-基}-2-{4,4-二甲基-9-氧代-7-硫杂-10,11-二氮杂三环[6.4.0.02,6]十二碳-1(8),(6),11-三烯-10-基}吡啶-3-甲醛292a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入3-(1,5-二甲基-1H-吡唑-3-基氨基)-1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮242a(344mg,1.0mmol)、4-氯-2-{4,4-二甲基-9-氧代-7-硫杂-10,11-二氮杂三环[6.4.0.02,6]十二碳-1(8),2(6),11-三烯-10-基}吡啶-3-甲醛282i(538.5mg,1.5mmol)、Pd2(dba)3(91.5mg,0.10mmol)、三环己基膦(112mg,0.40mmol)、碳酸铯(652mg,2.0mmol)、1,4-二噁烷(20mL)和水(0.5mL)。在经历三轮真空/氩气吹洗后,将混合物在75℃加热2小时。然后将其过滤并减压蒸发滤液。将残余物用石油醚洗涤得到292a(300mg,粗制),其为黑色固体。MS-ESI:[M+H]+542.2
实施例292 3-[4-[5-[(1,5-二甲基吡唑-3-基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-7,7-二甲基-6,8-二氢环戊二烯并[3,4]噻吩并[1,3-d]哒嗪-4-酮292
在0℃,向292a(162.6mg,0.30mmol)于甲醇(6mL)中的溶液加入硼氢化钠(114mg,3.0mmol)。将反应混合物在25℃搅拌0.5小时。然后将其用水(10mL)淬灭。将所得混合物减压蒸发并将残余物用二氯甲烷(3X20mL)萃取。将合并的二氯甲烷萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到292(35mg,22%),其为黄色固体。MS-ESI:[M+H]+543.8.1H NMR(500MHz,DMSO-d6)δ8.57(d,J=5.0Hz,1H),8.47(s,1H),8.08(s,1H),8.02(d,J=1.5Hz,1H),7.52(d,J=5.0Hz,1H),7.40(d,J=1.5Hz,1H),5.90(s,1H),4.88(s,1H),4.40(d,J=5.0Hz,2H),3.59(s,3H),3.58(s,3H),2.92(d,J=4.5Hz,2H),2.81(s,2H),2.18(s,3H),1.29(s,3H),1.28(s,6H).
实施例293a 1-甲基-4-硝基-1H-1,2,3-三唑293a
在0℃向装有4-硝基-2H-1,2,3-三唑(2.0g,17.5mmol)和THF(10mL)的100-mL单颈圆底烧瓶中加入NaH(1.7g,35.0mmol,2.0当量)。将混合物在0℃搅拌15分钟。加入碘甲烷(3.68g,26.3mmol,1.5当量)于丙酮(40mL)中的溶液并将所得反应混合物在室温搅拌2小时。之后,在0℃,将反应用水(20mL)淬灭并减压浓缩。将残余物用二氯甲烷(100mL)稀释。然后将其用盐水洗涤,用无水Na2SO4干燥并减压浓缩。将残余物通过硅胶柱色谱法来纯化(用6:1石油醚/乙酸乙酯洗脱)得到293a(800mg,35%),其为浅黄色固体,并得到区域异构体1-甲基-5-硝基-1H-1,2,3-三唑(1.34g,60%),其为白色固体。1H NMR(500MHz,CDCl3)δ8.34(s,1H),4.26(s,3H).
实施例293b 1-甲基-1H-1,2,3-三唑-4-胺293b
按照实施例130b中的操作,以293a(800mg,6.25mmol)和10%钯/炭(50%水分,160mg)开始得到293b,其为黄色固体(600mg,98%)。1H NMR(500MHz,CDCl3)δ6.91(s,1H),3.97(s,3H),3.65(brs,2H).
实施例293c 5-溴-1-甲基-3-(1-甲基-1H-1,2,3-三唑-4-基氨基)吡啶-2(1H)-酮293c
按照实施例130c中的操作,以293b(500mg,5.10mmol,1.0当量)和3,5-二溴-1-甲基吡啶-2(1H)-酮(2.04g,7.65mmol,1.5当量)开始得到293c,其为黄色固体(760mg,52%)。MS-ESI:[M+H]+283.9。
实施例293d乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{1-甲基-5-[(1-甲基-1H-1,2,3-三唑-4-基)氨基]-6-氧代-1,6-二氢吡啶-3-基}吡啶-3-基)甲酯293d
按照实施例283b中的操作,以293c(150mg,0.53mmol,1.0当量)和{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(629mg,1.59mmol,3.0当量)开始得到293d,其为黄色固体(110mg,37%)。MS-ESI:[M+H]+557.4.
实施例293 3-[3-(羟基甲基)-4-[1-甲基-5-[(1-甲基三唑-4-基)氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮293
按照实施例283中的操作,以293d(110mg,0.20mmol)开始得到293,其为浅黄色固体(78mg,75%)。MS-ESI:[M+H]+514.9.1H NMR(500MHz,CDCl3)δ8.49(d,J=4.5Hz,1H),7.78(s,1H),7.73(s,1H),7.60(s,1H),7.42(s,1H),7.33(d,J=4.0Hz,1H),6.87(s,1H),5.25(brs,1H),4.65-4.38(m,3H),4.21-4.20(m,2H),4.08(s,3H),3.89-3.85(m,1H),3.73(s,3H),2.59(s,2H),2.54(s,2H),1.29(s,6H).
实施例294 3-[4-[5-[(5-叔丁基异噁唑-3-基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮294
按照实施例273中的操作,用5-(叔丁基)异噁唑-3-胺代替2-氨基吡啶,制备了294(5.1mg,16%收率)。1H NMR(400MHz,DMSO-d6)δ8.93(s,1H),8.48(d,J=5.0Hz,1H),8.04(d,J=2.3Hz,1H),7.56(d,J=2.3Hz,1H),7.32(d,J=5.0Hz,1H),6.56(s,1H),6.22(s,1H),4.90(t,J=5.3Hz,1H),4.51–4.36(m,2H),4.26–4.16(m,3H),3.85(d,J=10.7Hz,1H),3.60(s,3H),2.58(d,J=7.7Hz,2H),2.43(s,2H),1.27(s,9H),1.22(s,6H).ES-MS m/z557.4[M+1].
实施例295a 5-乙基异噁唑-3-胺295a
向3-氧代戊腈(1.0g,10.3mmol)于水(20mL)中的溶液中加入NaOH(535.6mg,13.4mmol)。搅拌5分钟后,加入羟基胺盐酸盐(787.4mg,11.33mmol)并将混合物在40℃加热12小时。此时,加入浓HCl(3mL)并将反应混合物在50℃加热2小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。然后将其冷却至室温并用NaOH水溶液(30%)调整pH至10。将混合物用乙酸乙酯(3X50mL)萃取。将合并的有机层用盐水洗涤,用Na2SO4干燥并减压浓缩。将残余物通过硅胶柱色谱法来纯化(用2:1石油醚/乙酸乙酯洗脱)得到295a,其为黄色固体(300mg,25%)。MS-ESI:[M+H]+113.3.1H NMR(500MHz,DMSO-d6)5.55(s,1H),5.40(s,2H),2.56-2.52(m,2H),1.13(t,J=7.5Hz,3H).
实施例295b乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{5-[(5-乙基-1,2-噁唑-3-基)氨基]-1-甲基-6-氧代-1,6-二氢吡啶-3-基}吡啶-3-基)甲酯295b
在配备有磁力搅拌子和回流冷凝器的25-mL单颈圆底烧瓶中装入295a(24.8mg,0.222mmol)、乙酸[4-(5-溴-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-基]甲酯273a(100mg,0.185mmol)、Pd2(dba)3(8.5mg,0.0093mmol)、Xantphos(10.7mg,0.019mmol)、Cs2CO3(120.6mg,0.37mmol)和二噁烷(10mL)。使体系经历三轮真空/氮气吹洗并在氮气保护下在100℃加热3小时。通过LCMS分析反应混合物,显示完全转化成所期望的产物。将其冷却至室温并过滤。减压浓缩滤液。将残余物用乙腈(0.5mL)洗涤得到295b,其为白色固体(52mg,49.5%),将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+570.8
实施例295 3-[4-[5-[(5-乙基异噁唑-3-基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮295
向295b(42mg,0.0736mmol)于THF(4mL)、异丙醇(4mL)和水(4mL)中的溶液中加入氢氧化锂(17.7mg,0.736mmol)。将反应混合物在室温搅拌1小时并减压浓缩。将残余物用水(5mL)稀释并用二氯甲烷(3X20mL)萃取。将合并的萃取物用Na2SO4干燥,过滤并减压浓缩。将残余物通过反相制备性-HPLC来纯化得到295(22mg,57%),其为白色固体。MS-ESI:[M+H]+528.8.1H NMR(500MHz,DMSO-d6)δ8.99(s,1H),8.49(d,J=5.5Hz,1H),8.03(d,J=2.0Hz,1H),7.56(d,J=2.0Hz,1H),7.33(d,J=5.0Hz,1H),6.57(s,1H),6.25(s,1H),4.94-4.92(m,1H),4.48-4.38(m,2H),4.26-4.19(m,3H),3.87-3.85(m,1H),3.61(s,3H),2.68-2.66(m,2H),2.62-2.59(m,2H),2.43(s,2H),1.22(s,6H),1.19(t,J=7.5Hz,3H).
实施例296a(3-硝基-1H-吡唑-5-基)甲醇296a
将配备有氮气进气口的100-mL三颈圆底烧瓶用氮气吹洗并装入3-硝基吡唑-5-羧酸(0.56g,3.56mmol)和THF(8mL)。将体系用冰/丙酮浴冷却至-5℃。加入硼烷-THF复合物溶液(1.0M,11mL,11.0mmol),加入速度是维持内部温度低于5℃。添加结束后,移去冷却浴并将反应混合物在60℃搅拌3小时。之后,将反应混合物用冰/丙酮浴冷却至-5℃,加入水(2mL)和4N盐酸(2mL)。将反应混合物在70℃搅拌1小时,目的是破坏硼烷-吡唑复合物。将其冷却至室温并减压浓缩至体积为约1mL。加入乙酸乙酯(20mL)和水(10mL)并将混合物搅拌15分钟。分离出水层并用乙酸乙酯(4X10mL)萃取。将合并的有机层用饱和碳酸氢钠水溶液(2X10mL)、盐水(10mL)洗涤,并用硫酸钠干燥。过滤除去干燥剂并减压浓缩滤液得到296a(345mg,68%),其为浅黄色固体。MS-ESI:[M+H]+144
实施例296b(1-(2-溴乙基)-3-硝基-1H-吡唑-5-基)甲醇296b
将296a(345mg,2.41mmol)和碳酸铯(965mg,2.96mmol)于DMF(5mL)中的混合物用冰/丙酮浴冷却至0℃并逐份加入二溴乙烷(4.48g,24.1mmol)(无放热)。将反应混合物在0℃搅拌1小时并在室温搅拌4小时。之后,加入乙酸乙酯(20mL)和水(15mL)。分离出水层并用乙酸乙酯(2X10mL)萃取。将合并的有机层用水(10mL)、盐水(10mL)洗涤,并用硫酸钠干燥。通过过滤除去干燥剂,减压浓缩滤液得到粗制产物,将其通过硅胶柱色谱法来纯化(用6:1石油醚/乙酸乙酯洗脱)得到296b(300mg,50%)。MS-ESI:[M+H]+250
实施例296c 1-(2-溴乙基)-5-(氯甲基)-3-硝基-1H-吡唑296c
将配备有氮气进气口和回流冷凝器的50-mL三颈圆底烧瓶用氮气吹洗并装入296b(438mg,1.76mmol)和氯仿(10mL)。将反应混合物用冰/丙酮浴冷却至-5℃,逐份加入SOCl2(628mg,5.28mmol)。移去冷却浴并将反应混合物在70℃搅拌3小时。之后,减压除去溶剂,向残余物中加入乙酸乙酯并将所得溶液冷却至-5℃。加入饱和碳酸氢钠水溶液(3mL)直到达到pH 8.5。使混合物在乙酸乙酯和水之间分配。将合并的有机层用饱和碳酸钠水溶液(2X5mL)、盐水(10mL)洗涤,并用硫酸钠干燥。通过过滤除去干燥剂,减压浓缩滤液得到296c(284mg,60%).
实施例296d 5-(2-甲氧基乙基)-2-硝基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪296d
在配备有磁力搅拌子的微波小瓶中装入296c(2.67g,10.0mmol)、2-甲氧基乙胺(2.25g,30.0mmol)和DMSO(14mL)。将反应混合物在微波照射下在120℃加热1.0小时。将其冷却至室温并用乙酸乙酯(40mL)稀释。将混合物用水(3X15mL)洗涤。干燥有机层并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用30:1二氯甲烷/甲醇洗脱)得到296d(1.7g,75%),其为黄色固体。MS-ESI:[M+H]+227.0
实施例296e 5-(2-甲氧基乙基)-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-胺296e
向296d(1.7g,7.5mmol)于乙醇(50mL)中的溶液中加入Pd/C(10%,800mg)。向反应混合物中充入氢气(通过气囊)并在室温搅拌2小时。反应完成后,用塞过滤混合物。减压浓缩滤液得到296e,其为黄色固体(1.2g,82%),将其不经进一步纯化直接使用。MS-ESI:[M+H]+197.3
实施例296f 5-溴-3-(5-(2-甲氧基乙基)-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-1-甲基吡啶-2(1H)-酮296f
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(40mL)、296e(588mg,3.0mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(800mg,3.0mmol)和碳酸铯(1.96g,6.0mmol)。在使氮气鼓泡通过所述悬浮液20分钟后,加入xantphos(173mg,0.30mmol)和三(二亚苄基丙酮)二钯(0)(137mg,0.15mmol)。使体系经历三轮真空/氩气吹洗并回流加热5小时。然后将其冷却至室温并过滤。将固体用二氯甲烷(2X15mL)洗涤。将合并的滤液减压浓缩。将残余固体通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(80/1至30/1)洗脱)得到296f(745mg,65%),其为黄色固体。MS-ESI:[M+H]+382.9
实施例296g乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-(5-{[5-(2-甲氧基乙基)-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基]氨基}-1-甲基-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-基)甲酯296g
在配备有回流冷凝器的25-mL圆底烧瓶中装入{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(198mg,0.50mmol)、296f(190mg,0.50mmol)、K3PO4(212mg,1.0mmol)、乙酸钠(82mg,1.0mmol)、Pd(dppf)Cl2(21mg,0.025mmol)、乙腈(8mL)和水(0.5mL)。使体系经历三轮真空/氮气吹洗并在氮气保护下在100℃加热1小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将反应混合物冷却至室温并过滤。减压浓缩滤液。使残余物在二氯甲烷(20mL)和水(10mL)之间分配。将水层用二氯甲烷(2×20mL)萃取。将合并的有机萃取物用Na2SO4干燥,过滤并减压浓缩。将黑色残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(80/1至30/1)洗脱)得到296g(163mg,50%),其为黄色固体。MS-ESI:[M+H]+654.9
实施例296 3-[3-(羟基甲基)-4-[5-[[5-(2-甲氧基乙基)-6,7-二氢-4H-吡唑并[1,5-a]吡嗪-2-基]氨基]-1-甲基-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮296
向296g(160mg,0.245mmol)于THF/异丙醇/水(8/5/3mL)中的溶液中加入氢氧化锂(29mg,1.22mmol)。将混合物在室温搅拌1小时并减压蒸发。将残余物通过反相制备性-HPLC来纯化得到296,其为白色固体(117mg,78%)。MS-ESI:[M+H]+613.3.1H NMR(500MHz,CDCl3)δ8.48(d,J=5.0Hz,1H),7.93(d,J=2.0Hz,1H),7.73(d,J=2.5Hz,1H),7.41(s,1H),7.35(d,J=5.0Hz,1H),6.86(s,1H),5.71(s,1H),5.05(t,J=7.0Hz,1H),4.66-4.65(m,1H),4.52-4.50(m,1H),4.36-4.34(m,1H),4.17-4.05(m,2H),4.10-4.08(m,2H),3.88-3.87(m,1H),3.75-3.73(m,2H),3.71(s,3H),3.61-3.59(m,2H),2.40(s,3H),3.04-3.03(m,2H),2.80(t,J=5.5Hz,2H),2.59-2.57(m,2H),2.54-2.53(m,2H),1.29(s,6H).
实施例297a 6-氯-2-甲基-4-(5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)哒嗪-3(2H)-酮297a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(30mL)、5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-胺113e(1.70g,11.2mmol)、4-溴-6-氯-2-甲基哒嗪-3(2H)-酮(2.68g,12.0mmol)和碳酸铯(7.30g,22.4mmol)。在使氮气鼓泡通过所述悬浮液30分钟后,加入Xantphos(0.59g,1.02mmol)和三(二亚苄基丙酮)二钯(0)(467mg,0.51mmol)。使体系经历三轮真空/氩气吹洗并在90℃加热2小时。然后将其冷却至室温并过滤。真空蒸发滤液。将残余物通过硅胶柱色谱法来纯化(用30:1二氯甲烷/甲醇洗脱)得到297a(1.9g,60%),其为棕色固体。LCMS:[M+H]+295.1
实施例297b乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-[1-甲基-5-({5-甲基-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基}氨基)-6-氧代-1,6-二氢哒嗪-3-基]吡啶-3-基)甲酯297b
在配备有磁力搅拌子和回流冷凝器的25-mL圆底烧瓶中装入297a(195mg,0.66mmol)、乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-(四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-3-基)甲酯199e(315mg,0.66mmol)、PdCl2(dppf)(40mg,0.050mmol)、K3PO4(250mg,1.2mmol)、乙酸钠(100mg,1.20mmol)、乙腈(8mL)和水(1mL)。将体系排空,然后用氮气回填。然后将其在100℃加热1小时。将混合物冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用20:1二氯甲烷/甲醇洗脱)得到297b,其为黄色固体(150mg,38%)。MS-ESI:[M+H]+612.3.
实施例297 3-[3-(羟基甲基)-4-[1-甲基-5-[(5-甲基-6,7-二氢-4H-吡唑并[1,5-a]吡嗪-2-基)氨基]-6-氧代-哒嗪-3-基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮297
将297b(150mg,0.24mmol)和氢氧化锂水合物(96mg,2.4mmol)于THF(8mL)、异丙醇(8mL)和水(2mL)中的混合物在40℃搅拌0.5小时。将混合物减压蒸发,并将残余物在二氯甲烷(15mL)和水(10mL)之间分配。将合并的萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到297,其为浅黄色固体(98mg,70%)。MS-ESI:[M+H]+570.3.1H NMR(500MHz,DMSO-d6)δ9.30(s,1H),8.52(d,J=4.5Hz,1H),7.90(s,1H),7.38(d,J=5.0Hz,1H),6.55(s,1H),5.99(s,1H),4.74-4.73(m,1H),4.60-4.58(m,1H),4.40-4.37(m,1H),4.26-4.24(m,1H),4.19-4.18(m,2H),3.96-3.95(m,2H),3.89-3.87(m,1H),3.75(s,3H),3.53-3.52(m,2H),2.80-2.78(m,2H),2.57-2.55(m,2H),2.52-2.50(m,2H),2.35(s,3H),1.22(s,6H).
实施例298a乙酸(4-{5-[(5-氰基吡嗪-2-基)氨基]-1-甲基-6-氧代-1,6-二氢吡啶-3-基}-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-基)甲酯298a
在配备有回流冷凝器的50-mL圆底烧瓶中装入乙酸[4-(5-溴-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-基]甲酯273a(269mg,0.50mmol)、5-氨基吡嗪-2-甲腈(60mg,0.50mmol)、XantPhos(29mg,0.050mmol)、Pd2(dba)3(45mg,0.050mmol)、Cs2CO3(326mg,1.0mmol)和1,4-二噁烷(10mL)。在三次空气/氩气吹洗后,将反应混合物在微波照射下在100℃加热1小时。过滤混合物并将固体用甲醇(50mL)洗涤。将合并的滤液减压蒸发并将残余物用硅胶柱色谱法来纯化(用50:1二氯甲烷/甲醇洗脱)得到298a(200mg,69%),其为黄色固体。MS-ESI:[M+H]+579.3.
实施例298 5-[[5-[2-(7,7-二甲基-4-氧代-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-3-基)-3-(羟基甲基)-4-吡啶基]-1-甲基-2-氧代-3-吡啶基]氨基]吡嗪-2-甲腈298
将298a(200mg,0.35mmol)和氢氧化锂(84mg,3.5mmol)于异丙醇/THF(5mL/5mL)和水(2mL)中的混合物在室温搅拌2小时。将混合物减压蒸发,并将残余物在乙酸乙酯(20mL)和水(10mL)之间分配。将合并的萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到298(40mg,21%),其为黄色固体。MS-ESI:[M+H]+537.3.1H NMR(500MHz,DMSO-d6)δ9.96(s,1H),8.77(s,1H),8.701(d,J=2.5Hz,1H),8.67(s,1H),8.50(d,J=5.0Hz,1H),7.76(d,J=2.0Hz,1H),7.35(d,J=5.0Hz,1H),6.56(s,1H),5.00(t,J=5.0Hz,1H),4.42-4.39(m,2H),4.24-4.19(m,3H),3.84(m,1H),3.63(s,3H),2.57(m,2H),2.42(s,2H),1.23(s,6H)
实施例299a 5-苯基异噁唑-3-胺299a
向搅拌的3-氧代-3-苯基丙腈(1.5g,10.3mmol)和NaOH(452mg,11.3mmol)于水(10mL)/EtOH(10mL)中的溶液中加入羟基胺盐酸盐(785mg,11.3mmol)。将混合物在80℃搅拌整夜。此时,加入浓HCl(1.3mL,15.5mmol)并将所得混合物在80℃加热2小时。然后将其碱化至pH 10并用乙酸乙酯萃取。将合并的萃取物减压浓缩并将残余物通过硅胶柱色谱法来纯化(用乙酸乙酯/石油醚(1:50至1:10)洗脱)得到299a,其为黄色固体(1.1g,68%)。MS-ESI:[M+H]+161.3.
实施例299b 5-溴-1-甲基-3-(5-苯基异噁唑-3-基氨基)吡啶-2(1H)-酮299b
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(40mL)、299a(640mg,4.0mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(1.1g,4.0mmol)、Pd2(dba)3(366.8mg,0.40mmol)、XantPhos(462.4mg,0.80mmol)和碳酸铯(2.6g,8.0mmol)。在经历三轮真空/氩气吹洗后,将混合物在92℃加热3小时。然后将其冷却至室温并过滤。减压浓缩滤液并将所得残余物用乙腈洗涤得到299b(1.7g,87%)。MS-ESI:[M+H]+346.0.
实施例299c乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{1-甲基-6-氧代-5-[(5-苯基-1,2-噁唑-3-基)氨基]-1,6-二氢吡啶-吡啶-3-基}吡啶-3-基)甲酯299c
在配备有磁力搅拌子和回流冷凝器的50-mL圆底烧瓶中装入299b(138mg,0.40mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂-三环并[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(158.8mg,0.40mmol)、Pd(dppf)Cl2(32.7mg,0.040mmol)、K3PO4(169.6mg,0.80mmol)、乙酸钠(108.8mg,0.80mmol)、水(0.5mL)和乙腈(10mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热3小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用50:1二氯甲烷/甲醇洗脱)得到299c,其为棕色固体(120mg,49%)。MS-ESI:[M+H]+618.8.
实施例299 3-[3-(羟基甲基)-4-[1-甲基-6-氧代-5-[(5-苯基异噁唑-3-基)氨基]-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮299
将299c(100mg,0.16mmol)和氢氧化锂(96mg,4.0mmol)于异丙醇/THF(1:1,4mL)和水(1mL)中的混合物在40℃搅拌30分钟。减压浓缩反应混合物并用水(5mL)稀释。将所得混合物用二氯甲烷萃取三次。将合并的有机层减压浓缩并将所得残余物通过反相制备性-HPLC来纯化得到299,其为白色固体(35mg,31%)。MS-ESI:[M+H]+576.8.1H NMR(500MHz,DMSO-d6)δ9.17(s,1H),8.51(d,J=5.5Hz,1H),8.11(d,J=2.5Hz,1H),7.79-7.77(m,2H),7.60(d,J=2.0Hz,1H),7.55-7.49(m,3H),7.35(d,J=4.5Hz,1H),6.91(s,1H),6.57(s,1H),4.96-4.93(m,1H),4.50-4.40(m,2H),4.26-4.19(m,3H),3.88-3.85(m,1H),3.63(s,3H),2.62-2.59(m,2H),2.44-2.42(m,2H),1.23(s,6H).
实施例300a 5-(1-甲氧基丙烷-2-基)-2-硝基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪300a
在配备有磁力搅拌子的微波小瓶中装入1-(2-溴乙基)-5-(氯甲基)-3-硝基-1H-吡唑296c(1.0g,3.7mmol)、1-甲氧基丙烷-2-胺(1.0g,11.2mmol)和DMSO(6mL)。将混合物在微波照射下在120℃加热1.0小时。将其冷却至室温并用水(30mL)稀释。将所得混合物用乙酸乙酯(3X20mL)萃取。将合并的有机层干燥并减压浓缩。将残余物通过硅胶柱色谱法来纯化(用石油醚/乙酸乙酯(60/1至1/1)洗脱)得到300a(600mg,68%),其为黄色固体。MS-ESI:[M+H]+241.0
实施例300b 5-(1-甲氧基丙烷-2-基)-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-胺300b
向300a(600mg,2.5mmol)于EtOH(40mL)中的溶液中加入Pd/C(10%,60mg)。向反应混合物中充入氢气(通过气囊)并在室温搅拌2小时。反应完成后,用塞过滤混合物。减压浓缩滤液得到300b,其为黄色固体(467mg,89%),将其不经进一步纯化即使用。MS-ESI:[M+H]+211.1
实施例300c 5-溴-3-(5-(1-甲氧基丙烷-2-基)-4,5,6,7-四氢吡唑并[1,5-a]-吡嗪-2-基氨基)-1-甲基吡啶-2(1H)-酮300c
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(40mL)、300b(400mg,1.9mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(H-001)(508mg,1.9mmol)和碳酸铯(1.24g,3.8mmol)。在使氮气鼓泡通过所述悬浮液20分钟后,添加xantphos(109mg,0.19mmol)和Pd2(dba)3(87mg,0.095mmol)。使体系经历三轮真空/氩气吹洗并回流加热5小时。然后将其冷却至室温并过滤。将固体用二氯甲烷(2X30mL)洗涤。将合并的滤液减压浓缩。将残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(80/1至30/1)洗脱)得到300c(436mg,58%),其为黄色固体。MS-ESI:[M+H]+396.0
实施例300d乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-(5-{[5-(1-甲氧基丙烷-2-基)-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基]氨基}-1-甲基-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-基)甲酯300d
在配备有回流冷凝器的50-mL圆底烧瓶中装入{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(238mg,0.60mmol)、300c(240mg,0.80mmol)、K3PO4(254mg,1.2mmol)、乙酸钠(98mg,1.6mmol)、Pd(dppf)Cl2(22mg,0.030mmol)和乙腈/水(12/0.5mL)。使体系经历三轮真空/氮气吹洗并在氮气保护下在100℃加热1小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将反应混合物冷却至室温并过滤。减压浓缩滤液。使残余物在二氯甲烷(30mL)和水(30mL)之间分配。将水层用二氯甲烷(2×30mL)萃取。将合并的有机萃取物用Na2SO4干燥,过滤并减压浓缩。将黑色残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(80/1至30/1)洗脱)得到300d(200mg,50%),其为黄色固体。MS-ESI:[M+H]+669.4
实施例300(R)-2-(3'-(羟基甲基)-5-((5-(1-甲氧基丙烷-2-基)-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基)氨基)-1-甲基-6-氧代-1,6-二氢-[3,4'-联吡啶]-2'-基)-7,7-二甲基-2,3,4,6,7,8-六氢-1H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮300
向300d(200mg,0.30mmol)于THF/异丙醇/水(6/3/3mL)中的溶液中加入氢氧化锂(36mg,1.5mmol)。将混合物在30℃搅拌1小时并减压浓缩。使残余物在乙酸乙酯(15mL)和(10mL)之间分配。将水相用乙酸乙酯(3X10mL)萃取。将合并的有机层干燥,过滤并减压浓缩。制备性-HPLC和手性拆分得到两种对映异构体:300(35mg,18.6%),其为白色固体;和303(28mg,15%),其为白色固体。MS-ESI:[M+H]+627.4.1H NMR(500MHz,CDCl3)δ8.49(d,J=5.0Hz,1H),7.92(d,J=2.5Hz,1H),7.73(d,J=2.0Hz,1H),7.41(s,1H),7.35(d,J=5.0Hz,1H),6.85(s,1H),5.72(s,1H),5.05-5.03(m,1H),4.67-4.45(m,1H),4.52-4.50(m,1H),4.35-4.31(m,1H),4.18-4.16(m,2H),4.09-4.07(m,2H),3.87-3.85(m,3H),3.71(s,3H),3.56-3.52(m,1H),3.45-3.43(m,1H),3.38(s,3H),3.11-3.08(m,3H),2.60-2.58(m,2H),2.53(s,2H),1.29(s,6H),1.17(d,J=6.0Hz,3H).
实施例301a 6-(三氟甲基)哒嗪-3-胺301a
将3-氯-6-三氟甲基哒嗪(1.6g,8.80mmol)和氢氧化铵(9mL)于THF(3mL)中的混合物在微波反应器中在100℃加热1小时。之后,将反应混合物蒸发并将残余物用二氯甲烷萃取。将合并的萃取物用MgSO4干燥,过滤并减压蒸发得到301a(1.3g,93%),其为白色固体。MS-ESI:[M+H]+164.1
实施例301b 5-溴-1-甲基-3-(6-(三氟甲基)哒嗪-3-基氨基)吡啶-2(1H)-酮301b
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入301a(750mg,4.6mmol)、XantPhos(532mg,0.92mmol)、Pd2dba3(421mg,0.46mmol)、2-溴-4-氯吡啶-3-甲醛(H-001)(1.84g,6.9mmol)、Cs2CO3(3.0g,9.2mmol)和1,4-二噁烷(50mL)。使体系经历三轮真空/氩气吹洗并在90℃加热整夜。反应结束后,过滤混合物并将固体用甲醇(30mL)洗涤。将合并的滤液减压蒸发,将残余物通过硅胶柱色谱法来纯化(用20:1二氯甲烷/甲醇洗脱)得到301b(1.38g,89%),其为黄色固体。MS-ESI:[M+H]+350.8
实施例301c乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-(1-甲基-6-氧代-5-{[6-(三氟甲基)哒嗪-3-基]氨基}-1,6-二氢吡啶-3-基)吡啶-3-基)甲酯301c
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入301b(300mg,0.86mmol)、乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-(四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-3-基)甲酯199e(824mg,1.72mmol)、CH3COONa(140mg,1.72mmol)、PdCl2(dppf)(70mg,0.086mmol)、K3PO4(360mg,1.72mmol)、乙腈(20mL)和水(0.5mL)。使氮气鼓泡通过所得混合物20分钟后,将其在氮气中在100℃加热2小时。将混合物冷却至室温并过滤。减压蒸发滤液并将残余物通过硅胶柱色谱法来纯化(用50:1二氯甲烷/甲醇洗脱)得到301c,其为白色固体(125mg,23%)。MS-ESI:[M+H]+622.3
实施例301 3-[3-(羟基甲基)-4-[1-甲基-6-氧代-5-[[6-(三氟甲基)哒嗪-3-基]氨基]-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮301
将301c(90mg,0.14mmol)和氢氧化锂(24mg,0.56mmol)于异丙醇/THF/水(6mL/4mL/2mL)中的混合物在室温搅拌0.5小时。将混合物减压蒸发并使残余物在二氯甲烷(20mL)和水(10mL)之间分配。将合并的二氯甲烷萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到301c,其为白色固体(39mg,48%)。MS-ESI:[M+H]+580.3.1H NMR(500MHz,DMSO-d6)δ9.57(s,1H),8.87(d,J=2.5Hz,1H),8.51(d,J=5.0Hz,1H),7.96(d,J=9.0Hz,1H),7.88(d,J=9.0Hz,1H),7.74(d,J=2.0Hz,1H),7.38(d,J=5.0Hz,1H),6.58(s,1H),4.98-4.97(m,1H),4.48-4.40(m,2H),4.27-4.20(m,3H),3.88-3.86(m,1H),3.65(s,3H),2.62-2.53(m,2H),2.42-2.41(m,2H),1.2(s,6H).
实施例302a N-甲基(1-甲基-3-硝基-1H-吡唑-5-基)甲胺302a
在0℃(冰浴),向搅拌的MeNH2(30%wt于水中)(2.5g,20mmol)于丙酮(10mL)中的溶液中加入K2CO3(415mg,3mmol),然后滴加5-(溴甲基)-1-甲基-3-硝基-1H-吡唑(220mg,1mmol)于丙酮(5mL)中的溶液。然后将反应混合物温热至室温并搅拌3小时。除去溶剂并将残余物用二氯甲烷(3X15mL)萃取,用Na2SO4干燥并浓缩得到302a,其为黄色油状物(170mg,99%),将其不经额外纯化即用于下一步骤。LCMS:(M+H)+171
实施例302b N-甲基-N-((1-甲基-3-硝基-1H-吡唑-5-基)甲基)氧杂环丁烷-3-胺302b
在室温和氮气保护下,向302a(170mg,1mmol)于甲醇(4mL)中的溶液中加入ZnCl2(1mmol/L于乙醚中)(2mL,2mmol)和氧杂环丁烷-3-酮(150mg,2mmol),然后加入NaBH3CN(130mg,2mmol)。将反应混合物温热至50℃并搅拌3小时。然后将混合物冷却至室温并除去溶剂。将残余物在快速柱上纯化(用50:1二氯甲烷/甲醇洗脱)得到302b,其为黄色固体(180mg,80%,两步)。LCMS:(M+H)+227.1H NMR(500MHz,DMSO)δ6.99(s,1H),4.52(t,J=6.5,2H),4.42(t,J=6,2H),3.98(s,3H),3.63(m,1H),3.50(s,2H),2.03(s,3H).
实施例302c 1-甲基-5-((甲基(氧杂环丁烷-3-基)氨基)甲基)-1H-吡唑-3-胺302c
向302b(1.8g,7.96mmol)于乙醇(20mL)和水(20mL)中的溶液中加入NH4Cl(3.3g,63.6mmol)和铁粉(1.80g,31.8mmol)。将反应混合物在70℃加热2小时,之后,将混合物冷却至室温并过滤。蒸发滤液并将残余物用二氯甲烷(3X30mL)萃取,用Na2SO4干燥并浓缩得到粗制产物,将其在快速柱上纯化(用含有0.5%三乙胺的50:1二氯甲烷/甲醇洗脱)得到302c,其为黄色油状物(1.3g,83%)。LCMS:(M+H)+197
实施例302d 5-溴-1-甲基-3-(1-甲基-5-((甲基(氧杂环丁烷-3-基)氨基)甲基)-1H-吡唑-3-基氨基)吡啶-2(1H)-酮302d
按照实施例292c中的操作,以302c和3,5-二溴-1-甲基吡啶-2(1H)-酮开始得到302d,63%收率。LCMS:(M+H)+383.1H NMR(500MHz,DMSO)δ8.35(s,1H),7.99(d,J=2.5,1H),7.36(d,J=2.5,1H),5.99(s,1H),4.50(t,J=7,2H),4.40(t,J=6.5,2H),3.77(s,3H),3.57(m,1H),3.49(s,3H),3.35(s,2H),2.01(s,3H).
实施例302e(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{1-甲基-5-[(1-甲基-5-{[甲基(氧杂环丁烷-3-基)氨基]甲基}-1H-吡唑-3-基)氨基]-6-氧代-1,6-二氢吡啶-3-基}吡啶-3-基)甲基Acetate 302e
在配备有磁力搅拌子和回流冷凝器的25-mL圆底烧瓶中装入302d(200mg,0.52mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(210mg,0.53mmol)、PdCl2(dppf)(37mg,0.050mmol)、K3PO4(250mg,1.2mmol)、乙酸钠(100mg,1.20mmol)、乙腈(8mL)和水(0.5mL)。将体系排空,然后用氮气回填。将混合物在100℃加热1小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用20:1二氯甲烷/甲醇洗脱)得到302e,其为黄色固体(150mg,44%)。MS-ESI:[M+H]+655.3.
实施例302 3-[3-(羟基甲基)-4-[1-甲基-5-[[1-甲基-5-[[甲基(氧杂环丁烷-3-基)氨基]甲基]吡唑-3-基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮302
将302e(150mg,0.23mmol)和氢氧化锂水合物(90mg,2.3mmol)于THF(8mL)、异丙醇(8mL)和水(2mL)中的混合物在40℃搅拌0.5小时。将混合物减压浓缩。使残余物在水(10mL)和二氯甲烷(3X15mL)之间分配。将合并的有机萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到302,其为浅黄色固体(105mg,75%)。MS-ESI:[M+H]+612.8.1H NMR(500MHz,DMSO-d6)δ8.48(d,J=5.0Hz,1H),8.14(s,1H),8.05(d,J=2.5Hz,1H),7.40(d,J=2.0Hz,1H),7.33(d,J=5.0Hz,1H),6.55(s,1H),6.01(s,1H),4.99-4.97(m,1H),4.50-4.46(m,3H),4.40-4.38(m,3H),4.25-4.18(m,3H),3.85-3.84(m,1H),3.72(s,3H),3.59(s,3H),3.58-3.54(m,1H),2.58-2.56(m,2H),2.52-2.50(m,2H),2.43-2.42(m,2H),2.00(s,3H),1.22(s,6H).
实施例303(S)-10-[3-(羟基甲基)-4-[5-({5-[(2R)-1-甲氧基丙烷-2-基]-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基}氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基]吡啶-2-基]-4,4-二甲基-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-9-酮303
按照实施例300获得单一对映异构体303(28mg,15%),其为白色固体。MS-ESI:[M+H]+627.4。1H NMR(500MHz,CDCl3)δ8.49(d,J=5.0Hz,1H),7.92(d,J=2.5Hz,1H),7.73(d,J=2.0Hz,1H),7.41(s,1H),7.35(d,J=5.0Hz,1H),6.85(s,1H),5.72(s,1H),5.05-5.03(m,1H),4.67-4.45(m,1H),4.52-4.50(m,1H),4.35-4.31(m,1H),4.18-4.16(m,2H),4.09-4.07(m,2H),3.87-3.85(m,3H),3.71(s,3H),3.56-3.52(m,1H),3.45-3.43(m,1H),3.38(s,3H),3.11-3.08(m,3H),2.60-2.58(m,2H),2.53(s,2H),1.29(s,6H),1.17(d,J=6.0Hz,3H).
实施例304a 5-(2-甲氧基乙基)-2-硝基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪304a
向2-硝基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪(190mg,1.13mmol)125i于乙腈(10mL)中的溶液中加入K2CO3(311.9mg,2.26mmol)和1-溴-2-甲氧基乙烷(188.3mg,1.36mmol)。将反应混合物在微波照射下在80℃加热17小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将混合物冷却至室温并过滤。减压浓缩滤液得到304a,其为白色固体(230mg,90%),将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+227.0
实施例304b 5-(2-甲氧基乙基)-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-胺304b
向304a(286mg,1.26mmol)于甲醇(10mL)中的溶液中加入Pd/C(28.6mg)。将体系排空,然后用氮气回填。在室温搅拌2小时后,过滤混合物。减压浓缩滤液得到304b,其为黄色固体(240mg,97%),将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+197.0
实施例304c 5-溴-3-(5-(2-甲氧基乙基)-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-1-甲基吡啶-2(1H)-酮304c
在配备有磁力搅拌子和回流冷凝器的100-mL圆底烧瓶中装入304b(230mg,1.17mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(468.4mg,1.76mmol)、Pd2(dba)3(53.5mg,0.0585mmol)、Xantphos(67.6mg,0.117mmol)、Cs2CO3(762.8mg,2.34mmol)和二噁烷(20mL)。在经历三轮真空/氮气吹洗后,将混合物在100℃加热3小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将其冷却至室温并过滤。减压浓缩滤液。将残余物通过硅胶柱色谱法来纯化(用40:1二氯甲烷/甲醇洗脱)得到304c,其为黑色固体(380mg,85%)。MS-ESI:[M+H]+382.2
实施例304d 3-(5-(2-甲氧基乙基)-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮304d
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入304c(330mg,0.86mmol)、Pin2B2(329mg,1.30mmol)、Pd2(dba)3(40mg,0.043mmol)、X-phos(41mg,0.086mmol)、乙酸钾(169mg,1.726mmol)和二噁烷(10mL)。在经历三轮真空/氮气吹洗后,将混合物在70℃加热2小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将其冷却至室温并过滤。减压浓缩滤液。将残余物用石油醚洗涤得到304d,其为黑色油状物(240mg,80%),将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+348.3
实施例304e 2-{4,4-二甲基-9-氧代-7-硫杂-10,11-二氮杂三环[6.4.0.02,6]十二碳-1(8),2(6),11-三烯-10-基}-4-(5-{[5-(2-甲氧基乙基)-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基]氨基}-1-甲基-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-甲醛304e
在配备有回流冷凝器的50-mL圆底烧瓶中装入4-氯-2-{4,4-二甲基-9-氧代-7-硫杂-10,11-二氮杂三环[6.4.0.02,6]十二碳-1(8),2(6),11-三烯-10-基}吡啶-3-甲醛282i(60mg,0.167mmol)、304d(143.4mg,0.334mmol)、Pd(dppf)Cl2(6.8mg,0.0084mol)、K3PO4(70.8mg,0.334mmol)、乙酸钠(27.4mg,0.334mmol)、乙腈(10mL)和水(3滴)。使体系经历三轮真空/氮气吹洗并在氮气保护下在100℃加热1小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将其冷却至室温并过滤。减压浓缩滤液。将残余物通过硅胶柱色谱法来纯化(用40:1二氯甲烷/甲醇洗脱)得到304e(80mg,77%),其为白色固体。MS-ESI:[M+H]+626.8
实施例304 3-[3-(羟基甲基)-4-[5-[[5-(2-甲氧基乙基)-6,7-二氢-4H-吡唑并[1,5-a]吡嗪-2-基]氨基]-1-甲基-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-6,8-二氢环戊二烯并[3,4]噻吩并[1,3-d]哒嗪-4-酮304
向304e(80mg,0.128mmol)于二氯甲烷(4mL)和甲醇(4mL)中的溶液中加入NaBH4(9.7mg,0.256mmol)。将反应混合物在室温搅拌1小时。将其用NH4Cl水溶液(10mL)淬灭并减压浓缩,将残余物用二氯甲烷(3X20mL)萃取。将合并的萃取物用Na2SO4干燥并减压浓缩。将残余物通过反相制备性-HPLC来纯化得到304(23.5mg,29%),其为白色固体。MS-ESI:[M+H]+628.8.1H NMR(500MHz,DMSO-d6)δ8.57(d,J=4.5Hz,1H),8.46(s,1H),8.23(s,1H),8.05(d,J=2.0Hz,1H),7.52(d,J=5.5Hz,1H),7.40(d,J=2.5Hz,1H),5.89(s,1H),4.87(s,1H),4.39(s,2H),3.92-3.90(m,2H),3.61(s,2H),3.59(s,3H),3.50(t,J=5.5Hz,2H),3.26(s,3H),2.92-2.89(m,4H),2.81(s,2H),2.68-2.66(m,2H),1.29(s,3H),1.28(s,3H).
实施例305a 6-氯-4-(5-(2-甲氧基乙基)-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-2-甲基哒嗪-3(2H)-酮305a
在配备有回流冷凝器的100-mL圆底烧瓶中装入5-(2-甲氧基乙基)-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-胺304b(392mg,2.0mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(446mg,2.0mmol)、碳酸铯(1.30g,4.0mmol)和1,4-二噁烷(40mL)。在使氮气鼓泡通过所述悬浮液10分钟后,加入xantphos(115mg,0.20mmol)和三(二亚苄基丙酮)二钯(0)(92mg,0.10mmol)。使体系经历三轮真空/氩气吹洗并在100℃加热5小时。然后将其冷却至室温并过滤。将固体用二氯甲烷(2X15mL)洗涤。将合并的滤液减压浓缩。将残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(80/1至30/1)洗脱)得到305a(412mg,61%),其为黄色固体。MS-ESI:[M+H]+338.9
实施例305b乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-(5-{[5-(2-甲氧基乙基)-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基]氨基}-1-甲基-6-氧代-1,6-二氢哒嗪-3-基)吡啶-3-基)甲酯305b
在配备有回流冷凝器的25-mL圆底烧瓶中装入305a(200mg,0.60mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(238mg,0.60mmol)、K3PO4(254mg,1.2mmol)、乙酸钠(98mg,1.2mmol)和Pd(dppf)Cl2(22mg,0.030mmol)和乙腈/水(8/0.5mL)。使体系经历三轮真空/氮气吹洗并在氮气保护下在100℃加热1小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将反应混合物冷却至室温并过滤。减压浓缩滤液。使残余物在二氯甲烷(30mL)和水(20mL)之间分配。将水层用二氯甲烷(2×30mL)萃取。将合并的有机萃取物用Na2SO4干燥,过滤并减压浓缩。将黑色残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(80/1至30/1)洗脱)得到305b(169mg,43%),其为黄色固体。MS-ESI:[M+H]+655.9
实施例305 3-[3-(羟基甲基)-4-[5-[[5-(2-甲氧基乙基)-6,7-二氢-4H-吡唑并[1,5-a]吡嗪-2-基]氨基]-1-甲基-6-氧代-哒嗪-3-基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮305
向305b(160mg,0.24mmol)于THF/异丙醇/水(6/4/3mL)中的溶液中加入氢氧化锂(29mg,1.2mmol)。将混合物在室温搅拌1小时并减压浓缩。使残余物在水(15mL)和乙酸乙酯(20mL)之间分配。将水相用乙酸乙酯(3X20mL)萃取。将合并的有机层干燥并减压浓缩。将残余物通过反相制备性-HPLC来纯化得到305,其为白色固体(88mg,60%)。MS-ESI:[M+H]+614.3.1H NMR(500MHz,CDCl3)δ8.56(d,J=5.0Hz,1H),7.99(s,1H),7.87(s,1H),7.44(d,J=5.0Hz,1H),6.84(s,1H),5.96(s,1H),4.59-4.57(m,3H),4.49-4.47(m,1H),4.17-4.12(m,4H),3.92-3.90(m,4H,重叠),3.77-3.75(m,2H),3.61-3.60(m,2H),3.41(s,3H),3.05-3.03(m,2H),2.81-2.79(m,2H),2.60-2.58(m,2H),2.52-2.50(m,2H),1.28(s,6H).
实施例306a乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{5-[(6-甲氧基哒嗪-3-基)氨基]-1-甲基-6-氧代-1,6-二氢吡啶-3-基}吡啶-3-基)甲酯306a
在配备有磁力搅拌子和回流冷凝器的25-mL单颈圆底烧瓶中装入6-甲氧基哒嗪-3-胺(65mg,0.52mmol)、XantPhos(29mg,0.050mmol)、Pd2dba3(45mg,0.050mmol)、乙酸[4-(5-溴-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-基]甲酯273a(281mg,0.52mmol)、Cs2CO3(326mg,1.0mmol)和1,4-二噁烷(10mL)。使氮气鼓泡通过所得混合物20分钟后,将其回流加热2小时。反应结束后,将混合物减压蒸发,并将残余物在乙酸乙酯(20mL)和水(10mL)之间分配。将乙酸乙酯减压浓缩并将残余物通过硅胶柱色谱法来纯化(用20:1二氯甲烷/甲醇洗脱)得到306a(180mg,60%)。MS-ESI:[M+H]+584.3.
实施例306 3-[3-(羟基甲基)-4-[5-[(6-甲氧基哒嗪-3-基)氨基]-1-甲基-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮306
将306a(180mg,0.32mmol)和氢氧化锂一水合物(84mg,2.0mmol)于THF(5mL)、异丙醇(5mL)和水(1.5mL)中的混合物在40℃搅拌0.5小时。将混合物减压蒸发,并将残余物在乙酸乙酯(20mL)和水(10mL)之间分配。将乙酸乙酯减压浓缩并将残余物通过反相制备性-HPLC来纯化得到306(80mg,49%)。MS-ESI:[M+H]+542.3.1H NMR(500MHz,DMSO-d6)δ8.86(s,1H),8.76(d,J=2.5Hz,1H),8.51(d,J=5.0Hz,1H),7.73(d,J=10.0Hz,1H),7.56(d,J=2.5Hz,1H),7.35(d,J=5.0Hz,1H),7.11-7.10(m,1H),6.56(s,1H),4.94-4.93(m,1H),4.48-4.45(m,1H),4.40-4.38(m,1H),4.25-4.18(m,3H),3.91(s,3H),3.86-3.84(m,1H),3.62(s,3H),2.58-2.56(m,2H),2.50-2.49(m,2H),1.21(s,6H).
实施例307a 1,3-二甲基-5-硝基-1H-吲唑307a
氮气保护下,向1-(2-氯-5-硝基苯基)乙酮(500mg,2.5mmol)于无水乙醇(15mL)中的溶液中加入1,1-二甲基肼盐酸盐(3.38g,35.0mmol)。将混合物回流加热10小时并减压蒸发得到粗制307a(3.0g),将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+192.2
实施例307b 1,3-二甲基-1H-吲唑-5-胺307b
氮气保护下,向307a(粗制,2.5mmol)于乙醇(95%,30mL)中的溶液中加入NH2NH2.水(1.25g,25.0mmol)、Pd/C(100mg)。将混合物在50℃搅拌1.5小时。然后将其冷却至室温并用垫过滤。减压浓缩滤液并将残余物用无水乙醇(5mL)重结晶得到307b,其为白色固体(340mg,两步的收率为84%)。MS-ESI:[M+H]+162.3
实施例307c 5-溴-3-(1,3-二甲基-1H-吲唑-5-基氨基-1-甲基吡嗪-2(1H)-酮307c
向307b(280mg,1.74mmol)于异丙醇(7mL)中的溶液中加入三乙胺(352mg,3.48mmol)和3,5-二溴-1-甲基吡嗪-2(1H)-酮(H-005)(700mg,2.61mmol)。回流搅拌6小时后,将混合物冷却至室温。过滤析出物,用异丙醇(2X2mL)洗涤并在60℃减压干燥得到307c,其为棕色固体(560mg,92%)。MS-ESI:[M+H]+347.8.
实施例307d乙酸(4-{6-[(1,3-二甲基-1H-吲唑-5-基)氨基]-4-甲基-5-氧代-4,5-二氢-吡嗪-2-基}-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-基)甲酯307d
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入307c(300mg,0.86mmol)、1,4-二噁烷(20mL)、水(1mL)、乙酸[4-(二羟基硼烷基)-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-基]甲酯199e(512mg,1.28mmol)和碳酸铯(560mg,1.72mmol)。在使氮气鼓泡通过所述悬浮液10分钟后,加入Cy3P(96mg,0.34mmol)和Pd2(dba)3(79mg,0.086mmol)。使体系经历三轮真空/氩气吹洗并回流加热3小时。然后将其冷却至室温并过滤。将固体用二氯甲烷(3X20mL)洗涤。将合并的滤液减压浓缩,将残余物通过硅胶柱色谱法来纯化(用100:1二氯甲烷/甲醇洗脱)得到307d(230mg,43%),其为黄色固体。MS-ESI:[M+H]+620.9
实施例307 3-[4-[6-[(1,3-二甲基吲唑-5-基)氨基]-4-甲基-5-氧代-吡嗪-2-基]-3-(羟基甲基)-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮307
将307d(230mg,0.37mmol)、氢氧化锂(89mg,3.7mmol)于异丙醇/THF(1:1,10mL)和水(2mL)中的混合物在室温搅拌1小时。将其过滤并减压浓缩滤液。将所得残余物通过来纯化反相制备性-HPLC得到307(41mg,19%),其为白色固体。MS-ESI:[M+H]+578.4.1H NMR(500MHz,CDCl3)δ8.58(d,J=2.0Hz,1H),8.56(d,J=5.0Hz,1H),8.37(s,1H),8.11(s,1H),7.88(d,J=5.0Hz,1H),7.51(dd,J=2.0,9.0Hz,1H),7.33(d,J=9.0Hz,1H),6.86(s,1H),5.17-5.14(m,1H),4.75-4.73(m,1H),4.55-4.52(m,1H),4.48-4.43(m,1H),4.20-4.16(m,2H),4.02(s,3H),3.92-3.70(m,1H),3.70(s,3H),2.60(d,J=7.0Hz,2H),2.57(s,3H),2.54(s,2H),1.30(s,6H).
实施例308a 2-{4,4-二甲基-9-氧代-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-10-基}-4-(5-{[5-(2-甲氧基乙基)-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基]氨基}-1-甲基-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-甲醛308a
按照实施例304中的操作,以4-氯-2-{4,4-二甲基-9-氧代-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-10-基}吡啶-3-甲醛109a(250mg,0.693mmol)和3-(5-(2-甲氧基乙基)-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮304d(595mg,0.1.386mmol)开始,获得308a,其为黄色固体(250mg,57%)。MS-ESI:[M+H]+628.3
实施例308 3-[3-(羟基甲基)-4-[5-[[5-(2-甲氧基乙基)-6,7-二氢-4H-吡唑并[1,5-a]吡嗪-2-基]氨基]-1-甲基-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]噻吩并[1,3-c]吡啶-4-酮308
按照实施例304中的操作,以308a(230mg,0.366mmol)和NaBH4(27.7mg,0.732mmol)开始获得308,其为白色固体(53.2mg,23%)。MS-ESI:[M+H]+629.8.1H NMR(500MHz,DMSO-d6)δ8.49(d,J=5.0Hz,1H),8.19(s,1H),8.04(d,J=2.0Hz,1H),7.37(d,J=2.5Hz,1H),7.34(d,J=5.0Hz,1H),5.89(s,1H),4.95-4.93(m,1H),4.47-4.39(m,2H),4.20-4.14(m,1H),3.92-3.91(m,2H),3.84-3.80(m,1H),3.61(s,2H),3.58(s,3H),3.51-3.49(m,2H),3.25(s,3H),3.06-3.00(m,1H),2.91-2.87(m,3H),2.77(s,2H),2.68-2.53(m,4H),1.19(s,3H),1.18(s,3H).
实施例309a 5-(3-甲氧基丙基)-2-硝基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪309a
在配备有磁力搅拌子的微波小瓶中装入1-(2-溴乙基)-5-(氯甲基)-3-硝基-1H-吡唑296c(600mg,2.2mmol)、3-甲氧基丙烷-1-胺(595mg,6.6mmol)和DMSO(6mL)。将其在微波照射下在120℃加热0.5小时。然后将混合物冷却至室温并用乙酸乙酯(30mL)稀释。将所得混合物用水(3X10ml)洗涤。干燥有机层并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用30:1二氯甲烷/甲醇洗脱)得到309a(350mg,66%),其为黄色固体。MS-ESI:[M+H]+241.1
实施例309b 5-(3-甲氧基丙基)-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-胺309b
向309a(300mg,1.25mmol)于乙醇(20mL)中的溶液中加入Pd/C(10%,30mg)。向反应混合物中充入氢气(通过气囊)并在室温搅拌1小时。反应完成后,用塞过滤混合物。减压浓缩滤液得到309b,其为黄色固体(250mg,92%),将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+211.3
实施例309c 5-溴-3-(5-(3-甲氧基丙基)-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基-氨基)-1-甲基吡啶-2(1H)-酮309c
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入3,5-二溴-1-甲基吡啶-2(1H)-酮(320mg,1.2mmol)、309b(250mg,1.2mmol)、三(二亚苄基丙酮)二钯(0)(55mg,0.060mmol)、xantphos(70mg,0.12mmol)、碳酸铯(782mg,2.4mmol)和1,4-二噁烷(20mL)。使体系经历三轮真空/氩气吹洗并在100℃加热5小时。然后将其冷却至室温并过滤。将固体用二氯甲烷(2X10mL)洗涤。将合并的滤液减压浓缩。将残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(80:1至30:1)洗脱)得到309c(200mg,42%),其为黄色固体。MS-ESI:[M+H]+396.2
实施例309d乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-(5-{[5-(3-甲氧基丙基)-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基]氨基}-1-甲基-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-基)甲酯309d
在配备有回流冷凝器的25-mL圆底烧瓶中装入309c(120mg,0.30mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(240mg,0.60mmol)、K3PO4(127mg,0.60mmol)、乙酸钠一水合物(82mg,0.60mmol)、Pd(dppf)Cl2(12mg,0.015mmol)和乙腈/水(8/0.5mL)。使体系经历三轮真空/氮气吹洗并在氮气保护下在100℃加热2小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将反应混合物冷却至室温并减压浓缩。使残余物在二氯甲烷(20mL)和水(10mL)之间分配。将水层用二氯甲烷(2×10mL)萃取。将合并的有机萃取物用Na2SO4干燥,过滤并减压浓缩。将黑色残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(80:1至30:1)洗脱)得到309d(150mg,74%),其为黄色固体。MS-ESI:[M+H]+668.9
实施例309 3-[3-(羟基甲基)-4-[5-[[5-(3-甲氧基丙基)-6,7-二氢-4H-吡唑并[1,5-a]吡嗪-2-基]氨基]-1-甲基-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮309
向309d(120mg,0.18mmol)于THF/异丙醇/水(5/3/3mL)中的溶液中加入氢氧化锂一水合物(76mg,1.8mmol)。将混合物在30℃搅拌1小时。反应完成后,过滤混合物并减压蒸发溶剂。将残余物通过反相制备性-HPLC来纯化得到309,其为白色固体(85mg,76%)。MS-ESI:[M+H]+627.3.1H NMR(500MHz,CDCl3)δ8.48(d,J=5.0Hz,1H),7.95(d,J=2.0Hz,1H),7.72(d,J=2.0Hz,1H),7.42(s,1H),7.35(d,J=5.0Hz,1H),6.86(s,1H),5.71(s,1H),5.05(t,J=6.0Hz,1H),4.66-4.64(m,1H),4.52-4.50(m,1H),4.36-4.32(m,1H),4.17-4.16(m,2H),4.08-4.06(m,2H),3.88-3.85(m,1H),3.71(s,3H),3.65-3.64(m,2H),3.48(t,J=6.0Hz,2H),3.36(s,3H),2.93(t,J=6.0Hz,2H),2.65-2.62(m,2H),2.59-2.58(m,2H),2.53(s,2H),1.87-1.83(m,2H),1.29(s,6H).
实施例310a乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{1-甲基-5-[(5-甲基-1,2-噻唑-3-基)氨基]-6-氧代-1,6-二氢吡啶-3-基}吡啶-3-基)甲酯310a
在25-mL密封管中装入乙酸[4-(5-溴-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-基]甲酯273a(150mg,0.28mmol)、5-甲基异噻唑-3-胺盐酸盐(55mg,0.33mmol)、Cs2CO3(183mg,0.56mmol)、Pd2(dba)3(27mg,0.030mmol)、XantPhos(35mg,0.060mmol)和二噁烷(10mL)。在经历三轮真空/氩气吹洗后,将混合物在微波照射下在110℃加热0.5小时。将其冷却至室温并减压蒸发。将残余物通过硅胶柱来纯化(用20:1二氯甲烷/甲醇洗脱)得到310a,其为黄色固体(50mg,31%)。MS-ESI:[M+H]+573.2.
实施例310 3-[3-(羟基甲基)-4-[1-甲基-5-[(5-甲基异噻唑-3-基)氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮310
向310a(50mg,0.090mmol)于THF/异丙醇/水(4mL/4mL/1mL)中的溶液中加入氢氧化锂(21mg,0.90mmol)。将反应混合物在室温搅拌0.5小时并减压浓缩。将残余物用水(10mL)稀释并用乙酸乙酯(3X20mL)萃取。将合并的有机层用Na2SO4干燥并减压浓缩得到黄色固体,将其通过反相制备性-HPLC来纯化得到310,其为黄色固体(20mg,43%)。MS-ESI:[M+H]+530.8.1H NMR(500MHz,CDCl3)δ8.61(d,J=2.0Hz,1H),8.49(d,J=5.5Hz,1H),8.05(s,1H),7.93(d,J=2.0Hz,1H),7.37(d,J=5.0Hz,1H),6.84(s,1H),6.51(s,1H),5.09-5.06(m,1H),4.66-4.47(m,2H),4.28-4.27(m,1H),4.17-4.12(m,2H),3.89-3.82(m,1H),3.71(s,3H),2.57(d,J=6.0Hz,2H),2.52-2.50(m,重叠,5H),1.27(s,6H).
实施例311a乙酸(4-{5-[(5-环丙基-1,2-噁唑-3-基)氨基]-1-甲基-6-氧代-1,6-二氢-吡啶-3-基}-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-基)甲酯311a
在配备有磁力搅拌子和回流冷凝器的25-mL单颈圆底烧瓶中装入5-环丙基异噁唑-3-胺(80mg,0.65mmol)、XantPhos(29mg,0.050mmol)、Pd2dba3(45mg,0.050mmol)、乙酸[4-(5-溴-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-基]甲基酯273a(350mg,0.65mmol)、Cs2CO3(390mg,1.2mmol)和1,4-二噁烷(10mL)。使氮气鼓泡通过所得混合物10分钟后,将其回流加热2小时。然后减压蒸发混合物,并将残余物在乙酸乙酯(20mL)和水(10mL)之间分配。减压浓缩有机层并将残余物通过硅胶柱色谱法来纯化(用20:1二氯甲烷/甲醇洗脱)得到311a(120mg,32%),其为棕色固体。MS-ESI:[M+H]+583.2.
实施例311 3-[4-[5-[(5-环丙基异噁唑-3-基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮311
将311a(120mg,0.20mmol)和氢氧化锂一水合物(80mg,2.0mmol)于THF(5mL)、异丙醇(5mL)和水(1.5mL)中的混合物在40℃搅拌0.5小时。将混合物减压蒸发并将残余物用水(5mL)稀释。然后将其用乙酸乙酯(2X10mL)萃取。将合并的萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到311(65mg,58%),其为浅黄色固体。MS-ESI:[M+H]+541.3.1HNMR(500MHz,DMSO-d6)δ8.92(s,1H),8.48(d,J=5.0Hz,1H),7.99(d,J=2.0Hz,1H),7.55(d,J=2.0Hz,1H),7.31(d,J=5.0Hz,1H),6.56(s,1H),6.19(s,1H),4.92-4.90(m,1H),4.45-4.44(m,1H),4.40-4.39(m,1H),4.24-4.18(m,3H),3.86-3.83(m,1H),3.59(s,3H),2.58-2.56(m,2H),2.44-243(m,2H),2.07-2.04(m,1H),1.22(s,6H)1.03-0.99(m,2H),0.84-0.81(m,2H).
实施例312a 5-溴-1-甲基-3-(5-甲基-1-(氧杂环丁烷-3-基)-1H-吡唑-3-基氨基)吡啶-2(1H)-酮312a
将5-溴-1-甲基-3-(5-甲基-1H-吡唑-3-基氨基)吡啶-2(1H)-酮115a(200mg,0.71mmol)、3-碘氧杂环丁烷(647mg,3.53mmol)、Cs2CO3(1150mg,3.53mmol)和乙腈(5mL)的混合物在密封管中在80℃加热整夜。然后将混合物冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用20:1二氯甲烷/甲醇洗脱)得到312a,其为黄色固体(120mg,50%)。MS-ESI:[M+H]+339.1
实施例312b乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-(1-甲基-5-{[5-甲基-1-(氧杂环丁烷-3-基)-1H-吡唑-3-基]氨基}-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-基)甲酯312b
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入312a(170mg,0.50mmol)、(2-{4,4-二甲基-9-氧代-1,{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(200mg,0.50mmol)、CH3COONa(82mg,1.00mmol)、PdCl2(dppf)(41mg,0.050mmol)、K3PO4(212mg,1.00mmol)、乙腈(10mL)和水(0.5mL)。使氮气鼓泡通过所得混合物20分钟后,将其在氮气中在100℃加热2小时。将混合物冷却至室温并过滤。减压蒸发滤液并将残余物通过硅胶柱色谱法来纯化(用50:1二氯甲烷/甲醇洗脱)得到312b,其为白色固体(172mg,56%)。MS-ESI:[M+H]+612.4
实施例312 3-[3-(羟基甲基)-4-[1-甲基-5-[[5-甲基-1-(氧杂环丁烷-3-基)吡唑-3-基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮312
将312b(90mg,0.15mmol)和氢氧化锂(14mg,0.60mmol)于异丙醇/THF/水(6/4/2mL)中的混合物在室温搅拌0.5小时。将混合物减压浓缩。使残余物在水(10mL)和二氯甲烷(3X20mL)之间分配。将合并的二氯甲烷萃取物减压浓缩,并将残余物通过反相制备性-HPLC来纯化得到312,其为白色固体(54mg,64%)。MS-ESI:[M+H]+569.9.1H NMR(500MHz,DMSO-d6)δ8.47(d,J=5.0Hz,1H),8.24(d,J=2.0Hz,1H),8.23(s,1H),7.48(d,J=1.5Hz,1H),7.36(d,J=5.0Hz,1H),6.55(s,1H),5.95(s,1H),5.46-5.42(m,1H),4.99-4.91(m,3H),4.81-4.78(m,2H),4.52-4.41(m,2H),4.24-4.18(m,3H),3.87-3.84(m,1H),3.60(s,3H),2.61-2.56(m,2H),2.43(s,2H),2.15(s,3H),1.22(s,3H),1.19(s,3H).
实施例313a 2-(5-(羟基甲基)-3-硝基-1H-吡唑-1-基)乙酸乙酯313a
在配备有磁力搅拌子的100-mL单颈圆底烧瓶中装入乙腈(30mL)、(3-硝基-1H-吡唑-5-基)甲醇(1.43g,10.0mmol)、Cs2CO3(490mg,1.5mmol)和2-溴乙酸乙酯(2.00g,12mmol)。将混合物在40℃搅拌5小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用30:1二氯甲烷/甲醇洗脱)得到313a(1.65g,72%),其为黄色固体。MS-ESI:[M+H]+229.9
实施例313b 2-(5-(氯甲基)-3-硝基-1H-吡唑-1-基)乙酸乙酯313b
向在0℃冷却的313a(1.50g,6.55mmol)于CHCl3(60mL)中的混合物中加入SOCl2(2.34g,19.6mmol),同时维持内部温度低于5℃。将该反应混合物温热至50℃并在该温度搅拌3小时。然后将其冷却至0℃并用水淬灭。分离有机层并减压蒸发。将残余物通过硅胶柱色谱法来纯化(用30:1二氯甲烷/甲醇洗脱)得到313b(1.1g,68%),其为黄色固体。MS-ESI:[M+H]+247.9
实施例313c 5-甲基-2-硝基-4,5-二氢吡唑并[1,5-a]吡嗪-6(7H)-酮313c
向313b(1.0g,4.0mmol)于二氯甲烷(30mL)中的溶液中加入CH3NH2的溶液(1.07g,12.0mmol,35%于甲醇中)。将该反应混合物在室温搅拌3小时并用水(30mL)稀释。分离出有机层,用Na2SO4干燥并减压浓缩。将残余物通过硅胶柱色谱法来纯化(用30:1二氯甲烷/甲醇洗脱)得到313c(450mg,57%),其为黄色固体。MS-ESI:[M+H]+196.9
实施例313d 2-氨基-5-甲基-4,5-二氢吡唑并[1,5-a]吡嗪-6(7H)-酮313d
向313c(450mg,2.3mmol)于乙醇(30mL)中的溶液中加入Pd/C(10%,400mg)。向反应混合物中充入氢气(通过气囊)并在室温搅拌2小时。反应完成后,将混合物用塞过滤并减压浓缩滤液得到313d,其为黄色固体(320mg,84%),将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+167.1
实施例313e 2-(5-溴-1-甲基-2-氧代-1,2-二氢吡啶-3-基氨基)-5-甲基-4,5-二氢吡唑并[1,5-a]吡嗪-6(7H)-酮313e
在配备有磁力搅拌子和回流冷凝器的100-mL圆底烧瓶中装入313d(300mg,1.8mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(482mg,1.8mmol)、碳酸铯(1.17g,3.6mmol)和1,4-二噁烷(20mL)。在使氮气鼓泡通过所述悬浮液10分钟后,加入xantphos(104mg,0.18mmol)和三(二亚苄基丙酮)二钯(0)(82mg,0.090mmol)。使体系经历三轮真空/氩气吹洗并回流加热5小时。然后将其冷却至室温并过滤。将固体用二氯甲烷(2X30m)洗涤。将合并的滤液减压浓缩。将残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(80/1至30/1)洗脱)得到313e(390mg,61%),其为黄色固体。
实施例313f乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-[1-甲基-5-({5-甲基-6-氧代-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]吡啶-3-基)甲酯313f
在配备有磁力搅拌子和回流冷凝器的25-mL单颈圆底烧瓶中装入313e(150mg,0.43mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(170mg,0.43mmol)、K3PO4(183mg,0.86mmol)、乙酸钠(71mg,0.86mmol)、Pd(dppf)Cl2(35mg,0.043mmol)、乙腈(10mL)和水(0.5mL)。使体系经历三轮真空/氮气吹洗并在100℃加热3小时。之后,将反应混合物冷却至室温并过滤。减压浓缩滤液。将残余物通过硅胶柱色谱法来纯化(用30:1二氯甲烷/甲醇洗脱)得到313f(131mg,49%),其为黄色固体。MS-ESI:[M+H]+625.3.
实施例313 3-[3-(羟基甲基)-4-[1-甲基-5-[(5-甲基-6-氧代-4,7-二氢吡唑并[1,5-a]吡嗪-2-基)氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮313
将313f(130mg,0.21mmol)和氢氧化锂(10mg,0.42mmol)于异丙醇/THF(1:1,7mL)和水(2mL)中的混合物在0℃搅拌0.5小时。将混合物减压浓缩。使残余物在水(10mL)和乙酸乙酯(3X10mL)之间分配。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到313(60mg,49%),其为白色固体。MS-ESI:[M+H]+582.8.1H NMR(500MHz,DMSO-d6)δ8.48(d,J=5.0Hz,1H),8.37(s,1H),8.10(d,J=2.0Hz,1H),7.43(d,J=2.5Hz,1H),7.33(d,J=5.0Hz,1H),6.57(s,1H),6.07(s,1H),4.95(bs,1H),4.62-4.54(m,4H),4.46-4.42(m,2H),4.24-4.19(m,3H),3.89-3.82(m,1H),3.60(s,3H),2.99(s,3H),2.60-2.57(m,2H),2.45-2.44(m,2H),1.23(s,6H).
实施例314a 1-(6-硝基吡啶-3-基)氮杂环丁烷-3-醇314a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入乙腈(50mL)、5-氟-2-硝基吡啶(1.2g,7.9mmol)、K2CO3(2.1g,15.8mmol)和氮杂环丁烷-3-醇盐酸盐(1.3g,11.9mmol)。将混合物在60℃加热1小时。之后,将反应混合物冷却至室温。然后将其过滤并减压蒸发滤液。将残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(50:1至20:1)洗脱)得到314a(1.1g,73%),其为黄色固体。MS-ESI:[M+H]+196.0.
实施例314b 1-(6-氨基吡啶-3-基)氮杂环丁烷-3-醇314b
将100-mL单颈圆底烧瓶用氮气吹洗并装入314a(1.0g,5.1mmol)、10%钯/炭(10%水分,100mg)和乙醇(40mL)。将所述混合物排空、充入氢气并在室温搅拌5小时。然后将氢气排空并将氮气充入所述烧瓶中。通过用垫过滤除去催化剂,减压浓缩滤液得到314b,其为黄色固体(792mg,85%)。MS-ESI:[M+H]+166.1.
实施例314c 5-溴-3-(5-(3-羟基氮杂环丁烷-1-基)吡啶-2-基氨基)-1-甲基吡啶-2(1H)-酮314c
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入314b(792mg,4.8mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(1.9g,7.2mmol)、三-(二亚苄基丙酮)二钯(0)(440mg,0.48mmol)、XantPhos(555mg,0.96mmol)、Cs2CO3(3.1g,9.6mmol)和1,4-二噁烷(40mL)。在经历三轮真空/氩气吹洗后,将混合物在90℃加热3.0小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(50:1至20:1)洗脱)得到314c,其为黄色固体(1.5g,89%)。MS-ESI:[M+H]+351.1
实施例314d乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-(5-{[5-(3-羟基氮杂环丁烷-1-基)吡啶-2-基]氨基}-1-甲基-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-基)甲酯314d
在配备有回流冷凝器的50-mL圆底烧瓶中装入314c(176mg,0.50mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(198mg,0.50mmol)、Pd(dppf)Cl2(41mg,0.050mmol)、K3PO4(212.0mg,1.0mmol)、乙酸钠(82.0mg,1.0mmol)、水(0.5mL)和乙腈(10mL)。在经历三轮真空/氩气吹洗后,将混合物在95℃加热1小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用30:1二氯甲烷/甲醇洗脱得到粗制314d,其为棕色固体,将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+623.8.
实施例314 3-[4-[5-[[5-(3-羟基氮杂环丁烷-1-基)-2-吡啶基]氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮314
将314d(粗制产物,311.5mg,0.50mmol)和氢氧化锂水合物(300mg,12.5mmol)于异丙醇/THF/水(2:2:1,10mL)中的混合物在室温搅拌30分钟。将混合物减压浓缩。使残余物在水(10mL)和二氯甲烷(3X10mL)之间分配。将合并的萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到314(46mg,两步:16%),其为黄色固体。MS-ESI:[M+H]+581.9.1H NMR(500MHz,DMSO-d6)δ8.54(d,J=2.5Hz,1H),8.47(d,J=5.0Hz,1H),7.78(d,J=2.5Hz,1H),7.70(s,1H),7.54(d,J=2.5Hz,1H),7.35(d,J=5.0Hz,1H),6.83-6.81(m,2H),6.75(d,J=8.5Hz,1H),5.04-5.02(m,1H),4.77-4.75(m,1H),4.64-4.62(m,1H),4.50-4.48(m,1H),4.34-4.32(m,1H),4.17-4.14(m,4H),3.86-3.83(m,1H),3.70(s,3H),3.64-3.62(m,2H),2.57-2.56(m,2H),2.51(s,2H),2.31-2.30(m,1H),1.27(s,6H).
实施例315 3-[3-(羟基甲基)-4-[1-甲基-5-[[1-甲基-5-(吡咯烷-1-羰基)吡唑-3-基]氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮315
按照实施例273的操作,用(3-氨基-1-甲基-1H-吡唑-5-基)(吡咯烷-1-基)甲酮代替2-氨基吡啶制备了315。27.3mg,60%收率。1H NMR(400MHz,DMSO-d6)δ8.48(d,J=5.1Hz,1H),8.23(s,1H),8.05(d,J=2.4Hz,1H),7.43(d,J=2.4Hz,1H),7.34(d,J=5.1Hz,1H),6.55(s,1H),6.46(s,1H),4.95(t,J=5.2Hz,1H),4.42–4.47(m,1H),4.17–4.21(m,3H),3.79(s,2H),3.59(s,3H),3.48(dt,J=11.1,6.6Hz,3H),3.27(s,2H),2.57(d,J=7.5Hz,2H),2.43(s,2H),1.90–1.84(m,3H),1.22(s,6H).ES-MS m/z 611.4[M+1].
实施例316 3-[3-(羟基甲基)-4-[5-[[5-(甲氧基甲基)-1-甲基-吡唑-3-基]氨基]-1-甲基-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮316
按照实施例273的操作,用5-(甲氧基甲基)-1-甲基-1H-吡唑-3-胺代替2-氨基吡啶制备了316。43.2mg,84%收率。1H NMR(400MHz,DMSO-d6)δ8.47(d,J=5.0Hz,1H),8.15(s,1H),8.04(d,J=2.4Hz,1H),7.39(d,J=2.1Hz,1H),7.33(d,J=5.0Hz,1H),6.55(s,1H),6.11(s,1H),4.96–4.90(m,1H),4.38–4.46(m,1H),4.38(s,2H),4.19(d,J=9.8Hz,2H),3.82–3.96(m,1H),3.65(s,3H),3.58(s,3H),3.27(s,2H),2.57(d,J=7.5Hz,2H),2.43(s,2H),1.22(s,6H).ES-MS m/z 558.3[M+1].
实施例317a 5-甲基-2-(1-甲基-2-氧代-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)-1,2-二氢吡啶-3-基氨基)-4,5-二氢吡唑并[1,5-a]吡嗪-6(7H)-酮317a
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入2-(5-溴-1-甲基-2-氧代-1,2-二氢吡啶-3-基氨基)-5-甲基-4,5-二氢吡唑并[1,5-a]吡嗪-6(7H)-酮313e(270mg,1.0当量,0.68mmol)、Pin2B2(863.6mg,5.0当量,3.4mmol)、Pd2(dba)3(62.4mg,0.1当量,0.068mmol)、X-Phos(64.8mg,0.2当量,0.14mmol)、乙酸钾(200mg,3.0当量,2.04mmol)和二噁烷(15mL)。在经历三轮真空/氩气吹洗后,将混合物在65℃加热3小时。然后将其冷却至室温并过滤。减压浓缩滤液得到粗制317a,将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+399.9.
实施例317b 2-{4,4-二甲基-9-氧代-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-10-基}-4-[1-甲基-5-({5-甲基-6-氧代-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基}氨基)-6-氧代-1,6-二氢吡啶-3-基]吡啶-3-甲醛317b
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入317a(100mg,0.28mmol)、4-氯-2-{4,4-二甲基-9-氧代-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-10-基}吡啶-3-甲醛109a(112mg,0.28mmol)、Pd(dppf)Cl2(22.9mg,0.028mmol)、K3PO4(118.7mg,0.56mmol)、乙酸钠(45.9mg,0.56mmol)、水(0.5mL)和乙腈(10mL)。在经历三轮真空/氩气吹洗后,将混合物回流加热1小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(50:1至30:1)洗脱)得到317b,其为黄色固体(60mg,36%)。MS-ESI:[M+H]+597.8.
实施例317 3-[3-(羟基甲基)-4-[1-甲基-5-[(5-甲基-6-氧代-4,7-二氢吡唑并[1,5-a]吡嗪-2-基)氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]噻吩并[1,3-c]吡啶-4-酮317
将317b(60mg,0.10mmol)和NaBH4(11.3mg,0.30mmol)于甲醇(5mL)中的混合物在室温搅拌30分钟。将混合物用水(15mL)淬灭并减压浓缩。将残余物用二氯甲烷(3X10mL)萃取。将合并的萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到317(15mg,25%),其为黄色固体。MS-ESI:[M+H]+599.8.1H NMR(500MHz,CDCl3)δ8.50(d,J=5.0Hz,1H),8.0(d,J=2.0Hz,1H),7.69(d,J=2.5Hz,1H),7.50(s,1H),7.34(d,J=5.0Hz,1H),5.86(s,1H),4.82-4.66(m,4H),4.56(s,2H),4.42-4.33(m,2H),3.83-3.81(m,1H),3.70(s,3H),3.15(s,3H),2.98-2.94(m,2H),2.80(s,2H),2.57-2.52(m,2H),1.28(s,6H).
实施例318a乙酸{4-[5-({4,5-二甲基-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基}氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-基}甲酯318a
在配备有回流冷凝器的50-mL圆底烧瓶中装入4,5-二甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-胺287i(123mg,1.0当量,0.74mmol)、乙酸[4-(5-溴-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-基]甲酯273a(400mg,1.0当量,0.74mmol)、Pd2(dba)3(68mg,0.1当量,0.074mmol)、Xantphos(86mg,0.2当量,0.148mmol)、Cs2CO3(487mg,2.0当量,1.48mmol)和二噁烷(15mL)。在经历三轮真空/氮气吹洗后,将混合物在100℃搅拌2小时。将混合物冷却至室温并过滤。减压浓缩滤液。将所得残余物通过硅胶柱色谱法来纯化(用20:1乙酸乙酯/甲醇洗脱)得到318a,其为棕色固体(221mg,48%)。MS-ESI:[M+H]+624.9
实施例318b 10-{4-[5-({4,5-二甲基-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基}氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基]-3-(羟基甲基)吡啶-2-基}-4,4-二甲基-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-9-酮318b
在配备有磁力搅拌子的25-mL单颈圆底烧瓶中装入318a(200mg,1.0当量,0.32mmol)、氢氧化锂(38mg,5.0当量,1.60mmol)、异丙醇/THF(8/8mL)和水(2mL)。将混合物在室温搅拌1小时并减压浓缩。使残余物在水和二氯甲烷之间分配。将合并的有机层减压浓缩。将残余物通过反相制备性-HPLC来纯化得到外消旋混合物318b,其为黄色固体(91mg,43%)。
实施例318(R)-2-(5-((4,5-二甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基)氨基)-3'-(羟基甲基)-1-甲基-6-氧代-1,6-二氢-[3,4'-联吡啶]-2'-基)-7,7-二甲基-2,3,4,6,7,8-六氢-1H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮318
手性HPLC(柱:OZ-H,100%甲醇(0.1%乙酸乙酯))拆分318b分离出对映异构体318和319。318:MS-ESI:[M+H]+582.8.1H NMR(500MHz,CDCl3)δ8.49(d,J=5.0Hz,1H),7.99(s,1H),7.72(d,J=2.5Hz,1H),7.44(s,1H),7.36(d,J=5.0Hz,1H),6.86(s,1H),5.74(s,1H),5.04(t,J=6.5Hz,1H),4.66-4.64(m,1H),4.52-4.48(m,1H),4.36-4.34(m,1H),4.18-4.05(m,重叠,4H),3.88-3.86(m,1H),3.72(s,3H),3.43-3.41(m,1H),3.17-3.15(m,1H),2.87-2.85(m,1H),2.60-2.59(m,2H),2.53(s,2H),2.48(s,3H),1.46(d,J=6.5Hz,3H),1.29(s,6H).
实施例319(S)-2-(5-((4,5-二甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基)氨基)-3'-(羟基甲基)-1-甲基-6-氧代-1,6-二氢-[3,4'-联吡啶]-2'-基)-7,7-二甲基-2,3,4,6,7,8-六氢-1H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮319
手性HPLC(柱:OZ-H,100%甲醇(0.1%乙酸乙酯))拆分外消旋318b分离出对映异构体318和319。319:MS-ESI:[M+H]+582.8.1H NMR(500MHz,CDCl3)δ8.49(d,J=5.0Hz,1H),7.99(s,1H),7.72(d,J=2.5Hz,1H),7.44(s,1H),7.36(d,J=5.0Hz,1H),6.86(s,1H),5.74(s,1H),5.04(t,J=6.5Hz,1H),4.67-4.65(m,1H),4.52-4.48(m,1H),4.36-4.34(m,1H),4.18-4.05(m,重叠,4H),3.88-3.86(m,1H),3.72(s,3H),3.43-3.41(m,1H),3.17-3.15(m,1H),2.87-2.85(m,1H),2.60-2.59(m,2H),2.53(s,2H),2.48(s,3H),1.46(d,J=6.5Hz,3H),1.30(s,6H).
实施例320a(6-氨基吡啶-3-基)((3R,5S)-3,5-二甲基吗啉代)甲酮320a
在室温,向(3S,5R)-3,5-二甲基吗啉(1.15g,10mmol)于DMF(15mL)中的溶液中加入HATU(3.8g,10mmol)、DIPEA(2.6g,20mmol)和6-氨基吡啶-3-甲酸(1.38g,10mmol)。将反应混合物搅拌18小时。然后将其过滤并用Combiflash纯化所述滤液(A:1‰NH4HCO3/水,B:乙腈)得到320a(650mg,27%),其为黄色固体。MS-ESI:[M+H]+236.1.
实施例320b 5-溴-3-(5-((3R,5S)-3,5-二甲基吗啉-4-羰基)吡啶-2-基氨基)-1-甲基吡啶-2(1H)-酮320b
在配备有磁力搅拌子和回流冷凝器的50-mL圆底烧瓶中装入320a(160mg,1.0当量,0.68mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(273mg,1.5当量,1.02mmol)、Pd2(dba)3(64mg,0.1当量,0.070mmol)、Xantphos(79mg,0.2当量,0.14mmol)、Cs2CO3(444mg,2.0当量,1.36mmol)和二噁烷(20mL)。在三轮真空/氮气吹洗后,将混合物在100℃加热2小时。然后将其冷却至室温并过滤。减压蒸发滤液并将残余物通过硅胶柱色谱法来纯化(用乙酸乙酯洗脱)得到320b(190mg,66%),其为黄色固体。MS-ESI:[M+H]+420.8.
实施例320c乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{5-[(5-{[(3R,5S)-3,5-二甲基吗啉-4-基]羰基}吡啶-2-基)氨基]-1-甲基-6-氧代-1,6-二氢吡啶-3-基}吡啶-3-基)甲酯320c
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入320b(150mg,1.0当量,0.36mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(286mg,2.0当量,0.72mmol)、PdCl2(dppf)(29mg,0.10当量,0.040mmol)、K3PO4(153mg,2.0当量,0.72mmol)、乙酸钠(59mg,2.0当量,0.72mmol)、乙腈(10mL)和水(0.2mL)。在三轮真空/氮气吹洗后,将混合物在90℃加热2小时。然后将其冷却至室温并过滤。减压蒸发滤液并将残余物通过硅胶柱色谱法来纯化(用50:1二氯甲烷/甲醇洗脱)得到320c(161mg,64%),其为棕色固体。MS-ESI:[M+H]+693.8
实施例320 3-[4-[5-[[5-[(3S,5R)-3,5-二甲基吗啉-4-羰基]-2-吡啶基]氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮320
在配备有磁力搅拌子的25-mL单颈圆底烧瓶中装入320b(145mg,1.0当量,0.21mmol)、氢氧化锂(26mg,5.0当量,1.05mmol)、THF(4.0mL)、异丙醇(4.0mL)和水(1.0mL)。将混合物在室温搅拌1小时并过滤。减压浓缩滤液。将所得残余物用水(10mL)稀释并用二氯甲烷(3X15mL)萃取。将合并的有机层减压浓缩。将残余物通过反相制备性-HPLC来纯化得到320(35mg,26%),其为白色固体。MS-ESI:[M+H]+651.9
实施例321a 6-氯-4-(5-((3R,5S)-3,5-二甲基吗啉-4-羰基)吡啶-2-基氨基)-2-甲基哒嗪-3(2H)-酮321a
在配备有磁力搅拌子和回流冷凝器的25-mL圆底烧瓶中装入(6-氨基吡啶-3-基)((3R,5S)-3,5-二甲基吗啉代)甲酮320a(235mg,1.0mmol)、4-溴-6-氯-2-甲基哒嗪-3(2H)-酮(232mg,1.05mmol)、碳酸铯(652mg,2.0mmol)和1,4-二噁烷(6.0mL)。在使氮气鼓泡通过所述悬浮液10分钟后,加入Xantphos(116mg,0.20mmol)和三(二亚苄基丙酮)二钯(0)(70mg,0.10mmol)。使体系经历三轮真空/氮气吹洗并回流加热2.5小时。然后将其冷却至室温并过滤。将固体用二氯甲烷(3X10ml)洗涤。将合并的有机层减压浓缩。将残余物通过硅胶柱色谱法来纯化(用石油醚/乙酸乙酯(2:1至1:10)洗脱)得到321a(140mg,37%),其为黄色固体。MS-ESI:[M+H]+378.3
实施例321b乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{5-[(5-{[(3R,5S)-3,5-二甲基吗啉-4-基]羰基}吡啶-2-基)氨基]-1-甲基-6-氧代-1,6-二氢哒嗪-3-基}吡啶-3-基)甲酯321b
在配备有回流冷凝器的50-mL圆底烧瓶中装入321a(140mg,0.37mmol)、乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-3-基)甲酯199e(355mg,0.74mmol)、K3PO4(157mg,0.74mmol)、乙酸钠(61mg,0.74mmol)、1,1’-二(二苯基膦基)二茂铁二氯化钯(II)(36mg,0.040mmol)、乙腈(10mL)和水(0.2mL)。使体系经历三轮真空/氮气吹洗并在氮气保护下在100℃加热1.5小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将反应混合物冷却至室温并减压浓缩。使残余物在二氯甲烷(30mL)和水(30mL)之间分配。分离出水层并用二氯甲烷(3×20mL)萃取。将合并的有机层用Na2SO4干燥,过滤并减压浓缩。将黑色残余物通过硅胶柱色谱法来纯化(用60:1二氯甲烷/甲醇洗脱)得到320b(105mg,41%),其为黑色固体。MS-ESI:[M+H]+695.3
实施例321 3-[4-[5-[[5-[(3S,5R)-3,5-二甲基吗啉-4-羰基]-2-吡啶基]氨基]-1-甲基-6-氧代-哒嗪-3-基]-3-(羟基甲基)-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮321
在室温,向321b(105mg,0.15mmol)于THF/异丙醇/水(2/1/0.5mL)中的溶液中加入氢氧化锂(36mg,1.5mmol)。在将反应混合物搅拌3小时后,LCMS表明反应完成。然后将混合物倒入水(25mL)中并用二氯甲烷(3X20mL)萃取。将合并的有机层用盐水(30mL)洗涤,用Na2SO4干燥,过滤并减压浓缩。将残余物通过反相制备性-HPLC来纯化(A:1‰NH4HCO3/水,B:乙腈)得到321(100mg,95%),其为白色固体。MS-ESI:[M+H]+652.8.1H NMR(500MHz,DMSO-d6)δ9.69(s,1H),8.63(s,1H),8.53(d,J=5.0Hz,1H),8.31(d,J=1.5Hz,1H),7.77-7.75(m,1H),7.58(d,J=8.5Hz,1H),7.41(d,J=5.0Hz,1H),6.56(s,1H),4.78(t,J=5.5Hz,1H),4.60-4.57(m,1H),4.41-4.37(m,1H),4.30-4.25(m,1H),4.19(d,J=3.5Hz,2H),4.01-4.00(m,2H),3.92-3.88(m,1H),3.82(s,3H),3.65-3.61(m,2H),3.56-3.53(m,2H),2.61-2.58(m,2H),2.42(s,2H),1.25(d,J=6.0Hz,6H),1.21(s,6H)
实施例322a乙酸(4-(5-(5-((3R,5S)-3,5-二甲基吗啉-4-羰基)吡啶-2-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯322a
在配备有磁力搅拌子和回流冷凝器的25-mL圆底烧瓶中装入(6-氨基吡啶-3-基)((3R,5S)-3,5-二甲基吗啉代)甲酮320a(120mg,0.50mmol)、乙酸(4-(5-溴-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-2(1H)-基)吡啶-3-基)甲酯217a(262mg,0.50mmol)、碳酸铯(326mg,1.0mmol)和1,4-二噁烷(6mL)。在使氮气鼓泡通过所述悬浮液10分钟后,加入Xantphos(58mg,0.10mmol)和三(二亚苄基丙酮)二钯(0)(45mg,0.050mmol)。使体系经历三轮真空/氮气吹洗并回流加热2.5小时。然后将其冷却至室温并过滤。将固体用二氯甲烷(3X10mL)洗涤。将合并的滤液减压浓缩。将残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(80/1至50/1)洗脱)得到322a(200mg,59%),其为黄色固体。MS-ESI:[M+H]+680.3
实施例322 2-[4-[5-[[5-[(3S,5R)-3,5-二甲基吗啉-4-羰基]-2-吡啶基]氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-3,4,6,7,8,9-六氢吡嗪并[1,2-a]吲哚-1-酮322
在室温,向322a(136mg,0.20mmol)于THF/异丙醇/水(4/2/1mL)中的溶液中加入氢氧化锂(48mg,2.0mmol)。在将反应混合物搅拌2小时后,LCMS表明反应完成。然后将混合物倒入水(15mL)中并用二氯甲烷(3X15mL)萃取。将合并的有机层用盐水(30mL)洗涤,用Na2SO4干燥,过滤并减压浓缩。将残余物通过反相制备性-HPLC来纯化(A:1‰NH4HCO3/水,B:乙腈)得到322(50mg,40%),其为白色固体。MS-ESI:[M+H]+638.3.1HNMR(500MHz,DMSO-d6)δ8.94(s,1H),8.77(d,J=5.5Hz,1H),8.48(d,J=5.0Hz,1H),8.20(d,J=2.0Hz,1H),7.64-7.62(m,1H),7.59(d,J=2.5Hz,1H),7.37-7.35(m,2H),6.57(s,1H),4.95(t,J=4.5Hz,1H),4.47-4.38(m,2H),4.23-3.99(m,5H),3.88-3.87(m,1H),3.65-3.61(m,重叠,5H),3.56-3.53(m,2H),2.66-2.56(m,2H),2.47-2.44(m,2H),1.80-1.79(m,2H),1.70-1.66(m,2H),1.25(d,J=6.0Hz,6H)
实施例323a 5-(3-甲氧基氮杂环丁烷-1-基)-2-硝基吡啶323a
在配备有回流冷凝器的100-mL圆底烧瓶中装入3-甲氧基氮杂环丁烷盐酸盐(1.0g,8.09mmol)、5-溴-2-硝基吡啶(1.97g,9.71mmol)、Pd2(dba)3(370.1mg,0.404mmol)、Xantphos(467.6mg,0.809mmol)、Cs2CO3(7.9g,24.3mmol)和二噁烷(50mL)。在使氮气鼓泡通过反应混合物20分钟后,将其在氮气保护下在100℃加热3小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用50:1二氯甲烷/甲醇洗脱)得到323a,其为黄色固体(1.63g,96%).MS-ESI:[M+H]+210.2
实施例323b 5-(3-甲氧基氮杂环丁烷-1-基)吡啶-2-胺323b
向323a(1.5g,7.17mmol)于甲醇(150mL)中的溶液中加入10%Pd/C(150mg)。将体系排空,然后用氢气回填。在室温搅拌2小时后,过滤混合物。减压浓缩滤液得到323b,其为黄色油状物(1.2g,93%),将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+180.1
实施例323c 5-溴-3-(5-(3-甲氧基氮杂环丁烷-1-基)吡啶-2-基氨基)-1-甲基吡啶-2(1H)-酮323c
在配备有回流冷凝器的100-mL圆底烧瓶中装入323b(1.2g,6.7mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(2.14g,8.04mmol)、Pd2(dba)3(306.5mg,0.335mmol)、Xantphos(387.3mg,0.67mmol)、Cs2CO3(4.37g,13.4mmol)和二噁烷(50mL)。在使氮气鼓泡通过反应混合物20分钟后,将其在氮气保护下在100℃加热3小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将其冷却至室温并过滤。减压浓缩滤液。将残余物用石油醚洗涤得到323c,其为棕色固体(1.16g,47%),将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+364.8.
实施例323d乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-(5-{[5-(3-甲氧基氮杂环丁烷-1-基)吡啶-2-基]氨基}-1-甲基-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-基)甲酯323d
在配备有回流冷凝器的50-mL圆底烧瓶中装入323c(150mg,0.411mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(326.5mg,0.822mmol)、Pd(dppf)Cl2(16.8mg,0.0205mmol)、K3PO4(174.3mg,0.822mmol)、乙酸钠(67.5mg,0.822mmol)、乙腈(10mL)和水(5滴)。在使氮气鼓泡通过反应混合物20分钟后,将其在氮气保护下在100℃加热1小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将其冷却至室温并过滤。减压浓缩滤液。将残余物通过硅胶柱色谱法来纯化(用40:1二氯甲烷/甲醇洗脱)得到323d,其为黄色油状物(180mg,68.7%)。MS-ESI:[M+H]+637.8
实施例323 3-[3-(羟基甲基)-4-[5-[[5-(3-甲氧基氮杂环丁烷-1-基)-2-吡啶基]氨基]-1-甲基-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮323
向323d(160mg,0.251mmol)于THF(5mL)、异丙醇(5mL)和水(5mL)中的溶液中加入氢氧化锂(95mg,2.51mmol)。将反应混合物在室温搅拌1小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。然后将其减压浓缩并将残余物用水(10mL)稀释。将所得混合物用二氯甲烷(3X15mL)萃取。将合并的有机层用Na2SO4干燥,过滤并减压浓缩。将残余物通过反相制备性-HPLC来纯化得到323(33.8mg,23%),其为白色固体。MS-ESI:[M+H]+595.8.1H NMR(500MHz,DMSO-d6)δ8.55(d,J=2.0Hz,1H),8.49(d,J=5.0Hz,1H),8.31(s,1H),7.48(d,J=3.5Hz,1H),7.45(d,J=2.0Hz,1H),7.34(d,J=5.0Hz,1H),7.21(d,J=8.5Hz,1H),6.91(dd,J=2.5,8.5Hz,1H),6.56(s,1H),4.96-4.94(m,1H),4.47-4.39(m,2H),4.31-4.19(m,4H),4.03-4.00(m,2H),3.85-3.83(m,1H),3.60(s,3H),3.55-3.53(m,2H),3.23(s,3H),2.62-2.54(m,2H),2.44-2.42(m,2H),1.22(s,6H).
实施例324a(6-氨基吡啶-3-基)((3S,5S)-3,5-二甲基吗啉代)甲酮324a
在室温,向(3S,5S)-3,5-二甲基吗啉(115mg,1.0mmol)于DMF(2mL)中的溶液中加入HATU(380mg,1.0mmol)、DIPEA(260mg,2.0mmol)和6-氨基吡啶-3-甲酸(138mg,1.0mmol)。搅拌18小时后,将反应混合物过滤并用Combiflash纯化(A:1‰NH4HCO3/水,B:乙腈)得到324a(80mg,34%),其为黄色固体。MS(ESI):236.1(M+H).
实施例324b 6-氯-4-(5-((3S,5S)-3,5-二甲基吗啉-4-羰基)吡啶-2-基氨基)-2-甲基哒嗪-3(2H)-酮324b
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入1,4-二噁烷(8mL)、碳酸铯(221mg,0.68mmol)、324a(80mg,0.34mmol)和4-溴-6-氯-2-甲基哒嗪-3(2H)-酮(80mg,0.36mmol)。在使氮气鼓泡通过所述悬浮液5分钟后,加入Xantphos(40mg,0.068mmol)和三(二亚苄基丙酮)二钯(0)(24mg,0.034mmol)。使体系经历三轮真空/氮气吹洗并回流加热2.5小时。然后将其冷却至室温并过滤。将固体用二氯甲烷(3X10mL)洗涤。将合并的滤液减压浓缩。将残余物通过硅胶柱色谱法来纯化(用石油醚/乙酸乙酯(2/1至100%乙酸乙酯)洗脱)得到324b(40mg,31%),其为黄色固体。MS-ESI:[M+H]+378.3
实施例324c乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{5-[(5-{[(3S,5S)-3,5-二甲基吗啉-4-基]羰基}吡啶-2-基)氨基]-1-甲基-6-氧代-1,6-二氢哒嗪-3-基}吡啶-3-基)甲酯324c
在配备有回流冷凝器的50-mL圆底烧瓶中装入324b(40mg,0.11mmol)、乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-3-基)甲酯199e(105mg,0.22mmol)、K3PO4(47mg,0.22mmol)、乙酸钠(18mg,0.22mmol)、1,1’-二(二苯基膦基)二茂铁二氯化钯(II)(20mg,0.022mmol)、乙腈(10mL)和水(6滴)。使体系经历三轮真空/氮气吹洗并在氮气保护下在100℃加热1.5小时。LCMS分析显示完全转化成所期望的产物。将反应混合物冷却至室温并过滤。减压浓缩滤液。将残余物用二氯甲烷(50mL)和水(50mL)稀释。分离出水层并用二氯甲烷(3×20mL)萃取。将合并的萃取物用Na2SO4干燥,过滤并减压浓缩。将黑色残余物通过硅胶柱色谱法来纯化(用60:1二氯甲烷/甲醇洗脱)得到324c(40mg,52%),其为黑色固体。MS-ESI:[M+H]+695.3
实施例324 3-[4-[5-[[5-[(3S,5S)-3,5-二甲基吗啉-4-羰基]-2-吡啶基]氨基]-1-甲基-6-氧代-哒嗪-3-基]-3-(羟基甲基)-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮324
在室温,向324c(40mg,0.057mmol)于THF/异丙醇/水(1/1/0.5ml)中的溶液中加入氢氧化锂(14mg,0.57mmol)。在将反应混合物搅拌3小时后,LCMS表明反应完成。然后将混合物倒入水(20mL)中并用二氯甲烷(3X15mL)萃取。将合并的有机层用盐水(30mL)洗涤,用Na2SO4干燥,过滤并减压浓缩。将残余固体通过反相制备性-HPLC来纯化(A:1‰NH4HCO3/水,B:乙腈)得到324(10mg,27.7%),其为白色固体。MS-ESI:[M+H]+653.3.1H NMR(500MHz,DMSO-d6)δ9.69(s,1H),8.63(s,1H),8.53(d,J=5.0,1H),8.31(d,J=1.5Hz,1H),7.77-7.75(m,1H),7.58(d,J=8.5Hz,1H),7.41(d,J=5.0Hz,1H),6.56(s,1H),4.78(t,J=5.5Hz,1H),4.60-4.57(m,1H),4.41-4.37(m,1H),4.30-4.25(m,1H),4.19(d,J=3.5Hz,2H),4.01(s,2H),3.92-3.88(m,1H),3.82(s,3H),3.65-3.61(m,2H),3.56-3.53(m,2H),2.57(d,J=6.5Hz,2H),2.42(s,2H),1.25(d,J=6.0Hz,6H),1.21(s,6H)
实施例325a 3-氨基-5-溴-1-甲基吡啶-2(1H)-酮325a
向5-溴-3-(二苯基亚甲基氨基)-1-甲基吡啶-2(1H)-酮(3.82g,10.4mmol)于乙酸乙酯(10mL)中的溶液中加入4M HCl/二噁烷(7.8mL,31.3mmol)。将反应混合物搅拌0.5小时并减压浓缩。将残余物用叔丁基甲基醚洗涤并过滤。将所述固体溶解在乙酸乙酯(10mL)和水(10mL)中。通过逐渐加入K2CO3将将所得混合物的pH调整至7和8之间。分离出水相并用二氯甲烷萃取三次。将合并的有机层减压浓缩得到325a,其为黄色固体(1.1g,52%)。MS-ESI:[M+H]+202.9.
实施例325b 1-(2-溴-5-氟吡啶-4-基)乙醇325b
向250-mL 3-颈烧瓶中加入2-溴-5-氟吡啶(8.80g,50mmol)的THF溶液(20mL)。在-78℃,向所述溶液中滴加LDA(25.0mL,50mmol,2.5M于THF中)。搅拌5分钟后,通过注射器滴加二异丙胺(7.0mL,50mmol)并将混合物在-78℃搅拌4小时。通过注射器滴加乙醛的THF溶液(11mL,55mmol,5M于THF中)。从冷却浴移出内容物并搅拌,温热至室温,过夜。将混合物用水(150mL)稀释并剧烈搅拌5分钟。将内容物减压浓缩并将残余物用乙醚(3X150mL)萃取。将合并的有机层用MgSO4干燥,过滤并减压浓缩得到黄色油状物,将其通过硅胶柱色谱法来纯化(用石油醚/乙酸乙酯(10:1至5:1)洗脱)得到325b(8.0g,72.7%),其为黄色固体。MS-ESI:[M+H]+220.1.1H NMR(500MHz,CDCl3)δ8.15(d,J=1.5Hz,1H),7.68(d,J=5.5Hz,1H),5.17(d,J=6.5Hz,1H),2.18-2.16(m,1H),1.52(d,J=6.5Hz,3H).
实施例325c 1-(2-溴-5-氟吡啶-4-基)乙酮325c
将325b(7.5g,34.2mmol)和2-碘酰基苯甲酸(38.4g,137mmol)于乙酸乙酯(200mL)中的混合物在85℃搅拌20小时。将反应混合物过滤并减压浓缩滤液。将所得残余物通过硅胶柱色谱法来纯化(用石油醚/乙酸乙酯(20:1至10:1)洗脱)得到325c(6.8g,92%),其为黄色油状物。MS-ESI:[M+H]+217.9.
实施例325d 5-溴-3-甲基-1H-吡唑并[3,4-c]吡啶325d
向配备有回流冷凝器的250-mL圆底烧瓶中加入无水乙二醇(30mL)和325c(4.3g,20mmol)。然后通过注射器滴加水合肼(5.0mL,4.8g,81.6mmol)。将混合物在165℃加热3.5小时。将所得橙-褐色混合物冷却至室温并将内容物倒在搅拌的100mL冰/水(1:1)的混合物上,随即出现析出。搅拌10分钟后,收集灰白色析出物,将其真空干燥得到325d,其为灰白色固体(3.1g,74%)。MS-ESI:[M+H]+211.9.
实施例325e 5-溴-1,3-二甲基-1H-吡唑并[3,4-c]吡啶325e和5-溴-2,3-二甲基-2H-吡唑并[3,4-c]吡啶326a
将325d(3.0g,14.2mmol)、CH3I(2.40g,17.0mmol)和K2CO3(2.9g,21.3mmol)于乙腈(60mL)中的混合物在30℃搅拌1小时。将反应混合物过滤并减压浓缩滤液。将所得残余物通过硅胶柱色谱法来纯化,用8:1石油醚/乙酸乙酯洗脱得到325e(920mg,29.0%),其为白色固体,和用2:1石油醚/乙酸乙酯洗脱得到326a(390mg,12.0%),其为灰色固体。MS-ESI:[M+H]+226.1.
实施例325f 5-溴-3-(1,3-二甲基-1H-吡唑并[3,4-c]吡啶-5-基氨基)-1-甲基吡啶-2(1H)-酮325f
在密封管中装入325e(202mg,1.0mmol)、325a(337.5mg,1.5mmol)、Pd2(dba)3(91.7mg,0.10mmol)、BINAP(124.6mg,0.20mmol)、碳酸铯(650mg,2.0mmol)和1,4-二噁烷(10mL)。在三轮真空/氮气吹洗后,将密封管在100℃加热2小时。然后将其冷却至室温并过滤。减压浓缩滤液。将所得残余物通过硅胶柱色谱法来纯化(用石油醚/乙酸乙酯(5:1至2:1)洗脱)得到325f(140mg,40%),其为黄色固体。MS-ESI:[M+H]+348.2.
实施例325g乙酸{4-[5-({1,3-二甲基-1H-吡唑并[3,4-c]吡啶-5-基}氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-基}甲酯325g
在配备有磁力搅拌子和回流冷凝器的100-mL圆底烧瓶中装入325f(120mg,0.35mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(417mg,1.05mmol)、Pd(dppf)Cl2(29mg,0.035mmol)、K3PO4(148.0mg,0.70mmol)、乙酸钠(57.4mg,0.70mmol)、水(0.5mL)和乙腈(15mL)。在三轮真空/氮气吹洗后,将混合物回流加热1小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用30:1二氯甲烷/甲醇洗脱)得到325g,其为黄色固体(70mg,33%)。MS-ESI:[M+H]+620.8.
实施例325 3-[4-[5-[(1,3-二甲基吡唑并[3,4-c]吡啶-5-基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮325
将325g(60mg,0.10mmol)和氢氧化锂(60mg,2.5mmol)于异丙醇/THF(1:1,4mL)和水(1mL)中的混合物在35℃搅拌30分钟。向反应混合物中加入水(10mL)并将所得混合物减压浓缩。将残余物用二氯甲烷萃取三次。将合并的有机层减压浓缩并将所得残余物通过反相制备性-HPLC来纯化得到325,其为黄色固体(20mg,31%)。MS-ESI:[M+H]+578.8.1H NMR(500MHz,DMSO)δ8.80(s,1H),8.49(d,J=5.0Hz,1H),8.36(d,J=2.0Hz,1H),8.29(s,1H),7.55(s,1H),7.49(d,J=2.0Hz,1H),7.37(d,J=5.0Hz,1H),6.56(s,1H),5.06-5.05(m,1H),4.51-4.43(m,2H),4.25-4.19(m,3H),4.00(s,3H),3.86-3.84(m,1H),3.63(s,3H),2.62-2.59(m,2H),2.44-2.43(m,重叠,5H),1.22(s,6H).
实施例326b 5-溴-3-(2,3-二甲基-2H-吡唑并[3,4-c]吡啶-5-基氨基)-1-甲基吡啶-2(1H)-酮326b
在配备有磁力搅拌子和回流冷凝器的100-mL圆底烧瓶中装入来自实施例325的5-溴-2,3-二甲基-2H-吡唑并[3,4-c]吡啶326a(452mg,2.0mmol)、3-氨基-5-溴-1-甲基吡啶-2(1H)-酮325a(400mg,2.0mmol)、碳酸铯(1.3g,4.0mmol)和1,4-二噁烷(10mL)。在使氮气鼓泡通过所述悬浮液5分钟后,加入BINAP(124mg,0.2mmol)和三(二亚苄基丙酮)二钯(0)(140mg,0.2mmol)。使体系经历三轮真空/氮气吹洗并回流加热2.5小时。然后将其冷却至室温并过滤。将固体用二氯甲烷(3X10mL)洗涤。将合并的滤液减压浓缩。将残余物通过硅胶柱色谱法来纯化(用石油醚/乙酸乙酯(2/1至100%乙酸乙酯)洗脱)得到326b(160mg,23%),其为黄色固体。MS-ESI:[M+H]+348.3
实施例326c乙酸{4-[5-({2,3-二甲基-2H-吡唑并[3,4-c]吡啶-5-基}氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-基}甲酯326c
在配备有回流冷凝器的50-mL圆底烧瓶中装入326b(160mg,0.46mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(300mg,0.69mmol)、K3PO4(195mg,0.92mmol)、乙酸钠(75mg,0.92mmol)、1,1’-二(二苯基膦基)二茂铁二氯化钯(II)(42mg,0.046mmol)、乙腈(10mL)和水(6滴)。使体系经历三轮真空/氮气吹洗并在氮气保护下在100℃加热1.5小时。LCMS分析显示完全转化成所期望的产物。将反应混合物冷却至室温并过滤。减压浓缩滤液。将残余物用二氯甲烷(50mL)和水(50mL)稀释。分离出水层并用二氯甲烷(3×20mL)萃取。将合并的萃取物用Na2SO4干燥,过滤并减压浓缩。将黑色残余物通过硅胶柱色谱法来纯化(用60:1二氯甲烷/甲醇洗脱)得到326c(130mg,45%),其为黑色固体。MS-ESI:[M+H]+621.3
实施例326 3-[4-[5-[(2,3-二甲基吡唑并[3,4-c]吡啶-5-基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮326
在室温,向326c(130mg,0.21mmol)于THF/异丙醇/水(4/2/1mL)中的溶液中加入氢氧化锂(50mg,2.0mmol)。在将反应混合物搅拌3小时后,LCMS表明反应完成。然后将混合物倒入水(30mL)中并用二氯甲烷(3X30mL)萃取。将合并的有机层用盐水(30mL)洗涤,用Na2SO4干燥,过滤并减压浓缩。将残余固体通过反相制备性-HPLC来纯化(A:1‰NH4HCO3/水,B:乙腈)得到326(60mg,50%),其为白色固体。MS-ESI:[M+H]+579.3.1H NMR(500MHz,DMSO-d6)δ8.86(s,1H),8.48(d,J=5.0Hz,1H),8.06(d,J=1.5Hz,1H),7.99(s,1H),7.47(d,J=2.0Hz,1H),7.41(s,1H),7.38(d,J=5.0Hz,1H),6.57(s,1H),5.13(t,J=5.0Hz,1H),4.50-4.46(m,2H),4.24-4.19(m,3H),4.09(s,3H),3.86-3.85(m,1H),3.62(s,3H),2.62-2.53(m,重叠,5H),2.43(s,2H),1.22(s,6H)
实施例327a 5-(2-甲氧基乙基)-2-硝基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪327a
向2-硝基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪(190mg,1.13mmol)209a于乙腈(10mL)中的溶液中加入K2CO3(311.9mg,2.26mmol)和1-溴-2-甲氧基乙烷(188.3mg,1.36mmol)。将反应混合物在微波照射下在80℃加热17小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将混合物冷却至室温并过滤。减压浓缩滤液得到327a,其为白色固体(230mg,90%),将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+227.0
实施例327b 5-(2-甲氧基乙基)-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-胺327b
向327a(286mg,1.26mmol)于甲醇(10mL)中的溶液中加入Pd/C(28.6mg)。将体系排空并用氢气回填。在室温搅拌2小时后,过滤混合物。减压浓缩滤液得到327b,其为黄色固体(240mg,97%),将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+197.0
实施例327c 3,5-二溴-6-甲基吡啶-2(1H)-酮327c
将6-甲基-吡啶-2-醇(10.9g,0.10mol)悬浮在无水二氯甲烷(300mL)中并在环境温度搅拌。在用冰/水冷却浴冷却的条件下,以5分钟时间间隔缓慢地逐份加入N-溴琥珀酰亚胺(NBS)(11.4g,0.20mol)。将悬浮液搅拌回流2小时。之后,过滤悬浮液。将滤饼用甲醇充分洗涤并真空干燥得到327c,其为白色固体(22.7g,85%)。MS-ESI:[M+H]+266.
实施例327d 3,5-二溴-1,6-二甲基吡啶-2(1H)-酮327d
在配备有磁力搅拌子的100-mL单颈圆底烧瓶中装入DMF(50mL)、327c(10.0g,37.5mmol)、CH3I(5.3g,37.5mmol)和K2CO3(7.8g,56.2mmol)。将混合物在室温搅拌5小时。加入水(100mL)并收集所得白色固体得到327d(8.2g,78%),其为白色固体。MS-ESI:[M+H]+280.
实施例327e 5-溴-3-(5-(2-甲氧基乙基)-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-1,6-二甲基吡啶-2(1H)-酮327e
在配备有回流冷凝器的100-mL圆底烧瓶中装入327b(392mg,2.0mmol)、327d(562mg,2.0mmol)、碳酸铯(1.30g,4.0mmol)和1,4-二噁烷(20mL)。在使氮气鼓泡通过所述悬浮液10分钟后,加入xantphos(115mg,0.20mmol)和三(二亚苄基丙酮)二钯(0)(92mg,0.10mmol)。使体系经历三轮真空/氮气吹洗并回流加热5小时。然后将其冷却至室温并过滤。将固体用二氯甲烷(2X15mL)洗涤。将合并的滤液减压浓缩。将残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(80:1至30:1)洗脱)得到327e(490mg,62%),其为黄色固体。MS-ESI:[M+H]+396.2
实施例327f乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-(5-{[5-(2-甲氧基乙基)-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基]氨基}-1,2-二甲基-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-基)甲酯327f
在配备有磁力搅拌子和回流冷凝器的25-mL单颈圆底烧瓶中装入327e(158mg,0.40mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(159mg,0.40mmol)、K3PO4(170mg,0.80mmol)、乙酸钠(66mg,0.80mmol)、Pd(dppf)Cl2(15mg,0.020mmol)和乙腈/水(7/0.5mL)。在经历三轮真空/氮气吹洗后,将混合物在95℃加热1小时。LCMS分析显示完全转化成所期望的产物。将反应混合物冷却至室温并用二氯甲烷(50mL)和水(30mL)洗涤。将水层用二氯甲烷(2×30mL)萃取。将合并的有机萃取物用Na2SO4干燥,过滤并减压浓缩。将黑色残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(80:1至30:1)洗脱)得到327f(120mg,45%),其为黄色固体。MS-ESI:[M+H]+668.8
实施例327 3-[3-(羟基甲基)-4-[5-[[5-(2-甲氧基乙基)-6,7-二氢-4H-吡唑并[1,5-a]吡嗪-2-基]氨基]-1,2-二甲基-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮327
向327f(120mg,0.18mmol)于THF/异丙醇/水(6/4/3mL)中的溶液中加入氢氧化锂(22mg,0.90mmol)。将混合物在室温搅拌1小时。将混合物减压浓缩并将残余物用水(15mL)稀释。然后将其用乙酸乙酯(3X20mL)萃取。将合并的有机层用硫酸钠干燥并减压浓缩。将残余物通过反相制备性-HPLC来纯化得到327,其为白色固体(55mg,49%)。MS-ESI:[M+H]+626.9.1H NMR(500MHz,CDCl3)δ8.49(d,J=5.0Hz,1H),7.49(s,1H),7.32(s,1H),7.15(d,J=4.5Hz,1H),6.82(s,1H),5.61(bs,1H),4.53-4.45(m,3H),4.26-4.16(m,3H),4.03-3.97(m,3H),3.71-3.69(m,5H,重叠),3.58(t,J=5.5Hz,2H),3.39(s,3H),2.98(t,J=5.0Hz,2H),2.77(t,J=5.0Hz,2H),2.60-2.57(m,2H),2.53(s,2H),2.17(s,3H),1.29(s,6H).
实施例328a 3-(5-(2-甲氧基乙基)-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮328a
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入5-溴-3-(5-(2-甲氧基乙基)-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-1-甲基吡啶-2(1H)-酮296f(330mg,0.86mmol)、Pin2B2(329mg,1.30mmol)、Pd2(dba)3(40mg,0.043mmol)、X-phos(41mg,0.086mmol)、乙酸钾(169mg,1.726mmol)和二噁烷(10mL)。在经历三轮真空/氮气吹洗后,将混合物在70℃加热2小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将其冷却至室温并过滤。减压浓缩滤液。将残余物用石油醚洗涤得到328a,其为黑色油状物(240mg,80%),将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+348.3
实施例328b 3-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-5-(5-{[5-(2-甲氧基乙基)-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基]氨基}-1-甲基-6-氧代-1,6-二氢吡啶-3-基)吡啶-4-甲醛328b
在配备有磁力搅拌子的密封管中装入3-溴-5-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-甲醛107f(100mg,0.26mmol)、328a(110mg,0.26mmol)、Pd(dppf)Cl2(10mg,0.026mmol)、乙酸钠(50mg,0.50mmol)、K3PO4(100mg,0.50mmol)和乙腈/水(5mL/1mL)。在三轮真空/氮气吹洗后,将混合物在100℃加热2小时。然后将其过滤并减压蒸发滤液。将残余物通过硅胶柱色谱法来纯化(用10:1二氯甲烷/甲醇洗脱)得到328b(50mg,32%),其为棕色固体。MS-ESI:[M+H]+611.3.
实施例328 3-[4-(羟基甲基)-5-[5-[[5-(2-甲氧基乙基)-6,7-二氢-4H-吡唑并[1,5-a]吡嗪-2-基]氨基]-1-甲基-6-氧代-3-吡啶基]-3-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮328
将328b(50mg,0.08mmol)和NaBH4(8.0mg,0.20mmol)于甲醇(4mL)中的混合物在25℃搅拌0.5小时。将反应混合物用水(10mL)淬灭并减压蒸发。将残余物用二氯甲烷(2X10mL)萃取。将合并的萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到328(13mg,25%),其为浅黄色固体。MS-ESI:[M+H]+613.3.1H NMR(500MHz,CDCl3)δ8.62(s,1H),8.48(s,1H),7.92(d,J=2.0Hz,1H),7.38(s,1H),7.31(d,J=2.0Hz,1H),6.82(s,1H),5.67(s,1H),4.64-4.62(m,1H),4.57-4.55(m,1H),4.38-4.34(m,1H),4.22-4.17(m,3H),4.05-4.02(m,2H),3.99-3.96(m,1H),3.71-3.70(m,2H),3.69(s,3H),3.57(t,J=5.0Hz,2H),3.37(s,3H),2.99(t,J=5.0Hz,2H),2.77(t,J=5.0Hz,2H),2.56(s,2H),2.51(s,2H),1.27(s,6H).
实施例329a 2-氯-4-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-甲醛329a
在配备有回流冷凝器的100-mL圆底烧瓶中装入4,4-二甲基-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-9-酮107e(612mg,3.0mmol)、4-溴-2-氯吡啶-3-甲醛(2.0g,9.0mmol)、Pd2(dba)3(275mg,0.30mmol)、XantPhos(347mg,0.60mmol)、碳酸铯(1.95g,6.0mmol)和1,4-二噁烷(30mL)。在三轮真空/氮气吹洗后,将混合物在97℃加热整夜。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用1:2乙酸乙酯/石油醚洗脱)得到329a,其为黄色固体(660mg,65%)。MS-ESI:[M+H]+344.1.
实施例329b 4-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-2-(5-{[5-(2-甲氧基乙基)-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基]氨基}-1-甲基-6-氧代-1,6-二氢吡啶-3-基)吡啶-3-甲醛329b
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入329a(100mg,0.30mmol)、3-(5-(2-甲氧基乙基)-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基氨基)-1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮328a(257mg,0.60mmol)、Pd(dppf)Cl2(25mg,0.030mmol)、K3PO4(127mg,0.60mmol)、乙酸钠(49mg,0.60mmol)、水(0.50mL)和THF(10mL)。在三轮真空/氮气吹洗后,将混合物回流加热1小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用30:1二氯甲烷/甲醇洗脱)得到329b,其为棕色固体(60mg,34%)。MS-ESI:[M+H]+611.3.
实施例329 3-[3-(羟基甲基)-2-[5-[[5-(2-甲氧基乙基)-6,7-二氢-4H-吡唑并[1,5-a]吡嗪-2-基]氨基]-1-甲基-6-氧代-3-吡啶基]-4-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮329
将329b(50mg,0.080mmol)和NaBH4(9.1mg,0.24mmol)于甲醇(5mL)中的混合物在室温搅拌10分钟。将混合物用水淬灭(10mL)并减压蒸发。将残余物用二氯甲烷(3X10m)萃取。将合并的萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到329(15mg,30%),其为黄色固体。MS-ESI:[M+H]+613.3.1H NMR(500MHz,CDCl3)δ8.66(d,J=4.5Hz,1H),8.13(s,1H),7.63(s,1H),7.35(s,1H),7.12(d,J=5.0Hz,1H),6.83(s,1H),5.71(s,1H),4.67-4.63(m,1H),4.49-4.43(m,1H),4.24-4.23(m,2H),4.19-4.17(m,1H),4.06-4.04(m,2H),4.01-3.97(m,1H),3.74-3.71(m,2H),3.70(s,3H),3.59-3.55(m,2H),3.38(s,3H),3.00(t,J=5.0Hz,2H),2.77(t,J=5.0Hz,2H),2.56(s,2H),2.51(s,2H),1.27(s,6H).
实施例330a 10-[4-氯-3-(羟基甲基)吡啶-2-基]-4,4-二甲基-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-9-酮330a
将4-氯-2-{4,4-二甲基-9-氧代-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-10-基}吡啶-3-甲醛109a(1.2g,3.3mmol)、NaBH4(228mg,6.0mmol)和甲醇(10mL)的混合物在0℃搅拌0.5小时。将反应混合物用水(10mL)淬灭并减压浓缩。将残余物用二氯甲烷(2X15mL)萃取。将合并的二氯甲烷萃取物减压浓缩得到330a,其为浅黄色固体(1.0g,84%)。MS-ESI:[M+H]+362.9
实施例330b乙酸(4-氯-2-{4,4-二甲基-9-氧代-7-硫杂-10-氮杂三环[6.4.0.02 ,6]十二碳-1(8),2(6)-二烯-10-基}吡啶-3-基)甲酯330b
将330a(1.0g,2.76mmol)、三乙胺(610mg,6.0mmol)和乙酸酐(5mL)的混合物在25℃搅拌2小时。将反应混合物用水(10mL)淬灭并用NaHCO3(水溶液)将pH调整至约8。将混合物用二氯甲烷(2X15mL)萃取。将合并的二氯甲烷萃取物减压浓缩并将残余物通过硅胶柱色谱法来纯化(用1:1乙酸乙酯/石油醚洗脱)得到330b,其为浅黄色固体(1.0g,90%)。MS-ESI:[M+H]+405.2
实施例330c乙酸(2-{4,4-二甲基-9-氧代-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-10-基}-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-3-基)甲酯330c
在配备有磁力搅拌子和回流冷凝器的50-mL圆底烧瓶中装入330b(1.0g,2.47mmol)、4,4,4',4',5,5,5',5'-八甲基-2,2'-二(1,3,2-二氧杂硼杂戊环)(1.87g,7.40mmol)、Pd(dppf)Cl2(100mg,0.13mmol)、X-phos(125mg,0.25mmol)、乙酸钾(500mg,5.0mmol)和1,4-二噁烷(10mL)。在三轮真空/氮气吹洗后,将混合物在65℃加热4小时。然后将其过滤并减压蒸发滤液得到330c(1.0g,98%),其为棕色油状物并且未经进一步纯化。MS-ESI:[M+H]+415.2.
实施例330d(3-硝基-1H-吡唑-5-基)甲醇330d
将3-硝基-1H-吡唑-5-羧酸(4.71g,30mmol)、BH3/THF(75mL,1mol/L,75mmol)的混合物在60℃搅拌2小时。将混合物冷却至室温并加入4MHCl(19mL,75mmol)。将其在70℃搅拌2小时。冷却至室温后,将混合物减压浓缩。使残余物在乙酸乙酯和盐水(100:100mL)之间分配。将水相用乙酸乙酯(4X50mL)萃取。将合并的有机层在Na2SO4上干燥并减压蒸发。将残余物通过硅胶柱色谱法来纯化(用石油醚/乙酸乙酯(5:1至1:1)洗脱)得到330d(3.5g,79%),其为白色固体。MS-ESI:[M+H]+144.2
实施例330e 1-(5-(羟基甲基)-3-硝基-1H-吡唑-1-基)-2-甲基丙烷-2-醇330e
在密封管中装入330d(2.145g,15mmol)、Cs2CO3(978mg,3.0mmol)和2,2-二甲基环氧乙烷(15mL)。将混合物在70℃搅拌3小时。冷却至室温后,将混合物减压浓缩。将残余物通过硅胶柱色谱法来纯化(用石油醚/乙酸乙酯(5:1至1:1)洗脱)得到330e(1.2g,38%),其为白色固体。MS-ESI:[M+H]+216.2
实施例330f 6,6-二甲基-2-硝基-6,7-二氢-4H-吡唑并[5,1-c][1,4]噁嗪330f
在0℃,向330e(1.1g,5.1mmol)于DMF(10mL)中的溶液中加入NaH(60%分散于矿物油中,246mg,6.14mmol)。将所得悬浮液搅拌30分钟,然后加入对甲苯磺酰氯(1169mg,6.14mmol)。将混合物在60℃搅拌整夜。冷却至室温后,加入饱和氯化铵溶液并将混合物用二氯甲烷萃取。将合并的有机层用盐水洗涤,用Na2SO4干燥并减压蒸发。将残余物通过硅胶柱色谱法来纯化(用石油醚/乙酸乙酯梯度(9:1至2:1)洗脱)得到330f(228mg,22%)。MS-ESI:[M+H]+198.3
实施例330g 6,6-二甲基-6,7-二氢-4H-吡唑并[5,1-c][1,4]噁嗪-2-胺330g
将50-mL单颈圆底烧瓶用氮气吹洗并装入330f(0.21g,1.25mmol)、10%钯/炭(50%水分,125mg)和甲醇(10mL)。将所述混合物排空,充入氢气并在室温搅拌2小时。然后将氢气排空并将氮气充入所述烧瓶中。通过用垫过滤除去催化剂并减压浓缩滤液得到330g(167mg,93%)。MS-ESI:[M+H]+168.1
实施例330h 6-氯-4-(6,6-二甲基-6,7-二氢-4H-吡唑并[5,1-c][1,4]噁嗪-2-基氨基)-2-甲基哒嗪-3(2H)-酮330h
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入330g(250mg,1.5mmol)、4-溴-6-氯-2-甲基哒嗪-3(2H)-酮(669mg,3.0mmol)、Pd2(dba)3(137mg,0.15mmol)、Xantphos(173mg,0.30mmol)、Cs2CO3(978mg,3.0mmol)和1,4-二噁烷(20mL)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热3小时。然后将其冷却至室温并过滤。减压浓缩滤液并用乙酸乙酯洗涤得到330h,其为黄色固体(209mg,45%)。MS-ESI:[M+H]+310.1.
实施例330i乙酸{4-[5-({6,6-二甲基-4H,6H,7H-吡唑并[3,2-c][1,4]噁嗪-2-基}氨基)-1-甲基-6-氧代-1,6-二氢哒嗪-3-基]-2-{4,4-二甲基-9-氧代-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-10-基}吡啶-3-基}甲酯330i
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入330h(133mg,0.43mmol)、330c(178mg,0.43mmol)、乙酸钠(71mg,0.86mmol)、K3PO4(182mg,0.86mmol)、Pd(dppf)Cl2(35mg,0.043mmol)、乙腈(15mL)和水(0.5mL)。使氮气鼓泡通过所得混合物后20分钟,将反应混合物在95℃加热3小时。之后,将反应混合物冷却至室温并过滤。减压浓缩滤液。将残余物用硅胶柱色谱法来纯化(用30:1二氯甲烷/甲醇洗脱)得到330i,其为黄色固体(69mg,25%)。MS-ESI:[M+H]+644.3.
实施例330 3-[4-[5-[(6,6-二甲基-4,7-二氢吡唑并[5,1-c][1,4]噁嗪-2-基)氨基]-1-甲基-6-氧代-哒嗪-3-基]-3-(羟基甲基)-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]噻吩并[1,3-c]吡啶-4-酮330
将330i(69mg,0.11mmol)和氢氧化锂(10mg,0.42mmol)于异丙醇/THF(1:1,3.5mL)和水(1mL)中的混合物在室温搅拌1小时。然后减压浓缩混合物并将残余物用水(10mL)稀释。将其用乙酸乙酯(2X10mL)萃取。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到330(30mg,47%)。MS-ESI:[M+H]+602.5.1H NMR(500MHz,CDCl3)δ8.56(d,J=5.0Hz,1H),8.00(s,1H),7.90(s,1H),7.43(d,J=5.0Hz,1H),5.94(s,1H),4.82(s,2H),4.60-4.58(m,2H),4.38-4.36(m,2H),3.89(s,3H),3.89-3.87(m,3H),3.02-2.93(m,2H),2.79-2.75(m,2H),2.59-2.54(m,2H),1.37(s,6H),1.28(s,6H).
实施例331a 5-溴-1-甲基-3-(3-甲基异噻唑-5-基氨基)吡嗪-2(1H)-酮331a
在配备有磁力搅拌子的密封管中装入3-甲基异噻唑-5-胺(170mg,1.5mmol)、3,5-二溴-1-甲基吡嗪-2(1H)-酮(400mg,1.5mmol)、Pd(OAc)2(84mg,0.375mmol)、BINAP(116mg,0.188mmol)、K2CO3(450mg,4.5mmol)和1,4-二噁烷(4mL)。在三轮真空/氮气吹洗后,将混合物在密封管中在120℃加热18小时。然后将其冷却至室温并过滤。减压蒸发滤液。将残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(100:1至25:1)洗脱)得到331a(220mg,50%),其为黄色固体。MS-ESI:[M+H]+301.0.
实施例331b乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{4-甲基-6-[(3-甲基-1,2-噻唑-5-基)氨基]-5-氧代-4,5-二氢吡嗪-2-基}吡啶-3-基)甲酯331b
在配备有回流冷凝器的50-mL圆底烧瓶中装入331a(150mg,0.50mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(400mg,1.0mmol)、Pd(dppf)Cl2(25mg,0.025mmol)、K3PO4(220mg,1.0mmol)、乙酸钠三水合物(136mg,1.0mmol)、乙腈(10mL)和水(0.5mL)。将体系排空并用氮气回填。将反应混合物在100℃加热1小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(100/1至25/1)洗脱)得到331b(200mg,70%),其为黄色固体。MS-ESI:[M+H]+574.2.
实施例331 3-[3-(羟基甲基)-4-[4-甲基-6-[(3-甲基异噻唑-5-基)氨基]-5-氧代-吡嗪-2-基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮331
将331b(120mg,0.21mmol)和氢氧化锂一水合物(88mg,2.1mmol)于THF/异丙醇(4:2,6mL)和水(2mL)中的混合物在30℃搅拌1小时。将混合物减压蒸发并用水(10mL)稀释。然后将其用乙酸乙酯(2X15mL)萃取。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到331(50mg,45%),其为白色固体。MS-ESI:[M+H]+532.2.1H NMR(500MHz,CHCL3)δ9.13(s,1H),8.61(d,J=5Hz,1H),8.37(s,1H),7.99(d,J=5.0Hz,1H),6.87(s,1H),6.74(s,1H),5.32-5.39(m,1H),4.77-4.75(m,1H),4.58-4.56(m,1H),4.32-4.37(m,1H),4.21-4.18(m,2H),3.96-3.94(m,1H),3.72(s,3H),2.61-2.58(m,2H),2.54(s,2H),2.48(s,3H),1.30(s,6H).
实施例332a 5-溴-3-(5-乙基-1,3,4-噻二唑-2-基氨基)-1-甲基吡啶-2(1H)-酮332a
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入5-乙基-1,3,4-噻二唑-2-胺(500mg,3.88mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(1.55g,5.81mmol)、Pd2(dba)3(357mg,0.39mmol)、XantPhos(451mg,0.78mmol)、Cs2CO3(2.5g,7.67mmol)和1,4-二噁烷(40mL)。使体系经历三轮真空/氮气吹洗并在100℃加热2小时。将混合物冷却至90℃并过滤。将滤液在冰-水浴中冷却,然后再次过滤得到332a(574mg,47%),其为白色固体。MS-ESI:[M+H]+315.1
实施例332b乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-{5-[(5-乙基-1,3,4-噻二唑-2-基)氨基]-1-甲基-6-氧代-1,6-二氢吡啶-3-基}吡啶-3-基)甲酯332b
在配备有回流冷凝器的100-mL圆底烧瓶中装入332a(200mg,0.63mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(754mg,1.89mmol)、PdCl2(dppf)(51mg,0.063mmol)、K3PO4(267mg,1.26mmol)、CH3COONa(103mg,1.26mmol)、乙腈(15mL)和水(0.5mL)。使氮气鼓泡通过所得混合物20分钟后,将其在氮气中在100℃加热2小时。将所得混合物冷却至室温并过滤。减压蒸发滤液并将残余物通过硅胶柱色谱法来纯化(用50:1二氯甲烷/甲醇洗脱)得到332b,其为棕色固体(178mg,48%)。MS-ESI:[M+H]+588.2
实施例332 3-[4-[5-[(5-乙基-1,3,4-噻二唑-2-基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮332
将332b(158mg,0.27mmol)和氢氧化锂(19mg,0.81mmol)于异丙醇/THF/水(9mL/6mL/6mL)中的混合物在室温搅拌0.5小时。将混合物减压蒸发并将残余物用二氯甲烷(3X20mL)萃取。将合并的二氯甲烷萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到332,其为白色固体(80mg,54%)。MS-ESI:[M+H]+546.2.1H NMR(500MHz,DMSO-d6)δ10.20(s,1H),8.60(d,J=2.0Hz,1H),8.49(d,J=5.0Hz,1H),7.63(d,J=2.5Hz,1H),7.33(d,J=5.0Hz,1H),6.57(s,1H),4.92(t,J=4.5Hz,1H),4.49-4.39(m,2H),4.25-4.19(m,3H),3.87-3.85(m,1H),3.61(s,3H),2.92-2.88(m,2H),2.58-2.53(m,2H),2.43(s,2H),1.27-1.22(m,重叠,9H).
实施例333a乙酸(2-{4,4-二甲基-9-氧代-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-10-基}-4-{1-甲基-5-[(1-甲基-1H-1,2,3-三唑-4-基)氨基]-6-氧代-1,6-二氢吡啶-3-基}吡啶-3-基)甲酯333a
在配备有磁力搅拌子和回流冷凝器的50-mL圆底烧瓶中装入乙酸(2-{4,4-二甲基-9-氧代-7-硫杂-10-氮杂三环[6.4.0.02,6]十二碳-1(8),2(6)-二烯-10-基}-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-3-基)甲酯330c(180mg,0.37mmol)、5-溴-1-甲基-3-(1-甲基-1H-1,2,3-三唑-4-基氨基)吡啶-2(1H)-酮292c(125mg,0.43mmol)、Pd(dppf)Cl2(20mg,0.025mmol)、乙酸钾(80mg,0.80mmol)、K3PO4(165mg,0.80mmol)和乙腈/水(10mL/1mL)。在三轮真空/氮气吹洗后,将混合物在100℃加热1小时。然后将其过滤并减压蒸发滤液。将残余物通过硅胶柱色谱法来纯化(用20:1二氯甲烷/甲醇洗脱)得到333a(150mg,71%),其为棕色固体。MS-ESI:[M+H]+574.1
实施例333 3-[3-(羟基甲基)-4-[1-甲基-5-[(1-甲基三唑-4-基)氨基]-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]噻吩并[1,3-c]吡啶-4-酮333
将333a(150mg,0.26mmol)和氢氧化锂水合物(84mg,2.0mmol)于THF(5mL)、异丙醇(5mL)和水(1.5mL)中的混合物在40℃搅拌0.5小时。将混合物减压蒸发并用水(10mL)稀释。然后将其用二氯甲烷(2X10mL)萃取。将合并的有机层减压浓缩并将残余物通过反相制备性-HPLC来纯化得到333(52mg,38%),其为浅黄色固体。MS-ESI:[M+H]+532.3.1H NMR(500MHz,DMSO-d6)δ8.48-8.47(m,1H),8.28(s,1H),7.78-7.77(m,2H),7.42(d,J=2.5Hz,1H),7.34-7.33(m,1H),4.97-4.95(t,J=5.0Hz,1H),4.43-4.41(m,2H),4.17-4.16(m,1H),3.99(s,3H),3.94-3.92(m,1H),3.59(s,3H),3.04-3.02(m,1H),2.90-2.89(m,1H),2.77-2.75(m,2H),2.56-2.54(m,2H),1.23(s,3H),1.22(s,3H).
实施例334 3-[4-[5-[(5-环丙基-1,3,4-噻二唑-2-基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮334
按照实施例273的操作,用5-环丙基-1,3,4-噻二唑-2-胺代替2-氨基吡啶得到334(8.7mg,22%收率).1H NMR(400MHz,DMSO-d6)δ8.48(d,J=5.1Hz,1H),8.20(s,1H),8.10(d,J=2.4Hz,1H),7.53(d,J=2.4Hz,1H),7.44(d,J=5.1Hz,1H),6.53(s,1H),4.95(t,J=5.2Hz,1H),4.55–4.49(m,1H),4.27–4.23(m,3H),3.78(s,2H),3.51(s,3H),3.48(dt,J=12.3,5.2Hz,3H),3.24(s,2H),2.50(d,J=7.2Hz,2H),2.33(s,2H),1.85–1.82(m,3H),1.23(s,6H).ES-MS m/z 531.3[M+1].
实施例335a 5-溴-3-(6,6-二甲基-6,7-二氢-4H-吡唑并[5,1-c][1,4]噁嗪-2-基氨基)-1-甲基吡啶-2(1H)-酮335a
在配备有回流冷凝器的100-mL圆底烧瓶中装入1,4-二噁烷(10mL)、6,6-二甲基-6,7-二氢-4H-吡唑并[5,1-c][1,4]噁嗪-2-胺330g(167mg,1.0mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(320mg,1.2mmol)、Pd2(dba)3(91mg,0.10mmol)、XantPhos(116mg,0.20mmol)和碳酸铯(652mg,2.0mmol)。在经历三轮真空/氩气吹洗后,将混合物在100℃加热3小时。然后将其过滤并减压蒸发滤液。将残余物通过硅胶柱色谱法来纯化(用100:1二氯甲烷/甲醇洗脱)得到335a(210mg,60%),其为黄色固体。MS-ESI:[M+H]+352.9
实施例335b 3-(6,6-二甲基-6,7-二氢-4H-吡唑并[5,1-c][1,4]噁嗪-2-基氨基)-1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮335b
向335a(160mg,0.45mmol)和4,4,4',4',5,5,5',5'-八甲基-2,2'-二(1,3,2-二氧杂硼杂戊环)(572g,2.25mmol)于二噁烷(20mL)中的混合物中加入PdCl2(dppf)(36.8mg,0.045mmol)和乙酸钾(88.2mg,0.90mmol)。在三轮真空/氮气吹洗后,将混合物在氮气气氛下在90℃搅拌4小时。然后将其过滤并减压蒸发滤液得到335b,将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+401.3.
实施例335c 4-[5-({6,6-二甲基-4H,6H,7H-吡唑并[3,2-c][1,4]噁嗪-2-基}氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基]-2-{4,4-二甲基-9-氧代-7-硫杂-10,11-二氮杂三环[6.4.0.02,6]十二碳-1(8),2(6),11-三烯-10-基}吡啶-3-甲醛335c
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入335b(240mg,0.60mmol)、4-氯-2-{4,4-二甲基-9-氧代-7-硫杂-10,11-二氮杂三环[6.4.0.02,6]十二碳-1(8),2(6),11-三烯-10-基}吡啶-3-甲醛282i(107.7mg,0.30mmol)、Pd(dppf)Cl2(24.5mg,0.030mmol)、K3PO4(127.2mg,0.60mmol)、乙酸钠(49.2mg,0.60mmol)、水(0.5mL)和乙腈(10mL)。在三轮真空/氮气吹洗后,将混合物在95℃加热1小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用30:1二氯甲烷/甲醇洗脱)得到335c,其为棕色固体(60mg,两步的收率22%)。MS-ESI:[M+H]+598.2.
实施例335 3-[4-[5-[(6,6-二甲基-4,7-二氢吡唑并[5,1-c][1,4]噁嗪-2-基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-7,7-二甲基-6,8-二氢环戊二烯并[3,4]噻吩并[1,3-d]哒嗪-4-酮335
将335c(50mg,0.080mmol)和NaBH4(9.1mg,0.24mmol)于甲醇(5mL)中的混合物在室温搅拌10分钟。将混合物用水(10mL)淬灭并减压蒸发。将残余物用二氯甲烷(3X10mL)萃取。将合并的萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到335(15mg,30%),其为黄色固体。MS-ESI:[M+H]+600.2.1H NMR(500MHz,DMSO-d6)δ8.56(d,J=5.0Hz,1H),8.46(s,1H),8.31(s,1H),8.07(d,J=2.0Hz,1H),7.52(d,J=5.0Hz,1H),7.40(d,J=2.5Hz,1H),5.94(s,1H),4.85-4.83(m,1H),4.72(s,2H),4.38-4.37(m,2H),3.79-3.78(m,2H),3.3(s,3H),2.92-2.91(m,2H),2.81(s,2H),1.28(s,6H),1.25(s,6H).
实施例336a 5-(甲氧基甲基)-1-甲基-3-硝基-1H-吡唑336a
在配备有磁力搅拌子和回流冷凝器的250-mL单颈圆底烧瓶中装入5-(溴甲基)-1-甲基-3-硝基-1H-吡唑(8.8g,40mmol)、甲醇钠(4.3g,80mmol)和甲醇(50mL)。将反应混合物回流加热2小时。之后,将反应混合物冷却至室温并减压浓缩。使残余物在乙酸乙酯(60mL)和水(60mL)之间分配。分离出水层并用乙酸乙酯(2X50mL)萃取。将合并的有机层用盐水(50mL)洗涤并用硫酸钠干燥。过滤除去干燥剂并减压浓缩滤液得到336a,其为黄色油状物(6.1g,90%)。MS-ESI:[M+H]+172.
实施例336b 5-(甲氧基甲基)-1-甲基-1H-吡唑-3-胺336b
在配备有磁力搅拌子的250-mL单颈圆底烧瓶中装入336a(4.0g,23mmol)、Pd/C(1.0g)和乙醇(100mL)。将混合物在室温氢化15小时。然后将其过滤并减压浓缩滤液得到336b,其为黄色油状物(3.3g,99%),将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+142.
实施例336c 5-溴-3-(5-(甲氧基甲基)-1-甲基-1H-吡唑-3-基氨基)-1-甲基吡啶-2(1H)-酮336c
按照实施例335a中的操作,以335b(1.7g,12mmol)和3,5-二溴-1-甲基吡啶-2(1H)-酮(3.2g,12mmol)开始得到336c,其为黄色固体(2.8g,71%)。MS-ESI:[M+H]+327.1HNMR(500MHz,CDCl3)δ7.86(d,J=2.5Hz,1H),7.38(s,1H),6.88(d,J=2.5Hz,1H),5.86(s,1H),4.41(s,2H),3.82(s,3H),3.58(s,3H),3.36(s,3H).
实施例336d 3-(5-(甲氧基甲基)-1-甲基-1H-吡唑-3-基氨基)-1-甲基-5-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-2(1H)-酮336d
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入336c(600mg,1.83mmol)、4,4,4',4',5,5,5',5'-八甲基-2,2'-二(1,3,2-二氧杂硼杂戊环)(1.39g,5.49mmol)、Pd2(dba)3(183mg,0.20mmol)、X-phos(190mg,0.40mmol)、乙酸钾(392mg,4.0mmol)和1,4-二噁烷(30mL)。在三轮真空/氮气吹洗后,将混合物在85℃加热3小时。然后将其冷却至室温并过滤。减压浓缩滤液得到粗制336d,其为黑色油状物(400mg,75%),将其不经进一步纯化即用在下一步骤中。MS-ESI:[M+H]+293.1
实施例336e 4-(5-(5-(甲氧基甲基)-1-甲基-1H-吡唑-3-基氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-(1-氧代-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-3-甲醛336e
在配备有回流冷凝器的50-mL圆底烧瓶中装入336d(368mg,0.98mmol)、4-氯-2-(1-氧代-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-2(1H)-基)吡啶-3-甲醛139a(270mg,0.82mmol)、PdCl2(dppf)(60mg,0.082mmol)、K3PO4(348mg,1.64mmol))、乙酸钠(135mg,1.65mmol)、乙腈(15mL)和水(0.5mL)。使体系经历三轮真空/氮气吹洗并在95℃加热3小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用20:1乙酸乙酯/甲醇洗脱)得到336e(100mg,22%)。MS-ESI:[M+H]+542.2
实施例336 2-[3-(羟基甲基)-4-[5-[[5-(甲氧基甲基)-1-甲基-吡唑-3-基]氨基]-1-甲基-6-氧代-3-吡啶基]-2-吡啶基]-3,4,6,7,8,9-六氢吡啶并[3,4-b]吲嗪-1-酮336
向336e(100mg,0.18mmol)于甲醇(10mL)中的溶液中加入NaBH4(41mg,1.08mmol)。将混合物在室温搅拌1小时,LCMS显示起始物质已消失。将反应混合物用1.0M HCl溶液(10mL)淬灭并减压蒸发直到蒸馏掉大部分甲醇。将残余物用二氯甲烷(3X15mL)萃取。将合并的有机层用Na2SO4干燥并减压蒸发。将残余物通过反相制备性-HPLC来纯化得到336,其为白色固体(41mg,41%)。MS-ESI:[M+H]+544.2.1H NMR(500MHz,CDCl3)δ8.49(d,J=5.0Hz,1H),7.96(d,J=2.5Hz,1H),7.73(d,J=2.5Hz,1H),7.41(s,1H),7.33(d,J=5.0Hz,1H),6.33(s,1H),5.95(s,1H),4.99-4.96(m,1H),4.67-4.64(m,1H),4.42-4.41(m,3H),4.36-4.26(m,1H),3.98-3.91(m,1H),3.88-3.82(m,2H),3.79(s,3H),3.71(s,3H),3.37(s,3H),3.06-2.91(m,2H),2.87-2.79(m,2H),2.08-2.01(m,2H),1.91-1.86(m,2H).
实施例337a 1,2-二甲基-4-硝基-1H-咪唑337a
向2-甲基-4-硝基-1H-咪唑(10.0g,78.7mmol)和K2CO3(21.7g,160mmol)于DMF(80mL)中的混合物中滴加CH3I(13.4g,94mmol)同时在室温搅拌。将混合物搅拌2小时。然后向混合物中加入水(200mL)。过滤所得悬浮液,用水洗涤并真空干燥得到337a,其为白色固体(5.0g,45%)。MS-ESI:[M+H]+142.1.
实施例337b 1,2-二甲基-1H-咪唑-4-基氨基甲酸叔丁酯337b
将100-mL单颈圆底烧瓶用氮气吹洗并装入337a(2.0g,14.1mmol)、10%钯/炭(50%水分,400mg)、(Boc)2O(9.22g,43.3mmol)、三乙胺(2.85g,28.2mmol)和乙醇(20mL)。将混合物排空,充入氢气并在室温搅拌5小时。然后将氢气排空并将氮气充入所述烧瓶中。通过用垫过滤除去催化剂并减压浓缩滤液。将残余物通过硅胶柱色谱法来纯化(用40:1二氯甲烷/甲醇洗脱)得到337b(1.2g,40%),其为棕色固体。MS-ESI:[M+H]+212.1
实施例337c 1,2-二甲基-1H-咪唑-4-胺盐酸盐337c
向337b(1.2g,5.68mmol)于二氯甲烷(5.0mL)中的溶液中加入3M HCl/二噁烷(5.0mL)。将该混合物在室温搅拌4小时并减压浓缩。将粗制产物用乙酸乙酯洗涤得到337c(450mg,55%),其为浅黄色固体,将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+112.2
实施例337d 5-溴-3-(1,2-二甲基-1H-咪唑-4-基氨基)-1-甲基吡啶-2(1H)-酮337d
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入337c(400mg,3.60mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(960mg,3.60mmol)、XantPhos(240mg,0.40mmol)、三(二亚苄基丙酮)二钯(0)(360mg,0.40mmol)、Cs2CO3(4.69g,14.4mmol)和1,4-二噁烷(20mL)。在三轮真空/氮气吹洗后,将混合物在90℃加热2.5小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用二氯甲烷/甲醇(30:1至20:1)洗脱)得到337d,其为浅黄色固体(350mg,33%)。MS-ESI:[M+H]+297.1.
实施例337e乙酸(4-{5-[(1,2-二甲基-1H-咪唑-4-基)氨基]-1-甲基-6-氧代-1,6-二氢吡啶-3-基}-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]-十二碳-2(6),7-二烯-10-基}吡啶-3-基)甲酯337e
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入337d(20mg,0.67mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(270mg,0.67mmol)、Pd(dppf)Cl2(42mg,0.050mmol)、乙酸钠(82mg,1.0mmol)、K3PO4三水合物(266mg,1.0mmol)、水(6滴)和乙腈(6mL)。在三轮真空/氮气吹洗后,将混合物在95℃加热2小时。然后将其过滤并减压蒸发滤液。将残余物通过硅胶柱色谱法来纯化(用25:1二氯甲烷/甲醇洗脱)得到337e(200mg,50%),其为棕色固体。LCMS-ESI:[M+H]+570.3
实施例337 3-[4-[5-[(1,2-二甲基咪唑-4-基)氨基]-1-甲基-6-氧代-3-吡啶基]-3-(羟基甲基)-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮337
将337e(100mg,0.19mmol)和氢氧化锂(34mg,1.4mmol)于异丙醇/THF(1:1,4mL)和水(1mL)中的混合物在40℃搅拌0.5小时。将混合物减压蒸发并将残余物用水(10mL)稀释。然后将其用乙酸乙酯(2X10mL)萃取。将合并的乙酸乙酯萃取物减压浓缩并将残余物通过反相制备性-HPLC来纯化得到337(35mg,40%),其为白色固体。LCMS-ESI:[M+H]+528.3.1H NMR(500MHz,CDCl3)δ8.45(d,J=5.0Hz,1H),7.36(s,1H),7.28-7.27(m,2H),7.25(d,J=5.0Hz,1H),6.84(s,1H),6.79(s,1H),4.62-4.40(m,3H),4.15-4.14(m,2H),3.84-3.81(m,1H),3.67(s,3H),3.52(s,3H),2.57-2.56(m,2H),2.51(s,2H),2.32(s,3H),1.27(s,6H).
实施例338a 3-(2-硝基-6,7-二氢吡唑并[1,5-a]吡嗪-5(4H)-基)丙腈338a
按照实施例296d的操作,以1-(2-溴乙基)-5-(氯甲基)-3-硝基-1H-吡唑296d(268mg,1.00mmol)和3-氨基丙腈(210mg,3.00mmol)开始得到338a,其为白色固体(180mg,81%)。MS-ESI:[M+H]+222.1
实施例338b 3-(2-氨基-6,7-二氢吡唑并[1,5-a]吡嗪-5(4H)-基)丙腈338b
按照实施例296e的操作,并以338a(180mg,0.81mmol)开始,得到338b,其为黄色固体(120mg,77%)。MS-ESI:[M+H]+192.2
实施例338c 3-(2-(5-溴-1-甲基-2-氧代-1,2-二氢吡啶-3-基氨基)-6,7-二氢吡唑并[1,5-a]吡嗪-5(4H)-基)丙腈338c
按照实施例309c的操作,并以338b(120mg,0.63mmol)和3,5-二溴-1-甲基吡啶-2(1H)-酮(169mg,0.63mmol)开始,得到338c,其为黄色固体(150mg,63%)。MS-ESI:[M+H]+377.2
实施例338d乙酸[4-(5-{[5-(2-氰基乙基)-4H,5H,6H,7H-吡唑并[1,5-a]吡嗪-2-基]氨基}-1-甲基-6-氧代-1,6-二氢吡啶-3-基)-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-3-基]甲酯338d
按照实施例309d的操作,以338c(150mg,0.45mmol)和{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(358mg,0.90mmol)开始,得到338d,其为黄色固体(150mg,52%)。MS-ESI:[M+H]+650.3
实施例338 3-[2-[[5-[2-(7,7-二甲基-4-氧代-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-3-基)-3-(羟基甲基)-4-吡啶基]-1-甲基-2-氧代-3-吡啶基]氨基]-6,7-二氢-4H-吡唑并[1,5-a]吡嗪-5-基]丙腈338
按照实施例309的操作,以338e(150mg,0.23mmol)开始得到338,其为白色固体(55mg,40%)。MS-ESI:[M+H]+608.3.1H NMR(500MHz,CDCl3)δ8.49(d,J=5.0Hz,1H),7.96(d,J=2.5Hz,1H),7.71(d,J=2.0Hz,1H),7.42(s,1H),7.35(d,J=5.0Hz,1H),6.85(s,1H),5.74(s,1H),5.05(t,J=6.5Hz,1H),4.66-4.64(m,1H),4.52-4.50(m,1H),4.36-4.34(m,1H),4.17-4.16(m,2H),4.09-4.07(m,2H),3.88-3.84(m,1H),3.75(s,2H),3.71(s,3H),3.05-3.03(m,2H),2.93-2.90(m,2H),2.63-2.58(m,4H),2.53(s,2H),1.29(s,6H).
实施例339a 4-(6-硝基吡啶-3-基)哌嗪-1-羧酸叔丁酯339a
向5-溴-2-硝基吡啶(30.0g,148mmol)于DMSO(1L)中的溶液中加入K2CO3(40.0g,296mmol)和哌嗪-1-羧酸叔丁酯(28.0g,148mmol)。将混合物在65℃搅拌整夜。冷却下来后,将其倒入水(2L)中。收集析出的固体并真空干燥。然后将其进一步通过硅胶柱色谱法来纯化(用20:1石油醚/乙酸乙酯洗脱,然后用二氯甲烷洗脱)得到339a,其为黄色固体(17.0g,37%)。MS-ESI:[M+H]+309.
实施例339b 4-(6-氨基吡啶-3-基)哌嗪-1-羧酸叔丁酯339b
将500-mL圆底烧瓶用氮气吹洗并装入339a(3.1g,10mmol)、10%钯/炭(50%水分,1.0g)和乙醇(100mL)。将其排空,通过气囊充入氢气并在室温搅拌16小时。然后将氢气排空并将氮气充入所述烧瓶中。通过用垫过滤除去催化剂并减压浓缩滤液得到339b(2.7g,97%)。MS-ESI:[M+H]+279
实施例339c 4-(6-(5-溴-1-甲基-2-氧代-1,2-二氢吡啶-3-基氨基)吡啶-3-基)哌嗪-1-羧酸叔丁酯339c
在配备有磁力搅拌子和回流冷凝器的100-mL单颈圆底烧瓶中装入339b(1.3g,4.7mmol)、3,5-二溴-1-甲基吡啶-2(1H)-酮(1.24g,4.7mmol)、碳酸铯(3.8g,12mmol)和1,4-二噁烷(50mL)。使氮气鼓泡通过所得混合物30分钟后,加入XantPhos(272mg,0.47mmol)和三(二亚苄基丙酮)二钯(0)(430mg,0.47mmol)。使体系经历三轮氩气/真空吹洗并回流加热3小时。之后,将反应混合物冷却至室温并过滤。使滤液在乙酸乙酯(100mL)和水(100mL)之间分配。分离出水层并用乙酸乙酯(2X50mL)萃取。将合并的有机层用盐水(50mL)洗涤并用硫酸钠干燥。过滤除去干燥剂并减压浓缩滤液。将残余物通过硅胶柱色谱法来纯化(用50:1二氯甲烷/甲醇洗脱)得到339c(1.3g,59%)。MS-ESI:[M+H]+464.
实施例339d 4-{6-[(5-{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}-1-甲基-2-氧代-1,2-二氢吡啶-3-基)氨基]吡啶-3-基}哌嗪-1-羧酸叔丁酯339d
在配备有磁力搅拌子和回流冷凝器的50-mL单颈圆底烧瓶中装入乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼杂戊环-2-基)吡啶-3-基)甲酯199e(287.4mg,0.60mmol)、339c(145mg,0.30mmol)、Pd(dppf)Cl2(24.5mg,0.030mmol)、K3PO4(127.2mg,0.60mmol)、乙酸钠(49.2mg,0.60mmol)、水(0.50mL)和乙腈(10mL)。在三轮真空/氮气吹洗后,将混合物在95℃加热1小时。然后将其冷却至室温并过滤。减压浓缩滤液并将残余物通过硅胶柱色谱法来纯化(用乙酸乙酯洗脱)得到339d,其为黄色固体(140mg,61%)。MS-ESI:[M+H]+737.3.
实施例339e乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-(1-甲基-6-氧代-5-{[5-(哌嗪-1-基)吡啶-2-基]氨基}-1,6-二氢吡啶-3-基)吡啶-3-基)甲酯339e
将339d(130mg,0.18mmol)和HCl/甲醇(4.0mL)的混合物在室温搅拌4小时。然后将其减压浓缩得到粗制339e(100mg,87%),将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+637.3.
实施例339 3-[3-(羟基甲基)-4-[5-[[5-[4-(2-甲氧基乙基)哌嗪-1-基]-2-吡啶基]氨基]-1-甲基-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮339
将339e(100mg,0.18mmol)、1-溴-2-甲氧基乙烷(24.8mg,0.18mmol)和K2CO3(49.7mg,0.36mmol)于乙腈(5.0mL)中的混合物在密封管中在85℃搅拌整夜。将混合物冷却至室温并过滤。减压浓缩滤液。向残余物中加入水并将所得混合物用二氯甲烷萃取三次。将合并的有机层减压浓缩并将所得残余物通过反相制备性-HPLC来纯化得到339,其为黄色固体(31.1mg,30%)。MS-ESI:[M+H]+653.3.1H NMR(500MHz,DMSO)δ8.61(d,J=2.0Hz,1H),8.49(d,J=5.0Hz,1H),8.40(s,1H),7.84(d,J=3.0Hz,1H),7.46(d,J=2.0Hz,1H),7.38-7.34(m,2H),7.23(d,J=9.5Hz,1H),6.57(s,1H),4.97-4.95(m,1H),4.45-4.40(m,2H),4.23-4.19(m,3H),3.85-3.83(m,1H),3.60(s,3H),3.47-3.44(m,2H),3.24(s,3H),3.04-3.02(m,4H),2.59-2.53(m,重叠,8H),2.43(s,2H),1.23(s,6H).
实施例340a(3S)-3-甲基-4-(6-硝基吡啶-3-基)哌嗪-1-羧酸叔丁酯340a
按照实施例323a的操作,以(3S)-3-甲基哌嗪-1-羧酸叔丁酯(10.0g,50mmol)和5-溴-2-硝基吡啶(10.5g,50mmol)开始得到340a,其为黄色固体(8.05g,50%)。MS-ESI:[M+H]+323
实施例340b(3S)-4-(6-氨基吡啶-3-基)-3-甲基哌嗪-1-羧酸叔丁酯340b
按照实施例323b的操作,以340a(5.8g,18mmol)开始得到340b,其为棕色固体(4.9g,93%)。MS-ESI:[M+H]+293
实施例340c(3S)-4-(6-(5-溴-1-甲基-2-氧代-1,2-二氢吡啶-3-基氨基)吡啶-3-基)-3-甲基哌嗪-1-羧酸叔丁酯340c
按照实施例323c的操作,以340b(4.0g,13.7mmol)和3,5-二溴-1-甲基吡啶-2(1H)-酮(5.5g,20.6mmol)开始得到340c,其为黄色固体(5.4g,83%)。MS-ESI:[M+H]+478
实施例340d(3S)-5-溴-1-甲基-3-(5-(2-甲基哌嗪-1-基)吡啶-2-基氨基)吡啶-2(1H)-酮340d
按照实施例271c的操作,以340c(3.1g,6.5mmol)开始得到340d,其为黄色固体(2.3g,94%)。MS-ESI:[M+H]+378.
实施例340e(S)-5-溴-3-(5-(4-(2-甲氧基乙基)-2-甲基哌嗪-1-基)吡啶-2-基氨基)-1-甲基吡啶-2(1H)-酮340e
将340d(500mg,1.32mmol)、1-溴-2-甲氧基乙烷(239.1mg,1.72mmol)、K2CO3(364mg,2.64mmol)和乙腈(6mL)的混合物在密封管中在80℃加热12小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。将其冷却至室温并过滤。减压浓缩滤液。将残余物溶解在水(20mL)和乙酸乙酯(30mL)中。将水相用乙酸乙酯(3X30mL)萃取。将合并的有机层用盐水洗涤,用Na2SO4干燥,减压浓缩得到粗制340e,其为黑色油状物(600mg),将其不经进一步纯化即用于下一步骤。MS-ESI:[M+H]+436.1
实施例340f乙酸(2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}-4-[5-({5-[(2S)-4-(2-甲氧基乙基)-2-甲基哌嗪-1-基]吡啶-2-基}氨基)-1-甲基-6-氧代-1,6-二氢吡啶-3-基]吡啶-3-基)甲酯340f
在配备有回流冷凝器的50-mL圆底烧瓶中装入340e(180mg,0.412mmol)、{3-[(乙酰氧基)甲基]-2-{4,4-二甲基-9-氧代-1,10-二氮杂三环[6.4.0.02,6]十二碳-2(6),7-二烯-10-基}吡啶-4-基}硼酸199e(327.3mg,0.824mmol)、Pd(dppf)Cl2(16.8mg,0.0206mmol)、K3PO4(174.7mg,0.824mmol)、乙酸钠(67.6mg,0.824mmol)、乙腈(10mL)和水(3滴)。使体系经历三轮真空/氮气吹洗并在氮气保护下在100℃加热1小时。通过LCMS分析反应混合物,结果显示完全转化成所期望的产物。然后将其冷却至室温并过滤。减压浓缩滤液。将残余物通过硅胶柱色谱法来纯化(用20:1二氯甲烷/甲醇洗脱)得到340f,其为黄色油状物(190mg,65%)。MS-ESI:[M+H]+709.4
实施例340 3-[3-(羟基甲基)-4-[5-[[5-[(2S)-4-(2-甲氧基乙基)-2-甲基-哌嗪-1-基]-2-吡啶基]氨基]-1-甲基-6-氧代-3-吡啶基]-2-吡啶基]-7,7-二甲基-1,2,6,8-四氢环戊二烯并[3,4]吡咯并[3,5-b]吡嗪-4-酮340
向340f(170mg,0.24mmol)于THF(6mL)、异丙醇(6mL)和水(6mL)中的溶液中加入氢氧化锂(57.6mg,2.4mmol)。在室温搅拌1小时后,减压浓缩反应混合物。将残余物溶解在二氯甲烷(20mL)和水(10mL)中。将水相用二氯甲烷(3X20mL)萃取。将合并的有机层用盐水洗涤,用Na2SO4干燥,减压浓缩并通过反相制备性-HPLC来纯化得到340(48.5mg,30%),其为白色固体。MS-ESI:[M+H]+667.3.1H NMR(500MHz,DMSO-d6)δ8.62(d,J=2.5Hz,1H),8.49(d,J=5.0Hz,1H),8.42(s,1H),7.82(d,J=2.5Hz,1H),7.47(d,J=2.5Hz,1H),7.37-7.34(m,2H),7.24(d,J=9.0Hz,1H),6.56(s,1H),4.97-4.95(m,1H),4.47-4.41(m,2H),4.25-4.19(m,3H),3.85-3.83(m,1H),3.63-3.62(m,1H),3.61(s,3H),3.47-3.45(m,2H),3.25(s,3H),3.06-3.04(m,1H),2.93-2.89(m,1H),2.70-2.68(m,1H),2.62-2.32(m,重叠,9H),1.22(s,6H),0.91(d,J=6.5Hz,3H).
实施例901生物化学Btk测定
可被用于测试式I化合物的标准生物化学Btk激酶测定的一般操作如下所述。制备无Btk酶的标准混合物(master mix),其含有1X细胞信号传导激酶缓冲液(25mM Tris-HCl,pH 7.5,5mMβ-磷酸甘油,2mM二硫苏糖醇,0.1mM Na3VO4,10mM MgCl2)、0.5μM Promega PTK生物素化肽底物2和0.01%BSA。制备添加Btk酶的标准混合物,其含有1X细胞信号传导激酶缓冲液、0.5μM PTK生物素化肽底物2,0.01%BSA和100ng/孔(0.06mU/孔)的Btk酶。Btk酶如下制备:将具有C-末端V5和6x His标志的全长人野生型Btk(登录号NM-000061)亚克隆到pFastBac载体中,用于制备携带该表位-标志的Btk的杆状病毒。杆状病毒的生成是基于在Invitrogen公开的方案"Bac-to-Bac Baculovirus Expression Systems"(目录号10359-016和10608-016)中详细描述的说明完成的。通道3病毒用于感染Sf9细胞以过表达所述重组Btk蛋白。然后用Ni-NTA柱将所述Btk蛋白纯化为同质。基于敏感性Sypro-Ruby染色法,最终蛋白制剂的纯度大于95%。在水中制备200μM ATP的溶液并用1N NaOH调整至pH7.4。将1.25μL量的化合物/5%DMSO转移到96-孔1/2面积Costar聚苯乙烯板中。将化合物单独测试和以11-点剂量-应答曲线(起始浓度为10μM;1:2稀释)测试。将18.75μL量的无酶的标准混合物(其为阴性对照)和添加酶的标准混合物转移到96-孔1/2面积Costar聚苯乙烯板的适当的孔中。向于96-孔1/2面积Costar聚苯乙烯板中的混合物中加入5μL 200μM ATP以使最终ATP浓度为40μM。使反应混合物在室温孵育1小时。将反应用Perkin Elmer 1X检测缓冲液终止,所述检测缓冲液含有30mM EDTA,20nM SA-APC和1nM PT66Ab。将所述板通过PerkinElmer Envision使用时间分辨的荧光来读板,所述Perkin Elmer Envision使用激发滤光器330nm,发射滤光器665nm和第二发射滤光器615nm。随后计算IC50值。可选择地,Lanthascreen测定可用于通过量化其磷酸化肽产物来评估Btk活性。在肽产物上的荧光素与检测抗体上的铽之间出现的FRET(荧光共振能量转移)随着Btk抑制剂的添加而减少,所述Btk抑制剂降低了所述肽的磷酸化。在最终25uL反应体积中,将Btk(h)(0.1ng/25ul反应混合物)与50mM Hepes(pH 7.5)、10mM MgCl2、2mM MnCl2、2mM DTT、0.2mM NaVO4、0.01%BSA和0.4uM荧光素poly-GAT一起孵育。通过添加ATP至25uM(ATP的Km)来引发所述反应。在室温孵育60分钟后,通过以下方法来终止反应:添加在60mM EDTA中的最终浓度为2nM的Tb-PY20检测抗体并在室温保持30分钟。在Perkin Elmer Envision上使用在340nM的激发和在495nm和520nm的发射来确定检测。示例性Btk抑制IC50值在表1、2和3中。
实施例902 Ramos细胞Btk测定
可用于测试式I化合物的标准细胞Btk激酶测定的另一种一般化操作如下所述。在测试化合物的存在下,将Ramos细胞以0.5x107个细胞/ml的密度在37℃孵育1小时。然后通过与10μg/ml抗人IgM F(ab)2在37℃孵育5分钟来刺激细胞。使细胞成粒、溶解并对澄清的溶胞产物进行蛋白测定。使相同蛋白量的每种样品经历SDS-PAGE并用抗-磷酸Btk(Tyr223)抗体(Cell Signaling Technology#3531;Epitomics,目录号#2207-1)或磷酸Btk(Tyr551)抗体(BD Transduction Labs#558034)进行西式印迹法以评估Btk自磷酸化或抗-Btk抗体(BD Transduction Labs#611116)以控制每种溶胞产物中的Btk的总量。
实施例903 B-细胞增生测定
可用于测试式I化合物的标准细胞B-细胞增生测定的一般操作如下所述。用B-细胞分离试剂盒(Miltenyi Biotech,Cat#130-090-862)自8-16周龄Balb/c小鼠的脾脏纯化B-细胞。将测试化合物在0.25%DMSO中稀释并与2.5X105纯化的小鼠脾脏B-细胞孵育30分钟,然后添加10μg/ml抗-小鼠IgM抗体(Southern Biotechnology Associates Cat#1022-01)以使最终体积为100μl。孵育24小时后,添加1μCi 3H-胸腺嘧啶并再孵育额外36小时,然后用制造商就SPA[3H]胸腺嘧啶吸收测定系统(Amersham Biosciences#RPNQ0130)所述的方案收获。在Microbeta计数器(Wallace Triplex 1450,Perkin Elmer)中计数基于SPA-珠子的荧光。
实施例904 T细胞增生测定
可用于测试式I化合物的标准T细胞增生测定的一般操作如下所述。用Pan T细胞分离试剂盒(Miltenyi Biotech,Cat#130-090-861)自8-16周龄Balb/c小鼠的脾脏纯化T细胞。将测试化合物在0.25%DMSO中稀释并在透明平底板中在100μl最终体积中与2.5X105纯化的小鼠脾脏T细胞一起孵育,所述透明平底板用10μg/ml的抗-CD3(BD#553057)和抗-CD28(BD#553294)抗体中的每一种在37℃预孵育90分钟。孵育24小时后,加入1μCi 3H-胸腺嘧啶并将板孵育额外36小时,然后用制造商就SPA[3H]胸腺嘧啶吸收测定洗脱(AmershamBiosciences#RPNQ 0130)所描述的方案收获。在Microbeta计数器(Wallace Triplex1450,Perkin Elmer)中计数基于SPA-珠子的荧光。
实施例905 CD86抑制测定
可用于测试式I化合物的抑制B细胞活性的标准测定的一般操作如下所述。通过红血细胞溶解(BD Pharmingen#555899)自8-16周龄Balb/c小鼠纯化全鼠脾细胞。将测试化合物稀释至0.5%DMSO并在最终体积200μl中在透皮平底板(Falcon 353072)中在37℃孵育60分钟。然后通过添加15μg/ml IgM(Jackson ImmunoResearch 115-006-020)并在37℃,5%CO2孵育24小时来刺激细胞。孵育24小时后,将细胞转移到圆锥形底的透明96-孔板中并通过在1200XgX5分钟离心使其沉淀。将细胞用CD16/CD32(BD Pharmingen#553142)预阻断,然后用CD19-FITC(BD Pharmingen#553785)、CD86-PE(BD Pharmingen#553692)和7AAD(BDPharmingen#51-68981E)三重染色。将细胞贮存在BD FACSCalibur上并为CD19+/7AAD-数设置门控。相对于测试化合物浓度,测量CD86表面表达在门控数方面的水平。
实施例906 B-ALL细胞存活测定
下面的内容为使用XTT读数器测量活细胞数目的标准B-ALL(急性淋巴母细胞性白血病)细胞存活研究的操作。该测定可用于测试式I化合物抑制培养物中B-ALL细胞存活的能力。可使用的一种人B-细胞急性淋巴母细胞性白血病系为SUP-B15,其为自ATCC获得的Pre-B-细胞ALL系。
将SUP-B15pre-B-ALL细胞放置在于100μl Iscove培养基+20%FBS中的多个96-孔微量滴定板中,浓度为5X105个细胞/ml。然后添加测试化合物,最终浓度为0.4%DMSO。将细胞在37℃,5%CO2孵育最多3天。3天后,将细胞以1:3分装在新鲜的含有测试化合物的96-孔板中并使其生长额外3天。在每个24小时后,将50ul XTT溶液加至平行测定的96-孔板的每一个板中并按照制造商的指示在2、4和20小时读取吸收读数。然后用OD读取在所述测定线性范围内的仅DMSO处理细胞的读数,并且相对于DMSO处理的细胞测量化合物处理孔中的活细胞的百分比。
实施例907 CD69全血测定
从健康志愿者获得人血液,对所述志愿者具有以下限制:1周内未用药,不吸烟。通过静脉穿刺收集血液(约20mL,从而测试8个化合物),并装入含有肝素钠的(Becton,Dickinson and Co.)管中。
对于十点剂量响应曲线,将浓度为10μM的式I化合物的DMSO溶液在100%DMSO中以1:10稀释,然后在100%DMSO中三倍连续稀释。将化合物进一步在PBS中以1:10稀释,然后将每种化合物的5.5μl等分液一式两份地加至2mL 96-孔板中;加入5.5μl 10%DMSO/PBS作为对照和无刺激物孔。向每个孔中加入人全血–HWB(100μl)。搅拌后,将所述板在37℃,5%CO2,100%湿度孵育30分钟。在搅拌下,向每个孔(无刺激物孔除外)中加入羊F(ab’)2抗人IgM(10μl浓度为500μg/ml溶液,最终为50μg/ml),将板再孵育20小时。20小时孵育结束时,将样品与荧光标记的抗体一起在37℃,5%CO2,100%湿度孵育30分钟。该试验包括诱导的对照、未染色和单染色品,用于补偿调整和初始电压设置。然后将样品用PharM LyseTM(BDBiosciences Pharmingen)溶解。根据制造商的说明进行溶解。然后将样品转移到96孔板中,所述板适于在BD Biosciences HTS 96孔系统上在LSRII机器上运行。使用BDBiosciences DIVA软件得到获得性数据和平均荧光强度值。通过FACS分析软件(Flow Jo)对结果进行初始分析。将试验化合物的抑制浓度(IC50、IC70、IC90等)定义为使CD69细胞的阳性百分数(即由抗-IgM刺激的CD20阳性)减少50%的浓度(减去无刺激物背景的8个孔的平均值后获得的8个对照孔的平均值)。通过Prism版本5使用非线性回归曲线拟合计算IC70值,并且显示在表1和2中。
实施例908体外细胞增生测定
式I化合物的效力通过采用以下方案(Mendoza等人(2002)Cancer Res.62:5485-5488)进行的细胞增殖测定来测量。所述发光细胞存活力测定(包括试剂和方案)为商购的(Promega Corp.,Madison,WI,Technical Bulletin TB288)。所述测定评估化合物进入细胞和抑制细胞增殖的能力。测定原理基于通过对均质测定中存在的ATP进行定量确定存在的活细胞数目,其中加入Cell-Titer Glo试剂导致细胞溶解和通过荧光素酶反应生成发光信号。发光信号与存在的ATP的量成正比。
将一组B-细胞淋巴瘤细胞系(BJAB、SUDHL-4、TMD8、OCI-Ly10、OCI-Ly3、WSU-DLCL2)接板在于正常生长介质中的384-孔板中,并向每个孔中单独加入连续稀释的BTK抑制剂或DMSO。通过(Promega)孵育96小时后评估细胞存活力。数据可表现为BTK抑制剂处理的细胞相对于DMSO-处理的对照细胞的相对细胞存活力。数据点为每种剂量水平4个复制品的均值。误差棒代表偏离所述均质的SD。
操作:第1天–向细胞板(Cell Plates)(384-孔黑色,透明底部,microclear,来自Falcon#353962的带盖子的TC板)接种,收获细胞,以1000个细胞/54μl/孔在384孔细胞板中接种细胞,进行3天测定。细胞培养基:RPMI或DMEM高糖(high glucose)、10%胎牛血清、2mML-谷氨酰胺,P/S。在37℃、5%CO2条件下孵育过夜(O/N)。
第二天–将药物加入到细胞中,稀释化合物,DMSO板(对于9个点以1:2连续稀释),在96孔板的第2栏中加入20ul浓度为10mM的化合物。对于总共9个点,在整个板中使用Precision进行1:2连续稀释(10μl+20μl 100%DMSO)。培养基板为来自Nunc(目录编号:249946)的96-孔圆锥形底聚丙烯板(1:50稀释)。在所有孔中加入147μl培养基。使用Rapidplate将来自DMSO板每个孔中的3μl DMSO+化合物转移到培养基板上每个相应孔中。
向细胞中加入药物,细胞板(1:10稀释),向细胞中直接加入6μl培养基+化合物(在细胞上已有54μl培养基)。在37℃、5%CO2条件下,在不经常打开的培养箱中孵育3天。
第5天–培育板,在室温解冻Cell Titer Glo缓冲液。将细胞板从37℃移出并平衡至室温,保持约30分钟。向Cell Titer Glo底物中加入Cell Titer Glo缓冲液(瓶对瓶)。向每孔细胞中加入30μl Cell Titer Glo试剂(Promega目录编号:G7572)。在板震摇器上放置约30分钟。在Analyst HT板读数器上读取发光(半秒/孔)。
细胞存活力测定和组合测定:将细胞以1000-2000细胞/孔接种在384-孔板中,保持16小时。在第二天,在96孔板中在DMSO中制备9份化合物的1:2系列稀释液。使用Rapidplate robot(Zymark Corp.,Hopkinton,MA)将所述化合物进一步稀释成生长培养基。然后将稀释的化合物加入到384-孔细胞板的四倍孔中,在37℃和5%CO2孵育。4天后,使用Cell-TiterGlo(Promega)根据制造商的指示通过发光测量活细胞的相对数目并在Wallac Multilabel读数器(PerkinElmer,Foster City)上读数。使用4.0软件(GraphPad,San Diego)计算EC50值。在所有测定中同时加入式I化合物和化学治疗剂或相隔4小时(相继)加入式I化合物和化学治疗剂。
体外细胞增殖测定中的额外实例包括以下步骤:
1.将等份的100毫升细胞培养物(在培养基中含有约104细胞)沉积在384孔不透明壁板的每孔中。
2.制备含有培养基但不含细胞的对照孔。
3.将化合物加至实验孔中,然后孵育3-5天。
4.将板平衡至室温并保持约30分钟。
5.加入体积与每孔中存在的细胞培养基的体积相同的CellTiter-Glo试剂。
6.将内含物在定轨振荡器(orbital shaker)中混合2分钟以诱导细胞溶解。
7.将板在室温孵育10分钟以稳定发光信号。
8.记录发光信号并以图表形式报道,其为RLU=相对发光单位。
尽管出于清楚理解的目的已通过举例说明和实施例较详细地描述了前述发明,但所述描述和实施例不应被理解为限制本发明的范围。因此,所有适当的改变和等同物可被认为落入随附权利要求限定的本发明范围内。将本申请引用的所有专利和科技文献的全部内容专门并入本申请作为参考。
Claims (33)
1.选自式I的化合物或其可药用盐在制备用于治疗选自由Bruton酪氨酸蛋白激酶介导的免疫障碍、癌症、心血管疾病、病毒感染、炎症、代谢/内分泌机能障碍和神经障碍的疾病或障碍的药物中的用途:
其中:
X1为CR1或N;
X2为CR2或N;
X3为CR3或N;
其中X1、X2和X3中的一个或两个为N;
R1、R2和R3独立地选自H、F、Cl、-NH2、-NHCH3、-N(CH3)2、-OH、-OCH3、-OCH2CH3、-OCH2CH2OH和C1-C3烷基;
R4选自H、F、Cl、CN、-CH2OH、-CH(CH3)OH、-C(CH3)2OH、-CH(CF3)OH、-CH2F、-CHF2、-CH2CHF2、-CF3、-C(O)NH2、-C(O)NHCH3、-C(O)N(CH3)2、-NH2、-NHCH3、-N(CH3)2、-NHC(O)CH3、-OH、-OCH3、-OCH2CH3、-OCH2CH2OH、环丙基、环丙基甲基、1-羟基环丙基、咪唑基、吡唑基、3-羟基-氧杂环丁烷-3-基、氧杂环丁烷-3-基和氮杂环丁烷-1-基;
R5为任选取代的C6-C20芳基,其中所述芳基为苯基;任选取代的C1-C20杂芳基,其中所述杂芳基选自吡唑基、吡啶基、嘧啶基、吡嗪基、三嗪基、噁唑基、噻二唑基、咪唑基、异噁唑基、三唑基、哒嗪基、吲唑基、异噻唑基、5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基、5-乙酰基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基、6,7-二氢-4H-吡唑并[5,1-c][1,4]噁嗪-2-基和1-甲基-5-(5-(4-甲基哌嗪-1-基)吡啶-2-基;任选取代的-(C6-C20芳基)-(C2-C20杂环基),其中所述芳基为苯基,且所述杂环基为哌嗪基;任选取代的-(C1-C20杂芳基)-(C2-C20杂环基),其中所述杂芳基为吡啶基、吡嗪基或咪唑基,且所述杂环基为哌嗪基或氮杂环丁烷基;任选取代的-(C1-C20杂芳基)-(C2-C20杂环基)-(C1-C6烷基),其中所述杂芳基为吡啶基,且所述杂环基为哌嗪基;任选取代的-(C1-C20杂芳基)-(C1-C6烷基),其中所述杂芳基为嘧啶基、异噁唑基或吡唑基;或任选取代的-(C1-C20杂芳基)-C(=O)-(C2-C20杂环基),其中所述杂芳基为吡啶基或吡唑基,所述杂环基为吡咯烷基;
R6为H、-CH3、-CH2CH3、-CH2CH2OH、-CHF2、-NH2或-OH;
R7选自以下结构:
其中波浪线表示连接位点;和
Y1和Y2独立地选自CH和N,其中Y1和Y2不都是N;
其中烷基、碳环基、杂环基、芳基和杂芳基任选被一个或多个独立选自以下的基团取代:F、Cl、Br、I、-CN、-CH3、-CH2CH3、-CH(CH3)2、-CH2CH(CH3)2、-CH2OH、-CH2OCH3、-CH2CH2OH、-C(CH3)2OH、-CH(OH)CH(CH3)2、-C(CH3)2CH2OH、-CH2CH2SO2CH3、-CH2OP(O)(OH)2、-CH2F、-CHF2、-CF3、-CH2CF3、-CH2CHF2、-CH(CH3)CN、-C(CH3)2CN、-CH2CN、-CO2H、-COCH3、-CO2CH3、-CO2C(CH3)3、-COCH(OH)CH3、-CONH2、-CONHCH3、-CON(CH3)2、-C(CH3)2CONH2、-NH2、-NHCH3、-N(CH3)2、-NHCOCH3、-N(CH3)COCH3、-NHS(O)2CH3、-N(CH3)C(CH3)2CONH2、-N(CH3)CH2CH2S(O)2CH3、-NO2、=O、-OH、-OCH3、-OCH2CH3、-OCH2CH2OCH3、-OCH2CH2OH、-OCH2CH2N(CH3)2、-OP(O)(OH)2、-S(O)2N(CH3)2、-SCH3、-S(O)2CH3、-S(O)3H、环丙基、氧杂环丁烷基、氮杂环丁烷基、(1-甲基氮杂环丁烷-3-基)氧基、N-甲基-N-氧杂环丁烷-3-基氨基、氮杂环丁烷-1-基甲基和吗啉代。
2.选自式Ia的化合物或其可药用盐在制备用于治疗选自由Bruton酪氨酸蛋白激酶介导的免疫障碍、癌症、心血管疾病、病毒感染、炎症、代谢/内分泌机能障碍和神经障碍的疾病或障碍的药物中的用途:
其中:
X1为CR1或N;
X2为CR2或N;
X3为CR3或N;
其中X1、X2和X3中的一个或两个为N;
R1、R2和R3独立地选自H、F、Cl、-NH2、-NHCH3、-N(CH3)2、-OH、-OCH3、-OCH2CH3、-OCH2CH2OH和C1-C3烷基;
R4选自H、F、Cl、CN、-CH2OH、-CH(CH3)OH、-C(CH3)2OH、-CH(CF3)OH、-CH2F、-CHF2、-CH2CHF2、-CF3、-C(O)NH2、-C(O)NHCH3、-C(O)N(CH3)2、-NH2、-NHCH3、-N(CH3)2、-NHC(O)CH3、-OH、-OCH3、-OCH2CH3、-OCH2CH2OH、环丙基、环丙基甲基、1-羟基环丙基、咪唑基、吡唑基、3-羟基-氧杂环丁烷-3-基、氧杂环丁烷-3-基和氮杂环丁烷-1-基;
R5为任选取代的C6-C20芳基,其中所述芳基为苯基;任选取代的C1-C20杂芳基,其中所述杂芳基选自吡唑基、吡啶基、嘧啶基、吡嗪基、三嗪基、噁唑基、噻二唑基、咪唑基、异噁唑基、三唑基、哒嗪基、吲唑基、异噻唑基、5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基、5-乙酰基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基、6,7-二氢-4H-吡唑并[5,1-c][1,4]噁嗪-2-基和1-甲基-5-(5-(4-甲基哌嗪-1-基)吡啶-2-基;任选取代的-(C6-C20芳基)-(C2-C20杂环基),其中所述芳基为苯基,且所述杂环基为哌嗪基;任选取代的-(C1-C20杂芳基)-(C2-C20杂环基),其中所述杂芳基为吡啶基、吡嗪基或咪唑基,且所述杂环基为哌嗪基或氮杂环丁烷基;任选取代的-(C1-C20杂芳基)-(C2-C20杂环基)-(C1-C6烷基),其中所述杂芳基为吡啶基,且所述杂环基为哌嗪基;任选取代的-(C1-C20杂芳基)-(C1-C6烷基),其中所述杂芳基为嘧啶基、异噁唑基或吡唑基;或任选取代的-(C1-C20杂芳基)-C(=O)-(C2-C20杂环基),其中所述杂芳基为吡啶基或吡唑基,所述杂环基为吡咯烷基;
R6为H、-CH3、-CH2CH3、-CH2CH2OH、-CHF2、-NH2或-OH;
R7选自以下结构:
其中波浪线表示连接位点;和
其中烷基、碳环基、杂环基、芳基和杂芳基任选被一个或多个独立选自以下的基团取代:F、Cl、Br、I、-CN、-CH3、-CH2CH3、-CH(CH3)2、-CH2CH(CH3)2、-CH2OH、-CH2OCH3、-CH2CH2OH、-C(CH3)2OH、-CH(OH)CH(CH3)2、-C(CH3)2CH2OH、-CH2CH2SO2CH3、-CH2OP(O)(OH)2、-CH2F、-CHF2、-CF3、-CH2CF3、-CH2CHF2、-CH(CH3)CN、-C(CH3)2CN、-CH2CN、-CO2H、-COCH3、-CO2CH3、-CO2C(CH3)3、-COCH(OH)CH3、-CONH2、-CONHCH3、-CON(CH3)2、-C(CH3)2CONH2、-NH2、-NHCH3、-N(CH3)2、-NHCOCH3、-N(CH3)COCH3、-NHS(O)2CH3、-N(CH3)C(CH3)2CONH2、-N(CH3)CH2CH2S(O)2CH3、-NO2、=O、-OH、-OCH3、-OCH2CH3、-OCH2CH2OCH3、-OCH2CH2OH、-OCH2CH2N(CH3)2、-OP(O)(OH)2、-S(O)2N(CH3)2、-SCH3、-S(O)2CH3、-S(O)3H、环丙基、氧杂环丁烷基、氮杂环丁烷基、(1-甲基氮杂环丁烷-3-基)氧基、N-甲基-N-氧杂环丁烷-3-基氨基、氮杂环丁烷-1-基甲基和吗啉代。
3.权利要求1或2的用途,其中X1为N。
4.权利要求1或2的用途,其中X2为N。
5.权利要求1或2的用途,其中X3为N。
6.权利要求1或2的用途,其中X1和X3为N,X1和X2为N,或X2和X3为N。
7.权利要求1或2的用途,其中R5为任选取代的C1-C20杂芳基,所述杂芳基选自吡唑基、吡啶基、嘧啶基、5-甲基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基、5-乙酰基-4,5,6,7-四氢吡唑并[1,5-a]吡嗪-2-基、6,7-二氢-4H-吡唑并[5,1-c][1,4]噁嗪-2-基和1-甲基-5-(5-(4-甲基哌嗪-1-基)吡啶-2-基。
8.权利要求1或2的用途,其中R5为-(C1-C20杂芳基)-(C2-C20杂环基),其中杂芳基为任选取代的吡啶基,和杂环基为任选取代的哌嗪基。
9.权利要求1或2的用途,其中R5为苯基,其任选被一个或多个选自以下的基团取代:F、Cl、-CH3、-S(O)2CH3、环丙基、氮杂环丁烷基和氧杂环丁烷基。
12.权利要求1或2的用途,其中R6为CH3。
13.权利要求1的用途,其中Y1为CH,和Y2为N。
14.权利要求1的用途,其中Y1为N,和Y2为CH。
15.权利要求1的用途,其中Y1和Y2各自为CH。
16.权利要求1的用途,其中Y1和Y2各自为CH,和R6为CH3。
19.权利要求1的用途,其中所述化合物选自:
2-{4-羟基甲基-1'-甲基-5'-[5-(4-氧杂环丁烷-3-基-哌嗪-1-基)-吡啶-2-基氨基]-6'-氧代-1',6'-二氢-[3,3']联吡啶-5-基}-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮;
2-{3'-羟基甲基-1-甲基-5-[5-(4-氧杂环丁烷-3-基-哌嗪-1-基)-吡啶-2-基氨基]-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基}-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮;
2-{3'-羟基甲基-1-甲基-5-[5-((S)-2-甲基-4-氧杂环丁烷-3-基-哌嗪-1-基)-吡啶-2-基氨基]-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基}-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮;
2-[3'-羟基甲基-1-甲基-5-(5-甲基-4,5,6,7-四氢-吡唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基]-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮;
2-[3'-羟基甲基-1-甲基-6-氧代-5-(嘧啶-4-基氨基)-1,6-二氢-[3,4']联吡啶-2'-基]-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮;
2-[4-羟基甲基-1'-甲基-5'-(5-甲基-4,5,6,7-四氢-吡唑并[1,5-a]吡嗪-2-基氨基)-6'-氧代-1',6'-二氢-[3,3']联吡啶-5-基]-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮;
2-{3'-羟基甲基-1-甲基-5-[5-((R)-2-甲基-4-氧杂环丁烷-3-基-哌嗪-1-基)-吡啶-2-基氨基]-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基}-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮;
2-{5-[5-((2S,5R)-2,5-二甲基-4-氧杂环丁烷-3-基-哌嗪-1-基)-吡啶-2-基氨基]-3'-羟基甲基-1-甲基-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基}-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮;
2-[3'-羟基甲基-1-甲基-5-(5-氧杂环丁烷-3-基-4,5,6,7-四氢-吡唑并[1,5-a]吡嗪-2-基氨基)-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基]-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮;
2-{5-[5-((S)-2-乙基-4-氧杂环丁烷-3-基-哌嗪-1-基)-吡啶-2-基氨基]-3'-羟基甲基-1-甲基-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基}-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮;
2-[5-(6,7-二氢-4H-吡唑并[5,1-c][1,4]噁嗪-2-基氨基)-3'-羟基甲基-1-甲基-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基]-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮;
2-[5-(2,6-二甲基-嘧啶-4-基氨基)-3'-羟基甲基-1-甲基-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基]-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮;
2-[3'-羟基甲基-1-甲基-5-(2-甲基-嘧啶-4-基氨基)-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基]-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮;
2-[3'-羟基甲基-1-甲基-5-(6-甲基-嘧啶-4-基氨基)-6-氧代-1,6-二氢-[3,4']联吡啶-2'-基]-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮;
2-{3-羟基甲基-4-[6-(咪唑并[1,2-a]吡啶-7-基氨基)-4-甲基-5-氧代-4,5-二氢-吡嗪-2-基]-吡啶-2-基}-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮;和
2-[3'-羟基甲基-1-甲基-6-氧代-5-(吡嗪-2-基氨基)-1,6-二氢-[3,4']联吡啶-2'-基]-7,7-二甲基-3,4,7,8-四氢-2H,6H-环戊二烯并[4,5]吡咯并[1,2-a]吡嗪-1-酮。
21.权利要求1、2和13-20中任一项的用途,其中所述疾病或障碍为免疫障碍。
22.权利要求21的用途,其中所述免疫障碍为类风湿性关节炎。
23.权利要求1、2和13-20中任一项的用途,其中所述疾病或障碍为全身性炎症和局部炎症、器官移植排斥、变态反应、克罗恩氏病、哮喘、全身性红斑狼疮、舍格伦综合征、多发性硬化、硬皮病/全身性硬化症、特发性血小板减少性紫癜(ITP)、抗中性粒细胞胞质抗体(ANCA)或慢性阻塞性肺病(COPD)。
24.权利要求1、2和13-20中任一项的用途,其中所述疾病或障碍为关节炎、与免疫抑制相关的炎症、溃疡性结肠炎、皮炎、血管炎或牛皮癣。
25.权利要求1、2和13-20中任一项的用途,其中所述疾病或障碍为选自以下的癌症:乳癌、卵巢癌、前列腺癌、睾丸癌、泌尿生殖道癌、食道癌、喉癌、成胶质细胞瘤、神经母细胞瘤、胃癌、皮肤癌、角化棘皮瘤、肺癌、表皮样癌、小细胞癌、骨癌、结肠癌、胰腺癌、甲状腺癌、滤泡性癌、未分化癌、乳头状癌、精原细胞瘤、黑色素瘤、肉瘤、膀胱癌、肾癌、胰脏癌、骨髓障碍、淋巴瘤、毛细胞癌、口腔癌、鼻咽癌、咽癌、唇癌、舌癌、口癌、小肠癌、结肠-直肠癌、大肠癌、直肠癌、脑和中枢神经系统癌症、何杰金氏病、白血病、支气管癌、肝脏和肝内胆管癌、肝细胞癌、神经胶质瘤/成胶质细胞瘤、黑色素瘤、肾脏和肾盂癌、膀胱癌、子宫癌、多发性骨髓瘤、淋巴细胞白血病、髓细胞性白血病、非何杰金淋巴瘤和绒毛状结肠腺瘤。
26.权利要求1、2和13-20中任一项的用途,其中所述疾病或障碍为选自以下的癌症:子宫颈癌、大细胞癌、非小细胞肺癌(NSCLC)、腺瘤、子宫内膜癌、急性髓细胞性白血病、慢性髓细胞性白血病和慢性淋巴样白血病(CLL)。
27.权利要求1、2和13-20中任一项的用途,其中所述疾病或障碍为肺腺癌。
28.权利要求1、2和13-20中任一项的用途,进一步包括给药选自以下的额外治疗剂:抗炎剂、免疫调节剂、化疗剂、细胞凋亡增强剂、亲神经因子、用于治疗心血管疾病的药物、用于治疗肝病的药物、抗病毒药物、用于治疗血液障碍的药物、用于治疗糖尿病的药物和用于治疗免疫缺陷障碍的药物。
29.权利要求1、2和13-20中任一项的用途,其中所述疾病或障碍选自关节炎性疾病;贝赫切特病;脓毒病、脓毒性休克、内毒素性休克、革兰氏阴性脓毒病、革兰氏阳性脓毒病和中毒性休克综合征;继发于败血症的多发性器官损伤综合征、创伤或出血;眼部障碍;嗜酸细胞肉芽肿;肺或呼吸疾病;心肌膜、脑或骨端的再灌注损伤;纤维化;瘢痕疙瘩形成或瘢痕组织形成;动脉粥样硬化;自身免疫性疾病;和移植排斥障碍;慢性肾小球肾炎;炎症性肠病;炎症性皮肤病;由于感染引起的发热和肌痛;中枢或外周神经系统炎性疾病;斯耶格伦氏综合征;牵涉白细胞渗出的疾病;酒精性肝炎;细菌性肺炎;抗原-抗体复合物介导的疾病;低血容量性休克;I型糖尿病;急性和迟发型超敏反应;由于白细胞恶性增生和转移引起的病症;热损伤;粒细胞输注相关综合征;和细胞因子诱导的毒性的药物中的用途。
30.权利要求1、2和13-20中任一项的用途,其中所述疾病或障碍选自类风湿性关节炎、单关节炎、骨关节炎、痛风性关节炎、脊椎炎、变应性结膜炎、春季结膜炎、葡萄膜炎和甲状腺相关眼病、哮喘、慢性支气管炎、变应性鼻炎、ARDS、慢性肺部炎症性疾病、硅肺病、肺结节病、胸膜炎、肺泡炎、血管炎、肺气肿、肺炎、支气管扩张和肺型氧中毒、囊性纤维化、全身性红斑狼疮(SLE)、自身免疫性甲状腺炎、多发性硬化、糖尿病和Reynaud综合征、GVHD和同种异体移植物排斥、慢性炎症性肠病(CIBD)、克罗恩氏病、溃疡性结肠炎和坏死性小肠结肠炎、接触性皮炎、特应性皮炎、牛皮癣或荨麻疹、脑膜炎、脑炎和由于小创伤引起的脑或脊髓损伤。
31.权利要求1、2和13-20中任一项的用途,其中所述疾病或障碍为慢性阻塞性肺病。
32.权利要求1、2和13-20中任一项的用途,其中所述疾病或障碍选自类风湿性关节炎、全身性红斑狼疮、荨麻疹和多发性硬化。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201161555393P | 2011-11-03 | 2011-11-03 | |
| US61/555,393 | 2011-11-03 | ||
| CN201280065965.8A CN104125959B (zh) | 2011-11-03 | 2012-11-02 | 作为btk活性的抑制剂的杂芳基吡啶酮和氮杂‑吡啶酮化合物 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201280065965.8A Division CN104125959B (zh) | 2011-11-03 | 2012-11-02 | 作为btk活性的抑制剂的杂芳基吡啶酮和氮杂‑吡啶酮化合物 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN107011348A CN107011348A (zh) | 2017-08-04 |
| CN107011348B true CN107011348B (zh) | 2020-01-10 |
Family
ID=47146779
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201710227680.4A Active CN107011348B (zh) | 2011-11-03 | 2012-11-02 | 作为btk活性的抑制剂的杂芳基吡啶酮和氮杂-吡啶酮化合物 |
| CN201280065965.8A Active CN104125959B (zh) | 2011-11-03 | 2012-11-02 | 作为btk活性的抑制剂的杂芳基吡啶酮和氮杂‑吡啶酮化合物 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201280065965.8A Active CN104125959B (zh) | 2011-11-03 | 2012-11-02 | 作为btk活性的抑制剂的杂芳基吡啶酮和氮杂‑吡啶酮化合物 |
Country Status (34)
| Country | Link |
|---|---|
| US (10) | US8716274B2 (zh) |
| EP (5) | EP4050012A1 (zh) |
| JP (5) | JP5976827B2 (zh) |
| KR (2) | KR20160003328A (zh) |
| CN (2) | CN107011348B (zh) |
| AR (2) | AR088641A1 (zh) |
| AU (5) | AU2012332365B2 (zh) |
| CA (1) | CA2853975C (zh) |
| CL (1) | CL2014001103A1 (zh) |
| CO (1) | CO6950472A2 (zh) |
| CR (1) | CR20140194A (zh) |
| CY (1) | CY1117097T1 (zh) |
| DK (2) | DK2773638T3 (zh) |
| EA (1) | EA023263B1 (zh) |
| ES (3) | ES2898938T3 (zh) |
| HK (1) | HK1201265A1 (zh) |
| HR (2) | HRP20151442T1 (zh) |
| HU (2) | HUE028019T2 (zh) |
| IL (1) | IL232060A (zh) |
| IN (1) | IN2014CN03250A (zh) |
| LT (1) | LT3002284T (zh) |
| MA (1) | MA35819B1 (zh) |
| MX (2) | MX361807B (zh) |
| PE (1) | PE20141586A1 (zh) |
| PL (3) | PL3521288T3 (zh) |
| PT (2) | PT3002284T (zh) |
| RS (2) | RS54505B1 (zh) |
| SG (1) | SG11201401992YA (zh) |
| SI (2) | SI3002284T1 (zh) |
| TR (1) | TR201909849T4 (zh) |
| TW (4) | TW202124384A (zh) |
| UA (1) | UA111756C2 (zh) |
| WO (1) | WO2013067274A1 (zh) |
| ZA (1) | ZA201804727B (zh) |
Families Citing this family (58)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EA027561B1 (ru) * | 2011-11-03 | 2017-08-31 | Ф.Хоффманн-Ля Рош Аг | Алкилированные соединения пиперазина в качестве ингибиторов тирозинкиназы брутона |
| UA111756C2 (uk) * | 2011-11-03 | 2016-06-10 | Ф. Хоффманн-Ля Рош Аг | Сполуки гетероарилпіридону та азапіридону як інгібітори тирозинкінази брутона |
| EP3016943B1 (en) * | 2013-07-03 | 2019-08-21 | F. Hoffmann-La Roche AG | Heteroaryl pyridone and aza-pyridone amide compounds |
| WO2015050703A1 (en) * | 2013-10-04 | 2015-04-09 | Yi Chen | Inhibitors of bruton's tyrosine kinase |
| KR101813830B1 (ko) | 2013-12-05 | 2017-12-29 | 에프. 호프만-라 로슈 아게 | 친전자성 작용기를 갖는 헤테로아릴 피리돈 및 아자-피리돈 화합물 |
| CN106922146B (zh) * | 2014-10-02 | 2020-05-26 | 豪夫迈·罗氏有限公司 | 用于治疗由布鲁顿酪氨酸激酶(btk)介导的疾病的吡唑甲酰胺化合物 |
| WO2016066490A1 (en) | 2014-10-27 | 2016-05-06 | F. Hoffmann-La Roche Ag | Process for making tricyclic lactam compounds |
| CN106188063A (zh) * | 2015-05-08 | 2016-12-07 | 中国科学院上海药物研究所 | 用作Lp-PLA2抑制剂的双环类化合物、其制备方法及医药用途 |
| CR20180138A (es) | 2015-09-02 | 2018-07-16 | Glaxosmithkline Ip No 2 Ltd | Piridinona dicaboxamidas para uso como inhibidores de bromodominio |
| EP3365335B1 (en) | 2015-10-23 | 2024-02-14 | Array Biopharma, Inc. | 2-aryl- and 2-heteroaryl-substituted 2-pyridazin-3(2h)-one compounds as inhibitors of fgfr tyrosine kinases |
| UY37128A (es) * | 2016-02-19 | 2017-09-29 | Novartis Ag | Compuestos tetracíclicos de piridona como antivirales |
| IL300209A (en) * | 2016-02-29 | 2023-03-01 | Hoffmann La Roche | Dosage preparations containing Bruton's tyrosine kinase inhibitor |
| JP6983813B2 (ja) * | 2016-04-28 | 2021-12-17 | エフ.ホフマン−ラ ロシュ アーゲーF. Hoffmann−La Roche Aktiengesellschaft | 2−ピラゾロ[1,5−a]ピラジン−2−イルピリド[1,2−a]ピリミジン−4−オンの調製のためのプロセス |
| CN108101905A (zh) * | 2016-11-24 | 2018-06-01 | 中国科学院上海药物研究所 | 嘧啶并[5,4-b]吲嗪或嘧啶并[5,4-b]吡呤化合物、其制备方法及用途 |
| JP2020511462A (ja) | 2016-12-03 | 2020-04-16 | ジュノー セラピューティクス インコーポレイテッド | キナーゼ阻害剤との組み合わせで治療用t細胞を使用するための方法および組成物 |
| CN110381997A (zh) | 2016-12-12 | 2019-10-25 | 茂体外尔公司 | 用于治疗和预防癌症和感染性疾病的包含病毒基因治疗和免疫检查点抑制剂的方法和组合物 |
| MX2019005527A (es) * | 2016-12-15 | 2019-08-12 | Hoffmann La Roche | Proceso para preparar inhibidores de tirosina cinasa de bruton (btk). |
| WO2018113771A1 (en) | 2016-12-22 | 2018-06-28 | Betta Pharmaceuticals Co., Ltd | Benzimidazole derivatives, preparation methods and uses theirof |
| TW201836642A (zh) | 2017-03-24 | 2018-10-16 | 美商建南德克公司 | 治療自體免疫及發炎疾病的方法 |
| CN107445981B (zh) * | 2017-08-25 | 2018-06-22 | 牡丹江医学院 | 一种用于防治宫颈炎的活性化合物 |
| KR102613433B1 (ko) | 2017-10-11 | 2023-12-13 | 주식회사 대웅제약 | 신규한 페닐피리딘 유도체 및 이를 포함하는 약학 조성물 |
| AU2018354972B2 (en) | 2017-10-27 | 2021-07-08 | Fresenius Kabi Oncology Ltd. | An improved process for the preparation of ribociclib and its salts |
| US11100492B2 (en) * | 2018-02-19 | 2021-08-24 | Peter Garrett | General purpose re-loadable card aggregation implementation |
| US11702427B2 (en) | 2018-03-12 | 2023-07-18 | Arbutus Biopharma Corporation | Substituted 2-pyridone tricyclic compounds, analogues thereof, and methods using same |
| US20210113568A1 (en) | 2018-04-27 | 2021-04-22 | Ono Pharmaceutical Co., Ltd. | PREVENTIVE AND/OR THERAPEUTIC AGENT FOR AUTOIMMUNE DISEASE COMPRISING COMPOUND HAVING Btk INHIBITORY ACTIVITY AS ACTIVE INGREDIENT |
| PE20210406A1 (es) | 2018-07-25 | 2021-03-02 | Novartis Ag | Inhibidores de inflamasoma nlrp3 |
| KR102328682B1 (ko) * | 2018-08-27 | 2021-11-18 | 주식회사 대웅제약 | 신규한 헤테로사이클릭아민 유도체 및 이를 포함하는 약학 조성물 |
| WO2020043321A1 (en) | 2018-08-31 | 2020-03-05 | Stichting Katholieke Universiteit | Synergistic combinations of amino acid depletion agent sensitizers (aadas) and amino acid depletion agents (aada), and therapeutic methods of use thereof |
| WO2020081450A1 (en) | 2018-10-15 | 2020-04-23 | Nurix Therapeutics, Inc. | Bifunctional compounds for degrading btk via ubiquitin proteosome pathway |
| TW202033523A (zh) * | 2019-01-17 | 2020-09-16 | 美商愛彼特生物製藥股份有限公司 | 經取代的多環羧酸、其類似物及使用其之方法 |
| EP3914250A1 (en) | 2019-01-22 | 2021-12-01 | F. Hoffmann-La Roche AG | Methods of treating rheumatoid arthritis, chronic spontaneous urticaria, and systemic lupus erythematosis using an inhibitor of bruton's tyrosine kinase |
| CN113939292A (zh) * | 2019-02-25 | 2022-01-14 | 广州麓鹏制药有限公司 | Btk及其突变体的抑制剂 |
| WO2020188015A1 (en) | 2019-03-21 | 2020-09-24 | Onxeo | A dbait molecule in combination with kinase inhibitor for the treatment of cancer |
| EP3953346A1 (en) | 2019-04-09 | 2022-02-16 | Nurix Therapeutics, Inc. | 3-substituted piperidine compounds for cbl-b inhibition, and use of a cbl-b inhibitor in combination with a cancer vaccine and/or oncolytic virus |
| AU2020278592A1 (en) | 2019-05-17 | 2021-12-02 | Nurix Therapeutics, Inc. | Cyano cyclobutyl compounds for Cbl-b inhibition and uses thereof |
| AR119731A1 (es) | 2019-05-17 | 2022-01-05 | Novartis Ag | Inhibidores del inflamasoma nlrp3 |
| WO2021066958A1 (en) | 2019-10-05 | 2021-04-08 | Newave Pharmaceutical Inc. | Inhibitor of btk and mutants thereof |
| EP4055019A1 (en) * | 2019-11-08 | 2022-09-14 | Nurix Therapeutics, Inc. | Bifunctional compounds for degrading btk via ubiquitin proteosome pathway |
| WO2021089791A1 (en) | 2019-11-08 | 2021-05-14 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods for the treatment of cancers that have acquired resistance to kinase inhibitors |
| WO2021113557A1 (en) | 2019-12-04 | 2021-06-10 | Nurix Therapeutics, Inc. | Bifunctional compounds for degrading btk via ubiquitin proteosome pathway |
| WO2021148581A1 (en) | 2020-01-22 | 2021-07-29 | Onxeo | Novel dbait molecule and its use |
| IL295589A (en) * | 2020-02-20 | 2022-10-01 | Hutchison Medipharma Ltd | The heterocyclic heteroaryl compounds and their uses |
| KR20220148826A (ko) | 2020-02-28 | 2022-11-07 | 제넨테크, 인크. | 브루톤 티로신 키나아제의 저해제를 이용하여 원발성 진행형 다발성 경화증을 치료하는 방법 |
| EP4125906A1 (en) | 2020-04-03 | 2023-02-08 | Genentech, Inc. | Methods of treating relapsing multiple sclerosis using an inhibitor of bruton's tyrosine kinase |
| US20230348471A1 (en) * | 2020-06-18 | 2023-11-02 | Shanghai Synergy Pharmaceutical Sciences Co., Ltd. | Bruton's tyrosine kinase inhibitor and preparation method therefor |
| JP2023536339A (ja) * | 2020-08-04 | 2023-08-24 | エフ. ホフマン-ラ ロシュ アーゲー | 自己免疫疾患の処置のためのピリジノン化合物 |
| BR112023002031A2 (pt) | 2020-08-14 | 2023-03-07 | Novartis Ag | Derivados de espiropiperidinila substituídos por heteroarila e usos farmacêuticos dos mesmos |
| AU2021326530A1 (en) * | 2020-08-14 | 2023-04-20 | Guangzhou Lupeng Pharmaceutical Company Ltd. | Dosage form compositions comprising an inhibitor of btk and mutants thereof |
| AU2021343591A1 (en) | 2020-09-21 | 2023-05-04 | Hutchison Medipharma Limited | Heteroaryl heterocyclic compounds and uses thereof |
| US20230382900A1 (en) | 2020-10-30 | 2023-11-30 | Newave Pharmaceutical Inc. | Inhibitors of btk |
| EP4263552A1 (en) | 2020-12-20 | 2023-10-25 | Guangzhou Lupeng Pharmaceutical Company Ltd. | Btk degrader |
| WO2022212893A1 (en) | 2021-04-02 | 2022-10-06 | Biogen Ma Inc. | Combination treatment methods of multiple sclerosis |
| WO2022233801A1 (en) | 2021-05-05 | 2022-11-10 | F. Hoffmann-La Roche Ag | Process for preparing btk inhibitors |
| CN113603685A (zh) * | 2021-07-23 | 2021-11-05 | 都创(上海)医药开发有限公司 | Fenebrutinib化合物的晶型及其制备方法和用途 |
| WO2023110970A1 (en) | 2021-12-14 | 2023-06-22 | Netherlands Translational Research Center Holding B.V | Macrocyclic btk inhibitors |
| WO2023137225A1 (en) * | 2022-01-17 | 2023-07-20 | Newave Pharmaceutical Inc. | Btk degrader |
| WO2023143491A1 (zh) * | 2022-01-28 | 2023-08-03 | 和记黄埔医药(上海)有限公司 | 7,8-二氢-2h-环戊二烯并吡咯并吡嗪酮化合物的合成方法 |
| US20240067627A1 (en) | 2022-08-03 | 2024-02-29 | Novartis Ag | Nlrp3 inflammasome inhibitors |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN101610676A (zh) * | 2006-09-22 | 2009-12-23 | 药品循环公司 | 布鲁顿酪氨酸激酶的抑制剂 |
| WO2010100070A1 (en) * | 2009-03-02 | 2010-09-10 | F. Hoffmann-La Roche Ag | Inhibitors of bruton's tyrosine kinase |
| CN101861307A (zh) * | 2007-09-20 | 2010-10-13 | Cgi制药有限公司 | 取代的酰胺、其制备方法及其用于治疗疾病例如癌症的用途 |
| WO2010122038A1 (en) * | 2009-04-24 | 2010-10-28 | F. Hoffmann-La Roche Ag | Inhibitors of bruton's tyrosine kinase |
| CN101932573A (zh) * | 2008-02-05 | 2010-12-29 | 霍夫曼-拉罗奇有限公司 | 新型吡啶酮类和哒嗪酮类 |
Family Cites Families (38)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3773919A (en) | 1969-10-23 | 1973-11-20 | Du Pont | Polylactide-drug mixtures |
| US5583024A (en) | 1985-12-02 | 1996-12-10 | The Regents Of The University Of California | Recombinant expression of Coleoptera luciferase |
| US5543523A (en) | 1994-11-15 | 1996-08-06 | Regents Of The University Of Minnesota | Method and intermediates for the synthesis of korupensamines |
| JPH08336393A (ja) | 1995-04-13 | 1996-12-24 | Mitsubishi Chem Corp | 光学活性なγ−置換−β−ヒドロキシ酪酸エステルの製造法 |
| US6602677B1 (en) | 1997-09-19 | 2003-08-05 | Promega Corporation | Thermostable luciferases and methods of production |
| BR0211073A (pt) | 2001-07-12 | 2004-12-14 | Avecia Ltd | Sistema de catalisador, e, processos para a preparação de um catalisador microencapsulado, de bifenilas opcionalmente substituìdas, de alcenos opcionalmente substituìdos, de um produto hidrogenado e de dióis |
| US7405295B2 (en) | 2003-06-04 | 2008-07-29 | Cgi Pharmaceuticals, Inc. | Certain imidazo[1,2-a]pyrazin-8-ylamines and method of inhibition of Bruton's tyrosine kinase by such compounds |
| US7393848B2 (en) | 2003-06-30 | 2008-07-01 | Cgi Pharmaceuticals, Inc. | Certain heterocyclic substituted imidazo[1,2-A]pyrazin-8-ylamines and methods of inhibition of Bruton's tyrosine kinase by such compounds |
| AU2005271831A1 (en) | 2004-07-12 | 2006-02-16 | Idun Pharmaceuticals, Inc. | Tetrapeptide analogs |
| EP1812442A2 (en) | 2004-11-10 | 2007-08-01 | CGI Pharmaceuticals, Inc. | Imidazo[1,2-a]pyrazin-8-ylamines useful as modulators of kinase activity |
| KR101357524B1 (ko) | 2005-03-10 | 2014-02-03 | 질레드 코네티컷 인코포레이티드 | 특정 치환된 아미드, 그의 제조 방법, 및 사용 방법 |
| DK1934174T3 (da) | 2005-10-07 | 2011-08-01 | Exelixis Inc | Azetidiner som MEK inhibitorer til behandling af proliferative sygdomme |
| PE20080839A1 (es) | 2006-09-11 | 2008-08-23 | Cgi Pharmaceuticals Inc | Determinadas amidas sustituidas, metodo de elaboracion y metodo de uso de las mismas |
| AR063946A1 (es) | 2006-09-11 | 2009-03-04 | Cgi Pharmaceuticals Inc | Determinadas pirimidinas sustituidas, el uso de las mismas para el tratamiento de enfermedades mediadas por la inhibicion de la actividad de btk y composiciones farmaceuticas que las comprenden. |
| US7838523B2 (en) | 2006-09-11 | 2010-11-23 | Cgi Pharmaceuticals, Inc. | Certain substituted amides, method of making, and method of use thereof |
| EP2205564B1 (en) * | 2007-10-23 | 2014-07-30 | F. Hoffmann-La Roche AG | Novel kinase inhibitors |
| US8426441B2 (en) | 2007-12-14 | 2013-04-23 | Roche Palo Alto Llc | Inhibitors of bruton's tyrosine kinase |
| US7683064B2 (en) | 2008-02-05 | 2010-03-23 | Roche Palo Alto Llc | Inhibitors of Bruton's tyrosine kinase |
| US8426424B2 (en) | 2008-05-06 | 2013-04-23 | Cgi Pharmaceuticals, Inc. | Certain substituted amides, method of making, and method of use thereof |
| PE20100851A1 (es) * | 2008-06-24 | 2011-01-31 | Hoffmann La Roche | PIRIDIN-2-ONAS Y PIRIDAZIN-3-ONAS SUSTITUIDAS COMO INHIBIDORES DE Btk |
| PE20110164A1 (es) | 2008-07-02 | 2011-03-28 | Hoffmann La Roche | Nuevas fenilpirazinonas como inhibidores de quinasa |
| CA2636807A1 (en) | 2008-07-04 | 2010-01-04 | Steven Splinter | Methods for obtaining cyclopamine |
| EP2307413B1 (en) | 2008-07-15 | 2015-09-09 | F. Hoffmann-La Roche AG | Novel phenyl-imidazopyridines and pyridazines |
| US8598174B2 (en) | 2008-11-12 | 2013-12-03 | Genetech, Inc. | Pyridazinones, method of making, and method of use thereof |
| EP2424368B1 (en) * | 2009-04-29 | 2014-12-31 | Locus Pharmaceuticals, Inc. | Pyrrolotriazine compounds |
| PL2473049T3 (pl) * | 2009-09-04 | 2019-07-31 | Biogen Ma Inc. | Inhibitory kinazy tyrozynowej brutona |
| RU2017112518A (ru) * | 2010-05-07 | 2019-01-25 | Джилид Коннектикут, Инк. | Пиридоновые и азапиридоновые соединения и способы применения |
| AR082590A1 (es) | 2010-08-12 | 2012-12-19 | Hoffmann La Roche | Inhibidores de la tirosina-quinasa de bruton |
| JP5841602B2 (ja) | 2010-09-01 | 2016-01-13 | ジーアイリード コネチカット インコーポレーテッドGilead Connecticut,Inc. | ピリジノン/ピラジノン、その作製方法、および使用方法 |
| US8975260B2 (en) | 2010-09-01 | 2015-03-10 | Genetech, Inc | Pyridazinones, method of making, and method of use thereof |
| MX345170B (es) | 2011-05-17 | 2017-01-19 | Hoffmann La Roche | Inhibidores de la tirosina-cinasa de bruton. |
| KR20140052032A (ko) | 2011-08-17 | 2014-05-02 | 에프. 호프만-라 로슈 아게 | 브루톤 티로신 키나아제의 억제제 |
| EP2773632B1 (en) * | 2011-11-03 | 2017-04-12 | F. Hoffmann-La Roche AG | 8-fluorophthalazin-1(2h)-one compounds as inhibitors of btk activity |
| UA111756C2 (uk) * | 2011-11-03 | 2016-06-10 | Ф. Хоффманн-Ля Рош Аг | Сполуки гетероарилпіридону та азапіридону як інгібітори тирозинкінази брутона |
| EA027561B1 (ru) * | 2011-11-03 | 2017-08-31 | Ф.Хоффманн-Ля Рош Аг | Алкилированные соединения пиперазина в качестве ингибиторов тирозинкиназы брутона |
| EP3016943B1 (en) * | 2013-07-03 | 2019-08-21 | F. Hoffmann-La Roche AG | Heteroaryl pyridone and aza-pyridone amide compounds |
| KR101813830B1 (ko) * | 2013-12-05 | 2017-12-29 | 에프. 호프만-라 로슈 아게 | 친전자성 작용기를 갖는 헤테로아릴 피리돈 및 아자-피리돈 화합물 |
| IL300209A (en) * | 2016-02-29 | 2023-03-01 | Hoffmann La Roche | Dosage preparations containing Bruton's tyrosine kinase inhibitor |
-
2012
- 2012-02-11 UA UAA201405799A patent/UA111756C2/uk unknown
- 2012-11-02 SI SI201231643T patent/SI3002284T1/sl unknown
- 2012-11-02 TW TW109129648A patent/TW202124384A/zh unknown
- 2012-11-02 DK DK12783837.3T patent/DK2773638T3/en active
- 2012-11-02 HU HUE12783837A patent/HUE028019T2/en unknown
- 2012-11-02 LT LTEP15188086.1T patent/LT3002284T/lt unknown
- 2012-11-02 TW TW106130019A patent/TWI652270B/zh active
- 2012-11-02 DK DK15188086.1T patent/DK3002284T3/da active
- 2012-11-02 WO PCT/US2012/063194 patent/WO2013067274A1/en active Application Filing
- 2012-11-02 EP EP22157147.4A patent/EP4050012A1/en active Pending
- 2012-11-02 ES ES19152979T patent/ES2898938T3/es active Active
- 2012-11-02 CN CN201710227680.4A patent/CN107011348B/zh active Active
- 2012-11-02 EP EP19152979.1A patent/EP3521288B1/en active Active
- 2012-11-02 PL PL19152979T patent/PL3521288T3/pl unknown
- 2012-11-02 ES ES15188086T patent/ES2738329T3/es active Active
- 2012-11-02 CN CN201280065965.8A patent/CN104125959B/zh active Active
- 2012-11-02 US US13/667,133 patent/US8716274B2/en not_active Ceased
- 2012-11-02 SI SI201230367T patent/SI2773638T1/sl unknown
- 2012-11-02 EA EA201490858A patent/EA023263B1/ru unknown
- 2012-11-02 MX MX2015003514A patent/MX361807B/es unknown
- 2012-11-02 PL PL12783837T patent/PL2773638T3/pl unknown
- 2012-11-02 HU HUE15188086A patent/HUE044959T2/hu unknown
- 2012-11-02 ES ES12783837.3T patent/ES2555168T3/es active Active
- 2012-11-02 PT PT15188086T patent/PT3002284T/pt unknown
- 2012-11-02 CA CA2853975A patent/CA2853975C/en active Active
- 2012-11-02 MX MX2014005331A patent/MX2014005331A/es active IP Right Grant
- 2012-11-02 RS RS20160001A patent/RS54505B1/en unknown
- 2012-11-02 RS RS20190888A patent/RS59016B1/sr unknown
- 2012-11-02 KR KR1020157036122A patent/KR20160003328A/ko not_active Application Discontinuation
- 2012-11-02 TW TW101140919A patent/TWI609868B/zh active
- 2012-11-02 EP EP12783837.3A patent/EP2773638B1/en active Active
- 2012-11-02 TW TW107141781A patent/TWI701250B/zh active
- 2012-11-02 AR ARP120104128A patent/AR088641A1/es active IP Right Grant
- 2012-11-02 SG SG11201401992YA patent/SG11201401992YA/en unknown
- 2012-11-02 AU AU2012332365A patent/AU2012332365B2/en active Active
- 2012-11-02 PL PL15188086T patent/PL3002284T3/pl unknown
- 2012-11-02 JP JP2014541114A patent/JP5976827B2/ja active Active
- 2012-11-02 KR KR1020147014661A patent/KR101659193B1/ko active IP Right Grant
- 2012-11-02 PE PE2014000638A patent/PE20141586A1/es active IP Right Grant
- 2012-11-02 PT PT127838373T patent/PT2773638E/pt unknown
- 2012-11-02 IN IN3250CHN2014 patent/IN2014CN03250A/en unknown
- 2012-11-02 TR TR2019/09849T patent/TR201909849T4/tr unknown
- 2012-11-02 EP EP15188086.1A patent/EP3002284B1/en active Active
- 2012-11-02 EP EP21171114.8A patent/EP4019508A1/en active Pending
-
2014
- 2014-03-13 US US14/207,966 patent/US8921353B2/en active Active
- 2014-04-10 IL IL232060A patent/IL232060A/en active IP Right Grant
- 2014-04-28 CO CO14090476A patent/CO6950472A2/es active IP Right Grant
- 2014-04-28 CR CR20140194A patent/CR20140194A/es unknown
- 2014-04-29 CL CL2014001103A patent/CL2014001103A1/es unknown
- 2014-05-27 MA MA37075A patent/MA35819B1/fr unknown
- 2014-09-08 US US14/479,529 patent/US9238655B2/en active Active
-
2015
- 2015-02-18 HK HK15101799.4A patent/HK1201265A1/zh unknown
- 2015-08-24 JP JP2015165300A patent/JP2016028046A/ja not_active Withdrawn
- 2015-11-17 US US14/943,552 patent/US9782405B2/en active Active
- 2015-12-31 HR HRP20151442TT patent/HRP20151442T1/hr unknown
-
2016
- 2016-01-04 CY CY20161100003T patent/CY1117097T1/el unknown
- 2016-12-15 AU AU2016273930A patent/AU2016273930B2/en active Active
-
2017
- 2017-08-31 US US15/693,022 patent/US10045983B2/en active Active
-
2018
- 2018-01-04 JP JP2018000309A patent/JP6571215B2/ja active Active
- 2018-03-05 AU AU2018201557A patent/AU2018201557B2/en active Active
- 2018-06-27 US US16/020,270 patent/US20190194203A1/en not_active Abandoned
- 2018-07-16 ZA ZA2018/04727A patent/ZA201804727B/en unknown
- 2018-10-30 US US16/175,278 patent/USRE48239E1/en active Active
-
2019
- 2019-02-14 JP JP2019024668A patent/JP2019108342A/ja not_active Withdrawn
- 2019-07-18 HR HRP20191307TT patent/HRP20191307T1/hr unknown
- 2019-08-16 AU AU2019216728A patent/AU2019216728B2/en active Active
- 2019-10-31 US US16/670,898 patent/US20200062769A1/en not_active Abandoned
- 2019-12-23 AR ARP190103844A patent/AR117501A2/es unknown
-
2020
- 2020-04-22 AU AU2020202707A patent/AU2020202707B2/en active Active
- 2020-07-02 JP JP2020114594A patent/JP2020183397A/ja not_active Withdrawn
- 2020-08-24 US US17/001,205 patent/US20210079002A1/en not_active Abandoned
-
2022
- 2022-12-20 US US18/069,099 patent/US20230279012A1/en not_active Abandoned
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN101610676A (zh) * | 2006-09-22 | 2009-12-23 | 药品循环公司 | 布鲁顿酪氨酸激酶的抑制剂 |
| CN101861307A (zh) * | 2007-09-20 | 2010-10-13 | Cgi制药有限公司 | 取代的酰胺、其制备方法及其用于治疗疾病例如癌症的用途 |
| CN101932573A (zh) * | 2008-02-05 | 2010-12-29 | 霍夫曼-拉罗奇有限公司 | 新型吡啶酮类和哒嗪酮类 |
| WO2010100070A1 (en) * | 2009-03-02 | 2010-09-10 | F. Hoffmann-La Roche Ag | Inhibitors of bruton's tyrosine kinase |
| WO2010122038A1 (en) * | 2009-04-24 | 2010-10-28 | F. Hoffmann-La Roche Ag | Inhibitors of bruton's tyrosine kinase |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN107011348B (zh) | 作为btk活性的抑制剂的杂芳基吡啶酮和氮杂-吡啶酮化合物 | |
| JP5832524B2 (ja) | ピリドン及びアザピリドン化合物、並びにそれらの使用方法 | |
| BR122020017743B1 (pt) | Processo para fabricação de uma composição farmacêutica e uso de uma composição farmacêutica | |
| BR112014010459B1 (pt) | Compostos e composição farmacêutica |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| REG | Reference to a national code |
Ref country code: HK Ref legal event code: DE Ref document number: 1241873 Country of ref document: HK |
|
| GR01 | Patent grant | ||
| GR01 | Patent grant |