BRPI0411713B1 - Compostos, processo para a sua manufatura, composições farmacêuticas que compreendem os mesmos, método para tratamento e/ou profilaxia de enfermidades que estão associadas com dpp-iv e sua utilização - Google Patents
Compostos, processo para a sua manufatura, composições farmacêuticas que compreendem os mesmos, método para tratamento e/ou profilaxia de enfermidades que estão associadas com dpp-iv e sua utilização Download PDFInfo
- Publication number
- BRPI0411713B1 BRPI0411713B1 BRPI0411713-1A BRPI0411713A BRPI0411713B1 BR PI0411713 B1 BRPI0411713 B1 BR PI0411713B1 BR PI0411713 A BRPI0411713 A BR PI0411713A BR PI0411713 B1 BRPI0411713 B1 BR PI0411713B1
- Authority
- BR
- Brazil
- Prior art keywords
- pyrido
- isoquinolin
- amino
- dimethoxy
- hexahydro
- Prior art date
Links
- 0 *C(CN1C(C2)c3cc(*)c(*)c(*)c3CC1)C2NP Chemical compound *C(CN1C(C2)c3cc(*)c(*)c(*)c3CC1)C2NP 0.000 description 3
- RZLRUIOODAEHEX-JYJNAYRXSA-N CCCC(N[C@@H](CN(CCc1c2)[C@@H](C3)c1cc(OC)c2OC)[C@H]3N)=O Chemical compound CCCC(N[C@@H](CN(CCc1c2)[C@@H](C3)c1cc(OC)c2OC)[C@H]3N)=O RZLRUIOODAEHEX-JYJNAYRXSA-N 0.000 description 1
- NUBNLQCQSWLNCX-BASLNEPJSA-N C[C@H](C1)CN([C@H](CN(CC2)[C@H](C3)c(cc4OC)c2cc4OC)[C@@H]3N)C1=O Chemical compound C[C@H](C1)CN([C@H](CN(CC2)[C@H](C3)c(cc4OC)c2cc4OC)[C@@H]3N)C1=O NUBNLQCQSWLNCX-BASLNEPJSA-N 0.000 description 1
- KNVBAQYDHULIJB-KJEVXHAQSA-N C[C@H](CN1[C@@H](CN(CCc2c3)[C@@H](C4)c2cc(OC)c3O)[C@H]4N)OC1=O Chemical compound C[C@H](CN1[C@@H](CN(CCc2c3)[C@@H](C4)c2cc(OC)c3O)[C@H]4N)OC1=O KNVBAQYDHULIJB-KJEVXHAQSA-N 0.000 description 1
- CFRFQORFSQOVOA-KKUMJFAQSA-N N[C@@H](C[C@@H](c(c(CC1)c2)cc(O)c2O)N1C1)[C@H]1C(N1CCCC1)=O Chemical compound N[C@@H](C[C@@H](c(c(CC1)c2)cc(O)c2O)N1C1)[C@H]1C(N1CCCC1)=O CFRFQORFSQOVOA-KKUMJFAQSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1617—Organic compounds, e.g. phospholipids, fats
- A61K9/1623—Sugars or sugar alcohols, e.g. lactose; Derivatives thereof; Homeopathic globules
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/28—Dragees; Coated pills or tablets, e.g. with film or compression coating
- A61K9/2806—Coating materials
- A61K9/2833—Organic macromolecular compounds
- A61K9/286—Polysaccharides, e.g. gums; Cyclodextrin
- A61K9/2866—Cellulose; Cellulose derivatives, e.g. hydroxypropyl methylcellulose
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4816—Wall or shell material
- A61K9/4825—Proteins, e.g. gelatin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4841—Filling excipients; Inactive ingredients
- A61K9/4858—Organic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4841—Filling excipients; Inactive ingredients
- A61K9/4875—Compounds of unknown constitution, e.g. material from plants or animals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/02—Drugs for disorders of the urinary system of urine or of the urinary tract, e.g. urine acidifiers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/48—Drugs for disorders of the endocrine system of the pancreatic hormones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/48—Drugs for disorders of the endocrine system of the pancreatic hormones
- A61P5/50—Drugs for disorders of the endocrine system of the pancreatic hormones for increasing or potentiating the activity of insulin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/12—Antihypertensives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/28—Dragees; Coated pills or tablets, e.g. with film or compression coating
- A61K9/2806—Coating materials
- A61K9/2833—Organic macromolecular compounds
- A61K9/2853—Organic macromolecular compounds obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyethylene glycol, polyethylene oxide, poloxamers, poly(lactide-co-glycolide)
Abstract
"compostos, processo para a sua manufatura, composições farmacêuticas que compreendem os mesmos, método para tratamento e/ou profilaxia de enfermidades que estão associadas com dpp-iv e sua utilização". a presente invenção relaciona-se com compostos da fórmula (i) em que r^ 1^, r^ 2^, r^ 3^ e r^ 4^ são tais como definidos na descrição e nas reivindicações, e os seus sais farmaceuticamente aceitáveis. os compostos são de utilidade para o tratamento e/ou profilaxia de enfermidades que estão associadas com dpp-iv, tais como diabetes, particularmente diabetes mellitus não dependentes de insulina, e tolerância à glicose prejudicada.
Description
(54) Título: COMPOSTOS, PROCESSO PARA A SUA MANUFATURA, COMPOSIÇÕES FARMACÊUTICAS QUE COMPREENDEM OS MESMOS, MÉTODO PARA TRATAMENTO E/OU PROFILAXIA DE ENFERMIDADES QUE ESTÃO ASSOCIADAS COM DPP-IV E SUA UTILIZAÇÃO (51) Int.CI.: C07D 471/06; A61P 3/10 (30) Prioridade Unionista: 20/06/2003 EP 03013404.3 (73) Titular(es): F. HOFFMANN-LA ROCHE AG (72) Inventor(es): MARKUS BOEHRINGER; BERND KUHN; PATRIZIO MATTEI; ROBERT NARQUIZIAN • · ·
COMPOSTOS, PROCESSO PARA A SUA MANUFATURA, COMPOSIÇÕES
FARMACÊUTICAS QUE COMPREENDEM OS MESMOS, MÉTODO PARA
TRATAMENTO E/OU PROFIIAXIA DE ENFERMIDADES QUE ESTÃO
ASSOCIADAS COM DPP-IV E SUA UTILIZAÇÃO
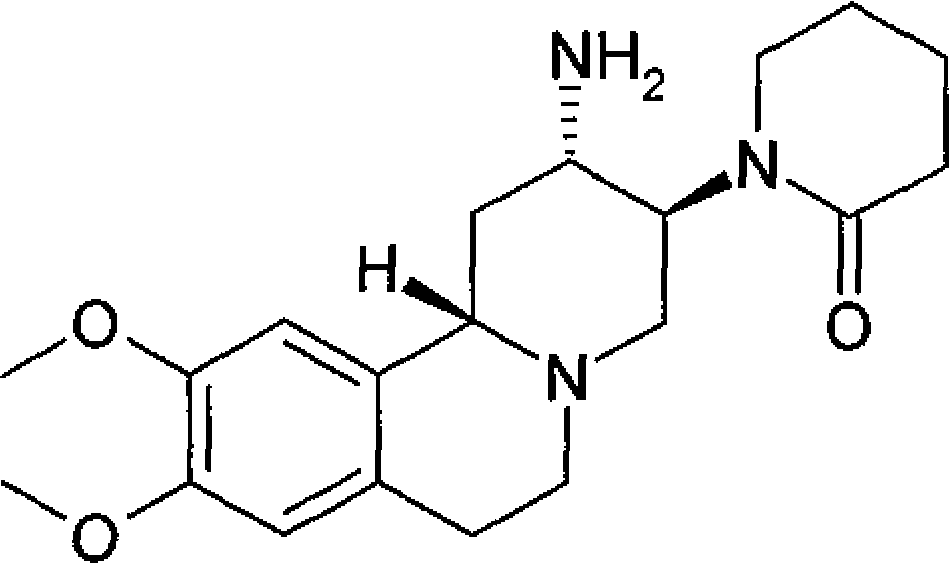
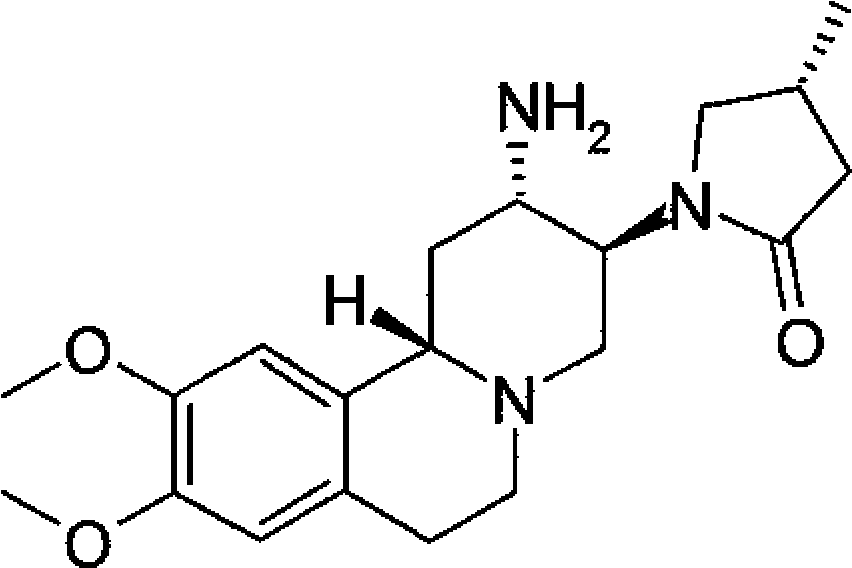
Refere-se a presente invenção a novos derivados de pirido[2,1-a]isoquinolina, à sua manufatura e ao seu uso como medicamentos.
Com particularidade, a invenção refere-se
em que
R1 é -C(O)-N(R5)R6 ou -N(R5)R6;
R2, R3 e R4 são, cada um deles, independentemente hidrogênio, halogênio, hidroxila, alquila inferi15 or, alcoxila inferior ou alquenila inferior, em que alquila inferior, alcoxila inferior e alquenila inferior podem opcionalmente ser substituídos por alcoxicarbonil inferior, arilo ou heterociclil;
R6 é hidrogênio, alquila inferior, alquila in20 ferior halogenado ou cicloalquila;
R6 é alquilsulfonil inferior, alquilsulfonil inferior halogenado, cicloalquilsulfonil, alquilcarbo«« «
> ♦ f» ♦ · • * * * • · ·· · • * * , « · * nil inferior, alquilcarbonil inferior halogenado, cicloalquilcarbonil; ou
R5 e R6, em conjunto com o átomo de nitrogênio ao qual eles estão fixados formam anel heterociclico saturado ou não-saturado de 4-, 5-, 6- ou 7-elementos contendo opcionalmente um outro heteroãtomo selecionado a partir de nitrogênio, oxigênio e enxofre, sendo o dito anel heterociclico opcionalmen.te mono-, di-, ou trisubstituído, independentemente, com alquila inferior, alquila inferior halogenado, oxo, dioxo e/ou ciano; e os seus sais farmaceuticamente aceitáveis.
A enzima dipeptidil peptidase IV (EC.3.4.14.5, que passa a ser doravante abreviada para DPP-IV) está envolvida na regularização das atividades de vários hormônios. Em particular, a DPP-IV degrada eficiente e rapidamente o peptídeo semelhante a glucagon 1 (GLP-1), que é um dos mais potentes estimuladores de produção e secreção de insulina. A inibição de DPPIV irá potencializar o efeito do GLP-1 endógeno, e conduzirá a concentrações de insulina de plasma mais altas. Em pacientes que sofrem de tolerância a glicose prejudicada e diabetes mellitus do tipo 2, concentração de insulina de plasma mais alta irá moderar a perigosa hiperglicemia e, conseqüentemente, reduzirá o risco de danificação dos tecidos. Conseqüentemente, os inibidores de DPP-IV foram sugeridos como candidatos a drogas para o tratamento de tolerância a glicose prejudicada e diabetes mellitus do tipo 2 (por exemplo, Villhauer,
| « * • · | • • | * | « • | • ·· | • | · + · • | ·· | |
| • · | • | • | r · | • | • | |||
| r | • | ·♦· | * | • | • | |||
| • « | • | • • | • • | • « ·· | • • o · | • • | ·· |
··· *
l·
WO98/19998). Outro estado da técnica relacionado pode ser encontrado em WO 99/38501, DE 19616486, DE 19834591, WO 01/40180, WO 01/55105, US 6110949, WO 00/34241 e US6011155.
Os inventores descobriram novos inibidores de DPP-IV que baixam muito eficientemente os niveis de glicose no sangue. Conseqüentemente, os compostos da presente invenção são de utilidade para o tratamento e/ou profilaxia de diabetes, particularmente diabetes mellitus não dependentes de insulina, e/ou tolerância a glicose prejudicada, bem como outras condições em que a amplificação da ação de um peptideo normalmente desativado por DPP-IV proporciona um benefício terapêutico. Surpreendentemente, os compostos da presente invenção também podem ser utilizados no tratamento e/ou profilaxia de obesidade, enfermidade inflamatória do intestino, Colitis Ulcerosa, Morbus Crohn, e/ou síndrome metabólica ou proteção de célula β. Além disso, os compostos da presente invenção podem ser usados como agentes diuréticos e para o tratamento e/ou profilaxia de hipertensão. Inesperadamente, os compostos da presente invenção exibem propriedades terapêuticas e farmacológicas aperfeiçoadas, em comparação com outros inibidores de DPP-IV conhecidos na técnica, tais como, por e25 xemplo, no contexto relacionado com farmacocinética e biodisponibilidade.
A não ser que de outro modo indicado, as definições seguintes são expostas para ilustrarem e de- 4
f<
finirem ο significado e escopo dos vários termos utilizados para descreverem a invenção neste contexto.
Neste relatório, o termo inferior é usado para significar um grupo que consiste de um a seis, de preferência de um a quatro, átomos de carbono.
O termo halogênio refere-se a flúor, cloro, bromo e iodo, com o flúor, bromo e o cloro sendo preferidos. O halogênio de maior preferência é flúor.
O termo alquila, individualmente ou em combinação com outros grupos, refere-se a um radical de hidrocarboneto alifático de cadeia ramificada ou normal, monovalente, saturado, de um a vinte átomos de carbono, preferentemente de um a dezesseis átomos de carbono, com maior preferência de um a dez átomos de carbono. O termo alquila inferior, individualmente ou em combinação com outros grupos, refere-se a um radical de alquila monovalente de cadeia ramificada ou normal de um a seis átomos de carbono, preferentemente de um a quatro átomos de carbono. Este termo é ainda exemplificado por radicais tais como metilo, etilo, npropilo, isopropilo, n-butilo, s-butilo, t-butilo, isobutilo, t-butilo, n-pentilo, 3-metilbutilo, n-hexilo, 2-etilbutilo, e assemelhados. Os resíduos de alquila inferior preferíveis compreendem metilo e etilo, em que o metilo é especialmente preferido.
O termo alquila inferior halogenado refere-se ao grupo de alquila em que pelo menos um dos hidrogênios do grupo de alquila inferior é substituído
por um átomo de halogênio, preferentemente fluoro ou cloro, com maior preferência fluoro. Entre os grupos de alquila inferior halogenado preferidos estão trifluorometil, difIuorometil, fluorometil e clorometil, em que o fluorometil é especialmente preferido.
termo alcoxila refere-se ao grupo R'0-, em que R' é alquila. O termo alcoxila inferior refere-se ao grupo R'-0-, em que R' é alquila inferior. Exemplos de grupos de alcoxila inferior são, por exem10 pio, metoxilo, etoxilo, propoxilo, isopropoxilo, butoxilo, isobutoxilo e hexiloxilo, em que o metoxilo é especialmente preferido.
O termo alcoxicarbonilo inferior referese ao grupo R'-0-C(0)-, em que R' é alquila inferior.
P termo arilo refere-se a um radical mono- ou policarboxilico monovalente aromático, tal como fenilo ou naftilo, preferentemente fenilo, que poderá ser opcionalmente mono-, di- ou tri-substituído, independentemente, por alquila inferior, alcoxila inferior, halo, cíano, azida, amino, alquil amino di-inferior ou hidroxila.
O termo cicloalquila refere-se a um radical carbociclico monovalente de três a seis, preferentemente de três a cinco átomos de carbono. Este termo é ainda exemplificado por radicais tais como ciclopropilo, ciclobutilo, ciclopentilo e cicloexilo, em que o ciclopropilo e ciclobutilo são preferidos.
1/ • · · • · · · • « · · · • · ·
Ο termo heterociclil refere-se a um resíduo N-heterocíclico aromático ou saturado de 5- ou 6elementos, que poderá opcionalmente conter um outro átomo de nitrogênio ou oxigênio, tal como imidazolil, pirazolil, tiazolil, piridil, pirimidil, morfolino, píperazino, piperidino ou pirrolidino, preferentemente piridil, tiazolil ou morfolino. Esses anéis heterocíclicos podem opcionalmente ser mono-, di- ou trisubstituídos, independentemente, por alquila inferior, alcoxila inferior, halo, ciano, azido, amino, dialquila inferior amino ou hidroxilo. O substituinte preferível é alquila inferior, com metilo sendo o preferido .
O termo um anel heterocíclico saturado ou não-saturado de 4-, 5-, 6- ou 7-elementos que contém opcionalmente um outro heteroátomo selecionado a partir de nitrogênio, oxigênio e enxofre refere-se a um anel heterocíclico não-aromático, sendo o dito anel heterocí clico opcionalmente mono-, di-, ou tri-substituído, independentemente, com alquila inferior, alquila inferior halogenado, oxo, dioxo e/ou ciano. Esses anéis heterocíclicos saturados são, por exemplo, pirrolidinil, piperidinil, azepanil, [1,2]tiazinanil, [1,3]oxazinanil, oxazolidinil, tiazolidinil ou azetidi25 nil. Exemplos desses anéis heterocíclicos nãosaturados são 5,6-diidro-lH-piridin-2-ona, pirrolinil, tetraidropiridina ou diidropiridina.
• · ·
O termo sais farmaceuticamente aceitáveis abrange sais dos compostos da fórmula (I) com ácidos inorgânicos ou orgânicos, tais como ácido clori* drico, ácido bromídrico, ácido nítrico, ácido sulfúri* 5 co, ácido fosfórico, ácido cítrico, ácido fórmico, ácido maléico, ácido acético, ácido fumárico, ácido succínico, ácido tartárico, ácido metanossulfônico, ácido salicílico, ácido p-toluenossulfônico, e outros assemelhados, que são ácidos não tóxicos para os organismos vivos. Os sais com ácidos preferidos são formatos, maleatos, citratos, cloridratos, bromidratós e sais de ácido metanossulfônico, em que os cloridratos são especialmente preferidos.
De acordo com uma concretização da presen15 te invenção, R1 é -C (O) -N (R5) R6. Em uma outra concretização, R1 é -N(R5)R6.
Em uma outra concretização, R2, R3 e R4 são cada um deles, independentemente, hidrogênio, hidroxila, alcoxila inferior, ou alcoxila inferior substituído por arilo, por heterociclíl ou por alcoxicarbonil inferior. Os resíduos de arilo preferíveis em R2, R3 e R4 w são fenilo ou fenilo substituído por alquilamino diinferior ou por ciano. Os resíduos de heterociclíl preferíveis em R2, R3 e R4 são morfolino, piridil, tia25 zolil ou tiazolil substituído por alquila inferior. Os resíduos de alcoxicarbonil inferior preferíveis em R2, R3 e R4 são metoxicarbonil e etoxicarbonil.
*· V
2«
«I «I 4
I íl 4
4. «I «; 4)
Em uma outra concretização, R2, R3 e R4 são cada um deles, independentemente, hidrogênio, hidroxila ou alcoxila inferior.
Em uma concretização preferível, o resíduo R2 é alcoxila inferior, preferencialmente metoxila, alcoxila inferior, preferentemente metoxila, hidrogênio ou hidroxila. Com maior preferência o resíduo R2 é metoxila .
Em uma outra concretização preferível, o resíduo R3 é alcoxila inferior, com metoxilo, etoxilo, propoxilo, n-butoxilo e isobutoxilo sendo preferidos, ou hidrogênio ou hidroxilo. O resíduo R3 de maior preferência é metoxilo ou hidroxilo, com metoxilo sendo especialmente preferido.
Em uma outra concretização preferida, o resíduo R4 é alcoxila inferior, preferentemente metóxiia, hidrogênio ou hidroxila. O resíduo R4 de maior preferência é hidrogênio.
De acordo com uma concretização, R5 é hidrogênio, alquila inferior, alquila inferior halogenado ou cicloalquila. Resíduos de alquila inferior preferíveis em R5 são metilo, etilo, n-propilo, isopropilo, n-butilo, sec-butilo e terfc-butilo, com metilo e etilo sendo especialmente preferidos. Os resíduos R5 de alquila inferior halogenado preferíveis são fluorometil, 2-fluoroetil e 3-fluoropropil, com fluorometil sendo especialmente preferido. Os resíduos R5 de cicloalquila preferidos são ciclopropilo não-substituído e ciclo« · * d
butilo não-substituído. Preferentemente, R5 é hidrogênio, alquila inferior tal como metilo ou alquila inferior halogenado tal como fluorometilo.
v Em uma concretização, R6 é alquilsulfonil * 5 inferior, alquilsulfonil inferior halogenado, cicloalquilsulfonil, alquilcarbonil inferior, alquilcarbonil inferior halogenado, cicloalquilcarbonil. Residuos R6 alquilsulfonil inferior preferíveis são metilsulfonil, etilsulfonil e propilsulfonil, com metilsulfonil e e10 tilsulfonil sendo especialmente preferidos. Os residuos Rô de alquilcarbonil inferior preferíveis são metilcarbonil, etilcarbonil e propilcarbonil, com metilcarbonil e etilcarbonil constituindo-se nqueles especialmente preferidos. Os resíduos R6 de alquilsulfonil inferior halogenado preferíveis são etilsulfonil e propilsulfonil. Os resíduos R6 de alquilcarbonil inferior halogenado preferíveis compreendem pentafluoroetilsulfonil e 2,2,2-trifluoroetilsulfonil. Os resíduos R6 de cicloalquilsulfonil preferíveis são ciclopropilsulfonil e ciclobutilsulfonil. Os resíduos R6 de cicloalquilcarbonil preferíveis compreendem ciclopropilcarbonil e v ciclobutilcarbonil.
De acordo com uma concretização preferida,
R6 é alquilsulfonil inferior, preferentemente etilsul25 fonil, ou alquilcarbonil inferior, preferentemente etilcarbonil, ou cicloalquilcarbonil, preferentemente ciclopropilcarbonil.
··
I « *
(. · • « ιν
De acordo com uma outra concretização, R5 e R6 em conjunto com o átomo de nitrogênio ao qual eles estão fixados formam um anel heterociclico saturado ou não saturado de 4-, 5-, 6- ou 7-elementos opcionalmente contendo um outro heteroátomo selecionado a partir de nitrogênio, oxigênio e enxofre, preferentemente enxofre, sendo o dito anel heterociclico opcionalmente mono-, di-, ou tri-substituido, preferentemente mono- ou di-substituido, independentemente, com alquila inferi10 or, tal como metil ou etil, alquila inferior halogenado tal como fluorometil, oxo, dioxo e/ou ciano.
Ainda de acordo com uma outra concretização, R5 e R6 em conjunto com o átomo de nitrogênio ao qual eles estão fixados formam um anel heterociclico saturado ou não-saturado de 4-, 5-, 6- ou 7-elementos contendo opcionalmente um átomo de enxofre ou um átomo de oxigênio como um outro heteroátomo no anel, sendo o dito anel heterociclico opcionalmente mono- ou disubstituído, independentemente, com alquila inferior tal como metilo ou etilo, alquila inferior halogenado tal como fluorometil, oxo, dioxo e/ou ciano.
De acordo com uma concretização preferida,
R5 e R6 em conjunto com o átomo de nitrogênio ao qual eles estão fixados são pirrolidina, pirrolidin-2-ona,
4-metil-pirrolidin-2-ona, 4-etil-pirrolidin-2-ona, 3metil-pirrolidin-2-ona, 5-metil-pirrolidin-2-ona, 4fluoro-metil-pirrolidin-2-ona, pirrolidina-2carbonitrilo, piperidina, piperidin-2-ona, 4-metil11 piperidin-2~ona, 5-metil-piperidin-2-ona, 5, 6-didro-lHpiridin-2-ona, tiazolidin-3-il, 1,1-dioxo-l,2tiazolidin-2-il, 1,1-dioxo[1,2]tiazinan-2-il, azetidine, azepan-2-ona, oxazolidin-2-ona, 5-metil- oxazoli5 din-2-ona, 5-fluorometil-oxazolidin-2-ona, ou [1,3]oxazinan-2-ona. Com maior preferência, R5 e R6 em conjunto com o átomo de nitrogênio ao qual eles estão fixados são tiazolidin-3-il, piperidin-2-ona, 4-metilpyrrolidin-2-ona, 4-fluorometil-pirrolidin-2-ona, 5,610 diidro-lH-piridin-2-ona, 5-metil-piperidin~2-ona, 5metil-oxazolidin-2-ona e 1,1-dioxo[1,2]tiazinan-2-il.
Ainda em uma outra concretização, a presente invenção refere-se a compostos da fórmula I, em que R1 é -C (0) -N (R5) R6 ou ~N(R5)R6; R2 é alcoxila inferi15 or tal como metoxilo; R3 é alcoxila inferior tal como metoxilo; e R4 é hidrogênio; e R5 e R6 em conjunto com o átomo de nitrogênio ao qual eles estão fixados formam um anel heterociclico saturado ou não-saturado de 4-, 5-, 6- ou 7-elementos contendo opcionalmente um átomo de enxofre como um outro heteroátomo no anel, sendo o dito anel heterociclico opcionalmente mono- ou bisubstituido, independentemente, com alquila inferior tal como metilo ou etilo, alquila inferior halogenado, tal como fluorometilo, oxo, dioxo e/ou ciano.
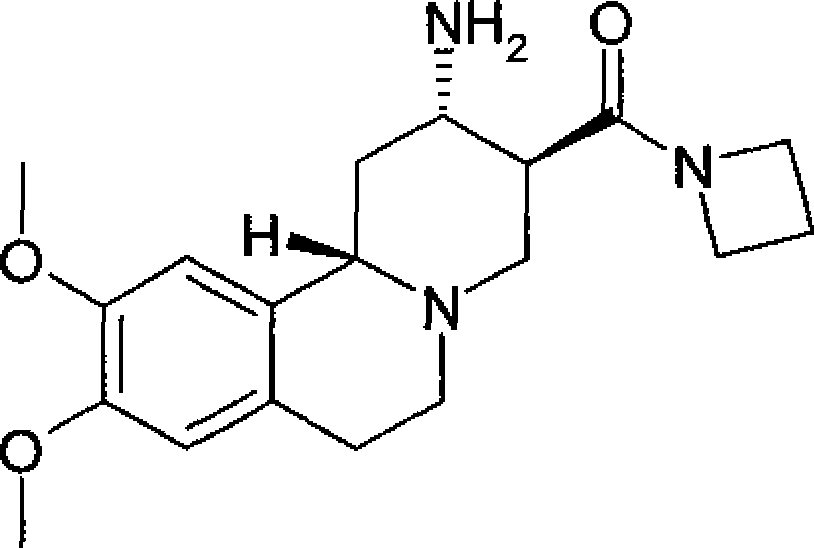
Os compostos da fórmula geral (I) de preferência são aqueles selecionados no grupo que consiste de:
• «····· · · * · ······· ·· · · ··· ·· ·· ·** • · ····*··· ··· · τλ (RS,RS,RS)-(2-amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-pirrolidinl-il-metanona, (RS,RS,RS)-(2-amino-9,10-dimetóxi-l,3,4,6,7,11b5 hexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-tiazolidin3-il-metanona, (RS,RS,RS)-(2-amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-azetidin-1il-metanona, (SS)-1-((RS,RS,RS)-2-amino-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolina-3carbonil)-pirrolidina-2-carbonitrilo,
1-((RS,RS,RS)-2-amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-piperidin-215 ona, ( —) — (S,S,S)—1 —(2-amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-piperidin-2ona, ( + ) - (R, R, R)-1-(2-amino-9,10-dimetóxi-l,3,4,6,7,11b20 hexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-piperidin-2ona,
1-((RS,RS,RS)-2-amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metilpiperidin-2-ona, (RS,RS,RS)-1-(2-amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-pirrolidin2-ona,
1-((RS,RS,RS)-2-amino-9,10-dimetóxi-l,3,4,6,7,11bw hexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metilpirrolidin-2-ona,
1-((RS,RS,RS)-2-amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-etilpirrolidin-2-ona, (RS,RS,RS)-1-(2-amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-5,6-diidrolH-pyridin-2-ona,
1-((RS,RS,RS)-2-amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-azepan-215 ona, (RS,RS,RS)-3-(1,1-dioxo-l,2-thiazolidin-2-il)-9,10dimetóxi-l, 3,4,6,7,llb-hexaidro-2H-pirido[2,1a]isoquinolin-2-ilamina, * (RS,RS,RS)-3-(1,1-dioxo[1,2]thiazinan-2-il)-9,1020 dimetóxi-1,3,4,6,7,llb-hexaidro-2H-pirido [2,1a]isoquinolin-2-ilamina, (S,S,S)-3-(1,1-dioxo-[1,2]tiazinan-2-il)-9,10dimetóxi-l, 3,4,6,7,llb-hexaidro-2H-pirido[2,1a]isoquinolin-2-ilamina,
« *······· *«· «
7f (SR)-1-((RS,RS,RS)-2-amino-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-4-metil-pirrolidin-2-ona, (RS,RS,RS,RS)-1-(2-amino-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-4-metil-pirrolidin-2-ona, (R) -1-((S,S,S)-2-amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metilpirrolidin-2-ona, (S) -1-((R, R, R)-2-amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metilpirrolídin-2-ona, (S,S,S,S)-1~(2-amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metilpirrolidin-2-ona, (R,R,R,R)-1-(2-amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metilpírrolidin-2-ona,
1-((RS,RS,RS)-2-amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4fluorometil-pirrolidin-2-ona,
1-((RS,RS,RS)-2-amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-5-metilpiperidin-2-ona,
,*
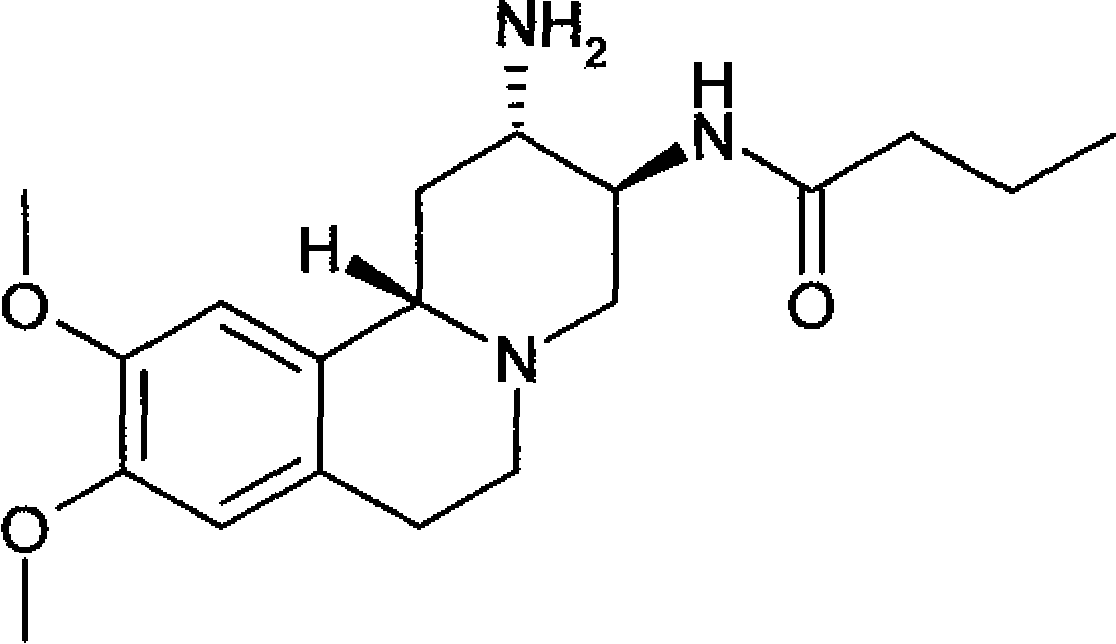
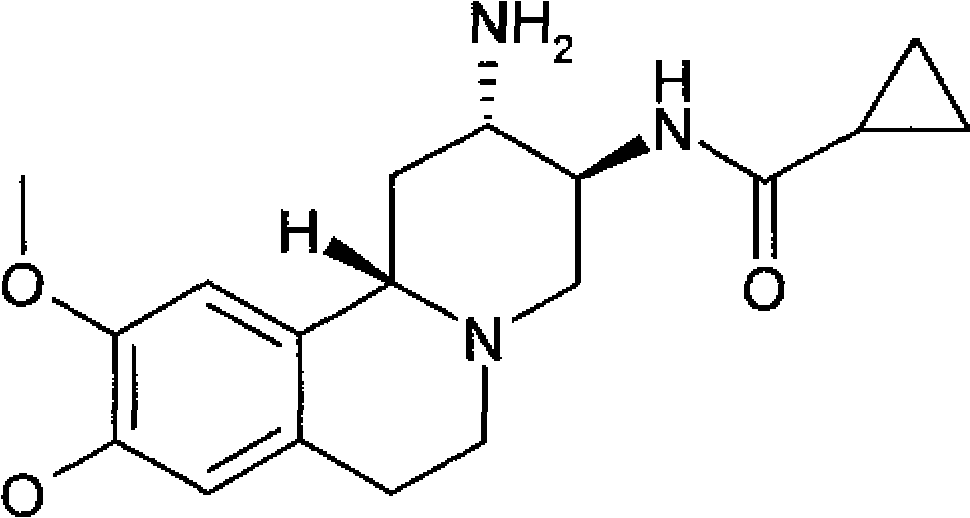
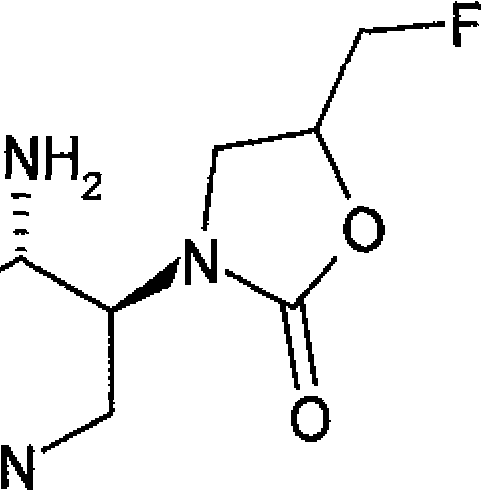
Β (RS,RS,RS)-N-(2-amino-9,10-dimetóxi-l,3,4,6,7,11bhexaídro-2H-pirido[2,1-a]isoquinolin-3-i1)propionamida, (RS,RS, RS)-N-(2-amino-9,10-dimetóxi-l,3,4,6,7,11b5 hexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-butiramida, ácido ((2RS,3RS,llbRS)-2-amino-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-amida ciclopropanocarboxilico, (SR)-1-((RS,RS,RS)-2-amino-9,10-dimetóxi10 1,3,4,6,7,llb-hexaídro-2H-pirido[2,1-a]isoquinolin-3il)-4-fluorometil-pirrolidin-2-ona (RS,RS,RS,RS)-1-(2-amino-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-4-fluorometil-pirrolidin-2-ona, (S)-1-((2S,3S,llbS)-2-amino~9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-4-fluorometil-pirrolidin-2-ona, (R)-1-((2S,3S,llbS)-2-amino-9,10-dimetóxi1,3,4,6,7,llb-hexaídro-2H-pirído[2,1-a]isoquínolin-320 il)-4-fluorometil-pirrolidin-2-ona, diidrocloridrato de (S)-1-((2S, 3S, llbS)-2-amino9,10-dimetóxi-l,3,4,6,7,llb-hexaidro-2H-pirido[2,1a]isoquinolin-3-il)-4-fluorometil-pirrolidin-2-ona, diidrocloridrato de (R)-1-((2S,3S,llbS)-2-amino25 9,10-dimetóxi-l,3,4,6,7,llb-hexaidro-2H-pirido[2,1a]isoquinolin-3-il)-4-fluorometil-pirrolidin-2-ona, • * « ·····
3-((RS,RS,RS)-2-amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-oxazolidin2-ona,
3-((2RS,3RS,llbRS)-2-amino-9,10-dimetóxi5 1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-3íl)- [1,3]oxazinan-2-ona,
1-((2RS,3RS,llbRS)-2-amino-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-5-metil-pirrolidin-2-ona,
3-((2RS,3RS,llbRS)-2-amino-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-5-fluorometil-oxazolidin-2-ona,
1-((2RS,3RS,llbRS)-2-amino-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-315 il)-3-metil-pirrolidin-2-ona,
3-((2RS,3RS,llbRS)-2-amino-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-5-metil-oxazolidin-2-ona, e os seus sais farmaceuticamente aceitáveis.
Os compostos da fórmula geral (I) especialmente preferidos são aqueles selecionados a partir do grupo que consiste de:
(RS,RS,RS)-(2-amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-tiazolidin25 3-il-metanona, ··· ·· ·· · ·· · ····· · · · · ···«·· · · · · • · ·· ·· · · · • ········ ··· · (—)—(S,S,S)—1—(2-amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido [2,1-a]isoquinolin-3-il)-piperidin-2ona,
1-{(RS,RS,RS)-2-amino-9,10-dimetóxi-l,3,4,6,7,11b5 hexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metilpirrolidin-2-ona, (RS,RS,RS)-1-(2-amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-5,6-diidrolH-piridin-2-ona, (S,S,S)-3-(1,1-dioxo-[1,2]tiazinan-2-il)-9,10dimetóxi-l, 3,4,6,7,llb-hexaidro-2H-pirido[2,1a]isoquinolin-2-ilamina, (R) -1-((S,S,S)-2-amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metil15 pirrolidin-2-ona, (S,S,S,S)-1-(2-amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metilpirrolidin~2-ona,
1-((RS,RS,RS)-2-amino-9,10-dimetóxi-l,3,4,6,7,11b20 hexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-5-metilpiperidin-2-ona, (S) -1-((2S,3S,llbS)-2-amino-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-4-fluorometil-pirrolidin-2-ona,
| * | • · | • | • | • · · | • | ♦ * · | |
| • | |||||||
| • · | • | • · · · | • | • | • | ♦ | • |
| • | • · ♦ * · | • | • | * | * | ♦ | |
| • | • · | • ·· | ·· · | • | • · · | 9 |
(R)-1-((2S,3S,llbS)-2-amino~9,10-dimetóxi1,3,4,6,7,llb-hexaídro-2H-pirido[2,1-a]isoquinolin-3il)-4-fluorometil-pirrolidin-2-ona,
3-((2RS, 3RS,llbRS)-2-amino-9,10-dimetóxi5 1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-5-metil-oxazolidin-2-ona, e os seus sais farmaceuticamente aceitáveis.
Os compostos da fórmula geral I têm três ou mais átomos de carbono assimétricos e podem existir na forma de enantiômeros opticamente puros, misturas de diastereômeros, racematos, ou misturas de racematos diastereoisoméricos. A invenção abrange todas estas formas .
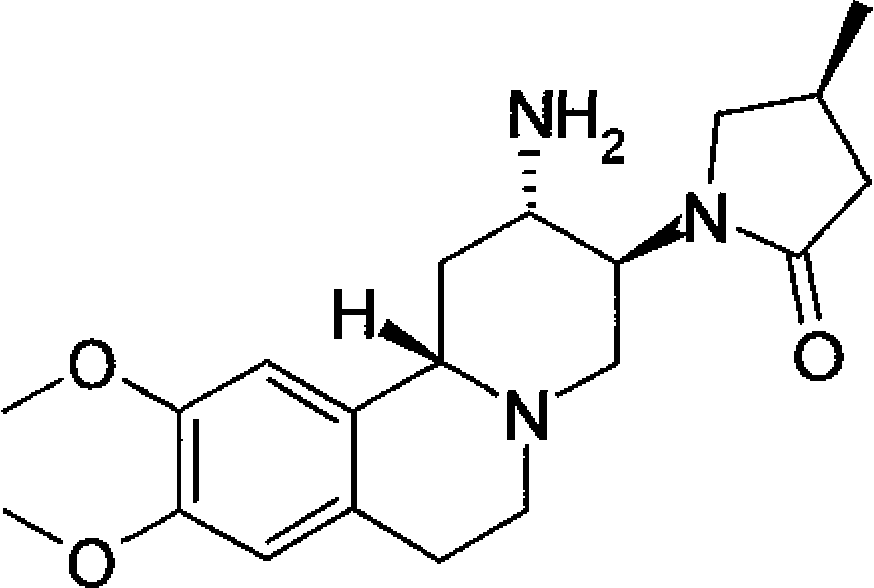
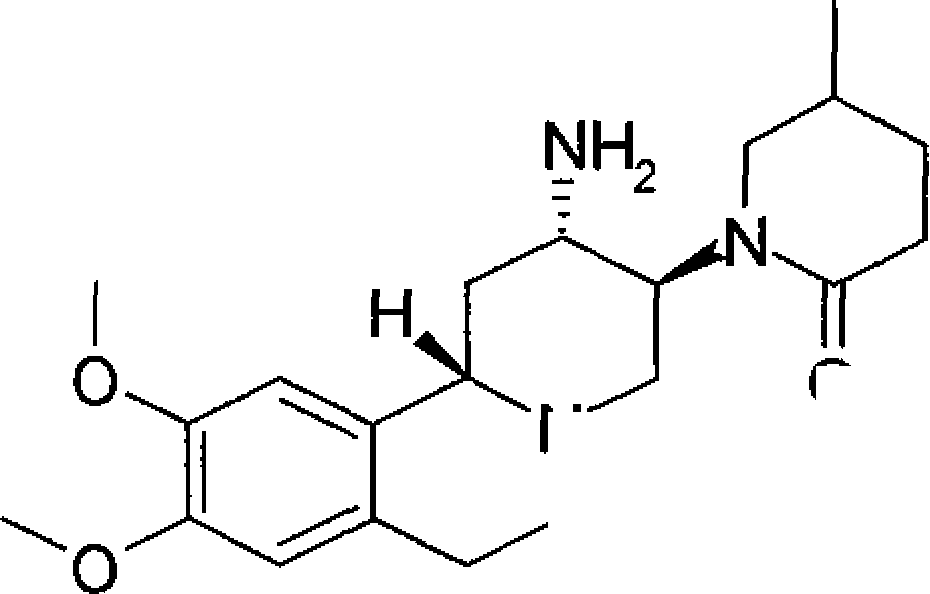
Em uma concretização preferível, R1, o grupo de amino na posição 2 e o hidrogênio na posição 11b da espinha dorsal de pirido[2,1-a]isoquinolina estão todos na configuração S, isto é,
Em uma outra concretização preferível, R1, o grupo de amino na posição 2 e o hidrogênio na posição 11b da espinha dorsal de pirido[2,1-a]isoquinolina são todos na configuração R, isto é, r
Deverá ser compreendido que os compostos da fórmula geral (I) na presente invenção podem ser derivados nos grupos funcionais para proporcionarem deri5 vados que são capazes de conversão de volta ao composto de origem in vivo.
A presente invenção também se refere a um processo para a manufatura dos compostos da fórmula I. Os compostos da presente invenção podem ser preparados como exposto adiante:
Nos esquemas de reação expostos em seguida (Esquemas 1 a 6) , os substituintes R1, R2, R3, R4, R5 e
R6 têm os significados tais como definidos anteriormente, a não ser que de outro modo indicado.
Os compostos da fórmula geral I são sintetizados a partir do carbamato A por meio de métodos que são conhecidos na técnica, de preferência utilizando-se cloreto de hidrogênio em dioxana ou ácido trifluoroacético ou ácido trifluoroacético em diclorometano quando
Pé Boc. O carbamato A pode ser obtido a partir de Nbenzilcarbamato A' por meio de métodos conhecidos na técnica, de preferência por meio de hidrogenação sob uma pressão de cerca de 3 bar, na presença de paládio em carvão vegetal ativado, em um solvente tal como etanol (Esquema 1).
P é um grupo de proteção amino adequado, tal como benziloxi-carbonil (Z) , aliloxicarbonil (Aloc), e, de preferência, tert-butoxicarbonil (Boc).
A conversão de um composto da fórmula I é realizada por divagem do grupo de proteção de amino.
A divagem do grupo de proteção de amino pode ser realizada por meio de métodos convencionais, tais como se encontram descritos, por exemplo, em P. Kocienski, Protecting groups, Thieme Verlag Stuttgart New York 1994, páginas 192-201. De preferência, a divagem do grupo de proteção de amino é realizada sob condições ácidas. O grupo de proteção de amino é tert-butoxicarbonil, o qual pode ser clivado por meio de acídólise com ácidos fortes, tais como cloreto de hidrogênio ou ácido trifluoroacético, ou com ácidos de Lewis. De preferência, ele é clivado com solução de cloreto de hidrogênio 4M em dioxana. Alternativamente, o grupo de proteção de amino é clivado por meio de hidrogenação catalítica sob • r *
3?
condições amplamente conhecidas daqueles versados na técnica.
A síntese dos derivados de amida Al encontra-se salientada no Esquema 2 e começa com ο β5 cetoéster B (Ra = metil or etil) . Os compostos da fórmula B são amplamente conhecidos na técnica (por exemplo, Helv. Chim. Acta 1958, 41, 119) . A reação de B com acetato de amônio em um solvente, tal como metanol, produz o β-enamino-éster C, o qual é reduzido, de pre10 ferência com boroidreto de sódio/ ácido trifluoroacético, para o correspondente β-amino-éster. O grupo de amino é opcionalmente benzilado e então convertido para o tert-butil carbamato da fórmula D. O grupo éster de D é hidrolisado utilizando-se uma base, de preferência hidróxido de potássio ou hidróxido de sódio em uma mistura de água /tetraidrofurano, para proporcionar o acido E. O composto E é levado a reagir com uma amina apropriada na presença de um agente de acoplamento adequado, por exemplo, hexafluorofosfato de O-(720 azobenzotriazol-l-il)-1,1,3,3-tetrametilurônio (HATU), e uma base, por exemplo, N-etildiisopropilamina, para proporcionar a amida A2.
• · * » · * ·»· w · ·» ·· · · • ♦ · · · · · . * ·«· · · * • · · · · · » · ··· ··· · ··· ·
A
Esquema 2
Ra = metil ou etil, Rp = H ou PhCH2.
A síntese de derivados de lactam ou sultam
A2 começa a partir de ácido carboxílico E e encontra-se salientado no Esquema 3. 0 ácido E é convertido para carbamato F através de uma recomposição de Curtius, utilizando-se métodos conhecidos na técnica (por exemplo, Tetrahedron 1974, 30, 2157 or Tetrahedron Lett.
1984, 25, 3515). A amina G é produzida a partir do carbamato F por meio de métodos padrão (H2, Pd-C, ácido acético no caso de Rb - benzilo; Bu4NF/THF, Et4NF/CH3CN, ou CsF/DMF no caso de Rb = Me3SiCH2CH2) . A amina G é levada a reagir com ácido clorídrico, cloreto de sulfonil, ou cloroformato H na presença de uma base (por exemplo, trietilamina) para proporcionar amida ou sulfo15 namida K. Alternativamente, amida K é obtida a partir de G mediante reação com lactona J, seguida por conver• · são do hidroxilo recém formado em um grupo retirante, utilizando-se métodos conhecidos na técnica. Finalmente, ciclisação de K utilizando-se uma base, por exemplo, hidreto de sódio, em um solvente tal como N,N5 dimetilformamida, opcionalmente na presença de iodeto de sódio, conduz a A2.
Rb - Me3SiCH2CH2 ou PhCH2; Rp = grupo retirante, por exemplo,
H ou PhCH2; W = C ou S{=0); Cl, Br, ou OTs.
Lactamas não-saturadas da fórmula A3 são sintetizadas a partir da amina G de acordo com o Esque10 ma 4. Desta maneira, a alquilação de G com halogeneto de alquila L (na presença de uma base, por exemplo, trietilamina), seguida por acilação (na presença de uma base, por exemplo, trietilamina) com halogeneto de acil
M, proporciona a amida N. O composto N é submetido a metatese de fechamento de anel (te. Chem. .Res. 2001, 34, 18), utilizando-se um catalsiador de rutênio, por exemplo, bicloreto de bis(tricicloexilfosfina)5 benzilidenorutênio(IV), e opcionalmente um ácido de Lewis, por exemplo, tetraisopropil-ortotitanato, para proporcionar A3.
Esquema 4
Rp = H ou PhCH2; X - grupo retirante, por exemplo, g., Cl ou Br.
As amidas e sulfonamidas da fórmula A4 são preparadas de acordo com o Esquema 5 mediante tratamento da amina G (no caso de R5 = H) ou P (no caso de R5 H) com cloretos de ácidos ou cloretos de sulfonil apropriados. A transformação de G na amina secundária P é realizada, por exemplo, por meio de alquilação, alquilação redutora, ou por acilação e subseqüente redução, utilizando-se métodos conhecidos na técnica..
• · ·
- 25 Esquema 5
Rp = H ou PhCH2.
cetoéster B pode ser produzido a partir de 1,2,3,4-tetraidro-l-isoquinolinoacetato Q por meio do intermediário diéster R {Esquema 6), de acordo com procedimentos da literatura (por exemplo, Helv. Chim. Acta 1958, 41, 119). Os compostos da formula Q são amplamente conhecidos na técnica e podem ser produzidos por meio de uma ampla variedade de métodos (por exemplo, Synthesis 1987, 474 e pelas referências citadas no mesmo).
Scheme 6
h^COORa
Ra = metilo ou etilo.
Os compostos da fórmula I têm três ou mais átomos de carbono assimétricos e podem existir na forma de enantiômeros opticamente puros, de misturas de diastereômeros, de racematos, ou de misturas de racematos diasteroisoméricos. As formas opticamente puras podem • · ·
5/ ser obtidas, por exemplo, por cristalização fracionária ou cromatografia assimétrica (cromatografia com adsorvente ou eluente quiral) dos racematos dos compostos da fórmula I. De forma assemelhada, precursores sintéti5 cos dos compostos da formula I podem ser separados nos enantiômeros puros.
Com particularidade, as formas opticamente puras de 1,2,3,4-tetraidro-l-isoquinolinoacetato (Q*) podem ser usadas como um material de partida para a síntese de compostos da formula I opticamente puros.
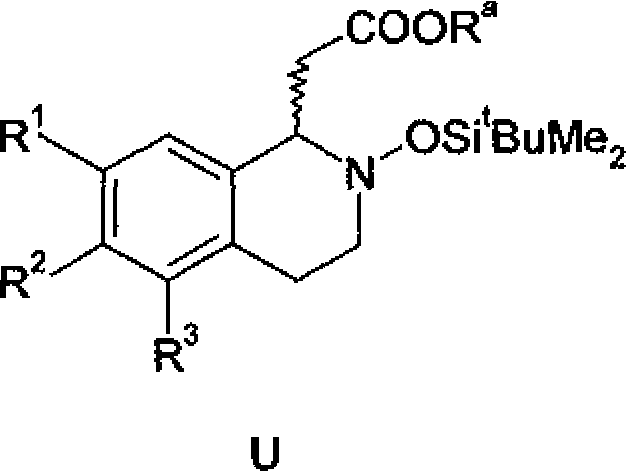
As formas opticamente puras de Q são amplamente conhecidas na literatura e podem ser produzidas a partir de racematos por meio de cristalização fracionária utilizando-se agentes de conversão quiral, por exemplo, áci15 dos tartranílicos, tais como descritos por Montzka et âl. (US3452086). Alternativamente, os enantiômeros Q* puros podem ser sintetizados a partir de precursores aquiraís , por exemplo, mediante adição de acetais S às nitronas da formula T na presença de ácidos de Lewis quirais, seguida por redução do intermediário U com zinco, tal como descrito por Murahashi e colaboradores (J. Ara. Chem, Soc. 2002, 124, 2888, Esquema 7).
Scheme 7
Ra = metilo ou etilo.
«
3^
A invenção relaciona-se ainda com os compostos da fórmula (I) tais como definidos anteriormente, quando manufaturados de acordo com um processo tal como definido anteriormente.
Conforme descrito anteriormente, os compostos da fórmula (I) da presente invenção podem ser usados como medicamentos para o tratamento e/ou profilaxia de enfermidades que estão associadas com DPP-IV, tais como diabetes, com particularidade diabetes melli10 tus não dependentes de insulina, tolerância a glicose prejudicada, enfermidade do intestino inflamatória, Colitis Ulcerosa, Morbus Crohn, obesidade, e/ou síndrome metabólica ou proteção de β-célula, de preferência diabetes mellitus não dependentes de insulina e/ou tole15 rância a glicose prejudicada. Além disso, os compostos da presente invenção podem ser usados como agentes diuréticos ou para o tratamento e/ou profilaxia de hipertensão.
A invenção também se relaciona com compo20 sições farmacêuticas que compreendem um composto tal como definido anteriormente e um veículo e/ou adjuvante farmaceuticamente aceitável.
Além disso, a invenção refere-se aos compostos tais como definidos anteriormente para o uso co25 mo substâncias terapeuticamente ativas, com particularidade como substâncias ativas terapêuticas para o tratamento e/ou profilaxia de enfermidades que estão associadas com DPP-IV, tais como diabetes, com particulari• · * dade diabetes mellitus não dependentes de insulina, tolerância a glicose prejudicada, enfermidade do intestino inflamatória, Colitis Ulcerosa, Morbus Crohn, obesidade, e/ou síndrome metabólica ou proteção de β-célula, de preferência para o uso como substâncias ativas terapêuticas para o tratamento e/ou profilaxia de diabetes mellitus não dependentes de insulina e/ou tolerância a glicose prejudicada. Além disso, a invenção aos compostos tais como definidos anteriormente para o uso co10 mo agentes diuréticos ou para o uso como substâncias ativas terapêuticas para o tratamento e/ou profilaxia de hipertensão.
Em uma outra concretização, a invenção refere-se a um método para o tratamento e/ou profilaxia de enfermidades que estão associadas com DPP-IV, tais como diabetes, com particularidade diabetes mellitus não dependentes de insulina, tolerância a glicose prejudicada, enfermidade do intestino inflamatória, Colitís Ulcerosa, Morbus Crohn, obesidade, e/ou síndrome metabólica ou proteção de β-célula, de preferência para o tratamento e/ou profilaxia de diabetes mellitus não dependentes de insulina e/ou tolerância a glicose prejudicada, método esse que compreende a administração de um composto tal como definido anteriormente a um ser humano ou animal. Além disso, a invenção refere-se a um método para o tratamento e/ou profilaxia tal como definido anteriormente, em que a enfermidade é hiper29
A tensão ou em que um agente diurético tem um efeito benéfico .
A invenção refere-se ainda ao uso dos compostos tais como definidos anteriormente para o trata5 mento e/ou profilaxia de enfermidades que estão associadas com DPP-IV, tais como diabetes, com particularidade diabetes mellitus não dependentes de insulina, tolerância a glicose prejudicada, enfermidade do intestino inflamatória, Colitis Ulcerosa, Morbus Crohn, obesida10 de, e/ou sindrome metabólica ou proteção de p-célula, de preferência para o tratamento e/ou profilaxia de diabetes mellitus não dependentes de insulina e/ou tolerância a glicose prejudicada. Além disso, a invenção refere-se ao uso tal como definido anteriormente, em que a enfermidade é hipertensão ou ao uso como agente diurético.
Além disso, a invenção refere-se ao uso dos compostos tais como definidos anteriormente para a preparação de medicamentos para o tratamento e/ou pro20 filaxia de enfermidades que estão associadas com DPPIV, tais como diabetes, com particularidade diabetes mellitus não dependentes de insulina, tolerância a glicose prejudicada, enfermidade do intestino inflamatória, Colitis Ulcerosa, Morbus Crohn, obesidade, e/ou sindrome metabólica ou proteção de β-célula, de preferência para o tratamento e/ou profilaxia de diabetes mellitus não dependentes de insulina e/ou tolerância a glicose prejudicada. Esses medicamentos compreendem um • · ·
- 30 composto tal como definido anteriormente. Além disso, a invenção refere-se ao uso tal como descrito anteriormente, em que a enfermidade é hipertensão ou para a preparação de agentes diuréticos.
No contexto com os métodos e usos definidos anteriormente, as enfermidades seguintes referem-se a uma concretização preferida: diabetes, com particularidade diabetes mellitus não dependentes de insulina, tolerância a glicose prejudicada, obesidade, e/ou sín10 drome metabólica ou proteção de β-célula, de preferência para o tratamento e/ou profilaxia de diabetes mellitus não dependentes de insulina e/ou tolerância a glicose prejudicada.
Os compostos da fórmula (I) podem ser raa15 nufaturados por meio dos métodos apresentados adiante, por meio dos métodos apresentados nos exemplos ou por meio de métodos análogos. Condições de reação apropriadas para as etapas de reação individuais são conhecidas daqueles versados na técnica. Os materiais de par20 tida são ou encontrados disponíveis comercialmente ou podem ser preparados por meio de métodos análogos aos métodos apresentados adiante ou nos exemplos ou por meio de métodos conhecidos na técnica
Os testes seguintes foram realizados com a finalidade de se determinar a atividade dos compostos da fórmula I.
A atividade dos inibidores de DPP-IV é testada com DPP-IV humano natural, derivado de um fundo
comum de plasma humano ou com DPP-IV recombinante humano. Plasma de citrato humano proveniente de diferentes doadores é reunido, filtrado através de uma membrana de 0.2 micrômetros sob condições estéreis e alíquotas de 1 ml são congeladas bruscamente e armazenadas a -120°C até serem usadas. No ensaio colorimétrico de DPP-IV, utilizam-se de 5 a 10 μΐ de plasma humano e no ensaio fluorométrico 1.0 μΐ de plasma humano, num volume de ensaio total de 100 μΐ, como uma fonte de enzimas. 0 cDNA da seqüência de aminoácidos 31 - a 766 de DPP-IV humano, restringido para o término-N e o domínio de transmembrana, é clonado em Pichia pastoris. O DPP-IV humano é expressado e purificado a partir do meio de cultura utilizando-se cromatografia de coluna convencional, incluindo exclusão de dimensão e cromatografia de ânion e cátion. A pureza do preparado de enzima final de azul Coomassie SDS-PAGE é > 95%. No ensaio colorímétrico de DPP-IV, utilizam-se 20 ng rec.-h DPP-IV, e no ensaio fluorométrico 2 ng rec-h DPP-IV, em um volume de ensaio total da ordem de 100 μΐ, como uma fonte de enzimas.
No ensaio fluorogênico utiliza-se Ala-Pro7-amido-4-trifluorometilcumarina (Calbiochem No 125510) como um substr.ato. Uma solução de suprimento de 20 mM em 10% DMF/H2O é armazenada a -20°C até ser usada. Nas determinações de IC50 utiliza-se uma concentração de substrato final de 50 μΜ. Nos ensaios usados para se determinarem os parâmetros cinéticos, tais como Km,
Vmax, Ki/ a concentração de substrato é variada entre 10 μΜ e 500 μΜ.
No ensaio colorimétrico utiliza-se H-AlaPro-pNA.HCl (Bachem L-1115) como um substrato. Uma so5 lução de suprimento de 10 mM em 10% Me0H/H2O é armazenada a -20°C até ser usada. Nas determinações de IC50 utiliza-se uma concentração de substrato final de 200 μΜ. Nos ensaios para se determinarem os parâmetros cinéticos, tais como Km, Vmax, Kiz a concentração de subs10 trato é variada entre 100 μΜ e 2000 μΜ.
Fluorescência é detectada em um Perkin Elmer Luminescence Spectrometer LS SOB sob um comprimento de onda de excitação de 400 nm e um comprimento de onda de emissão de 505 nm continuamente a cada 15 segundos durante 10 a 30 minutos. As constantes de taxa inicial são calculadas por meio de regressão linear de melhor ajuste.
A absorção de pNA liberada a partir do substrato colorimétrico é detectada em um Packard Spec20 traCount a 405 nm, continuamente, a cada 2 minutos, durante de 30 a 120 minutos. As constantes de taxa inicial são calculadas por meio de regressão linear de melhor ajuste.
Os ensaios de atividade de DPP-IV são rea25 lizados em placas de 96 cavidades a 37°C em um volume de ensaio total de 100 μΐ. 0 amortecedor de ensaio consiste de 50 mM Tris/HCl pH 7,8 contendo 0,1 mg/ml de BSA e 100 mM de NaCI. Os compostos de teste são dis• · *
-solvidos em DMSO a 100%, diluídos para a concentração desejada em DMSO a 10%/H20. A concentração de DMSO final desejada no ensaio é de 1% (v/v). Sob esta concentração, a desativação de enzimas por DMSO é < 5%. Os compostos estão com (10 minutos a 37 °C) e sem préincubação com a enzima. As reações enzimáticas são iniciadas com aplicação de substrato seguida por mistura imediata.
As determinações de IC50 dos compostos de 10 teste são calculadas por meio de regressão linear de melhor ajuste quanto à inibição de DPP-IV de, pelo menos, 5 diferentes concentrações de composto. Os parâmetros cinéticos da reação enzimática são calculados de acordo com pelo menos 5 diferentes concentrações de substrato e pelo menos 5 diferentes concentrações de composto de teste.
Os compostos da presente invenção exibem valores de IC5o de 0,1 nM até 10 μΜ, com maior preferência de 0,1 - 100 nM, tal como ilustrado na tabela exposta em seguida:
| Exemplo | ICso [μΜ] |
| 2 | 0,041 |
| 6 | 0,023 |
| 10 | 0,0093 |
| 12 | 0,033 |
| 16 | 0,131 |
• · ·
Os compostos da fórmula I e/ou seus sais
farmaceuticamente aceitáveis podem ser usados como medicamentos, por exemplo, na forma de preparados farmacêuticos para administração entérica, parenteral ou tópica. Eles podem ser administrados, por exemplo, de forma peroral, por exemplo, na forma de comprimidos, comprimidos revestidos, drágeas, cápsulas de gelatina dura e macia, soluções, emulsões ou suspensões, de forma retal, por exemplo, na forma de supositórios, de forma parenteral, por exemplo, na forma de soluções injetáveis ou soluções de infusão, ou topicamente, por exemplo, na forma de ungüentos, cremes ou óleos. Prefere-se a administração oral.
A produção dos preparados farmacêuticos pode ser realizada de uma maneira que será familiar a qualquer pessoa versada na técnica, ao trazer os compostos de fórmula I descritos e/ou seus sais e farmaceuticamente aceitáveis, opcionalmente em combinação com outras substâncias terapeuticamente valiosas, a uma forma de administração galênica em conjunto com materiais excipientes sólidos ou líquidos terapeuticamente compatíveis, inertes, não tóxicos, adequados e, se desejado, adjuvantes farmacêuticos usuais.
Materiais excipientes adequados são não apenas materiais excipientes inorgânicos, mas, também, materiais excipientes orgânicos. Assim, por exemplo, lactose, amido de milho ou seus derivados, talco, ácido esteárico ou seus sais poderão ser utilizados como ma·*· teriais excipientes para comprimidos, comprimidos revestidos, drágeas e cápsulas de gelatina dura. Os materiais excipientes adequados para cápsulas de gelatina macia são, por exemplo, óleos vegetais, ceras, gorduras e polióis semi-sólidos e líquidos (entretanto, na dependência da natureza do ingrediente ativo, nenhum excipiente será requerido no caso das cápsulas de gelatina macia). Os materiais excipientes adequados para a produção de soluções e xaropes compreendem, por exem10 pio, água, polióis, sacarina, açúcar invertido e outros assemelhados. Os materiais excipientes adequados para soluções injetáveis compreendem, por exemplo, água, álcoois, polióis, glicerol e óleos vegetais. Os materiais excipientes adequados para supositórios compreen15 dem, por exemplo, óleos naturais ou endurecidos, ceras, gorduras e polióis semi-líquidos ou líquidos. Os materiais excipientes adequados para preparados tópicos compreendem glicerídeos, glicerídeos semi-sintéticos e sintéticos, óleos hidrogenados, ceras líquidas, parafi20 nas líquidas, álcools graxos líquidos, esteróis, polietileno glicóis e derivados de celulose.
Estabilizadores, preservativos, agentes de umedecimento e de emulsionamento, agentes de aperfeiçoamento de consistência, agentes de aperfeiçoamento de aroma, sais para variação de pressão osmótica, substâncias amortecedoras, solubilizantes, corantes e agentes dissimulantes e antioxidantes usuais entram em consideração como adjuvantes farmacêuticos.
A dosagem dos compostos da fórmula I poderá variar dentro de amplos limites, dependentes da enfermidade a ser controlada, da idade e da condição individual do paciente, bem como da modalidade de admi5 nistração e será, naturalmente, ajustada aos requisitos individuais em cada caso particular. Para pacientes adultos, entra em consideração uma dosagem diária de cerca de 1 mg até cerca de 1000 mg, especialmente cerca de 1 mg até cerca de 100 mg. Na dependência da serie10 dade da enfermidade e do perfil farmacocinético preciso do composto, poderão ser administradas uma ou várias unidades de dosagem diária, por exemplo, em unidades de 1 a 3 dosagens.
Convenientemente, os preparados farmacêu15 ticos contêm cerca de 1-500 mg, de preferência 1-100 mg, de um composto da fórmula I.
Os exemplos seguintes servem para ilustrar a presente invenção de maneira mais detalhada. Não obstante, os mesmos não se destinam a limitar o seu es20 copo de forma alguma.
Exemplos:
Abreviaturas: MS - espectroscopia de massa, aq. = aquoso, r.t. = temperatura ambiente, THF = tetraidrofurano, NMR = espectroscopia por ressonância magnética, DMF = dimetilformamida, DMSO = dimetilsulfóxido, ISP - spray de ions.
• « * • ♦ · ' « · ··:
Exemplo 1 (RS,RS,RS)-(2-Amino~9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-pirrolidin1-il-metanona
a) Etil éster de ácido 2-amino-9,10-dimetóxi-l,6,7,11btetraidro-4H-pirido[2,1-a]isoquinolina-3-carboxílico
Uma mistura de etil éster de ácido 9, 10dimetóxi-2-oxo-l,3,4,6,7,llb~hexaidro-2H-pirido[2,ΙΙΟ a]isoquinolina-3-carboxílico (Helv. Chim. Acta 1958, 41, 119; 4,00 g, 12.0 mmol) e de acetate de amônio (13,9 g, 180 mmol) em metanol foi submetida a agitação 5 horas sob temperatura ambiente. Depois de evaporação do solvente, o resíduo foi dividido entre diclorometano e solução de hidróxido de sódio aquosa 1 Μ. A camada orgânica foi secada (MgSC>4) , e triturada com heptano para proporcionar o composto do título (3,71 g, 93%). Sólido não branco, MS (ISP) 333,2 (M+H)+.
b) Etil éster de ácido (RS,RS,RS)-2-tert-butoxicar20 bonilamino-9,10-dimetóxi-l,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquínolina-3-carboxílico
Ácido trif luoroacético (120 ml) foi adicionado a 0°C a uma solução de etil éster de ácido 2amino-9,10-dimetóxi-l,6,7,llb-tetraidro-4H-pirido[2,1- 38
5°
a]isoquinolina-3-carboxílico (6,90 g, 20,8 mmol) em tetraidrofurano (60 ml), então depois de 30 minutos a solução homogênea foi tratada com boroidreto de sódio (1,64 g, 41,5 mmol) e submetida a agitação durante ou5 tros 40 minutos. A mistura de reação foi concentrada in vacuo e o resíduo dividido entre solução de hidróxido de sódio 2 M aquosa e diclorometano. A camada orgânica foi lavada com salmoura, secada (MgSO^) e evaporada. O resíduo foi dissolvido em diclorometano (80 ml), e uma solução de di-tert-butil-bicarbonato (4,98 g,
22,8 mmol) em diclorometano (50 ml) foi adicionada sob temperatura ambiente. A solução foi submetida a agitação durante a noite sob temperatura ambiente, concentrada, e o resíduo foi triturado em heptano para pro15 porcionar o composto do título (7,44 g, 83%). Sólido amarelo claro, MS (ISP) 435,4 (M+H)+.
c) Ácido (RS,RS,RS)-2-tert-butoxicarbonilamino-9,10dímetóxi-1,3,4,6,7,llb-hexaidro-2H-pirido[2,1a]isoquinolina-3-carboxílico
Grânulos de hidróxido de potássio (8 6%,
4,47 g, 68,5 mmol) foram adicionados a uma suspensão de etil éster de ácido (RS,RS,RS)-2-tert-butoxicarbonilamino-9,10-dimetóxi-l,3,4,6,7,llb-hexaidro-2H-pirido [2,1-a]ísoquinolina-3-carboxílico (7,44 g, 17,1 mmol) em tetraidrofurano /água 1:1 (140 ml). Depois de aquecimento durante 5 horas sob refluxo, a mistura foi concentrada in vacuo. 0 resíduo foi recolhido em amortecedor de fosfato de potássio aquoso 1M (pH 6,85) e di·* · * «· * · *
_ * ι» » β clorometano, e adicionou-se etanol até ser obtida uma mistura transparente de duas fases. A camada orgânica foi separada, lavada com salmoura e evaporada para proporcionar o composto do titulo (6,91 g, 99%). Sólido amarelo claro, MS (ISP) 405,3 (M-H)“.
d) tert-Butil éster de ácido (RS,RS,RS)-[9,10-dimetóxi3-(pirrolidina-l-carbonil)-1,3,4,6,7,llb-hexaidro-2Hpirido[2,1-a]isoquinolin-2-il]-carbâmico
Adicionaram-se N-etildiisopropiiamina (96 mg, 0,74 mmol) e hexafluorofosfato de O-(7-azabenzotriazol-l-il)-N,N,N',N'-tetrametilurônio (HATU, 103 mg, 0,27 mmol) sob temperatura ambiente a uma suspensão de ácido (RS,RS,RS)-2-tert-butoxicarbonilamino-9,10-dimetóxi-l, 3,4,6,7,llb-hexaidro-2H-pirido[2,1-a] isoquino15 lina-3-carboxilico (100 mg, 0,25 mmol) em N,N,dimetilformamida (2 ml), então depois de 45 minutos adicionou-se pirrolidina (19 mg, 0,27 mmol). A solução homogênea foi submetida a agitação durante 90 minutos sob temperatura ambiente, então dividida entre hexano/etil acetato 1:1 e água. A camada orgânica foi lavada com salmoura, secada (MgSO4) , e evaporada, e o resíduo cromatografado (SiO2, CH2Cl2/MeOH/NH4OH 80:1:0,2) para produzir o composto do título (58 mg, 51%). Sólido amarelo claro, MS (ISP) 460,5 (M+H)+.
e) (RS,RS,RS)-(2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-pirrolidin1-il-metanona
Uma solução de tert-butil éster de ácido (RS,RS,RS)-[9,10-dimetóxi-3-(pirrolidina-l-carbonyl)1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-2il]-carbâmico (55 mg, 0,12 mmol) em solução de cloreto de hidrogênio (4 M em dioxana, 1 ml) foi submetida a agitação durante 1 hora sob temperatura ambiente, então neutralizada com CH2Cl2/MeOH/NH4OH 90:10:0,25 e evaporada. Cromatografia do resíduo (SiO2, CH2Cl2/MeOH/NH4OH 90:10:0.25) proporcionou o composto do título (32 mg, 74%). Espuma não branca, MS (ISP) 359, 6 (M+) .
Exemplo 2 (RS,RS,RS)-(2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-tiazolidin3-il-metanona
NH, O
a) tert-Butil éster de ácido (RS,RS,RS)-[9,10-dimetóxi3-(tiazolidina-3-carbonil)-1,3,4,6,7,llb-hexaidro-2Hpirido[2,1-a]isoquinolin-2-il]-carbâmico composto do título foi produzido de acordo com o método geral do Exemplo ld a partir de ácido (RS,RS,RS)-2~tert-butoxicarbonilamino-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolina-3carboxílico (Exemplo lc) e de tiazolidina. Sólido não branco, MS (ISP) 478,3 (M+H)+.
| • | ··· | ||||||
| ·· • · ·· | • • • • | • • · • · • · | • • • · ··· | *· • • | ·· • • a | • • • • | ·· |
| • • | • · • | • | • •9 | ··· | • | « · |
• * « ··*
b) (RS,RS,RS)-(2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-thiazolidin3-il-metanona composto do título foi produzido de a5 cordo com o método geral do Exemplo le a partir de tert-butil· éster de ácido (RS,RS,RS)-[9,10-dimetóxi-3(tiazolidina-3-carbonil)-1,3,4,6,7, llb-hexaidro-2Hpirido[2,1-a]isoquinolin-2-il]-carbâmico. Espuma branca, MS (ISP) 378,3 (M+H)+.
Exemplo 3 (RS,RS,RS)-(2-Amino-9,10-dimetóxi-l, 3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-azetidin-1il-metanona
a) tert-butil éster de ácido (RS,RS,RS)-[3-(azetidina1-carbonil)-9,10-dimetóxi-l,3,4,6,7,llb-hexaidro-2Hpirido[2,1-a]isoquinolin-2-il]-carbâmico
O composto do título foi produzido de acordo com o método geral do Exemplo Id a partir de ácido (RS,RS,RS)-2-tert-butoxicarbonilamino-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolina-3carboxílico (Exemplo lc) e azetidina. Sólido amarelo « *····· · * t · ···«·«· · · · ♦ a · ♦ · ♦» · · ·»« » claro, MS (ISP) 446,3 (M+H)+.
b) (RS,RS,RS)-(2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-azetidin-1il-metanona.
O composto do título foi produzido de acordo com o método geral do Exemplo le a partir de tert-butil éster de ácido (RS,RS,RS)-[3-(azetidina-1carboníl)-9,10-dimetóxi-l,3,4,6,7,llb-hexaidro-2Hpirido[2,1-a]isoquinolin-2-il]-carbâmico. Espuma bran10 ca, MS (ISP) 346,2 (M+H). + .
Exemplo 4 (SS)-l-((RS,RS,RS)-2-Amino-9,10-dimetóxi-l,3, 4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinoline-3-carbonil)pirrolidina-2-carbonitrilo
a) . tert-Butil éster de ácido [(RS,RS, RS)-3-((SS)-2ciano-pírrolídina-l-carbonil)-9,10-dimetóxi-l,3,4,6,7, llb-hexaidro-2H-pirido[2,1-a]ísoquínolin-2-íl]carbâmico
O composto do título foi produzido de acordo com o método geral do Exemplo Id a partir de ácido (RS,RS,RS)-2-tert-butoxicarbonilamino-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolina-343 carboxílico (Exemplo lc) e (S)-2-ciano-pirrolidina (EP1258476). Sólido amarelo, MS (ISP) 485,5 (M+H)+.
b) (S)-1-((RS,RS,RS)-2-Araino-9,10-dimetóxi-l,3,4,6,7, llb-hexaidro-2H-pirido[2,1-a]isoquinoline-3-carbonil)5 pirrolidina-2-carbonitrilo
O composto do título foi produzido de acordo com o método geral do Exemplo le a partir de tert-butil éster de ácido [(RS,RS,RS)-3-((SS)-2-cianopirrolidina- 1-carbonil) -9,10-dimetóxi-l,3,4,6,7,11b10 hexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico. Sólido amarelo claro, MS (ISP) 385,2 (M+H)+.
Exemplo 5
1-((RS,RS,RS)-2-Amino-9,10-dimetóxi-l,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-piperidin-2-ona
a) 2-Trimetilsilanil-etil éster de ácido (RS,RS,RS)-(2tert-butoxicarbonilamino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-carbâmico
Uma mistura de ácido (RS,RS,RS)-2-tert20 butoxicarbonilamino-9,10-dimetóxi-l,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolina-3-carboxílico (Exemplo lc, 6,91 g, 17,0 mmol), difenilfosforiyl azida (7,40 g, 25,6 mmol), trietilamina (1,72 g, 17,0 mmol), 244 •Μ-
(trimetilsilil)-etanol (30,2 g, 256 mmol) e tolueno (40 ml) foi aquecida durante 48 horas a 80°C sob uma suave corrente de nitrogênio. A mistura de reação mixture foi então concentrada in vacuo, o resíduo cromatografa5 do (SiO2, CH2Cl2/MeOH/NH4OH 80:1:0,2), e as frações de produto trituradas em hexano/etil acetato 1:1 para proporcionarem o composto do título (5,22 g, 59%). Solido branco, MS (ISP) 522,4 (M+H)+.
b) tert-Butil éster de ácido (RS,RS,RS)-(3-amino-9,1010 dimetóxi-1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-2-il)-carbâmico
Uma suspensão de etil éster de ácido 2trimetilsilanil-(RS,RS,RS)-(2-tert-butoxicarbonilamino9,10-dimetóxi-l,3,4,6,7,llb-hexaidro-2H-pirido[2,115 a]issoquinolin-3-il)-carbâmico (5,22 g, 10,0 mmol) em solução de fluoreto de tetrabutilamônio (1 M em THF, 42 ml, 42 mmol) foi aquecida durante 90 minutos a 50°C. A solução resultante foi concentrada in vacuo e cromatograf ada (CH2Cl2/MeOH/NH4OH 95:5:0,25) para proporcionar o composto do título (3,59 g, 95%). Sólido amarelo claro, MS (ISP) 378,4 (M+H)+; tR = 7,2 e 18,9 minutos (Chiralpak® AD 25*0,03 cm, heptano/etanol/trietilamina 70:30:0,3, velocidade de fluxo 4 μΐ/min).
c) tert-Butil éster de ácido (RS,RS,RS)-[3-(5-cloro25 pentanoilamino)-9,10-dimetóxi-l,3,4,6,7,llb-hexaidro2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico
Cloreto de 5-clorovaleril (466 mg, 2,91
- 45 10 mmol) foi adicionado a 0°C a uma solução de tert-butil éster de ácido (RS,RS,RS)-(3-amino-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-2il)-carbâmico (1,00 g, 2,65 mmol) e trietilamina (295 mg, 2,91 mmol), e a suspensão resultante foi deixada alcançar a temperatura ambiente durante 30 minutos. A mistura de reação foi então dividida entre diclorometano e água, a camada orgânica foi lavada com salmoura, secada (MgSO4) , e evaporada. Chromatrografia do resíduo (SiO2, CH2Cl2/MeOH/NH4OH 80:2:0,2) proporcionou o composto do título (1,23 g, 94%). Sólido branco, MS (ISP) 496,3 (M+H)+.
d) tert-Butil éster de ácido (RS,RS,RS)-[9,10-dimetóxi3-(2-oxo-piperidin-l~il)-1,3,4,6,7,llb-hexaidro-2H15 pirido[2,1-a]isoquinolin-2-il]-carbâmico
Uma solução de tert-butil éster de ácido (RS,RS, RS)-[3-(5-cloro-pentanoilamino)-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-2il] -carbâmico (1,22 g, 2,46 mmol) em N,N20 dimetilformamida (18 ml) foi tratada com iodeto de sódio (369 mg, 2,46 mmol) e sodium hydride (dispersão a 60%, em óleo, 197 mg, 4,92 mmol) e submetida a agitação durante 2 horas sob temperatura ambiente, então vazada em gelo e dividida entre heptano/etil acetato 1:1 e á25 gua. A camada orgânica foi lavada com salmoura, secada (MgSO4) , e evaporada. Cromatrografia do resíduo (SiO2,
CH2Cl2/MeOH/NH4OH 80:2:0,2) proporcionou o composto do
título (769 mg, 68%). Sólido branco, MS (ISP) 460,3 (M+H)+.
e) 1-((RS,RS,RS)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-piperidin-25 ona
O composto do título foi preparado de acordo com o método geral do Exemplo le a partir de tert-butil éster de ácido (RS,RS,RS)-[9,10-dimetóxi-3(2-oxo-piperidin-l-il)-1,3,4,6,7,llb-hexaidro-2H10 pirido[2,1-a]isoquinolin-2-il]-carbâmico. Sólido branco, MS (ISP) 360,3 (M+H)+.
Exemplos 6 e 7 (—)—(S,S,S)—1—(2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-piperidin-215 ona
e (+)”(R,R,R)-1-(2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-piperidin-2-
tert-Butil éster de ácido (RS, RS, RS) [9,10-dimetóxi-3-(2-oxo-piperidin-l-il)-1,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico ter (580 mg, 1,61 mmol) for dissolvido em eta10 nol/heptano 3:2 (5 ml) e submetido a HPLC de preparação (coluna Chiralpak® AD, heptano/etanol 80:20).
(-)-(S,S,S)-1-(2-Amino-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-piperidin-2-ona: Semi-sólido amarelo claro, 220 mg (38%), tR = 32,0 min (Chiralpak® AD 25x0,46 cm, heptano/etanol 80:20, velocidade de fluxo 1 ml/min).
(+)-(R,R,R)-1-(2-Amino-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-piperidin-2-ona: Semi-sólido amarelo claro, 207 mg (36%), tR - 55,4 min (Chiralpak® AD 25x0.46 cm, heptano/etanol 80:20, velocidade de fluxo 1 ml/min).
Exemplo 8
1-((RS,RS,RS)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11b48
hexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metil-
a) tert-Butil éster de ácido (RS,RS,RS)-[3-(5-cloro-35 metil-pentanoilamino)-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico composto do título foi produzido de acordo com o método geral do Exemplo 5c a partir de tert-butil éster de ácido (RS,RS,RS)-(3-amíno-9,1010 dimetóxi-1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-2-il)-carbâmico (Exemplo 5b) e de cloreto de 5cloro-3-metilvaleril (DE2621576). Sólido branco, MS (ISP) 510,4 (M+H)+.
b) tert-Butil éster de ácido (RS,RS,RS)-[9,10-dimetóxi15 3-(4-metil-2-oxo-piperidin-l-il)-1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico
O composto do título foi produzido de acordo com o método geral do Exemplo 5d a partir de tert-butil éster de ácido (RS,RS,RS)-[3-(5-cloro-320 metil-pentanoilamino)-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico. Sólido amarelo claro, MS (ISP) 474,3 (M+H)+.
c) 1-((RS,RS,RS)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metil49 piperidin-2-ona
O composto do título foi produzido de acordo com o método geral do Exemplo le a partir de tert-butil· éster de ácido (RS,RS,RS)-[9,10-dimetóxí-3(4-metil-2-oxo-piperidin-l-il)-1,3,4,6,7,llb-hexaidro2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico. Sólido branco, MS (ISP) 374,2 (M+H)+.
Exemplo 9 (RS,RS,RS)-1-(2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-pirrolidin2-ona
a) tert-Butil éster de ácido (RS,RS,RS)-[3-(4-clorobutirilamino)-9,10-dimetóxi-l,3,4,6,7,llb-hexaidro-2fípirido[2,1-a]isoquinolin-2-il]-carbâmico
O composto do título foi produzido de acordo com o método geral do Exemplo 5c a partir de tert-butil éster de ácido (RS,RS,RS)-(3-amino-9,10dimetóxi-l, 3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-2-il)-carbâmico (Exemplo 5b) e de cloreto de 4clorobutiril. Sólido branco Sólido branco, MS (ISP) 482,4 (M-t-H)+.
b) tert-Butil éster de ácido (RS,RS,RS)-[9,10-dimetóxi50
3-(2-oxo-pirrolidin-l-il)-1,3,4,6,7,llb-hexaidro-2Hpírido[2,1-a]isoquinolin-2-il]-carbâmico
O composto do título foi produzido de acordo com o método geral do Exemplo 5d a partir de tert-butil éster de ácido (RS,RS,RS)-[3-(4-clorobutirilamino)-9,10-dimetóxí-l,3,4,6, 7,llb-hexaidro-2Hpirido[2,1-a]isoquinolin-2-il]-carbâmico. Sólido amarelo claro, MS (ISP) 446,3 (M+H)+.
c) tert-Butil éster de ácido (RS,RS,RS)-[3-(4-cloro10 butirilamino)-9,10-dimetóxi-l,3,4,6,7,llb-hexaidro-2Hpirido[2,1-a]isoquinolin-2-il]-carbâmico
O composto do título foi produzido de acordo com o método geral do Exemplo le a partir de tert-butil éster de ácido (RS,RS,RS)-[9,10-dimetóxi-315 (2-oxo-pirrolidin-l-il)-1,3,4,6,7,llb-hexaidro-2Hpirido[2,1-a]isoquinolin-2-il]-carbâmico. Sólido branco, MS (ISP) 346,2 (M+H)+.
Exemplo 10
1-((RS,RS,RS)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11b20 hexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metil-
a) tert-Butil éster de ácido [(RS,RS,RS)-3-(4-cloro-3~ • · · • · * · ·· • · · · · * ··« · · · • · · * · * ·······* metil-butirilamino)-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-2-ii]-carbâmico composto do título foi produzido de acordo com o método geral do Exemplo 5c a partir de tert-butil éster de ácido (RS,RS,RS)-(3-amino-9,10dimetóxi-l, 3,4,6,7,llb-hexaidro-2H-pirido[2,1a]isoquinolin-2-il)-carbâmico (Exemplo 5b) e de cloreto de 4-cloro-3-metilbutiril (Chem. Ber. 1964, 97, 2544). Sólido branco, MS (ISP) 496,3 (M+H)+.
b) tert-Butil éster de ácido [(RS, RS, RS)-9,10-dimetóxi3-(4-metil-2-oxo-pirrolidin-l-il)-1,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico
O composto do titulo foi produzido de acordo com o método geral do Exemplo 5d a partir de tert-butil éster de ácido [(RS,RS,RS)-3-(4-cloro-3metil-butiriiamino)-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pírido[2,1-a]isoquinolin-2-il]-carbâmico. Sólido amarelo claro, MS (ISP) 460,3 (M+H)+.
c) 1-((RS,RS,RS)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11b20 hexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metilpirrolidin-2-ona composto do título foi produzido de acordo com o método geral do Exemplo le a partir de tert-butil éster de ácido [(RS,RS,RS)-9,10-dimetóxi-325 (4-metil-2-oxo-pirrolidin-l-il)-1,3,4,6,7,llb-hexaidro2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico. Sólido amarelo claro, MS (ISP) 360,3 (M+H)+.
··· · * ·· ··· · «···· « · * · • · ··· · · · · · « · · · ·· ··» • ·····«·· ··· *
Μ
Exemplo 11
1-((RS,RS,RS)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-etil-
a) tert-butil éster de ácido (RS,RS,RS)-[3-(3-clorometil-pentanoilamino)-9,10-dimetóxi-l,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico
O composto do título foi produzido de a10 cordo com o método geral do Exemplo 5c a partir de tert-butil éster de ácido (RS,RS,RS)-(3-amino-9,10dimetóxi-l, 3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-2-il) -carbâmico (Exemplo 5b) e de cloreto de 3(clorometil)-valeril (J. Korean Chem. Soc. 1991, 35r
756). Sólido branco, MS (ISP) 510,4 (M+H)+.
b) tert-Butil éster de ácido (RS,RS,RS)-[3-(4-etil-2oxo-pirrolidin-l-il)-9,10-dimetóxi-l,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico
O composto do título foi produzido de a20 cordo com o método geral do Exemplo 5d a partir de tert-butil éster de ácido (RS,RS,RS)-[3-(3-clorometilpentanoilamino)-9,10-dimetóxi-l,3,4,6,7, llb-hexaidro2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico. Sólido
amarelo claro, MS (ISP) 474,2 (M+H)+.
c) 1- ( (RS,RS,RS)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-etilpirrolidin-2-ona
O composto do título foi produzido de acordo com o método geral do Exemplo le a partir de tert-butil éster de ácido (RS,RS,RS)-[3-(4-etil-2-oxopirrolidin-l-il)-9,10-dimetóxi-l,3, 4,6,7,llb-hexaidro2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico. Sólido amarelo claro, MS (ISP) 374,5 (M+H)+.
Exemplo 12 (RS,RS,RS)-1-(2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-5,6-diidrolH-piridin-2-ona
a) fcert-Butil éster de ácido (RS,RS,RS)-(3-but-3enilamino-9,10-dimetóxi-l,3,4,6,7,llb-hexaidro-2Hpírido[2,1-a]isoquinolin-2-il)-carbâmico
4-Bromo-2-buteno (60 mg, 0,45 mmol) e tri20 etilamina (49 mg, 0,49 mmol) foram adicionados a uma solução de tert-butil éster de ácido (RS,RS,RS)-(3amino-9,10-dimetóxi-l,3,4,6,7,llb-hexaidro-2Hpirido[2,1-a]isoquinolin-2-il)-carbâmico (Exemplo 5b;
• ·
153 mg, 0,41 mmol), e a mistura foi aquecida sob refluxo, então depois de 18 horas, adicionou-se uma outra parte de 4-bromo-2-buteno {60 mg, 0,45 mmol) e de trietilamina (49 mg, 0,49 mmol). Depois de outras 24 horas sob refluxo, a mistura de reação foi vazada sobre gelo e dividida entre solução de hidróxido de sódio aquosa 1 M e etil acetato. A camada orgânica foi lavada com salmoura, secada (MgSO4) , e evaporada. Cromatografia (SiO2, CH2Cl2/MeOH/NH4OH 95:5:0,25) proporcionou o com10 posto do título (77 mg, 44%) . Sólido não branco, MS (ISP) 432,4 <M+H)+.
b) tert-Butil éster de ácido (RS,RS, RS)-[3-(acriloilbut-3-enil-amino)-9,10-dimetóxi-l, 3, 4,6,7,llb-hexaidro2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico
Adicionou-se cloreto de acriloil (18 mg,
0,20 mmol) gota a gota a 0°C a uma solução de tertbutil éster de ácido (RS,RS,RS)-(3-but-3-enilamino9,10-dimetóxi-l,3,4,6,7,llb-hexaidro-2H-pirido[2,1a]isoquinolin-2-il)-carbâmico (77 mg, 0,18 mmol) e tri20 etilamina (20 mg, 0,20 mmol) em diclorometano (1,5 ml). Depois 30 minutos a 0°C, a mistura de reação foi dividida entre solução de carbonato de sódio 2 M aquoso e etil acetato. A camada orgânica foi lavada com salmoura , secada (MgSO4) , e evaporada. Cromatografia (SiO2,
CH2Cl2/MeOH/NH4OH 95:5:0,25) proporcionou o composto do título (65 mg, 75%). Sólido branco, MS (ISP) 486,5 (M+H)+.
c) tert-Butil éster de ácido {RS,RS,RS)-[9,10-dimetóxi3-(6-ΟΧΟ-3,6-diidro-2H-piridin-l-il)-1,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico
Adicionaram-se tetraisopropil ortotitanato (7,6 mg, 27 μιηοΐ) e bicloreto de Bis(tricicloexilfosfina)-benzilidenorutênio(IV) (11 mg, 13 gmol) a uma solução de tert-butil éster de ácido (RS,RS,RS)-[3(acriloil-but-3-enil-amino)-9,10-dimetóxi-l,3,4,6,7,11b -hexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico (65 mg, 0,13 mmol) em diclorometano (2,5 ml). A mistura de reação foi submetida a agitação durante 45 minutos sob temperatura ambiente, então dividida entre etil acetato e água. A camada orgânica foi lavada com salmoura, secada (MgSO4) , e evaporada. Cromatografia (Si02, CH2Cl2/MeOH/NH4OH 95:5:0,25) proporcionou o composto do título (59 mg, 96%). Sólido branco, MS (ISP) 458,4 (M+H)+.
d) (RS,RS,RS)-1-(2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-5,6-diidrolH-piridin-2-ona
O composto do título foi produzido de acordo com o método geral do Exemplo le a partir de tert-butil éster de ácido (RS,RS, RS)-[9,10-dimetóxi-3(6-oxo-3,6-diidro-2H-piridin-l-il)-1,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico. Espuma branca, MS (ISP) 358,2 (M+H)+.
Exemplo 13 * * *
*
ΙΟ
1-((RS,RS,RS)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-azepan-2-ona
NH,
a) Etil éster de ácido (RS,RS,RS)-2-benzilamino-9,105 dimetóxi-1,3,4,6,7,llb-hexaidro-2H-pirído[2,1a]isoquinolina-3-carboxílico
Adicionou-se ácido trifluoroacético (20 ml) a 0°C e uma solução de etil éster de ácido 2-amino9,10-dimetóxi-l,6,7,llb-tetraidro-4H-pirido[2,1-a]isso10 quinolina-3-carboxílico (Exemplo la; 2,00 g, 6,02 mmol) em tetraidrofurano (20 ml), então depois de 30 minutos a solução homogênea foi tratada com boroidreto de sódio (474 mg, 12,0 mmol) e submetida a agitação durante outros 40 minutos. A mistura de reação foi concentrada in vacuo e o resíduo dividido entre solução de hidróxido de sódio aquosa 2 M e diclorometano. A camada orgânica foi lavada com salmoura, secada (MgSCh) e evaporada. O resíduo foi dissolvido em metanol (37 ml) e ácido acético (9 ml) e tratado com benzaldeído (723 mg,
6,81 mmol), então adicionou-se cianoboroidreto de sódio (526 mg, 7,95 mmol) por partes sob temperatura ambiente durante 1 hora. A mistura de reação foi submetida a agitação durante outros 15 minutos, então dividida ente solução de hidrogencarbonato de sódio aquosa e dicloro• * · * · · · · η « t · · · · ' < » · « «·· ·«· β ♦·· · (
metano. A camada orgânica foi lavada com salmoura, secada (MgSC>4), e evaporada. Cromatografia do residuo (SiO2, CH2Cl2/EtOAc 4:1, depois solução de subproduto dibenzilado, CH2Cl2/MeOH/NH4OH 95:5:0,25) proporcionou o composto do titulo (1,31 g, 51%). Óleo vermelho, MS (ISP) 425,2 (M+H)+.
b) Etil éster de ácido (RS,RS,RS)-2-(benzil-tertbutoxicarbonil-amino)-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolina-3-carboxilico
Adicionou-se di-tert-butil-dicarbonato (752 mg, 3,38 mmol) sob temperatura ambiente à solução de etil éster de ácido (RS,RS,RS)-2-benzilamino-9,10dimetóxi-l, 3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolina-3-carboxilíco (1,30 g, 3,07 mmol) em diclorometano (13 ml). Depois de 16 horas a solução foi evaporada e o residuo cromatografado (SiO2, gradiente heptano-EtOAc) para produzir o composto do título (1,24 g,
77%). Espuma amarela, MS (ISP) 525,3 (M+H)+.
c) Benzil éster de ácido (RS,RS,RS)-[2-(benzil-tertbutoxicarbonii-amíno)-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il]-carbâmico
Adicionaram-se pílulas de hidróxido de potássio (86%, 1,53 g, 23,4 mmol) a uma solução de etil éster de ácido (RS,RS,RS)-2-(benzil-tert-butoxicarbonil-amino)-9,10-dimetóxi-l,3,4,6,7,llb-hexaidro-2Hpirido[2,1-a]isoquinolína-3-carboxílico (1,20 g, 2,28 mmol) em água/tetraidrofurano 1:1 (24 ml), e a mistura foi aquecida sob refluxo durante 72 horas. Depois de «
»· ··· • ·· «·· • · ··· « · · · · · • ··· ··· · ··· ·
refrigeração, a solução foi neutralizada com amortecedor de fosfato de potássio aquoso 1 M (pH 6,85) e extraída três vezes com diclorometano. As camadas orgânicas foram agrupadas, secadas (MgSO4) , e evaporadas. O resíduo foi colocado em suspensão em tolueno (24 ml) e tratado com trietilamina (230 mg, 2,28 mmol) e difenilfosforil azida (659 mg, 2,28 mmol) . A reação foi mantida sob temperatura ambiente durante 90 minutos e aquecida a 80°C durante 90 minutos, então adicionou-se álcool benzílico (369 mg, 3,41 mmol), e a temperatura de reação foi mantida a 100°C durante 18 horas. A mistura de reação foi diluída com diclorometano e lavada com solução de ácido cítrico aquosa a 10%, solução de hidróxido de sódio aquosa 1 M, e salmoura, secada (MgSO4) , e evaporada. Cromatografia (SÍO2, gradiente heptano/EtOAc) proporcionou o composto do título (805 mg, 59%). Espuma amarelo claro, MS (ISP) 602,3 (M+H)+.
d) tert-Butil éster de ácido (RS,RS,RS)-(3-amino-9,10dimetóxi-l, 3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]issoquinolin-2-il)-benzil-carbâmico
Uma solução de benzil éster de ácido (RS,RS,RS)-[2-(benzil-tert-butoxicarbonil-amino)-9,10dimetóxi-l, 3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-3-il]-carbâmico (802 mg, 1,33 mmol) em ácido acético (24 ml) foi hidrogenada (1 bar, temperatura ambiente, 3 horas) na presença de paládio (10% em carvão vegetal ativado, 40 mg), então o catalisador foi remo59 « · vido por meio de filtragem e o filtrado foi evaporado. Cromatografia (SiO2, CH2Cl2/MeOH/NH4OH 90:10:0,25) proporcionou o composto do título (4 02 mg, 65%) . Espuma de cor amarelo claro, MS (ISP) 468,4 (M+H)+.
e) tert-Butil éster de ácido (RS,RS,RS)-benzil-[3-(6cloro-hexanoilamino)-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico
O composto do título foi produzido de acordo com o método geral do Exemplo 5c a partir de tert-butil éster de ácido (RS,RS,RS)-(3-amino-9,10dimetóxi-l, 3,4,6,7,llb-hexaidro-2H-pirido[2,1a]isoquinolin-2-il)-benzil-carbâmico e cloreto de 6cloroexanoil. Óleo amarelo, MS (ISP) 600,4 (M+H)+.
f) tert-Butil éster de ácido (RS,RS,RS)-benzil-[9,1015 dimetóxi-3-(2-oxo-azepan-l-il)-1,3,4,6,7,llb-hexaidro2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico
O composto do título foi produzido de acordo com o método geral do Exemplo 5d a partir de tert-butil éster de ácido (RS,RS,RS)-benzil-[3-(620 cloro-hexanoilamino)-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico. Sólido não branco, MS (ISP) 564,4 (M+H)+.
g) (RS,RS,RS)-1-(2-Benzilamino-9,10-dimetóxi-l,3,4,6,7, llb-hexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-azepan25 2-ona
O composto do título foi produzido de acordo com o método geral do Exemplo le a partir de • * ·
tert-butil éster de ácido (RS,RS,RS)-benzil-[9,10dimetóxi-3-(2-oxo-azepan-l-il)-1,3,4,6,7,llb-hexaidro2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico. Sólido amarelo claro, MS (ISP) 464,5 (M+H)+ .
h) 1-((RS,RS,RS)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-azepan-2-ona
Uma solução de (RS,RS,RS)-1-(2-benzilamino -9,10-dimetóxi-l,3,4,6,7,llb-hexaidro-2H-pirido[2,1a]isoquinolin-3-il)-azepan-2-ona (35 mg, 75 pmol) foi hidrogenada (3 bar, temperatura ambiente, 3 horas) na presença de paládio (10% em carvão vegetal ativado), então o catalisador foi removido por meio de filtragem e i filtrado evaporado. Cromatografia (SiO2,
CH2Cl2/MeOH/NH4OH 95:5:0,25) proporcionou o composto do título (10 mg, 43%). Sólido amarelo claro, MS (ISP) 374,2 (M+H)+.
Exemplo 14 (RS,RS,RS)-3-(1,1-Dioxo-1,2-tiazolidin-2-il)-9,10dimetóxi-l, 3,4,6,7,llb-hexaidro-2H-pirido[2,1a]isoquinolin-2-ilamina
a) tert-Butil éster de ácido (RS,RS,RS)-[3-(3-cloropropano-l-sulfonilamino)-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico
Β
Ο composto do título foi produzido de acordo com o método geral do Exemplo 5c a partir de tert-butil éster de ácido (RS,RS,RS)-(3-amino-9,10dimetóxi-l, 3,4,6,7,llb-hexaidro-2H-pirido[2,1a) isoquinolin-2-il)-carbâmico (Exemplo 5b) e de cloreto de 3-cloropropanossulfonil. Sólido branco, MS (ISP)
516,3 (M-H)~.
b) tert-Butil éster de ácido (RS,RS,RS)-[3-(1,1dioxoisotiazolidin-2-il)-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]rsoquinolin-2-il]-carbâmico
O composto do título foi produzido de acordo com o método geral do Exemplo 5d a partir de tert-butil éster de ácido (RS,RS,RS)-[3-(3-cloropropano-l-sulfonilamino)-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico.
Sólido não branco, MS (ISP) 482,3 (M+H)+.
c) (RS,RS,RS)-3-(1,1-Dioxo-l,2-tiazolidin-2-il)-9,10dimetóxi-l, 3,4,6,7,llb-hexaidro-2H-pirido [2,1a]isoquinolin-2-ilamina
O composto do título foi produzido de acordo com o método geral do Exemplo le a partir de tert-butil éster de ácido (RS,RS,RS)-[3-(1,1dioxoisotiazolidin-2-il)-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico.
Espuma branca, MS (ISP) 382,3 (M+H)+.
Exemplo 15 (RS,RS,RS)-3-(1,1-Dioxo[1,2]tiazinan-2-il)-9,1062 dimetóxi-1,3,4,6,7,llb-hexaidro-2H-pirido[2,1a]isoquinolin-2-ilamina
butano-l-sulfonilamino)-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico
O composto do título foi produzido de acordo com o método geral do Exemplo 5c a partir de tert-butil éster de ácido (RS,RS,RS)-(3-amino-9,1010 dimetóxi-1,3,4,6,7,1lb-hexaidro-2H-pirido[2, 1a] isoquínolín-2-il)-carbâmico (Exemplo 5b) e de cloreto de 4-clorobutanossulfonil (DE1300933). Sólido branco, MS (ISP) 532, 3 (M+H)+.
b) tert-Butil éster de ácido (RS,RS,RS)-[3-(1,1-dioxo [1,2]tiazinan-2-il)-9,10-dimetóxi-l,3,4,6,7, llb-hexaidro-2H-pirido [2,1-a]isoquinolin-2-il]-carbâmico
O composto do título foi produzido de acordo com o método geral do Exemplo 5d a partir de tert-butil éster de ácido (RS,RS,RS)-[3-(4-cloro20 butano-l-sulfonilamino)-9,10-dimetóxi-l, 3,4, 6, 7, 11bhexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico. Sólido branco, MS (ISP) 496,3 (M+H)+.
c) (RS,RS,RS)-3-(1,1-Dioxo[1,2]tiazinan-2-il)-9,10
dimetóxi-1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-2-ilamina composto do título foi produzido de acordo com o método geral do Exemplo le a partir de tert-butil éster de ácido (RS, RS, RS) - [3-(1,1dioxo[1,2]tiazinan-2-il)-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico. Sólido branco, MS (ISP) 396,3 (M+H)+.
Exemplo 16 (S,S,S)-3-(l,1-Dioxo-[1,2]tiazinan-2-il)-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-2ilamina
a) Etil éster de ácido (S)-(6,7-dimetóxi-l,2,3, 4tetraidro-isoquinolin-l-il)-acético
O composto do título foi produzido em >99,5% e.e. a partir de etil éster de ácido (6,7dimetóxi-1,2,3,4-tetraidro-isoquinoün-l-il)-acético (Synthesis 1987, 474) por meio de cristalização fracionária com ácido (-)-2'-nitrotartranílico, de acordo com o procedimento geral de Montzka et al. (US3452086). Sólido amarelo claro, MS (ISP) 280,2 (M+H)+, tR = 6,4 min (Chíralcel® ODH 15x0.21 cm, heptano/2-propanol/trietil64 amina 75:25:0,15, velocidade de fluxo 150 pL/min).
b) tert-Butil éster de ácido (S,S,S)-(3-amino-9,10dimetóxi-l, 3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-2-il)-carbâmico
O composto do título foi produzido a partir de etil éster de ácido (S)-(6,7-dimetóxi-l,2,3,4tetraidro-isoquinolin-l-il)-acético, de acordo com a síntese do racemato, tert-butil éster de ácido (RS,RS,RS)-(3-amino-9,10-dimetóxi-l,3,4,6,7,11b10 hexaidro-2H-pirido[2,1-a]isoquinolin-2-il)-carbâmico (Exemplo 5b). Sólido não branco, tR - 19,3 minutos (Chiralpak® AD 25x0.03 cm, heptano/etanol/trietilamina 70:30:0,3, velocidade de fluxo 4 pl/min).
c) (S, S, S)-3-(1,1-Dioxo-[1,2]tiazinan-2-il)-9,ΙΟΙ 5 dimetóxi-1,3,4,6,7,llb-hexaidro-2H-pirido[2,1a]isoquinolin-2-ilamina
O composto do título foi produzido de acordo com a síntese do racemato, (RS,RS,RS)-3-(1,1dioxo[1,2]tiazinan-2-il)-9,10-dimetóxi-l,3,4,6,7,11b20 hexaidro-2H-pirido[2,1-a]isoquinolin-2-ilamina (Exemplo 15). Espuma não branca.
Η
Exemplos 17 e 18 (SR) -1- ( (RS, RS, RS) -2-Amino--9,10-dimetóxi-l, 3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metilpirrolidin-2-ona
e (RS,RS,RS,RS)-1-(2-amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metilpirrolidin-2-ona
Os compostos dos títulos foram produzidos a partir de 1-((RS,RS,RS)-2-amíno-9,10-dimetóxi~ 1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-4-metil-pirrolidin-2-ona (Exemplo 10) por meio de separação cromatográfica (SiO2, CH2Cl2/MeOH/NH4OH 90:10:0,25).
(SR)-1-((RS,RS,RS)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metilpirrolidin-2-ona: Espuma de cor amarelo claro, Rf 20 0,20.
• · » · ··· · ··· ··· ·· ·♦ · ·· · ····· · * · * ······ ·· · · • » ·· »· · · · * ···«···· ·«· · (RS,RS,RS,RS)-1-(2-amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metilpirrolidin-2-ona: Sólido amarelo claro, Rf - 0,15.
Exemplos 19 e 20 (R)-1-((S,S,S)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metilpirrolidin-2-ona
(S)-1-((R,R,R)-2-amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metilpirrolidin-2-ona
Chiral
Os compostos dos títulos foram produzidos 15 de acordo com o método geral dos Exemplos 6 e 7 a partir de (SR)-1-((RS,RS,RS)-2-amino-9, 10-dimetóxi-l, 3, 4,
6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4metil-pirrolidin-2-ona (Exemplo 17).
(R)-1-((S,S,S)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11b20 hexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metil67
pirrolidin-2-ona: Espuma não branca, tR = 40,1 minutos (Chiralpak® AD 25x0,46 cm, heptano/etanol 80:20, velocidade de fluxo 1 ml/min).
(S)-1-((R,R,R)-2-amino-9,10-dimetóxi-l,3,4,6,7,11b5 hexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metilpirrolidin-2-ona: Espuma não branca, tR = 66,0 min (Chiralpak® AD 25x0,46 cm, heptano/etanol 80:20, velocidade de fluxo 1 ml/min).
Exemplos 21 e 22 (S,S,S,S)-1-(2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metilpirrolidin-2-ona
e (R,R,R,R)-1-(2-amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metilpirrolidin-2-ona
de acordo com o método geral dos Exemplos 6 e 7 a partir de (RS,RS,RS,RS)-1-(2-amino-9,10-dimetóxi-l,3,4,6,
7, llb-hexaidro-2H-pirido [2,1-a] isoquinolin-3-il) -4metil-pirrolidin~2-ona (Exemplo 18).
(S,S,S,S)-1-(2-Amino-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-4-metil-pirrolidin-2-ona: Espuma não branca, tR 29,4 minutos (Chiralpak® AD 25x0,46 cm, heptano/etanol 80:20, velocidade de fluxo 1 ml/min).
(R,R,R,R)-1-(2-Amino-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-4-metil-pirrolidin-2-ona: Espuma não branca, tR = 41,8 min (Chiralpak® AD 25x0,46 cm, heptano/etanol 80:20, velocidade de fluxo 1 ml/min).
Exemplo 23
1-((RS,RS,RS)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4fluorometil-pirrolidin-2-ona
O
a) 4-Fluorometil-diidro-furan-2-ona
Uma solução de 4-hidroximetil-diidrofuran-2-ona (Tetrahedron 1994, 50, 6839; 1,02 g, 8,78 mmol) e trifluoreto de bis(2-metoxietíl)amino-enxofre (3,88 g, 17,6 mmol) em clorofórmio (4,4 ml) foi submetida a agitação a 40°C durante 1 hora, então vazada em • · · · • · · · · • · · · · · • · * · · · • · · · • * · gelo e dividida entre solução de hidrogencarbonato de sódio aquosa saturada e diclorometano. Ά camada orgânica foi lavada com salmoura, secada (MgSO4) , e evaporada. Cromatografia (S1O2, gradiente de heptano-etil acetato) proporcionou o composto do título (576 mg, 56%). Liquido incolor, MS (EI) 118,9 (M+H)+.
b) Cloreto de 3-clorometil-4-fluoro-butiril
Uma mistura de 4-fluorometil-diidro-furan2-ona (871 mg, 7,37 mmol), cloreto de tionil (4,39 g, 36,9 mmol), e cloreto de zinco (60 mg, 0,44 mmol) foi submetida a agitação durante 72 horas a 80°C, então o excesso de cloreto de tionil foi removido por meio de destilação. Destilação de Kugelrohr do residuo (85°C, 0,2 mbar) proporcionou o composto do título (450 mg, 35%). Líquido incolor, 1H-NMR (300 MHz, CDC13) : 4,654,55 (m, 1 H), 4,50-4,40 (m, 1 H), 3,70-3, 60 (m, 2 H) , 3,25-3,05 (m, 2 H), 2,80-2,60 (m, 1 H).
c) tert-Butil éster de ácido (RS,RS,RS)-[3-(3-clorometil-4-fluoro-butirilamino)-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico
O composto do título foi produzido de acordo com o método geral do Exemplo 5c a partir de tert-butil éster de ácido (RS,RS,RS)-(3-amino-9,10dimetóxi-l, 3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-2-il)-carbâmico (Exemplo 5b) e de cloreto de 3clorometi1-4-fluoro-butiril. Sólido branco, MS (ISP) 514,5 (M+H)+.
d) tert-Butil éster de ácido (RS,RS,RS)-[3 - (4- 70 « * · * · · · • · · ·» • * · fluorometil-2-oxo-pirrolidin-l-il)-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-2il]-carbâmico composto do título foi produzido de a5 cordo com o método geral do Exemplo 5d a partir de tert-butil éster de ácido (RS,RS,RS)-[3-(3-clorometil4-fluoro-butirilamino)-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico. Espuma não branca, MS (ISP) 478,5 (M+H)+.
e) l-((RS,RS,RS)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-fluorometii-pírrolidin-2-ona
O composto do título foi produzido de acordo com o método geral do Exemplo le a partir de (RS,RS,RS)-[3-(4-fluorometi1-2-oxo-pirrolidin-l-il)9,10-dimetóxi-l,3,4,6,7,llb-hexaidro-2H-pirido[2,1a]isoquinolin-2-il]-carbâmico. Óleo amarelo claro, MS (ISP) 378,5 (M+H)+.
Exemplo 24
1-((RS,RS,RS)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-5-metilpiperidin-2-ona
N
O
a) Cloreto de 5-cloro-4-metil-pentanoil
| 0 composto | do | título foi produzido | de | a- | ||
| cordo | com o método geral | do | Exemplo 23b a | partir | de | 5- |
| metil- | -tetraidro-piran-2-ona | (Tetrahedron | 1995, | 51, | ||
| 6237) . | Líquido incolor, | 1H- | -NMR (300 MHz, | CDC13) : | 3, | 50- |
3,40 (m, 2 H), 2,95 (td, 2 H) , 2,00-1, 85 (m, 2 H) ,
1,70-1,60 (m, 1 H) , 1,04 (d, 3 H) .
b) tert-Butil éster de ácido (RS,RS,RS)-[3-(5-cloro-4metil-pentanoilamino)-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico
O composto do título foi produzido de acordo com o método geral do Exemplo 5c a partir de tert-butil éster de ácido (RS,RS,RS)-(3-amino-9,10dimetóxi-l, 3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-2-il)-carbâmico (Exemplo 5b) e de cloreto de 5cloro-4-metil-pentanoil. Sólido não branco, MS (ISP) 510,6 (M+H)+.
c) tert-Butil éster de ácido (RS,RS,RS)-[9,10-dimetóxi3-(5-metil-2-oxo-piperidin-l-il)-1,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico
O composto do título foi produzido de acordo com o método geral do Exemplo 5d a partir de tert-butil éster de ácido (RS,RS,RS)-[3-(5-cloro-4metil-pentanoylamino)-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico. Óleo amarelo claro, MS (ISP) 474,5 (M+H)+.
d) 1-((RS,RS,RS)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-ί1)-5-metíl- 72 • · · · ··· • · ·* ·· · ♦ · * · * · • * · · · · · • * · · » • · ··· ··· · piperidin-2-ona composto do título foi produzido de acordo com o método geral do Exemplo le a partir tertbutil éster de ácido (RS,RS,RS)-[9,10-dimetóxi-3-(55 metii-2-oxo-piperidin-l-il)-1,3,4,6,7,llb-hexaidro-2Hpirido[2,1-a]isoquinolin-2-il]-carbâmico. Sólido amarelo claro, MS (ISP) 374,5 (M+H)+.
Exemplo 25 (RS,RS, RS)-N-(2-Amino-9,10-dimetóxi-l,3,4,6,7,11b10 hexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-propionamida
a) tert-Butil éster de ácido (RS,RS,RS)-(9,10-dimetóxi3-propionilamino-l,3,4,6,7,llb-hexaidro-2H-pirido[2,1a] isoquinolin-2-il)-carbâmico
O composto do título foi produzido de acordo com o método geral do Exemplo 5c a partir de tert-butil éster de ácido (RS,RS,RS)-(3-amino-9,10dimetóxi-l, 3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-2-il)-carbâmico (Exemplo 5b) e cloreto de propio20 nil. Sólido amarelo claro, MS (ISP) 434,6 (M+H)+.
b) (RS,RS,RS)-N-(2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-propionamida composto do título foi produzido de acordo com o método geral do Exemplo le a partir de • »
• · « · · • * · · tert-butil éster de ácido (RS,RS,RS)-(9,10-dimetóxi-3propionylamino-1,3,4,6,7,llb-hexaidro-2H-pirido[2,1a] isoquinolin-2-il)-carbâmico·. Sólido não branco, MS (ISP) 334,5 (M+H)+.
Exemplo 26 (RS,RS,RS)-N-(2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-butiramlda
O composto do título foi produzido de a10 cordo com os métodos gerais dos Exemplos 5c e le a partir de tert-butil éster de ácido (RS,RS,RS)-(3-amino9,10-dimetóxi-l,3,4,6,7,llb-hexaidro~2H-pirido[2,1a]isoquinolin-2-il)-carbâmico (Exemplo 5b) e de cloreto de butiril. Sólido amarelo, MS (ISP) 348,5 (M+H)+.
Exemplo 27 ((RS,RS,RS)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-amida de ácido ciclopropanocarboxílico
»· * * · * * *«* · ♦·· «»<.«*« 1« «♦ * ·· ‘ ·Ί »«♦··· · * · * — 74 — · · * · *·· * · · ? „ ί ' » ,»,«··♦ · *> · • » » * ♦*» »«· · ♦*· *
Ο composto do título foi produzido de acordo com os métodos gerais dos Exemplos 5c e le a partir de tert-butil éster de ácido (RS,RS,RS)-(3-amino9,10-dimetóxi-l,3,4,6,7,llb-hexaidro-2H-pirido[2,15 a]isoquinoiin-2-il)-carbâmico (Exemplo 5b) e de cloreto de ciclopropanocarbonil. Sólido não branco, MS (ISP)
346,3 (M+H)+.
Exemplos 28 e 29 (SR) -1- ( (RS,RS>RS)-2-Amino-9,10-dimetóxi-l, 3, 4,6, 7,11b10 hexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4fluorometil-pirrolidin-2-ona
e (RS,RS,RS,RS)-1-(2-Amino-9,10-dimetóxi-l,3,4,6,7,11b15 hexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-
Os compostos dos títulos foram produzidos a partir de 1-((RS,RS,RS)-2-amino-9,10-dimetóxi20 1,3,4,6,7,llb-hexaidro-2H-pirido[2, 1-a]isoquinolin-3il)-4-fluorometil-pirrolidin-2-ona (Exemplo 23) por se- 75 -
| • 4 | « * | ·> | ♦ | « | • · · | ||
| • · | * * · | • | * · | t 9 | • | * · | |
| • * | • « * | • | • | « | « | • | |
| V « « | »· | • | • | • | • | ||
| • · · | ♦ | • | • | • | |||
| • · | • | *·· | * |
paração cromatográfica (SiO2, CH2Cl2/MeOH/NH4OH
80:1:0,2, então 95:5:0,25).
(SR)-1-((RS,RS,RS)-2-Amino-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-4-fluorometil-pirrolidin-2-ona: Óleo amarelo, Rf = 0,45 (CH2Cl2/MeOH/NH4OH 90:10:0,25).
(RS,RS,RS,RS)-1-(2-Amino—9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-4-fluorometil-pirrolidin-2-ona: Sólido amarelo claro, Rf = 0,40 (CH2Cl2/MeOH/NH4OH 90:10:0,25).
Exemplo 30
Dicloridrato de (S)-1-((S,S,S)-2-amíno-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-3-
a) tert-Butil éster de ácido [ (S,S,S)-3-(3-clorometil4-fluoro-butirilamino)-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico
O composto do título foi produzido de acordo com o método geral do Exemplo- 5c a partir de tert-butil éster de ácido (S,S,S)- (3-amino-9,10dimetóxi-l, 3,4,6,7,llb-hexaidro-2H-pirido[2,1a]isoquinolin-2-ί1)-carbâmico (Exemplo 16b) e de cloreto de 3-clorometil-4-fluoro-butiril (Exemplo 23b). Só-
• Γ · • · · · i, · *«· • ··· ··· · ···
lido não branco.
b) tert-Butil éster de ácido [(S,S,S)-3-((S)-4-fluorometil-2-oxo-pirrolidin-l-il)-9,10-dimetóxi-l,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolín-2-il]-carbâmi5 co e tert-butil éster de ácido [(S,S,S)-3-((R)-4fluorometil-2-oxo-pirrolidin-l-il)-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-2il]-carbâmico
Adicionou-se hidreto de sódio (dispersão em óleo 55-65%, 1,14 g, 28,5 mmol.) a uma suspensão de tert-butil éster de ácido [ (S,S,S)-3-(3-clorometil-4fluoro-butirilamino)-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico (6,72 g, 13,1 mmol) em N,N-dimetílformamida (95 ml) sob temperatura ambiente, então depois de 1 hora a mistura de reação foi vazada sobre gelo e dividida entre etil acetato e água. A camada orgânica foi lavada com salmoura, secada (MgSO4) , e evaporada. Cromatografia (SiO2, cícloexano/2-propanol 4:1) proporcionou tert-butil éster de ácido [(S,S,S)-3-((S)-4-fluorometil-2-oxopirrolidin-l-il)-9,10-dimetóxi-l,3,4,6,7,llb-hexaidro2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico (2,40 g, 38%) e o epimero, tert-butil éster de ácido [(S,S,S)-3((R)-4-fluorometil-2-oxo-pirrolidin-l-il)-9,10-dimetóxi
-1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-2il]-carbâmico (2,73 g, 44%).
tert-Butil éster de ácido [ (S, S, S)-3-( (S) 4-fluorometil-2-oxo-pirroiidin-l-il)-9,10-dimetóxi77 • · • * • *
1,3,4,6,7,1lb-hexaidro-2H-pirido[2,1-a]isoquinolin-2il]-carbâmico: Espuma de cor amarelo claro, Rf = 0,6 (SiO2, cicloexano/2-propanol 1:1).
fcerfc-Butil éster de ácido [(S,S,S)-3-((R)4-fluorometil-2-oxo-pirrolidin-l-il)-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-2il]-carbâmico: Espuma de cor amarelo claro, Rf - 0.4 (SiO2, cicloexano/2-propanol 1:1).
c) Dicloridrato de (S)-1-((S, S, S)-2-amino-9,10-dimetóxi-1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin3-il)-4-fluorometil-pirrolidin-2-ona terfc-Butil éster de ácido [(S,S,S)-3-( (S)4-fluorometil-2-oxo-pirrolidin-l-il)-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-2il]-carbâmico (2,40 g, 5,02 mmol) foi convertido para (S)—1—((S,S,S)-2-amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-fluorometil-pirrolidin-2-ona de acordo com o método geral do Exemplo le. O produto foi dissolvido em 2-propanol (10 ml) e tratado com cloreto de hidrogênio (5-6 M em 2propanol, 37 ml). A suspensão formada foi submetida a agitação durante 64 horas sob temperatura ambiente, então o precipitado foi coletado por filtragem e secado, para proporcionar o composto do título (2,04 g, 91%). Sólido branco, p.f. > 300 °C.
Exemplo 31
Diidrocloreto de (R)-1- ( (S,S,S)-2-amino-9,10-dimetóxi- 78
1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-4-fluorometil-pirrolidin-2-ona
O composto do titulo foi produzido de a5 cordo com o método geral do Exemplo 30c a partir tertbutil éster de ácido [{S,S,S)-3-{(R)-4-fluorometil-2oxo-pirrolidin-l-il)-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico {Exemplo 30b). Sólido branco, p.f. > 300 °C.
Exemplo 32
3-((RS,RS,RS)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-oxazolidin2-ona
15. O composto do titulo foi produzido de acordo com os métodos gerais dos Exemplos 5c, 5d e le a partir de tert-butil éster de ácido (RS,RS,RS)-(3amino-9,10-dimetóxi-l,3,4,6,7,llb-hexaidro-2H-pirido [2,1-a]isoquinolin-2-il)-carbâmico (Exemplo 5b) e 2-
cloroétil cloroformao. Sólido amarelo claro, MS- (ISP) 348,5 (M+H)+.
Exemplo 33
3-((RS,RS,PS)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)[1,3]oxazinan-2-ona
a) 3-Cloro-propil éster de ácido ((RS,RS,RS)-2-tertbutoxicarbonilainino-9,10-dimetóxi-l, 3,4,6,7,11b10 hexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-carbâmico
O composto do título foi produzido de acordo com o método geral do Exemplo 5c a partir de tert-butil éster de ácido (RS,RS,RS)-(3-amino-9,10dimetóxi-l, 3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoqui15 nolin-2-il)-carbâmico (Exemplo 5b) e de 3-cloropropil cloroformato. Sólido não branco, MS (ISP) 498,4 (M+H)+.
b) tert-Butil éster de ácido [(RS, RS, RS)-9,10-dimetóxi3-(2-oxo-[1,3]oxazinan-3-il)-1,3,4,6,7,llb-hexaidro-2H20 pirido[2,1-a]isoquinolin-2-il]-carbâmico
O composto do título foi produzido de acordo com o método geral do Exemplo 5d a partir de 3cloro-propil éster de ácido ((RS,RS,RS)-2-tertbutoxicarbonilamino-9,10-dimetóxi-l,3,4,6,7,11b80
hexaidro-2B-pirido[2,1-a]isoquinolin-3-il)-carbâmico. Sólido não branco, MS (ISP) 462,4 (M+H)+.
c) 3-((RS,RS,RS)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-[1,3]oxazinan-2-ona
O composto do título foi produzido de a~ cordo com o método geral do Exemplo le a partir de tert-butil éster de ácido [(RS,RS, RS)-9,10-dimetóxi-3(2-oxo- [1,3] oxazinan-3-il) -1,3,4,6,7, llb-hexaidro-2Hpirido[2,1-a]isoquinolin-2-il]-carbâmico. Sólido amarelo, MS (ISP) 362,5 (M+H)+.
Exemplo 34
1-((RS,RS,RS)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido [2,1-a] isoq.uinolin-3-il) -5-metil-
a) Cloreto de 4-cloro-pentanoil composto do título foi produzido de acordo com o método geral do Exemplo 23b a partir de γvalerolactona. Líquido incolor, 1H-NMR (300 MHz, CDCl3): 4,10-4,00 (m, 1 H), 3,25-3,05 (m, 2 H), 2,25-2,15 (m, 1 H), 2,05-1,95 (m, 1 H), 1,55 (d, 3 H).
b) tert-Butil éster de ácido [(RS,RS,RS)-3-(4-cloro81 • ·
pentanoilamino) - 9,10-dimetóxi-l, 3,4,6,-7, llb-hexaidro2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico composto do título foi produzido de acordo com o método geral do Exemplo 5c a partir de tert-butil éster de ácido (RS,.RS,RS) - (3-amino-9, 10dimetóxi-l, 3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-2-il)-carbâmico (Exemplo 5b) e de cloreto de 4cloro-pentanoil. Sólido não branco, MS (ISP) 496,4 (M+H)+.
c) l-( (RS,RS,RS)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-5-metilpirrolidin-2-ona
O composto do título foi produzido de acordo com- os métodos gerais dos Exemplos 5d e le a partir de tert-butil éster de ácido [(RS,RS,RS)-3-(4cioro-pentanoilamino)-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico. Sólido amarelo, MS (ISP) 360,1 (M+H)+.
Exemplo 35
3-((RS,RS,RS)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-5fluorometil-oxazolidin-2-ona
'0'
a) tert-Butil éster de ácido [(RS,RS,RS)-3-(2-cloro-lfluorometil-etoxicarbonilamino)-9,10-dimetóxi-l,3,4,6, 7,llb-hexaidro~2H-pirido[2,1-a]isoquinolin-2-il]carbâmico
Piridina (69 mg, 0,87 mmol) foi adicionada gota a gota a 0°C a uma solução de l-cloro-3fluoroisopropanol (34 mg, 0,29 mmol) em diclorometano (0,8 ml), então a solução foi deixada alcançar a temperatura ambiente durante 2 horas. Depois de refrigeração novamente para 0°C, adicionaram-se tert-butil éster de ácido (RS,RS,RS)-(3-amino-9,10-dímetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-2il)-carbâmico (Exemplo 5b, 100 mg, 0,26 mmol), piridina (23 mg, 0,29 mmol) , e 4-dimetilaminopiridina (1 mg, 8 pmol). Deixou-se que a mistura de reação alcançasse a temperatura ambiente durante 16 horas, então foi dividida entre solução de cloreto de amônio aquosa saturada e éter. A camada orgânica foi lavada com água, secada (MgSO4) , e evaporada. Cromatografia (SiO2, gradiente de heptano-etil acetato) produziu o composto do título (65 mg, 48%). Sólido branco, MS (ISP) 516,5 (M+H)+.
b) tert-Butil éster de ácido [(RS, RS,RS)-3-(5fluorometil-2-oxo-oxazolidin-3-il)-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirído[2,1-a]isoquinolin-2il]-carbâmico
O composto do título foi produzido de acordo com o método geral do Exemplo 5d a partir de • · · tert-butil éster de ácido- [ (RS, RS, RS) -3- (2-cloro-1fluorometil-etoxicarbonilamino)-9,10-dimetóxi-l,3,4,6,
7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico. Sólido branco, MS (ISP) 480,5 (M+H)+.
c) 3-((RS,RS,RS)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-5fluorometil-oxazolidin-2-ona
O composto do título foi produzido de acordo com o método gerai do Exemplo le a partir de tert-butil éster de ácido [(RS,RS, RS)-3-(5-fluorometil2-oxo-oxazolidin-3-il)-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico. Sólido amarelo, MS (ISP) 380,4 (M+H)+.
Exemplo 36
1-((RS,RS,RS)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-3-metilpirrolidin-2-ona
a) Cloreto de 4-cloro-2-metil-butyril
O composto do título foi produzido de acordo com o método geral do Exemplo 23b a partir de yvalerolactona. Líquido incolor, 1H-NMR (300 MHz, CDCl3): 3,61 (t, 2 H), 3,25-3,15 (m, 1 H), 2,40-2,25 (m, • ·
Η), 2,00-1,85 (m, 1 Η), 1,36 (d, 3 Η).
b) tert-Butil éster de ácido [(RS,RS,RS)-3-(4-cloro-2metil-butirilamino)· -9,10-dimetóxi-l, 3, 4,6,7, llb-hexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico
O composto do título foi produzido de acordo com o método geral do Exemplo 5c a partir de tert-butil éster de ácido (RS,RS,RS)-(3-amino-9,10dimetóxi-l, 3,4,6,7,llb-hexaidro-2H-pirido[2,1a]isoquinolin-2-il)-carbâmico (Exemplo 5b) e de cloreto de 4-cloro-2-metil-butiril. Sólido não branco, MS (ISP) 496,4 (M+H)+.
c) 1- ( (RS,RS,RS)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-3-metil-pirrolidin-2-ona
O composto do título foi produzido de acordo com o método geral do Exemplo 5d e le a partir de tert-butil éster de ácido [(RS,RS,RS)-3-(4-cloro-2metil-butirilamino)-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico.
Sólido amarelo, MS (ISP) 360,5 (M+H)+.
Exemplo 37
3-((RS,RS,RS)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-5-metiloxazolidin-2-ona • · ·
a) 2-Cloro-l-metil-etil éster de ácido ((RS,RS,RS)-2tert-butoxicarbonilamíno-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-carbâmico
0 composto do título foi produzido de acordo com o método geral do Exemplo 35a a partir tertbutil éster de ácido (RS,RS,RS)-(3-amino-9,10-dimetóxi1,3,4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-2il)-carbâmico (Exemplo 5b) e de l-cloro-propan-2-ol (J.
Chem. Soc. Perkin- Trans. 1 1983, 3019) . Sólido não branco, MS (ISP) 498,4 (M+H)+.
b) tert-Butil éster de ácido [(RS, RS, RS)-9,10-dimetóxi3-(5-metil-2-oxo-oxazolidin-3-il)-1,3, 4,6,7,llb-hexaidro-2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico
O composto do título foi produzido de acordo com o método geral do Exemplo 5d a partir de 2cloro-l-metil-etil éster de ácido ((RS,RS,RS)-2-tertbutoxicarbonilamino-9,10-dimetóxi-l, 3,4,6,7,llb-hexa-idro-2H-pirido[2,1-a]isoquinolin-3-il)-carbâmico. Sóli20 do branco, MS (ISP) 462,4 (M+H)+.
c) 3-((RS,RS,RS)-2-Amino-9,10-dimetóxi-l,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-5-metiloxazolidin-2-ona • · composto do título foi produzido de acordo com o método geral do Exemplo le a partir.de tert-butil éster de ácido [(RS,RS,RS)-9,10-dimetóxi-3(5-metíl-2-oxo-oxazolidin-3-il)-1,3,4,6,7,llb-hexaidro5 2H-pirido[2,1-a]isoquinolin-2-il]-carbâmico. Sólido amarelo claro, MS (ISP) 362,4 (M+H)+.
Exemplos Galênicos
Exemplo A
Comprimidos revestidos de película conten10 do os ingredientes expostos em seguida podem ser manufaturados de uma maneira convencional:
Ingredientes Por
Comprimido
Núcleo:
| Composto da formula (I) | 10,0 mg | 200,0 mg |
| Celulose microcristalina | 23,5 mg | 43,5 mg |
| Lactose hídrica | 60,0 mg | 70,0 mg |
| Povidone K30 | 12,5 mg | 15,0 mg |
| Glicolato de amido de sódio | 12,5 mg | 17,0 mg |
| Estearato de magnésio | 1,5 mg | 4,5 mg |
| (Peso do Núcleo) | 120,0 mg | 350,0 mg |
| Revestimento de pelicula: | ||
| Hidroxipropil metil celulose | 3,5 mg | 7,0 mg |
| Polietileno glicol 6000 | 0,8 mg | 1,6 mg |
| Talco | 1,3 mg | 2,6 mg |
| Óxido de ferro (amarelo) | 0,8 mg | 1,6 mg |
| Bióxido de titânio | 0,8 mg | 1,6 mg |
ingrediente ativo é peneirado e misturado com celulose microcristalina e a mistura é granulada com uma solução de polivinilpirrolidona em água. 0 granulado é misturado com glicolato de amido de sódio e estearato de magnésio e comprimido para se proporcionarem núcleos de 120 ou de 350 mg, respectivamente. Os núcleos são laqueados com uma solução / suspensão do revestimento de película mencionado anteriormente.
Exemplo B • · *
Cápsulas que contém os ingredientes expostos em seguida podem ser manufaturadas de uma maneira convencional:
Ingredientes Por cápsula
| Composto da fórmula (I) | 25,0 mg |
| Lactose | 150,0 mg |
| Amido de milho | 20,0 mg |
| Talco | 5,0 mg |
Os componentes são peneirados e misturados e preenchi5 dos em cápsulas de tamanho 2.
Exemplo C
Soluções para injeção podem ter a composição exposta em seguida:
Composto da fórmula (1)
Gelatina
Ácido Acético
Água para soluções de injeção
3,0 mg 150,0 mg para um pH final de 5,0 aj. 1,0 ml
O ingrediente ativo é dissolvido em uma mistura de polietileno glicol 400 e água para injeção (parte). O pH é ajustado para 5,0 por ácido acético. 0 volume é ajustado para 1,0 ml pela adição da quantidade residual de água. A solução é filtrada, vazada em frascos utilizando-se um excedente apropriado e esterilizada .
Exemplo D
Cápsulas de gelatina macia que contêm os « « ·
| ♦ · | . · ; | • c ·· | • * · » • · · |
| * · - 89 - : • | « * »·· · · « * · · · • *····· | • · · • * » · * · ·»· · | |
| ingredientes seguintes podem ser manufaturadas | de uma | ||
| maneira convencional: | |||
| Conteúdo da cápsula | |||
| Composto da fórmula (I) | 5,0 | mg | |
| Cera amarela | 8,0 | mg | |
| Óleo de soja hidrogenado | 8,0 | mg | |
| Óleos vegetais parciais hidrogenados | 34,0 | mg | |
| Óleo de soja | 110,0 | mg | |
| Peso do conteúdo da cápsula | 165,0 | mg | |
| Cápsula de gelatina | |||
| Gelatina | 75,0 | mg | |
| Glycerol 85 % | 32,0 | mg |
Karion 83 8,0 mg (mat seco)
| Bióxido de titânio | 0,4 mg |
| Óxido de ferro amarelo | 1,1 mg |
O ingrediente ativo é dissolvido em um 5 fundido morno dos outros ingredientes e a mistura é vazada em cápsulas de gelatina macia de dimensão apropriada. As cápsulas de gelatina macia enchidas são tratadas de acordo com os procedimentos usuais.
• « ·
Exemplo E
Sachês contendo os seguintes ingredientes podem ser manufaturados de uma maneira convencional:
| • | Composto da fórmula (I) | 50,0 | mg |
| Lactose, pó fino | 1015,0 | mg | |
| Celulose microcrist. (AVICEL PH 102) | 1400,0 | mg | |
| Carboximetil celulose de sódio | 14,0 | mg | |
| Polivinilpirrolidona K 30 | 10,0 | mg | |
| Estearato de magnésio | 10, 0 | mg |
Aditivos aromatizantes 1,0 mg
O ingrediente ativo é misturado com lacto5 se, celulose microcristalina e carboximetil celulose de sódio e então granulado com uma mistura de polivinilpirrolidona em água. 0 granulado é misturado com estearato de magnésio e os aditivos aromatizantes e vazado em sachês.
Claims (16)
- REIVINDICAÇÕES1 - Compostos caracterizados por compreenderem a fórmula (I)R'R5 em queR1 é -C(O)-N(R5)R6 ou -N(R5)R6;R2, R3 e R4 são, cada um deles, independentemente hidrogênio, halogênio, hidroxila, alquila inferior, alcoxila inferior ou alquenila inferior, em que al10 quila inferior, alcoxila inferior e alquenila inferior podem opcionalmente ser substituídos por alcoxicarbonila inferior, arila ou heterociclila;R é hidrogênio, alquila inferior, alquila inferior halogenada ou cicloalquila;15 R6 é alquilsulfonila inferior, alquilsulfonila inferior halogenada, cicloalquilsulfonila, alquilcarbonila inferior, alquilcarbonila inferior halogenada, cicloalquilcarbonila; ouR5 e R6, em conjunto com o átomo de nitrogênio20 ao qual eles estão fixados, formam um anel heterocíclico saturado ou insaturado de 4, 5, 6 ou 7 elementos contendo opcionalmente um outro heteroátomo selecionado a partir de nitrogênio, oxigênio e enxofre, sendo o diPetição 870180029814, de 13/04/2018, pág. 6/19 to anel heterocíclico opcionalmente mono-, di- ou trisubstituído, independentemente, com alquila inferior, alquila inferior halogenada, oxo, dioxo e/ou ciano; e os seus sais farmaceuticamente aceitáveis;5 em que o termo inferior significa um grupo que consiste em um a seis átomos de carbono e em que o termo heterocíclico se refere a um resíduo N-heterocíclico saturado ou aromático com 5 ou 6 elementos, que pode opcionalmente conter um átomo de10 nitrogênio ou oxigênio adicional.
- 2 - Compostos, de acordo com a reivindicação 1, caracterizados pelo fato de que R1 é —C(O)N(R5)R6.
- 3 — Compostos, de acordo com a reivindica15 ção 1, caracterizados pelo fato de que R1 é -N(R5)R6.
- 4 — Compostos, de acordo com qualquer uma das reivindicações 1 a 3, caracterizados pelo fato de que R2, R3 e R4 são cada um deles independentemente hidrogênio, hidroxila ou alcoxila inferior.20 5 — Compostos, de acordo com qualquer uma das reivindicações 1 a 4, caracterizados pelo fato de 2 que R2 é alcoxila inferior.6 — Compostos, de acordo com qualquer uma das reivindicações 1 a 5, caracterizados pelo fato de 325 que R3 é alcoxila inferior.7 — Compostos, de acordo com qualquer uma das reivindicações 1 a 6, caracterizados pelo fato de que R4 é hidrogênio.Petição 870180029814, de 13/04/2018, pág. 7/198 - Compostos, de acordo com qualquer uma das reivindicações 1 a 7, caracterizados pelo fato de que R é hidrogênio, alquila inferior ou alquila inferior halogenada.
- 5 9 - Compostos, de acordo com qualquer uma das reivindicações 1 a 8, caracterizados pelo fato de que R6 é alquilsulfonila inferior, alquilcarbonila inferior ou cicloalquilcarbonila.
- 10 - Compostos, de acordo com qualquer uma10 das reivindicações 1 a 9, caracterizados pelo fato de que R5 e R6 em conjunto com o átomo de nitrogênio ao qual eles estão fixados formam um anel heterocíclico saturado ou insaturado de 4, 5, 6 ou 7 elementos, contendo opcionalmente um átomo de enxofre ou um átomo de15 oxigênio como um heteroátomo adicional no anel, sendo o dito anel heterocíclico opcionalmente mono- ou disubstituído, independentemente, com alquila inferior tal como metila ou etila, alquila inferior halogenada tal como fluorometila, oxo, dioxo e/ou ciano.20
- 11 - Compostos, de acordo com a reivindi56 cação 10, caracterizados pelo fato de que R5 e R6 em conjunto com o átomo de nitrogênio ao qual eles estão fixados são pirrolidina, pirrolidin-2-ona, 4-metilpirrolidin-2-ona, 4-etil-pirrolidin-2-ona, 3-metil25 pirrolidin-2-ona, 5-metil-pirrolidin-2-ona, 4-fluorometil-pirrolidin-2-ona, pirrolidina-2-carbonitrila, piperidina, piperidin-2-ona, 4-metil-piperidin-2-ona, 5metil-piperidin-2-ona, 5,6-didro-1H-piridin-2-ona, tiPetição 870180029814, de 13/04/2018, pág. 8/19 azolidin-3-il, 1,1-dioxo-1,2-tiazolidin-2-il, 1,1-dioxo [1,2]tiazinan-2-il, azetidina, azepan-2-ona, oxazolidin-2-ona, 5-metil-oxazolidin-2-ona, 5-fluorometiloxazolidin-2-ona ou [1,3]oxazinan-2-ona.5
- 12 - Compostos, de acordo com qualquer uma das reivindicações 1 a 11, caracterizados pelo fato de serem selecionados a partir do grupo que consiste em:(RS,RS,RS)-(2-amino-9,10-dimetóxi-1,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-pirrolidin10 1-il-metanona, (RS,RS,RS)-(2-amino-9,10-dimetóxi-1,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-tiazolidin3-il-metanona, (RS,RS,RS)-(2-amino-9,10-dimetóxi-1,3,4,6,7,11b15 hexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-azetidin-1il-metanona, (SS)-1-((RS,RS,RS)-2-amino-9,10-dimetóxi1,3,4,6,7,11b-hexaidro-2H-pirido[2,1-a]isoquinolina-3carbonil)-pirrolidina-2-carbonitrila,20 1-((RS,RS,RS)-2-amino-9,10-dimetóxi-1,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-piperidin-2ona, (-)-(S,S,S)-1-(2-amino-9,10-dimetóxi-1,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-piperidin-225 ona,Petição 870180029814, de
- 13/04/2018, pág. 9/19 ( + ) -(R,R,R)-1-(2-amino-9,10-dimetóxi-1,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-piperidin-2ona,1-((RS,RS,RS)-2-amino-9,10-dimetóxi-1,3,4,6,7,11b5 hexaidro-2H-pirido[2,1-a]isoquinolin-3-il) -4-metilpiperidin-2-ona, (RS,RS,RS)-1-(2-amino-9,10-dimetóxi-1,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-pirrolidin2-ona,10 1-((RS,RS,RS)-2-amino-9,10-dimetóxi-1,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metilpirrolidin-2-ona,1-((RS,RS,RS)-2-amino-9,10-dimetóxi-1,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-etil15 pirrolidin-2-ona, (RS,RS,RS)-1-(2-amino-9,10-dimetóxi-1,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-5,6-diidro1H-piridin-2-ona,1-((RS,RS,RS)-2-amino-9,10-dimetóxi-1,3,4,6,7,11b20 hexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-azepan-2ona, (RS,RS,RS)-3-(1,1-dioxo-1,2-tiazolidin-2-il)-9,10dimetóxi-1,3,4,6,7,11b-hexaidro-2H-pirido[2,1a]isoquinolin-2-ilamina,Petição 870180029814, de 13/04/2018, pág. 10/19 (RS,RS,RS)-3-(1,1-dioxo[1,2]tiazinan-2-il)-9,10dimetóxi-1,3,4,6,7,11b-hexaidro-2H-pirido[2,1a]isoquinolin-2-ilamina, (5.5.5) -3-(1,1-dioxo-[1,2]tiazinan-2-il)-9,105 dimetóxi-1,3,4,6,7,11b-hexaidro-2H-pirido[2,1a]isoquinolin-2-ilamina, (SR)-1-((RS,RS,RS)-2-amino-9,10-dimetóxi1,3,4,6,7,11b-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-4-metil-pirrolidin-2-ona,10 (RS,RS,RS,RS)-1-(2-amino-9,10-dimetóxi1,3,4,6,7,11b-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-4-metil-pirrolidin-2-ona, (R) -1-((S,S,S)-2-amino-9,10-dimetóxi-1,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metil15 pirrolidin-2-ona, (S) -1-((R,R,R)-2-amino-9,10-dimetóxi-1,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metilpirrolidin-2-ona, (5.5.5.5) -1-(2-amino-9,10-dimetóxi-1,3,4,6,7,11b20 hexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metilpirrolidin-2-ona, (R,R,R,R)-1-(2-amino-9,10-dimetóxi-1,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metilpirrolidin-2-ona,Petição 870180029814, de 13/04/2018, pág. 11/191-((RS,RS,RS)-2-amino-9,10-dimetóxi-1,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4fluorometil-pirrolidin-2-ona,1-((RS,RS,RS)-2-amino-9,10-dimetóxi-1,3,4,6,7,11b5 hexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-5-metilpiperidin-2-ona, (RS,RS,RS)-N-(2-amino-9,10-dimetóxi-1,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)propionamida,10 (RS,RS,RS)-N-(2-amino-9,10-dimetóxi-1,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-butiramida, ácido ((2RS,3RS,11bRS)-2-amino-9,10-dimetóxi1,3,4,6,7,11b-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-amida ciclopropanocarboxílico,15 (SR)-1-((RS,RS,RS)-2-amino-9,10-dimetóxi1,3,4,6,7,11b-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-4-fluorometil-pirrolidin-2-ona (RS,RS,RS,RS)-1-(2-amino-9,10-dimetóxi1,3,4,6,7,11b-hexaidro-2H-pirido[2,1-a]isoquinolin-320 il)-4-fluorometil-pirrolidin-2-ona, (S)-1- ((2S,3S,11bS)-2-amino-9,10-dimetóxi1,3,4,6,7,11b-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-4-fluorometil-pirrolidin-2-ona, (R)-1-((2S,3S,11bS)-2-amino-9,10-dimetóxi25 1,3,4,6,7,11b-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-4-fluorometil-pirrolidin-2-ona,Petição 870180029814, de 13/04/2018, pág. 12/193-((RS,RS,RS)-2-amino-9,10-dimetóxi-1,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-oxazolidin2-ona,3-((2RS,3RS,11bRS)-2-amino-9,10-dimetóxi5 1,3,4,6,7,11b-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-[1,3]oxazinan-2-ona,1-((2RS,3RS,11bRS)-2-amino-9,10-dimetóxi1,3,4,6,7,11b-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-5-metil-pirrolidin-2-ona,10 3-((2RS,3RS,11bRS)-2-amino-9,10-dimetóxi1,3,4,6,7,11b-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-5-fluorometil-oxazolidin-2-ona,1-((2RS,3RS,11bRS)-2-amino-9,10-dimetóxi1,3,4,6,7,11b-hexaidro-2H-pirido[2,1-a]isoquinolin-315 il)-3-metil-pirrolidin-2-ona,3-((2RS,3RS,11bRS)-2-amino-9,10-dimetóxi-1,3,4,6,7, 11b-hexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-5-metiloxazolidin-2-ona, e os seus sais farmaceuticamente aceitáveis.20 13 - Compostos, de acordo com qualquer uma das reivindicações 1 a 11, caracterizados pelo fato de serem selecionados a partir do grupo que consiste em:(RS,RS,RS)-(2-amino-9,10-dimetóxi-1,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-tiazolidin25 3-il-metanona,Petição 870180029814, de 13/04/2018, pág. 13/19 (-)-(S,S,S)-1-(2-amino-9,10-dimetóxi-1,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-piperidin-2ona,1-((RS,RS,RS)-2-amino-9,10-dimetóxi-1,3,4,6,7,11b5 hexaidro-2H-pirido[2,1-a]isoquinolin-3-il) -4-metilpirrolidin-2-ona, (RS,RS,RS)-1-(2-amino-9,10-dimetóxi-1,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-5,6-diidro1H-piridin-2-ona,10 (S,S,S)-3-(1,1-dioxo-[1,2]tiazinan-2-il)-9,10dimetóxi-1,3,4,6,7,11b-hexaidro-2H-pirido[2,1a]isoquinolin-2-ilamina, (R) -1-((S,S,S)-2-amino-9,10-dimetóxi-1,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metil15 pirrolidin-2-ona, (S,S,S,S)-1-(2-amino-9,10-dimetóxi-1,3,4,6,7,11bhexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4-metilpirrolidin-2-ona,1-((RS,RS,RS)-2-amino-9,10-dimetóxi-1,3,4,6,7,11b20 hexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-5-metilpiperidin-2-ona, (S) -1- ((2S,3S,11bS)-2-amino-9,10-dimetóxi1,3,4,6,7,11b-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-4-fluorometil-pirrolidin-2-ona,Petição 870180029814, de 13/04/2018, pág. 14/19 (R)-1-((2S,3S,11bS)-2-amino-9,10-dimetóxi1,3,4,6,7,11b-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-4-fluorometil-pirrolidin-2-ona,3-((2RS,3RS,11bRS)-2-amino-9,10-dimetóxi5 1,3,4,6,7,11b-hexaidro-2H-pirido[2,1-a]isoquinolin-3il)-5-metil-oxazolidin-2-ona, e os seus sais farmaceuticamente aceitáveis.
- 14 - Processo para a fabricação de compostos de fórmula (I), conforme definido em qualquer uma10 das reivindicações 1 a 13, caracterizado pelo fato de que o processo compreende converter um composto da fórmula A:em que R1, R2, R3 e R4 são conforme definidos na 15 reivindicação 1 e P é um grupo de proteção de amina adequado, em um composto da fórmula (I):Petição 870180029814, de 13/04/2018, pág. 15/19 em que R1, R2, R3 e R4 são conforme definidos na reivindicação 1.
- 15 - Composições farmacêuticas caracterizadas pelo fato de compreenderem um composto, conforme definido em qualquer uma das reivindicações 1 a 13, e um veículo e/ou adjuvante farmaceuticamente aceitável.
- 16 - Composições farmacêuticas, de acordo com a reivindicação 15, caracterizadas pelo fato de se destinarem ao uso para o tratamento e/ou profilaxia de doenças que estão associadas com DPP-IV.
- 17 - Compostos, de acordo com qualquer uma das reivindicações 1 a 13, caracterizados pelo fato de se destinarem ao uso como substâncias terapêuticas ativas.
- 18 - Uso dos compostos, conforme definidos em qualquer uma das reivindicações 1 a 13, caracterizado pelo fato de ser na fabricação de medicamentos para o tratamento e/ou profilaxia de doenças que estão asso20 ciadas com DPP-IV.
- 19 - Uso dos compostos, conforme definidos em qualquer uma das reivindicações 1 a 13, caracterizado pelo fato de ser na fabricação de medicamentos paraPetição 870180029814, de 13/04/2018, pág. 16/19 o tratamento e/ou profilaxia de diabetes, diabetes mellitus não dependente de insulina, tolerância à glicose prejudicada, doença inflamatória intestinal, colite ulcerosa, doença de Crohn, hipertensão, doenças em que um5 agente diurético tem um efeito benéfico, obesidade, e/ou síndrome metabólica ou proteção de células β.
- 20 - Composto, de acordo com a reivindicação 1, caracterizado pelo fato de ser diidrocloreto de (S)-1-((S,S,S)-2-amino-9,10-dimetóxi-1,3,4,6,7,11b10 hexaidro-2H-pirido[2,1-a]isoquinolin-3-il)-4fluorometil-pirrolidin-2-ona.Petição 870180029814, de 13/04/2018, pág. 17/19
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP03013404 | 2003-06-20 | ||
| EP03013404.3 | 2003-06-20 | ||
| PCT/EP2004/006355 WO2005000848A1 (en) | 2003-06-20 | 2004-06-11 | Pyrido` 2, 1-a - isoquinoline derivatives as dpp-iv inhibitors |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| BRPI0411713A BRPI0411713A (pt) | 2006-08-08 |
| BRPI0411713B1 true BRPI0411713B1 (pt) | 2018-07-10 |
| BRPI0411713B8 BRPI0411713B8 (pt) | 2021-05-25 |
Family
ID=33515111
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0411713A BRPI0411713B8 (pt) | 2003-06-20 | 2004-06-11 | compostos, processo para a sua manufatura, composições farmacêuticas que compreendem os mesmos, método para tratamento e/ou profilaxia de enfermidades que estão associadas com dpp-iv e sua utilização |
Country Status (35)
| Country | Link |
|---|---|
| US (1) | US7122555B2 (pt) |
| EP (1) | EP1638970B1 (pt) |
| JP (1) | JP4160616B2 (pt) |
| KR (1) | KR100730867B1 (pt) |
| CN (1) | CN100374439C (pt) |
| AR (1) | AR044795A1 (pt) |
| AT (1) | ATE489387T1 (pt) |
| AU (1) | AU2004251830B8 (pt) |
| BR (1) | BRPI0411713B8 (pt) |
| CA (1) | CA2529443C (pt) |
| CO (1) | CO5640155A2 (pt) |
| CR (1) | CR8147A (pt) |
| CY (1) | CY1111425T1 (pt) |
| DE (1) | DE602004030244D1 (pt) |
| DK (1) | DK1638970T3 (pt) |
| EA (1) | EA009591B1 (pt) |
| EC (1) | ECSP056240A (pt) |
| ES (1) | ES2355105T3 (pt) |
| HK (1) | HK1093503A1 (pt) |
| HR (1) | HRP20110018T1 (pt) |
| IL (1) | IL172618A (pt) |
| MA (1) | MA27883A1 (pt) |
| MX (1) | MXPA05013904A (pt) |
| MY (1) | MY140039A (pt) |
| NO (1) | NO332126B1 (pt) |
| NZ (1) | NZ544221A (pt) |
| PL (1) | PL1638970T3 (pt) |
| PT (1) | PT1638970E (pt) |
| RS (1) | RS52397B (pt) |
| SI (1) | SI1638970T1 (pt) |
| TN (1) | TNSN05320A1 (pt) |
| TW (1) | TWI297011B (pt) |
| UA (1) | UA82242C2 (pt) |
| WO (1) | WO2005000848A1 (pt) |
| ZA (1) | ZA200510298B (pt) |
Families Citing this family (88)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| PL367527A1 (en) | 2001-06-27 | 2005-02-21 | Smithkline Beecham Corporation | Fluoropyrrolidines as dipeptidyl peptidase inhibitors |
| US7407955B2 (en) | 2002-08-21 | 2008-08-05 | Boehringer Ingelheim Pharma Gmbh & Co., Kg | 8-[3-amino-piperidin-1-yl]-xanthines, the preparation thereof and their use as pharmaceutical compositions |
| KR20050122220A (ko) | 2003-03-25 | 2005-12-28 | 다케다 샌디에고, 인코포레이티드 | 디펩티딜 펩티다제 억제제 |
| RU2339636C2 (ru) * | 2003-06-20 | 2008-11-27 | Ф.Хоффманн-Ля Рош Аг | Гексагидропиридоизохинолины в качестве ингибиторов дипептидилпептидазы iv (dpp-iv) |
| US7169926B1 (en) | 2003-08-13 | 2007-01-30 | Takeda Pharmaceutical Company Limited | Dipeptidyl peptidase inhibitors |
| US7678909B1 (en) | 2003-08-13 | 2010-03-16 | Takeda Pharmaceutical Company Limited | Dipeptidyl peptidase inhibitors |
| CN1867560A (zh) | 2003-08-13 | 2006-11-22 | 武田药品工株式会社 | 4-嘧啶酮衍生物及其作为肽基肽酶抑制剂的用途 |
| JP2007505121A (ja) | 2003-09-08 | 2007-03-08 | 武田薬品工業株式会社 | ジペプチジルぺプチダーゼ阻害剤 |
| US7501426B2 (en) | 2004-02-18 | 2009-03-10 | Boehringer Ingelheim International Gmbh | 8-[3-amino-piperidin-1-yl]-xanthines, their preparation and their use as pharmaceutical compositions |
| US7732446B1 (en) | 2004-03-11 | 2010-06-08 | Takeda Pharmaceutical Company Limited | Dipeptidyl peptidase inhibitors |
| CN102134231B (zh) | 2004-03-15 | 2020-08-04 | 武田药品工业株式会社 | 二肽基肽酶抑制剂 |
| JP2008501714A (ja) | 2004-06-04 | 2008-01-24 | 武田薬品工業株式会社 | ジペプチジルペプチダーゼインヒビター |
| WO2006019965A2 (en) | 2004-07-16 | 2006-02-23 | Takeda San Diego, Inc. | Dipeptidyl peptidase inhibitors |
| DE102004054054A1 (de) | 2004-11-05 | 2006-05-11 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Verfahren zur Herstellung chiraler 8-(3-Amino-piperidin-1-yl)-xanthine |
| CN101107247B (zh) * | 2004-11-30 | 2011-10-19 | 霍夫曼-拉罗奇有限公司 | 作为用于治疗糖尿病的dpp-iv抑制剂的取代的苯并喹嗪衍生物 |
| JP2008524331A (ja) | 2004-12-21 | 2008-07-10 | 武田薬品工業株式会社 | ジペプチジルペプチダーゼ阻害剤 |
| DOP2006000008A (es) | 2005-01-10 | 2006-08-31 | Arena Pharm Inc | Terapia combinada para el tratamiento de la diabetes y afecciones relacionadas y para el tratamiento de afecciones que mejoran mediante un incremento de la concentración sanguínea de glp-1 |
| JP4568361B2 (ja) | 2005-04-22 | 2010-10-27 | アラントス・ファーマシューティカルズ・ホールディング・インコーポレーテッド | ジペプチジルペプチダーゼ−iv阻害剤 |
| ES2313672T3 (es) * | 2005-05-24 | 2009-03-01 | F. Hoffmann-La Roche Ag | Praparacion de (s)-4-fluorometil-dihidro-furan-2-ona. |
| DE102005035891A1 (de) | 2005-07-30 | 2007-02-08 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | 8-(3-Amino-piperidin-1-yl)-xanthine, deren Herstellung und deren Verwendung als Arzneimittel |
| AU2006278039B2 (en) * | 2005-08-11 | 2010-10-21 | F. Hoffmann-La Roche Ag | Pharmaceutical composition comprising a DPP-lV inhibitor |
| EA015169B1 (ru) | 2005-09-14 | 2011-06-30 | Такеда Фармасьютикал Компани Лимитед | Применение ингибиторов дипептидилпептидазы |
| CA2622642C (en) | 2005-09-16 | 2013-12-31 | Takeda Pharmaceutical Company Limited | Dipeptidyl peptidase inhibitors |
| WO2007112347A1 (en) | 2006-03-28 | 2007-10-04 | Takeda Pharmaceutical Company Limited | Dipeptidyl peptidase inhibitors |
| PE20071221A1 (es) | 2006-04-11 | 2007-12-14 | Arena Pharm Inc | Agonistas del receptor gpr119 en metodos para aumentar la masa osea y para tratar la osteoporosis y otras afecciones caracterizadas por masa osea baja, y la terapia combinada relacionada a estos agonistas |
| DK1971862T3 (da) | 2006-04-11 | 2011-02-14 | Arena Pharm Inc | Fremgangsmåder til anvendelse af GPR119-receptor til identificering af forbindelser anvendelige til øgning af knoglemasse hos en person |
| CA2649209A1 (en) | 2006-04-12 | 2007-10-18 | Probiodrug Ag | Enzyme inhibitors |
| EP1852108A1 (en) | 2006-05-04 | 2007-11-07 | Boehringer Ingelheim Pharma GmbH & Co.KG | DPP IV inhibitor formulations |
| PE20080251A1 (es) | 2006-05-04 | 2008-04-25 | Boehringer Ingelheim Int | Usos de inhibidores de dpp iv |
| EA015687B1 (ru) | 2006-05-04 | 2011-10-31 | Бёрингер Ингельхайм Интернациональ Гмбх | Полиморфы |
| WO2007148185A2 (en) * | 2006-06-21 | 2007-12-27 | Pfizer Products Inc. | Substituted 3 -amino- pyrrolidino-4 -lactams as dpp inhibitors |
| US8324383B2 (en) | 2006-09-13 | 2012-12-04 | Takeda Pharmaceutical Company Limited | Methods of making polymorphs of benzoate salt of 2-[[6-[(3R)-3-amino-1-piperidinyl]-3,4-dihydro-3-methyl-2,4-dioxo-1(2H)-pyrimidinyl]methyl]-benzonitrile |
| EP2069343A2 (en) * | 2006-09-15 | 2009-06-17 | F. Hoffmann-Roche AG | Process for the preparation of pyrido[2,1-a]isoquinoline derivatives by catalytic asymmetric hydrogenation of an enamine |
| ES2371369T3 (es) * | 2006-09-15 | 2011-12-30 | F. Hoffmann-La Roche Ag | Procedimiento para la preparación de derivados pirido[2,1-a]isoquinolina, que comprende la resolución óptica de una enamina. |
| US7956201B2 (en) | 2006-11-06 | 2011-06-07 | Hoffman-La Roche Inc. | Process for the preparation of (S)-4-fluoromethyl-dihydro-furan-2-one |
| WO2008055945A1 (en) | 2006-11-09 | 2008-05-15 | Probiodrug Ag | 3-hydr0xy-1,5-dihydr0-pyrr0l-2-one derivatives as inhibitors of glutaminyl cyclase for the treatment of ulcer, cancer and other diseases |
| TW200838536A (en) | 2006-11-29 | 2008-10-01 | Takeda Pharmaceutical | Polymorphs of succinate salt of 2-[6-(3-amino-piperidin-1-yl)-3-methyl-2,4-dioxo-3,4-dihydro-2H-pyrimidin-1-ylmethy]-4-fluor-benzonitrile and methods of use therefor |
| ATE554085T1 (de) | 2006-11-30 | 2012-05-15 | Probiodrug Ag | Neue inhibitoren von glutaminylcyclase |
| US8093236B2 (en) | 2007-03-13 | 2012-01-10 | Takeda Pharmaceuticals Company Limited | Weekly administration of dipeptidyl peptidase inhibitors |
| EP2865670B1 (en) | 2007-04-18 | 2017-01-11 | Probiodrug AG | Thiourea derivatives as glutaminyl cyclase inhibitors |
| PE20090987A1 (es) * | 2007-08-16 | 2009-08-14 | Boehringer Ingelheim Int | Composicion farmaceutica que comprende un derivado de pirazol-o-glucosido |
| CL2008002427A1 (es) | 2007-08-16 | 2009-09-11 | Boehringer Ingelheim Int | Composicion farmaceutica que comprende 1-cloro-4-(b-d-glucopiranos-1-il)-2-[4-((s)-tetrahidrofurano-3-iloxi)bencil]-benceno combinado con 1-[(4-metilquinazolin-2-il)metil]-3-metil-7-(2-butin-1-il)-8-(3-(r)-aminopiperidin-1-il)xantina; y su uso para tratar diabetes mellitus tipo 2. |
| EP3542801A1 (en) * | 2007-08-17 | 2019-09-25 | Boehringer Ingelheim International GmbH | Purin derivatives for use in the treatment of fap-related diseases |
| US20090105480A1 (en) * | 2007-08-30 | 2009-04-23 | Ulrike Bromberger | Process for the preparation of a dpp-iv inhibitor |
| US20090163718A1 (en) * | 2007-12-19 | 2009-06-25 | Stefan Abrecht | PROCESS FOR THE PREPARATION OF PYRIDO[2,1-a] ISOQUINOLINE DERIVATIVES |
| AR071175A1 (es) | 2008-04-03 | 2010-06-02 | Boehringer Ingelheim Int | Composicion farmaceutica que comprende un inhibidor de la dipeptidil-peptidasa-4 (dpp4) y un farmaco acompanante |
| EP2146210A1 (en) | 2008-04-07 | 2010-01-20 | Arena Pharmaceuticals, Inc. | Methods of using A G protein-coupled receptor to identify peptide YY (PYY) secretagogues and compounds useful in the treatment of conditions modulated by PYY |
| PE20100156A1 (es) * | 2008-06-03 | 2010-02-23 | Boehringer Ingelheim Int | Tratamiento de nafld |
| KR20190016601A (ko) | 2008-08-06 | 2019-02-18 | 베링거 인겔하임 인터내셔날 게엠베하 | 메트포르민 요법이 부적합한 환자에서의 당뇨병 치료 |
| UY32030A (es) | 2008-08-06 | 2010-03-26 | Boehringer Ingelheim Int | "tratamiento para diabetes en pacientes inapropiados para terapia con metformina" |
| CN103816158A (zh) * | 2008-08-15 | 2014-05-28 | 勃林格殷格翰国际有限公司 | 用于治疗fab-相关疾病的嘌呤衍生物 |
| CA2736421A1 (en) | 2008-09-10 | 2010-03-18 | Boehringer Ingelheim International Gmbh | Combination therapy for the treatment of diabetes and related conditions |
| US20200155558A1 (en) | 2018-11-20 | 2020-05-21 | Boehringer Ingelheim International Gmbh | Treatment for diabetes in patients with insufficient glycemic control despite therapy with an oral antidiabetic drug |
| CN107011345A (zh) | 2008-12-23 | 2017-08-04 | 勃林格殷格翰国际有限公司 | 有机化合物的盐形式 |
| AR074990A1 (es) | 2009-01-07 | 2011-03-02 | Boehringer Ingelheim Int | Tratamiento de diabetes en pacientes con un control glucemico inadecuado a pesar de la terapia con metformina |
| TWI466672B (zh) | 2009-01-29 | 2015-01-01 | Boehringer Ingelheim Int | 小兒科病人糖尿病之治療 |
| UY32441A (es) | 2009-02-13 | 2010-09-30 | Boehringer Ingelheim Int | Composicion farmaceutica, metodos de tratamiento y sus usos |
| CN106177958A (zh) | 2009-02-13 | 2016-12-07 | 勃林格殷格翰国际有限公司 | 包含dpp‑4抑制剂(利拉列汀)任选地组合其它抗糖尿病药的抗糖尿病药物 |
| AR077642A1 (es) | 2009-07-09 | 2011-09-14 | Arena Pharm Inc | Moduladores del metabolismo y el tratamiento de trastornos relacionados con el mismo |
| NZ598685A (en) | 2009-09-11 | 2013-05-31 | Probiodrug Ag | Heterocylcic derivatives as inhibitors of glutaminyl cyclase |
| EA034869B1 (ru) | 2009-11-27 | 2020-03-31 | Бёрингер Ингельхайм Интернациональ Гмбх | Лечение генотипированных пациентов с диабетом ингибиторами дпп-4, такими как линаглиптин |
| EP2542549B1 (en) | 2010-03-03 | 2016-05-11 | Probiodrug AG | Inhibitors of glutaminyl cyclase |
| US8269019B2 (en) | 2010-03-10 | 2012-09-18 | Probiodrug Ag | Inhibitors |
| WO2011113947A1 (en) | 2010-03-18 | 2011-09-22 | Boehringer Ingelheim International Gmbh | Combination of a gpr119 agonist and the dpp-iv inhibitor linagliptin for use in the treatment of diabetes and related conditions |
| JP2013523819A (ja) | 2010-04-06 | 2013-06-17 | アリーナ ファーマシューティカルズ, インコーポレイテッド | Gpr119レセプターのモジュレーターおよびそれに関連する障害の処置 |
| JP5945532B2 (ja) | 2010-04-21 | 2016-07-05 | プロビオドルグ エージー | グルタミニルシクラーゼの阻害剤としてのベンゾイミダゾール誘導体 |
| EP2566469B1 (en) | 2010-05-05 | 2022-12-21 | Boehringer Ingelheim International GmbH | Combination therapy |
| CN102971005A (zh) | 2010-06-24 | 2013-03-13 | 贝林格尔.英格海姆国际有限公司 | 糖尿病治疗 |
| CA2812061A1 (en) | 2010-09-22 | 2012-03-29 | Arena Pharmaceuticals, Inc. | Modulators of the gpr119 receptor and the treatment of disorders related thereto |
| US9034883B2 (en) | 2010-11-15 | 2015-05-19 | Boehringer Ingelheim International Gmbh | Vasoprotective and cardioprotective antidiabetic therapy |
| AR085689A1 (es) | 2011-03-07 | 2013-10-23 | Boehringer Ingelheim Int | Composiciones farmaceuticas de metformina, linagliptina y un inhibidor de sglt-2 |
| EP2686313B1 (en) | 2011-03-16 | 2016-02-03 | Probiodrug AG | Benzimidazole derivatives as inhibitors of glutaminyl cyclase |
| WO2012135570A1 (en) | 2011-04-01 | 2012-10-04 | Arena Pharmaceuticals, Inc. | Modulators of the gpr119 receptor and the treatment of disorders related thereto |
| WO2012145361A1 (en) | 2011-04-19 | 2012-10-26 | Arena Pharmaceuticals, Inc. | Modulators of the gpr119 receptor and the treatment of disorders related thereto |
| WO2012145604A1 (en) | 2011-04-22 | 2012-10-26 | Arena Pharmaceuticals, Inc. | Modulators of the gpr119 receptor and the treatment of disorders related thereto |
| WO2012145603A1 (en) | 2011-04-22 | 2012-10-26 | Arena Pharmaceuticals, Inc. | Modulators of the gpr119 receptor and the treatment of disorders related thereto |
| WO2012170702A1 (en) | 2011-06-08 | 2012-12-13 | Arena Pharmaceuticals, Inc. | Modulators of the gpr119 receptor and the treatment of disorders related thereto |
| EP2731947B1 (en) | 2011-07-15 | 2019-01-16 | Boehringer Ingelheim International GmbH | Substituted dimeric quinazoline derivative, its preparation and its use in pharmaceutical compositions for the treatment of type i and ii diabetes |
| WO2013055910A1 (en) | 2011-10-12 | 2013-04-18 | Arena Pharmaceuticals, Inc. | Modulators of the gpr119 receptor and the treatment of disorders related thereto |
| US9555001B2 (en) | 2012-03-07 | 2017-01-31 | Boehringer Ingelheim International Gmbh | Pharmaceutical composition and uses thereof |
| JP6224084B2 (ja) | 2012-05-14 | 2017-11-01 | ベーリンガー インゲルハイム インターナショナル ゲゼルシャフト ミット ベシュレンクテル ハフツング | 糸球体上皮細胞関連障害及び/又はネフローゼ症候群の治療に用いるdpp−4阻害薬としてのキサンチン誘導体 |
| WO2013174767A1 (en) | 2012-05-24 | 2013-11-28 | Boehringer Ingelheim International Gmbh | A xanthine derivative as dpp -4 inhibitor for use in modifying food intake and regulating food preference |
| WO2014074668A1 (en) | 2012-11-08 | 2014-05-15 | Arena Pharmaceuticals, Inc. | Modulators of gpr119 and the treatment of disorders related thereto |
| JP6615109B2 (ja) | 2014-02-28 | 2019-12-04 | ベーリンガー インゲルハイム インターナショナル ゲゼルシャフト ミット ベシュレンクテル ハフツング | Dpp−4阻害薬の医学的使用 |
| JP2018507914A (ja) | 2015-03-09 | 2018-03-22 | インテクリン・セラピューティクス・インコーポレイテッド | 非アルコール性脂肪肝疾患および/またはリポジストロフィーの処置のための方法 |
| WO2017211979A1 (en) | 2016-06-10 | 2017-12-14 | Boehringer Ingelheim International Gmbh | Combinations of linagliptin and metformin |
| WO2018187350A1 (en) | 2017-04-03 | 2018-10-11 | Coherus Biosciences Inc. | PPARγ AGONIST FOR TREATMENT OF PROGRESSIVE SUPRANUCLEAR PALSY |
| EP3461819B1 (en) | 2017-09-29 | 2020-05-27 | Probiodrug AG | Inhibitors of glutaminyl cyclase |
Family Cites Families (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5681956A (en) | 1990-12-28 | 1997-10-28 | Neurogen Corporation | 4-aryl substituted piperazinylmethyl phenylimidazole derivatives; a new class of dopamine receptor subtype specific ligands |
| GB9313913D0 (en) | 1993-07-06 | 1993-08-18 | Smithkline Beecham Plc | Novel compounds |
| US5455351A (en) | 1993-12-13 | 1995-10-03 | Abbott Laboratories | Retroviral protease inhibiting piperazine compounds |
| DE19616486C5 (de) | 1996-04-25 | 2016-06-30 | Royalty Pharma Collection Trust | Verfahren zur Senkung des Blutglukosespiegels in Säugern |
| TW492957B (en) | 1996-11-07 | 2002-07-01 | Novartis Ag | N-substituted 2-cyanopyrrolidnes |
| US6011155A (en) | 1996-11-07 | 2000-01-04 | Novartis Ag | N-(substituted glycyl)-2-cyanopyrrolidines, pharmaceutical compositions containing them and their use in inhibiting dipeptidyl peptidase-IV |
| JP2002501889A (ja) | 1998-02-02 | 2002-01-22 | トラスティーズ オブ タフツ カレッジ | グルコース代謝を調節する方法、およびそれに関連する試薬 |
| DE19834591A1 (de) | 1998-07-31 | 2000-02-03 | Probiodrug Ges Fuer Arzneim | Verfahren zur Steigerung des Blutglukosespiegels in Säugern |
| GB9817118D0 (en) | 1998-08-07 | 1998-10-07 | Glaxo Group Ltd | Pharmaceutical compounds |
| CO5150173A1 (es) | 1998-12-10 | 2002-04-29 | Novartis Ag | Compuestos n-(glicilo sustituido)-2-cianopirrolidinas inhibidores de peptidasa de dipeptidilo-iv (dpp-iv) los cuales son efectivos en el tratamiento de condiciones mediadas por la inhibicion de dpp-iv |
| US6110949A (en) | 1999-06-24 | 2000-08-29 | Novartis Ag | N-(substituted glycyl)-4-cyanothiazolidines, pharmaceutical compositions containing them and their use in inhibiting dipeptidyl peptidase-IV |
| AU6875800A (en) | 1999-09-10 | 2001-04-17 | Takeda Chemical Industries Ltd. | Heterocyclic compounds and process for the preparation thereof |
| JP2003535034A (ja) | 1999-11-12 | 2003-11-25 | ギルフォード ファーマシューティカルズ インコーポレイテッド | ジペプチジルペプチダーゼiv阻害剤並びにジペプチジルペプチダーゼiv阻害剤の製造及び使用法 |
| GB9928330D0 (en) | 1999-11-30 | 2000-01-26 | Ferring Bv | Novel antidiabetic agents |
| AU2001228309A1 (en) | 2000-01-24 | 2001-08-07 | Novo-Nordisk A/S | N-substituted 2-cyanopyroles and -pyrrolines which are inhibitors of the enzyme dpp-iv |
| JP2003523396A (ja) | 2000-02-25 | 2003-08-05 | ノボ ノルディスク アクティーゼルスカブ | ベータ細胞変性の抑制 |
| HU227882B1 (hu) * | 2000-08-10 | 2012-05-29 | Mitsubishi Tanabe Pharma Corp | Prolinszármazékok és gyógyszerként való alkalmazásuk |
| CA2424600C (en) | 2000-10-06 | 2008-12-02 | Tanabe Seiyaku Co., Ltd. | Aliphatic nitrogenous five-membered ring compounds |
| US6861440B2 (en) * | 2001-10-26 | 2005-03-01 | Hoffmann-La Roche Inc. | DPP IV inhibitors |
| US6727261B2 (en) * | 2001-12-27 | 2004-04-27 | Hoffman-La Roche Inc. | Pyrido[2,1-A]Isoquinoline derivatives |
-
2004
- 2004-06-11 EA EA200501936A patent/EA009591B1/ru not_active IP Right Cessation
- 2004-06-11 CA CA2529443A patent/CA2529443C/en not_active Expired - Fee Related
- 2004-06-11 WO PCT/EP2004/006355 patent/WO2005000848A1/en active Application Filing
- 2004-06-11 BR BRPI0411713A patent/BRPI0411713B8/pt not_active IP Right Cessation
- 2004-06-11 SI SI200431593T patent/SI1638970T1/sl unknown
- 2004-06-11 DK DK04739841.7T patent/DK1638970T3/da active
- 2004-06-11 AU AU2004251830A patent/AU2004251830B8/en not_active Ceased
- 2004-06-11 MX MXPA05013904A patent/MXPA05013904A/es active IP Right Grant
- 2004-06-11 JP JP2006515913A patent/JP4160616B2/ja not_active Expired - Fee Related
- 2004-06-11 ES ES04739841T patent/ES2355105T3/es active Active
- 2004-06-11 PL PL04739841T patent/PL1638970T3/pl unknown
- 2004-06-11 NZ NZ544221A patent/NZ544221A/en not_active IP Right Cessation
- 2004-06-11 AT AT04739841T patent/ATE489387T1/de active
- 2004-06-11 EP EP04739841A patent/EP1638970B1/en active Active
- 2004-06-11 RS YU20050939A patent/RS52397B/en unknown
- 2004-06-11 KR KR1020057024424A patent/KR100730867B1/ko active IP Right Grant
- 2004-06-11 PT PT04739841T patent/PT1638970E/pt unknown
- 2004-06-11 DE DE602004030244T patent/DE602004030244D1/de active Active
- 2004-06-11 CN CNB200480017358XA patent/CN100374439C/zh not_active Expired - Fee Related
- 2004-06-16 TW TW093117363A patent/TWI297011B/zh not_active IP Right Cessation
- 2004-06-17 US US10/870,580 patent/US7122555B2/en active Active
- 2004-06-17 AR ARP040102105A patent/AR044795A1/es active IP Right Grant
- 2004-06-18 MY MYPI20042371A patent/MY140039A/en unknown
- 2004-11-06 UA UAA200600527A patent/UA82242C2/uk unknown
-
2005
- 2005-12-12 NO NO20055887A patent/NO332126B1/no not_active IP Right Cessation
- 2005-12-13 CR CR8147A patent/CR8147A/es unknown
- 2005-12-15 IL IL172618A patent/IL172618A/en active IP Right Grant
- 2005-12-15 MA MA28665A patent/MA27883A1/fr unknown
- 2005-12-16 TN TNP2005000320A patent/TNSN05320A1/en unknown
- 2005-12-19 ZA ZA200510298A patent/ZA200510298B/en unknown
- 2005-12-20 EC EC2005006240A patent/ECSP056240A/es unknown
- 2005-12-20 CO CO05128097A patent/CO5640155A2/es active IP Right Grant
-
2007
- 2007-01-10 HK HK07100369A patent/HK1093503A1/xx not_active IP Right Cessation
-
2011
- 2011-01-12 HR HR20110018T patent/HRP20110018T1/hr unknown
- 2011-01-27 CY CY20111100091T patent/CY1111425T1/el unknown
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| BRPI0411713B1 (pt) | Compostos, processo para a sua manufatura, composições farmacêuticas que compreendem os mesmos, método para tratamento e/ou profilaxia de enfermidades que estão associadas com dpp-iv e sua utilização | |
| RU2396257C2 (ru) | Производные 4-аминопиперидина | |
| JP5823476B2 (ja) | Nk1アンタゴニストとしてのピロリジンおよびピペリジンの誘導体 | |
| RU2339636C2 (ru) | Гексагидропиридоизохинолины в качестве ингибиторов дипептидилпептидазы iv (dpp-iv) | |
| EP2522664A1 (en) | Piperidine derivatives as NK1 antagonists | |
| TW201211028A (en) | Fused ring pyrrolidine derivatives | |
| EP4168406A1 (en) | Arylsulfonyl derivatives and their use as muscarinic acetylcholine receptor m5 inhibitors | |
| US20180155283A1 (en) | Dopamine d2 receptor ligands | |
| JPWO2004031171A1 (ja) | イソキノリン化合物及びその医薬用途 | |
| US7795267B2 (en) | Bicyclic piperazine compound having TGR23 antagonistic activity | |
| WO2001025199A1 (fr) | Composes d'uree, procede de production et d'utilisation de ces derniers | |
| JP6500201B2 (ja) | 置換トロパン誘導体 | |
| US20190263781A1 (en) | Tetrahydroisoquinoline Kappa Opioid Antagonists | |
| SG178319A1 (en) | Process for the preparation of cathepsin s inhibitors | |
| JP2023519605A (ja) | 核内受容体に対して活性な化合物 | |
| MX2007011769A (es) | Ciclohexano-1,4-diaminas sustituidas con piperidinilo. | |
| JP2005306839A (ja) | 二環性ピペラジン化合物およびその用途 | |
| Shah et al. | NK 1 antagonists |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B07D | Technical examination (opinion) related to article 229 of industrial property law [chapter 7.4 patent gazette] | ||
| B07E | Notification of approval relating to section 229 industrial property law [chapter 7.5 patent gazette] | ||
| B06A | Patent application procedure suspended [chapter 6.1 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] | ||
| B16C | Correction of notification of the grant [chapter 16.3 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 11/06/2004 OBSERVADAS AS CONDICOES LEGAIS. PATENTE CONCEDIDA CONFORME ADI 5.529/DF |
|
| B21F | Lapse acc. art. 78, item iv - on non-payment of the annual fees in time |
Free format text: REFERENTE A 18A ANUIDADE. |
|
| B24J | Lapse because of non-payment of annual fees (definitively: art 78 iv lpi, resolution 113/2013 art. 12) |
Free format text: EM VIRTUDE DA EXTINCAO PUBLICADA NA RPI 2674 DE 05-04-2022 E CONSIDERANDO AUSENCIA DE MANIFESTACAO DENTRO DOS PRAZOS LEGAIS, INFORMO QUE CABE SER MANTIDA A EXTINCAO DA PATENTE E SEUS CERTIFICADOS, CONFORME O DISPOSTO NO ARTIGO 12, DA RESOLUCAO 113/2013. |