(Pedido Dividido do PI0815474-0, depositado em 13/08/2008)
CAMPO DA INVENÇÃO
[001] A presente invenção relaciona-se aos métodos de produzir um alimento ou bebida à base de malte apropriado para consumo por um indivíduo com doença Celíaca. Em particular, a presente invenção relaciona-se aos métodos para produzir um alimento ou bebida à base de malte com baixos níveis de hordeínas. Também são fornecidas plantas de cevada que produzem grão que pode ser usado nos métodos da invenção.
FUNDAMENTO DA INVENÇÃO
[002] A doença celíaca (CD, também chamada enteropatia glúten-induzida) é uma doença autoimune mediada por célula T do intestino delgado que é provocada em indivíduos suscetíveis pela ingestão de proteínas de armazenamento particulares, coletivamente conhecidas como prolaminas, do trigo (glúten consistindo de gluteninas e gliadinas), cevada (hordeínas) ou centeio (secalinas). As prolaminas de aveia (aveninas) parecem ser tolerados pela maioria dos celíacos (Hogberg e col., 2004; Peraaho e col., 2004a), mas podem induzir reações positivas em uma minoria de celíacos (Lundin e col. 2003; Peraaho e col. 2004b). CD ocorre em aproximadamente 0,25 a 1% da população em pelo menos Austrália, América do Norte e Sul, Europa, África e Índia (Hovell e col. 2001; Fasano e col. 2003; Treem 2004), mas a doença é provavelmente não diagnosticada. A consciência aumentada dos sintomas e consequências de CD não tratado têm conduzido às taxas de diagnóstico na Austrália aumentando 15% por ano. Aproximadamente 1 em 4 Caucasianos e Asiáticos Ocidentais carregam o HLA-DQ8 ou alelos -DQ2 que são necessários, mas não determinante suficiente de CD (Treem 2004). Entretanto, somente aproximadamente 1 em 20 pessoas com estes alelos desenvolve CD. Presentemente o único tratamento é evitar totalmente trigo, cevada e centeio, pois as recorrências podem ser provocadas pelo pouco consumo de 10 miligramas de glúten por dia (Biagi e col., 2004).
[003] Se não diagnosticado ou não tratado, CD tem consequências sérias de saúde que podem ter risco de morte, particularmente em infantes. CD causa a deformação de vilosidades absorventes do intestino delgado e pode conduzir à destruição da vilosidade. Como resultado, os nutrientes são mal absorvidos e isto pode estar associado com perda de peso, fadiga, deficiências minerais, dermatite e perda de visão noturna, bem como estresse intestinal intenso que geralmente inclui inchaço, diarreia e cólicas. Os indivíduos com CD não tratados têm riscos aumentados de câncer, tais como um risco 10 vezes aumentado de carcinoma do intestino delgado, um aumento de 3-6 vezes no risco de linfoma não Hodgkin e risco 28 vezes aumentado de linfoma de célula T intestinal. CD também apresenta um aumento de 3 vezes no risco de diabetes tipo I (Peters e col. 2003; Peters e col. 2003; Verkarre e col. 2004). Um aumento de cinco vezes na incidência de depressão mental foi relatado em pacientes celíacos (Pynnonen e col. 2004).
[004] A base molecular de doença celíaca é agora razoavelmente bem compreendida (Sollid 2002; Hadjivassiliou e col. 2004) como sendo uma reação a uma sequência específica de aminoácidos em prolaminas. Os peptídeos de prolamina mal digeridos ricos em prolina e glutamina se conformam à porção de substrato alvo por trans-glutaminase de tecido humano (tTG) na mucosa intestinal permitindo resíduos de glutamina chaves serem desaminados. O ácido glutâmico negativamente carregado resultante permite a prolamina desaminada se ligar a uma classe específica de moléculas de HLA (DQ2 ou DQ8) (Kim e col. 2004). Os clones de célula T específicos, assim chamadas células T restritas de DQ2(8)/CD4+, enviados ao endotélio intestinal são estimulados para proliferar, liberando linfocinas que conduzem à atrofia de vilosidade ou produção de anticorpo (Hadjivassiliou e col. 2004). Estes clones de célula T alcançam uma concentração máxima no sangue periférico de celíacos em torno de seis dias após um desafio dietético (Anderson e col. 2000). A toxicidade celíaca de proteínas purificadas pode, portanto, ser sensivelmente e especificamente determinada medindo sua capacidade para estimular a células T para produzir IFN-Y, um citocina fundamental à patogênese da enteropatia vista na doença celíaca. Parece, portanto que a doença é causada pelo sistema imune do hospedeiro reagindo às prolaminas como se fossem um patógeno de invasão, montando uma resposta imune vigorosa, ao invés de uma alergia.
[005] O glúten de trigo é composto de muitas centenas de proteínas diferentes, mas relacionadas incluindo as gliadinas monoméricas e gluteninas poliméricas. As gliadinas contam como metade da fração de glúten e α- gliadinas compreendem mais de 50% das gliadinas (Wieser e col., 1994; Gellrich e col., 2003). Até agora, a maioria dos dados de toxicidade celíaca foram focados na α-gliadina, a primeira prolamina a ser clonada e inteiramente sequenciada (Kasarda e col. 1984). A toxicidade celíaca de α-gliadina de trigo é amplamente determinada por um único resíduo de glutamina dentro de um epítopo de aminoácido de chave 17 (Arentz-Hansen e col. 2000; Anderson e col. 2000; Shan e col. 2002). Os peptídeos naturais e sintéticos carregando mutações pontuais nesta região foram identificados, que não são tóxicos (Vader e col. 2003). Portanto, parece provavelmente que outras moléculas de prolamina não tóxicas, mas funcionais podem seridentificadas. Presentemente, a predição útil de toxicidade celíaca é limitada à fração pequena de prolaminas que foram caracterizadas em termos de sequência de aminoácido ou sequência de nucleotídeo dos genes codificando-as.
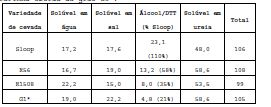
[006] A cevada é um cereal diplóide que é extensamente crescido em climas mais frescos para a produção de alimento e bebida. As proteínas de semente de cevada são classificadas em albumina, globulina, prolamina (hordeína) e glutelina de acordo com sua solubilidade em água, solução de sal, álcool aquoso e soluções básicas ou ácidas, respectivamente. Aproximadamente metade das proteínas de armazenamento de semente na cevada é encontrada na fração de prolamina. Estas prolaminas são primariamente proteínas de reserva que funcionam como fontes de carbono, nitrogênio ou enxofre para crescimento e desenvolvimento após a germinação. A hordeína constitui aproximadamente 40% da proteína de semente, embora isto seja dependente da fonte de nitrogênio da planta durante o crescimento. Os loci que codificam as prolaminas de cevada foram caracterizados, na maior parte por causa de sua contribuição à qualidade de maltagem de cevada e formação de espuma e turvação na produção de cerveja. Há quatro classes de prolaminas na cevada, as B, C, D e Y-hordeínas codificados por loci Hor2, Hor1, Hor3, e Hor5, respectivamente, no cromossomo 1H (Shewry e col. 1999). Estes loci codificam as proteínas que variam de uma única prolamina (por exemplo, D hordeína) às famílias de proteína contendo 20-30 membros (por exemplo, B e C hordeínas). As hordeínas B e C são relativamente mais abundantes, compreendendo aproximadamente 70% e 24% das hordeínas totais, respectivamente. As D e Y-hordeínas representam componentes menores em aproximadamente 2-4% cada. O peso molecular de hordeínas varia de aproximadamente 35 kDa a 100 kDa. Não há nenhuma prolamina de cevada que tenha homologia próxima às α-gliadina de trigo, porém é extensamente aceito que as hordeínas são tóxicas aos celíacos (Williamson & Marsh 2000). A extensão a qual as hordeínas individuais de cevada estão induzindo CD não foi relatada.
[007] A cerveja é um produto extensamente consumido feito de cevada maltada, portanto a cerveja é extensamente assumida não ser apropriada para celíacos e geralmente excluída de sua dieta. Kanerva e col. (2005) foram capazes de identificar prolaminas em baixos níveis em todas, com exceção de uma de várias cervejas. Os médicos e nutricionistas geralmente pressionam seus pacientes CD a assiduamente evitar quaisquer produtos contendo trigo, cevada ou centeio, incluindo cerveja. Nos EUA, a definição do FDA de “sem glúten” exige o produto ser feito das matérias-primas livres de glúten somente, isto é, não contendo nenhum trigo, cevada ou centeio. O Codex Alimentarius permite o rótulo “sem glúten” nos alimentos não contendo mais de 200 ppm de glúten (0,2g por quilograma ou litro) e este é também o padrão Europeu para “sem glúten”. A maioria de celíacos pode tolerar até aproximadamente 10 mg de glúten por dia sem grandes efeitos (Thompson, 2001).
[008] As prolaminas tóxicas aos pacientes celíacos podem ser especificamente detectadas com imunoensaios, tais como ELISA (Ellis e col., 1990; Sorell e col., 1998). Estes ensaios dependem da interação específica entre a proteína e o anticorpo. A eletroforese em gel de sulfato- poliacrilamida dodecil de sódio (SDS-PAGE) e HPLC também foram usadas (Kanerva e col., 2005; Marchilo e col., 1986; Sheehan e Skerritt, 1997).
[009] Há, portanto, uma necessidade para cevada com substancialmente níveis inferiores de hordeínas indutoras de CD que poderiam ser usadas em produtos de alimento e bebida para indivíduos suscetíveis à CD.
SUMÁRIO DA INVENÇÃO
[0010] Há quatro classes de prolaminas na cevada, B, C, D e Y-hordeínas codificados pelos loci Hor2, Hor1, Hor3, e Hor5, respectivamente. Os presentes inventores descobriram que pelo menos as classes B, C e D induzem respostas inflamatórias indesejáveis em indivíduos com doença celíaca.
[0011] Enquanto vários mutantes de cevada têm sido previamente identificados por produzir determinadas classes de hordeínas em níveis reduzidos, foi também observado que isto foi pelo menos compensado pela produção aumentada de outras classes de hordeínas. Isto sugere que a semente de cevada tem mecanismos compensatórios para assegurar determinados níveis de hordeínas exigidos para a semente ser viável. Surpreendentemente, os presentes inventores determinaram que a maioria, se não toda a produção de hordeína de cevada pode ser abolida e as sementes viáveis obtidas são capazes de germinar e produzir plantas de cevada no campo, apesar da perda da principal forma de armazenamento de nitrogênio na semente. Estas sementes são particularmente úteis para a produção de alimentos e bebidas para o consumo por indivíduos com doença celíaca.
[0012] Assim, em um aspecto a presente invenção fornece um método para produzir um alimento ou bebida à base de malte, o método compreendendo misturar grão de cevada, ou malte, farinha ou produto integral produzidos do referido grão, com pelo menos outro ingrediente de alimento ou bebida, em que o grão, malte, farinha ou produto integral compreendem aproximadamente 25% ou menos do nível de hordeínas quando comparados ao grão de uma planta de cevada ou malte do tipo selvagem correspondente, farinha ou produto integral produzidos na mesma maneira do grão de uma planta de cevada do tipo selvagem correspondente, desse modo produzindo o alimento ou bebida baseada em malte.
[0013] Preferivelmente, o grão, malte, farinha ou produto integral compreendem aproximadamente 15% ou menos, aproximadamente 10% ou menos, aproximadamente 7,5% ou menos, aproximadamente 5% ou menos ou mais preferivelmente aproximadamente 2,5% ou menos do nível de hordeínas quando comparado ao grão da planta de cevada do tipo selvagem correspondente, ou malte do tipo selvagem, farinha ou produto integral produzidos na mesma maneira.
[0014] Os exemplos de uma planta de cevada do tipo selvagem incluem, mas não são limitados a, Bomi, Sloop, Carlsberg II, K8 ou L1.
[0015] Em outra modalidade, o grão compreende aproximadamente 25% ou menos, aproximadamente 20% ou menos, aproximadamente 15% ou menos, aproximadamente 10% ou menos, aproximadamente 7,5% ou menos, aproximadamente 5% ou menos ou mais preferivelmente aproximadamente 2,5% ou menos do nível de hordeínas B, C e/ou D ou quaisquer combinações dos mesmos quando comparado ao grão da planta de cevada do tipo selvagem correspondente. O malte, farinha ou produto integral podem compreender a mesma extensão de redução no nível de hordeínas B, C e/ou D ou quaisquer combinações dos mesmos.
[0016] Em outra modalidade, a farinha que compreende menos do que aproximadamente 0,4%, menos do que em aproximadamente 0,3%, menos do que em aproximadamente 0,2% e mais preferivelmente menos do que em aproximadamente 0,1% de hordeínas. Os níveis de hordeína na farinha produzida do referido grão podem ser determinados por qualquer técnica conhecida na técnica, tal como fracionamento de álcool.
[0017] Em uma modalidade, a grão tem um peso médio (peso de 100 grãos) de pelo menos aproximadamente 2,4 g. Preferivelmente, o grão tem um peso médio de aproximadamente 2,4 g a aproximadamente 6 g, mais preferivelmente um peso médio de aproximadamente 3,5 g a aproximadamente 6 g.
[0018] Em outra modalidade, o teor de amido do grão é pelo menos aproximadamente 50% (peso/peso). Mais preferivelmente, o teor de amido do grão é aproximadamente 50% a aproximadamente 70% (peso/peso). O teor de amido pode ser determinado usando qualquer técnica conhecida na técnica. Por exemplo, um método como fornecido no exemplo 4 pode ser usado.
[0019] Em uma modalidade adicional, a toxicidade celíaca de farinha produzida do grão é menos do que aproximadamente 50%, menos do que aproximadamente 25%, mais preferivelmente aproximadamente 10% ou menos, de farinha produzida do grão de uma planta de cevada do tipo selvagem correspondente. A toxicidade celíaca pode ser determinada usando qualquer técnica conhecida na técnica. Por exemplo, um método como fornecido no exemplo 1 pode ser usado.
[0020] Em ainda outra modalidade, o malte produzido do grão compreende menos do que aproximadamente 200 ppm de hordeínas, menos do que aproximadamente 125 ppm de hordeínas, mais preferivelmente menos do que aproximadamente 75 ppm de hordeínas. O teor de hordeína pode também ser determinado usando qualquer técnica conhecida na técnica. Por exemplo, um método como fornecido no exemplo 7 pode ser usado.
[0021] Em outra modalidade, pelo menos aproximadamente 50% do genoma do grão de cevada é idêntico ao genoma de um cultivar Sloop de cevada.
[0022] Preferivelmente, o grão é de uma planta que é homozigota pelo menos um, pelo menos dois, pelo menos três ou mais loci para uma variação genética que resulta em níveis reduzidos de pelo menos uma, pelo menos duas ou todas as três classes de hordeína das classes B, C e D quando comparado a uma planta de cevada do tipo selvagem correspondente. Mais preferivelmente, estas variações genéticas são alelas que deletam a maioria ou todos os genes de codificação de B-hordeína no loci de Hor2 e/ou um alelo de mutante no loci de lys3 de cevada.
[0023] Em uma modalidade, o grão é de uma planta não transgênica. Por exemplo, o grão pode ser de um cruzamento entre Riso 56 e Riso 1508 ou progênia do mesmo compreendendo as mutações hor2 e lys3, respectivamente, presentes nestas linhagens progenitoras. Preferivelmente, tais plantas de progênia compreendem um contexto genético substancialmente diferente para Riso 56 ou Riso 1508, por exemplo, compreendendo menos do que aproximadamente 25% do contexto genético destas linhagens progenitoras.
[0024] Em outra modalidade, a grão é de uma planta transgênica.
[0025] Uma modalidade de uma planta transgênica é uma planta que compreende um transgene que codifica um polinucleotídeo que subregula a produção de pelo menos uma hordeína no grão. Preferivelmente, o polinucleotídeo desta modalidade é um polinucleotídeo antisenso, um polinucleotídeo senso, um polinucleotídeo catalítico, um microRNA artificial ou uma molécula de RNA duplex que subregula uma expressão de um ou preferivelmente mais genes codificando hordeínas.
[0026] Outra modalidade de uma planta transgênica é uma planta que compreende um transgene codificando uma prolamina que é menos tóxica, ou preferivelmente não tóxica, a um indivíduo com doença celíaca. Um exemplo de uma prolamina que é não tóxica a um indivíduo com doença celíaca inclui, mas não é limitada a aveninas de aveia e zeínas de milho.
[0027] Em uma modalidade, o método compreende a produção de farinha ou produto integral do grão.
[0028] Em uma modalidade particularmente preferida, o método ainda compreende a produção de malte do grão. Em uma modalidade, o método ainda compreende o fracionamento de grão germinado seco em dois ou mais de uma fração de endosperma, uma fração de camada endotelial, uma fração de casca, uma fração de plúmula, e uma fração de radículas de malte; e combinar e misturar quantidades predeterminadas de duas ou mais das frações.
[0029] Com relação à produção de malte e cerveja, um componente importante da semente de cevada é o amido. Entretanto, os níveis de amido em mutantes de cevada com níveis diminuídos de hordeínas têm sido previamente mostrados por ter níveis reduzidos de amido que seriam esperados fazer a semente não apropriada para produzir o malte e cerveja. Os inventores ficaram particularmente surpresos por descobrir que as sementes de cevada onde a maioria, se não toda a produção de hordeína de cevada foi abolida, poderia ser usada para produzir o malte e cerveja com características apropriadas para produção comercial. Assim, um uma modalidade particularmente preferida, a bebida à base de malte é cerveja ou uísque, e o método compreende germinar o grão.
[0030] Em uma modalidade, a bebida à base de malte é a cerveja que compreende pelo menos aproximadamente 2%, mais preferivelmente pelo menos aproximadamente 4% de álcool. Preferivelmente, o álcool é etanol.
[0031] Em ainda uma modalidade adicional, a bebida à base de malte é a cerveja que compreende menos do que aproximadamente 1 ppm de hordeínas.
[0032] Em uma modalidade adicional, pelo menos aproximadamente 50% do grão germina dentro de 3 dias após a imbebição sob condições típicas como usadas na maltagem.
[0033] Os exemplos de produtos de alimento que podem ser produzidos usando os métodos da invenção incluem, mas não são limitados a farinha, amido, pães fermentados ou não fermentados, massa, noodles, cereais de café da manhã, alimentos de petisco, bolos, malte, pastéis ou alimentos contendo molhos a base de farinha.
[0034] Preferivelmente, o alimento ou bebida à base de malte é para o consumo humano. Em uma modalidade preferida adicional, após o consumo do alimento ou bebida, pelo menos um sintoma de doença celíaca não é desenvolvido por um indivíduo com a referida doença.
[0035] Em outro aspecto, a presente invenção fornece um método para produzir um alimento ou bebida à base de malte, o método compreendendo misturar malte compreendendo uma ou mais proteínas de grão de cevada e menos do que aproximadamente 200 ppm hordeínas e/ou farinha compreendendo uma ou mais proteínas de grão de cevada e menos do que aproximadamente 0,4% de hordeínas, pelo menos outro ingrediente de alimento ou bebida desse modo produzindo o alimento ou bebida à base de malte.
[0036] Em uma modalidade, o método compreende a obtenção do malte e/ou farinha.
[0037] Em ainda outro aspecto, a presente invenção fornece um método para produzir um alimento ou bebida à base de malte, o método compreendendo o grão de mistura de cevada, ou malte, farinha ou produto integral produzidos do referido grão, com pelo menos outro ingrediente de alimento ou bebida, desse modo produzindo o alimento ou bebida à base de malte, em que a farinha produzida do grão compreende menos do que aproximadamente 0,4% de hordeínas, e/ou malte produzido do grão compreende menos do que aproximadamente 200 ppm de hordeínas.
[0038] Em uma modalidade, o método compreende a obtenção de malte e/ou farinha.
[0039] Em outro aspecto, a presente invenção fornece uma planta de cevada que produz grão compreendendo aproximadamente 25% ou menos do nível de hordeínas quando comparado ao grão de uma planta de cevada do tipo selvagem correspondente.
[0040] Preferivelmente, o grão compreende aproximadamente 15% ou menos, aproximadamente 10% ou menos, aproximadamente 7,5% ou menos, aproximadamente 5% ou menos ou mais preferivelmente aproximadamente 2,5% ou menos do nível de hordeínas quando comparado ao grão de planta de cevada do tipo selvagem correspondente.
[0041] Os exemplos de uma planta de cevada do tipo selvagem incluem, mas não são limitados a Bomi, Sloop, Carlsberg II, K8 ou L1.
[0042] Em outra modalidade, o grão compreende aproximadamente 25% ou menos, aproximadamente 20% ou menos, aproximadamente 15% ou menos, aproximadamente 10% ou menos, aproximadamente 7,5% ou menos, aproximadamente 5% ou menos ou mais preferivelmente aproximadamente 2,5% ou menos do nível de hordeínas B, C e/ou D ou quaisquer combinações dos mesmos quando comparado ao grão da planta de cevada do tipo selvagem correspondente.
[0043] Em outra modalidade, a farinha produzida do grão compreende menos do que aproximadamente 0,4%, menos do que aproximadamente 0,3%, menos do que aproximadamente 0,2% e mais preferivelmente menos do que aproximadamente 0,1% hordeínas.
[0044] Em uma modalidade, o grão tem um peso médio (peso de 100 grãos) de pelo menos aproximadamente 2,4 g. Preferivelmente, o grão tem um peso médio de aproximadamente 2,4 g a aproximadamente 6 g, mais preferivelmente um peso médio de aproximadamente 3,5 g a aproximadamente 6 g.
[0045] Em outra modalidade, o teor de amido do grão é pelo menos aproximadamente 50% (peso/peso). Mais preferivelmente, o teor de amido do grão é aproximadamente 50% a aproximadamente 70% (peso/peso).
[0046] Em uma modalidade mais adicional, a toxicidade celíaca da farinha de grão produzida é menos do que aproximadamente 50%, menos do que aproximadamente 25%, mais preferivelmente aproximadamente 10% ou menos, da farinha produzida do grão de uma planta de cevada do tipo selvagem correspondente.
[0047] Em ainda outra modalidade, o malte produzido do grão compreende menos do que aproximadamente 200 ppm de hordeínas, menos do que aproximadamente 125 ppm de hordeínas, mais preferivelmente menos do que aproximadamente 75 ppm de hordeínas.
[0048] Em outra modalidade, pelo menos aproximadamente 50% do genoma do grão de cevada é idêntico ao genoma de um cultivar Sloop de cevada.
[0049] Preferivelmente, o grão é de uma planta que é homozigota a pelo menos um, pelo menos dois, pelo menos três ou mais loci para uma variação genética que resulta em níveis reduzidos de pelo menos uma, pelo menos duas ou todas as três classes de hordeína das classes B, C e D quando comparado a uma planta de cevada do tipo selvagem correspondente.
[0050] Em uma modalidade, o grão é de uma planta não transgênica. Por exemplo, o grão pode ser de um cruzamento entre Riso 56 e Riso 1508 ou progênia do mesmo compreendendo as mutações hor2 e lys3, respectivamente, presentes nestas linhagens progenitoras. Preferivelmente, tal grão compreende um contexto genético substancialmente diferente para Riso 56 e Riso 1508, por exemplo, compreendendo menos de 25% do contexto genético destas linhagens progenitoras.
[0051] Em outra modalidade, o grão é de uma planta transgênica.
[0052] Uma modalidade de uma planta transgênica é uma planta que compreende um transgene que codifica um polinucleotídeo que subregula a produção de pelo menos uma hordeína no grão. Preferivelmente, o polinucleotídeo desta modalidade é um polinucleotídeo antisenso, um polinucleotídeo senso, um polinucleotídeo catalítico, um microRNA artificial ou uma molécula de RNA duplex que subregula a expressão de um ou preferivelmente mais genes codificando hordeínas.
[0053] Outra modalidade de uma planta transgênica é uma planta que compreende um transgene codificando uma prolamina que é menos tóxica, preferivelmente não tóxica a um indivíduo com doença celíaca. Um exemplo de uma prolamina que é não tóxica a um indivíduo com doença celíaca inclui, mas não é limitada à avenina de aveia.
[0054] Em uma modalidade adicional, pelo menos aproximadamente 50% do grão germina dentro de 3 dias após a imbebição sob condições típicas como usadas na maltagem.
[0055] Em outro aspecto, a presente invenção fornece uma planta de cevada que produz o grão, em que a farinha produzida do grão compreende menos do que aproximadamente 0,4% hordeínas, e/ou o malte produzido do grão compreende menos do que aproximadamente 200 ppm de hordeínas.
[0056] Em outro aspecto, a presente invenção fornece o grão de uma planta de cevada da invenção.
[0057] Em um aspecto adicional, a presente invenção fornece um método para produzir o grão de cevada, o método compreendendo: a) crescer uma planta de cevada da invenção, b) colher o grão, e c) opcionalmente processar o grão.
[0058] Preferivelmente, as plantas são crescidas em uma escala comercial em um campo. Por exemplo, em uma modalidade, o método compreende o crescimento de pelo menos 1.000, mais preferivelmente pelo menos 5.000, plantas em um campo em uma área de pelo menos um hectare (10.000 m2).
[0059] Também é fornecido um método para produzir a farinha, produto integral, amido ou outro produto obtido do grão, método compreendendo: d) obter o grão da invenção, e e) processar o grão para produzir a farinha, produto integral, amido ou outro produto.
[0060] Em um aspecto adicional, a presente invenção fornece um produto produzido de uma planta de cevada da invenção ou grão da invenção.
[0061] Em uma modalidade, o produto é um alimento ou produto de bebida à base de malte.
[0062] Preferivelmente, o produto de bebida à base de malte é cerveja ou uísque.
[0063] Em outra modalidade, o produto é um produto não alimentício, preferivelmente compreendendo amido ou consistindo de pelo menos aproximadamente 50% de amido. Os exemplos incluem, mas não são limitados a filmes, revestimentos, adesivos, papel, materiais de construção e materiais de embalagem, ou produtos de não amido, tais como etanol.
[0064] Em ainda outro aspecto, a presente invenção fornece um alimento ou bebida à base de malte produzido usando um método da invenção.
[0065] Em uma modalidade, a bebida à base de malte é cerveja compreendendo pelo menos aproximadamente 2%, mais preferivelmente pelo menos aproximadamente 4% de álcool. Preferivelmente, o álcool é etanol.
[0066] Em ainda uma modalidade adicional, a bebida à base de malte é cerveja compreendendo menos do que aproximadamente 1 ppm de hordeínas.
[0067] Em outro aspecto, a presente invenção fornece cerveja compreendendo uma ou mais proteínas de grão de cevada e menos do que aproximadamente 1 ppm de hordeínas. Em uma modalidade, a cerveja tem menos do que aproximadamente 0,05 ppm de hordeínas.
[0068] Preferivelmente, a cerveja compreende pelo menos aproximadamente 2%, mais preferivelmente pelo menos aproximadamente 4% de álcool. Preferivelmente, o álcool é etanol.
[0069] Os exemplos de proteínas de grão de cevada incluem, mas não são limitados à proteína 1 de cevada de lipídio de 9kDa (LTP1) e proteína Z.
[0070] Em outro aspecto, a presente invenção fornece farinha compreendendo uma ou mais proteínas de grão de cevada e menos do que aproximadamente 0,4% de hordeínas.
[0071] Em uma modalidade, a farinha compreende menos do que aproximadamente 0,3%, menos do que aproximadamente 0,2% e mais preferivelmente menos do que aproximadamente 0,1% de hordeínas.
[0072] Preferivelmente, a farinha compreende menos do que aproximadamente 7 mg, mais preferivelmente menos do que aproximadamente 5 mg, de proteína solúvel em álcool/g de peso seco de farinha.
[0073] Em ainda outro aspecto, a presente invenção fornece malte compreendendo uma ou mais proteínas de grão de cevada e menos do que aproximadamente 200 ppm de hordeínas.
[0074] Em uma modalidade, o malte compreende menos do que aproximadamente 125 ppm de hordeínas, mais preferivelmente menos do que aproximadamente 75 ppm de hordeínas.
[0075] Em um aspecto adicional, a presente invenção fornece um método para identificar o grão de cevada que pode ser usado para produzir um alimento e/ou bebida à base de malte para o consumo por um indivíduo com doença a celíaca compreendendo: f) obter um ou mais dos seguintes materiais: i) uma amostra de uma planta capaz de produzir o referido grão, ii) o grão, iii) malte produzido do grão, e/ou iv) um extrato do referido grão, g) analisando o material da etapa a) por pelo menos uma hordeína e/ou pelo menos um gene codificando uma hordeína, em que quanto maior a quantidade de hordeínas produzidas pelo grão menos apropriado é o grão para produzir um alimento e/ou bebida à base de malte para o consumo por um indivíduo com doença celíaca.
[0076] Em uma modalidade, a amostra é grão e a etapa b) compreende a análise do material para hordeínas B e/ou C. Isto pode ser realizado usando qualquer técnica conhecida na técnica, por exemplo, usando um método imunológico, tal como ensaios de ELISA. O método descrito no Exemplo 1 pode ser usado. Em uma modalidade, a etapa b) compreende oralmente administrar o material da etapa a) a um indivíduo com doença celíaca e determinar a imunoreatividade de células de T obtidas do indivíduo para um ou mais hordeínas de cevada.
[0077] Em outra modalidade, o material de amostra da etapa a) compreende DNA genômico e a etapa b) compreende detectar a ausência de um ou mais genes de hordeína funcionais. Novamente, isto pode ser realizado usando qualquer técnica conhecida na técnica. Por exemplo, realizando uma etapa de amplificação de gene de acordo com o exemplo 9.
[0078] Em uma modalidade, o método compreende a etapa de selecionar uma planta de cevada, um grão ou malte de acordo com a invenção de uma pluralidade de plantas, grãos ou maltes para a propagação ou uso. Tal seleção é baseada, diretamente ou indiretamente, na toxicidade celíaca reduzida do material.
[0079] Em um aspecto adicional, a presente invenção fornece um método para prevenir ou reduzir a incidência ou severidade de doença celíaca em um indivíduo, o método compreendendo oralmente administrar ao indivíduo um alimento ou uma bebida à base de malte da invenção, ou um grão da invenção. A incidência ou severidade reduzida da doença neste contexto é compreendida por ser relativa a administração de uma quantidade igual de alimento ou bebida preparado da cevada do tipo selvagem. O alimento ou bebida pode ser usado para fornecer nutrientes, ou uma quantidade aumentada de nutrientes, a um indivíduo tendo a doença celíaca enquanto diminui o risco de provocar sintomas de doença.
[0080] Em outro aspecto, a presente invenção fornece o uso de um alimento ou bebida à base de malte da invenção, ou um grão da invenção, para a fabricação de um medicamento para oralmente administrar a um indivíduo nutrientes enquanto ao mesmo tempo previne ou reduz a incidência ou severidade de doença celíaca.
[0081] Como será aparente, as características preferidas de um aspecto da invenção são aplicáveis a qualquer outro aspecto da invenção.
[0082] Através deste relatório descritivo a palavra “compreender”, ou variações, tais como “compreende” ou “compreendendo”, será compreendido para implicar a inclusão de um elemento, inteiro ou etapa, ou grupo de elementos, inteiros ou etapas indicadas, mas não a exclusão de qualquer outro elemento, inteiro ou etapa, ou grupo de elementos, inteiros ou etapas.
[0083] A invenção é descrita em seguida pelos seguintes exemplos não limitantes e em referência às figuras acompanhantes.
BREVE DESCRIÇÃO DOS DESENHOS ACOMPANHANTES
[0084] Figura 1: FPLC de fase reversa de extratos de prolamina totais, mostrando os cromatogramas de A280nm de trigo (a), cevada (b), aveias (c); milho (d) ou um gradiente em branco (e). As prolaminas equivalentes a 0,2g de farinha foram carregadas. DTT oxidada é mostrado (DTTox); cromatogramas foram deslocados para maior clareza.
[0085] Figura 2: FPLC de fase reversa de hordeínas. Um cromatograma representativo mostrando a A280nm (linha contínua) e composição solvente (linha quebrada) durante o isolamento da fração de hordeína 1 (#1), 2 (#2), 3 (#3), 4 (#4), 5 (#5), ou 6 (#6) de um extrato de cevada. As frações indicadas foram escolhidas como mostrado (linha em negrito) das injeções sequenciais.
[0086] Figura 3: Análise de 20 μg de frações de hordeína #1-6 por SDS-PAGE, manchando o gel com 0,06% Coomassie Blue G250. A posição de padrões de peso molecular (em kDa, BenchMark, Invitrogen) é indicada na linha de mão esquerda.
[0087] Figura 4: Estimulação de produção de IFN-y em células T, isolada dos celíacos seis dias após um desafio dietético, por preparações de prolamina total de cevada, trigo, aveias ou milho na presença (•, n=21), ou ausência (o, n=13) de pré-tratamento de tTG. As colônias de IFN-y positivas foram contadas e apresentadas como médias de UFC ± S.E. As barras de erro não são mostradas quando S.E. foi menor do que símbolos.
[0088] Figura 5: Estimulação de produção de IFN-y em células T, isolada dos celíacos seis dias após um desafio dietético, por frações de hordeína #1, 2, 3, 4, 5, e 6, na presença (•, n=21), ou ausência (o, n=13) de pré- tratamento de tTG. As colônias de IFN-y positivas foram contadas e apresentadas como médias UFC ± S.E. As barras de erro não são mostradas quando S.E. foi menor do que símbolos.
[0089] Figura 6: Cromatogramas de HPLC de fase reversa analíticos das frações de hordeína isoladas. Os cromatogramas representativos mostrando o A280nm durante o HPLC das frações de hordeína #1, 2, 3, 4, 5, 6 purificadas da cevada. Para a comparação os cromatogramas são mostrados para a cevada do tipo selvagem (Himalaya) mostrando a eluição (linha contínua) de hordeínas D, C, e B, bem como o mutante R56 que acumula principalmente hordeínas C.
[0090] Figura 7: Caracterização dos prolaminas em Riso56 e Riso1508 por SDS-PAGE e western blotting. 20 μg de prolamina, purificada como no exemplo 1, da linhagem de cevada indicada foram incubados por 30 min em temperatura ambiente em um tampão contendo ureia 6,6 M, 2% (peso/vol) SDS, 1% (peso/vol) DTT, Tris-HCl 62,5 mM (pH 6,8), e 0,01% (peso/vol) bromofenol azul e carregado em duplicata em géis de acrilamida 12% e feitos eletroforese em 200 V por 40 min. O gel foi enxaguado no tampão de transferência contendo 192 mM de glicina, 25 mM Tris-base, e 20% (vol/vol) metanol por 10 min e transferidos para nitrocelulose (Amersham Hybond C+) em 100 V por 1 h. A membrana esquerda foi tingida em 0,2% (peso/vol) Ponceau S em 3% (peso/vol) ácido tricloroacético, 3% de ácido 5-sulfosalicílico e destingido momentaneamente em água; a membrana direita foi bloqueada em 5% de nata em PBST por 1 h, então incubado com o anticorpo monoclonal de camundongo 12224 (Skerrit, 1988) em PBST, lavado em PBST por 3 x 10 minutos, incubado em anti- rato-HRP de carneiro (Selenius) em PBST, lavado em PBST 3 x 5 min, incubado no reagente ECL Amersham como nas instruções dos fabricantes, e exposto a Amersham Hyperfilm. MAb 12224 foi criado contra um extrato de glutenina total e detecta todas hordeínas e prolaminas (Skerrit, 1988).
[0091] Figura 8: FPLC de fase reversa de extratos de hordeína em Riso56 e Riso1508 comparados ao do tipo selvagem Bomi e Carlsberg II. As hordeínas foram purificadas das linhagens indicadas como no exemplo 1, e uma quantidade equivalente a 0,2 g de farinha foi injetada em uma coluna de FPLC usando o primeiro método de FPLC no exemplo 1. O tempo de eluição de C-hordeína (C-Hor) e B- hordeína (B-Hor) é indicado.
[0092] Figura 9: SDS-PAGE representativo de proteínas solúveis em álcool carregadas em uma base por semente. Os extratos de prolamina (10 μl) das sementes de cevada F2 individuais de um cruzamento entre Riso1508 e Riso56 foram extraídos como descrito acima. As posições de padrões de proteína de 30, 50, 70 e 100 kDa são indicadas sobre a linha esquerda. Os perfis de proteína das linhagens progenitoras Riso1508 e Riso56, e o tipo selvagem (Bomi) são também mostrados. Seis linhas de nulos duplos putativos contêm a proteína muito pequena (nula), outras seis linhas contêm níveis muito reduzidos de proteína (reduzida).
[0093] Figura 10: SDS-PAGE representativo de proteínas solúveis em álcool carregadas em uma base de proteína igual. As amostras contendo 20 μg de proteína solúvel em álcool extraído das sementes de cevada F2 individuais feitas eletroforese e gel tingidas com azul de Coomassie. As amostras das linhagens progenitoras (Riso 1508 e Riso 56) e tipo selvagem (Bomi) são também feitas. As linhas mais externas e centrais (10 kDa) continham padrões de proteína de pesos moleculares conhecidos, as posições para faixas de 30, 50, 70 e 100 kDa são indicados.
[0094] Figura 11: Cromatogramas de RP-FPLC de extratos solúveis em álcool das sementes de cevada F3. As proteínas solúveis em álcool foram extraídas das sementes F3 individuais como descrito; os sobrenadantes de duas sementes foram combinados de cada linhagem e 50 μl injetados em uma coluna FPLC de fase reversa e eluída como descrito no exemplo 1.
[0095] Figura 12: O teor de proteína solúvel em água (A), solúvel em sal (B), solúvel em álcool (C) e solúvel em ureia (D) em duplicatas de amostras de farinha da cevada do tipo selvagem (Sloop, Carlsberg II, Bomi), os únicos progenitores nulos (Riso 56, Riso 1508) e sementes F4 das plantas de linhagens J4, J1, BB5, G1, 5RB foi determinada como no exemplo 4. O teor de proteína extraível total (E) foi determinado somando o teor das frações individuais. O teor de proteína total foi também estimado pela análise elementar de acordo com o método de Dumas (F). Os teores de proteína são mostrados como a média + SE.
[0096] Figura 13: A toxicidade celíaca de hordeínas purificadas das várias amostras de farinha foi determinada com células T isoladas dos celíacos, 6 dias pós-desafio, como no exemplo 5, e a média de unidades formadoras de colônia (UFC) + SE traçado contra o peso fresco de farinha. Para maior clareza, UFC médios são mostrados somente para hordeínas purificadas da cevada do tipo selvagem (Sloop) ou a linhagem nula dupla (G1) na presença (+tTG) ou ausência (-tTG) da enzima, transglutaminase de tecido (A). Em todos os casos o tratamento com tTG aumentou a toxicidade de hordeínas como esperado para doença celíaca. UFC são também mostradas para hordeínas tratadas com tTG (b) purificadas das amostras de farinha de cevada do tipo selvagem (Sloop), os únicos progenitores nulos (R56, R1508) e sementes F4 (4BH).
[0097] Figura 14: Sequências de gene específicas para o gene de controle (gamma3-Hor), ou o gene de B- hordeína (B-Hor) foram amplificados dos extratos de DNA das plântulas F4 individuais das linhagens 9RE, 4BH ou linhagem progenitora R56 como no exemplo 9.
DESCRIÇÃO DETALHADA DA INVENÇÃO
Técnicas e definições gerais
[0098] A menos que especificamente definido de outra maneira, todos os termos técnicos e científicos usados aqui serão tomados para ter o mesmo significado como geralmente compreendido por um de habilidade ordinária na técnica (por exemplo, no cruzamento de planta, tecnologia de alimento, cultura de célula, genética molecular, imunologia, química de proteína, e bioquímica).
[0099] A menos que de outra maneira indicado, a proteína recombinante, cultura de célula, e técnicas imunológicas utilizadas na presente invenção são procedimentos padrões, conhecidos aos hábeis na técnica. Tais técnicas são descritas e explicadas através de toda a literatura nas fontes, tais como J. Perbal, A Practical Guide to Molecular Cloning, John Wiley and Sons (1984), J. Sambrook e col., Molecular Cloning: A loboratory Manual, Cold Spring Harbour Laboratory Press (1989), T.A. Brown (editor), Essential Molecular Biology: A Practical Approach, volumes 1 e 2, IRL Press (1991), D.M. Glover e B.D. Hames (editores), DNA Cloning: A Practical Approach, volumes 1-4, Press IRL (1995 e 1996), e F.M. Ausubel e col., (editores), Current Protocols in Molecular Biology, Greene Pub. Associates and Wiley-Interscience (1988, incluindo todas as atualizações até o presente), Ed Harlow and David Lane (editores) Antibodies: A Manual Laboratory, Cold Spring Harbour Laboratory, (1988), e J.E. Coligan e col., (editores) Current Protocols in Immunology, John Wiley & Sons (incluindo todas as atualizações até o presente).
[00100] Como usado aqui, o termo “cevada” refere-se a qualquer espécie do gênero Hordeum, incluindo progenitores do mesmo, bem como a progênia do mesmo produzida por cruzamento com outras espécies. Uma forma preferida de cevada é a espécie Hordeum vulgare.
[00101] A doença celíaca é um distúrbio autoimune do intestino delgado que ocorre em indivíduos geneticamente pré-dispostos em todos os grupos de idade após a primeira infância. Afeta aproximadamente 1% de populações indoeuropéias, embora não significativamente diagnosticada. A doença celíaca é causada por uma reação à gliadina, uma proteína de glúten encontrada no trigo (e proteínas similares de Triticeae que inclui outros cultivares, tais como cevada e centeio). Sob exposição à gliadina, a enzima transglutaminase de tecido modifica a proteína, e o sistema imune reage cruzadamente com o tecido do intestino, causando uma reação inflamatória. Isto conduz ao achatamento do revestimento do intestino delgado, que interfere com a absorção de nutrientes. O único tratamento eficaz é uma dieta sem glúten por toda a vida. Esta condição tem diversos outros nomes, incluindo: doença celíaca (com ligadura), enteropatia glúten-induzida, doença não tropical, doença endémica, enteropatia de glúten ou enteropatia sensível ao glúten, e intolerância ao glúten. Os sintomas da doença celíaca variam extensamente de pessoa para pessoa. Os sintomas da doença celíaca podem incluir um ou mais dos seguintes; gás, inchaço e dor abdominal recorrentes, diarreia crônica, constipação, palidez, fezes fedorentas ou gordurosas, perda de peso/ganho de peso, fadiga, anemia inexplicada (uma baixa contagem de glóbulos vermelhos causando fadiga), dor óssea ou articular, osteoporose, osteopenia, mudanças comportamentais, formigamento dormente nos pés (do dano no nervo), câimbras musculares, ataques, períodos menstruais perdidos (frequentemente por causa da perda de peso excessiva), infertilidade, aborto recorrente, crescimento atrasado, falha de prosperar em infantes, bolhas brancas dentro da boca chamada úlceras aftosas, descoloração de dente ou perda de esmalte, e irritação de pele chamada dermatite herpetiforme. Alguns dos sintomas mais comuns incluem: cansaço, diarreia intermitente, dor abdominal ou cólicas, indigestão, flatulência, inchamento; e perda de peso. A doença celíaca pode ser diagnosticada, por exemplo, como descrito em WO 01/025793.
[00102] Como usado aqui, o termo “não tóxico a um indivíduo com doença celíaca” refere-se ao consumo de alimento ou uma bebida não resultando do desenvolvimento de um sintoma de doença celíaca em um indivíduo sofrendo da referida doença. Como descrito aqui, o alimento ou bebida feita de uma planta de cevada do tipo selvagem correspondente resulta em sintomas da doença.
[00103] Os termos “semente” e “grão” são usados permutavelmente aqui. “Grão” geralmente refere-se ao grão maduro, colhido, mas pode também se referir ao grão após ser processado como, por exemplo, trituração ou polimento, onde a maioria dos grãos permanece intacta, ou após imbebição ou germinação, de acordo com o contexto. O grão maduro tem geralmente um teor de umidade de menos do que aproximadamente 18-20%. O grão de cevada do tipo selvagem (grão integral) contém geralmente 9-12% de proteína e aproximadamente 30-50% destas são prolamina, tipicamente 35%, então o grão de cevada do tipo selvagem tem aproximadamente 3-4% de prolamina por peso. As prolaminas são encontradas quase exclusivamente no endosperma, que é aproximadamente 70% de peso do grão inteiro.
[00104] Como usado aqui, o termo planta de cevada do “tipo selvagem correspondente” se refere a uma planta que compreende pelo menos 50%, mais preferivelmente pelo menos 75%, mais preferivelmente pelo menos 95%, mais preferivelmente pelo menos 97%, mais preferivelmente pelo menos 99%, e mais preferivelmente 99,5% do genótipo de uma planta da invenção, mas produz o grão com níveis de hordeína não modificados. Em uma modalidade, a planta de cevada do “tipo selvagem correspondente” é um cultivar usado em experimentos de cruzamento de planta para introduzir variantes genéticas que resultam em produção de hordeína reduzida no grão. Em outra modalidade, a planta de cevada do “tipo selvagem correspondente” é um cultivar progenitor em que um transgene foi introduzido que reduz a produção de hordeína no grão. Em uma modalidade adicional, a planta de cevada do “tipo selvagem correspondente” é um cultivar em que é usado até hoje para a produção comercial do grão de cevada, tal como, mas não limitado a, Bomi, Sloop, Carlsberg II, K8, L1, Vlamingh, Stirling, Hamelin, Schooner, Baudin, Gairdner, Buloke, WI3586-1747, WI3416, Flagship, Cowabbie, Franklin, SloopSA, Sloop Vic, Quasar, VB9104, Grimmett, Cameo*Arupo 31-04, Prior, Schooner, Unicom, Harrington, Torrens, Galleon, Morex, Dhow, Capstan, Fleet, Keel, MAritime, Yarra, Dash, Doolup, Fitzgerald, Molloy, Mundah, Onslow, Skiff, Unicorn, Yagan, Chebec, Hindmarsh, Chariot, Diamant, Koral, Rubin, Bonus, Zenit, Akcent, Forum, Amulet, Tolar, Heris, Maresi, Landora, Caruso, Miralix, Wikingett Brise, Caruso, Potter, Pasadena, Annabell, Maud, Extraxt, Saloon, Prestige, Astoria, Elo, Cork, Extract, Laura. Em uma modalidade, a planta de cevada do “tipo selvagem correspondente” produz o grão com níveis de hordeína não modificados devido a isso compreende um complemento total de genes de hordeína funcionais codificando proteínas de hordeína funcionais, incluindo B, C, D e Y-hordeínas codificadas por loci Hor2, Hor1, Hor3 e Hor5.
[00105] Como usado aqui, o termo “uma ou mais proteínas de grão de cevada” se refere às proteínas naturais produzidas pelo grão de cevada. Os exemplos de tais proteínas são conhecidos aos hábeis na técnica. Exemplos específicos incluem, mas não são limitados a albuminas de cevada, tais como proteína de transferência de lipídio 1 de 9kDa (LTP1) (veja Douliez e col. (2000) para uma revisão e Acesso de prot. Suíço N°. P07597 como um exemplo) e proteína Z (veja Brandt e col. (1990) e N°. de Acesso de Genbank P06293), incluindo formas (maduras) processadas do mesmo, bem como os formas e/ou fragmentos desnaturados produzidos dos mesmos como resultado da produção de malte, farinha, produto integral, alimento ou bebida à base de malte da invenção.
[00106] Como usado aqui, o termo “malte” é usado para se referir ao malte de cevada, “farinha” para se referir à farinha de cevada, “produto integral” para se referir ao produto integral de cevada, e “cerveja” para se referir à cerveja de cevada. Mais especificamente, uma fonte de malte, farinha, cerveja, produto integral, produto alimentício etc. da invenção são de processamento (por exemplo, trituração e/ou fermentação) de grão de cevada. Estes termos incluem malte, farinha, cerveja, produto integral, produto alimentício etc. produzidos de uma mistura de grãos. Em uma modalidade preferida, pelo menos 50% do grão usado para produzir o malte, farinha, cerveja, produto integral, produto alimentício etc. são grãos de cevada.
[00107] O termo “planta” como usado aqui como um substantivo se refere a uma planta inteira, tal como, por exemplo, uma planta crescendo em um campo para a produção de cevada comercial. Uma “parte de planta” se refere às estruturas vegetativas de planta (por exemplo, folhas, caules), raízes, órgãos florais/estruturas, semente (incluindo embrião, endosperma, e revestimento da semente), tecido de planta (por exemplo, tecido vascular, tecido de sustentação, e similares), células, grânulos de amido ou progênia dos mesmos.
[00108] Uma “planta transgênica”, “planta geneticamente modificada” ou variações das mesmas referem- se a uma planta que contém um elemento de gene (“transgene”) não encontrado em uma planta do tipo selvagem da mesma espécie, variedade ou cultivar. Um “transgene” como referido aqui tem o significado normal na técnica de biotecnologia e inclui uma sequência genética que foi produzida ou alterada pela tecnologia de DNA ou RNA recombinante e que foi introduzida na célula de planta. O transgene pode incluir sequências genéticas derivadas de uma célula de planta. Tipicamente, o transgene foi introduzido na planta pela manipulação humana, tal como, por exemplo, pela transformação, mas qualquer método pode ser usado como um de habilidade na técnica reconhece.
[00109] A “molécula de ácido nucleico” refere-se a um polinucleotídeo, tal como, por exemplo, DNA, RNA ou oligonucleotídeos. Pode ser DNA ou RNA de origem genômica ou sintética, de fita dupla ou fita simples, e combinado com carboidrato, lipídios, proteína, ou outros materiais para realizar uma atividade particular definida aqui.
[00110] “Operavelmente ligado” como usado aqui refere-se a um relacionamento funcional entre segmentos de dois ou mais ácidos nucleicos (por exemplo, DNA). Tipicamente, refere-se ao relacionamento funcional do elemento regulatório transcricional (promotor) a uma sequência transcrita. Por exemplo, um promotor é operavelmente ligado a uma sequência de codificação, tal como um polinucleotídeo definido aqui, se estimula ou modula a transcrição da sequência de codificação em uma célula apropriada. Geralmente, os elementos regulatórios transcricionais de promotor que são operavelmente ligados a uma sequência transcrita são fisicamente contíguos à sequência transcrita, isto é, eles atuam em cis. Entretanto, alguns elementos regulatórios transcricionais, tais como melhoradores, não precisam ser fisicamente contíguos ou localizados em grande proximidade às sequências de codificação cuja transcrição melhoram.
[00111] Como usado aqui, o termo “gene” deve ser considerado em seu contexto mais amplo e inclui as sequências de desoxiribonucleotídeo compreendendo a região de codificação de proteína de um gene estrutural e incluindo sequências situadas adjacentes à região de codificação em ambas extremidades 5’ e 3’ sobre pelo menos aproximadamente 2 kb na extremidade e que são envolvidas na expressão do gene. As sequências que são localizadas 5’ da região de codificação e que estão presentes no mRNA são referidas como sequências 5’ não traduzidas. As sequências que são localizadas 3’ ou a jusante da região de codificação e que estão presentes no mRNA são referidas como sequências 3’ não traduzidas. O termo “gene” engloba cDNA e formas genômicas de um gene. Uma forma genômica ou clone de um gene contém a região de codificação que pode ser interrompida com as sequências não codificantes denominadas “íntrons” ou “regiões de intervenção” ou “sequências de intervenção”. Os íntrons são segmentos de um gene que são transcritos no RNA nuclear (hnRNA); os íntrons podem conter elementos regulatórios, tais como melhoradores. Os íntrons são removidos ou “emendados” do transcrito nuclear ou preliminar; os íntrons estão, portanto, ausentes no transcrito de RNA mensageiro (mRNA). As funções de mRNA durante a tradução para especificar a sequência ou ordem de aminoácidos em um polipeptídeo nascente. O termo “gene” inclui uma molécula de fusão ou sintética codificando toda ou parte das proteínas da invenção descritas aqui e uma sequência de nucleotídeo complementar a qualquer uma da acima.
[00112] Como usado aqui, o termo “outro ingrediente de alimento ou bebida” refere-se a qualquer substância apropriada para o consumo por um animal, preferivelmente qualquer substância apropriada para consumo por um humano. Os exemplos incluem, mas não são limitados a água, grão de outras espécies de planta, açúcar, etc.
[00113] Como usado aqui, o termo “variação genética que resulta em níveis reduzidos de pelo menos uma hordeína” se refere a qualquer polimorfismo de uma planta de cevada que reduz a produção de hordeína. A variação genética pode ser, por exemplo, uma deleção de um gene de hordeína ou parte do mesmo, ou uma mutação que reduz a transcrição de gene de cevada. Os exemplos de tais variações genéticas estão presentes em Riso 56, Riso 527 e Riso 1508. Consequentemente, tais plantas podem ser usadas para os métodos da invenção. Além disso, uma planta da invenção pode ser um cruzamento entre quaisquer destes mutantes de cevada. Em uma modalidade preferida, uma planta da invenção é um cruzamento entre Riso 56 e Riso 1508 ou progênia do mesmo compreendendo as mutações hor2 e lys3 presentes nestas linhagens. Em uma modalidade, a planta não é um cruzamento entre Riso 527 e Riso 1508.
[00114] Como usado aqui, a menos que indicado ao contrário, a palavra “aproximadamente” se refere a qualquer faixa razoável em luz do valor em pergunta. Em uma modalidade preferida, o termo “aproximadamente” se refere a +/-10%, mais preferivelmente +/-5%, do valor especificado.
Prolaminas e Hordeínas
[00115] As prolaminas de cereal (conhecidas como gliadinas em trigo, hordeínas em cevada, secalinas em centeio, aveninas em aveia, e zeínas em milho) são as proteínas de armazenamento de endosperma principais em todos os grãos de cereal, com a exceção de aveias e arroz (Shewry e Halford, 2002). As hordeínas representam 35-50% da proteína total em sementes de cevada (Jaradat, 1991). São classificadas em quatro grupos, A (também conhecido como Y hordeína) , B, C, e D, em ordem de mobilidade decrescente (Field e col., 1982). As B hordeínas são a principal fração de proteína, diferindo das C hordeínas em seu teor de enxofre (Kreis e Shewry, 1989). As B hordeínas contam por 70-80% do total e C hordeínas por 10-20% (Davies e col., 1993). As A hordeínas não são geralmente consideradas por serem uma fração de armazenamento visto que as D hordeínas são homólogas às gluteninas de alto peso molecular. As hordeínas, junto com o resto das prolaminas relacionadas a cereal, não são expressas no próprio embrião zigótico, ao contrário de outras proteínas de armazenamento, tais como napinas; são acreditadas por ser expressas exclusivamente no endosperma de amido durante os estágios médio-a-tardio do desenvolvimento de semente.
[00116] Exemplos de sequências de aminoácido de hordeína de cevada (fornecidas com o N° de Acesso; descrição em NCBI; gi detalhes) incluem, mas não são necessariamente limitados a: 1103203A; hordeína B; gi|224385|prf||1103203A[224385]; 1103203B; hordeína B; gi|224386|prf||1103203B[224386] 1103203C; hordeína C; gi|224387|prf||1103203C[224387] 1210226A; hordeína B1; gi|225171|prf||1210226A[225171] 1307151A; hordeína C; gi|225588|prf||1307151A[225588] 1307151B; hordeína C; gi|225589|prf||1307151B[225589] 1604464A; gama hordeína; gi|226755|prf||1604464A [226755] AAA32942; C-hordeína; gi|167016|gb|AAA32942.1|[167016] AAA32943; proteína de armazenamento de C-hordeína; gi|167018|gb|AAA32943.1|[167018] AAA32944; proteína de armazenamento de C-hordeína; gi|167020|gb|AAA32944.1|[167020] AAA32955; precursor de gama-1 hordeína; gi|167042|gb|AAA32955.11[167042] AAA32967; hordeína; gi]530093|gb|AAA32967.1|[530093] AAA92333; C hordeína; gi|893242|gb|AAA92333.1|[893242] AAB28161; C-hordeína [Hordeum vulgare]; gi|442524)gb| AAB28161.1||bbm|324752|bbs|139926[442524] AAB71678; proteína de armazenamento de semente [Hordeum vulgare]; gi|2454599|gb|AAB71678.1|[2454599] AAB71679; proteína de armazenamento de semente [Hordeum vulgare]; gi|2454600|gb|AAB71679.1|[2454600] AAP31050; globulina [Hordeum vulgare]; gi |30421166|gb|AAP31050.1|[30421166] AAP31051; D-Hordeína [Hordeum vulgare]; gi |30421167|gb|AAP31051.1|[30421167] gi AAQ63842; gama 3 hordeína |34329251|gb|AAQ63842.1|[34329251] [Hordeum chilense]; gi AAQ63843; gama 3 hordeína |34329253|gb|AAQ63843.1|[34329253] [Hordeum chilense]; gi AAQ63844; gama 3 hordeína |34329255|gb|AAQ63844.1|[34329255] [Hordeum chilense]; gi AAQ63845; gama 3 hordeína |34329257|gb)AAQ63845.1|[34329257] [Hordeum chilense]; gi AAQ63846; gama 3 hordeína |34329259|gb|AAQ63846.1|[34329259] [Hordeum chilense]; gi AAQ63847; gama 3 hordeína |34329261|gb|AAQ63847.1|[34329261] [Hordeum chilense]; gi AAQ63848; gama 3 hordeína |34329263|gb|AAQ63848.1|[34329263] [Hordeum chilense]; gi AAQ63849; gama 3 hordeína |34329265|gb|AAQ63849.1|[34329265] [Hordeum chilense]; gi AAQ63850; gama 3 hordeína |34329267|gb|AAQ63850.1|[34329267] [Hordeum chilense]; gi AAQ63851; gama 3 hordeína |34329269|gb|AAQ63851.11[34329269] [Hordeum chilense]; AAQ63852; gama 3 hordeína [Hordeum chilense]; gi |34329271|gb AAQ63853; |AAQ63852.1| gama 3 [34329271] hordeína [Hordeum chilense]; gi |34329273|gb AAQ63854; |AAQ63853.1| gama 3 [34329273] hordeína [Hordeum chilense]; gi |34329275|gb AAQ63855; |AAQ63854.11 gama 3 [34329275] hordeína [Hordeum chilense]; gi |34329277|gb AAQ63866; |AAQ63855.1| gama 3 [34329277] hordeína [Hordeum chilense]; gi |34329299|gb AAQ63867; |AAQ63866.1| gama 3 [34329299] hordeína [Hordeum chilense]; gi |34329301|gb AAQ63868; |AAQ63867.1| gama 3 [34329301] hordeína [Hordeum chilense]; gi |34329303|gb AAQ63869; |AAQ63868.1| gama 3 [34329303] hordeína [Hordeum chilense]; gi |34329305|gb AAQ63870; |AAQ63869.1| gama 3 [34329305] hordeína [Hordeum chilense]; gi |34329307|gb AAQ63871; |AAQ63870.1| gama 3 [34329307] hordeína [Hordeum chilense]; gi]34329309|gb AAQ63872; |AAQ63871.1| gama 3 [34329309] hordeína [Hordeum chilense]; gi |34329311|gb AAU06227; |AAQ63872.1| B hordeína [34329311] [Hordeum brevisubulatum subsp. turkestanicum]; gi|51556914|gb|AAU06227.1][51556914] AAU06228; B hordeína [Hordeum brevisubulatum subsp. turkestanicum]; gi|51556916|gb|AAU06228.1|[51556916] AAU06229; B hordeína [Hordeum brevisubulatum subsp. turkestanicum]; gi|51556918|gb|AAU06229.1|[51556918] AAZ76368; B hordeína [Hordeum vulgare subsp. vulgare]; gi|73427781|gb|AAZ76368.1|[73427781] ABA06537; B hordeína [Hordeum vulgare subsp. vulgare]; gi|74422695|gb|ABA06537.1|[74422695] ABB82613; B hordeína [Hordeum vulgare subsp. vulgare]; gi|82548223|gb|ABB82613.1|[82548223] ABB82614; B hordeína [Hordeum vulgare subsp. vulgare]; gi|82548225|gb(ABB82614.1|[82548225] ABH01262; B hordeína [Hordeum vulgare subsp. vulgare]; gi|110832715|gb|ABH01262.1|[110832715] BAA11642; D hordeína [Hordeum vulgare subsp. vulgare]; gi|1167498|dbj|BAA11642.1|[1167498] CAA25509; produto de proteína não nomeado [Hordeum vulgare]; gi| 18907|emb|CAA25509.11[18907] CAA25912; produto de proteína não nomeado [Hordeum vulgare]; gi|18914|emb|CAA25912.1|[18914] CAA25913; produto de proteína não nomeado [Hordeum vulgare]; gi|829269|emb|CAA25913.1|[829269] CAA25914; produto de proteína não nomeado [Hordeum vulgare]; gi|18949|emb|CAA25914.1|[18949] CAA26889; produto de proteína não nomeado [Hordeum vulgare]; gi|18910|emb|CAA26889.1|[18910] CAA31861; produto de proteína não nomeado [Hordeum vulgare subsp. vulgare]; gi|18980|emb|CAA31861.1|[18980] CAA37729; Precursor de B hordeína [Hordeum vulgare subsp. vulgare]; gi|18929|emblCAA37729.1|[18929] CAA42642; produto de proteína não nomeado [Hordeum vulgare subsp. vulgare]; gi|19001|emb|CAA42642.1|[19001] CAA48209; D hordeína [Hordeum vulgare subsp. vulgare]; gi|18970)emb|CAA48209.1|[18970] CAA51204; gama 3 hordeína [Hordeum vulgare]; gi|288709|emb|CAA51204.1|[288709] CAA59104; D-hordeína [Hordeum vulgare. subsp. vulgare]; gi|671537|emb|CAA59104.1|[671537] CAA60681; B1 hordeína [Hordeum vulgare]; gi|809031|emb|CAA60681.1|[809031] CAE45747; gama 2 hordeína putativa [Hordeum vulgare]; gi|34365052|emb|CAE45747.1|[34365052] P06470; precursor de B1-hordeína; gi|123458|sp|P06470|Hor1_HORVU[123458] P06471; B3-hordeína; gi|123459|spiP06471|HOR3_HORVU [123459] P06472; C-hordeína (PCP387); gi|123460|sp|P06472|HOR7_HORVU[123460] P17990; precursor de gama-hordeína-1; gi|123464|sp|P17990|HOG1_HORVU[123464] P17991; C-hordeína (Clone PC Hor1-3); gi]123461|sp|P17991|HOR8_HORVU[123461] P17992; C-hordeína (Clone PC-919); gi|123462]sp|P17992|HOR9_HORVU[123462] P29835; precursor de globulina de 19 kDa (Alphaglobulin); gi|115505553|sp|P29835|GL19_ORYSJ[115505553] P80198; Gama-hordeína-3; gi|1708280|sp|P80198| HOG3_HORVU[1708280]
[00117] Exemplos de genes e/ou hordeínas de cevada codificando cDNAs (fornecido com o N de Acesso, descrição em NCBI, detalhes gi) incluem, mas não são necessariamente limitados a: AF016237; Proteína de armazenamento de semente Hordeum vulgare (HORDB3a) mRNA, cds parciais; gi|2454596|gb|AF016237.1|HVHORD1[2454596] AF016238; Proteína de armazenamento de semente Hordeum vulgare (HORDB3a) mRNA sequência de extremidade 3’, cds parciais; gi|2454597|gb|AF016238.1|HVHORD2[2454597] AH005570; proteína de armazenamento de semente gene Hordeum vulgare subsp. vulgare, cds parciais; gi|2454598|gb|AH005570.1 |SEG_HVHORD[2454598] AJ580585; gene gama-2hor de Hordeum vulgare para gama 2 hordeína putativa; gi|34365051|emb|AJ580585.1|[34365051] AY268139; Hordeum vulgare BAC 184G9, sequência completa; gi|30421164|gb|AY268139.1|[30421164] AY338365; clone 1 cultivar H1 gama 3 hordeína mRNA de Hordeum chilense, cds completos; gi|34329250|gb|AY338365.1|[34329250] AY338366; clone 2 cultivar H1 gama 3 hordeína mRNA de Hordeum chilense, cds completos; gi|34329252|gb|AY338366.1|[34329252] AY338367; clone 3 cultivar H1 gama 3 hordeína mRNA de Hordeum chilense, cds completos; gi|34329254|gb|AY338367.1|[34329254] AY338368; clone 4 cultivar H1 gama 3 hordeína mRNA de Hordeum chilense, cds completos; gi|34329256|gb|AY338368.1|[34329256] AY338369; clone 5 cultivar H1 gama 3 hordeína mRNA de Hordeum chilense, cds completos; gi|34329258|gb|AY338369.1|[34329258] AY338370; clone 6 cultivar H1 gama 3 hordeína mRNA de Hordeum chilense, cds completos; gi|34329260|gb|AY338370.1|[34329260] AY338371; clone 7 cultivar H7 gama 3 hordeína mRNA de Hordeum chilense, cds parciais; gi|34329262|gb|AY338371.1|[34329262] AY338372; clone 8 cultivar H7 gama 3 hordeína mRNA de Hordeum chilense, cds parciais; gi|34329264|gb|AY338372.1|[34329264] AY338373; clone 9 cultivar H7 gama 3 hordeína mRNA de Hordeum chilense, cds parciais; gi|34329266|gb|AY338373.1|[34329266] AY338374; clone 10 cultivar H7 gama 3 hordeína mRNA de Hordeum chilense, cds parciais; gi|34329268|gb|AY338374.1([34329268] AY338375; clone 11 cultivar H7 gama 3 hordeína mRNA de Hordeum chilense, cds parciais; gi|3432920|gb|AY338375.1|[34329270] AY338376; clone 12 cultivar H7 gama 3 hordeína mRNA de Hordeum chilense, cds parciais; gi|34329272|gb|AY338376.1|[34329272] AY338377; clone 13 cultivar H7 gama 3 hordeína mRNA de Hordeum chilense, cds parciais; gi|34329274|gb]AY338377.1|[34329274] AY338378; clone 14 cultivar H7 gama 3 hordeína mRNA de Hordeum chilense, cds parciais; gi|34329276|gb|AY338378.1|[34329276] AY338379; clone 1 cultivar H47 gene de gama 3 hordeína de Hordeum chilense, cds parciais; gi|34329298|gb|AY338379.1|[34329298] AY338380; clone 2 cultivar H47 gene de gama 3 hordeína de Hordeum chilense, cds parciais; gi|34329300|gb|AY338380.11[34329300] AY338381; clone 3 cultivar H210 gene de gama 3 hordeína de Hordeum chilense, cds parciais; gi|34329302|gb|AY338381.1|[34329302] AY338382; clone 4 cultivar H210 gene de gama 3 hordeína de Hordeum chilense, cds parciais; gi|34329304|gb]AY338382.1|[34329304] AY338383; clone 5 cultivar H210 gene de gama 3 hordeína de Hordeum chilense, cds parciais; gi|34329306|gb|AY338383.1|[34329306] AY338384; clone 6 cultivar H210 gene de gama 3 hordeína de Hordeum chilense, cds parciais; gi|34329308]gb|AY338384.11[34329308] AY338385; clone 7 cultivar H252 gene de gama 3 hordeína de Hordeum chilense, cds parciais; gi|34329310|gb|AY338385.1|[34329310] AY695367; gene de B hordeína Hordeum brevisubulatum subsp. turkestanicum, cds completos; gi|51556913|gb|AY695367.1|[51556913] AY695368; B hordeína gene de Hordeum brevisubulatum subsp. turkestanicum, cds completos; gi|51556915|gb|AY695368.1|[51556915] AY695369; B hordeína gene de Hordeum brevisubulatum subsp. turkestanicum, cds completos; gi|51556917|gb|AY695369.1|[51556917] AY700807; Hordeum chilense cultivar H7 clone pC63-2 B3-hordeína pseudogene mRNA, cds completos; gi|57118094|gb|AY700807.1|[57118094] AY998005; clone pC39-1 mRNA tipo D-hordeína de Hordeum chilense, sequência parcial; gi|66354246|gb|AY998005.1|[66354246] AY998008; clone pC36-2 (4) mRNA tipo D-hordeína de Hordeum chilense, sequência parcial; gi|66354251 |gb|AY998008.11[66354251] AY998009; gene de D-hordeína de Hordeum chilense, 5' UTR e cds parciais; gi|66354252|gb|AY998009.1|[66354252] AY998010; gene de B-hordeína de Hordeum chilense, 5' UTR e cds parcial; gi|66354254|gb|AY998010.1|[66354254] D82941; Hor3 mRNA de Hordeum vulgare para D hordeína, cds completos; gi| 1167497|dbJlD82941.1 |BLYHOR3[1167497] DQ 148297; gene de B hordeína cultivar XQ053 de Hordeum vulgare subsp. vulgare, cds completos; gi|73427780|gb|DQ148297.1|[73427780] DQ178602; gene de B hordeína cultivar Aba-siqing Hordeum vulgare subsp. vulgare, cds completos; gi|74422694|gb|DQ178602.1|[74422694] DQ 189997; pseudogene de B hordeína clone Hn3 de Hordeum vulgare subsp. vulgare, sequência completa; gi|75991848|gb|DQ189997.1|[75991848] DQ267476; pseudogene de B hordeína clone Hn4 Hordeum vulgare subsp. vulgare, sequência completa; gi|82548218 jgb|DQ267476.11[82548218] DQ267477; pseudogene de B hordeína clone Hn5 de Hordeum vulgare subsp. vulgare, sequência completa; gi|82548220|gb|DQ267477.1|[82548220] DQ267478; gene de B hordeína clone Hn6 de Hordeum vulgare subsp. vulgare, cds completos; gi|82548222|gb|DQ267478.1|[82548222] DQ267479; gene de B hordeína clone Hn7 de Hordeum vulgare subsp. vulgare, cds completos; gi|82548224|gb|DQ267479.11[82548224] DQ267480; pseudogene de B hordeína clone Hn8 de Hordeum vulgare subsp. vulgare, sequência completa; gi|82548226|gb|DQ267480.1|[82548226] DQ267481; pseudogene de B hordeína clone Hn9 de Hordeum vulgare subsp. vulgare, sequência completa; gi|82548228|gb|DQ267481.1|[82548228] DQ826387; gene de B hordeína de Hordeum vulgare subsp. vulgare, cds completos; gi|110832714jgb|DQ826387.1| [110832714] J01237; mRNA de B1 hordeína de cevada (parcial); gi|167002|gb|J01237.1|BLYBlHOR[167002] K03147; mRNA de C-hordeína Cevada (Hordeum vulgare L.), clone pHvE-c251; gi|167015|gb|K03147.1|BLYCHORD2[167015] M23836; mRNA de hordeína de Hordeum vulgare (hor2-l), 3' UTR; gi|530091|gb|M23836.1|BLYHOR21A[530091] M23869; mRNA de B1 hordeína de Hordeum vulgare, 3' end; gi|530092|gb|M23869.1|BLYHORDBlA[530092] M35610; proteína de armazenamento de C-hordeína de cevada, extremidade 3’; gi|167017|gb|M35610.1]BLYCHORDA [167017] M35611; proteína de armazenamento de C-hordeína de cevada, extremidade 3’; gi|167019|gb|M35611.1|BLYCHORDB [167019] M36378; Gene de proteína de armazenamento de gama-1 hordeína de cevada, cds completos; gi|167041|gb|M36378.1|BLYGlHORDA[167041] M36941; gene de C-hordeína de Hordeum vulgare, cds completos; gi|167062|gb|M36941.1|BLYHORDCA[167062] S66938; C-hordeína [Hordeum vulgare=cevada, M564, Genômico, 2806 nt]; gi|442523|bbm|324747lbbs|139925|gb|S66938.1|[442523] X01024; Fragmento de mRNA de cevada para B1 hordeína; gi|18906|emb|X01024.1|[18906] XOl 777; Fragmento de mRNA de cevada para B3-hordeína; X01778; Fragmento de mRNA de cevada para Bl-hordeína; gi|18908|emb|X01778.1|[18908] X01779; Fragmento de mRNA de cevada para C-hordeína (pcP387); gi|18948|emb|X01779.1|[18948] X03103; gene de cevada para B1 hordeína; gi|18909|emb|X03103.1|[18909] Xl 3508; gene de cevada proteína de armazenamento de gama-hordeína; gi|18979|emb|X13508.1|[18979] X53690; DNA de Hordeum vulgare para B-Hordeína (pcr31); gi|18928|emb|X53690.1|[18928] X53691; DNA de H.vulgare para B hordeína (pcr47); gi]18930]emb|X53691.1|[18930] X60037; gene de Hor1-17 H.vulgare para C-hordeína; gi|19000|emb|X60037.1|[19000] X68072; mRNA de H.vulgare para D hordeína; gi|18969|emb|X68072.11[18969] X72628; mRNA de H.vulgare para gama 3 hordeína, extremidade 3’;gi|288708|emb|X72628.11[288708] X84368; gene de Hor3 H.vulgare; gi|671536|emb|X84368.1|[671536] X87232; gene de B1 hordeína de H.vulgare; gi|809030|emb|X87232.1|[809030]
[00118] Uma modalidade da presente invenção se relaciona às plantas de cevada transgênica compreendendo uma prolamina que é não tóxica para um indivíduo com doença celíaca. Como mostrado aqui, os exemplos de tal prolamina são uma avenina de aveia e uma zeína de milho. Exemplos de sequências de aminoácido de avenina de aveia (fornecidos como N° de Acesso; descrição em NCBI; detalhes gi) incluem, mas não são limitados a: 1411172A; componente N9 de avenina rápido; gi|226123|prf||1411172A[226123] 1502200A; prolamina; gi]226227|prf||1502200A[226227] AAA32713; avenina; gi|166551|gb|AAA32713.1|[166551] AAA32714; avenina; gi|166553|gb|AAA32714.1|[166553] AAA32715; avenina; gi|166555|gb|AAA32715.1|[166555] AAA32716; avenina; gi|166557|gb|AAA32716.1|[166557] AAB23365; gama 3 avenina, proteína imunoreativa celíaca 2, CIP-2, prolamina 2; gi|256082|gb| AAB23365.1 ||bbm|240522|bbs| 113745 [256082] AAB32025; avenina solúvel em álcool-3=23.2 kda proteína [Avena sativa=oat, Narymsky 943, Peptídeo, 201 aa]; gi|693794|gb|AAB32025.1||bbm|352847|bbs|156888[693794] ABD14148; avenina [Avena sativa]; gi|86610884|gb|ABD14148.1|[86610884] CAE85306; produto de proteína não nomeado [Avena sativa]; gi|39923008|emb|CAE85306.1|[39923008] CAE85351; produto de proteína não nomeado [Avena sativa]; gi|39923098|emb|CAE85351.1|[39923098] P27919; precursor de avenina; gi|114720|sp|P27919|AVEN_AVESA[l 14720] P80356; precursor de avenina-3 (Prolamina); gi|728937|sp]P80356|AVE3_AVESA[728937] Q09095; Avenina-A (Gama-4 avenina) (Prolamina) (proteína imunoreativa celíaca 1) (CIP-1); gi|75107163|sp|Q09095|AVEA_AVESA[75107163] Q09097; Avenina-F (Gama-3 avenina) (Prolamina) (proteína imunoreativa celíaca 2) (CIP-2); gi|75107165|sp]Q09097| AVEF_AVES A[75107165] Q09114; Avenina-E (Alfa-2 avenina) (Avenina N9) (Prolamina) (proteína imunoreativa celíaca 3) (CIP-3); gi|75107166|sp|Q09114|AVEE_AVESA[75107166] S06211; alfa-2 avenina - aveia nua pequena (fragmento); gi|82325|pir||S06211[82325] S07621; gama-3 avenina - aveia nua pequena (fragmento); gi|2119756|pir||S07621[2119756] S07622; gama-4 avenina - aveia nua pequena (fragmento); gi|82327|pir||S07622[82327]
Maltagem
[00119] Uma bebida à base de malte fornecida pela presente invenção envolve as bebidas de álcool (incluindo bebidas destiladas) e bebidas sem álcool que são produzidas usando malte como uma parte ou inteiro de seu material de partida. Os exemplos incluem cerveja, happoshu (bebida de cerveja de baixo-malte), uísque, bebidas à base de maltes de pouco álcool (por exemplo, bebidas à base de malte contendo menos de 1% de álcool), e bebidas sem álcool.
[00120] A maltagem é um processo de maceração e germinação controladas seguido pela secagem do grão de cevada. Esta sequência de eventos é importante para a síntese de numerosas enzimas que causam a modificação do grão, um processo que principalmente despolimeriza as paredes celulares de endosperma inativas e mobiliza os nutrientes de grão. No processo de secagem subsequente, o sabor e a cor são produzidos devido às reações de escurecimento químicas. Embora o uso primário do malte seja para a produção de bebida, pode também ser utilizado em outros processos industriais, por exemplo, como uma fonte de enzima na indústria de cozimento, ou como um condimento e um agente de coloração na indústria alimentícia, por exemplo, como malte ou como farinha de malte, ou indiretamente como um xarope de malte, etc.
[00121] Em uma modalidade, a presente invenção relaciona-se aos métodos para produzir uma composição de malte. O método compreende preferivelmente as etapas de: (i) fornecendo o grão de uma planta de cevada da invenção, (ii) maceração do referido grão, (iii) germinando os grãos macerados sob condições predeterminadas e (iv) secando os referidos grãos germinados.
[00122] Por exemplo, o malte pode ser produzido por quaisquer dos métodos descritos em Hoseney (Principles of Cereal Science and Technology, segunda edição, 1994: American Association of Cereal Chemists, St. Paul, Minn.). Entretanto, qualquer outro método apropriado para produzir o malte pode também ser usado com a presente invenção, tal como métodos para a produção de maltes de especialidade, incluindo, mas limitado a, métodos de tostagem do malte. Um exemplo não limitante é descrito no exemplo 6.
[00123] O malte pode ser preparado usando somente o grão produzido das plantas de cevada da invenção ou em misturas compreendendo outros grãos.
[00124] O malte é principalmente usado para fabricação de cerveja, mas também para a produção de aguardentes destilados. A fabricação de cerveja compreende a produção de mosto, fermentações principal e secundária e pós-tratamento. Primeiramente o malte é moído, agitado em água e aquecido. Durante esta “brassagem”, as enzimas ativadas na maltagem degradam o amido da semente em açúcares fermentáveis. O mosto produzido é clarificado, o fermento é adicionado, a mistura é fermentada e um pós- tratamento é realizado.
[00125] Em outra modalidade, as composições de mosto podem ser preparadas do malte. O referido mosto pode ser primeiro e/ou segundo e/ou posteriormente mosto. Geralmente uma composição de mosto terá um teor elevado de nitrogênio de amino e carboidratos fermentáveis, principalmente maltose. Tipicamente, o mosto é preparado incubando malte com água, isto é, brassagem. Durante a brassagem, a composição de malte/água pode ser suplementada com composições ricas em carboidratos adicionais, por exemplo, adjunções de cevada, milho ou arroz. As adjunções de cereal sem malte não contêm geralmente nenhuma enzima ativa, e, portanto, confiam no malte ou enzimas exógenas para fornecer as enzimas necessárias para a conversão de açúcar.
[00126] Geralmente, a primeira etapa no processo de produção de mosto é a moagem de malte a fim de que a água possa ter acesso às partículas de grão na fase de brassagem, que é fundamentalmente uma extensão do processo de maltagem com despolimerização enzimática de substratos. Durante a brassagem, o malte moído é incubado com uma fração de líquido, tal como água. A temperatura é mantida constante (brassagem isotérmica) ou gradualmente aumentada. Em qualquer caso, as substâncias solúveis produzidas na maltagem e brassagem são extraídas na fração do referido líquido antes que seja separada por filtração no mosto e partículas sólidas residuais denotadas grãos gastos. Este mosto pode também ser denotado primeiro mosto. Após a filtração, um segundo mosto é obtido. Mostos adicionais podem ser preparados repetindo o procedimento. Exemplos não limitantes de procedimentos apropriados para a preparação de mosto são descritos em Hoseney (supra).
[00127] A composição de mosto pode também ser preparada incubando plantas de cevada da invenção ou partes das mesmas com uma ou mais enzimas apropriadas, tal como composições de enzima ou composições de mistura de enzima, por exemplo, Ultraflo ou Cereflo (Novozymes). A composição de mosto pode também ser preparada usando uma mistura de malte e plantas de cevada sem malte ou partes das mesmas, opcionalmente adicionando uma ou mais enzimas apropriadas durante a referida preparação. Além disso, as enzimas de prolil-endopeptidase que especificamente destroem as amino ligações tóxicos envolvidos na doença celíaca poderiam ser adicionadas durante a fermentação de mosto para reduzir a toxicidade dos hordeínas residuais (De Angelis e col., 2007; Marti e col., 2005; Stepniak e col., 2006).
Processamento de grão
[00128] O grão de cevada da invenção pode ser processado para produzir um alimento ou produto não alimentício usando qualquer técnica conhecida na técnica.
[00129] Em uma modalidade, o produto é a farinha de grão integral (uma farinha de grão integral moído ultrafino, tal como uma farinha de grão integral moído ultrafino; uma farinha de grão integral, ou uma farinha feita de aproximadamente 100% do grão). A farinha de grão integral inclui um constituinte de farinha refinada (farinha refinada) e uma fração grosseira (uma fração grosseira moída ultrafina).
[00130] A farinha refinada pode ser farinha que é preparada, por exemplo, moendo e peneirando a cevada limpa. A Agência de Medicamentos e Alimentos (FDA) exige que a farinha cumpra determinados padrões de tamanho de partícula a fim de ser incluído na categoria de farinha de cevada refinada. O tamanho de partícula da farinha refinada é descrito como farinha em que não menos do que 98% passa através de um pano tendo aberturas não maiores do que aquelas de pano de fio tecido designado “212 micrômetros (US Wire 70).
[00131] A fração grosseira inclui pelo menos um de: sêmea e gérmen. Por exemplo, o gérmen é uma planta embrionária encontrada dentro da semente de cevada. O gérmen inclui lipídios, fibra, vitaminas, proteína, minerais e fitonutrientes, tais como flavonóides. O sêmea inclui diversas camadas de célula e tem uma quantidade significativa de lipídios, fibra, vitaminas, proteína, minerais e fitonutrientes, tais como flavonóides. Além disso, a fração grosseira pode incluir uma camada de aleurona que também inclui lipídios, fibra, vitaminas, proteína, minerais e fitonutrientes, tais como flavonóides. A camada de aleurona, enquanto tecnicamente considerada parte do endosperma, exibe muitas das mesmas características que o sêmea e, portanto, é tipicamente removida com o sêmea e gérmen durante o processo de moagem. A camada de aleurona contém proteínas, vitaminas e fitonutrientes, tais como ácido ferúlico.
[00132] Além disso, a fração grosseira pode ser misturada com o constituinte de farinha refinada. Preferivelmente, a fração grosseira é misturada homogeneamente com o constituinte de farinha refinada. Homogeneamente misturando a fração grosseira e o constituinte de farinha refinada pode ajudar a reduzir a estratificação das partículas por tamanho durante o transporte. A fração grosseira pode ser misturada com o constituinte da farinha refinada para formar a farinha de grão integral, fornecendo assim uma farinha de grão integral com valor nutricional aumentado, teor de fibra, e capacidade antioxidante em comparação à farinha refinada. Por exemplo, a fração grosseira ou a farinha de grão integral pode ser usada em várias quantidades para substituir a farinha de grão refinada ou integral em produtos assados, produtos de petisco, e produtos alimentícios. A farinha de grão integral da presente invenção (isto é, farinha integral de grão moído ultrafino) pode também ser comercializada diretamente aos consumidores para uso em seus produtos cozidos caseiros. Em uma modalidade de exemplo, um perfil de granulação da farinha de grão integral é tal que 98% das partículas por peso da farinha de grão integral tem menos de 212 micrômetros.
[00133] Em modalidades adicionais, as enzimas encontradas dentro do sêmea e gérmen da farinha de grão integral e/ou fração grosseira são inativadas a fim de estabilizar a farinha de grão integral e/ou fração grosseira. É contemplado pela presente invenção que inativada pode também significar inibido, desnaturado ou similares. A estabilização é um processo que usa vapor, calor, radiação, ou outros tratamentos para inativar as enzimas encontradas na camada de sêmea e gérmen. As enzimas naturais na sêmea e gérmen catalisarão mudanças aos compostos na farinha, afetando adversamente as características de cozimento da farinha e vida útil. As enzimas inativadas não catalisam mudanças aos compostos encontrados na farinha, portanto, a farinha que foi estabilizada retém suas características de cozimento e tem uma vida útil mais longa. Por exemplo, a presente invenção pode realizar uma técnica de moagem de duas correntes para moer a fração grosseira. Uma vez que a fração grosseira é separada e estabilizada, a fração grosseira é então moída através de um moedor, preferivelmente um moinho de abertura, para formar uma fração grosseira tendo uma distribuição de tamanho de partícula inferior ou igual a aproximadamente 500 micrômetros. Em uma modalidade de exemplo, a velocidade de ponta de moinho de abertura funciona normalmente entre 115 m/s a 144 m/s, a velocidade de ponta elevada gera calor. O calor gerado durante o processo e o fluxo de ar conduzem a uma diminuição na carga microbiana da fração grosseira. Em modalidades adicionais, antes da moagem em um moinho de abertura, a fração grosseira pode ter uma contagem de placa aeróbia média de 95.000 unidades de formação de colónias/grama (cfu/g) e uma contagem de coliforme média de 1.200 cfu/g. Após a passagem através do moinho de abertura a fração grosseira pode ter uma contagem de placa aeróbia média de 10.000 cfu/g e uma contagem de coliforme média de 900 cfu/g. Assim, a carga microbiana pode ser visivelmente diminuída na fração grosseira da presente invenção. Após peneiração, qualquer fração grosseira moída tendo tamanho de partícula maior de 500 micrômetros pode ser retornada ao processo para uma moagem adicional.
[00134] Em modalidades adicionais, a farinha de grão integral ou a fração grosseira pode ser um componente de um produto alimentício. Por exemplo, o produto alimentício pode ser um bagel, um biscoito, um pão, um bolo, um croissant, um bolinho de massa, um muffin inglês, um muffin, um pão de pita, um pão rápido, produtos de massa refrigerados/congelados, massa de pão, feijões cozidos, um burrito, chili, um taco, um tamale, uma tortilha, uma torta, um cereal pronto para comer, uma refeição pronta para comer, recheio, uma refeição de microndas, um brownie, um bolo, um bolo de queijo, um bolo de café, um bolinho, uma sobremesa, um pastel, um rolo doce, uma barra de doce, uma crosta de torta, recheio de torta, comida para bebê, uma mistura de cozimento, uma massa, um pão, uma mistura de molho, um extensor de carne, um substituto de carne, uma mistura de tempero, uma mistura de sopa, um molho, uma massa, um molho de salada, uma sopa, creme azedo, um noodles, uma massa, ramen noodless, chow mein noodless, lo mein noodless, uma inclusão de sorvete, uma barra de sorvete, um cone de sorvete, um sanduíche de sorvete, um biscoito, um crouton, uma donuts, um rolo de ovo, um petisco extrudado, uma fruta e barra de cereal, um produto de petisco de microndas, uma barra nutritiva, uma panqueca, um produto de padaria par- cozido, um pretzel, um pudim, um produto à base de granola, uma batata de petisco, um alimento de petisco, uma mistura de petisco, um waffle, uma crosta de pizza, alimento animal ou alimento de animal de estimação.
[00135] Em modalidades alternativas, a farinha de grão integral ou fração grosseira pode ser um componente de um suplemento nutritivo. Por exemplo, o suplemento nutritivo pode ser um produto que é adicionado à dieta contendo um ou mais ingredientes, incluindo tipicamente: vitaminas, minerais, ervas, aminoácidos, enzimas, antioxidantes, ervas, especiarias, probióticos, extratos, prebióticos e fibra. A farinha de grão integral ou fração grosseira da presente invenção incluem vitaminas, minerais, aminoácidos, enzimas e fibra. Por exemplo, a fração grosseira contém uma quantidade concentrada de fibra dietética, bem como outros nutrientes essenciais, tais como vitaminas B, selênio, cromo, manganês, magnésio, e antioxidantes, que são essenciais para uma dieta saudável. Por exemplo, 22 gramas da fração grosseira da presente invenção liberam 33% de um consumo diário recomendado ao indivíduo de fibra. Além disso, 14 gramas é tudo que é necessário para liberar 20% do consumo diário recomendado ao indivíduo de fibra. Assim, a fração grosseira é uma fonte suplementar excelente para o consumo de uma exigência de fibra do indivíduo. Portanto, em uma modalidade presente, a farinha de grão ou fração grosseira integral pode ser um componente de um suplemento nutritivo. O suplemento nutritivo pode incluir quaisquer ingredientes nutritivos conhecidos que ajudam na saúde total de um indivíduo, os exemplos incluem, mas não são limitados às vitaminas, minerais, outros componentes de fibra, ácidos graxos, antioxidantes, aminoácidos, peptídeos, proteínas, luteína, ribose, ácidos omega-3 graxos, e/ou outros ingredientes nutritivos.
[00136] Em modalidades adicionais, a farinha de grão integral ou fração grosseira pode ser um suplemento de fibra ou um componente do mesmo. Muitos suplementos de fibra atuais, tais como cascas de psyllium, derivados de celulose, e goma guar hidrolizada tem limitado valor nutricional além de seu teor de fibra. Adicionalmente, muitos suplementos de fibra têm uma textura indesejável e um gosto pobre. Os suplementos de fibra feitos de farinha de grão integral ou fração grosseira podem ajudar a liberar fibra, bem como proteína, e antioxidantes. O suplemento de fibra pode ser liberado, mas não é limitado às seguintes formas: as misturas de bebida instantânea, bebidas prontas para beber, barras nutritivas, bolachas, bolinhos, biscoitos, bolas de gel, cápsulas, chicletes, comprimidos mastigáveis, e pílulas. Uma modalidade libera o suplemento de fibra na forma de um shake flavorizado ou bebida tipo malte, esta modalidade pode ser particularmente atrativa como um suplemento de fibra para crianças.
[00137] Em uma modalidade adicional, um processo de moagem pode ser usado para fazer uma farinha multi-grão, farinha de multi-cevada, ou uma fração grosseira de multi- grão. Por exemplo, a sêmea e gérmen de um tipo de cevada podem ser moídos e misturados com o endosperma moído ou farinha de cevada de grão integral de outro tipo de cevada. Alternativamente a sêmea e gérmen de um tipo de grão podem ser moídos e misturados com o endosperma moído ou farinha de grão integral de outro tipo de grão. Em uma modalidade adicional, o sêmea e o gérmen de um primeiro tipo de cevada ou de grão podem ser misturados com o sêmea e o gérmen de um segundo tipo de cevada ou de grão para produzir uma fração grosseira de multi-grão. Contempla-se que a presente invenção engloba a mistura de toda combinação de uma ou mais sêmeas, gérmen, endosperma, e farinha de grão integral de um ou mais grãos. Este multi-grão, multi-cevada abordada pode ser usada para fazer a farinha sob encomenda e para capitalizá-la nas qualidades e nos teores nutritivos de múltiplos tipos de grãos ou de cevadas para fazer uma farinha.
[00138] A farinha de grão integral da presente invenção pode ser produzida através de uma variedade de processos de moagem. Uma modalidade de exemplo envolve moer o grão em um único córrego sem separar o endosperma, sêmea, e gérmen de grão em córregos separados. O grão limpo e tratado é transportado a um primeiro moedor de passagem, tal como um moinho de martelo, moinho de rolo, moinho de pino, moinho de impacto, moinho de disco, moinho de atrito de ar, moinho de abertura, ou similares. Em uma modalidade, o moedor pode ser um moinho de abertura. Após a moagem, o grão é descarregado e transportado a uma peneira. Qualquer peneira conhecida na técnica para peneirar uma partícula moída pode ser usada. O material que passa através da tela da peneira é a farinha de grão integral da presente invenção e não exige nenhuma transformação posterior. O material que permanece na tela é referido como uma segunda fração. A segunda fração exige a redução adicional da partícula. Assim, esta segunda fração pode ser transportada a um segundo moedor de passagem. Após a moagem, a segunda fração pode ser transportada a uma segunda peneira. O material que passa através da tela da segunda peneira é a farinha de grão integral da presente invenção. O material que permanece na tela é referido como a quarta fração e exige uma transformação posterior para reduzir o tamanho da partícula. A quarta fração na tela da segunda peneira é transportada novamente ao primeiro moedor de passagem ou no segundo moedor de passagem para uma transformação posterior através de um retorno retroalimentado. Em uma modalidade alternativa da invenção, o processo pode incluir uma pluralidade de primeiros moedores de passagem para fornecer uma capacidade de sistema mais elevada.
[00139] Contempla-se que a farinha de grão integral, a fração grosseira e/ou os produtos de grão da presente invenção podem ser produzidos por todo o processo de moagem conhecido na técnica. Além disso, contempla-se que a farinha de grão integral, a fração grosseira e/ou os produtos de grão da presente invenção podem ser modificados ou melhorados por outros numerosos processos como: fermentação, instantaneização, extrusão, capsulagem, brindagem, tostagem ou similares.
Polinucleotídeo que regulam inferiormente a produção de uma Hordeína
[00140] Em uma modalidade, o grão da invenção, e/ou usado nos métodos da invenção, é de uma planta de cevada transgênica que compreenda um transgene que codifique um polinucleotídeo que subregula a produção de pelo menos um hordeína no grão. Os exemplos de tais polinucleotídeo incluem, mas não são limitados a polinucleotídeo antisenso, um polinucleotídeo senso, um polinucleotídeo catalítico, um microRNA artificial ou uma molécula de RNA duplex. Quando presente no grão, cada um destes polinucleotídeo conduz a uma redução no hordeína mRNA disponível para a tradução.
[00141] Polinucleotídeo antisenso
[00142] O termo “polinucleotídeo antisenso"; será tomado para significar um DNA ou um RNA, ou a combinação do mesmo, a molécula que é complementar pelo menos a uma parcela de uma molécula específica de mRNA codificando uma hordeína e capaz de interferir com um evento pós- transcricional tal como a tradução de mRNA. O uso de métodos antisenso é conhecido na técnica (veja por exemplo, G. Hartmann e S. Endres, manual de Metodologia antisenso, Kluwer (1999)). O uso de técnicas antisenso nas plantas foi revisto por Bourque (1995) e por Sênior (1998). Sênior (1998) indica que os métodos antisenso são agora uma técnica muito bem conhecida para manipular a expressão de gene.
[00143] Um polinucleotídeo antisenso em uma planta de cevada da invenção cruzará com um polinucleotídeo alvo sob condições fisiológicas. Como usado aqui, o termo “um polinucleotídeo antisenso que cruze sob condições fisiológicas”; significa que o polinucleotídeo (que é integralmente ou parcialmente único fixo) é pelo menos capaz de formar um polinucleotídeo fixo duplo com o mRNA codificando com uma proteína, tal como uma hordeína de cevada sob condições normais em uma célula de cevada.
[00144] As moléculas antisenso podem incluir as sequências que correspondem aos genes estruturais ou as sequências que efetuam o controle sobre a expressão de gene ou o evento de emenda. Por exemplo, a sequência antisenso pode corresponder à região de codificação alvejada dos genes da invenção, ou aos 5'-região não traduzida (UTR) ou 3'-UTR ou combinação destes. Pode ser complementar na parte às sequências íntron, que pode ser emendado para fora durante ou após a transcrição, preferivelmente somente às sequências de exon de gene alvo. Em virtude de divergência geralmente maior de UTRs, alvejar estas regiões fornece maior especificidade de inibição de gene.
[00145] O comprimento da sequência antisenso deve ser pelo menos 19 nucleotídeos contíguos, preferivelmente pelo menos 50 nucleotídeos, e melhor pelo menos 100, 200, 500 ou 1000 nucleotídeos. A sequência completa complementar transcrita inteira de gene pode ser usada. O comprimento preferível de 100-2000 nucleotídeos. O grau de identidade de sequência antisenso ao transcrito alvejado deve ser pelo menos 90% e preferível de 95-100%. A molécula antisenso de RNA pode naturalmente compreender as sequências não relacionadas que podem funcionar para estabilizar a molécula.
Polinucleotídeo catalíticos
[00146] O termo polinucleotídeo/nucleico ácido se refere a uma molécula de DNA ou DNA-contida molécula (também conhecida na técnica como uma "desoxiribozima") ou um RNA ou uma molécula de RNA-contenção (também conhecida como uma "ribozima") qual reconhece especificamente um substrato distinto e catalisa a modificação química deste substrato. As bases de ácido nucleico no ácido nucleico catalítico podem ser as bases A, C, G, T (e U para o RNA).
[00147] Tipicamente, o ácido nucleico catalítico contém uma sequência antisenso para o reconhecimento específico de um ácido nucleico de alvo, e um ácido nucleico que divide a atividade enzimática (também referida aqui como o "domínio catalítico"). Os tipos de ribozimas que são particulares úteis nesta invenção são a ribozima de cabeça de martelo (Haseloff e Gerlach, 1988, Perriman e col., 1992) e a ribozima de gancho de cabelo (Shippy e col., 1999).
[00148] As ribozimas em plantas de cevada da invenção e de DNA codificando as ribozimas podem ser quimicamente sintetizadas usando métodos conhecidos na técnica. As ribozimas podem também ser preparadas de uma molécula de DNA (que através de transcrição, obtém uma molécula de RNA) operavelmente ligada a um promotor de polimerase de RNA, por exemplo, promotor para polimerase de RNA T7 ou polimerase de RNA SP6. Quando o vetor também contiver um promotor de polimerase de RNA operavelmente ligado à molécula de DNA, a ribozima pode ser produzida in vitro através de incubação com polimerase e nucleotídeos de RNA. Em uma modalidade distinta, o DNA pode ser introduzido em uma gaveta de expressão ou na gaveta de transcrição. Após a síntese, a molécula de RNA pode ser modificada pela ligação a uma molécula de DNA tendo a habilidade de estabilizar a ribozima e de fazê-la resistente a RNase.
[00149] Como com os polinucleotídeo antisenso descritos aqui, os polinucleotídeo catalíticos devem também ser capazes de cruzar uma molécula de ácido nucleico de alvo (por exemplo um mRNA codificando uma hordeína de cevada) sob "condições fisiológicas", a saber aquelas condições dentro de uma célula de cevada.
Interferência de RNA
[00150] A interferência de RNA (RNAi) é particularmente útil para especificamente inibir a produção de uma proteína particular. Embora não desejando ser limitado pela teoria, Waterhouse e col. (1998) forneceram um modelo para o mecanismo na qual o dsRNA (RNA duplo) pode ser usado para reduzir a produção de proteína. Esta tecnologia confia na presença de moléculas de dsRNA contendo uma sequência que seja essencialmente idêntica ao mRNA de gene de interesse ou de parte do mesmo, neste caso um mRNA codificando a polipeptídeo de acordo com a invenção. Convenientemente, o dsRNA pode ser produzido de um único promotor em uma célula de recombinação de vetor ou hospedeira, onde o sentido e as sequências anti-senso sejam flanqueados por uma sequência não relacionada que permita o sentido e as sequências antisenso cruzarem para formar à molécula de dsRNA com a sequência não relacionada que dá forma a uma estrutura de retorno. O projeto e a produção de moléculas apropriadas de dsRNA para a presente invenção estão dentro da capacidade de uma pessoa hábil na técnica, considerando em particular Waterhouse e col. (1998), Smith e col. (2000), WO 99/32619, WO 99/53050, WO 99/49029, e WO 01/34815.
[00151] Em um exemplo, um DNA é introduzido que dirija a síntese de pelo menos um produto (duplo) fixo em parte dupla de RNA com homologia ao gene alvo inativada. O DNA compreende, portanto, o sentido e as sequências antisenso que, quando transcritos no RNA, podem cruzar para formar à região de fita dupla de RNA. Em uma modalidade preferida, o sentido e as sequências antisenso são separados por uma região de espaçador que compreenda um íntron que, quando transcrito no RNA, seja emendado para fora. Este arranjo foi mostrado para conduzir a uma eficiência mais elevada de silenciamento de gene. A região de fita dupla pode compreender uma ou dois moléculas de RNA, transcritas de uma região ou de dois de DNA. A presença de molécula fixa dupla é pensada para provocar uma resposta de um sistema endógeno de planta que destrua o RNA fixo duplo e também o transcrito homólogo de RNA de gene de planta alvo, eficientemente reduzindo ou eliminando a atividade de gene alvo.
[00152] O comprimento do senso e as sequências antisenso que se cruzam deve cada um ser de pelo menos 19 nucleotídeos contíguos, preferivelmente pelo menos 30 ou 50 nucleotídeos, e mais preferivelmente pelo menos 100, 200, 500 ou 1000 nucleotídeos. A sequência completa que corresponde ao transcrito inteiro de gene pode ser usada. Os comprimentos preferíveis são de 100-2000 nucleotídeos. O grau de identidade senso e das sequências antisenso ao transcrito alvejado deve ser pelo menos 85%, preferivelmente pelo menos 90% e mais preferivelmente 95100%. A molécula de RNA pode naturalmente compreender as sequências não relacionadas que podem funcionar para estabilizar a molécula. A molécula de RNA pode ser expressa sob o controle de um promotor de polimerase de RNA II ou de polimerase de RNA III. Os exemplos dos últimos incluem promotores de tRNA ou de snRNA.
[00153] As moléculas de RNA de pequena interferência preferidas ("siRNA") que compreendem uma sequência de nucleotídeo que seja idêntica a aproximadamente 19-21 nucleotídeos contíguos de alvo mRNA. Preferivelmente, a sequência de mRNA alvo começa com o dinucleotídeo AA, compreende um GC-teor de aproximadamente 30-70% (preferivelmente, 30-60%, mais preferivelmente 40 - 60% e mais preferivelmente aproximadamente 45%-55%), e não tem uma porcentagem de identidade elevada a nenhuma sequência de nucleotídeo à exceção de alvo no genoma de planta de cevada em que deve ser introduzida, por exemplo, como determinado pela busca padrão de EXPLOSÃO.
MicroRNA
[00154] O regulamento de MicroRNA é uma filial claramente especializada de RNA que silencia o caminho que evoluiu para o regulamento de gene, divergindo de convencional RNAi/PTGS. MicroRNAs é uma classe específica de RNAs pequeno que é codificado dentro de elementos similares a gene organizados em uma repetição invertida característica. Quando transcritos, os genes de microRNA causam o crescimento de RNAs precursores de caules com voltas dos quais os microRNAs são subsequentemente processados. Os microRNAs tem tipicamente aproximadamente 21 nucleotídeos de comprimento. Os miRNAs liberados são incorporados em complexos tipo RISC contendo um subconjunto particular de proteínas de Argonaute que exercem a repressão de gene de sequência específica (veja, por exemplo, Millar e Waterhouse, 2005; Pasquinelli e col., 2005; Almeida e Allshire, 2005).
Co-supressão
[00155] Outra abordagem biológica molecular que pode ser usada é a co-supressão. O mecanismo de co-supressão não é bem compreendido, mas é pensado envolver o silenciamento de gene pós-transcricional (PTGS) e nessa consideração pode ser muito similar a muitos exemplos de supressão antisenso. Envolve introduzir uma cópia extra de um gene ou um fragmento do mesmo em uma planta na orientação senso com relação a um promotor para sua expressão. O tamanho do fragmento senso, sua correspondência às regiões de gene alvo, e seu grau de identidade de sequência ao gene alvo são como para as sequências antisenso descritas acima. Em alguns casos a cópia adicional da sequência de gene interfere com a expressão do gene de planta alvo. A referência é feita a WO 97/20936 e EP 0465572 para métodos de implementar abordagens de co-supressão.
Elementos de ácido nucleico
[00156] Os elementos de ácido nucleico úteis para produzir plantas transgênicas podem ser prontamente produzidos usando técnicas padrões.
[00157] Ao introduzir uma região codificando um mRNA o elemento pode compreender sequências íntron. Estas sequências íntron podem ajudar na expressão do transgene na planta. O termo “íntron” é usado em seu sentido normal como significado de um segmento genético que é transcrito, mas não codifica a proteína e que é emendado de um RNA antes da tradução. Os íntrons podem ser incorporados em um 5’-UTR ou uma região de codificação se o transgene codifica um produto traduzido, ou em qualquer lugar na região transcrita, se não o faz. Entretanto, em uma modalidade preferida, qualquer região de codificação de polipeptídeo é fornecida como um único frame de leitura aberto. Como o hábil estaria ciente, tais frames de leitura abertos podem ser obtidos pela transcrição reversa de mRNA codificando o polipeptídeo.
[00158] Para assegurar a expressão apropriada do gene codificando um mRNA de interesse, o elemento de ácido nucleico compreende tipicamente um ou mais elementos regulatórios, tais como promotores, melhoradores, bem como sequências de terminação de transcrição ou poliadenilação. Tais elementos são bem conhecidos na técnica.
[00159] A região de iniciação transcricional compreendendo os elementos regulatórios pode fornecer a expressão regulada ou constitutiva na planta. Preferivelmente, a expressão ocorre pelo menos nas células da semente.
[00160] Vários promotores constitutivos que são ativos em células da planta foram descritos. Os promotores apropriados para a expressão constitutiva nas plantas incluem, mas não são limitados a, o promotor 35S de vírus mosaico de couve-flor (CaMV), o vírus mosaico de Scrophulariaceae (FMV) 35 S, o promotor baciliforme de vírus de cana-de-açúcar, o promotor de vírus de mancha mosqueada amarela de commelina, o promotor indutível de luz da subunidade pequena de carboxilase ribulose-1,5-bis- fosfato, o promotor de isomerase de triosefosfato citosólico de arroz, o promotor de adenina fosforibosiltransferase de Arabidopsis, o promotor de gene de actina 1 de arroz, os promotores de sintase de mannopina e sintase de octopina, o promotor de Adh, o promotor de sintase de sacarina, o promotor de complexo de gene R, e o promotor de gene de proteína de ligação de clorofila α/β. Estes promotores foram usados para criar os vetores de DNA que foram expressos nas plantas; veja, por exemplo, WO 84/02913. Todos estes promotores foram usados para criar vários tipos de vetores de DNA recombinante expressíveis de planta.
[00161] O promotor pode ser modulado por fatores, tais como temperatura, luz ou estresse. Ordinariamente, os elementos regulatórios serão fornecidos 5’ da sequência genética a ser expressa. O elemento pode também conter outros elementos que melhoram a transcrição, tal como as regiões de poliadenilação nos 3’ ou ocs 3’ ou terminadores de transcrição.
[00162] A 5’ sequência líder não traduzida pode ser derivada do promotor selecionado para expressar a sequência de gene heterólogo, e pode especificamente ser modificada se desejado para aumentar a tradução de mRNA. Para uma revisão de otimização de expressão de transgenes, veja Koziel e col. (1996). As regiões 5’ não traduzidas podem também ser obtidas de RNAs virais de planta (vírus mosaico de tabaco, vírus de enxerto de tabaco, vírus mosaico de milho anão, vírus mosaico de alfalfa, entre outros) dos genes eucarióticos apropriados, genes de planta (líder de gene proteína de ligação a/b de clorofila de trigo e de milho), ou de uma sequência de gene sintético. A presente invenção não é limitada ao uso de elementos em que a região não traduzida é derivada da sequência 5’ não traduzida que acompanha a sequência de promotor. A sequência líder poderia também ser derivada de uma sequência de codificação ou promotor não relacionada. As sequências líder úteis no contexto da presente invenção compreendem o líder de milho Hsp70 (US 5.362.865 e US 5.859.347), e o elemento ômega TMV.
[00163] A terminação de transcrição é realizada por uma sequência 3’ não traduzida de DNA operavelmente ligado no vetor quimérico ao polinucleotídeo de interesse. A região 3’ não traduzida de uma molécula de DNA recombinante contém um sinal de poliadenilação que funciona nas plantas para causar a adição de nucleotídeos de adenilato à extremidade 3’ do RNA. A região 3’ não traduzida pode ser obtida dos vários genes que são expressos em células de planta. A região 3’ não traduzida de sintase de nopaline, a região 3’ não traduzida do gene de Rubisco de subunidade de ervilha pequeno, a região 3’ não traduzida do gene de proteína de armazenamento 7S de semente de soja é comumente usada nesta capacidade. As regiões 3’ transcritas, não traduzidas contendo o sinal de poliadenilato de genes de plasmídeo indutores de tumor (Ti) de Agrobacterium são também apropriadas.
[00164] Tipicamente, o elemento de ácido nucleico compreende um marcador selecionável. Os marcadores selecionáveis ajudam na identificação e seleção de plantas ou células que foram transformadas com a molécula de ácido nucleico exógena. O gene de marcador selecionável pode fornecer a resistência ao antibiótico ou herbicida às células de cevada, ou permite a utilização de substratos, tais como manose. O marcador selecionável dá preferivelmente resistência à higromicina às células de cevada.
[00165] Preferivelmente, o elemento de ácido nucleico é estavelmente incorporado no genoma da planta. Consequentemente, o ácido nucleico compreende os elementos apropriados que permitem que a molécula seja incorporada no genoma, ou o elemento é colocado em um vetor apropriado que pode ser incorporado em um cromossomo de uma célula de planta.
[00166] Uma modalidade da presente invenção inclui o uso de um vetor de recombinação, que inclui pelo menos o transgene esboçado aqui, introduzido em qualquer vetor capaz de liberar a molécula de ácido nucleico em uma célula hospedeira. Tal vetor contém sequências de ácido nucleico heterólogas, que são sequências de ácido nucleico que não são encontradas naturalmente junto às moléculas de ácido nucleico da presente invenção e que são derivadas preferivelmente de uma espécie diferentes da espécie do que as moléculas de ácido nucleico são derivadas. O vetor pode ser de RNA ou DNA, procariótico ou eucariótico, e é tipicamente um vírus ou um plasmídeo.
[00167] Vários vetores apropriados para a transfecção estável de células de planta ou para o estabelecimento de plantas transgênicas foram descritos em, por exemplo, Pouwels e col., Cloning Vectors: A Manual Laboratory, 1985, supl. 1987; Weissbach and Weissbach, Methods for Plant Molecular Biology, Academic Press, 1989; e Gelvin e col., Plant Molecular Biology MAnual, Kluwer Academic Publishers, 1990. Tipicamente, os vetores de expressão de planta incluem, por exemplo, um ou mais genes de planta clonados sob o controle transcricional de sequências 5’ e 3’ regulatórias e um marcador selecionável dominante. Tais vetores de expressão de planta também podem conter uma região regulatória promotora (por exemplo, uma região regulatória controlando expressão indutível ou constitutiva, ambientalmente ou desenvolventemente-regulada, ou específica de célula ou tecido), uma transcrição sítio de partida de iniciação de região, um sítio de ligação de ribossomo, um sinal de processamento de RNA, um sítio de terminação de transcrição, e/ou um sinal de poliadenilação.
Plantas transgênicas
[00168] As plantas de cevada transgênicas, como definidas no contexto da presente invenção incluem as plantas (bem como partes e células das referidas plantas) e sua progênia que foram geneticamente modificadas usando técnicas de recombinação para causar a produção de pelo menos um polinucleotídeo e/ou polipeptídeo na planta desejada ou órgão de planta. As plantas transgênicas podem ser produzidas usando as técnicas conhecidas na técnica, tal como aquelas descritas geralmente em A. Slater e col., Plant Biotechnology - The Genetic Manipulation of Plants, Oxford University Press (2003), e P. Christou e H. Klee, Handbook of Plant Biotechnology, John Wiley and Sons (2004).
[00169] Em uma modalidade preferida, as plantas transgênicas são homozigóticas para cada gene que foi introduzido (transgene) de modo que sua progênia não segrega para o fenótipo desejado. As plantas transgênicas podem também ser heterozigóticas para os transgenes introduzidos, como, por exemplo, na progênia F1 que foi crescida da semente híbrida. Tais plantas podem fornecer vantagens, tais como vigor híbrido, conhecido na técnica.
[00170] Quatro métodos gerais para a liberação direta de um gene em células foram descritos: (1) métodos químicos (Graham e col., 1973); (2) métodos físicos, tais como microinjeção (Capecchi, 1980); eletroporação (veja, por exemplo, WO 87/06614, US 5.472.869, 5.384.253, WO92/09696 e WO 93/21335); e injetor de gene (veja, por exemplo, US 4.945.050 e US 5.141.131); (3) vetores virais (Clapp, 1993; Lu e col., 1993; Eglitis e col., 1988); e (4) mecanismos mediados por receptor (Curiel e col., 1992; Wagner e col., 1992).
[00171] Os métodos de aceleração que podem ser usados incluem, por exemplo, bombardeio de microprojétil e similares. Um exemplo de um método para liberar moléculas de transformação de ácido nucleico às células de planta é o bombardeio de microprojétil. Este método foi revisto por Yang e col., Particle Bombardment Technology for Gene Transfer, Oxford Press, Oxford, Inglaterra (1994). As partículas não biológicas (microprojéteis) podem ser revestidas com ácidos nucleicos e liberadas em células por uma força de propulsão. As partículas de exemplo incluem aquelas compreendidas de tungstênio, ouro, platina e similares. Uma vantagem particular de bombardeio de microprojétil, além dessa é que meios eficazes de reprodutivelmente transformar monocotiledôneas, é que nem o isolamento de protoplastos, nem a susceptibilidade de infecção de Agrobacterium são exigidas. Uma modalidade ilustrativa de um método para liberar o DNA em células de Zea mays por aceleração é um sistema de liberação de α- partícula biolísticos, que pode ser usado para propelir as partículas revestidas com DNA através de uma tela, tal como uma tela de aço inoxidável ou Nytex, em uma superfície de filtro coberta com células de milho cultivadas em suspensão. Um sistema de liberação de partícula apropriado para uso com a presente invenção é o injetor de aceleração de hélio PDS-1000/He disponível de Bio-Rad Laboratories.
[00172] Para o bombardeio, as células em suspensão podem ser concentradas em filtros. Os filtros contendo as células a serem bombardeadas são posicionados em uma distância apropriada abaixo da placa de parada de microprojétil. Se desejado, uma ou mais telas são posicionadas também entre o injetor e as células a serem bombardeadas.
[00173] Alternativamente, os embriões imaturos ou outras células alvo podem ser arranjados no meio de cultura sólido. As células a serem bombardeadas são posicionadas em uma distância apropriada abaixo da placa de parada de microprojétil. Se desejado, uma ou mais telas são também posicionadas entre o dispositivo de aceleração e as células a serem bombardeadas. Com o uso das técnicas determinadas aqui pode-se obter até 1000 ou mais foci de células transitoriamente expressando um gene marcador. O número de células em um focus que expressam o produto de gene exógeno 48 horas pós-bombardeio frequentemente varia de um a dez e média de um a três.
[00174] Na transformação de bombardeio, pode-se otimizar as condições de cultivo de pré-bombardeio e os parâmetros de bombardeio para render os números máximos de transformantes estáveis. Os parâmetros físicos e biológicos para o bombardeio são importantes nesta tecnologia. Os fatores físicos são aqueles que envolvem manipular o precipitado de DNA/microprojétil ou aqueles que afetam o voo e a velocidade de macro ou microprojéteis. Os fatores biológicos incluem todas as etapas envolvidas na manipulação de células antes e imediatamente depois do bombardeio, o ajuste osmótico de células alvo para ajudar a aliviar o traumatismo associado com o bombardeio, e também a natureza do DNA de transformação, tal como o DNA linearizado ou plasmídeos superenrolados intactos. Acredita-se que as manipulações de pré-bombardeio são especialmente importantes para a transformação bem-sucedida de embriões imaturos.
[00175] Em outra modalidade alternativa, os plastidos podem ser estavelmente transformados. O método divulgado para a transformação de plastido em plantas mais elevadas inclui a liberação de injetor de partícula de DNA contendo um marcador selecionável e direcionar o DNA ao genoma de plastido com a recombinação homóloga (US 5.451.513, US 5.545.818, US 5.877.402, US 5.932479, e WO 99/05265).
[00176] Consequentemente, é contemplado que pode-se desejar ajustar vários aspectos dos parâmetros de bombardeio em estudos de pequena escala para integralmente otimizar as condições. Pode-se particularmente desejar ajustar os parâmetros físicos, tais como distância de abertura, distância de voo, distância de tecido, e pressão de hélio. Pode-se também minimizar os fatores de redução de traumatismo modificando as condições que influenciam o estado fisiológico das células recipientes e que podem, portanto, influenciar eficiências de transformação e integração. Por exemplo, o estado osmótico, hidratação de tecido e o estágio de subcultura ou ciclo celular das células recipientes podem ser ajustados para transformação ótima. A execução de outros ajustes rotineiros será conhecida aos de habilidade na técnica em luz da presente divulgação.
[00177] A transferência mediada por Agrobacterium é um sistema extensamente aplicável para introduzir genes em células de planta, pois o DNA pode ser introduzido em tecidos de planta inteiros, desse modo contornando a necessidade para regeneração de uma planta intacta de um protoplasto. O uso de vetores de integração de planta mediados por Agrobacterium para introduzir o DNA em células de planta é conhecido na técnica (veja, por exemplo, US 5.177.010, US 5.104.310, US 5.004.863, US 5.159.135). Além disso, a integração de T-DNA é um processo relativamente preciso resultando em poucos rearranjos. A região de DNA a ser transferida é definida pelas sequências de borda, e o DNA de intervenção é geralmente introduzido no genoma de planta.
[00178] Os vetores de transformação de Agrobacterium modernos são capazes de replicação em E. coli bem como Agrobacterium, permitindo manipulações convenientes como descrito em (Klee e col., Plant DNA Infectious Agents, Hohn e Schell, eds., Springer-Verlag, New York, pp. 179-203 (1985)). Além disso, os avanços tecnológicos nos vetores para transferência de gene mediada por Agrobacterium melhoraram o arranjo de genes e sítios de restrição nos vetores para facilitar a construção de vetores capazes de expressar vários genes de codificação de polipeptídeo. Os vetores descritos têm as regiões convenientes multi- ligadoras flanqueadas por um promotor e um sítio de poliadenilação para a expressão direta de genes de codificação de polipeptídeo introduzidos e são apropriados para as presentes finalidades. Além disso, o Agrobacterium contendo genes Ti armados e desarmados pode ser usado para as transformações. Naquelas variedades de planta onde a transformação mediada por Agrobacterium é eficiente, é o método de escolha por causa da natureza fácil e definida da transferência de gene.
[00179] Uma planta transgênica formada usando métodos de transformação de Agrobacterium contém tipicamente um único lócus genético em um cromossomo. Tais plantas transgênicas podem ser referidas como sendo homozigóticas para o gene adicionado. Mais preferido é uma planta transgênica que seja homozigótica para o gene estrutural adicionado; isto é, uma planta transgênica que contenha dois genes adicionados, um gene no mesmo locus em cada cromossomo de um par de cromossomo. Uma planta transgênica homozigótica pode ser obtida sexualmente casando (autopolinização) uma planta transgênica segregante independente que contenha um único gene adicionado, germinando algumas das sementes produzidas e analisando as plantas resultantes para o gene de interesse.
[00180] Deve também ser compreendida que duas plantas transgênicas diferentes podem também ser casadas para produzir a prole contendo dois genes exógenos independentemente segregantes. Autopolinização de progênia apropriada pode produzir as plantas que são homozigóticas para ambos os genes exógenos. Cruzamento reverso para uma planta progenitora e cruzamento externo com uma planta não transgênica são também contemplados, como é a propagação vegetativa. Descrições de outros métodos de cruzamento que são comumente usados para traços diferentes e colheitas podem ser encontradas em Fehr, In: Breeding Methods for Cultivar Development, Wilcox J. ed., American Society of Agronomy, Madison Wis. (1987).
[00181] A transformação de protoplastos de planta pode ser conseguida usando os métodos baseados na precipitação de fosfato de cálcio, tratamento de polietileno glicol, eletroporação, e combinações destes tratamentos. A aplicação destes sistemas às variedades de planta diferentes depende da habilidade de regenerar essa cepa particular de planta dos protoplastos. Os métodos ilustrativos para a regeneração de cereais dos protoplastos são descritos (Fujimura e col., 1985; Toriyama e col., 1986; Abdullah e col., 1986).
[00182] Outros métodos de transformação de célula podem também ser usados e incluído, mas não são limitados à introdução de DNA em plantas por transferência direta de DNA no pólen, pela injeção direta de DNA em órgãos reprodutivos de uma planta, ou pela injeção direta de DNA nas células de embriões imaturos seguida pela reidratação de embriões secos.
[00183] A regeneração, desenvolvimento, e cultivo das plantas de únicos transformantes de protoplasto de planta ou vários explantados transformados são conhecidos na técnica (Weissbach e col., In: Methods for Plant Molecular Biology, Academic Press, San Diego, Califórnia, (1988). Este processo de regeneração e crescimento inclui tipicamente as etapas de seleção de células transformadas, cultivando aquelas células individualizadas através dos estágios usuais de desenvolvimento embrionário através do estágio enraizado de plântula. Os embriões e sementes transgênicas são similarmente regenerados. Os ramos enraizados transgênicos resultantes são plantados em um meio apropriado de crescimento de planta, tal como solo.
[00184] O desenvolvimento ou regeneração de plantas contendo o gene estrangeiro, exógeno é conhecido na técnica. Preferivelmente, as plantas regeneradas são auto- polinizadas para fornecer plantas transgênicas homozigóticas. Se não, o pólen obtido das plantas regeneradas é cruzado para plantas crescidas de semente de linhagens agronomicamente importantes. Inversamente, o pólen das plantas destas linhagens importantes é usado para polinizar plantas regeneradas. Uma planta transgênica da presente invenção contendo um ácido nucleico exógeno desejado é cultivada usando métodos conhecidos ao hábil na técnica.
[00185] Os métodos para transformar dicotiledôneas, primariamente por meio de Agrobacterium tumefaciens, e obter plantas transgênicas foram publicados para algodão (US 5.004.863, US 5.159.135, US 5.518.908); soja (US 5.569.834, US 5.416.011); Brassica (US 5.463.174); amendoim (Cheng e col., 1996); e ervilha (Grant e col., 1995).
[00186] Métodos para a transformação de plantas de cereal, tais como cevada para introduzir a variação genética na planta pela introdução de um ácido nucleico exógeno e para a regeneração de plantas dos protoplastos ou embriões de planta imaturos são conhecidos na técnica, veja por exemplo, CA 2.092.588, AU 61781/94, AU 667939, US 6.100.447, PCT/US97/10621, US 5.589.617, US 6.541.257, e WO 99/14314. Preferivelmente, as plantas de cevada transgênicas são produzidas por procedimentos de transformação mediados por Agrobacterium tumefaciens. Os vetores carregando o elemento de ácido nucleico desejado podem ser introduzidos em células de cevada regeneráveis de plantas ou explantados cultivados de tecido, ou sistemas de planta apropriados, tais como protoplastos.
[00187] As células de cevada regeneráveis são preferivelmente do escutelo de embriões imaturos, embriões maduros, calo derivado deste, ou tecido meristemático.
[00188] Para confirmar a presença dos transgenes em células e em plantas transgênicas, uma amplificação de reação em cadeia de polimerase (PCR) ou análise de Southern blot pode ser realizada usando os métodos conhecidos aos hábeis na técnica. Os produtos de expressão dos transgenes podem ser detectados em algumas de uma variedade de maneiras, dependendo da natureza do produto, e incluem o Western blot e ensaio de enzima. Uma maneira particularmente útil de dosar a expressão de proteína e detectar a replicação em tecidos de planta diferentes é usar um gene repórter, tal como GUS. Uma vez que as plantas transgênicas foram obtidas, podem ser crescidas para produzir tecidos de planta ou partes tendo o fenótipo desejado. O tecido de planta ou partes de planta podem ser colhido e/ou a semente ser coletada. A semente pode servir como uma fonte para crescer plantas adicionais com tecidos ou partes tendo as características desejadas.
TILLING
[00189] As plantas da invenção podem ser produzidas usando o processo conhecido como TILLING (Procura de Lesões Locais Induzidas em Genomas). Em uma primeira etapa, as mutações introduzidas, tais como novas únicas mudanças de pares de base são induzidas em uma população de plantas tratando sementes (ou pólen) com um mutagêneo químico, e então avançando plantas a uma geração onde as mutações serão herdadas estavelmente. O DNA é extraído, e as sementes são armazenadas de todos os membros da população para criar um recurso que pode ser acessado repetidamente com o tempo.
[00190] Para um ensaio de TILLING, os primers de PCR são projetados para especificamente amplificar um único alvo de gene de interesse. A especificidade é especialmente importante se um alvo é um membro de uma família de gene ou parte de um genoma poliplóide. Em seguida, os primers marcados por tinta podem ser usados para amplificar produtos de PCR do DNA escolhido de múltiplos indivíduos. Estes produtos de PCR são desnaturados e recozidos para permitir a formação de pares de base descombinados. As descombinações, ou heteroduplexes, representam polimorfismo de único nucleotídeo naturais (SNPs) (isto é, diversas plantas da população são prováveis de carregar o mesmo polimorfismo) e SNPs induzidos (isto é, somente as plantas individuais raras são prováveis de exobir a mutação). Após a formação de heteroduplex, o uso de uma endonuclease, tal como Cel I, que reconhece e cliva o DNA descombinado é a chave para descobrir SNPs novos dentro de uma população de TILLING.
[00191] Usando esta abordagem, muitos milhares de plantas podem ser selecionados para identificar o indivíduo com uma única mudança base, bem como inserções ou deleções pequenas (1-30 pb) em qualquer gene ou região específica do genoma. Os fragmentos genômicos sendo analisados podem variar no tamanho em qualquer lugar 0,3 a 1,6 kb. Na escolha em 8 vezes, fragmentos de 1,4 kb (discontando as extremidades de fragmentos onde a detecção de SNP é problemática devido ao ruído) e 96 linhas por ensaio, esta combinação permite até um milhão de pares de base de DNA genômico serem avaliados por um único ensaio, fazendo TILLING de uma técnica de alta produção.
[00192] TILLING é descrita em Slade e Knauf (2005) e Henikoff e col., (2004).
[00193] Além de permitir a detecção eficiente de mutações, a tecnologia de TILLING de alta produção é ideal para a detecção de polimorfismos naturais. Portanto, interrogar um DNA homólogo desconhecido por heteroduplexação a uma sequência conhecida revela o número e a posição de sítios polimórficos. O nucleotídeo muda e as inserções e deleções pequenas são identificadas, incluindo pelo menos alguns polimorfismos de número de repetição. Isto foi chamado Ecotilling (Comai e col., 2004).
[00194] Cada SNP é gravado por sua posição aproximada dentro de alguns nucleotídeos. Assim, cada haplotipo pode ser arquivado baseado em sua mobilidade. Os dados de sequência podem ser obtidos com um esforço incremental relativamente pequeno usando alíquota do mesmo DNA amplificado que é usado para o ensaio de clivagem descombinada. O primer de sequenciamento esquerdo ou direito para uma única reação é escolhido por sua proximidade ao polimorfismo. O software Sequencher realiza um alinhamento múltiplo e descobre a mudança de base, que em cada caso confirmou a faixa de gel.
[00195] Ecotilling pode ser realizado mais barato do que o sequenciamento completo, o método usado presentemente para a maioria da descoberta de SNP. As placas contendo o DNA ecotípico arranjado podem ser selecionadas ao invés de associações de DNA das plantas mutagenizadas. Pois a detecção é em géis com resolução de pares de base e padrões de fundamente são uniformes através das linhas, as faixas que são de tamanho idêntico podem ser combinadas, assim descobrindo e genotipando SNPs em uma única etapa. Desta maneira, o sequenciamento final do SNP é simples e eficiente, feito assim pelo fato que as alíquotas dos mesmos produtos de PCR usados para a seleção podem ser submetidas ao sequenciamento de DNA.
EXEMPLOS
Exemplo 1. Materiais e métodos
Isolamento e purificação de prolaminas
[00196] Para isolar prolaminas de cereais, a farinha integral (10 g) foi agitada por 30 min em 25°C em 200ml de tampão contendo 20 mM trietanolamina-HCl (TEA), 1% (peso/vol) ascorbato de sódio, 1% (peso/vol) polietileno glicol (MW 6000; PEG6000) e 200μl de coquetel inibidor de protease de planta (Sigma #P9599), ajustado ao pH 8. A suspensão foi centrifugada em 7.000 g para 15 min e os grânulos lavados duas vezes mais para remover as proteínas solúveis no tampão aquoso. Prolaminas nos grânulos lavados foram dissolvidas em 40ml de 50% (vol/vol) propan-2-ol contendo 1% (peso/vol) ditiotreitol (DTT), 1% (peso/vol) PEG6000, 1% (peso/vol) ascorbato de sódio agitando por30 min em 25°C. A suspensão foi centrifugada e as prolaminas foram precipitadas do sobrenadante com 2 volumes de propan- 2-ol e armazenadas em -20°C. Se necessário, uma alíquota equivalente a 10 g de farinha foi sedimentada pela centrifugação em 160 g em 4°C por 10 min, os grânulos foram redissolvidos em 10 ml de tampão (tampão A) que continha 25mM TEA, ureia recentemente deionizada 8M e 1% DTT, ajustados ao pH 6, ou outro tampões como descritos.
[00197] Uma fração de prolamina total foi purificada de cada amostra de grão por cromatografia líquida de proteína de fase-rápida reversa (RP-FPLC) como segue: Prolaminas (200μl) foram injetadas em uma coluna de Resource RPC 1 ml (Pharmacia) conectada em série com uma coluna de 3 ml similar. A coluna foi lavada com 2 ml de 95% solvente A/5% B solvente e prolaminas eluídas com um gradiente linear de 30 ml de 95% solvente A/5% solvente B para 100% de solvente B em 2 ml/min. O solvente A foi 0,1% (vol/vol) de ácido trifluoroacético (TFA) em água, solvente B foi 0,1% (vol/vol) de TFA em 60% (vol/vol) acetonitrila aquosa. O eluente correspondendo aos picos de proteína foi escolhido. Os controles solventes foram escolhidos similarmente dos exames sem injeção de proteína.
[00198] As hordeínas de cevada foram fracionadas por RP-FPLC como segue: Os procedimentos foram como acima exceto que o gradiente de eluição foi variado de modo que a concentração do solvente B fosse 50% em 4ml, 52% em 17ml, 56% em 34ml, 58% em 37ml, 60% em 41ml, 62% em 44ml, 64% em 47ml, 66% em 50ml, 100% em 53ml, 100% em 57ml. As frações de um ml foram coletadas e as frações 11-14 (#1), 19-23 (#2), 31-34 (#3), 43-51 (#4), 53-58 (#5) e 63-64 (#6) correspondendo aos picos A280 foram escolhidas.
Métodos analíticos
[00199] As frações de prolamina foram dissolvidas em ureia 6M, 2% (peso/vol) SDS, 1% (peso/vol) DTT, 0,01% (peso/vol) azul de bromofenol, Tris-HCL 0,0625 M (pH 6,8) em 25°C e examinadas por SDS-PAGE como segue. Uma alíquota de 5 μl da solução de prolamina-SDS foi carregada em géis de SDS-PAGE, usando pré-molde 245x110x0,5mm, 8-18% géis de gradiente de poliacrilamida (ExcelGel Pharmacia), e feita em 600V por 90 min em 15°C. Os géis foram lavados em 40% MeOH em ácido acético 10% por 30 min, então água por 10 min. As prolaminas foram tingidos por imersão no gel em 0,06% (peso/vol) Coomassie colloidal G250 em 8,5% ácido fosfórico por 30 min e os géis destingidos durante a noite em água. Cada gel foi calibrado com uma escada de proteína padrão de 10 kDa (BenchMark, Invitrogen).
[00200] As frações de hordeína foram dissolvidas também em 50% (vol/vol) álcool isopropílico aquoso, 1% (peso/vol) DTT, tratadas com um excesso de vinil-piridina para reduzir as ligações de disulfeto e examinadas por HPLC de fase reversa (RP-HPLC, Larroque e col., 2000) calibradas com prolaminas isoladas das linhagens de cevada Riso56 ou Riso1508 onde as famílias de hordeína B ou C inteiro, respectivamente, não são acumuladas devido à mutação (Doll, 1983).
[00201] Os níveis de proteína em extratos ou frações foram determinados pelo método de Bradford (1976). Tipicamente, o teor de proteína foi medido em um formato de 96 poços adicionando 10 μl de cada sobrenadante de DTT/propan-2-ol a 200μl de 1 em 5 diluição de concentrado de ensaio de proteína de Coomassie (BioRAD) em água, calibrada contra gamaglobulina, e medindo a absorvância em 595nm.
Ensaios de toxicidade de célula T ex vivo
[00202] Prolaminas (50 mg/ml em ureia 2M) foram diluídas com PBS contendo CaCl2 1 mM, para dar 62,5, 250, 625, 2500, ou 6250 μg de prolamina/ml e desaminadas adicionando 25 μl de cada solução a 100 μl de tTG de fígado de porquinho da Índia (transglutaminase (Sigma, T5398), 25μg/ml tTG em PBS contendo CaCl2 1 mM) e incubadas por 6 h em 37°C. As soluções não desaminadas foram preparadas similarmente pela incubação na ausência de tTG. Os controles solventes foram adicionados quanto para as concentrações mais elevadas de prolamina. Outros controles continham um peptídeo w-gliadina tóxico conhecido designado 626fEE em 50μg/ml, o peptídeo 626fEE sozinho ou com toxóide de tétano (50 unidades formadoras de luz/ml). O peptídeo w- gliadina 626fEE também conhecido como DQ2-w-l teve a sequência de aminoácido QPEQPFPQPEQPFPWQP (Id. de Seq. N°.: 1) e foi sintetizado por Mimotopes, Melbourne, Austrália. Sua identidade e pureza (91%) foram confirmadas pela espectrometria de massa e HPLC. O toxóide de tétano foi obtido de Commonwealth Serum Laboratories, Melbourne. Todas as soluções foram então congeladas em -20°C.
[00203] Vinte e um indivíduos com doença celíaca HLA-DQ24+ provados por biópsia, que tinham aderido a uma dieta sem glúten estrita por pelo menos três meses, foram fornecidos de 150g de cevada fervida diário por 3 dias, consumido como parte de sua dieta que permaneceu sem glúten. O sangue venoso heparinizado foi coletado imediatamente antes ou seis dias depois do começo do desafio dietético e células mononucleares de sangue periférico (PBMC) foram isoladas por centrifugação de densidade de Ficoll-Hypaque (Anderson e col., 2000) de cada amostra de sangue. As células PBMC foram ressuspensas no meio HT-RPMI completo (Invitrogen) contendo 10% de soro humano AB inativado por calor, escolhido. As prolaminas desaminadas ou não desaminadas e as soluções de controle foram descongeladas e 25μl adicionados aos poços contendo 100 μl de PBMC (3-8x105 PBMC por poço). Estes foram cultivados em 37°C durante a noite em placas de 96 poços (MAIP-S-45; Millipore, Bedford, MA). As culturas de controle foram feitas adicionando 25μl de PBS contendo CaCl2 1 mM (controles tampão sozinho). As concentrações finais de prolamina foram 2,5, 10, 25, 100 ou 250 μg/ml e a concentração final de ureia foi 50 mM. O nível de IFN-Y produzido em cada cultura, indicativo da toxicidade de cada prolamina, foi analisado visualmente pela formação de ponto usando anticorpos secundários de acordo com as instruções dos fornecedores (Mabtech, Estocolmo, Suécia) e o ponto de unidades formadoras de colônia (UFC) contado usando um leitor automatizado de ELISPOT (AID Autoimmun Diagnostika GmbH; Alemanha). Os resultados foram apresentados como o média de unidades de formação de colônia (UFC) + S.E. Tipicamente, o coeficiente percentual de intra-ensaio de variação de UFC/106 PBMC foi 14% baseado em seis ensaios duplicados de um controle positivo incubado com 0,5x106 células em seis indivíduos CD (todos com > 20UFC/poço).
Análise estatística
[00204] A análise de variância (ANOVA) ou t-testes que usam GenStat foi usada para determinar a significância das diferenças observadas para a UFC média produzida por células T isoladas dos indivíduos celíacos antes (n=10) ou após (n=21) um desafio dietético e incubadas com hordeínas, prolaminas ou controles.
[00205] As curvas de resposta para os 21 indivíduos pós-desafio foram muito diferentes e uma grande proporção da variabilidade foi devido a estas diferenças. A fim de considerar a resposta paciente diferente, um modelo de coeficientes aleatório foi feito. Esta é uma análise modelo misturada que é realizada usando a probabilidade máxima residual (REML) e que permite os termos aleatórios envolvendo o indivíduo (paciente) e o desafio (concentração de proteína) dentro do paciente. A fim de estabilizar a heterogeneidade substancial de variância os dados foram transformados em log antes desta análise. A fim de tratar o problema de contagens zero um foi adicionado a todos os dados antes de tomar registros. Os termos fixos no modelo foram a presença ou ausência de tTG e a fração de hordeína que foi envolvida, junto com sua interação.
[00206] Um modelo hiperbólico foi feito também à UFC média não transformada para células T de 21 pacientes de pós-desafio, expostos às seis frações de hordeína de tTG ou quatro preparações de prolamina de cereal tratadas tTG.
Transformação de cevada
[00207] As plantas de cevada transformadas podem ser produzidas pelo método de Tingay e col., (1997). Os elementos de gene em vetores binários podem ser introduzidos em uma cepa de Agrobacterium altamente virulenta (AGL1) por conjugação tri-progenitor, que é usado então para introduzir o T-DNA contendo o transgene e o gene marcador selecionável (codificando resistência à higromicina, expressa do promotor CaMV35S) em células regeneráveis do escutelo de embriões imaturos de cevada, como segue.
[00208] As sementes de cevada em desenvolvimento da variedade Golden Promise, 12-15 dias após a antese, são removidas do ponto de crescimento de plantas crescidas em estufa e esterelizadas por dez minutos em 20% (vol/vol) de descorante seguido pelo enxágue uma vez com etanol 95% e sete vezes com água estéril. Os embriões (aproximadamente 1,5 a 2,5mm em tamanho) são então removidos das sementes sob condições assépticas e o axila cortado de cada embrião. Os embriões são colocados de corte para baixo em uma placa de petri contendo o meio de indução de calo. Os transconjugants de Agrobacterium são crescidos em caldo MG/L (contendo 5g de manitol, 1g de ácido L-glutâmico, 0,2g de KH2PO4, 0,1 g de NaCl, 0,1 g de MgSO47H2O, 5 g de triptona, 2,5 g de extrato de levedura e 1 μg de biotina litro, pH 7,0) contendo espectinomicina (50mg/L) e rifampicina (20 mg/L) com aeração em 28°C a uma concentração de aproximadamente 2-3 x 108 células/ml. Então, aproximadamente 300μl da suspensão de célula é adicionado aos embriões em uma placa de petri. Após 2 min, o excesso de líquido é escorrido da placa e os embriões são virados de modo que o lado de corte (lado da axila do escutelo) esteja para cima. Os embriões então são transferidos para uma placa fresca de meio de indução de calo e colocados no escuro por 2-3 dias em 24°C. Os embriões são transferidos ao meio de indução de calo com seleção (50μg/ml de higromicina e 15 μg/ml de timentina).
[00209] Os embriões permanecem neste meio por 2 semanas no escuro em 24°C. Os calos saudáveis então são divididos e colocados em meios de seleção frescos e incubados por duas semanas adicionais em 24°C no escuro. Depois disto, os embriões são incubados em 24°C na luz por 2 semanas em meio de regeneração contendo citoquinina e transferidos aos meios de enraizamento contendo citoquinina e auxina por três períodos de 2 semanas. As plantas juvenis são transferidas então à mistura de solo e mantidas em um banco de bruma por duas semanas e finalmente transferidas a uma estufa.
Métodos de mutagênese incluindo a irradiação gama
[00210] A mutação de genes na cevada conduzindo à expressão reduzida de D, C, B ou Y-hordeínas pode ser conseguida com a irradiação de raio gama ou mutagênese química, por exemplo, com etil metano sulfonato (EMS). Para a mutação induzida por raio gama, sementes pode ser irradiada em uma dose de 20-50 kR de uma fonte 60Co (Zikiryaeva e Kasimov, 1972). A mutagênese de EMS pode ser realizada tratando as sementes com EMS (0,03%, vol/vol) como por Mullins e col. (1999). Em um fundo duplo nulo de B+C, os grãos mutantes podem ser identificados com base no teor de proteína ou hordeína diminuído ou na morfologia alterada do grão e confirmado pelos métodos descritos acima. Os mutantes em um gene de hordeína podem ser cruzados com um segundo mutante para combinar as mutações e produzir uma variedade não transgênica de cevada que falta substancialmente hordeínas no endosperma.
Exemplo 2. Toxicidade de hordeínas de cevada aos celíacos
Composição de prolamina de cevada e outros cereais
[00211] Prolaminas foram isoladas como proteínas solúveis em álcool aquoso dos cereais tóxicos aos celíacos, cevada e trigo, as aveias menos tóxicas e milho não tóxico e purificadas por uma rodada de RP-FPLC como descrito no Exemplo 1. Os perfis de eluição de proteína das prolaminas como determinados por A280nm no RP-FPLC (figura 1) mostraram uma série de picos parcialmente resolutos devido às proteínas individuais eluídas pelo gradiente de solvente altamente crescente. As frações contendo a proteína das 10 purificações para cada cereal foram combinadas e liofilizadas. O rendimento típico de prolamina de vários cereais (2g) foi: milho, 10 mg; aveia, 23mg; cevada, 73mg; e trigo, 114mg. As prolaminas totais de cada cereal foram liofilizadas e armazenadas para teste no ensaio de célula T ex vivo (abaixo). Os controles solventes foram preparados também do procedimento de RP-FPLC.
[00212] As prolaminas de cevada (hordeínas) foram também fracionados por RP-FPLC como descrito no exemplo 1. O perfil de eluição obtido durante o fracionamento em um experimento inicial é mostrado na figura 2. Seis picos foram obtidos e a proteína de cada um foi recuperada. As frações escolhidas correspondentes de vinte injeções sequenciais foram combinadas e liofilizadas. Os rendimentos típicos de 4g de farinha integral foram: fração 1, 19mg; fração 2, 26mg; fração 3, 14mg; fração 4, 104mg; fração 5, 24mg e fração 6, 11mg.
[00213] A identidade das hordeínas em cada fração foi estabelecida por SDS-PAGE como descrita no exemplo 1 e confirmada por RP-HPLC analítico. Os resultados são mostrados nas figuras 3 e 6. HPLC mostrou que a fração #1 continha aproximadamente 39% de hordeína D, que correu em 90 kDa em SDS-PAGE, e aproximadamente 61% de hordeína C que correu em 47 kDa e 48 em SDS-PAGE (figura 3, #1). A fração #2 continha C hordeínas como mostrados por SDS-PAGE e por HPLC. A fração #3 continha uma faixa larga de proteína que correu em aproximadamente 45 kDa em SDS-PAGE, mas que resolveu em 6 picos em HPLC, correspondendo à eluição de C e B hordeínas. A composição foi estimada por HPLC como contendo aproximadamente 43% e 57% de C e B hordeínas, respectivamente. Frações #4, 5, 6, continham B hordeínas; estas frações podem também conter uma pequena quantidade de gama-hordeína. A eletroforese bidimensional e impressão digital de massa tríptico destas frações de hordeína não produziram fragmentos originais de peptídeo suficientes para identificar inequivocadamente hordeínas individuais. Isto pode ser devido às leves variações de sequência entre as hordeínas isoladas e as sequências disponíveis nas bases de dados. O fracionamento neste experimento, portanto resultou no enriquecimento para hordeínas particulares de cevada, mas a purificação não completa. A purificação adicional pode ser conseguida por rodadas adicionais de RP- FPLC ou RP-FLPC combinado com os métodos de troca iônica.
[00214] As amostras de cada fração de hordeína foram tratadas ou não tratadas com tTG, que converte resíduos de glutamina nas proteínas ao glutamato, e então liofilizadas para uso nos ensaios de célula T.
Ensaios de toxicidade
[00215] Os ensaios de célula T que usam PBMC isolado dos indivíduos confirmados de doença celíaca foram realizados como descritos no exemplo 1 para estabelecer a toxicidade das preparações de prolamina totais e frações de hordeína. PBMC foram isolados antes e depois do desafio dietético com cevada, e as amostras de prolamina foram tratadas ou não tratadas com tTG. As células T isoladas de um subconjunto de 10 celíacos antes de um desafio dietético foram sem resposta às prolaminas. A análise estatística que usa ANOVA mostrou que não há nenhuma diferença significativa (P) entre o número médio de pontos positivos de IFN-Y para as concentrações mais elevadas de toda prolamina tratada com tTG, peptídeo ou frações de hordeína (média de grupo UFC±S.E. 1,52±0,18) e as culturas de controle (média UFC±S.E. 1,40±0,45). Ao contrário, a análise mostrou que as células T pré-desafio reagiram fortemente (P<0,001) ao toxóide de tétano de controle positivo (Média UFC±S.E. 22,3±4.72) comparado às prolaminas. Isto mostra que as células T isoladas eram funcionais e capazes de reação a uma toxina conhecida e confirma que havia poucas células T reativas de prolamina nas populações isoladas antes do desafio dietético.
[00216] Em contraste com a falta de resposta às prolaminas antes do desafio dietético, as células T isoladas depois do desafio dietético foram altamente reativas. As células T isoladas de 21 celíacos, 6 dias pós- desafio, responderam fortemente às prolaminas tratadas com tTG quando comparadas às células T de um subconjunto (n=13) deste grupo expostas às prolaminas não desaminadas. A Figura 4 mostra que dos cereais, as prolaminas totais de cevada induziram o número mais elevado de UFCs seguido por ordem decrescente pelas prolaminas de trigo, aveia e então milho (figura 4 painéis A, B, C, D, respectivamente). Embora a prolamina de milho provoque uma baixa resposta de célula T dose-dependente nestes ensaios, não provoca uma resposta em desafios dietéticos e é normalmente considerada um cereal seguro para celíaco. A digestão intestinal pode destruir epítopos presentes nas prolaminas de milho integral que permaneceram intactos em nosso ensaio e células T estimuladas in vitro.
[00217] Das frações de hordeína, as frações #1, #2 e #3 produziram números mais elevados de UFC do que as frações #4, #5 e #6 de hordeína (figura 5).
[00218] Como a concentração de prolamina nos ensaios foi aumentada, o número de pontos IFN-Y aumentou em uma maneira hiperbólico em uma forma similar à cinética de enzima de Michaelis-Menten vista frequentemente entre uma enzima e seu substrato (Figuras 4 e 5), embora não fosse claro porque isto ocorreu para estes ensaios celulares.
[00219] Cada placa de 96 poços continha um número de controles positivos e negativos internos. Havia uma pequena diferença, mas significativa (P<0,001) entre UFC média quando as culturas de controle e controles solventes foram comparados (culturas controle UFC 2,75±0,67 e 1,49±0,24; solvente controle UFC 2,64±0,23 e 2,75±0,23 na ausência e presença de tTG respectivamente). Embora estatisticamente significativos estes valores foram muito pequenos comparados ao UFC pós-desafio nos controles positivos ou a prolamina contendo ensaios. Isto confirmou que as impurezas de solvente não geraram falsos positivos. O peptídeo de controle positivo 626fEE, deu uma resposta consistentemente elevada (Média UFC±S.E. 29,55±4,38 e 33,60±2,97 na ausência e presença de tTG respectivamente). A falta de resposta de 626fEE ao tTG foi esperada já que este peptídeo foi sintetizado com um glutamato no 10° resíduo e não exige o tratamento de tTG para toxicidade. A adição de solvente controle não inibiu significativamente a resposta do peptídeo 626fEE positivo (P=0,13), confirmando que as impurezas de solvente não geraram falsos negativos. A consistência placa a placa dos controles de toxóide de tétano (P=0,193) confirmou que as diferenças na resposta de célula T às prolaminas não foram devidas a variação placa a placa, mas refletiu a sensibilidade deferente de populações de célula T dos indivíduos diferentes.
[00220] A variação entre indivíduos diferentes à mesma concentração de prolamina variou por 200 vezes. Portanto, um modelo de coeficientes REML aleatório foi feito aos dados normalizados de UFC e descobriu-se que um modelo permitindo a curvatura em respostas de pacientes devido às concentrações diferentes da proteína deu um ajuste significativamente melhor (P<0,001) aos dados do que um modelo que coubesse uma única resposta de paciente apesar da concentração, com o desvio mudando de 1982,28 (1616 df) para 1640,91 (1613 df). Os efeitos principais devido ao tTG (P<0,001) e a fração de prolamina (P<0,001) não foram altamente significativos e não houve nenhuma interação entre eles. Isto confirmou que as células T responsivas à prolamina foram induzidas em indivíduos celíacos seis dias após o desafio dietético com cevada. Os meios feitos, em uma escala de log, para os dados normalizados de UFC foram 1,613 (nenhum tTG) e 2,026 (mais tTG) com um erro padrão de diferença (SED) de 0,0527, confirmando que o pré-tratamento com tTG teve um efeito significativo nas respostas. Os meios feitos para as frações #1- #6 de hordeína foram 1,903, 1,909, 1,956, 1,693, 1,724 e 1,733 respectivamente com um SED de 0,0826. Estes resultados mostram que as frações de hordeína caem em dois grupos significativamente diferentes de toxicidade com frações de hordeína #1, #2 e #3 formando um grupo mais tóxico do que as frações de hordeína #4, #5 e #6.
[00221] Foi interessante notar que as frações de hordeína mais tóxicas foram eluídas primeiro do FPLC de fase reversa e HPLC, e, portanto, eram mais polares do que as últimas frações eluídas menos tóxicas.
Conclusões
[00222] As células T isoladas de 21 celíacos, 6 dias pós-desafio, responderam fortemente às prolaminas tratadas com tTG em comparação às prolaminas não desaminadas como esperado para a doença celíaca (Hadjivassiliou e col., 2004; Kim e col., 2004). Isto poderia ser explicado por uma interação entre as prolaminas desaminadas e um sítio de ligação em uma proteína chave, tal como a molécula HLA-DQ2, que apresentou as proteínas estimulatórias aos receptores em células T CD4+ envolvidas na resposta inflamatória.
[00223] Embora houvesse diferenças mensuráveis na toxicidade de frações de hordeína, todas as hordeínas foram significativamente mais tóxicas do que as prolaminas de milho e aveia, que são consideradas como seguras para a maioria dos celíacos. As análises estatísticas mostraram que as prolaminas de cevada e as frações de hordeína #1, #2 e #3 (contendo D e C hordeínas) formaram o grupo mais tóxico. As frações de hordeína #4, #5 e #6, contend principalmente hordeínas B, e prolaminas de trigo formaram um segundo grupo menos tóxico. A aveia e as prolaminas de milho formaram o grupo menos tóxico. Isto indicou que as células T induzidas nos celíacos por um desafio de cevada foram menos sensíveis ao trigo e a aveia. Isto pode ser devido aos epítopos dominantes em prolaminas de cevada diferirem consideravelmente daqueles em prolaminas de trigo e aveia. Embora os dados feitos indicassem que as prolaminas de aveia eram significativamente menos tóxicas do que as de cevada, havia uma variação de cinquenta vezes entre os indivíduos diferentes à mesma concentração de prolamina de aveia, com células T de cinco dos 21 indivíduos tendo mais de 20 UFC na concentração de prolamina mais elevada. Isto foi consistente com outros relatos dos indivíduos com respostas celíacas sérias às aveias (Arentz-Hansen e col., 2004; Lundin e col., 2003).
[00224] Considerou-se baseado provavelmente nestes dados que, em um desafio dietético, todas as frações de hordeína provocariam uma reação intestinal significativa em celíacos. Isto sugeriu que todas as frações de hordeína precisariam ser deletadas ou modificadas para produzir a cevada que fosse completamente não tóxica aos celíacos. Também sugeriu que as hordeínas B e C, os componentes principais, deveriam ser removidos ou modificados primeiramente.
Exemplo 3. Produção de grão de cevada reduzida para hordeínas B e C
[00225] Vários mutantes de cevada afetados na síntese ou acumulação de hordeína têm sido previamente identificados. Estes mutantes de cevada não foram isolados com a finalidade de reduzir hordeínas no grão, mas foram isolados e selecionados para níveis aumentados de lisina no grão e subsequentemente descobertos serem reduzidos por hordeínas.
[00226] O mutante Riso 7, descrito primeiramente por Doll e col. (1976), foi identificado após o tratamento de nêutron rápido do Bomi progenitor. Continha uma mutação recessiva em um gene que resultou em uma diminuição de 29% em prolaminas e um aumento de 10% no teor de lisina da proteína relativa ao Bomi. A redução nos prolaminas pobres em lisina foi compensada por um aumento em outras proteínas de armazenamento relativamente ricas em lisina, resultando no teor elevado de lisina. O rendimento de grão e teor de amido foram reduzidos por 6% e 7%, respectivamente, comparados ao progenitor (Talberg, 1982; Doll, 1983).
[00227] Riso 56, primeiramente descrito por Doll e col. (1973), foi criado pela mutação de raio gama do Carlsberg II progenitor. O tamanho de semente, rendimento de grão, e teor de prolamina foram diminuídos por 30%, 47%, e 25%, respectivamente, relativo ao progenitor quando o teor de lisina da proteína no grão mutante foi aumentado por 13% comparado ao progenitor. O teor de hordeína foi associado com nitrogênio de não proteína aumentado proteínas solúveis em sal e água (Shewry PR e col. 1980). O teor elevado de lisina de proteínas em Riso 56 foi devido a uma mutação recessiva no cromossomo 5 (Ullrich e Eslick, 1978) em um locus genético designado Hor2ca (Doll, 1980). A mutação incluiu uma deleção de 80-90 kb de DNA do locus Hor2 que codificou as hordeínas B na cevada. A expressão de proteínas de B hordeína foi reduzida em 75% no mutante enquanto a expressão C hordeína foi aumentada 2 vezes (Kreis e col., 1983). A deleção não foi relacionada à translocação entre o cromossomo 2 e 5 que estavam também presentes em Riso 56 (Olsen, 1977).
[00228] Riso 527, descrito primeiramente por Doll e col. (1973), foi criado também pela mutação de raio gama, mas do progenitor Bomi. O tamanho de semente, rendimento de grão e teor de prolamina do grão foram diminuídos por 13%, 25%, e 20%, respectivamente, relativo ao progenitor enquanto o teor de lisina de proteína no mutante foi aumentado por 12%. A mutação foi recessiva, em um gene no cromossomo 6 designado lys6i (Jensen, 1979). Este mutante tinha níveis diminuídos de D hordeína e níveis aumentados de B1 hordeína (Klemsdal e col., 1987).
[00229] Riso 1508 foi identificado após a mutação de EMS do progenitor Bomi (Doll e col., 1973; Ingerversen e col., 1973; Doll, 1973). O tamanho de semente, rendimento de grão e teor de prolamina de grão foram diminuídos por 8%, 12%, e 70%, respectivamente, relativo ao grão progenitor quando o teor de lisina de proteína no mutante foi aumentado por 42%. O teor elevado de lisina foi devido a uma mutação recessiva em um gene situado perto da região de centrômero do cromossomo 7 de cevada (Karlsson, 1977). Este gene foi designado primeiramente como sex3c xenia de endosperma encolhido (Ullrich e Eslick, 1977), mas é conhecido agora geralmente como lys3a (Tallberg, 1977). Os níveis relativos de tipos de proteína no grão utante foram mudados, com mais proteína solúvel em água (albumina/globulina) aumentada de 27% a 46% do nitrogênio de proteína de semente total e de menos prolamina, diminuída por 70% relativo ao progenitor, 29% a 9% de nitrogênio total da proteína de semente (Ingerversen e col., 1973; Doll, 1973). Havia um aumento de quatro vezes em aminoácidos livres e N não proteína em Riso 1508, comparado ao progenitor quando as plantas foram crescidas sob altos níveis de fertilizante de nitrogênio (Koeie e Kreis, 1978). Shewry e col. (1978) confirmaram que o nível de nitrogênio de proteína não solúvel em sal foi dobrado. A proporção de nitrogênio de semente quando a hordeína foi diminuída por 70% e as proteínas solúveis em sal aumentadas por 70% em Riso 1508 foi comparada a Bomi. A análise molecular detalhada mostrou que os níveis de hordeínas B e C foram reduzidos por 80% e 93%, respectivamente, quando as D hordeínas foram aumentadas quatro vezes. Estes efeitos na acumulação de proteína foram devido às mudanças na abundância ou estabilidade de mRNA (Kreis e col., 1984). Isto poderia ter sido mediado pela metilação aumentada dos promotores dos genes codificando as hordeínas B e C no mutante 1508 de Riso (Sorensen e col., 1996). O tamanho menor de semente de Riso 1508 foi principalmente devido à síntese reduzida de amido (Koeie e Breis, 1978; Kreis e Doll, 1980; Doll, 1983). Os açúcares foram aumentados o dobro enquanto a síntese de amido foi diminuída por aproximadamente 20-30% em Riso 1508 comparado ao progenitor. Kreis (1979) relatou que os níveis de β-amilase foram reduzidos em Riso 1508 quando Hejgaard e Boisen (1980) relataram níveis similares de e-amílase.
[00230] Hiproly foi um mutante espontâneo identificado de germplasm etiópio CI 3947 (Munck e col., 1970) que tinha níveis aumentados de proteína total e proteína lisina, aumentados por 20-30% relativo à cevada do tipo selvagens (Doll, 1983). Quando cruzado à cevada tipo selvagem, o alto teor de proteína foi perdido quando o teor aumentado de lisina de proteína foi retido, demonstrando que estes traços foram independentemente herdados. O teor de lisina aumentado foi devido a uma única mutação recessiva no gene lys no cromossomo 7. A mutação aumentou o nível de proteínas solúveis em água e sal e desse modo o teor de lisina. Ao contrário dos mutantes alta lisina de Riso, os níveis de hordeína e o peso de semente em Hiproly não foram diminuídos na progênia recruzada. O nitrogênio de não proteína foi também aumentado. O teor de e-amílase foi aumentado 4 vezes (Hejgaard e Boisen, 1980).
Caracterização das linhagens progenitoras Riso 56 e Riso 1508
[00231] As características de prolaminas acumuladas pelas linhagens progenitoras Riso 56 e Riso 1508 foram confirmadas por SDS-PAGE e HPLC de fase reversa. As proteínas solúveis em sal extraídas do grão foram separadas por eletroforese em gel e transferidas às membranas (western blotting). Os padrões de proteína nas membranas tingiram a proteína total (figura 7, lado esquerda) ou tratadas com um anticorpo monoclonal específico de prolamina (anticorpo monoclonal de camundongo MAb12224, criado contra um extrato de glutenina total, e que detecta todas hordeínas e prolaminas (Skerritt, 1988) (lado direito)) mostrou que os níveis de B hordeínas foram muito baixos em Riso 56 enquanto os níveis de C hordeínas foram aumentados relativos aos níveis de Riso 527. A detecção de anticorpo confirmou que o nível de B hordeínas no extrato de Riso 56 foi extremamente baixo (caixa pontilhada). As três proteínas vistas em Riso 56 que co-migraram com as B hordeínas eram mais provavelmente Y-hordeínas- Em Riso 1508, a acumulação de B hordeínas foi reduzida enquanto em C- hordeínas foi mal detectável (caixa pontilhada). Isto foi consistente com a literatura publicada. Os níveis de D hordeína, que era um componente de prolamina relativamente menor, não pareceram ser aumentados nos carregamentos de proteína usados neste gel.
[00232] A Figura 8 mostra os níveis relativos das hordeínas diferentes em extratos purificados após a análise de FPLC de fase reversa. Os extratos de hordeína equivalentes a 0,2 g de farinha foram analisados por FPLC como descrito no exemplo 1. Portanto, a área sob os cromatogramas A280 foi proporcional ao teor de proteína relativo de cada amostra. Em Riso 56, os níveis de C hordeínas foram aumentados por 400% e de B hordeínas diminuídos por 86% comparados ao progenitor Carlsberg II. Em Riso 1508, as hordeínas C e B foram reduzidas (91% e 86%, respectivamente) comparado ao progenitor Bomi. Estes padrões foram similares aos dados publicados.
Identificação de sementes tendo ambas mutações de hordeína
[00233] As plantas das linhagens Riso 56 e Riso 1508 foram cruzadas por emasculação de Riso 1508 e dois dias mais tarde polinizando-as com pólen fresco de Riso 56. Dez sementes F1 foram germinadas e as plantas F1 crescidas e reservadas para autofertilizar. As sementes F2 foram colhidas na maturidade.
[00234] Para identificar mutantes duplos na população, a metade de cada uma das 288 sementes F2 foi individualmente esmagada e moída a um pó em um microtubo de plástico com uma esfera de aço inoxidável, agitados em 30/s por 3 x 1,5 min em um moinho de vibração de 96 poços (Retsch Gmbh, Rheinische). Uma alíquota (400μl) de um tampão aquoso foi adicionada a cada tubo para extrair proteínas solúveis em água. O tampão continha 20 mM triethilamina-HCl (TEA), 1% (peso/vol) ascorbato de sódio, 1% (peso/vol) PEG6000 e 1/1000 de diluição de inibidor de protease de planta (Sigma P9599), pH 8 em temperatura ambiente (TA). Os teores de cada tubo foram agitados novamente e então centrifugados em 160 g por 10 min em TA. OS grânulos de farinha insolúveis em água foram lavados duas vezes mais na mesma maneira e os respectivos sobrenadantes retirados para as frações solúveis em água. As prolaminas solúveis em álcool nos grânulos foram então extraídas adicionando 400μl de 50% (vol/vol) propan-2-ol aquoso contendo 1% (peso/vol) DTT e agitação dos tubos como acima, seguido pela incubação por 30 min em TA, por uma segunda rodada de agitação e centrifugação como acima. Os respectivos sobrenadantes contendo as prolaminas extraídas foram escolhidos e transferidos aos tubos frescos. O teor de proteína em sobrenadantes de DTT/propan-2-ol foi medido com reagente de Coomassie (BioRAD) e as prolaminas em uma alíquota de 200μl foram precipitadas com 400μl de propan-2- ol e armazenadas durante a noite em -20°C.
[00235] Uma alíquota de cada extrato de meia semente de prolamina foi examinada para a perda de hordeínas B e C por SDS-PAGE como descrito no exemplo 1 (figura 9). Os géis de seleção foram carregados em uma base por semente, com cada linha carregando o equivalente de 1/20 de uma semente. Em particular, os extratos foram examinados para a ausência ou redução das faixas de proteína de hordeína características em 40 kDa (específico de hordeína B) e 70 kDa (específico de hordeína C). As sementes das linhagens progenitoras Riso 56 e Riso 1508 foram reduzidas para hordeínas B e C, respectivamente, mas ainda continham baixos níveis de hordeínas D em 100 kDa (figura 9). A maioria dos extratos de semente F2 continha um padrão do tipo selvagem com hordeínas D, C e B presentes (figura 9), confirmando que um cruzamento eficaz entre as duas linhagens progenitoras tinha sido feito. Dezesseis sementes pareceram faltar hordeínas B e C e foram, portanto, marcadas como homozigóticas para ambas as lesões genéticas presentes em progenitores. Estes foram identificados das 288 mais sementes (frequência 0,055). Isto foi similar a frequência de 1 em 16 (0,0625) esperada para a combinação de duas mutações simples recessivas.
[00236] Os níveis de proteína total nos extratos solúveis em álcool das meias sementes F2 foram comparados aos do tipo selvagem e sementes progenitoras. Os dados são mostrados na tabela 1. Os níveis de proteína nos extratos das sementes F2 foram reduzidos a menos de 20%, em alguns casos menos de 15% do tipo selvagem. Estes valores podem ter sido inflados pelos compostos de nitrogênio não proteína, tais como aminoácidos livres presentes nos extratos.
[00237] Tabela 1. Níveis de proteína em extratos solúveis em álcool de sementes de meia cevada F2.
[00238] As diferenças observadas em níveis de prolamina entre as linhagens F2 podem ter sido devido à segregação de outros genes ou mutações dos progenitores.
[00239] Os géis de proteína adicionais foram corridos tomando um volume do sobrenadante de DTT/propan-2- ol contendo 20μg de proteína, secando cada um sob vácuo em um SpeediVac, dissolvendo a proteína em 20μl de um tampão contendo 62,5 mM Tris-HCl (pH 6,8), 12,5% (peso/vol) glicerol, 2% (peso/vol) SDS, 1% (peso/vol) DTT, e 0,112% (peso/vol) azul de bromofenol, e aquecimento em um banho maria fervente por 90 s. Cada solução foi carregada em um gel pré-fabricado de SDS-poliacrilamida, feita eletroforese, tingida e examinada como descrito acima. Um gel típico é mostrado na figura 10. A maioria das sementes F2 selecionadas pareceram faltar as hordeínas B e C e foram presumidas serem “duplos nulos”. Mesmo que cada linha seja carregada com a mesma quantidade de proteína como medida pelo ensaio de proteína de ligação a corantes, a maioria dos extratos duplo nulos pareciam conter substancialmente menos proteínas do que os controles, em particular continham pouco mais de 20 kDa de material proteináceo. Isto poderia ser explicado pela presença dos compostos de nitrogênio de não proteína, tais como aminoácidos livres nos extratos que poderiam ter inflado os níveis de proteína aparentes como estimados pelo ensaio de proteína ligando ao corante. Este efeito foi visto também para extratos Riso 1508 onde o material tingível total correndo como faixas de proteína foi diminuído comparado ao Riso 56 ou Bomi. Riso 1508 foi mostrado por acumular mais N de não proteína como aminoácidos livres (Koie e Kreis, 1978).
[00240] A seção transversal de sementes F2 foi também examinada. Quando comparado ao tipo selvagem, em alguns casos, o endosperma de sementes duplo nulas aparentes pareceu moderadamente encolhido, em outros encolhidos mais severamente.
[00241] A segunda metade de cada uma das sementes F2 foi germinada em papel de filtro úmido, as plântulas F2 foram transferidas ao solo na estufa e crescidas à maturidade para fornecer a semente F3. Vários parâmetros de crescimento e rendimento de planta foram medidos (tabela 2).
[00242] Tabela 2. Parâmetros de crescimento e rendimento para plantas de cevada F2, classificadas de acordo com o peso de 100 sementes para a semente F3. Red. = reduzido para a hordeína especificada.
[00243] A altura de planta, cabeça e peso de caule, número de brotos, sementes per cabeça, e peso de 100 sementes foram medidos. O índice de colheita foi calculado da razão de peso de cabeça/(peso de caule + peso de cabeça). A semente F3 foi então crescida no campo para fornecer a semente F4 de cada linhagem.
[00244] As sementes F3 mostraram uma variação considerável em todos os parâmetros medidos quando comparadas aos progenitores e linhagem controle, Sloop. Muitas das linhagens duplo nulos aparentes, tais como J4 e 6RF, tiveram 100 pesos de semente reduzidos até por aproximadamente 40% ou números reduzidos de sementes por cabeça relativo ao K8 irmão tipo selvagem. Isto sugeriu que houve outros genes que segregam na população bem como as mutações de hordeína B ou C tendo um efeito no rendimento. Entretanto, diversas linhagens F3 tiveram pesos de semente superior ou igual aos progenitores e, portanto, era provável que os outros genes poderiam ser segregados longe das mutações de hordeína B e lys3a.
[00245] Na seção transversal, a aparência das sementes F3 variou de encolhida (similar ao Riso 1508) ao ligeiramente encolhido (similar ao Riso 56) quando comparada aos irmãos tipo selvagem ou controle Sloop.
[00246] As proteínas solúveis em álcool e solúveis em água totais de oito sementes F3 de diversas linhagens foram extraídas como descrito acima. O teor de proteína das frações solúveis em álcool e solúveis em água foi medido como descrito no exemplo 1 quantidades de uso conhecidas de gamaglobulina como um padrão de proteína. Entretanto os níveis de proteína solúvel em álcool totais em algumas amostras das sementes F3 foram essencialmente os mesmos que Riso 1508. Subsequentemente determinou-se que estas amostras de semente foram segregantes para o alelo do tipo selvagem do gene de lys3a e não foram uniformemente “duplo nulas”.
Quantificação de níveis de hordeína nas sementes F3 por RP-FPLC
[00247] Os extratos solúveis em álcool de duas sementes de cada linhagem foram combinados e 50μl foram examinados por RP-FPLC como descrito acima. Os cromatogramas são mostrados na figura 11. A área total sob os cromatogramas correspondendo à hordeína foi calculada e expressa relativo aos níveis em uma linhagem tipo selvagem. Os dados (tabela 3) mostraram que o grão F3 teve níveis de hordeína que foram menores do que 30% do nível tipo selvagem, em alguns casos menores de 20%, menores quanto 5,3%. A falta de faixas substanciais de proteína que seguem SDS-PAGE suporta a disputa que os níveis de proteína de álcool totais foram inflados devido aos níveis de nitrogênio de não proteína elevados nas sementes F3.
[00248] Tabela 3. Níveis de hordeína relativos nas sementes F3 medidas por RP-FPLC.
[00249] As características de sementes F4 crescidas no campo e crescidas na estufa das linhagens selecionadas (9RE, J1, G1, 4BH), progenitores único nulo (Riso 56 e Riso 1508), e cevada do tipo selvagem (Sloop; Bomi; e K8, um irmão tipo selvagem reconstituído do mesmo cruzamento que as linhagens duplo nulas) foram comparados.
Peso de semente
[00250] O peso de 100 sementes de sementes F4 crescidas na estufa variou de 60-76% de Sloop (5,47 + 0,16 g por 100 sementes), visto que o peso de 100 sementes F4 de grão crescido no campo foi menor, variando entre 58-65% de Sloop (4,75g + 0,04).
Germinação de grão
[00251] A germinação de sementes de duas linhagens de cevada F4 selecionadas foi comparada ao cv. Sloop tipo selvagem ao impregnar amostras de 100 grãos cada uma em papel úmido por seis dias. A germinação foi observada com o surgimento da ponta de raiz do revestimento de semente. Os grãos F4 pareceram germinar na mesma taxa que o grão do tipo selvagem, com aproximadamente 60-70% de germinação após 3 dias. O armazenamento do grão em 37°C por 4 semanas antes da imbebição aumentou ligeiramente o % de germinação de ambas as linhagens F4. Tratamento em 4°C por 3 dias também conseguiu o mesmo aumento sobre o material recentemente colhido.
[00252] Isto demonstrou que o grão das linhagens F4 não sofreu nenhum atraso sério de germinação, e, portanto, foi previsto por ser agronomicamente útil.
Níveis de proteína no grão F4
[00253] Os níveis de proteínas solúveis em água, sal, álcool, e ureia no grão das linhagens F4 foram medidos usando 20mg de amostras duplicadas de farinha integral das sementes F4 crescidas em estufa de linhagens selecionadas (9RE, J1, G1, 4BH), de progenitores único nulo (Riso 56 e Riso 1508), e cevada do tipo selvagem (Sloop; Bomi; e K8).
[00254] As proteínas solúveis em água foram extraídas de cada amostra de farinha usando 0,5 ml de água, misturando por 30 min, centrifugando a mistura em 13.000 rpm por 5 minutos, removendo o sobrenadante, e repetindo a extração nos grânulos duas vezes. Os sobrenadantes foram recolhidos (extrato solúvel em água) e os grânulos sequencialmente extraídos três vezes na mesma maneira usando 0,5 ml de NaCl 0,5M (extrato solúvel em sal), seguido por 0,5 ml de 50% (vol/vol) propan-1-ol contendo 1% (peso/vol) DTT (extrato solúvel em álcool (hordeínas)), seguido por ureia 8M contendo 1% (peso/vol) DTT (extrato solúvel em ureia). O teor de proteína de cada fração foi medido usando um ensaio de mistura de corantes (BioRad) de acordo com as instruções do fabricante, calibradas contra gamaglobulina como um padrão de proteína. Os dados são mostrados na figura 12. O teor de proteína extraível total (figura 12E), foi calculado da soma dos teores de proteína de todas as frações solúveis.
[00255] Além do nitrogênio total (N total; figura 12F) foi medido usando amostras duplicatas de 2,5 mg da mesma farinha pela análise elementar depois da combustão em 1800°C e redução ao N2 em 600°C, e quantificação por espectroscopia de massa (método de Dumas). O teor de proteína total foi calculado usando a expressão: teor de proteína = 6.63 x quantidade de N total. As figuras obtidas para níveis de proteína total por MS foram razoavelmente similares aos teores de proteína extraíveis totais estimados, mostrando que a extração da proteína foi eficiente.
[00256] O teor de hordeína (medido como o nível de proteína solúvel em álcool) do grão F4 foi reduzido a 1739% dos progenitores (R1508 e R56) e a 7-16% do cultivar Sloop tipo selvagem. Isto representou aproximadamente uma redução de 10 vezes no nível de hordeínas totais, mostrado acima por ser tóxico aos celíacos, destas amostras de grão relativas à cevada tipo selvagem, Sloop.
[00257] Os outros tipos de proteínas, em particular as proteínas solúveis em água e sal são pensadas por ter efeitos benéficos nas propriedades de fabricação de cerveja de grão de cevada. Já que os níveis de proteínas solúveis em água e sal dos grãos F4 foram similares aos do tipo selvagem Sloop, considerou-se que os grãos F4 teriam suficiente destas proteínas para finalidades de fabricação de cerveja.
Teor e composição de ácido graxo
[00258] Já que um principal reservatório de nitrogênio durante o crescimento e desenvolvimento das sementes tinha sido removido reduzindo as hordeínas, o grão mutante foi analisado para determinar se a semente em desenvolvimento poderia ter compensado aumentando o armazenamento de outros componentes, alguns do que poderia ser deletério ao uso do grão. Os ácidos graxos nas amostras 50mg duplicadas da farinha integral do grão F4 foram extraídos, misturados e analisados por cromatografia gasosa quantitativa (GC) usando o método de Folich e col. (1957).
[00259] A concentração de ácido graxo total no grão F4 de linhagens G1, BB5, J1, e J4 variou na faixa de aproximadamente 2,5% a 3% (peso/peso), e foram similares no nível em que no único nulo e o grão de cevada tipo selvagem. Concluiu-se que os grãos duplos nulos não continham níveis elevados de ácidos graxos.
[00260] Os ácidos graxos no lipídio de grão compreenderam principalmente ácidos linolêico (C18:2), olêico (C18:1) e palmítico (C16:0), com níveis inferiores de outros ácidos graxos. Não havia nenhuma diferença significativa nas concentrações de ácidos graxos individuais que tinham acumulado no grão F4 selecionado comparados aos únicos progenitores nulos ou a cevada do tipo selvagem. Em particular, a concentração de ácido erúcico (C22: 1n-9), que é tóxico aos humanos em concentração elevada, no grão F4 não foi aumentado. O grão mutante teve, portanto, teor e a composição de ácido graxo normais.
Níveis de amido
[00261] O amido é o componente principal de grão de cereal, compreendendo tipicamente aproximadamente 55 - 65% do peso seco. Os níveis de amido são particularmente importantes na cevada que é usada para maltagem. Um teor de amido que é muito baixo pode conduzir à formação de malte tendo teor de açúcar insuficiente para permitir a fermentação eficiente ocorrer durante a fabricação de cerveja, e, portanto, níveis de amido no grão de cevada foram medidos.
[00262] O amido do grão mutante foi isolado e essencialmente analisado como descrito no método Megazima (AACC76.13) usando 20 mg de amostras de farinha integral. Os níveis de amido totais no grão F4 estavam na faixa de 57% a 66% (peso/peso), e foram similares ao teor de amido dos progenitores único nulo e da cevada do tipo selvagem que estava na faixa de 51-64% (peso/peso).
[00263] Concluiu-se que os grãos de cevada F4 tiveram amido suficiente para permitir a produção de malte do grão.
Níveis de β glucano
[00264] O teor de β-glucan no grão mutante foi analisado como descrito no método de Megazima (AACC32.23), usando amostras de 20 mg de farinha integral, os níveis de β-glucan no grão de linhagens G1, BB5, J1, J4 estavam na faixa de 1,2 a 2,6% (peso/peso), e foram similares ao teor de β-glucan de grão progenitor de único nulo e o grão de cevada tipo selvagem que estavam na faixa de 2,4-3,3% (peso/peso).
[00265] Os níveis de β-glucan elevados estão envolvidos na formação de turvação de refrigeração na cerveja durante o armazenamento. Concluiu-se que o teor de β-glucan dos grãos F4 não foi elevado quando comparado aos grãos do tipo selvagem e os níveis eram improváveis de interferir com o desempenho da fabricação de cerveja destes grãos.
Níveis de aminoácido livre
[00266] A acumulação aumentada de aminoácidos livres poderia possivelmente ser deletéria para o uso do grão. Por exemplo, a asparagina livre em quantidades suficientes poderia formar o composto tóxico acrilamida se aquecida às altas temperaturas na presença de amido.
[00267] O teor e a composição de aminoácidos livres no grão foram medidos usando amostras replicatas de 20 mg de farinha integral crescida em estufa, sementes F4. As amostras foram dissolvidas em HCl 0,1N e uma alíquota foi tomada e seca, e os aminoácidos analisados usando a química de Waters AccQTag por Australian Proteome Analysis Facility (Sydney).
[00268] Os aminoácidos mais prevalentes nas farinhas de cevada foram prolina, asparagina, ácido glutâmico e aspártico por ordem decrescente, na faixa de 1,5 mg/g de farinha até 0,5 mg/g de farinha. O teor de prolina livre no grão F4 selecionada foi na faixa de 0,6-1,5 mg/g, e foi similar ao teor de prolina livre dos progenitores único nulo e cevada do tipo selvagem que estavam na faixa 0,2-1,2 mg/g. Os níveis de todos outros aminoácidos livres foram correspondentemente similares no F4 e grãos de controle. Em particular, o teor de asparagina livre no grão F4 foi aproximadamente 0,5 mg/g para as linhagens G1, BB5 e J1 e aproximadamente 1,0 mg/g na linhagem J4. Nos grãos progenitores de único nulo, o nível de asparagina livre foi 0,3 ou 0,9 mg/g, e nos grãos de cevada tipo selvagem, a asparagina livre estava na faixa de 0,3-0,6 mg/g.
[00269] Já que o teor de asparagina livre do grão F4 foi similar aos níveis no grão tipo selvagem correspondente, considerou-se que a produção de acrilamida da asparagina livre durante a maltagem ou outro uso do grão não seria diferente do que para o grão do tipo selvagem.
[00270] A lisina livre é conhecida por ser um aminoácido limitante na nutrição animal e, portanto, níveis deste aminoácido eram de interesse para uso potencial do grão como alimentação animal. O teor de lisina livre no grão F4 de linhagens G1, BB5 e J1 foi aproximadamente 0,5 mg/g e 1,0 mg/g no grão da linhagem J4. Isto representou um aumento de 181% - 1.020% comparado ao nível no grão do tipo selvagem de cultivar Sloop. Assim as linhagens F4 foram uma fonte mais nutritiva de lisina livre do que Sloop.
Exemplo 5. Teste de grãos F4 - teste de toxicidade de célula T
[00271] Para testar a toxicidade celíaca do grão F4, as hordeínas foram isoladas e purificadas das amostras de 10 g de farinha integral das sementes crescidas no campo de linhagens selecionadas 9JAE, J1, G1 e 4BH, progenitores de único nulo (Riso 56 e Riso 1508), e cevada do tipo selvagem (Sloop; Bomi; e K8) como descrito abaixo. As hordeínas purificadas foram adicionadas às células T isoladas de uma população de celíacos para testar para a toxicidade celíaca. O teste envolveu medir o número de células T que produziram gama-interferon seguindo a incubação durante a noite com a proteína purificada, usando um ensaio de anticorpo para o nível de gama-interferon. Isto é, o nível de gama- interferon foi uma indicação da extensão de toxicidade das proteínas no grão. Esta medida de toxicidade celíaca da farinha foi então traçada em função do peso fresco de farinha obtido do grão.
Purificação de prolaminas (hordeínas)
[00272] A farinha integral (10 g) foi agitada por 30 min em 25°C em 200ml de tampão contendo trietanolamina-HCl 20 mM (TEA), 1% (peso/vol) ascorbato de sódio, 1% (peso/vol) polietileno glicol (MW 6000; PEG 6000), e 1 μg/ml de inibidores de protease E64 e AEBSF (Sigma); o tampão ajustado ao pH 8. A suspensão foi centrifugada em 5.000 g por 5 min, o sobrenadante foi rejeitado e o grânulo lavado mais duas vezes. As proteínas nos grânulos lavados foram dissolvidas em 80ml de 50% (vol/vol) propan-2-ol, contendo 1% (peso/vol) DTT, agitando por 30 min em 60°C. A suspensão foi resfriada em 4°C por 10 minutos e centrifugada em 10.000g por 10 min em 4°C. As proteínas incluindo hordeínas no sobrenadante foram precipitadas com 2 volumes de propan- 2-ol durante a noite em -20°C, e sedimentadas em 10.000g por 10 min em 4°C, e os grânulos dissolvidos em 10 ml de tampão que continha ureia 8M recentemente deionizada, 1% DTT, 20 mM de TEA, ajustado ao pH 6.
[00273] As hordeínas foram purificadas por FPLC como segue. A solução de hordeína (1 ml) foi injetada em uma coluna de 8 ml de Cromatografia em fase reversa de fonte 15 (RPC, Pharmacia). A coluna foi lavada com 4 ml de 5% solvente B, e hordeínas eluídas com 2,5 ml de gradiente linear de 5% de solvente B a 35% de solvente B em 4 ml/min, seguido por um gradiente linear de 35% de solvente B a 83% de solvente B sobre 36 ml. O solvente A foi 0,1% (vol/vol) ácido trifluoroacético (TFA) em água, solvente B foi 0,1% (vol/vol) TFA em 60% (vol/vol) acetonitrila aquosa. As frações eluidas entre 25 e 43 ml foram escolhidas. Os controles de solvente foram similarmente escolhidos dos exames sem uma injeção. As seleções correspondentes de 10 injeções sequenciais foram combinadas, e liofilizadas.
Ensaios de célula T ex vivo
[00274] As hordeínas purificadas por FPLC (50 mg/ml em ureia 2M) foram diluídas com PBS contendo 1 mM CaCl2, para dar 25, 62,5, 125, 250, 625, 3.750, ou 6250μg de hordeína/ml e desaminadas adicionando 25 μl de cada solução a 100 μl de tTG de fígado de porquinho da Índia (Sigma; 25 μg/ml de tTG em PBS contendo CaCl2 1 mM) e incubado por 6 h em 37°C. As soluções não desaminadas foram similarmente preparadas pela incubação na ausência de tTG. Os controles solventes foram adicionados para as concentrações de hordeína mais elevadas. Outras amostras de controle continham controle de solvente, o controle solvente contendo uma toxina conhecida, o toxóide de tétano (50 unidades formadoras de luz/ml, obtido de Commonwealth Serum Laboratories, Melbourne); ou toxóide de tétano (50 unidades formadoras de luz/ml) sozinho. Todas as soluções foram então congeladas em -20°C.
[00275] As células T foram obtidas como segue. Seis, indivíduos celíacos HLA-DQ2+ provados por biópsia, aderindo a uma dieta estrita sem glúten por pelo menos três meses, consumiram 150g diários de cevada fervida por 3 dias. PBMC foi isolado por centrifugação de densidade Ficoll-Hypaque do sangue venoso heparinizado coletado imediatamente antes ou seis dias após o começo de desafio dietético, e foram ressuspensas em HT-RPMI completo contendo 10% de soro humano de AB escolhido inativado por calor. As hordeínas e desaminadas ou não desaminadas as soluções de controle foram descongeladas e 25 μl adicionados aos poços contendo 100 μl de PBMC (3-8x105 PBMC por poço), cultivado em 37°C durante a noite em placas de 96 poços (MAIP-S-45; Millipore, Bedford, MA) e comparado às culturas de controle (nenhuma adição) as quais foi adicionado 25 μl de PBS contendo CaCl2 1 mM sozinho. As concentrações de hordeína finais foram 0, 1, 2,5, 5, 10, 25, 150, ou 250 μg/ml. A concentração de ureia final mais elevada foi 10 mM. IFN-Y foi visualizado usando anticorpos secundários como nas notas dos fabricantes (Mabtech, Estocolmo, Suécia) como previamente descrito por Anderson e col. (2005), e o ponto unidades formadoras de colônia (UFC) contadas usando um leitor de ELISPOT automatizado (AID Autoimmun Diagnostika GmbH; Alemanha). Os resultados são apresentados como a média de unidades de formação de colônia (UFC)+S.E. contra o peso equivalente da farinha que conteria a quantidade calculada de hordeína. O teor de hordeína de cada amostra de farinha foi calculado no exemplo 5, permitindo o cálculo do peso de farinha.
[00276] Os dados foram analisados por GraphPAD Prisma e as curvas de melhor ajuste calculadas e mostradas com médias + S.E. Os valores r2 para os dados foram maiores do que 0,83, indicando um bom ajuste entre dados observados e a curva de melhor ajuste (figura 13).
Resultados
[00277] As células T isoladas de um único indivíduo celíaco antes de um desafio dietético foram menos responsivos às prolaminas adicionadas em 25 μg/ml do que as células T isoladas de mesmo indivíduo após um desafio dietético com cevada. A média UFC±S.E. de 29,5+3,0, e 104+15,9 foram observados para as células T isoladas antes e após um desafio dietético. Isto indicou que as células T específicas celíacos foram induzidas pelo desafio dietético.
[00278] Usando as células T isoladas de seis dias após o desafio dietético, o controle positivo, toxóide de tétano, deu uma resposta consistente na ausência e presença de tTG (Média UFC±S.E. 28,1±5,9 e 20,2±7,4, respectivamente). A adição do controle de solvente não significativamente inibiu a resposta do controle de toxóide de tétano positivo (Média UFC±S.E. 20,5+4,1 e 17,6±6,0 na ausência e presença de tTG respectivamente) confirmando as impurezas de solvente não geraram falsos negativos ou inibiram as respostas positivas.
[00279] As células T isoladas dos celíacos, 6 dias pós-desafio responderam mais fortemente a todas as frações de hordeína tratadas com tTG quando comparadas às células T expostas às hordeínas desaminadas como esperado para doença celíaca (Hadjivassiliou e col., 2004, Kim e col., 2004) (Figura 13 A; para maior clareza a resposta a somente duas amostras de hordeína, Sloop e G1, são mostradas). Isto confirmou que a resposta de célula T sendo medida foi relacionada à toxicidade celíaca.
[00280] Quando a concentração de hordeína foi aumentada, o número de UFC foi também aumentado em uma maneira hiperbólica como esperado para cinéticas de enzima de Michaelis-Menten normal entre uma enzima e seu substrato. Dois parâmetros são geralmente usados para descrever tais curvas: Bmax, o número máximo de UFC esperado na concentração mais elevada; e Kd, a concentração de proteína exigida para induzir metade do UFC máximo. Quanto mais tóxica a amostra de farinha, então mais baixo o Kd.
[00281] Os coeficientes Kd e Bmax foram calculados das curvas de melhor ajuste. Os valores de Bmax não variaram significativamente entre o tipo selvagem e mutantes, como esperado. Em contraste, os valores de Kd para as linhagens F4 foram mais elevados por um fator de 10 comparados às linhagens tipo selvagem (tabela 4). Isto é, aproximadamente 10 vezes mais farinha das linhagens mutantes foi exigida para induzir a resposta metade máxima de toxicidade do que para a farinha tipo selvagem (tabela 4). Assim foi concluído que a toxicidade celíaca do grão F4 tinha sido reduzida por aproximadamente 10 vezes comparado às linhagens tipo selvagem. Este nível de redução bem comparado com o nível de hordeína diminuído encontrado por determinação de proteína no grão F4.
[00282] Tabela 4. Toxicidade de célula T de farinha de cevada.
[00283] A toxicidade do grão F4 foi menor do que de Riso 56 como esperado. Entretanto a toxicidade do grão F4 foi similar a do outro progenitor Riso 1508. Subsequentemente, em uma caracterização genética adicional do grão F4, foi descoberto que isto foi devido à heterozigosidade da mutação da proteína de codificação de B-hordeína de gene nas linhagens F4 selecionadas, que tinha o efeito de elevar o teor de hordeína acima do esperado.
Exemplo 6. Maltagem de grão F4
[00284] Para determinar a conformidade do grão de cevada para maltagem, as análises incluindo testes de maltagem em faixa reduzida (micro-maltagem) foram realizadas.
[00285] Um fator que influencia a capacidade de maltagem é o tamanho de semente. As amostras do grão F4 foram analisadas para a distribuição de tamanho de semente contando a proporção de 1.000 sementes que foram retidas por telas de 2,8, 2,5 ou 2,2 mm. O grão F4 em média foi menor do que o tipo selvagem e similar aos grãos progenitores Riso 1508 e Riso 56 com menos de 5% da semente retida por uma peneira de 2,5 mm (tabela 5). Isto contrastou com as linhagens controle Galleon e Sloop onde 90% de semente foi maior do que 2,5 mm. Notou-se que os grãos de K8 que são uma linhagem do tipo selvagem derivada do mesmo cruzamento Riso 1508 X Riso 56 foram também reduzidos em tamanho, portanto pelo menos parte da redução no tamanho de semente foi relacionada ao contexto genético e não diretamente devido ao nível de hordeína reduzido. Além disso, o tamanho de semente menor poderia ser compensado por modificações no método para imersão do grão.
[00286] Tabela 5. Tamanho de semente usado para micromaltagem.
[00287] Os níveis de umidade de semente podem afetar o desempenho de maltagem. O % de umidade e % de nitrogênio foram medidos por análise próxima ao Infravermelho (NIR) antes de micro-maltagem. O nível de umidade de semente de todas as amostras de grão F4 foi na faixa entre 11 e 11,4% e foi similar às linhas de controle com exceção do grão de cv. Galleon (GA1, 8,9%). O nitrogênio de semente para as linhagens duplo nulas variou entre 2,3% e 2,5% que foi maior do que a linhagem de maltagem de controle cv. Galleon, em 1,6%. Para a maltagem, os níveis de nitrogênio de semente é otimamente entre 1,5 e 2,0%.
[00288] As amostras de cevada (170 g) de grão F4 crescido no campo de linhagens selecionadas 5RB, G1, J1, 9RE, 4BH, progenitores único nulo (Riso 56 e Riso 1508), e cevada do tipo selvagem K8, cultivares Bomi, Carlsberg II, Sloop e Galleon foram embebidos em 16°C por imersão por 6 h, seguido por descanso por 7 h em ar, seguido por imersão por 6 h, e então germinados em 15°C por 4 dias em um sistema de micromaltagem de JWM. O grão germinado foi dessecado por 21 h em uma temperatura mínima de 50°C, e uma temperatura máxima de 80°C, e os maltes resultantes foram limpos de suas raízes friccionando e peneirando.
[00289] Os maltes foram analisados para umidade (%), nitrogênio total (% de peso seco) pelo grão de NIR inteiro e rendimento (expresso como peso de malte limpo como uma porcentagem de peso inicial de cevada).
[00290] Além disso, as amostras de malte foram moídas em um moinho de martelo e 50 g de amostras foram dissolvidos em água aquecida de 45°C a 70°C, para dar 450 g de peso final de solução que foi analisada para extrato (% de peso de grão solubilizado), cor, nitrogênio solúvel (N), índice de Kohlbach (KI: % de proteína solúvel/proteína total), β-glucano, viscosidade, AAL (limite de atenuação aparente ou fermentabilidade, % de queda em densidade durante a fermentação com levedura de cervejas), cada um de acordo com os protocolos de Convenção de Cervejaria Europeia padrões, http://www.ebc-nl.com/ (tabela 6).
[00291] O teor de proteína dos maltes foi geralmente mais elevado do que a especificação desejável. Isto foi mostrado pelo malte total N, e pelo solúvel N, entretanto a proporção de proteína solúvel comparada ao total (KI) foi próxima à especificação. A cor e a viscosidade dos mostos F4 foram próximas à especificação e os níveis de β-glucan nos mostos foram baixos. Estas características foram aceitáveis para a maltagem.
[00292] O processo de maltagem envolveu três estágios: maltagem, mosto e fermentação. A eficiência total é calculada de três medidas da eficiência de cada estágio: rendimento, extrato, e AAL respectivamente. Estes indicam que em cada estágio o grão F4 é aproximadamente 10% menos eficiente do que o grão de BenchMark, cv Galleon. Geralmente aproximadamente 1,3 vezes mais grão das linhagens F4 seria exigido para produzir a cerveja de uma força equivalente ao padrão comercial, comparada a Galleon.
[00293] Todas estas indicações mostraram que o malte poderia ser feito dos grãos F4.
[00294] Aproximadamente amostras de 40 ml de mosto do Exemplo 6 foram congeladas, liofilizadas, e dissolvidas em 20 ml de ureia 6M, 1% (peso/vol) DTT, 20 mM de TEA (pH 6) na temperatura ambiente. O teor de proteína de cada amostra foi determinado usando o método de ligação de corante de Bradford. As diluições em série contendo 20μg de proteína de malte em 100 μl de ureia 6 M, 1% DTT, e 20 mM TEA (pH 6) foram aplicadas a uma membrana de nitrocelulose (Amersham Hybond C+) que foi pré-equilibrada em tampão de PBS, em um aparelho de dot blot (BioRad) e calibrado com um padrão de C-hordeína purificada (2 μg). A solução foi extraída através da membrana sob pressão reduzida, e a membrana enxaguada com o tampão de PBS contendo 0,1% Tween 20 (PBST), o aparelho foi desmontado e a membrana bloqueada incubando em 5% (peso/vol) de pó de nata em tampão de PBS contendo 0,1% Tween 20, por 1 h na temp. ambiente. As hordeínas foram detectadas com um anticorpo primário (gliadina anti- trigo de coelho, anticorpo conjugado à peroxidase de rábano, de Sigma), diluído 1 parte em 2000 de tampão de PBST, por 30 min em temperatura ambiente. A membrana foi lavada com três mudanças de tampão de PBST e desenvolvida incubando em 10 ml de uma mistura 1:1 (vol/vol) de reagentes de western blotting Amersham ECL de reagentes A e B (GE HealthCare) e o sinal detectado expondo a Amersham Hyperfilm por 30 s. A filme foi desenvolvido e quantificado usando o software Total Lab TL100 (Non-linear dynamics, 2006).
[00295] As soluções de malte bruto produzidas do grão F4 selecionado tiveram um nível médio de hordeína de 58+12,7 ppm.
[00296] Este nível foi substancialmente mais baixo do que o limite de 200 ppm estabelecido por FSANZ para alimento com pouco glúten na Austrália e consideravelmente menor do que a média de 687 + 158 ppm encontrada para o malte cultivar Galleon, Sloop. K8, Bomi, e Carlsberg II do tipo selvagem. Foi também consideravelmente mais baixo do que o teor de hordeína de malte feito dos progenitores Riso 56 e Riso 1508.
[00297] Ordinariamente, o teor de glúten (hordeína) de misturas cai dramaticamente através dos processos de maltagem, mosto e fermentação, e a cerveja estabilizada final pode conter 1/1000 de nível presente no malte bruto (Dostalek e col., 2006).
[00298] Portanto foi previsto que o nível de hordeína na cerveja processada feita dos maltes F4 seria reduzido a aproximadamente 0,05 ppm, bem abaixo da faixa de 3-40 ppm encontrados para cervejas feitas do grão de cevada do tipo selvagem (Dostalek e col., 2006).
[00299] Há diversas recomendações recentes na literatura para o limite de glúten na dieta de celíacos. O mais confiável destes é baseado em um experimento multicentro, placebo controlado, duplo cego e mostra que o consumo de menos do que 10 mg/dia é seguro para celíacos; e recomenda que o consumo deve ser mantido a menos do que 50 mg/dia (Catassi e col., 2007). Outro estudo recente confirma estas descobertas e (Collin e col., 2004) recomenda que o consumo de alimento com glúten de 100 ppm resultaria em consumo de aproximadamente 30 mg/dia e resulta em pouco dano aos celíacos. FSANZ estabelece os padrões de alimento para Nova Zelândia e Austrália. A Codex Alimentarius Commission foi criada em 1963 por FAO e WHO para desenvolver padrões de alimento, diretrizes e textos relativos, tais como códigos de prática sob os Joint FAO/WHO Food Standerds Programme e é a regulação estatutária aceitada para Europa, e Norte América. O Codex presentemente estabelece um limite sem glúten de menos do que 0,05 g de N (como glúten) por 100 g de alimento. Há uma proposta para revisar o Codex padrão e propor um limite de 20 ppm para o alimento feito sem glúten contendo cereais, e 200 ppm para o alimento feito de glúten contendo cereais (p32, PROPOSTA P264, REVIEW OF GLUTEN CLAIMS WITH SPECIFIC REFERENCE TO OATS AND MALT, FSANZ, website:
[00300] http://www.foodstandards.gov.au/_srcfiles/P2 64_Gluten_Claims_FAR.pdf#search=%22gluten%20free%22s).
[00301] Concluiu-se da análise acima que o consumo de cerveja produzida das linhagens de cevada F4 seria bem abaixo do limite de segurança estabelecido para o alimento livre de glúten para celíacos, nos estudos acima e incluindo as regulações estabelecidas por FSANZ e Codex Alimentarius.
Exemplo 8. Caracterização adicionais das linhagens F4
[00302] As proteínas solúveis em álcool purificadas da semente F4 colhida para cada uma das linhagens indicadas, como descrito acima. As amostras de proteína purificada (20μg) do grão F4 de linhagens G1, J1, 4BH, 5RB e 9RE foram dissolvidas em ureia 6M, 2% (peso/vol) SDS, 1% (peso/vol) DTT, 0,01% (peso/vol) azul de bromofenol, Tris-HCL 0,0625 M (pH 6,8) em 25°C, examinado por SDS-PAGE, tingido com 0,006% Commassie Blue coloidal, e comparado às hordeínas isoladas das linhagens Riso 56, Riso 1508, e tipo selvagem (K8). A migração foi comparada aos padrões de peso molecular para determinar a massa molecular (tabela 7).
[00303] As sequências de proteína foram obtidas por espectroscopia de massa de digestões tripticas dos pontos de proteína cortados dos géis, e processados para o sequenciamento de proteína por fragmentação de MS-MS como previamente descrito (Campbell e col., 2001) com uma busca na base de dados não redundante de NCBI.
[00304] Tabela 7. Identificação de proteína de SDS-PAGE.
A: Todas digestões também contêm peptídeos de tripsina suína, como esperado. B: Também continha um nível baixo de D-hordeína C: Também continha um nível baixo de B-hordeína. D: Também continha um nível baixo de precursor gama- hordeína-1 E: A contagem de busca de MSMS somada indica a confiança da atribuição de identidade. Do experimento anterior, uma contagem de mais de 15 é exigida para uma identificação de confiança, e uma contagem de mais de 50 indica quase certa a identificação.
[00305] Os peptídeos de cada amostra foram ligados a uma coluna de 150 x 0.5mm de 5μm de Agilent Zorbax SB-C 18 com uma taxa de fluxo de 0,1% (vol/vol) ácido fórmico 5% (vol/vol) 20μl/min de acetonitrila por um minuto então eluído com gradientes de concentração de acetonitrila crescente para 0,1% (vol/vol) ácido fórmico/20% (vol/vol) acetonitrila sobre um min em 5μl/min, então a 0,1% (vol/vol) ácido fórmico/50% (vol/vol) acetonitrila sobre 28 min, então a 0,1% (vol/vol) ácido fórmico/95% (vol/vol) acetonitrila sobre um min. A coluna foi lavada com um gradiente de 0,1% (vol/vol) ácido fórmico/95% (vol/vol) acetonitrila a 0,1% (vol/vol) ácido fórmico/100% (vol/vol) acetonitrila sobre 5 min em 20 μl/min e re-equilibrado com 0,1% (vol/vol) ácido fórmico/5% (vol/vol) acetonitrila por 7 min antes que peptídeos da amostra sejam aplicados.
[00306] O eluído da coluna foi introduzido em um espectrômetro de massa de armadilha de íon Agilent XCT através da fonte de íon eletropulverizador de micronebulisador do instrumento. Enquanto os peptídeos foram eluídos da coluna, a armadilha de íon coletou varreduras de íon positivo de espectro cheio (100-2200m/z) seguido por quatro varreduras de MS/MS de íons observados no espectro cheio de acordo com os ajustes “SmartFrag” e “Varredura de Peptídeo” do instrumento. Uma vez que dois espectros de fragmentação foram coletados para qualquer valor m/z particular foi excluído da seleção para análise por 30 s adicionais para evitar coletar dados redundantes.
[00307] Os dados espectrais de massa estabelecem combinados com bases de dados de sequência usando o software de Agilent’s Spectrum Mill (Rev A.03.02.060). As combinações falso positivas foram evitadas usando as configurações padrões de “autovalidação” do software. Isto inclui uma exigência para que as combinações de peptídeo sejam consideravelmente melhores do que a melhor combinação contra a base de dados reversa e várias pesagens favorecendo os padrões de ionização e fragmentação mais prováveis (“classificação de mobilidade de próton”). A metionina oxidada foi permitida como uma modificação variável.
[00308] Os resultados de sequenciamento de proteína estabeleceram que a semente F4 das linhagens selecionadas inesperadamente continha uma faixa de B3-hordeína, além da gama-1-hordeína e D-hordeína como esperado. A identidade das faixas de gama-1 e -3 hordeína foi estabelecida sequenciando proteínas do mutante Riso 56 onde estas proteínas não foram mascaradas por faixas de B-hordeína co- migrantes. Isto indicou que as linhagens F4 selecionadas não faltavam completamente a hordeína B3.
Exemplo 9. Identificação de grão de cevada faltando hordeínas B e C
[00309] As meias sementes individuais de uma única cabeça de plantas F4 crescida no campo de linhagem G1 foram inchadas durante a noite em água contendo os inibidores de protease E64 e AEBSF (1μg/ml), individualmente esmagadas e moídas em um microtubo plástico com uma esfera de aço inoxidável, agitada em 30/s por 3 x 1,5 min em um Moinho de Vibração de 96 poços (Retsch Gmbh, Rheinische) e então centrifugada em 3000 g por 5 min em TA e o sobrenadante descartado. O grânulo de farinha insolúvel em água foi lavado duas vezes mais na mesma maneira e os sobrenadantes descartados. As hordeínas solúveis em álcool no grânulo foram então extraídas adicionando 400 μl de 50% (vol/vol) propan-2-ol aquoso contendo 1% (peso/vol) DTT, seguido pela agitação e centrifugação como acima. Os sobrenadantes contendo hordeínas extraídas foram transferidos aos tubos frescos e o teor de proteína nos sobrenadantes de DTT/propan-2-ol foram medidos com reagente de Coomassie (BioRAD).
[00310] Uma alíquota de cada extrato de hordeína correspondendo a 20 μg de hordeína foi liofilizada sob vácuo durante a noite, dissolvida em 15 μl de tampão de ebulição SDS, aquecida por 3 min em 90°C, carregada em um gel de gradiente de 12-18% Excel pré-moldado (Pharmacia) e examinada por SDS-PAGE como descrito no Exemplo 1. Uma faixa proeminente em aproximadamente 43 kDa foi observada para segregar em sementes individuais e estava ausente em extratos de 5 das 16 sementes. A posição desta faixa foi a mesma como a faixa de B3-hordeína identificada previamente.
[00311] Os dados de proteína confirmaram que a semente F4 da linhagem G1 era heterozigótica e segregante para uma ou mais proteínas de B-hordeína. Esta situação foi também confirmada para outras linhagens F4.
Teste genético
[00312] Os testes genéticos foram realizados para confirmar os dados de proteína. As meias sementes individuais das linhagens F4 selecionadas crescidas no campo, foram germinadas no solo úmido, e crescidas por 2 semanas na estufa em 25°C dia e 20°C noite. O DNA foi isolado de 0,5 cm da lâmina de folha usando um Kit de PCR de Planta REDExtract-N-Amp (Sigma) de acordo com as instruções. As sequências de gene específicas para B1- hordeínas e gama-hordeínas foram amplificadas por reações de PCR separadas adicionando 10 μl de RMix, 1 μl cada um dos primers de B1-hordeína (5’B1hor e 3’B1hor) ou 0,5 μl cada um dos primers de gama3-hordeína (5’gama Hor3 e 3’gama 3-completas), 4 μl de DNA de planta e água MiIIiQ a 20 μl, em temperatura ambiente e então submetidas ao seguinte programa de temperatura em um ciclador térmico de Eppendorf: 95°C por 10 min; seguido por 35 ciclos de 95°C por 30 s, 56°C por 30 s, e 72°C por 1 min. Isto foi seguido por 72°C por 10 min, e refrigerando a 10°C.
[00313] As sequências dos primers de PCR foram como segue: 5’B1hor: 5’-CAACAATGAAGACCTTCCTC-3' (Id. de Seq. N°.: 2) 3’B1hor: 5’-TCGCAGGATCCTGTACAACG-3’ (Id. de Seq. N°.: 3) 5’ gama hor3: 5’-CGAGAAGGTACCATTACTCCAG-3’ (Id. de Seq. N°.: 4) 3’ gama-3 completa: 5’-AGTAACAATGAAGGTCCATCG-3’ (Id. de Seq. N°.: 5).
[00314] 20 μl de cada reação de PCR foram carregados em um 1 cm, 1% (peso/vol) de gel de agarose contendo EtBr, feitos eletroforese em 100 V por 1 h em tampão de TBE e uma imagem foi obtida da fluorescência dos produtos de DNA usando o sistema de imagem GelDoc (uvitec) (figura 14).
[00315] Uma faixa amplificada de DNA para o gene de controle de gama3 hordeína estava presente em todas as linhas como esperado (figura 14, painel inferior, gama3- Hor). O DNA de B-hordeína amplificado estava ausente em todas as linhas de PCR do Riso 56, como esperado o gene foi deletado em Riso 56 (figura 14, painel superior, R56). As faixas de DNA amplificado para genes de B-hordeína segregaram em extratos das sementes de uma única cabeça F4 de linhagens 9RE e 4BH (figura 14, painel superior 9RE, 4BH). Isto indicou que um ou mais genes de B-hordeína estavam presentes em algumas das sementes F4 e que as sementes F3 não eram homozigóticas para a deleção do locus de B-hordeína em Riso 56. Isto também foi mostrado para outras linhagens F4. Este método foi útil como um método a base de DNA para identificar e selecionar as sementes faltando B1 hordeína.
[00316] Os resultados do teste genético foram usados para selecionar para as plantas que não continham genes de B-hordeína. Doze plantas F5 individuais, nulas por PCR para genes de B-hordeína foram selecionadas, e crescidas para produzir uma população de sementes F5 conhecidas como G1*. G1* individuais, meias sementes F5, foram tomadas de uma única cabeça, germinada no solo úmido e crescida por 2 semanas na estufa em 25°C dia e 20°C noite antes do isolamento de DNA/análise de PCR como acima. A metade- semente correspondente foi usada para o isolamento de hordeína e análise tomando uma alíquota correspondendo a 40 μg de hordeína, liofilizada sob vácuo durante a noite, dissolvida em 15 μl de tampão de ebulição SDS, aquecida por 3 min em 90°C, carregada em um gel de 1mm 12% pré-fabricado Longlife (géis Longlife) e feita eletroforese em 150V por 40 min e tingida como no exemplo 1.
[00317] A análise de PCR mostrou que o DNA isolado das linhagens de controle positivas, Sloop e Riso 1508 deram uma faixa de B-hordeína como esperada. O tamanho da faixa de Sloop foi maior do que amplificada do Riso 1508, já que os genes de B1-hordeína foram ligeiramente diferentes. O gene de controle, gama3-hordeína, foi amplificado de todas as plantas. A faixa de PCR não foi amplificada dos extratos de seis G1* indivíduais confirmando a ausência do gene destas plantas. O padrão de hordeína em meias sementes correspondentes confirmou isto; nenhuma faixa de B-hordeína foi observada em G1*. Portanto concluiu-se que G1* faltou B-hordeínas detectáveis e foi pressuposta ser homozigóticas nula para o locus de codificação de B-hordeína.
[00318] As 250 sementes F5 G1* restantes foram germinadas e as plântulas foram testadas e confirmadas como nula para o gene de B-hordeína. As gerações subsequentes foram usadas para o aumento de semente desta linha.
Análise de teor de hordeína
[00319] As variedades de cevada Sloop, R56, R1508 e G1* foram crescidas em lotes adjacentes no campo, o grão maduro colhido e processado para fazer farinha. Os níveis de hordeína nas amostras de farinha foram analisados como descrito acima. As frações de proteína solúveis em água, solução salina, alcohol/DTT e solúvel em ureia foram obtidas como no exemplo 4 e o teor de proteína em cada uma medida. Os teores de proteína são mostrados na Tabela 8, e expressos como mg de proteína/g de peso seco de farinha. Cada teor de proteína total foi determinado somando o teor de proteína das frações para essa amostra. As hordeínas estavam contidas na fração solúvel em álcool junto com outras proteínas solúveis em álcool, tais como serpinas, inibidores de protease, LTP1 e proteína Z.
[00320] Tabela 8. Teor de proteína em frações na farinha obtida de grão G1*.
[00321] Os dados mostraram que o teor de proteína solúvel em álcool no grão de G1* e consequentemente a farinha foi reduzida a menos de 22% relativo ao cultivar Sloop do tipo selvagem.
[00322] As frações de proteína solúveis em álcool obtidas acima foram enriquecidas para hordeínas por FPLC como no exemplo 5. As proteínas em cada eluído de FPLC foram liofilizadas e o rendimento de proteína FPLC- purificada por 10 g de farinha foi determinado. Isto mostrou que o teor de hordeína de G1* foi reduzido para menos de 8 mg/10g de farinha comparada à farinha de 105 mg/10g para Sloop, 38 por R56 e 24 para R1508. Isto representou uma redução no teor de hordeína no grão de G1* e farinha de pelo menos 92% relativo ao Sloop.
Exemplo 10. Maltagem de maior escala e fabricação de cerveja usando grão F4
[00323] Os experimentos de maltagem de maior escala foram realizados para produzir quantidades suficientes de malte para testes de fabricação de cerveja usando o grão F4. Estes testes usaram procedimentos de imersão modificados, para considerar o tamanho de grão menor entre outros fatores, como segue. As amostras de grão de 800g por tonel de maltagem foram usadas. O regime de imersão foi 17°C por 5 horas, a temperatura de germinação foi 15°C por 94 horas. O programa de estufa foi 50-78°C por 17 horas, 50-74°C por 17 horas. A produção de malte não usou ácido giberélico, isto não foi necessário.Receita de brassagem: 4,65 kg de malte com pouco glúten, 10 litros água, 10 g cloreto de cálcio, 2g sulfato de cálcio, 64-65°C por 2 horas.Tanque: adicione 17 g de Grânulos de Lúpulo Alvo (10,0% AA) por 60 min, 21 g de Grânulos de Lúpulo de Hallertau (4,5% AA) por 10 minutos.
[00324] A fermentação foi no volume de batelada de 19 litros, na temperatura de fermentação 12°C, usando 12 g de levedura seca Fermentis W34/70, para fermentação primária de 8 dias, então 9 dias resfriado em 0°C. A cerveja foi então filtrada através de um filtro de 1 mícron, força carbonatada em um barril, e enchida com um recheio de frasco de pressão contrária. A gravidade específica original foi 1,044, a gravidade final do produto fermentado foi 1,013 com uma Amargura Aproximada de 30 IBU, e o Álcool Aproximado por volume foi 4,0%.
[00325] Outros parâmetros medidos durante o processo de produção foram como segue: Umidade de malte: 4,2%, Extrato 71,5; Cor 3,9; WC 1,0; TN 2,63% de base seca; SN 1,11; KI 51; Viscosidade 1,52; AAL 71,8%; beta-glucosidase 130 mg/l; DP 24.
[00326] Todas estas indicações mostraram que a cerveja poderia ser feita do malte dos grãos F4.
[00327] Os testes de maltagem e fabricação de cerveja de maior escala foram realizados também no grão de cevada de G1*. 800 g de grão foram maltadas em um malter automatizado de Joe White Maltings, de acordo com o protocolo indicado. As condições de maltagem preferidas para o grão de G1* foram determinadas como sendo: 3 horas embebendo em 17°C, germinação de 4 dias em 15°C, seguida por secagem em uma estufa 50-80°C. A duração ótima para imersão do grão de G1* diferiu ligeiramente comparados aos outros grãos: Sloop: 8h-9h-5h imersão/descanso/programa de etapa em 17°C; R1508: 7h-8h-3h imersão/descanso/programa de etapa em 17°C; R56: 8h-10h-5h imersão/descanso/programa de etapa em 17°C. Os protocolos de análise foram como especificados pela Convenção de Fabricação de Cerveja Europeia (EBC) ou Instituto de Fabricação de Cerveja (IOB). O teor de umidade do grão foi determinado por espectroscopia Infravermelha Próxima (NIR). O teor de nitrogênio total foi determinado pelo método de Dumas. Os dados para os maltes são mostrados na tabela 9. Uma diferença significativa entre o grão de G1* e as outras variedades testadas foi que as medidas de força diastática para G1* e R1508 eram muito mais baixas do que para grão Sloop ou R56. Isto foi, portanto, escolhido com a mutação lys3 em G1* e R1508.
[00328] As maltagens foram repetidas e combinadas para cada variedade. Aproximadamente 4 kg de malte de cada uma das linhagens G1*, R56, R1508 e Sloop (tipo selvagem) foram fabricados cerveja e engarrafados como segue. As amostras de malte foram amargadas com lúpulos de Tettnang por 60 min na temperatura de ebulição para conseguir 21-22 unidades amargas (IBU). A fermentação foi com levedura US- 05 (Fermentis) em 18-20°C. O produto fermentado foi embarrilado sem filtração e forçado e carbonatado antes de engarrafar. Todas as cervejas ainda estavam turvas quando engarrafadas, mas estavam mais claras após o armazenamento de 2-4 semanas. As cervejas tiveram um aroma “amanteigado” visível e saborizado devido ao diacetil quando embarrilado e engarrafado, mas isto também desvaneceu no armazenamento.
[00329] Os dados para os produtos fabricados de cerveja são mostrados na tabela 10. O teor de álcool para a cerveja feita do grão de G1* foi 4,2% por volume. A cerveja de G1* teve um topo de espuma ligeiramente reduzido, mas satisfatório, após derramamento. Tabela 9. Dados para características de maltagem de grão de G1*
[00330] Tabela 10. Dados para características de fabricação de cerveja do grão G1*.
[00331] Estes experimentos indicaram que o grão Gl* poderia ser com sucesso maltado e fabricado em cerveja.
[00332] Os níveis de hordeína na cerveja feita do grão de G1*, medida pelo imunoensaio, são esperados ser menos do que 1 ppm, e em algum caso menos do que 0,5 ppm. Isto compara a uma faixa em níveis de hordeína em uma cerveja de trigo de 10-41 ppm, na cerveja de malte de 915ppm, em lagers de 3-9 ppm.
[00333] Será apreciado por pessoas hábeis na técnica que numerosas variações e/ou modificações podem ser feitas à invenção como mostrado nas modalidades específicas sem sair do conceito inventivo ou escopo da invenção como amplamente descrita. As presentes modalidades devem ser, portanto, consideradas em todos os aspectos como ilustrativas e não restritivas.
[00334] O presente pedido reivindica prioridade da US 60/964.672, os conteúdos inteiros do qual são incorporados aqui por referência.
[00335] Todas as publicações discutidas e/ou referidas aqui são incorporadas aqui em sua totalidade.
[00336] Qualquer discussão de documentos, atos, materiais, dispositivos, artigos ou similares que foi incluída na presente especificação é unicamente com a finalidade de fornecer um contexto para a presente invenção. Não deve ser tomada como uma admissão que algumas ou todas estas matérias façam parte da de técnica prévia base nem eram de conhecimento geral comum no campo relevante à presente invenção enquanto existiu antes da data de prioridade de cada reivindicação desta aplicação. REFERÊNCIAS Abdullah e col. (1986) Biotechnology 4:1087. Almeida and Allshire (2005) TRENDS Cell Biol 15: 251-258. Anderson e col. (2000) Nature Medicine 6: 337-342. Anderson e col. (2005) Gut 54:1217-1223. Aventz-Hansen (2000) Journal of Experimental Medicine 191: 603-612. Biagi e col. (2004) Nutrition Reviews 62:360-363. Bourque (1995) Plant Sci. 105: 125-149. Bradford (1976) Analytical Chemistry 72: 248-254. Brandt e col. (1990) Eur J Biochem 194:499-505. Campbell e col. (2001) Insect Biochemistry and Molecular Biology 31: 513-520. Capecchi (1980) Cell 22:479-488. Catassi e col. (2007)Am. J. Clin. Nutr. 85:160-166. Cheng e col. (1996) Plant Cell Rep. 15:653-657. Clapp (1993) Clin. Perinatol. 20:155-168. Collin e col. (2004) Aliment Pharmacol Ther 19:1277-1283. Comai e col. (2004) Plant J 37: 778-786. Curiel e col. (1992) Hum. Gen. Ther. 3:147-154. Davies e col. (1993) Cell Biology International Reports 17: 195-202. De Anglis e col. (2007) J Food Protection 70:135-144. Doll (1976) Genetic studies of high lysine barley mutants. In "Barley Genetics III". Gaul H (ed). Verlag, Munchen:542-546. Doll (1980) Heriditas 93:217-222. Doll (1983) Barley seed proteins and possibilities for their improvement. In "Seed Proteins: Biochemistry, Genetics, Nutritional Value", Gottschalk W, Muller HP (eds). Martinus Nijhoff, The Hague:207-223. Doll e col (1973) Barley Genetics Newsletter 3:12-13. Douliez e col. (2000) J Cereal Sci 32:1-20. Dostalek e col. (2006) Food Additives and Contaminants 23:1074-1078. Eglitis e col. (1988) Biotechniques 6:608-614. Ellis e col. (1990) Clin Chim Acta 189: 123-130. Fasano e col. (2003) Archives of Internal Medicine 163: 286-292. Field e col. (1982) Theoretical and Applied Genetics 62:329-336. Folich e col. (1957) J Biol Chem. 226:497-509. Fujimura e col. (1985) Plant Tissue Culture Letters 2:74. Gellrich e col. (2003) Cereal Chem 80:102-109. Graham e col. (1973) Virology 54:536-539. Grant e col. (1995) Plant Cell Rep. 15:254-258. Hadjivassiliou e col. (2004) Trends Immunol 25:578-82. Haseloff and Gerlach (1988) Nature 334:585-591. Hejgaard and Boisen (1980) Hereditas 93:311-320. Henikoff e col. (2004) Plant Physiol 135: 630-636. Hogberg e col. (2004) Gut 53: 649-654. Hovell e col. (2001) Med J Aust 175: 247-250. Ingerversen e col. (1973) Experientia 29:1151-1152. Jaradat (1991) Theor Appl Genet 83:164-168. Jensen (1979). Chromosomal location of one dominant and four recessive high-lysine genes in barley mutants. In "Seed Protein Improvement in Cereals and Grain Legumes". IAEA/FAO/GSF, STI/PUB/496, Vienna:86-96. Kanerva e col. (2005) J Instit Brewing 111: 61-64. Karlsson (1977) Barley Genetics Newsletter 7:40-43. Kasarda e col. (1984) PNAS 81:4712-4716. Kim e col. (2004) Proc Natl Acad Sci USA 101:4175-9. Klemsdal (1987) Hereditas 107: 107-114. Koeie and Kreis (1978) Hordein and starch synthesis in developing high-lysine and normal barley seeds at different N-fertiliser levels. In "Carbohydrate and protein synthesis" Miflin BJ and Zoeschke M (eds). Commission of the European Communities, 1978; publication EUR 6043 En: 137-150. Koziel e col. (1996) Plant Mol. Biol. 32:393-405. Kreis (1979) Starch synthesis and prolamin level in single and double high-lysine barley mutants. Thesis Universsite Catholique de Louvain, Belgium 127pp. Kreis and Doll (1980) Physiol. Plant 48:139-143. Kreis e col. (1983) Cell 34:161-177. Kreis e col. (1984) Biochem. Genetics 22: 231-255. Kreis and Shewry (1989) BioEssays 10:201-207. Larroque e col. (2000) In Shewry and Tatham, eds. Seventh Internatl Workshop on Gluten Proteins, Bristol UK. Instit for Arable Crops Res 2000: 136-139. Lu e col. (1993) J. Exp. Med. 178:2089-2096. Lundin e col. (2003) Gut 52: 1649-1652. Marchylo e col. (1986) Cereal Chem 63: 219-231. Marti e col. (2005) J Pharmacol Exp Therapeut 312:19-26. Millar and Waterhouse (2005) Funct Integr Genomics 5: 129135. Mullins e col. (1999) Eur J Plant Pathol 105:465-475. Munck e col. (1970) Science 168:985-987. Olsen (1977) Hereditas 87: 11-20. Pasquinelli e col. (2005) Curr Opin Genet Develop 15: 200205. Peraaho e col. (2004a) Journal of the American Dietetic Association 104: 1148-1150. Peraaho e col. (2004b) Scandinavian Journal of Gastroenterology 39: 27-31. Perriman e col. (1992) Gene 113: 157-163. Peters e col. (2003) Arch Intern Med 163:1566-1572. Pynnonen e col. (2004) Psychosomatics 45: 325-335. Senior (1998) Biotech. Genet. Engin. Revs. 15: 79-119. Shan e col. (2002) Science 297: 2275-2279. Sheehan and Skerritt (1997) J Inst Brewing 103: 297-306. Shewry e col. (1980) Biochemical Genetics 18:33-151. Shewry e col. (1978) Journal of Experimental Botany 29:677692. Shewry e col. (1999) The prolamins of the Triticeae. In Shewry P.R., Casey R., eds Seed Proteins. Klewer, London, pp 35-78. Shewry and Halford (2002) Journal of Experimental Botany 53:947-958. Shippy e col. (1999) Mol. Biotech. 12: 117-129. Slade and Knauf (2005) Transgenic Res 14: 109-115. Skerritt (1988) J. Cereal Science 7:251-263. Smith e col. (2000) Nature 407: 319-320. • Sollid (2002) Nature Reviews Immunology 2: 647-655. Sorell e col. (1998) FEBS Letts 439:46-50. Sorensen e col. (1996). Mol Gen Genet 250:750-760. Stepniak e col. (2006) Am J Physiol-Gastrointest Liver Physiol 291:621-629. Tallberg (1977) Hereditas 87: 43-46. Thompson (2001) J. Amer Diet Assoc 101: 1456-1459. Tingay e col. (1997) Plant J 11 :1369-1376. Toriyama e col. (1986) Theor. Appl. Genet. 205:34. Treem (2004) Current Opinion in Pediatrics 16: 552-559. Ullrich and Eslick (1977) Barley Genetics Newsletter 7:6673. Ullrich and Eslick (1978) Barley Genetics Newsletter 8:114125. Vader e col. (2003) Gastroenterology 125: 1105-1113. Verkarre e col. (2004) J Pediatric Gastroenterology and Nutrition 38: 140-142. Wagner e col. (1992) Proc. Natl. Acad. Sci. USA 89:60996103. Waterhouse e col. (1998) Proc. Natl. Acad. Sci. USA 95: 13959-13964. Wieser e col. (1994) Journal of Cereal Science 19, 149-155. Williamson and Marsh (2000) Celiac Disease. In MN Marsh, ed Celiac Disease: Methods and Protocols. Humana Press, Totowa, NJ, pp 1-9. Zikiryaeva and Kasimov (1972) Uzbekskii Biologicheskii Zhurnal 6:18-20.