WO2023085236A1 - 骨接合材料及び骨接合材料の製造方法 - Google Patents
骨接合材料及び骨接合材料の製造方法 Download PDFInfo
- Publication number
- WO2023085236A1 WO2023085236A1 PCT/JP2022/041420 JP2022041420W WO2023085236A1 WO 2023085236 A1 WO2023085236 A1 WO 2023085236A1 JP 2022041420 W JP2022041420 W JP 2022041420W WO 2023085236 A1 WO2023085236 A1 WO 2023085236A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- osteosynthetic
- poly
- bending resistance
- lactic acid
- joint material
- Prior art date
Links
- 239000000463 material Substances 0.000 title claims abstract description 80
- 210000000988 bone and bone Anatomy 0.000 title claims abstract description 23
- 238000004519 manufacturing process Methods 0.000 title claims abstract description 15
- 238000005452 bending Methods 0.000 claims abstract description 35
- 229920001432 poly(L-lactide) Polymers 0.000 claims abstract description 33
- 230000001097 osteosynthetic effect Effects 0.000 claims description 51
- 238000000354 decomposition reaction Methods 0.000 abstract description 8
- 208000010392 Bone Fractures Diseases 0.000 abstract 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 15
- 238000000034 method Methods 0.000 description 11
- 230000000052 comparative effect Effects 0.000 description 8
- 229920001577 copolymer Polymers 0.000 description 5
- 238000011156 evaluation Methods 0.000 description 5
- 238000010438 heat treatment Methods 0.000 description 5
- 238000005259 measurement Methods 0.000 description 5
- 238000005520 cutting process Methods 0.000 description 4
- 230000004927 fusion Effects 0.000 description 4
- 229920001519 homopolymer Polymers 0.000 description 4
- 239000000203 mixture Substances 0.000 description 4
- 239000000919 ceramic Substances 0.000 description 3
- 238000000113 differential scanning calorimetry Methods 0.000 description 3
- 238000005227 gel permeation chromatography Methods 0.000 description 3
- 238000001746 injection moulding Methods 0.000 description 3
- 238000005096 rolling process Methods 0.000 description 3
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- AEMRFAOFKBGASW-UHFFFAOYSA-N Glycolic acid Chemical compound OCC(O)=O AEMRFAOFKBGASW-UHFFFAOYSA-N 0.000 description 2
- JVTAAEKCZFNVCJ-REOHCLBHSA-N L-lactic acid Chemical compound C[C@H](O)C(O)=O JVTAAEKCZFNVCJ-REOHCLBHSA-N 0.000 description 2
- 239000004793 Polystyrene Substances 0.000 description 2
- 239000000654 additive Substances 0.000 description 2
- 239000013078 crystal Substances 0.000 description 2
- 238000010586 diagram Methods 0.000 description 2
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 2
- 238000000465 moulding Methods 0.000 description 2
- 239000002953 phosphate buffered saline Substances 0.000 description 2
- 229920000747 poly(lactic acid) Polymers 0.000 description 2
- 239000004626 polylactic acid Substances 0.000 description 2
- 229920002223 polystyrene Polymers 0.000 description 2
- 238000001356 surgical procedure Methods 0.000 description 2
- 229910000619 316 stainless steel Inorganic materials 0.000 description 1
- 206010065687 Bone loss Diseases 0.000 description 1
- 208000005422 Foreign-Body reaction Diseases 0.000 description 1
- 238000002441 X-ray diffraction Methods 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 230000010478 bone regeneration Effects 0.000 description 1
- 238000007707 calorimetry Methods 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 239000003480 eluent Substances 0.000 description 1
- 238000001125 extrusion Methods 0.000 description 1
- 238000010101 extrusion blow moulding Methods 0.000 description 1
- 230000012010 growth Effects 0.000 description 1
- 238000007654 immersion Methods 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 238000004080 punching Methods 0.000 description 1
- 230000008929 regeneration Effects 0.000 description 1
- 238000011069 regeneration method Methods 0.000 description 1
- 238000002791 soaking Methods 0.000 description 1
- 229910001220 stainless steel Inorganic materials 0.000 description 1
- 239000010935 stainless steel Substances 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B17/00—Surgical instruments, devices or methods, e.g. tourniquets
- A61B17/56—Surgical instruments or methods for treatment of bones or joints; Devices specially adapted therefor
- A61B17/58—Surgical instruments or methods for treatment of bones or joints; Devices specially adapted therefor for osteosynthesis, e.g. bone plates, screws, setting implements or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/50—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
- A61L27/58—Materials at least partially resorbable by the body
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/04—Macromolecular materials
- A61L31/06—Macromolecular materials obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds
Definitions
- the present invention relates to an osteosynthetic material that has high strength and an appropriate rate of decomposition and that can be bent by hand, and a method for producing the osteosynthetic material.
- osteosynthetic materials have practically sufficient flexural strength of about 323 N/mm 2 for SUS-316 stainless steel and about 245 to 490 N/mm 2 for ceramic ones, while human bones Since the rigidity is too high compared to , there is a risk that the bone at the application site may be scraped, and continuous stimulation may cause localized bone melting, reduced strength of new bone, and retarded growth of regenerated bone. was there.
- Patent Literature 1 discloses a biodegradable surgical molded article (osteosynthesis material) comprising a polylactic acid molded article having a specific viscosity-average molecular weight, compressive bending strength and crystallinity.
- the osteosynthetic material composed of such poly-L-lactic acid has excellent properties such that it can fix the bone with sufficient strength until the bone is regenerated, and is eventually absorbed into the body.
- the conventional osteosynthesis material made of poly-L-lactic acid has high strength, there is a problem that a special tool is required to change the shape of the osteosynthesis material according to the shape of the application site.
- the osteosynthetic material can be obtained by using a copolymer of poly-L-lactic acid and other bioabsorbable polymer or a mixture of poly-L-lactic acid and an additive. It has been proposed that the wire can be bent by hand only by immersing it in hot water to heat it without using a special tool.
- the osteosynthesis material is a copolymer containing poly-L-lactic acid or a mixture with additives, although it can be bent by hand, the rate of decomposition in the body increases, resulting in bone loss. It was sometimes difficult to maintain sufficient strength until regeneration.
- an object of the present invention is to provide an osteosynthetic material that has high strength and an appropriate rate of decomposition and is bendable by hand, and a method for producing the osteosynthetic material.
- the present invention provides an osteosynthetic material used to fix bones at a fracture site, the osteosynthetic material comprising only poly-L-lactic acid, having a bending resistance of 10 N or more at 37° C., The osteosynthetic material has a bending resistance of 5 N or less at °C.
- the present invention will be described in detail below.
- the osteosynthetic material of the present invention consists only of poly-L-lactic acid. Since the osteosynthetic material of the present invention is composed of poly-L-lactic acid alone (homopolymer) instead of a copolymer or mixture, it can fix the bone with sufficient strength until the bone is regenerated. has a degradation rate that is rapidly absorbed into the body.
- the weight average molecular weight of the poly-L-lactic acid is preferably 100,000 or more and 500,000 or less. By making the weight average molecular weight equal to or higher than the above lower limit, the strength can be further increased. In addition, by setting the weight average molecular weight to the above upper limit or less, it is absorbed into the body at an early stage after bone regeneration, so that foreign body reaction in the body can be further suppressed.
- the weight average molecular weight of the poly-L-lactic acid is preferably 100,000 or more, more preferably 150,000 or more, preferably 500,000 or less, and even more preferably 450,000 or less.
- a weight average molecular weight is a weight average molecular weight of standard polystyrene conversion by GPC(Gel Permeation Chromatography) here. Specifically, it can be determined with a polystyrene standard using chloroform as an eluent at a column temperature of 40° C. and a multipore-dispersed organic solvent column.
- the poly-L-lactic acid preferably has a crystallinity of 10.0% or more and 25.6% or less.
- the crystallinity of the poly-L-lactic acid is more preferably 13.4% or more, still more preferably 15.4% or more, and more preferably 23.3% or less. It is more preferably 0% or less.
- the crystallinity of the poly-L-lactic acid can be adjusted by adjusting the temperature and time of heat treatment after stretching.
- the crystallinity can be measured by a conventionally known method, for example, X-ray diffraction or differential scanning calorimetry (DSC). preferable.
- DSC differential scanning calorimetry
- the osteosynthetic material of the present invention has a bending resistance of 10 N or more at 37°C.
- the bending resistance at 37° C. of the osteosynthetic material is within the above range, it is possible to obtain sufficient strength to fix the bones until the bones are regenerated.
- the bending resistance at 37° C. can be adjusted by adjusting the weight-average molecular weight of poly-L-lactic acid and the degree of stretching.
- the bending resistance at 37° C. can be measured by the following method.
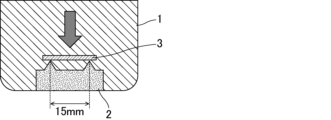
- FIG. 1 shows a schematic diagram for explaining the method of measuring the bending resistance.
- a jig 2 having two mutually parallel protrusions with a width of 15 mm is placed in a water bath 1 filled with water so that the protrusions face upward.
- an osteosynthetic material 3 is placed so as to bridge between the two projections.
- the osteosynthesis material 3 is arranged so as to be perpendicular to the advancing direction of the projections and so that the center of the osteosynthesis material 3 is positioned on the midline between the projections.
- the water temperature of the water bath 1 is set to 37° C. After reaching 37° C., the entire osteosynthesis material 3 is allowed to stand still for 2 minutes to equalize the water temperature.
- an autograph for example, AGS-5KNX manufactured by Shimadzu Corporation
- the bending resistance at 37° C. is preferably 10 N or more, more preferably 12 N or more. Although the upper limit of the bending resistance at 37° C. is not particularly limited, it is preferably 35 N or less.
- the osteosynthetic material of the present invention has a bending resistance of 5 N or less at 70°C.
- the osteosynthetic material of the present invention has a bending resistance of 10 N or more at 37°C and a bending resistance of 5 N or less at 70°C. Since it becomes soft, the osteosynthesis material can be deformed by hand, and the handling during surgery can be enhanced. In addition, while the osteosynthetic material of the present invention can be bent by hand, since the material is poly-L-lactic acid simple substance (homopolymer), the decomposition rate in the body does not increase unlike copolymers and mixtures. , can be fixed with sufficient strength until the bone regenerates.
- the bending resistance at 70°C can be measured in the same manner as the bending resistance at 37°C except that the water temperature is 70°C.
- the bending resistance at 70° C. can be adjusted by adjusting the degree of stretching of the poly-L-lactic acid.
- the bending resistance at 70° C. is preferably 5 N or less, more preferably 3 N or less.
- the lower limit of the bending resistance at 70° C. is not particularly limited, it is preferably 0.1 N or more from the viewpoint of ease of molding.
- the shape of the osteosynthetic material of the present invention is not particularly limited, and the shapes of conventional osteosynthetic materials such as dumbbell-shaped and plate-shaped can be used without particular limitations.
- the method for producing the osteosynthetic material of the present invention is not particularly limited as long as it satisfies the bending resistance at 37°C and the bending resistance at 70°C.
- a method of forming the shape of the osteosynthetic material afterwards is preferable.
- the steps of forming a plate consisting only of poly-L-lactic acid and stretching the plate by 1.1 times or more and 2.0 times or less are performed. , and the step of forming the plate after the stretching into the shape of the osteosynthetic material.
- a step of forming a plate made of only poly-L-lactic acid is performed.
- the method of forming a plate consisting of only poly-L-lactic acid is not particularly limited, and conventionally known methods such as injection molding, extrusion molding and blow molding can be used.
- the step of stretching the plate by 1.1 times or more and 2.0 times or less is then performed.
- a conventional osteosynthesis material made of poly-L-lactic acid stretches the plate four times or more in order to improve the strength.
- the plate made of poly-L-lactic acid obtained in the above steps is stretched within the above range to satisfy the bending resistance at 37°C and the bending resistance at 70°C. can be made easier.
- the draw ratio of the plate is preferably 1.1 times or more, and preferably 1.5 times or less.
- the stretching method is not particularly limited, but rolling is preferable from the viewpoint of productivity.
- heat treatment is preferably performed after the stretching step.
- the stretched poly-L-lactic acid By subjecting the stretched poly-L-lactic acid to a heat treatment, the crystallinity of the poly-L-lactic acid can be brought to a more optimal range.
- the heat treatment is appropriately adjusted on the basis of temperature or time.
- the step of forming the plate after the drawing into the shape of the osteosynthetic material is then performed.
- the osteosynthetic material is obtained by molding the stretched plate made of only poly-L-lactic acid into the shape of the osteosynthetic material.
- the method for forming the plate is not particularly limited, and conventionally known methods such as cutting and punching can be used without particular limitations.
- the osteosynthetic material of the present invention is used to fix bones at fracture sites.
- the osteosynthetic material of the present invention retains the excellent properties of poly-L-lactic acid, such as sufficient strength and moderate decomposition rate, and can be deformed by hand by soaking in hot water. very high in nature.
- Example 1 Production of osteosynthesis material A plate of 90 mm x 90 mm x 2 mm was prepared by injection molding a molten homopolymer of poly-L-lactic acid (weight average molecular weight: 300,000). The resulting plate was stretched 1.1 times by a rolling mill, heat-treated, and then cut to obtain an osteosynthesis material having a total length of 23 mm, a thickness of 1.5 mm, and a width of 5.7 mm.
- a plate of 45 mm ⁇ 45 mm ⁇ 11.5 mm was prepared by injection molding a molten homopolymer of poly-L-lactic acid (weight average molecular weight: 300,000). The obtained plate was stretched 6.0 times by a rolling mill. After that, by cutting the plate, an osteosynthetic material having a total length of 22 mm, a thickness of 1.5 mm, and a width of 5.1 mm was obtained.
- Lactosorb 915-2110 (copolymer of L-lactic acid and glycolic acid, length 21.2 mm, width 6.9 mm, thickness 1.4 mm, manufactured by Medical U&A) was used as it was as an osteosynthesis material.
- the osteosynthetic material was immersed in PBS (phosphate buffered saline) at a bath ratio of 100 and 50°C, and after 1 week, 2 weeks, 3 weeks, 5 weeks, and 7 weeks, GPC was performed. was used to measure the weight average molecular weight, and the ratio of the weight average molecular weight (molecular weight ratio) to the molecular weight before immersion being 100% was calculated to evaluate the degradability of the osteosynthetic material. The results are shown in FIG. For Comparative Example 4, measurements were performed after 2 weeks, 4 weeks, 6 weeks, and 8 weeks.
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Surgery (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Epidemiology (AREA)
- Chemical & Material Sciences (AREA)
- Heart & Thoracic Surgery (AREA)
- Engineering & Computer Science (AREA)
- Molecular Biology (AREA)
- Medical Informatics (AREA)
- Biomedical Technology (AREA)
- Dermatology (AREA)
- Medicinal Chemistry (AREA)
- Oral & Maxillofacial Surgery (AREA)
- Transplantation (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Vascular Medicine (AREA)
- Materials For Medical Uses (AREA)
Abstract
本発明は、高い強度と適度な分解速度を有しながらも手で曲げることが可能な骨接合材料及び該骨接合材料の製造方法を提供することを目的とする。本発明は、骨折部位において骨を固定するために用いられる骨接合材料であって、前記骨接合材料は、ポリ-L-乳酸のみからなり、37℃における曲げ抵抗力が10N以上であり、70℃における曲げ抵抗力が5N以下である骨接合材料である。
Description
本発明は、高い強度と適度な分解速度を有しながらも手で曲げることが可能な骨接合材料及び該骨接合材料の製造方法に関する。
従来から、骨折が治癒するまで骨を固定する骨接合材料としてステンレス、セラミック等より成るワイヤー、プレート、ねじ、ピン、ビス、ステープル、クリップ、ロッド等が用いられている。しかし、金属やセラミックからなる骨接合材料は、人体に吸収されないことから治癒後には摘出の為の再手術をする必要があった。また、これらの骨接合材料は、SUS-316のステンレス製のもので323N/mm2程度、セラミック製のもので245~490N/mm2程度と、実用上充分な曲げ強度を有する一方で、人骨に比べて剛性が高すぎることから、適用部の骨が削られたり、持続刺激によって局部の骨の融解、新生骨の強度低下、再生骨の成長遅延等を生じたりする恐れがあるという問題点があった。
これに対して、ポリ-L-乳酸等の生体吸収性材料からなる骨接合材料が開発されている。例えば、特許文献1には、特定の粘度平均分子量、圧縮曲げ強度、結晶化度を有するポリ乳酸成形物からなる生体内分解吸収性外科用成形物(骨接合材料)が開示されている。
このようなポリ-L-乳酸からなる骨接合材料は、骨が再生するまでの間充分な強度で骨を固定でき、最終的には体内に吸収されるという優れた性質を有する。しかしながら、従来のポリ-L-乳酸からなる骨接合材は強度が高いため、適用箇所の形状に応じて骨接合材料の形状を変えるためには専用の工具が必要であるという問題があった。これに対して、骨接合材料をポリ-L-乳酸と他の生体吸収性高分子との共重合体としたり、ポリ-L-乳酸と添加剤との混合物としたりすることで、骨接合材料を専用の工具を使うことなくお湯に浸漬して加温するだけで手で曲げることができるようにすることが提案されている。しかしながら、骨接合材料をポリ-L-乳酸を含む共重合体としたり添加剤との混合物としたりすると、手で曲げられるようにはなるものの、体内での分解速度が速くなってしまい、骨が再生するまでの間充分な強度を維持することが難しくなることがあった。
本発明は、上記現状に鑑み、高い強度と適度な分解速度を有しながらも手で曲げることが可能な骨接合材料及び該骨接合材料の製造方法を提供することを目的とする。
本発明は、骨折部位において骨を固定するために用いられる骨接合材料であって、前記骨接合材料は、ポリ-L-乳酸のみからなり、37℃における曲げ抵抗力が10N以上であり、70℃における曲げ抵抗力が5N以下である骨接合材料である。
以下に本発明を詳述する。
以下に本発明を詳述する。
本発明の骨接合材料は、ポリ-L-乳酸のみからなる。
本発明の骨接合材料は共重合体や混合物ではなくポリ-L-乳酸単体(単独重合体)のみからなるため、骨が再生するまでの間充分な強度で骨を固定でき、骨の再生後は速やかに体内へ吸収される分解速度を有している。
本発明の骨接合材料は共重合体や混合物ではなくポリ-L-乳酸単体(単独重合体)のみからなるため、骨が再生するまでの間充分な強度で骨を固定でき、骨の再生後は速やかに体内へ吸収される分解速度を有している。
上記ポリ-L-乳酸の重量平均分子量は10万以上50万以下であることが好ましい。
重量平均分子量を上記下限以上とすることで、強度をより高めることができる。また、重量平均分子量を上記上限以下とすることで、骨の再生後は早期に体内へ吸収されるため、体内での異物反応をより抑えることができる。上記ポリ-L-乳酸の重量平均分子量は10万以上が好ましく、15万以上がより好ましく、50万以下であることが好ましく、45万以下であることが更に好ましい。なお、ここで重量平均分子量とは、GPC(Gel Permeation Chromatography:ゲルパーミエーションクロマトグラフィ)による標準ポリスチレン換算の重量平均分子量である。具体的には、カラム温度40℃において溶出液としてクロロホルム、細孔多分散型有機溶媒系カラムを用いて、ポリスチレン標準により決定することができる。
重量平均分子量を上記下限以上とすることで、強度をより高めることができる。また、重量平均分子量を上記上限以下とすることで、骨の再生後は早期に体内へ吸収されるため、体内での異物反応をより抑えることができる。上記ポリ-L-乳酸の重量平均分子量は10万以上が好ましく、15万以上がより好ましく、50万以下であることが好ましく、45万以下であることが更に好ましい。なお、ここで重量平均分子量とは、GPC(Gel Permeation Chromatography:ゲルパーミエーションクロマトグラフィ)による標準ポリスチレン換算の重量平均分子量である。具体的には、カラム温度40℃において溶出液としてクロロホルム、細孔多分散型有機溶媒系カラムを用いて、ポリスチレン標準により決定することができる。
上記ポリ-L-乳酸は、結晶化度が10.0%以上25.6%以下であることが好ましい。ポリ-L-乳酸の結晶化度が上記範囲であることで、後述する37℃における曲げ抵抗力及び70℃における曲げ抵抗力を満たしやすくすることができる。上記ポリ-L-乳酸の結晶化度は、13.4%以上であることがより好ましく、15.4%以上であることが更に好ましく、23.3%以下であることがより好ましく、22.0%以下であることが更に好ましい。上記ポリ-L-乳酸の結晶化度は、延伸後の加熱処理の温度や時間によって調節することができる。
なお、上記結晶化度の測定方法は従来公知の方法を用いることができ、例えば、X線回析法や示差走査熱量分析法(DSC)によって測定することができるが、DSCが簡便であるため好ましい。DSCでは、得られるサンプルの融解熱量を用いて結晶化度を以下の式で算出できる。
結晶化度(%)=(ΔH/ΔH0)×100
ΔH(J/g):サンプルの融解熱量
ΔH0(J/g):ポリ-L-乳酸の完全結晶の理論融解熱量
なお、上記結晶化度の測定方法は従来公知の方法を用いることができ、例えば、X線回析法や示差走査熱量分析法(DSC)によって測定することができるが、DSCが簡便であるため好ましい。DSCでは、得られるサンプルの融解熱量を用いて結晶化度を以下の式で算出できる。
結晶化度(%)=(ΔH/ΔH0)×100
ΔH(J/g):サンプルの融解熱量
ΔH0(J/g):ポリ-L-乳酸の完全結晶の理論融解熱量
本発明の骨接合材料は、37℃における曲げ抵抗力が10N以上である。
骨接合材料の37℃における曲げ抵抗力が上記範囲であることで、骨が再生するまでの間充分に骨を固定できる強度とすることができる。
なお、上記37℃における曲げ抵抗力は、ポリ-L-乳酸の重量平均分子量や延伸の程度によって調節することができる。
また、上記37℃における曲げ抵抗力は、以下の方法で測定することができる。
骨接合材料の37℃における曲げ抵抗力が上記範囲であることで、骨が再生するまでの間充分に骨を固定できる強度とすることができる。
なお、上記37℃における曲げ抵抗力は、ポリ-L-乳酸の重量平均分子量や延伸の程度によって調節することができる。
また、上記37℃における曲げ抵抗力は、以下の方法で測定することができる。
ここで、曲げ抵抗力の測定方法を説明する模式図を図1に示した。図1に示すように、水が入ったウォーターバス1に幅15mmの互いに平行な2本の凸部を有する治具2を凸部が上となるように置く。次いで、2本の凸部間を架橋するように骨接合材料3を置く。この際、骨接合材料3を凸部の進行方向と垂直かつ骨接合材料3の中心が凸部間の中線上に位置するように配置する。次いで、ウォーターバス1の水温を37℃とし、37℃に到達後、骨接合材料3全体を水温と等しくするために2分静置する。その後、オートグラフ(例えば、島津製作所社製、AGS-5KNX等)を用いて骨接合材料3の中心に2.0mm/minの条件で力を加えて曲げ抵抗力を測定する。
上記37℃における曲げ抵抗力は10N以上であることが好ましく、12N以上であることがより好ましい。上記37℃における曲げ抵抗力の上限は特に限定されないが、35N以下であることが好ましい。
本発明の骨接合材料は、70℃における曲げ抵抗力が5N以下である。
本発明の骨接合材料の37℃における曲げ抵抗力が10N以上であり、70℃における曲げ抵抗力が5N以下であることで、体温程度の温度では高い強度を示しつつも、お湯につけることで柔らかくなるため、手で骨接合材料を変形させることができ、手術時の取り扱い性を高めることができる。また、本発明の骨接合材料は手で曲げられる一方、材料はポリ-L-乳酸単体(単独重合体)であるため、共重合体や混合物と異なり体内での分解速度が増加することはなく、骨を再生するまでの間充分な強度で固定することができる。
なお、上記70℃における曲げ抵抗力は、水温を70℃とすること以外は、上記37℃における曲げ抵抗力と同様の方法で測定することができる。
また、上記70℃における曲げ抵抗力は、ポリ-L-乳酸の延伸の程度によって調節することができる。
本発明の骨接合材料の37℃における曲げ抵抗力が10N以上であり、70℃における曲げ抵抗力が5N以下であることで、体温程度の温度では高い強度を示しつつも、お湯につけることで柔らかくなるため、手で骨接合材料を変形させることができ、手術時の取り扱い性を高めることができる。また、本発明の骨接合材料は手で曲げられる一方、材料はポリ-L-乳酸単体(単独重合体)であるため、共重合体や混合物と異なり体内での分解速度が増加することはなく、骨を再生するまでの間充分な強度で固定することができる。
なお、上記70℃における曲げ抵抗力は、水温を70℃とすること以外は、上記37℃における曲げ抵抗力と同様の方法で測定することができる。
また、上記70℃における曲げ抵抗力は、ポリ-L-乳酸の延伸の程度によって調節することができる。
上記70℃における曲げ抵抗力は、5N以下であることが好ましく、3N以下であることがより好ましい。上記70℃における曲げ抵抗力の下限は特に限定されないが、成形のしやすさの観点から0.1N以上であることが好ましい。
本発明の骨接合材料の形状は特に限定されず、ダンベル型、プレート型等従来の骨接合材料の形状を特に制限なく用いることができる。
本発明の骨接合材料の製造方法は上記37℃における曲げ抵抗力と70℃における曲げ抵抗力を満たしていれば特に限定されないが、ポリ-L-乳酸のみからなる板を特定の範囲で延伸した後、骨接合材料の形状に成形する方法が好ましい。
このような、本発明の骨接合材料の製造方法であって、ポリ-L-乳酸のみからなる板を形成する工程と、前記板を1.1倍以上2.0倍以下に延伸する工程と、前記延伸後の前記板を骨接合材料の形状に成形する工程とを有する骨接合材料の製造方法もまた、本発明の1つである。
このような、本発明の骨接合材料の製造方法であって、ポリ-L-乳酸のみからなる板を形成する工程と、前記板を1.1倍以上2.0倍以下に延伸する工程と、前記延伸後の前記板を骨接合材料の形状に成形する工程とを有する骨接合材料の製造方法もまた、本発明の1つである。
本発明の骨接合材料の製造方法は、まず、ポリ-L-乳酸のみからなる板を形成する工程を行う。
ポリ-L-乳酸のみからなる板を形成する方法は特に限定されず、例えば、射出成形、押出成形、ブロー成形等従来公知の方法を用いることができる。
ポリ-L-乳酸のみからなる板を形成する方法は特に限定されず、例えば、射出成形、押出成形、ブロー成形等従来公知の方法を用いることができる。
本発明の骨接合材料の製造方法は、次いで、上記板を1.1倍以上2.0倍以下に延伸する工程を行う。
従来のポリ-L-乳酸からなる骨接合材料は、強度を向上させるために板を4倍以上に延伸していた。本発明の骨接合材料の製造方法では、上記工程で得られたポリ-L-乳酸からなる板を上記範囲で延伸することにより、上記37℃における曲げ抵抗力と70℃における曲げ抵抗力を満たしやすくすることができる。
上記板の延伸倍率は1.1倍以上であることが好ましく、1.5倍以下であることが好ましい。上記延伸の方法は特に限定されないが、圧延加工が生産性の観点から好ましい。
従来のポリ-L-乳酸からなる骨接合材料は、強度を向上させるために板を4倍以上に延伸していた。本発明の骨接合材料の製造方法では、上記工程で得られたポリ-L-乳酸からなる板を上記範囲で延伸することにより、上記37℃における曲げ抵抗力と70℃における曲げ抵抗力を満たしやすくすることができる。
上記板の延伸倍率は1.1倍以上であることが好ましく、1.5倍以下であることが好ましい。上記延伸の方法は特に限定されないが、圧延加工が生産性の観点から好ましい。
本発明の骨接合材料の製造方法は、延伸工程後に加熱処理を行うことが好ましい。
延伸後のポリ-L-乳酸に加熱処理を施すことで、ポリ-L-乳酸の結晶化度をより最適な範囲とすることができる。上記加熱処理は温度又は時間を基準に適宜調整されるが、例えば、70℃以上80℃以下、45分以上120分以下の条件が挙げられる。
延伸後のポリ-L-乳酸に加熱処理を施すことで、ポリ-L-乳酸の結晶化度をより最適な範囲とすることができる。上記加熱処理は温度又は時間を基準に適宜調整されるが、例えば、70℃以上80℃以下、45分以上120分以下の条件が挙げられる。
本発明の骨接合材料の製造方法は、次いで、上記延伸後の上記板を骨接合材料の形状に成形する工程を行う。
延伸後のポリ-L-乳酸のみからなる板を骨接合材料の形状に成形することで骨接合材料が得られる。上記板を成形する方法は特に限定されず、切削加工、打ち抜き加工等従来の公知の方法を特に制限なく用いることができる。
延伸後のポリ-L-乳酸のみからなる板を骨接合材料の形状に成形することで骨接合材料が得られる。上記板を成形する方法は特に限定されず、切削加工、打ち抜き加工等従来の公知の方法を特に制限なく用いることができる。
本発明の骨接合材料は、骨折部位において骨を固定するために用いられる。本発明の骨接合材料は、充分な強度と適度な分解速度というポリ-L-乳酸が有する優れた性質はそのままに、お湯につけることで骨接合材料を手で変形させることができるため、取り扱い性が非常に高い。
本発明によれば、高い強度と適度な分解速度を有しながらも手で曲げることが可能な骨接合材料及び該骨接合材料の製造方法を提供することができる。
以下に実施例を掲げて本発明を更に詳しく説明するが、本発明はこれら実施例のみに限定されるものではない。
(実施例1)
(1)骨接合材料の製造
溶融したポリ-L-乳酸の単独重合体(重量平均分子量:30万)を射出成形することで90mm×90mm×2mmの板を作製した。得られた板を圧延機によって1.1倍に延伸し、加熱処理後に板を切削加工することで全長23mm、厚み1.5mm、幅5.7mmの骨接合材料を得た。
(1)骨接合材料の製造
溶融したポリ-L-乳酸の単独重合体(重量平均分子量:30万)を射出成形することで90mm×90mm×2mmの板を作製した。得られた板を圧延機によって1.1倍に延伸し、加熱処理後に板を切削加工することで全長23mm、厚み1.5mm、幅5.7mmの骨接合材料を得た。
(2)結晶化度の測定
得られた骨接合材料から10mgを切り出して測定サンプルとした。次いで、測定サンプルを専用の容器に封入し、示差走査熱量計(DSC-60、島津製作所社製)を用いて昇温温度10℃/minの条件で30℃から220℃までの範囲で示差走査熱量測定を行った。示差走査熱量測定によって得られた吸熱量、発熱量及びポリ乳酸の完全結晶の理論融解熱量から結晶化度を算出したところ、結晶化度は14.4%であった。
得られた骨接合材料から10mgを切り出して測定サンプルとした。次いで、測定サンプルを専用の容器に封入し、示差走査熱量計(DSC-60、島津製作所社製)を用いて昇温温度10℃/minの条件で30℃から220℃までの範囲で示差走査熱量測定を行った。示差走査熱量測定によって得られた吸熱量、発熱量及びポリ乳酸の完全結晶の理論融解熱量から結晶化度を算出したところ、結晶化度は14.4%であった。
(比較例1)
溶融したポリ-L-乳酸の単独重合体(重量平均分子量:30万)を射出成形することで45mm×45mm×11.5mmの板を作製した。得られた板を圧延機によって6.0倍に延伸した。その後、板を切削加工することで全長22mm、厚み1.5mm、幅5.1mmの骨接合材料を得た。
溶融したポリ-L-乳酸の単独重合体(重量平均分子量:30万)を射出成形することで45mm×45mm×11.5mmの板を作製した。得られた板を圧延機によって6.0倍に延伸した。その後、板を切削加工することで全長22mm、厚み1.5mm、幅5.1mmの骨接合材料を得た。
(比較例2)
切削後の厚みを1.0mmにした以外は比較例1と同様にして骨接合材料を得た。
切削後の厚みを1.0mmにした以外は比較例1と同様にして骨接合材料を得た。
(比較例3)
ラクトソーブ 915-2110(L-乳酸とグリコール酸の共重合体、全長21.2mm、幅6.9mm、厚み1.4mm、メディカルユーアンドエイ社製)をそのまま骨接合材料として用いた。
ラクトソーブ 915-2110(L-乳酸とグリコール酸の共重合体、全長21.2mm、幅6.9mm、厚み1.4mm、メディカルユーアンドエイ社製)をそのまま骨接合材料として用いた。
(比較例4)
切削後の厚みを0.95mm、幅を5.5mmにした以外は比較例1と同様にして骨接合材料を得た。
切削後の厚みを0.95mm、幅を5.5mmにした以外は比較例1と同様にして骨接合材料を得た。
<評価>
実施例、比較例で得られた骨接合材料について以下の方法により評価を行った。
結果を図2、図3に示した。
実施例、比較例で得られた骨接合材料について以下の方法により評価を行った。
結果を図2、図3に示した。
(1)曲げ抵抗力の評価
図1のように、水が入ったウォーターバスに幅15mmの互いに平行な2本の凸部を有する治具を凸部が上となるように置いた。次いで、2本の凸部間を架橋するように骨接合材料を置いた。この際、骨接合材料を凸部の進行方向と垂直かつ骨接合材料の中心が凸部間の中線上に位置するように配置した。次いで、ウォーターバスの水温を37℃とし、37℃に到達後、骨接合材料全体を水温と等しくするために2分静置した。その後、オートグラフ(島津製作所社製、AGS-5KNX)を用いて骨接合材料の中心に2.0mm/min、の条件で力を加えて37℃における曲げ抵抗力を測定した。
次いで、水温を50℃、60℃、70℃、80℃とする以外は同様の操作を行い、各温度における曲げ抵抗力を測定した。また、ウォーターバスを用いず、室温で測定を行う以外は上記と同様の操作で22℃における曲げ抵抗力を測定した。結果を表1、図2に示した。
図1のように、水が入ったウォーターバスに幅15mmの互いに平行な2本の凸部を有する治具を凸部が上となるように置いた。次いで、2本の凸部間を架橋するように骨接合材料を置いた。この際、骨接合材料を凸部の進行方向と垂直かつ骨接合材料の中心が凸部間の中線上に位置するように配置した。次いで、ウォーターバスの水温を37℃とし、37℃に到達後、骨接合材料全体を水温と等しくするために2分静置した。その後、オートグラフ(島津製作所社製、AGS-5KNX)を用いて骨接合材料の中心に2.0mm/min、の条件で力を加えて37℃における曲げ抵抗力を測定した。
次いで、水温を50℃、60℃、70℃、80℃とする以外は同様の操作を行い、各温度における曲げ抵抗力を測定した。また、ウォーターバスを用いず、室温で測定を行う以外は上記と同様の操作で22℃における曲げ抵抗力を測定した。結果を表1、図2に示した。
(2)分解性の評価
浴比100、50℃のPBS(リン酸緩衝生理食塩水)に骨接合材料を浸漬し、1週間、2週間、3週間、5週間及び7週間経過したものについてGPCを用いて重量平均分子量を測定し、浸漬前の分子量を100%としたときの重量平均分子量の割合(分子量比)を算出することで、骨接合材料の分解性を評価した。結果を図3に示した。なお、比較例4については2週間、4週間、6週間、8週間経過後に測定を行った。
浴比100、50℃のPBS(リン酸緩衝生理食塩水)に骨接合材料を浸漬し、1週間、2週間、3週間、5週間及び7週間経過したものについてGPCを用いて重量平均分子量を測定し、浸漬前の分子量を100%としたときの重量平均分子量の割合(分子量比)を算出することで、骨接合材料の分解性を評価した。結果を図3に示した。なお、比較例4については2週間、4週間、6週間、8週間経過後に測定を行った。
本発明によれば、高い強度と適度な分解速度を有しながらも手で曲げることが可能な骨接合材料及び該骨接合材料の製造方法を提供することができる。
1 ウォーターバス
2 治具
3 骨接合材料
2 治具
3 骨接合材料
Claims (2)
- 骨折部位において骨を固定するために用いられる骨接合材料であって、
前記骨接合材料は、ポリ-L-乳酸のみからなり、
37℃における曲げ抵抗力が10N以上であり、
70℃における曲げ抵抗力が5N以下である
ことを特徴とする骨接合材料。 - 請求項1記載の骨接合材料の製造方法であって、
ポリ-L-乳酸のみからなる板を形成する工程と、
前記板を1.1倍以上2.0倍以下に延伸する工程と、
前記延伸後の前記板を骨接合材料の形状に成形する工程
とを有することを特徴とする骨接合材料の製造方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202280040790.9A CN117440840A (zh) | 2021-11-10 | 2022-11-07 | 骨接合材料及骨接合材料的制造方法 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021183473 | 2021-11-10 | ||
| JP2021-183473 | 2021-11-10 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2023085236A1 true WO2023085236A1 (ja) | 2023-05-19 |
Family
ID=86335995
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2022/041420 WO2023085236A1 (ja) | 2021-11-10 | 2022-11-07 | 骨接合材料及び骨接合材料の製造方法 |
Country Status (2)
| Country | Link |
|---|---|
| CN (1) | CN117440840A (ja) |
| WO (1) | WO2023085236A1 (ja) |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH08196617A (ja) * | 1995-09-25 | 1996-08-06 | Takiron Co Ltd | 生体内分解吸収性の外科用材料及びその製造法 |
| JPH09173435A (ja) * | 1995-12-27 | 1997-07-08 | Takiron Co Ltd | インプラント材料及びその製造方法 |
| JP2000084064A (ja) * | 1998-09-14 | 2000-03-28 | Takiron Co Ltd | 生体内分解吸収性インプラント材とその形状調整方法 |
-
2022
- 2022-11-07 CN CN202280040790.9A patent/CN117440840A/zh active Pending
- 2022-11-07 WO PCT/JP2022/041420 patent/WO2023085236A1/ja active Application Filing
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH08196617A (ja) * | 1995-09-25 | 1996-08-06 | Takiron Co Ltd | 生体内分解吸収性の外科用材料及びその製造法 |
| JPH09173435A (ja) * | 1995-12-27 | 1997-07-08 | Takiron Co Ltd | インプラント材料及びその製造方法 |
| JP2000084064A (ja) * | 1998-09-14 | 2000-03-28 | Takiron Co Ltd | 生体内分解吸収性インプラント材とその形状調整方法 |
Non-Patent Citations (2)
| Title |
|---|
| MOCHIZUKI, MASATSUGU: "Crystallization Behaviors of highly LLA-rich PLA", SEN'I GAKKAISHI, vol. 66, no. 2, 1 January 2010 (2010-01-01), pages P_70 (24) - P_77 (31), XP009545642, DOI: 10.2115/fiber.66.P_70 * |
| SUGIYAMA, YOSHIKI: "Biodegradable osteosynthesis system for maxillofacial surgery ― focusing on high-strength PLLA materials ―", DENTAL JOURNAL OF IWATE MEDICAL UNIVERSITY, vol. 30, no. 2, 16 August 2005 (2005-08-16), pages 121 - 131, XP009545710, ISSN: 0385-1311, DOI: 10.20663/iwateshigakukaishi.30.2_121 * |
Also Published As
| Publication number | Publication date |
|---|---|
| CN117440840A (zh) | 2024-01-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US5227412A (en) | Biodegradable and resorbable surgical material and process for preparation of the same | |
| JP2619760B2 (ja) | 骨治療用具及びその製造法 | |
| US5705181A (en) | Method of making absorbable polymer blends of polylactides, polycaprolactone and polydioxanone | |
| JP2860663B2 (ja) | 生体内分解吸収性外科用成形物 | |
| KR100730432B1 (ko) | 재흡수가능한 고분자 조성물 | |
| JP2739974B2 (ja) | 生分解性の人工補装器として使用し得る乳酸ポリマーからつくられた物品及びその製造法 | |
| JP3418350B2 (ja) | 生体内分解吸収性インプラント材とその形状調整方法 | |
| JP2002505142A (ja) | 生体適合性を有する変形可能な固定板 | |
| JP3426460B2 (ja) | 骨接合具 | |
| JPS5827548A (ja) | 焼きもどししたポリジオキサノン外科器具及びその製造方法 | |
| EP0349656B1 (en) | Biodegradable and resorbable surgical materials and process for preparation of the same | |
| WO2023085236A1 (ja) | 骨接合材料及び骨接合材料の製造方法 | |
| JPH11206871A (ja) | 生体内分解吸収性の骨固定材およびその製造方法 | |
| JPH07216065A (ja) | p−ジオキサノンの共重合体 | |
| JP3148932B2 (ja) | 骨折部の内固定材用生体内分解吸収性プレート | |
| JP7313199B2 (ja) | 骨接合材料 | |
| KR100772966B1 (ko) | 유연성을 갖는 뼈 고정용 고강도 생분해성 고분자 소재 및그의 제조방법 | |
| JP7456733B2 (ja) | 骨接合材料 | |
| JPH06142182A (ja) | 骨接合用内固定材 | |
| JP2912923B2 (ja) | 生体内分解吸収性の外科用材料及びその製造法 | |
| JP3141088B2 (ja) | 生体内分解吸収性の外科用材料の製造法 | |
| JPH05237177A (ja) | 貫通孔を有する骨接合材料の製造方法 | |
| JP2009132769A (ja) | 医療用インプラント用ラクチド/ε−カプロラクトン共重合体 | |
| JP3262969B2 (ja) | 生体内分解吸収性骨接合材およびその製造方法 | |
| JPH09234242A (ja) | 骨接合材の製造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 22892735 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 202280040790.9 Country of ref document: CN |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2023559621 Country of ref document: JP |