WO2022102072A1 - リチウム2次電池 - Google Patents
リチウム2次電池 Download PDFInfo
- Publication number
- WO2022102072A1 WO2022102072A1 PCT/JP2020/042366 JP2020042366W WO2022102072A1 WO 2022102072 A1 WO2022102072 A1 WO 2022102072A1 JP 2020042366 W JP2020042366 W JP 2020042366W WO 2022102072 A1 WO2022102072 A1 WO 2022102072A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- secondary battery
- lithium secondary
- negative electrode
- lithium
- solvent
- Prior art date
Links
- 229910052744 lithium Inorganic materials 0.000 title claims abstract description 197
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 title claims abstract description 146
- 239000002904 solvent Substances 0.000 claims abstract description 67
- 150000001875 compounds Chemical class 0.000 claims abstract description 48
- 239000008151 electrolyte solution Substances 0.000 claims abstract description 48
- 239000007773 negative electrode material Substances 0.000 claims abstract description 32
- 229910052751 metal Inorganic materials 0.000 claims description 20
- 239000002184 metal Substances 0.000 claims description 20
- 229910052731 fluorine Inorganic materials 0.000 claims description 16
- 239000011737 fluorine Substances 0.000 claims description 16
- YCKRFDGAMUMZLT-UHFFFAOYSA-N Fluorine atom Chemical compound [F] YCKRFDGAMUMZLT-UHFFFAOYSA-N 0.000 claims description 13
- 229910045601 alloy Inorganic materials 0.000 claims description 10
- 239000000956 alloy Substances 0.000 claims description 10
- 239000011888 foil Substances 0.000 claims description 8
- 229910052759 nickel Inorganic materials 0.000 claims description 7
- 229910052802 copper Inorganic materials 0.000 claims description 6
- 239000010935 stainless steel Substances 0.000 claims description 6
- 229910001220 stainless steel Inorganic materials 0.000 claims description 6
- 150000002739 metals Chemical class 0.000 claims description 5
- 229910052742 iron Inorganic materials 0.000 claims description 4
- 229910052719 titanium Inorganic materials 0.000 claims description 4
- 229910052736 halogen Inorganic materials 0.000 claims description 3
- 150000002367 halogens Chemical class 0.000 claims description 3
- 229910052739 hydrogen Inorganic materials 0.000 claims description 3
- 239000001257 hydrogen Substances 0.000 claims description 3
- 150000002431 hydrogen Chemical class 0.000 claims description 3
- 125000001183 hydrocarbyl group Chemical group 0.000 claims 2
- 150000002641 lithium Chemical class 0.000 abstract 1
- 239000010410 layer Substances 0.000 description 53
- HBBGRARXTFLTSG-UHFFFAOYSA-N Lithium ion Chemical compound [Li+] HBBGRARXTFLTSG-UHFFFAOYSA-N 0.000 description 21
- 239000003792 electrolyte Substances 0.000 description 19
- -1 lithium metals Chemical class 0.000 description 19
- 229910001416 lithium ion Inorganic materials 0.000 description 16
- 235000019000 fluorine Nutrition 0.000 description 15
- 239000007774 positive electrode material Substances 0.000 description 12
- 238000000034 method Methods 0.000 description 11
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 8
- 239000011230 binding agent Substances 0.000 description 8
- 238000001556 precipitation Methods 0.000 description 8
- 239000002033 PVDF binder Substances 0.000 description 7
- 229910003002 lithium salt Inorganic materials 0.000 description 7
- 159000000002 lithium salts Chemical class 0.000 description 7
- 238000004519 manufacturing process Methods 0.000 description 7
- PXHVJJICTQNCMI-UHFFFAOYSA-N nickel Substances [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 7
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 7
- 239000007784 solid electrolyte Substances 0.000 description 7
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 6
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 6
- 239000011247 coating layer Substances 0.000 description 6
- 230000000052 comparative effect Effects 0.000 description 6
- 239000000203 mixture Substances 0.000 description 6
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 5
- 239000012752 auxiliary agent Substances 0.000 description 5
- 239000010949 copper Substances 0.000 description 5
- 150000002894 organic compounds Chemical class 0.000 description 5
- 230000009257 reactivity Effects 0.000 description 5
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 4
- 229910052782 aluminium Inorganic materials 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- 230000007423 decrease Effects 0.000 description 4
- 238000007599 discharging Methods 0.000 description 4
- 239000010408 film Substances 0.000 description 4
- 125000001153 fluoro group Chemical group F* 0.000 description 4
- 150000002430 hydrocarbons Chemical group 0.000 description 4
- 239000000463 material Substances 0.000 description 4
- 229910044991 metal oxide Inorganic materials 0.000 description 4
- 150000004706 metal oxides Chemical class 0.000 description 4
- 239000000243 solution Substances 0.000 description 4
- 239000000126 substance Substances 0.000 description 4
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 description 3
- 229910013075 LiBF Inorganic materials 0.000 description 3
- 239000004698 Polyethylene Substances 0.000 description 3
- 229920002125 Sokalan® Polymers 0.000 description 3
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 3
- 238000005275 alloying Methods 0.000 description 3
- 239000003575 carbonaceous material Substances 0.000 description 3
- 238000006243 chemical reaction Methods 0.000 description 3
- 150000002148 esters Chemical class 0.000 description 3
- 150000002484 inorganic compounds Chemical class 0.000 description 3
- 229910010272 inorganic material Inorganic materials 0.000 description 3
- XEEYBQQBJWHFJM-UHFFFAOYSA-N iron Substances [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 3
- PQXKHYXIUOZZFA-UHFFFAOYSA-M lithium fluoride Chemical compound [Li+].[F-] PQXKHYXIUOZZFA-UHFFFAOYSA-M 0.000 description 3
- IIPYXGDZVMZOAP-UHFFFAOYSA-N lithium nitrate Inorganic materials [Li+].[O-][N+]([O-])=O IIPYXGDZVMZOAP-UHFFFAOYSA-N 0.000 description 3
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 description 3
- 238000007747 plating Methods 0.000 description 3
- 229920000573 polyethylene Polymers 0.000 description 3
- 229920001721 polyimide Polymers 0.000 description 3
- 239000010936 titanium Substances 0.000 description 3
- ZNBGTBKGFZMWKR-UHFFFAOYSA-N 1,1,2,2,3,3,4,4-octafluoro-5-(1,1,2,2-tetrafluoroethoxy)pentane Chemical compound FC(F)C(F)(F)OCC(F)(F)C(F)(F)C(F)(F)C(F)F ZNBGTBKGFZMWKR-UHFFFAOYSA-N 0.000 description 2
- HCBRSIIGBBDDCD-UHFFFAOYSA-N 1,1,2,2-tetrafluoro-3-(1,1,2,2-tetrafluoroethoxy)propane Chemical compound FC(F)C(F)(F)COC(F)(F)C(F)F HCBRSIIGBBDDCD-UHFFFAOYSA-N 0.000 description 2
- LCGLNKUTAGEVQW-UHFFFAOYSA-N Dimethyl ether Chemical compound COC LCGLNKUTAGEVQW-UHFFFAOYSA-N 0.000 description 2
- 229910013716 LiNi Inorganic materials 0.000 description 2
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 2
- 239000004642 Polyimide Substances 0.000 description 2
- 239000004743 Polypropylene Substances 0.000 description 2
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 2
- MCMNRKCIXSYSNV-UHFFFAOYSA-N Zirconium dioxide Chemical compound O=[Zr]=O MCMNRKCIXSYSNV-UHFFFAOYSA-N 0.000 description 2
- 239000011149 active material Substances 0.000 description 2
- 125000000217 alkyl group Chemical group 0.000 description 2
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 2
- 239000006229 carbon black Substances 0.000 description 2
- 229910000428 cobalt oxide Inorganic materials 0.000 description 2
- IVMYJDGYRUAWML-UHFFFAOYSA-N cobalt(ii) oxide Chemical compound [Co]=O IVMYJDGYRUAWML-UHFFFAOYSA-N 0.000 description 2
- 238000000151 deposition Methods 0.000 description 2
- FKRCODPIKNYEAC-UHFFFAOYSA-N ethyl propionate Chemical compound CCOC(=O)CC FKRCODPIKNYEAC-UHFFFAOYSA-N 0.000 description 2
- AMWRITDGCCNYAT-UHFFFAOYSA-L hydroxy(oxo)manganese;manganese Chemical compound [Mn].O[Mn]=O.O[Mn]=O AMWRITDGCCNYAT-UHFFFAOYSA-L 0.000 description 2
- 229910003480 inorganic solid Inorganic materials 0.000 description 2
- 238000009830 intercalation Methods 0.000 description 2
- 230000002687 intercalation Effects 0.000 description 2
- 150000002500 ions Chemical class 0.000 description 2
- 238000010030 laminating Methods 0.000 description 2
- AMXOYNBUYSYVKV-UHFFFAOYSA-M lithium bromide Chemical compound [Li+].[Br-] AMXOYNBUYSYVKV-UHFFFAOYSA-M 0.000 description 2
- KWGKDLIKAYFUFQ-UHFFFAOYSA-M lithium chloride Chemical compound [Li+].[Cl-] KWGKDLIKAYFUFQ-UHFFFAOYSA-M 0.000 description 2
- 230000007246 mechanism Effects 0.000 description 2
- 229910001463 metal phosphate Inorganic materials 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- 239000002048 multi walled nanotube Substances 0.000 description 2
- LNOPIUAQISRISI-UHFFFAOYSA-N n'-hydroxy-2-propan-2-ylsulfonylethanimidamide Chemical compound CC(C)S(=O)(=O)CC(N)=NO LNOPIUAQISRISI-UHFFFAOYSA-N 0.000 description 2
- 239000005518 polymer electrolyte Substances 0.000 description 2
- 229920001155 polypropylene Polymers 0.000 description 2
- 238000004080 punching Methods 0.000 description 2
- 150000003839 salts Chemical group 0.000 description 2
- 229910052710 silicon Inorganic materials 0.000 description 2
- 239000002109 single walled nanotube Substances 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- 238000003860 storage Methods 0.000 description 2
- 229920003048 styrene butadiene rubber Polymers 0.000 description 2
- 229910052718 tin Inorganic materials 0.000 description 2
- YFNKIDBQEZZDLK-UHFFFAOYSA-N triglyme Chemical compound COCCOCCOCCOC YFNKIDBQEZZDLK-UHFFFAOYSA-N 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- 238000003466 welding Methods 0.000 description 2
- YLOUSLWKRLJSPV-UHFFFAOYSA-N 1,1,1,2,2,3,3-heptafluoro-4-(2,2,3,3,4,4,4-heptafluorobutoxy)butane Chemical compound FC(F)(F)C(F)(F)C(F)(F)COCC(F)(F)C(F)(F)C(F)(F)F YLOUSLWKRLJSPV-UHFFFAOYSA-N 0.000 description 1
- ZYAMKYAPIQPWQR-UHFFFAOYSA-N 1,1,1,2,2-pentafluoro-3-methoxypropane Chemical compound COCC(F)(F)C(F)(F)F ZYAMKYAPIQPWQR-UHFFFAOYSA-N 0.000 description 1
- YQQHEHMVPLLOKE-UHFFFAOYSA-N 1,1,2,2-tetrafluoro-1-methoxyethane Chemical compound COC(F)(F)C(F)F YQQHEHMVPLLOKE-UHFFFAOYSA-N 0.000 description 1
- XXTXKRUJTGNVOA-UHFFFAOYSA-N 1,1,2,2-tetrafluoro-3-(fluoromethoxy)propane Chemical compound FCOCC(F)(F)C(F)F XXTXKRUJTGNVOA-UHFFFAOYSA-N 0.000 description 1
- CTXZHYNQHNBVKL-UHFFFAOYSA-N 1,1,2,2-tetrafluoro-3-methoxypropane Chemical compound COCC(F)(F)C(F)F CTXZHYNQHNBVKL-UHFFFAOYSA-N 0.000 description 1
- DEYAWNMYIUDQER-UHFFFAOYSA-N 1-(1,1,2,2-tetrafluoroethoxy)propane Chemical compound CCCOC(F)(F)C(F)F DEYAWNMYIUDQER-UHFFFAOYSA-N 0.000 description 1
- DFUYAWQUODQGFF-UHFFFAOYSA-N 1-ethoxy-1,1,2,2,3,3,4,4,4-nonafluorobutane Chemical compound CCOC(F)(F)C(F)(F)C(F)(F)C(F)(F)F DFUYAWQUODQGFF-UHFFFAOYSA-N 0.000 description 1
- HBRLMDFVVMYNFH-UHFFFAOYSA-N 1-ethoxy-1,1,2,2-tetrafluoroethane Chemical compound CCOC(F)(F)C(F)F HBRLMDFVVMYNFH-UHFFFAOYSA-N 0.000 description 1
- DMECHFLLAQSVAD-UHFFFAOYSA-N 1-ethoxy-1,1,2,3,3,3-hexafluoropropane Chemical compound CCOC(F)(F)C(F)C(F)(F)F DMECHFLLAQSVAD-UHFFFAOYSA-N 0.000 description 1
- ZKNHDJMXIUOHLX-UHFFFAOYSA-N 2-ethoxy-1,1,1-trifluoroethane Chemical compound CCOCC(F)(F)F ZKNHDJMXIUOHLX-UHFFFAOYSA-N 0.000 description 1
- FNUBKINEQIEODM-UHFFFAOYSA-N 3,3,4,4,5,5,5-heptafluoropentanal Chemical compound FC(F)(F)C(F)(F)C(F)(F)CC=O FNUBKINEQIEODM-UHFFFAOYSA-N 0.000 description 1
- PCTQNZRJAGLDPD-UHFFFAOYSA-N 3-(difluoromethoxy)-1,1,2,2-tetrafluoropropane Chemical compound FC(F)OCC(F)(F)C(F)F PCTQNZRJAGLDPD-UHFFFAOYSA-N 0.000 description 1
- OYOKPDLAMOMTEE-UHFFFAOYSA-N 4-chloro-1,3-dioxolan-2-one Chemical compound ClC1COC(=O)O1 OYOKPDLAMOMTEE-UHFFFAOYSA-N 0.000 description 1
- 229920000178 Acrylic resin Polymers 0.000 description 1
- 239000004925 Acrylic resin Substances 0.000 description 1
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 1
- OIFBSDVPJOWBCH-UHFFFAOYSA-N Diethyl carbonate Chemical compound CCOC(=O)OCC OIFBSDVPJOWBCH-UHFFFAOYSA-N 0.000 description 1
- KMTRUDSVKNLOMY-UHFFFAOYSA-N Ethylene carbonate Chemical compound O=C1OCCO1 KMTRUDSVKNLOMY-UHFFFAOYSA-N 0.000 description 1
- GYHNNYVSQQEPJS-UHFFFAOYSA-N Gallium Chemical compound [Ga] GYHNNYVSQQEPJS-UHFFFAOYSA-N 0.000 description 1
- 229910018068 Li 2 O Inorganic materials 0.000 description 1
- 229910015015 LiAsF 6 Inorganic materials 0.000 description 1
- 229910013063 LiBF 4 Inorganic materials 0.000 description 1
- 229910012851 LiCoO 2 Inorganic materials 0.000 description 1
- 229910010707 LiFePO 4 Inorganic materials 0.000 description 1
- 229910015643 LiMn 2 O 4 Inorganic materials 0.000 description 1
- 229910013528 LiN(SO2 CF3)2 Inorganic materials 0.000 description 1
- 229910013553 LiNO Inorganic materials 0.000 description 1
- 229910015720 LiNi0.85Co0.12Al0.03O2 Inorganic materials 0.000 description 1
- 229910013290 LiNiO 2 Inorganic materials 0.000 description 1
- 229910013870 LiPF 6 Inorganic materials 0.000 description 1
- 229910012424 LiSO 3 Inorganic materials 0.000 description 1
- RJUFJBKOKNCXHH-UHFFFAOYSA-N Methyl propionate Chemical compound CCC(=O)OC RJUFJBKOKNCXHH-UHFFFAOYSA-N 0.000 description 1
- 238000005481 NMR spectroscopy Methods 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 1
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 1
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 description 1
- KXKVLQRXCPHEJC-UHFFFAOYSA-N acetic acid trimethyl ester Natural products COC(C)=O KXKVLQRXCPHEJC-UHFFFAOYSA-N 0.000 description 1
- 239000006230 acetylene black Substances 0.000 description 1
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 1
- 229910052787 antimony Inorganic materials 0.000 description 1
- 239000004760 aramid Substances 0.000 description 1
- 229920003235 aromatic polyamide Polymers 0.000 description 1
- 229910052797 bismuth Inorganic materials 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 239000002134 carbon nanofiber Substances 0.000 description 1
- 239000002041 carbon nanotube Substances 0.000 description 1
- 229910021393 carbon nanotube Inorganic materials 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 1
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 1
- 239000002800 charge carrier Substances 0.000 description 1
- GIPIUENNGCQCIT-UHFFFAOYSA-K cobalt(3+) phosphate Chemical class [Co+3].[O-]P([O-])([O-])=O GIPIUENNGCQCIT-UHFFFAOYSA-K 0.000 description 1
- 238000013329 compounding Methods 0.000 description 1
- 239000004020 conductor Substances 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- SBZXBUIDTXKZTM-UHFFFAOYSA-N diglyme Chemical compound COCCOCCOC SBZXBUIDTXKZTM-UHFFFAOYSA-N 0.000 description 1
- IEJIGPNLZYLLBP-UHFFFAOYSA-N dimethyl carbonate Chemical compound COC(=O)OC IEJIGPNLZYLLBP-UHFFFAOYSA-N 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 238000010828 elution Methods 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 150000002170 ethers Chemical class 0.000 description 1
- JBTWLSYIZRCDFO-UHFFFAOYSA-N ethyl methyl carbonate Chemical compound CCOC(=O)OC JBTWLSYIZRCDFO-UHFFFAOYSA-N 0.000 description 1
- 125000003784 fluoroethyl group Chemical group [H]C([H])(F)C([H])([H])* 0.000 description 1
- 229910052733 gallium Inorganic materials 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 229910052732 germanium Inorganic materials 0.000 description 1
- GNPVGFCGXDBREM-UHFFFAOYSA-N germanium atom Chemical compound [Ge] GNPVGFCGXDBREM-UHFFFAOYSA-N 0.000 description 1
- 229910021389 graphene Inorganic materials 0.000 description 1
- 229910002804 graphite Inorganic materials 0.000 description 1
- 239000010439 graphite Substances 0.000 description 1
- 229910021385 hard carbon Inorganic materials 0.000 description 1
- 238000000589 high-performance liquid chromatography-mass spectrometry Methods 0.000 description 1
- 229910052738 indium Inorganic materials 0.000 description 1
- 239000010954 inorganic particle Substances 0.000 description 1
- WBJZTOZJJYAKHQ-UHFFFAOYSA-K iron(3+) phosphate Chemical class [Fe+3].[O-]P([O-])([O-])=O WBJZTOZJJYAKHQ-UHFFFAOYSA-K 0.000 description 1
- 230000002427 irreversible effect Effects 0.000 description 1
- 238000005304 joining Methods 0.000 description 1
- 229910052745 lead Inorganic materials 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- XGZVUEUWXADBQD-UHFFFAOYSA-L lithium carbonate Chemical compound [Li+].[Li+].[O-]C([O-])=O XGZVUEUWXADBQD-UHFFFAOYSA-L 0.000 description 1
- 229910052808 lithium carbonate Inorganic materials 0.000 description 1
- HSZCZNFXUDYRKD-UHFFFAOYSA-M lithium iodide Inorganic materials [Li+].[I-] HSZCZNFXUDYRKD-UHFFFAOYSA-M 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- VTHJTEIRLNZDEV-UHFFFAOYSA-L magnesium dihydroxide Chemical compound [OH-].[OH-].[Mg+2] VTHJTEIRLNZDEV-UHFFFAOYSA-L 0.000 description 1
- 239000000347 magnesium hydroxide Substances 0.000 description 1
- 229910001862 magnesium hydroxide Inorganic materials 0.000 description 1
- 239000000395 magnesium oxide Substances 0.000 description 1
- CPLXHLVBOLITMK-UHFFFAOYSA-N magnesium oxide Inorganic materials [Mg]=O CPLXHLVBOLITMK-UHFFFAOYSA-N 0.000 description 1
- AXZKOIWUVFPNLO-UHFFFAOYSA-N magnesium;oxygen(2-) Chemical compound [O-2].[Mg+2] AXZKOIWUVFPNLO-UHFFFAOYSA-N 0.000 description 1
- 239000011572 manganese Substances 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- 238000000691 measurement method Methods 0.000 description 1
- 239000002923 metal particle Substances 0.000 description 1
- 229940017219 methyl propionate Drugs 0.000 description 1
- 239000012982 microporous membrane Substances 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 229910000480 nickel oxide Inorganic materials 0.000 description 1
- GNRSAWUEBMWBQH-UHFFFAOYSA-N oxonickel Chemical compound [Ni]=O GNRSAWUEBMWBQH-UHFFFAOYSA-N 0.000 description 1
- 125000004430 oxygen atom Chemical group O* 0.000 description 1
- 239000004584 polyacrylic acid Substances 0.000 description 1
- 229920002312 polyamide-imide Polymers 0.000 description 1
- 239000009719 polyimide resin Substances 0.000 description 1
- 229920001343 polytetrafluoroethylene Polymers 0.000 description 1
- 239000004810 polytetrafluoroethylene Substances 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- RUOJZAUFBMNUDX-UHFFFAOYSA-N propylene carbonate Chemical compound CC1COC(=O)O1 RUOJZAUFBMNUDX-UHFFFAOYSA-N 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 238000007789 sealing Methods 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- 229910052709 silver Inorganic materials 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 238000001179 sorption measurement Methods 0.000 description 1
- 239000010409 thin film Substances 0.000 description 1
- XOLBLPGZBRYERU-UHFFFAOYSA-N tin dioxide Chemical compound O=[Sn]=O XOLBLPGZBRYERU-UHFFFAOYSA-N 0.000 description 1
- 229910001887 tin oxide Inorganic materials 0.000 description 1
- OGIDPMRJRNCKJF-UHFFFAOYSA-N titanium oxide Inorganic materials [Ti]=O OGIDPMRJRNCKJF-UHFFFAOYSA-N 0.000 description 1
- DQWPFSLDHJDLRL-UHFFFAOYSA-N triethyl phosphate Chemical compound CCOP(=O)(OCC)OCC DQWPFSLDHJDLRL-UHFFFAOYSA-N 0.000 description 1
- WVLBCYQITXONBZ-UHFFFAOYSA-N trimethyl phosphate Chemical compound COP(=O)(OC)OC WVLBCYQITXONBZ-UHFFFAOYSA-N 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0566—Liquid materials
- H01M10/0569—Liquid materials characterised by the solvents
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0566—Liquid materials
- H01M10/0567—Liquid materials characterised by the additives
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0566—Liquid materials
- H01M10/0568—Liquid materials characterised by the solutes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/058—Construction or manufacture
- H01M10/0585—Construction or manufacture of accumulators having only flat construction elements, i.e. flat positive electrodes, flat negative electrodes and flat separators
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/42—Methods or arrangements for servicing or maintenance of secondary cells or secondary half-cells
- H01M10/44—Methods for charging or discharging
- H01M10/446—Initial charging measures
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/04—Processes of manufacture in general
- H01M4/0438—Processes of manufacture in general by electrochemical processing
- H01M4/044—Activating, forming or electrochemical attack of the supporting material
- H01M4/0445—Forming after manufacture of the electrode, e.g. first charge, cycling
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/13—Electrodes for accumulators with non-aqueous electrolyte, e.g. for lithium-accumulators; Processes of manufacture thereof
- H01M4/134—Electrodes based on metals, Si or alloys
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/38—Selection of substances as active materials, active masses, active liquids of elements or alloys
- H01M4/381—Alkaline or alkaline earth metals elements
- H01M4/382—Lithium
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/64—Carriers or collectors
- H01M4/66—Selection of materials
- H01M4/661—Metal or alloys, e.g. alloy coatings
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0017—Non-aqueous electrolytes
- H01M2300/0025—Organic electrolyte
- H01M2300/0028—Organic electrolyte characterised by the solvent
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0017—Non-aqueous electrolytes
- H01M2300/0025—Organic electrolyte
- H01M2300/0028—Organic electrolyte characterised by the solvent
- H01M2300/0034—Fluorinated solvents
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0017—Non-aqueous electrolytes
- H01M2300/0025—Organic electrolyte
- H01M2300/0028—Organic electrolyte characterised by the solvent
- H01M2300/0037—Mixture of solvents
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Definitions
- the present invention relates to a lithium secondary battery.
- lithium secondary battery that charges and discharges by moving lithium ions between a positive electrode and a negative electrode exhibits high voltage and high energy density.
- lithium ion 2 has an active material capable of holding lithium elements in the positive electrode and the negative electrode, and charges and discharges by exchanging lithium ions between the positive electrode active material and the negative electrode active material. The next battery is known.
- Patent Document 1 provides an ultrathin lithium metal anode to achieve a volumetric energy density of greater than 1000 Wh / L and / or a mass energy density of greater than 350 Wh / kg when discharged at room temperature at a rate of at least 1 C.
- the provided lithium secondary battery is disclosed.
- Patent Document 1 discloses that in such a lithium secondary battery, charging is performed by directly depositing a further lithium metal on the lithium metal as a negative electrode active material.
- Patent Document 2 in a lithium secondary battery including a positive electrode, a negative electrode, a separation film interposed between them, and an electrolyte, in the negative electrode, metal particles are formed on a negative electrode current collector, and the negative electrode is charged. A lithium secondary battery that is moved from the positive electrode and forms a lithium metal on the negative electrode current collector in the negative electrode is disclosed.
- Patent Document 2 provides a lithium secondary battery in which such a lithium secondary battery solves a problem caused by the reactivity of a lithium metal and a problem generated in the assembly process, and has improved performance and life. Discloses what can be done.
- a lithium secondary battery including a negative electrode having a negative electrode active material it is difficult to sufficiently increase the energy density and capacity due to the volume and mass occupied by the negative electrode active material.
- a dendrite-like lithium metal is likely to be formed on the surface of the negative electrode by repeated charging and discharging, and a short circuit and a capacity decrease are likely to occur. Therefore, the cycle characteristics are not sufficient.
- a method of applying a large physical pressure to the battery to keep the interface between the negative electrode and the separator at a high pressure has been developed in order to suppress discrete growth at the time of lithium metal precipitation.
- the application of such a high voltage requires a large mechanical mechanism, the weight and volume of the battery as a whole become large, and the energy density decreases.
- the present invention has been made in view of the above problems, and an object of the present invention is to provide a lithium secondary battery having a high energy density and excellent cycle characteristics.
- the lithium secondary battery according to the embodiment of the present invention includes a positive electrode, a separator, a negative electrode having no negative electrode active material, and an electrolytic solution, and the electrolytic solution is represented by the formulas (1) to (4). It contains at least one of the represented compounds as a solvent.
- R 1 to R 4 represent hydrogen, halogen, or a hydrocarbon-substituted, partially substituted, or unsubstituted hydrocarbon group, n is 1 or more, and R is fluorine-substituted, partially substituted, or unsubstituted. Indicates the hydrocarbon group of.
- lithium secondary battery is provided with a negative electrode having no negative electrode active material, lithium metal is deposited on the surface of the negative electrode, and the precipitated lithium metal is electrolytically eluted to perform charging and discharging. , High energy density.
- the present inventors also refer to the lithium secondary battery containing the above compounds (1) to (4) as a solvent in the electrolytic solution as a solid electrolyte interface layer (hereinafter, "SEI layer") on the surface of the negative electrode. ) Is likely to be formed. Since the SEI layer has ionic conductivity, the reactivity of the lithium precipitation reaction on the negative electrode surface on which the SEI layer is formed becomes uniform with respect to the surface direction of the negative electrode surface. Therefore, in the lithium secondary battery, the growth of dendrite-like lithium metal on the negative electrode is suppressed, and the cycle characteristics are excellent.
- the factor that facilitates the formation of the SEI layer by containing the compound as a solvent is not always clear, but factors described later can be considered in the embodiment for carrying out the invention.
- the content of the compound is preferably 30% by volume or more with respect to the total amount of the solvent components of the electrolytic solution. According to such an embodiment, the SEI layer is more easily formed, so that the lithium secondary battery has more excellent cycle characteristics.
- the above electrolytic solution may further contain a fluorine solvent. According to such an aspect, the solubility of the electrolyte in the electrolytic solution tends to be further improved, or the SEI layer tends to be more easily formed, and the lithium secondary battery has further excellent cycle characteristics.
- the electrolytic solution may further contain a non-fluorine solvent. According to such an aspect, the solubility of the electrolyte in the electrolytic solution tends to be further improved, or the SEI layer tends to be more easily formed, and the lithium secondary battery has further excellent cycle characteristics.
- the lithium secondary battery is preferably a lithium secondary battery in which lithium metal is deposited on the surface of the negative electrode and the deposited lithium is dissolved to charge and discharge the lithium secondary battery. According to such an embodiment, the energy density is further increased.
- the negative electrode is preferably an electrode made of at least one selected from the group consisting of Cu, Ni, Ti, Fe, and other metals that do not react with Li, alloys thereof, and stainless steel (SUS). Is. According to such an aspect, since it is not necessary to use a highly flammable lithium metal in the production, the safety and productivity are further improved. Moreover, since such a negative electrode is stable, the cycle characteristics of the lithium secondary battery are further improved.
- the lithium secondary battery preferably has no lithium foil formed on the surface of the negative electrode before the initial charge. According to such an aspect, since it is not necessary to use a highly flammable lithium metal in the production, the safety and productivity are further improved.
- the lithium secondary battery preferably has an energy density of 350 Wh / kg or more.
- the present embodiments will be described in detail with reference to the drawings as necessary.
- the same elements are designated by the same reference numerals, and duplicate description will be omitted.
- the positional relationship such as up, down, left, and right shall be based on the positional relationship shown in the drawings unless otherwise specified.
- the dimensional ratios in the drawings are not limited to the ratios shown.
- FIG. 1 is a schematic cross-sectional view of a lithium secondary battery according to the present embodiment.
- the lithium secondary battery 100 of the present embodiment has a positive electrode 120, a negative electrode 140 having no negative electrode active material, and a separator 130 arranged between the positive electrode 120 and the negative electrode 140. 1 includes an electrolytic solution (not shown).
- the positive electrode 120 has a positive electrode current collector 110 on a surface opposite to the surface facing the separator 130.
- the negative electrode 140 has no negative electrode active material, that is, lithium and an active material that hosts lithium. Therefore, the lithium secondary battery 100 has a smaller volume and mass of the entire battery and a higher energy density in principle than the lithium secondary battery having a negative electrode having a negative electrode active material.
- charge / discharge is performed by depositing lithium metal on the negative electrode 140 and electrolytically elution of the precipitated lithium metal.
- lithium metal precipitates on the negative electrode means that the lithium metal is formed on the surface of the negative electrode and at least one surface of the solid electrolyte interface (SEI) layer described later formed on the surface of the negative electrode.
- SEI solid electrolyte interface
- the "negative electrode active material” means a substance for holding lithium ion or lithium metal in the negative electrode 140, and may be paraphrased as a host substance of lithium element (typically lithium metal). good.
- the mechanism of such holding is not particularly limited, and examples thereof include intercalation, alloying, and occlusion of metal clusters, and typically intercalation.
- Examples of such a negative electrode active material include, but are not limited to, lithium metals and alloys containing lithium metals, carbon-based substances, metal oxides, metals alloyed with lithium, and alloys containing the metals. ..
- the carbon-based substance is not particularly limited, and examples thereof include graphene, graphite, hard carbon, mesoporous carbon, carbon nanotubes, and carbon nanohorns.
- the metal oxide is not particularly limited, and examples thereof include titanium oxide-based compounds, tin oxide-based compounds, and cobalt oxide-based compounds.
- Examples of the metal alloying with lithium include silicon, germanium, tin, lead, aluminum, and gallium.
- the negative electrode does not have a negative electrode active material means that the content of the negative electrode active material in the negative electrode is 10% by mass or less with respect to the entire negative electrode.
- the content of the negative electrode active material in the negative electrode is preferably 5.0% by mass or less, 1.0% by mass or less, or 0.1% by mass or less with respect to the entire negative electrode. , 0.0% by mass or less.
- the negative electrode 140 has a content of the negative electrode active material other than the lithium metal of 10% by mass or less, preferably 5.0% by mass or less, based on the entire negative electrode, regardless of the state of charge of the battery. Yes, it may be 1.0% by mass or less, 0.1% by mass or less, or 0.0% by mass or less. Further, the negative electrode 140 has a lithium metal content of 10% by mass or less, preferably 5.0% by mass or less, based on the entire negative electrode, before the initial charge and / or at the end of the discharge. It may be 0% by mass or less, 0.1% by mass or less, or 0.0% by mass or less.
- the "lithium secondary battery having a negative electrode having no negative electrode active material” can be paraphrased as an anode-free secondary battery, a zero-anode secondary battery, or an anodeless secondary battery. Further, the “lithium secondary battery having a negative electrode having no negative electrode active material” has a negative electrode having no negative electrode active material other than the lithium metal and having no lithium metal before the initial charge and / or at the end of the discharge. It may be paraphrased as "a lithium secondary battery” or "a lithium secondary battery provided with a negative electrode current collector having no lithium metal before the initial charge and / or at the end of discharge”.
- the term "before the initial charge” of the battery means the state from the time when the battery is assembled to the time when the battery is charged for the first time. Further, “at the end of discharge” of the battery means a state in which the voltage of the battery is 1.0 V or more and 3.8 V or less.
- the amount of lithium metal deposited on the negative electrode 140 when the battery voltage is 4.2 V is M 4.2
- the mass M 4.2 is deposited on the negative electrode 140 when the battery voltage is 3.0 V.
- the ratio M 3.0 / M 4.2 of the mass M 3.0 of the lithium metal is preferably 20% or less, more preferably 15% or less, still more preferably 10% or less.
- the capacity of the negative electrode (capacity of the negative electrode active material) is set to be about the same as the capacity of the positive electrode (capacity of the positive electrode active material). Since the negative electrode 130 does not have the negative electrode active material which is the host material of the lithium element, it is not necessary to specify the capacity thereof. Therefore, since the lithium secondary battery 100 is not limited by the charge capacity due to the negative electrode, the energy density can be increased in principle.
- the negative electrode 140 is not particularly limited as long as it does not have a negative electrode active material and can be used as a current collector, but for example, Cu, Ni, Ti, Fe, and other metals that do not react with Li, and , These alloys, as well as those consisting of at least one selected from the group consisting of stainless steel (SUS).
- SUS stainless steel
- various conventionally known types of SUS can be used.
- the negative electrode material as described above one type may be used alone or two or more types may be used in combination.
- the “metal that does not react with Li” means a metal that does not react with lithium ions or lithium metal to form an alloy under the operating conditions of the lithium secondary battery.
- the negative electrode 140 is preferably made of at least one selected from the group consisting of Cu, Ni, Ti, Fe, alloys thereof, and stainless steel (SUS), and more preferably Cu, Ni. , And these alloys, and at least one selected from the group consisting of stainless steel (SUS).
- the negative electrode 140 is more preferably Cu, Ni, an alloy thereof, or stainless steel (SUS). When such a negative electrode is used, the energy density and productivity of the battery tend to be further improved.
- the negative electrode 140 is an electrode that does not contain lithium metal. Therefore, since it is not necessary to use a highly flammable and highly reactive lithium metal during production, the lithium secondary battery 100 is excellent in safety, productivity, and cycle characteristics.
- the average thickness of the negative electrode 140 is preferably 4 ⁇ m or more and 20 ⁇ m or less, more preferably 5 ⁇ m or more and 18 ⁇ m or less, and further preferably 6 ⁇ m or more and 15 ⁇ m or less. According to such an embodiment, the volume occupied by the negative electrode 140 in the lithium secondary battery 100 is reduced, so that the energy density of the lithium secondary battery 100 is further improved.
- the electrolytic solution is a solution containing an electrolyte and a solvent and having ionic conductivity, and acts as a conductive path for lithium ions.
- the electrolytic solution may be infiltrated into the separator 130, or may be sealed in a closed container together with the laminate of the positive electrode 120, the separator 130 and the negative electrode 140.
- R 1 to R 4 represent hydrogen, halogen, or a hydrocarbon-substituted, partially substituted, or unsubstituted hydrocarbon group, n is 1 or more, and R is fluorine-substituted, partially substituted, or unsubstituted. Indicates the hydrocarbon group of.
- a SEI layer is formed on the surface of a negative electrode or the like by decomposing a solvent or the like in the electrolytic solution.
- the SEI layer suppresses further decomposition of components in the electrolytic solution, irreversible reduction of lithium ions, generation of gas, and the like in the lithium secondary battery.
- the SEI layer has ionic conductivity, the reactivity of the lithium precipitation reaction becomes uniform in the surface direction of the negative electrode surface on the negative electrode surface on which the SEI layer is formed. Therefore, promoting the formation of the SEI layer is very important for improving the performance of the anode-free lithium secondary battery.
- the present inventors tend to form an SEI layer on the surface of the negative electrode and suppress the growth of a dendrite-like lithium metal on the negative electrode, resulting in a cycle. We have found that the characteristics are improved. The factors are not always clear, but the following factors can be considered.
- the SEI layer is formed starting from the portion, it is presumed that the SEI layer is likely to be formed in the lithium secondary battery 100.
- the factors are not limited to the above.
- the SEI layer formed in the lithium secondary battery 100 containing any of the above compounds (1) to (4) is compared with the SEI layer formed in the conventional lithium secondary battery.
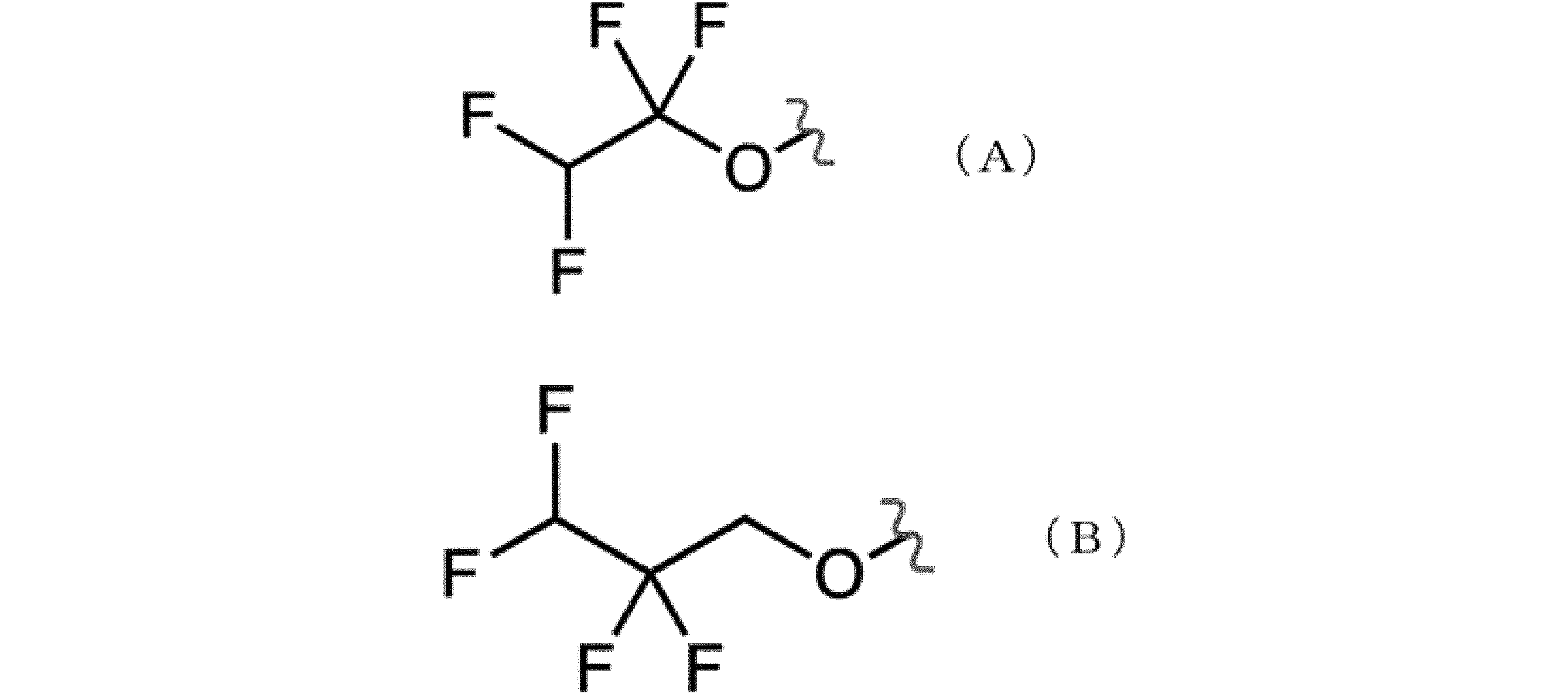
- the ion conductivity is high. This is because the portion represented by the above formula (A) and the portion represented by the above formula (B) are replaced with fluorine, so that the fluorine content of the SEI layer formed becomes high, and the SEI It is considered that this is because the movement path of lithium ions in the layer is increased or expanded.
- the factor is not limited to this.
- the lithium secondary battery 100 tends to form an SEI layer, the internal resistance of the battery is low and the rate performance is excellent. That is, the lithium secondary battery 100 is excellent in cycle characteristics and rate performance.
- the "rate performance” means the performance of being able to charge and discharge with a large current, and it is known that the rate performance is excellent when the internal resistance of the battery is low.
- a compound is "contained as a solvent” as long as the compound alone or a mixture with another compound is a liquid in the usage environment of the lithium secondary battery, and further, the electrolyte is dissolved. Anything can be used as long as it can produce an electrolytic solution in the solution phase.
- the compounds (1) to (4) used in the embodiment of the present invention are compounds (1), 1,1,2,2-tetra which are ethers having a 1,1,2,2-tetrafluoroethyl group as a skeleton.
- Compound (2) which is an ester having a fluoroethyl group in the skeleton Compound (3) which is an ether having a 2,2,3,3-tetrafluoropropyl group in the skeleton, 2,2,3,3-tetrafluoropropyl It is divided into compound (4), which is an ester having a group in its skeleton.
- the content of the compounds (1) to (4) in the electrolytic solution is not particularly limited, but is preferably 30% by volume or more, more preferably 40% by volume or more, based on the total amount of the solvent components of the electrolytic solution. It is more preferably 50% by volume or more, further preferably 60% by volume or more, and even more preferably 70% by volume or more. When the content of the compound is within the above range, the SEI layer is more easily formed, so that the lithium secondary battery 100 has further excellent cycle characteristics.
- the upper limit of the content of the compound is not particularly limited, and the content of the compound may be 100% by volume or less, 95% by volume or less, 90% by volume or less, or 80% by volume. It may be less than or equal to%.
- the electrolytic solution may contain a fluorine solvent other than the compounds (1) to (4).
- the fluorine solvent means a solvent composed of a compound having an alkyl group substituted with fluorine.
- the fluorine solvent is more preferably an ether or an ester containing the structure of the formula (A) or (B). Examples of such a fluorine solvent include 1,1,2,2-tetrafluoroethyl-2,2,3,3-tetrafluoropropyl ether and 1,1,2,2-tetrafluoroethyl-2,2.
- 2-trifluoroethyl ether methyl-1,1,2,2-tetrafluoroethyl ether, ethyl-1,1,2,2-tetrafluoroethyl ether, propyl-1,1,2,2-tetrafluoro Ethyl ether, 1H, 1H, 5H-perfluoropentyl-1,1,2,2-tetrafluoroethyl ether, and 1H, 1H, 5H-octafluoropentyl-1,1,2,2-tetrafluoroethyl ether, Difluoromethyl-2,2,3,3-tetrafluoropropyl ether, trifluoromethyl-2,2,3,3-tetrafluoropropyl ether, fluoromethyl-2,2,3,3-tetrafluoropropyl ether, and Methyl-2,2,3,3-tetrafluoropropyl ether, methylnonafluorobutyl ether,
- the electrolytic solution may further contain a non-fluorine solvent as a secondary solvent.
- the non-fluorine solvent means a solvent composed of a compound having no alkyl group substituted with fluorine.
- the non-fluorinated solvent include dimethyl ether, triethylene glycol dimethyl ether, dimethoxyethane, diethylene glycol dimethyl ether, acetonitrile, dimethyl carbonate, diethyl carbonate, ethylmethyl carbonate, ethylene carbonate, propylene carbonate, chloroethylene carbonate, methyl acetate, ethyl acetate and propyl.
- the ether compound or the ester compound is preferable as the by-solvent.
- the above compounds (1) to (4) and the auxiliary solvent can be freely used in combination, and the compounds (1) to (4) may be used alone or in combination of two or more. May be used.
- the auxiliary solvent may or may not be contained.
- the content of the auxiliary solvent is not particularly limited, but is preferably more than 0% by volume, more preferably 5% by volume or more, based on the total amount of the solvent components of the electrolytic solution. Yes, more preferably 10% by volume or more.
- the solubility of the electrolyte in the electrolytic solution tends to be further improved.
- the content of the by-solvent may be 20% by volume or more, or may be 30% by volume or more.
- the content of the auxiliary solvent may be 60% by volume or less, 50% by volume or less, 40% by volume or less, or 30% by volume or less.
- the electrolyte contained in the electrolytic solution is not particularly limited as long as it is a salt, and examples thereof include salts of Li, Na, K, Ca, and Mg.
- a lithium salt is preferably used as the electrolyte.
- the lithium salt is not particularly limited, but LiI, LiCl, LiBr, LiF, LiBF 4 , LiPF 6 , LiAsF 6 , LiSO 3 CF 3 , LiN (SO 2 F) 2 , LiN (SO 2 CF 3 ) 2 , LiN.
- LiN (SO 2 F) 2 and LiBF 2 (C 2 O 4 ) are preferable as the lithium salt.
- the electrolytic solution contains at least one of LiN (SO 2 F) 2 and LiBF 2 (C 2 O 4 )
- the formation and growth of the SEI layer on the negative electrode surface is further promoted, and the cycle characteristics are further excellent.
- the above lithium salts may be used alone or in combination of two or more.
- the concentration of the electrolyte in the electrolytic solution is not particularly limited, but is preferably 0.5 M or more, more preferably 0.7 M or more, still more preferably 0.9 M or more, still more preferably 1.0 M or more. be.
- concentration of the electrolyte is within the above range, the SEI layer is more likely to be formed, and the internal resistance tends to be lower.
- the lithium secondary battery 100 containing the compounds (1) to (4) as a solvent can increase the concentration of the electrolyte in the electrolytic solution, so that the cycle characteristics and the rate performance can be further improved.
- the upper limit of the concentration of the electrolyte is not particularly limited, and the concentration of the electrolyte may be 10.0 M or less, 5.0 M or less, or 2.0 M or less.
- the inclusion of the compound in the electrolytic solution can be confirmed by various conventionally known methods.
- Examples of such a method include an NMR measurement method, a mass spectrometry method such as HPLC-MS, and an IR measurement method.
- Solid electrolyte interface layer In the lithium secondary battery 100, it is presumed that a solid electrolyte interface layer (SEI layer) is formed on the surface of the negative electrode 140 by charging, particularly initial charging, but the lithium secondary battery 100 does not have the SEI layer. You may.
- the SEI layer formed is said to contain an organic compound derived from at least one of the portion represented by the above formula (A) and the portion represented by the above formula (B) of the compounds (1) to (4). It is presumed that, for example, other inorganic compounds containing lithium, organic compounds containing lithium, and the like may be contained.
- the lithium-containing organic compound and the lithium-containing inorganic compound are not particularly limited as long as they are contained in the conventionally known SEI layer.
- examples of the lithium-containing organic compound include organic compounds such as lithium carbonate, lithium alkoxide, and lithium alkyl ester
- examples of the lithium-containing inorganic compound include LiF. , Li 2 CO 3 , Li 2 O, LiOH, lithium borate compound, lithium phosphoric acid compound, lithium sulfuric acid compound, lithium nitrate compound, lithium nitrite compound, lithium sulfite compound and the like.
- the lithium secondary battery 100 contains the compounds (1) to (4) as a solvent, the formation of the SEI layer is promoted. Since the SEI layer has ionic conductivity, the reactivity of the lithium precipitation reaction on the negative electrode surface on which the SEI layer is formed becomes uniform with respect to the surface direction of the negative electrode surface. Therefore, in the lithium secondary battery 100, the growth of dendrite-like lithium metal on the negative electrode is suppressed, and the cycle characteristics are excellent.
- the typical average thickness of the SEI layer is 1 nm or more and 10 ⁇ m or less.
- the lithium metal deposited by charging the battery may be deposited at the interface between the negative electrode 140 and the SEI layer, or may be deposited at the interface between the SEI layer and the separator. May be good.
- the positive electrode 120 is not particularly limited as long as it is generally used for a lithium secondary battery, but a known material can be appropriately selected depending on the use of the lithium secondary battery. From the viewpoint of increasing the stability and output voltage of the lithium secondary battery 100, the positive electrode 120 preferably has a positive electrode active material.
- positive electrode active material means a substance for holding a lithium element (typically lithium ion) in a positive electrode in a battery, and is a lithium element (typically lithium ion). It may be paraphrased as a host substance.
- Such positive electrode active material is not particularly limited, and examples thereof include metal oxides and metal phosphates.
- the metal oxide is not particularly limited, and examples thereof include a cobalt oxide-based compound, a manganese oxide-based compound, and a nickel oxide-based compound.
- the metal phosphate is not particularly limited, and examples thereof include iron phosphate compounds and cobalt phosphate compounds.
- the positive electrode active material as described above is used alone or in combination of two or more.
- the positive electrode 120 may contain components other than the above-mentioned positive electrode active material. Such components include, but are not limited to, known conductive aids, binders, solid polymer electrolytes, and inorganic solid electrolytes.
- the conductive auxiliary agent in the positive electrode 120 is not particularly limited, and examples thereof include carbon black, single-walled carbon nanotubes (SW-CNT), multi-walled carbon nanotubes (MW-CNT), carbon nanofibers, and acetylene black. ..
- the binder is not particularly limited, and examples thereof include polyvinylidene fluoride, polytetrafluoroethylene, styrene butadiene rubber, acrylic resin, and polyimide resin.
- the content of the positive electrode active material in the positive electrode 120 may be, for example, 50% by mass or more and 100% by mass or less with respect to the entire positive electrode 120.
- the content of the conductive auxiliary agent may be, for example, 0.5% by mass and 30% by mass or less with respect to the entire positive electrode 120.
- the content of the binder may be, for example, 0.5% by mass and 30% by mass or less with respect to the entire positive electrode 120.
- the total content of the solid polymer electrolyte and the inorganic solid electrolyte may be, for example, 0.5% by mass and 30% by mass or less with respect to the entire positive electrode 120.
- a positive electrode current collector 110 is formed on one side of the positive electrode 120.
- the positive electrode current collector 110 is not particularly limited as long as it is a conductor that does not react with lithium ions in the battery. Examples of such a positive electrode current collector include aluminum.
- the average thickness of the positive electrode current collector 110 is preferably 4 ⁇ m or more and 20 ⁇ m or less, more preferably 5 ⁇ m or more and 18 ⁇ m or less, and further preferably 6 ⁇ m or more and 15 ⁇ m or less. According to such an embodiment, the volume occupied by the positive electrode current collector 110 in the lithium secondary battery 100 is reduced, so that the energy density of the lithium secondary battery 100 is further improved.
- the separator 130 is a member for ensuring the ionic conductivity of lithium ions serving as charge carriers between the positive electrode 120 and the negative electrode 140 while preventing the battery from short-circuiting by separating the positive electrode 120 and the negative electrode 140. It is made of a material that does not have electron conductivity and does not react with lithium ions.
- the separator 130 also plays a role of holding the electrolytic solution.
- the separator 130 is not limited as long as it plays the above role, but is composed of, for example, a porous polyethylene (PE) film, a polypropylene (PP) film, or a laminated structure thereof.
- the separator 130 may be covered with a separator coating layer.
- the separator coating layer may cover both sides of the separator 130, or may cover only one side.
- the separator coating layer is not particularly limited as long as it is a member having ionic conductivity and does not react with lithium ions, but it is preferable that the separator 130 and the layer adjacent to the separator 130 can be firmly adhered to each other. ..
- the separator coating layer is not particularly limited, and is, for example, polyvinylidene fluoride (PVDF), a mixture of styrene-butadiene rubber and carboxymethyl cellulose (SBR-CMC), polyacrylic acid (PAA), and lithium polyacrylic acid.
- the separator 130 includes a separator having a separator coating layer.
- the average thickness of the separator 130 is preferably 20 ⁇ m or less, more preferably 18 ⁇ m or less, and further preferably 15 ⁇ m or less. According to such an embodiment, the volume occupied by the separator 130 in the lithium secondary battery 100 is reduced, so that the energy density of the lithium secondary battery 100 is further improved.
- the average thickness of the separator 130 is preferably 5 ⁇ m or more, more preferably 7 ⁇ m or more, and further preferably 10 ⁇ m or more. According to such an aspect, the positive electrode 120 and the negative electrode 140 can be more reliably isolated, and the short circuit of the battery can be further suppressed.
- FIG. 2 shows one usage mode of the lithium secondary battery of the present embodiment.
- a positive electrode terminal 210 and a negative electrode terminal 220 for connecting the lithium secondary battery 200 to an external circuit are bonded to the positive electrode current collector 110 and the negative electrode 140, respectively.
- the lithium secondary battery 200 is charged and discharged by connecting the negative electrode terminal 220 to one end of the external circuit and the positive electrode terminal 210 to the other end of the external circuit.
- the lithium secondary battery 200 is charged by applying a voltage between the positive electrode terminal 210 and the negative electrode terminal 220 so that a current flows from the negative electrode terminal 220 to the positive electrode terminal 210 through an external circuit.
- a solid electrolyte interface layer (SEI layer) is formed on the surface of the negative electrode 140 (the interface between the negative electrode 140 and the separator 130) by the initial charge. It does not have to have the SEI layer.
- Charging the lithium secondary battery 200 causes precipitation of lithium metal at the interface between the negative electrode 140 and the SEI layer, the interface between the negative electrode 140 and the separator 130, and / or the interface between the SEI layer and the separator 130.
- the lithium secondary battery 200 when the positive electrode terminal 210 and the negative electrode terminal 220 are connected, the lithium secondary battery 200 is discharged. As a result, the precipitation of the lithium metal generated on the negative electrode is electrolytically eluted.
- the SEI layer is formed on the lithium secondary battery 200, the precipitation of lithium metal generated at at least one of the interface between the negative electrode 140 and the SEI layer and / or the interface between the SEI layer and the separator 130 is electrolytically eluted. ..
- the method for manufacturing the lithium secondary battery 100 as shown in FIG. 1 is not particularly limited as long as it can manufacture a lithium secondary battery having the above configuration, and examples thereof include the following methods. Be done.
- the positive electrode current collector 110 and the positive electrode 120 are manufactured, for example, as follows.
- the above-mentioned positive electrode active material, a known conductive auxiliary agent, and a known binder are mixed to obtain a positive electrode mixture.
- the compounding ratio is, for example, 50% by mass or more and 99% by mass or less of the positive electrode active material, 0.5% by mass or less of the conductive auxiliary agent, and 0.5% by mass or less of the binder with respect to the entire positive electrode mixture. It may be mass% or less.
- the obtained positive electrode mixture is applied to one side of a metal foil (for example, Al foil) as a positive electrode current collector having a predetermined thickness (for example, 5 ⁇ m or more and 1 mm or less), and press-molded.
- the obtained molded body is punched to a predetermined size by punching to obtain a positive electrode current collector 110 and a positive electrode 120.
- the above-mentioned negative electrode material for example, a metal foil of 1 ⁇ m or more and 1 mm or less (for example, an electrolytic Cu foil) is washed with a solvent containing sulfamic acid, punched to a predetermined size, and further ultrasonically washed with ethanol.
- the negative electrode 140 is obtained by drying.
- the separator 130 may be manufactured by a conventionally known method, or a commercially available one may be used.
- an electrolyte such as a lithium salt is dissolved in the solution using a solution obtained by mixing at least one of the above compounds (1) to (4) and, if necessary, the above auxiliary solvent as a solvent.
- This prepares an electrolytic solution.
- the mixing ratio of the solvent and the electrolyte may be appropriately adjusted so that the type of each solvent and the electrolyte and the content or concentration in the electrolytic solution are within the above-mentioned ranges.
- a laminated body is obtained by laminating the positive electrode current collector 110, the separator 130, and the negative electrode 140 on which the positive electrode 120 obtained as described above is formed so that the positive electrode 120 and the separator 130 face each other in this order.
- the lithium secondary battery 100 can be obtained by enclosing the obtained laminate together with the electrolytic solution in a closed container.
- the closed container is not particularly limited, and examples thereof include a laminated film.
- the present embodiment is an example for explaining the present invention, and the present invention is not limited to the present embodiment.
- the present invention can be modified in various ways as long as it does not deviate from the gist thereof. ..
- each component may not be a laminated body, but may be fixed at a distance and filled with an electrolytic solution between them.
- an auxiliary member may be arranged between the separator 130 and the negative electrode 140 to assist the lithium metal from being deposited and / or being eluted during charging and discharging.
- an auxiliary member include a member containing a metal alloying with a lithium metal, and may be, for example, a metal layer formed on the surface of the negative electrode 140.
- a metal layer include a layer containing at least one selected from the group consisting of Si, Sn, Zn, Bi, Ag, In, Pb, Sb, and Al.
- the average thickness of the metal layer may be, for example, 5 nm or more and 500 nm or less.
- the affinity between the negative electrode and the lithium metal deposited on the negative electrode is further improved, so that the lithium metal deposited on the negative electrode may peel off. It tends to be further suppressed and the cycle characteristics are further improved.
- the auxiliary member may contain a metal that alloys with the lithium metal, but its capacity is sufficiently smaller than the capacity of the positive electrode.
- the capacity of the negative electrode active material of the negative electrode is set to be about the same as the capacity of the positive electrode, but the capacity of the auxiliary member is sufficiently smaller than the capacity of the positive electrode.
- the lithium secondary battery 100 provided with such an auxiliary member can be said to "include a negative electrode having no negative electrode active material". Therefore, the capacity of the auxiliary member is sufficiently small with respect to the capacity of the positive electrode 120, for example, 20% or less, 15% or less, 10% or less, or 5% or less.
- the lithium secondary battery of the present embodiment has no lithium foil formed between the separator and the negative electrode before the initial charge.
- a lithium foil is not formed between the separator and the negative electrode before the initial charge, it is not necessary to use a lithium metal having a high possibility in manufacturing. It is a lithium secondary battery with even higher safety and productivity.
- the lithium secondary battery 100 may be provided with terminals for connecting to an external circuit on the positive electrode current collector and / or the negative electrode.
- terminals for connecting to an external circuit on the positive electrode current collector and / or the negative electrode.
- metal terminals of 10 ⁇ m or more and 1 mm or less (for example, Al, Ni, etc.) may be bonded to one or both of the positive electrode current collector and the negative electrode.
- the joining method a conventionally known method may be used, and for example, ultrasonic welding may be used.
- high energy density or “high energy density” means that the total volume of the battery or the capacity per total mass is high, but preferably 800 Wh / L or more or 350 Wh. It is / kg or more, more preferably 900 Wh / L or more or 400 Wh / kg or more, and further preferably 1000 Wh / L or more or 450 Wh / kg or more.
- excellent in cycle characteristics means that the rate of decrease in battery capacity is low before and after the number of charge / discharge cycles that can be expected in normal use. That is, when comparing the first discharge capacity after the initial charge / discharge with the capacity after the charge / discharge cycle of the number of times that can be expected in normal use, the capacity after the charge / discharge cycle is the capacity after the initial charge / discharge. It means that there is almost no decrease with respect to the first discharge capacity of.
- the "number of times that can be assumed in normal use” depends on the application in which the lithium secondary battery is used, but is, for example, 30 times, 50 times, 70 times, 100 times, 300 times, or 500 times. be.
- the capacity after the charge / discharge cycle is hardly reduced with respect to the first discharge capacity after the initial charge / discharge", depending on the application in which the lithium secondary battery is used, for example, charge.
- the capacity after the discharge cycle is 60% or more, 65% or more, 70% or more, 75% or more, 80% or more, or 85% or more with respect to the first discharge capacity after the initial charge / discharge. means.
- a lithium secondary battery was manufactured as follows. First, a 10 ⁇ m electrolytic Cu foil was washed with a solvent containing sulfamic acid, punched to a predetermined size (45 mm ⁇ 45 mm), ultrasonically washed with ethanol, and then dried. Then, the Cu foil was degreased, washed with pure water, and then immersed in a plating bath containing Sb ions. By electrolytically plating the surface of the Cu foil with the Cu foil standing horizontally, 100 nm-thick Sb was plated on the surface of the Cu foil as a metal layer. The Cu foil was taken out of the plating bath, washed with ethanol, and washed with pure water. A Cu foil coated with an Sb thin film was used as the negative electrode.
- a positive electrode was prepared.
- a mixture of 96 parts by mass of LiNi 0.85 Co 0.12 Al 0.03 O 2 as a positive electrode active material, 2 parts by mass of carbon black as a conductive auxiliary agent, and 2 parts by mass of polyvinylidene fluoride (PVDF) as a binder is 12 ⁇ m Al. It was applied to one side of the foil and press-molded. The obtained molded body was punched to a predetermined size (40 mm ⁇ 40 mm) by punching to obtain a positive electrode.
- PVDF polyvinylidene fluoride
- a separator As a separator, a separator having a predetermined size (50 mm ⁇ 50 mm) coated with 2 ⁇ m polyvinylidene fluoride (PVDF) on both sides of a 12 ⁇ m polyethylene microporous membrane was prepared.
- PVDF polyvinylidene fluoride
- the electrolytic solution was prepared as follows. In Example 1, only 1,1,2,2-tetrafluoroethoxymethoxyethaneethane was used as the first solvent (main solvent). An electrolytic solution was obtained by dissolving LiN (SO 2 F) 2 in this solvent so that the molar concentration of the electrolyte was 1.25 M.
- a laminated body was obtained by laminating the positive electrode current collector, the separator, and the negative electrode on which the positive electrode obtained as described above was formed so that the positive electrode faces the separator in this order. Further, a 100 ⁇ m Al terminal and a 100 ⁇ m Ni terminal were joined to the positive electrode current collector and the negative electrode by ultrasonic welding, respectively, and then inserted into the outer body of the laminate. Then, the electrolytic solution obtained as described above was injected into the above-mentioned exterior body. A lithium secondary battery was obtained by sealing the exterior body.
- Examples 2 to 24 A lithium secondary battery was obtained in the same manner as in Example 1 except that the electrolytic solution was prepared using the solvent and the electrolyte (lithium salt) shown in Table 1.
- TTFE is 1,1,2,2-tetrafluoroethyl-2,2,3,3-tetrafluoropropyl ether
- TFEE is 1,1,2,2-.
- Tetrafluoroethyl-2,2,2-trifluoroethyl ether "DME” stands for dimethoxyethane, "TGM” stands for triethylene glycol dimethyl ether, and "EA” stands for ethyl acetate.
- the first solvent (main solvent) is a compound corresponding to the above-mentioned compounds (1) to (4)
- the second solvent is a non-fluorine solvent as an auxiliary solvent
- the third solvent Is a fluorine solvent other than the compounds (1) to (4) as an auxiliary solvent.
- the content of the auxiliary solvent is described in volume% together with the type thereof, and the concentration of each lithium salt is described in volume molar concentration (M) together with the type.
- the content of the first solvent, which is the main solvent is not described in the table, but the content of the first solvent is the content obtained by subtracting the contents of the second solvent and the third solvent from 100% (the balance). ).
- the characteristics of the lithium secondary batteries prepared in each Example and Comparative Example were evaluated as follows.
- DCR Direct current resistance
- the prepared lithium secondary battery was CC-charged at 5.0 mA to 4.2 V, and then CC-discharged at 30 mA, 60 mA, and 90 mA for 30 seconds, respectively. At this time, the lower limit voltage was set to 2.5V, but this is an installed value and does not actually reach this point.
- CC charging was performed again at 5.0 mA to 4.2 V, and the next CC discharge was performed after the charging was completed.
- the current value I and the voltage drop V obtained as described above were plotted, and the direct current resistance (DCR) (unit: ⁇ ) was obtained from the slope of the IV characteristic obtained by linearly approximating each point.
- Examples 1 to 24 containing the compounds represented by the formulas (1) to (4) as a solvent have a very high number of cycles and cycle characteristics as compared with Comparative Examples 1 and 2 which do not contain the compounds. Turned out to be excellent. Further, Examples 1 to 24 have a DC resistance value lower than the DC resistance value predicted from the extremely high cycle characteristics, and have a DC resistance value equivalent to the DC resistance values of Comparative Examples 1 and 2. It turned out. From this, it was found that Examples 1 to 24 were excellent not only in cycle characteristics but also in rate performance.
- the lithium secondary battery of the present invention has a high energy density and excellent cycle characteristics, it has industrial applicability as a power storage device used for various purposes.
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Manufacturing & Machinery (AREA)
- Physics & Mathematics (AREA)
- Condensed Matter Physics & Semiconductors (AREA)
- General Physics & Mathematics (AREA)
- Inorganic Chemistry (AREA)
- Materials Engineering (AREA)
- Secondary Cells (AREA)
Abstract
Description
(リチウム2次電池)
図1は、本実施形態に係るリチウム2次電池の概略断面図である。図1に示すように、本実施形態のリチウム2次電池100は、正極120と、負極活物質を有しない負極140と、正極120と負極140との間に配置されているセパレータ130と、図1には図示されていない電解液とを備える。正極120は、セパレータ130に対向する面とは反対側の面に正極集電体110を有する。
負極140は、負極活物質を有さず、すなわち、リチウム及びリチウムのホストとなる活物質を有しないものである。したがって、リチウム2次電池100は、負極活物質を有する負極を備えるリチウム2次電池と比較して、電池全体の体積及び質量が小さく、エネルギー密度が原理的に高い。ここで、リチウム2次電池100は、リチウム金属が負極140上に析出し、及び、その析出したリチウム金属が電解溶出することによって充放電が行われる。
電解液は、電解質及び溶媒を含有し、イオン伝導性を有する溶液であり、リチウムイオンの導電経路として作用する。電解液は、セパレータ130に浸潤させてもよく、正極120とセパレータ130と負極140との積層体と共に密閉容器に封入してもよい。
リチウム2次電池100において、充電、特に初期充電により、負極140の表面に固体電解質界面層(SEI層)が形成されると推察されるが、リチウム2次電池100は、SEI層を有しなくてもよい。形成されるSEI層は、上記化合物(1)~(4)の上記式(A)で表される部分、及び上記式(B)で表される部分の少なくとも一方に由来する有機化合物を含むと推察されるが、例えば、その他の、リチウムを含有する無機化合物、及びリチウムを含有する有機化合物等を含んでいてもよい。
正極120としては、一般的にリチウム2次電池に用いられるものであれば、特に限定されないが、リチウム2次電池の用途によって、公知の材料を適宜選択することができる。リチウム2次電池100の安定性及び出力電圧を高める観点から、正極120は、好ましくは正極活物質を有する。
正極120の片側には、正極集電体110が形成されている。正極集電体110は、電池においてリチウムイオンと反応しない導電体であれば特に限定されない。そのような正極集電体としては、例えば、アルミニウムが挙げられる。
セパレータ130は、正極120と負極140とを隔離することにより電池が短絡することを防ぎつつ、正極120と負極140との間の電荷キャリアとなるリチウムイオンのイオン伝導性を確保するための部材であり、電子導電性を有さず、リチウムイオンと反応しない材料により構成される。また、セパレータ130は電解液を保持する役割も担う。セパレータ130は、上記役割を担う限りにおいて限定はないが、例えば、多孔質のポリエチレン(PE)膜、ポリプロピレン(PP)膜、又はこれらの積層構造により構成される。
図2に本実施形態のリチウム2次電池の1つの使用態様を示す。リチウム2次電池200は、正極集電体110及び負極140に、リチウム2次電池200を外部回路に接続するための正極端子210及び負極端子220がそれぞれ接合されている。リチウム2次電池200は、負極端子220を外部回路の一端に、正極端子210を外部回路のもう一端に接続することにより充放電される。
図1に示すようなリチウム2次電池100の製造方法としては、上述の構成を備えるリチウム2次電池を製造することができる方法であれば特に限定されないが、例えば、以下のような方法が挙げられる。
上記本実施形態は、本発明を説明するための例示であり、本発明をその本実施形態のみに限定する趣旨ではなく、本発明は、その要旨を逸脱しない限り、様々な変形が可能である。
以下のようにして、リチウム2次電池を作製した。
まず、10μmの電解Cu箔を、スルファミン酸を含む溶剤で洗浄した後に所定の大きさ(45mm×45mm)に打ち抜き、更に、エタノールで超音波洗浄した後、乾燥させた。その後、Cu箔を脱脂し、純水で洗浄した後、Sbイオンを含むめっき浴に浸漬した。Cu箔を水平に静置したままCu箔表面を電解めっきすることにより、Cu箔の表面に金属層として100nm厚のSbをめっきした。Cu箔をめっき浴から取り出し、エタノールで洗浄、純水で洗浄した。Sb薄膜がコーティングされたCu箔を負極として用いた。
表1に記載の溶媒及び電解質(リチウム塩)を用いて電解液を調製したこと以外は、実施例1と同様にしてリチウム2次電池を得た。
表1に記載の溶媒を用いて電解液を調製したこと以外は、実施例1と同様にしてリチウム2次電池を得た。なお、比較例1及び2は、化合物(1)~(4)を含有しない溶媒を使用したものである。
作製したリチウム2次電池を、3.2mAで、電圧が4.2VになるまでCC充電した(初期充電)後、3.2mAで、電圧が3.0VになるまでCC放電した(以下、「初期放電」という。)。次いで、13.6mAで、電圧が4.2VになるまでCC充電した後、20.4mAで、電圧が3.0VになるまでCC放電するサイクルを、温度25℃の環境で繰り返した。各例について、初期放電から求められた容量(以下、「初期容量」という。)を表1~14に示す。また、各例について、その放電容量が初期容量の80%になったときのサイクル回数(表中、「サイクル」という。)を表1に示す。
作製したリチウム2次電池を、5.0mAで4.2VまでCC充電した後、30mA、60mA、及び90mAでそれぞれ30秒間CC放電した。なお、この時、下限電圧は2.5Vに設定したが、これは設置値で実際はここまでは到達しない。また、各放電と放電の間は、5.0mAで再度4.2VまでCC充電し、充電完了後に次のCC放電を実施した。以上のようにして得られる電流値Iと電圧降下Vをプロットし、各点を直線近似することにより得られるI-V特性の傾きから直流抵抗(DCR)(単位:Ω)を求めた。
Claims (8)
- 前記式(1)~(4)で表される化合物の含有量が、前記電解液の溶媒成分の総量に対して、30体積%以上である、請求項1に記載のリチウム2次電池。
- 前記電解液が、下記式(1)~(4)で表される化合物以外のフッ素溶媒を更に含有する、請求項1又は2に記載のリチウム2次電池。
- 前記電解液が、非フッ素溶媒を更に含有する、請求項1~3のいずれかに記載のリチウム2次電池。
- 前記リチウム2次電池は、リチウム金属が前記負極の表面に析出し、及び、その析出したリチウムが電解溶出することによって充放電が行われるリチウム2次電池である、請求項1~4のいずれか1項に記載のリチウム2次電池。
- 前記負極は、Cu、Ni、Ti、Fe、及び、その他Liと反応しない金属、及び、これらの合金、並びに、ステンレス鋼(SUS)からなる群より選択される少なくとも1種からなる電極である、請求項1~5のいずれか1項に記載のリチウム2次電池。
- 初期充電の前に、前記負極の表面にリチウム箔が形成されていない、請求項1~6のいずれか1項に記載のリチウム2次電池。
- エネルギー密度が350Wh/kg以上である、請求項1~7のいずれか1項に記載のリチウム2次電池。
Priority Applications (6)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020237017070A KR20230092997A (ko) | 2020-11-13 | 2020-11-13 | 리튬 이차 전지 |
| CN202080106878.7A CN116438692A (zh) | 2020-11-13 | 2020-11-13 | 锂二次电池 |
| PCT/JP2020/042366 WO2022102072A1 (ja) | 2020-11-13 | 2020-11-13 | リチウム2次電池 |
| EP20961600.2A EP4246646A1 (en) | 2020-11-13 | 2020-11-13 | Lithium secondary battery |
| JP2022561798A JP7537789B2 (ja) | 2020-11-13 | 2020-11-13 | リチウム2次電池 |
| US18/196,291 US20230282885A1 (en) | 2020-11-13 | 2023-05-11 | Lithium secondary battery |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PCT/JP2020/042366 WO2022102072A1 (ja) | 2020-11-13 | 2020-11-13 | リチウム2次電池 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| US18/196,291 Continuation US20230282885A1 (en) | 2020-11-13 | 2023-05-11 | Lithium secondary battery |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2022102072A1 true WO2022102072A1 (ja) | 2022-05-19 |
Family
ID=81600936
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2020/042366 WO2022102072A1 (ja) | 2020-11-13 | 2020-11-13 | リチウム2次電池 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US20230282885A1 (ja) |
| EP (1) | EP4246646A1 (ja) |
| JP (1) | JP7537789B2 (ja) |
| KR (1) | KR20230092997A (ja) |
| CN (1) | CN116438692A (ja) |
| WO (1) | WO2022102072A1 (ja) |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000294295A (ja) * | 1999-04-08 | 2000-10-20 | Hitachi Maxell Ltd | 非水電解液二次電池 |
| JP2009211822A (ja) * | 2008-02-29 | 2009-09-17 | Panasonic Corp | 非水電解質二次電池 |
| JP2019517722A (ja) | 2016-06-08 | 2019-06-24 | ソリッドエナジー システムズ,エルエルシー | 高エネルギー密度、高出力密度、高容量及び室温対応「アノードフリー」二次電池 |
| JP2019537226A (ja) | 2017-06-21 | 2019-12-19 | エルジー・ケム・リミテッド | リチウム二次電池 |
| WO2020090986A1 (ja) * | 2018-11-01 | 2020-05-07 | 株式会社Gsユアサ | 非水電解液二次電池 |
| JP2020161428A (ja) * | 2019-03-28 | 2020-10-01 | 三洋電機株式会社 | 非水電解質二次電池 |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3902052A1 (en) | 2020-04-22 | 2021-10-27 | Solvay SA | Anode-less lithium battery |
-
2020
- 2020-11-13 WO PCT/JP2020/042366 patent/WO2022102072A1/ja unknown
- 2020-11-13 CN CN202080106878.7A patent/CN116438692A/zh active Pending
- 2020-11-13 KR KR1020237017070A patent/KR20230092997A/ko unknown
- 2020-11-13 JP JP2022561798A patent/JP7537789B2/ja active Active
- 2020-11-13 EP EP20961600.2A patent/EP4246646A1/en active Pending
-
2023
- 2023-05-11 US US18/196,291 patent/US20230282885A1/en active Pending
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2000294295A (ja) * | 1999-04-08 | 2000-10-20 | Hitachi Maxell Ltd | 非水電解液二次電池 |
| JP2009211822A (ja) * | 2008-02-29 | 2009-09-17 | Panasonic Corp | 非水電解質二次電池 |
| JP2019517722A (ja) | 2016-06-08 | 2019-06-24 | ソリッドエナジー システムズ,エルエルシー | 高エネルギー密度、高出力密度、高容量及び室温対応「アノードフリー」二次電池 |
| JP2019537226A (ja) | 2017-06-21 | 2019-12-19 | エルジー・ケム・リミテッド | リチウム二次電池 |
| WO2020090986A1 (ja) * | 2018-11-01 | 2020-05-07 | 株式会社Gsユアサ | 非水電解液二次電池 |
| JP2020161428A (ja) * | 2019-03-28 | 2020-10-01 | 三洋電機株式会社 | 非水電解質二次電池 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20230092997A (ko) | 2023-06-26 |
| US20230282885A1 (en) | 2023-09-07 |
| JP7537789B2 (ja) | 2024-08-21 |
| JPWO2022102072A1 (ja) | 2022-05-19 |
| CN116438692A (zh) | 2023-07-14 |
| EP4246646A1 (en) | 2023-09-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4743752B2 (ja) | リチウムイオン二次電池 | |
| JP4222519B2 (ja) | リチウムイオン二次電池およびこれを用いた機器 | |
| JP6304746B2 (ja) | リチウムイオン二次電池 | |
| WO2017154592A1 (ja) | 非水電解液電池 | |
| US20230246240A1 (en) | Lithium secondary battery | |
| US20240266608A1 (en) | Lithium secondary battery | |
| US20240120549A1 (en) | Lithium secondary battery | |
| US20230246238A1 (en) | Lithium secondary battery | |
| JP2019129147A (ja) | 非水電解質電池 | |
| WO2022102072A1 (ja) | リチウム2次電池 | |
| WO2021229635A1 (ja) | リチウム2次電池 | |
| WO2022144947A1 (ja) | リチウム2次電池 | |
| WO2022162822A1 (ja) | リチウム2次電池及びその製造方法 | |
| WO2022215160A1 (ja) | リチウム2次電池 | |
| JP2019129145A (ja) | 非水電解質電池 | |
| WO2022091407A1 (ja) | リチウム2次電池 | |
| WO2023053295A1 (ja) | リチウム2次電池 | |
| WO2022085046A1 (ja) | リチウム2次電池 | |
| WO2023002537A1 (ja) | リチウム2次電池 | |
| JP2023130894A (ja) | 非水系電解液二次電池 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 20961600 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2022561798 Country of ref document: JP Kind code of ref document: A |
|
| ENP | Entry into the national phase |
Ref document number: 20237017070 Country of ref document: KR Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 2020961600 Country of ref document: EP Effective date: 20230613 |