WO2015114679A1 - 量子ドット複合体、当該複合体を有する波長変換素子、光電変換装置および太陽電池 - Google Patents
量子ドット複合体、当該複合体を有する波長変換素子、光電変換装置および太陽電池 Download PDFInfo
- Publication number
- WO2015114679A1 WO2015114679A1 PCT/JP2014/000445 JP2014000445W WO2015114679A1 WO 2015114679 A1 WO2015114679 A1 WO 2015114679A1 JP 2014000445 W JP2014000445 W JP 2014000445W WO 2015114679 A1 WO2015114679 A1 WO 2015114679A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- cellulose acetate
- quantum dot
- composition distribution
- weight
- degree
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/02—Use of particular materials as binders, particle coatings or suspension media therefor
- C09K11/025—Use of particular materials as binders, particle coatings or suspension media therefor non-luminescent particle coatings or suspension media
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/08—Luminescent, e.g. electroluminescent, chemiluminescent materials containing inorganic luminescent materials
- C09K11/56—Luminescent, e.g. electroluminescent, chemiluminescent materials containing inorganic luminescent materials containing sulfur
- C09K11/562—Chalcogenides
- C09K11/565—Chalcogenides with zinc cadmium
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/08—Luminescent, e.g. electroluminescent, chemiluminescent materials containing inorganic luminescent materials
- C09K11/88—Luminescent, e.g. electroluminescent, chemiluminescent materials containing inorganic luminescent materials containing selenium, tellurium or unspecified chalcogen elements
- C09K11/881—Chalcogenides
- C09K11/883—Chalcogenides with zinc or cadmium
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01B—CABLES; CONDUCTORS; INSULATORS; SELECTION OF MATERIALS FOR THEIR CONDUCTIVE, INSULATING OR DIELECTRIC PROPERTIES
- H01B1/00—Conductors or conductive bodies characterised by the conductive materials; Selection of materials as conductors
- H01B1/20—Conductive material dispersed in non-conductive organic material
- H01B1/22—Conductive material dispersed in non-conductive organic material the conductive material comprising metals or alloys
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10F—INORGANIC SEMICONDUCTOR DEVICES SENSITIVE TO INFRARED RADIATION, LIGHT, ELECTROMAGNETIC RADIATION OF SHORTER WAVELENGTH OR CORPUSCULAR RADIATION
- H10F10/00—Individual photovoltaic cells, e.g. solar cells
- H10F10/10—Individual photovoltaic cells, e.g. solar cells having potential barriers
- H10F10/16—Photovoltaic cells having only PN heterojunction potential barriers
- H10F10/167—Photovoltaic cells having only PN heterojunction potential barriers comprising Group I-III-VI materials, e.g. CdS/CuInSe2 [CIS] heterojunction photovoltaic cells
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10F—INORGANIC SEMICONDUCTOR DEVICES SENSITIVE TO INFRARED RADIATION, LIGHT, ELECTROMAGNETIC RADIATION OF SHORTER WAVELENGTH OR CORPUSCULAR RADIATION
- H10F77/00—Constructional details of devices covered by this subclass
- H10F77/10—Semiconductor bodies
- H10F77/14—Shape of semiconductor bodies; Shapes, relative sizes or dispositions of semiconductor regions within semiconductor bodies
- H10F77/143—Shape of semiconductor bodies; Shapes, relative sizes or dispositions of semiconductor regions within semiconductor bodies comprising quantum structures
- H10F77/1433—Quantum dots
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10F—INORGANIC SEMICONDUCTOR DEVICES SENSITIVE TO INFRARED RADIATION, LIGHT, ELECTROMAGNETIC RADIATION OF SHORTER WAVELENGTH OR CORPUSCULAR RADIATION
- H10F77/00—Constructional details of devices covered by this subclass
- H10F77/10—Semiconductor bodies
- H10F77/16—Material structures, e.g. crystalline structures, film structures or crystal plane orientations
- H10F77/162—Non-monocrystalline materials, e.g. semiconductor particles embedded in insulating materials
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82Y—SPECIFIC USES OR APPLICATIONS OF NANOSTRUCTURES; MEASUREMENT OR ANALYSIS OF NANOSTRUCTURES; MANUFACTURE OR TREATMENT OF NANOSTRUCTURES
- B82Y20/00—Nanooptics, e.g. quantum optics or photonic crystals
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82Y—SPECIFIC USES OR APPLICATIONS OF NANOSTRUCTURES; MEASUREMENT OR ANALYSIS OF NANOSTRUCTURES; MANUFACTURE OR TREATMENT OF NANOSTRUCTURES
- B82Y30/00—Nanotechnology for materials or surface science, e.g. nanocomposites
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10H—INORGANIC LIGHT-EMITTING SEMICONDUCTOR DEVICES HAVING POTENTIAL BARRIERS
- H10H20/00—Individual inorganic light-emitting semiconductor devices having potential barriers, e.g. light-emitting diodes [LED]
- H10H20/80—Constructional details
- H10H20/85—Packages
- H10H20/851—Wavelength conversion means
- H10H20/8511—Wavelength conversion means characterised by their material, e.g. binder
- H10H20/8512—Wavelength conversion materials
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E10/00—Energy generation through renewable energy sources
- Y02E10/50—Photovoltaic [PV] energy
- Y02E10/541—CuInSe2 material PV cells
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S977/00—Nanotechnology
- Y10S977/70—Nanostructure
- Y10S977/773—Nanoparticle, i.e. structure having three dimensions of 100 nm or less
- Y10S977/774—Exhibiting three-dimensional carrier confinement, e.g. quantum dots
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S977/00—Nanotechnology
- Y10S977/902—Specified use of nanostructure
- Y10S977/932—Specified use of nanostructure for electronic or optoelectronic application
- Y10S977/948—Energy storage/generating using nanostructure, e.g. fuel cell, battery
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S977/00—Nanotechnology
- Y10S977/902—Specified use of nanostructure
- Y10S977/932—Specified use of nanostructure for electronic or optoelectronic application
- Y10S977/949—Radiation emitter using nanostructure
- Y10S977/95—Electromagnetic energy
Definitions
- the present invention relates to a quantum dot composite in which quantum dots are dispersed in a matrix, and in particular, a solar cell (photoelectric conversion device), a light emitting device such as an LED, a light receiving sensor such as an infrared region, a wavelength conversion element, and light light
- a quantum dot composite that can be used in a conversion device or the like.
- a PIN junction solar cell configured by bonding a P-type semiconductor, an I-type semiconductor, and an N-type semiconductor has energy equal to or higher than the band gap (Eg) between the conduction band and the valence band of the semiconductor.
- the solar light is absorbed, electrons are excited from the valence band to the conductor, holes are generated in the valence band, and an electromotive force is generated in the solar cell.
- a PN junction solar cell and a PIN junction solar cell have a single band gap and are called single junction solar cells.
- the PN junction solar cell and the PIN junction solar cell light having energy smaller than the band gap is transmitted without being absorbed.
- energy larger than the band gap is absorbed, but of the absorbed energy, the energy larger than the band gap is consumed as thermal energy as phonons. For this reason, the single band gap single-junction solar cell has a problem that the energy conversion efficiency is poor.
- Non-Patent Document 1 uses quantum dots having band gaps of 0.7 to 1.4 eV and 1.4 to 2.1 eV. Quantum dot solar cells that can absorb broadband solar energy by forming an intermediate band by overlapping wave functions between quantum dots by arranging them have been proposed.
- Non-Patent Document 2 proposes a novel optical device in which semiconductor nanoparticles are incorporated in a polymer matrix. This film exhibits the size quantum optical effect of semiconductor nanoparticles.
- the quantum dot (QD) / polymer composite film of this document is prepared by solvent casting a suspension of nanoparticles in which a CdSe / ZnS semiconductor is suspended in a cellulose triacetate (CTA) solution. It is described that QD can be directly added to a general CTA casting solution.
- CTA cellulose triacetate
- quantum dots When using quantum dots in devices as in Non-Patent Document 2, it is often necessary to use self-supporting materials by dispersing them in a polymer matrix.
- QD quantum dot
- concentration of the quantum dots increases, the quantum dots aggregate and the luminous efficiency (quantum yield) per unit quantum dot is significantly reduced. It is common. For this reason, the quantum dot density
- concentration of a nonpatent literature 2 is as low as 0.02 wt%.
- the quantum dot concentration is increased, the luminous efficiency per unit quantum dot is reduced due to the aggregation of the quantum dots. Therefore, if the luminous efficiency is maintained, the quantum dot concentration cannot be increased. there were.
- the present inventors have found that the quantum dot concentration can be increased while maintaining the luminous efficiency by constituting the matrix with cellulose acetate having a predetermined composition distribution index (CDI).
- CDI composition distribution index
- quantum dots are dispersed in a matrix, and the matrix is composed of cellulose acetate having a composition distribution index (CDI) of 3.0 or less, and the concentration of the quantum dots is 0.05% by weight or more.
- CDI composition distribution index
- the present invention provides a quantum dot composite characterized by the following.
- the concentration of the quantum dots is preferably 10% by weight or more.
- the cellulose acetate is preferably cellulose acetate having a composition distribution index (CDI) represented by the following formula of 2.0 kg or less.
- CDI composition distribution index
- the quantum dot is preferably a CdSe / ZnS quantum dot.
- the present invention also provides a wavelength conversion element, a photoelectric conversion device, and a solar cell having the quantum dot composite.
- the quantum dot composite of the present invention since the light emission efficiency per unit quantum dot (hereinafter sometimes referred to as quantum yield) can be maintained even when the quantum dot concentration is high, the light emission intensity is high. Obtainable.
- the matrix of the quantum dot composite according to the present invention is preferably a polymer material having low interaction energy with the quantum dots. Specifically, cellulose acetate having a high electron accepting property and low interaction energy with quantum dots can be mentioned.
- the cellulose acetate used in the matrix of the quantum dot composite according to the present invention has a small composition fluctuation.
- the fluctuation of the composition is expressed as a composition distribution index (CDI).
- CDI composition distribution index
- DPw weight average polymerization degree
- Total degree of acetyl substitution The total degree of acetyl substitution can be measured by a known titration method in which cellulose acetate is dissolved in water and the degree of substitution of cellulose acetate is determined. In addition, the total degree of acetyl substitution was determined in the same manner as in the case of obtaining an actual measurement value of the composition distribution half-width described later. After cellulose acetate (sample) was completely derivatized cellulose acetate propionate (CAP), deuterated chloroform It can also melt
- CAP derivatized cellulose acetate propionate
- the total degree of acetyl substitution can be obtained by converting the degree of acetylation determined according to the method for measuring the degree of acetylation in ASTM: D-817-91 (testing method for cellulose acetate, etc.) by the following formula. This is the most common method for determining the degree of substitution of cellulose acetate.
- DS 162.14 ⁇ AV ⁇ 0.01 / (60.052-42.037 ⁇ AV ⁇ 0.01)
- AV Degree of acetylation (%)
- 500 mg of dried cellulose acetate (sample) was precisely weighed and dissolved in 50 ml of a mixed solvent of ultrapure water and acetone (volume ratio 4: 1), and then 50 ml of 0.2N sodium hydroxide aqueous solution was added. Saponify for 2 hours at 25 ° C.
- AV degree of acetylation
- AV (%) (AB) ⁇ F ⁇ 1.201 / sample weight (g)
- the total acetyl substitution degree of cellulose acetate used in the matrix of the quantum dot composite according to the present invention can be appropriately selected according to the solubility in a solvent in preparing the composite.
- a solvent for example, when acetone is used as a solvent, It is preferably 2.1 to 2.5, more preferably 2.4 to 2.5.
- N-methylpyrrolidone when used as a solvent, it is preferably 0.5 to 2.9, and more preferably 0.6 to 2.9.
- the total degree of acetyl substitution of cellulose acetate used in the matrix of the quantum dot composite according to the present invention is determined by hydrolyzing cellulose acetate in the presence of acetic acid, an excess amount of water or alcohol with respect to the acetyl group, and a catalyst (partial desorption). Acetylation reaction; aging).
- the weight average degree of polymerization (DPw) is a value determined by GPC-light scattering method using cellulose acetate propionate obtained by propionylating all remaining hydroxyl groups of cellulose acetate (sample).
- the weight average degree of polymerization is the same as the method for obtaining the measured value of the half-value width of the composition distribution described later, and the cellulose acetate (sample) is completely derivatized cellulose acetate propionate (CAP), and the size is excluded. It is determined by performing chromatographic analysis (GPC-light scattering method).
- aqueous solvents generally have a large amount of foreign matter and are easily contaminated by secondary contamination once purified.
- aqueous solvents generally have a large amount of foreign matter and are easily contaminated by secondary contamination once purified.
- water-soluble inorganic salt for example, sodium chloride
- One effective method for avoiding this problem is to derivatize water-soluble cellulose acetate so that it is dissolved in an organic solvent that is less contaminated and less susceptible to secondary contamination, and GPC-light scattering measurement is performed in the organic solvent. That is.
- composition distribution index (CDI) The compositional distribution index (CDI) is defined as the ratio of the measured value to the theoretical value of the half-width of the composition distribution [(actual value of the half-width of the composition distribution) / (theoretical value of the half-width of the composition distribution)]. .
- the composition distribution half width is also simply referred to as “substitution degree distribution half width”.
- composition distribution index is 0, but this is achieved by a special synthetic technique such as acetylating only the 6th position of a glucose residue and not acetylating other positions with 100% selectivity. Such synthesis techniques are not known. In a situation where all of the hydroxyl groups of the glucose residue are acetylated and deacetylated with the same probability, the CDI is 1.0.
- composition distribution index (CDI) of cellulose acetate used in the matrix of the quantum dot composite according to the present invention can be determined by high performance liquid chromatography (HPLC) analysis.
- HPLC analysis derivatization of the residual hydroxyl group in cellulose acetate is performed as a pretreatment, and then HPLC analysis is performed.
- the purpose of this pretreatment is to convert the low-substituted cellulose acetate into a derivative that can be easily dissolved in an organic solvent to enable HPLC analysis. That is, the residual hydroxyl group in the molecule is completely propionylated, and the fully derivatized cellulose acetate propionate (CAP) is subjected to HPLC analysis to determine the composition distribution half width (actual value).
- CAP fully derivatized cellulose acetate propionate
- the derivatization is completely carried out, there should be no residual hydroxyl groups in the molecule, and only acetyl and propionyl groups must be present.
- composition distribution index is calculated by expressing the horizontal axis (elution time) of the elution curve of cellulose acetate propionate in HPLC (reverse phase HPLC) measured under predetermined processing conditions as the degree of acetyl substitution (0 to It can be obtained by converting to 3).
- a method for converting the elution time into the degree of acetyl substitution for example, the method described in JP-A-2003-201301 (paragraph numbers [0037] to [0040]) can be used.
- elution time is measured under the same measurement conditions using a plurality of (for example, 4 or more) samples having different degrees of total acetyl substitution, and elution time (T)
- a conversion formula (conversion formula) for obtaining the degree of acetyl substitution (DS) may be obtained. That is, from the relationship between the elution time (T) and the degree of acetyl substitution (DS), a calibration curve function [usually, the following quadratic equation] is obtained by the least square method.
- substitution degree distribution curve obtained from the calibration curve [substitution degree distribution curve of cellulose acetate propionate with the abundance of cellulose acetate propionate as the vertical axis and the acetyl substitution degree as the horizontal axis]
- the substitution degree distribution half-value width is obtained as follows. The base (A) on the low substitution degree side of the peak (E) and the base line (AB) in contact with the high substitution side base (B) are drawn, and from this peak, the maximum peak (E) Take a vertical line on the horizontal axis.
- An intersection (C) between the perpendicular and the base line (AB) is determined, and an intermediate point (D) between the maximum peak (E) and the intersection (C) is obtained.
- a straight line parallel to the base line (AB) is drawn through the intermediate point (D) to obtain two intersection points (A ′, B ′) with the intermolecular substitution degree distribution curve.
- a perpendicular line is drawn from the two intersections (A ′, B ′) to the horizontal axis, and the width between the two intersections on the horizontal axis is defined as the half-value width of the maximum peak (that is, the substitution value distribution half-value width).
- the half value width of the substitution degree distribution can be determined by high performance liquid chromatography (HPLC) analysis.
- HPLC high performance liquid chromatography
- the full width at half maximum of such a composition distribution curve depends on the degree of acetylation of the hydroxyl group of each glucose chain constituting the molecular chain of cellulose acetate propionate in the sample. It reflects the difference (also called retention time). Therefore, ideally, the holding time width indicates the width of the composition distribution (in units of substitution degree).
- a high-performance liquid chromatograph has a pipe portion (such as a guide column for protecting the column) that does not contribute to distribution. Therefore, depending on the configuration of the measurement apparatus, the width of the holding time that is not caused by the width of the composition distribution is often included as an error. As described above, this error is affected by the length and inner diameter of the column, the length from the column to the detector, the handling, and the like, and varies depending on the apparatus configuration.
- the half width of the cellulose acetate composition distribution curve (actually measured half value width of the composition distribution) can usually be determined by correction based on the correction formula represented by the following formula (1).
- the correction formula represented by the following formula (1) By using such a correction equation, even if the measurement apparatus (and measurement conditions) are different, it is possible to obtain a more accurate measured value of the composition distribution half-value width as the same (substantially the same) value.
- X is an uncorrected half-value width of the composition distribution curve obtained with a predetermined measuring apparatus and measuring conditions
- Y is an apparatus constant defined by the following equation.
- composition distribution index (CDI) is determined by the following equation (2).
- CDI Z / Z 0 (2)
- Z 0 is a composition distribution curve generated when acetylation and partial deacetylation in the preparation of all partially substituted cellulose acetates occur with equal probability for all hydroxyl groups (or acetyl groups) of all molecules. It is a theoretical value of the composition distribution half width.
- Z o (theoretical value of the half width of the composition distribution) can be calculated stochastically and is obtained by the following formula (3).
- m Total number of hydroxyl groups and acetyl groups in one molecule of cellulose acetate
- DPw weight average degree of polymerization (value determined by GPC-light scattering method using cellulose acetate propionate obtained by propionylating all remaining hydroxyl groups of cellulose acetate)
- DPw weight average degree of polymerization (value determined by GPC-light scattering method using cellulose acetate propionate obtained by propionylating all remaining hydroxyl groups of cellulose acetate)
- p Total degree of acetyl substitution of cellulose acetate / 3 q: 1-p
- the weight average polymerization degree (DPw) of cellulose acetate can be determined by conducting GPC-light scattering measurement after being led to propionylated cellulose acetate as described above.
- the polymerization degree distribution should be taken into account more strictly.
- the “DPw” in the formula (3) and the formula (4) is the polymerization degree. Substituting a distribution function, the entire equation should be integrated from 0 to infinity. However, as long as DPw is used, equations (3) and (4) give theoretical values with approximately sufficient accuracy. If DPn (number average degree of polymerization) is used, the influence of the degree of polymerization distribution cannot be ignored, so DPw should be used.
- the Z (actually measured half value width of composition distribution) of the cellulose acetate composition distribution curve used in the matrix of the quantum dot composite according to the present invention is preferably 0.12 to 0.34, more preferably 0.8. 13 to 0.25.
- the theoretical formula of the composition distribution explained above is a probabilistic calculation value assuming that all acetylation and deacetylation proceed independently and equally. That is, the calculated value according to the binomial distribution.
- Such an ideal situation is not realistic.
- the composition distribution of the cellulose ester is probabilistic. Therefore, it is much wider than what is determined by the binomial distribution.
- the composition distribution of cellulose acetate can be controlled by devising post-treatment conditions after the cellulose acetate hydrolysis step.
- Literature CiBment, L., and Rivibre, C., Bull. SOC. Chim., (5) 1, 1075 (1934), Sookne, A. M., Rutherford, H. A., Mark, H., and Harris, M. J. Research Natl. Bur. Standards, 29, 123 (1942), A. J. Rosenthal, B. B. White Ind. Eng. Chem., 1952, 44 (11), pp 2693-2696.
- composition distribution Another idea to narrow the composition distribution found by the present inventors is a hydrolysis reaction (aging reaction) of cellulose acetate at a high temperature of 90 ° C. or higher (or higher than 90 ° C.).
- aging reaction aging reaction
- decomposition of cellulose is preferred in a high-temperature reaction at 90 ° C. or higher.
- This idea can be said to be a belief (stereotype) based solely on the consideration of viscosity.
- the present inventors hydrolyze cellulose acetate to obtain low-substituted cellulose acetate, it is in a large amount of acetic acid at a high temperature of 90 ° C. or higher (or higher than 90 ° C.), preferably in the presence of a strong acid such as sulfuric acid. It was found that when the reaction was carried out with the above, the degree of polymerization was not lowered, but the viscosity was lowered with a decrease in CDI. That is, it has been clarified that the viscosity decrease due to the high temperature reaction is not due to a decrease in the degree of polymerization but based on a decrease in the structural viscosity due to a narrow substitution degree distribution (composition distribution).
- composition distribution index (CDI) of cellulose acetate used in the matrix of the quantum dot composite according to the present invention is small, which means that acetyl groups in cellulose acetate are relatively uniformly dispersed in cellulose acetate. ing.
- composition distribution index (CDI) is preferably 3.0 or less, more preferably 2.0 or less, because it is difficult to cause aggregation of quantum dots in the matrix and the dispersibility thereof can be improved. preferable.
- the quantum dot composite according to the present invention is composed of cellulose acetate having a composition distribution index (CDI) of 3.0 or less, so that the quantum dot concentration (hereinafter sometimes referred to as quantum dot fraction) is 0. Even if it is 05% by weight or more, it is possible to prevent a decrease in quantum yield, and the higher the concentration, the more the quantum dot composite composed of cellulose acetate having a composition distribution index (CDI) exceeding 3.0. The difference in quantum yield becomes significant.
- CDI composition distribution index
- the quantum dot fraction of the quantum dot composite according to the present invention is preferably 1% by weight or more, more preferably 5% by weight or more, and further preferably 10% by weight or more, Most preferably, it is 20% by weight or more.
- a quantum dot composite composed of cellulose acetate having a composition distribution index (CDI) of more than 3.0 or other resin has a quantum dot fraction of 10% by weight or more, particularly as the concentration becomes higher.
- CDI composition distribution index
- the quantum dot composite according to the present invention has a high quantum yield by being composed of cellulose acetate having a composition distribution index (CDI) of 3.0 or less. Can be maintained.
- the quantum dot composite according to the present invention is composed of cellulose acetate having a composition distribution index (CDI) of 2.0 or less, whereby cellulose acetate having a composition distribution index (CDI) exceeding 2.0, or Compared to a quantum dot composite composed of other resins, a very high quantum yield can be maintained even when the quantum dot fraction is high.
- CDI composition distribution index
- the cellulose acetate used in the matrix of the quantum dot composite according to the present invention is, for example, (A) a medium to high-substituted cellulose acetate hydrolysis step (aging step), (B) a precipitation step, and as necessary. (C) It can manufacture by the washing
- (A) Hydrolysis step (aging step)
- medium to high-substituted cellulose acetate (hereinafter sometimes referred to as “raw cellulose acetate”) is hydrolyzed.
- the total acetyl substitution degree of the medium to high substitution cellulose acetate used as a raw material is, for example, 1.5 to 3, preferably 2 to 3.
- As the raw material cellulose acetate commercially available cellulose diacetate (acetyl total substitution degree: 2.27 to 2.56) and cellulose triacetate (acetyl total substitution degree: more than 2.56 to 3) can be used.
- the hydrolysis reaction can be performed by reacting raw material cellulose acetate and water in an organic solvent in the presence of a catalyst (aging catalyst).
- a catalyst aging catalyst
- the organic solvent include acetic acid, acetone, alcohol (such as methanol), and mixed solvents thereof. Among these, a solvent containing at least acetic acid is preferable.
- a catalyst generally used as a deacetylation catalyst can be used.
- sulfuric acid is particularly preferable.
- the amount of the organic solvent (for example, acetic acid) used is, for example, 0.5 to 50 parts by weight, preferably 1 to 20 parts by weight, and more preferably 3 to 10 parts by weight with respect to 1 part by weight of the raw material cellulose acetate. .
- the amount of the catalyst (for example, sulfuric acid) used is, for example, 0.005 to 1 part by weight, preferably 0.01 to 0.5 part by weight, more preferably 0.02 to 1 part by weight based on 1 part by weight of the raw material cellulose acetate. 0.3 parts by weight. If the amount of the catalyst is too small, the hydrolysis time becomes too long, which may cause a decrease in the molecular weight of cellulose acetate. On the other hand, if the amount of the catalyst is too large, the degree of change in the depolymerization rate with respect to the hydrolysis temperature increases, and even if the hydrolysis temperature is low to some extent, the depolymerization rate increases and it is difficult to obtain cellulose acetate having a somewhat high molecular weight. Become.
- the amount of water in the hydrolysis step is, for example, 0.5 to 20 parts by weight, preferably 1 to 10 parts by weight, and more preferably 2 to 7 parts by weight with respect to 1 part by weight of the raw material cellulose acetate.
- the amount of the water is, for example, 0.1 to 5 parts by weight, preferably 0.3 to 2 parts by weight, more preferably 0.5 to 1 part per 1 part by weight of the organic solvent (for example, acetic acid). .5 parts by weight.
- all amounts of water may be present in the system at the start of the reaction, in order to prevent precipitation of cellulose acetate, a part of the water to be used is present in the system at the start of the reaction, and the remaining water is removed. It may be added to the system in 1 to several times.
- the reaction temperature in the hydrolysis step is, for example, 40 to 130 ° C, preferably 50 to 120 ° C, more preferably 60 to 110 ° C.
- the reaction temperature is 90 ° C. or higher (or a temperature exceeding 90 ° C.)
- the equilibrium of the reaction tends to increase in the direction in which the rate of the reverse reaction (acetylation reaction) to the normal reaction (hydrolysis reaction) increases.
- the substitution degree distribution becomes narrow, and a low-substituted cellulose acetate having an extremely small composition distribution index (CDI) can be obtained without any particular ingenuity in the post-treatment conditions.
- Step 2 After completion of the hydrolysis reaction, the temperature of the reaction system is cooled to room temperature, and a precipitation solvent is added to precipitate low-substituted cellulose acetate.
- a precipitation solvent an organic solvent miscible with water or an organic solvent having high solubility in water can be used. Examples thereof include ketones such as acetone and methyl ethyl ketone; alcohols such as methanol, ethanol and isopropyl alcohol; esters such as ethyl acetate; nitrogen-containing compounds such as acetonitrile; ethers such as tetrahydrofuran; and mixed solvents thereof.
- the mixed solvent include a mixed solvent of acetone and methanol, a mixed solvent of isopropyl alcohol and methanol, and the like.
- composition distribution is narrow and the composition distribution index (CDI) is Very low low substituted cellulose acetate can be obtained.
- low-substituted cellulose acetate (solid matter) obtained by precipitation is dissolved in water to obtain an aqueous solution having an appropriate concentration (for example, 2 to 10% by weight, preferably 3 to 8% by weight).
- a poor solvent is added to this aqueous solution (or the aqueous solution is added to the poor solvent), and maintained at an appropriate temperature (for example, 30 ° C. or less, preferably 20 ° C. or less) to precipitate low-substituted cellulose acetate, This can be done by collecting the precipitate.
- the poor solvent include alcohols such as methanol and ketones such as acetone.
- the amount of the poor solvent used is, for example, 1 to 10 parts by weight, preferably 2 to 7 parts by weight with respect to 1 part by weight of the aqueous solution.
- the low-substituted cellulose acetate (solid matter) obtained by the precipitation or the low-substituted cellulose acetate (solid matter) obtained by the precipitation fractionation is mixed with water and an organic solvent (for example, acetone or the like).
- an organic solvent for example, acetone or the like.
- a mixed solvent of an alcohol such as ketone and ethanol, and the like and after stirring at an appropriate temperature (for example, 20 to 80 ° C., preferably 25 to 60 ° C.), it is separated into a concentrated phase and a diluted phase by centrifugation, A precipitation solvent (for example, a ketone such as acetone or an alcohol such as methanol) is added to the dilute phase, and the precipitate (solid matter) is recovered.
- the concentration of the organic solvent in the mixed solvent of water and organic solvent is, for example, 5 to 50% by weight, preferably 10 to 40% by weight.
- the precipitate (solid matter) obtained in the precipitation step (B) is preferably washed with an organic solvent (poor solvent) such as alcohol such as methanol and ketone such as acetone. Moreover, it is also preferable to wash and neutralize with an organic solvent containing a basic substance (for example, alcohol such as methanol, ketone such as acetone).
- alkali metal compounds for example, alkali metal hydroxides such as sodium hydroxide and potassium hydroxide; alkali metal carbonates such as sodium carbonate and potassium carbonate; alkali metal carbonates such as sodium hydrogen carbonate) Hydrogen salts; alkali metal carboxylates such as sodium acetate and potassium acetate; sodium alkoxides such as sodium methoxide and sodium ethoxide), alkaline earth metal compounds (for example, alkaline earth such as magnesium hydroxide and calcium hydroxide) Alkaline earth metal carbonates such as metal hydroxide, magnesium carbonate and calcium carbonate; alkaline earth metal carboxylates such as magnesium acetate and calcium acetate; alkaline earth metal alkoxides such as magnesium ethoxide, etc.) can be used. .
- alkali metal compounds such as potassium acetate are particularly preferable.
- Impurities such as the catalyst (sulfuric acid, etc.) used in the hydrolysis step can be efficiently removed by washing and neutralization.
- the quantum dot of the quantum dot composite according to the present invention is a nano-sized particle, for example, a wavelength for wavelength conversion to a light having a lower energy than the absorbed light, for each specific wavelength region of the absorbed light. Consists of a conversion composition.
- the composition of the quantum dot is not particularly limited.
- a semiconductor such as CdSe / ZnS, CdS, CdSe, CI (G) S is used.
- the quantum dots are made of, for example, an organic material, fullerene, an organic fluorescent dye, an organic fluorescent dye molecule, or the like is used.
- CdSe / ZnS because it is easily available.
- Quantum dots preferably have a particle size of 1.5 nm to 9 nm. If the particle size is less than 1.5 nm, the band gap becomes too large and the desired wavelength conversion effect cannot be obtained. On the other hand, when the particle size exceeds 9 nm, the same characteristics as a so-called bulk semiconductor are exhibited, and a quantum size effect such as a different band gap depending on the particle size cannot be expected.
- the upper limit of the quantum dot fraction of the quantum dot composite according to the present invention is not particularly limited, but is preferably 40% by weight or less from the viewpoint of dispersibility of the quantum dots.
- the quantum dot composite according to the present invention can be obtained by drying a quantum dot / cellulose acetate solution obtained by mixing a quantum dot dispersion solution and a cellulose acetate solution.
- the quantum dot composite according to the present invention is formed into a film
- the quantum dot / cellulose acetate solution is concentrated under reduced pressure, and is obtained, for example, by casting on a substrate such as a glass plate with a bar coater and drying. be able to.
- light emitting devices such as LEDs, light receiving sensors in the infrared region, wavelength conversion elements, light-to-light conversion devices, etc.
- it is formed into a film shape It is preferable to do.
- the drying can be performed by, for example, drying at room temperature for 24 hours, drying at 80 ° C. for 24 hours, and further drying under reduced pressure at 40 ° C. for 24 hours to peel the film from the substrate. Furthermore, you may dry the peeled film as needed.
- a film with a uniform surface is obtained by leveling after casting.
- a stretched film is obtained by stretching the film. Stretching can be performed by a known method.
- the film can contain a plasticizer as long as the effects of the present invention are not hindered.
- the plasticizer is not particularly limited, but polyvalent carboxylic acid ester plasticizer, glycolate plasticizer, phthalate ester plasticizer, fatty acid ester plasticizer and polyhydric alcohol ester plasticizer, polyester plasticizer, acrylic System plasticizers and the like.
- the thickness of the film-like quantum dot composite depends on the use of a solar cell (photoelectric conversion device), a light emitting device such as an LED, a light receiving sensor such as an infrared region, a wavelength conversion element, and a light-light conversion device.
- a solar cell photoelectric conversion device
- a light emitting device such as an LED
- a light receiving sensor such as an infrared region
- a wavelength conversion element such as an infrared region
- a wavelength conversion element such as an infrared region
- a light-light conversion device preferably 0.01 to 0.3 mm (10 to 300 ⁇ m), preferably 0.02 to 0.1 mm. Is more preferable. If it is thicker than 0.3 mm, it may be difficult to obtain good photoelectric conversion efficiency and wavelength conversion efficiency by reducing the total light transmittance, and if it is thinner than 0.01 mm, it is difficult to handle the material. This is because there is a case where it becomes easy to cause a defect in the material.
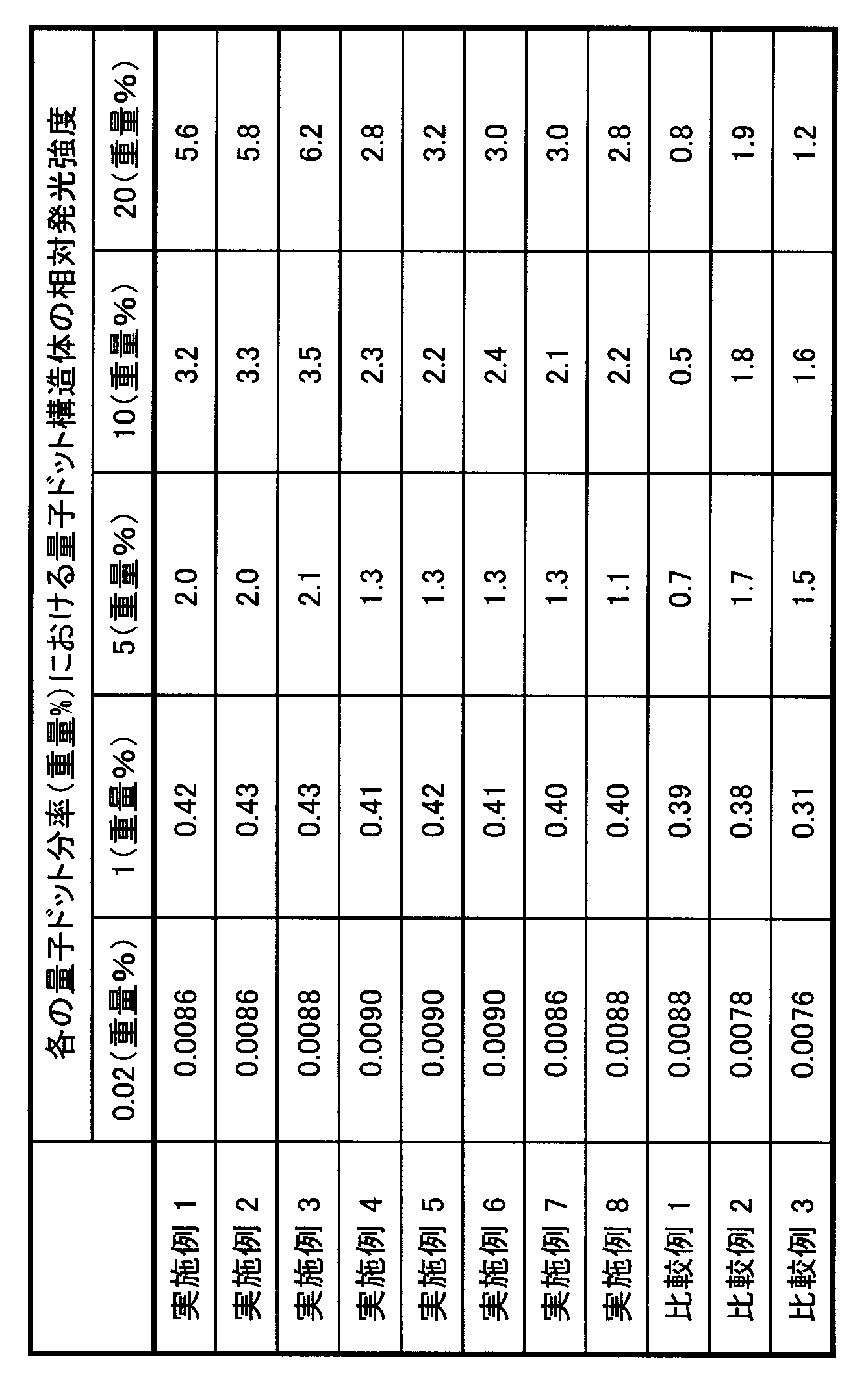
- the quantum yield of the quantum dot composite according to the present invention is the emission intensity based on the fluorescent substance Rhodamine 590, and can be specifically determined, for example, as follows.
- the polymer film which consists of a quantum dot composite and the matrix material which comprises the said quantum dot composite after calculating
- the ratio of the luminescence intensity of the quantum dot complex to the luminescence intensity of the control substance (ethanol substance solution of Rhodamine 590) having a concentration and cell thickness adjusted to have the same absorbance as the corrected absorbance is used as a control substance ( %) Is the quantum yield.
- the relative light emission intensity of the quantum dot composite according to the present invention can be determined as shown in the following formula (5).
- Relative emission intensity quantum yield x quantum dot fraction (wt%) / 100 (5)
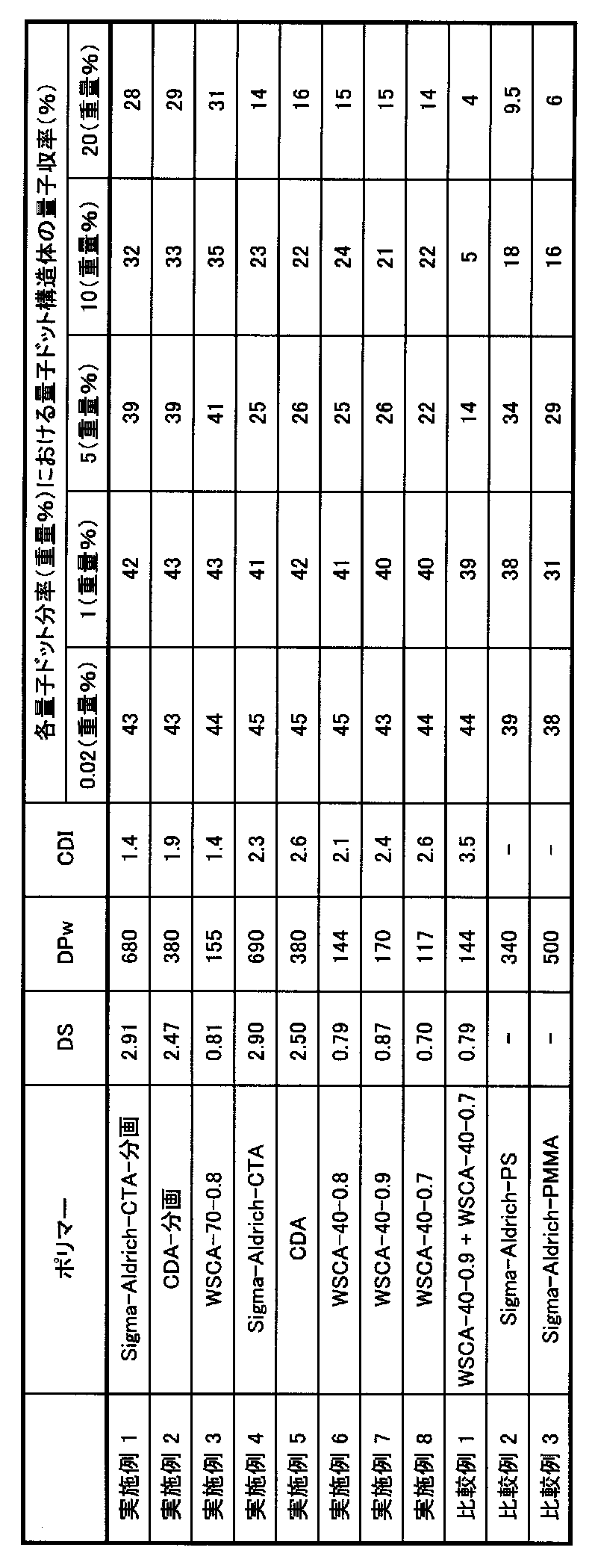
- Example 1 Cellulose acetate 100 parts by weight of cellulose triacetate (manufactured by Sigma-Aldrich) (Sigma-Aldrich-CTA) was dispersed in 1,000 parts by weight of acetone at room temperature (22 ° C.), and at 8000 rpm for 30 minutes at 15 ° C. Centrifugation was performed to obtain a gel-like sediment. The gel precipitate was dispersed in 2,000 parts by weight of methanol and centrifuged under the above-mentioned conditions to obtain a precipitate. This washing with methanol was performed twice. It dried under reduced pressure until it became constant weight at 40 degreeC.
- Quantum dot As the quantum dot, a CdSe / ZnS quantum dot (diameter 2.6 nm) dispersion (manufactured by Evident Technologies) was used. The concentration of the CdSe / ZnS quantum dot dispersion is 1.18 mg / mL, the solvent is toluene, and the emission wavelength of the quantum dots is 550 nm.
- Quantum dot / cellulose acetate solution As shown in Table 1, in order to prepare a quantum dot composite of each quantum dot fraction (% by weight), a predetermined volume of CdSe / ZnS quantum dots (diameter) with respect to 100 volume parts of cellulose acetate solution 2.6 nm) dispersion (Evident Technologies) was added.
- Quantum dot composite The quantum dot / polymer solution was concentrated under reduced pressure at 40 ° C. with a rotary evaporator to a polymer concentration of 8%. This concentrated solution is cast on a glass plate with a baker-type film applicator (wet film thickness of about 0.8 mm), dried at room temperature for 24 hours, dried at 80 ° C. for 24 hours, and further at 40 ° C. for 24 hours. The film was dried under reduced pressure to obtain a film-like quantum dot composite having a thickness of 0.07 mm.
- the obtained purified cellulose diacetate (Sigma-Aldrich-CTA-fraction) was propionylated in accordance with the method of Tezuka (Carbohydr. Res. 273, 83 (1995)) in the unsubstituted hydroxyl group of the low-substituted cellulose acetate sample. .
- the total degree of acetyl substitution in propionylated cellulose acetate was determined from 169 to 171 ppm acetylcarbonyl signal and 172 to 174 ppm propionylcarbonyl signal in 13C-NMR according to the Tezuka method (same).
- the weight average degree of polymerization (DPw) of the obtained purified cellulose diacetate was determined by conducting GPC-light scattering measurement under the following conditions after being led to propionylated cellulose acetate. did.
- composition distribution index (CDI) The composition distribution index (CDI) of the obtained purified cellulose diacetate (Sigma-Aldrich-CTA-fraction) was determined by conducting HPLC analysis under the following conditions after introduction into propionylated cellulose acetate.
- a calibration curve of elution time versus DS was prepared by HPLC analysis of a sample with a known DS in the range of 0 to 3 acetyl total substitution. Based on the calibration curve, the elution curve (time vs. detected intensity curve) of the unknown sample is converted to a DS vs. detected intensity curve (composition distribution curve), and an uncorrected half-value width X of this composition distribution curve is determined. ) To determine the corrected half-value width Z of the composition distribution. The Z is an actual measurement value of the composition distribution half width.
- X is an uncorrected half-value width of the composition distribution curve obtained with a predetermined measuring apparatus and measuring conditions
- Y is an apparatus constant defined by the following equation.
- Y (ab) x / 3 + b (0 ⁇ x ⁇ 3)
- a Apparent composition distribution half-value width of cellulose acetate having a total substitution degree of 3 determined by the same measuring apparatus and measurement conditions as X (actually, there is no substitution degree distribution because the total substitution degree is 3)
- b Apparent composition distribution half-value width of cellulose propionate having a total substitution degree of 3 determined using the same measuring apparatus and measurement conditions as X above
- x Total substitution degree of acetyl in the measurement sample (0 ⁇ x ⁇ 3)
- the composition distribution index (CDI) is determined from Z (actual value of the composition distribution half width) by the following equation (2).
- CDI Z / Z 0 (2)
- Z 0 is a composition distribution curve generated when acetylation and partial deacetylation in the preparation of all partially substituted cellulose acetates occur with equal probability for all hydroxyl groups (or acetyl groups) of all molecules.
- the theoretical value of the half-value width of the composition distribution is defined by the following formula (4).
- DPw weight average degree of polymerization (value determined by GPC-light scattering method using cellulose acetate propionate obtained by propionylating all remaining hydroxyl groups of cellulose acetate)
- p Acetyl total substitution degree / 3 q: 1-p
- Quantum yield measurement The obtained 0.07 mm thick film-like quantum dot composite and the 0.07 mm thick polymer film comprising the matrix material (Sigma-Aldrich-CTA-fraction) constituting the quantum dot composite, After obtaining the absorbance at 485 nm using a Cary 300 BIO spectrophotometer (manufactured by Varian), the absorbance of the polymer film was subtracted from the absorbance of the quantum dot complex to calculate the corrected absorbance.
- the relative light emission intensity was derived from the following formula (5) based on each quantum yield.
- Relative light emission intensity quantum yield ⁇ quantum dot fraction (% by weight) / 100 (5)
- Tables 2 and 3 show the measurement results of acetyl total substitution degree (DS), weight average polymerization degree (DPw), composition distribution index (CDI), quantum yield, and relative light emission intensity.
- Example 2 Cellulose acetate
- a hardwood prehydrolyzed kraft pulp having an ⁇ -cellulose content of 98.4 wt% was pulverized into a cotton shape with a disc refiner. After 26.8 parts by weight of acetic acid was sprayed on 100 parts by weight of pulverized pulp (water content 8%) and stirred well, the mixture was allowed to stand for 60 hours and activated as a pretreatment (activation step). The activated pulp is added to a mixture consisting of 323 parts by weight acetic acid, 245 parts by weight acetic anhydride, 13.1 parts by weight sulfuric acid and adjusted to a maximum temperature of 5 ° C to 40 ° C in 40 minutes, Vinegared for 90 minutes.
- a neutralizing agent (24% magnesium acetate aqueous solution) was added over 3 minutes so that the amount of sulfuric acid (aged sulfuric acid amount) was adjusted to 2.5 parts by weight. Furthermore, after raising the temperature of the reaction bath to 75 ° C., water was added to make the reaction bath moisture (ripening moisture) 56 mol% concentration. The aging water concentration was expressed in mol% by multiplying the ratio of the reaction bath water to acetic acid expressed in molar ratio by 100. Thereafter, aging was carried out at 75 ° C. for 210 minutes, and aging was stopped by neutralizing sulfuric acid with magnesium acetate to obtain a reaction mixture containing cellulose diacetate. A dilute aqueous acetic acid solution was added to the resulting reaction mixture to separate cellulose diacetate, and then washed with water, dried, and stabilized with calcium hydroxide to obtain cellulose diacetate (CDA).
- CDA cellulose diacetate
- cellulose diacetate (CDA) 100 parts by weight of the obtained cellulose diacetate (CDA) is dispersed in 1,000 parts by weight of methylene chloride at room temperature (about 22 ° C.) and centrifuged at 15 ° C. under conditions of 8,000 rpm-30 minutes. And a gel-like precipitate was obtained.
- the gel-like sediment was dispersed in 2,000 parts by weight of methanol, and centrifuged under the above-mentioned conditions to obtain a sediment.
- This washing with methanol was performed twice. Furthermore, it washed twice using 50 weight% of acetone aqueous solution instead of methanol. Thereafter, it was further washed twice with 1,000 parts by weight of water and dried under reduced pressure at 40 ° C. until a constant weight was obtained, to obtain 61 parts by weight of purified cellulose diacetate (CDA-fraction).
- Quantum dot composite A quantum dot composite was obtained in the same manner as in Example 1 except that purified cellulose diacetate (Sigma-Aldrich-CTA-fraction) was changed to purified cellulose diacetate (CDA-fraction).
- the measurement of the total degree of acetyl substitution (DS), the weight average degree of polymerization (DPw), the composition distribution index (CDI), the quantum yield, and the relative luminescence intensity was also carried out in the same manner as in Example 1, and the results are shown in Tables 2 and 3 Indicated.
- Example 3 Cellulose acetate
- cellulose acetate manufactured by Daicel, trade name “L-50”, acetyl total substitution degree 2.43, 6% viscosity: 110 mPa ⁇ s
- acetic acid a part by weight of acetic acid
- water was added and stirred at 40 ° C. for 5 hours to obtain a solution having a uniform appearance.
- 0.13 parts by weight of sulfuric acid was added to this solution, and the resulting solution was kept at 70 ° C. to carry out hydrolysis (partial deacetylation reaction; aging). In this aging process, water was added to the system twice in the middle.
- the third aging The first aging from the start of the reaction to the first water addition, the second aging from the first water addition to the second water addition, the reaction from the second water addition to the end of the reaction (ripening completed) This is called the third aging.
- the precipitate was recovered as a wet cake having a solid content of 15% by weight, and washed by adding 8 parts by weight of methanol and removing the liquid to a solid content of 15% by weight. This was repeated three times. The washed precipitate was further washed twice with 8 parts by weight of methanol containing 0.004% by weight of potassium acetate, neutralized and dried to obtain low-substituted cellulose acetate (WSCA-70-0.8). Obtained.
- Quantum dot composite A quantum dot composite was obtained in the same manner as in Example 1 except that the purified cellulose diacetate (Sigma-Aldrich-CTA-fraction) was changed to low-substituted cellulose acetate (WSCA-70-0.8). It was. The measurement of the total degree of acetyl substitution (DS), the weight average degree of polymerization (DPw), the composition distribution index (CDI), the quantum yield, and the relative luminescence intensity was also carried out in the same manner as in Example 1, and the results are shown in Tables 2 and 3 Indicated.
- Example 4 Cellulose acetate
- Cellulose triacetate Cellulose Triacetate, 43% acetyl, manufactured by Sigma-Aldrich
- This sample is Sigma-Aldrich-CTA.
- Quantum dot composite A quantum dot composite was obtained in the same manner as in Example 1 except that the purified cellulose diacetate (Sigma-Aldrich-CTA-fraction) was changed to cellulose triacetate (Sigma-Aldrich-CTA).
- the measurement of the total degree of acetyl substitution (DS), the weight average degree of polymerization (DPw), the composition distribution index (CDI), the quantum yield, and the relative luminescence intensity was also carried out in the same manner as in Example 1, and the results are shown in Tables 2 and 3 Indicated.
- Example 5 Cellulose acetate
- CDA Cellulose diacetate
- Quantum dot composite A quantum dot composite was obtained in the same manner as in Example 1 except that the purified cellulose diacetate (Sigma-Aldrich-CTA-fraction) was changed to cellulose diacetate (CDA).
- the measurement of the total degree of acetyl substitution (DS), the weight average degree of polymerization (DPw), the composition distribution index (CDI), the quantum yield, and the relative luminescence intensity was also carried out in the same manner as in Example 1, and the results are shown in Tables 2 and 3 Indicated.
- Example 6 Cellulose acetate Low in the same manner as in Example 3 except that the reaction temperature was 40 ° C., the first aging time was 8 hours, the second aging time was 16 hours, the third aging time was 42 hours, and the precipitating agent was changed to methanol. Substitution degree cellulose acetate (WSCA-40-0.8) was obtained.
- Quantum dot composite A quantum dot composite was obtained in the same manner as in Example 1 except that the purified cellulose diacetate (Sigma-Aldrich-CTA-fraction) was changed to low-substituted cellulose acetate (WSCA-40-0.8). It was. The measurement of the total degree of acetyl substitution (DS), the weight average degree of polymerization (DPw), the composition distribution index (CDI), the quantum yield, and the relative luminescence intensity was also carried out in the same manner as in Example 1, and the results are shown in Tables 2 and 3 Indicated.
- Example 7 Cellulose acetate Low in the same manner as in Example 3, except that the reaction temperature was 40 ° C., the first aging time was 8 hours, the second aging time was 16 hours, the third aging time was 36 hours, and the precipitating agent was changed to methanol. Substitution degree cellulose acetate (WSCA-40-0.9) was obtained.
- Quantum dot composite A quantum dot composite was obtained in the same manner as in Example 1, except that the purified cellulose diacetate (Sigma-Aldrich-CTA-fraction) was changed to low-substituted cellulose acetate (WSCA-40-0.9). It was. The measurement of the total degree of acetyl substitution (DS), the weight average degree of polymerization (DPw), the composition distribution index (CDI), the quantum yield, and the relative luminescence intensity was also carried out in the same manner as in Example 1, and the results are shown in Tables 2 and 3 Indicated.
- Example 8 Cellulose acetate Low as in Example 3, except that the reaction temperature was 40 ° C., the first aging time was 8 hours, the second aging time was 16 hours, the third aging time was 50 hours, and the precipitating agent was changed to methanol. Substitution degree cellulose acetate (WSCA-40-0.7) was obtained.
- Quantum dot composite A quantum dot composite was obtained in the same manner as in Example 1 except that the purified cellulose diacetate (Sigma-Aldrich-CTA-fraction) was changed to low-substituted cellulose acetate (WSCA-40-0.7). It was. The measurement of the total degree of acetyl substitution (DS), the weight average degree of polymerization (DPw), the composition distribution index (CDI), the quantum yield, and the relative luminescence intensity was also carried out in the same manner as in Example 1, and the results are shown in Tables 2 and 3 Indicated.
- Quantum dot composite A quantum dot composite was obtained in the same manner as in Example 1 except that the purified cellulose diacetate (Sigma-Aldrich-CTA-fraction) was changed to the low-substituted cellulose acetate mixed above.
- the measurement of the total degree of acetyl substitution (DS), the weight average degree of polymerization (DPw), the composition distribution index (CDI), the quantum yield, and the relative luminescence intensity was also carried out in the same manner as in Example 1, and the results are shown in Tables 2 and 3 Indicated.
- Example 2 A quantum dot composite was obtained in the same manner as in Example 1 except that the purified cellulose diacetate (Sigma-Aldrich-CTA-fraction) was changed to polystyrene (Mw 3,500, manufactured by Sigma-Aldrich). The measurement of acetyl total substitution degree (DS), composition distribution index (CDI), quantum yield, and relative luminescence intensity was performed in the same manner as in Example 1, and the weight average degree of polymerization (DPw) was converted from Mw. These results are shown in Tables 2 and 3.
- Example 3 A quantum dot composite was obtained in the same manner as in Example 1 except that purified cellulose diacetate (Sigma-Aldrich-CTA-fraction) was changed to polymethyl methacrylate (Mw 35,000, manufactured by Sigma-Aldrich). It was. The measurement of acetyl total substitution degree (DS), composition distribution index (CDI), quantum yield, and relative luminescence intensity was performed in the same manner as in Example 1, and the weight average degree of polymerization (DPw) was converted from Mw. These results are shown in Tables 2 and 3.
- the quantum dot composite according to the present invention can be used as a wavelength conversion element, a photoelectric conversion element, a light-light conversion element, or the like, and is a solar cell (photoelectric conversion device), a light emitting device such as an LED, or a light receiving sensor such as an infrared region. These devices and the like excellent in conversion efficiency can be realized by using them for wavelength conversion elements, light-to-light conversion devices, and the like.
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Organic Chemistry (AREA)
- Inorganic Chemistry (AREA)
- Physics & Mathematics (AREA)
- Dispersion Chemistry (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Compositions Of Macromolecular Compounds (AREA)
- Polysaccharides And Polysaccharide Derivatives (AREA)
- Life Sciences & Earth Sciences (AREA)
- Sustainable Energy (AREA)
Abstract
Description
本発明に係る量子ドット複合体のマトリクスは、量子ドットと相互作用エネルギーの低いポリマー材料であることが好ましい。具体的には、電子受容性が高く、量子ドットとの相互作用エネルギーが低い酢酸セルロースが挙げられる。
アセチル総置換度は、酢酸セルロースを水に溶解し、酢酸セルロースの置換度を求める公知の滴定法により測定できる。また、該アセチル総置換度は、後述する組成分布半値幅の実測値を求める場合と同様の方法で、酢酸セルロース(試料)を完全誘導体化セルロースアセテートプロピオネート(CAP)とした後、重クロロホルムに溶解し、NMRにより測定することもできる。
DS:アセチル総置換度
AV:酢化度(%)
まず、乾燥した酢酸セルロース(試料)500mgを精秤し、超純水とアセトンとの混合溶媒(容量比4:1)50mlに溶解した後、0.2N-水酸化ナトリウム水溶液50mlを添加し、25℃で2時間ケン化する。次に、0.2N-塩酸50mlを添加し、フェノールフタレインを指示薬として、0.2N-水酸化ナトリウム水溶液(0.2N-水酸化ナトリウム規定液)で、脱離した酢酸量を滴定する。また、同様の方法によりブランク試験(試料を用いない試験)を行う。そして、下記式にしたがってAV(酢化度)(%)を算出する。
A:0.2N-水酸化ナトリウム規定液の滴定量(ml)
B:ブランクテストにおける0.2N-水酸化ナトリウム規定液の滴定量(ml)
F:0.2N-水酸化ナトリウム規定液のファクター
本発明において、重量平均重合度(DPw)は、酢酸セルロース(試料)の残存水酸基をすべてプロピオニル化して得られるセルロースアセテートプロピオネートを用いてGPC-光散乱法により求めた値である。
組成分布指数(Compositional Distribution Index, CDI)とは、組成分布半値幅の理論値に対する実測値の比率[(組成分布半値幅の実測値)/(組成分布半値幅の理論値)]で定義される。組成分布半値幅は単に「置換度分布半値幅」ともいう。
(式中、DSはアセチル置換度であり、Tは溶出時間であり、a、bおよびcは変換式の係数である)
式(1)中、
Xは所定の測定装置および測定条件で求めた組成分布曲線の未補正半値幅、Yは次式で定義される装置定数である。
a: 前記Xと同じ測定装置および測定条件で求めた総置換度3の酢酸セルロースの見掛けの組成分布半値幅(実際は総置換度3なので、置換度分布は存在しない)
b: 前記Xと同じ測定装置および測定条件で求めた総置換度3のセルロースプロピオネートの見掛けの組成分布半値幅
x: 測定試料のアセチル総置換度(0≦x≦3)
上記式において、「アセチル総置換度=3」とは、酢酸セルロース(もしくはセルロースプロピオネート)のヒドロキシル基の全てがエステル化されたセルロースエステルを示し、実際には(又は理想的には)組成分布半値幅を有しない(すなわち、組成分布半値幅0の)酢酸セルロースである。
ここで、Z0は全ての部分置換酢酸セルロースの調製におけるアセチル化および部分脱アセチル化が全ての分子の全ての水酸基(又はアセチル基)に対して等しい確率で生じた場合に生成する組成分布曲線の組成分布半値幅の理論値である。
p:酢酸セルロース1分子中の水酸基がアセチル置換されている確率
q=1-p
DPw:重量平均重合度(酢酸セルロースの残存水酸基をすべてプロピオニル化して得られるセルロースアセテートプロピオネートを用いてGPC-光散乱法により求めた値)
p:酢酸セルロースのアセチル総置換度/3
q:1-p
本発明に係る量子ドット複合体のマトリクスに用いられる酢酸セルロースは、例えば、(A)中乃至高置換度酢酸セルロースの加水分解工程(熟成工程)、(B)沈殿工程、及び、必要に応じて行う(C)洗浄、中和工程により製造できる。
この工程では、中乃至高置換度酢酸セルロース(以下、「原料酢酸セルロース」と称する場合がある)を加水分解する。原料として用いる中乃至高置換度酢酸セルロースのアセチル総置換度は、例えば、1.5~3、好ましくは2~3である。原料酢酸セルロースとしては、市販のセルロースジアセテート(アセチル総置換度2.27~2.56)やセルローストリアセテート(アセチル総置換度2.56超~3)を用いることができる。
この工程では、加水分解反応終了後、反応系の温度を室温まで冷却し、沈殿溶媒を加えて低置換度酢酸セルロースを沈殿させる。沈殿溶媒としては、水と混和する有機溶剤若しくは水に対する溶解度の大きい有機溶剤を使用できる。例えば、アセトン、メチルエチルケトン等のケトン;メタノール、エタノール、イソプロピルアルコール等のアルコール;酢酸エチル等のエステル;アセトニトリル等の含窒素化合物;テトラヒドロフラン等のエーテル;これらの混合溶媒などが挙げられる。
10~40重量%である。
沈殿工程(B)で得られた沈殿物(固形物)は、メタノール等のアルコール、アセトン等のケトンなどの有機溶媒(貧溶媒)で洗浄するのが好ましい。また、塩基性物質を含む有機溶媒(例えば、メタノール等のアルコール、アセトン等のケトンなど)で洗浄、中和することも好ましい。
本発明に係る量子ドット複合体の量子ドットは、ナノサイズの粒子であり、例えば、それぞれ吸収した光の特定の波長領域に対して、その吸収した光よりも低いエネルギーの光に波長変換する波長変換組成物で構成される。量子ドットの組成は特に限定されるものではないが、量子ドットを、例えば、無機材料で構成する場合には、CdSe/ZnS、CdS、CdSe、CI(G)S等の半導体が用いられる。また、量子ドットを、例えば、有機材料で構成する場合には、フラーレン、有機系蛍光性色素または有機系蛍光性色素分子等が用いられる。
本発明に係る量子ドット複合体は、量子ドット分散溶液と酢酸セルロース溶液を混合した量子ドット/酢酸セルロース溶液を、乾燥させることにより得ることができる。
本発明に係る量子ドット複合体の量子収率は、蛍光物質ローダミン590(Rhodamine 590)を基準とした発光強度であり、具体的には、例えば、以下のとおり求めることができる。
本発明に係る量子ドット複合体の相対発光強度は、下記式(5)のとおり求めることができる。
(酢酸セルロース)
100重量部のセルローストリアセテート(Sigma-Aldrich社製)(Sigma-Aldrich-CTA)を1,000重量部のアセトンに室温(22℃)で分散し、15℃で8,000rpm-30分の条件で遠心分離を行い、ゲル状の沈降物を得た。ゲル状の沈降物を2,000重量部のメタノールに分散し、前述の条件で遠心分離を行い、沈降物を得た。このメタノールによる洗浄を2回行なった。40℃で恒量となるまで減圧乾燥した。この試料を2,500重量部の塩化メチレン/メタノール(=9/1(重量比))に溶解し、7,500重量部のヘキサンに滴下し沈澱物を得た。この沈澱物を40℃で恒量となるまで減圧乾燥し、80重量部の精製セルロースジアセテート(Sigma-Aldrich-CTA-分画)を得た。
精製セルロースジアセテート(Sigma-Aldrich-CTA-分画)をN-メチルピロリドン(NMP)に1.18mg/mLの濃度で溶解し、酢酸セルロース溶液を調製した。
量子ドットは、CdSe/ZnS量子ドット(直径2.6nm)分散液(Evident Technologies社製)を用いた。当該CdSe/ZnS量子ドット分散液の濃度は1.18mg/mL、溶媒はトルエン、量子ドットの発光波長は550nmである。
表1に記載のとおり、各量子ドット分率(重量%)の量子ドット複合体を調製するために、100容量部の酢酸セルロース溶液に対して、所定の容量部のCdSe/ZnS量子ドット(直径2.6nm)分散液(Evident Technologies社製)を加えた。
量子ドット/ポリマー溶液をロータリーエバポレーターで40℃で減圧濃縮し、ポリマー濃度8%とした。この濃縮した溶液を、ベーカー式フィルムアプリケーター(ウェット膜厚約0.8mm)でガラス板上に流延し、室温で24時間乾燥し、80℃で24時間乾燥し、さらに、40℃で24時間減圧乾燥し、厚さ0.07mmのフィルム状の量子ドット複合体を得た。
得られた精製セルロースジアセテート(Sigma-Aldrich-CTA-分画)を手塚の方法(Carbohydr. Res. 273, 83(1995))に準じて低置換度酢酸セルロース試料の未置換水酸基をプロピオニル化した。プロピオニル化低置換度酢酸セルロースのアセチル総置換度は、手塚の方法(同)に準じて13C-NMRにおける169~171ppmのアセチルカルボニルのシグナルおよび172~174ppmのプロピオニルカルボニルのシグナルから決定した。
得られた精製セルロースジアセテート(Sigma-Aldrich-CTA-分画)の重量平均重合度(DPw)は、プロピオニル化酢酸セルロースに導いた後、以下の条件でGPC-光散乱測定を行うことにより決定した。
溶媒:アセトン
カラム:GMHxl(東ソー)2本、同ガードカラム
流速:0.8ml/min
温度:29℃
試料濃度:0.25%(wt/vol)
注入量:100μl
検出:MALLS(多角度光散乱検出器)(Wyatt製、「DAWN-EOS」)
MALLS補正用標準物質:PMMA(分子量27600)
得られた精製セルロースジアセテート(Sigma-Aldrich-CTA-分画)の組成分布指数(CDI)は、プロピオニル化酢酸セルロースに導いた後に次の条件でHPLC分析を行うことで決定した。
カラム: Waters Nova-Pak phenyl 60Å 4μm(150mm×3.9mmΦ)+ガードカラム
カラム温度: 30℃
検出: Varian 380-LC
注入量: 5.0μL(試料濃度:0.1%(wt/vol))
溶離液: A液:MeOH/H2O=8/1(v/v),B液:CHCl3/MeOH=8/1(v/v)
グラジェント:A/B=80/20→0/100(28min);流量:0.7mL/min
Xは所定の測定装置および測定条件で求めた組成分布曲線の未補正半値幅、Yは次式で定義される装置定数である。
a: 前記Xと同じ測定装置および測定条件で求めた総置換度3の酢酸セルロースの見掛けの組成分布半値幅(実際は総置換度3なので、置換度分布は存在しない)
b: 前記Xと同じ測定装置および測定条件で求めた総置換度3のセルロースプロピオネートの見掛けの組成分布半値幅
x: 測定試料のアセチル総置換度(0≦x≦3)
Z(組成分布半値幅の実測値)から、下記式(2)により組成分布指数(CDI)が決定される。
ここで、Z0は全ての部分置換酢酸セルロースの調製におけるアセチル化および部分脱アセチル化が全ての分子の全ての水酸基(又はアセチル基)に対して等しい確率で生じた場合に生成する組成分布曲線の組成分布半値幅の理論値であり、下記式(4)で定義される。
p:アセチル総置換度/3
q:1-p
得られた厚さ0.07mmのフィルム状の量子ドット複合体および当該量子ドット複合体を構成するマトリクス材料(Sigma-Aldrich-CTA-分画)からなる厚さ0.07mmのポリマーフィルムについて、それぞれCary 300 BIO 分光光度計(Varian製)を用いて、485nmにおける吸光度を求めた後、量子ドット複合体の吸光度からポリマーフィルムの吸光度を差し引き、補正吸光度を算出した。
相対発光強度は、各量子収率に基づき下記式(5)から導いた。
アセチル総置換度(DS)、重量平均重合度(DPw)、組成分布指数(CDI)、量子収率、および相対発光強度の測定結果は表2および表3に示した。
(酢酸セルロース)
αセルロース含量98.4wt%の広葉樹前加水分解クラフトパルプをディスクリファイナーで綿状に解砕した。100重量部の解砕パルプ(含水率8%)に26.8重量部の酢酸を噴霧し、良くかき混ぜた後、前処理として60時間静置し活性化した(活性化工程)。活性化したパルプを、323重量部の酢酸、245重量部の無水酢酸、13.1重量部の硫酸からなる混合物に加え、40分を要して5℃から40℃の最高温度に調整し、90分間酢化した。中和剤(24%酢酸マグネシウム水溶液)を、硫酸量(熟成硫酸量)が2.5重量部に調整されるように3分間かけて添加した。さらに、反応浴を75℃に昇温した後、水を添加し、反応浴水分(熟成水分)を56mol%濃度とした。なお、熟成水分濃度は、反応浴水分の酢酸に対する割合をモル比で表わしたものに100を乗じてmol%で示した。その後、75℃で210分間熟成を行ない、酢酸マグネシウムで硫酸を中和することで熟成を停止し、セルロースジアセテートを含む反応混合物を得た。得られた反応混合物に希酢酸水溶液を加え、セルロースジアセテートを分離した後、水洗・乾燥・水酸化カルシウムによる安定化をしてセルロースジアセテート(CDA)を得た。
精製セルロースジアセテート(Sigma-Aldrich-CTA-分画)を精製セルロースジアセテート(CDA-分画)に変更したこと以外は、実施例1と同様にして、量子ドット複合体を得た。アセチル総置換度(DS)、重量平均重合度(DPw)、組成分布指数(CDI)、量子収率、および相対発光強度の測定も実施例1と同様に行い、結果は表2および表3に示した。
(酢酸セルロース)
1重量部の酢酸セルロース(ダイセル社製、商品名「L-50」、アセチル総置換度2.43、6%粘度:110mPa・s)に対して、5.1重量部の酢酸および2.0重量部の水を加え、40℃で5時間撹拌して外観均一な溶液を得た。この溶液に0.13重量部の硫酸を加え、得られた溶液を70℃に保持し、加水分解(部分脱アセチル化反応;熟成)を行った。なお、この熟成過程においては、途中で2回、水を系に添加した。すなわち、反応を開始して1時間後に0.67重量部の水を加え、さらに2時間後、1.67重量部の水を加え、さらに7時間反応させた。合計の加水分解時間は10時間である。なお、反応開始時から1回目の水の添加までを第1熟成、1回目の水の添加から2回目の水の添加までを第2熟成、2回目の水の添加から反応終了(熟成完了)までを第3熟成という。
精製セルロースジアセテート(Sigma-Aldrich-CTA-分画)を低置換度酢酸セルロース(WSCA-70‐0.8)に変更したこと以外は、実施例1と同様にして、量子ドット複合体を得た。アセチル総置換度(DS)、重量平均重合度(DPw)、組成分布指数(CDI)、量子収率、および相対発光強度の測定も実施例1と同様に行い、結果は表2および表3に示した。
(酢酸セルロース)
セルローストリアセテート(Cellulose Triacetate, 43% acetyl、Sigma-Aldrich社製)を用いた。なお、この試料は、Sigma-Aldrich-CTAとする。
精製セルロースジアセテート(Sigma-Aldrich-CTA-分画)をセルローストリアセテート(Sigma-Aldrich-CTA)に変更したこと以外は、実施例1と同様にして、量子ドット複合体を得た。アセチル総置換度(DS)、重量平均重合度(DPw)、組成分布指数(CDI)、量子収率、および相対発光強度の測定も実施例1と同様に行い、結果は表2および表3に示した。
(酢酸セルロース)
実施例2と同じ方法でセルロースジアセテート(CDA)を得た。
精製セルロースジアセテート(Sigma-Aldrich-CTA-分画)をセルロースジアセテート(CDA)に変更したこと以外は、実施例1と同様にして、量子ドット複合体を得た。アセチル総置換度(DS)、重量平均重合度(DPw)、組成分布指数(CDI)、量子収率、および相対発光強度の測定も実施例1と同様に行い、結果は表2および表3に示した。
(酢酸セルロース)
反応温度を40℃、第1熟成時間を8時間、第2熟成時間を16時間、第3熟成時間を42時間、沈殿化剤をメタノールに変更したこと以外は、実施例3と同様にして低置換度酢酸セルロース(WSCA-40‐0.8)を得た。
精製セルロースジアセテート(Sigma-Aldrich-CTA-分画)を低置換度酢酸セルロース(WSCA-40‐0.8)に変更したこと以外は、実施例1と同様にして、量子ドット複合体を得た。アセチル総置換度(DS)、重量平均重合度(DPw)、組成分布指数(CDI)、量子収率、および相対発光強度の測定も実施例1と同様に行い、結果は表2および表3に示した。
(酢酸セルロース)
反応温度を40℃、第1熟成時間を8時間、第2熟成時間を16時間、第3熟成時間を36時間、沈殿化剤をメタノールに変更したこと以外は、実施例3と同様にして低置換度酢酸セルロース(WSCA-40‐0.9)を得た。
精製セルロースジアセテート(Sigma-Aldrich-CTA-分画)を低置換度酢酸セルロース(WSCA-40‐0.9)に変更したこと以外は、実施例1と同様にして、量子ドット複合体を得た。アセチル総置換度(DS)、重量平均重合度(DPw)、組成分布指数(CDI)、量子収率、および相対発光強度の測定も実施例1と同様に行い、結果は表2および表3に示した。
(酢酸セルロース)
反応温度を40℃、第1熟成時間を8時間、第2熟成時間を16時間、第3熟成時間を50時間、沈殿化剤をメタノールに変更したこと以外は、実施例3と同様にして低置換度酢酸セルロース(WSCA-40‐0.7)を得た。
精製セルロースジアセテート(Sigma-Aldrich-CTA-分画)を低置換度酢酸セルロース(WSCA-40‐0.7)に変更したこと以外は、実施例1と同様にして、量子ドット複合体を得た。アセチル総置換度(DS)、重量平均重合度(DPw)、組成分布指数(CDI)、量子収率、および相対発光強度の測定も実施例1と同様に行い、結果は表2および表3に示した。
(酢酸セルロース)
低置換度酢酸セルロース(WSCA-40‐0.9)および低置換度酢酸セルロース(WSCA-40‐0.7)を1:1(重量比)で混合した。
精製セルロースジアセテート(Sigma-Aldrich-CTA-分画)を上記混合した低置換度酢酸セルロースに変更したこと以外は、実施例1と同様にして、量子ドット複合体を得た。アセチル総置換度(DS)、重量平均重合度(DPw)、組成分布指数(CDI)、量子収率、および相対発光強度の測定も実施例1と同様に行い、結果は表2および表3に示した。
精製セルロースジアセテート(Sigma-Aldrich-CTA-分画)をポリスチレン(Mw3,500、Sigma-Aldrich社製)に変更したこと以外は、実施例1と同様にして、量子ドット複合体を得た。アセチル総置換度(DS)、組成分布指数(CDI)、量子収率、および相対発光強度の測定は、実施例1と同様に行い、重量平均重合度(DPw)はMwから換算した。これらの結果は表2および表3に示した。
精製セルロースジアセテート(Sigma-Aldrich-CTA-分画)をポリメチルメタクリレート(Mw35,000、Sigma-Aldrich社製)に変更したこと以外は、実施例1と同様にして、量子ドット複合体を得た。アセチル総置換度(DS)、組成分布指数(CDI)、量子収率、および相対発光強度の測定は、実施例1と同様に行い、重量平均重合度(DPw)はMwから換算した。これらの結果は表2および表3に示した。
Claims (8)
- マトリクス中に、
量子ドットが分散され、
前記マトリクスは、下記式で表される組成分布指数(CDI)が3.0以下の酢酸セルロースで構成され、
前記量子ドットの濃度は0.05重量%以上であることを特徴とする量子ドット複合体。
CDI=Z(組成分布半値幅の実測値)/Zo(組成分布半値幅の理論値)
Z:前記酢酸セルロースの残存水酸基をすべてプロピオニル化して得られるセルロースアセテートプロピオネートをHPLC分析して求めたアセチル置換度の組成分布半値幅
DPw:重量平均重合度(前記酢酸セルロースの残存水酸基をすべてプロピオニル化して得られるセルロースアセテートプロピオネートを用いてGPC-光散乱法により求めた値)
p:前記酢酸セルロースのアセチル総置換度/3
q:1-p - 前記量子ドットの濃度が10重量%以上であることを特徴とする請求項1に記載の量子ドット複合体。
- 前記酢酸セルロースが、下記式で表される組成分布指数(CDI)が2.0以下の酢酸セルロースであることを特徴とする請求項1または2に記載の量子ドット複合体。
CDI=Z(組成分布半値幅の実測値)/Zo(組成分布半値幅の理論値)
Z:前記酢酸セルロースの残存水酸基をすべてプロピオニル化して得られるセルロースアセテートプロピオネートをHPLC分析して求めたアセチル置換度の組成分布半値幅
DPw:重量平均重合度(前記酢酸セルロースの残存水酸基をすべてプロピオニル化して得られるセルロースアセテートプロピオネートを用いてGPC-光散乱法により求めた値)
p:前記酢酸セルロースのアセチル総置換度/3
q:1-p - 前記量子ドットがCdSe/ZnS量子ドットである請求項1~3いずれかに記載の量子ドット複合体。
- フィルム状である請求項1~4のいずれかに記載の量子ドット複合体。
- 請求項1~5のいずれかに記載の量子ドット複合体を有する波長変換素子。
- 請求項1~5のいずれかに記載の量子ドット複合体を有する光電変換装置。
- 請求項1~5のいずれかに記載の量子ドット複合体を有する太陽電池。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US15/115,043 US9796920B2 (en) | 2014-01-29 | 2014-01-29 | Quantum dot composite and wavelength conversion element, photoelectric conversion device, and solar cell having the composite |
| PCT/JP2014/000445 WO2015114679A1 (ja) | 2014-01-29 | 2014-01-29 | 量子ドット複合体、当該複合体を有する波長変換素子、光電変換装置および太陽電池 |
| EP14880676.3A EP3101089B1 (en) | 2014-01-29 | 2014-01-29 | Quantum dot conjugate, wavelength conversion element comprising conjugate, photoelectric conversion device, and solar cell |
| CN201480074504.6A CN105980522B (zh) | 2014-01-29 | 2014-01-29 | 量子点复合体、具有该复合体的波长转换元件、光电转换装置及太阳能电池 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PCT/JP2014/000445 WO2015114679A1 (ja) | 2014-01-29 | 2014-01-29 | 量子ドット複合体、当該複合体を有する波長変換素子、光電変換装置および太陽電池 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2015114679A1 true WO2015114679A1 (ja) | 2015-08-06 |
Family
ID=53756311
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2014/000445 Ceased WO2015114679A1 (ja) | 2014-01-29 | 2014-01-29 | 量子ドット複合体、当該複合体を有する波長変換素子、光電変換装置および太陽電池 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US9796920B2 (ja) |
| EP (1) | EP3101089B1 (ja) |
| CN (1) | CN105980522B (ja) |
| WO (1) | WO2015114679A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9921343B2 (en) * | 2015-09-24 | 2018-03-20 | Shenzhen China Star Optoelectronics Technology Co., Ltd. | Quantum dot polarizer and manufacturing method thereof |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPWO2015156226A1 (ja) | 2014-04-08 | 2017-04-13 | Nsマテリアルズ株式会社 | 量子ドット及びその製造方法、並びに、前記量子ドットを用いた成形体、シート部材、波長変換部材、発光装置 |
| TWI634193B (zh) * | 2017-04-27 | 2018-09-01 | 中原大學 | 製造碳量子點的方法 |
| US11139444B2 (en) * | 2017-12-12 | 2021-10-05 | Universal Display Corporation | Organic electroluminescent devices containing a near-infrared down-conversion layer |
| CN114808141B (zh) * | 2022-06-23 | 2022-09-20 | 福建晶安光电有限公司 | 一种衬底改性处理方法及半导体发光器件的制造方法 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2003201301A (ja) | 2001-11-05 | 2003-07-18 | Daicel Chem Ind Ltd | セルロースアセテートのアセチル置換度の調整方法 |
| JP2007281484A (ja) * | 2006-04-10 | 2007-10-25 | Samsung Electro Mech Co Ltd | 白色発光ダイオードおよびその製造方法 |
| WO2008013069A1 (fr) * | 2006-07-28 | 2008-01-31 | Hoya Corporation | Dispositif el |
| JP2009200041A (ja) * | 2008-02-25 | 2009-09-03 | Korea Inst Of Science & Technology | 白色及びカラー光励起発光シート及びその製造方法 |
| WO2012132239A1 (ja) * | 2011-03-31 | 2012-10-04 | パナソニック株式会社 | 蛍光フィルムおよび表示フィルム |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6379622B1 (en) * | 2001-04-11 | 2002-04-30 | Motorola, Inc. | Sensor incorporating a quantum dot as a reference |
| US7820009B2 (en) * | 2006-08-18 | 2010-10-26 | The Royal Institution For The Advancement Of Learning/Mcgill University | Cellulose composites comprising hydrophobic particles and their use in paper products |
| JP4774121B2 (ja) * | 2010-01-29 | 2011-09-14 | ダイセル化学工業株式会社 | 位相差フィルム用セルロースジアセテート |
-
2014
- 2014-01-29 EP EP14880676.3A patent/EP3101089B1/en active Active
- 2014-01-29 US US15/115,043 patent/US9796920B2/en active Active
- 2014-01-29 CN CN201480074504.6A patent/CN105980522B/zh active Active
- 2014-01-29 WO PCT/JP2014/000445 patent/WO2015114679A1/ja not_active Ceased
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2003201301A (ja) | 2001-11-05 | 2003-07-18 | Daicel Chem Ind Ltd | セルロースアセテートのアセチル置換度の調整方法 |
| JP2007281484A (ja) * | 2006-04-10 | 2007-10-25 | Samsung Electro Mech Co Ltd | 白色発光ダイオードおよびその製造方法 |
| WO2008013069A1 (fr) * | 2006-07-28 | 2008-01-31 | Hoya Corporation | Dispositif el |
| JP2009200041A (ja) * | 2008-02-25 | 2009-09-03 | Korea Inst Of Science & Technology | 白色及びカラー光励起発光シート及びその製造方法 |
| WO2012132239A1 (ja) * | 2011-03-31 | 2012-10-04 | パナソニック株式会社 | 蛍光フィルムおよび表示フィルム |
Non-Patent Citations (6)
| Title |
|---|
| A. J. ROSENTHAL; B. B. WHITE, IND. ENG. CHEM., vol. 44, no. 11, 1952, pages 2693 - 2696 |
| CHEM. MATER., vol. 19, 2007, pages 4270 - 4276 |
| CIBMENT, L.; RIVIBRE, C., BULL. SOC. CHIM., vol. 1, no. 5, 1934, pages 1075 |
| PHYSICAL REVIEW LETTERS, vol. 78, 1997, pages 5014 |
| See also references of EP3101089A4 |
| SOOKNE, A. M.; RUTHERFORD, H. A.; MARK, H.; HARRIS, M. J., RESEARCH NATL. BUR. STANDARDS, vol. 29, 1942, pages 123 |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9921343B2 (en) * | 2015-09-24 | 2018-03-20 | Shenzhen China Star Optoelectronics Technology Co., Ltd. | Quantum dot polarizer and manufacturing method thereof |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3101089A4 (en) | 2017-02-15 |
| CN105980522B (zh) | 2019-03-22 |
| EP3101089A1 (en) | 2016-12-07 |
| US9796920B2 (en) | 2017-10-24 |
| US20160347996A1 (en) | 2016-12-01 |
| EP3101089B1 (en) | 2019-03-13 |
| CN105980522A (zh) | 2016-09-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Dong et al. | Improving physicochemical properties of edible wheat gluten protein films with proteins, polysaccharides and organic acid | |
| CN105073782B (zh) | 低取代度乙酸纤维素 | |
| WO2015114679A1 (ja) | 量子ドット複合体、当該複合体を有する波長変換素子、光電変換装置および太陽電池 | |
| KR101118879B1 (ko) | 위상차 필름용 셀룰로오스 디아세테이트 | |
| Li et al. | Concomitant degradation in periodate oxidation of carboxymethyl cellulose | |
| Zhang et al. | Preparation and characterization of a transparent amorphous cellulose film | |
| EP2690132A1 (en) | Solvent used for dissolving polysaccharide and method for manufacturing molded article and polysaccharide derivative using this solvent | |
| Nguyen et al. | A novel method for preparing microfibrillated cellulose from bamboo fibers | |
| JP6157472B2 (ja) | 導電性セルロース系樹脂組成物 | |
| CN101942041B (zh) | 一种硫酸酯化蔗渣木聚糖的制备方法 | |
| CN113214156B (zh) | 一种用于淀粉糊化度检测的转子型荧光分子及其制备和应用 | |
| Niu et al. | Preparation and sulfation of an α-glucan from Actinidia chinensis roots and their potential activities | |
| JP2014506279A5 (ja) | ||
| Gonzales et al. | Ulvan based materials doped with lithium sulfate salts as solid biopolymer electrolytes for energy storage applications | |
| CN104140468B (zh) | 一种纤维素混合酯、制备方法及其应用 | |
| CN104250415A (zh) | 一种抗紫外聚乙烯醇-木聚糖复合膜及其制备方法与应用 | |
| CN104497150A (zh) | 一种脂溶性纤维素混合酯的制备方法 | |
| JP2015140296A (ja) | シート状酸化グラフェンとその製造方法、及び電解質膜 | |
| CN116217753B (zh) | 木聚糖粘度荧光探针的制备方法及其应用 | |
| CN113861472A (zh) | 两亲性壳聚糖/改性结冷胶复合膜的制备方法 | |
| CN115236020B (zh) | 一种测定木质纤维素中交联木质素含量的方法 | |
| CN105928763A (zh) | 烤烟烟叶淀粉的分离提取方法及分析方法 | |
| TW202238101A (zh) | 乙酸纖維素及其製造方法 | |
| Greco et al. | Modified Polysaccharides as New Commodity Materials and for Light-Converting Systems: Syntheses, Characterization and Processing | |
| JP5774286B2 (ja) | カルボキシルエチルセルロース金属塩 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 14880676 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 15115043 Country of ref document: US |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| REEP | Request for entry into the european phase |
Ref document number: 2014880676 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2014880676 Country of ref document: EP |
|
| NENP | Non-entry into the national phase |
Ref country code: JP |