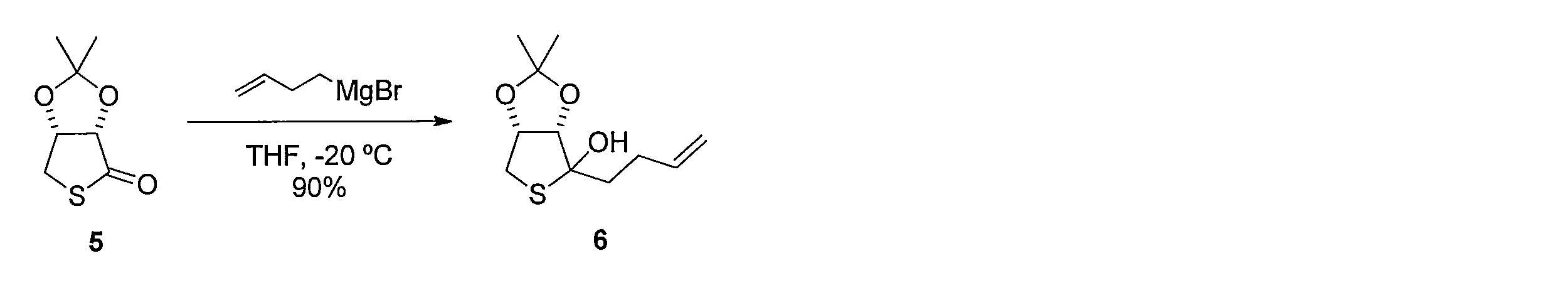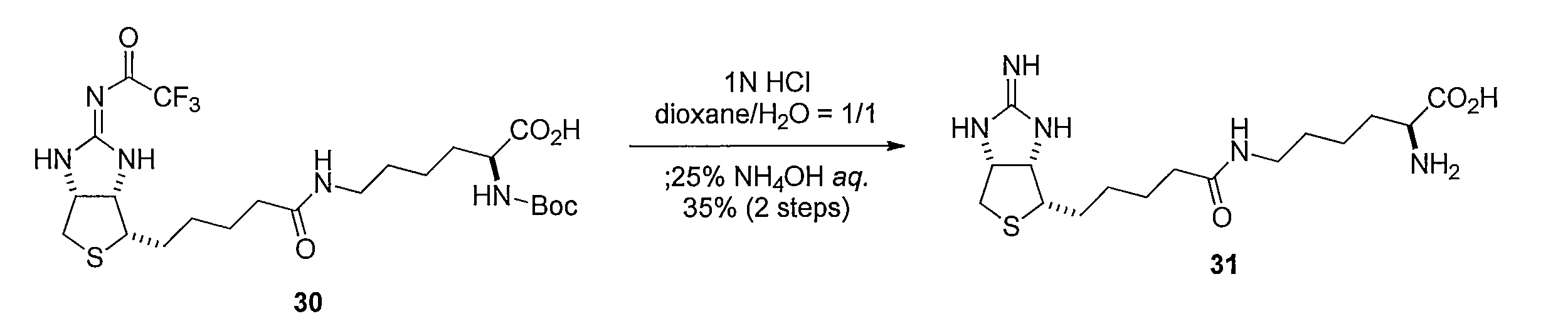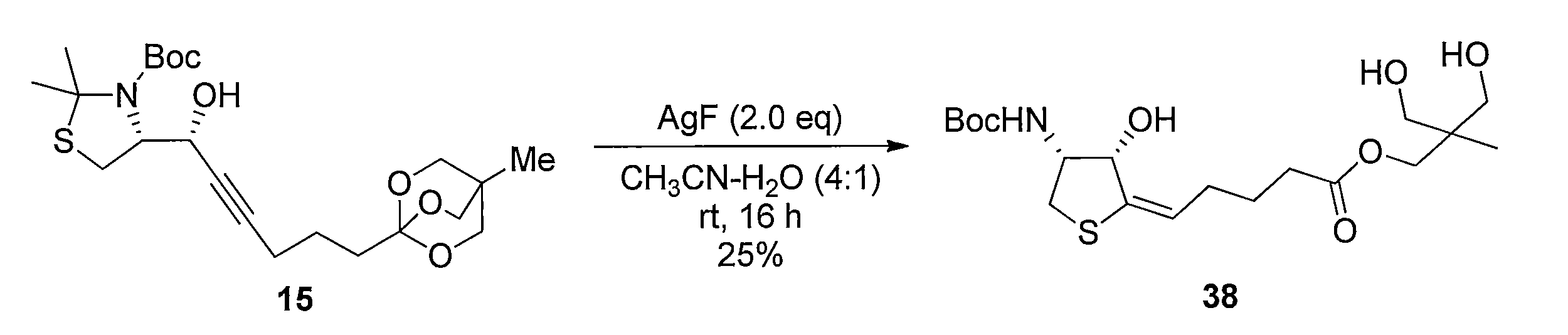WO2014129446A1 - ビオチン改変体、ストレプトアビジン変異体およびそれらの利用 - Google Patents
ビオチン改変体、ストレプトアビジン変異体およびそれらの利用 Download PDFInfo
- Publication number
- WO2014129446A1 WO2014129446A1 PCT/JP2014/053734 JP2014053734W WO2014129446A1 WO 2014129446 A1 WO2014129446 A1 WO 2014129446A1 JP 2014053734 W JP2014053734 W JP 2014053734W WO 2014129446 A1 WO2014129446 A1 WO 2014129446A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- streptavidin
- compound
- variant
- biotin
- added
- Prior art date
Links
- 0 CC(C*(*)=N)*C(CC[C@]1C)C*1=C Chemical compound CC(C*(*)=N)*C(CC[C@]1C)C*1=C 0.000 description 3
- HYAAZWJMWVJCNF-UHFFFAOYSA-N C=C1CSCC1 Chemical compound C=C1CSCC1 HYAAZWJMWVJCNF-UHFFFAOYSA-N 0.000 description 1
- QLLJIUXYLBUIOG-KYDWDHDXSA-N CC(C)(O[C@H]1COC2O)O[C@@H]1[C@H]2O Chemical compound CC(C)(O[C@H]1COC2O)O[C@@H]1[C@H]2O QLLJIUXYLBUIOG-KYDWDHDXSA-N 0.000 description 1
- DMIAYBYEIXQGCX-VYRNYKOWSA-N CC(CO)(CO)COC(CCC/C=C(\[C@H]1O2)/SCC1NC2=O)=O Chemical compound CC(CO)(CO)COC(CCC/C=C(\[C@H]1O2)/SCC1NC2=O)=O DMIAYBYEIXQGCX-VYRNYKOWSA-N 0.000 description 1
- YQUDUWGJSYNEES-NWDGAFQWSA-N CC(CO)(CO)COC(CCCC(SC[C@@H]1N2)=C[C@H]1OC2=O)=O Chemical compound CC(CO)(CO)COC(CCCC(SC[C@@H]1N2)=C[C@H]1OC2=O)=O YQUDUWGJSYNEES-NWDGAFQWSA-N 0.000 description 1
- GIMMHNSYTFPOLV-RTJIFQRUSA-N CC1(C)OCC(C)(COC(CCC/C=C(\[C@H]2O3)/SCC2NC3=O)=O)CO1 Chemical compound CC1(C)OCC(C)(COC(CCC/C=C(\[C@H]2O3)/SCC2NC3=O)=O)CO1 GIMMHNSYTFPOLV-RTJIFQRUSA-N 0.000 description 1
- OPBUERZOQCWTJW-YDHLFZDLSA-N CC1(C)OCC(C)(COC(CCCC[C@@H]([C@H]2O3)SC[C@@H]2NC3=O)=O)CO1 Chemical compound CC1(C)OCC(C)(COC(CCCC[C@@H]([C@H]2O3)SC[C@@H]2NC3=O)=O)CO1 OPBUERZOQCWTJW-YDHLFZDLSA-N 0.000 description 1
- RDRFHCAOXBKTQD-BULQSVBWSA-N CC1(C)SC[C@@H]([C@@H](C#CCCCC2(OC3)OCC3(C)CO2)O2)N1C2=O Chemical compound CC1(C)SC[C@@H]([C@@H](C#CCCCC2(OC3)OCC3(C)CO2)O2)N1C2=O RDRFHCAOXBKTQD-BULQSVBWSA-N 0.000 description 1
- IIQBFJORVAGSAQ-IEIXJENWSA-N OC(CCCCC([C@H]1O2)SCC1NC2=O)=O Chemical compound OC(CCCCC([C@H]1O2)SCC1NC2=O)=O IIQBFJORVAGSAQ-IEIXJENWSA-N 0.000 description 1
- BTLCIBOSEILEBJ-UHFFFAOYSA-N OC(CCCCCNC=O)=O Chemical compound OC(CCCCCNC=O)=O BTLCIBOSEILEBJ-UHFFFAOYSA-N 0.000 description 1
- SRBFZHDQGSBBOR-HWQSCIPKSA-N O[C@@H](COC([C@@H]1O)O)[C@@H]1O Chemical compound O[C@@H](COC([C@@H]1O)O)[C@@H]1O SRBFZHDQGSBBOR-HWQSCIPKSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D493/00—Heterocyclic compounds containing oxygen atoms as the only ring hetero atoms in the condensed system
- C07D493/02—Heterocyclic compounds containing oxygen atoms as the only ring hetero atoms in the condensed system in which the condensed system contains two hetero rings
- C07D493/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D493/00—Heterocyclic compounds containing oxygen atoms as the only ring hetero atoms in the condensed system
- C07D493/02—Heterocyclic compounds containing oxygen atoms as the only ring hetero atoms in the condensed system in which the condensed system contains two hetero rings
- C07D493/08—Bridged systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D495/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms
- C07D495/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D495/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D497/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having oxygen and sulfur atoms as the only ring hetero atoms
- C07D497/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having oxygen and sulfur atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D497/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D498/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D498/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D498/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D519/00—Heterocyclic compounds containing more than one system of two or more relevant hetero rings condensed among themselves or condensed with a common carbocyclic ring system not provided for in groups C07D453/00 or C07D455/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/195—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria
- C07K14/36—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria from Actinomyces; from Streptomyces (G)
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/543—Immunoassay; Biospecific binding assay; Materials therefor with an insoluble carrier for immobilising immunochemicals
- G01N33/54306—Solid-phase reaction mechanisms
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/195—Assays involving biological materials from specific organisms or of a specific nature from bacteria
- G01N2333/36—Assays involving biological materials from specific organisms or of a specific nature from bacteria from Actinomyces; from Streptomyces (G)
Definitions
- the present invention relates to a biotin variant, a streptavidin variant, and use thereof. More particularly, the present invention relates to a streptavidin variant having a reduced affinity for natural biotin, a biotin variant having an affinity for the streptavidin variant, and use thereof.
- the avidin / streptavidin-biotin interaction is widely applied in the fields of biochemistry, molecular biology, and medicine (Green, (1975), Adv. Protein Chem., 29: 85-133; Green, (1990), Methods Enzymol., 184: 51-67).
- Avidin is a basic glycoprotein derived from egg white and has an isoelectric point of more than 10.
- streptavidin is derived from Streptomyces avidinii, has an isoelectric point near neutral and does not contain sugar chains. Both proteins form a tetramer and bind to one molecule of biotin per subunit.
- the molecular weight is about 60 kDa.
- the above-mentioned low immunogenic streptavidin has a characteristic that immunogenicity to the human body is reduced, but it has an affinity for biotin inherent in the human body, so it is not suitable for diagnostic applications. There is a concern that the ground will be high and that there may be a possibility that the drug effect cannot be exhibited specifically in the case of therapeutic use. Therefore, the present invention provides a streptavidin variant with reduced affinity for natural biotin, and further provides a biotin variant having a high affinity for the low affinity streptavidin variant for natural biotin. This was a problem to be solved.
- the present invention provides a diagnostic agent / therapeutic agent using a combination of the above streptavidin variant and a biotin variant, and a diagnostic kit / therapeutic kit using a combination of the above streptavidin variant and a biotin variant.
- the present inventor has intensively studied in order to solve the above-mentioned problems, and further introduces a predetermined amino acid mutation into the low immunogenic streptavidin mutant described in International Publication WO 2010/095455, whereby affinity for natural biotin is obtained.
- various biotin modifications were synthesized by modifying a part of the structure of biotin.
- a combination having an affinity for each other was found, and the present invention was completed.
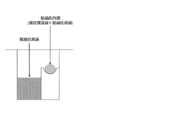
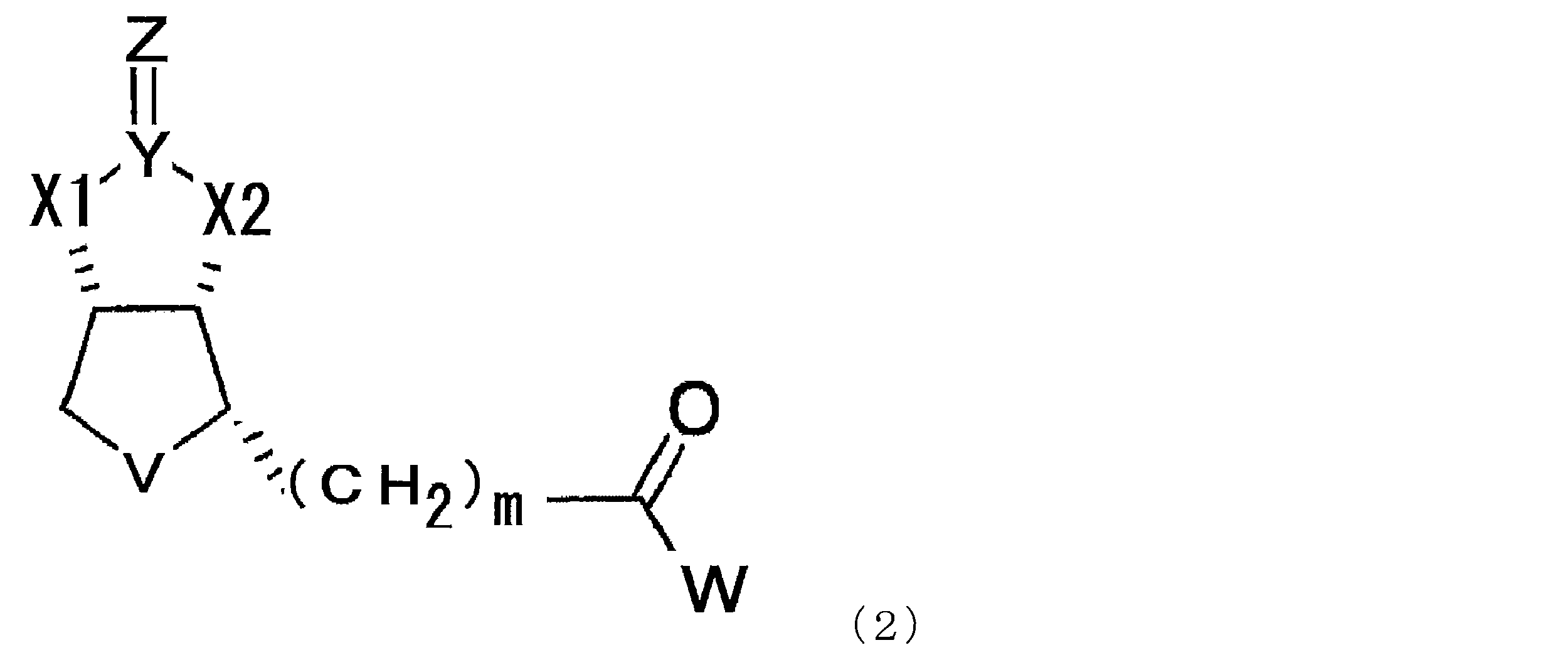
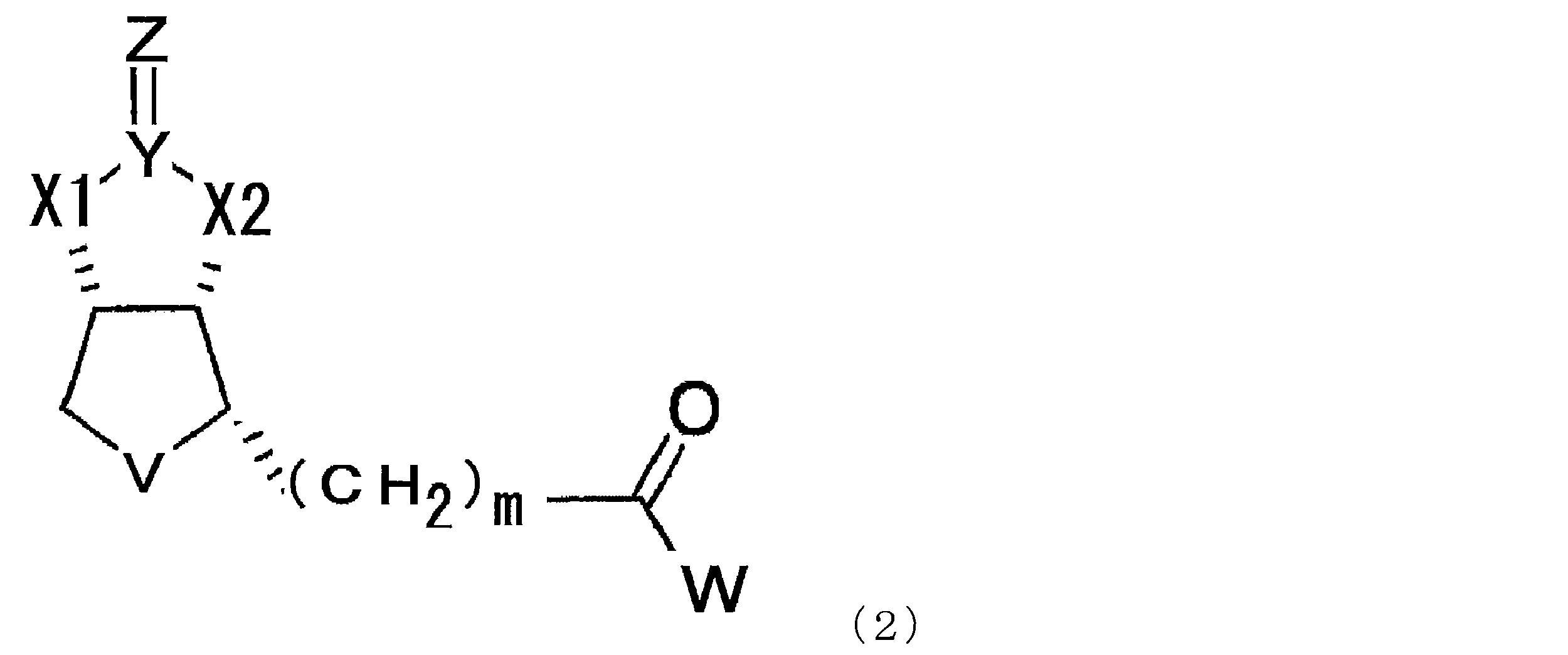
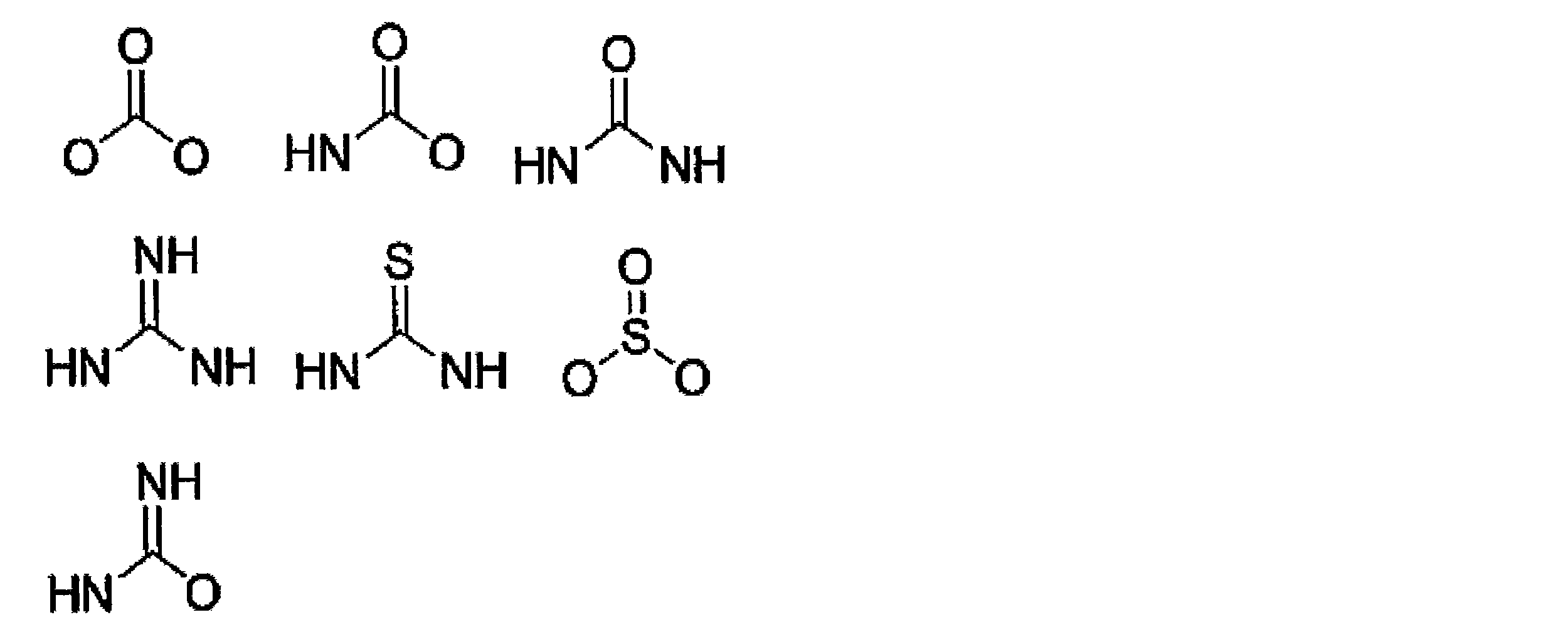
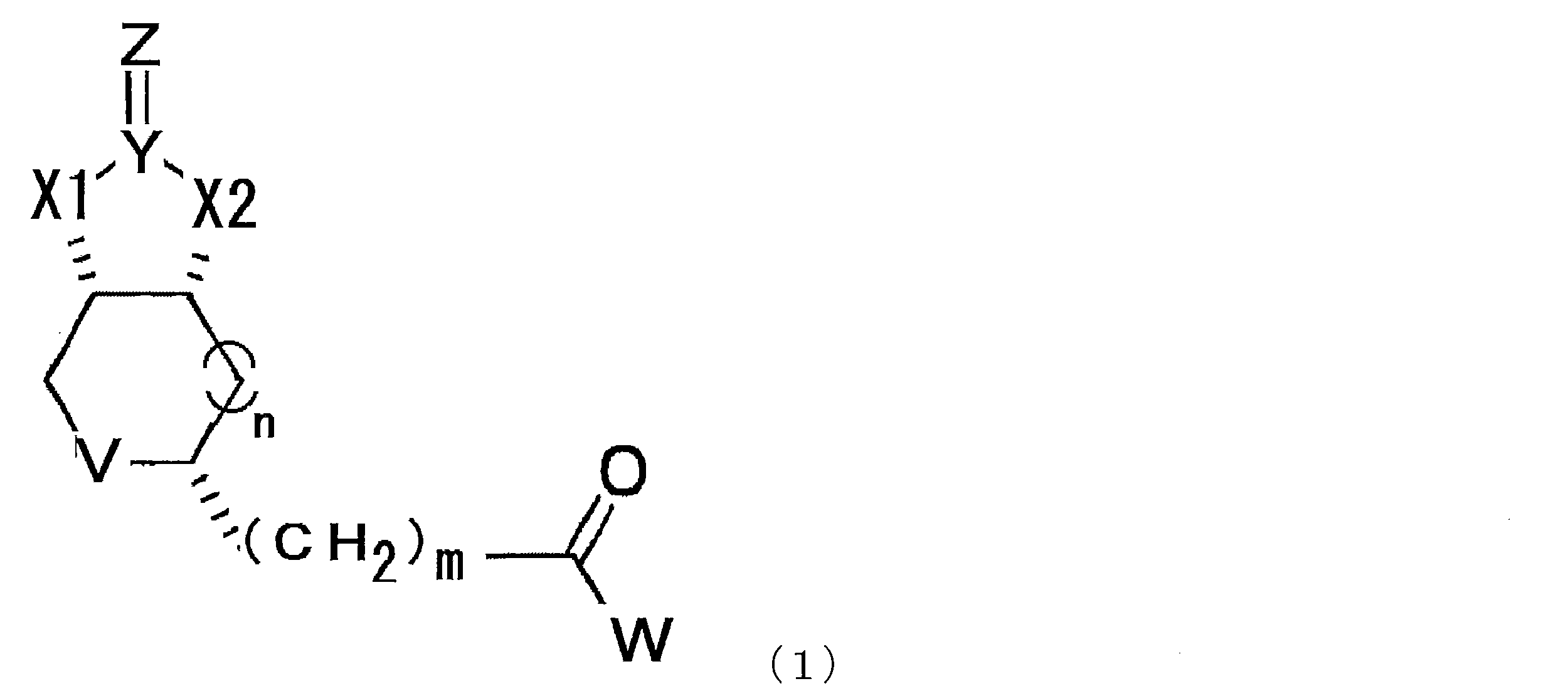
- a compound represented by the following formula (1) (In the formula, X1 and X2 each independently represent O or NH, Y represents C or S, Z represents O, S or NH, V represents S or S + —O ⁇ , and n represents 0. Or an integer of 1, m represents an integer of 1 to 10, and W represents —OH, —NH (CH 2 ) p COOH, or —NH (CH 2 ) q C (NH 2 ) COOH, where p and q each independently represent an integer of 1 to 10).
- a streptavidin mutant comprising the amino acid sequence of any one of SEQ ID NOs: 3 to 12.
- a streptavidin mutant-molecular probe conjugate obtained by binding a molecular probe to the streptavidin mutant according to [4].
- a therapeutic agent or an in-vivo or in-vitro diagnostic agent comprising the streptavidin mutant-molecular probe conjugate according to [6].
- a combination of a streptavidin variant with reduced immunogenicity and reduced affinity for natural biotin, and a biotin variant having high affinity for the streptavidin variant is provided.
- the combination of the streptavidin variant and the biotin variant of the present invention is useful in diagnostic methods and therapeutic methods based on the pretargeting method.
- FIG. 1 shows the result of crude purification of streptavidin mutant recombinant protein.
- FIG. 2 shows the results of competition analysis with biotin-HRP label.
- FIG. 3 shows the sitting drop vapor diffusion method.
- FIG. 4 shows the crystal structures of LISA314 and LISA314-V21.
- FIG. 5 shows the crystal structures of LISA314 and LISA314-V21.
- A Co-crystal structure of LISA314 and biotin.
- B Co-crystal structure of LISA314-V21 and iminobiotin long tail. Subunits A and C are indicated by line ribbon, and B and D are indicated by Flat ribbon.
- FIG. 6 shows an example of purification of the unwinding protein.
- FIG. 6 shows an example of purification of the unwinding protein.
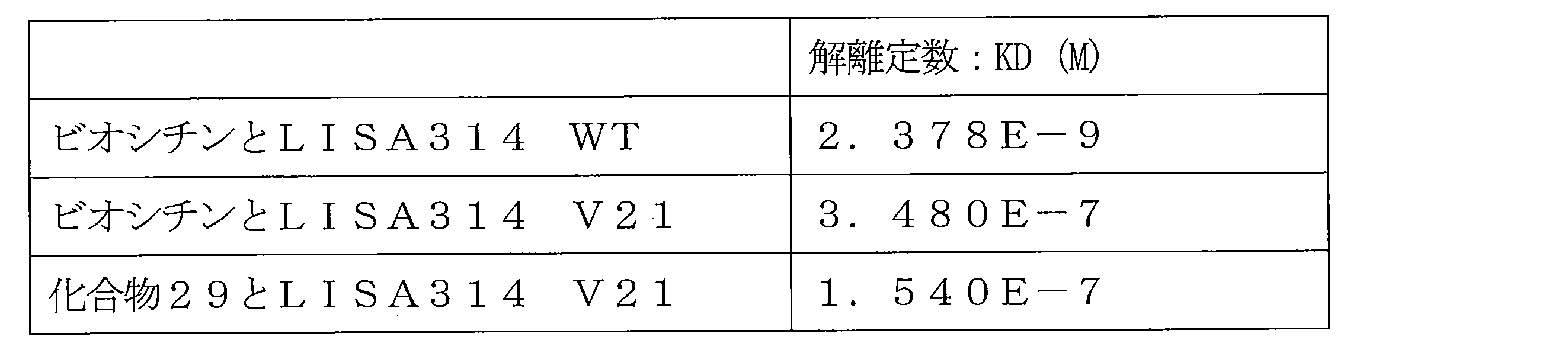
- FIG. 7 shows a sensorgram when the SPR analysis of the interaction between biocytin and LISA314 WT is performed.
- FIG. 8 shows a sensorgram when the SPR analysis of the interaction between biocytin and LISA314 V21 is performed.
- FIG. 9 shows a sensorgram when the SPR analysis of the interaction between Compound 29 and LISA314 V21 is performed.
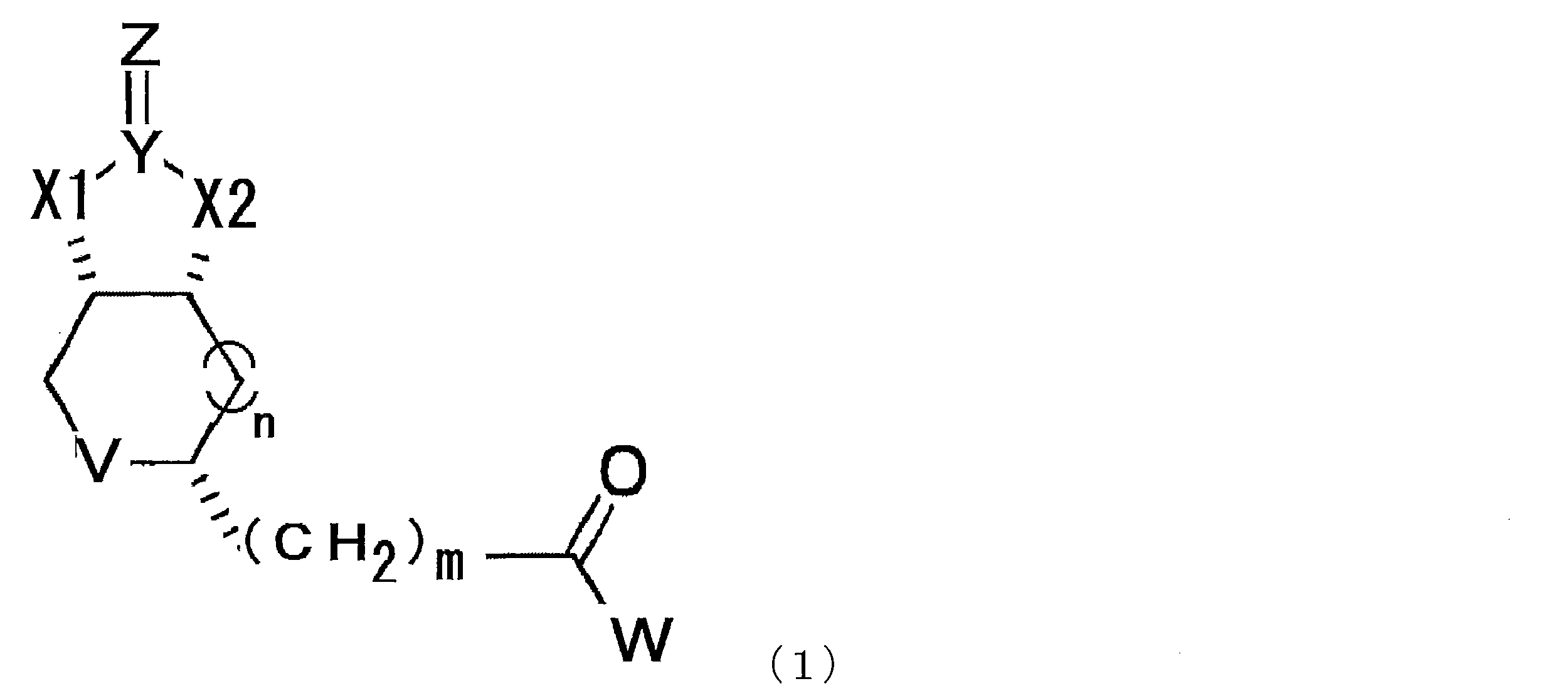
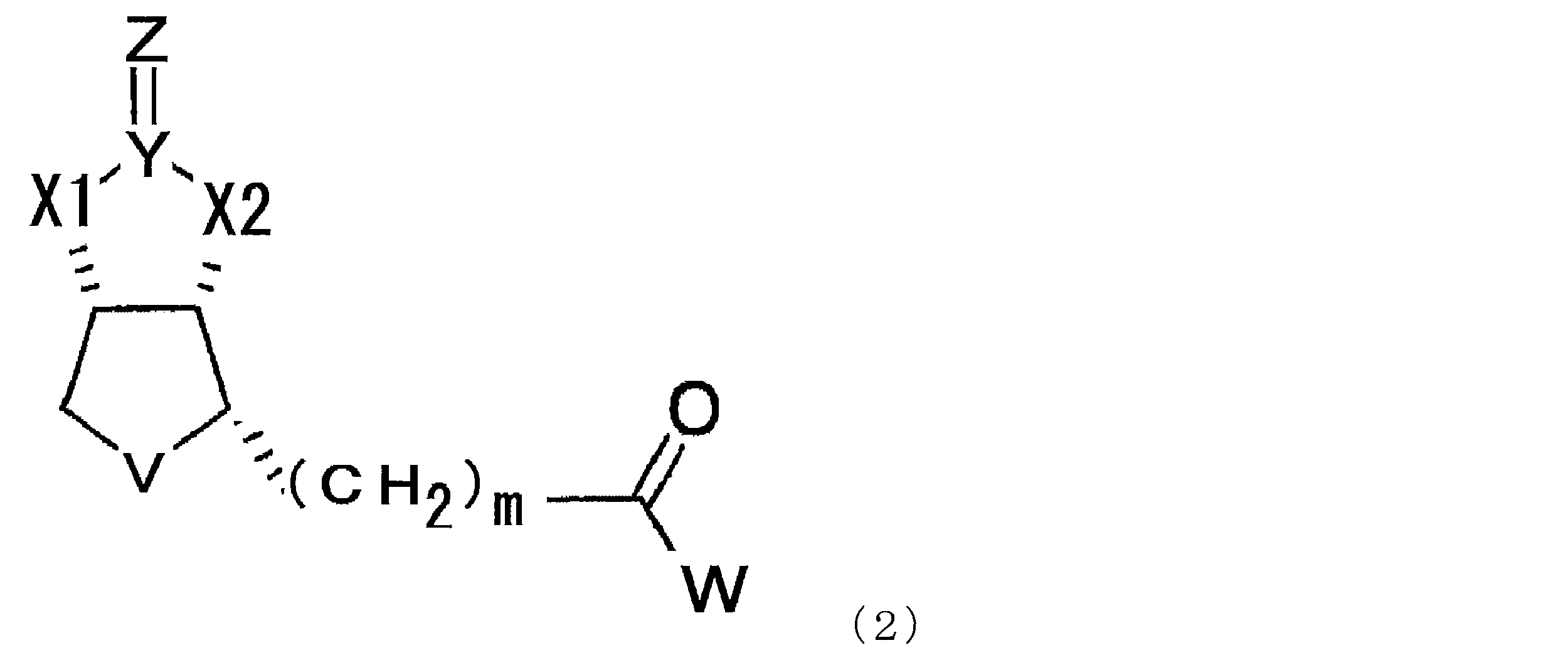
- the modified biotin of the present invention is a compound represented by the following formula (1), preferably a compound represented by the formula (2) in the case where n is 0 in the formula (1). is there.
- X1 and X2 each independently represent O or NH
- Y represents C or S
- Z represents O
- V represents S or S + —O ⁇
- n 0.
- m represents an integer of 1 to 10
- W represents —OH, —NH (CH 2 ) p COOH, or —NH (CH 2 ) q C (NH 2 ) COOH, where p and q each independently represent an integer of 1 to 10).
- m represents an integer of 1 to 10, preferably an integer of 2 to 10, more preferably an integer of 2 to 8, more preferably an integer of 2 to 6, and particularly preferably 4.
- p and q each independently represent an integer of 1 to 10, preferably an integer of 2 to 10, more preferably an integer of 2 to 8, more preferably an integer of 2 to 6, particularly preferably 4 or 5.
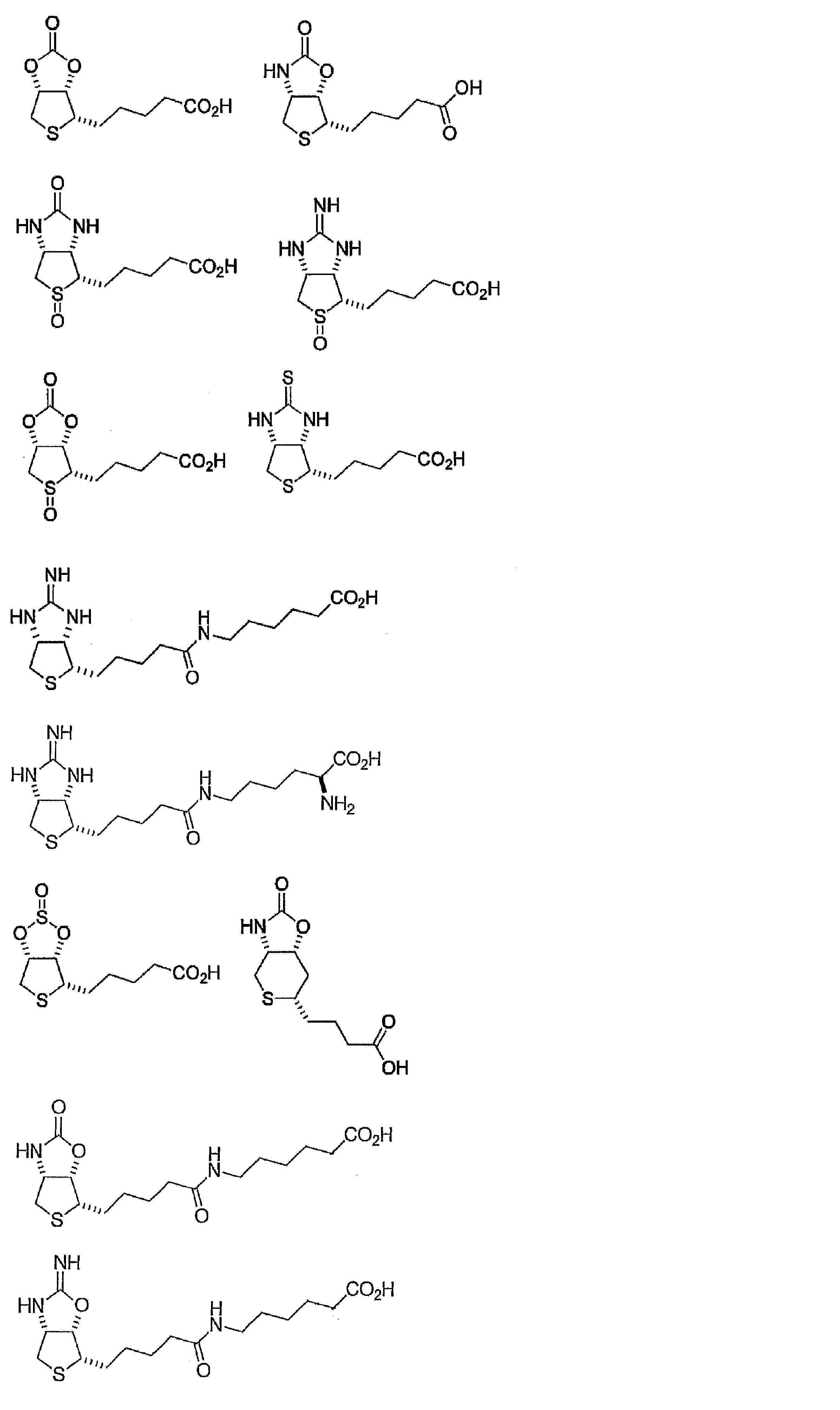
- the compound of formula (1) or formula (2) of the present invention can be synthesized by the synthesis method described in Example 1 below.
- Compounds 11, 19, 21, 23, 24, 27, 29, 31, 36, 37, 46 and 47 in Example 1 are compounds of formula (1) or formula (2) of the present invention.
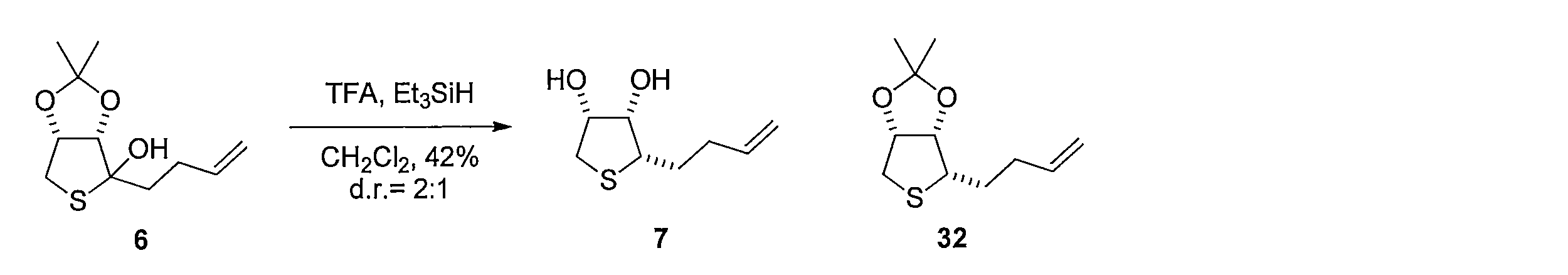
- Triethylsilane was added to the CH 2 Cl 2 solution of Compound 6 and stirred, and then trifluoroacetic acid (675 ⁇ L, 9.05 mmol) was added and reacted to give (2S, 3S, 4R) -2- (3- Buten-1-yl) tetrahydrothiophene-3,4-diol (compound 7) is obtained.
- (2S, 3S, 4R) -2- (3- Buten-1-yl) tetrahydrothiophene-3,4-diol compound 7
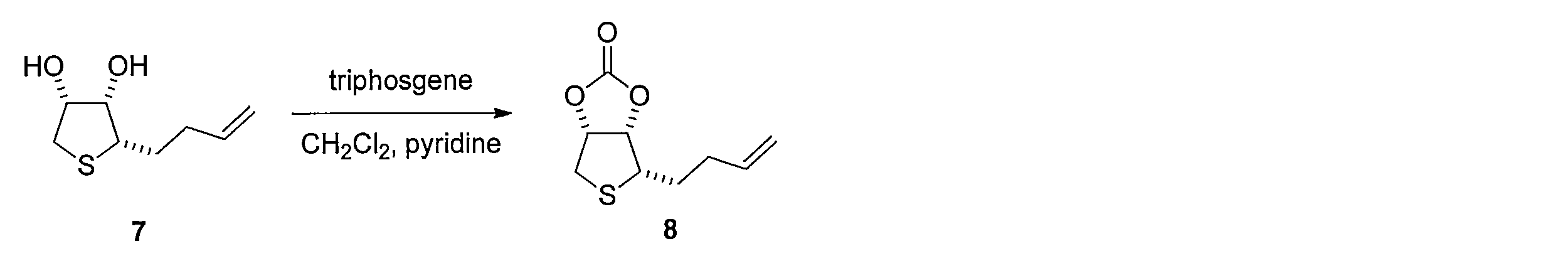
- 3aS, 4S, 6aR) -4- (3- buten-1-yl) tetrahydrothieno [3,4-d] [ 1,3] dioxol-2-one compound 8 is obtained.
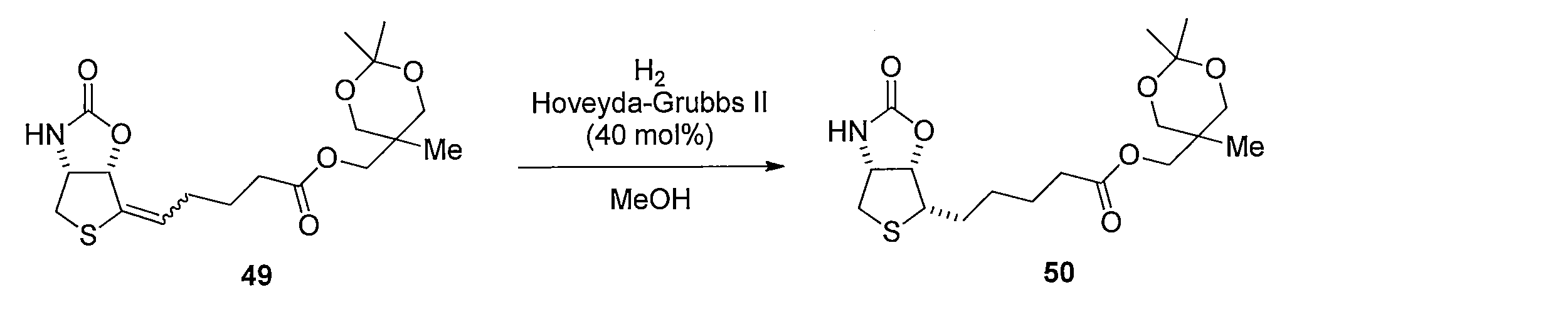
- Pearlman's catalyst (10% palladium) was added to a methanol solution of diacetonide 39, replaced with hydrogen gas (1 atm, balloon), and reacted at room temperature to give a mixture of compounds 40 and 41 with double bonds reduced. obtain.
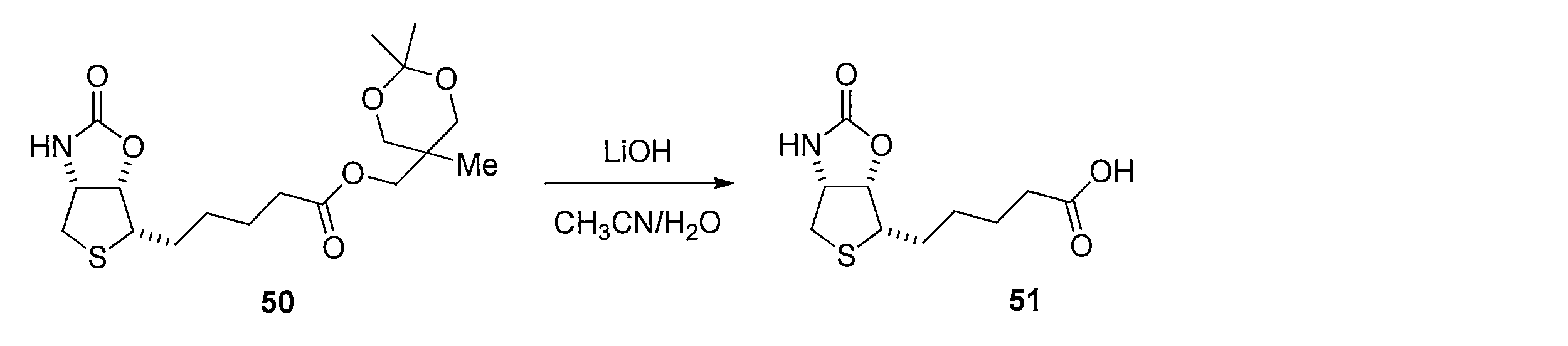
- This crude product is dissolved in a mixed solvent of acetonitrile and water, 2N aqueous lithium hydroxide solution is added, and the mixture is reacted at room temperature to obtain compound 42.
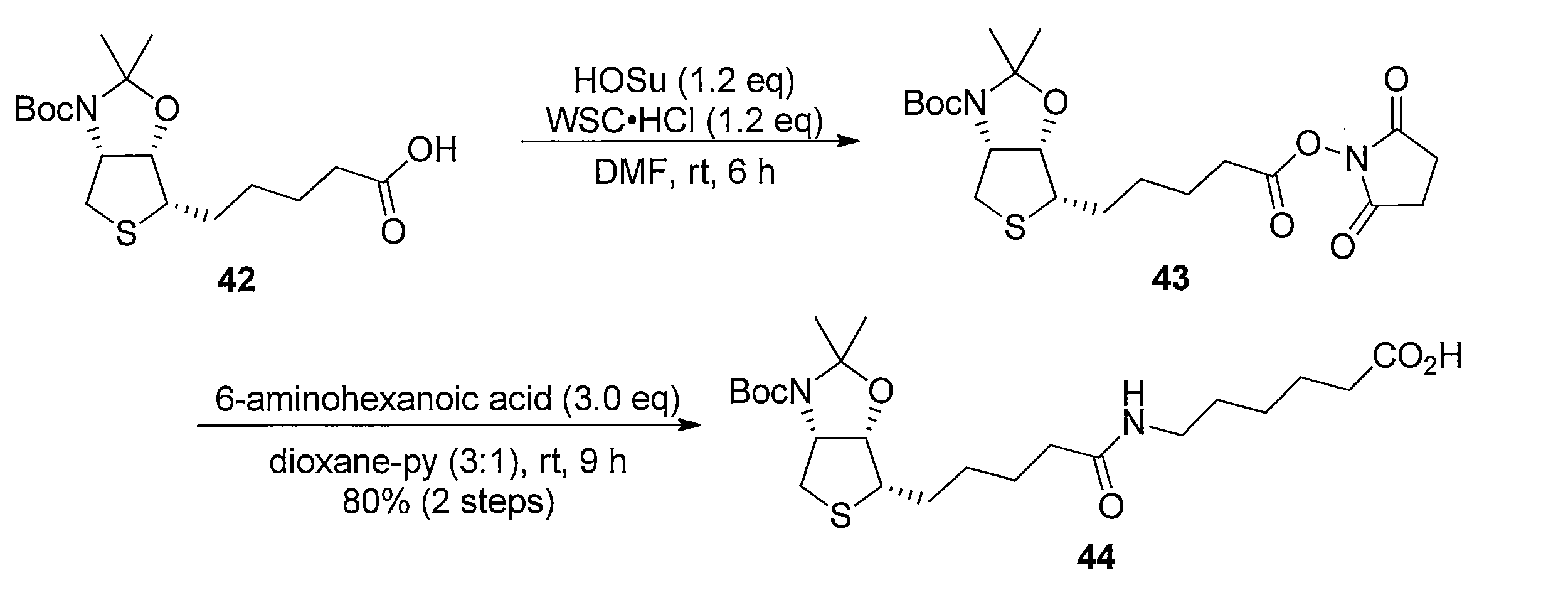
- 1-ethyl-3- (3-dimethylaminopropyl) carbodiimide hydrochloride is added to N, N-dimethylformamide solution of carboxylic acid 42 and N-hydroxysuccinimide, and the mixture is reacted by stirring at room temperature. Get 43.
- the obtained 43 is dissolved in a mixed solvent of dioxane and water, 6-aminohexanoic acid is added, and the mixture is reacted at room temperature to obtain compound 44.
- Compound 45 is obtained by adding 3N hydrochloric acid to a dioxane solution of carboxylic acid 44 and reacting the mixture at room temperature. Potassium carbonate and carbonyldiimidazole were added to a tetrahydrofuran solution of ammonium salt 45, and the mixture was reacted at 80 ° C., cooled to room temperature, then added with 2N aqueous sodium hydroxide solution, reacted at room temperature for 2 hours, and further reacted with 2N hydrochloric acid. Acidify (pH 3) to give compound 46.
- streptavidin mutant of the present invention has a predetermined amino acid mutation in the amino acid sequence of core streptavidin described in SEQ ID NO: 2, and is immunogenic compared to wild-type streptavidin. At the same time as the decrease in affinity for natural biotin or biocytin.
- amino acid sequence of wild-type (natural) core streptavidin is shown in SEQ ID NO: 2 in the sequence listing, and the base sequence encoding this is shown in SEQ ID NO: 1 in the sequence listing.
- the streptavidin variant of the present invention specifically has an amino acid sequence described in any one of SEQ ID NOs: 3 to 12 in the sequence listing.
- the immunogenicity is reduced compared to wild-type streptavidin means that the immunogenicity is reduced when a streptavidin variant is administered to a mammal such as a human. .
- the reduction in immunogenicity can be confirmed, for example, by the following method. That is, with respect to the streptavidin variant of the present invention, the reactivity to anti-streptavidin antiserum obtained by immunizing wild type streptavidin to cynomolgus monkeys was analyzed, and the reactivity to the above anti-streptavidin antiserum was If it is lower than that of the wild type streptavidin, it can be determined that the immunogenicity is lower than that of wild type streptavidin.
- the streptavidin variant of the present invention preferably has an immunogenicity of 80% or less, more preferably 60% or less, compared to wild-type streptavidin. It is preferably 20% or less, more preferably 15% or less, further preferably 10% or less, and particularly preferably 5% or less.
- the affinity with natural biotin or biocytin as referred to in the present invention means that the binding between a streptavidin variant and natural biotin or biocytin is compared with the binding between streptavidin and natural biotin or biocytin. It means that it is falling.
- the affinity / binding property between the streptavidin mutant and natural biotin or biocytin can be evaluated by SPR analysis or the like.
- the streptavidin variant of the present invention preferably has an affinity for natural biotin or biocytin of 80% or less, more preferably 70% or less, more preferably 60% or less, more preferably compared to wild-type streptavidin. It is reduced to 50% or less, more preferably 40% or less.
- a DNA encoding the above-described streptavidin mutant of the present invention can be prepared by site-directed mutagenesis on DNA encoding wild type (natural) streptavidin.
- the above-described DNA encoding the streptavidin variant of the present invention can be used by being incorporated into a vector.
- the DNA encoding the streptavidin mutant of the present invention is incorporated into an expression vector, and the expression vector is transformed into a host to thereby produce the streptavidin mutant of the present invention. Mutants can be expressed.
- the vector used in the present invention has an origin of replication (ori) and a gene for selecting a transformed host (for example, ampicillin, tetracycline, kanamycin or chloramphenic acid). It is preferable to have a drug resistance gene for a drug such as cole.
- a promoter capable of efficiently expressing the streptavidin variant of the present invention in the host for example, a lacZ promoter or a T7 promoter.
- vectors examples include M13 vectors, pUC vectors, pBR322, pBluescript, pCR-Script, pGEX-5X-1 (Pharmacia), “QIAexpress system” (Qiagen), pEGFP, or pET.
- the host preferably uses BL21 expressing T7 RNA polymerase.
- a signal sequence for increasing the yield of the streptavidin variant of the present invention can be added to the vector.
- the introduction of the vector into the host cell can be performed using, for example, the calcium chloride method or the electroporation method.
- a tag for improving solubility for example, a sequence encoding glutathione-S-transferase, thioredoxin, or maltose-binding protein may be added. It also encodes tags designed to facilitate purification, such as polyhistidine tags, Myc epitopes, hemagglutinin (HA) epitopes, T7 epitopes, Xpress tags and FLAG peptide tags, and other known tag sequences A sequence may be added.
- expression vectors derived from mammals for example, pcDNA3 (manufactured by Invitrogen), pEGF-BOS (Nucleic Acids. Res. 1990, 18 (17), p5322), pEF, pCDM8), derived from insect cells
- Expression vectors eg, “Bac-to-BAC baculovairus expression system” (manufactured by Gibco BRL), pBacPAK8), plant-derived expression vectors (eg, pMH1, pMH2), animal virus-derived expression vectors (eg, pHSV, pMV, pAdexLcw), retrovirus-derived expression vectors (for example, pZIPneo), yeast-derived expression vectors (for example, “Pichia® Expression® Kit” (manufactured by Invitrogen), pNV11®, SP-Q01), Bacillus subtilis-derived expression vectors (for example, PPL608, pKTH50).
- mammals for example,
- promoters necessary for expression in cells such as the SV40 promoter (Mulligan et al., Nature (1979) 277, 108), It is essential to have the MMLV-LTR promoter, EF1 ⁇ promoter (Mizushima et al., Nucleic Acids Res. (1990) 18, 5322), CMV promoter, etc., and genes for selecting transformation into cells (for example, More preferably, it has a drug resistance gene that can be discriminated by a drug (neomycin, G418, etc.). Examples of such a vector include pMAM, pDR2, pBK-RSV, pBK-CMV, pOPRSV, and pOP13.
- the host cell into which the vector is introduced is not particularly limited and may be either prokaryotic or eukaryotic.
- E. coli and various animal cells can be used.
- animal cells for example, animal cells, plant cells, and fungal cells can be used as the host.
- animal cells mammalian cells such as CHO cells, COS cells, 3T3 cells, HeLa cells, Vero cells, or insect cells such as Sf9, Sf21, and Tn5 can be used.
- CHO cells are particularly preferred for mass expression purposes.
- Introduction of a vector into a host cell can be performed by, for example, a calcium phosphate method, a DEAE dextran method, a method using a cationic ribosome DOTAP (Boehringer Mannheim), an electroporation method, a lipofection method, or the like.
- yeasts such as the genus Saccharomyces, such as Saccharomyces cerevisiae, filamentous fungi such as the genus Aspergillus, such as Aspergillus niger, are known. .
- E. coli for example, JM109, DH5 ⁇ , HB101, etc.
- Bacillus subtilis is also known.
- the culture can be performed according to a known method.
- DMEM, MEM, RPMI1640, and IMDM can be used as the culture medium for animal cells.
- a serum supplement such as fetal calf serum (FCS) can be used in combination, or serum-free culture may be performed.
- FCS fetal calf serum
- the pH during culture is preferably about 6-8.
- the culture is usually performed at about 30 to 40 ° C. for about 15 to 200 hours, and medium exchange, aeration, and agitation are added as necessary.
- a growth factor for promoting cell proliferation may be added.
- a streptavidin variant-molecular probe conjugate obtained by binding a molecular probe to the streptavidin variant of the present invention, and a streptavid A therapeutic or diagnostic agent comprising an avidin variant-molecular probe conjugate is provided.
- the above-described streptavidin variant-molecular probe conjugate is provided as a treatment or diagnostic kit in combination with a diagnostic or therapeutic substance labeled with a biotin variant having affinity for the streptavidin variant of the present invention. be able to.
- molecular probes include antibodies, peptides, nucleic acids, aptamers and the like.
- a fusion of a molecular probe such as a cancer antigen-specific antibody molecule and the streptavidin variant of the present invention is prepared and administered to a patient, so that the streptogram of the present invention specifically binds to cancer cells.
- Avidin variants can be accumulated.
- a diagnostic or therapeutic substance a fluorescent dye, a chemiluminescent agent, a radioisotope, a metal compound, a sensitizer, a metal compound, or the like bonded to a biotin variant having affinity for the above-mentioned streptavidin variant.
- antibody can be used as the antibody to be bound to the streptavidin variant. Both polyclonal and monoclonal antibodies can be used. Although subclass of the antibody is not particularly limited, preferably IgG, particularly IgG 1 is suitably used. “Antibody” includes all modified antibodies and antibody fragments. Humanized antibodies, human antibodies, human antibodies, antibodies derived from various animals such as mice, rabbits, rats, guinea pigs, monkeys, chimeric antibodies of human antibodies and antibodies derived from various animals, diabody, scFv, Fd, Fab, Fab ′, F (ab) ′ 2 may be mentioned, but is not limited thereto.
- a conjugate of a streptavidin variant and an antibody can be obtained using methods known to those skilled in the art. For example, it can be obtained by a chemical binding method (US5, 608, 060), or by ligating DNA encoding a streptavidin variant and DNA encoding an antibody, and expressing it in a host cell using an expression vector or the like, It can also be obtained as a fusion protein.
- the DNA encoding the streptavidin variant and the DNA encoding the antibody may be linked via DNA encoding an appropriate peptide called a linker. It is desirable that the streptavidin variant-antibody conjugate is produced while leaving the specific binding force between the antibody and the target molecule.
- a streptavidin variant with reduced affinity for natural biotin or biocytin; and (B) A biotin variant having high affinity for the streptavidin variant A reagent kit for treatment or diagnosis, comprising: (A) a conjugate of a streptavidin variant with a reduced affinity for natural biotin or biocytin and a molecular probe; and (b) a biotin variant having a high affinity for the streptavidin variant. Diagnostic or therapeutic substances: A therapeutic or diagnostic kit is provided.
- streptavidin variant with reduced affinity for natural biotin or biocytin in streptavidin having the amino acid sequence described in SEQ ID NO: 2, (1) Mutation in which tyrosine at the 10th amino acid residue is substituted with serine: (2) Mutation in which tyrosine at the 71st amino acid residue is substituted with serine: (3) Mutation in which arginine at the 72nd amino acid residue is substituted with lysine: (4) Mutation in which glutamic acid at the 89th amino acid residue is substituted with aspartic acid: (5) Mutation in which arginine at the 91st amino acid residue is substituted with lysine: (6) Mutation in which glutamic acid at the 104th amino acid residue is substituted with asparagine: (7) a mutation in which serine at the 33rd amino acid residue is substituted with another amino acid (for example, asparagine); and (8) the aspartic acid at 116th is other A streptavidin
- a compound represented by the formula (1) described in this specification preferably a compound represented by the formula (2) should be used. Can do.
- THF Anhydrous tetrahydrofuran
- the crude product containing 2 was dissolved in a mixed solvent of water (40 mL) and hexane (20 mL), sodium periodate (14.2 g, 66.5 mmol) was added, and the mixture was stirred for 2 hr. Sodium carbonate was added, and the mixture was further stirred for 1 hour. The organic layer was washed with saturated brine and dried, and then the solvent was distilled off under reduced pressure. The resulting crude product was purified by column chromatography on silica gel (dichloromethane-methanol) to give 2.17 g (two-stage yield 51%) of the title compound.
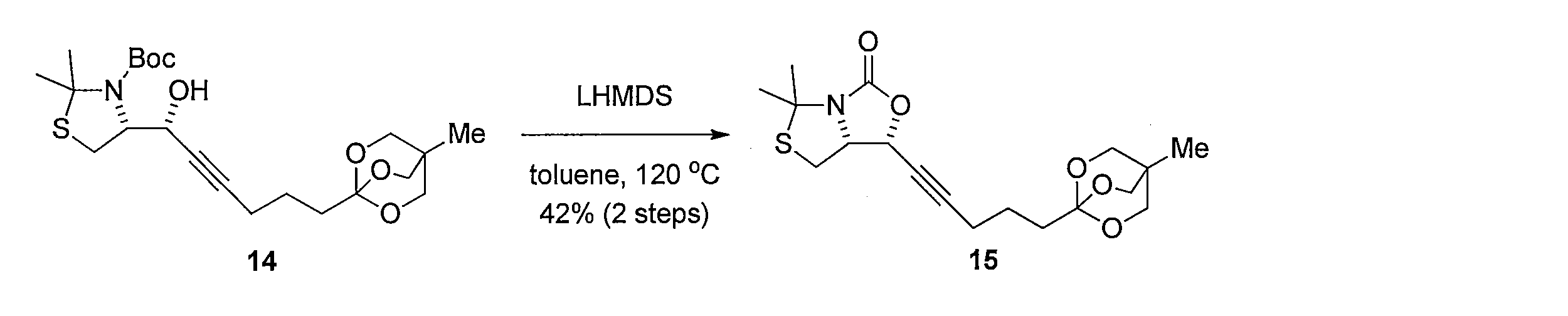
- Hexamethyldisilazane lithium solution (1 M THF solution 7.88 mmol) was added to a solution of the crude product containing 14 in anhydrous toluene 40 mL. After stirring at 120 ° C. for 12 hours, a saturated aqueous ammonium chloride solution was added, and the mixture was extracted with ethyl acetate. The organic layer was washed with saturated brine and dried, and then the solvent was distilled off under reduced pressure. The resulting crude product was purified by silica gel column chromatography (hexane-ethyl acetate) to obtain 1.82 g of the title compound (two-stage yield 42%, pale yellow oil).
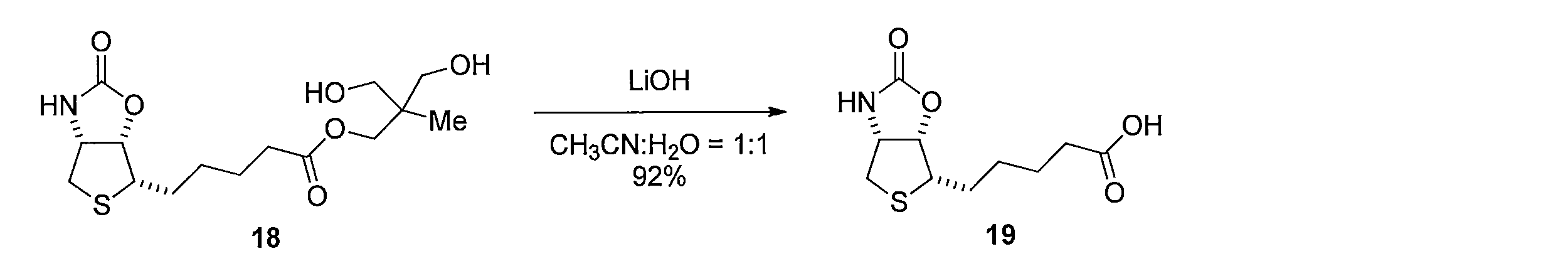
- Lithium hydroxide (5 ⁇ mol) was added to a mixed solution of 18 (1.1 mg, 3.2 ⁇ mol) of CH 3 CN (500 ⁇ L) and H 2 O (500 ⁇ L). After stirring for 12 hours, the reaction was quenched with 1 M hydrochloric acid, passed through silica gel column chromatography, and washed with methanol. The solvent was distilled off under reduced pressure, and the resulting crude product was purified by silica gel column chromatography (dichloromethane-methanol) to obtain 700 ⁇ g of the title compound (yield 92%, white solid).
- a sodium hydroxide aqueous solution was added to a mixed solution of 6-aminohexanoic acid (3 mg, 0.023 mmol) in dioxane (500 ⁇ L) and H 2 O (500 ⁇ L) to adjust the pH to about 9. 28 (10 mg, 0.023 mmol) (commercial product) was added and stirred for 12 hours, and then ether was added to remove the organic layer. The aqueous layer was neutralized with hydrochloric acid and filtered. The residue was washed with acetone, and the solvent was distilled off under reduced pressure.
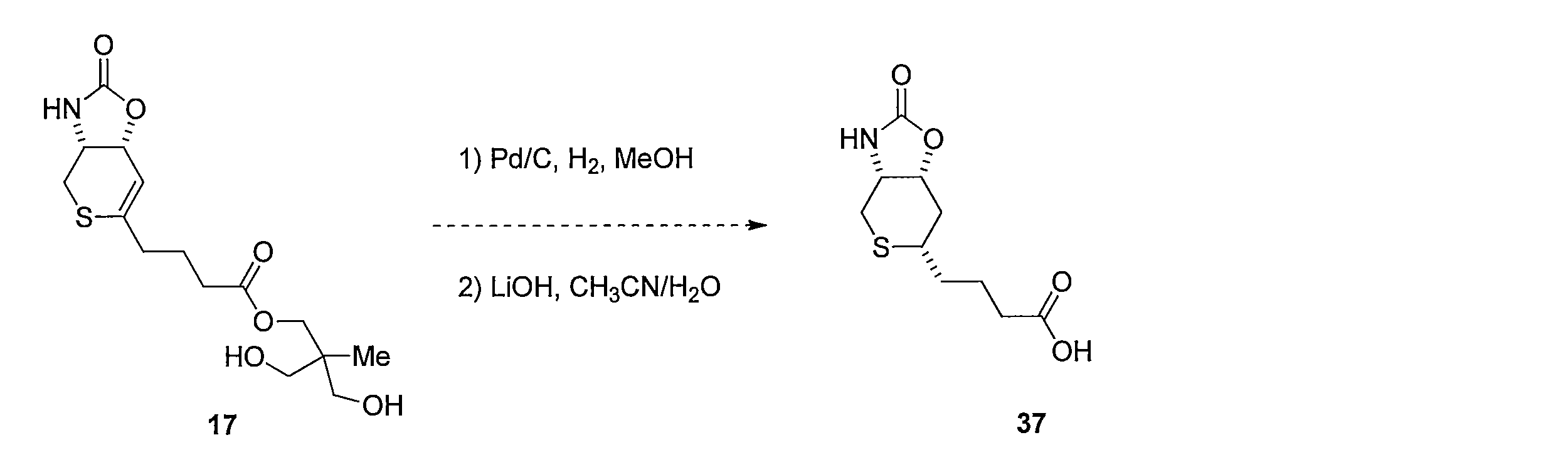
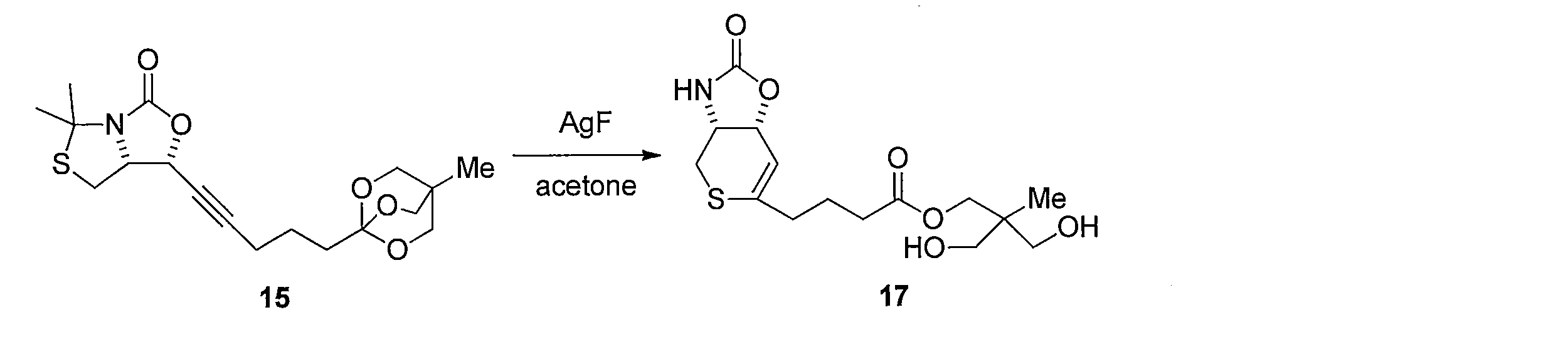
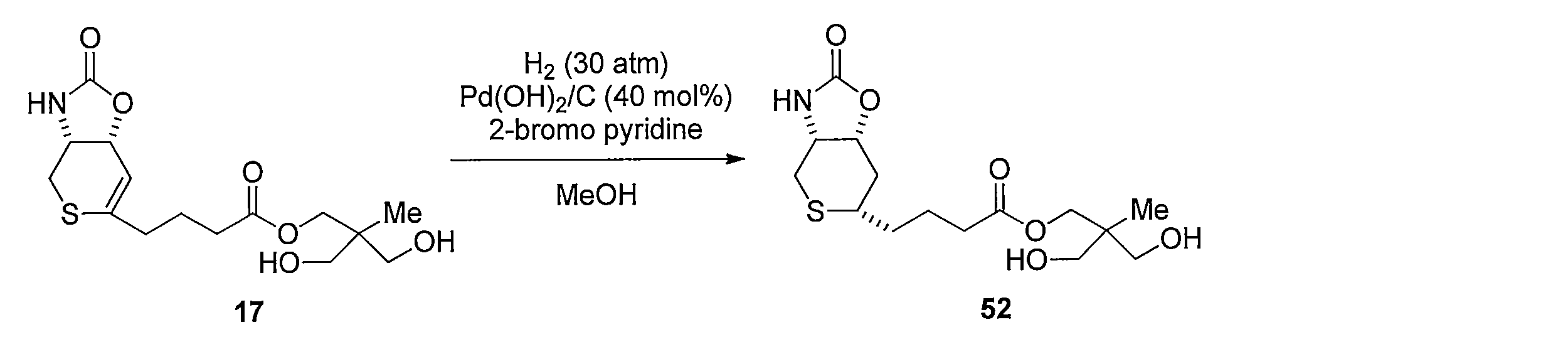
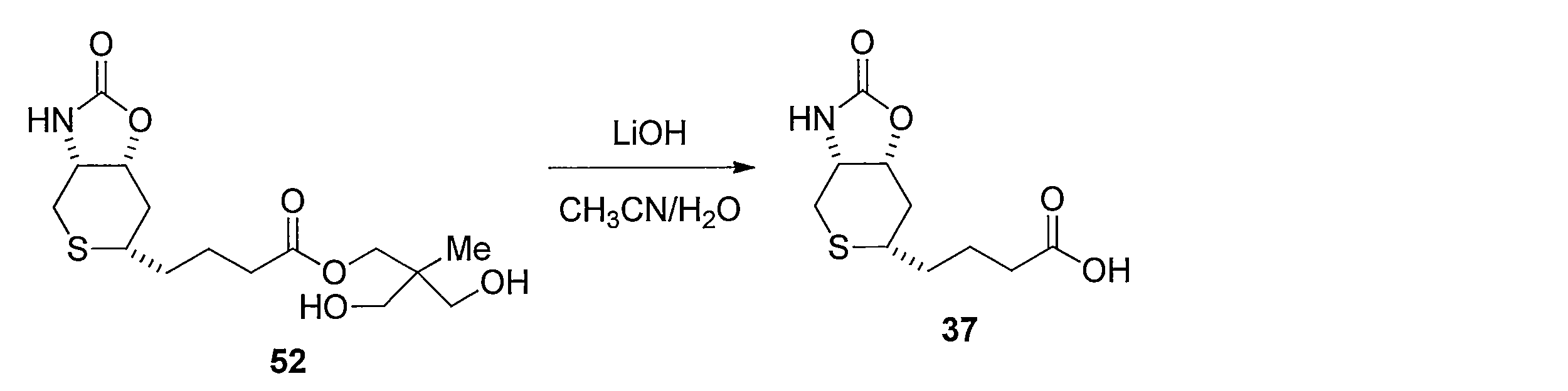
- Reduction of the double bond is carried out by dissolving compound 17 in MeOH and stirring under a hydrogen atmosphere using a catalytic amount of Pd / C. Subsequently, 37 is obtained by hydrolyzing the ester moiety of the obtained compound using LiOH in a CH 3 CN, H 2 O mixed solvent.
- Reversed phase high performance liquid chromatography was performed using the JASCO-HPLC system. Detection was performed using 210 nm or 254 nm ultraviolet light, and the mobile phase was a gradient solvent system (acetonitrile / 0.1% trifluoroacetic acid MQ solution). The analysis was performed using a YMC-Pack ODS-AM (150 ⁇ 4.6 mL) column at a flow rate of 1 mL / min. The fractionation was performed using a YMC-Pack ODS-AM (250 ⁇ 20 mL) column at a flow rate of 8-10 mL / min. Reagents were purchased from Aldrich, Tokyo Chemical Industry Co., Ltd. (TCI), Kanto Chemical Co., Ltd. (Kanto), Wako Pure Chemical Industries, Ltd., and Watanabe Chemical Industry Co., Ltd. All reagents and solvents were used as they were unless otherwise specified.
- the crude product was dissolved in a mixed solvent of acetonitrile (6.2 mL) and water (6.2 mL), 2N aqueous lithium hydroxide solution (0.47 mL, 0.93 mmol) was added, and the mixture was stirred at room temperature for 6 hr.
- the aqueous layer was washed with diethyl ether and acidified with 2N hydrochloric acid (pH ⁇ 5).
- the solvent was distilled off under reduced pressure, 1N aqueous sodium hydroxide solution was added, and the aqueous layer was washed twice with diethyl ether.
- the aqueous layer was acidified with 1N hydrochloric acid (pH ⁇ 5), extracted with ethyl acetate, and the organic layer was washed with saturated brine.
- Example 2 Production of mutant streptavidin (1) Construction of expression vector The nucleotide sequence of a gene encoding wild-type core streptavidin is shown in SEQ ID NO: 1 in the sequence listing.
- mcSA314 also referred to as LISA314WT or LISA314 in this specification
- mcSA314 is a streptavidin variant having all of the following mutations in the amino acid sequence of core streptavidin described in SEQ ID NO: 2.
- the expression vector was designed so that the fusion protein of the wild-type streptavidin and the modified streptavidin and the subtilisin prodomain part, which is a purification tag, was expressed.
- a vector that expresses was prepared. Specifically, using the above sequence as a template, the following primers 1 and 2 that add a HindIII site on the 5 ′ end side and an EcoRI site on the 3 ′ end side by PCR are used.
- Primer 1 GCTCTTCAAAGCTTTGGCCGAAGCTGGTATCACTG (SEQ ID NO: 13)
- Primer 2 CTCGAGGAATTCTTAGCTAGCAGCAGAAGGCTTAAC (SEQ ID NO: 14)
- the sample treated with the restriction enzyme was subjected to gel purification after electrophoresis.
- the pPAL7 vector (manufactured by BIO-RAD) was subjected to enzyme treatment and gel purification.
- the purified vector and PCR product were ligated by the designated method using 2 ⁇ Rapid Ligation Buffer and T4DNA Polymerase (Promega).
- the transformation of E. coli was performed by adding 2 microliters of ligation product to 50 microliters of DH5 ⁇ competent cell (manufactured by TOYOBO). Plasmid extraction was performed using Miniprep Kit (manufactured by QIAGEN), and the sequence of the obtained plasmid was confirmed by sequence analysis.
- S45N Fw TATGAAAACGCCGTGGGTAATGCGGAA (SEQ ID NO: 15)
- S45N Rv CACGGCGTTTTCATAGGTGCCGGTCAG (SEQ ID NO: 16)
- D128N Fw CGTTGGCGGTGCTGATGCTCGTATCAACAC (SEQ ID NO: 17)
- D128N Rv GGTGCTGATGCTAAGATCAACACTCAGTGG (SEQ ID NO: 18)
- S45N means a mutation in which serine (S) of the 33rd amino acid residue is substituted with asparagine (N) in the amino acid sequence of core streptavidin described in SEQ ID NO: 2.
- D128N means a mutation in which the 116th aspartic acid (D) is substituted with asparagine (N) in the amino acid sequence of core streptavidin described in SEQ ID NO: 2.
- a pPAL7 expression vector incorporating a mutant streptavidin gene sequence was transfected into Escherichia coli BL21 (BIO-RAD) according to a conventional method. Protein expression was performed as follows. That is, the cells are cultured at 37 ° C. until the cell density of the E. coli culture solution reaches OD (600 nm) 0.5-0.7, and IPTG (isopropyl- ⁇ -D-thiogalactocyanide) is added to a final concentration of 1 mM. Then, protein expression was induced, and culturing was performed at 10 ° C. to 30 ° C., preferably 16 ° C. for 24 hours or more. After culturing, the cells were collected by centrifugation, and stored at minus 20 ° C. until protein purification.
- IPTG isopropyl- ⁇ -D-thiogalactocyanide
- Binding buffer and wash buffer 1 10 mM sodium phosphate
- wash buffer 2 10 mM sodium phosphate, 300 mM
- elution buffer 10 mM sodium acetate, 100 mM sodium fluoride
- column regeneration buffer 100 mM phosphate
- column Storage buffer 10 mM sodium phosphate was used for purification.
- the buffer pH was adjusted to pH 6.1 for purification of natural streptavidin, and to pH 6.8 for purification of modified streptavidin.
- the buffer pH of the modified streptavidin is set to 7.0.
- the roughly purified recombinant protein was concentrated by centrifugal filtration using a 10,000 MWCO ultrafiltration membrane in preparation for purification using a ceramic hydroxyapatite column. After concentration, the buffer was replaced with 5 mM sodium phosphate solution using a desalting column.
- the ceramic hydroxyapatite column was CHT2-1 (BIO-RAD), and the flow rate of all operations was 2 ml / min. Initially, the column was equilibrated with 10 column volumes of 5 mM sodium phosphate. Next, the buffer-purified crude purified sample was applied and adsorbed onto the column. After 6 column volumes of washing, protein was eluted with 5 mM sodium phosphate and 500 mM sodium chloride buffer.
- Example 3 Competitive analysis with biotin-HRP label
- the purified variant protein was immobilized on an ELISA plate H (Sumitomo Bakelite) under conditions of 5 ⁇ g / mL, 100 ⁇ l, and 4 ° C. overnight. After solid-phase immobilization, blocking was performed at 200 ⁇ l / well for 5 minutes using a SuperBlock Blocking Buffer (Thermo Scientific).
- Example 4 Production of LISA314 variant (1) Preparation of expression vector of LISA314 variant According to the instructions of Primer STAR Mutagenesis Basit Kit (Takara Bio), the oligo DNA used for the preparation of each variant overlaps 15 bases on the 5 'side. Designed. Using the following primers, the pCold TF vector into which LISA314 was inserted was used as a template, and the amino acid sequence was converted by changing the codon sequence by substitution of the base sequence by the Site-Directed Mutagenesis method. Thereafter, the template plasmid was cleaved with the restriction enzyme DpnI, and E. coli was transformed.
- LISA314314V21 which is a LISA314 variant, has mutations N23D and S27D in addition to LISA314.
- N23D means a mutation in which the asparagine (N) of the 11th amino acid residue is substituted with aspartic acid (D) in the amino acid sequence of core streptavidin described in SEQ ID NO: 2.
- S27D means a mutation in which serine (S) at the 15th amino acid residue is substituted with aspartic acid (D) in the amino acid sequence of core streptavidin described in SEQ ID NO: 2.
- LISA314 V21 is the amino acid sequence of core streptavidin described in SEQ ID NO: 2, (1) Mutation in which tyrosine at the 10th amino acid residue is substituted with serine: (2) Mutation in which tyrosine at the 71st amino acid residue is substituted with serine: (3) Mutation in which arginine at the 72nd amino acid residue is substituted with lysine: (4) Mutation in which glutamic acid at the 89th amino acid residue is substituted with aspartic acid: (5) Mutation in which arginine at the 91st amino acid residue is substituted with lysine: (6) Mutation in which glutamic acid at the 104th amino acid residue is substituted with asparagine: (7) a mutation in which aspartic acid at the 11th amino acid residue is substituted with aspartic acid; (8) Mutation in which serine at the 15th amino acid residue is substituted with aspartic acid: A variant streptavidin having the amino acid sequence shown in SEQ ID NO: 4.
- IPTG isopropyl- ⁇ -D-thiogalactopanoside
- the column was equilibrated with 10 column volumes of binding / washing buffer (20 mM Tris-NaCl, 500 mM NaCl, pH 8) and the column washed after sample application.
- the bound protein was eluted with 3 column volumes of elution buffer (20 mM Tris-NaCl, 500 mM NaCl, 400 mM imidazole, pH 8).
- Example 5 Crystal structure analysis (1) Crystallization conditions Crystallization was performed at 20 ° C using the LISA314-biotin sitting drop vapor diffusion method ( Figure 3). The protein solution was 9 mg / ml LISA314, 15 mM tris-HCl pH 7.5, 150 mM NaCl. Biotin was added in excess during LISA314 purification. For the crystallization mother liquor (60 ⁇ l), 0.2 M Ammonium Sulfate, 0.1 M Sodium acetate trihydrate pH 5.2, 22% (w / v) Polyethylene glycol 4000 was used. 0.5 ⁇ l was mixed.
- LISA314-V21 ⁇ iminobiotintail Crystallization was performed at 20 ° C using the sitting drop vapor diffusion method.
- the protein solution was 10 mg / ml LISA314-V21, 20 mM tris-HCl pH 7.5, 250 mM NaCl.
- Iminobiotintail (Compound 29 of Example 1, the structure is shown below) was added in excess during LISA314-V21 purification.
- the crystallization mother liquor (60 ⁇ l) used 0.1 M Sodium acetate trihydrate pH4.5, 30% (w / v) lyPolyethylene glycol 1500. It was supposed to be.
- Asn23 interacts with neighboring Gly26 by forming a hydrogen bond (indicated by the dotted line connecting N23 and G26 in LISA314 in the upper right of Fig. 4), whereas in 1N43, Ala23 and Gly26 There is no hydrogen bond corresponding to this (the part indicated by the black arrow of 1N43 in the lower left of Fig. 4), so the N23A mutation in 1N43 does not alter the loop structure from N23 to S27 compared to LISA314.
- the mutant streptavidin LISA314-V21 was created with the expectation that the interaction with iminobiotin, rather than biotin, would be stronger, so the S27D mutation was applied in addition to the N23D mutation, and LISA314-V21 Asp27 interacts with the N atom of iminobiotin.
- Example 6 Affinity analysis by SPR (1) Construction of expression vector (LISA314 V21; N23D, S27, etc.) The protein used for affinity analysis by Biacore was expressed by the pET-21a (+) vector (Millipore Merck), and the recombinant protein was prepared by unwinding the inclusion bodies. Specifically, the pET-21a (+) vector was straightened using restriction enzymes BamHI and XhoI. Next, according to the manual of In-Fusion HD Cloning Kit (Clontech), design PCR primers that match the linearized vector, and perform PCR using each of the aforementioned variant LISA314 V21 expression vectors (pCold TF) as a template. did.
- the amplified sequence was purified by extracting a target band by agarose gel electrophoresis and extracting DNA.
- the linearized vector and the purified PCR product were ligated using In-Fusion HD Cloning Kit.
- LISA314 V21 variant expression vector The oligo DNA used for the preparation of various variants of LISA314 V21 was designed according to the instructions of Primer STAR Mutagenesis Basal Kit (Takara Bio) so that the 5 'side overlaps 15 bases. The following primers were used, and the amino acid sequence was converted by changing the codon sequence by substitution of the base sequence by the Site-Directed Mutagenesis method using the above-mentioned vector with LISA314 V21 inserted as a template. Thereafter, the template plasmid was cleaved with the restriction enzyme DpnI, and E. coli was transformed.
- S45A Fw TATGAAgcaGCCGTGGGTAATGCGGAA (SEQ ID NO: 23)
- S45A Rv CACGGCtgcTTCATAGGTGCCGGTCAG (SEQ ID NO: 24)
- S45Q Fw TATGAAcagGCCGTGGGTAATGCGGAA (SEQ ID NO: 25)
- S45Q Rw CACGGCctgTTCATAGGTGCCGGTCAG (SEQ ID NO: 26)
- S45L Fw TATGAActgGCCGTGGGTAATGCGGAA (SEQ ID NO: 27)
- S45L Rv CACGGCcagTTCATAGGTGCCGGTCAG (SEQ ID NO: 28)
- S45I Fw TATGAAatcGCCGTGGGTAATGCGGAA (SEQ ID NO: 29)
- S45I Rw CACGGCgatTTCATAGGTGCCGGTCAG (SEQ ID NO: 30)
- S45H Fw TATGAAcatGCCGTGGGTAATGCGG
- S45A, S45Q, S45L, S45I, S45H, S45T, S45V, and S45N the serine of the 33rd amino acid residue in the amino acid sequence of core streptavidin described in SEQ ID NO: 2 is alanine (A), glutamine (Q ), Leucine (L), isoleucine (I), histidine (H), threonine (T), valine (V) and asparagine (N). That is, a mutant in which any one of the amino acid mutations S45A, S45Q, S45L, S45I, S45H, S45T, S45V and S45N is further introduced into LISA314 V21 is produced. The amino acid sequences of these mutants are shown in SEQ ID NOs: 5 to 12 in the sequence listing.
- E. coli was prepared by adding 3 mL of B-PER (Thermo SCIETIFIC) and Lisonase Bioprocessing Reagent as a cell lysate per 1 mL of B-PER. The dissolution was performed at room temperature, and the dissolved solution was centrifuged at 27,000 ⁇ g for 20 minutes. After centrifugation, the supernatant was discarded and the pellet was collected as inclusion bodies. The collected inclusion bodies were resuspended in 10 mL of B-PER diluted 10-fold with MilliQ water and re-recovered by centrifugation at 27,000 ⁇ g for 20 minutes, and then washed three times. Finally, in order to remove the surfactant, it was resuspended with MilliQ and collected by centrifugation. The collected inclusion bodies were aliquoted and stored frozen at minus 80 ° C.
- B-PER Thermo SCIETIFIC
- Lisonase Bioprocessing Reagent as a cell lys
- the cryopreserved inclusion body was solubilized with a denaturing buffer (20 mM Tris-HCl, 6 M guanidine hydrochloride, 200 mM NaCl, pH 1.5). To remove biotin, 100 times volume of dialysis buffer (same as denaturation buffer) was performed twice for 4 hours. Thereafter, the concentration of the solubilized solution was adjusted with a dialysis buffer so that the protein concentration by absorbance 280 nm was 40-50 mg / mL. For the unwinding, a dilution method was used.
- the rewinding was performed by adding dropwise and diluting 100 microliters of the protein solution whose concentration was adjusted to 50 mL of dilution buffer (20 mM Tris-HCl, 200 mM NaCl, pH 8.0) stirred with a stirrer.
- Affinity analysis with compounds by SPR Biacore T100 was used for affinity analysis. Specifically, the protein fractionated by gel filtration chromatography was immobilized using Sensor Chip NTA. As the running buffer, 0.5% Tween 20, HBS-P + was used. The immobilization of nickel on NTA and the capture of the ligand were carried out by the attached template program.
- Biacore assay The amount of ligand immobilized on the sensor chip was adjusted to fall within the range of 1608 RU to 8042 RU in order to suppress mass transport limitation.
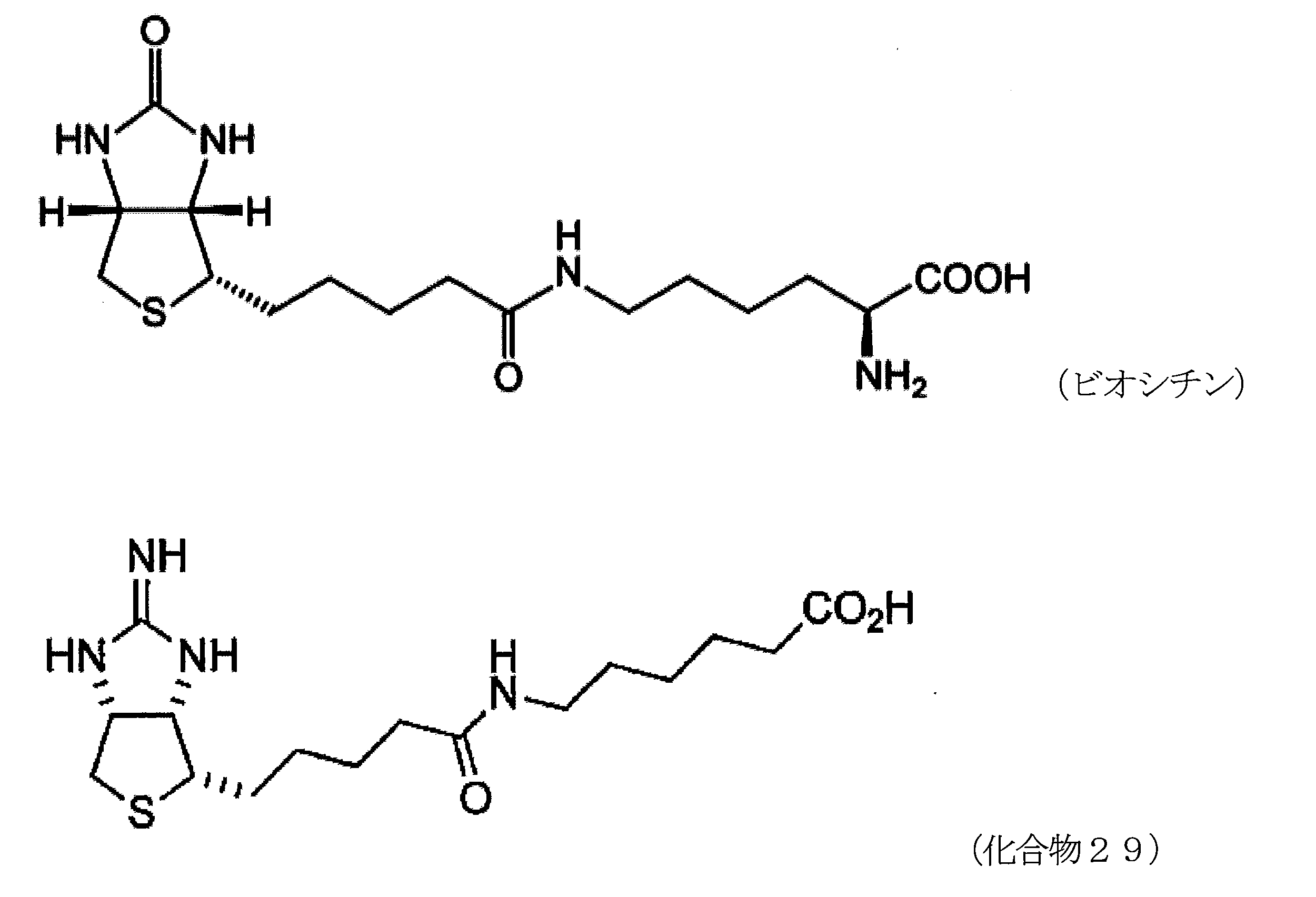
- biocytin and compound 29 (structure is shown below) synthesized in Example 1 were used as the analyte.
- Biocytin is the main form of biotin.
- the concentration of the analyte was prepared from 1 ⁇ M to a 2-fold diluted 8 series, and in the case of Compound 29, a 2-fold diluted 12 series was prepared.
- the measurement was performed at a flow rate of 30 ⁇ l / min, a contact time of 120 seconds, and a dissociation time of 600 seconds.
- sensorgrams of all concentrations were taken into analysis software, an equilibrium value analysis was performed, and a dissociation constant KD was calculated.
- the graphs are shown in FIGS. 7 to 9, and the calculated KD values are shown in Table 1.
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Immunology (AREA)
- Molecular Biology (AREA)
- Engineering & Computer Science (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Biochemistry (AREA)
- Biomedical Technology (AREA)
- Hematology (AREA)
- Urology & Nephrology (AREA)
- Biophysics (AREA)
- Gastroenterology & Hepatology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Genetics & Genomics (AREA)
- Microbiology (AREA)
- Food Science & Technology (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Biotechnology (AREA)
- Cell Biology (AREA)
- Analytical Chemistry (AREA)
- Physics & Mathematics (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Oxygen Or Sulfur (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
Abstract
Description
[1] 下記式(1)で示される化合物。
[5] [4]に記載のストレプトアビジン変異体をコードするDNA。
[6] [4]に記載のストレプトアビジン変異体に分子プローブを結合させることにより得られる、ストレプトアビジン変異体-分子プローブ結合物。
[7] [6]に記載のストレプトアビジン変異体-分子プローブ結合物を含む、治療剤又は体内あるいは体外診断剤。
[8] (a)[6]に記載のストレプトアビジン変異体―分子プローブ結合物;及び(b)[1]から[3]の何れかに記載の化合物で標識した体内あるいは体外診断用又は治療用物質:を含む治療又は体内あるいは体外診断キット。
(b)上記ストレプトアビジン変異体に対して高い親和性を有するビオチン改変体:
を含む、治療又は体内あるいは体外診断のための試薬キット。
(b)上記ストレプトアビジン変異体に対して高い親和性を有するビオチン改変体で標識した体内あるいは体外診断用又は治療用物質:
を含む治療又は体内あるいは体外診断キット。
(1)ビオチン改変体
本発明のビオチン改変体は、下記式(1)で示される化合物であり、好ましくは式(1)においてnが0である場合である式(2)で示される化合物である。
p及びqはそれぞれ独立に1から10の整数を示し、好ましくは2から10の整数、より好ましくは2から8の整数、より好ましくは2から6の整数、特に好ましくは4又は5を示す。
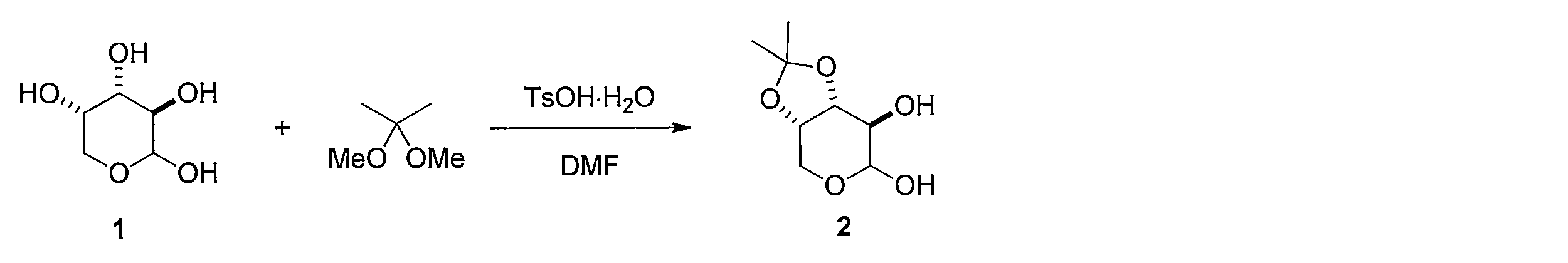
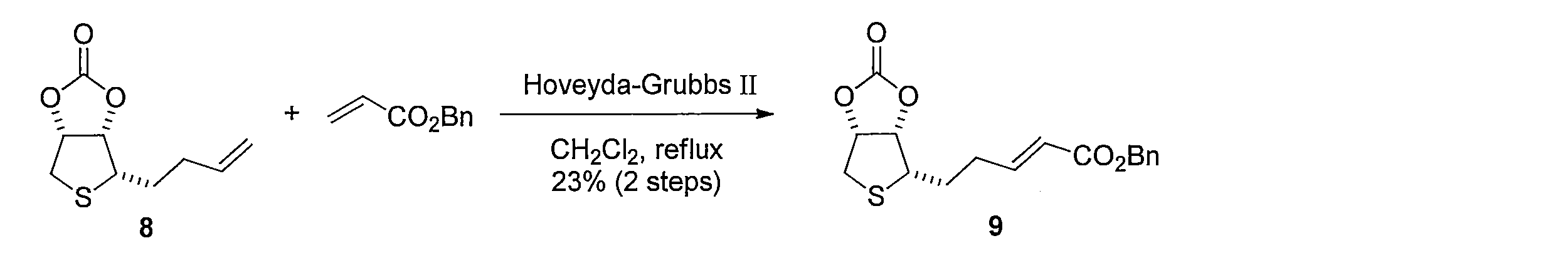
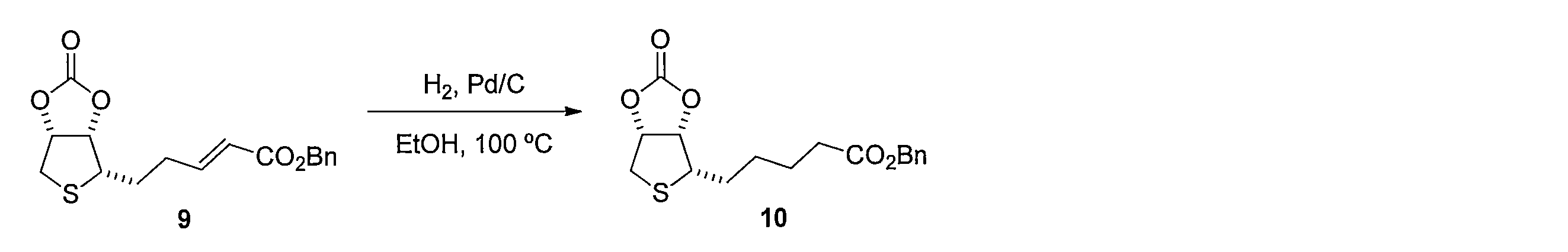
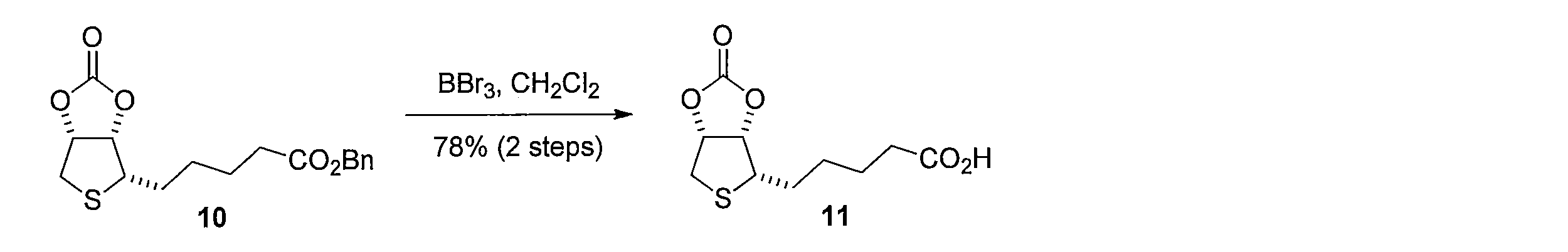
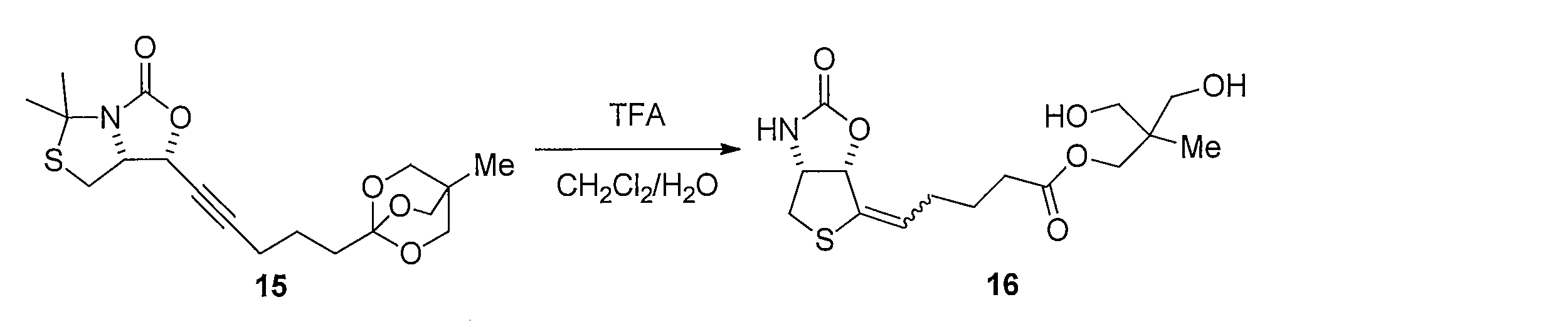
先ず、(L)-アラビノース(化合物1)のDMF溶液に2,2-ジメトキシプロパンとトルエンスルホン酸一水和物を加えることで、(3aS,7R,7aR)-2,2-ジメチルテトラヒドロ-3aH-[1,3]ジオキソロ[4,5-c]ピラン-6,7-ジオール (化合物2)を得る。化合物2を水及びヘキサンの混合溶媒に溶かし、過ヨウ素酸ナトリウムを加えて撹拌し、炭酸ナトリウムを加えることで、(3aS,6aS)-2,2-ジメチルテトラヒドロフロ[3,4-d][1,3]ジオキソール-4-オール(化合物3)を得る。化合物3 のDMF溶液に、セライトと二クロム酸ピリジニウムを加えて反応させることにより、(3aS,6aS)-2,2-ジメチルジヒドロフロ[3,4-d][1,3]ジオキソール-4(3aH)-オン(化合物4)を得る。化合物4の DMF溶液にチオ酢酸カリウムを加えて反応させることにより(3aS,6aR)-2,2-ジメチルジヒドロチエノ[3,4-d][1,3]ジオキソール-4(3aH)-オン(化合物5)を得る。化合物5のTHF溶液に、3-ブテニル-1-マグネシウム ブロミドを加えて反応させることにより、(3aS,6aR)-4-(3-ブテン-1-イル)-2,2-ジメチルテトラヒドロチエノ[3,4-d][1,3]ジオキソール-4-オール(化合物6)を得る。化合物6の CH2Cl2溶液に、トリエチルシラン を加えて攪拌した後、トリフルオロ酢酸 (675 μL, 9.05 mmol) を加えて反応させることにより、(2S,3S,4R)-2-(3-ブテン-1-イル)テトラヒドロチオフェン-3,4-ジオール(化合物7)を得る。化合物7の CH2Cl2溶液に、ピリジン及びトリホスゲンを加えて反応させることにより、(3aS,4S,6aR)-4-(3-ブテン-1-イル)テトラヒドロチエノ[3,4-d][1,3]ジオキソール-2-オン(化合物8)を得る。化合物8 を含むCH2Cl2溶液に、アクリル酸ベンジルと第二世代 Hoveyda-Grubbs 触媒を加えて加熱還流することにより、 (E)-ベンジル5-((3aS,4S,6aR)-2-オキソテトラヒドロチエノ[3,4-d][1,3]ジオキソール-4-イル)-2-ペンテノエート (化合物9)を得る。化合物9のエタノール溶液に、パラジウム炭素を加え、水素ガス存在下で撹拌して反応させることにより、ベンジル5-((3aS,4S,6aR)-2-オキソテトラヒドロチエノ[3,4-d][1,3]ジオキソール-4-イル)ペンタノエート(化合物10)を得る。化合物10 を含むCH2Cl2溶液に、三臭化ホウ素を加えて反応させることにより、本発明の式(1)で示される((3aS,4S,6aR)-2-オキソテトラヒドロチエノ[3,4-d][1,3]ジオキソール-4-イル)ペンタン酸(化合物11)を得る。
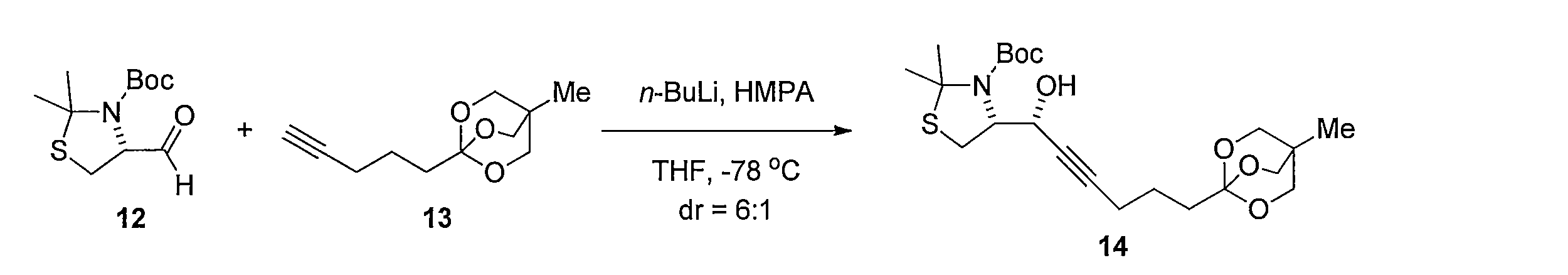
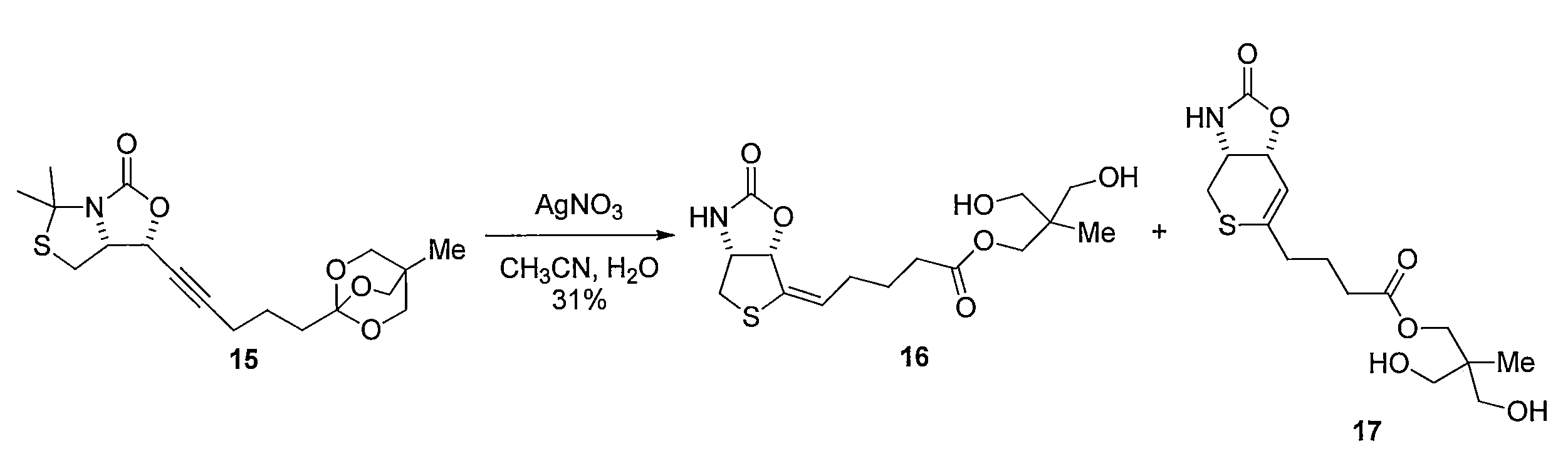
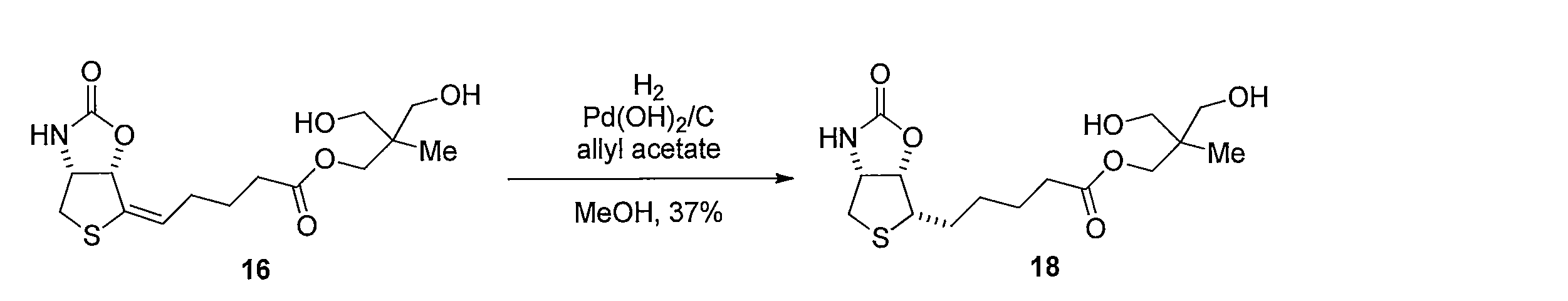
化合物13の無水 THF 溶液に、n-ブチルリチウム溶液 (2.6 M ヘキサン溶液) を滴下して撹拌後、化合物 12と HMPA無水 THF溶液を滴下して撹拌することにより、 (R)-tert-ブチル4-((R)-1-ヒドロキシ-6-(4-メチル-2,6,7-トリオキサビシクロ [2.2.2]オクタン-1-イル)-2-ヘキサニル-1-イルyl)-2,2-ジメチルチアゾリジン-3-カルボキシレート(化合物14)を得る。化合物14 を含む無水トルエン溶液に、ヘキサメチルジシラザンリチウム溶液を加えて反応させることにより (1R,7aR)-5,5-ジメチル-1-(5-(4-メチル-2,6,7-トリオキサビシクロ[2.2.2]オクタン-1-イル)-1-ペンチン-1-イル)ジヒドロ-1H-チアゾロ[3,4-c]オキサゾール-3(5H)-オン(化合物15)を得る。化合物15の CH3CNと H2O 混合溶液に、硝酸銀(I)を加えて反応させることにより(E)-3-ヒドロキシ-2-(ヒドロキシメチル)-2-メチルプロピル5-((3aR,6aS)-2-オキソテトラヒドロチエノ[3,4-d]オキサゾール-6(6aH)-イリデン)ペンタノエート(化合物16)を得る。化合物16及び酢酸アリルのメタノール溶液に水酸化パラジウム炭素を加え、水素ガス存在下で反応することにより、3-ヒドロキシ-2-(ヒドロキシメチル)-2-メチルプロピル 5-((3aR,6S,6aS)-2-オキソヘキサヒドロチエノ[3,4-d]オキサゾール-6-イル)ペンタノエート(化合物18)を得る。化合物18の CH3CNと H2Oの混合溶液に、水酸化リチウムを加えて反応させることにより、5-((3aR,6S,6aS)-2-オキサヘキサヒドロチエノ[3,4-d]オキサゾール-6-イル)ペンタン酸(化合物19)を得る。
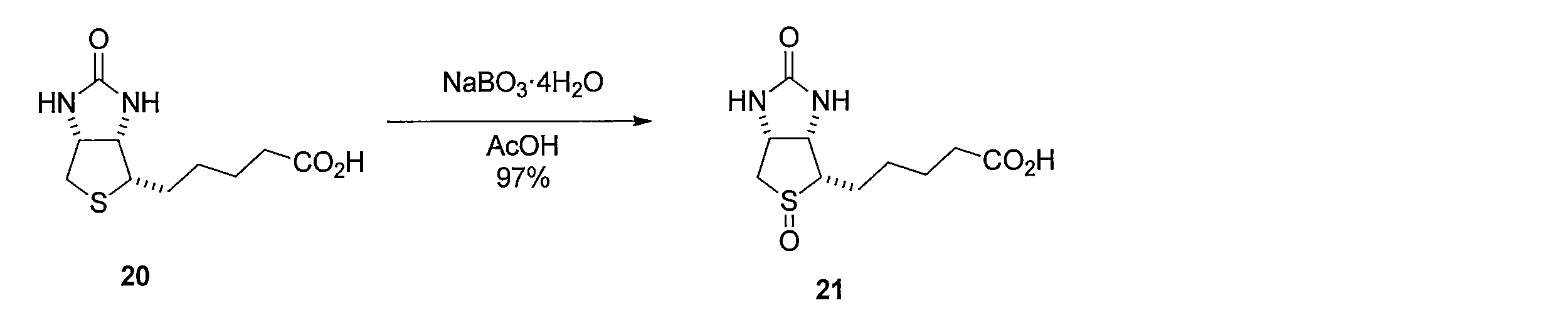
ビオチン (化合物20)の酢酸溶液にNaBO3・4H2Oを室温下加え、撹拌した後、チオ硫酸ナトリウムを加え、減圧下にて溶媒を留去することにより、5-((3aS,4S,6aR)-5-オキシド-2-オキソヘキサヒドロ-1H-チエノ[3,4-d]イミダゾール-4-イル)ペンタン酸(化合物21)を得る。
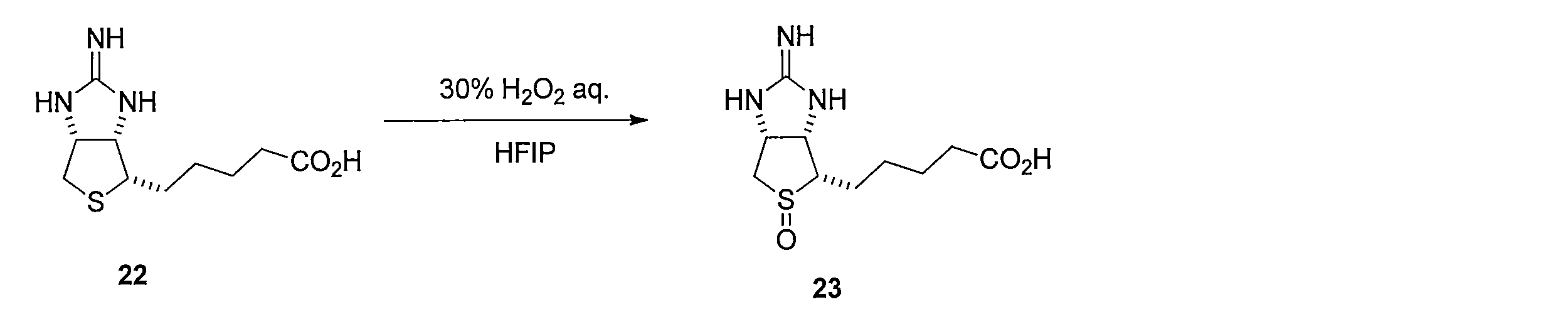
イミノビオチン(化合物22)の1,1,1,3,3,3-ヘキサフルオロイソプロパノール溶液にH2O2水溶液を加えて反応させることにより、5-((3aS,4S,6aR)-2-イミノ-5-オキシドヘキサヒドロ-1H-チエノ[3,4-d]イミダゾール-4-イル)ペンタン酸 (化合物23)を得る。
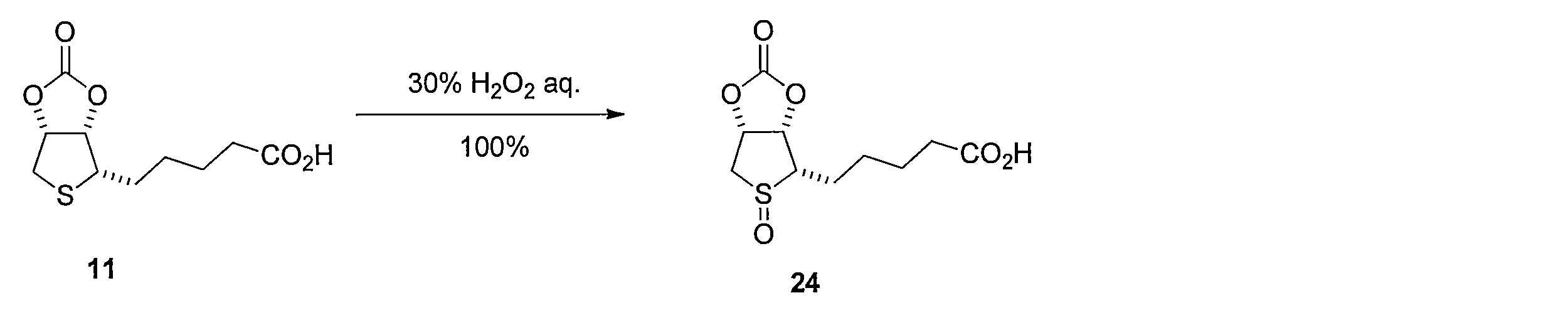
化合物11の1,1,1,3,3,3-ヘキサフルオロイソプロパノール溶液にH2O2水溶液を加えて反応させることにより、5-((3aS,4S,6aR)-5-オキシド-2-オキソテトラヒドロチエノ[3,4-d][1,3]ジオキソール-4-イル)ペンタン酸 (化合物24)を得る。
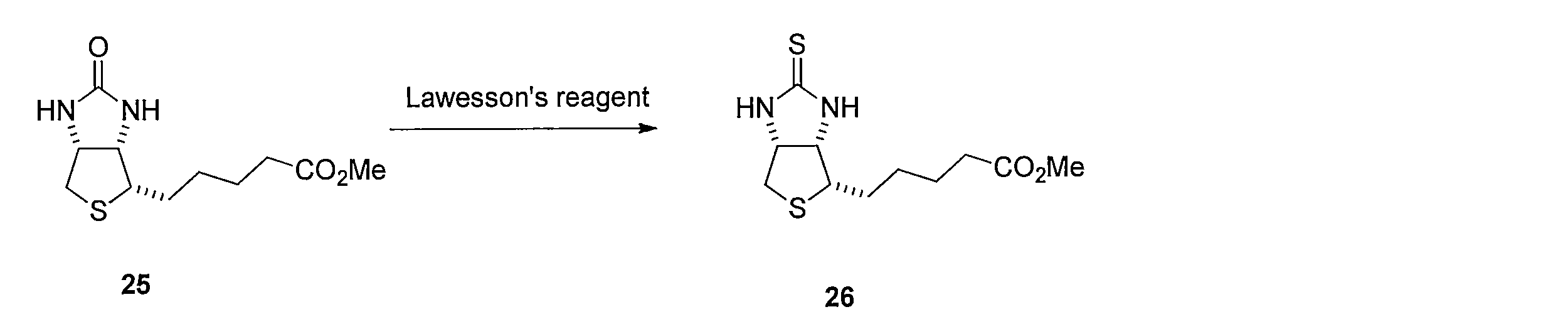
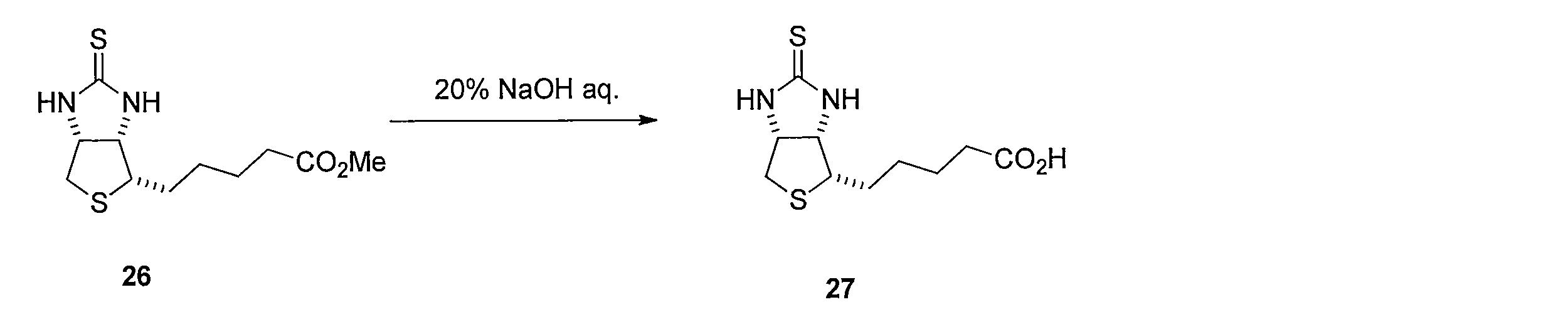
ビオチンメチルエステル (化合物25)のトルエン溶液にLawesson's reagentを加えて反応させることにより、メチル5-((3aS,4S,6aR)-2-チオキソヘキサヒドロ-1H-チエノ[3,4-d]イミダゾール-4-イル)ペンタノエート (化合物26)を得る。化合物26 を含むTHF溶液に水酸化ナトリウム水溶液を添加することにより、5-((3aS,4S,6aR)-2-チオキソヘキサヒドロ-1H-チエノ[3,4-d]イミダゾール-4-イル)ペンタン酸(化合物27)を得る。
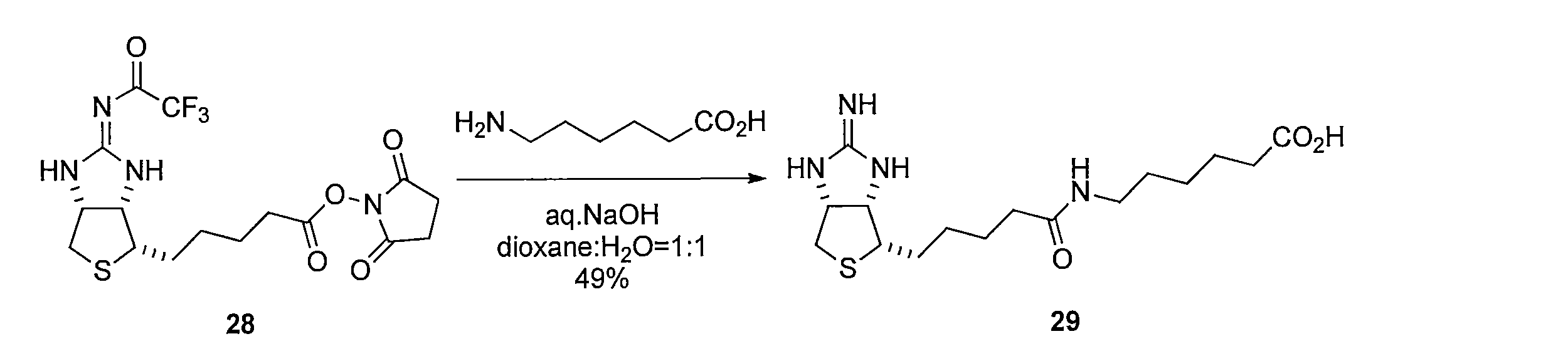
6-アミノヘキサン酸の dioxaneと H2Oの混合溶液に、水酸化ナトリウム水溶液を加え、pHが 9 程度になるよう調整する。化合物28を加えて反応させることにより、5-((3aR,6S,6aS)-2-オキソヘキサヒドロチエノ[3,4-d]オキサゾール-6-イル)ペンタン酸 (化合物29)を得る。
化合物28とNα-Boc-L-lysineのジオキサン/水の混合溶媒を撹拌することにより、
(S)-2-((tert-ブトキシカルボニル)アミノ)-6-(5-((3aS,4S,6aR,Z)-2-((2,2,2-トリフルオロアセチル)イミノ)ヘキサヒドロ-1H-チエノ[3,4-d]イミダゾール-4-イル)ペンタンアミド)ヘキサン酸 (化合物30)を得る。化合物30 をジオキサンと H2Oの混合溶液に、塩酸を加え、pHが 3 程度になるよう調整し5 時間撹拌した後、減圧下溶媒を留去して得た固体をdioxaneと H2Oに溶解してアンモニア水を加えることにより、 (S)-2-アミノ-6-(5-((3aS,4S,6aR)-2-イミノヘキサヒドロ-1H-チエノ[3,4-d]イミダゾール-4-イル)ペンタンアミド)ヘキサン酸(化合物31)を得る。
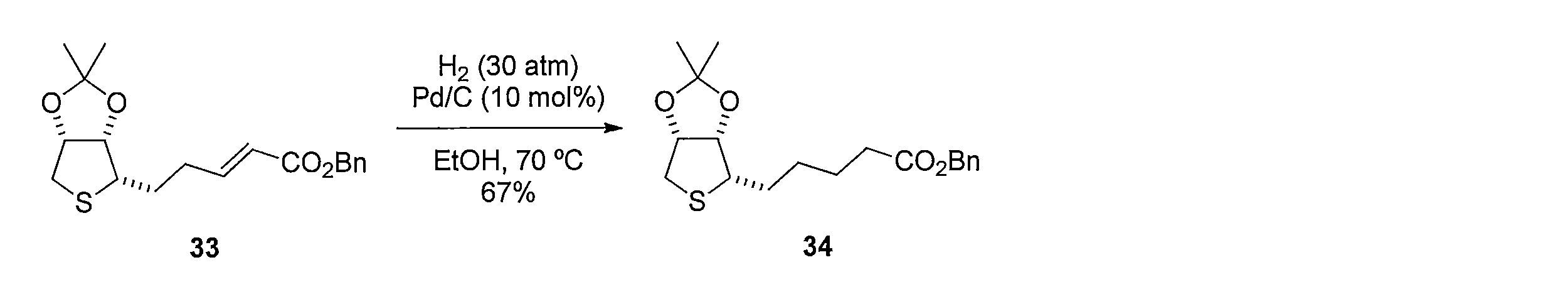
化合物32の CH2Cl2溶液に、アクリル酸ベンジルと第二世代 Hoveyda-Grubbs 触媒を加えて反応させることにより、(E)-ベンジル 5-((3aS,4S,6aR)-2,2-ジメチルテトラヒドロチエノ[3,4-d][1,3] ジオキソール-4-イル)-2-ペンテノエート(化合物33)を得る。化合物33のエタノール溶液に、パラジウム炭素 を加え、水素ガス存在下で反応させることにより、ベンジル5-((3aS,4S,6aR)-2,2-ジメチルテトラヒドロチエノ[3,4-d][1,3]ジオキソール-4-イル)ペンタノエート(化合物34)を得る。化合物34の CH2Cl2溶液に三臭化ホウ素を加えて反応させることにより5-((2S,3S,4R)-3,4-ジヒドロキテトラヒドロチオフェン-2-イル)ペンタン酸(化合物35)を得る。化合物35の CH3CN溶液に、塩化チオニルを加えて反応させることにより5-((3aS,4S,6aR)-2-オキシドテトラヒドロチエノ[3,4-d][1,3,2]ジオキサチオール-4-イル)ペンタン酸(化合物36)を得る。
化合物17をMeOHに溶解し触媒量のPd/Cを用いて水素雰囲気化で撹拌することにより2重結合の還元を行う。続いて得られた化合物のエステル部位をCH3CN、H2O混合溶媒下にLiOHを用いて加水分解することによって4-((3aR,6S,7aR)-2-オキソヘキサヒドロ-2H-チオピラノ[3,4-d]オキサゾール-6-イル)ブタン酸 (化合物37)を得る。
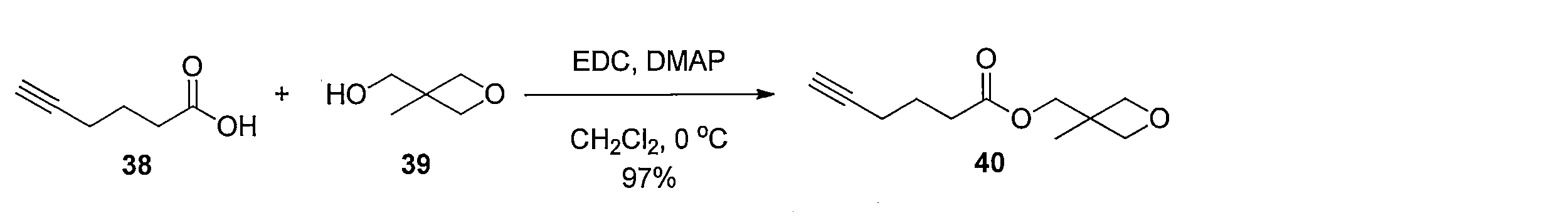
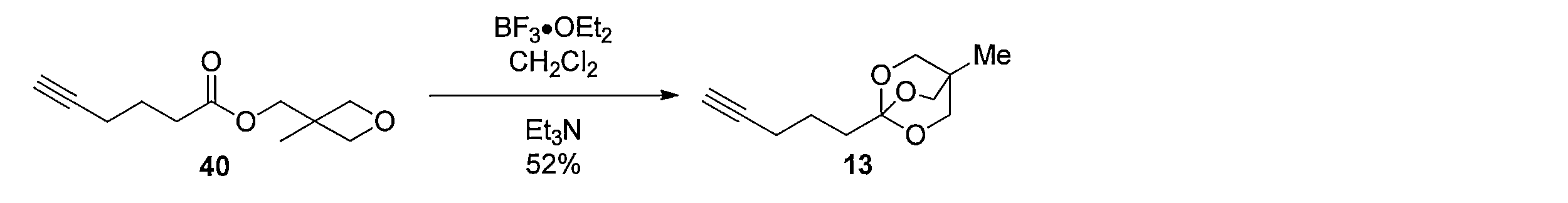
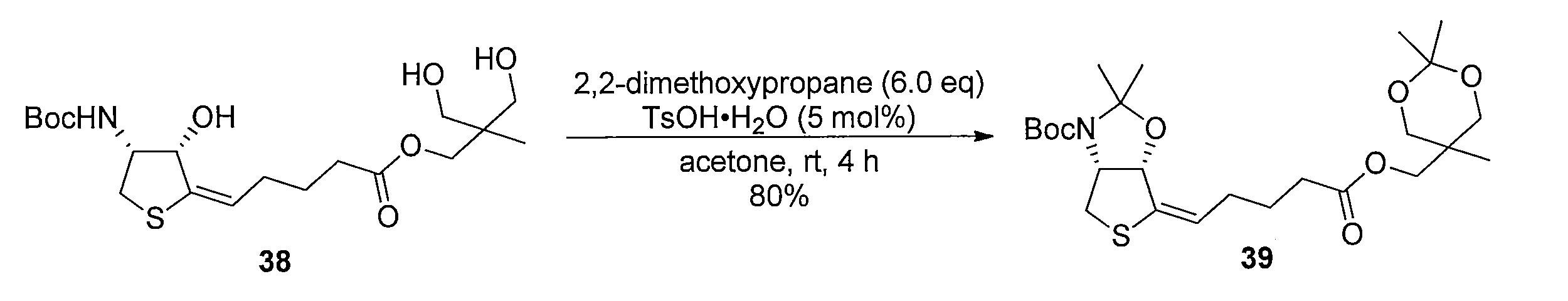
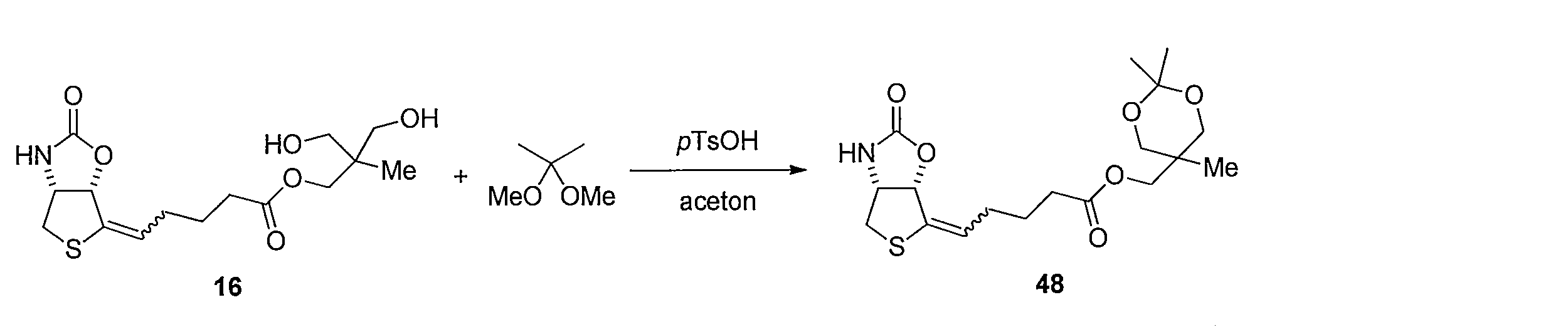
化合物15のアセトニトリル及び水の混合溶液に、フッ化銀を加え、室温で反応させることにより化合物38 を得る。トリオール体38と2,2-ジメトキシプロパンの無水アセトン溶液にp-トルエンスルホン酸一水和物を加え、混合物を室温で攪拌する。トリエチルアミンを加えた後、溶媒を減圧留去し、得られた粗生成物をシリカゲルカラムクロマトグラフィーで精製することで、化合物39を得る。ジアセトニド体39のメタノール溶液にPearlman触媒 (10% パラジウム) を加え、水素ガス (1気圧, 風船) で置換し、室温で反応させることにより、二重結合が還元された化合物40及び41の混合物を得る。この粗生成物をアセトニトリルと水の混合溶媒に溶解した後、2規定水酸化リチウム水溶液を加え、室温で反応させることにより化合物42を得る。カルボン酸42とN-ヒドロキシスクシンイミドのN,N-ジメチルホルムアミド溶液に1-エチル-3-(3-ジメチルアミノプロピル)カルボジイミド塩酸塩を加え、混合物を室温で攪拌して反応させることにより活性エステル体43を得る。得られた43をジオキサンと水の混合溶媒に溶解し、6-アミノヘキサン酸を加え、室温で反応させることにより、化合物44を得る。カルボン酸44のジオキサン溶液に3規定塩酸を加え、混合物を室温で反応させることにより化合物45を得る。アンモニウム塩45のテトラヒドロフラン溶液に炭酸カリウムとカルボニルジイミダゾールを加え、混合物を80℃で反応させ、室温まで冷却した後、2規定水酸化ナトリウム水溶液を加え、室温で2時間反応させ、さらに2規定塩酸で酸性にする (pH 3)ことにより、化合物46を得る。
アンモニウム塩45のメタノール溶液に酢酸ナトリウムと臭化シアンを加え、混合物を室温で攪拌する。2規定水酸化ナトリウム水溶液を加え、室温で攪拌する。水を加え、水層をジエチルエーテルで洗浄した後、2規定塩酸で酸性にする(pH 3)。溶媒を減圧留去した後、ジクロロメタン/メタノール (1:1) の混合溶液を加え、固体をろ過で分離除去する。溶媒を減圧留去し、得られた粗生成物を逆相HPLCで精製することで、化合物47を得る。
本発明のストレプトアビジン変異体は、配列番号2に記載のコアストレプトアビジンのアミノ酸配列において、所定のアミノ酸の変異を有し、野生型ストレプトアビジンと比較して免疫原性が低下していると同時に、天然ビオチン又はビオシチンとの親和性を低減していることを特徴とする。
さらに本発明によれば、本発明のストレプトアビジン変異体に分子プローブを結合させることにより得られる、ストレプトアビジン変異体―分子プローブ結合物、並びにストレプトアビジン変異体―分子プローブ結合物を含む治療剤又は診断剤が提供される。さらに、上記したストレプトアビジン変異体―分子プローブ結合物は、本発明のストレプトアビジン変異体に親和性を有するビオチン改変体で標識した診断用又は治療用物質と組み合わせて、治療又は診断キットとして提供することができる。分子プローブとしては、例えば抗体、ペプチド、核酸、アプタマー等を挙げることができる。
(a)天然ビオチン又はビオシチンとの親和性を低下させたストレプトアビジン変異体、及び;
(b)上記ストレプトアビジン変異体に対して高い親和性を有するビオチン改変体:
を含む、治療又は診断のための試薬キット、並びに、
(a)天然ビオチン又はビオシチンとの親和性を低下させたストレプトアビジン変異体と分子プローブとの結合物、及び
(b)上記ストレプトアビジン変異体に対して高い親和性を有するビオチン改変体で標識した診断用又は治療用物質:
を含む治療又は診断キットが提供される。
(1)10番目のアミノ酸残基のチロシンがセリンに置換している変異:
(2)71番目のアミノ酸残基のチロシンがセリンに置換している変異:
(3)72番目のアミノ酸残基のアルギニンがリジンに置換している変異:
(4)89番目のアミノ酸残基のグルタミン酸がアスパラギン酸に置換している変異:
(5)91番目のアミノ酸残基のアルギニンがリジンに置換している変異:及び
(6)104番目のアミノ酸残基のグルタミン酸がアスパラギンに置換している変異:
の全ての変異を有し、それに加えてさらに
(7)33番目のアミノ酸残基のセリンが他のアミノ酸(例えば、アスパラギン)に置換している変異;及び
(8)116番目のアスパラギン酸が他のアミノ酸(例えば、アスパラギン)に置換している変異
を有するストレプトアビジン変異体、又は、
上記(1)~(6)の全ての変異を有し、それに加えてさらに
(7‘)11番目のアミノ酸残基のアスパラギンが他のアミノ酸(例えば、アスパラギン酸)に置換している変異;
(8’)15番目のアミノ酸残基のセリンが他のアミノ酸(例えば、アスパラギン酸)に置換している変異:
を有するストレプトアビジン変異体が挙げられる。
(1)10番目のアミノ酸残基のチロシンがセリンに置換している変異:
(2)71番目のアミノ酸残基のチロシンがセリンに置換している変異:
(3)72番目のアミノ酸残基のアルギニンがリジンに置換している変異:
(4)89番目のアミノ酸残基のグルタミン酸がアスパラギン酸に置換している変異:
(5)91番目のアミノ酸残基のアルギニンがリジンに置換している変異:
(6)104番目のアミノ酸残基のグルタミン酸がアスパラギンに置換している変異:
(7‘)11番目のアミノ酸残基のアスパラギンが他のアミノ酸(例えば、アスパラギン酸)に置換している変異;及び
(8’)15番目のアミノ酸残基のセリンが他のアミノ酸(例えば、アスパラギン酸)に置換している変異:
の全ての変異を有し、さらに
(9)33番目のアミノ酸残基のセリンが、他のアミノ酸(例えば、アラニン、グルタミン、ロイシン、イソロイシン、ヒスチジン、トレオニン、バリン及びアスパラギン)に置換している変異:
を有するストレプトアビジン変異体を使用することができる。
一般的方法:NMRスペクトルはJEOL JNM-LA500又はECX500スペクトロメータで記録した(1H NMRについては500 MHz、13C NMR については125.65 MHz)。化学シフトは、内部参照としての残存CHCl3 (δ= 7.26 for 1H NMR、δ=77.0 for 13C NMR)に対するδスケールでppmで報告した。ESI質量スペクトルは、Waters-ZQ4000で測定した。カラムクロマトグラフィは、シリカゲルMerk 60 (230-400 mesh ASTM)又はシリカゲル60 N (KANTO CHEMICAL, spherical, neutral, 40-100 μm)を使用して行った。無水テトラヒドロフラン(THF)はKanto Chemical. Co., Inc.から購入するか、またはPh2CO-Naから新たに蒸留した。他の試薬は、特に明記ない限り市販品をそのまま使用した。
1H NMR (CDCl3): δ = 1.32 (s, 3H), 1.47 (s, 3H), 4.02 (d, J= 10 Hz, 1H), 4.08 (dd, J= 10, 3.7 Hz, 1H), 4.58 (d, J= 5.8 Hz, 1H), 4.84 (dd, J= 5.8, 3.7 Hz, 1H), 5.42 (s, 1H)
1H NMR (CDCl3): δ = 1.40 (s, 3H), 1.48 (s, 3H), 4.40 (dd, J= 11, 3.7 Hz, 1H), 4.46 (d, J= 11 Hz, 1H), 4.74 (d, J= 5.8 Hz, 1H), 4.87 (dd, J= 5.8, 3.7 Hz, 1H)
1H NMR (CDCl3): δ = 1.36 (s, 3H), 1.44 (s, 3H), 3.49 (d, J= 13 Hz, 1H), 3.60 (dd, J= 13, 4.6 Hz, 1H), 4.56 (d, J= 4.9 Hz, 1H), 4.81 (dd, J= 4.9, 4.6 Hz, 1H)
1H NMR (CDCl3): δ = 1.31 (s, 3H), 1.50 (s, 3H), 2.05 (t, J= 7.3 Hz, 2H), 2.05 (m, 2H), 2.90 (d, J= 13 Hz, 1H), 3.27 (dd, J= 13, 4.3 Hz, 1H), 4.38 (d, J= 5.5 Hz, 1H), 5.01 (d, J= 10 Hz, 1H), 5.12 (d, J=17 Hz, 1H) , 5.85-5.94 (m, 1H)
化合物7:1H NMR (CDCl3): δ = 1.65-1.74 (m, 1H), 1.89-1.96 (m, 1H), 2.05-2.19 (m, 2H), 2.81 (dd, J= 10, 8.8 Hz, 1H), 3.03 (dd, J= 10, 7.1 Hz, 1H), 3.39-3.45 (m, 1H), 4.10 (t, J= 3.5 Hz, 1H), 4.28-4.33 (m, 1H), 5.00 (d, J= 10 Hz, 1H), 5.06 (d, J=17 Hz, 1H) , 5.75-5.84 (m, 1H)
化合物32:1H NMR (CDCl3): δ = 1.32 (s, 3H), 1.51 (s, 3H), 1.75-1.84 (m, 1H), 1.89-1.97 (m, 1H), 2.15-2.23 (m, 2H), 2.82 (dd, J= 13, 4.0 Hz, 1H), 2.86 (d, J= 12 Hz, 1H), 3.10-3.12 (m, 1H), 4.60 (t, J= 4.3 Hz, 1H), 4.84 (t, J= 5.5 Hz, 1H), 5.00 (d, J= 9.0 Hz, 1H), 5.07 (d, J=16 Hz, 1H) , 5.78-5.87 (m, 1H)
1H NMR (CDCl3): δ = 1.93-2.02. (m, 1H), 2.03-2.10 (m, 1H), 2.31-2.45 (m, 2H), 2.96 (dd, J= 14, 4.3 Hz, 1H), 3.14 (d, J= 14 Hz, 1H), 3.19-3.23 (m, 1H), 5.03 (dd, J= 6.4, 4 Hz, 1H), 5.18 (s, 2H), 5.27 (dd, J= 6.4, 4.3 Hz, 1H), 5.95 (d, J= 15 Hz, 1H), 6.97 (dt, J=15, 7 Hz, 1H) , 7.32-7.36 (m, 2H), 7.37 (d, J= 4.6 Hz, 3H)
1H NMR (CDCl3): δ = 1.50-1.55 (m, 2H), 1.70 (q, J= 7.3 Hz, 2H), 1.74-1.84 (m, 1H), 1.88-1.95 (m, 1H), 2.39 (t, J= 7.4 Hz, 1H), 2.96 (dd, J= 14, 4.3 Hz, 1H), 3.14 (d, J= 14 Hz, 1H), 3.22 (ddd, J= 8.0, 6.7, 4.0 Hz, 1H), 5.05 (dd, J= 6.4, 4.0 Hz, 1H), 5.28 (dd, J= 6.4, 3.7 Hz, 1H)
1H NMR (CDCl3): δ = 1.33 (s, 3H), 1.83-1.89 (m, 2H), 2.04 (s, 1H), 2.27 (td, J= 6.9, 2.9 Hz, 2H), 2.51 (t, J= 7.5 Hz, 2H), 4.17 (s, 2H), 4.38 (d, J= 5.7 Hz, 2H), 4.51 (d, J= 5.7 Hz, 2H)
1H NMR (CDCl3): δ = 0.79 (s, 3H), 1.66-1.72 (m, 2H), 1.77-1.80 (m, 2H), 2.16 (s, 1H), 2.21 (td, J= 6.9, 2.9 Hz, 2H), 3.88 (s, 6H)
1H NMR (CDCl3): δ = 0.79 (s, 3H), 1.68 (s, 3H), 1.70-1.75 (m, 4H), 1.80 (s, 3H), 2.28 (td, J= 7.5, 1.7 Hz, 2H), 2.39 (t, J= 7.4 Hz, 1H), 2.96 (dd, J= 14, 4.3 Hz, 1H), 3.87 (s, 6H), 4.57-4.62 (m, 1H), 5.16 (d, J= 7.5 Hz, 1H)
1H NMR (CD3OD): δ = 0.93 (s, 3H), 1.79 (quin, J= 7.5 Hz, 2H), 2.16-2.31 (m, 2H), 2.40 (t, J= 7.5 Hz, 2H), 3.02 (d, J= 12 Hz, 1H), 3.25 (dd, J= 12, 5.2 Hz, 1H), 3.48 (dd, J= 18, 11 Hz, 4H), 4.03 (s, 2H), 4.64 (t, J= 5.2 Hz, 1H), 5.47 (d, J= 10 Hz, 1H), 5.93 (t, J= 7.5 Hz, 1H)
1H NMR (CD3OD): δ = 0.94 (s, 3H), 1.50-1.58 (m, 2H), 1.67-1.80 (m, 4H), 1.85-1.94 (m, 2H), 2.41 (t, J= 7.2 Hz, 2H), 2.76 (d, J= 13 Hz, 1H), 2.97 (dd, J= 13, 4.5 Hz, 1H), 3.29-3.32 (m, 1H), 3.48 (dd, J= 18, 11 Hz, 4H), 4.03 (s, 2H), 4.56 (dd, J= 6.7, 4.5 Hz, 1H), 5.09 (dd, J= 6.7, 4.0 Hz, 1H)
1H NMR (CD3OD): δ =1.47-1.55 (m, 2H), 1.65-1.74 (m, 4H), 1.85-1.94 (m, 2H), 2.38 (t, J= 7.5 Hz, 2H), 2.76 (d, J= 13 Hz, 1H), 2.98 (dd, J= 13, 4.6 Hz, 1H), 3.29-3.32 (m, 1H), 4.56 (dd, J= 6.9, 4.6 Hz, 1H), 5.08 (dd, J= 6.9, 4.0 Hz, 1H)
1H NMR (CD3OD): δ =1.49-1.63 (m, 2H), 1.63-1.75 (m, 2H), 1.83-1.95 (m, 2H), 2.26 (m, 2H), 3.06 (dd, J= 13, 2.1 Hz, 1H), 3.12-3.16 (m, 1H), 3.50 (dd, J= 13, 2.1 Hz, 1H), 4.60 (dd, J= 8.9, 5.2 Hz, 1H), 4.67 (dd, J= 8.9, 2.1 Hz, 1H)
1H NMR (CD3OD): δ =1.55-1.82 (m, 10.4H), 1.84-1.93 (m, 3.2H), 2.00-2.11 (m, 2H), 2.19-2.31 (m, 5.2H), 2.96 (dd, J= 14, 7.5 Hz, 1H), 3.01 (dd, J= 16, 6.9 Hz, 1H), 3.15 (dd, J= 13, 5.8 Hz, 1.6H),3.23-3.28 (m, 1.6H), 3.48 (d, J= 16 Hz, 1H), 3.60 (dd, J= 14, 1.7 Hz, 1.6H), 4.86-4.91 (m, 2.6H), 4.95 (dd, J= 8.6, 6.3 Hz, 1.6H), 5.08 (dd, J= 8.6, 6.3 Hz, 1H)
1H NMR (CD3OD): δ =1.60-1.80 (m, 8.4H), 1.90-2.18 (m, 4.2H), 2.33-2.39 (m, 4.2H), 3.03-3.10 (m, 2.1H), 3.20 (dd, J= 14, 5.8 Hz, 1H), 3.30-3.40 (m, 1.1H), 3.69 (d, J= 16 Hz, 1.1H), 3.96 (dd, J= 14, 1.2 Hz, 1H), 5.47 (dd, J= 7.4, 5.5 Hz, 1H), 5.53-5.58 (m, 2.1H), 5.73 (dd, J= 7.1, 5.5 Hz, 1.1H)
1H NMR (CD3OD): δ =1.42-1.51 (m, 2H), 1.57-1.72 (m, 3H), 1.75-1.82 (m, 1H), 2.28-2.34 (m, 2H), 2.79 (d, J= 13 Hz, 1H), 2.96 (dd, J= 13, 4.6 Hz, 1H), 3.25-3.28 (m, 1H), 4.48 (dd, J= 8.3, 4.6 Hz, 1H), 4.67 (dd, J= 4.3, 8.3 Hz, 1H)
MS (ESI) m/z 357 (M+H)+
MS: 371.80
1H NMR (CDCl3): δ = 1.31 (s, 3H), 1.49 (s, 3H), 1.83-1.92. (m, 1H), 1.96-2.03 (m, 1H), 2.32-2.38 (m, 2H), 2.83 (dd, J= 13, 4.3 Hz, 1H), 2.87 (d, J= 13 Hz, 1H), 3.06-3.11 (m, 1H), 4.59 (t, J= 5.5 Hz, 1H), 4.84 (t, J= 4.6 Hz, 1H), 5.18 (s, 2H), 5.93 (d, J= 16 Hz, 1H), 7.01 (dt, J=16, 7 Hz, 1H) , 7.32-7.36 (m, 2H), 7.37 (d, J= 4.6 Hz, 3H)
1H NMR (CDCl3): δ = 1.31 (s, 3H), 1.49 (s, 3H), 1.47-1.50 (m, 2H), 1.65-1.75 (m, 3H), 1.80-1.86 (m, 1H), 2.37 (t, J= 7.0 Hz, 2H), 2.80 (dd, J= 13, 3.5 Hz, 1H), 2.85 (d, J= 13 Hz, 1H), 3.06-3.10 (m, 1H), 4.58 (t, J= 4.3 Hz, 1H), 4.88 (t, J= 4.3 Hz, 1H), 5.11 (s, 2H), 7.32-7.37 (m, 5H)
1H NMR (CDCl3): δ = 1.43-1.50 (m, 2H), 1.65-1.75 (m, 3H), 1.80-1.88 (m, 1H), 2.38 (t, J= 7.3 Hz, 2H), 2.81 (t, J= 11 Hz, 1H), 3.03 (dd, J= 11, 7.0 Hz, 1H), 3.38-3.43 (m, 1H), 4.11 (t, J= 3.3 Hz, 1H), 4.31 (td, J= 9.1, 3.3 Hz, 1H)
1H NMR (CDCl3): δ = 1.50-1.74 (m, 12H), 1.85-1.95 (m, 6H), 2.39 (t, J= 7.4 Hz, 6H), 3.08 (dd, J= 14, 5.8 Hz, 1H), 3.14 (dd, J= 14, 2.1 Hz, 1H), 3.31-3.37 (m, 4H), 3.64 (br, 1H), 4.27-4.31 (m, 2H), 5.19 (dd, J= 5.5, 4.3 Hz, 1H), 5.33-5.36 (m, 1H), 5.36 (dd, J= 5.5, 4.3 Hz, 2H), 5.54-5.57 (m, 2H)
一般的方法
核磁気共鳴 (NMR) スペクトルは、JEOL ECX500 (1H NMR: 500MHz)、またはJEOL ECS400(1H NMR: 400MHz) スペクトロメータを用いて測定した。化学シフトは、内部参照として重溶媒中の残存溶媒ピークに対する値としてppmで記載した (CDCl3:δ= 7.26 ppm, CD3OD:δ= 3.31 ppm, D2O: δ= 4.79 ppm)。低分解能質量スペクトル (LHMS) は、Waters ZQ4000スペクトロメータによりESI-MSを用いて測定した。カラムクロマトグラフィーはシリカゲル Merk 60 (230-400 mesh ASTM) を用いて行った。反応は薄層クロマトグラフィー (TLC)、あるいは低分解能質量分析 (LRMS) によって追跡した。
試薬は、Aldrich、東京化成工業株式会社 (TCI)、関東化学株式会社 (Kanto)、和光純薬工業株式会社、渡辺化学工業株式会社から購入した。全ての試薬及び溶媒は、特に明記が無い限り市販品をそのまま使用した。
1H NMR (500 MHz, CD3OD) δ:0.91 (s, 3H), 1.45 (s, 9H), 1.75 (quint., 2H, J = 7.4 Hz), 2.05 (q, 2H, J = 7.4 Hz), 2.38, (t, 2H, J = 7.5 Hz), 3.02 (dd, 1H, J = 9.2, 10.3 Hz), 3.08 (1H, dd, J = 6.3, 10.3 Hz), 3.45 (dd, 4H, J = 14.9, 11.5 Hz), 3.98-4.01 (m, 1H), 4.00 (2H, s), 4.39 (d, 1H, J = 4.0 Hz), 5.66 (t, 1H, J = 6.9 Hz); LRMS (ESI): m/z 442 [M+Na]+.
1H NMR (500 MHz, CD3OD) δ: 0.86 (s, 3H), 1.35 (s, 3H), 1.43 (s, 3H), 1.48 (s, 5H), 1.47-1.53 (m, 12 H), 1.62 (s, 3H), 1.76 (quint., 2H, J = 7.5 Hz), 2.11 (q, 2H, J = 7.5 Hz), 2.39 (t, 2H, J = 7.5 Hz), 3.01 (td, 1H, J = 11.5, 7.4 Hz), 3.37 (m, 1H), 3.65 (s, 4H), 4.14 (dd, 2H, J = 13.8, 10.9 Hz), 4.50 (sext., 1H, J = 5.7 Hz), 4.96 (dd, 1H, J = 8.0, 5.7 Hz), 5.75 (t, 1H, J = 7.5 Hz); LRMS (ESI): m/z 522 [M+Na]+.
41:1H NMR (500 MHz, CD3OD) δ: 0.91 (s, 3H), 1.44-1.50 (m, 14H), 1.60 (s, 3H), 1.63-1.72 (m, 3H), 1.84 (sext., 1H, J = 6.9 Hz), 2.37 (t, 2H, J = 7.5 Hz), 2.81 (t, 1H, J = 10.9 Hz), 3.02 (tt, 1H, J = 12.6, 6.3 Hz), 3.23-3.29 (m, 1H), 3.45 (dd, 4H, J = 14.9, 10.9 Hz), 4.00 (s, 2H), (ddd, 1H, J = 18.9, 12.6, 6.3 Hz), 4.59-4.64 (m, 1H); LRMS (ESI): m/z 484 [M+Na]+.
42:1H NMR (500 MHz, CD3OD) δ: 1.43-1.51 (m, 14H), 1.60 (s, 3H), 1.61-1.72 (m, 3H), 1.84 (sext., 1H, J = 6.9 Hz), 2.30 (t, 2H, J = 7.5 Hz), 2.81 (t, 2H, J = 10.9 Hz), 3.03 (tt, 1H, J = 12.6, 6.3 Hz), 3.22-3.29 (m, 1H), (ddd, 1H, J = 18.9, 12.6, 6.3 Hz), 4.59-4.64 (m, 1H); LRMS (ESI): m/z 382 [M+Na]+.
1H NMR (500 MHz, CD3OD) δ: 1.35-1.40 (m, 3H), 1.42-1.54 (m, 16H), 1.60 (s, 3H), 1.61-1.72 (m, 4H), 1.84 (sext., 1H, J = 6.9 Hz), 2.19 (t, 2H, J = 7.5 Hz), 2.30 (t, 2H, J = 7.5 Hz), 2.80 (t, 2H, J = 10.9), 3.02 (tt, 1H, 1H, J = 12.6, 6.3 Hz),3.17 (t, 2H, J = 6.9 Hz), 3.22-3.29 (m, 1H), (ddd, 1H, J = 18.9, 12.6, 6.3 Hz), 4.58-4.64 (m, 1H); LRMS (ESI): m/z 495 [M+Na]+.
1H NMR (500 MHz, D2O) δ: 1.27-1.37 (m, 4H), 1.51 (quint., 2H, J = 7.5 Hz), 1.55-1.64 (m, 5H), 1.76-1.82 (m, 1H), 2.23 (t, 2H, J = 7.5 Hz), 2.38 (t, 2H, J = 7.5 Hz), 2.93 (t, 1H, J = 10.9 Hz), 3.14-3.18 (m, 3H), 3.58 (ddd, 1H, J = 9.2, 6.3, 2.9 Hz), 3.85 (ddd, 1H, J = 10.9, 7.5, 3.5 Hz), 4.39 (t, 1H, J = 2.9 Hz); LRMS (ESI): m/z 334 [M+H]+.
1H NMR (400 MHz, CD3OD) δ: 1.35-1.40 (m, 2H), 1.41-1.55 (m, 4H), 1.58-1.77 (m, 5H), 1.86 (sext., 1H, J = 6.3 Hz), 2.20 (t, 2H, J = 7.2 Hz), 2.30 (t, 2H, J = 7.2 Hz), 2.73 (d, 1H, J = 13 Hz), 2.95 (dd, 1H, J = 13.0, 4.5 Hz), 3.17 (t, 2H, J = 7.2 Hz), 3.28 (dd, 1H, J = 6.7, 3.6 Hz), 4.53 (dd, 1H, J = 6.7, 4.5 Hz), 5.05 (dd, 1H, J = 6.7, 3.6 Hz); LRMS (ESI): m/z 381 [M+Na]+.
1H NMR (500 MHz, D2O) δ: 1.31-1.38 (m, 2H), 1.41-1.49 (m, 2H), 1.53 (quint., 2H, J = 7.5 Hz), 1.58-1.68 (m, 4H), 1.69-1.76 (m, 2H), 2.26 (t, 2H, J = 7.5 Hz), 2.39 (t, 2H, J = 7.5 Hz), 3.19 (q, 2H, J = 6.9 Hz), 3.49 (ddd, 1H, J = 9.2, 6.3, 2. Hz), 4.94 (dd, 1H, J = 6.9, 5.2), 5.55 (dd, 1H, J = 7.0, 4.0 Hz); LRMS (ESI): m/z 358 [M+H]+.
1H NMR (CD3OD): δ = 0.89 (s, 3H), 1.37 (s, 3H), 1.45 (s, 3H), 1.76-1.83 (m, 2H), 1.85-1.94 (m, 2H), 2.41 (t, J= 7.2 Hz, 2H), 3.02 (d, J= 12 Hz, 1H), 3.24 (dd, J= 12, 5.5 Hz, 1H), 3.68 (s, 4H), 4.17 (s, 2H), 4.64 (m, 1H), 5.47 (d, J= 6.9 Hz, 1H), 5.92 (t, J= 7.3 Hz, 1H)
1H NMR (CD3OD): δ =1.47-1.55 (m, 2H), 1.65-1.74 (m, 2H), 1.85-1.94 (m, 2H), 2.38 (t, J= 7.5 Hz, 2H), 2.76 (d, J= 13 Hz, 1H), 2.98 (dd, J= 13, 4.6 Hz, 1H), 3.29-3.32 (m, 1H), 4.56 (dd, J= 6.9, 4.6 Hz, 1H), 5.08 (dd, J= 6.9, 4.0 Hz, 1H)
1H NMR (CD3OD): δ = 0.93 (s, 3H), 1.80-1.90 (m, 2H), 2.34 (t, J= 7.8 Hz, 2H), 2.40 (t, J= 7.5 Hz, 2H), 2.66 (dd, J= 13, 11 Hz, 1H), 2.99 (dd, J= 13, 4.1 Hz, 1H), 3.48 (dd, J= 18, 11 Hz, 4H), 4.03 (s, 2H), 4.64 (m, 1H), 4.97 (dd, J= 7.3, 4.6 Hz, 1H), 5.92 (d, J= 4.6 Hz, 1H)
1H NMR (CD3OD): δ = 1.08 (s, 3H), 1.82-1.91 (m, 2H), 1.95-2.05 (m, 4H), 2.56 (t, J= 7.8 Hz, 2H), 2.76 (dd, J= 14, 5.0 Hz, 1H), 3.00 (dd, J= 14, 9.2 Hz, 1H), 3.09-3.16 (m, 1H), 3.48 (dd, J= 15, 11 Hz, 4H), 4.18 (s, 2H), 4.24-4.31 (m, 1H), 4.96-5.00 (m, 1H)
1H NMR (CD3OD): δ =1.79-1.88 (m, 2H), 1.95-2.05 (m, 4H), 2.53 (t, J= 7.6 Hz, 2H), 2.76 (dd, J= 14, 5.1 Hz, 1H), 2.99 (dd, J= 14, 9.0 Hz, 1H), 3.07-3.13 (m, 1H), 4.24-4.30 (m, 1H), 4.97-5.00 (m, 1H)
(1)発現ベクターの構築
野生型コアストレプトアビジンをコードする遺伝子の塩基配列を配列表の配列番号1に示す。また、本発明では、低免疫原性(改変体)ストレプトアビジンとして国際公開WO2010/09455に記載されているmcSA314(本明細書中、LISA314WT又はLISA314とも称する)を使用した。mcSA314は、配列番号2に記載のコアストレプトアビジンのアミノ酸配列において以下の変異の全てを有する、ストレプトアビジン変異体である。
(1)10番目のアミノ酸残基のチロシンがセリンに置換している変異:
(2)71番目のアミノ酸残基のチロシンがセリンに置換している変異:
(3)72番目のアミノ酸残基のアルギニンがリジンに置換している変異:
(4)89番目のアミノ酸残基のグルタミン酸がアスパラギン酸に置換している変異:
(5)91番目のアミノ酸残基のアルギニンがリジンに置換している変異:及び
(6)104番目のアミノ酸残基のグルタミン酸がアスパラギンに置換している変異:
具体的には、上記の配列を鋳型にし、5’端側にHindIIIサイト、3’端側にEcoRIサイトをPCRにより付加する下記のプライマー1及び2を用い、PCR後、制限酵素HindIII、EcoRIにて処理を行った。
プライマー1: GCTCTTCAAAGCTTTGGCCGAAGCTGGTATCACTG (配列番号13)
プライマー2:CTCGAGGAATTCTTAGCTAGCAGCAGAAGGCTTAAC (配列番号14)
各バリアント作製に用いたオリゴDNAは5’側が15塩基オーバーラップするように、PrimerSTAR Mutagenesis Basal Kit(タカラバイオ)の説明書に従い設計した。下記のプライマーを使用し、 LISA314が挿入されたpCold TF ベクターを鋳型とし、SiteーDirected Mutagenesis法により塩基配列の置換によるコドン配列の変更を行いアミノ酸配列の変換を行った。その後、制限酵素DpnIにて鋳型プラスミドを切断し、大腸菌の形質転換を行った。
S45N Fw: TATGAAAACGCCGTGGGTAATGCGGAA (配列番号15)
S45N Rv: CACGGCGTTTTCATAGGTGCCGGTCAG (配列番号16)
D128N Fw: CGTTGGCGGTGCTGATGCTCGTATCAACAC (配列番号17)
D128N Rv: GGTGCTGATGCTAAGATCAACACTCAGTGG (配列番号18)
D128Nとは、配列番号2に記載のコアストレプトアビジンのアミノ酸配列において116番目のアスパラギン酸(D)がアスパラギン(N)に置換している変異を意味する。
(1)10番目のアミノ酸残基のチロシンがセリンに置換している変異:
(2)71番目のアミノ酸残基のチロシンがセリンに置換している変異:
(3)72番目のアミノ酸残基のアルギニンがリジンに置換している変異:
(4)89番目のアミノ酸残基のグルタミン酸がアスパラギン酸に置換している変異:
(5)91番目のアミノ酸残基のアルギニンがリジンに置換している変異:
(6)104番目のアミノ酸残基のグルタミン酸がアスパラギンに置換している変異:
(7)33番目のアミノ酸残基のセリンがアスパラギンに置換している変異;及び
(8)116番目のアスパラギン酸がアスパラギンに置換している変異
を有する変異体ストレプトアビジン(本書中、LISA314 N45 N128とも称する)を産生する大腸菌を作成した。配列番号2に記載のアミノ酸配列において上記(1)~(8)の変異を有するアミノ酸配列を配列番号3に示す。
変異体ストレプトアビジンの遺伝子配列を組み込んだpPAL7発現ベクターを大腸菌BL21(BIO-RAD社)に常法に従いトランスフェクションを行った。タンパク質の発現は以下のように実施した。すなわち、大腸菌培養液の細胞密度がOD(600nm)0.5-0.7となるまで37度にて培養を行い、最終濃度1mMになるようにIPTG(isopropyl-β-D-thiogalactopyanoside)を添加し、タンパク質発現を誘導し、10℃~30℃好ましくは16℃にて24時間以上の培養を行った。培養の後、菌体を遠心分離により細胞を集め、タンパク質精製までマイナス20℃で保存した。
組換えタンパク質(LISA314-V11)の粗精製は、改変ズブチリジンとズブチリジンプロドメインとの結合性を利用したアフィニティークロマトグラフィーを行った。具体的には、改変ズブチリジンをSperflow 6% agarose ビーズに固定したカラム(Bio-Scale Mini Profinity eXact Cartridge, BIO-RAD社)を使用した。
大腸菌の調製は細胞溶解液として10mM sodiumn phosphate, pH7.2 - 5.6、10xBugBuser reagent (Novagen)、核酸分解酵素(Benzonase) を添加し細胞の溶解を行った。溶解は室温で行い、溶解した液は35,000xg、30分間の遠心分離をおこなった。遠心分離後上清を総可溶性タンパク質とした。
10カラムボリュームのバッファーでカラムを平衡化した。次に、大腸菌の総可用性タンパク質を2ml/minの流速でカラムへアプライした。カラムへのアプライ後10カラムボリュームの洗浄バッファー1でカラムを洗浄した。次に10カラムボリュームの洗浄バッファー2でカラムの洗浄を行った。その後、1カラムボリュームの溶出バッファーを注入し30分間室温でインキュベーションを行った。インキュベーションの後、溶出バッファー3カラムボリュームでタンパク質の溶出を行った。その後、5カラムボリュームのカラム再生バッファーでカラムの再生を行った。最後に5カラムボリュームのカラム保存バッファーでカラムを洗浄し精製を終了した。
精製の結果を図1に示す。
以降、バッファーのpHについては、改変体ストレプトアビジンはpH7.0とする。
粗精製された組換えタンパク質は、セラミックハイドロキシアパタイトカラムによる精製の準備として10,000 MWCOの限外ろ過膜を使用し遠心ろ過にて濃縮をした。濃縮後、脱塩カラム用い、5 mM リン酸ナトリム溶液にバッファーを置換した。セラミックハイドロキシアパタイトカラムはCHT2-1(BIO-RAD社)を使用し、すべての作業の流速は2ml/minで行った。初めに10カラムボリュームの5mMリン酸ナトリムでカラムの平衡化を行った。次にバッファー置換された粗精製サンプルをアプライしカラムへ吸着させた。洗浄を6カラムボリューム行った後、5mM リン酸ナトリウム、500mM 塩化ナトリムバッファーでタンパク質の溶出を行った。
ELISA用プレートH(住友ベークライト)に精製された変異体タンパク質を5μg/mL、100μl、4℃オーバーナイトの条件で固相化を行った。固相化の後、SuperBlock Bloking Buffer(サーモサイエンティフィック社)を用いて200μl/ウエル、5分間のブロッキングを行った。その後、10μM、100μl/ウエルで実施例1に記載の化合物11(即ち、(3aS,4S,6aR)-2-オキソテトラヒドロチエノ[3,4-d][1,3]ジオキソール-4-イル)ペンタン酸)を1時間、室温で反応させた。洗浄の後、12.5nM、100μl/ウエル、1時間、室温でBiotin-HRP標識体を反応させた。洗浄後、100μl/ウエル、室温、30分で反応させた。発色の度合いを比較した結果(図2)、化合物11と標識体が競合している様子が確認された。
(1)LISA314バリアントの発現ベクターの調製
各バリアント作製に用いたオリゴDNAは5’側が15塩基オーバーラップするように、PrimerSTAR Mutagenesis Basal Kit(タカラバイオ)の説明書に従い設計した。下記のプライマーを使用し、 LISA314が挿入されたpCold TF ベクターを鋳型とし、SiteーDirected Mutagenesis法により塩基配列の置換によるコドン配列の変更を行いアミノ酸配列の変換を行った。その後、制限酵素DpnIにて鋳型プラスミドを切断し、大腸菌の形質転換を行った。
プライマー:
LISA314 V21 Fw: TGGAGCgatCAGCTGGGCgatACCTTT(配列番号19)
LISA314 V21 Rv: CAGCTGatcGCTCCAGGTGCCGGTAAT (配列番号20)
(1)10番目のアミノ酸残基のチロシンがセリンに置換している変異:
(2)71番目のアミノ酸残基のチロシンがセリンに置換している変異:
(3)72番目のアミノ酸残基のアルギニンがリジンに置換している変異:
(4)89番目のアミノ酸残基のグルタミン酸がアスパラギン酸に置換している変異:
(5)91番目のアミノ酸残基のアルギニンがリジンに置換している変異:
(6)104番目のアミノ酸残基のグルタミン酸がアスパラギンに置換している変異:
(7)11番目のアミノ酸残基のアスパラギンがアスパラギン酸に置換している変異;
(8)15番目のアミノ酸残基のセリンがアスパラギン酸に置換している変異:
を有する変異体ストレプトアビジンであり、このアミノ酸配列を配列番号4に示す。
各ミュータントタンパク質の発現は pCold TFベクター(タカラバイオ)のマニュアルに従い実施した。具体的には、発現ベクターを大腸菌BL21(タカラバイオ)に常法に従いトランスフォーメーションを行い、大腸菌培養液の細胞密度がOD(600nm)= 0.5-0.7となるまで37度で培養を行い、その後15度で1時間静置し最終濃度1mMになるようにIPTG(isopropyl-β-D-thiogalactopyanoside)を添加し、タンパク質発現を誘導し、15度で24時間の培養を行った。培養の後、菌体を遠心分離により細胞を集め、タンパク質精製までマイナス20℃で保存した。
組換えタンパク質の粗精製は、6xHis-tagを使用したアフィニティークロマトグラフィーを行った。具体的にはNi Sepharose 6 Fast Flow(GEヘルスケア)を担体として使用した。
大腸菌の調製は細胞溶解液としてB-PER(Thermo SCIETIFIC)、Lisonase Bioprocessing ReagentをB-PER1mLあたり3mL添加し細胞の溶解を行った。溶解は室温で行い、溶解した液は27,000xg、20分間の遠心分離を行った。遠心分離後、上清を総可溶性タンパク質とした。
10カラムボリュームの結合/洗浄バッファー(20mM Tris-NaCl、500mM NaCl、pH8)でカラムの平衡化およびサンプルアプライ後のカラムの洗浄を行った。また、3カラムボリュームの溶出バッファー(20mM Tris-NaCl、500mM NaCl、400mM イミダゾール、pH8)で結合タンパク質の溶出を行った。
5μgの粗精製タンパク質に対し、5UのHRV 3C Proteaseを使用しタグの切断を行った。4℃で24時間反応後、変性バッファー(20mM Tris-NaCl、6Mグアニジン塩酸塩、500mM NaCl、pH8)で変性を行い、Ni Sepharose 6 Fast Flow を使用したアフィニティークロマトグラフィーを行った。
(1)結晶化条件
LISA314―ビオチン
シッティングドロップ蒸気拡散法を用いて, 20 ℃で結晶化を行った(図3)。蛋白質溶液は, 9 mg/ml LISA314, 15 mM tris-HCl pH7.5, 150 mM NaClとした。ビオチンは, LISA314精製途中に過剰量添加した。結晶化母液(60 μl)には, 0.2 M Ammonium Sulfate, 0.1 M Sodium acetate trihydrate pH5.2, 22% (w/v) Polyethylene glycol 4000を用い, 結晶化内液は蛋白質溶液0.5 μl, 結晶化母液0.5 μlを混合したものとした。
シッティングドロップ蒸気拡散法を用いて, 20 ℃で結晶化を行った。蛋白質溶液は, 10 mg/ml LISA314-V21, 20 mM tris-HCl pH7.5, 250 mM NaClとした。Iminobiotintail(実施例1の化合物29、以下に構造を示す)は, LISA314-V21精製途中に過剰量添加した。
結晶構造の解析結果を図4及び図5に示す。
ストレプトアビジンのビオチンと水素結合を作っている23番目(配列番号2に記載のコアストレプトアビジンのアミノ酸配列において11番目)のアミノ酸Asn23をAlaに置き換えたN23Aの変異型ストレプトアビジンは、ビオチンとの結合力が大きく低下することが報告されている。また、この変異型ストレプトアビジンのビオチンと複合体を形成した結晶構造も報告されている(PDB ID、1N43。1N43の立体構造およびN23Aの近傍を、我々のLISA314の結晶構造を比較すると、LISA314ではAsn23は近傍のGly26と水素結合を形成し相互作用している(図4右上のLISA314のN23とG26を結ぶ点線、白抜き矢印で示されている)。一方、1N43では、Ala23とGly26にはこれに相当する水素結合は存在していない(図4左下の1N43の黒矢印で示された部分)。このため、LISA314と比較して1N43におけるN23Aの変異はN23からS27にかけてのloop構造を不安定化すると考えられ、N23Dの変異を施すことにより、この23番目(配列番号2に記載のコアストレプトアビジンのアミノ酸配列において11番目)のアミノ酸とGly26との水素結合が維持され、N23からS27にかけてのloop構造が安定するのではないかと考えた。実際、図4右下に示すようにN23Dの変異を施したLISA314-V21の結晶構造では、この水素結合が保存されている(白抜き矢印で示された点線)。変異型ストレプトアビジンLISA314-V21はビオチンではなくイミノビオチンとの相互作用が強くなることを期待して作成された。そのため、N23Dの変異に加えてS27Dの変異を施しており、LISA314-V21のAsp27はイミノビオチンのN原子と相互作用している。
(1)発現ベクターの構築(LISA314 V21;N23D、S27など)
Biacoreによるアフィニティー解析に用いるタンパク質は pET-21a(+)ベクター(ミリポア・メルク社) により発現させ、封入体を巻き戻すことでリコンビナントタンパク質を調整した。具体的には、 pET-21a(+)ベクター を制限酵素BamHIとXhoIを用いて直さかを行った。次に、In-Fusion HD Cloning Kit(クローンテック社)のマニュアルに従い直鎖化を実施したベクターに合うPCRプライマーを設計し、前述の各バリアントLISA314 V21発現ベクター(pCold TF)をテンプレートとしてPCRを実施した。増幅された配列はアガロースゲル電気泳動にて目的のバンドを切り出し、DNAを抽出して精製を行った。直鎖化されたベクターと精製されたPCR産物とをIn-Fusion HD Cloning Kitを使用しライゲーションを行った。
プライマー:
For pET21a(+) Fw: AATGGGTCGCGGATCCGCCGAAGCAGGTATTACCGGCAC(配列番号21)
For pET21a(+) Rv: GGTGGTGGTGCTCGAGGCTGGCCGCGCTCGGTTTAACTTTG(配列番号22)
LISA314 V21の各種バリアント作製に用いたオリゴDNAは5’側が15塩基オーバーラップするように、PrimerSTAR Mutagenesis Basal Kit(タカラバイオ)の説明書に従い設計した。以下のプライマーを使用し、上述のLISA314 V21が挿入されたベクターを鋳型とし、Site-Directed Mutagenesis法により塩基配列の置換によるコドン配列の変更を行いアミノ酸配列の変換を行った。その後、制限酵素DpnIにて鋳型プラスミドを切断し、大腸菌の形質転換を行った。
S45A Fw: TATGAAgcaGCCGTGGGTAATGCGGAA(配列番号23)
S45A Rv: CACGGCtgcTTCATAGGTGCCGGTCAG(配列番号24)
S45Q Fw: TATGAAcagGCCGTGGGTAATGCGGAA(配列番号25)
S45Q Rw: CACGGCctgTTCATAGGTGCCGGTCAG(配列番号26)
S45L Fw: TATGAActgGCCGTGGGTAATGCGGAA(配列番号27)
S45L Rv: CACGGCcagTTCATAGGTGCCGGTCAG(配列番号28)
S45I Fw: TATGAAatcGCCGTGGGTAATGCGGAA(配列番号29)
S45I Rw: CACGGCgatTTCATAGGTGCCGGTCAG(配列番号30)
S45H Fw: TATGAAcatGCCGTGGGTAATGCGGAA(配列番号31)
S45H Rv: CACGGCatgTTCATAGGTGCCGGTCAG(配列番号32)
S45T Fw: TATGAAaccGCCGTGGGTAATGCGGAA(配列番号33)
S45T Rw: CACGGCggtTTCATAGGTGCCGGTCAG(配列番号34)
S45V Fw: TATGAAgtgGCCGTGGGTAATGCGGAA(配列番号35)
S45V Rv: CACGGCcacTTCATAGGTGCCGGTCAG(配列番号36)
S45N Fw: TATGAAAACGCCGTGGGTAATGCGGAA(配列番号37)
S45N Rv: CACGGCGTTTTCATAGGTGCCGGTCAG(配列番号38)
各変異体タンパク質の発現は 目的のバリアント発現遺伝子が挿入されたpET-21a(+)ベクターを大腸菌BL21(DE3)( ミリポア・メルク社)に常法に従いトランスフォーメーションを行い、大腸菌培養液の細胞密度がOD(600nm)= 0.5-0.8となるまで37度で培養を行い、最終濃度1mMになるようにIPTG(isopropyl-β-D-thiogalactopyanoside)を添加し、タンパク質発現を誘導した。4-16時間で培養の後、菌体を遠心分離により細胞を集め、タンパク質精製までマイナス20℃で保存した。
大腸菌の調製は細胞溶解液としてB-PER(Thermo SCIETIFIC)、Lisonase Bioprocessing ReagentをB-PER1mLあたり3mL添加し細胞の溶解を行った。溶解は室温で行い、溶解した液は27,000xg、20分間の遠心分離を行った。遠心分離後、上清を破棄しペレットを封入体として回収した。回収した封入体はMilliQ水で10倍希釈したB-PER10mLにて再懸濁し27,000xg、20分間の遠心分離により再回収する洗浄作業を3回行った。最後に界面活性剤の除去のためにミリQにより再懸濁を行い遠心分離により回収を行った。回収した封入体は小分け分注をしマイナス80℃にて凍結保存した。
封入体の巻戻しは凍結保存した封入体を変性バッファー(20mM Tris-HCl、6Mグアニジン塩酸塩、200mM NaCl、pH1.5)で可溶化した。ビオチンの除去を行うために100倍のボリュームの透析バッファー(変性バッファーと同じ)に対して4時間、2回を実施した。その後、可溶化した液の吸光度280nmによるタンパク質濃度が40-50mg/mLとなるように濃度を透析バッファーで調節した。巻戻しは、希釈法を用いた。具体的にはスターラーで撹拌している50mLの希釈バッファー( 20mM Tris-HCl、200mM NaCl、pH8.0)に濃度調節したタンパク質溶液100マイクロリットルを滴下し希釈することで巻戻しを行った。
希釈法により巻き戻したタンパク質は、cOmplete His-Tag Purification Resin(ロシュ社)を用いてアフィニティークロマトグラフィーを実施した。これらの精製タンパク質を濃縮しゲル濾過クロマトグラフィーにより4量体画分の分取を実施した。
巻戻しタンパク質の精製の一例を図6に示す。
アフィニティー解析にはBiacore T100を用いた。具体的には、ゲル濾過クロマトグラフィーにより分取してきたタンパク質を Sensor Chip NTAを使用し固定化した。ランニングバッファーは、0.5% Tween20、HBS-P+を使用した。ニッケルのNTAへの固定化、リガンドのキャプチャーは附属のテンプレートプログラムにより実施した。
センサーチップへのリガンドの固定化量は、マストランスポートリミテーションを抑制するために1608RU~8042RUの範囲に収まるようにした。アナライトにはビオシチンおよび実施例1で合成した化合物29(構造を以下に示す)を使用した。なお、ビオシチンは、ビオチンの主たる存在形態である。
Claims (10)
- 配列番号3から12の何れかに記載のアミノ酸配列を含む、ストレプトアビジン変異体。
- 請求項4に記載のストレプトアビジン変異体をコードするDNA。
- 請求項4に記載のストレプトアビジン変異体に分子プローブを結合させることにより得られる、ストレプトアビジン変異体-分子プローブ結合物。
- 請求項6に記載のストレプトアビジン変異体-分子プローブ結合物を含む、治療剤又は体内あるいは体外診断剤。
- (a)請求項6に記載のストレプトアビジン変異体―分子プローブ結合物;及び(b)請求項1から3の何れかに記載の化合物で標識した体内あるいは体外診断用又は治療用物質:を含む治療又は体内あるいは体外診断キット。
- (a)天然ビオチン又はビオシチンとの親和性を低下させたストレプトアビジン変異体、及び;
(b)上記ストレプトアビジン変異体に対して高い親和性を有するビオチン改変体:
を含む、治療又は体内あるいは体外診断のための試薬キット。 - (a)天然ビオチン又はビオシチンとの親和性を低下させたストレプトアビジン変異体と分子プローブとの結合物、及び
(b)上記ストレプトアビジン変異体に対して高い親和性を有するビオチン改変体で標識した体内あるいは体外診断用又は治療用物質:
を含む治療又は体内あるいは体外診断キット。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015501452A JPWO2014129446A1 (ja) | 2013-02-20 | 2014-02-18 | ビオチン改変体、ストレプトアビジン変異体およびそれらの利用 |
| US14/768,916 US9670255B2 (en) | 2013-02-20 | 2014-02-18 | Modified biotin, mutant streptavidin, and use thereof |
| CN201480009625.2A CN104995196B (zh) | 2013-02-20 | 2014-02-18 | 生物素改变体、链霉亲和素突变体和它们的用途 |
| EP14753647.8A EP2960243B1 (en) | 2013-02-20 | 2014-02-18 | Biotin alterant, streptavidin mutant, and uses thereof |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013031038A JP6178586B2 (ja) | 2013-02-20 | 2013-02-20 | ビオチン改変体、ストレプトアビジン変異体およびそれらの利用 |
| JP2013-031038 | 2013-02-20 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2014129446A1 true WO2014129446A1 (ja) | 2014-08-28 |
Family
ID=51391236
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2014/053734 WO2014129446A1 (ja) | 2013-02-20 | 2014-02-18 | ビオチン改変体、ストレプトアビジン変異体およびそれらの利用 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US9670255B2 (ja) |
| EP (1) | EP2960243B1 (ja) |
| JP (2) | JP6178586B2 (ja) |
| CN (1) | CN104995196B (ja) |
| WO (1) | WO2014129446A1 (ja) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015125820A1 (ja) * | 2014-02-18 | 2015-08-27 | サヴィッド・セラピューティックス株式会社 | ビオチン改変体、ストレプトアビジン変異体およびそれらの利用 |
| WO2019230905A1 (ja) | 2018-05-30 | 2019-12-05 | 国立大学法人 東京大学 | ハロゲン化したビオチン改変二量体およびその利用 |
| WO2020032165A1 (ja) | 2018-08-08 | 2020-02-13 | 国立大学法人 東京大学 | ビオチン改変二量体とフタロシアニン染料とのコンジュゲート |
| WO2021210573A1 (ja) | 2020-04-14 | 2021-10-21 | 国立大学法人 東京大学 | ビオチン改変二量体およびその利用 |
| WO2021215534A1 (ja) | 2020-04-24 | 2021-10-28 | 国立大学法人 東京大学 | デュオカルマイシン誘導体及びその利用 |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11442066B2 (en) | 2017-02-17 | 2022-09-13 | Mitsui Chemicals, Inc | Method for identifying drug-discovery target protein for development of antibody drug, and method for producing antibody against target protein |
| JPWO2022080486A1 (ja) | 2020-10-16 | 2022-04-21 | ||
| CN114478725B (zh) * | 2022-01-19 | 2023-07-07 | 大连博格林生物科技有限公司 | 一种链霉亲和素突变体及其制备方法和应用 |
Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS58154508A (ja) * | 1982-02-19 | 1983-09-14 | ユニリ−バ−・ナ−ムロ−ゼ・ベンノ−トシヤ−プ | 皮膚処理用組成物 |
| US5608060A (en) | 1992-06-09 | 1997-03-04 | Neorx Corporation | Biotinidase-resistant biotin-DOTA conjugates |
| JPH09506594A (ja) * | 1993-12-07 | 1997-06-30 | ネオルクス コーポレーション | プレターゲティング方法及び化合物 |
| JPH1028589A (ja) * | 1996-04-01 | 1998-02-03 | Boehringer Mannheim Gmbh | 組換え不活性コア・ストレプトアビジン変異体 |
| JP2001514524A (ja) * | 1997-03-14 | 2001-09-11 | トラスティーズ オブ ボストン ユニバーシティー | マルチフレイバーストレプトアビジン |
| JP2008530565A (ja) * | 2005-02-15 | 2008-08-07 | エイディーライフ インコーポレイティッド | 誤って折り畳まれたタンパク質およびプリオンを検出する方法 |
| WO2010009455A2 (en) | 2008-07-18 | 2010-01-21 | Allen Jones | Wind powered energy amplification system and method |
| WO2010095455A1 (ja) | 2009-02-20 | 2010-08-26 | 国立大学法人 東京大学 | 低免疫原性ストレプトアビジンおよびその利用 |
| WO2012023579A1 (ja) * | 2010-08-19 | 2012-02-23 | 分子動力学抗体創薬技術研究組合 | ストレプトアビジンの製造方法 |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5976535A (en) | 1992-06-09 | 1999-11-02 | Neorx Corporation | Pretargeting protocols for the enhanced localization of cytotoxins to target sites and cytotoxic combinations useful therefore |
| US6015897A (en) | 1993-12-07 | 2000-01-18 | Neorx Corporation | Biotinamido-n-methylglycyl-seryl-o-succinamido-benzyl dota |
| US7249061B1 (en) | 1997-03-14 | 2007-07-24 | Kabushiki Kaisha Toshiba | Method of electronic commerce including receiving an acceptance signal indicating a change in a transaction available period based on a time adjustment day |
| US6391571B1 (en) | 1997-04-01 | 2002-05-21 | Roche Diagnostics Gmbh | Recombinant inactive avidin mutants |
-
2013
- 2013-02-20 JP JP2013031038A patent/JP6178586B2/ja active Active
-
2014
- 2014-02-18 US US14/768,916 patent/US9670255B2/en active Active
- 2014-02-18 JP JP2015501452A patent/JPWO2014129446A1/ja active Pending
- 2014-02-18 WO PCT/JP2014/053734 patent/WO2014129446A1/ja active Application Filing
- 2014-02-18 CN CN201480009625.2A patent/CN104995196B/zh active Active
- 2014-02-18 EP EP14753647.8A patent/EP2960243B1/en active Active
Patent Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS58154508A (ja) * | 1982-02-19 | 1983-09-14 | ユニリ−バ−・ナ−ムロ−ゼ・ベンノ−トシヤ−プ | 皮膚処理用組成物 |
| US5608060A (en) | 1992-06-09 | 1997-03-04 | Neorx Corporation | Biotinidase-resistant biotin-DOTA conjugates |
| JPH09506594A (ja) * | 1993-12-07 | 1997-06-30 | ネオルクス コーポレーション | プレターゲティング方法及び化合物 |
| JPH1028589A (ja) * | 1996-04-01 | 1998-02-03 | Boehringer Mannheim Gmbh | 組換え不活性コア・ストレプトアビジン変異体 |
| JP2001514524A (ja) * | 1997-03-14 | 2001-09-11 | トラスティーズ オブ ボストン ユニバーシティー | マルチフレイバーストレプトアビジン |
| JP2008530565A (ja) * | 2005-02-15 | 2008-08-07 | エイディーライフ インコーポレイティッド | 誤って折り畳まれたタンパク質およびプリオンを検出する方法 |
| WO2010009455A2 (en) | 2008-07-18 | 2010-01-21 | Allen Jones | Wind powered energy amplification system and method |
| WO2010095455A1 (ja) | 2009-02-20 | 2010-08-26 | 国立大学法人 東京大学 | 低免疫原性ストレプトアビジンおよびその利用 |
| WO2012023579A1 (ja) * | 2010-08-19 | 2012-02-23 | 分子動力学抗体創薬技術研究組合 | ストレプトアビジンの製造方法 |
Non-Patent Citations (12)
| Title |
|---|
| DATABASE CAPLUS 1993, MIYAMOTO, S. ET AL.: "ABOSLUTE AND RELATIVE BINDING FREE ENERGY CALCULATIONS OF THE INTERACTION OF BIOTIN AND ITS ANALOGS WITH STREPTAVIDIN USING MOLECULAR DYNAMICS/FREE ENERGY PERTURBATION APPROACHES, PROTEINS: STRUCTURE, FUNCTION, AND GENETICS", XP055300024, retrieved from STN Database accession no. 1994:72808 * |
| DATABASE FILE REGISTRY 16 November 1984 (1984-11-16), XP055300038, retrieved from STN Database accession no. 39871-28-8 * |
| DATABASE REGISTRY 14 April 2009 (2009-04-14), XP055300019, retrieved from STN Database accession no. 1134348-37-0 * |
| DATABASE REGISTRY 16 November 1984 (1984-11-16), XP055300029, retrieved from STN Database accession no. 66513-70-0 * |
| DATABASE REGISTRY 16 November 1984 (1984-11-16), XP055300034, retrieved from STN Database accession no. 76985-52-9 * |
| GREEN, ADV. PROTEIN CHEM., vol. 29, 1975, pages 85 - 133 |
| GREEN, METHODS ENZYMOL., vol. 184, 1990, pages 51 - 67 |
| HNATOWICH, J. NUCL. MED., vol. 28, 1987, pages 1294 - 1302 |
| MIZUSHIMA ET AL., NUCLEIC ACIDS RES., vol. 18, 1990, pages 5322 |
| MULLIGAN ET AL., NATURE, vol. 277, 1979, pages 108 |
| PAGANELLI, CANCER RES., vol. 51, 1991, pages 5960 - 5966 |
| RYUICHI YASUGI ET AL.: "Biotin", IWANAMI SEIBUTSUGAKU JITEN, 10 April 1997 (1997-04-10), pages 1133, XP008182030 * |
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015125820A1 (ja) * | 2014-02-18 | 2015-08-27 | サヴィッド・セラピューティックス株式会社 | ビオチン改変体、ストレプトアビジン変異体およびそれらの利用 |
| US11161884B2 (en) | 2014-02-18 | 2021-11-02 | Savid Therapeutics Inc. | Modified biotin, streptavidin mutant, and usage of them |
| US11286285B2 (en) | 2014-02-18 | 2022-03-29 | Savid Therapeutics Inc. | Modified biotin, streptavidin mutant, and usage of them |
| WO2019230905A1 (ja) | 2018-05-30 | 2019-12-05 | 国立大学法人 東京大学 | ハロゲン化したビオチン改変二量体およびその利用 |
| JPWO2019230905A1 (ja) * | 2018-05-30 | 2021-06-24 | 国立大学法人 東京大学 | ハロゲン化したビオチン改変二量体およびその利用 |
| WO2020032165A1 (ja) | 2018-08-08 | 2020-02-13 | 国立大学法人 東京大学 | ビオチン改変二量体とフタロシアニン染料とのコンジュゲート |
| WO2021210573A1 (ja) | 2020-04-14 | 2021-10-21 | 国立大学法人 東京大学 | ビオチン改変二量体およびその利用 |
| WO2021215534A1 (ja) | 2020-04-24 | 2021-10-28 | 国立大学法人 東京大学 | デュオカルマイシン誘導体及びその利用 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2016027006A (ja) | 2016-02-18 |
| JP6178586B2 (ja) | 2017-08-09 |
| CN104995196A (zh) | 2015-10-21 |
| CN104995196B (zh) | 2018-10-12 |
| EP2960243A4 (en) | 2016-08-03 |
| US20160137704A1 (en) | 2016-05-19 |
| EP2960243A1 (en) | 2015-12-30 |
| EP2960243B1 (en) | 2019-03-27 |
| JPWO2014129446A1 (ja) | 2017-02-02 |
| US9670255B2 (en) | 2017-06-06 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2014129446A1 (ja) | ビオチン改変体、ストレプトアビジン変異体およびそれらの利用 | |
| US11161884B2 (en) | Modified biotin, streptavidin mutant, and usage of them | |
| JP7413999B2 (ja) | 抗体に対する親和性物質、切断性部分および反応性基を有する化合物またはその塩 | |
| US20220088212A1 (en) | C-terminal lysine conjugated immunoglobulins | |
| JP2013501766A (ja) | 固体基材の官能化 | |
| US20190100518A1 (en) | Indole structure-selective crosslinking agent and composite in which same is used | |
| US11866457B2 (en) | Clearing agent | |
| Watanabe et al. | Gram-Scale Synthesis of Site-Specific Antibody-Drug Conjugates Using AJICAP Second-Generation Technology | |
| WO2022191283A1 (ja) | 化合物またはその塩、およびそれらにより得られる抗体 | |
| US20220348681A1 (en) | Fused protein of an antibody which recognizes cancer-cells and a streptavidin mutant |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 14753647 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2015501452 Country of ref document: JP Kind code of ref document: A |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 14768916 Country of ref document: US |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2014753647 Country of ref document: EP |