WO2010004139A1 - Nouveaux derives de benzothiadiazines cycloalkylees, leur procede de preparation et les compositions pharmaceutiques qui les contiennent - Google Patents
Nouveaux derives de benzothiadiazines cycloalkylees, leur procede de preparation et les compositions pharmaceutiques qui les contiennent Download PDFInfo
- Publication number
- WO2010004139A1 WO2010004139A1 PCT/FR2009/000841 FR2009000841W WO2010004139A1 WO 2010004139 A1 WO2010004139 A1 WO 2010004139A1 FR 2009000841 W FR2009000841 W FR 2009000841W WO 2010004139 A1 WO2010004139 A1 WO 2010004139A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- benzothiadiazine
- dioxide
- cyclopropyl
- dihydro
- stage
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
- 0 *c(c(*)c1*)c(*)c(NC=N2)c1S2(=O)=O Chemical compound *c(c(*)c1*)c(*)c(NC=N2)c1S2(=O)=O 0.000 description 2
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D285/00—Heterocyclic compounds containing rings having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by groups C07D275/00 - C07D283/00
- C07D285/15—Six-membered rings
- C07D285/16—Thiadiazines; Hydrogenated thiadiazines
- C07D285/18—1,2,4-Thiadiazines; Hydrogenated 1,2,4-thiadiazines
- C07D285/20—1,2,4-Thiadiazines; Hydrogenated 1,2,4-thiadiazines condensed with carbocyclic rings or ring systems
- C07D285/22—1,2,4-Thiadiazines; Hydrogenated 1,2,4-thiadiazines condensed with carbocyclic rings or ring systems condensed with one six-membered ring
- C07D285/24—1,2,4-Thiadiazines; Hydrogenated 1,2,4-thiadiazines condensed with carbocyclic rings or ring systems condensed with one six-membered ring with oxygen atoms directly attached to the ring sulfur atom
- C07D285/26—1,2,4-Thiadiazines; Hydrogenated 1,2,4-thiadiazines condensed with carbocyclic rings or ring systems condensed with one six-membered ring with oxygen atoms directly attached to the ring sulfur atom substituted in position 6 or 7 by sulfamoyl or substituted sulfamoyl radicals
- C07D285/28—1,2,4-Thiadiazines; Hydrogenated 1,2,4-thiadiazines condensed with carbocyclic rings or ring systems condensed with one six-membered ring with oxygen atoms directly attached to the ring sulfur atom substituted in position 6 or 7 by sulfamoyl or substituted sulfamoyl radicals with only hydrogen atoms or radicals containing only hydrogen and carbon atoms, directly attached in position 3
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/08—Antiepileptics; Anticonvulsants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
- A61P25/16—Anti-Parkinson drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/18—Antipsychotics, i.e. neuroleptics; Drugs for mania or schizophrenia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/24—Antidepressants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
Definitions
- the present invention relates to novel cycloalkylated benzothiadiazine derivatives, process for their preparation, pharmaceutical compositions containing them and their use as positive allosteric modulators of AMPA receptors.
- the AMPA receptor (“ ⁇ -amino-3-hydroxy-5-methyl-4-isoxazole-propionic acid”) appears to be the most involved in the phenomena of physiological neuronal excitability and in particular in those involved. in the memorization process. For example, learning has been shown to be associated with increased binding of AMPA to its receptor in the hippocampus, one of the brain areas essential to mnemocognitive processes. Similarly, nootropic agents such as aniracetam have been described as positively modulating the AMPA receptors of neuronal cells (J. Neurochemistry, 1992, 58, 1199-1204). In the literature, compounds of benzamide structure have been described to possess this same mechanism of action and to improve memory performance (Synapse, 1993, 15, 326-329). The compound BA 74, in particular, is the most active among these new pharmacological agents.
- EP 692 484 discloses a benzothiadiazine derivative having AMPA current facilitating activity and WO 99/42456 discloses, inter alia, certain benzothiadiazine derivatives as AMPA receptor modulators.
- a (C 3 -C 8 ) cycloalkyl group which is unsubstituted or substituted by one or more groups, which may be identical or different, chosen from linear or branched (C 1 -C 6 ) alkyl which is unsubstituted or substituted by one or more atoms of halogen; linear or branched (C 1 -C 6 ) alkoxy; hydroxy; and amino unsubstituted or substituted with one or two linear or branched (C 1 -C 6 ) alkyl groups; 1 or cycloalkyl (C 3 -C 8) alkyl (C 1 -C 6) linear or branched unsubstituted or substituted on the cyclic moiety by one or more groups, identical or different, chosen from alkyl (C 1 -C 6 ) linear or branched unsubstituted or substituted by one or more halogen atoms; linear or branched (C 1 -C 6 ) alkoxy;
- R 1 , R 2 , R 3 and R 4 which are identical or different, each represent a hydrogen or halogen atom or a nitro group; cyano; hydroxy; thio; linear or branched (C 1 -C 6 ) alkyl unsubstituted or substituted by one or more halogen atoms; linear or branched cyanoalkyl (C 1 -C 6 ); linear or branched hydroxy (C 1 -C 6 ) alkyl; linear or branched (C 1 -C 6 ) alkoxy unsubstituted or substituted by one or more halogen atoms; linear or branched alkylthio (C 1 -C 6 ); carboxy; linear or branched alkoxycarbonyl (C 1 -C e); aryloxycarbonyl; linear or branched (C 1 -C 6 ) acyl; amino unsubstituted or substituted with one or two alkyl groups (C 1 -(
- Aryl means the phenyl group which is unsubstituted or substituted with one or more groups, which may be identical or different, chosen from linear or branched (C 1 -C 6 ) alkyl which is unsubstituted or substituted by one or more atoms of halogen; linear or branched (C 1 -C 6 ) alkoxy; hydroxy; and amino unsubstituted or substituted with one or two linear or branched (C 1 -C 6 ) alkyl groups.
- pharmaceutically acceptable acids mention may be made, without limitation, of hydrochloric, hydrobromic, sulfuric, phosphoric, acetic, trifluoroacetic, lactic, pyruvic, malonic, succinic, glutaric, fumaric, tartaric, maleic, citric, ascorbic, oxalic and methanesulphonic acids. , benzenesulfonic, camphoric.
- pharmaceutically acceptable bases mention may be made, without limitation, of sodium hydroxide, potassium hydroxide, triethylamine and tertbutylamine.
- Rc are groups are cycloalkyl groups (C 3 -C 8), more particularly cyclopropyl.
- the cyclopropyl group may be substituted by a linear or branched (C 1 -C 0 ) alkyl group and, more particularly, the methyl group.
- Rc are groups are cycloalkyl groups (C 3 -C 8) alkyl (C 1 -C 6) linear or branched, more particularly cyclopropylmethyl group.
- the group R 1 preferably represents a hydrogen atom or a halogen atom, and more particularly the fluorine atom.
- the group R 2 preferably represents a hydrogen atom; a halogen atom, and more particularly the fluorine, chlorine or bromine atom; the cyano group; the carboxy group; or the linear or branched (C 1 -C 6 ) alkyl group, and more particularly the methyl group. . .
- the group R 3 preferably represents a hydrogen atom; a halogen atom, and more particularly the fluorine, chlorine or bromine atom; the linear or branched (C 1 -C 6 ) alkyl group, and more particularly the methyl group.
- the group R 4 represents a hydrogen atom or a halogen atom, and more particularly the fluorine, chlorine or bromine atom.
- the compounds for which Rc y represents a cyclopropyl group and two of the groups R 1 , R 2 , R 3 or R 4 on the benzene ring represent a hydrogen atom, while the two other substituents, which are identical or different, represent an atom of halogen, such as the fluorine, chlorine or bromine atom.
- the preferred compounds according to the invention are:
- the invention also extends to the process for preparing the compounds of formula (I) from the compound of formula (II):
- R 5 represents a linear or branched (Ci-C 6 ) alkyl group
- the present invention also relates to the process for preparing the compounds of formula (I), characterized in that a compound of formula (V) is used as starting material:
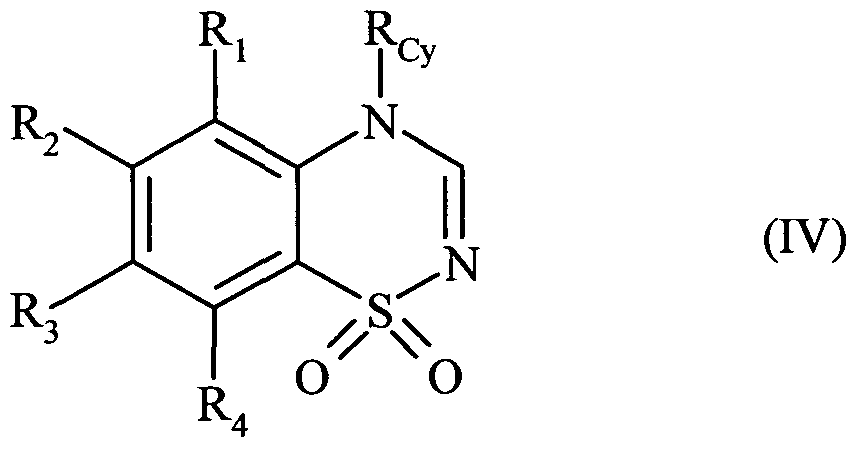
- the compounds of formula (IV) are new and are also part of the invention as synthesis intermediates of the compounds of formula (I).
- the compounds of formula (I) according to the invention have AMPA receptor activating properties which make them useful in the treatment or the prevention of mnemocognitive disorders associated with age, with anxiety or depressive syndromes, with progressive neurodegenerative diseases, with Alzheimer's disease, Parkinson's disease, Pick's disease, Huntington's disease, Korsakoff's disease, schizophrenia, the sequelae of acute neurodegenerative diseases, frontal and subcortical sequelae of ischemia and sequelae of epilepsy.
- the invention also extends to pharmaceutical compositions containing as active ingredient at least one compound of formula (I) with one or more inert, non-toxic and suitable excipients.
- pharmaceutical compositions according to the invention mention may be made more particularly of those which are suitable for oral, parenteral (intravenous or subcutaneous), nasal administration, single or coated tablets, sublingual tablets, capsules, lozenges, suppositories, creams, ointments, dermal gels, injectables, and oral suspensions.
- the useful dosage is adaptable according to the nature and severity of the condition, the route of administration and the age and weight of the patient. This dosage varies from 0.01 to 1000 mg per day in one or more doses.
- the starting materials used are known products or prepared according to known preparations.
- the expected product is obtained from 2-fluoro-5-methylaniline according to the process described in Step A of Example 1. Jusion point: 118-120 ° C.
- the expected product is obtained according to the method described (heating time of 72 hours) in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 3 hours) in stage C of Example 1. Jusion point: 192-195 ° C.
- the expected product is obtained from 4-chloro-2,5-difluoroaniline according to the process described in Step A of Example 1. Point of addition: 154-157 ° C
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 2 hours) in Stage C of Example 1. • 205-206 ° C.
- the expected product is obtained according to the process described in Step D of Example 1. Pressure point: 170-171 ° C.
- the expected product is obtained from 2,5-difluoroaniline according to the process described in Stage A of Example 1.
- MPP deJusiQn 135-137 ° C
- the expected product is obtained according to the method described (heating time of 96 hours) in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 24 hours at 130 ° C.) in Stage C of Example 1. Mp: 170-172 ° C.
- the expected product is obtained according to the process described in Step D of Example 1. Binding point: 163-164 ° C.
- the expected product is obtained from 5-chloro-2-fluoroaniline according to the process described in Step A of Example 1. Mp: 135-136 ° C
- the expected product is obtained according to the process described in Step D of Example 1. Melting point: 159-161 ° C.
- the expected product is obtained from 2,4-difluoroaniline according to the process described in Step A of Example 1. Melting point: 155-157 ° C.
- the expected product is obtained according to the process described (heating time of 10 hours at 130 ° C.) in stage C of Example 1. Melting point: 199-202 ° C.
- the expected product is obtained according to the process described in Stage D of Example 1. Melting point: 164-165 ° C.
- the expected product is obtained from 4-chloro-2-fluoroaniline according to the process described in Step A of Example 1. Melting point: 104 ° -106 ° C.
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described in Stage D of Example 1. Melting point: 174-176 ° C.
- the expected product is obtained from 2-fluoro-5-trifluoromethylaniline according to the process described in Step A of Example 1. Melting point: 128-130 ° C.
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 5 hours at 130 ° C.) in Stage C of Example 1. Melting point: 160 ° -162 ° C.
- Stage D 4-cyclopropyl-7-trifluoromethyl-S, 4-dihydro-2H-1,2,4-benzothiadiazine 1,1-dioxide
- the expected product is obtained from 2-fluoroaniline according to the process described in Step A of Example 1. Melting point: 160 ° -162 ° C.
- the expected product is obtained according to the process described (heating time of 96 hours) in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 5 hours at 130 ° C.) in Stage C of Example 1. Melting point: 191-194 ° C.
- the expected product is obtained according to the process described in Step D of Example 1. Jams ion: 165-166 ° C.
- the expected product is obtained from 5-cyano-2-fluoroaniline according to the process described in Step A of Example 1. Melting point: 195-196 ° C. 5-cyano-2-cyclopropylaminobenzessesulfonamide
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 3 hours at 130 ° C.) in stage C of Example 1. Jusion point: 268-270 ° C.
- the expected product is obtained according to the process described in Step D of Example 1. Melting point: 259-261 ° C.
- Step A 4-bromo-2-fluoro-5-trifluoromethylbenzenesulfonamide
- the expected product is obtained from 4-bromo-2-fluoro-5-trifluoromethylaniline according to the process described in Step A of Example 1.
- the expected product is obtained according to the process described (heating time of 3 hours at 130 ° C.) in stage C of Example 1. Mp. Decision: 204-206 ° C.
- the expected product is obtained according to the process described in Step D of Example 1. Melting point - 186-189 ° C.
- Step A 4-bromo-3-chloro-2-fluorobenzenesulfonamide
- the expected product is obtained from 4-bromo-3-chloro-2-fluoroaniline according to the process described in Step A of Example 1.
- Stage B 4-bromo-3-chloro-2-cyclopropylaminobenzenesulfonamide
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described in Stage D of Example 1. Melting point: 128-130 ° C.
- the expected product is obtained from 2-fluoro-3-trifluoromethylaniline according to the process described in Step A of Example 1. Melting point: 112-114 ° C.
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 5 hours at 130 ° C.) in stage C of Example 1. Melting point: 180 ° -182 ° C.
- the expected product is obtained from 2-chloro-4,6-difluoroaniline according to the process described in Step A of Example 1. Jusion point: 116-120 ° C.
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 3 hours at 130 ° C.) in stage C of Example 1. Melting point: 252-255 ° C.
- the expected product is obtained according to the process described in Step D of Example 1. Point of Jusion: 190-192 ° C.
- the expected product is obtained from 2-chloro-6-fluoro-3-methylaniline according to the process described in Step A of Example 1.
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 24 hours at 130 ° C.) in Stage C of Example 1. Melting point: 218-223 ° C.
- the expected product is obtained according to the process described in Stage D of Example 1. Melting point: 230 ° -232 ° C.
- the expected product is obtained from 4-cyano-2-fluoroaniline according to the process described in Step A of Example 1. Melting point: 149-152 ° C.
- the expected product is obtained according to the method described (heating time of 24 hours at 130 ° C.) in stage C of Example 1. Sugaring point: 273-276 ° C.
- the expected product is obtained according to the process described in Step D of Example 1. Melting temperature: 178-180 ° C.
- the expected product is obtained from 2-bromo-4,6-difluoroaniline according to the process described in Step A of Example 1. Melting point: 122-124 ° C.
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 3 hours at 130 ° C.) in Step C of Example 1. Melting point: 270 ° -273 ° C. ⁇ D; 8-bromo-4-cyclopropyl-6-fluoro-3,4-dihydro-2H-1,2,4-benzothiadiazine
- the expected product is obtained according to the process described in Step D of Example 1. PoiM of Jusion: 197-199 ° C.
- the expected product is obtained from 2-fluoro-6-trifluoromethylaniline according to the process described in Step A of Example 1. Melting point: 114-118 ° C.
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 10 hours at 130 ° C.) in stage C of Example 1. Jis ion point: 195-197 ° C.
- the expected product is obtained from 3-chloro-2-fluoroaniline according to the process described in Step A of Example 1. Deflection: 149-153 ° C.
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 24 hours at 130 ° C.) in stage C of Example 1. Point of Jk? ion: 159-160 ° C. . . . . .
- the expected product is obtained from 2-bromo-4-chloro-6-fluoroaniline according to the process described in Step A of Example 1. MMe Point: 122-126 ° C
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the method described (heating time of 3 hours) in Stage C of Example 1.
- the expected product is obtained according to the process described in Step D of Example 1. Point of addition - 177-180 ° C.
- the expected product is obtained from 2,3-difluoroaniline according to the process described in Step A of Example 1. Point of addition: 151-153 ° C.
- the expected product is obtained according to the process described (heating time of 48 hours) in Stage C of Example 1. Point of fusion: 151-152 ° C.
- the expected product is obtained according to the process described in Step D of Example 1. Starting point: 161 ° -163 ° C.
- the expected product is obtained from 4-bromo-2-fluoro-5-methylaniline according to the process described in Step A of Example 1. Melting point: 124 ° -125 ° C.
- the expected product is obtained according to the process described in Stage B of Example 1.
- Step C 6-bromo-4-cyclopropyl-7-methyl-4R-1,2,4-benzothiadiazine 1,1-dioxide
- the expected product is obtained according to the process described in Stage D of Example 1. Melting point: 199-200 ° C.
- the expected product is obtained from 3,4-dichloro-2-fluoroaniline according to the process described in Step A of Example 1.
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 2 hours at 130 ° C.) in stage C of Example 1. ⁇ jiqn point: 183-185 ° C.
- the expected product is obtained from 2-bromo-6-fluoroaniline according to the process described in Step A of Example 1. Point of addition: 185-187 ° C.
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 1.5 hours) in Stage C of Example 1.
- the expected product is obtained according to the process described in Stage D of Example 1. Melting point: 189-191 ° C.
- the expected product is obtained according to the method described (heating time of 40 hours) in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 3 hours at 130 ° C.) in Stage C of Example 1.
- PpJM of Jusion 160 ° -163 ° C.
- the expected product is obtained from 2,3-difluoro-4-methylaniline according to the process described in Step A of Example 1. Melting point: 171 ° -173 ° C.
- the expected product is obtained according to the process described (heating time of 24 hours at 130 ° C.) in Stage C of Example 1.
- the expected product is obtained according to the process described in Stage D of Example 1. Melting point: 135-138 ° C.
- the expected product is obtained from 2-chloro-3,6-difluoroaniline according to the process described in Step A of Example 1. Melting point: 175-178 ° C.
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 24 hours at 130 ° C.) in Stage C of Example 1. Melting point: 260 ° -263 ° C. Stage D: 8-chloro-4-cyclopropyl-7-fluoro-3,4-dihydro-2H-1,2,4-benzothiadiazine 1,1-dioxide
- the expected product is obtained from 2-fluoro-4-iodoaniline according to the process described in Step A of Example 1.
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 24 hours at 130 ° C.) in stage C of Example 1. Dip point: 304 ° -307 ° C.
- the expected product is obtained from commercial 2,6-difluorobenzenesulfonamide according to the process described in Step B of Example 1.
- the expected product is obtained according to the method described (heating time of 24 hours) in Stage C of Example 5. Melting point: 156-157 ° C.
- the expected product is obtained according to the process described in Step D of Example 1. Point of addition: 177-179 ° C.
- the expected product is obtained from 2,4-dibromo-6-fluoroaniline according to the process described in Step A of Example 1. Melting point: 153-157 ° C.
- the expected product is obtained according to the process described in Step C of Example 1. Melting point: 254-256 ° C.
- the expected product is obtained according to the process described in Stage D of Example 1. Melting point: 203-205 ° C.
- the expected product is obtained from 3-chloro-2,4-difluoroaniline according to the process described in Step A of Example 1.
- PpM deJ ⁇ siQn 128-132 ° C.
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described in Step D of Example 1. Melting point: 141-143 ° C.
- the expected product is obtained from 2-chloro-6-fluoroaniline according to the process described in Step A of Example 1. Melting point: 187-190 ° C.
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 2 hours at 130 ° C.) in Stage C of Example 1. Melting point: 207-209 ° C.
- Step A 4-bromo-2-fluoro-6-trifluoromethylbenzenesulfonamide
- the expected product is obtained from 4-bromo-2-fluoro-6-trifluoromethylaniline according to the process described in Step A of Example 1. Judage Point: 133-135 ° C.
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 6 hours) in Stage C of Example 1. Melting point: 253-254 ° C.
- the expected product is obtained from 4-bromo-2,5-difluoroaniline according to the process described in Step A of Example 1. Melting point: 159-163 ° C.
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 24 hours) in Stage C of Example 1. Melting point: 218-219 ° C.
- Stage D 6-bromo-4-cyclopropyl-7-fluoro-S, 4-dihydro-2H-1,2,4-benzothiadiazine 1,1-dioxide
- the expected product is obtained according to the process described in Stage D of Example 1. Melting point: 163-165 ° C.
- the expected product is obtained from commercial 4-bromo-2-fluorobenzenesulfonamide according to the process described in Step B of Example 1.
- Stage B 6-bromo-4-cyclopropyl-4H-1,2,4-benzothiadiazine 1,1-dioxide
- the expected product is obtained according to the process described (heating time of 24 hours at 130 ° C.) in Stage C of Example 1. Melting point: 268-271 ° C.
- the expected product is obtained according to the process described in Step D of Example 1. Point of addition: 180 ° -181 ° C.
- the expected product is obtained from 6-chloro-2-fluoro-3-methylaniline according to the process described in Step A of Example 1. Binding point: 174-176 ° C.
- the expected product is obtained according to the method described (heating time of 48 hours) in Stage B of Example 1.
- the expected product is obtained according to the process described in Step D of Example 1. Melting point: 215-217 ° C.
- the expected product is obtained from 2-fluoro-4-methylaniline according to the process described in Step A of Example 1. Melting point: 136-137 ° C.
- the expected product is obtained according to the method described (heating time of 24 hours) in Stage B of Example 1.
- the expected product is obtained according to the process described in Step C of Example 1. Demon point: 224-226 ° C.
- the expected product is obtained from 2,4,6-trifluoroaniline according to the process described in Step A of Example 1. Melting point: 102 ° -106 ° C.
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 24 hours) in Stage C of Example 1. Melting point: 167-168 ° C.
- the expected product is obtained according to the process described in Step D of Example 1. Melting point: 161 ° -164 ° C.
- the expected product is obtained from 2,3,4-trifluoroaniline according to the process described in Step A of Example 1. Mp: 111-114 ° C
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 6 hours) in Step C of Example 1. Melting point - 182-184 ° C.
- the expected product is obtained according to the process described in Step D of Example 1. Jusion point: 160 ° -162 ° C.
- the expected product is obtained from 5-bromo-2-fluoroaniline according to the process described in Step A of Example 1. Point Aejis ion: 149-151 ° C
- the expected product is obtained according to the process described (heating time of 5 hours at 130 ° C.) in stage C of Example 1. Point of formation: 242-244 ° C.
- the expected product is obtained according to the process described in Step D of Example 1. Melting point: 178 ° -179 ° C.
- 2-Chloro-5-nitroaniline (15 g) is dissolved in a mixture of glacial acetic acid (160 mL) and concentrated HCl (40 mL). To this solution cooled on an ice-bath and salt (-5 ° C.) is added dropwise and with stirring an aqueous solution of NaNO 2 (8 g in 20 ml). At the end of the addition, this solution is mixed slowly with stirring in suspension A. After stirring for 15 minutes, the suspension is poured onto ice (400 g). The precipitate formed is collected by filtration, washed with water and immediately redissolved in dioxane (15O mL).
- the solution obtained is added gradually with stirring to a concentrated aqueous solution of ammonia (300 mL) previously cooled in an ice bath. After stirring for 30 minutes, the organic solvent and a part of the ammonia are removed by evaporation under vacuum.
- the solution / aqueous suspension obtained is adjusted to neutral pH by addition of 6N HCl.
- precipitate formed is collected by filtration and washed with water. It is suspended in water (200 mL) and added with 10% NaOH to a clearly alkaline pH. The suspension is heated to promote dissolution of the title product. The persistent insoluble material is removed by hot filtration.
- the cooled filtrate is adjusted to neutral or slightly acidic pH by addition of 6N HCl.
- the precipitate is collected on a filter, washed with water and dried. Jusion point: 180-183 ° C
- the expected product is obtained from 4,5-dichloro-2-fluoroaniline according to the process described in Steps A and B of Example 1 with the addition of cyclobutylamine in step B.
- the expected product is obtained according to the process described (heating time of 24 hours) in Stage C of Example 1.
- PdM Jmion 238-240 ° C.
- the expected product is obtained according to the process described in Step D of Example 1. Jusion Point: 161-163 ° C.
- the expected product is obtained from 2-chloro-5-nitroaniline according to the process described in Steps A, B and C of Example 41 with the addition of cyclobutylamine in step B.
- the expected product is obtained according to the process described in Step A of Example 42. Melting point: 278-280 ° C.
- reaction medium (30 mL). After stirring for 30 minutes at room temperature, the reaction medium is treated with water (150 ml) and the precipitate obtained is collected by filtration, washed with water and dried.
- the expected product is obtained from 4-chloro-2-fluoroaniline according to the process described in Steps A and B of Example 1 with the addition of cyclobutylamine in step B.
- the expected product is obtained according to the process described (heating time of 6 hours at 130 ° C.) in stage C of Example 1. ⁇ sion: 224-226 ° C.
- the expected product is obtained from 4-cyclobutyl-7-nitro-4H-1,2,4-benzothiadiazine 1,1-dioxide (prepared in Step A of Example 44) according to the process described in Step D of Example 1.
- Step A 4,5-dichloro-2-cyclopentylaminobenzenesulfonamide
- the expected product is obtained from 4,5-dichloro-2-fluoroaniline according to the process described in Steps A and B of Example 1 with the addition of cyclopentylamine in step B.
- the expected product is obtained according to the process described (heating time of 72 hours at 140 ° C.) in stage C of Example 5. Melting point: 189-191 ° C.
- the expected product is obtained according to the process described in Stage D of Example 1. Melting point: 221-224 ° C.
- the expected product is obtained from 5-chloro-2-fluoroaniline according to the process described in Steps A and B of Example 1 with the addition of cyclopentylamine in step B. 7-chloro-4-cyclopentyl-4H-1,2,4-benzothiadiazine 1,1-dioxide
- the expected product is obtained according to the process described (heating time 96 hours) in Step C of Example 5. Melting point: 218-220 ° C.
- the expected product is obtained according to the process described in Step D of Example 1. Melting point: 193-194 ° C.
- Step A 4-chloro-2-cyclopentylaminobenzenesulfonamide
- the expected product is obtained from 4-chloro-2-fluoroaniline according to the process described in Steps A and B of Example 1 with the addition of cyclopentylamine in step B.
- the expected product is obtained according to the process described in Step C of Example 5. Melting point: 170-172 ° C.
- the expected product is obtained from 4,5-dichloro-2-fluoroaniline according to the process described in Steps A and B of Example 1 with the addition of cyclohexylamine heated at 80 ° C. in a hermetic enclosure for 72 hours. hours during step B.
- Step B 6,7-dichloro-4-cyclohexyl-4H-1,2,4-benzothiadiazine 1,1-dioxide
- the expected product is obtained according to the process described (heating time of 72 hours at 140 ° C.) in Stage C of Example 5. Melting point: 219-222 ° C.
- the expected product is obtained according to the process described in Stage D of Example 1. Melting point: 207-209 ° C.
- Step B 7-chloro-4-cyclohexyl-1,4-1,2,4-benzothiadiazine 1,1-dioxide
- the expected product is obtained according to the process described (heating time of 5 hours at 130 ° C.) in Stage C of Example 1. Deflection mp: 209-211 ° C.
- the expected product is obtained according to the process described in Stage D of Example 1. Melting point: 233-235 ° C.
- Step A 4-chloro-2-cyclohexylaminobenzenesulfonamide
- the expected product is obtained from 4-chloro-2-fluoroaniline according to the process described in Steps A and B of Example 1 with the addition of cyclohexylamine in step B.
- the expected product is obtained according to the process described (heating time of 48 hours at 130 ° C.) in stage C of Example 1. mMon point: 189-191 ° C.
- the expected product is obtained from 4,5-dichloro-2-fluoroaniline according to the process described in Steps A and B of Example 1 with the addition of cycloheptylamine in step B.
- Step B 6,7-dichloro-4-cycloheptyl-4H-1,2,4-benzothiadiazine 1,1-dioxide
- the expected product is obtained according to the process described (heating time of 72 hours at 140 ° C.) in stage C of Example 5. Jugging point: 222-224 ° C.
- the expected product is obtained according to the process described in Step D of Example 1. Melting point: 191-192 ° C.
- the expected product is obtained from 5-chloro-2-fluoroaniline according to the process described in Steps A and B of Example 1 with the addition of cycloheptylamine in step B.
- Stage B 7-chloro-4-cycloheptyl-4H-1,2,4-benzothiadiazine 1,1-dioxide
- the expected product is obtained according to the process described (heating time of 24 hours at 130 ° C.) in Stage C of Example 1. Melting point: 241-243 ° C.
- the expected product is obtained according to the process described in Stage D of Example 1. Melting point: 216-218 ° C.
- the expected product is obtained from 4-chloro-2-fluoroaniline according to the process described in Steps A and B of Example 1 with the addition of cycloheptylamine in step B.
- the expected product is obtained according to the process described (heating time of 72 hours at 130 ° C.) in stage C of Example 1. Melting point: 209-211 ° C.
- the expected product is obtained from 4,5-dichloro-2-fluoroaniline according to the process described in Steps A and B of Example 1 with the addition of cyclooctylamine heated at 80 ° C. in a hermetic enclosure for 72 hours in step B.
- the expected product is obtained according to the process described (heating time of 72 hours at 140 ° C.) in Stage C of Example 5. Melting point: 229-231 ° C.
- the expected product is obtained according to the process described in Stage D of Example 1. Deflection PoM: 154-155 ° C.
- the expected product is obtained from 5-chloro-2-fluoroaniline according to the process described in Steps A and B of Example 1 with the addition of cyclooctylamine in step B.
- Stage B 7-chloro-4-cyclooctyl-4H-1,2,4-benzothiadiazine 1,1-dioxide
- the expected product is obtained according to the process described (heating time of 24 hours at 130 ° C.) in Stage C of Example 1. Melting point: 235 ° -237 ° C.
- the expected product is obtained according to the process described in Step D of Example 1.
- Jude Point 184-186 ° C.
- the expected product is obtained from 4-chloro-2-fluoroaniline according to the process described in Steps A and B of Example 1 with the addition of cyclooctylamine in step B.
- the expected product is obtained according to the process described (heating time of 48 hours at 130 ° C.) in stage C of Example 1. Jusion point: 209-211 ° C.
- Step A 4,5-dichloro-2- (1-methyl) cyclopropylaminobenzenesulfonamide
- the expected product is obtained from 4,5-dichloro-2-fluoroaniline according to the process described in Steps A and B of Example 1 with the addition of (1-methyl) cyclopropylamine during step B.
- Step B 6,7-dichloro-4- (1-methyl) cyclopropyl-4H-1,2,4-benzothiadiazine 1,1-dioxide
- the expected product is obtained according to the method described (heating time of 24 hours) in Stage C of Example 1. Melting point: 230-232 ° C.
- Step C 6,7-dichloro-4- (1-methyl) cyclopropyl-2H-1,2,4-benzothiadiazine 1,1-dioxide
- the expected product is obtained according to the procedure described in Step D of Example 1 Melting point: 162-163 ° C
- Step C 7-chloro-4-cyclopropylmethyl-3,4-dihydro-2,2-1,2,4-benzothiadiazine 1,1-dioxide
- Step B 4-cyclopropylmethyl-7-fluoro-4H-1,2,4-benzothiadiazine 1,1-dioxide
- the expected product is obtained according to the process described in Stage B of Example 60. Point of fusion: 155-157 ° C.
- the expected product is obtained according to the process described in Step C of Example 60. Melting point: 102 ° -105 ° C.
- the expected product is obtained from 2,3,6-trifluoroaniline according to the process described in Step A of Example 1. Melting point: 148-151 ° C.
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 2 hours at 130 ° C.) in Stage C of Example 1. Melting point: 205-206 ° C. 4-cyclopropyl-7,8-difluoro-3,4-dihydro-2H-1,2,4-benzothiadiazine 1,1-dioxide
- the expected product is obtained according to the process described in Step D of Example 1. Jmiqn point: 199-201 ° C.
- the expected product is obtained from 4-cyano-2,5-difluoroaniline according to the process described in Step A of Example 1.
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 24 hours at 130 ° C.) in Stage C of Example 1. Melting point: 205 ° -207 ° C.
- the expected product is obtained from 4-bromo-2,6-difluoroaniline according to the process described in Step A of Example 1. Point of addition: 142-146 ° C.
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 72 hours at 130 ° C.) in Stage C of Example 1. Jusion Point - 285-287 ° C.
- the expected product is obtained from 4-bromo-2,3-difluoroaniline according to the process described in Step A of Example 1. Melting point: 155-157 ° C
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 3 hours at 130 ° C.) in stage C of Example 1. Jusion point: 244-247 ° C.
- Stage D 6-bromo-4-cyclopropyl-5-fluoro-S, 4-dihydro-2H-1,2,4-benzothiadiazine 1,1-dioxide
- the expected product is obtained from 5-bromo-2,4-difluoroaniline according to the process described in Step A of Example 1. Melting PoiM: 109-111 ° C.
- the expected product is obtained according to the process described (heating time of 4 hours at 130 ° C.) in Stage C of Example 1. Melting point: 228-231 ° C.
- Step D 7-bromo-4-cyclopropyl-6-fluoro-3,4-dihydro-2,2-l, 2,4-benzothiadiazine
- the expected product is obtained according to the process described in Step D of Example 1. Melting point: 175-177 ° C.
- the expected product is obtained from commercial 2,3,5,6-tetrafluorobenzenesulfonamide according to the process described in Step B of Example 1.
- the expected product is obtained according to the process described (heating time of 4 hours at 130 ° C.) in Stage C of Example 1. mp 166-168 ° C.
- the expected product is obtained from commercial 5-chloro-2,4-difluorobenzenesulfonamide according to the process described in Step B of Example 1.
- the expected product is obtained according to the process described (heating time of 5 hours at 130 ° C.) in Stage C of Example 1. Point of addition: 217-219 ° C.
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 3 hours at 130 ° C.) in Stage C of Example 1. Melting point: 278 ° -281 ° C.
- the expected product is obtained according to the process described in Step D of Example 1. Jusion Point: 269-271 ° C.
- Step A 4-Fluoro-N-methyl-3-sulfamoylbenzamide
- the expected product is obtained using methylamine in place of ammonia according to the process described in Step A of Example 69. Melting point: 242-244 ° C.
- the expected product is obtained according to the process described (heating time of 3 hours at 130 ° C.) in Stage C of Example 1. Melting point: 300 ° -305 ° C.
- the expected product is obtained according to the process described in Stage D of Example 1. Deflection PoM: 271-273 ° C.
- Step A 4-Fluoro-N, ⁇ N-dimethyl-3-sulfamoylbenzamide
- the expected product is obtained using dimethylamine in place of ammonia according to the process described in Step A of Example 69.
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained from 2-bromo-4-cyano-5-fluoroaniline according to the process described in Step A of Example 1.
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 3 hours at 130 ° C.) in Stage C of Example 1.
- the expected product is obtained according to the process described in Step D of Example 1, starting from 7-amino-4-cyclopropyl-4H-1,2,4-benzothiadiazine 1,1-dioxide prepared in Step A of Example 42.
- the expected product is obtained from 2-fluoro-4-nitroaniline according to the process described in Step A of Example 41. Melting point: 145-147 ° C.
- the expected product is obtained according to the process described in Stage B of Example 41.
- the expected product is obtained according to the process described in Step C of Example 41. Melting point: 254-257 ° C.
- Stage D 4-cyclopropyl-S, 4-dihydro-6-nitro-2H-1,2,4-benzothiadiazine 1,1-dioxide
- Step A 6-amino-4-cyclopropyl-4H-1,2,4-benzothiadiazine 1,1-dioxide
- the expected product is obtained from the compound of Example 74 according to the process described in Step A of Example 42. Yield: 177-180 ° C.
- the expected product is obtained according to the process described in Stage B of Example 42. MWO point: 265-267 ° C.
- the expected product is obtained according to the process described (heating time of 4 hours at 130 ° C.) in stage C of Example 1. Jusion point: 192-195 ° C.
- Example 80 4-cyclopropyl-3,4-dihydro-6-methoxycarbonyl-2 J fir-l, 2,4-benzothiadiazine 1,1-dioxide
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 4 hours at 130 ° C.) in Stage C of Example 1. Point of addition: 191-194 ° C.
- Stage D 4-cyclopropyl-3,4-dihydro-6-methoxycarbonyl-2W-1,2,4-benzothiadiazine 1,1-dioxide
- the expected product is obtained according to the process described in Step D of Example 1. pH: 162 ° -164 ° C.
- the expected product is obtained according to the method described in Example 78, using as starting material the compound of Example 80 in place of the compound of Example 77.
- Step A 4-Fluoro-N-phenyl-3-sulfamoylbenzamide
- the expected product is obtained in 4 steps from 4-fluoro-3-nitrotoluene.
- 4-Fluoro-3-nitrotoluene (6.5 mmol) is added in small portions to a solution of potassium dichromate (4 g) in glacial acetic acid (10 mL). After stirring for 15 minutes, sulfuric acid (4 mL) is added and the solution is refluxed for 2 hours. The medium is then cooled and added with water (100 mL) and extracted with ethyl acetate (3 x 100 mL). The organic phases are combined, dried over anhydrous MgSO 4 and evaporated. The residue is recrystallized from an ethyl acetate / hexane (1/1) mixture is engaged in the next step.
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the process described (heating time of 4 hours at 130 ° C.) in Stage C of Example 1. Point of addition: 293-296 ° C.
- the expected product is obtained according to the process described in Step D of Example 1. Melting point: 268-270 ° C.
- Example 83 4-cyclopropyl-3,4-dihydro-6 J-phenylaminocarbonyl-2-ff l, 2,4-benzothiadiazine 1,1-dioxide
- the expected product is obtained from 3-fluoro-4-nitrotoluene according to the process described in Stage A of Example 82. Melting point: 250-252 ° C.
- Step B 3-cyclopropylamino- N-phenyl-4-sulfamoylbenzamide
- the expected product is obtained according to the process described (heating time of 4 hours at 130 ° C.) in stage C of Example 1. JusIQU point: 278-281 ° C.
- Stage D 4-cyclopropyl-S, 4-dihydro-6-phenylaminocarbonyl-2H-1,2,4-benzothiadiazine 1,1-dioxide
- the expected product is obtained according to the process described in Step D of Example 1.
- the ion pressure 232 ° -234 ° C.
- the expected product is obtained according to the process described in Step C of Example 1. Melting point: 216-219 ° C.
- the expected product is obtained according to the process described in Stage D of Example 1. Melting point: 154-156 ° C.
- Example 85 The expected product is obtained according to the method described in Example 85 using as starting material the compound of Example 86 in place of the compound of Example 84. Melting point • 213-214 ° C
- the expected product is obtained from 2-amino-4,5-dichlorobenzenesulfonamide according to the process described in Step A of Example 60. Melting point: 237-240 ° C.
- the expected product is obtained according to the process described in Stage B of Example 60. Melting point: 192-195 ° C.
- the expected product is obtained from 3-chloro-2,6-difluoroaniline according to the method described in Step A of Example 1.
- the expected product is obtained according to the process described in Stage B of Example 1.
- the expected product is obtained according to the method described (heating time of 4 hours at 130 ° C.) in stage C of Example 1. Jusion point: 201-204 ° C.
- the expected product is obtained according to the process described in Step D of Example 1. Melting Point: 171 ° -174 ° C.
- the test consists in the in vitro fluorescence measurement of the membrane depolarization induced on rat embryonic neurons in culture, by the joint action of AMPA and the test product, in comparison with the action of AMPA. alone.
- Brain cells are cultured and maintained in a cell culture incubator for 18 days. After incubation, the culture medium is removed and replaced with fluorescence probe loading medium for measuring the membrane potential (20 ⁇ l Molecular Devices membrane potential kit) and left at room temperature for 1 hour.
- the basic fluorescence of the wells is read (Hamamatsu FDSS device), then the AMPA is injected onto the cells (20 ⁇ l, concentration range 3 to 100 ⁇ M) and the action of AMPA is measured in kinetics.
- test product is then introduced into the wells (20 .mu.l in concentration range, crossed with that of AMPA) and the action of the product is measured in kinetics.
- the value used for each well is the average of the reading over the last 15 seconds of the period.
- the effect curves of AMPA at different product concentrations are shown. For each product concentration, the value retained is the area under the AMPA curve at that concentration and the EC 2 ⁇ , product concentration that doubles the AMPA-induced membrane potential, is calculated.
- Example 34 1.8
- Example 37 4.4
- the object recognition test (Behav Brain Res., 1988, 31, 47-59) is based on the spontaneous exploratory activity of the animal and has the characteristics of episodic memory in humans. Sensitive to aging (Eur J Pharm 1997, 325, 173-180), as well as to cholinergic dysfunctions (Pharm Biochem Behav., 1996, 53 (2), 277-283), this memory test is based on the differential exploration of 2 objects of similar shape, one familiar, the other new.
- the experimental procedure, adapted to the CD1 mouse comprises 3 phases which take place in the same experimental chamber. During the era phase lasting 40 minutes, the mice are habituated to the environment. During the 2nd phase, which takes place the next day, an object is placed in the enclosure and the mouse is free to explore.
- the mouse When this exploration reaches a duration of 20 seconds, the mouse is removed from the enclosure. During the 3rd phase (5 minutes), 24 hours later, the same object is presented (it acquires the status of an object "familiar"), and a new object.
- the duration of exploration, expressed in seconds, of each of the two objects, is timed.
- the control animals having previously received the vehicle orally 60 minutes before each of the 3 phases, explore for an equivalent duration the "familiar" object and the "new" object, which means forgetting the object already present.
- the animals having received a mnemocognitive facilitator compound preferentially explore the new object, which means maintaining the memory of the object already presented.
- results obtained with the compounds of the present invention show a significantly greater exploration of the new object compared to the familiar object at doses of 1 and 3 mg / kg, PO, doubling or tripling the duration of exploration, which indicates that the compounds of the invention improve storage substantially.
- the difference in exploration of the two objects during the 3rd phase is between 5 and 10 seconds after administration of the compound of Example 1 when it is less than 3 seconds after the vehicle administration.
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Psychiatry (AREA)
- Pain & Pain Management (AREA)
- Hospice & Palliative Care (AREA)
- Psychology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen- Or Sulfur-Containing Heterocyclic Ring Compounds With Rings Of Six Or More Members (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
Composés de formule (I) dans laquelle Rcy représente un groupement cycloalkyle ou un groupement cycloalkylalkyle non- substitué ou substitué, R1, R2, R3 et R4, identiques ou différents, représentent chacun un atome d'hydrogène ou d'halogène ou un groupement nitro; cyano; hydroxy; alkoxy; alkyle; amino non-substitué ou substitué; carboxy; alkoxycarbonyle; loxycarbonyle; aminocarbonyle non-substitué ou substitué.
Description
NOUVEAUX DERIVES DE BENZOTHIADIAZINES CYCLOALKYLEES,
LEUR PROCEDE DE PREPARATION ET LES COMPOSITIONS
PHARMACEUTIQUES QUI LES CONTIENNENT
La présente invention concerne de nouveaux dérivés de benzothiadiazines cycloalkylées, leur procédé de préparation, les compositions pharmaceutiques qui les contiennent ainsi que leur utilisation en tant que modulateurs allostériques positifs des récepteurs AMPA.
Il est désormais reconnu que les aminoacides excitateurs et tout particulièrement le glutamate, jouent un rôle crucial dans les processus physiologiques de plasticité neuronale et dans les mécanismes sous-tendant l'apprentissage et la mémoire. Des études pathophysiologiques ont indiqué clairement qu'un déficit de la neurotransmission glutamatergique est associé étroitement avec le développement de la maladie d'Alzheimer (Neuroscience and Biobehavioral Reviews, 1992, J_6, 13-24 ; Progress in Neurobiology, 1992, 39, 517-545).
Par ailleurs, certains travaux ont démontré durant les dernières années l'existence de sous- types réceptoriels aux aminoacides excitateurs et de leurs interactions fonctionnelles (Molecular Neuropharmacology, 1992, 2, 15-31).
Parmi ces récepteurs, le récepteur à l'AMPA ("α-amino-3-hydroxy-5-methyl-4-isoxazole- propionic acid") apparaît être le plus impliqué dans les phénomènes d'excitabilité neuronale physiologique et notamment dans ceux impliqués dans les processus de mémorisation. Pour exemple, l'apprentissage a été montré comme étant associé à l'augmentation de la liaison de l'AMPA à son récepteur dans l'hippocampe, l'une des zones cérébrales essentielles aux processus mnémocognitifs. De même, les agents nootropes tels que l'aniracetam ont été décrits comme modulant positivement les récepteurs AMPA des cellules neuronales (J. Neurochemistry, 1992, 58, 1199-1204).
Dans la littérature, des composés de structure benzamide ont été décrits pour posséder ce même mécanisme d'action et pour améliorer les performances mnésiques (Synapse, 1993, 15, 326-329). Le composé BA 74, en particulier, est le plus actif parmi ces nouveaux agents pharmacologiques.
Enfin, le brevet EP 692 484 décrit un dérivé de benzothiadiazine possédant une activité facilitatrice sur le courant AMPA et la demande de brevet WO 99/42456 décrit, entre autres, certains dérivés de benzothiadiazine en tant que modulateurs des récepteurs AMPA.
Les dérivés de benzothiadiazine, objets de la présente invention, outre le fait qu'ils soient nouveaux, présentent, de manière surprenante, des activités pharmacologiques pour le récepteur AMPA nettement supérieures à celles des composés de structures proches décrits dans l'Art Antérieur.
Plus spécifiquement, la présente invention concerne les composés de formule (I)
dans laquelle :
> Rcy représente :
" un groupement cycloalkyle (C3-C8) non-substitué ou substitué par un ou plusieurs groupements, identiques ou différents, choisis parmi alkyle (C1-C6) linéaire ou ramifié non-substitué ou substitué par un ou plusieurs atomes d'halogène ; alkoxy (C1-C6) linéaire ou ramifié ; hydroxy ; et amino non-substitué ou substitué par un ou deux groupements alkyle (C1-C6) linéaire ou ramifié ;
1 ou un groupement cycloalkyle (C3-C8) alkyle (C1-C6) linéaire ou ramifié non- substitué ou substitué sur la partie cyclique par un ou plusieurs groupements, identiques ou différents, choisis parmi alkyle (C1-C6) linéaire ou ramifié non- substitué ou substitué par un ou plusieurs atomes d'halogène ; alkoxy (C1-C6) linéaire ou ramifié ; hydroxy ; et amino non-substitué ou substitué par un ou deux groupements alkyle (C1-C6) linéaire ou ramifié ;
> R1, R2, R3 et R4, identiques ou différents, représentent chacun un atome d'hydrogène ou d'halogène ou un groupement nitro ; cyano ; hydroxy ; thio ; alkyle (C1-C6) linéaire ou ramifié non-substitué ou substitué par un ou plusieurs atomes d'halogène ; cyanoalkyle (C1-C6) linéaire ou ramifié ; hydroxyalkyle (C1-C6) linéaire ou ramifié ; alkoxy (C1-C6) linéaire ou ramifié non-substitué ou substitué par un ou plusieurs atomes d'halogène ; alkylthio (C1-C6) linéaire ou ramifié ; carboxy ; alkoxycarbonyle (C1-Ce) linéaire ou ramifié ; aryloxycarbonyle ; acyle (C1-C6) linéaire ou ramifié ; amino non-substitué ou substitué par un ou deux groupements alkyle (C1-C6) linéaire ou ramifié ou par un groupement acyle (Ci-C6) linéaire ou ramifié ; aminocarbonyle non-substitué ou substitué par un ou deux groupements alkyle (C1-C6) linéaire ou . ramifié ; arylaminocarbonyle ; ou alkylsulfonylamino (C1TC6) linéaire ou ramifié ;
leurs énantiomères et leurs diastéréoisomères lorsqu'ils existent, ainsi que leurs sels d'addition avec un acide ou une base pharmaceutiquement acceptable.
On entend par « aryle », le groupement phényle non-substitué ou substitué par un ou plusieurs groupements, identiques ou différents, choisis parmi alkyle (C1-C6) linéaire ou ramifié non-substitué ou substitué par un ou plusieurs atomes d'halogène ; alkoxy (C1-C6) linéaire ou ramifié ; hydroxy ; et amino non-substitué ou substitué par un ou deux groupements alkyle (C1-C6) linéaire ou ramifié.
Parmi les acides pharmaceutiquement acceptables, on peut citer à titre non limitatif les acides chlorhydrique, bromhydrique, sulfurique, phosphorique, acétique, trifluoroacétique, lactique, pyruvique, malonique, succinique, glutarique, fumarique, tartrique, maléique, citrique, ascorbique, oxalique, méthanesulfonique, benzènesulfonique, camphorique.
Parmi les bases pharmaceutiquement acceptables, on peut citer à titre non limitatif l'hydroxyde de sodium, l'hydroxyde de potassium, la triéthylamine, la tertbutylamine.
Les groupements Rcy préférés sont les groupements cycloalkyles (C3-C8), et plus particulièrement le groupement cyclopropyle. De manière avantageuse, le groupement cyclopropyle peut être substitué par un groupement alkyle (C1-CO) linéaire ou ramifié et, plus particulièrement, le groupement méthyle.
Les groupements Rcy préférés sont les groupements cycloalkyle (C3-C8) alkyle (C1-C6) linéaire ou ramifié, et plus particulièrement le groupement cyclopropylméthyle.
Le groupement Rj représente préférentiellement un atome d'hydrogène ou un atome d'halogène, et plus particulièrement l'atome de fluor.
Le groupement R2 représente préférentiellement un atome d'hydrogène ; un atome d'halogène, et plus particulièrement l'atome de fluor, de chlore ou de brome ; le groupement cyano ; le groupement carboxy ; ou le groupement alkyle (C1-C6) linéaire ou ramifié, et plus particulièrement le groupement méthyle. . . Le groupement R3 représente préférentiellement un atome d'hydrogène ; un atome d'halogène, et plus particulièrement l'atome de fluor, de chlore ou de brome ; le groupement alkyle (C1-C6) linéaire ou ramifié, et plus particulièrement le groupement méthyle. Le groupement R4 représente un atome d'hydrogène ou un atome d'halogène, et plus particulièrement l'atome de fluor, de chlore ou de brome.
Sont plus particulièrement préférés les composés pour lesquels deux des groupements R1, R2, R3 ou R4 situés sur le noyau benzénique représentent un atome d'hydrogène, tandis que les deux autres substituants, identiques ou différents, représentent un groupement distinct d'un atome d'hydrogène, choisi préférentiellement parmi les atomes d'halogène, tels que l'atome de fluor, de chlore ou de brome.
De manière avantageuse, sont plus particulièrement préférés les composés pour lesquels
Rcy représente un groupement cyclopropyle et, deux des groupements R1, R2, R3 ou R4 situés sur le noyau benzénique représentent un atome d'hydrogène, tandis que les deux autres substituants, identiques ou différents, représentent un atome d'halogène, tels que l'atome de fluor, de chlore ou de brome.
Les composés préférés selon l'invention sont :
• le 6,7-dichloro-4-cyclopropyl-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1-dioxyde ;
• le 8-chloro-4-cyclopropyl-6-fluoro-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1- dioxyde ;
• le 8-bromo-4-cyclopropyl-6-fluoro-3 ,4-dihydro-2H- 1 ,2,4-benzothiadiazine 1,1- dioxyde ;
• le 6-cyano-4-cyclopropyl-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1 -dioxyde ;
• le 8-bromo-6-chloro-4-cyclopropyl-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1- dioxyde ;
• le 4-cyclopropyl-5-fluoro-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1 -dioxyde ; « le 8-bromo-4-cyclopropyl-3 ,4-dihydro-2H- 1 ,2,4-benzothiadiazine 1 , 1 -dioxyde ;
• le 4-cyclopropyl-5,7-difluoro-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1-dioxyde ;
• le 6-fluoro-4-cyclopropyl-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1-dioxyde ;
• le 8-chloro-4-cyclopropyl-7-fluoro-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1- dioxyde ; • le 4-cyclopropyl-3,4-dihydro-6-méthyl-2H-l,2,4-benzothiadiazine 1,1 -dioxyde ;
• le 4-cyclopropyl-8-fluoro-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1-dioxyde ;
• le 8-chloro-4-cyclopropyl-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1 -dioxyde ;
• le 6-bromo-4-cyclopropyl-7-fluoro-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1- dioxyde ; • le 6-bromo-4-cyclopropyl-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1-dioxyde ;
• le 4-cyclopropyl-6,8-difluoro-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1-dioxyde ;
• le 4-cyclopropyl-5,6-difluoro-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1-dioxyde ;
• le 4-cyclopropyl-3,4-dihydro-7-méthyl-2H-l,2,4-benzothiadiazine 1,1-dioxyde ;
• le 6-chloro-4-cyclopropyl-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1 -dioxyde ;
• le 4-cyclopropyl-3,4-dihydro-6-iodo-2H-l,2,4-benzothiadiazine 1,1-dioxyde ;
• le 6,7-dichloro-4-(l-méthyl)cyclopropyl-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1-dioxyde ;
• le 4-cyclopropylméthyl-7-fluoro-3 ,4-dihydro-2H- 1 ,2,4-benzothiadiazine 1,1- dioxyde ;
• le 6-carboxy-4-cyclopropyl-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1-dioxyde ;
• le 4-cyclopropyl-7,8-difluoro-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1-dioxyde ;
• le 8-bromo-6-cyano-4-cyclopropyl-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1- dioxyde ; • et le 7-bromo-4-cyclopropyl-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1 -dioxyde.
Les sels d'addition à un acide ou une base pharmaceutiquement acceptable des composés préférés de l'invention font partie intégrante de l'invention.
L'invention s'étend également au procédé de préparation des composés de formule (I) à partir du composé de formule (II) :
que l'on cyclise en présence d'un composé de formule (III) :
Η-C(OR5)3 (III)
dans laquelle R5 représente un groupement alkyle (Ci-C6) linéaire ou ramifié,
dans laquelle Rcy, R1, R2, R3 et R4 sont tels que définis précédemment,
que l'on met en réaction avec un agent réducteur, pour conduire au composé de formule (I),
une variante dans la préparation des composés de formule (I) consistant, après réalisation de l'étape de réduction du composé de formule (IV), en l'utilisation des réactions classiques de chimie afin de modifier, dans un deuxième temps, les substituants du noyau benzénique,
composé de formule (I) qui peut être ensuite purifié selon une technique classique de séparation, que l'on transforme, si on le souhaite en ses sels d'addition à un acide ou à une base pharmaceutiquement acceptable et dont on sépare éventuellement les isomères, s'ils existent, selon une technique classique de séparation.
La présente invention concerne également le procédé de préparation des composés de formule (I) caractérisé en ce que l'on utilise comme produit de départ un composé de formule (V) :
que l'on cyclise en présence d'un composé de formule (III) pour conduire au composé de formule (VI) :
dans laquelle R1, R2, R3 et R4 sont tels que définis précédemment,
que l'on met en réaction avec un composé de formule (VII) :
Y-RCy (VII) dans laquelle Rcy est tel que défini précédemment et Y représente un groupement partant choisi parmi les atomes d'iode, de brome et les groupements tosylate, mésylate et triflate pour conduire au composé de formule (IV),
que l'on met en réaction avec un agent réducteur, pour conduire au composé de formule (I),
une variante dans la préparation des composés de formule (I) consistant, après réalisation de l'étape de réduction du composé de formule (IV), en l'utilisation des réactions classiques de chimie afin de modifier, dans un deuxième temps, les substituants du noyau benzénique,
composé de formule (I) qui peut être ensuite purifié selon une technique classique de séparation, que l'on transforme, si on le souhaite en ses sels d'addition à un acide ou à une
base pharmaceutiquement acceptable et dont on sépare éventuellement les isomères, s'ils existent, selon une technique classique de séparation.
Les composés de formule (II) et de formule (V) sont aisément accessibles à l'homme du métier par des réactions de chimie classiques ou décrites dans la littérature.
Les composés de formule (IV) sont nouveaux et font également partie de l'invention à titre d'intermédiaires de synthèse des composés de formule (I).
Les composés de formule (I) selon l'invention présentent des propriétés activatrices des récepteurs AMPA qui les rendent utiles dans le traitement ou la prévention des désordres mnémocognitifs associés à l'âge, aux syndromes anxieux ou dépressifs, aux maladies neurodégénératives progressives, à la maladie d'Alzheimer, à la maladie de Parkinson, à la maladie de Pick, à la chorée d'Huntington, à la maladie de Korsakoff, à la schizophrénie, aux séquelles des maladies neurodégénératives aiguës, aux démences frontales et sous- corticales, aux séquelles de l'ischémie et aux séquelles de l'épilepsie.
L'invention s'étend aussi aux compositions pharmaceutiques renfermant comme principe actif au moins un composé de formule (I) avec un ou plusieurs excipients inertes, non toxiques et appropriés. Parmi les compositions pharmaceutiques selon l'invention, on pourra citer plus particulièrement celles qui conviennent pour l'administration orale, parentérale (intraveineuse ou sous-cutanée), nasale, les comprimés simples ou dragéifiés, les comprimés sublinguaux, les gélules, les tablettes, les suppositoires, les crèmes, les pommades, les gels dermiques, les préparations injectables, et les suspensions buvables.
La posologie utile est adaptable selon la nature et la sévérité de l'affection, la voie d'administration ainsi que l'âge et le poids du patient. Cette posologie varie de 0,01 à 1000 mg par jour en une ou plusieurs prises.
Les exemples suivants illustrent l'invention mais ne la limitent en aucune façon.
Les produits de départ utilisés sont des produits connus ou préparés selon des modes
préparatoires connus.
Les structures des composés décrits dans les exemples ont été déterminées selon les techniques spectrophotométriques usuelles (infrarouge, RMN, spectrométrie de masse).
EXEMPLE 1 : 6,7-dichloro-4-cyclopropyl-3,4-dihydro-2/T-l,2,4-benzothiadiazine 1,1-dioxyde
Stade A : 4,5-dichloro-2-fluorobenzènesulfonamide
Dans un ballon de 500 mL, une portion d'acide acétique glacial (30 mL) est saturée pendant 30 minutes par un courant d'anhydride sulfureux gazeux. A cette solution est ajoutée une solution de chlorure cuivrique (1,5 g) dans l'eau (10 mL) (suspension A). La 4,5-dichloro-2-fluoroaniline (5 g) est dissoute dans un mélange d'acide acétique glacial
(30 mL) et d'acide chlorhydrique concentré (15 mL). Cette solution est refroidie à -5 °C sur bain de glace et de sel. Ensuite, une solution de nitrite sodique (2,5 g) dans l'eau (1O mL) est ajoutée goutte à goutte sous agitation constante. Cette mixture est ajoutée lentement à la suspension A et est maintenue sous agitation sur bain de glace pendant 15 minutes. La mixture est ensuite versée sur un mélange d'eau (20O mL) et d'éther (200 mL). La phase éthérée est décantée et lavée à l'eau (100 mL). La phase organique est concentrée à siccité par distillation sous pression réduite et le résidu est redissous dans le dioxanne (25 mL). Cette solution est versée lentement sous agitation dans un mélange d'ammoniaque concentré (25 mL) et d'eau (10 mL) refroidi sur bain de glace. Après 30 minutes, la solution est évaporée à siccité par distillation sous pression réduite et le résidu obtenu est solubilisé dans le méthanol. La solution méthanolique est traitée au charbon adsorbant, filtrée et le filtrat évaporé à siccité. Le résidu est recristallisé dans un mélange méthanol-eau. Point dejusion : 144-145 0C
Stade B : 4,5-dichloro-2-cyclopropylaminobenzènesulfonamide
La solution de 4,5-dichloro-2-fluorobenzènesulfonamide (3 g) dans le dioxanne (30 mL) additionné de la cyclopropylamine (3 mL) est chauffée à 100-110 °C en enceinte hermétique pendant 24 heures. Le solvant et l'excès d'aminé sont éliminés par distillation sous pression réduite et le résidu est dissous dans le méthanol (20 mL). La solution méthanolique est refroidie sur bain de glace et additionnée d'eau (60 mL). Le précipité obtenu (produit du titre) est recueilli par filtration, lavé à l'eau et séché. Il est utilisé dans l'étape suivante sans autre purification.
Stade C : 6, 7 -dichloro-4-cyclopropyl-4Yi-l ,2,4-benzothiadiazine 1, 1-dioxyde
Dans un ballon, le mélange de 4,5-dichloro-2-cyclopropylaminobenzènesulfonamide de l'étape précédente (2,5 g) et d'orthoformiate d'éthyle (25 mL) est chauffé en vase ouvert à 150 °C pendant 1 heure. La suspension obtenue est refroidie sur bain de glace et l'insoluble est recueilli par filtration, lavé à l'éther et séché. Le solide est redissous dans un mélange d'acétone et de méthanol à chaud et la solution chaude est traitée au charbon absorbant puis filtrée et concentrée à siccité. Le résidu est recristallisé dans le méthanol. Point de Jusion : 260-262 °C
Stade D : 6, 7-dichloro-4-cyclopropyl-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1,1- dioxyde
La solution de 6,7-dichloro-4-cyclopropyl-4H-l,2,4-benzothiadiazine 1,1-dioxyde de l'étape précédente (1,9 g) dans l'isopropanol (5O mL) est additionnée de NaBH4 (1 g) finement broyé, puis chauffée pendant 5-10 minutes à 50-55 °C. Le solvant est éliminé par évaporation sous dépression. Le résidu est repris par de l'eau (50 mL) et amené à pH acide par addition de HCl 6 N. Le produit du titre est extrait par le dichlorométhane (3 x 30 mL). La phase organique est séchée sur MgSO4 et filtrée. Le filtrat est évaporé à siccité et le résidu obtenu est recristallisé dans le méthanol/eau 1/1 (60 mL). PoJM de 'Jusion : 174-176 °C
EXEMPLE 2 : 4-cyclopropyl-3,4-dihydro-7-inéthyl-2/_r-l,2,4-beiizothiadiazine 1,1- dioxyde
Stade A : 2-fluoro-5-méthylbenzènesulfonamide
Le produit attendu est obtenu à partir de la 2-fluoro-5-méthylaniline selon le procédé décrit dans le stade A de l'Exemple 1. Point de Jusion : 118-120 0C
Stade B : 2-cyclopropylamino-5-méthylbenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 72 heures) dans le stade B de l'Exemple 1.
Stade C : 4-cyclopropyl-7-méthyl-4ïl-l,2,4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 3 heures) dans le stade C de l'Exemple 1. Point de Jusion : 192-195 °C
Stade D : 4-cyclopropyl-3,4-dihydro-7-méthyl-2ïî-l,2,4-benzothiadiazme 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point de Jusion : 144-145 °C
EXEMPLE 3 : 6-chloro-4-cyclopropyl-7-fluoro-3,4-dihydro-2H-l,2,4- benzothiadiazine 1,1-dioxyde
Stade A : 4-chloro-2,5-difluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 4-chloro-2,5-difluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1. Point d_eju_s ion : 154-157 °C
Stade B : 4-chloro-2-cyclopropylamino-5-fluorobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 6-chloro-4-cyclopropyl-7-fluoro-4ϋ-l,2,4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 2 heures) dans le stade C de l'Exemple 1. Pojni de jusion • 205-206 0C
Stade D : ό-chloro-4-cyclopropyl- 7-fluoro-S, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point de jusion : 170-171 0C
EXEMPLE 4 : 4-cydopropyl-7-fluoro-3,4-dihydro-2JÏ-l,2,4-benzothiadiazine 1,1- dioxyde
Stade A : 2,5-difluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 2,5-difluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1.
PpM deJusiQn : 135-137 °C
Stade B : 2-cyclopropylamino-5-fluorobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 96 heures) dans le stade B de l'Exemple 1.
: 4-cyclopropyl- 7-fluoro-4H-l, 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 24 heures à 130 °C) dans le stade C de l'Exemple 1. Point dejusiqn : 170-172 0C
Stade D : 4-cyclopropyl- 7-fluoro-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejβisiqn : 163-164 °C
EXEMPLE 5 : 7-chloro-4-cyclopropyI-3,4-dihydro-2fir-l,2,4-benzothiadiazine 1,1- dioxyde
Stade A : 5-chloro-2-fluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 5-chloro-2-fluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1. PoM dejusiqn : 135-136 °C
Stade B : 5-chloro-2-cyclopropylaminobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
ie C : 7-chloro-4-cyclopropyl-4H-l, 2, 4-benzothiadiazine 1, 1 -dioxyde
Dans un autoclave scellé, le mélange de 2-cyclopropylaminobenzènesulfonamide de l'étape précédente (2,5 g) et d'orthoformiate d'éthyle (25 mL) est chauffé à 150 °C pendant 96 heures. La mixture est refroidie sur bain de glace et l'insoluble est recueilli par filtration, lavé à l'éther et séché. Le solide est redissous dans un mélange d'acétone et de méthanol à chaud et la solution chaude est traitée au charbon absorbant puis filtrée et concentrée à siccité. Le résidu est recristallisé dans le méthanol. Point de Jusion : 229-231 °C
7-chloro-4-cyclopropyl-3, 4-dihydro-2R-l, 2, 4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejusion : 159-161 0C
EXEMPLE 6 : 4-cycIopropyl-6-fluoro-3,4-dihydro-2//-l,2,4-beiizothiadiazine 1,1- dioxyde
Stade A : 2,4-difluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 2,4-difluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1. Point dejusion : 155-157 °C
: 2-cyclopropylamino-4-fluorobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
4-cyclopropyl-6-fluoro-4H-l, 2, 4-benzothiadiazine 1, 1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 10 heures à 130 °C) dans le stade C de l'Exemple 1. Point de Jusion : 199-202 °C
Stade D : 4-cyclopropyl-6-fluoro-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejusion : 164-165 °C
EXEMPLE 7 : 6-chIoro-4-cyclopropyI-3,4-dihydro-2//-l,2,4-benzothiadiazine 1,1- dioxyde
Stade A : 4-chloro-2-fluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 4-chloro-2-fluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1. Point dejusion : 104-106 °C
Stade B : 4-chloro-2-cyclopropylaminobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 6-chloro-4-cyclopropyl-4H-l, 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 5 heures à 130 °C) dans le stade C de l'Exemple 1. Point dejusion : 239-242 °C
Stade D : 6-chloro-4-cyclopropyl-S, 4-dihydro-2H- 1, 2, 4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejusion : 174-176 °C
EXEMPLE 8 : 4-cyclopropyl-7-trifluorométhyl-3,4-dihydro-2^-l,2,4- benzothiadiazine 1,1-dioxyde
Stade A : 2-fluoro-5-trifluorométhylbenzènesulfonamide
Le produit attendu est obtenu à partir de la 2-fluoro-5-trifluorométhylaniline selon le procédé décrit dans le stade A de l'Exemple 1. Point dejusion : 128-130 0C
2-cyclopropylamino-5-trifluorométhylbenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 4-cyclopropyl-7-trifluorométhyl-4H-l,2,4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 5 heures à 130 °C) dans le stade C de l'Exemple 1. Point dejusion : 160-162 °C
Stade D : 4-cyclopropyl- 7-trifluorométhyl-S, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1, 1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. PpM dejusion : 155-157 0C
EXEMPLE 9 : 4-cyclopropyI-3,4-dihydro-2//-l,2,4-benzothiadiazine 1,1-dioxyde
Stade A : 2-fluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 2-fluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1. Point dejusion : 160-162 °C
Stade B : 2-cyclopropylaminobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 96 heures) dans le stade B de l'Exemple 1.
' : 4-cycîopropyl-4H-l , 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 5 heures à 130 °C) dans le stade C de l'Exemple 1. Point dejusion : 191-194 0C
Stade D : 4-cyclopropyl-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point _de Jks ion : 165-166 0C
EXEMPLE 10 : 7-cyano-4-cyclopropyl-3,4-dihydro-2//-l,2,4-benzothiadiazine 1,1- dioxyde
Stade A : 5-cyano-2-fluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 5-cyano-2-fluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1. PpM dejusion : 195-196 °C
5-cyano-2-cyclopropylaminobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 7-cyano-4-cyclopropyl-4H- 1, 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 3 heures à 130 °C) dans le stade C de l'Exemple 1. Point de Jusion : 268-270 0C
Stade D : 7-cyano-4-cyclopropyl-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point de 'Jusion : 259-261 °C
EXEMPLE 11 : 6-bromo-4-cyclopropyl-7-trifluorométhyl-3,4-dihydro-2//-l,2,4- benzothiadiazine 1,1-dioxyde
Stade A : 4-bromo-2-fluoro-5-trifluorométhylbenzènesulfonamide
Le produit attendu est obtenu à partir de la 4-bromo-2-fluoro-5-trifluorométhylaniline selon le procédé décrit dans le stade A de l'Exemple 1.
Stade B : 4-bromo-2-cyclopropylamino-5-trifluorométhylbenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 6-bromo-4-cyclopropyl- 7-trifluorométhyl-4H-l , 2, 4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 3 heures à 130 °C) dans le stade C de l'Exemple 1. PoJM décision : 204-206 0C
Stade D : 6-bromo-4-cyclopropyl- 7-trifluorométhyl-3, 4-dihydro-2H-l, 2, 4- benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. PoJM dejusion - 186-189 °C
EXEMPLE 12 : 6-bromo-5-chloro-4-cyclopropyl-3,4-dihydro-2H-l,2,4- benzothiadiazine 1,1-dioxyde
Stade A : 4-bromo-3-chloro-2-fluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 4-bromo-3-chloro-2-fluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1. Stade B : 4-bromo-3-chloro-2-cyclopropylaminobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 6-bromo-5-chloro-4-cyclopropyl-4H-l, 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 3 heures à 130 °C) dans le stade C de l'Exemple 1. PpM dejusion : 199-201 °C
Stade D : 6-bromo-5-chloro-4-cyclopropyl-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejusion : 128-131 0C
EXEMPLE 13 : 4-cyclopropyl-5-trifluorométhyl-3,4-dihydro-2/ï-l,2,4- benzothiadiazine 1,1-dioxyde
Stade A : 2-fluoro-3-trifluorométhylbenzènesulfonamide
Le produit attendu est obtenu à partir de la 2-fluoro-3-trifluorométhylaniline selon le procédé décrit dans le stade A de l'Exemple 1. Point dejusion : 112-114 °C
: 2-cyclopropylamino-3-trifluorométhylbenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 4-cyclopropyl-5-trifluorométhyl-4ïl- 1, 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 5 heures à 130 °C) dans le stade C de l'Exemple 1. Point dejusion : 180-182 0C
Stade D : 4-cyclopropyl-5-trifluorométhyl-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejusion : 165-167 °C
EXEMPLE 14 : 8-chloro-4-cyclopropyl-6-fluoro-3,4-dihydro-2H-l,2,4- benzothiadiazine 1,1-dioxyde
2-chloro-4, 6-difluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 2-chloro-4,6-difluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1. Point de Jusion : 116-120 0C
Stade B : 2-chloro-6-cyclopropylamino-4-fluorobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 8-chloro-4-cyclopropyl-6-fluoro-4R-l,2,4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 3 heures à 130 °C) dans le stade C de l'Exemple 1. Point de Jusion : 252-255 °C
Stade D : 8-chloro-4-cyclopropyl-6-fluoro-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point de Jus ion : 190-192 °C
EXEMPLE 15 : 8-chloro-4-cyclopropyI-3,4-dihydro-7-méthyl-2^-l,2,4- benzothiadiazine 1,1-dioxyde
Stade A : 2-chloro-6-fluoro-3-méthylbenzènesulfonamide
Le produit attendu est obtenu à partir de la 2-chloro-6-fiuoro-3-méthylaniline selon le procédé décrit dans le stade A de l'Exemple 1.
2-chloro-6-cyclopropylamino-3-méthylbenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : δ-chloro^-cyclopropyl- 7-méthyl-4H-l, 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 24 heures à 130 °C) dans le stade C de l'Exemple 1. Point dejusion : 218-223 °C
Stade D : 8-chloro-4-cyclopropyl-3, 4-dihydro- 7-méthyl-2ïi-l, 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejusion : 230-232 °C
EXEMPLE 16 : 6τcyano-4-cyclopropyl-3,4-dihydro-2//-l,2,4-benzothiadiazine 1,1- dioxyde
Stade A : 4-cyano-2-fluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 4-cyano-2-fluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1. Point dejusion : 149-152 °C
[ : 4-cyano-2-cyclopropylaminobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 6-cyano-4-cycîopropyl-4H-l , 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 24 heures à 130 °C) dans le stade C de l'Exemple 1. Point de Jus ion : 273-276 °C
6-cyano-4-cyclopropyl-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1, 1 - dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. PoJM de 'Jusion : 178-180 °C
EXEMPLE 17 : 8-bromo-4-cycIopropyl-6-fluoro-3,4-dihydro-2^-l,2,4- benzothiadiazine 1,1-dioxyde
: 2-bromo-4, 6-difluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 2-bromo-4,6-difluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1. Point de 'Jusion : 122-124 °C
Stade B : 2-bromo-6-cyclopropylamino-4-fluorobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 8-bromo-4-cyclopropyl-6-fluoro-4H-l,2,4-benzothiadiazine 1,1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 3 heures à 130 0C) dans le stade C de l'Exemple 1. Pojnt de Jusion : 270-273 °C
^D ; 8-bromo-4-cyclopropyl-6-fluoro-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine
1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. PoiM de Jusion : 197-199 °C
EXEMPLE 18 : 4-cyclopropyl-8-trifluorométhyI-3,4-dihydro-2Jy-l,2,4- benzothiadiazine 1,1-dioxyde
Stade A : 2-fluoro-6-trifluorométhylbenzènesulfonamide
Le produit attendu est obtenu à partir de la 2-fluoro-6-trifluorométhylaniline selon le procédé décrit dans le stade A de l'Exemple 1. Point de 'Jusion : 114-118 °C
Stade B : 2-cyclopropylamino-6-trifluorométhylbenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 4-cyclopropyl-8-trifluorométhyl-4\{-l,2,4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 10 heures à 130 °C) dans le stade C de l'Exemple 1. Point de Jis ion : 195-197 °C
Stade D : 4-cyclopropyl-8-trifluorométhyl-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1, 1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point de Jusion : 239-241 °C
EXEMPLE 19 : 5-chloro-4-cyclopropyl-3,4-dihydro-2iy-l,2,4-benz(>thiadiazine 1,1- dioxyde
Stade A : 3-chloro-2-fluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 3-chloro-2-fluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1. PoJM dejusion : 149-153 °C
Stade B : 3-chloro-2-cyclopropylaminobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 5-chloro-4-cyclopropyl-4Yi-l,2,4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 24 heures à 130 °C) dans le stade C de l'Exemple 1. Point de Jk? ion : 159-160 °C . . . . . .
Stade D : 5-chloro-4-cyclopropyl-3 \4-dihydro-2Yi-l ,2,4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. P Qint _de Jus ion : 142-143 °C
EXEMPLE 20 : 8-bromo-6-chloro-4-cyclopropyl-3,4-dihydro-2/T-l,2,4- benzothiadiazine 1,1-dioxyde
Stade A : 2-bromo-4-chloro-6-fluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 2-bromo-4-chloro-6-fluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1.
Point dejMqn : 122-126 °C
Stade B : 2-bromo-4-chloro-6-cyclopropylaminobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 8-bromo-6-chloro-4-cyclopropyl-4H-l,2,4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 3 heures) dans le stade C de l'Exemple 1.
Stade D : 8-bromo-6-chloro-4-cyclopropyl-3, 4-dihydro-2K-l, 2, 4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejus ion - 177-180 °C
EXEMPLE 21 : 4-cyclopropyl-5-fluoro-3,4-dihydro-2/M,2,4-benzothiadiazine 1,1- dioxyde
Stade A : 2,3-difluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 2,3-difluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1. Point _de Jis ion : 151-153 °C
Stade B : 2-cyclopropylamino-3-fluorobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
4-cyclopropyl-5-fluoro-4H-l , 2, 4-benzothiadiazine 1, 1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 48 heures) dans le stade C de l'Exemple 1. Point dejusion : 151-152 0C
Stade D : 4-cyclopropyl-5-fluoro-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejusi on : 161-163 °C
EXEMPLE 22 : 6-bromo-4-cyclopropyl-3,4-dihydro-7-méthyl-2JÏ-l,2,4- benzothiadiazine 1,1-dioxyde
Stade A : 4-bromo-2-fluoro-5-méthylbenzènesulfonamide
Le produit attendu est obtenu à partir de la 4-bromo-2-fluoro-5-méthylaniline selon le procédé décrit dans le stade A de l'Exemple 1. Point dejusion : 124-125 °C
Stade B : 4-bromo-2-cyclopropylamino-5-méthylbenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 6-bromo-4-cyclopropyl- 7-méthyl-4R-l, 2, 4-benzothiadiazine 1, 1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 24 heures) dans le stade C de l'Exemple 1. Point dejusion : 219-2200C
Stade D : 6-bromo-4-cyclopropyl-3, 4-dïhydro- 7-méthyl-2H-l, 2, 4-benzothiadiazine 1, 1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. PpM deJusion : 199-200 °C
EXEMPLE 23 : 5,6-dichIoro-4-cyclopropyl-3,4-dihydro-2/y-l,2,4-benzothiadiazine
1,1-dioxyde
Stade A : 3,4-dichloro-2-fluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 3,4-dichloro-2-fluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1.
Stade B : 3,4-dichloro-2-cyclopropylaminobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 5, 6-dichloro-4-cyclopropyl-4H-l , 2, 4-benzothiadiazine 1, 1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 2 heures à 130 °C) dans le stade C de l'Exemple 1. Point de φjiqn : 183-185 0C
Stade D : 5, 6-dichloro-4-cyclopropyl-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejusiqn : 132-133 °C
EXEMPLE 24 : 8-bromo-4-cyclopropyl-3,4-dihydro-2/T-l,2,4-benzothiadiazine 1,1- dioxyde
Stade A : 2-bromo-6-fluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 2-bromo-6-fluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1. Point dejm ion : 185-187 °C
Stade B : 2-bromo-6-cyclopropylaminobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 8-bromo-4-cyclopropyl-4H-l, 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 1,5 heures) dans le stade C de l'Exemple 1.
Stade D : 8-bromo-4-cyclopropyl-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejusion : 189-191 °C
EXEMPLE 25 : 4-cyclopropyl-5,7-difluoro-3,4-dihydro-2,-ï-l,2,4-benzothiadiazine 1,1-dioxyde
Stade A : 2,3,5-trifluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 2,3,5-trifluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1. PpM dejusion : 115-117 °C
Stade B : 2-cyclopropylamino-3,5-difluorobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 40 heures) dans le stade B de l'Exemple 1.
; 4-cyclopropyl-5, 7-difluoro-4H-l, 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 3 heures à 130 °C) dans le stade C de l'Exemple 1. PpJM de Jusion : 160-163 °C
Stade D : 4-cyclopropyl-5, 7-difluoro-3, 4-dihydro-2H- 1, 2, 4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. P oint de Jus ion : 149-151 °C
EXEMPLE 26 : 4-cyclopropyI-5-fluoro-3,4-dihydro-6-méthyl-2i/-l,2,4- benzothiadiazine 1,1 -dioxyde
2,3-difluoro-4-méthylbenzènesulfonamide
Le produit attendu est obtenu à partir de la 2,3-difluoro-4-méthylaniline selon le procédé décrit dans le stade A de l'Exemple 1. PoJM de Jusion : 171-173 °C
Stade B : 2-cyclopropylamino-3-fluoro-4-méthylbenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 4-cyclopropyl-5-fluoro-6-méthyl-4H-l,2,4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 24 heures à 130 °C) dans le stade C de l'Exemple 1. PpJM dejusion : 189-192 °C
Stade D : 4-cyclopropyl-5-fluoro-3,4-dihydro-6-méthyl-2H-l,2,4-benzothiadiazine
1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejusion : 135-138 °C
EXEMPLE 27 : 8-chloro-4-cyclopropyl-7-fluoro-3,4-dihydro-2iï-l,2,4- benzothiadiazine 1,1-dioxyde
Stade A : 2-chloro-3, 6-difluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 2-chloro-3,6-difluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1. Point dejusion : 175-178 °C
Stade B : 2-chloro-6-cyclopropylamino-3-fluorobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 8-chloro-4-cyclopropyl-7-fluoro-4H-l,2,4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 24 heures à 130 °C) dans le stade C de l'Exemple 1. Point dejusion : 260-263 0C
Stade D : 8-chloro-4-cyclopropyl- 7-fluoro-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. PjoJnt dejMQn : 198-200 °C
EXEMPLE 28 : 4-cyclopropyl-3,4-dihydro-6-iodo-2/y-l,2,4-benzothiadiazine 1,1- dioxyde
Stade A : 2-fluoro-4-iodobenzènesulfonamide
Le produit attendu est obtenu à partir de la 2-fluoro-4-iodoaniline selon le procédé décrit dans le stade A de l'Exemple 1.
Stade B : 2-cyclopropylamino-4-iodobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 4-cyclopropyl-6-iodo-4B.-l,2,4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 24 heures à 130 °C) dans le stade C de l'Exemple 1. Point d_e Jus ion : 304-307 0C
Stade D : 4-cyclopropyl-3, 4-dihydro-6-iodo-2H-l , 2, 4-benzothiadiazine 1, 1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejusion : 183-185 °C
EXEMPLE 29 : 4-cyclopropyl-8-fluoro-3,4-dihydro-2iï-l,2,4-benzothiadiazine 1,1- dioxyde
Stade A : 2-cyclopropylamino-6-fluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 2,6-difluorobenzènesulfonamide commerciale selon le procédé décrit dans le stade B de l'Exemple 1.
Stade B : 4-cyclopropyl-8-fluoro-4H-l , 2, 4-benzothiadiazine 1, 1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 24 heures) dans le stade C de l'Exemple 5. Point de 'Jusion : 156-157 °C
Stade C : 4-cyclopropyl-8-fluoro-3, 4-dihydro-2ïl-l, 2, 4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejus ion : 177-179 °C
EXEMPLE 30 : 6,8-dibromo-4-cyclopropyl-3,4-dihydro-2//-l,2,4-benzothiadiazine 1,1-dioxyde
Stade A : 2,4-dibromo-6-fluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 2,4-dibromo-6-fluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1. Point de Jusion : 153-157 °C
Stade B : 2,4-dibromo-6-cyclopropylaminobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 6, 8-dibromo-4-cyclopropyl-4H-l ', 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade C de l'Exemple 1. Point dejμsion : 254-256 °C
_D : 6, 8-dibromo-4-cyclopropyl-3, 4-dihydro-2VL-l, 2, 4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejusion : 203-205 °C
EXEMPLE 31 : 5-chloro-4-cyclopropyl-6-fluoro-3,4-dihydro-2J7-l,2,4- benzothiadiazine 1,1-dioxyde
Stade A : 3-chloro-2,4-difluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 3-chloro-2,4-difluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1. PpM deJμsiQn : 128-132 °C
Stade B : 3-chloro-2-cyclopropylamino-4-fluorobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 5-chloro-4-cyclopropyl-6-fluoro-4H-l,2,4-benzothiadiazine 1,1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 2 heures à 130 °C) dans le stade C de l'Exemple 1. P_oint deju_siqn : 147-148 0C
Stade D : 5-chloro-4-cyclopropyl-6-fluoro-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point de Jusion : 141-143 °C
EXEMPLE 32 : 8-chloro-4-cyclopropyl-3,4-dihydro-2/M,2,4-benzothiadiazine 1,1- dioxyde
je A : 2-chloro-6-fluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 2-chloro-6-fluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1. Point de Jusion : 187-190 °C
Stade B : 2-chloro-6-cyclopropylaminobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 8-chloro-4-cyclopropyl-4\i-l,2,4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 2 heures à 130 °C) dans le stade C de l'Exemple 1. Point dejusion : 207-209 0C
Stade D : 8-chloro-4-cyclopropyl-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejusion : 182-184 °C
EXEMPLE 33 : 6-bromo-4-cycIopropyl-8-trifluorométhyl-3,4-dihydro-2/y-l,2,4- benzothiadiazine 1,1-dioxyde
Stade A : 4-bromo-2-fluoro-6-trifluorométhylbenzènesulfonamide
Le produit attendu est obtenu à partir de la 4-bromo-2-fluoro-6-trifluorométhylaniline selon le procédé décrit dans le stade A de l'Exemple 1. Point de Ju_sion : 133-135 0C
Stade B : 4-bromo-2-cyclopropylamino-6-trifluorométhylbenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 6-bromo-4-cyclopropyl-8-trifluorométhyl-4H-l,2,4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 6 heures) dans le stade C de l'Exemple 1. Point de Jusion : 253-254 °C
Stade D : 6-bromo-4-cyclopropyl-8-trifluorométhyl-3, 4-dihydro-2H-l, 2, 4- benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point de 'Jusion : 200-201 °C
EXEMPLE 34 : 6-bromo-4-cyclopropyl-7-fluoro-3,4-dihydro-2/M,2,4- benzothiadiazine 1,1-dioxyde
: 4-bromo-2,5-difluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 4-bromo-2,5-difluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1. Point dejusion : 159-163 0C
4-bromo-2-cyclopropylamino-5-fluorobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 6-bromo-4-cyclopropyl-7-fluoro-4YL-l,2,4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 24 heures) dans le stade C de l'Exemple 1. PpM dejusion : 218-219 0C
Stade D : 6-bromo-4-cyclopropyl- 7-fluoro-S, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1, 1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. PpM dejusion : 163-165 °C
EXEMPLE 35 : 6-bromo-4-cyclopropyl-3,4-dihydro-2/-r-l,2,4-benzothiadiazine 1,1- dioxyde
L4 : 4-bromo-2-cyclopropylaminobenzènesulfonamide
Le produit attendu est obtenu à partir de la 4-bromo-2-fluorobenzènesulfonamide commerciale selon le procédé décrit dans le stade B de l'Exemple 1.
Stade B : 6-bromo-4-cyclopropyl-4Yi-l,2,4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 24 heures à 130 °C) dans le stade C de l'Exemple 1. Point de 'Jusion : 268-271 °C
Stade C : 6-bromo-4-cyclopropyl-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejm ion : 180-181 °C
EXEMPLE 36 : 8-chloro-4-cycIopropyl-3,4-dihydro-5-méthyl-2Jy-l,2,4- benzothiadiazine 1,1-dioxyde
ie A : 6-chloro-2-fluoro-3-méthylbenzènesulfonamide
Le produit attendu est obtenu à partir de la 6-chloro-2-fluoro-3-méthylaniline selon le procédé décrit dans le stade A de l'Exemple 1. Point _dβjks ion : 174-176 °C
Stade B : 6-chloro-2-cyclopropylamino-3-méthylbenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 48 heures) dans le stade B de l'Exemple 1.
: 8-chloro-4-cyclopropyl-5-méthyl-4H-l, 2, 4-benzothiadiazine 1, 1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade C de l'Exemple 1.
Stade D : 8-chloro-4-cyclopropyl-3, 4-dihydro-5-méthyî-2H-l , 2, 4-benzothiadiazine 1, 1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejmion : 215-217 °C
EXEMPLE 37 : 4-cyclopropyl-3,4-dihydro-6-méthyl-2^-l,2,4-benzothiadiazine 1,1- dioxyde
Stade A : 2-fluoro-4-méthylbenzènesulfonamide
Le produit attendu est obtenu à partir de la 2-fluoro-4-méthylaniline selon le procédé décrit dans le stade A de l'Exemple 1. Point dejmion : 136-137 °C
J? : 2-cyclopropylamino-4-méthylbenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 24 heures) dans le stade B de l'Exemple 1.
Stade C : 4-cyclopropyl-6-méthyl-4Y{-l , 2, 4-benzothiadiazine 1, 1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade C de l'Exemple 1. Point dejmion : 224-226 0C
Stade D : 4-cyclopropyl-3, 4-dihydro-6-méthyl-2H-l , 2, 4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejusion : 157-158 °C
EXEMPLE 38 : 4-cyclopropyl-6,8-difluoro-3,4-dihydro-2//-l,2,4-benzothiadiazine 1,1-dioxyde
: 2, 4, 6-trifluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 2,4,6-trifluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1. Point de 'Jusion : 102-106 °C
; ; 2-cyclopropylamino-4, 6-difluorobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 4-cyclopropyl-6, 8-difluoro-4H-l, 2, 4-benzothiadiazine 1, 1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 24 heures) dans le stade C de l'Exemple 1. Point dejusion : 167-168 °C
4-cyclopropyl-6, 8-difluoro-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1, 1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. ?_ojnt dejusion : 161-164 °C
EXEMPLE 39 : 4-cyclopropyl-5,6-difluoro-3,4-dihydro-2iï-l,2,4-benzothiadiaziiie 1,1-dioxyde
2,3,4-trifluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 2,3,4-trifluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1.
PoM deJmion : 111-114 °C
2-cyclopropylamino-3,4-difluorobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 4-cyclopropyl-5, 6-difluoro-4H-l, 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 6 heures) dans le stade C de l'Exemple 1. Point dejusiqn - 182-184 °C
Stade D : 4-cyclopropyl-5, 6-difluoro-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point de Jusion : 160-162 °C
EXEMPLE 40 : 7-bromo-4-cycIopropyl-3,4-dihydro-2JfiT-l,2,4-benzothiadiazine 1,1- dioxyde
Stade A : 5-bromo-2-fluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 5-bromo-2-fluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1. Point Aejis ion : 149-151 °C
5-bromo-2-cyclopropylaminobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
7-bromo-4-cyclopropyl-4H-l , 2,4-benzothiadiazine I11-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 5 heures à 130 °C) dans le stade C de l'Exemple 1. Point de Ju_sion : 242-244 °C
7-bromo-4-cyclopropyl-3 , 4-dihydro-2H-l, 2, 4-benzothiadiazine 1, 1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. PpM de 'Jusion : 178-179 °C
EXEMPLE 41 : 4-cyclopropyl-3,4-dihydro-7-nitro-2#-l,2,4-benzothiadiazine 1,1- dioxyde
2-chloro-5-nitrobenzènesulfonamide
Une portion d'acide acétique glacial (16O mL) est saturé pendant 30 minutes par de l'anhydride sulfureux gazeux. A cette solution refroidie sur bain de glace est ajoutée sous agitation une solution aqueuse de CuCl2 (7 g dans 20 mL) (suspension A).
La 2-chloro-5-nitroaniline (15 g) est dissoute dans un mélange d'acide acétique glacial (160 mL) et de HCl concentré (40 mL). A cette solution refroidie sur bain de glace et de sel (-5 °C) est ajoutée goutte à goutte et sous agitation une solution aqueuse de NaNO2 (8 g dans 20 mL). Au terme de l'addition, cette solution est mélangée lentement sous agitation à la suspension A. Après 15 minutes d'agitation, la suspension est versée sur de la glace (400 g). Le précipité formé est recueilli par filtration, lavé à l'eau et redissous immédiatement dans le dioxanne (15O mL). La solution obtenue est ajoutée progressivement sous agitation à une solution aqueuse concentrée d'ammoniaque (300 mL) préalablement refroidie sur bain de glace. Après 30 minutes d'agitation, le solvant organique et une partie de l'ammoniaque sont éliminés par évaporation sous dépression. La solution/suspension aqueuse obtenue est ajustée à pH neutre par addition de HCl 6 N. Le
précipité formé est recueilli par filtration et lavé à l'eau. Il est mis en suspension dans de l'eau (200 mL) et additionné de NaOH 10 % jusqu'à pH clairement alcalin. La suspension est chauffée pour favoriser la dissolution du produit du titre. L'insoluble persistant est éliminé par filtration à chaud. Le filtrat refroidi est ajusté à pH neutre ou légèrement acide par addition de HCl 6 N. Le précipité est recueilli sur filtre, lavé à l'eau et séché. Point de Jusion : 180-183 °C
2-cyclopropyla.mino-5-nitrobenzenesulfona.mide
Dans une enceinte hermétique contenant un mélange de dioxanne (70 mL) et de cyclopropylamine (3,5 mL) est introduit le 2-chloro-5-nitrobenzènesulfonamide (5 g) préparé lors de l'étape précédente. L'enceinte hermétique est placée à l'étuve à 100 °C pendant 24 heures. Après ce laps de temps, le solvant et le réactif sont éliminés par concentration sous dépression. Le résidu est repris par du méthanol (20 mL) et l'insoluble constitué du produit du titre est recueilli par filtration, lavé au méthanol et séché.
4-cyclopropyl- 7-nitro-4H-l, 2, 4-benzothiadiazine 1, 1-dioxyde
Dans un ballon, le mélange de 2-cyclopropylamino-5-nitrobenzènesulfonamide (5 g), issue de l'étape précédente, et d'orthoformiate d'éthyle (50 mL) est chauffé en vase ouvert à 130 °C pendant 3 heures. La suspension obtenue est refroidie sur bain de glace et l'insoluble est recueilli par filtration, lavé à l'éther et séché. Point dejusion : 233-235 °C
Stade D : 4-cyclopropyl-3,4-dihydro-7-nitro-2H-l,2,4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejusion : 198-201 0C
EXEMPLE 42 : 7-acétamido-4-cyclopropyl-3,4-dihydro-2//-l,2,4-benzothiadiazine 1,1-dioxyde
7-amino-4-cyclopropyl-4H-l , 2, 4-benzothiadiazine 1, 1-dioxyde
Une solution de 4-cyclopropyl-7-nitro-4H-l,2,4-benzothiadiazine 1,1-dioxyde (5 g ; préparé lors du stade C de l'Exemple 41) dans l'éthanol (18O mL) est additionné de charbon palladié à 10 % (500 mg). La suspension est placée à l'hydrogénateur sous 10 atmosphères de H2 pendant 30 minutes à température ambiante. La suspension est concentrée à siccité sous dépression et le résidu est repris par de l'acétone bouillant (300 mL). L'insoluble est éliminé par filtration à chaud et lavé avec de l'acétone bouillant. Le filtrat est concentré à siccité et le résidu est recristallisé dans le méthanol. Point dejusion - 283-285 °C
Stade B : 7-acétamido-4-cyclopropyl-3 , 4-dihydro-2H-l, 2, 4-benzothiadiazine 1,1- dioxyde
La solution de 7-amino-4-cyclopropyl-4H-l,2,4-benzothiadiazine 1,1-dioxyde préparé dans l'étape précédente (0,5 g) dans le dioxanne (2O mL) est additionnée de chlorure d'acétyle (0,5 mL) et mise sous agitation à température ambiante pendant 16 heures. Après élimination du solvant par distillation sous pression réduite, le résidu est repris par de l'eau et le précipité de 7-acétamido-4-cyclopropyl-4H-l,2,4-benzothiadiazine 1,1-dioxyde est recueilli par filtration, lavé à l'eau et séché. Il est engagé directement dans l'étape suivante afin d'obtenir le produit attendu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejusion : 230-232 °C
EXEMPLE 43 : 6,7-dichloro-4-cyclobutyl-3,4-dihydro-2J7-l,2,4-benzothiadiazine 1,1- dioxyde
Stade A : 4,5-dichloro-2-cyclobutylarninobenzènesulfonamide
Le produit attendu est obtenu à partir de la 4,5-dichloro-2-fluoroaniline selon le procédé décrit dans les stades A et B de l'Exemple 1 avec l'addition de la cyclobutylamine lors de l'étape B.
Stade B : 6, 7-dichloro-4-cyclobutyl-4H-l , 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 24 heures) dans le stade C de l'Exemple 1. PpJM de Jmion : 238-240 °C
Stade C : 6, 7-dichloro-4-cyclobutyl-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point de Jusion : 161-163 0C
EXEMPLE 44 : 7-chloro-4-cyclobutyl-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1- dioxyde
: 4-cyclobutyl-7-nitro-4H-l,2,4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu à partir de la 2-chloro-5-nitroaniline selon le procédé décrit dans les stades A, B et C de l'Exemple 41 avec l'addition de la cyclobutylamine lors de l'étape B.
Point de Jusion : 229-232 °C
Stade B : 7-amino-4-cyclobutyl-4H-l,2,4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade A de l'Exemple 42. Point de Jusion : 278-280 °C
7-chloro-4-cyclobutyl-4Yi-l,2,4-benzothiadiazine 1,1-dioxyde
Une solution de CuSO4.5H2O (84 g) et de NaCl (22,5 g) dans l'eau (200 mL) est refroidie sur bain de glace et additionnée goutte à goutte d'une solution aqueuse de Na2S2O5 (22,5 g dans 10O mL). Après 15 minutes d'agitation, le précipité de Cu2Cl2 est recueilli par filtration et lavé à l'eau.
Une solution de 7-amino-4-cyclobutyl-4H-l,2,4-benzothiadiazine 1,1-dioxyde préparé lors de l'étape précédente (3,48 g) dans le HCl 6 N (40 mL) est refroidie sur bain de glace, puis additionnée goutte à goutte d'une solution aqueuse de NaNO2 (2 g dans 15 mL). La solution obtenue est ajoutée progressivement à la solution de Cu2Cl2 dans le HCl concentré
(30 mL). Après 30 minutes d'agitation à température ambiante, le milieu réactionnel est additionné d'eau (150 mL) et le précipité obtenu est recueilli par filtration, lavé à l'eau et séché.
Point de Jusion : 229-231 0C
7-chloro-4-cyclobutyl-3, 4-dihydro-2R-l, 2, 4-benzothiadiazine 1,1- dioxyde
La solution de 7-chloro-4-cyclobutyl-4H-l,2,4-benzothiadiazine 1,1-dioxyde issue de l'étape précédente (3 g) dans l'isopropanol (10O mL) est additionnée de NaBH4 (2,5 g) finement broyé, puis chauffée pendant 10 minutes à 55 °C. Le solvant est éliminé par évaporation sous dépression. Le résidu est repris par de l'eau (100 mL) et amené à pH acide par addition de HCl 6 N. Le produit du titre est extrait par le chloroforme
(3 x 50 mL). La phase organique est séchée sur MgSO4 et filtrée. Le filtrat est évaporé à siccité et le résidu est purifié par chromatographie sur colonne de silice (phase mobile : chloroforme). Le produit obtenu est recristallisé dans le méthanol.
Point dejusiqn : 162-164 0C
EXEMPLE 45 : 6-chloro-4-cyclobutyl-3,4-dihydro-2/y-l,2,4-benzothiadiazine 1,1- dioxyde
Stade A : 4-chloro-2-cyclobutylaminobenzènesulfonamide
Le produit attendu est obtenu à partir de la 4-chloro-2-fluoroaniline selon le procédé décrit dans les stades A et B de l'Exemple 1 avec l'addition de la cyclobutylamine lors de l'étape B.
Stade B : 6-chloro-4-cyclobutyl-4\i-l,2,4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 6 heures à 130 °C) dans le stade C de l'Exemple 1. PoJM de φsion : 224-226 °C
6-chloro-4-cyclobutyl-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. PpM de Jusion : 183-185 °C
EXEMPLE 46 : 4-cydobutyl-3,4-dihydro-7-nitro-2/M,2,4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu à partir de la 4-cyclobutyl-7-nitro-4H-l,2,4-benzothiadiazine 1,1-dioxyde (préparée lors du stade A de l'Exemple 44) selon le procédé décrit dans le stade D de l'Exemple 1.
PoM dejusion : 188-190 °C
EXEMPLE 47 : 6,7-dichloro-4-cycIopentyl-3,4-dihydπ>-2/y-l,2,4-beiizothiadiazine 1,1-dioxyde
Stade A : 4,5-dichloro-2-cyclopentylaminobenzènesulfonamide
Le produit attendu est obtenu à partir de la 4,5-dichloro-2-fluoroaniline selon le procédé décrit dans les stades A et B de l'Exemple 1 avec l'addition de la cyclopentylamine lors de l'étape B.
: 6, 7-dichloro-4-cyclopentyl-4H-l , 2, 4-benzothiadiazine 1, 1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 72 heures à 140 °C) dans le stade C de l'Exemple 5. Point de Jusion : 189-191 °C
Stade C : 6, 7-dichloro-4-cyclopentyl-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejusion : 221-224 °C
EXEMPLE 48 : 7-chloro-4-cycIopentyl-3,4-dihydro-2/r-l,2,4-benzothiadiazine 1,1- dioxyde
5-chloro-2-cyclopentylaminobenzènesulfonamide
Le produit attendu est obtenu à partir de la 5-chloro-2-fluoroaniline selon le procédé décrit dans les stades A et B de l'Exemple 1 avec l'addition de la cyclopentylamine lors de l'étape B.
7-chloro-4-cyclopentyl-4H-l, 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 96 heures) dans le stade C de l'Exemple 5. Point de 'Jusion : 218-220 °C
Stade C : 7-chloro-4-cyclopentyl-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejusion : 193-194 0C
EXEMPLE 49 : 6-chloro-4-cyclopentyl-3,4-dihydro-2#-l,2,4-benzothiadiazine 1,1- dioxyde
Stade A : 4-chloro-2-cyclopentylaminobenzènesulfonamide
Le produit attendu est obtenu à partir de la 4-chloro-2-fluoroaniline selon le procédé décrit dans les stades A et B de l'Exemple 1 avec l'addition de la cyclopentylamine lors de l'étape B.
Stade B : 6-chloro-4-cyclopentyl-4YL-l,2,4-benzothiadiazine 1,1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade C de l'Exemple 5. Point dejusion : 170-172 °C
6-chloro-4-cyclopentyl-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1, 1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejus ion : 175-177 0C
EXEMPLE 50 : 6,7-dichloro-4-cyclohexyl-3,4-dihydro-2#-l,2,4-beiizothiadiazine 1,1- dioxyde
Stade A : 4,5-dichloro-2-cyclohexylaminobenzènesulfonamide
Le produit attendu est obtenu à partir de la 4,5-dichloro-2-fluoroaniline selon le procédé décrit dans les stades A et B de l'Exemple 1 avec l'addition de la cyclohexylamine chauffée à 80 °C en enceinte hermétique pendant 72 heures lors de l'étape B.
Stade B : 6, 7-dichloro-4-cyclohexyl-4ïl-l, 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 72 heures à 140 °C) dans le stade C de l'Exemple 5. Point dejusion : 219-222 °C
6, 7-dichloro-4-cyclohexyl-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. PpJM dejusion : 207-209 °C
EXEMPLE 51 : 7-chloro-4-cyclohexyl-3,4-dihydro-2iy-l,2,4-benzothiadiazine 1,1- dioxyde
L4 : 5-chloro-2-cyclohexylaminobenzènesulfonamide
Le produit attendu est obtenu à partir de la 5-chloro-2-fluoroaniline selon le procédé décrit dans les stades A et B de l'Exemple 1 avec l'addition de la cyclohexylamine lors de l'étape B.
Stade B : 7-chloro-4-cyclohexyl-4îî-l, 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 5 heures à 130 °C) dans le stade C de l'Exemple 1. PoM dejusion : 209-211 °C
Stade C : 7-chloro-4-cyclohexyl-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. PpM dejusion : 233-235 °C
EXEMPLE 52 : 6-chloro-4-cyclohexyl-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1- dioxyde
Stade A : 4-chloro-2-cyclohexylaminobenzènesulfonamide
Le produit attendu est obtenu à partir de la 4-chloro-2-fluoroaniline selon le procédé décrit dans les stades A et B de l'Exemple 1 avec l'addition de la cyclohexylamine lors de l'étape B.
Stade B : 6-chloro-4-cyclohexyl-4W-l,2,4-benzothiadiazine 1,1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 48 heures à 130 0C) dans le stade C de l'Exemple 1. Point de jMon : 189-191 0C
: 6-chloro-4-cyclohexyl-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejusion : 178-180 °C
EXEMPLE 53 : 6,7-dichloro-4-cycloheptyl-3,4-dihydro-2i7-l,2,4-benzothiadiaziiie 1,1-dioxyde
Stade A : 4,5-dichloro-2-cycloheptylaminobenzènesulfonamide
Le produit attendu est obtenu à partir de la 4,5-dichloro-2-fluoroaniline selon le procédé décrit dans les stades A et B de l'Exemple 1 avec l'addition de la cycloheptylamine lors de l'étape B.
Stade B : 6, 7-dichloro-4-cycloheptyl-4H-l , 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 72 heures à 140 °C) dans le stade C de l'Exemple 5. Point de Jusion : 222-224 °C
6, 7-dichloro-4-cycloheptyl-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point de Jusion : 191-192 °C
EXEMPLE 54 : 7-chloro-4-cycIoheptyl-3,4-dihydro-2//-l,2,4-benzothiadiazine 1,1- dioxyde
: 5-chloro-2-cycloheptylaminobenzènesulfonamide
Le produit attendu est obtenu à partir de la 5-chloro-2-fluoroaniline selon le procédé décrit dans les stades A et B de l'Exemple 1 avec l'addition de la cycloheptylamine lors de l'étape B.
Stade B : 7-chloro-4-cycloheptyl-4H-l, 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 24 heures à 130 °C) dans le stade C de l'Exemple 1. Point dejusion : 241-243 °C
Stade C : 7-chloro-4-cycloheptyl-3,4-dihydro-2\l-l,2,4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejusion : 216-218 0C
EXEMPLE 55 : 6-chloro-4-cycloheptyl-3,4-dihydro-2iï-l,2,4-benzothiadiazine 1,1- dioxyde
L^ : 4-chloro-2-cycloheptylaminobenzènesulfonamide
Le produit attendu est obtenu à partir de la 4-chloro-2-fluoroaniline selon le procédé décrit dans les stades A et B de l'Exemple 1 avec l'addition de la cycloheptylamine lors de l'étape B.
Stade B : 6-chloro-4-cycloheptyl-4H-l,2,4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 72 heures à 130 °C) dans le stade C de l'Exemple 1. Point dejusion : 209-211 °C
Stade C : 6-chloro-4-cycloheptyl-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. PpM dejusion : 149-151 °C
EXEMPLE 56 : 6,7-dichloro-4-cyclooctyl-3,4-dihydro-2J7-l,2,4-benzothiadiazine 1,1- dioxyde
4,5-dichloro-2-cyclooctylaminobenzènesulfonamide
Le produit attendu est obtenu à partir de la 4,5-dichloro-2-fluoroaniline selon le procédé décrit dans les stades A et B de l'Exemple 1 avec l'addition de la cycloocty lamine chauffée à 80 °C en enceinte hermétique pendant 72 heures lors de l'étape B.
6, 7-dichloro-4-cyclooctyl-4H-l , 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 72 heures à 140 °C) dans le stade C de l'Exemple 5. Point de 'Jusion : 229-231 °C
Stade C : 6, 7-dichloro-4-cyclooctyl-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. PoM dejusion : 154-155 °C
EXEMPLE 57 : 7-chloro-4-cyclooctyl-3,4-dihydro-2/-r-l,2,4-benzothiadiazine 1,1- dioxyde
Stade A : 5-chloro-2-cyclooctylaminobenzènesulfonamide
Le produit attendu est obtenu à partir de la 5-chloro-2-fluoroaniline selon le procédé décrit dans les stades A et B de l'Exemple 1 avec l'addition de la cycloocty lamine lors de l'étape B.
Stade B : 7-chloro-4-cyclooctyl-4H-l , 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 24 heures à 130 °C) dans le stade C de l'Exemple 1. Point Je Jusion : 235-237 °C
7-chloro-4-cyclooctyl-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point de Jusion : 184-186 °C
EXEMPLE 58 : 6-chloro-4-cyclooctylO,4-dihydro-2iï-l,2,4-beiizothiadiaziiie 1,1- dioxyde
4-chloro-2-cyclooctylaminobenzènesulfonamide
Le produit attendu est obtenu à partir de la 4-chloro-2-fluoroaniline selon le procédé décrit dans les stades A et B de l'Exemple 1 avec l'addition de la cyclooctylamine lors de l'étape B.
Stade B : 6-chloro-4-cyclooctyl-4W-l,2,4-benzothiadiazine 1,1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 48 heures à 130 0C) dans le stade C de l'Exemple 1. Point de Jusion : 209-211 °C
Stade C : 6-chloro-4-cyclooctyl-3, 4-dihydro-2ïi- 1, 2, 4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point de Jusion : 141-143 °C
EXEMPLE 59 : 6,7-dichloro-4-(l-méthyl)cyclopropyl-3,4-dihydro-2iy-l,2,4- benzothiadiazine 1,1-dioxyde
Stade A : 4, 5-dichloro-2-(l -méthyl)cyclopropylaminobenzènesulfonamide
Le produit attendu est obtenu à partir de la 4,5-dichloro-2-fluoroaniline selon le procédé décrit dans les stades A et B de l'Exemple 1 avec l'addition de la (l-méthyl)cyclopropylamine lors de l'étape B. Point de Jusion : 130-132 °C
Stade B : 6, 7-dichloro-4-(l -méthyl)cyclopropyl-4H-l ,2,4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 24 heures) dans le stade C de l'Exemple 1. Point dejusion : 230-232 0C
Stade C : 6, 7-dichîoro-4-(l-méthyî)cyclopropyl-2H-l,2,4-benzothiadiazine 1,1- dioxyde Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejusion : 162-163 °C
EXEMPLE 60 : 7-chloro-4-cy clopropylméthyl-3,4-dihydro-2//-l ,2,4-benzothiadiazine 1,1-dioxyde
Stade A : 7-chloro-4\ϋ-l,2,4-benzothiadiazine 1,1-dioxyde
Le mélange de 2-amino-5-chlorobenzènesulfonamide (obtenu selon J. Chem. Soc. Perkin I, 1043-1047, 1979) et d'orthoformiate d'éthyle (4O mL) est porté à ébullition pendant 30 minutes en vase ouvert. Le volume du milieu est réduit de moitié sous pression réduite. Le précipité obtenu est recueilli par filtration, lavé à l'éther et séché. PQM Ae Jis ion : 243-244 °C
Stade B : 7-chloro-4-cyclopropylméthyl-4H-l,2,4-benzothiadiazine 1,1-dioxyde
La solution de 7-chloro-4H-l,2,4-benzothiadiazine 1,1-dioxyde (1 g) dans l'acétonitrile (40 mL) est additionnée de carbonate potassique (2,5 g) et de bromure de cyclopropylméthyle (0,7 mL) et le mélange est porté à reflux pendant 24 heures. Le milieu réactionnel est évaporé sous pression réduite et le résidu est repris par de l'eau (40 mL). L'insoluble est recueilli par filtration, lavé à l'eau et séché. Il est recristallisé dans le méthanol. Point de Jusion : 183-185 °C
Stade C : 7-chloro-4-cyclopropylméthyl-3, 4-dihydro-2îî-l, 2, 4-benzothiadiazine 1,1-dioxyde
La solution de 7-chloro-4-cyclopropylméthyl-4H-l,2,4-benzothiadiazine 1,1-dioxyde (0,7 g) dans Pisopropanol (50 mL) est additionnée de borohydrure sodique (0,2 g) et le mélange est chauffé à 50 °C pendant 5 minutes. Le milieu réactionnel est évaporé sous pression réduite et le résidu est repris par de l'eau (30 mL). Le pΗ du milieu est ajusté à 5-6 par ajout d'acide chlorhydrique .6 N et la suspension est extraite trois fois par le chloroforme (30 mL). Les phases organiques sont rassemblées, séchées sur MgSO4 anhydre et filtrées. Le filtrat est évaporé sous pression réduite et le résidu est repris par du méthanol (5 mL). A la solution méthanolique est ajoutée de l'eau (50 mL) et le précipité qui apparaît est recueilli par filtration, lavé à l'eau et séché. PpM de Jusion : 106-109 0C
EXEMPLE 61 : 4-cyclopropylméthyl-7-fluoro-3,4-dihydro-2//-l,2,4-benzothiadiazine 1,1-dioxyde
Stade A : 7-fluoro-4H-l,2,4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu à partir de la 2-amino-5-fiuorobenzènesulfonamide selon le procédé décrit dans le stade A de l'Exemple 60. Point de Jusion : 269-270 0C
Stade B : 4-cyclopropylméthyl- 7-fluoro-4H-l, 2, 4-benzothiadiazine 1, 1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 60. Point dejusion : 155-157 °C
Stade C : 4-cyclopropylméthyl- 7-fluoro-S, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade C de l'Exemple 60. Point dejusion : 102-105 °C
EXEMPLE 62 : 4-cyclopropyl-7,8-difluoro-3,4-dihydro-2iy-l,2,4-benzothiadiazme 1,1-dioxyde
Stade A : 2,3,6-trifluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 2,3,6-trifluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1. Point dejusion : 148-151 °C
Stade B : 2-cyclopropylamino-5,6-difluorobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 4-cyclopropyl- 7, 8-difluoro-4H-l, 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 2 heures à 130 °C) dans le stade C de l'Exemple 1. Point dejusion : 205-206 °C
4-cyclopropyl- 7, 8-difluoro-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1, 1 - dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point de Jmiqn : 199-201 °C
EXEMPLE 63 : 6-cyano-4-cyclopropyl-7-fluoro-3,4-dihydro-2#-l,2,4- benzothiadiazine 1,1-dioxyde
L4 ; 2,5-difluoro-4-sulfamoylbenzonitrile
Le produit attendu est obtenu à partir de la 4-cyano-2,5-difluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1.
Stade B : 2-cyclopropylamino-2-fluoro-4-sulfamoylbenzonitrile
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : ό-cyano-4-cyclopropyl- 7-fluoro-4H-l, 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 24 heures à 130 0C) dans le stade C de l'Exemple 1. Point dejusion : 205-207 °C
Stade D : 6-cyano-4-cyclopropyl- 7-fluoro-S, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1,1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point de Jis ion : 208-210 °C
EXEMPLE 64 : 6-bromo-4-cycIopropyl-8-fluoro-3,4-dihydro-2/7-l,2,4- benzothiadiazine 1,1-dioxyde
Stade A : 4-bromo-2, 6-difluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 4-bromo-2,6-difluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1. Point dejus ion : 142-146 0C
Stade B : 4-bromo-2-cyclopropylamino-6-fluorobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 6-bromo-4-cyclopropyl-8-fluoro-4H-l,2,4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 72 heures à 130 °C) dans le stade C de l'Exemple 1. Point de Jusion - 285-287 0C
Stade D : 6-bromo-4-cyclopropyl-8-fluoro-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point de Jmiqn : 195-198 °C
EXEMPLE 65 : 6-bromo-4-cyclopropyl-5-fluoro-3,4-dihydro-2/T-l,2,4- benzothiadiazine 1,1-dioxyde
Stade A : 4-bromo-2,3-difluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 4-bromo-2,3-difiuoroaniline selon le procédé décrit dans le stade A de l'Exemple 1.
Point deJmiQn : 155-157 °C
Stade B : 4-bromo-2-cyclopropylamino-3-fluorobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 6-bromo-4-cyclopropyl-5-fluoro-4H-l, 2, 4-benzothiadiazine 1, 1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 3 heures à 130 °C) dans le stade C de l'Exemple 1. Point de Jusion : 244-247 °C
Stade D : 6-br omo-4-cyclopropyl-5 -fluor o-S, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point de Jus JQU • 197-199 °C
EXEMPLE 66 : 7-bromo-4-cyclopropyl-6-fluoro-3,4-dihydro-2iï-l,2,4- benzothiadiazine 1,1-dioxyde
: 5-bromo-2,4-difluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 5-bromo-2,4-difluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1. PoiM de 'Jusion : 109-111 0C
Stade B : 5-bromo-2-cyclopropylamino-4-fluorobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 7 -bromo-4-cyclopropyl-6-fluoro-4Α-l ,2,4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 4 heures à 130 °C) dans le stade C de l'Exemple 1. Point dejusion : 228-231 °C
Stade D : 7-bromo-4-cyclopropyl-6-fluoro-3,4-dihydro-2\i-l,2,4-benzothiadiazine
1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejusion : 175-177 0C
EXEMPLE 67 : 4-cyclopropyl-5,7,8-trifluoro-3,4-dihydro-2iy-l,2,4-benzothiadiazine 1,1-dioxyde
Stade A : 2-cyclopropylamino-3,5,6-trifluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 2,3,5,6-tétrafluorobenzènesulfonamide commerciale selon le procédé décrit dans le stade B de l'Exemple 1.
\ : 4-cyclopropyl-5, 7, 8-trifluoro-4H-l, 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 4 heures à 130 °C) dans le stade C de l'Exemple 1. Point Je Jusion : 166-168 °C
Stade C : 4-cyclopropyl-5, 7,8-trifluoro-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejusion : 149-151 °C
EXEMPLE 68 : 7-chIoro-4-cyclopropyl-6-fluoro-3,4-dihydro-2i/-l,2,4- benzothiadiazine 1,1-dioxyde
5-chloro-2-cyclopropylamino-4-fluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 5-chloro-2,4-difluorobenzènesulfonamide commerciale selon le procédé décrit dans le stade B de l'Exemple 1.
Stade B : 7-chloro-4-cyclopropyl-6-fluoro-4H-l,2,4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 5 heures à 130 °C) dans le stade C de l'Exemple 1. Point dejus ion : 217-219 0C
Stade C : 7-chloro-4-cyclopropyl-6-fluoro-3,4-dihydro-2\{-l,2,4-benzothiadiazine
1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. P oint de Jis ion : 155-158 0C
EXEMPLE 69 : 7-aminocarbonyl-4-cyclopropyl-3,4-dihydro-2i/-l,2,4- benzothiadiazine 1,1-dioxyde
Stade A : 4-fluoro-3-sulfamoylbenzamide
La solution d'acide 4-fluoro-3-sulfamoylbenzoïque (5,4 mmol) dans le chlorure de thionyle (10 mL) est portée à reflux pendant 4 heures. Le réactif est ensuite éliminé par distillation sous pression réduite et le résidu est redissous dans le toluène sec (10 mL). Le solvant est éliminé par distillation sous pression réduite. Cette opération est renouvelée à deux reprises, puis le résidu est dissous dans le dioxanne sec (10 mL) et additionné d'ammoniaque (6 mmol) et de pyridine (6 mmol). Après une heure, le solvant est éliminé
sous dépression et le résidu est repris par le méthanol (5 mL), puis additionné d'eau (30 mL). Le précipité obtenu est recueilli par filtration, lavé à l'eau et séché. Point dejusiqn : 212-214 °C
: 4-cyclopropylamino-3-sulfamoylbenzamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 7-aminocarbonyl-4-cyclopropyl-4H-l,2,4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 3 heures à 130 °C) dans le stade C de l'Exemple 1. Point dejusiqn : 278-281 °C
Stade D : 7-aminocarbonyl-4-cyclopropyl-3,4-dihydro-2H-l,2,4-benzothiadiazine
1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point de Jusion : 269-271 0C
EXEMPLE 70 : 7-aminocarbonyl-4-cyclopropyl-3,4-dihydro-iV-méthyl-2/-r-l,2,4- benzothiadiazine 1,1-dioxyde
Stade A : 4-fluoro-N-méthyl-3-sulfamoylbenzamide
Le produit attendu est obtenu en utilisant la méthy lamine à la place de l'ammoniaque selon le procédé décrit dans le stade A de l'Exemple 69. Point dejusiqn : 242-244 °C
Stade B : 4-cyclopropylamino-N-méthyl-3-sulfamoylbenzamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
7-aminocarbonyl-4-cyclopropyl-N-méthyl-4H-l,2,4-benzothiadiazine 1, 1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 3 heures à 130 0C) dans le stade C de l'Exemple 1. Point dejusion : 300-305 °C
7-aminocarbonyl-4-cyclopropyl-3, 4-dihydro-N-méthyl-2H-l, 2, 4- benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. PoM dejusion : 271-273 °C
EXEMPLE 71 : 7-aminocarbonyl-4-cyclopropyl-3,4-dihydro-iV^V-diméthyl-2fl-l,2,4- benzothiadiazine 1,1-dioxyde
Stade A : 4-fluoro-N,~N-diméthyl-3-sulfamoylbenzamide
Le produit attendu est obtenu en utilisant la diméthylamine à la place de l'ammoniaque selon le procédé décrit dans le stade A de l'Exemple 69.
Stade B : 4-cyclopropylamino-N,N-diméthyl-3-sulfamoylbenzamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
7-aminocarbonyl-4-cyclopropyl-Η£i-diméthyl-4Y{-l, 2, 4- benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 3 heures à 130 °C) dans le stade C de l'Exemple 1. PoM dejusion : 173-175 °C
Stade D : 7-aminocarbonyl-4-cyclopropyl-3 , 4-dihydro-N,N-diméthyl-2Y{-l , 2, 4- benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point de Jmiqn : 216-219 0C
EXEMPLE 72 : 8-bromo-6-cyano-4-cyclopropyI-3,4-dihydro-2/7-l,2,4- benzothiadiazine 1,1-dioxyde
Stade A : 3-bromo-5-fluoro-4-sulfamoylbenzonitrile
Le produit attendu est obtenu à partir de la 2-bromo-4-cyano-5-fluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1.
Stade B : 3-bromo-5-cyclopropylamino-4-sulfamoylbenzonitrile
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 8-bromo-6-cyano-4-cyclopropyl-4H-l, 2, 4-benzothiadiazine 1, 1-dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 3 heures à 130 °C) dans le stade C de l'Exemple 1.
Stade D : 8-bromo-6-cyano-4-cyclopropyl-3,4-dihydro-2H-l,2,4-benzothiadiazine
1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point de Jusion : 250-253 °C
EXEMPLE 73 : 7-amino-4-cyclopropyl-3,4-dihydro-2//-l,2,4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1, à partir du 7-amino-4-cyclopropyl-4//-l,2,4-benzothiadiazine 1,1-dioxyde préparé au stade A de l'Exemple 42.
Point dejusion : 187-189 °C
EXEMPLE 74 : 4-cyclopropyl-3,4-dihydro-6-nitro-2/M,2,4-benzothiadiazine 1,1- dioxyde
Stade A : 2-fluoro-4-nitrobenzènesulfonamide
Le produit attendu est obtenu à partir de la 2-fluoro-4-nitroaniline selon le procédé décrit dans le stade A de l'Exemple 41. Point dejusion : 145-147 °C
2-cyclopropylamino-4-nitrobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 41.
Stade C : 4-cyclopropyl-6-nitro-4H-l, 2, 4-benzothiadiazine 1, 1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade C de l'Exemple 41. Point dejusion : 254-257 °C
Stade D : 4-cyclopropyl-S, 4-dihydro-6-nitro-2H-l , 2, 4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. P Qint de Jus ion : 166-169 °C
EXEMPLE 75 : 6-acétamido-4-cyclopropyl-3,4-dihydro-2//-l ,2,4-benzothiadiazine 1,1-dioxyde
Stade A : 6-amino-4-cyclopropyl-4H-l, 2, 4-benzothiadiazine 1, 1-dioxyde
Le produit attendu est obtenu à partir du composé de l'Exemple 74 selon le procédé décrit dans le stade A de l'Exemple 42. Point de Jusion : 177-180 0C
Stade B : 6-acétamido-4-cyclopropyl-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 42. Point de Jmwn : 265-267 °C
EXEMPLE 76 : 6-amino-4-cyclopropyl-3,4-dihydro-2//-l,2,4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1, à partir du 6-amino-4-cyclopropyl-4H-l,2,4-benzothiadiazine 1,1-dioxyde préparé au stade A de l'Exemple 75.
Point dejusiqn : 185-188 °C
EXEMPLE 77 : 4-cyclopropyl-3,4-dihydro-7-méthoxycarbonyI-2JÏ-l,2,4- benzothiadiazine 1,1-dioxyde
Stade A : Acide 4-fluoro-3-sulfamoylbenzoïque
La suspension de 2-fluoro-5-méthylbenzènesulfonamide (5,3 mmol), obtenu à partir de la 2-fluoro-5-méthylaniline selon le procédé décrit dans le stade A de l'Exemple 1, dans l'eau (50 mL) est chauffée à 70 °C puis additionnée goutte à goutte de NaOH 10 % m/v jusqu'à dissolution complète du composé. Le permanganate de potassium (3 g) est ajouté par
petites portions. Après 4 heures sous agitation, la suspension est éliminée par filtration à chaud et le filtrat est amené à pH 1 par addition de HCl 12 N. Le précipité obtenu est recueilli par filtration, lavé à l'eau et séché pour donner le produit du titre sous la forme d'un solide blanc. Point de 'Jusion : 237-239 °C
Stade B : 4-cyclopropylamino-3-sulfamoylbenzoate de méthyle
Préparé à partir du composé obtenu dans l'étape précédente selon le procédé décrit dans le stade B de l'Exemple 1, l'acide 4-cyclopropylamino-3-sulfamoylbenzoïque (3,9 mmol) est alors mis en solution dans l'acide sulfurique (0,5 mL) et le méthanol (10 mL) et le mélange est chauffé à reflux pendant 4 heures. Le solvant est ensuite éliminé par distillation sous pression réduite et le résidu est mis en suspension dans l'eau (20 mL). Le précipité obtenu est recueilli par filtration, lavé à l'eau et séché pour donner le produit du titre sous la forme d'un solide blanc. PoM de 'Jusion : 158-161 °C
Stade C : 4-cyclopropyl-7-méthoxycarbonyl-4H-l,2,4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 4 h à 130 °C) dans le stade C de l'Exemple 1. Point de Jusion : 192-195 0C
Stade D : 4-cyclopropyl-3,4-dihydro-7-méthoxycarbonyl-2Yi-l,2,4- benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejusion : 178-180 °C
EXEMPLE 78 : 7-carboxy-4-cyclopropyl-3,4-dihydro-2//-l,2,4-benzothiadiazine 1,1- dioxyde
La solution du composé de l'Exemple 77 (3,5 mmol) dans un mélange méthanol/eau 1/1 (100 mL) contenant du NaOH (0,5 g) est chauffée à 40 °C pendant 3 heures. Le méthanol est ensuite éliminé par distillation sous pression réduite et la solution aqueuse résultante est ajustée à pH 2 par addition de HCl 6 N. Le précipité obtenu est recueilli par fïltration, lavé à l'eau et séché pour donner le produit du titre sous la forme d'un solide blanc. Point de Ju_siqn : 263-265 °C
EXEMPLE 79 : 4-cyclopropyl-3,4-dihydro-7-phénoxycarbonyI-2i/-l,2,4- benzothiadiazine 1,1-dioxyde
Le TV.TV'-carbonyldiimidazole (0,6 g) est additionné dans une solution du composé de l'Exemple 78 (3,5 mmol) dans le DMF (7 mL). Au bout de 1 heure d'agitation à température ambiante, le phénol (0,5 g) et le DBU (0,5 mL) sont ajoutés. Après 2 heures d'agitation à température ambiante, de l'eau (40 mL) est ajoutée et le milieu est extrait trois fois par. de l'acétate d'éthyle (3O mL). Les phases organiques sont rassemblées, séchées sur MgSO4 anhydre et filtrées. Le filtrat est évaporé à siccité et le résidu est redissous dans le méthanol (5 mL). La solution est additionné d'eau (50 mL) et le précipité obtenu est recueilli par filtration, lavé à l'eau et séché pour donner le produit du titre sous la forme d'un solide blanc. Point dejusion : 160-162 °C
EXEMPLE 80 : 4-cyclopropyl-3,4-dihydro-6-méthoxycarbonyl-2Jfir-l,2,4- benzothiadiazine 1,1-dioxyde
3-fluoro-4-sulfamoylbenzoate de méthyle
Une solution d'acide 3-fluoro-4-sulfamoylbenzoïque (4,5 mmol), obtenu en 2 étapes à partir de la 2-fluoro-4-méthylaniline selon le procédé décrit dans le stade A de l'Exemple
77, et d'acide sulfurique (0,5 mL) dans le méthanol (10 mL) est chauffée à reflux pendant
1 heure. Le solvant est ensuite éliminé par distillation sous pression réduite et le résidu est mis en suspension dans l'eau (20 mL). Le précipité obtenu est recueilli par filtration, lavé à l'eau et séché pour donner le produit du titre sous la forme d'un solide blanc. PoM dejusion : 153-156 0C
Stade B : 3-cyclopropylamino-4-sulfamoylbenzoate de méthyle
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 4-cyclopropyl-6-méthoxycarbonyl-4H-l, 2, 4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 4 heures à 130 °C) dans le stade C de l'Exemple 1. Point de Jis ion : 191-194 0C
Stade D : 4-cyclopropyl-3 ,4-dihydro-6-méthoxycarbonyl-2W-l ,2,4- benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point de Ji_s ion : 162-164 °C
EXEMPLE 81 : 6-carboxy-4-cyclopropyl-3,4-dihydro-2/7-l,2,4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans l'Exemple 78, en utilisant comme produit de départ le composé de l'Exemple 80 à la place du composé de l'Exemple 77.
PoM dejusion : 243-245 0C
EXEMPLE 82 : 4-cyclopropyl-3,4-dihydro-7-phénylaminocarbonyl-2/M,2,4- benzothiadiazine 1,1-dioxyde
Stade A : 4-fluoro-N-phényl-3-sulfamoylbenzamide
Le produit attendu est obtenu en 4 étapes à partir du 4-fluoro-3-nitrotoluène. Le 4-fluoro-3-nitrotoluène (6,5 mmol) est ajouté par petites portions à une solution de bichromate potassique (4 g) dans l'acide acétique glacial (1O mL). Après 15 minutes d'agitation, l'acide sulfurique (4 mL) est ajouté et la solution est portée à reflux pendant 2 heures. Le milieu est ensuite refroidi puis additionné d'eau (10O mL) et extrait par l'acétate d'éthyle (3 x 100 mL). Les phases organiques sont rassemblées, séchées sur MgSO4 anhydre et évaporées. Le résidu est recristallisé dans un mélange acétate d'éthyle/hexane (1/1) est engagé dans l'étape suivante.
La solution d'acide 4-fluoro-3-nitrobenzoïque (5,4 mmol) dans le chlorure de thionyle (1O mL) est portée à reflux pendant 4 heures. Après évaporation du solvant sous dépression, le résidu est redissous dans le toluène sec (10 mL) et la solution est évaporée à siccité. Cette opération est répétée à deux reprises. Le résidu est dissous dans le dioxanne sec (1O mL) et la solution est additionnée d'aniline (6 mmol) et de pyridine (6 mmol). Après 1 heure d'agitation à température ambiante, le solvant est éliminé sous dépression et le résidu est dissous dans le méthanol (5 mL). Cette solution est additionnée d'eau (30 mL) et le précipité obtenu est recueilli par filtration, lavé à l'eau et séché pour être engagé dans l'étape suivante.
La suspension de 4-fluoro-3-nitro-iV-phénylbenzamide (4 mmol) dans un mélange éthanol/eau 2/1 (3O mL) est portée à reflux puis additionnée de chlorure ammonique (0,5 g) et de poudre de fer (2 g). Après 15 minutes, la suspension est filtrée à chaud et l'insoluble est rincé à l'aide d'éthanol chaud (50 mL). Le filtrat est traité au charbon adsorbant et filtré. L'éthanol du filtrat est éliminé par distillation sous dépression. Le précipité obtenu est recueilli par filtration, lavé à l'eau et séché.
Le produit ainsi obtenu est mis en réaction selon le procédé décrit dans le stade A de l'Exemple 1 pour donner le produit du titre. Point de Jusion : 219-221 °C
Stade B : 4-cyclopropylamino-N-phényl-3-sulfamoylbenzamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
4-cyclopropyl- 7-phénylaminocarbonyl-4Yi-l, 2, 4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 4 heures à 130 °C) dans le stade C de l'Exemple 1. Point dejus ion : 293-296 °C
4-cyclopropyl-3, 4-dihydro- 7-phénylaminocarbonyl-2Y[-l, 2, 4- benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point de 'Jusion : 268-270 °C
EXEMPLE 83 : 4-cyclopropyl-3,4-dihydro-6-phénylaminocarbonyl-2Jff-l,2,4- benzothiadiazine 1,1-dioxyde
3-fluoro-N-phényl-4-sulfamoylbenzamide
Le produit attendu est obtenu à partir du 3-fiuoro-4-nitrotoluène selon le procédé décrit dans le stade A de l'Exemple 82. Point dejusign : 250-252 °C
Stade B : 3-cyclopropylamino-'N-phényl-4-sulfamoylbenzamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 4-cyclopropyl-6-phénylaminocarbonyl-4H-l, 2, 4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 4 heures à 130 °C) dans le stade C de l'Exemple 1. Point de JusiQU : 278-281 °C
Stade D : 4-cyclopropyl-S, 4-dihydro-6-phénylaminocarbonyl-2H-l, 2, 4- benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. P oint de Jks ion : 232-234 °C
EXEMPLE 84 : 4-cyclopropyl-3,4-dihydro-7-méthoxy-2//-l,2,4-benzothiadiazine 1,1- dioxyde
Stade A : 2-cyclopropylamino-5-méthoxybenzènesulfonamide
La solution de 2-amino-5-méthoxybenzènesulfonamide (4,9 mmol) dans le méthanol (2O mL) est additionnée de (l-éthoxycyclopropyloxy)triméthylsilane (4 mL) et d'acide acétique glacial (4 mL) puis portée à reflux pendant 18 heures. Le milieu est ensuite évaporé à siccité sous dépression. L'huile obtenue est reprise par de l'eau (30 mL) et extraite au chloroforme (3 x 30 mL). Les phases organiques sont rassemblées et séchées sur MgSO4 anhydre. Après filtration, le filtrat est évaporé à siccité et l'huile résiduelle est mis en solution dans le THF (50 mL). Le borohydrure de sodium (2 g) et l'éthérate de trifluorure de bore (2 mL) sont ajoutés puis le mélange est chauffé à reflux pendant 18 heures. Le solvant est ensuite éliminé par évaporation sous pression réduite et le résidu est repris par de l'eau (30 mL), ajusté à pH légèrement acide par ajout de HCl 6 N, puis extrait au chloroforme (3 x 30 mL). Les phases organiques sont rassemblées et séchées sur MgSO4 anhydre. Après filtration, le filtrat est évaporé à siccité et le composé attendu est obtenu sous forme d'une huile directement engagée dans l'étape suivante.
ie B : 4-cyclopropyl- 7-méthoxy-4H-l, 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade C de l'Exemple 1. Point de 'Jusion : 216-219 0C
Stade C : 4-cyclopropyl-3, 4-dïhydro- 7-méthoxy-2H-l , 2, 4-benzothiadiazine 1,1- dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point dejusion : 154-156 °C
EXEMPLE 85 : 4-cyclopropyl-3,4-dihydro-7-hydroxy-2//-l,2,4-benzothiadiazine 1,1- dioxyde
Une solution du composé de l'Exemple 84 (50 mg) dans le chloroforme (3 mL) est refroidie sur bain de glace, puis additionnée de tribromure de bore (0,15 mL). Après 20 heures d'agitation, le milieu est additionné d'eau (5 mL), puis concentré sous dépression, et ensuite extrait par l'acétate d'éthyle (3 x 20 mL). Les phases organiques sont rassemblées et séchées sur MgSO4 anhydre. Après filtration, le filtrat est évaporé à siccité et le résidu est dissous dans l'acétate d'éthyle (1 mL) puis additionné d'hexane (5 mL). Le précipité obtenu est recueilli par filtration, lavé à l'hexane et séché pour donner le produit attendu sous la forme d'un solide blanc. Point dejusion : 187-189 °C
EXEMPLE 86 : 6-chloro-4-cyclopropyl-3,4-dihydro-7-méthoxy-2^-l,2,4- benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans les stades A, B et C de l'Exemple 84 en utilisant comme produit de départ le 2-amino-4-chloro- 5-méthoxybenzènesulfonamide à la place du 2-amino-5-méthoxybenzènesulfonamide. Point dejusion : 188-190 °C
EXEMPLE 87 : 6-chloro-4-cyclopropyl-3,4-dihydro-7-hydroxy-2/7-l,2,4- benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans l'Exemple 85 en utilisant comme produit de départ le composé de l'Exemple 86 à la place du composé de l'Exemple 84. Point dejusion • 213-214 °C
EXEMPLE 88 : 6,7-dichloro-4-cyclopropylméthyl-3,4-dihydro-2/7-l,2,4- benzothiadiazine 1,1-dioxyde
Stade A : 6, 7-dichloro-4H-l, 2, 4-benzothiadiazine 1, 1-dioxyde
Le produit attendu est obtenu à partir de la 2-amino-4,5-dichlorobenzènesulfonamide selon le procédé décrit dans le stade A de l'Exemple 60. Point dejusion : 237-240 0C
Stade B : 6, 7-dichloro-4-cyclopropylméthyl-4H-l,2,4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 60. PpM dejusion : 192-195 °C
Stade C : 6, 7-dichloro-4-cyclopropylméthyl-3,4-dihydro-2\{-l,2,4- benzothiadiazine 1, 1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade C de l'Exemple 60. PoJM dejusion : 171-173 °C
EXEMPLE 89 : 5-chIoro-4-cyclopropyl-8-fluoro-3,4-dihydro-2/y-l,2,4- benzothiadiazine 1,1-dioxyde
Stade A : 3-chloro-2, 6-difluorobenzènesulfonamide
Le produit attendu est obtenu à partir de la 3-chloro-2,6-difluoroaniline selon le procédé décrit dans le stade A de l'Exemple 1. Point de Jus ion : 144-146 QC
Stade B : 3-chloro-2-cyclopropylamino-6-fluorobenzènesulfonamide
Le produit attendu est obtenu selon le procédé décrit dans le stade B de l'Exemple 1.
Stade C : 5-chloro-4-cyclopropyl-8-fluoro-4H-l, 2, 4-benzothiadiazine 1, 1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit (temps de chauffe de 4 heures à 130 °C) dans le stade C de l'Exemple 1. Point de Jusion : 201-204 0C
5-chloro-4-cyclopropyl-8-fluoro-3, 4-dihydro-2H-l, 2, 4-benzothiadiazine 1,1 -dioxyde
Le produit attendu est obtenu selon le procédé décrit dans le stade D de l'Exemple 1. Point de Jusion : 171-174 °C
EXEMPLE 90 : 4-cyclopropyl-6,7-difluoro-3,4-dihydro-2/-r-l,2,4-benzothiadiazine 1,1-dioxyde
Le produit attendu est obtenu selon le procédé décrit dans les stades A, B et C de l'Exemple 84 en utilisant comme produit de départ le 2-amino-4,5-difluoro benzènesulfonamide à la place du 2-amino-5-méthoxybenzènesulfonamide. Point _d_e Jus ion : 146-148 0C
ETUDE PHARMACOLOGIQUE
EXEMPLE A : Etude de l'effet des produits sur le courant ionique induit par l'AMPA sur des cultures primaires de neurones de rat.
Le test consiste en la mesure in vitro, par fluorescence, de la dépolarisation membranaire induite sur des neurones embryonnaires de rat en culture, par l'action conjointe de l'AMPA et du produit testé, en comparaison à l'action de l'AMPA seul. Les cellules du cerveau sont mises en culture et maintenues dans un incubateur de culture cellulaire pendant 18 jours. Après incubation, le milieu de culture est retiré et remplacé par du milieu de chargement en sonde de fluorescence pour mesure du potentiel membranaire (20 μl ; kit de potentiel de membrane de Molecular Devices) et laissées à température ambiante pendant 1 heure. La fluorescence de base des puits est lue (appareil FDSS de Hamamatsu), puis l'AMPA est injecté sur les cellules (20 μl ; gamme de concentration de 3 à 100 μM) et l'action de l'AMPA est mesurée en cinétique. Le produit testé est ensuite introduit dans les puits (20 μl; en gamme de concentration, croisée avec celle de l'AMPA) et l'action du produit est mesurée en cinétique. A l'issue de chacune des 2 périodes de mesure en cinétique, la valeur retenue pour chaque puits est la moyenne de la lecture sur les 15 dernières secondes de la période. On représente les courbes d'effet de l'AMPA aux différentes concentrations de produit. Pour chaque concentration de produit, la valeur retenue est l'aire sous la courbe d'AMPA à cette concentration et l'EC2χ, concentration de produit qui double le potentiel membranaire induit par l'AMPA, est calculée.
Les composés de l'invention potentialisent fortement les effets excitateurs de l'AMPA comme le montre le tableau ci-dessous pour quelques exemples de composés de la présente invention :
EC2x (μM)
Exemple 1 1,0
Exemple 2 5,0
Exemple 21 2,0
Exemple 34 1,8
Exemple 37 4,4
Exemple 39 4,8
Exemple 62 0,8
EXEMPLE B : Reconnaissance d'objet chez la souris CDl
Le test de reconnaissance d'objet (Behav. Brain Res., 1988, 31, 47-59) est basé sur l'activité exploratoire spontanée de l'animal et possède les caractéristiques de la mémoire épisodique chez l'Homme. Sensible au vieillissement (Eur. J. Pharm. 1997, 325, 173-180), ainsi qu'aux dysfonctionnements cholinergiques (Pharm. Biochem. Behav., 1996, 53(2), 277-283), ce test de mémoire est fondé sur l'exploration différentielle de 2 objets de forme assez similaire, l'un familier, l'autre nouveau. La procédure expérimentale, adaptée à la souris CDl, comporte 3 phases qui se déroulent dans la même enceinte expérimentale. Pendant la lere phase qui dure 40 minutes, les souris sont habituées à l'environnement. Pendant la 2e phase, qui a lieu le lendemain, un objet est placé dans l'enceinte et la souris est libre de l'explorer. Lorsque cette exploration atteint une durée de 20 secondes, la souris est retirée de l'enceinte. Au cours de la 3e phase (5 minutes), 24 heures plus tard, le même objet est présenté (il acquiert le statut d'objet « familier »), ainsi qu'un nouvel objet. La durée d'exploration, exprimée en secondes, de chacun des deux objets, est chronométrée. Les animaux témoins, ayant reçu préalablement le véhicule par voie orale 60 minutes avant chacune des 3 phases, explorent pendant une durée équivalente l'objet « familier » et l'objet « nouveau », ce qui signifie l'oubli de l'objet déjà présenté. Les animaux ayant reçu un composé facilitateur mnémocognitif, explorent de façon préférentielle l'objet nouveau, ce qui signifie le maintien du souvenir de l'objet déjà présenté.
Les résultats obtenus avec les composés de la présente invention montrent une exploration signifïcativement plus importante de l'objet nouveau par rapport à l'objet familier aux doses de 1 et 3 mg/kg, PO, en doublant voire triplant la durée d'exploration, ce qui indique que les composés de l'invention améliorent la mémorisation de façon importante.
Par exemple, la différence d'exploration des deux objets au cours de la 3e phase est comprise entre 5 et 10 secondes après administration du composé de l'Exemple 1 alors qu'elle est inférieure à 3 secondes après administration du véhicule.
EXEMPLE C : Composition pharmaceutique
Formule de préparation pour 1000 comprimés dosés à 10 mg en 6,7-dichloro-4- cyclopropyl-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1-dioxyde (Exemple 1) 10 g
Hydroxypropylcellulose 2 g
Amidon de blé 10 g
Lactose 100 g Stéarate de magnésium 3 g
Talc 3 g
Claims
1. Composés de formule (I) :
dans laquelle :
> Rcy représente :
" un groupement cycloalkyle (C3-C8) non-substitué ou substitué par un ou plusieurs groupements, identiques ou différents, choisis parmi alkyle (C1-C6) linéaire ou ramifié non-substitué ou substitué par un ou plusieurs atomes d'halogène ; alkoxy (C1-C6) linéaire ou ramifié ; hydroxy ; et amino non-substitué ou substitué par un ou deux groupements alkyle (C1-C6) linéaire ou ramifié ;
" ou un groupement cycloalkyle (C3-C8) alkyle (C1-C6) linéaire ou ramifié non- substitué ou substitué sur la partie cyclique par un ou plusieurs groupements, identiques ou différents, choisis parmi alkyle (C1-C6) linéaire ou ramifié non- substitué ou substitué par un ou plusieurs atomes d'halogène ; alkoxy (Cj-C6) linéaire ou ramifié ; hydroxy ; et amino non-substitué ou substitué par un ou deux groupements alkyle (C1-C6) linéaire ou ramifié ;
y R1, R2, R3 et R4, identiques ou différents, représentent chacun un atome d'hydrogène ou d'halogène ou un groupement nitro ; cyano ; hydroxy ; thio ; alkyle (C1-C6) linéaire ou ramifié non-substitué ou substitué par un ou plusieurs atomes d'halogène ; cyanoalkyle (C1-C6) linéaire ou ramifié ; hydroxyalkyle (Ci-C6) linéaire ou ramifié ; alkoxy (C1-C6) linéaire ou ramifié non-substitué ou substitué par un ou plusieurs atomes d'halogène ; alkylthio (C1-C6) linéaire ou ramifié ; carboxy ; alkoxycarbonyle (Ci-C6) linéaire ou ramifié ; aryloxycarbonyle ; acyle (Ci-C6) linéaire ou ramifié ; amino non-substitué ou substitué par un ou deux groupements alkyle (C1-C6) linéaire ou ramifié ou par un groupement acyle (C1-C6) linéaire ou ramifié ; aminocarbonyle non-substitué ou substitué par un ou deux groupements alkyle (C1-C6) linéaire ou ramifié ; arylaminocarbonyle ; ou alkylsulfonylamino (C1-C6) linéaire ou ramifié ;
leurs énantiomères et leurs diastéréoisomères lorsqu'ils existent, ainsi que leurs sels d'addition avec un acide ou une base pharmaceutiquement acceptable,
on entend par « aryle », le groupement phényle non-substitué ou substitué par un ou plusieurs groupements, identiques ou différents, choisis parmi alkyle (C1-C6) linéaire ou ramifié non-substitué ou substitué par un ou plusieurs atomes d'halogène ; alkoxy (C1-C6) linéaire ou ramifié ; hydroxy ; et amino non-substitué ou substitué par un ou deux groupements alkyle (C1-C6) linéaire ou ramifié.
2. Composés de formule (I) selon la revendication 1, caractérisés en ce que Rcy représente un groupement cycloalkyle (C3-C8).
3. Composés de formule (I) selon la revendication 1 ou 2, caractérisés en ce que Rcy représente un groupement cyclopropyle.
4. Composés de formule (I) selon la revendication 1, caractérisés en ce que Rcy représente un groupement cycloalkyle (C3-C8) alkyle (C1-C6) linéaire ou ramifié.
5. Composés de formule (I) selon la revendication 1 ou 4, caractérisés en ce que Rcy représente un groupement cyclopropylméthyle.
6. Composés de formule (I) selon l'une quelconque des revendications 1 à 5, caractérisés en ce que R1 représente un atome d'hydrogène ou un atome d'halogène.
7. Composés de formule (I) selon l'une quelconque des revendications 1 à 6, caractérisés en ce que R2 représente un atome d'hydrogène, un atome d'halogène, un groupement méthyle, un groupement cyano ou un groupement carboxy.
8. Composés de formule (I) selon l'une quelconque des revendications 1 à 7, caractérisés en ce que R3 représente un atome d'hydrogène, un atome d'halogène ou un groupement méthyle.
9. Composés de formule (I) selon l'une quelconque des revendications 1 à 8, caractérisés en ce que R4 représente un atome d'hydrogène ou un atome d'halogène.
10. Composés de formule (I) selon l'une quelconque des revendications 1 à 9, caractérisés en ce que deux des groupements R1, R2, R3 et R4 sont différents d'un atome d'hydrogène.
11. Composés de formule (I) selon la revendication 1, caractérisés en ce que deux des groupements R1, R2, R3 et R4 représentent un atome d'halogène et Rcy représente un groupement cyclopropyle.
12. Composés de formule (I) selon la revendication 1, qui sont le :
• 6,7-dichloro-4-cyclopropyl-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1-dioxyde ;
• 8-chloro-4-cyclopropyl-6-fluoro-3 ,4-dihydro-2H- 1 ,2,4-benzothiadiazine 1,1- dioxyde ;
• 8-bromo-4-cyclopropyl-6-fluoro-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1- dioxyde ;
• 6-cyano-4-cyclopropyl-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1 -dioxyde ;
• 8-bromo-6-chloro-4-cyclopropyl-3 ,4-dihydro-2H- 1 ,2,4-benzothiadiazine 1,1- dioxyde ;
• 4-cyclopropyl-5-fluoro-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1 -dioxyde ; • 8-bromo-4-cyclopropyl-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1 -dioxyde ;
• 4-cyclopropyl-5 ,7-difluoro-3 ,4-dihydro-2H- 1 ,2,4-benzothiadiazine 1 , 1 -dioxyde ; • 6-fluoro-4-cyclopropyl-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1-dioxyde ;
• δ-chloro^-cyclopropyl-T-fluoro-S ,4-dihydro-2H- 1 ,2,4-benzothiadiazine 1,1- dioxyde ;
• 4-cyclopropyl-3,4-dihydro-6-méthyl-2H-l,2,4-benzothiadiazine 1,1-dioxyde ; • 4-cyclopropyl-8-fluoro-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1-dioxyde ;
• δ-chloro^-cyclopropyl-S ,4-dihydro-2H- 1 ,2,4-benzothiadiazine 1 , 1 -dioxyde ;
• 6-bromo-4-cyclopropyl-7-fluoro-3 ,4-dihydro-2H- 1 ,2,4-benzothiadiazine 1,1- dioxyde ;
• 6-bromo-4-cyclopropyl-3 ,4-dihydro-2H- 1 ,2,4-benzothiadiazine 1 , 1 -dioxyde ; • 4-cyclopropyl-6,8-difluoro-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1 -dioxyde ;
• 4-cyclopropyl-5,6-difluoro-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1 -dioxyde ;
• le 4-cyclopropyl-3 ,4-dihydro-7-méthyl-2H- 1 ,2,4-benzothiadiazine 1 , 1 -dioxyde ;
• le 6-chloro-4-cyclopropyl-3 ,4-dihydro-2H- 1 ,2,4-benzothiadiazine 1 , 1 -dioxyde ;
• le 4-cyclopropyl-3,4-dihydro-6-iodo-2H-l,2,4-benzothiadiazine 1,1 -dioxyde ; • le 6,7-dichloro-4-(l-méthyl)cyclopropyl-3,4-dihydro-2H-l,2,4-benzothiadiazine
1,1 -dioxyde ;
• le 4-cyclopropylméthyl-7-fluoro-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1- dioxyde ;
• le 6-carboxy-4-cyclopropyl-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1 -dioxyde ; • le 4-cyclopropyl-7,8-difluoro-3,4-dihydro-2H-l,2,4-benzothiadiazine 1, 1 -dioxyde ;
• le 8-bromo-6-cyano-4-cyclopropyl-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1- dioxyde ;
• le 7-bromo-4-cyclopropyl-3,4-dihydro-2H-l,2,4-benzothiadiazine 1,1 -dioxyde,
ainsi que leurs sels d'addition à un acide ou à une base pharmaceutiquement acceptable.
13. Procédé de préparation des composés de formule (I) selon la revendication 1, caractérisé en ce que l'on utilise comme produit de départ un composé de formule (II) :
dans laquelle Rcy, Ri, R2, R3 et R4 sont tels que définis dans la revendication 1,
que l'on cyclise en présence d'un composé de formule (III) :
H-C(OR 5,)^3 (III)
dans laquelle R5 représente un groupement alkyle (Ci-C6) linéaire ou ramifié,
pour conduire au composé de formule (IV) :
dans laquelle Rcy, R1, R2, R3 et R4 sont tels que définis précédemment,
que l'on met en réaction avec un agent réducteur, pour conduire au composé de formule (I),
une variante dans la préparation des composés de formule (I) consistant, après réalisation de l'étape de réduction du composé de formule (IV), en l'utilisation des réactions classiques de chimie afin de modifier, dans un deuxième temps, les substituants du noyau benzénique, composé de formule (I) qui peut être ensuite purifié selon une technique classique de séparation, que l'on transforme, si on le souhaite en ses sels d'addition à un acide ou à une base pharmaceutiquement acceptable et dont on sépare éventuellement les isomères, s'ils existent, selon une technique classique de séparation.
14. Procédé de préparation des composés de formule (I) selon la revendication 1, caractérisé en ce que l'on utilise comme produit de départ un composé de formule (V) :
dans laquelle R1, R2, R3 et R4 sont tels que définis dans la revendication 1,
que l'on cyclise en présence d'un composé de formule (III)
H-C(OR V5)3 (III)
dans laquelle R5 représente un groupement alkyle (C1-C6) linéaire ou ramifié,
pour conduire au composé de formule (VI)
dans laquelle Rcy est tel que défini précédemment et Y représente un groupement partant choisi parmi les atomes d'iode, de brome et les groupements tosylate, mésylate et triflate pour conduire au composé de formule (IV),
dans laquelle Rcy, Ri, R2, R3 et R4 sont tels que définis précédemment,
que l'on met en réaction avec un agent réducteur, pour conduire au composé de formule (I),
une variante dans la préparation des composés de formule (I) consistant, après réalisation de l'étape de réduction du composé de formule (IV), en l'utilisation des réactions classiques de chimie afin de modifier, dans un deuxième temps, les substituants du noyau benzénique,
composé de formule (I) qui peut être ensuite purifié selon une technique classique de séparation, que l'on transforme, si on le souhaite en ses sels d'addition à un acide ou à une base pharmaceutiquement acceptable et dont on sépare éventuellement les isomères, s'ils existent, selon une technique classique de séparation.
15. Composés de formule (IV) selon les revendications 13 ou 14 :
dans laquelle Rcy, R1, R2, R3 et R4 sont tels que définis dans la revendication 1,
caractérisés en ce qu'ils sont utiles en tant qu'intermédiaires de synthèse des composés de formule (I).
16. Composition pharmaceutique contenant comme principe actif un composé selon l'une quelconque des revendications 1 à 12, en combinaison avec un ou plusieurs véhicules inertes, non toxiques et pharmaceutiquement acceptables.
17. Compositions pharmaceutiques selon la revendication 16 utiles en tant que modulateurs du récepteur AMPA.
18. Compositions pharmaceutiques selon la revendication 16 utiles pour le traitement ou la prévention des désordres mnémocognitifs associés à l'âge, aux syndromes anxieux ou dépressifs, aux maladies neurodégénératives progressives, à la maladie d'Alzheimer, à la maladie de Parkinson, à la maladie de Pick, à la chorée d'Huntington, à la maladie de Korsakoff, à la schizophrénie, aux séquelles des maladies neurodégénératives aiguës, aux démences frontales et sous-corticales, aux séquelles de l'ischémie et aux séquelles de l'épilepsie.
19. Utilisation des composés de formule (I) selon l'une quelconque des revendications 1 à 12 pour la fabrication de médicaments utiles en tant que modulateurs du récepteur AMPA.
20. Utilisation des composés de formule (I) selon l'une quelconque des revendications 1 à 12 pour la fabrication de médicaments utiles pour le traitement ou la prévention des désordres mnémocognitifs associés à l'âge, aux syndromes anxieux ou dépressifs, aux maladies neurodégénératives progressives, à la maladie d'Alzheimer, à la maladie de Parkinson, à la maladie de Pick, à la chorée d'Huntington, à la maladie de Korsakoff, à la schizophrénie, aux séquelles des maladies neurodégénératives aiguës, aux démences frontales et sous-corticales, aux séquelles de l'ischémie et aux séquelles de l'épilepsie.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR08.03898 | 2008-07-09 | ||
| FR0803898A FR2933698A1 (fr) | 2008-07-09 | 2008-07-09 | Nouveaux derives de benzothiadiazines cycloalkylees, leur procede de preparation et les compositions pharmaceutiques qui les contiennent. |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2010004139A1 true WO2010004139A1 (fr) | 2010-01-14 |
Family
ID=40345046
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/FR2009/000841 Ceased WO2010004139A1 (fr) | 2008-07-09 | 2009-07-07 | Nouveaux derives de benzothiadiazines cycloalkylees, leur procede de preparation et les compositions pharmaceutiques qui les contiennent |
Country Status (18)
| Country | Link |
|---|---|
| US (1) | US7741320B2 (fr) |
| EP (1) | EP2147915B1 (fr) |
| AR (1) | AR072486A1 (fr) |
| AT (1) | ATE481393T1 (fr) |
| AU (1) | AU2009202704B2 (fr) |
| CA (1) | CA2671236C (fr) |
| CY (1) | CY1110944T1 (fr) |
| DE (1) | DE602009000183D1 (fr) |
| DK (1) | DK2147915T3 (fr) |
| ES (1) | ES2352873T3 (fr) |
| FR (1) | FR2933698A1 (fr) |
| HR (1) | HRP20100622T8 (fr) |
| PL (1) | PL2147915T3 (fr) |
| PT (1) | PT2147915E (fr) |
| RS (1) | RS51518B (fr) |
| SI (1) | SI2147915T1 (fr) |
| TW (1) | TW201006805A (fr) |
| WO (1) | WO2010004139A1 (fr) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2014062044A1 (fr) | 2012-10-15 | 2014-04-24 | Vilnius University | Benzènesulfonamides fluorés à utiliser en tant qu'inhibiteurs d'anhydrase carbonique |
| JP2017014225A (ja) * | 2011-07-01 | 2017-01-19 | バルーク エス.ブルームバーグ インスティテュート | Hbv感染に対する抗ウイルス剤としてのスルファモイルベンズアミド誘導体 |
| EP3597653A1 (fr) * | 2018-07-19 | 2020-01-22 | Irbm S.P.A. | Inhibiteurs cycliques du virus de l'hépatite b |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN105175284B (zh) * | 2015-07-21 | 2017-06-16 | 中国药科大学 | 酰胺类化合物、制备方法及其医药用途 |
| AR119971A1 (es) | 2019-09-16 | 2022-01-26 | Takeda Pharmaceuticals Co | Derivados de piridazin-3(2h)-ona fusionados con azol |
| CN120247899B (zh) * | 2025-05-06 | 2025-09-30 | 汕头职业技术学院 | 一种苯并噻二嗪-1,1-二酮-喹啉衍生物及其制备方法和应用 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2003031422A1 (fr) * | 2001-10-10 | 2003-04-17 | Neurosearch A/S | Nouveaux derives de benzothiazine, leur preparation et leur utilisation |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2722502B1 (fr) | 1994-07-12 | 1996-08-23 | Adir | Nouveau derive de benzothiadiazine, son procede depreparation et les compositions pharmaceutiques qui le contiennent |
| RU2214405C2 (ru) | 1998-02-18 | 2003-10-20 | НьюроСёрч А/С | Новые соединения и их применение в качестве положительных модуляторов амра-рецепторов |
| DE19854096A1 (de) * | 1998-11-24 | 2000-05-25 | Merck Patent Gmbh | Anschlußträger für plattenförmige Mikrokomponenten |
-
2008
- 2008-07-09 FR FR0803898A patent/FR2933698A1/fr active Pending
-
2009
- 2009-07-03 AU AU2009202704A patent/AU2009202704B2/en not_active Ceased
- 2009-07-03 CA CA2671236A patent/CA2671236C/fr not_active Expired - Fee Related
- 2009-07-07 WO PCT/FR2009/000841 patent/WO2010004139A1/fr not_active Ceased
- 2009-07-08 DE DE602009000183T patent/DE602009000183D1/de active Active
- 2009-07-08 SI SI200930008T patent/SI2147915T1/sl unknown
- 2009-07-08 AT AT09290547T patent/ATE481393T1/de active
- 2009-07-08 DK DK09290547.0T patent/DK2147915T3/da active
- 2009-07-08 ES ES09290547T patent/ES2352873T3/es active Active
- 2009-07-08 PL PL09290547T patent/PL2147915T3/pl unknown
- 2009-07-08 TW TW098123134A patent/TW201006805A/zh unknown
- 2009-07-08 RS RSP-2010/0540A patent/RS51518B/sr unknown
- 2009-07-08 PT PT09290547T patent/PT2147915E/pt unknown
- 2009-07-08 EP EP09290547A patent/EP2147915B1/fr active Active
- 2009-07-08 AR ARP090102578A patent/AR072486A1/es unknown
- 2009-07-09 US US12/459,844 patent/US7741320B2/en not_active Expired - Fee Related
-
2010
- 2010-11-17 HR HR20100622T patent/HRP20100622T8/xx unknown
- 2010-11-29 CY CY20101101087T patent/CY1110944T1/el unknown
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2003031422A1 (fr) * | 2001-10-10 | 2003-04-17 | Neurosearch A/S | Nouveaux derives de benzothiazine, leur preparation et leur utilisation |
Non-Patent Citations (4)
| Title |
|---|
| DATABASE CAPLUS [online] CHEMICAL ABSTRACTS SERVICE, COLUMBUS, OHIO, US; WHEATLEY, DAVID ET AL: "Hypertension. Results of treatment [with various drugs]", XP002515882, retrieved from STN Database accession no. 1964:12490 * |
| PHILLIPS, DEAN ET AL: "5'-Alkyl-benzothiadiazides: A New Subgroup of AMPA Receptor Modulators with Improved Affinity", BIOORGANIC & MEDICINAL CHEMISTRY , 10(5), 1229-1248 CODEN: BMECEP; ISSN: 0968-0896, 2002, XP002515881 * |
| PROCEEDINGS OF THE ROYAL SOCIETY OF MEDICINE , 56(5), 400-6 CODEN: PRSMA4; ISSN: 0035-9157, 1963 * |
| WHITEHEAD, CALVERT W. ET AL: "Diuretics. VI. 1,2,4-Benzothiadiazine 1,1-dioxides substituted at 2,3,4- and 7-N-sulfamoyl positions", JOURNAL OF ORGANIC CHEMISTRY , 27, 951-6 CODEN: JOCEAH; ISSN: 0022-3263, 1962, XP002515880 * |
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2017014225A (ja) * | 2011-07-01 | 2017-01-19 | バルーク エス.ブルームバーグ インスティテュート | Hbv感染に対する抗ウイルス剤としてのスルファモイルベンズアミド誘導体 |
| WO2014062044A1 (fr) | 2012-10-15 | 2014-04-24 | Vilnius University | Benzènesulfonamides fluorés à utiliser en tant qu'inhibiteurs d'anhydrase carbonique |
| LT6064B (lt) | 2012-10-15 | 2014-08-25 | Vilniaus Universitetas | Fluorinti benzensulfonamidai kaip karboanhidrazės inhibitoriai |
| US9725467B2 (en) | 2012-10-15 | 2017-08-08 | Vilnius University | Fluorinated benzenesulfonamides as inhibitors of carbonic anhydrase |
| EP3597653A1 (fr) * | 2018-07-19 | 2020-01-22 | Irbm S.P.A. | Inhibiteurs cycliques du virus de l'hépatite b |
| WO2020016434A1 (fr) | 2018-07-19 | 2020-01-23 | Ospedale San Raffaele S.R.L. | Inhibiteurs cycliques du virus de l'hépatite b |
Also Published As
| Publication number | Publication date |
|---|---|
| EP2147915A1 (fr) | 2010-01-27 |
| RS51518B (sr) | 2011-06-30 |
| DE602009000183D1 (de) | 2010-10-28 |
| US20100009974A1 (en) | 2010-01-14 |
| PT2147915E (pt) | 2010-10-13 |
| ES2352873T3 (es) | 2011-02-23 |
| SI2147915T1 (sl) | 2010-11-30 |
| US7741320B2 (en) | 2010-06-22 |
| AR072486A1 (es) | 2010-09-01 |
| CA2671236C (fr) | 2012-06-19 |
| AU2009202704A1 (en) | 2010-01-28 |
| CY1110944T1 (el) | 2015-06-10 |
| TW201006805A (en) | 2010-02-16 |
| HRP20100622T1 (hr) | 2010-12-31 |
| FR2933698A1 (fr) | 2010-01-15 |
| AU2009202704B2 (en) | 2013-01-17 |
| EP2147915B1 (fr) | 2010-09-15 |
| CA2671236A1 (fr) | 2010-01-09 |
| PL2147915T3 (pl) | 2011-03-31 |
| ATE481393T1 (de) | 2010-10-15 |
| HRP20100622T8 (en) | 2011-01-31 |
| DK2147915T3 (da) | 2010-12-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP0557171B1 (fr) | Azaindoles, procédés de préparation et médicaments les contenant | |
| EP2246339B1 (fr) | Dérivés de benzothiazépine et leur utilisation en tant que modulateurs des récepteurs AMPA et NMDA | |
| EP1070716A1 (fr) | Nouveaux dérivés de beta-carboline, leur procédé de préparation et les compositions pharmaceutiques qui les contiennent | |
| WO2010004139A1 (fr) | Nouveaux derives de benzothiadiazines cycloalkylees, leur procede de preparation et les compositions pharmaceutiques qui les contiennent | |
| NO167916B (no) | Analogifremgangsmaate for fremstilling av terapeutisk aktive tiolaktam-n-eddiksyrederivater | |
| EP0162776B1 (fr) | Dérivés hétérocycliques, leurs procédés de préparation,médicaments les contenant, utiles notamment comme inhibiteurs de l'aldose réductase | |
| CA2524377C (fr) | Nouveaux derives de thiadiazine, leur procede de preparation et les compositions pharmaceutiques qui les contiennent | |
| EP1176148B1 (fr) | Nouveaux dérivés de benzothiadiazine, leur procédé de préparation et les compositions pharmaceutiques qui les contiennent | |
| EP1486503B1 (fr) | Dérivés de benzothiazine et benzothiadiazine, leur procédé de préparation et les compositions pharmaceutiques qui les contiennent | |
| CA2471263A1 (fr) | Nouveaux derives de benzothiazine et benzothiadiazine, leur procede de preparation et les compositions pharmaceutiques qui les contiennent | |
| EP1456189B1 (fr) | Derives de benzothia(dia)zine et leur utilisation comme modulateurs ampa | |
| CA2513059A1 (fr) | Nouveaux derives d'azepines tricycliques, leur procede de preparation et les compositions pharmaceutiques qui les contiennent | |
| KR100842485B1 (ko) | 벤조티아진 및 벤조티아디아진 화합물, 이들의 제조 방법및 이들을 함유하는 약학적 조성물 | |
| CA2492161C (fr) | Nouveaux derives de benzothiadiazines fluorees, leur procede de preparation et les compositions pharmaceutiques qui les contiennent | |
| FR2565980A1 (fr) | Nouveaux esters de 1,1-dioxydes de n-heteroaryl-4-hydroxy-2-methyl- 2h -1,2-benzothiazine- (ou thieno(2,3-e)-1,2-thiazine)-3-carboxamide precurseurs de medicaments et composition pharmaceutiques les contenant | |
| EP2431360B1 (fr) | Derives de dihydrobenzoxathiazepines, leur procede de preparation et les compositions pharmaceutiques qui les contiennent ainsi que leur utilisation comme modulateurs des recepteurs AMPA | |
| MC593A1 (fr) | Nouveaux benzène sulfonyl-semicarbazides et leur préparation | |
| WO2011083265A1 (fr) | Nouveaux derives de benzothiadiazines cyclopropylees, leur procede de preparation et les compositions pharmaceutiques qui les contiennent | |
| WO2003053978A1 (fr) | Nouveaux derives de benzothiazine et benzothiadiazine, leur procede de preparation et les compositions pharmaceutiques qui les contiennent | |
| CA2449189A1 (fr) | Modulateurs allosteriques positifs des recepteurs ampa naphtothiazine (paarm) | |
| FR2877342A1 (fr) | Nouveaux derives de benzothiadiazine, leur procede de preparation et les compositions pharmaceutiques qui les contiennent | |
| LU83861A1 (fr) | Nouveaux derives pyridothiaziniques,leur preparation et leur utilisation | |
| OA16341A (fr) | Nouveaux dérivés dihydrobenzoxathiazépines, leur procédé de préparation et les compositions pharmaceutiques qui les contiennent. | |
| FR2578542A2 (fr) | Nouveaux derives heterocycliques, leurs procedes de preparation, medicaments les contenant, utiles notamment comme inhibiteurs de l'aldose reductase | |
| FR2955107A1 (fr) | Nouveaux derives thiochromanes, leur procede de preparation et les compositions pharmaceutiques qui les contiennent |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 09794011 Country of ref document: EP Kind code of ref document: A1 |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| 122 | Ep: pct application non-entry in european phase |
Ref document number: 09794011 Country of ref document: EP Kind code of ref document: A1 |