Propiόnsäurederivate
Die vorliegende Anmeldung betrifft neue, potente PPAR-alpha aktivierende Nerbin- düngen zur Behandlung von zum Beispiel der koronaren Herzkrankheit sowie deren
Herstellung.
Trotz vielfacher Therapieerfolge bleiben koronare Herzkrankheiten (KHK) ein ernstes Problem der öffentlichen Gesundheit. Während die Behandlung mit Staunen durch Hemmung der HMG-CoA-Reduktase sehr erfolgreich sowohl die Plasmakonzentrationen von LDL-Cholesterin als auch die Mortalität von Risikopatienten senken, so fehlen heute überzeugende Behandlungsstrategien zur Therapie von Patienten mit ungünstigem HDL/LDL-Cholesterin-Nerhältnis oder der Hypertri- glyceridämie.
Fibrate stellen heute die einzige Therapieoption für Patienten dieser Risikogruppen dar. Sie wirken als schwache Agonisten des Peroxisom-Proliferator-aktivierten Rezeptors (PPAR)-alpha (Nature 1990, 347, 645-50). Ein Nachteil von bisher zugelassenen Fibraten ist ihre nur schwache Interaktion mit dem Rezeptor, die zu hohen Tagesdosen und deutlichen Nebenwirkungen führt.
In der WO 00/23407 werden PPAR-Modulatoren zur Behandlung von Obesitas, Atherosklerose und/oder Diabetes beschrieben.
Aufgabe der vorliegenden Erfindung war die Bereitstellung neuer Verbindungen, die als PPAR-alpha-Modulatoren eingesetzt werden können.
Es wurde nun gefunden, dass Verbindungen der allgemeinen Formel (I)
woπn
A für eine Bindung oder für eine -CH2- oder -CH2CH2- Gruppe steht,
X für O, S oder CH2 steht,
R1, R2 und R3 gleich oder verschieden sind und unabhängig voneinander für Wasserstoff, (Cι-C6)-Alkyl, (C3-C7)-Cycloalkyl, Hydroxy, (Cι-C6)-Alkoxy, (C6-Cιo)-Aryloxy, Halogen, Trifluormethyl, Trifluormethoxy, (CrC6)-
Alkylaminosulfonyl, Nitro oder Cyano stehen,
oder
R1 und R2 an zwei benachbarte Kohlenstoffatome gebunden sind und gemeinsam mit diesen einen annelierten Cyclohexan- oder Benzolring bilden, wobei letzterer gegebenenfalls durch eine (Cι-C4)-Alkylsulfonylmethyl-Gruppe substituiert ist,
und
R die oben angegebene Bedeutung hat,
R4 für Wasserstoff oder (Ci -C4)-Alkyl steht,
R5 und R6 Wasserstoff bedeuten oder gemeinsam mit dem Kohlenstoffatom, an das sie gebunden sind, eine Carbonylgruppe bilden,
R7 für Wasserstoff, (d-C6)-Alkyl, Phenyl oder Benzyl, worin die genannten Aromaten ihrerseits jeweils ein- bis dreifach gleich oder verschieden durch ( -C^-Alkyl, (d-C^-Alkoxy, Hydroxy oder Halogen substituiert sein können, steht,
R8 für Wasserstoff, (C6-Cιo)-Aryl oder für (C -C4)-Alkyl steht, das seinerseits durch Hydroxy, Trifluormethoxy, ( -C^-Alkoxy oder Phenoxy, welche ihrerseits gegebenenfalls ein- bis zweifach durch Trifluormethyl substituiert sind, oder durch (C6-C10)-Aryl oder 5- bis 6-gliedriges Heteroaryl mit bis zu drei Heteroatomen aus der Reihe N, O und oder S substituiert sein kann, wobei alle genannten Aryl- und Heteroaryl-Ringe ihrerseits jeweils ein- bis dreifach, gleich oder verschieden, durch Halogen, Hydroxy, (C C^-Alkyl, ( -C^-Alkoxy, Trifluormethyl, Trifluormethoxy, Cyano, Nitro oder A ino substituiert sein können,
R9 und R10 gleich oder verschieden sind und unabhängig voneinander für Wasserstoff, (C C6)-Alkyl, (CrC6)-Alkoxy, Trifluormethyl, Trifluormethoxy oder Halogen stehen,
11 1 R und R gleich oder verschieden sind und unabhängig voneinander für
Wasserstoff oder (d-C^-Alkyl stehen oder gemeinsam mit dem Kohlenstoffatom, an das sie gebunden sind, einen (C4-C7)-Cycloalkylring bilden,
und
R für Wasserstoff oder für eine hydrolysierbare Gruppe steht, die zur entsprechenden Carbonsäure abgebaut werden kann,
sowie deren pharmazeutisch verträgliche Salze, Hydrate und Solvate,
diese Aufgabe erfüllen und eine pharmakologische Wirkung zeigen sowie als Arzneimittel oder zur Herstellung von Arzneimittel-Formulierungen verwendet werden können.
Im Rahmen der Erfindung bedeutet in der Definition von R13 eine hydrolysi erbare
Gruppe eine Gruppe, die insbesondere im Körper zu einer Umwandlung der -C(O)OR -Gruppierung in die entsprechende Carbonsäure (R = Wasserstoff) führt. Solche Gruppen sind beispielhaft und vorzugsweise: Benzyl, (d-C6)-Alkyl oder (C3- C8)-Cycloalkyl, die jeweils gegebenenfalls ein- oder mehrfach, gleich oder verschieden, durch Halogen, Hydroxy, Amino, (d-C6)-Alkoxy, Carboxyl, (d-C6)-
Alkoxycarbonyl, (d-C6)-Alkoxycarbonylamino oder (d-C6)-Alkanoyloxy substituiert sind, oder insbesondere (d-C )-Alkyl, das gegebenenfalls ein- oder mehrfach, gleich oder verschieden, durch Halogen, Hydroxy, Amino, (Cι-Q)-AIkoxy, Carboxyl, (d-C )-Alkoxycarbonyl, (d-C^-Alkoxycarbonylamino oder (d-C4)- Alkanoyloxy substituiert ist.
(Cι-C6)-Alkyl und (d-C4)-Alkyl stehen im Rahmen der Erfindung für einen gerad- kettigen oder verzweigten Alkylrest mit 1 bis 6 bzw. 1 bis 4 Kohlenstoffatomen. Bevorzugt ist ein geradkettiger oder verzweigter Alkylrest mit 1 bis 4 Kohlenstoff- atomen. Beispielhaft und vorzugsweise seien genannt: Methyl, Ethyl, n-Propyl,
Isopropyl und t-Butyl.
(C6-do)-Aryl steht im Rahmen der Erfindung für einen aromatischen Rest mit 6 bis 10 Kohlenstoffatomen. Beispielhaft und vorzugsweise ist der Arylrest Phenyl.
(C3-C8)-Cycloalkyl und (C4-C7)-Cycloalkyl stehen im Rahmen der Erfindung für eine Cycloalkylgruppe mit 3 bis 8 bzw. 4 bis 7 Kohlenstoffatomen. Beispielhaft und vorzugsweise seien genannt: Cyclobutyl, Cyclopentyl und Cyclohexyl.
(d-Cö^Alkoxy steht im Rahmen der Erfindung für einen geradkettigen oder verzweigten Alkoxyrest mit 1 bis 6 Kohlenstoffatomen. Bevorzugt ist ein geradkettiger
oder verzweigter Alkoxyrest mit 1 bis 4 Kohlenstoffatomen. Beispielhaft und vorzugsweise seien genannt: Methoxy, Ethoxy, n-Propoxy, Isopropoxy, t-Butoxy, n-Pentoxy und n-Hexoxy.
(C6-C10)-Aryloxy steht im Rahmen der Erfindung für einen aromatischen Rest mit 6 bis 10 Kohlenstoffatomen, der über ein Sauerstoffatom verknüpft ist. Beispielhaft und vorzugsweise ist der Aryloxy-Rest Phenoxy.
(d-C6)-Alkoxycarbonyl steht im Rahmen der Erfindung für einen geradkettigen oder verzweigten Alkoxyrest mit 1 bis 6 Kohlenstoffatomen, der über eine Carbonylgruppe verknüpft ist. Bevorzugt ist ein geradkettiger oder verzweigter Alkoxycarbonylrest mit 1 bis 4 Kohlenstoffatomen. Beispielhaft und vorzugsweise seien genannt: Methoxy- carbonyl, Ethoxycarbonyl, n-Propoxycarbonyl, Isopropoxycarbonyl und t-Butoxy- carbonyl.
(Cι-C6)-Alkoxycarbonylamino steht im Rahmen der Erfindung für eine A ino- Gruppe mit einem geradkettigen oder verzweigten Alkoxycarbonyl-Substituenten, der im Alkoxyrest 1 bis 6 Kohlenstoffatome aufweist und über die Carbonylgruppe verknüpft ist. Bevorzugt ist ein Alkoxycarbonylamino-Rest mit 1 bis 4 Kohlenstoff- atomen. Beispielhaft und vorzugsweise seien genannt: Methoxycarbonylamino,
Ethoxycarbonylamino, n-Propoxycarbonylamino, Isopropoxycarbonylamino und t-Butoxycarbonylamino .
(d-C6)-Alkanoyloxy steht im Rahmen der Erfindung für einen geradkettigen oder verzweigten Alkyl-Rest mit 1 bis 6 Kohlenstoffatomen, der in der 1 -Position ein doppelt gebundenes Sauerstoffatom trägt und in der 1 -Position über ein weiteres Sauerstoffatom verknüpft ist. Beispielhaft und vorzugsweise seien genannt: Acetoxy, Propionoxy, n-Butyroxy, i-Butyroxy, Pivaloyloxy, n-Hexanoyloxy.
(d-C^-Alkylaminosulfonyl steht im Rahmen der Erfindung für eine Aminogruppe, die über eine Sulfonylgruppe verknüpft ist und die einen geradkettigen oder ver-
zweigten Alkylsubstituenten mit 1 bis 6 Kohlenstoffatomen aufweist. Bevorzugt ist ein Alkylaminosulfonyl-Rest mit 1 bis 4 Kohlenstoffatomen. Beispielhaft und vorzugsweise seien genannt: Methylaminosulfonyl, Ethylaminosulfonyl, n-Propyl- aminosulfonyl, Isopropylaminosulfonyl und t-Butylaminosulfonyl.
Halogen steht im Rahmen der Erfindung für Fluor, Chlor, Brom und lod. Bevorzugt sind Chlor oder Fluor.
5- bis 6-gliedriges Heteroaryl mit bis zu 3 Heteroatomen aus der Reihe S, N und/oder O steht im Rahmen der Erfindung im Allgemeinen für einen monocyclischen
Heteroaromaten, der über ein Ringkohlenstoffatom des Heteroaromaten, gegebenenfalls auch über ein Ringstickstoffatom des Heteroaromaten verknüpft ist. Beispielhaft und vorzugsweise seien genannt: Furanyl, Pyrrolyl, Thienyl, Thiazolyl, Oxazolyl, Imidazolyl, Triazolyl, Pyridyl, Pyrimidyl, Pyridazinyl. Bevorzugt sind Furanyl, Thienyl und Oxazolyl.
Die erfindungsgemäßen Nerbindungen können in Abhängigkeit von dem Substitutionsmuster in stereoisomeren Formen, die sich entweder wie Bild und Spiegelbild (Enantiomere), oder die sich nicht wie Bild und Spiegelbild (Diastereomere) verhalten, existieren. Die Erfindung betrifft sowohl die Enantiomeren oder
Diastereomeren als auch deren jeweilige Mischungen. Die Racemformen lassen sich ebenso wie die Diastereomeren in bekannter Weise in die stereoisomer einheitlichen Bestandteile trennen.
Weiterhin können bestimmte Nerbindungen in tautomeren Formen vorliegen. Dies ist dem Fachmann bekannt, und derartige Nerbindungen sind ebenfalls vom Umfang der Erfindung umfasst.
Die erfindungsgemäßen Nerbindungen können auch als Salze vorliegen. Im Rahmen der Erfindung sind physiologisch unbedenkliche Salze bevorzugt.
Physiologisch unbedenkliche Salze können Salze der erfindungsgemäßen Nerbindungen mit anorganischen oder organischen Säuren sein. Bevorzugt werden Salze mit anorganischen Säuren wie beispielsweise Chlorwasserstoffsäure, Bromwasserstoffsäure, Phosphorsäure oder Schwefelsäure, oder Salze mit organischen Carbon- oder Sulfonsäuren wie beispielsweise Essigsäure, Propionsäure, Maleinsäure, Fumar- säure, Äpfelsäure, Zitronensäure, Weinsäure, Milchsäure, Benzoesäure, oder Methan- sulfonsäure, Ethansulfonsäure, Benzolsulfonsäure, Toluolsulfonsäure oder Νaphthalindisulfonsäure.
Physiologisch unbedenkliche Salze können ebenso Salze der erfindungsgemäßen
Nerbindungen mit Basen sein, wie beispielsweise Metall- oder Ammoniumsalze. Bevorzugte Beispiele sind Alkalimetallsalze (z.B. Natrium- oder Kaliumsalze), Erdalkalisalze (z.B. Magnesium- oder Calciumsalze), sowie Ammoniumsalze, die abgeleitet sind von Ammoniak oder organischen Aminen, wie beispielsweise Ethylamin, Di- bzw. Triethylamin, Ethyldiisopropylamin, Monoethanolamin, Di- bzw. Tri- ethanolamin, Dicyclohexylamin, Dimethylaminoethanol, Dibenzylamin, N-Methyl- morpholin, Dihydroabietylamin, 1-Ephenamin, Methylpiperidin, Arginin, Lysin, Ethylendiamin oder 2-Phenylethylamin.
Die erfindungsgemäßen Nerbindungen können auch in Form ihrer Solvate, insbesondere in Form ihrer Hydrate vorliegen.
Bevorzugt sind Nerbindungen der allgemeinen Formel (I),
worin
A für eine Bindung oder für eine -CH2- oder -CH2CH2- Gruppe steht,
X für O, S oder CH2 steht,
R1, R2 und R3 gleich oder verschieden sind und unabhängig voneinander für Wasserstoff, (d-C6)-Alkyl, (d-C6)-Alkoxy, Hydroxy, Halogen, Trifluormethyl, Trifluormethoxy, Nitro oder Cyano stehen,
R4 für Wasserstoff oder (d-C )-Alkyl steht,
R und R Wasserstoff bedeuten oder gemeinsam mit dem Kohlenstoffatom, an das sie gebunden sind, eine Carbonylgruppe bilden,
R7 für Wasserstoff, (d-C6)-Alkyl, Phenyl oder Benzyl, worin die genannten
Aromaten ihrerseits jeweils ein- bis dreifach gleich oder verschieden durch (Cι-C6)-Alkyl, (d-C6)-Alkoxy, Hydroxy oder Halogen substituiert sein können, steht,
R8 für Wasserstoff, (C6-do)-Aryl oder für (d-C4)-Alkyl, das seinerseits gegebenenfalls durch (C6-do)-Aryl oder 5- bis 6-gliedriges Heteroaryl mit bis zu drei Heteroatomen aus der Reihe N, O und/oder S substituiert ist, steht, wobei alle genannten Ringsysteme ihrerseits jeweils ein- bis dreifach gleich oder verschieden durch Halogen, Hydroxy, (d-C6)-Alkyl, (d-C6)-Alkoxy, Trifluormethyl, Trifluormethoxy, Cyano, Nitro oder Amino substituiert sein können,
R9 und R10 gleich oder verschieden sind und unabhängig voneinander für Wasserstoff, (d-C6)-Alkyl, (d-C6)-Alkoxy, Trifluormethyl, Trifluor- methoxy oder Halogen stehen,
R und R gleich oder verschieden sind und unabhängig voneinander für Wasserstoff oder (d-C6)-Alkyl stehen oder gemeinsam mit dem Kohlenstoffatom, an das sie gebunden sind, einen (C4-C7)-Cycloalkylring bilden,
und
R13 für Wasserstoff oder für eine hydrolysierbare Gruppe steht, die zur entsprechenden Carbonsäure abgebaut werden kann,
sowie deren pharmazeutisch verträgliche Salze, Hydrate und Solvate.
Besonders bevorzugt sind Nerbindungen der allgemeinen Formel (I),
worin
A für eine -CH - oder -CH2CH2-Gruppe steht,
X für O, S oder CH2 steht,
R1, R2 und R3 gleich oder verschieden sind und unabhängig voneinander für
Wasserstoff, (d-C4)-Alkyl, (d-C4)-Alkoxy, Chlor, Fluor, Trifluormethyl, Trifluormethoxy, Νitro oder Cyano stehen,
R4 für Wasserstoff oder Methyl steht,
R5 und R6 Wasserstoff bedeuten oder gemeinsam mit dem Kohlenstoffatom, an das sie gebunden sind, eine Carbonylgruppe bilden,
R7 für Wasserstoff, (d-C4)-Alkyl oder Benzyl steht,
R8 für Wasserstoff, Phenyl, Benzyl oder 5-gliedriges Heteroarylmethyl mit bis zu zwei Heteroatomen aus der Reihe Ν, O und/oder S steht, wobei die genannten aromatischen Ringsysteme ihrerseits jeweils ein- bis dreifach gleich oder verschieden durch Chlor, Fluor, Brom, Hydroxy, (d-C4)-Alkyl, (d-C4)-Alkoxy, Trifluormethyl oder Amino substituiert sein können,
R9 und R10 gleich oder verschieden sind und unabhängig voneinander für Wasserstoff, (d-C3)-Alkyl, (d-C3)-Alkoxy, Trifluormethyl, Fluor oder Chlor stehen,
R11 und R12 gleich oder verschieden sind und unabhängig voneinander für
Wasserstoff, Methyl oder Ethyl stehen oder gemeinsam mit dem Kohlenstoffatom, an das sie gebunden sind, einen Cyclopentyl- oder Cyclohexylring bilden,
und
R13 für Wasserstoff oder für eine hydrolysierbare Gruppe steht, die zur entsprechenden Carbonsäure abgebaut werden kann,
sowie deren pharmazeutisch verträgliche Salze, Hydrate und Solvate.
Ganz besonders bevorzugt sind Nerbindungen der allgemeinen Formel (I),
woπn
A für eine -CH2- oder -CH2CH2- Gruppe steht,
X für O, S oder CH2 steht,
R1 für Wasserstoff, Methyl oder Methoxy steht,
9
R und R gleich oder verschieden sind und unabhängig voneinander für Methyl, Trifluormethyl, Methoxy, Trifluormethoxy, Chlor oder Fluor stehen,
R4 für Wasserstoff steht,
R5 und R6 gemeinsam mit dem Kohlenstoffatom, an das sie gebunden sind, eine Carbonylgruppe bilden,
R7 für Methyl, Ethyl, n-Propyl oder insbesondere für Wasserstoff steht,
R8 für Phenyl, Furanylmethyl oder Thienylmethyl steht, wobei die genannten
Ringsysteme ihrerseits jeweils ein- bis zweifach gleich oder verschieden durch Methyl oder Ethyl substituiert sein können,
R9 und R10 gleich oder verschieden sind und für Wasserstoff oder Methyl und insbesondere für Wasserstoff stehen,
Ru und R12 gleich oder verschieden sind und für Wasserstoff oder Methyl und insbesondere für Methyl stehen,
und
R13 für eine hydrolysierbare Gruppe steht, die zur entsprechenden Carbonsäure abgebaut werden kann, oder insbesondere für Wasserstoff steht,
sowie deren pharmazeutisch verträgliche Salze, Hydrate und Solvate.
Die oben aufgeführten allgemeinen oder in Norzugsbereichen angegebenen Reste- definitionen gelten sowohl für die Endprodukte der Formel (I) als auch entsprechend für die jeweils zur Herstellung benötigten Ausgangsstoffe bzw. Zwischenprodukte.
Die in den jeweiligen Kombinationen bzw. bevorzugten Kombinationen von Resten im einzelnen angegebenen Restedefinitionen werden unabhängig von den jeweilig angegebenen Kombinationen der Reste beliebig auch durch Restedefinitionen ande- rer Kombinationen ersetzt.
Von besonderer Bedeutung sind Verbindungen der Formel (I), in denen R für Wasserstoff steht.
Von besonderer Bedeutung sind Verbindungen der Formel (I), in denen R5 und R6 gemeinsam mit dem Kohlenstoffatom, an das sie gebunden sind, eine Carbonylgruppe bilden.
Von besonderer Bedeutung sind Verbindungen der Formel (I), in denen
R1 für Wasserstoff, Methyl oder Methoxy steht,
und
9 * •
R und R gleich oder verschieden sind und unabhängig voneinander für Methyl, Isopropyl, tert.-Butyl, Cyclohexyl, Trifluormethyl, Methoxy, Trifluormethoxy, Chlor oder Fluor stehen.
Von besonderer Bedeutung sind Verbindungen der Formel (I), in denen
R für Phenyl, Furanylmethyl, Thienylmethyl oder Oxazolylmethyl, wobei die genannten Ringsysteme ihrerseits jeweils ein- bis zweifach durch Methyl substituiert sein können, oder für 2-Methoxyethyl steht.
Von ganz besonderer Bedeutung sind Verbindungen der Formel (IA)
in der
A für eine -CH2- oder -CH2CH2- Gruppe steht,
X für O oder S steht,
R1 für Wasserstoff, Methyl oder Methoxy steht,
R2 und R3 gleich oder verschieden sind und unabhängig voneinander für Methyl, Isopropyl, tert.-Butyl, Cyclohexyl, Trifluormethyl, Methoxy, Trifluor- methoxy, Chlor oder Fluor stehen,
und
R für Phenyl, Furanylmethyl, Thienylmethyl oder Oxazolylmethyl, wobei die genannten Ringsysteme ihrerseits jeweils ein- bis zweifach durch Methyl substituiert sein können, oder für 2-Methoxyethyl steht.
Außerdem wurde ein Verfahren zur Herstellung der erfindungsgemäßen Verbin- düngen der allgemeinen Formel (I) gefunden, dadurch gekennzeichnet, dass man
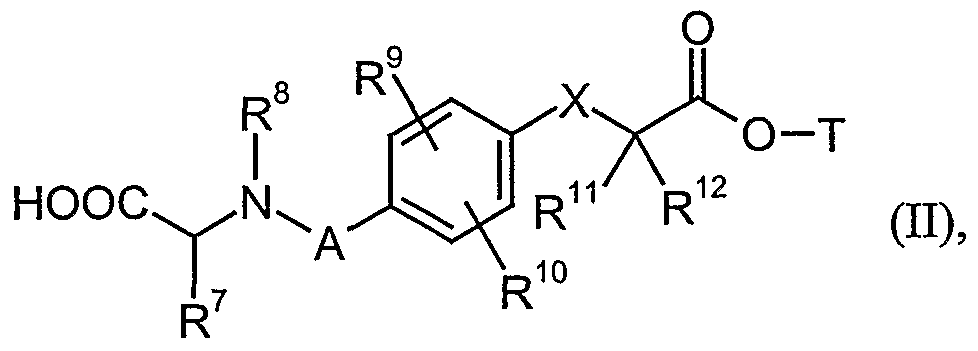
[A] Verbindungen der allgemeinen Formel (II)
in welcher
A, X, R , R°, Ry, R , R11 und R die oben angegebene Bedeutung haben
und
T für Benzyl, (d-C6)-Alkyl oder für einen für die Festphasen-Synthese geeigneten polymeren Träger steht,
zunächst unter Aktivierung der Carbonsäure-Gruppe in (II) mit Verbindungen der allgemeinen Formel (III)
in welcher
R1, R2 und R3 die oben angegebene Bedeutung haben,
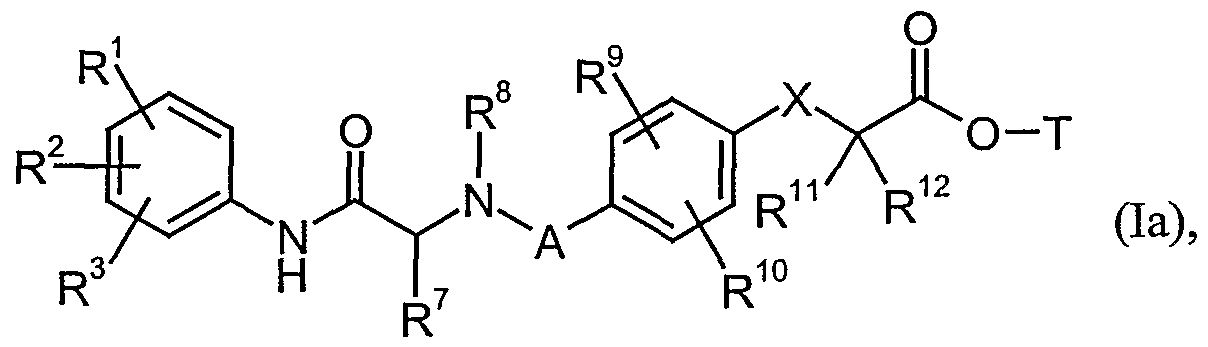
zu Verbindungen der allgemeinen Formel (Ia)
in welcher
A, X, T, R1, R2, R3, R7, R8, R9, R10, R11 und R12 die oben angegebene Bedeutung haben,
umsetzt,
oder
[B] Verbindungen der allgemeinen Formel (IV)
in welcher
A, X, T, R8, R9, R10, R1 x und R12 die oben angegebene Bedeutung haben,
in Gegenwart einer Base mit Verbindungen der allgemeinen Formel (V)
in welcher
R1, R2, R3 und R7 die oben angegebene Bedeutung haben
und
Q für eine geeignete Abgangsgrappe, wie beispielsweise Halogen, Mesylat oder Tosylat, vorzugsweise für Brom oder lod steht,
gleichfalls zu Verbindungen der allgemeinen Formel (Ia) umsetzt,
dann die Verbindungen der allgemeinen Formel (Ia) gegebenenfalls nach bekannten Methoden zur Amid-Alkylierung bzw. Amid-Reduktion in Verbindungen der allgemeinen Formel (Ib)
in welcher
A, X, T, R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R11 und R12 die oben angegebene
Bedeutung haben,
überführt,
anschließend mit Säuren oder Basen in die entsprechenden Carbonsäuren der allgemeinen Formel (Ic)
in welcher
A, X, R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R11 und R12 die oben angegebene Bedeutung haben,
überführt,
und diese gegebenenfalls nach bekannten Methoden zur Veresterung durch Umsetzung mit Verbindungen der allgemeinen Formel (VI)
Rl3-Z (VI),
woπn
R13 die oben angegebene Bedeutung hat
und
Z für eine geeignete Abgangsgruppe, wie beispielsweise Halogen, Mesylat oder Tosylat, oder für eine Hydroxy-Gruppe steht,
weiter modifiziert.
Das erfindungsgemäße Verfahren wird im Allgemeinen bei Normaldruck durchge- führt. Es ist aber auch möglich, das Verfahren bei Überdruck oder bei Unterdruck durchzuführen (z.B. in einem Bereich von 0,5 bis 5 bar).
Als Lösemittel für das Verfahren eignen sich übliche organische Lösemittel, die sich unter den Reaktionsbedingungen nicht verändern. Hierzu gehören Ether wie Diethyl- ether, Dioxan, Tetrahydrofuran, Glykoldimethylether, oder Kohlenwasserstoffe wie
Benzol, Toluol, Xylol, Hexan, Cyclohexan oder Erdölfraktionen, oder Halogenkohlenwasserstoffe wie Dichlormethan, Trichlormethan, Tetrachlormethan, Dichlor- ethylen, Trichlorethylen oder Chlorbenzol, oder Ethylacetat, Pyridin, Dimethylsulf- oxid, Dimethylformamid, N,N'-Dimethylpropylenharnstoff (DMPU), N-Methyl- pyrrolidon (NMP), Acetonitril, Aceton oder Nitromethan. Ebenso ist es möglich, Gemische der genannten Lösemittel zu verwenden.
Bevorzugte Lösemittel für den Verfahrensschritt (II) + (III) — » (Ia) sind Dichlor- methan und Dimethylformamid. Für den Verfahrensschritt (IN) + (N) — » (Ia) ist Dimethylformamid bevorzugt.
Der erfindungsgemäße Nerfahrensschritt (II) + (III) - (Ia) wird im Allgemeinen in einem Temperaturbereich von 0°C bis +100°C, bevorzugt von 0°C bis +40°C, durchgeführt. Der Nerfahrensschritt (IV) + (V) -» (Ia) wird im Allgemeinen in einem Temperaturbereich von 0°C bis +120°C, bevorzugt von +50°C bis +100°C durchgeführt.
Als Hilfsstoffe für die Amidbildung im Verfahrensschritt (II) + (III) - (Ia) werden bevorzugt übliche Kondensationsmittel eingesetzt, wie Carbodiimide, z.B. Ν,Ν'- Diethyl-, N,N'-Dipropyl-, N,N'-Diisopropyl-, N,N'-Dicyclohexylcarbodiimid (DCC), N-(3-Dimethylaminoisopropyl)-N'-ethylcarbodiimid-Hydrochlorid (EDC), oder
Carbonylverbindungen wie Carbonyldiimidazol, oder 1,2-Oxazoliumverbindungen wie 2-Ethyl-5-phenyl-l,2-oxazolium-3-sulfat oder 2-tert.-Butyl-5-methyl-isoxazo- lium-perchlorat, oder Acylaminoverbindungen wie 2-Ethoxy-l-ethoxycarbonyl-l,2- dihydrochinolin, oder Propanphosphonsäureanhydrid, oder Isobutylchlorformiat, oder Bis-(2-oxo-3-oxazolidinyl)-phosphorylchlorid oder Benzotriazolyloxy- tris(dimethylamino)phosphonium-hexafluorophosphat, oder O-(Benzotriazol-l-yl)- N^N^N'-tetramethyluronium-hexafluorophosphat (HBTU), 2-(2-Oxo-l -(2H)- pyridyl)-lJ,3,3-tetramethyluronium-tetrafluoroborat (TPTU) oder O-(7-Azabenzo- triazol-1 -yl)-N,N,N',N'-tetramethyluronium-hexafluorophosphat (HATU), gegebe- nenfalls in Kombination mit weiteren Hilfsstoffen wie 1-Hydroxybenzotriazol oder
N-Hydroxysuccinimid, sowie als Basen Alkalicarbonate, z.B. Natrium- oder Kalium- carbonat oder -hydrogencarbonat, oder organische Basen wie Trialkylamine, z.B. Triethylamin, N-Methylmorpholin, N-Methylpiperidin oder Diisopropylethylamin. Besonders bevorzugt ist die Kombination von EDC, N-Methylmorpholin und 1- Hydroxybenzotriazol, EDC, Triethylamin und 1-Hydroxybenzotriazol sowie von
HATU und Diisopropylethylamin.
Als Base für die Reaktion (IV) + (V) -» (Ia) eignen sich die üblichen anorganischen Basen wie Alkalihydroxide, wie beispielsweise Lithium-, Natrium- oder Kaliumhydroxid, Alkali- oder Erdalkalicarbonate wie Natrium-, Kalium-, Calcium- oder Cäsiumcarbonat oder Natrium- oder Kaliumhydrogencarbonat, oder organische
Basen wie Trialkylamine, z.B. Triethylamin, N-Methylmorpholin, N-Methyl- piperidin oder Diisopropylethylamin. Bevorzugt ist Natriumhydrogencarbonat.
Die Hydrolyse der Carbonsäureester im Verfahrensschritt (Ia) bzw. (Ib) - (Ic) erfolgt nach üblichen Methoden, indem man die Ester in inerten Lösemitteln mit
Basen behandelt, wobei die zunächst entstehenden Salze durch Behandeln mit Säure in die freien Carbonsäuren überführt werden. Im Falle der tert.-Butylester erfolgt die Hydrolyse bevorzugt mit Säuren.
Als Lösemittel eignen sich für die Hydrolyse der Carbonsäureester Wasser oder die für eine Esterspaltung üblichen organischen Lösemittel. Hierzu gehören bevorzugt Alkohole wie Methanol, Ethanol, Propanol, Isopropanol oder Butanol, oder Ether wie Tetrahydrofuran oder Dioxan, Dimethylformamid, Dichlormethan oder Dime- thylsulfoxid. Ebenso ist es möglich, Gemische der genannten Lösemittel einzusetzen. Bevorzugt sind Wasser/Tetrahydrofuran und im Falle der Umsetzung mit Tri- fluoressigsäure Dichlormethan sowie im Falle von Chlorwasserstoff Tetrahydrofuran, Diethylether, Dioxan oder Wasser.
Als Basen eignen sich für die Hydrolyse die üblichen anorganischen Basen. Hierzu gehören bevorzugt Alkalihydroxide oder Erdalkalihydroxide wie beispielsweise
Natriumhydroxid, Lithiumhydroxid, Kaliumhydroxid oder Bariumhydroxid, oder Alkalicarbonate wie Natrium- oder Kaliumcarbonat oder Natriumhydrogencarbonat. Besonders bevorzugt werden Natriumhydroxid oder Lithiumhydroxid eingesetzt.
Als Säuren eignen sich im Allgemeinen Trifluoressigsäure, Schwefelsäure,
Chlorwasserstoff, Bromwasserstoff und Essigsäure oder deren Gemische
gegebenenfalls unter Zusatz von Wasser. Bevorzugt sind Chlorwasserstoff oder Trifluoressigsäure im Falle der tert.-Butylester und Salzsäure im Falle der Methylester.
Im Falle der über Festphasen-Synthese hergestellten, über die Carbonsäure-Gruppe an einen polymeren Träger gebundenen Verbindungen der allgemeinen Formel (Ia) bzw. (Ib) erfolgt die Abspaltung vom Harz zu den Verbindungen der allgemeinen Formel (Ic) gleichfalls nach den zuvor beschriebenen üblichen Methoden zur Carbonsäureester-Hydrolyse. Bevorzugt wird hier Trifluoressigsäure eingesetzt.
Bei der Durchführung der Hydrolyse wird die Base oder die Säure im Allgemeinen in einer Menge von 1 bis 100 mol, bevorzugt von 1,5 bis 40 mol bezogen auf 1 mol des Esters eingesetzt.
Die Hydrolyse wird im Allgemeinen in einem Temperaturbereich von 0°C bis
+100°C, bevorzugt von 0°C bis +50°C, durchgeführt.
Die Verbindungen der allgemeinen Formel (II) sind neu und können hergestellt werden, indem man zunächst
[a] Verbindungen der allgemeinen Formel (VII)
worin
X, T, R9, R10, R11 und R12 die oben angegebene Bedeutung haben
und
B für eine Bindung oder eine Methylengruppe steht,
in Gegenwart eines geeigneten Reduktionsmittels mit Nerbindungen der allgemeinen
Formel (NIII)
R14-ΝH2 (NIII),
in welcher
R .14 [a-1] die oben angegebene Bedeutung von R hat
oder
[a-2] für eine Gruppe der Formel steht,
worin
R7 die oben angegebene Bedeutung hat
und
R15 für (C C4)-Alkyl oder Trimethylsilyl steht,
zu Nerbindungen der allgemeinen Formel (IX)
B, X, T, R9, R10, R11, R12 und R14 die oben angegebene Bedeutung haben
umsetzt,
diese dann in Gegenwart einer Base mit Nerbindungen der allgemeinen Formel (X)
R16-Y (X),
in welcher
R .16 im Falle der Nerfahrensvariante [a-1] für eine Gruppe der Formel
7 1 ^ worin R und R die oben angegebene Bedeutung haben,
oder
im Falle der Nerfahrensvariante [a-2] die oben angegebene Bedeutung von R hat,
und
Y für eine geeignete Abgangsgruppe, wie beispielsweise Halogen, Mesylat oder Tosylat, vorzugsweise für Brom oder lod steht,
zu Verbindungen der allgemeinen Formel (XI)
in welcher
B, X, T, R7, R8, R9, R10, R11, R12 und R15 die oben angegebene Bedeutung haben,
umsetzt,
und abschließend in diesen Verbindungen selektiv die Carbonsäureester-Gruppierung -COOR15 zur Carbonsäure hydrolysiert,
oder
[b] Verbindungen der allgemeinen Formel (XII)
worin
A, X, T, R9, R10, R11 und R12 die oben angegebene Bedeutung haben,
in Gegenwart eines geeigneten Reduktionsmittels mit Verbindungen der allgemeinen Formel (XIII)
in welcher
R17 für Wasserstoff, (C6-C10)-Aryl, 5- bis 6-gliedriges Heteroaryl mit bis zu drei Heteroatomen aus der Reihe N, O und/oder S oder für (d-C3)-Alkyl steht, das seinerseits durch Hydroxy, Trifluormethoxy, (d-C4)-Alkoxy oder
Phenoxy, welche ihrerseits gegebenenfalls ein- bis zweifach durch Trifluormethyl substituiert sind, oder durch (C6-C10)-Aryl oder 5- bis 6- gliedriges Heteroaryl mit bis zu drei Heteroatomen aus der Reihe N, O und/oder S substituiert sein kann, wobei alle genannten Aryl- und Heteroaryl- Ringe ihrerseits jeweils ein- bis dreifach, gleich oder verschieden, durch
Halogen, Hydroxy, (d-C6)-Alkyl, (d-C6)-Alkoxy, Trifluormethyl, Trifluormethoxy, Cyano, Nitro oder Amino substituiert sein können,
zu Verbindungen der allgemeinen Formel (XIV)
worin
A, X, T, R9, R10, R11, R12 und R17 die oben angegebene Bedeutung haben,
umsetzt,
diese dann in Gegenwart einer Base mit Nerbindungen der allgemeinen Formel (XV)
in welcher
R7, R15 und Y die oben angegebene Bedeutung haben,
zu Nerbindungen der allgemeinen Formel (XNI)
in welcher
A, X, T, R7, R9, R10, R11, R12, R15 und R17 die oben angegebene Bedeutung haben,
umsetzt,
und abschließend in diesen Nerbindungen selektiv die Carbonsäureester-Gruppierung -COOR15 zur Carbonsäure hydrolysiert.
Das gesamte Nerfahren kann auch als Festphasen-Synthese durchgeführt werden. In diesem Fall werden die Nerbindungen der allgemeinen Formel (NU) bzw. (XII) als
Carbonsäureester an ein geeignetes Trägerharz geknüpft, die weiteren Reaktionen an fester Phase durchgeführt und die Zielverbindung abschließend vom Harz abge-
spalten. Festphasen-Synthese sowie die Anknüpfung und die Abspaltung vom Harz sind geläufige Standardtechniken. Als ein Beispiel aus der umfangreichen Literatur wird auf die Publikation "Linkers for Solid Phase Organic Synthesis", Ian W. James, Tetrahedron 55, 4855-4946 (1999) verwiesen.
Die Umsetzung (VII) + (VIII) - (IX) bzw. (XII) + (XIII) -> (XIV) erfolgt in den für eine reduktive Aminierung üblichen, unter den Reaktionsbedingungen inerten Lösemitteln, gegebenenfalls in Gegenwart einer Säure. Zu diesen Lösemitteln gehören beispielsweise Wasser, Dimethylformamid, Tetrahydrofuran, Dichlormethan, Dichlorethan oder Alkohole wie Methanol, Ethanol, Propanol, Isopropanol oder
Butanol; ebenso ist es möglich, Gemische der genannten Lösemittel einzusetzen. Bevorzugt sind Methanol und Ethanol jeweils unter Zusatz von Essigsäure.
Als Reduktionsmittel für die Umsetzung (VII) + (VIII) → (IX) bzw. (XII) + (XIII) — » (XIV) eignen sich komplexe Aluminium- oder Borhydride, wie beispielsweise
Diisobutylaluminmmhydrid, Natriumborhydrid, Natriumtriacetoxyborhydrid, Natriumcyanoborhydrid oder Tetrabutylammoniumborhydrid, oder auch die katalytische Hydrierung in Gegenwart von Übergangsmetall-Katalysatoren wie beispielsweise Palladium, Platin, Rhodium oder Raney-Nickel. Bevorzugte Reduktions- mittel sind Natriumcyanoborhydrid, Natriumtriacetoxyborhydrid und Tetrabutylammoniumborhydrid.
Die Umsetzung (VII) + (VIII) → (IX) bzw. (XII) + (XIII) → (XIV) erfolgt im Allgemeinen in einem Temperaturbereich von 0°C bis +40°C.
Der Umsetzung (IX) + (X) - (XI) bzw. (XIV) + (XV) -» (XVI) erfolgt in den üblichen unter den Reaktionsbedingungen inerten Lösemitteln. Bevorzugt sind Dimethylformamid, Tetrahydrofuran und Dioxan.
Als Base für die Reaktion (IX) + (X) - (XI) bzw. (XIV) + (XV) → (XVI) eignen sich die üblichen anorganischen oder organischen Basen. Bevorzugt ist Triethylamin.
Die Umsetzung (IX) + (X) → (XI) bzw. (XIV) + (XV) → (XVI) erfolgt im Allgemeinen in einem Temperaturbereich von 0°C bis +100°C.
Die Reaktion (XI) - (II) bzw. (XVI) -» (II) erfolgt in den für eine Esterspaltung üblichen, unter den Reaktionsbedingungen inerten Lösemitteln. Im Fall der Ester- Hydrolyse sind dies bevorzugt Tetrahydrofuran, Dioxan und Alkohole wie Methanol und Ethanol jeweils im Gemisch mit Wasser. Im Fall der Silylester-Spaltung wird bevorzugt Dioxan oder Tetrahydrofuran eingesetzt.
Als Base für die Reaktion (XI) -» (II) bzw. (XVI) → (II) eignen sich im Fall der Hydrolyse die üblichen anorganischen Basen. Bevorzugt sind Lithium-, Natrium- und Kaliumhydroxid. Im Fall der Silylester-Spaltung wird bevorzugt Tetrabutyl- ammoniumfluorid verwendet.
Die Umsetzung (XI) -» (II) bzw. (XVI) -» (II) erfolgt im Allgemeinen in einem Temperaturbereich von 0°C bis +100°C.
Die Verbindungen der allgemeinen Formel (IV) entsprechen den Verbindungen der allgemeinen Formel (IX) bzw. (XIV) und können wie zuvor beschrieben hergestellt werden.
Die Verbindungen der allgemeinen Formeln (III), (V), (VI), (VII), (VIII), (X), (XII), (XIII) und (XV) sind kommerziell erhältlich, bekannt oder nach üblichen Methoden herstellbar [vgl. z.B. PJ. Brown et al., J. Med. Chem. 42, 3785-88 (1999)].
Die erfindungsgemäßen Nerbindungen der Formel (I) zeigen ein überraschendes und wertvolles pharmakologisches Wirkungsspektrum und lassen sich daher als vielseitige Medikamente einsetzen. Insbesondere eignen sie sich zur Behandlung der koronaren Herzkrankheit, zur Myokardinfarkt-Prophylaxe sowie zur Behandlung von
Restenose nach Koronarangioplastie oder Stenting. Bevorzugt eignen sich die
erfindungsgemäßen Nerbindungen der Formel (I) zur Behandlung der Arteriosklerose und Hypercholesterolämie, zur Erhöhung krankhaft niedriger HDL-Spiegel sowie zur Senkung erhöhter Triglycerid-, Fibrinogen- und LDL-Spiegel. Darüber hinaus können sie zur Behandlung von Obesitas, Diabetes, zur Behandlung des metabolischen Syndroms (Glucose-Intoleranz, Hyperinsulinämie, Dyslipidämie und
Bluthochdruck infolge von Insulinresistenz), der Leberfibrose und Krebs angewendet werden.
Die Wirksamkeit der erfindungsgemäßen Nerbindungen lässt sich z.B. in vitro durch den im Beispielteil beschriebenen Transaktivierungsassay prüfen.
Die Wirksamkeit der erfindungsgemäßen Nerbindungen in vivo lässt sich z.B. durch die im Beispielteil beschriebenen Untersuchungen prüfen.
Für die Applikation der Nerbindungen der allgemeinen Formel (I) kommen alle üblichen Applikationsformen in Betracht, d.h. also oral, parenteral, inhalativ, nasal, sub- lingual, rektal oder äußerlich wie z.B. transdermal, insbesondere bevorzugt oral oder parenteral. Bei der parenteralen Applikation sind insbesondere intravenöse, intramuskuläre, subkutane Applikation zu nennen, z.B. als subkutanes Depot. Ganz be- sonders bevorzugt ist die orale Applikation.
Hierbei können die Wirkstoffe allein oder in Form von Zubereitungen verabreicht werden. Für die orale Applikation eignen sich als Zubereitungen u.a. Tabletten, Kapseln, Pellets, Dragees, Pillen, Granulate, feste und flüssige Aerosole, Sirupe, Emul- sionen, Suspensionen und Lösungen. Hierbei muss der Wirkstoff in einer solchen
Menge vorliegen, dass eine therapeutische Wirkung erzielt wird. Im Allgemeinen kann der Wirkstoff in einer Konzentration von 0,1 bis 100 Gew.-%, insbesondere 0,5 bis 90 Gew.-%, vorzugsweise 5 bis 80 Gew.-%, vorliegen. Insbesondere sollte die Konzentration des Wirkstoffs 0,5 - 90 Gew.-% betragen, d.h. der Wirkstoff sollte in Mengen vorliegen, die ausreichend sind, den angegebenen Dosierungsspielraum zu erreichen.
Zu diesem Zweck können die Wirkstoffe in an sich bekannter Weise in die üblichen Zubereitungen überführt werden. Dies geschieht unter Verwendung inerter, nichttoxischer, pharmazeutisch geeigneter Trägerstoffe, Hilfsstoffe, Lösungsmittel, Vehikel, Emulgatoren und oder Dispergiermittel.
Als Hilfsstoffe seien beispielsweise aufgeführt: Wasser, nichttoxische organische Lösungsmittel wie z.B. Paraffine, pflanzliche Öle (z.B. Sesamöl), Alkohole (z.B. Ethanol, Glycerin), Glykole (z.B. Polyethylenglykol), feste Trägerstoffe wie natür- liehe oder synthetische Gesteinsmehle (z.B. Talkum oder Silikate), Zucker (z.B.
Milchzucker), Emulgiermittel, Dispergiermittel (z.B. Polyvinylpyrrolidon) und Gleitmittel (z.B. Magnesiumsulfat).
Im Falle der oralen Applikation können Tabletten selbstverständlich auch Zusätze wie Natriumeitrat zusammen mit Zuschlagstoffen wie Stärke, Gelatine und dergleichen enthalten. Wässrige Zubereitungen für die orale Applikation können weiterhin mit Geschmacksaufbesserern oder Farbstoffen versetzt werden.
Bei oraler Applikation werden vorzugsweise Dosierungen von 0,001 bis 5 mg/kg, bevorzugt von 0,005 bis 3 mg/kg Körpergewicht je 24 Stunden appliziert.
Die nachfolgenden Ausführungsbeispiele erläutern die Erfindung. Die Erfindung ist nicht auf die Beispiele beschränkt.
Die folgenden verwendeten Abkürzungen stehen für:
Ac Acetyl
Bu Butyl
DC Dünnschichtchromatographie
DCI direkte chemische Ionisation (bei MS)
DCM Dichlormethan
DIC Diisopropylcarbodiimid
DMAP 4-N, N-Dimethylaminopyridin
DMF N, N-Dimethylformamid
DMSO Dimethylsulfoxid
EDC N-(3-Dimethylaminopropyl)-N-ethylcarbodiimid x HCl
EI Elektronenstoß-Ionisation (bei MS)
ESI Elektrospray-Ionisation (bei MS)
Et Ethyl ges. gesättigt
HATU O-(7- Azabenzotriazol- 1 -yl)-N, N, N', N -tetramethyluromum-
Hexafluorphosphat
HOBt 1-Hydroxy-lH-benzotriazol x H2O
HPLC Hochdruck-, Hochleistungsflüssigchromatographie
LC-MS Flüssigchromatographie-gekoppelte Massenspektroskopie
Me Methyl
MS Massenspektroskopie
NMR Kernresonanzspektroskopie
RF Rückfluss f Retentionsindex (bei DC)
RT Raumtemperatur
Rt Retentionszeit (bei HPLC)
TBAF Tetrabutylammoniumfluorid
TB AI Tetrabutylammomumiodid
TFA Trifluoressigsäure
THF Tetrahydroftiran
Ausgangsverbindungen I
Beispiel 1-1 tert-Butyl-2-methylpropionat
Eine Lösung von 73,0 g (0,985 mol) tert-Butanol, 190 g (1,877 mol) Triethylamin und 0,573 g (0,0047 mol) DMAP in 750 ml Dichlormethan wird unter Eiskühlung mit einer Lösung von 100 g (0,939 mmol) Isobuttersäurechlorid in 150 ml Dichlormethan versetzt und nach Zugabe über Nacht gerührt. Anschließend werden 500 ml 2 M Salzsäure zugegeben, die wässrige Phase wird mit Dichlormethan extrahiert, die vereinigten organischen Phasen werden mit Wasser, ges. NaHCO3-Lsg. und ges. NaCl-Lsg. gewaschen, über Natriumsulfat getrocknet und eingeengt. DestiUative Reinigung des Rohproduktes ergibt 65,5 g (48 %) des tert-Butyl-2-methyl- propionates. 1H-NMR (200 MHz, CDC13): δ = 1.11 (d, 6H); 1.44 (s, 9H); 2.42 (sept, 1H).
Beispiel 1-2 tert-Butyl-3-(4-bromphenyl)-2,2-dimethylpropionat
Zu einer Lösung von 10,0 g (69,34 mmol) tert-Butyl-2-methylpropionat (Beispiel I- 1) in 100 ml Tetrahydrofuran werden bei -78°C 34,7 ml (69,4 mmol) einer 2 M
Lithiumdiisopropylamid-Lsg. langsam zugetropft. Nach beendeter Zugabe wird das
Gemisch 1 h bei -78°C gerührt, dann wird eine Lösung von 15,76 g (63,04 mmol) 4- Brombenzylbromid in 10 ml Tetrahydrofuran zugegeben und 1 h bei -78°C gerührt. Anschließend erwärmt man die Reaktion auf Raumtemperatur, gießt auf 100 ml I N Salzsäure, trennt die Phasen und extrahiert die wässrige Phase 3x mit Diethylether. Die vereinigten organischen Phasen werden mit NaHCO3-Lsg. gewaschen, über
Natriumsulfat getrocknet und im Vakuum vom Lösungsmittel befreit. Die destiUative Reinigung des Rückstandes im Ölpumpenvakuum ergibt 16,75 g (85 %) des tert- Butyl-3-(4-bromphenyl)-2,2-dimethylpropionates.
1H-NMR (200 MHz, DMSO): δ - 1.06 (s, 6H); 1-38 (s, 9H); 2.74 (s, 2H); 7.10 (d, 2H); 7.47 (d, 2H).
Beispiel 1-3 tert-Butyl-3-(4-formylphenyl)-2,2-dimethylpropionat
Eine Lösung von 6,00 g (19,16 mmol) tert-Butyl-3-(4-bromophenyl)-2,2-dimethy- lpropionat (Beispiel 1-2) in 80 ml Tetrahydrofuran wird bei -75°C langsam mit 13,5 ml (22,98 mmol) einer 1,7 M tert-Butyllithium-Lsg. in Pentan versetzt, wobei die Temperatur unter -60°C gehalten wird. Das Gemisch wird 15 min nachgerührt, dann werden 1,82 g (24,90 mmol) N,N-Dimethylformamid zugegeben und das Gemisch weitere 4 h bei -75°C gerührt. Es wird langsam auf -20°C erwärmt, unter kräftigem Rühren mit 20 ml Wasser versetzt und anschließend auf Raumtemperatur erwärmt. Die wässrige Phase wird 3x mit Diethylether extrahiert, die vereinigten organischen Phasen werden über Natriumsulfat Natriumcarbonat getrocknet und im
Vakuum vom Lösungsmittel befreit. Durch Destillation des Rückstandes im Ölpumpenvakuum erhält man 2,54 g (51 %) des tert-Butyl-3-(4-formylphenyl)-2,2- dimethylpropionates.
1H-NMR (300 MHz, CDC13): δ = 1.16 (s, 6H); 1.42 (s, 9H); 2.90 (s, 2H); 7.32 (d, 2H); 7.78 (d, 2H); 9.98 (s, 1H).
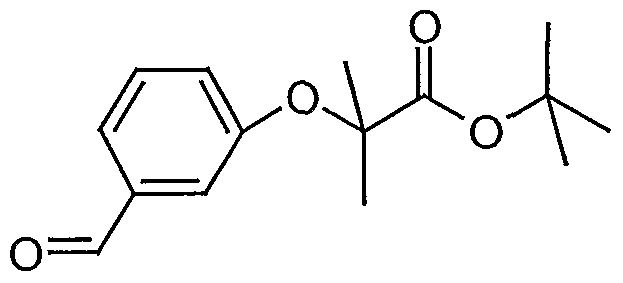
Beispiel 1-4 tert-Butyl-2-(4-formylphenoxy)-2-methylpropionat
Eine Lösung von 24,4 g (200 mmol) 4-Hydroxybenzaldehyd in 100 ml Dimethylformamid wird mit 97,75 g (300 mmol) Cäsiumcarbonat versetzt und 1 h bei 90°C gerührt. Anschließend wird eine Lösung von 66,93 g (300 mmol) 2-Brom- isobuttersäure-tert-butylester in 100 ml Dimethylformamid zugetropft und das Gemisch über Nacht bei 90°C gerührt. Nach Abdestillieren des Dimethylformamids im Vakuum wird der Rückstand in Ethylacetat aufgenommen, 2x mit Wasser, 2x mit 1 N Natronlauge und lx mit ges. NaCl-Lsg. gewaschen, über Natriumsulfat getrocknet und im Vakuum vom Lösungsmittel befreit. Es werden 16,6 g (31 %) des tert-Butyl-2-(4-formylphenoxy)-2-methylpropionates gewonnen. 1H-NMR (200 MHz, CDC13): δ = 1.40 (s, 9H); 1.63 (s, 6H); 6.90 (d, 2H); 7.78 (d, 2H); 9.88 (s, 1H).
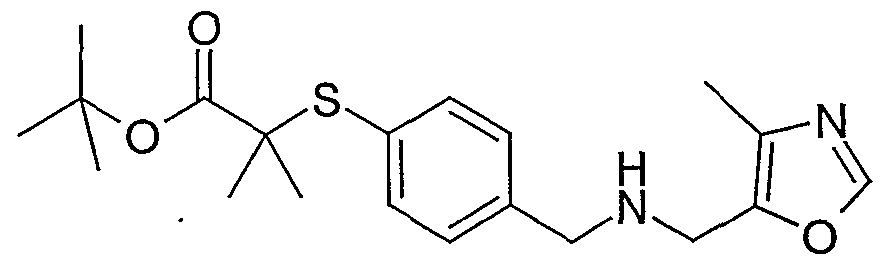
Beispiel 1-5 tert-Butyl-3-(4-{[(2-furylmethyl)amino]methyl}phenyl)-2,2-dimethylpropionat
Eine Lösung von 1,00 g (3,81 mmol) tert-Butyl-3-(4-formylphenyl)-2,2-dimethyl- propionat (Beispiel 1-3) und 0,37 g (3,81 mmol) Furfurylamin in 10 ml Dichlorethan wird bei Raumtemperatur 30 min gerührt, mit 1,21 g (5,72 mmol) Natriumtriacetoxyborhydrid versetzt und dann 22 h bei Raumtemperatur gerührt. An- schließend werden 6 ml ges. NaHCO
3-Lsg. und 10 ml Ethylacetat zugegeben, die
Phasen werden getrennt, die wässrige Phase wird 2x mit Ethylacetat extrahiert und die vereinigten organischen Phasen werden über Natriumsulfat getrocknet. Nach Entfernen des Lösungsmittels im Vakuum ergibt die chromatographische Reinigung an Kieselgel (Cyclohexan -> Cyclohexan/Ethylacetat 10:1 -> 2:1) 720 mg (55 %) des tert-Butyl-3-(4- { [(2-furylmethyl)amino]methyl}phenyl)-2,2-dimethylpropionates.
1H-NMR (300 MHz, CDC13): δ = 1.11 (s, 6H); 1.42 (s, 9H); 1.62 (breites s, 1H); 2.70 (s, 2H); 3.76 (s, 2H); 3.80 (s, 2H); 6.18 (d, 1H); 6.32 (dd, 1H); 7.10 (d, 2H); 7.20 (d, 2H); 7.35 (d, 1H).
Beispiel 1-6 tert-Butyl-3-[4-(anilinomethyl)phenyl]-2,2-dimethylpropionat
Analog zur Vorschrift des Beispiels 1-5 werden 200 mg (0,762 mmol) tert-Butyl-3-
(4-formylphenyl)-2,2-dimethylpropionat (Beispiel 1-3), 71 mg (0,762 mmol) Anilin und 210 mg (0,991 mmol) Natriumtriacetoxyborhydrid in 2 ml Dichlorethan zu 223 mg (86 %) des tert-Butyl-3-[4-(anilinomethyl)phenyl]-2,2-dimethylpropionates umgesetzt. 1H-NMR (400 MHz, CDC13): δ = 1.11 (s, 6H); 1.42 (s, 9H); 2.81 (s, 2H); 3.98
(breites s, 1H); 4.29 (s, 2H); 6.64 (d, 2H); 6.71 (t, 1H); 7.12 (d, 2H); 7.17 (t, 2H); 7.25 (d, 2H).
Beispiel 1-7 tert-Butyl-2,2-dimethyl-3-(4-{[(4-methylphenyl)amino]methyl}phenyl)propionat
Analog zur Vorschrift des Beispiels 1-5 werden 200 mg (0,762 mmol) tert-Butyl-3- (4-foraιylphenyl)-2,2-dimethylpropionat (Beispiel 1-3), 82 mg (0,762 mmol) Toluidin und 210 mg (0,991 mmol) Natriumtriacetoxyborhydrid in 2 ml Dichlorethan zu 206 mg (76 %) des tert-Butyl-2,2-dimethyl-3-(4-{[(4-methylphenyl)- amino]methyl} -phenyl)propionats umgesetzt.
1H-NMR (400 MHz, CDC13): δ = 1.11 (s, 6H); 1.42 (s, 9H); 2.23 (s, 3H); 2.81 (s, 2H); 3.87 (breites s, IH); 4.27 (s, 2H); 6.57 (d, 2H); 6.98 (d, 2H); 7.12 (d, 2H); 7.25 (d, 2H).
Beispiel 1-8
Methyl-2- { [4-(2-tert-butoxy- 1 , 1 -dimethyl-2-oxoethoxy)benzyl] amino }butyrat
Analog zur Vorschrift des Beispiels 1-5 werden 1,20 g (4,54 mmol) tert-Butyl-2-(4- formylphenoxy)-2-methylpropionat (Beispiel 1-4) und 0,70 g (4,54 mmol) DL-2- Aminobuttersäuremethylester mit 0,92 g (9,08 mmol) Triethylamin und 1,44 g (6,81 mmol) Natriumtriacetoxyborhydrid bei Raumtemperatur in 10 ml Dichlorethan
umgesetzt. Nach weiterer Zugabe von 0,9 g (4,25 mmol) Natriumtriacetoxyborhydrid und 0,35 g (2,27 mmol) DL-2-Aminobuttersäuremethylester und Erhitzen auf 40°C für 3 h werden 1,47 g (89 %) des Methyl-2-{[4-(2-tert-butoxy-lJ-dimethyl-2-oxo- ethoxy)b enzy 1] amino } butyrates gewonnen. 1H-NMR (300 MHz, DMSO): δ = 0.84 (t, 3H); 1.38 (s, 9H); 1.47 (s, 6H); 1.57 (dt,
2H); 2.29 (breites s, IH); 3.08 (t, IH); 3.47 (d, IH); 3.62 (s, 3H); 3.65 (d, IH); 6J3 (d, 2H); 7.18 (d, 2H).
Beispiel 1-9 tert-Butyl-3-(4-{[(2-ethoxy-2-oxoethyl)(2-furylmethyl)amino]methyl}phenyl)-2,2- dimethylpropionat
Eine Lösung von 600 mg (1,75 mmol) tert-Butyl-3-(4-{[(2-furylmethyl)amino]- methyl}phenyl)-2,2-dimethylpropionat (Beispiel 1-5), 323 mg (0,87 mmol) Tetra-n- butylammoniumiodid und 265 mg (2,62 mmol) Triethylamin in 10 ml THF wird mit 438 mg (2,62 mmol) Bromessigsäureethylester versetzt und über Nacht unter Rück- fluss erhitzt. Nach Abkühlen wird das Gemisch im Vakuum eingeengt, mit Wasser und Ethylacetat aufgenommen, die wässrige Phase 2x mit Ethylacetat extrahiert, die vereinigten organischen Phasen mit NaCl-Lsg. gewaschen und über Natriumsulfat getrocknet. Nach Entfernen des Lösungsmittels im Vakuum ergibt die chromato- graphische Reinigung an Kieselgel (Cyclohexan -> Cyclohexan/Ethylacetat 10:1) 702 mg (94 %) des 'tert-Butyl-3-(4-{[(2-ethoxy-2-oxoethyl)(2-furylmethyl)amino]- methyl}phenyl)-2,2-dimethylpropionates.
1H-NMR (400 MHz, CDC13): δ = 1.11 (s, 6H); 1.27 (t, 3H); 1.42 (s, 9H); 2.80 (s, 2H); 3.31 (s, 2H); 3.76 (s, 2H); 3.84 (s, 2H); 4.17 (q, 2H); 6.20 (d, IH); 6.32 (dd, IH); 7.10 (d, 2H); 7.25 (d, 2H); 7.38 (d, IH).
Beispiel 1-10 tert-Butyl-3-(4-{[N-(2-ethoxy-2-oxo)ethyl-N-phenylamino]methyl}phenyl)-2,2- dimethylpropionat
Analog zur Vorschrift des Beispiels 1-9 werden aus 198 mg (0,583 mmol) tert-Butyl- 3-[4-(anilinomethyl)phenyl]-2,2-dimethylpropionat (Beispiel 1-6), 108 mg (0,292 mmol) Tefra-n-butylammoniumiodid, zweimaliger Gabe von je 89 mg (0,875 mmol) Triethylamin und dreimaliger Gabe von je 146 mg (0,875 mmol)
Bromessigsäureethylester in 2 ml Tetrahydrofuran und 2 ml Dimethylformamid 191 mg (77 %) des tert-Butyl-3-(4-{[(2-ethoxy-2-oxoethyl)(2-phenyl)amino]- methyl} phenyl)-2,2-dimethylpropionates gewonnen. 1H-ΝMR (200 MHz, CDC13): δ = 1.11 (s, 6H); 1.25 (t, 3H); 1.42 (s, 9H); 2.70 (s, 2H); 4.05 (s, 2H); 4.20 (q, 2H); 4.62 (s, 2H); 6.69 (d, 2H); 6.73 (t, IH); 7.07 - 7.25
(m, 6H).
Beispiel 1-11 tert-Butyl-3-(4-{[N-(2-ethoxy-2-oxo)ethyl-N-(4-methylphenyl)amino]methyl}- phenyl)-2,2-dimethylpropionat
Analog zur Vorschrift des Beispiels 1-9 werden aus 181 mg (0,512 mmol) tert-Butyl- 2,2-dimethyl-3-(4-{[(4-methylphenyl)amino]methyl}phenyl)propionat (Beispiel 1-7), 95 mg (0,256 mmol) Tetra-n-butylammoniumiodid, zweimaliger Gabe von je 78 mg (0,768 mmol) Triethylamin und dreimaliger Gabe von je 128 mg (0,768 mmol) Bromessigsäureethylester in 2 ml Tetrahydrofuran und 2 ml Dimethylformamid
176 mg (78 %) des tert-Butyl-3-(4-{[N-(2-ethoxy-2-oxo)ethyl-N-(4-methylphenyl)- amino]methyl}phenyl)-2,2-dimethylpropionates gewonnen.
1H-NMR (200 MHz, CDC13): 1.11 (s, 6H); 1.25 (t, 3H); 1.42 (s, 9H); 2.22 (s, 3H); 2.80 (s, 2H); 4.02 (s, 2H); 4.19 (q, 2H); 4.59 (s, 2H); 6.60 (d, 2H); 7.00 (d, 2H); 7.10 (d, 2H); 7.17 (d, 2H).
Beispiel 1-12
N-[4-(3-tert-Butoxy-2J-dimethyl-3-oxopropyl)benzyl]-N-(2-furylmethyl)glycin
Eine Lösung von 785 mg (1,83 mmol) tert-Butyl-3-(4-{[(2-ethoxy-2-oxoethyl)(2- furylmethyl)amino]methyl}phenyl)-2,2-dimethylpropionat (Beispiel 1-9) in 15 ml Ethanol wird mit 5,5 ml (5,5 mmol) 1 Ν Natronlauge versetzt und 1 h auf 80°C erhitzt. Nach Abkühlung wird das Gemisch im Vakuum eingeengt, mit wenig Wasser aufgenommen, mit 1 N Salzsäure angesäuert und 3x mit Ethylacetat extrahiert. Die vereinigten organischen Extrakte werden 2x mit ges. NaCl-Lsg. gewaschen, über Natriumsulfat getrocknet und im Vakuum vom Lösungsmittel befreit. Man erhält 728 mg (99 %) des N-[4-(3-tert-Butoxy-2,2-dimethyl-3-oxoρropyl)benzyl]-N-(2-furyl- methyl)glycins.
1H-NMR (200 MHz, DMSO): δ = 1.06 (s, 6H); 1.37 (s, 9H); 2.74 (s, 2H); 3.24 (s, 2H); 3.76 (s, 2H); 3.84 (s, 2H); 6.32 (m, IH); 6.41 (m, IH); 7.11 (d, 2H); 7.26 (d, 2H); 7.63 (d, IH); 12.20 (breites s, IH).
Beispiel 1-13
N-[4-(3-tert-Butoxy-2,2-dimethyl-3-oxopropyl)benzyl]-N-phenylglycin
Analog zur Vorschrift des Beispiels 1-12 werden aus 175 mg (0,411 mmol) tert- Butyl-3-(4-{[(2-ethoxy-2-oxoethyl)(2-phenyl)amino]methyl}phenyl)-2,2-dimethyl- propionat (Beispiel 1-10) und 1,23 ml (1,23 mmol) 1 Ν Natronlauge in 3 ml Ethanol 162 mg (99 %) des N-[4-(3-tert-Butoxy-2,2-dimethyl-3-oxopropyl)benzyl]-N- phenylglycins gewonnen.
1H-ΝMR (300 MHz, DMSO): δ = 1.04 (s, 6H); 1.36 (s, 9H); 2J3 (s, 2H); 4.12 (s, 2H); 4.56 (s, 2H); 6.56 (d, 2H); 6.61 (t, IH); 7.07 (d, 2H); 7.11 (d, 2H); 7.19 (d, IH); 12.53 (breites s, IH).
Beispiel 1-14
N-[4-(3-tert-Butoxy-2,2-dimethyl-3-oxopropyl)benzyl]-N-(4-methylphenyl)glycin
Analog zur Vorschrift des Beispiels 1-12 werden aus 153 mg (0,348 mmol) tert- Butyl-3-(4-{[N-(2-ethoxy-2-oxo)ethyl-N-(4-methylphenyl)amino]methyl}phenyl)- 2,2-dimethylpropionat (Beispiel I-ll) und 1,23 ml (1,23 mmol) 1 Ν Natronlauge in
3 ml Ethanol 141 mg (99 %) des N-[4-(3-tert-Butoxy-2,2-dimethyl-3-oxopropyl benzyl]-N-(4-methylphenyl)glycins gewonnen.
1H-ΝMR (300 MHz, DMSO): δ = 1.04 (s, 6H); 1.36 (s, 9H); 2.14 (s, 3H); 2.72 (s, 2H); 4.08 (s, 2H); 4.52 (s, 2H); 6.48 (d, 2H); 6.90 (d, 2H); 7.08 (d, 2H); 7.18 (d, 2H); 12.48 (breites s, IH).
Beispiel 1-15
2-{[4-(2-tert-Butoxy-lJ-dimethyl-2-oxoethoxy)benzyl]amino}buttersäure
Analog zur Vorschrift des Beispiels 1-12 werden aus 750 mg (2,05 mmol) Methyl-2- {[4-(2-tert-butoxy- 1 , 1 -dimethyl-2-oxoethoxy)benzyl]amino}butyrat (Beispiel 1-8) und 6,20 ml (6,20 mmol) 1 N Natronlauge in 6 ml Ethanol 640 mg (89 %) der 2-{[4- (2-tert-Butoxy-l J -dimethyl-2-oxoethoxy)benzyl]amino}buttersäure gewonnen. 1H-NMR (300 MHz, DMSO): δ = 0.91 (t, 3H); 1.40 (s, 9H); 1.51 (s, 6H); 1.84 (m, 2H); 3.25 (breites s, IH); 3.57 (t, IH); 3.99 (s, 2H); 6.81 (d, 2H); 7.38 (d, 2H).
Ausfflhrungsbeispiele 1
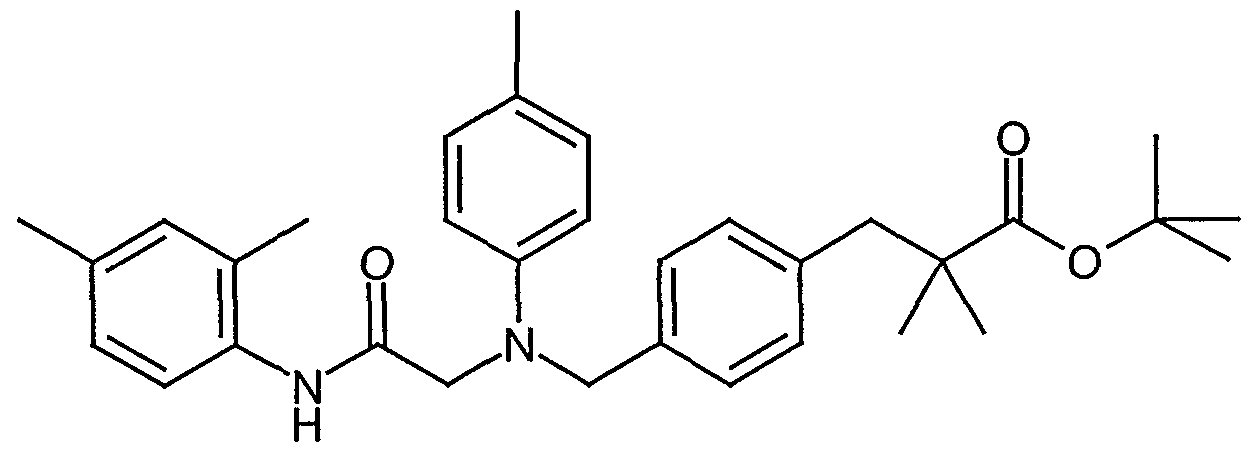
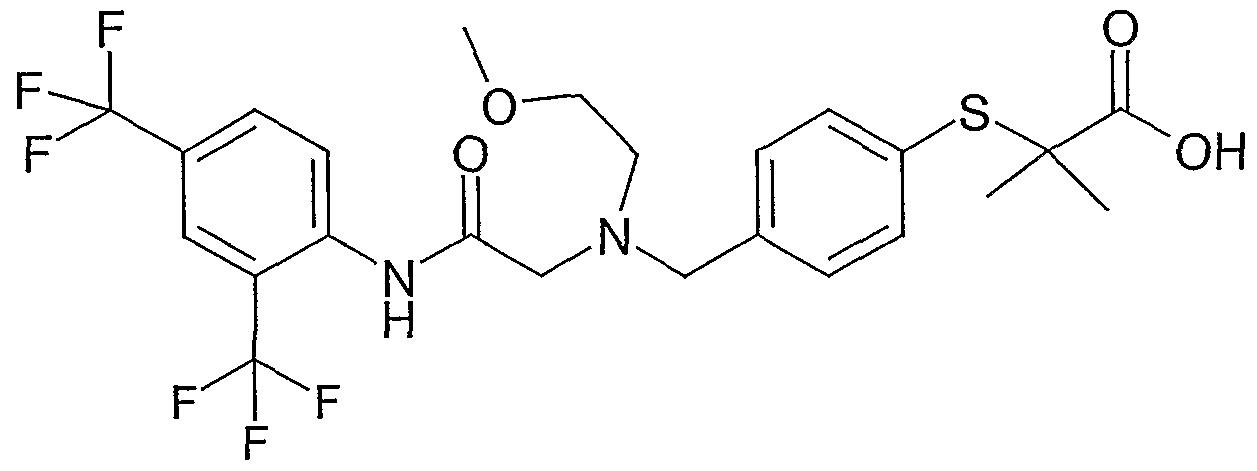
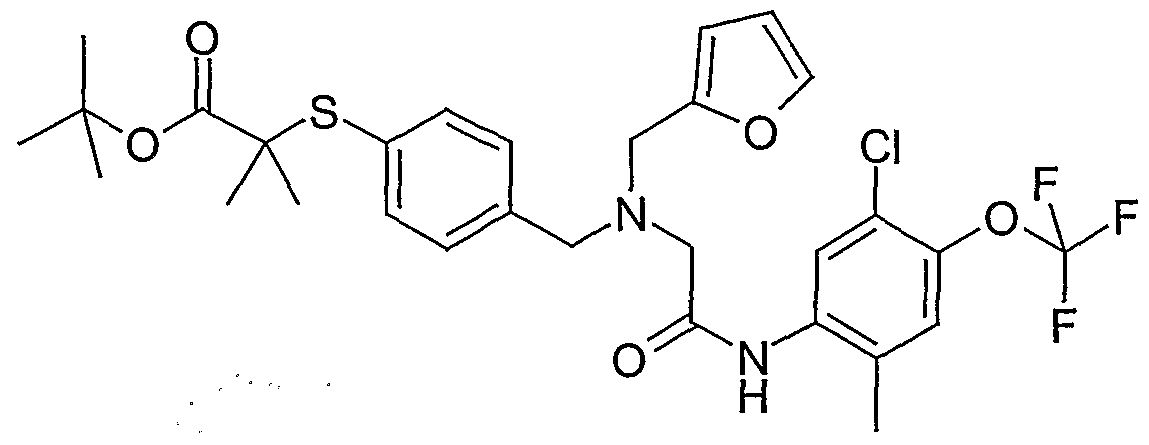
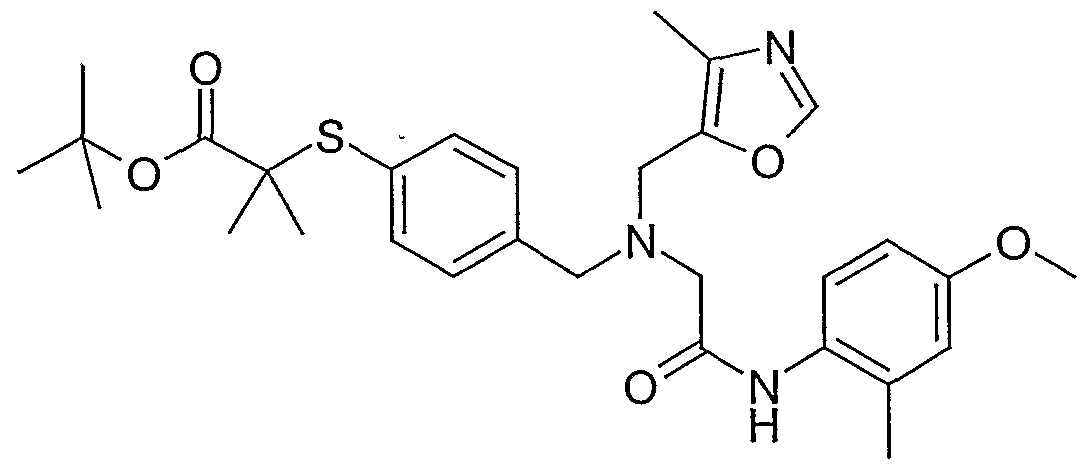
Beispiel 1-1 tert-Butyl-3-(4-{[(2-(2,4-dimethylphenyl)amino-2-oxoethyl)(2-furylmethyl)amino]- methyl}phenyl)-2,2-dimethylpropionat
Zu einer Lösung von 200 mg (0,498 mmol) N-[4-(3-tert-Butoxy-2,2-dimethyl-3- oxopropyl)benzyl]-N-(2-furylmethyl)glycin (Beispiel 1-12) und 91 mg (0,747 mmol)
2,4-Dimethylanilin in 8 ml Dimethylformamid werden bei 0°C 88 mg (0,648 mmol) 1 -Hydroxy- lH-benzotriazol, 124 mg (0,648 mmol) l-Ethyl-3-(3-dimethylamino)- propylcarbodiimid-Hydrochlorid, 151 mg (1,494 mmol) N-Methylmorpholin und 3 mg (0,025 mmol) 4-Dimethylaminopyridin zugegeben und die Lösung 1 h bei dieser Temperatur gerührt. Anschließend wird das Gemisch 9 h bei Raumtemperatur gerührt und dann mit 10 ml Wasser versetzt. Die wässrige Phase wird 2x mit Ethylacetat extrahiert, die vereinigten organischen Phasen werden mit 1 Ν Salzsäure, ges. ΝaHCO3-Lsg. und ges. NaCl-Lsg. gewaschen, über Natriumsulfat getrocknet und im Vakuum vom Lösungsmittel befreit. Die chromatographische Reinigung des Rück- Standes an Kieselgel (Cyclohexan/Ethylacetat 10: 1 -> 3 : 1) ergibt 228 mg (91 %) des tert-Butyl-3-(4-{[(2-(2,4-dimethylphenyl)amino-2-oxoethyl)(2-furylmethyl)amino]- methyl}phenyl)-2,2-dimethylpropionates.
1H-NMR (200 MHz, CDC13): δ = 1.10 (s, 6H); 1.40 (s, 9H); 2.26 (s, 3H); 2.28 (s, 3H); 2.80 (s, 2H); 3.29 (s, 2H); 3.71 (s, 2H); 3.74 (s, 2H); 6.25 (d, IH); 6.32 (dd, IH); 6.99 (m, 2H); 7.11 (d, 2H); 7.23 (d, 2H); 7.37 (d, IH); 7.84 (d, IH); 9.12
(breites s, IH).
Beispiel 1-2 tert-Butyl-3-(4-{[(2-(4-methoxy-2,5-dimethylphenyl)amino-2-oxoethyl)(2-furyl- methyl)amino]methyl}ρhenyl)-2,2-dimethylpropionat
Analog zur Vorschrift des Beispiels 1-1 werden 200 mg (0,498 mmol) N-[4-(3-tert- Butoxy-2,2-dimethyl-3-oxopropyl)benzyl]-N-(2-furylmethyl)glycin (Beispiel 1-12), 113 mg (0,747 mmol) 4-Methoxy-2,5-dimethylanilin, 88 mg (0,648 mmol) 1- Hydroxy- lH-benzotriazol, 124 mg (0,648 mmol) l-Ethyl-3-(3-dimethylamino)- propylcarbodiimid-Hydrochlorid, 151 mg (1,494 mmol) N-Methylmorpholin und 3 mg (0,025 mmol) 4-Dimethylaminopyridin in 8 ml Dimethylformamid zu 241 mg (90 %) des tert-Butyl-3-(4-{[(2-(4-methoxy-2,5-dimethylphenyl)amino-2-oxoethyl)- (2-fiιrylmethyl)amino]methyl}phenyl)-2,2-dimethylpropionates umgesetzt. 1H-ΝMR (200 MHz, DMSO): δ = 1.05 (s, 6H); 1.35 (s, 9H); 2.08 (s, 3H); 2.14 (s,
3H); 2.75 (s, 2H); 3.18 (s, 2H); 3.69 (s, 2H); 3.74 (s, 3H); 3.76 (s, 2H); 6.35 (d, IH); 6.41 (dd, IH); 6.75 (s, IH); 7.11 (d, 2H); 7.28 (d, 2H); 7.31 (s, IH); 7.61 (d, IH); 9.02 (breites s, IH).
Beispiel 1-3 tert-Butyl-3-(4-{[N-(2-(2,4-dimethylphenyl)amino-2-oxo)ethyl-N-phenylamino]- methyl}phenyl)-2,2-dimethylpropionat
Analog zur Vorschrift des Beispiels 1-1 werden 65 mg (0,164 mmol) N-[4-(3-tert- Butoxy-2,2-dimethyl-3-oxopropyl)benzyl]-N-phenylglycin (Beispiel 1-13), 30 mg (0,245 mmol) 2,4-Dimethylanilin, 29 mg (0,213 mmol) 1-Hydroxy-lH-benzotriazol, 41 mg (0,213 mmol) l-Ethyl-3-(3-dimethylamino)propylcarbodiimid-Hydrochlorid, 50 mg (0,491 mmol) N-Methylmorpholin und 0,2 mg (0,002 mmol) 4-Dimethyl- aminopyridin in 2 ml Dimethylformamid zu 65 mg (79 %) des tert-Butyl-3-(4-{[N- (2-(2,4-dimethylphenyl)amino-2-oxo)ethyl-N-phenylamino]methyl}phenyl)-2,2- dimethylpropionates umgesetzt.
1H-ΝMR (200 MHz, CDC13): δ = 1.10 (s, 6H); 1.41 (s, 9H); 1.90 (s, 3H); 2.26 (s, 3H); 2.79 (s, 2H); 4.09 (s, 2H); 4.66 (s, 2H); 6.80 - 6.95 (m, 4H); 6.98 (d, IH); 7.12 (s, 4H); 7.27 (m, 2H); 7.67 (d, IH); 8.11 breites s, IH).
Beispiel 1-4 tert-Butyl-3-(4- {[N-(2-(4-methoxy-2,5-dimethylphenyl)amino-2-oxo)ethyl-N- phenylamino]methyl}phenyl)-2,2-dimethylpropionat
Analog zur Vorschrift des Beispiels 1-1 werden 65 mg (0,164 mmol) N-[4-(3-tert-
Butoxy-2,2-dimethyl-3-oxopropyl)benzyl]-N-phenylglycin (Beispiel 1-13), 37 mg (0,245 mmol) 4-Methoxy-2,5-dimethylanilin, 29 mg (0,213 mmol) 1-Hydroxy-lH- benzotriazol, 41 mg (0,213 mmol) l-Ethyl-3-(3-dimethylamino)propylcarbodiimid- Hydrochlorid, 50 mg (0,491 mmol) N-Methylmorpholin und 0,2 mg (0,002 mmol) 4- Dimethylaminopyridin in 2 ml Dimethylforamid zu 78 mg (90 %) des tert-Butyl-3-
(4-{[N-(2-(4-methoxy-2,5-dimemylphenyl)amino-2-oxo)ethyl-N-phenylamino]- methyl} phenyl)-2,2-dimethylpropionates umgesetzt.
1H-NMR (200 MHz, CDC13): δ = 1.11 (s, 6H); 1.42 (s, 9H); 1.96 (s, 3H); 2.16 (s, 3H); 2.80 (s, 2H); 3.77 (s, 3H); 4.09 (s, 2H); 4.67 (s, 2H); 6.57 (s, IH); 6.83 (dd, IH); 6.89 (d, 2H); 7.13 (s, 4H); 7.24 (d, 2H); 7.34 (m, IH); 7.94 (breites s, IH).
Beispiel 1-5 tert-Butyl-3-(4-{[N-(2-(2,4-dimethylphenyl)amino-2-oxo)ethyl-N-(4-methylphenyl)- amino]methyl } phenyl)-2,2-dimethylpropionat
Analog zur Vorschrift des Beispiels 1-1 werden 50 mg (0,121 mmol) N-[4-(3-tert- Butoxy-2,2-dimethyl-3-oxopropyl)benzyl]-N-(4-methylphenyl)glycin (Beispiel I- 14), 22 mg (0,182 mmol) 2,4-Dimethylanilin, 21 mg (0,158 mmol) 1-Hydroxy-lH- benzotriazol, 30 mg (0,158 mmol) l-Ethyl-3-(3-dimethylamino)propylcarbodiimid- Hydrochlorid, 37 mg (0,364 mmol) N-Methylmorpholin und 0,1 mg (0,001 mmol) 4- Dimethylaminopyridin in 2 ml Dimethylformamid zu 40 mg (64 %) des tert-Butyl-3- (4-{[N-(2-(2,4-dimethylphenyl)amino-2-oxo)ethyl-N-(4-methylphenyl)amino]- methyl}phenyl)-2,2-dimethylpropionates umgesetzt.
1H-ΝMR (300 MHz, CDC13): δ = 1.10 (s, 6H); 1.40 (s, 9H); 1.92 (s, 3H); 2.27 (s, 6H); 2.79 (s, 2H); 4.02 (s, 2H); 4.58 (s, 2H); 6.80 (d, 2H); 6.91 (s, IH); 6.98 (d, IH); 7.06 (d, 2H); 7.11 (d, 2H); 7.13 (d, 2H); 7.67 (d, IH); 8.18 (breites s, IH).
Beispiel 1-6 tert-Butyl-3-(4-{[N-(2-(4-methoxy-2,5-dimethylphenyl)amino-2-oxo)ethyl-N-(4- methylphenyl)amino]methyl}phenyl)-2,2-dimethylpropionat
Analog zur Vorschrift des Beispiels 1-1 werden 50 mg (0,121 mmol) N-[4-(3-tert- Butoxy-2,2-dimethyl-3-oxopropyl)benzyl]-N-(4-methylphenyl)glycin (Beispiel 1-14), 28 mg (0,182 mmol) 4-Methoxy-2,5-dimethylanilin, 21 mg (0,158 mmol) 1- Hydroxy-lH-benzόtriazol, 30 mg (0,158 mmol) l-Ethyl-3-(3-dimethylamino)propyl- carbodiimid-Hydrochlorid, 37 mg (0,364 mmol) N-Methylmorpholin und 0,1 mg (0,001 mmol) 4-Dimethylaminopyridin in 2 ml Dimethylformamid zu 58 mg (88 %) des tert-Butyl-3-(4-{[N-(2-(4-methoxy-2,5-dimethylphenyl)amino-2-oxo)ethyl-N-(4- methylphenyl)amino]methyl}phenyl)-2,2-dimethylpropionates umgesetzt. 1H-ΝMR (300 MHz, CDC13): δ = 1.10 (s, 6H); 1.41 (s, 9H); 1.96 (s, 3H); 2.15 (s, 3H); 2.26 (s, 3H); 2.79 (s, 2H); 3.11 (s, 3H); 4.02 (s, 2H); 4.60 (s, 2H); 6.57 (s, IH); 6.80 (d, 2H); 7.07 (d, 2H); 7.10 (d, 2H); 7.13 (d, 2H); 7.37 (s, IH); 8.01 (breites s, IH).
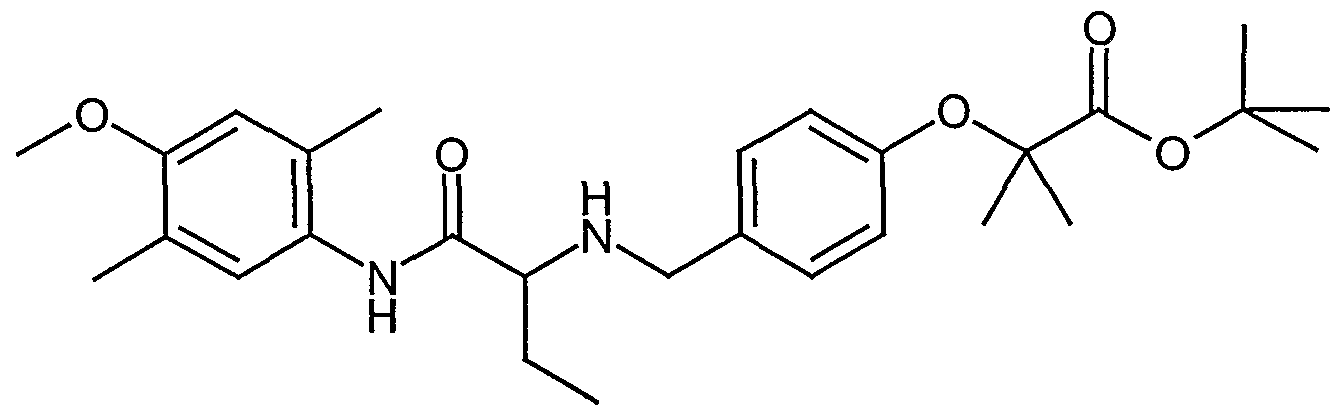
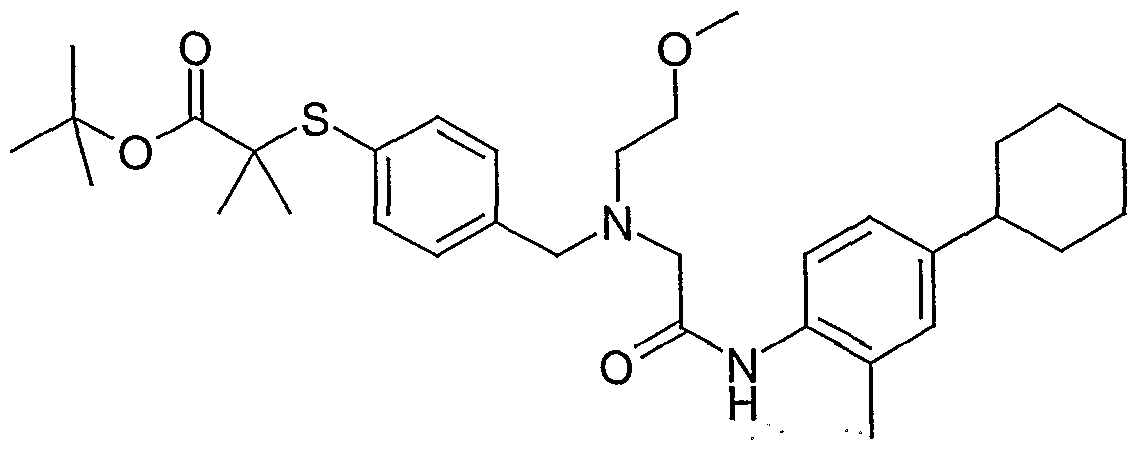
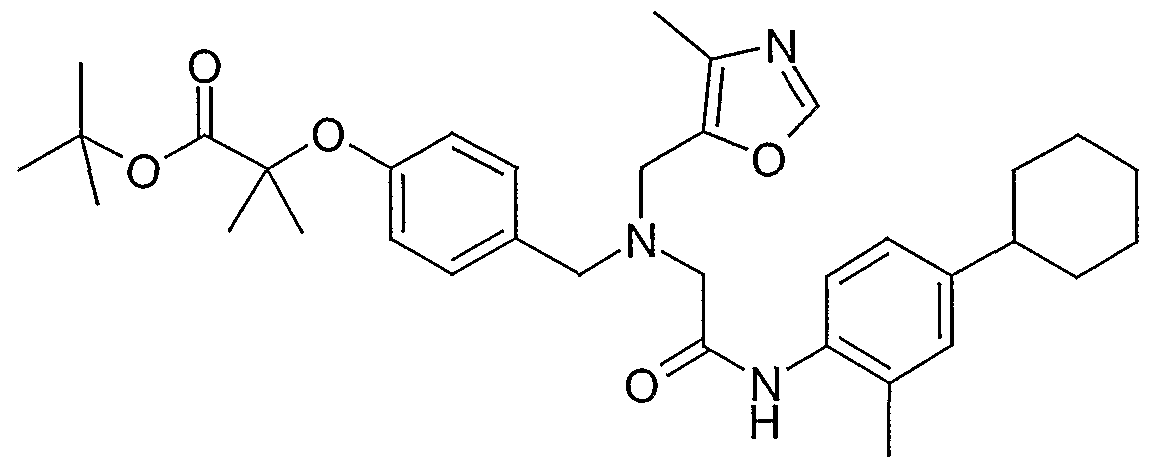
Beispiel 1-7 tert-Butyl-2-(4-{[(l-{[(2,4-dimethylphenyl)amino]carbonyl}propyl)-amino]methyl}- phenoxy)-2-methylpropionat
Analog zur Vorschrift des Beispiels 1-1 werden 320 mg (0,90 mmol) 2-{[4-(2-tert- Butoxy-lJ-dimethyl-2-oxoethoxy)benzyl]amino}buttersäure (Beispiel 1-15), 160 mg (1,36 mmol) 2,4-Dimethylanilin, 160 mg (1,18 mmol) 1-Hydroxy-lH-benzotriazol, 230 mg (1,18 mmol) l-Ethyl-3-(3-dimethylamino)propylcarbodiimid-Hydrochlorid, 270 mg (2,71 mmol) N-Methylmorpholin und 1 mg (0,01 mmol) 4-Dimethylamino- pyridin in 5 ml Dimethylformamid zu 190 mg (46 %) des tert-Butyl-2-(4-{[(l-{[(2,4- dimethylphenyl)amino]carbonyl}propyl)amino]methyl}phenoxy)-2-methylpropiona- tes umgesetzt.
1H-ΝMR (200 MHz, CDC13): δ = 0.99 (t, 3H); 1.43 (s, 9H); 1.56 (s, 6H); 1.74 (m, 2H); 2.21 (s, 3H); 2.28 (s, 3H); 3.22 (dd, IH); 3.69 (d, IH); 3.82 (d, IH); 6.83 (d,
2H); 6.98 (s, IH); 7.02 (d, IH); 7.18 (d, 2H); 7.93 (d, IH); 9.32 (breites s, IH).
Beispiel 1-8 tert-Butyl-2-(4- { [( 1 - { [(4-methoxy-2,5-dimethylphenyl)amino]carbonyl}propyl)- amino]methyl} phenoxy)-2-methylpropionat
Analog zur Vorschrift des Beispiels 1-1 werden 320 mg (0,90 mmol) 2-{[4-(2-tert- Butoxy-l,l-dimethyl-2-oxoethoxy)benzyl]amino}buttersäure (Beispiel 1-15), 210 mg
(1,36 mmol) 4-Methoxy-2,5-dimethylanilin, 160 mg (1,18 mmol) 1-Hydroxy-lH- benzotriazol, 230 mg (1,18 mmol) l-Ethyl-3-(3-dimeιhylamino)propylcarbodiimid- Hydrochlorid, 270 mg (2,71 mmol) N-Methylmorpholin und 1 mg (0,01 mmol) 4- Dimethylaminopyridin in 5 ml Dimethylformamid zu 130 mg (30 %) des tert-Butyl- 2-(4- { [(1 - { [(4-methoxy-2,5-dimethylphenyl)amino]carbonyl}propyl)amino]methyl} - phenoxy)-2-methylpropionates umgesetzt.
1H-NMR (200 MHz, CDC13): δ = 0.99 (t, 3H); 1.44 (s, 9H); 1.56 (s, 6H); 1.74 (m, 2H); 2.19 (s, 3H); 2.22 (s, 3H); 3.22 (dd, IH); 3.71 (d, IH); 3.80 (s, 3H); 3.82 (d, IH); 6.64 (s, IH); 6.83 (d, 2H); 7.19 (d, 2H); 7.65 (s, IH); 9.13 (breites s, IH).
Beispiel 1-9
3-(4-{[(2-(2,4-Dimethylphenyl)amino-2-oxoethyl)(2-furylmethyl)amino]methyl}- phenyl)-2,2-dimethylpropionsäure
Eine Lösung von 192 mg (0,380 mmol) tert-Butyl-3-(4-{[(2-(2,4-dimethylρhenyl)- amino-2-oxoethyl)(2-furylmethyl)amino]methyl}phenyl)-2,2-dimethylpropionat (Beispiel 1-1) in 1 ml Dichlormethan wird mit 1 ml Trifluoressigsäure versetzt und 2 h bei Raumtemperatur gerührt. Anschließend wird das Gemisch im Vakuum ein- geengt, mit Ethylacetat aufgenommen, die organische Phase wird 2x mit Wasser, lx mit 20%iger Natriumacetat-Lsg., lx mit Wasser und lx mit ges. NaCl-Lsg. gewaschen, über Natriumsulfat getrocknet und im Vakuum vom Lösungsmittel befreit. Die chromatographische Reinigung des Rückstandes an Kieselgel (Dichlormethan -> Dichlormethan/Methanol 20:1) ergibt 150 mg (88 %) der 3-(4-{[(2-(2,4-Dimethyl- phenyl)amino-2-oxoethyl)(2-furylmethyl)amino]methyl}-phenyl)-2,2-dimethyl- propionsäure.
1H-NMR (200 MHz, CDC13): δ = 1.16 (s, 6H); 2.26 (s, 3H); 2.28 (s, 3H); 2.87 (s, 2H); 3.30 (s, 2H); 3.71 (s, 2H); 3.74 (s, 2H); 6.26 (d, IH); 6.32 (dd, IH); 6.99 (m, 2H); 7.12 (d, 2H); 7.24 (d, 2H); 7.37 (d, IH); 7.83 (d, IH); 9.12 (breites s, IH).
Beispiel 1-10
3-(4-{[(2-(4-Methoxy-2,5-dimethylphenyl)amino-2-oxoethyl)(2-furylmethyl)- amino]methyl}phenyl)-2,2-dimethylpropionsäure
Analog zur Vorschrift des Beispiels 1-9 werden 170 mg (0,318 mmol) tert-Butyl-3-
(4-{[(2-(4-methoxy-2,5-dimethylphenyl)amino-2-oxoethyl)(2-furylmethyl)amino]- methyl}phenyl)-2,2-dimethylpropionat (Beispiel 1-2) mit 1 ml Trifluoressigsäure in
1 ml Dichlormethan zu 133 mg (87 %) der 3-(4-{[(2-(4-Methoxy-2,5-dimethyl- phenyl)amino-2-oxoethyl)(2----urylmethyl)amino]methyl}phenyl)-2,2-dimethyl- propionsäure umgesetzt.
1H-NMR (200 MHz, DMSO): δ = 1.04 (s, 6H); 2.07 (s, 3H); 2.13 (s, 3H); 2.76 (s, 2H); 3.18 (s, 2H); 3.70 (s, 2H); 3.74 (s, 3H); 3.76 (s, 2H); 6.39 (d, 2H); 6.87 (s, IH);
7.12 (d, 2H); 7.28 (d, 2H); 7.30 (s, IH); 7.61 (s, IH); 9.02 (breites s, IH); 12.18
(breites s, IH).
Beispiel 1-11 3-(4-{[N-(2-(2,4-Dimethylphenyl)amino-2-oxo)ethyl-N-phenylamino]methyl}- phenyl)-2,2-dimethylpropionsäure
Analog zur Vorschrift des Beispiels 1-9 werden 48 mg (0,096 mmol) tert-Butyl-3-(4- {[N-(2-(2,4-dimethylphenyl)amino-2-oxo)ethyl-N-phenylamino]methyl}phenyl)-2,2- dimethylpropionat (Beispiel 1-3) mit 1 ml Trifluoressigsäure in 2 ml Dichlormethan zu 36 mg (85 %) der 3-(4-{[N-(2-(2,4-Dimethylphenyl)amino-2-oxo)ethyl-N-phenyl- amino]methyl}phenyl)-2,2-dimethylpropionsäure umgesetzt.
1H-ΝMR (200 MHz, CDC13): δ = 1.19 (s, 6H); 1.90 (s, 3H); 2.26 (s, 3H); 2.87 (s, 2H); 4.08 (s, 2H); 4.66 (s, 2H); 6.80 - 6.95 (m, 4H); 6.98 (d, IH); 7.14 (s, 4H); 7.27 (m, 2H); 7.67 (d, IH); 8.08 (breites s, IH).
Beispiel 1-12
3-(4-{[N-(2-(4-Methoxy-2,5-dimethylphenyl)amino-2-oxo)ethyl-N-phenylamino]- methyl}phenyl)-2,2-dimethylpropionsäure
Analog zur Vorschrift des Beispiel 1-9 werden 61 mg (0,115 mmol) tert-Butyl-3-(4- {[N-(2-(4-methoxy-2,5-dimethylphenyl)amino-2-oxo)ethyl-N-phenylamino]methyl}- phenyl)-2,2-dimethylpropionat (Beispiel 1-4) mit 1 ml Trifluoressigsäure in 2 ml Dichlormethan zu 46 mg (85 %) der 3-(4-{[N-(2-(4-Methoxy-2,5-Dimethylρhenyl)- amino-2-oxo)ethyl-N-phenylamino]methyl}phenyl)-2,2-dimethylpropionsäure umgesetzt.
1H-ΝMR (200 MHz, CDC13): δ - 1.19 (s, 6H); 1.94 (s, 3H); 2.15 (s, 3H); 2.86 (s, 2H); 3.77 (s, 3H); 4.08 (s, 2H); 4.66 (s, 2H); 6.56 (s, IH); 6.83 (dd, IH); 6.88 (d, 2H); 7.13 (s, 4H); 7.24 (d, 2H); 7.34 (m, IH); 7.93 (breites s, IH).
Beispiel 1-13
3-(4-{[N-(2-(2,4-Dimethylphenyl)amino-2-oxo)ethyl-N-(4-methylphenyl)amino]- methyl}phenyl)-2J-dimethylpropionsäure
Analog zur Vorschrift des Beispiels 1-9 werden 23 mg (0,049 mmol) tert-Butyl-3-(4- {[N-(2-(2,4-dimethylphenyl)amino-2-oxo)ethyl-N-(4-methylphenyl)amino]methyl}- phenyl)-2,2-dimethylpropionat (Beispiel 1-5) mit 1 ml Trifluoressigsäure in 2 ml Di- chlormethan zu 20 mg (91 %) der 3-(4-{[N-(2-(2,4-Dimethylphenyl)amino-2-oxo)- ethyl-N-(4-methylphenyl)amino]methyl}phenyl)-2,2-dimethylpropionsäure umgesetzt.
1H-ΝMR (200 MHz, CDC13): δ = 1.17 (s, 6H); 1.92 (s, 3H); 2.25 (s, 6H); 2.86 (s, 2H); 4.02 (s, 2H); 4.60 (s, 2H); 6.79 (d, 2H); 6.91 (s, IH); 6.98 (d, IH); 7.06 (d, 2H); 7.13 (s, 2H); 7.17 (d, 2H); 7.68 (d, IH); 8.19 (breites s, IH).
Beispiel 1-14
3-(4-{[N-(2-(4-Methoxy-2,5-dimethylphenyl)amino-2-oxo)ethyl-N-(4-methyl- phenyl)amino]methyl}phenyl)-2,2-dimethylpropionsäure
Analog zur Vorschrift des Beispiels 1-9 werden 40 mg (0,073 mmol) tert-Butyl-3-(4- {[N-(2-(4-methoxy-2,5-dimethylphenyl)amino-2-oxo)ethyl-N-(4-methylphenyl)- amino]methyl}phenyl)-2,2-dimethylpropionat (Beispiel 1-6) mit 1 ml Trifluoressigsäure in 2 ml Dichlormethan zu 33 mg (93 %) der 3-(4-{[N-(2-(4-Methoxy-2,5- Dimethylphenyl)amino-2-oxo)ethyl-N-(4-methylphenyl)amino]methyl}phenyl)-2,2- dimethylpropionsäure umgesetzt.
1H-ΝMR (200 MHz, CDC13): δ = 1.18 (s, 6H); 1.96 (s, 3H); 2.15 (s, 3H); 2.26 (s, 3H); 2.86 (s, 2H); 3.76 (s, 3H); 4.03 (s, 2H); 4.61 (s, 2H); 6.57 (s, IH); 6.80 (dd, 2H); 7.07 (d, 2H); 7.14 (s, 4H); 7.36 (s, IH); 8.02 (breites s, IH).
Beispiel 1-15
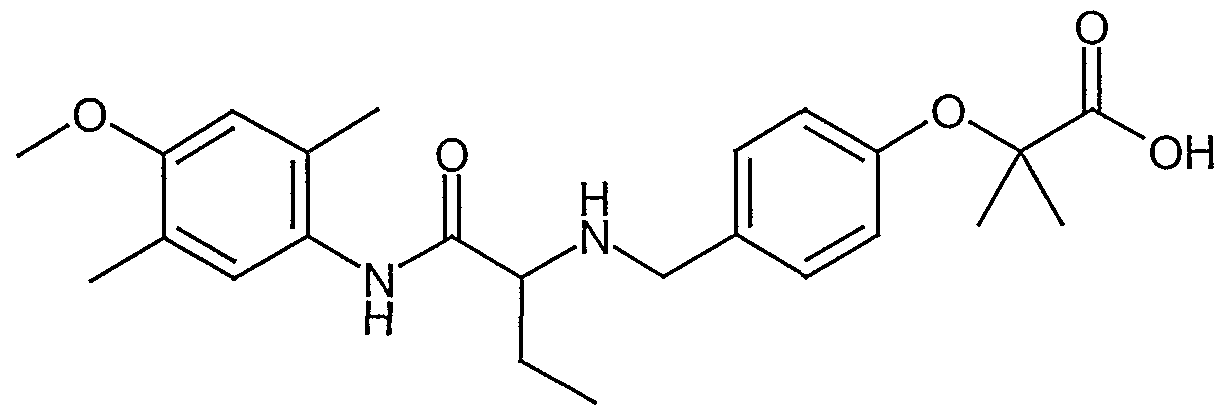
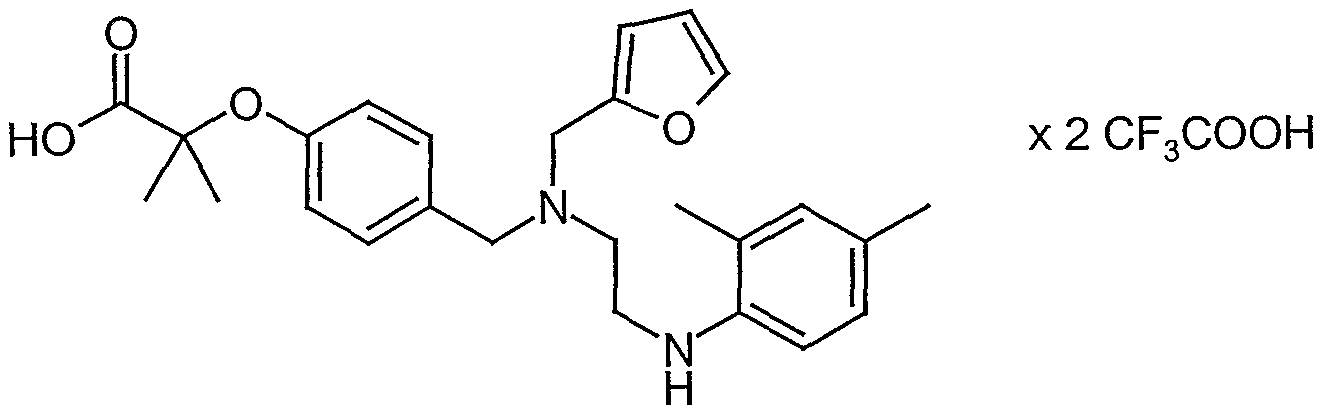
2-(4- {[(1 - {[(2,4-Dimethylphenyl)amino]carbonyl}propyl)amino]methyl}phenoxy)- 2-methylpropionsäure
Analog vor Vorschrift des Beispiels 1-9 werden 170 mg (0,374 mmol) tert-Butyl-2- (4-{[(l-{[(2,4-dimethylphenyl)amino]carbonyl}propyl)amino]methyl}phenoxy)-2- methylpropionat (Beispiel 1-7) mit 0,72 ml (9,35 mmol) Trifluoressigsäure in 3 ml Dichlormethan zu 113 mg (72 %) der 2-(4-{[(l-{[(2,4-Dimethylρhenyl)amino]- carbonyl}propyl)amino]methyl}phenoxy)-2-methylpropionsäure umgesetzt. 1H-NMR (300 MHz, CDC13): δ = 1.01 (t, 3H); 1.53 (d, 6H); 1.95 (m, 2H); 2.10 (s, 3H); 2.23 (s, 3H); 3.67 (breites s, IH); 4.02 (m, IH); 4.55 (m, IH); 6.61 (d, 2H); 6.82 (d, IH); 6.89 (s, IH); 7.10 (d, 2H); 7.11 (s, IH); 9.53 (breites s, IH).
Beispiel 1-16
2-(4-{[(l-{[(4-Methoxy-2,5-dimethylphenyl)amino]carbonyl}propyl)amino]- methyl}phenoxy)-2-methylpropionsäure
Analog zur Vorschrift des Beispiels 1-9 werden 115 mg (0,237 mmol) tert-Butyl-2- (4-{[(l-{[(4-methoxy-2,5-dimethylphenyl)amino]carbonyl}propyl)amino]-methyl}- phenoxy)-2-methylpropionat (Beispiel 1-8) mit 0,46 ml (5,93 mmol) Trifluoressig- säure in 3 ml Dichlormethan zu 100 mg (93 %) der 2-(4-{[(l-{[(4-Methoxy-2,5- dimethylphenyl)amino]carbonyl}propyl)amino]methyl}phenoxy)-2-methyl- propionsäure umgesetzt.
1H-NMR (300 MHz, CDC13): δ = 1.05 (t, 3H); 1.55 (d, 6H); 1.97 (m, 2H); 2.10 (s, 6H); 3.75 (s, 3H); 3.78 (m, IH); 4.08 (m, 2H); 4.50 (m, 2H); 6.50 (s, IH); 6.64 (d, 2H); 6.94 (s, IH); 7.14 (d, 2H); 7.65 (s, IH); 9.38 (breites s, IH).
Ausgangsverbindungen II
Beispiel IM
2-[(4-Bromphenyl)thio]-2-methyl-propansäure-l,l-dimethylethylester
4-Bromthiophenol (100 g) und t-Butyl-2-bromisobutyrat (118 g) werden in 1 1 Ethanol gelöst und mit 29 g KOH versetzt. Man rührt 2 h bei Rückfluss, kühlt ab und filtriert von KBr ab. Das Filtrat wird eingeengt und aus n-Hexan umkristallisiert.
Man erhält 93,6 g farblosen Feststoff. 1H-NMR (200 MHz, CDC13): 1.48 (s, 15H); 7.38 (m, 4H).
Beispiel II-2
2-[(4-Formylphenyl)thio]-2-methyl-propansäure-l,l-dimethylethylester
1,0 g 2-[(4-Bromphenyl)thio]-2-methyl-propansäure-l,l-dimethylethylester werden in 20 ml THF gelöst und mit 189 ml (3,02 mmol, 1 eq) n-Butyllithium-Lsg. in Hexan versetzt. Direkt danach wird mit 0,46 ml Dimethylformamid versetzt und auf Raumtemperatur erwärmt und 1 h nachgerührt. Die Reaktion wird durch Zugabe von 1 ml 1 N HCl abgebrochen, eingeengt und in Ethylacetat aufgenommen. Man schüttelt mit ges. NaHCO3-Lsg. sowie mit NaCl-Lsg. aus und trocknet (MgSO4). Die chromatographische Reinigung (Dichlormethan) ergibt 550 mg hellgelbes Öl. LC-MS: Acetonitril/30% wässr. HCl/Wasser (Gradient): Rt = 4.86 min ([M+H]+ - 281).
Beispiel II-3
2-[[4-[[(2-Furanylmethyl)amino]methyl]phenyl]thio]-2-methyl-propansäure- 1,1- dimethylethylester
550 mg 2-[(4-Formylphenyl)thio]-2-methyl-propansäure-l,l-dimethylethylester wer- den mit 381 mg Furfurylamin in 100 ml Methanol vorgelegt und mit 1 ml Eisessig versetzt. Man rührt 15 min bei Raumtemperatur, kocht kurz auf und versetzt dann bei 0°C portionsweise mit 493 mg Natriumcyanoborhydrid. Nach Rühren über Nacht bei Raumtemperatur versetzt man mit 1 N HCl und lässt 30 min rühren. Dann wird mit Na2CO -Lsg. basisch gestellt und 2x mit Ethylacetat extrahiert. Die org. Phase wird gewaschen (ges. NaCl-Lsg.) und getrocknet (MgSO4). Einengen und chromato- graphische Reinigung (Dichlormethan/Ethylacetat 10+1) ergibt 430 mg eines farblosen Öls.
1H-NMR (300 MHz, CDC13): 1.42 (s, 15H); 3J9 (s, 2H); 3.80 (s, 2H); 6.15 (m, IH); 6.28 (m, IH); 7.25-7.45 (m, 5H).
Beispiel II-4
2-[[4-[2-[(2-Ethoxy-2-oxoethyl)(2-füranylmethyl)amino]methyl]phenyl]thio]-2- methyl-propansäure- 1 , 1 -dimethylethylester
5,4 g 2-[[4-[[(2-Furanylmethyl)amino]methyl]phenyl]thio]-2-methyl-propansäure-
1,1 -dimethylethylester werden in 270 ml Tetrahydrofuran gelöst und mit 2,27 g Triethylamin sowie 3,74 g Bromessigsäureethylester und 14,85 g Tetra-n-butyl- ammoniumiodid versetzt. Man rührt 48 h bei 90°C, kühlt ab und versetzt mit Wasser und Ethylacetat. Die org. Phase wird abgetrennt und zweimal mit ges. NaCl-Lsg. ge- waschen. Trocknen (MgSO4), einengen und chromatographische Reinigung (Cyclo- hexan/Ethylacetat 5+1) liefert 6,4 g eines farblosen Öls!
1H-NMR (CDC13, 200 MHz): 1.28 (t, 3 H, J=8.7 Hz); 1.40 (s, 9H); 1.42 (s, 6H); 3.32 (s, 2H); 3.78 (s, 2H); 3.84 (s, 2H); 4.15 (q, J=8.7 Hz); 6.17 (m, IH); 6.30 ( , IH); 7.25-7.45 (m, 5H).
Beispiel II-5
Propansäure-2-[[4-[2-[(carboxymethyl)(2-furanylmethyl)amino]methyl]phenyl]thio]- 2-methyl- 1 , 1 -dimethylethylester
192 mg 2-[[4-[2-[(2-Ethoxy-2-oxoethyl)(2-furanylmethyl)amino]methyl]ρhenyl]- thio]-2-methyl-propansäure-l,l-dimethylethylester werden in 5 ml Ethanol vorgelegt und mit 0,4 ml 1 N NaOH versetzt. Man rührt 1 h bei 80°C. Nach DC-Kontrolle (CH2C12/Methanol=10+1) wird abgekühlt, eingeengt und der Rückstand in wenig Wasser gelöst. Man säuert mit 1 N HCl an und extrahiert dreimal mit Ethylacetat. Die vereinigten org. Phasen werden 2x mit Wasser und 2x mit ges. NaCl-Lsg. gewaschen und über MgSO getrocknet. Man engt ein, zieht auf Kieselgel und reinigt über Flash-Chromatographie in CH2C12 -> CH2Cl2/Methanol 50+1 -> 25+1. Man erhält 132 mg eines sich am Hochvakuum verfestigenden farblosen Öls. 1H-NMR (DMSO, 200 MHz): 1.32 (s, 9H); 1.39 (s, 6H); 3.18 (s, 2H); 3.22 (s, 2H); 3.23 (s, 2H); 6.27 (m, IH); 6.40 (m, IH); 7.34 (d, 2H, J= 9.0 Hz); 7.50 (d, 2H, J=9.0
Hz); 7.59 (m, IH); 12.38 (breites s, IH).
Beispiel II-6
2-[[4-[2-[(2-Furanylmethyl)amino]ethyl]phenyl]thio]-2-methyl-propansäure-lJ- dimethylethylester
4,0 g 2-[[4-(2-Aminoethyl)phenyl]thio]-2-methyl-propansäure-l , 1 -dimethylethylester [(P.J. Brown et al., J. Med. Chem. 42, 3785-88 (1999)] werden in 100 ml Methanol gelöst und mit 2,6 g Furfüral versetzt. Man gibt 9,3 ml Eisessig hinzu und kocht kurz auf (10 min). Dann wird auf 0°C gekühlt und 4,25 g Natriumcyano- borhydrid portionsweise hinzugegeben. Dann wird über Nacht bei Raumtemperatur gerührt. Mit 1 N HCl wird bis zur sauren Reaktion versetzt und 30 min gerührt. Man engt etwas ein und stellt mit ges. NaHCO3-Lsg. basisch. Dann wird zweimal mit Ethylacetat extrahiert, die Extrakte gewaschen (ges. NaCl-Lsg.) und getrocknet und eingeengt. Chromatographische Reinigung (Dichlormethan/Methanol 15+1) liefert 2,4 g der Titelverbindung als farbloses Öl.
Rf (Dichlormethan/Methanol 10+1) = 0,57.
Beispiel II-7
2-[[4-[2-[(2-Ethoxy-2-oxoethyl)(2-füranylmethyl)amino]ethyl]phenyl]thio]-2- methyl-propansäure- 1 , 1 -dimethylethylester
2,4 g 2-[[4-[2-[(2-Furanylmethyl)amino]ethyl]phenyl]thio]-2-methyl-propansäure- 1,1 -dimethylethylester werden mit 1,5 g Bromessigsäureethylester, 0,97 g Triethylamin, 7,08 g Tetra-«-butylammoniumiodid in 100 ml Tetrahydrofuran gelöst und über Nacht zum Rückfluss erhitzt. Man versetzt mit Ethylacetat und Wasser und schüttelt mit Wasser und ges. NaCl-Lsg. aus. Einengen und Chromatographie (Petrolether/ Ethylacetat 10+1) liefert 1,38 g der Titelverbindung. 1H-NMR (DMSO, 200 MHz): 1.18 (t, 3H, J=7.8 Hz); 1.37 (s, 15H); 2.77 (m 4H); 3.32 (s, 2H); 3.81 (s, 2H); 4.06 (q, 2H, J=7.8 Hz); 6.21 (m, IH); 6.34 (m, IH); 7.16 (d, 2H, J=9.6 Hz); 7.32 (d, 2H, J=9.6 Hz); 7.58 (m, IH).
Beispiel II-8
2-[[4-[2-[(Carboxymethyl)(2-füranylmethyl)amino]ethyl]phenyl]thio]-2-methyl- propansäure-1 , 1 -dimethylethylester
1,0 g 2-[[4-[2-[(2-Ethoxy-2-oxoethyl)(2-furanylmethyl)amino]ethyl]phenyl]thio]-2- methyl-propansäure- 1,1 -dimethylethylester werden mit 6,5 ml 1 N NaOH in 10 ml Ethanol versetzt. Man rührt 1 h bei 80°C, engt ein, löst in Wasser und säuert mit 1 N HCl an. Dreifache Extraktion mit Ethylacetat und Chromatographie (Dichlormethan/Methanol 5+1) liefert 744 mg als farbloses Öl. 1H-NMR (DMSO, 200 MHz): 1.36 (s, 15H); 2.75 (m, 4H); 3.20 (s, 2H); 3.72 (s, 2H);
6.18 (m, IH); 6.88 (m, IH); 7.12 (d, 2H, J=9.5 Hz); 7.32 (d, 2H, J=9.5 Hz); 7.56 (m, IH).
Beispiel II-9 2-[[4-[[(2-Methoxyethyl)amino]methyl]phenyl]thio]-2-methyl-propansäure-lJ- dimethylethylester
7,9 g 2-[(4-Formylphenyl)thio]-2-methyl-propansäure-l , 1 -dimethylethylester werden mit 4,23 g Methoxy ethylamin in 100 ml Methanol vorgelegt und mit 19 ml Essigsäure versetzt. Man rührt 15 min bei RT, kocht kurz auf und versetzt dann bei
0°C portionsweise mit 8,9 g Natriumcyanoborhydrid. Nach Rühren über Nacht bei Raumtemperatur versetzt man mit 1 N HCl und lässt 30 min rühren. Dann wird mit Natriumcarbonat-Lösung basisch gestellt und 2 x mit Ethylacetat extrahiert. Die org. Phase wird mit ges. Kochsalz-Lösung gewaschen und über Magnesiumsulfat getrocknet. Einengen und chromatographische Reinigung ergibt 5,6 g (58%) eines farblosen Öls.
1H-NMR (200 MHz, CDC13): δ = 1.38 (s, 6H), 1.42 (s, 9H), 2.45 (m, 3H, CH2 + NH), 3.37 (s, 3H), 3.88 (s, 2H), 7.25-7.52 (m, 4H).
Beispiel 11-10
2-[[4-[[(2-(5-Methylfüranmethyl)amino]methyl]phenyl]thio]-2-methyl-propansäure- 1 , 1 -dimethylethylester
8,0 g 2- [(4-Formylphenyl)thio]-2-methyl-propansäure-lJ -dimethylethylester werden mit 6,3 g 5-Methyl-2-furanmethanamin in 100 ml Methanol vorgelegt und mit 16 ml Essigsäure versetzt. Man rührt 15 min bei RT, kocht kurz auf und versetzt dann bei 0°C portionsweise mit 5,7 g Natriumcyanoborhydrid. Nach Rühren über Nacht bei Raumtemperatur versetzt man mit 1 N HCl und lässt 30 min rühren. Dann wird mit Natriumcarbonat-Lösung basisch gestellt und 2 x mit Ethylacetat extrahiert. Die org.
Phase wird mit ges. Kochsalz-Lösung gewaschen und über Magnesiumsulfat getrocknet. Einengen und chromatographische Reinigung ergibt 4,8 g (45%) eines farblosen Öls, das zur Zersetzung neigt und bei -25 °C gelagert wird. 1H-NMR (200 MHz, CDC13): δ = 1.42 (s, 15H), 1.72 (s, IH, NH), 2.28 (s, 3H), 3.79 (s, 2H), 3.78 (s, 2H), 5.88 (m, IH), 6.03 (m, IH), 7.28 (dd, 2 H, J=llHz), 7.45 (m,
2H, J=l lHz).
Beispiel 11-11
2-Brom-N-(2,4-dimethylphenyl)-acetamid
117 g Triethylamin und 140 g 2,4-Dimethylanilin werden in 2 1 Methylenchlorid gelöst und mit einer Lösung aus 233 g alpha-Bromacetylbromid in 400 ml Methylenchlorid bei maximal 15°C in 30 min unter Eiskühlung versetzt. Nach 30 min Reaktionszeit wird der Niederschlag abgesaugt, der Rückstand in 3 1 Methylenchlorid gelöst, mit dem Filtrat vereinigt und zweimal mit 2 1 Wasser sowie 2 1 ges. Kochsalzlösung gewaschen. Man trocknet über Natriumsulfat, saugt ab, engt ein, und kristallisiert den Rückstand aus Ethanol um. Man erhält 193 g der Titelverbindung.
Beispiel 11-12 2-Brom-N-(2,4-dichlorphenyl)-acetamid
Diese Verbindung wurde analog zu Beispiel 11-11 hergestellt aus 4,2 g 2,4-Dichlor- anilin und 5,76 g Bromacetylbromid sowie 2,89 g Triethylamin in Methylenchlorid. Es wurden 5,9 g (80,4 %) der Titelverbindung erhalten. Rf (Dichlormethan): 0,38 MS (EI pos.): M+ = 283.
Ausführungsbeispiele 2
Beispiel 2-1
2-[[4-[[[2-[(2,4-Dimethylphenyl)amino]-2-oxoethyl](2-furanylmethyl)amino]- methyl]phenyl]thio]-2-methyl-propansäure-tert-butylester
Methode a): 250 mg Propansäure-2-[[4-[2-[(carboxymethyl)(2-furanylmethyl)amino]methyl]- phenyl]thio] -2 -methyl- 1,1 -dimethylethylester werden gemeinsam mit 89 mg Hydroxybenztriazol, 249 ml Triethylamin, 82 mg 2,4-Dimethylanilin und 131 mg N'- (3-Dimethylaminopropyl)-N-ethylcarbodiimid-Hydrochlorid versetzt und in 5 ml Dichlormethan gelöst. Man rührt 20 h bei Raumtemperatur und extrahiert mit 1 N NaOH, 1 N HCl, Wasser und ges. NaCl-Lsg. Die vereinigten organischen Phasen werden getrocknet (MgSO ) und chromatographisch gereinigt (Dichlormethan/Ethyl- acetat 25+1). Man erhält 200 mg eines zähen Öls.
LC-MS: Acetonitril/30% wässr. HCl/Wasser (Gradient): Rt = 4.87 min ([M+H]+ = 523).
Methode b):
1,5 g 2-[[4-[[(2-Furanylmethyl)amino]methyl]phenyl]thio]-2-methyl-propansäure- 1,1 -dimethylethylester (Beispiel II-3) und 1,1 g 2-Brom-N-(2,4-dimethylphenyl)- acetamid (Beispiel II-9) werden in 20 ml DMF gelöst und mit 0,4 g Natrium- hydrogencarbonat versetzt. Man erwärmt über Nacht auf 90°C, engt ein und reinigt
chromatographisch (Dichlormethan/Ethylacetat 10:1 und 5:1). Man erhält 2,1 g der Titelverbindung.
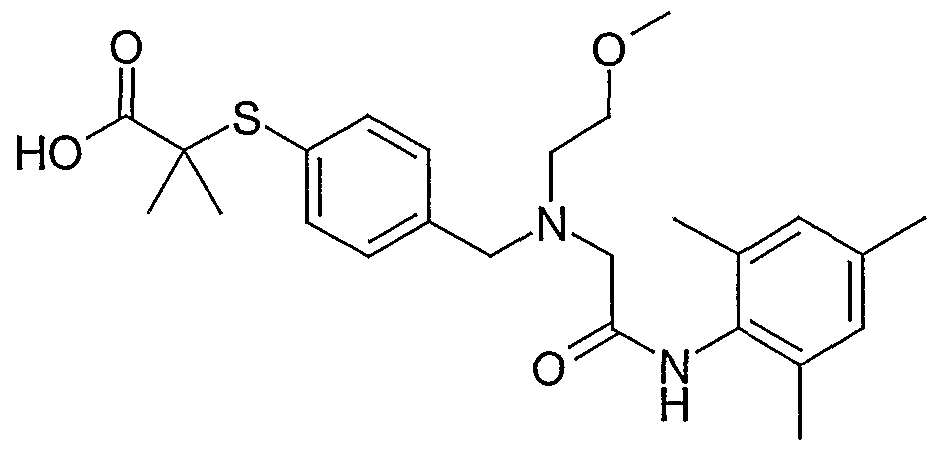
Beispiel 2-2 2-[[4-[[[2-[(2,4,6-Trimethylphenyl)amino]-2-oxoethyl](2-furanylmethyl)amino]- methyl]phenyl]thio]-2-methyl-propansäure-tert.-butylester
250 mg Propansäure-2- [ [4- [2- [(carboxymethy l)(2-furanylmethyl)amino]methyl] - phenyl]thio]-2-methy 1-1,1 -dimethylethylester werden gemeinsam mit 90 mg Hydroxybenztriazol, 250 ml Triethylamin, 80 mg 2,4,6-Trimethylanilin und 130 mg
N'-(3-Dimethylaminopropyl)-N-ethylcarbodiimid-Hydrochlorid versetzt und in 5 ml Dichlormethan gelöst. Man rührt 20 h bei Raumtemperatur und extrahiert mit 1 N NaOH, 1 N HCl, Wasser und ges. NaCl-Lsg. Die vereinigten organischen Phasen werden getrocknet (MgSO ) und chromatographisch gereinigt (Dichlormethan Ethyl- acetat 25+1). Man erhält 210 mg eines zähen Öls.
LC-MS: Acetoriitril/30% wässr. HCl/Wasser (Gradient): Rt = 5.32 min ([M+H]+ = 537).
Beispiel 2-3 2-[[4-[[[2-[(2,5-Dimethyl-4-meti oxyphenyl)amino]-2-oxoethyl](2-furanylmethyl)- amino]methyl]phenyl]thio]-2-methyl-propansäure-tert.-butylester
250 mg Propansäιιre-2-[[4-[2-[(carboxymethyl)(2-furanylmethyl)amino]-ethyl]- phenyl]t-hio]-2 -methyl- 1,1 -dimethylethylester werden gemeinsam mit 90 mg Hydroxybenztriazol, 250 ml Triethylamin, 80 mg 2,5-Dimethyl-4-methoxyanilin und
130 mg N,-(3-Dimethylaminopropyl)-N-ethylcarbodiimid-Hydrochlorid versetzt und in 5 ml Dichlormethan gelöst. Man rührt 20 h bei Raumtemperatur und extrahiert mit 1 N NaOH, 1 N HCl, Wasser und ges. NaCl-Lsg. Die vereinigten organischen Phasen werden getrocknet (MgSO ) und chromatographisch gereinigt (Dichlormethan/Ethyl- acetat 25+1). Man erhält 190 mg eines zähen Öls.
LC-MS: Acetonitril/30% wässr. HCl/Wasser (Gradient): Rt = 4.90 min ([M+H]+ = 552).
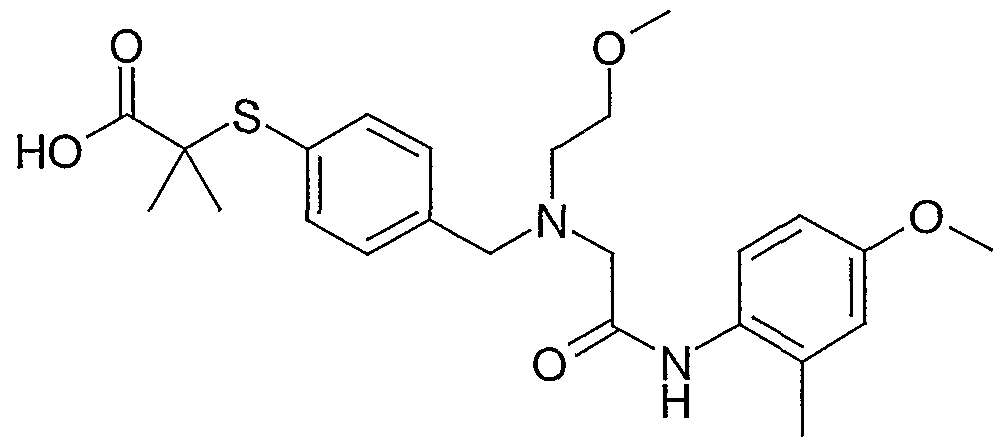
Beispiel 2-4 2-[[4-[[[2-[(2-Methyl-4-methoxyphenyl)amino]-2-oxoethyl](2-furanylmethyl)- amino]-methyl]phenyl]thio]-2-methyl-propansäure-tert.-butylester
250 mg Propansäure-2-[[4-[2-[(carboxymethyl)(2-füranylmethyl)amino]-ethyl]- phenyl]thio]-2-methyl-l,l -dimethylethylester werden gemeinsam mit 90 mg Hydroxybenztriazol, 250 ml Triethylamin, 80 mg 2-Methyl-4-methoxyanilin und
130 mg N'-(3-Dimethylaminopropyl)-N-ethylcarbodiimid-Hydrochlorid versetzt und in 5 ml Dichlormethan gelöst. Man rührt 20 h bei Raumtemperatur und extrahiert mit 1 N NaOH, 1 N HCl, Wasser und ges. NaCl-Lsg. Die vereinigten organischen Phasen werden getrocknet (MgSO4) und chromatographisch gereinigt (Dichlormethan/Ethyl- acetat 25+1). Man erhält 190 mg eines zähen Öls.
LC-MS: Acetonitril/30%wässr. HCl/Wasser (Gradient): Rt = 4.69 min ([M+H]+ = 538).
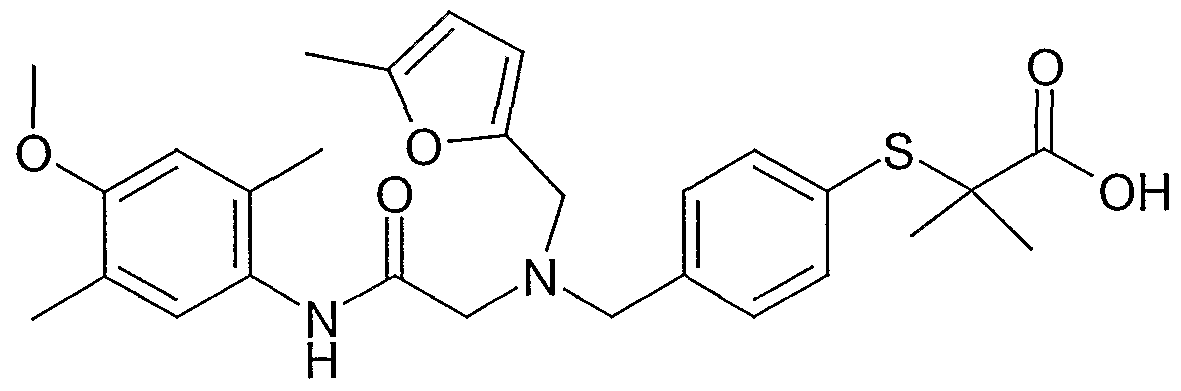
Beispiel 2-5 2-[[4-[[[2-[(2,4-Dimethylphenyl)amino]-2-oxoethyl](2-furanylmethyl)amino]- methyl]phenyl]thio]-2-methyl-propansäure
90 mg 2-[[4-[[[2-[(2,4-Dimethylρhenyl)amino]-2-oxoethyl](2-furanylmethyl)amino]- methyl]phenyl]thio]-2-methyl-propansäure-tert-butylester werden in 5 ml Dichlormethan gelöst und mit 0,1 ml Trifluoressigsäure umgesetzt. Nach 4 h Rühren bei
Raumtemperatur wird eingeengt und chromatographisch (Dichloπnethan/Methanol
100+1) gereinigt. Man erhält 80 mg der Titelverbindung als festen Schaum.
Rf (Dichloπnethan Methanol 10+1) = 0.3
1H-NMR (400 MHz, D6-DMSO): δ = 1.34 (s, 6H, CH3), 2.16 (s, 3H, CH3), 2.23 (s,
3H, CH3), 3.24 (s, 2H, CH2), 3.16 (s, 2H, CH2), 3.78 (s, 2H, CH2), 6.38-6.40 (m, 2H,
2x Furanyl-H), 6.93-6.95 (d, 2H, Ar-H), 7.0 (s, IH, Ar-H), 7.38-7.51 (m, 4H, Ar-H),
7.60-7.61 (m, IH, Furanyl-H), 9.14 (s, IH, NH).
MS (ESI pos.): m/z - 467 ([M+HJ^ m/z = 489 ([M+Naf)
LC-MS: Acetonitril/30% wässr. HCl/Wasser (Gradient): Rt = 3J6 min ([M+H]+ =
467).
Beispiel 2-5a
2-[[4-[[[2-[(2,4-Dimethylphenyl)amino]-2-oxoethyl](2-furanylmethyl)amino]- methyl]phenyl]thio]-2-methyl-propansäure Dicyclohexylammonmmsalz
500 mg 2-[[4-[[[2-[(2,4-Dimethylphenyl)amino]-2-oxoethyl](2-furanylmethyl)- amino]methyl]phenyl]thio]-2-methyl-propansäure (Beispiel 2-5) werden in 500 mg
Acetonitril gelöst und 194 mg Dicyclohexylamin zugesetzt. Man gibt Wasser hinzu, destilliert Teile des Acetonitrils bis zur Eintrübung ab und lyophilisiert. Man erhält
445 mg eines Pulvers.
LC-MS: Acetonitril/30%wässr. HCl/Wasser (Gradient): Rt = 3J6 min ([M+H]+ -
467).
Beispiel 2-5b
2-[[4-[[[2-[(2,4-Dimethylphenyl)amino]-2-oxoethyl](2-furanylmethyl)amino]- methyl]phenyl]thio]-2-methyl-propansäure Hydrochlorid
1 ,20 g 2-[[4-[[[2-[(2,4-Dimethylphenyl)amino]-2-oxoethyl](2-furanylmethyl)amino]- methyl]phenyl]thio]-2-methyl-prop ansäure (Beispiel 2-5) werden in 100 ml Ethylacetat heiß gelöst und bis zur Eintrübung mit IN HCl/Diethylether versetzt. Die anfallenden Kristalle werden abgesaugt und mit trockenem Ether gewaschen. Man erhält 1 g der Titelverbindung. Fp.: 158° C (aus Ethanol/Diethylether).
Beispiel 2-6 2-[[4-[[[2-[(2,4,6-Trimethylphenyl)amino]-2-oxoethyl](2-furanylmethyl)amino]- methyl]phenyl]thio]-2-methyl-propansäure
210 mg 2-[[4-[[[2-[(2,4,6-Trimethylphenyl)amino]-2-oxoethyl](2-furanylmethyl)- amino]methyl]phenyl]thio]-2-methyl-propansäure-tert.-butylester werden in 5 ml Dichlormethan gelöst und mit 1 ml Trifluoressigsäure umgesetzt. Nach 4 h Rühren bei
Raumtemperatur wird eingeengt und chromatographisch (Dichlormethan/Ethylacetat 50+1) gereinigt. Man erhält 187 mg der Titelverbindung als festen Schaum. 1H-NMR (DMSO, 200 MHz): 1.42 (s, 6H); 2.04 (s, 6H); 2.23 (s, 3H); 3.58 (breites s, 2H); 4.05 (s, 2H); 4.12 (s, 2H); 6.55 (m, 2H); 6.87 (s, 2H); 7.48 (d, 2H, J= 9.0 Hz); 7.51 (d, 2H, J= 9.0 Hz); 7.72 (m, IH); 9.40 (breites s, IH).
Beispiel 2-7
2-[[4-[[[2-[(2,5-Dimethyl-4-methoxyphenyl)amino]-2-oxoethyl](2-furanylmethyl)- amino]methyl]phenyl]thio]-2-methyl-propansäure
190 mg 2-[[4-[[[2-[(2,5-Dimethyl-4-methoxyphenyl)amino]-2-oxoethyl](2-füranyl- methyl)amino]methyl]phenyl]thio]-2-methyl-propansäure-tert.-butylester werden in 5 ml Dichlormethan gelöst und mit 1 ml Trifluoressigsäure umgesetzt. Nach 20 h
Rühren bei Raumtemperatur wird eingeengt und chromatographisch (Dichlormethan/Methanol 50+1) gereinigt. Man erhält 166 mg der Titelverbindung als festen Schaum. 1H-NMR (DMSO, 200 MHz): 1.39 (s, 6H); 2.08 (s, 3H); 2.11 (s, 3H); 3.7 (s, 3H); 4.00 (breites s, 4H); 6.48 (m, IH); 6.51 (m, IH); 6.16 (s, IH); 7.08 (s, IH); 7.48 (m,
4H); 7.72 (m, IH); 9.35, (breites s, IH); 12.65 (breites s, IH).
Beispiel 2-8
2-[[4-[[[2-[(2-Methyl-4-methoxyphenyl)amino]-2-oxoethyl](2-furanylmethyl)- amino]methyl]phenyl]thio]-2-methyl-propansäure
200 mg 2-[[4-[[[2-[(2-Methyl-4-methoxyphenyl)amino]-2-oxoethyl](2-furanyl- methyl)amino]methyl]phenyl]thio] -2-methyl-propansäure-tert.-butylester werden in 5 ml Dichlormethan gelöst und mit 1 ml Trifluoressigsäure umgesetzt. Nach 20 h
Rühren bei Raumtemperatur wird eingeengt und chromatographisch (Dichlormethan/Methanol 50+1) gereinigt. Man erhält 174 mg der Titelverbindung als festen Schaum.
1H-NMR (DMSO, 200 MHz): 1.38 (s, 6H); 2.12 (s, 3H); 3.7 (s, 3H); 3.80 (breites s, 2H); 4.00 (breites s, 2H); 6.45 (m, IH); 6.55 (m, IH); 6.65 (m, IH); 6.78 (m, IH);
7.25 (m, IH); 7.48 (m, 4H); 7.71 (m, IH); 9.37 (breites s, IH); 12.65 (breites s, IH).
Beispiel 2-9
2-[[4-[2-[[2-[(2,4-Dimethylphenyl)amino]-2-oxoethyl](2-fiιranylmethyl)amino]- ethyl]phenyl]thio]-2-methyl-propansäure tert.-butylester
104 mg 2-[[4-[2-[(Carboxymethyl)(2-füranylmethyl)amino]ethyl]phenyl]thio]-2- methyl-propansäure- 1,1 -dimethylethylester werden gemeinsam mit 36 mg Hydroxybenztriazol, 0,1 ml Triethylamin, 29 mg 2,4-Dimethylanilin und 53 mg N'- (3-Dimethylaminopropyl)-N-ethylcarbodiimid-Hydrochlorid versetzt und in 5 ml
Dichlormethan gelöst. Man rührt 20 h bei Raumtemperatur und extrahiert mit 1 N NaOH, 1 N HCl, Wasser und ges. NaCl-Lsg. Die vereinigten organischen Phasen werden getrocknet (MgSO4) und chromatographisch gereinigt (Dichlormethan/Ethylacetat 5+1). Man erhält 190 mg eines zähen Öls. LC-MS: Acetonitril/30% wässr. HCl/Wasser (Gradient): Rt = 5,3 min ([M+H]+ =
537).
1H-NMR (CDC13, 200 MHz): 1.38 (s, 9H); 1.40 (s, 6H); 2.08 (s, 3H); 2.28 (s, 3H) 2.82 (m, 4H); 3.32 (s, 2H); 3.78 (s, 2H); 6.22 (m, IH); 6.95 (m, IH); 7.00 (m, IH) 7.05 (d, 2H, J=10.0 Hz); 7.35 (d, 2H, J=10.0 Hz), darunter: (m, IH); 7.79 (m, IH) 8.95 (breites s, IH); 12.60 (breites s, IH).
Beispiel 2-10
2-[[4-[2-[[2-[(2,5-Dimethyl-4-methoxyphenyl)amino]-2-oxoethyl](2-furanylmethyl)- amino]ethyl]phenyl]thio]-2 -methyl- propansäure tert.-butylester
98 mg 2-[[4-[2-[(Carboxymethyl)(2-furanylmethyl)amino]ethyl]phenyl]thio]-2- methyl-propansäure- 1,1 -dimethylethylester werden gemeinsam mit 33 mg Hydroxybenztriazol, 0,09 ml Triethylamin, 34 mg 2,5-Dimethyl-4-methoxyanilin und 49 mg N'-(3-Dimethylaminopropyl)-N-ethylcarbodiimid-Hydrochlorid versetzt und in 5 ml Dichlormethan gelöst. Man rührt 20 h bei Raumtemperatur und extrahiert mit 1 N NaOH, 1 N HCl, Wasser und ges. NaCl-Lsg. Die vereinigten organischen Phasen werden getrocknet (MgSO4) und chromatographisch gereinigt (Dichlormethan/Ethylacetat 5+1). Man erhält 48 mg eines zähen Öls. DC: Rf = 0.65 (Dichlormethan/Ethylacetat =10+1).
Beispiel 2-11
2-[[4-[2-[[2-[(2,4-Dimethylphenyl)amino]-2-oxoethyl](2-furanylmethyl)amino]- ethyl]phenyl]thio]-2-methyl-proρansäure
38 mg 2-[[4-[2-[[2-[(2,4-Dimethylphenyl)amino]-2-oxoethyl](2-furanylmethyl)- amino]ethyl]phenyl]thio]-2-methyl-propansäure tert.-butylester werden in 5 ml
Dichlormethan gelöst und mit 0,27 ml Trifluoressigsäure versetzt. Man rührt 24 h bei Raumtemperatur, zieht mit Toluol ab und chromatographiert (Dichlormethan/ Methanol 10+1) den Rückstand. Man erhält 33 mg farbloses Öl. LC-MS: Acetonitril/30% wässr. HCl/Wasser (Gradient): Rt = 3.38 min ([M+H]+ = 481).
Beispiel 2-12
2-[[4-[2-[[2-[(2,5-Dimethyl-4-methoxyphenyl)amino]-2-oxoethyl](2-furanylmethyl)- amino]ethyl]phenyl]thio]-2-methyl-propansäure
30 mg 2-[[4-[2-[[2-[(2,5-Dimethyl-4-methoxyphenyl)amino]-2-oxoethyl](2-füranyl- methyl)amino]ethyl]phenyl]thio]-2-methyl-propansäure tert.-butylester werden in 5 ml Dichlormethan gelöst und mit 0,20 ml Trifluoressigsäure versetzt. Man rührt
24 h bei Raumtemperatur, zieht mit Toluol ab und chromatographiert den Rückstand (Dichloπnethan/Methanol 10+1). Man erhält 27 mg an der Luft dunkelndes Öl. LC-MS: Acetonitril/30% wässr. HCl/Wasser (Gradient): Rt = 3.78 min ([M+H]+ = 511). 1H-NMR (DMSO, 200 MHz): 1.35 (s, 9H); 2.05 (s, 3H); 2.10 (s, 3H); 2.82 (m, 4H);
3.25 (s, 2H); 3J2 (s, 3H); 3.82 (s, 2H); 6.33 (m, 2H); 6J2 (m, IH); 7.15 (d, 2H, J=9.8 Hz); 7.24 (d, 2H, J=9.8 Hz), darunter: (m, IH); 7.62 (m, IH); 8.88 (breites s, IH); 12.55 (breites s, IH).
In analoger Weise wurden die folgenden Beispielverbindungen hergestellt:
Beispiel 2-13
2-Methyl-2-[[4-[[[(5-methyl-2-furanyl)methyl][2-oxo-2-[(2,4-dichlorphenyl)amino]- ethyl]amino]methyl]phenyl]thio]-propansäure
Ausbeute: 343 mg (68%).
1H-NMR: (200 MHz, CDC13): δ = 1.50 (s, 6H, 2xCH3), 2.19 (s, 3H, CH3), 3.38 (s, 2H, CH2), 3J8 (s, 2H, CH2), 3.83 (s, 2H, CH2), 4.30 (s, br, IH, COOH), 5.85 (m, IH, Furanyl-H), 6.16 (m, IH, Furanyl-H), 7.18-7.49 (m, 6H, Ar-H), 8.30 (m, IH, Ar-
H), 9.68 (s, IH, NH).
LC-MS: Acetonitril/30%wässr. HCl/Wasser (Gradient): Rt = 3.42 min ([M+H]+ = 521)
Beispiel 2-14
2-Methyl-2-[[4-[[[(5-methyl-2-furanyl)methyl][2-oxo-2-[(2,4,6-trichlorphenyl)- amino]ethyl]amino]methyl]phenyl]tl io]-propansäure
Ausbeute: 90 mg (36%)
1H-NMR (200 MHz, CDC13): δ = 1.53 (s, 6H, 2xCH3), 2.29 (s, 3H, CH3), 3.75 (s, 2H, CH2), 4.25 (s, 2H, CH2), 4.28 (s, 2H, CH2), 5.95 (m, IH, Furanyl-H), 6.49 (m, IH, Furanyl-H), 7.35 (s, 2H, Ar-H), 7.38-7.51 (m, 4H, Ar-H), 9.51 (s, IH, NH). LC-MS: Acetonitril/30%wässr. HCl/Wasser (Gradient): Rt = 3.05 min ([M+H]+= 555)
Beispiel 2-15
2-Methyl-2-[[4-[[[(5-methyl-2-füranyl)methyl][2-oxo-2-[(2,4,6- trimethylphenyl)amino]ethyl]amino]methyl]phenyl]thio]-propansäure
Ausbeute: 46 mg (26%)
LC-MS: Acetonitril/30%wässr. HCl/Wasser (Gradient): Rt - 4,18 min ([M+H]4 494)
Beispiel 2-16
2-Methyl-2-[[4-[[[(5-methyl-2-firranyl)methyl][2-oxo-2-[(2,4-dimethylphenyl)- amino]ethyl]amino]methyl]phenyl]thio]-propansäure
Ausbeute: 183 mg (41%)
LC-MS: Acetonitril/30%wässr. HCl/Wasser (Gradient): Rt = 2,80 min ([M+H]+ 481)
Beispiel 2-17 2-Methyl-2-[[4-[[[(5-methyl-2-furanyl)methyl][2-oxo-2-[(2,5-dimethyl-4-methoxy- phenyl)amino]ethyl]amino]methyl]phenyl]thio]-propansäure
Ausbeute: 149 mg (67%)
LC-MS: Acetonitril/30%wässr. HCl/Wasser (Gradient): Rt = 4,10 min ([M+H]+ 511)
Beispiel 2-18 2-Methyl-2-[[4-[[[(5-methyl-2-furanyl)methyl] [2-oxo-2-[(4-chlor-2-trifluormethyl- phenyl)amino]ethyl]amino]methyl]phenyl]thio]-propansäure
Ausbeute: 63 mg (22%)
LC-MS: Acetonitril/30%wässr. HCl/Wasser (Gradient): Rt = 3.48 min ([M+H]' 555)
Beispiel 2-19
2-Methyl-2-[[4-[[[(5-methyl-2-furanyl)methyl][2-oxo-2-[(4-methoxy-2-methyl- phenyl)amino]ethyl]amino]methyl]phenyl]thio]-propansäure
Ausbeute: 24 mg (18%)
LC-MS: Acetonitril/30%wässr. HCl/Wasser (Gradient): R, = 2,59 min ([M+H]+
497)
Beispiel 2-20
2-[[4-[[[2-[(2,5-Dimethyl-4-methoxy-phenyl)amino]-2-oxoethyl](2-methoxyethyl)- amino]methyl]phenyl]thio]-2-methyl-propionsäure
Ausbeute: 60 mg (60%)
LC-MS: Acetonitril/30%wässr. HCl/Wasser (Gradient): Rt = 2,15 min ([M+H]+
475).
Beispiel 2-21
2-Methyl-2-[[4-[[[(5-methyl-2--fiιranyl)methyl][2-oxo-2-[(2,4-bistrifluormethyl- phenyl)amino]ethyl]amino]methyl]phenyl]thio]-propansäure
Ausbeute: 16 mg (20%)
LC-MS: Acetonitril/30%wässr. HCl/Wasser (Gradient): Rt = 3.59 min ([M+H]+
589)
Beispiel 2-22
2-Methyl-2-[[4-[[[(5-methyl-2-mranyl)methyl][2-oxo-2-[(2-methyl-4-trifluor- methoxy-5-chlorphenyl)amino]ethyl]amino]methyl]phenyl]thio]-propansäure
Ausbeute: 89 mg (81%) LC-MS: Acetonitril/30%wässr. HCl/Wasser (Gradient): Rt = 3.36 min ([M+H]+
585)
Beispiel 2-23
2-Methyl-2-[[4-[[[(5-methyl-2-furanyl)methyl][2-oxo-2-[(2-trifluormethyl-4- trifluormethoxyphenyl)amino]ethyl]amino]methyl]phenyl]thio]-propansäure
Ausbeute: 22 mg (34%)
LC-MS: Acetonitril/30%wässr. HCl/Wasser (Gradient): Rt = 3.52min ([M+H] 605)
Beispiel 2-24
2-[[4-[[[2-[[2,4-Bis(trifluormethyl)phenyl]amino]-2-oxoethyl](2-methoxyethyl)- amino]methyl]phenyl]thio]-2-methyl-propansäure
Ausbeute: 26 mg (20%)
LC-MS: Acetonitril 30%wässr. HCl/Wasser (Gradient): Rt = 3.05 min ([M+H]+
553).
Beispiel 2-25
2-[[4-[[[2-[[2,4-Dichlorphenyl]amino]-2-oxoethyl](2-methoxyethyl)amino]- methyl]phenyl]thio]-2-methyl-propansäure
Ausbeute: 61 mg (27%).
1H-NMR (300 MHz, CDC13): δ = 1.38 (s, 6H, 2xCH3), 2.82 (m, 2H, CH2), 3.23 (s, 3H, OMe), 3.32 (s, 2H, CH2), 3.50 (m, 2H, CH2), 3.73 (s, 2H, CH2), 5.28 (s, IH,
COOH), 7.15-7.48 (m, 6H, Ar-H), 8.35 (m, IH, Ar-H), 9.90 (s, IH, NH). LC-MS: Acetonitril/30%wässr. HCl/Wasser (Gradient): Rt = 2,76 min ([M+H]+ = 485).
Beispiel 2-26
2-[[4-[[[2-[[2,4-Dimethylphenyl]amino]-2-oxoethyl](2-methoxyethyl)amino]- methyl]phenyl]thio]-2-methyl-propansäure
Ausbeute: 50 mg (75%)
1H-NMR (200 MHz, CDC13): δ = 1.50 (s, 6H, 2xCH3), 2.15 (s, 3H, Me), 2.28 (s, 3H,
Me), 3.34 (s, 3H, OMe), 3.40 (m, 2H, CH2), 3.68 (m, 2H, CH2), 3.83 (s, 2H, CH2),
4.32 (s, 2H, CH2), 5.40 (s, IH, COOH), 7.00 (m, 2H, Ar-H), 7.32-7.52 (m, 7H, Ar-
H), 9.00 (s, IH, NH).
LC-MS: Acetonitril/30%wässr. HCl/Wasser (Gradient): Rt = 2,22 min ([M+H]+ =
445).
Beispiel 2-27
2-Methyl-2-[[4-[[[(2-thiophenyl)methyl][2-oxo-2-[(2-methyl-4-trifluormethoxy-5- chlo henyl)amino]ethyl]amino]methyl]phenyl]thio]-propansäure
Ausbeute: 200 mg (99%)
1H-NMR (300 MHz, CDC13): δ = 1.50 (s, 6H, 2xCH3), 2.20 (s, 3H, Me), 3.61 (s, 2H, CH2), 4.20 (s, 2H, CH2), 4.48 (s, 2H, CH2), 5.60 (s, IH, COOH), 7.00 (m, 2H, Ar-H), 7.02-7.17 (m, 3H, Ar-H und Thienyl-H), 7.36 (m, 3H, Ar-H), 7.50 (m, 2H, Ar-H),
8.00 (s, IH, Ar H), 8.88 (s, IH, NH).
LC-MS: Acetonitril/30%wässr. HCl/Wasser (Gradient): Rt = 3,40 min ([M+H/]+ = 587).
Beispiel 2-28
2-Methyl-2-[[4-[[[(2-thiophenyl)methyl][2-oxo-2-[(2-trifluormethyl-4-trifluor- methoxy-phenyl)amino]ethyl]amino]methyl]phenyl]thio]-propansäure
Ausbeute: 80 mg (98%)
LC-MS: Acetonitril/30%wässr. HCl/Wasser (Gradient): Rt = 3.56 min ([M+H]+ 606).
Beispiel 2-29
2-Methyl-2-[[4-[[[(2-thiophenyl)methyl][2-oxo-2-[(2-methyl-4-methoxy-phenyl)- amino]ethyl]amino]methyl]phenyl]thio]-propansäure
Ausbeute: 83 mg (83%)
LC-MS: Acetonitril/30%wässr. HCl/Wasser (Gradient): Rt = 2,74 min ([M+H]4 498).
Beispiel 2-30 2-Methyl-2-[[4-[[[(2-raranyl)methyl][2-oxo-2-[(2,4-dimethoxyphenyl)amino]- ethyl]amino]methyl]phenyl]thio]-propansäure
Ausbeute: 75 mg (60%)
LC-MS: Acetonitril/30%wässr. HCl/Wasser (Gradient): Rt = 4,19 min ([M+H]4" 499).
Beispiel 2-31
2-[[4-[[[2-[(2-Methyl-4-methoxyphenyl)amino]-2-oxoethyl](2-methoxyethyl)amino]- methyl]phenyl]thio]-2-methyl-propansäure
Ausbeute: 65 % d.Th.
1H-NMR (300 MHz, CDC13): δ = 1,51 (s, 6H); 2,18 (s, 3H); 3,34 (s, 3H); 3,37-3,45 (m, 2H); 3,65-3,75 (m, 2H); 3,77 (s, 3H); 3,89 (s, 2H); 4,34 (s, 2H); 6,67-6,78 (m, 2H); 7,35-7,44 (m, 3H); 7,52 (d, 2H); 9,05 (s, IH).
Beispiel 2-32
2-[[4-[[[2-[(2,4,6-Trimethylphenyl)amino]-2-oxoethyl](2-methoxyethyl)amino]- methyl]phenyl]thio]-2-methyl-propansäure
Ausbeute: 89 % d.Th. 1H-NMR (300 MHz, CDC13): δ = 1,51 (s, 6 H); 2,12 (s, 6H); 2,25 (s, 3H); 3,35 (s,
3H); 3,38-3,54 (m, 2H); 3,65-3,77 (m, 2H); 3,85-3,94 (m, 2H); 4,30-4,45 (m, 2H); 6,87 (s, 2H); 7,39 (d, 2H); 7,53 (d, 2H); 8,82 (br s, IH).
Ausgangsverbindungen III
Beispiel III-l tert-Butyl (4-foιmylphenoxy)acetat
Zu einer Lösung aus 27,50 g (225,18 mmol) 4-Hydroxybenzaldehyd in 200 ml
Dioxan werden bei Raumtemperatur 31,60 g (281,48 mmol) Kalium-t-butylat und 52,70 (270,22 mmol) Bromessigsäure-t-butylester gegeben und über Nacht bis zum Sieden erhitzt. Nach Zugabe von 1 1 Wasser wird mit Diethylether extrahiert, mit 1 N Natriumhydroxid-Lösung, Wasser und gesättigter Natriumchlorid-Lösung ge- waschen, über Magnesiumsulfat getrocknet und das Lösungsmittel abdestilliert.
Flash-Chromatographie an Kieselgel (Cyclohexan -> Cyclohexan/Essigsäureethyl- ester 20:1 -> 10:1 -> 5:1) ergibt nach Umkristallisation aus Pentan die Zielverbindung. Ausbeute: 31 % Schmelzpunkt: 58 - 60°C
Beispiel III-2 tert-Butyl 2-(4-formylphenoxy)-2-methylpropanoat
In 250 ml N,N-Dimethylformamid werden 24,42 g (200 mmol) 4-Hydroxybenz- aldehyd gelöst und mit 27,64 g (200 mmol) Kaliumcarbonat versetzt. Bei 100°C werden 53,55 g (240 mmol) α-Bromisobuttersäure-t-butylester zugetropft. Es wird eine Stunde nachge-rührt, weitere 200 mmol Kaliumcarbonat und 240 mmol α-Brom- iso-buttersäure-t-butylester zugegeben und nach 4 Stunden bei 100°C mit 1 1 Wasser versetzt. Nach Extraktion mit Diethylether, Waschen mit 1 N Natronlauge und gesättigter Natriumchlorid-Lösung sowie Trocknen über Magnesiumsulfat wird das Lösungsmittel abdestilliert und der Rückstand durch Flash-Chromatographie an Kieselgel (Cyclohexan -> Cyclohexan/Essigsäureethylester 20:1 -> 10:1 -> 5:1) gereinigt und im Vakuum getrocknet. Die Zielverbmdung wird in Form farbloser Kristalle in einer Ausbeute von 42 % erhalten.
1H-NMR (200 MHz, CDC13): δ = 1,40 (s, 9 H), 1,62 (s, 6 H), 6,91 (d, 2 H), 7,79 (d, 2 H), 9,88 (s IH). MS (ESI): 265 [M+H]+.
Analog der Vorschrift von Beispiel 111-2 werden erhalten:
Beispiel III-3
Ethyl 2-(4-formylphenoxy)-2-methylbutanoat
Ausbeute: 11,71 %
1H-NMR (200 MHz, CDC13): δ = 1,00 (t, 3 H), 1,22 (t, 3 H), 1,61 (s, 3 R), 1,90 - 2,20 (m, 2 H), 4,24 (q, 2 H), 6,90 (d, 2 H), 7,80 (d, 2 H), 9,85 (s, 1 H).
MS (ESI): 251 [M+H]4", 273 [M+Na]4".
Beispiel III-4 tert-Butyl 2-[(3 -bromophenyl)sulfanyl]-2-methylpropanoat
Ausbeute: 87 %
1H-NMR (200 MHz, CDC13): δ = 1,43 (s, 9 H), 1,45 (s, 6 H), 7,14 - 7,28 (m, 1 H),
7,39 - 7,53 (m, 2 H), 7,67 (t, 1 H).
MS (DCI/ H3): 348 [M+NH4 +].
Beispiel III-5 tert -Butyl 2-(3-formylphenoxy)-2-methylpropanoat
Ausbeute: 35 %
1H-NMR (300 MHz, CDC13): δ = 1,44 (s, 9 H), 1,61 (s, 6 H), 7,14 (dd, 1 H), 7,31-
7,35 (m, 1 H), 7,41 (t, 1 H), 7,45- 5,52 (m, 1 H).
MS (DCI/ H3): 282 [M+NH4 +].
Beispiel III-6 tert-Butyl-2-(3-bromophenoxy)-2-methylpropanoat
Ausbeute: 21 %
1H-NMR (300 MHz, CDC13): δ = 1,44 (s, 9H), 1,56 (s, 6 H), 6,74 - 6,83 (m, 1 H), 7,00 - 7,04 (m, 1 H), 7,06 - 7,11 (m, 2H).
MS (DCI H3) 332 [M+NH4 +].
Beispiel III-7 tert-Butyl 2-[4-(l ,3-dioxo-l ,3-dihydro-2H-isoindol-2-yl)phenoxy]-2-methyl- propanoat
Ausbeute: 24 % Schmelzpunkt: 142 - 143 °C
Beispiel III-8 tert-Butyl 2-[(3-formylphenyl)sulfanyl]-2-methylpropanoat
Bei -78 °C werden 30,00 g (90,56 mmol) der Verbindung aus Beispiel III-4 in Tetrahydrofuran gelöst und mit 36,2 ml einer 2,5 M n-Butyllithium-Lösung in Hexan versetzt. Anschließend werden 13,94 ml (181,12 mmol) N,N-Dimethylformamid zugegeben. Nach 30 min wird auf Raumtemperatur erwärmt und 1 Stunde gerührt. Es werden 30 ml 1 N Salzsäure zugegeben, das Lösungsmittel abdestilliert und der
Rückstand mit Essigsäureethylester extrahiert, mit gesättigter Natriumhydrogencarbonat- und Natriumchlorid-Lösung gewaschen und anschließend über Magnesiumsulfat getrocknet. Nach Flashchromatographie an Kieselgel (Dichlormethan) wird die Zielverbindung mittels NP-HPLC (Cyclohexan/Essigsäureethylester) gereinigt und in einer Ausbeute von 10% erhalten.
1H-NMR (300 MHz, CDC13): δ = 1,43 (s, 9 H), 1,46 (s, 6 H), 7,50 (t, 1 H), 7,77 - 7,80 (m, 1 H), 7,87 (d, 1 H), 7,98 - 8,05 (m, 1 H), 10,00 (s, 1 H). MS (DCI/NH3): 298 [M+NH4 +].
Beispiel III-9 tert-Butyl 2-{3-[2-(l,3-dioxo-l,3-dihydro-2H-isoindol-2-yl)ethenyl]phenoxy}-2- methyl-propanoat
In einem Autoklaven werden bei 130°C 14,93 g (47,37 mmol) der Verbindung aus Beispiel πi-6, 10,25 g (59,21 mmol) Vinylphthalimid, 0,39 g (1,27 mmol) Tris-o- tolylphosphin, 0,07 g (0,32 mmol) und 21,78 g (215,23 mmol) Triethylamin erhitzt. Nach Zugabe von Wasser/Methanol wird der Niederschlag abgesaugt und aus Cyclo- hexan/Essigsäureethylester kristallisiert.
Ausbeute: 66%.
1H-NMR (200 MHz, CDC13): δ = 1,40 (s, 9 H), 1,50 (s, 6 H), 6,73 (dd, 1 H), 6,86 - 6,93 (m, 1 H), 7,16 (t, 1 H), 7,21-7,34 (m, 2 H), 7,43 (d, 1 H), 7,80 - 8,00 (m, 4 H). MS (DCI/NH3): 425 [M+NH4 +].
Beispiel 111-10 tert-Butyl 2-{3-[2-(l,3-dioxo-l,3-dihydro-2H-isoindol-2-yl)ethyl]phenoxy}-2- methyl-propanoat
In 200 ml Tetrahydrofuran werden 15,00 g (36,81 mmol) der Verbindung aus Beispiel III-9 gelöst und über Nacht in einer Wasserstoff- Atmosphäre unter Normaldruck in Gegenwart einer Suspension aus 2,00 g (2,16 mmol) Wilkinson-Katalysator in 40 ml Ethanol gerührt. Zweifache Flash-Chromatographie an Kieselgel (Cyclo- hexan/Dichlormethan 10:1 -> Cyclohexan/Essigsäureethylester 10:1 -> 5:1 und
Cyclohexan -> Cyclohexan/Dichlormethan -> Dichlormethan) ergibt die Zielverbindung in einer Ausbeute von 64%.
1H-NMR (200 MHz, CDC13): δ = 1,45 (s, 9 H), 1,52 (s, 6 H), 2,85 -3,00 (m, 2 H), 3,82-3,95 (m, 2 H), 6,65 - 6,80 (m, 2 H), 6,88 (d, 1 H), 7,15 (t, 1 H), 7,62 - 7,76 (m, 2 H), 7,77 - 7,89 (m, 2 H).
MS (ESI): 432 [M+Na+], 841 [2M+Na+].
Beispiel III-ll tert-Butyl 2-(4-aminophenoxy)-2-methylρropanoat
In 25 ml Ethanol werden 18,88 g (49,50 mmol) der Verbindung aus Beispiel III-7 gelöst und mit 12,04 ml (247,49 mmol) Hydrazinhydrat 2 h bis zum Sieden erhitzt und anschließend 12 Stunden bei Raumtemperatur gerührt. Der Niederschlag wird abgetrennt, mit Ethanol gewaschen, das Filtrat eingeengt und anschließend mit 1 1 Diethylether verdünnt. Diese Lösung wird mit 1 N Natriumhydroxid- und gesättigter Natriumchlorid-Lösung gewaschen sowie über Magnesiumsulfat getrocknet. Nach Entfernen des Lösungsmittels wird die Zielverbindung in einer Ausbeute von 87% erhalten.
Schmelzpunkt: 87 - 88°C.
Analog der Vorschrift des Beispiels III-l 1 wird erhalten:
Beispiel 111-12 tert-Butyl 2-[3-(2-aminoethyl)phenoxy]-2-methylpropanoat
Ausbeute: 70%«
1H-NMR (200 MHz, CDC13): δ = 1,31 (breites s, 2 H), 1,44 (s, 9 H), 1,56 (s, 6 H), 2,69 (t, 2 H), 2,94 (t, 2 H), 6,64 - 6,75 (m, 2 H), 6,81 (d, 1 H), 7,15 (t, 1 H). MS (EI): 279 [M4].
Beispiel 111-13 tert-Butyl 2-(4-{[(2-furylmethyl)amino]methyl}phenoxy)-2-methylpropanoat
In 350 ml 1,2-Dichlorethan werden 20,00 g (75,67 mmol) der Verbindung aus Beispiel III-2 und 7,35 g (75,67 mmol) 2-Furfurylamin mit 24,06 g (113,50 mmol) Natriumtriacetoxyborhydrid 5 Stunden bei Raumtemperatur gerührt. Die Reaktionsmischung wird mit gesättigter Natriumhydrogencarbonat-Lösung und Essigsäure- ethylester versetzt. Nach Trocknen der organischen Phase über Magnesiumsulfat und
Abdestillieren des Lösungsmittels wird der Rückstand mittels Flashchromatographie an Kieselgel (Cyclohexan -> Cyclohexan/Essigsäureethylester 10:1 -> 2:1) gereinigt. Die Zielverbindung wird in einer Ausbeute von 72% erhalten. 1H-NMR (200 MHz, CDC13): δ = 1,61 (breites s, 1 H), 1,44 (s, 9 H), 1,55 (s, 6 H), 3,71 (s, 2 H), 3,77 (s, 2 H), 6,17 (d, 1 H), 6,26-6,36 (m, 1 H), 6,70 - 6,88 (m, 2 H),
7,18 (d, 2 H), 7,32-7,40 (m, 1 H). MS (ESI): 346 [M+H]4".
Beispiel 111-14 tert. -Butyl 2- {4-[(2-furylmethyl)amino]phenoxy} -2-methylpropanoat
In 80 ml 1,2-Dichlorethan werden 4,79 g (19,06 mmol) der Verbindung aus Beispiel iπ-11 und 1,83 g (19,06 mmol) Furfüral gelöst und in Gegenwart von 6,06 g (28,59 mmol) Natriumtriacetoxyborhydrid 5 Stunden bei Raumtemperatur gerührt. Die
Reaktionslösung wird mit gesättigter Natriumhydrogencarbonat-Lösung und Essig-
säureethylester versetzt. Nach Trocknen der organischen Phase über Magnesiumsulfat und Abdestillieren des Lösungsmittels wird der Rückstand durch Flashchromatographie an Kieselgel (Cyclohexan -> Cyclohexan/Essigsäureethylester 10:1 -> 2:1) und mittels NP-HPLC (Cyclohexan/Essigsäureethylester 10:1) gereinigt. Die Zielverbindung wird in einer Ausbeute von 79% erhalten.
1H-NMR (200 MHz, CDC13): δ = 1,46 (s, 9 H), 1,48 (s, 6 H), 3,80 (breites s, 1 H), 4,26 (s, 2 H), 6,21 (d, 1 H), 6,25-6,35 (m, 1 H), 6,50-6,61 (m, 2 H), 6,72-6,85 (m, 2 H), 7,30 -7,39 (m, I H). MS (DCI H3): 332 [M+H4"], 349[M+NH4 +].
Beispiel 111-15 tert. -Butyl 2-[4-[[(2-ethoxy-2-oxoethyl)(2-furanylmethyl)amino]methyl]phenoxy]-2- methyl-propanoat
In 200 ml Tetrahydrofuran werden 18,14 g (52,50 mmol) der Verbindung aus Beispiel 111-13, 11 ml Triethylamin und 1,10 g (2,97 mmol) Tetra-n-butyl- ammoniumiodid vorgelegt, mit 8,77 ml (78,75 mmol) Bromessigsäureethylester versetzt und 1 Stunde bei Raumtemperatur sowie 2 Stunden bei 60°C gerührt.
Anschließend wird mit Wasser und Essigsäureethylester versetzt, mit gesättigter Natriumchlorid-Lösung gewaschen, über Magnesiumsulfat getrocknet und nach Entfernung des Lösungsmittels der Rückstand mittels Flash-Chromatographie an Kieselgel (Cyclohexan/Dichlormethan 4:1 -> Cyclohexan/Essigsäureethylester 10:1 -> 5:1) gereinigt. Die Ausbeute an Zielverbindung ist quantitativ.
1H-NMR (300 MHz, CDC13): δ = 1,26 (t, 3 H), 1,43 (s, 9H), 1,55 (s, 6 H), 3,30 (s, 2 H), 3,71 (s, 2 H), 3,83 (s, 2 H), 4,15 (q, 2 H), 6,19 (d, IH), 6,28-6,34 (m, 1 H), 6,77 - 6,85 (m, 2 H), 7,22 (d, 2 H), 7,35-7,41 (m, 1 H). MS (ESI): 432 [M+H]4".
Beispiel 111-16 tert. -Butyl 2-[4-[[(carboxymethyl)(2-füranylmethyl)amino]methyl]phenoxy]-2- methyl-propanoat
In 785 ml Ethanol werden 22,01g (51,00 mmol) der Verbindung aus Beispiel III- 15 in Gegenwart von 6,12 g (153,00 mmol) Natriumhydroxid 1 Stunde bei 80°C gerührt. Nach Abdestilheren des Lösungsmittels und Zugabe von Wasser wird mit 1 N Salzsäure angesäuert und mit Essigsäureethylester extrahiert. Anschließend wird mit
Wasser und gesättigter Natriumchlorid-Lösung gewaschen. Nach Trocknen über Magnesiumsulfat und Reduktion der Menge an Lösungsmittel wird das Produkt abgesaugt und getrocknet, wobei die Zielverbindung in einer Ausbeute von 74% erhalten wird. Schmelzpunkt: 152 - 155°C
Beispiel 111-17
2-Brom-N-[4-isopropyl-2-(trifluormethyl)phenyl]acetamid
50 g (246,06 mmol) 4-Isopropyl-2-(trifluoromethyl)anilin werden zusammen mit 27,39 g (270,66 mmol) Triethylamin in 1000 ml Dichlormethan vorgelegt. Bei 0°- 5°C tropft man 54,63 g (270,66 mmol) Bromacetylbromid, gelöst in 200 ml
Dichlormethan, zu. Der Ansatz wird 20 Stunden bei Raumtemperatur gerührt. Anschließend extrahiert man die Reaktionsmischung nacheinander mit Wasser, IN Salzsäure, Wasser, gesättigter Natriumhydrogencarbonat-Lösung und Wasser. Die organische Phase wird über Natriumsulfat getrocknet und das Lösungsmittel im Vakuum entfernt. Der Rückstand wird chromatographisch gereinigt. Das Produkt wird aus Cyclohexan/n-Pentan umkristallisiert, abgesaugt und bei 40°C 20 Stunden im Vakuum getrocknet. Man erhält 32,45 g (41 % d.Th.) der Titelverbindung. 1H-NMR (300 MHz, CDC13): δ = 1,25 (d, 6H); 2,95 (sept, IH); 4,05 (s, 2H); 7,45 (d, IH); 7,49 (s, IH); 8,02 (d, IH); 8,50 (br s, IH).
Beispiel 111-18
2-Brom-N-(4-tert.-butyl-2-methylphenyl)acetamid
5,5 g (33,69 mmol) 4-tert.-Butyl-2-methylanilin werden zusammen mit 3,75 g (37,06 mmol) Triethylamin in 150 ml Dichlormethan vorgelegt. Bei 0°-5°C tropft man 7,48 g (37,06 mmol) Bromacetylbromid, gelöst in 90 ml Dichlormethan, zu, wobei ein hellbrauner Niederschlag entsteht. Über Nacht wird der Ansatz bei Raumtemperatur gerührt. Anschließend versetzt man das Reaktionsgemisch mit 150 ml Essigsäure-
ethylester und extrahiert nacheinander mit Wasser, IN Salzsäure, Wasser, gesättigter Natriumhydrogencarbonat-Lösung und Wasser. Die organische Phase wird über Magnesiumsulfat getrocknet und im Vakuum vom Lösungsmittel befreit. Der Rückstand wird chromatographisch gereinigt. Das Produkt wird aus Essigsäureethylester und n-Pentan umkristallisiert, abgesaugt und bei 40°C im Vakuum getrocknet. Man erhält 6,53 g (68 % d.Th.) der Titelverbindung.
1H-NMR (400 MHz, CDC13): δ = 1,3 (s, 9H); 2,3 (s, 3H); 4,06 (s, 2H); 7,20-7,23 (m, IH); 7,25 (d, IH); 7,7 (d, IH); 8,05 (br s, IH).
Beispiel 111-19
2-Brom-N-(4-cyclohexyl-2-methylphenyl)acetamid
Ausbeute: 41 ,0 % d.Th.
1H-NMR (200 MHz, CDC13): δ = 1,20-1,50 (m, 5H); 1,65-1,95 (m, 5H); 2,28 (s, 3H); 2,35-2,55 (m, IH); 4,07 (s, 2H); 7,00-7,13 (m, 2H); 7,69 (d, IH); 8,05 (br s, IH).
Beispiel 111-20 2-Brom-N-(5,6,7,8-tetrahydro-l-naphthalenyl)acetamid
Ausbeute: 95,6 % d.Th.
1H-NMR (200 MHz, CDC13): δ = 1,70-1,90 (m, 4H); 2,55-2,70 (m, 2H); 2,75-2,85 (m, 2H); 4,08 (s, 2H); 6,95 (d, IH); 7,14 (t, IH); 7,69 (d, IH); 8,09 (br s, IH).
Beispiel 111-21 2-Brom-N-[4-(l -naphthyloxy)-2-(trifluormethyl)phenyl]acetamid
Ausbeute: 80,5% d.Th. 1H-NMR (200 MHz, CDC13): δ = 4,08 (s, 2H); 7,01 (d, IH); 7,18 (dd, IH); 7,30-7,62
(m, 4H); 7,70 (d, IH); 7,85-8,17 (m, 3H); 8,47 (br s, IH).
Beispiel 111-22
2-Brom-N-[5-chlor-2-(2-naphthyloxy)phenyl]acetamid
Ausbeute: 77,9 % d.Th.
1H-NMR (200 MHz, CDC13): δ = 3,99 (s, 2H); 6,88 (d, IH); 7,06 (dd, IH); 7,21-7,36 (m, 2H); 7,38-7,57 (m, 2H); 1,68-1,19 (m, IH); 7,80-7,95 ( , 2H); 8,51 (d, IH); 8,85
(br s, IH).
Beispiel 111-23
N-[2,4-Bis(trifluormethyl)phenyl]-2-bromacetamid
Ausbeute: 28 % d.Th.
1H-NMR (200 MHz, CDC13): δ = 4,10 (s, 2H); 7,80-7,91 (m, 2H); 8,50 (d, IH); 8,80
(br s, IH).
Beispiel 111-24
2-Brom-N-(2-ethoxy- 1 -naphthyl)acetamid
Ausbeute: 24 % d.Th.
1H-NMR (300 MHz, CDC13): δ = 1,46 (t, 3H); 4,10-4,30 (m, 4H); 7,26-7,30 (d, IH);
7,36 (t, IH); 7,50 (t, IH); 7,70-7,87 (m, 3H); 8,07 (br s, IH).
Beispiel 111-25
2-Brom-N- {5-[(ethylsulfonyl)methyl]-l -naphthyl} acetamid
Ausbeute: 16 % d.Th.
1H-NMR (200 MHz, CDC13): δ = 1,37 (t, 3H); 1,54 (s, IH); 2,91 (q, 2H); 4,20 (s, 2H); 4,72 (s, 2H); 1,53-1,10 (m, 3H); 7,90-8, 11 (m, 3H); 8,65 (br s, IH).
Beispiel 111-26
2-Brom-N-[5-chlor-2-methyl-4-(trifluonnethoxy)phenyl]acetamid
Ausbeute: 84,0 % d.Th.
1H-NMR (200 MHz, CDCI3): δ = 2,35 (s, 3H); 4,08 (s, 2H); 7,18 (s, IH); 8,05-8,20
(m, 2H).
Beispiel 111-27
4-Methyl-l,3-oxazol-5-carbaldehydoxim
In 3 ml Wasser werden 0,50 g (4,50 mmol) 4-Methyl-l,3-oxazol-5-carbaldehyd [hergestellt aus dem entsprechendem Alkohol (Chem. Ber. 1961, 1248) durch Swern- Oxidation (Tetrahedron 34, 1651 (1978))] vorgelegt und mit 0,66 g (9,45 mmol) Hydroxylamin-Hydrochlorid in 2 ml Wasser versetzt. Anschließend werden 0,68 g (4,95 mmol) Kaliumcarbonat zugegeben. Nach 2 h wird abgesaugt, mit Wasser gewaschen und bei Raumtemperatur getrocknet. Die Ausbeute beträgt 0,41 g (72,2 % d.Th.).
1H-NMR (200 MHz, DMSO): δ = 2,21 (s, 3H); 8,20 (s, IH); 8,33 (s, IH); 11,48 (s, IH).
Beispiel 111-28
(4-Methyl-l,3-oxazol-5-yl)methylamin
4,00 g (31,72 mmol) 4-Methyl-l,3-oxazol-5-carbaldehydoxim werden in 70 ml Essigsäure vorgelegt. Bei Raumtemperatur gibt man in kleinen Portionen 47,70 g (729,50 mmol) Zinkstaub zu. Man lässt 2 Stunden bei Raumtemperatur rühren. Anschließend saugt man den Zinkstaub ab und wäscht diesen noch zweimal mit 50 ml Essigsäure. Das Filtrat wird im Vakuum vom Lösungsmittel befreit. Der
Rückstand wird so lange mit 20%-iger Natronlauge versetzt, bis ein pH- Wert von 11 erreicht ist. Dabei fällt ein weißer kristalliner Niederschlag aus. Dieser wird mit Essigsäureethylester ausgerührt und abgesaugt. Die vereinigten Filtrate werden im Vakuum vom Lösungsmittel befreit und der Rückstand chromatographisch gereinigt. Man erhält 1,34 g (38 % d.Th.) der Titelverbindung.
1H-NMR (300 MHz, CDC13): δ = 1,5 (s, 2H); 2,15 (s, 3H); 3,83 (s, 2H); 7,73 (s, IH).
Beispiel 111-29
2-[(4-Bromphenyl)thio]-2-ethyl-butansäure-l , 1 -dimethylethylester
Die Synthese erfolgte analog Beispiel II- 1 aus 4-Bromthiophenol und 2-Brom-2- ethyl-butansäure- 1,1 -dimethylethylester [Herstellung z.B. analog Liebigs Ann.
Chem. 725, 106-115 (1969); J. Am. Chem. Soc. 77, 946-947 (1955), und Bromie- rung mit N-Bromsuccinimid bzw. Brom analog z.B. Tetrahedron Lett. 1970, 3431; J. Org. Chem. 40, 3420 (1975)]. Ausbeute: 15,9 % d.Th. 1H-NMR (300 MHz, CDC13): δ = 0,96 (t, 6H); 1,58-1,74 (m, 4H); 7,28-7,35 (m, 2H);
7,39-7,46 (m, 2H).
Beispiel 111-30
2-Ethyl-2-[(4-formylphenyl)thio]-butansäure-l , 1 -dimethylethylester
Die Synthese erfolgte analog Beispiel II-2 ausgehend von Beispiel 111-29. Ausbeute: 70,4 % d.Th. 1H-NMR (300 MHz, CDC13): δ = 0,96 (t, 6H); 1,64-1,87 (m, 4H); 7,60 (d, 2H); 7,78
(d, 2H); 10,l (s, lH).
Beispiel 111-31 tert.-Butyl-2-ethyl-2-[(4-{[(2----urylmethyl)ammo]methyl}phenyl)-sulfanyl]butanoat
Die Synthese erfolgte analog Beispiel III- 13 ausgehend von Beispiel 111-30 und Furfurylamin. Ausbeute: 83,1 % d.Th.
1H-NMR (300 MHz, CDC13): δ = 0,93 (t, 6H); 1,43 (s, 9H); 1,60-1,75 (m, 4H); 3,78 (s, 4H); 6,18 (d, IH); 6,28-6,35 (m, IH); 7,25 (d, 2H); 7,35-7,38 (m, IH); 7,43 (d, 2H).
Beispiel 111-32 tert.-Butyl-2-methyl-2-[4-({[(4-methyl-l,3-oxazol-5-yl)methyl]amino}methyl)- phenoxy]-propanoat
1,25 g (4,73 mmol) tert.-Butyl-2-(4-formylphenoxy)-2-methylpropanoat (Beispiel I- 4) und 0,64 g (5,67 mmol) 4-Methyl-l,3-oxazol-5-yl)methylamin (Beispiel 111-28) werden zusammen in 1,2-Dichlorethan vorgelegt. Bei Raumtemperatur versetzt man mit 1,50 g (7,09 mmol) Natriumtriacetoxyborhydrid. Die Reaktionsmischung wird 4 Stunden bei Raumtemperatur gerührt. Anschließend versetzt man mit gesättigter
Natriumhydrogencarbonat-Lösung und extrahiert mit Essigsäureethylester. Die organische Phase wird über Magnesiumsulfat getrocknet und im Vakuum vom Lösungsmittel befreit. Der Rückstand wird chromatographisch an Kieselgel (Dichlormethan/Methanol 30:1) gereinigt und anschließend im Vakuum getrocknet. Man erhält 1 , 104 g (65 % d.Th.) der Titelverbindung.
1H-NMR (200 MHz, CDC13): δ = 1,45 (s, 9H); 1,55 (s, 6H); 2,11 (s, 3H); 3,70 (s, 2H); 3,77 (s, 2H); 6,70-6,90 (m, 2H); 7,10-7,20 (m, 2H); 7,29 (s, IH); 7.75 (br s, IH).
Analog der Vorschrift von Beispiel 111-32 wurden erhalten:
Beispiel 111-33 tert.-Butyl-2-(4-{[(2-methoxyethyl)amino]methyl}phenoxy)-2-methylpropanoat
Ausbeute: 92,8 % d.Th.
1H-NMR (300 MHz, CDC13): δ = 1,44 (s, 9H); 1,55 (s, 6H); 2,48 (br s, IH); 2,83 (t,
2H); 3,35 (s, 3H); 3,54 (t, 2H); 3,77 (s, 2H); 6,75-6,86 (m, 2H); 7,19 (d, 2H).
Beispiel 111-34 tert.-Butyl-2-methyl-2-[4-({[(5-methyl-2-füryl)methyl]amino}methyl)- phenoxy]propanoat
Ausbeute: 55,1 % d.Th.
1H-NMR (300 MHz, CDC13): δ = 1,44 (s, 9H); 1,55 (s, 6H); 2,27 (s, 3H); 3,71 (s,
4H); 5,83-5,92 (m, IH); 6,00-6,08 (m, IH); 6,75-6,88 (m, 2H); 7,12-7,24 (m, 2H).
Beispiel 111-35 tert.-Butyl-2-[(4-{[(2-methoxyethyl)amino]methyl}phenyl)-sulfanyl]-2- methylpropanoat
In 80 ml 1,2-Dichlorethan werden 4,00 g (14,27 mmol) tert.-Butyl-2-[(4- formylphenyl)sulfanyl]-2-methylpropanoat (Beispiel II-2) und 1,07 g (14,27 mmol) 2-Methoxyethylamin gelöst und nach 30 min. sowie nach 10 Stunden mit 4,54 g (21,40 mmol) Natriumtriacetoxyborhydrid versetzt. Nach DC-Kontrolle werden
Essigsäureethylester und gesättigte Natriumhydrogencarbonat-Lösung zugegeben und das Produkt mit Essigsäureethylester extrahiert. Die organische Phase wird mit IN HCl gewaschen, über Magnesiumsulfat getrocknet und nach Abdestilheren des Lösungsmittels durch Chromatographie an Kieselgel (Essigsäureethyl-ester/Cyclo- hexan 1 :1) gereinigt.
Ausbeute: 2,69 g (55,6 % d.Th.)
1H-NMR (300 MHz, CDC13): δ = 1,45 (s, 15 H); 2,96 (t, 2H); 3,37 (s, 3H); 3,72 (t,
2H); 4,13 (s, 2H); 7,52 (s, 4H).
Analog der Vorschrift von Beispiel 111-35 wurde erhalten:
Beispiel 111-36 tert.-Butyl-2-methyl-2- {[4-( {[(4-methyl- 1 ,3-oxazol-5-yl)methyl]amino}methyl)- phenyl] -sulfanyl} propanoat
1H-NMR (200 MHz, CDC13): δ = 1,43 (s, 15H); 2,12 (s, 3H); 3,77 (s, 2H); 3,78 (s,
2H); 7,22- 7,33 (m, 2H); 7,46 (d, 2H); 7,75 (s, IH).
Ausführungsbeispiele 3
Beispiel 3-1 tert. -Butyl 2-[4-[[[2-[(2,4-dimethylphenyl)amino]-2-oxoethyl](2-furanylmethyl)- amino]methyl]phenoxy]-2-methyl-propanoat
In 30 ml N,N-Dimethylformamid werden 0,50 g (1,25 mmol) der Verbindung aus
Beispiel 111-16 mit 0,23 g (1,88 mmol) 2,4-Dimethylanilin, 0,22 g (1,63 mmol) 1- Hydroxy-lH-benzotriazol, 0,31 g (1,63 mmol) EDCxHCl, 0,38 g (3,75 mmol) 4- Methylmorpholin und 0,01 g (0,08 mmol) 4-Dimethylaminopyridin 2 Stunden bei 0°C und über Nacht bei Raumtemperatur gerührt. Nach Versetzen mit Wasser und Extraktion mit Essigsäureethylester werden die organischen Phasen mit 1 N Salzsäure, Wasser, gesättigter Natriumhydrogencarbonat- und gesättigter Natriumchlorid- Lösung gewaschen und anschließend über Magnesiumsulfat getrocknet. Das Lösungsmittel wird abdestilliert und der Rückstand durch Flash-Chromatographie an Kieselgel (Cyclohexan Dichlorethan 2:1 -> Cyclohexan/Essigsäureethylester 10:1 -> 4:1) gereinigt. Umkristallisation aus n-Heptan ergibt die Zielverbindung in einer
Ausbeute von 78%. Schmelzpunkt: 90 - 91°C.
Beispiel 3-2 tert. -Butyl 2-[4-[[[2-[(2,4-dimethylphenyl)methylamino]-2-oxoethyl](2-furanyl- methyl)amino]methyl]phenoxy]-2-methyl-propanoat
Bei 0°C werden 0,51 g (1,00 mmol) der Verbindung aus Beispiel 3-1 und 0,04 g (1,10 mmol) Natriumhydrid 30 min gerührt, mit 0,07 ml (1,10 mmol) Iodmethan und anschließend mit Wasser versetzt. Nach Extraktion mit Essigsäureethylester wird mit
Wasser und gesättigter Natriumchlorid-Lösung gewaschen, über Magnesiumsulfat getrocknet, das Lösungsmittel abdestilliert und der Rückstand mit Flash-Chromatographie an Kieselgel (Cyclohexan/Dichlormethan 3:1 -> Dichloπnethan -> Dichlor- methan/Essigsäureeethylester 15:1) gereinigt. Umkristallisation aus n-Pentan ergibt die Zielverbindung in einer Ausbeute von 51 %.
Schmelzpunkt: 80 - 81°C.
Beispiel 3-3 tert. -Butyl 2-[4-[[[2-[(2,4-dimethylphenyl)amino]ethyl](2-furanylmethyl)-amino]- methyl]phenoxy]-2-methyl-propanoat
In 5 ml Toluol werden 0,25 g (0,50 mmol) der Verbindung aus Beispiel 3-1 mit 0,30 ml 2 M Boran-Dimethylsulfid-Lösung in Tetrahydrofuran versetzt und 2 Stunden bis zum Sieden erhitzt. Anschließend wird 1 Stunde in Gegenwart von 5 ml 2 N Natriumcarbonat-Lösung gerührt und die organische Phase mit Wasser sowie mit gesättigter Natriumchlorid-Lösung gewaschen. Nach Trocknen über Magnesiumsulfat und Abdestilheren des Lösungsmittels wird der Rückstand mit Hilfe von Flash-Chromatographie an Kieselgel (Cyclohexan/Dichlormethan 3:1 -> Cyclo- hexan/Essigsäureethylester 10:1) gereinigt. Dabei wird die Zielverbindung in einer Ausbeute von 37% erhalten. 1H-NMR (200 MHz, CDC1
3): δ = 1,43 (s, 9 H), 1,55 (s, 6 H), 2,15 (s, 3 H), 2,22 (s, 3
H), 2,73 - 2,87 (m, 2 H), 3,09 - 3,22 (m, 2 H); 3,57 (s, 2 H), 3,63 (s, 2 H), 6,12 - 6,19 (m, 1 H), 6,28 - 6,35 (m, 1 H), 6,47 (d, 1 H), 6,73 - 6,95 (m, 4 H), 7,20 (d, 1 H), 7,34 - 7,40 (m, I H). MS (ESI): 493 [M+H]4", 985 [2M+H]4".
Beispiel 3-4
2-[4-[[[2-[(2,4-Dimethylphenyl)amino]-2-oxoethyl](2-furanylmethyl)amino]- methyl]phenoxy]-2-methyl-propionsäure
In 35 ml Dichlormethan werden 7,09 g (14,00 mmol) der Verbindung aus Beispiel 3-1 zusammen mit 35 ml Trifluoressigsäure 2 Stunden bei Raumtemperatur gerührt. Nach Abdestilheren des Lösungsmittels wird der Rückstand in Essigsäureethylester gelöst, mit Wasser, 20proz. Natriumacetat- und gesättigter Natriumchlorid-Lösung gewaschen und anschließend über Magnesiumsulfat getrocknet. Der Rückstand wird nach Entfernen des Lösungsmittels mittels Flash-Chromatographie an Kieselgel (Di-
chlormethan -> Dichlormethan/Essigsäureethylester 5:1 -> 2:1 -> 1:1) gereinigt. Die Zielverbindung wird dabei in einer Ausbeute von 82% erhalten. 1H-NMR (200 MHz, CDC13): δ = 1,57 (s, 6 H), 2,24 (s, 3 H), 2,27 (s, 3 H), 3,31 (s, 2 H), 3,67 (s, 2 H), 3,75 (s, 2 H), 6,22 - 6,36 (m, 2 H), 6,88 (d, 2 H), 6,93 - 7,03 (m, 2 H), 7,23 (d, 2 H), 7,34 - 7,40 (m, 1 H), 7,78 (d, 1 H), 8,00 (breites s, 1 H), 9,09 (s, 1
H). MS (ESI): 451 [M+H]4", 901 [2M+H]4".
Analog der Vorschrift von Beispiel 3-4 werden erhalten:
Beispiel 3-5
2-[4-[[[2-[(2,4-Dimethylphenyl)methylamino]-2-oxoethyl](2-furanyhnethyl)amino]- methyl]phenoxy]-2-methyl-propionsäure
Ausbeute: 85%
1H-NMR (200 MHz, CDC13): δ = 1,46 (s, 6 H), 1,92 (s, 3 H), 2,24 (s, 3 H), 2,73 (q, 2 H), 3,00 (s, 3 H), 3,30 (breites s 1 H), 3,63 (d, 2 H), 3,78 (d, 2 H), 6,19 (d, 1 H), 6,30- 6,40 (m, 1 H), 6,74 (d, 2 H), 6,80 - 7,10 (m, 5 H), 7,52 - 7,57 (m, 1 H).
MS (ESI): 465 [M+H]4", 487 [M+Na .
Beispiel 3-6
2-[4-[[[2-[(2,4-Dimethylphenyl)ammo]ethyl](2-furanyh-nethyl)amino]-methyl]phen- oxy]-2-methyl-propionsäure
Ausbeute: 60%
1H-NMR (200 MHz, DMSO-d6): δ = 1,49 (s, 6 H), 2,01 (s, 3 H), 2,12 (s, 3 H), 2,55 - 2,72 (breites m,2 H), 2,97 - 3,20 (breites m, 2 H), 3,46 - 3,78 (m, 4 H), 4,40 (breites s, 1 H), 6,20 - 6,50 (m, 3 H), 6,68 - 6,88 (m, 4 H), 7,12 - 7,30 (m, 2 H), 7,56 - 7,68 (m, 1 H), 13,00 (breites s, 1 H). MS (ESI): 437 [M+H]+, 873 [2M+H]4".
Beispiel 3-7
2-[4-[[(2-Methoxyethyl)[2-[[4-(l-methylethyl)-2-(trifluormethyl)phenyl]amino]-2- oxoethyl] amino]methyl]phenoxy] -2-methyl-propionsäure- 1 , 1 -dimethylethylester
0,533 g (1,65 mmol) tert.-Butyl-2-(4-{[(2-methoxyethyl)amino]methyl}phenoxy)-2- methylpropanoat (Beispiel 111-33) werden in 6 ml Dimethylformamid vorgelegt. Bei Raumtemperatur versetzt man mit 0,588 g (1,81 mmol) 2-Brom-N-[4-isopropyl-2- (trifluormethyl)phenyl]acetamid (Beispiel 111-17) und 0,152 g (1,81 mmol) Natriumhydrogencarbonat. • Der Ansatz wird 2 Stunden bei 90°C gerührt.
Anschließend lässt man die Reaktionsmischung abkühlen und gibt Wasser hinzu. Man extrahiert einmal mit Essigsäureethylester und wäscht die organische Phase dann dreimal mit Wasser und einmal mit gesättigter Natriumchlorid-Lösung. Die
organische Phase wird über Natriumsulfat getrocknet und im Vakuum vom Lösungsmittel befreit. Der Rückstand wird chromatographisch an Kieselgel (Cyclohexan/Esssigsäureethylester 4:1) gereinigt und das Produkt anschließend im Vakuum getrocknet. Man erhält 0,885 g (95 % d.Th.) der Titelverbindung. 1H-NMR (400 MHz, CDC13): δ = 1.25 (d, 6H); 1.42 (s, 9H); 1.55 (s, 6H); 2.80 (t,
2H); 2.93 (sept, IH); 3.28 (s, 3H); 3.30 (s, 2H); 3.54 (t, 2H); 3.70 (s, 2H); 6.80 (d, 2H); 7.20 (d, 2H); 7.39 (dd, IH); 7.45 (d, IH); 8.17 (d, IH); 9.65 (br s, IH).
Beispiel 3-8 2-[4-[[(2-Methoxyethyl)[2-[[4-(l-methylethyl)-2-(trifluormethyl)phenyl]amino]-2- oxoethyl]amino]methyl]phenoxy]-2-methyl-propionsäure
0,842 g (1,49 mmol) der Verbindung aus Beispiel 3-7 werden in 10 ml
Dichlormethan vorgelegt. Bei Raumtemperatur gibt man 10 ml Trifluoressigsäure zu. Die Reaktionsmischung wird 2 Stunden bei Raumtemperatur gerührt. Anschließend wird der Ansatz im Vakuum einrotiert. Der Rückstand wird in Essigsäureethylester aufgenommen und mit Wasser, 20%-iger Natriumacetat-Lösung, Wasser und gesättigter Natriumchlorid-Lösung gewaschen. Die organische Phase wird über
Magnesiumsulfat getrocknet und im Vakuum vom Lösungsmittel befreit. Das Produkt wird chromatographisch an Kieselgel (Dichlormethan/Methanol 30:1) gereinigt und das Produkt anschließend im Vakuum getrocknet. Man erhält 0,648 g (85 % d.Th.) der Titelverbindung. 1H-NMR (200 MHz, CDC13): δ = 1.26 (d, 6H); 1.55 (s, 6H); 2.81 (t, 2H); 2.91 (sept.,
IH); 3.28 (s, 3H); 3.31 (s, 2H); 3.55 (t, 2H); 3.72 (s, 2H); 6.90 (d, 2H); 7.25 (d, 2H); 7.35-7.49 (m, 2H); 8.12 (d, IH); 9.62 (br s, IH).
Beispiel 3-9
2-[4-[[(2-Methoxyethyl)[2-[[4-(l-methylethyl)-2-(trifluormethyl)phenyl]amino]-2- oxoethyl]amino]methyl]phenoxy]-2-methyl-propionsäure-Hydrochlorid
0,4 g (0,78 mmol) der Verbindung aus Beispiel 3-7 werden in 4 ml Essigsäureethylester gelöst. Bei 40°C versetzt man zunächst mit 8 ml IN Salzsäure (in Diethylether) und anschließend mit 12 ml Diethylether. Dann lässt man den Ansatz eine Stunde bei 4°C stehen. Die ausgefallenen Kristalle werden abgesaugt und mit einer Mischung aus Essigsäureethylester und Diethylether (Verhältnis 1:1) gewaschen und anschließend 20 Stunden bei 40°C im Vakuum getrocknet. Man erhält 0,362 g (84,5 % d.Th.) der Titelverbindung. 1H-NMR (200 MHz, DMSO): δ = 1.22 (d, 6H); 1.55 (s, 6H); 2.94-3.08 (m, IH); 3.28 (s, 3H); 3.30-3.40 (m, 2H); 3.60-3.80 (m, 2H); 4.00-4.20 (m, 2H); 4.30-4.50 (m, 2H);
6.86 (d, 2H); 7.20-7.70 (m, 5H); 10.25 (br s, IH); 13.18 (br s, IH).
Beispiel 3-10 2-[4-[[[2-[(4-Cyclohexyl-2-methylphenyl)amino]-2-oxoethyl](2-methoxyethyl)- amino]methyl]phenoxy] -2-methyl-propionsäure- 1 , 1 -dimethylethylester
0,303 g (0,94 mmol) tert.-Butyl-2-(4-{[(2-methoxyethyl)amino]methyl}phenoxy)-2- methylpropanoat (Beispiel 111-33) werden in 5 ml Dimethylformamid vorgelegt. Bei Raumtemperatur versetzt man mit 0,319 g (1,03 mmol) 2-Brom-N-(4-cyclohexyl-2- methylphenyl)acetamid (Beispiel 111-19) und 0,086 g (1,03 mmol) Natriumhydrogencarbonat. Der Ansatz wird 2 Stunden bei 90°C gerührt. Anschließend lässt man die Reaktionsmischung abkühlen und gibt Wasser hinzu. Man extrahiert mit Essigsäureethylester und wäscht die organische Phase mit Wasser und gesättigter Natriumchlorid-Lösung. Die organische Phase wird über Natriumsulfat getrocknet und im Vakuum vom Lösungsmittel befreit. Der Rückstand wird chromatographisch an Kieselgel (Cyclohexan/Esssigsäureethylester 3:1) gereinigt und das Produkt im Vakuum getrocknet. Man erhält 0,464 g (90 % d.Th.) der Titelverbindung. 1H-NMR (300 MHz, CDC1
3): δ = 1.20-1.45 (m, 14H); 1.50 (s, 6H); 1.70-1.90 (m, 5H); 2.25 (s, 3H); 2.36-2.48 (m, IH); 2.80 (t, 2H); 3.25 (s, 5H); 3.5 (t, 2H); 3.69 (s, 2H); 6.80 (d, 2H); 6.98- 7.06 (m, 2H); 7.15-7.25 (m, 2H); 7.85 (d, IH); 9.25 (br s, IH).
Beispiel 3-11
2-[4-[[[2-[(4-Cyclohexyl-2-methylphenyl)amino]-2-oxoethyl](2-methoxyethyl)- amino]methyl]phenoxy]-2-methyl-propionsäure-Hydrochlorid
0,398 g (0,72 mmol) der Verbindung aus Beispiel 3-10 werden in 5 ml Dichlor- methan vorgelegt. Bei Raumtemperatur gibt man 5 ml Trifluoressigsäure zu. Die
Reaktionsmischung wird 2 Stunden bei Raumtemperatur gerührt. Anschließend wird der Ansatz im Vakuum einrotiert. Der Rückstand wird in Essigsäureethylester
aufgenommen und mit Wasser, 20%-iger Natriumacetat-Lösung, Wasser und gesättigter Natriumchlorid-Lösung gewaschen. Die organische Phase wird über Magnesiumsulfat getrocknet und im Vakuum vom Lösungsmittel befreit. Das Produkt wird chromatographisch an Kieselgel (Dichlormethan/Methanol 30:1) gereinigt. Der Rückstand wird unter Erwärmung in Dichlormethan gelöst, IN Salzsäure in Diethylether zugegeben und bis zur leichten Trübung n-Heptan zugetropft. Das Produkt wird abgesaugt, mit Diethylether gewaschen und im Vakuum bei 40°C getrocknet. Man erhält 0,187 g (49 % d.Th.) der Titelverbindung.
1H-NMR (300 MHz, CDC13): δ = 1.15-1.47 (m, 5H); 1.55 (s, 6H); 1.68-1.90 (m, 5H); 2.25 (s, 3H); 2.36-2.49 (m, IH); 2.85 (t, 2H); 3.28 (s, 3H); 3.30 (s, 2H); 3.52 (t, 2H); 3.12 (s, 2H); 6.87 (d, 2H); 6.99-7.10 (m, 2H); 7.25 (d, 2H); 7.80 (d, IH); 9.25 (br s, IH).
Die folgenden Verbindungen wurden analog zur Vorschrift der Beispiele 3-7 und 3- 10 erhalten:
Beispiel 3-12
2-[4-[[[2-[[2,4-Bis(trifluormethyl)phenyl]amino]-2-oxoethyl][(5-methyl-2-füranyl)- methyl]amino]methyl]phenoxy]-2-methyl-propionsäure- 1 , 1 -dimethylethylester
Ausbeute: 88 % d.Th.
1H-NMR (300 MHz, CDC13): δ = 1.40 (s, 9H); 1.55 (s, 6H); 2.15 (s, 3H); 3.30 (s, 2H); 3.65 (s, 4H); 5.85 (m, IH); 6.12 (d, IH); 6.81 (m, 2H); 7.20 ( , 2H); 7.25 (m, IH); 7.35 (s, IH); 8.57 (d, IH); 9.85 (br s, IH).
Beispiel 3-13
2-[[4-[[[2-[[5-Chlor-2-methyl-4-(trifluormethoxy)phenyl]amino]-2-oxoethyl][(4- methyl-5 -oxazolyl)methyl] amino]methyl]phenyl]thio] -2-methyl-propionsäure- 1 , 1 - dimethylethylester
Ausbeute: 80,2 % d.Th.
1H-NMR (300 MHz, CDC13): δ = 1,40 (s, 9H); 1,41 (s, 6H); 2,14 (s, 3H); 2,29 (s, 3H); 3,32 (s, 2H); 3,73 (s, 2H); 3,77 (s, 2H); 7,13 (s, IH); 7,23-7,31 (m, 2H); 7,49 (d, 2H); 7,78 (s, IH); 8,30 (s, IH); 9,05 (s, IH).
Beispiel 3-14
2-[[4-[[[2-[[5-Chlor-2-methyl-4-(trifluormethoxy)ρhenyl]amino]-2-oxoethyl](2- fiιranylmethyl)amino]methyl]phenyl]thio]-2 -methyl -propionsäure- 1 , 1 -dimethylethylester
1H-NMR (300 MHz, CDC13): δ = 1,39 (s, 9H); 1,41 (s, 6H); 2,30 (s, 3H); 3,31 (s, 2H); 3,74 (s, 4H); 6,28 (d, IH); 6,31-6,35 (m, IH); 7,12 (s, IH); 7,27 (d, 2H); 7,35- 7,38 (m, IH); 7,48 (d, 2H); 8,31 (s, IH); 9,19 (s, IH).
Beispiel 3-15
2-[[4-[[[2-[(2,4-Dimethylphenyl)amino]-2-oxoethyl](2-furanylmethyl)amino]- methyl]phenyl]thio]-2-ethyl-butansäure- 1 , 1 -dimethylethylester
Ausbeute: 73,4 % d.Th.
1H-NMR (200 MHz, CDC13): δ = 0,95 (t, 6H); 1,41 (s, 9H); 1,55-1,78 (m, 4H); 2,26 (s, 3H); 2,28 (s, 3H); 3,30 (s, 2H); 3,73 (s, 2H); 3,74 (s, 2H); 6,20-6,38 (m, 2H); 6,90-7,08 (m, 2H); 7,28 (d, 2H); 7,35-7,50 (m, 3H); 7,75-7,88 (m, IH); 9,05 (s, IH).
Beispiel 3-16
2-[[4-[[[2-[(4-Cyclohexyl-2-methylphenyl)amino]-2-oxoethyl](2-methoxyethyl)- amino]methyl]phenyl]thio] -2-methyl-propionsäure- 1 , 1 -dimethylethylester
1H-NMR (200 MHz, CDC13): δ = 1,31-1,47 (m, 18H); 1,70-1,95 (m, 6H); 2,20-2,31 (m, 4H); 2,35-2,51 ( , IH); 2,82 (t, 2H); 3,28 (s, 5H); 3,51 (t, 2H); 3,77 (s, 2H); 7,03 (d, 2H); 7,31 (d, 2H); 7,46 (d, 2H); 7,83 (d, IH); 9,24 (s, IH).
Beispiel 3-17
2-[[4-[[[2-[[4-(l,l-Dimethylethyl)-2-methylphenyl]amino]-2-oxoethyl](2-methoxy- ethyl)amino]methyl]phenyl]thio]-2-methyl-propionsäure-l,l-dimethylethylester
Ausbeute: 82,9 % d.Th.
1H-NMR (300 MHz, CDC13): δ = 1,29 (s, 12 H); 1,40 (s, 9H); 1,42 (s, 6H); 2,82 (t, 2H); 3,29 (s, 5H); 3,51 (t, 2H); 3,77 (s, 2H); 7,13-7,40 (m, 4H); 7,40-7,53 (m, 2H); 7,86 (d, IH); 9,26 (br s, IH).
Beispiel 3-18
2-[[4-[[[2-[[5-Chlor-2-methyl-4-(trifluormethoxy)phenyl]amino]-2-oxoethyl](2- furanylmethyl)amino]methyl]phenyl]thio]-2-ethyl-butansäure-l,l-dimethylethylester
1H-NMR (200 MHz, CDC13): δ = 0,94 (t, 6H); 1,41 (s, 9H); 1,55-1,75 (m, 4H); 2,30 (s, 3H); 3,31 (s, 2H); 3,73 (s, 2H); 3,75 (s, 2H); 6,24-6,38 (m, 2H); 7,12 (s, IH); 7,26 (d, 2H); 7,36 (d, IH); 7,44 (d, 2H); 8,31 (s, IH); 9,19 (s, IH).
Beispiel 3-19
2-[[4-[[[2-[[5-Chlor-2-methyl-4-(trifluormethoxy)phenyl]amino]-2-oxoethyl](2- methoxyethyl)amino]methyl]phenyl]thio]-2-methyl-propionsäure- 1 , 1 -dimethylethylester
Ausbeute: 57,4 % d.Th.
1H-NMR (300 MHz, CDC13): δ = 1,40 (s, 9H); 1,41 (s, 6H); 2,29 (s, 3H); 2,83 (t, 2H); 3,27 (s, 3H); 3,29 (s, 2H); 3,51 (t, 2H); 3,77 (s, 2H); 7,11 (s, IH); 7,30 (d, 2H); 7,46 (d, 2H); 8,29 (s, IH); 9,44 (s, IH).
Beispiel 3-20
2-Methyl-2-[4-[[[2-[[4-(l-methylethyl)-2-(trifluormethyl)phenyl]amino]-2- oxoethyl] [(5-methyl-2-fiιranyl)methyl]amino]methyl]phenoxy]-propionsäure-l , 1 - dimethylethylester
Ausbeute: 94 % d.Th.
1H-NMR (400 MHz, CDC13): δ = 1.25 (d, 6H); 1.40 (s, 9H); 1.55 (s, 6H); 2.17 (s, 3H); 2.88 (sept., IH); 3.25 (s, 2H); 3.15 (m, 4H); 5.85 (m, IH); 6.10 (d, IH); 6.81 (d, 2H); 7.21 (d, 2H); 7.35 (m, IH); 7.43 (m, IH); 8.15 (d, IH); 9.67 (s, IH).
Beispiel 3-21
2-[4-[[[2-[(2-Ethoxy- 1 -naphthalenyl)amino]-2-oxoethyl] [(5-methyl-2-ftιranyl)- methyl]amino]methyl]phenoxy]-2-methyl-propionsäure-lJ-dimethylethylester
Ausbeute: 95 % d.Th.
1H-NMR (200 MHz, CDC13): δ = 1,30 (t, 3H); 1,43 (s, 9H); 1,54 (s, 6H); 2,25 (s, 3H); 3,44 (s, 2H); 3,78-3,82 (m, 4H); 4,15 (q, 2H); 5,89-5,94 (m, IH); 6,15-6,18 (m,
IH); 6,84 (d, 2H); 7,20-7,38 (m, 4H); 7,45 (t, IH); 7,65 (d, IH); 7,75-7,85 (m, 2H); 9,05 (br s, IH).
Beispiel 3-22 2-Methyl-2-[4-[[[(5-methyl-2-furanyl)methyl] [2-oxo-2-[(5,6,7,8-tetrahydro-l - naphthalenyl)amino] ethyl] amino]methyl]phenoxy] -propionsäure- 1 , 1 -dimethylethylester
Ausbeute: 91 % d.Th.
1H-NMR (300 MHz, CDC13): δ = 1,40 (s, 9H); 1,55 (s, 6H); 1,70-1,95 (m, 4H); 2,20 (s, 3H); 2,65-2,82 (m, 4H); 3,24 (s, 2H); 3,67 (s, 4H); 5,86-5,90 (m, IH); 6,10-6,14 (d, IH); 6,78-6,93 (m, 3H); 7,08 (t, IH); 7,22 (d, 2H); 7,89 (d, IH); 9,20 (br s, IH).
Beispiel 3-23
2-[4-[[[2-[(2,4-Dichlorphenyl)amino]-2-oxoethyl](2-methoxyethyl)amino]methyl]- phenoxy]-2-methyl-propionsäure- 1 , 1 -dimethylethylester
Ausbeute: 87 % d.Th. 1H-NMR (300 MHz, CDC13): δ = 1.39 (s, 9H); 1.53 (s, 6H); 2.81 (t, 2H); 3.24 (s,
3H); 3.29 (s, 2H); 3.51 (t, 2H); 3.70 (s, 2H); 6.80 (m, 2H); 7.10-7.30 (m, 3H); 7.38 (d, IH); 8.42 (d, IH); 9.93 (br s, IH).
Beispiel 3-24 2-[4-[[(2-Methoxyethyl)[2-[[4-( 1 -naphthalenyloxy)-2-(trifluormethyl)phenyl]amino]-
2-oxoethyl] amino]methyl]ρhenoxy] -2-methy 1-propionsäure- 1 , 1 -dimethylethylester
Ausbeute: 95,5 % d.Th. 1H-NMR (300 MHz, CDC13): δ = 1.41 (s, 9H); 1.55 (s, 6H); 2.80 (t, 2H); 3.28 (s,
3H); 3.30 (s, 2H); 3.54 (t, 2H); 3.70 (s, 2H); 6.80 (d, 2H); 6.95 (d, IH); 7.13-7.25 (m, 3H); 7.34 (d, IH); 7.40 (t, IH); 7.47-7.58 (m, 2H); 7.66 (d, 1H); 7.89 (dd, IH); 8.07- 8.21 (m, 2H); 9.68 (br s, IH).
Beispiel 3-25
2-[4-[[[2-[[5-[(Ethylsulfonyl)methyl]-l-naphthalenyl]amino]-2-oxoethyl](2- methoxyethyl)amino]methyl]phenoxy]-2-methyl-propionsäure-l,l- dimethylethylester
Ausbeute: 91 % d.Th.
1H-NMR (200 MHz, CDC13): δ = 1.20-1.37 (m, 12H); 1.55 (s, 6H); 2.83-2.94 (m, 4H); 3.22 (s, 3H); 3.39 (s, 2H); 3.55 (t, 2H); 3.77 (s, 2H); 4.77 (s, 2H); 6.81 (d, 2H); 7.15-7.30 (m, 2H); 7.50-7.70 (m, 3H); 7.91 (d, IH); 8.12 (d, IH); 8.22 (d, IH); 10.18 (br s, IH).
Beispiel 3-26
2-Methyl-2-[4-[[[2-[[4-(l-methylethyl)-2-(trifluormethyl)phenyl]amino]-2- oxoethyl] [(4-methyl-5-oxazolyl)methyl] amino]methyl]phenoxy]-propionsäure- 1 , 1 - dimethylethylester
Ausbeute: 83,5 % d.Th.
1H-NMR (300 MHz, CDC13): δ = 1.25 (d, 6H); 1.40 (s, 9H); 1.55 (s, 6H); 2.10 (s, 3H); 2.85-3.00 (sept, IH); 3.28 (s, 2H); 3.66 (s, 2H); 3.75 (s, 2H); 6.82 (d, 2H); 7.20 (d, 2H); 7.38 (dd, IH); 7.40-7.45 (m, IH); 7.75 (s, IH); 8.14 (d, IH); 9.45 (br s, IH).
Beispiel 3-27
2-[4-[[[2-[[2,4-Bis(trifluormethyl)phenyl]amino]-2-oxoethyl][(4-methyl-5-oxazolyl)- methyl] amino]methyl]phenoxy] -2-methyl-propionsäure- 1 , 1 -dimethylethylester
Ausbeute: 79,5 % d.Th. 1H-NMR (300 MHz, CDC13): δ = 1.40 (s, 9H); 1.55 (s, 6H); 2.11 (s, 3H); 3.30 (s,
2H); 3.68 (s, 2H); 3.76 (s, 2H); 6.81 (d, 2H); 7.18 (d, 2H); 7.70-7.80 (m, 2H); 7.86 (s, IH); 8.56 (d, IH); 9.71 (br s, IH).
Beispiel 3-28
2-[4-[[[2-[[4-(lJ-Dimethylethyl)-2-methylphenyl]amino]-2-oxoethyl](2-methoxy- ethyl)amino]methyl]phenoxy]-2-methyl-propionsäure-l , 1 -dimethylethylester
Ausbeute: 81 % d.Th.
1H-NMR (300 MHz, CDC13): δ = 1.30 (s, 9H); 1.40 (s, 9H); 1.55 (s, 6H); 2.38 (s, 3H); 2.80 (t, 2H); 3.29 (s, 5H); 3.50 (t, 2H); 3J0 (s, 2H); 6.80 (d, 2H); 7.15-7.25 (m, 4H); 7.78 (d, IH); 9.30 (br s, IH).
Beispiel 3-29
2-[4-[[[2-[[2,4-Bis(trifluormethyl)phenyl]amino]-2-oxoethyl](2-methoxyethyl)- amino]methyl]phenoxy] -2-methyl-propionsäure- 1 , 1 -dimethylethylester
Ausbeute: 80 % d.Th.
1H-NMR (300 MHz, CDC13): δ = 1,39 (s, 9H); 1,55 (s, 6H); 2,82 (t, 2H); 3,28 (s, 3H); 3,33 (s, 2H); 3,52 (t, 2H); 3,71 (s, 2H); 6,80 (d, 2H); 7,18 (d, 2H); 7,78 (d, IH); 7,84 (s, IH); 8,60 (d, IH); 9,98 (br s, IH).
Beispiel 3-30
2-[4-[[[2-[[2,4-Bis(trifluormethyl)phenyl]amino]-2-oxoethyl](2-furanylmethyl)- amino]methyl]phenoxy]-2-methyl-propionsäure- 1 , 1 -dimethylethylester
Ausbeute: 84 % d.Th.
1H-NMR (300 MHz, CDC13): δ = 1,40 (s, 9H); 1,55 (s, 6H); 3,30 (s, 2H); 3,65 (s, 2H); 3,75 (s, 2H); 6,20-6,30 (m, IH); 6,30-6,38 (m, IH); 6,82 (d, 2H); 7,18 (d, 2H); 7,36-7,39 (m, IH); 7,75 (d, IH); 7,90 (s, IH); 8,60 (d, IH); 9,82 (br s, IH).
Beispiel 3-31
2-[[4-[[[2-[[2,4-Bis(trifluormethyl)phenyl]amino]-2-oxoethyl](2-furanylmethyl)- amino]methyl]phenyl]thio]-2-methyl-ρropionsäure- 1 , 1 -dimethylethylester
1H-NMR (300 MHz, CDC13): δ = 1,40 (s, 9H); 1,45 (s, 6H); 3,31 (s, 2H); 3,74-3,80 (m, 4H); 6,25 (d, IH); 6,30-6,38 (m, IH); 7,22-7,40 (m, 3H); 7,50 (d, 2H); 7,78 (d, IH); 7,90 (s, IH); 8,61 (d, IH); 9,78 (br s, IH).
Die folgenden Verbindungen wurden analog zur Vorschrift des Beispiels 3-8 erhalten:
Beispiel 3-32 2-[4-[[[2-[[2,4-Bis(trifluormethyl)phenyl]amino]-2-oxoethyl] [(5-methyl-2-furanyl)- methyl]amino]methyl]phenoxy]-2-methyl-propionsäure
Ausbeute: 83,4 % d.Th.
1H-NMR (300 MHz, CDCI3): δ = 1,56 (s, 6H); 2,15 (s, 3H); 3,29 (s, 2H); 3,69 (s, 2H); 3,71 (s, 2H); 5,80-5,88 (m, IH); 6,13 (d, IH); 6,89-6,98 (m, 2H); 7,20-7,35 (m, 2H); 7,74 (d, IH); 7,86 (s, IH); 8,56 (d, IH); 9,79 (s, IH).
Beispiel 3-33
2-[[4-[[[2-[[5-Chlor-2-methyl-4-(trifluormethoxy)phenyl]amino]-2-oxoethyl][(4- methyl-5-oxazolyl)methyl]amino]methyl]phenyl]thio]-2-methyl-propionsäure
Ausbeute: 62,8 % d.Th.
1H-NMR (200 MHz, CDC13): δ = 1,47 (s, 6H); 2,11 (s, 3H); 2,28 (s, 3H); 3,35 (s, 2H); 3,74 (s, 2H); 3,77 (s, 2H); 7,11 (s, IH); 7,20-7,30 (m, 2H); 7,49 (d, 2H); 7,80 (s, IH); 8,28 (s, IH); 9,04 (s, IH).
Beispiel 3-34
2-[[4-[[[2-[[5-Chlor-2-methyl-4-(trifluormethoxy)phenyl]amino]-2-oxoethyl](2- furanylmethyl)amino]methyl]phenyl]thio]-2-methyl-propionsäure
Ausbeute: 90,9 % d.Th. 1H-NMR (300 MHz, CDC13): δ = 1,46 (s, 6H); 2,28 (s, 3H); 3,32 (s, 2H); 3,75 (s,
4H); 6,30 (dd, 2H); 7,10 (s, IH); 7,29 (d, 2H); 7,36 (d, IH); 7,48 (d, 2H); 8,27 (s, IH); 9,16 (s, IH).
Beispiel 3-35 2-[[4-[[[2-[(2,4-Dimethylphenyl)amino]-2-oxoethyl](2-füranylmethyl)amino]- methyl]phenyl]thio]-2-ethyl-butansäure
Ausbeute: 96,6 % d.Th.
1H-NMR (300 MHz, CDC13): δ = 0,97 (t, 6H); 1,60-1,90 (m, 4H); 2,25 (s, 3H); 2,28 (s, 3H); 3,31 (s, 2H); 3,73 (s, 2H); 3,74 (s, 2H); 6,26 (d, IH); 6,29-6,35 (m, IH);
6,95-7,05 (m, 2H); 7,29 (d, 2H); 7,37 (d, IH); 7,46 (d, 2H); 7,80 (d, IH); 9,03 (s, IH).
Beispiel 3-36 2-[[4-[[[2-[[5-Chlor-2-methyl-4-(trifluormethoxy)phenyl]amino]-2-oxoethyl](2- fiιranylmethyl)amino]methyl]phenyl]thio]-2-ethyl-butansäure
Ausbeute: 90,9 % d.Th.
1H-NMR (300 MHz, CDC13): δ = 0,96 (t, 6 H); 1,58-1,87 (m, 4H); 2,28 (s, 3H); 3,31 (s, 2H); 3,73 (s, 2H); 3,76 (s, 2H); 6,26 (d, IH); 6,30-6,36 (m, IH); 7,10 (s, IH); 7,27 (d, 2H); 7,34- 7,40 (m, IH); 7,45 (d, 2H); 8,28 (s, IH); 9,16 (s, IH).
Beispiel 3-37
2-[[4-[[[2-[[5-Chlor-2-methyl-4-(trifluormethoxy)phenyl]ammo]-2-oxoethyl](2- methoxyethyl)amino]methyl]phenyl]thio]-2-methyl-ρropionsäure
Ausbeute: 83,9 % d.Th. 1H-NMR (200 MHz, CDC13): δ = 1,46 (s, 6H); 2,27 (s, 3H); 2,84 (t, 2H); 3,27 (s,
3H); 3,31 (s, 2H); 3,50 (t, 2H); 3,77 (s, 2H); 7,10 (br s, IH); 7,31 (d, 2H); 7,48 (d, 2H); 8,24 (s, IH); 9,43 (s, IH).
Beispiel 3-38 2-Methyl-2-[4-[[[2-[[4-(l-methylethyl)-2-(trif!uormethyl)phenyl]amino]-2- oxoethyl][(5-methyl-2-furanyl)methyl]amino]methyl]phenoxy]-propionsäure
Ausbeute: 91 % d.Th.
1H-NMR (200 MHz, CDC13): δ = 1.25 (d, 6H); 1.55 (s, 6H); 2.17 (s, 3H); 2.91 (sept, IH); 3.28 (s, 2H); 3.1 (s, 4H); 5.80-5.90 (m, IH); 6.13 (d, IH); 6.90 (m, 2H); 7.17- 7.30 (m, 2H); 7.32- 7.47 (m, 2H); 8.12 (d, IH); 9.55 (br s, IH).
Beispiel 3-39
2-[4-[[[2-[(2-Ethoxy-l-naphthalenyl)amino]-2-oxoethyl][(5-methyl-2-furanyl)- methyl]amino]methyl]phenoxy]-2-methyl-propionsäure
Ausbeute: 64 % d.Th.
1H-NMR (300 MHz, CDC13): δ = 1.25-1.32 (t, 3H); 1.60 (s, 3H); 2.25 (s, 3H); 3.45 (s, 2H); 3.82 (s, 4H); 4.15 (quart., 2H); 5.94 (m, IH); 6.17 (d, IH); 6.90-7.00 (m, 2H); 7.23-7.46 (m, 5H); 7.60-7.70 (m, IH); 7.75-7.80 (m, 2H); 9.05 (br s, IH).
Beispiel 3-40
2-Methyl-2-[4-[[[(5-methyl-2-füranyl)-methyl][2-oxo-2-[(5,6J,8-tetrahydro-l- naphthalenyl)amino]ethyl]amino]methyl]phenoxy]-propionsäure
Ausbeute: 76 % d.Th.
1H-NMR (300 MHz, CDC13): δ = 1.55 (s, 6H); 1.75-1.95 ( , 4H); 2.20 (s, 3H); 2.36 (t, 2H); 2.78 (t, 2H); 3.30 (s, 2H); 3.69 (s, 4H); 5.89 (m, IH); 6.12 (d, IH); 6.83-6.94 (m, 4H); 7.09 (t, IH); 7.20-7.32 (m, IH); 7.85 (d, IH); 9.15 (s, IH).
Beispiel 3-41
2-[4-[[[2-[(2,4-Dichlorphenyl)amino]-2-oxoethyl](2-methoxyethyl)ammo]methyl]- phenoxy]-2-methyl-propionsäure
Ausbeute: 69 % d.Th.
1H-NMR (300 MHz, CDC13): δ = 1.55 (s, 6H); 2.82 (t, 2H); 3.28 (s, 3H); 3.00 (s, 2H); 3.54 (t, 2H); 3.75 (s, 2H); 6.90 (m, 2H); 7.18-7.36 (m, 3H); 7.39 (d, IH); 8.40 (d, IH); 9.90 (br s, IH).
Beispiel 3-42
2-[4-[[(2-Methoxyethyl)[2-[[4-(l-naphthalenyloxy)-2-(trifluormethyl)phenyl]amino]- 2-oxoethyl]amino]methyl]phenoxy]-2-methyl-propionsäure
Ausbeute: 74 % d.Th.
1H-NMR (300 MHz, DMSO): δ = 1.45 (s, 6H); 2.72 (t, 2H); 3.18 (s, 3H); 3.25 (s, 2H); 3.47 (t, 2H); 3.68 (s, 2H); 6.78 (d, 2H); 7.10 (d, IH); 7.21 (d, 2H); 7.28 (dd,
IH); 7.40 (d, IH); 7.48-7.66 (m, 3H); 7.80 (d, IH); 7.90 (d, IH); 8.05 (t, 2H); 9.60 (br s, IH).
Beispiel 3-43
2-[4-[[[2-[[5-[(Ethylsulfonyl)methyl]-l-naphthalenyl]amino]-2-oxoethyl](2- methoxyethyl)amino]methyl]phenoxy]-2-methyl-propionsäure
Ausbeute: 40,5 % d.Th.
1H-NMR (400 MHz, CD2C12): δ = 1,34 (t, 3H); 1,46 (s, 6H); 2,83-3,04 (m, 4H); 3,24 (s, 3H); 3,37 (s, 2H); 3,32-3,64 (m, 2H); 3,78 (s, 2H); 4,72 (s, 2H); 6,83 (d, 2H); 7,31 (d, 2H); 7,46-7,65 (m, 3H); 7,90 (d, IH); 8,04-8,20 (m, 2H); 10,10 (br s, IH).
Beispiel 3-44
2-Methyl-2-[4-[[[2-[[4-(l-methylethyl)-2-(trifluormethyl)phenyl]amino]-2- oxoethyl][(4-methyl-5-oxazolyl)methyl]amino]methyl]phenoxy]-propionsäure
Ausbeute: 69 % d.Th.
1H-NMR (200 MHz, CDC13): δ = 1.25 (d, 6H); 1.58 (s, 6H); 2.09 (s, 3H); 2.82-3.04 (sept, IH); 3.30 (s, 2H); 3.66 (s, 2H); 3.76 (s, 2H); 6.90 (d, 2H); 7.25 (d, 2H); 7.35- 7.48 (m, 2H); 7.80 (s, IH); 8.11 (d, IH); 9.40 (br s, IH).
Beispiel 3-45
2-[4-[[[2-[[2,4-Bis(trifluormethyl)phenyl]amino]-2-oxoethyl][(4-methyl-5- oxazolyl)methyl]amino]methyl]phenoxy]-2-methyl-propionsäure
Ausbeute: 76 % d.Th.
1H-NMR (200 MHz, CDC13): δ = 1.60 (s, 6H); 2.10 (s, 3H); 3.32 (s, 2H); 3.70 (s,
2H); 3.11 (s, 2H); 6.90 (d, 2H); 7.21 (d, 2H); 1.13-1.90 (m, 3H); 8.55 (d, IH); 9.68
(br s, lH).
Beispiel 3-46
2-[4-[[[2-[[2,4-Bis(trifluormethyl)phenyl]amino]-2-oxoethyl](2-methoxyethyl)- amino]methyl]phenoxy]-2-methyl-propionsäure
Ausbeute: 77 % d.Th.
1H-NMR (300 MHz, CDC13): δ = 1.55 (s, 6H); 2.84 (t, 2H); 3.25 (s, 3H); 3.35 (s, 2H); 3.55 (t, 2H); 3.75 (s, 2H); 6.90 (d, 2H); 7.15-7.30 (m, 2H); 7.75 (d, IH); 7.88 (s, IH); 8.59 (d, IH); 9.91 (br s, IH).
Beispiel 3-47
2-[4-[[[2-[[2,4-Bis(trifluormethyl)phenyl]amino]-2-oxoethyl](2-furanylmethyl)- amino]methyl]phenoxy]-2-methyl-propionsäure
Ausbeute: 91 % d.Th.
1H-NMR (300 MHz, CDC13): δ = 1,57 (s, 6H); 3,30 (s, 2H); 3,70 (s, 2H); 3,77 (s, 2H); 6,30 (dd, 2H); 6,88 (d, 2H); 7,20-7,35 (m, 2H); 7,37-7,42 (m, IH); 7,75 (d, IH); 7,86 (s, IH); 8,56 (d, IH); 9,80 (br s, IH).
Beispiel 3-48
2-[[4-[[[2-[[2,4-Bis(trifluormethyl)phenyl]amino]-2-oxoethyl](2-furanylmethyl)- amino]methyl]phenyl]thio]-2-methyl-propionsäure
Ausbeute: 91 % d.Th.
1H-NMR (300 MHz, CDC13): δ = 1,46 (s, 6H); 3,32 (s, 2H); 3,75 (s, 4H); 6,25 (dd, 2H); 7,20-7,40 (m, 3H); 7,50 (d, 2H); 7,78 (d, IH); 7,90 (s, IH); 8,59 (d, IH); 9,78 (br s, IH).
Die folgenden Verbindungen wurden analog zur Vorschrift der Beispiele 3-9 und 3- 11 erhalten:
Beispiel 3-49
2-[[4-[[[2-[(4-Cyclohexyl-2-methylρhenyl)amino]-2-oxoethyl](2-methoxyethyl)- amino]methyl]phenyl]thio]-2-methyl-propionsäure-Hydrochlorid
Ausbeute: 53,3 % d.Th.
1H-NMR (300 MHz, DMSO): δ = 1,20-1,48 (m, 12H); 1,62-1,87 (m, 5H); 2,14 (s, 3H); 3,27 (s, 3H); 3,51 (br s, 2H); 3,74 (br s, 2H); 4,12 (br s, 2H); 4,51 (br s, 2H); 7,02 (d, 2H); 7,16- 7,30 (br s, IH); 7,46-7,68 (m, 4H); 9,93 (br s, IH); 10,36 (br s, IH); 12,74 (br s, IH).
Beispiel 3-50
2-[[4-[[[2-[[4-(l , 1 -Dimethylethyl)-2-methylphenyl]amino]-2-oxoethyl](2- methoxyethyl)amino]methyl]phenyl]thio]-2-methyl-propionsäure-Hydrochlorid
Ausbeute: 85,3 % d.Th.
1H-NMR (300 MHz, CDC13): δ = 1,29 (s, 9H); 1,56 (s, 6H); 2,26 (s, 3H); 2,86 (t, 2H); 3,29 (s, 3H); 3,35 (s, 2H); 3,53 (t, 2H); 3,74 (s, 2H); 6,88 (d, 2H); 7,15-7,26 (m, 4H); 7,79 (d, IH); 9,26 (s, IH).
Beispiel 3-51
2-Methyl-2-[4-[[[2-[[4-(l-methylethyl)-2-(trifluormethyl)phenyl]amino]-2- oxoethyl][(5-methyl-2-furanyl)methyl]amino]methyl]phenoxy]-propionsäure-
Hydrochlorid
Ausbeute: 99 % d.Th.
1H-NMR (300 MHz, DMSO): δ - 1.20 (d, 6H); 1.50 (s, 6H); 2.27 (br s, 3H); 2.96- 3.05 (sept., IH); 3.95 (br s, 2H); 4.31 (br s, 4H); 6.17 (br s, IH); 6.63 (br s, IH); 6.85 (d, 2H); 7.46-7.57 (m, 5H); 10.23 (br s, IH); 10.55 (br s, IH); 13.15 (br s, IH).
Beispiel 3-52
2-[4-[[[2-[[4-(l,l-Dimethylethyl)-2-methylphenyl]amino]-2-oxoethyl](2- methoxyethyl)amino]methyl]phenoxy]-2-methyl-propionsäure-Hydrochlorid
x HCI
Ausbeute: 54 % d.Th. LC-MS: 470 [M
+]
Beispiel 3-53 2-[4-[[[2-[(2,4-Dimethylphenyl)amino]-2-oxoethyl](2-füranylmethyl)amino]- methyl]phenoxy]-2-methyl-propionsäure-Natriumsalz
0,015 g (0,03 mmol) der Verbindung aus Beispiel 3-4 werden in 0,5 ml Ethanol gelöst und mit 0,3 ml IN Natronlauge versetzt. Man rührt den Ansatz 5 min. nach und rotiert die Reaktionsmischung dann ein. Der Rückstand wird in wenig Toluol aufgenommen und das Lösungsmittel im Vakuum entfernt. Dann wird das Produkt 20 Stunden im Vakuum getrocknet. Man erhält 0,015 g (95,5 % d.Th.) der Titelverbindung.
1H-NMR (200 MHz, CDC13): δ = 1.21 (s, 6H); 2J0-2.20 (m, 6H); 3.16 (s, 2H); 3.58- 3.64 (m, 4H); 6.18-6.25 (m, 2H); 6.73-6.82 (m, 2H); 7.09-7.35 (m, 3H); 7.71 (d, IH); 9.00 (br s, IH).
Die folgenden Verbindungen wurden analog zur Vorschrift der Beispiele 3-7 und 3-
10 erhalten:
Beispiel 3-54
2-[[4-[[[2-[[4-(l-Methylethyl)-2-(trifluormethyl)phenyl]amino]-2-oxoethyl](2- methoxyethyl)amino]metlιyl]phenyl]thio]-2-methyl-propionsäure-l,l- dimethylethylester
Ausbeute: 61 % d.Th.
1H-NMR (200 MHz, CDC13): δ = 1,24 (d, 6H); 1,39 (s, 9H); 1,42 (s, 6H); 2,80 (t, 2H); 2,90-3,1 (m, IH); 3,28 (s, 3H); 3,32 (s, 2H); 3,53 (t, 2H); 3,78 (s, 2H); 7,25- 7,50 (m, 6H); 8,14 (d, IH); 9,62 (br s, IH).
Beispiel 3-55
2-Methyl-2-[[4-[[[2-[[4-(l-methylethyl)-2-(trifluormethyl)phenyl]amino]-2-oxo- ethyl][(4-methyl-5-oxazolyl)methyl]amino]methyl]phenyl]thio]-propionsäure-l,l- dimethylethylester
Ausbeute: 66 % d.Th.
1H-NMR (300 MHz, CDC13): δ = 1,25 (d, 6H); 1,40 (s, 9H); 1,43 (s, 6H); 2,10 (s, 3H); 2,90-3,10 (m, IH); 3,29 (s, 2H); 3,70-3,80 (m, 4H); 7,30-7,55 (m, 6H); 7,77 (s, IH); 8,13 (d, IH); 9,40 (br s, IH).
Beispiel 3-56
2-[[4-[[[2-[(2-Methyl-4-methoxyphenyl)amino]-2-oxoethyl][(4-methyl-5-oxazolyl)- methyl]amino]methyl]phenyl]thio]-2-methyl-propionsäure-l,l-dimethylethylester
Ausbeute: 86 % d.Th.
1H-NMR (200 MHz, CDC13): δ - 1,41 (s, 9H); 1,43 (s, 9H); 2,13 (s, 3H); 2,24 (s, 3H); 3,31 (s, 2H); 3,70-3,81 (m, 7H); 6,68-6,80 (m, 2H); 7,30 (d, 2H); 7,50 (d, 2H); 1,61-1,15 (m, IH); 7,78 (s, IH); 8,80 (br s, IH).
Beispiel 3-57
2-[[4-[[[2-[[2,4-Bis(trifluormethyl)phenyl]amino]-2-oxoethyl][(4-methyl-5- oxazolyl)methyl]amino]methyl]phenyl]thio]-2-methyl-propionsäure-lJ-dimethyl- ethylester
Ausbeute: 84 % d.Th.
1H-NMR (200 MHz, CDC13): δ = 1,40 (s, 9H); 1,42 (s, 6H); 2,1 l(s, 3H); 3,32 (s, 2H); 3,74-3,82 (m, 4H); 7,29 (d, 2H); 7,49 (d, 2H); 7,70-7,85 (m, 2H); 7,87 (s, IH); 8,57 (d, IH); 9,67 (br s, IH).
Beispiel 3-58
2-[4-[[[2-[(4-Cyclohexyl-2-methylphenyl)amino]-2-oxoethyl][(4-methyl-5-oxazolyl)- methyl] amino]methyl]phenoxy] -2-methyl-propionsäure- 1 , 1 -dimethylethylester
Ausbeute: 54,8 % d.Th.
1H-NMR (200 MHz, CDC13): δ = 1.30-1.46 (m, 14 H); 1,55 (s, 6H); 1.62-1.94 (m, 6H); 2.12 (s, 3H); 2.26 (s, 3H); 3.29 (s, 2H); 3.65 (s, 2H); 3.74 (s, 2H); 6.82 (d, 2H); 6.98-7.08 ( , 2H); 7.18 (d, 2H); 7.77 (s, IH); 7.83 (d, IH); 8.96 (br s, IH).
Beispiel 3-59
2-[4-[[[2-[[4-(lJ-Dimethylethyl)-2-methylphenyl]amino]-2-oxoethyl][(4-methyl-5- oxazolyl)methyl]amino]methyl]phenoxy]-2-methyl-propionsäure- 1 , 1 -dimethylethylester
Ausbeute: 64,7 % d.Th.
1H-NMR (200 MHz, CDC13): δ = 1.29 (s, 9H); 1.41 (s, 9H); 1.55 (s, 6H); 2.12 (s, 3H); 2.28 (s, 3H); 3.29 (s, 2H); 3.65 (s, 2H); 3.75 (s, 2H); 6.82 (d, 2H); 7.10-7.30 (m, 4H); 7.77 (s, IH); 7.85 (d, IH); 8.98 (br s, IH).
Beispiel 3-60
2-[[4-[[[2-[[4-(l-Methylethyl)-2-(trifluormethyl)phenyl]amino]-2-oxoethyl](2- methoxyethyl)amino]methyl]phenyl]thio]-2-methyl-propionsäure
0,248 g (0,43 mmol) der Verbindung aus Beispiel 3-54 werden in 5 ml Dichlormethan vorgelegt. Bei Raumtemperatur gibt man 5 ml Trifluoressigsäure zu. Die Reaktionsmischung wird 2 Stunden bei Raumtemperatur gerührt. Anschließend wird der Ansatz im Vakuum einrotiert. Der Rückstand wird in Essigsäureethylester aufgenommen und mit Wasser, 20%-iger Natriumacetat-Lösung, Wasser und gesättigter Natriumchlorid-Lösung extrahiert. Die organische Phase wird über Magnesiumsulfat getrocknet und im Vakuum vom Lösungsmittel befreit. Das Produkt wird chromatographisch an Kieselgel (Dichlormethan, Dichlormethan/Methanol 30:1) gereinigt und anschließend im Vakuum getrocknet. Man erhält 197 mg (88% d.Th.) der Titelverbindung.
1H-NMR (200 MHz, CDC13): δ = 1.25 (d, 6H); 1.49 (s, 6H); 2.80 (t, 2H); 2.85-3.00 (m, IH); 3.30 (s, 3H); 3.32 (s, 2H); 3.49-3.59 (m, 2H); 3.80 (s, 2H); 7.24-7.53 (m, 6H); 8.12 (d, IH); 9.58 (br s, IH).
Die folgenden Verbindungen wurden analog zur Vorschrift des Beispiels 3-60 erhalten:
Beispiel 3-61
2-Methyl-2-[[4-[[[2-[[4-(l-methylethyl)-2-(trifluormethyl)phenyl]amino]-2-oxo- ethyl][(4-methyl-5-oxazolyl)methyl]amino]methyl]phenyl]thio]-propionsäure
Ausbeute: 81 % d.Th.
1H-NMR (300 MHz, CDC13): δ = 1,25 (d, 6H); 1,50 (s, 6H); 2,07 (s, 3H); 2,85-3,00 (m, IH); 3,39 (s, 2H); 3,74-3,78 (m, 4H); 7,30 (d, 2H); 7,36-7,53 (m, 4H); 7,79 (s, IH); 8,11 (d, IH); 9,39 (br s, IH).
Beispiel 3-62
2-[[4-[[[2-[(2-Methyl-4-methoxyphenyl)amino]-2-oxoethyl][(4-methyl-5-oxazolyl)- methyl]amino]methyl]phenyl]thio]-2-methyl-propionsäure
Ausbeute: 84 % d.Th.
1H-NMR (200 MHz, CDC13): δ = 1,51 (s, 6H); 2,08 (s, 3H); 2,23 (s, 3H); 3,35 (s, 2H); 3,70-3,82 (m, 7H); 6,70-6,80 (m, 2H); 7,28 (d, 2H); 7,48 (d, 2H); 7,63-7,73 (m, IH); 7,80 (s, IH); 8,81 (br s, IH).
Beispiel 3-63
2-[[4-[[[2-[[2,4-Bis(trifluormethyl)ρhenyl]amino]-2-oxoethyl][(4-methyl-5- oxazolyl)methyl]amino]methyl]phenyl]thio]-2-methyl-propionsäure
Ausbeute: 76 % d.Th.
1H-NMR (300 MHz, CDC13): δ = 1,49 (s, 6H); 2,09 (s, 3H); 3,35 (s, 2H); 3,74-3,80 (m, 4H); 7,29 (d, 2H); 7,49 (d, 2H); 1,15-1,82 (m, 2H); 7,87 (s, IH); 8,56 (d, IH); 9,66 (br s, IH).
Beispiel 3-64
2-[4-[[[2-[(4-Cyclohexyl-2-methylphenyl)amino]-2-oxoethyl][(4-methyl-5-oxazolyl)- methyl]amino]methyl]phenoxy]-2-methyl-propionsäure
Ausbeute: 80 % d.Th. LC-MS: Acetonitril / 30% wässr. HCl Wasser (Gradient): Rt = 2.64 min ([M+H]4
534).
Beispiel 3-65
2-[4-[[[2-[[4-(l,l-Dimethylethyl)-2-methylphenyl]amino]-2-oxoethyl][(4-methyl-5- oxazolyl)methyl] amino]methyl]phenoxy] -2-methy 1-propionsäure
Ausbeute: 80 % d.Th.
LC-MS: Acetonitril / 30%wässr. HCl/Wasser (Gradient): R = 2.43 min ([M+H]4
508).
Ausführungsbeispiele 4
Beispiel 4-1
2-[4-[[[2-[(2,5-Dimethylphenyl)amino]-2-oxoethyl](2-füranylmethyl)amino]methyl]- phenoxy]-2-methyl-propansäure
Stufe a)
Wang-Harz (Fa. Rapp Polymere, Best.-Nr. H 1011) (48,0 g, 14,06 mmol reaktive Gruppen) wird in Dichlormethan suspendiert. Nach der Zugabe von 2-(4-Formyl-
phenoxy)-2-methyl-propionsäure [GJ. Ellymes, C. Glynis, J. Chem. Soc. Perkin Trans. 2, 1993, 43-48] (8,78 g, 42,18 mmol), Diisopropylcarbodiimid (10,65 g, 84,35 mmol) und DMAP (3,44 g, 28,12 mmol) wird die Mischung 18 h bei Raumtemperatur geschüttelt. Anschließend wird die Mischung filtriert, das Harz mit Dichlor- methan, DMF und Methanol gewaschen und Harz A erhalten.
Stufe b)
Harz A (2,50 g, 0,72 mmol reaktive Gruppen) und 2-Furfürylamin (352 mg, 3,62 mmol) werden in 20 ml Trimethylorthoformiat suspendiert. Die Mischung wird 20 h bei Raumtemperatur geschüttelt, dann filtriert und das Harz mit DMF gewaschen.
Anschließend wird das Harz in 20 ml DMF suspendiert, mit Tetrabutylammonium- borhydrid (559 mg, 2,17 mmol) und Essigsäure (0,42 ml, 7,25 mmol) versetzt und 7 h bei Raumtemperatur geschüttelt. Anschließend wird die Mischung filtriert, das Harz mit Dichlormethan, DMF und Methanol gewaschen und Harz Bl erhalten.
Stufe c)
Harz Bl (2,5 g, 0,72 mmol reaktive Gruppen) wird in 40 ml Dioxan suspendiert und mit Triethylamin (3,03 ml, 21,75 mmol) und Bromessigsäuretrimethylsilylester (2,38 ml, 14,5 mmol) versetzt. Die Mischung wird über Nacht bei 60°C geschüttelt. An- schließend wird die Mischung filtriert und das Harz mit Dichlormethan, DMF und
Methanol gewaschen. Die Silyl-Schutzgruppe wird entfernt, indem das Harz in 25 ml Dioxan suspendiert und mit Tetrabutylammoniumfluorid-Lösung (1 M in THF, 1 ml) versetzt wird. Die Mischung wird 1 h bei Raumtemperatur geschüttelt und dann filtriert. Anschließend wird das Harz mit Dichlormethan, DMF und Methanol ge- waschen und Harz Cl erhalten.
Stufe d)
Harz Cl (2,5 g, 0,72 mmol reaktive Gruppen) wird in 20 ml DMF suspendiert und mit Diisopropylethylamin (656 mg, 5,08 mmol), HATU (1,38 g, 3,63 mmol) und 2,5- Dimethylanilin (615 mg, 5,08 mmol) versetzt. Die Mischung wird 18 h bei
Raumtemperatur geschüttelt, dann filtriert und das Harz mit Dichlormethan, DMF
und Methanol gewaschen. Anschließend wird das Harz in einer Mischung von Dichlormethan und Trifluoressigsäure suspendiert. Die Mischung wird 30 min. bei Raumtemperatur geschüttelt, dann filtriert und eingedampft. Die Zielverbindung wird als farbloser Film erhalten. LC-MS: Rt = 3.68 min; [M+H]4" = 451.3 (100%), [M-H]4" = 449.3 (100%)
[Methode: Symmetry C18 Säule (Waters), Fluss: 0.5 ml/min, Ofentemp. 40°C, Druck 400 bar, Gradient: t=0min: 10% A, 90% B; 1=4.0 min: 90% A, 10% B; t=6.0 min: 90%A, 10% B; 1=6.1 min 10% A, 90%B; 1=7.5 min 10 % A, 90 % B. A: CH3CN + 0.1% HCOOH; B: H2O +0.1% HCOOH]. 1H-NMR (d6-DMSO): δ = 1.4 (s, 6H), 2.3 (s, 3H), 2.4 (s, 3H), 3.3 (s, 2H), 3.7 (s,
2H), 3.8 (s, 2H), 6.3 (d, IH), 6.4 (d, IH), 6.8 (d, IH), 6.9 (d, 2H), 7.05 (d, IH), 7.2 (m, 2H), 7.4 (s, lH), 7.8 (s, IH).
Beispiel 4-2 2-[4-[[[2-[(4-Methoxy-2,5-dimethylphenyl)amino]-2-oxoethyl](2-furanylmethyl)- amino]-methyl]phenoxy]-2-methyl-propansäure
Harz Cl aus Beispiel 4-1 Stufe c) (2,5 g, 0,72 mmol reaktive Gruppen) wird in 20 ml
DMF suspendiert und mit Diisopropylethylamin (656 mg, 5,08 mmol), HATU (1,38 g, 3,63 mmol) und 2,5-Dimethyl-4-methoxyanilin (756 mg, 5,08 mmol) versetzt. Die Mischung wird 18 h bei Raumtemperatur geschüttelt, dann filtriert und das Harz mit Dichlormethan, DMF und Methanol gewaschen. Anschließend wird das Harz in einer Mischung von Dichlormethan und Trifluoressigsäure suspendiert. Die Mischung wird 30 min. bei Raumtemperatur geschüttelt, dann filtriert und eingedampft. Die Zielverbindung wird als farbloser Film erhalten. LC-MS: Rt = 3.48 min; [M+H]4" = 481.226 (100%), [M-H]4" = 479.226 (100%)
[Methode: Symmetry C18 Säule (Waters), Fluss: 0.5 ml/min, Ofentemp. 40°C, Druck 400 bar, Gradient: t=0min: 10% A, 90% B; t=4.0 min: 90% A, 10% B; t=6.0 min: 90%A, 10% B; 1=6.1 min 10% A, 90%B; 1=7.5 min 10 % A, 90 % B. A: CH3CN + 0.1% HCOOH; B: H2O +0.1% HCOOH].
Beispiel 4-3
2-[4-[[[2-[(4-Methoxy-2,5-dimethylphenyl)amino]-2-oxoethyl](2-thienylmethyl)- amino]-methyl]phenoxy]-2-methyl-propansäure
Stufe a)
Harz A aus Beispiel 4-1 Stufe a) (2,50 g, 0,72 mmol reaktive Gruppen) und 2- Aminomethylthiophen (409 mg, 3,62 mmol) werden in 20 ml Trimethylorthoformiat suspendiert. Die Mischung wird über Nacht bei Raumtemperatur geschüttelt, dann filtriert und das Harz mit DMF gewaschen. Anschließend wird das Harz in 20 ml DMF suspendiert und mit Tetrabutylammoniumborhydrid (559 mg, 2,17 mmol) und Essigsäure (0,42 ml, 7,25 mmol) versetzt und 7 h bei Raumtemperatur geschüttelt. Anschließend wird die Mischung filtriert, das Harz mit Dichlormethan, DMF und Methanol gewaschen und Harz B2 erhalten.
Stufe b)
Harz B2 (2,5 g, 0,72 mmol reaktive Gruppen) wird in 40 ml Dioxan suspendiert und mit Triethylamin (3,03 ml, 21,75 mmol) und Bromessigsäuretrimethylsilylester (2,38 ml, 14,5 mmol) versetzt. Die Mischung wird über Nacht bei 60°C geschüttelt. Anschließend wird die Mischung filtriert und das Harz mit Dichlormethan, DMF und Methanol gewaschen. Die Silyl-Schutzgruppe wird entfernt, indem das Harz in 25 ml Dioxan suspendiert und mit Tefrabutylammoniumfluorid-Lösung (1 M in THF, 1 ml)
versetzt wird. Die Mischung wird 1 h bei Raumtemperatur geschüttelt und dann filtriert. Anschließend wird das Harz mit Dichlormethan, DMF und Methanol gewaschen und Harz C2 erhalten.
Stufe c)
Harz C2 (2,5 g, 0,72 mmol reaktive Gruppen) wird in 20 ml DMF suspendiert und mit Diisopropylethylamin (656 mg, 5,08 mmol), HATU (1,38 g, 3,63 mmol) und 2,5- Dimethyl-4-methoxyanilin (657 mg, 5,08 mmol) versetzt. Die Mischung wird 18 h bei Raumtemperatur geschüttelt, dann filtriert und das Harz mit Dichloπnethan, DMF und Methanol gewaschen. Anschließend wird das Harz in einer Mischung von
Dichlormethan und Trifluoressigsäure suspendiert. Die Mischung wird 30 min. bei Raumtemperatur geschüttelt, dann filtriert und eingedampft. Die Zielverbindung wird als farbloser Film erhalten. LC-MS: Rt = 3.90 min; [M+H]4" = 497.4 (100%), [M-H]4" = 495.4 (100%) [Methode: Symmetry C18 Säule (Waters), Fluss: 0.5 ml/min, Ofentemp. 40°C,
Druck 400 bar, Gradient: t=0min: 10% A, 90% B; 1=4.0 min: 90% A, 10% B; 1=6.0 min: 90%A, 10% B; 1=6.1 min 10% A, 90%B; 1=7.5 min 10 % A, 90 % B. A: CH3CN + 0.1% HCOOH; B: H2O +0.1% HCOOH]. 1H-NMR ( ,y-DMSO): δ = 1.5 (s, 6H), 2.1 (s, 3H), 2.2 (s, 3H), 3.3 (s, 2H), 3.7 (s, 2H), 3.8 (s, 3H), 4.0 (s, 2H), 6.8-7.5 (m, 9H).
Auf analoge Weise wird erhalten:
Beispiel 4-4 2-[4-[[[2-[(4-Methoxy-2,5-dimethylphenyl)amino]-2-oxoethyl][(5-methyl-2-fixranyl)- methyl]-amino]methyl]phenoxy]-2-methyl-propansäure
LC-MS: R
t = 2.76 min; [M+H]
4" = 495 (100%), [M-H]
4" = 493 (100%) [Methode: Symmetry C18 Säule (Waters), Fluss: 0.5 ml/min, Ofentemp. 40°C, Druck 400 bar, Gradient: t=0min: 10% A, 90% B; 1=4.0 min: 90% A, 10% B; 1=6.0 min: 90%A, 10% B; 1=6.1 min 10% A, 90%B; t=7.5 min 10 % A, 90 % B. A:
CH3CN + 0.1% HCOOH; B: H2O +0.1% HCOOH].
Beispiel A Zellulärer Transaktivierungs-Assay:
Testprinzip:
Ein zellulärer Assay wird eingesetzt zur Identifizierung von Aktivatoren des
Peroxisom-Proliferator-aktivierten Rezeptors alpha (PPAR-alpha).
Da Säugetierzellen verschiedene endogene nukleare Rezeptoren enthalten, die eine eindeutige Interpretation der Ergebnisse komplizieren könnten, wird ein etabliertes Chimärensystem eingesetzt, in dem die Liganden-Bindungsdomäne des humanen PPARα-Rezeptors an die DNA-Bindungsdomäne des Hefe-Transkriptionsfaktors GAL4 fusioniert wird. Die so entstehende GAL4-PPARα-Chimäre wird in CHO-
Zellen mit einem Reporterkonstrukt co-transfiziert und stabil exprimiert.
Klonierung:
Das GAL4-PPARα-Expressions-Konstrukt enthält die Ligandenbindungsdomäne von PPARα (Aminosäuren 167-468), welche PCR-amplifiziert wird und in den
Vektor pcDNA3.1 hineinkloniert wird. Dieser Vektor enthält bereits die GAL4- DNA-Bindungsdomäne (Aminosäuren 1-147) des Vektors pFC2-dbd (Stratagene). Das Reporterkonstrukt, welches fünf Kopien der GAL4-Bindestelle, vorgeschaltet vor einem Thymidinkinasepromoter enthält, führt zur Expression der Firefly- Luciferase (Photinus pyralis) nach Aktivierung und Bindung von GAL4-PPARα.
Transaktivierungs-Assay (Luciferase-Reporter):
CHO (chinese hamster ovary)-Zellen werden in DMEM/F12-Medium (BioWhittaker), supplementiert mit 10% fötalem Kälberserum, 1% Penicillin/ Streptomycin (GIBCO), mit einer Zelldichte von 2 x 10 Zellen pro well in einer 384 well-Platte (Greiner) ausgesät. Nach Kultivierung über 48 h bei 37°C werden die
Zellen stimuliert. Dazu werden die zu prüfenden Substanzen in CHO-A-SFM- Medium (GIBCO), supplementiert mit 10% fötalem Kälberserum, 1% Penicillin/Streptomycin (GIBCO) aufgenommen und zu den Zellen dazu gegeben. Nach einer Stimulationszeit von 24 Stunden wird die Luciferaseaktivität mit Hilfe einer Videokamera gemessen. Die gemessenen relativen Lichteinheiten ergeben in
Abhängigkeit von der Substanzkonzentration eine sigmoide Stimulationskurve. Die Berechnung der EC50- Werte erfolgt mit Hilfe des Computerprogramms GraphPad PRISM (Version 3.02).
Die erfindungsgemäßen Verbindungen der Beispiele 3-4, 3-6, 3-60, 1-9, 2-7 und 2-12 zeigen in diesem Test EC50- Werte von 0,04 bis 200 nM.
Beispiel B Fibrinogenbestimmung: Zur Bestimmung der Wirkung auf die Plasma-Fibrinogen-Konzentration werden männliche Wistar-Ratten für einen Zeitraum von 4-9 Tagen per Schlundsonden- Applikation oder über Futterbeimischung mit der zu untersuchenden Substanz behandelt. Anschließend wird in Terminalnarkose Citratblut durch Herzpunktion gewonnen. Die Plasma-Fibrinogen-Spiegel werden nach der Clauss-Methode [Clauss A., Acta Haematol 17, 237-46 (1957)] durch Messung der Thrombinzeit mit humanem Fibrinogen als Standard bestimmt. In einigen Fällen werden Parallelbestimmungen mit einer rurbidometrischen Methode [Becker U., Bartl K., Wahlefeld A. W., Thrombosis Res. 35, 475-84 (1984)] durchgeführt, bei der Batroxobin anstelle von Thrombin eingesetzt wird.
Beispiel C
Testbeschreibung zur Auffindung von pharmakologisch wirksamen Substanzen, die das Apoprotein AI (ApoAl) und das HDL-Cholesterin (HDL-C) im Serum von transgenen Mäusen, die mit dem humanen ApoAl-Gen (hApoAl) transfiziert sind, erhöhen:
Die Substanzen, die auf ihre HDL-C erhöhende Wirkung in vivo untersucht werden sollen, werden männlichen transgenen hApo AI -Mäusen oral verabreicht. Die Tiere werden einen Tag vor Versuchsbeginn randomisiert Gruppen mit gleicher Tierzahl, in der Regel n = 7-10, zugeordnet. Während des gesamten Versuches steht den
Tieren Trinkwasser und Futter ad libitum zur Verfügung. Die Substanzen werden einmal täglich 7 Tage lang oral verabreicht. Zu diesem Zwecke werden die Testsubstanzen in einer Lösung aus Solutol HS 15 + Ethanol + Kochsalzlösung (0.9%) im Verhältnis 1+1+8 oder in einer Lösung aus Solutol HS 15 + Kochsalzlösung (0.9%) im Verhältnis 2+8 gelöst. Die Applikation der gelösten Substanzen erfolgt in einem Volumen von 10 ml/kg Körpergewicht mit einer Schlundsonde. Als Kontrollgruppe dienen Tiere, die genauso behandelt werden, aber nur das Lösungsmittel (10 ml/kg Körpergewicht) ohne Testsubstanz erhalten.
Vor der ersten Substanzapplikation wird jeder Maus zur Bestimmung von ApoAl,
Serumcholesterin, HDL-C und Serumtriglyceriden (TG) Blut durch Punktion des refroorbitalen Venenplexus entnommen (Vorwert). Anschließend wird den Tieren mit einer Schlundsonde die Testsubstanz zum ersten Mal verabreicht. 24 Stunden nach der letzten Substanzapplikation, (am 8.Tag nach Behandlungsbeginn), wird jedem Tier zur Bestimmung der gleichen Parameter erneut Blut durch Punktion des refroorbitalen Venenplexus entnommen. Die Blutproben werden zentrifugiert und nach Gewinnung des Serums werden Cholesterin und TG photometrisch mit einem EPOS Analyzer 5060 (Eppendorf-Gerätebau, Netheler & Hinz GmbH, Hamburg) bestimmt. Die Bestimmung erfolgt mit handelsüblichen Enzymtests (Boehringer Mannheim, Mannheim).
Zur Bestimmung des HDL-C wird die nicht-HDL-C Fraktion mit 20% PEG 8000 in 0,2 M Glycinpuffer pH 10 gefällt. Aus dem Überstand wird das Cholesterin in einer 96 Lochplatte mit handelsüblichem Reagenz (Ecoline 25, Merck, Darmstadt) UV- photometrisch bestimmt (BIO-TEK Instruments Inc. USA).
Das humane Maus ApoAl wird mit einer Sandwich ELISA-Methode unter Verwendung eines polyklonalen antihuman ApoAl und eines monoklonalen antihuman ApoAl Antikörpers (Biodesign International, USA) bestimmt. Die Quantifizierung erfolgt UV-photometrisch (BIO-TEK Instruments, USA) mit Peroxidase-gekoppelten anti-Maus-IGG Antikörper (KPL, USA) und
Peroxidasesubstrat (KPL, USA)
Die Wirkung der Testsubstanzen auf die HDL-C - Konzentration wird durch Subtraktion des Messwertes der 1. Blutentnahme (Vorwert) von dem Messwert der 2. Blutentnahme (nach Behandlung) bestimmt Es werden die Differenzen aller
HDL-C-Werte einer Gruppe gemittelt und mit dem Mittelwert der Differenzen der Kontrollgruppe verglichen.
Die statistische Auswertung erfolgt mit Student' s t-Test nach vorheriger Überprüfung der Varianzen auf Homogenität.
Substanzen, die das HDL-C der behandelten Tiere, verglichen mit dem der Kontrollgruppe, statistisch signifikant (p<0.05) um mindestens 20% erhöhen, werden als phannakologisch wirksam angesehen.