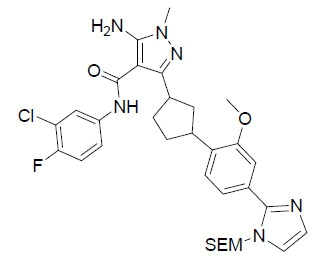
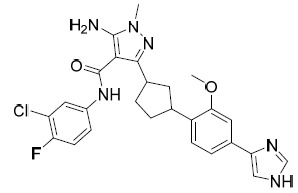
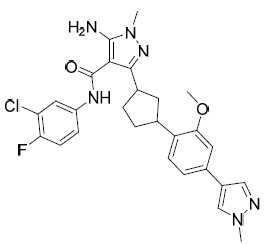
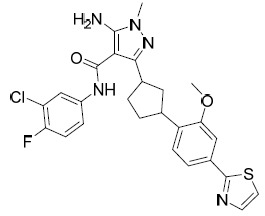
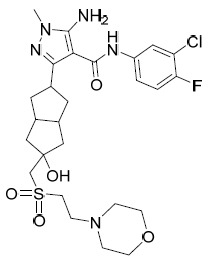
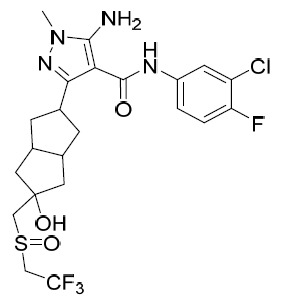
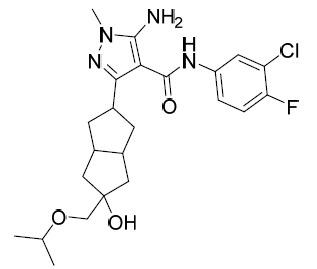
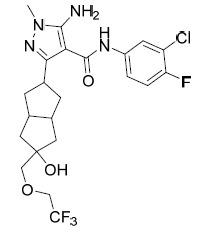
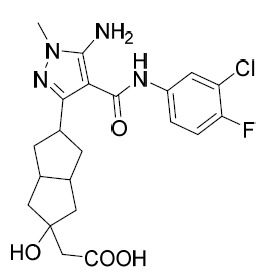
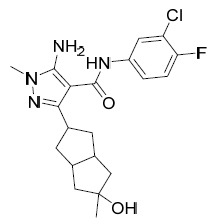
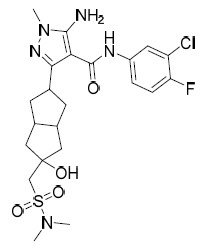
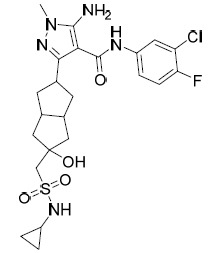
TW202028190A - 用於治療hbv之5員雜芳甲醯胺化合物 - Google Patents
用於治療hbv之5員雜芳甲醯胺化合物 Download PDFInfo
- Publication number
- TW202028190A TW202028190A TW108138129A TW108138129A TW202028190A TW 202028190 A TW202028190 A TW 202028190A TW 108138129 A TW108138129 A TW 108138129A TW 108138129 A TW108138129 A TW 108138129A TW 202028190 A TW202028190 A TW 202028190A
- Authority
- TW
- Taiwan
- Prior art keywords
- alkyl
- methyl
- aia
- amino
- chloro
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/08—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a carbon chain containing alicyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/415—1,2-Diazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4164—1,3-Diazoles
- A61K31/4178—1,3-Diazoles not condensed 1,3-diazoles and containing further heterocyclic rings, e.g. pilocarpine, nitrofurantoin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/20—Antivirals for DNA viruses
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D231/00—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings
- C07D231/02—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings
- C07D231/10—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D231/14—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D231/38—Nitrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/08—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a carbon chain containing alicyclic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/10—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/10—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/04—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings
- C07D409/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/08—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a carbon chain containing alicyclic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/08—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a carbon chain containing alicyclic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/10—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a carbon chain containing aromatic rings
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Virology (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Oncology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Communicable Diseases (AREA)
- Engineering & Computer Science (AREA)
- Biotechnology (AREA)
- Molecular Biology (AREA)
- Epidemiology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Peptides Or Proteins (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
本發明部分地提供可用於破壞HBV核心蛋白組裝之5員雜芳甲醯胺化合物及其醫藥組合物以及治療B型肝炎(HBV)感染之方法。
Description
B型肝炎(HBV)會引起病毒性肝炎,其進一步會引起慢性肝病且增加肝硬化及肝癌(肝細胞癌)之風險。在全世界,約20億人已感染HBV,約3億6千萬人發生慢性感染,且每年之HBV感染會引起大於五十萬例之死亡。HBV可藉由體液(自母親至孩子)、藉由性活動及經由血液產品來傳播。除非在出生時接種疫苗,否則HBV陽性母親所生之孩子亦可發生感染。
肝炎病毒顆粒係由脂質包膜構成,該脂質包膜上散佈有環繞病毒核心之表面蛋白(HBsAg)。核心係由蛋白質殼體或衣殼構成,該蛋白質殼體或衣殼係由120個核心蛋白(Cp)二聚體構成且繼而含有松環DNA (rcDNA)病毒基因體以及病毒及宿主蛋白。在經感染細胞中發現,基因體呈於宿主細胞核中之共價閉環DNA (cccDNA)之形式。cccDNA係用於病毒RNA且由此用於病毒蛋白之模板。在細胞質中,Cp組裝於全長病毒RNA (所謂的前基因體RNA或pgRNA)及病毒聚合酶(P)之複合物周圍。在組裝之後,P在衣殼範圍內將pgRNA逆轉錄成rcDNA以生成經DNA填充之病毒核心。
當前,主要使用核苷(酸)類似物(例如恩替卡韋(entecavir))來治療慢性HBV,該等核苷(酸)類似物在患者仍在治療的同時抑制病毒,但並不消除感染,即使在治療許多年之後。一旦患者開始服用核苷(酸)類似物,大多數人必須繼續服用該等藥劑或冒著因病毒反彈而可能具有危及生命之免疫反應之風險。另外,核苷酸療法可導致出現抗病毒藥物抗性。
核苷(酸)類似物之經FDA批准之唯一替代方式係使用干擾素α或聚乙二醇化干擾素α進行治療。不幸的是,干擾素α之不良事件發生率及特徵概述產生較差耐受性,且許多患者不能完成療法。此外,僅小部分患者可視為適用於干擾素療法,此乃因僅較小子組之患者可能對干擾素療法過程具有持續臨床反應。因此,基於干擾素之療法僅用於所有選擇治療之經診斷患者之小部分中。
因此,當前HBV治療範圍係從緩和性治療至觀察性等待。核苷酸類似物可抑制病毒產生,從而治療症狀,但完整保留感染。干擾素α在患者中具有嚴重副效應及較小耐受性且僅在少數患者中成功地用作有限治療策略。顯而易見,持續需要HBV感染之更有效治療。
本發明部分地提供可用於破壞HBV核心蛋白組裝之5員雜芳甲醯胺化合物及其醫藥組合物以及治療HBV感染之方法。
或其醫藥上可接受之鹽,其中變量闡述於實施方式中。
在另一態樣中,本發明提供醫藥組合物,其包括式I化合物或其醫藥上可接受之鹽及醫藥上可接受之賦形劑。
在另一態樣中,本發明提供治療有需要之個體之HBV感染之方法,其包括:向該個體投與治療有效量之式I化合物或其醫藥上可接受之鹽。
在另一態樣中,本發明提供治療有需要之個體之HBV感染之方法,其包括:向該個體投與包括治療有效量之式I化合物或其醫藥上可接受之鹽及醫藥上可接受之賦形劑之醫藥組合物。
相關申請案交叉參考 本申請案主張2018年10月22日提出申請之美國臨時專利申請案第62/748,906號及2019年6月7日提出申請之美國臨時專利申請案第62/858,790號之權益,該等申請案之全部內容以引用方式併入本文中。
現將更具體地闡述本發明之特徵及其他細節。在進一步闡述本發明之前,在此收集說明書、實例及隨附申請專利範圍中所採用之某些術語。應根據本發明之其餘部分且如由熟習此項技術者所理解來解讀該等定義。除非另外定義,否則本文所用之所有技術及科學術語皆具有與通常由熟習此項技術者所理解相同之含義。
I. 定義
本文所用之術語「烯基」係指具有至少一個碳-碳雙鍵之不飽和直鏈或具支鏈烴。實例性烯基包含(但不限於)具有2-6個碳原子之直鏈或具支鏈基團,其在本文中稱為C2-6
烯基。實例性烯基包含(但不限於)乙烯基、烯丙基、丁烯基、戊烯基等。
本文所用之術語「烷氧基」係指連接至氧之直鏈或具支鏈烷基(亦即烷基-O-)。實例性烷氧基包含(但不限於)具有1-6或1-4個碳原子之烷氧基,其在本文中分別稱為C1-6
烷氧基及C1-4
烷氧基。實例性烷氧基包含(但不限於)甲氧基、乙氧基、異丙氧基等。
本文所用之術語「烷氧基烷基」係指經烷氧基取代之烷基。實例包含(但不限於) CH3
CH2
OCH2
-、CH3
OCH2
CH2
-及CH3
OCH2
-。
本文所用之術語「烷基」係指飽和直鏈或具支鏈烴。實例性烷基包含(但不限於)具有1-6或1-4個碳原子之直鏈或具支鏈烴,其在本文中分別稱為C1-6
烷基及C1-4
烷基。實例性烷基包含(但不限於)甲基、乙基、正丙基、異丙基、2-甲基-1-丁基、3-甲基-2-丁基、2-甲基-1-戊基、3-甲基-1-戊基、4-甲基-1-戊基、2-甲基-2-戊基、3-甲基-2-戊基、4-甲基-2-戊基、2,2-二甲基-1-丁基、3,3-二甲基-1-丁基、2-乙基-1-丁基、正丁基、異丁基、第三丁基、正戊基、異戊基、新戊基、正己基等。本文所用之術語「伸烷基」係指雙自由基烷基。
本文所用之術語「炔基」係指具有至少一個碳-碳三鍵之不飽和直鏈或具支鏈烴。實例性炔基包含(但不限於)具有2-6個碳原子之直鏈或具支鏈基團,其在本文中稱為C2-6
炔基。實例性炔基包含(但不限於)乙炔基、丙炔基、丁炔基、戊炔基、己炔基、甲基丙炔基等。
本文所用之術語「羰基」係指雙自由基-C(O)-。
本文所用之術語「氰基」係指基團-CN。
本文所用之術語「環烷基」係指具有(例如) 3-6個碳之飽和單環烴基(在本文中稱為C3-6
單環烷基)或具有(例如) 8-12個碳之雙環烴環結構(在本文中稱為C8-12
雙環烷基)。對於雙環環烷基而言,兩個環可經由相同或不同碳進行連接。實例性單環環烷基包含(但不限於)環己基、環戊基、環戊烯基、環丁基及環丙基。實例性雙環環烷基包含(但不限於)螺[2.5]辛烷基、螺[3.5]壬烷基、雙環[2.2.2]辛烷基、雙環[4.1.0]庚烷基、八氫并環戊二烯基、雙環[4.2.0]辛烷基、雙環[1.1.1]戊烷基、雙環[2.2.1]庚烷基及雙環[2.2.2]辛烷基。
本文所用之術語「環烯基」係指具有(例如) 4-6個碳之部分地不飽和之單環烴基(在本文中稱為C4-6
單環烯基)或具有(例如) 8-12個碳之雙環烴環結構(在本文中稱為C8-12
雙環烯基)。對於雙環環烯基而言:1)一或兩個環可含有一或多個雙鍵,且2)兩個環可經由相同或不同環碳進行連接。實例性單環環烯基包含(但不限於)環丙烯基、環丁烯基、環戊烯基、環己烯基及環庚烯基。實例性雙環環烯基包含(但不限於)螺[2.5]辛-5-烯基、螺[2.5]辛-4-烯基、螺[3.5]壬-5-烯基、螺[3.5]壬-6-烯基、雙環[4.1.0]庚-3-烯基、雙環[4.1.0]庚-2-烯基及雙環[2.2.2]辛-2-烯基。
本文所用之術語「碳環基」係指藉由使苯環稠合至C3-6
單環烷基或C4-6
單環烯基環所形成之雙環系統。碳環基之實例包含(但不限於) 2,3-二氫-1H-茚基、1,2,3,4-四氫萘基及1H-茚基。
本文所用之術語「鹵基」或「鹵素」係指F、Cl、Br或I。
本文所用之術語「鹵代烷基」係指經一或多個鹵素原子取代之烷基。舉例而言,鹵代C1-6
烷基係指經一或多個鹵素原子取代之具有1-6個碳原子之直鏈或具支鏈烷基。實例包含(但不限於) CH2
F-、CHCl2
-、-CHF2
、CF3
-、CF3
CH2
-、CH3
CF2
、CF3
CCl2
-及CF3
CF2
-。
本文所用之術語「鹵代烷氧基」係指經一或多個鹵素原子取代之烷氧基。實例包含(但不限於) CCl3
O-、CF3
O-、CHF2
O-CF3
CH2
O-及CF3
CF2
O-。
本文所用之術語「雜芳基」係指含有一至四個獨立選擇之雜原子(例如氮、氧及硫)之5-6員單環或8-12員雙環芳香族環系統。在可能之情形下,雜芳基環可經由碳或氮連接至毗鄰基團。5-6員單環雜芳基之實例包含(但不限於)呋喃基、噻吩基(thiophenyl,亦稱為thienyl)、吡咯基、噻唑基、噁唑基、異噻唑基、異噁唑基、咪唑基、吡唑基、1H-1,2,3-三唑基、2H-1,2,3-三唑基、1,2,4-三唑基、吡啶基(pyridinyl,亦稱為pyridyl)、噠嗪基、嘧啶基、吡嗪基、1,3,5-三嗪基、1,2,4-三嗪基、1,2,3-三嗪基、1,2,4-噁二唑基、1,3,4-噁二唑基、1,2,5-噁二唑基、1,2,4-噻二唑基、1,3,4-噻二唑基、1,2,5-噻二唑基及四唑基。8-12員雙環雜芳基之實例包含(但不限於)苯并呋喃基、異苯并呋喃基、苯并[b
]噻吩基、苯并[c
]噻吩基、吲哚基、異吲哚基、苯并[d
]異噁唑基、苯并[c
]異噁唑基、苯并[d
]噁唑基、苯并[d
]異噻唑基、苯并[c
]異噻唑基、苯并[d
]噻唑基、吲唑基、苯并[d
]咪唑基、苯并[d
]咪唑基及苯并[d
][1,2,3]三唑基。
術語「雜環烷基」係指含有一至四個獨立選擇之雜原子(例如氮、氧及硫,包含其氧化狀態:S、S(O)及SO2
)之飽和3-6員單環或8-12員雙環系統,其在本文中稱為C3-6
單雜環烷基及C8-12
雙雜環烷基。在可能之情形下,雜環烷基環可經由碳或氮連接至毗鄰基團。C3-6
單雜環烷基之實例包含(但不限於)氮丙啶基、環氧乙烷基、硫雜環丙基1,1-二氧化物、環氧丙烷基、氮雜環丁基、硫雜環丁基1,1-二氧化物、吡咯啶基、四氫呋喃基、六氫吡啶基、四氫-2H-吡喃基、嗎啉基、硫嗎啉基及六氫吡嗪基。C8-12
雙雜環烷基之實例包含(但不限於) 1,4-二氧雜螺[4.5]癸烷基及1,5-二氧雜螺[5.5]十一烷基。
術語「雜環烯基」係指含有一至四個獨立選擇之雜原子(例如氮、氧及硫,包含其氧化狀態:S、S(O)或S(O)2
之部分地不飽和之3-6員單環或8-12員雙環系統,其在本文中稱為C3-6
單雜環烯基及C8-12
雙雜環烯基。在可能之情形下,雜環烯基環可經由碳或氮連接至毗鄰基團。對於雜環烯基而言:1)一或兩個環可含有一或多個雙鍵,且2)兩個環可經由相同或不同環原子進行連接。C3-6
單雜環烯基之實例包含(但不限於) 2,3-二氫-1H-吡咯基、2,5-二氫-1H-吡咯基、4,5-二氫-1H-吡唑基、2,3-二氫-1H-吡唑基、4,5-二氫-1H-咪唑基、2,3-二氫-1H-咪唑基、2,3-二氫噻吩基、2,5-二氫噻吩基、4,5-二氫噻唑基、2,3-二氫噻唑基、4,5-二氫異噻唑基、2,3-二氫異噻唑基、2,3-二氫呋喃基、2,5-二氫呋喃基、4,5-二氫噁唑基、2,3-二氫噁唑基、4,5-二氫異噁唑基、2,3-二氫異噁唑基、3,4-二氫吡啶基、2,3-二氫吡啶基、2,3,4,5-四氫吡啶基、1,6-二氫噠嗪基、4,5-二氫噠嗪基、3,4,5,6-四氫噠嗪基、4,5-二氫嘧啶基、1,2,5,6-四氫嘧啶基、1,2-二氫嘧啶基、1,2-二氫吡嗪基、2,3-二氫吡嗪基、1,2,3,6-四氫吡嗪基、4H-1,4-噁嗪基、3,4-二氫-2H-1,4-噁嗪基、4H-1,4-噻嗪基及3,4-二氫-2H-1,4-噻嗪基。C8-12
雙雜環烯基之實例包含(但不限於) 6,7-二氫吲哚基、4,5-二氫吲哚基、7,8-二氫咪唑并[1,2-a]吡啶基、5,6-二氫咪唑并[1,2-a]吡啶基、4,5-二氫苯并[d]咪唑基、6,7-二氫-1H-吲唑基、4,5-二氫-1H-吲唑基、4,5-二氫吡唑并[1,5-a]吡啶基及6,7-二氫吡唑并[1,5-a]吡啶基。
本文所用之術語「雜環基」係指藉由以下方式形成之雙環系統:(1)使苯環稠合至3-6員單環雜環烷基或4-7員單環雜環烯基環,或(2)使5-6員單環雜芳基環稠合至C3-6
環烷基、C4-7
環烯基、3-6員單環雜環烷基或4-6員單環雜環烯基環。在可能之情形下,該等環可經由碳或氮連接至毗鄰基團。雜環基之實例包含(但不限於)異烷基、2H-喹啉基、6,7,8,9-四氫-5H-[1,2,4]三唑并[4,3-a]氮呯、5,6,8,9-四氫-[1,2,4]三唑并[4,3-d][1,4]氧氮雜環庚烷、6,7-二氫-5H,9H-[1,2,4]三唑并[3,4-c][1,4]氧氮雜環庚烷、5,6,8,9-四氫-7l2-[1,2,4]三唑并[4,3-d][1,4]二氮呯、8,9-二氫-5H-[1,2,4]三唑并[4,3-a]氮呯、6,9-二氫-5H-[1,2,4]三唑并[4,3-a]氮呯、5,6,7,8-四氫-[1,2,4]三唑并[4,3-a]吡啶、5,6-二氫-8H-[1,2,4]三唑并[3,4-c][1,4]噁嗪、5,6,7,8-四氫咪唑并[1,2-a]吡啶及5H,9H-[1,2,4]三唑并[3,4-c][1,4]氧氮呯。
本文所用之術語「羥基(hydroxy及hydroxyl)」係指基團-OH。
本文所用之術語「羥基烷基」係指經一或多個羥基取代之烷基。實例包含(但不限於) HOCH2
-、HOCH2
CH2
-、CH3
CH(OH)CH2
-及HOCH2
CH(OH)CH2
-。
本文所用之術語「羥基烷氧基」係指經一或多個羥基取代之烷氧基。實例包含(但不限於) HOCH2
O-、HOCH2
CH2
O-、CH3
CH(OH)CH2
O-及HOCH2
CH(OH)CH2
O-。
本文所用之術語「Ra
Rb
NC1-6
烷基-」係指經如本文所定義之Ra
Rb
N-基團取代之烷基。實例包含(但不限於) NH2
CH2
-、NH(CH3
)CH2
-、N(CH3
)2
CH2
CH2
-及CH3
CH(NH2
)CH2
-。
本文所用之術語「Ra
Rb
NC1-6
烷氧基」係指經如本文所定義之Ra
Rb
N-基團取代之烷氧基。實例包含(但不限於) NH2
CH2
-、NH(CH3
)CH2
O-、N(CH3
)2
CH2
CH2
O-及CH3
CH(NH2
)CH2
O-。
本文所用之術語「側氧基」係指基團=O。
術語「個體(Individual)」、「患者」或「個體(subject)」可互換使用且包含任一動物,包含哺乳動物,較佳係小鼠、大鼠、其他齧齒類動物、兔、狗、貓、豬、牛、綿羊、馬或靈長類動物,且最佳係人類。本發明之化合物或醫藥組合物可投與哺乳動物(例如人類),但亦可投與其他哺乳動物,例如需要獸醫治療之動物,例如家養動物(例如狗、貓及諸如此類)、農場動物(例如牛、綿羊、豬、馬及諸如此類)及實驗室動物(例如大鼠、小鼠、天竺鼠、狗、靈長類動物及諸如此類)。期望地,本發明方法中所治療之哺乳動物係其中期望治療HBV感染之哺乳動物。
術語「調節」包含拮抗作用(例如抑制)、激動作用、部分拮抗作用及/或部分激動作用。
術語「醫藥上可接受」包含視需要在投與動物或人類時不產生不良、過敏或其他不利反應之分子實體及組合物。對於人類投與而言,製劑應滿足如由FDA生物製劑標準辦公室(FDA Office of Biologics standards)所要求之無菌性、熱原性及一般安全性與純度標準。
本文所用之術語「醫藥上可接受之載劑」或「醫藥上可接受之賦形劑」係指與醫藥投與相容之任何及所有溶劑、分散介質、包衣、等滲及吸收延遲劑、填充劑及諸如此類。用於醫藥活性物質之該等介質及試劑之使用在業內已眾所周知。組合物亦可含有其他活性化合物以提供補充、其他或增強之治療功能。
本文所用之術語「醫藥組合物」係指包括調配至一起之至少一種如本文所揭示之化合物及一或多種醫藥上可接受之賦形劑的組合物。
本文所用之術語「醫藥上可接受之鹽」係指可存在於組合物中所用之化合物中之酸性或鹼性基團之鹽。本發明組合物中所包含之天然鹼性化合物能夠與眾多種無機及有機酸形成各種鹽。可用於製備該等鹼性化合物之醫藥上可接受之酸加成鹽之酸係形成無毒酸加成鹽者,該等無毒酸加成鹽亦即含有藥理學可接受之陰離子之鹽,包含(但不限於)蘋果酸鹽、草酸鹽、氯化物、溴化物、碘化物、硝酸鹽、硫酸鹽、硫酸氫鹽、磷酸鹽、酸式磷酸鹽、異菸鹼酸鹽、乙酸鹽、乳酸鹽、水楊酸鹽、檸檬酸鹽、酒石酸鹽、油酸鹽、鞣酸鹽、泛酸鹽、酒石酸氫鹽、抗壞血酸鹽、琥珀酸鹽、馬來酸鹽、龍膽酸鹽、富馬酸鹽、葡萄糖酸鹽、葡糖醛酸鹽、糖二酸鹽、甲酸鹽、苯甲酸鹽、麩胺酸鹽、甲磺酸鹽、乙磺酸鹽、苯磺酸鹽、對甲苯磺酸鹽及雙羥萘酸鹽(亦即1,1'-亞甲基-雙
-(2-羥基-3-萘酸鹽))。本發明組合物中所包含之天然酸性化合物能夠與各種藥理上可接受之陽離子形成鹼式鹽。該等鹽之實例包含鹼金屬或鹼土金屬鹽,尤其係鈣、鎂、鈉、鋰、鋅、鉀及鐵鹽。本發明組合物中所包含之包含鹼性或酸性部分之化合物亦可與各種胺基酸形成醫藥上可接受之鹽。本發明化合物可含有酸性基團及鹼性基團;例如一個胺基及一個羧酸基團。在此一情形下,化合物可以酸加成鹽、兩性離子或鹼式鹽之形式存在。
本文所用之術語「治療有效量」或「有效量」係指將使組織、系統或動物(例如哺乳動物或人類)引發研究者、獸醫、醫師或其他臨床醫師正尋求之生物或醫學反應之標的化合物的量。以治療有效量投與本發明之化合物或醫藥組合物以治療疾病。或者,化合物之治療有效量係達成期望治療及/或防治效應所需之量。
術語「治療」包含經由破壞HBV核心蛋白組裝來改良疾病之任一效應,例如減弱、減小、調節或消除。「破壞」包含抑制HBV病毒組裝及感染。
本發明化合物可含有一或多個對掌性中心且由此以立體異構體形式存在。本文所用之術語「立體異構體」由所有對映異構體或非對映異構體組成。端視立體碳原子周圍之取代基之構形,該等化合物可由符號「(+)」、「(-)」、「R」或「S」來指定,但熟習此項技術者應認識到,某一結構可隱含地表示對掌性中心。本發明涵蓋該等化合物之各種立體異構體及其混合物。對映異構體或非對映異構體之混合物之命名可指定為「(±)」,但熟習此項技術者應認識到,某一結構可隱含地表示對掌性中心。
本發明化合物可含有一或多個雙鍵且由此以幾何異構體形式存在,該等幾何異構體係源自碳-碳雙鍵周圍之取代基之配置。符號表示可為如本文所闡述之單鍵、雙鍵或三鍵之鍵。碳-碳雙鍵周圍之取代基指定為呈「Z
」或「E
」構形,其中術語「Z
」及「E
」係根據IUPAC標準來使用。除非另外指定,否則繪示雙鍵之結構涵蓋「E
」及「Z
」異構體。或者,碳-碳雙鍵周圍之取代基可稱為「順式」或「反式」,其中「順式」代表取代基位於雙鍵之同一側且「反式」代表取代基位於雙鍵之相反側。
本發明化合物可含有碳環或雜環且由此以幾何異構體形式存在,該等幾何異構體係源自環周圍之取代基之配置。碳環或雜環周圍之取代基之配置指定為呈「Z
」或「E
」構形,其中術語「Z
」及「E
」係根據IUPAC標準來使用。除非另外指定,否則繪示碳環或雜環之結構涵蓋「Z
」及「E
」異構體。碳環或雜環周圍之取代基亦可稱為「順式」或「反式」,其中術語「順式」代表取代基位於環平面之同一側且術語「反式」代表取代基位於環平面之相反側。取代基佈置於環平面之同一側及相反側之化合物之混合物指定為「順式/反式」。
本發明化合物之個別對映異構體及非對映異構體可以合成方式自含有不對稱或立體中心之市售起始材料來製得,或藉由製備外消旋混合物且隨後實施熟習此項技術者熟知之拆分方法來製得。該等拆分方法之實例為:(1)使對映異構體混合物連接至對掌性輔助劑,藉由重結晶或層析分離所得非對映異構體混合物且自輔助劑釋放光學純產物,(2)採用光學活性拆分劑形成鹽,(3)在對掌性液體層析管柱上直接分離光學對映異構體混合物,或(4)使用立體選擇性化學或酶促試劑實施動力學拆分。亦可藉由熟知方法(例如對掌相液相層析或在對掌性溶劑中使化合物結晶)來將外消旋混合物拆分成其組分對映異構體。立體選擇性合成在業內已眾所周知,其係其中單一反應物在產生新立體中心期間或在轉變預存在立體中心期間形成立體異構體不等混合物之化學或酶促反應。立體選擇性合成涵蓋對映異構體及非對映異構體選擇性轉變且可涉及使用對掌性輔助劑。例如參見Carreira及Kvaerno,Classics in Stereoselective Synthesis
, Wiley-VCH: Weinheim, 2009。
本文所揭示之化合物可以與醫藥上可接受之溶劑(例如水、乙醇及諸如此類)形成之溶劑化形式以及未溶劑化形式存在,且本發明預計涵蓋溶劑化形式及未溶劑化形式。在一實施例中,化合物係非晶形。在一實施例中,化合物係單一多晶型。在另一實施例中,化合物係多晶型混合物。在另一實施例中,化合物係呈結晶形式。
本發明亦涵蓋經同位素標記之本發明化合物,該等化合物與本文所列舉者相同,只是一或多個原子經原子質量或質量數不同於自然界中通常發現之原子質量或質量數之原子代替。可納入本發明化合物中之同位素之實例包含氫、碳、氮、氧、磷、硫、氟及氯之同位素,例如分別為2
H、3
H、13
C、14
C、15
N、18
O、17
O、31
P、32
P、35
S、18
F及36
Cl。舉例而言,本發明化合物中之一或多個H原子可經氘代替。
所揭示之某些同位素標記之化合物(例如使用3
H及14
C標記者)可用於化合物及/或基質組織分佈分析。氚化(亦即3
H)及碳-14 (亦即14
C)同位素因其易於製備及可檢測性而尤佳。另外,使用諸如氘(亦即2
H)等較重同位素取代可提供源自較高代謝穩定性之某些治療優點(例如活體內半衰期增加或劑量要求降低),且由此在一些情況下可為較佳。經同位素標記之本發明化合物通常可藉由下列與本文實例中所揭示之彼等類似之程序、藉由使用經同位素標記之試劑取代未經同位素標記之試劑來製備。
術語「前藥」係指在活體內經轉變以產生所揭示化合物或該化合物之醫藥上可接受之鹽、水合物或溶劑合物之化合物。轉變可藉由各種機制(例如藉由酯酶、醯胺酶、磷酸酶、氧化及或還原代謝)發生於不同位置(例如腸腔中或在通過腸、血液或肝時)。前藥在業內已眾所周知(例如參見Rautio, Kumpulainen
等人,Nature Reviews Drug Discovery 2008, 7, 255)。
II. 5 員雜芳甲醯胺化合物
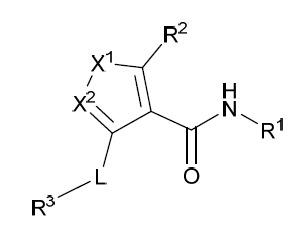
在一態樣中,本發明提供式I化合物:式I
或其醫藥上可接受之鹽,其中:
X1
係NRx1
、O或S;
X2
係N或CRx2
;
X3
係O、NR7
、CR4
R8
、C(O)、S(O)t
、C=CR4
R0
或C=NR4
;
X4
及X6
獨立地係O或S;
X5
係O、S或NR0
;
L係鍵或C1-6
伸烷基;
L1
係鍵、C1-6
伸烷基、O、NRc
、C(O)、C(O)NRc
、S(O)t
或S(O)t
NRc
;
Rx1
及Rx2
獨立地選自由以下組成之群:氫、C1-6
烷基、鹵代C1-6
烷基及C3-6
單環烷基;
Ra
、Rb
及Rc
在每次出現時獨立地選自由以下組成之群:氫、C1-6
烷基、鹵代C1-6
烷基及C3-6
單環烷基;
Rd
係氫、OH、C1-6
烷基或C1-6
烷氧基;
R0
、R6
、R8
及R11
在每次出現時獨立地選自由以下組成之群:氫、鹵素、OH、CN、NO2
、側氧基、Rd
N=、肼基、甲醯基、疊氮基、矽基、矽氧基、HOC(O)-、Ra
Rb
N-、Ra
Rb
NS(O)t
-、C1-6
烷基、C2-6
烯基、C2-6
炔基、C3-6
單環烷基、鹵代C1-6
烷基、羥基C1-6
烷基-、Ra
Rb
NC1-6
烷基-、HOC(O)C1-6
烷基-、Ra
Rb
NC1-6
烷基NRc
-、C1-6
烷基NRa
C1-6
烷基NRc
-、C1-6
烷氧基、鹵代C1-6
烷氧基、羥基C1-6
烷氧基-、Ra
Rb
NC1-6
烷氧基-、C1-6
烷氧基C1-6
烷基-、鹵代C1-6
烷氧基C1-6
烷基-、Ra
Rb
NC(O)-、C1-6
烷基C(O)-、C1-6
烷氧基C(O)-、C1-6
烷基C(O)O-、C1-6
烷基S(O)q
-、C1-6
烷基S(O)t
NRc
-、C1-6
烷基S(O)t
C1-6
烷基-、C1-6
烷基S(O)t
NRa
C1-6
烷基-、C3-6
環烷基S(O)t
C1-6
烷基-、C1-6
烷基C(O)C1-6
烷基-及C1-6
烷基C(O)OC1-6
烷基-;
R0a
在每次出現時獨立地選自由以下組成之群:氫、鹵素、OH、CN、NO2
、Ra
Rb
N-、C1-6
烷基及鹵代C1-6
烷基;
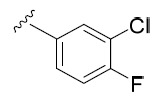
R1
係苯基、萘基、C3-6
單環烷基、C3-6
單雜環烷基或5-6員單環雜芳基,其中:苯基、C3-6
單環烷基、C3-6
單雜環烷基或5-6員單環雜芳基視情況經一個、兩個或三個獨立選擇之R11
基團取代;
R2
係氫、鹵素、Ra
Rb
N、C1-6
烷基、鹵代C1-6
烷基、C3-6
單環烷基或C1-6
烷氧基;
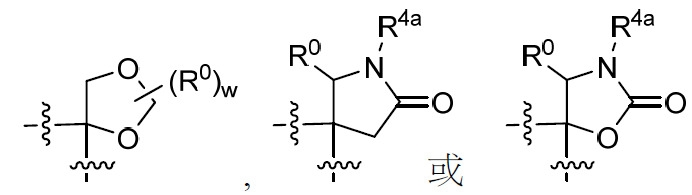
R3
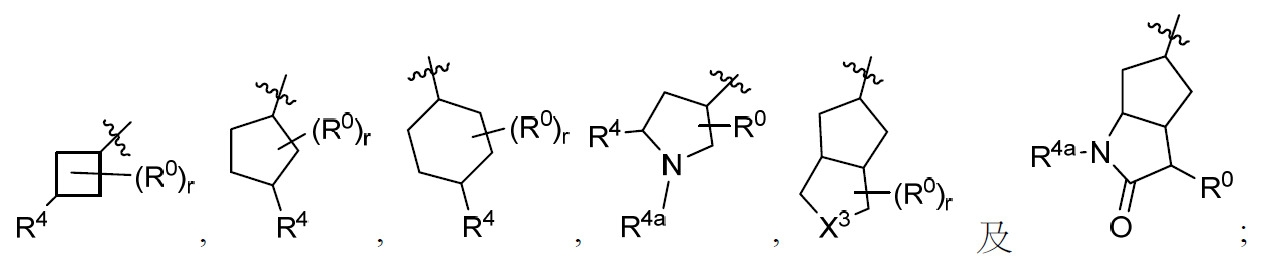
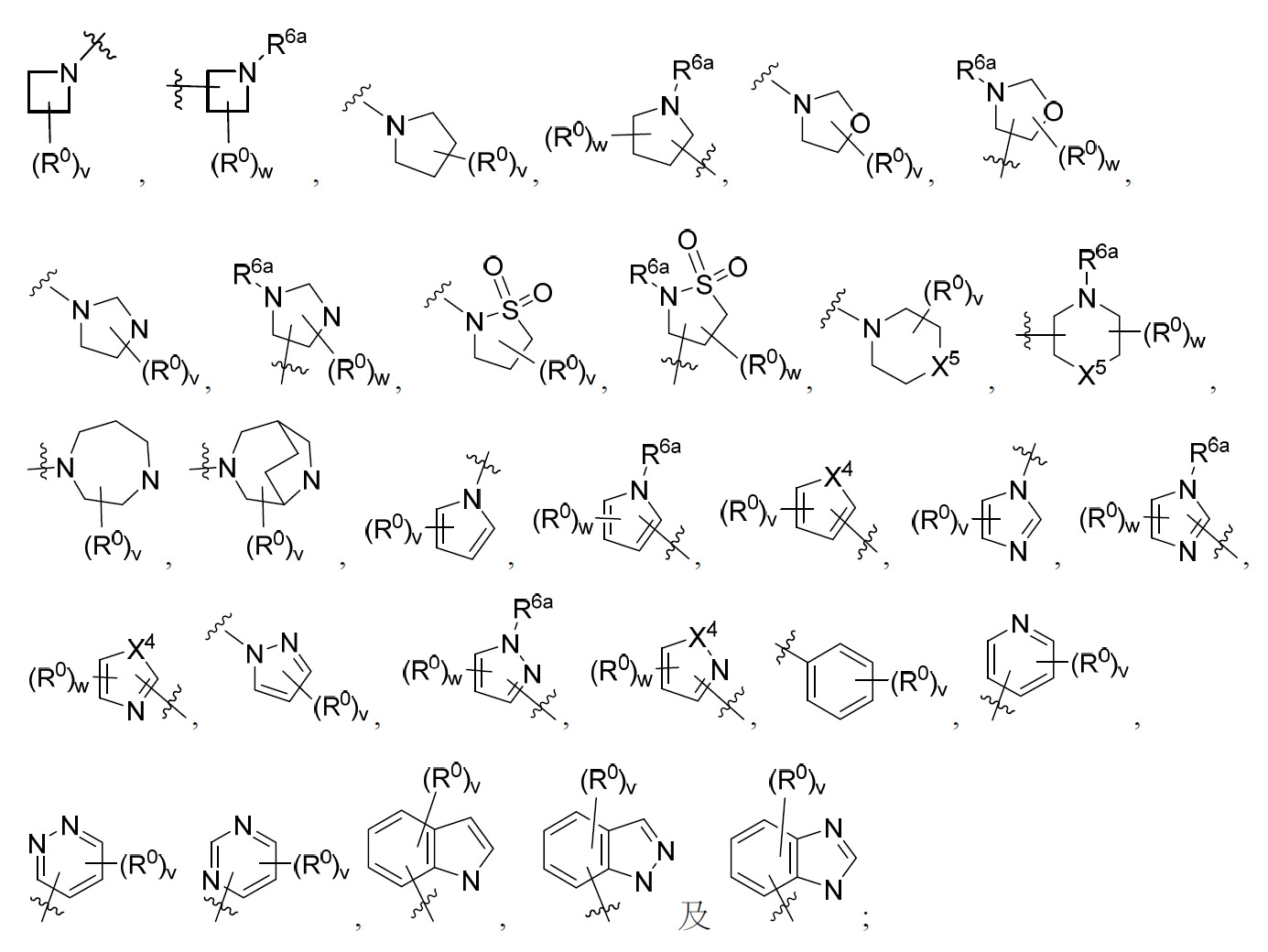
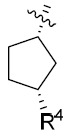
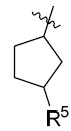
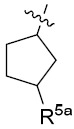
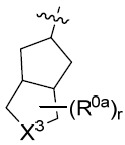
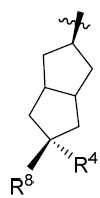
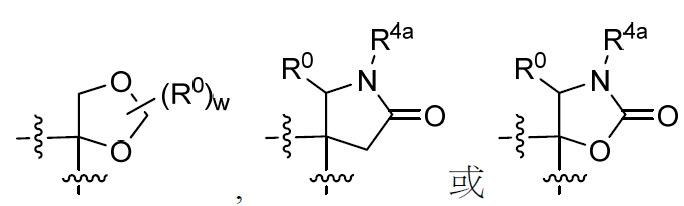
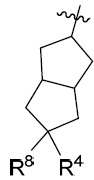
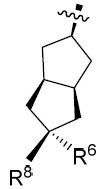
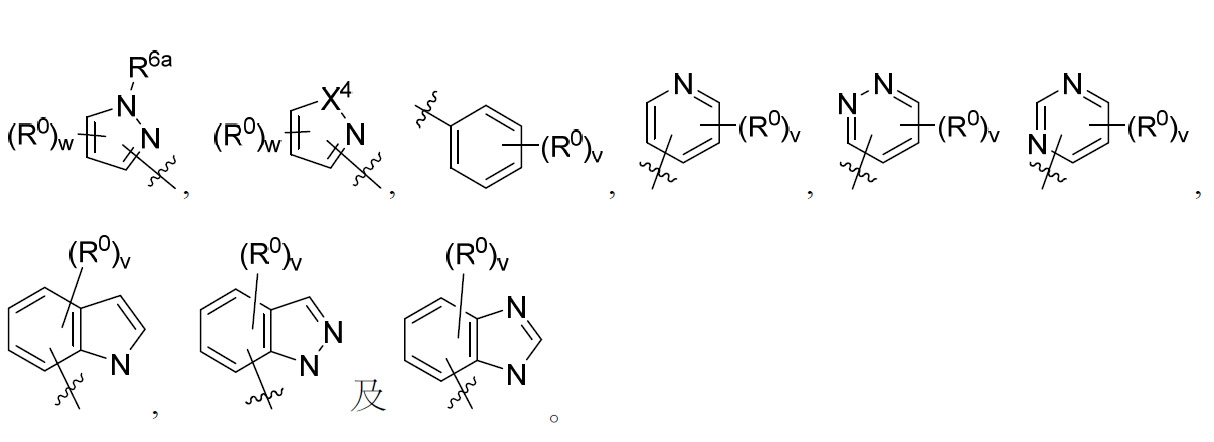
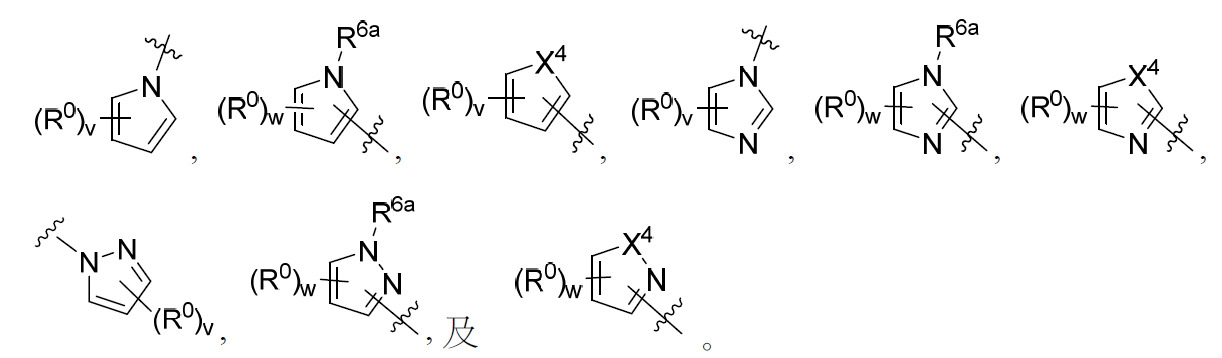
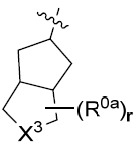
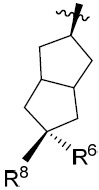
係選自由以下組成之群:
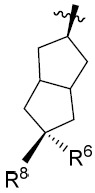
R4
係R5
、R6
或R5
-L1
-;
或R4
及R8
與其所連接之碳原子一起形成基團;
R4a
係氫或C1-6
烷基;
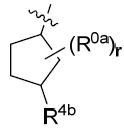
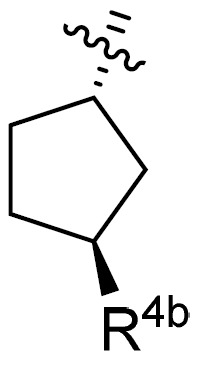
R4b
係R5
、R5a
、R6
或R5
-L1
-;
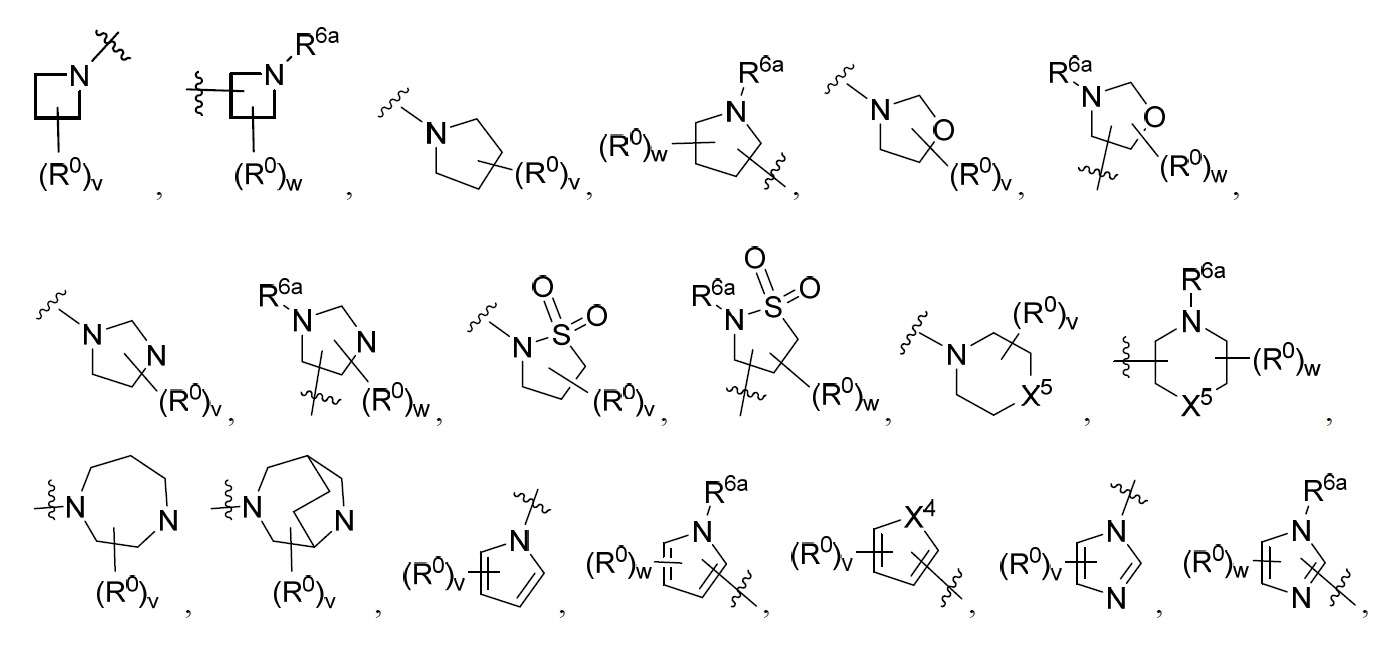
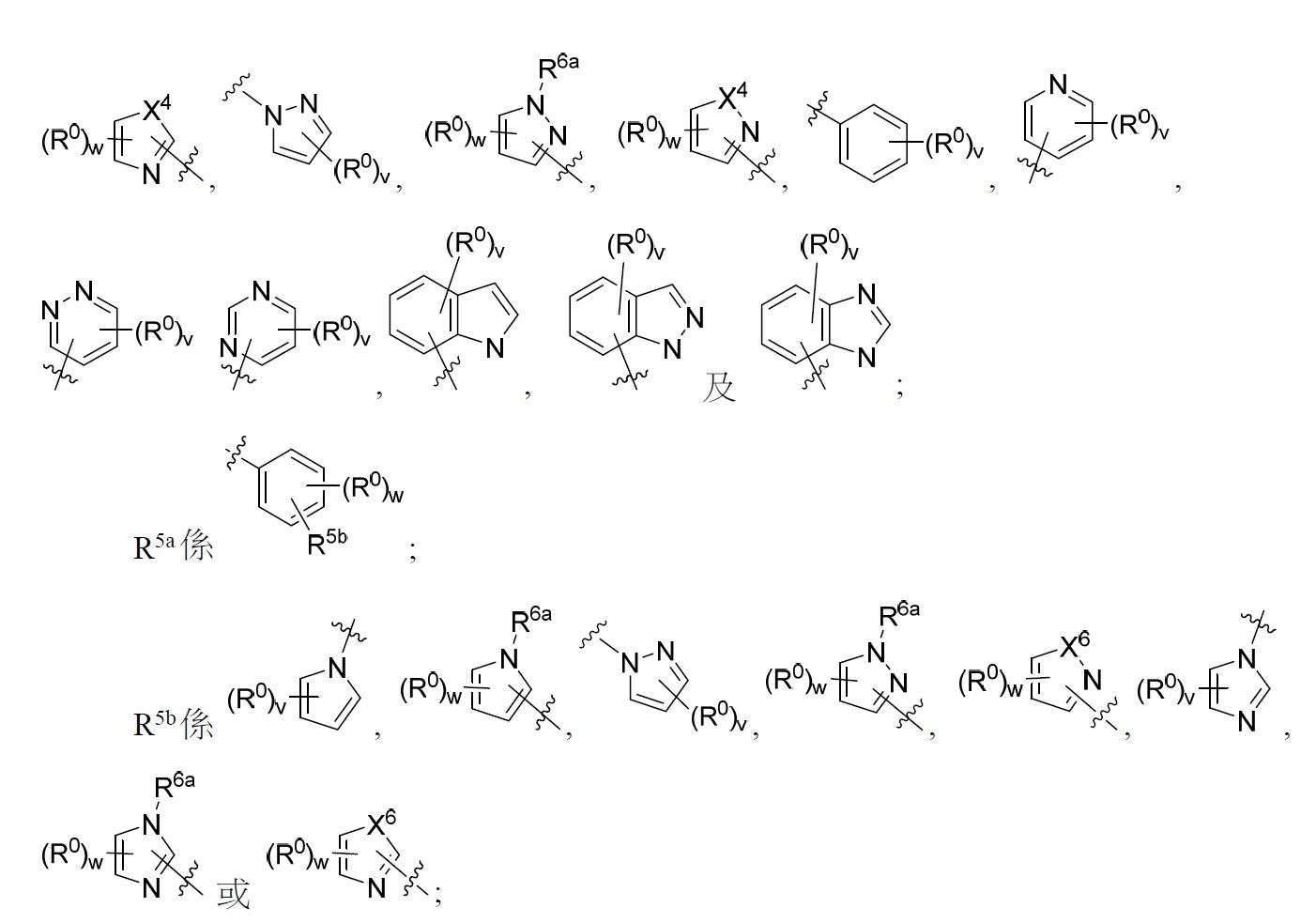
R5
係選自由以下組成之群:
R6a
係氫或C1-6
烷基;
R7
係氫、C1-6
烷基、C1-6
鹵代烷基、C1-6
烷氧基C1-6
烷基-、NRa
Rb
C(O)-、R7a
C(O)-、C1-6
烷基氧基C(O)-、C1-6
烷基S(O)q
-或C1-6
鹵代烷基S(O)q
-;
R7a
係C1-6
烷基或C3-6
單環烷基;
q、r、t及w在每次出現時獨立地選自0、1及2;且
v在每次出現時獨立地選自0、1、2及3。
在一態樣中,本發明提供式I化合物:式I
或其醫藥上可接受之鹽,其中:
X1
係NRx1
、O或S;
X2
係N或CRx2
;
X3
係O、NR7
、CR4
R8
、C(O)、S(O)t
、C=CR4
R0
或C=NR4
;
X4
係O或S;
X5
係O、S或NR0
;
L係鍵或C1-6
伸烷基;
L1
係鍵、C1-6
伸烷基、O、NRc
、C(O)、C(O)NRc
、S(O)t
或S(O)t
NRc
;
Rx1
及Rx2
獨立地選自由以下組成之群:氫、C1-6
烷基、鹵代C1-6
烷基及C3-6
單環烷基;
Ra
、Rb
及Rc
在每次出現時獨立地選自由以下組成之群:氫、C1-6
烷基、鹵代C1-6
烷基及C3-6
單環烷基;
Rd
係氫、OH、C1-6
烷基或C1-6
烷氧基;
R0
、R6
、R8
及R11
在每次出現時獨立地選自由以下組成之群:氫、鹵素、OH、CN、NO2
、側氧基、Rd
N=、肼基、甲醯基、疊氮基、矽基、矽氧基、HOC(O)-、Ra
Rb
N-、Ra
Rb
NS(O)t
-、C1-6
烷基、C2-6
烯基、C2-6
炔基、C3-6
單環烷基、鹵代C1-6
烷基、羥基C1-6
烷基-、Ra
Rb
NC1-6
烷基-、HOC(O)C1-6
烷基-、Ra
Rb
NC1-6
烷基NRc
-、C1-6
烷基NRa
C1-6
烷基NRc
-、C1-6
烷氧基、鹵代C1-6
烷氧基、羥基C1-6
烷氧基-、Ra
Rb
NC1-6
烷氧基-、C1-6
烷氧基C1-6
烷基-、鹵代C1-6
烷氧基C1-6
烷基-、Ra
Rb
NC(O)-、C1-6
烷基C(O)-、C1-6
烷氧基C(O)-、C1-6
烷基C(O)O-、C1-6
烷基S(O)q
-、C1-6
烷基S(O)t
NRc
-、C1-6
烷基S(O)t
C1-6
烷基-、C1-6
烷基S(O)t
NRa
C1-6
烷基-、C3-6
環烷基S(O)t
C1-6
烷基-、C1-6
烷基C(O)C1-6
烷基-及C1-6
烷基C(O)OC1-6
烷基-;
R1
係苯基、萘基、C3-6
單環烷基、C3-6
單雜環烷基或5-6員單環雜芳基,其中:苯基、C3-6
單環烷基、C3-6
單雜環烷基或5-6員單環雜芳基視情況經一個、兩個或三個獨立選擇之R11
基團取代;
R2
係氫、鹵素、Ra
Rb
N、C1-6
烷基、鹵代C1-6
烷基、C3-6
單環烷基或C1-6
烷氧基;
R3
係選自由以下組成之群:
R4
係R5
、R6
或R5
-L1
-;
R4a
係氫或C1-6
烷基;
R5
係選自由以下組成之群:
R6a
係氫或C1-6
烷基;
R7
係氫、C1-6
烷基、C1-6
鹵代烷基、C1-6
烷氧基C1-6
烷基-、NRa
Rb
C(O)-、R7a
C(O)-、C1-6
烷基氧基C(O)-、C1-6
烷基S(O)q
-或C1-6
鹵代烷基S(O)q
-;
R7a
係C1-6
烷基或C3-6
單環烷基;
q、r、t及w在每次出現時獨立地選自0、1及2;且
v在每次出現時獨立地選自0、1、2及3。
下列實施例進一步闡述式I化合物或其醫藥上可接受之鹽。應瞭解,本文所闡述實施例之所有化學容許組合可視為本發明之其他實施例。
在某些實施例中,X1
係NRx1
且X2
係N。
在某些實施例中,X1
係NRx1
,X2
係N,且Rx1
係氫或甲基。
在某些實施例中,X1
係NRx1
,X2
係N,且Rx1
係甲基。
在某些實施例中,X1
係O且X2
係N。
在某些實施例中,X3
係CR4
R8
。
在某些實施例中,L係鍵。
在某些實施例中,X1
係NRx1
,X2
係N,Rx1
係甲基,且L係鍵。
在某些實施例中,L係C1-6
伸烷基。
在某些實施例中,L1
係鍵。
在某些實施例中,L1
係C1-6
伸烷基。
在某些實施例中,R0a
係氫。
在某些實施例中,R11
在每次出現時獨立地選自由以下組成之群:鹵素及CN。
在某些實施例中,R11
在每次出現時獨立地選自由以下組成之群:F、Cl、Br及I。
在某些實施例中,R1
係C3-6
單環烷基,其視情況經一個、兩個或三個獨立地選自由以下組成之群之取代基取代:鹵素、CN、C1-6
烷基及鹵代C1-6
烷基。
在某些實施例中,R1
係C3-6
單雜環烷基,其視情況經一個、兩個或三個獨立地選自由以下組成之群之取代基取代:鹵素、CN、C1-6
烷基及鹵代C1-6
烷基。
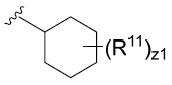
在某些實施例中,R1
係或,其中:
R11
在每次出現時獨立地選自由以下組成之群:氫、鹵素、CN、C1-6
烷基及鹵代C1-6
烷基;
R12
係氫或C1-6
烷基;
X6
係O或S;
z1為0、1、2或3;且
z2為0、1或2。
在某些實施例中,R1
係5-6員單環雜芳基,其視情況經一個、兩個或三個獨立地選自由以下組成之群之取代基取代:鹵素、CN、C1-6
烷基及鹵代C1-6
烷基。
在某些實施例中,R2
係Ra
Rb
N;
在某些實施例中,R2
係Ra
Rb
N,且Ra
及Rb
獨立地選自由以下組成之群:氫及C1-6
烷基。
在某些實施例中,R2
係NH2
。
在某些實施例中,R4
係R5
。
在某些實施例中,R4
係R6
。
在某些實施例中,R4
係R5
-L1
-。
在某些實施例中,R6
係C1-6
烷基S(O)t
C1-6
烷基-或C1-6
烷基S(O)t
NRa
C1-6
烷基-。
在某些實施例中,R6
係C1-6
烷基S(O)t
C1-6
烷基-。
在某些實施例中,R6
係C1-6
烷基S(O)t
C1-6
烷基-,且t為1或2。
在某些實施例中,R6
係C1-6
烷基S(O)t
C1-6
烷基-,且t為2。
在某些實施例中,R8
係氫、OH或C1-6
烷氧基。
在某些實施例中,R8
係OH。
在某些實施例中,X1
係NRx1
,X2
係N,Rx1
係甲基,L係鍵,R1
係,R2
係NH2
,R3
係;
R6
係C1-6
烷基S(O)t
C1-6
烷基-或C1-6
烷基S(O)t
NRa
C1-6
烷基-;且
R8
係氫、OH或C1-6
烷氧基。
在某些實施例中,X1
係NRx1
,X2
係N,Rx1
係甲基,L係鍵,R1
係,R2
係NH2
,R3
係;
R6
係C1-6
烷基S(O)t
C1-6
烷基-;且
R8
係氫、OH或C1-6
烷氧基。
III. 醫藥組合物及套組
在另一態樣中,本發明提供醫藥組合物,其包括式I化合物或其醫藥上可接受之鹽及醫藥上可接受之賦形劑。特定而言,本發明提供包括調配至一起之如本文所揭示之化合物及一或多種醫藥上可接受之載劑的醫藥組合物。該等調配物包含適用於經口、直腸、局部、經頰、非經腸(例如皮下、肌內、真皮內或靜脈內)、直腸、陰道或氣溶膠投與者,但任一既定情形下之最適宜投與形式將取決於所治療病狀之程度及嚴重程度及所用特定化合物之性質。舉例而言,所揭示組合物可調配為單位劑量,且/或可經調配用於經口或皮下投與。
在另一態樣中,本發明提供包括表17之化合物或其醫藥上可接受之鹽及/或立體異構體之醫藥組合物。
本發明之實例性醫藥組合物可以醫藥製劑形式來使用,例如以固體、半固體或液體形式,其含有一或多種本發明化合物作為活性成分;以與適用於外部、經腸或非經腸應用之有機或無機載劑或賦形劑之混合物形式。活性成分可與(例如)用於錠劑、沈澱物、膠囊、栓劑、溶液、乳液、懸浮液及任一其他適用形式之醫藥上可接受之常用無毒載劑進行複合。以足以對製程或疾病病狀產生期望效應之量將活性目標化合物包含於醫藥組合物中。
對於製備固體組合物(例如錠劑)而言,可將主要活性成分與醫藥載劑(例如習用製錠成分,例如玉米澱粉、乳糖、蔗糖、山梨醇、滑石粉、硬脂酸、硬脂酸鎂、磷酸二鈣或樹膠)及其他醫藥稀釋劑(例如水)混合以形成含有本發明化合物或其醫藥上可接受之無毒鹽之均質混合物的固體預調配組合物。在提及該等預調配組合物呈均相時,其意指活性成分均勻分散於整個組合物中,從而可容易地將組合物再分成等效單位劑型(例如錠劑、丸劑及膠囊)。
在用於經口投與之固體劑型(膠囊、錠劑、丸劑、糖衣錠、粉劑、粒劑及諸如此類)中,可將標的組合物與一或多種醫藥上可接受之載劑(例如檸檬酸鈉或磷酸二鈣)及/或以下中之任一者混合:(1)填充劑或增量劑,例如澱粉、乳糖、蔗糖、葡萄糖、甘露醇及/或矽酸;(2)黏合劑,例如羧甲基纖維素、海藻酸鹽、明膠、聚乙烯基吡咯啶酮、蔗糖及/或阿拉伯膠;(3)保濕劑,例如甘油;(4)崩解劑,例如瓊脂、碳酸鈣、馬鈴薯或木薯澱粉、海藻酸、某些矽酸鹽及碳酸鈉;(5)緩溶劑,例如石蠟;(6)吸收加速劑,例如四級銨化合物;(7)潤濕劑,例如乙醯醇及甘油單硬脂酸酯;(8)吸收劑,例如高嶺土及膨潤土;(9)潤滑劑,例如滑石粉、硬脂酸鈣、硬脂酸鎂、固體聚乙二醇、月桂基硫酸鈉及其混合物;及(10)著色劑。在膠囊、錠劑及丸劑之情形中,組合物亦可包括緩衝劑。在使用諸如乳糖(lactose或milk sugar)以及高分子量聚乙二醇及諸如此類等賦形劑之軟質及硬質填充明膠膠囊中,亦可使用類似類型之固體組合物作為填充劑。
可藉由壓縮或模製來製備錠劑,其視情況含有一或多種輔助成分。壓縮錠劑可使用黏合劑(例如明膠或羥丙基甲基纖維素)、潤滑劑、惰性稀釋劑、防腐劑、崩解劑(例如羥乙酸澱粉鈉或交聯羧甲基纖維素鈉)、表面活性劑或分散劑來製備。可藉由在適宜機器中模製經惰性液體稀釋劑潤濕之標的組合物之混合物來製備模製錠劑。可視情況使用包衣及包殼(例如腸溶包衣及醫藥調配領域中熟知之其他包衣)刻痕或製備錠劑及其他固體劑型(例如糖衣錠、膠囊、丸劑及粒劑)。
供吸入或吹入用之組合物包含於醫藥上可接受之水性或有機溶劑或其混合物中之溶液及懸浮液及粉劑。用於經口投與之液體劑型包含醫藥上可接受之乳液、微乳液、溶液、懸浮液、糖漿及酏劑。除標的組合物外,該等液體劑型亦可含有業內常用之惰性稀釋劑,例如水或其他溶劑、增溶劑及乳化劑,例如乙醇、異丙醇、碳酸乙酯、乙酸乙酯、苄醇、苯甲酸苄酯、丙二醇、1,3-丁二醇、油(尤其棉籽油、花生油、玉米油、胚芽油、橄欖油、蓖麻油及芝麻油)、甘油、四氫呋喃醇、聚乙二醇及山梨醇酐脂肪酸酯、環糊精及其混合物。
除標的組合物外,懸浮液亦可含有懸浮劑,例如乙氧基化異硬脂醇、聚環氧乙烷山梨醇及山梨醇酐酯、微晶纖維素、偏氫氧化鋁、膨潤土、瓊脂及黃蓍膠及其混合物。
用於直腸或陰道投與之調配物可作為栓劑呈遞,該栓劑可藉由將標的組合物與一或多種適宜非刺激性賦形劑或載劑(包括(例如)可可脂、聚乙二醇、栓劑蠟或水楊酸鹽)混合來製備,且該栓劑在室溫下為固體,但在體溫下為液體,且由此將在體腔中融化並釋放活性劑。
用於經皮投與標的組合物之劑型包含粉劑、噴霧劑、軟膏、膏糊、乳霜、洗劑、凝膠、溶液、貼劑及吸入劑。可在無菌條件下將該活性組分與醫藥上可接受之載劑且與任何可需要之防腐劑、緩衝劑或推進劑混合。
除標的組合物外,軟膏劑、糊劑、乳膏及凝膠亦可含有賦形劑,例如動物及植物脂肪、油、蠟、石蠟、澱粉、黃蓍膠、纖維素衍生物、聚乙二醇、聚矽氧、膨潤土、矽酸、滑石粉及氧化鋅或其混合物。
除標的組合物外,粉劑及噴霧劑亦可含有賦形劑,例如乳糖、滑石粉、矽酸、氫氧化鋁、矽酸鈣及聚醯胺粉末或該等物質之混合物。噴霧劑可另外含有常用推進劑,例如氯氟烴及未經取代之揮發性烴(例如丁烷及丙烷)。
或者,可藉由氣溶膠投與本發明之組合物及化合物。此可藉由製備含有該化合物之水性氣溶膠、脂質體製劑或固體顆粒來達成。可使用非水性(例如氟碳推進劑)懸浮液。可使用音波噴霧器,此乃因其使藥劑在可使得標的組合物中所含之化合物降解之剪切中之暴露降至最低。通常,藉由將標的組合物之水溶液或懸浮液與習用醫藥上可接受之載劑及穩定劑調配在一起來製得水性氣溶膠。載劑及穩定劑隨特定標的組合物之需要而有所變化,但通常包含非離子型表面活性劑(吐溫(Tween)、普朗尼克(Pluronic)
或聚乙二醇)、無害蛋白質(如血清白蛋白)、山梨醇酐酯、油酸、卵磷脂、胺基酸(例如甘胺酸)、緩衝劑、鹽、糖或糖醇。氣溶膠通常係自等滲溶液製備。
適用於非經腸投與之本發明醫藥組合物包括標的組合物與一或多種醫藥上可接受之無菌等滲之含水或不含水溶液、分散液、懸浮液或乳液或無菌粉劑之組合,該等無菌粉劑可在即將使用前重構成無菌可注射溶液或分散液,該等醫藥組合物可含有抗氧化劑、緩衝劑、抑菌劑、可使調配物與預期接受者之血液等滲之溶質或懸浮劑或增稠劑。
可用於本發明醫藥組合物中之適宜水性及非水性載劑之實例包含水、乙醇、多元醇(例如甘油、丙二醇、聚乙二醇及諸如此類)及其適宜混合物、植物油(例如橄欖油)及可注射有機酯(例如油酸乙酯及環糊精)。舉例而言,可藉由使用諸如卵磷脂等包覆材料、藉由維持所需粒徑(在分散劑情況下)及藉由使用表面活性劑來維持適當流動性。
在另一態樣中,本發明提供經腸醫藥調配物,其包含所揭示化合物及腸溶材料以及其醫藥上可接受之載劑或賦形劑。腸溶材料係指實質上不溶於酸性胃環境中且大部分可在特定pH下溶於腸液中之聚合物。小腸係胃與大腸之間之胃腸道(腸道)部分,且包含十二指腸、空腸及回腸。十二指腸之pH為約5.5,空腸之pH為約6.5且遠端回腸之pH為約7.5。因此,舉例而言,腸溶材料並不可溶,直至pH為約5.0、約5.2、約5.4、約5.6、約5.8、約6.0、約6.2、約6.4、約6.6、約6.8、約7.0、約7.2、約7.4、約7.6、約7.8、約8.0、約8.2、約8.4、約8.6、約8.8、約9.0、約9.2、約9.4、約9.6、約9.8或約10.0。實例性腸溶材料包含鄰苯二甲酸乙酸纖維素(CAP)、鄰苯二甲酸羥丙基甲基纖維素(HPMCP)、聚乙酸鄰苯二甲酸乙烯酯(PVAP)、乙酸琥珀酸羥丙基甲基纖維素(HPMCAS)、乙酸偏苯三酸纖維素、琥珀酸羥丙基甲基纖維素、乙酸琥珀酸纖維素、乙酸六氫鄰苯二甲酸纖維素、丙酸鄰苯二甲酸纖維素、乙酸馬來酸纖維素、乙酸丁酸纖維素、乙酸丙酸纖維素、甲基甲基丙烯酸及甲基丙烯酸甲酯之共聚物、丙烯酸甲酯、甲基丙烯酸甲酯及甲基丙烯酸之共聚物、甲基乙烯基醚及馬來酸酐之共聚物(Gantrez ES系列)、甲基丙烯酸乙酯-甲基丙烯酸甲酯-氯三甲基銨丙烯酸乙酯共聚物、天然樹脂(例如玉米醇溶蛋白、蟲膠及柯己脂松香(copal collophorium))及若干市售腸溶分散液系統(例如Eudragit L30D55、Eudragit FS30D、Eudragit L100、Eudragit S100、Kollicoat EMM30D、Estacryl 30D、Coateric及Aquateric)。上述材料中之每一者之溶解度係已知的或可易於在活體外測得。上文係可能材料之清單,但熟習此項技術者藉助本發明將認識到,其並非全面的且存在滿足本發明目標之其他腸溶材料。
有利的是,本發明亦提供由(例如)需要HBV感染治療之消費者使用之套組。該等套組包含適宜劑型(例如上文所闡述者)及闡述使用該等劑型來調介、減小或預防HBV感染之方法之說明書。說明書將指導消費者或醫學人員根據熟習此項技術者已知之投與模式來投與劑型。該等套組可有利地以單一或多個套組單元來包裝及出售。此一套組之實例係所謂的泡罩包裝。泡罩包裝為包裝工業所熟知且廣泛用於醫藥單位劑型(錠劑、膠囊及諸如此類)之包裝。泡罩包裝通常係由一片覆蓋有較佳透明塑膠材料箔之相對堅硬的材料組成。在包裝製程期間,在塑膠箔中形成凹陷。凹陷具有擬包裝之錠劑或膠囊之大小及形狀。隨後,將錠劑或膠囊置於凹陷中並使相對堅硬的材料片在與凹陷形成方向相對之箔表面上緊貼塑膠箔密封。因此,將錠劑或膠囊密封於塑膠箔與片之間之凹陷中。較佳地,薄片之強度應使得可藉由在凹陷上人工施加壓力並借此在薄片中在凹陷處形成開口而將錠劑或膠囊自泡罩包裝移出。然後可經由該開口移出錠劑或膠囊。
可期望在套組上提供記憶輔助物,例如呈數字形式緊挨著錠劑或膠囊,由此該等數字對應於方案中應攝取所指定之錠劑或膠囊之天數。此一記憶輔助物之另一實例係印刷於卡上之日曆,例如如下「第一周,星期一,星期二……等……第二周,星期一,星期二……」等。可易於明瞭記憶輔助物之其他變化形式。「日劑量」可為擬在給定天數服用之單一錠劑或膠囊或若干丸劑或膠囊。此外,第一化合物之日劑量可由一個錠劑或膠囊組成,而第二化合物之日劑量可由若干錠劑或膠囊組成,且反之亦然。記憶輔助物應反映此情況。
IV . 方法
在另一態樣中,提供治療有需要之患者之B型肝炎感染之方法,其包括向個體或患者投與有效量之所揭示化合物及/或投與第一所揭示化合物及視情況其他不同所揭示化合物。在另一實施例中,提供治療有需要之患者之B型肝炎感染之方法,其包括向個體或患者投與治療有效量之所揭示醫藥組合物或包括所揭示化合物或兩種或更多種所揭示化合物及醫藥上可接受之賦形劑之醫藥組合物。
對於此態樣中之應用而言,適當劑量預計端視(例如)以下因素而有所變化:所用特定化合物、投與模式及擬治療感染之性質及嚴重程度以及擬治療具體感染,且為治療醫師所熟知。通常,所指示投與劑量可介於約0.1 μg/kg體重至約1000 μg/kg體重之間。在一些情形下,化合物之投與劑量可小於400 μg/kg體重。在其他情形下,投與劑量可小於200 μg/kg體重。在其他情形下,投與劑量可介於約0.1 μg/kg體重至約100 μg/kg體重之間。劑量可便利地每天投與一次,或以分開劑量最多每天投與(例如) 4次,或以持續釋放形式來投與。
可藉由任一習用途徑來投與本發明化合物,特定途徑如下:經腸、經局部、經口、經鼻(例如以錠劑或膠囊形式)、經由栓劑或非經腸(例如以用於靜脈內、肌內、皮下或腹膜腔內注射之可注射溶液或懸浮液形式)。適宜調配物及醫藥組合物包含以習用方式使用一或多種生理上可接受之載劑或賦形劑及任一已知且市面有售且當前用於臨床環境中者所調配者。因此,化合物可經調配用於經口、經頰、局部、非經腸、直腸或經皮投與,或調配成適於藉由吸入或吹入(經口或經鼻)投與之形式。
對於經口投與而言,醫藥組合物可採用(例如)錠劑或膠囊之形式,該等錠劑或膠囊可藉由習用方式以諸如以下等醫藥上可接受之賦形劑來製備:黏合劑(例如預膠凝玉米澱粉、聚乙烯基吡咯啶酮或羥丙基甲基纖維素)、填充劑(例如乳糖、微晶纖維素或磷酸氫鈣)、潤滑劑(例如硬脂酸鎂、滑石粉或二氧化矽)、崩解劑(例如馬鈴薯澱粉或澱粉乙醇酸鈉)或潤濕劑(例如月桂基硫酸鈉)。錠劑可藉由業內熟知之方法加包衣。經口投與之液體製劑可採取(例如)溶液、糖漿或懸浮液形式,或可將其製備為乾燥產物以供在使用前使用水或其他適宜媒劑構造。該等液體製劑可藉由習用方式使用醫藥上可接受之添加劑來製備,例如懸浮劑(例如山梨醇糖漿、纖維素衍生物或氫化食用脂肪);乳化劑(例如卵磷脂或阿拉伯樹膠);非水性媒劑(例如杏仁油、油性酯、乙醇或經分餾植物油);及防腐劑(例如對羥基苯甲酸甲酯或對羥基苯甲酸丙酯或山梨酸)。若適宜,製劑亦可含有緩衝鹽、矯味劑、著色劑及甜味劑。
亦可適宜地調配用於口服投與之製劑以在延長時段內受控釋放或持續釋放活性化合物。對於經頰側投與,組合物可採用以熟習此項技術者已知之習用方式調配之錠劑或菱形錠劑形式。
所揭示化合物亦可經調配以用於藉由注射(例如藉由濃注或連續輸注)來非經腸投與。用於注射之調配物可以單位劑型存在,例如存於安瓿(ampoule)或存於多劑量容器中,同時添加有防腐劑。該等組合物可呈於油性或水性媒劑中之懸浮液、溶液或乳液形式,且可含有諸如懸浮劑、穩定劑及/或分散劑等添加劑。或者,化合物可呈粉劑形式,以便在使用之前使用適宜媒劑(例如無菌無致熱源水)構造。該等化合物亦可經調配以用於經直腸投與(如含有例如習用栓劑基質(例如可可油或其他甘油酯)之栓劑或保留灌腸劑)。
本文亦涵蓋包含第二活性劑或投與第二活性劑之方法及組合物。舉例而言,除經HBV感染外,個體或患者可進一步患有HBV感染相關共病,亦即與HBV感染有關、由其加劇或由其促成之疾病及其他不良健康病狀。本文涵蓋所揭示化合物與至少一種先前已展示可治療該等HBV感染相關病狀之其他藥劑之組合。
在一些情形下,所揭示化合物可與一或多種抗病毒劑一起作為組合療法之一部分來投與。實例性抗病毒劑包含核苷類似物、干擾素α及其他組裝效應物(例如雜芳基二氫嘧啶(HAP),例如4-(2-氯-4-氟苯基)-6-甲基-2-(吡啶-2-基)-1,4-二氫嘧啶-5-甲酸甲酯(HAP-1))。舉例而言,本文提供治療患有B型肝炎感染之患者之方法,其包括向患者投與第一量之所揭示化合物及第二量之抗病毒劑或其他抗HBV劑,例如第二量之選自由以下組成之群之第二化合物:HBV衣殼組裝促進劑(例如GLS4、BAY 41-4109、AT-130、DVR-23 (例如如下文所繪示):;
NVR 3-778、NVR1221 (根據代碼);及N890 (如下文所繪示):;
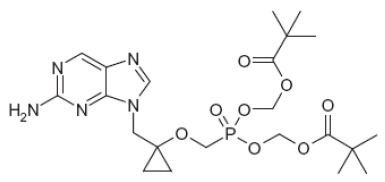
其他衣殼抑制劑,例如揭示於以引用方式併入本文中之下列專利申請案中者:WO2014037480、WO2014184328、WO2013006394、WO2014089296、WO2014106019、WO2013102655、WO2014184350、WO2014184365、WO2014161888、WO2014131847、WO2014033176、WO2014033167及WO2014033170;干擾病毒聚合酶之核苷(酸)類似物,例如恩替卡韋(Baraclude)、拉米夫定(Lamivudine) (Epivir-HBV)、替比夫定(Telbivudine) (Tyzeka、Sebivo)、阿德福韋二匹伏酯(Adefovir dipivoxil) (Hepsera)、替諾福韋(Tenofovir) (Viread)、富馬酸替諾福韋埃拉酚胺(Tenofovir alafenamide fumarate) (TAF)、替諾福韋前藥(例如AGX-1009)、L-FMAU (克來夫定(Clevudine))、LB80380 (倍司福韋(Besifovir))及:;
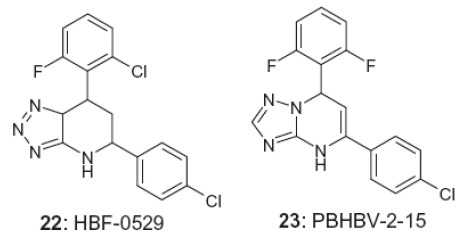
病毒進入抑制劑,例如米爾戴克(Myrcludex) B及相關脂肽衍生物;HBsAg分泌抑制劑,例如REP 9AC’及相關核酸基兩親性聚合物、HBF-0529 (PBHBV-001)、PBHBV-2-15,如下文所繪示:;
及BM601,如下文所繪示:;
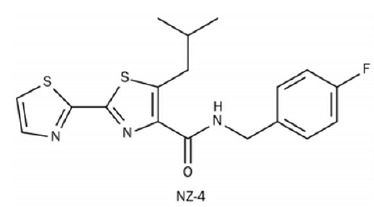
核衣殼形成或完整性破壞劑,例如NZ-4/W28F:;
cccDNA形成抑制劑,例如BSBI-25、CCC-0346、CCC-0975 (如下文所繪示):。
HBc定向反式體,例如闡述於Wang Y等人,Transbody against hepatitis B virus core protein inhibits hepatitis B virus replication in vitro, Int. Immunopharmacol (2014) (位於//dx.doi.org/10.1016/j.intimp.2015.01.028處)中者;抗病毒核心蛋白突變體(例如Cp183-V124W及相關突變,如WO/2013/010069、WO2014/074906中所闡述,每一案件以引用方式併入本文中);HBx-相互作用抑制劑,例如靶向HBV RNA之RNAi、反義及核酸基聚合物,例如RNAi (例如ALN-HBV、ARC-520、TKM-HBV、ddRNAi)、反義(ISIS-HBV)或核酸基聚合物:(REP 2139-Ca);免疫刺激劑,例如干擾素α 2a (Roferon)、內含子A (干擾素α 2b)、派羅欣(Pegasys) (聚乙二醇化干擾素α 2a)、聚乙二醇化IFN 2b、IFNλ 1a及PEG IFNλ 1a、Wellferon、Roferon、Infergen;淋巴毒素β激動劑,例如CBE11及BS1);非干擾素免疫增強劑,例如胸腺素α-1 (Zadaxin)及介白素-7 (CYT107);TLR-7/9激動劑,例如GS-9620、CYT003、瑞喹莫德(Resiquimod);親環素抑制劑,例如NVP018;OCB-030;SCY-635;阿利泊韋(Alisporivir);NIM811及相關環孢素類似物;疫苗,例如GS-4774、TG1050、核心抗原疫苗;SMAC模擬物,例如比瑞那帕(birinapant)及其他IAP-拮抗劑;表觀遺傳調節劑,例如KMT抑制劑(EZH1/2、G9a、SETD7、Suv39抑制劑)、PRMT抑制劑、HDAC抑制劑、SIRT激動劑、HAT抑制劑、WD拮抗劑(例如OICR-9429)、PARP抑制劑、APE抑制劑、DNMT抑制劑、LSD1抑制劑、JMJD HDM抑制劑及溴結構域拮抗劑;激酶抑制劑,例如TKB1拮抗劑、PLK1抑制劑、SRPK抑制劑、CDK2抑制劑、ATM及ATR激酶抑制劑;STING激動劑;利巴韋林(Ribavirin);N-乙醯基半胱胺酸;NOV-205 (BAM205);硝唑尼特(Nitazoxanide) (Alinia)、替唑尼特(Tizoxanide);SB 9200小分子核酸雜合體(SMNH);DV-601;阿比朵爾(Arbidol);FXR激動劑(例如GW 4064及非沙拉明(Fexaramin));抗體、治療蛋白、基因療法及針對病毒組分或相互作用之宿主蛋白之生物製劑。
在一些實施例中,本發明提供治療有需要之患者之B型肝炎感染之方法,其包括投與選自任一所揭示化合物之第一化合物及一或多種其他HBV藥劑,每一HBV藥劑選自由以下組成之群:HBV衣殼組裝促進劑、HBF病毒聚合酶干擾核苷、病毒進入抑制劑、HBsAg分泌抑制劑、核衣殼形成破壞劑、cccDNA形成抑制劑、抗病毒核心蛋白突變體、HBc定向反式體、靶向HBV RNA之RNAi、免疫促進劑、TLR-7/9激動劑、親環素抑制劑、HBV疫苗、SMAC模擬物、表觀遺傳調節劑、激酶抑制劑及STING激動劑。在一些實施例中,本發明提供治療有需要之患者之B型肝炎感染之方法,其包括投與一定量之所揭示化合物且投與另一HBV衣殼組裝促進劑。
在一些實施例中,第一量及第二量一起構成醫藥有效量。第一量、第二量或二者可相同於、大於或小於作為單一療法投與之每一化合物之有效量。治療有效量之所揭示化合物及抗病毒劑可共投與個體,亦即以任一既定順序且藉由相同或不同投與途徑同時或分開投與個體。在一些情況下,可有利地首先投與所揭示化合物,例如在開始投與抗病毒之前一或多天或一或多週。此外,可聯合上述組合療法給予其他藥物。
在另一實施例中,所揭示化合物可與檢測部分(例如螢光團部分,此一部分在結合至病毒時及/或在光子激發時可(例如)再發射某一光頻率)偶聯(例如直接或經由分子連接體共價結合至所揭示化合物之游離碳、氮(例如胺基)或氧(例如活性酯))。所涵蓋螢光團包含AlexaFluor® 488 (Invitrogen)及BODIPY FL (Invitrogen)以及螢光黃、玫瑰紅、青色素、吲哚羰花青、蒽醌、螢光蛋白、胺基香豆素、甲氧基香豆素、羥基香豆素、Cy2、Cy3及諸如此類。該等偶聯至檢測部分之所揭示化合物可用於(例如)檢測HBV或HBV感染生物路徑之方法(例如在活體外或在活體內)及/或評價新化合物之生物活性的方法中。
V. 實例 可以諸多方式基於本文所含之教示內容及業內已知之合成程序來製備本文所闡述之化合物。在闡述下述合成方法時,應理解,除非另外指示,否則所提出之所有反應條件(包含所選溶劑、反應氣氛、反應溫度、實驗持續時間及後處理程序)可選擇為標準反應條件。熟習有機合成技術者應理解,分子之不同位置上存在之官能基應與所提出之試劑及反應相容。熟習此項技術者易於明瞭與反應條件不相容之取代基,且由此指示替代方法。用於該等實例之起始材料市面有售或係容易地藉由標準方法自已知材料製備。
至少一些在本文中鑑別為「中間體」之化合物涵蓋為本發明化合物。
縮寫:
DCM 二氯甲烷
EtOAc 乙酸乙酯
MeOH 甲醇
DMSO 二甲基亞碸
ACN 乙腈
DIAD 偶氮二甲酸二異丙基酯
DIEA 二異丙基乙胺
nBuLi 正丁基鋰
iPrOH 異丙醇
AcOH 乙酸
BOC2
O 二碳酸二-第三丁基酯
Et3
N 三乙胺
DMF N,N-二甲基甲醯胺
THF 四氫呋喃
TEA 三乙胺
TFA 三氟乙酸
TLC 薄層層析
LCMS 液相層析-質譜
HPLC 高效液相層析
XPhos 2-二環己基膦基-2′,4′,6′-三異丙基聯苯
DPPF 1,1'-雙(二苯基膦基)二茂鐵
NMO N-甲基嗎啉-N-氧化物
HATU 六氟磷酸氮雜苯并三唑四甲基脲鎓)
SFC 超臨界流體層析
NBS N-溴琥珀醯亞胺
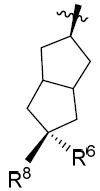
可用於本發明化合物之合成之方法展示於下文之反應圖中。在反應圖I中,羧酸酯或氯化物I-1可與I-2縮合以提供中間體I-3,隨後使用適宜烷基鹵化物(I-4)進行處理。可使用經適當取代之醯肼(I-6)處理所得化合物(I-5)以形成5-胺基吡唑模板。皂化及醯胺鍵形成可產生最終化合物I-10。
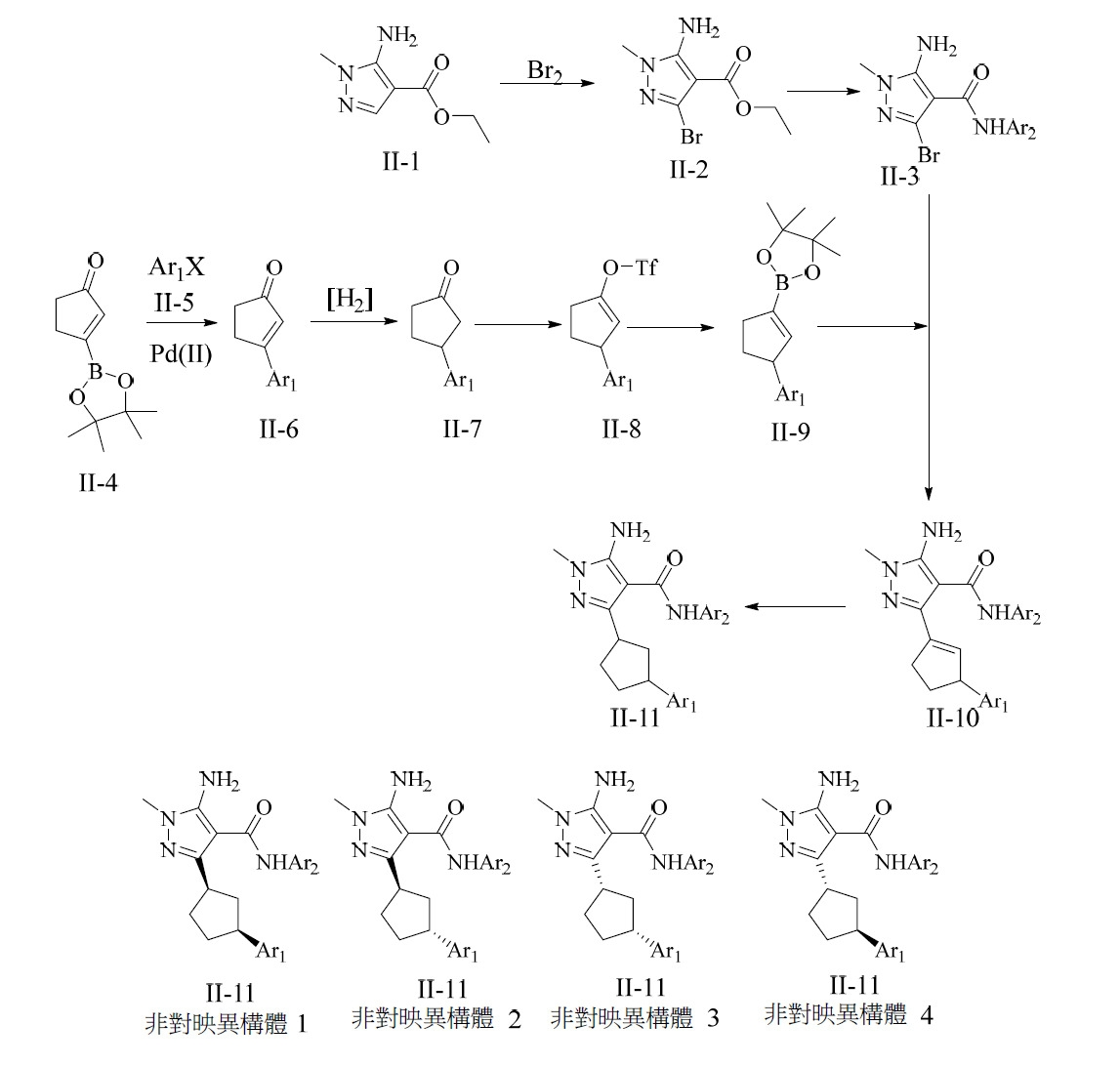
在反應圖II中,對5-胺基-吡唑酯II-1實施溴化並使用Ar2
NH2
在適當條件下處理以實現酯/醯胺交換反應。可使所得中間體II-3與II-9在催化(Pd(0)或Pd(II))條件下偶合以產生倒數第二個中間體II-10。對II-10實施氫化以產生最終化合物II-11。如反應圖II中所展示,II-11含有2個對掌性中心,此意味著存在4種可能之非對映異構體構形。可選擇性合成單一非對映異構體或選擇性分離單一非對映異構體與混合物之其他非對映異構體之方法已眾所周知(Stereoselective Synthesis of Drugs and Natural Products
,由Vasyl Andrushko及Natalia Andrushko編輯,由John Wiley & Sons, Inc於2013年出版)。
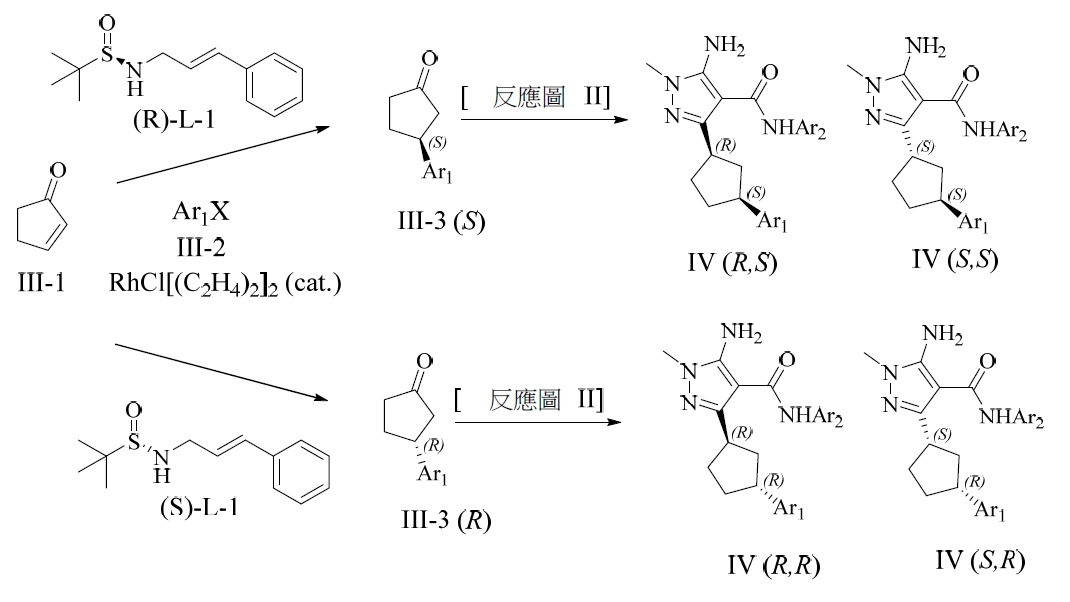
反應圖III圖解說明某些本發明化合物之立體選擇性合成。根據Org. Biomol. Chem
., 2012,10
, 1764中所闡述之方法,分別使用對掌性配體(R)-L-1或(S)-L-2,將芳基或雜-芳基(III-2)對映異構體選擇性加成至III-1可提供S-
對映異構體III-3(S
)或III-3(R
)。中間體III-3(S
)及III-3(R
)可各自分別進行至非對映異構體混合物IV (R,S
)/IV (S,S
)及IV (R,R
)/IV (S,R
)。可在已知方法下分離非對映異構體混合物。
合成本發明化合物之其他方法圖解說明於反應圖IV中。選擇性改質二酮IV-1 (Tetrahedron,
1982,38
, 63)以產生酸酯IV-3,可使該酸酯偶合至溴-吡唑中間體II-3。還原所得化合物IV-4以產生IV-5。實施酮還原且活化IV-6之所得醇基團以提供中間體IV-7,其可經由使用NucH (IV-8)進行親核性取代而進行至IV-9。或者,IV-5之酮基團適於使用IV-10進行還原胺化以產生IV-11。IV-9及IV-11皆可以至少4種不同非對映異構體構形(展示於反應圖中)存在。可基於已知立體選擇性反應原理來選擇反應條件及路徑以較其他非對映異構體偏好於形成一種非對映異構體。另外,使用已知條件分離IV-9及IV-11之個別非對映異構體。
在反應圖V中,可還原自IV-5合成之肟V-1以產生胺V-2。胺基團可進一步反應以提供磺醯胺(V-4)或醯胺(V-6)。
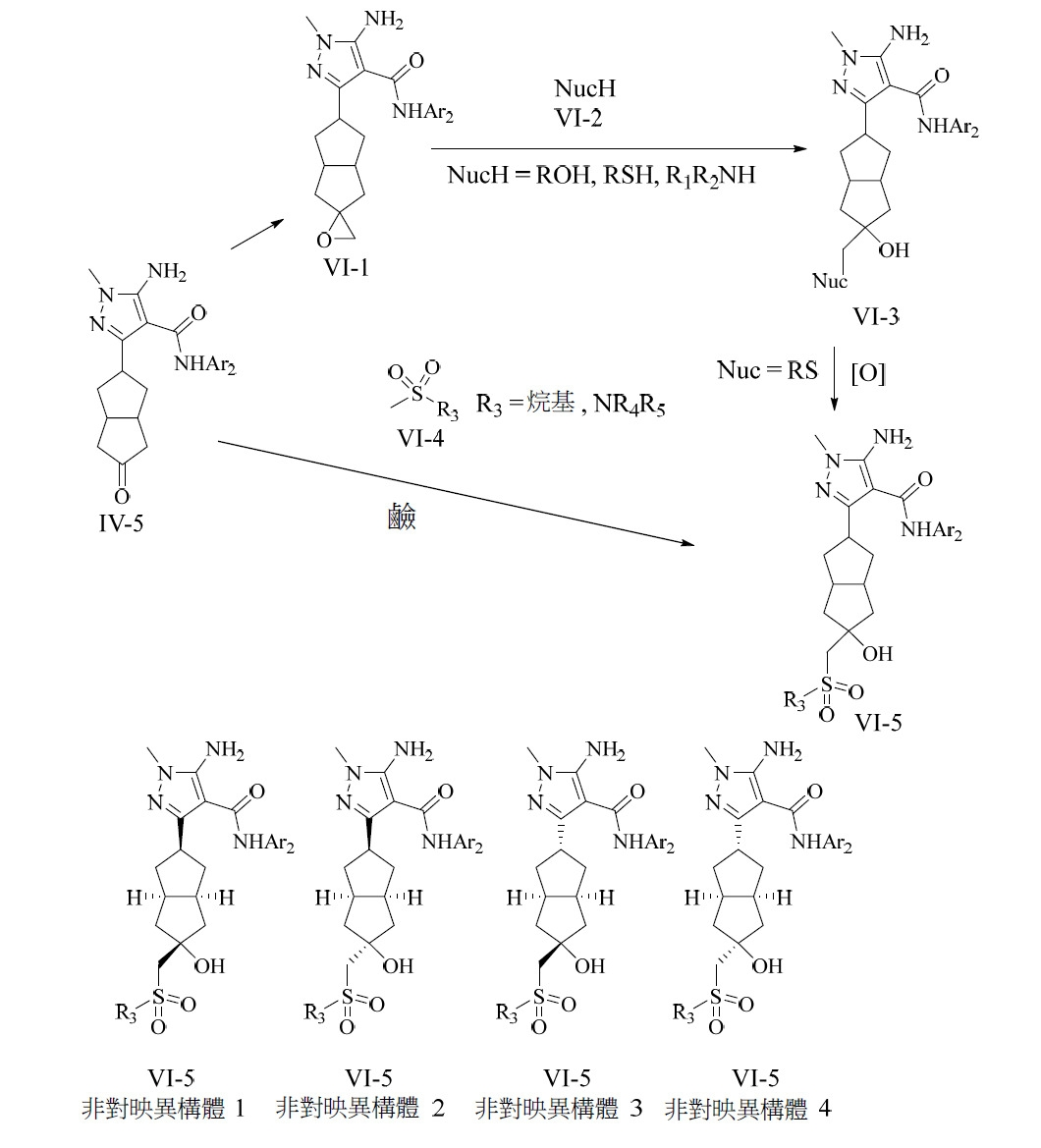
另一合成方法圖解說明於反應圖VI中。可使用已知條件將中間體IV-5轉化成相應環氧化物VI-1。此中間體可經由與各種親核試劑(NucH, VI-2)反應進行轉變以形成由VI-3代表之化合物。倘若VI-3係硫化物,則可藉由將硫原子氧化成相應碸VI-5來達成進一步修飾。形成VI-5之第二方法涉及使IV-5與磺醯胺VI-4之碸之相應陰離子進行反應。VI-5及VI-3可以至少4種不同非對映異構體構形存在,如反應圖中所圖解說明。可基於已知立體選擇性反應原理來選擇反應條件及路徑以較其他非對映異構體偏好於形成一種非對映異構體。另外,使用已知條件分離VI-3及VI-5之個別非對映異構體。
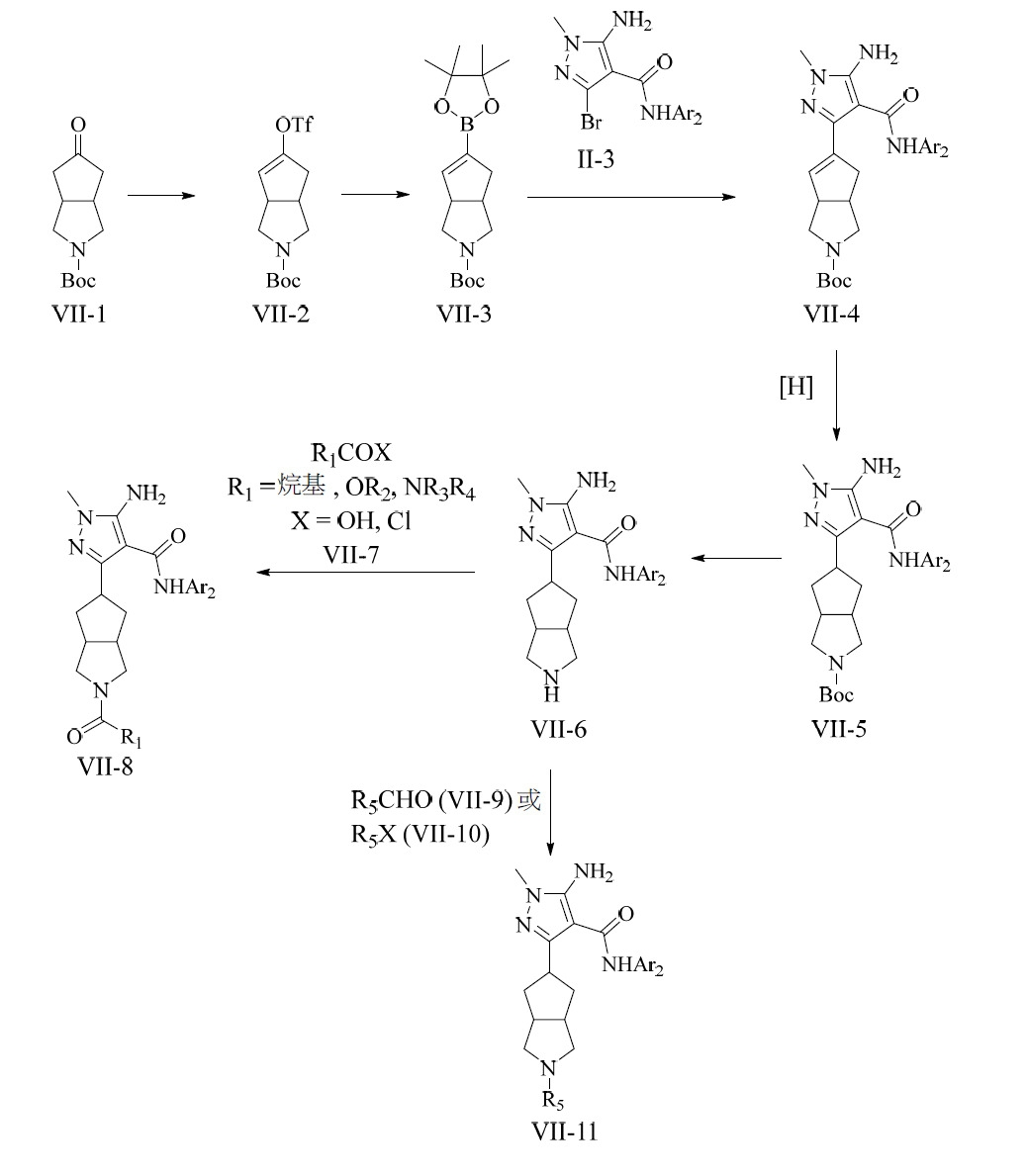
在反應圖VII中,將經Boc保護之VII-I轉化成相應酸酯VI-3且根據先前反應圖中所闡述之方法偶合至II-3。在偶合反應後,對VII-4實施氫化以提供VII-5。在去除Boc保護基團之後,化合物VII-6可經由與適當親電子劑反應進行至VII-8或經由烷基化或還原烷基化進行至VII-11。
反應圖VIII圖解說明含亞碸化合物VIII-6之合成。使用上述方法,合成化合物VIII-5,其可經氧化以形成VIII-6。反應圖 I 反應圖 II 反應圖 III 反應圖 IV 反應圖 V 反應圖 VI 反應圖 VII 反應圖 VIII
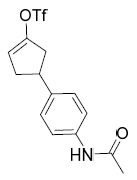
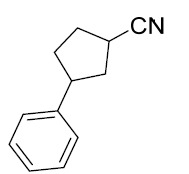
中間體1 3- 苯基環丁烷 -1- 羰基氯
。將3-苯基環丁烷甲酸(1 g, 5.68 mmol, 1當量)於SOCl2
(5 mL)中之澄清溶液在80℃下攪拌1hr。在真空下濃縮反應液以得到粗製淺黃色油狀物。使用DCM (10 mL)稀釋該油狀物。在真空下濃縮溶液以得到淺黃色油狀物形式之3-苯基環丁烷羰基氯(1.1 g,粗製物)。
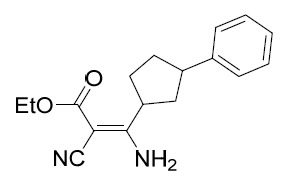
中間體2 2- 氰基 -3- 羥基 -3-(3- 苯基環丁基 ) 丙烯酸乙酯
。在0℃下,向2-氰基乙酸乙酯(1.28 g, 11.30 mmol, 1.21 mL, 2當量)於THF (20 mL)中之溶液中添加於礦物油中之60% NaH (565.04 mg, 14.13 mmol, 60%純度,2.5當量)。將反應液攪拌1 hr。在0℃下,逐滴添加3-苯基環丁烷羰基氯(1.1 g, 5.65 mmol, 1當量)於THF (10 mL)中之溶液。將反應液升溫至25℃並攪拌16 hr。使用NH4
Cl水溶液(20 mL)終止反應並使用乙酸乙酯(10 mL × 2)萃取。合併有機層,使用鹽水(10 mL)洗滌,藉由Na2
SO4
乾燥,過濾並在真空下濃縮以得到褐色油狀物形式之2-氰基-3-羥基-3-(3-苯基環丁基)丙烯酸乙酯(1.8 g,粗製物)。1
H NMR (400 MHz,氯仿-d) δ ppm 1.37 - 1.43 (m, 3 H) 2.51 - 2.74 (m, 3 H) 2.76 - 2.84 (m, 1 H) 3.63 - 3.73 (m, 1 H) 3.74 -3.87 (m, 1 H) 4.33 - 4.41 (m, 2 H) 7.21 - 7.40 (m, 5 H)。
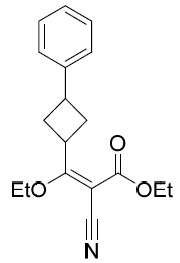
中間體3 2- 氰基 -3- 乙氧基 -3-(3- 苯基環丁基 ) 丙烯酸乙酯。
將2-氰基-3-羥基-3-(3-苯基環丁基)丙-2-烯酸乙酯(1.7 g, 6.27 mmol, 1當量)、Ag2
CO3
(4.32 g, 15.66 mmol, 0.710 mL, 2.5當量)及EtI (4.89 g, 31.33 mmol, 2.51 mL, 5當量)於DCM (50 mL)中之懸浮液在25℃下攪拌16 hr。經由Celite®墊過濾反應液,並使用DCM (10 mL × 2)洗滌濾餅。在真空下濃縮濾液以得到黃色油狀物形式之粗產物(1.8 g)。藉由急速層析(Combi-flash®;12 g SepaFlash®二氧化矽急速管柱,0~5%乙酸乙酯/石油醚梯度之洗脫劑,在20 mL/min下)純化殘餘物以提供無色油狀物形式之2-氰基-3-乙氧基-3-(3-苯基環丁基)丙烯酸乙酯(1.2 g)。1
H NMR (400 MHz,氯仿-d) δ ppm 1.29 - 1.37 (m, 3 H) 1.45 - 1.55 (m, 3 H) 2.18 (d, J=7.03 Hz, 1 H) 2.25 - 2.42 (m, 1 H) 2.45 - 2.70 (m, 3 H) 3.39 - 3.49 (m, 1 H) 4.16 - 4.42 (m, 2 H) 4.67 - 4.84 (m, 2 H) 7.18 - 7.35 (m, 5 H)。
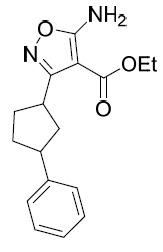
中間體4 5- 胺基 -1- 甲基 -3-(3- 苯基環丁基 )-1H- 吡唑 -4- 甲酸乙酯
。將2-氰基-3-乙氧基-3-(3-苯基環丁基)丙-2-烯酸乙酯(1.2 g, 4.01 mmol, 1當量)、甲基肼-硫酸(577.83 mg, 4.01 mmol, 1當量)及TEA (1.42 g, 14.03 mmol, 1.95 mL, 3.5當量)於EtOH (15 mL)中之黃色混合物在70℃下攪拌1hr。LCMS展示若干新峰,且檢測到25.1%之期望化合物。使用NH4
Cl水溶液(10 mL)終止反應並使用乙酸乙酯(10 mL × 2)萃取。合併有機層並使用鹽水(10 mL)洗滌,藉由Na2
SO4
乾燥,過濾,並在真空下濃縮以得到褐色油狀物形式之粗製物(1.6 g)。藉由急速矽膠層析(Combi-flash®;4 g SepaFlash®二氧化矽急速管柱,0~31%乙酸乙酯/石油醚梯度之洗脫劑,在20 mL/min下)純化殘餘物以得到黃色油狀物形式之5-胺基-1-甲基-3-(3-苯基環丁基)吡唑-4-甲酸乙酯(220 mg, 0.652 mmol, 15.3%產率,88.7%純度)。1
H NMR (400 MHz,氯仿-d) δ ppm 1.26 - 1.42 (m, 3 H) 2.36 - 2.84 (m, 4 H) 3.04 - 3.92 (m, 2 H) 4.14 - 4.33 (m, 2 H) 4.92 - 5.10 (m, 1 H) 7.13 -7.28 (m, 2 H) 7.29 - 7.36 (m, 3 H);LC-MS: 300.2 [M+1]+
。
中間體5 5- 胺基 -1- 甲基 -3-(3- 苯基環丁基 )-1H- 吡唑 -4- 甲酸
。將5-胺基-1-甲基-3-(3-苯基環丁基)吡唑-4-甲酸乙酯(220 mg, 0.652 mmol, 1當量)及LiOH-H2
O (273.43 mg, 6.52 mmol, 10當量)於THF (3 mL)、MeOH (3 mL)及H2
O (3 mL)中之混合物在70℃下攪拌64 hr。在真空下濃縮反應液以去除THF及MeOH。使用1N HCl將混合物調節至pH 6並使用乙酸乙酯(50 mL × 2)萃取。合併有機層,使用鹽水(40 mL)洗滌,藉由Na2
SO4
乾燥,過濾並在真空下濃縮以得到黃色油狀物形式之粗製5-胺基-1-甲基-3-(3-苯基環丁基)-1H-吡唑-4-甲酸(200 mg,粗製物)。LC-MS: 272.1 [M+1]+
。
中間體6 5- 胺基 -1- 甲基 -3-(3- 苯基環丁基 )-1H- 吡唑 -4- 羰基氯
。將5-胺基-1-甲基-3-(3-苯基環丁基)吡唑-4-甲酸(190 mg, 0.70 mmol)於SOCl2
(3 mL)中之溶液在80℃下攪拌1 hr。在真空下濃縮反應液以得到黃色油狀物形式之粗製5-胺基-1-甲基-3-(3-苯基環丁基)-1H-吡唑-4-羰基氯(200 mg),其未經進一步純化即用於下一步驟中。
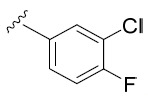
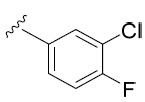
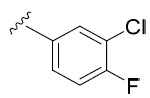
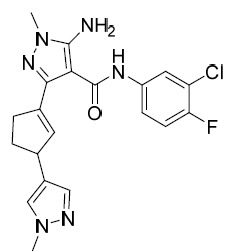
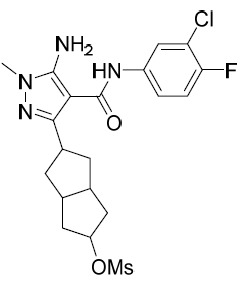
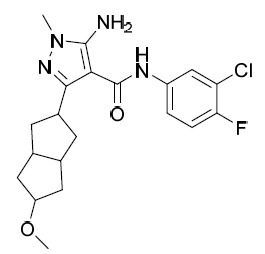
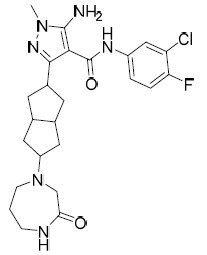
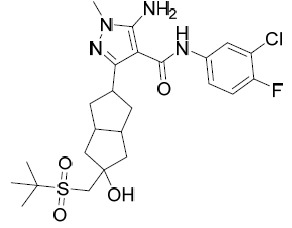
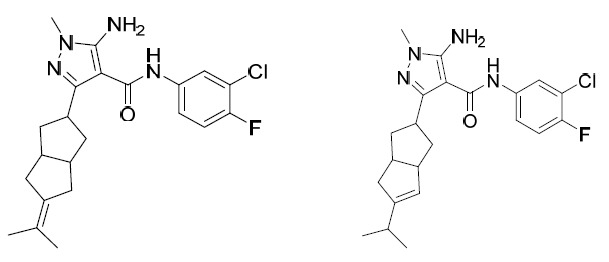
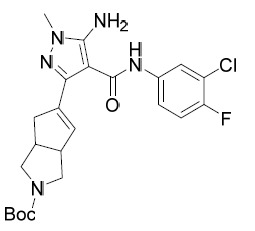
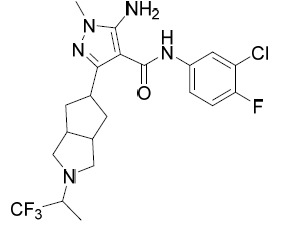
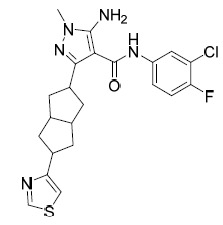
AIA 224A及AIA 224B 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(3- 苯基環丁基 )-1H- 吡唑 -4- 甲醯胺 , 非對映異構體 1 及非對映異構體 2
。在0℃及N2
下,向5-胺基-1-甲基-3-(3-苯基環丁基)吡唑-4-羰基氯(200 mg, 0.690 mmol)及3-氯-4-氟-苯胺(100.47 mg, 0.690 mmol)於DCM (5 mL)中之溶液中逐滴添加Et3
N (209.53 mg, 2.07 mmol, 0.288 mL, 3當量)。將反應液升溫至25℃並攪拌15 hr以得到褐色溶液。使用NH4
Cl (20 mL)終止反應。分離水層並對於DCM (10 mL)萃取。合併有機層並使用鹽水(10 mL)洗滌,藉由Na2
SO4
乾燥,過濾並在真空下濃縮以得到褐色油狀物形式之粗製5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(3-苯基環丁基)-1H-吡唑-4-甲醯胺(300 mg)。藉由急速矽膠層析(Combi-flash®;4 g SepaFlash®二氧化矽急速管柱,0~30%乙酸乙酯/石油醚梯度之洗脫劑,在20 mL/min下)純化殘餘物以得到呈2種非對映異構體之混合物形式之5-胺基-N-(3-氯-4-氟-苯基)-1-甲基-3-(3-苯基環丁基)吡唑-4-甲醯胺(100 mg, 0.225 mmol, 32.56%產率,89.637%純度)。藉由製備型HPLC (管柱:Xtimate C18 150 × 25mm × 5um;移動相:[水(0.05%氫氧化氨,v/v)-ACN];B%: 52%-92%, 12min)分離非對映異構體。5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(3-苯基環丁基)-1H-吡唑-4-甲醯胺(AIA-224A);1
H NMR (400 MHz, DMSO-d6) δ ppm 2.21 - 2.33 (m, 2 H) 2.62 - 2.69 (m, 2 H) 3.45 - 3.54 (m, 4 H) 3.84 - 3.98 (m, 1 H) 6.10 (s, 2 H) 7.11 - 7.24 (m, 3 H) 7.25 - 7.32 (m, 2 H) 7.36 (t, J=9.11 Hz, 1 H) 7.57 (ddd, J=9.05, 4.28, 2.69 Hz, 1 H) 7.95 (dd, J=6.91, 2.63 Hz, 1 H) 8.70 (s, 1 H);LC-MS: 399.2 [M+1]+
。5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(3-苯基環丁基)-1H-吡唑-4-甲醯胺(AIA-224B);1
H NMR (400 MHz, DMSO-d6) δ ppm 2.21 - 2.33 (m, 2 H) 2.62 - 2.69 (m, 2 H) 3.45 - 3.54 (m, 4 H) 3.84 - 3.98 (m, 1 H) 6.10 (s, 2 H) 7.11 - 7.24 (m, 3 H) 7.25 - 7.32 (m, 2 H) 7.36 (t, J=9.11 Hz, 1 H) 7.57 (ddd, J=9.05, 4.28, 2.69 Hz, 1 H) 7.95 (dd, J=6.91, 2.63 Hz, 1 H) 8.70 (s, 1 H);LC-MS: 399.2 [M+1]+
。
中間體7 5- 胺基 -3- 溴 -1- 甲基 -1H- 吡唑 -4- 甲酸乙酯。
向5-胺基-1-甲基-吡唑-4-甲酸乙酯(0.206 g, 1.22 mmol, 1當量)於EtOH (5 mL)中之黃色溶液中添加乙酸鈉(929.89 mg, 11.34 mmol, 9.28當量)於H2
O (8 mL)中之溶液,隨後逐滴添加Br2
(1.12 g, 7.04 mmol, 362.82 uL, 5.78當量)。將橙色懸浮液在15℃下攪拌3 hr。將反應混合物傾倒至H2
O (15 mL)中。使用乙酸乙酯(3 × 20 mL)萃取混合物。合併有機層並使用硫代硫酸鈉飽和水溶液(2 × 5 mL)洗滌,乾燥(Na2
SO4
),過濾並在減壓下濃縮。使用甲基第三丁基醚:石油醚(1:10)之溶液(10 mL)將固體研磨5 min。獲得黃色固體形式之5-胺基-3-溴-1-甲基-吡唑-4-甲酸乙酯(0.24 g, 967.44 umol, 79.45%產率)。1H NMR (400 MHz,氯仿-d) δ ppm 1.38 (t, J=7.15 Hz, 3 H) 3.61 (s, 3 H) 4.32 (q, J=7.13 Hz, 2 H) 5.14 (br s, 2 H)。
中間體8
.5- 胺基 -3- 溴 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺
在0℃下,向3-氯-4-氟-苯胺(281.65 mg, 1.93 mmol, 2當量)於甲苯(6 mL)中之無色溶液中添加Me3
Al (2 M於甲苯中) (2 M, 1.45 mL, 3當量)。將淺褐色溶液升溫至15℃並攪拌0.5 hr。向溶液中添加5-胺基-3-溴-1-甲基-吡唑-4-甲酸乙酯(0.24 g, 967.44 umol, 1當量)。將褐色溶液在80℃下攪拌16 hr。觀察到深褐色懸浮液。將混合物冷卻至0℃並使用1 N HCl (2 mL)驟冷。觀察到褐色懸浮液。過濾混合物。使用水(10 mL)稀釋濾液,使用EtOAc (15 mL × 3)萃取。合併有機層,藉由MgSO4乾燥,過濾並在真空下濃縮以得到黃色固體形式之殘餘物。使用甲基第三丁基醚(3 mL)將殘餘物研磨5 min。獲得淺黃色固體形式之5-胺基-3-溴-N-(3-氯-4-氟-苯基)-1-甲基-吡唑-4-甲醯胺(0.1 g, 275.30 umol, 28.46%產率,95.732%純度)。1
H NMR (400 MHz,氯仿-d) δ ppm 1.57 (s, 3 H) 3.64 (s, 3 H) 5.53 (br s, 2 H) 7.12 (t, J=8.74 Hz, 1 H) 7.29 - 7.41 (m, 1 H) 7.80 (dd, J=6.54, 2.63 Hz, 1 H) 8.34 (br s, 1 H)
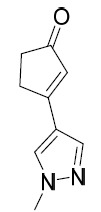
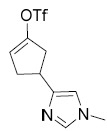
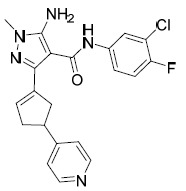
中間體9 3-(1- 甲基 -1H- 吡唑 -4- 基 ) 環戊 -2- 烯 -1- 酮。
將3-(4,4,5,5-四甲基-1,3,2-二氧硼㖦-2-基)環戊-2-烯-1-酮(5.0 g, 24.0 mmol)、4-溴-1-甲基-1H-吡唑(3.9 g, 24.0 mmol)、K3
PO4
(10.2 mg, 48.0 mmol)及Pd(dppf)Cl2
(880 mg, 1.2 mmol)於二噁烷(80 mL)及H2
O (20 mL)中之混合物在80℃及N2
氣氛下攪拌過夜。在真空下去除溶劑且藉由矽膠管柱層析使用1:9石油醚/乙酸乙酯純化殘餘物以提供黃色固體形式之3-(1-甲基-1H-吡唑-4-基)環戊-2-烯-1-酮(1.8 g, 46%產率)。MS計算值:162.1,MS實驗值:163.4 [M+1]+
。
中間體10 3-(1- 甲基 -1H- 吡唑 -4- 基 ) 環戊酮 , 對映異構體 1 及對映異構體 2 。
將3-(1-甲基-1H-吡唑-4-基)環戊-2-烯-1-酮(1.8 g, 11.1 mmol)及Pd/C (900 mg, 10%純度)於EtOH (50 mL)中之混合物脫氣並使用H2
氣氛吹掃5次。將混合物在H2
(5 atm)及80℃下攪拌過夜。經由Celite®墊過濾反應液,並使用EtOH (10 mL × 3)洗滌濾餅。在真空下濃縮濾液並藉由矽膠管柱層析使用1:1石油醚/乙酸乙酯純化殘餘物以提供黃色油狀物形式之3-(1-甲基-1H-吡唑-4-基)環戊酮(1.0 g, 56%產率)。MS計算值:164.1,MS實驗值:165.4 [M+1]+
。藉由SFC分離此材料以得到(提供) 3-(1-甲基-1H-吡唑-4-基)環戊酮之純對映異構體1及對映異構體2。
中間體11 三氟甲烷磺酸 3-(1- 甲基 -1H- 吡唑 -4- 基 ) 環戊 -1- 烯基酯 , 對映異構體 1 。
在-78℃下,向3-(1-甲基-1H-吡唑-4-基)環戊酮(400 mg, 2.4 mmol)之對映異構體1於THF (10 mL)中之溶液中添加LiHMDS (3.6 mmol, 1 M, 3.6 mL)。將反應混合物在-78℃下攪拌1 h且然後使用1,1,1-三氟-N-苯基-N-(三氟甲基磺醯基)甲烷磺醯胺(1.3 g, 3.6 mmol)於THF (5 mL)中之溶液進行處理。將反應混合物升溫至30℃並攪拌4 h。在25℃下藉由添加NH4
Cl (2 mL)來驟冷反應混合物,使用H2
O (10 mL)稀釋並使用EtOAc (20 mL × 2)萃取。使用鹽水(20 mL)洗滌合併之有機層,藉由Na2
SO4
乾燥,過濾,並在減壓下濃縮。藉由矽膠管柱層析使用3:1石油醚/乙酸乙酯純化殘餘物以提供無色油狀物形式之三氟甲烷磺酸3-(1-甲基-1H-吡唑-4-基)環戊-1-烯基酯之對映異構體1 (450 mg, 63%產率)。MS計算值:296.0,MS實驗值:297.2 [M+1]+
。
中間體12 1- 甲基 -4-(3-(4,4,5,5- 四甲基 -1,3,2- 二氧硼㖦 -2- 基 ) 環戊 -2- 烯基 )-1H- 吡唑 , 對映異構體 1
將三氟甲烷磺酸3-(1-甲基-1H-吡唑-4-基)環戊-1-烯基酯之對映異構體1 (450 mg, 1.5 mmol)、4,4,5,5-四甲基-2-(4, 4,5,5-四甲基-1,3,2-二氧硼㖦-2-基)-1,3,2-二氧硼㖦(580 mg, 2.3 mmol)、Pd(dppf)Cl2
(55 mg, 0.075 mmol)及乙酸鉀(230 mg, 2.3 mmol)於二噁烷(10 mL)中之混合物在80℃及N2
氣氛下攪拌4 h。經由矽藻土墊過濾反應液,使用EtOAc (10 mL × 3)洗滌濾餅。在真空下濃縮濾液且藉由矽膠管柱層析使用3:1石油醚/乙酸乙酯純化殘餘物以提供無色油狀物形式之1-甲基-4-(3-(4,4,5,5-四甲基-1,3,2-二氧硼㖦-2-基)環戊-2-烯基)-1H-吡唑之對映異構體1 (330 mg, 79%產率)。MS計算值:274.2,MS實驗值:275.4 [M+1]+
。
中間體13 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(3-(1- 甲基 -1H- 吡唑 -4- 基 ) 環戊 -1- 烯基 )-1H- 吡唑 -4- 甲醯胺對映異構體 1 。
將5-胺基-3-溴-N-(3-氯-4-氟苯基)-1-甲基-1H-吡唑-4-甲醯胺(348 mg, 1.0 mmol)、1-甲基-4-(3-(4,4,5,5-四甲基-1,3,2-二氧硼㖦-2-基)環戊-2-烯基)-1H-吡唑之對映異構體1 (330 mg, 1.2 mmol)、K3
PO4
(510 mg, 2.4 mmol)及Pd(dppf)Cl2
(44 mg, 0.06 mmol)於二噁烷(10 mL)及H2
O (2 mL)中之混合物在95℃及N2
氣氛下攪拌2 h。在真空下去除溶劑且藉由矽膠管柱層析使用1:9石油醚/乙酸乙酯純化殘餘物以提供白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(3-(1-甲基-1H- 吡唑-4-基)環戊-1-烯基)-1H-吡唑-4-甲醯胺之對映異構體1 (250 mg, 64%產率)。MS計算值:414.1,MS實驗值:415.3 [M+1]+
。
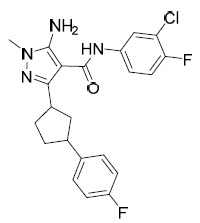
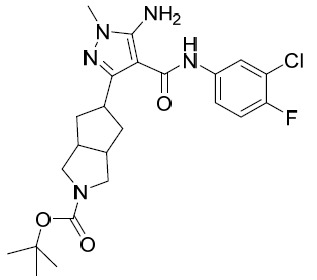
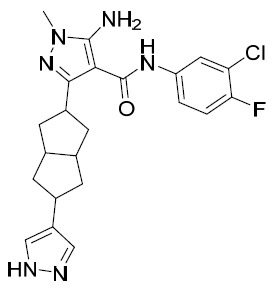
AIA004-A及AIA-004-B 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(3-(1- 甲基 -1H- 吡唑 -4- 基 ) 環戊基 )-1H- 吡唑 -4- 甲醯胺 , 非對映異構體 1 (AIA-004A) 及非對映異構體 2 (AIA-004B) 。
將5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(3-(1-甲基-1H- 吡唑-4-基)環戊-1-烯基)-1H-吡唑-4-甲醯胺之對映異構體1 (250 mg, 0.6 mmol)及RhCl(PPh3
)3
(28 mg, 0.03 mmol)於MeOH (20 mL)中之混合物在10 atm H2
及60℃下攪拌過夜。在真空下去除溶劑且藉由矽膠管柱層析使用1:9石油醚/乙酸乙酯純化殘餘物以提供呈非對映異構體混合物形式之5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(3-(1-甲基-1H-吡唑-4-基)環戊基)-1H-吡唑-4-甲醯胺,藉由SFC分離以得到白色固體形式之非對映異構體1 (AIA-004-A) (20 mg)及白色固體形式之非對映異構體2 (AIA-004-B) (6 mg)。AIA-004-A:1
H-NMR (DMSO-d6
, 400 MHz): δ 8.91 (s, 1H), 7.91 (dd, J = 6.8, 2.4 Hz, 1H), 7.53-7.49 (m, 1H), 7.44 (s, 1H), 7.34 (t, J = 9.2 Hz, 1H), 7.24 (s, 1H), 6.02 (s, 2H), 3.77-3.74 (m, 4H), 3.51 (s, 3H), 3.02-2.98 (m, 1H), 2.16-2.11 (m, 1H), 2.08-2.00 (m, 2H), 1.94-1.89 (m, 2H), 1.55-1.50 (m, 1H)。AIA-004-B:1
H-NMR (DMSO-d6
, 400 MHz): δ 8.91 (s, 1H), 7.91 (dd, J = 6.8, 2.4 Hz, 1H), 7.52-7.48 (m, 1H), 7.44 (s, 1H), 7.34 (t, J = 9.2 Hz, 1H), 7.24 (s, 1H), 6.01 (s, 2H), 3.77-3.74 (m, 4H), 3.51 (s, 3H), 3.02-2.98 (m, 1H), 2.16-2.11 (m, 1H), 2.08-2.00 (m, 2H), 1.94-1.89 (m, 2H), 1.55-1.50 (m, 1H)。
AIA-004C及AIA-004D 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(3-(1- 甲基 -1H- 吡唑 -4- 基 ) 環戊基 )-1H- 吡唑 -4- 甲醯胺 , 非對映異構體 3 (AIA-004C) 及非對映異構體 4 (AIA-004D) 。
自3-(1-甲基-1H-吡唑-4-基)環戊酮之對映異構體2使用針對5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(3-(1-甲基-1H-吡唑-4-基)環戊基)-1H-吡唑-4-甲醯胺所闡述之相同方法來合成標題化合物,非對映異構體1 (AIA-004A)及非對映異構體2 (AIA-004B)。AIA-004C:1
H-NMR (DMSO-d6
, 400 MHz): δ 8.90 (s, 1H), 7.91 (dd, J = 6.8, 2.4 Hz, 1H), 7.53-7.49 (m, 1H), 7.44 (s, 1H), 7.34 (t, J = 9.2 Hz, 1H), 7.24 (s, 1H), 6.01 (s, 2H), 3.78-3.74 (m, 4H), 3.51 (s, 3H), 3.02-2.98 (m, 1H), 2.16-2.11 (m, 1H), 2.08-2.00 (m, 2H), 1.94-1.89 (m, 2H), 1.55-1.50 (m, 1H)。AIA-004D:1
H-NMR (DMSO-d6
, 400 MHz): δ 8.94 (s, 1H), 7.93 (dd, J = 6.8, 2.4 Hz, 1H), 7.56-7.52 (m, 1H), 7.45 (s, 1H), 7.35 (t, J = 9.2 Hz, 1H), 7.23 (s, 1H), 6.00 (s, 2H), 3.74 (s, 3H), 3.67-3.62 (m, 1H), 3.50 (s, 3H), 2.97-2.93 (m, 1H), 2.28-2.23 (m, 1H), 2.01-1.97 (m, 2H), 1.90-1.86 (m, 1H), 1.78-1.69 (m, 1H), 1.56-1.51 (m, 1H)。
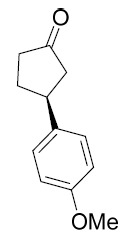
中間體14 (S)-3-(4- 甲氧基苯基 ) 環戊酮 。
在氮氣氛下,將RhCl[(C2
H4
)2
]2
(30 mg, 0.08 mmol)、(R
)-N-肉桂基-2-甲基丙烷-2-亞磺醯胺(R)-L-1 (Org. Biomol. Chem., 2012, 10, 1764) (38 mg, 0.16 mmol)及(4-甲氧基苯基)酸(1.2 g, 8.0 mmol)於二噁烷(10 mL)中之溶液在40℃下攪拌0.5 h。向此混合物中添加環戊-2-烯-1-酮(330 mg, 4.0 mmol)及K3
PO4
水溶液(1.6 mL, 1.5 mmol/L, 2.5 mmol)。在40℃下攪拌1 h之後,在減壓下濃縮混合物且藉由矽膠管柱層析使用6:1石油醚/乙酸乙酯純化殘餘物以提供無色油狀物形式之(S)-3-(4-甲氧基苯基)環戊酮(690 mg, 91%產率及97%對映異構體過量)。MS計算值:190.1,MS實驗值:191.3 [M+1]+
。
中間體15 (S)- 三氟甲烷磺酸 3-(4- 甲氧基苯基 ) 環戊 -1- 烯基酯。
在0℃下,向(S)-3-(4-甲氧基苯基)環戊酮(690 mg, 3.6 mmol)及Tf2
O (1.5 g, 5.4 mmol)於DCM (10 mL)中之溶液中逐滴添加2,6-二-第三丁基-4-甲基-吡啶(1.5 g, 7.2 mmol)。將反應液升溫至40℃並攪拌2 h以產生深色懸浮液。在真空下濃縮反應液。將石油醚 (5 mL)添加至褐色固體中,將混合物攪拌2 min,過濾,並使用石油醚(2 mL)洗滌濾餅。在真空下濃縮濾液以提供褐色油狀物形式之(S)-三氟甲烷磺酸3-(4-甲氧基苯基)環戊-1-烯基酯(1.1 g粗製物,92%產率)。MS計算值:322.0,MS實驗值:323.0 [M+1]+
。
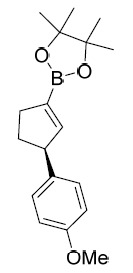
中間體16 (S)-2-(3-(4- 甲氧基苯基 ) 環戊 -1- 烯基 )-4,4,5,5- 四甲基 -1,3,2- 二氧硼㖦。
將(S)-三氟甲烷磺酸3-(4-甲氧基苯基)環戊-1-烯基酯(1.1 g, 3.4 mmol)、4,4,5,5-四甲基-2-(4, 4,5,5-四甲基- 1,3,2-二氧硼㖦-2-基)-1,3,2-二氧硼㖦(1.3 g, 5.1 mmol)、Pd(dppf)Cl2
(125 mg, 0.17 mmol)及乙酸鉀(500 mg, 5.1 mmol)於二噁烷(10 mL)中之混合物在80℃及N2
氣氛下攪拌4 h。經由Celite®墊過濾反應液,並使用EtOAc (10 mL × 3)洗滌濾餅。在真空下濃縮濾液並藉由矽膠管柱層析使用15:1石油醚/乙酸乙酯純化殘餘物以提供黃色油狀物形式之(S)-2-(3-(4-甲氧基苯基)環戊-1-烯基)-4,4,5,5-四甲基-1,3,2-二氧硼㖦(700 mg, 68%產率)。MS計算值:300.2,MS實驗值:301.3 [M+1]+
。
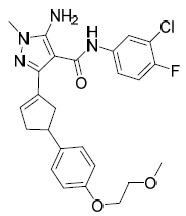
中間體17 (S)-5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(3-(4- 甲氧基苯基 ) 環戊 -1 - 烯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。
將5-胺基-3-溴-N-(3-氯-4-氟苯基)-1-甲基-1H-吡唑-4-甲醯胺(348 mg, 1.0 mmol)、(S)-2-(3-(4-甲氧基苯基)環戊-1-烯基)-4,4,5,5-四甲基-1,3,2-二氧硼㖦(700 mg, 2.3 mmol)、K3
PO4
(424 mg, 2.0 mmol)及Pd(dppf)Cl2
(73 mg, 0.1 mmol)於二噁烷(10 mL)及H2
O (2 mL)中之混合物在95℃及N2
氣氛下攪拌2 h。在真空下去除溶劑並藉由矽膠管柱層析使用1:1石油醚/乙酸乙酯純化殘餘物以提供黃色固體形式之(S)-5-胺基-N-(3-氯-4-氟苯基)-3-(3-(4-甲氧基苯基)環戊-1 -烯基)-1-甲基-1H-吡唑-4-甲醯胺(300 mg, 68%產率)。MS計算值:440.1,MS實驗值:441.1 [M+1]+
。
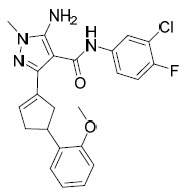
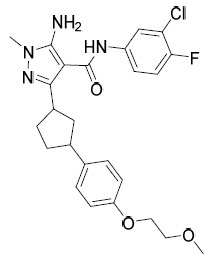
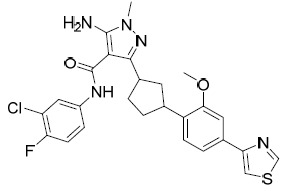
AIA-003A及AIA-003B 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-((1R,3S)-3-(4- 甲氧基苯基 ) 環戊基 )- 1- 甲基 -1H- 吡唑 -4- 甲醯胺 (AIA-003A) 及 5- 胺基 -N- (3- 氯 -4- 氟苯基 )- 3-((1S,3S)-3-(4- 甲氧基苯基 ) 環戊基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺 (AIA-003B) :
將(S)-5-胺基-N-(3-氯-4-氟苯基)-3-(3-(4-甲氧基苯基)環戊-1 -烯基)-1-甲基-1H-吡唑-4-甲醯胺(300 mg, 0.68 mmol)及RhCl(PPh3
)3
(31 mg, 0.034 mmol)於MeOH (20 mL)中之混合物在60℃及10 atm H2
下攪拌過夜。在真空下去除溶劑並藉由矽膠管柱層析使用1:1石油醚/乙酸乙酯純化殘餘物以提供5-胺基-N-(3-氯-4-氟苯基)-3-3-(4-甲氧基苯基)環戊基)- 1-甲基-1H-吡唑-4-甲醯胺(AP-AIA-003A及AIA-003B之混合物),藉由SFC分離以得到白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-3-((1R,3S)-3-(4-甲氧基苯基)環戊基)-1-甲基-1H-吡唑-4-甲醯胺(AIA-003A) (80 mg)及白色固體形式之5-胺基-N-(3-氯-4-氟苯基)- 3-((1S,3S)-3-(4-甲氧基苯基)環戊基)-1-甲基-1H-吡唑-4-甲醯胺(AIA-003 (10 mg)。AIA-003-A:1
H-NMR (DMSO-d6
, 400 MHz): δ 8.97 (s, 1H), 7.93 (dd, J = 6.8, 2.8 Hz, 1H), 7.57-7.53 (m, 1H), 7.35 (t, J = 9.2 Hz, 1H), 7.17 (d, J = 8.8 Hz, 2H), 6.83 (d, J = 8.8 Hz, 2H), 6.00 (s, 2H), 3.72-3.67 (m, 4H), 3.52 (s, 3H), 3.08-3.03 (m, 1H), 2.29-2.03 (m, 1H), 2.07-1.99 (m, 2H), 1.95-1.80 (m, 2H), 1.64-1.58 (m, 1H)。AIA-003-B:1
H-NMR (DMSO-d6
, 400 MHz): δ 8.96 (s, 1H), 7.91 (dd, J = 6.8, 2.8 Hz, 1H), 7.56-7.52 (m, 1H), 7.34 (t, J = 9.2 Hz, 1H), 7.16 (d, J = 8.4 Hz, 2H), 6.81 (d, J = 8.8 Hz, 2H), 6.03 (s, 2H), 3.85-3.82 (m, 1H), 3.70 (s, 3H), 3.52 (s, 3H), 3.10-3.06 (m, 1H), 2.17-2.05 (m, 3H), 1.99-1.88 (m, 2H), 1.62-1.56 (m, 1H)。
AIA-003C及AIA-003D 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-((1S,3R)-3-(4- 甲氧基苯基 ) 環戊基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺 (AIA-003C) 及 5- 胺基 -N- (3- 氯 -4- 氟苯基 )-3-((1R,3R)-3-(4- 甲氧基苯基 ) 環戊基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺 (AIA-003D) :
根據針對AIA-003A及AIA-003B所闡述之程序使用對掌性配體(S)-N-肉桂基-2-甲基丙烷-2-亞磺醯胺(S)-L-1來合成標題化合物(Org. Biomol. Chem., 2012, 10, 1764)。AIA-003C:1
H-NMR (DMSO-d6
, 400 MHz): δ 8.96 (s, 1H), 7.91 (dd, J = 6.8, 2.8 Hz, 1H), 7.56-7.52 (m, 1H), 7.34 (t, J = 9.2 Hz, 1H), 7.16 (d, J = 8.4 Hz, 2H), 6.81 (d, J = 8.8 Hz, 2H), 6.03 (s, 2H), 3.86-3.82 (m, 1H), 3.70 (s, 3H), 3.52 (s, 3H), 3.10-3.06 (m, 1H), 2.17-2.05 (m, 3H), 1.99-1.88 (m, 2H), 1.62-1.56 (m, 1H)。AIA-003D:1
H-NMR (DMSO-d6
, 400 MHz): δ 8.97 (s, 1H), 7.93 (dd, J = 6.8, 2.8 Hz, 1H), 7.57-7.53 (m, 1H), 7.35 (t, J = 9.2 Hz, 1H), 7.17 (d, J = 8.8 Hz, 2H), 6.83 (d, J = 8.8 Hz, 2H), 6.00 (s, 2H), 3.72-3.67 (m, 4H), 3.52 (s, 3H), 3.08-3.03 (m, 1H), 2.29-2.03 (m, 1H), 2.07-1.99 (m, 2H), 1.95-1.80 (m, 2H), 1.64-1.58 (m, 1H)。
AIA-005A及AIA-005B 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-((1R,3S)-3-(4-(1- 甲基 -1H- 吡唑 -4- 基 ) 苯基 ) 環戊基 )-1H- 吡唑 -4- 甲醯胺 (AIA-050A) 及 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-((1S,3S)-3-(4-(1- 甲基 -1H- 吡唑 -4- 基 ) 苯基 ) 環戊基 )-1H- 吡唑 -4- 甲醯胺 (AIA-050B) :
根據針對AIA-003A及AIA-003B所闡述之程序來合成標題化合物。AIA-050-A:1
H-NMR (DMSO-d6
, 400 MHz): δ 8.94 (s, 1H), 8.05 (s, 1H), 7.93 (dd, J = 7.2, 2.8 Hz, 1H), 7.79 (s, 1H), 7.56-7.52 (m, 1H), 7.43 (d, J = 8.4 Hz, 2H), 7.34 (t, J = 9.2 Hz, 1H), 7.23 (d, J = 8.0 Hz, 2H), 6.04 (s, 2H), 3.88-3.84 (m, 4H), 3.53 (s, 3H), 3.15-3.09 (m, 1H), 2.20-2.08 (m, 3H), 2.03-1.91 (m, 2H), 1.67-1.62 (m, 1H)。AIA-050-B:1
H-NMR (DMSO-d6
, 400 MHz): δ 8.98 (s, 1H), 8.06 (s, 1H), 7.94 (dd, J = 6.8, 2.8 Hz, 1H), 7.79 (s, 1H), 7.58-7.54 (m, 1H), 7.45 (d, J = 8.4 Hz, 2H), 7.36 (t, J = 9.2 Hz, 1H), 7.23 (d, J = 8.0 Hz, 2H), 6.01 (s, 2H), 3.85 (s, 3H), 3.73-3.67 (m, 1H), 3.53 (s, 3H), 3.13-3.07 (m, 1H), 2.33-2.26 (m, 1H), 2.09-1.95 (m, 2H), 1.92-1.86 (m, 2H), 1.69-1.63 (m, 1H)。
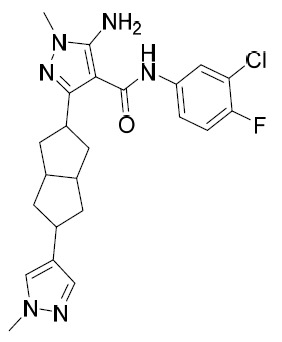
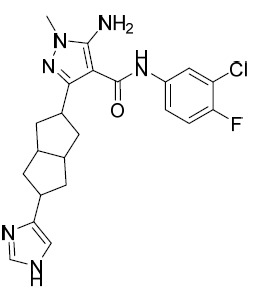
AIA-124-A及AIA-124-B 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-((1R,3S)-3-(4-(1- 甲基 -1H- 咪唑 -4- 基 ) 苯基 ) 環戊基 )-1H- 吡唑 -4- 甲醯胺 (CP-AIA-124-B) 及 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-((1S,3S)-3-(4-(1- 甲基 -1H- 咪唑 -4- 基 ) 苯基 ) 環戊基 )-1H- 吡唑 -4- 甲醯胺 (CP-AIA-124-A) 。
根據針對AIA-003A及AIA-003B所闡述之程序來合成標題化合物。CP-AIA-124-A:1
H-NMR (DMSO-d6
, 400 MHz): δ 8.94 (s, 1H) , 7.92 (dd,J
= 2.4, 6.8Hz, 1H), 7.60 (t,J
= 8.0Hz, 3H), 7.54-7.51 (m, 2H), 7.33 (t,J
= 9.2Hz, 1H), 7.21 (d,J
= 8.4Hz, 2H), 6.05 (s, 2H), 3.86 (t,J
= 8.0Hz, 1H), 3.67 (s, 3H), 3.53 (s, 3H), 3.12 (t,J
= 8.0Hz, 1H), 2.20-2.08 (m, 3H), 2.00-1.94 (m, 2H), 1.65 (t,J
= 8.4Hz, 1H)。CP-AIA-124-B:1
H-NMR (DMSO-d6
, 400 MHz): δ 8.98 (s, 1H) , 7.93 (dd,J
= 2.4, 6.8Hz, 1H), 7.65-7.52 (m, 5H), 7.36 (t,J
= 9.2Hz, 1H), 7.23 (d,J
= 8.4Hz, 2H), 6.02 (s, 2H), 3.71 (t,J
= 9.6Hz, 1H), 3.67 (s, 3H), 3.53 (s, 3H), 2.33-2.27 (m, 1H), 2.10-2.04 (m, 2H), 2.02-1.87 (m, 2H), 1.70-1.64 (m, 2H)。
中間體18 3-( 吡啶 -4- 基 ) 環戊 -2- 烯 -1- 酮
。向4-溴吡啶(2 g, 10.29 mmol, 1當量,HCl)於二噁烷(30 mL)及H2
O (6 mL)中之溶液中添加3-(4,4,5,5-四甲基-1,3,2-二氧硼㖦-2-基)環戊-2-烯-1-酮(3.21 g, 15.43 mmol, 1.5當量)、Pd(dppf)Cl2
(752.56 mg, 1.03 mmol, 0.1當量)及K3
PO4
(6.55 g, 30.87 mmol, 3當量)。將懸浮液脫氣並使用N2
吹掃3次。將混合物在N2
及80℃下攪拌16 hr。過濾反應混合物,且使用水(20 mL)稀釋濾液並使用EtOAc (30 mL × 3)萃取。使用鹽水(15 mL × 2)洗滌合併之有機層,藉由Na2
SO4
乾燥,過濾並在減壓下濃縮以得到殘餘物,藉由急速矽膠層析(ISCO®;40 g SepaFlash®二氧化矽急速管柱,0~100%乙酸乙酯/石油醚梯度之洗脫劑,在40 mL/min下)純化以得到黃色固體形式之3-(4-吡啶基)環戊-2-烯-1-酮(1.2 g, 7.54 mmol, 73.26%產率)。1
H NMR (400 MHz,氯仿-d) δ 2.52-2.67 (m, 2H), 3.00 (dt, J=4.85, 2.21 Hz, 2H), 6.65 (d, J=1.76 Hz, 1H), 7.40-7.47 (m, 2H), 8.69 (br d, J=4.41 Hz, 2H)。
中間體 19-23.
根據針對中間體18所闡述之程序來合成中間體19-23。
| 中間體 | 結構 | 表徵 |
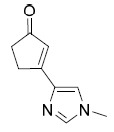
| 19 | 3-(1- 甲基 -1H- 咪唑 -4- 基 ) 環戊 -2- 烯 -1- 酮 1 H NMR (400 MHz,氯仿-d) δ ppm 2.49-2.59 (m, 2H), 2.98 (td, J=4.85, 1.54 Hz, 1H), 2.96-2.98 (m, 1H), 3.76 (s, 3H), 6.49 (s, 1H), 7.31 (s, 1H), 7.48-7.62 (m, 1H)。 | |
| 20 | 3-(4-( 二甲基胺基 ) 苯基 ) 環戊 -2- 烯 -1- 酮 LCMS: 202.2 [M+1]+ 。 | |
| 21 | 3-( 吡啶 -3- 基 ) 環戊 -2- 烯 -1- 酮 1 H NMR (400 MHz,氯仿-d) δ ppm 2.58 - 2.65 (2 H, m), 3.03 - 3.11 (2 H, m), 6.64 (1 H, t, J=1.76 Hz), 7.40 (1 H, ddd, J=7.99, 4.80, 0.66 Hz), 7.93 (1 H, dt, J=7.94, 1.98 Hz), 8.69 (1 H, dd, J=4.85, 1.54 Hz), 8.90 - 8.92 (1 H, m)。 | |
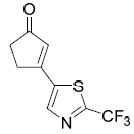
| 22 | 3-(2-( 三氟甲基 ) 噻唑 -5- 基 ) 環戊 -2- 烯 -1- 酮 MS 計算值:233.2,MS實驗值:234.0 [M + 1]+ | |
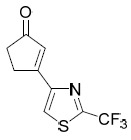
| 23 | 3-(2-( 三氟甲基 ) 噻唑 -4- 基 ) 環戊 -2- 烯酮 . MS 計算值:233.2,MS 實驗值:234.4 [M + 1]+ 。 |
中間體24 3-(4-( 二甲基胺基 ) 苯基 ) 環戊烷 -1- 酮。
在N2
氣氛下,向3-[4-(二甲基胺基)苯基]環戊-2-烯-1-酮(1.05 g, 4.97 mmol, 1當量)於MeOH (20 mL)中之溶液中添加Pd/C (200 mg, 10%純度)。將懸浮液脫氣並使用H2
吹掃3次。將混合物在H2
(40 psi)及20℃下攪拌16 hr。過濾混合物,並在真空下濃縮濾液以得到黃色油狀物形式之3-[4-(二甲基胺基)苯基]環戊酮(900 mg, 2.51 mmol, 50.6%產率,56.7%純度)。LCMS: 203.9 [M+1]+
。
中間體 25-26.
根據針對中間體24所闡述之程序來合成中間體25-26。
| 中間體 | 結構 | 表徵 |
| 25 | 3-( 吡啶 -3- 基 ) 環戊烷 -1- 酮 1 H NMR (400 MHz,氯仿-d) δ ppm 1.94 - 2.07 (1 H, m), 2.29 - 2.41 (2 H, m), 2.46 - 2.57 (2 H, m), 2.66 - 2.78 (1 H, m), 3.38 - 3.52 (1 H, m), 7.27 - 7.31 (1 H, m), 7.56 - 7.60 (1 H, m), 8.52 (1 H, dd, J=4.74, 1.65 Hz), 8.56 (1 H, d, J=2.20 Hz)。 | |
| 26 | 3-( 吡啶 -4- 基 ) 環戊烷 -1- 酮 1 H NMR (400 MHz,氯仿-d) δ 1.91-1.95 (m, 1H), 2.17-2.30 (m, 2H), 2.37-2.48 (m, 2H), 2.63 (dd, J=18.19, 7.61 Hz, 1H), 3.29-3.40 (m, 1H), 7.03-7.18 (m, 2H), 8.37-8.53 (m, 2H)。 |
中間體27 3-(2- 氯苯基 ) 環戊烷 -1- 酮
。將(2-氯苯基)酸(1.14 g, 7.31 mmol)、環戊-2-烯-1-酮(500 mg, 6.09 mmol, 0.510 mL)及[Rh(COD)2
Cl]2
(60.06 mg, 0.122 mmol)於7.7 mL 10:1 EtOH/H2
O中之黃色懸浮液在50℃下攪拌50 hr。然後過濾黃色懸浮液,並在真空下濃縮濾液。藉由矽膠層析(於石油醚中之0至9.4% EtOAc梯度之洗脫劑)純化所得殘餘物以產生黃色油狀物形式之標題化合物。1
H NMR (400 MHz,氯仿-d) δ ppm 1.96 - 2.07 (1 H, m), 2.26 - 2.49 (4 H, m), 2.72 (1 H, dd, J=18.19, 7.83 Hz), 3.81 - 3.90 (1 H, m), 7.16 - 7.22(1 H, m), 7.25 - 7.28 (2 H, m), 7.39 (1 H, dt, J=7.77, 0.85 Hz)。中間體 28-38
根據針對中間體27所闡述之程序來合成中間體28-38。
| 中間體 | 結構 | 表徵 |
| 28 | 3-(3- 氯苯基 ) 環戊烷 -1- 酮 1 H NMR (400 MHz,氯仿-d) δ ppm 1.86 - 2.02 (m, 1H), 2.19 - 2.58 (m, 4H), 2.59 - 2.71 (m, 1H), 3.29 - 3.52 (m, 1H), 7.18 - 7.38 (m, 4H)。 | |
| 29 | 3-(4- 氯苯基 ) 環戊烷 -1- 酮 1 H NMR (400 MHz,氯仿-d) δ ppm 1.88 - 2.03 (m, 1H) 2.22 - 2.37 (m, 2H) 2.39 - 2.53 (m, 2H) 2.59 - 2.73 (m, 1H) 3.40 (tt,J =10.95, 6.87Hz,1H) 7.16 - 7.22 (m, 2H) 7.29 - 7.34 (m, 2H) | |
| 30 | 3-(2- 甲氧基苯基 ) 環戊烷 -1- 酮 1 H NMR (400 MHz,氯仿-d) δ ppm 2.01 - 2.13 (m, 1H) 2.27 - 2.50 (m, 4H) 2.66 (dd, J=18.40, 8.13 Hz, 1H) 3.66 - 3.76 (m, 1H) 3.86 (s, 3H) 6.89 - 6.99 (m, 2H) 7.18 - 7.28 (m, 2H)。 | |
| 31 | 3-(3- 甲氧基苯基 ) 環戊烷 -1- 酮 1 H NMR (400 MHz,氯仿-d) δ ppm 1.95 - 2.08 (m, 1H) 2.27 - 2.53 (m, 4H) 2.69 (dd, J=18.10, 7.46 Hz, 1H) 3.42 (ddd, J=10.85, 6.69, 3.85 Hz,1H) 3.84 (s, 3H) 6.78 - 6.90 (m, 3H) 7.26 - 7.32 (m, 1H)。 | |
| 32 | 3-(4- 氟苯基 ) 環戊烷 -1- 酮 1 H NMR (400 MHz,氯仿-d) δ ppm 1.88 - 2.05 (m, 1H) 2.23 - 2.36 (m, 2H) 2.38 - 2.51 (m, 2H) 2.66 (dd, J=17.86, 7.50 Hz, 1H) 3.33 - 3.47 (m, 1H) 6.97 - 7.07 (m, 2H) 7.17 - 7.24 (m, 2H)。 | |
| 33 | 3-(4-( 三氟甲氧基 ) 苯基 ) 環戊烷 -1- 酮 1 H NMR (400 MHz,氯仿-d) δ ppm 1.93 - 2.05 (m, 1H) 2.28 - 2.40 (m, 2H) 2.43 - 2.59 (m, 2H) 2.72 (br dd,J =18.19, 7.61 Hz, 1H) 3.36 - 3.57 (m, 1H) 7.22 (br d,J =8.16 Hz, 2H) 7.27 - 7.36 (m, 2H)。 | |
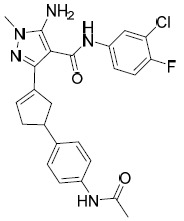
| 34 | N-(4-(3- 側氧基環戊基 ) 苯基 ) 乙醯胺 1 H NMR (400 MHz,氯仿-d) δ ppm 1.83 - 1.99 (m, 1H) 2.11 (s, 3H) 2.24 (br dd, J=18.08, 10.58 Hz, 2H) 2.30 - 2.46 (m, 2H) 2.58 (br dd, J=18.30, 7.28Hz, 1H) 3.24 - 3.42 (m, 1H) 7.14 (br d, J=8.38 Hz, 2H) 7.40 (br d, J=8.38 Hz, 2H);LC-MS: 217.9 [M+1]+ 。 | |
| 35 | 3-(4- 異丙氧基苯基 ) 環戊烷 -1- 酮 1 H NMR (400 MHz,氯仿-d) δ ppm 1.34 (d, J=5.95 Hz, 6H) 1.88 - 2.02 (m, 1H) 2.23 - 2.36 (m, 2H) 2.38 - 2.51 (m, 2H) 2.58 - 2.71 (m, 1H) 3.27 - 3.45 (m, 1H) 4.54 (spt, J=5.92 Hz, 1H) 6.87 (d, J=8.16 Hz, 2H) 7.15 (s, 2H)。 | |
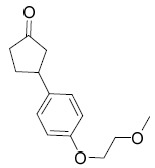
| 36 | 3-(4-(2- 甲氧基乙氧基 ) 苯基 ) 環戊烷 -1- 酮 1 H NMR (400 MHz,氯仿-d) δ ppm 1.87-2.02 (m, 1H), 2.23-2.47 (m, 4H), 2.59-2.77 (m, 1H), 3.31-3.49 (m, 4H), 3.76 (dd, J=5.40, 4.08 Hz, 2H), 4.07-4.15 (m, 2H), 6.87-6.94 (m, 2H), 7.17 (d, J=8.60 Hz, 2H);LCMS: 235.0 [M+1]+ 。 | |
| 37 | 3-(2-( 三氟甲基 ) 噻唑 -5- 基 ) 環戊酮 MS 計算值:235.2,MS實驗值:236.0 [M + 1]+ 。 | |
| 38 | 3-(2-( 三氟甲基 ) 噻唑 -4- 基 ) 環戊酮 MS 計算值:235.0,MS 實驗值:236.2 [M + 1]+ 。 |
中間體 39-55.
根據針對中間體11或15所闡述之程序來合成中間體39-55。
| 中間體 | 結構 | 表徵 |
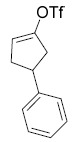
| 39 | 三氟甲烷磺酸 4- 苯基環戊 -1- 烯 -1- 基酯 1 H NMR (400 MHz,氯仿-d) ppm 2.44 - 2.63 (m, 1 H) 2.67 - 2.82 (m, 1 H) 2.86 - 2.97 (m, 1 H) 2.99 -3.08 (m, 1 H) 3.62 - 3.71 (m, 1 H) 5.71 - 5.77 (m, 1 H) 7.18 - 7.28 (m, 2 H) 7.32 - 7.40 (m, 3 H)。 | |
| 40 | 三氟甲烷磺酸 4-(1- 甲基 -1H- 咪唑 -4- 基 ) 環戊 -1- 烯 -1- 基酯 1 H NMR (400 MHz,氯仿-d) δ ppm 2.40-2.98 (m, 4H), 3.62-3.65 (m, 3H), 3.98 (ddd, J=8.43, 5.57, 2.76 Hz, 1H), 5.60-5.79 (m, 1H), 6.57-6.70 (m, 1H), 7.33-7.42 (m, 1H)。 | |
| 41 | 三氟甲烷磺酸 4-(4-( 二甲基胺基 ) 苯基 ) 環戊 -1- 烯 -1- 基酯 1 H NMR (400 MHz,氯仿-d) δ ppm 1.83-1.95 (m, 1H), 2.44-2.59 (m, 1H), 2.60-2.81 (m, 2H), 2.91-2.95 (m, 7H), 5.70 (br s, 1H), 6.72 (br d, J=8.38 Hz, 3H), 7.01-7.19 (m, 2H) | |
| 42 | 三氟甲烷磺酸 4-( 吡啶 -3- 基 ) 環戊 -1- 烯 -1- 基酯 1 H NMR (400 MHz,氯仿-d) δ ppm 1.72 - 1.80 (m, 1H), 2.38 - 2.49 (m, 1H), 2.53 - 2.62 (m, 2H, m, 1H, 3.87 (ddd, J=8.71, 5.95, 2.98 Hz, 1H), 5.54 -5.60 (m, 1H), 7.11 - 7.14 (m, 1H), 7.35 (dt, J=7.94, 1.98 Hz, 1H), 8.28 - 8.38 (m, 1H);LCMS: 294.2 [M+1]+ 。 | |
| 43 | 三氟甲烷磺酸 4-( 吡啶 -4- 基 ) 環戊 -1- 烯 -1- 基酯 LCMS: 294.2 [M+1]+ 。 | |
| 44 | 三氟甲烷磺酸 4-(2- 氯苯基 ) 環戊 -1- 烯 -1- 基酯 1 H NMR (400 MHz,氯仿-d) δ ppm 2.38 - 2.52 (m, 1H), 2.63 - 2.70 (m, 1H), 2.76 - 2.92 (m, 1H), 2.99 (dddt, J=16.37, 9.65, 3.36, 1.74, 1.74 Hz, 1H), 3.99 - 4.11 (m, 1H), 5.63 - 5.66 (m, 1H), 7.08 - 7.18 (m, 1H), 7.23 - 7.32 (m, 1H)。 | |
| 45 | 三氟甲烷磺酸 4-(3- 氯苯基 ) 環戊 -1- 烯 -1- 基酯 1 H NMR (400 MHz,氯仿-d) δ ppm 2.47 - 2.60 (m, 1H), 2.69 - 2.74 (m, 1H, 2.85 - 2.94 (m, 1H, 2.98 - 3.06 (m, 1H, 3.55 - 3.67 (m, 1H, 5.70 (d, J=2.21 Hz), 7.10 - 7.17 (m, 1H, 7.20 - 7.26 (m, 3H) | |
| 46 | 三氟甲烷磺酸 4-(3- 氯苯基 ) 環戊 -1- 烯 -1- 基酯 1 H NMR (400 MHz,氯仿-d) δ ppm 1.80 - 1.95 (m, 1H) 2.43 - 2.62 (m, 1H) 2.64 - 2.78 (m, 1H) 2.90 (ddtd,J =16.41, 9.07, 2.89, 2.89, 1.38 Hz, 1H) 3.03 (dddt,J =16.19, 9.60, 3.20, 1.57, 1.57 Hz, 1H) 3.62 (tt,J =9.29, 6.78 Hz, 1H) 3.97 (ddq,J =8.66, 5.87, 2.77, 2.77, 2.77 Hz, 1H) 5.71 (dq,J =4.83, 2.32Hz, 1H) 7.09 - 7.15 (m, 1H) 7.16 - 7.22 (m, 1H) 7.28 - 7.33 (m, 2H)。 | |
| 47 | 三氟甲烷磺酸 4-(2- 甲氧基苯基 ) 環戊 -1- 烯 -1- 基酯 未經進一步純化即用於下一反應中。 | |
| 48 | 三氟甲烷磺酸 4-(3- 甲氧基苯基 ) 環戊 -1- 烯 -1- 基酯 未經進一步純化即用於下一反應中。 | |
| 49 | 三氟甲烷磺酸 4-(4- 氟苯基 ) 環戊 -1- 烯 -1- 基酯 未經進一步純化即用於下一反應中。 | |
| 50 | 三氟甲烷磺酸 4-(4-( 三氟甲氧基 ) 苯基 ) 環戊 -1- 烯 -1- 基酯 1 H NMR (400 MHz,氯仿-d) δ ppm 2.45 - 2.64 (m, 1H) 2.65 - 2.81 (m, 2H) 2.85 - 3.10 (m, 1H) 3.60 - 4.05 (m, 1H) 5.67 - 5.76 (m, 1H) 7.14 - 7.23 (m, 3H) 7.27 - 7.31 (m, 1H)。 | |
| 51 | 三氟甲烷磺酸 4-(4- 乙醯胺基苯基 ) 環戊 -1- 烯 -1- 基酯 LC-MS: 349.9 [M+1]+ . | |
| 52 | 三氟甲烷磺酸 4-(4- 異丙氧基苯基 ) 環戊 -1- 烯 -1- 基酯 1 H NMR (400 MHz,氯仿-d) δ ppm 1.32 - 1.34 (m, 6H) 2.43 - 2.77 (m, 3H) 2.80 - 3.05 (m, 1H) 3.52 - 3.98 (m, 1H) 4.46 - 4.60 (m, 1H) 5.62 - 5.79 (m, 1H) 6.77 - 6.89 (m, 2H) 7.03 - 7.21 (m, 2H)。 | |
| 53 | 三氟甲烷磺酸 3-(4-(2- 甲氧基乙氧基 ) 苯基 ) 環戊 -1- 烯 -1- 基酯 1 H NMR (400 MHz,氯仿-d) δ ppm 2.36-2.62 (m, 1H), 2.65-2.73 (m, 1H), 2.80-2.92 (m, 1H), 2.93-3.05 (m, 1H), 3.45 (s, 3H), 3.53-3.66 (m, 1H), 3.72-3.79 (m, 2H), 4.07-4.13 (m, 2H), 5.69 (br d, J=2.01 Hz, 1H), 6.85-6.92 (m, 2H), 7.06-7.20 (m, 2H)。 | |
| 54 | 三氟甲烷磺酸 3-(2-( 三氟甲基 ) 噻唑 -5- 基 ) 環戊 -1- 烯基酯 MS 計算值:367.3,MS實驗值:367.9 [M + 1]+ 。 | |
| 55 | 三氟甲烷磺酸 3-(2-( 三氟甲基 ) 噻唑 -4- 基 ) 環戊 -1- 烯基酯 MS 計算值:367.0,MS 實驗值:368.0 [M + 1]+ |
中間體 56-72.
根據針對中間體16所闡述之程序來合成中間體56-72。
| 中間體 | 結構 | 表徵 |
| 56 | 4,4,5,5- 四甲基 -2-(3- 苯基環戊 -1- 烯 -1- 基 )-1,3,2- 二氧硼㖦 1 H NMR (400 MHz,氯仿-d) δ ppm 1.28 - 1.32 (m, 12 H) 2.36 - 2.69 (m, 3 H) 2.86 - 3.00 (m, 1 H) 3.49 (t, J=8.41 Hz, 1 H) 6.51 - 6.60 (m, 1 H) 7.15 - 7.34 (m, 5 H)。 | |
| 57 | (4-(1- 甲基 -1H- 咪唑 -4- 基 ) 環戊 -1- 烯 -1- 基 ) 酸 1 H NMR (400 MHz,氯仿-d) δ ppm 1.90 (br s, 1H), 1.92-2.06 (m, 1H), 2.30-2.63 (m, 4H), 3.55 (s, 3H), 3.93 (br s, 1H), 5.52-5.72 (m, 1H), 6.52 (s, 1H), 7.31 (s, 1H)。 | |
| 58 | N,N- 二甲基 -4-(3-(4,4,5,5- 四甲基 -1,3,2- 二氧硼㖦 -2- 基 ) 環戊 -3- 烯 -1- 基 ) 苯胺 1 H NMR (400 MHz,氯仿-d) δ ppm 1.27 (br d, J=4.41 Hz, 12H), 1.60-1.77 (m, 1H), 2.26-2.65 (m, 3H), 2.68-2.95 (m, 7H), 6.44-6.59 (m, 1H), 6.98-7.16 (m, 2H), 7.36-7.40 (m, 2H)。 | |
| 59 | 3-(3-(4,4,5,5- 四甲基 -1,3,2- 二氧硼㖦 -2- 基 ) 環戊 -3- 烯 -1- 基 ) 吡啶 1 H NMR (400 MHz,氯仿-d) δ ppm 1.26 - 1.30 (m, 12H), 1.69 - 1.76 (m, 1H), 2.47 - 2.57 (m, 2H), 2.59 - 2.68 (m, 1H), 3.87 - 3.98 (m, 1H), 6.40 - 6.58 (m, 1H), 7.19 (dd, J=7.72, 4.85 Hz, 1H), 7.46 (dt, J=7.83, 1.82 Hz, 1H), 8.37 - 8.48 (m, 2H)。 | |
| 60 | 4-(3-(4,4,5,5- 四甲基 -1,3,2- 二氧硼㖦 -2- 基 ) 環戊 -3- 烯 -1- 基 ) 吡啶 1 H NMR (400 MHz, DMSO-d6 ) δ ppm 1.80 (s, 12H), 2.20-2.31 (m, 1H), 2.95-3.00 (m, 2H), 4.36-4.58 (m, 1H), 6.84-7.04 (m, 1H), 7.68-7.78 (m, 2H), 8.97-9.02 (m, 2H);LCMS: 272.3 [M+1]+ 。 | |
| 61 | 2-(4-(2- 氯苯基 ) 環戊 -1- 烯 -1- 基 )-4,4,5,5- 四甲基 -1,3,2- 二氧硼㖦 1 H NMR (400 MHz,氯仿-d) δ ppm 1.29 (d, J=7.50 Hz, 12H), 2.39 - 2.64 (m, 3H), 2.89 - 3.00 (m, 1H), 3.90 - 3.98 (m, 1H), 6.46 - 6.58 (m, 1H), 7.07 - 7.20 (m, 3H), 7.33 (d, J=7.50 Hz, 1H)。 | |
| 62 | 2-(4-(3- 氯苯基 ) 環戊 -1- 烯 -1- 基 )-4,4,5,5- 四甲基 -1,3,2- 二氧硼㖦 1 H NMR (400 MHz,氯仿-d) δ ppm 1.29 (13H, d, J=4.63 Hz), 2.34 - 2.69 (m, 3H), 2.85 - 2.98 (m, 1H), 3.38 - 3.52 (m, 1H), 6.47- 6.56 (m, 1H), 7.04 - 7.12 (m, 1H), 7.13 - 7.22 (m, 3H)。 | |
| 63 | 2-(4-(4- 氯苯基 ) 環戊 -1- 烯 -1- 基 )-4,4,5,5- 四甲基 -1,3,2- 二氧硼㖦 1 H NMR (400 MHz,氯仿-d) δ ppm 1.30 (d,J =4.03 Hz, 12H) 1.71 (ddt,J =12.55, 8.91, 7.18, 7.18 Hz, 1H) 2.23 - 2.71 (m, 3H) 2.82 - 3.02 (m, 1H) 3.36 - 3.53 (m, 1H) 3.87 - 3.97 (m, 1H) 6.43 - 6.59 (m, 1H) 7.09 - 7.19 (m, 2H) 7.21 - 7.26 (m, 2H)。 | |
| 64 | 2-(4-(2- 甲氧基苯基 ) 環戊 -1- 烯 -1- 基 )-4,4,5,5- 四甲基 -1,3,2- 二氧硼㖦 1 H NMR (400 MHz,氯仿-d) δ ppm 1.25 - 1.34 (m, 12H) 2.37 - 2.63 (m, 3H) 2.71 - 2.98 (m, 1H) 3.77 - 3.88 (m, 3H) 4.29 - 4.35 (m, 1H) 6.53 - 6.59 (m, 1H) 6.80 - 6.93 (m, 2H) 7.09 - 7.22 (m, 2H)。 | |
| 65 | 2-(4-(3- 甲氧基苯基 ) 環戊 -1- 烯 -1- 基 )-4,4,5,5- 四甲基 -1,3,2- 二氧硼㖦 1 H NMR (400 MHz,氯仿-d) δ ppm 1.24 - 1.32 (m, 12H) 2.34 - 2.71 (m, 3H) 2.85 - 2.99 (m, 1H) 3.46 (t, J=8.28 Hz, 1H) 3.76 -3.83 (m, 3H) 6.51 - 6.58 (m, 1H) 6.70 - 6.86 (m, 3H) 7.17 - 7.24 (m, 1H)。 | |
| 66 | 2-(4-(4- 氟苯基 ) 環戊 -1- 烯 -1- 基 )-4,4,5,5- 四甲基 -1,3,2- 二氧硼㖦 1 H NMR (400 MHz,氯仿-d) δ ppm 1.22 - 1.30 (m, 12H) 2.33 - 2.68 (m, 3H) 2.78 - 2.99 (m, 1H) 3.37 - 3.51 (m, 1H) 6.43 - 6.56 (m, 1H) 6.88 - 6.99 (m, 2H) 7.06 - 7.21 (m, 2H)。 | |
| 67 | 4,4,5,5- 四甲基 -2-(4-(4-( 三氟甲氧基 ) 苯基 ) 環戊 -1- 烯 -1- 基 )-1,3,2- 二氧硼㖦 1 H NMR (400 MHz,氯仿-d) δ ppm 1.30 (d,J =3.51 Hz, 12H) 1.73 (ddt,J =12.64, 8.82, 7.09, 7.09 Hz, 1H) 2.35 - 2.60 (m, 2H) 2.86 - 3.01 (m, 1H) 3.43 - 3.99 (m, 1H) 6.42 - 6.62 (m, 1H) 7.09 - 7.15 (m, 2H) 7.17 - 7.21 (m, 1H) 7.22 - 7.26 (m, 1H)。 | |
| 68 | N-(4-(3-(4,4,5,5- 四甲基 -1,3,2- 二氧硼㖦 -2- 基 ) 環戊 -3- 烯 -1- 基 ) 苯基 ) 乙醯胺 LC-MS: 328.1 [M+1]+ 。 | |
| 69 | 2-(4-(4- 異丙氧基苯基 ) 環戊 -1- 烯 -1- 基 )-4,4,5,5- 四甲基 -1,3,2- 二氧硼㖦 1 H NMR (400 MHz,氯仿-d) δ ppm 1.29 - 1.34 (m, 12H) 1.70 - 2.43 (m, 1H) 2.45 - 2.66 (m, 2H) 2.80 - 2.99 (m, 1H) 3.33 - 3.96 (m, 1H) 4.50 (dt, J=12.18, 6.15 Hz, 1H) 6.49 - 6.58 (m, 1H) 6.80 (d, J=8.60 Hz, 2H) 7.04 - 7.17 (m, 2H)。 | |
| 70 | 2-(4-(4-(2- 甲氧基乙氧基 ) 苯基 ) 環戊 -1- 烯 -1- 基 )-4,4,5,5- 四甲基 -1,3,2- 二氧硼㖦 1 H NMR (400 MHz,氯仿-d) δ ppm 1.31 (d, J=3.31 Hz, 12H), 2.32-2.70 (m, 3H), 2.80-3.02 (m, 1H), 3.36-3.51 (m, 3H), 3.76 (dd, J=5.51, 3.97 Hz, 2H), 3.87-3.98 (m, 1H), 4.07-4.14 (m, 2H), 6.47-6.63 (m, 1H), 6.86 (br d, J=8.60 Hz, 2H), 7.07-7.20 (m, 2H);LCMS:345.1 [M+1]+ 。 | |
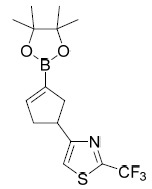
| 71 | 5-(3-(4,4,5,5- 四甲基 -1,3,2- 二氧硼㖦 -2- 基 ) 環戊 -2- 烯基 )-2-( 三氟甲基 ) 噻唑 MS 計算值:345.2,MS實驗值:346.1 [M + 1]+ 。 | |
| 72 | 4-(3-(4,4,5,5- 四甲基 -1,3,2- 二氧硼㖦 -2- 基 ) 環戊 -2- 烯基 )-2-( 三氟甲基 ) 噻唑 MS 計算值:345.1,MS 實驗值:346.4 [M + 1]+ 。 |
中間體 73-89.
根據針對中間體18所闡述之程序來合成中間體73-89。
AIA-202A、AIA-202B、AIA-202C及CP-202D 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(3- 苯基環戊基 )-1H- 吡唑 -4- 甲醯胺非對映異構體 1 (AIA-202A) 、非對映異構體 2 (AIA-202B) 、非對映異構體 3 (AIA-202C) 、非對映異構體 4 (AIA-202D) 。
將5-胺基-N-(3-氯-4-氟-苯基)-1-甲基-3- (3-苯基環戊烯-1-基)吡唑-4-甲醯胺(400 mg, 0.801 mmol, 1當量)及RhCl(PPh3
)3
(37.05 mg, 0.040 mmol, 0.05當量)於MeOH (20 mL)中之褐色溶液在50 Psi H2
及45℃下攪拌16 hr。在真空下濃縮反應液以得到粗製褐色油狀物。藉由急速矽膠層析(Combi-flash®;4 g SepaFlash®二氧化矽急速管柱, 0~5.5% MeOH/DCM梯度之洗脫劑,在20 mL/min下)純化殘餘物,隨後藉由SFC純化以提供5-胺基-N-(3-氯-4-氟-苯基)-1-甲基-3-(3-苯基環戊基)吡唑-4-甲醯胺之4種非對映異構體。AIA-202A:1
H NMR (400 MHz, DMSO-d6) δ ppm 1.67 (dt, J=9.87, 4.91 Hz, 1 H) 1.86 - 1.99 (m, 2 H) 2.01 - 2.12 (m, 2 H) 2.26 - 2.35 (m, 1 H) 3.07 - 3.16 (m, 1 H) 3.52 (s, 3 H) 3.66 - 3.76 (m, 1 H) 6.01 (s, 2 H) 7.14 - 7.22 (m, 1 H) 7.24 - 7.38 (m, 5 H) 7.56 (ddd, J=9.05, 4.34, 2.63 Hz, 1 H) 7.94 (d, J=6.71 Hz, 1 H) 8.99 (s, 1 H);LC-MS: 413.3 [M+1]+
;及de: 100 %。AIA-202B:1
H NMR (400 MHz, DMSO-d6) δ ppm 1.60 - 1.74 (m, 1 H) 1.85 - 2.01 (m, 2 H) 2.01 - 2.13 (m, 2 H) 2.31 (br dd, J=12.05, 6.27 Hz, 1 H) 3.05 - 3.20 (m, 1 H) 3.48 - 3.56 (m, 3 H) 3.65 - 3.79 (m, 1 H) 6.01 (s, 2 H) 7.05 - 7.22 (m, 1 H) 7.24 - 7.39 (m, 5 H) 7.47 - 7.74 (m, 1 H) 7.94 (d, J=6.59 Hz, 1 H) 8.98 (s, 1 H);LC-MS: 413.3 [M+1]+
;及de: 100 %。AIA-202C:1
H NMR (400 MHz, DMSO-d6) δ ppm 1.59 - 1.70 (m, 1 H) 1.91 - 2.04 (m, 2 H) 2.07 - 2.23 (m, 3 H) 3.10 - 3.23 (m, 1 H) 3.53 (s, 3 H) 3.82 - 3.90 (m, 1 H) 6.04 (s, 2 H) 7.12 - 7.19 (m, 1 H) 7.24 - 7.37 (m, 5 H) 7.54 (ddd, J=9.02, 4.31, 2.57 Hz, 1 H) 7.91 (d, J=6.74 Hz, 1 H) 8.94 (s, 1 H);LC-MS: 413.3 [M+1]+
;及de: 97.6 %。AIA-202D:1
H NMR (400 MHz, DMSO-d6) δ ppm 1.12 - 1.33 (m, 4 H) 1.57 - 1.72 (m, 1 H) 1.90 - 2.02 (m, 2 H) 2.04 - 2.20 (m, 3 H) 2.26 - 2.39 (m, 1 H) 3.07 - 3.21 (m, 1 H) 3.53 (d, J=1.47 Hz, 3 H) 3.71 (br s, 1 H) 3.79 - 3.91 (m, 1 H) 5.96 - 6.09 (m, 2 H) 7.13 - 7.38 (m, 7 H) 7.45 - 7.59 (m, 1 H) 7.86 - 7.96 (m, 1 H) 8.91 - 9.00 (m, 1 H);LC-MS: 413.3 [M+1]+
。表 1.
根據針對CP-AIA-202A-D所闡述之程序來合成表1中之化合物
| 中間體 | 結構 | 表徵 |
| 73 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(3- 苯基環戊 -1- 烯 -1- 基 )-1H- 吡唑 -4- 甲醯胺 LC-MS: 411.1 [M+1]+ 。 | |
| 74 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(4-(1- 甲基 -1H- 咪唑 -4- 基 ) 環戊 -1- 烯 -1- 基 )-1H- 吡唑 -4- 甲醯胺 LCMS: 437.0 [M+23]+ 。 | |
| 75 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(4-(4-( 二甲基胺基 ) 苯基 ) 環戊 -1- 烯 -1- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺 LCMS: 476.0 [M+1]+ 。 | |
| 76 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(4-( 吡啶 -3- 基 ) 環戊 -1- 烯 -1- 基 )-1H- 吡唑 -4- 甲醯胺 LCMS: 412.0 [M+1]+ 。 | |
| 77 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(4-( 吡啶 -4- 基 ) 環戊 -1- 烯 -1- 基 )-1H- 吡唑 -4- 甲醯胺 LCMS: 412.0 [M+1]+ 。 | |
| 78 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(4-(2- 氯苯基 ) 環戊 -1- 烯 -1- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺 LCMS: 445.0 [M+1]+ 。 | |
| 79 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(4-(3- 氯苯基 ) 環戊 -1- 烯 -1- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺 LCMS: 445.0 [M+1]+ 。 | |
| 80 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(4-(4- 氯苯基 ) 環戊 -1- 烯 -1- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺, 未經進一步純化即用於下一反應中 | |
| 81 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(4-(2- 甲氧基苯基 ) 環戊 -1- 烯 -1- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺 LCMS: 441.0 [M+1]+ 。 | |
| 82 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(4-(3- 甲氧基苯基 ) 環戊 -1- 烯 -1- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺 LCMS: 441.0 [M+1]+ 。 | |
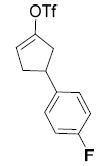
| 83 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(4-(4- 氟苯基 ) 環戊 -1- 烯 -1- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺 LCMS: 429.0 [M+1]+ 。 | |
| 84 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(4-(4-( 三氟甲氧基 ) 苯基 ) 環戊 -1- 烯 -1- 基 )-1H- 吡唑 -4- 甲醯胺 LCMS: 495.0 [M+1]+ 。 | |
| 85 | 3-(4-(4- 乙醯胺基苯基 ) 環戊 -1- 烯 -1- 基 )-5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺 LCMS 490.2 [M+23]+ 。 | |
| 86 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(4-(4- 異丙氧基苯基 ) 環戊 -1- 烯 -1- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺 LCMS: 469.0 [M+1]+ 。 | |
| 87 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(4-(4-(2- 甲氧基乙氧基 ) 苯基 ) 環戊 -1- 烯 -1- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺 LCMS: 485.0 [M+1]+ 。 | |
| 88 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(3-(2-( 三氟甲基 ) 噻唑 -5- 基 ) 環戊 -1- 烯基 )-1H- 吡唑 -4- 甲醯胺 MS 計算值:485.9,MS實驗值:486.1 [M + 1]+ | |
| 89 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(3-(2-( 三氟甲基 ) 噻唑 -4- 基 ) 環戊 -1- 烯基 )-1H- 吡唑 -4- 甲醯胺 MS 計算值:485.1,MS 實驗值:486.3 [M + 1]+ |
| 化合物 | 結構及表徵 |
| CP-AIA-280 | 5- 胺基 -N-(3- 氯 -4- 氟 - 苯基 )-1- 甲基 -3-[3-(1- 甲基咪唑 - 4- 基 ) 環戊基 ] 吡唑 -4- 甲醯胺 。1 H NMR (400 MHz,氯仿-d) δ 1.81-1.92 (m, 1H), 2.01 (ddd, J=12.36, 10.10, 8.41 Hz, 1H), 2.12-2.36 (m, 3H), 2.39-2.51 (m, 1H), 3.30-3.46 (m, 1H), 3.62 (d, J=15.81 Hz, 6H), 5.34-5.43 (m, 2H), 6.63 (s, 1H), 7.08 (t, J=8.91 Hz, 1H), 7.29-7.36 (m, 1H), 7.58 (ddd, J=8.97, 4.20, 2.64 Hz, 1H), 7.66 (dd, J=6.65, 2.64 Hz, 1H), 7.89 (s, 1H);LCMS: 439.0 [M+23]+ 。 |
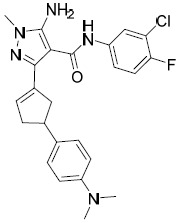
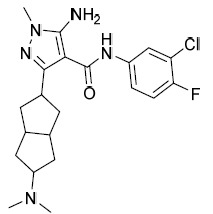
| CP-AIA-293 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(3-(4-( 二甲基胺基 ) 苯基 ) 環戊基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺 1 H NMR (400 MHz,氯仿-d) δ 1.79-1.96 (m, 1H), 2.05-2.39 (m, 4H), 2.44 (dt, J=12.86, 6.49 Hz, 1H), 2.89-2.97 (m, 6H), 3.06-3.23 (m, 1H), 3.30-3.52 (m, 1H), 3.61 (s, 3H), 5.21-5.39 (m, 2H), 6.62-6.81 (m, 2H), 7.02-7.24 (m, 3H), 7.32 (ddd, J=8.91, 4.02, 2.64 Hz, 1H), 7.37 (s, 1H), 7.68-7.80 (m, 1H);LCMS: 456.2 [M+1]+ 。 |
| CP-AIA-270 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(3-( 吡啶 -3- 基 ) 環戊基 )-1H- 吡唑 -4- 甲醯胺 |
| CP-AIA-271 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(3-( 吡啶 -4- 基 ) 環戊基 )-1H- 吡唑 -4- 甲醯胺。 1 H NMR (400 MHz,氯仿-d) δ 1.86-2.05 (m, 1H), 2.13-2.42 (m, 4H), 2.43-2.57 (m, 1H), 3.14-3.26 (m, 1H), 3.41-3.51 (m, 1H), 3.61 (s, 3H), 5.27 (s, 2H), 7.12 (t, J=8.66 Hz, 1H), 7.24 (br s, 2H), 7.30-7.36 (m, 2H), 7.71 (dd, J=6.40, 2.64 Hz, 1H), 8.51 (br d, J=5.02 Hz, 2H);LCMS: 414.0 [M+1]+ 。 |
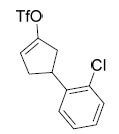
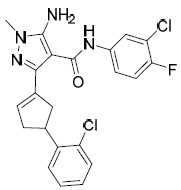
| CP-AIA-272 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(3-(2- 氯苯基 ) 環戊基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 1 H NMR (400 MHz, DMSO-d6) δ ppm 1.65 (1 H, td, J=9.70, 5.51 Hz), 1.84 - 1.96 (2 H, m), 2.01 - 2.12 (2 H, m), 2.25 - 2.32 (1 H, m), 3.46 - 3.53 (4 H, m), 3.65 - 3.79 (1 H, m), 5.96 - 6.03 (2 H, m), 7.15 - 7.20 (1 H, m), 7.25 - 7.38 (3 H, m), 7.43 (1 H, dd, J=7.83, 1.65 Hz), 7.54 (1 H, ddd, J=8.99, 4.24, 2.65 Hz), 7.91 (1 H, dd, J=6.84, 2.65 Hz), 8.92 - 8.97 (1 H, m);LCMS: 446.9 [M+1]+ 。 |
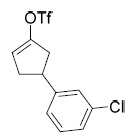
| CP-AIA-273 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(3-(3- 氯苯基 ) 環戊基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 1 H NMR (400 MHz, DMSO-d6) δ ppm 1.57 - 1.68 (1 H, m), 1.84 - 1.96 (2 H, m), 1.98 - 2.10 (2 H, m), 2.25 - 2.33 (1 H, m), 3.07 - 3.17 (1 H, m), 3.50 (3 H, s), 3.62 - 3.86 (1 H, m), 5.92 - 6.05 (2 H, m), 7.15 - 7.37 (5 H, m), 7.53 (1 H, ddd, J=9.04, 4.41, 2.65 Hz), 7.91 (1 H, dd, J=6.95, 2.54 Hz), 8.97 (1 H, s);LCMS: 446.9 [M+1]+ 。 |
| CP-AIA-274 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(3-(4- 氯苯基 ) 環戊基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 1 H NMR (400 MHz, DMSO-d6) δ ppm 1.62 (td, J=9.98, 5.18 Hz, 1 H) 1.82 - 1.96 (m, 2 H) 2.00 - 2.11 (m, 2 H) 2.24 - 2.35 (m, 1 H) 3.04 - 3.19 (m, 1 H) 3.51(s, 3 H) 3.62 - 3.87 (m, 1 H) 5.95 - 6.08 (m, 2 H) 7.26 - 7.38 (m, 5 H) 7.50 - 7.57 (m, 1 H) 7.85 - 7.95 (m, 1 H) 8.91 - 9.02 (m, 1 H);LCMS: 446.9 [M+1]+ 。 |
| CP-AIA-275A | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(3-(2- 甲氧基苯基 ) 環戊基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺,非對映異構體 1 (CP-AIA-275A) 1 H NMR (400 MHz,氯仿-d) δ ppm 1.85 - 1.91 (m, 1 H) 2.09 - 2.32 (m, 5 H) 3.36 - 3.45 (m, 1 H) 3.53 (s, 3 H) 3.55 - 3.62 (m, 1 H) 3.73 (s, 3 H) 5.25 (s, 2 H) 6.82 - 6.90 (m, 2 H) 6.97 (d, J=8.60 Hz, 1 H) 7.01 - 7.05 (m, 1 H) 7.14 - 7.19 (m, 2 H) 7.23 (s, 1 H) 7.54 (dd, J=6.62, 2.65 Hz, 1 H);LC-MS: 443.0 [M+1]+ 。 |
| CP-AIA-275B | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(3-(2- 甲氧基苯基 ) 環戊基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺,非對映異構體 2 (CP-AIA-275B) 。 1 H NMR (400 MHz, DMSO-d6) δ ppm 1.61 (br d, J=10.04 Hz, 1 H) 1.78 - 2.11 (m, 4 H) 2.18 - 2.25 (m, 1 H) 3.40 - 3.47 (m, 1 H) 3.51 (s, 2 H) 3.48 - 3.56 (m,1 H) 3.66 - 3.78 (m, 4 H) 6.03 (s, 2 H) 6.88 (t, J=7.50 Hz, 1 H) 6.92 (d, J=7.77 Hz, 1 H) 7.15 (t, J=7.77 Hz, 1 H) 7.23 (d, J=7.20 Hz, 1 H) 7.36 (t, J=9.14 Hz,1 H) 7.53 - 7.58 (m, 1 H) 7.93 (d, J=6.56 Hz, 1 H) 8.92 - 8.96 (m, 1 H);LC-MS: 443.0 [M+1]+ 。 |
| CP-AIA-275C/CP-AIA-D | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(3-(2- 甲氧基苯基 ) 環戊基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺,非對映異構體 3 及 4 (CP-AIA-275C 、 CP-AIA0275D) 之混合物 1 H NMR (400 MHz, DMSO-d6) δ ppm 1.61 (br dd, J=9.79, 5.52 Hz, 1 H) 1.80 - 2.10 (m, 4 H) 2.18 - 2.26 (m, 1 H) 3.45 - 3.61 (m, 4 H) 3.63 - 3.84 (m, 4 H) 6.03 (br s, 2 H) 6.84 - 6.94 (m, 2 H) 7.11 - 7.18 (m, 1 H) 7.23 (d, J=7.53 Hz, 1 H) 7.36 (t, J=9.21 Hz, 1 H) 7.48 - 7.59 (m, 1 H) 7.93 (dd, J=6.78, 2.26 Hz, 1H) 8.94 (br s, 1 H);LC-MS: 443.0 [M+1]+ 。 |
| AIA-276D | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(3-(3- 甲氧基苯基 ) 環戊基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺,單一非對映異構體 (AIA-276D) 。 1 H NMR (400 MHz, DMSO-d6) δ ppm 1.64 (dt, J=9.65, 4.77 Hz, 1 H) 1.84 - 2.06 (m, 4 H) 2.26 (dt, J=12.62, 6.59 Hz, 1 H) 3.02 - 3.11 (m, 1 H) 3.49 (s, 3 H) 3.64 - 3.74 (m, 4 H) 5.98 (s, 2 H) 6.70 (d, J=8.41 Hz, 1 H) 6.79 (s, 1 H) 6.81 (d, J=7.69 Hz, 1 H) 7.16 (t, J=7.53 Hz, 1 H) 7.33 (t, J=9.15 Hz, 1 H) 7.53 (ddd, J=8.99, 4.35, 2.54 Hz, 1 H) 7.90 (d, J=6.57 Hz, 1 H) 8.96 (s, 1 H);LC-MS: 443.0 [M+1]+ 。 |
| AIA-281 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(3-(4- 氟苯基 ) 環戊基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 1 H NMR (400 MHz, DMSO-d6) δ ppm 1.60 (td, J=10.03, 5.07 Hz, 1 H) 1.81 - 1.95 (m, 2 H) 1.96 - 2.11 (m, 2 H) 2.23 - 2.31 (m, 1 H) 3.05 - 3.15 (m, 1 H) 3.50 (s, 3 H) 3.64 - 3.87 (m, 1 H) 5.96 - 6.02 (m, 2 H) 7.02 - 7.09 (m, 2 H) 7.24 - 7.36 (m, 3 H) 7.49 - 7.55 (m, 1 H) 7.87 - 7.92 (m, 1 H) 8.89 - 8.97 (m, 1 H);LC-MS: 431.0 [M+1]+ 。 |
| AIA-292 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(3-(4-( 三氟甲氧基 ) 苯基 ) 環戊基 )-1H- 吡唑 -4- 甲醯胺。 1 H NMR (400 MHz, DMSO-d6) δ ppm 1.59 - 1.76 (m, 1 H) 1.86 - 2.02 (m, 2 H) 2.03 - 2.16 (m, 2 H) 2.28 - 2.35 (m, 1 H) 3.10 - 3.27 (m, 1 H) 3.54 (s, 3 H) 3.67 - 3.81 (m, 1 H) 5.99 - 6.07 (m, 2 H) 7.24 - 7.31 (m, 2 H) 7.34 - 7.45 (m, 3 H) 7.52 - 7.62 (m, 1 H) 7.89 - 7.98 (m, 1 H) 8.94 - 9.05 (m, 1 H);LCMS: 497.0 [M+1]+ 。 |
| AIA-294 | 3-(3-(4- 乙醯胺基苯基 ) 環戊基 )-5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 1 H NMR (400 MHz, DMSO-d6) δ ppm 1.59 (dt, J=9.70, 4.85 Hz, 1 H) 1.77 - 1.93 (m, 2 H) 1.93 - 2.04 (m, 5 H) 2.19 - 2.27 (m, 1 H) 2.97 - 3.09 (m, 1 H) 3.45 - 3.52 (m, 3 H) 3.66 (br dd, J=9.59, 7.61 Hz, 1 H) 5.93 - 6.03 (m, 2 H) 7.08 - 7.20 (m, 2 H) 7.32 (t, J=9.10 Hz, 1 H) 7.39 - 7.46 (m, 2 H) 7.52 (ddd, J=8.99, 4.35, 2.54 Hz, 1 H) 7.90 (d, J=6.59 Hz, 1 H) 8.92 - 9.22 (m, 1 H) 9.77 - 9.82 (m, 1 H);LC-MS: 470.0 [M+1]+ 。 |
| AIA-296 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(3-(4- 異丙氧基苯基 ) 環戊基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 1 H NMR (400 MHz, DMSO-d6) δ ppm 1.25 (d, J=6.17 Hz, 6 H) 1.56 - 1.67 (m, 1 H) 1.80 - 1.98 (m, 2 H) 2.00 - 2.16 (m, 2 H) 2.21 - 2.33 (m, 1 H) 2.99 - 3.12 (m, 1 H) 3.53 (s, 3 H) 3.65 - 3.76 (m, 1 H) 4.48 - 4.61 (m, 1 H) 5.98 - 6.07 (m, 2 H) 6.76 - 6.86 (m, 2 H) 7.11 - 7.19 (m, 2 H) 7.31 - 7.42 (m, 1 H) 7.52 - 7.60 (m, 1 H) 7.90 - 7.98 (m, 1 H) 8.93 - 9.01 (m, 1 H)。LCMS: 471.0 [M+1]+ 。 |
| AIA297 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(3-(4-(2- 甲氧基乙氧基 ) 苯基 ) 環戊基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 1 H NMR (400 MHz, DMSO-d6) δ 1.51-1.69 (m, 1H), 1.80-2.15 (m, 4H), 2.20-2.31 (m, 1H), 2.97-3.16 (m, 1H), 3.29 (s, 3H), 3.51 (s, 3H), 3.59-3.89 (m, 3H), 4.00-4.32 (m, 2H), 5.93-6.10 (m, 2H), 6.76-6.88 (m, 2H), 7.10-7.23 (m, 2H), 7.29-7.43 (m, 1H), 7.48-7.61 (m, 1H), 7.86-8.01 (m, 1H), 8.88-9.06 (m, 1H);LCMS: 487.0 [M+1]+ 。 |
| AIA-354 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-((1R,3R)-3-(2-( 三氟甲基 ) 噻唑 -5- 基 ) 環戊基 )-1H- 吡唑 -4- 甲醯胺。 1 H-NMR (DMSO-d6 , 400 MHz): δ 9.03 (s, 1H), 7.93 (d,J = 9.6 Hz, 2H), 7.55 (t,J = 4.8 Hz, 1H), 7.36 (t,J = 8.8 Hz, 1H), 6.02 (s, 2H), 3.79-3.71 (m, 2H), 3.61-3.51 (m, 1H), 3.46 (s, 2H), 2.25-1.68 (m, 5H), 1.29 (s, 1H)。 |
| AIA-355 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(3-(2-( 三氟甲基 ) 噻唑 -4- 基 ) 環戊基 )-1H- 吡唑 -4- 甲醯胺。 MS計算值:487.1;MS實驗值:488.2 [M +1]+ ;1 H NMR (DMSO-d6, 400 MHz): δ 8.99 (s, 1H), 7.94-7.91 (m, 1H), 7.84 (s, 1H), 7.57-7.53 (m, 1H), 7.38-7.32 (m, 1H), 6.01 (s, 2H), 3.73-3.69 (m, 1H), 3.56-3.51(m, 3H), 3.43-3.38 (m, 1H), 2.37-2.32 (m, 1H), 2.12-2.03 (m, 2H), 2.00-1.90 (m, 2H), 1.89-1.77 (m, 1H)。 |
中間體90 5- 胺基 -1- 甲基 -3-(3- 苯基環戊基 )-1H- 吡唑 -4- 羰基氯。
將5-胺基-1-甲基-3-(3-苯基環戊基)吡唑-4-甲酸(50 mg, 0.175 mmol, 1當量)於SOCl2
(2 mL)中之溶液在80℃下攪拌1 hr。在真空下濃縮反應液以得到黃色油狀物形式之5-胺基-1-甲基-3-(3-苯基環戊基)吡唑-4-羰基氯(50 mg,粗製物)。粗製物未經進一步純化即用於下一步驟中。
AIA-278 5- 胺基 -N-(3- 溴 -4,5- 二氟苯基 )-1- 甲基 -3-(3- 苯基環戊基 )-1H- 吡唑 -4- 甲醯胺。
在0℃下,向5-胺基-1-甲基-3-(3-苯基環戊基)吡唑-4-羰基氯(50 mg, 0.165 mmol, 1當量)及3-溴-4,5-二氟-苯胺(51.35 mg, 0.247 mmol, 0.032 mL, 1.5當量)於DCM (3 mL)中之溶液中逐滴添加Et3
N (33.31 mg, 0.329 mmol, 0.046 mL, 2.0當量)。將反應液升溫至25℃並攪拌2 hr。使用DCM (20 mL)稀釋反應液並使用NH4
Cl (10 mL)、鹽水(10 mL)洗滌,藉由Na2
SO4
乾燥,過濾並在真空下濃縮以得到褐色油狀物形式之粗產物。藉由製備型HPLC (管柱:Gemini 150×25 5u;移動相:[水(0.05%氫氧化氨,v/v)-ACN];B%: 55%-85%, 10min)純化粗產物。藉由凍乾乾燥期望部分以獲得灰色固體形式之5-胺基-N-(3-溴-4,5-二氟-苯基)-1-甲基-3-(3-苯基環戊基)吡唑-4-甲醯胺(7.5 mg, 0.015 mmol, 9.30%產率,96.97%純度)。1
H NMR (400 MHz, DMSO-d6) δ ppm 1.65 - 1.78 (m, 1 H) 1.95 - 2.21 (m, 4 H) 2.22 - 2.39 (m, 1 H) 3.13 - 3.24 (m, 1 H) 3.56 - 3.61 (m, 3 H) 3.75 (br t, J=8.71 Hz, 1 H) 6.09 - 6.16 (m, 2 H) 7.17 - 7.26 (m, 1 H) 7.29 - 7.36 (m, 4 H) 7.79 - 7.89 (m, 2 H) 9.08 - 9.17 (m, 1 H);LC-MS: 475.0 [M+1]+
。
AIA-279 5- 胺基 -N-(3- 氰基 -4- 氟苯基 )-1- 甲基 -3-(3- 苯基環戊基 )-1H- 吡唑 -4- 甲醯胺。
根據針對AIA-278所闡述之程序來合成標題化合物。1
H NMR (400 MHz, DMSO-d6) δ ppm 1.63 - 1.69 (m, 1 H) 1.89 - 2.14 (m, 4 H) 2.15 - 2.32 (m, 1 H) 3.07 - 3.23 (m, 1 H) 3.47 - 3.55 (m, 3 H) 3.65 - 3.77 (m, 1 H) 6.02 - 6.20 (m, 2 H) 7.13 - 7.21 (m, 1 H) 7.24 - 7.31 (m, 4 H) 7.44 - 7.53 (m, 1 H) 7.93 (tdd, 1 H) 8.08 - 8.17 (m, 1 H) 9.06 - 9.15 (m, 1 H);LC-MS: 404.0 [M+1]+
。
中間體91 2- 溴 -1-((2-( 三甲基矽基 ) 乙氧基 ) 甲基 )-1H- 咪唑。
向2-溴-咪唑(10.0 g, 68.0 mmol)於丙酮(100 mL)中之溶液中添加K2
CO3
(23.5 g, 170.0 mmol)及SEMCl (13.6 g, 81.6 mmol)。將反應混合物在室溫下攪拌過夜。經由Celite®墊過濾混合物,並濃縮濾液以得到粗產物,藉由矽膠管柱層析使用10:1石油醚/乙酸乙酯純化以提供黃色油狀物形式之2-溴-1-((2-(三甲基矽基)乙氧基)甲基)-1H-咪唑(12.0 g, 63.7%)。MS計算值:276.0,MS實驗值:277.1 [M
+ 1]+
。
中間體92 2-(4- 溴 -3- 甲氧基苯基 )-4,4,5,5- 四甲基 -1,3,2- 二氧硼㖦。
將1-溴-4-碘-2-甲氧基苯(8.0 g, 25.6 mmol)、pin2
B2
(6.8 g, 26.9 mmol)、Pd(dppf)Cl2
(940.0 mg, 1.3 mmol)及乙酸鉀(6.3 g, 64.0 mmol)於二噁烷(100 mL)中之混合物在80℃及N2
氣氛下攪拌過夜。經由Celite®墊過濾反應液,並使用EtOAc (50 mL × 3)洗滌濾餅。在真空下濃縮濾液並藉由矽膠管柱層析使用15:1石油醚/乙酸乙酯純化殘餘物以提供黃色油狀物形式之2-(4-溴-3-甲氧基苯基)-4,4,5,5-四甲基-1,3,2-二氧硼㖦(6.0 g, 75.0%)。MS計算值:312.0;1
H-NMR (CDCl3
, 400 MHz): δ 7.53 (d,J
= 7.6 Hz, 1H), 7.28-7.25 (m, 2H), 3.93 (s, 3H), 1.34 (s, 12H)。
中間體93 2-(4- 溴 -3- 甲氧基苯基 )-1-((2-( 三甲基矽基 ) 乙氧基 ) 甲基 )-1H- 咪唑。
向2-(4-溴-3-甲氧基苯基)-4,4,5,5-四甲基-1,3,2-二氧硼㖦(6.0 g, 19.2 mmol)於二噁烷/H2
O (60 mL, v/v=5:1)中之溶液中添加2-溴-1-((2-(三甲基矽基)乙氧基)甲基)-1H-咪唑(5.9 g, 21.1 mmol)、Pd(dppf)Cl2
(1.4 g, 1.9 mmol)及Na2
CO3
(5.1 g, 48.0 mmol)。將反應液在90℃及N2
氣氛下攪拌過夜。去除溶劑,且添加水,並使用EtOAc (50 mL × 3)萃取混合物。藉由Na2
SO4
乾燥合併之有機層,然後濃縮以得到粗產物,藉由矽膠管柱層析使用10:1石油醚/乙酸乙酯純化以提供灰色固體形式之2-(4-溴-3-甲氧基苯基)-1-((2-(三甲基矽基)乙氧基)甲基)-1H-咪唑(1.5 g, 20.4%)。MS計算值:382.1,MS實驗值:383.2 [M
+ 1]+
。
中間體94 3-(2- 甲氧基 -4-(1-((2-( 三甲基矽基 ) 乙氧基 ) 甲基 )-1H- 咪唑 -2- 基 ) 苯基 ) 環戊 -2- 烯酮。
向2-(4-溴-3-甲氧基苯基)-1-((2-(三甲基矽基)乙氧基)甲基)-1H-咪唑(1.5 g, 3.9 mmol)於二噁烷/H2
O (60 mL, v/v=5:1)中之溶液中添加3-(4,4,5,5-四甲基-1,3,2-二氧硼㖦-2-基)環戊-2-烯-1-酮(1.0 g, 4.7 mmol)、Pd(dppf)Cl2
(500.0 mg, 0.4 mmol)及K3
PO4
(2.1 g, 9.8 mmol)。將反應液在90℃及N2
氣氛下攪拌過夜。去除溶劑,添加水,並使用EtOAc (50 mL × 3)萃取混合物。藉由Na2
SO4
乾燥合併之有機層並濃縮以得到粗產物,藉由矽膠管柱層析使用10:1石油醚/乙酸乙酯純化以提供灰色固體形式之3-(2-甲氧基-4-(1-((2-(三甲基矽基)乙氧基)甲基)-1H-咪唑-2-基)苯基)環戊-2-烯酮(1.0 g, 66.7%)。MS計算值:384.2,MS實驗值:385.3 [M
+ 1]+
。
中間體95 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(3-(2- 甲氧基 -4-(1-((2-( 三甲基矽基 ) 乙氧基 ) 甲基 )-1H- 咪唑 -2- 基 ) 苯基 ) 環戊基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。
根據上述程序來合成標題化合物。MS計算值:638.2,MS實驗值:639.3 [M
+ 1]+
。
AIA-352-1及AIA-352-2 3-(3-(4-(1H- 咪唑 -2- 基 )-2- 甲氧基苯基 ) 環戊基 )-5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 1 (AIA-352-1) 及非對映異構體 2 (AIA-352-2) 。
將5-胺基-N-(3-氯-4-氟苯基)-3-(3-(2-甲氧基-4-(1-((2-(三甲基矽基)乙氧基)甲基)-1H-咪唑-2-基)苯基)環戊基)-1-甲基-1H-吡唑-4-甲醯胺(230.0 mg, 0.4 mmol)及TFA (2 mL)於DCM (10 mL)中之混合物在室溫下攪拌過夜。去除溶劑並添加氫氧化銨(2 mL)。將所得混合物在室溫下攪拌15分鐘。去除溶劑以得到粗產物,藉由製備型HPLC純化以提供AIA-352-1 (11 mg, 5.4%)及AIA-352-2 (7 mg, 3.4%) AIA-352-1:1
H-NMR (DMSO-d6
, 400 MHz): δ 12.42 (s, 1H), 8.93 (s, 1H), 7.92 (dd, J = 6.8, 2.4 Hz, 1H), 7.49-7.44 (m, 3H), 7.33-7.27 (m, 2H), 7.22 (s, 1H), 6.98 (s, 1H), 6.03 (s, 2H), 3.90-3.86 (m, 1H), 3.84 (s, 3H), 3.53 (s, 3H), 3.45-3.39 (m, 1H), 2.14-1.92 (m, 5H), 1.68-1.63 (m, 1H)。AIA-352-2:1
H-NMR (DMSO-d6
, 400 MHz): δ 12.43 (s, 1H), 8.94 (s, 1H), 7.94 (dd, J = 6.8, 2.8 Hz, 1H), 7.58-7.54 (m, 1H), 7.51-7.45 (m, 2H), 7.36 (t, J = 8.8 Hz, 1H), 7.28 (d, J = 8.0 Hz, 1H), 7.22 (s, 1H), 6.98 (s, 1H), 6.03 (s, 2H), 3.83 (s, 3H), 3.73-3.67 (m, 1H), 3.52 (s, 3H), 3.46-3.38 (m, 1H), 2.27-2.20 (m, 1H), 2.07-1.83 (m, 4H), 1.65-1.60 (m, 1H)。表 2.
根據針對AIA-352-1及AIA-352-2所闡述之程序來合成表2中之化合物
| 化合物 | 結構及表徵 |
| AIA-365-1 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(3-(2- 甲氧基 -4-(1- 甲基 -1H- 咪唑 -4- 基 ) 苯基 ) 環戊基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 1 (AIA-365-1) 。 MS計算值:522.2;MS實驗值:523.3 [M + 1]+ 。1 H-NMR (DMSO-d6 , 400 MHz): δ 8.89 (s, 1H), 7.90 (dd,J = 6.8, 2.4 Hz, 1H), 7.57 (s, 1 H), 7.53 (s, 1 H), 7.48-7.44 (m, 1H), 7.32-7.26 (m, 2H), 7.22-7.15 (m, 2H), 6.01 (s, 2H), 3.81-3.79 (m, 1H), 3.76 (s, 3H), 3.65 (s, 3H), 3.50 (s, 3H), 3.40-3.33 (m, 1H), 2.10-1.91 (m, 5H), 1.64-1.59 (m, 1H)。 |
| AIA-365-2 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(3-(2- 甲氧基 -4-(1- 甲基 -1H- 咪唑 -4- 基 ) 苯基 ) 環戊基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 2 (AIA-365-2) 。 MS計算值:522.2;MS實驗值:523.3 [M + 1]+ 。1 H-NMR (DMSO-d6 , 400 MHz): δ 8.93 (s, 1H), 7.94 ((dd,J = 6.8, 2.4 Hz, 1H), 7.58-7.53 (m, 3H), 7.38-7.30 (m, 2H), 7.26-7.17 (m, 2 H), 6.03(s, 2H), 3.80 (s, 3H),3.70-3.68 (m, 1H), 3.67 (s, 3H), 3.52 (s, 3H), 3.40-3.35 (m, 1H), 2.33-2.32 (m, 1H), 2.02 -1.90 (m, 4H), 1.62-1.58 (m, 1H)。 |
| AIA-366-1 | 3-(3-(4-(1H- 咪唑 -4- 基 )-2- 甲氧基苯基 ) 環戊基 )-5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 1 (AIA-366-1) 。 MS計算值:508.2;MS實驗值:509.3 [M + 1]+ 。1 H-NMR (DMSO-d6 , 400 MHz): δ 12.2 (s, 1H), 8.93 (s, 1H), 7.92 (dd,J = 6.8, 2.4 Hz, 1H), 7.67 (s, 1H), 7.56-7.46 (m, 2H), 7.40-7.18(m, 4H), 6.03 (s, 2H), 3.84-3.83 (m, 1H), 3.80 (s, 3H), 3.52 (s, 3H), 3.43-3.38 (m, 1H), 2.12-1.91 (m, 5H), 1.65-1.60 (m, 1H)。 |
| AIA-366-2 | 3-(3-(4-(1H- 咪唑 -4- 基 )-2- 甲氧基苯基 ) 環戊基 )-5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 2 (AIA-366-2) 。 MS計算值:508.2;MS實驗值:509.3 [M + 1]+ 。1 H-NMR (DMSO-d6 , 400 MHz): δ 12.2 (s, 1H), 8.93 (s, 1H), 7.97 (dd,J = 6.8, 2.4 Hz, 1H), 7.93 (s, 1H), 7.54-7.38 (m, 2H), 7.36-7.20(m, 4H), 6.03 (s, 2H), 3.83 (s, 3H), 3.80-3.79 (m, 1H), 3.71 (s, 3H), 3.49-3.46 (m, 1H), 2.25-2.18 (m, 1H), 2.02-1.85 (m, 4H), 1.63-1.52 (m, 1H)。 |
| AIA-367-1 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(3-(2- 甲氧基 -4-(1- 甲基 -1H- 咪唑 -2- 基 ) 苯基 ) 環戊基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 1 (AIA-367-1) 。 MS計算值:522.2;MS實驗值:523.3 [M + 1]+ 。1 H-NMR (DMSO-d6 , 400 MHz): δ 8.95 (s, 1H), 7.93 (dd,J = 7.2, 2.8 Hz, 1H), 7.49-7.46 (m, 1 H), 7.36-7.31 (m, 2 H), 7.22 (s, 1H), 7.18-7.14 (m, 2H), 6.94 (s, 1H), 6.03 (s, 2H), 3.85-3.83 (m, 1H), 3.82 (s, 3H), 3.73 (s, 3H), 3.53(s, 3H), 3.49-3.44 (m, 1H), 2.13-1.97 (m, 5H), 1.67-1.58 (m, 1H)。 |
| AIA-367-2 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(3-(2- 甲氧基 -4-(1- 甲基 -1H- 咪唑 -2- 基 ) 苯基 ) 環戊基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 2 (AIA-367-2) 。 MS計算值:522.2;MS實驗值:523.3 [M + 1]+ 。1 H-NMR (DMSO-d6 , 400 MHz): δ 8.92 (s, 1H), 7.92 ((dd,J = 7.2, 2.8 Hz, 1H), 7.56-7.53 (m, 1H), 7.36-7.31 (m, 2H), 7.21-7.15 (m, 3 H),6.92 (s, 1H), 6.01 (s, 2H), 3.82 (s, 3H), 3.77 (s, 3H), 3.72-3.68 (m, 1H), 3.50 (s, 3H), 3.45-3.40 (m, 1H), 2.25-2.22 (m, 1H), 2.05 -1.98 (m, 2H), 1.92 -1.86 (m, 2H), 1.65-1.58 (m, 1H)。 |
| AIA-369 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(3-(2- 甲氧基 -4-(1- 甲基 -1H- 吡唑 -4- 基 ) 苯基 ) 環戊基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺 (AIA-369) 。 MS計算值:522.2,MS實驗值:523.3 [M+1]+ ;1 H-NMR (CD3 OD, 400 MHz):δ 7.91 (s, 1H), 7.74-7.84 (m, 2H), 7.42-7.45 (m, 0.7H), 7.03-7.24(m, 4.3 H), 3.81-3.91 (m, 6H), 3.46-3.73 (m, 5H), 1.74-2.36 (m, 6H)。 |
| AIA-370 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(3-(2- 甲氧基 -4-(1H- 吡唑 -4- 基 ) 苯基 ) 環戊基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺 (AIA-370): MS計算值:508.1,MS實驗值:509.2 [M+1]+ ;1 H-NMR (CD3 OD, 400 MHz):δ 7.92 (s, 1H), 7.82-7.84 (m, 2H), 7.42-7.46 (m, 1 H), 7.03-7.25(m, 4 H), 3.85 (s, 3H), 3.64-3.68 (m, 1H), 3.57 (s, 3H), 3.52 (m, 1H), 2.34-2.37 (m, 2H), 1.77-2.19(m, 4H)。 |
| AIA-371 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(3-(2- 甲氧基 -4-( 噻唑 -2- 基 ) 苯基 ) 環戊基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 MS計算值:525.14;MS實驗值:526.3 [M+1]+ ;1 H NMR (DMSO-d6 , 400 MHz): δ 8.95 (brs, 1H), 7.95-7.89 (m, 2H), 7.76 (d,J =3.2 Hz, 1H), 7.58-7.42 (m, 3H), 7.38-7.29 (m, 2H), 6.04 (s, 2H), 3.89-3.68 (m, 4H), 3.53-3.42 (m, 4H), 2.28-1.91 (m, 5H), 1.67-1.58 (m, 1H)。 |
| AIA-372 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(3-(2- 甲氧基 -4-( 噻唑 -4- 基 ) 苯基 ) 環戊基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 MS計算值:525.1;MS實驗值:526.3 [M + 1]+ ;1 H NMR (DMSO-d6+D2 O, 400 MHz): δ 9.12 (m, 1H), 8.08-8.07 (m, 1H), 7.89-7.84 (m, 1H), 7.54-7.46 (m, 3H), 7.35-7.25 (m, 2H), 3.81-3.79 (m, 3H), 3.69-3.62 (m, 1H), 3.49-3.48 (m, 3H), 3.42-3.37 (m, 1H), 2.23-2.20 (m, 1H), 2.06-1.82 (m, 4H), 1.63-1.60 (m, 1H)。 |
中間體96 3- 甲氧基 -4-(4,4,5,5- 四甲基 -1,3,2- 二氧硼㖦 -2- 基 ) 苯甲酸甲酯。
將4-溴-3-甲氧基苯甲酸甲酯(3.0 g, 12.2 mmol)、4,4,5,5-四甲基-2-(4,4,5,5-四甲基-1,3,2-二氧硼㖦-2-基)-1,3,2-二氧硼㖦(4.8 g, 19 mmol)、Pd(dppf)Cl2
(450 mg, 0.6 mmol)及乙酸鉀(1.9 g, 19.0 mmol)於二噁烷(50 mL)中之混合物在80℃及N2
氣氛下攪拌4 h。經由Celite®墊過濾反應液,並使用EtOAc (10 mL × 3)洗滌濾餅。在真空下濃縮濾液並藉由矽膠管柱層析使用15:1石油醚/乙酸乙酯純化殘餘物以提供白色固體形式之3-甲氧基-4-(4,4,5,5-四甲基-1,3,2-二氧硼㖦-2-基)苯甲酸甲酯(2.5 g, 70%產率)。MS計算值:292.1,MS實驗值:293.4 [M+1]+
。
中間體97 3- 甲氧基 -4-(3- 側氧基環戊 -1- 烯基 ) 苯甲酸甲酯。
將3-甲氧基-4-(4,4,5,5-四甲基-1,3,2-二氧硼㖦-2-基)苯甲酸甲酯(2.5 g, 8.6 mmol)、3-溴環戊-2-烯-1-酮(1.3 g, 8.6 mmol)、Pd(PPh3
)4
(500 mg, 0.43 mmol)及碳酸鉀(1.8 g, 12.9 mmol)於二噁烷(50 mL)及水(10 mL)中之混合物在100℃及N2
氣氛下攪拌4 h。經由Celite®墊過濾反應液並使用EtOAc (10 mL × 3)洗滌濾餅。在真空下濃縮濾液並藉由矽膠管柱層析使用3:1石油醚/乙酸乙酯純化殘餘物以提供微黃色固體形式之3-甲氧基-4-(3-側氧基環戊-1-烯基)苯甲酸甲酯(1.8 g, 86%產率)。MS計算值:246.1,MS實驗值:247.4 [M+1]+
。
中間體98 4-(3-(5- 胺基 -4-(3- 氯 -4- 氟苯基胺甲醯基 )-1- 甲基 -1H- 吡唑 -3- 基 ) 環戊基 )-3- 甲氧基苯甲酸甲酯。
根據上述程序自3-甲氧基-4-(3-側氧基環戊-1-烯基)苯甲酸甲酯及5-胺基-3-溴-N-(3-氯-4-氟苯基)-1-甲基-1H-吡唑-4-甲醯胺合成標題化合物。MS計算值:500.2,MS實驗值:501.3 [M+1]+
。
中間體99 4-(3-(5- 胺基 -4-(3- 氯 -4- 氟苯基胺甲醯基 )-1- 甲基 -1H- 吡唑 -3- 基 ) 環戊基 )-3- 甲氧基苯甲酸。
將4-(3-(5-胺基-4-(3-氯-4-氟苯基胺甲醯基)-1-甲基-1H-吡唑-3-基)環戊基)-3-甲氧基苯甲酸甲酯(800 mg, 1.6 mmol)及LiOH-H2
O (670 mg, 16.0 mmol)於THF/H2
O=1:1 (10 mL)中之混合物在60℃下加熱過夜。使用2N HCl中和反應液,並在真空下去除溶劑。藉由矽膠管柱層析使用乙酸乙酯純化殘餘物以提供白色固體形式之4-(3-(5-胺基-4-(3-氯-4-氟苯基胺甲醯基)-1-甲基-1H-吡唑-3-基)環戊基)-3-甲氧基苯甲酸(700 mg, 90%產率)。MS計算值:486.1,MS實驗值:487.3 [M+1]+
。
AIA-150-C、AIA-150-D 5- 胺基 -3-(3-(4- 胺甲醯基 -2- 甲氧基苯基 ) 環戊基 )-N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 1 (AP-AIA-150-C) , 非對映異構體 2 (AIA-150-D) 。
將4-(3-(5-胺基-4-(3-氯-4-氟苯基胺甲醯基)-1-甲基-1H-吡唑-3-基)環戊基)-3-甲氧基苯甲酸(700 mg, 1.4 mmol)、HCOONH4
(180 mg, 2.9 mmol)、HATU (1.1 g, 2.9 mmol)及TEA (300 mg, 2.9 mmol)於DMF (5 mL)中之混合物在室溫下攪拌過夜。使用水(20 mL)終止反應,然後使用EtOAc (20 mL × 3)萃取。在減壓下濃縮有機層並藉由矽膠管柱層析使用乙酸乙酯純化所得殘餘物以提供白色固體形式之AIA-150-1 (30 mg, 4%產率)及白色固體形式之AIA-150-2 (300 mg, 43%產率)。MS計算值:485.2,MS實驗值:486.3 [M+1]+
。藉由SFC分離100 mg AIA-150-2以得到白色固體形式之AIA-150-C (30 mg)及白色固體形式之AIA-150-D (30 mg)。AIA-150-C:1
H-NMR (DMSO-d6
, 400 MHz): δ 8.94 (s, 1H), 7.93 (dd, J = 6.8, 2.4 Hz, 1H), 7.91 (brs, 1H), 7.58-7.54 (m, 1H), 7.44-7.41 (m, 2H), 7.36 (t, J = 9.2 Hz, 1H), 7.30-7.27 (m, 2H), 6.03 (s, 2H), 3.81 (s, 3H), 3.73-3.69 (m, 1H), 3.52 (s, 3H), 3.46-3.41 (m, 1H), 2.27-2.20 (m, 1H), 2.08-2.00 (m, 2H), 1.99-1.83 (m, 2H), 1.65-1.59 (m, 1H)。AIA-150-D:1
H-NMR (DMSO-d6
, 400 MHz): δ 8.94 (s, 1H), 7.93 (dd, J = 6.8, 2.4 Hz, 1H), 7.91 (brs, 1H), 7.58-7.54 (m, 1H), 7.44-7.41 (m, 2H), 7.36 (t, J = 9.2 Hz, 1H), 7.30-7.27 (m, 2H), 6.03 (s, 2H), 3.81 (s, 3H), 3.73-3.69 (m, 1H), 3.52 (s, 3H), 3.46-3.41 (m, 1H), 2.27-2.20 (m, 1H), 2.08-2.00 (m, 2H), 1.99-1.83 (m, 2H), 1.65-1.59 (m, 1H)。
AIA-070-2 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(3-(4- 氰基 -2- 甲氧基苯基 ) 環戊基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺
向AIA-150-2 (150 mg, 0.3 mmol)於吡啶(5 mL)中之溶液中添加POCl3
(140 mg, 0.9 mmol)並將混合物在-40℃下攪拌10 min。使用水(10 mL)終止反應並使用EtOAc (10 mL × 3)萃取。在真空下濃縮合併之有機層。藉由矽膠管柱層析使用1:1石油醚/乙酸乙酯純化所得殘餘物以提供白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-3-(3-(4-氰基-2-甲氧基苯基)環戊基)-1-甲基-1H-吡唑-4-甲醯胺(7 mg, 5%產率)。MS計算值:467.2,MS實驗值:468.2 [M+1] +
。1
H-NMR (DMSO-d6
, 400 MHz):δ
8.94 (s, 1H), 7.93 (dd,J
= 6.8, 2.4 Hz, 1H), 7.58-7.54 (m, 1H), 7.44 (d,J
= 8.0 Hz, 1H), 7.38-7.33 (m, 3H), 6.03 (s, 2H), 3.83 (s, 3H), 3.74-3.70 (m, 1H), 3.51 (s, 3H), 3.48-3.43 (m, 1H), 2.28-2.22 (m, 1H), 2.08-2.00 (m, 2H), 1.99-1.83 (m, 2H), 1.65-1.59 (m, 1H)。表 3.
根據針對AIA-150-C及AIA-150-D所闡述之程序來合成表3中之化合物
AIA-262 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(1- 苯基吡咯啶 -3- 基 )-1H- 吡唑 -4- 甲醯胺。
將5-胺基-N-(3-氯-4-氟-苯基)-1-甲基-3-吡咯啶-3-基-吡唑 -4-甲醯胺(100 mg, 0.296 mmol, 1當量)、溴苯(46.48 mg, 0.296 mmol, 0.031 mL, 1當量)、Pd2
(dba)3
(8.13 mg, 0.009 mmol, 0.03當量)、XPhos (4.23 mg, 0.009 mmol, 0.03當量)及NaOtBu (85.35 mg, 0.888 mmol, 3當量)於二噁烷(3 mL)中之混合物在105℃及N2
下攪拌2 hr。觀察到褐色懸浮液。藉由在105℃及N2
下攪拌2 hr來繼續反應。向反應液中添加乙酸乙酯(10 mL)及水(10 mL)。分離水層並使用乙酸乙酯(10 mL)萃取。合併有機層並使用鹽水(10 mL)洗滌,藉由Na2
SO4
乾燥,過濾並在真空下濃縮以得到褐色油狀物形式之5-胺基-N-(3-氯- 4-氟-苯基)-1-甲基-3-(1-苯基吡咯啶-3-基)吡唑-4-甲醯胺(150 mg,粗製物)。藉由製備型TLC (1:1石油醚/EtOAc)純化殘餘物以得到黃色油狀物形式之5-胺基-N- (3-氯-4-氟-苯基)-1-甲基-3-(1-苯基吡咯啶-3-基)吡唑-4-甲醯胺(5 mg,粗製物),藉由製備型HPLC (管柱:Gemini 150 × 25 5 u;移動相: [水(0.05%氫氧化氨,v/v)-ACN];B%: 50%-80%,10min)純化以得到黃色固體形式之5-胺基-N- (3-氯-4-氟-苯基)-1-甲基-3-(1-苯基吡咯啶-3-基)吡唑-4-甲醯胺(1.8 mg, 0.004 mmol, 36.00%產率,100%純度)。1
H NMR (400 MHz,氯仿-d) ppm 2.35 - 2.57 (m, 2 H) 3.13 - 3.23 (m, 1 H) 3.46 - 3.60 (m, 4 H) 3.75 - 3.82 (m, 2 H) 5.47 (br s, 2 H) 6.75 (br d,J=7.72 Hz, 2 H) 6.80 - 6.98 (m, 2 H) 7.11 (ddd, J=8.99, 4.02, 2.65 Hz, 1 H) 7.25 - 7.32 (m, 2 H) 7.39 - 7.48 (m, 1 H) 8.66 (br s, 1 H);LC-MS: 414.0 [M+1]+
。
| 化合物 | 結構及表徵 |
| AIA-387-1 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(3-(2- 甲氧基 -4-((2-( 甲基磺醯基 ) 乙基 ) 胺甲醯基 ) 苯基 ) 環戊基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 1 (AIA-387-1) 。 1 H-NMR (D2 O/DMSO-d6 , 400 MHz):δ 7.83-7.85 (m, 1H), 7.46-7.50 (m, 1H), 7.28-7.35 (m, 4H), 3.76(s, 3H), 3.62-3.65 (m, 3H), 3.46(s, 3H), 3.31-3.38 (m, 3H), 2.97 (s, 3H), 2.17-2.21 (m, 1H), 1.78-2.02(m, 4H), 1.57-1.61 (m, 1H)。 |
| AIA-387-2 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(3-(2- 甲氧基 -4-((2-( 甲基磺醯基 ) 乙基 ) 胺甲醯基 ) 苯基 ) 環戊基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 2 (AIA-387-2) 。 1 H-NMR (D2 O/DMSO-d6 , 400 MHz):δ 7.82-7.84 (m, 1H), 7.45-7.49 (m, 1H), 7.28-7.34 (m, 4H), 3.61-3.65 (m, 3H), 3.46(s, 3H), 3.30-3.38 (m, 3H), 2.97 (s, 3H), 2.17-2.20 (m, 1H), 1.77-2.01(m, 4H), 1.57-1.61 (m, 1H)。 |
| AIA-388 | 5- 胺基 -3-(3-(4-((2- 胺基乙基 ) 胺甲醯基 )-2- 甲氧基苯基 ) 環戊基 )-N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 MS計算值:528.2,MS實驗值:529.3 [M+1] + 。1 H-NMR (D2 O/DMSO-d6 , 400 MHz):δ 7.83-7.85 (m, 1H), 7.47-7.51 (m, 1H), 7.27-7.37 (m, 4H), 3.78 (s, 3H), 3.62-3.66(m, 1H), 3.47(s, 3H), 3.37-3.42 (m, 1H), 3.17-3.25 (m, 2H), 3.03-3.06 (m, 1H), 2.56-2.63 (m, 1H), 2.19-2.22 (m, 1H), 1.77-2.06(m, 4H), 1.57-1.61 (m, 1H)。 |
中間體100 三氟甲烷磺酸 5- 側氧基 -1,3a,4,5,6,6a- 六氫并環戊二烯 -2- 基酯。
在室溫下,向1,3,3a,4,6,6a-六氫并環戊二烯-2,5-二酮(40.0g, 289.5 mmol)及吡啶(24.0 g, 304.0 mmol)於DCM (600 ml)中之溶液中逐滴添加Tf2
O (89.8 g, 318.5 mmol)。將混合物在室溫下攪拌3 h。添加鹽水(300 mL)並使用DCM (200 mL × 3)萃取水層。分離有機層,藉由Na2
SO4
乾燥並濃縮以得到粗產物,藉由矽膠管柱層析使用8:1石油醚/乙酸乙酯純化以提供黃色油狀物形式之三氟甲烷磺酸5-側氧基-1,3a,4,5,6,6a-六氫并環戊二烯-2-基酯(36.0 g, 46%產率)。1
H NMR (400 MHz,氯仿-d
) δ ppm 2.17 (ddd,J
=19.14, 7.34, 1.63 Hz, 1 H) 2.26 - 2.34 (m, 1 H) 2.40 - 2.56 (m, 2 H) 2.58 - 2.67 (m, 1 H) 3.00 -3.14 (m, 2 H) 3.50 - 3.57 (m, 1 H) 5.63 (q,J
=1.92 Hz, 1 H)。
中間體101 5-(4,4,5,5- 四甲基 -1,3,2- 二氧硼㖦 -2- 基 )-3,3a,6,6a- 四氫并環戊二烯 -2(1H)- 酮。
將三氟甲烷磺酸5-側氧基-1,3a,4,5,6,6a-六氫并環戊二烯-2-基酯(110.0 g, 407.0 mmol)、4,4,5,5-四甲基-2-(4, 4,5,5-四甲基-1,3,2-二氧硼㖦-2-基)-1,3,2-二氧硼㖦(108.5 g, 427.4 mmol)、Pd(dppf)Cl2
(8.9 g, 12.2 mmol)及乙酸鉀(119.7 g, 1221.0 mmol)於二噁烷(1000 ml)中之混合物在80℃及N2
氣氛下攪拌2 h。經由Celite®墊過濾反應混合物且使用EtOAc (250 mL × 3)洗滌濾餅。在真空下濃縮濾液且藉由矽膠管柱層析使用8:1石油醚/乙酸乙酯純化殘餘物以提供黃色油狀物形式之5-(4,4,5,5-四甲基-1,3,2-二氧硼㖦-2-基)-3,3a,6,6a-四氫并環戊二烯-2(1H)-酮(90.0 g, 89%產率)。1
H NMR (400 MHz,氯仿-d
) δ ppm 1.28 (s, 13 H) 1.95 - 2.07 (m, 1 H) 2.24 - 2.55 (m, 4 H) 2.79 (ddt,J
=16.48, 7.58, 2.64, 2.64 Hz, 1 H) 2.93 -3.05 (m, 1 H) 3.41 - 3.54 (m, 1 H) 6.37 (q,J
=2.08 Hz, 1 H)。
中間體102 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5- 側氧基 -1,3a,4,5,6,6a- 六氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺。
將 5-胺基-3-溴-N-(3-氯-4-氟苯基)-1-甲基-1H-吡唑-4-甲醯胺(68.6 g, 197.5 mmol)、5-(4,4,5,5-四甲基-1,3,2-二氧硼㖦-2-基)-3,3a,6,6a-四氫并環戊二烯-2(1H)-酮(70.0 g, 282.1 mmol)、Pd(dppf)Cl2
(10.1 g, 13.8 mmol)及Na2
CO3
(41.9 g, 395.0 mmol)於二噁烷(1200 mL)及H2
O (150 mL)中之混合物在80℃及N2
下攪拌過夜。 混合物係褐色懸浮液。在真空下蒸發溶劑。藉由矽膠管柱層析使用1:2石油醚/乙酸乙酯純化殘餘物以提供黃色固體形式之5-
胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-側氧基-1,3a,4,5,6,6a-六氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺(55.0 g, 72%產率)。MS計算值:388.1,MS實驗值:389.0 [M+1]+
。1
H NMR (400 MHz,氯仿-d
) δ ppm 2.19 (dd,J
=19.20, 5.26 Hz, 1 H) 2.33 (br d,J
=18.83 Hz, 1 H) 2.55 - 2.79 (m, 3 H) 3.15 - 3.28 (m, 2 H) 3.63 (s, 3 H) 3.66 (s, 1 H) 3.68 - 3.77 (m, 1 H) 5.24 - 5.45 (m, 2 H) 6.05 (d,J
=1.71 Hz, 1 H) 6.95 - 7.20 (m, 2 H) 7.47 - 7.58 (m, 1 H) 7.68 - 7.86 (m, 2 H);LCMS: 389.0 [M+1]+
。
AIA-002 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5- 側氧基八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺。
向5-(4,4,5,5-四甲基-1,3,2-二氧硼㖦-2-基)-3,3a,6,6a-四氫并環戊二烯-2(1H)-酮(5.0 g, 12.9 mmol)於EtOAc (500 ml)中之溶液中添加Pd/C (2.5 g, 10% w/w Pd)。將混合物在40℃及H2
下攪拌2 h 。過濾混合物並在真空下蒸發以得到白色固體形式之目標化合物(4.6 g, 92%)。粗製物未經任何進一步純化即直接使用。MS計算值:390.1;MS實驗值:391.0 [M+1]+
。1
H NMR (400 MHz,氯仿-d
) δ ppm 1.85 - 2.01 (m, 2 H) 2.07 - 2.29 (m, 2 H) 2.41 - 2.67 (m, 4 H) 2.83 - 3.06 (m, 2 H) 3.32 - 3.50 (m, 1 H) 3.54 - 3.61 (m, 3 H) 5.15 - 5.32 (m, 2 H) 7.12 (t,J
=8.74 Hz, 1 H) 7.27 - 7.35 (m, 2 H) 7.65 - 7.83 (m, 1 H);LCMS: 391.2 [M+1]+
。
AIA-290 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-( 六氫 -1H- 螺 [ 并環戊二烯 -2,2'-[1,3] 二氧雜環戊烷 ]-5- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺
。向5-胺基-N-(3-氯-4-氟-苯基)-1-甲基-3-(5-側氧基-2,3,3a,4,6,6a-六氫-1H-并環戊二烯-2-基)吡唑-4-甲醯胺(30 mg, 0.071 mmol, 1當量)及乙二醇(4.39 mg, 0.0708 mmol, 1當量)於甲苯(3 mL)中之淺褐色溶液中添加p-TsOH (12.19 mg, 0.0708 mmol, 1.0當量)。將混合物在110℃下攪拌16 hr。使用EtOAc (10 mL)稀釋混合物,使用飽和NaHCO3
溶液(10 mL)洗滌,藉由Na2
SO4
乾燥,過濾並在真空下濃縮以得到殘餘物。藉由製備型TLC (SiO2
, 10:1 DCM: MeOH)純化殘餘物。獲得無色膠狀化合物5-胺基-N-(3-氯-4-氟-苯基)-1-甲基-3-螺[1,3-二氧雜環戊烷-2,5'-2,3,3a,4,6,6a-六氫-1H-并環戊二烯]-2'-基-吡唑-4-甲醯胺(30 mg, 0.0659 mmol, 55.9%產率,95.6%純度),並藉由製備型HPLC (鹼性)進一步純化。1
H NMR (400 MHz,氯仿-d) δ ppm 1.74 (2 H, br dd, J=13.45, 4.85 Hz), 1.81 - 1.92 (2 H, m), 2.00 - 2.10 (2 H, m), 2.30 - 2.42 (2 H, m), 2.60 -2.74 (2 H, m), 3.07 - 3.19 (1 H, m), 3.60 (3 H, s), 3.85 - 3.95 (4 H, m), 5.28 (2 H, s), 7.11 (1 H, t, J=8.71 Hz), 7.27 - 7.33 (2 H, m), 7.72 (1 H, dd, J=6.62, 2.65 Hz);LCMS: 435.0 [M+1]+
。
中間體103 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-( 六氫 -1H- 螺 [ 并環戊二烯 -2,2'-[1,3] 二硫㖦 ]-5- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺
。向5-胺基-N-(3-氯-4-氟-苯基)-1-甲基-3-(5-側氧基-2,3,3a,4,6,6a- 六氫-1H-并環戊二烯-2-基)吡唑-4-甲醯胺(0.2 g, 0.512 mmol, 1當量)及乙烷-1,2-二硫醇(77.13 mg, 0.819 mmol, 0.069 mL, 1.6當量)於DCM (5 mL)中之混合物中添加BF3
.Et2
O (290.51 mg, 2.05 mmol, 0.253 mL, 4當量)。將混合物在25℃下攪拌3 hr。使用H2
O (15 mL)將混合物洗滌三次,然後使用鹽水(20 mL)洗滌。藉由Na2
SO4
乾燥有機層並在真空下蒸發以得到黃色固體。藉由急速矽膠層析(combi flash®;4 g SepaFlash®二氧化矽急速管柱, 0~41.4%乙酸乙酯/石油醚梯度之洗脫劑,在18 mL/min下)純化黃色固體。獲得黃色固體形式之5-胺基-N-(3-氯-4-氟-苯基)-1-甲基-3-螺[1,3-二硫㖦-2,5'-2,3,3a,4,6,6a-六氫- 1H-并環戊二烯]-2'-基-吡唑-4-甲醯胺(190 mg, 0.397 mmol, 77.58%產率,97.580%純度)。LCMS: 467.0 [M+1]+
。
AIA-232 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-( 八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺
。向拉尼鎳(Raney-Ni) (100 mg, 1.17 mmol)於EtOH (10 mL)中之溶液中添加5-胺基-N- (3-氯-4-氟-苯基)-1-甲基-3-螺[1,3-二硫㖦-2,5'-2,3,3a,4,6,6a-六氫-1H-并環戊二烯]-2'-基-吡唑-4-甲醯胺(50 mg, 0.078 mmol, 1當量)。將混合物在80℃下攪拌4 hr。過濾混合物,且在真空下蒸發濾液以得到黃色膠狀物。藉由製備型HPLC (管柱:Gemini 150 × 25 5u;移動相: [水(0.05%氫氧化銨,v/v)-ACN];B%: 55%-85%,10min) 純化粗產物以產生白色固體形式之3-(1,2,3,3a,4,5,6,6a-八氫并環戊二烯-2-基)-5-胺基-N- (3-氯-4-氟-苯基)-1-甲基-吡唑-4-甲醯胺(10 mg, 0.0265 mmol, 16.9%產率,100%純度)。1
H NMR (400 MHz, DMSO-d
6) δ ppm 1.16 - 1.29 (m, 2 H) 1.36 (br s, 2 H) 1.41 - 1.54 (m, 4 H) 2.07 - 2.18 (m, 2 H) 2.43 (br s, 2 H) 3.26 - 3.34 (m, 1 H) 3.48 (s, 3 H) 5.95 (s, 2 H) 7.34 (t,J
=9.15 Hz, 1 H) 7.51 (ddd,J
=9.04, 4.41, 2.65 Hz, 1 H) 7.91 (dd,J
=6.84, 2.65 Hz, 1 H) 8.97 (s, 1 H);LCMS: 376.9 [M+1]+
。
AIA-026 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺
。向AIA-002 (39 mg, 0.1 mmol, 1當量)於THF / MeOH (1 mL/1 mL)中之懸浮液中逐份添加NaBH4
(6 mg, 0.15 mmol, 1.5當量)。將反應液在室溫下攪拌30分鐘。觀察到黃色溶液。使用水終止反應並使用乙酸乙酯(10 mL × 2)萃取。在真空下濃縮有機相並藉由製備型HPLC純化殘餘物以得到白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-3-(5-羥基八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺(28 mg, 71%產率)。MS計算值:392.1;MS實驗值:393.0 [M+1]+
。1
H-NMR (DMSO-d6
, 400 MHz): δ 8.93 (s, 1H), 7.91 (dd,J
= 6.8, 2.8 Hz, 1H), 7.53-7.49 (m, 1H), 7.34 (t,J
= 9.2 Hz, 1H), 5.96 (s, 2H), 4.45 (d,J
= 3.2 Hz, 1H), 4.04-4.02 (m, 1H), 3.49 (s, 3H), 3.45-3.39 (m, 1H), 2.38-2.32 (m, 2H), 2.17-2.11 (m, 2H), 1.92-1.89 (m, 2H), 1.62-1.54 (m, 2H), 1.30-1.24 (m, 2H)
中間體104 甲烷磺酸 5-(5- 胺基 -4-((3- 氯 -4- 氟苯基 )arbamoyl)-1- 甲基 -1H- 吡唑 -3- 基 ) 八氫并環戊二烯 -2- 基酯
向AIA-026 (400 mg, 1 mmol)及TEA (204 mg, 2 mmol)於DCM (20 mL)中之混合物中添加MsCl (172 mg, 1.5 mmol)並將混合物在25℃下攪拌4 h。在真空下濃縮反應液並藉由矽膠管柱層析使用5-10%乙酸乙酯/石油醚純化殘餘物以得到淺白色固體形式之甲烷磺酸5-(5-胺基-4-((3-氯-4-氟苯基)胺甲醯基)-1-甲基-1H-吡唑-3-基)八氫并環戊二烯-2-基酯(311 mg, 65%產率)。MS計算值:470.9;MS實驗值:471.7 [M+1]+
。
AIA-027 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 氰基八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺
向甲烷磺酸5-(5-胺基-4-((3-氯-4-氟苯基)胺甲醯基)-1-甲基-1H-吡唑-3-基)八氫并環戊二烯-2-基酯(46.7 mg, 0.10 mmol)於乙腈(5 mL)中之溶液中添加TMSCN (100 mg, 1.01 mmol)及TBAF (100mg, 0.38 mmol)並將所得混合物在70℃下攪拌4 h。在真空中濃縮混合物並藉由製備型HPLC純化殘餘物以提供白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-3-(5-氰基八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺(6.7 mg, 16%產率)。MS計算值:401.8;MS實驗值:402.7 [M + 1]+
。V1
H-NMR (DMSO-d6
, 400 MHz): δ 8.96 (s, 1H), 7.91 (dd, J = 6.8, 2.8 Hz, 1H), 7.53-7.49 (m, 1H), 7.34 (t, J = 9.2 Hz, 1H), 5.97 (s, 2H), 3.48 (s, 3H), 3.31-3.29 (m, 1H), 2.93-2.88 (m, 1H), 2.60-2.57 (m, 2H), 2.17-2.11 (m, 2H), 1.85-1.73 (m, 4H), 1.30-1.22 (m, 2H)
AIA-028 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5-( 甲基硫基 ) 八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺。
將甲烷磺酸5-(5-胺基-4-((3-氯-4-氟苯基)胺甲醯基)-1-甲基-1H-吡唑-3-基)八氫并環戊二烯-2-基酯(46 mg, 0.1 mmol)及MeSNa (28 mg, 0.4 mmol)於DMF (4 mL)中之混合物在70℃下攪拌4 h。向混合物中添加H2
O (10 mL)。使用乙酸乙酯(10 mL × 3)萃取溶液。藉由Na2
SO4
乾燥合併之有機層,濃縮,然後藉由矽膠管柱層析使用5-30%乙酸乙酯/石油醚純化以提供淺白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(甲基硫基)八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺(10 mg, 23%產率)。MS計算值:422.13;MS實驗值:423.2 [M+1]+
。1
H-NMR (DMSO-d6
, 400 MHz): δ 8.96 (s, 1H), 7.91 (d, J = 4.8, 1H), 7.52-7.50 (m, 1H), 7.34 (t, J = 9.2 Hz, 1H), 5.96 (s, 2H), 3.48 (s, 3H), 3.05-3.02 (m, 1H), 2.45-2.50 (m, 3H), 2.16-2.14 (m, 2H), 2.00 (s, 3H), 1.76-1.72 (m, 2H), 1.50-1.48 (m, 2H), 1.31-1.25 (m, 2H)表 4.
根據針對5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(甲基硫基)八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺所闡述之程序來合成表4中之化合物
AIA-030 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5-( 甲基磺醯基 ) 八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺。
向5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(甲基硫基)八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺(35 mg, 0.08 mmol)於DCM (5 mL)中之溶液中添加m-CPBA (14 mg, 0.08 mmol),並將所得混合物在25℃下攪拌1 h。在真空下去除溶劑並藉由製備型HPLC純化殘餘物以提供白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(甲基磺醯基)八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺(6 mg, 17%產率)。MS計算值:454.12;MS實驗值:455.3 [M+1]+
。1
H-NMR (DMSO-d6
, 400 MHz): δ 8.96 (s, 1H), 7.91 (dd, J = 6.8, 2.8 Hz, 1H), 7.53-7.49 (m, 1H), 7.34 (t, J = 9.2 Hz, 1H), 5.98 (s, 2H), 3.69-3.66 (m, 1H), 3.49 (s, 3H), 3.35-3.34 (m, 1H), 2.92 (s, 3H), 2.67-2.62 (m, 2H), 2.21-2.15 (m, 2H), 1.90-1.83 (m, 2H), 1.78-1.73 (m, 2H), 1.39-1.31 (m, 2H)。
AIA-074 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5-( 甲基亞磺醯基 ) 八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺。
向5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(甲基硫基)八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺(50 mg, 0.11 mmol)於DCM (5 mL)中之溶液中添加m-CPBA (10 mg, 0.05 mmol),且將所得混合物在25℃下攪拌1 h。在真空中去除溶劑並藉由製備型HPLC純化殘餘物以提供白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(甲基亞磺醯基)八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺(8 mg, 15%產率)。MS計算值:438.13;MS實驗值:439.3 [M+1]+
。1
H-NMR (DMSO-d6
, 400 MHz): δ 8.96 (s, 1H), 7.92 (dd, J = 7.2, 2.8 Hz, 1H), 7.54-7.50 (m, 1H), 7.34 (t, J = 8.8 Hz, 1H), 5.97 (s, 2H), 3.49 (s, 3H), 3.37-3.31 (m, 1H), 3.31-3.12 (m, 1H), 2.60-2.58 (m, 2H), 2.50-2.47 (m, 3H), 2.21-2.17 (m, 2H), 1.93-1.90 (m, 1H), 1.68-1.62 (m, 3H), 1.40-1.32 (m, 2H)表 5.
根據針對5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(甲基磺醯基)八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺及5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(甲基亞磺醯基)八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺所闡述之程序來合成表5中之化合物。
AIA-285 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 甲氧基八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺
。向5-胺基-N-(3-氯-4-氟-苯基)-3-(5-羥基-1,2,3,3a,4,5,6,6a -八氫并環戊二烯-2-基)-1-甲基吡唑-4-甲醯胺(50 mg, 0.127 mmol, 1當量)於DCM (3 mL)中之溶液中添加四氟硼酸三甲基氧鎓(37.65 mg, 0.255 mmol, 2.0當量)及N1,N1,N8,N8-四甲基萘-1,8-二胺(54.55 mg, 0.255 mmol, 2.0當量)。將混合物在25℃下及N2
下攪拌16 hr。添加額外四氟硼酸三甲基氧鎓(37.65 mg, 0.255 mmol, 2.0當量)並在N2
下攪拌繼續48 hr。水(10 mL)添加至反應混合物中。使用乙酸乙酯(10 mL × 2)萃取水層。藉由Na2
SO4
乾燥合併之有機層,過濾並濃縮以得到淺色殘餘物。藉由製備型TLC (SiO2
, 1:1石油醚:乙酸乙酯)純化殘餘物以得到粗產物(25 mg)。藉由製備型HPLC進一步純化粗產物。管柱:Gemini 150 × 25 5u;移動相:[水(0.05%氫氧化氨,v/v)-ACN];B%: 40%-70%, 10min。藉由凍乾乾燥期望部分以提供白色固體形式之5-胺基-N-(3-氯-4-氟-苯基)-3- (5-甲氧基-1,2,3,3a,4,5,6,6a-八氫并環戊二烯-2-基)-1-甲基-吡唑-4-甲醯胺(10.8 mg, 0.027 mmol, 20.9%產率,100%純度)。1
H NMR (400 MHz,氯仿-d) δ ppm 1.60 - 1.64 (m, 2 H) 1.81 - 1.93 (m, 2 H) 2.06 (ddd, J=13.40, 8.10, 5.62 Hz, 2 H) 2.33 (br d, J=5.95 Hz, 2 H) 2.49 - 2.62 (m, 2 H) 3.11 (tt, J=11.85, 5.79 Hz, 1 H) 3.28 (s, 3 H) 3.57 (s, 3 H) 3.84 (quin, J=6.01 Hz, 1 H) 5.25 (s, 2 H) 7.10 (t, J=8.71 Hz, 1 H) 7.26 - 7.30 (m, 1 H) 7.30 (s, 1 H) 7.70 (dd, J=6.50, 2.76 Hz, 1 H);LC-MS: 406.9 [M+1]+
。
AIA-009 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5-( 三氟甲氧基 ) 八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺。
將AIA-026 (100 mg, 0.25 mmol)、1-(三氟甲基)-1λ3
-苯并[d][1,2]碘醯-3(1H)-酮(157 mg, 0.5 mmol)及雙(三氟甲基磺醯基)亞醯胺鋅(306 mg, 0.5 mmol)於DCM (15 mL)中之混合物在室溫下攪拌8 h。添加水且使用DCM (20 mL × 3)萃取混合物。乾燥有機層並濃縮。藉由矽膠管柱層析(使用20 - 60%乙酸乙酯/石油醚)及製備型HPLC純化所得殘餘物以得到白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(三氟甲氧基)八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺(5 mg, 4.3%)。MS計算值:460.1;MS實驗值:461.3 [M + 1]+
。1
H-NMR (DMSO-d6
, 400 MHz): δ 8.97 (s, 1H), 7.91 (dd, J = 6.8, 2.4 Hz, 1H), 7.54-7.50 (m, 1H), 7.34 (t, J = 3.2 Hz, 1H), 5.96 (s, 2H), 4.79 (t, J = 6.0 Hz, 1H), 3.46 (t, J = 6.0 Hz, 4H), 2.22-2.09 (m, 5H), 1.65-1.51 (m, 5H)。
AIA-286 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5-( 二甲基胺基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺
。在25℃下,向5-胺基-N-(3-氯-4-氟-苯基)-1-甲基-3-(5-側氧基- 2,3,3a,4,6,6a- 六氫-1H-并環戊二烯-2-基)吡唑-4-甲醯胺(54.21 mg, 0.128 mmol, 1當量)、N-甲基甲胺鹽酸鹽(12.52 mg, 0.154 mmol, 1.2當量)、TEA (19.42 mg, 0.192 mmol, 0.027 mL, 1.5當量)及MgSO4
(76.99 mg, 0.640 mmol, 5當量)於DCM (3 mL)中之混合物中逐份添加三乙醯氧基硼氫化鈉(54.23 mg, 0.256 mmol, 2當量)。將AcOH(催化量)添加至混合物中並攪拌16 hr。使用DCM (10 mL)稀釋反應液並使用NaHCO3
水溶液(10 mL)洗滌。分離水層並使用乙酸乙酯(10 mL)萃取。合併有機層並使用鹽水(10 mL)洗滌,藉由Na2
SO4
乾燥,過濾並濃縮以得到黃色油狀物形式之粗產物。藉由製備型HPLC (管柱:Phenomenex Gemini C18 250 × 50 10u;移動相:[水(0.225%FA)-ACN];B%: 28%-58%,11.2min)純化粗產物以得到白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-3-(5-(二甲基胺基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺 (8 mg, 0.017 mmol, 13.42%產率,100%純度,FA鹽)。1
H NMR (400 MHz, DMSO-d6) δ ppm 1.18 - 1.31 (m, 2 H) 1.47 (td, J=11.86, 8.16 Hz, 2 H) 2.05 - 2.24 (m, 4 H) 2.32 (s, 6 H) 2.37 - 2.44 (m, 2 H) 2.52 - 2.55 (m, 1 H) 2.73 - 2.89 (m, 1 H) 3.50 - 3.50 (m, 3 H) 5.98 (br s, 2 H) 7.35 (t, J=9.04 Hz, 1 H) 7.49 - 7.54 (m, 1 H) 7.90 (d, J=6.56 Hz, 1 H) 8.27 (s, 1 H) 9.00 (s,1 H);LC-MS: 420.0 [M+1]+
。表 6.
根據針對5-胺基-N-(3-氯-4-氟苯基)-3-(5-(二甲基胺基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺所闡述之程序來合成表6中之化合物
AIA-102 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5-( 甲基胺基 ) 八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺。
向AIA-002 (300 mg, 0.7 mmol)於Ti(OiPr)4
(5 mL)中之溶液中添加MeNH2
(100 mg, 1.05 mmol)。將混合物在40℃下攪拌1 h。使用MeOH (5 mL)稀釋混合物,添加NaBH4
(100 mg, 1.4mmol),並在室溫下繼續攪拌1h。使用水將混合物驟冷,然後過濾並在真空中濃縮。藉由管柱層析使用10:3 H2
O/MeCN純化殘餘物以提供白色固體形式之粗製化合物(200 mg, 64.3%)。藉由製備型HPLC進一步純化此材料以產生白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(甲基胺基)八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺。1
H NMR (DMSO-d6 ,
400 MHz): δ 8.94 (s, 1H), 7.90 (dd,J
= 2.8, 2.4 Hz, 1H), 7.51-7.49 (m, 1H), 7.34 (t,J
= 8.8, 9.2 Hz, 1H), 5.95 (s, 2H), 3.52-3.47 (m, 5H), 2.87 (s, 1H), 2.37 (s, 2H), 2.22 (s, 3H), 2.17-2.12 (m, 2H), 2.02 (t,J
= 5.6 Hz, 2H), 1.48-1.46 (m, 2H), 1.03-1.01 (m, 2H);MS計算值:405.1;MS實驗值:406.2 [M+1]+
。表 7.
根據針對5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(甲基胺基)八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺所闡述之程序來合成表7中之化合物
AIA-043 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5-(N- 甲基甲基磺醯胺基 ) 八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺。
向5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(甲基胺基)八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺(100 mg, 0.2 mmol)於DCM (10 mL)中之溶液中添加TEA (50 mg, 0.4 mmol)及MsCl (28 mg, 0.2 mmol)。將混合物在室溫下攪拌2h。使用MeOH將混合物驟冷並在真空中濃縮。藉由製備型HPLC純化殘餘物以提供白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(N-甲基甲基磺醯胺基)八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺(10.5 mg, 8.8%)。1
H NMR (DMSO-d6,
400 MHz): δ 8.96 (s, 1H), 7.90 (dd, J = 2.4, 2.8 Hz, 1H), 7.54-7.50 (m, 1H), 7.34 (t, J = 2.8, 10.0 Hz, 1H), 5.97 (s, 2H), 4.06-4.00 (m, 1H), 3.57-3.52 (m, 4H), 2.83 (s, 3H), 2.67 (s, 3H), 2.42-2.32 (m, 2H), 2.20-2.14 (m, 2H), 1.90-1.84(m, 2H), 1.55-1.48(m, 2H), 1.43-1.35 (m, 2H);MS計算值:483.1;MS實驗值:484.2 [M+1]+
。
AIA-047 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5-(2- 側氧基咪唑啶 -1- 基 ) 八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺。
將5-胺基-3-(5-((2-胺基乙基)胺基)八氫并環戊二烯-2-基)-N-(3-氯-4-氟苯基)-1-甲基-1H-吡唑-4-甲醯胺(120 mg, 0.28 mmol)、CDI (68 mg, 0.42 mmol)及DIPEA (108 mg, 0.84 mmol)於DCM (10 mL)中之溶液在室溫下攪拌過夜。在真空中濃縮混合物並藉由製備型HPLC純化殘餘物以提供白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(2-側氧基咪唑啶-1-基)八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺(20 mg, 15%)。1
H-NMR (DMSO-d6
, 400 MHz): δ 8.96 (s, 1H), 7.91 (dd, J = 6.8, 2.4 Hz, 1H), 7.54-7.50 (m, 1H), 7.35 (t, J = 9.2 Hz, 1H), 6.17 (s, 1H), 5.98 (s, 2H), 4.06-4.00 (m, 1H), 3.57-3.54 (m, 1H), 3.32-3.17 (m, 7H), 2.43-2.37 (m, 2H), 2.21-2.16 (m, 2H), 1.82-1.76 (m, 2H), 1.52-1.44 (m, 2H), 1.37-1.29 (m, 2H);MS計算值:460.2;MS實驗值:461.3 [M+1]+
。
AIA-046 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5-(2- 側氧基噁唑啶 -3- 基 ) 八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺。
將5-胺基-N-(3-氯-4-氟苯基)-3-(5-((2-羥乙基)胺基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺(110 mg, 0.25 mmol)、CDI (62 mg, 0.38 mmol)及DIPEA (97 mg, 0.75 mmol)於DCM (10 mL)中之溶液在室溫下攪拌過夜。在真空中濃縮混合物並藉由製備型HPLC純化殘餘物以提供白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(2-側氧基噁唑啶-3-基)八氫 并環戊二烯-2-基)-1H-吡唑-4-甲醯胺(20 mg, 17%)。1
H-NMR (DMSO-d6
, 400 MHz): δ 8.99 (s, 1H), 7.91 (dd,J
= 6.8, 2.4 Hz, 1H), 7.54-7.50 (m, 1H), 7.35 (t,J
= 9.2 Hz, 1H), 5.99 (s, 2H), 4.24 (t,J
= 7.6 Hz, 2H), 4.02-3.97 (m, 1H), 3.58-3.48 (m, 6H), 2.44-2.40 (m, 2H), 2.22-2.16 (m, 2H), 1.93-1.87 (m, 2H), 1.54-1.47 (m, 2H), 1.43-1.35 (m, 2H);MS計算值:461.2;MS實驗值:462.3 [M+1]+
。
AIA-032 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5-( 羥基亞胺基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。
向AIA-002 (800 mg, 2.1 mmol)於混合溶劑(THF:EtOH =10:10 mL)中之溶液中添加NH2
OH-HCl (440 mg, 6.3 mmol)及NaOAc
(1.2 g, 14.7 mmol)。將混合物在室溫下攪拌過夜,然後過濾並在真空中濃縮。藉由矽膠管柱層析使用10:1 DCM/MeOH純化殘餘物以提供白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-3-(5-(羥基亞胺基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺(800 mg, 96.0%)。MS計算值:405.1;MS實驗值:406.2 [M+1]+
。
AIA-073 5- 胺基 -3-(5- 胺基八氫并環戊二烯 -2- 基 )-N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。
向5-胺基-N-(3-氯-4-氟苯基)-3-(5-(羥基亞胺基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺(300 mg, 0.4 mmol)於MeOH (15 mL)中之溶液中添加NiCl2
6H2
O (23 mg, 0.08 mmol)。將混合物在-30℃下攪拌0.5 h。向此混合物中添加NaBH4
(94mg, 2mmol)並將混合物攪拌1 h,且返回室溫。使用水將混合物驟冷並使用乙酸乙酯萃取。在真空中濃縮有機層以提供淺黃色固體形式之粗製化合物,藉由製備型HPLC純化以提供白色固體形式之5-胺基-3-(5-胺基八氫并環戊二烯-2-基)-N-(3-氯-4-氟苯基)-1-甲基-1H-吡唑-4-甲醯胺(10 mg, 10%產率)。1
H NMR (DMSO-d6,
400 MHz): δ 8.96 (s, 1H), 7.90 (dd, J = 2.8, 2.4 Hz, 1H), 7.53-7.49 (m, 1H), 7.34 (t, J = 9.2, 9.2 Hz, 1H), 5.97 (s, 2H), 3.49-3.33 (m, 5H), 3.14-3.11 (m, 1H), 2.34 (d, J = 5.6 Hz, 2H), 2.17-2.12 (m, 2H), 1.99-1.93 (m, 2H), 1.57-1.42 (m, 2H), 1.23 (s, 1H), 1.02-0.95 (m, 2H);MS計算值:391.1;MS實驗值:392.2 [M+1]+
。
AIA-042 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5-( 甲基磺醯胺基 ) 八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺。
向5-胺基-3-(5-胺基八氫并環戊二烯-2-基)-N-(3-氯-4-氟苯基)-1-甲基-1H-吡唑-4-甲醯胺(200 mg, 0.2 mmol)於DCM (10 mL)中之溶液中添加TEA (52 mg, 0.4 mmol)及MsCl (39 mg, 0.2 mmol)。將混合物在室溫下攪拌2 h。去除溶劑,且藉由製備型HPLC純化殘餘物以提供白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(甲基磺醯胺基)八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺(19.3 mg, 16.8%)。1
H NMR (DMSO-d6,
400 MHz): δ ppm 8.96 (s, 1H), 7.90 (dd, J = 2.4, 4.0 Hz, 1H), 7.53-7.49 (m, 1H), 7.34 (t, J = 8.8, 9.2 Hz, 1H), 7.10 (d, J = 7.6 Hz, 1H), 5.97 (s, 2H), 3.60-3.50 (m, 2H), 3.47 (s, 3H), 2.87 (s, 3H), 2.34 (t, J = 8.0 Hz, 2H ), 2.20-2.11 (m, 4H), 1.48-1.40 (m, 2H), 1.23-1.16 (m, 2H);MS計算值:469.1;MS實驗值:470.2 [M+1]+
。
AIA-086 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5-(( 三氟甲基 ) 磺醯胺基 ) 八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺。
根據針對5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(甲基磺醯胺基)八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺所闡述之程序來合成標題化合物。1
H NMR (DMSO-d6,
400 MHz): δ 9.46 (s, 1H), 8.97 (s, 1H), 7.89 (dd, J = 2.4, 2.4 Hz, 1H), 7.53-7.49 (m, 1H), 7.34 (t, J = 9.2 Hz, 1H), 5.98 (s, 2H), 3.74 (s, 1H), 3.54-3.33 (m, 4H), 2.39-2.37 (m, 2H), 2.21-2.09 (m, 4H), 1.48-1.40 (m, 2H), 1.32-1.24 (m, 2H);MS計算值:523.1;MS實驗值:524.2 [M+1]+
。
AIA-087 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5-((1- 甲基 -1H- 咪唑 )-4- 磺醯胺基 ) 八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺
根據針對5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(甲基磺醯胺基)八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺所闡述之程序來合成標題化合物。MS計算值:535.1;MS實驗值:536.2 [M+1]+
。1
H NMR (DMSO-d6,
400 MHz): δ 8.95 (s, 1H), 7.88 (dd, J = 2.4, 2.4 Hz, 1H), 7.74 (s, 1H), 7.65 (d, J = 0.8 Hz, 1H), 7.52-7.47 (m, 2H),7.33 (t, J = 9.2, 9.2 Hz, 1H), 5.96 (s, 2H), 3.68 (s, 3H), 3.49-3.43 (m, 5H), 2.23(t, J = 4.8, 8.4 Hz, 2H), 2.14-2.07 (m, 2H), 1.92-1.85 (m, 2H), 1.37 (dd, J = 12.4, 12.0 Hz, 2H), 1.11 (t, J = 12.0, 11.6 Hz, 2H)。
| 化合物 | 結構及表徵 |
| AIA-029 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5-( 乙基硫基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 MS計算值:436.9;MS實驗值:437.7 [M+1]+ 。 |
| AIA-048 | 3-(5-(1H- 吡唑 -1- 基 ) 八氫并環戊二烯 -2- 基 )-5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 1 H NMR (DMSO-d 6 , 400 MHz): δ 8.98 (s, 1H), 7.92 (dd,J = 6.8, 2.4 Hz, 1H), 7.77 (d,J = 2.0 Hz, 1H), 7.55-7.51 (m, 1H), 7.43 (d,J = 4.0 Hz, 1H), 7.40-7.33 (m, 1H), 6.19 (t,J = 2.0 Hz, 1H), 5.99 (s, 2H), 4.77-4.69 (m, 1H), 3.51 (s, 3H), 3.38-3.35 (m, 1H), 2.68-2.59 (m, 2H), 2.26-2.20 (m, 2H), 2.11-2.04 (m ,2H), 1.86-1.82 (m, 2H), 1.45-1.37 (m ,2H);MS計算值:442.2;MS實驗值:443.2 [M + 1]+ 。 |
| AIA-058 | 5- 胺基 -3-(5-( 第三丁氧基 ) 八氫并環戊二烯 -2- 基 )-N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 MS計算值:448.2;MS實驗值:449.4 [M+1]+ 。 |
| AIA-101 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5-(2,2,2- 三氟乙氧基 ) 八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺。 MS計算值:474.1;MS實驗值:475.2[M + 1]+ 。 |
| 中間體105 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5-( 環丙基硫基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 MS計算值:448.1;MS實驗值:449.2 [M + 1]+ 。 |
| AIA-170 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5-(2- 羥基乙氧基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 MS計算值:436.2;MS實驗值:437.3 [M + 1]+ ;1 HNMR (DMSO-d6, 400 MHz): δ 8.94 (s, 1H), 7.89 (dd,J = 7.2, 2.4 Hz, 1H), 7.51-7.47 (m, 1H), 7.33 (t,J = 9.2Hz, 1H), 5.95 (s, 2H), 4.50 (t,J = 5.6 Hz, 1H), 3.92 (t,J = 5.6 Hz, 1H) 3.47 (s, 3H) 3.44-3.40 (m, 2H), 3.38-3.31 (m, 5H), 2.15-2.12 (m, 2H), 1.59-1.57 (m, 4H), 1.32-1.24 (m, 2H)。 |
| 實例 | 結構及表徵 |
| AIA-031 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5-( 乙基磺醯基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺: MS計算值:468.9;MS實驗值:469.7 [M+1]+ 。1 H-NMR (DMSO-d6 , 400 MHz): δ 8.95 (s, 1H), 7.90 (dd,J = 6.8, 2.8 Hz, 1H), 7.50-7.47 (m, 1H), 7.32 (t,J = 9.2 Hz, 1H), 5.95 (s, 2H), 3.64-3.62 (m, 1H), 3.47 (s, 3H), 3.33-3.32 (m, 1H), 3.02 (q,J = 7.6 Hz, 2H), 2.65-2.61 (m, 2H), 2.18-2.12 (m, 2H), 1.86-1.82 (m, 2H), 1.75-1.71 (m, 2H), 1.39-1.31 (m, 2H), 1.18 (t,J = 7.6 Hz, 3H) |
| AIA-075 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5-( 乙基亞磺醯基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺: MS計算值:452.9;MS實驗值:453.7 [M+1]+ 。1 H-NMR (DMSO-d6 , 400 MHz): δ 8.95 (s, 1H), 7.90 (dd,J = 6.8, 2.4 Hz, 1H), 7.51-7.47 (m, 1H), 7.32 (t,J = 8.8 Hz, 1H), 5.95 (s, 2H), 3.46 (s, 3H), 3.34-3.29 (m, 1H), 3.14-3.12 (m, 1H), 2.70-2.65 (m, 1H), 2.58-2.51 (m, 3H), 2.18-2.14 (m, 2H), 1.91-1.86 (m, 1H), 1.66-1.58 (m, 3H), 1.38-1.30 (m, 2H), 1.15 (t,J = 7.4) |
| AIA-105 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5-( 環丙基磺醯基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 MS計算值:480.1;MS實驗值:481.2 [M + 1]+ 。 |
| 化合物 | 結構及表徵 |
| AIA-012 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5-( 二乙基胺基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺 。MS計算值:447.9;MS實驗值:448.7 [M+1]+ 。1 H-NMR (DMSO-d6 , 400 MHz): δ 8.96 (s, 1H), 7.91 (dd,J = 6.8, 2.8 Hz, 1H), 7.53-7.49 (m, 1H), 7.34 (t,J = 9.2 Hz, 1H), 5.95 (s, 2H), 3.54-3.51 (m, 1H), 3.49 (s, 3H), 2.94-2.91 (m, 1H), 2.37 (s, 2H), 2.18-2.13 (m, 2H), 1.98 (s, 2H), 1.48-1.40 (m, 2H), 1.09-1.08 (m, 2H), 0.90 (s, 6H) |
| AIA-013 | 5- 胺基 -3-(5-( 氮雜環丁烷 -1- 基 ) 八氫并環戊二烯 -2- 基 )-N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺 。MS計算值:431.9;MS實驗值:432.7 [M+1]+ 。H-NMR (DMSO-d6 , 400 MHz): δ 8.93 (s, 1H), 7.91 (dd,J = 6.8, 2.4 Hz, 1H), 7.52-7.48 (m, 1H), 7.34 (t,J = 9.2 Hz, 1H), 5.95 (s, 2H), 3.49 (s, 3H), 3.45-3.42 (m, 1H), 2.99 (t,J = 6.8 Hz, 4H), 2.61-2.58 (m, 1H), 2.40-2.38 (m, 2H), 2.14-2.07 (m, 2H), 1.87-1.03 (m, 2H), 1.78-1.71 (m, 2H), 1.55-1.47 (m, 2H), 1.08-1.01 (m, 2H) |
| AIA-040 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5-( 吡咯啶 -1- 基 ) 八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺 MS計算值:445.2;MS實驗值:446.3 [M + 1]+ ;448.3 [M + 2 + 1]+ ;1 H NMR (DMSO-d6 , 400 MHz): 1H-NMR (DMSO-d6 , 400 MHz): δ 8.95 (s, 1H), 7.90 (dd, J = 6.8, 2.4 Hz, 1H), 7.50 (dq, J = 8.8, 4.4 Hz, 1H), 7.34 (t, J = 9.2 Hz, 1H), 5.95 (s, 2H), 3.52-3.49 (m, 1H), 3.49 (s, 3H), 2.44-2.38 (m, 7H), 2.18-2.12 (m, 2H), 2.03-1.97 (m, 2H) , 1.65-1.58 (m, 4H) , 1.49-1.41 (m, 2H) , 1.20-1.12 (m, 2H)。 |
| AIA-041 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5- 嗎啉基八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺 1 H-NMR (DMSO-d6 , 400 MHz): δ 8.95 (s, 1H), 7.88 (dd, J = 6.8, 2.8 Hz, 1H), 7.49 (dq, J = 8.8, 4.0 Hz, 1H), 7.32 (t, J = 8.8 Hz, 1H), 5.94 (s, 2H), 3.52 (t, J = 4.4 Hz, 5H), 3.47 (s, 3H), 2.48 -2.45(m, 1H), 2.39-2.33 (m, 6H), 2.17-2.11 (m, 2H), 2.05-1.98 (m, 2H) , 1.47-1.40 (m, 2H) , 1.12-1.04 (m, 2H);MS計算值:461.2;MS實驗值:462.3 [M + 1]+ ;464.3 [M + 2 + 1]+ 。 |
| AIA-246 | 5- 胺基 -N-(3- 氰基 -4- 氟苯基 )-1- 甲基 -3-(5-(3- 側氧基六氫吡嗪 -1- 基 ) 八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺 MS 計算值:465.2;MS實驗值:466.1 [M+1]+ 。1 H-NMR (DMSO-d6 , 400 MHz): δ 9.09 (s, 1H), 8.10 (dd, J = 5.6, 2.8 Hz, 1H), 7.91-7.87 (m, 1H), 7.70 (s, 1H), 7.47 (t, J = 9.2 Hz, 1H), 6.00 (s, 2H), 3.55-3.52 (m, 1H), 3.49 (s, 3H), 3.11 (s, 2H), 2.90 (s, 2H), 2.62-2.52 (m, 3H), 2.42-2.36 (m, 2H), 2.19-2.13 (m, 2H), 2.08-2.02 (m, 2H), 1.50-1.43 (m, 2H), 1.17-1.09 (m, 2H)。 |
| AIA-199 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5-(5- 側氧基 -1,4- 二氮雜環庚烷 -1- 基 ) 八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺。 MS計算值:488.2;MS實驗值:489.3 [M+1]+ ;1H NMR (DMSO-d6, 400 MHz): δ 7.79 (dd,J = 6.8, 2.8 Hz, 1H), 7.42-7.39 (m, 1H), 7.18 (t,J = 8.8 Hz,1 H), 3.55 (s,3 H), 3.54-3.51 (m, 1H), 3.30-3.27 (m,2 H), 2.93-2.87 (m, 1H), 2.72-2.68 (m, 4H), 2.59-2.48 (m, 4H), 2.34-2.28 (m, 2H), 2.21-2.15 (m, 2H), 1.61-1.53 (m, 2H), 1.33-1.25 (m, 2H)。 |
| 化合物 | 結構及表徵 |
| AIA-160 | 5- 胺基 -3-(5-((2- 胺基乙基 ) 胺基 ) 八氫并環戊二烯 -2- 基 )-N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 MS計算值:434.2,MS實驗值:435.3 [M+1]+ 。 |
| AIA-103 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5-((2- 羥乙基 ) 胺基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 1 H-NMR (DMSO-d6 , 400 MHz): δ 8.96 (s, 1H), 7.91 (dd,J = 6.8, 2.4 Hz, 1H), 7.53-7.49 (m, 1H), 7.35 (t,J = 9.2 Hz, 1H), 5.97 (s, 2H), 4.42-4.39 (m, 1H), 3.52-3.47 (m, 4H), 3.42-3.38 (m, 2H), 3.02-2.97 (m, 1H), 2.55-2.52 (m, 2H), 2.37-2.33 (m, 2H), 2.18-2.12 (m, 2H), 2.07-2.01 (m, 2H), 1.52-1.44 (m, 2H), 1.06-0.98 (m, 2H);MS計算值:435.2,MS實驗值:436.3 [M+1]+ 。 |
| AIA-079 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5-(2,2- 二甲基嗎啉基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 MS計算值:489.2;MS實驗值:490.3 [M+1]+ 。1 H-NMR (CDCl3 , 400 MHz): δ 7.71 (dd,J = 6.4, 2.8 Hz, 1H), 7.29 (t,J = 4 Hz, 1H), 7.11 (t,J = 8.8 Hz, 1H), 5.26 (s, 2H), 3.72 (t,J = 4.8 Hz, 2H), 3.58 (s, 3H), 3.25-3.16 (m, 1H), 2.57-2.50 (m, 3H), 2.39-2.31 (m, 4H), 2.22 (s, 2H), 2.15-2.09 (m, 2H), 1.84-1.76 (m, 2H), 1.37-1.30 (m, 2H), 1.23 (s, 6H) |
| AIA-202 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5-(3- 甲基 -5- 側氧基六氫吡嗪 -1- 基 ) 八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺。 MS計算值:488.2;MS實驗值:489.4 [M + 1]+ 。1 H NMR (DMSO-d6 , 400 MHz): δ 8.95 (s,1 H), 7.89-7.87 (dd,J = 6.8, 2.4 Hz, 1 H), 7.51 (s, 1H), 7.50-7.47 (m, 1H), 7.32 (t,J = 8.8 Hz, 2H), 5.95 (s, 2H), 3.53-3.47 (m, 4H), 3.39-3.36 (m, 1H), 3.01 (d,J = 16 Hz, 1H), 2.78-2.68 (m, 2H),2.57-2.53 (m, 1H), 2.37-2.33 (m, 2H), 2.17-2.12 (m, 2H), 2.06-1.96 (m,3H), 1.48-1.43 (m, 2H), 1.12-1.02 (m, 2H), 1.01 (d,J = 6.4 Hz, 3H)。 |
| AIA-082 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5-( 六氫吡嗪 -1- 基 ) 八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺。 MS計算值:460.2;MS實驗值:461.3 [M+1]+ ,1 H-NMR (DMSO-d6 , 400 MHz): δ 8.97 (s, 1H), 7.90 (dd,J = 6.8, 2.4 Hz, 1H), 7.52-7.49 (m, 1H), 7.34 (t,J = 9.2 Hz, 1H), 5.96 (s, 2H), 3.54-3.49 (m, 4H), 3.28-3.14 (m, 2H), 2.64 (s, 3H), 2.44-2.22 (m, 6H), 2.17-2.09 (m, 2H), 2.04-2.01 (m, 2H), 1.48-1.39 (m, 2H), 1.10-1.07 (m, 2H)。 |
| AIA-203 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5-(2- 甲基 -3- 側氧基六氫吡嗪 -1- 基 ) 八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺。 MS計算值:488.2;MS實驗值:489.4 [M + 1]+ 。1 H NMR (DMSO-d6 , 400 MHz): δ 8.95 (s,1 H), 7.90-7.87 (dd,J = 7.2, 2.4 Hz, 1H), 7.55 (2, 1H), 7.51-7.47 (m, 1H), 7.35-7.30 (t,J = 8.8 Hz, 2H),5.95 (s, 2H), 3.53-3.50 (m, 1H), 3.47 (s, 3H), 3.19-3.14 (m, 2H), 3.04-2.95 (m, 2H),2.80-2.75 (m, 1H), 2.60-2.56 (m, 1H), 2.43-2.30 (m, 2H), 2.15-2.12 (m,2H), 2.00 (s, 2H), 1.48-1.40 (m, 2H), 1.14-1.06 (m, 5H)。 |
| AIA-211 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5-(3- 側氧基 -1,4- 二氮雜環庚烷 -1- 基 ) 八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺。 MS計算值:488.2;MS實驗值:489.2 [M + 1]+ ;1 H NMR (DMSO-d 6 , 400 MHz): 8.96 (s, 1H), 7.91 (dd,J = 6.8, 2.4 Hz, 1H), 7.54-7.48 (m, 2H), 7.34 (t,J = 9.2 Hz, 1H), 5.97 (s, 2H), 3.56-3.52 (m, 1H), 3.50 (s, 3H), 3.29 (s, 2H), 3.10-3.09 (m, 2H), 3.02-2.94 (m, 1H), 2.89-2.88 (m ,2H), 2.38-2.32 (m ,2H), 2.19-2.10 (m ,4H), 1.54 (s, 2H), 1.48-1.41 (m ,2H), 1.10-1.02 (m ,2H) |
中間體106 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5-((3- 氯丙基 ) 磺醯胺基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺
:根據針對5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(甲基磺醯胺基)八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺所闡述之程序來合成標題化合物。MS計算值:531.1;MS實驗值:532.2 [M+1]+
。
AIA-044 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5-(1,1- 二側氧基異噻唑啶 -2- 基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。
向5-胺基-N-(3-氯-4-氟苯基)-3-(5-((3-氯丙基)磺醯胺基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺(100 mg, 0.2 mmol)於DMF (5 mL)中之溶液中添加NaH (13 mg, 0.6 mmol)。將混合物在室溫下攪拌1h,然後使用水驟冷並使用乙酸乙酯萃取。在真空中濃縮有機層。藉由製備型HPLC純化殘餘物以提供白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-3-(5-(1,1-二側氧基異噻唑啶-2-基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺(47.3 mg, 51%產率)。1
H NMR (DMSO-d6,
400 MHz): δ 8.97 (s, 1H), 7.90 (dd, J = 2.8, 2.4 Hz, 1H), 7.53-7.49 (m, 1H), 7.34 (t, J = 9.2, 9.2 Hz, 1H), 5.97 (s, 2H), 3.55-3.49 (m, 5H), 3.17-3.13 (m, 4H), 2.41-2.39 (m, 2H), 2.21-2.14 (m, 4H), 2.06-1.99 (m, 2H), 1.52-1.44 (m, 2H), 1.41-1.33 (m, 2H);MS計算值:495.1;MS實驗值:496.2 [M+1]+
AIA-288 3-(5- 乙醯胺基八氫并環戊二烯 -2- 基 )-5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺
根據針對5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(甲基磺醯胺基)八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺所闡述之程序來合成標題化合物1
H NMR (400 MHz,氯仿-d) δ ppm 1.19 - 1.31 (2 H, m), 1.71 - 1.83 (2 H, m), 1.95 (3 H, s), 2.28 - 2.42 (4 H, m), 2.52 - 2.63 (2 H, m), 3.23 (1 H, dt, J=11.30, 5.71 Hz), 3.58 (3 H, s), 4.24 - 4.37 (1 H, m), 5.25 (2 H, s), 5.49 - 5.58 (1 H, m), 7.11 (1 H, t, J=8.77 Hz), 7.22 - 7.25 (2 H, m), 7.71 (1 H, dd, J=6.39, 2.21 Hz);LCMS: 434.0 [M+1]+
。
AIA-033A、AIA-033B 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(3- 側氧基八氫 -1H- 環戊 [c] 吡啶 -6- 基 )-1H- 吡唑 -4- 甲醯胺。非對映異構體 1 (AIA-033A) 及非對映異構體 2(AIA-033B) 。
將5-胺基-N-(3-氯-4-氟苯基)-3-(5-(羥基亞胺基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺(90 mg, 0.22 mmol)、TsCl (90 mg, 1.47 mmol)、Na2
CO3
(90 mg, 0.85 mmol)於H2
O (5 mL)/丙酮(5 mL)中之混合物在80℃下攪拌4 h。在真空中濃縮反應混合物且藉由對掌性HPLC純化殘餘物以提供AIA-033A及AIA-03-B。AIA-033-A (20 mg, 22%產率)呈白色固體形式。MS計算值:405.14;MS實驗值:406.3 [M+1]+
;1
H-NMR (DMSO-d6
, 400 MHz): δ 8.95 (s, 1H), 7.91 (dd, J = 6.8, 2.4 Hz, 1H), 7.52-7.45 (m, 2H), 7.32 (t, J = 9.2 Hz, 1H), 5.95 (s, 2H), 3.47 (s, 3H), 3.38-3.35 (m, 1H), 3.16-3.12 (m, 1H), 2.84-2.81 (m, 1H), 2.42-2.41 (m, 1H), 2.31-2.21 (m, 2H), 2.09-2.04 (m, 2H), 1.96-1.91 (m, 1H), 1.48-1.45 (m, 1H), 1.29-1.27 (m, 1H)。AIA-033-B (20 mg, 22%產率)呈白色固體形式。MS計算值:405.14;MS實驗值:406.3 [M+1]+
。1
H-NMR (DMSO-d6
, 400 MHz): δ 8.95 (s, 1H), 7.91 (dd, J = 6.8, 2.4 Hz, 1H), 7.52-7.45 (m, 2H), 7.32 (t, J = 9.2 Hz, 1H), 5.95 (s, 2H), 3.47 (s, 3H), 3.38-3.35 (m, 1H), 3.16-3.12 (m, 1H), 2.84-2.81 (m, 1H), 2.42-2.41 (m, 1H), 2.31-2.21 (m, 2H), 2.09-2.04 (m, 2H), 1.96-1.91 (m, 1H), 1.48-1.45 (m, 1H), 1.30-1.27 (m, 1H)。
中間體107 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-( 六氫 -1'H- 螺 [ 環氧乙烷 -2,2'- 并環戊二烯 ]-5'- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。
向2-甲基丙烷-2-醇鉀(230 mg, 2.05 mmol)於THF (30 mL)中之溶液中添加三甲基碘化亞碸(450 mg, 2.05 mmol)。將混合物在室溫及N2
下攪拌1h。然後向混合物中添加AIA-002(200mg, 0.53mmol)並在60℃及N2
氣氛下繼續攪拌5h。在真空下去除溶劑並藉由矽膠管柱層析使用1:1乙酸乙酯/石油醚純化產物以提供黃色固體形式之5-胺基-N-(3-氯-4-氟苯基)-3-(六氫-1'H-螺[環氧乙烷-2,2'-并環戊二烯]-5'-基)-1-甲基-1H-吡唑-4-甲醯胺(200 mg, 96.6%)。MS計算值:404.1;MS實驗值:405.2 [M
+1]+
。
AIA-225 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-( 甲基硫基甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。
向5-胺基-N-(3-氯-4-氟苯基)-3-(六氫-1'H-螺[環氧乙烷-2,2'-并環戊二烯]-5'-基)-1-甲基-1H-吡唑-4-甲醯胺(200 mg, 0.495 mmol)於THF/H2
O (6 mL/2 mL)中之溶液中添加NaSMe (138.6 mg, 1.98 mmol)。將混合物在室溫下攪拌過夜。去除溶劑並藉由矽膠管柱層析使用3:1石油醚/乙酸乙酯純化粗產物以提供黃色固體形式之5-胺基-N-(3-氯-4-氟苯基)-3-(5-羥基-5-(甲基硫基甲基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺(100 mg, 44.7%)。MS計算值:452.1;MS實驗值:452.2 [M
+1]+
。表 8.
根據針對5-胺基-N-(3-氯-4-氟苯基)-3-(5-羥基-5-(甲基硫基甲基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺所闡述之程序來合成表8中之化合物
AIA-227-1、AIA-227-2 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-((2r,5r)-5- 羥基 -5-( 甲基磺醯基甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺 (AIA-227-1) 及 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-((2s,5s)-5- 羥基 -5-( 甲基磺醯基甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺 (AIA-227-2) 。
向5-胺基-N-(3-氯-4-氟苯基)-3-(5-羥基-5-(甲基硫基甲基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺(100 mg, 0.22 mmol)於DCM (5 mL)中之溶液中添加m-CPBA (114.8 mg, 0.66 mmol)。將混合物在室溫下攪拌過夜。去除溶劑並藉由矽膠管柱層析使用3:1 DCM/MeOH純化粗製材料以提供白色固體形式之AIA-227 (40 mg, 37.3%)。MS計算值:484.1;MS實驗值:484.3 [M+1]+
。藉由SFC分離AIA-227以得到白色固體形式之AIA-227-1 (4 mg)及白色固體形式之AIA-227-2 (4 mg)。AIA-227-1:1
H-NMR (DMSO, 400 MHz): δ 8.95 (s, 1H), 7.91 (dd,J
= 6.8, 2.4 Hz, 1H), 7.54-7.50 (m, 1H), 7.35 (t,J
= 9.2 Hz, 1H), 5.97 (s, 2H), 4.79 (s, 1H), 3.59-3.53 (m, 1H), 3.49 (s, 3H), 3.35 (s, 2H), 2.97 (s, 3H), 2.67-2.60 (m, 2H), 2.18-2.12 (m, 2H), 2.07-2.02 (m, 2H), 1.45-1.36 (m,4H)。AIA-227-2:1
H-NMR (DMSO, 400 MHz): δ 8.94 (s, 1H), 7.91 (dd,J
= 2.8, 2.4 Hz, 1H), 7.53-7.49 (m, 1H), 7.34 (t,J
= 9.2 Hz, 1H), 5.97 (s, 2H), 4.87 (s, 1H), 3.49 (s, 3H), 3.43-3.35 (m, 1H), 3.25 (s, 2H), 2.97 (s, 3H), 2.49 (s, 2H), 2.15-2.09 (m, 2H), 2.02-1.97 (m, 2H), 1.73-1.60 (m, 4H)。表 9.
根據針對5-胺基-N-(3-氯-4-氟苯基)-3-((2r,5r)-5-羥基-5-(甲基磺醯基甲基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺(AIA-227-1)及5-胺基-N-(3-氯-4-氟苯基)-3-((2s,5s)-5-羥基-5-(甲基磺醯基甲基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺(AIA-227-2)所闡述之程序來合成表9中之化合物。
AIA-227-2 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-((2s,5s)-5- 羥基 -5-( 甲基磺醯基甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺之替代合成。
在-78℃下,向二甲基碸(77.0 g, 818.7 mmol)於THF (800 mL)中之溶液中逐滴添加n-BuLi (327.5 mL, 818.7 mmol, 2.5M)。將所得溶液升溫至-20℃並攪拌1小時。將反應液冷卻至-78℃,且經2小時添加AIA-002 (40.0 g, 102.3 mmol)於無水四氫呋喃(1200 mL)中之溶液。將混合物升溫至室溫並再攪拌4小時。使用飽和氯化銨水溶液(200 mL)將反應混合物驟冷。去除溶劑,隨後使用水稀釋,使用乙酸乙酯(3 × 200 mL)萃取,藉由Na2
SO4
乾燥,過濾,並濃縮以得到粗產物。藉由管柱層析(使用於DCM中之0-5%甲醇)及鹼性製備型HPLC純化粗產物以提供白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-3-((2s,5s)-5-羥基-5-(甲基磺醯基甲基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺(26.0 g, 52.4%)。MS計算值:484.1,MS實驗值:485.2 [M
+ 1]+
;1
H NMR (DMSO-d6
, 400 MHz): δ 8.96 (s, 1H), 7.92 (dd, J = 6.8, 2.8 Hz, 1H), 7.54-7.50 (m, 1H), 7.35 (t, J = 8.8 Hz, 1H), 5.98 (s, 2H), 4.88 (s, 1H), 3.49 (s, 3H), 3.42-3.37 (m, 1H), 3.25 (s, 2H), 2.97 (s, 3H), 2.15-2.10 (m, 2H), 2.03-1.97 (m, 2H), 1.73-1.60 (m, 4H)。
| 化合物 | 結構及表徵 |
| 中間體108 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5-(( 乙基硫基 ) 甲基 )-5- 羥基八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 MS計算值:466.1;MS實驗值:467.2 [M+1]+ 。 |
| 中間體109 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5-(( 環丙基硫基 ) 甲基 )-5- 羥基八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 MS計算值:478.2;MS實驗值:479.3 [M+H]+ 。 |
| AIA-258-1 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-(((2,2,2- 三氟乙基 ) 硫基 ) 甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 1 。 MS計算值:520.1;MS實驗值:521.2 [M + H]+ 。AIA-258-1:1 H NMR (DMSO-d6, 400 MHz): δ 8.94 (s, 1H), 7.91 (dd,J = 6.8, 2.4 Hz, 1H), 7.54-7.50 (m, 1H), 7.35 (t,J = 9.2 Hz, 1H), 5.97 (s, 2H), 4.47 (s, 1H) 3.58-3.45 (m, 6H), 2.86 (s, 2H), 2.67-2.62 (m, 2H), 2.18-2.11 (m, 2H), 1.89-1.84 (m, 2H), 1.44-1.32 (m, 4H)。 |
| AIA-258-2 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-(((2,2,2- 三氟乙基 ) 硫基 ) 甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 2 。 1 H NMR (DMSO-d6, 400 MHz): δ 8.94 (s, 1H), 7.91 (dd,J = 6.8, 2.8 Hz, 1H), 7.53-7.49 (m, 1H), 7.34 (t,J = 8.8 Hz, 1H), 5.97 (s, 2H), 4.60 (s, 1H) 3.54-3.46 (m, 5H), 3.42-3.39 (m, 1H), 2.79 (s, 2H), 2.42-2.41 (m, 2H), 2.14-2.10 (m, 2H), 1.92-1.87 (m, 2H), 1.65-1.63 (m, 2H), 1.51-1.47 (m, 2H)。 |
| AIA-283-1 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-(((2- 羥乙基 ) 硫基 ) 甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 1 。 MS計算值:483.0;MS實驗值:484.1 [M + 1]+ 。1 H NMR (CDCl3 , 400 MHz): δ 7.74-7.72 (m, 1H), 7.30-7.26 (m, 2H), 7.11 (t,J = 8.4 Hz, 1H), 5.28 (s, 2H), 3.80-3.77 (m, 2H), 3.59 (s, 3H), 3.29-3.24 (m, 2H), 2.92-2.79 (m, 6H), 2.41-2.35 (m, 2H), 2.10-2.04 (m, 2H), 1.75-1.60 (m, 2H), 1.50-1.46 (m, 2H)。 |
| AIA-283-2 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-(((2- 羥乙基 ) 硫基 ) 甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 2 。 1 H NMR (DMSO-d6 , 400 MHz): δ 8.94(s, 1H), 7.92-7.90 (m, 1H), 7.51-7.50 (m, 1H), 7.35 (t,J = 9.2 Hz, 1H), 5.98 (s, 2H), 4.76-4.74 (m, 1H), 3.42 (s, 1H), 3.52-3.49 (m, 6H), 2.62-2.57 (m, 4H), 2.42 (s, 2H), 2.13-2.10 (m, 2H), 1.91-1.86 (m, 2H), 1.67-1.65 (m, 2H), 1.46-1.44 (m, 2H)。 |
| AIA-284-1 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-(((2- 嗎啉基乙基 ) 硫基 ) 甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 1 。 MS計算值:551.2;MS實驗值:552.3 [M + H]+ 。1 H NMR (DMSO-d6 , 400 MHz) δ 8.94 (s, 1H), 7.91 (dd,J = 6.8, 2.0 Hz, 1H ), 7.53-7.49 (m, 1H), 7.37-7.32 (m, 1H), 5.98 (s, 2H), 4.48 (s, 1H), 3.56-3.53 (m, 4H), 3.49 (s, 3H), 3.42-3.38 (m, 1H), 2.66-2.62 (m, 4H), 2.47-2.36 (m, 8H), 2.15-2.08 (m, 2H), 1.90-1.85 (m, 2H), 1.68-1.65 (m, 2H), 1.46-1.43 (m, 2H)。 |
| AIA-284-2 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-(((2- 嗎啉基乙基 ) 硫基 ) 甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 2 。 1 H NMR (DMSO-d6 , 400 MHz) δ 8.95 (s, 1H), 7.91 (dd,J = 6.8, 2.4 Hz, 1H), 7.54-7.50 (m, 1H), 7.37-7.33 (m, 1H) 5.98 (s, 2H), 4.37 (s, 1H), 3.59-3.53 (m, 5H), 3.51-3.49 (s, 3H), 2.68-2.61 (m, 6H), 2.51-2.30 (m, 6H), 2.17-2.11 (m, 2H), 1.83-1.78 (m, 2H), 1.43-1.23 (m, 4H)。 |
| AIA-262-1 | 5- 胺基 -3-(5-(( 第三丁基硫基 ) 甲基 )-5- 羥基八氫并環戊二烯 -2- 基 )-N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 1 。 MS計算值:494.19;MS實驗值:495.3 [M+H]+ 。1 H-NMR (DMSO, 400 MHz): δ 8.94 (s, 1H), 7.90-7.93(dd,J = 7.2, 2.8 Hz, 1H), 7.54-7.50 (m, 1H), 7.35 (t,J = 9.2 Hz, 1H), 5.96 (s, 2H), 4.29 (s, 1H), 3.55-3.52 (m, 1H), 3.49 (s, 3H), 2.66-2.51 (m, 4H), 2.16-2.08 (m, 2H), 1.79-1.74 (m, 2H), 1.42-1.34 (m, 4H), 1.24 (s, 9H)。 |
| AIA-262-2 | 5- 胺基 -3-(5-(( 第三丁基硫基 ) 甲基 )-5- 羥基八氫并環戊二烯 -2- 基 )-N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 2 。 1 H-NMR (DMSO, 400 MHz): δ 8.92 (s, 1H), 7.92-7.90 (dd,J = 6.8, 2.4 Hz, 1H), 7.53-7.49 (m, 1H), 7.35 (t,J = 9.2 Hz, 1H), 5.97 (s, 2H), 4.33 (s, 1H), 3.49 (s, 3H), 3.43-3.34 (m, 1H), 2.61 (s, 2H), 2.45-2.44 (m, 2H), 2.14-2.08 (m, 2H), 1.92-1.87 (m, 2H), 1.72-1.34 (m, 2H), 1.46-1.40 (m, 2H), 1.24 (s, 9H)。 |
| AIA-295-2A | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-(((3- 羥丙基 ) 硫基 ) 甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺非對映異構體 1 。 MS計算值:496.17;MS實驗值:497.13 [M+H]+ 。 |
| AIA-295-2B | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-(((3- 羥丙基 ) 硫基 ) 甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺非對映異構體 2 。 MS計算值:496.17;MS實驗值:497.13 [M+H]+ 。 |
| 化合物 | 結構及表徵 |
| AIA-250-1 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5-(( 乙基磺醯基 ) 甲基 )-5- 羥基八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 1 。 1 H-NMR (DMSO, 400 MHz): δ 8.95 (s, 1H), 7.91 (dd,J = 6.8, 2.4 Hz, 1H), 7.54-7.50 (m, 1H), 7.35 (t,J = 9.2 Hz, 1H), 5.98 (s, 2H), 4.77 (s, 1H), 3.58-3.55 (m,1H), 3.49 (s, 3H), 3.31 (s, 2H), 3.11 (q,J = 7.2 Hz, 2H), 2.63-2.61 (m, 2H), 2.18-2.12 (m, 2H), 2.06-2.02 (m, 2H), 1.47-1.36 (m, 4H), 1.20 (t,J =7.6 Hz, 3H)。 |
| AIA-250-2 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5-(( 乙基磺醯基 ) 甲基 )-5- 羥基八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 2 。1 H-NMR (DMSO, 400 MHz): δ 8.94 (s, 1H), 7.91 (dd,J = 7.2, 2.8 Hz, 1H), 7.53-7.49 (m, 1H), 7.35 (t,J = 9.2 Hz, 1H), 5.97 (s, 2H), 4.87 (s, 1H), 3.49 (s, 3H), 3.41-3.37 (m, 1H), 3.21 (s, 2H), 3.11 (q,J = 7.6 Hz, 2H), 2.49 (s, 2H), 2.15-2.09 (m, 2H), 2.03-1.98 (m, 2H), 1.73-1.60 (m, 4H), 1.20 (t,J = 7.6 Hz, 3H)。 |
| AIA-252-1 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5-(( 環丙基磺醯基 ) 甲基 )-5- 羥基八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 1 。 1 H-NMR (DMSO, 400 MHz): δ 8.95 (s, 1H), 7.90-7.93(dd,J = 6.8, 2.4 Hz, 1H), 7.55-7.51 (m, 1H), 7.35 (t,J = 9.2 Hz, 1H), 5.98 (s, 2H), 4.73 (s, 1H), 3.60-3.54 (m, 1H), 3.49 (s, 3H), 3.37 (s, 2H), 2.79-2.72 (m, 1H), 2.68-2.61 (m, 2H), 2.19-2.13 (m, 2H), 2.09-2.04 (m, 2H), 1.50-1.37 (m, 4H), 0.97 (d,J = 6.4 Hz, 4H)。 |
| AIA-252-2 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5-(( 環丙基磺醯基 ) 甲基 )-5- 羥基八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 2 。 MS計算值:510.2;MS實驗值:511.2 [M+H]+ 。1 H-NMR (DMSO, 400 MHz): δ 8.94 (s, 1H), 7.92 (d,J = 6.0 Hz, 1H), 7.53-7.50 (m, 1H), 7.35 (t,J = 9.2 Hz, 1H), 5.97 (s, 2H), 4.80 (s, 1H), 3.49 (s, 3H), 3.41-3.36 (m, 1H), 3.28 (s, 2H), 2.78-2.75 (m, 1H), 2.60 (m, 2H), 2.13-2.11 (m, 2H), 2.04-2.01 (m, 2H), 1.76-1.64 (m, 4H), 0.96 (d,J = 6.0 Hz, 4H)。 |
| AIA-266-1 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-(((2- 羥乙基 ) 磺醯基 ) 甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 1 。 MS計算值:515.0;MS實驗值:515.15 [M + 1]+ ;1 H NMR (DMSO-d6 , 400 MHz): δ 8.96 (s, 1H), 7.93-7.90 (m, 1H), 7.55-7.51 (m, 1H), 7.35 (t,J = 9.2 Hz, 1H), 5.55 (s, 1H), 5.02 (t,J = 5.6 Hz, 1H), 4.76 (s, 1H), 3.78 (dd,J = 11.6, 5.6 Hz, 1H), 3.58-3.55 (m, 1H), 3.49 (s, 3H), 3.38 (s, 2H), 3.28 (t,J = 6.4 Hz, 2H), 2.26 (s, 2H), 2.17-2.01 (m, 4H), 1.48-1.39 (m, 4H)。 |
| AIA-266-2 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-(((2- 羥乙基 ) 磺醯基 ) 甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 2 。 MS計算值:515.0;MS實驗值:515.15 [M + 1]+ ;1 H NMR (DMSO-d6 , 400 MHz): δ 8.95 (s, 1H), 7.93-7.90 (m, 1H), 7.53-7.49 (m, 1H), 7.35 (t,J = 8.8 Hz, 1H), 5.98 (s, 2H), 5.02-4.99 (m, 1H), 4.82 (s, 1H), 3.80-3.76 (m, 2H), 3.49 (s, 3H), 3.42-3.40 (m, 2H), 3.37-3.28 (m, 5H), 2.13-1.98 (m, 4H), 1.74-1.61 (m, 4H)。 |
| AIA-260-1 | 5- 胺基 -3-(5-(( 第三丁基磺醯基 ) 甲基 )-5- 羥基八氫并環戊二烯 -2- 基 )-N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 1 。 MS計算值:526.18;MS實驗值:527.2 [M+H]+ 。1 H-NMR (CDCl3 , 400 MHz): δ 7.68-7.66 (dd,J = 6.4, 2.4 Hz, 1H), 7.23-7.17 (m,2H), 7.04 (t, J = 8.8 Hz, 1H), 5.20 (s, 2H), 3.66 (s, 1H), 3.51 (s, 3H), 3.24-3.20 (m, 1H), 3.17 (s, 2H),2.88-2.83 (m, 2H), 2.36-2.28 (m, 4H), 1.70-1.51 (m, 4H), 1.35 (s, 9H)。 |
| AIA-260-2 | 5- 胺基 -3-(5-(( 第三丁基磺醯基 ) 甲基 )-5- 羥基八氫并環戊二烯 -2- 基 )-N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 2 。 MS計算值:526.18;MS實驗值:527.2 [M + H]+ 。1 H-NMR ( (CD3 )2 CO, 400 MHz): δ 8.14 (s, 1H), 8.03-8.00 (dd,J = 6.8, 2.4 Hz, 2H), 7.58-7.54 (t,J = 8.8 Hz, 1H), 5.90 (s, 2H), 3.96 (s, 1H), 3.56 (s, 3H), 3.45-3.39 (m, 1H), 3.35 (s, 2H),2.71-2.69 (m, 2H), 2.32-2.26 (m, 2H), 2.17-2.11 (m, 2H), 2.01-1.85 (m, 2H), 1.88-1.83 (dd,J = 13.2, 2.8 Hz, 2H), 1.38 (s, 9H)。 |
中間體110 甲烷磺酸 3-(((5-(5- 胺基 -4-((3- 氯 -4- 氟苯基 ) 胺甲醯基 )-1- 甲基 -1H- 吡唑 -3- 基 )-2- 羥基八氫并環戊二烯 -2- 基 ) 甲基 ) 硫基 ) 丙基酯非對映異構體 1 。
向5-胺基-N-(3-氯-4-氟苯基)-3-(5-羥基-5-(((3-羥丙基)硫基)甲基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺非對映異構體1 (AIA-295-2A) (198.8 mg, 0.4 mmol)於DCM (15 mL)中之溶液中添加TEA (121.4 mg, 1.2 mmol )及MsCl (91.6 mg, 0.8 mmol)。將混合物在室溫下攪拌1h。在完成反應之後,使用H2
O將混合物驟冷並使用DCM萃取。在減壓下去除有機層,且藉由管柱層析純化殘餘物以提供白色固體形式之甲烷磺酸3-(((5-(5-胺基-4-((3-氯-4-氟苯基)胺甲醯基)-1-甲基-1H-吡唑-3-基)-2-羥基八氫并環戊二烯-2-基)甲基)硫基)丙基酯非對映異構體1 (200.0 mg, 86.9%)。MS計算值:574.15;MS實驗值:575.2 [M+1]+
。
中間體111 甲烷磺酸 3-(((5-(5- 胺基 -4-((3- 氯 -4- 氟苯基 ) 胺甲醯基 )-1- 甲基 -1H- 吡唑 -3- 基 )-2- 羥基八氫并環戊二烯 -2- 基 ) 甲基 ) 硫基 ) 丙基酯非對映異構體 2 。
向5-胺基-N-(3-氯-4-氟苯基)-3-(5-羥基-5-(((3-羥丙基)硫基)甲基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺非對映異構體2 (AIA-295-2B) (452.3 mg, 0.91 mmol)於DCM (15 mL)中之溶液中添加TEA (276.2 mg, 2.73 mmol )及MsCl (208.5 mg, 1.82 mmol)。將混合物在室溫下攪拌1h。在完成反應之後,使用H2
O將混合物驟冷並使用DCM萃取。在減壓下去除有機層,且藉由管柱層析純化殘餘物以提供白色固體形式之甲烷磺酸3-(((5-(5-胺基-4-((3-氯-4-氟苯基)胺甲醯基)-1-甲基-1H-吡唑-3-基)-2-羥基八氫并環戊二烯-2-基)甲基)硫基)丙基酯非對映異構體2 (460.0 mg, 87.9%)。MS計算值:574.15;MS實驗值:575.2 [M+1]+
。
中間體112 5- 胺基 -3-(5-(((3- 溴丙基 ) 硫基 ) 甲基 )-5- 羥基八氫并環戊二烯 -2- 基 )-N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 1 。
在80℃下攪拌甲烷磺酸3-(((5-(5-胺基-4-((3-氯-4-氟苯基)胺甲醯基)-1-甲基-1H-吡唑-3-基)-2-羥基八氫并環戊二烯-2-基)甲基)硫基)丙基酯非對映異構體1 (201.3 mg, 0.35 mmol )及LiBr
(76.4 mg, 0.88 mmol)於NMP中之混合物。在完成反應之後,藉由製備型HPLC純化混合物以提供白色固體形式之5-胺基-3-(5-(((3-溴丙基)硫基)甲基)-5-羥基八氫并環戊二烯-2-基)-N-(3-氯-4-氟苯基)-1-甲基-1H-吡唑-4-甲醯胺非對映異構體1 (120 mg, 61.2 %)。MS計算值:558.09;MS實驗值:559.13 [M+1]+
。
中間體113 5- 胺基 -3-(5-(((3- 溴丙基 ) 硫基 ) 甲基 )-5- 羥基八氫并環戊二烯 -2- 基 )-N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 2 。
在80℃下攪拌甲烷磺酸3-(((5-(5-胺基-4-((3-氯-4-氟苯基)胺甲醯基)-1-甲基-1H-吡唑-3-基)-2-羥基八氫并環戊二烯-2-基)甲基)硫基)丙基酯非對映異構體2 (460.1 mg, 0.8 mmol )及LiBr
(173.7 mg, 2.0 mmol)於NMP中之混合物。在完成反應之後,藉由製備型HPLC純化混合物以提供白色固體形式之5-胺基-3-(5-(((3-溴丙基)硫基)甲基)-5-羥基八氫并環戊二烯-2-基)-N-(3-氯-4-氟苯基)-1-甲基-1H-吡唑-4-甲醯胺非對映異構體2 (200 mg, 44.6 %)。MS計算值:558.09;MS實驗值:559.1 [M+1]+
, 561.2 [M+2+H]+
。
中間體114 5- 胺基 -3-(5-(((3- 溴丙基 ) 磺醯基 ) 甲基 )-5- 羥基八氫并環戊二烯 -2- 基 )-N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 1 。
將5-胺基-3-(5-(((3-溴丙基)硫基)甲基)-5-羥基八氫并環戊二烯-2-基)-N-(3-氯-4-氟苯基)-1-甲基-1H-吡唑-4-甲醯胺非對映異構體1 (117.6 mg, 0.21 mmol )及m
-CPBA
(108.7 mg, 0.63 mmol)於DCM中之混合物在室溫下攪拌2h。在完成反應之後,使用NaHCO3
將混合物驟冷並使用DCM萃取。在減壓下去除有機層,並藉由管柱層析純化殘餘物以提供白色固體形式之5-胺基-3-(5-(((3-溴丙基)磺醯基)甲基)-5-羥基八氫并環戊二烯-2-基)-N-(3-氯-4-氟苯基)-1-甲基-1H-吡唑-4-甲醯胺非對映異構體1 (60 mg, 48.3%)。MS計算值:590.08;MS實驗值:591.13 [M+1]+
。
中間體115 5- 胺基 -3-(5-(((3- 溴丙基 ) 磺醯基 ) 甲基 )-5- 羥基八氫并環戊二烯 -2- 基 )-N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 2 。
將5-胺基-3-(5-(((3-溴丙基)硫基)甲基)-5-羥基八氫并環戊二烯-2-基)-N-(3-氯-4-氟苯基)-1-甲基-1H-吡唑-4-甲醯胺非對映異構體1 (117.6 mg, 0.21 mmol )及m
-CPBA
(108.7 mg, 0.63 mmol)於DCM中之混合物在室溫下攪拌2h。在完成反應之後,使用NaHCO3
將混合物驟冷並使用DCM萃取。在減壓下去除有機層,並藉由管柱層析純化殘餘物以提供白色固體形式之5-胺基-3-(5-(((3-溴丙基)磺醯基)甲基)-5-羥基八氫并環戊二烯-2-基)-N-(3-氯-4-氟苯基)-1-甲基-1H-吡唑-4-甲醯胺非對映異構體1 (150 mg, 72.4%)。MS計算值:590.08;MS實驗值:591.1 [M+1]+
, 593.2 [M+2+H]+
。
AIA-295-1 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-(((3- 嗎啉基丙基 ) 磺醯基 ) 甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 1 (AIA-295-1) 。
在80℃下攪拌5-胺基-3-(5-(((3-溴丙基)磺醯基)甲基)-5-羥基八氫并環戊二烯-2-基)-N-(3-氯-4-氟苯基)-1-甲基-1H-吡唑-4-甲醯胺非對映異構體1 (50.0 mg, 0.08 mmol )、嗎啉(14.0mg , 0.16 mmol)及K2
CO3
(22.1mg, 0.16 mmol)於ACN中之混合物。在完成反應之後,使用H2
O將混合物驟冷並使用DCM萃取。在減壓下去除有機層,並藉由製備型HPLC純化殘餘物以提供白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-3-(5-羥基-5-(((3-嗎啉基丙基)磺醯基)甲基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺非對映異構體1 (AIA-295-1) (10.0 mg, 21.3%)。MS計算值:597.22;MS實驗值:598.22 [M+1]+
;1
H NMR (DMSO-d6
, 400 MHz) of AIA -295-1: δ 8.95 (S, 1H), 7.92-7.90 (m, 1H), 7.53-7.51 (m, 1H), 7.38-7.33 (t,J
=8.6 Hz, 1H), 5.98 (S, 2H), 4.89 (S, 1H), 3.60 (S, 4H), 3.60 (S, 3H), 3.42-3.38 (m, 1H), 3.28-3.10 (m, 4H), 2.64-2.57 (m, 2H), 2.42-2.33 (m, 6H), 2.14-2.11 (m, 2H), 2.03-1.96 (m, 2H), 1.87-1.83 (m, 2H), 1.73-1.58 (m, 4H)。
AIA-295-B 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-(((3- 嗎啉基丙基 ) 磺醯基 ) 甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 2 (AIA-295-B) 。
在80℃下攪拌5-胺基-3-(5-(((3-溴丙基)磺醯基)甲基)-5-羥基八氫并環戊二烯-2-基)-N-(3-氯-4-氟苯基)-1-甲基-1H-吡唑-4-甲醯胺非對映異構體12 (50.0 mg, 0.08 mmol )、嗎啉(14.0mg , 0.16 mmol)及K2
CO3
(22.1mg, 0.16 mmol)於ACN中之混合物。在完成反應之後,使用H2
O將混合物驟冷並使用DCM萃取。在減壓下去除有機層,並藉由製備型HPLC純化殘餘物以提供白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-3-(5-羥基-5-(((3-嗎啉基丙基)磺醯基)甲基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺非對映異構體1 (AIA-295-B) (33 mg, 55.2%)。MS計算值:597.22;MS實驗值:598.2 [M+1]+
;1
H NMR (DMSO-d6
, 400 MHz): δ 8.95 (s, 1H), 7.91 (dd,J
=2.4 Hz, 6.8 Hz, 1H), 7.54-7.50 (m, 1H), 7.35 (t,J
=9.2 Hz, 1H), 5.97(s, 2H), 4.78(s, 1H), 3.57-3.54 (m, 5H), 3.49 (s, 3H), 3.32 (brs, 2H), 3.16-3.12 (m, 2H), 2.63-2.61 (m, 2H), 2.36-2.33 (m, 6H), 2.18-2.11 (m, 2H), 2.06-2.01 (m, 2H), 1.85-1.81 (m, 2H), 1.47-1.36 (m, 4H)。表 10.
根據針對5-胺基-N-(3-氯-4-氟苯基)-3-(5-羥基-5-(((3-嗎啉基丙基)磺醯基)甲基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺非對映異構體1及2所闡述之程序來合成表10中之化合物。
AIA-351-A 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-(((3-(2- 側氧基六氫吡嗪 -1- 基 ) 丙基 ) 磺醯基 ) 甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。
將4-(3-(((5-(5-胺基-4-((3-氯-4-氟苯基)胺甲醯基)-1-甲基-1H-吡唑-3-基)-2-羥基八氫并環戊二烯-2-基)甲基)磺醯基)丙基)-3-側氧基六氫吡嗪-1-甲酸第三丁基酯非對映異構體1 (50.0 mg, 0.08 mmol )於HCl/CH3
OH (5 mL)中之溶液在室溫下攪拌1h,在完成反應之後,在減壓下去除溶劑,並藉由製備型HPLC純化所得殘餘物以提供白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-3-(5-羥基-5-(((3-(2-側氧基六氫吡嗪-1-基)丙基)磺醯基)甲基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺(10.0 mg, 47.6%)。MS計算值:610.21;MS實驗值:611.1 [M+1]+
;1
H NMR (DMSO-d6
, 400 MHz): δ 8.92 (s, 1H), 7.89 (dd, J=2.8 Hz, 7.2 Hz, 1H), 7.51-7.47 (m, 1H), 7.33 (t, J=5.2 Hz, 1H), 5.95 (s, 2H), 4.96-4.94 (m, 1H), 4.87 (s, 1H), 3.47 (s, 3H), 3.45-3.36 (m, 3H), 3.33-3.32 (m, 1H), 3.29-3.28 (m, 1H), 3.18-3.12 (m, 5H), 2.83-2.82 (m, 2H), 2.47 (brs, 2H), 2.14-2.09 (m, 2H), 2.02-1.93 (m, 2H), 1.70-1.59 (m, 4H), 1.16 (d, J=6.8 Hz, 3H)。
AIA-259-A、AIA-259-B 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-((2r,5r)-5- 羥基 -5-((2,2,2- 三氟乙基亞磺醯基 ) 甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺 , 非對映異構體 1 (AIA-259-A) , 非對映異構體 2 (AIA-259-B) 。
向5-胺基-N-(3-氯-4-氟苯基)-3-(5-羥基-5-(((2,2,2-三氟乙基)硫基)甲基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺非對映異構體1 (100 mg, 0.2 mmol)於無水DCM (10 mL)中之溶液中添加m
-CPBA (99 mg, 0.6 mmol),並將混合物在室溫下攪拌4小時。在減壓下去除溶劑,並藉由製備型HPLC純化殘餘物以提供AIA-259-1。藉由對掌性HPLC進一步純化此材料以得到AIA-259-A (9 mg)及AIA-259-B (12 mg)。AIA-259-A:1
H NMR (DMSO-d6, 400 MHz): δ 8.95 (s, 1H), 7.91 (dd,J
= 6.8, 2.4 Hz, 1H), 7.54-7.51 (m, 1H), 7.35 (t,J
= 9.2 Hz, 1H), 5.98 (s, 2H), 4.91 (s, 1H) 4.06-3.89 (m, 2H), 3.59-3.56 (m, 1H), 3.49 (s, 3H), 3.16 (dd,J
= 28.8, 13.6 Hz, 2H), 2.68-2.62 (m, 2H), 2.18-2.14 (m, 2H), 2.08-2.00 (m,1H), 1.92-1.89 (m, 1H) 1.49-1.37 (m, 4H)。AIA-259-B:1
H NMR (DMSO-d6, 400 MHz): δ 8.95 (s, 1H), 7.91 (dd,J
= 6.8, 2.4 Hz, 1H), 7.54-7.50 (m, 1H), 7.35 (t,J
= 9.2 Hz, 1H), 5.98 (s, 2H), 4.91 (s, 1H) 4.03-3.89 (m, 2H), 3.58-3.56 (m, 1H), 3.49 (s, 3H), 3.22-3.11 (m, 2H), 2.68-2.62 (m, 2H), 2.18-2.14 (m, 2H), 2.08-2.00 (m, 2H), 1.92-1.89 (m, 2H), 1.49-1.37 (m, 4H)。
AIA-259-C、AIA-259-D 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-((2r,5r)-5- 羥基 -5-((2,2,2- 三氟乙基亞磺醯基 ) 甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺 , 非對映異構體 3 (AIA-259-C) , 非對映異構體 4 (AIA-259-D) 。
向5-胺基-N-(3-氯-4-氟苯基)-3-(5-羥基-5-(((2,2,2-三氟乙基)硫基)甲基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺非對映異構體2 (200 mg, 0.4 mmol)於無水DCM (10 mL)中之溶液中添加m
-CPBA (331 mg, 1.9 mmol),且將混合物在室溫下攪拌4小時。在起始材料完全消耗之後,在減壓下去除溶劑,且藉由製備型HPLC純化殘餘物以提供AIA-259-2,藉由對掌性HPLC進一步純化以得到AIA-259-C (6 mg)及AIA-259-D (6 mg)。AIA-259-C:1
H NMR (DMSO-d6, 400 MHz): δ 8.96 (s, 1H), 7.92 (dd,J
= 7.2, 2.8 Hz, 1H), 7.54-7.50 (m, 1H), 7.35 (t,J
= 9.2 Hz, 1H), 5.98 (s, 2H), 4.99 (s, 1H) 4.05-3.90 (m, 2H), 3.49 (s, 3H), 3.45-3.39 (m, 1H), 3.10 (dd,J
= 16.8, 13.2 Hz, 2H), 2.33-2.32 (m, 2H), 2.14-2.12 (m, 2H), 2.07-2.02 (m, 1H), 1.89-1.82(m, 1H), 1.69-1.56 (m, 4H)。AIA-259-D:1
H NMR (DMSO-d6, 400 MHz): δ 8.96 (s, 1H), 7.91 (dd,J
= 6.8, 2.4 Hz, 1H), 7.54-7.50 (m, 1H), 7.35 (t,J
= 9.2 Hz, 1H), 5.98 (s, 2H), 4.99 (s, 1H) 4.02-3.90 (m, 2H), 3.49 (s, 3H), 3.44-3.37 (m, 1H), 3.10 (dd,J
= 16.8, 13.6 Hz, 2H), 2.44-2.33 (m, 2H), 2.14-2.12 (m, 2H), 2.07-2.02 (m, 1H), 1.88-1.82 (m, 1H), 1.69-1.56 (m, 4H)。
AIA-339-1、AIA-339-2 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-( 異丙氧基甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 1 (AIA-339-1) , 非對映異構體 2 (AIA-339-2) 。
將5-胺基-N-(3-氯-4-氟苯基)-3-(六氫-1'H-螺[環氧乙烷-2,2'-并環戊二烯]-5'-基)-1-甲基-1H-吡唑-4-甲醯胺(420 mg粗製物,1.0 mmol)及丙烷-2-醇鈉(410 mg, 5.0 mmol)於iPrOH (20 mL)中之混合物在回流下攪拌過夜。藉由製備型HPLC純化反應混合物以提供白色固體形式之AIA-339-1 (9 mg, 2%)及白色固體形式之化合物AIA-339-2 (10 mg, 2%)。AIA-339-1: MS計算值:464.20;MS實驗值:465.3 [M+H]+
。1
H-NMR (d6
-DMSO, 400 MHz): δ 8.92 (s, 1H), 7.90 (dd,J
= 6.8, 2.4 Hz, 1H), 7.52-7.48 (m, 1H), 7.33 (t,J
= 9.2 Hz, 1H), 5.95 (s, 2H), 4.07 (s, 1H), 3.52-3.45 (m, 5H), 3.20 (s, 2H), 2.63-2.60 (m, 2H), 2.13-2.09 (m, 2H), 1.67-1.61 (m, 2H), 1.39-1.34 (m, 4H), 1.05 (d,J
= 6.0 Hz, 6H)。AIA-339-2: MS計算值:464.20;MS實驗值:465.3 [M+
+H]+
。1
H-NMR (d6
-DMSO, 400 MHz): δ 8.90 (s, 1H), 7.89 (dd,J
= 6.8, 2.8 Hz, 1H), 7.51-7.46 (m, 1H), 7.32 (t,J
= 9.2 Hz, 1H), 5.95 (s, 2H), 4.13 (s, 1H), 3.51-3.47 (m, 4H), 3.38-3.35 (m, 1H), 3.15 (s, 2H), 2.40-2.39 (m, 2H), 2.13-2.06 (m, 2H), 1.80-1.86 (m, 2H), 1.72-1.66 (m, 2H), 1.34-1.30 (m, 2H), 1.05 (d,J
= 6.4 Hz, 6H)。表 11.
根據針對5-胺基-N-(3-氯-4-氟苯基)-3-(5-羥基-5-(異丙氧基甲基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺所闡述之程序來合成表11中之化合物
AIA-217-3 5- 胺基 -3-(5-( 胺基甲基 )-5- 羥基八氫并環戊二烯 -2- 基 )-N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。
向5-胺基-N-(3-氯-4-氟苯基)-3-(六氫-1'H-螺[環氧乙烷-2,2'-并環戊二烯]-5'-基)-1-甲基-1H-吡唑-4-甲醯胺(200 mg, 0.495 mmol)於THF (5 mL)中之溶液中添加NH4
OH (5 mL)。將混合物在室溫下攪拌過夜。去除溶劑並藉由矽膠管柱層析使用乙酸乙酯純化以提供白色固體形式之5-胺基-3-(5-(胺基甲基)-5-羥基八氫并環戊二烯-2-基)-N-(3-氯-4-氟苯基)-1-甲基-1H-吡唑-4-甲醯胺(80 mg, 38.4%)。MS計算值:421.1;MS實驗值:422.3 [M+1]+
AIA-218-1及AIA-218-2 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(2- 側氧基六氫 -1'H- 螺 [ 噁唑啶 -5,2'- 并環戊二烯 ]-5'- 基 )-1H- 吡唑 -4- 甲醯胺。非對映異構體 1 (CP-AIA-218-1) 。非對映異構體 2(CP-AIA-218-2) :
向5-胺基-3-(5-(胺基甲基)-5-羥基八氫并環戊二烯-2-基)-N-(3-氯-4-氟苯基)-1-甲基-1H-吡唑-4-甲醯胺(80 mg, 0.19 mmol)於DCM (6 mL)中之溶液中添加CDI (43 mg, 0.266 mmol)。將混合物在室溫下攪拌4h。去除溶劑並藉由矽膠管柱層析使用DCM/MeOH=3/1純化以提供白色固體形式之CP-AIA-218 (40 mg, 47.1%)。MS計算值:447.1;MS實驗值:448.2 [M+1]+
。藉由SFC分離CP-AIA-218以得到白色固體形式之CP-AIA-218-1(4 mg)及白色固體形式之CP-AIA-218-2(4 mg)。CP-AIA-218-1:1
H-NMR (DMSO, 400 MHz): δ 8.95 (s, 1H), 7.92 (dd,J
= 2.4, 2.4 Hz, 1H), 7.55-7.51 (m, 1H), 7.37-7.33 (m, 2H), 5.98 (s, 2H), 3.62-3.56 (m, 1H), 3.49 (s, 3H), 3.38 (s, 2H), 2.67-2.61 (m, 2H), 2.22-2.10 (m, 4H), 1.55 (dd,J
= 8.0, 7.2 Hz, 2H), 1.50-1.42 (m, 2H)。CP-AIA-218-2:1
H-NMR (DMSO, 400 MHz): δ 8.96 (s, 1H), 7.91 (dd,J
= 2.8, 2.4 Hz, 1H), 7.54-7.50 (m, 1H), 7.40-7.32 (m, 2H), 5.98 (s, 2H), 3.51 (s, 3H), 3.42-3.35 (m, 1H), 3.34 (s, 2H), 2.55 (s, 2H), 2.20-2.13 (m, 2H), 1.91 (dd,J
= 8.8, 8.0 Hz, 2H), 1.80-1.76 (m, 2H), 1.64-1.56 (m, 2H)。
AIA-255-3及AIA-255-4 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(2'- 乙基六氫 -1H- 螺 [ 并環戊二烯 -2,4'-[1,3] 二氧雜環戊烷 ]-5- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 1 (CP-AIA-255-3) , 非對映異構體 2 (CP-AIA-255-4) 。
向5-胺基-N-(3-氯-4-氟苯基)-3-(六氫-1'H-螺[環氧乙烷-2,2'-并環戊二烯]-5'-基)-1-甲基-1H-吡唑-4-甲醯胺(200 mg, 0.49 mmol)於THF (3 mL)中之溶液中添加環丙醇(287 mg, 4.90 mmol)。將混合物冷卻至0℃且添加H2
SO4
(濃,1滴)。將所得混合物在0℃下攪拌1 h,且升溫至室溫並保持1 h,隨後使用Na2
CO3
溶液驟冷並使用乙酸乙酯(15 mL × 3)萃取。乾燥有機層並濃縮,且藉由製備型TLC、然後製備型HPLC純化殘餘物以提供白色固體形式之CP-AIA-255-3 (5 mg, 2.2%)及CP-AIA-255-4 (3 mg, 0.7%)。CP-AIA-255-3: MS計算值:462.2。1
H-NMR (DMSO-d6
, 400 MHz): δ 8.94 (s, 1H), 7.91 (dd, J = 6.8, 2.4 Hz, 1H), 7.54-7.50 (m, 1H), 7.34 (t, J = 9.2 Hz, 1H), 5.97 (s, 2H), 4.79 (t, J = 4.8 Hz, 1H), 3.70 (dd, J = 34.8, 8.0 Hz, 2H), 3.57-3.51 (m, 1H), 3.48 (s, 3H), 2.62-2.58 (m, 2H), 2.19-2.13 (m, 2H), 2.05-2.00 (m, 1H), 1.93-1.88 (m, 1H), 1.56-1.49 (m, 3H), 1.45-1.38 (m, 3H), 0.84 (t, J = 7.2 Hz, 3H);MS實驗值:463.2 [M+1]+
。CP-AIA-255-4:1
H-NMR (DMSO-d6
, 400 MHz): δ 8.95 (s, 1H), 7.91 (dd, J = 6.8, 2.4 Hz, 1H), 7.53-7.49 (m, 1H), 7.34 (t, J = 9.2 Hz, 1H), 5.96 (s, 2H), 4.80 (t, J = 4.4 Hz, 1H), 3.65 (dd, J = 48.4, 8.0 Hz, 2H), 3.48 (s, 3H), 3.42-3.37 (m, 1H), 2.45-2.41 (m, 2H), 2.15-2.12 (m, 2H), 1.87-1.77 (m, 2H), 1.65-1.48 (m, 6H), 0.84 (t, J = 7.2 Hz, 3H) MS計算值:462.2;MS實驗值:463.2 [M+1]+
。
AIAI-253 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5-(( 二氟甲氧基 ) 甲基 )-5- 羥基八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。
向5-胺基-N-(3-氯-4-氟苯基)-3-(5-羥基-5-(羥甲基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺(480 mg, 1.14 mmol)於CHCl3
/H2
O (20 mL/4 mL)中之溶液中添加KHF2
(450 mg, 5.7 mmol)及(溴二氟甲基)三甲基矽烷(1.2 g, 5.7 mmol)。將混合物在室溫下攪拌過夜。去除溶劑,並藉由矽膠管柱層析使用1:1乙酸乙酯/石油醚純化產物以提供白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-3-(5-((二氟甲氧基)甲基)-5-羥基八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺(1.4 mg, 0.3%)。MS計算值:472.15;MS實驗值:473.3 [M+H]+
。1
H-NMR (DMSO, 400 MHz): δ 8.95 (s, 1H), 7.90-7.93(dd,J
= 6.8, 2.4 Hz, 1H), 7.54-7.50 (m, 1H), 7.35 (t,J
= 9.2 Hz, 1H), 6.66 (t,J
= 76 Hz, 1H), 5.98 (s, 2H), 4.54 (s, 1H), 3.69 (s, 2H), 3.59-3.51 (m, 1H), 3.49 (s, 3H), 2.70-2.64 (m, 2H), 2.18-2.12 (m, 2H), 1.79-1.74 (m, 2H), 1.41-1.34 (m, 4H)。
AIA-267-1、AIA-267-2 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-(2-( 甲基磺醯基 ) 乙基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 1
(AIA-267-1) , 非對映異構體 2 (AIA-267-2) :
在-78℃下,向二甲基碸(1.5 g, 15.8 mmol)於無水THF (20 mL)中之溶液中緩慢添加n-BuLi於THF中之溶液(6.3 mL, 15.8 mmol, 2.5 M),且將混合物在此溫度下攪拌1小時。緩慢添加5-胺基-N-(3-氯-4-氟苯基)-3-(六氫-1'H-螺[環氧乙烷-2,2'-并環戊二烯]-5'-基)-1-甲基-1H-吡唑-4-甲醯胺(800.0 mg, 2.0 mmol)於THF (15 mL)中之溶液且將反應液升溫至室溫並攪拌過夜。在使用NH4
Cl (水溶液,30 mL)驟冷之後,使用乙酸乙酯(3 × 25 mL)萃取懸浮液,藉由Na2
SO4
乾燥並在真空中濃縮以得到粗產物。藉由鹼性製備型HPLC純化粗產物以提供白色固體形式之AIA-267-1 (42.0 mg, 4.2%)及白色固體形式之AIA-267-2 (34.0 mg, 3.4%)。MS計算值:499.0;MS實驗值:500.2 [M
+ 1]+
。AIA-267-1:1
H NMR (DMSO-d6
, 400 MHz) δ 8.96 (s, 1H), 7.92-7.90 (m, 1H), 7.54-7.50 (m, 1H), 7.35 (t,J
= 9.2 Hz, 1H), 5.99 (s,
2H), 4.33 (s, 1H), 3.56 (s, 1H), 3.49 (s, 3H), 3.13-3.09 (m, 2H), 2.96 (s, 3H), 2.66-2.64 (m, 2H), 2.16-2.13 (m, 2H), 1.89-1.80 (m, 4H), 1.45-1.40 (m, 2H), 1.30-1.24 (m, 2H)。AIA-267-2:1
H NMR (DMSO-d6
, 400 MHz) δ 8.94 (s, 1H), 7.93-7.91 (m, 1H), 7.53-7.49 (m, 1H), 7.35 (t,J
= 9.2 Hz, 1H), 5.99 (s,
2H), 4.45 (s, 1H), 3.49 (s, 1H), 3.42-3.37 (m, 3H), 3.13-3.09 (m, 2H), 2.96 (s, 3H), 2.47-2.46 (m, 2H), 2.16-2.11 (m, 2H), 1.81-1.62 (m, 6H), 1.50-1.46 (m, 2H)。
| 化合物 | 結構及表徵 |
| AIA-349 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-(((3-( 六氫吡啶 -1- 基 ) 丙基 ) 磺醯基 ) 甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺,非對映異構體 1 。 (AIA-349) 。 MS計算值:595.24;MS實驗值:596.2 [M+1]+ ;1 H NMR (DMSO-d6 , 400 MHz): δ 8.91 (s, 1H), 7.89 (dd,J =2.8 Hz, 7.2Hz , 1H), 7.50-7.47 (m, 1H), 7.32 (t,J =9.2 Hz, 1H), 5.95 (s, 2H), 4.85 (s, 1H), 3.46 (s, 3H), 3.40-3.34(m, 2H), 3.20 (s, 1H), 3.20-3.08 (m, 2H), 2.40 (m, 1H), 2.29-2.26 (m, 6H), 2.13-2.08 (m, 2H), 2.00-1.95 (m, 2H), 1.83-1.76 (m, 2H), 1.73-1.55 (m, 4H), 1.47-1.42 (m, 4H), 1.35-1.34 (m, 2H)。 |
| AIA-349-B | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-(((3-( 六氫吡啶 -1- 基 ) 丙基 ) 磺醯基 ) 甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺,非對映異構體 2 。 (AIA-349-B) 。 MS計算值:595.24;MS實驗值:596.2 [M+1]+ ;1 H NMR (DMSO-d6 , 400 MHz): δ8.95 (s, 1H), 7.91 (dd,J =2.8 Hz, 6.8 Hz, 1H), 7.54-7.50 (m, 1H), 7.35 (s,J =9.2 Hz, 1H), 5.98 (s, 2H), 4.78 (s, 1H), 3.56-3.55 (m, 1H), 3.49 (s, 3H), 3.33 (brs, 2H), 3.14-3.10 (m, 2H), 2.62-2.60 (m, 2H), 2.32-2.28 (m, 6H), 2.16-2.13 (m, 2H), 2.06-2.01 (m, 2H), 1.83-1.79 (m, 2H), 1.50-1.36 (m, 10H)。 |
| AIA-350 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-(((3-(3- 側氧基六氫吡嗪 -1- 基 ) 丙基 ) 磺醯基 ) 甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 1 (AIA-350) 。 MS計算值:610.21;MS實驗值:611.2 [M+1]+ ;1 H NMR (CDCl3 , 400 MHz) δ 7.80 (dd,J= 2.4 Hz, 6.8 Hz, 1H), 7.43-7.39 (m , 1H), 7.19 (t,J =8.8 Hz, 1H), 4.72 (brs, 1H), 4.60 (s, 1H), 3.55 (s, 3H), 3.47-3.37(m, 2H), 3.25 (brs, 6H), 3.12 (s, 2H), 2.69-2.63 (m, 4H), 2.59-2.55 (m, 2H), 2.31-2.26 (m, 2H), 2.18-2.13(m, 2H), 2.05-1.97 (m, 2H), 1.84-1.74 (m, 4H)。 |
| AIA-350-b | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-(((3-(3- 側氧基六氫吡嗪 -1- 基 ) 丙基 ) 磺醯基 ) 甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 2 (AIA-350-b): MS計算值:610.21;MS實驗值:611.2 [M+1]+ ;1 H NMR (DMSO-d6 , 400 MHz) δ 8.96 (s, 1H), 7.90 (dd,J =2.4 Hz, 7.2 Hz, 1H), 7.73 (s, 1H), 7.54-7.50 (m, 1H), 7.35 (t,J =9.2 Hz, 1H), 5.97 (s, 2H), 4.81 (s, 1H), 3.57-3.53 (m, 1H), 3.48 (s, 3H), 3.34 (s, 2H), 3.16-3.12 (m, 4H), 2.89 (s, 2H), 2.63-2.62 (m, 2H), 2.54-2.51 (m, 2H), 2.44-2.41 (m, 2H), 2.18-2.12 (m, 2H), 2.07-2.01 (m, 2H), 1.86-1.82 (m, 2H), 1.46-1.39 (m, 4H)。 |
| AIA-351-1 | 4-(3-(((5-(5- 胺基 -4-((3- 氯 -4- 氟苯基 ) 胺甲醯基 )-1- 甲基 -1H- 吡唑 -3- 基 )-2- 羥基八氫并環戊二烯 -2- 基 ) 甲基 ) 磺醯基 ) 丙基 )-3- 側氧基六氫吡嗪 -1- 甲酸第三丁基酯。非對映異構體 1 (AIA-351-1) 。 MS計算值:710.27;MS實驗值:711.3 [M+1]+ 。 |
| AIA-269-1 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-(((2- 嗎啉基乙基 ) 磺醯基 ) 甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 1 。 (AIA-269-1): MS計算值:583.20;MS實驗值:584.20 [M+1]+ ;1 H NMR (DMSO-d6 , 400 MHz) δ 7.80 (dd,J = 6.4, 2.4, 1H), 7.43-7.39 (m, 1H ), 7.18 (t,J = 9.2, 1H),4.91 (s, 1H), 3.69-3.66 (m, 4H), 3.46 (s, 3H), 3.47-3.36 (m, 7H), 2.85-2.82 (m, 2H), 2.64-2.51 (m, 7H), 2.33-2.27 (m, 2H), 2.19-2.14 (m, 2H), 1.84-1.74 (m, 4H)。 |
| 化合物 | 結構及表徵 |
| AIA-254 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-((2s,5s)-5- 羥基 -5-((2,2,2- 三氟乙氧基 ) 甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺 MS計算值:504.1;MS實驗值:505.1[M+1]+ 。1 H-NMR (DMSO-d6 , 400 MHz): δ 8.93 (s, 1H), 7.91 (dd, J = 7.2, 2.8 Hz, 1H), 7.53-7.49 (m, 1H), 7.34 (t, J = 9.2 Hz, 1H), 5.97 (s, 2H), 4.46 (s, 1H), 4.08 (q, J = 9.2 Hz, 2H), 3.49 (s, 3H), 3.42 (s, 2H), 3.40-3.37 (m, 1H), 2.45-2.41 (m, 2H), 2.16-2.09 (m, 2H), 1.87-1.82 (m, 2H), 1.71-1.63 (m, 2H), 1.41-1.36 (m, 2H); |
| AIA-168-A | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-( 羥甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 1 (AIA-168-A) 。 1 H NMR (DMSO-d6, 400 MHz): δ 8.92 (brs, 1H), 7.89 (dd, 1H, J = 6.8 Hz, 2.8 Hz, 1H), 7.52-7.48 (m, 1H), 7.33 (t, J = 9.2 Hz, 1H), 5.95 (brs, 2H), 4.50 (t, J = 5.6 Hz, 1H), 4.00 (brs, 1H), 3.50-3.47 (m, 4H), 3.22 (d, J = 5.6 Hz, 2H), 2.65-2.61 (m, 2H), 2.14-2.08 (m, 2H), 1.62-1.57 (m, 2H), 1.40-1.31 (m, 4H)。AIA-168-A MS計算值:422.2;MS實驗值:423.3 [M + 1] +。 |
| AIA-168-B | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-( 羥甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 2 (AIA-168-B)。1 H NMR (DMSO-d6, 400 MHz): δ 8.90 (brs, 1H), 7.89 (dd, 1H, J = 6.8 Hz, 2.8 Hz, 1H), 7.51-7.47 (m, 1H), 7.92 (t, J = 9.2 Hz, 1H), 6.00 (brs, 2H), 4.44 (t, J = 5.6 Hz, 1H), 4.07 (brs, 1H), 3.47 (s, 3H), 3.39-3.34 (m, 1H), 3.17 (d, J = 5.6 Hz, 2H), 2.42-2.36 (m, 2H), 2.13-2.09 (m, 2H), 1.85-1.80 (m, 2H), 1.70-1.65 (m, 2H), 1.31-1.27 (m, 2H)。 |
| AIA-225-A | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-( 甲氧基甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 1 。 1 H-NMR (DMSO, 400 MHz): δ 8.94 (s, 1H), 7.91 (dd,J = 2.4, 2.8 Hz, 1H), 7.54-7.50 (m, 1H), 7.34 (t,J = 9.2 Hz, 1H), 5.97 (s, 2H), 4.22 (s, 1H), 3.56-3.52 (m, 1H), 3.48 (s, 3H), 3.28 (s, 3H), 3.20 (s, 2H), 2.67-2.60 (m, 2H), 2.15-2.12 (m, 2H), 1.71-1.66 (m, 2H), 1.41-1.34 (m, 4H)。 |
| AIA-225-B | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-( 甲氧基甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 2 。 1 H-NMR (DMSO, 400 MHz): δ 8.92 (s, 1H), 7.91 (dd,J = 2.8, 2.8 Hz, 1H), 7.53-7.49 (m, 1H), 7.34 (t,J = 9.2 Hz, 1H), 5.97 (s, 2H), 4.27 (s, 1H), 3.49 (s, 3H), 3.40-3.36 (m, 1H), 3.25 (s, 3H), 3.15(s, 2H), 2.45-2.41 (m, 2H), 2.14-2.08 (m, 2H), 1.85-1.79 (m, 2H), 1.73-1.65 (m, 2H), 1.37 (dd,J = 2.8, 3.2 Hz, 2H)。 |
| AIA-363-1 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-( 六氫吡啶 -1- 基甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 1 (AIA-363-1) 1 H NMR (DMSO-d6 , 400 MHz): δ 8.92 (s, 1H), 7.89 (dd,J = 7.2, 2.8 Hz, 1H), 7.52-7.48 (m, 1H), 7.33 (t,J = 9.2 Hz, 1H), 5.95 (s, 2H), 3.90 (s, 1H), 3.55-3.49 (m, 1H), 3.46 (s, 3H), 2.65-2.59 (m, 2H), 2.41-2.35 (m, 4H), 2.25 (s, 2H), 2.14-2.08 (m, 2H), 1.71-1.66 (m, 2H), 1.45-1.25 (m, 10H)。 |
| AIA-363-2 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-( 六氫吡啶 -1- 基甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 2 (AIA-363-2) 1 H NMR (DMSO-d6 , 400 MHz): δ 8.92 (s, 1H), 7.90 (dd,J = 7.2, 2.8 Hz, 1H), 7.52-7.48 (m, 1H), 7.34 (t,J = 9.2 Hz, 1H), 5.97 (s, 2H), 4.08 (s, 1H), 3.49 (s, 3H), 3.43-3.36 (m, 1H), 2.43-2.32 (m, 6H), 2.20 (s, 2H), 2.15-2.08 (m, 2H), 1.86-1.81 (m, 2H), 1.69-1.61 (m, 2H), 1.47-1.45 (m, 4H), 1.35-1.31 (m, 4H)。 |
| AIA-364-1 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-( 嗎啉基甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺非對映異構體 1 (AIA-364-1) 。 1 H NMR (DMSO-d6 , 400 MHz): δ 8.92 (s, 1H), 7.90 (dd,J = 6.8, 2.4 Hz, 1H), 7.52-7.48 (m, 1H), 7.33 (t,J = 9.2 Hz, 1H), 5.95 (s, 2H), 3.96 (s, 1H), 3.53-3.50 (m, 5H), 3.46 (s, 3H), 2.65-2.59 (m, 2H), 2.45-2.44 (m, 4H), 2.31-2.30 (m, 2H), 2.14-2.08 (m, 2H), 1.77-1.72 (m, 2H), 1.41-1.25 (m, 4H)。 |
| AIA-364-2 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-( 嗎啉基甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺非對映異構體 2 (AIA-364-2) 。 1 H NMR (DMSO-d6 , 400 MHz): δ 8.93 (s, 1H), 7.90 (dd,J = 6.8, 2.8 Hz, 1H), 7.52-7.48 (m, 1H), 7.34 (t,J = 9.2 Hz, 1H), 5.97 (s, 2H), 4.18 (s, 1H), 3.55-3.52 (m, 4H), 3.49 (s, 3H), 3.42-3.37 (m, 1H), 2.49-2.46 (m, 4H), 2.36-2.32 (m, 2H), 2.22 (s, 2H), 2.16-2.11 (m, 2H), 1.91-1.86 (m, 2H), 1.66-1.58 (m, 2H), 1.37-1.32 (m, 2H)。 |
中間體116 2-(5-(5- 胺基 -4-((3- 氯 -4- 氟苯基 ) 胺甲醯基 )-1- 甲基 -1H- 吡唑 -3- 基 )-2- 羥基八氫并環戊二烯 -2- 基 ) 乙酸乙酯
。在-78℃下,向EtOAc (338 mg, 3.9 mmol)於THF (15 mL)中之溶液中添加LDA (1.9 mL, 3.9 mmol)並將所得溶液攪拌10 min。添加AIA-002 (300 mg, 0.8 mmol)並將混合物在-78℃下攪拌4h。使用MeOH將混合物驟冷且在真空中濃縮有機層,且藉由矽膠管柱層析使用1:5乙酸乙酯/石油醚純化殘餘物以提供白色固體形式之2-(5-(5-胺基-4-((3-氯-4-氟苯基)胺甲醯基)-1-甲基-1H-吡唑-3-基)-2-羥基八氫并環戊二烯-2-基)乙酸乙酯(200 mg, 54%)。MS計算值:478.2;MS實驗值:479.2 [M+1]+
。
AIA-241 2-(5-(5- 胺基 -4-((3- 氯 -4- 氟苯基 ) 胺甲醯基 )-1- 甲基 -1H- 吡唑 -3- 基 )-2- 羥基八氫并環戊二烯 -2- 基 ) 乙酸
。向2-(5-(5-胺基-4-((3-氯-4-氟苯基)胺甲醯基)-1-甲基-1H-吡唑-3-基)-2-羥基八氫并環戊二烯-2-基)乙酸乙酯(200 mg, 0.5 mmol)於THF/H2
O (10/10 mL)中之溶液中添加LiOH-H2
O (21 mg, 0.5 mmol)且將混合物在40℃下攪拌過夜。使用乙酸乙酯萃取混合物且在真空中濃縮有機層以提供白色固體形式之2-(5-(5-胺基-4-((3-氯-4-氟苯基)胺甲醯基)-1-甲基-1H-吡唑-3-基)-2-羥基八氫并環戊二烯-2-基)乙酸(200 mg)。MS計算值:450.1;MS實驗值:451.2 [M+1]+
。1
H-NMR (DMSO, 400 MHz): δ 8.91 (s, 1H), 7.92 (dd,J
= 7.2, 2.8 Hz, 1H), 7.53-7.49 (m, 1H), 7.34 (t,J
= 9.2 Hz, 1H), 5.98 (s, 2H), 3.49 (s, 3H), 3.42-3.35 (m, 1H), 2.39 (s, 2H), 2.12-2.08 (m, 4H), 1.73-1.63 (m, 4H), 1.43-1.39 (m, 2H)。
AIA-215 5- 胺基 -3-(5-(2- 胺基 -2- 側氧基乙基 )-5- 羥基八氫并環戊二烯 -2- 基 )-N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺
。向2-(5-(5-胺基-4-((3-氯-4-氟苯基)胺甲醯基)-1-甲基-1H-吡唑-3-基)-2-羥基八氫并環戊二烯-2-基)乙酸(200 mg 0.4 mmol)於DMF(5 mL)中之溶液中添加HCOONH4
(60 mg, 0.8 mmol), HATU (370 mg, 0.8 mmol)及Et3
N (88 mg, 0.8 mmol)。將混合物在室溫下攪拌過夜。使用乙酸乙酯萃取混合物並使用飽和NaCl洗滌。在真空中濃縮有機層,且藉由製備型HPLC純化殘餘物以提供白色固體形式之AIA-215 (94 mg, 46%)。MS計算值:449.2;MS實驗值:450.2 [M+1]+
。1
H-NMR (DMSO-d6
, 400 MHz): δ 8.94 (s, 1H) , 7.90 (dd,J
= 2.8, 4.4Hz, 1H), 7.53-7.49 (m, 1H), 7.34 (t,J
= 8.8Hz, 2H), 7.00 (s, 1H), 5.96 (s, 2H), 4.98 (s, 1H), 3.49 (s, 3H), 3.46-3.36 (m, 1H), 2.43 (d,J
= 11.6Hz, 2H), 2.22 (s, 2H), 2.12 (t,J
= 5.6Hz, 2H), 1.79 (dd,J
= 7.6, 12.0Hz, 2H), 1.64 (t,J
= 8.8Hz, 2H), 1.45 (dd,J
= 4.0, 12.8Hz, 2H)。
中間體117 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 氰基 -5-( 三甲基矽基氧基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。
向AIA-002 (200 mg, 0.51 mmol)於三甲基矽基氰化物(3.0 mL)之溶液中添加ZnCl2
(0.05 mL, 0.1 mmol, 2 M)且將混合物在60℃下攪拌4小時。使用水稀釋反應混合物,使用乙酸乙酯(3 × 20 mL)萃取,藉由Na2
SO4
乾燥,過濾並在減壓下濃縮。藉由管柱層析純化殘餘物以提供黃色油狀物形式之5-胺基-N-(3-氯-4-氟苯基)-3-(5-氰基-5-(三甲基矽基氧基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺(180.0 mg, 72.2%)。MS計算值:489.2,MS實驗值:490.2 [M
+ 1]+
。
中間體118 5-(5- 胺基 -4-(3- 氯 -4- 氟苯基胺甲醯基 )-1- 甲基 -1H- 吡唑 -3- 基 )-2- 羥基八氫并環戊二烯 -2- 甲酸。
將5-胺基-N-(3-氯-4-氟苯基)-3-(5-氰基-5-(三甲基矽基氧基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺(180.0 mg, 0.37 mmol)及HCl (濃) (5 mL)之混合物在60℃下攪拌4小時。使用冰冷水稀釋反應混合物並使用飽和NaHCO3
中和。在減壓下去除水層,且藉由管柱層析及鹼性製備型HPLC純化殘餘物以提供白色固體形式之5-(5-胺基-4-(3-氯-4-氟苯基胺甲醯基)-1-甲基-1H-吡唑-3-基)-2-羥基八氫并環戊二烯-2-甲酸(90.0 mg, 55.8%)。MS計算值:436.1,MS實驗值:437.1 [M
+ 1]+
。
AIA-274-1、AIA-274-2 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5-( 環丙基胺甲醯基 )-5- 羥基八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。非對映異構體 1 (AIA-274-1) , 非對映異構體 2(AIA-274-2) 。
向5-(5-胺基-4-(3-氯-4-氟苯基胺甲醯基)-1-甲基-1H-吡唑-3-基)-2-羥基八氫并環戊二烯-2-甲酸(90.0 mg, 0.21 mmol)於DMF (3 mL)中之溶液中添加環丙胺(12.9 mg, 0.23 mmol)、HATU (119.7 mg, 0.32 mmol)及Et3
N (60.6 mg, 0.6 mmol)。將反應混合物在室溫下攪拌過夜。添加水並使用乙酸乙酯(15 mL × 3)萃取混合物,藉由Na2
SO4
乾燥,然後濃縮以得到粗產物。藉由製備型TLC純化粗產物,隨後藉由製備型HPLC純化以提供白色固體形式之AIA-274-1 (10.0 mg, 10.0%)及AIA-274-2 (4.0 mg, 4.0%)。MS計算值:475.2,MS實驗值:476.2 [M
+ 1]+
。AIA-274-1:1
H NMR (DMSO-d6
, 400 MHz): δ 8.91 (s, 1H), 7.92 (dd, J = 6.8, 2.4 Hz, 1H), 7.60 (d, J = 4.8, 1H), 7.53-7.49 (m, 1H), 7.35 (t, J = 8.8 Hz, 1H), 5.99 (s, 2H), 5.06 (s, 1H), 3.48 (s, 3H), 3.40-3.36 (m, 1H), 2.67-260 (m, 3H), 2.10-2.05 (m, 4H), 1.82-1.74 (m, 2H), 1.56-1.53 (m, 2H), 0.61-0.56 (m , 2H), 0.49-0.45 (m , 2H)。AIA-274-2:1
H NMR (DMSO-d6
, 400 MHz): δ 8.96 (s, 1H), 7.91 (dd, J = 6.8, 2.4 Hz, 1H), 7.65 (d, J = 4.8 Hz, 1H), 7.55-7.51 (m, 1H), 7.35 (t, J = 9.2 Hz, 1H), 5.98 (s, 2H), 5.12 (s, 1H), 3.61-3.57 (m, 1H), 3.50 (s, 3H), 2.69-2.65 (m, 3H), 2.18-2.12 (m, 2H), 1.82-1.70 (m, 4H), 1.50-1.42 (m, 2H), 0.61-0.46 (m , 4H)。
AIA-076 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5- 異丙基八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺
。在-10℃下經30 min,將異丙基氯化鎂(1.3 mL, 2.55 mmol)緩慢添加至AIA-002 (200 mg, 0.51 mmol)於無水THF (5 mL)中之溶液中。將反應混合物升溫至室溫且攪拌2 h。然後使用NH4
Cl (水溶液)將此混合物驟冷,並使用DCM (10 mL × 3)萃取溶液。藉由Na2
SO4
乾燥合併之有機層,濃縮並藉由製備型HPLC純化以提供淺白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-3-(5-羥基-5-異丙基八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺(6.6 mg, 3.1%產率)。MS計算值:434.1;MS實驗值:435.2 [M + 1]+
。表 12.
根據針對5-胺基-N-(3-氯-4-氟苯基)-3-(5-羥基-5-異丙基八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺所闡述之程序來合成表12中之化合物
| 化合物 | 結構及表徵 |
| AIA-077 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 環丙基 -5- 羥基八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 MS計算值:432.1;MS實驗值:433.2 [M + 1]+ 。 |
| AIA-011 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5- 甲基八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 MS計算值:406.8;MS實驗值:407.7 [M+1]+ 。 |
| AIA-265 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5-((N,N- 二甲基胺磺醯基 ) 甲基 )-5- 羥基八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 MS計算值:513.2;MS實驗值:514.2 [M + 1]+ ;1 H NMR (DMSO-d6 , 400 MHz): δ 7.71-7.68 (m, 1H), 7.34-7.27 (m, 2H), 7.11 (t,J = 8.8 Hz, 1H), 5.26 (s, 2H), 3.65 (s, 3H), 3.11 (s, 3H), 2.87 (s, 6H), 2.77-2.73 (m, 2H), 2.38-2.32 (m, 2H), 2.13-1.94 (m, 6H)。 |
| 中間體119 | (((5-(5- 胺基 -4-((3- 氯 -4- 氟苯基 ) 胺甲醯基 )-1- 甲基 -1H- 吡唑 -3- 基 )-2- 羥基八氫并環戊二烯 -2- 基 ) 甲基 ) 磺醯基 )( 環丙基 ) 胺基甲酸第三丁基酯。 MS計算值:625.2,MS實驗值:626.2 [M + 1]+ 。 |
| AIA-273 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5-((N- 環丙基胺磺醯基 ) 甲基 )-5- 羥基八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 MS計算值:525.2,MS實驗值:526.2 [M + 1]+ 。1 H NMR (DMSO-d6 , 400 MHz): δ 8.94 (s, 1H), 7.92 (dd,J = 6.8, 2.4 Hz, 1H), 7.54-7.50 (m, 1H), 7.35 (t,J = 9.2 Hz, 1H), 7.11 (s, 1H), 5.98 (s, 2H), 4.55 (s, 1H), 3.49 (s, 3H), 3.41-3.35 (m, 1H), 3.25 (s, 2H), 2.15-2.08 (m, 2H), 2.02-1.97 (m, 2H), 1.79-1.71 (m, 2H), 1.66-1.63 (m , 2H), 0.57-0.51 (m ,4H)。 |
| AIA-270 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5-(2-( 二甲基胺基 )-2- 側氧基乙基 )-5- 羥基八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 MS計算值:477.19;MS實驗值:478.3 [M + H]+ ;1 H NMR (DMSO-d6 , 400 MHz): δ 8.94 (s, 1H), 7.91 (dd,J = 6.8, 1.6 Hz, 1H), 7.52-7.50 (m, 1H), 7.35 (t,J = 9.2 Hz, 1H), 5.97 (s, 2H), 4.95 (s, 1H), 3.49 (s, 3H), 3.40-3.36 (m, 1H), 2.98 (s, 3H), 2.82 (s, 3H), 2.51-2.47 (m, 4H), 2.14-2.11 (m, 2H), 1.82-1.79 (m, 2H), 1.70-1.65 (m, 2H), 1.52-1.49 (m, 2H)。 |
| AIA-271 | 2-(5-(5- 胺基 -4-((3- 氯 -4- 氟苯基 ) 胺甲醯基 )-1- 甲基 -1H- 吡唑 -3- 基 )-2- 羥基八氫并環戊二烯 -2- 基 ) 乙酸甲酯。 MS計算值:464.2;MS實驗值:465.2 [M + 1]+ ;1 H NMR (DMSO-d6 , 400 MHz): δ 8.93 (s, 1H), 7.91 (dd,J = 4.0, 2.8 Hz, 1H), 7.53-7.50 (m, 1H), 7.35 (t,J = 9.2 Hz, 1H), 5.97 (s, 2H), 4.49 (s, 1H), 3.56 (s, 3H), 3.48 (s, 3H), 3.40-3.37 (m, 1H), 2.44 (brs, 4H), 2.11-2.08 (m, 2H), 1.88-1.85 (m, 2H), 1.72-1.64 (m, 2H), 1.55-1.51 (m, 2H)。 |
中間體120及中間體121 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5-( 丙烷 -2- 亞基 ) 八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺及 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 異丙基 -1,2,3,3a,4,6a- 六氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。
在室溫下,向5-胺基-N-(3-氯-4-氟苯基)-3-(5-羥基-5-異丙基八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺(600 mg, 1.38 mmol)於甲苯(40 mL)中之溶液中添加對甲基苯磺酸(48 mg, 0.28 mmol),且將混合物在回流下攪拌過夜。將所得混合物傾倒至水中並使用乙酸乙酯(40 mL × 3)萃取。乾燥有機層並濃縮,且藉由矽膠管柱層析純化殘餘物以提供5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(丙烷-2-亞基)八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺及5-胺基-N-(3-氯-4-氟苯基)-3-(5-異丙基-1,2,3,3a,4,6a-六氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺之混合物(180 mg)。藉由製備型對掌性HPLC分離混合物以得到化合物5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(丙烷-2-亞基)八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺。MS計算值:416.2;MS實驗值:417.2 [M+1]+
。5-胺基-N-(3-氯-4-氟苯基)-3-(5-異丙基-1,2,3,3a,4,6a-六氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺。MS計算值:416.2;MS實驗值:417.2 [M+1]+
。
AIA-257 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-(2- 羥基丙烷 -2- 基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。
將5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(丙烷-2-亞基)八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺(35 mg, 0.08 mmol)、OsO4
(10 mg, 0.04 mmol)、NMO (45 mg, 0.40 mmol)於THF/H2
O (5 mL/1 mL)中之混合物在室溫下攪拌4 h。在真空下濃縮反應混合物並藉由製備型HPLC純化殘餘物以提供白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-3-(5-羥基-5-(2-羥基丙烷-2-基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺(4 mg, 11%)。TLC: 10% MeOH / DCM (Rf: 0.3);MS計算值:450.2;MS實驗值:451.3 [M + 1]+
。1
H-NMR (DMSO-d6
, 400 MHz): δ 8.91 (s, 1H), 7.89 (dd, J = 6.8, 2.0 Hz, 1H), 7.52-7.48 (m, 1H), 7.32 (t, J = 3.2 Hz, 1H), 5.96 (s, 2H), 4.03 (s, 1H), 3.86 (s, 1H), 3.54-3.39 (m, 4H), 2.57 (t, J = 5.6 Hz, 2H), 2.09 (t, J = 5.6 Hz, 2H), 1.57 (s, 4H), 1.37 (dd, J = 11.6, 19.2 Hz, 2H), 1.03 (s, 6H)。
AIA-257-1 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(4,5- 二羥基 -5- 異丙基八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。
將5-胺基-N-(3-氯-4-氟苯基)-3-(5-異丙基-1,2,3,3a,4,6a-六氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺(20 mg, 0.05 mmol)、OsO4
(7 mg, 0.03 mmol)、NMO (23 mg, 0.20 mmol)於THF/H2
O (5 mL/1 mL)中之混合物在室溫下攪拌4 h。在真空下濃縮反應混合物且藉由製備型HPLC純化殘餘物以提供白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-3-(4,5-二羥基-5-異丙基八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺(2 mg, 9%)。MS計算值:450.2;MS實驗值:451.3 [M + 1]+
。1
H NMR (DMSO-d6
, 400 MHz): δ 8.94 (s, 1H), 7.91 (dd, J = 6.8, 2.4 Hz, 1H), 7.54-7.50 (m, 1H), 7.35 (t, J = 9.2 Hz, 1H), 5.97 (s, 2H), 4.47 (s, 1H) 3.58-3.45 (m, 6H), 2.86 (s, 2H), 2.67-2.62 (m, 2H), 2.18-2.11 (m, 2H), 1.89-1.84 (m, 2H), 1.44-1.32 (m, 4H)。
AIA-275 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(3- 側氧基八氫環戊 [c] 吡喃 -6- 基 )-1H- 吡唑 -4- 甲醯胺。
向m-CPBA (528.1 mg, 3.06 mmol)於無水DCM (15 mL)中之溶液中添加TFA (247.4 mg, 2.55 mmol),且將混合物在室溫下攪拌0.5小時。添加CP-AIA-002 (199.3 mg, 0.51 mmol),且將混合物在室溫下攪拌過夜。使用NaHCO3
(水溶液)將混合物驟冷,使用乙酸乙酯萃取。使用鹽水洗滌有機相,藉由Na2
SO4
乾燥,過濾並濃縮以得到粗產物,藉由管柱層析純化以提供白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(3-側氧基八氫環戊[c]吡喃-6-基)-1H-吡唑-4-甲醯胺(30 mg, 14.5 %)。MS計算值:406.1;MS實驗值:407.2 [M + 1]+
。1
H NMR (DMSO-d6
, 400 MHz): δ 9.02 (s, 1H), 7.91 (dd,J
= 4.4, 2.4 Hz, 1H), 7.54-7.51 (m, 1H), 7.35 (t,J
= 9.2 Hz, 1H), 5.99 (s, 2H), 4.29-4.25 (m, 1H), 4.08-4.03 (m, 1H), 3.50 (s, 3H), 3.46-3.41 (m, 1H), 2.67-2.58 (m, 2H), 2.50-2.48 (m, 1H), 2.33 (dd,J
= 9.6, 4.8 Hz, 1H), 2.22-2.08 (m, 2H), 1.51 (dd,J
= 4.4, 2.4 Hz, 1H), 1.34-1.26 (m, 1H)。
中間體122 3-(5-(1,3- 二噻烷 -2- 亞基 ) 八氫并環戊二烯 -2- 基 )-5- 胺基 -N- (3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。
在-78℃下,向(1,3-二噻烷-2-基)三甲基矽烷(2.1 g, 10.8 mmol)於THF (30 mL)中之混合物溶液中添加n-BuLi (2.5 M, 4.3 mL)。在將混合物在-78℃下攪拌1 hr之後,緩慢添加AIA-002 (600 mg, 1.5 mmol)於THF中之溶液並繼續攪拌3 hr。使用飽和NH4
Cl將混合物驟冷,蒸發溶劑,並藉由矽膠管柱(使用1:1石油醚/乙酸乙酯洗脫)純化殘餘物以提供白色固體形式之3-(5-(1,3-二噻烷-2-亞基)八氫并環戊二烯-2-基)-5-胺基-N- (3-氯-4-氟苯基)-1-甲基-1H-吡唑-4-甲醯胺(300 mg, 40%)。MS計算值:492.1;MS實驗值:493.1 [M+1]+
。
中間體123 5-(5- 胺基 -4-(3- 氯 -4- 氟苯基胺甲醯基 )-1- 甲基 -1H- 吡唑 -3- 基 ) 八氫并環戊二烯 -2- 甲酸甲酯。
向3-(5-(1,3-二噻烷-2-亞基)八氫并環戊二烯-2-基)-5-胺基-N- (3-氯-4-氟苯基)-1-甲基-1H-吡唑-4-甲醯胺(200 mg, 0.4 mmol)於MeOH (20 mL)中之溶液中連續添加HCl (6 N, 0.2 mL)、HgCl2
(232 mg, 0.9 mmol)及TFA (118 mg, 1.0 mmol)。將混合物在室溫下攪拌3小時,然後經由Celite®過濾。使用甲醇洗滌濾餅。使用NaBH4
在0℃下處理濾液,去除溶劑,並藉由矽膠管柱層析(使用2:1石油醚/乙酸乙酯洗脫)純化殘餘物以提供白色固體形式之5-(5-胺基-4-(3-氯-4-氟苯基胺甲醯基)-1-甲基-1H- 吡唑-3-基)八氫并環戊二烯-2-甲酸甲酯(120 mg, 68%)。MS計算值:434.2;MS實驗值:435.1 [M+1]+
。
AIA-014 5-(5- 胺基 -4-(3- 氯 -4- 氟苯基胺甲醯基 )-1- 甲基 -1H- 吡唑 -3- 基 ) 八氫并環戊二烯 -2- 甲酸。
將5-(5-胺基-4-(3-氯-4-氟苯基胺甲醯基)-1-甲基-1H- 吡唑-3-基)八氫并環戊二烯-2-甲酸甲酯(120 mg, 0.28 mmol)溶於甲醇(20 mL)及水(2 mL)之溶液中,然後一次性添加LiOH-H2
O (232 mg, 5.5 mmol)。將混合物溶液在室溫下攪拌3 hr。使溶液升溫至40℃並攪拌過夜。添加1N HCl以將pH調節至7。蒸發溶劑,並藉由矽膠管柱層析(10:1 DCM/MeOH)純化殘餘物以提供白色固體形式之5-(5-胺基-4-(3-氯-4-氟苯基胺甲醯基)-1-甲基-1H- 吡唑-3-基)八氫并環戊二烯-2-甲酸(100 mg, 86%)。MS計算值:420.1;MS實驗值:421.2 [M+1]+
;1H NMR (DMSO-d6, 400 MHz): δ 11.98 (s, 1H), 8.96 (s, 1H), 7.92-7.89 (m, 1H), 7.54-7.50 (m, 1H), 7.34 (t, J = 9.2, 1H), 5.97 (s, 2H), 3.49 (s, 3H), 3.31-3.27 (m, 1H), 2.69-2.64 (m, 1H), 2.55-2.53 (m, 2H), 2.17-2.02 (m, 2H), 1.73-1.59 (m, 3H), 1.51-1.43 (m, 1H), 1.30-1.25 (m, 2H)。
AIA-015 5- 胺基 -3-(5- 胺甲醯基八氫并環戊二烯 -2- 基 )-N-(3- 氯 -4- 氟苯基 )- 1- 甲基 -1H- 吡唑 -4- 甲醯胺。
合併5-(5-胺基-4-(3-氯-4-氟苯基胺甲醯基)-1-甲基-1H- 吡唑-3-基)八氫并環戊二烯-2-甲酸(30 mg, 0.07 mmol)、HATU (33 mg, 0.09 mmol)、DIEA (14 mg, 0.11 mmol)及HCOONH4
(6 mg, 0.08 mmol)並溶於DMF (1 mL)中。將所得溶液在室溫下攪拌過夜。採用製備型HPLC (鹼性)純化最終目標,且獲得白色固體形式之5-胺基-3-(5-胺甲醯基八氫并環戊二烯-2-基)-N-(3-氯-4-氟苯基)- 1-甲基-1H-吡唑-4-甲醯胺(19 mg, 64%)。MS計算值:419.2;MS實驗值:420.3 [M+1]+
;1H NMR (DMSO-d6, 400 MHz): δ 8.96 (s, 0.3H), 8.95 (s, 0.7H), 7.93-7.89 (m, 1H), 7.54-7.50 (m, 1H), 7.35 (t, J = 9.2 Hz, 1H), 7.28 (s, 0.7 H), 7.16 (s, 0.3 H), 6.68 (s, 1H), 5.98 (s, 1.4 H), 5.96 (s, 0.6 H), 3.53-3.49 (m, 4H), 3.30-3.26 (m, 1H), 2.65-2.60 (m, 1H), 2.46-2.43 (m, 1H), 2.18-2.12 (m, 2H), 1.97-1.94 (m, 2H), 1.68-1.39 (m, 4H), 1.30-1.27 (m, 1H)。表 13.
根據針對5-胺基-3-(5-胺甲醯基八氫并環戊二烯-2-基)-N-(3-氯-4-氟苯基)- 1-甲基-1H-吡唑-4-甲醯胺所闡述之程序來合成表13中之化合物。
AIA-017 2-(5-(5- 胺基 -4-((3- 氯 -4- 氟苯基 ) 胺甲醯基 )-1- 甲基 -1H- 吡唑 -3- 基 ) 六氫并環戊二烯 -2(1H)- 亞基 ) 乙酸乙酯。
在0℃下,向2-(二乙氧基磷醯基)乙酸乙酯(33 mg, 0.2 mmol, 2.0當量)於THF (5 mL)中之溶液中添加NaH (12 mg, 0.3 mmol, 3當量)。將所得溶液在0℃下攪拌30 mins,然後添加AIA-002 (39 mg, 0.1 mmol, 1當量)。將溶液在55℃下攪拌1 h,然後使用水驟冷並使用乙酸乙酯萃取。在真空下濃縮有機相並藉由製備型HPLC純化以得到白色固體形式之2-(5-(5-胺基-4-((3-氯-4-氟苯基)胺甲醯基)-1-甲基-1H-吡唑-3-基)六氫并環戊二烯-2(1H)-亞基)乙酸乙酯(22 mg, 48%)。TLC: 30%乙酸乙酯/石油醚(Rf
: 0.35);MS計算值:460.2;MS實驗值:461.3 [M+1]+
。1
H-NMR (DMSO-d6
, 400 MHz): δ 8.95 (s, 1H), 7.91 (dd,J
= 7.2, 2.8 Hz, 1H), 7.53-7.50 m, 1H), 7.34 (t,J
= 8.8 Hz, 1H), 5.96 (s, 2H), 5.74 (s, 1H), 4.05 (q,J
= 7.2 Hz , 2H), 3.49-3.47 (m, 1H), 3.47 (s, 3H), 2.75-2.73 (m, 2H), 2.66-2.61 (m, 2H), 2.49-2.13 (m, 4H), 1.38-1.33 (m, 2H), 1.18 (t,J
= 7.2 Hz, 3H)。
AIA-018 2-(5-(5- 胺基 -4-((3- 氯 -4- 氟苯基 ) 胺甲醯基 )-1- 甲基 -1H- 吡唑 -3- 基 ) 八氫并環戊二烯 -2- 基 ) 乙酸乙酯。
將2-(5-(5-胺基-4-((3-氯-4-氟苯基)胺甲醯基)-1-甲基-1H-吡唑-3-基)六氫并環戊二烯-2(1H)-亞基)乙酸酯(30 mg, 0.06 mmol)溶於THF中,添加Pt/C (10 mg),且將懸浮液在35℃及H2
氣氛下攪拌3 h。經由Celite®過濾混合物並使用THF洗滌。在真空下濃縮濾液並藉由製備型HPLC純化殘餘物以提供白色固體形式之2-(5-(5-胺基-4-((3-氯-4-氟苯基)胺甲醯基)-1-甲基-1H-吡唑-3-基)八氫并環戊二烯-2-基)乙酸乙酯(15 mg, 50%)。MS計算值:462.2;MS實驗值:463.2 [M+1]+
。1
H-NMR (DMSO-d6
, 400 MHz): δ 8.95 (s, 1H), 7.91 (dd,J
= 6.8, 2.4 Hz, 1H), 7.53-7.49 (m, 1H), 7.34 (t,J
= 9.2 Hz, 1H), 5.96 (s, 2H), 4.02 (q,J
= 7.2 Hz , 2H), 3.56-3.52 (m, 1H), 3.49 (s, 3H), 2.44-2.42 (m, 2H), 2.31-2.29 (m, 2H), 2.21-2.10 (m, 3H), 2.00-1.94 (m, 2H), 1.44-1.36 (m, 2H), 1.16 (t,J
= 7.2 Hz, 3H), 0.96-0.88 (m, 2H)。
AIA-019 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5-(2- 羥乙基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺
。向2-(5-(5-胺基-4-((3-氯-4-氟苯基)胺甲醯基)-1-甲基-1H-吡唑-3-基)八氫并環戊二烯-2-基)乙酸乙酯(46 mg, 0.1 mmol, 1當量)於THF (2 mL)中之溶液中逐份添加LiAlH4
(8 mg, 0.2 mmol, 2.0當量)。混合物變成黃色溶液。使用水及NaOH (水溶液)將混合物驟冷,然後過濾並使用THF洗滌。在真空下濃縮濾液並藉由製備型HPLC純化殘餘物以提供白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-3-(5-(2-羥乙基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺(20 mg, 48%)。MS計算值:420.2;MS實驗值:421.3 [M+1]+
。1
H-NMR (DMSO-d6
, 400 MHz): δ 8.95 (s, 1H), 7.91 (dd, J = 6.8, 2.4 Hz, 1H), 7.53-7.49 (m, 1H), 7.34 (t, J = 9.2 Hz, 1H), 5.96 (s, 2H), 4.29 (t, J = 5.2 Hz, 1H), 3.56-3.51 (m, 1H), 3.49 (s, 3H), 3.38-3.35 (m, 2H), 2.40 (s, 2H), 2.16-2.09 (m, 2H), 1.97-1.94 (m, 3H), 1.48-1.35 (m, 4H), 0.86-0.84 (m, 2H)。
| 化合物 | 結構及表徵 |
| AIA-016 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5-( 甲基胺甲醯基 ) 八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺 。MS計算值:433.2;MS實驗值:434.3 [M+1]+ ;1H NMR (DMSO-d6, 400 MHz): δ 8.96 (s, 0.3H), 8.94 (s,0.7 H), 7.92-7.89 (m, 1H), 7.76-7.75 (m,0.7 H), 7.64-7.63 (m, 0.3H), 7.53-7.49 (m, 1H), 7.35 (t,J = 9.2 Hz, 1H), 5.98 (s, 1.4H), 5.96 (s, 0.6H), 3.53-3.49 (m, 6H), 3.29-3.24 (m, 1H), 2.64-2.59 (m, 1H), 2.55-2.54 (m, 3H), 2.16-2.12 (m, 2H), 1.94-1.91 (m, 1H), 1.69-1.61 (m, 1H), 1.51-1.31 (m, 2H), 1.29-1.23 (m, 1H)。 |
| AIA-109 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5-( 環丙基胺甲醯基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺 MS計算值:459.2;MS實驗值:460.3 [M+1]+ ;1H NMR (DMSO-d6, 400 MHz): δ 8.95 (s, 1H), 7.92-7.76 (m, 2H), 7.53-7.49 (m,1 H), 7.35 (t,J = 9.2 Hz,1H), 5.99 (s, 2H), 3.50 (s,3 H), 3.48-3.27 (m, 1H), 2.63-2.57 (m, 3H), 2.46-2.43 (m, 1H), 2.17-2.10 (m, 2H), 2.10-1.88 (m, 1H), 1.68-1.39 (m, 4H), 1.28-1.20 (m, 1H), 0.59-0.54 (m, 2H), 0.36-0.32 (m, 2H)。 |
中間體124 2-(5-(5- 胺基 -4-(3- 氯 -4- 氟苯基胺甲醯基 )-1- 甲基 -1H- 吡唑 -3- 基 ) 八氫并環戊二烯 -2- 基 ) 乙酸。
向2-(5-(5-胺基-4-((3-氯-4-氟苯基)胺甲醯基)-1-甲基-1H-吡唑-3-基)八氫并環戊二烯-2-基)乙酸乙酯(462 mg, 1.0 mmol)於MeOH / H2
O (5 mL / 1 mL)中之溶液中添加LiOH-H2
O (84 mg, 2.0 mmol)。將混合物在50℃下攪拌4 h。在真空下去除MeOH並使用3M HCl將殘餘物中和至pH約為5。凍乾所得溶液以得到白色固體形式之粗製2-(5-(5-胺基-4-(3-氯-4-氟苯基胺甲醯基)-1-甲基-1H- 吡唑-3-基)八氫并環戊二烯-2-基)乙酸(510 mg, 100%)。MS計算值:434.2;MS實驗值:435.3 [M+1]+
。表 14.
根據針對5-胺基-3-(5-胺甲醯基八氫并環戊二烯-2-基)-N-(3-氯-4-氟苯基)- 1-甲基-1H-吡唑-4-甲醯胺所闡述之程序來合成表14中之化合物。
| 化合物 | 結構及表徵 |
| AIA-020 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5-(2-( 二甲基胺基 )-2- 側氧基乙基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺 MS計算值: 461.2;MS實驗值:462.3 [M+1]+ 。1 H-NMR (DMSO-d6 , 400 MHz): δ 8.95 (s, 1H), 7.91 (d,J = 4.4 Hz, 1H), 7.50 (s, 1H), 7.34 (t,J = 9.2 Hz, 1H), 5.96 (s, 2H), 3.54-3.53 (m, 1H), 3.49 (s, 3H), 2.93 (s, 3H), 2.78 (s, 3H), 2.41 (s, 2H), 2.32-2.31 (m, 2H), 2.22-2.13 (m, 3H), 1.99 (s, 2H), 1.41-1.40 (m, 2H), 0.91-0.89 (m, 2H) |
| AIA-021 | 5- 胺基 -3-(5-(2- 胺基 -2- 側氧基乙基 ) 八氫并環戊二烯 -2- 基 )-N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 MS計算值:433.2;MS實驗值:434.3 [M+1]+ 。1 H-NMR (DMSO-d6 , 400 MHz): δ 8.94 (s, 1H), 7.91 (dd,J = 6.8, 2.4 Hz, 1H), 7.53-7.49 (m, 1H), 7.34 (t,J = 8.8 Hz, 1H), 7.17 (s, 1H), 6.62 (s, 1H), 5.96 (s, 2H), 3.56-3.51 (m, 1H), 3.49 (s, 3H), 2.41-2.39 (m, 2H), 2.15-2.13 (m, 3H), 2.06-2.04 (m, 2H), 1.96-1.93 (m, 2H), 1.41-1.38 (m, 2H), 0.90-0.88 (m, 2H)。 |
中間體125 2-(5-(5- 胺基 -4-((3- 氯 -4- 氟苯基 ) 胺甲醯基 )-1- 甲基 -1H- 吡唑 -3- 基 )-2-( 硝基甲基 ) 八氫并環戊二烯 -2- 基 ) 乙酸乙酯。
在0℃下,向2-(5-(5-胺基-4-((3-氯-4-氟苯基)胺甲醯基)-1-甲基-1H
-吡唑-3-基)六氫并環戊二烯-2(1H
)-亞基)乙酸酯(0.8 g, 1.73 mmol)於DMSO (3 mL)中之經攪拌溶液中添加K2
CO3
(0.703 g, 5.09 mmol)。向此溶液中緩慢添加MeNO2
(0.265 g, 4.34 mmol)。將所得反應混合物在70℃下攪拌16 h。在完成之後,使用冰冷水稀釋反應混合物並使用乙酸乙酯萃取。藉由無水硫酸鈉乾燥合併之有機層,過濾並在減壓下濃縮以提供灰白色固體形式之2-(5-(5-胺基-4-((3-氯-4-氟苯基)胺甲醯基)-1-甲基-1H-吡唑-3-基)-2-(硝基甲基)八氫并環戊二烯-2-基)乙酸乙酯(0.7 g,粗製物)。C24
H29
ClFN5
O5
之LCMS計算值:521.18;觀察值:522.20 [M+1]+
。
HBV-AIA-039 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5'- 側氧基六氫 -1H- 螺 [ 并環戊二烯 -2,3'- 吡咯啶 ]-5- 基 )-1H- 吡唑 -4- 甲醯胺
。向2-(5-(5-胺基-4-((3-氯-4-氟苯基)胺甲醯基)-1-甲基-1H-吡唑-3-基)-2-(硝基甲基)八氫并環戊二烯-2-基)乙酸酯(0.5 g, 0.95 mmol)於AcOH (5 mL)中之經攪拌溶液中添加鐵粉(0.321g, 4.87 mmol)並將所得反應混合物在80℃下攪拌16 h。在完成之後,在真空中濃縮反應混合物。使用NaHCO3
水溶液中和殘餘物並使用乙酸乙酯萃取。使用水、鹽水洗滌合併之有機層,藉由硫酸鈉乾燥,過濾並在真空中濃縮以提供粗製化合物,藉由製備型HPLC純化以提供5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5'-側氧基六氫-1H-螺[并環戊二烯-2,3'-吡咯啶]-5-基)-1H-吡唑-4-甲醯胺。H NMR (400 MHz, DMSO-d 6
): δ 8.96 (s, 1H), 7.89 (d,J
= 6.4 Hz, 1H), 7.51-7.49 (m, 1H), 7.45 (s, 1H), 7.34 (t,J
= 8.8 Hz, 1H), 5.96 (s, 2H), 3.57-3.49 (m, 4H), 3.00 (s, 2H), 2.53-2.45 (m, 2H,合併), 2.17-2.11 (m, 4H), 1.88-1.86 (m, 2H), 1.46-1.32 (m, 4H)。
中間體126 5- 胺基 -3- 溴 -1H- 吡唑 -4- 甲酸乙酯。
向5-胺基-1H-吡唑-4-甲酸乙酯(20 g, 0.13 mol)於CHCl3
(200 mL)中之溶液中緩慢添加NBS (34.5 g, 0.19 mol)以維持溫度介於20℃至30℃之間。將溶液在室溫下攪拌3 h。使用水(200 ml)終止反應,使用DCM (100 mL × 3)萃取,乾燥,過濾並在減壓下濃縮。藉由管柱層析使用20 - 30%乙酸乙酯/石油醚純化粗產物以提供黃色固體形式之5-胺基-3-溴-1H-吡唑-4-甲酸乙酯(12.6 g, 42%)。MS計算值:233.0;MS實驗值:234.1 [M+H]+
。
中間體127 5- 胺基 -3- 溴 -N-(3- 氯 -4- 氟苯基 )-1H- 吡唑 -4- 甲醯胺。
在0℃下,向3-氯-4-氟-苯胺(9.3 g, 64 mmol)於甲苯(100 mL)中之溶液中添加三甲基鋁(2 M於甲苯中,129 mL, 258 mmol)。將淺褐色溶液攪拌30 min。在0℃下,向溶液中添加5-胺基-3-溴-1H-吡唑-4-甲酸乙酯(10 g, 43 mmol)並繼續攪拌30 min。將褐色溶液加熱至回流並保持48 h。將混合物冷卻至0℃,使用H2
O (200 mL)、5% NaOH (100 mL)驟冷並將所得混合物攪拌10 min。在真空下去除溶劑並藉由管柱層析使用20 - 30%乙酸乙酯/石油醚純化殘餘物以提供白色固體形式之5-胺基-3-溴-N-(3-氯-4-氟苯基)-1H-吡唑-4-甲醯胺(5 g, 36%)。MS計算值:331.9;MS實驗值:333.1[M
+ 1]+
中間體128 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 側氧基 -1,3a,4,5,6,6a- 六氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺
。將5-(4,4,5,5-四甲基-1,3,2-二氧硼㖦-2-基)-3,3a,6,6a-四氫并環戊二烯-2(1H)-酮(5 g, 20 mmol)、5-胺基-3-溴-N-(3-氯-4-氟苯基)-1H-吡唑-4-甲醯胺(5 g, 15 mmol)、Pd(dppf)Cl2
(736 mg, 1.0 mmol)及Na2
CO3
(2.4 g, 23 mmol)於二噁烷/水(80 mL / 15 mL)中之混合物在80℃及N2
下攪拌過夜。將EtOAc (30 mL)添加至混合物中。過濾混合物,且使用H2
O (35 mL × 2)洗滌濾液。分離有機層,藉由Na2
SO4
乾燥並在真空下濃縮以得到黃色殘餘物。藉由矽膠管柱層析使用20 - 30%乙酸乙酯石油醚純化殘餘物以得到黃色固體形式之5-胺基-N-(3-氯-4-氟苯基)-3-(5-側氧基-1,3a,4,5,6,6a-六氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺(2.6 g, 46%)。MS計算值:374.1;MS實驗值:375.2 [M + 1]+
。
AIA-286 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 側氧基八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺
向5-胺基-N-(3-氯-4-氟苯基)-3-(5-側氧基-1,3a,4,5,6,6a-六氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺(500 mg, 1.3 mmol)於THF (20 mL)中之溶液中添加Pd/C (500 mg)及NH4
OH (12滴)。將燒瓶抽真空並使用H2
回填。將溶液在35℃下攪拌8 h。添加DMF (8 mL)並過濾混合物,且然後在真空下濃縮。藉由製備型HPLC純化所得殘餘物以得到5-胺基-N-(3-氯-4-氟苯基)-3-(5-側氧基八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺(200 mg, 40%) MS計算值:376.1;MS實驗值:377.1 [M + 1]+
。1
H-NMR (DMSO-d6, 400 MHz): δ 12.05 (s, 0.55H), 11.49 (s, 0.46 H ), 9.54 (s, 0.46H), 8.96 (s, 0.48H), 7.94 (d, J = 4.8 Hz, 1H), 7.55-7.50 (m, 1H), 7.36 (t, J = 9.2 Hz, 1H), 5.76 (s, 1H), 4.97 (s, 1H), 3.67-3.60 (m, 1H), 2.72-2.66 (m, 2H), 2.50-2.44 (m, 2H), 2.33-2.25 (m, 2H), 2.08-2.04 (m, 2H), 1.59-1.54 (m, 2H)。
中間體129 (4-((3- 氯 -4- 氟苯基 ) 胺甲醯基 )-3-(5- 側氧基八氫并環戊二烯 -2- 基 )-1H- 吡唑 -5- 基 ) 胺基甲酸第三丁基酯
。在0℃下,向5-胺基-N-(3-氯-4-氟苯基)-3-(5-側氧基八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺(200 mg, 0.5 mmol)於THF (10 mL)中之溶液中添加NaH (32 mg, 1.3 mmol),將淺褐色溶液在0℃下攪拌30 min。添加Boc2
O (150 mg, 0.7 mmol)並在室溫下再繼續攪拌30 min。將混合物冷卻至0℃,使用H2
O驟冷,使用乙酸乙酯(20 mL × 3)萃取,乾燥,過濾並在減壓下濃縮濾液。藉由管柱層析使用10 - 20%乙酸乙酯/石油醚純化粗產物以提供淺白色固體形式之(4-((3-氯-4-氟苯基)胺甲醯基)-3-(5-側氧基八氫并環戊二烯-2-基)-1H-吡唑-5-基)胺基甲酸第三丁基酯(200 mg, 80%)。MS計算值:476.1;MS實驗值:421.2 [M - 56 + 1]+
。
中間體130 (4-((3- 氯 -4- 氟苯基 ) 胺甲醯基 )-3-(5- 羥基 -5-(( 甲基磺醯基 ) 甲基 ) 八氫并環戊二烯 -2- 基 )-1H- 吡唑 -5- 基 ) 胺基甲酸第三丁基酯
。在-45℃及N2
下,向二甲基碸(237 mg, 2.5 mmol)於THF (10 mL)中之溶液中添加n
-BuLi (1 mL, 2.5 M, 2.5 mmol)。將混合物在-45℃下攪拌30 min。將(4-((3-氯-4-氟苯基)胺甲醯基)-3-(5-側氧基八氫并環戊二烯-2-基)-1H-吡唑-5-基)胺基甲酸第三丁基酯(200 mg, 0.4 mmol)一次性添加至混合物中。將溶液在室溫下攪拌過夜。使用NH4
Cl水溶液將反應混合物驟冷並使用乙酸乙酯(10 mL × 3)萃取。乾燥合併之有機層並濃縮,藉由矽膠管柱層析使用95:5 DCM/MeOH純化殘餘物以提供白色固體形式之(4-((3-氯-4-氟苯基)胺甲醯基)-3-(5-羥基-5-((甲基磺醯基)甲基)八氫并環戊二烯-2-基)-1H-吡唑-5-基)胺基甲酸第三丁基酯(140 mg, 60%)。MS計算值:570.2;MS實驗值:571.2 [M+1]+
。
AIA-310 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-(( 甲基磺醯基 ) 甲基 ) 八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺
。向(4-((3-氯-4-氟苯基)胺甲醯基)-3-(5-羥基-5-((甲基磺醯基)甲基)八氫并環戊二烯-2-基)-1H-吡唑-5-基)胺基甲酸第三丁基酯(140 mg, 0.25 mmol)於DCM (5 mL)中之溶液中添加三氟乙酸(1 mL)。將所得混合物在室溫下攪拌1 h。使用NaHCO3
將反應混合物調節至pH 8 - 9並使用DCM (10 mL × 3)萃取。乾燥合併之有機層並濃縮。藉由矽膠管柱層析(使用95:5 DCM/MeOH)及製備型HPLC純化殘餘物以提供白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-3-(5-羥基-5-((甲基磺醯基)甲基)八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺(30 mg, 26% )。MS計算值:470.1;MS實驗值:471.2 [M + 1]+
。1
H-NMR (DMSO-d6, 400 MHz): δ 11.88 (s, 0.55H), 11.44 (s, 0.45H), 9.49 (s, 0.53H), 8.93 (s, 0.41H), 7.93 (s, 1H), 7.53-7.49 (m, 1H), 7.35 (t, J = 8.8 Hz, 1H), 5.73 (s, 1H), 4.92 (t, J = 12.0 Hz, 2H), 3.47-3.45 (m, 1H), 3.28-3.26 (m, 2H), 2.98 (s, 3H), 2.51-2.49 (m, 2H), 2.17 (s, 2H), 2.02 (s, 2H), 1.64 (d, J = 10.0 Hz, 4H)。
中間體131 5-( 三氟甲基磺醯基氧基 )-3,3a,6,6a- 四氫環戊 [c] 吡咯 -2(1H)- 甲酸第三丁基酯 :
在-78℃下經30 min,將LDA (10 mL, 20 mmol)緩慢添加至5-側氧基六氫環戊[c]吡咯-2(1H)-甲酸第三丁基酯(3 g, 13.3 mmol)於無水THF (50 mL)中之溶液中。緩慢添加於THF (20 mL)中之1,1,1-三氟-N-苯基-N-(三氟甲基磺醯基)甲烷磺醯胺(5.7 g, 16.1 mmol)並將溶液攪拌2 h。將反應混合物升溫至室溫並使用NH4
Cl (水溶液)驟冷。使用乙酸乙酯(50 mL × 3)萃取溶液。藉由Na2
SO4
乾燥合併之有機層,濃縮並藉由矽膠管柱層析使用5 - 10%乙酸乙酯/石油醚純化以提供淺黃色固體形式之5-(三氟甲基磺醯基氧基)-3,3a,6,6a-四氫環戊[c]吡咯-2(1H)-甲酸第三丁基酯(3.7 g, 78%)。
中間體132 5-(4,4,5,5- 四甲基 -1,3,2- 二氧硼㖦 -2- 基 )-3,3a,6,6a- 四氫環戊 [c] 吡咯 -2(1H)- 甲酸第三丁基酯。
將5-(三氟甲基磺醯基氧基)-3,3a,6,6a-四氫環戊[c]吡咯-2(1H)-甲酸第三丁基酯(2.8 g, 7.8 mmol)、4,4,5,5-四甲基-2-(4,4,5,5-四甲基-1,3,2-二氧硼㖦 -2-基)-1,3,2-二氧硼㖦(2.4 g, 9.4 mmol)、1,1'-雙(二苯基膦基)二茂鐵(0.13 g, 0.24 mmol)、[1,1'-雙(二苯基 膦基)二茂鐵]二氯鈀(II) (0.17 g, 0.24 mmol)及乙酸鉀(2.3 g, 23.5 mmol)於二噁烷(30 mL)中之褐色混合物在80℃及N2
下攪拌16 h。觀察到深色懸浮液。經由Celite®墊過濾反應液,並使用乙酸乙酯(20 mL)洗滌濾餅。在真空下濃縮濾液並藉由矽膠管柱層析使用5 - 10%乙酸乙酯/石油醚純化以得到淺黃色固體形式之5-(4,4,5,5-四甲基-1,3,2-二氧硼㖦-2-基)-3,3a,6,6a- 四氫環戊[c]吡咯-2(1H)-甲酸第三丁基酯(2.2 g, 85%產率)。
中間體133 5-(5- 胺基 -4-(3- 氯 -4- 氟苯基胺甲醯基 )-1- 甲基 -1H- 吡唑 -3- 基 )-3,3a,6,6a- 四氫環戊 [c] 吡咯 -2(1H)- 甲酸第三丁基酯。
將5-(4,4,5,5-四甲基-1,3,2-二氧硼㖦-2-基)-3,3a,6,6a-四氫環戊[c]吡咯- 2(1H)-甲酸第三丁基酯(1 g, 3.0 mmol)、5-胺基-3-溴-N-(3-氯-4-氟苯基)-1-甲基-1H-吡唑-4-甲醯胺(1 g, 3.0 mmol)、Pd(dppf)Cl2
(66 mg, 0.09 mmol)及K2
CO3
(0.82 g, 6.0 mmol)於二噁烷(20 mL)及H2
O (4 mL)中之混合物在80℃及N2
下攪拌16 h。將EtOAc (20 mL)添加至混合物中。過濾混合物,且使用H2
O (35 mL × 2)洗滌濾液。分離有機層,藉由Na2
SO4
乾燥並在真空下濃縮以得到黃色殘餘物。藉由矽膠管柱層析使用5 - 10%乙酸乙酯/石油醚純化殘餘物以得到黃色固體形式之5-(5-胺基-4-(3-氯-4-氟苯基胺甲醯基)-1-甲基-1H- 吡唑-3-基)-3,3a,6,6a-四氫環戊[c]吡咯-2(1H)-甲酸第三丁基酯(0.8 g, 57%)。MS計算值:475.2;MS實驗值:420.3 [M-56+1]+
, 476.4 [M+1]+
。
AIA-005 5-(5- 胺基 -4-(3- 氯 -4- 氟苯基胺甲醯基 )-1- 甲基 - 1H- 吡唑 -3- 基 ) 六氫環戊 [c] 吡咯 -2(1H)- 甲酸第三丁基酯。
向5-(5-胺基-4-(3-氯-4-氟苯基胺甲醯基)-1-甲基-1H-吡唑-3-基)- 3,3a,6,6-四氫環戊烷[c]吡咯-2(1H)-甲酸第三丁基酯(800 mg, 1.7 mmol)於THF (20 mL)中之溶液中添加Pt/C (160 mg)。然後將燒瓶抽真空並使用H2
回填。將溶液在30℃下攪拌16 h。過濾混合物並濃縮以得到白色固體形式之5-(5-胺基-4-(3-氯-4-氟苯基胺甲醯基)-1-甲基- 1H-吡唑-3-基)六氫環戊[c]吡咯-2(1H)-甲酸第三丁基酯(600 mg, 75%)。MS計算值:477.2;MS實驗值:422.3 [M-56+1]+
, 478.4 [M+1]+
。1
H-NMR (DMSO-d6
, 400 MHz): δ 8.98 (s, 1H), 7.91 (dd, J = 6.8, 2.4 Hz, 1H), 7.54-7.50 (m, 1H), 7.34 (t, J = 9.6 Hz, 1H), 5.98 (s, 2H), 3.59-3.52 (m, 1H), 3.49 (s, 3H), 3.32 (s, 2H), 3.14-3.10 (m, 2H), 2.61-2.57 (m, 2H), 2.21-2.14 (m, 2H), 1.56-1.48 (m, 2H), 1.38 (s, 9H)
AIA-006 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-( 八氫環戊 [c] 吡咯 -5- 基 )-1H- 吡唑 -4- 甲醯胺。
向5-(5-胺基-4- (3-氯-4-氟苯基胺甲醯基)-1-甲基-1H-吡唑-3-基)六氫環戊[c]吡咯-2(1H)-甲酸第三丁基酯(600 mg, 1.26 mmol)於DCM (10 mL)中之溶液中添加1M HCl
(0.5 mL),將所得混合物在室溫下攪拌1 h。使用NaHCO3
水溶液將反應混合物調節至pH 8 ~ 9並使用DCM (10 mL × 3)萃取溶液。乾燥合併之有機層,並在真空中去除溶劑。藉由製備型HPLC純化殘餘物以提供白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(八氫環戊[c] 吡咯-5-基)-1H-吡唑-4-甲醯胺(355 mg, 75%)。MS計算值:377.1;MS實驗值:378.4 [M + 1]+
。1
H-NMR (DMSO-d6
, 400 MHz): δ 8.97 (s, 1H), 7.91 (dd, J = 6.8, 2.8 Hz, 1H), 7.53-7.51 (m, 1H), 7.34 (t, J = 9.2 Hz, 1H), 5.97 (s, 2H), 3.55-3.53 (m, 1H), 3.49 (s, 3H), 3.44-3.41 (m, 3H), 3.22-3.14 (m, 1H), 2.57 (s, 3H), 2.19-2.13 (m, 2H), 1.52-1.50 (m, 1H), 1.34-1.32 (m, 1H)。
AIA-007 3-(2- 乙醯基八氫環戊 [c] 吡咯 -5- 基 )-5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。
在0℃下,向含有5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(八氫環戊[c] 吡咯- 5-基)-1H-吡唑-4-甲醯胺(80 mg, 0.21 mmol)及Et3
N (43 mg, 0.42 mmol)於DCM (2 mL)中之經攪拌混合物之燒瓶中添加乙酸酐(32 mg, 0.32 mmol)。將混合物在室溫下攪拌16 h,然後使用水驟冷,使用乙酸乙酯萃取,乾燥並濃縮。藉由製備型HPLC純化粗產物以提供白色固體形式之3-(2-乙醯基八氫環戊[c]吡咯-5-基)-5-胺基-N-(3-氯-4- 氟苯基)-1-甲基-1H-吡唑-4-甲醯胺(30 mg, 34%)。MS計算值:419.2;MS實驗值:420.2 [M+1]+
。1
H-NMR (DMSO-d6
, 400 MHz): δ 8.96 (s, 1H), 7.89 (dd, J = 6.8, 2.8 Hz, 1H), 7.53-7.49 (m, 1H), 7.32 (t, J = 9.2 Hz, 1H), 5.95 (s, 2H), 3.59-3.48 (m, 2H), 3.46 (s, 3H), 3.36-3.33 (m, 1H), 3.26-3.18 (m, 2H), 2.68-2.57 (m, 2H), 2.21-2.13 (m, 2H), 1.88 (s, 3H), 1.55-1.48 (m, 2H)。表 15.
根據針對3-(2-乙醯基八氫環戊[c]吡咯-5-基)-5-胺基-N-(3-氯-4- 氟苯基)-1-甲基-1H-吡唑-4-甲醯胺所揭示之程序來合成表15中之化合物。
| 化合物 | 結構及表徵 |
| AIA-022 | 5-(5- 胺基 -4-((3- 氯 -4- 氟苯基 ) 胺甲醯基 )-1- 甲基 -1H- 吡唑 -3- 基 ) 六氫環戊 [c] 吡咯 -2(1H)- 甲酸甲酯 。MS計算值:435.1;MS實驗值:436.2 [M+1]+ 。1 H-NMR (DMSO-d6 , 400 MHz): δ 8.95 (s, 1H), 7.89 (dd,J = 6.8, 2.4 Hz, 1H), 7.52-7.49 (m, 1H), 7.32 (t,J = 9.2 Hz, 1H), 5.96 (s, 2H), 3.55-3.53 (m, 4H), 3.47 (s, 3H), 3.38-3.33 (m, 2H), 3.18-3.15 (m, 2H), 2.61 (s, 2H), 2.19-2.15 (m, 2H), 1.52-1.48 (m, 2H) |
| AIA-023 | 5-(5- 胺基 -4-(3- 氯 -4- 氟苯基胺甲醯基 )-1- 甲基 -1H- 吡唑 -3- 基 )-N- 甲基六氫環戊 [c] 吡咯 -2(1H)- 甲醯胺 。MS計算值:434.1;MS實驗值:435.3 [M+1]+ 。1 H-NMR (DMSO-d6 , 400 MHz): δ 8.95 (s, 1H), 7.89 (dd,J = 6.8, 2.4 Hz, 1H), 7.53-7.49 (m, 1H), 7.32 (t,J = 9.2 Hz, 1H), 5.99-5.95 (m, 3H), 3.52-3.50 (m, 1H), 3.47 (s, 3H), 3.25-3.20 (m, 2H), 3.13-3.10 (m, 2H), 2.59-2.58 (m, 2H), 2.52 (d,J = 4.0 Hz, 3H), 2.20-2.13 (m, 2H), 1.52-1.45 (m, 2H) |
| AIA-025 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(2-( 吡咯啶 -1- 羰基 ) 八氫環戊 [c] 吡咯 -5- 基 )-1H- 吡唑 -4- 甲醯胺。 MS計算值:474.2;MS實驗值:475.3 [M+1]+ 。1 H-NMR (DMSO-d6 , 400 MHz): δ 8.95 (s, 1H), 7.89 (dd,J = 6.8, 2.4 Hz, 1H), 7.52-7.48 (m, 1H), 7.32 (t,J = 8.8 Hz, 1H), 5.95 (s, 2H), 3.53-3.49 (m, 1H), 3.47 (s, 3H), 3.27-3.17 (m, 8H), 2.56-2.55 (m, 2H), 2.18-2.12 (m, 2H), 1.72-1.68 (m, 4H), 1.53-1.46 (m, 2H) |
| AIA-053 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(2- 異丙基八氫環戊 [c] 吡咯 -5- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 MS計算值:419.2;MS實驗值:420.3 [M+1]+ 。1 H-NMR (DMSO-d6 , 400 MHz): δ 8.94 (s, 1H), 7.91 (dd,J = 6.8, 2.4 Hz, 1H), 7.53-7.49 (m, 1H), 7.34 (t,J = 8.8 Hz, 1H), 5.96 (s, 2H), 3.49 (s, 3H), 3.32-3.26 (m, 1H), 2.59-2.57 (m, 2H), 2.50-2.49 (m, 2H), 2.25-2.19 (m, 1H), 2.15-2.12 (m, 4H), 1.47-1.39 (m, 2H), 0.99 (d,J = 6.4 Hz, 6H) |
| AIA-052 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(2- 甲基八氫環戊 [c] 吡咯 -5- 基 )-1H- 吡唑 -4- 甲醯胺。 MS計算值:391.2;MS實驗值:392.3 [M+1]+ 。1 H-NMR (DMSO-d6 , 400 MHz): δ 8.93 (s, 1H), 7.91 (dd,J = 6.8, 2.4 Hz, 1H), 7.53-7.49 (m, 1H), 7.34 (t,J = 8.8 Hz, 1H), 5.96 (s, 2H), 3.48 (s, 3H), 3.30-3.29 (m, 1H), 2.49-2.46 (m, 4H), 2.18 (s, 3H), 2.16-2.10 (m, 2H), 2.06-2.03 (m, 2H), 1.47-1.44 (m, 2H) |
| AIA-054 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(2-(1,1,1- 三氟丙烷 -2- 基 ) 八氫環戊 [c] 吡咯 -5- 基 )-1H- 吡唑 -4- 甲醯胺。 MS計算值:473.2;MS實驗值:474.3 [M+1]+ 。1 H-NMR (DMSO-d6 , 400 MHz): δ 8.93 (s, 1H), 7.89 (dd,J = 6.8, 2.4 Hz, 1H), 7.51-7.47 (m, 1H), 7.32 (t,J = 8.8 Hz, 1H), 5.94 (s, 2H), 3.47 (s, 3H), 3.41-3.37 (m, 1H), 2.60-2.48 (m, 4H), 2.48-2.47 (m, 3H), 2.16-2.12 (m, 2H), 1.40-1.38 (m, 2H), 1.11 (d,J = 6.4 Hz, 3H) |
| AIA-024 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(2-( 甲基磺醯基 ) 八氫環戊 [c] 吡咯 -5- 基 )-1H- 吡唑 -4- 甲醯胺。 MS計算值:455.1;MS實驗值:456.2 [M+1]+ 。1 H-NMR (DMSO-d6 , 400 MHz): δ 8.97 (s, 1H), 7.89 (dd,J = 7.2, 2.8 Hz, 1H), 7.53-7.49 (m, 1H), 7.32 (t,J = 9.2 Hz, 1H), 5.96 (s, 2H), 3.48 (s, 3H), 3.47-3.42 (m, 1H), 3.16-3.12 (m, 2H), 3.01-2.99 (m, 2H), 2.85 (s, 3H), 2.69-2.67 (m, 2H), 2.24-2.21 (m, 2H), 1.53-1.45 (m, 2H) |
| AIA-085 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(2-( 異丙基磺醯基 ) 八氫環戊基 [c] 吡咯 -5- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。 MS計算值:483.2;MS實驗值:484.2 [M+1]+ 。1 H-NMR (DMSO-d6 , 400 MHz): δ 8.97 (s, 1H), 7.89 (dd,J = 6.8, 2.4 Hz, 1H), 7.52-7.48 (m, 1H), 7.32 (t,J = 8.8 Hz, 1H), 5.96 (s, 2H), 3.47 (s, 3H), 3.44-3.41 (m, 1H), 3.34-3.33 (m, 1H), 3.27-3.23(m, 2H), 3.13-3.11 (m, 2H), 2.65-2.64 (m, 2H), 2.22-2.17 (m, 2H), 1.51-1.43(m, 2H), 1.19 (d,J = 6.8, 6H) |
中間體134 5-(1- 甲基 -1H- 吡唑 -4- 基 )-3,3a,6,6a- 四氫并環戊二烯 -2(1H)- 酮。
將4-溴-1-甲基-1H-吡唑(2.0 g, 8.1 mmol)、5-(4,4,5,5-四甲基-1,3,2-二氧硼㖦-2-基)-3,3a,6,6a-四氫并環戊二烯-2(1H)-酮(1.4 g, 8.9 mmol)、K3
PO4
(3.4 g, 16.1 mmol)及Pd(dppf)Cl2
(589.8 mg, 0.8 mmol)於二噁烷(10 mL)及H2
O (2 mL)中之混合物在80℃及N2
氣氛下攪拌過夜。在真空下去除溶劑並藉由矽膠管柱層析使用2:1石油醚/乙酸乙酯純化殘餘物以提供黃色固體形式之5-(1-甲基-1H-吡唑-4-基)-3,3a,6,6a-四氫并環戊二烯-2(1H)-酮(1.0 g, 62.5%)。MS計算值:202.1,MS實驗值:203.4 [M
+ 1]+
。
中間體135 5-(1- 甲基 -1H- 吡唑 -4- 基 ) 六氫并環戊二烯 -2(1H)- 酮。
將5-(1-甲基-1H-吡唑-4-基)-3,3a,6,6a-四氫并環戊二烯-2(1H)-酮(1.0 g, 4.9 mmol)及Pd/C (0.1 g)於乙酸乙酯(20 mL)中之混合物在H2
及30℃下攪拌過夜。藉由Celite®墊過濾混合物。濃縮濾液,然後藉由矽膠管柱層析使用1:1石油醚/乙酸乙酯純化以提供黃色固體形式之5-(1-甲基-1H-吡唑-4-基)六氫并環戊二烯-2(1H)-酮(800.0 mg, 80.0%) MS計算值:204.1,MS實驗值:205.4 [M
+ 1]+
。
中間體136 三氟甲烷磺酸 5-(1- 甲基 -1H- 吡唑 -4- 基 )-1,3a,4,5,6,6a- 六氫并環戊二烯 -2- 基酯。
在-78℃下,向5-(1-甲基-1H-吡唑-4-基)六氫并環戊二烯-2(1H)-酮(550.0 mg, 2.7 mmol)於THF (20 mL)中之溶液中添加LiHMDS (4.0 mmol, 1 M, 4.0 mL)。將反應混合物在-78℃下攪拌1小時,然後逐滴添加1,1,1-三氟-N-苯基-N-((三氟甲基)磺醯基)甲烷磺醯胺(1.4 g, 4.0 mmol)於THF (5 mL)中之溶液。將反應混合物升溫至30℃並攪拌過夜。在25℃下藉由添加NH4
Cl (2 mL)來將反應混合物驟冷,然後使用H2
O (10 mL)稀釋並使用EtOAc (20 mL × 2)萃取。使用鹽水(20 mL)洗滌合併之有機層,藉由Na2
SO4
乾燥,過濾並在減壓下濃縮,並藉由矽膠管柱層析使用3:1石油醚/乙酸乙酯純化殘餘物以提供黃色油狀物形式之三氟甲烷磺酸5-(1-甲基-1H-吡唑-4-基)-1,3a,4,5,6,6a-六氫并環戊二烯-2-基酯(800.0 mg, 88.4%)。MS計算值:336.1,MS實驗值:337.3 [M
+ 1]+
。
中間體137 1- 甲基 -4-(5-(4,4,5,5- 四甲基 -1,3,2- 二氧硼㖦 -2- 基 )-1,2,3,3a,4,6a- 六氫并環戊二烯 -2- 基 )-1H- 吡唑。
將三氟甲烷磺酸5-(1-甲基-1H-吡唑-4-基)-1,3a,4,5,6,6a-六氫并環戊二烯-2-基酯(90.0 mg, 0.3 mmol)、4,4,5,5-四甲基-2-(4, 4,5,5-四甲基-1,3,2-二氧硼㖦-2-基)-1,3,2-二氧硼㖦(81.5 mg, 0.3 mmol)、Pd(dppf)Cl2
(19.6 mg, 0.03 mmol)及乙酸鉀(52.5 mg, 0.5 mmol)於二噁烷(5 mL)中之混合物在80℃及N2
氣氛下攪拌4小時。經由Celite®墊過濾反應混合物,並使用EtOAc (10 mL × 3)洗滌濾餅。在真空下濃縮濾液並藉由矽膠管柱層析使用3:1石油醚/乙酸乙酯純化殘餘物以提供黃色油狀物形式之1-甲基-4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼㖦-2-基)-1,2,3,3a,4,6a- 六氫并環戊二烯-2-基)-1H-吡唑(50.0 mg, 59.5%)。MS計算值:314.2,MS實驗值:315.4 [M
+ 1]+
。
中間體138 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5-(1- 甲基 -1H- 吡唑 - 4- 基 )-1,3a,4,5,6,6a- 六氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺。
將5-胺基-3-溴-N-(3-氯-4-氟苯基)-1-甲基-1H-吡唑-4-甲醯胺(55.3 mg, 0.2 mmol)、1-甲基-4-(5-(4,4,5,5-四甲基-1,3,2-二氧硼㖦-2-基)-1,2,3,3a,4,6a- 六氫并環戊二烯-2-基)-1H-吡唑(50.0 mg, 0.2 mmol)、K3
PO4
(67.6 mg, 0.3 mmol)及Pd(dppf)Cl2
(11.6 mg, 0.02 mmol)於二噁烷(5 mL)及H2
O (1 mL)中之混合物在100℃及N2
氣氛下攪拌4小時。在真空下去除溶劑並藉由矽膠管柱層析使用1:1石油醚/乙酸乙酯純化殘餘物以提供黃色固體形式之5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(1-甲基-1H-吡唑- 4-基)-1,3a,4,5,6,6a-六氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺(50.0 mg, 69.4%)。(Rf
: 0.2);MS計算值:454.2,MS實驗值:455.3 [M
+ 1]+
。
AIA-049 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5-(1- 甲基 -1H- 吡唑 -4- 基 ) 八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺。
將5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(1-甲基-1H-吡唑- 4-基)-1,3a,4,5,6,6a-六氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺(800.0 mg, 1.8 mmol)及RhCl(PPh3
)3
(81.3 mg, 0.09 mmol)於MeOH (50 mL)中之混合物在10 atm H2
及70℃下攪拌過夜。在真空下去除溶劑並藉由矽膠管柱層析使用1:石油醚/乙酸乙酯純化殘餘物以提供白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(1-甲基-1H-吡唑-4-基)八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺(55 mg, 6.8%)。1
H-NMR (DMSO-d6
, 400 MHz): δ 8.97 (s, 1H), 7.91 (dd, J = 6.8, 2.4 Hz, 1H), 7.54-7.50 (m, 1H), 7.44 (s, 1H), 7.35 (t, J = 9.2 Hz, 1H), 7.22 (s, 1H), 5.97 (s, 2H), 3.74 (s, 3H), 3.64-3.53 (m, 1H), 3.50 (m, 3H), 2.99-2.90 (m, 1H), 2.51-2.50 (m, 2H), 2.20-2.10 (m, 4H), 1.52-1.44 (m, 2H), 1.27-1.19 (m, 2H);MS計算值:456.2,MS實驗值:457.4 [M
+1]+
。表 16.
根據針對5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(1-甲基-1H-吡唑-4-基)八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺所闡述之程序來合成表16中之化合物。
| 化合物 | 結構及表徵 |
| AIA-119 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5-( 噻唑 -2- 基 ) 八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺。 MS計算值:459.1;MS實驗值:460.2 [M + 1]+ ;1 H NMR (DMSO-d 6 , 400 MHz): δ8.97 (brs, 1H), 7.92 (dd,J = 7.2, 2.8 Hz, 1H), 7.66 (d,J = 3.2 Hz, 1H), 7.55-7.51 (m, 2H), 7.35 (t,J = 8.8 Hz, 1H), 5.98 (brs, 2H), 3.66-3.61 (m, 1H), 3.56-3.50 (m, 4H), 2.60-2.59 (m, 2H), 3.36-2.30 (m, 2H), 2.22-2.18 (m, 2H), 1.57-1.49 (m, 4H)。 |
| AIA-121 | 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5-( 噻唑 -4- 基 ) 八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺 MS 計算值:459.1,MS實驗值:460.2 [M+1]+ 。1 H-NMR (DMSO-d6 , 400 MHz): δ 8.99 (d,J = 2.4 Hz, 2H), 7.92 (dd,J = 6.8, 2.8 Hz, 1H), 7.55-7.51 (m, 1H), 7.35 (t,J = 9.2 Hz, 1H), 7.32 (d,J = 2.4 Hz, 1H), 5.98 (s, 2H), 3.65-3.59 (m, 1H), 3.50 (s, 3H), 3.35-3.30 (m, 1H), 2.58-2.54 (m, 2H), 2.22-2.18 (m, 4H), 1.56-1.45 (m, 4H)。 |
中間體139 5-(1H- 咪唑 -4- 基 )-3,3a,6,6a- 四氫并環戊二烯 -2(1H)- 酮。
將5-(4,4,5,5-四甲基-1,3,2-二氧硼㖦-2-基)-3,3a,6,6a-四氫并環戊二烯-2(1H)-酮(1.5 g, 6.0 mmol)、4-溴-1H-咪唑(0.88 g, 6.0 mmol)、Pd(dppf)Cl2
(0.44 g, 0.6 mmol)及K3
PO4
(2.6 g, 12 mmol)於二噁烷(50 mL)及H2
O (8 mL)中之混合物在80℃及N2
下攪拌16 h。混合物係褐色懸浮液。將EtOAc (40 mL)添加至混合物中。過濾混合物,並使用H2
O (35 mL × 2)洗滌濾液。藉由Na2
SO4
乾燥有機層並在真空下蒸發以得到黃色殘餘物。藉由矽膠管柱層析使用5 - 50%乙酸乙酯/石油醚純化殘餘物以得到黃色固體形式之5-(1H-咪唑-4-基)-3,3a,6,6a-四氫并環戊二烯-2(1H)-酮(0.6 g, 55%)。MS計算值:188.1;MS實驗值:189.2 [M + 1]+
。
中間體140 4-(5- 側氧基 -1,3a,4,5,6,6a- 六氫并環戊二烯 -2- 基 )-1H- 咪唑 -1- 甲酸第三丁基酯。
向5-(1H-咪唑-4-基)-3,3a,6,6a-四氫并環戊二烯-2(1H)-酮(600 mg, 3.2 mmol)於DCM (20 mL)中之溶液中添加Boc2
O (765 mg, 3.5 mmol)及DMAP (39 mg, 0.32 mmol)。將溶液在室溫下攪拌0.5 h。在真空中去除溶劑並藉由矽膠管柱層析使用5 - 10%乙酸乙酯/石油醚純化粗產物以提供淺黃色固體形式之4-(5-側氧基-1,3a,4,5,6,6a-六氫并環戊二烯-2-基)-1H-咪唑-1-甲酸第三丁基酯(500 mg, 75%)。MS計算值:288.1;MS實驗值:232.2 [M-56 + 1]+
, 288.2 [M + 1]+
。
中間體141 4-(5- 側氧基八氫并環戊二烯 -2- 基 )-1H- 咪唑 -1- 甲酸第三丁基酯。
向4-(5-側氧基-1,3a,4,5,6,6a-六氫并環戊二烯-2-基)-1H-咪唑-1-甲酸第三丁基酯(500 mg, 1.7 mmol)於乙酸乙酯(20 mL)中之溶液中添加Pd/C (100 mg)。然後將燒瓶抽真空並使用H2
回填。將溶液在40℃下攪拌16 h。過濾混合物,且濃縮濾液以得到淺黃色固體形式之4-(5-側氧基八氫并環戊二烯-2-基)-1H-咪唑-1-甲酸第三丁基酯(480 mg, 95%)。MS計算值:290.2;MS實驗值:234.2 [M-56 + 1]+
, 291.2 [M + 1]+
。
中間體142 4-(5-(5- 胺基 -4-((3- 氯 -4- 氟苯基 ) 胺甲醯基 )-1- 甲基 -1H- 吡唑 -3- 基 ) 八氫并環戊二烯 -2- 基 )-1H- 咪唑 -1- 甲酸第三丁基酯。
根據針對5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(5-(1-甲基-1H-吡唑-4-基)八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺所闡述之程序來合成標題化合物。MS計算值:542.2;MS實驗值:487.2 [M-56 + 1]+
, 543.3 [M + 1]+
。
AIA-118 3-(5-(1H- 咪唑 -4- 基 ) 八氫并環戊二烯 -2- 基 )-5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。
向4-(5-(5-胺基-4-((3-氯-4-氟苯基)胺甲醯基)-1-甲基-1H-吡唑-3-基)八氫并環戊二烯-2-基)-1H-咪唑-1-甲酸第三丁基酯(70 mg, 0.13 mmol)於DCM (5 mL)中之溶液中添加三氟乙酸(0.5 mL)並將所得混合物在室溫下攪拌1 h。使用NaHCO3
將反應混合物調節至pH 8 - 9,過濾並在真空中濃縮濾液。藉由製備型HPLC純化粗產物以提供白色固體形式之3-(5-(1H-咪唑-4-基)八氫并環戊二烯-2-基)-5-胺基-N-(3-氯-4-氟苯基)-1-甲基-1H-吡唑-4-甲醯胺(30 mg, 53%)。MS計算值:442.2;MS實驗值:443.3 [M + 1]+
。
AIA-129 3-(5-(1H- 吡唑 -4- 基 ) 八氫并環戊二烯 -2- 基 )-5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。
根據針對3-(5-(1H-咪唑-4-基)八氫并環戊二烯-2-基)-5-胺基-N-(3-氯-4-氟苯基)-1-甲基-1H-吡唑-4-甲醯胺所闡述之程序來合成標題化合物。MS計算值:442.2,MS實驗值:443.3 [M+1]+
;1
H-NMR (DMSO-d6
, 400 MHz): δ 12.47 (brs, 1H), 8.97 (s, 1H), 7.92 (dd,J
= 6.8, 2.4 Hz, 1H), 7.55-7.51 (m, 1H), 7.40 (s, 2H), 7.35 (t,J
= 9.2 Hz, 1H), 5.97 (s, 2H), 3.63-3.57 (m, 1H), 3.50 (s, 3H), 3.01-2.95 (m, 1H), 2.50-2.51 (m, 2H), 2.18-2.17 (m, 4H), 1.52-1.45 (m, 2H), 1.30-1.21 (m, 2H)。
AIA-394 N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(5- 側氧基八氫并環戊二烯 -2- 基 )-1H- 吡唑 -4- 甲醯胺。
在0℃下,向AIA-002 (200.0 mg, 0.51 mmol)於無水THF (10 mL)中之溶液中添加t-BuNO2
(210.1 mg, 2.04 mmol),並將混合物在室溫下攪拌5小時。使用NaHSO3
飽和水溶液(5.0 mL)終止反應。使用水(10 mL)稀釋溶液並使用DCM (10 mL × 3)萃取。分離有機層,藉由無水Na2
SO4
乾燥並濃縮以得到粗產物,藉由管柱層析純化以提供黃色固體形式之N-(3-氯-4-氟苯基)-1-甲基-3-(5-側氧基八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺(80.0 mg, 41.8%)。MS計算值:375.1;MS實驗值:376.1 [M + 1]+
。1
H-NMR (CDCl3
, 400 MHz): δ7.74 (dd, J = 2.4 Hz, 6.4 Hz, 1H), 7.68 (s, 1H), 7.36-7.31 (m, 1H), 7.11 (t, J = 8.8 Hz, 1H), 3.87 (s, 3H), 3.80-3.70 (m, 1H), 2.86-2.78 (m, 2H), 2.57-2.42 (m, 4H), 2.23-2.16 (m, 2H), 1.78-1.65 (m, 2H)。
AIA-397 N-(3- 氯 -4- 氟苯基 )-3-(5- 羥基 -5-(( 甲基磺醯基 ) 甲基 ) 八氫并環戊二烯 -2- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺
將甲碸(160 mg, 1.7 mmol)於無水四氫呋喃(10 mL)中之溶液冷卻至-78℃且然後使用正丁基鋰溶液(0.68 mL, 1.7 mmol, 2.5 M)進行處理。將所得溶液在-78℃至-30℃下攪拌2小時。然後,將反應混合物冷卻至-78℃並N-(3-氯-4-氟苯基)-1-甲基-3-(5-側氧基八氫并環戊二烯-2-基)-1H-吡唑-4-甲醯胺(80.0 mg, 0.21 mmol)於無水四氫呋喃(2.0 mL)中之溶液進行處理。將混合物在-78℃下攪拌2小時。然後將反應液升溫至室溫且在室溫下攪拌3小時。藉由氯化銨飽和水溶液(2.0 mL)將反應混合物驟冷。在真空中濃縮此混合物,使用水稀釋,並使用DCM (10 mL × 4)萃取,藉由Na2
SO4
乾燥,過濾並在減壓下濃縮。藉由矽膠管柱層析使用1:15 MeOH/DCM純化殘餘物,隨後藉由製備型HPLC純化以提供白色固體形式之N-(3-氯-4-氟苯基)-3-(5-羥基-5-((甲基磺醯基)甲基)八氫并環戊二烯-2-基)-1-甲基-1H-吡唑-4-甲醯胺(40.0 mg, 40.6%)。MS計算值:469.1,MS實驗值:470.1 [M
+ 1]+
。1
H NMR (DMSO-d6
, 400 MHz): δ 9.85 (s, 1H), 8.24 (s, 1H), 8.02 (dd,J
= 2.8 Hz, 7.2 Hz, 1H), 7.60-7.56 (m, 1H), 7.37 (t,J
= 9.2 Hz, 1H), 4.90 (s, 1H), 3.83 (s, 3H), 3.51-3.48 (m, 1H), 3.27 (s, 2H), 2.99 (s, 3H), 2.51-2.49 (m, 2H), 2.20-2.13 (m, 2H), 2.06-1.99 (m, 2H), 1.80-1.63 (m, 4H)。
中間體143 三氟甲烷磺酸 3,3a,4,6a- 四氫 -1H- 環戊 [c] 噻吩 -5- 基酯
在0℃下,將吡啶(3.3 g, 42 mmol)添加至四氫-1H-環戊[c]噻吩-5(3H)-酮(4.0 g, 28 mmol)於無水DCM (50 mL)中之溶液中。緩慢添加Tf2
O (12.2 g, 34 mmol)並攪拌4 h。將反應混合物升溫至室溫並使用H2
O驟冷,且使用乙酸乙酯(50 mL × 3)萃取溶液。藉由Na2
SO4
乾燥合併之有機層,濃縮並藉由矽膠管柱層析使用5-10%乙酸乙酯/石油醚純化以提供淺黃色固體形式之三氟甲烷磺酸3,3a,4,6a-四氫-1H-環戊[c]噻吩-5-基酯(3.2 g, 44%產率)。MS計算值:274.2;MS實驗值:275.7 [M+1]+
。
中間體144 4,4,5,5- 四甲基 -2-(3,3a,4,6a- 四氫 -1H- 環戊 [c] 噻吩 -5- 基 )-1,3,2- 二氧硼㖦。
將化合物三氟甲烷磺酸3,3a,4,6a-四氫-1H-環戊[c]噻吩-5-基酯(3.20 g, 11.34 mmol)、pin2
B2
(2.80 g, 11.34 mmol)、Pd(dppf)Cl2
(0.68 g, 0.56 mmol)、dppf (0.68 g, 0.56 mmol)及乙酸鉀(3.33 g, 34.02 mmol)於二噁烷(30 mL)中之褐色混合物在80℃及N2
下攪拌2 h。觀察到深色懸浮液。經由Celite®墊過濾反應液,使用乙酸乙酯(20 mL)洗滌濾餅。在真空下濃縮濾液並藉由矽膠管柱層析使用5 - 10%乙酸乙酯/石油醚純化殘餘物以得到淺黃色固體形式之4,4,5,5-四甲基-2-(3,3a,4,6a-四氫-1H-環戊[c]噻吩-5-基)-1,3,2-二氧硼㖦(1.8 g, 60%產率)。MS計算值:252.1;MS實驗值:253.7 [M+1]+
。
中間體145 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(3,3a,4,6a- 四氫 -1H- 環戊 [c] 噻吩 -5- 基 )-1H- 吡唑 -4- 甲醯胺。
將4,4,5,5-四甲基-2-(3,3a,4,6a-四氫-1H-環戊[c]噻吩-5-基)-1,3,2-二氧硼㖦(1.8 g, 7 mmol)、5-胺基-3-溴-N-(3-氯-4-氟苯基)-1-甲基-1H-吡唑- 4-甲醯胺(2.4 g, 7 mmol)、Pd(dppf)Cl2
(0.6 g, 0.35 mmol)及碳酸鈉(14.9 g, 14 mmol)於二噁烷/ H2
O (36 mL ,v/v = 5:1)中之混合物在80℃及N2
下攪拌2 h。觀察到深色懸浮液。經由Celite®墊過濾反應液,並使用乙酸乙酯(20 mL)洗滌濾餅。在真空下濃縮濾液並藉由矽膠管柱層析使用1-5%乙酸乙酯/石油醚純化殘餘物以得到淺黃色固體形式之5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(3,3a,4,6a-四氫-1H-環戊[c]噻吩-5-基)-1H-吡唑-4-甲醯胺(0.3 g, 10%產率)。MS計算值:392.8;MS實驗值:393.7 [M+1]+
。
AIA-055 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-( 六氫 -1H- 環戊 [c] 噻吩 -5- 基 )-1- 甲基 -1H- 吡唑 -4- 甲醯胺。
向化合物5-胺基-N-(3-氯-4-氟苯基)-1-甲基-3-(3,3a,4,6a-四氫-1H-環戊[c]噻吩-5-基)-1H-吡唑-4-甲醯胺(300 mg, 0.7 mmol)於EtOAc (20 mL)中之溶液中添加Pt/C (160 mg)。然後將燒瓶抽真空並使用H2
回填。將溶液在45℃下攪拌16 h。過濾混合物並濃縮以得到白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-3-(六氫-1H-環戊[c]噻吩-5-基)-1-甲基-1H-吡唑-4-甲醯胺(280 mg, 93%)。MS計算值:394.8;MS實驗值:395.7 [M+1]+
。1
H-NMR (DMSO-d6
, 400 MHz): δ 8.87 (s, 1H), 7.94 (dd,J
= 7.2, 2.8 Hz, 1H), 7.53-7.52 (m, 1H), 7.36 (t,J
= 8.8 Hz, 1H), 6.03 (s, 2H), 3.77-3.74 (m, 1H), 3.48 (s, 3H), 2.92-2.87 (m, 2H), 2.82-2.77 (m, 2H), 2.49-2.48 (m, 2H), 2.02-1.95 (m, 2H), 1.73-1.67 (m, 2H)。
AIA-056-A及AIA-056-B 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-1- 甲基 -3-(2- 氧負離子基六氫 -1H- 環戊 [c] 噻吩 -5- 基 )-1H- 吡唑 -4- 甲醯胺。非對映異構體 1 (CP-AIA-056-A) , 非對映異構體 2 (CP-AIA-056-B)
向5-胺基-N-(3-氯-4-氟苯基)-3-(六氫-1H-環戊[c]噻吩-5-基)-1-甲基-1H-吡唑-4-甲醯胺(150 mg, 0.4 mmol)於DCM (5 mL)中之溶液中添加m-CPBA (32 mg, 0.2 mmol),且將所得混合物在25℃下攪拌1 h。在真空中去除溶劑,並藉由對掌性HPLC純化殘餘物以提供CP-AIA-056-A及CP-AIA-05-6B。CP-AIA-056-A (9 mg, 5%產率)呈白色固體形式。MS計算值:410.9;MS實驗值:411.7 [M + 1]+
;且CP-AIA-056-B (8.5 mg, 5%產率)呈灰色固體形式。MS計算值:410.9;MS實驗值:411.7 [M + 1]+
。
中間體146 2-(3- 苯亞環戊基 )-1,3- 二噻烷。
在-78℃下,向 (1,3-二噻烷-2-基)三甲基矽烷(10.8 g, 56.3 mmol)於THF中之溶液中逐滴添加n-BuLi (22.5 mL, 2.5 M於THF中,56.3 mmol)。將混合物在-78℃下攪拌1 h,然後添加3-苯基環戊烷-1-酮(6.0 g, 37.5 mmol)。將混合物在相同溫度下攪拌2 h。使用NH4
Cl水溶液終止反應。在真空下去除溶劑以得到殘餘物,藉由管柱層析使用石油醚/乙酸乙酯=10:1純化以提供微黃色油狀物形式之2-(3-苯亞環戊基)-1,3-二噻烷(4.5 g, 46%產率)。MS計算值:262.1,MS實驗值:262.3 [M+1]+
。
中間體147 3- 苯基環戊烷甲酸甲酯。
將2-(3-苯亞環戊基)-1,3-二噻烷(4.5 g, 17.2 mmol)、HgCl2
(9.4 g, 34.4 mmol)、6 N HCl (5.7 mL, 34.4 mmol)及TFA (3.9 g, 34.4 mmol)於MeOH中之混合物在室溫下攪拌4 h。在過濾後,在真空中濃縮濾液並藉由管柱層析使用石油醚/乙酸乙酯=10:1純化殘餘物以提供無色油狀物形式之3-苯基環戊烷甲酸甲酯(2.9 g, 83%產率)。MS計算值:204.1,MS實驗值:205.3 [M+1]+
。
中間體148 3- 苯基環戊烷甲酸
將3-苯基環戊烷甲酸甲酯(2.9 g, 14.2 mmol) 及LiOH-H2
O (3.0 g, 71.0 mmol)於THF/H2
O=1:1 (20 mL)中之混合物在60℃下加熱過夜。 使用2N HCl中和反應液。在真空下去除溶劑並藉由矽膠管柱層析使用石油醚/乙酸乙酯=1:4純化殘餘物以提供白色固體形式之3-苯基環戊烷甲酸(2.4 g, 89%產率)。MS計算值:190.1,MS實驗值:191.1 [M+1] +
。
中間體149 3- 苯基環戊烷甲醯胺。
將3-苯基環戊烷甲酸(2.4 g, 12.6 mmol)、HCOONH4
(1.6 g, 25.2 mmol)、HATU (7.2 g, 18.9 mmol)及TEA (2.5 g, 25.2 mmol)於DMF (20 mL)中之混合物在室溫下攪拌過夜。使用水(100 mL)終止反應並使用EtOAc (100 mL × 3)萃取。在減壓下濃縮合併之有機層。藉由矽膠管柱層析使用石油醚/乙酸乙酯=1:2純化殘餘物以提供白色固體形式之3-苯基環戊烷甲醯胺(2.0 g, 83%產率)。MS計算值:189.1,MS實驗值:190.4 [M+1] +
。
中間體150 3- 苯基環戊烷甲腈。
在-40℃下,向3-苯基環戊烷甲醯胺(2.0 g, 10.6 mmol)於吡啶(20 mL)中之溶液中添加POCl3
(4.9 g, 31.8 mmol)並將混合物攪拌30 min。使用水(30 mL)終止反應,使用EtOAc (30 mL × 3)萃取。在真空下濃縮合併之有機層並藉由矽膠管柱層析使用石油醚/乙酸乙酯=10:1純化殘餘物以提供無色油狀物形式之3-苯基環戊烷甲腈(1.1 g, 61%產率)。MS計算值:171.1,MS實驗值:172.2 [M+1] +
。
中間體151 3- 苯基環戊烷甲亞胺酸甲酯鹽酸鹽。
使HCl (氣體)鼓泡通過3-苯基環戊烷甲腈(1.1 g, 6.4 mmol)於MeOH (10 mL)中之溶液並將反應液攪拌2 h。在真空下去除溶劑且殘餘物未經進一步純化即用於下一步驟中。獲得白色固體形式之3-苯基環戊烷甲亞胺酸甲酯鹽酸鹽(1.3 g粗製物,100%產率)。MS計算值:203.1,MS實驗值:204.3 [M+1] +
。
中間體152 3- 胺基 -2- 氰基 -3-(3- 苯基環戊基 ) 丙烯酸乙酯。
將3-苯基環戊烷甲亞胺酸甲酯鹽酸鹽(1.3 g, 6.4 mmol)、2-氰基乙酸乙酯(1.4 g, 12.8 mmol)及TEA (1.3 g, 12.8 mmol)於MeOH中之混合物在室溫下攪拌過夜。在真空下去除溶劑並藉由矽膠管柱層析使用石油醚/乙酸乙酯=2:1純化殘餘物以提供白色固體形式之3-胺基-2-氰基-3-(3-苯基環戊基)丙烯酸乙酯(500 mg, 28%產率)。MS計算值:284.2,MS實驗值:285.3 [M+1] +
。
中間體153 5- 胺基 -3-(3- 苯基環戊基 ) 異噁唑 -4- 甲酸乙酯。
將3-胺基-2-氰基-3-(3-苯基環戊基)丙烯酸乙酯(500 mg, 1.8 mmol)及羥基胺/EtOH (1 mL)於EtOH (2 mL)中之混合物在回流下加熱4 h。在真空下去除溶劑並藉由矽膠管柱層析使用石油醚/乙酸乙酯=10:1純化殘餘物以提供白色固體形式之5-胺基-3-(3-苯基環戊基)異噁唑-4-甲酸乙酯(200 mg, 38%產率)。MS計算值:300.1,MS實驗值:301.3 [M+1] +
。
中間體154 5- 胺基 -3-(3- 苯基環戊基 ) 異噁唑 -4- 甲酸。
將5-胺基-3-(3-苯基環戊基)異噁唑-4-甲酸乙酯(100 mg, 0.3 mmol) 及LiOH-H2
O (140 mg, 71.03.3 mmol)於THF/H2
O=1:1 (10 mL)中之混合物在60℃下加熱過夜。 使用2N HCl中和反應液。在真空下去除溶劑並藉由矽膠管柱層析使用石油醚/乙酸乙酯=1:4純化殘餘物以提供白色固體形式之5-胺基-3-(3-苯基環戊基)異噁唑-4-甲酸(70 mg, 78%產率)。MS計算值:272.1,MS實驗值:273.1 [M+1] +
。
AIA-149 5- 胺基 -N-(3- 氯 -4- 氟苯基 )-3-(3- 苯基環戊基 ) 異噁唑 -4- 甲醯胺 :
將5-胺基-3-(3-苯基環戊基)異噁唑-4-甲酸(70 mg, 0.3 mmol)、3-氯-4-氟苯胺(60 mg, 0.4 mmol)、HATU (170 mg, 0.4 mmol)及TEA (60 mg, 0.6 mmol)於DCM (5 mL)中之混合物在室溫下攪拌1 h。使用水(20 mL)終止反應並使用EtOAc (20 mL × 3)萃取。在減壓下濃縮合併之有機層並藉由矽膠管柱層析使用石油醚/乙酸乙酯=1:1及製備型HPLC純化殘餘物以提供白色固體形式之5-胺基-N-(3-氯-4-氟苯基)-3-(3-苯基環戊基)異噁唑-4-甲醯胺(3 mg, 3%產率)。MS計算值:399.1,MS實驗值:400.0 [M+1] +
。1
H-NMR (DMSO-d6
, 400 MHz): δ 9.26-9.21 (m, 1H), 7.89-7.85 (m, 1H), 7.52 (brs, 3H), 7.37-7.15 (m, 6H), 3.85-3.66 (m, 1H), 3.19-3.10 (m, 1H), 2.35-2.32 (m, 1H), 2.19-1.83 (m, 4H), 1.67-1.62 (m, 1H)。
VI. 生物學數據 量測測試化合物對來自 HepAD38 細胞之病毒產生之活性之分析
使用0.25%胰蛋白酶-EDTA (Invitrogen,目錄號:25200-056)剝離生長於含有生長培養基(DMEM/F12 (1:1) (Hyclone,目錄號:SH30023.02)、1X Pen/Strep (Invitrogen,目錄號:15140-122)、10% FBS (Tissue Culture Biologics,目錄號:101)、250 µg/mL G418 (Alfa Aesar,目錄號:J62671)、1µg/mL四環素(Tetracycline) (Teknova,目錄號:T3320))之T-150燒瓶(Corning,目錄號:430825)中之HepAD38細胞。然後向混合物中添加無四環素處理培養基(15 mL DMEM/F12 (1:1))、1x Pen/step、Tet系統專用2% FBS (Clontech,目錄號:631106),轉移至50 ml圓錐管(Falcon,目錄號:21008-918)中並在1300 rpm下旋轉5 min。然後使用50 mL 1X DPBS (Invitrogen,目錄號:14190-136)再懸浮/洗滌粒化細胞2次並使用50 mL處理培養基處理兩次。然後使用10 mL處理培養基再懸浮HepAD38細胞,沖洗並計數。在96孔透明底部TC板(Corning,目錄號:3904)之孔之180 µL處理培養基中以50,000細胞/孔進行接種,且向處理培養基中添加20 µL 10% DMSO (Sigma,目錄號:D4540,作為對照)或測試化合物於10% DMSO中之10X溶液直至最終化合物濃度(始於10 µM),且將板在37℃下於5% CO2
培育器中培育5天。
隨後,藉由HBV核心序列之定量PCR (qPCR)分析病毒負荷產生。製備含有正向引子HBV-f 5'-CTGTGCCTTGGGTGGCTTT-3’ (IDT DNA)、反向引子HBV-r 5'-AAGGAAAGAAGTCAGAAG GCAAAA-3' (IDT DNA)、螢光TaqMantm
探針HBV探針5′-FAM/AGCTCCAAA/ZEN/TTCTTTATAAGGGTCGATGTC/3IABkFQ -3′ (IDT DNA)、10 µL/孔PerfeCTa® qPCR ToughMix® (Quanta Biosciences,目錄號:95114-05K)及6 µL/孔DEPC水(Alfa Aesar,目錄號:J62087)之PCR反應混合物。將4 µL上清液添加至qPCR板(Applied Biosytems,目錄號:4309849)中之16 µL反應混合物中,使用膜(Applied Biosystems,目錄號:4311971)密封,離心數秒,且隨後在Applied Biosystems VIIA7上運行。將PCR混合物在45℃下培育5 min,然後在95℃下培育10 min,隨後實施40個循環之95℃下培育10秒及60℃下培育20秒。針對已知HBV DNA標準藉由使用ViiA™ 7軟體來量化病毒負荷。對含有經處理細胞之孔上清液中之病毒負荷與來自DMSO對照孔(每板≥ 3)之上清液中之病毒負荷進行比較。使用經修改之CellTiter-Glo發光細胞活力分析(Promega,目錄號:G7573)實施細胞活力分析。以1:1比率混合適當量之CellTiter-Glo (CTG) 1X DPBS,將100 uL混合物添加至每一孔中,隨後在不觸碰細胞表面下完全去除每一孔中之所有上清液。將板在室溫下於定軌振盪器上培育10 min,且然後使用讀板儀(TECAN M1000或Envision)讀取板。經由4參數非線性邏輯回歸模型(GraphPad Prism或Dotmatics)之曲線擬合來計算EC50
或CC50
值。CC50
值皆>10 μM。
表17給出本發明之例示化合物之病毒負荷降低EC50
值且以下列範圍分組:A
指示EC50
< 0.1 μM;B
指示EC50
為0.1-0.5 μM;C
指示EC50
為0.5-10 μM。
表17 本發明之例示化合物之病毒負荷降低。
| 化合物 | 病毒負荷 EC50 活性範圍 |
| AIA-202A | A |
| AIA-202B | A |
| AIA-202C | C |
| AIA-202D | A |
| AIA-224A | A |
| AIA-224B | B |
| AIA-232 | A |
| AIA-249 | A |
| AIA-249A | A |
| AIA-249B | B |
| AIA-262 | B |
| AIA-268 | A |
| AIA-270 | A |
| AIA-271 | A |
| AIA-272 | A |
| AIA-273 | B |
| AIA-274 | B |
| AIA-275 | A |
| AIA-275A | B |
| AIA-275B | B |
| AIA-275D | A |
| AIA-276 | A |
| AIA-276C | A |
| AIA-276D | A |
| AIA-278 | B |
| AIA-279 | A |
| AIA-280 | B |
| AIA-281 | A |
| AIA-282 | A |
| AIA-283 | A |
| AIA-284 | A |
| AIA-285 | A |
| AIA-286 | B |
| AIA-288 | A |
| AIA-290 | A |
| AIA-292 | C |
| AIA-293 | A |
| AIA-294 | A |
| AIA-296 | A |
| AIA-297 | A |
| AIA-027 | A |
| AIA-032-B | A |
| AIA-011 | A |
| AIA-042 | A |
| AIA-049 | A |
| AIA-050-A | A |
| AIA-048 | A |
| AIA-077 | A |
| AIA-100 | A |
| AIA-021 | A |
| AIA-031 | A |
| AIA-044 | A |
| AIA-020 | A |
| AIA-019 | A |
| AIA-072 | A |
| AIA-075 | A |
| AIA-032-A | A |
| AIA-030 | A |
| AIA-046 | A |
| AIA-015 | A |
| AIA-016 | A |
| AIA-018 | A |
| AIA-074 | A |
| AIA-058 | A |
| AIA-050-B | A |
| AIA-029 | A |
| AIA-028 | A |
| AIA-014 | A |
| AIA-085 | A |
| AIA-043 | A |
| AIA-022 | A |
| AIA-041 | A |
| AIA-047 | A |
| AIA-025 | A |
| AIA-024 | A |
| AIA-101 | A |
| AIA-004-D | A |
| AIA-007 | A |
| AIA-005 | A |
| AIA-003-B | A |
| AIA-004-A | A |
| AIA-023 | A |
| AIA-017 | A |
| AIA-054 | A |
| AIA-003-D | A |
| AIA-003-A | A |
| AIA-033-B | A |
| AIA-086 | A |
| AIA-092 | A |
| AIA-033 | A |
| AIA-055 | A |
| AIA-040 | A |
| AIA-227-1 | A |
| AIA-227-2 | A |
| AIA-004-C | B |
| AIA-073 | B |
| AIA-004-B | B |
| AIA-013 | B |
| AIA-102 | B |
| AIA-003-C | B |
| AIA-033-A | B |
| AIA-103 | B |
| AIA-012 | B |
| AIA-057 | B |
| AIA-052 | C |
| AIA-053 | C |
| AIA-006 | C |
| AIA-056-A | C |
| AIA-056-B | C |
| AIA-009 | A |
| AIA-241 | A |
| AIA-242 | B |
| AIA-244-1 | A |
| AIA-244-2 | A |
| AIA-246 | A |
| AIA-248 | A |
| AIA-249 | C |
| AIA-250-1 | A |
| AIA-250-2 | A |
| AIA-252-1 | A |
| AIA-252-2 | A |
| AIA-253-1 | A |
| AIA-254 | A |
| AIA-255-3 | A |
| AIA-255-4 | A |
| AIA-255-5 | A |
| AIA-257 | A |
| AIA-257-1 | A |
| AIA-258-1 | A |
| AIA-258-2 | A |
| AIA-259-A | A |
| AIA-259-B | A |
| AIA-259-C | A |
| AIA-259-D | A |
| AIA-260-1 | A |
| AIA-260-2 | A |
| AIA-262-1 | A |
| AIA-262-2 | A |
| AIA-263-1 | A |
| AIA-263-2 | A |
| AIA-264 | A |
| AIA-265 | A |
| AIA-266-1 | A |
| AIA-266-2 | A |
| CP-AIA-270 | A |
| AIA-271 | A |
| AIA-273 | A |
| AIA-274-1 | A |
| AIA-274-2 | A |
| AIA-275 | A |
| AIA-283-1 | A |
| AIA-283-2 | A |
| AIA-284-1 | A |
| AIA-284-2 | A |
| AIA-149 | B |
| AIA-310 | A |
| HBV-AIA-039 | A |
| AIA-339-1 | C |
| AIA-339-2 | B |
| AIA-349-b | B |
| AIA-350 | C |
| AIA-351-a | C |
| AIA-352-1 | C |
| AIA-352-2 | A |
| AIA-354 | C |
| AIA-355 | C |
| AIA-363-1 | B |
| AIA-363-2 | B |
| AIA-364-1 | C |
| AIA-364-2 | B |
| AIA-365-1 | B |
| AIA-365-2 | A |
| AIA-366-1 | B |
| AIA-366-2 | A |
| AIA-367-1 | B |
| AIA-367-2 | A |
| AIA-369 | B |
| AIA-371 | C |
| AIA-372 | A |
| AIA-387-1 | B |
| AIA-387-2 | A |
| AIA-388 | B |
| AIA-394 | C |
| AIA-397 | C |
VII. 實例之立體化學 在揮發20天之後自EtOH獲得化合物AIA-227-2之0.08 × 0.10 × 0.20mm大小晶體且用於X射線繞射數據收集。在室溫下於Bruker SMART CCD面探繞射儀使用CuKα
輻射藉由ω/φ
掃描模式來收集數據。收集10846個反射,其中3754個反射係獨特的(Rint = 0.0507)。
晶體屬單斜晶體系統且具有空間群P21
/c。單位晶胞參數如下:a
= 6.6143(3),b
=14.0381(8),c
=23.6870(14)Å,α
=γ
=90.0°,β
=97.702(3)°,V= 2179.5(2)Å3
,Z=4。
藉由直接方法解析結構且針對F 2
藉由全矩陣最小平方方法使用SHELXTL程式來精修所有非H原子。將所有H原子皆置於幾何理想位置且迫使其騎於其親代原子上。使用多掃描吸收校正方法,且最大及最小透射參數分別為0.7531及0.6017。最終R
、wR 2
、GOF分別為0.0457、0.1293及1.024。
在不對稱單元中存在一個C21
H26
FClN4
O4
S分子且可在其間發現氫鍵,氫鍵在晶體結構之穩定堆積中發揮重要作用。
化合物AIA-227-2之ORTEP繪圖呈現於圖1中。化合物AIA-227-2之相對立體化學圖展示於圖2中。相關實例之化學結構中之所繪示立體化學係基於此指派。
以引用方式併入
本文所提及之所有公開案及專利(包含下文所列示之項目)之全部內容出於所有目的以引用方式併入本文中,其併入程度如同將每一個別公開案或專特定地及個別地以引用方式併入一般。倘若出現衝突,則以本申請案(包含本文中之任何定義)為準。
等效內容
儘管已論述本發明之具體實施例,但上述說明書具有闡釋性而非限制性。熟習此項技術者可在審閱本說明書後瞭解本發明之多個變化形式。本發明之完整範圍應參照申請專利範圍連同其等效內容之完整範圍及說明書且連同該等變化形式來確定。
除非另有指示,否則本說明書及申請專利範圍中用於表示成分量、反應條件等之所有數值皆應理解為在所有情況下皆受術語「約」修飾。因此,除非指示相反之情形,否則本說明書及隨附申請專利範圍中所列示之數字參數皆係可隨本發明尋求獲得之所要性質而變化之近似值。
圖1展示化合物CP-AIA-227-2之ORTEP繪圖。
圖2展示化合物CP-AIA-227-2之相對立體化學圖。
Claims (27)
- 一種式I化合物,式I 或其醫藥上可接受之鹽,其中: X1 係NRx1 、O或S; X2 係N或CRx2 ; X3 係O、NR7 、CR4 R8 、C(O)、S(O)t 、C=CR4 R0 或C=NR4 ; X4 及X6 獨立地係O或S; X5 係O、S或NR0 ; L係鍵或C1-6 伸烷基; L1 係鍵、C1-6 伸烷基、O、NRc 、C(O)、C(O)NRc 、S(O)t 或S(O)t NRc ; Rx1 及Rx2 獨立地選自由以下組成之群:氫、C1-6 烷基、鹵代C1-6 烷基及C3-6 單環烷基; Ra 、Rb 及Rc 在每次出現時獨立地選自由以下組成之群:氫、C1-6 烷基、鹵代C1-6 烷基及C3-6 單環烷基; Rd 係氫、OH、C1-6 烷基或C1-6 烷氧基; R0 、R6 、R8 及R11 在每次出現時獨立地選自由以下組成之群:氫、鹵素、OH、CN、NO2 、側氧基、Rd N=、肼基、甲醯基、疊氮基、矽基、矽氧基、HOC(O)-、Ra Rb N-、Ra Rb NS(O)t -、C1-6 烷基、C2-6 烯基、C2-6 炔基、C3-6 單環烷基、鹵代C1-6 烷基、羥基C1-6 烷基-、Ra Rb NC1-6 烷基-、HOC(O)C1-6 烷基-、Ra Rb NC1-6 烷基NRc -、C1-6 烷基NRa C1-6 烷基NRc -、C1-6 烷氧基、鹵代C1-6 烷氧基、羥基C1-6 烷氧基-、Ra Rb NC1-6 烷氧基-、C1-6 烷氧基C1-6 烷基-、鹵代C1-6 烷氧基C1-6 烷基-、Ra Rb NC(O)-、C1-6 烷基C(O)-、C1-6 烷氧基C(O)-、C1-6 烷基C(O)O-、C1-6 烷基S(O)q -、C1-6 烷基S(O)t NRc -、C1-6 烷基S(O)t C1-6 烷基-、C1-6 烷基S(O)t NRa C1-6 烷基-、C3-6 環烷基S(O)t C1-6 烷基-、C1-6 烷基C(O)C1-6 烷基-及C1-6 烷基C(O)OC1-6 烷基-; R0a 在每次出現時獨立地選自由以下組成之群:氫、鹵素、OH、CN、NO2 、Ra Rb N-、C1-6 烷基及鹵代C1-6 烷基; R1 係苯基、萘基、C3-6 單環烷基、C3-6 單雜環烷基或5至6員單環雜芳基,其中:該苯基、C3-6 單環烷基、C3-6 單雜環烷基或5至6員單環雜芳基視情況經一個、兩個或三個獨立經選擇之R11 基團取代; R2 係氫、鹵素、Ra Rb N、C1-6 烷基、鹵代C1-6 烷基、C3-6 單環烷基或C1-6 烷氧基; R3 係選自由以下組成之群:; R4 係R5 、R6 或R5 -L1 -; 或R4 及R8 與其所連接之碳原子一起形成基團; R4a 係氫或C1-6 烷基; R4b 係R5 、R5a 、R6 或R5 -L1 -; R5 係選自由以下組成之群: R6a 係氫或C1-6 烷基; R7 係氫、C1-6 烷基、C1-6 鹵代烷基、C1-6 烷氧基C1-6 烷基-、NRa Rb C(O)-、R7a C(O)-、C1-6 烷基氧基C(O)-、C1-6 烷基S(O)q -或C1-6 鹵代烷基S(O)q -; R7a 係C1-6 烷基或C3-6 單環烷基; q、r、t及w在每次出現時獨立地選自0、1及2;且 v在每次出現時獨立地選自0、1、2及3。
- 如請求項1之化合物或其醫藥上可接受之鹽,其中X1 係NRx1 ,X2 係N,且Rx1 係氫或甲基。
- 如請求項1或2之化合物或其醫藥上可接受之鹽,其中Rx1 係甲基。
- 如請求項1至3中任一項之化合物或其醫藥上可接受之鹽,其中L係鍵。
- 如請求項1至3中任一項之化合物或其醫藥上可接受之鹽,其中L1 係鍵。
- 如請求項1至5中任一項之化合物或其醫藥上可接受之鹽,其中R2 係Ra Rb N。
- 如請求項6之化合物或其醫藥上可接受之鹽,其中R2 係NH2 。
- 如請求項8之化合物或其醫藥上可接受之鹽,其中R11 在每次出現時獨立地選自由以下組成之群:F、Cl、Br及I。
- 如請求項18或19之化合物或其醫藥上可接受之鹽,其中R6 係C1-6 烷基S(O)t C1-6 烷基-或C1-6 烷基S(O)t NRa C1-6 烷基-。
- 如請求項20之化合物或其醫藥上可接受之鹽,其中R6 係C1-6 烷基S(O)t C1-6 烷基-,且t為1或2。
- 如請求項21之化合物或其醫藥上可接受之鹽,其中t為2。
- 如請求項18至22中任一項之化合物或其醫藥上可接受之鹽,其中R8 係氫、OH或C1-6 烷氧基。
- 如請求項23之化合物或其醫藥上可接受之鹽,其中R8 係OH。
- 一種醫藥組合物,其包括如請求項1至24中任一項之化合物或其醫藥上可接受之鹽及醫藥上可接受之賦形劑。
- 一種治療有需要個體中B型肝炎(HBV)感染之方法,該方法包括:向該個體投與治療有效量之如請求項1至24中任一項之化合物或其醫藥上可接受之鹽。
- 一種治療有需要個體中B型肝炎(HBV)感染之方法,該方法包括:向該個體投與治療有效量之如請求項25之醫藥組合物。
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201862748906P | 2018-10-22 | 2018-10-22 | |
| US62/748,906 | 2018-10-22 | ||
| US201962858790P | 2019-06-07 | 2019-06-07 | |
| US62/858,790 | 2019-06-07 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| TW202028190A true TW202028190A (zh) | 2020-08-01 |
Family
ID=68610300
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| TW108138129A TW202028190A (zh) | 2018-10-22 | 2019-10-22 | 用於治療hbv之5員雜芳甲醯胺化合物 |
Country Status (15)
| Country | Link |
|---|---|
| US (2) | US11560370B1 (zh) |
| EP (1) | EP3870296A1 (zh) |
| JP (1) | JP2022508953A (zh) |
| KR (1) | KR20210095143A (zh) |
| CN (1) | CN113195055A (zh) |
| AU (1) | AU2019364352A1 (zh) |
| BR (1) | BR112021007602A2 (zh) |
| CA (1) | CA3117449A1 (zh) |
| IL (1) | IL282433A (zh) |
| MA (1) | MA53983A (zh) |
| MX (1) | MX2021004580A (zh) |
| PH (1) | PH12021550887A1 (zh) |
| SG (1) | SG11202104086PA (zh) |
| TW (1) | TW202028190A (zh) |
| WO (1) | WO2020086533A1 (zh) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN111205264A (zh) * | 2020-02-25 | 2020-05-29 | 成都睿智化学研究有限公司 | 一种合成同位羟基和甲磺酰甲基化合物的新方法 |
| US20230295096A1 (en) * | 2020-04-22 | 2023-09-21 | Assembly Biosciences, Inc. | Pyrazole carboxamide compounds for treatment of hbv |
| WO2023069547A1 (en) * | 2021-10-20 | 2023-04-27 | Assembly Biosciences, Inc. | 5-membered heteroaryl carboxamide compounds for treatment of hbv |
| CN118339163A (zh) * | 2021-10-20 | 2024-07-12 | 组装生物科学股份有限公司 | 新的晶型 |
| WO2023105481A1 (en) * | 2021-12-10 | 2023-06-15 | Assembly Biosciences, Inc. | Pharmaceutical compositions for the treatment of hbv |
| WO2024173196A1 (en) * | 2023-02-17 | 2024-08-22 | Merck Sharp & Dohme Llc | Plasma kallikrein inhibitors |
Family Cites Families (25)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| BR0211742A (pt) * | 2001-08-06 | 2004-08-24 | Pharmacia Italia Spa | Derivados de aminoisoxazole ativos como inibidores de cinase |
| GB0228417D0 (en) * | 2002-12-05 | 2003-01-08 | Cancer Rec Tech Ltd | Pyrazole compounds |
| JP2010524941A (ja) | 2007-04-20 | 2010-07-22 | シェーリング コーポレイション | ピリミジノン誘導体およびそれらの使用方法 |
| JP5918124B2 (ja) * | 2009-05-12 | 2016-05-18 | ロマーク ラボラトリーズ エル.シー. | ハロアルキルヘテロアリールベンズアミド化合物 |
| WO2013006394A1 (en) | 2011-07-01 | 2013-01-10 | Institute For Hepatitis And Virus Research | Sulfamoylbenzamide derivatives as antiviral agents against hbv infection |
| US9968650B2 (en) | 2011-07-13 | 2018-05-15 | Indiana University Research And Technology Corporation | Modified viral structural protein with antiviral activity |
| UY34566A (es) | 2012-01-06 | 2013-07-31 | Janssen R & D Ireland | 1,4?dihidropirimidinas 4,4?disustituidas y su uso como medicamentos para el tratamiento de la hepatitis b |
| PL2890683T3 (pl) | 2012-08-28 | 2017-06-30 | Janssen Sciences Ireland Uc | Pochodne skondensowanego bicyklicznego sulfamylu i ich zastosowanie jako leki do leczenia wirusowego zapalenia wątroby typu B |
| UA123256C2 (uk) | 2012-08-28 | 2021-03-10 | ЯНССЕН САЙЄНСІЗ АЙРЛЕНД ЮСі | Сульфамоїлариламіди та їх застосування як лікарських препаратів для лікування гепатиту b |
| MA37942B1 (fr) | 2012-09-10 | 2020-01-31 | Hoffmann La Roche | Hétéroaryldihydropyrimidines d'acide 6-aminé pour le traitement et la prophylaxie d'une infection par le virus de l'hépatite b |
| CA2889892A1 (en) | 2012-11-09 | 2014-05-15 | Indiana University Research And Technology Corporation | Alternative uses for hbv assembly effectors |
| AU2013355220B2 (en) | 2012-12-06 | 2018-08-02 | Baruch S. Blumberg Institute | Functionalized benzamide derivatives as antiviral agents against HBV infection |
| BR112015015584A2 (pt) | 2012-12-27 | 2017-12-12 | Baruch S Blumberg Inst | novos agentes antivirais contra infecção por hbv |
| HUE034820T2 (en) | 2013-02-28 | 2018-02-28 | Janssen Sciences Ireland Uc | Sulphamoyl arylamides and their use as medicaments for the treatment of hepatitis B |
| ES2640063T3 (es) | 2013-04-03 | 2017-10-31 | Janssen Sciences Ireland Uc | Derivados de n-fenil-carboxamida y su uso como medicamentos para el tratamiento de la hepatitis B |
| AU2014267235B2 (en) | 2013-05-17 | 2017-10-05 | Janssen Sciences Ireland Uc | Sulphamoylthiophenamide derivatives and the use thereof as medicaments for the treatment of hepatitis B |
| JO3603B1 (ar) | 2013-05-17 | 2020-07-05 | Janssen Sciences Ireland Uc | مشتقات سلفامويل بيرولاميد واستخدامها كادوية لمعالجة التهاب الكبد نوع بي |
| US9266904B2 (en) | 2013-05-17 | 2016-02-23 | Hoffmann-La Roche Inc. | 6-bridged heteroaryldihydropyrimidines for the treatment and prophylaxis of hepatitis B virus infection |
| JP6348978B2 (ja) | 2013-07-25 | 2018-06-27 | ヤンセン・サイエンシズ・アイルランド・ユーシー | グリオキサミド置換ピロールアミド誘導体およびb型肝炎を処置するための医薬品としてのその使用 |
| ES2777248T3 (es) * | 2013-11-14 | 2020-08-04 | Novira Therapeutics Inc | Derivados de azepano y métodos de tratar infecciones por hepatitis B |
| CN110483484A (zh) | 2014-02-06 | 2019-11-22 | 爱尔兰詹森科学公司 | 氨磺酰基吡咯酰胺衍生物及其作为药物用于治疗乙型肝炎的用途 |
| US9884831B2 (en) * | 2015-03-19 | 2018-02-06 | Novira Therapeutics, Inc. | Azocane and azonane derivatives and methods of treating hepatitis B infections |
| CN105503730B (zh) * | 2015-12-25 | 2018-06-22 | 山东大学 | 吡唑类衍生物及其制备方法与应用 |
| JOP20180008A1 (ar) * | 2017-02-02 | 2019-01-30 | Gilead Sciences Inc | مركبات لعلاج إصابة بعدوى فيروس الالتهاب الكبدي b |
| CN108250112B (zh) * | 2018-01-30 | 2019-08-27 | 西北大学 | 一种1-烷基-1-芳硫基-2-(1h)-萘酮衍生物及其制备方法 |
-
2019
- 2019-10-22 CN CN201980082985.8A patent/CN113195055A/zh active Pending
- 2019-10-22 US US17/287,681 patent/US11560370B1/en active Active
- 2019-10-22 SG SG11202104086PA patent/SG11202104086PA/en unknown
- 2019-10-22 JP JP2021547054A patent/JP2022508953A/ja active Pending
- 2019-10-22 MX MX2021004580A patent/MX2021004580A/es unknown
- 2019-10-22 TW TW108138129A patent/TW202028190A/zh unknown
- 2019-10-22 WO PCT/US2019/057362 patent/WO2020086533A1/en active Application Filing
- 2019-10-22 KR KR1020217015135A patent/KR20210095143A/ko unknown
- 2019-10-22 CA CA3117449A patent/CA3117449A1/en active Pending
- 2019-10-22 BR BR112021007602-6A patent/BR112021007602A2/pt unknown
- 2019-10-22 MA MA053983A patent/MA53983A/fr unknown
- 2019-10-22 AU AU2019364352A patent/AU2019364352A1/en active Pending
- 2019-10-22 EP EP19805797.8A patent/EP3870296A1/en active Pending
-
2021
- 2021-04-19 IL IL282433A patent/IL282433A/en unknown
- 2021-04-21 PH PH12021550887A patent/PH12021550887A1/en unknown
-
2022
- 2022-11-17 US US17/989,237 patent/US12030869B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| WO2020086533A1 (en) | 2020-04-30 |
| JP2022508953A (ja) | 2022-01-19 |
| MX2021004580A (es) | 2021-09-08 |
| US11560370B1 (en) | 2023-01-24 |
| PH12021550887A1 (en) | 2022-02-21 |
| EP3870296A1 (en) | 2021-09-01 |
| IL282433A (en) | 2021-06-30 |
| KR20210095143A (ko) | 2021-07-30 |
| AU2019364352A1 (en) | 2021-06-03 |
| US12030869B2 (en) | 2024-07-09 |
| CN113195055A (zh) | 2021-07-30 |
| CA3117449A1 (en) | 2020-04-30 |
| MA53983A (fr) | 2021-12-15 |
| SG11202104086PA (en) | 2021-05-28 |
| BR112021007602A2 (pt) | 2021-07-27 |
| US20240150324A1 (en) | 2024-05-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7150903B2 (ja) | B型肝炎ウイルスコアタンパク質モジュレーター | |
| US11759462B2 (en) | Spirocyclic compounds as tryptophan hydroxylase inhibitors | |
| TW202028190A (zh) | 用於治療hbv之5員雜芳甲醯胺化合物 | |
| AU2013272701A1 (en) | Imidazo[1,2-b]pyridazine derivatives as kinase inhibitors | |
| MX2011001333A (es) | Derivados de pirazolo [3, 4] pirimidin-4-ilo y sus usos para tratar la diabetes y obesidad. | |
| US20230183213A1 (en) | 5-membered heteroaryl carboxamide compounds for treatment of hbv | |
| KR20230142745A (ko) | Cdk2 억제제 및 그의 사용 방법 | |
| TW202315870A (zh) | 布魯頓氏酪胺酸激酶之抑制劑 | |
| CN113166086A (zh) | 用于治疗hbv的环状磺酰胺化合物 | |
| US20230295096A1 (en) | Pyrazole carboxamide compounds for treatment of hbv | |
| WO2023079294A1 (en) | Phthalazine derivatives as pyruvate kinase modulators | |
| WO2023069547A1 (en) | 5-membered heteroaryl carboxamide compounds for treatment of hbv | |
| WO2021216661A1 (en) | Pyrazole carboxamide compounds for treatment of hbv | |
| TW202409010A (zh) | 人類呼吸道融合病毒及人類間質肺炎病毒之抑制劑 | |
| EP4426681A1 (en) | Phthalazine derivatives as pyruvate kinase modulators |